 |
|
con_1_1 |
정 정 신 고 (보고)
| 2026년 04월 29일 |
| 1. 정정대상 공시서류 : | 주주총회소집 공고 |
| 2. 정정대상 공시서류의 최초제출일 : | 2026.04.16 |
| 3. 정정사항 |
| 항 목 | 정정사유 | 정 정 전 | 정 정 후 |
|---|---|---|---|
| 1. 일시 | 임시주총일 연기 | 2026.04.30 | 2026.05.28 |
| 2. 장소 | 임시주총장소 변경 | 서울시 강남구 테헤란로 7길22(역삼동635-4)한국과학기술회관2관 지하1층 소회의실 3 | 서울시 구로구 디지털로 26길5, 에이스하이엔드타워1차 옥상층 세미나실 |
| 제2호의안 : 자본 감소 승인의 건 | 임시주총일 연기에 따른 일정조정 | 3. 주주총회 일자 : 2026년 04월 30일 | 3. 주주총회 일자 : 2026년 05월 28일 |
| 감자기준일(권리배정기준일) | 임시주총일 연기에 따른 일정조정 | 2026년 05월 16일 | 2026년 06월 14일 |
| 5. 감자일정 | 임시주총일 연기에 따른 일정조정 | 1) 주주총회 예정일 : 2026년 04월 30일 | 1) 주주총회 예정일 : 2026년 05월 28일 |
| 2) 병합기준일 : 2026년 05월17일 | 2) 병합기준일 : 2026년 06월15일 | ||
| 3) 효력발생일 : 2026년 5월17일 | 3) 효력발생일 : 2026년 06월15일 | ||
| 4) 매매거래 정지기간 : 2026년 05월 15일~2026년 06월 04일 | 4) 매매거래 정지기간 : 2026년 06월 11일~2026년 07월 02일 |
||
| 4) 신주상장 예정일 : 2026년 06월 05일 | 4) 신주상장 예정일 : 2026년 07월 03일 | ||
| 주주총회 목저사항별 기재사항 | 자본의 감소 : 감자 기준일 변경 | 2026년 05월16일 | 2026년 06월 14일 |
| 사업보고서 및 감사보고서 첨부 | 제출 예정일 | 2026년 04월 23일 | 2026년 05월 21일 |
주주총회소집공고
| 2026년 04월 15일 | ||
| 회 사 명 : | 진원생명과학(주) | |
| 대 표 이 사 : | 고광연, 한우근 | |
| 본 점 소 재 지 : | 서울 구로구 디지털로26길 5 | |
| (전 화)02-6949-4056 | ||
| (홈페이지)https://www.genels.com | ||
| 작 성 책 임 자 : | (직 책)상무이사 | (성 명)전경하 |
| (전 화)02-6949-4056 | ||
주주총회 소집공고
| (제51기 임시) |
제51기 임시주주총회 소집통지서
주주님의 건승과 댁내의 평안을 기원합니다.
당사는 상법 제365조와 정관 제15조에 따라 제51기 임시주주총회를 아래와 같이 소집하오니 참석하여 주시기 바라오며, 상법 제542조의4 및 정관 제15조의2에 의거하여 발행주식총수의 1% 이하 소유주주에 대한 소집통지는 본 공고로 갈음하오니 양지하여 주시기 바랍니다.
- 아 래 -
1. 일 시 : 2026년 5월 28일(목) 오전 09시 00분
2. 장 소 : 서울시 구로구 디지털로 26길5, 에이스하이엔드타워1차 옥상층 세미나실
3. 회의 목적 사항
가. 보고사항 : 감사보고 및 제50기(2025년도) 별도 및 연결 재무제표 승인 보고(상법 제449조의 2에 의한 요건 충족); 2026년 4월13일 이사회 결의로 재무제표 승인함.
나. 부의안건 :
제1호 의안 : 이사 선임의 건
제1-1호 의안 : 사내이사 이준규 선임의 건
제1-2호 의안 : 사내이사 전경하 선임의 건
제1-3호 의안 : 사내이사 김훈범 선임의 건
| 후보자 성명 | 주된 직업 | 약력 | 해당법인과의 최근 3년간 거래내역 |
|---|---|---|---|
| 이준규 | 전문경영인 | (전) 군인공제회 (전) (주)디에이치산업 대표이사 (전) (주)제주컨트리구락부 사장 |
없음 |
| 전경하 | 전문경영인 | 고려대학교 법학과 졸업 (전) 어린이집안전공제회 본부장 (현) 진원생명과학 상무이사 |
앖음 |
| 김훈범 | 전문경영인 | Drexel University, 마케팅&국제경제학과 졸업(B.A) Widener University School of Law 졸업 (현) Mirage Entertainment & Design 이사 |
없음 |
제2호 의안 : 자본 감소 승인의 건
1. 자본 감소의 목적 : 결손금 보전을 위한 재무구조 개선
2. 자본 감소의 방법 : 기명식 보통주 5주를 동일한 액면주식 1주로 무상병합
3. 주주총회 일자 : 2026년 5월 28일
4. 자본 감소의 목적인 주식의 종류와 수, 감소비율 및 기준일
| 감자 주식의 종류 | 진원생명과학㈜ 기명식 보통주 |
| 감자 주식 수 | 72,706,326 |
| 감자 비율 | 80% |
| 감자 기준일(권리배정기준일) | 2026년 06월14일 |
|
감자 전 자본금 (발행 주식수) |
90,882,907,000원 (90,882,907주) |
|
감자 후 자본금 (발행 주식수) |
18,176,581,000원 (18,176,581주) |
5. 감자일정
1) 주주총회 예정일 : 2026년 5월 28일
2) 병합기준일 : 2026년 06월 15일
3) 효력발생일 : 2026년 06월 15일
4) 매매거래 정지기간 : 2026년 06월 11일~2026년 07월 02일
5) 신주상장 예정일 : 2026년 07월 03일
6. 단주수 처리방법 : 주식병합으로 1주 미만의 단주에 대해서는 신주상장 초일 종가 기준으로 계산 하여 현금 지급
7. 상기 일정 및 감소사항은 주주총회 결의 과정 및 자본감소 절차 진행에 따라 필요한 경우 관계기관 과의 협의 실무처리 과정에서 변경될 수 있으며, 기타 상기에 결정되지 않은 세부사항의 결정은 대 표이사에게 그 결정을 위임함.
4. 경영참고사항 비치
상법 제542조의 4에 의거하여 경영참고사항을 당사의 본점, 금융위원회, 한국거래소 및 명의개서대행기관 하나은행에 비치하오니 참고하시기 바랍니다.
5. 예탁결제원 의결권 행사(섀도우보팅)제도 폐지에 따른 실질주주의 의결권 행사에 관한 사항
예탁결제원의 의결권 행사(섀도우보팅)제도가 2018년 1월 1일부터 폐지됨에 따라 금번 주주총회는 한국예탁결제원이 주주님들의 의결권을 행사할 수 없습니다. 따라서 주주님께서는 한국예탁결제원에 의결권행사에 관한 의사 표시를 하실 필요가 없으며, 종전과 같이 주주총회에 참석하여 의결권을 직접 행사하시거나 또는 위임장에 의거 의결권을 간접행사 할 수 있습니다.
7. 주주총회 참석시 준비물
가. 직접행사: 신분증
나. 대리행사: 위임장(주주와 대리인의 인적사항 기재, 인감 날인), 대리인의 신분증
2026년 4월 15일
진원생명과학 주식회사
대표이사 고광연, 한우근 (직인 생략)
I. 사외이사 등의 활동내역과 보수에 관한 사항
1. 사외이사 등의 활동내역
가. 이사회 출석률 및 이사회 의안에 대한 찬반여부
| 회차 | 개최일자 | 의안내용 | 사외이사 등의 성명 | |||||
|---|---|---|---|---|---|---|---|---|
| 고광연 (출석률: 95.5%) |
한우근 (출석률:95.5 %) |
사중진 (출석률:95.5 %) |
신문식사외이사 (출석률:72.7%) |
정봉기사오이이사 (출석률:22.7%) |
김용묵 감사 (출석률:54.5%) |
|||
| 찬 반 여 부 | ||||||||
| 제50-54차 | 2026.01.19 | 의안 제1호 :담보제공 진행의 건 | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 |
| 제50-55차 | 2026.01.26 | 의안 제1호 : [4차정정]유상증자의 건(제3자배정) | 찬성 | 찬성 | 찬성 | 불참 | 불참 | 찬성 |
| 제50-56차 | 2026.01.30 | 의안 제1호 : [2차정정]제7회차 무기명식 무보증 사모전환사채 발행 결정의 건 |
찬성 | 찬성 | 불참 | 찬성 | 찬성 | 찬성 |
| 제50-57차 | 2026.02.02 | 의안 제1호 : 차입 진행의 건 | 찬성 | 불참 | 찬성 | 찬성 | 불참 | 찬성 |
| 제50-58차 | 2026.02.09 | 의안 제1호 : [5차정정]유상증자의 건(제3자배정) | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 |
| 제50-59차 | 2026.02.09 | 의안 제1호 : 차입 진행의 건 | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 |
| 제50-60차 | 2026.02.24 | 의안 제1호 : [6차정정]유상증자의 건(제3자 배정) | 찬성 | 찬성 | 찬성 | 찬성 | 불참 | 찬성 |
| 제50-61차 | 2026.03.04 | 의안 제1호 : [7차정정]유상증자의 건(제3자 배정) | 찬성 | 찬성 | 찬성 | 불참 | 불참 | 불참 |
| 제50-62차 | 2026.03.04 | 의안 제1호 : 질권설정 진행 건 | 찬성 | 찬성 | 찬성 | 불참 | 불참 | 불참 |
| 제50-63차 | 2026.03.05 | 의안 제1호 : 제6회차 전환사채 만기전 취득의 건 | 찬성 | 찬성 | 찬성 | 불참 | 불참 | 불참 |
| 제50-64차 | 2026.03.13 | 의안 제1호 : 제50기 정기주주총회 소집의 건 | 찬성 | 찬성 | 찬성 | 찬성 | 불참 | 찬성 |
| 의안 제2호 : 전자투표 및 전자위임장권유제도 이용의 건 | 찬성 | 찬성 | 찬성 | 찬성 | 불참 | 찬성 | ||
| 제50-65차 | 2026.03.20 | 의안 제1호 : 대출 진행의 건 | 찬성 | 찬성 | 찬성 | 불참 | 불참 | 불참 |
| 제50-66차 | 2026.03.20 | 의안 제1호 : 제51기 임시주주총회 소집의 건 | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 |
| 의안 제2호 : 자본 감소 결정의 건 | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 | ||
| 제50-67차 | 2026.03.20 | 의안 제1호 : 제51기 임시주주총회 소집의 건(문구 수정) | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 |
| 의안 제2호 : 자본 감소 결정의 건 | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 | 찬성 | ||
| 제50-68차 | 2026.03.25 | 의안 제1호 : 2차정정]제7회차 무기명식 무보증 사모전환사채 발행 결정의 건 |
찬성 | 찬성 | 찬성 | 찬성 | 불참 | 찬성 |
| 제50-69차 | 2026.03.30 | 의안 제1호 : 감사전 연결 및 별도 재무제표 결정의 건 | 찬성 | 찬성 | 찬성 | 찬성 | 불참 | 찬성 |
| 제51-01차 | 2026.03.31 | 의안 제1호 : 임원 보수 결정의 건 | 불참 | 찬성 | 찬성 | 찬성 | 불참 | 불참 |
| 의안 제2호 : 미등기임원 선임 및 담당업무 위촉의 건 | 불참 | 찬성 | 찬성 | 찬성 | 불참 | 불참 | ||
| 의안 제3호 : 미등기임원의 보수한도 및 임기 결정의 건 | 불참 | 찬성 | 찬성 | 찬성 | 불참 | 불참 | ||
| 제51-02차 | 2026.04.02 | 의안 제1호 : [4차정정]제7회차 무기명식 무보증 사모전환사채 발행 결정의 건 |
찬성 | 찬성 | 찬성 | 찬성 | 불참 | 불참 |
| 제51-03차 | 2026.04.13 | 의안 제1호 : 본점 이전의 건 | 찬성 | 찬성 | 찬성 | 불참 | 불참 | 불참 |
| 제51-04차 | 2026.04.13 | 의안 제1호 : 제50기(2025년도) 별도 및 연결재무제표 승인의 건 | 찬성 | 찬성 | 찬성 | 찬성 | 불참 | 불참 |
| 의안 제2호 : 제51기 임시주주총회 의안 확정의 건 | 찬성 | 찬성 | 찬성 | 찬성 | 불참 | 불참 | ||
| 제51-05차 | 2026.04.13 | 의안 제1호 : 제7회 전환사채 수납대행 및 사채원리금 지급대행 은행 변경의 건 | 찬성 | 찬성 | 찬성 | 찬성 | 불참 | 불참 |
| 제51-06차 | 2026.04.14 | 의안 제1호 : 해외 종속회사(DIV) 채권 출자전환의 건 | 찬성 | 찬성 | 찬성 | 찬성 | 불참 | 불참 |
나. 이사회내 위원회에서의 사외이사 등의 활동내역
| 위원회명 | 구성원 | 활 동 내 역 | ||
|---|---|---|---|---|
| 개최일자 | 의안내용 | 가결여부 | ||
| 보수위원회 | 사외이사 | 2026.04.13 | 의안 제1호 : 2026년도 보수 결정의 건 | 가결 |
2. 사외이사 등의 보수현황
| (단위 : 백만원) |
| 구 분 | 인원수 | 주총승인금액 | 지급총액 | 1인당 평균 지급액 |
비 고 |
|---|---|---|---|---|---|
| 사외이사 | 2 | 50,000 | 23 | 12 | 2025년 기준 |
| 사내이사 | 3 | 119 | 40 | 2025년 기준 | |
| 감사 | 1 | 500 | 11 | 11 | 2025년 기준 |
II. 최대주주등과의 거래내역에 관한 사항
1. 단일 거래규모가 일정규모이상인 거래
| (단위 : 억원) |
| 거래종류 | 거래상대방 (회사와의 관계) |
거래기간 | 거래금액 | 비율(%) |
|---|---|---|---|---|
| - | - | - | - | - |
2. 해당 사업연도중에 특정인과 해당 거래를 포함한 거래총액이 일정규모이상인 거래
| (단위 : 억원) |
| 거래상대방 (회사와의 관계) |
거래종류 | 거래기간 | 거래금액 | 비율(%) |
|---|---|---|---|---|
| Dong-il Interlining Ltd. (종속회사) |
매출 | 2025.01.01~2025.12.31 | 34 | 2.48 |
| 매입 | 2025.01.01~2025.12.31 | 17 | 1.24 | |
| VGXI, Inc. (종속회사) |
이자수익 | 2025.01.01~2025.12.31 | 74 | 5.40 |
| 매입 | 2025.01.01~2025.12.31 | 103 | 9.13 |
III. 경영참고사항
1. 사업의 개요
가. 업계의 현황
1) 산업의 특성
① 바이오의약품 산업
21세기 들어 바이오텍 회사들의 성장과 함께 바이오산업이 빠르게 약진하고 있으며 단클론 항체, 단백질 치료제, 그리고 백신 관련 분야의 약진이 돋보이고 있습니다.
특히 백신 개발 다국적 제약사들은 차세대 백신의 연구개발에 집중하여 보다 효과적이고 안전한 백신들이 개발되고 있습니다.
백신 사업 분야는 암, HIV, 자가면역질환 등으로 적응증이 확대되고 있으며, 특히 예방백신 분야에서 치료백신 분야로 넓혀지고 있는 추세입니다.
일반적으로 바이오 의약품의 개발은 장기간 대규모 자금이 소요되면서도 성공 확률이 높지 않은 특성으로 인하여 리스크가 큰 사업입니다.
하지만, 리스크가 큰 만큼 성공할 경우 반대 급부 또한 큰 특성을 가지고 있습니다.
② 바이오의약품 CDMO 산업
바이오 의약품은 신약 개발에서 제품 판매에 이르기까지 오랜 시간과 대규모의 투자를 필요로 하기에 전체 프로세스를 일원화할 수 있는 기업은 몇몇 소수의 대규모 다국적 제약회사를 제외하고는 많지 않습니다.
특히, 바이오 의약품 CDMO 산업은 첨단생명공학 기술이 요구되고, 첨단설비를 갖추는데 막대한 설비투자비 및 품질관리 기술을 필요로 하고 있음에 따라 최적의 비용과 고효율로
제품의 생산을 전담할 수 있는 위탁생산 전문기업(CDMO)의 출현이 요구되고 있고 관련 시장도 급격히 성장하고 있습니다.
③ 섬유산업
섬유산업은 섬유 원료 및 원사에서 최종 의류, 산업용 섬유 소재 및 제품생산까지 전 제조 산업 분야를 비롯하여 디자인, 유통, 마케팅 등의 전 연관 산업을 포함하는 산업이며, 생산구조는 원료, 사, 직물, 염색, 의류, 제조, 유통으로 이어지는 다단계로 형성되어 있고 고용 창출 효과와 고부가가치를 실현할 수 있는 가공 산업입니다.
2) 산업의 성장성
① DNA 백신 및 핵산 기반 치료제 분야
시장 분석 기관인 리서취앤마켓닷컴(ResearchAndMarkets.com)은 DNA 백신 시장을 2019년부터 2027년까지의 연평균성장률(CAGR) 42.03%를 예측하였습니다. 또 다른 보고서인 DNA 백신 시장 보고서 2030 (DNA Vaccine Market Report: Trends,Forecast and Competitive Analysis to 2030 (2030년 10월, 리서치사: Lucintel)에 따르면, DNA 백신 시장은 2024년부터 2030년까지 6.5%의 연평균 복합 성장률
(CAGR) 로 성장을 지속하여 2030년까지 약 8억 달러 규모에 이를 것으로 예상하고, 시장조사기관인 모르도르 인텔리전스(Mordor Intelligence)가 2023년 8월 발행한 시장보고서 '핵산 기반 치료제 시장의 규모 및 시장의 성장 경향과 이의 예측(Nucleic
Acid-based Therapeutics Market Size & Share Analysis-Growth Trends &
Forecasts) 2023-2028)에 따르면, 세계의 핵산 기반 치료제 시장규모는 2023년 48억 9,000만달러이며 2023년부터 2028년까지 연평균성장률(CAGR) 14.29%로 2028년에는 95억4,000만 달러 규모에 달할 것으로 예측하였습니다. 특히, mRNA 백신과 치료제 시장은 “mRNA 백신과 치료제 시장의 산업의 경향과 이의 성장 예측 2025-2030(mRNA Vaccine and Therapeutics-Market Share Analysis, Industry Trends & Statistics, Growth Forecast, 2025-2030; 2023년 3월, 리서치사: Mordor
Intelligence)에 따르면, 2025년 638억 9,000만 달러, 2030년에는 1,388억 8,000만 달러에 달할 것으로 예측 기간(2025-2030년)의 CAGR은 16.8%를 나타낼 것이라 전망하였습니다.
핵산 기반 치료제 시장은 주로 유전질환과 유전적 장애를 대상으로 하는 치료제로 개발이 되고 있습니다. 기존 치료제들이 치료 효능이 거의 없거나 크지 않아, 혁신 의약품으로 평가를 받고 있습니다.
② 플라스미드 DNA CDMO 산업
플라스미드 DNA는 최근 미국 및 전 세계에 시판된 바이러스 운반체 기반 유전자치료제들의 원료물질로 이용되고 있고, 플라스미드 DNA 유전자치료제에서는 주성
분으로 이용되고 있어, 전 세계 유전자치료제 의약품 생산의 근간을 이루는 중요한 역할을 하고 있습니다. 즉, AAV 운반체 기반 유전자치료제 또는 렌티바이러스 운반
체 기반 유전자치료제를 생산하기 위해서는 반드시 플라스미드 DNA의 의약품 생산이 전제되어야 합니다. 따라서, 최근 전 세계 유전자치료제 시장의 급속한 성장에 힘입어, 플라스미드 DNA의 의약품 위탁개발생산 산업의 성장이 가속화되고 있습니다.
글로벌 시장조사기관 프레시던스 리서치(Precedence Research)에 따르면, 글로벌 플라스미드 DNA 제조시장 규모는 2022년 4억 4,613만 달러로 추정되며, 2022년부
터 2030년까지 연평균성장률(CAGR) 21.7%로 2030년에는 21억 5,658만 달러에 이를 것으로 예상됩니다.
③ 섬유산업
- 섬유 산업의 구조
- 산업구조
우리나라의 섬유산업은 원자재의 1/3을 해외에서 수입, 가공하여 완제품을 만들어 그 완제품의 2/3를 해외로 수출하는 해외의존형, 수출주도형 산업구조
- 생산구조
원료·사·직물·염색·의류·제조·유통으로 이어지는 다단계로 형성되어 있고 고용 창출 효과와 고부가가치를 실현할 수 있는 가공산업
 |
|
con_1_1 |
- 섬유산업의 위상
4차 산업혁명을 선도하는 미래 핵심산업
섬유산업 업체수는 ‘23년 기준 53,537개로 제조업대비 10.0% 차지, 고용인원은
240,091명으로 5.2%를 점유
- 섬유패션산업 일반현황(‘23년, 조사기준)
| 구분 | 업체수(개사) | 고용(명) | 생산(십억원) | 부가가치(십억원) |
|---|---|---|---|---|
| 제조업 | 537,580 | 4,156,969 | 1,995,947 | 672,555 |
| 섬유패션산업 | 53,357 | 240,091 | 40,298 | 17,403 |
| 비중(%) | 10.0 | 5.8 | 2.0 | 2.6 |
자료: (업체수, 고용) 전국사업체조사(1인이상, `23년), (생산, 부가가치) 광업제조업 조사 (10인이상, `23년)
- 세계 17위의 섬유·의류 수출국
섬유·의류 수출 세계 17위 : 섬유소재 수출 세계 9위, 의류수출 세계 35위
중국(1), 방글라데시(2), 독일(3), 이탈리아(4), 베트남(5), 인도(6), 튀르키예(7), 네덜란드(8), 프랑스(9), 스페인(10)(‘23년 기준)
※ 주 : 중국은 홍콩, 마카오 포함, EU 통합 집계시 한국 11위
'24년 섬유류 수출은 104.6억불, 수입 192.6억불로 무역수지 88.0억불 적자
섬유패션산업 무역수지는 단일산업 최초로 수출 100억불을 달성한 ‘87년부터 ‘01년까지 매년 100억불 이상 흑자 기록
- 국민의 의(衣)생활을 선도하는 주요 생활산업
국내 섬유·패션산업은 제조업체가 62,101개(1인이상), 섬유패션 도소매업 및 서비스업 포함시 관련 업체가 291,390개사에 달하는 등 국민 경제·생활에 기여 효과가 매우 큰 산업임
- 우리나라 섬유패션산업은 원사, 직물, 염색가공, 패션의류 등 Up Stream에서
Down Stream까지 균형된 생산기반을 보유하고 있으며 생산기술도 고르게 발달됨
의류용의 경우 중·저가 범용품보다 고부가가치 기능성 섬유, 친환경섬유에 치중 하는 한편 산업용섬유 등 신섬유 개발 및 생산 확대를 위한 기술력과 제품화 수준 을 고도화하고 있음
- 수출
섬유류 수출 추이(단위: 백만불, 천톤, $/kg)
| 구분 | '90년 | '95년 | '00년 | '05년 | '10년 | '15년 | '16년 | '17년 | '18년 | '19년 | '20년 | '21년 | '22년 | '23년 | '24년 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 금액 | 14,766 | 18,656 | 18,783 | 13,650 | 13,980 | 14,490 | 13,807 | 13,742 | 14,080 | 12,959 | 11,238 | 12,807 | 12,301 | 10,922 | 10,463 |
| 물량 | 2,863 | 2,399 | 3,593 | 2,863 | 2,747 | 2,710 | 2,768 | 2,868 | 2,879 | 2,734 | 2,418 | 2,658 | 2,323 | 2,142 | 2,102 |
| 단가 | 5.16 | 7.78 | 5.23 | 4.77 | 5.09 | 5.35 | 4.99 | 4.79 | 4.89 | 4.74 | 4.65 | 4.82 | 5.29 | 5.10 | 5.20 |
자료 : 한국무역협회 무역통계(KITA)
- 수입
섬유류 수입 추이(단위: 백만불, 천톤, $/kg)
| 구분 | '90년 | '95년 | '00년 | '05년 | '10년 | '15년 | '16년 | '17년 | '18년 | '19년 | '20년 | '21년 | '22년 | '23년 | '24년 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 금액 | 2,316 | 5,214 | 4,788 | 6,723 | 9,739 | 14,287 | 14,491 | 15,175 | 17,120 | 17,110 | 16,203 | 18,299 | 19,901 | 18,873 | 19,261 |
| 물량 | 404 | 861 | 1,089 | 1,307 | 1,656 | 1,909 | 2,073 | 2,101 | 2,176 | 2,238 | 2,238 | 2,348 | 2,271 | 2,293 | 2,388 |
| 단가 | 5.74 | 6.05 | 4.39 | 5.14 | 5.88 | 7.48 | 6.99 | 7.22 | 7.87 | 7.65 | 7.24 | 7.79 | 8.77 | 8.23 | 8.06 |
자료 : 한국무역협회 무역통계(KITA)
- 무역수지
섬유산업은 ‘87년부터 ’02년까지 매년 100억불 이상의 무역수지 흑자를 기록하였으나, 이후 의류 수출감소에 반해 수입은 지속적으로 증가하여 무역수지는 점차 감소
- 섬유산업 무역수지 추이(단위: 백만불)
| 구분 | '90년 | '95년 | '00년 | '05년 | '10년 | '15년 | '16년 | '17년 | '18년 | '19년 | '20년 | '21년 | '22년 | '23년 | '24년 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수출 | 14,766 | 18,656 | 18,783 | 13,650 | 13,980 | 14,490 | 13,807 | 13,742 | 14,080 | 12,959 | 11,238 | 12,807 | 12,301 | 10,922 | 10,463 |
| 수입 | 2,316 | 5,214 | 4,788 | 6,723 | 9,739 | 14,287 | 14,491 | 15,175 | 17,120 | 17,110 | 16,203 | 18,299 | 19,901 | 18,873 | 19,261 |
| 수지 | 12,450 | 13,442 | 13,995 | 6,928 | 4,241 | 203 | -684 | -1,433 | -3,040 | -4,151 | -4,965 | -5,492 | -7,601 | -7,951 | -8,798 |
자료 : 한국무역협회 무역통계(KITA)
- 해외투자
섬유산업의 해외투자는 ‘80년대 중반까지 거의 이루어지지 않았으나, 80년 후반 인력난, 높은 임금 상승률 등으로 생산여건이 악화되면서 크게 증가
- 섬유산업 해외투자 추이(단위: 건, 백만불,%)
| 구분 | ‘90년 | ‘00년 | ‘10년 | ‘15년 | ‘20년 | ‘24년 | 누계 | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 법인 | 금액 | 법인 | 금액 | 법인 | 금액 | 법인 | 금액 | 법인 | 금액 | 법인 | 금액 | 법인 | 금액 | |
| 제조업 | 207 | 591 | 1,098 | 1,648 | 1,174 | 7,721 | 1,174 | 8,046 | 654 | 13,978 | 818 | 16,170 | 39,173 | 259,880 |
| 섬유 | 64 | 85 | 234 | 156 | 135 | 373 | 110 | 451 | 44 | 568 | 67 | 503 | 6,208 | 12,914 |
| 비중 | 30.9 | 14.4 | 21.3 | 9.5 | 11.5 | 4.8 | 9.4 | 5.6 | 6.7 | 4.1 | 8.2 | 3.1 | 15.8 | 5.0 |
자료 : 한국수출입은행
주 : 비중은 제조업내 섬유산업 비중, 누계는 1968년부터 2024년까지 누계치임
업종별로는 노동집약적인 특성을 지니고 있는 봉제산업 진출이 활발하며, 최근에는 화섬, 면방 대기업의 해외진출이 확대됨.
(한국섬유산업연합회 발췌)
3) 경기변동의 특성
① 바이오 의약품 산업
최근 국내를 포함한 글로벌 제약산업 및 바이오 의약품 시장도 세계 경기침체의 영향을 받고 있어 지적재산권의 보호, R&D 생산성, 그리고 효과성이 중시되고 있습니다.
하지만, 사람의 건강과 직결되는 산업의 특징상 타 산업에 비해 경기변동의 영향을 상대적으로 적게 받는다고 할 수 있습니다. 특히 평균연령의 증가, 다양한 질병 및 새로운 감염성 질환들의 등장 등으로 인하여 바이오 의약품에 대한 요구와 수요가 증가하여 경기변동과 무관하게 지속적인 성장을 보이고 있습니다.
② 바이오의약품 CDMO 산업
바이오 의약품 CDMO 산업은 주로 정부의 지원을 통해 의약품을 개발하는 바이오 벤처사 또는 전문연구기관인 특성을 가지고 있으면서, 임상시험에 소요되는 바이오 의약품을 생산해 주는 산업으로이니만큼 임상시험이 진행되는 1~3년 단위의 생산계약이 이루어져 여타의 산업에 비하여 경기변동에 상대적으로 덜 민감하다고 할 수 있습니다. 하지만 경기가 극도로 악화되는 경우에는 제약산업의 시장규모 축소로
CDMO 산업도 영향을 받을 수 있습니다.
③ 섬유산업
섬유산업은 국제경기, 환율변동 및 유가 상승 등의 외적인 영향으로 인한 경기변동이
심한 편입니다.
4) 경쟁 요소 및 향후 전망
① 핵산 기반 치료제 분야
DNA 백신 개발 기술은 약독화 생백신 또는 불활성화 바이러스 백신과 같이 기존 백신 플랫폼에 비해 본질적으로 더 안전하고 개발 비용이 저렴하여 상대적으로 높은 안정성과 온도 민감성이 낮아 대량생산 및 유통 경비가 적게 소요되는 이점이 있습니다. 반면에, 낮은 수준의 세포내/핵내 수송으로 면역원성이 낮아서 적절한 효능을 확인하기 위해서는 DNA 백신의 양을 늘려야 하고 비임상에서 확인된 효능이 임상에 완전히 적용되지 않고 있어 임상용 DNA 백신 개발 경쟁사가 많지 않습니다. 당사는
DNA 백신이 갖는 한계를 보완해서 중증열성혈소판감소증후군(SFTS) 예방용 DNA 백신 후보물질을 개발하여 임상시험 진입을 위해 필요한 비임상 시험을 마쳤으며,
임상1상 시험을 준비하고 있습니다. 국내외 경쟁사로 모더나/국립감염병연구소를 비롯하여 15여 곳이 있지만 대부분 mRNA 백신, 약독화 혹은 재조합 형태입니다. 뿐만
아니라 이들 물질들은 후보물질 검증단계 혹은 비임상 연구 단계라 개발 속도면에 있어 당사가 세계적으로 선두라 할 수 있습니다. 임상 1상 시험으로 안전성과 내약성이
확인되고, 임상 2상 시험에서 예방 효능이 검증되면 향후 수년 내에 시판 허가 및 상업화 가능성이 높아질 것입니다. 또한, 코로나19 팬데믹을 기점으로 국내외 많은 개발사에서 다양한 유형의 코로나 19감염병 백신들이 개발되었습니다.
모더나(Moderna), 화이자(Pfizer) 등의 대형 글로벌 제약사와 대부분의 개발사는
mRNA 백신 개발에 주력하였고, 인도 제약회사 자이더스 캐딜라(Zydus Cadila)는 사람을 대상으로 한 DNA 백신 ZyCoV-D를 개발해서 임상 승인을 받은 사례가 있습니다. 당사에서도 코로나 19 발병 초기에 신속하게 기초접종용 예방 DNA 백신을 개발하여 국내에서 1/2a상 임상시험을 진행하면서, 추가접종으로 1상 임상시험을 미국
FDA에서 승인을 받아 진행하였습니다.
핵산 기반 치료제 중 mRNA 치료제 분야는 다국적 제약사들의 자금 및 협력을 지원받은 바이오텍 기업들이 신종 감염병 치료제 및 항암치료제를 대상으로 임상 개발을 진행 중에 있습니다. 대표적인 바이오텍 기업들로는 모더나(Moderna), 큐어백
(CureVac), 바이오엔텍(BioNTech)사등이 있습니다. 현재 개발 중인 제품들은 대부분은 1상 또는 2상 임상 연구를 진행하고 있습니다.
② 플라스미드 DNA CDMO 산업
비록 유전자치료제 시장의 급속한 성장으로 이들의 원료물질인 플라스미드 DNA의 전 세계 의약품 생산 수요는 증가하고 있지만, 원료물질이라는 점과 고순도, 고농도의 플라스미드 GMP 생산기술이 필요 하다는 점들로 인해, 전문적인 위탁 생산기업이 전 세계적으로 많지 않고, 기업들간 기술력의 차이가 있습니다.
나. 회사의 현황
(1) 영업개황 및 사업부문의 구분
(가) 영업개황
① 바이오의약품 사업
당사의 바이오 의약품 사업은 바이오 의약품 CDMO 사업과 차세대 바이오 신약 개발사업으로 구분됩니다.
바이오 의약품 CDMO 사업은 임상 및 비임상 시험에 필요한 유전자 치료제 및 DNA백신의 원료인 국제규격(cGMP) 플라스미드(Plasmid) DNA 제품을 2008년 6월 미국에 설립한 현지 법인인 VGXI, Inc.에서 생산하여 해외 판매 지점인 VGXI USA를 통해 판매하고 있습니다. 또한, 2018년 9월 미국 휴스턴 매소디스트 병원 연구소
(Houston Methodist Research Institute, HMRI)와 독점적 라이선스 계약을 통해
VGXI, Inc.는 mRNA 생산기술을 확보하였고, mRNA 백신 및 mRNA치료제의 위탁개발 생산 서비스 제공을 위해서 생산공정 스케일업을 진행 중에 있습니다.
신약 개발 사업은 핵산 기반 바이오 신약과 항염증 치료 신약으로 나뉩니다.
핵산 기반 바이오 신약은 다시 DNA 기반 의약품과 RNA 기반 의약품으로 나뉘며,
치료 기전에 따라 핵산 기반 백신과 핵산 기반 유전자 의약품으로 구분됩니다.
DNA 백신은 신변종 감염병 DNA 백신과 만성화된 감염 질병에 대비하는 만성 감염병 DNA 백신으로 구분되며, 당사의 개발 개황을 정리하면 다음과 같습니다.
메르스 DNA 백신(GLS-5300)은 중동호흡기증후군 코로나 바이러스의 예방 백신입니다. 메르스 바이러스에 의한 감염병은 중증 급성 호흡기 질환으로 치사율이 40% 이상으로 높으며, 국내에서는 2022년 7월에 중동지역을 포함한 해외방문으로 국내 메르스 감염병 환자 의심 신고를 포함하여 116건 접수되어 우리나라 정부는 지속해서 메르스 감염에 대한 조기발견 및 지역 사회 전파 차단에 심혈을 기울인 바 있습니다.
당사는 2015년 5월 27일 이노비오와 메르스 DNA 백신의 공동연구 계약을 체결하여, 비임상 연구와 임상 연구에서는 IND 신청 및 승인, 임상시험관리, 그리고 임상시료의 대량생산을 담당하여 해외 1상 및 국내 1/2a상 임상연구를 주도적으로 진행했습니다.
2015년 11월 19일 미국 FDA로부터 1상 임상 시험계획 승인을 받아, 2015년 11월
11일 미국 국방부 산하 월터리드 미육군 연구소(Walter Reed Army Institute of
Research)가 임상시험 관련 비용을 부담하는 조건으로 공동연구 개발 계약을 체결하여 임상 1상 연구를 착수하였습니다.
2017년 2월 24일 신종감염병 글로벌 준비 혁신 협력체(CEPI)가 주관하는 '신종감염병 백신-글로벌 보험' 1차 학술대회에서 해당 임상 연구의 매우 우수한 면역학적 중간 결과를 발표하였고, 2018년 6월 27일 세계보건기구(WHO)와 국제백신연구소
(IVI) 공동 주최 메르스 백신 국제심포지엄에서 1상 임상시험 예비 결과를 발표하였습니다.
2019년 7월 25일 완료된 해당 임상시험 결과를 국제 저명 의학전문학술지인 란셋 인펙셔스 디지즈(Lancet Infectious Disease)에 발표하였습니다.
메르스 DNA 백신의 우수한 안전성과 높은 백신 면역 반응을 확인하였을 뿐만 아니라, 2015년 국내 메르스 사태에서 확보한 메르스 감염 환자의 혈액을 임상시험 대상자의 혈액과 비교 평가한 결과로부터 백신 접종 60주 후에도 메르스 완치 환자와 유사한 면역반응이 유지됨을 확인하였습니다.
또한, 당사는 국내에서 메르스 DNA 백신의 개발 및 국가 기관에 응급 백신을 공급하기 위한 목적으로 2016년 12월 7일 국제백신연구소(IVI)로부터 관련 임상시험 1/2a 임상시험 개발비 전액을 지원을 받는 계약을 체결하였습니다.
2017년 6월 30일 국내에서 1/2a 상 임상시험을 수행하기 위해 한국 식품의약품안전처에 임상시험 계획 승인을 신청하여, 2017년 9월 14일 임상시험 계획승인을 받았습니다.
2018년 6월 메르스 DNA 백신(GLS-5300)의 1/2a 상 임상시험을 위한 임상시험기관의 임상시험 심사위원회(IRB)의 허가를 받았고, 2018년 9월 5일 첫 번째 임상시험 대상자의 첫 접종을 시작으로 서울대병원과 분당서울대병원에서 1/2a 상 임상시험을 진행하여, 2019년 5월 30일 모든 임상시험 대상자들의 백신 접종을 완료하였으며,
2020년 4월에 해당 임상시험이 종료되었습니다.
해당 임상시험 기간 동안 GLS- 5300을 투여한 모든 접종군에서 백신과 관련 있는 중대한 이상반응은 발현되지 않았으며, 백신을 투여한 그룹에서 접종용량과 접종횟수에 상관없이 그룹간 내약성의 차이는 없었으며, 백신의 효과가 잘 유지되는 것을 확인하였습니다.
이노비오와의 계약에 의해 GLS-5300의 후속 개발은 이노비오에서 담당하며 당사는
일정 지분을 갖습니다.
지카 바이러스 DNA 백신(GLS-5700)은 지카(Zika) 바이러스 감염병을 예방하거나 치료를 목적으로 하는 백신입니다. 임산부가 지카(Zika) 바이러스에 감염이 되면,
태아의 소두증을 유발하는 감염병으로 현재까지 상용화된 백신 및 치료제가 없습니다.
2016년 1월 22일 이노비오와 DNA 백신 개발의 공동연구 계약을 체결하였으며, 당사에서는 비임상 연구와 임상시료의 대량생산, 임상 1상 시험개발을 담당하여 수행했습니다.
2016년 6월 20일 미국 FDA로부터 임상시험 계획승인을 받았고, 2017년 10월 10일 GLS-5700의 임상시험 중간결과를 국제 저명 의학 전문 학술잡지인 뉴 잉글랜드 저널 오브 메드신(New England Journal of Medicine)에 발표하였습니다.
또한, 2016년 8월 30일 푸에르토 리코에서 160명의 피험자를 대상으로 하는 추가
1상(1b상) 임상시험도 미국 FDA로부터 승인을 받아, 2017년 6월 16일 임상시험 대상자 160명의 등록이 완료된 후 모든 임상시험 대상자들에게 백신 접종을 완료하였으며, 2018년 6월 GLS-5700의 해당 임상시험이 종료되었습니다.
GLS-5700 백신을 단회 혹은 다회 투여한 두 그룹 모두에서 접종부위에 이상반응이 일시적으로 발현했지만 경미했고, 두 그룹에서 용량에 따른 발현의 차이는 없었습니다. 또한, GLS-5700과 관련 있는 중대한 이상반응은 관찰되지 않았고, 두 그룹간 내약성의 차이는 없었으며 백신의 효과가 잘 유지되는 것을 확인했습니다.
이노비오와의 계약에 의해 GLS-5700의 후속개발은 이노비오에서 담당하고 당사는 일정지분을 갖습니다.
SFTS DNA 백신(GLS-5140)은 중증열성혈소판감소증후군(SFTS) 예방하기 위한 열성 질환 백신입니다. 중증열성혈소판감소증후군(SFTS)은 SFTS 바이러스에 감염된 진드기에 물려 감염되며, 고열등의 증상을 동반하는 중증열성질환입니다.
2015년 12월 한국과학기술원(KAIST) 산학협력단과 보건복지부 기술개발 사업에 참여하여 개발을 시작하였으며, 이 과정에서 살인진드기 바이러스 항원 후보물질 4종을 도출하였습니다. 마우스 및 페럿 동물모델을 이용한 실험을 통해 예방 효과를 확인하였고, 해당 연구결과는 2019년 8월 23일 국제 저명학술지인 네이처 커뮤니케이션즈(Nature Communications)에 발표되었습니다.
아울러, 2018년 6월 29일 한국과학기술원(KAIST)과 공동으로 "중증열성혈소판감소증후군(SFTS) 예방 DNA 백신"에 대한 특허를 대한민국 특허청에 출원하였으며,
2020년 2월 4일 특허등록을 완료하였습니다.
이후 2019년 6월 26일 미국, 일본, 중국에 특허 출원을 위한 특허협력조약(PCT)을 출원하였고, 그 결과 2024년 4월 2일 일본 특허청과 2024년 10월 11일 중국 특허청으로부터 중증열성혈소판감소증후군(SFTS) 바이러스 감염 질환 예방 또는 치료용 백신 조성물에 대한 특허등록을 받았습니다.
2020년 10월 보건복지부 백신실용화기술개발 사업단의 미래 대응 미해결 감염병 신규 백신 개발 분야의 지원 과제로 선정되어 임상시험 1상의 임상시험계획 승인까지의 연구개발비용을 지원받았으며, 해당 정부지원 과제를 2023년 12월에 성공적으로 종료하였습니다.
비임상 시험을 통해 선정한 후보물질이 설치류 동물에서 우수한 면역 효능을 보였으며, 백신을 접종한 페럿 동물모델에서는 SFTS 바이러스 감염에 의한 사망 사례가 나타나지 않아 백신의 뛰어난 방어능이 확인되었습니다. 또한, 백신의 독성을 평가하기
위해 GLP 기관에 반복 투여 독성 시험을 의뢰하였고, 약물로 인한 유해 반응이 관찰되지 않아 안전성이 확보된 백신임을 확인하였습니다. 수행한 모든 비임상시험 결과를 토대로, 임상시험에 적용하기 위한 적절한 용량 및 용법을 최종 결정하였습니다. 해당 실험 결과는 2022년 11월 10일과 11일에 열린 화순 국제 백신 포럼에 연자로 초청받아 발표한 바 있습니다.
한국 식품의약품안전처(식약처)와 2022년 8월 31일, 12월 5일, 2023년 6월 7일에 걸쳐 총 3차례의 사전 상담 회의를 진행하며, 제1상 임상시험계획 승인 신청을 위한 제출 자료에 대해 논의를 하였고, 2023년 11월 8일에 제1상 임상시험에 대한 IND 신청서를 제출하였습니다. 하지만, 식약처는 해당 임상시험이 전 세계적으로 전례 없는 최초 사례이며, 참고 가능한 자료가 전무하다는 점을 들어 제출된 IND 자료에 대해 보다 면밀하고 엄격한 검토가 필요하다는 의견을 제시하였습니다. 이에 따라 기 제출된 IND 자료의 보완 필요성을 인지하고 식약처와의 협의를 통해 2024년 1월 17일 해당 IND 신청을 자진 취하하였습니다. IND 자료를 보완한 후, 식약처로부터 승인을 받는 즉시 임상개발에 착수할 예정입니다
코로나19 DNA 백신(GLS-5310)은 코로나 바이러스 감염병의 예방목적의 백신입니다.
2020년 2월 우리나라에 코로나19 확진사례가 발생한 직 후 코로나 바이러스(SARS-CoV2) 감염병 백신 후보물질의 디자인 및 제작을 추진하다가 2020년 3월 27일
"2020년도 질병관리본부 긴급 현안 지정학술연구개발 용역과제"인 "핵산 백신 플랫폼을 활용한 코로나19 백신 후보물질 개발사업"에 우선 순위 협상대상자로 선정되었습니다.
2020년 4월 GLS-5310 후보물질을 제작한 후 생체 외에서 후보물질로부터 코로나
19 바이러스 항원이 생성되는 것을 확인하였습니다.
2020년 5월 VGXI, Inc.사에서 후보물질의 cGMP 생산공정 개발연구를 완료하여
2020년 7월 후보물질을 마우스에 접종한 후 우수한 항원 특이적 T세포 면역반응과 항원 특이적 결합 항체 반응, 그리고 중화항체의 생성을 확인하였습니다.
2020년 12월 4일 임상에서의 투여 경로를 실험동물에 적용한 후보물질의 용량 증량에 따른 면역원성 평가를 완료하여, 한국 식품의약품안전처로부터 1/2a상 임상시험계획 승인을 받았습니다. 임상시험 1상 착수를 위해 고대구로병원과 2020년 12월 18일 임상시험 계약을 체결하였고, 12월 31일 첫 대상자의 접종을 완료하고, 2021년
1월 21일 고용량군의 대상자 등록이 시작되어, 2021년 3월 4일 임상 1상 임상시험 대상자 45명의 등록이 완료되어, 2021년 5월 모든 대상자의 접종을 완료하였습니다.
2021년 7월 8일 임상 1상 중간 분석 결과가 자료 안전성 모니터링 위원회(DSMB) 심의를 통과하여 임상 2a상 시험에 진입하였습니다.
임상 2a상은 총 5개 기관에서 실시하였고, 위약 대조군이 있고 이중눈가림 임상시험으로 120명을 계획하였습니다. 총 126명이 등록되었고, 2023년 1월 6일 마지막 대상자의 최종 방문이 완료되었으며, 2023년 5월 10일 위약을 접종한 대상자중에서 본인
동의하에 GLS-5310을 재접종한 마지막 대상자까지 최종 방문을 마쳤습니다.
2024년 8월 21일 임상시험수탁기관(CRO)에서 해당 임상 시험 결과 분석이 완료되었으며, 2024년 12월 12일 임상 1/2a상에 대한 임상시험결과보고서 작성이 완료되었습니다.
GLS-5310의 글로벌 개발을 위해 기존 피내 접종과 비강 내 접종을 병용하는 임상시험을 미국에서 수행하고자 2020년 1월 19일 미국 FDA에 임상시험계획 승인을 신청하여, 2021년 7월 27일 승인을 받은 후, 2022년 1월 3일 미국 FDA로부터 코로나19백신 접종자들을 대상으로 하여 GLS-5310을 부스터 샷으로 접종하는 임상시험계획의 변경 승인을 받았습니다. 본 임상 연구의 변경 승인을 통해 미국에서 mRNA 백신과 아데노바이러스 전달체 백신을 접종한 대상자에게 진덤(Gene-Derm) 흡인압력을
이용 피내 접종군과 피내 접종 및 코 스프레이를 이용한 비강 내 접종을 병용한 접종군을 비교하고자 하였습니다. 2022년 9월 말 기준으로 69명 중 69명이 등록되었고, 임상시험 완료 및 결과 분석이 완료되었습니다.
2020년 12월 29일 코로나19 `백신인 GLS-5310의 1/2a상 임상개발 비용인 98억원 중 73억원의 연구비를 지원받는 내용으로 “코로나19 치료제 백신 신약개발사업단”과 협약을 체결하였습니다. 또한, 2021년 9월 6일 국가임상시험지원재단과 코로나19 백신 임상2a상 대상자 모집지원 협약을 체결하였습니다. 2025년 7월 9일 보건복지부는 GLS-5310의 1/2a상 임상개발 과제에 대한 제재처분을 통지하였습니다.
부과 사유로는 국가연구개발혁신법 제12조제2항에 따른 최종평가 결과 연구개발과제의 수행과정과 결과가 극히불량으로 부과금액 73억과 2년간 국가과제 참여제한 처분을 받았습니다. 본 처분 결과에 대한 집행정지 신청을 2025년 9월 8일 제기하였으며, 2025년 9월 23일 집행정지 신청이 인용되었습니다.
2021년 7월 22일 코로나19 DNA 백신인 GLS-5310의 백신조성물 특허에 대한 국내
및 특허협력조약(PCT) 출원을 완료하였으며, 2024년 9월 19일 대한민국 특허청으로부터 특허 등록을 받았습니다.
2023년 1월, 자체개발 흡인작용 피내접종기 진덤(Gene-Derm)을 이용한 코로나19 DNA 백신(GLS-5310)의 안전성 및 면역원성에 대한 임상 1상 결과를 국제감염병학회(International Society for Infectious Diseases, ISID) 학술지인 국제감염질환저널(International Journal of Infectious Diseases;2021년 인용지수: 12.074)에 발표했습니다.
2023년 5월 SARS-CoV-2를 포함한 전염병 대비를 위한 DNA 백신 관련 내용의 리뷰 논문을 백신(Vaccines;MDPI)에 발표하였고, 2023년 6월 임상 1상 분석 결과 중에서 GLS-5310 DNA 기초접종 후 mRNA 백신을 추가접종한 대상자들에 대한 면역원성 결과를 백신(Vaccine; Elsevier) 학술지에 게재하였습니다.
당사는 DNA 백신을 피내에 타겟팅하고 항원의 발현 효율성을 높이기 위해 흡인작용피내 접종 의료기기인 진덤(Gene-Derm)을 적용하고 있습니다.
2021년 8월 26일 진덤(Gene-Derm)의 이물질 및 분비물에 의한 오염 방지의 흡인기 플랫 모듈의 개량 특허를 국내 출원하여 2023년 6월 29일에는 해당 특허가 등록되었으며, 2022년 11월 11일 특허 협력조약(PCT) 출원이 완료되었습니다. 또한, 2021년
4월 14일 분비물에 의한 디바이스 오염을 방지하는 흡인기 모듈에 대해 국내 특허를 출원하여,2023년 7월 10일 이의 특허가 등록되었으며, 2022년 4월 13일 특허 협력조약(PCT)출원과 2023년 10월 6일 미국 특허 출원이 완료되었습니다.
진덤(Gene-Derm) 기기는 물리적/화학적/생물학적 성능시험 및 전기/전자파 성능시험을 포함한 각종 시험검사들과 제조 및 품질관리기준(GMP) 인정서 및 ISO-13485 취득을 완료하여 기술문서 심사를 통과하게 되어 2022년 4월 29일 식품의약품안전처로부터 의료기기(품목명: 전동식의료용 흡인기, 2등급)로 승인을 득하였습니다.
해당 흡인기를 2021년 10월 햄스터 공격 감염 모델을 이용한 동물실험에 적용하여 GLS-5310이 야생형 및 베타 변이 코로나 19 바이러스에 대한 감염을 완벽하게 예방함을 확인하였습니다. 이는 진덤(Gene-Derm) 기기가 효과적으로 항원의 발현을 유도하는 DNA 백신 접종 방식임을 입증함을 보여주는 결과입니다.
2021년 11월 5일 DNA 백신의 흡인작용 피내 접종 의료기기인 진덤(Gene-Derm)의 플랫폼 개발과 이를 이용해서 확인된 연구 결과를 사이언스 어드밴시스(Science
Advances)에 게재하였습니다. 또한, 진덤(Gene-Derm)의 약물 전달 메커니즘 연구를 미국 뉴저지 주립대학인 럿거스(Rutgers) 대학 연구진과 공동연구로 진행하여,
2023년 1월 그 결과를 국제학술지인 약물 전달 프론티어스(Frontiers in Drug
Delivery)에 게재했습니다.
2022년 1월 3일 미국 FDA로부터 코로나19백신 접종자들을 대상으로 하여 GLS-
5310을 부스터 샷으로 접종하는 임상시험계획을 승인을 받았습니다.
해당 임상시험은 지난 2021년 7월 27일 승인을 받은 임상시험 계획서에 대해 계획을
변경하여 승인을 받은 것으로 미국에서 mRNA 백신과 아데노바이러스 전달체 백신을 접종한 대상자에게 진덤(Gene-Derm) 흡인압력을 이용 피내 접종군과 피내 접종 및 코 스프레이를 이용한 비강 내 접종을 병용한 접종군을 비교하고자 하였습니다.
2022년 9월 말 기준으로 69명 중 69명이 등록되었고, 임상시험 완료 및 결과 분석이 완료되었습니다.
당사는 만성 감염병 DNA 백신으로 C형 간염 DNA 백신을 개발하고자 2011년 10월 7일 이노비오사와 계약을 체결하여 일본을 제외한 아시아지역의 개발 및 판권을 확보하였습니다.
만성 C형 간염환자의 치료를 위한 백신인 VGX-6150은 2013년 10월 18일 국내
식품의약품안전처로부터 임상시험 계획을 승인을 받아 연세대 세브란스병원과 부산대병원에서 18명의 만성 C형 간염 임상시험 대상자 대상으로 1상 임상시험을 진행하였습니다. 또한, 추가 접종 후 면역기억에 의한 장기간 치료효과를 확인하기 위해
2014년 9월 26일 국내 식품의약품안전처로부터 상기 1상 임상시험이 종료된 임상시험 대상자중 희망자에 한해 후속 임상시험 계획을 승인을 받아 추가 임상시험을 완료하였습니다.
2017년 9월 26일 HCV 2017 국제심포지엄에서 VGX-6150 안전성과 면역원성에 대한 결과를 발표하였고, 2020년 2월 20일 심각한 부작용없이 매우 안전하면서도 C형 간염바이러스에 대한 T세포 면역반응을 높인다는 1상 임상시험 결과를 간 연구분야의 국제 전문학술지인 저널 오브 헤파톨로지(Journal of Hepatology) 온라인판에 게재하였습니다.
C형 간염 예방 백신으로 기존 치료제로 완치된 만성 C형 간염 환자를 대상으로 재감염 예방하고자 하는 DNA 백신(GLS-6150)과 C형 간염 고위험군을 대상으로 만성 C형 간염 예방하고자 하는 DNA 백신(GLS-6100)이 있습니다.
2017년 6월 9일 보건복지부 기술개발사업단 주관과제로 선정되어 C형 간염 예방을 위한 DNA 백신인 GLS-6150과 GLS-6100 개발에 정부로부터 지원을 받게 되었습니다.
2021년 1월 4일 한국 식약처에 GLS-6100의 국내 1상 임상시험 계획승인신청서를 제출하였고, 2021년 5월 20일 이의 승인을 받았습니다. 하지만, 이후 정부로부터 해당 임상과제의 후속 지원이 없어 개발을 종료했습니다.
2017년 10월 31일 한국 식약처에 GLS-6150의 국내 1상 임상시험 계획승인을 신청하였고, 2018년 2월 2일 이의 승인을 득하였습니다.
2018년 7월 임상시험 기관의 임상시험 심사위원회(IRB)의 1상 임상시험의 허가를 받았고, 2018년 9월 4일 첫 번째 임상시험 대상자의 첫 접종이 이뤄진 후, 1상 임상시험을 연세 의료원 세브란스 병원과 부산대 병원에서 진행하였습니다.
2020년 5월 11일 해당 임상시험을 종료하여 식약처에 종료 보고를 완료하였습니다.
1상 임상시험 전반에 대한 안전성 결과와 면역원성 결과에 대한 통계분석이 완료되었으며, 2022년 12월 12일 임상결과보고서(CSR) 최종본을 수령하여 보고서 작성이 완료되었습니다.
당사는 DNA 기반 단백질 의약품 및 단클론 항체 의약품은 기존 단백질 의약품 및
단클론 항체 의약품 대비 우수한 가격 경쟁력, 체내 안전성 및 약효 지속성을 장점으로 하여, 자체 R&D 기술력으로 DNA기반 의약품을 직접 개발하고 있습니다.
당사의 R&D 기술에 의해 개발하고 당사가 보유하고 있는 DNA 백신 플랫폼은 감염성 질환에 대한 예방백신 개발에 적용할 수 있는 기술이기도 합니다. 2021년 12월
17일 DNA 백신 플랫폼에 이용하여 개발한 DNA 백신을 동물에 접종 시 면역원성이 잘 유도됨을 확인 및 검증하여 DNA 백신의 기술과 이의 효능을 국제 학술지인 메소드 인 몰리큘러 바이올로지(Methods in Molecular Biology) 온라인판으로 출판하였습니다.
DNA 기반 단백질의약품으로는 혈우병 치료제의 개발 타당성에 대한 검증 연구를 진행하고 있습니다.
DNA 기반 혈우병 치료제는 2014년 10월 강원대 의생명과학대학의 혈우병 치료제의
의약품 개발 타당성 검증 연구를 참고하여, 당사 자체적으로 혈액응고 8인자를 이용하여 후보물질에 대한 개선 연구를 진행하고 있었습니다만, 2019년 이후 코로나 바이러스의 갑작스러운 확산에 따른 팬데믹 시기에는 코로나 백신 연구개발에 집중하고자 본 연구를 중단하였었습니다. 팬데믹이 종식이 된 후, 혈액응고 8인자의 체내 생성량과 활성을 높이기 위한 제품 개발을 위해 혈우병 치료제 후보물질 발굴을 위한
연구를 재개하여 진행하고 있습니다.
DNA 기반 단클론 항체 의약품으로 B형 간염 면역글로불린의 개발타당성에 대한 검증 연구를 진행하고 있습니다.
DNA 기반 B형간염 면역글로불린은 2017년 4월 강원대학교 산학협력단 보유의 B형간염 바이러스의 preS1에 특이하게 결합하는 항체 2종에 대한 특허와 기술이전을 받아, 이의 타당성 검증 연구에 착수하였습니다. 그 결과, 2018년 5월 30일 대한민국
특허청으로부터 특허 등록을 받았고, 2019년 2월 5일 미국 특허 등록을 받았습니다.
타당성 검증을 위해 DNA 기반 B형 간염 항preS1 면역글로불린 2종의 후보물질 플라스미드와 항S 면역글로불린 2종의 후보물질 플라스미드를 제작하여, 연구용 시료를 이용하여 동물세포에서 항체 생성과 항원 결합능력을 확인하였고, 실험동물에서는 이들 4종의 후보물질 플라스미드로부터 항체 생성 및 체내 분포 경향 분석을 진행하였습니다. 2019년 9월에는 B형 간염바이러스 연구 분야의 세계적 권위자인 건국대 의학전문대학원 김균환 교수 연구팀과 함께 실험동물을 이용한 효능평가 연구를 수행하여 항preS1 면역글로불린과 항S 면역글로불린을 동시에 처리한 조건에서 우수한 바이러스 억제 효과가 있음을 확인하였습니다.
현재, 당사 자체적으로 높은 국내 분포를 보이는 B형 간염바이러스 유전자 C형에 대하여 4종 후보물질들의 억제 효과를 평가중에 있습니다.
또한, 당사는 류머티즘 관절염 치료 목적으로 DNA 기반의 항 TNF 알파 단클론 항체후보 물질을 개발하여 해당 후보물질이 동물세포에서의 항체 생성, TNF 알파와 아밀로이드 베타와의 결합력, 및 TNF 알파의 세포 살상 반응 억제능이 있음을 확인하였으나, 생산된 제품의 상업화 적합성 문제로 연구개발을 중단하였습니다.
당사는 mRNA 기반 의약품의 연구개발을 수행하기 위해 mRNA 기반 플랫폼 구축을
완료하여, mRNA 백신 후보물질의 효능 및 안전성 평가 연구를 진행하고 있습니다.
2018년 9월 17일 자회사 VGXI, Inc.가 임상용 의약품 mRNA를 생산하기 위해 미국 휴스턴 매소디스트 병원 연구소(Houston Methodist Research Institute)와 독점적
라이선스-인 계약을 체결함에 따라, mRNA 백신 및 mRNA 치료제 생산의 핵심 기술과 mRNA 백신 설계 및 연구 기술을 이전 받아 mRNA 백신 및 mRNA 치료제 연구 개발사업에 진출하게 되었습니다.
자회사인 VGXI, Inc.는 mRNA 기반 의약품의 상업적 생산을 위한 파일럿 생산공정을 성공적으로 구축한 후 대규모 cGMP 생산공정을 구축하기 위한 공정 스케일 업 및 최적화 단계를 진행하고 있습니다.
코로나19 mRNA 백신은 2020년 2월 우리나라에 코로나19 확진 사례가 발생한 직후
휴스턴 매소디스트 병원 연구소의 존 쿡(John Cooke) 박사 연구팀으로부터 mRNA 백신 설계 및 연구 기술을 이전 받아 mRNA 백신 후보물질의 디자인 및 제작을 진행하였습니다.
2020년 3월 27일 "2020년도 질병관리본부 긴급 현안 지정 학술연구개발 용역과제"인 "핵산 백신 플랫폼을 활용한 코로나19 백신 후보물질 개발 사업"에 우선 순위 협상대상자로 선정되어, 2020년 5월 후보물질을 2종을 제작한 후, 2020년 9월 생체 외에서 후보물질로부터 코로나19 바이러스 항원이 생성되는 것을 확인하였습니다. 2020년 11월 실험동물에서 후보물질 접종 후 항체 면역반응과 T세포 면역반응이 유도됨을 확인하였으나, LNP 기술을 보유한 기관들로부터 해당 mRNA 백신의 평가를 진행하였으나, 상업적 타당성 문제로 연구개발을 종료하였습니다.
당사는 mRNA 기반의 항암 백신과 단클론 항체 플랫폼 개발을 위한 연구를 진행하고
있습니다.
당사는 2021년 5월 31일 한미 사이언스와 mRNA 백신 대규모 생산기반 및 글로벌 네트워크 구축을 위한 협력 계약을 체결하였습니다.
해당 계약에 따라 당사와 한미 사이언스는 양사가 보유한 핵심 기술을 상호 협력하여
mRNA 백신의 글로벌 대규모 생산을 위한 차세대 생산기술을 함께 연구하고자 하였습니다. 이는 mRNA 백신 기술을 더욱 최적화하여 코로나19 및 신종 감염병 mRNA 백신의 공동 연구 및 사업화를 포함하며, 양사가 파트너로서 핵산 사업 글로벌 네트워크 구축을 통해 기술 확보 및 시장개척 등을 논의하였습니다.
당사는 2021년 6월 17일 보건복지부 백신실용화기술개발사업단의 미래 대응, 미해결 신변종 감염병백신 플랫폼 개발 분야의 지원 과제로 선정되어 mRNA 기반 신속 백신 제작 플랫폼을 구축하고 지카(Zika) 바이러스 mRNA백신 선도 물질 발굴 및 유효성을 평가하는 연구를 진행하였습니다.
지카(Zika) 바이러스 백신 항원 기술은 질병관리청으로부터 이전 받아 과제에 적용하였으며, 지카 바이러스 mRNA 백신의 선도물질 발굴 및 유효성 평가하여 원부자재의
국산화 여부를 확인하여 비임상 및 초기 임상시험용 mRNA 백신 생산 공정 최적화를
포함하고 있었습니다. 당사는 자체 mRNA 기반 신속 백신 제작플랫폼의 구축하여,
2022년 12월 31일 지카(Zika) 바이러스 mRNA 백신 선도물질의 유효성 및 안전성 평가하여 해당 국책 과제는 완료하였으며, 2024년 11월 14일 이의 연구결과를 국제 학술지인 백신(Vaccine; Elsevier) 저널에 게재를 하였습니다.
당사의 원형(circular) RNA 기술을 활용한 새로운 mRNA 백신용 플랫폼 연구를 통해
2021년 6월 25일 과학기술정보통신부 주도 신변종 감염병 대응 플랫폼 기술 개발사업의 참여연구개발기관으로 선정되었습니다. 총 43개월 동안 원형(circular) RNA 플랫폼의 구축, 생산 및 유효성 평가를 수행하고, 신변종 감염병 선정을 위한 대상 감염병(Disease X) 3종의 대량생산 공정 최적화 및 임상용 백신의 생산 내용을 포함하고 있었으며, 당사는 사업의 결과로써 백신의 비임상 시험용 시험물질인 SARS-CoV2 Omicron 원형(circular) RNA의 대량 생산을 완료하여 2023년 12월 주관 연구개발기관에 공급하였습니다. 본 국책과제는 국가 예산 편성 변경 정책에 따라 갑작스럽게 연구 개발 비용의 삭감되어, 예산 부족으로 인하여 당사가 담당하기로 한 연구개발 업무의 진행이 불가하여, 2024년 1월부터는 담당 국책과제에 더 이상 참여하지 않는
것으로 사업을 종결하였습니다.
2021년 9월에 도입한 원형(circular) RNA 플랫폼의 원형(circular) RNA의 공정 최적화를 위한 연구개발을 지속적으로 수행함으로써 보다 우월한 생산효율을 확보한 플랫폼 기술을 완성하여 2023년 12월 15일에 국내특허를 출원하였으며, 현재 심사 중에 있습니다.
당사는 R&D 역량 강화를 위한 전략적인 오픈 이노베이션(Open Innovation)을 지속해서 추진 중에 있습니다.
당사가 확보하고 있는 mRNA 플랫폼을 적용하여 미충족 수요(Unmet Need)가 많은 암 치료 분야에서 mRNA 기반의 항암 백신과 단클론 항체를 개발하여, 현 수준의 치료용 mRNA의 단점을 극복하고 이의 장점은 극대화하고자 하는 목적으로 다수의 기관과 공동연구를 진행하고 있습니다. 그 외에도 여러 방면으로 오픈 이노베이션을 진행하여, 다양한 난치성 전염병의 백신 연구개발을 비롯하여, 암, 자가면역 질환, 퇴행성 만성질환 등에 적용 가능한 혁신적인 치료 방법과 당사의 mRNA 플랫폼에 적용할
수 있는 새로운 치료 방법을 개발하고자 하고 있습니다.
당사는 2022년 12월 8일 애스톤 사이언스와 전략적 업무 제휴 양해각서(MOU)를 체결함으로써, 오픈 이노베이션을 통해 차세대 핵산 기반 백신의 연구 및 개발을 위해 역량을 공유하여 새로운 타깃 물질을 연구 개발하는 파트너로서 협력하기로 하였습니다. 본 MOU의 후속 조치로써 치료 목적의 백신 신약 연구 및 이의 개발을 위하여 인공지능(AI) 스크리닝 방법을 적용한 새로운 항원 결정기의 정보를 공유하고, DNA 백신을 mRNA 기반 백신으로 전환하기 위한 연구를 수행하기 위한 논의를 우선 진행하였으며, mRNA 항암 백신 신약 개발 공동 프로젝트를 구성하여 새로운 항원 결정기를 찾고 효능 및 안정성을 검토하는 연구에 착수하였습니다.
당사는 축적된 DNA 기반 백신 임상 연구 개발 결과와 자체적으로 개발한 mRNA 기반 백신 플랫폼 기술력을 인정받아 2023년과 2024년 2년 연속 연례 백신 세계 아시아의회의 초청을 받아 핵산 기반 백신 연구개발 성과를 발표하였습니다. 싱가포르에서 개최된 2023년 제5회 아시아태평양 백신 우수상(Asia-Pacific Vaccine
Excellence Award, AVEA) 시상식에서는 '대한민국의 가장 유망한 백신부문' 최우수상을 수상했습니다.
항염증 치료 신약은 천연물 유래성분 의약품과 저분자 화학합성 의약품으로 나눌 수 있습니다.
천연물 유래성분 의약품으로 쓴맛 수용체를 이용한 항바이러스 및 항균 코 스프레이 약물이 있으며, 저분자 화학합성 의약품으로 항염증 면역제어 경구 약물이 있습니다.
쓴맛수용체를 이용한 항바이러스 및 항균 코 스프레이 약물(GLS-1200)은 2018년
6월 26일 미국 펜실베이니아 대학교로부터 호흡기 감염에 대한 혁신 치료제 및 진단법 개발을 위한 쓴맛 수용체 신호전달물질 및 관련기술을 기술이전 받았습니다.
2019년 8월 5일 만성 축농증 치료를 위해 임상용 의약품의 생산을 완료하여 미국
FDA에 2상 임상시험 진행을 위한 임상시험 계획승인을 신청하였습니다. 본 임상은 미국 펜실베이니아 대학교 임상시험센터에서 실시되며 만성 축농증환자의 부비동 수술이후 7주에 거쳐 만성 축농증 치료제(GLS-1200)인 코 스프레이를 비강을 통해 투여한 후 4개월 동안 급성 축농증의 재발 여부를 확인하는 목적으로 위약 대조군과 함께 99명의 환자를 대상으로 진행할 것을 계획하였습니다.
2020년 4월 13일 미국 FDA로부터 2상 임상시험계획의 승인을 받았지만, 코로나 19 감염병 사태로 인해 임상 시험이 잠정 중단되었습니다.
GLS-1200에 대해 펜실베이니아 대학교와 공동으로 2020년 4월 21일 코로나19 및 독감을 포함한 다른 바이러스에 의한 감염을 예방하는 용도에 대한 특허를 미국 특허청에 출원하였으며, 호흡기 질환 진단 및 치료에 대한 특허는 2021년 1월 5일 미국 특허청에 등록을 받았습니다.
코 스프레이 GLS-1200은 비강에 분무되어 비강부위 세포의 쓴맛 수용체와 결합하여 산화질소를 생성 분비하게 하여 코로나19 바이러스를 사멸하는 MOA를 예상하고있습니다.
2020년 4월 29일 코로나19 감염 예방 코스프레이 약물로써 2상 임상시험 계획승인을 미국 FDA로부터 받았습니다.
2020년 6월 11일 펜실베이니아 대학교 임상시험센터에서 의료계 종사자들을 대상으로 한 첫 임상시험 대상자 투약이 진행되었고, 2020년 9월 계획된 225명 임상시험 대상자에서 50% 이상 대상자 등록이 완료되었습니다.
2021년 1월 18일 GLS-1200은 코 부위에 분포하고 있는 코로나19 바이러스 농도를 감소시켰고, 족제비 감염동물 모델을 통해 비강세포내 감염을 억제하는 것으로 확인되었습니다.
미국 루이지애나주 바톤 루지시에 2차 임상시험 실시기관을 추가하였고, 2021년 4월
임상대상자를 일반인으로 확대해서 진행할 수 있도록 하는 IRB 승인을 받았습니다. 대상자 모집에 지속해서 노력하여 2022년 12월 기준 184명이 등록되었으나, 코로나19에 감염된 대상자를 모집하는데 어려움이 있어 임상시험 대상자 모집을 조기 종료하였습니다. 이로써, 2023년에 임상2상 연구를 종료하였고, 임상시험 결과보고서를 작성하였습니다.
항염증 면역제어 경구 약물(GLS-1027)은 당사가 보유한 1상 임상시험이 종료된
GLS-1027(구VGX-1027)을 이용하여 자가면역성 신장질환등의 치료를 위한 임상개발을 준비하였으나, 전 세계적 코로나 19 감염병의 유행으로 인해 GLS-1027은 코로나19 치료제 임상 개발로 연구개발 방향을 전환하였습니다.
공정개발연구를 통해 불순물이 제거된 GLS-1027을 생산하였고, 기존 물질과의 항염증 반응을 평가하기 위해 이탈리아 카타리나 대학 니콜라티 교수 연구팀과 협력하여 진행한 동물실험에서, GLS-1027이 코로나19 감염 후 생성되는 다수의 염증유발물질(사이토카인)들이 억제됨을 보여주는 결과를 근거로 하여, 2020년 10월 28일
코로나19 감염 후 과대 면역에 의한 심각한 폐질환을 방지하는 치료제로서의 개발을
착수하였습니다.
GLS-1027의 2상 임상시험 계획승인 신청서를 미국 FDA에 제출했고, 11월 30일
미국 FDA로부터 승인을 받았습니다.
GLS-1027(국제일반명 zenozulac)은 경구용 캡슐 약제로 빠른 체내 소실과 우수한 안전성을 임상 1상연구를 통해 확인되었습니다. GLS-1027은 선천성 면역세포에만
작용하여 사이토카인 분비를 억제함으로써 바이러스 감염 시 과대면역을 제어하여 정상 범위의 수치로 면역이 회복될 수 있게 합니다.
본 약제에 대한 2상 임상시험은 코로나19 확진자를 대상으로 132명을 계획하고 코로나19 바이러스 감염시부터 GLS-1027을 선제적으로 투약하여 코로나19에 의한 심각한 폐렴 발병을 예방할 수 있는지를 평가하였습니다.
코로나19 DNA 백신(GLS-5310)은 코로나 바이러스 감염병의 예방목적의 백신입니다.
2020년 2월 우리나라에 코로나19 확진사례가 발생한 직 후 코로나 바이러스(SARS-CoV2) 감염병 백신 후보물질의 디자인 및 제작을 추진하다가 2020년 3월 27일
"2020년도 질병관리본부 긴급 현안 지정학술연구개발 용역과제"인 "핵산 백신 플랫폼을 활용한 코로나19 백신 후보물질 개발사업"에 우선 순위 협상대상자로 선정되었습니다.
2020년 4월 GLS-5310 후보물질을 제작한 후 생체 외에서 후보물질로부터 코로나
19 바이러스 항원이 생성되는 것을 확인하였습니다.
2020년 5월 VGXI, Inc.사에서 후보물질의 cGMP 생산공정 개발연구를 완료하여
2020년 7월 후보물질을 마우스에 접종한 후 우수한 항원 특이적 T세포 면역반응과 항원 특이적 결합 항체 반응, 그리고 중화항체의 생성을 확인하였습니다.
2020년 12월 4일 임상에서의 투여 경로를 실험동물에 적용한 후보물질의 용량 증량에 따른 면역원성 평가를 완료하여, 한국 식품의약품안전처로부터 1/2a상 임상시험계획 승인을 받았습니다. 임상시험 1상 착수를 위해 고대구로병원과 2020년 12월 18일 임상시험 계약을 체결하였고, 12월 31일 첫 대상자의 접종을 완료하고, 2021년
1월 21일 고용량군의 대상자 등록이 시작되어, 2021년 3월 4일 임상 1상 임상시험 대상자 45명의 등록이 완료되어, 2021년 5월 모든 대상자의 접종을 완료하였습니다.
2021년 7월 8일 임상 1상 중간 분석 결과가 자료 안전성 모니터링 위원회(DSMB) 심의를 통과하여 임상 2a상 시험에 진입하였습니다.
임상 2a상은 총 5개 기관에서 실시하였고, 위약 대조군이 있고 이중눈가림 임상시험으로 120명을 계획하였습니다. 총 126명이 등록되었고, 2023년 1월 6일 마지막 대상자의 최종 방문이 완료되었으며, 2023년 5월 10일 위약을 접종한 대상자중에서 본인
동의하에 GLS-5310을 재접종한 마지막 대상자까지 최종 방문을 마쳤습니다.
2024년 8월 21일 임상시험수탁기관(CRO)에서 해당 임상 시험 결과 분석이 완료되었으며, 2024년 12월 12일 임상 1/2a상에 대한 임상시험결과보고서 작성이 완료되었습니다.
GLS-5310의 글로벌 개발을 위해 기존 피내 접종과 비강 내 접종을 병용하는 임상시험을 미국에서 수행하고자 2020년 1월 19일 미국 FDA에 임상시험계획 승인을 신청하여, 2021년 7월 27일 승인을 받은 후, 2022년 1월 3일 미국 FDA로부터 코로나19백신 접종자들을 대상으로 하여 GLS-5310을 부스터 샷으로 접종하는 임상시험계획의 변경 승인을 받았습니다. 본 임상 연구의 변경 승인을 통해 미국에서 mRNA 백신과 아데노바이러스 전달체 백신을 접종한 대상자에게 진덤(Gene-Derm) 흡인압력을
이용 피내 접종군과 피내 접종 및 코 스프레이를 이용한 비강 내 접종을 병용한 접종군을 비교하고자 하였습니다. 2022년 9월 말 기준으로 69명 중 69명이 등록되었고, 임상시험 완료 및 결과 분석이 완료되었습니다.
2020년 12월 29일 코로나19백신인 GLS-5310의 1/2a상 임상개발 비용인 98억원 중
73억원의 연구비를 지원받는 내용으로 "코로나19 치료제 백신 신약개발사업단”과 협약을 체결하였습니다. 또한, 2021년 9월 6일 국가임상시험지원재단과 코로나
19 백신 임상2a상 대상자 모집지원 협약을 체결하였습니다. 2025년 7월 9일 보건복지부는 GLS-5310의 1/2a상 임상개발 과제에 대한 제재처분을 통지하였습니다. 부과 사유로는 국가연구개발혁신법 제12조제2항에 따른 최종평가 결과 연구개발과제의 수행과정과 결과가 극히불량으로 부과금액 73억과 2년간 국가과제 참여제한 처분을 받았습니다. 본 처분 결과에 대한 집행정지 신청을 2025년 9월 8일 제기하였으며,
2025년 9월 23일 집행정지 신청이 인용되었습니다.
2021년 7월 22일 코로나19 DNA 백신인 GLS-5310의 백신조성물 특허에 대한 국내
및 특허협력조약(PCT) 출원을 완료하였으며, 2024년 9월 19일 대한민국 특허청으로부터 특허 등록을 받았습니다 .
2023년 1월, 자체개발 흡인작용 피내접종기 진덤(Gene-Derm)을 이용한 코로나19 DNA 백신(GLS-5310)의 안전성 및 면역원성에 대한 임상 1상 결과를 국제감염병학회(International Society for Infectious Diseases, ISID) 학술지인 국제감염질환저널
(International Journal of Infectious Diseases;2021년 인용지수: 12.074)에 발표했습니다.
2023년 5월 SARS-CoV-2를 포함한 전염병 대비를 위한 DNA 백신 관련 내용의 리뷰 논문을 백신(Vaccines) 학술지에 발표하였고, 2023년 6월 임상 1상 분석 결과중에서 GLS-5310 DNA 기초접종 후 mRNA 백신을 추가접종한 대상자들에 대한 면역원성 결과를 백신(Vaccine; Elsevier) 학술지에 게재하였습니다.
2021년 6월 30일 코로나19 중증 폐렴을 유발하는 햄스터 공격 감염 모델을 이용하여
GLS-1027(국제 일반명 zenozulac)이 용량 의존적으로 폐렴 증상 마커들의 발현을 감소시키며, 해부학적으로는 폐 부위 조직에서 바이러스에 의해 유도되는 세포융합체(syncytia)와 세포이형성(atypia)이 탁월하게 감소시키는 것을 확인하였습니다. 해당 치료 효과는 코로나19 바이러스 남아공 변이주인 B.1.351 β variant에 대해서도 동일한 반응이 보이는 것을 확인하였습니다.
당사는 2010년 2월 과학기술정보통신부로부터 기업부설연구소 인가를 받아 당사 기술력으로 신약개발 사업을 직접 수행 및 운영하고 있습니다.
2013년 9월 중소기업청으로부터 당사의 우수한 연구개발 능력을 평가받아 기술혁신형 중소기업(INNO-BIZ) 인증을 받았고, 2019년 3월 기술보증기금으로부터 벤처기업 확인서를 받았습니다.
또한 메르스 DNA 백신, 지카 바이러스 DNA 백신, 코로나19 백신, 쓴맛수용체를 이용한 항바이러스 및 항균 코스프레이 약물, 항염증 면역제어 경구약물의 글로벌 임상개발을 효율적으로 수행하기 위해 미국 펜실베이니아주 포트 워싱턴(Fort
Washington)시에 글로벌 임상개발본부를 설립하였고 최고 의학책임자를 임명하였습니다.
당사는 핵산기반 바이오 신약의 개발을 위하여 국내외 기업 및 전문 연구기관과 적극적이고 지속적인 협력연구를 진행하고 있습니다.
지카 바이러스 DNA 백신의 개발을 위해 이노비오(Inovio), 미국 위스타(Wistar) 백신연구소, 캐나다 라발(Laval) 대학교와 협력하고, 메르스 DNA 백신의 개발을 위해
이노비오(Inovio), 미국 국방부 월터리드 미육군연구소(WRAIR), 국제백신연구소(IVI), 서울대병원, 분당서울대병원과 협력하고, C형간염예방 및 치료 DNA 백신개발을 위 연세의료원 세브란스병원, 부산대병원, 한국과학기술원(KAIST)과 협력하고 있으며,SFTS DNA 백신개발을 위해 한국과학기술원(KAIST)과 협력하고, 코로나19
DNA 백신개발을 위해 질병관리청 공공백신개발지원센터, 고대구로병원, 고대안산병원, 한림대강남성심병원, 가천대길병원, 인하대병원, 국가임상시험지원재단과 협력하고 있습니다. mRNA 기반 의약품의 개발을 위해 미국 휴스턴 매소디스트 병원 연구소(Houston Methodist Research Institute)와 항염증 치료 신약개발을 위하여 쓴맛 수용체를 이용한 항바이러스 및 항균 코스프레이 약물 개발 연구는 미국 펜실베이니아 대학교와 협력하고 있습니다.
② 섬유사업
심지 사업은 의류 및 모자용 심지 류 국내시장 수요의 약 20~30% 선 점유율을 차지
하는 것으로 추정합니다.
③ 회사 매출액과 영업손익 및 손익
당기말 연결재무제표기준으로 회사의 매출액은 230여억원이었으며, 영업손실 440여억원, 당기순손실 518여억원을 기록하였습니다.
(나) 공시대상 사업부문의 구분
(1) 연결실체의 영업부문은 2개로 구성되어 있으며 그 내용은 다음과 같습니다.
| 구 분 | 제품 및 용역의 유형 |
|---|---|
| 제약사업 | Contract Development Manufacturing Organization (CDMO) |
| 패브릭사업 | 의류용 심지제품 제조, 판매 |
(2) 영업부문별 정보는 다음과 같습니다.
1) 영업부문의 당기손익정보는 다음과 같습니다.
<당기>
| (단위: 원) | |||
|---|---|---|---|
| 구분 | 제약사업 | 패브릭사업 | 합계 |
| 총매출액 | 11,970,434,673 | 11,074,356,997 | 23,044,791,670 |
| 내부거래 | - | - | - |
| 외부거래 | 11,970,434,673 | 11,074,356,997 | 23,044,791,670 |
| 영업이익(손실) | (40,364,101,399) | (3,672,147,895) | (44,036,249,294) |
| 당기순이익(손실) | (48,449,612,095) | (3,401,367,506) | (51,850,979,601) |
| 감가상각비와상각비 | 17,667,393,832 | 471,272,741 | 18,138,666,573 |
| 이자수익 | 61,080,213 | 125,495,388 | 186,575,601 |
| 이자비용 | (4,878,496,577) | (261,970,232) | (5,140,466,809) |
| 법인세비용(수익) | 173,760,582 | (87,404,976) | 86,355,606 |
<전기>
| (단위: 원) | |||
|---|---|---|---|
| 구분 | 제약사업 | 패브릭사업 | 합계 |
| 총매출액 | 22,427,160,608 | 13,292,938,241 | 35,720,098,849 |
| 내부거래 | - | - | - |
| 외부거래 | 22,427,160,608 | 13,292,938,241 | 35,720,098,849 |
| 영업이익(손실) | (42,197,649,271) | (841,464,185) | (43,039,113,456) |
| 전기순이익(손실) | (48,319,993,315) | (216,614,055) | (48,536,607,370) |
| 감가상각비와상각비 | 17,452,199,406 | 451,711,912 | 17,903,911,318 |
| 이자수익 | 74,982,943 | 50,192,335 | 125,175,278 |
| 이자비용 | (1,905,768,560) | (250,226,368) | (2,155,994,928) |
| 법인세비용(수익) | 228,770,094 | (12,582,224) | 216,187,870 |
2) 영업부문의 자산 및 부채정보는 다음과 같습니다.
<당기말>
| (단위: 원) | |||
|---|---|---|---|
| 구분 | 제약사업 | 패브릭사업 | 합계 |
| 총자산 | 103,726,000,298 | 15,481,168,704 | 119,207,169,002 |
| 총부채 | 76,850,714,597 | 1,458,392,734 | 78,309,107,331 |
<전기말>
| (단위: 원) | |||
|---|---|---|---|
| 구분 | 제약사업 | 패브릭사업 | 합계 |
| 총자산 | 132,431,364,334 | 18,903,043,478 | 151,334,407,812 |
| 총부채 | 64,112,007,357 | 1,617,157,851 | 65,729,165,208 |
3) 주요 고객에 대한 매출 정보는 다음과 같습니다.
<당기>
| (단위: 원) | ||
|---|---|---|
| 구분 (*) | 금액 | 영업부문 |
| A 회사 | 4,305,312,352 | 제약사업 |
| B 회사 | 2,926,269,981 | 제약사업 |
| C 회사 | 2,615,869,875 | 패브릭사업 |
| 합계 | 9,847,452,208 | |
(*) 회사명은 기밀유지 계약조건 등으로 기재하지 않았습니다.
<전기>
| (단위: 원) | ||
|---|---|---|
| 구분 (*) | 금액 | 영업부문 |
| 가 회사 | 3,192,081,505 | 제약사업 |
| 나 회사 | 2,480,824,025 | 제약사업 |
| 다 회사 | 2,341,239,608 | 제약사업 |
| 라 회사 | 2,649,681,365 | 패브릭사업 |
| 합계 | 10,663,826,503 | |
(*) 회사명은 기밀유지 계약조건 등으로 기재하지 않았으며, 전기의 발주처명을 영어 알파벳에서 당기의 발주처 영어 알파벳과 혼동을 주지 않기 위하여 한글명으로 변경 하였습니다.
4) 영업부문의 수익 내역은 다음과 같습니다.
<당기>
| (단위: 원) | |||
|---|---|---|---|
| 구분 | 제약사업 | 패브릭사업 | 합계 |
| 주요 제품/상품/용역 계열 | |||
| 상품매출 | - | 3,674,935,760 | 3,674,935,760 |
| 제품매출 | - | 7,399,421,237 | 7,399,421,237 |
| CDMO매출 | 11,048,700,532 | - | 11,048,700,532 |
| 기타 | 921,734,141 | - | 921,734,141 |
| 합계 | 11,970,434,673 | 11,074,356,997 | 23,044,791,670 |
| 수익 인식시기 | |||
| 한 시점에 인식 | 639,463,663 | 11,074,356,997 | 11,713,820,660 |
| 기간에 걸쳐 인식 | 11,330,971,010 | - | 11,330,971,010 |
| 합계 | 11,970,434,673 | 11,074,356,997 | 23,044,791,670 |
<전기>
| (단위: 원) | |||
|---|---|---|---|
| 구분 | 제약사업 | 패브릭사업 | 합계 |
| 주요 제품/상품/용역 계열 | |||
| 상품매출 | - | 5,049,035,072 | 5,049,035,072 |
| 제품매출 | - | 8,243,903,169 | 8,243,903,169 |
| CDMO매출 | 21,353,599,829 | - | 21,353,599,829 |
| 기타 | 1,073,560,779 | - | 1,073,560,779 |
| 합계 | 22,427,160,608 | 13,292,938,241 | 35,720,098,849 |
| 수익 인식시기 | |||
| 한 시점에 인식 | 607,940,645 | 13,292,938,241 | 13,900,878,886 |
| 기간에 걸쳐 인식 | 21,819,219,963 | - | 21,819,219,963 |
| 합계 | 22,427,160,608 | 13,292,938,241 | 35,720,098,849 |
(3) 지역별 부문정보는 다음과 같습니다.
| (단위: 원) | ||||
|---|---|---|---|---|
| 구분 | 당기 / 당기말 | 전기 / 전기말 | ||
| 매출 | 비유동자산 | 매출 | 비유동자산 | |
| 국내 | 2,915,476,214 | 4,503,092,861 | 2,100,544,702 | 5,964,221,842 |
| 해외 | 20,129,315,456 | 95,267,018,500 | 33,619,554,147 | 116,734,959,084 |
| 합계 | 23,044,791,670 | 99,770,111,361 | 35,720,098,849 | 122,699,180,926 |
(2) 시장점유율
① 바이오의약품 사업
플라스미드 DNA 기반의 바이오의약품 연구/개발 사업과 플라스미드 DNA 생산/공
급(CDMO)사업은 아직 전 세계적으로 완제의약품으로 승인을 받은 의약품이 없는
관계로 시장점유율을 예측하기 곤란합니다.
② 섬유사업
심지 사업은 의류 및 모자용 심지 류 국내시장 수요의 약 20~30% 선 점유율을 차지
하는 것으로 추정합니다.
(3) 시장의 특성
① DNA 백신 및 핵산 기반 치료제 분야
DNA 백신 시장 보고서 2030 (DNA Vaccine Market Report: Trends; Forecast and Competitive Analysis to 2030 (2023년 10월, 리서치사: Lucintel)에 따르면, DNA 백신 시장은 2024년부터 2030년까지 6.5%의 연평균 복합 성장률(CAGR) 로 성장을지속하여 2030년까지 약 8억 달러 규모에 이를 것으로 예상하고, 시장조사기관인 모르도르 인텔리전스(Mordor Intelligence)가 2023년 8월 발행한 시장보고서 '핵산 기반 치료제 시장의 규모 및 시장의 성장 경향과 이의 예측(Nucleic Acid-based
Therapeutics Market Size & Share Analysis-Growth Trends & Forecasts (2023-
2028)'에 따르면, 세계의 핵산 기반 치료제 시장규모는 2023년 48억 9,000만달러이며 2023년부터 2028년까지 연평균성장률(CAGR) 14.29%로 2028년에는 95억
4,000만 달러 규모에 달할 것으로 예측하였습니다. 특히, mRNA 백신과 치료제 시장은 “mRNA 백신과 치료제 시장의 산업의 경향과 이의 성장 예측 보고서(mRNA
Vaccine and Therapeutics-Market Share Analysis, Industry Trends & Statistics, Growth Forecast (2025-2030) (2023년 3월, Mordor Intelligence)에서, 2025년 638억 9,000만 달러, 2030년에는 1,388억 8,000만 달러에 달할 것으로 예측 기간(2025-2030년)의 CAGR은 16.8%를 나타낼 것이라 전망하였습니다.
핵산 기반 치료제 시장은 주로 유전질환과 유전적 장애를 대상으로 하는 치료제로 개발이 되고 있습니다. 기존 치료제들이 치료 효능이 거의 없거나 크지 않아, 혁신 의약품으로 평가를 받고 있습니다.
핵산 기반 치료제 중 mRNA 치료제 분야는 다국적 제약사들의 자금 및 협력을 지원받은 바이오텍 기업들이 신종 감염병 치료제 및 항암치료제를 대상으로 임상 개발을 진행 중에 있습니다. 대표적인 바이오텍 기업들로는 모더나(Moderna), 화이자(Pfizer), 바이오엔텍(BioNTech)사등이 있습니다. 대형 글로벌 제약사에 의해 개발중인 제품들은 대부분은 1상 혹은 2상 임상 연구를 진행하고 있으나, 일부 제품들은 임상 3상을 진입하기도 하였습니다.
② 플라스미드 DNA CDMO 산업
플라스미드 DNA는 최근 미국 및 전 세계에 시판된 바이러스 운반체 기반 유전자 치료제들의 원료물질로 이용되고 있고, 플라스미드 DNA 유전자 치료제에서는 주성분으로 이용되고 있어, 전 세계 유전자치료제 의약품 생산의 근간을 이루는 중요한 역할을 하고 있습니다.
즉, AAV 운반체 기반 유전자치료제 또는 렌티바이러스 운반체 기반 유전자치료제를
생산하기 위해서는 반드시 플라스미드 DNA의 의약품 생산이 전제되어야 합니다.
따라서, 최근 전 세계 유전자치료제 시장의 급속한 성장에 힘입어, 플라스미드 DNA의 의약품 위탁개발생산 산업의 성장이 가속화 되고 있습니다.
글로벌 시장조사기관 프레시던스 리서치(Precedence Research)에 따르면, 글로벌 플라스미드 DNA 제조시장 규모는 2022년 4억 4,613만 달러로 추정되며, 2022년부터 2030년까지 연평균 성장률(CAGR) 21.7%로 2030년에는 21억 5,658만 달러에 이를 것으로 예상됩니다.
비록 유전자치료제 시장의 급속한 성장으로 이들의 원료물질인 플라스미드 DNA의 전 세계 의약품 생산 수요는 증가하고 있지만, 원료물질이라는 점과 고순도, 고농도의 플라스미드 GMP 생산기술이 필요하다는 점들로 인해, 전문적인 위탁 생산기업이전 세계적으로 많지 않고, 기업들 간 기술력의 차이가 있습니다.
대표적인 플라스미드 DNA 위탁개발생산기업으로는 미국의 VGXI, Inc.(진원생명과학자회사)사, 벨기에의 유로젠텍(Eurogentec)사, 미국의 알데브론(Aldevron)사, 영국의 코브라(Cobra)사 등이 있습니다.
최근 플라스미드 DNA의 전 세계 위탁개발생산 수요가 증가함에 따라, 몇몇 기업들의 생산시설 확장 보도가 이어지고 있습니다.
미국의 VGXI, Inc.사와 Aldevron사는 2020년대 초까지 연 매출 10억 달러의 생산시설을 확장하였습니다.
③ 섬유 사업
당사는 상기 바이오 의약품 사업과 별도로 면, P/C 및 CVC 등을 소재로 한 의류용
접착, 비 접착 심지를 주 ITEM으로 하여 VIETNAM 해외공장에서 제조한 심지
(Dress Shirts, Caps등의 부자재로 쓰임)를 판매하고 있습니다.
동남아 저개발국에서 저가 심지 제품이 일부 생산되고 있음을 고려할 때 제품차별화를 통한 비교우위와 다품종 소 Lot 화로 다양한 수요자의 욕구에 신속히 대응하는 판매 전략이 요구됨에 따라 고부가가치제품개발과 다양한 소재 개발로 해외 수출 확대
에 노력하고 있습니다.
주거래처는 국내외의류업체(수출 및 내수용 봉제업체) 및 해외 Buyer로서 다양한
Sales Network를 가지고 있습니다.
비록 심지 시장이 직물 제품시장에 비해 협소한 편이나 품질 우위 및 가격 경쟁력을
유지하며 판매 확대에 힘쓰고 있습니다.
(4) 신규사업 등의 내용 및 전망
① 신약개발사업 부문
신약개발사업은 핵산 기반 바이오 신약과 항염증 치료 신약으로 나눌 수 있습니다. 핵산 기반 바이오 신약은 DNA 기반 의약품과 mRNA 기반 의약품으로 나눌 수 있으며, 치료 기전에 따라 핵산 기반 백신, 핵산 기반 유전자 의약품으로 구성되어 있습니다.
DNA 기반 의약품 중 DNA 백신은 다수의 제품이 비임상 시험 및 국내외 임상시험 수행 중에 있으며, DNA 기반 단백질의약품 및 단클론 항체 의약품은 타당성 검증 연구를 통해 비임상 후보물질을 도출하고 있습니다. 또한 mRNA 기반 의약품은 연구개발 기반 플랫폼 구축을 완료하고, mRNA 백신 후보물질을 이용한 효능 및 안전성 평가 연구를 진행하고 있습니다.
DNA 백신은 신변종 바이러스로부터 초래하는 질병을 사전에 예방하기 위한 신변종 감염병 DNA 백신과 만성화된 감염 질병에 대비하기 위한 만성 감염병 DNA 백신으로 구분됩니다.
당사는 신변종 감염병 DNA 백신으로, 메르스와 지카 바이러스 백신의 후보물질을 개발하여 각 질환에 대해 메르스 DNA 백신의 1상(미국)과 1/2a상(한국) 임상시험을,지카 바이러스 DNA 백신의 1상(미국)과 1b상(미국) 임상시험을 완료하였고, 현재
코로나19 DNA 백신, SFTS DNA 백신을 개발하고 있습니다.
메르스 DNA 백신(GLS-5300)은 중동호흡기증후군 코로나 바이러스의 예방 백신입니다. 메르스 바이러스에 의한 감염병은 중증 급성 호흡기 질환으로 치사율이 40% 이상으로 높으며, 국내에서는 2022년 7월에 중동지역을 포함한 해외방문으로 국내 메르스 감염병 환자 의심 신고를 포함하여 116건 접수되어 우리나라 정부는 지속해서 메르스 감염에 대한 조기발견 및 지역 사회 전파 차단에 심혈을 기울인 바 있습니다.
당사는 2015년 5월 27일 이노비오와 메르스 DNA 백신의 공동연구 계약을 체결하여, 비임상 연구와 임상 연구에서는 IND 신청 및 승인, 임상시험관리, 그리고 임상시료의 대량생산을 담당하여 해외 1상 및 국내 1/2a상 임상연구를 주도적으로 진행했습니다.
2015년 11월 19일 미국 FDA로부터 1상 임상 시험계획 승인을 받아, 2015년 11월
11일 미국 국방부 산하 월터리드 미육군 연구소(Walter Reed Army Institute of
Research)가 임상시험 관련비용을 부담하는 조건으로 공동연구 개발 계약을 체결하여 임상 1상 연구를 착수하였습니다.
2017년 2월 24일 신종감염병 글로벌 준비 혁신 협력체(CEPI)가 주관하는 ‘신종감염병 백신-글로벌 보험’1차 학술대회에서 해당 임상 연구의 매우 우수한 면역학적 중간 결과를 발표하였고, 2018년 6월 27일 WHO와 IVI 공동 주최 메르스 백신 국제심포지엄에서 1상 임상시험 예비 결과를 발표하였습니다.
2019년 7월 25일 완료된 해당 임상시험 결과를 국제 저명 의학전문학술지인 란셋 인펙셔서 디지즈(Lancet Infectious Disease)에 발표하였습니다.
메르스 DNA 백신의 우수한 안전성과 높은 백신 면역 반응을 확인하였을 뿐만 아니라, 2015년 국내 메르스 사태에서 확보한 메르스 감염 환자의 혈액을 임상시험 대상자의 혈액과 비교 평가한 결과로부터 백신 접종 60주 후에도 메르스 완치 환자와 유사한 면역반응이 유지됨을 확인하였습니다.
또한, 당사는 국내에서 메르스 DNA 백신의 개발 및 국가 기관에 응급 백신을 공급하기 위한 목적으로 2016년 12월 7일 국제백신연구소(IVI)로부터 관련 임상시험 1/2a 임상시험 개발비 전액을 지원을 받는 계약을 체결하였습니다.
2017년 6월 30일 국내에서 1/2a 상 임상시험을 수행하기 위해 한국 식품의약품안전처에 임상시험 계획 승인을 신청하여, 2017년 9월 14일 임상시험 계획승인을 받았습니다.
2018년 6월 메르스 DNA 백신(GLS-5300)의 1/2a 상 임상시험을 위한 임상시험기관의 임상시험 심사위원회(IRB)의 허가를 받았고, 2018년 9월 5일 첫 번째 임상시험 대상자의 첫 접종을 시작으로 서울대병원과 분당서울대병원에서 1/2a 상 임상시험을 진행하여, 2019년 5월 30일 모든 임상시험 대상자들의 백신 접종을 완료하였으며,
2020년 4월에 해당 임상시험을 종료되었습니다.
해당 임상시험 기간 동안 GLS- 5300을 투여한 모든 접종군에서 백신과 관련 있는 중대한 이상반응은 발현되지 않았으며, 백신을 투여한 그룹에서 접종용량과 접종횟수에 상관없이 그룹간 내약성의 차이는 없었으며, 백신의 효과가 잘 유지되는 것을 확인하였습니다.
이노비오와의 계약에 의해 GLS-5300의 후속 개발은 이노비오에서 담당하며 당사는
일정 지분을 갖습니다
지카 바이러스 DNA 백신(GLS-5700)은 지카(Zika) 바이러스 감염병을 예방하거나 치료를 목적으로 하는 백신입니다. 임산부가 지카(Zika) 바이러스에 감염이 되면,
태아의 소두증을 유발하는 감염병으로 현재까지 상용화된 백신 및 치료제가 없습니다.
2016년 1월 22일 이노비오와 DNA 백신 개발의 공동연구 계약을 체결하였으며, 당사에서는 비임상 연구와 임상시료의 대량생산, 임상 1상 시험개발을 담당하여 수행했습니다.
2016년 6월 20일 미국 FDA로부터 임상시험 계획승인을 받았고, 2017년 10월 10일 GLS-5700의 임상시험 중간결과를 국제 저명 의학 전문 학술잡지인 뉴 잉글랜드 저널 오브 메드신(New England Journal of Medicine)에 발표하였습니다.
또한, 2016년 8월 30일 푸에르토 리코에서 160명의 피험자를 대상으로 하는 추가
1상(1b상) 임상시험도 미국 FDA로부터 승인을 받아, 2017년 6월 16일 임상시험 대상자 160명의 등록이 완료된 후 모든 임상시험 대상자들에게 백신 접종을 완료하였으며, 2018년 6월 GLS-5700의 해당 임상시험이 종료되었습니다.
GLS-5700 백신을 단회 혹은 다회 투여한 두 그룹 모두에서 접종부위에 이상반응이 일시적으로 발현했지만 경미했고, 두 그룹에서 용량에 따른 발현의 차이는 없었습니다. 또한, GLS-5700과 관련 있는 중대한 이상반응은 관찰되지 않았고, 두 그룹간 내약성의 차이는 없었으며 백신의 효과가 잘 유지되는 것을 확인했습니다.
이노비오와의 계약에 의해 GLS-5700의 후속개발은 이노비오에서 담당하고 당사는 일정지분을 갖습니다.
SFTS DNA 백신(GLS-5140)은 중증열성혈소판감소증후군(SFTS) 예방하기 위한 열성 질환 백신입니다. 중증열성혈소판감소증후군(SFTS)은 SFTS 바이러스에 감염된 진드기에 물려 감염되며, 고열등의 증상을 동반하는 중증열성질환입니다.
2015년 12월 한국과학기술원(KAIST) 산학협력단과 보건복지부 기술개발 사업에 참여하여 개발을 시작하였으며, 이 과정에서 살인진드기 바이러스 항원 후보물질 4종을 도출하였습니다. 마우스 및 페럿 동물모델을 이용한 실험을 통해 예방 효과를 확인하였고, 해당 연구 결과는 2019년 8월 23일 국제 저명학술지인 네이쳐 커뮤니케이션(Nature Communications)에 발표되었습니다.
아울러, 2018년 6월 29일 한국과학기술원(KAIST)과 공동으로 "중증열성혈소판감소증후군(SFTS) 예방DNA 백신"에 대한 특허를 대한민국 특허청에 출원하였으며,
2020년 2월 4일 특허등록을 완료하였습니다.
이후 2019년 6월 26일 미국, 일본, 중국에 특허 출원을 위한 특허협력조약(PCT)을 출원하였고, 그 결과 2024년 4월 2일 일본 특허청과 2024년 10월 11일 중국 특허청으로부터 중증열성혈소판감소증후군(SFTS) 바이러스 감염 질환 예방 또는 치료용 백신 조성물에 대한 특허등록을 받았습니다.
2020년 10월 보건복지부 백신실용화기술개발 사업단의 미래 대응 미해결 감염병 신규 백신 개발 분야의 지원 과제로 선정되어 임상시험 1상의 임상시험계획 승인까지의 연구개발비용을 지원받았으며, 해당 정부지원 과제를 2023년 12월에 성공적으로 종료하였습니다.
비임상 시험을 통해 선정한 후보물질이 설치류 동물에서 우수한 면역 효능을 보였으며, 백신을 접종한 페럿 동물모델에서는 SFTS 바이러스 감염에 의한 사망 사례가 나타나지 않아 백신의 뛰어난 방어능이 확인되었습니다. 또한, 백신의 독성을 평가하기
위해 GLP 기관에 반복 투여 독성 시험을 의뢰하였고, 약물로 인한 유해 반응이 관찰되지 않아 안전성이 확보된 백신임을 확인하였습니다. 수행한 모든 비임상시험 결과를 토대로, 임상시험에 적용하기 위한 적절한 용량 및 용법을 최종 결정하였습니다. 해당 실험 결과는 2022년 11월 10일과 11일에 열린 화순 국제 백신 포럼에 연자로 초청받아 발표한 바 있습니다.
한국 식품의약품안전처(식약처)와 2022년 8월 31일, 12월 5일, 2023년 6월 7일에 걸쳐 총 3차례의 사전 상담 회의를 진행하며, 제1상 임상시험계획 승인 신청을 위한 제출 자료에 대해 논의를 하였고, 2023년 11월 8일에 제1상 임상시험에 대한 IND 신청서를 제출하였습니다. 하지만, 식약처는 해당 임상시험이 전 세계적으로 전례 없는 최초 사례이며, 참고 가능한 자료가 전무하다는 점을 들어 제출된 IND 자료에 대해 보다 면밀하고 엄격한 검토가 필요하다는 의견을 제시하였습니다. 이에 따라 기 제출된 IND 자료의 보완 필요성을 인지하고 식약처와의 협의를 통해 2024년 1월 17일 해당 IND 신청을 자진 취하하였습니다. IND 자료를 보완한 후, 식약처로부터 승인을 받는 즉시 임상개발에 착수할 예정입니다.
코로나19 DNA 백신(GLS-5310)은 코로나 바이러스 감염병의 예방목적의 백신입니다.
2020년 2월 우리나라에 코로나19 확진사례가 발생한 직 후 코로나 바이러스(SARS-CoV2) 감염병 백신 후보물질의 디자인 및 제작을 추진하다가 2020년 3월 27일
"2020년도 질병관리본부 긴급 현안 지정학술연구개발 용역과제"인 "핵산 백신 플랫폼을 활용한 코로나19 백신 후보물질 개발사업"에 우선 순위 협상대상자로 선정되었습니다.
2020년 4월 GLS-5310 후보물질을 제작한 후 생체 외에서 후보물질로부터 코로나
19 바이러스 항원이 생성되는 것을 확인하였습니다.
2020년 5월 VGXI, Inc.사에서 후보물질의 cGMP 생산공정 개발연구를 완료하여
2020년 7월 후보물질을 마우스에 접종한 후 우수한 항원 특이적 T세포 면역반응과 항원 특이적 결합 항체 반응, 그리고 중화항체의 생성을 확인하였습니다.
임상에서의 투여 경로를 실험동물에 적용한 후보물질의 용량 증량에 따른 면역원성 평가를 완료하여, 2020년 12월 4일 한국 식품의약품안전처로부터 1/2a상 임상시험계획 승인을 받았습니다. 임상시험 1상 착수를 위해 고대구로병원과 2020년 12월 18일 임상시험 계약을 체결하였고, 12월 31일 첫 대상자의 접종을 완료하고, 2021년
1월 21일 고용량군의 대상자 등록이 시작되어, 2021년 3월 4일 임상 1상 임상시험 대상자 45명의 등록이 완료되어, 2021년 5월 모든 대상자의 접종을 완료하였습니다.
2021년 7월 8일 임상 1상 중간 분석 결과가 자료 안전성 모니터링 위원회(DSMB) 심의를 통과하여 임상 2a상 시험에 진입하였습니다.
임상 2a상은 총 5개 기관에서 실시하였고, 위약 대조군이 있고 이중눈가림 임상시험으로 120명을 계획하였었습니다. 총 126명이 등록되었고, 2023년 1월 6일 마지막 대상자의 최종 방문이 완료되었으며, 2023년 5월 10일 위약을 접종한 대상자중에서
본인 동의하에 GLS-5310을 재접종한 마지막 대상자까지 최종 방문을 마쳤습니다.
2024년 8월 21일 임상시험수탁기관(CRO)에서 해당 임상 시험 결과 분석이 완료되었으며, 2024년 12월 12일 임상 1/2a상에 대한 임상시험결과보고서 작성이 완료되었습니다.
GLS-5310의 글로벌 개발을 위해 기존 피내 접종과 비강 내 접종을 병용하는 임상시험을 미국에서 수행하고자 2020년 1월 19일 미국 FDA에 임상시험계획 승인을 신청하여, 2021년 7월 27일 승인을 받은 후, 2022년 1월 3일 미국 FDA로부터 코로나19백신 접종자들을 대상으로 하여 GLS-5310을 부스터 샷으로 접종하는 임상시험계획의 변경 승인을 받았습니다. 본 임상 연구의 변경 승인을 통해 미국에서 mRNA 백신과 아데노바이러스 전달체 백신을 접종한 대상자에게 진덤(Gene-Derm) 흡인압력을
이용 피내 접종군과 피내 접종 및 코 스프레이를 이용한 비강 내 접종을 병용한 접종군을 비교하고자 하였습니다. 2022년 9월 말 기준으로 69명 중 69명이 등록되었고, 임상시험 완료 및 결과 분석이 완료되었습니다.
2020년 12월 29일 코로나19 백신인 GLS-5310의 1/2a상 임상개발 비용인 98억원 중 73억원의 연구비를 지원받는 내용으로 "코로나19 치료제 백신 신약개발사업단"과
협약을 체결하였습니다. 또한, 2021년 9월 6일 국가임상시험지원재단과 코로나19 백신 임상2a상 대상자 모집지원 협약을 체결하였습니다. 2025년 7월 9일 보건복지부는 GLS-5310의 1/2a상 임상개발 과제에 대한 제재처분을 통지하였습니다. 부과 사유로는 국가연구개발혁신법 제12조제2항에 따른 최종평가 결과 연구개발과제의 수행과정과 결과가 극히불량으로 부과금액 73억과 2년간 국가과제 참여제한 처분을 받았습니다. 본 처분 결과에 대한 집행정지 신청을 2025년 9월 8일 제기하였으며,
2025년 9월 23일 집행정지 신청이 인용되었습니다.
2021년 7월 22일 코로나19 DNA 백신인 GLS-5310의 백신조성물 특허에 대한 국내
및 특허협력조약(PCT) 출원을 완료하였으며, 2024년 9월 19일 대한민국 특허청으로부터 특허 등록을 받았습니다 .
2023년 1월, 자체개발 흡인작용 피내접종기 진덤(Gene-Derm)을 이용한 코로나19 DNA 백신(GLS-5310)의 안전성 및 면역원성에 대한 임상 1상 결과를 국제감염병학회(International Society for Infectious Diseases, ISID) 학술지인 국제감염질환저널(International Journal of Infectious Diseases;2021년 인용지수: 12.074)에 발표했습니다.
2023년 5월 SARS-CoV-2를 포함한 전염병 대비를 위한 DNA 백신 관련 내용의 리뷰 논문을 백신(Vaccines) 학술지에 발표하였고, 2023년 6월 임상 1상 분석결과중에서 GLS-5310 DNA 기초접종 후 mRNA 백신을 추가접종한 대상자들에 대한 면역원성 결과를 백신(Vaccine (Elsevier)) 학술지에 게재하였습니다.
당사는 DNA 백신을 피내에 타겟팅하고 항원의 발현 효율성을 높이기 위해 흡인작용피내 접종 의료기기인 진덤(Gene-Derm)을 적용하고 있습니다.
2021년 8월 26일 진덤(Gene-Derm)의 이물질 및 분비물에 의한 오염 방지의 흡인기 플랫 모듈의 개량 특허를 국내 출원하여 2023년 6월 29일에는 해당 특허가 등록되었으며, 2022년 11월 11일 특허협력조약(PCT) 출원이 완료되었습니다. 또한, 2021년 4월 14일 분비물에 의한 디바이스 오염을 방지하는 흡인기 모듈에 대해 국내 특허를 출원하여, 2023년 7월 10일 이의 특허가 등록되었으며, 2022년 4월 13일 특허 협력조약(PCT) 출원과 2023년 10월 6일 미국 특허 출원이 완료되었습니다.
진덤(Gene-Derm) 기기는 물리적/화학적/생물학적 성능시험 및 전기/전자파 성능시험을 포함한 각종 시험검사들과 제조 및 품질관리기준(GMP) 인정서 및 ISO-13485 취득을 완료하여 기술문서 심사를 통과하게 되어 2022년 4월 29일 식품의약품안전처로부터 의료기기(품목명: 전동식의료용 흡인기, 2등급)로 승인을 득하였습니다.
해당 흡인기를 2021년 10월 햄스터 공격 감염 모델을 이용한 동물실험에 적용하여 GLS-5310이 야생형 및 베타 변이 코로나 19 바이러스에 대한 감염을 완벽하게 예방함을 확인하였습니다.
2021년 11월 5일 DNA 백신의 흡인작용 피내 접종 의료기기인 진덤(Gene-Derm)의 플랫폼 개발과 이를 이용해서 확인된 연구 결과를 사이언스 어드밴시스(Science
Advances)에 게재하였습니다. 또한, 진덤(Gene-Derm)의 약물 전달 메커니즘 연구를 미국 뉴저지 주립대학인 럿거스(Rutgers) 대학 연구진과 공동연구로 진행하여,
2023년 1월 그 결과를 국제학술지인 약물 전달 프론티어스(Frontiers in Drug
Delivery)에 게재했습니다.
당사는 만성 감염병 DNA 백신으로 C형 간염 DNA 백신을 개발하고자 2011년 10월 7일 이노비오사와 계약을 체결하여 일본을 제외한 아시아 지역의 개발 및 판권을 확보하였습니다.
만성 C형 간염 환자의 치료를 위한 백신인 VGX-6150은 2013년 10월 18일 국내
식품의약품안전처로부터 임상시험 계획을 승인을 받아 연세대 세브란스병원과 부산대 병원에서 18명의 만성 C형 간염 임상시험 대상자 대상으로 1상 임상시험을 진행하였습니다.
또한, 추가접종 후 면역기억에 의한 장기간 치료 효과를 확인하기 위해 2014년 9월 26일 국내 식품의약품안전처로부터 상기 1상 임상시험이 종료된 임상시험 대상자 중
희망자에 한해 후속 임상시험 계획을 승인을 받아 추가 임상시험을 완료하였습니다.
2017년 9월 26일 HCV 2017 국제심포지엄에서 VGX-6150 안전성과 면역원성에 대한 결과를 발표하였고, 2020년 2월 20일 심각한 부작용없이 매우 안전하면서도 C형 간염바이러스에 대한 T세포 면역반응을 높인다는 1상 임상시험 결과를 간연구분야의 국제적 전문학술지인 저널 오브 헤파톨로지(Journal of Hepatology) 온라인판에 게재하였습니다.
C형 간염 예방 백신으로 기존 치료제로 완치된 만성 C형 간염 환자를 대상으로 재감염 예방하고자 하는 DNA 백신(GLS-6150)과 C형 간염 고위험군을 대상으로 만성 C형 간염 예방하고자 하는 DNA 백신(GLS-6100)이 있습니다.
2017년 6월 9일 보건복지부 기술개발사업단 주관과제로 선정되어 C형 간염 예방을 위한 DNA 백신인 GLS-6150과 GLS-6100 개발에 정부로부터 지원을 받게 되었습니다.
2021년 1월 4일 한국 식약처에 GLS-6100의 국내 1상 임상시험 계획승인신청서를 제출하였고, 2021년 5월 20일 이의 승인을 받았습니다. 하지만, 이후 정부로부터 해당 임상과제의 후속 지원이 없어 개발을 종료했습니다.
2017년 10월 31일 한국 식약처에 GLS-6150의 국내 1상 임상시험 계획승인을 신청하였고, 2018년 2월 2일 이의 승인을 득하였습니다.
2018년 7월 임상시험 기관의 임상시험 심사위원회(IRB)의 1상 임상시험의 허가를 받았고, 2018년 9월 4일 첫 번째 임상시험 대상자의 첫 접종이 이뤄진 후, 1상 임상시험을 연세 의료원 세브란스 병원과 부산대 병원에서 진행하였습니다.
2020년 5월 11일 해당 임상시험을 종료하여 식약처에 종료 보고를 완료하였습니다.
1상 임상시험 전반에 대한 안전성 결과와 면역원성 결과에 대한 통계분석이 완료되었으며, 2022년 12월 12일 임상결과보고서(CSR) 최종본을 수령하여 보고서 작성이 완료되었습니다
당사는 DNA 기반 단백질 의약품 및 단클론 항체 의약품은 기존 단백질의약품 및
단클론 항체 의약품 대비 우수한 가격 경쟁력, 체내 안전성 및 약효 지속성을 장점으로 하여, 자체 R&D 기술력으로 DNA기반 의약품을 직접 개발하고 있습니다.
당사의 R&D 기술에 의해 개발하고 당사가 보유하고 있는 DNA 백신 플랫폼은 감염성 질환에 대한 예방백신 개발에 적용할 수 있는 기술이기도 합니다. 2021년 12월
17일 DNA 백신 플랫폼에 이용하여 개발한 DNA 백신을 동물에 접종 시 면역원성이 잘 유도됨을 확인 및 검증하여 DNA 백신의 기술과 이의 효능을 국제 학술지인 매서드 인 몰리큘러 바이올로지(Methods in Molecular Biology)온라인판으로 출판하였습니다.
DNA 기반 단백질의약품으로는 혈우병 치료제의 개발 타당성에 대한 검증 연구를 진행하고 있습니다.
DNA 기반 혈우병 치료제는 2014년 10월 강원대 의생명과학대학의 혈우병 치료제의
의약품 개발 타당성 검증 연구를 참고하여, 당사 자체적으로 혈액응고 8인자를 이용하여 후보물질에 대한 개선 연구를 진행하고 있었습니다만, 2019년 이후 코로나 바이러스의 갑작스러운 확산에 따른 팬데믹 시기에는 코로나 백신 연구개발에 집중하고자 본 연구를 중단하였었습니다. 팬데믹이 종식이 된 후, 혈액응고 8인자의 체내 생성량과 활성을 높이기 위한 제품 개발을 위해 혈우병 치료제 후보물질 발굴을 위한
연구를 재개하여 진행하고 있습니다.
DNA 기반 단클론항체 의약품으로 B형 간염 면역글로불린의 개발타당성에 대한 검증 연구를 진행하고 있습니다.
DNA 기반 B형간염 면역글로불린은 2017년 4월 강원대학교 산학협력단 보유의 B형간염 바이러스의 preS1에 특이하게 결합하는 항체 2종에 대한 특허와 기술이전을 받아, 이의 타당성 검증 연구에 착수하였습니다. 그 결과, 2018년 5월 30일 대한민국
특허청으로부터 특허 등록을 받았고, 2019년 2월 5일 미국 특허 등록을 받았습니다.
타당성 검증을 위해 DNA 기반 B형 간염 항preS1 면역글로불린 2종의 후보물질 플라스미드와 항S 면역글로불린 2종의 후보물질 플라스미드를 제작하여, 연구용 시료를 이용하여 동물세포에서 항체 생성과 항원 결합능력을 확인하였고, 실험동물에서는 이들 4종의 후보물질 플라스미드로부터 항체 생성 및 체내 분포 경향 분석을 진행하였습니다. 2019년 9월에는 B형 간염바이러스 연구 분야의 세계적 권위자인 건국대 의학전문대학원 김균환 교수 연구팀과 함께 실험동물을 이용한 효능평가 연구를 수행하여 항preS1 면역글로불린과 항S 면역글로불린을 동시에 처리한 조건에서 우수한 바이러스 억제 효과가 있음을 확인하였습니다.
현재, 당사 자체적으로 높은 국내 분포를 보이는 B형 간염바이러스 유전자 C형에 대하여 4종 후보물질들의 억제 효과를 평가중에 있습니다.
또한, 당사는 류머티즘 관절염 치료 목적으로 DNA 기반의 항 TNF 알파 단클론항체 후보 물질을 개발하여 해당 후보물질이 동물세포에서의 항체 생성, TNF 알파와 아밀로이드 베타와의 결합력, 및 TNF 알파의 세포 살상 반응 억제능이 있음을 확인하였으나, 생산된 제품의 상업화 적합성 문제로 연구개발을 중단하였습니다.
당사는 mRNA 기반 의약품의 연구개발을 수행하기 위해 mRNA 기반 플랫폼 구축을
완료하여, mRNA 백신 후보물질의 효능 및 안전성 평가 연구를 진행하고 있습니다.
2018년 9월 17일 자회사 VGXI, Inc.가 임상용 의약품 mRNA를 생산하기 위해 미국 휴스턴 매소디스트 병원 연구소(Houston Methodist Research Institute)와 독점적 라이선스-인 계약을 체결함에 따라, mRNA 백신 및 mRNA 치료제 생산의 핵심 기술과
mRNA 백신 설계 및 연구 기술을 이전 받아 mRNA 백신 및 mRNA 치료제 연구 개발사업에 진출하게 되었습니다.
자회사인 VGXI, Inc.는 mRNA 기반 의약품의 상업적 생산을 위한 파일럿 생산공정을 성공적으로 구축한 후 대규모 cGMP 생산공정을 구축하기 위한 공정 스케일 업 및 최적화 단계를 진행하고 있습니다.
코로나19 mRNA 백신은 2020년 2월 우리나라에 코로나19 확진 사례가 발생한 직후
휴스턴 매소디스트 병원 연구소의 존 쿡(John Cooke) 박사 연구팀으로부터 mRNA 백신 설계 및 연구 기술을 이전 받아 mRNA 백신 후보물질의 디자인 및 제작을 진행하였습니다.
2020년 3월 27일 "2020년도 질병관리본부 긴급 현안 지정 학술연구개발 용역과제"인 "핵산 백신 플랫폼을 활용한 코로나19 백신 후보물질 개발 사업"에 우선 순위 협상대상자로 선정되어, 2020년 5월 후보물질을 2종을 제작한 후, 2020년 9월 생체 외에서 후보물질로부터 코로나19 바이러스 항원이 생성되는 것을 확인하였습니다. 2020년 11월 실험동물에서 후보물질 접종 후 항체 면역반응과 T세포 면역반응이 유도됨을 확인하였으나, LNP 기술을 보유한 기관들로부터 해당 mRNA 백신의 평가를 진행하였으나, 상업적 타당성 문제로 연구개발을 종료하였습니다.
당사는 mRNA 기반의 항암 백신과 단클론 항체 플랫폼 개발을 위한 연구를 진행하고
있습니다.
당사는 2021년 5월 31일 한미 사이언스와 mRNA 백신 대규모 생산기반 및 글로벌 네트워크 구축을 위한 협력 계약을 체결하였습니다.
해당 계약에 따라 당사와 한미 사이언스는 양사가 보유한 핵심 기술을 상호 협력하여
mRNA 백신의 글로벌 대규모 생산을 위한 차세대 생산기술을 함께 연구하고자 하였습니다. 이는 mRNA 백신 기술을 더욱 최적화하여 코로나19 및 신종 감염병 mRNA 백신의 공동 연구 및 사업화를 포함하며, 양사가 파트너로서 핵산 사업 글로벌 네트워크 구축을 통해 기술 확보 및 시장개척 등을 논의하였습니다.
당사는 2021년 6월 17일 보건복지부 백신실용화기술개발사업단의 미래 대응, 미해결 신변종 감염병백신 플랫폼 개발 분야의 지원 과제로 선정되어 mRNA 기반 신속 백신 제작 플랫폼을 구축하고 지카(Zika) 바이러스 mRNA백신 선도 물질 발굴 및 유효성을 평가하는 연구를 진행하였습니다.
지카(Zika) 바이러스 백신 항원 기술은 질병관리청으로부터 이전 받아 과제에 적용하였으며, 지카 바이러스 mRNA 백신의 선도물질 발굴 및 유효성 평가하여 원부자재의
국산화 여부를 확인하여 비임상 및 초기 임상시험용 mRNA 백신 생산 공정 최적화를
포함하고 있었습니다. 당사는 자체 mRNA 기반 신속 백신 제작플랫폼의 구축하여,
2022년 12월 31일 지카(Zika) 바이러스 mRNA 백신 선도물질의 유효성 및 안전성 평가하여 해당 국책 과제는 완료하였으며, 2024년 11월 14일 이의 연구결과를 국제 학술지인 백신(Vaccine; Elsevier) 저널에 게재를 하였습니다.
당사의 원형(circular) RNA 기술을 활용한 새로운 mRNA 백신용 플랫폼 연구를 통해
2021년 6월 25일 과학기술정보통신부 주도 신변종 감염병 대응 플랫폼 기술 개발사업의 참여연구개발기관으로 선정되었습니다. 총 43개월 동안 원형(circular) RNA 플랫폼의 구축, 생산 및 유효성 평가를 수행하고, 신변종 감염병 선정을 위한 대상 감염병(Disease X) 3종의 대량생산 공정 최적화 및 임상용 백신의 생산 내용을 포함하고 있었으며, 당사는 사업의 결과로써 백신의 비임상 시험용 시험물질인 SARS-CoV2 Omicron 원형(circular) RNA의 대량 생산을 완료하여 2023년 12월 주관 연구개발기관에 공급하였습니다. 본 국책과제는 국가 예산 편성 변경 정책에 따라 갑작스럽게 연구 개발 비용의 삭감되어, 예산 부족으로 인하여 당사가 담당하기로 한 연구개발 업무의 진행이 불가하여, 2024년 1월부터는 담당 국책과제에 더 이상 참여하지 않는
것으로 사업을 종결하였습니다.
2021년 9월에 도입한 원형(circular) RNA 플랫폼의 원형(circular) RNA의 공정 최적화를 위한 연구개발을 지속적으로 수행함으로써 보다 우월한 생산효율을 확보한 플랫폼 기술을 완성하여 2023년 12월 15일에 국내특허를 출원하였으며, 현재 심사 중에 있습니다.
당사는 R&D 역량 강화를 위한 전략적인 오픈 이노베이션(Open Innovation)을 지속해서 추진 중에 있습니다.
당사가 확보하고 있는 mRNA 플랫폼을 적용하여 미충족 수요(Unmet Need)가 많은 암 치료 분야에서 mRNA 기반의 항암 백신과 단클론 항체를 개발하여, 현 수준의 치료용 mRNA의 단점을 극복하고 이의 장점은 극대화하고자 하는 목적으로 다수의 기관과 공동연구를 진행하고 있습니다. 그 외에도 여러 방면으로 오픈 이노베이션을 진행하여, 다양한 난치성 전염병의 백신 연구개발을 비롯하여, 암, 자가면역 질환, 퇴행성 만성질환 등에 적용 가능한 혁신적인 치료 방법과 당사의 mRNA 플랫폼에 적용할
수 있는 새로운 치료 방법을 개발하고자 하고 있습니다.
당사는 2022년 12월 8일 애스톤 사이언스와 전략적 업무 제휴 양해각서(MOU)를 체결함으로써, 오픈 이노베이션을 통해 차세대 핵산 기반 백신의 연구 및 개발을 위해 역량을 공유하여 새로운 타깃 물질을 연구 개발하는 파트너로서 협력하기로 하였습니다. 본 MOU의 후속 조치로써 치료 목적의 백신 신약 연구 및 이의 개발을 위하여 인공지능(AI) 스크리닝 방법을 적용한 새로운 항원 결정기의 정보를 공유하고, DNA 백신을 mRNA 기반 백신으로 전환하기 위한 연구를 수행하기 위한 논의를 우선 진행하였으며, mRNA 항암 백신 신약 개발 공동 프로젝트를 구성하여 새로운 항원 결정기를 찾고 효능 및 안정성을 검토하는 연구에 착수하였습니다.
당사는 축적된 DNA 기반 백신 임상 연구 개발 결과와 자체적으로 개발한 mRNA 기반 백신 플랫폼 기술력을 인정받아 2023년과 2024년 2년 연속 연례 백신 세계 아시아의회의 초청을 받아 핵산 기반 백신 연구개발 성과를 발표하였습니다. 싱가포르에서 개최된 2023년 제5회 아시아태평양 백신 우수상 (Asia-Pacific Vaccine
Excellence Award, AVEA) 시상식에서는 '대한민국의 가장 유망한 백신부문' 최우수상을 수상했습니다.
항염증 치료 신약은 천연물 유래성분 의약품과 저분자 화학합성 의약품으로 나눌 수 있습니다.
천연물 유래성분 의약품으로 쓴맛 수용체를 이용한 항바이러스 및 항균 코스프레이 약물이 있으며, 저분자 화학합성 의약품으로 항염증 면역제어 경구약물이 있습니다.
쓴맛수용체를 이용한 항바이러스 및 항균 코 스프레이 약물(GLS-1200)은 2018년 6월 26일 미국 펜실베이니아 대학교로부터 호흡기 감염에 대한 혁신 치료제 및 진단법개발을 위한 쓴맛 수용체 신호전달물질 및 관련기술을 기술이전 받았습니다.
2019년 8월 5일 만성 축농증 치료를 위해 임상용 의약품의 생산을 완료하여 미국
FDA에 2상 임상시험 진행을 위한 임상시험 계획승인을 신청하였습니다. 본 임상은 미국 펜실베이니아 대학교 임상시험센터에서 실시되며 만성 축농증 환자의 부비동 수술이후 7주에 거쳐 만성 축농증 치료제(GLS-1200)인 코 스프레이를 비강을 통해 투여한 후 4개월 동안 급성 축농증의 재발 여부를 확인하는 목적으로 위약 대조군과 함께 99명의 환자를 대상으로 진행할 것을 계획하였습니다.
2020년 4월 13일 미국 FDA로부터 2상 임상시험계획의 승인을 받았지만, 코로나 19 감염병 사태로 인해 임상 시험이 잠정 중단되었습니다.
GLS-1200에 대해 펜실베이니아 대학교와 공동으로 2020년 4월 21일 코로나19 및 독감을 포함한 다른 바이러스에 의한 감염을 예방하는 용도에 대한 특허를 미국 특허청에 출원하였으며, 호흡기 질환 진단 및 치료에 대한 특허는 2021년 1월 5일 미국 특허청에 등록을 받았습니다.
코 스프레이GLS-1200은 비강에 분무되어 비강부위 세포의 쓴맛수용체와 결합하여 산화질소를 생성 분비하게 하여 코로나19 바이러스를 사멸하는 작용기전(MOA)를 예상하고 있습니다.
2020년 4월 29일 코로나19 감염 예방 코스프레이 약물로써 2상 임상시험 계획승인을 미국 FDA로부터 받았습니다.
2020년 6월 11일 펜실베이니아 대학교 임상시험센터에서 의료계 종사자들을 대상으로 한 첫 임상시험 대상자 투약이 진행되었고, 2020년 9월 계획된 225명 임상시험 대상자에서 50% 이상 대상자 등록이 완료되었습니다.
2021년 1월 18일 GLS-1200은 코 부위에 분포하고 있는 코로나19 바이러스 농도를 감소시켰고, 족제비 감염동물 모델을 통해 비강세포내 감염을 억제하는 것으로 확인되었습니다.
미국 루이지애나주 바톤 루지시를 2차 임상시험 실시기관을 추가하고, 2021년 4월 임상대상자를 일반인으로 확대해서 진행할 수 있도록 하는 IRB 승인을 받았습니다. 대상자 모집에 지속적으로 노력하여 2022년 12월 기준 184명이 등록되었으나, 코로나19에 감염된 대상자를 모집하는데 어려움이 있어 임상시험 대상자 모집을 조기 종료하였습니다. 이로써, 2023년에 임상2상 연구를 종료하였고, 임상시험 결과보고서를 작성하였습니다.
항염증 면역제어 경구 약물(GLS-1027)은 당사가 보유한 1상 임상시험이 종료된
GLS-1027(구VGX-1027)을 이용하여 자가면역성 신장 질환등의 치료를 위한 임상개발을 준비하였으나, 전 세계적 코로나 19 감염병의 유행으로 인해 GLS-1027은
코로나19 치료제 임상 개발로 연구개발 방향을 전환하였습니다.
공정개발연구를 통해 불순물이 제거된 GLS-1027을 생산하였고, 기존 물질과의 항염증 반응을 평가하기 위해 이탈리아 카타리나 대학 니콜라티 교수 연구팀과 협력하여 진행한 동물실험에서, GLS-1027이 코로나19 감염 후 생성되는 다수의 염증유발물질(사이토카인)들이 억제됨을 보여주는 결과를 근거로 하여, 2020년 10월 28일
코로나19 감염 후 과대면역에 의한 심각한 폐질환을 방지하는 치료제로서의 개발을 착수하였습니다.
GLS-1027의 2상 임상시험 계획승인 신청서를 미국 FDA에 제출했고, 11월 30일
미국 FDA로부터 승인을 받았습니다.
GLS-1027(국제일반명 zenozulac)은 경구용 캡슐약제로 빠른 체내 소실과 우수한 안전성을 임상 1상연구를 통해 확인되었습니다. GLS-1027은 선천성 면역세포에만 작용하여 사이토카인 분비를 억제함으로써 바이러스 감염 시 과대면역을 제어하여 정상 범위의 수치로 면역이 회복될 수 있게 합니다.
본 약제에 대한 2상 임상시험은 코로나19 확진자를 대상으로 132명을 계획하고 코로나19 바이러스 감염시부터 GLS-1027을 선제적으로 투약하여 코로나19에 의한 심각한 폐렴 발병을 예방할 수 있는지를 평가하였습니다.
우리나라를 포함한 총 4개국(대한민국, 미국, 북 마케도니아, 불가리아)에서 수행하는 다지역 임상시험(MRCT)으로 설계되었습니다.
2021년 3월 1일 바톤 루지 임상시험센터의 IRB 승인을 받았고, 2021년 7월 2일 북 마케도니아 식약처로부터 승인을 받아 임상시험을 착수하였습니다.
2021년 11월 1일 유럽의약품청(EMA)과 불가리아 허가 당국으로부터 GLS-1027의 임상 2상 시험계획을 승인을 받았습니다.
2022년 3월 25일 기준으로 3개국(미국, 북마케도니아, 불가리아)에서 임상시험대상자 118명의 등록을 완료하였습니다.
국내에서는 2021년 1월 29일 임상시험 대상자 15명에 대한 GLS-1027의 2상 임상시험계획 승인 신청서를 식약처에 제출하였고, 2021년 9월 8일 승인을 받았습니다. 임상시험 대상자의 빠른 등록을 위해 국내 5개 임상시험 실시기관에서 진행되었으며, 2022년 4월 8일 마지막 임상시험 개시 방문(SIV)을 완료하여 임상 시험대상자 모집과 등록을 진행하였습니다만, 국내에서는 코로나 19에 감염된 중등증 입원환자 수의
급격한 감소로 인해 환자 모집의 어려움이 있었습니다.
이후, 한국을 제외한 3개국에서 계획한 환자 모집을 완료하여 국내에서의 환자 모집은 조기 종료되었습니다.
2022년 6월 22일 임상 2상 임상시험에 계획된 132명 대상자 모두 등록이 완료되었고, 2022년 12월 기준 대상자 모두 임상시험을 완료했습니다.
임상시험 결과는 약물 효능, 약동학, 그리고 안전성을 변수로 하여 분석하였습니다. 코로나 19 확진자에게 위약 또는 GLS-1027(저용량 또는 고용량)을 매일 경구 투여했을 때 GLS-1027을 투여한 2개 군간 비교에서 이상사례 발현빈도와 중증도는 복용량에 비례하지 않았고, 혈액학적 검사와 활력 징후 등의 검사결과에서도 유의미한 변화는 없었기에 GLS-1027 약물의 안전성과 내약성은 우수함을 확인하였습니다.
다만, 위약군과 GLS-1027의 각 2개군의 효능 비교에서 중증으로 진행되는 빈도와 호흡기 장착일수 등을 유의미하게 줄이지 못하는 것으로 나타났습니다.
해당 임상과제는 모두 완료되었고 2024년 4월 15일 식약처에 종료보고서를 제출하였습니다.
2021년 6월 30일 코로나19 중증 폐렴을 유발하는 햄스터 공격 감염 모델을 이용하여
GLS-1027(국제 일반명 zenozulac)이 용량 의존적으로 폐렴 증상 마커들의 발현을 감소시키며, 해부학적으로는 폐 부위 조직에서 바이러스에 의해 유도되는 세포융합체(syncytia)와 세포이형성(atypia)이 탁월하게 감소되는 것을 확인하였습니다.
해당 치료 효과는 코로나19 바이러스 남아공 변이주인 B.1.351 β variant에 대해서도 동일한 반응이 보이는 것을 확인하였습니다.
당사는 2010년 2월 과학기술정보통신부로부터 기업부설연구소 인가를 받아 당사 기술력으로 신약개발 사업을 직접 수행 및 운영하고 있습니다.
2013년 9월 중소기업청으로부터 당사의 우수한 연구개발 능력을 평가받아 기술혁신형 중소기업(INNO-BIZ) 인증을 받았고, 2019년 3월 기술보증기금으로부터 벤처기업 확인서를 받았습니다.
또한 메르스 DNA 백신, 지카 바이러스 DNA 백신, 코로나19 백신, 쓴맛수용체를 이용한 항바이러스 및 항균 코스프레이 약물, 항염증 면역제어 경구약물의 글로벌 임상개발을 효율적으로 수행하기 위해 미국 펜실베이니아주 포트 워싱톤
(Fort Washington)시에 글로벌 임상개발본부를 설립하였고 최고 의학책임자를 임명하였습니다.
당사는 핵산기반 바이오 신약의 개발을 위하여 국내외 기업 및 전문연구기관과 적극적이고 지속적인 협력 연구를 진행하고 있습니다.
지카 DNA 백신의 개발을 위해 이노비오(Inovio), 미국 위스타(Wistar) 백신연구소, 캐나다 라발(Laval) 대학교와 협력하고, 메르스 DNA 백신의 개발을 위해 이노비오
(Inovio), 미국 국방부 월터리드 미육군연구소(WRAIR), 국제백신연구소(IVI), 서울대병원, 분당서울대병원과 협력하고, C형 간염 예방 및 치료 DNA 백신 개발을 위해 연세의료원 세브란스병원, 부산대병원, 한국 과학기술원(KAIST)과 협력하고 있으며,
SFTS DNA 백신 개발을 위해 한국과학기술원 (KAIST)과 협력하고, 코로나19 DNA 백신 개발을 위해 질병관리청 공공백신개발지원센터, 고려대 구로병원, 고려대 안산병원, 한림대 강남성심병원, 가천대 길병원, 인하대병원, 국가임상시험지원재단과 협력하고 있습니다. mRNA 기반 의약품의 개발을 위해 미국 휴스턴 매소디스트 병원연구소(Houston Methodist Research Institute)와 항염증 치료 신약 개발을 위하여 쓴맛 수용체를 이용한 항바이러스 및 항균 코스프레이 약물의 개발 연구는 미국 펜실베이니아 대학교와 협력하고 있습니다.
② 바이오의약품 CDMO 사업 부문
2016년 3월 VGXI, Inc.의 생산시설을 추가로 확충하여 10리터에서 40리터까지의 발효 공정 시설을 확보되어 고객수요에 맞춰 소규모 임상용 플라스미드 DNA 생산이 가능해졌습니다. 이로써, 기존 500리터 규모 생산시설에 새로운 정제 시설이 추가됨으로써 전체 생산 용량이 증가하였을 뿐만 아니라, 동시에 여러 제품의 생산이 가능하게 되었습니다.
2018년 11월, 유전자 치료제 시장이 급속히 성장함에 따라 유전자 치료제의 원료 또는 제품으로 이용되는 고품질 플라스미드 DNA의 전 세계적인 수요 증가에 대응하고자 자회사 VGXI, Inc.의 생산 면적의 확장을 통해 기존 전체 면적 대비 17%, 우수 의약품 제조 및 품질관리 기준(cGMP) 생산시설 면적은 70% 이상 확충하게 되었습니다.
2018년 9월 미국 휴스턴 매소디스트 병원연구소(Houston Methodist Research
Institute, HMRI)와 독점적 라이선스 계약을 통해 임상 등급의 mRNA 생산을 위한 기술 이전을 실행하여, mRNA 백신 및 RNA 치료제의 위탁생산 서비스 제공을 위한 준비를 시작하였습니다.
2019년 12월 임상시험용 파일럿 규모의 mRNA 생산공정의 구축을 완료하였고, 공정 스케일 업 및 최적화 단계를 착수하였습니다.
2019년 7월 개인 맞춤형 신생항원(neoantigen) 암 백신 개발 기업인 지니어스 테라퓨틱스(Geneos Therapeutics)와 장기 공급계약을 체결하고 개인 맞춤형 신생 항원 암 백신의 우수 의약품 제조 및 품질관리 기준(cGMP) 생산 시스템 구축에 착수하였습니다.
각광받고 있는 개인 맞춤형 신생항원 암 백신은 빠른 기간에 고순도의 암 백신을 생산하는 것이 성공의 관건인데, VGXI, Inc.는 회사가 보유한 플라스미드의 고순도 고수율 생산공정을 최적화함으로써 생산기간을 기존의 1/10 수준으로 단축할 수 있습니다.
2019년 12월 VGXI, Inc.가 기존 생산시설과는 별도로 약 10배 이상 규모로 유전자 치료제 원료물질인 플라스미드 DNA와 mRNA에 대한 새로운 생산시설 건설을 결정하고, BE&K Building Group을 시행사로 선정했습니다. 유전자 치료제 제품들이 미국시장에 성공적으로 진입함에 따라 형성된 플라스미드 DNA 및 mRNA의 폭발적 생산 수요에 적극적으로 대응하기 위해 이번 확장뿐만 아니라 추가 확장도 추진할 계획이며, 첫 번째 단계로 약 6,800평 규모의 가변형 플라스미드 DNA와 mRNA 생산 시설을 구축하기로 하고 2-3년 후 완공을 목표로 하였습니다.
2020년 1월 VGXI, Inc.가 미국 나스닥 상장기업인 이노비오가 추진하는 신종 코로나 바이러스(2019-nCoV) 감염병 예방 DNA 백신의 연구개발에 참여하여 임상용 백신 생산을 수행하게 되었습니다. 전염병대비혁신연합(CEPI)은 중국 우한에서 발원한 변종 코로나바이러스(2019-nCoV) 감염병 예방 백신을 개발하도록 이노비오에
9백만 달러까지 지원하였습니다. VGXI, Inc.는 에볼라, 지카 바이러스 및 메르스 등의 신종 감염병에 대해 긴급한 백신 개발 일정에 맞춰 지연 없이 지원함으로써 신변종 감염병예방백신의 생산능력 및 생산시설로서의 역할을 입증한 바 있습니다.
2020년 5월 VGXI, Inc.가 DNA 기반 개인 맞춤형 신생항원(neoantigen) 암 백신 제품을 5일 만에 cGMP 생산을 마치고 2주 이내에 품질평가를 거쳐 출시한 후 환자의 첫 접종을 수행함으로써 신속 생산 시스템의 구축을 성공적으로 완료했습니다. 해당 제품은 미국 지니어스 테라퓨틱스(Geneos Therapeutics)가 암 환자의 종양 유전자 정보를 이용하여 개인 맞춤형 신생 항원을 설계한 후 DNA 백신 형태로 암을 치료하는 백신으로, 환자의 암 조직 채취부터 cGMP 생산 및 환자 접종까지 6~8주를 목표로 하고 있습니다. 해당 제품의 성공적인 개발을 위해서는 평균 6~8개월이 소요되는
DNA 백신의 cGMP 생산 및 출시 기간을 수주 이내로 축소하는 것이 핵심이며,
VGXI, Inc.의 탁월한 고순도 생산 기술력이 있었기에 가능했습니다.
2020년 11월 VGXI, Inc.가 미국 텍사스주 콘로시에 마련한 생산시설 부지에서 유전자 치료제 및 코로나19 RNA 백신 등에 사용되는 플라스미드의 폭발적인 수요에 대응하기 위한 1차 신규 생산시설 건설에 착수함에 따라 기공식을 개최했습니다. 데이슨 테크놀로지 파크(Deison Technology Park)에 건설되는 신규 생산시설은 본사로 이용될 예정이며, 해당 시설은 품질평가 실험실, 정제 및 충전, 포장 설비와 원부자재
창고 그리고 공정 지원에 필요한 공간은 물론 사무실과 편의시설 등을 갖춘 2층 규모입니다.
2021년 3월 VGXI, Inc.가 진행성 간세포암종(HCC)에 대한 치료제를 개발하고 있는 미국 지니어스 테라퓨틱스(Geneos Therapeutics)와 협력을 강화하기로 하고, 1b/2a 임상시험을 위한 추가 공급 계약을 체결했습니다.
2021년 4월 VGXI, Inc.가 미국 텍사스주 콘로시에 건설 중인 신규 생산시설에 대한 마지막 강철빔이 세워져 골조 공사가 마무리됨에 따라 시공사인 BE&K Building
Group 주최로 상량식을 진행하였습니다.
2021년 8월 VGXI, Inc.가 "레어 트레이트 호프 펀드(Rare Trait Hope Fund)"가 지원하는 아스파르틸글루코사민뇨(Aspartylglucosaminuria) 유전자 치료제 개발 프로젝트에 파트너로 참여하여 지원하기로 하였습니다.
2021년 9월 VGXI, Inc.가 플라스미드 DNA 및 mRNA 생산 능력을 최대한 높이기 위해 신규 2공장 건설에 투입되고, 신규 3공장 건설도 추진하기 위해, 지분을 통한 자금을 조달하기 위해 JP모건을 주간사로 선정했습니다.
2021년 10월 VGXI, Inc.는 미국 텍사스주 콘로시 데이슨 테크놀로지 파크(Deison
Technology Park)에 건설 중인 신규 1공장의 외관 공사를 마무리하였습니다.
2022년 1월 VGXI, Inc.가 제40회 JP모건 헬스케어 컨퍼런스(J.P. Morgan
Healthcare Conference)에 공식 초청을 받아 참가하였습니다.
2022년 10월에는 미국 텍사스주 콘로시 데이슨 테크놀로지파크(Deison TechnologyPark)에 자회사 VGXI, Inc.의 신규 1공장을 증설하였습니다.
2023년 1월 VGXI, Inc.가 제41회 JP모건 헬스케어 컨퍼런스(J.P. Morgan
Healthcare Conference)에 공식 초청을 받아 참가하였습니다.
2024년 1월 VGXI, Inc.가 제42회 JP모건 헬스케어 컨퍼런스(J.P. Morgan
Healthcare Conference)에 3년 연속 공식 초청을 받아 참가하였습니다.
2025년 1월 VGXI, Inc.가 제43회 JP모건 헬스케어 컨퍼런스(J.P. Morgan
Healthcare Conference)에 4년 연속 공식 초청을 받아 참가하였습니다.
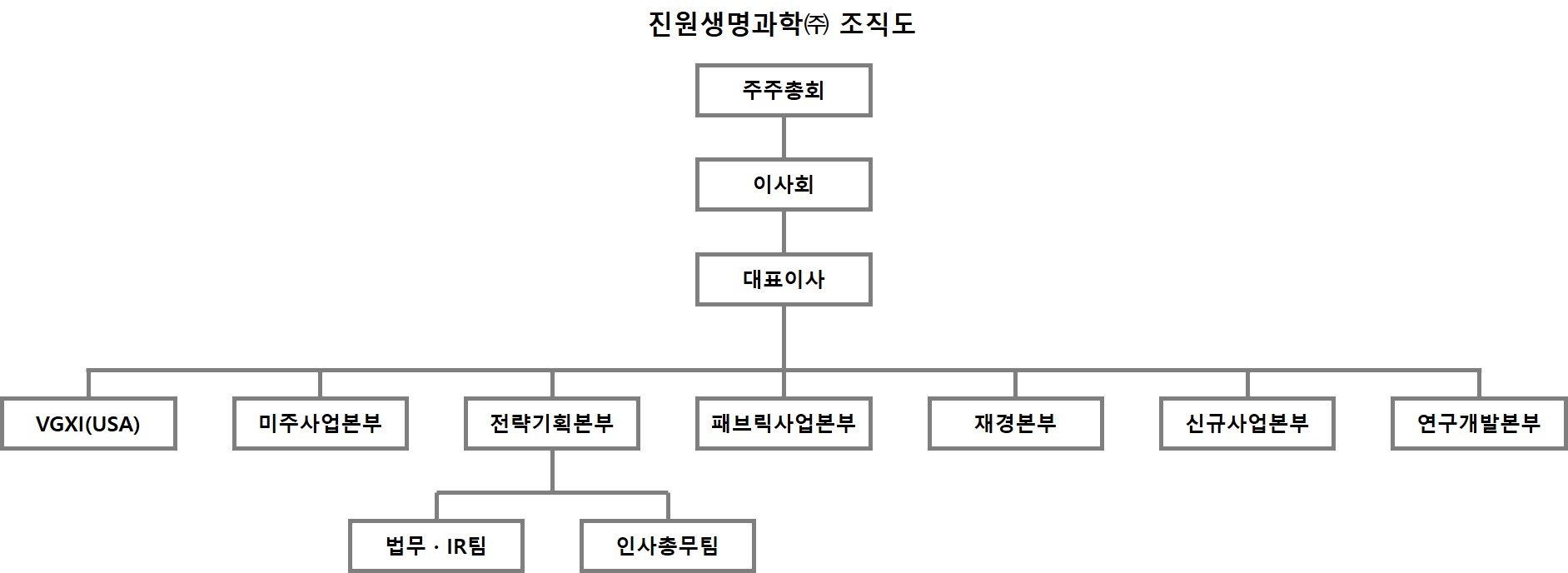
(5) 조직도
 |
|
진원생명과학(주) 조직도 |
2. 주주총회 목적사항별 기재사항
□ 이사의 선임
가. 후보자의 성명ㆍ생년월일ㆍ추천인ㆍ최대주주와의 관계ㆍ사외이사후보자 등 여부
| 후보자성명 | 생년월일 | 사외이사 후보자여부 |
감사위원회 위원인 이사 분리선출 여부 |
최대주주와의 관계 | 추천인 |
|---|---|---|---|---|---|
| 이준규 | 1965.04.13 | 부 | 부 | 발행회사 미등기임원 | 이사회 |
| 전경하 | 1974.08.24 | 부 | 부 | 발행회사 미등기임원 | 이사회 |
| 김훈범 | 1975.01.23 | 부 | 부 | 없음 | 이사회 |
| 총 ( 3 ) 명 | |||||
나. 후보자의 주된직업ㆍ세부경력ㆍ해당법인과의 최근3년간 거래내역
| 후보자성명 | 주된직업 | 세부경력 | 해당법인과의 최근3년간 거래내역 |
|---|---|---|---|
| 내용 | |||
| 이준규 | 전문경영인 | (전) 군인공제회 (전) (주)디에이치산업 대표이사 (전) (주)제주컨트리구락부 사장 |
없음 |
| 전경하 | 전문경영인 | 고려대학교 법학과 졸업 (전) 어린이집안전공제회 본부장 (현) 진원생명과학 상무이사 |
없음 |
| 김훈범 | 전문경영인 | Drexel University, 마케팅&국제경제학과 졸업(B.A) Widener University School of Law 졸업 (현) Mirage Entertainment & Design 이사 |
없음 |
다. 후보자의 체납사실 여부ㆍ부실기업 경영진 여부ㆍ법령상 결격 사유 유무
| 후보자성명 | 체납사실 여부 | 부실기업 경영진 여부 | 법령상 결격 사유 유무 |
|---|---|---|---|
| 이준규 | 부 | 부 | 부 |
| 전경하 | 부 | 부 | 부 |
| 김훈범 | 부 | 부 | 부 |
라. 후보자의 직무수행계획(사외이사 선임의 경우에 한함)
| 해당사항 없음 |
마. 후보자에 대한 이사회의 추천 사유
| <사내이사 후보자 이준규> 후보자는 사업 전반에 대한 전문적인 식견과 노하우를 가지고 있으며 이를 바탕으로 회사의 지속성장 발전에 기여할 것으로 판단되어 후보자로 추천함. <사내이사 후보자 전경하> 후보자는 다년간의 업무수행경험으로 비추어 회사의 지속적인 성장 발전에 기여할 것으로 판단되어 후보자로 추천함. <사외이사 후보자 김상돈> 후보자는 기업활동에 대한 풍부한 경험과 지식을 갖추고 있는 바, 이와 같은 전문성을 바탕으로 당사의 경쟁력 제고에 기여할 수 있으리라 기대되어 후보자로 추천함. |
확인서
 |
|
확인서(이준규) |
 |
|
확인서(전경하) |
 |
|
확인서(김훈범) |
※ 기타 참고사항
해당사항 없음
□ 자본의 감소
가. 자본의 감소를 하는 사유
결손금 보전을 위한 재무구조 개선
나. 자본감소의 방법
기명식 보통주 5주를 동일한 액면주식 1주로 무상병합
다. 자본감소의 목적인 주식의 종류와 수, 감소비율 및 기준일
| 감자주식의 종류 |
감자주식수 | 감자비율 | 감자기준일 | 감자전자본금 (발행주식수) |
감자후자본금 (발행주식수) |
|---|---|---|---|---|---|
| 진원생명과학(주) 기명식 보통주 | 72,706,326주 | 80% | 2026.06.15 | 90,882,907,000원 (90,882,907주) |
18,176,581,000원 (18,176,581주) |
※ 기타 참고사항
해당사항 없음
IV. 사업보고서 및 감사보고서 첨부
가. 제출 개요
| 제출(예정)일 | 사업보고서 등 통지 등 방식 |
|---|---|
| 2026년 05월 21일 | 1주전 회사 홈페이지 게재 |
나. 사업보고서 및 감사보고서 첨부
「DART-정기공시」에 제출된 사업보고서를 참고하십시요.
※ 참고사항
|
해당사항 없음 |