 |
|
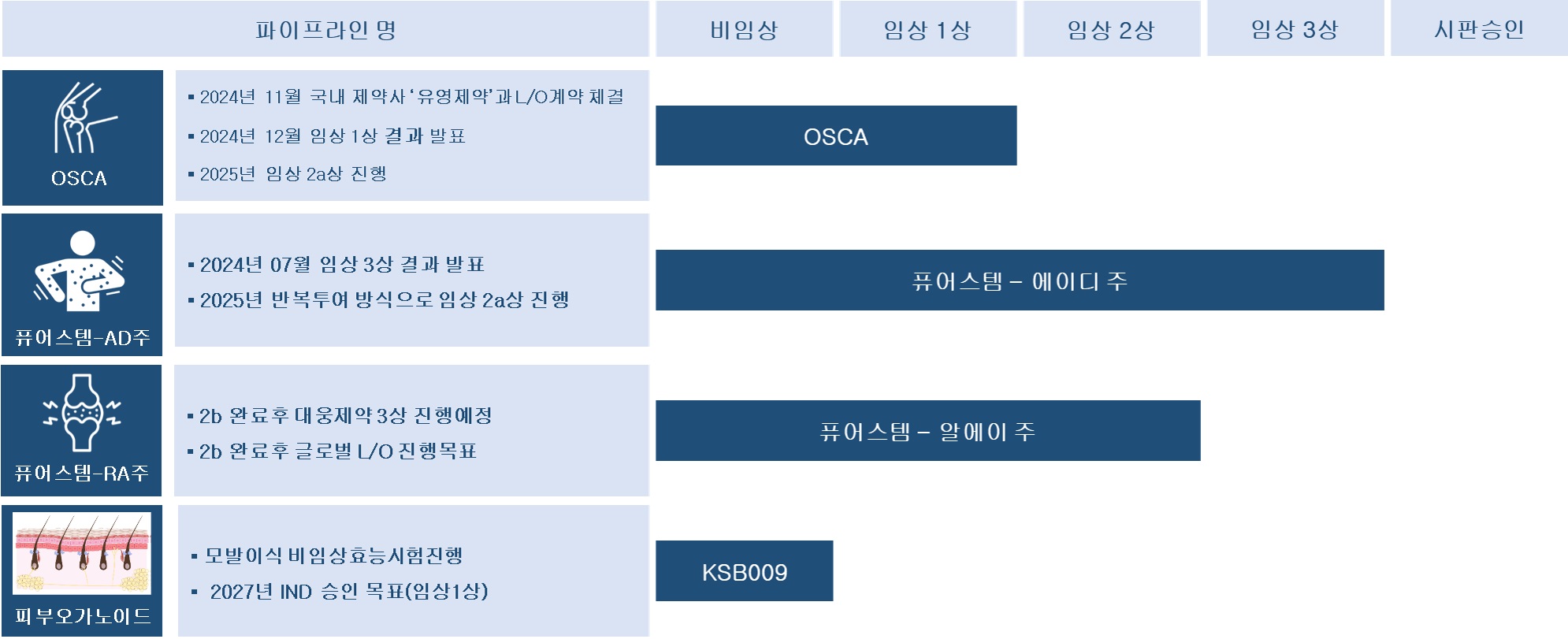
파이프라인별 임상 단계 |
정 정 신 고 (보고)
| 2025년 06월 24일 |
| 1. 정정대상 공시서류 : | 증권신고서(지분증권) |
| 2. 정정대상 공시서류의 최초제출일 : | 2025년 06월 10일 |
| [증권신고서 제출 및 정정 연혁] |
| 제출일자 | 문서명 | 비고 |
|---|---|---|
| 2025년 06월 10일 | 증권신고서(지분증권) | 최초 제출 |
| 2025년 06월 24일 | [기재정정]증권신고서(지분증권) | 기재 정정(파란색) |
| 3. 정정사항 |
| 항 목 | 정정요구ㆍ명령 관련 여부 |
정정사유 | 정 정 전 | 정 정 후 |
|---|---|---|---|---|
| ※금번 정정사항은 공시서류 기재사항 보완에 따른 자진정정으로, 정정사항 확인의 편의를 위해 정정사항은 '굵은 파란색'을 사용하여 기재하였습니다. ※ 요약정보는 본문의 정정사항을 반영하였으며, 정오표를 별도로 기재하지 않았습니다 ※ 단순 오타 및 목차 순서 변경의 경우 별도의 색깔 표시 없이 정정하였습니다. ※ [요약정보 - 1. 핵심투자위험]의 정정사항은 [제1부 모집 또는 매출에 관한 일반사항 - Ⅲ. 투자위험요소]의 정정사항과 동일하여,별도의 정오표를 작성하지 아니하고 본문에 직접 정정하였으니 참고하시기 바랍니다 |
||||
| 제1부 모집 또는 매출에 관한 사항 | ||||
| III. 투자위험요소 | ||||
| 내용 본문 | 아니오 | 자진정정 | (주1) 정정 전 | (주1) 정정 후 |
| 1. 사업위험 | ||||
| 가. 국내외 거시경기 침체 및 불확실성이 미치는 위험 | 아니오 | 자진정정 | (주2) 정정 전 | (주2) 정정 후 |
| 나. 임상시험의 지연 및 실패 위험 | 아니오 | 자진정정 | (주3) 정정 전 | (주3) 정정 후 |
| 다. 연구개발의 지연 및 실패 위험 | 아니오 | 자진정정 | (주4) 정정 전 | (주4) 정정 후 |
| 라. 파이프라인별 경쟁 심화로 인한 수익성 부진 위험 | 아니오 | 자진정정 | (주5) 정정 전 | (주5) 정정 후 |
| 마. 국내외 정부정책 및 규제 변화에 따른 위험 | 아니오 | 자진정정 | (주6) 정정 전 | (주6) 정정 후 |
| 자. 기술이전 지연 및 실패에 따른 위험 | 아니오 | 자진정정 | (주7) 정정 전 | (주7) 정정 후 |
| 2. 회사위험 | ||||
| 내용 본문 | 아니오 | 자진정정 | (주8) 정정 전 | (주8) 정정 후 |
| 나. 성장성 및 수익성 하락에 따른 위험 | 아니오 | 자진정정 | (주9) 정정 전 | (주9) 정정 후 |
| 다. 재무안정성 위험 | 아니오 | 자진정정 | (주10) 정정 전 | (주10) 정정 후 |
| 마. 관리종목 편입 및 상장폐지 가능성에 따른 위험 |
아니오 | 자진정정 | (주11) 정정 전 | (주11) 정정 후 |
| 사. GMP를 포함한 생산시설 관련 위험 | 아니오 | 자진정정 | (주12) 정정 전 | (주12) 정정 후 |
| 아. 특수관계자 및 지분투자기업과의 거래 관련 위험 | 아니오 | 자진정정 | (주13) 정정 전 | (주13) 정정 후 |
| 차. 잦은 자금조달 관련 위험 | 아니오 | 자진정정 | (주14) 정정 전 | (주14) 정정 후 |
| 카. 매출처 편중 관련 위험 | 아니오 | 자진정정 | (주15) 정정 전 | (주15) 정정 후 |
| 타. 소송 및 우발채무 관련 위험 | 아니오 | 자진정정 | (주16) 정정 전 | (주16) 정정 후 |
| 파. 합병 철회 등에 따른 관계기업 관련 위험 | 아니오 | 자진정정 | (주17) 정정 전 | (주17) 정정 후 |
| 3. 기타위험 | ||||
| 가. 금융감독기관의 규제 강화에 따른 위험 | 아니오 | 자진정정 | (주18) 정정 전 | (주18) 정정 후 |
| 나. 최대주주 지분희석 및 경영권 관련 위험 | 아니오 | 자진정정 | (주19) 정정 전 | (주19) 정정 후 |
| 차. 관리감독기준 위반에 따른 위험 | 아니오 | 자진정정 | (주20) 정정 전 | (주20) 정정 후 |
| IV. 인수인의 의견(분석기관의 평가의견) | ||||
| 내용 본문 | 아니오 | 자진정정 | (주21) 정정 전 | (주21) 정정 후 |
| V. 자금의 사용목적 | ||||
| 내용 본문 | 아니오 | 자진정정 | (주22) 정정 전 | (주22) 정정 후 |
| 제2부 발행인에 관한 사항 | ||||
| II. 사업의 내용 | ||||
| 6. 주요계약 및 연구개발활동 | 아니오 | 자진정정 | (주23) 정정 전 | (주23) 정정 후 |
(주1) 정정 전
| [당사 주요 파이프라인 임상 및 사업화 계획] |
| 구분 | 품목 | 적응증 | 연구 시작일 |
현재 진행단계 | 비고 | |
| 단계(국가) | 승인일 | |||||
| 바이오 신약 |
퓨어스템-에이디 주 | 아토피피부염 | 2011년 | 임상3상(한국) | 2017년 | 주1) |
| 임상1/2a상(한국) | 2019년 | 주2) | ||||
| 퓨어스템-알에이 주 | 류마티스관절염 | 2012년 | 임상2b상(한국) | 2023년 | 주3) | |
| 퓨어스템-시디 주 | 크론병 | 2012년 | 임상1/2a상(한국) | 2013년 | 주4) | |
| 판상형 건선 | 2013년 | 임상1상(한국) | 2014년 | 주5) | ||
| 퓨어스템-오에이 키트 주 | 골관절염 | 2015년 | 임상 1/2a상(한국) | 2022년 | 주6) | |
| 주1) | 2021년 05월 국내 두번째 3상 승인 완료되어 임상 진행하였으며, 2024년 11월 CSR 결과발표하였습니다. |
| 주2) | 반복투여 임상으로 2024년 11월 1/2a 임상시험 변경승인신청하였으며, 2025년 4월 자진취하 하였습니다. 2025년 4월 30일 식약처에 자료를 보완하여 변경승인신청 하였습니다. |
| 주3) | 2023년 9월 2b상 IND 승인을 받았으며, 임상 개시 준비 중입니다. |
| 주4) | 2019년 5월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. |
| 주5) | 2019년 1월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. |
| 주6) | 2022년 11월 15일 식약처로부터 IND 승인받았으며, 2a 임상시험을 진행 중입니다. |
(주1) 정정 후
| [당사 주요 파이프라인 임상 및 사업화 계획] |
| 구분 | 품목 | 적응증 | 연구 시작일 |
현재 진행단계 | 비고 | |
| 단계(국가) | 승인일 | |||||
| 바이오 신약 |
퓨어스템-에이디 주 | 아토피피부염 | 2011년 | 임상3상(한국) | 2017년 | 주1) |
| 임상1/2a상(한국) | 2019년 | 주2) | ||||
| 퓨어스템-알에이 주 | 류마티스관절염 | 2012년 | 임상2b상(한국) | 2023년 | 주3) | |
| 퓨어스템-시디 주 | 크론병 | 2012년 | 임상1/2a상(한국) | 2013년 | 주4) | |
| 판상형 건선 | 2013년 | 임상1상(한국) | 2014년 | 주5) | ||
| 퓨어스템-오에이 키트 주 | 골관절염 | 2015년 | 임상 1/2a상(한국) | 2022년 | 주6) | |
| 주1) | 2021년 05월 국내 두번째 3상 승인 완료되어 임상 진행하였으며, 2024년 11월 CSR 결과발표하였습니다. |
| 주2) | 반복투여 임상으로 2024년 11월 1/2a 임상시험 변경승인신청하였으며, 2025년 4월 자진취하 하였습니다. 2025년 4월 30일 식약처에 자료를 보완하여 변경승인신청 하였습니다. |
| 주3) | 2023년 9월 2b상 IND 승인을 받았으며, 임상 개시 시기는 2027년 하반기로 예상하고 있습니다. |
| 주4) | 2019년 5월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주5) | 2019년 1월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주6) | 2022년 11월 15일 식약처로부터 IND 승인받았으며, 2a 임상시험을 진행 중입니다. |
(주2) 정정 전
| 가. 국내외 거시경기 침체 및 불확실성이 미치는 위험 IMF는 세계경제의 리스크가 하방 요인에 집중되어있다 진단하면서, 무역갈등 등 정책 불확실성 확대에 따른 소비ㆍ투자 위축, 고금리 및 높은 부채수준으로 인한 재정ㆍ통화 정책 여력 부족, 주가 및 시장가격 재조정 가능성 등 금융ㆍ외환시장의 높은 변동성 등을 위험 요인으로 제시하였습니다. 또한, 한국은행은 국내 경제가 대내외 불확실성으로 경제심리 회복이 예상보다 지연되었고, 미국 관세 정책도 연초보다 강화되며 직전 예상 수치 대비 크게 하향 조정하였습니다. 당사가 영위하고 있는 사업은 국내외 거시경제의 직ㆍ간접적인 영향을 받고 있으며, 고금리, 고환율, 저성장 등에 따른 글로벌 경기침체로 인해 투자가 위축되거나 지연된 바 있습니다. 이러한 거시경제 불확실성은 국내외 경기 전반에 걸쳐 영향을 미칠 수 있으며, 당사가 영위하는 사업 및 실적에도 부정적인 요인으로 작용할 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
(중략)
상기 기재된 바와 같이 트럼프 행정부의 경제 정책 및 글로벌 무역갈등 등으로 국내외 거시경제는 불확실성이 증대된 상황입니다. 당사가 영위하고 있는 사업은 국내외 거시경제의 직ㆍ간접적인 영향을 받고 있으며, 고금리, 고환율, 저성장 등에 따른 글로벌 경기침체로 인해 투자가 위축되거나 지연된 바 있습니다. 이러한 거시경제 불확실성은 국내외 경기 전반에 걸쳐 영향을 미칠 수 있으며, 당사가 영위하는 사업 및 실적에도 부정적인 요인으로 작용할 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
(주2) 정정 후
| 가. 국내외 거시경기 침체 및 불확실성이 미치는 위험 IMF는 세계경제의 리스크가 하방 요인에 집중되어있다 진단하면서, 무역갈등 등 정책 불확실성 확대에 따른 소비ㆍ투자 위축, 고금리 및 높은 부채수준으로 인한 재정ㆍ통화 정책 여력 부족, 주가 및 시장가격 재조정 가능성 등 금융ㆍ외환시장의 높은 변동성 등을 위험 요인으로 제시하였습니다. 또한, 한국은행은 국내 경제가 대내외 불확실성으로 경제심리 회복이 예상보다 지연되었고, 미국 관세 정책도 연초보다 강화되며 직전 예상 수치 대비 크게 하향 조정하였습니다. 당사가 영위하고 있는 사업은 국내외 거시경제의 직ㆍ간접적인 영향을 받고 있으며, 고금리, 고환율, 저성장 등에 따른 글로벌 경기침체로 인해 투자가 위축되거나 지연될 위험이 존재합니다. 당사는 2021년 6월부터 주요 파이프라인인 아토피 피부염 치료제(퓨어스템-에이디주)의 2차 임상 3상을 위해 환자 모집을 시작하였으나, 코로나19 확산에 따라 원활한 환자모집이 되지 않으면서 일정이 지연되었던 경험이 있습니다. 기존에 2022년 12월까지 예정되어있던 환자 모집기간을 연장하여 2023년 08월 최종인원 환자를 모두 모집할 수 있었으며, 이와 같은 일정 지연으로 인해 추가적인 임상비용 지출이 발생하였습니다. 이처럼 거시경제 불확실성은 국내외 경기 전반에 걸쳐 영향을 미칠 수 있으며, 당사가 영위하는 사업 및 실적에도 부정적인 요인으로 작용할 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
(중략)
상기 기재된 바와 같이 트럼프 행정부의 경제 정책 및 글로벌 무역갈등 등으로 국내외 거시경제는 불확실성이 증대된 상황입니다. 당사가 영위하고 있는 사업은 국내외 거시경제의 직ㆍ간접적인 영향을 받고 있으며, 고금리, 고환율, 저성장 등에 따른 글로벌 경기침체로 인해 투자가 위축되거나 지연될 위험이 존재합니다. 당사는 2021년 6월부터 주요 파이프라인인 아토피 피부염 치료제(퓨어스템-에이디주)의 2차 임상 3상을 위해 환자 모집을 시작하였으나, 코로나19 확산에 따라 원활한 환자모집이 되지 않으면서 일정이 지연되었던 경험이 있습니다. 기존에 2022년 12월까지 예정되어있던 환자 모집기간을 연장하여 2023년 08월 최종인원 환자를 모두 모집할 수 있었으며, 이와 같은 일정 지연으로 인해 추가적인 임상비용 지출이 발생하였습니다. 이처럼 거시경제 불확실성은 국내외 경기 전반에 걸쳐 영향을 미칠 수 있으며, 당사가 영위하는 사업 및 실적에도 부정적인 요인으로 작용할 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
(주3) 정정 전
 |
|
파이프라인별 임상 단계 |
| 출처) 당사 제시 |
(중략)
② 류마티스 관절염 치료제(Furestem-RA Inj.)
당사의 류마티스 관절염 치료제(Furestem-RA Inj.)는 중증도 이상의 류마티스 관절염 환자를 대상으로 개발 중인 치료제입니다. 다양한 면역조절인자가 분비되어 류마티스 관절염을 유발하는 대식세포의 활성을 억제하는 등의 효능을 가지고 있습니다.
류마티스 관절염 치료제(Furestem-RA Inj.)는 2014년 10월부터 2015년 10월까지 진행된 임상 1상(단회투여) 진행하였고, 그 이후 반복투여(4주간격 3회투여) 치료제로 2016년에 임상 1/2a 계획서를 제출했고 2018년 2월에 한국 식약처에서 승인되었습니다. 2018년 07월 1/2a상 임상 개시 이후, 2018년 12월 임상 1상이 완료되었으며, 2021년 10월에 1/2a상을 통해 안정성을 확인하였으며, 2023년 01월 임상 2b상 IND를 제출하였습니다. 2023년 09월 임상2b상 IND 승인을 받았으며, 차후 임상 개시 시기를 결정 후 진행할 예정입니다.
 |
|
퓨어스템-RA 주: 2a상 임상결과 |
| 출처) 당사 제시 |
임상 2b상까지는 당사가 진행하며, 임상 3상부터는 대웅제약과 공동개발을 진행할 예정입니다. 다만, 대웅제약과의 계약이 해지될 경우, 새로운 국내 임상 3상을 진행할 파트너를 찾는 과정에서 임상 시기가 지연될 수 있으며, 임상 3상을 진행하더라도 환자모집이 장기화되어 임상 3상 일정이 지연될 위험도 존재하니 투자자께서는 이 점 유의하시기 바랍니다.
③ 골관절염 치료제 OSCA (구. Furestem-OA Kit Inj.)
당사의 골관절염 치료제 OSCA (구. Furestem-OA Kit Inj.)는 골관절염의 증상개선이 아닌, 연골조직의 재생 및 연골하골의 구조개선을 통한 근본적인 치료제로 개발 중입니다. 제대혈 유래 중간엽 중기세포와 무세포성 연골기질을 함께 투여하며, 수술 없이 무릎관절강 내 주사를 1회 투약합니다.
골관절염 치료제 OSCA(구. Furestem-OA Kit Inj.)는 2015년 비임상 시험 개시 이후 2020년 비임상 시험으로 소형/대형 동물 대상 임상을 완료하였습니다. 이후 2022년 07월 한국 식약처에 임상 1/2a상 IND를 제출하였으며, 2022년 11월에 IND 승인이 완료되었습니다. 2023년 07월 초 국내 임상 1상 임상시험개시모임(임상시험에 필요한 전반적인 내용을 최종적으로 검토 및 확인하는 자리)을 완료하였으며, 2023년 08월 저용량, 10월 중용량, 2024년 02월 고용량 기준으로 환자에게 투여를 완료하였습니다. 2024년 08월 1/2a상 식약처 IND 변경승인 신청 후 10월에 승인 완료받았으며 2024년 12월 초 임상 1상 결과를 수령, 모든 투약군에서 유의미한 개선이 있었음을 발표하였습니다. 이후 2025년 3월 임상 2a상을 진행중이며, 2026년 하반기 임상 2b상을 진행할 예정입니다.
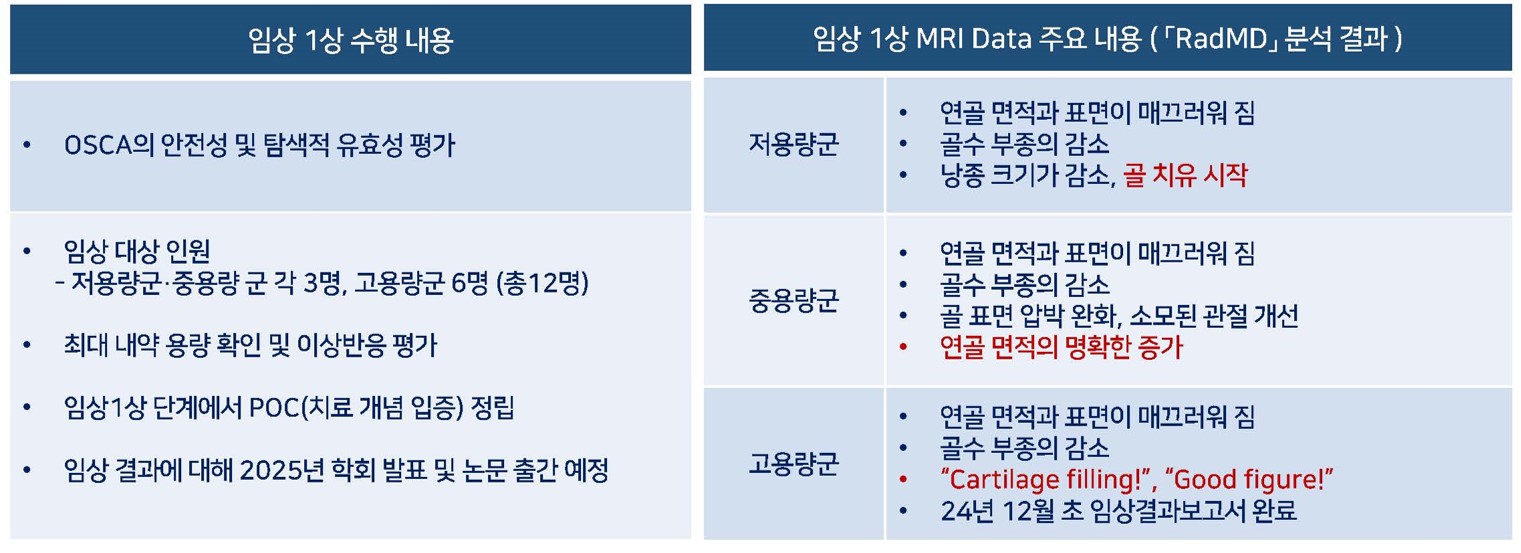 |
|
OSCA: 1상 임상결과 |
| 출처) 당사 제시 |
| 주) 2024년 11월 07일 국내 제약사 유영제약과 140억원 규모의 라이선스아웃 계약을 체결하였습니다. 다만, 임상시험, 허가, 규제 승인 미실현 등으로 본 라이선스아웃 계약은 중도에 해지될 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
(주3) 정정 후
 |
|
파이프라인별 임상 단계 |
| 출처) 당사 제시 |
(중략)
② 류마티스 관절염 치료제(Furestem-RA Inj.)
당사의 류마티스 관절염 치료제(Furestem-RA Inj.)는 중증도 이상의 류마티스 관절염 환자를 대상으로 개발 중인 치료제입니다. 다양한 면역조절인자가 분비되어 류마티스 관절염을 유발하는 대식세포의 활성을 억제하는 등의 효능을 가지고 있습니다.
류마티스 관절염 치료제(Furestem-RA Inj.)는 2014년 10월부터 2015년 10월까지 진행된 임상 1상(단회투여) 진행하였고, 그 이후 반복투여(4주간격 3회투여) 치료제로 2016년에 임상 1/2a 계획서를 제출했고 2018년 2월에 한국 식약처에서 승인되었습니다. 2018년 07월 1/2a상 임상 개시 이후, 2018년 12월 임상 1상이 완료되었으며, 2021년 10월에 1/2a상을 통해 안정성을 확인하였으며, 2023년 01월 임상 2b상 IND를 제출하였습니다. 2023년 09월 임상2b상 IND 승인을 받았으나, 당사 내부 파이프라인 우선순위에 따라 골관절염 치료제(OSCA) 임상과 아토피 피부염 치료제(퓨어스템-에이디주) 임상 시험에 우선적으로 예산을 사용하여, 류마티스 관절염 치료제의 2b 임상시험을 바로 개시하지 않고 보류 중입니다. 현재 류마티스 관절염 치료제(Furestem-RA Inj.)의 임상 2b상은 2027년 하반기 개시를 목표로 하고 있습니다. 다만, 우선순위로 집중하고 있는 OSCA와 퓨어스템-에이디주의 연구개발 일정이 지연되거나 성과가 좋지 않아 당사 수익성에 영향을 미칠 경우 수익화 달성에 따른 임상 진행 재원 마련 여부 등에 의해 류마티스 관절염 치료제(Furestem-RA Inj.)의 임상 2b상의 개시 일정이 추가 지연될 가능성이 존재하므로 투자자께서는 이 점 유의하시기 바랍니다.
 |
|
퓨어스템-RA 주: 2a상 임상결과 |
| 출처) 당사 제시 |
한편, 임상 2b상까지는 당사가 진행하며, 임상 3상부터는 대웅제약과 공동개발을 진행할 예정입니다. 해당 공동개발 계약서 상 임상 지연 및 실패에 따른 해지 조항은 별도로 없습니다. 다만, 임상 진행 과정에서 이견이 발생하여 양측 합의로 공동개발계약이 해지될 수 있으며, 이 경우 새로운 국내 임상 3상을 진행할 파트너를 찾는 과정에서 임상 시기가 지연될 수 있으며, 임상 3상을 진행하더라도 환자모집이 장기화되어 임상 3상 일정이 지연될 위험도 존재하니 투자자께서는 이 점 유의하시기 바랍니다.
③ 골관절염 치료제 OSCA (구. Furestem-OA Kit Inj.)
당사의 골관절염 치료제 OSCA (구. Furestem-OA Kit Inj.)는 골관절염의 증상개선이 아닌, 연골조직의 재생 및 연골하골의 구조개선을 통한 근본적인 치료제로 개발 중입니다. 제대혈 유래 중간엽 중기세포와 무세포성 연골기질을 함께 투여하며, 수술 없이 무릎관절강 내 주사를 1회 투약합니다.
골관절염 치료제 OSCA(구. Furestem-OA Kit Inj.)는 2015년 비임상 시험 개시 이후 2020년 비임상 시험으로 소형/대형 동물 대상 임상을 완료하였습니다. 이후 2022년 07월 한국 식약처에 임상 1/2a상 IND를 제출하였으며, 2022년 11월에 IND 승인이 완료되었습니다. 2023년 07월 초 국내 임상 1상 임상시험개시모임(임상시험에 필요한 전반적인 내용을 최종적으로 검토 및 확인하는 자리)을 완료하였으며, 2023년 08월 저용량, 10월 중용량, 2024년 02월 고용량 기준으로 환자에게 투여를 완료하였습니다. 2024년 08월 1/2a상 식약처 IND 변경승인 신청 후 10월에 승인 완료받았으며 2024년 12월 초 임상 1상 결과를 수령, 모든 투약군에서 유의미한 개선이 있었음을 발표하였습니다. 이후 2025년 3월 임상 2a상을 진행중입니다.
골관절염 치료제 OSCA(구. Furestem-OA Kit Inj.)는 개발 초기 비임상 연구 단계에서는 동물 모델을 활용해 연골 재생 및 관절 구조 개선 효과를 입증했으며, 항염증 및 재생 효과를 증명하고 안전성을 확보했습니다. 이후 임상 1상에서는 저용량, 중용량, 고용량으로 구분된 세 군을 대상으로 안전성, 내약성, 그리고 유효성을 평가했습니다. 중용량과 고용량에서 통증 및 관절 기능 개선과 구조적 개선에서 유의미한 효과가 관찰되었고, 주요 통계 지표들(IKDC, WOMAC, KOOS, VAS)에서도 긍정적인 결과가 나타났습니다.
 |
|
OSCA: 1상 임상결과 |
| 출처) 당사 제시 |
| 주) 2024년 11월 07일 국내 제약사 유영제약과 140억원 규모의 라이선스아웃 계약을 체결하였습니다. 다만, 임상시험, 허가, 규제 승인 미실현 등으로 본 라이선스아웃 계약은 중도에 해지될 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
임상 1상에서 확인된 안전성 및 유효성에 대한 전반적인 평가 결과를 바탕으로 중용량과 고용량을 임상 2a상의 시험군으로 선정하였으며, 대상자를 50명에서 108명으로 확대하여 위약 대비 시험약의 효과를 보다 정밀하게 평가할 계획입니다. 2025년 3월 임상시험을 시작해 2026년 2분기까지 완료를 목표로 하고 있으며, 성공 시 임상 2b 단계를 생략하고 임상 3상으로 직행할 가능성도 있을 것으로 예상됩니다.
다만, 당사의 임상일정에 차질이 생길 수 있으며 임상에 맞는 환자들을 선별하는 과정에서 예상치 못한 난관들로 인해 환자모집이 장기화되어 임상 일정이 지연될 가능성 존재 및 임상을 진행하더라도 임상이 실패할 위험이 존재하니 투자자께서는 이 점 유의하시기 바랍니다.
(주4) 정정 전
당사가 보유하고 있는 파이프라인별 연구개발 진행 단계는 아래와 같습니다.
| [연구개발 진행 총괄표] |
| 구분 | 품목 | 적응증 | 연구 시작일 |
현재 진행단계 | 비고 | |
| 단계(국가) | 승인일 | |||||
| 바이오 신약 |
퓨어스템-에이디 주 | 아토피피부염 | 2011년 | 임상3상(한국) | 2017년 | 주1) |
| 임상1/2a상(한국) | 2019년 | 주2) | ||||
| 퓨어스템-알에이 주 | 류마티스관절염 | 2012년 | 임상2b상(한국) | 2023년 | 주3) | |
| 퓨어스템-시디 주 | 크론병 | 2012년 | 임상1/2a상(한국) | 2013년 | 주4) | |
| 판상형 건선 | 2013년 | 임상1상(한국) | 2014년 | 주5) | ||
| 퓨어스템-오에이 키트 주 | 골관절염 | 2015년 | 임상1/2a상(한국) | 2022년 | 주6) | |
| 주1) | 2021년 05월 국내 두번째 3상 승인 완료되어 임상 진행하였으며, 2024년 11월 CSR 결과발표하였습니다. |
| 주2) | 반복투여 임상으로 2024년 11월 1/2a 임상시험 변경승인 신청하였으며, 2025년 4월 자진취하 하였습니다. 2025년 4월 30일 식약처에 자료를 보완하여 변경승인 신청 하였습니다. |
| 주3) | 2023년 9월 2b상 IND 승인을 받았으며, 임상 개시 준비 중입니다. |
| 주4) | 2019년 5월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. |
| 주5) | 2019년 1월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. |
| 주6) | 2022년 11월 15일 식약처로부터 IND 승인받았으며, 2a 임상시험을 진행 중입니다. |
당사의 연구개발 자금 계획표는 다음과 같습니다.
| (단위 : 백만원) |
| 구분 | 2025년 | 2026년 | 2027년 | 2028년 | 합계 | |
|---|---|---|---|---|---|---|
| 이월 | 19,059 | 49,867 | 79,159 | 60,643 | 19,059 | |
| 수입 | 58,356 | 58,903 | 13,535 | 112,857 | 243,651 | |
| 자금조달 | 49,210 | - | - | - | 49,210 | |
| 제품매출(배양액) | 783 | 1,018 | 1,323 | 1,720 | 4,843 | |
| 제품매출(배지,해동기 등) | 111 | 145 | 188 | 245 | 689 | |
| 제품매출(퓨어스템-에이디주) | 1,240 | 2,380 | 3,990 | 6,728 | 14,338 | |
| 제품매출(OSCA) | - | 210 | - | 300 | 510 | |
| 제품매출(CDMO) | 1,000 | 1,100 | 1,155 | 1,155 | 4,410 | |
| 제품매출(화장품) | 1,032 | 1,135 | 1,249 | 1,374 | 4,791 | |
| 상품매출(홈쇼핑) | 1,260 | 1,386 | 1,524 | 1,676 | 5,846 | |
| 상품매출(의약품) | - | - | - | - | - | |
| 기타매출(L/O 등) | - | 53,000 | 3,000 | 100,000 | 156,000 | |
| 기타매출 | - | - | - | - | - | |
| 기타 | 3,000 | - | - | - | 3,000 | |
| 비현금비용보정 | 720 | -1,470 | 1,105 | -340 | 15 | |
| 지출 | 27,548 | 29,611 | 32,051 | 32,836 | 122,046 | |
| 제품원가(배양액) | 470 | 611 | 794 | 1,032 | 2,906 | |
| 제품원가(배지,해동기 등) | 67 | 87 | 113 | 147 | 413 | |
| 제품원가(OSCA/퓨어스템-에이디주) | 620 | 1,190 | 1,796 | 2,691 | 6,297 | |
| 제품원가(CDMO) | 900 | 990 | 982 | 982 | 3,854 | |
| 제품원가(화장품) | 568 | 625 | 687 | 756 | 2,635 | |
| 상품원가(홈쇼핑) | 693 | 762 | 838 | 922 | 3,215 | |
| 상품원가(의약품) | - | - | - | - | - | |
| 연구개발비용 | - | - | - | - | - | |
| 퓨어스템-에이디주 | 1,838 | 510 | 1,550 | 1,550 | 5,448 | |
| 퓨어스템-알에이주 | 3 | 510 | 1,020 | 1,020 | 2,553 | |
| 퓨어스템-씨디주 | - | - | - | - | - | |
| OSCA | 2,701 | 5,210 | 3,630 | 1,440 | 12,981 | |
| DDS | - | - | - | - | - | |
| 국책과제 | 600 | 600 | 600 | 600 | 2,400 | |
| 기타연구비 | 1,000 | 500 | 1,080 | 1,260 | 3,840 | |
| 기타 | 1,425 | 400 | 400 | 400 | 2,625 | |
| 판매비와관리비(일반) | 16,664 | 17,617 | 18,562 | 20,037 | 72,880 | |
| 법인세 | - | - | - | - | - | |
| 잔액 | 49,867 | 79,159 | 60,643 | 140,664 | 140,664 | |
| 출처) 당사 제시 |
당사 주요 파이프라인의 임상개요 및 임상 목표 및 결과 현황은 다음과 같습니다.
| 구분 | 임상개요 | 임상 목표 | 결과 현황 |
|---|---|---|---|
| 퓨어스템-AD주(반복투여) -아토피 피부염 치료제 |
중등도 이상의 성인아토피 피부염 환자에서 1개월 간격 3회 피하 반복투여 시 저용량(5x10^7cell)과 고용량(1x10^8cell)에 대한 안전성 및 탐색적 유효성 평가를 위한 1/2a 임상시험 | (1상) 3회 반복투여 시 투여용량군에 대한 안전성확립(DLT 및 MTD)과 EASI50/75와 같은 변수를 이용하여 탐색적 유효성 평가 (2a상) 단회투여 3상 임상시험결과를 반영한 수정 임상시험계획서를 바탕으로 16주-24주 시점에 시판중인 항체치료제와 대등한 유효성(EASI75 및 IGA 1 또는 0 비율)을 보여줄 수 있는지를 위약군과 비교하여 반복투여에 따른 유효성의 효과크기를 확인 |
(1상/완료) 투여된 두 용량 모두에서 DLT 및 MTD 평가에서 뛰어난 안전성 확인. 탐색적 유효성 평가에서는 업그레이드된 임상시험용의약품이 적용된 고용량군 대상자들 모두 50%-80% EASI 변화율이 확인되어 단회투여에 비교할 때, 보다 빠른 시기에 효과가 나타날 수 있는 가능성 확인 (2a상/진행 중) 단회 3상 임상결과에 대한 심층분석결과를 바탕으로 2a 임상시험계획서 변경신청서를 11월 제출하였고, 식약처 자료 보완 요청에 대해 행정처리기간내 회신이 어려울 것으로 보여 2025년 4월에 신청을 자진 취하하였고 2025년 4월 30일에 재신청함 |
| 퓨어스템-RA주 -류마티스관절염 치료제 |
기존의 DMARD제제에 불응인 중등도 이상의 류마티스 관절염 환자에서 1개월 간격으로 시험약(5x10^7cell) 3회 투여 시 위약대비 안전성 검토 및 유효성 평가를 위한 2b 임상시험 | (2b상) 이전 2a 임상시험에서 1개월 간격으로 3회 정맥내 투여할 때 저용량(5x10^7 cells)의 유효성이 확인되었으며, 보다 큰 규모의 모집단에서 위약대비 효과의 크기를 측정하고자 함 |
(2a상/완료) 임상시험을 통해 저용량-고용량 모두 6개월 관찰에서 안전성 확보하였고, 유효성 측면에서 저용량군이 더 뛰어난 결과를 보여 이를 바탕으로 2b 임상시험계획서를 준비하고 진행하였음 (2b상/보류) 2023년 9월 2b상 임상시험계획 승인되었지만, 우선순위 프로젝트인 OSCA 임상과 아토피 임상시험에 예산을 우선 투여하여 2b 임상시험의 개시를 보류 중. 바로는 개시 계획이 없으며 재정상황을 고려하면서 차후 2b 임상시험의 재개 시기를 결정하고 진행 예정임 |
| OSCA (구. 퓨어스템 OA주) -골관절염 치료제 -주력 파이프라인 |
중등도 무릎골관절염 환자(Kellgren & Lawrence grade 2-3)에서 안전성 및 탐색적 유효성을 평가하기 위한 1/2a 임상시험 | (1상) 무릎관절낭내로 3가지 용량(저/중/고) 단회투여 후 안전성 확인 (DLT & MTD), 투약 후 6개월 시점에서 통증과 관절기능, 구조적 개선에 대한 탐색적 유효성을 평가 (2a상) 무릎관절낭내로 단회투여 후 1상에서 안전성과 탐색적 유효성이 확인된 중용량/고용량을 위약 대비 6개월 시점에서 통증과 관절기능, 구조개선에 대해 시험약의 유효성의 크기를 측정하고자 함 |
(1상/완료) 투약된 세 용량 모두에서 독성이 확인되지 않아 안전성이 확립되었음. 탐색적 유효성의 경우, 중용량과 고용량에서 통증조절과 기능개선이 빠르게 나타났으며(100mmVAS, IKDC, WOMAC, KOOS), MRI를 이용한 구조적 개선평가에서도 의미있는 개선이 확인되었음 : 연골재생, 연골하골 구조개선 등 (1상 장기추적조사/진행 중) 12개월 통증 및 관절기능에 대해 저용량 및 중용량 데이터 확보하였고, 6개월 시점대비 저용량의 증상과 영상의학적 평가결과 눈에 띄는 개선이 확인되었으며, 중용량군의 경우 6개월에서 보여준 증상개선이 유지 및 추가개선이 확인되었음. 중·고용량군의 12개월 영상평가결과, 다수의 중·고용량군 환자들에게서 연골재생과 손상된 연골하골의 회복이 지속된 것으로 확인됨. 고용량군은 장기추적조사에 참여한 환자 모두 연골의 마모, 이상구조, 부종, 활막염, 반월판 손상 등 전반적인 부분에서 개선이 나타남 (2상/진행 중) 2025년 3월 25일 분당차병원을 시작으로 중용량에 대해 첫환자 투약 개시함 |
| 출처) 당사 제시 |
당사 주요 파이프라인의 ① 개발 단계별 주요 목표 및 예상 달성 시기, ② 개발 단계별 예상 비용, ③ 연구개발 자금계획은 다음과 같습니다.
① 개발 단계별 주요 목표 및 예상 달성 시기
| 구분 | 1상 | 2a상 | 2b상 | 3상 | 장기 추적 |
|---|---|---|---|---|---|
| 퓨어스템-에이디주(반복투여) | 2022년 06월 | 2027년 02월 | 2028년 10월 | 2030년 02월 | 2035년 02월 |
| 퓨어스템-알에이주 | 2015년 10월 | 2021년 10월 | 2028년 12월 | 2030년 12월 | 2035년 12월 |
| OSCA | 2024년 08월 | 2026년 03월 | 2028년 03월 | 2029년 09월 | 2034년 09월 |
| 출처) 당사 제시 |
② 개발 단계별 예상 비용
| 구분 | 1상 | 2a상 | 2b상 | 3상 |
|---|---|---|---|---|
| 퓨어스템-에이디주(반복투여) | - | 80억원 (장기추적 포함) |
86억원 (장기추적 포함) |
175억원 (장기추적 포함) |
| 퓨어스템-알에이주 | - | - | 84억원 (장기추적 포함) |
249억원 (장기추적 포함) |
| OSCA | 4억원(장기추적) | 239억원 (장기추적 포함, 해외임상IND 포함) |
131억원 (장기추적포함) |
239억원 (장기추적 포함) |
| 출처) 당사 제시 |
③ 연구개발 자금계획
| 구분 | 2025년 | 2026년 | 2027년 | 2028년 |
|---|---|---|---|---|
| 퓨어스템-에이디주(반복투여) | - | 35억원 | 45억원 | 49억원 |
| 퓨어스템-알에이주 | - | 20억원 | 20억원 | 25억원 |
| OSCA | 46억원 | 96억원 | 69억원 | 35억원 |
| 출처) 당사 제시 |
(중략)
(2) 류마티스관절염 치료제(퓨어스템-알에이 주)
| ①구분 | - 바이오 신약 |
| ②적응증 | - 중등도 이상의 류마티스관절염 |
| ③작용기전 | - 퓨어스템-알에이 주를 류마티스 관절염 환자에 투여시, TSG-6, PGE2 등 다양한 면역조절인자가 분비되어 염증성 세포인 M1 phase macrophage의 활성을 억제하고, 항염증성 세포인 M2 phase macrophage의 활성을 촉진하여, 환자의 염증을 억제하고 증상개선효과를 나타냄. |
| ④제품의특성 | - 세계 최초의 류마티스관절염 줄기세포치료제로서, 단일인자에 대한 차단이 아닌, 질환유발과 관련된 면역세포의 반응을 다각적으로 조절함으로서, 부작용이 거의 없으면서 근본적인 치료제로서 역할을 할 수 있는 신개념의 치료제임. |
| ⑤진행경과 | - 2014년 퓨어스템-알에이 주 1상 임상시험계획 식약처 승인 - 2015년 1상 임상시험 종료 - 2018년 1/2a상 반복투여 임상시험(K0202) 식약처 승인 - 2021년 4월 대상자 등록 완료 - 2021년 10월 임상종료 - 2021년 12월 K0202 결과 확보 (2022년 5월 임상시험결과보고서 최종화) - 2023년 1월 2b상 IND 승인 신청 - 2023년 9월 2b상 IND 승인 |
| ⑥향후계획 | - 2b상 임상 개시 준비 |
| ⑦경쟁제품 |
- AbbVie사의 Humira - Johnson & Johnson사의 Remicade - Amgen/Pfizer사의Enbrel 등 |
| ⑧관련논문등 |
- Human umbilical cord blood-stem cells direct macrophage polarization and block inflammasome activation to alleviate rheumatoid arthritis. Cell Death Dis. 2016;7(12):e2524. - Intravenous Infusion of Umbilical Cord Blood-Derived Mesenchymal Stem Cells in Rheumatoid Arthritis: A Phase 1a Clinical Trial. Stem Cells Transl Med. 2018;7(9):636-642. |
| ⑨시장규모 | - 2019년 류마티스 관절염 치료제 매출이 262억 달러로 2029년까지 연평균 성장률(CAGR) 1% 로 291억 달러까지 완만한 성장을 예상됨. (출처: GlobalData) |
| ⑩기타사항 | - 정부 정책 과제 수주 1건 제대혈 유래 줄기세포를 이용한 류마티스 관절염 치료제의 상업화 임상 2a상 연구 (보건복지부) |
(중략)
(5) 골관절염 치료제 (퓨어스템-오에이 키트 주)
| ①구분 | - 바이오 신약 |
| ②적응증 | - ICRS grade 3 또는 4에 해당하는 무릎골관절염 |
| ③작용기전 | - 골관절염 환자의 관절강내에 줄기세포와 생체소재를 함께 주입하여, 염증을 억제하면서, 손상된 연골조직의 재생을 유도함. |
| ④제품의특성 | - 기존의 골관절염 줄기세포치료제의 한계점을 극복할 수 있는 치료제로, 줄기세포와 생체소재를 혼합하여 연골 재생 기능이 탁월한 치료제를 주사제 형태로 개발중에 있음. |
| ⑤진행경과 | - 2021년 8월 한국 식약처 임상시험계획 승인 신청 - 2022년 4월 보완답변 제출 - 2022년 6월 20일 IND 자진취하 - 2022년 7월 15일 IND 재신청 - 2022년 11월 15일 IND 승인완료 - 2022년 11월 28일 IND 변경승인 신청 - 2023년 2월 7일 IND 변경승인 완료 - 2023년 7월 1상 코호트1 대상자 투약ㅉ- 2023년 9월 1상 코호트1 대상자 DLT 평가완료 - 2023년 11월 1상 코호트2 대상자 투약 완료 - 2024년 1월 코호트2 대상자 DLT 평가완료, 코호트1 대상자 6개월 방문완료 - 2024년 3월 코호트3 대상자 DLT 평가완료, 전체 코호트에 대한 MTD 평가완료 - 2024년 4월 코호트1 대상자 6개월 영상평가 평가완료 - 2024년 8월 1/2a상 식약처 IND 변경승인신청, 10월 변경승인 완료 - 2024년 12월 1상 topline data 발표, 1/2a상 식약처 IND 변경승인신청 - 2025년 1월 1/2a상 IND 변경승인 - 2025년 2월 2a 임상시험 개시 |
| ⑥향후계획 | - 1상 전체 대상자 영상평가 완료 - 1상 결과 국제학회 발표 - 2a 임상시험 개시 |
| ⑦경쟁제품 | - 무릎골관절염 근복적 치료제로 시판승인된 제품 없음. |
| ⑧관련논문등 | - Therapeutic Effects of Human Umbilical Cord Blood-Derived Mesenchymal Stem Cells Combined with Cartilage Acellular Matrix Mediated Via Bone Morphogenic Protein 6 in a Rabbit Model of Articular Cruciate Ligament Transection 2020 Jun;16(3):596-611 - Combined Mesenchymal Stem Cells and Cartilage Acellular Matrix Injection Therapy for Osteoarthritis in Goats 2022 Feb; 19(1): 177-187 |
| ⑨시장규모 | - 골관절염 시장은 2032년까지 183억 6000만달러(24조2021억원)으로 성장할 것으로 전망함. (출처 : Precedence Research) |
| ⑩기타사항 | - 독일Heraeus Medical GmbH 공동개발 계약 체결(2017.09) - 정부 정책과제 수주 1건 차세대 골관절염 줄기세포 치료제 개발을 위한 유효성 안전성 평가 연구 |
(중략)
OSCA의 강점은 첨단 세포 선별 기술과 대량생산 기술로, 고활성 세포의 안정적인 유지가 가능하다는 점입니다. 또한 다중 기전 작용을 통해 기존 치료제보다 우수한 효과와 안전성을 기대할 수 있습니다. 이미 임상 1상 결과를 통해 구조적 개선을 포함한 근본적인 치료제로서의 가능성을 입증했으며, 장기적인 효과를 확인하기 위해 5년까지의 추적 관찰이 계획되어 있습니다.
상업적 측면에서는 국내외 파트너와의 협력으로 개발 비용을 최소화하고 초기 매출 실현 가능성을 높였습니다. 특히, 국내에서는 유영제약과 라이선스 계약을 체결하여 임상 2b상 단계 이후의 개발 비용 부담을 줄이는 동시에 매출 조기 실현이라는 장점을 확보했습니다. 이러한 전략은 안정적인 회사 운영과 글로벌 파트너십 확장을 위한 유리한 환경을 제공합니다.
다만, OSCA의 성공을 위해서는 대규모 임상시험에서 일관성 있는 결과가 필수적이며, 장기적 효과를 지속적으로 증명해야하며 글로벌 시장에서 경쟁 중인 다른 DMOAD 후보들과의 차별화를 이루는 것도 중요한 과제로 판단됩니다. 또한, 당사가 환자모집 지연 등 예상치 못한 이유로 인해 연구개발 일정이 지연된다면 제품화까지 당사 예상 대비 장기간이 소요될 수 있으며, 연구개발을 진행하는 동안에도 성과가 나오지 않을 경우 연구를 중단하게 되고 사용된 연구개발비용은 따로 회수할 수 없어 당사의 수익성 및 성장성에 악영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
(주4) 정정 후
당사가 보유하고 있는 파이프라인별 연구개발 진행 단계는 아래와 같습니다.
| [연구개발 진행 총괄표] |
| 구분 | 품목 | 적응증 | 연구 시작일 |
현재 진행단계 | 비고 | |
| 단계(국가) | 승인일 | |||||
| 바이오 신약 |
퓨어스템-에이디 주 | 아토피피부염 | 2011년 | 임상3상(한국) | 2017년 | 주1) |
| 임상1/2a상(한국) | 2019년 | 주2) | ||||
| 퓨어스템-알에이 주 | 류마티스관절염 | 2012년 | 임상2b상(한국) | 2023년 | 주3) | |
| 퓨어스템-시디 주 | 크론병 | 2012년 | 임상1/2a상(한국) | 2013년 | 주4) | |
| 판상형 건선 | 2013년 | 임상1상(한국) | 2014년 | 주5) | ||
| 퓨어스템-오에이 키트 주 | 골관절염 | 2015년 | 임상1/2a상(한국) | 2022년 | 주6) | |
| 주1) | 2021년 05월 국내 두번째 3상 승인 완료되어 임상 진행하였으며, 2024년 11월 CSR 결과발표하였습니다. |
| 주2) | 반복투여 임상으로 2024년 11월 1/2a 임상시험 변경승인 신청하였으며, 2025년 4월 자진취하 하였습니다. 2025년 4월 30일 식약처에 자료를 보완하여 변경승인 신청 하였습니다. |
| 주3) | 2023년 9월 2b상 IND 승인을 받았으며, 임상 개시 시기는 2027년 하반기로 예상하고 있습니다. |
| 주4) | 2019년 5월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주5) | 2019년 1월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주6) | 2022년 11월 15일 식약처로부터 IND 승인받았으며, 2a 임상시험을 진행 중입니다. |
당사의 최근 3개년 및 향후 연구개발 자금 계획표는 다음과 같습니다.
| [연구개발 자금 계획표(상세)] |
| (단위 : 백만원) |
| 구분 | 2022년 | 2023년 | 2024년 | 소계 | 2025년(E) | 2026년(E) | 2027년(E) | 2028년(E) | 소계 | 총계 | ||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 이월 | 55,955 | 36,036 | 36,974 | 19,059 | 49,867 | 79,159 | 60,643 | |||||
| 수입 | 7,010 | 26,911 | 9,673 | 43,595 | 58,356 | 58,903 | 13,535 | 112,857 | 243,651 | 287,246 | ||
| 자금조달 | - | 20,970 | - | 20,970 | 49,210 | - | - | - | 49,210 | 70,180 | ||
| 제품매출(배양액) | 247 | 912 | 333 | 1,492 | 783 | 1,018 | 1,323 | 1,720 | 4,843 | 6,335 | ||
| 제품매출(배지,해동기 등) | 256 | 132 | 97 | 485 | 111 | 145 | 188 | 245 | 689 | 1,174 | ||
| 제품매출(퓨어스템-에이디주) | - | - | - | - | 1,240 | 2,380 | 3,990 | 6,728 | 14,338 | 14,338 | ||
| 제품매출(OSCA) | - | - | - | - | - | 210 | - | 300 | 510 | 510 | ||
| 제품매출(CDMO) | 839 | 404 | 1,914 | 3,158 | 1,000 | 1,100 | 1,155 | 1,155 | 4,410 | 7,568 | ||
| 제품매출(화장품) | 1,463 | 2,283 | 1,475 | 5,220 | 1,032 | 1,135 | 1,249 | 1,374 | 4,791 | 10,011 | ||
| 상품매출(홈쇼핑) | 2,546 | 1,835 | 1,799 | 6,181 | 1,260 | 1,386 | 1,524 | 1,676 | 5,846 | 12,027 | ||
| 상품매출(의약품) | 563 | 347 | 86 | 996 | - | - | - | - | - | 996 | ||
| 기타매출(L/O 등) | - | - | 2,000 | 2,000 | - | 53,000 | 3,000 | 100,000 | 156,000 | 158,000 | ||
| 기타매출 | - | - | 42 | 42 | - | - | - | - | - | 42 | ||
| 기타 | - | - | - | - | 3,000 | - | - | - | 3,000 | 3,000 | ||
| 비현금비용보정 | 1,096 | 29 | 1,927 | 3,052 | 720 | -1,470 | 1,105 | -340 | 15 | 3,067 | ||
| 지출 | 26,929 | 25,973 | 27,588 | 80,491 | 27,548 | 29,611 | 32,051 | 32,836 | 122,046 | 202,537 | ||
| 원가비용 | 3,430 | 3,429 | 3,420 | 10,280 | 3,318 | 4,265 | 5,210 | 6,530 | 19,320 | 29,600 | ||
| 제품원가(배양액) | 145 | 550 | 158 | 853 | 470 | 611 | 794 | 1,032 | 2,906 | 3,759 | ||
| 제품원가(배지,해동기 등) | 151 | 70 | 58 | 279 | 67 | 87 | 113 | 147 | 413 | 692 | ||
| 제품원가(OSCA/퓨어스템-에이디주) | - | - | - | - | 620 | 1,190 | 1,796 | 2,691 | 6,297 | 6,297 | ||
| 제품원가(CDMO) | 769 | 527 | 1,317 | 2,613 | 900 | 990 | 982 | 982 | 3,854 | 6,467 | ||
| 제품원가(화장품) | 1,080 | 1,341 | 1,076 | 3,496 | 568 | 625 | 687 | 756 | 2,635 | 6,131 | ||
| 상품원가(홈쇼핑) | 779 | 637 | 734 | 2,150 | 693 | 762 | 838 | 922 | 3,215 | 5,365 | ||
| 상품원가(의약품) | 506 | 305 | 77 | 888 | - | - | - | - | - | 888 | ||
| 연구개발비용 주1) |
14,241 | 14,365 | 12,562 | 41,167 | 9,667 | 14,123 | 11,781 | 8,819 | 44,389 | 85,556 | ||
| 퓨어스템-에이디주 (반복투여) 주2) |
1,157 | 833 | 604 | 2,594 | 2 | - | - | - | 2 | 2,596 | ||
| 퓨어스템-에이디주 (단회투여) 주3) | 4,692 | 5,707 | 5,446 | 15,845 | 2,608 | - | - | - | 2,608 | 18,453 | ||
| 퓨어스템-에이디주 (단회투여-장기추적) | 462 | 450 | 715 | 1,627 | 871 | 1,353 | 1,155 | 938 | 4,312 | 5,945 | ||
| 퓨어스템-알에이주 | 1,951 | 1,988 | 45 | 3,984 | 3 | 2,040 | 2,040 | 2,472 | 6,555 | 10,539 | ||
| 퓨어스템-시디주 | 142 | - | - | 142 | - | - | - | - | - | 142 | ||
| OSCA | 2,039 | 4,211 | 2,795 | 9,045 | 4,583 | 9,629 | 6,906 | 3,549 | 24,667 | 33,712 | ||
| DDS | - | - | - | - | - | - | - | - | - | - | ||
| 국책과제 | 527 | 397 | 266 | 1,191 | 600 | 600 | 600 | 600 | 2,400 | 3,591 | ||
| 기타연구비 | 3,271 | 779 | 2,690 | 6,739 | 1,000 | 500 | 1,080 | 1,260 | 3,840 | 10,579 | ||
| 기타 | 400 | 400 | 5,400 | 6,200 | 1,425 | 400 | 400 | 400 | 2,625 | 8,825 | ||
| 판매비와관리비(일반) | 8,858 | 7,779 | 6,206 | 22,844 | 13,139 | 10,824 | 14,661 | 17,088 | 55,718 | 78,556 | ||
| 법인세 | - | - | - | - | - | - | - | - | - | - | ||
| 잔액 | 36,036 | 36,974 | 19,059 | 49,867 | 79,159 | 60,643 | 140,664 | |||||
| 출처) 당사 제시 |
| 주1) 해당 예상 연구개발비용 항목은 각 파이프라인 별 발생 예상되는 전체 비용 중 당사가 지출 예상되는 비용을 기준으로 작성되었습니다. 직접비용과 간접비용을 모두 포함한 기준으로 작성되었습니다. 주2) 퓨어스템-에이디주 반복투여 방식의 임상시험 비용은 컨소시엄 등 임상 프로젝트 그룹 구성을 통해 해당 외부 자금으로 처리할 예정으로 이를 가정하여 해당 비용에 반영되어있지 않습니다. 주3) 퓨어스템-에이디주 단회투여 방식의 3상 임상비용 잔금, 3상 위약군 연장 연구 관련 직접비용과 이에 따른 간접비용이 포함되어 있습니다. |
상기 연구개발 자금계획표에 기재한 예상 수입 중 '기타매출(L/O 등)'의 경우 OSCA의 임상 2a상이 완료된 후 글로벌 라이선스 아웃 성공 가정 시의 예상 매출 금액과 유영제약과의 기술이전 계약 마일스톤에 따른 예상 수취 금액으로 작성되었습니다. 당사는 OSCA 글로벌 라이선스 아웃을 다수의 고객사와 대륙 단위(혹은 특정 지역 단위)로 진행할 계획입니다. 이에 2026년과 2028년 라이선스 아웃 예상 매출 금액은 무릎골관절염치료제 OSCA의 유럽지역, 미주지역, 아시아 지역별 라이선스 아웃 계약 체결을 가정한 것으로 통상적인 무릎치환술 가격을 기준으로 예상 시장점유율을 고려하여 산정하였습니다. 2026년은 유럽지역 소재 고객사로의 라이선스 아웃 가정으로 총 라이선스 아웃의 10% 해당 계약금 수취에 따른 매출을 가정하였고, 2028년에는 미주지역과 아시아지역 고객사로의 라이선스 아웃에 따른 10% 해당 계약금 수취에 따른 매출을 가정하였습니다. 당사가 현재까지 기술이전 계약 관련하여 논의한 바 있는 글로벌 고객사의 관심 수준, 논의 수준 등을 고려하여 유럽지역, 미주지역, 아시아 지역 순으로의 라이선스 아웃을 가정하였으나, 현재 구체적인 계약 조건이나 상대방이 확정된 것은 아니므로, 기술이전의 성공 여부, 시기, 금액 등은 불확실할 수 있다는 점을 유의해주시기 바랍니다. 한편, 유영제약과의 OCSA 국내 기술이전 계약 상 마일스톤 달성을 가정하여 마일스톤에 따른 2026년 30억원(경상기술료 2차), 2027년 30억원(경상기술료 3차)을 포함하였습니다.
예상 수입 중 '제품매출(OSCA)'은 국내 기술이전 계약에 따라 유영제약에서 임상 2b상~3상 진행 시 IP공급에 따른 예상 매출을 반영하였으며, '제품매출(퓨어스템-에이디주)'은 국내외 재생의료 사업 관련 매출로, 일본 재생의료 자가줄기세포 공급에 따른 예상 매출 또한 포함하고 있습니다. 국내 첨생법 매출의 경우 임상연구 시작 후 2년의 임상연구 기관이 필요한 관계로 매출 상승폭이 크지 않으나 일본 재생의료의 경우 2025년 하반기부터 현지 환자 투여를 목표로 하고 있으며, 환자 모집에 따라 매출 변화가 클 것으로 예상되는 바, 적극적인 모객 활동으로 매출이 빠르게 증가하는 것으로 가정하였습니다. 그 외 '배양액 및 배지 등 매출'은 줄기세포 사업 본격화에 따라 매년 일정 비율만큼의 상승을 가정하였으며, 'CDMO, 화장품, 홈쇼핑 매출'은 타사와의 서비스 경쟁을 고려하여 상대적으로 낮은 폭의 상승을 가정하였습니다. 한편, 각 제품매출 및 상품매출을 위해 예상되는 원가 비용을 각 제품원가비용과 상품원가비용으로 기재하였습니다.
예상 비용 중 '연구개발비용'의 경우 각 파이프라인의 연구개발을 위해 각 임상 단계별 발생 예상되는 전체 비용 중 실제 당사가 지출 예상되는 비용을 기준으로 연도별 작성되었으며, 직접 비용과 간접 비용을 모두 포함하여 작성되었습니다. 최초 증권신고서 공시 시에는 각 임상 단계별 임상과 관련된 직접비용만 '연구개발비용'으로 분류하고, 간접비용은 '판매비와관리비(일반)'로 구분하여 기재하였으나, 금번 공시 시에는 각 '연구개발비용' 항목에 각 임상연구와 관련된 직접비용과 간접비용을 모두 포함하는 기준으로 통일하여 기재하였습니다. 한편, 각 임상 시험 단계별 필요 예상되는 간접 비용은 주로 임상 진행에 따른 당사의 연구소, GMP 인원의 인건비입니다. 퓨어스템-에이디주는 단회투여 방식과 반복투여 방식을 구분하여 세분화하였습니다. 퓨어스템-에이디주의 연구개발비용에는 단회투여 방식의 비용에는 단회투여 3상 임상비용 잔금 등과 장기추적에 필요한 비용이 반영되었으며, 반복투여 방식의 임상시험 비용은 컨소시엄 등 임상 프로젝트 그룹 구성을 통해 해당 외부 자금으로 처리할 예정으로 이를 가정하여 해당 비용에 반영되어 있지 않습니다. 퓨어스템-알에이주의 연구개발비용에는 향후 국내 임상과 장기추적조사에 필요한 비용을 포함하였으며, OSCA는 국내임상, 장기추적조사 및 해외임상에 필요한 비용까지 모두 포함하여 산정하였습니다.
당사는 해당 연구개발 자금 계획표 산정 시 논의 중인 글로벌 파트너사의 관심도와 가능성 예상치, 예상 매출 상승률과 원가 비용, 임상 필요 예상 비용 등을 종합적으로 고려하여 합리적이고 신뢰성 있게 산출하고자 노력하였습니다. 또한, 당사는 이 추정치에 근거하여 내부전략 및 연구개발전략을 수립하고 있습니다. 다만, 최대한 합리적이고 신뢰성 있는 추정치 산출을 위한 당사의 노력에도 불구하고, 미래의 정확한 수치를 예측하는 것에는 한계가 있을 수 있습니다. 또한, 임상 일정이 지연되거나, 임상을 진행하더라도 임상이 실패할 경우, 또는 예상보다 매출 상승률이 낮거나 비용이 늘어나는 경우 당사의 매출액 및 수익성에 부정적인 영향이 미칠 수 있으며, 이에 따라 당사가 현재 추정하고 있는 연구개발 자금계획이 향후 변동될 가능성이 있으니 투자자께서는 이 점 유의하시기 바랍니다.
당사 주요 파이프라인의 임상개요 및 임상 목표 및 결과 현황은 다음과 같습니다.
| 구분 | 임상개요 | 임상 목표 | 결과 현황 |
|---|---|---|---|
| 퓨어스템-AD주(반복투여) -아토피 피부염 치료제 |
중등도 이상의 성인아토피 피부염 환자에서 1개월 간격 3회 피하 반복투여 시 저용량(5x10^7cell)과 고용량(1x10^8cell)에 대한 안전성 및 탐색적 유효성 평가를 위한 1/2a 임상시험 | (1상) 3회 반복투여 시 투여용량군에 대한 안전성확립(DLT 및 MTD)과 EASI50/75와 같은 변수를 이용하여 탐색적 유효성 평가 (2a상) 단회투여 3상 임상시험결과를 반영한 수정 임상시험계획서를 바탕으로 16주-24주 시점에 시판중인 항체치료제와 대등한 유효성(EASI75 및 IGA 1 또는 0 비율)을 보여줄 수 있는지를 위약군과 비교하여 반복투여에 따른 유효성의 효과크기를 확인 |
(1상/완료) 투여된 두 용량 모두에서 DLT 및 MTD 평가에서 뛰어난 안전성 확인. 탐색적 유효성 평가에서는 업그레이드된 임상시험용의약품이 적용된 고용량군 대상자들 모두 50%-80% EASI 변화율이 확인되어 단회투여에 비교할 때, 보다 빠른 시기에 효과가 나타날 수 있는 가능성 확인 (2a상/임상시험계획 변경승인신청) 단회 3상 임상결과에 대한 심층분석결과를 바탕으로 2a 임상시험계획서 변경신청서를 11월 제출하였고, 식약처 자료 보완 요청에 대해 행정처리기간내 회신이 어려울 것으로 보여 2025년 4월에 신청을 자진 취하하였고 2025년 4월 30일에 재신청함 |
| 퓨어스템-RA주 -류마티스관절염 치료제 |
기존의 DMARD제제에 불응인 중등도 이상의 류마티스 관절염 환자에서 1개월 간격으로 시험약(5x10^7cell) 3회 투여 시 위약대비 안전성 검토 및 유효성 평가를 위한 2b 임상시험 | (2b상) 이전 2a 임상시험에서 1개월 간격으로 3회 정맥내 투여할 때 저용량(5x10^7 cells)의 유효성이 확인되었으며, 보다 큰 규모의 모집단에서 위약대비 효과의 크기를 측정하고자 함 |
(2a상/완료) 임상시험을 통해 저용량-고용량 모두 6개월 관찰에서 안전성 확보하였고, 유효성 측면에서 저용량군이 더 뛰어난 결과를 보여 이를 바탕으로 2b 임상시험계획서를 준비하고 진행하였음 (2b상/보류) 2023년 9월 2b상 임상시험계획 승인되었지만, 우선순위 프로젝트인 OSCA 임상과 아토피 임상시험에 예산을 우선 투여하여 2b 임상시험의 개시를 보류 중. 바로는 개시 계획이 없으며 재정상황을 고려하면서 차후 2b 임상시험의 재개 시기를 결정하고 진행 예정임 |
| OSCA (구. 퓨어스템 OA주) -골관절염 치료제 -주력 파이프라인 |
중등도 무릎골관절염 환자(Kellgren & Lawrence grade 2-3)에서 안전성 및 탐색적 유효성을 평가하기 위한 1/2a 임상시험 | (1상) 무릎관절낭내로 3가지 용량(저/중/고) 단회투여 후 안전성 확인 (DLT & MTD), 투약 후 6개월 시점에서 통증과 관절기능, 구조적 개선에 대한 탐색적 유효성을 평가 (2a상) 무릎관절낭내로 단회투여 후 1상에서 안전성과 탐색적 유효성이 확인된 중용량/고용량을 위약 대비 6개월 시점에서 통증과 관절기능, 구조개선에 대해 시험약의 유효성의 크기를 측정하고자 함 |
(1상/완료) 투약된 세 용량 모두에서 독성이 확인되지 않아 안전성이 확립되었음. 탐색적 유효성의 경우, 중용량과 고용량에서 통증조절과 기능개선이 빠르게 나타났으며(100mmVAS, IKDC, WOMAC, KOOS), MRI를 이용한 구조적 개선평가에서도 의미있는 개선이 확인되었음 : 연골재생, 연골하골 구조개선 등 (1상 장기추적조사/진행 중) 12개월 통증 및 관절기능에 대해 저용량 및 중용량 데이터 확보하였고, 6개월 시점대비 저용량의 증상과 영상의학적 평가결과 눈에 띄는 개선이 확인되었으며, 중용량군의 경우 6개월에서 보여준 증상개선이 유지 및 추가개선이 확인되었음. 중·고용량군의 12개월 영상평가결과, 다수의 중·고용량군 환자들에게서 연골재생과 손상된 연골하골의 회복이 지속된 것으로 확인됨. 고용량군은 장기추적조사에 참여한 환자 모두 연골의 마모, 이상구조, 부종, 활막염, 반월판 손상 등 전반적인 부분에서 개선이 나타남 (2상/진행 중) 2025년 3월 25일 분당차병원을 시작으로 중용량에 대해 첫환자 투약 개시함 |
| 출처) 당사 제시 |
당사 주요 파이프라인의 ① 개발 단계별 주요 목표 및 예상 달성 시기, ② 개발 단계별 예상 비용, ③ 연구개발 자금계획은 다음과 같습니다.
① 개발 단계별 주요 목표 및 예상 달성 시기
| 구분 | 1상 | 2a상 | 2b상 | 3상 | 장기 추적 |
|---|---|---|---|---|---|
| 퓨어스템-에이디주(반복투여) | 2022년 06월 | 2027년 02월 | 2028년 10월 | 2030년 02월 | 2035년 02월 |
| 퓨어스템-에이디주(단회투여-3상 장기추적조사) | - | - | - | - | 2028년 08월 |
| 퓨어스템-알에이주 | 2015년 10월 | 2021년 10월 | 2028년 12월 | 2030년 12월 | 2035년 12월 |
| OSCA | 2024년 08월 | 2026년 04월 | 2028년 12월 | 2030년 10월 | 2034년 09월 |
| 출처) 당사 제시 |
| 주1) 해당 예상 달성 시기는 LPO(마지막 환자 방문 완료)시점으로 기재되어 있습니다. |
상기 각 임상 단계별 예상 달성 시기는 LPO(마지막 환자 방문 완료)시점으로 기재되어 있습니다. 통상적으로 임상 시험의 Top-line 데이터 확보는 LPO 시점으로부터 약 3개월 소요, 임상시험 결과보고서(CSR) 수령은 Top-line 데이터 확보로부터 약 3개월 소요됩니다. 다만, 후속 결과 분석, 범위 등에 따라 추가적인 시간이 소요될 수 있습니다.
한편, 당사는 2024년 12월 공시한 합병신고서 당시 예상했던 OSCA의 임상시험 달성 시점이 예상보다 일부 지연되었습니다. 당시 OSCA의 개발 단계별 목표 및 예상 달성 시기가 2a상의 경우 2026년 03월, 2b상은 2028년 03월, 3상은 2029년 09월이었습니다. 그러나 OSCA의 임상 2a상 개시 이후 2a상의 환자 모집 및 투약 개시의 실제 속도에 따라 2a상의 LPO 시점을 최신화하였으며, 이에 임상 2a상 예상 달성 시점이 당시 계획했던 일정과 한 달 차이가 발생하게 되었습니다. 또한, 2024년 12월 공시 시점에는 임상 2b상과 3상에 대해 투약 후 6개월 관찰을 가정하였으나, 이후 내부 논의에 따라 임상 2b상과 3상의 관찰기간을 6개월에서 12개월로 변경 가정하여 이를 반영하였습니다. 이에 따라 임상 2b상 예상시점이 약 6개월 연기되었으며, 2a상과 2b상 예상 시점 연기에 따라 임상 3상의 예상시점도 약 1년 연기되었습니다. 장기추적조사의 경우 5년 진행 예정으로 2034년 9월로 변동없습니다. 또한, 퓨어스템-에이디주와 퓨어스템-알에이주의 경우 2024년 12월 공시한 합병신고서 당시 예상과 금번 예상 달성 시기 간에 변동 사항 없습니다.
당사는 금번 계획한 상기 단계별 목표 및 예상 달성 시기에 맞춰 신약 개발을 위해 노력하고 있으나, 해당 예상 달성 시기는 당사 내부의 파이프라인 우선순위 조정 등에 따라 향후에도 지연될 가능성을 배제할 수 없습니다. 당사는 현실적 여건상 한정된 자원을 가능성이 높은 파이프라인에 우선적으로 집중할 수 밖에 없어 금번 조달된 자금은 OSCA 임상을 위해 사용되며, 우선적으로는 OSCA의 국내 및 해외 임상에 집중할 계획입니다. 퓨어스템-에이디주의 경우 파트너사를 찾아 컨소시엄을 구성하여 임상 비용을 부담할 계획이며, 현재 2025년 하반기 임상 1/2a상 개시를 계획하고 있으나, 임상시험 계획변경 승인 시기가 지연되거나, 컨소시엄 등 결성 시기 지연 시 임상1/2a상 개시 일정도 지연될 수 있습니다. 이후 OSCA의 해외 라이선스 아웃, 국내외 첨단재생의료 진출, 오가노이드 기술 등을 통한 자체적인 재원 확보 등이 성공적으로 이루어질 경우 해당 재원을 기반으로 퓨어스템-에이디주, 퓨어스템-알에이주의 임상 시험을 순차적으로 개시할 예정입니다. 이에 특히 퓨어스템-알에이주의 경우 임상 2b상을 2027년 하반기 개시 후 마지막 환자 방문 완료 시점은 2028년 12월로 현재 목표하고 있으나, 수익화 달성에 따른 임상 진행 재원 마련 여부 등에 의해 추가 지연될 가능성이 존재하므로 이점 투자자께서는 유의하시기 바랍니다.
② 개발 단계별 예상 비용
| 구분 | 1상 | 2a상 | 2b상 | 3상 |
|---|---|---|---|---|
| 퓨어스템-에이디주(반복투여) | - | 80억원 (장기추적 포함) |
86억원 (장기추적 포함) |
175억원 (장기추적 포함) |
| 퓨어스템-에이디주(단회투여-3상 장기추적조사) | - | - | - |
54억원 (장기추적 조사) |
| 퓨어스템-알에이주 | - | - | 84억원 (장기추적 포함) |
249억원 (장기추적 포함) |
| OSCA | 4억원(장기추적) | 239억원 (장기추적 포함, 해외임상IND 포함) |
131억원 (장기추적포함) |
239억원 (장기추적 포함) |
| 출처) 당사 제시 |
| 주1) 해당 예상 비용은 각 파이프라인의 각 개발 단계별 발생 예상되는 전체 비용 기준으로 작성되었습니다. 즉, 당사 및 파트너사 지출 등 모두 포함한 각 단계별 전체 예상 비용 입니다. 직접비용과 간접비용을 모두 포함한 기준으로 작성되었습니다. |
③ 연구개발 자금계획
| 구분 | 2025년 | 2026년 | 2027년 | 2028년 |
|---|---|---|---|---|
| 퓨어스템-에이디주(반복투여) | - | - | - | - |
| 퓨어스템-에이디주(단회투여-3상 장기추적조사) | 9억원 | 13억원 | 12억원 | 9억원 |
| 퓨어스템-알에이주 | - | 20억원 | 20억원 | 25억원 |
| OSCA | 46억원 | 96억원 | 69억원 | 35억원 |
| 출처) 당사 제시 |
| 주1) 해당 예상 비용은 각 파이프라인의 각 개발 단계별 발생 예상되는 전체 비용 중 당사가 지출 예상되는 비용을 기준으로 작성되었습니다. 직접비용과 간접비용을 모두 포함한 기준으로 작성되었습니다. 주2) 퓨어스템-에이디주(반복투여) 임상시험 비용은 컨소시엄 등 임상 프로젝트 그룹 구성을 통해 해당 외부 자금으로 처리할 예정으로 이를 가정하여 해당 비용에 반영되어있지 않습니다. |
당사가 2024년 12월 공시한 합병신고서 당시 예상했던 개발 단계별 예상 비용 및 연구개발 자금계획 대비 금번 ② 개발 단계별 예상 비용 및 ③ 연구개발 자금계획 상 금액이 증가한 이유는 다음과 같습니다. 1) 2024년 12월 공시 당시에는 예상 비용 기재 시, 각 항목의 직접 비용만 산정하여 기재하였습니다. 반면 금번의 경우, 금번 조달한 자금의 사용목적 상 직접 비용 뿐 아니라 간접 비용도 포함되는 바 금번에는 간접 비용까지 모두 포함한 기준으로 변경하여 반영하였습니다. 간접 비용은 임상 진행에 따른 당사의 연구소, GMP 인원의 인건비가 주된 비용이며, 거의 대부분 외주로 진행되는 임상기관연구비, CRO, 위탁연구개발비 항목에는 포함되지 않고, 인허가, 약물감시, 기타 임상진행비 항목에 포함 및 반영되어 있습니다. 2) 또한, 각 예상 비용도 증권신고서 제출일 전일 기준으로 상승률 등 반영하여 최신화하여 재산출 진행하였습니다. 3) OSCA 관련 예상 비용의 경우, 관찰기간 연장 등 변경 계획에 따른 변화를 반영하였으며, 해외 임상 계획도 추가 포함되며 2a상 예상 비용이 크게 증가하였습니다. 다만, OSCA 임상 2b상, 3상의 경우에는 유영제약과의 기술이전 계약 체결에 따라 유영제약 주도로 진행 예정되는 바, 당사가 해당 예상 비용을 대신 최신화 하여 산정하는 것이 어려운 부분이 있어 당시 논의된 예상 임상 비용을 추가 변동 없이 그대로 사용하였으니, 투자자께서는 이 점 유의하시기 바랍니다. 4) 최초 증권신고서 공시 시에는 퓨어스템-에이디주(반복투여) 방식만 표기하였으나, 금번에는 퓨어스템-에이디주를 단회투여방식(3상 장기추적조사)과 반복투여 방식으로 세분화하여 기재 추가하였습니다. 5) 한편, 퓨어스템-에이디주 반복투여 방식의 임상시험 비용은 컨소시엄 등 임상 프로젝트 그룹 구성을 통해 해당 외부 자금으로 처리할 계획을 갖고 있습니다. 이에 이를 가정 시 최초 증권신고서 공시 시 '③ 연구개발 자금계획'에 기재하였던 퓨어스템-에이디주(반복투여)에 예상 비용은, 각 개발 단계별 발생 예상되는 전체 비용 중 당사가 지출 예상되는 비용 기준에 해당하지 않는다고 판단하여 금번 공시에는 제외하여 작성하였으니 이 점 유의하시기 바랍니다.
당사는 각 파이프라인의 각 단계별 예상 비용 및 자금계획 산정 시 필수 비용을 제외한 비용 최소화를 기본 원칙으로 산정하였으며, 유사 임상 진행 시 사용된 비용 등을 종합적으로 분석하여 최대한 객관적이고 신뢰성 있게 산출하고자 노력하였습니다. 그럼에도 불구하고, 임상 일정이 당사 계획보다 지연되거나, 임상을 진행하더라도 임상이 실패할 경우 각 단계별 임상 비용이 증가할 수 있으며 이는 당사의 매출액 및 수익성에 부정적인 영향을 미칠 가능성이 있으니 투자자께서는 이 점 유의하시기 바랍니다.
(중략)
(2) 류마티스관절염 치료제(퓨어스템-알에이 주)
| ①구분 | - 바이오 신약 |
| ②적응증 | - 중등도 이상의 류마티스관절염 |
| ③작용기전 | - 퓨어스템-알에이 주를 류마티스 관절염 환자에 투여시, TSG-6, PGE2 등 다양한 면역조절인자가 분비되어 염증성 세포인 M1 phase macrophage의 활성을 억제하고, 항염증성 세포인 M2 phase macrophage의 활성을 촉진하여, 환자의 염증을 억제하고 증상개선효과를 나타냄. |
| ④제품의특성 | - 세계 최초의 류마티스관절염 줄기세포치료제로서, 단일인자에 대한 차단이 아닌, 질환유발과 관련된 면역세포의 반응을 다각적으로 조절함으로서, 부작용이 거의 없으면서 근본적인 치료제로서 역할을 할 수 있는 신개념의 치료제임. |
| ⑤진행경과 | - 2014년 퓨어스템-알에이 주 1상 임상시험계획 식약처 승인 - 2015년 1상 임상시험 종료 - 2018년 1/2a상 반복투여 임상시험(K0202) 식약처 승인 - 2021년 4월 대상자 등록 완료 - 2021년 10월 임상종료 - 2021년 12월 K0202 결과 확보 (2022년 5월 임상시험결과보고서 최종화) - 2023년 1월 2b상 IND 승인 신청 - 2023년 9월 2b상 IND 승인 |
| ⑥향후계획 | - 2b상 임상 개시 준비 |
| ⑦경쟁제품 |
- AbbVie사의 Humira - Johnson & Johnson사의 Remicade - Amgen/Pfizer사의Enbrel 등 |
| ⑧관련논문등 |
- Human umbilical cord blood-stem cells direct macrophage polarization and block inflammasome activation to alleviate rheumatoid arthritis. Cell Death Dis. 2016;7(12):e2524. - Intravenous Infusion of Umbilical Cord Blood-Derived Mesenchymal Stem Cells in Rheumatoid Arthritis: A Phase 1a Clinical Trial. Stem Cells Transl Med. 2018;7(9):636-642. |
| ⑨시장규모 | - 2019년 류마티스 관절염 치료제 매출이 262억 달러로 2029년까지 연평균 성장률(CAGR) 1% 로 291억 달러까지 완만한 성장을 예상됨. (출처: GlobalData) |
| ⑩기타사항 | - 정부 정책 과제 수주 1건 제대혈 유래 줄기세포를 이용한 류마티스 관절염 치료제의 상업화 임상 2a상 연구 (보건복지부) |
당사 류마티스 관절염 치료제(Furestem-RA Inj.)는 2014년 10월부터 2015년 10월까지 진행된 임상 1상(단회투여) 진행하였고, 그 이후 반복투여(4주간격 3회투여) 치료제로 2016년에 임상 1/2a 계획서를 제출했고 2018년 2월에 한국 식약처에서 승인되었습니다. 2018년 07월 1/2a상 임상 개시 이후, 2018년 12월 임상 1상이 완료되었으며, 2021년 10월에 1/2a상을 통해 안정성을 확인하였으며, 2023년 01월 임상 2b상 IND를 제출하였습니다.
2023년 09월 임상2b상 IND 승인을 받았으나, 선순위 프로젝트인 골관절염 치료제(OSCA) 임상과 아토피 피부염 치료제(퓨어스템-에이디주) 임상 시험에 예산을 우선 사용하여 류마티스 관절염 치료제의 2b 임상시험을 바로 개시하지 않고 보류 중입니다. 현재 류마티스 관절염 치료제(Furestem-RA Inj.)의 임상 2b상은 2027년 하반기 개시 후 마지막 환자 방문 완료 시점은 2028년 12월로 현재 목표하고 있습니다. 다만, 우선순위로 집중하고 있는 OSCA와 퓨어스템-에이디주의 연구개발 일정이 지연되거나 성과가 좋지 않아 당사 수익성에 영향을 미칠 경우, 수익화 달성에 따른 임상 진행 재원 마련 여부 등에 의해 류마티스 관절염 치료제의 임상 2b상의 개시 일정이 추가 지연될 가능성이 존재하므로 투자자께서는 이 점 유의하시기 바랍니다.
(중략)
(5) 골관절염 치료제 (퓨어스템-오에이 키트 주)
| ①구분 | - 바이오 신약 |
| ②적응증 | - ICRS grade 3 또는 4에 해당하는 무릎골관절염 |
| ③작용기전 | - 골관절염 환자의 관절강내에 줄기세포와 생체소재를 함께 주입하여, 염증을 억제하면서, 손상된 연골조직의 재생을 유도함. |
| ④제품의특성 | - 기존의 골관절염 줄기세포치료제의 한계점을 극복할 수 있는 치료제로, 줄기세포와 생체소재를 혼합하여 연골 재생 기능이 탁월한 치료제를 주사제 형태로 개발중에 있음. |
| ⑤진행경과 | - 2021년 8월 한국 식약처 임상시험계획 승인 신청 - 2022년 4월 보완답변 제출 - 2022년 6월 20일 IND 자진취하 - 2022년 7월 15일 IND 재신청 - 2022년 11월 15일 IND 승인완료 - 2022년 11월 28일 IND 변경승인 신청 - 2023년 2월 7일 IND 변경승인 완료 - 2023년 7월 1상 코호트1 대상자 투약ㅉ- 2023년 9월 1상 코호트1 대상자 DLT 평가완료 - 2023년 11월 1상 코호트2 대상자 투약 완료 - 2024년 1월 코호트2 대상자 DLT 평가완료, 코호트1 대상자 6개월 방문완료 - 2024년 3월 코호트3 대상자 DLT 평가완료, 전체 코호트에 대한 MTD 평가완료 - 2024년 4월 코호트1 대상자 6개월 영상평가 평가완료 - 2024년 8월 1/2a상 식약처 IND 변경승인신청, 10월 변경승인 완료 - 2024년 12월 1상 topline data 발표, 1/2a상 식약처 IND 변경승인신청 - 2025년 1월 1/2a상 IND 변경승인 - 2025년 3월 2a상 첫환자 투약 개시 |
| ⑥향후계획 | - 1상 전체 대상자 영상평가 완료 - 1상 결과 국제학회 발표 - 2a 임상시험 개시 |
| ⑦경쟁제품 | - 무릎골관절염 근복적 치료제로 시판승인된 제품 없음. |
| ⑧관련논문등 | - Therapeutic Effects of Human Umbilical Cord Blood-Derived Mesenchymal Stem Cells Combined with Cartilage Acellular Matrix Mediated Via Bone Morphogenic Protein 6 in a Rabbit Model of Articular Cruciate Ligament Transection 2020 Jun;16(3):596-611 - Combined Mesenchymal Stem Cells and Cartilage Acellular Matrix Injection Therapy for Osteoarthritis in Goats 2022 Feb; 19(1): 177-187 |
| ⑨시장규모 | - 골관절염 시장은 2032년까지 183억 6000만달러(24조2021억원)으로 성장할 것으로 전망함. (출처 : Precedence Research) |
| ⑩기타사항 | - 독일Heraeus Medical GmbH 공동개발 계약 체결(2017.09) - 정부 정책과제 수주 1건 차세대 골관절염 줄기세포 치료제 개발을 위한 유효성 안전성 평가 연구 |
(중략)
OSCA의 강점은 첨단 세포 선별 기술과 대량생산 기술로, 고활성 세포의 안정적인 유지가 가능하다는 점입니다. 또한 다중 기전 작용을 통해 기존 치료제보다 우수한 효과와 안전성을 기대할 수 있습니다. 이미 임상 1상 결과를 통해 구조적 개선을 포함한 근본적인 치료제로서의 가능성을 입증했으며, 장기적인 효과를 확인하기 위해 5년까지의 추적 관찰이 계획되어 있습니다.
상업적 측면에서는 국내외 파트너와의 협력으로 개발 비용을 최소화하고 초기 매출 실현 가능성을 높였습니다. 특히, 국내에서는 임상 1상 이후 유영제약과 라이선스 계약을 체결하여 임상 2b상 단계 이후의 개발 비용 부담을 줄이는 동시에 매출 조기 실현이라는 장점을 확보했습니다. 이러한 전략은 안정적인 회사 운영과 글로벌 파트너십 확장을 위한 유리한 환경을 제공합니다.
한편, 당사는 2023년 유상증자 당시 OCSA 임상 1상 완료 후 글로벌 라이선스 아웃을 계획하였으나, 이는 예상보다 지체되었습니다. 당사는 OSCA 임상 1상 이후 다수의 글로벌 제약사와 기술이전 협의를 위해 노력하였으나, 1)위약 대비 시험약의 효과 비교 가능한 데이터, 2)시험군의 효과크기를 비교하기 적절한 규모의 데이터를 보강 요청하는 곳이 다수였습니다. 이에 당사는 OSCA 임상 2a상 대상자를 50명에서 108명으로 본래 계획보다 확대하여 위약 대비 시험약의 효과를 보다 정밀하게 평가할 수 있게 수정하였으며, 임상 2a상 완료 후 확보하게 되는 임상 데이터를 기반으로 다시 글로벌 라이선스 아웃 달성을 목표로 하고 있습니다. 다만, 당사가 추진하는 글로벌 기술이전 계약의 구체적인 계약 조건이나 상대방이 확정된 것은 아니므로, 기술이전의 성공 여부 및 시기 등은 불확실할 수 있다는 점을 투자자께서는 유의하시기 바랍니다.
OSCA의 성공을 위해서는 대규모 임상시험에서 일관성 있는 결과가 필수적이며, 장기적 효과를 지속적으로 증명해야하며 글로벌 시장에서 경쟁 중인 다른 DMOAD 후보들과의 차별화를 이루는 것도 중요한 과제로 판단됩니다. 또한, 당사가 환자모집 지연 등 예상치 못한 이유로 인해 연구개발 일정이 지연된다면 제품화까지 당사 예상 대비 장기간이 소요될 수 있으며, 연구개발을 진행하는 동안에도 성과가 나오지 않을 경우 연구를 중단하게 되고 사용된 연구개발비용은 따로 회수할 수 없어 당사의 수익성 및 성장성에 악영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
(주5) 정정 전
| [당사 파이프라인 현황] |
| 구분 | 품목 | 적응증 | 연구 시작일 |
현재 진행단계 | 비고 | |
| 단계(국가) | 승인일 | |||||
| 바이오 신약 |
퓨어스템-에이디 주 | 아토피피부염 | 2011년 | 임상3상(한국) | 2017년 | 주1) |
| 임상1/2a상(한국) | 2019년 | 주2) | ||||
| 퓨어스템-알에이 주 | 류마티스관절염 | 2012년 | 임상2b상(한국) | 2023년 | 주3) | |
| 퓨어스템-시디 주 | 크론병 | 2012년 | 임상1/2a상(한국) | 2013년 | 주4) | |
| 판상형 건선 | 2013년 | 임상1상(한국) | 2014년 | 주5) | ||
| 퓨어스템-오에이 키트 주 | 골관절염 | 2015년 | 임상1/2a상(한국) | 2022년 | 주6) | |
| 주1) | 2021년 05월 국내 두번째 3상 승인 완료되어 임상 진행하였으며, 2024년 11월 CSR 결과발표하였습니다. |
| 주2) | 반복투여 임상으로 2024년 11월 1/2a 임상시험 변경승인 신청하였으며, 2025년 4월 자진취하 하였습니다. 2025년 4월 30일 식약처에 자료를 보완하여 변경승인 신청 하였습니다. |
| 주3) | 2023년 9월 2b상 IND 승인을 받았으며, 임상 개시 준비 중입니다. |
| 주4) | 2019년 5월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. |
| 주5) | 2019년 1월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. |
| 주6) | 2022년 11월 15일 식약처로부터 IND 승인받았으며, 2a 임상시험을 진행 중입니다. |
(주5) 정정 후
| [당사 파이프라인 현황] |
| 구분 | 품목 | 적응증 | 연구 시작일 |
현재 진행단계 | 비고 | |
| 단계(국가) | 승인일 | |||||
| 바이오 신약 |
퓨어스템-에이디 주 | 아토피피부염 | 2011년 | 임상3상(한국) | 2017년 | 주1) |
| 임상1/2a상(한국) | 2019년 | 주2) | ||||
| 퓨어스템-알에이 주 | 류마티스관절염 | 2012년 | 임상2b상(한국) | 2023년 | 주3) | |
| 퓨어스템-시디 주 | 크론병 | 2012년 | 임상1/2a상(한국) | 2013년 | 주4) | |
| 판상형 건선 | 2013년 | 임상1상(한국) | 2014년 | 주5) | ||
| 퓨어스템-오에이 키트 주 | 골관절염 | 2015년 | 임상1/2a상(한국) | 2022년 | 주6) | |
| 주1) | 2021년 05월 국내 두번째 3상 승인 완료되어 임상 진행하였으며, 2024년 11월 CSR 결과발표하였습니다. |
| 주2) | 반복투여 임상으로 2024년 11월 1/2a 임상시험 변경승인 신청하였으며, 2025년 4월 자진취하 하였습니다. 2025년 4월 30일 식약처에 자료를 보완하여 변경승인 신청 하였습니다. |
| 주3) | 2023년 9월 2b상 IND 승인을 받았으며, 임상 개시 시기는 2027년으로 예상하고 있습니다. |
| 주4) | 2019년 5월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주5) | 2019년 1월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주6) | 2022년 11월 15일 식약처로부터 IND 승인받았으며, 2a 임상시험을 진행 중입니다. |
(주6) 정정 전
당사는 일본 재생의료시장 진출을 위해 2024년 일본 후생노동성에 제1종(동종제대혈줄기세포(를 이용한 아토피 피부염 치료)) 및 제2종(자가지방줄기세포) 재생의료 제공계획에 대한 심의 및 승인 절차를 진행하였습니다. 제2종(자가지방줄기세포)의 경우, 특정인정재생의료위원회의 심의를 거쳐 승인을 받고, 2025년 2월 후생노동성 최종 승인까지 완료되었습니다. 이에 현재 일본 내 공급을 위해 동경, 오사카, 나고야 소재의 현지 의료기관과 계약을 완료하였고, 2분기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 한편, 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며, 후생노동성 권고사항에 따라 소규모 임상시험 진행 등을 검토 중입니다.
(주6) 정정 후
당사는 일본 재생의료시장 진출을 위해 2024년 일본 후생노동성에 제1종(동종제대혈줄기세포(를 이용한 아토피 피부염 치료)) 및 제2종(자가지방줄기세포) 재생의료 제공계획에 대한 심의 및 승인 절차를 진행하였습니다. 제2종(자가지방줄기세포)의 경우, 특정인정재생의료위원회의 심의를 거쳐 승인을 받고, 2025년 2월 후생노동성 최종 승인까지 완료되었습니다. 이에 현재 일본 내 공급을 위해 동경, 오사카, 나고야 소재의 현지 의료기관과 계약을 완료하였고, 2025년 하반기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 기존 계획으로는 2025년 2분기부터 제2종(자가지방줄기세포)의 환자 투약이 가능할 것으로 예상하였으나, 1) 당사 기존시설은 자가줄기세포가 아닌 동종줄기세포 생산에 초점이 맞춰져 있어 자가줄기세포 초도 생산 설비 및 시설 세팅 등 제반 사항 준비 과정의 지연이 있었으며, 2) 최초 투약으로 인한 환자 모객의 지연 등으로 인해 최초 환자 투약은 2025년 하반기부터 가능할 것으로 예상됩니다. 다만, 당사의 노력에도 불구하고 추가 환자 모객의 지연, 현지 상황 변동 등으로 제2종(자가지방줄기세포)의 일본 공급이 지연될 가능성이 존재하므로 투자자께서는 이 점 유의하시기 바랍니다. 한편, 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며, 후생노동성 권고사항에 따라 소규모 임상시험 진행 등을 검토 중입니다.
(주7) 정정 전
| 자. 기술이전 지연 및 실패에 따른 위험 당사와 같은 세포치료제 등 신약개발전문 기업은 대규모 자금이 소요 되는 임상 과정, 다년간의 개발 기간 등의 리스크 분산을 위해 대형제약사 등을 대상으로 기술이전을 통해 조기에 수익을 시현하고 비용 부담을 경감하는 전략을 펼치고 있습니다. 당사는 3건의 라이센스아웃 계약을 체결하였으나, 퓨어스템 에이디주 품목에 대한 현대바이오랜드 와의 라이선스아웃 계약은 3상 임상 결과에서 유효성 차이를 입증하지 못하며 2024년 11월부로 해지되었습니다. 해당 계약 해지에 따라, 지급 받았던 선급기술료 50억은 반환 완료하였습니다. 이처럼 라이선스 아웃 계약이 이루어지더라도, 계약 후 개발 진행 단계가 더디거나, 계약 당시 예상치 못했던 사유 등으로 인해 해지될 수 있는 성격을 가지고 있습니다. 당사가 2024년 11월에 맺은 OSCA의 유영제약 라이센스 아웃 계약의 경우, 통상적인 경우와 다르게 1상에서 진행되었으며 이는 계약 상대방인 유영제약은 정형외과 분야에서 300억 가량의 매출을 발생하고 있는 관절염에 대해 이해가 높은 중견제약사라는 점과, 2b상 이후 유영제약의 임상비용 부담으로 많은 비용이 절감이 가능하고, 동시에, 현재 국내 기술이전을 바탕으로 해외 파트너와의 글로벌 기술이전을 체결하는데 유리한 장점 때문입니다. 또한, 유영제약 입장에서도, 비임상 동물실험과 임상1상 시험 단계에서 당사의 OSCA 통증 감소 및 기능 개선, 연골재생 효과까지 확인하여 근본적인 골관절염 치료제(DMOAD)로서의 가능성을 확인하여 게약을 체결하게 되었습니다. 한편,해당 계약은 선급금에 대한 반환 조건이 없습니다. 당사는 상기 개발 중인 파이프라인의 기술이전을 위해 노력함에도 불구하고 당사가 보유한 파이프라인의 향후 기술개발이 지연되거나 중단되어 추가 기술이전이 발생하지 않거나, 기술개발이 성공해도 잠재 기술이전 파트너사의 협의가 원활하지 않아 기술이전 계약이 지연되거나 실패할 경우에는 당사의 수익성이 악화되거나 사업에 부정적 영향을 줄 수 있습니다. 투자자 여러분들께서는 이 점을 반드시 유의하여 주시기 바랍니다. |
(중략)
가) 퓨어스템-에이디 주(아토피 피부염)
| 계약상대방 | - SK바이오랜드(주) (대한민국) *주1) |
| 계약내용 | - 제대혈유래줄기세포치료제(적응증:아토피 피부염)의 국내 독점판매권/통상 실시권 설정 및 기술전수 계약 |
| 대상지역 | - 대한민국 |
| 계약기간 | - 계약체결일 : 2019.03.25. - 계약종료일 : 2024.11.18. |
| 총 계약금 | - 선급기술료 : 150 억원 (경상기술료는 미공개) |
| 수취금액 | - 50 억원 |
| 계약조건 | - 계약제품에 대한 국내 독점판매권을 현대바이오랜드(구.SK바이오랜드)에 허여함 - 국내 통상실시권 부여 및 기술 전수 - 계약기술 : 당사 보유의 특허권 4건 및 노하우 - 전수시기 : 제품 품목허가 승인 후 현대바이오랜드(구.SK바이오랜드)가 공정 설계 및 투자를 준비하는 시점 - 선급기술료는 총 150억원으로 분할 수령함 1) 계약체결일로부터 15일 이내 50억원 2) 품목허가 후 2년 이내 계약상대방과 협의하에 완제품 협의수량 이상을 연속 생산하고 연속생상된 완제품의 제품공급가 평균값이 vial당 협의된 가격이하가 되는 것을 양사가 확인한 날로부터 90일 이내 20억원 *주2) 3) 현대바이오랜드(SK바이오랜드)가 판매개시 이후 누적판매량이 협의된 수량을 초과한 날로부터 90일 이내 30억원 4) 본 계약에 따라 Know-how 기술전수 요청일로부터 90일 이내 30억원 5) 본 계약에 따라 Know-how 기술전수 종결일로부터 90일 이내 20억원 - 계약제품의 생산은 양사가 공동 협력하며, 당사는 3만 바이알 이내 물량에 대한 제품공급의무를 갖고 있음 |
| 회계처리방법 | - 계약금(Upfront payment) : 라이선스 제공에 대해서는 라이선스 제공과 제품 공급 의무를 단일의 수행의무로 회계처리하며 제품 공급 기간에 걸쳐 수익을 인식하고, 제품의 Know-how 기술이전과 관련 된 수행의무에 대해서는 기술전수가 완료되는 시점에 일시에 수익을 인식 |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 아토피 피부염) - 계약기술 특허는 다음과 같습니다. (1) ZNF281을 발현하는 제대혈 유래 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195호) (2) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량 배양방법(대한민국 특허 등록 제10-1158664호) (3) Isolating Method for Umbilical Cord Blood-Derived Pluripotent Stem Cells Expressing ZNF281(PCT/KR2010/001338) (4) 줄기세포를 유효성분으로 함유하는 면역질환 또는 염증질환의 예방 또는 치료용 조성물(대한민국 특허등록 제10-1512171호) |
| 개발 진행경과 |
- 2013년 퓨어스템-에이디 주 1/2a상 임상시험계획 식약처 승인 - 2015년 1/2a상 임상시험 종료 (2018년 장기추적관찰 종료) - 2017년 3상 임상시험계획 식약처 승인 |
| 기타사항 | 해당 계약에 대하여 (주)현대바이오랜드로부터 2024년 11월 18일 계약해제를 통고 받아 계약이 해제되었습니다. |
| *주1) | 사명 변경 SK바이오랜드 → 현대바이오랜드 |
| *주2) | 2020.12.10 지급조건 변경 |
| 출처) 당사 공시보고서 |
나) Cart-T 기술(암질환군 한정)
| 계약상대방 | - 마루테라퓨틱스(주) (대한민국) |
| 계약내용 | - Car-T 기술(암질환군에 한정)에 대한 전용실시권 부여하는 기술이전계약 |
| 대상지역 | - 국내 및 국외 |
| 계약기간 | - 계약체결일 : 2021.04.16. - 계약종료일 : 대상기술 특허 존속기간 만료시까지 |
| 총 계약금 | - *주) |
| 수취금액 | - *주) |
| 계약조건 | * 계약조건은 영업비밀로 자세한 기재는 생략하며, 대략적인 내용은 다음과 같습니다. - 계약금은 ** 원이며 반환의무가 없음 - 1차선정 파이프라인은 두가지로 하며 단계별 기술료는 각각 **원으로 최대 **원 - 향후 제품 생산시 당사에게 CMO생산 위탁 |
| 회계처리방법 | - 계약금 수취액은 계약 조건에 따라 일시에 수익 인식 |
| 대상기술 | - Car-T 기술(대상 적응증 : 암질환군) - 계약기술 특허는 다음과 같습니다. * off-the-shelf 줄기세포 및 면역세포, 이를 포함하는 약학적 조성물 (출원번호 제10-2021-0009773호) 외 1건 |
| 개발 진행경과 | - 2021년 기술이전 완료 |
| 기타사항 | - |
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
| 출처) 당사 공시보고서 |
다) OSCA(구. 퓨어스템-오에이 키트 주, 골관절염)
| 계약상대방 | - (주)유영제약 (대한민국) |
| 계약내용 | - 무릎골관절염치료제(OSCA(구. 퓨어스템-오에이 키트 주)) 공동개발 및 국내 독점판매권·통상실시권에 대한 라이선스 계약 체결 |
| 대상지역 | - 국내 |
| 계약기간 | - 계약체결일 : 2024.11.07. - 계약종료일 : 품목허가일로부터 10년째 되는 해의 12월 말 |
| 총 계약금 | - 선급기술료: 140억원 |
| 수취금액 | - 20억원 |
| 계약조건 | - 무릎골관절염치료제(OSCA(구. 퓨어스템-오에이 키트 주))의 공동개발 포함 국내 독점판매권·통상실시권에 대한 라이선스 계약 - 총계약금액 : 140억원 1) 경상기술료 1차 : 20억원 (계약체결시) 2) 경상기술료 2차 : 30억원 (국내 공동개발사 선정시 또는 2026년 말 중 빠른 시점) 3) 경상기술료 3차 : 30억원 (유영제약 또는 공동개발사 첫번째 IND 승인시(2b상 또는 통합 임상 2상)) 4) 경상기술료 4차 : 30억원 (유영제약의 3상 임상 IND 승인시) 5) 경상기술료 5차 : 30억원 (유영제약의 품목허가 취득시) - 로열티 별도지급 (시판 후 12개월 간 발주수량에 따라 합의된 금액 수령) - 조건부 허가로 임상3상 진행시 합의된 금액 수령 |
| 회계처리방법 | - 경상기술료 수취액은 계약 조건에 따라 일시에 수익 인식 |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 아토피 피부염) - 계약기술 특허는 다음과 같습니다. (1) 연골 무세포 파쇄물 및 줄기세포를 포함하는 연골분화 촉진용 복합체 및 그의 용도(대한민국 특허 등록 제10-1901568호) (2)연골 분화능이 증진된 줄기세포의 선별 방법 및 이를 포함하는 세포 치료제(대한민국 특허 출원 제10-2023-0189178호) (3) ZNF281을 발현하는 제대혈 유래만능 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195) (4) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량배양 방법 (대한민국 특허등록 제10-1158664호) |
| 개발 진행경과 | - 2023년 1/2a상 식약처 IND 변경승인 완료 및 임상시험 진행 - 2024년 8월 1/2a상 식약처 IND 변경승인신청, 10월 변경승인 완료 - 2024년 12월 1상 topline data 발표, 1/2a상 식약처 IND 변경승인신청 - 2025년 1월 1/2a상 IND 변경승인 - 2025년 2월 2a 임상시험 개시 |
| 기타사항 | - |
| 출처) 당사 공시보고서 |
(중략)
당사는 상기 명시한 기술이전 외에 현재 연구개발 진행 중이거나, 연구개발 진행 예정인 파이프라인의 기술이전을 위해 다양한 경로로 국내외 잠재적 파트너사와 접촉할 계획입니다. 그러나 당사의 파이프라인의 기술이전을 위한 노력에도 불구하고 당사가 보유한 파이프라인의 향후 기술개발이 지연되거나 중단되어 추가 기술이전이 발생하지 않거나, 기술개발이 성공해도 잠재 기술이전 파트너사의 협의가 원활하지 않아 기술이전 계약이 지연되거나 실패할 수 있습니다. 또한, 추가적인 기술이전에 성공하더라도, 해당 기술이전 계약에서 목표하는 기간 내에 효능이 기대에 미치지 못하는 등 임상이 원활하게 진행되지 않을 경우 해당 계약에서 규정한 조건에 따라 계약금을 반환해야할 의무가 있을 수 있으며, 마일스톤 및 로열티 금액 등을 추가로 수령할 수 없을 가능성이 존재합니다.
이처럼 당사의 이러한 기술이전 계약의 지연 및 실패를 축소ㆍ회피하기 위한 노력에도 불구하고, 기술이전 계약이 지연되거나 실패하는 경우에는 당사의 수익성이 악화되거나 사업에 부정적 영향을 줄 수 있습니다. 투자자 여러분들께서는 이 점을 반드시 유의하여 주시기 바랍니다.
(주7) 정정 후
| 자. 기술이전 지연 및 실패에 따른 위험 당사와 같은 세포치료제 등 신약개발전문 기업은 대규모 자금이 소요 되는 임상 과정, 다년간의 개발 기간 등의 리스크 분산을 위해 대형제약사 등을 대상으로 기술이전을 통해 조기에 수익을 시현하고 비용 부담을 경감하는 전략을 펼치고 있습니다. 당사는 3건의 라이센스아웃 계약을 체결하였으나, 퓨어스템 에이디주 품목에 대한 현대바이오랜드 와의 라이선스아웃 계약은 3상 임상 결과에서 유효성 차이를 입증하지 못하며 2024년 11월부로 해지되었습니다. 해당 계약 해지에 따라, 지급 받았던 선급기술료 50억은 반환 완료하였습니다. 이처럼 라이선스 아웃 계약이 이루어지더라도, 계약 후 개발 진행 단계가 더디거나, 계약 당시 예상치 못했던 사유 등으로 인해 해지될 수 있는 성격을 가지고 있습니다. 당사가 2024년 11월에 맺은 OSCA의 유영제약 라이센스 아웃 계약의 경우, 통상적인 경우와 다르게 1상에서 진행되었으며 이는 계약 상대방인 유영제약은 정형외과 분야에서 300억 가량의 매출을 발생하고 있는 관절염에 대해 이해가 높은 중견제약사라는 점과, 2b상 이후 유영제약의 임상비용 부담으로 많은 비용이 절감이 가능하고, 동시에, 현재 국내 기술이전을 바탕으로 해외 파트너와의 글로벌 기술이전을 체결하는데 유리한 장점 때문입니다. 또한, 유영제약 입장에서도, 비임상 동물실험과 임상1상 시험 단계에서 당사의 OSCA 통증 감소 및 기능 개선, 연골재생 효과까지 확인하여 근본적인 골관절염 치료제(DMOAD)로서의 가능성을 확인하여 계약을 체결하게 되었습니다. 한편,해당 계약은 선급금에 대한 반환 조건이 없습니다. 한편, 당사는 2023년 유상증자 및 2024년 12월 공시한 합병 증권신고서 당시 계획했던 기술이전 일정이 현재 전반적으로 지연되고 있습니다. 당사는 상기 개발 중인 파이프라인의 기술이전을 위해 노력함에도 불구하고 당사가 보유한 파이프라인의 향후 기술개발이 지연되거나 중단되어 추가 기술이전이 발생하지 않거나, 기술개발이 성공해도 잠재 기술이전 파트너사의 협의가 원활하지 않아 기술이전 계약이 지연되거나 실패할 경우에는 당사의 수익성이 악화되거나 사업에 부정적 영향을 줄 수 있습니다. 투자자 여러분들께서는 이 점을 반드시 유의하여 주시기 바랍니다. |
(중략)
가) 퓨어스템-에이디 주(아토피 피부염)
| 계약상대방 | - SK바이오랜드(주) (대한민국) *주1) |
| 계약내용 | - 제대혈유래줄기세포치료제(적응증:아토피 피부염)의 국내 독점판매권/통상 실시권 설정 및 기술전수 계약 |
| 대상지역 | - 대한민국 |
| 계약기간 | - 계약체결일 : 2019.03.25. - 계약종료일 : 2024.11.18. |
| 총 계약금 | - 선급기술료 : 150 억원 (경상기술료는 미공개) |
| 수취금액 | - 50 억원 (반환완료 *주3) |
| 계약조건 | - 계약제품에 대한 국내 독점판매권을 현대바이오랜드(구.SK바이오랜드)에 허여함 - 국내 통상실시권 부여 및 기술 전수 - 계약기술 : 당사 보유의 특허권 4건 및 노하우 - 전수시기 : 제품 품목허가 승인 후 현대바이오랜드(구.SK바이오랜드)가 공정 설계 및 투자를 준비하는 시점 - 선급기술료는 총 150억원으로 분할 수령함 1) 계약체결일로부터 15일 이내 50억원 2) 품목허가 후 2년 이내 계약상대방과 협의하에 완제품 협의수량 이상을 연속 생산하고 연속생상된 완제품의 제품공급가 평균값이 vial당 협의된 가격이하가 되는 것을 양사가 확인한 날로부터 90일 이내 20억원 *주2) 3) 현대바이오랜드(SK바이오랜드)가 판매개시 이후 누적판매량이 협의된 수량을 초과한 날로부터 90일 이내 30억원 4) 본 계약에 따라 Know-how 기술전수 요청일로부터 90일 이내 30억원 5) 본 계약에 따라 Know-how 기술전수 종결일로부터 90일 이내 20억원 - 계약제품의 생산은 양사가 공동 협력하며, 당사는 3만 바이알 이내 물량에 대한 제품공급의무를 갖고 있음 |
| 회계처리방법 | - 계약금(Upfront payment) : 라이선스 제공에 대해서는 라이선스 제공과 제품 공급 의무를 단일의 수행의무로 회계처리하며 제품 공급 기간에 걸쳐 수익을 인식하고, 제품의 Know-how 기술이전과 관련 된 수행의무에 대해서는 기술전수가 완료되는 시점에 일시에 수익을 인식 |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 아토피 피부염) - 계약기술 특허는 다음과 같습니다. (1) ZNF281을 발현하는 제대혈 유래 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195호) (2) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량 배양방법(대한민국 특허 등록 제10-1158664호) (3) Isolating Method for Umbilical Cord Blood-Derived Pluripotent Stem Cells Expressing ZNF281(PCT/KR2010/001338) (4) 줄기세포를 유효성분으로 함유하는 면역질환 또는 염증질환의 예방 또는 치료용 조성물(대한민국 특허등록 제10-1512171호) |
| 개발 진행경과 |
- 2013년 퓨어스템-에이디 주 1/2a상 임상시험계획 식약처 승인 - 2015년 1/2a상 임상시험 종료 (2018년 장기추적관찰 종료) - 2017년 3상 임상시험계획 식약처 승인 |
| 기타사항 | 해당 계약에 대하여 (주)현대바이오랜드로부터 2024년 11월 18일 계약해제를 통고 받아 계약이 해제되었습니다. |
| *주1) | 사명 변경 SK바이오랜드 → 현대바이오랜드 |
| *주2) | 2020.12.10 지급조건 변경 |
| *주3) | 2024년 11월 18일 계약해제되었으며, 이에 당사는 ㈜현대바이오랜드로부터 수령한 선급기술료 50억원을 반환하였습니다. 해당 선급기술료는 회계 계정 상 선수수익으로 처리했다가 계약부채로 변경한 후 현대바이오랜드에 반환 후 계약부채에 대한 역분개 처리하였습니다. 이에 관련 분개로 손익에 미치는 영향은 없었습니다. |
| 출처) 당사 공시보고서 |
나) Cart-T 기술(암질환군 한정)
| 계약상대방 | - 마루테라퓨틱스(주) (대한민국) |
| 계약내용 | - Car-T 기술(암질환군에 한정)에 대한 전용실시권 부여하는 기술이전계약 |
| 대상지역 | - 국내 및 국외 |
| 계약기간 | - 계약체결일 : 2021.04.16. - 계약종료일 : 대상기술 특허 존속기간 만료시까지 |
| 총 계약금 | - *주) |
| 수취금액 | - *주) |
| 계약조건 | * 계약조건은 영업비밀로 자세한 기재는 생략하며, 대략적인 내용은 다음과 같습니다. - 계약금은 ** 원이며 반환의무가 없음 - 1차선정 파이프라인은 두가지로 하며 단계별 기술료는 각각 **원으로 최대 **원 - 향후 제품 생산시 당사에게 CMO생산 위탁 |
| 회계처리방법 | - 계약금 수취액은 계약 조건에 따라 일시에 수익 인식 |
| 대상기술 | - Car-T 기술(대상 적응증 : 암질환군) - 계약기술 특허는 다음과 같습니다. * off-the-shelf 줄기세포 및 면역세포, 이를 포함하는 약학적 조성물 (출원번호 제10-2021-0009773호) 외 1건 |
| 개발 진행경과 | - 2021년 기술이전 완료 |
| 기타사항 | - |
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
| 출처) 당사 공시보고서 |
다) OSCA(구. 퓨어스템-오에이 키트 주, 골관절염)
| 계약상대방 | - (주)유영제약 (대한민국) |
| 계약내용 | - 무릎골관절염치료제(OSCA(구. 퓨어스템-오에이 키트 주)) 공동개발 및 국내 독점판매권·통상실시권에 대한 라이선스 계약 체결 |
| 대상지역 | - 국내 |
| 계약기간 | - 계약체결일 : 2024.11.07. - 계약종료일 : 품목허가일로부터 10년째 되는 해의 12월 말 |
| 총 계약금 | - 선급기술료: 140억원 |
| 수취금액 | - 20억원 |
| 계약조건 | - 무릎골관절염치료제(OSCA(구. 퓨어스템-오에이 키트 주))의 공동개발 포함 국내 독점판매권·통상실시권에 대한 라이선스 계약 - 총계약금액 : 140억원 1) 경상기술료 1차 : 20억원 (계약체결시) 2) 경상기술료 2차 : 30억원 (국내 공동개발사 선정시 또는 2026년 말 중 빠른 시점) 3) 경상기술료 3차 : 30억원 (유영제약 또는 공동개발사 첫번째 IND 승인시(2b상 또는 통합 임상 2상)) 4) 경상기술료 4차 : 30억원 (유영제약의 3상 임상 IND 승인시) 5) 경상기술료 5차 : 30억원 (유영제약의 품목허가 취득시) - 로열티 별도지급 (시판 후 12개월 간 발주수량에 따라 합의된 금액 수령) - 조건부 허가로 임상3상 진행시 합의된 금액 수령 |
| 회계처리방법 | - 경상기술료 수취액은 계약 조건에 따라 일시에 수익 인식 |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 아토피 피부염) - 계약기술 특허는 다음과 같습니다. (1) 연골 무세포 파쇄물 및 줄기세포를 포함하는 연골분화 촉진용 복합체 및 그의 용도(대한민국 특허 등록 제10-1901568호) (2)연골 분화능이 증진된 줄기세포의 선별 방법 및 이를 포함하는 세포 치료제(대한민국 특허 출원 제10-2023-0189178호) (3) ZNF281을 발현하는 제대혈 유래만능 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195) (4) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량배양 방법 (대한민국 특허등록 제10-1158664호) |
| 개발 진행경과 | - 2023년 1/2a상 식약처 IND 변경승인 완료 및 임상시험 진행 - 2024년 8월 1/2a상 식약처 IND 변경승인신청, 10월 변경승인 완료 - 2024년 12월 1상 topline data 발표, 1/2a상 식약처 IND 변경승인신청 - 2025년 1월 1/2a상 IND 변경승인 - 2025년 3월 2a상 첫환자 투약 개시 |
| 기타사항 | - |
| 출처) 당사 공시보고서 |
(중략)
당사는 상기 명시한 기술이전 외에 현재 연구개발 진행 중이거나, 연구개발 진행 예정인 파이프라인의 기술이전을 위해 다양한 경로로 국내외 잠재적 파트너사와 접촉할 계획입니다.
한편, 당사는 2023년 유상증자 및 2024년 12월 공시한 합병 증권신고서 당시 계획했던 기술이전 일정이 현재 전반적으로 지연되고 있습니다. 퓨어스템-에이디주의 경우 진행중이던 임상 3상 결과를 바탕으로 2024년/2025년 글로벌 라이센스 아웃을 목표로 설정한 바 있습니다. 그러나 2024년 11월 2차 임상 3상 결과, 1차 평가지표인 12주차 시점 EASI-50 평가에서 시험군과 위약 대조군 간 유효성 차이를 입증하지 못하였으며, 이에 따라 글로벌 라이센스 아웃 역시 계획했던 일정보다 지연되었습니다. 당사는 2025년 4월 퓨어스템-에이디주의 반복투여 제1/2a 임상시험계획변경승인신청을 하였으며, 퓨어스템-에이디주의 경우 파트너사를 찾아 컨소시엄을 구성하여 임상 비용을 부담할 계획이며, 현재 2025년 하반기 임상 1/2a상 개시를 계획하고 있습니다. 다만, 임상시험 계획변경 승인 시기가 지연되거나, 컨소시엄 등 결성 시기 지연 시 임상1/2a상 개시 일정도 지연될 수 있습니다. 향후 해당 임상 진행 추이 및 결과를 바탕으로 퓨어스템-에이디주의 기술이전 계획을 재수립할 예정입니다.
퓨어스템-알에이주의 경우 2023년 유상증자 당시 2025년 상반기 임상 2b상 개시 및 임상 2b상 완료 후 글로벌 라이센스 아웃 진행을 목표로 하였으며, 2024년 12월 공시한 합병 증권신고서에는 2028년을 글로벌 라이센스 아웃 목표로 계획하였습니다. 이에 2023년 9월 식약처로부터 임상 2b상 IND를 승인 받았으나, 퓨어스템-에이디주의 사업화가 지연되며 내부적으로 파이프라인 전반에 대한 임상계획 조정이 필요하였습니다. 이에 따라, 우선순위 프로젝트인 OSCA와 퓨어스템-에이디주 임상시험에 예산 투여를 위해 퓨어스템-알에이주 2b 임상시험의 개시를 보류 중이며 기술이전 일정 역시 함께 지연될 수밖에 없었습니다. 당사는 우선순위 파이프라인의 임상 계획 등을 감안하여 퓨어스템-알에이주 2b상을 2027년 하반기에 개시, 2028년 12월 완료를 목표로 계획 중입니다. 향후 해당 임상 진행 추이 및 결과를 바탕으로 퓨어스템-알에이주의 라이센스 아웃 계획을 수립할 예정입니다. 한편, 임상 2b상까지는 당사가 진행 후 임상 3상부터는 대웅제약과 공동개발을 진행할 예정이며, 임상2b상이 지연되거나 실패하더라도 별도의 공동개발 계약 해지 조항은 없습니다.
OSCA의 경우 2023년 유상증자 당시 2024년 임상 1상 결과를 바탕으로 글로벌 라이센스 아웃을 계획하였고, 2024년 12월 합병 증권신고서 당시 2025년 말 혹은 2026년 상반기를 글로벌 라이센스 아웃 목표로 계획하였습니다. OSCA 1상의 경우 실제로 중용량, 고용량군에서 우수한 임상 결과를 수령하였습니다. 당사는 OSCA 임상 1상 이후 다수 글로벌 제약사와 기술이전 협의를 위해 접촉하였으나, 1)위약 대비 시험약의 효과 비교 가능한 데이터, 2)시험군의 효과크기를 비교하기 적절한 규모의 데이터를 보강 요청하는 곳이 다수였습니다. 이에 당사는 위약 대조와 더 많은 실험군을 바탕으로 OSCA의 우수한 효과와 안전성을 2a상에서 입증하고, 글로벌 라이센스 아웃 규모를 확대하는 방향으로 전략을 수정하였습니다. 또한, 국내 라이센스 아웃을 선제적으로 체결하고, 해당 레퍼런스 기반으로 글로벌 라이센스 아웃 계약을 준비하기로 결정하였으며, 이에 따라 2024년 11월 유영제약과 국내 라이센스 아웃 계약을 체결하는데 성공하였습니다. 금번 증권신고서 제출일 기준, 당사는 OSCA의 글로벌 라이센스 아웃 시점을 임상 2a상 종료 후인 2026년 하반기 또는 2027년 상반기로 목표하고 있습니다. 그러나, OSCA의 임상 진행 과정 및 기술이전 협의 과정 등에서 차질이 발생할 경우 글로벌 라이센스 아웃의 목표 시점이 지연될 수 있으며, 이에 당사의 핵심 파이프라인 상업화가 지연됨에 따라 당사의 재무적 성과에 직접적 영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
그러나 당사의 파이프라인의 기술이전을 위한 노력에도 불구하고 당사가 보유한 파이프라인의 향후 기술개발이 지연되거나 중단되어 추가 기술이전이 발생하지 않거나, 기술개발이 성공해도 잠재 기술이전 파트너사의 협의가 원활하지 않아 기술이전 계약이 지연되거나 실패할 수 있습니다. 또한, 추가적인 기술이전에 성공하더라도, 해당 기술이전 계약에서 목표하는 기간 내에 효능이 기대에 미치지 못하는 등 임상이 원활하게 진행되지 않을 경우 해당 계약에서 규정한 조건에 따라 계약금을 반환해야할 의무가 있을 수 있으며, 마일스톤 및 로열티 금액 등을 추가로 수령할 수 없을 가능성이 존재합니다.
이처럼 당사의 이러한 기술이전 계약의 지연 및 실패를 축소ㆍ회피하기 위한 노력에도 불구하고, 기술이전 계약이 지연되거나 실패하는 경우에는 당사의 수익성이 악화되거나 사업에 부정적 영향을 줄 수 있습니다. 투자자 여러분들께서는 이 점을 반드시 유의하여 주시기 바랍니다.
(주8) 정정 전
| [주요재무사항 총괄표] | |
| (K-IFRS, 연결) | (단위 : 백만원, %) |
| 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | 비고 | |
|---|---|---|---|---|---|---|
| 감사인 | 안진회계법인 | 안진회계법인 | 안진회계법인 | 안진회계법인 | - | |
| 외부감사인의 감사(검토)의견 | 적정 | 적정 | 적정 | 적정 | - | |
| 감사인 강조사항 | 해당없음 | 해당없음 | 해당없음 | 해당없음 | - | |
| 계속기업 존속불확실성 사유 해당여부 | 미해당 | 미해당 | 미해당 | 미해당 | - | |
| 1. 자산총계 | 50,204 | 55,986 | 81,253 | 80,592 | - | |
| 유동자산 | 23,576 | 28,528 | 47,366 | 45,907 | - | |
| 비유동자산 | 26,628 | 27,458 | 33,887 | 34,685 | - | |
| 2. 부채총계 | 11,925 | 12,804 | 36,735 | 33,331 | - | |
| 유동부채 | 7,019 | 7,732 | 24,199 | 19,709 | - | |
| 비유동부채 | 4,906 | 5,072 | 12,536 | 13,623 | - | |
| 3. 자본총계 | 38,279 | 43,182 | 44,518 | 47,260 | - | |
| 자본금 | 28,027 | 28,027 | 28,003 | 19,003 | - | |
| 주식발행초과금 | 174,869 | 174,869 | 174,895 | 163,374 | - | |
| 기타자본항목 | 7,172 | 7,172 | 4,469 | 4,194 | - | |
| 결손금 | (171,789) | (166,886) | (159,354) | (137,201) | - | |
| 4. 부채비율(%) | 31.2% | 29.7% | 82.5% | 70.5% | 부채총계 ÷ 자본총계 | |
| 5. 유동비율(%) | 335.9% | 368.9% | 195.7% | 232.9% | 유동자산 ÷ 유동부채 | |
| 6. 총차입금 | 8,430 | 8,456 | 19,214 | 18,811 | - | |
| 유동성 차입금 | 4,031 | 4,048 | 14,560 | 12,460 | - | |
| 비유동성 차입금 | 4,399 | 4,408 | 4,654 | 6,350 | - | |
| - 총차입금 의존도(%) | 16.8% | 15.1% | 23.6% | 23.3% | 총차입금 ÷ 자산총계 | |
| - 유동성 차입금 비중(%) | 47.8% | 47.9% | 75.8% | 66.2% | 유동성 차입금 ÷ 총차입금 | |
| 7. 영업활동 현금흐름 | (321) | (18,987) | (16,498) | (18,864) | - | |
| - 영업활동현금흐름 총부채 비율(%) | -2.7% | -148.3% | -44.9% | -56.6% | 영업활동현금흐름 ÷ 부채총계 | |
| 8. 투자활동 현금흐름 | (195) | 15,014 | (2,304) | 16,236 | - | |
| 9. 재무활동 현금흐름 | (85) | 884 | 19,977 | (231) | - | |
| 10. 현금 및 현금성자산 | 18,596 | 19,197 | 37,360 | 36,678 | 현금 및 현금성자산 + 단기금융상품 | |
| 11. 순차입금 | (10,166) | (10,741) | (18,146) | (17,867) | 총차입금 - 현금 및 현금성자산 | |
| - 순차입금 의존도(%) | -20.2% | -19.2% | -22.3% | -22.2% | 순차입금 ÷ 자산총계 | |
| 12. 매출액 | 954 | 7,746 | 12,704 | 16,301 | - | |
| 13. 매출원가 | 749 | 3,420 | 11,061 | 11,428 | - | |
| - 매출원가율(%) | 78.5% | 44.2% | 87.1% | 70.1% | 매출원가 ÷ 매출액 | |
| 14. 영업이익(손실) | (4,745) | (14,842) | (22,777) | (20,558) | - | |
| - 영업이익률(%) | -497.2% | -191.6% | -179.3% | -126.1% | 영업이익 ÷ 매출액 | |
| 15. 기타수익 | 21 | 152 | 173 | 459 | - | |
| 16. 기타비용 | 10 | 47 | 300 | 321 | - | |
| 17. 금융수익 | 175 | 1,457 | 1,547 | 1,335 | - | |
| 18. 금융원가 | 270 | 1,170 | 1,060 | 1,129 | - | |
| 이자비용 | 127 | 426 | 893 | 761 | - | |
| - 이자비용배수(배) | -37.36 | -34.85 | -25.49 | -27.01 | 영업이익 ÷ 이자비용 | |
| 21. 법인세비용차감전계속사업이익(손실) | (4,903) | (7,083) | (23,137) | (20,215) | - | |
| 22. 당기순이익(손실) | (4,903) | (7,990) | (23,221) | (20,176) | - | |
| - 당기순이익률(%) | -513.8% | -103.2% | -182.8% | -123.8% | 당기순이익 ÷ 매출액 | |
| 출처) 당사 정기보고서 제시 |
(주8) 정정 후
| [주요재무사항 총괄표] | |
| (K-IFRS, 연결) | (단위 : 백만원, %) |
| 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | 비고 | |
|---|---|---|---|---|---|---|
| 감사인 | 삼일회계법인 | 안진회계법인 | 안진회계법인 | 안진회계법인 | - | |
| 외부감사인의 감사(검토)의견 | - | 적정 | 적정 | 적정 | - | |
| 감사인 강조사항 | 해당없음 | 해당없음 | 해당없음 | 해당없음 | - | |
| 계속기업 존속불확실성 사유 해당여부 | 미해당 | 미해당 | 미해당 | 미해당 | - | |
| 1. 자산총계 | 50,204 | 55,986 | 81,253 | 80,592 | - | |
| 유동자산 | 23,576 | 28,528 | 47,366 | 45,907 | - | |
| 비유동자산 | 26,628 | 27,458 | 33,887 | 34,685 | - | |
| 2. 부채총계 | 11,925 | 12,804 | 36,735 | 33,331 | - | |
| 유동부채 | 7,019 | 7,732 | 24,199 | 19,709 | - | |
| 비유동부채 | 4,906 | 5,072 | 12,536 | 13,623 | - | |
| 3. 자본총계 | 38,279 | 43,182 | 44,518 | 47,260 | - | |
| 자본금 | 28,027 | 28,027 | 28,003 | 19,003 | - | |
| 주식발행초과금 | 174,869 | 174,869 | 174,895 | 163,374 | - | |
| 기타자본항목 | 7,172 | 7,172 | 4,469 | 4,194 | - | |
| 결손금 | (171,789) | (166,886) | (159,354) | (137,201) | - | |
| 4. 부채비율(%) | 31.2% | 29.7% | 82.5% | 70.5% | 부채총계 ÷ 자본총계 | |
| 5. 유동비율(%) | 335.9% | 368.9% | 195.7% | 232.9% | 유동자산 ÷ 유동부채 | |
| 6. 총차입금 | 8,430 | 8,456 | 19,214 | 18,811 | - | |
| 유동성 차입금 | 4,031 | 4,048 | 14,560 | 12,460 | - | |
| 비유동성 차입금 | 4,399 | 4,408 | 4,654 | 6,350 | - | |
| - 총차입금 의존도(%) | 16.8% | 15.1% | 23.6% | 23.3% | 총차입금 ÷ 자산총계 | |
| - 유동성 차입금 비중(%) | 47.8% | 47.9% | 75.8% | 66.2% | 유동성 차입금 ÷ 총차입금 | |
| 7. 영업활동 현금흐름 | (321) | (18,987) | (16,498) | (18,864) | - | |
| - 영업활동현금흐름 총부채 비율(%) | -2.7% | -148.3% | -44.9% | -56.6% | 영업활동현금흐름 ÷ 부채총계 | |
| 8. 투자활동 현금흐름 | (195) | 15,014 | (2,304) | 16,236 | - | |
| 9. 재무활동 현금흐름 | (85) | 884 | 19,977 | (231) | - | |
| 10. 현금 및 현금성자산 | 18,596 | 19,197 | 37,360 | 36,678 | 현금 및 현금성자산 + 단기금융상품 | |
| 11. 순차입금 | (10,166) | (10,741) | (18,146) | (17,867) | 총차입금 - 현금 및 현금성자산 | |
| - 순차입금 의존도(%) | -20.2% | -19.2% | -22.3% | -22.2% | 순차입금 ÷ 자산총계 | |
| 12. 매출액 | 954 | 7,746 | 12,704 | 16,301 | - | |
| 13. 매출원가 | 749 | 3,420 | 11,061 | 11,428 | - | |
| - 매출원가율(%) | 78.5% | 44.2% | 87.1% | 70.1% | 매출원가 ÷ 매출액 | |
| 14. 영업이익(손실) | (4,745) | (14,842) | (22,777) | (20,558) | - | |
| - 영업이익률(%) | -497.2% | -191.6% | -179.3% | -126.1% | 영업이익 ÷ 매출액 | |
| 15. 기타수익 | 21 | 152 | 173 | 459 | - | |
| 16. 기타비용 | 10 | 47 | 300 | 321 | - | |
| 17. 금융수익 | 175 | 1,457 | 1,547 | 1,335 | - | |
| 18. 금융원가 | 270 | 1,170 | 1,060 | 1,129 | - | |
| 이자비용 | 127 | 426 | 893 | 761 | - | |
| - 이자비용배수(배) | -37.36 | -34.85 | -25.49 | -27.01 | 영업이익 ÷ 이자비용 | |
| 21. 법인세비용차감전계속사업이익(손실) | (4,903) | (7,083) | (23,137) | (20,215) | - | |
| 22. 당기순이익(손실) | (4,903) | (7,990) | (23,221) | (20,176) | - | |
| - 당기순이익률(%) | -513.8% | -103.2% | -182.8% | -123.8% | 당기순이익 ÷ 매출액 | |
| 출처) 당사 정기보고서 제시 |
(주9) 정정 전
당사는 줄기세포 치료제 개발 및 제조회사로, 연구개발하는 신약이 상업화되기까지 많은 시간과 비용이 소요되며 임상 시험의 경우 최소 8~9년의 연구개발 기간과 이에 따른 비용 소요를 필요로 합니다. 이에 연구개발 활동 이외의 수익 창출을 위해 H&B(health & beauty) 사업을 확장하여 홈쇼핑, 전략적 유통 파트너를 통한 줄기세포 기반의 기능성 화장품, 샴푸 매출을 창출하고 있으며, 최근에는 매출 지역, 제품 다각화를 위해 일본 시장을 겨냥한 재생의료사업을 계획하고 있습니다. 다만, 신약 개발과 연계한 제품 제조를 위해 2019년 05월 15일 GMP 센터 설립 등의 비용으로 175억원 소요 및 퓨어스템-에이디 주 2차 임상 진행 기간 중 코로나19 팬데믹에 따른 임상 지연으로 추가 비용이 발생하는 등 10년 간 신약 파이프라인 임상 진행에 따른 비용이 가중되었습니다. 2019년 이후 2025년 1분기까지 각 파이프라인별 소요 비용은 퓨어스템-에이디 379억원, OSCA 105억원, 퓨어스템-알에이 38억원으로, 총 522억원이 소요되었습니다. 이에 당사는 CDMO 사업 진행을 통해 관련 매출을 발생시켜 유지 및 보수 비용을 충당하였으며, 개발 중인 신약과 관련한 다양한 국가 과제 수행을 통해 연구개발비용을 절감하고 긴축 재정 관리로 운용 비용을 절감하고 있습니다. 2025년 1분기 기준, 총 26개의 과제를 수행완료 및 진행 중에 있으며 총 정부출연금은 약 217억원입니다.
이러한 당사의 노력에도 불구하고 2010년 설립 이후 적자가 지속되고 있으며 매출액 대비 연구개발비용(개별기준)이 2022년부터 2024년까지 평균 212.3% 수준으로, 신약개발기업 특성상 매출 대비 현저히 많은 연구개발비용이 소요되고 있습니다. 이에 당사는 수익성 개선을 위해 2020년 12월부터 첨단바이오의약품 제조업 허가 및 CDMO 사업을 개시하며 누적매출 36억원을 기록하였습니다. 또한, 2015년 줄기세포배양액 화장품 GD11 런칭, 2021년 화장품사업부 인수 및 2021년 CJ홈쇼핑, 2022년 GS홈쇼핑를 통해 제품 판매를 시작하며 화장품사업부 누적매출 289억원을 기록하였습니다.
또한, 당사는 일본 재생의료시장 진출을 위해 특정인정재생의료위원회의 심의를 거쳐 제2종(자가지방줄기세포) 승인을 받고, 2025년 2월 후생노동성 최종 승인까지 완료된 상황입니다. 현재 일본 내 공급을 위해 동경, 오사카, 나고야 소재의 현지 의료기관과 계약을 완료하였고, 2분기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 또한 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며, 후생노동성 권고사항에 따라 소규모 임상시험 진행 등을 검토 중입니다. 제1종의 경우, 현재까지 후생노동성 최종 승인 사례가 단 1건에 불과하여 승인이 쉽지 않을 것으로 예상되지만, 승인을 받을 경우 당사의 줄기세포 사업 전반에 걸쳐 큰 수혜를 받을 것으로 예상됩니다.
(주9) 정정 후
당사는 줄기세포 치료제 개발 및 제조회사로, 연구개발하는 신약이 상업화되기까지 많은 시간과 비용이 소요되며 임상 시험의 경우 최소 8~9년의 연구개발 기간과 이에 따른 비용 소요를 필요로 합니다. 이에 연구개발 활동 이외의 수익 창출을 위해 H&B(health & beauty) 사업을 확장하여 홈쇼핑, 전략적 유통 파트너를 통한 줄기세포 기반의 기능성 화장품, 샴푸 매출을 창출하고 있으며, 최근에는 매출 지역, 제품 다각화를 위해 일본 시장을 겨냥한 재생의료사업을 계획하고 있습니다. 다만, 신약 개발과 연계한 제품 제조를 위해 2019년 05월 15일 GMP 센터 설립 등의 비용으로 175억원 소요 및 퓨어스템-에이디 주 2차 임상 3상 진행 기간 중 코로나19 팬데믹에 따른 임상 지연으로 추가 비용이 발생하는 등 10년 간 신약 파이프라인 임상 진행에 따른 비용이 가중되었습니다. 2019년 이후 2025년 1분기까지 각 파이프라인별 소요 비용은 퓨어스템-에이디 379억원, OSCA 105억원, 퓨어스템-알에이 38억원으로, 총 522억원이 소요되었습니다. 이에 당사는 CDMO 사업 진행을 통해 관련 매출을 발생시켜 유지 및 보수 비용을 충당하였으며, 개발 중인 신약과 관련한 다양한 국가 과제 수행을 통해 연구개발비용을 절감하고 긴축 재정 관리로 운용 비용을 절감하고 있습니다. 2025년 1분기 기준, 총 26개의 과제를 수행완료 및 진행 중에 있으며 총 정부출연금은 약 217억원입니다.
이러한 당사의 노력에도 불구하고 2010년 설립 이후 적자가 지속되고 있으며 매출액 대비 연구개발비용(개별기준)이 2022년부터 2024년까지 평균 212.3% 수준으로, 신약개발기업 특성상 매출 대비 현저히 많은 연구개발비용이 소요되고 있습니다. 이에 당사는 수익성 개선을 위해 2020년 12월부터 첨단바이오의약품 제조업 허가 및 CDMO 사업을 개시하며 누적매출 36억원을 기록하였습니다. 또한, 2015년 줄기세포배양액 화장품 GD11 런칭, 2021년 화장품사업부 인수 및 2021년 CJ홈쇼핑, 2022년 GS홈쇼핑를 통해 제품 판매를 시작하며 화장품사업부 누적매출 289억원을 기록하였습니다.
또한, 당사는 일본 재생의료시장 진출을 위해 특정인정재생의료위원회의 심의를 거쳐 제2종(자가지방줄기세포) 승인을 받고, 2025년 2월 후생노동성 최종 승인까지 완료된 상황입니다. 현재 일본 내 공급을 위해 동경, 오사카, 나고야 소재의 현지 의료기관과 계약을 완료하였고, 2025년 하반기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 또한 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며, 후생노동성 권고사항에 따라 소규모 임상시험 진행 등을 검토 중입니다. 제1종의 경우, 현재까지 후생노동성 최종 승인 사례가 단 1건에 불과하여 승인이 쉽지 않을 것으로 예상되지만, 승인을 받을 경우 당사의 줄기세포 사업 전반에 걸쳐 큰 수혜를 받을 것으로 예상됩니다.
(주10) 정정 전
2022년~2024년 및 2025년 1분기 연결기준 차입부채의 내역은 다음과 같습니다.
| (단위: 백만원) |
| 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| 유동 | ||||
| 단기차입금 | 3,330 | 3,330 | 900 | 900 |
| 유동성장기차입금 | 400 | 400 | 5,530 | 3,700 |
| 전환사채(크로엔 CB) | - | - | 1,716 | 1,666 |
| 상환전환우선주부채(크로엔 RCPS) | - | - | 5,605 | 5,442 |
| 소 계 | 3,730 | 3,730 | 13,751 | 11,709 |
| 비유동 | ||||
| 장기차입금 | 2,980 | 2,980 | 3,380 | 5,230 |
| 소 계 | 2,980 | 2,980 | 3,380 | 5,230 |
| 합 계 | 6,710 | 6,710 | 17,131 | 16,938 |
| 출처) 당사 정기보고서 |
| 주1) 당사는 2024년 05월 HLB바이오코드(주)의 보유주식 1,183,676주 중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류되었으며 연결 대상에서 제외되었습니다. |
2025년 1분기말 현재 장단기차입금 내역은 다음과 같습니다.
| [차입금 상세 내역] | |
| (K-IFRS, 연결) | (단위 : 백만원) |
| 구분 | 차입처 | 내역 | 만기일 | 연이자율(%) | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|---|---|---|
| 단기차입금 | 기업은행 | 중소기업자금 | 2025-05-31 | 4.959 | 1,500 | 1,500 | 300 | 300 |
| 중소기업시설자금 | 2025-06-11 | 4.349 | 1,480 | 1,480 | 600 | 600 | ||
| 2025-06-11 | 4.521 | 350 | 350 | - | - | |||
| 유동성장기차입금 | 400 | 400 | 5,530 | 3,500 | ||||
| 단기차입금 소계 | 3,730 | 3,730 | 6,430 | 4,400 | ||||
| 장기차입금 | 기업은행 | 중소기업시설자금 | 2032-06-08 | 4.945 | 3,000 | 3,000 | 3,400 | 3,800 |
| 2025-06-11 | 5.551 | - | - | 1,480 | 1,480 | |||
| 2025-06-11 | 5.490 | - | - | 350 | 350 | |||
| 2026-12-21 | 4.911 | 380 | 380 | 380 | - | |||
| 2024-09-22 | 5.669 | - | - | 3,300 | 3,300 | |||
| 소계 | 3,380 | 3,380 | 8,910 | 8,930 | ||||
| 유동성 대체 | (400) | (400) | (5,530) | (3,700) | ||||
| 장기 차입금 소계 | 2,980 | 2,980 | 3,380 | 5,230 | ||||
| 합계 | 6,710 | 6,710 | 9,810 | 9,630 | ||||
| 출처) 당사 정기보고서 |
한편, 당사는 2025년 1분기 기준 금융기관으로부터 토지 및 시설자금 명목으로 대출을 받았으며, 이와 관련하여 토지 및 건물 등을 담보로 제공하고 있습니다. 2025년 1분기 기준 차입금과 관련하여 담보로 제공된 자산의 내역은 다음과 같습니다.
| [유형자산 담보제공 내역] |
| (단위: 천원) |
| 담보제공자산 | 장부금액 | 담보설정금액 | 관련 계정과목 | 관련 차입금액 | 담보권자 |
|---|---|---|---|---|---|
| 토지 | 3,660,774 | 8,796,000 | 차입금 | 6,710,000 | 기업은행 |
| 건물 | 7,758,009 |
| 출처) 당사 정기보고서 |
(주10) 정정 후
2022년~2024년 및 2025년 1분기 연결기준 차입부채의 내역은 다음과 같습니다.
| [차입금 상세 내역] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| 유동 | ||||
| 단기차입금 | 3,330 | 3,330 | 900 | 900 |
| 유동성장기차입금 | 400 | 400 | 5,530 | 3,700 |
| 전환사채(크로엔 CB) | - | - | 1,716 | 1,666 |
| 상환전환우선주부채(크로엔 RCPS) | - | - | 5,605 | 5,442 |
| 소 계 | 3,730 | 3,730 | 13,751 | 11,709 |
| 비유동 | ||||
| 장기차입금 | 2,980 | 2,980 | 3,380 | 5,230 |
| 소 계 | 2,980 | 2,980 | 3,380 | 5,230 |
| 합 계 | 6,710 | 6,710 | 17,131 | 16,938 |
| 출처) 당사 정기보고서 |
| 주1) 당사는 2024년 05월 HLB바이오코드(주)의 보유주식 1,183,676주 중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류되었으며 연결 대상에서 제외되었습니다. |
2025년 1분기말 현재 장단기차입금 내역은 다음과 같습니다.
| [장단기차입금 상세 내역] | |
| (K-IFRS, 연결) | (단위 : 백만원) |
| 구분 | 차입처 | 내역 | 만기일 | 연이자율(%) | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|---|---|---|
| 단기차입금 | 기업은행 | 중소기업자금 | 2025-05-31 | 4.959 | 1,500 | 1,500 | 300 | 300 |
| 중소기업시설자금 | 2025-06-11 | 4.349 | 1,480 | 1,480 | 600 | 600 | ||
| 2025-06-11 | 4.521 | 350 | 350 | - | - | |||
| 유동성장기차입금 | 400 | 400 | 5,530 | 3,700 | ||||
| 단기차입금 소계 | 3,730 | 3,730 | 6,430 | 4,600 | ||||
| 장기차입금 | 기업은행 | 중소기업시설자금 | 2032-06-08 | 4.945 | 3,000 | 3,000 | 3,400 | 3,800 |
| 2025-06-11 | 5.551 | - | - | 1,480 | 1,480 | |||
| 2025-06-11 | 5.490 | - | - | 350 | 350 | |||
| 2026-12-21 | 4.911 | 380 | 380 | 380 | - | |||
| 2024-09-22 | 5.669 | - | - | 3,300 | 3,300 | |||
| 소계 | 3,380 | 3,380 | 8,910 | 8,930 | ||||
| 유동성 대체 | (400) | (400) | (5,530) | (3,700) | ||||
| 장기 차입금 소계 | 2,980 | 2,980 | 3,380 | 5,230 | ||||
| 합계 | 6,710 | 6,710 | 9,810 | 9,830 | ||||
| 출처) 당사 정기보고서 |
한편, 당사는 2025년 1분기 기준 금융기관으로부터 토지 및 시설자금 명목으로 대출을 받았으며, 이와 관련하여 토지 및 건물 등을 담보로 제공하고 있습니다. 2025년 1분기 기준 차입금과 관련하여 담보로 제공된 자산의 내역은 다음과 같습니다.
| [유형자산 담보제공 내역] |
| (단위: 천원) |
| 담보제공자산 | 장부금액 | 담보설정금액 | 담보감정가격 | 관련 계정과목 | 차입금액 | 담보권자 |
|---|---|---|---|---|---|---|
| 토지 | 3,660,774 | 8,796,000 | 11,028,000 | 차입금 | 6,710,000 | 기업은행 |
| 건물 | 7,758,009 |
| 출처) 당사 정기보고서 |
| 주1) 담보제공자산인 토지 및 건물은 글로벌R&D센터줄기세포재생의학연구소(서울 금천구 소재)와 줄기세포GMP센터(경기도 광명시 소재)입니다. |
| 주2) 담보감정가격 감정일은 2021년입니다. |
(주11) 정정 전
| 마. 관리종목 편입 가능성에 따른 위험 당사는 기술성장특례 적용 기업으로 2015년에 12월에 상장하여 관리종목 지정요건 중 유예 항목들에 대한 적용 기간이 만료되었습니다. 이에 따라 당사가 매출액 및 법인세비용차감전계속사업손실 요건, 자본잠식 요건 등을 충족하지 못할 경우 향후 관리종목으로 지정될 가능성이 있습니다. 당사는 2023년 법인세비용차감전계속사업손실률이 51.9%까지 증가하였으며 관리종목 지정 리스크가 발생하였습니다. 2024년 법차손률이 16.4%를 기록하며 대폭 개선되었으나, 2025년 사업연도말의 법차손률이 50%를 상회할 경우 최근 3사업연도중 2사업연도(2023년, 2025년)의 법차손률이 50%를 상회함에 따라 관리종목으로 지정될 수 있습니다. 당사는 2024년 5월 HLB바이오코드 주식회사 지분 매각을 통해 연결 손실 인식을 방지하고, 동시에 98억원의 처분이익이 발생하며 2024년 법차손률 16.4%로 큰 폭으로 개선되었습니다. 또한, 현재 당사는 OSCA 라이선스 아웃 계약에 따른 단계별 선급기술료 수취 및 임상비용 절약, 일본 재생의료 매출 발생 등 수익성 향상을 위해 노력중입니다. 동시에, 금번 유상증자를 통한 자본규모 확충을 기대중입니다. 이러한 당사의 노력에도 불구하고 사업환경이 급격히 악화되어 당사의 임상 및 연구개발 지연으로 매출 저조 등 재무성과를 나타내지 못할 경우 관리종목으로 지정 요건에 해당할 수 있으니 투자자들께서는 이점 유의하시기 바랍니다. |
「코스닥시장 상장규정」제53조(관리종목)은 매출액, 법인세비용차감전계속사업손실, 자본잠식 등 코스닥시장 상장법인으로서의 경영성과 및 재무상태에 미달하는 경우 관리종목을 지정하도록 명시되어 있습니다. 당사는 기술성장특례 적용 기업으로 2015년에 12월에 상장하여 관리종목 지정요건 중 유예 항목들에 대한 적용 기간이 만료되었습니다.이에 따라 당사가 매출액 및 법인세비용차감전계속사업손실 요건, 자본잠식 요건 등을 충족하지 못할 경우 향후 관리종목으로 지정될 가능성이 있습니다.
| [코스닥시장 관리종목 지정요건 및 해당여부 검토] |
| 구 분 | 관리종목 지정(코스닥 상장규정 제53조) | 관리종목지정유예 | 관리종목 지정요건 적용여부 |
회사현황 | ||
|---|---|---|---|---|---|---|
| 해당여부 | 유예기간 | 사업연도 | 금액(백만원) / 비율(%) / 내용 | |||
| (1) 매출액 미달 | 최근 사업연도 30억원 미만 (지주회사는 연결기준) - 이익미실현기업 또는 기술성장기업은 상장후 5년간 미적용 - 기술성장기업 중 A), B), C) 중 어느 하나에 해당하는 제약·바이오기업은 최근 사업연도 미적용 A) 최근 사업연도 말「제약산업 육성 및 지원에 관한 특별법」에 따른 혁신제약기업이 세칙으로 정한 요건을 충족하는 경우 B) 최근 사업연도의 일평균 시가총액 4,000억 이상이며, 그 금액이 현재의 자본금을 초과하는 기업이 세칙으로 정하는 요건을 충족하는 경우 C) 최근 3사엽언도의 매출액 합계 90억 이상이며, 최근 사업연도의 직전 사업연도의 매출액이 30억 이상인 경우 |
- | - | 현재 미해당 | 2024년말 | 매출액 : 7,746백만원 (K-IFRS 별도기준) |
| 2025년 1분기말 | 매출액 : 954백만원 (K-IFRS 별도기준) |
|||||
| (2) 법인세비용차감전 계속사업손실 |
최근 3사업연도중 2사업연도에 각각 10억원 이상이면서 해당 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 있고 최근사업연도에 법인세비용차감전계속사업손실이 있는 경우 - 이익미실현 기업은 상장 후 5년간 미적용 (다만, 상장일부터 상장일이 속한 사업연도의 말일까지의 기간이 3개월 미만인 경우에는 상장일이 속하는 사업연도와 그 이후 5개 사업연도로 한다) - 기술성장기업은 상장후 3년간 미적용(다만, 상장일부터 상장일이 속한 사업연도의 말일까지의 기간이 3개월 미만인 경우에는 상장일이 속하는 사업연도와 그 이후 3개 사업연도로 한다) |
- | - | 2023년이 해당되며 2024년은 미해당, 2025년 해당될 경우 관리종목 지정 |
2023년말 | 세전손실 : (23,137)백만원 자기자본 : 44,517백만원 (자기자본 대비 52.0%) |
| 2024년말 | 세전손실 : (7,083)백만원 자기자본 : 43,182백만원 (자기자본 대비 16.4%) |
|||||
| 2025년 1분기말 | 세전손실 : (4,903)백만원 자기자본 : 38,279백만원 (자기자본 대비 12.8%) |
|||||
| (3) 자본잠식 등 | 최근 사업연도말 현재 자본잠식률이 100분의 50 이상인 경우 | - | - | 현재 미해당 | 2024년말 | 자본금 : 28,027백만원 지배주주지분 : 43,182백만원 자본잠식률 : 해당없음 |
| 2025년 1분기말 | 자본금 : 28,027백만원 지배주주지분 : 38,279백만원 자본잠식률 : 해당없음 |
|||||
| (4)자기자본 미달 | 최근 사업연도말 현재 자기자본이 10억원 미만인 경우 | - | - | 현재 미해당 | 2024년말 | 지배주주지분 : 43,182백만원 |
| 2025년 1분기말 | 지배주주지분 : 38,279백만원 | |||||
| (5) 시가총액 미달 | 보통주 시가총액 40억원미만 30일간 지속 - 천재지변, 시장상황의 급격한 변동 등으로 거래소가 시장 관리를 위하여 필요하다고 인정될 경우 적용배제 가능 |
- | - | 현재 미해당 | 2024년 12월 31일 |
시가총액 : 113,229백만원 |
| 증권신고서 제출일 기준 |
시가총액 : 116,873백만원 |
|||||
| (6) 정기보고서 미제출 | 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않은 경우 | - | - | 현재 미해당 | 현재 기준 | 현재 특이사항 없음 |
| (7) 지배구조 미달 | 최근 사업연도 사업보고서상 A)사외이사의 수가 「상법」 제542조의8의 규정에서 정하는 수에 미달하는 경우 B) 「상법」 제542조의11의 규정에서 정하는 감사위원회를 구성하지 않거나 감사위원회의 구성요건을 충족하지 못하는 경우 *「상법」 제542조의8에 의거 자산총액 1,000억원 미만의 코스닥 상장 벤처기업은 사외이사 선임 의무 면제 **「상법」 제542조의11에 의거 자산총액 2조원 미만의 상장회사는 감사위원회 설치 의무 면제 |
- | - | 현재 미해당 | 2024년말 | 현재 특이사항 없음 |
| (8) 거래량 미달 | 분기월평균거래량이 유동주식수의 1%에 미달 다만, 다음 어느 하나에 해당하는 경우에는 이 호에 적용 받지 않습니다. - 신규상장법인(신규상장일이 속하는 분기에 한정) - 분기의 월평균거래량 1만주 이상(액면가액 5,000원 기준) - 「코스닥시장 업무규정」(이하 “업무규정”이라 한다) 제12조의3제1항에 따른 유동성공급계약이 체결된 경우 - 소액주주가 소유한 보통주식의 총수가 유동주식수의 100분의 20 이상이고, 해당 소액주주의 수가 300명 이상인 경우. |
- | - | 현재 미해당 | 2025년 1분기말 | 소액주주 - 지분율 77.58% - 19,291명 |
| (9) 주식분산 미달 | 소액주주 200인미만 or 소액주주지분 20%미만 - 300인이상의 소액주주가 유동주식수의 10%이상으로서 100만주이상을 소유, 해외증권시장에 상장된 경우는 적용배제 |
- | - | 현재 미해당 | 2025년 1분기말 | 소액주주 - 지분율 77.58% - 19,291명 |
| (10) 회생절차 개시신청 | "채무자 회생 및 파산에 관한 법률" 제34조에 의한 회생 절차개시 신청이 있는 경우 | - | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| (11) 파산신청 | 코스닥시장 상장법인에 대하여 "채무자 회생 및 파산에 관한 법률" 제294조에 의한 파산신청이 있는 경우 | - | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| (12) 기타 | - 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 - 변경·추가상장이 유예된 기간 중에「증권의 발행 및 공시 등에 관한 규정」에 따른 재무관리기준을 위반한 경우 |
- | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| 출처)「코스닥시장 상장규정」, 당사 정기보고서 |
| 주1) 상기 도표 중 (1)매출액 미달 요건 관련하여, 별도재무제표를 기준으로 합니다. 그 외 요건은 연결재무제표를 기준으로 합니다. |
| 주2) (2)법인세비용차감전계속사업손실 요건 관련하여, 자기자본은 비지배지분을 제외하지 않은 금액 기준을 적용합니다. (3)자본잠식 등, (4)자기자본 미달 요건 관련하여, 자기자본은 비지배지분을 제외한 지배기업지분금액 기준을 적용합니다. |
한편, 당사는 2023년 법인세비용차감전계속사업손실률이 51.9%까지 증가하였으며 관리종목 지정 리스크가 발생하였습니다(최근 3개년 중 1년 해당됨). 2024년 법차손률이 16.4%를 기록하며 대폭 개선되었으나, 2025년 사업연도말의 법차손률이 50%를 상회할 경우 최근 3사업연도중 2사업연도(2023년, 2025년)의 법차손률이 50%를 상회함에 따라 관리종목으로 지정될 수 있습니다.
2023년 당사의 연결대상 종속회사인 HLB바이오코드(구.주식회사 크로엔)의 매출 및 손익이 크게 악화되었고, 그에 따른 연결 손실을 인식함으로써 법인세비용차감전계속사업손실률이 51.9%까지 증가하였습니다. 2024년 HLB바이오코드의 손실이 지속될 것으로 예상되어, 계속해서 지분을 보유할 경우 당사의 재무적 악화 및 관리종목 지정 리스크에 여전히 영향을 미칠 것으로 예상되었고, 2024년 5월 HLB바이오코드 주식회사 지분 매각을 결정하였습니다. 이를 통해 연결 손실 인식을 방지하고, 동시에 98억원의 처분이익이 발생하며 2024년 법차손률 16.4%로 큰 폭으로 개선되었습니다.
현재 당사는 OSCA 라이선스 아웃 계약에 따른 단계별 선급기술료 수취 및 임상비용 절약, 일본 재생의료 매출 발생 등 수익성 향상을 위해 노력중입니다. 동시에, 금번 유상증자를 통한 자본규모 확충을 기대중입니다. 이러한 당사의 노력에도 불구하고 사업환경이 급격히 악화되어 당사의 임상 및 연구개발 지연으로 매출 저조 등 재무성과를 나타내지 못할 경우 관리종목으로 지정 요건에 해당할 수 있으니 투자자들께서는 이점 유의하시기 바랍니다.
| [최근 3개년 법인세비용차감전계속사업손실] | |||
| (단위 : 백만원) | |||
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| (법인세비용차감전계속사업손실/자기자본)×100(%) | 12.8% | 16.4% | 52.0% | 42.7% |
| 법인세비용차감전계속사업손실 | 4,903 | 7,083 | 23,137 | 20,215 |
| 자기자본 | 38,279 | 43,182 | 44,517 | 47,260 |
| 출처) 당사 정기보고서 |
관리종목 지정사유 확인 당일에는 코스닥시장에서의 거래는 정지되며, 이를 기한 내에 해결하지 못한다면 코스닥시장 상장폐지 사유에 해당하여, 당사 주식은 향후 장내에서 거래가 이루어지지 못할 수 있습니다. 투자자 여러분들께서는 당사의 주식이 상장폐지될 경우, 투자금액을 회수하지 못하게 될 수도 있는 점을 반드시 유의하여 주시기 바랍니다. 이에 투자자 여러분들께서는 코스닥시장에서의 관리종목, 상장폐지와 관련된 규정을 반드시 유의하시고, 당사의 영업 수익성 추이에 대하여 지속적으로 모니터링하시기 바랍니다.
| [IPO 및 상장 폐지 제도개선 방안 및 해당여부 검토] |
| 구 분 | IPO 및 상장 폐지 제도개선 방안 | 상장폐지 지정요건 적용여부 |
회사현황 | |
|---|---|---|---|---|
| 사업연도 | 금액(백만원) / 내용 | |||
| (1) 시가총액 요건 기준 강화 | 정량요건으로서 시장평가 관련 시가총액 기준을 단계적으로 상향하여 코스피 500억원, 코스닥 300억원을 목표로 합니다. - 코스피 : 50억원(현행) → 200억원(2026년) → 300억원(2027년) → 500억원(2028년) - 코스닥 : 40억원(현행) → 150억원(2026년) → 200억원(2027년) → 300억원(2028년) |
현재 미해당 | 2024년 12월 31일 |
시가총액 : 113,229백만원 |
| 증권신고서 제출일 기준 |
시가총액 : 백만원 | |||
| (2) 매출액 요건 기준 강화 | 정량요건으로서 기업실적 관련 매출액 기준을 단계적으로 상향하여 코스피 300억원(시가총액 1,000원 미만 기업만 적용), 코스닥 100억원(시가총액 600억원 미만 기업만 적용)을 목표로 합니다. - 코스피 : 50억원(현행) → 100억원(2027년) → 200억원(2028년) → 300억원(2029년) - 코스닥 : 30억원(현행) → 50억원(2027년) → 750억원(2028년) → 100억원(2029년) |
현재 미해당 | 2024년말 | 매출액 : 7,746백만원 (K-IFRS 별도기준) |
| 2025년 1분기말 | 매출액 : 954백만원 (K-IFRS 별도기준) |
|||
| (3) 감사의견 미달 요건 기준 강화 | - 2회 연속 감사의결 미달시 즉시 상장폐지 : 감사의견 미달(한정, 부적정, 의견거절)의 경우 2회 연속발생시 즉시 상장폐지되고(회생 ·워크아웃기업에 대해서는 예외인정), 이의신청은 허용되지 않습니다. | 현재 미해당 | 2024년말 | 해당사항 없음 |
| 2025년 1분기말 | 해당사항 없음 | |||
| 출처) 금융위원회, 당사 정기보고서 |
또한, 2025년 01월 21일, 정부와 유관기관(금융위원회, 금융감독원, 한국거래소, 금융투자협회)은 주식시장의 질적수준 제고를 위한「IPO 및 상장 폐지 제도개선 방안」을 발표하였습니다. 이 중 상장폐지 제도개선 방안은 상자유지 요건을 강화하고, 절차는 효율화함으로써 주식시장 내 저성과 기업을 적시에 퇴출시키고 상장기업의 밸류업을 주요 목적으로 하고 있습니다. 이와 같이 상장폐지 요건이 강화됨에 따라 당사의 영업환경 악화, 재무요건 악화 등을 원인으로 강화된 상장폐지 요건에 해당되어 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있음을 투자자분들은 유의하시기 바랍니다.
(주11) 정정 후
| 마. 관리종목 편입 및 상장폐지 가능성에 따른 위험 당사는 기술성장특례 적용 기업으로 2015년에 12월에 상장하여 관리종목 지정요건 중 유예 항목들에 대한 적용 기간이 만료되었습니다. 이에 따라 당사가 매출액 및 법인세비용차감전계속사업손실 요건, 자본잠식 요건 등을 충족하지 못할 경우 향후 관리종목으로 지정될 가능성이 있습니다. 당사는 2023년 법인세비용차감전계속사업손실률이 51.9%까지 증가하였으며 관리종목 지정 리스크가 발생하였습니다. 2024년 법차손률이 16.4%를 기록하며 대폭 개선되었으나, 2025년 사업연도말의 법차손률이 50%를 상회할 경우 최근 3사업연도중 2사업연도(2023년, 2025년)의 법차손률이 50%를 상회함에 따라 관리종목으로 지정될 수 있습니다. 당사는 2024년 5월 HLB바이오코드 주식회사 지분 매각을 통해 연결 손실 인식을 방지하고, 동시에 98억원의 처분이익이 발생하며 2024년 법차손률 16.4%로 큰 폭으로 개선되었습니다. 다만, 2024년 지분 매각으로 인한 처분이익 98억원의 경우 일회성 이익에 해당하여 당사의 2025년 영업수익성에 미치는 영향은 미미한 것으로 판단됩니다. 따라서, 2025년 법인세비용차감전계속사업손실이 전년도 대비 증가할 가능성이 있으니 투자자들께서는 이 점을 유의하여 주시기 바랍니다. 또한, 현재 당사는 OSCA 라이선스 아웃 계약에 따른 단계별 선급기술료 수취 및 임상비용 절약, 일본 재생의료 매출 발생 등 수익성 향상을 위해 노력중입니다. 동시에, 금번 유상증자를 통한 자본규모 확충을 기대 중이며, 계획한 수익성 향상 노력과 자금조달이 모두 성공적으로 이루어질 경우 2025년 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 발생할 가능성은 낮을 것으로 판단됩니다. 다만. 이러한 당사의 노력에도 불구하고 사업환경이 급격히 악화되어 당사의 임상 및 연구개발 지연으로 매출 저조 등 재무성과를 나타내지 못하거나 유상증자에 실패하여 법인세비용차감전계속사업손실률이 50%를 상회할 경우 관리종목으로 지정 요건에 해당할 수 있으니 투자자들께서는 이점 유의하시기 바랍니다. 2025년 01월 21일 금융위원회와 금융감독원, 한국거래소, 금융투자협회, 자본시장연구원이 발표한 'IPO 및 상장폐지 제도 개선 방안'에 따르면 시가총액이 600억원 미만인 코스닥 상장 법인의 상장 유지를 위한 매출 요건이 강화되었습니다. 당사의 최근 3년간 별도기준 매출액 중 2022년과 2023년은 각각 59.2억원, 59.1억원으로 2028년부터 적용되는 매출요건 75억을 하회합니다. 한편, 2024년 매출액은 77.5억원으로, 2029년부터 적용되는 매출요건 100억원을 하회합니다. 다만, 당사의 최근 시가총액은 2028년부터 적용되는 최소 시가총액 요건인 600억원을 상회하고 있기 때문에, 현재 시가총액 수준을 유지한다면 해당 사항은 없을 것으로 보입니다. 그러나, 향후 당사의 매출 성장성이 둔화되어 매출이 악화되고 시가총액 수준이 지속적으로 하락할 경우 금융당국의 강화된 상장폐지 요건에 해당될 가능성이 있습니다. 투자자들께서는 투자 판단 시 최근 상장폐지 요건 강화에 따른 상장폐지 위험에 대해서 충분히 인지하시길 바랍니다. |
「코스닥시장 상장규정」제53조(관리종목)은 매출액, 법인세비용차감전계속사업손실, 자본잠식 등 코스닥시장 상장법인으로서의 경영성과 및 재무상태에 미달하는 경우 관리종목을 지정하도록 명시되어 있습니다. 당사는 기술성장특례 적용 기업으로 2015년에 12월에 상장하여 관리종목 지정요건 중 유예 항목들에 대한 적용 기간이 만료되었습니다. 이에 따라 당사가 매출액 및 법인세비용차감전계속사업손실 요건, 자본잠식 요건 등을 충족하지 못할 경우 향후 관리종목으로 지정될 가능성이 있습니다.
| [코스닥시장 관리종목 지정요건 및 해당여부 검토] |
| 구 분 | 관리종목 지정(코스닥 상장규정 제53조) | 관리종목지정유예 | 관리종목 지정요건 적용여부 |
회사현황 | ||
|---|---|---|---|---|---|---|
| 해당여부 | 유예기간 | 사업연도 | 금액(백만원) / 비율(%) / 내용 | |||
| (1) 매출액 미달 | 최근 사업연도 30억원 미만 (지주회사는 연결기준) - 이익미실현기업 또는 기술성장기업은 상장후 5년간 미적용 - 기술성장기업 중 A), B), C) 중 어느 하나에 해당하는 제약·바이오기업은 최근 사업연도 미적용 A) 최근 사업연도 말「제약산업 육성 및 지원에 관한 특별법」에 따른 혁신제약기업이 세칙으로 정한 요건을 충족하는 경우 B) 최근 사업연도의 일평균 시가총액 4,000억 이상이며, 그 금액이 현재의 자본금을 초과하는 기업이 세칙으로 정하는 요건을 충족하는 경우 C) 최근 3사엽언도의 매출액 합계 90억 이상이며, 최근 사업연도의 직전 사업연도의 매출액이 30억 이상인 경우 |
- | - | 현재 미해당 | 2024년말 | 매출액 : 7,746백만원 (K-IFRS 별도기준) |
| 2025년 1분기말 | 매출액 : 954백만원 (K-IFRS 별도기준) |
|||||
| (2) 법인세비용차감전 계속사업손실 |
최근 3사업연도중 2사업연도에 각각 10억원 이상이면서 해당 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 있고 최근사업연도에 법인세비용차감전계속사업손실이 있는 경우 - 이익미실현 기업은 상장 후 5년간 미적용 (다만, 상장일부터 상장일이 속한 사업연도의 말일까지의 기간이 3개월 미만인 경우에는 상장일이 속하는 사업연도와 그 이후 5개 사업연도로 한다) - 기술성장기업은 상장후 3년간 미적용(다만, 상장일부터 상장일이 속한 사업연도의 말일까지의 기간이 3개월 미만인 경우에는 상장일이 속하는 사업연도와 그 이후 3개 사업연도로 한다) |
- | - | 2023년이 해당되며 2024년은 미해당, 2025년 해당될 경우 관리종목 지정 |
2023년말 | 세전손실 : (23,137)백만원 자기자본 : 44,517백만원 (자기자본 대비 51.9%) |
| 2024년말 | 세전손실 : (7,083)백만원 자기자본 : 43,182백만원 (자기자본 대비 16.4%) |
|||||
| 2025년 1분기말 | 세전손실 : (4,903)백만원 자기자본 : 38,279백만원 (자기자본 대비 12.8%) |
|||||
| (3) 자본잠식 등 | 최근 사업연도말 현재 자본잠식률이 100분의 50 이상인 경우 | - | - | 현재 미해당 | 2024년말 | 자본금 : 28,027백만원 지배주주지분 : 43,182백만원 자본잠식률 : 해당없음 |
| 2025년 1분기말 | 자본금 : 28,027백만원 지배주주지분 : 38,279백만원 자본잠식률 : 해당없음 |
|||||
| (4)자기자본 미달 | 최근 사업연도말 현재 자기자본이 10억원 미만인 경우 | - | - | 현재 미해당 | 2024년말 | 지배주주지분 : 43,182백만원 |
| 2025년 1분기말 | 지배주주지분 : 38,279백만원 | |||||
| (5) 시가총액 미달 | 보통주 시가총액 40억원미만 30일간 지속 - 천재지변, 시장상황의 급격한 변동 등으로 거래소가 시장 관리를 위하여 필요하다고 인정될 경우 적용배제 가능 |
- | - | 현재 미해당 | 2024년 12월 31일 |
시가총액 : 113,229백만원 |
| 증권신고서 제출일 전일 기준 |
시가총액 : 84,754백만원 |
|||||
| (6) 정기보고서 미제출 | 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않은 경우 | - | - | 현재 미해당 | 현재 기준 | 현재 특이사항 없음 |
| (7) 지배구조 미달 | 최근 사업연도 사업보고서상 A)사외이사의 수가 「상법」 제542조의8의 규정에서 정하는 수에 미달하는 경우 B) 「상법」 제542조의11의 규정에서 정하는 감사위원회를 구성하지 않거나 감사위원회의 구성요건을 충족하지 못하는 경우 *「상법」 제542조의8에 의거 자산총액 1,000억원 미만의 코스닥 상장 벤처기업은 사외이사 선임 의무 면제 **「상법」 제542조의11에 의거 자산총액 2조원 미만의 상장회사는 감사위원회 설치 의무 면제 |
- | - | 현재 미해당 | 2024년말 | 현재 특이사항 없음 |
| (8) 거래량 미달 | 분기월평균거래량이 유동주식수의 1%에 미달 다만, 다음 어느 하나에 해당하는 경우에는 이 호에 적용 받지 않습니다. - 신규상장법인(신규상장일이 속하는 분기에 한정) - 분기의 월평균거래량 1만주 이상(액면가액 5,000원 기준) - 「코스닥시장 업무규정」(이하 “업무규정”이라 한다) 제12조의3제1항에 따른 유동성공급계약이 체결된 경우 - 소액주주가 소유한 보통주식의 총수가 유동주식수의 100분의 20 이상이고, 해당 소액주주의 수가 300명 이상인 경우. |
- | - | 현재 미해당 | 2025년 1분기말 | 소액주주 - 지분율 77.58% - 19,291명 |
| (9) 주식분산 미달 | 소액주주 200인미만 or 소액주주지분 20%미만 - 300인이상의 소액주주가 유동주식수의 10%이상으로서 100만주이상을 소유, 해외증권시장에 상장된 경우는 적용배제 |
- | - | 현재 미해당 | 2025년 1분기말 | 소액주주 - 지분율 77.58% - 19,291명 |
| (10) 회생절차 개시신청 | "채무자 회생 및 파산에 관한 법률" 제34조에 의한 회생 절차개시 신청이 있는 경우 | - | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| (11) 파산신청 | 코스닥시장 상장법인에 대하여 "채무자 회생 및 파산에 관한 법률" 제294조에 의한 파산신청이 있는 경우 | - | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| (12) 기타 | - 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 - 변경·추가상장이 유예된 기간 중에「증권의 발행 및 공시 등에 관한 규정」에 따른 재무관리기준을 위반한 경우 |
- | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| 출처)「코스닥시장 상장규정」, 당사 정기보고서 |
| 주1) 상기 도표 중 (1)매출액 미달 요건 관련하여, 별도재무제표를 기준으로 합니다. 그 외 요건은 연결재무제표를 기준으로 합니다. |
| 주2) (2)법인세비용차감전계속사업손실 요건 관련하여, 자기자본은 비지배지분을 제외하지 않은 금액 기준을 적용합니다. (3)자본잠식 등, (4)자기자본 미달 요건 관련하여, 자기자본은 비지배지분을 제외한 지배기업지분금액 기준을 적용합니다. |
(1) 매출액 미달 여부 검토
| [최근 3개년 매출액] |
| (단위 : 백만원) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| 매출액 (별도) | 954 | 7,746 | 5,913 | 5,915 |
| 자료 : 당사 정기보고서 |
「코스닥시장 상장규정」 제53조 1항 1호에 따라 최근 사업연도의 매출액이 30억 미만일 경우 관리종목으로 지정됩니다. 상기한 바와 같이 당사는 기술성장특례 적용 기업으로서, 최근사업연도의 매출액 미달 요건으로 인한 관리종목 지정 유예를 받았으나, 현재는 유예기간이 종료되었습니다. 따라서 당사는 매년 매출액(K-IFRS 개별/별도 기준) 30억원 이상 달성해야 관리종목에 지정되지 않습니다. 당사의 별도 기준 매출액은 2022년 약 59억원, 2023년 약 59억원, 2024년 약 77억원으로, 최근 3개년 모두 30억원을 초과하여 관리종목 지정 사유에 해당되지 않습니다.
한편, 2025년 01월 21일 금융위원회와 금융감독원, 한국거래소, 금융투자협회, 자본시장연구원이 발표한 'IPO 및 상장폐지 제도 개선 방안'에 따르면 상장 유지를 위한 매출 요건이 강화되었습니다. 향후 시가총액이 600억원 미만인 코스닥 상장 법인은 2027년 50억원, 2028년 75억원, 2029년 100억원 이상의 매출을 달성해야합니다. 증권신고서 제출일 기준, 당사의 시가총액은 600억원 이상이기 때문에, 향후 현 수준의 시가총액을 유지할 경우 해당 사항이 없을 것으로 판단됩니다.
당사는 2022년 이후 매출액이 지속적으로 50억원을 상회하고 있으며, 현재 매출액 기준으로 관련 요건을 충족하고 있습니다. 다만, 향후 현재 수준보다 매출이 큰 폭으로 감소되어 매출액(별도 기준) 30억원을 유지하지 못하거나, 시가총액이 600억원 미만으로 떨어지고 당사의 매출액이 강화된 기준에 하회할 경우 금융당국의 상장폐지 요건 강화 정책에 의해 2027년 이후 해당 사유가 발생할 수 있으니, 투자자 여러분께서는 이 점 유의하시기 바랍니다.
(2) 법인세비용차감전계속사업손실 발생 여부 검토
| [최근 3개년 법인세비용차감전계속사업손실] |
| (단위 : 백만원) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| (법인세비용차감전계속사업손실/자기자본)×100(%) | 12.8% | 16.4% | 51.9% |
42.7% |
| 법인세비용차감전계속사업손실 | 4,903 | 7,083 | 23,137 | 20,215 |
| 자기자본 | 38,279 | 43,182 | 44,517 | 47,260 |
| 출처) 당사 정기보고서 |
한편, 당사는 2023년 법인세비용차감전계속사업손실률이 51.9%까지 증가하였으며 관리종목 지정 리스크가 발생하였습니다(최근 3개년 중 1년 해당됨). 2024년 법차손률이 16.4%를 기록하며 대폭 개선되었으나, 2025년 사업연도말의 법차손률이 50%를 상회할 경우 최근 3사업연도중 2사업연도(2023년, 2025년)의 법차손률이 50%를 상회함에 따라 관리종목으로 지정될 수 있습니다.
2023년 당사의 연결대상 종속회사인 HLB바이오코드(구.주식회사 크로엔)의 매출 및 손익이 크게 악화되었고, 그에 따른 연결 손실을 인식함으로써 법인세비용차감전계속사업손실률이 51.9%까지 증가하였습니다. 2024년 HLB바이오코드의 손실이 지속될 것으로 예상되어, 계속해서 지분을 보유할 경우 당사의 재무적 악화 및 관리종목 지정 리스크에 여전히 영향을 미칠 것으로 예상되었고, 2024년 5월 HLB바이오코드 주식회사 지분 매각을 결정하였습니다. 이를 통해 연결 손실 인식을 방지하고, 동시에 98억원의 처분이익이 발생하며 2024년 법차손률 16.4%로 큰 폭으로 개선되었습니다. 다만, 2024년 지분 매각으로 인한 처분이익 98억원의 경우 일회성 이익에 해당하여 당사의 2025년 영업수익성에 미치는 영향은 미미한 것으로 판단됩니다. 따라서, 2025년 법인세비용차감전계속사업손실이 전년도 대비 증가할 가능성이 있으니 투자자들께서는 이 점을 유의하여 주시기 바랍니다.
현재 당사는 OSCA의 국내 라이선스 아웃 계약에 따른 단계별 선급기술료 수취 및 임상비용 절약, 일본 재생의료 매출 발생 등 수익성 향상을 위해 노력중입니다. 동시에, 금번 유상증자를 통한 자본규모 확충을 기대 중이며, 계획한 수익성 향상 노력과 자금조달이 모두 성공적으로 이루어질 경우 2025년 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 발생할 가능성은 낮을 것으로 판단됩니다. 다만, 이러한 당사의 노력에도 불구하고 사업환경이 급격히 악화되어 당사의 임상 및 연구개발 지연으로 매출 저조 등 재무성과를 나타내지 못하거나 유상증자에 실패하여 법인세비용차감전계속사업손실률이 50%를 상회할 경우 관리종목으로 지정 요건에 해당할 수 있으니 투자자들께서는 이점 유의하시기 바랍니다.
(3) 자본잠식 여부 검토
| [자본잠식 여부 검토] |
| (단위 : 백만원) |
| 구분 | 2025년 1분기말 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| 비지배지분 제외 자기자본(연결) | 38,279 | 43,182 | 48,012 | 49,370 |
| 자기자본(연결) | 38,279 | 43,182 | 44,518 | 47,260 |
| 자본금 | 28,027 | 28,027 | 28,003 | 19,003 |
| 자본잠식률 | - | - | - | - |
| 자본잠식여부 | 미해당 | 미해당 | 미해당 | 미해당 |
| 출처) 당사 정기보고서 |
| 주1) 자본잠식률 = 1-{비지배지분 제외 자본총계 / 자본금} |
「코스닥시장 상장규정」 제53조 1항 4호에 따라 최근 사업연도 말을 기준으로 자본잠식률 50%이상인 경우 관리종목으로 지정됩니다. 당사는 최근 사업연도 말(2024년 말) 기준으로 자본잠식 상태가 아니며, 2025년 1분기말 기준으로도 자본잠식 요건에 의한 관리종목 지정 요건에 해당하지 않습니다. 또한, 본 유상증자 후에는 자본금 대비 자기자본 확대가 다시 한번 이루어지므로 2025년 중 자본잠식에 의한 관리종목 지정 위험은 대응 가능할 것으로 판단하고 있습니다. 다만, 대규모 손실 발생시에는 자기자본이 크게 감액될 경우 자본잠식으로 인한 관리종목 지정 가능성이 있으므로 투자자 여러분들께서는 이 점 유의하시기 바랍니다.
(4) 시가총액 미달여부 검토
| [최근 3개년 시가총액 추이] |
| (단위: 백만원) |
| 구분 | 시가총액(최고) | 시가총액(최저) |
|---|---|---|
| 2025년 1분기 | 135,090 | 109,306 |
| 2024년 | 200,258 | 78,812 |
| 2023년 | 133,971 | 49,699 |
| 2022년 | 160,477 | 95,414 |
| 출처) KRX 정보데이터시스템 |
「코스닥시장 상장규정」 제53조 1항 5호에 따라 보통주 시가총액 40억원 미만 30일간 지속되는 경우 관리종목으로 지정됩니다. 당사의 2025년 1분기 시가총액은 최고 1,351억원, 최저 1,093억원입니다. 또한 최근 3개년 최저 시가총액은 2022년 954억원, 2023년 497억원, 2024년 788억원으로 40억원 미만을 기록한 바 없어 해당 관리종목 지정요건에 해당하지 않습니다.
한편, 2025년 01월 21일 금융위원회와 금융감독원, 한국거래소, 금융투자협회, 자본시장연구원이 발표한 'IPO 및 상장폐지 제도 개선 방안'에 따르면 상장 유지를 위한 시가총액 요건이 강화되었습니다. 향후 코스닥 상장 법인은 2026년 150억원, 2027년 200억원, 2028년 300억원 이상의 시가총액을 달성해야합니다. 증권신고서 제출일 기준, 당사의 시가총액은 2028년 최종 상향 목표치인 300억원 이상으로, 현재 수준의 시가총액을 유지할 경우 해당 사항은 없을 것으로 판단됩니다. 다만, 향후 당사의 시가총액이 감소하여 강화된 기준에 하회할 경우 금융당국의 상장폐지 요건 강화 정책에 의해 상장폐지 사유에 해당될 수 있으니 투자자 여러분께서는 이 점 유의하시기 바랍니다.
(5) 정기보고서 미제출 여부 검토
「코스닥시장 상장규정」제53조 1항 6호에 따라 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않은 경우 관리종목으로 지정됩니다. 당사는 최근일 현재까지 정기보고서를 법정제출기한 내에 제출한 바 관리종목 지정요건에 해당하지 않습니다.
(6) 지배구조 미달 여부 검토
「코스닥시장 상장규정」 제53조 1항 7호에 따라 최근 사업연도 사업보고서상 A)사외이사의 수가 법에서 정하는 수에 미달, B) 법에서 정하는 감사위원회를 구성하지 않거나 구성요건을 충족하지 아니하는 경우 관리종목으로 지정됩니다.
당사는 벤처기업에 해당되며, 2025년 1분기말 기준 자산총액이 약 502억원으로 상법 시행령」 제34조제1항1호에 따라 자산총액이 1천억원 미만입니다. 이에 따라, 사외이사 선임 및 감사위원회 구성 의무가 면제되기 때문에, 현재까지는 지배구조 요건 미달에 따른 관리종목 지정 요건에 해당하지 않습니다.
(7) 거래량 미달 여부 검토
「코스닥시장 상장규정」 제53조 1항 8호에 따라 분기월평균거래량이 유동주식수의 1%에 미달하는 경우 관리종목으로 지정됩니다. 다만, 다음 어느 하나에 해당하는 경우에는 이 호에 적용 받지 않습니다. 가) 신규 신규상장법인의 경우. 다만, 신규상장일이 속하는 분기에 한정하는 경우, 나) 분기의 월평균거래량이 1만주 이상인 경우. 이 경우 보통주식 상장법인이 액면주식을 발행한 때에는 액면가액 5,000원을 기준, 다) 세칙으로 정하는 소액주주가 소유한 보통주식의 총수가 유동주식수의 100분의 20 이상이고, 해당 소액주주의 수가 300명 이상인 경우. 이 경우 소액주주가 소유한 주식 수와 소액주주의 수는 최근 사업연도 말을 기준으로 하되, 최근 사업연도 말 이후 주주명부를 폐쇄한 경우에는 그 폐쇄시점 현재를 기준으로 거래소에 제출한 주주명부 및 「주식·사채 등의 전자등록에 관한 법률」에 따른 소유자명세를 기준으로 하는 경우입니다.
| [관리종목 지정 관련 주요 거래량 검토] | |
| (단위 : 주, %) | |
| 구분 | 2025년 1분기 |
|---|---|
| 월평균 거래량 | 381,396 |
| 분기말 유동주식수 | 56,054,149 |
| 비율 (주1) | 0.68% |
| 출처) 한국거래소 정보데이터시스템, Dart 전자공시시스템 주1): 비율 = 분기월평균거래량 / 유동주식수 |
당사는 2025년 1분기 기준 월평균거래량이 381,396주로 유동주식수의 0.68%에 해당하여 1% 이하이지만 소액주주 지분율 78.75%, 소액주주 수 18,315명임에 따라 상기 다) 항목에 해당되어 거래량 미달에 의한 관리종목 지정요건에 해당하지 않습니다.
(8) 주식분산 미달 여부 검토
「코스닥시장 상장규정」 제53조 1항 9호에 따라 최근 사업연도말 소액주주가 200인 미만이거나 소액주주지분이 20% 미만일 경우 관리종목으로 지정됩니다.
당사는 최근사업연도말(2024년) 소액주주 지분율 77.58%, 소액주주 수 19,291명이며, 2025년 1분기 기준 소액주주 지분율 78.75%, 소액주주 수 18,315명임에 따라 주식분산 미달에 의한 관리종목 지정요건에 해당하지 않습니다.
(9) 기타사항
「코스닥시장 상장규정」 제53조 1항 10호에서 13호까지에 따라 회생절차개시신청, 파산신청, 상장폐지사유발생, 재무관리기준 위반 요건에 해당하는 경우 관리종목으로 지정됩니다. 당사는 현재까지는 상기 기타사항 관련하여, 관리종목 지정 요건에 해당되지 않습니다.
관리종목 지정사유 확인 당일에는 코스닥시장에서의 거래는 정지되며, 이를 기한 내에 해결하지 못한다면 코스닥시장 상장폐지 사유에 해당하여, 당사 주식은 향후 장내에서 거래가 이루어지지 못할 수 있습니다. 투자자 여러분들께서는 당사의 주식이 상장폐지될 경우, 투자금액을 회수하지 못하게 될 수도 있는 점을 반드시 유의하여 주시기 바랍니다. 이에 투자자 여러분들께서는 코스닥시장에서의 관리종목, 상장폐지와 관련된 규정을 반드시 유의하시고, 당사의 영업 수익성 추이에 대하여 지속적으로 모니터링하시기 바랍니다.
(10) 상장폐지 요건 강화
| [IPO 및 상장 폐지 제도개선 방안 및 해당여부 검토] |
| 구 분 | IPO 및 상장 폐지 제도개선 방안 | 상장폐지 지정요건 적용여부 |
회사현황 | |
|---|---|---|---|---|
| 사업연도 | 금액(백만원) / 내용 | |||
| (1) 시가총액 요건 기준 강화 | 정량요건으로서 시장평가 관련 시가총액 기준을 단계적으로 상향하여 코스피 500억원, 코스닥 300억원을 목표로 합니다. - 코스피 : 50억원(현행) → 200억원(2026년) → 300억원(2027년) → 500억원(2028년) - 코스닥 : 40억원(현행) → 150억원(2026년) → 200억원(2027년) → 300억원(2028년) |
현재 미해당 | 2024년 12월 31일 |
시가총액 : 113,229백만원 |
| 증권신고서 제출일 전일 기준 |
시가총액 : 84,754백만원 |
|||
| (2) 매출액 요건 기준 강화 | 정량요건으로서 기업실적 관련 매출액 기준을 단계적으로 상향하여 코스피 300억원(시가총액 1,000원 미만 기업만 적용), 코스닥 100억원(시가총액 600억원 미만 기업만 적용)을 목표로 합니다. - 코스피 : 50억원(현행) → 100억원(2027년) → 200억원(2028년) → 300억원(2029년) - 코스닥 : 30억원(현행) → 50억원(2027년) → 75억원(2028년) → 100억원(2029년) |
현재 미해당 | 2024년말 | 매출액 : 7,746백만원 (K-IFRS 별도기준) |
| 2025년 1분기말 | 매출액 : 954백만원 (K-IFRS 별도기준) |
|||
| (3) 감사의견 미달 요건 기준 강화 | - 2회 연속 감사의결 미달시 즉시 상장폐지 : 감사의견 미달(한정, 부적정, 의견거절)의 경우 2회 연속발생시 즉시 상장폐지되고(회생 ·워크아웃기업에 대해서는 예외인정), 이의신청은 허용되지 않습니다. | 현재 미해당 | 2024년말 | 해당사항 없음 |
| 2023년말 | 해당사항 없음 | |||
| 출처) 금융위원회, 당사 정기보고서 |
또한, 2025년 01월 21일, 정부와 유관기관(금융위원회, 금융감독원, 한국거래소, 금융투자협회)은 주식시장의 질적수준 제고를 위한「IPO 및 상장 폐지 제도개선 방안」을 발표하였습니다. 이 중 상장폐지 제도개선 방안은 상장유지 요건을 강화하고, 절차는 효율화함으로써 주식시장 내 저성과 기업을 적시에 퇴출시키고 상장기업의 밸류업을 주요 목적으로 하고 있습니다. 이와 같이 상장폐지 요건이 강화됨에 따라 당사의 영업환경 악화, 재무요건 악화 등을 원인으로 강화된 상장폐지 요건에 해당되어 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있음을 투자자분들은 유의하시기 바랍니다.
당사의 최근 3년간 별도기준 매출액 중 2022년과 2023년은 각각 59.2억원, 59.1억원으로 2028년부터 적용되는 매출요건 75억을 하회합니다. 한편, 2024년 매출액은 77.5억원으로, 2029년부터 적용되는 매출요건 100억원을 하회합니다. 다만, 당사의 최근 시가총액은 2028년부터 적용되는 최소 시가총액 요건인 600억원을 상회하고 있기 때문에, 현재 시가총액 수준을 유지한다면 해당 사항은 없을 것으로 보입니다. 그러나, 향후 당사의 매출 성장성이 둔화되어 매출이 악화되고 시가총액 수준이 지속적으로 하락할 경우 금융당국의 강화된 상장폐지 요건에 해당될 가능성이 있습니다. 투자자들께서는 투자 판단 시 최근 상장폐지 요건 강화에 따른 상장폐지 위험에 대해서 충분히 인지하시길 바랍니다.
한편, 비재무적 요건 중 감사의견 관련 기준도 강화될 예정입니다. 현재는 감사의견 거절 또는 부적정 발생 시 이의신청이 가능하며, 이후 사업연도까지 개선기간이 부여되는 완화된 제도가 적용되고 있으나, 2025년 7월 1일부로 개정안이 시행되면 2개 사업연도 연속으로 감사의견이 미달되는 경우 이의신청 없이 곧바로 상장폐지 절차가 진행됩니다.
금융당국은 이와 같은 제도 강화를 통해 상장기업의 회계 투명성과 신뢰성을 제고하고, 시장 건전성을 확보하고자 하고 있으며, 이에 따라 향후 유가증권시장 및 코스닥시장에서 상장폐지 요건은 점차 엄격하게 적용될 전망입니다. 이에 따라 현행 기준으로 당사는 어떠한 재무적 또는 비재무적 상장폐지 요건에도 해당되지 않으나, 당사가 이후 영업실적의 악화나 재무구조의 급격한 변화 등에 의해 강화된 상장폐지 요건에 해당될 가능성도 존재하므로, 투자자께서는 이 점 유의하여 주시기 바랍니다.
당사는 증권신고서 제출일 전일 기준 「코스닥시장 상장규정」 상 관리종목 지정 및 상장폐지요건에 해당하는 경우는 없습니다. 하지만 당사는 코스닥시장에서의 주요 관리종목 지정 요건 중 법인세비용차감전계속사업손실 요건에 해당될 수 있는 위험이 큰 상태입니다. 2025년 사업연도말 자기자본총계 대비 50%를 초과하는 법인세비용차감전계속사업손실이 발생할 경우 당사는 관리종목으로 지정됩니다. 또한, 향후 당사의 시가총액이 600억 원 미만으로 떨어져 당사의 매출액이 강화된 기준에 하회할 경우 금융당국의 상장폐지 요건 강화 정책에 의해 해당 사유가 발생할 수 있으며, 향후 적자 상태가 지속될 경우 관리종목 및 상장폐지 요건에 해당될 가능성이 존재하므로, 투자자께서는 이 점 유의하시기 바랍니다.
(주12) 정정 전
| 사. GMP를 포함한 생산시설 관련 위험 당사는 신축 GMP공장을 본격적인 가동 시, 판매용 완제품 생산을 통해 시장 수요 충족과 더불어 대량생산으로 원가 절감으로 수익성 확대를 이룰 것으로 기대하였으나, 2019년 10월 '퓨어스템-에이디 주' 3상 결과가 통계적 유의성 입증에 실패하면서 당사가 계획했던 GMP공장의 본격 가동 일정이 미뤄지게 되었습니다. 이후 2021년 05월 임상 3상 재도전을 위해 환자모집에 힘썼지만, 코로나19 확산에 따라 원활한 환자모집이 되지 않으면서 일정이 지연되었습니다. 기존에 2022년 12월까지 예정되어있던 환자 모집기간을 연장하여 2023년 08월 최종인원 315명의 환자를 모두 투약하였습니다. 다만, 12주차 시점 위약 대비 시험군과 대조군 간 유효성 차이를 입증하지 못하였습니다. 이에 기존 단회투여에서 반복투여 방식으로 프로토콜을 수정하여 2024년 11월 임상 1/2a상 IND를 변경승인신청하였으나, 식품의약품안전처(MFDS)의 추가 자료보완 요청을 기한 내 회신이 어려울 것으로 판단하여 자진취하 신청을 하였습니다. 그리고 2025년 4월 퓨어스템-에이디주의 반복투여 제1/2a 임상시험계획변경승인신청을 하였으며, 2025년 하반기 임상1/2a상 개시를 계획하고 있습니다. 이와 같이 아토피 피부염 치료제 상업화에 대한 허가 일정이 또 한번 장기간 미루어질 경우, 당사 GMP공장의 고정비는 당사의 재무구조 및 수익성에 부정적인 영향을 미칠 것으로 예상됩니다. 또한, 당사의 신축 GMP공장을 활용한 의약품 위탁개발생산(CDMO)이라는 신사업의 매출 증대 전략이 수주 지연 및 GMP공장 시설 문제 등의 이유로 계획대로 진행되지 않는다면, 상기 생산시설의 연구인력 및 생산력 충원으로 인해 과도한 고정비의 지출이 선행되었기 때문에, 이는 당사의 재무구조 및 수익성에 부정적인 영향이 장기간 이어질 가능성이 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
당사는 2018년 11월에 준공을 시작하여 신축 GMP공장을 2019년 05월에 완공하였습니다. 당시 국내 줄기세포 치료제 생산 공장으로서는 가장 큰 규모로, 당사의 기존 아토피 피부염 치료제의 상업화 허가 일정에 맞춘 완공이었습니다. 당사는 신축 GMP공장을 본격적인 가동 시, 판매용 완제품 생산을 통해 시장 수요 충족과 더불어 대량생산으로 원가 절감으로 수익성 확대를 이룰 것으로 기대하였으나, 2019년 10월 '퓨어스템-에이디 주' 3상 결과가 통계적 유의성 입증에 실패하면서 당사가 계획했던 GMP공장의 본격 가동 일정이 미뤄지게 되었습니다. 이후 2021년 05월 임상 3상 재도전을 위해 환자모집에 힘썼지만, 코로나19 확산에 따라 원활한 환자모집이 되지 않으면서 일정이 지연되었습니다. 기존에 2022년 12월까지 예정되어있던 환자 모집기간을 연장하여 2023년 08월 최종인원 308명의 환자를 모두 투약하였습니다. 다만, 12주차 시점 위약 대비 시험군과 대조군 간 유효성 차이를 입증하지 못하였습니다.
(중략)
당사는 GMP공장의 활용도를 높이고자 2020년 12월 식약처로부터 첨단바이오의약품 제조업 허가 승인을 받았으며, 이에 「첨단재생바이오법」 규정에 따라 사람 또는 동물의 줄기세포와 조혈모세포, 체세포 등을 채취·검사 처리해 재생의료기관에 공급할 수 있게 되었습니다. 또한, 당사는 2020년 07월 의약품 제조에 대한 허가를 취득했으며, 인체 세포 등의 관리업 허가 취득과 재생의료기관의 임상 연구를 위한 세포 처리시설 허가도 받을 계획입니다. 이에 당사는 본격적으로 의약품 위탁개발생산(CDMO)을 신사업으로 체택하여 2021년말부터 매출이 발생하고 있습니다.
다만, 당사의 신축 GMP공장을 활용한 의약품 위탁개발생산(CDMO)이라는 신사업의 매출 증대 전략이 수주 지연 및 GMP공장 시설 문제 등의 이유로 계획대로 진행되지 않는다면, 상기 생산시설의 연구인력 및 생산력 충원으로 인해 과도한 고정비의 지출이 선행되었기 때문에, 이는 당사의 재무구조 및 수익성에 부정적인 영향이 장기간 이어질 가능성이 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
(주12) 정정 후
| 사. GMP를 포함한 생산시설 관련 위험 당사는 2018년 11월에 준공을 시작하여 신축 GMP공장을 2019년 05월에 완공하였습니다. 당시 국내 줄기세포 치료제 생산 공장으로서는 가장 큰 규모로, 당사의 기존 아토피 피부염 치료제(퓨어스템-에이디주)의 상업화 허가 기대 일정에 맞춘 완공이었습니다. 당사는 퓨어스템-에이디주가 임상 3상에서 유의성이 달성되었을 경우, 신축 GMP공장을 본격적으로 가동하며 퓨어스템-에이디주의 판매용 완제품을 생산함으로써 시장 수요 충족과 더불어 대량생산으로 원가 절감으로 수익성 확대를 이룰 것으로 기대하였으나, 2019년 10월 퓨어스템-에이디주 3상 결과가 통계적 유의성 입증에 실패하면서 당사가 계획했던 GMP공장의 본격 가동 일정이 미뤄지게 되며, 가동률이 저하되었습니다. 이와 같이 아토피 피부염 치료제 상업화에 대한 허가 일정이 또 한번 장기간 미루어질 경우, 당사 GMP공장의 고정비는 당사의 재무구조 및 수익성에 부정적인 영향을 미칠 것으로 예상됩니다. 당사는 GMP공장의 활용도를 높이고 고정비 부담을 낮추기 위해 완공 이후 해당 GMP 공장에서 제대혈 유래 줄기세포 배양액, 줄기세포 배양 배지 등을 직접 생산하여 줄기세포 치료제를 제조하여 당사의 주요 파이프라인의 전임상시험 및 임상시험에 사용하고 있습니다. 이에 줄기세포 배양액과 줄기세포 배양 배지 생산을 위한 구획을 구분하여 생산 라인이 가동되고 있습니다. 또한, 당사는 GMP공장의 활용도를 높이고자 2020년 12월 식약처로부터 첨단바이오의약품 제조업 허가 승인을 받았으며, 이에 「첨단재생바이오법」 규정에 따라 사람 또는 동물의 줄기세포와 조혈모세포, 체세포 등을 채취·검사 처리해 재생의료기관에 공급할 수 있게 되었습니다. 다만, 당사의 신축 GMP공장을 활용한 주요 파이프라인 임상시험에 필요한 약물의 직접 생산 및 의약품 위탁개발생산(CDMO)이라는 신사업의 매출 증대 전략 등과 같은 당사의 노력에도 불구하고 수주 지연 및 GMP공장 시설 문제 등의 이유로 계획대로 진행되지 않는다면, 상기 생산시설의 연구인력 및 생산력 충원으로 인해 과도한 고정비의 지출이 선행되었기 때문에, 이는 당사의 재무구조 및 수익성에 부정적인 영향이 장기간 이어질 가능성이 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
당사는 2018년 11월에 준공을 시작하여 신축 GMP공장을 2019년 05월에 완공하였습니다. 당시 국내 줄기세포 치료제 생산 공장으로서는 가장 큰 규모로, 당사의 기존 아토피 피부염 치료제(퓨어스템-에이디주)의 상업화 허가 기대 일정에 맞춘 완공이었습니다. 당사는 퓨어스템-에이디주가 임상 3상에서 유의성이 달성되었을 경우, 신축 GMP공장을 본격적으로 가동하며 퓨어스템-에이디주의 판매용 완제품을 생산함으로써 시장 수요 충족과 더불어 대량생산으로 원가 절감으로 수익성 확대를 이룰 것으로 기대하였으나, 2019년 10월 퓨어스템-에이디주 3상 결과가 통계적 유의성 입증에 실패하면서 당사가 계획했던 GMP공장의 본격 가동 일정이 미뤄지게 되며, 가동률이 저하되었습니다. 이후 2021년 05월 퓨어스템-에이디주의 임상 3상 재도전을 위해 환자모집에 힘썼지만, 코로나19 확산에 따라 원활한 환자모집이 되지 않으면서 일정이 지연되었습니다. 기존에 2022년 12월까지 예정되어있던 환자 모집기간을 연장하여 2023년 08월 최종인원 308명의 환자를 모두 투약하였습니다. 다만, 12주차 시점 위약 대비 시험군과 대조군 간 유효성 차이를 입증하지 못하였습니다.
(중략)
상기한 바와 같이 아토피 피부염 치료제(퓨어스템-에이디주)의 임상 3상 실패 및 이로 인한 상업화에 대한 허가 계획 차질에 따라 GMP 공장 가동률이 완공 당시 예상보다 매우 저하되었으나, 당사는 GMP공장의 활용도를 높이고 고정비 부담을 낮추기 위해 완공 이후 해당 GMP 공장에서 제대혈 유래 줄기세포 배양액, 줄기세포 배양 배지 등을 직접 생산하여 줄기세포 치료제를 제조하여 당사의 주요 파이프라인의 전임상시험 및 임상시험에 사용하고 있습니다. 이에 줄기세포 배양액과 줄기세포 배양 배지 생산을 위한 구획을 구분하여 생산 라인이 가동되고 있습니다. 또한, 당사는 GMP공장의 활용도를 높이고자 2020년 12월 식약처로부터 첨단바이오의약품 제조업 허가 승인을 받았으며, 이에 「첨단재생바이오법」 규정에 따라 사람 또는 동물의 줄기세포와 조혈모세포, 체세포 등을 채취·검사 처리해 재생의료기관에 공급할 수 있게 되었습니다. 또한, 당사는 2020년 07월 의약품 제조에 대한 허가를 취득했으며, 인체 세포 등의 관리업 허가 취득과 재생의료기관의 임상 연구를 위한 세포 처리시설 허가도 받을 계획입니다. 이에 당사는 본격적으로 의약품 위탁개발생산(CDMO)을 신사업으로 채택하여 2021년 말부터 매출이 발생하고 있습니다. 당사 GMP 공장의 생산시설 가동률 추이는 아래와 같습니다.
| [GMP 생산시설 가동률 추이] |
| 품 목 | 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | 2021년 |
|---|---|---|---|---|---|---|
|
줄기세포 배양액(주1) (단위: ℓ) |
생산능력 | 600 | 2,400 | 2,400 | 2,400 | 2,400 |
| 생산실적 | 386 | 1,140 | 855 | 188 | 191 | |
| 가 동 률 | 64.3% | 47.5% | 35.6% | 7.8% | 8.0% | |
|
세포배양 배지(주2) (단위: 개) |
생산능력 | 1,500 | 6,000 | 6,000 | 6,000 | 6,000 |
| 생산실적 | 0 | 1,469 | 3,242 | 1,871 | 2,240 | |
| 가 동 률 | 0.0% | 24.5% | 54.0% | 31.2% | 37.3% | |
| 세포배양 배지(주3) (단위: 개) |
생산능력 | 600 | 1,800 | - | - | - |
| 생산실적 | 0 | 379 | - | - | - | |
| 가 동 률 | 0.0% | 21.1% | - | - | - |
| 출처) | 당사 정기보고서 |
| (주1) | 월 200ℓ생산 가능합니다. |
| (주2) | 월 500개 생산 가능합니다. |
| (주3) | 월 200개 생산 가능합니다. |
| (주4) | 2024년 기존 생산 설비를 활용하여 줄기세포 배양 배지(StemVie XF Supplments 제품)를 신규 생산하게 됨에 따라 추가된 내용입니다. |
다만, 당사의 신축 GMP공장을 활용한 주요 파이프라인 임상시험에 필요한 약물의 직접 생산 및 의약품 위탁개발생산(CDMO)이라는 신사업의 매출 증대 전략 등과 같은 당사의 노력에도 불구하고 수주 지연 및 GMP공장 시설 문제 등의 이유로 계획대로 진행되지 않는다면, 상기 생산시설의 연구인력 및 생산력 충원으로 인해 과도한 고정비의 지출이 선행되었기 때문에, 이는 당사의 재무구조 및 수익성에 부정적인 영향이 장기간 이어질 가능성이 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
(주13) 정정 전
특수관계자와의 주요 거래 내역은 다음과 같습니다.
| (단위: 천원) |
| 특수관계자 명칭 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | ||||
|---|---|---|---|---|---|---|---|---|
| 영업수익 등 | 영업비용 등 | 영업수익 등 | 영업비용 등 | 영업수익 등 | 영업비용 등 | 영업수익 등 | 영업비용 등 | |
| HLB바이오코드(주) | 2,268 | - | 9,353 | 816,966 | - | - | - | - |
| (주)프리모리스인터내셔널(주1) | 364,806 | 29,053 | 1,838,666 | 159,222 | 2,631,960 | 292,285 | 1,451,717 | 350,114 |
| (주)프리모리스테라퓨틱스 | 17,280 | 78,117 | 64,725 | 55 | 73,044 | 4 | 729,899 | - |
| 합 계 | 384,354 | 107,170 | 1,912,744 | 976,243 | 2,705,004 | 292,289 | 2,181,616 | 350,114 |
| 출처) 당사 정기보고서 |
| 주1) 당사는 특수관계자인 (주)프리모리스인터내셔널과 연간 상품공급계약을 맺고 있습니다. |
특수관계자 간 주요 채권ㆍ채무잔액은 다음과 같습니다.
| (단위: 천원) |
| 특수관계자 명칭 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 채권 | 채무 | 채권 | 채무 | 채권 | 채무 | 채권 | 채무 | |||||||||
| 매출채권 등 (주1) |
계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | 매출채권 등 | 계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | 매출채권 등 | 계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | 매출채권 등 | 계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | |
| HLB바이오코드(주) | 2,268 | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - |
| (주)프리모리스인터내셔널 | 172,992 | - | 10,453 | - | 403,923 | - | 14,160 | - | 417,682 | - | 21,062 | - | 549,527 | - | 35,753 | - |
| (주)프리모리스테라퓨틱스 | 67,555 | - | - | 2,000 | 49,375 | - | - | 2,000 | - | 13,409 | - | 3,333 | 510,047 | 400 | - | 11,333 |
| 합 계 | 242,815 | - | 10,453 | 2,000 | 453,298 | - | 14,160 | 2,000 | 417,682 | 13,409 | 21,062 | 3,333 | 1,059,574 | 400 | 35,753 | 11,333 |
| 출처) 당사 정기보고서 |
| 주1) 당분기말 채권은 대손충당금 차감전 금액이 기재되어 있습니다. 상기 특수관계자 채권에 설정되어 있는 대손충당금은 18백만원입니다. |
특수관계자와의 지분거래내역은 다음과 같습니다.
| (단위 : 천원) |
| 특수관계자 명칭 | 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|
| HLB바이오코드(주) | 보통주 유상증자(주1) | - | 989,998 | - | - |
| (주)프리모리스테라퓨틱스 | 보통주 무상수증(주2) | - | - | - | - |
| 출처) 당사 정기보고서 |
| 주1) 전기 중 보통주 유상증자로 183,333주를 취득하였습니다. |
| 주2) 전기까지 최대주주 및 당사 임원으로부터 프리모리스테라퓨틱스 보통주 87,200주를 무상수증받아, 취득금액은 영(0)입니다. |
특수관계자와의 자금거래내역은 다음과 같습니다.
| (단위 : 천원) |
| 특수관계자 명칭 | 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|
| HLB바이오코드(주) | 대여금 | - | 200,000 | - | - |
| (주)프리모리스테라퓨틱스 | 대여금 | - | 730,000 | - | - |
| (주)프리모리스테라퓨틱스 | 상환전환우선주 | - | - | 2,000,050 | - |
| 출처) 당사 정기보고서 |
당사는 특수관계자 등과 일부 자금거래가 발생하고 있으나, 특수관계자와 거래를 함에 있어 특별히 유리하거나 불리한 조건을 제시하는 등 거래상대방에 따라 계약조건을 달리한 사실이 없으며, 특수관계자와 계약을 체결할 때 통상 시장가로 계약을 체결하고 있습니다. 하지만 당사의 적법한 절차 및 법규 준수에도 불구하고 향후 당사와 특수관계자 간의 부적절한 거래가 발생될 가능성을 완전히 배제할 수 없으니 투자자께서는 이점 유의하시어 투자에 임하시기 바랍니다.
(주13) 정정 후
당사의 2025년 1분기말 기준 특수관계자에 대한 영업수익은 3.8억원으로 전체 매출액 9.5억원 가운데 약 40.3%를 차지합니다. 또한, 2024년 기준으로 전체 매출액 77.5억원 중 약 24.7%에 해당하는 19.1억원이 특수관계자 거래로부터 발생하였습니다. 한편, 2025년 1분기말 기준 특수관계자에 대한 영업비용은 약 10.7억원이 발생하였으며, 2024년에는 약 9.8억원이 발생하였습니다. 특수관계자와 주요 거래 발생 내역은 다음과 같습니다.
1) HLB바이오코드(주)
당사는 HLB바이오코드㈜에 의뢰하여 줄기세포, 오가노이드의 독성시험, 조직분석, 안정성 평가 등 다양한 비임상시험용역을 진행 중입니다. 이에 따른 용역 비용으로 2024년 약 8억원의 비용이 발생하였습니다. 한편, 2024년 및 2025년 발생한 영업수익은 2022년 HLB바이오코드(주)가 당사로부터 대여한 대여금 잔액에 대한 이자수익입니다.
2) (주)프리모리스인터내셔널
(주)프리모리스인터내셔널은 당사의 줄기세포 화장품, 샴푸 및 줄기세포 배양액 등의 유통을 담당하며 2023년 26억원, 2024년 18억원, 2025년 1분기 3억원의 매출거래가 발생하였습니다. 특히, 당사의 줄기세포 화장품 단독 유통 채널로서, 2024년 전체 매출의 23.7%, 2025년 1분기의 38.2%가 발생하는 등 당사의 매출에 기여하는 비중이 상대적으로 높습니다. 한편, 영업비용은 당사와 H&B 사업부 사무실 공동사용에 대한 임차료 및 기본 관리비 지급 과정에서 발생하였습니다.
3) (주)프리모리스테라퓨틱스
관계회사인 (주)프리모리스테라퓨틱스에 대해서는 2022년 7.29억원, 2023년 7.3천만원의 매출이 발생하였으며, 이는 2021~2023년 진행된 CDMO 프로젝트 관련 매출입니다. 2024년과 2025년 1분기에는 각각 6.4천만원, 1.7천만원의 매출이 발생하였으며, 이는 CDMO 프로젝트 완료 이후 MCB(Master Cell Bank) 세포보관료 및 품질시험 등으로 인한 매출, 대여금에 대한 이자수익, 사무실 임대에 의한 수입임대료에서 발생하였습니다. 한편, 당사의 (주)프리모리스테라퓨틱스에 대한 영업비용은 2025년 1분기 7.8천만원으로 증가하였는데, 이는 엑소좀 관련 위탁연구용역비 약 6천만원과 당사가 (주)프리모리스테라퓨틱스로부터 받아야하는 외상매출금 및 미수금 대한 대손충당금 약 2천만원 설정에 기인합니다.
| [최근 3개년 특수관계자와의 영업수익 및 영업비용 발생 내역] |
| (단위: 천원) |
| 특수관계자 명칭 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | ||||
|---|---|---|---|---|---|---|---|---|
| 영업수익 등 | 영업비용 등 | 영업수익 등 | 영업비용 등 | 영업수익 등 | 영업비용 등 | 영업수익 등 | 영업비용 등 | |
| HLB바이오코드(주) | 2,268 | - | 9,353 | 816,966 | - | - | - | - |
| (주)프리모리스인터내셔널(주1) | 364,806 | 29,053 | 1,838,666 | 159,222 | 2,631,960 | 292,285 | 1,451,717 | 350,114 |
| (주)프리모리스테라퓨틱스 | 17,280 | 78,117 | 64,725 | 55 | 73,044 | 4 | 729,899 | - |
| 합 계 | 384,354 | 107,170 | 1,912,744 | 976,243 | 2,705,004 | 292,289 | 2,181,616 | 350,114 |
| 출처) 당사 정기보고서 |
| 주1) 당사는 특수관계자인 (주)프리모리스인터내셔널과 연간 상품공급계약을 맺고 있습니다. |
당사는 위와 같이 특수관계자들과 다양한 매출, 매입 관련 거래가 발생하고 있으며, 이에 따라 매출채권, 미수금, 미지급금 등의 채권 및 채무가 발생합니다. 2025년 1분기말 당사의 특수관계자에 대한 채권은 총 약 2.4억원, 채무는 약 0.1억원입니다. 또한, 2024년말 기준 당사의 특수관계자에 대한 채권은 약 4.5억원, 채무는 약 1.6억원이었습니다. 특히, (주)프리모리스인터내셔널의 경우 당사 화장품 및 줄기세포 배양액의 주요 유통사로서 2024년 4억원, 2025년 1분기 1억7천만원의 상거래채권이 발생하였습니다. 한편,(주)프리모리스테라퓨틱스의 2022,2023년 계약자산 및 계약이행원가는 2023년 종료된 CDMO 프로젝트 진행시 발생하였습니다. 2024년과 2025년 1분기 발생한 계약부채의 경우 CDMO 프로젝트 종료 이후 MCB(Master Cell Bank) 세포보관료에 대해 매 3개월마다 계약을 갱신하여 발생한 보관료 선수금액입니다. 특수관계자 간 주요 채권ㆍ채무잔액은 다음과 같습니다.
| [최근 3개년 특수관계자와의 채권, 채무 발생 내역] |
| (단위: 천원) |
| 특수관계자 명칭 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 채권 | 채무 | 채권 | 채무 | 채권 | 채무 | 채권 | 채무 | |||||||||
| 매출채권 등 (주1) |
계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | 매출채권 등 | 계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | 매출채권 등 | 계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | 매출채권 등 | 계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | |
| HLB바이오코드(주) | 2,268 | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - |
| (주)프리모리스인터내셔널 | 172,992 | - | 10,453 | - | 403,923 | - | 14,160 | - | 417,682 | - | 21,062 | - | 549,527 | - | 35,753 | - |
| (주)프리모리스테라퓨틱스 | 67,555 | - | - | 2,000 | 49,375 | - | - | 2,000 | - | 13,409 | - | 3,333 | 510,047 | 400 | - | 11,333 |
| 합 계 | 242,815 | - | 10,453 | 2,000 | 453,298 | - | 14,160 | 2,000 | 417,682 | 13,409 | 21,062 | 3,333 | 1,059,574 | 400 | 35,753 | 11,333 |
| 출처) 당사 정기보고서 |
| 주1) 당분기말 채권은 대손충당금 차감전 금액이 기재되어 있습니다. 상기 특수관계자 채권에 설정되어 있는 대손충당금은 18백만원입니다. |
한편, 당사는 2024년 유상증자에 참여하여 HLB바이오코드㈜(구.㈜크로엔) 보통주 183,333주를 약 9.9억원에 취득한 사실이 있습니다. 당사는 자회사였던 HLB바이오코드㈜ 지분을 HLB바이오스텝에 일부 매각하면서 경영권을 이전하였습니다. 경영권 이전 후에도 오가노이드 활용 동물대체시험법 및 오가노이드 치료제 연구개발 등 업무 협업 유지, 사업 시너지를 발휘하고자 후속하여 진행된 HLB바이오코드㈜ 유상증자에 참여하였고, 현재 22.15%의 지분을 보유하고 있습니다. 특수관계자와의 지분거래내역은 다음과 같습니다.
| [최근 3개년 특수관계자와의 지분거래내역] |
| (단위 : 천원) |
| 특수관계자 명칭 | 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|
| HLB바이오코드(주) | 보통주 유상증자(주1) | - | 989,998 | - | - |
| (주)프리모리스테라퓨틱스 | 보통주 무상수증(주2) | - | - | - | - |
| 출처) 당사 정기보고서 |
| 주1) 전기 중 보통주 유상증자로 183,333주를 취득하였습니다. |
| 주2) 전기까지 최대주주 및 당사 임원으로부터 프리모리스테라퓨틱스 보통주 87,200주를 무상수증받아, 취득금액은 영(0)입니다. |
2025년 1분기 기준 당사의 특수관계인에 대한 대여금 잔액은 총 9.3억원 입니다. 당사는 2022년 당시 종속기업인 HLB바이오코드(주)(구.(주)크로엔)의 운영자금 지원 목적으로 6억원을 대여한 바 있습니다. 해당 대여금은 2023년까지 매분기 1억원씩 상환되었으며, 2025년 1분기 기준 잔액은 2억원 입니다. 2025년말 만기 도래 예정이며, 해당 대여금에 대해서 당좌대출이자율을 적용한 이자를 수취하고, 대여 원금 잔액을 상환받을 예정입니다.
또한, 당사는 관계회사인 ㈜프리모리스테라퓨틱스의 운영자금 지원 목적으로 2024년 2월 4억 5천만원, 9월 9천만원, 10월 1억 9천만원을 대여하며, 총 7억 3천만원을 대여한 바 있습니다. 향후 대여기간 만료 시, 당사는 해당 대여금에 대해 당좌대출이자율을 적용한 이자를 수취하고, 대여 원금 전액을 상환받을 예정입니다. 한편, 당사는 2023년 2월 ㈜프리모리스테라퓨틱스와 기술 및 사업 시너지를 발휘하고자 2023년 2월 8일 상환전환우선주 11,765주를 약 20억원에 취득하였습니다. 특수관계자와의 자금거래내역은 다음과 같습니다.
| [최근 3개년 특수관계자와의 자금거래내역 발생 내역] |
| (단위 : 천원) |
| 특수관계자 명칭 | 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|
| HLB바이오코드(주) | 대여금 | - | - | - | 600,000 |
| (주)프리모리스테라퓨틱스 | 대여금 | - | 730,000 | - | - |
| (주)프리모리스테라퓨틱스 | 상환전환우선주 | - | - | 2,000,050 | - |
| 출처) 당사 정기보고서 |
| 주1) 대여금 최초 발생 시점 기준입니다. |
| 주2) 2025년 1분기 기준 HLB바이오코드(주)에 대한 대여금 잔액은 2억원입니다. |
한편, 「상법」 제542조의9(주요주주 등 이해관계자와의 거래) 제3항에 의하면 최근 사업연도 말 현재의 자산총액이 2조원 이상인 상장회사는 특수관계인과의 거래에 있어 이사회 승인을 받아야 하는 규정이 있습니다. 당사의 경우 최근 결산일인 2024년 말 연결 기준 총 자산규모가 약 560억원으로 동 조항에 해당되지 않아 특수관계인과의 거래에 있어 제한적인 규제를 적용받고 있습니다.
또한,「상법」제542조의9(주요주주 등 이해관계자와의 거래) 제1항에 따르면 상장회사는 주요주주 및 그의 특수관계인, 이사 및 집행임원, 감사에 대해서는 신용공여를 하여서는 안된다고 규정하고 있습니다. 다만, 동법 제2항에 따라 복리후생을 위한 이사 및 집행 임원 또는 감사에 대한 금전대여 등으로서 대통령령으로 정하는 신용공여나 그 밖에 상장회사의 경영건전성을 해칠 우려가 없는 금전대여 등으로서 대통령령으로 정하는 신용공여는 가능합니다. 「상법시행령」제35조제3항에 따르면 '대통령령으로 정하는 신용공여'란 회사의 경영상 목적을 달성하기 위하여 필요한 경우라고 규정하고 있고 그 대상을 회사의 지분율에 따라 제한하고 있습니다. 당사가 당사의 주요주주 및 주요주주의 특수관계인과의 자금거래와 관련하여 상법 충족 여부를 검토한 결과, 당사는 대여금 제공이 상법시행령 제35조 제3항 제1호 및 제2호에서 정하는 법인이 '경영상 목적을 달성하기 위하여 필요한 경우' 해당한다고 판단하였습니다. 이에 따라, 당사가 종속기업 및 관계기업을 대상으로 수행한 출자 및 금전대여는 「상법」 제542조의9 제2항 제3호에서 정한 신용공여 제한의 예외 사유인 '상장회사의 경영건전성을 해칠 우려가 없는 신용공여'에 해당하는 것으로 판단됩니다.
| 상법 제542조의9(주요주주 등 이해관계자와의 거래) |
|---|
| ① 상장회사는 다음 각 호의 어느 하나에 해당하는 자를 상대방으로 하거나 그를 위하여 신용공여(금전 등 경제적 가치가 있는 재산의 대여, 채무이행의 보증, 자금 지원적 성격의 증권 매입, 그 밖에 거래상의 신용위험이 따르는 직접적ㆍ간접적 거래로서 대통령령으로 정하는 거래를 말한다. 이하 이 조에서 같다)를 하여서는 아니 된다. <개정 2011. 4. 14.> 1. 주요주주 및 그의 특수관계인 2. 이사(제401조의2제1항 각 호의 어느 하나에 해당하는 자를 포함한다. 이하 이 조에서 같다) 및 집행임원 3. 감사 ② 제1항에도 불구하고 다음 각 호의 어느 하나에 해당하는 경우에는 신용공여를 할 수 있다.<개정 2011. 4. 14.> 1. 복리후생을 위한 이사ㆍ집행임원 또는 감사에 대한 금전대여 등으로서 대통령령으로 정하는 신용공여 2. 다른 법령에서 허용하는 신용공여 3. 그 밖에 상장회사의 경영건전성을 해칠 우려가 없는 금전대여 등으로서 대통령령으로 정하는 신용공여 ③ 자산 규모 등을 고려하여 대통령령으로 정하는 상장회사는 최대주주, 그의 특수관계인 및 그 상장회사의 특수관계인으로서 대통령령으로 정하는 자를 상대방으로 하거나 그를 위하여 다음 각 호의 어느 하나에 해당하는 거래(제1항에 따라 금지되는 거래는 제외한다)를 하려는 경우에는 이사회의 승인을 받아야 한다. 1. 단일 거래규모가 대통령령으로 정하는 규모 이상인 거래 2. 해당 사업연도 중에 특정인과의 해당 거래를 포함한 거래총액이 대통령령으로 정하는 규모 이상이 되는 경우의 해당 거래 ④ 제3항의 경우 상장회사는 이사회의 승인 결의 후 처음으로 소집되는 정기주주총회에 해당 거래의 목적, 상대방, 그 밖에 대통령령으로 정하는 사항을 보고하여야 한다. ⑤ 제3항에도 불구하고 상장회사가 경영하는 업종에 따른 일상적인 거래로서 다음 각 호의 어느 하나에 해당하는 거래는 이사회의 승인을 받지 아니하고 할 수 있으며, 제2호에 해당하는 거래에 대하여는 그 거래내용을 주주총회에 보고하지 아니할 수 있다. 1. 약관에 따라 정형화된 거래로서 대통령령으로 정하는 거래 2. 이사회에서 승인한 거래총액의 범위 안에서 이행하는 거래 [본조신설 2009. 1. 30.] |
| 상법시행령 제35조(주요주주 등 이해관계자와의 거래) |
| ① 법 제542조의9제1항 각 호 외의 부분에서 "대통령령으로 정하는 거래"란 다음 각 호의 어느 하나에 해당하는 거래를 말한다. 1. 담보를 제공하는 거래 2. 어음(「전자어음의 발행 및 유통에 관한 법률」에 따른 전자어음을 포함한다)을 배서(「어음법」 제15조제1항에 따른 담보적 효력이 없는 배서는 제외한다)하는 거래 3. 출자의 이행을 약정하는 거래 4. 법 제542조의9제1항 각 호의 자에 대한 신용공여의 제한(금전ㆍ증권 등 경제적 가치가 있는 재산의 대여, 채무이행의 보증, 자금 지원적 성격의 증권 매입, 제1호부터 제3호까지의 어느 하나에 해당하는 거래의 제한을 말한다)을 회피할 목적으로 하는 거래로서 「자본시장과 금융투자업에 관한 법률 시행령」 제38조제1항제4호 각 목의 어느 하나에 해당하는 거래 5. 「자본시장과 금융투자업에 관한 법률 시행령」 제38조제1항제5호에 따른 거래 ② 법 제542조의9제2항제1호에서 "대통령령으로 정하는 신용공여"란 학자금, 주택자금 또는 의료비 등 복리후생을 위하여 회사가 정하는 바에 따라 3억원의 범위에서 금전을 대여하는 행위를 말한다. ③ 법 제542조의9제2항제3호에서 "대통령령으로 정하는 신용공여"란 회사의 경영상 목적을 달성하기 위하여 필요한 경우로서 다음 각 호의 자를 상대로 하거나 그를 위하여 적법한 절차에 따라 이행하는 신용공여를 말한다. 1. 법인인 주요주주 2. 법인인 주요주주의 특수관계인 중 회사(자회사를 포함한다)의 출자지분과 해당 법인인 주요주주의 출자지분을 합한 것이 개인인 주요주주의 출자지분과 그의 특수관계인(해당 회사 및 자회사는 제외한다)의 출자지분을 합한 것보다 큰 법인 3. 개인인 주요주주의 특수관계인 중 회사(자회사를 포함한다)의 출자지분과 제1호 및 제2호에 따른 법인의 출자지분을 합한 것이 개인인 주요주주의 출자지분과 그의 특수관계인(해당 회사 및 자회사는 제외한다)의 출자지분을 합한 것보다 큰 법인 ④ 법 제542조의9제3항 각 호 외의 부분에서 "대통령령으로 정하는 상장회사"란 최근 사업연도 말 현재의 자산총액이 2조원 이상인 상장회사를 말한다. ⑤ 법 제542조의9제3항 각 호 외의 부분에서 "대통령령으로 정하는 자"란 제34조제4항의 특수관계인을 말한다. ⑥ 법 제542조의9제3항제1호에서 "대통령령으로 정하는 규모"란 자산총액 또는 매출총액을 기준으로 다음 각 호의 구분에 따른 규모를 말한다. 1. 제4항의 회사가 「금융위원회의 설치 등에 관한 법률」 제38조에 따른 검사 대상 기관인 경우: 해당 회사의 최근 사업연도 말 현재의 자산총액의 100분의 1 2. 제4항의 회사가 「금융위원회의 설치 등에 관한 법률」 제38조에 따른 검사 대상 기관이 아닌 경우: 해당 회사의 최근 사업연도 말 현재의 자산총액 또는 매출총액의 100분의 1 ⑦ 법 제542조의9제3항제2호에서 "대통령령으로 정하는 규모"란 다음 각 호의 구분에 따른 규모를 말한다. 1. 제4항의 회사가 「금융위원회의 설치 등에 관한 법률」 제38조에 따른 검사 대상 기관인 경우: 해당 회사의 최근 사업연도 말 현재의 자산총액의 100분의 5 2. 제4항의 회사가 「금융위원회의 설치 등에 관한 법률」 제38조에 따른 검사 대상 기관이 아닌 경우: 해당 회사의 최근 사업연도 말 현재의 자산총액 또는 매출총액의 100분의 5 ⑧ 법 제542조의9제4항에서 "대통령령으로 정하는 사항"이란 다음 각 호의 사항을 말한다. 1. 거래의 내용, 날짜, 기간 및 조건 2. 해당 사업연도 중 거래상대방과의 거래유형별 총거래금액 및 거래잔액 ⑨ 법 제542조의9제5항제1호에서 “대통령령으로 정하는 거래”란 「약관의 규제에 관한 법률」 제2조제1호의 약관에 따라 이루어지는 거래를 말한다. |
| 자료 : 국가법령정보센터 |
이처럼 당사는 특수관계자 등과 일부 자금거래가 발생하고 있으나, 특수관계자와 거래를 함에 있어 특별히 유리하거나 불리한 조건을 제시하는 등 거래상대방에 따라 계약조건을 달리한 사실이 없으며, 특수관계자와 계약을 체결할 때 통상 시장가로 계약을 체결하고 있습니다. 하지만 당사의 적법한 절차 및 법규 준수에도 불구하고 향후 당사와 특수관계자 간의 부적절한 거래가 발생될 가능성을 완전히 배제할 수 없으니 투자자께서는 이점 유의하시어 투자에 임하시기 바랍니다.
(주14) 정정 전
당사는 지난 11월 초에 국내 제약사인 유영제약과 체결한 라이선스 아웃 계약에 따른 경상기술료를 단계별로 수취함에 따라 운영 자금을 확보할 계획에 있습니다. 총 140억원의 경상기술료 중 1차 경상기술료 20억원을 수취하였으며, 개발 단계에 따라 지속적으로 경상기술료를 수취함으로 운영자금을 확보할 예정입니다.
최근 임상 1상을 성공적으로 마친 골관절염 치료제 OSCA에 대해서는 임상 2b상부터 유영제약에서 전액 임상 비용을 부담하는 조건으로 계약을 맺으며 막대한 임상 비용 조달에 대한 부담이 감소하였습니다. 또한, 골관절염 치료제 OSCA에 대한 해외 라이선스 아웃에 대해 관심을 가지고 있는 수요처와 논의 중에 있습니다. 독일, 스위스 등 유럽 지역에 소재한 해당 수요처들은 OSCA에 대한 큰 관심을 보이고 있으며 임상 1상의 결과에 대해 매우 고무적으로 반응하고 있습니다. 다만, 임상 1상은 대상 인원이 적은 관계로(12명) 임상 2a상의 진행 상황에 따라 좀 더 구체적인 기술 라이선스 아웃에 대한 논의가 이뤄질 것으로 예상됩니다.
당사의 계획대로 해외 라이선스 아웃이 진행될 경우의 예상 시점은 2025년말 혹은 2026년 상반기가 될 것으로 예상하며 성공적으로 해외 라이선스 아웃이 이뤄질 경우, 임상 및 운영 비용에 대한 추가 확충이 필요하지 않을 것으로 판단됩니다. 다만, 당사가 예상하는 시점에 국내 제약사인 유영제약과의 라이선스 아웃에 따른 경상기술료의 수취 및 해외 라이선스 아웃이 이뤄지지 않을 경우에는 주주배정 혹은 제3자 배정을 통한 유상증자, 채무증권 발행 등을 통한 자금확충 계획을 고려하고 있습니다.
(주14) 정정 후
당사는 지난 11월 초에 국내 제약사인 유영제약과 체결한 라이선스 아웃 계약에 따른 경상기술료를 단계별로 수취함에 따라 운영 자금을 확보할 계획에 있습니다. 총 140억원의 경상기술료 중 1차 경상기술료 20억원을 수취하였으며, 개발 단계에 따라 지속적으로 경상기술료를 수취함으로 운영자금을 확보할 예정입니다.
최근 임상 1상을 성공적으로 마친 골관절염 치료제 OSCA에 대해서는 임상 2b상부터 유영제약에서 전액 임상 비용을 부담하는 조건으로 계약을 맺으며 막대한 임상 비용 조달에 대한 부담이 감소하였습니다. 또한, 골관절염 치료제 OSCA에 대한 해외 라이선스 아웃에 대해 관심을 가지고 있는 수요처와 논의 중에 있습니다. 독일, 스위스 등 유럽 지역에 소재한 해당 수요처들은 OSCA에 대한 큰 관심을 보이고 있으며 임상 1상의 결과에 대해 매우 고무적으로 반응하고 있습니다. 다만, 임상 1상은 대상 인원이 적은 관계로(12명) 임상 2a상의 진행 상황에 따라 좀 더 구체적인 기술 라이선스 아웃에 대한 논의가 이뤄질 것으로 예상됩니다.
당사의 계획대로 해외 라이선스 아웃이 진행될 경우의 예상 시점은 2026년 하반기혹시 2027년 상반기가 될 것으로 예상하며 성공적으로 해외 라이선스 아웃이 이뤄질 경우, 임상 및 운영 비용에 대한 추가 확충이 필요하지 않을 것으로 판단됩니다. 다만, 당사가 예상하는 시점에 국내 제약사인 유영제약과의 라이선스 아웃에 따른 경상기술료의 수취 및 해외 라이선스 아웃이 이뤄지지 않을 경우에는 주주배정 혹은 제3자 배정을 통한 유상증자, 채무증권 발행 등을 통한 자금확충 계획을 고려하고 있습니다.
(주15) 정정 전
| 카. 매출처 편중 관련 위험 당사의 주요 매출처인 프리모리스인터내셔널, CJ홈쇼핑, GS홈쇼핑사의 경우 2022년 71.0%, 2023년 85.0%로 꾸준히 증가하였으나 2024년 46.9%를 기록하며 매출처 편중이 일부 해소되었습니다. 해당 매출처들의 경우 당사의 주요 매출제품인 화장품 제품군의 매출처입니다. 당사의 경우 이러한 매출 편중을 해소하기 위해 일본 재생의료 사업 진출을 통한 신규 매출을 발생시키고자 적극적으로 영업 활동 중입니다. 현재 일본 재생의료심의위원회의 제2종(자가지방줄기세포)의 후생성 승인이 완료되어 2분기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 한편, 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며 마찬가지로 승인 시 후생성 승인 후 바로 시장에 공급될 수 있도록 준비 중입니다. 또한 OSCA의 해외 라이선스 아웃 또한 준비 중에 있습니다. 다만, 당사의 이러한 노력에도 불구하고 매출처 다각화가 예상보다 지체되고 주요 매출처 및 잠재 매출처들의 경영전략 변경에 따라 사업관계에 부정적인 변화가 발생하거나 주요 매출처의 매출 및 영업성과가 부진할 경우 당사의 영업실적 및 재무상태에 부정적인 영향을 미칠 수 있으므로 투자자께서는 이 점 유의하시기 바랍니다. |
(중략)
당사의 경우 이러한 매출 편중을 해소하기 위해 일본 재생의료 사업 진출을 통한 신규 매출을 발생시키고자 적극적으로 영업 활동 중이며 거래처 다변화를 위해 노력하고 있습니다. 현재 일본 재생의료심의위원회의 제2종(자가지방줄기세포)의 후생성 승인이 완료되어 2분기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 한편, 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며 마찬가지로 후생성 승인 시 바로 시장에 공급될 수 있도록 준비 중입니다. 또한 OSCA의 해외 라이선스 아웃 또한 준비 중에 있습니다.
다만, 당사의 이러한 노력에도 불구하고 매출처 다각화가 예상보다 지체되고 주요 매출처 및 잠재 매출처들의 경영전략 변경에 따라 사업관계에 부정적인 변화가 발생하거나 주요 매출처의 매출 및 영업성과가 부진할 경우 당사의 영업실적 및 재무상태에 부정적인 영향을 미칠 수 있으므로 투자자께서는 이 점 유의하시기 바랍니다.
(주15) 정정 후
| 카. 매출처 편중 관련 위험 당사의 주요 매출처인 프리모리스인터내셔널, CJ홈쇼핑, GS홈쇼핑사의 경우 2022년 71.0%, 2023년 85.0%로 꾸준히 증가하였으나 2024년 46.9%를 기록하며 매출처 편중이 일부 해소되었습니다. 해당 매출처들의 경우 당사의 주요 매출제품인 화장품 제품군의 매출처입니다. 당사의 경우 이러한 매출 편중을 해소하기 위해 일본 재생의료 사업 진출을 통한 신규 매출을 발생시키고자 적극적으로 영업 활동 중입니다. 현재 일본 재생의료심의위원회의 제2종(자가지방줄기세포)의 후생성 승인이 완료되어 2025년 하반기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 한편, 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며 마찬가지로 승인 시 후생성 승인 후 바로 시장에 공급될 수 있도록 준비 중입니다. 또한 OSCA의 해외 라이선스 아웃 또한 준비 중에 있습니다. 다만, 당사의 이러한 노력에도 불구하고 매출처 다각화가 예상보다 지체되고 주요 매출처 및 잠재 매출처들의 경영전략 변경에 따라 사업관계에 부정적인 변화가 발생하거나 주요 매출처의 매출 및 영업성과가 부진할 경우 당사의 영업실적 및 재무상태에 부정적인 영향을 미칠 수 있으므로 투자자께서는 이 점 유의하시기 바랍니다. |
(중략)
당사의 경우 이러한 매출 편중을 해소하기 위해 일본 재생의료 사업 진출을 통한 신규 매출을 발생시키고자 적극적으로 영업 활동 중이며 거래처 다변화를 위해 노력하고 있습니다. 현재 일본 재생의료심의위원회의 제2종(자가지방줄기세포)의 후생성 승인이 완료되어 2025년 하반기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 한편, 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며 마찬가지로 후생성 승인 시 바로 시장에 공급될 수 있도록 준비 중입니다. 또한 OSCA의 해외 라이선스 아웃 또한 준비 중에 있습니다.
다만, 당사의 이러한 노력에도 불구하고 매출처 다각화가 예상보다 지체되고 주요 매출처 및 잠재 매출처들의 경영전략 변경에 따라 사업관계에 부정적인 변화가 발생하거나 주요 매출처의 매출 및 영업성과가 부진할 경우 당사의 영업실적 및 재무상태에 부정적인 영향을 미칠 수 있으므로 투자자께서는 이 점 유의하시기 바랍니다.
(주16) 정정 전
당사의 2025년 1분기 기준유형자산 담보제공 내역은 다음과 같습니다.
| (단위: 천원) |
| 담보제공자산 | 장부금액 | 담보설정금액 | 관련 계정과목 | 차입금액 | 담보권자 |
|---|---|---|---|---|---|
| 토지 | 3,660,774 | 8,796,000 | 차입금 | 6,710,000 | 기업은행 |
| 건물 | 7,758,009 |
| 출처) 당사 정기보고서 |
(주16) 정정 후
당사의 2025년 1분기 기준유형 자산 담보제공 내역은 다음과 같습니다.
| [유형자산 담보제공 내역] |
| (단위: 천원) |
| 담보제공자산 | 장부금액 | 담보설정금액 | 담보감정가격 | 관련 계정과목 | 차입금액 | 담보권자 |
|---|---|---|---|---|---|---|
| 토지 | 3,660,774 | 8,796,000 | 11,028,000 | 차입금 | 6,710,000 | 기업은행 |
| 건물 | 7,758,009 |
| 출처) 당사 정기보고서 |
| 주1) 담보제공자산인 토지 및 건물은 글로벌R&D센터줄기세포재생의학연구소(서울 금천구 소재)와 줄기세포GMP센터(경기도 광명시 소재)입니다. |
| 주2) 담보감정가격의 감정일은 2021년입니다. |
(주17) 정정 전
(1) (주)프리모리스테라퓨틱스 합병 결정(2024.11.28)
당사는 2023년 2월 2일 (주)프리모리스테라퓨틱스 최대주주로부터 보통주식 60,000주(지분율 39.26%)를 무상으로 수증받고, 2023년 2월 09일 (주)프리모리스테라퓨틱스 전환우선주 11,764주(지분율 7.7%)를 금 20억원에 취득하여 공동지배력을 획득하였으며, 이에 당사 공동 기업에 포함되었습니다. 이후 2024년 10월 31일 당사 임직원 2인으로부터 27,200주(각 20,200주, 7,000주)(지분율 17.80%)를 무상수증 받아 지분율은 64.76%(보통주 57.06%, RCPS 7.7%)로 증가하였습니다.
(주17) 정정 후
(1) (주)프리모리스테라퓨틱스 합병 결정(2024.11.28)
당사는 2023년 01월 20일 이사회를 통해 계열회사 지분 인수 및 계열회사 증자 출자 안건을 승인받은 뒤, 2023년 2월 2일 (주)프리모리스테라퓨틱스 최대주주였던 강경선으로부터 보통주식 60,000주(지분율 42.5%, 총 발행 주식수 141,061주 기준)를 무상으로 수증받았습니다. 이후 2023년 2월 08일 (주)프리모리스테라퓨틱스 전환우선주 11,765주(지분율 7.7%, 총 발행 주식수 152,826주 기준)를 금 20억원에 취득하여 공동지배력을 획득하였으며, 이에 당사 공동 기업에 포함되었습니다. 이후 2024년 10월 31일 당사 임직원 2인(이동열, 이미혜)으로부터 총 27,200주(각 20,200주, 7,000주)(지분율 17.80%, 총 발행 주식수 152,826주 기준)를 무상수증 받아 지분율은 64.76%(보통주 57.06%, RCPS 7.7%, 총 발행 주식수 152,826주 기준)로 증가하였습니다. 당사는 강경선, 이동열, 이미혜로부터의 무상 증여와 신주 인수를 통해 (주)프리모리스테라퓨틱스의 지분율을 높이며 실질 지배력을 강화하였습니다. 이러한 지분 확보를 통해 당사는 (주)프리모리스테라퓨틱스와의 계열사 간 협력 및 차세대 치료제 및 융복합 치료제 개발과 같은 기술적 시너지를 강화하고자 하였습니다.
| [당사의 (주)프리모리스테라퓨틱스 RCPS 취득 및 보통주 무상수증 내역] |
| 구분 | RCPS 취득 | 보통주 무상수증 | |||
|---|---|---|---|---|---|
| 구분 | 1차 | 2차 | 3차 | ||
| 계약일 | 기명식 상환전환우선주 | 증여자 | 강경선 | 이동열 | 이미혜 |
| 발행주식총수 | 11,765주 | 증여일 | 2023년 02월 02일 | 2024년 10월 31일 | 2024년 10월 31일 |
| 액면가액 | 5,000원 | 주식수 | 60,000주 | 20,200주 | 7,000주 |
| 발행가액 | 170,000원 | 지분율 | 13.2% | 4.6% | |
| 발행주식총액 | 2,000,050,000원 | 액면가액 | 5,000원 | 5,000원 | 5,000원 |
| 청약일 | 2023년 02월 08일 | - | - | - | - |
| 출처) 당사 제시 |
(주18) 정정 전
(2) 줄기세포 치료제의 일본 및 국내(첨생법) 재생의료사업 진출 추진
당사는 안정적인 수익 기반을 확보하기 위해 일본 재생의료 시장 및 국내(첨생법) 재생의료 사업 진출을 계획하고 있습니다. 일본 재생의료시장 진출을 위해 2024년 일본 후생노동성에 제1종(동종제대혈줄기세포) 및 제2종(자가지방줄기세포) 재생의료 제공계획에 대한 심의 및 승인 절차를 진행하였습니다. 제2종(자가지방줄기세포)의 경우, 2025년 2월 후생노동성 최종 승인까지 완료되어 2분기부터 일본 내 환자 투여를 계획하고 있습니다. 이에 금번 조달 자금의 일부는 일본 현지 환자 수급을 위한 본격적인 영업활동 및 투자를 진행을 위한 운영자금으로 활용될 예정입니다.
한편, 국내 첨단재생바이오법 개정안 시행에 따라 첨단재생의료 임상연구 및 첨단재생의료 치료 제도를 통해 희귀/난치 질환자가 당사의 줄기세포치료제를 조기에 사용할 수 있도록 치료 기회를 확대할 계획을 가지고 있습니다. 당사 주요 파이프라인 치료제의 대상 적응증인 중증아토피와 골관절염은 난치질환에 해당합니다. 금번 조달 자금의 일부는 국내 협력기관과의 협업을 통한 2025년 재생의료 임상연구 계약 개시 및 2026년 임상연구 계획 제출 및 임상연구 시작 등에 활용될 예정이며, 이는 당사의 아토피 피부염 치료제(퓨어스템-에이디 주)와 골관절염 치료제(OSCA) 등의 임상연구데이터를 확보하고 치료제 조기 공급을 통한 수익화 기회 확대의 토대를 마련해 줄 것 입니다.
(3) 기타 파이프라인 연구개발 투자 및 지속 가능한 성장 기반 마련
당사는 기타 파이프라인 중 하나로 오가노이드를 연구개발 중에 있습니다. 특히 당사의 피부 오가노이드 기술의 경우, 공기-액체 계면(ALI) 배양을 통해 불필요한 연골 조직의 형성을 억제하여 실제 피부와 같은 평평한 구조를 완벽 재현하여 다양한 유효물질에 대한 약물 스크리닝 및 효력평가 등에 적용 가능하여, 일부 대형 글로벌 제약사들로부터 관심을 받고 있는 상황입니다. 이러한 파이프라인들의 포트폴리오를 지속적으로 확장하기 위해서는 선제적이고 적극적인 연구개발 투자가 필수적입니다. 이는 단기적인 성과뿐만 아니라 중장기적인 기업 성장의 발판을 마련하는 데 중요한 역할을 할 것입니다.
(4) 실권주 일반공모를 통한 투자자 참여 기회 확대
당사는 주주배정 후 실권주 일반공모 방식을 채택함으로써 기존 주주의 권리를 보호하는 동시에 신규 투자자들에게도 투자 기회를 제공하고자 합니다. 이를 통해 기존 주주들의 지분희석화를 최소화함과 동시에 실권주 일반공모를 통해 다양한 투자자층을 확보하고 기업의 지속 가능한 성장을 위한 기반을 마련할 것입니다.
상기한 바와 같이, 당사는 금번 유상증자를 통해 조달되는 자금을 핵심 파이프라인의 경쟁력 강화, 재생의료 시장 진출 및 추가 성장 동력 확보라는 명확한 목표 하에 투명하고 효율적으로 사용할 계획입니다. 이를 통해 기업가치를 지속적으로 증대시키고, 궁극적으로 주주분들의 이익을 극대화하기 위한 최선의 노력을 다할 것입니다.
당사는 금번 유상증자로 인해 기존 주주들의 지분이 희석될 수 있음을 충분히 인지하고 있으며, 이사회결의시 조달규모 등 정량적인 조건뿐만 아니라, 유상증자의 당위성과 소액주주 등의 유상증자 이해 고려, 주주보호(소통) 방안 등 정성적인 기준도 감안하여 본 유상증자의 목적과 필요성을 논의하였습니다.
2. 주주 권익 보호를 위한 회사 정책
당사는 금번 유상증자로 인해 주주들의 지분이 다소 희석될 수 있음을 충분히 인지하고 있으며, 이에 따라 유상증자 이후의 명확한 비전 제시 등을 통해 지속적으로 주주 소통을 강화할 예정입니다. 금번 유상증자 납입대금을 전략적으로 사용하여 회사의 경쟁력을 강화할 예정이며 이를 통해 기업 가치 상승을 유도하여 중장기적으로 주주 가치를 극대화하도록 노력할 예정입니다.
1) 주주와의 소통 강화 방안
당사는 주주 대상으로 적극적인 IR 활동을 통해 주주 신뢰를 제고하기 위해 노력할 계획입니다. 또한, 당사는 2025년 06월 10일 증권신고서 공시 직후, 금번 주주배정 유상증자 결정과 관련된 주요 내용을 주주들에게 설명하기 위하여 당사 홈페이지 주주 서한을 게재할 계획입니다.
가) IR자료 및 보도자료 배포를 통한 회사에 대한 이해도 증진
당사는 소액주주의 정보 접근성을 높이고 소통을 활성화하여 주주 권익을 보호하고자 합니다. 구체적으로 당사는 추후 당사 홈페이지에 IR 자료를 즉시 게재하여 주주들이 관련 내용을 신속하게 확인할 수 있도록 할 예정입니다. 더불어, 당사는 유상증자와 관련된 전반적인 내용을 다양한 이해관계자들이 확인할 수 있도록 보도자료를 배포할 예정입니다. 이를 통해 개인, 기관, 외국인 투자자 등 다양한 이해관계자들에게 언론을 통해 당사의 비전과 전략을 정확히 전달할 수 있도록 노력할 계획입니다.
나) 투자설명회(IR) 개최
당사는 공모 유상증자 기간 중 오프라인 투자설명회(IR)를 개최하여 질의응답 세션을 운영하여 당사의 경영전략에 대해 충분히 이해할 수 있도록 진행할 계획입니다. 특히, 당사는 금번 유상증자의 목적 및 회사의 향후 성장 전략 등에 대해 주주분들에게 상세히 설명드리고 의견을 경청하기 위해 증권신고서 공시 익일인 2025년 06월 11일에 첫 번째 투자설명회(IR)를 개최할 예정입니다. 간담회의 구체적인 시간 및 장소, 참여 방법 등은 2025년 6월 10일 증권신고서 공시 직후 당사 홈페이지 공지를 통해 신속히 알려드리겠습니다. 또한, 추가적으로 주주분들의 수요를 조사하여 수도권 외에 지방거점에서도 투자설명회를 개최할 계획이 있습니다. 이를 통해 당사의 파이프라인 임상 현황, 기술이전 현황, 향후 비전 등을 상세히 설명하고 질의응답 시간을 통해 주주분들의 궁금증을 해소하겠습니다.
다) IR응대 전용 라인 강화를 통한 소통 강화
당사는 보다 적극적인 투자자 의사 소통 강화를 위해, 기존에 있는 IR응대 전용 라인을 강화할 계획입니다. IR 응대 전용 이메일 및 유선을 통해 유상증자와 관련한 문의에 신속하고 누락 없이 응대할 수 있도록 하겠습니다. 특히, 소액주주를 포함한 다양한 주주의 의견을 수렴할 수 있도록 당사와 사전 일정 조율 등을 신청한 소액주주에 대해서는 개별적인 대면 미팅 또는 유선 의견청취를 적극 활용하여 실시간 소통을 강화하겠습니다.
2) 주요 기관투자자 대상 IR 진행
주요 기관투자자 대상으로 IR을 진행하여 유상증자의 배경, 목적, 기대 효과와 당사의 중장기 사업전략 등에 대해 상세히 설명을 진행할 예정이며, 증권사 애널리스트 대상으로도 적극적으로 소통하여, 시장 내에 충분한 정보가 전달될 수 있도록 노력할 계획입니다.
당사는 상기와 같이 주주 및 시장과의 적극적인 소통을 통해 회사의 경영 전략 및 본 유상증자의 배경과 필요성을 명확히 전달하는 한편, 본 유상증자와 관련 후속 정보를 지속적으로 제공해 나가겠습니다.
(증자비율, 할인율 등) 본 공모 유상증자의 증자비율은 67.79%이며, 할인율은 25%입니다. 최근 4개년 공모 유상증자 증자비율 및 할인율 추이를 살펴보면 본 공모처럼 주주배정 후 실권주 일반공모의 경우, 2021년 증자비율 42%, 할인율 22%, 2022년 증자비율 36%, 할인율 22%, 2023년 증자비율 41%, 할인율 23%, 2024년 증자비율 47%, 할인율 24% 입니다. 이를 고려했을 때, 본 공모 유상증자의 할인율은 적정수준이라 판단되지만, 증자비율은 다소 높은 편으로, 주식가치 희석에 미흡한 부분이 존재합니다. 다만, 당사는 최근 임상 1상을 성공적으로 마친 OSCA의 추가 임상에 대규모 자금을 투입을 통해 차세대 파이프라인 구축이 필요한 시점입니다. 또한 본격적인 일본 재생의료 사업 진출을 위한 추가 자금 투입과 자본 확충을 통한 재무구조의 건전성 확보가 필요한 상황임으로 67.79% 증자비율의 발행조건을 결정하게 되었습니다. 당사는 이러한 사항을 충분히 인지하며 주주권익 보호를 위해 소통을 강화하고, 지속가능한 성장을 통해 주주가치를 증대해 나가겠습니다.
| [최근 4개년 공모 유상증자 증자비율 및 할인율] |
| 구분 | 2021년 | 2022년 | 2023년 | 2024년 | ||||
|---|---|---|---|---|---|---|---|---|
| 증자비율 | 할인율 | 증자비율 | 할인율 | 증자비율 | 할인율 | 증자비율 | 할인율 | |
| 일반공모 | 107.89% | 12.22% | 39.26% | 30.00% | 18.98% | 15.00% | 59.34% | 26.25% |
| 주주배정 | 1.79% | 45.00% | 33.30% | 16.67% | 127.09% | 20.83% | 45.32% | 17.50% |
| 주주우선공모 | 118.27% | 27.50% | 69.26% | 28.50% | 76.95% | 28.75% | 92.26% | 27.50% |
| 주주배정 후 실권주 일반공모 | 42.11% | 21.99% | 36.17% | 22.08% | 40.85% | 23.09% | 47.13% | 23.94% |
| 평균 | 52.43% | 60.85% | 38.69% | 37.93% | 51.50% | 22.97% | 50.96% | 24.12% |
| 자료 : Dart 전자공시시스템 |
| 주) 최초 증권신고서 제출일 기준으로 해당 사업연도 산정 |
(신사업투자 등) 당사의 금번 주주배정 후 실권주 일반공모 유상증자의 자금의 사용목적은 연구개발비, 인건비 등 운영자금으로 신사업투자에는 해당사항이 없습니다. 당사는 기술성장기업으로서 코스닥시장에 상장하였으며 매출 확대를 위하여 추가적인 운영자금(연구개발비용, 기타운전자금)이 필요한 것으로 판단되어 금번 주주배정 후 실권주 일반공모 유상증자를 통해 추가적인 자금을 확보할 계획이고 이를 통해 재무안정성 제고 및 영업활동을 지속하고자 합니다. 세부 자금사용 계획에 대해서는 '제1부 모집 또는 매출에 관한 사항 - Ⅴ. 자금의 사용목적'을 참고하여 주시기 바랍니다.
(경영권 분쟁발생) 증권신고서 제출일 현재 최대주주인 주식회사 세종은 14.27%의 지분율을 확보하고 있습니다. 금번 주주배정 후 실권주 일반공모에 당사의 최대주주인 주식회사 세종은 배정분의 약 100% 내외로 참여를 계획 중입니다. 또한, 당사 발행주식총수의 5% 이상 지분율을 보유한 주주는 최대주주 이외에 존재하지 않고, 소액주주들에게 지분율이 분산되어 있어 최대주주의 변경 및 경영권 분쟁발생 가능성은 제한적일 것으로 판단하고 있습니다. 최대주주 지분율 약화에 따른 경영권 변동 및 분쟁 관련 위험은 '제1부 모집 또는 매출에 관한 사항 - III. 투자위험요소 - 3. 기타위험 - 나. 최대주주 지분희석 및 경영권 관련 위험'을 참고하여 주시기 바랍니다.
(한계기업 등) 당사는 매출이 부진한 가운데, 지속적으로 임상시험 등 연구개발비용이 발생하고 있습니다. 이에 따라 2022년 영업손실 205.6억원, 2023년 영업손실 227.8억원, 2024년 영업손실 148.4억원, 2025년 1분기 영업손실 47.5억원이 발생하였습니다. 또한 영업 외적 측면에서도, 금융비용 등의 발생 영향으로 인해 2022년 당기순손실 201.8억원, 2023년 당기순손실 232.2억원, 2024년 당기순손실 70.8억원, 2025년 1분기 당기순손실 49.0억원이 발생하는 등 지속적인 적자 구조를 면하지 못하고 있습니다. 바이오 업종의 특성 상 당사의 파이프라인에서 임상 성공을 통한 기술이전, 제품화 등의 성과를 이루어내지 못한다면 당사의 적자 구조를 개선하는 것은 불가능할 수 있으며, 자본력이 지속적으로 감소하여 지속적인 연구개발비용 등의 지출이 필요한 당사의 영업활동을 영위하는데 상당한 제약이 생길 수 있습니다. 한편, 2024년말 감사보고서상 외부감사인의 감사 결과 계속기업 관련 중요한 불확실성은 없는 상황입니다. 당사의 재무 관련 위험은 '제1부 모집 또는 매출에 관한 사항 중 III. 투자위험요소 - 2. 회사위험'을 전반적으로 참고하여 주시기 바랍니다.
(주18) 정정 후
(2) 줄기세포 치료제의 일본 및 국내(첨생법) 재생의료사업 진출 추진
당사는 안정적인 수익 기반을 확보하기 위해 일본 재생의료 시장 및 국내(첨생법) 재생의료 사업 진출을 계획하고 있습니다. 일본 재생의료시장 진출을 위해 2024년 일본 후생노동성에 제1종(동종제대혈줄기세포) 및 제2종(자가지방줄기세포) 재생의료 제공계획에 대한 심의 및 승인 절차를 진행하였습니다. 제2종(자가지방줄기세포)의 경우, 2025년 2월 후생노동성 최종 승인까지 완료되어 2025년 하반기부터 일본 내 환자 투여를 계획하고 있습니다. 이에 금번 조달 자금의 일부는 일본 현지 환자 수급을 위한 본격적인 영업활동 및 투자를 진행을 위한 운영자금으로 활용될 예정입니다.
한편, 국내 첨단재생바이오법 개정안 시행에 따라 첨단재생의료 임상연구 및 첨단재생의료 치료 제도를 통해 희귀/난치 질환자가 당사의 줄기세포치료제를 조기에 사용할 수 있도록 치료 기회를 확대할 계획을 가지고 있습니다. 당사 주요 파이프라인 치료제의 대상 적응증인 중증아토피와 골관절염은 난치질환에 해당합니다. 금번 조달 자금의 일부는 국내 협력기관과의 협업을 통한 2025년 재생의료 임상연구 계약 개시 및 2026년 임상연구 계획 제출 및 임상연구 시작 등에 활용될 예정이며, 이는 당사의 아토피 피부염 치료제(퓨어스템-에이디 주)와 골관절염 치료제(OSCA) 등의 임상연구데이터를 확보하고 치료제 조기 공급을 통한 수익화 기회 확대의 토대를 마련해 줄 것 입니다.
(3) 기타 파이프라인 연구개발 투자 및 지속 가능한 성장 기반 마련
당사는 기타 파이프라인 중 하나로 오가노이드를 연구개발 중에 있습니다. 특히 당사의 피부 오가노이드 기술의 경우, 공기-액체 계면(ALI) 배양을 통해 불필요한 연골 조직의 형성을 억제하여 실제 피부와 같은 평평한 구조를 완벽 재현하여 다양한 유효물질에 대한 약물 스크리닝 및 효력평가 등에 적용 가능하여, 일부 대형 글로벌 제약사들로부터 관심을 받고 있는 상황입니다. 이러한 파이프라인들의 포트폴리오를 지속적으로 확장하기 위해서는 선제적이고 적극적인 연구개발 투자가 필수적입니다. 이는 단기적인 성과뿐만 아니라 중장기적인 기업 성장의 발판을 마련하는 데 중요한 역할을 할 것입니다.
(4) 실권주 일반공모를 통한 투자자 참여 기회 확대
당사는 주주배정 후 실권주 일반공모 방식을 채택함으로써 기존 주주의 권리를 보호하는 동시에 신규 투자자들에게도 투자 기회를 제공하고자 합니다. 이를 통해 기존 주주들의 지분희석화를 최소화함과 동시에 실권주 일반공모를 통해 다양한 투자자층을 확보하고 기업의 지속 가능한 성장을 위한 기반을 마련할 것입니다.
상기한 바와 같이, 당사는 금번 유상증자를 통해 조달되는 자금을 핵심 파이프라인의 경쟁력 강화, 재생의료 시장 진출 및 추가 성장 동력 확보라는 명확한 목표 하에 투명하고 효율적으로 사용할 계획입니다. 이를 통해 기업가치를 지속적으로 증대시키고, 궁극적으로 주주분들의 이익을 극대화하기 위한 최선의 노력을 다할 것입니다.
당사는 금번 유상증자로 인해 기존 주주들의 지분이 희석될 수 있음을 충분히 인지하고 있으며, 이사회결의시 조달규모 등 정량적인 조건뿐만 아니라, 유상증자의 당위성과 소액주주 등의 유상증자 이해 고려, 주주보호(소통) 방안 등 정성적인 기준도 감안하여 본 유상증자의 목적과 필요성을 논의하였습니다. 당사는 금번 유상증자 자금조달 방안 이외에 다음과 같은 조달 방안들도 함께 검토하였습니다.
1) 회사채 발행
당사는 증권신고서 제출일 현재 공모 회사채 발행을 위한 적격 신용평가기관의 신용등급은 존재하지 않은 상태입니다. 신용평가기관의 등급 평가 방식으로는 정량적 평가(재무분석 : 수익성, 재무건정성, 현금흐름, 성장성 등) 및 정성적 평가(산업전망, 경쟁력, 경영진의 역량, 정부규제 등)과 함께 계량 모델 및 비교분석을 통해 진행되고 있습니다. 이후 신용등급이 확정되어 투자적격 등급 이상(BBB- 이상)의 등급으로 구분될 시 회사채 금융시장에서의 원활한 자금조달이 가능할 것으로 예상한 바, 당사는 공모 회사채 발행을 통한 자금조달은 현재 어려울 것으로 판단하였습니다. 또한, 사모 회사채 발행도 검토하였으나 높은 금리, 짧은 만기, 담보 및 지급보증 요구 등으로 인해 재무적 부담이 과도할 수 있다는 판단하에 실제 발행으로 이어지지 못하였습니다.
2) 주식 관련 사채 발행
주식 관련 사채로는 주식으로 전환될 수 있는 전환사채, 신주인수권 권리를 보유하고 있는 신주인수권부사채, 특정 주식으로 교환할 수 있는 교환사채 등이 존재합니다. 당사는 주식 관련 사채 또한 자금조달의 방안 중 하나로 고려하였으나, 회사의 재무 여건 등을 고려할 때 투자자 모집에 어려움이 있어 선택할 수 없었습니다.
3) 담보 제공을 통한 추가 차입
2025년 1분기 기준 당사 유형자산 중 담보력이 존재한다고 생각되는 토지 및 건물의 총 장부 금액은 약 12,025백만원입니다. 이 중 당사는 토지 및 건물(장부금액 약 11,418백만원)에 대해 8,796백만원 담보 설정하여 6,710백만원을 이미 차입하고 있습니다. 당사는 복수의 금융기관을 통해 현 담보물을 통한 추가 차입 가능 여부를 사전 검토하였으나, 추가 차입 가능성이 매우 낮은 것으로 확인하여 담보 제공을 통한 추가 차입 조달을 선택할 수 없었습니다.
| [2025년 1분기말 유형자산 상세 현황] |
| (단위: 천원) |
| 구 분 | 취득금액 | 감가상각누계액 | 정부보조금 | 장부금액 |
|---|---|---|---|---|
| 토지 | 3,927,206 | - | - | 3,927,206 |
| 건물 | 9,241,382 | (1,143,426) | - | 8,097,956 |
| 시설장치 | 7,998,885 | (3,919,893) | - | 4,078,992 |
| 연구시험용자산 | 7,968,351 | (7,194,122) | (29,906) | 744,323 |
| 비품 | 412,784 | (380,371) | - | 32,413 |
| 합 계 | 29,548,608 | (12,637,812) | (29,906) | 16,880,890 |
| 출처) 당사 정기보고서 |
| [2025년 1분기말 유형자산 담보제공 내역] |
| (단위: 천원) |
| 담보제공자산 | 장부금액 | 담보설정금액 | 담보감정가격 | 관련 계정과목 | 차입금액 | 담보권자 |
|---|---|---|---|---|---|---|
| 토지 | 3,660,774 | 8,796,000 | 11,028,000 | 차입금 | 6,710,000 | 기업은행 |
| 건물 | 7,758,009 |
| 출처) 당사 정기보고서 |
| 주1) 담보제공자산인 토지 및 건물은 글로벌R&D센터줄기세포재생의학연구소(서울 금천구 소재)와 줄기세포GMP센터(경기도 광명시 소재)입니다. |
| 주2) 담보감정가격의 감정일은 2021년입니다. |
또한, 상기 회사채 및 주식 관련 사채 발행과 담보제공을 통한 추가 차입방안의 경우, 금융비용(이자비용) 부담과 함께 수익성 악화가 이루어질 수 있고 부채총계 증가에 따라 재무안정성에 악영향을 줄 수 있는 점 또한 선택되지 않은 사유로 고려되었습니다. 지속적인 영업손실 및 당기순손실에 기인한 당사의 열위한 재무안정성을 고려하였을 때, 유상증자를 통해 자본을 확충하는 경우 차입금 및 부채비율을 보다 안정적으로 관리하여 건실한 재무안정성을 기대할 수 있으며, 추가적인 금융비용 발생을 방지하여 재무적 부담을 완화시킬 수 있을 것이라 판단하였습니다.
이러한 일련의 자금조달 방안 검토 과정을 거쳐, 이사회는 기존 주주에게 신주인수권을 우선적으로 부여하고, 실권주 발생 시 일반 투자자에게도 참여 기회를 제공할 수 있는 주주배정 후 실권주 일반공모 방식의 유상증자를 추진하는 것이 주주 권익 보호와 자금조달 안정성 확보 측면에서 가장 적절하다는 판단에 이르게 되었으며, 이에 대표주관회사와 인수회사의 잔액인수를 조건으로 한 주주배정 후 실권주 일반공모 방식의 유상증자를 최종적으로 결의하였습니다.
2. 주주 권익 보호를 위한 회사 정책
당사는 금번 유상증자로 인해 주주들의 지분이 다소 희석될 수 있음을 충분히 인지하고 있으며, 이에 따라 유상증자 이후의 명확한 비전 제시 등을 통해 지속적으로 주주 소통을 강화할 예정입니다. 금번 유상증자 납입대금을 전략적으로 사용하여 회사의 경쟁력을 강화할 예정이며 이를 통해 기업 가치 상승을 유도하여 중장기적으로 주주 가치를 극대화하도록 노력할 예정입니다.
1) 주주와의 소통 강화 방안
당사는 주주 대상으로 적극적인 IR 활동을 통해 주주 신뢰를 제고하기 위해 노력할 계획입니다. 또한, 당사는 2025년 06월 10일 증권신고서 공시 직후, 금번 주주배정 유상증자 결정과 관련된 주요 내용을 주주들에게 설명하기 위하여 당사 홈페이지 주주 서한을 게재하였습니다.
![이미지: [주주서한]](%EC%A3%BC%EC%A3%BC%EC%84%9C%ED%95%9C.jpg) |
|
[주주서한] |
가) IR자료 및 보도자료 배포를 통한 회사에 대한 이해도 증진
당사는 소액주주의 정보 접근성을 높이고 소통을 활성화하여 주주 권익을 보호하고자 합니다. 구체적으로 당사는 추후 당사 홈페이지에 IR 자료를 즉시 게재하여 주주들이 관련 내용을 신속하게 확인할 수 있도록 할 예정입니다. 더불어, 당사는 유상증자와 관련된 전반적인 내용을 다양한 이해관계자들이 확인할 수 있도록 보도자료를 배포할 예정입니다. 이를 통해 개인, 기관, 외국인 투자자 등 다양한 이해관계자들에게 언론을 통해 당사의 비전과 전략을 정확히 전달할 수 있도록 노력할 계획입니다.
나) 투자설명회(IR) 개최
당사는 공모 유상증자 기간 중 오프라인 투자설명회(IR)를 개최하여 질의응답 세션을 운영하여 당사의 경영전략에 대해 충분히 이해할 수 있도록 진행할 계획입니다. 특히, 당사는 금번 유상증자의 목적 및 회사의 향후 성장 전략 등에 대해 주주분들에게 상세히 설명드리고 의견을 경청하기 위해 증권신고서 공시 익일인 2025년 06월 11일에 첫 번째 투자설명회(IR)를 개최하였습니다. 간담회의 구체적인 시간 및 장소, 참여 방법 등은 2025년 6월 10일 증권신고서 공시 직후 당사 홈페이지 및 공시를 통해 안내하였습니다.
또한, 추가적으로 주주분들의 수요를 조사하여 수도권 외에 지방거점에서도 투자설명회를 개최할 계획이 있습니다. 이를 통해 당사의 파이프라인 임상 현황, 기술이전 현황, 향후 비전 등을 상세히 설명하고 질의응답 시간을 통해 주주분들의 궁금증을 해소하겠습니다.
다) IR응대 전용 라인 강화를 통한 소통 강화
당사는 보다 적극적인 투자자 의사 소통 강화를 위해, 기존에 있는 IR응대 전용 라인을 강화할 계획입니다. IR 응대 전용 이메일 및 유선을 통해 유상증자와 관련한 문의에 신속하고 누락 없이 응대할 수 있도록 하겠습니다. 특히, 소액주주를 포함한 다양한 주주의 의견을 수렴할 수 있도록 당사와 사전 일정 조율 등을 신청한 소액주주에 대해서는 개별적인 대면 미팅 또는 유선 의견청취를 적극 활용하여 실시간 소통을 강화하겠습니다.
2) 주요 기관투자자 대상 IR 진행
주요 기관투자자 대상으로 IR을 진행하여 유상증자의 배경, 목적, 기대 효과와 당사의 중장기 사업전략 등에 대해 상세히 설명을 진행할 예정이며, 증권사 애널리스트 대상으로도 적극적으로 소통하여, 시장 내에 충분한 정보가 전달될 수 있도록 노력할 계획입니다.
당사는 상기와 같이 주주 및 시장과의 적극적인 소통을 통해 회사의 경영 전략 및 본 유상증자의 배경과 필요성을 명확히 전달하는 한편, 본 유상증자와 관련 후속 정보를 지속적으로 제공해 나가겠습니다.
(증자비율, 할인율 등) 본 공모 유상증자의 증자비율은 67.79%이며, 할인율은 25%입니다. 최근 4개년 공모 유상증자 증자비율 및 할인율 추이를 살펴보면 본 공모처럼 주주배정 후 실권주 일반공모의 경우, 2021년 증자비율 42%, 할인율 22%, 2022년 증자비율 36%, 할인율 22%, 2023년 증자비율 41%, 할인율 23%, 2024년 증자비율 47%, 할인율 24% 입니다. 이를 고려했을 때, 본 공모 유상증자의 할인율은 적정수준이라 판단되지만, 증자비율은 다소 높은 편으로, 주식가치 희석에 미흡한 부분이 존재합니다. 다만, 당사는 최근 임상 1상을 성공적으로 마친 OSCA의 추가 임상에 대규모 자금을 투입을 통해 차세대 파이프라인 구축이 필요한 시점입니다. 또한 본격적인 국내외 재생의료 사업 진출을 위한 추가 자금 투입과 자본 확충을 통한 재무구조의 건전성 확보가 필요한 상황임으로 67.79% 증자비율의 발행조건을 결정하게 되었습니다. 당사는 이러한 사항을 충분히 인지하며 주주권익 보호를 위해 소통을 강화하고, 지속가능한 성장을 통해 주주가치를 증대해 나가겠습니다.
| [최근 4개년 공모 유상증자 증자비율 및 할인율] |
| 구분 | 2021년 | 2022년 | 2023년 | 2024년 | ||||
|---|---|---|---|---|---|---|---|---|
| 증자비율 | 할인율 | 증자비율 | 할인율 | 증자비율 | 할인율 | 증자비율 | 할인율 | |
| 일반공모 | 107.89% | 12.22% | 39.26% | 30.00% | 18.98% | 15.00% | 59.34% | 26.25% |
| 주주배정 | 1.79% | 45.00% | 33.30% | 16.67% | 127.09% | 20.83% | 45.32% | 17.50% |
| 주주우선공모 | 118.27% | 27.50% | 69.26% | 28.50% | 76.95% | 28.75% | 92.26% | 27.50% |
| 주주배정 후 실권주 일반공모 | 42.11% | 21.99% | 36.17% | 22.08% | 40.85% | 23.09% | 47.13% | 23.94% |
| 평균 | 52.43% | 60.85% | 38.69% | 37.93% | 51.50% | 22.97% | 50.96% | 24.12% |
| 자료 : Dart 전자공시시스템 |
| 주) 최초 증권신고서 제출일 기준으로 해당 사업연도 산정 |
(신사업투자 등) 당사의 금번 주주배정 후 실권주 일반공모 유상증자의 자금의 사용목적은 연구개발비, 인건비 등 운영자금으로 신사업투자에는 해당사항이 없습니다. 당사는 기술성장기업으로서 코스닥시장에 상장하였으며 매출 확대를 위하여 추가적인 운영자금(연구개발비용, 기타운전자금)이 필요한 것으로 판단되어 금번 주주배정 후 실권주 일반공모 유상증자를 통해 추가적인 자금을 확보할 계획이고 이를 통해 재무안정성 제고 및 영업활동을 지속하고자 합니다. 세부 자금사용 계획에 대해서는 '제1부 모집 또는 매출에 관한 사항 - Ⅴ. 자금의 사용목적'을 참고하여 주시기 바랍니다.
(경영권 분쟁발생) 증권신고서 제출일 현재 최대주주인 주식회사 세종은 14.27%의 지분율을 확보하고 있습니다. 금번 주주배정 후 실권주 일반공모에 당사의 최대주주인 주식회사 세종은 배정분의 100% 참여를 계획 중입니다. 초과 청약 및 추가 신주인수권증서 매매 여부는 검토 중이나, 현재 미정입니다. 또한, 당사 발행주식총수의 5% 이상 지분율을 보유한 주주는 최대주주 이외에 존재하지 않고, 소액주주들에게 지분율이 분산되어 있어 최대주주의 변경 및 경영권 분쟁발생 가능성은 제한적일 것으로 판단하고 있습니다. 최대주주 지분율 약화에 따른 경영권 변동 및 분쟁 관련 위험은 '제1부 모집 또는 매출에 관한 사항 - III. 투자위험요소 - 3. 기타위험 - 나. 최대주주 지분희석 및 경영권 관련 위험'을 참고하여 주시기 바랍니다.
(한계기업 등) 당사는 매출이 부진한 가운데, 지속적으로 임상시험 등 연구개발비용이 발생하고 있습니다. 이에 따라 2022년 영업손실 205.6억원, 2023년 영업손실 227.8억원, 2024년 영업손실 148.4억원, 2025년 1분기 영업손실 47.5억원이 발생하였습니다. 또한 영업 외적 측면에서도, 금융비용 등의 발생 영향으로 인해 2022년 당기순손실 201.8억원, 2023년 당기순손실 232.2억원, 2024년 당기순손실 70.8억원, 2025년 1분기 당기순손실 49.0억원이 발생하는 등 지속적인 적자 구조를 면하지 못하고 있습니다. 바이오 업종의 특성 상 당사의 파이프라인에서 임상 성공을 통한 기술이전, 제품화 등의 성과를 이루어내지 못한다면 당사의 적자 구조를 개선하는 것은 불가능할 수 있으며, 자본력이 지속적으로 감소하여 지속적인 연구개발비용 등의 지출이 필요한 당사의 영업활동을 영위하는데 상당한 제약이 생길 수 있습니다.
이에 당사는 주요 파이프라인 개발과 더불어 다른 연관 사업 수익화를 통해 자체 재원 역량을 강화하고자 노력하고 있습니다. 구체적으로는 1) 오가노이드 사업으로 피부 오가노이드를 활용한 3D 약물평가 구축을 통해 글로벌 픽파마와의 협업 및 기술이전 등을 통한 수익화 노력 계획이며, 2) 일본 재생의료 사업으로 일본 후생노동성 최종 승인이 완료된 2종(자가지방줄기세포)의 일본 내 공급 통한 수익화를 준비 중이며, 3) 국내 첨생법 사업으로 국내 첨생법 개정에 따라 당사의 아토피 피부염 치료제(퓨어스템-에이디 주)와 골관절염 치료제(OSCA)를 조기에 사용할 수 있도록 협력 의료기관을 통한 해당 파이프라인의 임상 연구 지원, IP 생산 등을 위해 노력할 계획입니다. 다만 그럼에도 불구하고 지속적인 영업손실과 당기순손실 발생 및 부의 영업현금흐름 발생, 그리고 이에 따른 결손금 누적과 재무상태 악화가 발생한다면 당사의 계속기업으로서의 존속능력에 유의적인 불확실성이 존재할 수 있는 상황입니다. 한편, 2024년말 감사보고서상 외부감사인의 감사 결과 계속기업 관련 중요한 불확실성은 없는 상황입니다. 당사의 재무 관련 위험은 '제1부 모집 또는 매출에 관한 사항 중 III. 투자위험요소 - 2. 회사위험'을 전반적으로 참고하여 주시기 바랍니다.
(주19) 정정 전
| 나. 최대주주 지분희석 및 경영권 관련 위험 증권신고서 제출일 현재 최대주주인 주식회사 세종은 당사 주식을 8,000,000주 보유하고 있으며, 지분율은 14.27%로 낮은 수준을 유지하고 있습니다. 금번 유상증자로 인해 발행될 신주의 수는 38,000,000주이며, 당사의 구주주는 유상증자 참여시 1주당 0.6779159202주의 비율로 신주를 배정받게 됩니다. 이에 따라 최대주주인 주식회사 세종은 5,423,327를 배정받게 됩니다. 금번 유상증자에서 최대주주는 자금 여력에 따라 최대한 참여할 예정으로, 현재는 최대주주인 주식회사 세종은 배정분의 약 100% 내외로 참여를 계획 중이며, 최대주주가 배정분 약 100%만 청약 참여할 경우 유상증자 후 지분율은 약 14.27%이 됩니다. 당사 발행주식총수의 5% 이상 지분율을 보유한 주주는 최대주주 이외에 존재하지 않고, 소액주주들에게 지분율이 분산되어 있어 최대주주의 변경 및 경영권 분쟁발생 가능성은 제한적일 것으로 판단하고 있습니다. 다만, 당사는 상장 이후 증권신고서 제출 전일까지 경영권 분쟁 사례가 존재하지 않지만 금번 증자로 인해 최대주주의 지분율은 감소할 수 있으며, 향후 적대적 기업인수 등으로 인한 경영권 분쟁이 대두될 가능성도 있습니다. 이러한 경영 안정성 악화, 경영권 분쟁 등은 주가의 급등락에 영향에 미칠 수 있으며, 이에 따른 투자자 손실을 야기할 가능성이 존재하오니 투자자께서는 이 점 유의하시기 바랍니다. |
증권신고서 제출일 전일 기준 최대주주인 주식회사 세종은 당사 주식을 8,000,000주 보유하고 있으며, 지분율은 14.27%로 낮은 수준을 유지하고 있습니다. 최대주주 및 특수관계인의 보유지분 현황 및 최대주주의 지분 변동 내역은 다음과 같습니다.
| [최대주주 및 특수관계인 현황] |
| (2025년 1분기 기준) |
| 성명 (회사명) |
관계 | 주식의 종류 |
소유주식수 | 소유 비율 | 비고 |
|---|---|---|---|---|---|
| (주)세종 | 최대주주 | 보통주 | 8,000,000 | 14.27 | - |
| 계 | - | 8,000,000 | 14.27 | - | |
| 출처) 당사 분기보고서 제시 |
| [최대주주의 당사 지분 변동 내역] |
| (단위: 주) |
| 구분 | 거래일자 | 거래방식 | 거래주식수 | 보유주식수 | 거래단가 | 지분율 | 비고 |
|---|---|---|---|---|---|---|---|
| 취득 | 2023-10-11 | 장내매수 | 305,421 | 305,421 | 1,652 | 0.81% | 5% 미만, 수회 취득 |
| 2023-10-24 | 장내매수 | 260,000 | 565,421 | 1,526 | 1.49% | ||
| 2023-10-25 | 장내매수 | 160,000 | 725,421 | 1,576 | 1.91% | ||
| 2023-10-27 | 장내매수 | 66,000 | 791,421 | 1,319 | 2.09% | ||
| 2023-10-30 | 유상신주 취득 | 5,633,494 | 6,424,915 | 1,165 | 11.49% | 유상신주 초과청약 | |
| 2023-10-31 | 장내매수 | 110,000 | 6,534,915 | 1,345 | 11.68% | ||
| 2023-11-01 | 장내매수 | 40,331 | 6,575,246 | 1,367 | 11.75% | ||
| 2023-11-02 | 장내매수 | 93,737 | 6,668,983 | 1,455 | 11.92% | ||
| 2023-11-03 | 장내매수 | 16,094 | 6,685,077 | 1,496 | 11.95% | ||
| 2023-11-06 | 장내매수 | 86,923 | 6,772,000 | 1,567 | 12.11% | ||
| 2023-11-07 | 장내매수 | 28,000 | 6,800,000 | 1,658 | 12.16% | ||
| 2023-11-16 | 장내매수 | 640,000 | 7,440,000 | 1,238 | 13.30% | ||
| 2023-11-17 | 장내매수 | 160,000 | 7,600,000 | 1,324 | 13.59% | ||
| 2023-11-27 | 장내매수 | 20,000 | 7,620,000 | 1,332 | 13.62% | ||
| 2023-12-12 | 장내매수 | 80,000 | 7,700,000 | 1,808 | 13.77% | ||
| 2023-12-13 | 장내매수 | 110,000 | 7,810,000 | 1,827 | 13.96% | ||
| 2023-12-14 | 장내매수 | 54,704 | 7,864,704 | 1,982 | 14.06% | ||
| 2023-12-15 | 장내매수 | 65,296 | 7,930,000 | 2,114 | 14.18% | ||
| 2023-12-18 | 장내매수 | 40,000 | 7,970,000 | 2,193 | 14.25% | ||
| 2023-12-19 | 장내매수 | 30,000 | 8,000,000 | 2,279 | 14.27% |
| 출처) 당사 제시 |
금번 유상증자로 인해 발행될 신주의 수는 38,000,000주이며 이는 기존 발행주식 대비 67.79% 수준으로, 당사의 주주는 유상증자 참여시 1주당 0.6779159202주의 비율로 신주를 배정받게 됩니다. (신주배정기준일 전 주식매수선택권의 행사, 자기주식 수의 변동 등에 의하여 변동 가능성이 있습니다.) 이에 따라 최대주주인 주식회사 세종은 5,423,327주를 배정받게 됩니다. 금번 유상증자에서 최대주주는 자금 여력에 따라 최대한 참여할 예정으로, 현재는 최대주주인 주식회사 세종은 배정분의 약 100% 참여를 계획 중입니다. 최대주주가 배정분 약 100%만 청약 참여할 경우 유상증자 후 지분율은 약 14.27%이 됩니다.
| [최대주주 청약률에 따른 지분변동 가정] |
| 성명 | 증자 전 | 증자 후 | |||||
|---|---|---|---|---|---|---|---|
| (최대주주 100% 참여) | (최대주주 미참여) | ||||||
| 주식수(주) | 지분율(%) | 배정주식수(주) | 주식수(주) | 지분율(%) | 주식수(주) | 지분율(%) | |
| (주)세종 | 8,000,000 | 14.27 | 5,423,327 | 13,423,327 | 14.27 | 8,000,000 | 8.51 |
| 출처: 당사 제공 |
| 주1) 증자 전 발행주식 총수 : 56,054,149주 → 증자 후 발행주식 총수 : 94,054,149주 |
(중략)
상기한 바와 같이 증권신고서 제출일 현재 최대주주인 주식회사 세종은 14.27%의 지분율을 확보하고 있으며, 금번 주주배정 후 실권주 일반공모에 배정분의 약 100% 내외로 참여를 계획 중입니다. 또한, 당사 발행주식총수의 5% 이상 지분율을 보유한 주주는 최대주주 이외에 존재하지 않고, 소액주주들에게 지분율이 분산되어 있어 최대주주의 변경 및 경영권 분쟁발생 가능성은 제한적일 것으로 판단하고 있습니다. 다만, 당사는 상장 이후 증권신고서 제출 전일까지 경영권 분쟁 사례가 존재하지 않지만 금번 증자로 인해 최대주주의 지분율은 감소할 수 있으며, 향후 적대적 기업인수 등으로 인한 경영권 분쟁이 대두될 가능성도 있습니다. 이러한 경영 안정성 악화, 경영권 분쟁 등은 주가의 급등락에 영향에 미칠 수 있으며, 이에 따른 투자자 손실을 야기할 가능성이 존재하오니 투자자께서는 이 점 유의하시기 바랍니다.
(주19) 정정 후
| 나. 최대주주 지분희석 및 경영권 관련 위험 증권신고서 제출일 현재 최대주주인 주식회사 세종은 당사 주식을 8,000,000주 보유하고 있으며, 지분율은 14.27%로 낮은 수준을 유지하고 있습니다. 금번 유상증자로 인해 발행될 신주의 수는 38,000,000주이며, 당사의 구주주는 유상증자 참여시 1주당 0.6779159202주의 비율로 신주를 배정받게 됩니다. 이에 따라 최대주주인 주식회사 세종은 5,423,327를 배정받게 됩니다. 금번 유상증자에서 최대주주는 자금 여력에 따라 최대한 참여할 예정으로, 현재 최대주주인 주식회사 세종은 배정분의 100% 참여를 계획 중입니다. 초과 청약 및 추가 신주인수권증서 매매 여부는 검토 중이나, 현재 미정입니다. 최대주주가 배정분 100%만 청약 참여할 경우 유상증자 후 지분율은 약 14.27%이 됩니다. 당사 발행주식총수의 5% 이상 지분율을 보유한 주주는 최대주주 이외에 존재하지 않고, 소액주주들에게 지분율이 분산되어 있어 최대주주의 변경 및 경영권 분쟁발생 가능성은 제한적일 것으로 판단하고 있습니다. 다만, 당사는 상장 이후 증권신고서 제출 전일까지 경영권 분쟁 사례가 존재하지 않지만 금번 증자로 인해 최대주주의 지분율은 감소할 수 있으며, 향후 적대적 기업인수 등으로 인한 경영권 분쟁이 대두될 가능성도 있습니다. 이러한 경영 안정성 악화, 경영권 분쟁 등은 주가의 급등락에 영향에 미칠 수 있으며, 이에 따른 투자자 손실을 야기할 가능성이 존재하오니 투자자께서는 이 점 유의하시기 바랍니다. |
증권신고서 제출일 전일 기준 최대주주인 주식회사 세종은 당사 주식을 8,000,000주 보유하고 있으며, 지분율은 14.27%로 낮은 수준을 유지하고 있습니다. 최대주주 및 특수관계인의 보유지분 현황 및 최대주주의 지분 변동 내역은 다음과 같습니다.
| [최대주주 및 특수관계인 현황] |
| (2025년 1분기 기준) |
| 성명 (회사명) |
관계 | 주식의 종류 |
소유주식수 | 소유 비율 | 비고 |
|---|---|---|---|---|---|
| (주)세종 | 최대주주 | 보통주 | 8,000,000 | 14.27 | - |
| 계 | - | 8,000,000 | 14.27 | - | |
| 출처) 당사 분기보고서 제시 |
| [최대주주의 당사 지분 변동 내역] |
| (단위: 주, 원) |
| 구분 | 거래일자 | 거래방식 | 거래주식수 | 보유주식수 | 거래단가 | 지분율 | 비고 |
|---|---|---|---|---|---|---|---|
| 취득 | 2023-10-11 | 장내매수 | 305,421 | 305,421 | 1,652 | 0.81% | 5% 미만, 수회 취득 |
| 2023-10-24 | 장내매수 | 260,000 | 565,421 | 1,526 | 1.49% | ||
| 2023-10-25 | 장내매수 | 160,000 | 725,421 | 1,576 | 1.91% | ||
| 2023-10-27 | 장내매수 | 66,000 | 791,421 | 1,319 | 2.09% | ||
| 2023-10-30 | 유상신주 취득 | 5,633,494 | 6,424,915 | 1,165 | 11.49% | 유상신주 청약 및 초과청약 |
|
| 2023-10-31 | 장내매수 | 110,000 | 6,534,915 | 1,345 | 11.68% | ||
| 2023-11-01 | 장내매수 | 40,331 | 6,575,246 | 1,367 | 11.75% | ||
| 2023-11-02 | 장내매수 | 93,737 | 6,668,983 | 1,455 | 11.92% | ||
| 2023-11-03 | 장내매수 | 16,094 | 6,685,077 | 1,496 | 11.95% | ||
| 2023-11-06 | 장내매수 | 86,923 | 6,772,000 | 1,567 | 12.11% | ||
| 2023-11-07 | 장내매수 | 28,000 | 6,800,000 | 1,658 | 12.16% | ||
| 2023-11-16 | 장내매수 | 640,000 | 7,440,000 | 1,238 | 13.30% | ||
| 2023-11-17 | 장내매수 | 160,000 | 7,600,000 | 1,324 | 13.59% | ||
| 2023-11-27 | 장내매수 | 20,000 | 7,620,000 | 1,332 | 13.62% | ||
| 2023-12-12 | 장내매수 | 80,000 | 7,700,000 | 1,808 | 13.77% | ||
| 2023-12-13 | 장내매수 | 110,000 | 7,810,000 | 1,827 | 13.96% | ||
| 2023-12-14 | 장내매수 | 54,704 | 7,864,704 | 1,982 | 14.06% | ||
| 2023-12-15 | 장내매수 | 65,296 | 7,930,000 | 2,114 | 14.18% | ||
| 2023-12-18 | 장내매수 | 40,000 | 7,970,000 | 2,193 | 14.25% | ||
| 2023-12-19 | 장내매수 | 30,000 | 8,000,000 | 2,279 | 14.27% |
| 출처) 당사 제시, 세종 제출 지분공시 |
| [최대주주의 유상신주 청약 상세 내역] |
| (단위: 주, 원) |
| 거래일자 | 거래방식 | 주식종류 | 거래주식수 | 보유주식수 | 거래단가 | 비고 |
|---|---|---|---|---|---|---|
| 2023-10-12 | 장내매수 | 신주인수권이표시된것 | 1,500,000 | 1,500,000 | 86 | |
| 2023-10-13 | 장내매수 | 신주인수권이표시된것 | 850,000 | 2,350,000 | 124 | |
| 2023-10-16 | 장내매수 | 신주인수권이표시된것 | 674,602 | 3,024,602 | 130 | |
| 2023-10-17 | 장내매수 | 신주인수권이표시된것 | 619,088 | 3,643,690 | 151 | |
| 2023-10-18 | 장내매수 | 신주인수권이표시된것 | 1,050,889 | 4,694,579 | 207 | |
| 2023-10-30 | 기타(-) | 신주인수권이표시된것 | -4,694,579 | 0 | - | 유상신주 청약 |
| 2023-10-30 | 구주주청약 | 의결권이있는 주식 | 4,694,579 | |||
| 2023-10-30 | 초과청약 | 의결권이있는 주식 | 938,915 |
| 출처) 당사 제시, 세종 제출 지분공시 |
금번 유상증자로 인해 발행될 신주의 수는 38,000,000주이며 이는 기존 발행주식 대비 67.79% 수준으로, 당사의 주주는 유상증자 참여시 1주당 0.6779159202주의 비율로 신주를 배정받게 됩니다. (신주배정기준일 전 주식매수선택권의 행사, 자기주식 수의 변동 등에 의하여 변동 가능성이 있습니다.) 이에 따라 최대주주인 주식회사 세종은 5,423,327주를 배정받게 됩니다. 금번 유상증자에서 최대주주는 자금 여력에 따라 최대한 참여할 예정으로, 현재 최대주주인 주식회사 세종은 배정분의 100% 참여를 계획 중입니다. 초과 청약 및 추가 신주인수권증서 매매 여부는 검토 중이나, 현재 미정입니다. 최대주주가 배정분 100%만 청약 참여할 경우 유상증자 후 지분율은 약 14.27%이 됩니다.
| [최대주주 청약률에 따른 지분변동 가정] |
| 성명 | 증자 전 | 증자 후 | |||||
|---|---|---|---|---|---|---|---|
| (최대주주 100% 참여) | (최대주주 미참여) | ||||||
| 주식수(주) | 지분율(%) | 배정주식수(주) | 주식수(주) | 지분율(%) | 주식수(주) | 지분율(%) | |
| (주)세종 | 8,000,000 | 14.27 | 5,423,327 | 13,423,327 | 14.27 | 8,000,000 | 8.51 |
| 출처: 당사 제공 |
| 주1) 증자 전 발행주식 총수 : 56,054,149주 → 증자 후 발행주식 총수 : 94,054,149주 |
현재 최대주주 세종의 당사 지분 보유 목적은 '일반투자'입니다. 세종은 금번
유상증자 참여를 통해 지분 보유 목적을 '경영참여'로 변경하는 것을 검토 중에 있으며, 경영참여를 확정하는 경우 즉시 공시를 통해 의사를 밝힐 예정입니다. 다만, 증권신고서 제출일 전일 기준 확정된 사항은 없으며, 변경하지 않을 가능성도 존재하니 투자자께서는 이 점 유의하시기 바랍니다. 또한, 세종은 당사에 대한 경영참여를 결정한 후에도 현 경영진을 최대한 유지하여 당사의 신약개발 등 사업의 일관성 및 지속성을 유지하기 위해 노력할 예정입니다.
한편, 최대주주 및 특수관계인을 제외한 주요 주주 현황 및 전 최대주주인 강경선의 지분 변동 내역은 다음과 같습니다.
| [최대주주 제외 주요주주 현황] |
| (2025.03.31 기준) |
| 성명 (회사명) |
관계 | 주식의 종류 |
소유주식수 | 소유 비율 | 비고 |
|---|---|---|---|---|---|
| 강경선 | 주요주주 | 보통주 | 2,628,526 | 4.69 | - |
| 김신현 | 주주 | 보통주 | 79,000 | 0.14 | - |
| 강영민 | 주주 | 보통주 | 22,700 | 0.04 | - |
| 강영준 | 주주 | 보통주 | 11,400 | 0.02 | - |
| 강영은 | 주주 | 보통주 | 11,300 | 0.02 | - |
| 나종천 | 등기임원 | 보통주 | 111,729 | 0.2 | |
| 김원균 | 등기임원 | 보통주 | 6,272 | 0.01 | - |
| 이승희 | 등기임원 | 보통주 | 19,337 | 0.03 | |
| 최정호 | 등기임원 | 보통주 | 195,283 | 0.35 | |
| 이동열 | 미등기임원 | 보통주 | 86,000 | 0.15 | |
| 이미혜 | 미등기임원 | 보통주 | 35,000 | 0.06 | |
| 이상균 | 주주 | 보통주 | 67,167 | 0.12 |
| 출처) 당사 제공 |
| [주요주주 강경선(전 최대주주)의 당사 지분 변동 내역] |
| (단위: 주, 원) |
| 구분 | 거래일자 | 거래방식 | 거래주식수 | 보유주식수 | 거래단가 | 지분율 | 비고 |
|---|---|---|---|---|---|---|---|
| 변동 | 2015-12-21 | 신규상장 | 2,520,000 | 2,520,000 | 6,000 | 18.24% | |
| 2018-07-28 | 유상신주 취득 | 131,445 | 2,651,445 | 8,560 | 12.75% | 유상신주 청약 및 초과청약 | |
| 2019-10-25 | 장내매도 | -600 | 2,650,845 | 9,650 | 12.71% | ||
| 2019-10-28 | 장내매도 | -620,845 | 2,030,000 | 8,204 | 9.73% | ||
| 2020-02-27 | 장내매도 | -27,000 | 2,003,000 | 6,476 | 9.67% | ||
| 2020-02-28 | 장내매도 | -25,000 | 1,978,000 | 7,061 | 9.42% | ||
| 2020-03-02 | 장내매도 | -20,000 | 1,958,000 | 6,726 | 9.33% | ||
| 2020-03-03 | 장내매도 | -28,000 | 1,930,000 | 6,687 | 9.19% | ||
| 2021-10-22 | 유상신주 취득 | 371,515 | 2,301,515 | 3,150 | 6.06% | 유상신주 청약 및 초과청약 | |
| 2023-11-08 | 유상신주 취득 | 327,011 | 2,628,526 | 1,165 | 4.69% | 유상신주 청약 |
| 출처) 당사 제시, 강경선 제출 지분공시 |
(중략)
상기한 바와 같이 증권신고서 제출일 현재 최대주주인 주식회사 세종은 14.27%의 지분율을 확보하고 있으며, 금번 주주배정 후 실권주 일반공모에 배정분의 100% 참여를 계획 중입니다. 초과 청약 및 추가 신주인수권증서 매매 여부는 검토 중이나, 현재 미정입니다. 또한, 당사 발행주식총수의 5% 이상 지분율을 보유한 주주는 최대주주 이외에 존재하지 않고, 소액주주들에게 지분율이 분산되어 있어 최대주주의 변경 및 경영권 분쟁발생 가능성은 제한적일 것으로 판단하고 있습니다. 다만, 당사는 상장 이후 증권신고서 제출 전일까지 경영권 분쟁 사례가 존재하지 않지만 금번 증자로 인해 최대주주의 지분율은 감소할 수 있으며, 향후 적대적 기업인수 등으로 인한 경영권 분쟁이 대두될 가능성도 있습니다. 이러한 경영 안정성 악화, 경영권 분쟁 등은 주가의 급등락에 영향에 미칠 수 있으며, 이에 따른 투자자 손실을 야기할 가능성이 존재하오니 투자자께서는 이 점 유의하시기 바랍니다.
(주20) 정정 전
| [코스닥시장 관리종목 지정요건 및 해당여부 검토] |
| 구 분 | 관리종목 지정(코스닥 상장규정 제53조) | 관리종목지정유예 | 관리종목 지정요건 적용여부 |
회사현황 | ||
|---|---|---|---|---|---|---|
| 해당여부 | 유예기간 | 사업연도 | 금액(백만원) / 비율(%) / 내용 | |||
| (1) 매출액 미달 | 최근 사업연도 30억원 미만 (지주회사는 연결기준) - 이익미실현기업 또는 기술성장기업은 상장후 5년간 미적용 - 기술성장기업 중 A), B), C) 중 어느 하나에 해당하는 제약·바이오기업은 최근 사업연도 미적용 A) 최근 사업연도 말「제약산업 육성 및 지원에 관한 특별법」에 따른 혁신제약기업이 세칙으로 정한 요건을 충족하는 경우 B) 최근 사업연도의 일평균 시가총액 4,000억 이상이며, 그 금액이 현재의 자본금을 초과하는 기업이 세칙으로 정하는 요건을 충족하는 경우 C) 최근 3사엽언도의 매출액 합계 90억 이상이며, 최근 사업연도의 직전 사업연도의 매출액이 30억 이상인 경우 |
- | - | 현재 미해당 | 2024년말 | 매출액 : 7,746백만원 (K-IFRS 별도기준) |
| 2025년 1분기말 | 매출액 : 954백만원 (K-IFRS 별도기준) |
|||||
| (2) 법인세비용차감전 계속사업손실 |
최근 3사업연도중 2사업연도에 각각 10억원 이상이면서 해당 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 있고 최근사업연도에 법인세비용차감전계속사업손실이 있는 경우 - 이익미실현 기업은 상장 후 5년간 미적용 (다만, 상장일부터 상장일이 속한 사업연도의 말일까지의 기간이 3개월 미만인 경우에는 상장일이 속하는 사업연도와 그 이후 5개 사업연도로 한다) - 기술성장기업은 상장후 3년간 미적용(다만, 상장일부터 상장일이 속한 사업연도의 말일까지의 기간이 3개월 미만인 경우에는 상장일이 속하는 사업연도와 그 이후 3개 사업연도로 한다) |
- | - | 2023년이 해당되며 2024년은 미해당, 2025년 해당될 경우 관리종목 지정 |
2023년말 | 세전손실 : (23,137)백만원 자기자본 : 44,517백만원 (자기자본 대비 52.0%) |
| 2024년말 | 세전손실 : (7,083)백만원 자기자본 : 43,182백만원 (자기자본 대비 16.4%) |
|||||
| 2025년 1분기말 | 세전손실 : (4,903)백만원 자기자본 : 38,279백만원 (자기자본 대비 12.8%) |
|||||
| (3) 자본잠식 등 | 최근 사업연도말 현재 자본잠식률이 100분의 50 이상인 경우 | - | - | 현재 미해당 | 2024년말 | 자본금 : 28,027백만원 지배주주지분 : 43,182백만원 자본잠식률 : 해당없음 |
| 2025년 1분기말 | 자본금 : 28,027백만원 지배주주지분 : 38,279백만원 자본잠식률 : 해당없음 |
|||||
| (4)자기자본 미달 | 최근 사업연도말 현재 자기자본이 10억원 미만인 경우 | - | - | 현재 미해당 | 2024년말 | 지배주주지분 : 43,182백만원 |
| 2025년 1분기말 | 지배주주지분 : 38,279백만원 | |||||
| (5) 시가총액 미달 | 보통주 시가총액 40억원미만 30일간 지속 - 천재지변, 시장상황의 급격한 변동 등으로 거래소가 시장 관리를 위하여 필요하다고 인정될 경우 적용배제 가능 |
- | - | 현재 미해당 | 2024년 12월 31일 |
시가총액 : 113,229백만원 |
| 증권신고서 제출일 기준 |
시가총액 : 116,873백만원 |
|||||
| (6) 정기보고서 미제출 | 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않은 경우 | - | - | 현재 미해당 | 현재 기준 | 현재 특이사항 없음 |
| (7) 지배구조 미달 | 최근 사업연도 사업보고서상 A)사외이사의 수가 「상법」 제542조의8의 규정에서 정하는 수에 미달하는 경우 B) 「상법」 제542조의11의 규정에서 정하는 감사위원회를 구성하지 않거나 감사위원회의 구성요건을 충족하지 못하는 경우 *「상법」 제542조의8에 의거 자산총액 1,000억원 미만의 코스닥 상장 벤처기업은 사외이사 선임 의무 면제 **「상법」 제542조의11에 의거 자산총액 2조원 미만의 상장회사는 감사위원회 설치 의무 면제 |
- | - | 현재 미해당 | 2024년말 | 현재 특이사항 없음 |
| (8) 거래량 미달 | 분기월평균거래량이 유동주식수의 1%에 미달 다만, 다음 어느 하나에 해당하는 경우에는 이 호에 적용 받지 않습니다. - 신규상장법인(신규상장일이 속하는 분기에 한정) - 분기의 월평균거래량 1만주 이상(액면가액 5,000원 기준) - 「코스닥시장 업무규정」(이하 “업무규정”이라 한다) 제12조의3제1항에 따른 유동성공급계약이 체결된 경우 - 소액주주가 소유한 보통주식의 총수가 유동주식수의 100분의 20 이상이고, 해당 소액주주의 수가 300명 이상인 경우. |
- | - | 현재 미해당 | 2025년 1분기말 | 소액주주 - 지분율 77.58% - 19,291명 |
| (9) 주식분산 미달 | 소액주주 200인미만 or 소액주주지분 20%미만 - 300인이상의 소액주주가 유동주식수의 10%이상으로서 100만주이상을 소유, 해외증권시장에 상장된 경우는 적용배제 |
- | - | 현재 미해당 | 2025년 1분기말 | 소액주주 - 지분율 77.58% - 19,291명 |
| (10) 회생절차 개시신청 | "채무자 회생 및 파산에 관한 법률" 제34조에 의한 회생 절차개시 신청이 있는 경우 | - | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| (11) 파산신청 | 코스닥시장 상장법인에 대하여 "채무자 회생 및 파산에 관한 법률" 제294조에 의한 파산신청이 있는 경우 | - | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| (12) 기타 | - 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 - 변경·추가상장이 유예된 기간 중에「증권의 발행 및 공시 등에 관한 규정」에 따른 재무관리기준을 위반한 경우 |
- | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| 출처)「코스닥시장 상장규정」, 당사 정기보고서 |
| 주1) 상기 도표 중 (1)매출액 미달 요건 관련하여, 별도재무제표를 기준으로 합니다. 그 외 요건은 연결재무제표를 기준으로 합니다. |
| 주2) (2)법인세비용차감전계속사업손실 요건 관련하여, 자기자본은 비지배지분을 제외하지 않은 금액 기준을 적용합니다. (3)자본잠식 등, (4)자기자본 미달 요건 관련하여, 자기자본은 비지배지분을 제외한 지배기업지분금액 기준을 적용합니다. |
또한, 2025년 01월 21일, 정부와 유관기관(금융위원회, 금융감독원, 한국거래소, 금융투자협회)은 주식시장의 질적수준 제고를 위한「IPO 및 상장 폐지 제도개선 방안」을 발표하였습니다. 이 중 상장폐지 제도개선 방안은 상장유지 요건을 강화하고, 절차는 효율화함으로써 주식시장 내 저성과 기업을 적시에 퇴출시키고 상장기업의 밸류업을 주요 목적으로 하고 있습니다. 이와 같은 상장폐지 요건이 강화됨에 따라 당사의 영업환경 악화, 재무요건 악화 등을 원인으로 강화된 상장폐지 요건에 해당되어 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있음을 투자자분들은 유의하시기 바랍니다.
| [IPO 및 상장 폐지 제도개선 방안 및 해당여부 검토] |
| 구 분 | IPO 및 상장 폐지 제도개선 방안 | 상장폐지 지정요건 적용여부 |
회사현황 | |
|---|---|---|---|---|
| 사업연도 | 금액(백만원) / 내용 | |||
| (1) 시가총액 요건 기준 강화 | 정량요건으로서 시장평가 관련 시가총액 기준을 단계적으로 상향하여 코스피 500억원, 코스닥 300억원을 목표로 합니다. - 코스피 : 50억원(현행) → 200억원(2026년) → 300억원(2027년) → 500억원(2028년) - 코스닥 : 40억원(현행) → 150억원(2026년) → 200억원(2027년) → 300억원(2028년) |
현재 미해당 | 2024년 12월 31일 |
시가총액 : 113,229백만원 |
| 증권신고서 제출일 기준 |
시가총액 : 116,873백만원 |
|||
| (2) 매출액 요건 기준 강화 | 정량요건으로서 기업실적 관련 매출액 기준을 단계적으로 상향하여 코스피 300억원(시가총액 1,000원 미만 기업만 적용), 코스닥 100억원(시가총액 600억원 미만 기업만 적용)을 목표로 합니다. - 코스피 : 50억원(현행) → 100억원(2027년) → 200억원(2028년) → 300억원(2029년) - 코스닥 : 30억원(현행) → 50억원(2027년) → 750억원(2028년) → 100억원(2029년) |
현재 미해당 | 2024년말 | 매출액 : 7,746백만원 (K-IFRS 별도기준) |
| 2025년 1분기말 | 매출액 : 954백만원 (K-IFRS 별도기준) |
|||
| (3) 감사의견 미달 요건 기준 강화 | - 2회 연속 감사의결 미달시 즉시 상장폐지 : 감사의견 미달(한정, 부적정, 의견거절)의 경우 2회 연속발생시 즉시 상장폐지되고(회생 ·워크아웃기업에 대해서는 예외인정), 이의신청은 허용되지 않습니다. | 현재 미해당 | 2024년말 | 해당사항 없음 |
| 2025년 1분기말 | 해당사항 없음 | |||
| 출처) 금융위원회, 당사 정기보고서 |
(주20) 정정 후
| [코스닥시장 관리종목 지정요건 및 해당여부 검토] |
| 구 분 | 관리종목 지정(코스닥 상장규정 제53조) | 관리종목지정유예 | 관리종목 지정요건 적용여부 |
회사현황 | ||
|---|---|---|---|---|---|---|
| 해당여부 | 유예기간 | 사업연도 | 금액(백만원) / 비율(%) / 내용 | |||
| (1) 매출액 미달 | 최근 사업연도 30억원 미만 (지주회사는 연결기준) - 이익미실현기업 또는 기술성장기업은 상장후 5년간 미적용 - 기술성장기업 중 A), B), C) 중 어느 하나에 해당하는 제약·바이오기업은 최근 사업연도 미적용 A) 최근 사업연도 말「제약산업 육성 및 지원에 관한 특별법」에 따른 혁신제약기업이 세칙으로 정한 요건을 충족하는 경우 B) 최근 사업연도의 일평균 시가총액 4,000억 이상이며, 그 금액이 현재의 자본금을 초과하는 기업이 세칙으로 정하는 요건을 충족하는 경우 C) 최근 3사엽언도의 매출액 합계 90억 이상이며, 최근 사업연도의 직전 사업연도의 매출액이 30억 이상인 경우 |
- | - | 현재 미해당 | 2024년말 | 매출액 : 7,746백만원 (K-IFRS 별도기준) |
| 2025년 1분기말 | 매출액 : 954백만원 (K-IFRS 별도기준) |
|||||
| (2) 법인세비용차감전 계속사업손실 |
최근 3사업연도중 2사업연도에 각각 10억원 이상이면서 해당 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 있고 최근사업연도에 법인세비용차감전계속사업손실이 있는 경우 - 이익미실현 기업은 상장 후 5년간 미적용 (다만, 상장일부터 상장일이 속한 사업연도의 말일까지의 기간이 3개월 미만인 경우에는 상장일이 속하는 사업연도와 그 이후 5개 사업연도로 한다) - 기술성장기업은 상장후 3년간 미적용(다만, 상장일부터 상장일이 속한 사업연도의 말일까지의 기간이 3개월 미만인 경우에는 상장일이 속하는 사업연도와 그 이후 3개 사업연도로 한다) |
- | - | 2023년이 해당되며 2024년은 미해당, 2025년 해당될 경우 관리종목 지정 |
2023년말 | 세전손실 : (23,137)백만원 자기자본 : 44,517백만원 (자기자본 대비 52.0%) |
| 2024년말 | 세전손실 : (7,083)백만원 자기자본 : 43,182백만원 (자기자본 대비 16.4%) |
|||||
| 2025년 1분기말 | 세전손실 : (4,903)백만원 자기자본 : 38,279백만원 (자기자본 대비 12.8%) |
|||||
| (3) 자본잠식 등 | 최근 사업연도말 현재 자본잠식률이 100분의 50 이상인 경우 | - | - | 현재 미해당 | 2024년말 | 자본금 : 28,027백만원 지배주주지분 : 43,182백만원 자본잠식률 : 해당없음 |
| 2025년 1분기말 | 자본금 : 28,027백만원 지배주주지분 : 38,279백만원 자본잠식률 : 해당없음 |
|||||
| (4)자기자본 미달 | 최근 사업연도말 현재 자기자본이 10억원 미만인 경우 | - | - | 현재 미해당 | 2024년말 | 지배주주지분 : 43,182백만원 |
| 2025년 1분기말 | 지배주주지분 : 38,279백만원 | |||||
| (5) 시가총액 미달 | 보통주 시가총액 40억원미만 30일간 지속 - 천재지변, 시장상황의 급격한 변동 등으로 거래소가 시장 관리를 위하여 필요하다고 인정될 경우 적용배제 가능 |
- | - | 현재 미해당 | 2024년 12월 31일 |
시가총액 : 113,229백만원 |
| 증권신고서 제출일 전일 기준 |
시가총액 : 84,754백만원 |
|||||
| (6) 정기보고서 미제출 | 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않은 경우 | - | - | 현재 미해당 | 현재 기준 | 현재 특이사항 없음 |
| (7) 지배구조 미달 | 최근 사업연도 사업보고서상 A)사외이사의 수가 「상법」 제542조의8의 규정에서 정하는 수에 미달하는 경우 B) 「상법」 제542조의11의 규정에서 정하는 감사위원회를 구성하지 않거나 감사위원회의 구성요건을 충족하지 못하는 경우 *「상법」 제542조의8에 의거 자산총액 1,000억원 미만의 코스닥 상장 벤처기업은 사외이사 선임 의무 면제 **「상법」 제542조의11에 의거 자산총액 2조원 미만의 상장회사는 감사위원회 설치 의무 면제 |
- | - | 현재 미해당 | 2024년말 | 현재 특이사항 없음 |
| (8) 거래량 미달 | 분기월평균거래량이 유동주식수의 1%에 미달 다만, 다음 어느 하나에 해당하는 경우에는 이 호에 적용 받지 않습니다. - 신규상장법인(신규상장일이 속하는 분기에 한정) - 분기의 월평균거래량 1만주 이상(액면가액 5,000원 기준) - 「코스닥시장 업무규정」(이하 “업무규정”이라 한다) 제12조의3제1항에 따른 유동성공급계약이 체결된 경우 - 소액주주가 소유한 보통주식의 총수가 유동주식수의 100분의 20 이상이고, 해당 소액주주의 수가 300명 이상인 경우. |
- | - | 현재 미해당 | 2025년 1분기말 | 소액주주 - 지분율 77.58% - 19,291명 |
| (9) 주식분산 미달 | 소액주주 200인미만 or 소액주주지분 20%미만 - 300인이상의 소액주주가 유동주식수의 10%이상으로서 100만주이상을 소유, 해외증권시장에 상장된 경우는 적용배제 |
- | - | 현재 미해당 | 2025년 1분기말 | 소액주주 - 지분율 77.58% - 19,291명 |
| (10) 회생절차 개시신청 | "채무자 회생 및 파산에 관한 법률" 제34조에 의한 회생 절차개시 신청이 있는 경우 | - | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| (11) 파산신청 | 코스닥시장 상장법인에 대하여 "채무자 회생 및 파산에 관한 법률" 제294조에 의한 파산신청이 있는 경우 | - | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| (12) 기타 | - 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 - 변경·추가상장이 유예된 기간 중에「증권의 발행 및 공시 등에 관한 규정」에 따른 재무관리기준을 위반한 경우 |
- | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| 출처)「코스닥시장 상장규정」, 당사 정기보고서 |
| 주1) 상기 도표 중 (1)매출액 미달 요건 관련하여, 별도재무제표를 기준으로 합니다. 그 외 요건은 연결재무제표를 기준으로 합니다. |
| 주2) (2)법인세비용차감전계속사업손실 요건 관련하여, 자기자본은 비지배지분을 제외하지 않은 금액 기준을 적용합니다. (3)자본잠식 등, (4)자기자본 미달 요건 관련하여, 자기자본은 비지배지분을 제외한 지배기업지분금액 기준을 적용합니다. |
또한, 2025년 01월 21일, 정부와 유관기관(금융위원회, 금융감독원, 한국거래소, 금융투자협회)은 주식시장의 질적수준 제고를 위한「IPO 및 상장 폐지 제도개선 방안」을 발표하였습니다. 이 중 상장폐지 제도개선 방안은 상장유지 요건을 강화하고, 절차는 효율화함으로써 주식시장 내 저성과 기업을 적시에 퇴출시키고 상장기업의 밸류업을 주요 목적으로 하고 있습니다. 이와 같은 상장폐지 요건이 강화됨에 따라 당사의 영업환경 악화, 재무요건 악화 등을 원인으로 강화된 상장폐지 요건에 해당되어 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있음을 투자자분들은 유의하시기 바랍니다.
| [IPO 및 상장 폐지 제도개선 방안 및 해당여부 검토] |
| 구 분 | IPO 및 상장 폐지 제도개선 방안 | 상장폐지 지정요건 적용여부 |
회사현황 | |
|---|---|---|---|---|
| 사업연도 | 금액(백만원) / 내용 | |||
| (1) 시가총액 요건 기준 강화 | 정량요건으로서 시장평가 관련 시가총액 기준을 단계적으로 상향하여 코스피 500억원, 코스닥 300억원을 목표로 합니다. - 코스피 : 50억원(현행) → 200억원(2026년) → 300억원(2027년) → 500억원(2028년) - 코스닥 : 40억원(현행) → 150억원(2026년) → 200억원(2027년) → 300억원(2028년) |
현재 미해당 | 2024년 12월 31일 |
시가총액 : 113,229백만원 |
| 증권신고서 제출일 전일 기준 |
시가총액 : 84,754백만원 |
|||
| (2) 매출액 요건 기준 강화 | 정량요건으로서 기업실적 관련 매출액 기준을 단계적으로 상향하여 코스피 300억원(시가총액 1,000원 미만 기업만 적용), 코스닥 100억원(시가총액 600억원 미만 기업만 적용)을 목표로 합니다. - 코스피 : 50억원(현행) → 100억원(2027년) → 200억원(2028년) → 300억원(2029년) - 코스닥 : 30억원(현행) → 50억원(2027년) → 75억원(2028년) → 100억원(2029년) |
현재 미해당 | 2024년말 | 매출액 : 7,746백만원 (K-IFRS 별도기준) |
| 2025년 1분기말 | 매출액 : 954백만원 (K-IFRS 별도기준) |
|||
| (3) 감사의견 미달 요건 기준 강화 | - 2회 연속 감사의결 미달시 즉시 상장폐지 : 감사의견 미달(한정, 부적정, 의견거절)의 경우 2회 연속발생시 즉시 상장폐지되고(회생 ·워크아웃기업에 대해서는 예외인정), 이의신청은 허용되지 않습니다. | 현재 미해당 | 2024년말 | 해당사항 없음 |
| 2023년말 | 해당사항 없음 | |||
| 출처) 금융위원회, 당사 정기보고서 |
상세 내용은 본 증권신고서 "제1부. - III.투자위험요소 - 2.회사위험 - 마. 관리종목 편입 및 상장폐지 가능성에 따른 위험을 참고하여 주시기 바랍니다.
(주21) 정정 전
3. 기업실사 일정 및 주요 내용
| 일자 | 실사 내용 |
|---|---|
| 2025.04.24 | * 발행회사 방문 - 자금조달 금액, 목적 등 발행회사 의견 청취 - 공시 및 뉴스 등을 통한 발행회사 및 소속 산업 사전조사 - 주요사항 및 일정 체크 - 실사 사전 요청자료 송부 |
| 2025.04.25 ~ 2025.04.29 |
* 발행회사 및 해당 산업 조사 - 실사 사전 요청 자료 송부 - 관련 Q&A 등 * 유상증자 리스크검토 - 발행시장 상황, 자금조달규모 적정성, 공모가액 희망 할인율 |
| 2025.04.30 | * 발행회사 방문 - 공시 및 뉴스 내용 등을 통한 발행회사 및 산업 이해 - 발행회사 및 산업 관련 Q&A - 발행시장 상황, 자금조달 규모 적정성, 최대주주 및 주요주주 청약 참여 등 유상증자 관련 리스크 검토 |
| 2025.05.01 ~ 2025.05.06 |
* 실사 사전 요청 자료 목록 및 Check List 제공 |
| 2025.05.07 | * 현장 방문을 통한 실사 * Due-diligence checklist에 따라 투자위험요소 실사 1) 사업위험관련 실사 - 영위중인 사업의 임상 진행현황 및 기술적 진입 난이도 - 경쟁사 대비 유효성 및 장단점 확인 - 신규 사업에 대한 세부사항 체크 2) 회사위험관련 실사 - 재무관련 위험 등 체크 |
| 2025.05.08 ~ 2025.05.28. |
* 실사 추가 자료 요청 * 발행 세부일정 협의 * 기업실사 관련 Q&A 정리 |
| 2025.05.28 |
* 현장 방문을 통한 실사 * 투자위험요소 세부사항 체크 |
| 2025.05.28 ~ 2025.06.09 |
* 실사 추가자료 요청 * 증권신고서 작성 및 조언 * 이사회의사록 검토/인수계약서 작성 및 검토 * 실사이행보고서 작성 및 증권신고서 검토 |
(중략)
| 2025년 06월 10일 |
| 공동대표주관회사 : 삼성증권 주식회사 |
| 대표이사 박 종 문 |
| 공동대표주관회사 : NH투자증권 주식회사 |
| 대표이사 윤 병 운 |
(주21) 정정 후
3. 기업실사 일정 및 주요 내용
| 일자 | 실사 내용 |
|---|---|
| 2025.04.24 | * 발행회사 방문 - 자금조달 금액, 목적 등 발행회사 의견 청취 - 공시 및 뉴스 등을 통한 발행회사 및 소속 산업 사전조사 - 주요사항 및 일정 체크 - 실사 사전 요청자료 송부 |
| 2025.04.25 ~ 2025.04.29 |
* 발행회사 및 해당 산업 조사 - 실사 사전 요청 자료 송부 - 관련 Q&A 등 * 유상증자 리스크검토 - 발행시장 상황, 자금조달규모 적정성, 공모가액 희망 할인율 |
| 2025.04.30 | * 발행회사 방문 - 공시 및 뉴스 내용 등을 통한 발행회사 및 산업 이해 - 발행회사 및 산업 관련 Q&A - 발행시장 상황, 자금조달 규모 적정성, 최대주주 및 주요주주 청약 참여 등 유상증자 관련 리스크 검토 |
| 2025.05.01 ~ 2025.05.06 |
* 실사 사전 요청 자료 목록 및 Check List 제공 |
| 2025.05.07 | * 현장 방문을 통한 실사 * Due-diligence checklist에 따라 투자위험요소 실사 1) 사업위험관련 실사 - 영위중인 사업의 임상 진행현황 및 기술적 진입 난이도 - 경쟁사 대비 유효성 및 장단점 확인 - 신규 사업에 대한 세부사항 체크 2) 회사위험관련 실사 - 재무관련 위험 등 체크 |
| 2025.05.08 ~ 2025.05.28. |
* 실사 추가 자료 요청 * 발행 세부일정 협의 * 기업실사 관련 Q&A 정리 |
| 2025.05.28 |
* 현장 방문을 통한 실사 * 투자위험요소 세부사항 체크 |
| 2025.05.28 ~ 2025.06.09 |
* 실사 추가자료 요청 * 증권신고서 작성 및 조언 * 이사회의사록 검토/인수계약서 작성 및 검토 * 실사이행보고서 작성 및 증권신고서 검토 |
| 2025.06.17 ~ 2025.06.23 |
* 실사 추가 자료 요청 * (정정) 증권신고서 작성 / 검토 * (정정) 실사이행보고서 작성 및 증권신고서 검토 |
4. 기업실사 참여자
[공동대표주관회사]
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 | 참여기간 | 주요 경력 |
|---|---|---|---|---|---|---|
| 삼성증권(주) | Corporate Finance3팀 | 김준한 | 그룹장 | 기업실사 총괄 | 2025년 05월 08일 ~ 2025년 06월 23일 |
기업금융업무 27년 |
| 삼성증권(주) | Corporate Finance3팀 | 강동진 | 이사 | 기업실사 책임 | 2025년 05월 08일 ~ 2025년 06월 23일 |
기업금융업무 19년 |
| 삼성증권(주) | Corporate Finance3팀 | 홍지연 | 과장 | 기업실사 실무 | 2025년 05월 08일 ~ 2025년 06월 23일 |
기업금융업무 8년 |
| 삼성증권(주) | Corporate Finance3팀 | 김정현 | 대리 | 기업실사 실무 | 2025년 05월 08일 ~ 2025년 06월 23일 |
기업금융업무 2년 |
| 삼성증권(주) | ECM1팀 | 김한룡 | 부장 | 기업실사 실무 | 2025년 05월 08일 ~ 2025년 06월 23일 |
기업금융업무 9년 |
| 삼성증권(주) | ECM1팀 | 이근영 | 대리 | 기업실사 실무 | 2025년 05월 08일 ~ 2025년 06월 23일 |
기업금융업무 2년 |
| NH투자증권 | SME부 | 김기훈 | 이사 | 기업실사 총괄 | 2025년 04월 24일 ~ 2025년 06월 23일 |
기업금융업무 12년 |
| NH투자증권 | SME부 | 노동혁 | 차장 | 기업실사 책임 | 2025년 04월 24일 ~ 2025년 06월 23일 |
기업금융업무 9년 |
| NH투자증권 | SME부 | 김건 | 대리 | 기업실사 실무 | 2025년 04월 24일 ~ 2025년 06월 23일 |
기업금융업무 5년 |
(중략)
| 2025년 06월 24일 |
| 공동대표주관회사 : 삼성증권 주식회사 |
| 대표이사 박 종 문 |
| 공동대표주관회사 : NH투자증권 주식회사 |
| 대표이사 윤 병 운 |
(주22) 정정 전
나. 공모자금 세부 사용목적
당사는 금번 유상증자를 통해 조달된 자금을 골관절염 치료제(OSCA(구.Furestem-OA Kit Inj.)) 및 아토피 피부염 치료제(Furestem-AD Inj.)의 연구개발비(국내 및 해외 임상시험 수행비, 장기추적조사), 당사 배양 지방줄기세포(제2종 재생의료)의 일본재생의료 시장 공급, 국내첨생법 사업 진출 및 오가노이드 연구개발 위한 운영 경비, 그리고 첨단줄기세포 GMP 시설투자, 기타 운영경비 및 채무상환자금으로 사용할 계획입니다. 금번 유상증자 자금 사용의 우선순위는 아래와 같습니다.
| [금번 유상증자 자금사용의 우선순위] |
| (단위 : 원) |
| 우선순위 | 자금용도 | 세부 내용 | 사용(예정)시기 | 금 액 |
|---|---|---|---|---|
| 1 | 운영자금(임상시험비) | 골관절염 치료제(국내 임상) | 2025년 하반기 ~ 2028년 | 14,200,000,000 |
| 골관절염 치료제(해외 임상) | 5,900,000,000 | |||
| 아토피 치료제(장기추적조사) | 2026년 ~ 2028년 | 2,600,000,000 | ||
| 2 | 운영자금(운영경비) | 일본재생의료/국내첨생법 사업 | 2025년 하반기 ~ 2028년 | 5,905,000,000 |
| 오가노이드 연구개발 | 6,340,000,000 | |||
| 시설자금 | GMP 시설투자 | 2026년 ~ 2028년 | 4,010,000,000 | |
| 3 | 운영자금(운영경비) | 기타운영경비 | 2026년 ~ 2028년 | 7,830,000,000 |
| 4 | 채무상환자금 | GMP 시설 취득 용도 차입금 상환 | 2025년 하반기 ~ 2028년 | 1,400,000,000 |
| - | 기타자금 | 발행제비용 | - | 1,025,000,000 |
| 합 계 | 49,210,000,000 | |||
| 주1) 상기 금액은 예정발행가액을 기준으로 산정한 금액으로 모집가액 확정 시 변경될 수 있습니다. |
| 주2) 자금의 사용 시기는 증권신고서 제출일 전일 기준으로 작성되었으며, 향후 실제자금 집행 과정에서 금액 또는 사용시기가 변경될 수 있습니다. |
(1) 운영자금(임상시험비)
| [임상시험에 따른 세부 자금 사용 계획] | |
| (단위:백만원) | |
| 우선 순위 |
적응증 | 구분 | 구성 | 2023년 증자 잔액 (2025.03.31 기준) |
2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고사항 |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 골관절염 치료제 (OSCA) |
국내임상 2a상 |
임상 기관연구비 | 1,181 | 250 | 500 | 100 | - | 850 | *주요 임상 비용 1. 2a 임상시험 기간(FPI-LPO): 2025. 03-2026. 04 2. 2a 위약군에 대해 1년 시점의 보상투여 관련 비용은 장기추적조사에 포함됨 |
| CRO | 811 | 1,100 | 2,500 | 500 | - | 4,100 | ||||
| 위탁연구개발비 | -834 | 50 | 100 | 100 | - | 250 | ||||
| 인허가 | 63 | 19 | 611 | 178 | 16 | 825 | ||||
| 약물감시 | 157 | - | 932 | 283 | 24 | 1,239 | ||||
| 기타 임상진행비 | 123 | - | 1,253 | 437 | 83 | 1,772 | ||||
| 소계 | 1,501 | 1,419 | 5,896 | 1,598 | 123 | 9,036 | - | |||
| 장기추적조사(K0701-E) | 임상 기관연구비 | -38 | - | - | 300 | 300 | 600 | *주요 비용 1. LTFU 기간(EV1-EV5): ~2031. 3Q (2a 위약군 보상투여 개시 +5년) 2. Scope: 1상 + 2a (위약군 보상투여 포함) - 총 118명 대상 3. 방문시점: 12M/24M/60M |
||
| CRO | 806 | - | - | 1,000 | 1,000 | 2,000 | ||||
| 위탁연구개발비 | 136 | - | - | - | - | - | ||||
| 인허가 | 3 | - | - | 279 | 462 | 741 | ||||
| 약물감시 | 491 | - | - | 212 | 709 | 921 | ||||
| 기타 임상진행비 | 855 | - | - | - | 955 | 955 | ||||
| 소계 | 2,252 | - | - | 1,791 | 3,426 | 5,217 | - | |||
| 해외임상 | GAP분석/RFD | - | 8 | 50 | - | - | 130 | *주요 일정: 1. 융복합제제에 대한 분류 (CAM의 FDA 분류지정): 4Q 2025 2. US preIND Meeting: 3Q/4Q 2026 3. US preIND 보완사항 F/U 4. US IND 승인 5. RMAT/BTD 지정 *주요 비용: -Pre-IND & IND: 관련 신청 및 F/U에 필요한 CRO 비용 및 부대비용 -RMAT & BTD: 준비 및 지정에 필요한 전체비용 -IP supply: 해외임상시험 수행을 위해 필요한 IP 공급방식/밸리데이션/임대료/물품 등 제반사항의 준비비용 -CMC/Preclinical/Clinical: 해외임상시험 승인을 위해 추가/보완/임상시험 디자인 등의 준비에 필요한 비용 |
||
| Pre-IND | - | 80 | 200 | - | - | 280 | ||||
| IND | - | - | 150 | 150 | - | 300 | ||||
| RMAT | - | - | 50 | 50 | - | 100 | ||||
| BTD | - | - | 50 | 50 | - | 100 | ||||
| IP supply 준비 | - | 50 | 200 | 500 | - | 750 | ||||
| Preclinical | - | - | 200 | 100 | - | 300 | ||||
| CMC | - | - | 300 | 300 | - | 600 | ||||
| Clinical | - | - | 300 | 300 | - | 600 | ||||
| 인허가 | - | 45 | 283 | 291 | - | 619 | ||||
| 약물감시 | - | 68 | 424 | 436 | - | 928 | ||||
| 기타 임상진행비 | - | 91 | 565 | 582 | - | 1,238 | ||||
| 소계 | - | 414 | 2,772 | 2,759 | - | 5,945 | - | |||
| 합계 | 3,752 | 1,833 | 8,668 | 6,147 | 3,549 | 20,198 | - | |||
| 1 | 아토피 피부염 치료제 (Furestem-AD Inj.) |
장기추적조사 | 임상 기관연구비 | -74 | - | 200 | 200 | 200 | 600 | *주요 비용 1. LTFU 기간(EV1-EV5): ~2030 2. Scope: 3상(단회) (위약군 보상투여 포함) - 총 315명 3. 방문시점: 12M/24M/60M |
| CRO | 128 | - | 280 | 300 | 300 | 880 | ||||
| 위탁연구개발비 | -4 | - | - | - | - | - | ||||
| 인허가 | 199 | - | - | 149 | 99 | 248 | ||||
| 약물감시 | 645 | - | - | 228 | 154 | 383 | ||||
| 기타 임상진행비 | 851 | - | - | 278 | 184 | 462 | ||||
| 소계 | 1,745 | - | 480 | 1,155 | 938 | 2,572 | - | |||
| 총합계 | 5,497 | 9,148 | 7,303 | 4,487 | 22,770 | - | ||||
| 출처) 당사 정기보고서 및 당사 제시 |
| 주1) CRO비용에는 영상의학평가, Lab 분석비용 등이 포함되어 있습니다. |
| 주2) 인허가 비용에는 임상에 필요한 각종 인허가비용과 등록비용 그리고 담당인력의 인건비가 포함되어 있습니다. |
| 주3) 약물감시 비용에는 임상에 투여하는 약물에 대한 모니터링 비용과 담당인력의 인건비가 포함되어 있습니다. |
| 주4) 기타 임상진행비에는 임상에 필요한 물품과 약품 제조비용 그리고 담당인력의 인건비가 포함되어 있습니다. |
| 주5) 상기 '2023년 증자 잔액' 합계는 골관절염 치료제(OSCA) 국내임상시험비/장기추적 및 아토피 치료제(퓨어스템-에이디주) 장기추적에 해당하는 잔액만 포함하고 있으며, 나머지 잔액을 포함하고 있지 않습니다. |
(중략)
(2) 운영자금(운영경비) 및 시설자금
| [운영자금(운영경비) 사용 계획] | |
| (단위:백만원) | |
| 우선 순위 |
구분 | 구성 | 2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고 |
|---|---|---|---|---|---|---|---|---|
| 2 | 운영자금(운영경비) | 일본재생의료/국내첨생법 사업 | 600 | 2,000 | 1,650 | 1,655 | 5,905 | - 일본재생의료 공급 및 국내 첨단재생바이오법 개정안 시행에 따른 준비 비용 |
| 운영자금(운영경비) | 오가노이드 연구개발 | 150 | 990 | 2,340 | 2,860 | 6,340 | - 피부 및 췌도 오가노이드 임상 전 연구소의 연구인건비 및 재료비 등의 개발 비용 | |
| 시설자금 | GMP 시설투자 | - | 2,537 | - | 1,473 | 4,010 | - 신규시설 투자 및 기존 노후 시설 개보수 |
|
| 합 계 | 750 | 5,527 | 3,990 | 5,988 | 16,255 | |||
| 출처) 당사 제시 |
(2)-1 일본재생의료/국내첨생법 사업
당사는 일본 재생의료시장 진출을 위해 2024년 일본 후생노동성에 제1종(동종제대혈줄기세포(를 이용한 아토피 피부염 치료)) 및 제2종(자가지방줄기세포) 재생의료 제공계획에 대한 심의 및 승인 절차를 진행하였습니다. 제2종(자가지방줄기세포)의 경우, 특정인정재생의료위원회의 심의를 거쳐 승인을 받고, 2025년 2월 후생노동성 최종 승인까지 완료되었습니다. 현재 일본 내 공급을 위해 동경, 오사카, 나고야 소재의 현지 의료기관과 계약을 완료하였으며, 2분기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 이에 금번 조달 자금 중 2,500백만원은 제2종(자가지방줄기세포)의 일본재생의료 시장 진출 및 공급을 위해 사용할 계획입니다.
한편, 국내 첨단재생바이오법 개정안 시행에 따라 첨단재생의료 기반 바이오 신약의 경우 첨생법에 따른 연구계획 및 치료계획이 승인되는 경우 환자에게 임상 목적이 아닌 치료 목적으로 첨단재생의료 치료를 제공할 수 있게되고, 매출을 발생시킬 수 있게 되었습니다. 따라서 기존 바이오 신약 대비 매출 발생 시점이 앞당겨짐과 동시에 매출 발생 경로 및 가능성이 확대되며, 이를 통해 자체 연구개발 비용을 충당함으로써 전체적인 연구개발 안정성을 증대시킬 수 있게 되었습니다. 당사 주요 파이프라인 치료제의 대상 적응증인 중증아토피와 골관절염은 난치질환에 해당되며, 첨단재생바이오법 개정에 따라 당사의 아토피 피부염 치료제(퓨어스템-에이디 주)와 골관절염 치료제(OSCA)를 조기에 사용할 수 있도록 금번 조달 자금 중 3,405백만원은 협력 의료기관을 통한 해당 파이프라인의 임상 연구 지원, IP 생산 등을 위해 사용할 계획입니다.
| [일본재생의료/국내첨생법 사업 비용 상세 내역] | |
| (단위:백만원) | |
| 구성 | 2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고 | |
|---|---|---|---|---|---|---|---|
| 일본재생의료 사업 | - 일본내 유통망구축, 공급용 해동기 구매, 해외 공급용 안전재고 확보, 기본 운영 등을 위한 비용 | ||||||
| 해외 유통망 구축 | 150 | 700 | 350 | 350 | 1,550 | ||
| 공급설비(해동기 등)구입/안전재고 확보 | 100 | 200 | 200 | 200 | 700 | ||
| 운영비용 | 50 | 100 | 50 | 50 | 250 | ||
| 소계 | 300 | 1,000 | 600 | 600 | 2,500 | ||
| 국내 첨생법 개정에 따른 사업 | - 국내 첨단재생바이오법 개정안 시행에 따른 임상기관에 대한 연구 지원, IP생산 등을 위한 비용 | ||||||
| 임상연구 지원 | 100 | 200 | 200 | 200 | 700 | ||
| IP생산 | 200 | 800 | 850 | 855 | 2,705 | ||
| 소계 | 300 | 1,000 | 1,050 | 1,055 | 3,405 | ||
| 합 계 | 600 | 2,000 | 1,650 | 1,655 | 5,905 | ||
| 출처) 당사 제시 |
(2)-2 오가노이드 연구개발
당사는 기타 파이프라인 중 하나로 오가노이드를 연구개발 중에 있습니다. 오가노이드란 장기유사체 혹은 미니 장기라고도 불리며, 당사의 피부 오가노이드 기술은 공기-액체 계면(ALI) 배양을 통해 불필요한 연골 조직의 형성을 억제하여 기존 기술의 한계를 극복하고 실제 피부와 같은 평평한 구조를 형성하여 정상피부와 기능적으로 동등한 피부 오가노이드 플랫폼을 구축하고자 합니다. 최근 선진국 중심으로 동물 임상시험에 대한 규모를 축소 및 최종적으로는 타 시험법으로 완전히 대체하고자 하는 점진적 규제가 진행되는 중이기 때문에 오가노이드는 동물 임상시험 규제에 따른 가장 적합한 대체법 시험물로 잠재적 가능성이 있습니다. 또한, 당사의 오가노이드 기술은 어떠한 세포로도 분화가 가능한 유도만능줄기세포(iPSC) 기반으로 적응 분야를 확대하고 있으며, 현재 모발 오가노이드를 활용한 연구개발도 진행 중에 있습니다. 이에 당사는 오가노이드 R&D 비용으로 2028년까지 6,784백만원의 연구개발비 지출이 필요할 것으로 생각하고 있으며, 이는 2023년 증자 잔액 450백만원과 금번 조달 자금 중 6,340백만원으로 사용할 예정입니다.
| [오가노이드 연구개발 비용 상세 내역] | |
| (단위:백만원) | |
| 구성 | 2023년 증자 잔액 (2025.03.31 기준) |
2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고 |
|---|---|---|---|---|---|---|---|
| 원재료 구입 | 450 | 350 | 600 | 1,200 | 1,800 | 3,950 | -오가노이드 연구용 원재료 구입 -오가노이드 연구개발 인력 증원 반영 -27년부터 임상 시작 목표로 임상 관련 인허가/약물감시 등 반영 |
| 인건비 | 250 | 389 | 537 | 623 | 1,799 | ||
| 인허가 | - | - | 134 | 96 | 230 | ||
| 약물감시 | - | - | 200 | 144 | 345 | ||
| 기타 임상진행비 | - | - | 267 | 193 | 460 | ||
| 합계 | 450 | 600 | 989 | 2,338 | 2,856 | 6,784 | - |
| 출처) 당사 제시 |
(2)-3 시설자금 (GMP 시설투자)
금번 유상증자로 조달된 자금 중 4,010백만원을 활용하여 GMP 시설 투자에 사용할 예정입니다. 당사가 추진 중인 일본재생의료 사업 및 국내 첨단재생바이오법 개정안에 따른 사업 성장 시 2026년부터 신규시설 투자하여 생산 CAPA를 확대하고, 한편으로는 장비 노후화에 따라 2028년부터 기존 시설 개보수 투자를 진행하고자 합니다. 시설투자에 따른 자금사용의 상세 내역은 아래와 같습니다.
| [GMP 시설투자에 따른 세부 자금 사용 계획] | |
| (단위:백만원) | |
| 우선 순위 |
구분 | 구성 | 2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고사항 | |
|---|---|---|---|---|---|---|---|---|---|
| 2 | 일본재생의료/첨생법 | 신규시설투자 | - 2026년 이후 해당 사업 성장 시 사용 예정 - 제조실4 확장을 통한 재생의료 사업지원 - 생산 CAPA 20lot/월 ->최대 100lot/월 증가 : 제조 배양기 15대등 1090백만원 : 실험 유세포분석기등 1040백만원 |
||||||
| 건물 | - | - | - | - | - | ||||
| 연구기자재 | - |
2,277 | - | - | 2,277 | ||||
| 비품 | - | - | - | - | - | ||||
| 시설장치 | - | 60 | - | - | 60 | ||||
| 기타 | 200 | 200 | |||||||
| 소계 | - | 2,537 | - | - | 2,337 | - | |||
| 장비노후화에 따른 교체 투자 | 기존 시설 개보수 | - 배양기 노후화에 따른 교체투자 (수명주기 10년 도래) - 19년 설비투자된 약 50여대 대체액 반영 |
|||||||
| 건물 | - | - | - | - | - | ||||
| 연구기자재 | - | - | 1,300 | 1,300 | |||||
| 비품 | - | - | - | - | - | ||||
| 시설장치 | - | - | - | - | - | ||||
| 기타 | - | - | - | 173 | 173 | ||||
| 소계 | - | - | - | 1,473 | 1,473 | - | |||
| 합 계 | - | 2,537 | - | 1,473 | 4,010 | - | |||
| 출처) 당사 제시 |
(3) 기타운영경비 (GMP 및 본사 경비)
금번 유상증자로 조달된 자금 중 연구소와 치료제 및 임상약물제조를 담당하는 GMP의 시설관리에 사용되는 전력비, 수수료 등 실험약물제조경비로 약 7,830백만원이 소요될 예정입니다. 이는 GMP 생산, 운영, 본사 운영과 관련하여 직간접적으로 필요한 비용으로 월 평균 250~300백만원 수준으로 집행할 예정입니다.
| [기타운영경비(GMP 및 본사 경비) 비용 상세 내역] |
|
| (단위:백만원) | |
| 구성 | 2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고 |
|---|---|---|---|---|---|---|
| 지급수수료 | - | - | 1,720 | 1,806 | 3,526 | - GMP 및 본사 경비: 전력비, 수수료, GMP 실험약물제조를 위한 경비 등 - GMP생산,운영, 본사 운용과 관련한 직간접적으로 필요한 경비 등 |
| 연구기자재와 시설장치 운영비 | - | 504 | 529 | 556 | 1,589 | |
| 수선소모품비 | - | - | 529 | 556 | 1,085 | |
| 세금과공과 | - | - | 132 | 139 | 271 | |
| 관리비 | - | - | 662 | 694 | 1,356 | |
| 합계 | - | 504 | 3,572 | 3,751 | 7,827 | - |
| 출처) 당사 제시 |
(4) 채무상환자금
금번 유상증자로 조달된 자금 중 1,400백만원을 활용하여 부채비율 개선, 금융비용 절감을 위해 시설자금 차입금을 상환할 예정입니다. 당사는 2017년 GMP 시설 및 연구소 취득을 위해 중소기업시설자금을 차입하였으며, 금번 유상자금으로 매반기 200백만씩 분할 상환 중인 해당 차입금 총 1,400백만원을 2028년까지 상환할 예정입니다. 금번 유상증자 자금조달로 차입금 일부를 상환함으로써 이자비용을 절감하고 재무구조 건전성을 확보하고자 합니다. 자금사용의 상세 내역은 아래와 같습니다.
| [상환 예정인 차입금 상세 현황] | |
| (기준일: 2025.06.09) | (단위: 백만원) |
| 차입처 | 내역 | 최초 대여일 | 만기일 | 이자율 | 잔액 | 상환예정금액 | 상환예정시기 |
|---|---|---|---|---|---|---|---|
| 기업은행 | 중소기업시설자금 | 2017.06.08 | 2032.06.08 | 4.95% | 2,800 | 200 | 2025년 하반기 |
| 2017.06.08 | 2032.06.08 | 4.95% | 2,600 | 400 | 2026년 | ||
| 2017.06.08 | 2032.06.08 | 4.95% | 2,200 | 400 | 2027년 | ||
| 2017.06.08 | 2032.06.08 | 4.95% | 1,800 | 400 | 2028년 | ||
| 합 계 | 1,400 | 1,400 | |||||
| 출처) 당사 제시 |
(중략)
(2) 줄기세포 치료제의 일본 및 국내(첨생법) 재생의료사업 진출 추진
당사는 안정적인 수익 기반을 확보하기 위해 일본 재생의료 시장 및 국내(첨생법) 재생의료 사업 진출을 계획하고 있습니다. 일본 재생의료시장 진출을 위해 2024년 일본 후생노동성에 제1종(동종제대혈줄기세포) 및 제2종(자가지방줄기세포) 재생의료 제공계획에 대한 심의 및 승인 절차를 진행하였습니다. 제2종(자가지방줄기세포)의 경우, 2025년 2월 후생노동성 최종 승인까지 완료되어 2분기부터 일본 내 환자 투여를 계획하고 있습니다. 이에 금번 조달 자금의 일부는 일본 현지 환자 수급을 위한 본격적인 영업활동 및 투자를 진행을 위한 운영자금으로 활용될 예정입니다
(3) 기타 파이프라인 연구개발 투자 및 지속 가능한 성장 기반 마련
당사는 기타 파이프라인 중 하나로 오가노이드를 연구개발 중에 있습니다. 특히 당사의 피부 오가노이드 기술의 경우, 공기-액체 계면(ALI) 배양을 통해 불필요한 연골 조직의 형성을 억제하여 실제 피부와 같은 평평한 구조를 완벽 재현하여 다양한 유효물질에 대한 약물 스크리닝 및 효력평가 등에 적용 가능하여, 일부 대형 글로벌 제약사들로부터 관심을 받고 있는 상황입니다. 이러한 파이프라인들의 포트폴리오를 지속적으로 확장하기 위해서는 선제적이고 적극적인 연구개발 투자가 필수적입니다. 이는 단기적인 성과뿐만 아니라 중장기적인 기업 성장의 발판을 마련하는 데 중요한 역할을 할 것입니다.
(4) 실권주 일반공모를 통한 투자자 참여 기회 확대
당사는 주주배정 후 실권주 일반공모 방식을 채택함으로써 기존 주주의 권리를 보호하는 동시에 신규 투자자들에게도 투자 기회를 제공하고자 합니다. 이를 통해 기존 주주들의 지분희석화를 최소화함과 동시에 실권주 일반공모를 통해 다양한 투자자층을 확보하고 기업의 지속 가능한 성장을 위한 기반을 마련할 것입니다.
상기한 바와 같이, 당사는 금번 유상증자를 통해 조달되는 자금을 핵심 파이프라인의 경쟁력 강화, 재생의료 시장 진출 및 추가 성장 동력 확보라는 명확한 목표 하에 투명하고 효율적으로 사용할 계획입니다. 이를 통해 기업가치를 지속적으로 증대시키고, 궁극적으로 주주분들의 이익을 극대화하기 위한 최선의 노력을 다할 것입니다.
마. 주주 권익 보호를 위한 사항
당사는 금번 유상증자로 인해 주주들의 지분이 다소 희석될 수 있음을 충분히 인지하고 있으며, 이에 따라 유상증자 이후의 명확한 비전 제시 등을 통해 지속적으로 주주 소통을 강화할 예정입니다. 금번 유상증자 납입대금을 전략적으로 사용하여 회사의 경쟁력을 강화할 예정이며 이를 통해 기업 가치 상승을 유도하여 중장기적으로 주주 가치를 극대화하도록 노력할 예정입니다.
1) 주주와의 소통 강화 방안
당사는 주주 대상으로 적극적인 IR 활동을 통해 주주 신뢰를 제고하기 위해 노력할 계획입니다. 또한, 당사는 2025년 06월 10일 증권신고서 공시 직후, 금번 주주배정 유상증자 결정과 관련된 주요 내용을 주주들에게 설명하기 위하여 당사 홈페이지 주주 서한을 게재할 계획입니다.
가) IR자료 및 보도자료 배포를 통한 회사에 대한 이해도 증진
당사는 소액주주의 정보 접근성을 높이고 소통을 활성화하여 주주 권익을 보호하고자 합니다. 구체적으로 당사는 추후 당사 홈페이지에 IR 자료를 즉시 게재하여 주주들이 관련 내용을 신속하게 확인할 수 있도록 할 예정입니다. 더불어, 당사는 유상증자와 관련된 전반적인 내용을 다양한 이해관계자들이 확인할 수 있도록 보도자료를 배포할 예정입니다. 이를 통해 개인, 기관, 외국인 투자자 등 다양한 이해관계자들에게 언론을 통해 당사의 비전과 전략을 정확히 전달할 수 있도록 노력할 계획입니다.
나) 투자설명회(IR) 개최
당사는 공모 유상증자 기간 중 오프라인 투자설명회(IR)를 개최하여 질의응답 세션을 운영하여 당사의 경영전략에 대해 충분히 이해할 수 있도록 진행할 계획입니다. 특히, 당사는 금번 유상증자의 목적 및 회사의 향후 성장 전략 등에 대해 주주분들에게 상세히 설명드리고 의견을 경청하기 위해 증권신고서 공시 익일인 2025년 06월 11일에 첫 번째 투자설명회(IR)를 개최할 예정입니다. 간담회의 구체적인 시간 및 장소, 참여 방법 등은 2025년 6월 10일 증권신고서 공시 직후 당사 홈페이지 공지를 통해 신속히 알려드리겠습니다. 또한, 추가적으로 주주분들의 수요를 조사하여 수도권 외에 지방거점에서도 투자설명회를 개최할 계획이 있습니다. 이를 통해 당사의 파이프라인 임상 현황, 기술이전 현황, 향후 비전 등을 상세히 설명하고 질의응답 시간을 통해 주주분들의 궁금증을 해소하겠습니다.
다) IR응대 전용 라인 강화를 통한 소통 강화
당사는 보다 적극적인 투자자 의사 소통 강화를 위해, 기존에 있는 IR응대 전용 라인을 강화할 계획입니다. IR 응대 전용 이메일 및 유선을 통해 유상증자와 관련한 문의에 신속하고 누락 없이 응대할 수 있도록 하겠습니다. 특히, 소액주주를 포함한 다양한 주주의 의견을 수렴할 수 있도록 당사와 사전 일정 조율 등을 신청한 소액주주에 대해서는 개별적인 대면 미팅 또는 유선 의견청취를 적극 활용하여 실시간 소통을 강화하겠습니다.
2) 주요 기관투자자 대상 IR 진행
주요 기관투자자 대상으로 IR을 진행하여 유상증자의 배경, 목적, 기대 효과와 당사의 중장기 사업전략 등에 대해 상세히 설명을 진행할 예정이며, 증권사 애널리스트 대상으로도 적극적으로 소통하여, 시장 내에 충분한 정보가 전달될 수 있도록 노력할 계획입니다.
당사는 상기와 같이 주주 및 시장과의 적극적인 소통을 통해 회사의 경영 전략 및 본 유상증자의 배경과 필요성을 명확히 전달하는 한편, 본 유상증자와 관련 후속 정보를 지속적으로 제공해 나가겠습니다.
바. 미사용 자금의 운용 계획
당사가 금번 유상증자를 통해 조달한 자금 중 일부 자금은 조달시기와 사용시기가 다소 차이가 생길 수 있습니다. 이에 조달로부터 사용 시까지 미사용 자금에 대해서는 자금 사용시점 및 금리에 따라 적격금융기관의 수시입출금 예금, 정기예금 등 금융상품 또는 A등급 이상의 단기금융상품으로 운용할 예정입니다.
(주22) 정정 후
나. 공모자금 세부 사용목적
당사는 금번 유상증자를 통해 조달된 자금을 골관절염 치료제(OSCA(구.Furestem-OA Kit Inj.)) 및 아토피 피부염 치료제(Furestem-AD Inj.)의 연구개발비(국내 및 해외 임상시험 수행비, 장기추적조사), 당사 배양 지방줄기세포(제2종 재생의료)의 일본재생의료 시장 공급, 국내첨생법 사업 진출 및 오가노이드 연구개발 위한 운영 경비, 그리고 첨단줄기세포 GMP 시설투자, 기타 운영경비 및 채무상환자금으로 사용할 계획입니다. 금번 유상증자 자금 사용의 우선순위는 아래와 같습니다.
| [금번 유상증자 자금사용의 우선순위] |
| (단위 : 원) |
| 우선순위 | 자금용도 | 세부 내용 | 사용(예정)시기 | 금 액 |
|---|---|---|---|---|
| 1 | 운영자금(임상시험비) | 골관절염 치료제(국내 임상) | 2025년 하반기 ~ 2028년 | 14,200,000,000 |
| 골관절염 치료제(해외 임상) | 5,900,000,000 | |||
| 아토피 치료제(장기추적조사) | 2026년 ~ 2028년 | 2,600,000,000 | ||
| 2 | 운영자금(운영경비) | 일본재생의료/국내첨생법 사업 | 2025년 하반기 ~ 2028년 | 5,905,000,000 |
| 오가노이드 연구개발 | 6,340,000,000 | |||
| 시설자금 | GMP 시설투자 | 2026년 ~ 2028년 | 4,010,000,000 | |
| 3 | 운영자금(운영경비) | 기타운영경비 | 2026년 ~ 2028년 | 7,830,000,000 |
| 4 | 채무상환자금 | GMP 시설 취득 용도 차입금 상환 | 2025년 하반기 ~ 2028년 | 1,400,000,000 |
| - | 기타자금 | 발행제비용 | - | 1,025,000,000 |
| 합 계 | 49,210,000,000 | |||
| 주1) 상기 금액은 예정발행가액을 기준으로 산정한 금액으로 모집가액 확정 시 변경될 수 있습니다. |
| 주2) 자금의 사용 시기는 증권신고서 제출일 전일 기준으로 작성되었으며, 향후 실제자금 집행 과정에서 금액 또는 사용시기가 변경될 수 있습니다. |
(1) 운영자금(임상시험비)
| [임상시험에 따른 세부 자금 사용 계획] |
| (단위:백만원) |
| 우선 순위 |
적응증 | 구분 | 구성 | 2023년 증자 잔액 (2025.03.31 기준) |
2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고사항 |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 골관절염 치료제 (OSCA) |
국내임상 2a상 |
임상 기관연구비 | 1,181 | 250 | 500 | 100 | - | 850 | *주요 임상 비용 1. 2a 임상시험 기간(FPI-LPO): 2025. 03-2026. 04 2. 2a 위약군에 대해 1년 시점의 보상투여 관련 비용은 장기추적조사에 포함됨 |
| CRO | 811 | 1,100 | 2,500 | 500 | - | 4,100 | ||||
| 위탁연구개발비 | -834 | 50 | 100 | 100 | - | 250 | ||||
| 인허가 | 63 | 19 | 611 | 178 | 16 | 825 | ||||
| 약물감시 | 157 | - | 932 | 283 | 24 | 1,239 | ||||
| 기타 임상진행비 | 123 | - | 1,253 | 437 | 83 | 1,772 | ||||
| 소계 | 1,501 | 1,419 | 5,896 | 1,598 | 123 | 9,036 | - | |||
| 장기추적조사(K0701-E) | 임상 기관연구비 | -38 | - | - | 300 | 300 | 600 | *주요 비용 1. LTFU 기간(EV1-EV5): ~2031. 3Q (2a 위약군 보상투여 개시 +5년) 2. Scope: 1상 + 2a (위약군 보상투여 포함) - 총 118명 대상 3. 방문시점: 12M/24M/60M |
||
| CRO | 806 | - | - | 1,000 | 1,000 | 2,000 | ||||
| 위탁연구개발비 | 136 | - | - | - | - | - | ||||
| 인허가 | 3 | - | - | 279 | 462 | 741 | ||||
| 약물감시 | 491 | - | - | 212 | 709 | 921 | ||||
| 기타 임상진행비 | 855 | - | - | - | 955 | 955 | ||||
| 소계 | 2,252 | - | - | 1,791 | 3,426 | 5,217 | - | |||
| 해외임상 | GAP분석/RFD | - | 8 | 50 | - | - | 130 | *주요 일정: 1. 융복합제제에 대한 분류 (CAM의 FDA 분류지정): 4Q 2025 2. US preIND Meeting: 3Q/4Q 2026 3. US preIND 보완사항 F/U: 2Q 2027 4. US IND 승인: 3Q/4Q 2027 5. RMAT/BTD 지정: 4Q 2027 *주요 비용: -Pre-IND & IND: 관련 신청 및 F/U에 필요한 CRO 비용 및 부대비용 -RMAT & BTD: 준비 및 지정에 필요한 전체비용 -IP supply: 해외임상시험 수행을 위해 필요한 IP 공급방식/밸리데이션/임대료/물품 등 제반사항의 준비비용 -CMC/Preclinical/Clinical: 해외임상시험 승인을 위해 추가/보완/임상시험 디자인 등의 준비에 필요한 비용 |
||
| Pre-IND | - | 80 | 200 | - | - | 280 | ||||
| IND | - | - | 150 | 150 | - | 300 | ||||
| RMAT | - | - | 50 | 50 | - | 100 | ||||
| BTD | - | - | 50 | 50 | - | 100 | ||||
| IP supply 준비 | - | 50 | 200 | 500 | - | 750 | ||||
| Preclinical | - | - | 200 | 100 | - | 300 | ||||
| CMC | - | - | 300 | 300 | - | 600 | ||||
| Clinical | - | - | 300 | 300 | - | 600 | ||||
| 인허가 | - | 45 | 283 | 291 | - | 619 | ||||
| 약물감시 | - | 68 | 424 | 436 | - | 928 | ||||
| 기타 임상진행비 | - | 91 | 565 | 582 | - | 1,238 | ||||
| 소계 | - | 414 | 2,772 | 2,759 | - | 5,945 | - | |||
| 합계 | 3,752 | 1,833 | 8,668 | 6,147 | 3,549 | 20,198 | - | |||
| 1 | 아토피 피부염 치료제 (Furestem-AD Inj.) |
장기추적조사 | 임상 기관연구비 | -74 | - | 200 | 200 | 200 | 600 | *주요 비용 1. LTFU 기간(EV1-EV5): ~2030 2. Scope: 3상(단회) (위약군 보상투여 포함) - 총 315명 3. 방문시점: 12M/24M/60M |
| CRO | 128 | - | 280 | 300 | 300 | 880 | ||||
| 위탁연구개발비 | -4 | - | - | - | - | - | ||||
| 인허가 | 199 | - | - | 149 | 99 | 248 | ||||
| 약물감시 | 645 | - | - | 228 | 154 | 383 | ||||
| 기타 임상진행비 | 851 | - | - | 278 | 184 | 462 | ||||
| 소계 | 1,745 | - | 480 | 1,155 | 938 | 2,572 | - | |||
| 총합계 | 5,497 | 9,148 | 7,303 | 4,487 | 22,770 | - | ||||
| 출처) 당사 정기보고서 및 당사 제시 |
| 주1) 상기 '비고사항'의 각 임상 및 장기추적조사의 주요 일정은 당사가 목표로 하는 일정이며, 임상 대상 환자모집 난관 등 예상치 못한 상황 발생에 따라 목표와 달리 일정이 지연될 가능성도 존재합니다. |
| 주2) 상기 '2023년 증자 잔액' 합계는 골관절염 치료제(OSCA) 국내임상시험비/장기추적 및 아토피 치료제(퓨어스템-에이디주) 장기추적에 해당하는 잔액만 포함하고 있으며, 나머지 잔액을 포함하고 있지 않습니다. |
상기 임상시험에 따른 세부 자금 계획 시 각 항목별 아래와 같은 비용을 포함하여 산정하였습니다.
| 구분 | 항목 | 내용 |
| 국내임상 및 장기추적조사 |
임상 기관연구비 | 임상 환자 모집에 따른 연구비, 검체 채취 및 임상병리 시험비용, 연구자/부연구자/연구간호사 등의 기본 인건비가 포함되어 있습니다. |
| CRO | 임상시험 수행에 따른 CRO 서비스에 대한 직접비용을 의미하며, 영상의학평가, Lab 분석비용, Lab 검사비용, 임상시험 수행을 위한 시스템(EDC, eCOA 등) 운용 비용 등이 포함되어 있습니다. | |
| 위탁연구개발비 | 위탁연구개발비는 임상시험기간 중 추가로 연구되어야 하는 작용기전 및 생물검정(bioassay)와 같은 비용, 그리고 이제까지 확보한 데이터에 대한 추가분석 및 해석을 위한 자문비용 등이 포함되어 있습니다. | |
| 인허가 | 임상에 필요한 각종 인허가비용과 등록비용 그리고 담당인력의 인건비등이 포함되어 있습니다. | |
| 약물감시 | 임상에 투여하는 약물에 대한 모니터링 비용, 장기추적조사 연차보고 및 안전성 관련 자문비용, 담당인력의 인건비 등이 포함되어 있습니다. | |
| 기타 임상진행비 | 임상과 관련된 논문 및 학회발표, 통계자문 비용, 담당인력의 인건비가 포함되어 있습니다. | |
해외임상 |
GAP분석/RFD | US FDA 관련 신청에 앞서 내부생성 자료에 대한 적합성 및 보완영역 평가 준비에 필요한 비용이 포함되어 있습니다. |
| Pre-IND & IND |
Pre-IND 및 IND의 각 신청 및 F/U에 필요한 각 CRO 비용 및 부대비용(출장 등) 등이 포함되어 있습니다. | |
| RMAT & BTD |
RMAT 및 BTD 각 준비 및 지정에 필요한 전체 비용 등이 포함되어 있습니다. | |
| IP supply 준비 | 해외임상시험 수행을 위해 필요한 IP 공급방식/밸리데이션/임대료/물품 등 제반사항의 준비비용 등이 포함되어 있습니다. | |
| Preclinical | 기존 비임상자료 정리, 번역, gap assessment, 추가 비임상 시험 또는 보완 비임상시험 수행, 후속 단계 IP에 대한 동등성연구 자료 검토 비용 등이 포함되어 있습니다. | |
| CMC | 기존 CMC 자료 정리 및 번역, gap assessment, cell banking 교체에 따른 계획 검토 및 보완, 미국 FDA 관련 규정에 따른 보완 및 수정사항 파악 관련 비용 등이 포함되어 있습니다. | |
| Clinical | 기존 1/2a 임상시험 데이터에 대한 해석, 미국 FDA DMOAD 가이드라인에 맞는 시놉시스 개발, PreIND meeting 관련 질의 및 대응 관련 비용 등이 포함되어 있습니다. | |
| 인허가 | FDA 가이드라인에 맞춰 허가요건을 검토하고 제반 서류 제출, 보완 조율 역할 등과 관련한 비용, 국내 담당인력의 인건비가 포함되어 있습니다. | |
| 약물감시 | 치료제 부작용이나 안정성 문제가 발생할 수 있으므로 임상에 투여하는 약물에 대한 지속한 모니터링이 필요합니다. 이와 관련한 모니터링 비용, 안전성 관련 자문 비용, 국내 담당인력의 인건비가 포함되어 있습니다. | |
| 기타 임상진행비 | 임상 진행에 필요한 물품과 약품 제조비용, 국내 담당인력의 인건비가 포함되어 있습니다. |
(중략)
(2) 운영자금(운영경비) 및 시설자금
| [운영자금(운영경비) 사용 계획] |
| (단위:백만원) |
| 우선 순위 |
구분 | 구성 | 2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고 |
|---|---|---|---|---|---|---|---|---|
| 2 | 운영자금(운영경비) | 일본재생의료/국내첨생법 사업 | 600 | 2,000 | 1,650 | 1,655 | 5,905 | - 일본재생의료 공급 및 국내 첨단재생바이오법 개정안 시행에 따른 준비 비용 |
| 운영자금(운영경비) | 오가노이드 연구개발 | 150 | 990 | 2,340 | 2,860 | 6,340 | - 피부 및 췌도 오가노이드 임상 전 연구소의 연구인건비 및 재료비 등의 개발 비용 | |
| 시설자금 | GMP 시설투자 | - | 2,537 | - | 1,473 | 4,010 | - 신규시설 투자 및 기존 노후 시설 개보수 |
|
| 합 계 | 750 | 5,527 | 3,990 | 5,988 | 16,255 | |||
| 출처) 당사 제시 |
(2)-1 일본재생의료/국내첨생법 사업
당사는 일본 재생의료시장 진출을 위해 2024년 일본 후생노동성에 제1종(동종제대혈줄기세포(를 이용한 아토피 피부염 치료)) 및 제2종(자가지방줄기세포) 재생의료 제공계획에 대한 심의 및 승인 절차를 진행하였습니다. 제2종(자가지방줄기세포)의 경우, 특정인정재생의료위원회의 심의를 거쳐 승인을 받고, 2025년 2월 후생노동성 최종 승인까지 완료되었습니다. 현재 일본 내 공급을 위해 동경, 오사카, 나고야 소재의 현지 의료기관과 계약을 완료하였으며, 2025년 하반기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 이에 금번 조달 자금 중 2,500백만원은 제2종(자가지방줄기세포)의 일본재생의료 시장 진출 및 공급을 위해 사용할 계획입니다.
한편, 국내 첨단재생바이오법 개정안 시행에 따라 첨단재생의료 기반 바이오 신약의 경우 첨생법에 따른 연구계획 및 치료계획이 승인되는 경우 환자에게 임상 목적이 아닌 치료 목적으로 첨단재생의료 치료를 제공할 수 있게되고, 매출을 발생시킬 수 있게 되었습니다. 따라서 기존 바이오 신약 대비 매출 발생 시점이 앞당겨짐과 동시에 매출 발생 경로 및 가능성이 확대되며, 이를 통해 자체 연구개발 비용을 충당함으로써 전체적인 연구개발 안정성을 증대시킬 수 있게 되었습니다. 당사 주요 파이프라인 치료제의 대상 적응증인 중증아토피와 골관절염은 난치질환에 해당되며, 첨단재생바이오법 개정에 따라 당사의 아토피 피부염 치료제(퓨어스템-에이디 주)와 골관절염 치료제(OSCA)를 조기에 사용할 수 있도록 금번 조달 자금 중 3,405백만원은 협력 의료기관을 통한 해당 파이프라인의 임상 연구 지원, IP 생산 등을 위해 사용할 계획입니다.
| [일본재생의료/국내첨생법 사업 비용 상세 내역] |
| (단위:백만원) |
| 구성 | 2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고 | |
|---|---|---|---|---|---|---|---|
| 일본재생의료 사업 | - 일본내 유통망구축, 공급용 해동기 구매, 해외 공급용 안전재고 확보, 기본 운영 등을 위한 비용 | ||||||
| 해외 유통망 구축 | 150 | 700 | 350 | 350 | 1,550 | ||
| 공급설비(해동기 등)구입/안전재고 확보 | 100 | 200 | 200 | 200 | 700 | ||
| 운영비용 | 50 | 100 | 50 | 50 | 250 | ||
| 소계 | 300 | 1,000 | 600 | 600 | 2,500 | ||
| 국내 첨생법 개정에 따른 사업 | - 국내 첨단재생바이오법 개정안 시행에 따른 임상기관에 대한 연구 지원, IP생산 등을 위한 비용 | ||||||
| 임상연구 지원 | 100 | 200 | 200 | 200 | 700 | ||
| IP생산 | 200 | 800 | 850 | 855 | 2,705 | ||
| 소계 | 300 | 1,000 | 1,050 | 1,055 | 3,405 | ||
| 합 계 | 600 | 2,000 | 1,650 | 1,655 | 5,905 | ||
| 출처) 당사 제시 |
상기 일본재생의료/국내첨생법 사업 비용 자금 계획 시 각 항목별 아래와 같은 비용을 포함하여 산정하였습니다.
| 구분 | 항목 | 내용 |
| 일본재생의료 사업 | 해외 유통망 구축 | 일본 현지 공급을 위해 해외 시술병원을 추가로 섭외하여 실제 투약가능시까지 소요되는 비용으로 병원 섭외 시 소요 비용, 투약 허가 승인, 변경, 실사 대응 등 위한 비용, 모객 관련 마케팅 비용 등이 포함되어 있습니다. |
| 공급설비(해동기 등)구입/안전재고 확보 | 생산한 줄기세포의 해외 시술 병원 공급(운송)을 위한 해동기/디프리저의 구입 비용, 배양을 위한 조직채취, 혈액검사 비용, 안전재고 확보를 위한 세포 보관 비용 등이 포함되어 있습니다. | |
| 운영비용 | 재생의료 사업 컨설팅, 사업 대행, 허가 대행 등과 관련한 비용이 포함되어 있습니다. | |
| 국내 첨생법 개정에 따른 사업 | GAP분석/RFD | 임상연구 실시 기관(대학병원 등)의 당사 치료제를 활용한 임상연구 진행과 관련한 연구 진행 지원, 컨설팅, 신고 서류 준비 등 담당인력의 인건비가 포함되어 있습니다. |
| Pre-IND & IND |
임상연구 실시 기관(대학병원 등)의 당사 치료제를 활용한 임상연구 진행과 관련한 IP생산 관련 비용 등이 포함되어 있습니다. |
(2)-2 오가노이드 연구개발
당사는 기타 파이프라인 중 하나로 오가노이드를 연구개발 중에 있습니다. 오가노이드란 장기유사체 혹은 미니 장기라고도 불리며, 당사의 피부 오가노이드 기술은 공기-액체 계면(ALI) 배양을 통해 불필요한 연골 조직의 형성을 억제하여 기존 기술의 한계를 극복하고 실제 피부와 같은 평평한 구조를 형성하여 정상피부와 기능적으로 동등한 피부 오가노이드 플랫폼을 구축하고자 합니다. 최근 선진국 중심으로 동물 임상시험에 대한 규모를 축소 및 최종적으로는 타 시험법으로 완전히 대체하고자 하는 점진적 규제가 진행되는 중이기 때문에 오가노이드는 동물 임상시험 규제에 따른 가장 적합한 대체법 시험물로 잠재적 가능성이 있습니다. 또한, 당사의 오가노이드 기술은 어떠한 세포로도 분화가 가능한 유도만능줄기세포(iPSC) 기반으로 적응 분야를 확대하고 있으며, 현재 모발 오가노이드를 활용한 연구개발도 진행 중에 있습니다. 이에 당사는 오가노이드 R&D 비용으로 2028년까지 6,784백만원의 연구개발비 지출이 필요할 것으로 생각하고 있으며, 이는 2023년 증자 잔액 450백만원과 금번 조달 자금 중 6,340백만원으로 사용할 예정입니다.
| [오가노이드 연구개발 비용 상세 내역] |
| (단위:백만원) |
| 구성 | 2023년 증자 잔액 (2025.03.31 기준) |
2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고 |
|---|---|---|---|---|---|---|---|
| 원재료 구입 | 450 | 350 | 600 | 1,200 | 1,800 | 3,950 | -오가노이드 연구용 원재료 구입 -오가노이드 연구개발 인력 증원 반영 -27년부터 임상 시작 목표로 임상 관련 인허가/약물감시 등 반영 |
| 인건비 | 250 | 389 | 537 | 623 | 1,799 | ||
| 인허가 | - | - | 134 | 96 | 230 | ||
| 약물감시 | - | - | 200 | 144 | 345 | ||
| 기타 임상진행비 | - | - | 267 | 193 | 460 | ||
| 합계 | 450 | 600 | 989 | 2,338 | 2,856 | 6,784 | - |
| 출처) 당사 제시 |
상기 오가노이드 연구개발 비용 자금 계획 시 각 항목별 아래와 같은 비용을 포함하여 산정하였습니다.
| 구분 | 항목 | 내용 |
| 오가노이드 연구개발 |
원재료 구입 | 오가노이드 연구개발을 위한 모낭 오가노이드, iPSC 등의 원재료 구입 비용이 포함되어 있습니다. GMP 오가노이드 공정개발과 관련한 특성분석시험법 및 단계별 제조공정개발비용, scale-up 공정개발비용 등이 포함되어 있습니다. |
| 인건비 | 오가노이드 연구 개발 기존 인력의 인건비, 추가 인력 증원 반영한 인건비가 포함되어 있습니다. | |
| 인허가 | 2027년 임상 1상 목표로 임상 관련 인허가에 필요한 비용으로 임상에 필요한 각종 인허가비용과 등록비용 그리고 담당인력의 인건비 등이 포함되어 있습니다. | |
| 약물감시 | 2027년 임상 1상 목표로 임상 관련 약물감시에 필요한 비용으로 임상에 투여하는 약물에 대한 모니터링 비용, 장기추적조사 연차보고 및 안전성 관련 자문비용, 담당인력의 인건비 등이 포함되어 있습니다. | |
| 기타 임상진행비 | 2027년 임상 1상 목표로 임상과 관련된 논문 및 학회발표, 통계자문 비용, 담당인력의 인건비가 포함되어 있습니다. |
(2)-3 시설자금 (GMP 시설투자)
금번 유상증자로 조달된 자금 중 4,010백만원을 활용하여 GMP 시설 투자에 사용할 예정입니다. 당사가 추진 중인 일본재생의료 사업 및 국내 첨단재생바이오법 개정안에 따른 사업 성장 시 2026년부터 신규시설 투자하여 생산 CAPA를 확대하고, 한편으로는 장비 노후화에 따라 2028년부터 기존 시설 개보수 투자를 진행하고자 합니다. 시설투자에 따른 자금사용의 상세 내역은 아래와 같습니다.
| [GMP 시설투자에 따른 세부 자금 사용 계획] | |
| (단위:백만원) | |
| 우선 순위 |
구분 | 구성 | 2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고사항 | |
|---|---|---|---|---|---|---|---|---|---|
| 2 | 일본재생의료/첨생법 | 신규시설투자 | - 2026년 이후 해당 사업 성장 시 사용 예정 - 제조실4 확장을 통한 재생의료 사업지원 - 생산 CAPA 20lot/월 ->최대 100lot/월 증가 : 제조 배양기 15대등 1090백만원 : 실험 유세포분석기등 1040백만원 |
||||||
| 건물 | - | - | - | - | - | ||||
| 연구기자재 | - |
2,277 | - | - | 2,277 | ||||
| 비품 | - | - | - | - | - | ||||
| 시설장치 | - | 60 | - | - | 60 | ||||
| 기타 | 200 | 200 | |||||||
| 소계 | - | 2,537 | - | - | 2,337 | - | |||
| 장비노후화에 따른 교체 투자 | 기존 시설 개보수 | - 배양기 노후화에 따른 교체투자 (수명주기 10년 도래) - 19년 설비투자된 약 50여대 대체액 반영 |
|||||||
| 건물 | - | - | - | - | - | ||||
| 연구기자재 | - | - | 1,300 | 1,300 | |||||
| 비품 | - | - | - | - | - | ||||
| 시설장치 | - | - | - | - | - | ||||
| 기타 | - | - | - | 173 | 173 | ||||
| 소계 | - | - | - | 1,473 | 1,473 | - | |||
| 합 계 | - | 2,537 | - | 1,473 | 4,010 | - | |||
| 출처) 당사 제시 |
상기 GMP 시설투자 자금 계획 시 각 항목별 아래와 같은 비용을 포함하여 산정하였습니다.
| 구분 | 항목 | 내용 |
| 일본재생의료/국내첨생법 진출에 따른 신규시설투자 | 연구기자재 | 제조실 4 확장을 위한 제조 배양기, 실험용 유세포 분석기 등의 신규 구입 비용 등이 포함되어 있습니다. |
| 시설장치 | ||
| 기타 | 신규 배양기, 유세포 분석기 구입에 따른 설치, 교정 비용 등 기타 비용이 포함되었습니다. | |
| 장비노후화에 따른 기존 시설 개보수 | 연구기자재 | GMP생산 설비 중 수명주기가 도래한 배양기(약 50여대) 교체를 위한 배양기 구입 비용 등이 포함되어 있습니다. |
| 기타 | 배양기 교체에 따른 설치, 교정 비용 등 기타 비용이 포함되었습니다. |
당사 GMP 생산시설의 2024년 기준 줄기세포 배양액 가동률은 47.5%, 세포배양배지 가동률은 약 21~24% 수준이며, 2025년 1분기 기준 줄기세포 배양액 가동률은 64.3%, 세포배양배지 가동률는 0.0%입니다.
| [GMP 생산시설 가동률 추이] |
| 품 목 | 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | 2021년 |
|---|---|---|---|---|---|---|
|
줄기세포 배양액(주1) (단위: ℓ) |
생산능력 | 600 | 2,400 | 2,400 | 2,400 | 2,400 |
| 생산실적 | 386 | 1,140 | 855 | 188 | 191 | |
| 가 동 률 | 64.3% | 47.5% | 35.6% | 7.8% | 8.0% | |
|
세포배양 배지(주2) (단위: 개) |
생산능력 | 1,500 | 6,000 | 6,000 | 6,000 | 6,000 |
| 생산실적 | 0 | 1,469 | 3,242 | 1,871 | 2,240 | |
| 가 동 률 | 0.0% | 24.5% | 54.0% | 31.2% | 37.3% | |
| 세포배양 배지(주3) (단위: 개) |
생산능력 | 600 | 1,800 | - | - | - |
| 생산실적 | 0 | 379 | - | - | - | |
| 가 동 률 | 0.0% | 21.1% | - | - | - |
| 출처) | 당사 정기보고서 |
| (주1) | 월 200ℓ생산 가능합니다. |
| (주2) | 월 500개 생산 가능합니다. |
| (주3) | 월 200개 생산 가능합니다. |
| (주4) | 2024년 기존 생산 설비를 활용하여 줄기세포 배양 배지(StemVie XF Supplments 제품)를 신규 생산하게 됨에 따라 추가된 내용입니다. |
당사는 현재 당사의 GMP 공장에서 제대혈 유래 줄기세포 배양액, 줄기세포 배양 배지 등을 직접 생산하여 줄기세포 치료제를 제조하여 당사의 주요 파이프라인의 전임상시험 및 임상시험에 사용하고 있습니다. GMP 시설 내에 줄기세포 배양액과 줄기세포 배양 배지 생산을 위한 구획을 구분하여 생산 라인이 가동되어야 하며, 해당 구역들은 당사의 임상 약물 기본 생산 라인이기 때문에 이는 가동률이 낮아도 유지를 해야 하는 구획입니다. 현재 GMP 생산 시설의 가동률이 낮은 편이지만, 상기한 바와 같이 가동률과 별개로 당사 주요 파이프라인의 임상 시험 및 신약개발을 위해 점유되는 구획이 존재하여, 이에 나머지 구역을 개조하여 국내외 재생의료사업 진출을 위한 시설 확충이 필요한 상황입니다.
당사가 금번 GMP시설투자에 사용 예정인 비용은 국내외 재생의료사업을 위한 시설 확충 용도 및 기존시설 노후화에 따른 신규 장비 매입 비용입니다. 현재 당사의 주력 생산시설은 동종줄기세포 생산에 초점이 맞춰져 있으므로 일본 재생의료 사업을 위한 2종(자가지방줄기세포)의 대량 생산설비 구축이 추가로 필요합니다. 2025년은 현재 생산라인을 활용하여 2종(자가지방줄기세포)의 생산량이 가능할 것으로 보이나, 공급이 본격적으로 증가할 것으로 예상되는 2026년부터는 별도 추가 설비 구축을 통해 생산 CAPA를 증설하는 것이 불가피할 것으로 예상되어 금번 자금 사용 목적에 시설투자를 포함하였습니다.
(3) 기타운영경비 (GMP 및 본사 경비)
금번 유상증자로 조달된 자금 중 연구소와 치료제 및 임상약물제조를 담당하는 GMP의 시설관리에 사용되는 전력비, 수수료 등 실험약물제조경비로 약 7,830백만원이 소요될 예정입니다. 이는 GMP 생산, 운영, 본사 운영과 관련하여 직간접적으로 필요한 비용으로 월 평균 250~300백만원 수준으로 집행할 예정입니다.
| [기타운영경비(GMP 및 본사 경비) 비용 상세 내역] |
|
| (단위:백만원) | |
| 구성 | 2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고 |
|---|---|---|---|---|---|---|
| 지급수수료 | - | - | 1,720 | 1,806 | 3,526 | - GMP 및 본사 경비: 전력비, 수수료, GMP 실험약물제조를 위한 경비 등 - GMP생산,운영, 본사 운용과 관련한 직간접적으로 필요한 경비 등 |
| 연구기자재와 시설장치 운영비 | - | 504 | 529 | 556 | 1,589 | |
| 수선소모품비 | - | - | 529 | 556 | 1,085 | |
| 세금과공과 | - | - | 132 | 139 | 271 | |
| 관리비 | - | - | 662 | 694 | 1,356 | |
| 합계 | - | 504 | 3,572 | 3,751 | 7,827 | - |
| 출처) 당사 제시 |
(4) 채무상환자금
금번 유상증자로 조달된 자금 중 1,400백만원을 활용하여 부채비율 개선, 금융비용 절감을 위해 시설자금 차입금을 상환할 예정입니다. 당사는 2017년 GMP 시설 및 연구소 취득을 위해 중소기업시설자금을 차입하였으며, 금번 유상자금으로 매반기 200백만씩 분할 상환 중인 해당 차입금 총 1,400백만원을 2028년까지 상환할 예정입니다. 금번 유상증자 자금조달로 차입금 일부를 상환함으로써 이자비용을 절감하고 재무구조 건전성을 확보하고자 합니다. 자금사용의 상세 내역은 아래와 같습니다.
| [상환 예정인 차입금 상세 현황] | |
| (기준일: 2025.06.23) |
(단위: 백만원) |
| 차입처 | 내역 | 최초 대여일 | 만기일 | 이자율 | 잔액 | 상환예정금액 | 상환예정시기 |
|---|---|---|---|---|---|---|---|
| 기업은행 | 중소기업시설자금 | 2017.06.08 | 2032.06.08 | 4.95% | 2,800 | 200 | 2025년 하반기 |
| 2017.06.08 | 2032.06.08 | 4.95% | 2,600 | 400 | 2026년 | ||
| 2017.06.08 | 2032.06.08 | 4.95% | 2,200 | 400 | 2027년 | ||
| 2017.06.08 | 2032.06.08 | 4.95% | 1,800 | 400 | 2028년 | ||
| 합 계 | 1,400 | 1,400 | |||||
| 출처) 당사 제시 |
(중략)
(2) 줄기세포 치료제의 일본 및 국내(첨생법) 재생의료사업 진출 추진
당사는 안정적인 수익 기반을 확보하기 위해 일본 재생의료 시장 및 국내(첨생법) 재생의료 사업 진출을 계획하고 있습니다. 일본 재생의료시장 진출을 위해 2024년 일본 후생노동성에 제1종(동종제대혈줄기세포) 및 제2종(자가지방줄기세포) 재생의료 제공계획에 대한 심의 및 승인 절차를 진행하였습니다. 제2종(자가지방줄기세포)의 경우, 2025년 2월 후생노동성 최종 승인까지 완료되어 2025년 하반기부터 일본 내 환자 투여를 계획하고 있습니다. 이에 금번 조달 자금의 일부는 일본 현지 환자 수급을 위한 본격적인 영업활동 및 투자를 진행을 위한 운영자금으로 활용될 예정입니다.
(3) 기타 파이프라인 연구개발 투자 및 지속 가능한 성장 기반 마련
당사는 기타 파이프라인 중 하나로 오가노이드를 연구개발 중에 있습니다. 특히 당사의 피부 오가노이드 기술의 경우, 공기-액체 계면(ALI) 배양을 통해 불필요한 연골 조직의 형성을 억제하여 실제 피부와 같은 평평한 구조를 완벽 재현하여 다양한 유효물질에 대한 약물 스크리닝 및 효력평가 등에 적용 가능하여, 일부 대형 글로벌 제약사들로부터 관심을 받고 있는 상황입니다. 이러한 파이프라인들의 포트폴리오를 지속적으로 확장하기 위해서는 선제적이고 적극적인 연구개발 투자가 필수적입니다. 이는 단기적인 성과뿐만 아니라 중장기적인 기업 성장의 발판을 마련하는 데 중요한 역할을 할 것입니다.
(4) 실권주 일반공모를 통한 투자자 참여 기회 확대
당사는 주주배정 후 실권주 일반공모 방식을 채택함으로써 기존 주주의 권리를 보호하는 동시에 신규 투자자들에게도 투자 기회를 제공하고자 합니다. 이를 통해 기존 주주들의 지분희석화를 최소화함과 동시에 실권주 일반공모를 통해 다양한 투자자층을 확보하고 기업의 지속 가능한 성장을 위한 기반을 마련할 것입니다.
상기한 바와 같이, 당사는 금번 유상증자를 통해 조달되는 자금을 핵심 파이프라인의 경쟁력 강화, 재생의료 시장 진출 및 추가 성장 동력 확보라는 명확한 목표 하에 투명하고 효율적으로 사용할 계획입니다. 이를 통해 기업가치를 지속적으로 증대시키고, 궁극적으로 주주분들의 이익을 극대화하기 위한 최선의 노력을 다할 것입니다.
당사는 금번 유상증자로 인해 기존 주주들의 지분이 희석될 수 있음을 충분히 인지하고 있으며, 이사회결의시 조달규모 등 정량적인 조건뿐만 아니라, 유상증자의 당위성과 소액주주 등의 유상증자 이해 고려, 주주보호(소통) 방안 등 정성적인 기준도 감안하여 본 유상증자의 목적과 필요성을 논의하였습니다. 당사는 금번 유상증자 자금조달 방안 이외에 다음과 같은 조달 방안들도 함께 검토하였습니다.
1) 회사채 발행
당사는 증권신고서 제출일 현재 공모 회사채 발행을 위한 적격 신용평가기관의 신용등급은 존재하지 않은 상태입니다. 신용평가기관의 등급 평가 방식으로는 정량적 평가(재무분석 : 수익성, 재무건정성, 현금흐름, 성장성 등) 및 정성적 평가(산업전망, 경쟁력, 경영진의 역량, 정부규제 등)과 함께 계량 모델 및 비교분석을 통해 진행되고 있습니다. 이후 신용등급이 확정되어 투자적격 등급 이상(BBB- 이상)의 등급으로 구분될 시 회사채 금융시장에서의 원활한 자금조달이 가능할 것으로 예상한 바, 당사는 공모 회사채 발행을 통한 자금조달은 현재 어려울 것으로 판단하였습니다. 또한, 사모 회사채 발행도 검토하였으나 높은 금리, 짧은 만기, 담보 및 지급보증 요구 등으로 인해 재무적 부담이 과도할 수 있다는 판단하에 실제 발행으로 이어지지 못하였습니다.
2) 주식 관련 사채 발행
주식 관련 사채로는 주식으로 전환될 수 있는 전환사채, 신주인수권 권리를 보유하고 있는 신주인수권부사채, 특정 주식으로 교환할 수 있는 교환사채 등이 존재합니다. 당사는 주식 관련 사채 또한 자금조달의 방안 중 하나로 고려하였으나, 회사의 재무 여건 등을 고려할 때 투자자 모집에 어려움이 있어 선택할 수 없었습니다.
3) 담보 제공을 통한 추가 차입
2025년 1분기 기준 당사 유형자산 중 담보력이 존재한다고 생각되는 토지 및 건물의 총 장부 금액은 약 12,025백만원입니다. 이 중 당사는 토지 및 건물(장부금액 약 11,418백만원)에 대해 8,796백만원 담보 설정하여 6,710백만원을 이미 차입하고 있습니다. 당사는 복수의 금융기관을 통해 현 담보물을 통한 추가 차입 가능 여부를 사전 검토하였으나, 추가 차입 가능성이 매우 낮은 것으로 확인하여 담보 제공을 통한 추가 차입 조달을 선택할 수 없었습니다.
| [2025년 1분기말 유형자산 상세 현황] |
| (단위: 천원) |
| 구 분 | 취득금액 | 감가상각누계액 | 정부보조금 | 장부금액 |
|---|---|---|---|---|
| 토지 | 3,927,206 | - | - | 3,927,206 |
| 건물 | 9,241,382 | (1,143,426) | - | 8,097,956 |
| 시설장치 | 7,998,885 | (3,919,893) | - | 4,078,992 |
| 연구시험용자산 | 7,968,351 | (7,194,122) | (29,906) | 744,323 |
| 비품 | 412,784 | (380,371) | - | 32,413 |
| 합 계 | 29,548,608 | (12,637,812) | (29,906) | 16,880,890 |
| 출처) 당사 정기보고서 |
| [2025년 1분기말 유형자산 담보제공 내역] |
| (단위: 천원) |
| 담보제공자산 | 장부금액 | 담보설정금액 | 담보감정가격 | 관련 계정과목 | 차입금액 | 담보권자 |
|---|---|---|---|---|---|---|
| 토지 | 3,660,774 | 8,796,000 | 11,028,000 | 차입금 | 6,710,000 | 기업은행 |
| 건물 | 7,758,009 |
| 출처) 당사 정기보고서 |
| 주1) 담보제공자산인 토지 및 건물은 글로벌R&D센터줄기세포재생의학연구소(서울 금천구 소재)와 줄기세포GMP센터(경기도 광명시 소재)입니다. |
| 주2) 담보감정가격의 감정일은 2021년입니다. |
또한, 상기 회사채 및 주식 관련 사채 발행과 담보제공을 통한 추가 차입방안의 경우, 금융비용(이자비용) 부담과 함께 수익성 악화가 이루어질 수 있고 부채총계 증가에 따라 재무안정성에 악영향을 줄 수 있는 점 또한 선택되지 않은 사유로 고려되었습니다. 지속적인 영업손실 및 당기순손실에 기인한 당사의 열위한 재무안정성을 고려하였을 때, 유상증자를 통해 자본을 확충하는 경우 차입금 및 부채비율을 보다 안정적으로 관리하여 건실한 재무안정성을 기대할 수 있으며, 추가적인 금융비용 발생을 방지하여 재무적 부담을 완화시킬 수 있을 것이라 판단하였습니다.
이러한 일련의 자금조달 방안 검토 과정을 거쳐, 이사회는 기존 주주에게 신주인수권을 우선적으로 부여하고, 실권주 발생 시 일반 투자자에게도 참여 기회를 제공할 수 있는 주주배정 후 실권주 일반공모 방식의 유상증자를 추진하는 것이 주주 권익 보호와 자금조달 안정성 확보 측면에서 가장 적절하다는 판단에 이르게 되었으며, 이에 대표주관회사와 인수회사의 잔액인수를 조건으로 한 주주배정 후 실권주 일반공모 방식의 유상증자를 최종적으로 결의하였습니다.
마. 주주 권익 보호를 위한 사항
당사는 금번 유상증자로 인해 주주들의 지분이 다소 희석될 수 있음을 충분히 인지하고 있으며, 이에 따라 유상증자 이후의 명확한 비전 제시 등을 통해 지속적으로 주주 소통을 강화할 예정입니다. 금번 유상증자 납입대금을 전략적으로 사용하여 회사의 경쟁력을 강화할 예정이며 이를 통해 기업 가치 상승을 유도하여 중장기적으로 주주 가치를 극대화하도록 노력할 예정입니다.
1) 주주와의 소통 강화 방안
당사는 주주 대상으로 적극적인 IR 활동을 통해 주주 신뢰를 제고하기 위해 노력할 계획입니다. 또한, 당사는 2025년 06월 10일 증권신고서 공시 직후, 금번 주주배정 유상증자 결정과 관련된 주요 내용을 주주들에게 설명하기 위하여 당사 홈페이지 주주 서한을 게재하였습니다.
![이미지: [주주서한]](%EC%A3%BC%EC%A3%BC%EC%84%9C%ED%95%9C.jpg) |
|
[주주서한] |
가) IR자료 및 보도자료 배포를 통한 회사에 대한 이해도 증진
당사는 소액주주의 정보 접근성을 높이고 소통을 활성화하여 주주 권익을 보호하고자 합니다. 구체적으로 당사는 추후 당사 홈페이지에 IR 자료를 즉시 게재하여 주주들이 관련 내용을 신속하게 확인할 수 있도록 할 예정입니다. 더불어, 당사는 유상증자와 관련된 전반적인 내용을 다양한 이해관계자들이 확인할 수 있도록 보도자료를 배포할 예정입니다. 이를 통해 개인, 기관, 외국인 투자자 등 다양한 이해관계자들에게 언론을 통해 당사의 비전과 전략을 정확히 전달할 수 있도록 노력할 계획입니다.
나) 투자설명회(IR) 개최
당사는 공모 유상증자 기간 중 오프라인 투자설명회(IR)를 개최하여 질의응답 세션을 운영하여 당사의 경영전략에 대해 충분히 이해할 수 있도록 진행할 계획입니다. 특히, 당사는 금번 유상증자의 목적 및 회사의 향후 성장 전략 등에 대해 주주분들에게 상세히 설명드리고 의견을 경청하기 위해 증권신고서 공시 익일인 2025년 06월 11일에 첫 번째 투자설명회(IR)를 개최하였습니다. 간담회의 구체적인 시간 및 장소, 참여 방법 등은 2025년 6월 10일 증권신고서 공시 직후 당사 홈페이지 및 공시를 통해 안내하였습니다.
또한, 추가적으로 주주분들의 수요를 조사하여 수도권 외에 지방거점에서도 투자설명회를 개최할 계획이 있습니다. 이를 통해 당사의 파이프라인 임상 현황, 기술이전 현황, 향후 비전 등을 상세히 설명하고 질의응답 시간을 통해 주주분들의 궁금증을 해소하겠습니다.
다) IR응대 전용 라인 강화를 통한 소통 강화
당사는 보다 적극적인 투자자 의사 소통 강화를 위해, 기존에 있는 IR응대 전용 라인을 강화할 계획입니다. IR 응대 전용 이메일 및 유선을 통해 유상증자와 관련한 문의에 신속하고 누락 없이 응대할 수 있도록 하겠습니다. 특히, 소액주주를 포함한 다양한 주주의 의견을 수렴할 수 있도록 당사와 사전 일정 조율 등을 신청한 소액주주에 대해서는 개별적인 대면 미팅 또는 유선 의견청취를 적극 활용하여 실시간 소통을 강화하겠습니다.
2) 주요 기관투자자 대상 IR 진행
주요 기관투자자 대상으로 IR을 진행하여 유상증자의 배경, 목적, 기대 효과와 당사의 중장기 사업전략 등에 대해 상세히 설명을 진행할 예정이며, 증권사 애널리스트 대상으로도 적극적으로 소통하여, 시장 내에 충분한 정보가 전달될 수 있도록 노력할 계획입니다.
당사는 상기와 같이 주주 및 시장과의 적극적인 소통을 통해 회사의 경영 전략 및 본 유상증자의 배경과 필요성을 명확히 전달하는 한편, 본 유상증자와 관련 후속 정보를 지속적으로 제공해 나가겠습니다.
바. 미사용 자금의 운용 계획
당사가 금번 유상증자를 통해 조달한 자금 중 일부 자금은 조달시기와 사용시기가 다소 차이가 생길 수 있습니다. 이에 조달로부터 사용 시까지 미사용 자금에 대해서는 자금 사용시점 및 금리에 따라 적격금융기관의 수시입출금 예금, 정기예금 등 금융상품 또는 A등급 이상의 단기금융상품으로 운용할 예정입니다.
(주23) 정정 전
2) 품목별 라이선스아웃 계약 세부내용
가) 퓨어스템-에이디 주(아토피 피부염)
| 계약상대방 | - SK바이오랜드(주) (대한민국) *주1) |
| 계약내용 | - 제대혈유래줄기세포치료제(적응증:아토피 피부염)의 국내 독점판매권/통상 실시권 설정 및 기술전수 계약 |
| 대상지역 | - 대한민국 |
| 계약기간 | - 계약체결일 : 2019.03.25. - 계약종료일 : 2024.11.18. |
| 총 계약금 | - 선급기술료 : 150 억원 (경상기술료는 미공개) |
| 수취금액 | - 50 억원 |
| 계약조건 | - 계약제품에 대한 국내 독점판매권을 현대바이오랜드(구.SK바이오랜드)에 허여함 - 국내 통상실시권 부여 및 기술 전수 - 계약기술 : 당사 보유의 특허권 4건 및 노하우 - 전수시기 : 제품 품목허가 승인 후 현대바이오랜드(구.SK바이오랜드)가 공정 설계 및 투자를 준비하는 시점 - 선급기술료는 총 150억원으로 분할 수령함 1) 계약체결일로부터 15일 이내 50억원 2) 품목허가 후 2년 이내 계약상대방과 협의하에 완제품 협의수량 이상을 연속 생산하고 연속생상된 완제품의 제품공급가 평균값이 vial당 협의된 가격이하가 되는 것을 양사가 확인한 날로부터 90일 이내 20억원 *주2) 3) 현대바이오랜드(SK바이오랜드)가 판매개시 이후 누적판매량이 협의된 수량을 초과한 날로부터 90일 이내 30억원 4) 본 계약에 따라 Know-how 기술전수 요청일로부터 90일 이내 30억원 5) 본 계약에 따라 Know-how 기술전수 종결일로부터 90일 이내 20억원 - 계약제품의 생산은 양사가 공동 협력하며, 당사는 3만 바이알 이내 물량에 대한 제품공급의무를 갖고 있음 |
| 회계처리방법 | - 계약금(Upfront payment) : 라이선스 제공에 대해서는 라이선스 제공과 제품 공급 의무를 단일의 수행의무로 회계처리하며 제품 공급 기간에 걸쳐 수익을 인식하고, 제품의 Know-how 기술이전과 관련 된 수행의무에 대해서는 기술전수가 완료되는 시점에 일시에 수익을 인식 |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 아토피 피부염) - 계약기술 특허는 다음과 같습니다. (1) ZNF281을 발현하는 제대혈 유래 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195호) (2) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량 배양방법(대한민국 특허 등록 제10-1158664호) (3) Isolating Method for Umbilical Cord Blood-Derived Pluripotent Stem Cells Expressing ZNF281(PCT/KR2010/001338) (4) 줄기세포를 유효성분으로 함유하는 면역질환 또는 염증질환의 예방 또는 치료용 조성물(대한민국 특허등록 제10-1512171호) |
| 개발 진행경과 |
- 2013년 퓨어스템-에이디 주 1/2a상 임상시험계획 식약처 승인 - 2015년 1/2a상 임상시험 종료 (2018년 장기추적관찰 종료) - 2017년 3상 임상시험계획 식약처 승인 |
| 기타사항 | 해당 계약에 대하여 (주)현대바이오랜드로부터 2024년 11월 18일 계약해제를 통고 받아 계약이 해제되었습니다. |
| *주1) | 사명 변경 SK바이오랜드 → 현대바이오랜드 |
| *주2) | 2020.12.10 지급조건 변경 |
나) Cart-T 기술(암질환군 한정)
| 계약상대방 | - 마루테라퓨틱스(주) (대한민국) |
| 계약내용 | - Car-T 기술(암질환군에 한정)에 대한 전용실시권 부여하는 기술이전계약 |
| 대상지역 | - 국내 및 국외 |
| 계약기간 | - 계약체결일 : 2021.04.16. - 계약종료일 : 대상기술 특허 존속기간 만료시까지 |
| 총 계약금 | - *주) |
| 수취금액 | - *주) |
| 계약조건 | * 계약조건은 영업비밀로 자세한 기재는 생략하며, 대략적인 내용은 다음과 같습니다. - 계약금은 ** 원이며 반환의무가 없음 - 1차선정 파이프라인은 두가지로 하며 단계별 기술료는 각각 **원으로 최대 **원 - 향후 제품 생산시 당사에게 CMO생산 위탁 |
| 회계처리방법 | - 계약금 수취액은 계약 조건에 따라 일시에 수익 인식 |
| 대상기술 | - Car-T 기술(대상 적응증 : 암질환군) - 계약기술 특허는 다음과 같습니다. * off-the-shelf 줄기세포 및 면역세포, 이를 포함하는 약학적 조성물 (출원번호 제10-2021-0009773호) 외 1건 |
| 개발 진행경과 | - 2021년 기술이전 완료 |
| 기타사항 | - |
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
다) OSCA(구. 퓨어스템-오에이 키트 주, 골관절염)
| 계약상대방 | - (주)유영제약 (대한민국) |
| 계약내용 | - 무릎골관절염치료제(OSCA(구. 퓨어스템-오에이 키트 주)) 공동개발 및 국내 독점판매권·통상실시권에 대한 라이선스 계약 체결 |
| 대상지역 | - 국내 |
| 계약기간 | - 계약체결일 : 2024.11.07. - 계약종료일 : 품목허가일로부터 10년째 되는 해의 12월 말 |
| 총 계약금 | - 선급기술료: 140억원 |
| 수취금액 | - 20억원 |
| 계약조건 | - 무릎골관절염치료제(OSCA(구. 퓨어스템-오에이 키트 주))의 공동개발 포함 국내 독점판매권·통상실시권에 대한 라이선스 계약 - 총계약금액 : 140억원 1) 경상기술료 1차 : 20억원 (계약체결시) 2) 경상기술료 2차 : 30억원 (국내 공동개발사 선정시 또는 2026년 말 중 빠른 시점) 3) 경상기술료 3차 : 30억원 (유영제약 또는 공동개발사 첫번째 IND 승인시(2b상 또는 통합 임상 2상)) 4) 경상기술료 4차 : 30억원 (유영제약의 3상 임상 IND 승인시) 5) 경상기술료 5차 : 30억원 (유영제약의 품목허가 취득시) - 로열티 별도지급 (시판 후 12개월 간 발주수량에 따라 합의된 금액 수령) - 조건부 허가로 임상3상 진행시 합의된 금액 수령 |
| 회계처리방법 | - 경상기술료 수취액은 계약 조건에 따라 일시에 수익 인식 |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 아토피 피부염) - 계약기술 특허는 다음과 같습니다. (1) 연골 무세포 파쇄물 및 줄기세포를 포함하는 연골분화 촉진용 복합체 및 그의 용도(대한민국 특허 등록 제10-1901568호) (2)연골 분화능이 증진된 줄기세포의 선별 방법 및 이를 포함하는 세포 치료제(대한민국 특허 출원 제10-2023-0189178호) (3) ZNF281을 발현하는 제대혈 유래만능 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195) (4) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량배양 방법 (대한민국 특허등록 제10-1158664호) |
| 개발 진행경과 | - 2023년 1/2a상 식약처 IND 변경승인 완료 및 임상시험 진행 - 2024년 8월 1/2a상 식약처 IND 변경승인신청, 10월 변경승인 완료 - 2024년 12월 1상 topline data 발표, 1/2a상 식약처 IND 변경승인신청 - 2025년 1월 1/2a상 IND 변경승인 - 2025년 2월 2a 임상시험 개시 |
| 기타사항 | - |
나. 라이선스인(License-in) 계약
1) 라이센스인 계약 총괄표
| 품목 | 계약상대방 | 대상지역 | 계약체결일 | 계약종료일 | 총 계약금액 | 수취금액 | 진행단계 |
| 피부오가노이드 기술 (아토피피부염 모델) |
서울대학교 산학협력단 |
국내 국외 |
2021.08.30. | 체결일로부터 특허 존속만료일까지 |
*주) | *주) | 기술이전 중 |
| 인공장기제작 기술 | 서울대학교 산학협력단 |
국내 국외 |
2021.10.01. | 체결일로부터 특허 존속만료일까지 |
*주) | *주) | 기술이전 중 |
| 모낭 오가노이드 기술 (모낭제작 및 배양기술) |
서울대학교 산학협력단 |
국내 국외 |
2023.12.22 | 체결일로부터 특허 존속만료일 중 가장 늦은 날까지 |
*주) | *주) | 기술이전 중 |
| UV 손상 피부 오가노이드 기술 |
서울대학교 산학협력단 |
국내 국외 |
2024.02.29 | 체결일로부터 특허 존속만료일 중 가장 늦은 날까지 |
*주) | *주) | 기술이전 중 |
| 합 계 | *주) | *주) | - | ||||
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
(주23) 정정 후
2) 품목별 라이선스아웃 계약 세부내용
가) 퓨어스템-에이디 주(아토피 피부염)
| 계약상대방 | - SK바이오랜드(주) (대한민국) *주1) |
| 계약내용 | - 제대혈유래줄기세포치료제(적응증:아토피 피부염)의 국내 독점판매권/통상 실시권 설정 및 기술전수 계약 |
| 대상지역 | - 대한민국 |
| 계약기간 | - 계약체결일 : 2019.03.25. - 계약종료일 : 2024.11.18. |
| 총 계약금 | - 선급기술료 : 150 억원 (경상기술료는 미공개) |
| 수취금액 | - 50 억원 (반환완료 *주3) |
| 계약조건 | - 계약제품에 대한 국내 독점판매권을 현대바이오랜드(구.SK바이오랜드)에 허여함 - 국내 통상실시권 부여 및 기술 전수 - 계약기술 : 당사 보유의 특허권 4건 및 노하우 - 전수시기 : 제품 품목허가 승인 후 현대바이오랜드(구.SK바이오랜드)가 공정 설계 및 투자를 준비하는 시점 - 선급기술료는 총 150억원으로 분할 수령함 1) 계약체결일로부터 15일 이내 50억원 2) 품목허가 후 2년 이내 계약상대방과 협의하에 완제품 협의수량 이상을 연속 생산하고 연속생상된 완제품의 제품공급가 평균값이 vial당 협의된 가격이하가 되는 것을 양사가 확인한 날로부터 90일 이내 20억원 *주2) 3) 현대바이오랜드(SK바이오랜드)가 판매개시 이후 누적판매량이 협의된 수량을 초과한 날로부터 90일 이내 30억원 4) 본 계약에 따라 Know-how 기술전수 요청일로부터 90일 이내 30억원 5) 본 계약에 따라 Know-how 기술전수 종결일로부터 90일 이내 20억원 - 계약제품의 생산은 양사가 공동 협력하며, 당사는 3만 바이알 이내 물량에 대한 제품공급의무를 갖고 있음 |
| 회계처리방법 | - 계약금(Upfront payment) : 라이선스 제공에 대해서는 라이선스 제공과 제품 공급 의무를 단일의 수행의무로 회계처리하며 제품 공급 기간에 걸쳐 수익을 인식하고, 제품의 Know-how 기술이전과 관련 된 수행의무에 대해서는 기술전수가 완료되는 시점에 일시에 수익을 인식 |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 아토피 피부염) - 계약기술 특허는 다음과 같습니다. (1) ZNF281을 발현하는 제대혈 유래 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195호) (2) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량 배양방법(대한민국 특허 등록 제10-1158664호) (3) Isolating Method for Umbilical Cord Blood-Derived Pluripotent Stem Cells Expressing ZNF281(PCT/KR2010/001338) (4) 줄기세포를 유효성분으로 함유하는 면역질환 또는 염증질환의 예방 또는 치료용 조성물(대한민국 특허등록 제10-1512171호) |
| 개발 진행경과 |
- 2013년 퓨어스템-에이디 주 1/2a상 임상시험계획 식약처 승인 - 2015년 1/2a상 임상시험 종료 (2018년 장기추적관찰 종료) - 2017년 3상 임상시험계획 식약처 승인 |
| 기타사항 | 해당 계약에 대하여 (주)현대바이오랜드로부터 2024년 11월 18일 계약해제를 통고 받아 계약이 해제되었습니다. |
| *주1) | 사명 변경 SK바이오랜드 → 현대바이오랜드 |
| *주2) | 2020.12.10 지급조건 변경 |
| *주3) | 2024년 11월 18일 계약해제되었으며, 이에 당사는 ㈜현대바이오랜드로부터 수령한 선급기술료 50억원을 반환하였습니다. 해당 선급기술료는 회계 계정 상 선수수익으로 처리했다가 계약부채로 변경한 후 현대바이오랜드에 반환 후 계약부채에 대한 역분개 처리하였습니다. 이에 관련 분개로 손익에 미치는 영향은 없었습니다. |
나) Cart-T 기술(암질환군 한정)
| 계약상대방 | - 마루테라퓨틱스(주) (대한민국) |
| 계약내용 | - Car-T 기술(암질환군에 한정)에 대한 전용실시권 부여하는 기술이전계약 |
| 대상지역 | - 국내 및 국외 |
| 계약기간 | - 계약체결일 : 2021.04.16. - 계약종료일 : 대상기술 특허 존속기간 만료시까지 |
| 총 계약금 | - *주) |
| 수취금액 | - *주) |
| 계약조건 | * 계약조건은 영업비밀로 자세한 기재는 생략하며, 대략적인 내용은 다음과 같습니다. - 계약금은 ** 원이며 반환의무가 없음 - 1차선정 파이프라인은 두가지로 하며 단계별 기술료는 각각 **원으로 최대 **원 - 향후 제품 생산시 당사에게 CMO생산 위탁 |
| 회계처리방법 | - 계약금 수취액은 계약 조건에 따라 일시에 수익 인식 |
| 대상기술 |
- Car-T 기술(대상 적응증 : 암질환군) |
| 개발 진행경과 |
- 2021년 기술이전 완료 |
| 기타사항 | - |
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
다) OSCA(구. 퓨어스템-오에이 키트 주, 골관절염)
| 계약상대방 | - (주)유영제약 (대한민국) |
| 계약내용 | - 무릎골관절염치료제(OSCA(구. 퓨어스템-오에이 키트 주)) 공동개발 및 국내 독점판매권·통상실시권에 대한 라이선스 계약 체결 |
| 대상지역 | - 국내 |
| 계약기간 | - 계약체결일 : 2024.11.07. - 계약종료일 : 품목허가일로부터 10년째 되는 해의 12월 말 |
| 총 계약금 | - 선급기술료: 140억원 |
| 수취금액 | - 20억원 |
| 계약조건 | - 무릎골관절염치료제(OSCA(구. 퓨어스템-오에이 키트 주))의 공동개발 포함 국내 독점판매권·통상실시권에 대한 라이선스 계약 - 총계약금액 : 140억원 1) 경상기술료 1차 : 20억원 (계약체결시) 2) 경상기술료 2차 : 30억원 (국내 공동개발사 선정시 또는 2026년 말 중 빠른 시점) 3) 경상기술료 3차 : 30억원 (유영제약 또는 공동개발사 첫번째 IND 승인시(2b상 또는 통합 임상 2상)) 4) 경상기술료 4차 : 30억원 (유영제약의 3상 임상 IND 승인시) 5) 경상기술료 5차 : 30억원 (유영제약의 품목허가 취득시) - 로열티 별도지급 (시판 후 12개월 간 발주수량에 따라 합의된 금액 수령) - 조건부 허가로 임상3상 진행시 합의된 금액 수령 |
| 회계처리방법 | - 경상기술료 수취액은 계약 조건에 따라 일시에 수익 인식 |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 아토피 피부염) - 계약기술 특허는 다음과 같습니다. (1) 연골 무세포 파쇄물 및 줄기세포를 포함하는 연골분화 촉진용 복합체 및 그의 용도(대한민국 특허 등록 제10-1901568호) (2)연골 분화능이 증진된 줄기세포의 선별 방법 및 이를 포함하는 세포 치료제(대한민국 특허 출원 제10-2023-0189178호) (3) ZNF281을 발현하는 제대혈 유래만능 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195) (4) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량배양 방법 (대한민국 특허등록 제10-1158664호) |
| 개발 진행경과 | - 2023년 1/2a상 식약처 IND 변경승인 완료 및 임상시험 진행 - 2024년 8월 1/2a상 식약처 IND 변경승인신청, 10월 변경승인 완료 - 2024년 12월 1상 topline data 발표, 1/2a상 식약처 IND 변경승인신청 - 2025년 1월 1/2a상 IND 변경승인 - 2025년 3월 2a상 첫환자 투약 개시 |
| 기타사항 | - |
나. 라이선스인(License-in) 계약
1) 라이센스인 계약 총괄표
| 품목 | 계약상대방 | 대상지역 | 계약체결일 | 계약종료일 | 총 계약금액 | 수취금액 | 진행단계 |
| 피부오가노이드 기술 (아토피피부염 모델) |
서울대학교 산학협력단 |
국내 국외 |
2021.08.30. | 체결일로부터 특허 존속만료일까지 |
*주) | *주) | 기술이전 완료 |
| 인공장기제작 기술 | 서울대학교 산학협력단 |
국내 국외 |
2021.10.01. | 체결일로부터 특허 존속만료일까지 |
*주) | *주) | 기술이전 완료 |
| 모낭 오가노이드 기술 (모낭제작 및 배양기술) |
서울대학교 산학협력단 |
국내 국외 |
2023.12.22 | 체결일로부터 특허 존속만료일 중 가장 늦은 날까지 |
*주) | *주) | 기술이전 완료 |
| UV 손상 피부 오가노이드 기술 |
서울대학교 산학협력단 |
국내 국외 |
2024.02.29 | 체결일로부터 특허 존속만료일 중 가장 늦은 날까지 |
*주) | *주) | 기술이전 완료 |
| 합 계 | *주) | *주) | - | ||||
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
【 대표이사 등의 확인 】
 |
|
대표이사 등의 확인(250624) |
증 권 신 고 서
| ( 지 분 증 권 ) |
| [증권신고서 제출 및 정정 연혁] |
| 제출일자 | 문서명 | 비고 |
|---|---|---|
| 2025년 06월 10일 | 증권신고서(지분증권) | 최초 제출 |
| 2025년 06월 24일 | [기재정정]증권신고서(지분증권) | 기재 정정(파란색) |
| 금융위원회 귀중 | 2025년 06월 24일 |
| 회 사 명 : |
주식회사 강스템바이오텍 |
| 대 표 이 사 : |
나종천 |
| 본 점 소 재 지 : |
서울특별시 강남구 테헤란로 522 홍우빌딩 9층 |
| (전 화) 02-888-1590 | |
| (홈페이지) http:// http://www.kangstem.com |
|
| 작 성 책 임 자 : | (직 책) 경영지원실장 (성 명) 이계종 |
| (전 화) 02-888-1590 |
|
| 모집 또는 매출 증권의 종류 및 수 : | 기명식 보통주 38,000,000주 | |
| 모집 또는 매출총액 : | 49,210,000,000 | 원 |
| 증권신고서 및 투자설명서 열람장소 |
| 가. 증권신고서 |
| 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 나. 투자설명서 |
| 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 서면문서 : (주)강스템바이오텍 → 서울시 강남구 테헤란로 513 홍우빌딩 9층 삼성증권(주) → 서울특별시 서초구 서초대로74길 11 엔에이치투자증권(주) → 서울특별시 영등포구 여의대로 108 한양증권(주) → 서울특별시 영등포구 국제금융로6길 7 |
【 대표이사 등의 확인 】
 |
|
대표이사 등의 확인(250610) |
요약정보
1. 핵심투자위험
| 하단의 핵심투자위험은 증권신고서 본문에 기재된 투자위험요소 중 중요한 항목만을 투자자의 이해도 제고를 위하여 간단ㆍ명료하게 요약한 것입니다. 자세한 투자위험요소는 "본문-제1부 모집 또는 매출에 관한 사항-Ⅲ. 투자위험요소"에 기재되어 있으니 참고하시기 바랍니다. |
| 구 분 | 내 용 |
| 사업위험 |
가. 국내외 거시경기 침체 및 불확실성이 미치는 위험 다. 연구개발의 지연 및 실패 위험 당사가 주요사업으로 영위하는 바이오신약개발 산업은 특허권에 의해 일정기간 동안 독점권으로 보호받게 되며 특허의 존속기간과 관계없이 신약의 경우 시장독점권을 보장받을 수 있습니다. 이처럼 특허권 및 독점판매권(시장독점권)을 통해 일정기간 수익을 보장받을 수 있기 때문에 글로벌 블록버스터급 신약 개발에 성공 시 막대한 수익을 창출할 수 있는 고부가가치 사업입니다. |
| 회사위험 | 가. 지속적인 연구개발 투자 필요에 따른 유동성 위험 연구개발을 통한 신약 개발은 일반적으로 막대한 연구개발비와 장기에 걸친 투자 및 연구기간이 소요되며, 신약 개발에 성공한다 하더라도 기투자된 금액과 시간을 상쇄할 수 있을 정도의 수익 창출이 가능할지 여부는 불확실합니다. 또한 내외부적인 요인으로 인하여 개발이 지연되거나 추가적인 비용 지출이 요구될 경우도 존재합니다. 당사는 연구개발비용으로 2025년 1분기말 기준 32.3억원을 사용하였으며, 이는 2025년 1분기말 매출액(9.5억원) 대비 338.6% 수준입니다. 최근 3개년(2022, 2023, 2024년) 연결기준 매출액 대비 평균 118.1% 수준을 연구개발비용으로 사용하고 있습니다. 연구개발비는 발생시점에 전액 비용 처리하고 있으며, 개발비 자산화 시점에 대한 고려는 하지 않을 계획입니다. 다만, 증권신고서 제출일 현재까지 연구개발에 대한 성과가 수익성으로 연결되지 않아 지속적인 영업적자를 기록하고 있습니다. 당사의 연구개발 계획이 실패하거나, 장기적인 연구개발 전략과 사업계획, 그리고 그에 맞는 자금운용계획을 적정하게 수립하지 못할 경우 당사의 수익성 및 재무안정성에 부정적인 영향이 발생할 수 있습니다. 또한, 당사는 지속적인 적자로 인해 자체적으로 연구개발비를 조달하는데 어려움이 있어 계속적으로 자금조달을 유치하고 있습니다. 향후에도 추가적인 자금조달 가능성이 존재하며 적절한 시점에 유동자금을 확보하지 못할 경우 회사 운영이 어려워지는 상황에 직면할 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. 나. 성장성 및 수익성 하락에 따른 위험 2025년 1분기 기준 매출액은 9.5억원을 기록하며 전년 동기 대비 감소하였습니다. 아토피 피부염 줄기세포 치료제인 '퓨어스템-에이디 주' 임상 3상 결산 수수료 및 골관절염 치료제 '퓨어스템-오에이 키트 주' 임상을 위한 연구비용이 발생하였지만 비임상시험 사업부의 연결 제외로 전체 판관비가 감소하였으며, 이에 영업손실 적자 폭은 작아졌습니다. 영업손실의 경우 2022년 206억원, 2023년 228억원, 2024년 148억원, 2025년 1분기 47억원을 기록하며 손실이 지속되는 추이를 보이고 있습니다. 이는 바이오산업 특성상 가시적인 성과가 발생하기까지 지속적인 연구개발자금이 소요되는 것이 주요 원인으로, 진행 중인 파이프라인의 임상연구가 지속되는 한 높은 판관비는 지속적으로 발생할 것으로 예상되고 있습니다. 이에 당사는 CDMO 사업 진행을 통해 관련 매출을 발생시켜 유지 및 보수 비용을 충당하였으며, 개발 중인 신약과 관련한 다양한 국가 과제 수행을 통해 연구개발비용을 절감하고 긴축 재정 관리로 운용 비용을 절감하고 있습니다. 이러한 노력에도 불구하고 당사가 계획하고 있는 연구개발 지연 및 실패하는 경우, 또는 품목허가 및 출시 지연에 따른 화장품 및 바이오파마 제품 생산ㆍ판매 지연 등으로 인해 당사의 매출 계획이 지연될 가능성이 존재합니다. 이에 따라 당사의 영업활동 및 수익성은 부정적인 영향을 받을 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. 다. 재무안정성 위험 2025년 1분기말 기준 총자산 502억원 및 유동자산 236억원, 총 차입금 84억원, 차입금 의존도 16.8%, 부채비율 31.2%, 유동비율 335.9%를 나타내고 있습니다. 당사의 최근 3개년 부채비율은 2022년 70.5%, 2023년 82.5% 로 증가하는 추세를 보였으나 2024년 29.7%, 2025년 1분기에는 31.2%를 기록하였습니다. 이는 HLB바이오코드 주식회사가 발행했던 제1회 전환사채 및 상환전환우선주부채가 연결 대상에서 제외된 것이 기인했습니다. 당사의 차입금 규모는 2022년 188.1억원, 2023년 192.1억원, 2024년 85억원, 2025년 1분기 84억원입니다. 당사는 2021년 10월 390억원, 2023년 11월 210억원 규모의 유상증자를 통해 재무안정성이 개선되었으나, 지속해서 손실 폭이 커짐에 따라 재무안정성이 다시 악화될 수 있습니다. 향후 각 사업부문 영업 환경이 지속적으로 악화되거나, 줄기세포치료제 등에 지속적인 투자로 인한 자금 소요 등의 예상치 못한 환경의 변화에 따라 외부자금 조달 수요가 발생할 경우 당사에 차입금 상환 부담이 일시적으로 가중될 수 있으며, 당사의 재무안정성 약화로 이어질 위험이 나타날 수 있습니다. 또한, 갑작스러운 영업환경의 변화나 담보가치의 하락으로 인한 담보제공이 현실화될 가능성을 배제할 수는 없으며, 증권신고서 제출 전일 기준 진행 중인 소송은 없지만, 향후 유사의약품 등에 대한 특허권 분쟁, 거래상대방과의 공급계약 또는 수수료 지급, 핵심인력 유출입, 임직원 및 관련자가 당사에 중대한 손해를 입히는 경우 등과 관련된 다양한 종류의 분쟁 또는 소송이 발생할 수 있으며, 이러한 소송이나 분쟁이 발생할 경우 당사의 영업 및 재무구조에 부정적인 영향을 미칠 수 있으므로 투자자께서 유의하시어 투자에 임하시기를 바랍니다. 라. 영업현금흐름 및 유동성 관련 위험 당사는 수익성 악화 및 지속적인 연구개발 활동으로 인해 음(-)의 영업활동현금흐름을 보이고 있으며, 투자활동현금흐름의 경우, 2022년, 2024년에는 단기금융상품의 처분으로 인해 양(+)의 현금흐름을 보였습니다. 재무활동현금흐름의 경우, 2021년 유상증자를 통해 자금을 조달하며 양(+)의 현금흐름을 보인 이후, 2022년에는 차입금 및 전환사채 등을 상환하며 다시 음(-)의 현금흐름을 보였으며 2023년 유상증자를 통해 자금을 조달하며 양(+)의 현금흐름을 보였습니다. 2024년은 차입금이 증가하며 2개년 연속으로 양(+)의 현금흐름을 보였습니다. 당사의 주요 파이프라인으로는 아토피 피부염 치료제(퓨어스템-에이디 주), 류마티스 관절염(퓨어스템-알에이 주), 골관절염(OSCA, 구.퓨어스템-오에이 키트 주)이 있습니다. 이에 대한 임상시험을 진행하면서 2022년 14,220백만 원, 2023년 14,030백만원, 2024년 12,143백만원, 2025년 1분기 3,231백만 원의 정부보조금을 제외한 경상연구개발비용이 지출되었습니다. 향후 파이프라인별 임상 단계 진전 및 신규 파이프라인 개발에 따라 더 많은 연구개발비가 투입될 예정이며 이에 따라 영업비용 또한 확대될 것으로 예상됩니다. 당사는 상장 이후 지속적인 임상개발과 연구개발활동으로 인해 유동성 지표가 악화되어 왔으며, 향후에도 유의미한 수준의 매출이 발생하지 않아 음(-)의 영업활동현금흐름이 계속 발생할 경우 유동성 리스크가 부각될 위험이 있습니다. 또한, 지속적으로 영업 성과에 부정적인 영향으로 음(-)의 영업활동현금흐름이 발생할 경우 장기적으로 회사의 현금흐름에 문제가 발생할 소지가 있습니다. 투자자께서는 회사의 현금흐름 및 유동성 관련 위험요인을 면밀히 검토하시고 투자에 임해주시기 바랍니다. 마. 관리종목 편입 및 상장폐지 가능성에 따른 위험 당사는 기술성장특례 적용 기업으로 2015년에 12월에 상장하여 관리종목 지정요건 중 유예 항목들에 대한 적용 기간이 만료되었습니다. 이에 따라 당사가 매출액 및 법인세비용차감전계속사업손실 요건, 자본잠식 요건 등을 충족하지 못할 경우 향후 관리종목으로 지정될 가능성이 있습니다. 당사는 2023년 법인세비용차감전계속사업손실률이 51.9%까지 증가하였으며 관리종목 지정 리스크가 발생하였습니다. 2024년 법차손률이 16.4%를 기록하며 대폭 개선되었으나, 2025년 사업연도말의 법차손률이 50%를 상회할 경우 최근 3사업연도중 2사업연도(2023년, 2025년)의 법차손률이 50%를 상회함에 따라 관리종목으로 지정될 수 있습니다. 당사는 2024년 5월 HLB바이오코드 주식회사 지분 매각을 통해 연결 손실 인식을 방지하고, 동시에 98억원의 처분이익이 발생하며 2024년 법차손률 16.4%로 큰 폭으로 개선되었습니다. 다만, 2024년 지분 매각으로 인한 처분이익 98억원의 경우 일회성 이익에 해당하여 당사의 2025년 영업수익성에 미치는 영향은 미미한 것으로 판단됩니다. 따라서, 2025년 법인세비용차감전계속사업손실이 전년도 대비 증가할 가능성이 있으니 투자자들께서는 이 점을 유의하여 주시기 바랍니다. 또한, 현재 당사는 OSCA 라이선스 아웃 계약에 따른 단계별 선급기술료 수취 및 임상비용 절약, 일본 재생의료 매출 발생 등 수익성 향상을 위해 노력중입니다. 동시에, 금번 유상증자를 통한 자본규모 확충을 기대 중이며, 계획한 수익성 향상 노력과 자금조달이 모두 성공적으로 이루어질 경우 2025년 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 발생할 가능성은 낮을 것으로 판단됩니다. 다만. 이러한 당사의 노력에도 불구하고 사업환경이 급격히 악화되어 당사의 임상 및 연구개발 지연으로 매출 저조 등 재무성과를 나타내지 못하거나 유상증자에 실패하여 법인세비용차감전계속사업손실률이 50%를 상회할 경우 관리종목으로 지정 요건에 해당할 수 있으니 투자자들께서는 이점 유의하시기 바랍니다. 2025년 01월 21일 금융위원회와 금융감독원, 한국거래소, 금융투자협회, 자본시장연구원이 발표한 'IPO 및 상장폐지 제도 개선 방안'에 따르면 시가총액이 600억원 미만인 코스닥 상장 법인의 상장 유지를 위한 매출 요건이 강화되었습니다. 당사의 최근 3년간 별도기준 매출액 중 2022년과 2023년은 각각 59.2억원, 59.1억원으로 2028년부터 적용되는 매출요건 75억을 하회합니다. 한편, 2024년 매출액은 77.5억원으로, 2029년부터 적용되는 매출요건 100억원을 하회합니다. 다만, 당사의 최근 시가총액은 2028년부터 적용되는 최소 시가총액 요건인 600억원을 상회하고 있기 때문에, 현재 시가총액 수준을 유지한다면 해당 사항은 없을 것으로 보입니다. 그러나, 향후 당사의 매출 성장성이 둔화되어 매출이 악화되고 시가총액 수준이 지속적으로 하락할 경우 금융당국의 강화된 상장폐지 요건에 해당될 가능성이 있습니다. 투자자들께서는 투자 판단 시 최근 상장폐지 요건 강화에 따른 상장폐지 위험에 대해서 충분히 인지하시길 바랍니다. 바. 매출채권 및 재고자산 관련 위험 당사의 2025년 1분기 매출채권 총액은 16.0억원으로 2024년말 매출채권 52.7억원 대비 36.7억원 감소하였습니다. 매출채권 회수를 측정하는 주요 지표인 매출채권 회전율은 2022년 3.0회, 2023년는 2.4회, 2024년 1.5회, 2025년 1분기 1.1회로 매출액의 증감에 따라 변동성이 나타나고 있습니다. 향후 파이프라인의 기술이전 및 화장품 사업부와 바이오파마 사업부의 제품 라인업 확대 및 온라인 시장 점유 확대 등의 여부에 따른 매출 증대로 인하여 매출채권이 현 수준보다 증가할 수 있습니다. 한편, 당사의 재고자산회전율은 2022년 18.6회, 2023년 21.2회, 2024년 4.8회, 2025년 1분기 0.9회로 업종 평균인 5.0회에 하회하고 있습니다. 다만, 2022~2023년 기준 당사의 재고자산 회전율이 업종평균을 상회한 주된 원인은 자체 줄기세포 배양액을 기반으로 한 제품을 위주로 화장품을 제조해서 판매하는 화장품 사업, 의약품 도매 총판 및 일반의약품을 유통하는 바이오파마 사업 등 사업다각화로 인한 홈쇼핑 판매 재고 증가, 화장품 원료로 사용되는 줄기세포배양액과 세포배양배지 생산으로 인한 원재료 구매 증가 등이 기인했습니다. 재고자산이 증가할 경우 창고에 보관된 기간이 길어지는 것을 의미하므로 회사 입장에서는 재고 보관비용의 증가, 재고자산의 노후화 위험을 동시에 부담할 가능성을 시사합니다. 당사는 향후 보다 정확한 수요예측 및 생산량조절을 통해 적정수준의 재고자산 보유를 위해 노력하고, 진부화된 재고자산에 대한 적시 평가를 통한 관리를 지속할 예정입니다. 다만, 향후 매출 증가 및 품목 다변화에 의한 재고자산 증가 및 산업환경 변화에 대한 적응 미숙으로 인한 재고자산의 진부화 가능성은 여전히 존재하며, 이에 따라 재고자산의 평가손실이 확대된다면 수익성에 악영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. 사. GMP를 포함한 생산시설 관련 위험 당사는 2018년 11월에 준공을 시작하여 신축 GMP공장을 2019년 05월에 완공하였습니다. 당시 국내 줄기세포 치료제 생산 공장으로서는 가장 큰 규모로, 당사의 기존 아토피 피부염 치료제(퓨어스템-에이디주)의 상업화 허가 기대 일정에 맞춘 완공이었습니다. 당사는 퓨어스템-에이디주가 임상 3상에서 유의성이 달성되었을 경우, 신축 GMP공장을 본격적으로 가동하며 퓨어스템-에이디주의 판매용 완제품을 생산함으로써 시장 수요 충족과 더불어 대량생산으로 원가 절감으로 수익성 확대를 이룰 것으로 기대하였으나, 2019년 10월 퓨어스템-에이디주 3상 결과가 통계적 유의성 입증에 실패하면서 당사가 계획했던 GMP공장의 본격 가동 일정이 미뤄지게 되며, 가동률이 저하되었습니다. 이와 같이 아토피 피부염 치료제 상업화에 대한 허가 일정이 또 한번 장기간 미루어질 경우, 당사 GMP공장의 고정비는 당사의 재무구조 및 수익성에 부정적인 영향을 미칠 것으로 예상됩니다. 당사는 GMP공장의 활용도를 높이고 고정비 부담을 낮추기 위해 완공 이후 해당 GMP 공장에서 제대혈 유래 줄기세포 배양액, 줄기세포 배양 배지 등을 직접 생산하여 줄기세포 치료제를 제조하여 당사의 주요 파이프라인의 전임상시험 및 임상시험에 사용하고 있습니다. 이에 줄기세포 배양액과 줄기세포 배양 배지 생산을 위한 구획을 구분하여 생산 라인이 가동되고 있습니다. 또한, 당사는 GMP공장의 활용도를 높이고자 2020년 12월 식약처로부터 첨단바이오의약품 제조업 허가 승인을 받았으며, 이에 「첨단재생바이오법」 규정에 따라 사람 또는 동물의 줄기세포와 조혈모세포, 체세포 등을 채취·검사 처리해 재생의료기관에 공급할 수 있게 되었습니다. 다만, 당사의 신축 GMP공장을 활용한 주요 파이프라인 임상시험에 필요한 약물의 직접 생산 및 의약품 위탁개발생산(CDMO)이라는 신사업의 매출 증대 전략 등과 같은 당사의 노력에도 불구하고 수주 지연 및 GMP공장 시설 문제 등의 이유로 계획대로 진행되지 않는다면, 상기 생산시설의 연구인력 및 생산력 충원으로 인해 과도한 고정비의 지출이 선행되었기 때문에, 이는 당사의 재무구조 및 수익성에 부정적인 영향이 장기간 이어질 가능성이 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. 아. 특수관계자 및 지분투자기업과의 거래 관련 위험 당사는 특수관계자 등과 일부 자금거래가 발생하고 있으나, 특수관계자와 거래를 함에 있어 특별히 유리하거나 불리한 조건을 제시하는 등 거래상대방에 따라 계약조건을 달리한 사실이 없으며, 특수관계자와 계약을 체결할 때 통상 시장가로 계약을 체결하고 있습니다. 하지만 당사의 적법한 절차 및 법규 준수에도 불구하고 향후 당사와 특수관계자 간의 부적절한 거래가 발생될 가능성을 완전히 배제할 수 없으니 투자자께서는 이점 유의하시어 투자에 임하시기 바랍니다. 자. 환율 변동 관련 위험 당사의 매출액을 살펴보면 2022년 16,301백만원, 2023년 12,704백만원, 2024년 7,746백만원, 2025년 1분기 954백만원을 기록하였습니다. 이중 수출액은 2022년 272백만원, 2023년 673백만원, 2024년 860백만원, 2025년 1분기 95백만원을 기록하였으며 매출액 중 수출 비중은 미미한 수준을 나타냈습니다. 다만, 당사가 후생노동성으로부터 제2종(자가지방줄기세포) 최종 승인을 받은 상태로서, 금년도부터 일본 재생의료 시장 진출이 유력하기 때문에, 일본향 매출 비중이 증가할 가능성이 있습니다. 당사는 매출액 중 더마 코스메틱 브랜드 지디일레븐(GD11)의 매출 일부가 수출 형태로 판매되고 있습니다. 국가별 수출 비중을 살펴보면 주로 일본의 비중이 2022년 55%, 2023년 60%, 2024년 82%, 2025년 1분기 86%를 기록하고 있습니다. 최근 원/달러 환율은 글로벌 경기 불확실성 확대 및 국내 정치적 불안 요소 부각 등 대내외 환경의 영향으로 2024년 12월 31일 1,470.00원까지 급등한 뒤, 2025년 2월 24일 1,434.1원으로 일시적으로 안정되었으나, 이후 1,440원에서 1,475원 사이의 고환율 구간을 형성하며 원화 가치가 빠르게 하락하는 추세를 보였습니다. 다만, 2025년 5월 들어 미중 관세 협상과 같은 주요국 간 외교적 긴장 완화, 대외거래 수지 개선, 통화정책 변화에 대한 기대 등 대내외 여건의 변화에 따라 원/달러 환율이 급락하는 흐름을 보이며 높은 변동성을 보이고 있습니다. 아울러 원/엔 환율은 2024년 12월 31일 936.48원에서 2025년 4월 29일 기준 1,011.85원까지 상승하였으나 2025년 5월 들어 글로벌 외환시장 환경 변화에 따라 다시 하락세로 전환하는 등 글로벌 경제 변화와 일본의 통화정책 영향을 강하게 받으며 뚜렷한 변동성을 보였습니다.이처럼 갑작스러운 환율 변동성의 확대는 당사의 해외 글로벌 임상비용 지출 등에 영향을 미칠 수 있는 바 투자자 여러분께서는 이 점 유의하시기 바랍니다. 차. 잦은 자금조달 관련 위험 당사는 신주 상장으로 주주가치가 훼손될 수 있는 자금조달방법인 유상증자나 주식연계채권을 통해 자금을 조달한 이력이 있습니다. 당사의 경우 바이오의약품 기업 특성 상 추가적인 자금조달 가능성을 배제할 수 없습니다. 추가 자금조달 필요성이 지속될 경우 당사의 자금 유동성이 크게 악화될 수 있고 추가적인 자금조달을 진행할 수 있으며, 반복적인 유상증자 및 주식연계채권 발행으로 주주가치가 심각하게 훼손될 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. 카. 매출처 편중 관련 위험 당사의 주요 매출처인 프리모리스인터내셔널, CJ홈쇼핑, GS홈쇼핑사의 경우 2022년 71.0%, 2023년 85.0%로 꾸준히 증가하였으나 2024년 46.9%를 기록하며 매출처 편중이 일부 해소되었습니다. 해당 매출처들의 경우 당사의 주요 매출제품인 화장품 제품군의 매출처입니다. 당사의 경우 이러한 매출 편중을 해소하기 위해 일본 재생의료 사업 진출을 통한 신규 매출을 발생시키고자 적극적으로 영업 활동 중입니다. 현재 일본 재생의료심의위원회의 제2종(자가지방줄기세포)의 후생성 승인이 완료되어 2025년 하반기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 한편, 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며 마찬가지로 승인 시 후생성 승인 후 바로 시장에 공급될 수 있도록 준비 중입니다. 또한 OSCA의 해외 라이선스 아웃 또한 준비 중에 있습니다. 다만, 당사의 이러한 노력에도 불구하고 매출처 다각화가 예상보다 지체되고 주요 매출처 및 잠재 매출처들의 경영전략 변경에 따라 사업관계에 부정적인 변화가 발생하거나 주요 매출처의 매출 및 영업성과가 부진할 경우 당사의 영업실적 및 재무상태에 부정적인 영향을 미칠 수 있으므로 투자자께서는 이 점 유의하시기 바랍니다. 타. 소송 및 우발채무 관련 위험 당사는 2025년 1분기 현재기준으로 토지, 건물 등 유형자산을 기업은행에게 차입금에 대한 담보로 제공하고 있으며, 유형자산과 관련된 담보설정액은 88.0억원입니다. 당사의 유동성 및 재무안정성 지표를 살펴볼 때 당사의 2025년 1분기 단기 및 장기차입금은 67.1억원으로 현금성자산 186.0억원을 고려하였을 때 단기적인 채무불이행이 발생할 위험은 매우 낮은 상황입니다. 공시서류 제출 전일 현재 당사가 피고로서 계류 중인 소송사건은 없습니다. 상기 서술한 우발채무가 당사에게 어떤 시점에 부정적인 영향을 미칠지는 예측하기가 어려운 것으로 판단됩니다. 당사는 이와 같은 우발부채가 현재 존재하지 않지만 향후 사업운영에 따라 발생할 가능성이 존재하는 소송현황을 적절하게 관리하지 못한다면, 예상하지 못한 시점에 경영 활동에 중대한 부정적인 금전적 손실이 발생하여 투자자에게 대규모 피해를 끼칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. 파. 합병 철회 등에 따른 관계기업 관련 위험 당사는 주요 사업부문의 파이프라인 다각화, 경영효율성 및 주주가치 제고 등을 달성하기 위하여 2024년 11월 28일 이사회 결의를 통해 관계회사인 (주)프리모리스테라퓨틱스를 피합병회사로 하여 흡수합병(소규모합병)을 결정하였으나, 최근 국제 경제의 불확실성 증대 및 주식시장의 변동성 확대 등 제반 여건을 고려하여 합병 자진 철회를 결정하였습니다. 당사는 향후 수익원 다각화 및 기업가치 증대를 위해 신규 파이프라인 강화 등의 다양한 방안을 꾸준히 강구하고 있습니다. 방안 중 하나로 합병 여부와 무관하게 관계사인 (주)프리모리스테라퓨틱스와 엑소좀을 활용한 재생의료 사업 분야의 공동개발 및 국내외 사업화를 모색하는 등 계속하여 사업적 시너지를 도모할 예정입니다. 이는 당사의 연구개발 약물 형태를 확장하고 차세대 기술 개발 및 파이프라인 다각화 가능성이 생긴다는 긍정적인 측면이 있으나, 동시에 진행 과정에서 당사의 전망과 달리 비경상적 투자로 인한 재무적 여력 소진 추세가 가속화될 수 있으며, 이는 당사의 수익성과 재무안정성에 부정적인 영향을 미칠 가능성이 존재합니다. 또한, (주)프리모리스테라퓨틱스가 추후 자체적인 자금 조달을 진행할 경우, 당사의 보유 지분율 감소에 따른 지배력 감소로 인해 협업 효율을 약화하는 요인으로 작용할 수 있으니 투자자 여러분께서는 유의하여 주시기 바랍니다. 하. 내부회계관리제도 및 내부통제 관련 위험 당사는 내부통제를 위한 규정 및 조직을 구축하고 있으며, 우발상황 등이 발생하지 않도록 상시 모니터링을 통해 내부통제 강화를 위하여 상당한 노력을 기울이며 대비하고 있습니다. 그럼에도 불구하고, 내부회계관리조직이 적절하게 운영되지 않거나 혹은 외부감사인의 내부회계관리 운영실태를 검토한 결과 중요한 취약점이 발견될 시 각종 제재사항에 해당할 수 있습니다. 투자자 여러분들께서는 이 점을 반드시 유의하여 주시기 바랍니다. |
| 기타 투자위험 |
가. 금융감독기관의 규제 강화에 따른 위험 당사가 중점심사 대상 기준에 해당하는 경우, 중점 심사항목 위주로 1주일 이내 집중심사를 진행하고 최소 1회 이상의 대면협의를 진행하게 되며, 본 증권신고서는 공시 심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우에는 본 신고서상의 일정이 예상보다 지연될 가능성이 있습니다. 투자자 여러분께서는 이 점 유의하시기 바랍니다. |
2. 모집 또는 매출에 관한 일반사항
| (단위 : 원, 주) |
| 증권의 종류 |
증권수량 | 액면가액 | 모집(매출) 가액 |
모집(매출) 총액 |
모집(매출) 방법 |
|---|---|---|---|---|---|
| 보통주 | 38,000,000 | 500 | 1,295 | 49,210,000,000 | 주주배정후 실권주 일반공모 |
| 인수(주선) 여부 | 지분증권 등 상장을 위한 공모여부 | ||
|---|---|---|---|
| 인수 | 아니오 | 해당없음 | 해당없음 |
| 인수(주선)인 | 증권의 종류 |
인수수량 | 인수금액 | 인수대가 | 인수방법 | |
|---|---|---|---|---|---|---|
| 대표 | 삼성증권 | 보통주 | 19,000,000 | 24,605,000,000 | 대표주관수수료 : 모집총액의 0.50% 中 62.5% 인수수수료: 모집총액의 1.30% 中 50.0% 실권수수료: 잔액인수금액의 15.0% |
잔액인수 |
| 대표 | NH투자증권 | 보통주 | 11,400,000 | 14,763,000,000 | 대표주관수수료 : 모집총액의 0.50% 中 37.5% 인수수수료: 모집총액의 1.30% 中 30.0% 실권수수료: 잔액인수금액의 15.0% |
잔액인수 |
| 인수 | 한양증권 | 보통주 | 7,600,000 | 9,842,000,000 | 인수수수료: 모집총액의 1.30% 中 20.0% 실권수수료: 잔액인수금액의 15.0% |
잔액인수 |
| 청약기일 | 납입기일 | 청약공고일 | 배정공고일 | 배정기준일 |
|---|---|---|---|---|
| 2025년 08월 14일 ~ 2025년 08월 18일 | 2025년 08월 25일 | 2025년 08월 19일 | 2025년 08월 25일 | 2025년 07월 11일 |
| 청약이 금지되는 공매도 거래 기간 | |
|---|---|
| 시작일 | 종료일 |
| 2025년 06월 11일 | 2025년 08월 11일 |
| 자금의 사용목적 | |
|---|---|
| 구 분 | 금 액 |
| 운영자금 | 42,775,000,000 |
| 시설자금 | 4,010,000,000 |
| 채무상환자금 | 1,400,000,000 |
| 발행제비용 | 1,025,000,000 |
| 신주인수권에 관한 사항 | ||
|---|---|---|
| 행사대상증권 | 행사가격 | 행사기간 |
| - | - | - |
| 매출인에 관한 사항 | ||||
|---|---|---|---|---|
| 보유자 | 회사와의 관계 |
매출전 보유증권수 |
매출증권수 | 매출후 보유증권수 |
| - | - | - | - | - |
| 일반청약자 환매청구권 | ||||
|---|---|---|---|---|
| 부여사유 | 행사가능 투자자 | 부여수량 | 행사기간 | 행사가격 |
| - | - | - | - | - |
| 【주요사항보고서】 | 주요사항보고서(유상증자결정)-2025.06.10 |
| 【기 타】 |
|
제1부 모집 또는 매출에 관한 사항
I. 모집 또는 매출에 관한 일반사항
1. 공모개요
당사는 이사회 결의를 통하여 「자본시장과 금융투자업에 관한 법률」 제165조의6제2항제1호에 의거 당사와 공동대표주관회사인 삼성증권(주) 및 엔에이치투자증권(주), 인수회사인 한양증권(주) 간에 주주배정 후 실권주를 인수하는 계약을 체결하고 사전에 그 실권주를 일반에 공모하기로 하여, 당사 기명식 보통주 38,000,000주를 주주배정 후 실권주 일반공모 방식으로 발행하기로 결정하였으며, 동 증권의 개요는 다음과 같습니다.
■ 모집(매출) 정보
| (단위 : 원, 주) |
| 증권의 종류 | 증권수량 | 액면가액 | 모집가액 | 모집총액 | 모집방법 |
| 기명식 보통주 | 38,000,000 | 500 | 1,295 | 49,210,000,000 | 주주배정후 실권주 일반공모 |
| 주1) | 이사회 결의일: 2025년 06월 10일 |
| 주2) | 1주의 모집가액 및 모집총액은 예정 발행가액 기준으로 한 예정금액이며, 확정되지 않은 금액입니다. |
발행가액은「증권의 발행 및 공시 등에 관한 규정」 제5-18조에서 의거, 주주배정 증자시 가격산정 절차 폐지 및 가격산정의 자율화에 따라 발행가격을 자유롭게 산정할 수 있으나, 시장 혼란 우려 및 기존 관행 등으로 (구)「유가증권의 발행 및 공시 등에 관한 규정」 제57조를 일부 준용하여 산정할 예정입니다.
■ 예정 발행가액의 산출근거
본 증권신고서의 예정발행가액은 이사회결의일 직전 거래일(2025년 6월 9일)을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와 1주일 가중산술평균주가 및 최근일 가중산술평균주가를 산술평균하여 산정한 가액과 기산일 가중산술평균주가 중 낮은 금액을 기준주가로 하여 할인율 25%를 적용, 아래의 산식에 의하여 산정된 발행가액으로 합니다. 단, 호가 단위 미만은 호가 단위로 절상하며, 그 가액이 액면가액 미만인 경우 액면가액으로 합니다.
| ▶ 예정발행가액(1,295원) |
= | 기준주가 ×【 1 - 할인율(25%)】 |
| -------------------------------------------- | ||
| 1 + 【증자비율 × 할인율(25%)】 |
상기 방법에 따라 산정된 예정발행가액은 참고용이며, 구주주 청약일전 3거래일에 확정발행가액이 결정될 예정입니다.
| [ 예정발행가액 산정표] | |
| 기산일 : 2025년 06월 09일 |
(단위 : 원, 주) |
| 일자 | 가중산술평균주가 | 거래량 | 거래대금 |
| 2025-06-09 | 2,019 | 307,520 | 620,792,508 |
| 2025-06-05 | 2,072 | 475,494 | 985,030,013 |
| 2025-06-04 | 2,051 | 103,082 | 211,393,250 |
| 2025-06-02 | 2,021 | 235,247 | 475,340,281 |
| 2025-05-30 | 2,029 | 547,296 | 1,110,403,552 |
| 2025-05-29 | 1,976 | 294,254 | 581,489,062 |
| 2025-05-28 | 1,954 | 69,771 | 136,301,394 |
| 2025-05-27 | 1,953 | 168,181 | 328,491,158 |
| 2025-05-26 | 1,952 | 341,453 | 666,545,156 |
| 2025-05-23 | 1,938 | 138,721 | 268,850,639 |
| 2025-05-22 | 1,956 | 255,361 | 499,503,849 |
| 2025-05-21 | 1,975 | 141,808 | 280,006,860 |
| 2025-05-20 | 1,991 | 209,343 | 416,816,292 |
| 2025-05-19 | 1,975 | 425,950 | 841,345,572 |
| 2025-05-16 | 2,023 | 314,600 | 636,552,465 |
| 2025-05-15 | 2,046 | 465,855 | 952,982,348 |
| 2025-05-14 | 2,131 | 477,617 | 1,017,725,540 |
| 2025-05-13 | 2,169 | 193,951 | 420,696,459 |
| 2025-05-12 | 2,174 | 364,829 | 793,127,678 |
| 1개월 가중산술평균주가 (A) | 2,033 | 5,530,333 | 11,243,394,076 |
| 1주일 가중산술평균주가 (B) | 2,051 | 886,096 | 1,817,215,771 |
| 기산일 가중산술평균주가 (C) | 2,019 | 307,520 | 620,792,508 |
| (A),(B),(C)의 산술평균 (D) | 2,034 | (A+B+C)/3 | |
| 기준주가 (E) | 2,019 | (C와 D중 낮은가액) | |
| 할인율 (F) | 25% | - | |
| 증자비율 (G) | 67.79% | - | |
| 예정발행가액 | 1,295 | 기준주가 × (1-할인율) / 1 + (유상증자비율 × 할인율 ) (단, 호가 단위 미만은 호가 단위로 절상하기로 하며, 그 가액이 액면가액 미만인 경우 액면가액으로 합니다.) |
|
■ 공모일정 등에 관한 사항
당사는 2025년 06월 10일 이사회를 통해 유상증자를 결의하였으며, 세부 일정은 다음과 같습니다.
| [주요일정] |
| 날 짜 | 내 용 | 비 고 |
| 2025년 06월 10일 | 이사회결의 | - |
| 2025년 06월 10일 | 신주발행 및 기준일 공고 | 당사 인터넷 홈페이지 (www.kangstem.com) |
| 2025년 06월 10일 | 증권신고서(예비투자설명서) 제출 | - |
| 2025년 07월 08일 | 1차 발행가액 확정 | 신주배정기준일 3거래일 전 |
| 2025년 07월 10일 | 권리락 | - |
| 2025년 07월 11일 | 신주배정기준일(주주확정) | - |
| 2025년 07월 23일 | 신주배정 통지 | - |
| 2025년 07월 30일 ~ 2025년 08월 05일 |
신주인수권증서 상장 거래기간 | 5거래일 이상 거래 |
| 2025년 08월 06일 | 신주인수권증서 상장폐지 | 구주주 청약초일 5거래일 이전에 폐지 |
| 2025년 08월 11일 | 확정 발행가액 산정 | 구주주 청약초일 3거래일 전 |
| 2025년 08월 12일 | 확정 발행가액 공고 | 당사 인터넷 홈페이지 (www.kangstem.com) Dart전자공시시스템 (http://dart.fss.or.kr) |
| 2025년 08월 14일 ~ 2025년 08월 18일 |
구주주 청약 및 초과청약 | - |
| 2025년 08월 19일 | 일반공모 청약 공고 | 당사 인터넷 홈페이지 (www.kangstem.com) 삼성증권(주) 홈페이지 (http://www.samsungpop.com) 엔에이치투자증권(주) 홈페이지 (http://www.nhqv.com) 한양증권(주) 홈페이지 (www.hygood.co.kr) |
| 2025년 08월 20일 ~ 2025년 08월 21일 |
일반공모 청약 | - |
| 2025년 08월 25일 | 환불 및 배정 공고 | 삼성증권(주) 홈페이지 (http://www.samsungpop.com) 엔에이치투자증권(주) 홈페이지 (http://www.nhqv.com) 한양증권(주) 홈페이지 (www.hygood.co.kr) |
| 2025년 08월 25일 | 주금 납입 | - |
| 2025년 09월 04일 | 신주상장 예정일 | - |
| 주1) | 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. |
| 주2) | 2019년 9월 16일부터 전자증권제도가 시행됨에 따라 금번 유상증자 시 발행되는 신주인수권증서 및 신주는 전자증권으로 발행될 예정이며, 신주상장과 동시에 신주가 유통될 예정입니다. |
| 주3) | 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
2. 공모방법
| [공모방법 : 주주배정후 실권주 일반공모] |
| 모집대상 | 주식수 | 비 고 |
|---|---|---|
| 구주주 (신주인수권증서 보유자) 청약 |
38,000,000주(100.0%) | - 구주 1주당 신주 배정비율 : 1주당 0.6779159202주 - 신주배정 기준일 : 2025년 07월 11일 - 구주주 청약일 : 2025년 08월 14일 ~ 2025년 08월 18일 (2일간) - 보유한 신주인수권증서의 수량 한도로 청약가능(구주주에게는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율을 곱한 수량만큼의 신주인수권증서가 배정됨) |
| 초과 청약 | - | -「자본시장과 금융투자업에 관한 법률」제165조의6의 제2항 제2호에 의거 초과청약 - 초과청약비율 : 배정신주(신주인수권증서) 1주당 0.2주 - 신주인수권증서 거래를 통해서 신주인수권증서를 매매시 보유자 기준으로 초과청약 가능 |
| 일반공모 청약 (고위험고수익투자신탁등, 벤처기업투자신탁 청약 포함) |
- | - 구주주 및 초과청약 후 발생하는 단수주 및 실권주에 대해 배정됨 - 일반공모 청약일 : 2025년 08월 20일 ~ 2025년 08월 21일 (2일간) |
| 합 계 | 38,000,000주(100.0%) | - |
| 주1) | 본 건 유상증자는 주주배정후 실권주 일반공모 방식으로 진행되며, 구주주 청약결과 발생하는 실권주 및 단수주는 우선적으로 초과청약자에게 배정되며, 이후 실권이 발생할 경우에 대해서는 일반에게 공모합니다. |
| 주2) | 구주주의 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율인 0.6779159202주를 곱하여 산정된 배정주식수로 하되, 1주 미만은 절사합니다. 단, 신주배정기준일 전 주식관련사채의 권리행사, 주식매수선택권의 권리행사, 자기주식수의 변동 등으로 인하여 1주당 배정주식수가 변동될 수 있습니다. |
| 주3) |
신주인수권증서 보유자는 보유한 신주인수권증서 수량의 한도로 증서청약을 할 수 있고, 동 주식수에 초과청약비율(20%)를 곱한 수량을 한도로 초과청약 할 수 있습니다. 단, 1주 미만은 절사합니다. (ii) 신주인수권증서 청약한도 주식수 = 보유한 신주인수권증서의 수량 (iii) 초과청약 한도주식수 = 신주인수권증서 청약한도 주식수 X 초과청약 비율(20%) |
| 주4) |
"고위험고수익투자신탁등"이란 다음 각 호의 어느 하나에 해당하는 투자신탁 등을 말합니다. (1) 「조세특례제한법」 제91조의15 제1항에 따른 고위험고수익채권투자신탁을 말합니다. 다만, 해당 투자신탁 등의 최초 설정일ㆍ설립일이 속하는 분기 또는 그 다음 분기 말일 전 영업일까지 수요예측에 참여하는 경우에는 같은 법 시행령 제93조 제1항 제1호 및 같은 조 제5항에도 불구하고 수요예측 참여일 직전 영업일의 고위험고수익채권의 보유비율이 같은 법 시행령 제93조 제1항 제1호 각 목의 비율 이상이어야 합니다. (2) 법률 제19328호「조세특례제한법」의 시행일 이전의 제91조의15제1항에 따른 고위험고수익투자신탁으로서 최초 설정일ㆍ설립일이 2023년 12월 31일 이전인 것을 말합니다. 다만, 해당 투자신탁 등의 설정일ㆍ설립일부터 배정일까지의 기간이 6개월 미만인 경우에는 대통령령 제33499호「조세특례제한법 시행령」시행령 시행일 이전의 제93조 제3항 제1호 및 같은 조 제7항에도 불구하고 수요예측 참여일 직전 영업일의 비우량채권과 코넥스 상장주식을 합한 보유비율이 100분의 45 이상이고 이를 포함한 국내 채권의 보유비율이 100분의 60 이상이어야 합니다. |
| 주5) | "벤처기업투자신탁"이란 「조세특례제한법」 제16조제1항제2호의 벤처기업투자신탁(대통령령 제28636호 「조세특례제한법 시행령 일부개정령」 시행 이후 설정된 벤처기업투자신탁에 한한다. 이하 같다)을 말합니다. 다만 해당 벤처기업투자신탁의 최초 설정일로부터 배정일까지의 기간이 1년 미만인 경우에는 같은 법 시행령 제14조제1항제3호에도 불구하고 배정일 직전영업일의 벤처기업투자신탁 재산총액에서 같은 호 각 목에 따른 비율의 합계가 100분의 35 이상이어야 합니다. |
| 주6) |
구주주 청약(초과청약 포함) 결과 발생한 미청약주식 및 단수주는 공동대표주관회사와 인수회사가 일반에게 공모하되「증권 인수업무 등에 관한 규정」 제9조 제2항 제6호에 따라 "고위험고수익투자신탁등"에 일반공모 배정분의 10%를 배정하고, "벤처기업투자신탁"에 일반공모 배정분의 25%를 배정합니다. 나머지 주식은 개인청약자 및 기관투자자에 구분없이 배정합니다. "고위험고수익투자신탁등"에 대한 일반공모 배정분 10%, "벤처기업투자신탁"에 대한 일반공모 배정분 25% 및 개인투자자 및 기관투자자에 대한 일반공모 배정분 65%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정합니다. 다만, 한 그룹만 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다. 일반공모 청약결과 일반공모 총 청약자의 청약주식수가 일반공모 배정분에 미달하는 경우에는 청약주식수대로 배정합니다. 배정결과 발생하는 잔여주식은 "공동대표주관회사"와 "인수회사"가 각 인수의무비율대로 자기계산으로 잔액인수하기로 합니다. |
| 주7) | 단, 공동대표주관회사와 인수회사는 「증권 인수업무 등에 관한 규정」 제9조제2항에 의거 "고위험고수익투자신탁등", "벤처기업투자신탁" 및 일반청약자에 대하여 배정하여야 할 주식이 50,000주 이하(액면가 500원 기준)이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 이를 청약자에게 배정하지 아니하고 공동대표주관회사 및 인수회사가 자기계산으로 인수할 수 있습니다. |
| 주8) |
자본시장법 제180조의4 및 같은 법 시행령 제208조의4제1항에 따라 2025년 06월 11일부터 2025년 08월 11일까지 공매도를 하거나 공매도 주문을 위탁한 자는 금번 모집(매출)에 청약할 수 없으며, 이를 위반하여 주식을 취득할 경우 같은 법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만 모집(매출)가액의 공정한 가격형성을 저해하지 않는 경우로서 같은 법 시행령 제208조의4제2항 및 금융투자업규정 제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다. ※ 예외적으로 모집(매출)에 따른 주식 취득이 허용되는 경우 ① 모집(매출)에 따른 주식 취득이 금지되는 공매도 거래 기간 중에 전체 공매도 주문수량보다 많은 수량의 주식을 가격경쟁에 의한 거래 방식으로 매수한 경우 (매매계약 체결일 기준으로 정규시장의 매매거래시간에 매수한 경우로 한정) ② 한국거래소의 증권시장업무규정 또는 파생상품시장업무규정에서 정한 유동성 공급 및 시장조성 목적을 위해 해당 주식을 공매도하거나 공매도 주문을 위탁한 경우 ③ 동일한 법인 내에서 모집(매출)에 따른 주식 취득 참여가 금지되는 공매도 거래 기간 중 공매도를 하지 않거나 공매도 주문을 위탁하지 않은 독립거래단위(*)가 모집(매출)에 따른 주식을 취득하는 경우 (*)「금융투자업규정」 제6-30조 제5항에 따라 의사결정이 독립적이고 상이한 증권계좌를 사용하는 등의 요건을 갖춘 거래단위 |
▶ 구주주 1주당 배정비율 산출근거
| 구 분 | 상세 내역 |
|---|---|
| A. 보통주식 | 56,054,149주 |
| B. 우선주식 | - |
| C. 발행주식총수(A+B) | 56,054,149주 |
| D. 자기주식 + 자기주식신탁 | - |
| E. 자기주식을 제외한 발행주식총수 (C-D) | 56,054,149주 |
| F. 유상증자 주식수 | 38,000,000주 |
| G. 증자비율 (F/C) | 67.79% |
| H. 우리사주조합 배정 | - |
| I. 구주주배정 (F-H) | 38,000,000주 |
| J. 구주주 1주당 배정비율 (I/E) | 0.6779159202 |
3. 공모가격 결정방법
「증권의 발행 및 공시 등에 관한 규정」 제5-18조에서 주주배정 증자시 가격산정 절차 폐지 및 가격산정의 자율화에 따라 발행가격을 자유롭게 산정할 수 있으나, 시장 혼란 우려 및 기존 관행 등으로 (구)「유가증권의 발행 및 공시 등에 관한 규정」 제57조를 일부 준용하여 아래와 같이 발행가액을 산정합니다.
(1) 1차 발행가액 : 신주배정기준일 전 제3거래일을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와 1주일 가중산술평균주가 및 기산일 가중산술평균주가를 산술평균하여 산정한 가액과 기산일 가중산술평균주가 중 낮은 금액을 기준주가로 하여 할인율 25%를 적용, 아래의 산식에 의하여 산정된 발행가액을 1차 발행가액으로 합니다. 단, 호가 단위 미만은 호가 단위로 절상하며, 그 가액이 액면가액 미만인 경우에는 액면가액을 발행가액으로 합니다.
| 기준주가 ×【 1 - 할인율(25%)】 | ||
| ▶ 1차 발행가액 | = | ------------------------------------- |
| 1 + 【증자비율 × 할인율(25%)】 |
(2) 2차 발행가액 : 구주주 청약 초일 전 제3거래일을 기산일로 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1주일 가중산술평균주가 및 기산일 가중산술평균주가를 산술평균하여 산정한 가액과 기산일 가중산술평균주가 중 낮은 금액을 기준주가로 하여 할인율 25%를 적용, 아래의 산식에 의하여 산정된 발행가액을 2차 발행가액으로 합니다. 단, 호가 단위 미만은 호가 단위로 절상하며, 그 가액이 액면가액 미만인 경우에는 액면가액을 발행가액으로 합니다.
| ▶ 2차 발행가액 = 기준주가 ×【1 - 할인율(25%)】 |
(3) 확정 발행가액 : 확정발행가액은 1차 발행가액과 2차 발행가액 중 낮은 가액으로 합니다. 다만, 「자본시장과 금융투자업에 관한 법률」 제165조의6 및 「증권의 발행 및 공시 등에 관한 규정」 제5-15조의2에 의거하여 1차 발행가액과 2차 발행가액중 낮은 가액이 구주주 청약일 전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 할인율 40%를 적용하여 산정한 가액보다 낮은 경우에는 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 할인율 40%를 적용하여 산정한 가액을 확정발행가액으로 합니다. 단, 호가 단위 미만은 호가 단위로 절상하며, 그 가액이 액면가액 미만인 경우에는 액면가액을 발행가액으로 합니다.
| ▶ 확정 발행가액 = MAX【MIN(1차 발행가액, 2차 발행가액), 청약일 전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가의 60%】 |
(4) 최종 발행가액은 구주주 청약일 초일 전 제3거래일에 결정되어 익영업일에 금융감독원 전자공시시스템에 공시될 예정이며, 회사의 인터넷 홈페이지(www.kangstem.com)에 공고하여 개별통지에 갈음할 예정입니다.
※ 일반공모 발행가액은 구주주 청약시에 적용된 확정 발행가액을 동일하게 적용합니다.
4. 모집 또는 매출절차 등에 관한 사항
가. 모집 또는 매출조건
| (단위 : 주, 원) |
| 항 목 | 내 용 | |||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 모집 또는 매출주식의 수 | 38,000,000 | |||||||||||||||||||||||||||||||||||
| 주당 모집가액 | 예정가액 | 1,295 | ||||||||||||||||||||||||||||||||||
| 확정가액 | - | |||||||||||||||||||||||||||||||||||
| 모집총액 | 예정가액 | 49,210,000,000 | ||||||||||||||||||||||||||||||||||
| 확정가액 | - | |||||||||||||||||||||||||||||||||||
| 청 약 단 위 |
(1) 구주주의 청약단위는 1주로 하며, 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식수에 신주배정비율("주주 배정분"에 해당하는 주식수를 자기주식을 제외한 발행주식 총수로 나눈 비율을 말하며, 자기주식과 발행주식총수는 신주배정기준일 현재의 주식수를 말한다)을 곱하여 산정된 배정주식수(1주 미만은 절사)와 초과청약가능 주식수(보유하고 있는 신주인수권증서 1주당 0.2주를 곱하여 산정된 수, 단 1주 미만은 절사)를 합한 주식수입니다. 다만, 신주배정기준일 현재 신주배정비율은 주식관련사채의 행사, 주식매수선택권의 행사, 자기주식수의 변동 등으로 인하여 변경될 수 있습니다.
|
|||||||||||||||||||||||||||||||||||
| 청약기일 | 구주주 | 개시일 | 2025년 08월 14일 | |||||||||||||||||||||||||||||||||
| 종료일 | 2025년 08월 18일 | |||||||||||||||||||||||||||||||||||
| 실권주 일반공모 | 개시일 | 2025년 08월 20일 | ||||||||||||||||||||||||||||||||||
| 종료일 | 2025년 08월 21일 | |||||||||||||||||||||||||||||||||||
| 청약 증거금 |
구주주 | 청약금액의 100% | ||||||||||||||||||||||||||||||||||
| 초 과 청 약 | 청약금액의 100% | |||||||||||||||||||||||||||||||||||
| 일반모집 또는 매출 | 청약금액의 100% | |||||||||||||||||||||||||||||||||||
| 납 입 기 일 | 2025년 08월 25일 | |||||||||||||||||||||||||||||||||||
| 배당기산일(결산일) | 2025년 01월 01일 | |||||||||||||||||||||||||||||||||||
| 주1) | 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. |
| 주2) | 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
나. 모집 또는 매출의 절차
1) 공고의 일자 및 방법
| 구 분 | 공고일자 | 공고방법 |
|---|---|---|
| 신주 발행 및 배정기준일(주주확정일) 공고 |
2025년 07월 11일 |
회사 인터넷 홈페이지 (www.kangstem.com) |
| 모집가액 확정의 공고 | 2025년 08월 12일 |
회사 인터넷 홈페이지 (www.kangstem.com) 전자공시시스템(http://dart.fss.or.kr) |
| 실권주 일반공모 청약공고 | 2025년 08월 19일 |
회사 인터넷 홈페이지 (www.kangstem.com) 삼성증권(주) 홈페이지(http://www.samsungpop.com) 엔에이치투자증권(주) 홈페이지 (http://www.nhqv.com) 한양증권(주) 홈페이지 (www.hygood.co.kr) |
| 실권주 일반공모 배정공고 | 2025년 08월 25일 |
삼성증권(주) 홈페이지(http://www.samsungpop.com) 엔에이치투자증권(주) 홈페이지 (http://www.nhqv.com) 한양증권(주) 홈페이지 (www.hygood.co.kr) |
| 주1) | 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
| 주2) | 모집가액은 2025년 08월 11일을 기준으로 확정되며, 다음 영업일인 2025년 08월 12일까지 공고할 예정입니다. |
| 주3) | 청약결과 초과청약금 환불에 대한 통지는 공동대표주관회사 및 인수회사 홈페이지에 게시함으로써 개별통지에 갈음합니다. |
| 주4) | 전산장애 또는 그 밖의 부득이한 사유로 회사의 인터넷 홈페이지에 공고를 할 수 없는 때에는 서울특별시에서 발행되는 일간 매일경제신문에 게재할 예정입니다. |
2) 청약방법
(1) 구주주 청약(신주인수권증서 보유자 청약): 구주주 중 주권을 증권회사에 예탁한 주주(기존 "실질주주")는 주권을 예탁한 증권회사의 본ㆍ지점 및 공동대표주관회사의 본ㆍ지점에서 청약할 수 있습니다. 다만, 구주주 중 명의개서대행기관 특별계좌에 주식을 가지고 있는 주주(기존 "명부주주")는 신주배정통지서를 첨부하여 실명확인증표를 제시한 후 공동대표주관회사의 본ㆍ지점에서 청약할 수 있습니다. 청약시에는 소정의 청약서 2통에 필요한 사항을 기입하여 청약증거금과 함께 제출하여야 합니다.
| 2019년 9월 16일 전자증권제도가 시행되며, 주권 상장법인의 상장주식은 전자증권 의무전환대상으로 전자증권제도 시행일에 전자증권으로 일괄전환됩니다. 전자증권제도 시행전까지 증권회사에 예탁하고 있는 실질주주 주식은 해당 증권회사 계좌에 전자증권으로 일괄 전환되며, 기존 명부주주가 보유한 주식은 명의개서대행기관이 개설하는 특별계좌에 발행되어 소유자별로 관리됩니다. 금번 유상증자시 신주인수권증서는 전자증권제도 시행일 이후에 발행되고 상장될 예정으로 전자증권으로 발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다. '특별계좌 보유자(기존 '명부주주')'는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후 금번 유상증자 청약 참여또는 신주인수권증서의 매매가 가능합니다. '특별계좌 보유자(기존 '명부주주')'는 신주인수권증서의 '일반 전자등록계좌(증권회사 계좌)'로 이전 없이 "공동대표주관회사"의 본ㆍ지점에서 직접 청약하는 방법으로도 금번 유상증자에 청약이 가능합니다. 다만 신주인수권증서의 매매는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후에만 가능하므로 이 점 유의하시기 바랍니다. |
| 「주식ㆍ사채 등의 전자등록에 관한 법률」 제29조(특별계좌의 개설 및 관리) ① 발행인이 제25조부터 제27조까지의 규정에 따라 이미 주권등이 발행된 주식등을 전자등록하는 경우 제25조제1항에 따른 신규 전자등록의 신청을 하기 전에 제27조제1항제2호에 따른 통지를 하지 아니하거나 주권등을 제출하지 아니한 주식등의 소유자 또는 질권자를 위하여 명의개서대행회사, 그 밖에 대통령령으로 정하는 기관(이하 이 조에서 "명의개서대행회사등"이라 한다)에 기준일의 직전 영업일을 기준으로 주주명부등에 기재된 주식등의 소유자 또는 질권자를 명의자로 하는 전자등록계좌(이하 "특별계좌"라 한다)를 개설하여야 한다. ② 제1항에 따라 특별계좌가 개설되는 때에 제22조제2항 또는 제23조제2항에 따라 작성되는 전자등록계좌부(이하 이 조에서 "특별계좌부"라 한다)에 전자등록된 주식등에 대해서는 제30조부터 제32조까지의 규정에 따른 전자등록을 할 수 없다. 다만, 다음 각 호의 어느 하나에 해당하는 경우에는 그러하지 아니하다. 1. 해당 특별계좌의 명의자가 아닌 자가 주식등이 특별계좌부에 전자등록되기 전에 이미 주식등의 소유자 또는 질권자가 된 경우에 그 자가 발행인에게 그 주식등에 관한 권리가 표시된 주권등을 제출(주권등을 제출할 수 없는 경우에는 해당 주권등에 대한 제권판결의 정본·등본을 제출하는 것을 말한다. 이하 제2호 및 제3호에서 같다)하고 그 주식등을 제30조에따라 자기 명의의 전자등록계좌로 계좌간 대체의 전자등록을 하려는 경우(해당 주식등에 질권이 설정된 경우에는 다음 각 목의 어느 하나에 해당하는 경우로 한정한다) 가. 해당 주식등에 설정된 질권이 말소된 경우 나. 해당 주식등의 질권자가 그 주식등을 특별계좌 외의 소유자 명의의 다른 전자등록계좌로 이전하는 것에 동의한 경우 2. 해당 특별계좌의 명의자인 소유자가 발행인에게 전자등록된 주식등에 관한 권리가 표시된 주권등을 제출하고 그 주식등을 제30조에 따라 특별계좌 외의 자기 명의의 다른 전자등록계좌로 이전하려는 경우(해당 주식등에 질권이 설정된 경우에는 제1호 각 목의 어느 하나에 해당하는 경우로 한정한다) 3. 해당 특별계좌의 명의자인 질권자가 발행인에게 주권등을 제출하고 그 주식등을 제30조에 따라 특별계좌 외의 자기 명의의 전자등록계좌로 이전하려는 경우 4. 그 밖에 특별계좌에 전자등록된 주식등의 권리자의 이익을 해칠 우려가 없는 경우로서 대통령령으로 정하는 경우 ③ 누구든지 주식등을 특별계좌로 이전하기 위하여 제30조에 따른 계좌간 대체의 전자등록을 신청할 수 없다. 다만, 제1항에 따라 특별계좌를 개설한 발행인이 대통령령으로 정하는 사유에 따라 신청을 한 경우에는 그러하지 아니하다. ④ 명의개서대행회사등이 발행인을 대행하여 제1항에 따라 특별계좌를 개설하는 경우에는 「금융실명거래 및 비밀보장에 관한 법률」 제3조에도 불구하고 특별계좌부에 소유자 또는질권자로 전자등록될 자의 실지명의를 확인하지 아니할 수 있다. |
(2) 초과청약: 신주인수권증서 청약을 한 자에 한하여 신주인수권증서 청약 한도 주식수의 20%를 추가로 청약할 수 있습니다. 이때, 신주인수권증서 청약 한도주식수의 20%에 해당하는 주식 중 소수점 이하인 주식은 청약할 수 없습니다.
a. 청약한도 주식수 = 신주인수권증서청약 한도주식수 + 초과청약 한도주식수
b. 신주인수권증서청약 한도주식수 = 보유한 신주인수권 증서의 수량
c. 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 * 초과청약 비율(20%)
(3) 일반공모청약: 고위험고수익투자신탁등, 벤처기업투자신탁 및 일반청약자는 「금융실명거래 및 비밀보장에 관한 법률」의 규정에 의한 실명자이어야 하며, 청약사무 취급처에 실명확인증표를 제시하고 청약합니다. 고위험고수익투자신탁등, 벤처기업투자신탁 및 일반청약자의 청약 시, 각 청약처별로 다중청약은 가능하나, 한 개의 청약처에서 이중청약은 불가능하며, 집합투자기구 중 운용주체가 다른 집합투자기구를 제외한 청약자의 한 개 청약처에 대한 복수청약은 불가능합니다. 또한 고위험고수익투자신탁등은 청약 시, 청약사무 취급처에 「증권 인수업무 등에 관한 규정」 제2조제18호에 따른 요건을 충족함을 확약하는 서류 및 자산총액이 기재되어 있는 서류를 함께 제출하여야 합니다. 벤처기업투자신탁은 청약 시, 청약사무 취급처에 「증권 인수업무 등에 관한 규정」 제2조제20호에 따른 요건을 충족하고, 제9조제10항에 따른 확약서 및 자산총액이 기재되어 있는 서류를 함께 제출하여야 합니다.
(4) 일반청약자의 청약은 청약주식의 단위에 따라 될 수 있으며, 1인당 청약한도를 초과하는 청약부분에 대하여는 청약이 없는 것으로 하고 청약사무 취급처는 그 차액을 납입일까지 당해 청약자에게 반환하며, 이때 받은 날부터의 이자는 지급하지 않습니다.
(5) 본 유상증자에 청약하고자 하는 투자자(「자본시장과 금융투자업에 관한 법률」 제9조제5항에 규정된 전문투자자 및 「자본시장과 금융투자업에 관한 법률 시행령」 제 132조에 따라 투자설명서의 교부가 면제되는자 제외)는 청약 전 반드시 투자설명서를 교부 받아야 하고, 이를 확인하는 서류에 서명 또는 기명날인하여야 합니다.
(6) 청약 한도
a. 구주주(신주인수권증서 보유자)의 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율인 0.6779159202주를 곱하여 산정된 신주인수권증서(단, 1주 미만은 절사)와 초과청약가능 주식수(보유하고 있는 신주인수권증서 1주당 0.2주를 곱하여 산정된 수, 단 1주 미만은 절사)를 합한 주식수로 하되, 자기주식, 자사주신탁, 주식관련사채의 권리행사 등의 변동으로 인하여 구주주의 1주당 배정비율은 변동될 수 있습니다.
b. 일반공모 청약자의 청약한도는 일반공모 총 공모주식 범위 내로 하며, 청약한도를초과하는 부분에 대해서는 청약이 없는 것으로 간주합니다.
(7) 기타
① 일반공모 배정을 함에 있어 이중청약이 있는 경우에는 그 청약자의 청약 전부를 청약하지 아니한 것으로 봅니다. 단, 구주주가 신주배정비율에 따라 배정받은 주식을 청약한 후 일반공모에 참여하는 경우에는 금지되는 이중청약이 있는 경우로 보지 않습니다. 단, 동일한 집합투자기구라도 운용주체(집합투자업자)가 다른 경우는 예외로 합니다.
② 1인당 청약한도를 초과하는 청약부분에 대하여는 청약이 없는 것으로 합니다.
③ 청약자는 「금융실명거래 및 비밀보장에 관한 법률」에 의거 실지 명의에 의해 청약해야 합니다.
④「자본시장법과 금융투자업에 관한 법률」 제180조의4 및 동법 시행령 제208조의4제1항에 의거, 2025년 06월 11일부터 2025년 08월 11일까지 당사의 주식을 공매도 하거나 공매도 주문을 위탁한 자는 금번 모집(매출)에 청약할 수 없으며, 이를 위반하여 주식을 취득할 경우 동법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만, 모집(매출)가액의 공정한 가격형성을 저해하지 않는 경우로서 동법 시행령 제208조의4제2항 및 「금융투자업규정」제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다.
|
※ 예외적으로 모집(매출)에 따른 주식 취득이 허용되는 경우 ① 모집(매출)에 따른 주식 취득이 금지되는 공매도 거래 기간 중에 전체 공매도 주문수량보다 많은 수량의 주식을 가격경쟁에 의한 거래 방식으로 매수한 경우(매매계약 체결일 기준으로 정규시장의 매매거래시간에 매수한 경우로 한정) ② 한국거래소의 증권시장업무규정 또는 파생상품시장업무규정에서 정한 유동성 공급 및 시장조성 목적을 위해 해당 주식을 공매도하거나 공매도 주문을 위탁한 경우 ③ 동일한 법인 내에서 모집(매출)에 따른 주식 취득 참여가 금지되는 공매도 거래 기간 중 공매도를 하지 않거나 공매도 주문을 위탁하지 않은 독립거래단위(*)가 모집(매출)에 따른 주식을 취득하는 경우 (*)「금융투자업규정」제6-30조 제5항에 따라 의사결정이 독립적이고 상이한 증권계좌를 사용하는 등의 요건을 갖춘 거래단위 |
3) 청약취급처
| 청약대상자 | 청약취급처 | 청약일 | |
|---|---|---|---|
| 구주주 (신주인수권증서 보유자) |
특별계좌 보유자 (기존 '명부주주') |
1) 삼성증권(주) 본ㆍ지점 2) 엔에이치투자증권(주) 본ㆍ지점 |
2025년 08월 14일~ 2025년 08월 18일 |
| 일반주주 (기존 '실질주주') |
1) 주주확정일 현재 (주)강스템바이오텍의 주식을 예탁하고 있는 당해 증권회사 본ㆍ지점 2) 삼성증권(주) 본ㆍ지점 3) 엔에이치투자증권(주) 본ㆍ지점 |
||
| 일반공모청약 (고위험고수익투자신탁등, 벤처기업투자신탁 청약 포함) |
1) 삼성증권(주) 본ㆍ지점 2) 엔에이치투자증권(주) 본ㆍ지점 3) 한양증권(주) 본ㆍ지점 |
2025년 08월 20일~ 2025년 08월 21일 |
|
| ※ | 청약취급처에 따라 청약창구 및 방법(본ㆍ지점 외 홈페이지, HTS, MTS, ARS 등)과 규정이 상이하오니 해당 증권사에 청약전 확인하여 주시기 바랍니다. |
4) 청약결과 배정방법
가) 구주주(신주인수권증서 보유자) 청약 : 신주배정기준일(2025년 07월 11일 예정) 18시 현재 주주명부에 등재된 주주(이하 "구주주"라 한다)에게 "본 주식"을 1주당 "신주배정비율"인 0.6779159202주를 곱하여 산정된 배정주식수(단, 1주 미만은 절사함)로 하고, 배정범위 내에서 청약한 수량만큼 배정합니다. 단, 신주배정기준일 전 주식관련사채의 행사, 주식매수선택권의 행사, 자기주식수의 변동 등으로 인하여 1주당 배정주식수가 변동될 수 있습니다.
나) 초과청약 : 구주주(신주인수권증서 보유자) 청약 이후 발생한 실권주 및 단수주가 있는 경우, 실권주 및 단수주를 구주주(신주인수권증서 보유자)가 초과청약(초과청약비율 : 배정 신주 1주당 0.2주)한 주식수에 비례하여 배정하며, 1주 미만의 주식은 절사하여 배정하지 않습니다. (단, 초과청약 주식수가 실권주 및 단수주에 미달한 경우 100% 배정)
(ⅰ) 청약한도 주식수 = 신주인수권증서 청약한도 주식수 + 초과청약한도 주식수
(ⅱ) 신주인수권증서 청약한도 주식수 = 보유한 신주인수권증서의 수량
(ⅲ) 초과청약한도 주식수 = 신주인수권증서청약 한도주식수 × 초과청약 비율(20%)
다) 일반공모 청약:
(1) 상기 구주주 청약 및 초과청약 결과 발생한 실권주 및 단수주(이하 "일반공모 배정분"이라 한다)는 공동대표주관회사와 인수회사가 일반에게 공모하되, 「증권 인수업무 등에 관한 규정」 제9조 제2항 제6호에 따라 "고위험고수익투자신탁등"에 공모주식의 10%를 배정하고, "벤처기업투자신탁"에 공모주식의 25%를 배정합니다. 나머지 65%에 해당하는 주식은 개인청약자 및 기관투자자(집합투자업자 포함)에게 구분 없이 배정합니다. "고위험고수익투자신탁등"에 대한 일반공모 배정분 10%, "벤처기업투자신탁"에 대한 일반공모 배정분 25% 및 개인투자자 및 기관투자자에 대한 일반공모 배정분 65%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정합니다. 다만, 어느 한 그룹에서 청약미달이 발생할 경우「증권인수업무등에 관한 규정」제9조 제3항에 따라, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다.
(2) 일반공모에 관한 배정수량 계산시 "공동대표주관회사"와 "인수회사"의 "청약물량"(공동대표주관회사와 인수회사의 각 청약처에서 일반공모 방식으로 접수를 받은 청약주식수를 의미하며, 공동대표주관회사와 인수회사에 대하여 개별적으로 산정한 청약주식수를 말한다)에 대해서는 "공동대표주관회사"와 "인수회사"의 "총청약물량"(공동대표주관회사와 인수회사가 일반공모 방식으로 접수를 받은 청약물량의 합을 말한다)을 "일반공모 배정분" 주식수로 나눈 통합 청약경쟁률에 따라 "공동대표주관회사"와 "인수회사"의 각 청약자에 배정하는 방식(이하 "통합배정"이라 한다)으로 합니다.
(3) 일반공모에 관한 배정시 "공동대표주관회사"와 "인수회사"의 "총청약물량"이 "일반공모 배정분" 주식수를 초과하는 경우에는 청약경쟁률에 따라 5사6입을 원칙으로 안분 배정하여 잔여주식이 최소화되도록 합니다.다만, 고위험고수익투자신탁등에 대한 공모주식 10%와 벤처기업투자신탁에 대한 공모주식 25%, 개인투자자 및 기관투자자(집합투자업자포함)에 대한 공모주식 65%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정합니다. 다만, 어떤 그룹에 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다. 이후 최종 잔여주식은 최대청약자부터 순차적으로 우선 배정하되, 동순위 최고청약자가 최종 잔여 주식보다 많은 경우에는 "공동대표주관회사"와 "인수회사"가 합리적으로 판단하여 배정합니다.
(4) 일반공모 청약결과 "공동대표주관회사"와 "인수회사"의 "총청약물량"이 "일반공모 배정분" 주식수에 미달하는 경우에는 청약주식수대로 배정하며, 배정결과 발생하는 잔여주식은 "공동대표주관회사"와 "인수회사"가 잔액인수계약서 제2조 제5항에 따른 인수비율에 따라 각각 자기의 계산으로 인수합니다.
(5) 단, "공동대표주관회사" 및 "인수회사"는「증권 인수업무 등에 관한 규정」 제9조 제2항에 의거 고위험고수익투자신탁등, 벤처기업투자신탁, 일반청약자에 대하여 배정하여야 할 주식이 50,000주 이하(액면가 500원 기준)이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 이를 청약자에게 배정하지 아니하고 자기계산으로 인수할 수 있습니다.
5) 투자설명서 교부에 관한 사항
- 「자본시장과 금융투자업에 관한 법률」 제124조에 의거, 본 주식의 청약에 대한 투자설명서 교부 의무는 당사 및 공동대표주관회사, 인수회사가 부담하며, 금번 유상증자의 청약에 참여하시는 투자자께서는 투자설명서를 의무적으로 교부받으셔야 합니다.
- 금번 유상증자에 청약하고자 하는 투자자께서는 (「자본시장과 금융투자업에 관한 법률」제9조 제5항에 규정된 전문투자자 및「자본시장과 금융투자업에 관한 법률 시행령」제132조에 따라 투자설명서의 교부가 면제되는 자 제외) 청약하시기 전 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
- 투자설명서 수령거부 의사 표시는 서면, 전화, 전신, 모사전송, 전자우편 및 이와 비슷한 전자통신, 그 밖의 금융위원회가 정하여 고시하는 방법으로 가능합니다.
- 전자문서의 방법으로 투자설명서를 교부받고자 하는 투자자는 「자본시장과 금융투자업에 관한 법률」 제124조제1항 각호의 요건을 모두 충족하여야 합니다.
가) 투자설명서 교부 방법 및 일시
| 구분 | 교부방법 | 교부일시 |
|---|---|---|
| 구주주 청약자 |
1),2),3)을 병행 1) 등기우편 송부 2) "공동대표주관회사"의 본, 지점 교부 3) "공동대표주관회사"의 홈페이지나 HTS, MTS에서 교부 |
1) 우편송부 시: 구주주 청약초일(2025년 08월 14일) 전 수취 가능 2) "공동대표주관회사"의 본, 지점 3) "공동대표주관회사"의 홈페이지 또는 HTS, MTS 교부 |
| 일반 청약자 |
1), 2)를 병행 1) "공동대표주관회사" 및 "인수회사"의 본, 지점에서 교부 2) "공동대표주관회사" 및 "인수회사"의 홈페이지나 HTS, MTS 에서 교부 |
1) "공동대표주관회사" 및 "인수회사"의 본, 지점 2) "공동대표주관회사" 및 "인수회사"의 홈페이지 또는 HTS, MTS 교부 |
| ※ | 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다. |
나) 확인절차
(1) 우편을 통한 투자설명서 수령 시
(가) 청약하시기 위해 지점을 방문하셨을 경우, 직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
(나) HTS 또는 MTS를 통한 청약을 원하시는 경우, 청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
(다) 주주배정 유상증자 경우 유선청약이 가능합니다. 유선 상으로 신분확인을 하신 후, 투자설명서 교부 확인을 해주시고 청약을 진행하여 주시기 바랍니다.
(2) 지점 방문을 통한 투자설명서 수령 시
직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
(3) 홈페이지 또는 HTS, MTS를 통한 교부
청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
다) 기타
(1) 금번 유상증자에서 당사는 본 증권신고서의 효력발생 이후 주주명부상 주주분들에게 투자설명서를 우편으로 발송할 예정입니다. 우편의 반송 등에 의한 사유로 교부를 받지 못하신 투자자께서는 지점 방문을 통해 인쇄물을 받으실 수 있으며, 또한 동일한 내용의 투자설명서를 전자문서의 형태로 공동대표주관회사의 홈페이지에서 다운로드 받으실 수 있습니다. 한편, 일반공모 청약시 투자자께서는 공동대표주관회사 및 인수회사의 본ㆍ지점에 방문하여 투자설명서 인쇄물을 수령하시거나 공동대표주관회사 및 인수회사의 홈페이지에서 동일한 내용의 투자설명서를 전자문서의 형태로 다운로드 받으시는 2가지 방법으로 투자설명서를 교부받으실 수 있습니다. 다만, 전자문서의 형태로 교부 받으실 경우,「자본시장과 금융투자업에 관한 법률」제124조 제1항 각 호의 요건을 모두 충족해야만 청약이 가능합니다.
(2) 구주주 청약 시 공동대표주관회사인 삼성증권(주) 및 엔에이치투자증권(주) 이외의 증권회사를 이용한 청약 방법
- 해당 증권회사의 청약 방법 및 규정에 의해 청약을 진행하시기 바랍니다. 이 경우에도, 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
※ 투자설명서 교부를 받지 않거나, 수령거부의사를 서면 등의 방법으로 표시하지 않을 경우, 본 유상증자의 청약에 참여할 수 없습니다.
| ※ 관련법규 「자본시장과 금융투자업에 관한 법률」 제9조 (그 밖의 용어의 정의) ⑤ 이 법에서 "전문투자자"란 금융투자상품에 관한 전문성 구비 여부, 소유자산규모 등에 비추어 투자에 따른 위험감수능력이 있는 투자자로서 다음 각 호의 어느 하나에 해당하는 자를 말한다. 다만, 전문투자자 중 대통령령으로 정하는 자가 일반투자자와 같은 대우를 받겠다는 의사를 금융투자업자에게 서면으로 통지하는 경우 금융투자업자는 정당한 사유가 있는 경우를 제외하고는 이에 동의하여야 하며, 금융투자업자가 동의한 경우에는 해당 투자자는 일반투자자로 본다. <개정 2009.2.3> 1. 국가 2. 한국은행 3. 대통령령으로 정하는 금융기관 4. 주권상장법인. 다만, 금융투자업자와 장외파생상품 거래를 하는 경우에는 전문투자자와 같은 대우를 받겠다는 의사를 금융투자업자에게 서면으로 통지하는 경우에 한한다. 5. 그 밖에 대통령령으로 정하는 자 제124조 (정당한 투자설명서의 사용) ① 누구든지 증권신고의 효력이 발생한 증권을 취득하고자 하는 자(전문투자자, 그 밖에 대통령령으로 정하는 자를 제외한다)에게 제123조에 적합한 투자설명서(집합투자증권의 경우 투자자가 제123조에 따른 투자설명서의 교부를 별도로 요청하지 아니하는 경우에는 제2항제3호에 따른 간이투자설명서를 말한다. 이하 이 항 및 제132조에서 같다)를 미리 교부하지 아니하면 그 증권을 취득하게 하거나 매도하여서는 아니 된다. 이 경우 투자설명서가 제436조에 따른 전자문서의 방법에 따르는 때에는 다음 각 호의 요건을 모두 충족하는 때에 이를 교부한 것으로 본다.<개정 2013.5.28> 1. 전자문서에 의하여 투자설명서를 받는 것을 전자문서를 받을 자(이하 "전자문서수신자"라 한다)가 동의할 것 2. 전자문서수신자가 전자문서를 받을 전자전달매체의 종류와 장소를 지정할 것 3. 전자문서수신자가 그 전자문서를 받은 사실이 확인될 것 4. 전자문서의 내용이 서면에 의한 투자설명서의 내용과 동일할 것 「자본시장과 금융투자업에 관한 법률 시행령」 제11조(증권의 모집ㆍ매출) ① 법 제9조제7항 및 제9항에 따라 50인을 산출하는 경우에는 청약의 권유를 하는 날 이전 6개월 이내에 해당 증권과 같은 종류의 증권에 대하여 모집이나 매출에 의하지 아니하고 청약의 권유를 받은 자를 합산한다. 다만, 다음 각 호의 어느 하나에 해당하는 자는 합산 대상자에서 제외한다. <개정 2009. 10. 1., 2010. 12. 7., 2013. 6. 21., 2013. 8. 27., 2016. 6. 28., 2016. 7. 28.> 1. 다음 각 목의 어느 하나에 해당하는 전문가 가. 전문투자자 나. 삭제<2016. 6. 28.> 다. 「공인회계사법」에 따른 회계법인 라. 신용평가회사(법 제335조의3에 따라 신용평가업인가를 받은 자를 말한다. 이하 같다) 마. 발행인에게 회계, 자문 등의 용역을 제공하고 있는 공인회계사ㆍ감정인ㆍ변호사ㆍ변리사ㆍ세무사 등 공인된 자격증을 가지고 있는 자 바. 그 밖에 발행인의 재무상황이나 사업내용 등을 잘 알 수 있는 전문가로서 금융위원회가 정하여 고시하는 자 2. 다음 각 목의 어느 하나에 해당하는 연고자 가. 발행인의 최대주주[「금융회사의 지배구조에 관한 법률」 제2조제6호가목에 따른 최대주주를 말한다. 이 경 우 "금융회사"는 "법인"으로 보고, "발행주식(출자지분을 포함한다. 이하 같다)"은 "발행주식"으로 본다. 이하 같다]와 발행주식 총수의 100분의 5 이상을 소유한 주주 나. 발행인의 임원(「상법」 제401조의2제1항 각 호의 자를 포함한다. 이하 이 호에서 같다) 및 「근로복지기본 법」에 따른 우리사주조합원 다. 발행인의 계열회사와 그 임원 라. 발행인이 주권비상장법인(주권을 모집하거나 매출한 실적이 있는 법인은 제외한다)인 경우에는 그 주주 마. 외국 법령에 따라 설립된 외국 기업인 발행인이 종업원의 복지증진을 위한 주식매수제도 등에 따라 국내 계열 회사의 임직원에게 해당 외국 기업의 주식을 매각하는 경우에는 그 국내 계열회사의 임직원 바. 발행인이 설립 중인 회사인 경우에는 그 발기인 사. 그 밖에 발행인의 재무상황이나 사업내용 등을 잘 알 수 있는 연고자로서 금융위원회가 정하여 고시하는 자 제132조 (투자설명서의 교부가 면제되는 자) 법 제124조제1항 각 호 외의 부분 전단에서 "대통령령으로 정하는 자"란 다음 각 호의 어느 하나에 해당하는 자를 말한다. <개정 2009.7.1, 2013.6.21> 1. 제11조 제1항 제1호 다목부터 바목까지 및 같은 항 제2호 각 목의 어느 하나에 해당하는 자 1의2. 제11조제2항제2호 및 제3호에 해당하는 자 2. 투자설명서를 받기를 거부한다는 의사를 서면, 전화·전신·팩스, 전자우편 및 이와 비슷한 전자통신, 그 밖에 금융위원회가 정하여 고시하는 방법으로 표시한 자 3. 이미 취득한 것과 같은 집합투자증권을 계속하여 추가로 취득하려는 자. 다만, 해당 집합투자증권의 투자설명서의 내용이 직전에 교부한 투자설명서의 내용과 같은 경우만 해당한다. |
6) 주권유통에 관한 사항
주권유통개시(예정)일: 2025년 09월 04일(신주 상장예정)
(2019년 9월 16일 전자증권제도가 시행됨에 따라 실물 주권의 교부 없이 각 주주의 보유 증권계좌로 상장일에 주식이 등록발행되어 입고되며, 상장일부터 유통이 가능합니다. 단, 유관기관과의 업무 협의 과정에서 상기 일정은 변경될 수 있음을 유의하시기 바랍니다.)
7) 청약증거금의 대체 및 반환 등에 관한 사항
청약증거금은 청약금액의 100%로 하고, 주금납입기일에 주금납입금으로 대체하며, 청약증거금에 대해서는 무이자로 합니다. 일반공모 총 청약주식수(기관투자자 포함)가 일반공모주식수를 초과하여 청약증거금이 발생한 경우, 그 초과 청약증거금은 2025년 08월 25일부터 해당 청약사무 취급처에서 환불합니다.
8) 주금납입장소 : 신한은행 삼성역기업금융센터 지점
다. 신주인수권증서에 관한 사항
| 신주배정기준일 | 신주인수권증서의 매매 금융투자업자 | |
|---|---|---|
| 회사명 | 회사고유번호 | |
| 2025년 07월 11일 |
삼성증권(주) | 00104856 |
| 엔에이치투자증권(주) | 00120182 | |
1) 금번과 같이 주주배정방식의 유상증자를 실시할 때, 주주가 소유하고 있는 주식수 비율대로 신주를 인수할 권리인 신주인수권에 대하여 당사는 「자본시장과 금융투자업에 관한 법률」 제165의6조3항 및 「증권의 발행 및 공시 등에 관한 규정」 제5-19조에 의거하여 주주에게 신주인수권증서를 발행합니다.
2) 금번 유상증자시 신주인수권증서는 전자증권제도 시행일(2019년 9월 16일) 이후에 발행되고 상장될 예정으로 전자증권으로 발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여 배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다.
3) 신주인수권증서 매매의 중개를 할 증권회사는 공동대표주관회사인 삼성증권(주) 및 엔에이치투자증권(주)로 합니다.
4) 신주인수권증서 매매 등
신주인수권증서를 매매하고자 하는 주주는 신주인수권증서를 예탁하고 있는 증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자 계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약 기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
5) 신주인수권증서를 양수한 투자자의 청약방법
신주인수권증서를 증권회사에 예탁하고 있는 양수인은 당해 증권회사 점포 및 공동대표주관회사인 삼성증권(주) 및 엔에이치투자증권(주)의 본점 및 지점을 통해 해당 신주인수권증서에 기재되어 있는 수량(초과청약이 있는 경우 초과청약 가능수량이 합산된 수량)만큼 청약할 수 있으며, 청약 기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
6) 신주인수권증서의 상장
당사는 금번 주주배정후 실권주 일반공모 유상증자 관련 신주인수권증서의 상장을 한국거래소에 신청할 예정입니다. 동 신주인수권증서가 상장될 경우 상장기간은 2025년 07월 30일부터 2025년 08월 05일까지 5거래일간으로 예정하고 있으며, 동 기간 중 상장된 신주인수권증서를 한국거래소에서 매매할 수 있습니다. 동 신주인수권증서는 2025년 08월 06일에 상장폐지될 예정입니다. (「코스닥시장 상장규정」 제83조(신주인수권증권 및 신주인수권증서의 신규상장)에 따라 5거래일 이상 상장되어야 하며, 동 규정 제85조(신주인수권증권 및 신주인수권증서의 상장폐지)에 따라 주주청약 개시일 5거래일 전에 상장폐지되어야 함.)
7) 신주인수권증서의 거래 관련 추가사항
당사는 금번 유상증자의 신주인수권증서를 상장신청할 예정인 바, 현재까지 관계기관과의 협의를 통해 확인된 신주인수권증서 상장시의 제반 거래 관련 사항은 다음과 같습니다.
가) 상장방식 : 전자등록발행된 신주인수권증서 전부를 상장합니다.
나) 주주의 신주인수권증서 거래
| 구분 | 상장거래방식 | 계좌대체 거래방식 |
|---|---|---|
| 방법 | 주주의 신주인수권증서를 전자등록발행하여 상장합니다. 상장된 신주인수권증서를 장내거래를 통하여 매수하여 증권사 계좌에 보유한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. 주주의 신주인수권증서는 전자등록발행되므로 실물 증서는 발행되지 않습니다. | 신주인수권증서를 매매하고자 하는 실질주주는 위탁증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. |
| 기간 | 2025년 07월 30일부터 2025년 08월 05일까지(5거래일간) 거래 | 신주배정통지일(2025년 07월 23일(예정))부터 신주인수권증서의 상장거래 마지막 날 이후 제2영업일(2025년 08월 07일)까지 거래 |
| 주1) | 상장거래 : 2025년 07월 30일부터 2025년 08월 05일(5영업일간) 거래 가능합니다. |
| 주2 | 계좌대체거래 : 신주배정통지일인 2025년 07월 23일(예정)부터 2025년 08월 07일까지 거래 가능 합니다. → 신주인수권증서 상장거래의 결제일인 2025년 08월 07일까지 계좌대체(장외거래)가 가능하며, 동일 이후부터는 신주인수권증서의 청약권리 명세를 확정하므로 신주인수권증서의 계좌대체(장외거래)가 제한됩니다. |
| 주3) | 신주인수권증서는 전자등록발행되므로 실물은 발행되지 않습니다. |
다) 특별계좌 소유자(기존 '명부주주')의 신주인수권증서 거래
(1) '특별계좌 보유자(기존 '명부주주')'는 명의개서대행기관에 '특별계좌'에서 '일반전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후 금번 유상증자 청약 참여 또는 신주인수권증서의 매매가 가능합니다.
(2) '특별계좌 보유자(기존 '명부주주')'는 신주인수권증서의 '일반 전자등록계좌(증권회사 계좌)'로 이전 없이 공동대표주관회사의 본ㆍ지점에서 직접 청약하는 방법으로도 금번 유상증자에 청약이 가능합니다. 다만 신주인수권증서의 매매는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후에만 가능하므로 이 점 유의하시기 바랍니다.
라. 기타 모집 또는 매출에 관한 사항
1) 본 증권신고서는 공시심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요 내용의 변경시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있으므로 투자자 여러분께서는 투자시 이러한 점을 감안하시기 바랍니다.
2) 「자본시장과 금융투자업에 관한 법률」 제120조3항에 의거 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다.
3) 당사는 본 증권신고서를 통하여 청약 전에 투자자께서 숙지하셔야 하는 부분에 대하여 성실히 기재하고자 노력하고 있습니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 아래 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수 없으므로, 투자자는 본 증권신고서 제1부.III.투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안 되며, 투자자 자신의 독자적이고도 세밀한 판단에 의해야 합니다. 따라서 본 공시서류에 기재된 사항은 투자 판단 시 참고 자료로 활용하실 것을 권고 드리며, 투자자의 투자 판단에 대한 결과는 투자자 본인에게 귀속됩니다.
4) 금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서, 반기보고서, 분기보고서 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있사오니 투자의사를 결정하시는 데 참조하시기 바랍니다.
5) 본 증권신고서의 예정 모집가액은 확정되어 있는 것은 아니며, 청약일 3거래일 전에 확정 발행가액을 산정함으로써 확정될 예정입니다. 또한, 본 증권신고서의 발행예정금액은 추후 주당 발행가액이 확정되는 내용에 따라 변경될 수 있음을 유의하여 주시기 바랍니다.
5. 인수 등에 관한 사항
| [공모방법: 잔액인수] |
| 인수인 | 인수주식 종류 및 수 | 인수대가 | |
|---|---|---|---|
| 공동대표주관회사 | 삼성증권(주) | 인수주식의 종류: 기명식 보통주식 인수주식의 수: 최종 실권주 ×인수비율(50.00%) |
대표주관수수료 : 모집총액의 0.50% 中 62.5% 인수수수료: 모집총액의 1.30% 中 50.0% 실권수수료: 잔액인수금액의 15.0% |
| 공동대표주관회사 | 엔에이치투자증권(주) | 인수주식의 종류: 기명식 보통주식 인수주식의 수: 최종 실권주 ×인수비율(30.00%) |
대표주관수수료 : 모집총액의 0.50% 中 37.5% 인수수수료: 모집총액의 1.30% 中 30.0% 실권수수료: 잔액인수금액의 15.0% |
| 인수회사 | 한양증권(주) | 인수주식의 종류: 기명식 보통주식 인수주식의 수: 최종 실권주 ×인수비율(20.00%) |
인수수수료: 모집총액의 1.30% 中 20.0% 실권수수료: 잔액인수금액의 15.0% |
| 주1) 최종 실권주 : 구주주청약 및 일반공모 후 발생한 배정잔여주 또는 청약미달주식 주2) 모집총액 : 최종 발행가액 X 총 발행주식수 주3) 상기 일반공모를 거친 후에도 미청약된 잔여주식에 대하여는 공동대표주관회사 및 인수회사가 인수계약서 상 인수의무주식수를 한도로 하여 각각 인수의무주식수만큼 자기 책임 하에 인수하기로 합니다. 주4) 「증권 인수업무 등에 관한 규정」 제9조제2항제7호에 의거 고위험고수익투자신탁, 벤처기업투자신탁 및 일반청약자에 대하여 배정하여야 할 주식이 50,000주(액면가 500원 기준) 이하이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 이를 청약자에게 배정하지 아니하고 공동대표주관회사 및 인수회사가 자기 계산으로 인수할 수 있습니다. |
II. 증권의 주요 권리내용
당사가 금번 주주배정후 실권주 일반공모 유상증자를 통하여 발행할 증권은 기명식 보통주이며, 동 증권의 주요 권리내용은 다음과 같습니다.
1. 액면금액
| ※ 당사의 정관 (이하 동일) 제7조(1주의 금액) 주식 1주의 금액은 500원으로 한다. |
2. 주식에 관한 사항
|
제5조(발행예정주식총수) 회사가 발행할 주식의 총수는 100,000,000주로 한다.
제6조(설립시에 발행하는 주식의 총수) 회사가 설립시에 발행하는 주식의 총수는 20,000주(액면가 5,000원)로 한다.
제8조(주권의 발행과 종류) 삭 제
제8조2(주식등의 전자등록) 회사는 주식,사채 등의 전자등록에 관한 법률 제2조 제1호에 따른 주식등을 발행하는 경우에는 전자등록기관의 전자등록계좌부에 주식등을 전자등록하여야 한다. 다만, 회사가 법령에 따른 등록의무를 부담하지 않는 주식등의 경우에는 그러하지 아니할 수 있다.
제9조(주식의 종류) ① 회사가 발행할 주식은 보통주식과 종류주식으로 한다. ② 회사가 발행하는 종류주식은 이익배당 또는 잔여재산분배에 관한 우선주식, 의결권 배제 또는 제한에 관한 주식, 상환주식, 전환주식 및 이들의 전부 또는 일부를 혼합한 주식으로 한다. 제5조의 발행예정주식 중 종류주식의 발행한도는 발행주식총수의 1/4 범위 내로 한다. 제14조(명의개서대리인) ① 회사는 주식의 명의개서대리인을 둔다. ② 명의개서대리인 및 그 영업소와 대행업무의 범위는 이사회의 결의로 정한다. ③ 회사는 주주명부 또는 그 복본을 명의개서대리인의 사무취급장소에 비치하고, 주식의 전자등록, 주주명부의 관리, 기타 주식에 관한 사무는 명의개서대리인으로 하여금 취급케 한다. ④ 제3항의 사무취급에 관한 절차는 명의개서대리인의 증권명의개서대행업무 규정에 따른다.
제16조(주주명부의 폐쇄 및 기준일) ① 회사는 의결권을 행사하거나 배당을 받을 자 기타 주주 또는 질권자로서 권리를 행사할 자를 정하기 위하여 이사회 결의로 일정한 기간을 정하여 주주명부의 기재변경을 정지하거나 일정한 날에 주주명부에 기재된 주주 또는 질권자를 그 권리를 행사할 주주 또는 질권자로 볼 수 있다. ② 회사가 제1항의 기간 또는 날을 정하는 경우 3개월을 경과하지 아니하는 일정한 기간을 정하여 권리에 관한 주주명부의 기재변경을 정지하거나, 3개월 내로 정한 날에 주주명부에 기재되어 있는 주주를 그 권리를 행사할 주주로 할 수 있다. ③ 회사가 제1항의 기간 또는 날을 정한 때에는 그 기간 또는 날의 2주 전에 이를 공고하여야 한다. |
3. 신주인수권에 관한 사항
|
제10조(신주인수권) ① 당회사의 주주는 신주발행에 있어 그가 소유한 주식의 수에 비례하여 신주의 배정을 받을 권리를 갖는다. ② 회사는 제1항의 규정에도 불구하고 다음 각 호의 어느 하나에 해당하는 경우 이사회의 결의로 주주 외의 자에게 신주를 배정할 수 있다. 1. 발행주식총수의 100분의 50을 초과하지 않는 범위 내에서 자본시장과 금융투자업에 관한 법률 제165조의6에 따라 일반공모증자 방식으로 신주를 발행하는 경우 2. 상법 제542조의3에 따른 주식매수선택권의 행사로 인하여 신주를 발행하는 경우 3. 발행하는 주식총수의 100분의 20 범위 내에서 우리사주조합원에게 주식을 우선 배정하는 경우 4. 근로복지기본법 제39조의 규정에 의한 우리사주매수선택권의 행사로 인하여 신주를 발행하는 경우 5. 발행주식총수의 100분의 30을 초과하지 않는 범위 내에서 긴급한 자금조달을 위하여 국내외 금융기관 또는 기관투자자에게 신주를 발행하는 경우 6. 발행주식총수의 100분의 30을 초과하지 않는 범위 내에서 사업상 중요한 기술 도입, 연구개발, 생산·판매·자본제휴를 위하여 그 상대방에게 신주를 발행하는 경우 7. 주권을 코스닥시장에 상장하기 위하여 신주를 모집하거나 인수인에게 인수 하게 하는 경우 ③ 제2항 각 호 중 어느 하나의 규정에 의해 신주를 발행할 경우 발행할 주식의 종류와 수 및 발행가격 등은 이사회의 결의로 정한다. ④ 신주인수권의 포기 또는 상실에 따른 주식과 신주배정에서 발생한 단주에 대한 처리방법은 이사회의 결의로 정한다. |
4. 의결권에 관한 사항
|
28조(주주의 의결권) 주주의 의결권은 1주마다 1개로 한다.
제29조(상호주에 대한 의결권 제한) 회사, 회사와 회사의 자회사 또는 회사의 자회사가 다른 회사의 발행주식총수의 10분의 1을 초과하는 주식을 가지고 있는 경우, 그 다른 회사가 가지고 있는 이 회사의 주식은 의결권이 없다.
제30조(의결권의 불통일행사) ① 2 이상의 의결권을 가지고 있는 주주가 의결권의 불통일행사를 하고자 할 때에는 회일의 3일전에 회사에 대하여 서면 또는 전자문서로 그 뜻과 이유를 통지하여야 한다. ② 회사는 주주의 의결권의 불통일행사를 거부할 수 있다. 그러나 주주가 주식의 신탁을 인수하였거나 기타 타인을 위하여 주식을 가지고 있는 경우에는 그러 하지 아니하다.
제31조(의결권의 대리행사) ① 주주는 대리인으로 하여금 그 의결권을 행사하게 할 수 있다. ② 제1항의 대리인은 주주총회 개시 전에 그 대리권을 증명하는 서면(위임장)을 제출하여야 한다.
제32조(주주총회의 결의방법) 주주총회의 결의는 법령과 정관에 다른 정함이 있는 경우를 제외하고는 출석한 주주의 의결권의 과반수와 발행주식총수의 4분의 1 이상의 수로써 한다. |
5. 배당에 관한 사항
|
제12조(신주의 동등배당) ① 회사가 정한 배당기준일 전에 유상증자, 무상증자 및 주식배당에 의하여 발행한 주식에 대하여는 동등배당한다. ② 제1항의 규정에도 불구하고 배당기준일을 정하는 이사회 결의일로부터 그 배당기준일까지 발행한 신주에 대하여는 배당을 하지 아니한다. 제16조(주주명부의 폐쇄 및 기준일) ① 회사는 의결권을 행사하거나 배당을 받을 자 기타 주주 또는 질권자로서 권리를 행사할 자를 정하기 위하여 이사회 결의로 일정한 기간을 정하여 주주명부의 기재변경을 정지하거나 일정한 날에 주주명부에 기재된 주주 또는 질권자를 그 권리를 행사할 주주 또는 질권자로 볼 수 있다. ② 회사가 제1항의 기간 또는 날을 정하는 경우 3개월을 경과하지 아니하는 일정한 기간을 정하여 권리에 관한 주주명부의 기재변경을 정지하거나, 3개월 내로 정한 날에 주주명부에 기재되어 있는 주주를 그 권리를 행사할 주주로 할 수 있다. ③ 회사가 제1항의 기간 또는 날을 정한 때에는 그 기간 또는 날의 2주 전에 이를 공고하여야 한다. 제57조(이익배당) ① 이익배당은 금전 또는 금전 외의 재산으로 할 수 있다. ② 이익의 배당을 주식으로 하는 경우 회사가 종류주식을 발행한 때에는 주주총회의 결의로 그와 다른 종류의 주식으로도 할 수 있다. ③ 제1항의 배당은 이사회 결의로 정하는 배당기준일 현재의 주주명부에 기재된 주주 또는 등록된 질권자에게 지급한다. ④ 이익배당은 주주총회의 결의로 정한다. 다만, 제54조제6항에 따라 재무제표를 이사회가 승인하는 경우 이사회 결의로 이익배당을 정한다. ⑤ 제1항의 배당금은 지급개시일로부터 5년 이내에 지급청구를 하지 아니한 때에는 그 청구권을 포기한 것으로 간주하고 이는 회사에 귀속한다. |
III. 투자위험요소
| [ 주요 용어 설명 ] |
| 용어 | 설명 |
|---|---|
| live cell 제형 의약품 | 일반 제형, 라이브셀 제형 이라고 부르나 '냉장보관' 제형으로 봐야함 원료의약품 상태에서 동결 저장 하였다가 해동 및 세척을 거쳐서 완제의약품으로 제조 최종 제품 출하시 4°C 상태로 운송되는 제형으로 약 48시간 정도의 유효시간 |
| 동결 제형 | '동결보관' 제형 동결 보관된 완제의약품으로 최종 제품 출하시 동결(영하 70°C 이하)상태로 운송이 되며, 약 3~4년의 유효기간 |
| Vial(바이알) | 주사용 유리 용기 단위 주사용 약제를 넣을 수 있고 무균 상태로 만든 뒤 고무마개로 밀폐가 가능한 유리용기 |
| GMP | Good Manufaturing Practice' 의약품 제조 위한 품질관리의 전반적인 규범으로, 이러한 규범하에 관리되는 제조시설 |
| CDMO | 위탁생산(CMO·Contract Manufacturing Organization) +위탁개발(CDO·Contract Development Organization) |
| 배지 | 세포가 필요로 하는 영양물질을 넣은 증식 환경을 말하며, 기체상으로 얻어지는 것을 제외한 생존 및 발육에 불가결한 물을 비롯하여 영양물질로서 탄소원, 질소원, 발육인자 등을 공급해 줌. |
| 배양용기 | 세포를 배양하기 위해 배지를 넣는 용기로 크기와 소재가 다양하며 petri dish, flask, plate 등으로 구분되어 세포의 특성에 따라 사용함 |
| Flask(플래스크) | 세포배양 시 주로 사용되는 배양용기로, 밑이 넓고 작은 뚜껑이 있으며 크기에 따라 T25(25㎠), T75(75㎠), T175(175㎠) flask로 구분됨. |
| 다분화능 | 세포가 여러 종류의 세포로 분화하는 능력을 가지고 있는 것을 말함 |
| IRB | 임상시험심사위원회 (Institutional Review Board) |
| 크론성 누공 치료제 | 크론병으로 인한 누공에 대한 치료제 |
| 제대혈 | 분만 후 아기의 탯줄에서 나온 혈액인 탯줄혈액을 뜻하며, 조혈모세포와 간엽줄기세포가 풍부하게 들어 있어 의료적인 가치가 있음. |
| GLP | 비임상시험규정 (Good Laboratory Practice); 의약품, 화학품 등의 안전성 평가를 위하여 실시하는 각종 독성시험의 신뢰성을 보증하기 위하여 인구인력, 실험시설 및 장비 등 시험의 전과정에 관련된 모든 사항을 관리하는 규정임. |
| IND | 임상시험계획승인신청(Investigational New Drug Application): 인체를 대상으로 한 안전성·유효성자료 수집을 목적으로 해당 의약품을 사용하여 임상시험을 실시하고자 하는 자가 식품의약품안전처장의 승인을 신청하는 과정을 말함. |
| EASI | 습진중증도평가지수(Eczema Area and Severity Index): 아토피피부염의 중증도를 평가하는 지표 중 하나로 신체의 네 부위로 나누어 아토피 피부염 병변의 면적과 증상(홍반, 구진, 찰상, 태선화)에 대한 중증도를 측정하여 평가함 |
| DLT | 용량제한독성(Dose Limiting Toxicity): 약제 복용에 의해 나타나는 독성반응 중 관심을 가지고 용량을 조절해야하는 반응을 특정한 것 |
| MTD | 최대허용용량(Maximum Tolerated dose): 독성이 나타나지 않는 용량 범위 내에서의 최대복용량를 뜻하거나, 또는 독성반응이 나타나는 용량 범위 중에서의 최소복용량을 뜻함 |
| 100mmVAS | 일반적으로 길이 100mm의 수직 또는 수평의 직선을 이용하여 현재 환자가 느끼고 있는 통증의 정도를 직선의 길이를 측정하여 표현하는 방법으로, 숫자가 클수록 통증이 심하다는 것을 의미함. |
| IKDC | 국제 무릎기능활동성평가지수 (International Knee Documentation Committee): 무릎 통증, 기능성 및 활동성을 평가하는 지수로 점수가 높을수록 증상 개선을 의미함 |
| WOMAC | 골관절염 평가지수(Western Ontario and McMaster Universities Osteoarthritis Index): 관절염, 관절질환에 관한 설문 도구로 통증(5개의 항목), 뻣뻣함(2개의 항목), 신체적 기능(17개의 항목)을 평가하는 도구로 점수가 높을수록 통증, 뻣뻣함, 일상 활동 수행의 어려움이 많은 것을 의미함 |
| KOOS | 무릎 부상 및 골관절염 결과점수(Knee Injury and Osteoarthritis Outcome Score): 무릎 부상 및 골관절염 결과 점수로 무릎 관절의 통증, 증상, 일상생활, 스포츠 활동, 기능 및 삶의 질 등을 평가하며, 무릎 관절의 상태와 치료 효과를 판단하는데 사용됨 |
| JAK 억제제 | 야누스키나제(Janus Kinase) 억제제: 세포내에서 면역과 염증을 조절하는 JAK라는 효소의 활동을 억제하여 염증 반응을 줄이는 약물를 의미함 |
| TNF-α억제제 | 종양괴사인자(Tumor necrosis factor-α)억제제: 우리 몸에서 염증 반응을 일으키는 주요 물질 중 하나인 TNF-α의 작용을 막아 염증을 줄이는 약물을 의미함. |
| PCT | 특허협력조약(Patent Cooperation Treaty): 특허 및 실용신안에 관한 해외 출원절차의 통일화와 간소화를 위해 체결된 다자조약으로 PCT 규정에 따라 1회의 국제출원으로 출원인이 모든 PCT 체약국의 특허청에 직접 출원한 효과가 발생함. |
당사는 2010년 10월 설립되어 2015년 12월 코스닥시장에 상장된 법인으로, 줄기세포 치료제의 개발 및 제조 등을 주요 사업으로 영위하고 있습니다. 당사의 사업부문별 현황을 요약하면 아래와 같습니다.
| [당사 사업 분야] |
| 구 분 | 주요 사업 내용 |
|---|---|
| 줄기세포 사업 | 줄기세포 치료제 연구개발, 줄기세포 배양액 및 배양배지 공급 |
| 화장품 사업 | 줄기세포 배양액 화장품 제조, 판매 |
| 바이오파마 사업 | 일반의약품(OTC) |
| 비임상시험 사업 (주1) |
의약품, 화학물질, 작물보호제, 동물의약품 등의 효능 및 유해성 평가 |
| (주1) | 비임상시험 사업부는 HLB바이오코드(주)(구.(주)크로엔)의 지분 매각으로 연결에서 제외되었습니다. |
| [사업부문별 매출액(연결기준)] |
| (단위: 백만원) |
| 구 분 | 매출 유형 |
품 목 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | 설 명 | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 매출액 | 비 율 | 매출액 | 비 율 | 매출액 | 비 율 | 매출액 | 비 율 | ||||
| 줄기세포 사업부 | 제 품 | 줄기세포 배양액 | 183 | 19.2 | 430 | 5.6 | 1,023 | 8.1 | 370 | 2.3 | 화장품 원료 및 세포배양배지 |
| CDMO | 251 | 26.2 | 1,914 | 24.7 | 404 | 3.2 | 839 | 5.1 | 공정개발 및 위탁생산 | ||
| 상 품 | 해동기 | - | - | - | - | - | - | 128 | 0.8 | - | |
| 기 타 | 줄기세포 치료제 | - | - | - | - | - | - | - | - | 판권이전 기술료 | |
| 기타 | 30 | 3.1 | 2,042 | 26.4 | 17 | 0.1 | 5 | - | - | ||
| 화장품 사업부 | 제 품 | GD11 | 244 | 25.6 | 1,475 | 19.0 | 2,283 | 18.0 | 1,463 | 9.0 | 줄기세포배양액 화장품 |
| 상 품 | BIO-3 | 247 | 25.8 | 1,799 | 23.2 | 1,833 | 14.4 | 2,536 | 15.6 | 줄기세포배양액 기반 기능성 샴푸 | |
| 기타 | - | - | - | - | 2 | - | 11 | 0.1 | - | ||
| 바이오파마 사업부 | 상 품 | 일반의약품 | - | - | 86 | 1.1 | 347 | 2.7 | 548 | 3.4 | 일반의약품 |
| 기타 | 기타 | - | - | - | - | 4 | - | 14 | 0.1 | 용역, 교정 등 기타매출 | |
| 합 계 | 955 | 100.0 | 7,746 | 100.0 | 5,913 | 100.0 | 5,915 | 100.0 | |||
| 중단영업 (주1) | - | - | - | - | 6,791 | 114.8 | 10,386 | 175.6 | 비임상시험 사업부(주1) | ||
| (주1) | 비임상시험 사업부는 HLB바이오코드(주)(구.(주)크로엔)의 지분 매각으로 연결에서 제외되었습니다. |
[주요 파이프 라인]
당사는 자체 개발한 다분화능을 가진 줄기세포를 인간 제대혈로부터 고순도(high-purity)로 분리하고, 대량배양(massive culture)하는 기술을 기반으로 동종 제대혈유래 줄기세포치료제(의약품) 연구개발을 주요 사업으로 영위하고 있으며 파이프라인 현황은 다음과 같습니다.
| [당사 주요 파이프라인 임상 및 사업화 계획] |
| 구분 | 품목 | 적응증 | 연구 시작일 |
현재 진행단계 | 비고 | |
| 단계(국가) | 승인일 | |||||
| 바이오 신약 |
퓨어스템-에이디 주 | 아토피피부염 | 2011년 | 임상3상(한국) | 2017년 | 주1) |
| 임상1/2a상(한국) | 2019년 | 주2) | ||||
| 퓨어스템-알에이 주 | 류마티스관절염 | 2012년 | 임상2b상(한국) | 2023년 | 주3) | |
| 퓨어스템-시디 주 | 크론병 | 2012년 | 임상1/2a상(한국) | 2013년 | 주4) | |
| 판상형 건선 | 2013년 | 임상1상(한국) | 2014년 | 주5) | ||
| 퓨어스템-오에이 키트 주 | 골관절염 | 2015년 | 임상 1/2a상(한국) | 2022년 | 주6) | |
| 주1) | 2021년 05월 국내 두번째 3상 승인 완료되어 임상 진행하였으며, 2024년 11월 CSR 결과발표하였습니다. |
| 주2) | 반복투여 임상으로 2024년 11월 1/2a 임상시험 변경승인신청하였으며, 2025년 4월 자진취하 하였습니다. 2025년 4월 30일 식약처에 자료를 보완하여 변경승인신청 하였습니다. |
| 주3) | 2023년 9월 2b상 IND 승인을 받았으며, 임상 개시 시기는 2027년 하반기로 예상하고 있습니다. |
| 주4) | 2019년 5월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주5) | 2019년 1월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주6) | 2022년 11월 15일 식약처로부터 IND 승인받았으며, 2a 임상시험을 진행 중입니다. |
1. 사업위험
| 가. 국내외 거시경기 침체 및 불확실성이 미치는 위험 IMF는 세계경제의 리스크가 하방 요인에 집중되어있다 진단하면서, 무역갈등 등 정책 불확실성 확대에 따른 소비ㆍ투자 위축, 고금리 및 높은 부채수준으로 인한 재정ㆍ통화 정책 여력 부족, 주가 및 시장가격 재조정 가능성 등 금융ㆍ외환시장의 높은 변동성 등을 위험 요인으로 제시하였습니다. 또한, 한국은행은 국내 경제가 대내외 불확실성으로 경제심리 회복이 예상보다 지연되었고, 미국 관세 정책도 연초보다 강화되며 직전 예상 수치 대비 크게 하향 조정하였습니다. 당사가 영위하고 있는 사업은 국내외 거시경제의 직ㆍ간접적인 영향을 받고 있으며, 고금리, 고환율, 저성장 등에 따른 글로벌 경기침체로 인해 투자가 위축되거나 지연될 위험이 존재합니다. 당사는 2021년 6월부터 주요 파이프라인인 아토피 피부염 치료제(퓨어스템-에이디주)의 2차 임상 3상을 위해 환자 모집을 시작하였으나, 코로나19 확산에 따라 원활한 환자모집이 되지 않으면서 일정이 지연되었던 경험이 있습니다. 기존에 2022년 12월까지 예정되어있던 환자 모집기간을 연장하여 2023년 08월 최종인원 환자를 모두 모집할 수 있었으며, 이와 같은 일정 지연으로 인해 추가적인 임상비용 지출이 발생하였습니다. 이처럼 거시경제 불확실성은 국내외 경기 전반에 걸쳐 영향을 미칠 수 있으며, 당사가 영위하는 사업 및 실적에도 부정적인 요인으로 작용할 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
(1) 글로벌 경기 동향
국제통화기금(IMF)이 2025년 04월 22일 발표한 "World Economic Outlook"에서는, 최근의 높은 정책 불확실성을 감안하여, 기존의 단일 전망(baseline)대신, 전망 기준일에 따른 '기준 전망(reference forecast)'과 '보완 전망(alternatives)'을 함께 제시하였습니다. 해당 내용에 따르면 기준 전망에서 2025년 4월 4일 기준 반영 가능한 정보를 기반으로 국가별 성장률을 전망하되, 보완 전망을 통해 4월 2일 상호관세 부과 이전 및 4월 9일 상호관세 유예 및 미중 보복관세 이후 기준 전망으로 세계 성장률 범위를 추가로 제시하였습니다. 다만, 보완 전망은 지역, 국가별 전망에 대해서는 공개하지 않았습니다.
2025년 4월 4일을 기준점으로 한 기준전망에서 무역긴장 등 글로벌 불확실성을 반영하여 대부분 국가의 성장률 전망을 하향하면서 2025년 세계경제성장률을 2.8%로 전망하였습니다. 이는 2025년 01월 추정치 대비 0.5%p 하향 조정된 수치입니다. 한편, 4월 2일 상호관세 부과 이전 기준으로는, 미국의 2~3월 무역정책, 높은 유가 전망으로 중국 캐나다, 멕시코의 성장률이 대폭 둔화됨에 따라 세계경제성장률을 3.2%로 전망하였습니다. 4월 9일 이후 기준으로는 2025년 상호관세 90일 유예의 효과가 미국과 중국의 성장률 하락으로 상쇄되어 세계경제성장률 2.8%로 전망하였고, 2026년에는 미국과 중국의 손실이 다른 국가의 이득을 넘어섬에 따라 2.9%의 성장률을 전망하였습니다.
| [세계경제성장률 전망] |
| (단위 : %, %p.) |
| 구분 | 2025년 세계 경제 성장률 | 2026년 세계 경제 성장률 |
|---|---|---|
| 2025년 1월 전망 | 3.3% | 3.3% |
| 기준전망(4.4 기준) | 2.8%(-0.5%p.) | 3.0%(-0.3%p.) |
| 보완전망(4.2 이전 기준) | 3.2%(-0.1%p.) | 3.2%(-0.1%p.) |
| 보완전망(4.9 이후 기준) | 2.8%(-0.5%p.) | 2.9%(-0.4%p.) |
| 출처 : IMF World Economic Outlook(세계경제전망)(2025.04) 주) 기준전망 및 보완전망 괄호 내 수치는 2025년 1월 전망치 대비 변동 수치입니다. |
IMF가 전망한 한국의 2025년 경제성장률은 1.0%로 2025년 1월 대비 1.0%p 하향되었습니다. 선진국 그룹의 2025년 경제성장률 전망치는 1.4%로 하향 조정되었으며, 미국은 정책 불확실성, 무역 긴장, 소비 회복 지연을 이유로 성장률을 1.8%로 대폭 하락 조정했습니다. 대부분의 유럽국가와 일본도 하향 조정되었습니다. 신흥개도국 그룹(중국, 인도, 러시아, 브라질 등)의 2025년 경제성장률 전망치는 3.7%로 전망 되었습니다.
IMF는 세계경제의 리스크가 하방 요인에 집중되어있다 진단하면서, 무역갈등 등 정책 불확실성 확대에 따른 소비ㆍ투자 위축, 고금리 및 높은 부채수준으로 인한 재정ㆍ통화 정책 여력 부족, 주가 및 시장가격 재조정 가능성 등 금융ㆍ외환시장의 높은 변동성 등을 위험 요인으로 제시하였습니다.
IMF는 고조된 불확실성과 성장 둔화에 대응하기 위해 예측가능한 무역환경 조성을 위해 무분별한 산업 보조금 지양을 권고했습니다. 또한 지역, 다자간 무역협정 확대를 통한 무역 분절화 방지 노력의 필요성을 강조했습니다. 또한 금융시장 안정과 기대 인플레이션간 균형을 유지하는 신중한 통화정책과 건전한 재정운용의 필요성을 역설하고, 자본 변동성 확대에 대응하여 국가별 금융, 외환시장 성숙도에 맞는 적절합 개입 및 건전성 조치를 시행할 것을 권고했습니다. 그 밖에 중기 성장잠재력 회복을 위한 여성, 고령층 노동 참여 제고와 AI 디지털 기술 투자확대, 규제 정비 등의 노력도 촉구하였습니다. 2025년 4월 IMF의 세계 및 주요 경제 성장률 전망은 아래와 같습니다.
| [2025년 04월 국제통화기금 세계 경제성장률 전망] |
| (단위: %, %p) |
| 구분 | 2024년 | 2025년(E) | 2026년(E) | ||||
| 25년 01월 | 25년 04월 | 조정폭 | 25년 01월 | 25년 04월 | 조정폭 | ||
| (A) | (B) | (B-A) | (C) | (D) | (D-C) | ||
| 세 계 | 3.2 | 3.3 | 2.8 | -0.5 | 3.3 | 3.0 | -0.3 |
| 선진국 | 1.7 | 1.9 | 1.4 | -0.5 | 1.8 | 1.5 | -0.3 |
| 미국 | 2.8 | 2.7 | 1.8 | -0.9 | 2.1 | 1.7 | -0.4 |
| 유로존 | 0.8 | 1.0 | 0.8 | -0.2 | 1.4 | 1.2 | -0.2 |
| 독일 | -0.2 | 1.1 | 0.0 | -1.1 | 1.1 | 0.9 | -0.2 |
| 영국 | 0.9 | 1.6 | 1.1 | -0.5 | 1.5 | 1.4 | -0.1 |
| 일본 | -0.2 | 2.0 | 0.6 | -1.4 | 0.8 | 0.6 | -0.2 |
| 한국 | 2.2 | 2.0 | 1.0 | -1.0 | 2.1 | 1.4 | -0.7 |
| 신흥국 | 4.2 | 4.2 | 3.7 | -0.5 | 4.3 | 3.9 | -0.4 |
| 중국 | 4.8 | 4.6 | 4.0 | -0.6 | 4.5 | 4.0 | -0.5 |
| 인도 | 6.5 | 6.5 | 6.2 | -0.3 | 6.5 | 6.3 | -0.2 |
| 출처) | 국제통화기금(World Economic Oulook, 2025.04) |
(2) 국내 경기 동향
한국은행이 2025년 5월 발간한 '경제전망보고서'에 따르면 2024년 국내 경제성장률을 2.0% 기록하였습니다. 2025년 국내 경제성장률은 0.8%로 전망되었으며, 이는 직전('25년 2월) 전망치 대비 0.7%p 감소한 수치입니다. 한국은행은 국내 경제가 대내외 불확실성으로 경제심리 회복이 예상보다 지연되었고, 미국 관세 정책이 연초보다 강화되었다고 평가하며 국내 경제성장률을 크게 하향 조정하였습니다.
한국은행은 각 부문에 대해서 다음과 같이 전망하고 있습니다. 민간소비는 예상보다 부진이 길어졌으나 앞으로는 심리회복, 금융 여건 완화 등의 영향으로 점차 개선될 것으로 전망하였습니다. 건설투자는 상반기 큰 폭 부진 영향으로 금년중 감소폭이 크게 확대될 것으로 보고 있습니다. 설비투자의 경우 반도체 기업의 투자가 지속되겠으나 통상여건 악화로 비IT 부문 부진이 심화되며 당초 예상을 하회할 것으로 전망하였습니다. 지적재산생산물 투자는 주요 기업의 연구개발투자 지속과 정부의 예산 확대에 힘입어 성장세를 이어갈 전망입니다. 재화수출은 강화된 미국 관세정책의 영향으로 당초 예상에 못 미칠 것으로 전망됩니다.
| [한국은행 국내 경제전망] |
| (단위: %) |
| 구분 | 2024년 | 2025년(E) | 2026년(E) | ||||
|---|---|---|---|---|---|---|---|
| 연간 | 상반기 | 하반기 | 연간 | 상반기 | 하반기 | 연간 | |
| GDP | 2.0 | 0.1 | 1.4 | 0.8 | 2.0 | 1.3 | 1.6 |
| 민간소비 | 1.1 | 0.8 | 1.4 | 1.1 | 1.8 | 1.3 | 1.6 |
| 건설투자 | (3.0) | (11.3) | (1.1) | (6.1) | 4.9 | 0.9 | 2.8 |
| 설비투자 | 1.6 | 4.9 | (1.0) | 1.8 | 1.0 | 0.9 | 1.0 |
| 지적재산생산물투자 | 0.7 | 1.4 | 4.8 | 3.2 | 3.7 | 1.4 | 2.5 |
| 재화수출 | 6.3 | (0.1) | 0.0 | (0.1) | 0.6 | 0.8 | 0.7 |
| 재화수입 | 1.2 | 0.8 | (0.3) | 0.2 | 1.8 | 1.3 | 1.5 |
| 출처) | 한국은행 경제전망보고서(2025년 05월) |
상기 기재된 바와 같이 트럼프 행정부의 경제 정책 및 글로벌 무역갈등 등으로 국내외 거시경제는 불확실성이 증대된 상황입니다. 당사가 영위하고 있는 사업은 국내외 거시경제의 직ㆍ간접적인 영향을 받고 있으며, 고금리, 고환율, 저성장 등에 따른 글로벌 경기침체로 인해 투자가 위축되거나 지연될 위험이 존재합니다. 당사는 2021년 6월부터 주요 파이프라인인 아토피 피부염 치료제(퓨어스템-에이디주)의 2차 임상 3상을 위해 환자 모집을 시작하였으나, 코로나19 확산에 따라 원활한 환자모집이 되지 않으면서 일정이 지연되었던 경험이 있습니다. 기존에 2022년 12월까지 예정되어있던 환자 모집기간을 연장하여 2023년 08월 최종인원 환자를 모두 모집할 수 있었으며, 이와 같은 일정 지연으로 인해 추가적인 임상비용 지출이 발생하였습니다. 이처럼 거시경제 불확실성은 국내외 경기 전반에 걸쳐 영향을 미칠 수 있으며, 당사가 영위하는 사업 및 실적에도 부정적인 요인으로 작용할 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| 나. 임상시험의 지연 및 실패 위험 당사의 주요 파이프라인은 ① 아토피 피부염 치료제(Furestem-AD Inj.), ② 류마티스 관절염 치료제(Furestem-RA Inj.), ③ 골관절염 치료제(OSCA(구.Furestem-OA Kit Inj.))입니다. 한편, 2019년 10월 아토피 피부염 치료제(Furestem-AD Inj.)의 임상3상 통계분석 결과는 일차유효성 평가변수인 위약군 대비 통계적 유의성을 확보하지 못하며 입증에 실패했습니다. 이후 2020년 10월 국내 임상 3상을 다시 신청하였고, 2021년 5월 임상 3상 IND가 승인되었습니다. 다만, 코로나19 확산으로 병원 내원의 어려움 등 환자 모집이 지연됨에 따라 기존에 2022년 12월까지 예정되어있던 환자 모집기간을 연장하여 2023년 08월 최종인원 315명의 환자를 모두 투약하였습니다. 임상 결과, 1차 평가지표인12주차 시점 위약 대비 시험군과 대조군 간 유효성 차이를 입증하지 못하였으나 내부 시뮬레이션을 통해 16주차 이후에는 통계적 유의성 달성 가능성을 확인하였고 특정 연령대의 시험약군에서는 위약군 대비 통계적 유의성 달성을 확인하였습니다. 이에 기존 단회투여에서 반복투여 방식으로 프로토콜을 수정하여 2024년 11월 임상 1/2a상 IND를 변경 승인신청하였으나, 식품의약품안전처(MFDS)의 추가 자료보완 요청을 기한 내 회신이 어려울 것으로 판단하여 자진취하 신청을 하였습니다. 그리고 2025년 4월 퓨어스템-에이디주의 반복투여 제1/2a 임상시험계획변경승인신청을 하였으며, 2025년 하반기 임상1/2a상 개시를 계획하고 있습니다. 다만, 당사의 임상일정에 차질이 생길 수 있으며 임상에 맞는 환자들을 선별하는 과정에서 예상치 못한 난관들로 인해 환자모집이 장기화되어 임상 일정이 지연될 위험도 충분히 존재하며, 일정 연기 없이 임상을 진행하게 되더라도 임상 결과 유효성 지표 달성에 실패하여 최종적으로 임상이 실패할 위험이 있으며, 이로 인해 당사의 기업 가치가 크게 훼손될 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
당사의 줄기세포 사업은 자체 개발한 다분화능을 가진 줄기세포를 인간 제대혈로부터 고순도(high-purity)로 분리하고, 대량배양(massive culture)하는 기술을 기반으로 동종 제대혈유래 줄기세포치료제(의약품) 연구개발을 주요 사업으로 영위하고 있으며, 태아로부터 얻은 제대혈의 80% 이상에서 줄기세포 분리가 가능하고, 채취한 제대혈은 채취 후 최대 72시간까지 분리가 가능한 기술을 개발했습니다.
이를 바탕으로 ① 아토피 피부염 치료제(Furestem-AD Inj.), ② 류마티스 관절염 치료제(Furestem-RA Inj.), ③ 골관절염 치료제 OSCA(구. Furestem-OA Kit Inj.) 등의 주요 파이프라인을 구축했습니다. 각 파이프별 임상 단계 및 향후 계획은 아래와 같습니다.
 |
|
파이프라인별 임상 단계 |
| 출처) 당사 제시 |
① 아토피 피부염 치료제(Furestem-AD Inj.)
당사의 아토피 피부염 치료제(Furestem-AD Inj.)는 국소 및 전신 스테로이드제 등 기존 치료제에 효과를 보지 못한 중등도 이상의 만성 아토피피부염 환자를 대상으로 개발 중인 치료제입니다. 기존 의약품과 달리 아토피 피부염 유발에 관여하는 면역세포의 활성을 조절하여 증상을 개선하는데 초점을 두고 있습니다.
아토피 피부염 치료제(Furestem-AD Inj.)는 2013년 01월에 임상승인을 받은 이후 2013년 11월부터 2015년 05월까지 서울 성모병원에서 임상 1/2a까지 진행하였으며, 2017년 12월에 임상 3상 임상시험계획(IND) 승인을 받은 이후 2018년 04월에 첫 환자 등록/투여하였습니다. 이후 2019년 10월 임상 3상 통계분석 결과는 일차유효성 평가변수인 EASI-50(Baseline 대비 50%이상 감소한 환자의 비율) 평가에서 위약군(27.16%) 대비 시험약군(31.82%)이 약 4% 정도 유효성이 높은 것으로 나타났지만, EASI-50 달성율에서 통계적 유의성을 확보하지 못했습니다.
당사는 기존 3상 임상에서 통계적 유의성을 확보하지 못한 요인으로 1) 임상 결과에 영향을 미칠 수 있는 병용 약물에 대한 통제 미흡(알레르기성 반응에 관여하는 히스타민의 작용을 억제하는 항히스타민제를 사용한 환자와 사용하지 않은 환자 간의 통제)과 2) live cell 제형 의약품 제조 후 보관 시간(투약까지의 시간 지연 등으로 임상의약품의 약효 저하)에 따른 치료제의 효과를 충분히 고려하지 못하였으며, 3) 이전 임상시험은 당사가 실시한 최초의 줄기세포치료제 3상 임상시험으로써 대규모 임상시험에 관한 경험이 없었다는 점(임상1/2a상은 1개 기관에서 30명을 수행한 반면, 임상 3상은 11개 기관에서 197명 수행) 등이 있습니다.
다음은 3상 실패 이후 전반적인 임상 프로토콜의 재설계 내용입니다.
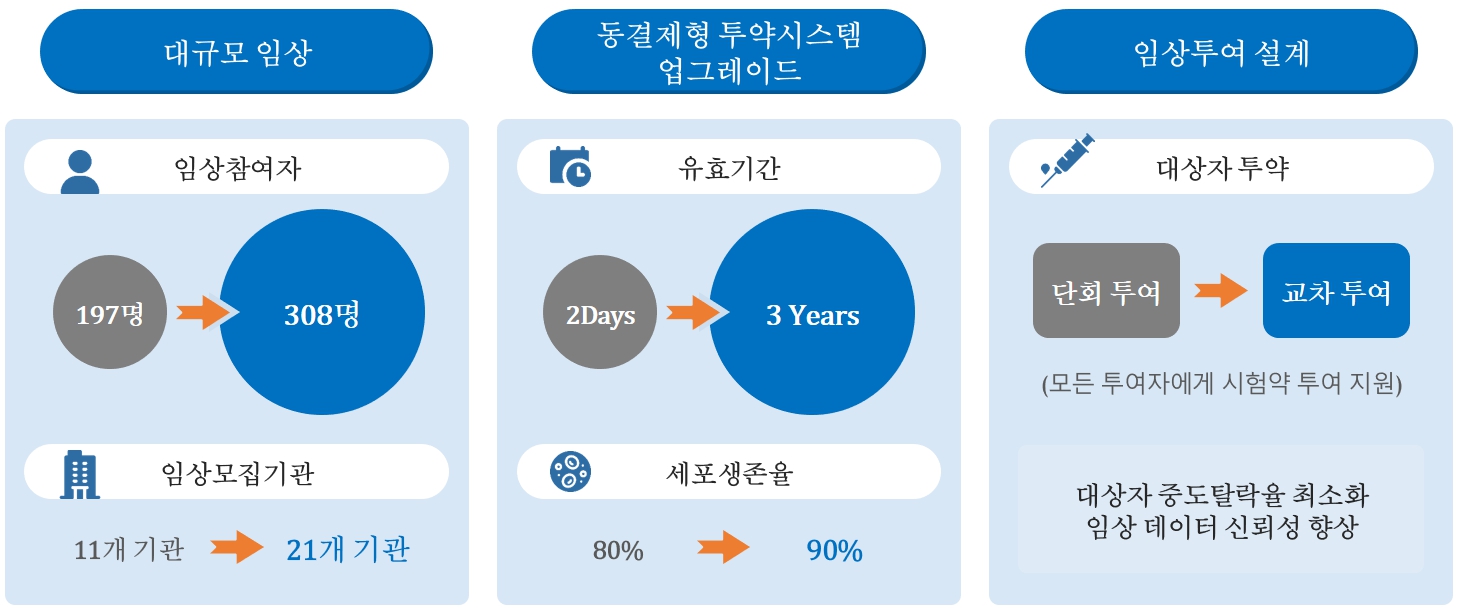 |
|
퓨어스템-AD주 임상 프로토콜 재설계 |
| 출처) 당사 제시 |
재설계된 주요 내용은 1) live cell 제형 의약품에서 동결(영하 70°C 이하) 제형 의약품으로 방식을 변경하였으며, 2) 기관수(11개 기관->21개 기관) 및 환자수 (197명 → 308명) 확대로 유효한 데이터군을 확보 및 마련하였으며, 3) 치료제의 효능을 저하시키는 면역억제 치료제인 '피메크로리무스' 약물을 금기 목록에 추가하였습니다.
당사는 2020년 10월 국내 임상 3상을 다시 신청하였고, 2021년 05월 임상 3상이 승인되었습니다. 다만, 코로나19 확산으로 병원 내원의 어려움 등 환자 모집이 지연됨에 따라 기존에 2022년 12월까지 예정되어있던 환자 모집기간을 연장하여 2023년 08월 최종인원 315명의 환자를 모두 투약하였습니다. 임상 결과, 1차 평가지표인 12주차 시점 EASI-50 평가에서 시험군과 위약 대조군 간 유효성 차이를 입증하지 못하였으나, 내부 시뮬레이션을 통해 16주차 이후에는 통계적 유의성 달성 가능성을 확인하였고 특정 연령대의 시험약군에서는 위약군 대비 통계적 유의성 달성을 확인하였습니다. 이에 기존 단회투여에서 반복투여 방식으로 프로토콜을 수정하여 2024년 11월 임상 1/2a상 IND를 변경승인신청하였으나, 식품의약품안전처(MFDS)의 추가 자료보완 요청을 기한 내 회신이 어려울 것으로 판단하여 자진취하 신청을 하였습니다. 그리고 2025년 4월 퓨어스템-에이디주의 반복투여 제1/2a 임상시험계획변경승인신청을 하였으며, 2025년 하반기 임상1/2a상 개시를 계획하고 있습니다.
다만, 당사의 임상일정에 차질이 생길 수 있으며 임상에 맞는 환자들을 선별하는 과정에서 예상치 못한 난관들로 인해 환자모집이 장기화되어 임상 일정이 지연될 위험도 충분히 존재하며, 일정 연기 없이 임상을 진행하게 되더라도 임상 결과 유효성 지표 달성에 실패하여 최종적으로 임상이 실패할 위험이 있으며, 이로 인해 당사의 기업 가치가 크게 훼손될 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
② 류마티스 관절염 치료제(Furestem-RA Inj.)
당사의 류마티스 관절염 치료제(Furestem-RA Inj.)는 중증도 이상의 류마티스 관절염 환자를 대상으로 개발 중인 치료제입니다. 다양한 면역조절인자가 분비되어 류마티스 관절염을 유발하는 대식세포의 활성을 억제하는 등의 효능을 가지고 있습니다.
류마티스 관절염 치료제(Furestem-RA Inj.)는 2014년 10월부터 2015년 10월까지 진행된 임상 1상(단회투여) 진행하였고, 그 이후 반복투여(4주간격 3회투여) 치료제로 2016년에 임상 1/2a 계획서를 제출했고 2018년 2월에 한국 식약처에서 승인되었습니다. 2018년 07월 1/2a상 임상 개시 이후, 2018년 12월 임상 1상이 완료되었으며, 2021년 10월에 1/2a상을 통해 안정성을 확인하였으며, 2023년 01월 임상 2b상 IND를 제출하였습니다. 2023년 09월 임상2b상 IND 승인을 받았으나, 당사 내부 파이프라인 우선순위에 따라 골관절염 치료제(OSCA) 임상과 아토피 피부염 치료제(퓨어스템-에이디주) 임상 시험에 우선적으로 예산을 사용하여, 류마티스 관절염 치료제의 2b 임상시험을 바로 개시하지 않고 보류 중입니다. 현재 류마티스 관절염 치료제(Furestem-RA Inj.)의 임상 2b상은 2027년 하반기 개시를 목표로 하고 있습니다. 다만, 우선순위로 집중하고 있는 OSCA와 퓨어스템-에이디주의 연구개발 일정이 지연되거나 성과가 좋지 않아 당사 수익성에 영향을 미칠 경우 수익화 달성에 따른 임상 진행 재원 마련 여부 등에 의해 류마티스 관절염 치료제(Furestem-RA Inj.)의 임상 2b상의 개시 일정이 추가 지연될 가능성이 존재하므로 투자자께서는 이 점 유의하시기 바랍니다.
 |
|
퓨어스템-RA 주: 2a상 임상결과 |
| 출처) 당사 제시 |
한편, 임상 2b상까지는 당사가 진행하며, 임상 3상부터는 대웅제약과 공동개발을 진행할 예정입니다. 해당 공동개발 계약서 상 임상 지연 및 실패에 따른 해지 조항은 별도로 없습니다. 다만, 임상 진행 과정에서 이견이 발생하여 양측 합의로 공동개발계약이 해지될 수 있으며, 이 경우 새로운 국내 임상 3상을 진행할 파트너를 찾는 과정에서 임상 시기가 지연될 수 있으며, 임상 3상을 진행하더라도 환자모집이 장기화되어 임상 3상 일정이 지연될 위험도 존재하니 투자자께서는 이 점 유의하시기 바랍니다.
③ 골관절염 치료제 OSCA (구. Furestem-OA Kit Inj.)
당사의 골관절염 치료제 OSCA (구. Furestem-OA Kit Inj.)는 골관절염의 증상개선이 아닌, 연골조직의 재생 및 연골하골의 구조개선을 통한 근본적인 치료제로 개발 중입니다. 제대혈 유래 중간엽 중기세포와 무세포성 연골기질을 함께 투여하며, 수술 없이 무릎관절강 내 주사를 1회 투약합니다.
골관절염 치료제 OSCA(구. Furestem-OA Kit Inj.)는 2015년 비임상 시험 개시 이후 2020년 비임상 시험으로 소형/대형 동물 대상 임상을 완료하였습니다. 이후 2022년 07월 한국 식약처에 임상 1/2a상 IND를 제출하였으며, 2022년 11월에 IND 승인이 완료되었습니다. 2023년 07월 초 국내 임상 1상 임상시험개시모임(임상시험에 필요한 전반적인 내용을 최종적으로 검토 및 확인하는 자리)을 완료하였으며, 2023년 08월 저용량, 10월 중용량, 2024년 02월 고용량 기준으로 환자에게 투여를 완료하였습니다. 2024년 08월 1/2a상 식약처 IND 변경승인 신청 후 10월에 승인 완료받았으며 2024년 12월 초 임상 1상 결과를 수령, 모든 투약군에서 유의미한 개선이 있었음을 발표하였습니다. 이후 2025년 3월 임상 2a상을 진행중입니다.
골관절염 치료제 OSCA(구. Furestem-OA Kit Inj.)는 개발 초기 비임상 연구 단계에서는 동물 모델을 활용해 연골 재생 및 관절 구조 개선 효과를 입증했으며, 항염증 및 재생 효과를 증명하고 안전성을 확보했습니다. 이후 임상 1상에서는 저용량, 중용량, 고용량으로 구분된 세 군을 대상으로 안전성, 내약성, 그리고 유효성을 평가했습니다. 중용량과 고용량에서 통증 및 관절 기능 개선과 구조적 개선에서 유의미한 효과가 관찰되었고, 주요 통계 지표들(IKDC, WOMAC, KOOS, VAS)에서도 긍정적인 결과가 나타났습니다.
 |
|
OSCA: 1상 임상결과 |
| 출처) 당사 제시 |
| 주) 2024년 11월 07일 국내 제약사 유영제약과 140억원 규모의 라이선스아웃 계약을 체결하였습니다. 다만, 임상시험, 허가, 규제 승인 미실현 등으로 본 라이선스아웃 계약은 중도에 해지될 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
임상 1상에서 확인된 안전성 및 유효성에 대한 전반적인 평가 결과를 바탕으로 중용량과 고용량을 임상 2a상의 시험군으로 선정하였으며, 대상자를 50명에서 108명으로 확대하여 위약 대비 시험약의 효과를 보다 정밀하게 평가할 계획입니다. 2025년 3월 임상시험을 시작해 2026년 2분기까지 완료를 목표로 하고 있으며, 성공 시 임상 2b 단계를 생략하고 임상 3상으로 직행할 가능성도 있을 것으로 예상됩니다.
다만, 당사의 임상일정에 차질이 생길 수 있으며 임상에 맞는 환자들을 선별하는 과정에서 예상치 못한 난관들로 인해 환자모집이 장기화되어 임상 일정이 지연될 가능성 존재 및 임상을 진행하더라도 임상이 실패할 위험이 존재하니 투자자께서는 이 점 유의하시기 바랍니다.
|
다. 연구개발의 지연 및 실패 위험 당사가 주요사업으로 영위하는 바이오신약개발 산업은 특허권에 의해 일정기간 동안 독점권으로 보호받게 되며 특허의 존속기간과 관계없이 신약의 경우 시장독점권을 보장받을 수 있습니다. 이처럼 특허권 및 독점판매권(시장독점권)을 통해 일정기간 수익을 보장받을 수 있기 때문에 글로벌 블록버스터급 신약 개발에 성공 시 막대한 수익을 창출할 수 있는 고부가가치 사업입니다. |
당사가 주요사업으로 영위하는 바이오신약개발 산업은 특허권에 의해 일정기간 동안 독점권으로 보호받게 되며 특허의 존속기간과 관계없이 신약의 경우, 미국은 시판 승인 후 7년, EU는 10년, 국내는 4년의 시장독점권을 보장받을 수 있습니다. 이처럼 특허권 및 독점판매권(시장독점권)을 통해 일정기간 수익을 보장받을 수 있기 때문에 글로벌 블록버스터급 신약 개발에 성공 시 막대한 수익을 창출할 수 있는 고부가가치 사업입니다. 따라서, 신약허가를 받기 위해서는 비임상 시험을 거쳐 임상시험에서 안정성과 유효성을 인정받아야하며, 이 과정을 수행함으로써 신약의 인체 위해성평가를 검증받아야합니다.
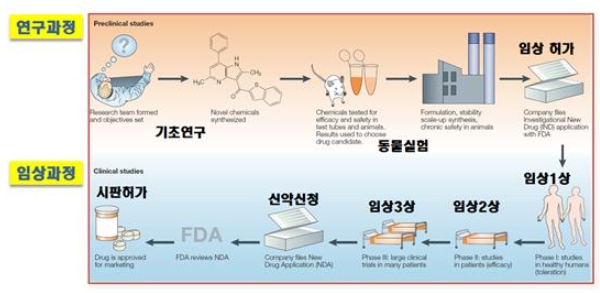 |
|
신약 허가를 받기 위한 개발 과정 |
| 출처) 당사 및 Nature Reviews Drug Discovery 제시 |
반면, 연구개발하고 있는 신약이 상업화되기까지 막대한 비용과 시간이 소요되며 특히, 임상시험 진입 시 최소 8~9년이 소요되며 그에 필요한 비용이 요구됩니다. 또한, 임상시험을 진행한다고 하더라도 시험결과 효능이 부족하거나 안전성 평가에 적합하지 못한 결과가 나올 경우 해당 신약의 연구개발은 중단될 수 있으며, 이러할 경우 당사의 비용 및 시간 투자에도 불구하고 엄청난 손실을 야기할 수밖에 없습니다.
당사가 보유하고 있는 파이프라인별 연구개발 진행 단계는 아래와 같습니다.
| [연구개발 진행 총괄표] |
| 구분 | 품목 | 적응증 | 연구 시작일 |
현재 진행단계 | 비고 | |
| 단계(국가) | 승인일 | |||||
| 바이오 신약 |
퓨어스템-에이디 주 | 아토피피부염 | 2011년 | 임상3상(한국) | 2017년 | 주1) |
| 임상1/2a상(한국) | 2019년 | 주2) | ||||
| 퓨어스템-알에이 주 | 류마티스관절염 | 2012년 | 임상2b상(한국) | 2023년 | 주3) | |
| 퓨어스템-시디 주 | 크론병 | 2012년 | 임상1/2a상(한국) | 2013년 | 주4) | |
| 판상형 건선 | 2013년 | 임상1상(한국) | 2014년 | 주5) | ||
| 퓨어스템-오에이 키트 주 | 골관절염 | 2015년 | 임상1/2a상(한국) | 2022년 | 주6) | |
| 주1) | 2021년 05월 국내 두번째 3상 승인 완료되어 임상 진행하였으며, 2024년 11월 CSR 결과발표하였습니다. |
| 주2) | 반복투여 임상으로 2024년 11월 1/2a 임상시험 변경승인 신청하였으며, 2025년 4월 자진취하 하였습니다. 2025년 4월 30일 식약처에 자료를 보완하여 변경승인 신청 하였습니다. |
| 주3) | 2023년 9월 2b상 IND 승인을 받았으며, 임상 개시 시기는 2027년 하반기로 예상하고 있습니다. |
| 주4) | 2019년 5월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주5) | 2019년 1월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주6) | 2022년 11월 15일 식약처로부터 IND 승인받았으며, 2a 임상시험을 진행 중입니다. |
당사의 최근 3개년 및 향후 연구개발 자금 계획표는 다음과 같습니다.
| [연구개발 자금 계획표(상세)] |
| (단위 : 백만원) |
| 구분 | 2022년 | 2023년 | 2024년 | 소계 | 2025년(E) | 2026년(E) | 2027년(E) | 2028년(E) | 소계 | 총계 | ||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 이월 | 55,955 | 36,036 | 36,974 | 19,059 | 49,867 | 79,159 | 60,643 | |||||
| 수입 | 7,010 | 26,911 | 9,673 | 43,595 | 58,356 | 58,903 | 13,535 | 112,857 | 243,651 | 287,246 | ||
| 자금조달 | - | 20,970 | - | 20,970 | 49,210 | - | - | - | 49,210 | 70,180 | ||
| 제품매출(배양액) | 247 | 912 | 333 | 1,492 | 783 | 1,018 | 1,323 | 1,720 | 4,843 | 6,335 | ||
| 제품매출(배지,해동기 등) | 256 | 132 | 97 | 485 | 111 | 145 | 188 | 245 | 689 | 1,174 | ||
| 제품매출(퓨어스템-에이디주) | - | - | - | - | 1,240 | 2,380 | 3,990 | 6,728 | 14,338 | 14,338 | ||
| 제품매출(OSCA) | - | - | - | - | - | 210 | - | 300 | 510 | 510 | ||
| 제품매출(CDMO) | 839 | 404 | 1,914 | 3,158 | 1,000 | 1,100 | 1,155 | 1,155 | 4,410 | 7,568 | ||
| 제품매출(화장품) | 1,463 | 2,283 | 1,475 | 5,220 | 1,032 | 1,135 | 1,249 | 1,374 | 4,791 | 10,011 | ||
| 상품매출(홈쇼핑) | 2,546 | 1,835 | 1,799 | 6,181 | 1,260 | 1,386 | 1,524 | 1,676 | 5,846 | 12,027 | ||
| 상품매출(의약품) | 563 | 347 | 86 | 996 | - | - | - | - | - | 996 | ||
| 기타매출(L/O 등) | - | - | 2,000 | 2,000 | - | 53,000 | 3,000 | 100,000 | 156,000 | 158,000 | ||
| 기타매출 | - | - | 42 | 42 | - | - | - | - | - | 42 | ||
| 기타 | - | - | - | - | 3,000 | - | - | - | 3,000 | 3,000 | ||
| 비현금비용보정 | 1,096 | 29 | 1,927 | 3,052 | 720 | -1,470 | 1,105 | -340 | 15 | 3,067 | ||
| 지출 | 26,929 | 25,973 | 27,588 | 80,491 | 27,548 | 29,611 | 32,051 | 32,836 | 122,046 | 202,537 | ||
| 원가비용 | 3,430 | 3,429 | 3,420 | 10,280 | 3,318 | 4,265 | 5,210 | 6,530 | 19,320 | 29,600 | ||
| 제품원가(배양액) | 145 | 550 | 158 | 853 | 470 | 611 | 794 | 1,032 | 2,906 | 3,759 | ||
| 제품원가(배지,해동기 등) | 151 | 70 | 58 | 279 | 67 | 87 | 113 | 147 | 413 | 692 | ||
| 제품원가(OSCA/퓨어스템-에이디주) | - | - | - | - | 620 | 1,190 | 1,796 | 2,691 | 6,297 | 6,297 | ||
| 제품원가(CDMO) | 769 | 527 | 1,317 | 2,613 | 900 | 990 | 982 | 982 | 3,854 | 6,467 | ||
| 제품원가(화장품) | 1,080 | 1,341 | 1,076 | 3,496 | 568 | 625 | 687 | 756 | 2,635 | 6,131 | ||
| 상품원가(홈쇼핑) | 779 | 637 | 734 | 2,150 | 693 | 762 | 838 | 922 | 3,215 | 5,365 | ||
| 상품원가(의약품) | 506 | 305 | 77 | 888 | - | - | - | - | - | 888 | ||
| 연구개발비용 주1) |
14,241 | 14,365 | 12,562 | 41,167 | 9,667 | 14,123 | 11,781 | 8,819 | 44,389 | 85,556 | ||
| 퓨어스템-에이디주 (반복투여) 주2) |
1,157 | 833 | 604 | 2,594 | 2 | - | - | - | 2 | 2,596 | ||
| 퓨어스템-에이디주 (단회투여) 주3) | 4,692 | 5,707 | 5,446 | 15,845 | 2,608 | - | - | - | 2,608 | 18,453 | ||
| 퓨어스템-에이디주 (단회투여-장기추적) | 462 | 450 | 715 | 1,627 | 871 | 1,353 | 1,155 | 938 | 4,312 | 5,945 | ||
| 퓨어스템-알에이주 | 1,951 | 1,988 | 45 | 3,984 | 3 | 2,040 | 2,040 | 2,472 | 6,555 | 10,539 | ||
| 퓨어스템-시디주 | 142 | - | - | 142 | - | - | - | - | - | 142 | ||
| OSCA | 2,039 | 4,211 | 2,795 | 9,045 | 4,583 | 9,629 | 6,906 | 3,549 | 24,667 | 33,712 | ||
| DDS | - | - | - | - | - | - | - | - | - | - | ||
| 국책과제 | 527 | 397 | 266 | 1,191 | 600 | 600 | 600 | 600 | 2,400 | 3,591 | ||
| 기타연구비 | 3,271 | 779 | 2,690 | 6,739 | 1,000 | 500 | 1,080 | 1,260 | 3,840 | 10,579 | ||
| 기타 | 400 | 400 | 5,400 | 6,200 | 1,425 | 400 | 400 | 400 | 2,625 | 8,825 | ||
| 판매비와관리비(일반) | 8,858 | 7,779 | 6,206 | 22,844 | 13,139 | 10,824 | 14,661 | 17,088 | 55,718 | 78,556 | ||
| 법인세 | - | - | - | - | - | - | - | - | - | - | ||
| 잔액 | 36,036 | 36,974 | 19,059 | 49,867 | 79,159 | 60,643 | 140,664 | |||||
| 출처) 당사 제시 |
| 주1) 해당 예상 연구개발비용 항목은 각 파이프라인 별 발생 예상되는 전체 비용 중 당사가 지출 예상되는 비용을 기준으로 작성되었습니다. 직접비용과 간접비용을 모두 포함한 기준으로 작성되었습니다. 주2) 퓨어스템-에이디주 반복투여 방식의 임상시험 비용은 컨소시엄 등 임상 프로젝트 그룹 구성을 통해 해당 외부 자금으로 처리할 예정으로 이를 가정하여 해당 비용에 반영되어있지 않습니다. 주3) 퓨어스템-에이디주 단회투여 방식의 3상 임상비용 잔금, 3상 위약군 연장 연구 관련 직접비용과 이에 따른 간접비용이 포함되어 있습니다. |
상기 연구개발 자금계획표에 기재한 예상 수입 중 '기타매출(L/O 등)'의 경우 OSCA의 임상 2a상이 완료된 후 글로벌 라이선스 아웃 성공 가정 시의 예상 매출 금액과 유영제약과의 기술이전 계약 마일스톤에 따른 예상 수취 금액으로 작성되었습니다. 당사는 OSCA 글로벌 라이선스 아웃을 다수의 고객사와 대륙 단위(혹은 특정 지역 단위)로 진행할 계획입니다. 이에 2026년과 2028년 라이선스 아웃 예상 매출 금액은 무릎골관절염치료제 OSCA의 유럽지역, 미주지역, 아시아 지역별 라이선스 아웃 계약 체결을 가정한 것으로 통상적인 무릎치환술 가격을 기준으로 예상 시장점유율을 고려하여 산정하였습니다. 2026년은 유럽지역 소재 고객사로의 라이선스 아웃 가정으로 총 라이선스 아웃의 10% 해당 계약금 수취에 따른 매출을 가정하였고, 2028년에는 미주지역과 아시아지역 고객사로의 라이선스 아웃에 따른 10% 해당 계약금 수취에 따른 매출을 가정하였습니다. 당사가 현재까지 기술이전 계약 관련하여 논의한 바 있는 글로벌 고객사의 관심 수준, 논의 수준 등을 고려하여 유럽지역, 미주지역, 아시아 지역 순으로의 라이선스 아웃을 가정하였으나, 현재 구체적인 계약 조건이나 상대방이 확정된 것은 아니므로, 기술이전의 성공 여부, 시기, 금액 등은 불확실할 수 있다는 점을 유의해주시기 바랍니다. 한편, 유영제약과의 OCSA 국내 기술이전 계약 상 마일스톤 달성을 가정하여 마일스톤에 따른 2026년 30억원(경상기술료 2차), 2027년 30억원(경상기술료 3차)을 포함하였습니다.
예상 수입 중 '제품매출(OSCA)'은 국내 기술이전 계약에 따라 유영제약에서 임상 2b상~3상 진행 시 IP공급에 따른 예상 매출을 반영하였으며, '제품매출(퓨어스템-에이디주)'은 국내외 재생의료 사업 관련 매출로, 일본 재생의료 자가줄기세포 공급에 따른 예상 매출 또한 포함하고 있습니다. 국내 첨생법 매출의 경우 임상연구 시작 후 2년의 임상연구 기관이 필요한 관계로 매출 상승폭이 크지 않으나 일본 재생의료의 경우 2025년 하반기부터 현지 환자 투여를 목표로 하고 있으며, 환자 모집에 따라 매출 변화가 클 것으로 예상되는 바, 적극적인 모객 활동으로 매출이 빠르게 증가하는 것으로 가정하였습니다. 그 외 '배양액 및 배지 등 매출'은 줄기세포 사업 본격화에 따라 매년 일정 비율만큼의 상승을 가정하였으며, 'CDMO, 화장품, 홈쇼핑 매출'은 타사와의 서비스 경쟁을 고려하여 상대적으로 낮은 폭의 상승을 가정하였습니다. 한편, 각 제품매출 및 상품매출을 위해 예상되는 원가 비용을 각 제품원가비용과 상품원가비용으로 기재하였습니다.
예상 비용 중 '연구개발비용'의 경우 각 파이프라인의 연구개발을 위해 각 임상 단계별 발생 예상되는 전체 비용 중 실제 당사가 지출 예상되는 비용을 기준으로 연도별 작성되었으며, 직접 비용과 간접 비용을 모두 포함하여 작성되었습니다. 최초 증권신고서 공시 시에는 각 임상 단계별 임상과 관련된 직접비용만 '연구개발비용'으로 분류하고, 간접비용은 '판매비와관리비(일반)'로 구분하여 기재하였으나, 금번 공시 시에는 각 '연구개발비용' 항목에 각 임상연구와 관련된 직접비용과 간접비용을 모두 포함하는 기준으로 통일하여 기재하였습니다. 한편, 각 임상 시험 단계별 필요 예상되는 간접 비용은 주로 임상 진행에 따른 당사의 연구소, GMP 인원의 인건비입니다. 퓨어스템-에이디주는 단회투여 방식과 반복투여 방식을 구분하여 세분화하였습니다. 퓨어스템-에이디주의 연구개발비용에는 단회투여 방식의 비용에는 단회투여 3상 임상비용 잔금 등과 장기추적에 필요한 비용이 반영되었으며, 반복투여 방식의 임상시험 비용은 컨소시엄 등 임상 프로젝트 그룹 구성을 통해 해당 외부 자금으로 처리할 예정으로 이를 가정하여 해당 비용에 반영되어 있지 않습니다. 퓨어스템-알에이주의 연구개발비용에는 향후 국내 임상과 장기추적조사에 필요한 비용을 포함하였으며, OSCA는 국내임상, 장기추적조사 및 해외임상에 필요한 비용까지 모두 포함하여 산정하였습니다.
당사는 해당 연구개발 자금 계획표 산정 시 논의 중인 글로벌 파트너사의 관심도와 가능성 예상치, 예상 매출 상승률과 원가 비용, 임상 필요 예상 비용 등을 종합적으로 고려하여 합리적이고 신뢰성 있게 산출하고자 노력하였습니다. 또한, 당사는 이 추정치에 근거하여 내부전략 및 연구개발전략을 수립하고 있습니다. 다만, 최대한 합리적이고 신뢰성 있는 추정치 산출을 위한 당사의 노력에도 불구하고, 미래의 정확한 수치를 예측하는 것에는 한계가 있을 수 있습니다. 또한, 임상 일정이 지연되거나, 임상을 진행하더라도 임상이 실패할 경우, 또는 예상보다 매출 상승률이 낮거나 비용이 늘어나는 경우 당사의 매출액 및 수익성에 부정적인 영향이 미칠 수 있으며, 이에 따라 당사가 현재 추정하고 있는 연구개발 자금계획이 향후 변동될 가능성이 있으니 투자자께서는 이 점 유의하시기 바랍니다.
당사 주요 파이프라인의 임상개요 및 임상 목표 및 결과 현황은 다음과 같습니다.
| 구분 | 임상개요 | 임상 목표 | 결과 현황 |
|---|---|---|---|
| 퓨어스템-AD주(반복투여) -아토피 피부염 치료제 |
중등도 이상의 성인아토피 피부염 환자에서 1개월 간격 3회 피하 반복투여 시 저용량(5x10^7cell)과 고용량(1x10^8cell)에 대한 안전성 및 탐색적 유효성 평가를 위한 1/2a 임상시험 | (1상) 3회 반복투여 시 투여용량군에 대한 안전성확립(DLT 및 MTD)과 EASI50/75와 같은 변수를 이용하여 탐색적 유효성 평가 (2a상) 단회투여 3상 임상시험결과를 반영한 수정 임상시험계획서를 바탕으로 16주-24주 시점에 시판중인 항체치료제와 대등한 유효성(EASI75 및 IGA 1 또는 0 비율)을 보여줄 수 있는지를 위약군과 비교하여 반복투여에 따른 유효성의 효과크기를 확인 |
(1상/완료) 투여된 두 용량 모두에서 DLT 및 MTD 평가에서 뛰어난 안전성 확인. 탐색적 유효성 평가에서는 업그레이드된 임상시험용의약품이 적용된 고용량군 대상자들 모두 50%-80% EASI 변화율이 확인되어 단회투여에 비교할 때, 보다 빠른 시기에 효과가 나타날 수 있는 가능성 확인 (2a상/임상시험계획 변경승인신청) 단회 3상 임상결과에 대한 심층분석결과를 바탕으로 2a 임상시험계획서 변경신청서를 11월 제출하였고, 식약처 자료 보완 요청에 대해 행정처리기간내 회신이 어려울 것으로 보여 2025년 4월에 신청을 자진 취하하였고 2025년 4월 30일에 재신청함 |
| 퓨어스템-RA주 -류마티스관절염 치료제 |
기존의 DMARD제제에 불응인 중등도 이상의 류마티스 관절염 환자에서 1개월 간격으로 시험약(5x10^7cell) 3회 투여 시 위약대비 안전성 검토 및 유효성 평가를 위한 2b 임상시험 | (2b상) 이전 2a 임상시험에서 1개월 간격으로 3회 정맥내 투여할 때 저용량(5x10^7 cells)의 유효성이 확인되었으며, 보다 큰 규모의 모집단에서 위약대비 효과의 크기를 측정하고자 함 |
(2a상/완료) 임상시험을 통해 저용량-고용량 모두 6개월 관찰에서 안전성 확보하였고, 유효성 측면에서 저용량군이 더 뛰어난 결과를 보여 이를 바탕으로 2b 임상시험계획서를 준비하고 진행하였음 (2b상/보류) 2023년 9월 2b상 임상시험계획 승인되었지만, 우선순위 프로젝트인 OSCA 임상과 아토피 임상시험에 예산을 우선 투여하여 2b 임상시험의 개시를 보류 중. 바로는 개시 계획이 없으며 재정상황을 고려하면서 차후 2b 임상시험의 재개 시기를 결정하고 진행 예정임 |
| OSCA (구. 퓨어스템 OA주) -골관절염 치료제 -주력 파이프라인 |
중등도 무릎골관절염 환자(Kellgren & Lawrence grade 2-3)에서 안전성 및 탐색적 유효성을 평가하기 위한 1/2a 임상시험 | (1상) 무릎관절낭내로 3가지 용량(저/중/고) 단회투여 후 안전성 확인 (DLT & MTD), 투약 후 6개월 시점에서 통증과 관절기능, 구조적 개선에 대한 탐색적 유효성을 평가 (2a상) 무릎관절낭내로 단회투여 후 1상에서 안전성과 탐색적 유효성이 확인된 중용량/고용량을 위약 대비 6개월 시점에서 통증과 관절기능, 구조개선에 대해 시험약의 유효성의 크기를 측정하고자 함 |
(1상/완료) 투약된 세 용량 모두에서 독성이 확인되지 않아 안전성이 확립되었음. 탐색적 유효성의 경우, 중용량과 고용량에서 통증조절과 기능개선이 빠르게 나타났으며(100mmVAS, IKDC, WOMAC, KOOS), MRI를 이용한 구조적 개선평가에서도 의미있는 개선이 확인되었음 : 연골재생, 연골하골 구조개선 등 (1상 장기추적조사/진행 중) 12개월 통증 및 관절기능에 대해 저용량 및 중용량 데이터 확보하였고, 6개월 시점대비 저용량의 증상과 영상의학적 평가결과 눈에 띄는 개선이 확인되었으며, 중용량군의 경우 6개월에서 보여준 증상개선이 유지 및 추가개선이 확인되었음. 중·고용량군의 12개월 영상평가결과, 다수의 중·고용량군 환자들에게서 연골재생과 손상된 연골하골의 회복이 지속된 것으로 확인됨. 고용량군은 장기추적조사에 참여한 환자 모두 연골의 마모, 이상구조, 부종, 활막염, 반월판 손상 등 전반적인 부분에서 개선이 나타남 (2상/진행 중) 2025년 3월 25일 분당차병원을 시작으로 중용량에 대해 첫환자 투약 개시함 |
| 출처) 당사 제시 |
당사 주요 파이프라인의 ① 개발 단계별 주요 목표 및 예상 달성 시기, ② 개발 단계별 예상 비용, ③ 연구개발 자금계획은 다음과 같습니다.
① 개발 단계별 주요 목표 및 예상 달성 시기
| 구분 | 1상 | 2a상 | 2b상 | 3상 | 장기 추적 |
|---|---|---|---|---|---|
| 퓨어스템-에이디주(반복투여) | 2022년 06월 | 2027년 02월 | 2028년 10월 | 2030년 02월 | 2035년 02월 |
| 퓨어스템-에이디주(단회투여-3상 장기추적조사) | - | - | - | - | 2028년 08월 |
| 퓨어스템-알에이주 | 2015년 10월 | 2021년 10월 | 2028년 12월 | 2030년 12월 | 2035년 12월 |
| OSCA | 2024년 08월 | 2026년 04월 | 2028년 12월 | 2030년 10월 | 2034년 09월 |
| 출처) 당사 제시 |
| 주1) 해당 예상 달성 시기는 LPO(마지막 환자 방문 완료)시점으로 기재되어 있습니다. |
상기 각 임상 단계별 예상 달성 시기는 LPO(마지막 환자 방문 완료)시점으로 기재되어 있습니다. 통상적으로 임상 시험의 Top-line 데이터 확보는 LPO 시점으로부터 약 3개월 소요, 임상시험 결과보고서(CSR) 수령은 Top-line 데이터 확보로부터 약 3개월 소요됩니다. 다만, 후속 결과 분석, 범위 등에 따라 추가적인 시간이 소요될 수 있습니다.
한편, 당사는 2024년 12월 공시한 합병신고서 당시 예상했던 OSCA의 임상시험 달성 시점이 예상보다 일부 지연되었습니다. 당시 OSCA의 개발 단계별 목표 및 예상 달성 시기가 2a상의 경우 2026년 03월, 2b상은 2028년 03월, 3상은 2029년 09월이었습니다. 그러나 OSCA의 임상 2a상 개시 이후 2a상의 환자 모집 및 투약 개시의 실제 속도에 따라 2a상의 LPO 시점을 최신화하였으며, 이에 임상 2a상 예상 달성 시점이 당시 계획했던 일정과 한 달 차이가 발생하게 되었습니다. 또한, 2024년 12월 공시 시점에는 임상 2b상과 3상에 대해 투약 후 6개월 관찰을 가정하였으나, 이후 내부 논의에 따라 임상 2b상과 3상의 관찰기간을 6개월에서 12개월로 변경 가정하여 이를 반영하였습니다. 이에 따라 임상 2b상 예상시점이 약 6개월 연기되었으며, 2a상과 2b상 예상 시점 연기에 따라 임상 3상의 예상시점도 약 1년 연기되었습니다. 장기추적조사의 경우 5년 진행 예정으로 2034년 9월로 변동없습니다. 또한, 퓨어스템-에이디주와 퓨어스템-알에이주의 경우 2024년 12월 공시한 합병신고서 당시 예상과 금번 예상 달성 시기 간에 변동 사항 없습니다.
당사는 금번 계획한 상기 단계별 목표 및 예상 달성 시기에 맞춰 신약 개발을 위해 노력하고 있으나, 해당 예상 달성 시기는 당사 내부의 파이프라인 우선순위 조정 등에 따라 향후에도 지연될 가능성을 배제할 수 없습니다. 당사는 현실적 여건상 한정된 자원을 가능성이 높은 파이프라인에 우선적으로 집중할 수 밖에 없어 금번 조달된 자금은 OSCA 임상을 위해 사용되며, 우선적으로는 OSCA의 국내 및 해외 임상에 집중할 계획입니다. 퓨어스템-에이디주의 경우 파트너사를 찾아 컨소시엄을 구성하여 임상 비용을 부담할 계획이며, 현재 2025년 하반기 임상 1/2a상 개시를 계획하고 있으나, 임상시험 계획변경 승인 시기가 지연되거나, 컨소시엄 등 결성 시기 지연 시 임상1/2a상 개시 일정도 지연될 수 있습니다. 이후 OSCA의 해외 라이선스 아웃, 국내외 첨단재생의료 진출, 오가노이드 기술 등을 통한 자체적인 재원 확보 등이 성공적으로 이루어질 경우 해당 재원을 기반으로 퓨어스템-에이디주, 퓨어스템-알에이주의 임상 시험을 순차적으로 개시할 예정입니다. 이에 특히 퓨어스템-알에이주의 경우 임상 2b상을 2027년 하반기 개시 후 마지막 환자 방문 완료 시점은 2028년 12월로 현재 목표하고 있으나, 수익화 달성에 따른 임상 진행 재원 마련 여부 등에 의해 추가 지연될 가능성이 존재하므로 이점 투자자께서는 유의하시기 바랍니다.
② 개발 단계별 예상 비용
| 구분 | 1상 | 2a상 | 2b상 | 3상 |
|---|---|---|---|---|
| 퓨어스템-에이디주(반복투여) | - | 80억원 (장기추적 포함) |
86억원 (장기추적 포함) |
175억원 (장기추적 포함) |
| 퓨어스템-에이디주(단회투여-3상 장기추적조사) | - | - | - |
54억원 (장기추적 조사) |
| 퓨어스템-알에이주 | - | - | 84억원 (장기추적 포함) |
249억원 (장기추적 포함) |
| OSCA | 4억원(장기추적) | 239억원 (장기추적 포함, 해외임상IND 포함) |
131억원 (장기추적포함) |
239억원 (장기추적 포함) |
| 출처) 당사 제시 |
| 주1) 해당 예상 비용은 각 파이프라인의 각 개발 단계별 발생 예상되는 전체 비용 기준으로 작성되었습니다. 즉, 당사 및 파트너사 지출 등 모두 포함한 각 단계별 전체 예상 비용 입니다. 직접비용과 간접비용을 모두 포함한 기준으로 작성되었습니다. |
③ 연구개발 자금계획
| 구분 | 2025년 | 2026년 | 2027년 | 2028년 |
|---|---|---|---|---|
| 퓨어스템-에이디주(반복투여) | - | - | - | - |
| 퓨어스템-에이디주(단회투여-3상 장기추적조사) | 9억원 | 13억원 | 12억원 | 9억원 |
| 퓨어스템-알에이주 | - | 20억원 | 20억원 | 25억원 |
| OSCA | 46억원 | 96억원 | 69억원 | 35억원 |
| 출처) 당사 제시 |
| 주1) 해당 예상 비용은 각 파이프라인의 각 개발 단계별 발생 예상되는 전체 비용 중 당사가 지출 예상되는 비용을 기준으로 작성되었습니다. 직접비용과 간접비용을 모두 포함한 기준으로 작성되었습니다. 주2) 퓨어스템-에이디주(반복투여) 임상시험 비용은 컨소시엄 등 임상 프로젝트 그룹 구성을 통해 해당 외부 자금으로 처리할 예정으로 이를 가정하여 해당 비용에 반영되어있지 않습니다. |
당사가 2024년 12월 공시한 합병신고서 당시 예상했던 개발 단계별 예상 비용 및 연구개발 자금계획 대비 금번 ② 개발 단계별 예상 비용 및 ③ 연구개발 자금계획 상 금액이 증가한 이유는 다음과 같습니다. 1) 2024년 12월 공시 당시에는 예상 비용 기재 시, 각 항목의 직접 비용만 산정하여 기재하였습니다. 반면 금번의 경우, 금번 조달한 자금의 사용목적 상 직접 비용 뿐 아니라 간접 비용도 포함되는 바 금번에는 간접 비용까지 모두 포함한 기준으로 변경하여 반영하였습니다. 간접 비용은 임상 진행에 따른 당사의 연구소, GMP 인원의 인건비가 주된 비용이며, 거의 대부분 외주로 진행되는 임상기관연구비, CRO, 위탁연구개발비 항목에는 포함되지 않고, 인허가, 약물감시, 기타 임상진행비 항목에 포함 및 반영되어 있습니다. 2) 또한, 각 예상 비용도 증권신고서 제출일 전일 기준으로 상승률 등 반영하여 최신화하여 재산출 진행하였습니다. 3) OSCA 관련 예상 비용의 경우, 관찰기간 연장 등 변경 계획에 따른 변화를 반영하였으며, 해외 임상 계획도 추가 포함되며 2a상 예상 비용이 크게 증가하였습니다. 다만, OSCA 임상 2b상, 3상의 경우에는 유영제약과의 기술이전 계약 체결에 따라 유영제약 주도로 진행 예정되는 바, 당사가 해당 예상 비용을 대신 최신화 하여 산정하는 것이 어려운 부분이 있어 당시 논의된 예상 임상 비용을 추가 변동 없이 그대로 사용하였으니, 투자자께서는 이 점 유의하시기 바랍니다. 4) 최초 증권신고서 공시 시에는 퓨어스템-에이디주(반복투여) 방식만 표기하였으나, 금번에는 퓨어스템-에이디주를 단회투여방식(3상 장기추적조사)과 반복투여 방식으로 세분화하여 기재 추가하였습니다. 5) 한편, 퓨어스템-에이디주 반복투여 방식의 임상시험 비용은 컨소시엄 등 임상 프로젝트 그룹 구성을 통해 해당 외부 자금으로 처리할 계획을 갖고 있습니다. 이에 이를 가정 시 최초 증권신고서 공시 시 '③ 연구개발 자금계획'에 기재하였던 퓨어스템-에이디주(반복투여)에 예상 비용은, 각 개발 단계별 발생 예상되는 전체 비용 중 당사가 지출 예상되는 비용 기준에 해당하지 않는다고 판단하여 금번 공시에는 제외하여 작성하였으니 이 점 유의하시기 바랍니다.
당사는 각 파이프라인의 각 단계별 예상 비용 및 자금계획 산정 시 필수 비용을 제외한 비용 최소화를 기본 원칙으로 산정하였으며, 유사 임상 진행 시 사용된 비용 등을 종합적으로 분석하여 최대한 객관적이고 신뢰성 있게 산출하고자 노력하였습니다. 그럼에도 불구하고, 임상 일정이 당사 계획보다 지연되거나, 임상을 진행하더라도 임상이 실패할 경우 각 단계별 임상 비용이 증가할 수 있으며 이는 당사의 매출액 및 수익성에 부정적인 영향을 미칠 가능성이 있으니 투자자께서는 이 점 유의하시기 바랍니다.
당사 주요 파이프라인의 연구개발 세부 실적은 다음과 같습니다.
(1) 아토피 피부염 치료제(퓨어스템-에이디 주)
| ①구분 | - 바이오 신약 |
| ②적응증 | - 중등도 이상의 아토피피부염 |
| ③작용기전 | - 퓨어스템-에이디 주를 아토피환자에 투여시, TGF-b, PGE2 등 다양한 면역조절인자가 분비되어 비만세포의 활성화 및 탈과립을 억제하고, 그 외에 Th2, Dendritic cell 등 다양한 염증세포의 반응을 조절함으로서 소양감 및 염증증상을 개선하는 효능을 나타냄 |
| ④제품의특성 | - 세계 최초의 아토피피부염 줄기세포치료제로서, 단일인자에 대한 차단이 아닌, 질환유발과 관련된 면역세포의 반응을 다각적으로 조절함으로서, 부작용이 거의 없으면서 근본적인 치료제로서 역할을 할 수 있는 신개념의 치료제임. |
| ⑤진행경과 | - 2013년 퓨어스템-에이디 주 1/2a상 줄기세포 단회 투여 임상시험계획 식약처 승인 - 2015년 1/2a상 줄기세포 단회 투여 임상시험 종료 (2018년 장기추적관찰 종료) - 2017년 3상 줄기세포 단회 투여 임상시험계획(K0102) 식약처 승인 - 2019년 6월 3상 임상시험(K0102) 종료 - 2019년 7월 1/2a상(반복투여) 임상시험계획(K0104) 식약처 승인 - 2020년 10월 한국 식약처 추가 3상 임상시험(K0106) 승인 신청 - 2021년 1월 1/2a상(반복투여)첫 환자 등록 및 투여 실시 - 2021년 5월 한국 식약처 추가 3상 임상시험(K0106) 승인 - 2021년 6월 3상 임상시험(K0106) 개시, 대상자 모집 시작 - 2023년 8월 3상 임상시험(K0106) 대상자 모집 완료 - 2023년 11월 3상 임상시험(K0106) 2차 투약 완료 - 2024년 2월 3상 임상시험(K0106) 마지막 대상자 최종방문 완료 - 2024년 7월 3상 임상시험(K0106) Top Line 발표, 11월 CSR 발표 - 2024년 11월 반복 2a 임상시험(K0104) 임상시험계획서 변경신청 - 2025년 4월 반복 2a 임상시험(K0104) 변경신청 자진취하 후 변경승인신청 |
| ⑥향후계획 | - 3상 결과활용 기술수출 진행 - 2a상 임상시험계획서 승인 |
| ⑦경쟁제품 | - Sanofi Genzyme사의 듀필루맙 등 |
| ⑧관련논문등 |
- Human umbilical cord blood mesenchymal stem cell-derived PGE2 and TGF-β1 alleviate atopic dermatitis by reducing mast cell degranulation. Stem Cells. 2015;33(4):1254-66. - Clinical Trial of Human Umbilical Cord Blood-Derived Stem Cells for the Treatment of Moderate-to- Severe Atopic Dermatitis: Phase I/IIa Studies. Stem Cells. 2017;35(1):248-255 |
| ⑨시장규모 | - 세계 아토피 치료제 시장은 오는 2030년 276억 8,000달러(37조원) 규모로 성장할 것으로 전망됨 (출처 : Grand View Research) |
| ⑩기타사항 |
- 정부정책과제 수주 4건 1) 아토피 피부염 치료를 위한 제대혈 줄기세포의 실용화 연구(중소기업청) |
당사 아토피 피부염 치료제(Furestem-AD Inj.)는 두차례 임상3상을 진행하였지만 통계적 유의성을 확보하지 못하여 2025년 4월 반복투여 임상1/2a상 임상시험계획 변경승인신청을 완료하였으며, 2025년 하반기 임상1/2a상 개시를 계획하고 있습니다.
1차 3상 임상시험의 경우, 2a임상시험에서 확인된 55% 수준의 EASI50 결과를 바탕으로 식약처로부터 2b임상시험을 면제하고 3상 임상시험으로 직행할 수 있었습니다. 당시 국내에 괄목할만한 아토피 치료제가 부재한 상태에서 당사 치료제의 우수한 임상 결과가 확인되었기 때문에 2b임상시험 면제라는 큰 수혜를 받을 수 있었습니다.그럼에도 불구하고 다음과 같은 사유로 1차 3상 임상에서 좋은 결과를 얻지 못했다고 판단됩니다. ① 위약과의 비교를 하지 않고 3상으로 직행하였다는 점, ② 이전에 수행된 2a 임상의 경우 1개 기관에서 수행되었지만, 3상의 경우 11개 기관에서 수행됨으로써 발생된 임상기관 관리 리스크 증가, ③ 2a와 3상 임상시험 모두 임상시험용 의약품이 냉장보관으로 공급되는 방식으로 진행되었는데, 2a 임상은 1개 기관이 참여하였기에 당사의 광명 소재 GMP센터에서 임상기관까지 4시간 이내 배송 및 투약이 가능했지만, 3상의 경우는 배송 및 투약에 평균 24시간 이상 소요되었습니다. 이는 시간경과에 따른 줄기세포의 세포활성에 부정적인 영향을 주었습니다. ④ 구제약물 및 허용약물, 그리고 12주 이후 적극적 치료약물의 사용을 허용하였기 때문으로 판단됩니다. 결과적으로 3상 임상이 2a 임상과 비교할 때, 임상시험용 의약품의 세포활성도가 저하된 것과 당시 내부적으로 충분하지 않았던 대규모 임상경험으로 1차 3상 임상에서 12주 시점에서 위약군 대비 통계적 유의성을 확보하지 못한 것으로 추정됩니다.
2차 3상 임상시험의 경우, 1차 3상 임상 수행의 경험을 바탕으로 ① 세포활성을 유지할 수 있도록 당사의 SELAF 플랫폼을 통해 임상시험용 의약품에 대한 관리를 개선하였고, ② 3종의 국소코르티코스테로이드(TCS)만 구제약으로 허용함으로써 1차 3상에서 확인된 교란 효과를 최소화하고자 했으며, ③ 시험약과 위약의 비율을 2:1로 하고 투약 후 12주 평가 후 시험약 투여군은 위약으로, 위약 투여군은 시험약으로 교체투약을 허용하여 중도탈락을 예방하였고, ④ 대규모 3상 임상시험에 필수적인 임상환경구축(eCOA, mediData)과 임상시험운영위원회를 통해 임상시험에 대한 관리 통제를 강화하였습니다.
이 결과 1차 3상 임상시험에 비해 2차 3상 임상시험의 중도탈락률은 10% 이상 감소하였고, 투약 후 12주를 포함한 시험약의 EASI50 평가에서 dataset 별로 2~8% 수준의 개선이 확인되는 등 전반적인 임상 품질이 제고됨을 확인하었습니다.
그러나 1차 유효성 평가변수인 투약 후 12주 시점에서의 EASI50에서 위약군 대비 통계적 유의성을 보여주지 못했습니다.
그 이유는 ① 단 회 투여시 시험약물의 경우 투약 후 시간이 경과함에 따라 지속적으로 EASI50와 기준치 대비 EASI 변화량 등에서 꾸준히 개선됨을 확인했지만 특정 시점인 12주 시점에서는 위약군 대비 개선도가 크지 않았기 때문이며, ② 구제약에 의한 영향 또한 있었습니다. 임상 기간 중 최소한으로 사용된 구제약이지만, 위약군의 경우 투약 후 12주 이전 구제약 사용자에게서 더 높은 EASI50 (비사용자 : 사용자 = 25.6% : 30.6%)를 보이는 반면, 시험군에서는 구제약 미 사용자에서 훨씬 더 높은 EASI50를 확인하였습니다(비사용자 : 사용자 = 44.9% : 23.5%).
아직 구체적인 기술수출이 체결된 바는 없으며 2차 3상 임상결과를 바탕으로 2025년 4월 30일 반복투여 임상 1/2a상 변경 승인 재신청을 완료하였으며, 2025년 하반기 임상 1/2a상 개시를 계획하고 있습니다. 다만, 당사가 환자모집 지연 등 예상치 못한 이유로 인해 연구개발 일정이 지연된다면 제품화까지 당사 예상 대비 장기간이 소요될 수 있으며, 연구개발을 진행하는 동안에도 성과가 나오지 않을 경우 연구를 중단하게 되고 사용된 연구개발비용은 따로 회수할 수 없어 당사의 수익성 및 성장성에 악영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
(2) 류마티스관절염 치료제(퓨어스템-알에이 주)
| ①구분 | - 바이오 신약 |
| ②적응증 | - 중등도 이상의 류마티스관절염 |
| ③작용기전 | - 퓨어스템-알에이 주를 류마티스 관절염 환자에 투여시, TSG-6, PGE2 등 다양한 면역조절인자가 분비되어 염증성 세포인 M1 phase macrophage의 활성을 억제하고, 항염증성 세포인 M2 phase macrophage의 활성을 촉진하여, 환자의 염증을 억제하고 증상개선효과를 나타냄. |
| ④제품의특성 | - 세계 최초의 류마티스관절염 줄기세포치료제로서, 단일인자에 대한 차단이 아닌, 질환유발과 관련된 면역세포의 반응을 다각적으로 조절함으로서, 부작용이 거의 없으면서 근본적인 치료제로서 역할을 할 수 있는 신개념의 치료제임. |
| ⑤진행경과 | - 2014년 퓨어스템-알에이 주 1상 임상시험계획 식약처 승인 - 2015년 1상 임상시험 종료 - 2018년 1/2a상 반복투여 임상시험(K0202) 식약처 승인 - 2021년 4월 대상자 등록 완료 - 2021년 10월 임상종료 - 2021년 12월 K0202 결과 확보 (2022년 5월 임상시험결과보고서 최종화) - 2023년 1월 2b상 IND 승인 신청 - 2023년 9월 2b상 IND 승인 |
| ⑥향후계획 | - 2b상 임상 개시 준비 |
| ⑦경쟁제품 |
- AbbVie사의 Humira - Johnson & Johnson사의 Remicade - Amgen/Pfizer사의Enbrel 등 |
| ⑧관련논문등 |
- Human umbilical cord blood-stem cells direct macrophage polarization and block inflammasome activation to alleviate rheumatoid arthritis. Cell Death Dis. 2016;7(12):e2524. - Intravenous Infusion of Umbilical Cord Blood-Derived Mesenchymal Stem Cells in Rheumatoid Arthritis: A Phase 1a Clinical Trial. Stem Cells Transl Med. 2018;7(9):636-642. |
| ⑨시장규모 | - 2019년 류마티스 관절염 치료제 매출이 262억 달러로 2029년까지 연평균 성장률(CAGR) 1% 로 291억 달러까지 완만한 성장을 예상됨. (출처: GlobalData) |
| ⑩기타사항 | - 정부 정책 과제 수주 1건 제대혈 유래 줄기세포를 이용한 류마티스 관절염 치료제의 상업화 임상 2a상 연구 (보건복지부) |
당사 류마티스 관절염 치료제(Furestem-RA Inj.)는 2014년 10월부터 2015년 10월까지 진행된 임상 1상(단회투여) 진행하였고, 그 이후 반복투여(4주간격 3회투여) 치료제로 2016년에 임상 1/2a 계획서를 제출했고 2018년 2월에 한국 식약처에서 승인되었습니다. 2018년 07월 1/2a상 임상 개시 이후, 2018년 12월 임상 1상이 완료되었으며, 2021년 10월에 1/2a상을 통해 안정성을 확인하였으며, 2023년 01월 임상 2b상 IND를 제출하였습니다.
2023년 09월 임상2b상 IND 승인을 받았으나, 선순위 프로젝트인 골관절염 치료제(OSCA) 임상과 아토피 피부염 치료제(퓨어스템-에이디주) 임상 시험에 예산을 우선 사용하여 류마티스 관절염 치료제의 2b 임상시험을 바로 개시하지 않고 보류 중입니다. 현재 류마티스 관절염 치료제(Furestem-RA Inj.)의 임상 2b상은 2027년 하반기 개시 후 마지막 환자 방문 완료 시점은 2028년 12월로 현재 목표하고 있습니다. 다만, 우선순위로 집중하고 있는 OSCA와 퓨어스템-에이디주의 연구개발 일정이 지연되거나 성과가 좋지 않아 당사 수익성에 영향을 미칠 경우, 수익화 달성에 따른 임상 진행 재원 마련 여부 등에 의해 류마티스 관절염 치료제의 임상 2b상의 개시 일정이 추가 지연될 가능성이 존재하므로 투자자께서는 이 점 유의하시기 바랍니다.
(3) 크론병 치료제(퓨어스템-시디 주)
| ①구분 | - 바이오 신약 |
| ②적응증 | - 중등도 활동성 크론병(염증성 장질환) |
| ③작용기전 | - 퓨어스템-시디 주를 크론병 환자에 투여시, NOD2 수용체의 활성화를 통해 PGE2 등 다양한 면역조절인자가 분비되어, 항염증성세포인 regulatory T cell의 활성을 촉진하고, Th1/Th17의 활성을 억제하여 염증억제, 조직재생등의 증상개선의 효과를 나타냄. |
| ④제품의특성 | - 희귀난치성 질환 치료제이며, 해외진출 가능성이 높은 치료제임. 단일인자에 대한 차단이 아닌, 질환유발과 관련된 면역세포의 반응을 다각적으로 조절함으로서, 부작용이 거의 없으면서 근본적인 치료제로서 역할을 할 수 있는 신개념의 치료제임. |
| ⑤진행경과 | - 2013년 퓨어스템-시디 주 1/2a상 임상시험계획 식약처 승인 - 크론병 성인환자 대상으로 1상 임상시험 진행 후 장기추적관찰 종료 |
| ⑥향후계획 | - 검토 중 |
| ⑦경쟁제품 |
- 존슨앤존슨의 인터류킨 12/23 (IL-12/23) 저해제 '스텔라라(Stelara, ustekinumab)' - 애브비의 IL- 23 저해제 리산키주맙(risankizumab) - 로슈/제넨테크의 에트롤리주맙(etrolizumab) - 다케다의'엔티바이오(Entyvio) 등 |
| ⑧관련논문등 | - Human umbilical cord blood mesenchymal stem cells reduce colitis in mice by activating NOD2 signaling to COX2. Gastroenterology. 2013;145(6):1392-403.e1-8. |
| ⑨시장규모 | - 크론병 치료제 시장이 미국, 프랑스, 독일, 이태리, 스페인, 영국, 일본 등 주요7개 국가에서 2029년 126억달러로 추정됨.(출처: GlobalData 2020년) |
| ⑩기타사항 |
- 크론병 중개연구센터 컨소시엄 참여 기업 - 정부정책과제 수주 2건 1) 크론병 치료제 개발을 위한 제대혈유래 줄기세포 상업화 임상연구 (보건복지부) |
(4) 건선 치료제(퓨어스템-시디 주)
| ①구분 | - 바이오 신약 |
| ②적응증 | - 중등도 이상의 건선 |
| ③작용기전 | - 퓨어스템-시디 주를 건선 환자에 투여시, PGE2와 같은 면역조절인자가 분비되어 건선유발에 중요한 역할을 하는 Th17세포를 억제하고, IL-17 과 같은 염증성사이토카인을 억제함으로서, 증상 개선에 대한 효능을 나타냄. |
| ④제품의특성 | - 세계 최초의 건선 줄기세포치료제로서, 단일인자에 대한 차단이 아닌, 질환유발과 관련된 면역세포의 반응을 다각적으로 조절함으로서, 부작용이 거의 없으면서 근본적인 치료제로서 역할을 할 수 있는 신개념의 치료제임. |
| ⑤진행경과 | - 2014년 퓨어스템-시디 주 1상 임상시험계획 식약처 승인 - 판상형 건선 성인환자 대상으로 1상 임상시험 진행 후 장기추적관찰 종료 |
| ⑥향후계획 | - 검토 중 |
| ⑦경쟁제품 |
- 얀센의 스텔라라(우스테키누맙) - 노바티스의 코센틱스(세쿠키누맙) - 릴리의 탈츠(이젝키주맙) - 밸리언트의 실리크(브로달루맙) - 존슨앤존슨의 트렘피야(구셀쿠맙) 등 |
| ⑧관련논문등 | - |
| ⑨시장규모 | - 건선치료제 글로벌 시장 규모는 2030년 275억 달러로 추정됨 (출처: 메디팜스투데이 2021년) |
| ⑩기타사항 |
- 정부정책과제 수주 1건 1) 제대혈유래 만능줄기세포를 이용한 건선치료를 위한 비임상연구(보건복지부) |
(5) 골관절염 치료제 (퓨어스템-오에이 키트 주)
| ①구분 | - 바이오 신약 |
| ②적응증 | - ICRS grade 3 또는 4에 해당하는 무릎골관절염 |
| ③작용기전 | - 골관절염 환자의 관절강내에 줄기세포와 생체소재를 함께 주입하여, 염증을 억제하면서, 손상된 연골조직의 재생을 유도함. |
| ④제품의특성 | - 기존의 골관절염 줄기세포치료제의 한계점을 극복할 수 있는 치료제로, 줄기세포와 생체소재를 혼합하여 연골 재생 기능이 탁월한 치료제를 주사제 형태로 개발중에 있음. |
| ⑤진행경과 | - 2021년 8월 한국 식약처 임상시험계획 승인 신청 - 2022년 4월 보완답변 제출 - 2022년 6월 20일 IND 자진취하 - 2022년 7월 15일 IND 재신청 - 2022년 11월 15일 IND 승인완료 - 2022년 11월 28일 IND 변경승인 신청 - 2023년 2월 7일 IND 변경승인 완료 - 2023년 7월 1상 코호트1 대상자 투약ㅉ- 2023년 9월 1상 코호트1 대상자 DLT 평가완료 - 2023년 11월 1상 코호트2 대상자 투약 완료 - 2024년 1월 코호트2 대상자 DLT 평가완료, 코호트1 대상자 6개월 방문완료 - 2024년 3월 코호트3 대상자 DLT 평가완료, 전체 코호트에 대한 MTD 평가완료 - 2024년 4월 코호트1 대상자 6개월 영상평가 평가완료 - 2024년 8월 1/2a상 식약처 IND 변경승인신청, 10월 변경승인 완료 - 2024년 12월 1상 topline data 발표, 1/2a상 식약처 IND 변경승인신청 - 2025년 1월 1/2a상 IND 변경승인 - 2025년 3월 2a상 첫환자 투약 개시 |
| ⑥향후계획 | - 1상 전체 대상자 영상평가 완료 - 1상 결과 국제학회 발표 - 2a 임상시험 개시 |
| ⑦경쟁제품 | - 무릎골관절염 근복적 치료제로 시판승인된 제품 없음. |
| ⑧관련논문등 | - Therapeutic Effects of Human Umbilical Cord Blood-Derived Mesenchymal Stem Cells Combined with Cartilage Acellular Matrix Mediated Via Bone Morphogenic Protein 6 in a Rabbit Model of Articular Cruciate Ligament Transection 2020 Jun;16(3):596-611 - Combined Mesenchymal Stem Cells and Cartilage Acellular Matrix Injection Therapy for Osteoarthritis in Goats 2022 Feb; 19(1): 177-187 |
| ⑨시장규모 | - 골관절염 시장은 2032년까지 183억 6000만달러(24조2021억원)으로 성장할 것으로 전망함. (출처 : Precedence Research) |
| ⑩기타사항 | - 독일Heraeus Medical GmbH 공동개발 계약 체결(2017.09) - 정부 정책과제 수주 1건 차세대 골관절염 줄기세포 치료제 개발을 위한 유효성 안전성 평가 연구 |
OSCA는 동종 제대혈 유래 중간엽 줄기세포(UCB-MSC, Osiramestrocel)와 연골 세포 기질(CAM)을 결합한 무릎 골관절염(DMOAD) 치료제입니다. 기존 치료제가 특정 기전에만 작용하는 반면, OSCA는 다양한 질환 유발 요인에 동시에 작용하여 통증 개선, 관절 기능 회복, 구조적 개선을 목표로 하고 있습니다.
개발 초기 비임상 연구 단계에서는 동물 모델을 활용해 연골 재생 및 관절 구조 개선 효과를 입증했으며, 항염증 및 재생 효과를 증명하고 안전성을 확보했습니다. 이후 임상 1상에서는 저용량, 중용량, 고용량으로 구분된 세 군을 대상으로 안전성, 내약성, 그리고 유효성을 평가했습니다. 중용량과 고용량에서 통증 및 관절 기능 개선과 구조적 개선에서 유의미한 효과가 관찰되었고, 주요 통계 지표들(IKDC, WOMAC, KOOS, VAS)에서도 긍정적인 결과가 나타났습니다.
임상 1상에서 확인된 안전성 및 유효성에 대한 전반적인 평가 결과를 바탕으로 중용량과 고용량을 임상 2a상의 시험군으로 선정하였으며, 대상자를 50명에서 108명으로 확대하여 위약 대비 시험약의 효과를 보다 정밀하게 평가할 계획입니다. 2025년 3월 임상시험을 시작해 2026년 2분기까지 완료를 목표로 하고 있으며, 성공 시 임상 2b 단계를 생략하고 임상 3상으로 직행할 가능성도 검토 중입니다. 이는 뛰어난 효과와 안전성이 입증된다면, 개발 기간을 2~3년 단축할 수 있는 잠재력을 가지고 있음을 의미합니다.
OSCA의 강점은 첨단 세포 선별 기술과 대량생산 기술로, 고활성 세포의 안정적인 유지가 가능하다는 점입니다. 또한 다중 기전 작용을 통해 기존 치료제보다 우수한 효과와 안전성을 기대할 수 있습니다. 이미 임상 1상 결과를 통해 구조적 개선을 포함한 근본적인 치료제로서의 가능성을 입증했으며, 장기적인 효과를 확인하기 위해 5년까지의 추적 관찰이 계획되어 있습니다.
상업적 측면에서는 국내외 파트너와의 협력으로 개발 비용을 최소화하고 초기 매출 실현 가능성을 높였습니다. 특히, 국내에서는 임상 1상 이후 유영제약과 라이선스 계약을 체결하여 임상 2b상 단계 이후의 개발 비용 부담을 줄이는 동시에 매출 조기 실현이라는 장점을 확보했습니다. 이러한 전략은 안정적인 회사 운영과 글로벌 파트너십 확장을 위한 유리한 환경을 제공합니다.
한편, 당사는 2023년 유상증자 당시 OCSA 임상 1상 완료 후 글로벌 라이선스 아웃을 계획하였으나, 이는 예상보다 지체되었습니다. 당사는 OSCA 임상 1상 이후 다수의 글로벌 제약사와 기술이전 협의를 위해 노력하였으나, 1)위약 대비 시험약의 효과 비교 가능한 데이터, 2)시험군의 효과크기를 비교하기 적절한 규모의 데이터를 보강 요청하는 곳이 다수였습니다. 이에 당사는 OSCA 임상 2a상 대상자를 50명에서 108명으로 본래 계획보다 확대하여 위약 대비 시험약의 효과를 보다 정밀하게 평가할 수 있게 수정하였으며, 임상 2a상 완료 후 확보하게 되는 임상 데이터를 기반으로 다시 글로벌 라이선스 아웃 달성을 목표로 하고 있습니다. 다만, 당사가 추진하는 글로벌 기술이전 계약의 구체적인 계약 조건이나 상대방이 확정된 것은 아니므로, 기술이전의 성공 여부 및 시기 등은 불확실할 수 있다는 점을 투자자께서는 유의하시기 바랍니다.
OSCA의 성공을 위해서는 대규모 임상시험에서 일관성 있는 결과가 필수적이며, 장기적 효과를 지속적으로 증명해야하며 글로벌 시장에서 경쟁 중인 다른 DMOAD 후보들과의 차별화를 이루는 것도 중요한 과제로 판단됩니다. 또한, 당사가 환자모집 지연 등 예상치 못한 이유로 인해 연구개발 일정이 지연된다면 제품화까지 당사 예상 대비 장기간이 소요될 수 있으며, 연구개발을 진행하는 동안에도 성과가 나오지 않을 경우 연구를 중단하게 되고 사용된 연구개발비용은 따로 회수할 수 없어 당사의 수익성 및 성장성에 악영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
| 라. 파이프라인별 경쟁 심화로 인한 수익성 부진 위험 당사 파이프라인의 전방산업인 아토피 피부염 치료제, 류마티스 관절염 치료제 및 골관절염 치료제 시장 등이 안정적이고 지속적으로 성장한다면, 당사의 성장성을 견인할 수 있습니다. 아토피 피부염의 최근 환자가 증가하는 추세에 따라 큰 규모의 시장을 노리고 대형 제약사에서는 아토피 관련 제품들을 출시하고 있으며 경쟁 또한 치열해지며,글로벌 아토피 피부염 환자수는 2023년 2억 400만명으로 추정됩니다. 아직 아토피 피부염의 발병 원인이 정확하게 분석되지 않았음에도 최근 치료비의 증가세에 힘입어 아토피 관련 수많은 제품들이 시중에 출시되어 있습니다.류마티스 관절염 또한 고령의 환자들에게서 높은 유병률을 보이며, 노령화 사회가 지속됨에 따라 환자 수 또한 지속적으로 증가할 것으로 예상됩니다. 최근 새로운 기전으로 작용하는 약물들이 개발되어 당사를 비롯한 제약사들이 류마티스 관절염 치료제시장에 도전하고 있습니다. 골관절염은 노화와 비만이 가장 흔한 원인이며, 이로 인해 골관절염 환자 수는 지속적으로 증가하고 있습니다. 수년간 혁신이 일어나지 않았던 무릎관절염분야가 최근 급격하게 진전되고 있고, 많은 후보물질들이 활발하게 개발되고 있습니다. 당사의 기술을 포함한 줄기세포치료제가 자가면역질환의 치료성능으로써 임상이 진행중에 있어 성능과 그 상용화 전망에는 긍정적인 요인은 있으나, 당사와 같은 파이프라인 중 이미 개발 완료된 치료제가 존재할 경우 당사는 후발 진입에 따른 경쟁력 확보해야될 과제를 안고 있습니다. 이러한 잠재적 경쟁회사의 연구개발 제품이 시장에 성공적으로 출시될 경우 당사가 장기간 신약 개발에 쓰인 막대한 투자 비용과 시간을 감안할 시 당사의 경영성과 및 재무구조에 부정적인 영향을 미칠 수 있음을 투자자께서는 유의하시기 바랍니다. |
당사 파이프라인의 전방산업인 아토피 피부염 치료제, 류마티스 관절염 치료제 및 골관절염 치료제 시장 등이 안정적이고 지속적으로 성장한다면, 당사의 성장성을 견인할 수 있습니다.
| [당사 파이프라인 현황] |
| 구분 | 품목 | 적응증 | 연구 시작일 |
현재 진행단계 | 비고 | |
| 단계(국가) | 승인일 | |||||
| 바이오 신약 |
퓨어스템-에이디 주 | 아토피피부염 | 2011년 | 임상3상(한국) | 2017년 | 주1) |
| 임상1/2a상(한국) | 2019년 | 주2) | ||||
| 퓨어스템-알에이 주 | 류마티스관절염 | 2012년 | 임상2b상(한국) | 2023년 | 주3) | |
| 퓨어스템-시디 주 | 크론병 | 2012년 | 임상1/2a상(한국) | 2013년 | 주4) | |
| 판상형 건선 | 2013년 | 임상1상(한국) | 2014년 | 주5) | ||
| 퓨어스템-오에이 키트 주 | 골관절염 | 2015년 | 임상1/2a상(한국) | 2022년 | 주6) | |
| 주1) | 2021년 05월 국내 두번째 3상 승인 완료되어 임상 진행하였으며, 2024년 11월 CSR 결과발표하였습니다. |
| 주2) | 반복투여 임상으로 2024년 11월 1/2a 임상시험 변경승인 신청하였으며, 2025년 4월 자진취하 하였습니다. 2025년 4월 30일 식약처에 자료를 보완하여 변경승인 신청 하였습니다. |
| 주3) | 2023년 9월 2b상 IND 승인을 받았으며, 임상 개시 시기는 2027년으로 예상하고 있습니다. |
| 주4) | 2019년 5월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주5) | 2019년 1월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주6) | 2022년 11월 15일 식약처로부터 IND 승인받았으며, 2a 임상시험을 진행 중입니다. |
① 아토피 피부염 치료제(Furestem-AD Inj.)
Oxford Academic의 Global epidemiology of atopic dermatitis: a comprehensive systematic analysis and modelling study에 따르면 글로벌 아토피 피부염 환자수는 2023년 전세계 인구의 2.6%인 2억 400만명으로 추정됩니다. 이 중 성인 환자의 비율은 55.2%, 아동 환자의 비율은 44.8%로 추정됩니다. 여성이 남성보다 더 아토피 환자가 될 가능성이 높았으며, 여성의 유병률은 2.8%, 남성의 경우 2.4%로 추정되었습니다.
아토피 피부염의 최근 환자가 증가하는 추세에 따라 큰 규모의 시장을 노리고 대형 제약사에서는 아토피 관련 제품들을 출시하고 있으며 경쟁 또한 치열해지고 있습니다. 글로벌 아토피 피부염 치료제 시장 규모는 2024년 약 147.2억달러에서 2034년 약 314.4억 달러 규모까지 성장할 것으로 전망되며, 이는 연평균 7.9% 수준의 성장성을 보입니다.
| [글로벌 아토피 치료제 시장 규모] | ||
| (단위: 십억달러) | ||
|
| 출처) Precedence Research, Atopic Dermatitis Drugs Market Size, Share, and Trends 2024 to 2034, 2024 |
건강보험심사평가원에 따르면, 국내 전체 인구대비 아토피 피부염 진료실 인원 비중과 절대수치를 보았을 때, 그 수는 약 100만명에 이르며, 소아 및 청소년을 넘어 성인에게도 꾸준히 발생하고 있습니다. 국내 아토피 치료제 시장만 고려했을 때도 아토피 피부염 시장은 큰 규모입니다. 다음은 연도별 아토피 피부염 환자 증감 추이 현황입니다.
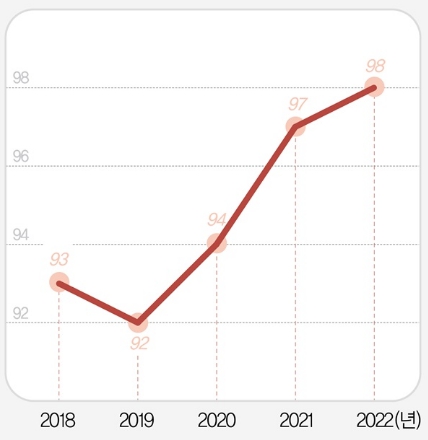 |
|
연도별 아토피 피부염 환자 증감 추이(단위: 만명) |
| 출처) 건강보험심사평가원, 2020 |
진료실 인원 비중과 상반되게 치료비 규모는 2018년 435억원 규모에서 2022년 1,201억원 규모로 증가하고 있으며, 일시적 증상 완화만 가능한 상태로, 효과적인 치료제에 대한 해법은 아직 없는 상황입니다. 해당 질환은 삶의 질을 급격히 저하시키는 질환으로 전 세계적으로 환자가 꾸준히 발생하고 있어, 당사는 해당 치료제 개발에 매진하고 있습니다.
| [최근 5년 아토피 피부염 질환에 대한 진료환자, 요양급여비 추이] |
| 구 분 | 2018 | 2019 | 2020 | 2021 | 2022 | 5개년 성장률 |
|---|---|---|---|---|---|---|
| 진료환자 (명) | 921,070 | 949,990 | 972,928 | 989,750 | 973,636 | 1.1% |
| 요양급여비 총액 (천원) | 43,562,688 | 45,837,611 | 51,847,661 | 86,472,525 | 120,118,801 | 22.5% |
| 출처) 건강보험심사평가원 보건의료빅데이터개방시스템 |
아직 아토피 피부염의 발병 원인이 정확하게 분석되지 않았음에도 최근 치료비의 증가세에 힘입어 아토피 관련 수많은 제품들이 시중에 출시 되어 있습니다. 아토피 피부염은 면역학적, 유전적, 환경적 요인이 상호작용해 나타나는 대표적인 알러지 질환으로 현재로서는 적절한 치료제가 없기 때문에 병원 치료 외에도 보습제 또는 DIY 천연제품 등 환자 개인마다 다양한 방법으로 관리를 하고 있으며, 이러한 대증요법은 질병의 근본적인 치료보다는 표면적이고 일시적인 증상 완화에 불과합니다. 이에 당사 뿐만 아니라 국내 제약회사들도 부작용을 최소화 할 수 있는 다양한 방법으로 치료제를 개발하고 있습니다.
2018년 03월 사노피의 듀피젠트(성분명 두필루맙; 글로벌 시장 점유율: 2023년 69%, 국내 중증 아토피 치료제 시장 90% 점유, 출처: 헬스조선)가 국내에서 성인 중등증에서 중증 아토피 피부염 치료제로 허가받으면서 새로운 치료 대안으로 제시되었습니다. 다양한 연령의 중등증에서 중증의 아토피 피부염 환자에게 사용 가능한 주력 옵션으로 자리매김해오고 있습니다. 다만, 듀피젠트가 시장에서 큰 비중을 차지하고 있으나, 2주 간격으로 주사를 맞아야 하는 등 단점이 있습니다. 치료효과와 함께 복약 편의성을 높인 신제품 출시 경쟁으로 이러한 아토피 피부염 시장에 국내 제약사들도 앞다퉈 임상에 진입하고 있습니다.
JAK 억제제로 2021년 5월 릴리의 올루미언트(성분명 바리시티닙), 2021년 10월 애브비의 린버크(성분명 유파다시티닙), 2022년 4월 화이자의 시빈코(성분명 아브로시티닙), 2023년 8월 레오파마의 아트랄자(성분명: 트랄로키누맙)이 국내에서 아토피피부염 치료제로 허가를 받으며 새로운 대안으로 선택할 수 있게 되었습니다. 그러나 이러한 JAK억제제는 대상포진, 결핵, 심혈관 질환 등의 감염 위험을 증가시키며, 혈전 생성 촉진 가능성이 있고, 림프종 및 피부암 등 암 발생 위험도 상승시키는 등 안전성에 있어 결함을 보유 중입니다.
| [국내 아토피 치료제 개발 현황] |
| 제약사 | 프로젝트명 | 특징 | 개발단계 |
|---|---|---|---|
| 강스템바이오텍 | Furestem-AD | 제대혈 줄기세포 치료제 | 임상 3상 완료 (단일투여) 임상 1/2a 진행 (반복투여) |
| 큐리언트 | Q301 | 류코트리엔 합성 저해 | 미국 임상 2b상 완료 |
| JW중외제약 | JW1601 | 염증, 가려움증 개선 | 글로벌 2b상 완료 |
| 에스씨엠생명과학 | SCM-AGH | 중등증-중증 아토피피부염 줄기세포 치료제 | 국내 임상 2상 완료 |
| 대웅제약 | DWP212525 | JAK3/TFK 이중 표적 | 전임상 |
| DWP213388 | ITK/BTK 동시 저해 | 미국 임상 1상 진행 | |
| 노바셀 | NCP112 | FPR2 표적 | 국내 1상 완료 |
| 엔지켐생명과학 | EC-18 | 경구투여, 화학합성신약 | 국내 2상 승인 |
| 샤페론 | NuGel | GPCR19 수용체 표적 | 국내 2상, 미국 2상 |
| HK이노엔 | IN-115314 | JAK-1 선택적 억제 | 국내 2상 |
| 출처) 언론사 보도 자료 및 당사 자체 집계(2025.03) |
당사는 아토피 피부염 치료제(Furestem-AD Inj.)의 임상 3상에서 12주차 시점 위약 대비 시험군과 대조군 간 유효성 차이를 입증하지 못하였습니다. 이에 기존 단회투여에서 반복투여 방식으로 프로토콜을 수정하여 2024년 11월 임상2a상 IND를 신청하였으나, 식품의약품안전처(MFDS)의 추가 자료보완 요청을 기한 내 회신이 어려울 것으로 판단하여 자진취하 신청을 하였습니다. 그리고 2025년 4월 30일 퓨어스템-에이디주의 반복투여 제1/2a 임상시험계획변경승인신청을 하였으며, 2025년 하반기 임상 1/2a상 개시를 계획하고 있습니다.
다만, 당사가 예상하지 못한 다른 방식의 새로운 치료제가 개발되거나, 타 줄기세포치료제와의 경쟁이 심화될 경우 당사의 장기간 신약 개발에 쓰인 막대한 투자 비용과 시간을 감안할 시 당사의 경영성과 및 수익성에 부정적인 영향을 미칠 수 있습니다.
② 류마티스 관절염 치료제(Furestem-RA Inj.)
글로벌 류마티스 관절염 시장은 2024년 182.7억달러에서 2033년 273.8억달러 규모까지 성장할 것으로 예상되고 있습니다. 류마티스 관절염은 가장 만성 염증성 골질환으로, 고령의 환자들에게서 높은 유병률을 보이고 있으며 노령화 사회가 지속됨에 따라 환자 수 또한 지속적으로 증가할 것으로 예상됩니다.
| [글로벌 류마티스 골관절염 치료제 시장 규모] | ||
| (단위: 십억달러) | ||
|
| 출처) Precedence Research, Rheumatoid Arthritis Drugs Market Size 2023 to 2033, 2024 |
과거 비스테로이드성 항염제나 스테로이드 제제들이 부작용 등으로 시장에서 외면 받은 반면 생물학적 제제들은 비생물학적 항류마티스제제에 대한 반응이 좋지 않았던 환자들의 70% 이상에게서 증상이 호전되어 생물학적제제가 류마티스 관절염 시장을 이끌어 가고 있습니다. 대표적인 생물학제 제제인 종양괴사인자(TNF-α) 억제제는 10년 이상 류마티스관절염 시장을 장악하였으며, TNF-α억제제와 JAK억제제, IL-6억제제가 혼전하는 양상 속에서도 에브비사의 휴미라(TNF-α억제제)는 다수의 적응증 확보와 오랜 투약 경험에서 나오는 안전성 등 강점을 내세우며 국내 시장도 장악하고 있습니다.
다만, 치료 후 약 2년 정도 지나면 TNF-α억제제에 대한 내성으로 인해 치료효과를 보이지 않는 것으로 확인되어 TNF-α억제제를 대체할 만한 치료제의 개발이 요구되고 있는 상황입니다. 이에 최근 새로운 기전으로 작용하는 약물들이 개발되어 당사를 비롯한 제약사들이 류마티스 관절염 치료제 TNF-α억제제 시장에 도전하고 있습니다.
| [2020년 글로벌 류마티스 관절염 치료제 시장 Top10 제약사] |
| (단위 : 십억달러) |
| 순위 | 작용기전 | 제품명 | Trade name (Biological name) | 제약사 | 출시 년도 | 매출 (USD) |
|---|---|---|---|---|---|---|
| 1 | TNF-a 억제제 | 휴미라 | Humira® (adalimumab) | 애브비 | 2002 | 20.39 |
| 2 | TNF-α, β 억제제 | 엔브렐 | Enbrel® (etanercept) | 암젠/화이자 | 1998 | 6.37 |
| 3 | CD20 | 리툭산 | Rituxan® (rituximab) | 로슈 | 2006 | 4.52 |
| 4 | TNF-a 억제제 | 레미케이드 | Remicade® (infliximab) | J&J/MSD | 1999 | 4.195 |
| 5 | IL-6 억제제 | 악템라 | Actemra® (tocilizumab) | 로슈 | 2010 | 3.12 |
| 6 | T세포 활성 조절제 | 오렌시아 | Orencia® (abatacept) | BMS | 2005 | 3.2 |
| 7 | TNF-a 억제제 | 심퍼니 | Simponi® (golimumab) | J&J/MSD | 2009 | 2.25 |
| 8 | TNF-a 억제제 | 심지아 | Cimzia® (certolizumab pegol) | UCB | 2009 | 2.1 |
| 9 | JAK 억제제 | 올루미언트 | Olumiant® (baricitinib) | 릴리 | 2020 | 638.9 |
| 10 | IL-1R 억제제 | 키네레트 | Kineret® (anakinra) | 소비 | 2001 | 239 |
| 자료: 각사 Annual Report 및 당사 자체 집계 |
| [류마티스 관절염 치료제 비교] |
| 제품 | Furestem-RA® | 휴미라 | 레미케이드 | 엔브렐 |
|---|---|---|---|---|
| 구분 | 제대혈 줄기세포 치료제 | 단크론항체 치료제 | ||
| 개발사 | 강스템바이오텍 | AbbVie | Johnson & Johnson | Pfizer |
| 투여주기 | 단회투여 | 2주 1회 | 2주~6주 1회 | 주 1~2회 |
| 부작용 | 면역조절이 이루어지기 때문에 중대한 부작용 없음 | 감염, 결핵, 신경계 이상, 악성종양 및 림프구증식 질환, B형간염, 울혈성 심부전 | ||
| 효과지속성 | 현재까지 발견된 내성 반응 없음 | 전체 투여 환자의 1/3 가량이 불응, 지속사용에 따라 효능 저하 발생 | ||
| 출처) 당사 제시 |
당사는 류마티스 관절염 치료제(Furestem-RA Inj.)에 대해 2014년 10월부터 2015년 10월까지 진행된 임상 1상(단회투여) 진행하였고, 그 이후 반복투여(4주간격 3회투여) 치료제로 2016년에 임상 1/2a 계획서를 제출했고 2018년 2월에 한국 식약처에서 승인되었습니다. 2018년 07월 1/2a상 임상 개시 이후, 2018년 12월 임상 1상이 완료되었으며, 2021년 10월에 1/2a상을 통해 안정성을 확인하였으며, 2023년 01월 임상 2b상 IND를 제출하였습니다. 2023년 09월 임상2b상 IND 승인을 받았으며, 임상 개시 시기를 결정 후 진행할 예정입니다.
③ 골관절염 치료제(OSCA (구. Furestem-OA Inj.))
프레시던스 리서치에 따르면, 글로벌 골관절염 치료제 시장은 2024년 99.1억 달러에서 2034년 243.4억 달러까지 성장할 것으로 전망하였습니다. 국내 시장의 골관절염 환자 규모는 2023년 기준 약 430만명(건강보험심사평가원 자료)에 달하며, 고령화로 환자수는 갈수록 늘어날 전망입니다.
| [글로벌 골관절염 치료제 시장 규모] | ||
| (단위: 십억달러) | ||
|
| 출처) Precedence Research, Osteoarthritis Therapeutics Market Size, Share, and Trends 2024 to 2034 |
노화와 비만(보통 체중을 가진 개인에 비해 비만인 경우 무릎 골관절염에 걸릴 확률이 14배 높음.)은 무릎 골관절염의 가장 흔한 원인이며, 이로 인해 골관절염 환자 수는 지속적으로 증가하고 있습니다. 수년간 혁신이 일어나지 않았던 무릎관절염분야가 최근 급격하게 진전되고 있고, 많은 후보물질들이 활발하게 개발되고 있는 중입니다. 그러나 항체와 같은 물질은 개발에 실패하는 사례가 보고되고 있으며, 골관절염의 통증완화, 기능개선 효과 뿐만 아니라 구조적 질병진행을 억제하거나 회복시키는 근복적인 치료제인 DMOAD(Disease-Modifying Osteoarthritis Drugs)는 여전히 전무한 상태입니다.
골관절염은 진행단계와 환자 상태에 따라 초기, 중기, 말기로 구분되며 초기 단계는 통증치료를 위한 진통소염제, 히알루론신치료제, 물리치료등의 보존적 방법으로 치료하고, 중기단계는 연골재생을 촉진하는 자가세포치료제, 줄기세포 치료제를 이용한 수술적 요법을 적용합니다. 말기단계는 연골 소실로 보행장애증상으로 인공관절 수술을 실시합니다. 연골재생의 촉진 및 통증완화 등 DMOAD로써 수술을 시행하지 않으며, off-the-shelf의 Injection치료법에 대해 절실히 요구되고 있으며, 현재 골관절염치료제로써 DMOAD로써 동종유래줄기세포치료제가 미충족 의료 시장의 해결책이 될 수 있습니다.
| [골관절염 치료제 비교] |
| 제품 | OSCA | C치료제 | C치료제 | I치료제 |
|---|---|---|---|---|
| 개발사 | 강스템바이오텍 | B사 | M사 | K사 |
| 주요 성분 | 동종 제대혈 유래 중간엽 줄기세포+ CAM (무세포성 연골 ECM) | 자가연골유래연골세포 | 동종 제대혈유래 중간엽줄기세포 | 토노젠콜셀 동종유래 연골세포+형질전환세포 |
| 적응증 | 국제연골재생학회(ICRS) grade 3 또는 4의 무릎 연골이 퇴행된 환자 | 무릎 연골결손 (ICRS grade 3 또는 4, 결손면적 2 내지 10 cm2)의 치료 | 골관절염환자(ICRS grade 4)의 무릎 연골 결손 치료 | 중증도 무릎 골관절염(K&L grade3)의 치료 |
| 투여방식 | 무릎강 주사 (줄기세포 + 무세포성 연골) |
관절강 개방 후 투약 | 무릎수술 후 투약 | 무릎강 주사 (연골세포 + 형질전환세포) |
| 개발단계 | - 국내: 임상 2a상 진행 중 | - 국내: 시판 중(임상2상 이후 3상 조건부 허가), 임상3상 완료(25/12/11) - 미국: RMAT 지정 |
- 국내: 시판 중 - 미국: 임상 3상 준비 중 - 일본: 임상 3상 진행 중 |
- 국내: 허가 취하(19/07/09) - 미국: 임상 3상 진행 중 |
| 특징 | - 투약의 편의성 - 신속한 통증조절 및 관절기능 개선 - 연골재생 및 연하골 구조개선이 확인됨 (DMOAD) |
- 환자 본인의 늑연골 채취 및 투약을 위한 수술 필요 - 관절 손상부위 재생효과 |
- 투약을 위한 미세천공술 필요 - 품목허가 후 장기간에 걸친 데이터를 통해 치료 효과와 안전성 확인 |
- 투약의 편의성 |
| 출처) 당사 제시 |
당사는 골관절염 치료제(OSCA)에 대해 2022년 07월 한국 식약처에 임상 1/2a상 IND를 제출하였으며, 2022년 11월에 IND 승인이 완료되었습니다. 2023년 07월 초 국내 임상 1상 임상시험개시모임(임상시험에 필요한 전반적인 내용을 최종적으로 검토 및 확인하는 자리)을 완료하였으며, 2023년 08월 저용량,10월 중용량, 2024년 02월 고용량 기준으로 환자에게 투여를 완료하였습니다. 2024년 08월 1/2a상 식약처 IND 변경승인 신청 후 10월에 승인 완료받았으며 임상 1상 결과보고서를 수령하였습니다. 그 결과에 따라 2025년 3월 임상 2a상이 진행중이며, 2026년 하반기 임상 2b상을 진행할 예정입니다.
이처럼 당사의 기술을 포함한 줄기세포치료제가 자가면역질환의 치료성능으로써 임상이 진행 중에 있어 성능과 그 상용화 전망에는 긍정적인 요인은 있으나, 다른 방식의 치료제 및 타 줄기세포치료제와의 경쟁은 치료제를 개발 진행 중인 당사 영업전망에 위험요소가 될 수 있습니다.
또한, 당사와 같은 파이프라인 중 이미 개발 완료된 치료제가 존재할 경우 당사는 후발 진입에 따른 경쟁력을 확보해야할 과제를 안고 있습니다. 또한, 당사의 연구개발 영역 또는 타겟 질병이 겹치는 잠재적인 경쟁회사의 출현 가능성을 배제 할 수 없으며, 이러한 잠재적 경쟁회사의 연구개발 제품이 시장에 성공적으로 출시될 경우 당사가 장기간 신약 개발에 쓰인 막대한 투자 비용과 시간을 감안할 시 당사의 경영성과 및 재무구조에 부정적인 영향을 미칠 수 있음을 투자자께서는 유의하시기 바랍니다.
| 마. 국내외 정부정책 및 규제 변화에 따른 위험 제약바이오 산업은 인간의 생명 및 건강과 직결되는 의약품을 개발ㆍ제조ㆍ판매하는 산업으로, 제품의 개발 및 제조, 임상시험, 인허가, 유통 및 판매에 이르기까지 전 과정에 걸쳐 각 국가의 규제 당국이 제시하는 엄격한 규정과 절차를 따라야 합니다. 동시에 제약바이오 산업은 핵심 미래 성장 산업으로, 국내를 포함한 주요 선진국들을 중심으로 바이오 의약품을 미래 성장 동력으로 확보하고 기술 선점을 위하여 바이오 의약품 규제 개선 및 연구개발 확대 등 다양한 정책적 지원 체계를 통해 바이오 의약품 산업 경쟁력 강화를 추진하고 있습니다. 이처럼 제약바이오 산업에 대한 관심도가 증가함에 따라 정부의 우호적인 시장 정책이 다수 도입되고 있는 실정이지만, 이와 같은 정책지원이 조속히 실행되지 않거나, 정책 기조의 변화에 따라 정부지원이 축소되는 등의 상황이 발생하는 경우에는 당사의 재무상태 및 영업실적 등에 부정적인 영향이 있을 수 있습니다. 당사는 정책 및 규제 변화에 신속한 대응을 위한 지속적인 모니터링을 진행하고 있지만, 그럼에도 불구하고 국내외 정책 등의 변동 위험이 존재하니 투자자께서는 이 점 유의하시기 바랍니다. |
당사가 영위하고 있는 세포치료제 등 제약바이오 산업은 핵심 미래 성장 산업으로 각국 정부에서 적극적인 육성 정책을 시행하지만, 환자 보호 측면에서 인허가 및 약가 결정에 각국 정부는 엄격하게 개입하는 양면적인 특성을 가지고 있습니다. 따라서, 정책의 성과를 제약 관련 산업계, 학계, 연구계 등과 공유하고 요구를 반영함으로써 원활한 정책 운영의 선순환 구조를유지하는 등 제약산업 현장에 실질적으로 반영될 수 있는 다양한 방안을 강구하고 있습니다.
제약바이오 산업은 긴 투자기간과 높은 위험을 수반하지만, 개발에 성공할 경우 막대한 가치 창출이 가능하며, 신약 개발을 통해 국민들에게 양질의 의약품을 보급함으로써 국민의 생명 연장과 삶의 질 향상이라는 공공적 가치 달성도 가능합니다. 또한, 양질의 일자리 창출을 선도하고 있습니다. 저성장기조에 따른 제조업계 전반의 고용감축 흐름과는 달리 매년 지속적인 인력 채용으로 제약산업 종사자는 지속 증가하고 있으며, 전세계적으로 제약산업은 제조업은 물론 전 산업 평균 부가가치율을 크게 상회하고 있습니다. 이에 미국, 일본 등 주요 선진국들을 중심으로 바이오 의약품을 미래 성장 동력으로 확보하고 기술 선점을 위하여 바이오 의약품 규제 개선 및 연구개발 확대 등 다양한 정책적 지원 체계를 통해 바이오 의약품 산업 경쟁력 강화를 추진하고 있습니다.
국내 정부의 경우, 한-미 FTA 발효, 약가제도 개편 등 제약산업의 환경 악화로 2012년 제약산업 육성대책 마련 필요성이 제기되었으며, 제약산업 발전기반 조성 및 국제 경쟁력 강화를 촉진하기 위하여, 2012년 '제약산업 육성 및 지원에 관한 특별법'을 시행하였습니다. 이에 따라 2013년부터 5년 단위의 제약산업육성ㆍ지원 종합계획과 1년 단위의 제약산업육성ㆍ지원 시행계획을 수립ㆍ시행하여 세부 과제를 추진하고 있습니다.
2023년 03월에 발표한 '바이오헬스 글로벌 중심국가 도약을 위한 제3차 제약바이오 산업 육성ㆍ지원 종합계획(2023~2027년)'에 따르면, 글로벌 블록버스터급 신약 창출, 글로벌 수준의 제약바이오 기업 육성, 의약품 수출 2배 달성, 제약바이오 산업 양질 일자리 창출, 임상시험 글로벌 3위 달성을 목표로 설정하였으며, 신약 창출을 위한 R&D 투자 확대, 글로벌 수준의 규제 혁신 및 공급망 인프라 확대 등의 10대 중점 과제를 추진하겠다고 공표하였습니다.
| [제3차 제약바이오산업 육성ㆍ지원 5개년 종합계획] |
 |
|
바이오헬스 글로벌 중심국가 도약을 위한 제3차 제약바이오 산업 육성 지원 종합계획(2023~2027년) |
| 출처) 보건복지부 |
또한, 2023년 07월 산업통상자원부에서 발표한 '바이오경제 2.0 추진방향'에 따르면, 최근 세포 치료제, 유전자 치료제 등 혁신 바이오의약품이 글로벌 시장을 주도하고 있으며, 신약개발과 제조(위탁생산, CMO)간 분업화가 가속화 되고 있습니다. 또한, 바이오 빅데이터, 디지털 의료기기 등 AI 및 디지털과 바이오간의 융합이 가속화되고 있기 때문에 높은 성장 잠재력을 가지고 있다고 판단되고 있습니다.
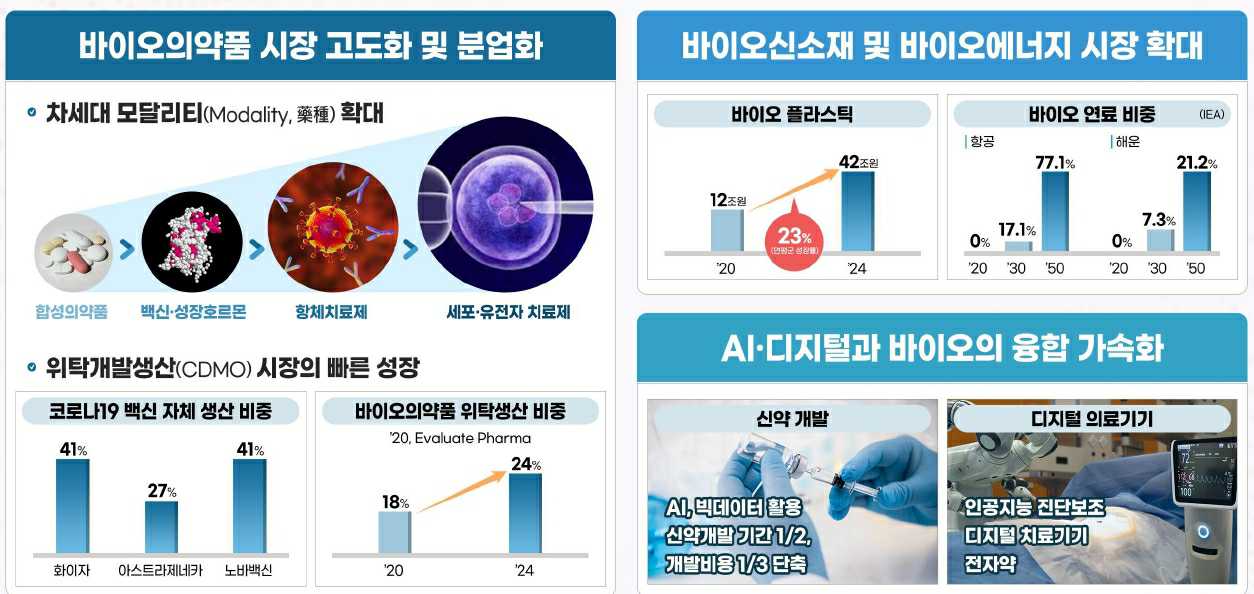 |
|
바이오경제 2.0 추진방향 -1 |
| 출처) 산업통상자원부 |
다만, 이를 뒷받침할 국내 기반은 부족한 상황이기 때문에 미래 유망 바이오 신산업을 본격적으로 육성하기 위해 2030년 바이오경제 생산 100조원, 수출 500억달러 달성을 목표로, 다음과 같이 추진방향을 공표하였습니다.
1) 바이오기업 성장 지원 및 부지, 전력, 상하수도 등의 인프라 지원 등 2030년까지 15.7조원 규모의 투자를 지원할 계획입니다. 이를 통해 바이오의약품 시장의 제조역량 강화를 지원하고, 글로벌 원부자재기업의 국내 투자유치를 통해 바이오 원부자재 국산화율 10%(2027년 달성), 15%(2030년 달성)을 목표하고 있습니다. 또한, 바이오 국가첨단전략산업 특화단지를 조성하여 한국판 보스턴 바이오 클러스터를 육성할 계획입니다.
2) 다양한 바이오신소재 제품 개발 및 원료 기술을 개발할 수 있는 산업을 육성하여 경쟁력을 키우기 위해 지원할 계획이며
3) 차세대 바이오 연료 기술 개발을 통해 친환경 바이오에너지를 상용화할 수 있는 연구 및 법령 개정을 추진할 계획입니다.
4) AI 및 디지털 전환의 가속화가 심해지고 있는 상황에서, 바이오산업과 AI, ICT 산업과의 융복합을 통해 고부가가치 창출이 가능한 생태계를 조성할 계획입니다.
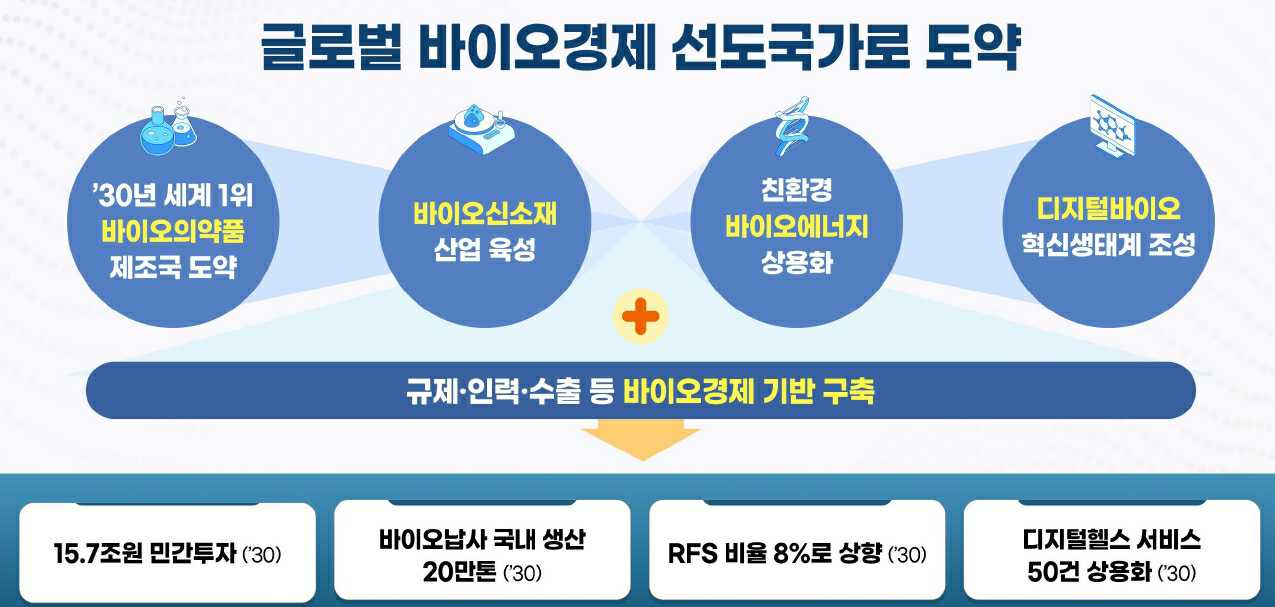 |
|
바이오경제 2.0 추진방향 -2 |
| 출처) 산업통상자원부 |
동시에, 제약바이오 산업은 인간의 생명 및 건강과 직결되는 의약품을 개발ㆍ제조ㆍ판매하는 산업으로, 제품의 개발 및 제조, 임상시험, 인허가, 유통 및 판매에 이르기까지 전 과정에 걸쳐 각 국가의 규제 당국이 제시하는 엄격한 규정과 절차를 따라야 합니다. 제약 및 신약개발 사업과 관련된 국내 법률 중 당사의 사업과 밀접하게 연관된 법률로는 식품의약품안전처 및 보건복지부 소관의「약사법」이 대표적이며, 그 외 보건복지부 소관의 「국민건강보험법」, 「생명윤리 및 안전에 관한 법률」, 「제약산업 육성 및 지원에 관한 특별법', 「희귀질환관리법」, 「첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률」과 식품의약품안전처 소관의 「실험동물에 관한 법률」 등이 있습니다.
| [제약바이오 산업 주요 유관 법률] |
| 법규 | 주요 목적 |
|---|---|
| 약사법 | - 약사(藥事)에 관한 일들이 원활하게 이루어질 수 있도록 필요한 사항을 규정하여 국민보건 향상에 기여하는 것을 목적 |
| 첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률 | - 첨단재생의료의 안전성 확보 체계 및 기술 혁신ㆍ실용화 방안을 마련하고 첨단바이오의약품의 품질과 안전성ㆍ유효성 확보 및 제품화 지원을 위하여 필요한 사항을 규정함으로써 국민 건강 및 삶의 질 향상에 이바지함을 목적 |
| 첨단재생의료 안전 및 지원에 관한 규칙 | - 「첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률」 및 같은 법 시행령에서 보건복지부령으로 정하도록 위임된 사항과 그 시행에 필요한 사항을 규정함을 목적 - 첨단재생의료기관, 안전관리기관의 운영 등에 관한 사항을 규정함 |
| 첨단바이오의약품 안전 및 지원에 관한 규칙 | - 「첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률」 및 같은 법 시행령에서 총리령으로 정하도록 위임된 사항과 그 시행에 필요한 사항을 규정함을 목적 - 첨단바이오의약품의 범위에 대한 정의, 첨단재생의료처리시설의 허가ㆍ운영에 관한 사항을 정의 |
| 국민건강보험법 | - 국민의 질병ㆍ부상에 대한 예방ㆍ진단ㆍ치료ㆍ재활과 출산ㆍ사망 및 건강증진에 대하여 보험급여를 실시함으로써 국민보건 향상과 사회보장 증진에 이바지함을 목적 |
| 생명윤리 및 안전에 관한 법률 | - 인간과 인체유래물 등을 연구하거나, 배아나 유전자 등을 취급할 때 인간의 존엄과 가치를 침해하거나 인체에 위해(危害)를 끼치는 것을 방지함으로써 생명윤리 및 안전을 확보하고 국민의 건강과 삶의 질 향상에 이바지함을 목적 |
| 제약산업 육성 및 지원에 관한 특별법 | - 제약산업의 체계적인 육성ㆍ지원과 혁신성 증진 및 국제협력 강화를 통하여 제약산업의 발전기반을 마련하고 외국 제약기업의 국내투자유치환경을 조성하여 제약산업이 국제적인 경쟁력을 갖추도록 함으로써 국민의 건강증진과 국가경제의 발전에 이바지하는 것을 목적 |
| 희귀질환관리법 | - 희귀질환의 예방, 진료 및 연구 등에 관한 정책을 종합적으로 수립ㆍ시행하여 희귀질환으로 인한 개인적ㆍ사회적 부담 감소시키고, 국민의 건강 증진 및 복지 향상에 이바지하는 것을 목적 |
| 실험동물에 관한 법률 | - 실험동물 및 동물실험의 적절한 관리를 통하여 동물실험에 대한 윤리성 및 신뢰성을 높여 생명과학 발전과 국민보건 향상에 이바지함을 목적 |
특히, 「약사법」 하위 시행령/시행규칙 중 의약품 등의 안전에 관한 규칙, 의약품 등의 제조업 및 수입자의 시설기준령 시행규칙, 생물학적 제제 등의 제조ㆍ판매관리 규칙, 동물용 의약품등 취급규칙 등과 이의 하위 규정을 준수해야 합니다. 이에 따라, 신약 후보물질의 발굴에서부터 동물을 대상으로 하는 비임상시험, 인체를 대상으로 하는 임상시험, 품목허가에 이르기까지 임상 승인에 관한 규정, 의약품의 약리 및 독성, 안정성 시험 기준, 임상시험 실시기관 지정에 관한 규정, 품목허가ㆍ심사 등의 규정 등을 반드시 준수하여 진행해야 합니다. 또한 제조 및 판매 단계에서도 제조소 시설 기준, 제조 및 품질관리 규정, 포장 및 공급에 관한 규정, 표시 등에 관한 규정을 준수해야 하며, 사후에도 정기적으로 규제기관으로부터 제품 생산 공정 및 품질관리 전반에 대한 실사 및 관리, 감독을 받게 됩니다. 이러한 규제 및 검증을 통해 제약산업의 선진화 정책을 시현할 수 있지만, 각종 규제 및 절차, 검증 강화로 인한 부담이 높아지는 경우, 당사의 사업에 부정적인 영향을 미칠 수 있습니다.
한편, 「첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률(첨단재생바이오법, 첨생법)」은 재생의료 임상연구실시 및 첨단바이오의약품 패스트트랙을 골자로 하며, 2020년 8월부터 시행된 바 있습니다. 첨단바이오의약품은 세포치료제, 유전자치료제, 조직공학제제 등 살아있는 세포ㆍ조직 또는 유전자를 원료로 제조한 의약품을 의미합니다. 첨단재생바이오법은 첨단재생의료의 안전성 확보 체계 및 기술 혁신ㆍ실용화 방안을 마련하고, 약사법, 생명윤리법 등에 산재한 바이오의약품 관련 규제를 일원화하며, 신속허가제도 도입 및 안전관리체계를 구축하는 것을 주요 목표로 하고 있습니다.
이후 첨단재생바이오법 개정안이 2024년 2월 국회 본회의를 통과하면서 2025년 2월 21일 시행되었습니다. 첨단재생바이오법 개정안은 첨단재생의료의 적용 범위를 확대하고, 관련 절차를 명확히 하여 국내 바이오 산업의 경쟁력을 강화하는 것을 목표로 하고 있습니다. 시행령 개정 이전에는 중대ㆍ희귀ㆍ난치 질환자에 한해 임상연구 목적으로만 첨단재생의료 기술을 적용할 수 있었습니다. 하지만, 개정된 첨단재생바이오법은 임상연구를 통해 안전성과 유효성이 확인된 재생의료기술을 '첨단재생의료 치료' 제도로 승인하여, 정식 허가 없이도 중대ㆍ희귀ㆍ난치 질환자 치료에 적용 할 수 있도록 허용하고 있습니다.
| [개정 첨단재생바이오법 주요 내용] |
![이미지: 개정 첨단재생바이오법 주요 내용 ['25.2.21 시행]](%EA%B0%9C%EC%A0%95%20%EC%B2%A8%EB%8B%A8%EC%9E%AC%EC%83%9D%EB%B0%94%EC%9D%B4%EC%98%A4%EB%B2%95%20%EC%A3%BC%EC%9A%94%20%EB%82%B4%EC%9A%A9%20%5B%2725.2.21%20%EC%8B%9C%ED%96%89%5D.jpg) |
|
개정 첨단재생바이오법 주요 내용 ['25.2.21 시행] |
| 출처) 보건복지부 |
개정된 첨단재생바이오법에 따라, 첨단재생의료 치료를 실시하고자 하는 의료기관은 사전에 시설, 장비 및 인력 요건을 갖춰 실시기관(재생의료기관)으로 지정 받은 후 치료계획을 마련하여 심의위원회에 심의를 신청할 수 있으며, 계획 승인 이후 해당 기관은 정해진 기간 내에 치료를 실시할 수 있게 됩니다. 또한, 재생의료기관은 치료 실시 중에는 환자 안전 확보 등을 위해 재생의료기관에 대한 정기 현황보고를 진행하고, 안전관리기관인 국립보건연구원이 이상반응 모니터링하는 등 보완 장치가 마련됩니다. 이를 통해 대체 치료제가 없는 희귀ㆍ난치 질환자에게 새로운 치료기회를 제공하여 국내에서의 희귀ㆍ난치 질환에 대한 치료 접근성을 높일 수 있게 되었습니다.
당사 주요 파이프라인 치료제의 대상 적응증인 중증아토피와 골관절염은 난치질환에 해당합니다. 첨단재생바이오법 개정안 시행을 통해 당사의 아토피 피부염 치료제(퓨어스템-에이디 주)와 골관절염 치료제(OSCA)의 환자 적용 치료 조기 실시 가능성이 생겼으며, 이와 같은 정부의 우호적인 정책은 당사의 신약 개발 사업에도 긍정적인 요인으로 작용할 것으로 기대됩니다.
| [개정 첨단재생바이오법 주요 내용] |
| 구분 | 개정 전 | 개정 후 |
|---|---|---|
| 첨단재생의료 치료 도입 | 제2조(정의) 이 법에서 사용하는 용어의 뜻은 다음과 같다. 1. “첨단재생의료”란 사람의 신체 구조 또는 기능을 재생, 회복 또는 형성하거나 질병을 치료 또는 예방하기 위하여 인체세포등을 이용하여 실시하는 세포치료, 유전자치료, 조직공학치료 등 대통령령으로 정하는 것을 말한다. 다만, 세포ㆍ조직을 생물학적 특성이 유지되는 범위에서 단순분리, 세척, 냉동, 해동 등의 최소한의 조작을 통하여 시술하는 것으로서 대통령령으로 정하는 것은 제외한다. 2. “인체세포등”이란 인체에서 유래한 줄기세포ㆍ조혈모세포ㆍ체세포ㆍ면역세포, 이종세포 등 대통령령으로 정하는 세포, 조직 및 장기를 말한다. 다만, 「인체조직안전 및 관리 등에 관한 법률」 제3조제1호에 따른 인체조직과 「장기등 이식에 관한 법률」 제4조제1호에 따른 장기등은 제외한다. 3. “첨단재생의료 임상연구”란 환자의 삶의 질 향상 및 질병 치료 기회 확대를 목적으로 사람을 대상으로 첨단재생의료에 관하여 실시하는 연구로서 다음 각 목의 구분에 따라 대통령령으로 정하는 연구를 말한다. 가. 사람의 생명 및 건강에 미치는 영향이 불확실하거나 그 위험도가 큰 임상연구 나. 사람의 생명 및 건강에 부정적인 영향을 미칠 우려가 있어 상당한 주의를 요하는 임상연구 다. 사람의 생명 및 건강에 미치는 영향이 잘 알려져 있고 그 위험도가 미미한 임상연구 4. “연구대상자”란 대체치료제가 없거나 생명을 위협하는 중대한 질환, 「희귀질환관리법」 제2조제1호에 따른 희귀질환, 그 밖에 난치질환 등을 가진 사람으로서 첨단재생의료 임상연구의 대상이 되는 사람을 말한다 5. “첨단바이오의약품”이란 「약사법」 제2조제4호에 따른 의약품으로서 다음 각 목의 어느 하나에 해당하는 것을 말한다. 가. 세포치료제: 사람 또는 동물의 살아 있는 세포를 체외에서 배양ㆍ증식하거나 선별하는 등 물리적, 화학적 또는 생물학적 방법으로 조작하여 제조한 의약품. 다만, 생물학적 특성이 유지되는 범위에서 단순분리, 세척, 냉동, 해동 등의 최소한의 조작을 통하여 제조된 것으로서 총리령으로 정하는 것은 제외한다. 나. 유전자치료제: 유전물질의 발현에 영향을 주기 위하여 투여하는 것으로서 유전물질을 함유한 의약품 또는 유전물질이 변형ㆍ도입된 세포를 함유한 의약품 다. 조직공학제제: 조직의 재생, 복원 또는 대체 등을 목적으로 사람 또는 동물의 살아 있는 세포나 조직에 공학기술을 적용하여 제조한 의약품 라. 첨단바이오융복합제제: 세포치료제, 유전자치료제, 조직공학제제와 「의료기기법」 제2조제1항에 따른 의료기기가 물리적ㆍ화학적으로 결합(융합, 복합, 조합 등을 포함한다)하여 이루어진 의약품. 다만, 주된 기능이 의료기기에 해당하는 경우는 제외한다. 마. 그 밖에 세포나 조직 또는 유전물질 등을 함유하는 의약품으로서 총리령으로 정하는 의약품 |
제2조(정의) 이 법에서 사용하는 용어의 뜻은 다음과 같다. <개정 2024. 2. 20.> 1. “첨단재생의료”란 사람의 신체 구조 또는 기능을 재생, 회복 또는 형성하거나 질병을 치료또는 예방하기 위하여 인체세포등을 이용하여 실시하는 세포치료, 유전자치료, 조직공학치료 등 대통령령으로 정하는 것을 말한다. 다만, 세포ㆍ조직을 생물학적 특성이 유지되는 범위에서 단순분리, 세척, 냉동, 해동 등의 최소한의 조작을 통하여 시술하는 것으로서 대통령령으로 정하는 것은 제외한다. 2. “인체세포등”이란 인체에서 유래한 줄기세포ㆍ조혈모세포ㆍ체세포ㆍ면역세포, 이종세포 등 대통령령으로 정하는 세포, 조직 및 장기를 말한다. 다만, 「인체조직안전 및 관리 등에 관한 법률」 제3조제1호에 따른 인체조직과 「장기등 이식에 관한 법률」 제4조제1호에 따른 장기등은 제외한다. 3. “첨단재생의료 임상연구”란 환자의 삶의 질 향상 및 질병 치료 기회 확대를 목적으로 사람을 대상으로 첨단재생의료에 관하여 실시하는 연구로서 다음 각 목의 구분에 따라 대통령령으로 정하는 연구를 말한다. 가. 사람의 생명 및 건강에 미치는 영향이 불확실하거나 그 위험도가 큰 임상연구 나. 사람의 생명 및 건강에 부정적인 영향을 미칠 우려가 있어 상당한 주의를 요하는 임상연구 다. 사람의 생명 및 건강에 미치는 영향이 잘 알려져 있고 그 위험도가 미미한 임상연구 4. “연구대상자”란 첨단재생의료 임상연구의 대상이 되는 사람을 말한다. 5. “첨단재생의료 치료”란 「의료법」 제12조에 따른 의료행위가 이루어지는 과정에서 첨단재생의료를 이용하는 의학적 치료로서 다음 각 목의 구분에 따라 대통령령으로 정하는 치료를 말한다. 가. 사람의 생명 및 건강에 미치는 영향이 불확실하거나 그 위험도가 큰 치료 나. 사람의 생명 및 건강에 부정적인 영향을 미칠 우려가 있어 상당한 주의를 요하는 치료 다. 사람의 생명 및 건강에 미치는 영향이 잘 알려져 있고 그 위험도가 미미한 치료 6. “치료대상자”란 대체치료제가 없거나 생명을 위협하는 중대한 질환, 「희귀질환관리법」 제2조제1호에 따른 희귀질환, 그 밖에 난치질환 등을 가진 사람으로서 첨단재생의료 치료의 대상이 되는 사람을 말한다. 7. “첨단바이오의약품”이란 「약사법」 제2조제4호에 따른 의약품으로서 다음 각 목의 어느 하나에 해당하는 것을 말한다. 가. 세포치료제: 사람 또는 동물의 살아 있는 세포를 체외에서 배양ㆍ증식하거나 선별하는 등 물리적, 화학적 또는 생물학적 방법으로 조작하여 제조한 의약품. 다만, 생물학적 특성이 유지되는 범위에서 단순분리, 세척, 냉동, 해동 등의 최소한의 조작을 통하여 제조된 것으로서 총리령으로 정하는 것은 제외한다. 나. 유전자치료제: 유전물질의 발현에 영향을 주기 위하여 투여하는 것으로서 유전물질을 함유한 의약품 또는 유전물질이 변형ㆍ도입된 세포를 함유한 의약품 다. 조직공학제제: 조직의 재생, 복원 또는 대체 등을 목적으로 사람 또는 동물의 살아 있는 세포나 조직에 공학기술을 적용하여 제조한 의약품 라. 첨단바이오융복합제제: 세포치료제, 유전자치료제, 조직공학제제와 「의료기기법」 제2조제1항에 따른 의료기기가 물리적ㆍ화학적으로 결합(융합, 복합, 조합 등을 포함한다)하여 이루어진 의약품. 다만, 주된 기능이 의료기기에 해당하는 경우는 제외한다. 마. 그 밖에 세포나 조직 또는 유전물질 등을 함유하는 의약품으로서 총리령으로 정하는 의약품 |
| 첨단재생의료 실시기관 | 제10조(첨단재생의료실시기관) ① 첨단재생의료 임상연구를 하려는 「의료법」 제3조에 따른 의료기관(이하 “의료기관”이라 한다)은 보건복지부장관으로부터 첨단재생의료실시기관으로 지정을 받아야 한다. ② 제1항에 따라 첨단재생의료실시기관으로 지정을 받고자 하는 자는 보건복지부령으로 정하는 시설, 장비 및 인력 등을 갖추어야 한다. ③ 제1항에 따라 첨단재생의료실시기관으로 지정을 받은 자(이하 “재생의료기관”이라 한다)는 첨단재생의료 임상연구를 하는 경우 제15조에 따른 첨단재생의료세포처리시설로부터 공급받은 인체세포등으로 첨단재생의료 임상연구를 하여야 한다.다만, 재생의료기관이 제2조제3호다목에 해당하는 첨단재생의료 임상연구를 하는 경우에는 보건복지부령으로 정하는 바에 따라 해당 재생의료기관에서 처리한 인체세포등을 이용할 수 있다. ④ 재생의료기관은 첨단재생의료 임상연구에 관한 사항을 보건복지부령으로 정하는 바에 따라 기록하여 관리ㆍ보관하고, 그 기록을 제19조에 따른 첨단재생의료안전관리기관의 장에게 보고하여야 하며, 그 밖에 대통령령으로 정하는 첨단재생의료 임상연구의 실시기준을 지켜야 한다. ⑤ 재생의료기관은 연구대상자에게 첨단재생의료 임상연구와 관련된 비용을 청구해서는 아니 된다. ⑥ 재생의료기관은 제42조에 따라 지정이 취소되는 경우 인체세포등의 처리ㆍ보관 등에 관한 사항을 보건복지부장관에게 보고하여야 한다. ⑦ 연구대상자는 자신에 관한 정보의 공개를 요청할 수 있으며, 그 요청을 받은 재생의료기관은 정당한 사유가 없으면 정보를 공개하여야 한다. ⑧ 제1항ㆍ제6항 및 제7항에 따른 재생의료기관 지정, 인체세포등의 처리ㆍ보관 등의 보고 또는 정보 공개 절차ㆍ방법 등에 필요한 사항은 보건복지부령으로 정한다. |
제10조(첨단재생의료실시기관) ① 첨단재생의료 실시를 하려는 「의료법」 제3조에 따른 의료기관(이하 “의료기관”이라 한다)은 보건복지부장관으로부터 첨단재생의료실시기관으로 지정을 받아야 한다. <개정 2024. 2. 20.> ② 제1항에 따라 첨단재생의료실시기관으로 지정을 받고자 하는 자는 첨단재생의료 임상연구 및 첨단재생의료 치료의 위험도에 따라 보건복지부령으로 정하는 시설, 장비 및 인력 등을 갖추어야 한다. <개정 2024. 2. 20.> ③ 제1항에 따라 첨단재생의료실시기관으로 지정을 받은 자(이하 “재생의료기관”이라 한다)는 첨단재생의료 실시를 하는 경우 제15조에 따른 첨단재생의료세포처리시설로부터 공급받은 인체세포등으로 첨단재생의료 실시를 하여야 한다. 다만, 재생의료기관이 제2조제3호다목에 해당하는 첨단재생의료 임상연구 또는 같은 조 제5호다목에 해당하는 첨단재생의료 치료를 하는 경우에는 보건복지부령으로 정하는 바에 따라 해당 재생의료기관에서 처리한 인체세포등을 이용할 수 있다. <개정 2024. 2. 20.> ④ 재생의료기관은 첨단재생의료 실시에 관한 사항(첨단재생의료 치료 비용에 관한 사항을 포함한다)을 보건복지부령으로 정하는 바에 따라 기록하여 관리ㆍ보관하고, 그 기록을 제19조에 따른 첨단재생의료안전관리기관의 장에게 보고하여야 하며, 그 밖에 대통령령으로 정하는 첨단재생의료 실시의 제공기준을 지켜야 한다. <개정 2024. 2. 20.> ⑤ 재생의료기관은 첨단재생의료의 안전성 확보를 위하여 제2항에 따른 재생의료기관 인력에 대하여 정기적으로 보건복지부장관이 정하는 교육을 이수하도록 하여야 한다. 이 경우 첨단재생의료 임상연구와 첨단재생의료 치료에 따라 이수기준을 달리 적용할 수 있다.<신설 2024. 2. 20.> ⑥ 재생의료기관은 연구대상자에게 첨단재생의료 임상연구와 관련된 비용을 청구해서는 아니 된다. <개정 2024. 2. 20.> ⑦ 재생의료기관은 제42조에 따라 지정이 취소되는 경우 인체세포등의 처리ㆍ보관 등에 관한 사항을 보건복지부장관에게 보고하여야 한다. <개정 2024. 2. 20.> ⑧ 연구대상자 및 치료대상자(이하 “실시대상자”라 한다)는 자신에 관한 정보의 공개를 요청할 수 있으며, 그 요청을 받은 재생의료기관은 정당한 사유가 없으면 정보를 공개하여야 한다. <개정 2024. 2. 20.> ⑨ 보건복지부장관은 제19조에 따른 첨단재생의료안전관리기관의 장에게 제4항에 따라 재생의료기관이 보고한 첨단재생의료 치료 비용에 관한 정보의 제공을 요청할 수 있다. 이 경우 첨단재생의료안전관리기관의 장은 특별한 사유가 없으면 그 요청에 따라야 한다. <신설 2024. 2. 20.> ⑩ 보건복지부장관은 제9항에 따라 제공받은 내용을 바탕으로 첨단재생의료 치료 비용 현황을 조사ㆍ분석하여 그 결과를 공개할 수 있다. <신설 2024. 2. 20.> ⑪ 제1항ㆍ제4항ㆍ제5항 및 제7항부터 제10항까지에 따른 재생의료기관 지정, 인체세포등의 처리ㆍ보관 등의 보고 또는 정보 공개 절차ㆍ방법, 재생의료기관의 첨단재생의료 치료 비용에 대한 보고, 현황조사ㆍ분석 및 결과 공개의 범위ㆍ방법ㆍ절차, 교육 이수기준 등에 필요한 사항은 보건복지부령으로 정한다. <개정 2024. 2. 20.> |
| 첨단재생의료 연구계획에 대한 심의 및 승인 | 제12조(첨단재생의료 연구계획에 대한 심의 및 승인) ① 재생의료기관이 첨단재생의료 임상연구를 하기 위해서는 대통령령으로 정하는 바에 따라 연구에 관한 실시계획(이하 “첨단재생의료 연구계획”이라 한다)을 작성하여 제13조제1항에 따른 첨단재생의료 및 첨단바이오의약품 심의위원회(이하 “심의위원회”라 한다)의 심의를 받아야 한다. ② 보건복지부장관 또는 식품의약품안전처장은 첨단재생의료 연구계획의 적합여부에 관한 심의위원회의 심의 결과를 재생의료기관에 통보하여야 하며, 적합 통보를 받은 재생의료기관은 첨단재생의료 임상연구를 할 수 있다. ③ 제1항 및 제2항에도 불구하고 제2조제3호가목에 해당하는 첨단재생의료 임상연구를 하기 위해서는 제1항에 따른 심의위원회의 심의를 거쳐 식품의약품안전처장의 승인을 받아야 한다. 이 경우 현재 이용가능한 치료법이 없거나 다른 치료법과 비교하여 현저히 효과가 우수할 것으로 예측되는 치료법에 해당하는지를 고려하여야 한다. ④ 첨단재생의료 연구계획에 대하여 심의위원회의 심의를 받은 경우에는 「생명윤리 및 안전에 관한 법률」 제10조에 따른 기관생명윤리위원회의 심의를 받은 것으로 본다. ⑤ 그 밖에 첨단재생의료 연구계획 심의ㆍ승인의 절차 및 방법 등에 필요한 사항은 대통령령으로 정한다. |
(좌동) |
| 첨단재생의료 치료계획에 대한 심의 | (신설) | 제12조의2(첨단재생의료 치료계획에 대한 심의)① 재생의료기관이 첨단재생의료 치료를 하기 위하여서는 대통령령으로 정하는 바에 따라 치료에 관한 실시계획(이하 "첨단재생의료 치료계획"이라 한다)을 작성하여 심의위원회의 심의를 받아야 한다. ② 재생의료기관은 동일한 목적 및 내용의 첨단재생의료 임상연구가 사전에 실시되어 완료된 경우에만 제2조제5호가목(동일 기관에서 임상연구를 완료한 경우에 한정한다) 또는 나목(다른 기관에서 임상연구가 완료된 경우를 포함한다)에 해당하는 첨단재생의료 치료를 할 수 있다. ③ 재생의료기관은 첨단재생의료 치료계획 적합 통보를 받은 날부터 최대 5년간 첨단재생의료 치료를 제공할 수 있으며, 제공 기간이 종료된 후에도 첨단재생의료 치료를 제공하려는 재생의료기관은 첨단재생의료 치료계획에 대하여 다시 심의를 받아야 한다. ④ 첨단재생의료 치료계획 심의 결과의 통보에 관하여는 제12조제2항을 준용한다. 이 경우 "첨단재생의료 연구계획"은 "첨단재생의료 치료계획"으로, "첨단재생의료 임상연구"는 "첨단재생의료 치료"로 본다. ⑤ 그 밖에 첨단재생의료 치료계획 심의의 절차 및 방법 등에 필요한 사항은 대통령령으로 정한다. [본조신설 2024.2.20.] |
해외 주요국 역시 재생의료의 성장 가능성에 주목하여 기존 합성의약품과 구분되는 재생의료 특성에 맞는 별도의 제도를 선제적으로 마련하고, 국가 차원의 전략적 투자를 지속 확대하고 있습니다. 각 국의 주요 제도는 다음과 같습니다.
| [해외 주요국들의 재생의료 분야 주요 제도] |
| 구분 | 내용 |
|---|---|
| 미국 | - 법령명 : 「21세기 치유법」, 「치료받을 권리법」 - 주요 내용 : 2016년 FDCA(Food, Drug, and Cosmetic Act)에 새로운 의약품 분류로 재생의료치료제(Regenerative Medicine Therapy, RMT)을 신설 : 첨단재생의료치료제(Regenerative Medicine Advanced Therapy, RMAT) 지정 제도 도입 |
| 유럽 | - 법령명 : 「Regulation 1394/2007/EC」 - 주요 내용 : 2007년 ATMP(Advanced Therapy Medicinal Product)를 정의하여 다른 생명공학 제품과 구별하고 새로운 첨단치료제들을 별도로 규제하기 시작 : 병원면제제도(Hospital Exemption)도입 |
| 일본 | - 법령명 : 「재생의료등 안전성확보등에 관한 법률」, 「의약품, 의료기기 등의 품질, 유효성 및 안전성 확보 등에 관한 법률」 - 주요 내용 : 2013년 재생의료 연구, 개발 및 실용화에 이르는 종합적인 정책을 추진하기 위해 임상연구와 자유진료를 관리하는 '재생의료법'을 제정 : 약사법의 명칭을 「의약품, 의료기기 등의 품질, 유효성 및 안전성 확보 등에 관한 법률」로 변경하고, 재생의료 제품의 정의를 새롭게 포함하도록 규정 |
| 대만 | - 법령명 : 「재생의료제재관리특별법」 - 주요 내용 : 2018년 세포치료 기술을 특별 의료기술로 정의 : 정부가 인증한 재생의료 영역의 치료기술들은 환자에게 비용을 받고 시술 가능하도록 「재생의료제재관리특별법」 제정 |
| 한국 | - 법령명 : 「첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률(첨단재생바이오법, 첨생법)」 - 주요 내용 : 첨단재생의료의 안전성 확보 체계 및 기술 혁신, 실용화 방안 마련하고 첨단바이오의약품의 품질과 안전성ㆍ유효성 확보 및 제품화 지원을 위하여 필요한 사항을 규정함으로써 국민 건강 및 삶의 질 향상 |
| 출처) 첨단재생의료포털 |
특히, 일본의 경우 2013년 11월 재생의료 특화 법률인 「재생의료 등의 안전성의 확보 등에 관한 법률(재생의료안전법)」을 제정하며 재생의료를 선제적으로 제도권 내에서 적극적으로 육성해왔습니다.
일본의 재생의료안전법에서는 재생의료를 사람의 생명 및 건강에 미치는 영향을 기준으로 위험도(총 3종)를 분류하고 그 명칭을 정했으며, 고위험 세포(역분화줄기세포 등) 치료는 '제1종', 중위험 세포(성체줄기세포 등) 치료는 '제2종', 저위험 세포(체세포 등) 치료는 '제3종' 재생의료 기술로 구분하고 있습니다. 또한, 재생의료 제공(연구, 치료) 신고 체계를 마련하고, (특정) 인정 재생의료 위원회를 설치하였으며, 의료기관이 세포배양가공을 기업에 외부 위탁할 수 있도록 허용하였습니다.
당사는 일본 재생의료시장 진출을 위해 2024년 일본 후생노동성에 제1종(동종제대혈줄기세포(를 이용한 아토피 피부염 치료)) 및 제2종(자가지방줄기세포) 재생의료 제공계획에 대한 심의 및 승인 절차를 진행하였습니다. 제2종(자가지방줄기세포)의 경우, 특정인정재생의료위원회의 심의를 거쳐 승인을 받고, 2025년 2월 후생노동성 최종 승인까지 완료되었습니다. 이에 현재 일본 내 공급을 위해 동경, 오사카, 나고야 소재의 현지 의료기관과 계약을 완료하였고, 2025년 하반기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 기존 계획으로는 2025년 2분기부터 제2종(자가지방줄기세포)의 환자 투약이 가능할 것으로 예상하였으나, 1) 당사 기존시설은 자가줄기세포가 아닌 동종줄기세포 생산에 초점이 맞춰져 있어 자가줄기세포 초도 생산 설비 및 시설 세팅 등 제반 사항 준비 과정의 지연이 있었으며, 2) 최초 투약으로 인한 환자 모객의 지연 등으로 인해 최초 환자 투약은 2025년 하반기부터 가능할 것으로 예상됩니다. 다만, 당사의 노력에도 불구하고 추가 환자 모객의 지연, 현지 상황 변동 등으로 제2종(자가지방줄기세포)의 일본 공급이 지연될 가능성이 존재하므로 투자자께서는 이 점 유의하시기 바랍니다. 한편, 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며, 후생노동성 권고사항에 따라 소규모 임상시험 진행 등을 검토 중입니다.
2024년 9월 30일 기준 일본의 재생의료 제공 계획 건수는 아래와 같으며, 합계 치료 건수는 5,888건, 합계 연구 건수는 103건으로 연구 시장에 비해 치료 시장이 활성화된 것을 확인할 수 있습니다.
| [2024년 일본 재생의료 제공 계획 건수(2024.09.30 기준)] |
| 위험도 분류 | 치료연구구분 | 건수 |
|---|---|---|
| 1종(고위험) | 치료 | 8 |
| 연구 | 11 | |
| 2종(중위험) | 치료 | 1,855 |
| 연구 | 44 | |
| 3종(저위험) | 치료 | 4,025 |
| 연구 | 48 | |
| 합계 | 치료 | 5,888 |
| 연구 | 103 |
| (출처 : 일본 후생노동성) |
국내에서 매년 2~5만 명이 일본으로 건너가 줄기세포 치료 등 재생의료를 받고 있다는 언론 보도가 이어지고 있으며, 이는 재생의료에 대한 높은 수요를 반영하는 사례입니다. 2025년 2월 첨단재생바이오법 개정을 통해 국내 기업은 임상 단계에서 환자에 대한 판매가 가능해지는 만큼 치료제 상업화 시점을 앞당기고, 해외 원정 치료를 가는 환자들은 국내에서 치료받을 수 있는 경로를 확보하게 됩니다. 따라서, 법 개정 이후 국내 역시 일본 사례와 같이 첨단재생의료 치료 시장이 활성화될 수 있을 것으로 보여집니다. 그럼에도 불구하고, 시행규칙 등 세부적인 제도 측면에서의 일부 불확실성이 존재합니다. 첨단재생의료 치료 시행을 위해서는 연구계획 및 첨단재생의료 치료 승인 등 추가 절차가 필요하나, 구체적인 심사 가이드라인은 미비한 상태입니다. 이에 따라, 제도 시행 초기 심사 지연 등에 따른 계획 승인 지연으로 치료 절차 수행 및 조기 상용화 관련 일정이 지연될 수 있습니다.
상기 언급된 바와 같이 제약바이오 산업에 대한 관심도가 증가함에 따라 정부의 우호적인 시장 정책이 다수 도입되고 있지만, 지원 정책이 이루어지지 않거나 향후 정책 기조의 변화에 따라 정부지원이 축소 또는 규제 강화 등의 대외적 변수가 발생될 수 있습니다. 이에 당사는 정책 및 규제 변화에 신속한 대응을 위한 지속적인 모니터링을 항시적으로 진행하고 있지만, 그럼에도 불구하고 각국 또는 국제기관의 정책 및 규제의 방향성, 적용시기 등의 변동 위험이 존재할 가능성이 존재함으로 당사의 줄기세포치료제 연구 개발 사업 전망에도 부정적인 영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
| 바. 화장품 산업의 경쟁 심화에 따른 위험 최근 제약기반의 신규 카테고리 형성 및 고성장 추세에 따라, 제약회사들의 화장품산업 진출 및 효능 중심의 화장품이 급부상되며, 코스메슈티컬 카테고리가 고성장세의 새로운 화장품 트렌드로 주목받고 있습니다. 진입장벽이 높지 않아 새로운 중소형 브랜드와 제품들이 꾸준히 출시되고 있으며, 경쟁이 치열해지고 있습니다. 당사의 화장품 제품은 줄기세포 배양액 기반의 제품으로, 주름 및 미백 개선 등의 기능성 화장품을 판매하고 있습니다. 당사 제품의 주요 판매 채널은 온라인 및 SNS를 활용한 인플루언서를 통한 판매이며, 제품 및 브랜드에 따라 오프라인, 홈쇼핑 등으로 넓혀 나갈 계획입니다. 다만, 소비자들의 구매 트렌드 변화에 따라 당사의 매출은 직접적인 영향을 받을 것으로 예상되며, 온라인 및 홈쇼핑 채널을 통해 제품을 판매할 시 일정 수수료를 지급하여야 하며 향후 수수료가 상승할 경우, 당사의 수익성에 부정적인 영향을 미칠 수 있습니다. 당사는 다양한 고객층의 욕구를 만족시키기 위하여 고가부터 중저가의 제품라인업을 형성하였으며, 고정비가 많이 들어가는 오프라인 유통망보다는 다양한 소비층을 만날 수 있는 온라인 유통망을 강화하고 있지만, 아직 국내 화장품 시장의 경쟁 업체들과 비교했을 때, 시장 점유율은 현저히 낮은 상태입니다. 당사의 이러한 노력에도 불구하고 화장품 산업의 성장이 정체되는 가운데, 경쟁기업수의 증가로 인한 경쟁 심화로 제품 판매가격 하락, 마케팅 비용 과다지출, 신규 제품의 판매채널에 의한 가격 및 매출 변동 위험성 등으로 판매비와 관리비 상승 가능성이 존재합니다. 차별화된 경쟁력을 확보하지 못한다면 당사의 영업실적 악화로 이어질 수 있으니 이 점 주의하시길 바랍니다. |
화장품 산업은 유행에 민감한 전형적인 트렌드 기반의 산업으로 경기변동과도 밀접한 영향을 받습니다. 최근 제약기반의 신규 카테고리 형성 및 고성장 추세에 따라, 제약회사들의 화장품산업 진출 및 효능 중심의 화장품이 급부상되며, 코스메슈티컬(Costmetic 화장품+Pharmaceutical 의약품) 카테고리가 고성장세의 새로운 화장품 트렌드로 주목받고 있습니다. 특히 당사가 보유한 첨단 바이오원료인 제대혈줄기세포배양액 함유 화장품은 대표적인 바이오 코스메슈티컬 화장품으로 인지되고 있습니다.
초기의 화장품 산업은 대형사 위주의 시장이 형성되어있었으나 OEM 및 ODM 방식의 제조 및 판매가 용이해짐에 따라 진입장벽이 높지 않아 새로운 중소형 브랜드와 제품들이 꾸준히 출시되고 있으며, 경쟁이 치열해지고 있습니다. 또한, 백화점, 브랜드샵과 같은 전통의 오프라인 유통 채널 외에도 멀티브랜드샵, H&B스토어와 같은 신규 오프라인 유통 채널이 생겨남에 따라 소비자의 다양성을 고려한 제품들이 출시되고 있습니다. 최근에는 브랜드 자사온라인몰이나 대형 온라인 쇼핑몰뿐만 아니라 개인 SNS 채널 등을 이용한 온라인 채널이 등장함에 따라 다품종 소량 생산, 급격한 트렌드 대응으로 소비자의 욕구를 만족시키는 브랜드들이 늘어나고 있습니다.
바이오 및 피부과학을 기반으로 첨단 바이오 원료를 함유한 화장품에 대한 수요는 지속적이며 안정적으로 창출될 것으로 예상되며, 타겟 수요층이 밀집한 판매채널을 확보하고 효율적인 마케팅이 진행된다면, 안정적 내수시장 확보가 가능할 것으로 전망하고 있습니다. 향후의 내수시장 및 수출 상황 등을 고려하였을 때, 지속적인 성장세를 이어갈 것으로 예상됩니다.
| [글로벌 화장품 산업 현황 및 전망] |
| 구분 | 2019년 | 2020년 | 2021년 | 2022년 | 2023년 | 2024년 | 2025년(E) | 2026년(E) | 2027년(E) | 2028년(E) |
| 시장규모 (십억 달러) |
465 | 456 | 488 | 521 | 568 | 619 | 669 | 723 | 786 | 854 |
| 증가율 (%) |
-1.9% | 7.0% | 6.8% | 9.0% | 9.0% | 8.1% | 8.1% | 8.7% | 8.7% | 8.7% |
| 출처) Euromonitor |
| [국내 화장품 산업 현황] |
| 구분 | 2019년 | 2020년 | 2021년 | 2022년 | 2023년 | 2024년 |
| 수출금액(백만달러) | 6,525 | 7,572 | 9,184 | 7,953 | 8,462 | 10,177 |
| 성장률(%) | 4.2% | 16.0% | 21.3% | -13.4% | 6.4% | 20.5% |
| 출처) 식약처, 2024 식품의약품 산업동향통계 |
식약의약품안전처에 따르면 2024년 국내 화장품 수출액은 101억 7731만달러로 전년(84억6237만달러) 대비 20.3% 증가한 성장세를 기록하였습니다. 국내 화장품 시장은 과거 아모레퍼시픽, LG생활건강 등과 같은 대형사와 토니모리, 클리오 등과 같은 중형사들이 대부분의 시장을 점유하였으나, 최근에는 중소형 인디브랜드가 소비자들의 다변화된 요구와 트렌드 변화에 빠르게 대응하며 인디 브랜드 중심으로 성장세를 보이고 있습니다.
향후 화장품 시장의 성장은 유지될 것으로 전망되지만 화장품 산업의 성장이 정체될 경우, 신규 경쟁 기업 증가에 따른 경쟁 심화로 제품 판매가격 하락 및 마케팅 비용 과다지출 등의 판매비와 관리비 상승 가능성이 존재합니다. 또한, 경쟁이 심화되는 시장에서 차별화된 경쟁력을 확보하지 못한다면 당사의 화장품 사업부분 매출에 부정적인 영향을 미칠 수 있습니다.
당사의 화장품 제품은 줄기세포 배양액 기반의 제품으로, 주름 및 미백 개선 등의 기능성 화장품을 판매하고 있습니다. 최근 인터넷, SNS 등이 활발해지면서 다양하고 스마트한 정보를 바탕으로 자신만의 화장품을 찾는 소비자층은 증가 추세에 있으며, 최근 고령화 사회 진입에 따른 시대적 요구와 더불어 아름다워지고 싶은 욕구가 점차 높아지면서 소비자들의 새로운 기대를 충족시킬 수 있는 기능성 화장품 및 코스메슈티컬로의 화장품 트렌드 변화가 나타나고 있습니다. 당사의 화장품 매출액 추이는 다음과 같습니다.
| [당사의 화장품 사업 부문 매출액 추이] |
| (단위: 백만원) |
| 구분 | 2021년 | 2022년 | 2023년 | 2024년 | 2025년 1분기 |
|---|---|---|---|---|---|
| 매출액 | 3,182 | 4,010 | 4,117 | 3,274 | 491 |
| 출처) 당사 정기보고서 제시 |
당사 제품의 주요 판매채널은 온라인 및 SNS를 활용한 인플루언서를 통한 판매이며, 제품 및 브랜드에 따라 오프라인, 홈쇼핑 등으로 판매채널을 넓혀 나갈 계획입니다. 다만, 소비자들의 구매 트렌드 변화에 따라 당사의 매출은 직접적인 영향을 받을 것으로 예상되며, 온라인 및 홈쇼핑 채널을 통해 제품을 판매할 시 일정 수수료를 지급하여야 하며, 향후 수수료가 상승할 경우 당사의 수익성에 부정적인 영향을 미칠 수 있습니다.
당사는 다양한 고객층의 욕구를 만족시키기 위하여 고가부터 중저가의 제품라인업을 형성하였으며, 고정비가 많이 들어가는 오프라인 유통망보다는 다양한 소비층을 만날 수 있는 온라인 유통망을 강화하고 있지만, 아직 국내 화장품 시장의 경쟁 업체들과 비교했을 때, 시장 점유율은 현저히 낮은 상태입니다.
당사의 이러한 노력에도 불구하고 화장품 산업의 성장이 정체되는 가운데, 경쟁기업수의 증가로 인한 경쟁 심화로 제품 판매가격 하락, 마케팅 비용 과다지출, 신규 제품의 판매채널에 의한 가격 및 매출 변동 위험성 등으로 판매비와 관리비 상승 가능성이 존재합니다. 차별화된 경쟁력을 확보하지 못한다면 당사의 영업실적 악화로 이어질 수 있으니 이 점 주의하시길 바랍니다.
| 사. 핵심연구인력유출 위험 당사가 영위하는 있는 제약바이오 산업은 높은 기술 수준과 빠른 변화로 인해 핵심연구 인력을 확보하는 것이 중요하며, 원활한 임상시험과 줄기세포치료제 생산을 위한 구체적인 노하우를 터득한 전문인력 등 인적 자원에 대한 의존도가 높은 사업입니다. 당사는 연구개발부문 산하에 우수 연구인력을 채용하여 연구개발을 진행하고 있으며, 우수 연구개발인력 확보 및 기존 인력 이탈 최소화를 위해 합리적 보상체계를 마련하고 있습니다. 그럼에도 불구하고 핵심인력의 이탈 가능성을 배제할 수는 없는 상황입니다. 특히, 경쟁 심화에 따른 당사 우수 인력 스카우트 등은 핵심기술 노하우 유출 등으로 이어질 수 있으며 이는 당사의 경쟁력을 약화시키며 지속적인 성장에 부정적인 영향을 끼칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
당사는 영위하고 있는 제약바이오 산업은 높은 기술 수준과 빠른 변화로 인하여 핵심연구 인력을 확보하는 것이 중요하며, 희귀ㆍ난치성 질환의 줄기세포치료제를 연구개발하는 바이오 벤처기업으로서 원활한 임상시험과 생산을 위한 구체적인 노하우를 터득한 전문인력 등 인적 자원에 대한 의존도가 높습니다.
당사의 연구개발 조직은 임상개발본부 산하 4개팀과 줄기세포재생의학연구소 산하 3개팀으로 구성되어 있으며, 각 조직별 업무분장은 다음과 같습니다.
| [연구개발 조직 구성] |
| 본부 | 구성 | 주 요 업 무 |
|---|---|---|
|
임상개발 본부 |
본부장 | 임상개발 총괄 |
| 임상개발팀 | 치료제별 임상시험 관리 | |
| 임상전략팀 | 신규 파이프라인 임상전략 및 임상중 및 후 데이터해석 | |
| RA팀 | 국내외 규제기관 인허가업무 | |
| 임상안전팀 | 약물 감시 | |
| 연구소 | 연구소장 | 연구소 총괄관리 |
| 연구관리팀 | 연구과제 기획 및 관리업무, 특허등록 관리 업무 등 | |
| 연구1파트 | 임상개발단계 파이프라인 연구 | |
| 연구2파트 | 세포선별, 제품제형, 생산공정 등에 관한 연구 |
| 출처) 당사 제시 |
2025년 1분기 기준 당사는 박사급 10명(연구소장 포함), 석사급 10명(임상개발본부장 포함) 등 총 26명의 연구인력을 보유하고 있습니다. 당사의 연구소 인력은 의학, 생명공학 및 수의학등을 전공한 줄기세포 전문 연구인력으로 줄기세포 및 줄기세포치료제에 대한 기초연구 및 비임상 연구분야에서 오랜 경험을 바탕으로 최신 연구동향 파악, 비임상 치료효능 및 치료기전에 대한 연구 뿐만 아니라 후속 파이프라인 기반기술 개발을 위한 신기술 발굴, 검증을 수행하고 있습니다. 당사의 연구개발 조직 구성과 연구 인력 현황은 다음과 같습니다.
| [연구개발 인력 현황] |
| (2025년 1분기 기준, 단위: 명) |
| 구 분 | 인 원 | ||||
|---|---|---|---|---|---|
| 박 사 | 석 사 | 기 타 | 합 계 | ||
| 임상개발본부 | 임상개발팀 | - | 1 | 1 | 2 |
| 임상전략팀 | 1 | - | - | 1 | |
| RA팀 | 1 | 1 | - | 2 | |
| 임상안전팀 | - | 1 | 2 | 3 | |
| 연구소 | 연구관리팀 | - | - | 2 | 2 |
| 연구1파트 | 6 | 3 | - | 9 | |
| 연구2파트 | 1 | 3 | 1 | 5 | |
| 합 계 | 9 | 9 | 6 | 24 | |
| 출처) 당사 정기보고서 제시 |
| 주) 연구소장, 임상개발본부장 미포함 |
당사의 핵심 연구인력은 연구소장 이승희, 연구1파트장 안종찬, 연구2파트장 이송 등 입니다. 연구소장은 줄기세포 분야의 활발한 연구 활동으로 다수의 논문을 출간하였습니다. 당사의 핵심 연구인력의 주요경력 및 연구실적은 다음과 같습니다.
| [핵심 연구개발인력 현황] |
| 성명 | 직급 | 담당업무 | 주요경력 | 주요 연구실적 |
|---|---|---|---|---|
| 이승희 | 연구소장 | 연구총괄 및 관리 |
해마루 동물병원 인턴수료('06~'07) 인천 노성남 동물병원 진료수의사('07) 서울대학교 수의과대학 석사 ('08~'10) 서울대학교 수의과대학 박사 ('10~'12) |
[논문] - Human umbilical cord blood-stem cells direct macrophage polarization and block inflammasome activation to alleviate rheumatoid arthritis, Cell Death Dis (2016) - DNA methyltransferase inhibition accelerates the immunomodulation and migration of human mesenchymal stem cells. Sci Rep. (2015) - miR-543 and miR-590-3p regulate human mesenchymal stem cell aging via direct targeting of AIMP3/p18. Age (Dordr). (2014) [학회발표] - Practical Cost Reduction Strategies on Mass Production of Stem Cell Therapies, 5th Annual Biologics World Korea (2016) - Possible application of stem cell and its result, 제6차 대한색소학회 및 제17차 대한코스메틱피부과학회 학술대회 (2016) |
| 안종찬 | 수석연구원 | 연구1파트장 |
서울대학교 이학박사 ('10) 식품의약품안전평가원 전문연구원('10~'11) 차의과학대학교 의생명과학과 포스닥 ('11~'14) 에이비온(주) 책임연구원 ('15) (주)엑셀세라퓨틱스 책임연구원 ('15~'17) |
[논문] - AIMP1 down-regulation restores chondrogenic characteristics of dedifferentiated/degenerated chondrocytes by enhancing TGF-β1 signal, Cell Death and Disease (2016) - Aminoacyl-tRNA synthetase interacting multi-functional protein 1 attenuates liver fibrosis by inhibiting TGFβ signaling, International journal of oncology (2016) - Transplantation of human Wharton’s jelly-derived mesenchymal stem cells highly expressing TGFβ receptors in a rabbit model of disc degeneration, Stem Cell Res Ther. (2015) [학회발표] - 탈분화 연골세포의 기능회복을 위한 유전자 조절 연구, 대한정형외과연구학회 (2014) |
| 이송 | 수석연구원 | 연구2파트장 | 고려대학교 의과대학 이학석사('05) 인하대학교 의과대학 이학박사('08) 서울아산병원 의생명연구소('13~'21) |
[ 논문 ] - Continuous Inhibition of Sonic Hedgehog Signaling Leads to Differentiation of Human-Induced Pluripotent Stem Cells into Functional Insulin-Producing β Cells. Lee S, Joo JH, Oh JY, Seo EH, Kim YH, Jun E, Shim IK, Kim SC. Stem cells international. (2021) - Long-term reversal of diabetes by subcutaneous transplantation of pancreatic islet cells and adipose-derived stem cell sheet using surface-immobilized heparin and engineered collagen scaffold. Kim YH, Ko JH, Lee S, Oh JY, Jeong GS, Park SN, Shim IK, Kim SC. BMJ Open Diabetes Res Care. (2020) - Enhanced insulin production and reprogramming efficiency of mesenchymal stem cells derived from porcine pancreas using suitable induction medium. Lee S, Moon S, Oh JY, Seo EH, Kim YH, Jun E, Shim IK, Kim SC. Xenotransplantation. (2019) - Role of High-Mobility Group Box 1 (HMGB1) in Transplantation of Rat Pancreatic Islets. Jeong S, Lee S, Mee-Lee C, Shim IK, Kim SC. Ann Transplant. (2017) - Mesenchymal Stem Cells Derived from Human Exocrine Pancreas Spontaneously Express Pancreas Progenitor-Cell Markers in a Cell-Passage-Dependent Manner. Lee S, Jeong S, Lee C, Oh J, Kim SC.Stem Cells Int. (2016) - Adult human pancreas-derived cells expressing stage-specific embryonic antigen 4 differentiate into Sox9-expressing and Ngn3-expressing pancreatic ducts in vivo. Lee S, Lee CM, Kim SC. Stem Cell Res Ther. (2016) |
| 출처) 당사 제시 |
당사는 지식과 경험이 풍부한 인력이 신약 연구개발 사업의 핵심 경쟁력이라는 사실을 인지하고 우수한 인력을 지속적으로 확보하고자 노력하고 있으며, 현재 보유하고 있는 핵심 인력을 유지하기 위하여 2011년 이후 10차에 걸쳐 부여한 주식매수선택권(발행 2년 후 행사 가능), 직무발명보상제도(출원보상, 등록보상, 공동발명자 등으로 구분), 능력에 따른 연봉제, 회사 비전 공유, 각종 복리후생제도 강화 등 합리적인 보상구조 및 애사심 고취에 힘쓰고 있으며 향후에도 이와 같은 정책을 확대할 계획입니다. 그럼에도 불구하고 불가피하게 연구개발인력의 유출이 발생할 경우 당사의 사업 수행 및 연구개발 활동에 차질이 발생하여 영업활동 및 지속적인 성장에 부정적인 영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
| 아. 지식재산권 분쟁 관련 위험 당사는 증권신고서 제출일 현재 총 303건의 지식재산권을 보유하고 있습니다. 줄기세포 사업부문은 특허권은 98건의 등록과 PCT를 포함한 110건의 출원을 합하여 총 208건이 있으며, 상표권은 등록 35건과 1건의 출원이 있습니다. 또한, 화장품 사업무문은 43건의 상표권 등록과 1건의 출원이 있으며, 2건의 디자인권을 보유하고 있습니다. 한편, 특허권 방어를 위하여 국책과제 및 IP 지원사업을 적극 활용하여 특허 선행조사 및 전략 분석을 실시하고 있습니다. 특허 조사를 통해 경쟁자 특허 분쟁 위험에 대한 분석, 현재의 기술문제 해결방안, 제품 결과물 보호 및 핵심특허 대응 전략 등 특허권 방어 전략을 지속적으로 펼쳐 가고 있습니다. 이를 위해 특허 관리 전담부서(연구관리팀)을 지정하여 일원화된 특허 관리를 체계적으로 수행하고 있습니다. 현재 당사에 대한 지식재산권 및 특허권에 대한 침해 소송을 제기할 계획이 있는 대상은 없는 것으로 파악되고 있지만, 향후에도 당사가 지식재산권 관련 소송의 대상이 되지 않을 것이라고 단언할 수 없습니다. 지식재산권 소송의 법정공방, 특허의 신청 및 관련 법률적 재판 및 행정재판 등은 막대한 비용과 시간의 소모를 야기할 수 있고 당사 기술인력 및 경영진의 상당한 시간과 노력을 소요할 수 있습니다. 지적재산권이 적절히 보호받지 못하는 상황이 발생한다면 사업 경쟁력이 약화될 수 있으며, 향후 제3자에 의하여 당사가 보유하고 있는 특허에 대한 소송 또는 기타 분쟁이 발생할 가능성을 배제할 수 없습니다. 이는 당사의 영업활동 및 손익에 부정적인 영향을 미칠 수 있습니다. |
당사가 영위하는 제약바이오 산업은 특허확보가 핵심 성공 요인으로, 특허를 확보하지 못할 경우 원천적으로 사업이 불가능하거나 특허 소유자로부터 기술이전에 대한 비용을 지불해야 합니다. 당사는 특허기간을 최대한 보호하기 위한 다양한 전략 및 정책을 도입하고 있으며, 제약사를 비롯하여 개발사들 역시 제품화 이후 자사의 특허를 보호하기 위한 전략으로 공정 특허, 제법 특허 등의 방법을 활용하고 있습니다.
당사는 증권신고서 제출일 현재 총 303건의 지식재산권을 보유하고 있습니다. 줄기세포 사업부문은 특허권은 98건의 등록과 PCT를 포함한 110건의 출원을 합하여 총 208건이 있으며, 상표권은 등록 35건과 1건의 출원이 있습니다. 또한, 화장품 사업무문은 43건의 상표권 등록과 1건의 출원이 있으며, 2건의 디자인권을 보유하고 있습니다.
| 구분 | 국내 | 해외 | PCT | 합계 | ||
| 줄기세포 사업부문 |
특허권 | 등록 | 34 | 64 | - | 98 |
| 출원 | 23 | 53 | 34 | 110 | ||
| 상표권 | 등록 | 25 | 11 | - | 35 | |
| 출원 | 1 | - | - | 1 | ||
| 디자인권 | 등록 | 5 | 3 | - | 8 | |
| 출원 | - | 4 | - | 5 | ||
| 화장품 사업부문 |
상표권 | 등록 | 24 | 19 | - | 43 |
| 출원 | - | 1 | - | 1 | ||
| 디자인권 | 등록 | 2 | - | - | 2 | |
| 출원 | - | - | - | - | ||
| 합계 | 114 | 155 | 34 | 303 | ||
| 출처) 당사 정기보고서 제시 |
1) 특허권
| 구분 | 내 용 | 권리자 | 국 가 | 출원일 | 등록일 | 적용제품 |
|---|---|---|---|---|---|---|
| 1 | ZNF281을 발현하는 제대혈 유래 만능 줄기세포의 분리방법 |
서울대학교 산학협력단 (전용실시권 : 강스템바이오텍) |
한국 | 2009.03.20 | 2010.03.23 | 줄기세포 분리배양 원천기술 |
| 2 | PCT | 2010.03.03 | 해당없음 | |||
| 3 | 미국 | 2011.09.20 | 2020.03.10 | |||
| 4 | 일본 | 2011.09.20 | 2016.09.28 | |||
| 5 | 일본 (분할 출원) |
2015.01.05 | 2016.11.11 | |||
| 6 | 중국 | 2011.10.14 | 2015.07.22 | |||
| 7 | 유럽 | 2011.10.19 | 2018.12.13 | |||
| 8 | 영국 | 2011.10.19 | 2018.12.13 | |||
| 9 | 독일 | 2011.10.19 | 2018.12.13 | |||
| 10 | 프랑스 | 2011.10.19 | 2018.12.13 | |||
| 11 | 이탈리아 | 2011.10.19 | 2018.12.13 | |||
| 12 | 스페인 | 2011.10.19 | 2018.12.13 | |||
| 13 | 네덜란드 | 2011.10.19 | 2018.12.13 | |||
| 14 | 스위스 | 2011.10.19 | 2018.12.13 | |||
| 15 | 폴란드 | 2011.10.19 | 2018.12.13 | |||
| 16 | 벨기에 | 2011.10.19 | 2018.12.13 | |||
| 17 | 러시아 | 2011.10.18 | 2014.04.10 | |||
| 18 | 말레이시아 | 2011.09.20 | 2017.02.28 | |||
| 19 | 호주 | 2011.10.18 | 2014.10.09 | |||
| 20 | 베트남 | 2011.09.20 | 2018.10.17 | |||
| 21 | 인도 | 2011.10.18 | 2019.01.01 | |||
| 22 | 인도네시아 | 2011.09.20 | 2018.05.15 | |||
| 23 | ZNF281을 발현하는 제대혈 유래 줄기세포의 대량 배양방법 |
서울대학교 산학협력단 (전용실시권 : 강스템바이오텍) |
한국 | 2009.09.14 | 2012.06.14 | 줄기세포 분리배양 원천기술 |
| 24 | 한국(분할) | 2014.04.14 | 2016.05.31 | |||
| 25 | HMGA2를 이용하여 비신경세포로부터 리프로그래밍된 유도신경 줄기 세포를 제조하는 방법 (Method for Producing Reprogrammed Induced Neural Stem Cells from Non-Neuronal Cells Using HMGA2) |
강스템바이오텍/ 서울대학교 산학협력단 |
한국 | 2014.04.04 | 2018.06.18 | 유도신경 줄기세포 |
| 26 | 호주 | 2015.10.19 | 2017.10.16 | |||
| 27 | PCT | 2014.04.04 | 해당없음 | |||
| 28 | 일본 | 2015.10.05 | 2018.03.28 | |||
| 29 | 중국 | 2015.12.04 | 2020.11.10 | |||
| 30 | 미국 | 2015.10.05 | 2022.11.29 | |||
| 31 | NOD2의 아고니스트를 처리한 줄기세포 또는 그 배양물을 포함하는 면역질환 또는 염증질환의 예방 또는 치료용 약학조성물 (Pharmaceutical Composition Comprising Stem Cells Treated with NOD2 Agonist or Culture Thereof for Prevention and Treatment of Immune Disorders and Inflammatory Diseases) |
강스템바이오텍 | 한국 | 2011.08.19 | 2015.01.02 | 아토피, 크론병 |
| 32 | PCT | 2011.08.19 | 해당없음 | |||
| 33 | 일본 | 2013.02.22 | 2015.09.11 | |||
| 34 | 중국 | 2013.03.22 | 2016.08.24 | |||
| 35 | 중국(분할) | 2016.02.23 | 2023.11.07 | |||
| 36 | 유럽 | 2013.03.21 | 2019.03.27 | |||
| 37 | 영국 | 2013.03.21 | 2019.02.14 | |||
| 38 | 독일 | 2013.03.21 | 2019.02.14 | |||
| 39 | 프랑스 | 2013.03.21 | 2019.02.14 | |||
| 40 | 이탈리아 | 2013.03.21 | 2019.02.14 | |||
| 41 | 스페인 | 2013.03.21 | 2019.02.14 | |||
| 42 | 스위스 | 2013.03.21 | 2019.02.14 | |||
| 43 | 미국 | 2013.04.09 | 2016.06.29 | |||
| 44 | 미국-CIP | 2016.08.08 | - | |||
| 45 | PI3K/AKT/GSK3 경로를 통해 성체줄기세포의 증식, 다분화능 및 재프로그래밍을 촉진하는 CD49f (CD49f Promoting Proliferation, Multipotency and Reprogramming of Adult Stem Cells through PI3K/AKT/GSK4 Pathway) |
강스템바이오텍 | 한국(분할) | 2018.10.29 | 2020.08.26 | 줄기세포 분리배양 원천기술 |
| 46 | PCT | 2011.02.18 | 해당없음 | |||
| 47 | 미국 | 2012.09.28 | 2015.09.22 | |||
| 48 | 중국 | 2012.10.18 | 2015.06.10 | |||
| 49 | 유럽 | 2012.09.18 | 2021.04.21 | |||
| 50 | 독일 | 2012.09.18 | 2021.04.21 | |||
| 51 | 영국 | 2012.09.18 | 2021.04.21 | |||
| 52 | 프랑스 | 2012.09.18 | 2021.04.21 | |||
| 53 | 말과동물 양수 유래 다분화능 줄기세포 및 그 제조방법 (Equine Amniotic Fluid-Derived Multipotent Stem Cells and a Method for Producing the Same) |
강스템바이오텍 | 한국 | 2011.09.07 | 2014.03.24 | 동물 줄기세포 |
| 54 | PCT | 2011.09.07 | 해당없음 | |||
| 55 | 일본 | 2013.03.07 | 2015.11.06 | |||
| 56 | 미국 | 2013.04.24 | 2016.03.22 | |||
| 57 | 유럽 | 2013.04.04 | 2018.08.15 | |||
| 58 | 영국 | 2013.04.04 | 2018.08.15 | |||
| 59 | 프랑스 | 2013.04.04 | 2018.08.15 | |||
| 60 | 독일 | 2013.04.04 | 2018.08.15 | |||
| 61 | 말과동물 양막-유래 중간엽 줄기세포 (Equine Amniotic Membrane-Derived Mesenshymal Stem Cells) |
강스템바이오텍 | PCT | 2012.11.22 | 해당없음 | 동물 줄기세포 |
| 62 | 한국 | 2011.11.22 | 2018.10.02 | |||
| 63 | 미국 | 2014.05.22 | 2017.05.16 | |||
| 64 | 개과동물 양막-유래 다분화능 줄기세포 (Canine Amniotic Membrane-Derived Multipotent Stem Cells) |
강스템바이오텍 | PCT | 2012.12.06 | 해당없음 | 동물 줄기세포 |
| 65 | 미국 | 2014.06.05 | 2017.09.26 | |||
| 66 | 비만세포 과립을 처리한 줄기세포 또는 그 배양물을 포함하는 면역질환 또는 염증질환의 예방 또는 치료용 약학조성물 |
강스템바이오텍 | 한국 | 2015.09.24 | 2017.08.02 | 아토피 |
| 67 | PCT | 2015.09.24 | 해당없음 | |||
| 68 | GDF11을 포함하는 조성물 및 그의 용도 | 강스템바이오텍 | 한국 | 2016.02.04 | 2017.12.13 | 화장품원료 |
| 69 | 한국(분할) | 2017.09.19 | 2018.08.24 | |||
| 70 | PCT | 2016.12.02 | 해당없음 | |||
| 71 | 망막색소상피 분화 유도용 조성물 | 강스템바이오텍/ 서울대학교 산학협력단 |
한국 | 2015.10.28 | 2019.05.21 | 안과질환 |
| 72 | SOD3를 과발현하는 줄기세포를 유효성분으로 포함하는 염증성 질환의 예방 또는 치료용 조성물 |
강스템바이오텍 | 한국 | 2016.09.19 | 2021.04.21 | 아토피, 건선 |
| 73 | PCT | 2016.09.15 | 해당없음 | |||
| 74 | 미국 | 2018.03.14 | 2023.08.22 | |||
| 75 | 미국(CA) | 2023.06.14 | - | |||
| 76 | 일본 | 2018.03.15 | 2021.12.13 | |||
| 77 | 중국 | 2018.05.14 | 2022.08.02 | |||
| 78 | 퇴행성 뇌질환을 예방, 개선 또는 치료하는 유황의 법제방법 및 상기 방법으로 법제된 유황 | 강스템바이오텍/ 원광대 산학협력단 |
한국 | 2014.10.08 | 2016.07.18 | 신경계질환 |
| 79 | 퇴행성 신경계질환에 유효한 오공을 포함하는 복합약침의 제조방법 및 상기 방법으로 제조 된 복합약침 |
강스템바이오텍/ 원광대 산학협력단 |
한국 | 2014.10.10 | 2016.09.26 | 신경계질환 |
| 80 | 뇌신경세포 보호 기능이 있는 천연물 조성물 및 그를 이용한 건강 음료 |
강스템바이오텍/ 원광대 산학협력단 |
한국 | 2014.10.08 | 2016.11.01 | 신경계질환 |
| 81 | DNA메탈기전달효소 억제제를 처리한 줄기세포 또는 그 배양물을 포함하는 면역질환 또는 염증질환의 예방 또는 치료용 약학조성물 |
강스템바이오텍 | 한국 | 2014.03.06 | 2015.04.24 | 크론병 |
| 82 | 줄기세포를 유효 성분으로 함유하는 면역질환 또는 염증 질환의 예방 또는 치료용 조성물 | 강스템바이오텍 | 한국 | 2013.02.21 | 2015.04.08 | 퓨어스템 |
| 83 | PCT | 2013.02.22 | 해당없음 | |||
| 84 | 피부세포로부터 기능성 인슐린생산 세포의 직접 제조 방법 |
강스템바이오텍/ 서울대학교 산학협력단 |
한국 | 2012.10.24 | 2015.02.02 | 당뇨병 |
| 85 | 제대혈 유래 중간엽 줄기세포의 세포외기질을 유효성분으로 함유하는 암치료용 약제학적 조성물 | 강스템바이오텍 | 한국 | 2012.06.26 | 2014.06.30 | 항암제 |
| 86 | PCT | 2011.01.13 | 해당없음 | |||
| 87 | 성체 줄기세포로부터 췌장 베타 유사세포를 제조하는 방법 |
강스템바이오텍 | 한국 | 2011.02.18 | 2013.11.25 | 당뇨병 |
| 88 | miRNA의 발현 억제를 이용한 성체줄기세포의 노화 억제방법 |
강스템바이오텍 | 한국 | 2011.03.31 | 2013.08.19 | 줄기세포 분리배양 원천기술 |
| 89 | 제대혈 또는 지방조직유래 성체줄기세포를 함유한 항암용 조성물 |
강스템바이오텍 | 한국 | 2009.04.15 | 2013.04.24 | 항암제 |
| 90 | 개의 제대혈, 태반 및 개 태아의 심장 유래 다분화능 성체줄기세포, 그 제조방법 및 이를 함유하는 세포 치료제 |
강스템바이오텍 | 한국 | 2006.05.12 | 2007.12.31 | 동물 줄기세포 |
| 91 | Oct-4, Cripto-1, ABCG2 또는 에스트로겐 수용체를 마커로 이용한 줄기세포 또는 종양줄기세포의 검출방법 및 항암물질의 스크리닝 방법 |
강스템바이오텍 | 한국 | 2006.11.28 | 2008.08.01 | 항암제 |
| 92 | 비신경 세포를 이용한 유도신경줄기세포의 제조방법 |
강스템바이오텍/ 서울대학교 산학협력단 |
한국 | 2016.05.25 | 2017.09.11 | 신경계질환 |
| 93 | PCT | 2016.05.25 | 해당없음 | |||
| 94 | 연골 무세포 파쇄물 및 줄기세포를 포함하는 연골분화 촉진용 복합체 및 그의 용도 | 강스템바이오텍 | 한국 | 2017.07.04 | 2018.09.18 | 퇴행성 관절염 |
| 95 | PCT | 2017.07.04 | 해당없음 | |||
| 96 | 일본 | 2017.07.04 | 2021.08.12 | |||
| 97 | 미국 | 2019.01.04 | - | |||
| 98 | 중국 | 2019.03.01 | - | |||
| 99 | 유럽 | 2019.01.30 | 2022.09.07 | |||
| 100 | 영국 | 2019.01.30 | 2022.09.07 | |||
| 101 | 독일 | 2019.01.30 | 2022.09.07 | |||
| 102 | 프랑스 | 2019.01.30 | 2022.09.07 | |||
| 103 | 이탈리아 | 2019.01.30 | 2022.09.07 | |||
| 104 | 스페인 | 2019.01.30 | 2022.09.07 | |||
| 105 | 네덜란드 | 2019.01.30 | 2022.09.07 | |||
| 106 | 스위스 | 2019.01.30 | 2022.09.07 | |||
| 107 | 터키 | 2019.01.30 | 2022.09.07 | |||
| 108 | 벨기에 | 2019.01.30 | 2022.09.07 | |||
| 109 | Sox2, C-myc을 이용하여 비신경 세포로부터 직접 리프로그래밍 된 유도신경줄기 세포를 제조하는 방법 |
강스템바이오텍 | 한국 | 2018.05.09 | 2020.10.14 | 신경계질환 |
| 110 | PCT | 2019.05.09 | 해당없음 | |||
| 111 | HLA 유전자가 제거된 인간 유도만능줄기세포 유래 중간엽 줄기세포 및 그의 제조방법 | 강스템바이오텍 | 한국 | 2019.05.30 | 2021.09.15 | 이식적합성 치료제개발 |
| 112 | PCT | 2019.05.30 | 해당없음 | |||
| 113 | 유럽 | 2020.12.16 | - | |||
| 114 | 미국 | 2020.11.30 | - | |||
| 115 | 효능이 증진된 줄기세포의 제조방법 | 강스템바이오텍 | PCT | 2020.12.16 | 해당없음 | |
| 116 | 미국 | 2022.06.16 | - | |||
| 117 | 유럽 | 2022.07.11 | - | |||
| 118 | 세포해동기 | 강스템바이오텍/ ㈜아모그린텍 |
한국 | 2021.06.25 | - | 세포치료제 해동기 |
| 119 | PCT | 2022.06.20 | 해당없음 | |||
| 120 | 미국 | 2023.12.25 | - | |||
| 121 | 유럽 | 2023.12.20 | - | |||
| 122 | 세포해동기 및 이의 운전방법 (1) | 한국 | 2021.07.27 | 2024.06.26 | ||
| 123 | 세포해동기 및 이의 운전방법 (2) | 한국 | 2021.07.27 | 2025.01.13 | ||
| 124 | 세포해동기 및 이의 운전방법 (3) | 한국 | 2021.07.27 | 2025.01.13 | ||
| 125 | 세포해동기 | 한국 | 2021.11.05 | - | ||
| 126 | 한국 | 2021.11.05 | - | |||
| 127 | 한국 | 2021.11.05 | - | |||
| 128 | 세포해동기 및 이의 운전방법 | PCT | 2022.06.20 | 해당없음 | ||
| 129 | 미국 | 2023.12.25 | - | |||
| 130 | 유럽 | 2023.12.20 | - | |||
| 131 | 세포해동기 및 이의 운전방법 | PCT | 2022.06.20 | 해당없음 | ||
| 132 | 미국 | 2023.12.25 | - | |||
| 133 | 유럽 | 2023.12.20 | - | |||
| 134 | 세포해동기 및 이의 운전방법 | PCT | 2022.06.20 | 해당없음 | ||
| 135 | 미국 | 2023.12.25 | - | |||
| 136 | 유럽 | 2023.12.20 | - | |||
| 137 | off-the-shelf 줄기세포 및 면역세포, 이를 포함하는 약학적 조성물 |
강스템바이오텍 | 한국 | 2020.01.23 | 2024.06.04 | 혈액암 |
| 138 | PCT | 2021.01.22 | 해당없음 | |||
| 139 | 미국 | 2021.01.22 | - | |||
| 140 | 일본 | 2021.01.22 | - | |||
| 141 | 중국 | 2021.01.22 | - | |||
| 142 | 유럽 | 2021.01.22 | - | |||
| 143 | 주입이 가능한 동물 연골유래 주사제의 제조 방법 및 이의 이용 |
강스템바이오텍 | 한국 | 2021.11.26 | - | 퇴행성 관절염 |
| 144 | PCT | 2021.11.26 | 해당없음 | |||
| 145 | 유럽 | 2023.06.23 | - | |||
| 146 | 미국 | 2023.03.10 | - | |||
| 147 | 중국 | 2023.05.26 | - | |||
| 148 | 일본 | 2023.05.26 | - | |||
| 149 | 일본(분할) | 2025.02.07 | - | |||
| 150 | 호주 | 2023.06.27 | - | |||
| 151 | 강스템바이오/에이템즈㈜ | 한국(분할) | 2023.04.10 | - | ||
| 152 | 미국(분할) | 2023.06.13 | - | |||
| 153 | 중국(분할) | 2023.08.04 | - | |||
| 154 | 유럽(분할) | 2023.07.03 | - | |||
| 155 | 칼시뉴린 억제제와 줄기세포를 사용하여 면역질환을 치료하는 방법 |
강스템바이오텍 | 한국 | 2022.08.19 | - | 줄기세포 제조기술 |
| 156 | PCT | 2022.08.19 | 해당없음 | |||
| 157 | 미국 | 2024.02.13 | - | |||
| 158 | 중국 | 2024.03.20 | - | |||
| 159 | 일본 | 2024.02.19 | - | |||
| 160 | 유럽 | 2024.02.27 | - | |||
| 161 | 만능성 줄기세포 유래 피부 오가노이드를 이용한 아토피 피부염 모델 제작 방법 |
강스템바이오텍 | 한국 | 2021.10.20 | 2025.02.04 | 이식적합성 치료제개발 |
| 162 | PCT | 2021.10.21 | 해당없음 | |||
| 163 | 미국 | 2023.04.19 | - | |||
| 164 | 호주 | 2023.04.19 | - | |||
| 165 | 일본 | 2023.04.20 | - | |||
| 166 | 중국 | 2023.04.20 | - | |||
| 167 | 유럽 | 2023.04.21 | - | |||
| 168 | 한국 | 2024.09.12 | - | |||
| 169 | 앱타머를 이용한 고기능성 인공장기 제작 방법 | 강스템바이오텍 | 한국 | 2020.11.12 | - | 이식적합성 치료제개발 |
| 170 | 한국(분할) | 2024.03.20 | - | |||
| 171 | 한국(분할) | 2024.07.02 | - | |||
| 172 | PCT | 2021.07.27 | 해당없음 | |||
| 173 | 유럽 | 2023.03.03 | - | |||
| 174 | 호주 | 2023.02.02 | 2024.09.26 | |||
| 175 | 미국 | 2023.02.03 | - | |||
| 176 | 일본 | 2023.02.06 | - | |||
| 177 | 일본(분할) | 2025.03.05 | - | |||
| 178 | 중국 | 2023.02.06 | - | |||
| 179 | 무혈청배지를 이용한 줄기세포 배양 방법 | 강스템바이오텍 | 한국 | 2023.02.27 | - | 줄기세포 제조기술 |
| 180 | PCT | 2023.02.27 | 해당없음 | |||
| 181 | 미국 | 2024.08.23 | - | |||
| 182 | 유럽 | 2024.09.24 | - | |||
| 183 | 일본 | 2024.08.26 | - | |||
| 184 | 중국 | 2024.08.26 | - | |||
| 185 | 마이크로캐리어를 이용한 줄기세포 배양 방법 | 강스템바이오텍 | 한국 | 2023.02.27 | - | 줄기세포 제조기술 |
| 186 | PCT | 2023.02.27 | 해당없음 | |||
| 187 | 미국 | 2024.08.23 | - | |||
| 188 | 유럽 | 2024.09.24 | - | |||
| 189 | 일본 | 2024.08.26 | - | |||
| 190 | 중국 | 2024.08.26 | - | |||
| 191 | 면역질환 또는 염증질환 치료용 조성물 | 강스템바이오텍 | 한국 | 2019.12.26 | - | |
| 192 | 정적 부유 배양법을 이용한 췌도 오가노이드의 제조방법 |
강스템바이오텍 | 한국 | 2023.10.11 | - | |
| 193 | PCT | 2023.12.20 | 해당없음 | |||
| 194 | 연골 분화능이 증진된 줄기세포의 선별 방법 및 이를 포함하는 세포 치료제 |
강스템바이오텍 | 한국 | 2023.12.22 | - | 줄기세포 제조기술 |
| 195 | PCT | 2023.12.22 | 해당없음 | |||
| 196 | 프라이밍 중간엽 줄기세포를 유효성분으로 포함하는 급성 호흡곤란 증후군 예방 또는 치료용 조성물 | 강스템바이오텍 | 한국 | 2024.11.07 | - | ARDS |
| 197 | 강스템바이오텍 | PCT | 2024.11.07 | 해당없음 | ||
| 198 | 모낭 오가노이드 제작 및 배양방법과 이를 이용한 모발 약물 스크리닝 방법 및 모발 이식 소재 | 강스템바이오텍 | 한국 | 2024.03.18 | - | |
| 199 | PCT | 2024.03.18 | 해당없음 | |||
| 200 | 피부 손상 오가노이드 모델 및 이를 이용한 약물 스크리닝 방법 |
강스템바이오텍 | 한국 | 2024.10.04 | - | |
| 201 | 강스템바이오텍 | PCT | 2024.10.08 | 해당없음 | ||
| 202 | 강스템바이오텍 | 미국 | 2024.11.28 | - | ||
| 203 | 라파마이신을 함유 약물 전달체가 접합된 줄기세포 및 이의 용도 | 부산대산단, 성균관대산단, 강스템바이오텍 | 한국 | 2024.05.10 | - | |
| 204 | 미국 | 2025.02.18 | - | |||
| 205 | 피부 오가노이드를 이용한 의료/미용기기 유효성 평가 모델 및 평가 방법 | 강스템바이오텍 | 한국 | 2024.11.28 | - | |
| 206 | 무릎 골관절염 환자에서 동종 제대혈 유래 중간엽 줄기세포(OSCA)의 관절내 주입을 이용한 1상 연구 | 강스템바이오텍 | 한국 | 2024.11.29 | - | |
| 207 | 액티빈 A를 분비하는 중간엽 줄기세포를 포함하는 M1 대식세포의 활성 또는 분화 억제 및 M2 대식세포로의 분화 유도용 조성물 | 강스템바이오텍 | 한국 | 2025.01.24 | - | |
| 208 | PCT | 2025.01.24 | 해당없음 |
2) 디자인권
| 구분 | 내 용 | 권리자 | 국 가 | 출원일 | 등록일 | 적용제품 |
| 1 | 실험실용 트레이 | 강스템바이오텍 | 한국 | 2020.03.24 | 2020.11.12 | 퓨어스템 |
| 2 | 바이알병 보관용 박스 | 강스템바이오텍 | 한국 | 2020.03.24 | 2021.01.07 | 퓨어스템 |
| 3 | 헤이그 | 2022.09.06 | - | |||
| 4 | 일본 | 2022.08.19 | 2023.10.10 | |||
| 5 | 2023.11.07 | |||||
| 6 | 미국 | 2022.08.19 | 2024.12.17 | |||
| 7 | 독일 | 2022.08.19 | - | |||
| 8 | 영국 | 2022.08.19 | - | |||
| 9 | 싱가포르 | 2022.08.19 | - | |||
| 10 | 베네룩스(벨기에, 네덜란드, 룩셈부르크) | 2022.08.19 | - | |||
| 11 | 바이알병 보관용 박스 | 강스템바이오텍 | 한국 | 2021.01.15 | 2022.01.18 | 퓨어스템 |
| 12 | 바이알병 보관용 박스(64 셀박스) | 강스템바이오텍 | 한국 | 2020.08.11 | 2021.10.27 | 퓨어스템 |
| 13 | 실험용 플로팅 바이알 랙 | 강스템바이오텍 | 한국 | 2020.08.11 | 2021.06.04 | 퓨어스템 |
한편, 당사는 증권신고서 제출일 현재 총 303건의 지식재산권을 보유하고 있으며, 각 분야별 전문 업체로 특허 내용에 맞게 선별하여 평균 매년 5건 이상 특허 출원을 진행하고 있습니다. 특허권 방어를 위하여 국책과제 및 IP 지원사업을 적극 활용하여 특허 선행조사 및 전략 분석을 실시하고 있습니다.
| [당사의 IP 지원사원 내역] |
| 부처명 | 사업명 | 지원기간 | 지원금 |
|---|---|---|---|
| 특허청 | IP-R&D 전략지원 사업 | 2018.05 ~ 2018.08 | 60백만원 |
| 특허청 | IP-R&D 전략지원 사업 | 2019.02 ~ 2019.07 | 80백만원 |
| 특허청 | 2020년 IP-R&D 전략지원 사업 |
2020.04 ~ 2020.09 | 96백만원 |
| 특허청 | IP-R&D 후속지원 특허컨설팅 | 2020.11 ~ 2020.12 | 16.5백만원 |
| 특허청 | 2021년 상반기 IP-R&D 전략지원 사업 | 2021.03 ~ 2021.09 | 84백만원 |
| 한국무역협회 | 2024년 비관세장벽 대응 지원사업 | 2024.07 ~ 2024.12 | 5백만원 |
| 서울대학교 산학협력단 | 기술이전사업화 실용화 고도화 지원사업 | 2024.12 ~ 2025.01 | 20백만원 |
| 출처) 당사 제시 |
특허 조사를 통해 경쟁자 특허 분쟁 위험에 대한 분석, 현재의 기술문제 해결방안, 제품 결과물 보호 및 핵심특허 대응 전략 등 특허권 방어 전략을 지속적으로 펼쳐 가고 있습니다. 이를 위해 특허 관리 전담부서(연구관리팀)을 지정하여 일원화된 특허 관리를 체계적으로 수행하고 있습니다.
증권신고서 제출 전일 현재 당사에 대한 지식재산권 및 특허권에 대한 침해 소송을 제기할 계획이 있는 대상은 없는 것으로 파악되고 있지만, 향후에도 당사가 지식재산권 관련 소송의 대상이 되지 않을 것이라고 단언할 수 없습니다. 지식재산권 소송의 법정공방, 특허의 신청 및 관련 법률적 재판 및 행정재판 등은 막대한 비용과 시간의 소모를 야기할 수 있고 당사 기술인력 및 경영진의 상당한 시간과 노력을 소요할 수 있습니다.
당사가 보유하고 있는 지적재산권이 적절히 보호받지 못하는 상황이 발생한다면 사업 경쟁력이 약화될 수 있으며, 향후 제3자에 의하여 당사가 보유하고 있는 특허에 대한 소송 또는 기타 분쟁이 발생할 가능성을 배제할 수 없습니다. 이는 당사의 영업활동 및 손익에 부정적인 영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
| 자. 기술이전 지연 및 실패에 따른 위험 당사와 같은 세포치료제 등 신약개발전문 기업은 대규모 자금이 소요 되는 임상 과정, 다년간의 개발 기간 등의 리스크 분산을 위해 대형제약사 등을 대상으로 기술이전을 통해 조기에 수익을 시현하고 비용 부담을 경감하는 전략을 펼치고 있습니다. 당사는 3건의 라이센스아웃 계약을 체결하였으나, 퓨어스템 에이디주 품목에 대한 현대바이오랜드 와의 라이선스아웃 계약은 3상 임상 결과에서 유효성 차이를 입증하지 못하며 2024년 11월부로 해지되었습니다. 해당 계약 해지에 따라, 지급 받았던 선급기술료 50억은 반환 완료하였습니다. 이처럼 라이선스 아웃 계약이 이루어지더라도, 계약 후 개발 진행 단계가 더디거나, 계약 당시 예상치 못했던 사유 등으로 인해 해지될 수 있는 성격을 가지고 있습니다. 당사가 2024년 11월에 맺은 OSCA의 유영제약 라이센스 아웃 계약의 경우, 통상적인 경우와 다르게 1상에서 진행되었으며 이는 계약 상대방인 유영제약은 정형외과 분야에서 300억 가량의 매출을 발생하고 있는 관절염에 대해 이해가 높은 중견제약사라는 점과, 2b상 이후 유영제약의 임상비용 부담으로 많은 비용이 절감이 가능하고, 동시에, 현재 국내 기술이전을 바탕으로 해외 파트너와의 글로벌 기술이전을 체결하는데 유리한 장점 때문입니다. 또한, 유영제약 입장에서도, 비임상 동물실험과 임상1상 시험 단계에서 당사의 OSCA 통증 감소 및 기능 개선, 연골재생 효과까지 확인하여 근본적인 골관절염 치료제(DMOAD)로서의 가능성을 확인하여 계약을 체결하게 되었습니다. 한편,해당 계약은 선급금에 대한 반환 조건이 없습니다. 한편, 당사는 2023년 유상증자 및 2024년 12월 공시한 합병 증권신고서 당시 계획했던 기술이전 일정이 현재 전반적으로 지연되고 있습니다. 당사는 상기 개발 중인 파이프라인의 기술이전을 위해 노력함에도 불구하고 당사가 보유한 파이프라인의 향후 기술개발이 지연되거나 중단되어 추가 기술이전이 발생하지 않거나, 기술개발이 성공해도 잠재 기술이전 파트너사의 협의가 원활하지 않아 기술이전 계약이 지연되거나 실패할 경우에는 당사의 수익성이 악화되거나 사업에 부정적 영향을 줄 수 있습니다. 투자자 여러분들께서는 이 점을 반드시 유의하여 주시기 바랍니다. |
당사와 같은 세포치료제 등 신약개발전문 기업은 일반적으로 대규모 자금이 소요 되는 임상 과정, 다년간의 개발 기간 등의 리스크 분산을 위해 대형제약사 등을 대상으로 기술이전을 통해 조기에 수익을 시현하고 비용 부담을 경감하는 전략을 펼치고 있습니다. 일반적으로 바이오 신약 파이프라인 기술 이전 시, 기술이전의 대가로 초기 계약금을 수령하게 되며, 이후에는 임상 및 허가 단계 성공마다 마일스톤 수입이 발생하고, 경우에 따라 신약 발매 후 매출액의 일정 비율에 해당하는 로열티 수입, 특정 금액 이상의 매출 발생 시 지급되는 마일스톤 수입 등을 수령하게 됩니다.
기술이전이란 개발된 기술을 계약 파트너에게 이전하여 해당기술의 독점실시권을 허락하는 것으로, 일반적으로 기술을 이전할 때는 계약 파트너가 해당 기술을 활용하여제품을 개발하고 판매할 수 있는 권리도 이전하게 됩니다. 이 과정에서 기술을 이전한 바이오 기업은 계약 조건에 따라 계약체결 직후 선수금, 향후 일정 개발 단계의 달성 시점에 따라 중도금 및 완제 의약품의 시장 출시 후 판매대금의 일정비율을 지급받는 로열티를 지급받고, 이러한 기술료 수입이 바이오 기업들의 주요 수익원이라 할 수 있습니다. 따라서, 기술이전 계약 시점 이후에 이루어지는 임상 개발, 품목 허가 및 판매 등의 업무는 기술이전 대상 회사의 역량에 따라 좌우된다고 볼 수 있습니다. 특히 대규모 비용이 요구되는 임상 3상 단계부터는 글로벌 제약사와의 파트너쉽 또는 기술 이전을 통하여 자금을 확보하는 것이 필요합니다.
라이센스 거래는 제약기업간 전략적 제휴의 대표적인 형태 중 하나로 최근 건수가 감소하고 있으나 거래규모는 확대되고 있습니다. 양질의 기술을 보유했으나 자금력과 경험 부족 등으로 높은 임상비용을 감당하기 어려운 소규모 업체는 라이센싱 아웃(기술이전)을 통해 각종 기술료를 받음으로써 회사 재무구조 개선에 활용하고 있습니다. 라이센싱 아웃은 Upfront fee(초기계약금), Milestone(개발단계별 기술료), Running Royalty(매출의 일정 비중을 로열티로 지급) 등의 기술료 수익이 발생하게 됩니다. 반대로 라이센싱 인을 하는 기업은 오랜 기간이 소요되는 연구 단계를 거치지 않고 양질의 기술을 신속하게 확보함으로써 신약개발의 효율성 제고가 가능합니다. 라이센스 거래는 다양한 파이프라인을 보유 목적 외에 파이프라인 독점 수단으로도 활용되고 있습니다.
| [2023년 글로벌 빅파마 병증 및 치료방법별 라이센싱 규모] |
| (단위 : 십억 달러) |
|
| 출처) JP Morgan(2023 Annual Biopharma Licensing and Venture Report, 2023년 12월) |
질환영역별로는 종양, 중추신경계, 심혈관 질환 순으로 라이센스 거래가 이루어지고 있으며, 임상단계별로 글로벌 라이센스 거래를 살펴본 결과 2008~2023년간 물질 발견단계 및 전임상 단계에서의 거래건수와 규모가 모두 높게 나타나고 있습니다.
| [글로벌 빅파마 라이센싱 시기 추이] |
|
| 출처) JP Morgan(2023 Annual Biopharma Licensing and Venture Report, 2023년 12월) |
일반적으로 기술이전이 이루어지게 되면, 추가개발은 라이선스인을 한 기업에서 진행하며 계약에 따라 별도로 추가개발을 진행할 수도 있습니다. 라이선스인한 기업에서는 추가개발 상황 및 임상시험 결과에 따라 마일스톤 및 로열티를 지급하게 되는데 이러한 수익구조는 다음과 같이 정리할 수 있습니다.
| [라이센스 계약 수익 구조] |
| 구분 | 내용 | |
|---|---|---|
| 총 계약금액 | 계약금 | - 계약 체결 직후 또는 일정기간 내에 받게 되는 금액 |
| 마일스톤 | - 전임상, 임상, 허가신청, 허가완료 등 개발 단계별로 성공시 받게 되는 금액 | |
| 로열티 | - 기술 이전으로 생산된 제품의 매출에 따라 받게 되는 금액(통상 매출액 대비 비율로 책정) | |
| 출처) 금융감독원 보도자료 "제약ㆍ바이오 기업의 공시실태 및 투자자 보호방안"(2018.08) |
계약금은 계약 직후 수령하게 되는데, 계약조건에 따라 반환의무가 있을 수 있습니다. 마일스톤의 경우 추가개발 진행상황에 따라 수취하게 되는 금액이며, 로열티는 최종 허가 이후 해당 제품이 매출을 발생시킬 경우 받게 되는 수수료입니다.
당사 역시 임상 또는 전임상 단계에서 기술이전을 성공시켜 기술이전 관련 수익을 최대화하고 이후 계약상대방인 제약사가 제품을 판매함에 따른 로열티 수익을 추가 수령하는 전략을 취하고 있습니다. 당사는 증권신고서 제출일 현재까지 총 3건의 라이선스아웃 계약을 체결하였으나, 퓨어스템-에이디주 품목에 대한 SK바이오랜드 와의 라이선스아웃 계약은 2024년 11월부로 해지되었습니다.
| [라이센스아웃 계약 총괄표] |
| (단위: 억원) |
| 품목 | 계약상대방 | 대상지역 | 계약체결일 | 계약종료일 | 총 계약금액 | 수취금액 | 진행단계 |
| 퓨어스템 -에이디 주 |
SK바이오랜드(주) (대한민국) *주1) |
국내 | 2019.03.25. | 2024.11.18 | 150 (로열티 별도) |
50 | 국내 3상 종료 국내 1/2a (반복투여)변경신청 *주2) |
| Car-T 기술 (암질환군 한정) |
마루테라퓨틱스(주) (대한민국) |
국내, 국외 |
2021.04.16. | 계약기술 특허존속기간 만료일까지 |
*주3) | *주3) | 기술이전 완료 |
| OSCA(구. 퓨어스템-오에이 키트 주) | (주)유영제약 (대한민국) |
국내 | 2024.11.07 | 품목허가일로부터 10년째 되는 해의 12월 말 | 140 (로열티 별도,임상2b 및 3상 비용 유영제약 부담) |
20 | 국내 1/2a상 진행중 |
| 합 계 | *주3) | *주3) | - | ||||
| 출처) 당사 제시 |
| *주1) | 사명 변경 SK바이오랜드 → 현대바이오랜드 2024년 11월 18일자로 (주)현대바이오랜드로부터 계약해제 통고를 받아 계약이 해제되었습니다. |
| *주2) | 반복투여 임상으로 2024년 11월 1/2a 임상시험 변경승인 신청하였으며, 2025년 4월 자진취하 하였습니다. 2025년 4월 30일 식약처에 자료를 보완하여 변경승인 신청 하였습니다. |
| *주3) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
가) 퓨어스템-에이디 주(아토피 피부염)
| 계약상대방 | - SK바이오랜드(주) (대한민국) *주1) |
| 계약내용 | - 제대혈유래줄기세포치료제(적응증:아토피 피부염)의 국내 독점판매권/통상 실시권 설정 및 기술전수 계약 |
| 대상지역 | - 대한민국 |
| 계약기간 | - 계약체결일 : 2019.03.25. - 계약종료일 : 2024.11.18. |
| 총 계약금 | - 선급기술료 : 150 억원 (경상기술료는 미공개) |
| 수취금액 | - 50 억원 (반환완료 *주3) |
| 계약조건 | - 계약제품에 대한 국내 독점판매권을 현대바이오랜드(구.SK바이오랜드)에 허여함 - 국내 통상실시권 부여 및 기술 전수 - 계약기술 : 당사 보유의 특허권 4건 및 노하우 - 전수시기 : 제품 품목허가 승인 후 현대바이오랜드(구.SK바이오랜드)가 공정 설계 및 투자를 준비하는 시점 - 선급기술료는 총 150억원으로 분할 수령함 1) 계약체결일로부터 15일 이내 50억원 2) 품목허가 후 2년 이내 계약상대방과 협의하에 완제품 협의수량 이상을 연속 생산하고 연속생상된 완제품의 제품공급가 평균값이 vial당 협의된 가격이하가 되는 것을 양사가 확인한 날로부터 90일 이내 20억원 *주2) 3) 현대바이오랜드(SK바이오랜드)가 판매개시 이후 누적판매량이 협의된 수량을 초과한 날로부터 90일 이내 30억원 4) 본 계약에 따라 Know-how 기술전수 요청일로부터 90일 이내 30억원 5) 본 계약에 따라 Know-how 기술전수 종결일로부터 90일 이내 20억원 - 계약제품의 생산은 양사가 공동 협력하며, 당사는 3만 바이알 이내 물량에 대한 제품공급의무를 갖고 있음 |
| 회계처리방법 | - 계약금(Upfront payment) : 라이선스 제공에 대해서는 라이선스 제공과 제품 공급 의무를 단일의 수행의무로 회계처리하며 제품 공급 기간에 걸쳐 수익을 인식하고, 제품의 Know-how 기술이전과 관련 된 수행의무에 대해서는 기술전수가 완료되는 시점에 일시에 수익을 인식 |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 아토피 피부염) - 계약기술 특허는 다음과 같습니다. (1) ZNF281을 발현하는 제대혈 유래 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195호) (2) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량 배양방법(대한민국 특허 등록 제10-1158664호) (3) Isolating Method for Umbilical Cord Blood-Derived Pluripotent Stem Cells Expressing ZNF281(PCT/KR2010/001338) (4) 줄기세포를 유효성분으로 함유하는 면역질환 또는 염증질환의 예방 또는 치료용 조성물(대한민국 특허등록 제10-1512171호) |
| 개발 진행경과 |
- 2013년 퓨어스템-에이디 주 1/2a상 임상시험계획 식약처 승인 - 2015년 1/2a상 임상시험 종료 (2018년 장기추적관찰 종료) - 2017년 3상 임상시험계획 식약처 승인 |
| 기타사항 | 해당 계약에 대하여 (주)현대바이오랜드로부터 2024년 11월 18일 계약해제를 통고 받아 계약이 해제되었습니다. |
| *주1) | 사명 변경 SK바이오랜드 → 현대바이오랜드 |
| *주2) | 2020.12.10 지급조건 변경 |
| *주3) | 2024년 11월 18일 계약해제되었으며, 이에 당사는 ㈜현대바이오랜드로부터 수령한 선급기술료 50억원을 반환하였습니다. 해당 선급기술료는 회계 계정 상 선수수익으로 처리했다가 계약부채로 변경한 후 현대바이오랜드에 반환 후 계약부채에 대한 역분개 처리하였습니다. 이에 관련 분개로 손익에 미치는 영향은 없었습니다. |
| 출처) 당사 공시보고서 |
나) Cart-T 기술(암질환군 한정)
| 계약상대방 | - 마루테라퓨틱스(주) (대한민국) |
| 계약내용 | - Car-T 기술(암질환군에 한정)에 대한 전용실시권 부여하는 기술이전계약 |
| 대상지역 | - 국내 및 국외 |
| 계약기간 | - 계약체결일 : 2021.04.16. - 계약종료일 : 대상기술 특허 존속기간 만료시까지 |
| 총 계약금 | - *주) |
| 수취금액 | - *주) |
| 계약조건 | * 계약조건은 영업비밀로 자세한 기재는 생략하며, 대략적인 내용은 다음과 같습니다. - 계약금은 ** 원이며 반환의무가 없음 - 1차선정 파이프라인은 두가지로 하며 단계별 기술료는 각각 **원으로 최대 **원 - 향후 제품 생산시 당사에게 CMO생산 위탁 |
| 회계처리방법 | - 계약금 수취액은 계약 조건에 따라 일시에 수익 인식 |
| 대상기술 | - Car-T 기술(대상 적응증 : 암질환군) - 계약기술 특허는 다음과 같습니다. * off-the-shelf 줄기세포 및 면역세포, 이를 포함하는 약학적 조성물 (출원번호 제10-2021-0009773호) 외 1건 |
| 개발 진행경과 | - 2021년 기술이전 완료 |
| 기타사항 | - |
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
| 출처) 당사 공시보고서 |
다) OSCA(구. 퓨어스템-오에이 키트 주, 골관절염)
| 계약상대방 | - (주)유영제약 (대한민국) |
| 계약내용 | - 무릎골관절염치료제(OSCA(구. 퓨어스템-오에이 키트 주)) 공동개발 및 국내 독점판매권·통상실시권에 대한 라이선스 계약 체결 |
| 대상지역 | - 국내 |
| 계약기간 | - 계약체결일 : 2024.11.07. - 계약종료일 : 품목허가일로부터 10년째 되는 해의 12월 말 |
| 총 계약금 | - 선급기술료: 140억원 |
| 수취금액 | - 20억원 |
| 계약조건 | - 무릎골관절염치료제(OSCA(구. 퓨어스템-오에이 키트 주))의 공동개발 포함 국내 독점판매권·통상실시권에 대한 라이선스 계약 - 총계약금액 : 140억원 1) 경상기술료 1차 : 20억원 (계약체결시) 2) 경상기술료 2차 : 30억원 (국내 공동개발사 선정시 또는 2026년 말 중 빠른 시점) 3) 경상기술료 3차 : 30억원 (유영제약 또는 공동개발사 첫번째 IND 승인시(2b상 또는 통합 임상 2상)) 4) 경상기술료 4차 : 30억원 (유영제약의 3상 임상 IND 승인시) 5) 경상기술료 5차 : 30억원 (유영제약의 품목허가 취득시) - 로열티 별도지급 (시판 후 12개월 간 발주수량에 따라 합의된 금액 수령) - 조건부 허가로 임상3상 진행시 합의된 금액 수령 |
| 회계처리방법 | - 경상기술료 수취액은 계약 조건에 따라 일시에 수익 인식 |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 아토피 피부염) - 계약기술 특허는 다음과 같습니다. (1) 연골 무세포 파쇄물 및 줄기세포를 포함하는 연골분화 촉진용 복합체 및 그의 용도(대한민국 특허 등록 제10-1901568호) (2)연골 분화능이 증진된 줄기세포의 선별 방법 및 이를 포함하는 세포 치료제(대한민국 특허 출원 제10-2023-0189178호) (3) ZNF281을 발현하는 제대혈 유래만능 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195) (4) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량배양 방법 (대한민국 특허등록 제10-1158664호) |
| 개발 진행경과 | - 2023년 1/2a상 식약처 IND 변경승인 완료 및 임상시험 진행 - 2024년 8월 1/2a상 식약처 IND 변경승인신청, 10월 변경승인 완료 - 2024년 12월 1상 topline data 발표, 1/2a상 식약처 IND 변경승인신청 - 2025년 1월 1/2a상 IND 변경승인 - 2025년 3월 2a상 첫환자 투약 개시 |
| 기타사항 | - |
| 출처) 당사 공시보고서 |
당사는 2019년 3월 ㈜현대바이오랜드(舊 SK바이오랜드㈜)와 아토피 피부염 치료제(퓨어스템-에이디주) 라이센스아웃 계약을 체결한 바 있습니다. 그러나 단회투여 방식의 3상 임상 결과에서 유효성 차이를 입증하지 못하며 해당 계약은 2024년 11월부로 해제되었으며, 당사는 지급 받았던 선급기술료 50억을 반환 완료하였습니다. 이처럼 라이선스 아웃 계약은 계약이 이루어지더라도, 계약 후 개발 진행 단계가 더디거나, 예상치 못했던 사유 등으로 인해 해지될 수 있는 성격을 가지고 있습니다. 한편, 당사는 해당 계약 해제 여부와 상관없이 퓨어스템-에이디주에 대해 2025년 4월 30일 반복투여 임상 1/2a상 변경 승인 재신청을 완료하였으며, 2025년 하반기 임상 1/2a상 개시를 계획하고 있습니다. 이미 계약이 해지된 상태이므로, 당사의 퓨어스템-에이디주 파이프라인은 현재 다른 대상자에게 라이선스 아웃을 시도할 수 있는 상황입니다.
| [투자판단관련주요경영사항(2024.11.18) -제대혈 유래 줄기세포 아토피피부염 치료제 국내 독점판권/통상실시권 설정 및 기술전수 계약 해제] |
|
|||||||||||||||||||||||||||||
| 출처) DART 전자공시시스템 |
또한, 당사는 2024년 11월 무릎골관절염치료체(OSCA)의 공동개발 및 국내 독점판매권ㆍ통상실시권에 대하여 유영제약과 라이선스 아웃 계약을 체결하였습니다. 해당 계약에 따라 당사는 유영제약으로부터 선급금으로 금 20억원을 수취하였으며, 해당 계약금은 환수불가한 금액입니다. 계약에 대한 세부 내용은 다음과 같습니다.
| [투자판단관련주요경영사항(2024.11.07) -무릎골관절염치료제(OSCA) 공동개발 및 국내 독점판매권ㆍ통상실시권에 대한 라이선스 계약 체결] |
【계약상 특이사항 등 투자위험요소】
|
||||||||||||||||||||||||||||||
| 출처) DART 전자공시시스템 |
2024년 11월에 맺은 OSCA의 유영제약 라이센스 아웃 계약의 경우, 통상적인 경우와 다르게 임상 1상을 완료한 초기 단계에서 진행되었으며, 이는 당사 입장에서 다음과 같은 장점이 있습니다. 1) 계약 상대방인 유영제약은 2023년 기준 매출액 1,290억원 중 정형외과 분야 매출이 약 300억원으로 관절염에 대한 이해가 높은 중견제약사입니다. 당사의 줄기세포 관련 전문기술과 더불어 유영제약의 골관절염 치료제의 임상개발 및 영업 마케팅 경험을 통한 노하우를 활용함으로써 보다 시장 중심적(market-oriented)제품을 개발 하여 시장 성공 가능성을 높일 수 있는 시너지 효과가 기대됩니다. 2) 또한, 임상 2a상 까지는 당사가 비용을 부담하지만, 이후 임상 2b상부터 3상, 장기추적조사까지 유영제약이 비용을 부담하여 당사는 많은 비용의 절감이 가능합니다. 3) 동시에, 해당 국내 기술이전 계약이 해외 파트너와의 글로벌 라이센스 아웃 계약 체결을 준비하는데 있어서도 유리하게 작용할 것으로 예상됩니다.
한편, 2024년 11월 계약 해지된 퓨어스템-에이디주 건과 다르게, 해당 계약은 선급금에 대한 반환 조건이 없습니다.
당사는 상기 명시한 기술이전 외에 현재 연구개발 진행 중이거나, 연구개발 진행 예정인 파이프라인의 기술이전을 위해 다양한 경로로 국내외 잠재적 파트너사와 접촉할 계획입니다.
한편, 당사는 2023년 유상증자 및 2024년 12월 공시한 합병 증권신고서 당시 계획했던 기술이전 일정이 현재 전반적으로 지연되고 있습니다. 퓨어스템-에이디주의 경우 진행중이던 임상 3상 결과를 바탕으로 2024년/2025년 글로벌 라이센스 아웃을 목표로 설정한 바 있습니다. 그러나 2024년 11월 2차 임상 3상 결과, 1차 평가지표인 12주차 시점 EASI-50 평가에서 시험군과 위약 대조군 간 유효성 차이를 입증하지 못하였으며, 이에 따라 글로벌 라이센스 아웃 역시 계획했던 일정보다 지연되었습니다. 당사는 2025년 4월 퓨어스템-에이디주의 반복투여 제1/2a 임상시험계획변경승인신청을 하였으며, 퓨어스템-에이디주의 경우 파트너사를 찾아 컨소시엄을 구성하여 임상 비용을 부담할 계획이며, 현재 2025년 하반기 임상 1/2a상 개시를 계획하고 있습니다. 다만, 임상시험 계획변경 승인 시기가 지연되거나, 컨소시엄 등 결성 시기 지연 시 임상1/2a상 개시 일정도 지연될 수 있습니다. 향후 해당 임상 진행 추이 및 결과를 바탕으로 퓨어스템-에이디주의 기술이전 계획을 재수립할 예정입니다.
퓨어스템-알에이주의 경우 2023년 유상증자 당시 2025년 상반기 임상 2b상 개시 및 임상 2b상 완료 후 글로벌 라이센스 아웃 진행을 목표로 하였으며, 2024년 12월 공시한 합병 증권신고서에는 2028년을 글로벌 라이센스 아웃 목표로 계획하였습니다. 이에 2023년 9월 식약처로부터 임상 2b상 IND를 승인 받았으나, 퓨어스템-에이디주의 사업화가 지연되며 내부적으로 파이프라인 전반에 대한 임상계획 조정이 필요하였습니다. 이에 따라, 우선순위 프로젝트인 OSCA와 퓨어스템-에이디주 임상시험에 예산 투여를 위해 퓨어스템-알에이주 2b 임상시험의 개시를 보류 중이며 기술이전 일정 역시 함께 지연될 수밖에 없었습니다. 당사는 우선순위 파이프라인의 임상 계획 등을 감안하여 퓨어스템-알에이주 2b상을 2027년 하반기에 개시, 2028년 12월 완료를 목표로 계획 중입니다. 향후 해당 임상 진행 추이 및 결과를 바탕으로 퓨어스템-알에이주의 라이센스 아웃 계획을 수립할 예정입니다. 한편, 임상 2b상까지는 당사가 진행 후 임상 3상부터는 대웅제약과 공동개발을 진행할 예정이며, 임상2b상이 지연되거나 실패하더라도 별도의 공동개발 계약 해지 조항은 없습니다.
OSCA의 경우 2023년 유상증자 당시 2024년 임상 1상 결과를 바탕으로 글로벌 라이센스 아웃을 계획하였고, 2024년 12월 합병 증권신고서 당시 2025년 말 혹은 2026년 상반기를 글로벌 라이센스 아웃 목표로 계획하였습니다. OSCA 1상의 경우 실제로 중용량, 고용량군에서 우수한 임상 결과를 수령하였습니다. 당사는 OSCA 임상 1상 이후 다수 글로벌 제약사와 기술이전 협의를 위해 접촉하였으나, 1)위약 대비 시험약의 효과 비교 가능한 데이터, 2)시험군의 효과크기를 비교하기 적절한 규모의 데이터를 보강 요청하는 곳이 다수였습니다. 이에 당사는 위약 대조와 더 많은 실험군을 바탕으로 OSCA의 우수한 효과와 안전성을 2a상에서 입증하고, 글로벌 라이센스 아웃 규모를 확대하는 방향으로 전략을 수정하였습니다. 또한, 국내 라이센스 아웃을 선제적으로 체결하고, 해당 레퍼런스 기반으로 글로벌 라이센스 아웃 계약을 준비하기로 결정하였으며, 이에 따라 2024년 11월 유영제약과 국내 라이센스 아웃 계약을 체결하는데 성공하였습니다. 금번 증권신고서 제출일 기준, 당사는 OSCA의 글로벌 라이센스 아웃 시점을 임상 2a상 종료 후인 2026년 하반기 또는 2027년 상반기로 목표하고 있습니다. 그러나, OSCA의 임상 진행 과정 및 기술이전 협의 과정 등에서 차질이 발생할 경우 글로벌 라이센스 아웃의 목표 시점이 지연될 수 있으며, 이에 당사의 핵심 파이프라인 상업화가 지연됨에 따라 당사의 재무적 성과에 직접적 영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
그러나 당사의 파이프라인의 기술이전을 위한 노력에도 불구하고 당사가 보유한 파이프라인의 향후 기술개발이 지연되거나 중단되어 추가 기술이전이 발생하지 않거나, 기술개발이 성공해도 잠재 기술이전 파트너사의 협의가 원활하지 않아 기술이전 계약이 지연되거나 실패할 수 있습니다. 또한, 추가적인 기술이전에 성공하더라도, 해당 기술이전 계약에서 목표하는 기간 내에 효능이 기대에 미치지 못하는 등 임상이 원활하게 진행되지 않을 경우 해당 계약에서 규정한 조건에 따라 계약금을 반환해야할 의무가 있을 수 있으며, 마일스톤 및 로열티 금액 등을 추가로 수령할 수 없을 가능성이 존재합니다.
이처럼 당사의 이러한 기술이전 계약의 지연 및 실패를 축소ㆍ회피하기 위한 노력에도 불구하고, 기술이전 계약이 지연되거나 실패하는 경우에는 당사의 수익성이 악화되거나 사업에 부정적 영향을 줄 수 있습니다. 투자자 여러분들께서는 이 점을 반드시 유의하여 주시기 바랍니다.
2. 회사위험
| [주요재무사항 총괄표] | |
| (K-IFRS, 연결) | (단위 : 백만원, %) |
| 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | 비고 | |
|---|---|---|---|---|---|---|
| 감사인 | 삼일회계법인 | 안진회계법인 | 안진회계법인 | 안진회계법인 | - | |
| 외부감사인의 감사(검토)의견 | - | 적정 | 적정 | 적정 | - | |
| 감사인 강조사항 | 해당없음 | 해당없음 | 해당없음 | 해당없음 | - | |
| 계속기업 존속불확실성 사유 해당여부 | 미해당 | 미해당 | 미해당 | 미해당 | - | |
| 1. 자산총계 | 50,204 | 55,986 | 81,253 | 80,592 | - | |
| 유동자산 | 23,576 | 28,528 | 47,366 | 45,907 | - | |
| 비유동자산 | 26,628 | 27,458 | 33,887 | 34,685 | - | |
| 2. 부채총계 | 11,925 | 12,804 | 36,735 | 33,331 | - | |
| 유동부채 | 7,019 | 7,732 | 24,199 | 19,709 | - | |
| 비유동부채 | 4,906 | 5,072 | 12,536 | 13,623 | - | |
| 3. 자본총계 | 38,279 | 43,182 | 44,518 | 47,260 | - | |
| 자본금 | 28,027 | 28,027 | 28,003 | 19,003 | - | |
| 주식발행초과금 | 174,869 | 174,869 | 174,895 | 163,374 | - | |
| 기타자본항목 | 7,172 | 7,172 | 4,469 | 4,194 | - | |
| 결손금 | (171,789) | (166,886) | (159,354) | (137,201) | - | |
| 4. 부채비율(%) | 31.2% | 29.7% | 82.5% | 70.5% | 부채총계 ÷ 자본총계 | |
| 5. 유동비율(%) | 335.9% | 368.9% | 195.7% | 232.9% | 유동자산 ÷ 유동부채 | |
| 6. 총차입금 | 8,430 | 8,456 | 19,214 | 18,811 | - | |
| 유동성 차입금 | 4,031 | 4,048 | 14,560 | 12,460 | - | |
| 비유동성 차입금 | 4,399 | 4,408 | 4,654 | 6,350 | - | |
| - 총차입금 의존도(%) | 16.8% | 15.1% | 23.6% | 23.3% | 총차입금 ÷ 자산총계 | |
| - 유동성 차입금 비중(%) | 47.8% | 47.9% | 75.8% | 66.2% | 유동성 차입금 ÷ 총차입금 | |
| 7. 영업활동 현금흐름 | (321) | (18,987) | (16,498) | (18,864) | - | |
| - 영업활동현금흐름 총부채 비율(%) | -2.7% | -148.3% | -44.9% | -56.6% | 영업활동현금흐름 ÷ 부채총계 | |
| 8. 투자활동 현금흐름 | (195) | 15,014 | (2,304) | 16,236 | - | |
| 9. 재무활동 현금흐름 | (85) | 884 | 19,977 | (231) | - | |
| 10. 현금 및 현금성자산 | 18,596 | 19,197 | 37,360 | 36,678 | 현금 및 현금성자산 + 단기금융상품 | |
| 11. 순차입금 | (10,166) | (10,741) | (18,146) | (17,867) | 총차입금 - 현금 및 현금성자산 | |
| - 순차입금 의존도(%) | -20.2% | -19.2% | -22.3% | -22.2% | 순차입금 ÷ 자산총계 | |
| 12. 매출액 | 954 | 7,746 | 12,704 | 16,301 | - | |
| 13. 매출원가 | 749 | 3,420 | 11,061 | 11,428 | - | |
| - 매출원가율(%) | 78.5% | 44.2% | 87.1% | 70.1% | 매출원가 ÷ 매출액 | |
| 14. 영업이익(손실) | (4,745) | (14,842) | (22,777) | (20,558) | - | |
| - 영업이익률(%) | -497.2% | -191.6% | -179.3% | -126.1% | 영업이익 ÷ 매출액 | |
| 15. 기타수익 | 21 | 152 | 173 | 459 | - | |
| 16. 기타비용 | 10 | 47 | 300 | 321 | - | |
| 17. 금융수익 | 175 | 1,457 | 1,547 | 1,335 | - | |
| 18. 금융원가 | 270 | 1,170 | 1,060 | 1,129 | - | |
| 이자비용 | 127 | 426 | 893 | 761 | - | |
| - 이자비용배수(배) | -37.36 | -34.85 | -25.49 | -27.01 | 영업이익 ÷ 이자비용 | |
| 21. 법인세비용차감전계속사업이익(손실) | (4,903) | (7,083) | (23,137) | (20,215) | - | |
| 22. 당기순이익(손실) | (4,903) | (7,990) | (23,221) | (20,176) | - | |
| - 당기순이익률(%) | -513.8% | -103.2% | -182.8% | -123.8% | 당기순이익 ÷ 매출액 | |
| 출처) 당사 정기보고서 제시 |
| 가. 지속적인 연구개발 투자 필요에 따른 유동성 위험 연구개발을 통한 신약 개발은 일반적으로 막대한 연구개발비와 장기에 걸친 투자 및 연구기간이 소요되며, 신약 개발에 성공한다 하더라도 기투자된 금액과 시간을 상쇄할 수 있을 정도의 수익 창출이 가능할지 여부는 불확실합니다. 또한 내외부적인 요인으로 인하여 개발이 지연되거나 추가적인 비용 지출이 요구될 경우도 존재합니다. 당사는 연구개발비용으로 2025년 1분기말 기준 32.3억원을 사용하였으며, 이는 2025년 1분기말 매출액(9.5억원) 대비 338.6% 수준입니다. 최근 3개년(2022, 2023, 2024년) 연결기준 매출액 대비 평균 118.1% 수준을 연구개발비용으로 사용하고 있습니다. 연구개발비는 발생시점에 전액 비용 처리하고 있으며, 개발비 자산화 시점에 대한 고려는 하지 않을 계획입니다. 다만, 증권신고서 제출일 현재까지 연구개발에 대한 성과가 수익성으로 연결되지 않아 지속적인 영업적자를 기록하고 있습니다. 당사의 연구개발 계획이 실패하거나, 장기적인 연구개발 전략과 사업계획, 그리고 그에 맞는 자금운용계획을 적정하게 수립하지 못할 경우 당사의 수익성 및 재무안정성에 부정적인 영향이 발생할 수 있습니다. 또한, 당사는 지속적인 적자로 인해 자체적으로 연구개발비를 조달하는데 어려움이 있어 계속적으로 자금조달을 유치하고 있습니다. 향후에도 추가적인 자금조달 가능성이 존재하며 적절한 시점에 유동자금을 확보하지 못할 경우 회사 운영이 어려워지는 상황에 직면할 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
연구개발을 통한 신약 및 기술개발은 바이오벤처기업의 지속적인 성장을 위한 중요한 요소이며, 연구개발을 위한 투자 또한 필연적인 사항입니다. 당사 역시 기존 제품의 향상 및 새로운 파이프라인 등 미래성장동력 확보를 위하여 연구개발 투자를 지속적으로 해왔으며 향후에도 계속 진행할 예정입니다.
연구개발을 통한 신약 개발은 일반적으로 막대한 연구개발비와 장기에 걸친 투자 및 연구기간이 소요되며, 신약 개발에 성공한다 하더라도 기투자된 금액과 시간을 상쇄할 수 있을 정도의 수익 창출이 가능할지 여부는 불확실합니다. 또한 내외부적인 요인으로 인하여 개발이 지연되거나 추가적인 비용 지출이 요구될 경우도 존재합니다.
당사는 연구개발비용으로 2025년 1분기말 기준 32.3억원을 사용하였으며, 이는 2025년 1분기말 매출액(9.5억원) 대비 338.6% 수준입니다. 최근 3개년(2022, 2023, 2024년) 연결기준 매출액 대비 평균 118.1% 수준을 연구개발비용으로 사용하고 있습니다. 연구개발비는 발생시점에 전액 비용 처리하고 있습니다. 2019년 10월 아토피 피부염 치료제(Furestem-AD Inj.)의 국내 임상 3상 실패 및 통계분석 결과 '유의성 미확보'로 기술적 실현가능성을 입증하지 못하여 무형자산으로 인식할 수 없다는 K-IFRS 제1038호 자산성 검토 의견에 따라 그동안 개발비(무형자산)로 계상하던 금액을 손상인식하였습니다. 이에 개발비 자산화 시점에 대한 고려는 하지 않을 계획입니다. 다만, 증권신고서 제출일 현재까지 연구개발에 대한 성과가 수익성으로 연결되지 않아 지속적인 영업적자를 기록하고 있습니다. 이에 따라 당사는 자체 사업으로만 운영자금을 확보하지 못해 외부로부터 펀딩을 통해 연구개발비를 포함한 운영자금을 조달하고 있습니다.
2021년 10월 및 2023년 11월 유상증자 자금은 당시 기재했던 자금사용목적에 따라 계획대로 사용 중이며 자금 사용내역은 다음과 같습니다.
(1) 공모자금의 사용내역
| (기준일 : 2025년 03월 31일) | (단위 : 백만원) |
| 구 분 | 납입일 | 증권신고서 등의 자금사용 계획 | 실제 자금사용 내역 | 차이발생 사유 등 | ||
|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | |||
| 기업공개 (코스닥상장) |
2015.12.15 | 시설자금 5,740 운영자금 6,060 발행제비용 560 |
12,360 | 시설자금 3,648 운영자금 8,152 발행제비용 560 |
12,360 | 신약개발일정이 조정됨에 따라 설비 신축계획을 일부증축으로 변경하고, 차액분을 연구개발비로 사용 |
| 주주배정 유상증자 |
2018.07.27 | 운영자금 | 35,952 | 운영자금 | 35,952 | - |
| 주주배정 유상증자 |
2021.10.21 | 운영자금 | 38,985 | 운영자금 | 37,781 | 미사용자금 1,204 / 단기금융상품 예치 |
| 주주배정 유상증자 |
2023.11.08 | 운영자금 | 20,970 | 운영자금 | 12,545 | 미사용자금 8,425 / 단기금융상품 예치 |
| 출처) 당사 제시 |
(2) 사모자금의 사용내역
| (기준일 : 2025년 03월 31일) | (단위 : 백만원) |
| 구 분 | 납입일 | 주요사항보고서의 자금사용 계획 | 실제 자금사용 내역 | 차이발생 사유 등 | ||
|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | |||
| 제3자배정 유상증자 |
2015.01.22 | 임상연구비 및 운영자금 |
6,000 | 임상연구비 및 운영자금 |
6,000 | - |
| 제3자배정 유상증자 |
2015.03.05 | 임상연구비 및 운영자금 |
3,000 | 임상연구비 및 운영자금 |
3,000 | - |
| 제3자배정 유상증자 |
2015.04.01 | 임상연구비 및 운영자금 |
1,000 | 임상연구비 및 운영자금 |
1,000 | - |
| 전환사채 발행(주1) |
2016.09.08 | 시설자금 15,000 운영자금 15,000 |
30,000 | 시설자금 15,000 운영자금 15,000 |
30,000 | - |
| 제3자배정 유상증자 |
2017.04.28 | 운영자금 | 1,400 | 운영자금 | 1,400 | - |
| 제3자배정 유상증자 |
2019.07.11 | 운영자금 | 48,000 | 운영자금 | 48,000 | - |
| 출처) 당사 제시 |
| 주1) 당사가 발행한 전환사채 300억원 중 150억원은 GMP 신축 등 시설투자를 목적으로 발행되었습니다. 2017년 12월말 150억원 중 91억원은 토지 및 건물 취득 등에 사용하였고, 나머지 59억원은 2018년 중 시설장치 및 연구시험용 자산 취득에 사용되었습니다. |
| [연구개발비용 현황(연결기준)] |
| (단위 : 백만원, %) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | |
|---|---|---|---|---|---|
|
비용의 성격별 분류 |
원재료 | 110 | 726 | 917 | 880 |
| 인건비 | 1,238 | 4,481 | 4,989 | 4,675 | |
| 감가상각비 | 560 | 2,168 | 2,117 | 2,112 | |
| 위탁용역비 | 937 | 2,898 | 3,573 | 4,029 | |
| 기타 | 519 | 2,689 | 2,961 | 3,701 | |
| 연구개발비용 합계 | 3,365 | 12,962 | 14,558 | 15,398 | |
|
회계처리 내역 |
판매비와관리비 | 3,231 | 12,143 | 14,030 | 14,220 |
| 정부보조금 | 134 | 819 | 528 | 1,178 | |
| 연구개발비용 합계 | 3,365 | 12,962 | 14,558 | 15,398 | |
|
연구개발비/매출액 비율 [연구개발비용합계/당기매출액*100] |
353 | 167 | 114.6 | 94.5 | |
| 출처) 당사 정기보고서 |
| 주1) 상기 연구개발비는 연결기준이고, 당사의 연구개발비는 향후 발생시점에 전액 비용 처리할 계획입니다. |
당사의 연구개발 계획이 실패하거나, 장기적인 연구개발 전략과 사업계획, 그리고 그에 맞는 자금운용계획을 적정하게 수립하지 못할 경우 당사의 수익성 및 재무안정성에 부정적인 영향이 발생할 수 있습니다. 또한, 당사는 지속적인 적자로 인해 자체적으로 연구개발비를 조달하는데 어려움이 있어 계속적으로 자금조달을 유치하고 있습니다. 향후에도 추가적인 자금조달 가능성이 존재하며 적절한 시점에 유동자금을 확보하지 못할 경우 회사 운영이 어려워지는 상황에 직면할 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
| 나. 성장성 및 수익성 하락에 따른 위험 2025년 1분기 기준 매출액은 9.5억원을 기록하며 전년 동기 대비 감소하였습니다. 아토피 피부염 줄기세포 치료제인 '퓨어스템-에이디 주' 임상 3상 결산 수수료 및 골관절염 치료제 '퓨어스템-오에이 키트 주' 임상을 위한 연구비용이 발생하였지만 비임상시험 사업부의 연결 제외로 전체 판관비가 감소하였으며, 이에 영업손실 적자 폭은 작아졌습니다. 영업손실의 경우 2022년 206억원, 2023년 228억원, 2024년 148억원, 2025년 1분기 47억원을 기록하며 손실이 지속되는 추이를 보이고 있습니다. 이는 바이오산업 특성상 가시적인 성과가 발생하기까지 지속적인 연구개발자금이 소요되는 것이 주요 원인으로, 진행 중인 파이프라인의 임상연구가 지속되는 한 높은 판관비는 지속적으로 발생할 것으로 예상되고 있습니다. 이에 당사는 CDMO 사업 진행을 통해 관련 매출을 발생시켜 유지 및 보수 비용을 충당하였으며, 개발 중인 신약과 관련한 다양한 국가 과제 수행을 통해 연구개발비용을 절감하고 긴축 재정 관리로 운용 비용을 절감하고 있습니다. 이러한 노력에도 불구하고 당사가 계획하고 있는 연구개발 지연 및 실패하는 경우, 또는 품목허가 및 출시 지연에 따른 화장품 및 바이오파마 제품 생산ㆍ판매 지연 등으로 인해 당사의 매출 계획이 지연될 가능성이 존재합니다. 이에 따라 당사의 영업활동 및 수익성은 부정적인 영향을 받을 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
당사 사업부문은 크게 줄기세포 사업부, 화장품 사업부, 바이오파마 사업부로 구성되어 있습니다. 당사는 자체 개발한 다분화능을 가진 줄기세포를 인간 제대혈로부터 고순도(high-purity)로 분리하고, 대량배양(massive culture)하는 기술을 기반으로 동종 제대혈 유래 줄기세포치료제(의약품) 연구개발을 진행하고 있습니다. 또한 이와 별도로 줄기세포 배양액을 이용한 화장품사업과 의약품 도매 총판 및 일반의약품 유통사업을 영위하는 바이오파마 사업을 진행하고 있습니다. 자회사(HLB바이오코드 주식회사)를 통해 영위해오던 비임상 CRO 사업은 2024년 05월 보유 주식 일부를 매각함에 따라 더 이상 영위하지 않고 있으며 연결 대상에서 제외되었습니다.
2025년 1분기 매출액 기준으로 줄기세포 사업부가 48.5%, 화장품 사업부가 51.5%의 비중을 차지하고 있습니다. 사업부문별 주요사업 내용과 재무현황은 다음과 같습니다.
| 구 분 | 주요 사업 내용 |
|---|---|
| 줄기세포 사업 | 줄기세포 치료제 연구개발, 줄기세포 배양액 및 배양배지 공급 |
| 화장품 사업 | 줄기세포 배양액 화장품 제조, 판매 |
| 바이오파마 사업 | 일반의약품(OTC) 및 건강기능식품 판매 |
| 비임상시험 사업 | 의약품, 화학물질, 작물보호제, 동물의약품 등의 효능 및 유해성 평가 |
| 출처) 당사 정기보고서 |
| 주) HLB바이오코드(주)를 통해 영위하던 비임상시험 사업은 2024년 05월 보유 주식 일부를 매각함에 따라 연결 대상에서 제외되었습니다. |
당사의 주요 경쟁회사의 실적 비교 추이는 다음과 같습니다.
| [당사와 주요 경쟁회사의 실적 비교 추이] | |
| (K-IFRS, 개별) | (단위: 백만원) |
| 구분 | 강스템바이오텍 | A사 | B사 | C사 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2024년 | 2023년 | 2022년 | 2024년 | 2023년 | 2022년 | 2024년 | 2023년 | 2022년 | 2024년 | 2023년 | 2022년 | |
| 매출액 | 7,746 | 5,913 | 5,915 | 12,889 | 12,462 | 10,102 | 74,113 | 69,707 | 61,394 | 159,671 | 124,922 | 161,017 |
| 영업이익(손실) | (14,842) | (20,061) | (21,014) | (5,069) | (5,142) | (5,229) | 3,780 | 3,598 | (10,767) | (13,998) | (14,935) | 10,155 |
| 당기순이익(손실) | (7,990) | (19,016) | (19,765) | (11,928) | (1,356) | (8,040) | (62,221) | 7,254 | 6,020 | (94,171) | (31,039) | 2,476 |
| 자본총계 | 43,182 | 53,211 | 51,432 | 31,257 | 42,130 | 43,822 | 252,810 | 312,749 | 180,373 | 148,462 | 137,672 | 167,777 |
| 미처리결손금 | (166,886) | (159,354) | (137,201) | (38,116) | (26,322) | (24,458) | (94,475) | (31,468) | (38,800) | (228,967) | (133,289) | (101,483) |
| 경상연구개발비 | 12,143 | 14,960 | 15,544 | 5,755 | 4,388 | 3,837 | 8,305 | 5,498 | 15,152 | 17,670 | 14,794 | 13,551 |
| 출처) 당사 제시 |
| 주) 경쟁회사는 당사의 주요 제품인 OSCA(골관절염 치료제)의 경쟁 제품을 개발하고 있는 곳으로 선정하였습니다. |
A사의 경우 매출의 대부분이 생체 세포를 활용한 화상 및 무릎 연골손상 질환을 대상으로 재생치료제를 생산 및 판매하고 있으며, 관련 세포 치료제 매출이 95억원 발생하고 있습니다. 그 외 인체조직모델을 활용한 각막, 기관지 점막, 피부 대상 대체독성시험 및 유효성 시험 등의 용역 제공과 화장품 사업부를 영위하고 있습니다. 2024년말 기준 매출액이 3.4% 증가하였으며 영업손실 1.4% 감소하였습니다.
B사의 경우 매출의 대부분이 제대혈채취 및 보관매출 392억원과 동종 줄기세포 치료제 제조 및 판매 등 CDMO로 202억원의 매출을 기록하였습니다. 또한, 국내 경상연구개발비 절감으로 영업이익이 개선되며 2023년말 기준 흑자전환에 성공한 이후 2개년 연속 흑자를 기록 중입니다.
C사의 경우 매출의 대부분이 Chemical 사업부문의 의약사업 및 기능소재 사업에서 발생하고 있으며 수출 비중이 82%로 매우 높은 편입니다.
당사의 경우, 화장품 사업부(출기세포배양액 화장품 GD11 및 줄기세포배양액 기반 기능성 샴푸 Bio-3) 매출이 33억원을 기록 중입니다. 특히, OSCA 기술이전 경상기술료 1차로 20억원을 수취하는 등 줄기세포 사업부에서 전년도 대비 203.7% 증가한 44억원의 매출이 발생하였습니다. 다만, 주요 파이프라인인 퓨어스템-에이디 및 OSCA의 임상 시험 등 경상 연구개발비가 매출을 크게 상회하며 영업손실과 당기순손실을 기록하고 있습니다.
| [사업부문별 재무현황] |
| (단위 : 백만원, %) |
| 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | |||||
|---|---|---|---|---|---|---|---|---|---|
| 금 액 | 비 중 | 금 액 | 비 중 | 금 액 | 비 중 | 금 액 | 비 중 | ||
| 줄기세포 사업부 | 자산 | 49,803 | 99.2 | 55,274 | 98.7 | 70,630 | 86.9 | 68,166 | 84.6 |
| 부채 | 11,739 | 98.4 | 12,635 | 98.7 | 17,809 | 48.5 | 17,008 | 51.0 | |
| 매출액 | 463 | 48.5 | 4,386 | 56.6 | 1,444 | 11.4 | 1,343 | 8.2 | |
| 영업이익 | (4,575) | 96.4 | (14,262) | 96.1 | (18,787) | 82.5 | (19,339) | 94.1 | |
| 화장품 사업부 | 자산 | 401 | 0.8 | 712 | 1.3 | 642 | 0.8 | 588 | 0.7 |
| 부채 | 186 | 1.6 | 169 | 1.3 | 369 | 1.0 | 394 | 1.2 | |
| 매출액 | 491 | 51.5 | 3,274 | 42.3 | 4,117 | 32.4 | 4,009 | 24.6 | |
| 영업이익 | (169) | 3.6 | (465) | 3.1 | (1,063) | 4.7 | (1,425) | 6.9 | |
| 바이오파마 사업부 | 자산 | 0.0 | 0.0 |
0.0 |
0.0 | 120 | 0.1 | 97 | 0.1 |
| 부채 | 0.0 | 0.0 |
0.0 |
0.0 | 3 | 0.0 | 16 | 0.0 | |
| 매출액 | 0.0 | 0.0 |
86 | 1.1 | 351 | 2.8 | 563 | 3.5 | |
| 영업이익 | 0.0 | 0.0 |
(115) | 0.8 | (211) | 0.9 | (251) | 1.2 | |
| 비임상시험 사업부 | 자산 | 11,083 | 13.6 | 12,245 | 15.2 | ||||
| 부채 | 20,948 | 57 | 18,193 | 54.6 | |||||
| 매출액 | 7,123 | 56.1 | 10,480 | 64.3 | |||||
| 영업이익 | (2,787) | 12.2 | 400 | (1.9) | |||||
| 연결조정 | 자산 | (1,222) | -1.5 | (504) | (0.6) | ||||
| 부채 | (2,393) | -6.5 | (2,280) | (6.8) | |||||
| 매출액 | (332) | -2.6 | (94) | (0.6) | |||||
| 영업이익 | 71 | -0.3 | 57 | (0.3) | |||||
| 연결 후 금액 | 자산 | 50,204 | 100.0 | 55,986 | 100.0 | 81,253 | 100.0 | 80,592 | 100.0 |
| 부채 | 11,925 | 100.0 | 12,804 | 100.0 | 36,735 | 100.0 | 33,331 | 100.0 | |
| 매출액 | 954 | 100.0 | 7,746 | 100.0 | 12,704 | 100.0 | 16,301 | 100.0 | |
| 영업이익 | (4,745) | 100.0 | (14,842) | 100.0 | (22,777) | 100.0 | (20,558) | 100.0 | |
| 출처) 당사 제시 |
| 주1) HLB바이오코드(주)는 2017년 04월에 연결종속회사로 편입되었지만, 2024년 05월 보유주식 1,183,676주 중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류되었습니다. |
| 주2) 2024년 05월 (주)크로엔에서 HLB바이오코드(주)로 사명을 변경하였습니다. |
| [설립 이후부터 현재(2025년 1분기)까지의 적자 추이(별도/연결)] |
| (단위 : 백만원) |
| 별도기준 | 2010년 | 2011년 | 2012년 | 2013년 | 2014년 | 2015년 | 2016년 | 2017년 | 2018년 | 2019년 | 2020년 | 2021년 | 2022년 | 2023년 | 2024년 | 2025년 1분기 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 제1기 | 제2기 | 제3기 | 제4기 | 제5기 | 제6기 | 제7기 | 제8기 | 제9기 | 제10기 | 제11기 | 제12기 | 제13기 | 제14기 | 제15기 | 제16기 | |
| K-Gaap/ 감사받지않음 |
K-Gaap | K-Gaap | K-IFRS/ 감사받지않음 |
K-IFRS/ 감사받지않음 |
K-IFRS | K-IFRS | K-IFRS | K-IFRS | K-IFRS | K-IFRS | K-IFRS | K-IFRS | K-IFRS | K-IFRS | K-IFRS | |
| 매출액 | - | - | 139 | 410 | 208 | 1,484 | 843 | 983 | 1,001 | 282 | 295 | 3,757 | 5,915 | 5,913 | 7,746 | 954 |
| 영업손익 | (71) | (873) | (826) | (2,803) | (4,454) | (5,125) | (9,117) | (9,977) | (10,525) | (19,411) | (16,745) | (21,748) | (21,014) | (20,061) | (14,842) | (4,745) |
| 당기순손익 | (71) | (774) | (722) | (2,836) | (3,713) | (5,754) | (7,146) | (14,938) | (13,501) | (25,001) | (19,492) | (20,437) | (19,765) | (19,016) | (7,083) | (4,903) |
| 자본총계 | 29 | 6,177 | 5,448 | 1,776 | (1,913) | 21,237 | 22,500 | 23,591 | 47,945 | 70,845 | 51,431 | 70,138 | 51,432 | 53,211 | 43,182 | 38,279 |
| 미처리결손금 | (71) | (845) | (1,574) | (6,649) | (10,352) | (16,106) | (23,252) | (38,190) | (51,691) | (76,693) | (96,185) | (116,622) | (136,387) | (155,403) | (166,886) | (171,789) |
| 출처) 당사 제시 |
| 연결기준 | 2010년 | 2011년 | 2012년 | 2013년 | 2014년 | 2015년 | 2016년 | 2017년 | 2018년 | 2019년 | 2020년 | 2021년 | 2022년 | 2023년 | 2024년 | 2025년 1분기 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 제1기 | 제2기 | 제3기 | 제4기 | 제5기 | 제6기 | 제7기 | 제8기 | 제9기 | 제10기 | 제11기 | 제12기 | 제13기 | 제14기 | 제15기 | 제16기 | |
| - | - | - | - | - | - | - | K-IFRS/ 연결재무제표 작성의무 |
K-IFRS | K-IFRS | K-IFRS | K-IFRS | K-IFRS | K-IFRS | K-IFRS | K-IFRS | |
| 매출액 | - | - | - | - | - | - | - | 9,133 | 9,165 | 6,004 | 9,138 | 12,405 | 16,300 | 12,704 | 7,746 | 954 |
| 영업손익 | - | - | - | - | - | - | - | (11,738) | (11,694 | (23,154) | (18,725) | (22,735) | (20,558) | (22,777) | (14,842) | (4,745) |
| 당기순손익 | - | - | - | - | - | - | - | (15,614) | (14,294) | (26,394) | (19,746) | (21,827) | (20,176) | (23,221) | (7,083) | (4,903) |
| 자본총계 | - | - | - | - | - | - | - | 23,405 | 47,581 | 68,719 | 48,639 | 66,003 | 47,260 | 44,517 | 43,182 | 38,279 |
| 미처리결손금 | - | - | - | - | - | - | - | (38,722) | (52,360) | (77,232) | (95,670) | (117,054) | (137,201) | (159,354) | (166,886) | (171,789) |
| 출처) 당사 제시 |
당사는 줄기세포 치료제 개발 및 제조회사로, 연구개발하는 신약이 상업화되기까지 많은 시간과 비용이 소요되며 임상 시험의 경우 최소 8~9년의 연구개발 기간과 이에 따른 비용 소요를 필요로 합니다. 이에 연구개발 활동 이외의 수익 창출을 위해 H&B(health & beauty) 사업을 확장하여 홈쇼핑, 전략적 유통 파트너를 통한 줄기세포 기반의 기능성 화장품, 샴푸 매출을 창출하고 있으며, 최근에는 매출 지역, 제품 다각화를 위해 일본 시장을 겨냥한 재생의료사업을 계획하고 있습니다. 다만, 신약 개발과 연계한 제품 제조를 위해 2019년 05월 15일 GMP 센터 설립 등의 비용으로 175억원 소요 및 퓨어스템-에이디 주 2차 임상 3상 진행 기간 중 코로나19 팬데믹에 따른 임상 지연으로 추가 비용이 발생하는 등 10년 간 신약 파이프라인 임상 진행에 따른 비용이 가중되었습니다. 2019년 이후 2025년 1분기까지 각 파이프라인별 소요 비용은 퓨어스템-에이디 379억원, OSCA 105억원, 퓨어스템-알에이 38억원으로, 총 522억원이 소요되었습니다. 이에 당사는 CDMO 사업 진행을 통해 관련 매출을 발생시켜 유지 및 보수 비용을 충당하였으며, 개발 중인 신약과 관련한 다양한 국가 과제 수행을 통해 연구개발비용을 절감하고 긴축 재정 관리로 운용 비용을 절감하고 있습니다. 2025년 1분기 기준, 총 26개의 과제를 수행완료 및 진행 중에 있으며 총 정부출연금은 약 217억원입니다.
이러한 당사의 노력에도 불구하고 2010년 설립 이후 적자가 지속되고 있으며 매출액 대비 연구개발비용(개별기준)이 2022년부터 2024년까지 평균 212.3% 수준으로, 신약개발기업 특성상 매출 대비 현저히 많은 연구개발비용이 소요되고 있습니다. 이에 당사는 수익성 개선을 위해 2020년 12월부터 첨단바이오의약품 제조업 허가 및 CDMO 사업을 개시하며 누적매출 36억원을 기록하였습니다. 또한, 2015년 줄기세포배양액 화장품 GD11 런칭, 2021년 화장품사업부 인수 및 2021년 CJ홈쇼핑, 2022년 GS홈쇼핑를 통해 제품 판매를 시작하며 화장품사업부 누적매출 289억원을 기록하였습니다.
또한, 당사는 일본 재생의료시장 진출을 위해 특정인정재생의료위원회의 심의를 거쳐 제2종(자가지방줄기세포) 승인을 받고, 2025년 2월 후생노동성 최종 승인까지 완료된 상황입니다. 현재 일본 내 공급을 위해 동경, 오사카, 나고야 소재의 현지 의료기관과 계약을 완료하였고, 2025년 하반기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 또한 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며, 후생노동성 권고사항에 따라 소규모 임상시험 진행 등을 검토 중입니다. 제1종의 경우, 현재까지 후생노동성 최종 승인 사례가 단 1건에 불과하여 승인이 쉽지 않을 것으로 예상되지만, 승인을 받을 경우 당사의 줄기세포 사업 전반에 걸쳐 큰 수혜를 받을 것으로 예상됩니다.
2016년 KOTRA 오사카 무역관 자료에 따르면, 일본 줄기세포 시장은 2012년 90억엔, 2020년 950억엔, 2030년 1조엔으로 급성장할 것으로 전망할 것으로 예상되는 시장이며 줄기세포를 제조, 배양하는 업체가 후생성으로부터 제조승인을 받고, 시술병원(의원)은 치료승인을 받으면 시술이 가능한 시장입니다. 이에 당사는 하기 일본 재생의료 제공계획 허가 절차에 따라 승인 완료된 제2종(자가지방줄기세포)의 현지 공급 및 환자투약이 성공적으로 개시되고, 제 1종(동종제대혈줄기세포) 또한 최종 승인되어 수익화가 가능해진다면, 수익성 개선과 더불어 일본 줄기세포 시장 진출 레퍼런스를 통해 글로벌 시장 동력을 얻고 영위하는 사업 전반에 긍정적인 영향을 미칠 수 있을 것으로 예상하고 있습니다.
| [일본 재생의료 제공계획 허가 절차] |
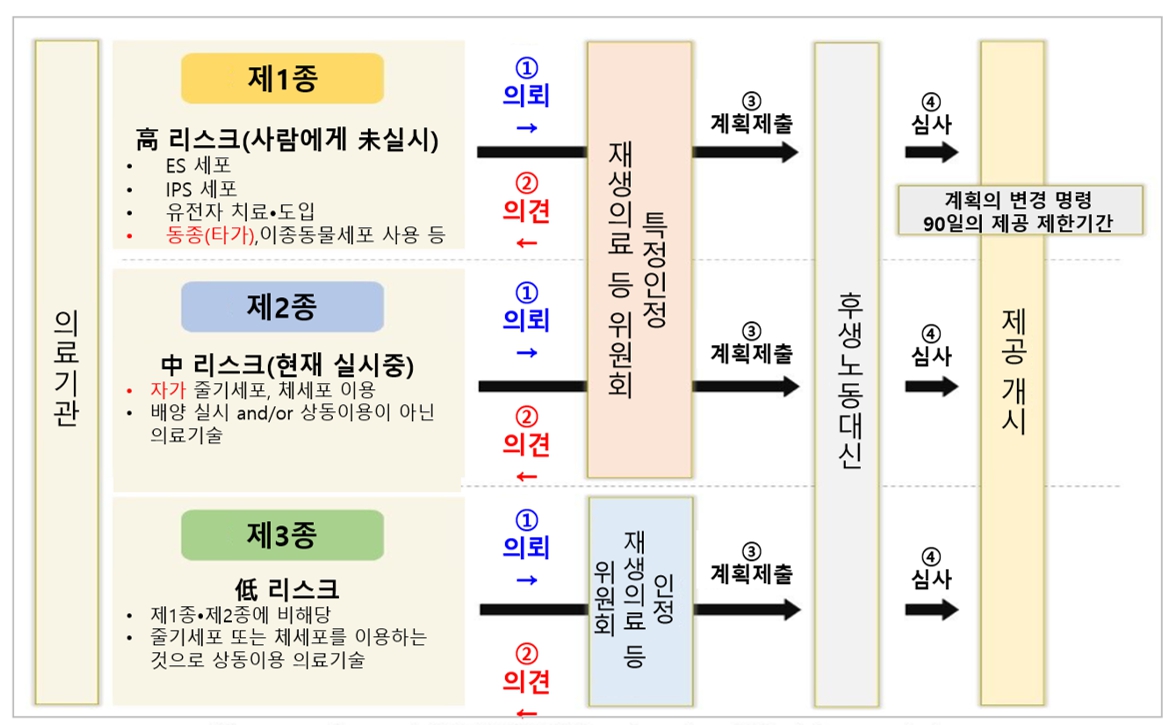 |
|
재생의료 제공계획 |
| 출처) 당사 제시 |
한편, 당사는 2024년 05월 비임상시험 사업을 영위하던 HLB바이오코드 주식회사(구.주식회사 크로엔) 지분 매각을 통해 처분이익 98억원이 발생하며 법인세비용차감전순손실 감소로 관리종목 편입 우려를 해소하였습니다. 또한, 지분 매각을 통해 발생한 매각대금 28억원은 임상비용 외 운영자금 및 일본 재생의료사업 진출을 위한 운영비로 사용할 계획입니다. 자회사 HLB바이오코드의 지분 및 경영권 매각 관련 세부 내용은 다음과 같습니다.
| [HLB바이오코드의 지분 및 경영권 매각 관련 세부 내용] |
| 일정 | 이사회결의일 | 2024년 04월 25일 | |
| 처분일 | 2024년 05월 09일 | ||
| 목적 | 지분 매각을 통한 자금 확보 및 경영 효율성 증대 | ||
| 적자가 지속되는 자회사의 지분을 일부 매각하여 관계기업투자주식으로 계정 대체(연결기업→관계기업투자주식 변경으로 손실의 일부만 적용) | |||
| 처분이익 인식을 통한 법인세차감전순손실 감소로 관리종목 편입 우려 해소 | |||
| HLB 그룹사인 HLB바이오스텝과의 업무 협업을 통한 시장 인지도 확대 | |||
| 처분 내용 | 지분율 변동 | 64.5% → 24.6% | |
| 계정 대체 | 종속회사(연결대상) → 관계회사(연결제외, 지분법) |
||
| 매각대금 및 활용계획 |
현금 | 1,438,165,800원 | 임상비용 외 일반 운영자금 편입 사용 / 일본 재생의료사업 진출을 위한 운영비 |
| 영구전환사채 | 1,438,165,800원 (HLB바이오스텝 영구전환사채) |
2025년 05월 09일 이후 전환청구 가능, 이후 주가 추이에 따라 매각 후 운영비 사용 가능 | |
| 합계 | 2,876,331,600원 | - | |
| 출처) 당사 제시 |
당사는 HLB바이오코드 주식회사(구.주식회사 크로엔)의 연결 인식으로 인하여 그동안 매출 금액에 대한 수혜는 받았으나, 2023년 HLB바이오코드의 매출 및 손익이 크게 악화되었고, 그에 따른 연결 손실을 인식함으로 법인세비용차감전계속사업손실률이 51.9%까지 증가하였으며 관리종목 지정 리스크가 발생하였습니다(최근 3개년 중 1년 해당됨). 2024년에도 HLB바이오코드의 손실이 지속될 것으로 예상되어, 계속해서 지분을 보유할 경우 당사의 재무적 악화 및 관리종목 지정 리스크에 여전히 영향을 미칠 것으로 예상되었습니다. 이에 따라 비임상시험 사업을 영위하는 HLB바이오코드와도 사업적 시너지를 낼 수 있고 당사와도 오가노이드 연구 등 여러 시너지가 발생할 수 있는 HLB바이오스텝에게 지분 일부를 매각함으로써 당사의 관리종목 지정 리스크 해소 뿐만 아니라 HLB바이오코드의 사업 강화 측면에서도 긍정적인 영향을 미쳤습니다.
결과적으로 당사는 지분 일부 매각을 통해 처분이익이 반영되어 2024년 기준 법인세비용차감전계속사업손실률이 16.4%로 크게 감소하여 코스닥 상장 유지 조건을 충족하게 되었고, HLB바이오코드의 매출이 연결에서 제외되면서 매출액이 77억원 규모로 축소되었으나, 당사의 자체 매출만으로 코스닥 상장 유지 규정인 30억원은 충족하고 있습니다. 또한 25%의 지분은 유지하고 있으므로 향후 이익 발생 시 관계기업으로서 지분법이익을 인식할 수 있고, 모회사인 HLB바이오스텝과의 협업을 통해 사업 경쟁력을 더욱 강화할 계획입니다. 다만, HLB바이오코드의 영업손익이 계속해서 적자를 유지할 경우 당사의 보유 지분 만큼 손실은 계속해서 발생할 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
| [손익계산서 주요 계정 및 수익성 추이(연결기준)] | |
| (K-IFRS, 연결) | (단위 : 백만원) |
| 구 분 | 2025년 1분기 | 2024년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|
| 매출액 | 954 | 2,916 | 7,746 | 12,704 | 16,301 |
| 매출액증가율 | -25.70% | - | -39.0% | -22.06% | 31.41% |
| 매출원가 | 749 | 2,288 | 3,420 | 11,061 | 11,428 |
| 매출총이익 | 206 | 628 | 4,325 | 1,643 | 4,873 |
| 매출총이익률 | 2.65% | 21.54% | 55.84% | 12.93% | 29.89% |
| 판매비와관리비 | 4,950 | 4,936 | 19,168 | 24,420 | 25,431 |
| 판매비와관리비율 | 63.91% | 169.27% | 247.46% | 192.23% | 156.01% |
| 영업이익(손실) | (4,745) | (4,308) | (14,842) | (22,777) | (20,558) |
| 영업이익률 | -61.26% | -147.74% | -191.62% | -179.29% | -126.11% |
| 기타수익 | 21 | 63 | 152 | 173 | 459 |
| 기타비용 | 10 | 3 | 47 | 300 | 321 |
| 금융수익 | 175 | 436 | 1,457 | 1,547 | 1,335 |
| 금융비용 | 270 | 224 | 1,170 | 1,060 | 1,129 |
| 당기순이익(손실) | (4,903) | (4,172) | (7,990) | (23,221) | (20,176) |
| 당기순이익률 | -63.30% | -143.07% | -103.15% | -182.78% | -123.77% |
| 출처) 당사 정기보고서 |
2022년말 기준 매출액 또한 전년대비 39억원 증가한 163억원을 기록하였습니다. 이는 화장품 사업 및 비임상시험 사업의 호조와 의약품 도매 총판업 및 일반의약품 유통 등을 영위하는 바이오파마 사업부의 호조 등이 기인했습니다.
2023년말 기준 매출액은 전년대비 36억원 감소한 127억원을 기록하였습니다. 이는 크로엔을 통해 영위하던 비임상시험 사업부 및 바이오파마 사업부의 매출 부진 등이 기인했습니다.
2024년 말 기준 매출액은 77억원을 기록하며 비임상 사업부 연결 제외 기준 전년 대비 31.0% 상승하였습니다. 이는 전년도 대비 203.7% 상승한 줄기세포 사업부 매출에 힘입었습니다. 한편, 아토피 피부염 줄기세포 치료제인 '퓨어스템-에이디 주' 임상 3상 결산 수수료 및 골관절염 치료제 '퓨어스템-오에이 키트 주' 임상을 위한 연구비용이 발생하였지만 비임상시험 사업부의 연결 제외로 전체 판관비가 감소하였으며, 이에 영업손실 적자 폭은 작아졌습니다.
2025년 1분기 기준 매출액은 9.5억원을 기록하며 비임상 사업부 연결 제외 기준 전년 동기 대비 약 3억원 감소하였으며, 이는 화장품 사업부의 부진에 따른 것으로, 줄기세포 사업부의 매출은 217.3% 상승하여 5억원을 기록하였습니다.
영업손실의 경우 2022년 206억원, 2023년 228억원, 2024년 148억원, 2025년 1분기 47억원을 기록하며 손실이 지속되는 추이를 보이고 있습니다. 이는 바이오산업 특성상 가시적인 성과가 발생하기까지 지속적인 연구개발자금이 소요되는 것이 주요 원인으로, 진행 중인 파이프라인의 임상연구가 지속되는 한 높은 판관비는 지속적으로 발생할 것으로 예상되고 있습니다.
이러한 노력에도 불구하고 당사가 계획하고 있는 연구개발 지연 및 실패하는 경우, 또는 품목허가 및 출시 지연에 따른 화장품 및 바이오파마 제품 생산ㆍ판매 지연 등으로 인해 당사의 매출 계획이 지연될 가능성이 존재합니다. 이에 따라 당사의 영업활동 및 수익성은 부정적인 영향을 받을 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
| 다. 재무안정성 위험 2025년 1분기말 기준 총자산 502억원 및 유동자산 236억원, 총 차입금 84억원, 차입금 의존도 16.8%, 부채비율 31.2%, 유동비율 335.9%를 나타내고 있습니다. 당사의 최근 3개년 부채비율은 2022년 70.5%, 2023년 82.5% 로 증가하는 추세를 보였으나 2024년 29.7%, 2025년 1분기에는 31.2%를 기록하였습니다. 이는 HLB바이오코드 주식회사가 발행했던 제1회 전환사채 및 상환전환우선주부채가 연결 대상에서 제외된 것이 기인했습니다. 당사의 차입금 규모는 2022년 188.1억원, 2023년 192.1억원, 2024년 85억원, 2025년 1분기 84억원입니다. 당사는 2021년 10월 390억원, 2023년 11월 210억원 규모의 유상증자를 통해 재무안정성이 개선되었으나, 지속해서 손실 폭이 커짐에 따라 재무안정성이 다시 악화될 수 있습니다. 향후 각 사업부문 영업 환경이 지속적으로 악화되거나, 줄기세포치료제 등에 지속적인 투자로 인한 자금 소요 등의 예상치 못한 환경의 변화에 따라 외부자금 조달 수요가 발생할 경우 당사에 차입금 상환 부담이 일시적으로 가중될 수 있으며, 당사의 재무안정성 약화로 이어질 위험이 나타날 수 있습니다. 또한, 갑작스러운 영업환경의 변화나 담보가치의 하락으로 인한 담보제공이 현실화될 가능성을 배제할 수는 없으며, 증권신고서 제출 전일 기준 진행 중인 소송은 없지만, 향후 유사의약품 등에 대한 특허권 분쟁, 거래상대방과의 공급계약 또는 수수료 지급, 핵심인력 유출입, 임직원 및 관련자가 당사에 중대한 손해를 입히는 경우 등과 관련된 다양한 종류의 분쟁 또는 소송이 발생할 수 있으며, 이러한 소송이나 분쟁이 발생할 경우 당사의 영업 및 재무구조에 부정적인 영향을 미칠 수 있으므로 투자자께서 유의하시어 투자에 임하시기를 바랍니다. |
당사의 최근 3개년 부채비율은 2022년 70.5%, 2023년 82.5%, 2024년 29.7%로 감소하는 추세를 보였으며 2025년 1분기에는 35.1%를 기록하였습니다. 이는 HLB바이오코드 주식회사가 발행했던 제1회 전환사채 및 상환전환우선주부채가 연결 대상에서 제외된 것이 기인했습니다. 2025년 1분기말 기준 총자산 502억원 및 유동자산 236억원, 총 차입금 84억원, 차입금 의존도 16.8%, 부채비율 31.2%, 유동비율 335.9%를 나타내고 있습니다.
| [요약 재무 현황(연결기준)] | |
| (K-IFRS, 연결) | (단위: 백만원) |
| 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| 자산총계 | 50,204 | 55,986 | 81,253 | 80,592 |
| 유동자산 | 23,576 | 28,528 | 47,366 | 45,907 |
| 비유동자산 | 26,628 | 27,458 | 33,887 | 34,685 |
| 부채총계 | 11,925 | 12,804 | 36,735 | 33,331 |
| 유동부채 | 7,019 | 7,732 | 24,199 | 19,709 |
| 비유동부채 | 4,906 | 5,072 | 12,536 | 13,623 |
| 자본총계 | 38,279 | 43,182 | 44,518 | 47,260 |
| 자본금 | 28,027 | 28,027 | 28,003 | 19,003 |
| 부채비율 | 31.2% | 29.7% | 82.5% | 70.5% |
| 유동비율 | 335.9% | 368.9% | 195.7% | 232.9% |
| 총차입금 | 8,430 | 8,456 | 19,214 | 18,811 |
| 단기 차입금 | 3,330 | 3,330 | 900 | 900 |
| 유동성 장기차입금 | 400 | 400 | 5,530 | 3,700 |
| 유동성전환사채 | - | - | 1,716 | 1,666 |
| 장기차입금 | 2,980 | 2,980 | 3,380 | 5,230 |
| 상환전환우선주부채 | - | - | 5,605 | 5,442 |
| 유동 리스부채 | 301 | 318 | 809 | 752 |
| 비유동 리스부채 | 1,419 | 1,428 | 1,274 | 1,120 |
| 현금및현금성자산 | 2,166 | 2,767 | 5,856 | 4,681 |
| 단기금융상품 | 15,500 | 15,500 | 31,504 | 31,008 |
| 차입금의존도 | 16.8% | 15.1% | 23.6% | 23.3% |
| 출처) 당사 정기보고서 |
한편, 당사의 차입금 규모는 2022년 188.1억원, 2023년 192.1억원, 2024년 85억원, 2025년 1분기 84억원 입니다. 당사는 2021년` 10월 390억원, 2023년 11월 210억원 규모의 유상증자를 통해 재무안정성이 개선되었으나, 지속해서 손실 폭이 커짐에 따라 재무안정성이 다시 악화될 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
2022년~2024년 및 2025년 1분기 연결기준 차입부채의 내역은 다음과 같습니다.
| [차입금 상세 내역] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| 유동 | ||||
| 단기차입금 | 3,330 | 3,330 | 900 | 900 |
| 유동성장기차입금 | 400 | 400 | 5,530 | 3,700 |
| 전환사채(크로엔 CB) | - | - | 1,716 | 1,666 |
| 상환전환우선주부채(크로엔 RCPS) | - | - | 5,605 | 5,442 |
| 소 계 | 3,730 | 3,730 | 13,751 | 11,709 |
| 비유동 | ||||
| 장기차입금 | 2,980 | 2,980 | 3,380 | 5,230 |
| 소 계 | 2,980 | 2,980 | 3,380 | 5,230 |
| 합 계 | 6,710 | 6,710 | 17,131 | 16,938 |
| 출처) 당사 정기보고서 |
| 주1) 당사는 2024년 05월 HLB바이오코드(주)의 보유주식 1,183,676주 중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류되었으며 연결 대상에서 제외되었습니다. |
2025년 1분기말 현재 장단기차입금 내역은 다음과 같습니다.
| [장단기차입금 상세 내역] | |
| (K-IFRS, 연결) | (단위 : 백만원) |
| 구분 | 차입처 | 내역 | 만기일 | 연이자율(%) | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|---|---|---|
| 단기차입금 | 기업은행 | 중소기업자금 | 2025-05-31 | 4.959 | 1,500 | 1,500 | 300 | 300 |
| 중소기업시설자금 | 2025-06-11 | 4.349 | 1,480 | 1,480 | 600 | 600 | ||
| 2025-06-11 | 4.521 | 350 | 350 | - | - | |||
| 유동성장기차입금 | 400 | 400 | 5,530 | 3,700 | ||||
| 단기차입금 소계 | 3,730 | 3,730 | 6,430 | 4,600 | ||||
| 장기차입금 | 기업은행 | 중소기업시설자금 | 2032-06-08 | 4.945 | 3,000 | 3,000 | 3,400 | 3,800 |
| 2025-06-11 | 5.551 | - | - | 1,480 | 1,480 | |||
| 2025-06-11 | 5.490 | - | - | 350 | 350 | |||
| 2026-12-21 | 4.911 | 380 | 380 | 380 | - | |||
| 2024-09-22 | 5.669 | - | - | 3,300 | 3,300 | |||
| 소계 | 3,380 | 3,380 | 8,910 | 8,930 | ||||
| 유동성 대체 | (400) | (400) | (5,530) | (3,700) | ||||
| 장기 차입금 소계 | 2,980 | 2,980 | 3,380 | 5,230 | ||||
| 합계 | 6,710 | 6,710 | 9,810 | 9,830 | ||||
| 출처) 당사 정기보고서 |
한편, 당사는 2025년 1분기 기준 금융기관으로부터 토지 및 시설자금 명목으로 대출을 받았으며, 이와 관련하여 토지 및 건물 등을 담보로 제공하고 있습니다. 2025년 1분기 기준 차입금과 관련하여 담보로 제공된 자산의 내역은 다음과 같습니다.
| [유형자산 담보제공 내역] |
| (단위: 천원) |
| 담보제공자산 | 장부금액 | 담보설정금액 | 담보감정가격 | 관련 계정과목 | 차입금액 | 담보권자 |
|---|---|---|---|---|---|---|
| 토지 | 3,660,774 | 8,796,000 | 11,028,000 | 차입금 | 6,710,000 | 기업은행 |
| 건물 | 7,758,009 |
| 출처) 당사 정기보고서 |
| 주1) 담보제공자산인 토지 및 건물은 글로벌R&D센터줄기세포재생의학연구소(서울 금천구 소재)와 줄기세포GMP센터(경기도 광명시 소재)입니다. |
| 주2) 담보감정가격 감정일은 2021년입니다. |
2025년 1분기 기준 금융기관과의 주요 약정사항은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 금융기관 | 약정금액 | 실행금액 |
|---|---|---|---|
| 시설자본 대출약정 | 기업은행 | 4,000,000 | 3,000,000 |
| 시설자본 대출약정 | 기업은행 | 1,480,000 | 1,480,000 |
| 시설자본 대출약정 | 기업은행 | 350,000 | 350,000 |
| 시설자본 대출약정 | 기업은행 | 380,000 | 380,000 |
| 운전자본 대출약정 | 기업은행 | 1,500,000 | 1,500,000 |
| 출처) 당사 정기보고서 |
더불어, 당사의 대출 및 한도약정과 관련하여 상환을 보증하기 위하여 2025년 1분기 기준 당사가 특수관계자를 제외한 타인으로부터 제공받은 지급보증의 내용은 다음과 같습니다
| [타인으로부터 제공받은 보증내용] |
| (단위 : 천원) |
| 제공자 | 보증자 | 보증일 | 보증금액 | 보증내용 |
|---|---|---|---|---|
| ㈜지에스리테일 | 서울보증보험 | 2024.11.03 ~ 2026.11.02 | 10,000 | 홈쇼핑계약등에 따른 손해배상금 |
| ㈜씨제이이엔엠 | 서울보증보험 | 2023.09.27 ~ 2025.09.26 | 40,000 | 홈쇼핑계약등에 따른 손해배상금 |
| 출처) 당사 정기보고서 |
향후 각 사업부문 영업 환경이 지속적으로 악화되거나, 줄기세포치료제 등에 지속적인 투자로 인한 자금 소요 등의 예상치 못한 환경의 변화에 따라 외부자금 조달 수요가 발생할 경우 당사에 차입금 상환 부담이 일시적으로 가중될 수 있으며, 당사의 재무안정성 약화로 이어질 위험이 나타날 수 있습니다. 또한, 갑작스러운 영업환경의 변화나 담보가치의 하락으로 인한 담보제공이 현실화될 가능성을 배제할 수는 없으며, 증권신고서 제출 전일 기준 진행 중인 소송은 없지만, 향후 유사의약품 등에 대한 특허권 분쟁, 거래상대방과의 공급계약 또는 수수료 지급, 핵심인력 유출입, 임직원 및 관련자가 당사에 중대한 손해를 입히는 경우 등과 관련된 다양한 종류의 분쟁 또는 소송이 발생할 수 있으며, 이러한 소송이나 분쟁이 발생할 경우 당사의 영업 및 재무구조에 부정적인 영향을 미칠 수 있으므로 투자자께서 유의하시어 투자에 임하시기를 바랍니다.
| 라. 영업현금흐름 및 유동성 관련 위험 당사는 수익성 악화 및 지속적인 연구개발 활동으로 인해 음(-)의 영업활동현금흐름을 보이고 있으며, 투자활동현금흐름의 경우, 2022년, 2024년에는 단기금융상품의 처분으로 인해 양(+)의 현금흐름을 보였습니다. 재무활동현금흐름의 경우, 2021년 유상증자를 통해 자금을 조달하며 양(+)의 현금흐름을 보인 이후, 2022년에는 차입금 및 전환사채 등을 상환하며 다시 음(-)의 현금흐름을 보였으며 2023년 유상증자를 통해 자금을 조달하며 양(+)의 현금흐름을 보였습니다. 2024년은 차입금이 증가하며 2개년 연속으로 양(+)의 현금흐름을 보였습니다. 당사의 주요 파이프라인으로는 아토피 피부염 치료제(퓨어스템-에이디 주), 류마티스 관절염(퓨어스템-알에이 주), 골관절염(OSCA, 구.퓨어스템-오에이 키트 주)이 있습니다. 이에 대한 임상시험을 진행하면서 2022년 14,220백만 원, 2023년 14,030백만원, 2024년 12,143백만원, 2025년 1분기 3,231백만 원의 정부보조금을 제외한 경상연구개발비용이 지출되었습니다. 향후 파이프라인별 임상 단계 진전 및 신규 파이프라인 개발에 따라 더 많은 연구개발비가 투입될 예정이며 이에 따라 영업비용 또한 확대될 것으로 예상됩니다. 당사는 상장 이후 지속적인 임상개발과 연구개발활동으로 인해 유동성 지표가 악화되어 왔으며, 향후에도 유의미한 수준의 매출이 발생하지 않아 음(-)의 영업활동현금흐름이 계속 발생할 경우 유동성 리스크가 부각될 위험이 있습니다. 또한, 지속적으로 영업 성과에 부정적인 영향으로 음(-)의 영업활동현금흐름이 발생할 경우 장기적으로 회사의 현금흐름에 문제가 발생할 소지가 있습니다. 투자자께서는 회사의 현금흐름 및 유동성 관련 위험요인을 면밀히 검토하시고 투자에 임해주시기 바랍니다. |
당사는 수익성 악화 및 지속적인 연구개발 활동으로 인해 음(-)의 영업활동현금흐름을 보이고 있으며, 투자활동현금흐름의 경우 2022년, 2024년에는 단기금융상품의 처분으로 인해 양(+)의 현금흐름을 보였습니다. 재무활동현금흐름의 경우, 2021년 유상증자를 통해 자금을 조달하며 양(+)의 현금흐름을 보인 이후, 2022년에는 차입금 및 전환사채 등을 상환하며 다시 음(-)의 현금흐름을 보였으며 2023년 유상증자를 통해 자금을 조달하며 양(+)의 현금흐름을 보였습니다. 2024년은 차입금이 증가하며 2개년 연속으로 양(+)의 현금흐름을 보였습니다. 당사의 최근 3년간 요약 현금흐름 추이는 다음과 같습니다.
| [당사 연결기준 주요 현금흐름 추이] | |
| (K-IFRS, 연결) | (단위: 백만원) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| 영업활동으로 인한 현금흐름 | (321) | (18,987) | (16,498) | (18,864) |
| - 당기순이익(손실) | (4,903) | (7,990) | (23,221) | (20,176) |
| - 이자수취(영업) | 111 | 1,217 | 1,324 | 786 |
| - 이자지급(영업) | (85) | (434) | (567) | (364) |
| - 배당금수취(영업) | - | - | 25 | - |
| - 법인세납부(환급) | (17) | 17 | (73) | (73) |
| 투자활동으로 인한 현금흐름 | (195) | 15,014 | (2,304) | 16,236 |
| - 단기금융상품의 취득 | (163) | (35,600) | (40,080) | (56,742) |
| - 단기금융상품의 처분 | (163) | 51,604 | 39,584 | 64,752 |
| - 대여금의 증가 | - | (730) | - | - |
| - 유형자산의 취득 | (164) | (593) | (1,392) | (712) |
| - 유형자산의 처분 | - | 73 | 28 | 19 |
| - 무형자산의 취득 | - | - | (17) | (135) |
| - 무형자산의 처분 | - | - | 559 | - |
| - 매각예정자산의 처분 | - | - | - | - |
| - 당기손익-공정가치측정금융자산의 취득 | - | - | (2,000) | (1,985) |
| - 당기손익-공정가치측정금융자산의 처분 | - | - | 1,000 | 11,079 |
| - 종속기업투자주식의 처분 | - | 1,270 | - | - |
| - 관계기업투자주식의 취득 | - | (990) | - | - |
| - 임차보증금의 증가 | (57) | (291) | (30) | (67) |
| - 임차보증금의 감소 | 26 | 200 | 29 | 28 |
| - 장기금융상품의 취득 | - | (100) | - | - |
| - 장기금융상품의 처분 |
- | 170 | - | - |
| - 임대보증금의 증가 | - | - | 15 | - |
| 재무활동으로 인한 현금흐름 | (85) | 884 | 19,977 | (231) |
| - 유상증자 | - | - | 20,521 | - |
| - 유동성장기부채의 상환 | - | - | - | - |
| - 차입금의 증가 | - | 3,530 | 380 | 1,100 |
| - 주식발행비용의 환급 | - | - | - | - |
| - 주식선택권행사 | - | - | - | 237 |
| - 전환우선주의 전환 | - | (1) | - | - |
| - 정부보조금의 사용 | - | - | - | - |
| - 차입금의 상환 | - | (2,230) | (400) | (400) |
| - 전환사채의 감소 | - | - | - | (600) |
| - 상환할증금의 상환 | - | - | - | 61 |
| - 리스상환 | (85) | (415) | 523 | 507 |
| 현금및현금성자산의순증가(감소) | (601) | (3,089) | 1,175 | (2,860) |
| 기초 현금및현금성자산 | 2,767 | 5,856 | 4,681 | 7,542 |
| 현금및현금성자산의 환율변동효과 | - | - | - | (1) |
| 기말 현금및현금성자산 | 2,166 | 2,767 | 5,856 | 4,681 |
| 출처) 당사 정기보고서 |
2022년에는 화장품 사업 및 비임상시험 사업의 호조, 바이오파마 사업의 신규 전개 등으로 전년대비 매출은 상승하였지만, 판관비 증가로 당기순손실 20,176백만원이 발생하며 음(-)의 영업활동현금흐름을 보였습니다. 투자활동현금흐름의 경우 단기금융상품 및 당기손익-공정가치측정금융자산의 취득 대비 처분 금액이 높아 16,236백만원의 양(+)의 투자활동현금흐름을 보이고 있습니다. 재무활동현금흐름의 경우 차입금 상환 400백만원, 전환사채 상환 600백만원 및 리스상환 507백만원 등으로 231백만원의 음(-)의 현금흐름을 보이고 있습니다. 이에 2022년말 기준 4,681백만원의 현금 및 현금성자산을 보유하게 되었습니다.
2023년은 당기순손실이 지속됨에 따라 16,498백만원의 음(-)의 영업활동현금흐름을 보였습니다. 투자활동현금흐름의 경우 단기금융상품 40,080백만원 취득 및 유동당기손익인식금융자산 2,000백만원을 취득하는 등 2,304백만원의 음(-)의 투자활동현금흐름을 보이고 있습니다. 재무활동현금흐름의 경우 2023년 11월 유상증자로 자금을 조달하며 19,977백만원의 양(+)의 현금흐름이 발생하였습니다. 이에 2023년말 기준 5,856백만원의 현금 및 현금성자산을 보유하게 되었습니다.
2024년은 당기순손실이 지속됨에 따라 18,987백만원의 음(-)의 영업활동현금흐름을 보였습니다. 투자활동현금흐름의 경우 단기금융상품 51,604백만원을 처분하는 등 15,013백만원의 양(+)의 투자활동현금흐름을 보였습니다. 재무활동현금흐름의 경우 차입금 3,530백만원 증가 등 884백만원의 양(+)의 현금흐름을 보이고 있습니다. 이에 2024년 말 2,767백만원의 현금 및 현금성자산을 보유하게 되었습니다.
2025년 1분기는 당기순손실 지속됨에 따라 320백만원의 음(-)의 영업활동현금흐름을 보였으나 전년도 대비 53.6억 증가하며 크게 개선되었습니다. 투자활동현금흐름의 경우 단기금융상품 163백만원 취득 및 유형자산 164백만원 취득 등으로 195백만원의 음(-)의 투자활동현금흐름을 보이고 있습니다. 재무활동현금흐름의 경우 리스 상환으로 인해 85백만원의 음(-)의 현금흐름을 보이고 있습니다. 이에 2025년 1분기 기준 2,166백만원의 현금 및 현금성자산을 보유하게 되었습니다.
당사의 주요 파이프라인으로는 아토피 피부염 치료제(퓨어스템-에이디 주), 류마티스 관절염(퓨어스템-알에이 주), 골관절염(OSCA, 구.퓨어스템-오에이 키트 주)이 있습니다. 이에 대한 임상시험을 진행하면서 2022년 14,220백만 원, 2023년 14,030백만원, 2024년 12,143백만원, 2025년 1분기 3,231백만 원의 정부보조금을 제외한 경상연구개발비용이 지출되었습니다. 향후 파이프라인별 임상 단계 진전 및 신규 파이프라인 개발에 따라 더 많은 연구개발비가 투입될 예정이며 이에 따라 영업비용 또한 확대될 것으로 예상됩니다.
| [연구개발비용 현황(연결기준)] |
| (단위 : 백만원, %) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | |
|---|---|---|---|---|---|
|
비용의 성격별 분류 |
원재료 | 110 | 726 | 917 | 880 |
| 인건비 | 1,238 | 4,481 | 4,989 | 4,675 | |
| 감가상각비 | 560 | 2,168 | 2,117 | 2,112 | |
| 위탁용역비 | 937 | 2,898 | 3,573 | 4,029 | |
| 기타 | 519 | 2,689 | 2,961 | 3,701 | |
| 연구개발비용 합계 | 3,365 | 12,962 | 14,558 | 15,398 | |
|
회계처리 내역 |
판매비와관리비 | 3,231 | 12,143 | 14,030 | 14,220 |
| 정부보조금 | 134 | 819 | 528 | 1,178 | |
| 연구개발비용 합계 | 3,365 | 12,962 | 14,558 | 15,398 | |
|
연구개발비/매출액 비율 [연구개발비용합계/당기매출액*100] |
353 | 167 | 114.6 | 94.5 | |
| 출처) 당사 정기보고서 |
| 주1) 상기 연구개발비는 연결기준이고, 당사의 연구개발비는 향후 발생시점에 전액 비용 처리할 계획입니다. |
당사는 2022년 현금및현금성자산 46.8억원 및 단기금융상품 310.1억원, 2023년 현금및현금성자산 58.6억원 및 단기금융상품 315.0억원, 2024년 현금및현금성자산 27.7억원 및 단기금융상품 155.0억원, 2025년 1분기 현금및현금성자산 21.7억원 및 단기금융상품 155.0억원을 보유하고 있습니다.
당사는 2018년 07월(359억원), 2019년 07월(480억원), 2021년 10월(390억원), 2023년 11월(210억원) 네 차례 유상증자를 통해 자금을 조달했습니다. 조달한 공모자금은 코로나19 확산, 임상시험 지연, 운영 상황 등에 따라 사용 시기가 변경되거나 지연되었지만, 주로 주요 파이프라인의 임상시험비용과 후속 파이프라인의 임상시험 및 기초연구비와 운영경비로 사용되어 왔습니다.
한편, 당사의 2025년 1분기 유동비율은 335.9%로 최근 3개년 유동비율 추이는 다음과 같습니다.
| [유동비율 추이] |
| (단위 : 백만원) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| 유동자산 | 23,576 | 28,528 | 47,366 | 45,907 |
| 유동부채 | 7,019 | 7,732 | 24,199 | 19,709 |
| 유동비율(%) | 335.9% | 368.9% | 195.7% | 232.9% |
| 출처) 당사 정기보고서 |
당사의 최근 3개년 영업활동현금흐름은 연결기준으로 각각 2022년 (-)188.6억원, 2023년 (-)165.0억원, 2024년 (-)190.0억원, 2025년 1분기 (-)3억원입니다. 당사의 영업활동현금흐름은 부(-)의 흐름이 지속되고 있으며, 그 밖에 유형자산 취득 등으로 자금이 소요되었으나, 유상증자로 자금이 유입되면서 양호한 수준의 유동성을 유지하고 있습니다.
당사는 현금흐름 및 유동성에 대하여 지속적으로 모니터링하면서 유동성 이슈가 발생하지 않도록 대응하고 있으나, 당사는 상장 이후 지속적인 임상개발과 연구개발활동으로 인해 유동성 지표가 악화되어 왔으며, 향후에도 유의미한 수준의 매출이 발생하지 않아 음(-)의 영업활동현금흐름이 계속 발생할 경우 유동성 리스크가 부각될 위험이 있습니다. 또한, 지속적으로 영업 성과에 부정적인 영향으로 음(-)의 영업활동현금흐름이 발생할 경우 장기적으로 회사의 현금흐름에 문제가 발생할 소지가 있습니다. 투자자께서는 회사의 현금흐름 및 유동성 관련 위험요인을 면밀히 검토하시고 투자에 임해주시기 바랍니다.
| 마. 관리종목 편입 및 상장폐지 가능성에 따른 위험 당사는 기술성장특례 적용 기업으로 2015년에 12월에 상장하여 관리종목 지정요건 중 유예 항목들에 대한 적용 기간이 만료되었습니다. 이에 따라 당사가 매출액 및 법인세비용차감전계속사업손실 요건, 자본잠식 요건 등을 충족하지 못할 경우 향후 관리종목으로 지정될 가능성이 있습니다. 당사는 2023년 법인세비용차감전계속사업손실률이 51.9%까지 증가하였으며 관리종목 지정 리스크가 발생하였습니다. 2024년 법차손률이 16.4%를 기록하며 대폭 개선되었으나, 2025년 사업연도말의 법차손률이 50%를 상회할 경우 최근 3사업연도중 2사업연도(2023년, 2025년)의 법차손률이 50%를 상회함에 따라 관리종목으로 지정될 수 있습니다. 당사는 2024년 5월 HLB바이오코드 주식회사 지분 매각을 통해 연결 손실 인식을 방지하고, 동시에 98억원의 처분이익이 발생하며 2024년 법차손률 16.4%로 큰 폭으로 개선되었습니다. 다만, 2024년 지분 매각으로 인한 처분이익 98억원의 경우 일회성 이익에 해당하여 당사의 2025년 영업수익성에 미치는 영향은 미미한 것으로 판단됩니다. 따라서, 2025년 법인세비용차감전계속사업손실이 전년도 대비 증가할 가능성이 있으니 투자자들께서는 이 점을 유의하여 주시기 바랍니다. 또한, 현재 당사는 OSCA 라이선스 아웃 계약에 따른 단계별 선급기술료 수취 및 임상비용 절약, 일본 재생의료 매출 발생 등 수익성 향상을 위해 노력중입니다. 동시에, 금번 유상증자를 통한 자본규모 확충을 기대 중이며, 계획한 수익성 향상 노력과 자금조달이 모두 성공적으로 이루어질 경우 2025년 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 발생할 가능성은 낮을 것으로 판단됩니다. 다만. 이러한 당사의 노력에도 불구하고 사업환경이 급격히 악화되어 당사의 임상 및 연구개발 지연으로 매출 저조 등 재무성과를 나타내지 못하거나 유상증자에 실패하여 법인세비용차감전계속사업손실률이 50%를 상회할 경우 관리종목으로 지정 요건에 해당할 수 있으니 투자자들께서는 이점 유의하시기 바랍니다. 2025년 01월 21일 금융위원회와 금융감독원, 한국거래소, 금융투자협회, 자본시장연구원이 발표한 'IPO 및 상장폐지 제도 개선 방안'에 따르면 시가총액이 600억원 미만인 코스닥 상장 법인의 상장 유지를 위한 매출 요건이 강화되었습니다. 당사의 최근 3년간 별도기준 매출액 중 2022년과 2023년은 각각 59.2억원, 59.1억원으로 2028년부터 적용되는 매출요건 75억을 하회합니다. 한편, 2024년 매출액은 77.5억원으로, 2029년부터 적용되는 매출요건 100억원을 하회합니다. 다만, 당사의 최근 시가총액은 2028년부터 적용되는 최소 시가총액 요건인 600억원을 상회하고 있기 때문에, 현재 시가총액 수준을 유지한다면 해당 사항은 없을 것으로 보입니다. 그러나, 향후 당사의 매출 성장성이 둔화되어 매출이 악화되고 시가총액 수준이 지속적으로 하락할 경우 금융당국의 강화된 상장폐지 요건에 해당될 가능성이 있습니다. 투자자들께서는 투자 판단 시 최근 상장폐지 요건 강화에 따른 상장폐지 위험에 대해서 충분히 인지하시길 바랍니다. |
「코스닥시장 상장규정」제53조(관리종목)은 매출액, 법인세비용차감전계속사업손실, 자본잠식 등 코스닥시장 상장법인으로서의 경영성과 및 재무상태에 미달하는 경우 관리종목을 지정하도록 명시되어 있습니다. 당사는 기술성장특례 적용 기업으로 2015년에 12월에 상장하여 관리종목 지정요건 중 유예 항목들에 대한 적용 기간이 만료되었습니다. 이에 따라 당사가 매출액 및 법인세비용차감전계속사업손실 요건, 자본잠식 요건 등을 충족하지 못할 경우 향후 관리종목으로 지정될 가능성이 있습니다.
| [코스닥시장 관리종목 지정요건 및 해당여부 검토] |
| 구 분 | 관리종목 지정(코스닥 상장규정 제53조) | 관리종목지정유예 | 관리종목 지정요건 적용여부 |
회사현황 | ||
|---|---|---|---|---|---|---|
| 해당여부 | 유예기간 | 사업연도 | 금액(백만원) / 비율(%) / 내용 | |||
| (1) 매출액 미달 | 최근 사업연도 30억원 미만 (지주회사는 연결기준) - 이익미실현기업 또는 기술성장기업은 상장후 5년간 미적용 - 기술성장기업 중 A), B), C) 중 어느 하나에 해당하는 제약·바이오기업은 최근 사업연도 미적용 A) 최근 사업연도 말「제약산업 육성 및 지원에 관한 특별법」에 따른 혁신제약기업이 세칙으로 정한 요건을 충족하는 경우 B) 최근 사업연도의 일평균 시가총액 4,000억 이상이며, 그 금액이 현재의 자본금을 초과하는 기업이 세칙으로 정하는 요건을 충족하는 경우 C) 최근 3사엽언도의 매출액 합계 90억 이상이며, 최근 사업연도의 직전 사업연도의 매출액이 30억 이상인 경우 |
- | - | 현재 미해당 | 2024년말 | 매출액 : 7,746백만원 (K-IFRS 별도기준) |
| 2025년 1분기말 | 매출액 : 954백만원 (K-IFRS 별도기준) |
|||||
| (2) 법인세비용차감전 계속사업손실 |
최근 3사업연도중 2사업연도에 각각 10억원 이상이면서 해당 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 있고 최근사업연도에 법인세비용차감전계속사업손실이 있는 경우 - 이익미실현 기업은 상장 후 5년간 미적용 (다만, 상장일부터 상장일이 속한 사업연도의 말일까지의 기간이 3개월 미만인 경우에는 상장일이 속하는 사업연도와 그 이후 5개 사업연도로 한다) - 기술성장기업은 상장후 3년간 미적용(다만, 상장일부터 상장일이 속한 사업연도의 말일까지의 기간이 3개월 미만인 경우에는 상장일이 속하는 사업연도와 그 이후 3개 사업연도로 한다) |
- | - | 2023년이 해당되며 2024년은 미해당, 2025년 해당될 경우 관리종목 지정 |
2023년말 | 세전손실 : (23,137)백만원 자기자본 : 44,517백만원 (자기자본 대비 51.9%) |
| 2024년말 | 세전손실 : (7,083)백만원 자기자본 : 43,182백만원 (자기자본 대비 16.4%) |
|||||
| 2025년 1분기말 | 세전손실 : (4,903)백만원 자기자본 : 38,279백만원 (자기자본 대비 12.8%) |
|||||
| (3) 자본잠식 등 | 최근 사업연도말 현재 자본잠식률이 100분의 50 이상인 경우 | - | - | 현재 미해당 | 2024년말 | 자본금 : 28,027백만원 지배주주지분 : 43,182백만원 자본잠식률 : 해당없음 |
| 2025년 1분기말 | 자본금 : 28,027백만원 지배주주지분 : 38,279백만원 자본잠식률 : 해당없음 |
|||||
| (4)자기자본 미달 | 최근 사업연도말 현재 자기자본이 10억원 미만인 경우 | - | - | 현재 미해당 | 2024년말 | 지배주주지분 : 43,182백만원 |
| 2025년 1분기말 | 지배주주지분 : 38,279백만원 | |||||
| (5) 시가총액 미달 | 보통주 시가총액 40억원미만 30일간 지속 - 천재지변, 시장상황의 급격한 변동 등으로 거래소가 시장 관리를 위하여 필요하다고 인정될 경우 적용배제 가능 |
- | - | 현재 미해당 | 2024년 12월 31일 |
시가총액 : 113,229백만원 |
| 증권신고서 제출일 전일 기준 |
시가총액 : 84,754백만원 |
|||||
| (6) 정기보고서 미제출 | 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않은 경우 | - | - | 현재 미해당 | 현재 기준 | 현재 특이사항 없음 |
| (7) 지배구조 미달 | 최근 사업연도 사업보고서상 A)사외이사의 수가 「상법」 제542조의8의 규정에서 정하는 수에 미달하는 경우 B) 「상법」 제542조의11의 규정에서 정하는 감사위원회를 구성하지 않거나 감사위원회의 구성요건을 충족하지 못하는 경우 *「상법」 제542조의8에 의거 자산총액 1,000억원 미만의 코스닥 상장 벤처기업은 사외이사 선임 의무 면제 **「상법」 제542조의11에 의거 자산총액 2조원 미만의 상장회사는 감사위원회 설치 의무 면제 |
- | - | 현재 미해당 | 2024년말 | 현재 특이사항 없음 |
| (8) 거래량 미달 | 분기월평균거래량이 유동주식수의 1%에 미달 다만, 다음 어느 하나에 해당하는 경우에는 이 호에 적용 받지 않습니다. - 신규상장법인(신규상장일이 속하는 분기에 한정) - 분기의 월평균거래량 1만주 이상(액면가액 5,000원 기준) - 「코스닥시장 업무규정」(이하 “업무규정”이라 한다) 제12조의3제1항에 따른 유동성공급계약이 체결된 경우 - 소액주주가 소유한 보통주식의 총수가 유동주식수의 100분의 20 이상이고, 해당 소액주주의 수가 300명 이상인 경우. |
- | - | 현재 미해당 | 2025년 1분기말 | 소액주주 - 지분율 77.58% - 19,291명 |
| (9) 주식분산 미달 | 소액주주 200인미만 or 소액주주지분 20%미만 - 300인이상의 소액주주가 유동주식수의 10%이상으로서 100만주이상을 소유, 해외증권시장에 상장된 경우는 적용배제 |
- | - | 현재 미해당 | 2025년 1분기말 | 소액주주 - 지분율 77.58% - 19,291명 |
| (10) 회생절차 개시신청 | "채무자 회생 및 파산에 관한 법률" 제34조에 의한 회생 절차개시 신청이 있는 경우 | - | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| (11) 파산신청 | 코스닥시장 상장법인에 대하여 "채무자 회생 및 파산에 관한 법률" 제294조에 의한 파산신청이 있는 경우 | - | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| (12) 기타 | - 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 - 변경·추가상장이 유예된 기간 중에「증권의 발행 및 공시 등에 관한 규정」에 따른 재무관리기준을 위반한 경우 |
- | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| 출처)「코스닥시장 상장규정」, 당사 정기보고서 |
| 주1) 상기 도표 중 (1)매출액 미달 요건 관련하여, 별도재무제표를 기준으로 합니다. 그 외 요건은 연결재무제표를 기준으로 합니다. |
| 주2) (2)법인세비용차감전계속사업손실 요건 관련하여, 자기자본은 비지배지분을 제외하지 않은 금액 기준을 적용합니다. (3)자본잠식 등, (4)자기자본 미달 요건 관련하여, 자기자본은 비지배지분을 제외한 지배기업지분금액 기준을 적용합니다. |
(1) 매출액 미달 여부 검토
| [최근 3개년 매출액] |
| (단위 : 백만원) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| 매출액 (별도) | 954 | 7,746 | 5,913 | 5,915 |
| 자료 : 당사 정기보고서 |
「코스닥시장 상장규정」 제53조 1항 1호에 따라 최근 사업연도의 매출액이 30억 미만일 경우 관리종목으로 지정됩니다. 상기한 바와 같이 당사는 기술성장특례 적용 기업으로서, 최근사업연도의 매출액 미달 요건으로 인한 관리종목 지정 유예를 받았으나, 현재는 유예기간이 종료되었습니다. 따라서 당사는 매년 매출액(K-IFRS 개별/별도 기준) 30억원 이상 달성해야 관리종목에 지정되지 않습니다. 당사의 별도 기준 매출액은 2022년 약 59억원, 2023년 약 59억원, 2024년 약 77억원으로, 최근 3개년 모두 30억원을 초과하여 관리종목 지정 사유에 해당되지 않습니다.
한편, 2025년 01월 21일 금융위원회와 금융감독원, 한국거래소, 금융투자협회, 자본시장연구원이 발표한 'IPO 및 상장폐지 제도 개선 방안'에 따르면 상장 유지를 위한 매출 요건이 강화되었습니다. 향후 시가총액이 600억원 미만인 코스닥 상장 법인은 2027년 50억원, 2028년 75억원, 2029년 100억원 이상의 매출을 달성해야합니다. 증권신고서 제출일 기준, 당사의 시가총액은 600억원 이상이기 때문에, 향후 현 수준의 시가총액을 유지할 경우 해당 사항이 없을 것으로 판단됩니다.
당사는 2022년 이후 매출액이 지속적으로 50억원을 상회하고 있으며, 현재 매출액 기준으로 관련 요건을 충족하고 있습니다. 다만, 향후 현재 수준보다 매출이 큰 폭으로 감소되어 매출액(별도 기준) 30억원을 유지하지 못하거나, 시가총액이 600억원 미만으로 떨어지고 당사의 매출액이 강화된 기준에 하회할 경우 금융당국의 상장폐지 요건 강화 정책에 의해 2027년 이후 해당 사유가 발생할 수 있으니, 투자자 여러분께서는 이 점 유의하시기 바랍니다.
(2) 법인세비용차감전계속사업손실 발생 여부 검토
| [최근 3개년 법인세비용차감전계속사업손실] |
| (단위 : 백만원) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| (법인세비용차감전계속사업손실/자기자본)×100(%) | 12.8% | 16.4% | 51.9% |
42.7% |
| 법인세비용차감전계속사업손실 | 4,903 | 7,083 | 23,137 | 20,215 |
| 자기자본 | 38,279 | 43,182 | 44,517 | 47,260 |
| 출처) 당사 정기보고서 |
한편, 당사는 2023년 법인세비용차감전계속사업손실률이 51.9%까지 증가하였으며 관리종목 지정 리스크가 발생하였습니다(최근 3개년 중 1년 해당됨). 2024년 법차손률이 16.4%를 기록하며 대폭 개선되었으나, 2025년 사업연도말의 법차손률이 50%를 상회할 경우 최근 3사업연도중 2사업연도(2023년, 2025년)의 법차손률이 50%를 상회함에 따라 관리종목으로 지정될 수 있습니다.
2023년 당사의 연결대상 종속회사인 HLB바이오코드(구.주식회사 크로엔)의 매출 및 손익이 크게 악화되었고, 그에 따른 연결 손실을 인식함으로써 법인세비용차감전계속사업손실률이 51.9%까지 증가하였습니다. 2024년 HLB바이오코드의 손실이 지속될 것으로 예상되어, 계속해서 지분을 보유할 경우 당사의 재무적 악화 및 관리종목 지정 리스크에 여전히 영향을 미칠 것으로 예상되었고, 2024년 5월 HLB바이오코드 주식회사 지분 매각을 결정하였습니다. 이를 통해 연결 손실 인식을 방지하고, 동시에 98억원의 처분이익이 발생하며 2024년 법차손률 16.4%로 큰 폭으로 개선되었습니다. 다만, 2024년 지분 매각으로 인한 처분이익 98억원의 경우 일회성 이익에 해당하여 당사의 2025년 영업수익성에 미치는 영향은 미미한 것으로 판단됩니다. 따라서, 2025년 법인세비용차감전계속사업손실이 전년도 대비 증가할 가능성이 있으니 투자자들께서는 이 점을 유의하여 주시기 바랍니다.
현재 당사는 OSCA의 국내 라이선스 아웃 계약에 따른 단계별 선급기술료 수취 및 임상비용 절약, 일본 재생의료 매출 발생 등 수익성 향상을 위해 노력중입니다. 동시에, 금번 유상증자를 통한 자본규모 확충을 기대 중이며, 계획한 수익성 향상 노력과 자금조달이 모두 성공적으로 이루어질 경우 2025년 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 발생할 가능성은 낮을 것으로 판단됩니다. 다만, 이러한 당사의 노력에도 불구하고 사업환경이 급격히 악화되어 당사의 임상 및 연구개발 지연으로 매출 저조 등 재무성과를 나타내지 못하거나 유상증자에 실패하여 법인세비용차감전계속사업손실률이 50%를 상회할 경우 관리종목으로 지정 요건에 해당할 수 있으니 투자자들께서는 이점 유의하시기 바랍니다.
(3) 자본잠식 여부 검토
| [자본잠식 여부 검토] |
| (단위 : 백만원) |
| 구분 | 2025년 1분기말 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| 비지배지분 제외 자기자본(연결) | 38,279 | 43,182 | 48,012 | 49,370 |
| 자기자본(연결) | 38,279 | 43,182 | 44,518 | 47,260 |
| 자본금 | 28,027 | 28,027 | 28,003 | 19,003 |
| 자본잠식률 | - | - | - | - |
| 자본잠식여부 | 미해당 | 미해당 | 미해당 | 미해당 |
| 출처) 당사 정기보고서 |
| 주1) 자본잠식률 = 1-{비지배지분 제외 자본총계 / 자본금} |
「코스닥시장 상장규정」 제53조 1항 4호에 따라 최근 사업연도 말을 기준으로 자본잠식률 50%이상인 경우 관리종목으로 지정됩니다. 당사는 최근 사업연도 말(2024년 말) 기준으로 자본잠식 상태가 아니며, 2025년 1분기말 기준으로도 자본잠식 요건에 의한 관리종목 지정 요건에 해당하지 않습니다. 또한, 본 유상증자 후에는 자본금 대비 자기자본 확대가 다시 한번 이루어지므로 2025년 중 자본잠식에 의한 관리종목 지정 위험은 대응 가능할 것으로 판단하고 있습니다. 다만, 대규모 손실 발생시에는 자기자본이 크게 감액될 경우 자본잠식으로 인한 관리종목 지정 가능성이 있으므로 투자자 여러분들께서는 이 점 유의하시기 바랍니다.
(4) 시가총액 미달여부 검토
| [최근 3개년 시가총액 추이] |
| (단위: 백만원) |
| 구분 | 시가총액(최고) | 시가총액(최저) |
|---|---|---|
| 2025년 1분기 | 135,090 | 109,306 |
| 2024년 | 200,258 | 78,812 |
| 2023년 | 133,971 | 49,699 |
| 2022년 | 160,477 | 95,414 |
| 출처) KRX 정보데이터시스템 |
「코스닥시장 상장규정」 제53조 1항 5호에 따라 보통주 시가총액 40억원 미만 30일간 지속되는 경우 관리종목으로 지정됩니다. 당사의 2025년 1분기 시가총액은 최고 1,351억원, 최저 1,093억원입니다. 또한 최근 3개년 최저 시가총액은 2022년 954억원, 2023년 497억원, 2024년 788억원으로 40억원 미만을 기록한 바 없어 해당 관리종목 지정요건에 해당하지 않습니다.
한편, 2025년 01월 21일 금융위원회와 금융감독원, 한국거래소, 금융투자협회, 자본시장연구원이 발표한 'IPO 및 상장폐지 제도 개선 방안'에 따르면 상장 유지를 위한 시가총액 요건이 강화되었습니다. 향후 코스닥 상장 법인은 2026년 150억원, 2027년 200억원, 2028년 300억원 이상의 시가총액을 달성해야합니다. 증권신고서 제출일 기준, 당사의 시가총액은 2028년 최종 상향 목표치인 300억원 이상으로, 현재 수준의 시가총액을 유지할 경우 해당 사항은 없을 것으로 판단됩니다. 다만, 향후 당사의 시가총액이 감소하여 강화된 기준에 하회할 경우 금융당국의 상장폐지 요건 강화 정책에 의해 상장폐지 사유에 해당될 수 있으니 투자자 여러분께서는 이 점 유의하시기 바랍니다.
(5) 정기보고서 미제출 여부 검토
「코스닥시장 상장규정」제53조 1항 6호에 따라 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않은 경우 관리종목으로 지정됩니다. 당사는 최근일 현재까지 정기보고서를 법정제출기한 내에 제출한 바 관리종목 지정요건에 해당하지 않습니다.
(6) 지배구조 미달 여부 검토
「코스닥시장 상장규정」 제53조 1항 7호에 따라 최근 사업연도 사업보고서상 A)사외이사의 수가 법에서 정하는 수에 미달, B) 법에서 정하는 감사위원회를 구성하지 않거나 구성요건을 충족하지 아니하는 경우 관리종목으로 지정됩니다.
당사는 벤처기업에 해당되며, 2025년 1분기말 기준 자산총액이 약 502억원으로 상법 시행령」 제34조제1항1호에 따라 자산총액이 1천억원 미만입니다. 이에 따라, 사외이사 선임 및 감사위원회 구성 의무가 면제되기 때문에, 현재까지는 지배구조 요건 미달에 따른 관리종목 지정 요건에 해당하지 않습니다.
(7) 거래량 미달 여부 검토
「코스닥시장 상장규정」 제53조 1항 8호에 따라 분기월평균거래량이 유동주식수의 1%에 미달하는 경우 관리종목으로 지정됩니다. 다만, 다음 어느 하나에 해당하는 경우에는 이 호에 적용 받지 않습니다. 가) 신규 신규상장법인의 경우. 다만, 신규상장일이 속하는 분기에 한정하는 경우, 나) 분기의 월평균거래량이 1만주 이상인 경우. 이 경우 보통주식 상장법인이 액면주식을 발행한 때에는 액면가액 5,000원을 기준, 다) 세칙으로 정하는 소액주주가 소유한 보통주식의 총수가 유동주식수의 100분의 20 이상이고, 해당 소액주주의 수가 300명 이상인 경우. 이 경우 소액주주가 소유한 주식 수와 소액주주의 수는 최근 사업연도 말을 기준으로 하되, 최근 사업연도 말 이후 주주명부를 폐쇄한 경우에는 그 폐쇄시점 현재를 기준으로 거래소에 제출한 주주명부 및 「주식·사채 등의 전자등록에 관한 법률」에 따른 소유자명세를 기준으로 하는 경우입니다.
| [관리종목 지정 관련 주요 거래량 검토] | |
| (단위 : 주, %) | |
| 구분 | 2025년 1분기 |
|---|---|
| 월평균 거래량 | 381,396 |
| 분기말 유동주식수 | 56,054,149 |
| 비율 (주1) | 0.68% |
| 출처) 한국거래소 정보데이터시스템, Dart 전자공시시스템 주1): 비율 = 분기월평균거래량 / 유동주식수 |
당사는 2025년 1분기 기준 월평균거래량이 381,396주로 유동주식수의 0.68%에 해당하여 1% 이하이지만 소액주주 지분율 78.75%, 소액주주 수 18,315명임에 따라 상기 다) 항목에 해당되어 거래량 미달에 의한 관리종목 지정요건에 해당하지 않습니다.
(8) 주식분산 미달 여부 검토
「코스닥시장 상장규정」 제53조 1항 9호에 따라 최근 사업연도말 소액주주가 200인 미만이거나 소액주주지분이 20% 미만일 경우 관리종목으로 지정됩니다.
당사는 최근사업연도말(2024년) 소액주주 지분율 77.58%, 소액주주 수 19,291명이며, 2025년 1분기 기준 소액주주 지분율 78.75%, 소액주주 수 18,315명임에 따라 주식분산 미달에 의한 관리종목 지정요건에 해당하지 않습니다.
(9) 기타사항
「코스닥시장 상장규정」 제53조 1항 10호에서 13호까지에 따라 회생절차개시신청, 파산신청, 상장폐지사유발생, 재무관리기준 위반 요건에 해당하는 경우 관리종목으로 지정됩니다. 당사는 현재까지는 상기 기타사항 관련하여, 관리종목 지정 요건에 해당되지 않습니다.
관리종목 지정사유 확인 당일에는 코스닥시장에서의 거래는 정지되며, 이를 기한 내에 해결하지 못한다면 코스닥시장 상장폐지 사유에 해당하여, 당사 주식은 향후 장내에서 거래가 이루어지지 못할 수 있습니다. 투자자 여러분들께서는 당사의 주식이 상장폐지될 경우, 투자금액을 회수하지 못하게 될 수도 있는 점을 반드시 유의하여 주시기 바랍니다. 이에 투자자 여러분들께서는 코스닥시장에서의 관리종목, 상장폐지와 관련된 규정을 반드시 유의하시고, 당사의 영업 수익성 추이에 대하여 지속적으로 모니터링하시기 바랍니다.
(10) 상장폐지 요건 강화
| [IPO 및 상장 폐지 제도개선 방안 및 해당여부 검토] |
| 구 분 | IPO 및 상장 폐지 제도개선 방안 | 상장폐지 지정요건 적용여부 |
회사현황 | |
|---|---|---|---|---|
| 사업연도 | 금액(백만원) / 내용 | |||
| (1) 시가총액 요건 기준 강화 | 정량요건으로서 시장평가 관련 시가총액 기준을 단계적으로 상향하여 코스피 500억원, 코스닥 300억원을 목표로 합니다. - 코스피 : 50억원(현행) → 200억원(2026년) → 300억원(2027년) → 500억원(2028년) - 코스닥 : 40억원(현행) → 150억원(2026년) → 200억원(2027년) → 300억원(2028년) |
현재 미해당 | 2024년 12월 31일 |
시가총액 : 113,229백만원 |
| 증권신고서 제출일 전일 기준 |
시가총액 : 84,754백만원 |
|||
| (2) 매출액 요건 기준 강화 | 정량요건으로서 기업실적 관련 매출액 기준을 단계적으로 상향하여 코스피 300억원(시가총액 1,000원 미만 기업만 적용), 코스닥 100억원(시가총액 600억원 미만 기업만 적용)을 목표로 합니다. - 코스피 : 50억원(현행) → 100억원(2027년) → 200억원(2028년) → 300억원(2029년) - 코스닥 : 30억원(현행) → 50억원(2027년) → 75억원(2028년) → 100억원(2029년) |
현재 미해당 | 2024년말 | 매출액 : 7,746백만원 (K-IFRS 별도기준) |
| 2025년 1분기말 | 매출액 : 954백만원 (K-IFRS 별도기준) |
|||
| (3) 감사의견 미달 요건 기준 강화 | - 2회 연속 감사의결 미달시 즉시 상장폐지 : 감사의견 미달(한정, 부적정, 의견거절)의 경우 2회 연속발생시 즉시 상장폐지되고(회생 ·워크아웃기업에 대해서는 예외인정), 이의신청은 허용되지 않습니다. | 현재 미해당 | 2024년말 | 해당사항 없음 |
| 2023년말 | 해당사항 없음 | |||
| 출처) 금융위원회, 당사 정기보고서 |
또한, 2025년 01월 21일, 정부와 유관기관(금융위원회, 금융감독원, 한국거래소, 금융투자협회)은 주식시장의 질적수준 제고를 위한「IPO 및 상장 폐지 제도개선 방안」을 발표하였습니다. 이 중 상장폐지 제도개선 방안은 상장유지 요건을 강화하고, 절차는 효율화함으로써 주식시장 내 저성과 기업을 적시에 퇴출시키고 상장기업의 밸류업을 주요 목적으로 하고 있습니다. 이와 같이 상장폐지 요건이 강화됨에 따라 당사의 영업환경 악화, 재무요건 악화 등을 원인으로 강화된 상장폐지 요건에 해당되어 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있음을 투자자분들은 유의하시기 바랍니다.
당사의 최근 3년간 별도기준 매출액 중 2022년과 2023년은 각각 59.2억원, 59.1억원으로 2028년부터 적용되는 매출요건 75억을 하회합니다. 한편, 2024년 매출액은 77.5억원으로, 2029년부터 적용되는 매출요건 100억원을 하회합니다. 다만, 당사의 최근 시가총액은 2028년부터 적용되는 최소 시가총액 요건인 600억원을 상회하고 있기 때문에, 현재 시가총액 수준을 유지한다면 해당 사항은 없을 것으로 보입니다. 그러나, 향후 당사의 매출 성장성이 둔화되어 매출이 악화되고 시가총액 수준이 지속적으로 하락할 경우 금융당국의 강화된 상장폐지 요건에 해당될 가능성이 있습니다. 투자자들께서는 투자 판단 시 최근 상장폐지 요건 강화에 따른 상장폐지 위험에 대해서 충분히 인지하시길 바랍니다.
한편, 비재무적 요건 중 감사의견 관련 기준도 강화될 예정입니다. 현재는 감사의견 거절 또는 부적정 발생 시 이의신청이 가능하며, 이후 사업연도까지 개선기간이 부여되는 완화된 제도가 적용되고 있으나, 2025년 7월 1일부로 개정안이 시행되면 2개 사업연도 연속으로 감사의견이 미달되는 경우 이의신청 없이 곧바로 상장폐지 절차가 진행됩니다.
금융당국은 이와 같은 제도 강화를 통해 상장기업의 회계 투명성과 신뢰성을 제고하고, 시장 건전성을 확보하고자 하고 있으며, 이에 따라 향후 유가증권시장 및 코스닥시장에서 상장폐지 요건은 점차 엄격하게 적용될 전망입니다. 이에 따라 현행 기준으로 당사는 어떠한 재무적 또는 비재무적 상장폐지 요건에도 해당되지 않으나, 당사가 이후 영업실적의 악화나 재무구조의 급격한 변화 등에 의해 강화된 상장폐지 요건에 해당될 가능성도 존재하므로, 투자자께서는 이 점 유의하여 주시기 바랍니다.
당사는 증권신고서 제출일 전일 기준 「코스닥시장 상장규정」 상 관리종목 지정 및 상장폐지요건에 해당하는 경우는 없습니다. 하지만 당사는 코스닥시장에서의 주요 관리종목 지정 요건 중 법인세비용차감전계속사업손실 요건에 해당될 수 있는 위험이 큰 상태입니다. 2025년 사업연도말 자기자본총계 대비 50%를 초과하는 법인세비용차감전계속사업손실이 발생할 경우 당사는 관리종목으로 지정됩니다. 또한, 향후 당사의 시가총액이 600억 원 미만으로 떨어져 당사의 매출액이 강화된 기준에 하회할 경우 금융당국의 상장폐지 요건 강화 정책에 의해 해당 사유가 발생할 수 있으며, 향후 적자 상태가 지속될 경우 관리종목 및 상장폐지 요건에 해당될 가능성이 존재하므로, 투자자께서는 이 점 유의하시기 바랍니다.
| 바. 매출채권 및 재고자산 관련 위험 당사의 2025년 1분기 매출채권 총액은 16.0억원으로 2024년말 매출채권 52.7억원 대비 36.7억원 감소하였습니다. 매출채권 회수를 측정하는 주요 지표인 매출채권 회전율은 2022년 3.0회, 2023년는 2.4회, 2024년 1.5회, 2025년 1분기 1.1회로 매출액의 증감에 따라 변동성이 나타나고 있습니다. 향후 파이프라인의 기술이전 및 화장품 사업부와 바이오파마 사업부의 제품 라인업 확대 및 온라인 시장 점유 확대 등의 여부에 따른 매출 증대로 인하여 매출채권이 현 수준보다 증가할 수 있습니다. 한편, 당사의 재고자산회전율은 2022년 18.6회, 2023년 21.2회, 2024년 4.8회, 2025년 1분기 0.9회로 업종 평균인 5.0회에 하회하고 있습니다. 다만, 2022~2023년 기준 당사의 재고자산 회전율이 업종평균을 상회한 주된 원인은 자체 줄기세포 배양액을 기반으로 한 제품을 위주로 화장품을 제조해서 판매하는 화장품 사업, 의약품 도매 총판 및 일반의약품을 유통하는 바이오파마 사업 등 사업다각화로 인한 홈쇼핑 판매 재고 증가, 화장품 원료로 사용되는 줄기세포배양액과 세포배양배지 생산으로 인한 원재료 구매 증가 등이 기인했습니다. 재고자산이 증가할 경우 창고에 보관된 기간이 길어지는 것을 의미하므로 회사 입장에서는 재고 보관비용의 증가, 재고자산의 노후화 위험을 동시에 부담할 가능성을 시사합니다. 당사는 향후 보다 정확한 수요예측 및 생산량조절을 통해 적정수준의 재고자산 보유를 위해 노력하고, 진부화된 재고자산에 대한 적시 평가를 통한 관리를 지속할 예정입니다. 다만, 향후 매출 증가 및 품목 다변화에 의한 재고자산 증가 및 산업환경 변화에 대한 적응 미숙으로 인한 재고자산의 진부화 가능성은 여전히 존재하며, 이에 따라 재고자산의 평가손실이 확대된다면 수익성에 악영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
(1) 매출채권
매출채권 회수율을 측정하는 주요지표인 매출채권 회전율은 2022년 3.0회, 2023년는 2.4회, 2024년 1.5회, 2025년 1분기 기준 1.1회로, 업종 평균인 5.0회 대비 하회하고 있으며 매출채권 회수가 빠른 편에 속하지 않습니다. 당사의 기존 매출채권은 화장품 사업과 비임상시험 사업 비중이 높았지만, 2024년 05월 비임상시험 사업을 영위하던 HLB바이오코드 주식회사(구.주식회사 크로엔)의 지분 매각에 따른 연결 대상 제외로 매출이 감소하며 매출채권회전율이 감소하였습니다.
당사의 2025년 1분기 매출채권 총액은 16.0억원으로 2024년말 매출채권 52.7억원 대비 36.7억원 감소하였습니다. 자산총계 대비 매출채권의 비중은 2025년 1분기 기준 3%대의 낮은 비중을 차지중으로, 연구개발을 주요 사업으로 영위하고 있으므로 매출채권 규모는 상대적으로 적은 편이며 자산에 유의적인 영향을 미치고 있지 않습니다. 그러나 향후 파이프라인의 기술이전 및 화장품 사업부와 바이오파마 사업부의 제품 라인업 확대 및 온라인 시장 점유 확대 등의 여부에 따른 매출 증대로 인하여 매출채권이 현 수준보다 증가할 수 있습니다.
또한, 2018년말 기준 발생한 매출에 대해 2019년부터 2022년까지 회수되지 못한 매출채권에 대한 회수가 지연되었으나 2023년말 모두 회수하였습니다. 2024년 상반기에는 매출 부진으로 매출채권 회수가 일부 지연되었으나 하반기 중으로 대부분 회수하여 2025년 1분기 기준 매출채권 잔액은 3억원입니다. 특히, 주요 매출처인 주식회사 프리모리스인터내셔널향 매출 증가로 매출채권이 증가하였으나 2020년 이후 매출액 대비 매출채권 비중이 감소하는 추세입니다. 프리모리스인터내셔널향 매출 및 매출채권 추이는 상세내역은 다음과 같습니다.
| [주요 매출처인 (주)프리모리스인터내셔널향 매출 및 매출채권 추이] |
| (단위: 백만원) |
| 구분 | 2019년 | 2020년 | 2021년 | 2022년 | 2023년 | 2024년 | 2025년 1분기 |
|---|---|---|---|---|---|---|---|
| 상품매출 | - | - | 12 | 80 | 23 | 25 | 7 |
| 제품매출_줄기세포 | 114 | 143 | 84 | 247 | 912 | 354 | 113 |
| 제품매출_화장품 | - | - | 1,127 | 1,125 | 1386 | 1,454 | 244 |
| 기타매출 | - | - | - | - | - | 6 | - |
| 합계 | 114 | 143 | 1,223 | 1,452 | 2,321 | 1,839 | 365 |
| 매출채권 잔액 | 687 | 647 | 555 | 549 | 418 | 404 | 173 |
| 매출액 대비 매출채권 비율 | 600.4% | 452.9% | 45.4% | 37.9% | 18.0% | - | - |
| 출처) 당사 제시 |
향후 매출 성장 또는 매출처와의 계약에 따라 회전율은 변동할 수 있으며, 추후 매출채권 회수가 지연되어 매출채권회전율이 지금보다 더욱 감소할 경우 당사 유동성 및 손익에 악영향을 미칠 수 있습니다. 당사의 매출채권 현황은 다음과 같습니다.
| [매출채권 현황(연결기준)] |
| (단위: 백만원) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | 업종평균 |
|---|---|---|---|---|---|
| 매출액 | 954 | 7,746 | 12,704 | 16,301 | - |
| 매출채권 | 1,599 | 5,273 | 4,761 | 5,779 | - |
| 매출채권 대손충당금 | 12 | - | 48 | 311 | - |
| 매출채권회전율 | 1.1회 | 1.5회 | 2.4회 | 3.0회 | 5.0회 |
| 자산총계 | 50,204 | 55,986 | 81,253 | 80,592 | - |
| 자산총계 대비 매출채권 비중 | 3.2% | 9.4% | 5.9% | 7.2% | - |
| 출처) 당사 정기보고서 |
| 주1) 매출채권회전율 = 연환산 매출액÷{(전기매출채권+당기매출채권)÷2} |
| 주2) 업종평균은 한국은행 2023년 기업경영분석 "C21. 의료용 물질 및 의약품"을 적용하였습니다. |
2025년 1분기 기준 당사의 충당금 설정률표에 기초한 매출채권의 위험정보의 세부내용은 다음과 같습니다. 당사의 과거 경험상 매출채권의 연체일수에 따라 기대신용손실을 설정하고 있습니다.
| (단위: 백만원) |
| 구 분 | 발생이후 일수 | ||||
|---|---|---|---|---|---|
| 미연체 | ~30일 | 30~90일 | 90일초과 | 계 | |
| 총장부금액 | 282 | 3 | - | 15 | 301 |
|
전체기간 기대신용손실 |
- | - | - | -12 | -12 |
| 순장부금액 | 282 | 3 | - | 4 | 289 |
| 출처) 당사 정기보고서 |
당사는 제대혈 줄기세포의 연구, 개발 및 세포치료제 개발, 제조 그리고 판매를 주 사업으로 영위하고 있어, 매출채권 규모가 상대적으로 적습니다. 하지만 현재 회수가 지연되거나 거래상대방의 채무불이행으로 인하여 매출채권이 손상 된다면 대손충당금 설정에 대해 완전히 배제할 수 없으며 당사의 수익성에 부정적 영향을 미칠 수 있습니다.
(2) 재고자산
한편, 당사의 재고자산회전율은 2022년 18.6회, 2023년 21.2회, 2024년 4.8회, 2025년 1분기 0.9회로 업종 평균인 5.0회에 하회하고 있습니다. 다만, 2022~2023년 기준 당사의 재고자산 회전율이 업종평균을 상회한 주된 원인은 자체 줄기세포 배양액을 기반으로 한 제품을 위주로 화장품을 제조해서 판매하는 화장품 사업, 의약품 도매 총판 및 일반의약품을 유통하는 바이오파마 사업 등 사업다각화로 인한 홈쇼핑 판매 재고 증가, 화장품 원료로 사용되는 줄기세포배양액과 세포배양배지 생산으로 인한 원재료 구매 증가 등이 기인했습니다.
2024년 재고자산회전율 악화 원인은 1)주요 매출처인 주식회사 프리모리스인터내셔널의 매출 계획에 따라 배양액을 선 제조하였으나, 프리모리스인터내셔널의 매출 계획 대비 실적 부진으로 인해 배양액 출고가 지연되면서 재고가 증가하였습니다. 이는 2025년에 순차적으로 출고하여 소진될 예정입니다. 또한, 2)2024년 일본 재생의료사업 진출이 예상되어 배양액을 선 제조하였으나, 재생의료 심사 지연으로 인한 매출 개시가 미뤄짐에 따라 재고가 증가하였습니다. 2024년 11월 자가지방줄기세포를 이용한 제2종 재생의료 제공계획에 대한 심의위원회 승인 및 2025년 2월 후생노동성 승인이 완료됨에 따라, 일본 현지재생의료 전문 기관에 공급 및 환자 투여 준비를 진행하고 있으며, 이후 매출화 및 재고 소진이 가능할 것으로 판단됩니다. 당사의 재고자산 현황은 다음과 같습니다.
| [재고자산 관련 재무지표 현황] |
| (단위: 백만원) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | 업종평균 |
|---|---|---|---|---|---|
| 매출액 | 954 | 7,746 | 12,704 | 16,301 | - |
| 매출원가 | 749 | 3,420 | 11,061 | 11,428 | - |
| 재고자산 | 867 | 858 | 578 | 467 | - |
| 재고자산회전율 | 0.9회 | 4.8회 | 21.2회 | 18.6회 | 5.0회 |
| 자산총계 | 50,204 | 55,986 | 81,253 | 80,592 | - |
| 자산총계 대비 재고자산비중 | 1.7% | 1.5% | 0.7% | 0.6% | - |
| 출처) 당사 정기보고서 |
| 주1) 재고자산 회전율 = 매출원가/(기초재고+기말재고/2) |
2022년의 재고자산은 3.0억원 감소하였는데, 이는 화장품 제품 중 장기 재고 관련 손실 반영 및 부재료 폐기 등이 기인하며 4.7억원을 기록하였습니다. 2023년 재고자산은 홈쇼핑 화장품 신제품인 '메가셀'을 개발하여 생긴 제품 재고와 바이오파마 사업 관련 의약품 입고 물량 증가 등의 이유로 2022년 대비 소폭 증가한 5.8억원을 기록하였습니다. 2024년의 경우 화장품 시장의 호조가 지속됨에 따른 제품 재고 증가 등의 이유로 8.6억원을 기록했습니다. 2025년 1분기 기준 재고자산은 직접 사업년도 말과 유사한 수준인 8.7억을 기록했습니다. 당사의 재고자산 세부 내역은 다음과 같습니다.
| [재고자산 내역] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 취득원가 | 평가손실 | 장부금액 | 취득원가 | 평가손실 | 장부금액 | 취득원가 | 평가손실 | 장부금액 | 취득원가 | 평가손실 | 장부금액 | |
| 상품 | 85 | -66 | 19 | 119 | -21 | 98 | 138 | -9 | 129 | 146 | -43 | 103 |
| 제품 | 776 | -136 | 639 | 703 | -152 | 551 | 490 | -114 | 376 | 389 | -99 | 290 |
| 재공품 | 209 | 0 | 209 | 209 | 0 | 209 | 74 | - | 74 | 74 | - | 74 |
| 원재료 | - | - | - | - | - | - | - | - | - | - | - | - |
| 저장품 | - | - | - | - | - | - | - | - | - | - | - | - |
| 합 계 | 1069 | -202 | 867 | 1032 | -173 | 858 | 701 | -123 | 578 | 609 | -142 | 467 |
| 출처) 당사 정기보고서 |
재고자산이 증가할 경우 창고에 보관된 기간이 길어지는 것을 의미하므로 회사 입장에서는 재고 보관비용의 증가, 재고자산의 노후화 위험을 동시에 부담할 가능성을 시사합니다. 당사는 향후 보다 정확한 수요예측 및 생산량조절을 통해 적정수준의 재고자산 보유를 위해 노력하고, 진부화된 재고자산에 대한 적시 평가를 통한 관리를 지속할 예정입니다. 다만, 향후 매출 증가 및 품목 다변화에 의한 재고자산 증가 및 산업환경 변화에 대한 적응 미숙으로 인한 재고자산의 진부화 가능성은 여전히 존재하며, 이에 따라 재고자산의 평가손실이 확대된다면 수익성에 악영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
| 사. GMP를 포함한 생산시설 관련 위험 당사는 2018년 11월에 준공을 시작하여 신축 GMP공장을 2019년 05월에 완공하였습니다. 당시 국내 줄기세포 치료제 생산 공장으로서는 가장 큰 규모로, 당사의 기존 아토피 피부염 치료제(퓨어스템-에이디주)의 상업화 허가 기대 일정에 맞춘 완공이었습니다. 당사는 퓨어스템-에이디주가 임상 3상에서 유의성이 달성되었을 경우, 신축 GMP공장을 본격적으로 가동하며 퓨어스템-에이디주의 판매용 완제품을 생산함으로써 시장 수요 충족과 더불어 대량생산으로 원가 절감으로 수익성 확대를 이룰 것으로 기대하였으나, 2019년 10월 퓨어스템-에이디주 3상 결과가 통계적 유의성 입증에 실패하면서 당사가 계획했던 GMP공장의 본격 가동 일정이 미뤄지게 되며, 가동률이 저하되었습니다. 이와 같이 아토피 피부염 치료제 상업화에 대한 허가 일정이 또 한번 장기간 미루어질 경우, 당사 GMP공장의 고정비는 당사의 재무구조 및 수익성에 부정적인 영향을 미칠 것으로 예상됩니다. 당사는 GMP공장의 활용도를 높이고 고정비 부담을 낮추기 위해 완공 이후 해당 GMP 공장에서 제대혈 유래 줄기세포 배양액, 줄기세포 배양 배지 등을 직접 생산하여 줄기세포 치료제를 제조하여 당사의 주요 파이프라인의 전임상시험 및 임상시험에 사용하고 있습니다. 이에 줄기세포 배양액과 줄기세포 배양 배지 생산을 위한 구획을 구분하여 생산 라인이 가동되고 있습니다. 또한, 당사는 GMP공장의 활용도를 높이고자 2020년 12월 식약처로부터 첨단바이오의약품 제조업 허가 승인을 받았으며, 이에 「첨단재생바이오법」 규정에 따라 사람 또는 동물의 줄기세포와 조혈모세포, 체세포 등을 채취·검사 처리해 재생의료기관에 공급할 수 있게 되었습니다. 다만, 당사의 신축 GMP공장을 활용한 주요 파이프라인 임상시험에 필요한 약물의 직접 생산 및 의약품 위탁개발생산(CDMO)이라는 신사업의 매출 증대 전략 등과 같은 당사의 노력에도 불구하고 수주 지연 및 GMP공장 시설 문제 등의 이유로 계획대로 진행되지 않는다면, 상기 생산시설의 연구인력 및 생산력 충원으로 인해 과도한 고정비의 지출이 선행되었기 때문에, 이는 당사의 재무구조 및 수익성에 부정적인 영향이 장기간 이어질 가능성이 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
당사는 2018년 11월에 준공을 시작하여 신축 GMP공장을 2019년 05월에 완공하였습니다. 당시 국내 줄기세포 치료제 생산 공장으로서는 가장 큰 규모로, 당사의 기존 아토피 피부염 치료제(퓨어스템-에이디주)의 상업화 허가 기대 일정에 맞춘 완공이었습니다. 당사는 퓨어스템-에이디주가 임상 3상에서 유의성이 달성되었을 경우, 신축 GMP공장을 본격적으로 가동하며 퓨어스템-에이디주의 판매용 완제품을 생산함으로써 시장 수요 충족과 더불어 대량생산으로 원가 절감으로 수익성 확대를 이룰 것으로 기대하였으나, 2019년 10월 퓨어스템-에이디주 3상 결과가 통계적 유의성 입증에 실패하면서 당사가 계획했던 GMP공장의 본격 가동 일정이 미뤄지게 되며, 가동률이 저하되었습니다. 이후 2021년 05월 퓨어스템-에이디주의 임상 3상 재도전을 위해 환자모집에 힘썼지만, 코로나19 확산에 따라 원활한 환자모집이 되지 않으면서 일정이 지연되었습니다. 기존에 2022년 12월까지 예정되어있던 환자 모집기간을 연장하여 2023년 08월 최종인원 308명의 환자를 모두 투약하였습니다. 다만, 12주차 시점 위약 대비 시험군과 대조군 간 유효성 차이를 입증하지 못하였습니다.
이에 기존 단회투여에서 반복투여 방식으로 프로토콜을 수정하여 2024년 11월 임상 1/2a상 IND를 변경승인신청하였으나, 식품의약품안전처(MFDS)의 추가 자료보완 요청을 기한 내 회신이 어려울 것으로 판단하여 자진취하 신청을 하였습니다. 그리고 2025년 4월 퓨어스템-에이디주의 반복투여 제1/2a 임상시험계획변경승인신청을 하였으며, 2025년 하반기 임상 1/2a상 개시를 계획하고 있습니다. 이와 같이 아토피 피부염 치료제 상업화에 대한 허가 일정이 또 한번 장기간 미루어질 경우, 당사 GMP공장의 고정비는 당사의 재무구조 및 수익성에 부정적인 영향을 미칠 것으로 예상됩니다.
당사의 신축 GMP공장과 관련된 공시 사항은 아래와 같습니다.
| [신규 시설투자 등] |
| 1. 투자구분 | 신규시설 투자 | |
| 2. 투자내역 | 투자금액(원) | 8,756,334,000 |
| 자기자본(원) | 62,950,891,061 | |
| 자기자본대비(%) | 13.91 | |
| 대규모법인여부 | 미해당 | |
| 3. 투자목적 | GMP제조소 신축 | |
| 4. 투자기간 | 시작일 | 2018-10-22 |
| 종료일 | 2019-06-28 | |
| 5. 이사회결의일(결정일) | 2019-04-30 | |
| -사외이사 참석여부 | 참석(명) | 2 |
| 불참(명) | - | |
| 6. 감사(감사위원) 참석여부 | 참석 | |
| 7. 공시유보 관련내용 | 유보사유 | - |
| 유보기한 | - | |
| 8. 기타 투자판단에 참고할 사항 | - 상기 '2. 투자내역의 자기자본'은 K-IFRS에따라 작성된 최근 사업연도말(2017년) 연결재무제표 에서 최근 사업연도말 경과 후 공시사유 발생일 까지의 자본금 및 자본잉여금 증가액을 가산한 금액입니다. - 상기 '2. 투자내역의 투자금액'은 GMP제조소 신축 시 시설공사 및 장비구입 비용으로 부가 가치세가 제외된 금액이고, 재원은 기발행한 전환사채 및 자체자금입니다. - 상기 '4.투자기간의 종료일'은 시설공사 완료 후 공사내역에 대한 당사의 검수 완료일입니다. - 상기 투자금액과 투자기간은 공사 진행과정에 따라 변경될 수 있습니다. - 상기 GMP제조소 신축을 위하여 2016년 9월에 토지 및 건물을 매수하였습니다. (2016.09.07 유형자산 양수 결정 공시 참조) |
|
| 출처) 당사 정기 보고서 제시 |
| [유형자산 양수 결정] |
| 1. 자산구분 | 토지 및 건물 | |
| - 자산명 | 경기도 광명시 소하동 1345 소재 토지(659.58㎡) 및 건물(4,611.93㎡) |
|
| 2. 양수내역 | 양수금액(원) | 7,318,780,000 |
| 자산총액(원) | 24,982,626,487 | |
| 자산총액대비(%) | 29.30 | |
| 3. 양수목적 | 세포치료제 양산시설 구축 | |
| 4. 양수영향 | 향후 세포치료제 시판에 대비한 생산시설 확보 | |
| 5. 양수예정일자 | 계약체결일 | 2016년 09월 30일 |
| 양수기준일 | 2017년 04월 28일 | |
| 등기예정일 | 2017년 04월 28일 | |
| 6. 거래상대방 | 회사명(성명) | 팅크웨어(주)(THINKWARE Corporation) |
| 자본금(원) | 4,888,002,500 | |
| 주요사업 | 차량용 블랙박스, 지도서비스, 모바일서비스 사업 | |
| 본점소재지(주소) | 경기도 성남시 분당구 판교역로 240, A동 9층(삼환하이펙스) | |
| 회사와의 관계 | - | |
| 7. 거래대금지급 | - 현금지급 - 계약금(10%) : 2016.09.30 / 731,878,000원 - 잔 금(90%) : 2017.04.28 / 6,586,902,000원 - 자금조달 방법 : 전환사채 발행 |
|
| 8. 외부평가에 관한 사항 | 외부평가 여부 | 예 |
| - 근거 및 사유 | 자본시장과 금융투자업에 관한 법률 제161조제1항제7호 및 동법 시행령 제176조의6제3항에 의한 적정성 평가 |
|
| 외부평가기관의 명칭 | 한미회계법인 | |
| 외부평가 기간 | 2016년 09월 01일 ~ 2016년 09월 06일 | |
| 외부평가 의견 | 적 정 | |
| 9. 주주총회 특별결의 여부 | 미해당 | |
| - 주주총회 예정일자 | - | |
| - 주식매수청구권에 관한 사항 |
행사요건 | - |
| 매수예정가격 | - | |
| 행사절차, 방법, 기간, 장소 |
- | |
| 지급예정시기, 지급방법 |
- | |
| 주식매수청구권 제한 관련 내용 |
- | |
| 계약에 미치는 효력 | - | |
| 10. 이사회결의일(결정일) | 2016년 09월 07일 | |
| - 사외이사참석여부 | 참석(명) | 2 |
| 불참(명) | - | |
| - 감사(사외이사가 아닌 감사위원) 참석여부 | 참석 | |
| 11. 공정거래위원회 신고대상 여부 | 미해당 | |
| 12. 풋옵션 등 계약 체결여부 | 아니오 | |
| - 계약내용 | - | |
| 출처) 당사 공시자료 제시 |
상기한 바와 같이 아토피 피부염 치료제(퓨어스템-에이디주)의 임상 3상 실패 및 이로 인한 상업화에 대한 허가 계획 차질에 따라 GMP 공장 가동률이 완공 당시 예상보다 매우 저하되었으나, 당사는 GMP공장의 활용도를 높이고 고정비 부담을 낮추기 위해 완공 이후 해당 GMP 공장에서 제대혈 유래 줄기세포 배양액, 줄기세포 배양 배지 등을 직접 생산하여 줄기세포 치료제를 제조하여 당사의 주요 파이프라인의 전임상시험 및 임상시험에 사용하고 있습니다. 이에 줄기세포 배양액과 줄기세포 배양 배지 생산을 위한 구획을 구분하여 생산 라인이 가동되고 있습니다. 또한, 당사는 GMP공장의 활용도를 높이고자 2020년 12월 식약처로부터 첨단바이오의약품 제조업 허가 승인을 받았으며, 이에 「첨단재생바이오법」 규정에 따라 사람 또는 동물의 줄기세포와 조혈모세포, 체세포 등을 채취·검사 처리해 재생의료기관에 공급할 수 있게 되었습니다. 또한, 당사는 2020년 07월 의약품 제조에 대한 허가를 취득했으며, 인체 세포 등의 관리업 허가 취득과 재생의료기관의 임상 연구를 위한 세포 처리시설 허가도 받을 계획입니다. 이에 당사는 본격적으로 의약품 위탁개발생산(CDMO)을 신사업으로 채택하여 2021년 말부터 매출이 발생하고 있습니다. 당사 GMP 공장의 생산시설 가동률 추이는 아래와 같습니다.
| [GMP 생산시설 가동률 추이] |
| 품 목 | 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | 2021년 |
|---|---|---|---|---|---|---|
|
줄기세포 배양액(주1) (단위: ℓ) |
생산능력 | 600 | 2,400 | 2,400 | 2,400 | 2,400 |
| 생산실적 | 386 | 1,140 | 855 | 188 | 191 | |
| 가 동 률 | 64.3% | 47.5% | 35.6% | 7.8% | 8.0% | |
|
세포배양 배지(주2) (단위: 개) |
생산능력 | 1,500 | 6,000 | 6,000 | 6,000 | 6,000 |
| 생산실적 | 0 | 1,469 | 3,242 | 1,871 | 2,240 | |
| 가 동 률 | 0.0% | 24.5% | 54.0% | 31.2% | 37.3% | |
| 세포배양 배지(주3) (단위: 개) |
생산능력 | 600 | 1,800 | - | - | - |
| 생산실적 | 0 | 379 | - | - | - | |
| 가 동 률 | 0.0% | 21.1% | - | - | - |
| 출처) | 당사 정기보고서 |
| (주1) | 월 200ℓ생산 가능합니다. |
| (주2) | 월 500개 생산 가능합니다. |
| (주3) | 월 200개 생산 가능합니다. |
| (주4) | 2024년 기존 생산 설비를 활용하여 줄기세포 배양 배지(StemVie XF Supplments 제품)를 신규 생산하게 됨에 따라 추가된 내용입니다. |
다만, 당사의 신축 GMP공장을 활용한 주요 파이프라인 임상시험에 필요한 약물의 직접 생산 및 의약품 위탁개발생산(CDMO)이라는 신사업의 매출 증대 전략 등과 같은 당사의 노력에도 불구하고 수주 지연 및 GMP공장 시설 문제 등의 이유로 계획대로 진행되지 않는다면, 상기 생산시설의 연구인력 및 생산력 충원으로 인해 과도한 고정비의 지출이 선행되었기 때문에, 이는 당사의 재무구조 및 수익성에 부정적인 영향이 장기간 이어질 가능성이 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| 아. 특수관계자 및 지분투자기업과의 거래 관련 위험 당사는 특수관계자 등과 일부 자금거래가 발생하고 있으나, 특수관계자와 거래를 함에 있어 특별히 유리하거나 불리한 조건을 제시하는 등 거래상대방에 따라 계약조건을 달리한 사실이 없으며, 특수관계자와 계약을 체결할 때 통상 시장가로 계약을 체결하고 있습니다. 하지만 당사의 적법한 절차 및 법규 준수에도 불구하고 향후 당사와 특수관계자 간의 부적절한 거래가 발생될 가능성을 완전히 배제할 수 없으니 투자자께서는 이점 유의하시어 투자에 임하시기 바랍니다. |
2025년 1분기 연결 기준 당사의 특수관계자 현황은 다음과 같습니다.
| 관 계 | 2025년 1분기 | 2024년 |
|---|---|---|
| 관계기업 | HLB바이오코드(주)(주2) | HLB바이오코드(주) |
| (주)디앤케이코퍼레이션 | (주)디앤케이코퍼레이션 | |
| (주)블루진 | (주)블루진 | |
| (주)프리모리스테라퓨틱스 | (주)프리모리스테라퓨틱스 | |
| 기타 특수관계자 | (주)프리모리스인터내셔널(주1) | (주)프리모리스인터내셔널 |
| 마루테라퓨틱스(주)(주1) | 마루테라퓨틱스(주) | |
| 주요경영진 | 주요경영진 |
| 출처) 당사 제시 |
| 주1) 당사에 대한 지배력을 보유하고 있는 개인 등이 지배력을 보유하고 있는 회사입니다. |
| 주2) 전기 중 사명을 (주)크로엔에서 HLB바이오코드(주)로 변경하였으며, 보유 주식 1,183,676주(64.50%) 중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류하였습니다. |
당사의 2025년 1분기말 기준 특수관계자에 대한 영업수익은 3.8억원으로 전체 매출액 9.5억원 가운데 약 40.3%를 차지합니다. 또한, 2024년 기준으로 전체 매출액 77.5억원 중 약 24.7%에 해당하는 19.1억원이 특수관계자 거래로부터 발생하였습니다. 한편, 2025년 1분기말 기준 특수관계자에 대한 영업비용은 약 10.7억원이 발생하였으며, 2024년에는 약 9.8억원이 발생하였습니다. 특수관계자와 주요 거래 발생 내역은 다음과 같습니다.
1) HLB바이오코드(주)
당사는 HLB바이오코드㈜에 의뢰하여 줄기세포, 오가노이드의 독성시험, 조직분석, 안정성 평가 등 다양한 비임상시험용역을 진행 중입니다. 이에 따른 용역 비용으로 2024년 약 8억원의 비용이 발생하였습니다. 한편, 2024년 및 2025년 발생한 영업수익은 2022년 HLB바이오코드(주)가 당사로부터 대여한 대여금 잔액에 대한 이자수익입니다.
2) (주)프리모리스인터내셔널
(주)프리모리스인터내셔널은 당사의 줄기세포 화장품, 샴푸 및 줄기세포 배양액 등의 유통을 담당하며 2023년 26억원, 2024년 18억원, 2025년 1분기 3억원의 매출거래가 발생하였습니다. 특히, 당사의 줄기세포 화장품 단독 유통 채널로서, 2024년 전체 매출의 23.7%, 2025년 1분기의 38.2%가 발생하는 등 당사의 매출에 기여하는 비중이 상대적으로 높습니다. 한편, 영업비용은 당사와 H&B 사업부 사무실 공동사용에 대한 임차료 및 기본 관리비 지급 과정에서 발생하였습니다.
3) (주)프리모리스테라퓨틱스
관계회사인 (주)프리모리스테라퓨틱스에 대해서는 2022년 7.29억원, 2023년 7.3천만원의 매출이 발생하였으며, 이는 2021~2023년 진행된 CDMO 프로젝트 관련 매출입니다. 2024년과 2025년 1분기에는 각각 6.4천만원, 1.7천만원의 매출이 발생하였으며, 이는 CDMO 프로젝트 완료 이후 MCB(Master Cell Bank) 세포보관료 및 품질시험 등으로 인한 매출, 대여금에 대한 이자수익, 사무실 임대에 의한 수입임대료에서 발생하였습니다. 한편, 당사의 (주)프리모리스테라퓨틱스에 대한 영업비용은 2025년 1분기 7.8천만원으로 증가하였는데, 이는 엑소좀 관련 위탁연구용역비 약 6천만원과 당사가 (주)프리모리스테라퓨틱스로부터 받아야하는 외상매출금 및 미수금 대한 대손충당금 약 2천만원 설정에 기인합니다.
| [최근 3개년 특수관계자와의 영업수익 및 영업비용 발생 내역] |
| (단위: 천원) |
| 특수관계자 명칭 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | ||||
|---|---|---|---|---|---|---|---|---|
| 영업수익 등 | 영업비용 등 | 영업수익 등 | 영업비용 등 | 영업수익 등 | 영업비용 등 | 영업수익 등 | 영업비용 등 | |
| HLB바이오코드(주) | 2,268 | - | 9,353 | 816,966 | - | - | - | - |
| (주)프리모리스인터내셔널(주1) | 364,806 | 29,053 | 1,838,666 | 159,222 | 2,631,960 | 292,285 | 1,451,717 | 350,114 |
| (주)프리모리스테라퓨틱스 | 17,280 | 78,117 | 64,725 | 55 | 73,044 | 4 | 729,899 | - |
| 합 계 | 384,354 | 107,170 | 1,912,744 | 976,243 | 2,705,004 | 292,289 | 2,181,616 | 350,114 |
| 출처) 당사 정기보고서 |
| 주1) 당사는 특수관계자인 (주)프리모리스인터내셔널과 연간 상품공급계약을 맺고 있습니다. |
당사는 위와 같이 특수관계자들과 다양한 매출, 매입 관련 거래가 발생하고 있으며, 이에 따라 매출채권, 미수금, 미지급금 등의 채권 및 채무가 발생합니다. 2025년 1분기말 당사의 특수관계자에 대한 채권은 총 약 2.4억원, 채무는 약 0.1억원입니다. 또한, 2024년말 기준 당사의 특수관계자에 대한 채권은 약 4.5억원, 채무는 약 1.6억원이었습니다. 특히, (주)프리모리스인터내셔널의 경우 당사 화장품 및 줄기세포 배양액의 주요 유통사로서 2024년 4억원, 2025년 1분기 1억7천만원의 상거래채권이 발생하였습니다. 한편,(주)프리모리스테라퓨틱스의 2022,2023년 계약자산 및 계약이행원가는 2023년 종료된 CDMO 프로젝트 진행시 발생하였습니다. 2024년과 2025년 1분기 발생한 계약부채의 경우 CDMO 프로젝트 종료 이후 MCB(Master Cell Bank) 세포보관료에 대해 매 3개월마다 계약을 갱신하여 발생한 보관료 선수금액입니다. 특수관계자 간 주요 채권ㆍ채무잔액은 다음과 같습니다.
| [최근 3개년 특수관계자와의 채권, 채무 발생 내역] |
| (단위: 천원) |
| 특수관계자 명칭 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 채권 | 채무 | 채권 | 채무 | 채권 | 채무 | 채권 | 채무 | |||||||||
| 매출채권 등 (주1) |
계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | 매출채권 등 | 계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | 매출채권 등 | 계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | 매출채권 등 | 계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | |
| HLB바이오코드(주) | 2,268 | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - |
| (주)프리모리스인터내셔널 | 172,992 | - | 10,453 | - | 403,923 | - | 14,160 | - | 417,682 | - | 21,062 | - | 549,527 | - | 35,753 | - |
| (주)프리모리스테라퓨틱스 | 67,555 | - | - | 2,000 | 49,375 | - | - | 2,000 | - | 13,409 | - | 3,333 | 510,047 | 400 | - | 11,333 |
| 합 계 | 242,815 | - | 10,453 | 2,000 | 453,298 | - | 14,160 | 2,000 | 417,682 | 13,409 | 21,062 | 3,333 | 1,059,574 | 400 | 35,753 | 11,333 |
| 출처) 당사 정기보고서 |
| 주1) 당분기말 채권은 대손충당금 차감전 금액이 기재되어 있습니다. 상기 특수관계자 채권에 설정되어 있는 대손충당금은 18백만원입니다. |
한편, 당사는 2024년 유상증자에 참여하여 HLB바이오코드㈜(구.㈜크로엔) 보통주 183,333주를 약 9.9억원에 취득한 사실이 있습니다. 당사는 자회사였던 HLB바이오코드㈜ 지분을 HLB바이오스텝에 일부 매각하면서 경영권을 이전하였습니다. 경영권 이전 후에도 오가노이드 활용 동물대체시험법 및 오가노이드 치료제 연구개발 등 업무 협업 유지, 사업 시너지를 발휘하고자 후속하여 진행된 HLB바이오코드㈜ 유상증자에 참여하였고, 현재 22.15%의 지분을 보유하고 있습니다. 특수관계자와의 지분거래내역은 다음과 같습니다.
| [최근 3개년 특수관계자와의 지분거래내역] |
| (단위 : 천원) |
| 특수관계자 명칭 | 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|
| HLB바이오코드(주) | 보통주 유상증자(주1) | - | 989,998 | - | - |
| (주)프리모리스테라퓨틱스 | 보통주 무상수증(주2) | - | - | - | - |
| 출처) 당사 정기보고서 |
| 주1) 전기 중 보통주 유상증자로 183,333주를 취득하였습니다. |
| 주2) 전기까지 최대주주 및 당사 임원으로부터 프리모리스테라퓨틱스 보통주 87,200주를 무상수증받아, 취득금액은 영(0)입니다. |
2025년 1분기 기준 당사의 특수관계인에 대한 대여금 잔액은 총 9.3억원 입니다. 당사는 2022년 당시 종속기업인 HLB바이오코드(주)(구.(주)크로엔)의 운영자금 지원 목적으로 6억원을 대여한 바 있습니다. 해당 대여금은 2023년까지 매분기 1억원씩 상환되었으며, 2025년 1분기 기준 잔액은 2억원 입니다. 2025년말 만기 도래 예정이며, 해당 대여금에 대해서 당좌대출이자율을 적용한 이자를 수취하고, 대여 원금 잔액을 상환받을 예정입니다.
또한, 당사는 관계회사인 ㈜프리모리스테라퓨틱스의 운영자금 지원 목적으로 2024년 2월 4억 5천만원, 9월 9천만원, 10월 1억 9천만원을 대여하며, 총 7억 3천만원을 대여한 바 있습니다. 향후 대여기간 만료 시, 당사는 해당 대여금에 대해 당좌대출이자율을 적용한 이자를 수취하고, 대여 원금 전액을 상환받을 예정입니다. 한편, 당사는 2023년 2월 ㈜프리모리스테라퓨틱스와 기술 및 사업 시너지를 발휘하고자 2023년 2월 8일 상환전환우선주 11,765주를 약 20억원에 취득하였습니다. 특수관계자와의 자금거래내역은 다음과 같습니다.
| [최근 3개년 특수관계자와의 자금거래내역 발생 내역] |
| (단위 : 천원) |
| 특수관계자 명칭 | 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|
| HLB바이오코드(주) | 대여금 | - | - | - | 600,000 |
| (주)프리모리스테라퓨틱스 | 대여금 | - | 730,000 | - | - |
| (주)프리모리스테라퓨틱스 | 상환전환우선주 | - | - | 2,000,050 | - |
| 출처) 당사 정기보고서 |
| 주1) 대여금 최초 발생 시점 기준입니다. |
| 주2) 2025년 1분기 기준 HLB바이오코드(주)에 대한 대여금 잔액은 2억원입니다. |
한편, 「상법」 제542조의9(주요주주 등 이해관계자와의 거래) 제3항에 의하면 최근 사업연도 말 현재의 자산총액이 2조원 이상인 상장회사는 특수관계인과의 거래에 있어 이사회 승인을 받아야 하는 규정이 있습니다. 당사의 경우 최근 결산일인 2024년 말 연결 기준 총 자산규모가 약 560억원으로 동 조항에 해당되지 않아 특수관계인과의 거래에 있어 제한적인 규제를 적용받고 있습니다.
또한,「상법」제542조의9(주요주주 등 이해관계자와의 거래) 제1항에 따르면 상장회사는 주요주주 및 그의 특수관계인, 이사 및 집행임원, 감사에 대해서는 신용공여를 하여서는 안된다고 규정하고 있습니다. 다만, 동법 제2항에 따라 복리후생을 위한 이사 및 집행 임원 또는 감사에 대한 금전대여 등으로서 대통령령으로 정하는 신용공여나 그 밖에 상장회사의 경영건전성을 해칠 우려가 없는 금전대여 등으로서 대통령령으로 정하는 신용공여는 가능합니다. 「상법시행령」제35조제3항에 따르면 '대통령령으로 정하는 신용공여'란 회사의 경영상 목적을 달성하기 위하여 필요한 경우라고 규정하고 있고 그 대상을 회사의 지분율에 따라 제한하고 있습니다. 당사가 당사의 주요주주 및 주요주주의 특수관계인과의 자금거래와 관련하여 상법 충족 여부를 검토한 결과, 당사는 대여금 제공이 상법시행령 제35조 제3항 제1호 및 제2호에서 정하는 법인이 '경영상 목적을 달성하기 위하여 필요한 경우' 해당한다고 판단하였습니다. 이에 따라, 당사가 종속기업 및 관계기업을 대상으로 수행한 출자 및 금전대여는 「상법」 제542조의9 제2항 제3호에서 정한 신용공여 제한의 예외 사유인 '상장회사의 경영건전성을 해칠 우려가 없는 신용공여'에 해당하는 것으로 판단됩니다.
| 상법 제542조의9(주요주주 등 이해관계자와의 거래) |
|---|
| ① 상장회사는 다음 각 호의 어느 하나에 해당하는 자를 상대방으로 하거나 그를 위하여 신용공여(금전 등 경제적 가치가 있는 재산의 대여, 채무이행의 보증, 자금 지원적 성격의 증권 매입, 그 밖에 거래상의 신용위험이 따르는 직접적ㆍ간접적 거래로서 대통령령으로 정하는 거래를 말한다. 이하 이 조에서 같다)를 하여서는 아니 된다. <개정 2011. 4. 14.> 1. 주요주주 및 그의 특수관계인 2. 이사(제401조의2제1항 각 호의 어느 하나에 해당하는 자를 포함한다. 이하 이 조에서 같다) 및 집행임원 3. 감사 ② 제1항에도 불구하고 다음 각 호의 어느 하나에 해당하는 경우에는 신용공여를 할 수 있다.<개정 2011. 4. 14.> 1. 복리후생을 위한 이사ㆍ집행임원 또는 감사에 대한 금전대여 등으로서 대통령령으로 정하는 신용공여 2. 다른 법령에서 허용하는 신용공여 3. 그 밖에 상장회사의 경영건전성을 해칠 우려가 없는 금전대여 등으로서 대통령령으로 정하는 신용공여 ③ 자산 규모 등을 고려하여 대통령령으로 정하는 상장회사는 최대주주, 그의 특수관계인 및 그 상장회사의 특수관계인으로서 대통령령으로 정하는 자를 상대방으로 하거나 그를 위하여 다음 각 호의 어느 하나에 해당하는 거래(제1항에 따라 금지되는 거래는 제외한다)를 하려는 경우에는 이사회의 승인을 받아야 한다. 1. 단일 거래규모가 대통령령으로 정하는 규모 이상인 거래 2. 해당 사업연도 중에 특정인과의 해당 거래를 포함한 거래총액이 대통령령으로 정하는 규모 이상이 되는 경우의 해당 거래 ④ 제3항의 경우 상장회사는 이사회의 승인 결의 후 처음으로 소집되는 정기주주총회에 해당 거래의 목적, 상대방, 그 밖에 대통령령으로 정하는 사항을 보고하여야 한다. ⑤ 제3항에도 불구하고 상장회사가 경영하는 업종에 따른 일상적인 거래로서 다음 각 호의 어느 하나에 해당하는 거래는 이사회의 승인을 받지 아니하고 할 수 있으며, 제2호에 해당하는 거래에 대하여는 그 거래내용을 주주총회에 보고하지 아니할 수 있다. 1. 약관에 따라 정형화된 거래로서 대통령령으로 정하는 거래 2. 이사회에서 승인한 거래총액의 범위 안에서 이행하는 거래 [본조신설 2009. 1. 30.] |
| 상법시행령 제35조(주요주주 등 이해관계자와의 거래) |
| ① 법 제542조의9제1항 각 호 외의 부분에서 "대통령령으로 정하는 거래"란 다음 각 호의 어느 하나에 해당하는 거래를 말한다. 1. 담보를 제공하는 거래 2. 어음(「전자어음의 발행 및 유통에 관한 법률」에 따른 전자어음을 포함한다)을 배서(「어음법」 제15조제1항에 따른 담보적 효력이 없는 배서는 제외한다)하는 거래 3. 출자의 이행을 약정하는 거래 4. 법 제542조의9제1항 각 호의 자에 대한 신용공여의 제한(금전ㆍ증권 등 경제적 가치가 있는 재산의 대여, 채무이행의 보증, 자금 지원적 성격의 증권 매입, 제1호부터 제3호까지의 어느 하나에 해당하는 거래의 제한을 말한다)을 회피할 목적으로 하는 거래로서 「자본시장과 금융투자업에 관한 법률 시행령」 제38조제1항제4호 각 목의 어느 하나에 해당하는 거래 5. 「자본시장과 금융투자업에 관한 법률 시행령」 제38조제1항제5호에 따른 거래 ② 법 제542조의9제2항제1호에서 "대통령령으로 정하는 신용공여"란 학자금, 주택자금 또는 의료비 등 복리후생을 위하여 회사가 정하는 바에 따라 3억원의 범위에서 금전을 대여하는 행위를 말한다. ③ 법 제542조의9제2항제3호에서 "대통령령으로 정하는 신용공여"란 회사의 경영상 목적을 달성하기 위하여 필요한 경우로서 다음 각 호의 자를 상대로 하거나 그를 위하여 적법한 절차에 따라 이행하는 신용공여를 말한다. 1. 법인인 주요주주 2. 법인인 주요주주의 특수관계인 중 회사(자회사를 포함한다)의 출자지분과 해당 법인인 주요주주의 출자지분을 합한 것이 개인인 주요주주의 출자지분과 그의 특수관계인(해당 회사 및 자회사는 제외한다)의 출자지분을 합한 것보다 큰 법인 3. 개인인 주요주주의 특수관계인 중 회사(자회사를 포함한다)의 출자지분과 제1호 및 제2호에 따른 법인의 출자지분을 합한 것이 개인인 주요주주의 출자지분과 그의 특수관계인(해당 회사 및 자회사는 제외한다)의 출자지분을 합한 것보다 큰 법인 ④ 법 제542조의9제3항 각 호 외의 부분에서 "대통령령으로 정하는 상장회사"란 최근 사업연도 말 현재의 자산총액이 2조원 이상인 상장회사를 말한다. ⑤ 법 제542조의9제3항 각 호 외의 부분에서 "대통령령으로 정하는 자"란 제34조제4항의 특수관계인을 말한다. ⑥ 법 제542조의9제3항제1호에서 "대통령령으로 정하는 규모"란 자산총액 또는 매출총액을 기준으로 다음 각 호의 구분에 따른 규모를 말한다. 1. 제4항의 회사가 「금융위원회의 설치 등에 관한 법률」 제38조에 따른 검사 대상 기관인 경우: 해당 회사의 최근 사업연도 말 현재의 자산총액의 100분의 1 2. 제4항의 회사가 「금융위원회의 설치 등에 관한 법률」 제38조에 따른 검사 대상 기관이 아닌 경우: 해당 회사의 최근 사업연도 말 현재의 자산총액 또는 매출총액의 100분의 1 ⑦ 법 제542조의9제3항제2호에서 "대통령령으로 정하는 규모"란 다음 각 호의 구분에 따른 규모를 말한다. 1. 제4항의 회사가 「금융위원회의 설치 등에 관한 법률」 제38조에 따른 검사 대상 기관인 경우: 해당 회사의 최근 사업연도 말 현재의 자산총액의 100분의 5 2. 제4항의 회사가 「금융위원회의 설치 등에 관한 법률」 제38조에 따른 검사 대상 기관이 아닌 경우: 해당 회사의 최근 사업연도 말 현재의 자산총액 또는 매출총액의 100분의 5 ⑧ 법 제542조의9제4항에서 "대통령령으로 정하는 사항"이란 다음 각 호의 사항을 말한다. 1. 거래의 내용, 날짜, 기간 및 조건 2. 해당 사업연도 중 거래상대방과의 거래유형별 총거래금액 및 거래잔액 ⑨ 법 제542조의9제5항제1호에서 “대통령령으로 정하는 거래”란 「약관의 규제에 관한 법률」 제2조제1호의 약관에 따라 이루어지는 거래를 말한다. |
| 자료 : 국가법령정보센터 |
이처럼 당사는 특수관계자 등과 일부 자금거래가 발생하고 있으나, 특수관계자와 거래를 함에 있어 특별히 유리하거나 불리한 조건을 제시하는 등 거래상대방에 따라 계약조건을 달리한 사실이 없으며, 특수관계자와 계약을 체결할 때 통상 시장가로 계약을 체결하고 있습니다. 하지만 당사의 적법한 절차 및 법규 준수에도 불구하고 향후 당사와 특수관계자 간의 부적절한 거래가 발생될 가능성을 완전히 배제할 수 없으니 투자자께서는 이점 유의하시어 투자에 임하시기 바랍니다.
| 자. 환율 변동 관련 위험 당사의 매출액을 살펴보면 2022년 16,301백만원, 2023년 12,704백만원, 2024년 7,746백만원, 2025년 1분기 954백만원을 기록하였습니다. 이중 수출액은 2022년 272백만원, 2023년 673백만원, 2024년 860백만원, 2025년 1분기 95백만원을 기록하였으며 매출액 중 수출 비중은 미미한 수준을 나타냈습니다. 다만, 당사가 후생노동성으로부터 제2종(자가지방줄기세포) 최종 승인을 받은 상태로서, 금년도부터 일본 재생의료 시장 진출이 유력하기 때문에, 일본향 매출 비중이 증가할 가능성이 있습니다. 당사는 매출액 중 더마 코스메틱 브랜드 지디일레븐(GD11)의 매출 일부가 수출 형태로 판매되고 있습니다. 국가별 수출 비중을 살펴보면 주로 일본의 비중이 2022년 55%, 2023년 60%, 2024년 82%, 2025년 1분기 86%를 기록하고 있습니다. 최근 원/달러 환율은 글로벌 경기 불확실성 확대 및 국내 정치적 불안 요소 부각 등 대내외 환경의 영향으로 2024년 12월 31일 1,470.00원까지 급등한 뒤, 2025년 2월 24일 1,434.1원으로 일시적으로 안정되었으나, 이후 1,440원에서 1,475원 사이의 고환율 구간을 형성하며 원화 가치가 빠르게 하락하는 추세를 보였습니다. 다만, 2025년 5월 들어 미중 관세 협상과 같은 주요국 간 외교적 긴장 완화, 대외거래 수지 개선, 통화정책 변화에 대한 기대 등 대내외 여건의 변화에 따라 원/달러 환율이 급락하는 흐름을 보이며 높은 변동성을 보이고 있습니다. 아울러 원/엔 환율은 2024년 12월 31일 936.48원에서 2025년 4월 29일 기준 1,011.85원까지 상승하였으나 2025년 5월 들어 글로벌 외환시장 환경 변화에 따라 다시 하락세로 전환하는 등 글로벌 경제 변화와 일본의 통화정책 영향을 강하게 받으며 뚜렷한 변동성을 보였습니다.이처럼 갑작스러운 환율 변동성의 확대는 당사의 해외 글로벌 임상비용 지출 등에 영향을 미칠 수 있는 바 투자자 여러분께서는 이 점 유의하시기 바랍니다. |
당사의 매출액을 살펴보면 2022년 16,301백만원, 2023년 12,704백만원, 2024년 7,746백만원, 2025년 1분기 954백만원을 기록하였습니다. 이중 수출액은 2022년 272백만원, 2023년 673백만원, 2024년 860백만원, 2025년 1분기 95백만원을 기록하였으며 매출액 중 수출 비중은 미미한 수준을 나타냈습니다. 다만, 당사가 후생노동성으로부터 제2종(자가지방줄기세포) 최종 승인을 받은 상태로서, 금년도부터 일본 재생의료 시장 진출이 유력하기 때문에, 일본향 매출 비중이 증가할 가능성이 있습니다.
| [최근 3개년 수출 비중] | |
| (K-IFRS, 연결) | (단위 : 백만원) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| 수출 | 95 | 860 | 673 | 272 |
| 내수 | 859 | 6,886 | 12,032 | 16,028 |
| 수출 비중 | 9.96% | 11.10% | 5.29% | 1.67% |
| 총 매출액 | 954 | 7,746 | 12,704 | 16,301 |
| 출처) 당사 정기보고서 |
| [최근 3개년 수출 비중(상세 내역)] | |
| (K-IFRS, 연결) | (단위 : 백만원) |
| 사업부문 | 품목 | 매출 유형 |
구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | |
| 줄기세포 사업부 |
줄기세포 치료제 | 제품 | CDMO | 내수 | 251 | 1,914 | 404 | 839 |
| 수출 | - | - | - | - | ||||
| 소계 | 251 | 1,914 | 404 | 839 | ||||
| 줄기세포 배양액 | 제품 | 줄기세포 배양액등 |
내수 | 183 | 430 | 1,024 | 363 | |
| 수출 | - | - | - | - | ||||
| 소계 | 183 | 430 | 1,024 | 363 | ||||
| 해동기 | 상품 | Purple Vie | 내수 | - | - | - | 128 | |
| 수출 | - | - | - | - | ||||
| 소계 | - | - | - | 128 | ||||
| 기타 | 기술 | OSCA 기술이전 | 내수 | - | 2,000 | - | - | |
| 수출 | - | - | - | - | ||||
| 소계 | - | 2,000 | - | - | ||||
| 제품 등 | 연구용역 등 | 내수 | 30 | 42 | 17 | 12 | ||
| 수출 | - | - | - | - | ||||
| 소계 | 30 | 42 | 17 | 12 | ||||
| 화장품 사업부 |
화장품 | 제품 | GD11 | 내수 | 150 | 615 | 1,610 | 1,190 |
| 수출 | 95 | 860 | 673 | 272 | ||||
| 소계 | 244 | 1,475 | 2,283 | 1,463 | ||||
| 상품 | 기타 | 내수 | - | - | 2 | 11 | ||
| 수출 | - | - | - | - | ||||
| 소계 | - | - | 2 | 11 | ||||
| 샴푸 | 상품 | BIO-3 | 내수 | 246 | 1,799 | 1,833 | 2,536 | |
| 수출 | - | - | - | - | ||||
| 소계 | 246 | 1,799 | 1,833 | 2,536 | ||||
| 바이오파마 사업부 |
일반 의약품 |
상품 | 일반의약품 | 내수 | - | 86 | 347 | 548 |
| 수출 | - | - | - | - | ||||
| 소계 | - | 86 | 347 | 548 | ||||
| 기타 | 기타 | 기타 | 내수 | - | - | 4 | 14 | |
| 수출 | - | - | - | - | ||||
| 소계 | - | - | 4 | 14 | ||||
| 비임상시험 사업부 |
비임상 시험 |
용역 | 비임상시험 | 내수 | - | - | 7,123 | 10,480 |
| 수출 | - | - | - | - | ||||
| 소계 | - | - | 7,123 | 10,480 | ||||
| (-) 연결 조정 | 내수 | - | - | (332) | (94) | |||
| 수출 | - | - | - | - | ||||
| 소계 | - | - | (332) | (94) | ||||
| 합 계 | 내수 | 859 | 6,886 | 12,032 | 16,028 | |||
| 수출 | 95 | 860 | 673 | 272 | ||||
| 합계 | 954 | 7,746 | 12,704 | 16,301 | ||||
| 출처) 당사 정기보고서 |
| [최근 3개년 국가별 수출 비중] | |
| (K-IFRS, 연결) | (단위 : 백만원) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 국가명 | 매출액 | 비중 | 국가명 | 매출액 | 비중 | 국가명 | 매출액 | 비중 | 국가명 | 매출액 | 비중 | |
| 1 | 일본 | 82 | 86% | 일본 | 665 | 82% | 일본 | 402 | 60% | 일본 | 149 | 55% |
| 2 | 태국 | 4 | 4% | 태국 | 45 | 6% | 대만 | 103 | 15% | 미국 | 52 | 19% |
| 3 | 미얀마 | 4 | 4% | 말레이시아 | 28 | 4% | 태국 | 76 | 11% | 홍콩 | 36 | 13% |
| - | 기타 | 5 | 6% | 기타 | 70 | 8% | 기타 | 92 | 14% | 기타 | 36 | 13% |
| 합계 | - | 95 | 100% | - | 798 | 100% | - | 673 | 100% | - | 272 | 100% |
| 출처) 당사 정기보고서 |
당사는 매출액 중 더마 코스메틱 브랜드 지디일레븐(GD11)의 매출 일부가 수출 형태로 판매되고 있습니다. 국가별 수출 비중을 살펴보면 주로 일본의 비중이 2022년 55%, 2023년 60%, 2024년 82%, 2025년 86%를 기록하고 있습니다.
당사의 22년부터 2025년 1분기까지 원재료 수입 내역은 없습니다.
한편, 당사의 보유 자산 및 부채를 살펴보면 USD 등의 통화 가격 변동에 주로 영향을 받고 있으며, 매출을 살펴보면 수출 비중이 크진 않으나, 주로 일본향 매출 비중이 큰 편입니다. 당사는 내부적으로 환율 변동에 대한 환위험을 정기적으로 측정하고 있으며, 환율을 지속적으로 모니터링하고 전망에 근거한 경영진의 의사결정을 통해 외화자산을 관리하고 있습니다.
당사의 최근 3개년 환율변동 위험 노출정도와 각 외화에 대한 환율 10% 변동시 환율변동이 실적에 미치는 영향은 하기와 같습니다.
| [환율변동위험 노출정도] |
| (단위 : 천원, USD) |
| 구 분 | 통 화 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | ||||
|---|---|---|---|---|---|---|---|---|---|
| 외화금액 | 원화환산금액 | 외화금액 | 원화환산금액 | 외화금액 | 원화환산금액 | 외화금액 | 원화환산금액 | ||
| 현금및현금성자산 | USD | 2,157.47 | 3,155 | 2,157.47 | 3,163 | 2,151.25 | 2,774 | 101,776.46 | 128,981 |
| 출처) 당사 정기보고서 |
한편, 최근 3개년 기준 다른 모든 변수가 일정하고 각 외화에 대한 원화의 환율 10% 변동 시 회사의 당기손익에 미치는 영향은 다음과 같습니다.
| [환율 변동 영향] |
| (단위 : 천원) |
| 구분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|
| 10% 상승 | 316 | 316 | 277 | 12,898 |
| 10% 하락 | (316) | (316) | (277) | (12,898) |
| 출처) 당사 정기보고서 |
원/달러 환율의 추이를 살펴보면, 2022년초 발발한 러시아-우크라이나 전쟁으로 인한 지정학적 리스크와 더불어 2022년부터 한-미 금리격차가 벌어지며 원/달러 환율은 상승하기 시작했고 2022년 9월 1,445.0원까지 고점을 기록하고 급등세는 다시금 진정되며 2023년 1월 1,230.0원까지 하락했습니다. 그러나 2023년 중국의 경기 둔화 및 미국 경기가 상대적으로 빠르게 회복하는 모습을 보이며 다시금 환율은 상승했으나 박스권에서 등락하다 2023년 10월 이스라엘-하마스 전쟁이 발발하며 다시금 지정학적 리스크가 불거져 2024년 초 1,315원 수준에서 2024년 7월 1,380원 수준까지 상승하였습니다. 2024년 8월에 들어서는 일본의 금리 인상 진행 및 미국 고용시장 침체에 대한 우려와 이에 따른 조기 금리 인하 가능성이 높아졌고 달러가 약세로 들어서면서 환율은 1,300원 중반 이하로 하락하는 추세를 보였으나, 이후 미국 경기침체 우려가 다소 해소되면서 재차 1,300원 후반대로 상승하였습니다.
그러나, 2025년 1월 트럼프 정부 출범으로 인해 글로벌 보호무역 기조 및 정책 불확실성은 더욱 확대되고 있는 상황입니다. 이러한 글로벌 경기 불확실성 확대 및 국내 정치적 불안 요소 부각 등 대내외 환경의 영향으로 원/달러 환율은 2024년 12월 31일 1,470.00원까지 급등한 뒤, 2025년 2월 24일 1,434.1원으로 일시적으로 안정되었으나, 이후 1,440원에서 1,475원 사이의 고환율 구간을 형성하며 원화 가치가 빠르게 하락하는 추세를 보였습니다. 다만, 2025년 5월 들어 미중 관세 협상과 같은 주요국 간 외교적 긴장 완화, 대외거래 수지 개선, 통화정책 변화에 대한 기대 등 대내외 여건의 변화에 따라 원/달러 환율이 급락하는 흐름을 보이며 현재 1,360원대 전후를 기록 중입니다. 향후 트럼프 정부 관세 정책 향방 및 금융시장 변동에 따라 환율 변동성이 크게 확대될 수 있으므로 투자자 분들은 이 점 유의하시기 바랍니다.
| [최근 3년간 원/달러 환율 동향] | ||
|
| 출처) 서울외국환중개 |
원/엔 환율의 추이를 살펴보면, 글로벌 경제 변화와 일본의 통화정책 영향을 강하게 받으며 뚜렷한 변동성을 보였습니다.
2022년에는 러시아-우크라이나 전쟁으로 글로벌 불확실성이 확대되었지만, 일본은행(BOJ)의 초완화적 통화정책이 지속되면서 엔화 약세가 두드러졌습니다.
2023년에는 일본 엔화의 회복과 원화 강세가 겹치며 환율이 1,000엔당 950원 수준으로 하락했습니다. 이후 중국 경기 둔화와 일본 경제 회복 기대가 맞물리며 환율은 100엔당 970~1,020원 범위에서 박스권 움직임을 보였습니다.
2024년에는 엔화가 강세를 보였습니다. 특히 하반기에는 일본 금리 인상과 글로벌 지정학적 리스크 완화가 겹쳐 엔화가 추가 강세를 나타내면서 2024년 11월 중순 최저치인 895.87원을 기록하였습니다. 그러나 연말에는 그간의 약세를 되돌리며 꾸준히 상승, 2024년 12월 31일에는 936.48원을 기록하였습니다.
2025년에는 전년도 말의 상승흐름이 지속되며 4월 29일 기준으로는 1,011.85원에 도달하는 등 명확한 오름세를 나타내고 있습니다. 다만, 2025년 5월 중 주요국 통화정책 기대 변화와 글로벌 환율 시장의 방향성 전환 등 외부 여건 변화에 따라 원/엔 환율은 다시 급락세로 전환되는 모습을 보이며 현재 940원대 전후를 기록 중입니다.
| [최근 3년간 원/엔화 환율 동향] | ||
|
| 출처) 서울외국환중개 |
2025년 트럼프 행정부의 대외 정책, 글로벌 경제 변화 등으로 인해 통화의 환율 변동성이 심화된 상황입니다. 이처럼 갑작스러운 환율 변동성의 확대는 당사의 해외 원재료 매입 및 글로벌 임상비용 지출에 영향을 미칠 수 있는 바 투자자 여러분께서는 이 점 유의하시기 바랍니다.
| 차. 잦은 자금조달 관련 위험 당사는 신주 상장으로 주주가치가 훼손될 수 있는 자금조달방법인 유상증자나 주식연계채권을 통해 자금을 조달한 이력이 있습니다. 당사의 경우 바이오의약품 기업 특성 상 추가적인 자금조달 가능성을 배제할 수 없습니다. 추가 자금조달 필요성이 지속될 경우 당사의 자금 유동성이 크게 악화될 수 있고 추가적인 자금조달을 진행할 수 있으며, 반복적인 유상증자 및 주식연계채권 발행으로 주주가치가 심각하게 훼손될 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
(1) 발행 내역 및 향후 자금조달 계획
당사는 신주 상장으로 주주가치가 훼손될 수 있는 자금조달방법인 유상증자나 주식연계채권을 통해 자금을 조달한 이력이 있습니다. 당사는 2010년 상장 이후 2016년 09월 08일 제1회 사모 전환사채(CB) 300억원(시설자금 150억원, 운영자금 150억원), 2017년 04월 29일 유상증자 14억원(제3자배정 보통주, 운영자금), 2018년 07월 28일 유상증자 359억원(주주배정후 실권주 일반공모, 운영자금), 2019년 07월 12일 유상증자 480억원(제3자배정 전환우선주, 운영자금), 2021년 10월 21일 유상증자 390억원(주주배정후 실권주 일반공모, 운영자금), 2023년 11월 08일 유상증자 210억원(주주배정후 실권주 일반공모, 운영자금) 을 통해 자금을 조달하였습니다. 당사가 상장 이후 조달한 자금 현황은 다음과 같습니다.
| [상장 이후 조달한 자금 현황] |
| (단위: 백만원, 원) |
| 발행일 | 종류 | 사용용도 | 발행금액 | 주당 발행 /전환가 |
자금사용목적 | 실제 자금사용 용도 | 배정대상자 및 인수자 |
차이발생 사유 |
| 2015-12-15 | 코스닥 상장 유상증자(일반공모) |
시설자금 운영자금 |
12,360 | 6,000 | - 시설자금 57.4억원 - 운영자금 60.6억원 - 발행제비용 5.6억원 |
- 시설자금 36.5억원 - 운영자금 81.5억원 - 발행제비용 5.6억원 |
일반공모 | 신약개발일정이 조정됨에 따라 설비 신축계획을 일부증축으로 변경하고, 차액분을 연구개발비로 사용 |
| 2016-09-18 | 제1회 사모 전환사채 | 기타자금 | 30,000 | 10,115 | - 운영 경비 150억원 - 시설자금 150억원 |
- 운영 경비 150억원 - 시설자금 150억원 |
키움증권 등 | - |
| 2017-04-29 | 유상증자(제3자배정 보통주) | 운영자금 | 1,400 | 10,200 | - 연구개발비 7억원 - 운영 경비 7억원 |
- 연구개발비 7억원 - 운영 경비 7억원 |
박영찬 | - |
| 2018-07-28 | 유상증자(주주배정후 실권주 일반공모) | 운영자금 | 35,952 | 8,560 | - 아토피 피부염 치료제의 유럽 임상비 240억원 - 류마티스관절염 치료제의 국내 임상비 68억원 - 골관절염 국내 임상비 8억원 - 공정개발연구를 위해 기기 및 장비 개발, 원재료 구매 44억원 |
- 아토피 피부염 치료제의 유럽 임상비 240억원 - 류마티스관절염 치료제의 국내 임상비 68억원 - 골관절염 국내 임상비 8억원 - 공정개발연구를 위해 기기 및 장비 개발, 원재료 구매 44억원 |
주주배정 후 실권주 일반공모 | - |
| 2019-07-12 | 유상증자(제3자배정 전환우선주) | 운영자금 | 48,000 | 14,815 | - 연구개발비 300억원 - 운영 경비 180억원 |
- 연구개발비 300억원 - 운영 경비 180억원 - 미사용금액 77억원 정기예금 보관 |
신한투자증권 등 | - |
| 2021-10-21 | 유상증자(주주배정후 실권주 일반공모) | 운영자금 | 38,985 | 3,150 | - 임상시험비 377억원 - 운영 경비 13억원 |
- 임상시험비 300억원 (아토피 피부염 173억원, 류마티즘 관절염 38억원, OSCA 89억원) - 운영 경비 13억원 - 미사용금액 77억 정기예금 보관 |
주주배정 후 실권주 일반공모 | 미사용자금 1,204 / 단기금융상품 예치 |
| 2023-11-08 | 유상증자(주주배정후 실권주 일반공모) | 운영자금 | 20,970 | 1,165 | - 임상시험비 107억원 - 운영 경비 103억원 |
- 임상시험비 26억원 (아토피 피부염 21억원, OSCA 5억원) - 운영 경비 36억원 - 미사용금액 147억원 정기예금 보관 |
주주배정 후 실권주 일반공모 | 미사용자금 8,425 / 단기금융상품 예치 |
| 합계 | 187,667 | - | - | - | - | - | ||
| 출처) 감사보고소 및 당사 제시 |
당사는 지난 11월 초에 국내 제약사인 유영제약과 체결한 라이선스 아웃 계약에 따른 경상기술료를 단계별로 수취함에 따라 운영 자금을 확보할 계획에 있습니다. 총 140억원의 경상기술료 중 1차 경상기술료 20억원을 수취하였으며, 개발 단계에 따라 지속적으로 경상기술료를 수취함으로 운영자금을 확보할 예정입니다.
최근 임상 1상을 성공적으로 마친 골관절염 치료제 OSCA에 대해서는 임상 2b상부터 유영제약에서 전액 임상 비용을 부담하는 조건으로 계약을 맺으며 막대한 임상 비용 조달에 대한 부담이 감소하였습니다. 또한, 골관절염 치료제 OSCA에 대한 해외 라이선스 아웃에 대해 관심을 가지고 있는 수요처와 논의 중에 있습니다. 독일, 스위스 등 유럽 지역에 소재한 해당 수요처들은 OSCA에 대한 큰 관심을 보이고 있으며 임상 1상의 결과에 대해 매우 고무적으로 반응하고 있습니다. 다만, 임상 1상은 대상 인원이 적은 관계로(12명) 임상 2a상의 진행 상황에 따라 좀 더 구체적인 기술 라이선스 아웃에 대한 논의가 이뤄질 것으로 예상됩니다.
당사의 계획대로 해외 라이선스 아웃이 진행될 경우의 예상 시점은 2026년 하반기혹시 2027년 상반기가 될 것으로 예상하며 성공적으로 해외 라이선스 아웃이 이뤄질 경우, 임상 및 운영 비용에 대한 추가 확충이 필요하지 않을 것으로 판단됩니다. 다만, 당사가 예상하는 시점에 국내 제약사인 유영제약과의 라이선스 아웃에 따른 경상기술료의 수취 및 해외 라이선스 아웃이 이뤄지지 않을 경우에는 주주배정 혹은 제3자 배정을 통한 유상증자, 채무증권 발행 등을 통한 자금확충 계획을 고려하고 있습니다.
이처럼 당사는 다양한 방법으로 자금조달을 하고 있기 때문에 현재 영위하고 있는 연구개발이 제품화에 실패하거나 CDMO 사업 관련 장기적인 사업계획과 자금운용계획을 적정하게 수립하지 못할 경우 향후에도 추가적인 자금조달을 할 수 있습니다. 또한 시장 상황으로 인해 자금조달이 원활하지 않을시에는 유동성 위험에 직면하여 큰 어려움에 처할 수 있으니, 투자자께서는 이 점 유의하시기 바랍니다.
| 카. 매출처 편중 관련 위험 당사의 주요 매출처인 프리모리스인터내셔널, CJ홈쇼핑, GS홈쇼핑사의 경우 2022년 71.0%, 2023년 85.0%로 꾸준히 증가하였으나 2024년 46.9%를 기록하며 매출처 편중이 일부 해소되었습니다. 해당 매출처들의 경우 당사의 주요 매출제품인 화장품 제품군의 매출처입니다. 당사의 경우 이러한 매출 편중을 해소하기 위해 일본 재생의료 사업 진출을 통한 신규 매출을 발생시키고자 적극적으로 영업 활동 중입니다. 현재 일본 재생의료심의위원회의 제2종(자가지방줄기세포)의 후생성 승인이 완료되어 2025년 하반기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 한편, 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며 마찬가지로 승인 시 후생성 승인 후 바로 시장에 공급될 수 있도록 준비 중입니다. 또한 OSCA의 해외 라이선스 아웃 또한 준비 중에 있습니다. 다만, 당사의 이러한 노력에도 불구하고 매출처 다각화가 예상보다 지체되고 주요 매출처 및 잠재 매출처들의 경영전략 변경에 따라 사업관계에 부정적인 변화가 발생하거나 주요 매출처의 매출 및 영업성과가 부진할 경우 당사의 영업실적 및 재무상태에 부정적인 영향을 미칠 수 있으므로 투자자께서는 이 점 유의하시기 바랍니다. |
당사의 줄기세포 사업은 자체 개발한 다분화능을 가진 줄기세포를 인간 제대혈로부터 고순도(high-purity)로 분리하고, 대량배양(massive culture)하는 기술을 기반으로 동종 제대혈유래 줄기세포치료제(의약품) 연구개발을 주요 사업으로 영위하고 있습니다. 줄기세포 사업의 경우 당사가 예상하지 못한 다른 방식의 새로운 치료제가 개발되거나, 타 줄기세포치료제와의 경쟁이 심화될 경우 당사의 장기간 신약 개발에 쓰인 막대한 투자 비용과 시간을 감안할 시 당사의 경영성과 및 수익성에 부정적인 영향을 미칠 수 있습니다. 특히, 연구개발하고 있는 신약이 상업화되기까지 막대한 비용과 시간이 소요되며 특히, 임상시험 진입 시 최소 8~9년이 소요되며 그에 필요한 비용이 요구됩니다. 또한, 임상시험을 진행한다고 하더라도 시험결과 효능이 부족하거나 안전성 평가에 적합하지 못한 결과가 나올 경우 해당 신약의 연구개발은 중단될 수 있으며, 이러할 경우 당사의 비용 및 시간 투자에도 불구하고 엄청난 손실을 야기할 수밖에 없습니다.
한편, 화장품 제품은 줄기세포 배양액 기반의 제품으로, 주름 및 미백 개선 등의 기능성 화장품을 판매하고 있습니다. 향후 화장품 시장의 성장은 유지될 것으로 전망되지만 화장품 산업의 성장이 정체될 경우, 신규 경쟁 기업 증가에 따른 경쟁 심화로 제품 판매가격 하락 및 마케팅 비용 과다지출 등의 판매비와 관리비 상승 가능성이 존재합니다. 또한, 경쟁이 심화되는 시장에서 차별화된 경쟁력을 확보하지 못한다면 당사의 화장품 사업부분 매출에 부정적인 영향을 미칠 수 있습니다.
당사의 주요 제품별 비중 및 주요 거래처 현황은 다음과 같습니다.
| [주요 제품별 현황] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| (단위: 백만원) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 출처) 당사 제시 |
당사의 주요 매출처인 프리모리스인터내셔널, CJ홈쇼핑, GS홈쇼핑사의 경우 2022년 71.0%, 2023년 85.0%로 꾸준히 증가하였으나 2024년 46.9%를 기록하며 매출처 편중이 일부 해소되었습니다. 해당 매출처들의 경우 당사의 주요 매출제품인 화장품 제품군의 매출처입니다.
현재 당사의 매출의 가장 큰 비중을 차지하고 있는 화장품 사업은 당사가 생산한 줄기세포 배양액을 기반으로 한 제품을 주로 판매하고 있으며, 당사가 생산하는 제대혈유래줄기세포는 지방이나 늑골 추출 줄기세포에 비해 세포의 성장과 분화가 매우 뛰어나 기능성 원료로서의 활용가치가 높습니다. 고정비가 많이 드는 오프라인 유통망보다 CJ홈쇼핑(Bio-3 샴푸)와 GS홈쇼핑(GD11 화장품), 인터넷몰 등 온라인 유통망을 적극 활용하고 있으며 영업/판매 전담부서(H&B사업부)를 통해 직접 또는 대리점과 거래하고 있습니다. 영업적 운용 측면에서 오랜 업력으로 관련 국내ㆍ외 시장에서 판매 및 영업 인프라를 구축하고 있는 전략적 파트너(프리모리스인터내셔널 등)와 연계를 통하여 영업 유지ㆍ관리 강화와 고정비용 절감, 수주의 불확실성을 최소화하고 있습니다. 주요한 전략적 사업 파트너인 프리모리스인터내셔널은 당사와 밀접한 관계(특수관계인)로서 영업환경이 다변화할지라도 거래가 단절될 가능성은 적은 편입니다. 해당 회사는 2025년도에 국내 최대 소매 유통 채널(D사)로의 납품 판로 개척을 준비 중이므로 공급 계약이 체결될 경우 판매량이 대폭 늘어날 것으로 기대하고 있습니다.
당사의 최근 5개년 및 2025년 1분기 기준 주요 매출처별 현황은 다음과 같습니다.
| [최근 5개년 및 2025년 1분기 기준 주요 매출처별 현황] |
| (단위: 백만원) |
| 거래처명 | 계정과목 | 제품 | 거래구조 | 2020년 | 2021년 | 2022년 | 2023년 | 2024년 | 2025년 1분기 | 합계 | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 매출액 | 비중 | 매출액 | 비중 | 매출액 | 비중 | 매출액 | 비중 | 매출액 | 비중 | 매출액 | 비중 | 매출액 | 비중 | ||||
| (주)프리모리스인터내셔널 | 상품매출 | 샴푸(Bio-3) | 영세매출 | - | 0.0% | 12 | 0.3% | 80 | 1.4% | 23 | 0.4% | 25 | 0.3% | 7 | 0.78% | 55 | 0.4% |
| 제품매출_줄기세포 | 배양액 | 국내매출 | 143 | 48.4% | 84 | 2.2% | 247 | 4.2% | 912 | 15.4% | 354 | 4.6% | 113 | 11.8% | 1,379 | 9.4% | |
| 제품매출_화장품 | 화장품 | 영세매출 | - | 0.0% | 1,127 | 30.0% | 1,125 | 19.0% | 1,386 | 23.4% | 1,454 | 18.8% | 244 | 25.6% | 3,084 | 21.1% | |
| 기타매출 | 용액매출 | - | - | 0.0% | - | 0.0% | - | 0.0% | - | 0.0% | 6.237 | 0.1% | - | 0.0% | 6 | 0.0% | |
| (주)프리모리스인터내셔널 매출 합계 | 143 | 48.4% | 1,223 | 32.5% | 1,452 | 24.5% | 2,321 | 39.3% | 1,839 | 23.7% | 365 | 38.2% | 4,524 | 31.0% | |||
| CJ홈쇼핑 | 상품매출 | 샴푸(Bio-3) | 홈쇼핑 방송 | - | 0.0% | 1,723 | 45.9% | 2,465 | 41.7% | 1,809 | 30.6% | 1,774 | 22.9% | 239 | 25.0% | 3,823 | 26.2% |
| CJ홈쇼핑 매출 합계 | - | 0.0% | 1,723 | 45.9% | 2,646 | 41.7% | 1,809 | 30.6% | 1,774 | 22.9% | 239 | 25.0% | 3,823 | 26.2% | |||
| GS홈쇼핑(주) |
제품매출_화장품 | GD11 | 홈쇼핑 방송, 홈페이지 | - | 0.0% | - | 0.0% | 282 | 4.8% | 894 | 15.0% | 20.868 | 0.3% | - | 0.0% | 915 | 6.3% |
| GS홈쇼핑(주) 매출 합계 | - | 0.0% | - | 0.0% | 282 | 4.8% | 894 | 15.0% | 20.868 | 0.3% | - | 0.0% | 915 | 6.3% | |||
| 주요 매출처 3사 매출 합계 | 143 | 48.4% | 2,946 | 78.4% | 4,199 | 71.0% | 5,025 | 85.0% | 3,634 | 46.9% | 604 | 63.3% | 9,262 | 63.4% | |||
| 전체 매출 합계 | 295 | 100.0% | 3,756 | 100.0% | 5,915 | 100.0% | 5,913 | 100.0% | 7,746 | 100.0% | 954 | 100.0% | 14,613 | 100.0% | |||
| 출처) 당사 제시 |
당사의 경우 이러한 매출 편중을 해소하기 위해 일본 재생의료 사업 진출을 통한 신규 매출을 발생시키고자 적극적으로 영업 활동 중이며 거래처 다변화를 위해 노력하고 있습니다. 현재 일본 재생의료심의위원회의 제2종(자가지방줄기세포)의 후생성 승인이 완료되어 2025년 하반기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 한편, 제 1종(동종제대혈줄기세포)의 경우 특정인정재생의료위원회 승인까지 완료하였고, 후생노동성 승인 절차를 진행 중에 있으며 마찬가지로 후생성 승인 시 바로 시장에 공급될 수 있도록 준비 중입니다. 또한 OSCA의 해외 라이선스 아웃 또한 준비 중에 있습니다.
다만, 당사의 이러한 노력에도 불구하고 매출처 다각화가 예상보다 지체되고 주요 매출처 및 잠재 매출처들의 경영전략 변경에 따라 사업관계에 부정적인 변화가 발생하거나 주요 매출처의 매출 및 영업성과가 부진할 경우 당사의 영업실적 및 재무상태에 부정적인 영향을 미칠 수 있으므로 투자자께서는 이 점 유의하시기 바랍니다.
| 타. 소송 및 우발채무 관련 위험 당사는 2025년 1분기 현재기준으로 토지, 건물 등 유형자산을 기업은행에게 차입금에 대한 담보로 제공하고 있으며, 유형자산과 관련된 담보설정액은 88.0억원입니다. 당사의 유동성 및 재무안정성 지표를 살펴볼 때 당사의 2025년 1분기 단기 및 장기차입금은 67.1억원으로 현금성자산 186.0억원을 고려하였을 때 단기적인 채무불이행이 발생할 위험은 매우 낮은 상황입니다. 공시서류 제출 전일 현재 당사가 피고로서 계류 중인 소송사건은 없습니다. 상기 서술한 우발채무가 당사에게 어떤 시점에 부정적인 영향을 미칠지는 예측하기가 어려운 것으로 판단됩니다. 당사는 이와 같은 우발부채가 현재 존재하지 않지만 향후 사업운영에 따라 발생할 가능성이 존재하는 소송현황을 적절하게 관리하지 못한다면, 예상하지 못한 시점에 경영 활동에 중대한 부정적인 금전적 손실이 발생하여 투자자에게 대규모 피해를 끼칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
당사의 2025년 1분기 기준 금융기관과의 주요 약정사항은 다음과 같습니다.
| (단위: 천원) |
| 구분 | 금융기관 | 약정금액 | 실행금액 |
|---|---|---|---|
| 시설자본 대출약정 | 기업은행 | 4,000,000 | 3,000,000 |
| 시설자본 대출약정 | 기업은행 | 1,480,000 | 1,480,000 |
| 시설자본 대출약정 | 기업은행 | 350,000 | 350,000 |
| 시설자본 대출약정 | 기업은행 | 380,000 | 380,000 |
| 운전자본 대출약정 | 기업은행 | 1,500,000 | 1,500,000 |
| 합계 | 7,710,000 | 6,710,000 | |
| 출처) 정기보고서 |
당사의 2025년 1분기 기준 특수관계자를 제외한 타인으로부터 제공받은 지급보증의 내용은 다음과 같습니다.
| (단위: 천원) |
| 제공자 | 보증자 | 보증일 | 보증금액 | 보증내용 |
|---|---|---|---|---|
| ㈜지에스리테일 | 서울보증보험 | 2024.11.03 ~ 2026.11.02 | 10,000 | 홈쇼핑계약등에 따른 손해배상금 |
| ㈜씨제이이엔엠 | 서울보증보험 | 2023.09.27 ~ 2025.09.26 | 40,000 | 홈쇼핑계약등에 따른 손해배상금 |
| 출처) 정기보고서 |
당사의 2025년 1분기 기준유형 자산 담보제공 내역은 다음과 같습니다.
| [유형자산 담보제공 내역] |
| (단위: 천원) |
| 담보제공자산 | 장부금액 | 담보설정금액 | 담보감정가격 | 관련 계정과목 | 차입금액 | 담보권자 |
|---|---|---|---|---|---|---|
| 토지 | 3,660,774 | 8,796,000 | 11,028,000 | 차입금 | 6,710,000 | 기업은행 |
| 건물 | 7,758,009 |
| 출처) 당사 정기보고서 |
| 주1) 담보제공자산인 토지 및 건물은 글로벌R&D센터줄기세포재생의학연구소(서울 금천구 소재)와 줄기세포GMP센터(경기도 광명시 소재)입니다. |
| 주2) 담보감정가격의 감정일은 2021년입니다. |
당사는 2025년 1분기 현재기준으로 토지, 건물 등 유형자산을 기업은행에게 차입금에 대한 담보로 제공하고 있으며, 유형자산과 관련된 담보설정액은 88.0억원입니다. 당사의 유동성 및 재무안정성 지표를 살펴볼 때 당사의 2025년 1분기 단기 및 장기차입금은 67.1억원으로 현금성자산 186.0억원을 고려하였을 때 단기적인 채무불이행이 발생할 위험은 매우 낮은 상황입니다.
공시서류 제출 전일 현재 당사가 피고로서 계류 중인 소송사건은 없습니다.
상기 서술한 우발채무가 당사에게 어떤 시점에 부정적인 영향을 미칠지는 예측하기가 어려운 것으로 판단됩니다. 당사는 이와 같은 우발부채가 현재 존재하지 않지만 향후 사업운영에 따라 발생할 가능성이 존재하는 소송현황을 적절하게 관리하지 못한다면, 예상하지 못한 시점에 경영 활동에 중대한 부정적인 금전적 손실이 발생하여 투자자에게 대규모 피해를 끼칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| 파. 합병 철회 등에 따른 관계기업 관련 위험 당사는 주요 사업부문의 파이프라인 다각화, 경영효율성 및 주주가치 제고 등을 달성하기 위하여 2024년 11월 28일 이사회 결의를 통해 관계회사인 (주)프리모리스테라퓨틱스를 피합병회사로 하여 흡수합병(소규모합병)을 결정하였으나, 최근 국제 경제의 불확실성 증대 및 주식시장의 변동성 확대 등 제반 여건을 고려하여 합병 자진 철회를 결정하였습니다. 당사는 향후 수익원 다각화 및 기업가치 증대를 위해 신규 파이프라인 강화 등의 다양한 방안을 꾸준히 강구하고 있습니다. 방안 중 하나로 합병 여부와 무관하게 관계사인 (주)프리모리스테라퓨틱스와 엑소좀을 활용한 재생의료 사업 분야의 공동개발 및 국내외 사업화를 모색하는 등 계속하여 사업적 시너지를 도모할 예정입니다. 이는 당사의 연구개발 약물 형태를 확장하고 차세대 기술 개발 및 파이프라인 다각화 가능성이 생긴다는 긍정적인 측면이 있으나, 동시에 진행 과정에서 당사의 전망과 달리 비경상적 투자로 인한 재무적 여력 소진 추세가 가속화될 수 있으며, 이는 당사의 수익성과 재무안정성에 부정적인 영향을 미칠 가능성이 존재합니다. 또한, (주)프리모리스테라퓨틱스가 추후 자체적인 자금 조달을 진행할 경우, 당사의 보유 지분율 감소에 따른 지배력 감소로 인해 협업 효율을 약화하는 요인으로 작용할 수 있으니 투자자 여러분께서는 유의하여 주시기 바랍니다. |
당사는 주요 사업부문의 파이프라인 다각화, 경영효율성 및 주주가치 제고 등을 달성하기 위하여 2024년 11월 28일 이사회 결의를 통해 관계회사인 (주)프리모리스테라퓨틱스를 피합병회사로 하여 흡수합병(소규모합병)을 결정하였으나, 최근 국제 경제의 불확실성 증대 및 주식시장의 변동성 확대 등 제반 여건을 고려하여 합병 자진 철회를 결정하였습니다. 해당 합병 결정 및 철회 관련 세부 내용은 다음과 같습니다.
(1) (주)프리모리스테라퓨틱스 합병 결정(2024.11.28)
당사는 2023년 01월 20일 이사회를 통해 계열회사 지분 인수 및 계열회사 증자 출자 안건을 승인받은 뒤, 2023년 2월 2일 (주)프리모리스테라퓨틱스 최대주주였던 강경선으로부터 보통주식 60,000주(지분율 42.5%, 총 발행 주식수 141,061주 기준)를 무상으로 수증받았습니다. 이후 2023년 2월 08일 (주)프리모리스테라퓨틱스 전환우선주 11,765주(지분율 7.7%, 총 발행 주식수 152,826주 기준)를 금 20억원에 취득하여 공동지배력을 획득하였으며, 이에 당사 공동 기업에 포함되었습니다. 이후 2024년 10월 31일 당사 임직원 2인(이동열, 이미혜)으로부터 총 27,200주(각 20,200주, 7,000주)(지분율 17.80%, 총 발행 주식수 152,826주 기준)를 무상수증 받아 지분율은 64.76%(보통주 57.06%, RCPS 7.7%, 총 발행 주식수 152,826주 기준)로 증가하였습니다. 당사는 강경선, 이동열, 이미혜로부터의 무상 증여와 신주 인수를 통해 (주)프리모리스테라퓨틱스의 지분율을 높이며 실질 지배력을 강화하였습니다. 이러한 지분 확보를 통해 당사는 (주)프리모리스테라퓨틱스와의 계열사 간 협력 및 차세대 치료제 및 융복합 치료제 개발과 같은 기술적 시너지를 강화하고자 하였습니다.
| [당사의 (주)프리모리스테라퓨틱스 RCPS 취득 및 보통주 무상수증 내역] |
| 구분 | RCPS 취득 | 보통주 무상수증 | |||
|---|---|---|---|---|---|
| 구분 | 1차 | 2차 | 3차 | ||
| 계약일 | 기명식 상환전환우선주 | 증여자 | 강경선 | 이동열 | 이미혜 |
| 발행주식총수 | 11,765주 | 증여일 | 2023년 02월 02일 | 2024년 10월 31일 | 2024년 10월 31일 |
| 액면가액 | 5,000원 | 주식수 | 60,000주 | 20,200주 | 7,000주 |
| 발행가액 | 170,000원 | 지분율 | 13.2% | 4.6% | |
| 발행주식총액 | 2,000,050,000원 | 액면가액 | 5,000원 | 5,000원 | 5,000원 |
| 청약일 | 2023년 02월 08일 | - | - | - | - |
| 출처) 당사 제시 |
(주)프리모리스테라퓨틱스는 엑소좀 및 약물전달 플랫폼 개발에 특화된 바이오 신약개발 전문성을 보유하고 있습니다. 이에 당사는 합병을 통해 (주)프리모리스테라퓨틱스의 엑소좀 전문 연구개발 역량을 통합함으로서 줄기세포 치료제와 더불어 엑소좀을 활용한 창상(화상) 치료제 및 약물전달 플랫폼 기술을 활용한 신약 개발 파이프라인을 강화를 극대화할 수 있을 것으로 생각하였습니다. 이에 당사는 2024년 11월 28일 이사회 결의를 통해 (주)프리모리스테라퓨틱스를 피합병회사로 하여 흡수합병(소규모합병)을 결정하였습니다.
| [회사합병결정(2024.11.28)] |
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 출처) 금융감독원 전자공시시스템 |
당시 합병 목적과 관련된 상세 내용은 다음과 같습니다.
| ③ 합병의 목적 - 기술적ㆍ사업적 시너지 (주)강스템바이오텍은 이번 합병을 통해 기술적ㆍ사업적 시너지를 발휘할 예정입니다. 엑소좀은 세포 간 신호전달의 핵심물질인 핵산과 그 외 유효성분을 포함한 Bio-material(생체재료)로서 줄기세포의 파라크라인효과(Paracrine effect) 등을 모사하면서 세포치료제가 가질 수 있는 한계점, 예를 들면 세포의 Lung Trapping(폐 조직내 세포 밀집 현상)에 따른 치료효과 감소, 세포 보관을 위한 영하 70℃ 이하의 저온 운송, 세포가 변이시 발생할 수 있는 안정성 변수 등을 극복할 수 있는 '무세포(Cell-Free)' 치료제로 급부상하고 있습니다. ㈜프리모리스테라퓨틱스는 엑소좀 생산을 위한 분리, 배양,대량 생산까지 기술 노하우를 확보하였으며, ㈜강스템바이오텍은 엑소좀 생산의 근간이 되는 줄기세포의 원천기술 및 임상에 대한 1상부터 3상까지의 경험을 보유하고 있습니다. 이는 양사의 기술적 유사성, 보완성이 매우 큼을 의미합니다. 이에 양사의 기술적 측면에서의 합병 시너지 발현을 통해 창상(화상) 치료제 및 차세대 융복합 치료제 등의 개발 및 사업화를 도모할 계획입니다. - 파이프라인의 다각화 피합병회사의 기술을 내재화하여 합병회사의 파이프라인을 강화할 계획입니다. 기존, 줄기세포 치료제 중심의 파이프라인을 보유한 (주)강스템바이오텍의 기술력과 (주)프리모리스테라퓨틱스의 엑소좀 활용 화상 치료제 및 약물전달 플랫폼 기술을 활용한 신약 개발 등 파이프라인을 강화하여 궁극적으로는 합병회사의 수익성과 성장성에 크게 기여할 것으로 기대하고 있습니다. 특히, (주)프리모리스테라퓨틱스가 보유한 화상 치료제의 경우 소규모 임상 시험을 통해 신속한 임상이 가능하여 빠른 매출 실현이 가능할 것으로 기대됩니다. 뿐만 아니라 폐렴 및 탈모 치료제의 비임상시험 진행을 또한 순차적으로 계획하고 있어, (주)강스템바이오텍의 다양한 임상 경험을 바탕으로 임상 파이프라인의 다각화 및 임상 성공 가능성 증대를 기대하고 있습니다. 또한 (주)강스템바이오텍이 기존에 진행해 왔던 국내 임상 경험 외에, 호주에서의 임상을 진행함으로써 약물에 대한 다인종 간 유효성 검증 및 해외 임상 경험을 축적할 수 있습니다. 이는, ㈜강스템바이오텍이 현재 추진중인 북미, 유럽 임상 및 시장 진출에 많은 도움이 될 것으로 기대하고 있습니다. - CDMO 사업확대 CDMO 신규 수주를 통한 매출 증대가 기대됩니다. (주)강스템바이오텍은 CDMO사업을 영위하고 있습니다. 이미 (주)프리모리스테라퓨틱스와의 CMO 수주 계약을 통해 20억 원 규모의 연구개발생산을 진행 중이며, 합병으로 엑소좀 개발 업체간 경업금지 의무가 해소되어 치료 질환이 중복되지 않는 엑소좀 개발 업체를 대상으로 CDMO 신규 수주를 추진할 예정입니다. 이를 통해 GMP의 가동률의 증가 효과도 기대하고 있습니다. - 사업화 시너지 엑소좀을 활용한 재생의료 사업 분야의 공동개발 및 국내외 사업화를 모색 중입니다.합병회사는 기존 화장품(H&B사업)을 통해 엑소좀 활용 제품에 대한 피부과 수요를 확인한 바 있으며, 이에 양사는 제품의 사업화를 위해 (주)프리모리스테라퓨틱스는 식약처 승인과 판매를, (주)강스템바이오텍은 제품의 독점 생산 및 공급 역할을 분리하여 진행하고자 하였으나, 합병을 통해 단일 조직내에서 사업을 추진함으로서 신속한 매출 실현 등 사업적 시너지를 도모하고자 합니다. - 경영효율성 극대화 (주)강스템바이오텍은 퓨어스템-에이디주(아토피 피부염 치료제)의 대규모 임상 및 오스카(OSCA, 골관절염 치료제,구. 퓨어스템-오에이 키트 주) 1상 임상 경험과 전문 지식을 갖춘 임상 인력과 기술이전계약을 위한 사업개발 인력 및 cGMP 수준의 최신 생산시설을 보유하고 있습니다. 본 합병을 통해 (주)프리모리스테라퓨틱스가 진행 중인 호주 임상 1상에 대한 기술적 협업, 레퍼런스 활용 및 향후 엑소좀 치료제 생산을 위한 중복 투자 및 외부 비용을 절감하여 경영의 효율성을 극대화 할 수 있을 것으로 예상됩니다. |
| 출처) 금융감독원 전자공시시스템 |
(2) (주)프리모리스테라퓨틱스 합병 철회 결정(2025.05.09)
다만, 당사는 합병 결정 이후 최근 국제경제의 불확실성 증대 및 주식시장의 변동성 확대 등 제반 여건을 고려하여 합병 일정 재검토를 위해 해당 합병을 철회하는 것으로 결정하였으며, ㈜프리모리스테라퓨틱스와 합병계약 해제를 합의하였습니다. 이에 따라 해당 합병과 관련된 사항은 철회되었으니 투자자분들께서는 이점 유의하시기 바랍니다.
| [철회신고서(2025.05.09)] |
|
| 출처) 금융감독원 전자공시시스템 |
당사는 향후 수익원 다각화 및 기업가치 증대를 위해 신규 파이프라인 강화 등의 다양한 방안을 꾸준히 강구하고 있습니다. 방안 중 하나로 합병 여부와 무관하게 관계사인 (주)프리모리스테라퓨틱스와 엑소좀을 활용한 재생의료 사업 분야의 공동개발 및 국내외 사업화를 모색하는 등 계속하여 사업적 시너지를 도모할 예정입니다. 이는 당사의 연구개발 약물 형태를 확장하고 차세대 기술 개발 및 파이프라인 다각화 가능성이 생긴다는 긍정적인 측면이 있습니다. 다만, 동시에 진행 과정에서 당사의 전망과 달리 비경상적 투자로 인한 재무적 여력 소진 추세가 가속화될 수 있으며, 이는 당사의 수익성과 재무안정성에 부정적인 영향을 미칠 가능성이 존재합니다. 또한, (주)프리모리스테라퓨틱스가 추후 자체적인 자금 조달을 진행할 경우, 당사의 보유 지분율 감소에 따른 지배력 감소로 인해 협업 효율을 약화하는 요인으로 작용할 수 있으니 투자자 여러분께서는 유의하여 주시기 바랍니다.
한편, 2025년 6월 5일 한국거래소는 당사의 회사합병 결정 철회 건에 대하여 공시번복 건에 해당한다고 판단하여 불성실 공시 법인 지정을 예고하였습니다. 코스닥시장 공시규정 제32조에 따라 당사는 상기 예고 내용에 대하여 이의를 신청할 수 있고, 코스닥시장공시위원회의 심의에 따라 불성실공시법인 해당여부, 부과벌점, 공시위반제재금의 부과 여부 등이 결정될 수 있습니다. 당사는 추후 불성실공시법인 지정여부 등 그 구체적인 결과가 확정되는 대로 공시할 예정이오니 투자자 여러분께서는 참고 바랍니다.
| [불성실공시법인지정예고 공시(2025.06.05)] |
|
||||||||||||||||||||
| 출처) 금융감독원 전자공시시스템 |
| [불성실공시 관련 코스닥시장 공시규정] |
|
제28조(공시번복) (중략) 제32조(불성실공시 법인 지정 절차 등) ② 제1항의 규정에 의하여 불성실공시법인 지정예고를 통보받은 법인은 통보를 받은 날부터 7일 이내에 거래소에 이의신청할 수 있다. ③ 거래소는 특별한 사유가 없는 한 제2항의 이의신청기간이 종료한 날부터 10일 이내에 제50조의 규정에 의한 코스닥시장공시위원회(이하 "위원회"라 한다)의 심의를 거쳐 심의일로부터 3일 이내에 해당 코스닥시장상장법인의 불성실공시법인 해당여부, 부과벌점, 제34조의 공시위반제재금의 부과 여부 및 제34조의2에 따른 공시책임자·공시담당자에 대한 교체요구 여부 등을 결정하여야 하며, 이 경우 거래소는 위반행위의 동기, 중요성, 투자자 영향 및 해당 법인의 성실공시 관행 등 세칙에서 정하는 사항을 고려하여 해당 불성실공시법인 부과벌점, 벌점의 가중·감경을 결정한다. 다만, 해당 코스닥시장상장법인의 성실공시 이행정도 등을 고려하여 세칙으로 정하는 바에 따라 불성실공시법인 지정을 6개월간 유예할 수 있다. ④ 거래소는 제3항의 규정에 의하여 해당 코스닥시장상장법인의 불성실공시법인 해당 여부 및 부과벌점 등을 결정하기 위하여 필요하다고 인정하는 경우 해당 사실을 증명하는 서류 등의 제출을 요구할 수 있으며, 코스닥시장상장법인은 특별한 사유가 없는 한 지체없이 이에 응하여야 한다. ⑤ 거래소는 제3항의 규정에 의하여 해당 법인을 불성실공시법인으로 지정하거나 지정을 유예하는 경우 그 사실 등을 세칙으로 정하는 바에 따라 공시매체에 게재하고 해당 법인에게 통보하며, 불성실공시법인으로 지정하지 않는 경우에도 해당 코스닥시장상장법인에 대하여 성실공시 이행촉구 등의 조치를 할 수 있다 |
자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융감독법규정보시스템(http://law.fss.or.kr)", "KRX법무포털(https://rule.krx.co.kr)" 등을 참고하시기 바랍니다.
| 하. 내부회계관리제도 및 내부통제 관련 위험 당사는 내부통제를 위한 규정 및 조직을 구축하고 있으며, 우발상황 등이 발생하지 않도록 상시 모니터링을 통해 내부통제 강화를 위하여 상당한 노력을 기울이며 대비하고 있습니다. 그럼에도 불구하고, 내부회계관리조직이 적절하게 운영되지 않거나 혹은 외부감사인의 내부회계관리 운영실태를 검토한 결과 중요한 취약점이 발견될 시 각종 제재사항에 해당할 수 있습니다. 투자자 여러분들께서는 이 점을 반드시 유의하여 주시기 바랍니다. |
당사는 코스닥 상장법인으로「주식회사 등의 외부감사에 관한 법률」(이하 '외감법')에 따라 신뢰할 수 있는 회계정보의 작성과 공시를 위해 내부회계관리규정 및 내부회계관리제도를 갖추고 있어야 합니다. 또한, 외부감사인은 당사의 내부회계관리제도 운영실태를 검토를 진행하여야 하며, 해당 결과는 감사보고서에 표명하도록 되어 있습니다. 최근 사업연도 기준 당사 외부감사인의 내부회계관리제도 검토 의견은 아래와 같습니다.
| [내부회계관리제도 검토의견] |
| 사업연도 | 감사인 | 감사의견 및 검토 의견 | 지적사항 |
|---|---|---|---|
| 제15기 (2024년) |
안진회계법인 | 경영자의 내부회계관리제도 운영실태평가보고서에 대한 우리의 검토결과, 상기 경영자의 운영실태보고 내용이 중요성의 관점에서 내부회계관리제도 모범규준 제5장 '중소기업에 대한 적용'의 규정에 따라 작성되지 않았다고 판단하게 하는 점이 발견되지 아니하였습니다. | 해당사항 없음 |
| 제14기 (2023년) |
안진회계법인 | 경영자의 내부회계관리제도 운영실태평가보고서에 대한 우리의 검토결과, 상기 경영자의 운영실태보고 내용이 중요성의 관점에서 내부회계관리제도 모범규준 제5장 '중소기업에 대한 적용'의 규정에 따라 작성되지 않았다고 판단하게 하는 점이 발견되지 아니하였습니다. | 해당사항 없음 |
| 제13기 (2022년) |
안진회계법인 | 경영자의 내부회계관리제도 운영실태평가보고서에 대한 우리의 검토결과, 상기 경영자의 운영실태보고 내용이 중요성의 관점에서 내부회계관리제도 모범규준 제5장 '중소기업에 대한 적용'의 규정에 따라 작성되지 않았다고 판단하게 하는 점이 발견되지 아니하였습니다. | 해당사항 없음 |
| 출처) 당사 감사보고서 |
당사는 재무활동 건전성 및 타당성을 검토하고 내부회계관리제도 운영실태를 평가하며, 현 내부회계관리제도를 철저히 운영하여 외부감사인의 내부회계관리제도에 대한 의견을 받고 있습니다.
다만, 내부회계관리를 철저히 운영함에도 불구하고 회계처리 위반, 혹은 관련 임직원의 배임 및 횡령 등 발생으로 내부회계관리가 적절하게 운영되지 않을 경우 과태료 등의 법적 제재가 부과될 수 있습니다. 과태료 부과 시 법정최고금액에 과태료 예정금액 산정표에 따른 비율을 적용하여 예정금액을 산정하고, 가증, 감경하여 최종 과태료부과금액을 결정하고 있습니다.
특히, 이사 등 내부회계관리제도 운영 관련자가 회계정보를 내부회계관리제도에 의하지 아니하고 위조, 변조, 훼손 또는 파기한 사실이 확인되는 경우, 5년 이하의 징역 또는 5천만원 이하의 벌금이 부과될 수 있습니다.
또한, 코스닥시장 상장규정에 따라 내부회계관리제도 비적정 시 투자주의환기종목에 지정될 수 있으며(「코스닥시장 상장규정」제52조), 2년 연속 내부회계관리제도 비적정 의견을 받는 경우 상장적격성 실질심사에 따른 상장폐지 요건에 해당할 수 있습니다(「코스닥시장 상장규정」제56조).
종합적으로 당사는 내부통제를 위한 규정 및 조직을 구축하고 있으며, 우발상황 등이 발생하지 않도록 상시 모니터링을 통해 내부통제 강화를 위하여 상당한 노력을 기울이며 대비하고 있습니다. 그럼에도 불구하고, 내부회계관리조직이 적절하게 운영되지 않거나 혹은 외부감사인의 내부회계관리 운영실태를 검토한 결과 중요한 취약점이 발견될 시 각종 제재사항에 해당할 수 있습니다. 투자자 여러분들께서는 이 점을 반드시 유의하여 주시기 바랍니다.
3. 기타위험
|
가. 금융감독기관의 규제 강화에 따른 위험 당사가 중점심사 대상 기준에 해당하는 경우, 중점 심사항목 위주로 1주일 이내 집중심사를 진행하고 최소 1회 이상의 대면협의를 진행하게 되며, 본 증권신고서는 공시 심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우에는 본 신고서상의 일정이 예상보다 지연될 가능성이 있습니다. 투자자 여러분께서는 이 점 유의하시기 바랍니다. |
최근 금융감독기관 등의 관리감독기준이 엄격해지고 있는 상황으로 관련 규정을 위반할 경우 주권매매정지, 관리종목지정, 투자주의환기종목 지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다. 향후 감독기관으로부터 당사가 현재 파악하지 못한 제재가 부과될 경우 주가하락 및 유동성(환금성)제약 등으로 인해 투자금에 막대한 손실이 발생할 수 있습니다. 투자자 여러분들께서는 관련 규정을 충분히 검토하신 후 투자에 임해주시기 바랍니다. 상세 내용은 본 증권신고서 "제1부 모집 또는 매출에 관한 사항 - III.투자위험요소 - 3.기타위험 - 마.관리종목 편입 가능성에 따른 위험'을 참고하여 주시기 바랍니다.
특히, "코스닥시장 상장규정 제28조(관리종목), 코스닥시장 상장규정 제38조(상장의 폐지) 및 코스닥시장 상장규정 제38조의2(실질심사위원회의 심사 등"에 유의하시기 바랍니다. 자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융법규서비스(http://fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
또한 2025년 2월 27일, 금융감독원은 기업공개(IPO), 유상증자 주관 업무 관련하여 16개 증권사와 간담회를 갖고 주관 업무 관련 불공정거래 및 위규 행위에 대해 엄정하게 대응하겠다고 밝혔습니다. 주주권익 훼손 우려가 있는 유상증자에 대해서는 증권신고서가 주주와의 공식적 소통 창구가 될 수 있도록 심사 절차 및 기준을 정비하고 이를 공개하였습니다. 특히, △ 주주 가치 희석화, △ 일반주주 권익 훼손 우려, △ 주관사의 의무 소홀 등 7개 사유 중 하나에 해당하는 경우 '중점심사 유상증자' 대상으로 선정해 유상증자의 당위성, 의사결정 과정, 이사회 논의 내용, 주주 소통계획 등 기재 사항을 집중심사한다고 밝혔습니다. 중점심사 유상증자 선정기준 상세 항목 및 중점심사 유상증자 해당시 심사절차는 아래와 같습니다.
| [중점심사 유상증자 선정기준] |
| 대분류 | 소분류 | 선정기준 |
|---|---|---|
| 주식가치 희석화 우려 | ① 증자비율 | 증자규모 및 증자비율 등 고려 |
| ② 할인율 | 증자규모 및 할인율 등 고려 | |
| 일반주주 권익훼손 우려 | ③ 신사업투자 등 | 자금사용목적의 타법인출자 또는 신규사업 연관성 고려 |
| ④ 경영권 분쟁발생 | 경영권 분쟁 소송이 진행되었거나 진행중 | |
| 재무위험 과다 | ⑤ 한계기업 등 | 최근 3년 연속 재무실적 부실 또는 재무구조 악화 등 |
| 주관사의 주의의무 소흘 | ⑥ IPO 실적 과다 추정 | IPO 후 실적 괴리율 등 고려 |
| ⑦ Due Diligence 소흘 | 다수의 정정요구를 받은 주관사의 인수·주선 참여 |
| 출처) 금융감독원 보도자료 |
| 주1) 주식 관련 사채(CB, BW 등) 발행 포함 |
| 주2) ③, ④ 외 정성적 중점심사 유상증자 기준을 탄력적으로 운용 예정 |
| 주3) 규모, 비율 등 계량기준은 비공개 운영 |
|
[중점심사 유상증자 심사절차] |
||
|
| 출처) 금융감독원 보도자료 |
중점심사 유상증자에 해당하는 경우 공통 심사항목으로 1) 유상증자의 당위성 및 의사결정 과정, 2) 이사회 논의 내용, 3) 주주 소통절차, 4) 기업실사 내용 등 기재사항을 집중심사할 예정입니다. 특히, 현행 IPO 심사절차를 준용해 제출 1주일 내 집중심사를 진행하고, 최소 1회 이상 대면협의를 할 계획입니다. 이와 함께 중점심사 유상증자 대상으로 지정된 사유와 해당 이슈가 발생하게 된 경위와 향후 대응 방안 등을 심사할 예정입니다.
| [중점심사 지정사유별 심사항목] |
| 중점심사 지정사유 | 심사항목 |
|---|---|
| ① 공통 심사항목 | 유상증자 당위성 및 의사결정과정, 동 사항들의 이사회 논의 여부 및 그 논의내용, 소액주주 등의 이해 고려여부 및 주주 보호 방안 관련 개선계획, 기업실사 합리적 수행여부 등 |
| ② 증자비율, 할인율 | 증자비율, 할인율 적정성에 대한 검토여부 및 검토내용, 이에 대한 이사회 논의여부 및 그 내용 등 |
| ③ 신사업투자 등 | 신규사업 진출위험, 기존 사업에 미치는 영향, 타법인 인수시 가격 적정성 검토여부 및 주요 검토내용 등 |
| ④ 경영권 분쟁발생 | 경영권 분쟁 상황에서 유상증자 추진 배경 및 목적, 관련 법률적 위험 등 |
| ⑤ 한계기업 등 | 재무지표 악화 경위, 이로 인해 발생할 수 있는 위험 및 이를 극복하기 위한 회사의 대응방안 등 |
| ⑥ IPO실적 과다 추정 | 상장시 자금사용 계획과 달리 자금이 추가로 필요하게 된 경위, 괴리율 발생원인 및 회사의 대응방안 등 |
| 출처 : 금융감독원 보도자료 |
증권신고서 제출일 현재 유상증자 중점심사 지정사유별 심사항목에 대한 당사의 검토 내용은 다음과 같습니다.
(공통 심사항목)
1. 주주배정 후 실권주 일반공모 유상증자 당위성
당사가 영위하는 신약 개발업은 지속적인 연구개발 비용이 소요되며, 경쟁력 확보를 위해서는 높은 기술력의 파이프라인 확보를 위한 투자가 필수적입니다. 특히, 당사의 주요 파이프라인이 속해있는 아토피 치료제, 골관절염 치료제 등의 분야는 잠재적인 시장 규모가 거대한 만큼, 글로벌 시장에서 치열한 경쟁이 전개되고 있습니다. 이에 따라 당사는 금번 유상증자를 통해 기존 파이프라인의 임상 개발을 더욱 빠르게 추진하여 기술력을 확보하고자 합니다. 동시에, 선제적 투자를 통해 기타 매출처를 확대하고, 자본 건전성을 제고하여 향후 글로벌 시장 내에서 경쟁력을 보유하기 위한 발판을 마련하고자 합니다.
(1) 핵심 파이프라인인 골관절염 치료제(OSCA)의 임상 가속화
당사의 골관절염 치료제(OSCA)는 1상에서 염증 완화 및 연골 재생에서 뛰어난 효과를 입증해내며 2024년 11월 유영제약과 라이센스 아웃 계약을 체결하였습니다. 이후, 세계골관절염학회(OASRI) 등 여러 국제학회에서 성공적인 1상 결과를 발표하며 근본적인 골관절염 치료제(DMOAD)로서의 잠재력을 보여주었습니다. 이로 인해 현재 여러 글로벌 제약사들로부터 OSCA의 기술력에 대한 관심을 받고 있는 상황입니다. 이러한 레퍼런스를 바탕으로 임상 규모를 확대하여 국내 임상 2a상 진행 및 해외임상 등 추가 임상을 진행하여 글로벌 라이센스 아웃을 위한 임상 전략을 수립하는데 있어 최적의 시기로 판단하였습니다.
이러한 핵심 파이프라인의 임상시험은 대규모 자금이 소요되나, 자체 임상 데이터 확보를 통해 신약의 가치를 최대한 높이고, 향후 글로벌 기술이전 시 유리한 협상 위치를 확보하며 파트너사 선택의 폭을 넓히기 위한 필수적인 과정입니다. 당사는 2023년 주주배정 후 실권주 일반공모 유상증자룰 통해 OSCA 임상시험비 약 43.8억원을 확보하였으며 잔액으로 약 37.5억원을 보유 중입니다. 2023년 증자 당시에는 OSCA의 국내임상 1/2a상 및 장기추적조사만을 계획하였지만 현재 당사가 국내 2a 임상 규모 확대 및 해외임상까지 범위를 확대한만큼 2028년까지 예상되는 총 비용은 약 238.5억원으로 증가하였습니다. 이에 따라 기존에 OSCA 임상을 위해 확보한 자금은 현재의 임상 계획을 진행하기에 부족한 수준이며, 추가 재원 확보를 위해 증자를 통한 자금조달을 계획하게 되었습니다. 금번 조달 자금은 이러한 핵심 파이프라인의 임상시험을 계획대로 신속하게 진행하고, 조기에 의미 있는 결과를 도출하여 기업가치를 극대화하는 데 사용될 것입니다.
(2) 줄기세포 치료제의 일본 및 국내(첨생법) 재생의료사업 진출 추진
당사는 안정적인 수익 기반을 확보하기 위해 일본 재생의료 시장 및 국내(첨생법) 재생의료 사업 진출을 계획하고 있습니다. 일본 재생의료시장 진출을 위해 2024년 일본 후생노동성에 제1종(동종제대혈줄기세포) 및 제2종(자가지방줄기세포) 재생의료 제공계획에 대한 심의 및 승인 절차를 진행하였습니다. 제2종(자가지방줄기세포)의 경우, 2025년 2월 후생노동성 최종 승인까지 완료되어 2025년 하반기부터 일본 내 환자 투여를 계획하고 있습니다. 이에 금번 조달 자금의 일부는 일본 현지 환자 수급을 위한 본격적인 영업활동 및 투자를 진행을 위한 운영자금으로 활용될 예정입니다.
한편, 국내 첨단재생바이오법 개정안 시행에 따라 첨단재생의료 임상연구 및 첨단재생의료 치료 제도를 통해 희귀/난치 질환자가 당사의 줄기세포치료제를 조기에 사용할 수 있도록 치료 기회를 확대할 계획을 가지고 있습니다. 당사 주요 파이프라인 치료제의 대상 적응증인 중증아토피와 골관절염은 난치질환에 해당합니다. 금번 조달 자금의 일부는 국내 협력기관과의 협업을 통한 2025년 재생의료 임상연구 계약 개시 및 2026년 임상연구 계획 제출 및 임상연구 시작 등에 활용될 예정이며, 이는 당사의 아토피 피부염 치료제(퓨어스템-에이디 주)와 골관절염 치료제(OSCA) 등의 임상연구데이터를 확보하고 치료제 조기 공급을 통한 수익화 기회 확대의 토대를 마련해 줄 것 입니다.
(3) 기타 파이프라인 연구개발 투자 및 지속 가능한 성장 기반 마련
당사는 기타 파이프라인 중 하나로 오가노이드를 연구개발 중에 있습니다. 특히 당사의 피부 오가노이드 기술의 경우, 공기-액체 계면(ALI) 배양을 통해 불필요한 연골 조직의 형성을 억제하여 실제 피부와 같은 평평한 구조를 완벽 재현하여 다양한 유효물질에 대한 약물 스크리닝 및 효력평가 등에 적용 가능하여, 일부 대형 글로벌 제약사들로부터 관심을 받고 있는 상황입니다. 이러한 파이프라인들의 포트폴리오를 지속적으로 확장하기 위해서는 선제적이고 적극적인 연구개발 투자가 필수적입니다. 이는 단기적인 성과뿐만 아니라 중장기적인 기업 성장의 발판을 마련하는 데 중요한 역할을 할 것입니다.
(4) 실권주 일반공모를 통한 투자자 참여 기회 확대
당사는 주주배정 후 실권주 일반공모 방식을 채택함으로써 기존 주주의 권리를 보호하는 동시에 신규 투자자들에게도 투자 기회를 제공하고자 합니다. 이를 통해 기존 주주들의 지분희석화를 최소화함과 동시에 실권주 일반공모를 통해 다양한 투자자층을 확보하고 기업의 지속 가능한 성장을 위한 기반을 마련할 것입니다.
상기한 바와 같이, 당사는 금번 유상증자를 통해 조달되는 자금을 핵심 파이프라인의 경쟁력 강화, 재생의료 시장 진출 및 추가 성장 동력 확보라는 명확한 목표 하에 투명하고 효율적으로 사용할 계획입니다. 이를 통해 기업가치를 지속적으로 증대시키고, 궁극적으로 주주분들의 이익을 극대화하기 위한 최선의 노력을 다할 것입니다.
당사는 금번 유상증자로 인해 기존 주주들의 지분이 희석될 수 있음을 충분히 인지하고 있으며, 이사회결의시 조달규모 등 정량적인 조건뿐만 아니라, 유상증자의 당위성과 소액주주 등의 유상증자 이해 고려, 주주보호(소통) 방안 등 정성적인 기준도 감안하여 본 유상증자의 목적과 필요성을 논의하였습니다. 당사는 금번 유상증자 자금조달 방안 이외에 다음과 같은 조달 방안들도 함께 검토하였습니다.
1) 회사채 발행
당사는 증권신고서 제출일 현재 공모 회사채 발행을 위한 적격 신용평가기관의 신용등급은 존재하지 않은 상태입니다. 신용평가기관의 등급 평가 방식으로는 정량적 평가(재무분석 : 수익성, 재무건정성, 현금흐름, 성장성 등) 및 정성적 평가(산업전망, 경쟁력, 경영진의 역량, 정부규제 등)과 함께 계량 모델 및 비교분석을 통해 진행되고 있습니다. 이후 신용등급이 확정되어 투자적격 등급 이상(BBB- 이상)의 등급으로 구분될 시 회사채 금융시장에서의 원활한 자금조달이 가능할 것으로 예상한 바, 당사는 공모 회사채 발행을 통한 자금조달은 현재 어려울 것으로 판단하였습니다. 또한, 사모 회사채 발행도 검토하였으나 높은 금리, 짧은 만기, 담보 및 지급보증 요구 등으로 인해 재무적 부담이 과도할 수 있다는 판단하에 실제 발행으로 이어지지 못하였습니다.
2) 주식 관련 사채 발행
주식 관련 사채로는 주식으로 전환될 수 있는 전환사채, 신주인수권 권리를 보유하고 있는 신주인수권부사채, 특정 주식으로 교환할 수 있는 교환사채 등이 존재합니다. 당사는 주식 관련 사채 또한 자금조달의 방안 중 하나로 고려하였으나, 회사의 재무 여건 등을 고려할 때 투자자 모집에 어려움이 있어 선택할 수 없었습니다.
3) 담보 제공을 통한 추가 차입
2025년 1분기 기준 당사 유형자산 중 담보력이 존재한다고 생각되는 토지 및 건물의 총 장부 금액은 약 12,025백만원입니다. 이 중 당사는 토지 및 건물(장부금액 약 11,418백만원)에 대해 8,796백만원 담보 설정하여 6,710백만원을 이미 차입하고 있습니다. 당사는 복수의 금융기관을 통해 현 담보물을 통한 추가 차입 가능 여부를 사전 검토하였으나, 추가 차입 가능성이 매우 낮은 것으로 확인하여 담보 제공을 통한 추가 차입 조달을 선택할 수 없었습니다.
| [2025년 1분기말 유형자산 상세 현황] |
| (단위: 천원) |
| 구 분 | 취득금액 | 감가상각누계액 | 정부보조금 | 장부금액 |
|---|---|---|---|---|
| 토지 | 3,927,206 | - | - | 3,927,206 |
| 건물 | 9,241,382 | (1,143,426) | - | 8,097,956 |
| 시설장치 | 7,998,885 | (3,919,893) | - | 4,078,992 |
| 연구시험용자산 | 7,968,351 | (7,194,122) | (29,906) | 744,323 |
| 비품 | 412,784 | (380,371) | - | 32,413 |
| 합 계 | 29,548,608 | (12,637,812) | (29,906) | 16,880,890 |
| 출처) 당사 정기보고서 |
| [2025년 1분기말 유형자산 담보제공 내역] |
| (단위: 천원) |
| 담보제공자산 | 장부금액 | 담보설정금액 | 담보감정가격 | 관련 계정과목 | 차입금액 | 담보권자 |
|---|---|---|---|---|---|---|
| 토지 | 3,660,774 | 8,796,000 | 11,028,000 | 차입금 | 6,710,000 | 기업은행 |
| 건물 | 7,758,009 |
| 출처) 당사 정기보고서 |
| 주1) 담보제공자산인 토지 및 건물은 글로벌R&D센터줄기세포재생의학연구소(서울 금천구 소재)와 줄기세포GMP센터(경기도 광명시 소재)입니다. |
| 주2) 담보감정가격의 감정일은 2021년입니다. |
또한, 상기 회사채 및 주식 관련 사채 발행과 담보제공을 통한 추가 차입방안의 경우, 금융비용(이자비용) 부담과 함께 수익성 악화가 이루어질 수 있고 부채총계 증가에 따라 재무안정성에 악영향을 줄 수 있는 점 또한 선택되지 않은 사유로 고려되었습니다. 지속적인 영업손실 및 당기순손실에 기인한 당사의 열위한 재무안정성을 고려하였을 때, 유상증자를 통해 자본을 확충하는 경우 차입금 및 부채비율을 보다 안정적으로 관리하여 건실한 재무안정성을 기대할 수 있으며, 추가적인 금융비용 발생을 방지하여 재무적 부담을 완화시킬 수 있을 것이라 판단하였습니다.
이러한 일련의 자금조달 방안 검토 과정을 거쳐, 이사회는 기존 주주에게 신주인수권을 우선적으로 부여하고, 실권주 발생 시 일반 투자자에게도 참여 기회를 제공할 수 있는 주주배정 후 실권주 일반공모 방식의 유상증자를 추진하는 것이 주주 권익 보호와 자금조달 안정성 확보 측면에서 가장 적절하다는 판단에 이르게 되었으며, 이에 대표주관회사와 인수회사의 잔액인수를 조건으로 한 주주배정 후 실권주 일반공모 방식의 유상증자를 최종적으로 결의하였습니다.
2. 주주 권익 보호를 위한 회사 정책
당사는 금번 유상증자로 인해 주주들의 지분이 다소 희석될 수 있음을 충분히 인지하고 있으며, 이에 따라 유상증자 이후의 명확한 비전 제시 등을 통해 지속적으로 주주 소통을 강화할 예정입니다. 금번 유상증자 납입대금을 전략적으로 사용하여 회사의 경쟁력을 강화할 예정이며 이를 통해 기업 가치 상승을 유도하여 중장기적으로 주주 가치를 극대화하도록 노력할 예정입니다.
1) 주주와의 소통 강화 방안
당사는 주주 대상으로 적극적인 IR 활동을 통해 주주 신뢰를 제고하기 위해 노력할 계획입니다. 또한, 당사는 2025년 06월 10일 증권신고서 공시 직후, 금번 주주배정 유상증자 결정과 관련된 주요 내용을 주주들에게 설명하기 위하여 당사 홈페이지 주주 서한을 게재하였습니다.
![이미지: [주주서한]](%EC%A3%BC%EC%A3%BC%EC%84%9C%ED%95%9C.jpg) |
|
[주주서한] |
가) IR자료 및 보도자료 배포를 통한 회사에 대한 이해도 증진
당사는 소액주주의 정보 접근성을 높이고 소통을 활성화하여 주주 권익을 보호하고자 합니다. 구체적으로 당사는 추후 당사 홈페이지에 IR 자료를 즉시 게재하여 주주들이 관련 내용을 신속하게 확인할 수 있도록 할 예정입니다. 더불어, 당사는 유상증자와 관련된 전반적인 내용을 다양한 이해관계자들이 확인할 수 있도록 보도자료를 배포할 예정입니다. 이를 통해 개인, 기관, 외국인 투자자 등 다양한 이해관계자들에게 언론을 통해 당사의 비전과 전략을 정확히 전달할 수 있도록 노력할 계획입니다.
나) 투자설명회(IR) 개최
당사는 공모 유상증자 기간 중 오프라인 투자설명회(IR)를 개최하여 질의응답 세션을 운영하여 당사의 경영전략에 대해 충분히 이해할 수 있도록 진행할 계획입니다. 특히, 당사는 금번 유상증자의 목적 및 회사의 향후 성장 전략 등에 대해 주주분들에게 상세히 설명드리고 의견을 경청하기 위해 증권신고서 공시 익일인 2025년 06월 11일에 첫 번째 투자설명회(IR)를 개최하였습니다. 간담회의 구체적인 시간 및 장소, 참여 방법 등은 2025년 6월 10일 증권신고서 공시 직후 당사 홈페이지 및 공시를 통해 안내하였습니다.
또한, 추가적으로 주주분들의 수요를 조사하여 수도권 외에 지방거점에서도 투자설명회를 개최할 계획이 있습니다. 이를 통해 당사의 파이프라인 임상 현황, 기술이전 현황, 향후 비전 등을 상세히 설명하고 질의응답 시간을 통해 주주분들의 궁금증을 해소하겠습니다.
다) IR응대 전용 라인 강화를 통한 소통 강화
당사는 보다 적극적인 투자자 의사 소통 강화를 위해, 기존에 있는 IR응대 전용 라인을 강화할 계획입니다. IR 응대 전용 이메일 및 유선을 통해 유상증자와 관련한 문의에 신속하고 누락 없이 응대할 수 있도록 하겠습니다. 특히, 소액주주를 포함한 다양한 주주의 의견을 수렴할 수 있도록 당사와 사전 일정 조율 등을 신청한 소액주주에 대해서는 개별적인 대면 미팅 또는 유선 의견청취를 적극 활용하여 실시간 소통을 강화하겠습니다.
2) 주요 기관투자자 대상 IR 진행
주요 기관투자자 대상으로 IR을 진행하여 유상증자의 배경, 목적, 기대 효과와 당사의 중장기 사업전략 등에 대해 상세히 설명을 진행할 예정이며, 증권사 애널리스트 대상으로도 적극적으로 소통하여, 시장 내에 충분한 정보가 전달될 수 있도록 노력할 계획입니다.
당사는 상기와 같이 주주 및 시장과의 적극적인 소통을 통해 회사의 경영 전략 및 본 유상증자의 배경과 필요성을 명확히 전달하는 한편, 본 유상증자와 관련 후속 정보를 지속적으로 제공해 나가겠습니다.
(증자비율, 할인율 등) 본 공모 유상증자의 증자비율은 67.79%이며, 할인율은 25%입니다. 최근 4개년 공모 유상증자 증자비율 및 할인율 추이를 살펴보면 본 공모처럼 주주배정 후 실권주 일반공모의 경우, 2021년 증자비율 42%, 할인율 22%, 2022년 증자비율 36%, 할인율 22%, 2023년 증자비율 41%, 할인율 23%, 2024년 증자비율 47%, 할인율 24% 입니다. 이를 고려했을 때, 본 공모 유상증자의 할인율은 적정수준이라 판단되지만, 증자비율은 다소 높은 편으로, 주식가치 희석에 미흡한 부분이 존재합니다. 다만, 당사는 최근 임상 1상을 성공적으로 마친 OSCA의 추가 임상에 대규모 자금을 투입을 통해 차세대 파이프라인 구축이 필요한 시점입니다. 또한 본격적인 국내외 재생의료 사업 진출을 위한 추가 자금 투입과 자본 확충을 통한 재무구조의 건전성 확보가 필요한 상황임으로 67.79% 증자비율의 발행조건을 결정하게 되었습니다. 당사는 이러한 사항을 충분히 인지하며 주주권익 보호를 위해 소통을 강화하고, 지속가능한 성장을 통해 주주가치를 증대해 나가겠습니다.
| [최근 4개년 공모 유상증자 증자비율 및 할인율] |
| 구분 | 2021년 | 2022년 | 2023년 | 2024년 | ||||
|---|---|---|---|---|---|---|---|---|
| 증자비율 | 할인율 | 증자비율 | 할인율 | 증자비율 | 할인율 | 증자비율 | 할인율 | |
| 일반공모 | 107.89% | 12.22% | 39.26% | 30.00% | 18.98% | 15.00% | 59.34% | 26.25% |
| 주주배정 | 1.79% | 45.00% | 33.30% | 16.67% | 127.09% | 20.83% | 45.32% | 17.50% |
| 주주우선공모 | 118.27% | 27.50% | 69.26% | 28.50% | 76.95% | 28.75% | 92.26% | 27.50% |
| 주주배정 후 실권주 일반공모 | 42.11% | 21.99% | 36.17% | 22.08% | 40.85% | 23.09% | 47.13% | 23.94% |
| 평균 | 52.43% | 60.85% | 38.69% | 37.93% | 51.50% | 22.97% | 50.96% | 24.12% |
| 자료 : Dart 전자공시시스템 |
| 주) 최초 증권신고서 제출일 기준으로 해당 사업연도 산정 |
(신사업투자 등) 당사의 금번 주주배정 후 실권주 일반공모 유상증자의 자금의 사용목적은 연구개발비, 인건비 등 운영자금으로 신사업투자에는 해당사항이 없습니다. 당사는 기술성장기업으로서 코스닥시장에 상장하였으며 매출 확대를 위하여 추가적인 운영자금(연구개발비용, 기타운전자금)이 필요한 것으로 판단되어 금번 주주배정 후 실권주 일반공모 유상증자를 통해 추가적인 자금을 확보할 계획이고 이를 통해 재무안정성 제고 및 영업활동을 지속하고자 합니다. 세부 자금사용 계획에 대해서는 '제1부 모집 또는 매출에 관한 사항 - Ⅴ. 자금의 사용목적'을 참고하여 주시기 바랍니다.
(경영권 분쟁발생) 증권신고서 제출일 현재 최대주주인 주식회사 세종은 14.27%의 지분율을 확보하고 있습니다. 금번 주주배정 후 실권주 일반공모에 당사의 최대주주인 주식회사 세종은 배정분의 100% 참여를 계획 중입니다. 초과 청약 및 추가 신주인수권증서 매매 여부는 검토 중이나, 현재 미정입니다. 또한, 당사 발행주식총수의 5% 이상 지분율을 보유한 주주는 최대주주 이외에 존재하지 않고, 소액주주들에게 지분율이 분산되어 있어 최대주주의 변경 및 경영권 분쟁발생 가능성은 제한적일 것으로 판단하고 있습니다. 최대주주 지분율 약화에 따른 경영권 변동 및 분쟁 관련 위험은 '제1부 모집 또는 매출에 관한 사항 - III. 투자위험요소 - 3. 기타위험 - 나. 최대주주 지분희석 및 경영권 관련 위험'을 참고하여 주시기 바랍니다
(한계기업 등) 당사는 매출이 부진한 가운데, 지속적으로 임상시험 등 연구개발비용이 발생하고 있습니다. 이에 따라 2022년 영업손실 205.6억원, 2023년 영업손실 227.8억원, 2024년 영업손실 148.4억원, 2025년 1분기 영업손실 47.5억원이 발생하였습니다. 또한 영업 외적 측면에서도, 금융비용 등의 발생 영향으로 인해 2022년 당기순손실 201.8억원, 2023년 당기순손실 232.2억원, 2024년 당기순손실 70.8억원, 2025년 1분기 당기순손실 49.0억원이 발생하는 등 지속적인 적자 구조를 면하지 못하고 있습니다. 바이오 업종의 특성 상 당사의 파이프라인에서 임상 성공을 통한 기술이전, 제품화 등의 성과를 이루어내지 못한다면 당사의 적자 구조를 개선하는 것은 불가능할 수 있으며, 자본력이 지속적으로 감소하여 지속적인 연구개발비용 등의 지출이 필요한 당사의 영업활동을 영위하는데 상당한 제약이 생길 수 있습니다.
이에 당사는 주요 파이프라인 개발과 더불어 다른 연관 사업 수익화를 통해 자체 재원 역량을 강화하고자 노력하고 있습니다. 구체적으로는 1) 오가노이드 사업으로 피부 오가노이드를 활용한 3D 약물평가 구축을 통해 글로벌 픽파마와의 협업 및 기술이전 등을 통한 수익화 노력 계획이며, 2) 일본 재생의료 사업으로 일본 후생노동성 최종 승인이 완료된 2종(자가지방줄기세포)의 일본 내 공급 통한 수익화를 준비 중이며, 3) 국내 첨생법 사업으로 국내 첨생법 개정에 따라 당사의 아토피 피부염 치료제(퓨어스템-에이디 주)와 골관절염 치료제(OSCA)를 조기에 사용할 수 있도록 협력 의료기관을 통한 해당 파이프라인의 임상 연구 지원, IP 생산 등을 위해 노력할 계획입니다. 다만 그럼에도 불구하고 지속적인 영업손실과 당기순손실 발생 및 부의 영업현금흐름 발생, 그리고 이에 따른 결손금 누적과 재무상태 악화가 발생한다면 당사의 계속기업으로서의 존속능력에 유의적인 불확실성이 존재할 수 있는 상황입니다. 한편, 2024년말 감사보고서상 외부감사인의 감사 결과 계속기업 관련 중요한 불확실성은 없는 상황입니다. 당사의 재무 관련 위험은 '제1부 모집 또는 매출에 관한 사항 중 III. 투자위험요소 - 2. 회사위험'을 전반적으로 참고하여 주시기 바랍니다.
(IPO 실적 과다 추정 등) 당사는 2010년 10월 29일 줄기세포치료제의 개발, 제조 및 공급 등의 사업 영위를 목적으로 설립되었으며 2015년 12월 21일 코스닥 시장에 주식을 상장하여 매매를 개시하였습니다. 당사는 상장 당시에 가정한 임상시험 및 기술이전 일정이 지연되어, 사업계획 및 추정 손익과 실제 경영성과 간 괴리를 보였으며, 괴리율은 아래와 같습니다.
| [상장 당시 추정손익과 실제 손익 비교] |
| (단위: 백만원) |
| 추정대상 | 계정과목 | 예측치 | 실적 | 예측달성여부 | 괴리율(%) |
| 2016년 | 매출액 | 5,483 | 843 | 미달성 | -84.63 |
| 영업이익 | -2,688 | - 9,118 | 미달성 | 239.21 | |
| 2017년 | 매출액 | 9,471 | 9,133 | 미달성 | -3.57 |
| 영업이익 | 992 | -11,738 | 미달성 | -1,283.27 | |
| 2018년 | 매출액 | 17,870 | 9,165 | 미달성 | -48.71 |
| 영업이익 | 5,935 | -11,694 | 미달성 | -297.03 | |
| 2019년 | 매출액 | 28,696 | 6,005 | 미달성 | -79.07 |
| 영업이익 | 13,619 | -23,154 | 미달성 | -270.01 |
| 출처) 당사 정기보고서 및 당사 증권신고서 및 당사 제공 |
| 주1) 괴리율 = (실적치 - 예측치) / 예측치 * 100 |
상기 기재한 바와 같이 당사는 유상증자 중점심사대상 선정 항목에 일부 해당 가능성이 있는 사항들이 있습니다. 증권신고서 제출일 기준 당사는 중점심사 대상에 지정되었는지 그 여부를 알 수 없으나, 중점심사 대상 선정을 가정한 주요 심사항목에 대한 내용은 최대한 본 증권신고서에 기재하였습니다. 당사가 중점심사 대상 기준에 해당하는 경우, 중점 심사항목 위주로 1주일 이내 집중심사를 진행하고 최소 1회 이상의 대면협의를 진행하게 되며, 본 증권신고서는 공시 심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우에는 본 신고서상의 일정이 예상보다 지연될 가능성이 있습니다. 투자자 여러분께서는 이 점 유의하시기 바랍니다.
| 나. 최대주주 지분희석 및 경영권 관련 위험 증권신고서 제출일 현재 최대주주인 주식회사 세종은 당사 주식을 8,000,000주 보유하고 있으며, 지분율은 14.27%로 낮은 수준을 유지하고 있습니다. 금번 유상증자로 인해 발행될 신주의 수는 38,000,000주이며, 당사의 구주주는 유상증자 참여시 1주당 0.6779159202주의 비율로 신주를 배정받게 됩니다. 이에 따라 최대주주인 주식회사 세종은 5,423,327를 배정받게 됩니다. 금번 유상증자에서 최대주주는 자금 여력에 따라 최대한 참여할 예정으로, 현재 최대주주인 주식회사 세종은 배정분의 100% 참여를 계획 중입니다. 초과 청약 및 추가 신주인수권증서 매매 여부는 검토 중이나, 현재 미정입니다. 최대주주가 배정분 100%만 청약 참여할 경우 유상증자 후 지분율은 약 14.27%이 됩니다. 당사 발행주식총수의 5% 이상 지분율을 보유한 주주는 최대주주 이외에 존재하지 않고, 소액주주들에게 지분율이 분산되어 있어 최대주주의 변경 및 경영권 분쟁발생 가능성은 제한적일 것으로 판단하고 있습니다. 다만, 당사는 상장 이후 증권신고서 제출 전일까지 경영권 분쟁 사례가 존재하지 않지만 금번 증자로 인해 최대주주의 지분율은 감소할 수 있으며, 향후 적대적 기업인수 등으로 인한 경영권 분쟁이 대두될 가능성도 있습니다. 이러한 경영 안정성 악화, 경영권 분쟁 등은 주가의 급등락에 영향에 미칠 수 있으며, 이에 따른 투자자 손실을 야기할 가능성이 존재하오니 투자자께서는 이 점 유의하시기 바랍니다. |
증권신고서 제출일 전일 기준 최대주주인 주식회사 세종은 당사 주식을 8,000,000주 보유하고 있으며, 지분율은 14.27%로 낮은 수준을 유지하고 있습니다. 최대주주 및 특수관계인의 보유지분 현황 및 최대주주의 지분 변동 내역은 다음과 같습니다.
| [최대주주 및 특수관계인 현황] |
| (2025년 1분기 기준) |
| 성명 (회사명) |
관계 | 주식의 종류 |
소유주식수 | 소유 비율 | 비고 |
|---|---|---|---|---|---|
| (주)세종 | 최대주주 | 보통주 | 8,000,000 | 14.27 | - |
| 계 | - | 8,000,000 | 14.27 | - | |
| 출처) 당사 분기보고서 제시 |
| [최대주주의 당사 지분 변동 내역] |
| (단위: 주, 원) |
| 구분 | 거래일자 | 거래방식 | 거래주식수 | 보유주식수 | 거래단가 | 지분율 | 비고 |
|---|---|---|---|---|---|---|---|
| 취득 | 2023-10-11 | 장내매수 | 305,421 | 305,421 | 1,652 | 0.81% | 5% 미만, 수회 취득 |
| 2023-10-24 | 장내매수 | 260,000 | 565,421 | 1,526 | 1.49% | ||
| 2023-10-25 | 장내매수 | 160,000 | 725,421 | 1,576 | 1.91% | ||
| 2023-10-27 | 장내매수 | 66,000 | 791,421 | 1,319 | 2.09% | ||
| 2023-10-30 | 유상신주 취득 | 5,633,494 | 6,424,915 | 1,165 | 11.49% | 유상신주 청약 및 초과청약 |
|
| 2023-10-31 | 장내매수 | 110,000 | 6,534,915 | 1,345 | 11.68% | ||
| 2023-11-01 | 장내매수 | 40,331 | 6,575,246 | 1,367 | 11.75% | ||
| 2023-11-02 | 장내매수 | 93,737 | 6,668,983 | 1,455 | 11.92% | ||
| 2023-11-03 | 장내매수 | 16,094 | 6,685,077 | 1,496 | 11.95% | ||
| 2023-11-06 | 장내매수 | 86,923 | 6,772,000 | 1,567 | 12.11% | ||
| 2023-11-07 | 장내매수 | 28,000 | 6,800,000 | 1,658 | 12.16% | ||
| 2023-11-16 | 장내매수 | 640,000 | 7,440,000 | 1,238 | 13.30% | ||
| 2023-11-17 | 장내매수 | 160,000 | 7,600,000 | 1,324 | 13.59% | ||
| 2023-11-27 | 장내매수 | 20,000 | 7,620,000 | 1,332 | 13.62% | ||
| 2023-12-12 | 장내매수 | 80,000 | 7,700,000 | 1,808 | 13.77% | ||
| 2023-12-13 | 장내매수 | 110,000 | 7,810,000 | 1,827 | 13.96% | ||
| 2023-12-14 | 장내매수 | 54,704 | 7,864,704 | 1,982 | 14.06% | ||
| 2023-12-15 | 장내매수 | 65,296 | 7,930,000 | 2,114 | 14.18% | ||
| 2023-12-18 | 장내매수 | 40,000 | 7,970,000 | 2,193 | 14.25% | ||
| 2023-12-19 | 장내매수 | 30,000 | 8,000,000 | 2,279 | 14.27% |
| 출처) 당사 제시, 세종 제출 지분공시 |
| [최대주주의 유상신주 청약 상세 내역] |
| (단위: 주, 원) |
| 거래일자 | 거래방식 | 주식종류 | 거래주식수 | 보유주식수 | 거래단가 | 비고 |
|---|---|---|---|---|---|---|
| 2023-10-12 | 장내매수 | 신주인수권이표시된것 | 1,500,000 | 1,500,000 | 86 | |
| 2023-10-13 | 장내매수 | 신주인수권이표시된것 | 850,000 | 2,350,000 | 124 | |
| 2023-10-16 | 장내매수 | 신주인수권이표시된것 | 674,602 | 3,024,602 | 130 | |
| 2023-10-17 | 장내매수 | 신주인수권이표시된것 | 619,088 | 3,643,690 | 151 | |
| 2023-10-18 | 장내매수 | 신주인수권이표시된것 | 1,050,889 | 4,694,579 | 207 | |
| 2023-10-30 | 기타(-) | 신주인수권이표시된것 | -4,694,579 | 0 | - | 유상신주 청약 |
| 2023-10-30 | 구주주청약 | 의결권이있는 주식 | 4,694,579 | |||
| 2023-10-30 | 초과청약 | 의결권이있는 주식 | 938,915 |
| 출처) 당사 제시, 세종 제출 지분공시 |
금번 유상증자로 인해 발행될 신주의 수는 38,000,000주이며 이는 기존 발행주식 대비 67.79% 수준으로, 당사의 주주는 유상증자 참여시 1주당 0.6779159202주의 비율로 신주를 배정받게 됩니다. (신주배정기준일 전 주식매수선택권의 행사, 자기주식 수의 변동 등에 의하여 변동 가능성이 있습니다.) 이에 따라 최대주주인 주식회사 세종은 5,423,327주를 배정받게 됩니다. 금번 유상증자에서 최대주주는 자금 여력에 따라 최대한 참여할 예정으로, 현재 최대주주인 주식회사 세종은 배정분의 100% 참여를 계획 중입니다. 초과 청약 및 추가 신주인수권증서 매매 여부는 검토 중이나, 현재 미정입니다. 최대주주가 배정분 100%만 청약 참여할 경우 유상증자 후 지분율은 약 14.27%이 됩니다.
| [최대주주 청약률에 따른 지분변동 가정] |
| 성명 | 증자 전 | 증자 후 | |||||
|---|---|---|---|---|---|---|---|
| (최대주주 100% 참여) | (최대주주 미참여) | ||||||
| 주식수(주) | 지분율(%) | 배정주식수(주) | 주식수(주) | 지분율(%) | 주식수(주) | 지분율(%) | |
| (주)세종 | 8,000,000 | 14.27 | 5,423,327 | 13,423,327 | 14.27 | 8,000,000 | 8.51 |
| 출처: 당사 제공 |
| 주1) 증자 전 발행주식 총수 : 56,054,149주 → 증자 후 발행주식 총수 : 94,054,149주 |
현재 최대주주 세종의 당사 지분 보유 목적은 '일반투자'입니다. 세종은 금번
유상증자 참여를 통해 지분 보유 목적을 '경영참여'로 변경하는 것을 검토 중에 있으며, 경영참여를 확정하는 경우 즉시 공시를 통해 의사를 밝힐 예정입니다. 다만, 증권신고서 제출일 전일 기준 확정된 사항은 없으며, 변경하지 않을 가능성도 존재하니 투자자께서는 이 점 유의하시기 바랍니다. 또한, 세종은 당사에 대한 경영참여를 결정한 후에도 현 경영진을 최대한 유지하여 당사의 신약개발 등 사업의 일관성 및 지속성을 유지하기 위해 노력할 예정입니다.
한편, 최대주주 및 특수관계인을 제외한 주요 주주 현황 및 전 최대주주인 강경선의 지분 변동 내역은 다음과 같습니다.
| [최대주주 제외 주요주주 현황] |
| (2025.03.31 기준) |
| 성명 (회사명) |
관계 | 주식의 종류 |
소유주식수 | 소유 비율 | 비고 |
|---|---|---|---|---|---|
| 강경선 | 주요주주 | 보통주 | 2,628,526 | 4.69 | - |
| 김신현 | 주주 | 보통주 | 79,000 | 0.14 | - |
| 강영민 | 주주 | 보통주 | 22,700 | 0.04 | - |
| 강영준 | 주주 | 보통주 | 11,400 | 0.02 | - |
| 강영은 | 주주 | 보통주 | 11,300 | 0.02 | - |
| 나종천 | 등기임원 | 보통주 | 111,729 | 0.2 | |
| 김원균 | 등기임원 | 보통주 | 6,272 | 0.01 | - |
| 이승희 | 등기임원 | 보통주 | 19,337 | 0.03 | |
| 최정호 | 등기임원 | 보통주 | 195,283 | 0.35 | |
| 이동열 | 미등기임원 | 보통주 | 86,000 | 0.15 | |
| 이미혜 | 미등기임원 | 보통주 | 35,000 | 0.06 | |
| 이상균 | 주주 | 보통주 | 67,167 | 0.12 |
| 출처) 당사 제공 |
| [주요주주 강경선(전 최대주주)의 당사 지분 변동 내역] |
| (단위: 주, 원) |
| 구분 | 거래일자 | 거래방식 | 거래주식수 | 보유주식수 | 거래단가 | 지분율 | 비고 |
|---|---|---|---|---|---|---|---|
| 변동 | 2015-12-21 | 신규상장 | 2,520,000 | 2,520,000 | 6,000 | 18.24% | |
| 2018-07-28 | 유상신주 취득 | 131,445 | 2,651,445 | 8,560 | 12.75% | 유상신주 청약 및 초과청약 | |
| 2019-10-25 | 장내매도 | -600 | 2,650,845 | 9,650 | 12.71% | ||
| 2019-10-28 | 장내매도 | -620,845 | 2,030,000 | 8,204 | 9.73% | ||
| 2020-02-27 | 장내매도 | -27,000 | 2,003,000 | 6,476 | 9.67% | ||
| 2020-02-28 | 장내매도 | -25,000 | 1,978,000 | 7,061 | 9.42% | ||
| 2020-03-02 | 장내매도 | -20,000 | 1,958,000 | 6,726 | 9.33% | ||
| 2020-03-03 | 장내매도 | -28,000 | 1,930,000 | 6,687 | 9.19% | ||
| 2021-10-22 | 유상신주 취득 | 371,515 | 2,301,515 | 3,150 | 6.06% | 유상신주 청약 및 초과청약 | |
| 2023-11-08 | 유상신주 취득 | 327,011 | 2,628,526 | 1,165 | 4.69% | 유상신주 청약 |
| 출처) 당사 제시, 강경선 제출 지분공시 |
최대주주 제외 주요주주의 경우, 자금여력 부족 등을 이유로 청약에 전량 참여할 가능성은 낮은 상황입니다. 다만, 전 최대주주인 강경선의 경우 배정분의 약 30% 내외로 참여를 계획중이며 자금여력에 따라 참여율은 변동될 수 있습니다.
| [최대주주 제외 주요주주 예상 지분 변동] |
| 성명 | 증자 전 | 증자 후 | |||
|---|---|---|---|---|---|
| 주식수(주) | 지분율(%) | 배정주식수(주) | 주식수(주) | 지분율(%) | |
| 강경선 | 2,628,526 | 4.69 | 1,781,919 | 3,163,101 | 3.36% |
| 김신현 | 79,000 | 0.14 | 53,555 | 79,000 | 0.08% |
| 강영민 | 22,700 | 0.04 | 15,388 | 22,700 | 0.02% |
| 강영준 | 11,400 | 0.02 | 7,728 | 11,400 | 0.01% |
| 강영은 | 11,300 | 0.02 | 7,660 | 11,300 | 0.01% |
| 나종천 | 111,729 | 0.2 | 75,742 | 111,729 | 0.12% |
| 김원균 | 6,272 | 0.01 | 4,251 | 6,272 | 0.01% |
| 이승희 | 19,337 | 0.03 | 13,108 | 19,337 | 0.02% |
| 최정호 | 195,283 | 0.35 | 132,385 | 195,283 | 0.21% |
| 이동열 | 86,000 | 0.15 | 58,300 | 86,000 | 0.09% |
| 이미혜 | 35,000 | 0.06 | 23,727 | 35,000 | 0.04% |
| 이상균 | 67,167 | 0.12 | 45,533 | 67,167 | 0.07% |
| 출처: 당사 제공 |
| 주1) 증자 전 발행주식 총수 : 56,054,149주 → 증자 후 발행주식 총수 : 94,054,149주 |
| 주2) 주요주주 중 강경선의 경우 배정분의 약 30% 내외로 참여를 가정하였으며, 나머지 주요 주주의 경우 청약하지 않는 것을 가정한 지분율입니다. |
한편, 당사는 증권신고서 제출 전일 기준, 추가 주식 발행에 따른 기존 주주의 지분 희석을 야기할 수 있는 미행사 주식매수선택권이 존재합니다. 당사가 임직원에게 부여한 주식매수선택권 중 미행사수량은 총 634,000주이며, 모두 신고서 제출 전일 기준 행사 가능합니다. 해당 주식매수선택권은 행사 시 보호예수 없이 곧바로 출회가 가능하므로, 이에 따른 주가 하락 위험이 존재하오니 투자자께서는 이 점 유의하시기 바랍니다. 또한 행사될 경우 기존 주주의 지분 희석을 야기할 수 있으며, 금번 유상증자의 신주배정기준일 전에 주식매수선택권의 일부가 행사될 경우 구주주 배정비율이 변동될 수 있습니다. 당사의 미행사 주식매수선택권 현황은 아래와 같습니다.
| [행사 가능한 주식매수선택권 부여현황] | |
| (기준일 : 2025.03.31) | (단위 : 원, 주) |
| 부여 받은자 |
관 계 | 부여일 | 부여방법 | 주식의 종류 |
기말 미행사수량 |
행사기간 | 행사 가격 |
의무 보유 여부 |
의무 보유 기간 |
|---|---|---|---|---|---|---|---|---|---|
| 나종천 | 등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 100,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 배요한 | 미등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 70,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 김원균 | 등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 60,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 노경환 | 계열회사 임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 70,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 이계종 | 미등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 50,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 이승희 | 미등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 50,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 유연실 | 미등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 25,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| OOO 외 14명 | 직원 | 2021년 03월 25일 | 신주교부 | 보통주 | 149,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 서명관 | - | 2021년 03월 25일 | 신주교부 | 보통주 | 60,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 합계 | 634,000 | ||||||||
유상증자 후 주식매수선택권 미행사수량인 634,000주가 전량 행사될 경우, 최대주주 및 특별관계자의 지분율은 최대 14.18%까지 감소할 수 있습니다.
| [최대주주 지분율 시뮬레이션] |
| 성명 | 증자 후 (최대주주 100% 참여) |
주식매수선택권 전량 행사 | |||
|---|---|---|---|---|---|
| 주식수(주) | 지분율(%) | 배정주식수(주) | 주식수(주) | 지분율(%) | |
| (주)세종 | 8,000,000 | 14.27 | 5,423,327 | 13,423,327 | 14.18% |
| 출처: 당사 제공 |
| 주1) 증자 전 발행주식 총수 : 56,054,149주 → 증자 후 발행주식 총수 : 94,054,149주 → 주식매수선택권 전량 행사 후 발행주식 총수 94,688,149주 |
상기한 바와 같이 증권신고서 제출일 현재 최대주주인 주식회사 세종은 14.27%의 지분율을 확보하고 있으며, 금번 주주배정 후 실권주 일반공모에 배정분의 100% 참여를 계획 중입니다. 초과 청약 및 추가 신주인수권증서 매매 여부는 검토 중이나, 현재 미정입니다. 또한, 당사 발행주식총수의 5% 이상 지분율을 보유한 주주는 최대주주 이외에 존재하지 않고, 소액주주들에게 지분율이 분산되어 있어 최대주주의 변경 및 경영권 분쟁발생 가능성은 제한적일 것으로 판단하고 있습니다. 다만, 당사는 상장 이후 증권신고서 제출 전일까지 경영권 분쟁 사례가 존재하지 않지만 금번 증자로 인해 최대주주의 지분율은 감소할 수 있으며, 향후 적대적 기업인수 등으로 인한 경영권 분쟁이 대두될 가능성도 있습니다. 이러한 경영 안정성 악화, 경영권 분쟁 등은 주가의 급등락에 영향에 미칠 수 있으며, 이에 따른 투자자 손실을 야기할 가능성이 존재하오니 투자자께서는 이 점 유의하시기 바랍니다.
| 다. 주가희석화 및 인수인의 실권주 인수분 물량 출회에 따른 주가하락 위험 신주 상장예정일은 유관기관과의 협의에 따라 변경될 수 있으며, 금번 유상증자에 따른 38,000,000주의 유상신주가 코스닥시장에 추가 상장됩니다. 또한, 구주주 청약주식 및 실권주 일반공모 청약시 기관 및 일반 투자자들의 청약으로 추가 발행되는 주식은 보호예수되지 않으므로 일시적인 물량출회에 따른 주가하락의 가능성이 있습니다. 또한, 공동대표주관회사 및 인수회사가 잔액인수한 물량은 수익을 확정하기 위해 신주상장일 2영업일 전부터 장내에서 대량 매도할 수 있습니다. 이 경우 일시적 물량 출회에 따른 주가 하락의 가능성이 존재하며, 인수한 실권주를 일정 기간 보유하더라도 동 인수물량이 잠재매각물량으로 존재하여 주가 상승에는 부담으로 작용할 가능성이 높습니다. 공동대표주관회사 및 인수회사가 최종 실권주를 인수하게 되면 실권주 인수금액의 15%를 추가수수료로 지급하게 되며, 이를 고려 시 공동대표주관회사 및 인수회사의 실권주 매입단가는 일반청약자들보다 15% 낮은 것과 같은 결과가 초래되어 공동대표주관회사 및 인수회사의 실권주 매도단가가 신주의 발행가액보다 낮게 될 가능성이 존재합니다. 투자자께서는 이 점을 반드시 유의하여 주시기 바랍니다. |
| [당사 잠재주식수 비율] |
| 구분 | 주식수 |
|---|---|
| 총발행주식수 (A) | 56,054,149주 |
| 주식매수선택권 (B) | 634,000주 |
| 총발행주식수 대비 잠재주식수 (B) / (A) | 1.13% |
| 금번 유상증자 발행예정 주식 수 (C) | 38,000,000주 |
| 총발행주식수 및 발행예정 주식 수 대비 잠재주식수 (B) / (A+C) | 0.7% |
| 출처) 당사 제시 |
금번 유상증자에 따른 모집가액은 「증권의 발행 및 공시 등에 관한 규정」 제5-18조에 의거 주주배정 증자 시 가격 산정절차 폐지 및 가격 산정의 자율화에 따라 발행가액을 자유롭게 산정할 수 있으나, (구)「유가증권의 발행 및 공시 등에 관한 규정」 제57조를 적용하여 산정합니다(Ⅰ. 모집 또는 매출에 관한 일반사항, 3. 공모가격 결정방법 참조). 그러나 주식시장의 특성상 향후 주가에 대한 변동성이 있는 관계로 증자에 따른 모집가격 산정시 결정된 1주당 모집가액보다 향후 추가 상장 후 거래 시점의 주가가 낮아져 투자자에게 금전적 손실을 끼칠 가능성이 있습니다.
신주 상장예정일은 유관기관과의 협의에 따라 변경될 수 있으며, 금번 유상증자에 따른 38,000,000주의 유상신주가 코스닥시장에 추가 상장됩니다.
한편, 구주주 청약주식 및 실권주 일반공모 청약시 기관 및 일반 투자자들의 청약으로 추가 발행되는 주식은 보호예수되지 않으므로 일시적인 물량출회에 따른 주가하락의 가능성이 있습니다.
또한, 공동대표주관회사 및 인수회사가 잔액인수한 물량은 수익을 확정하기 위해 신주상장일 2영업일 전부터 장내에서 대량 매도할 수 있습니다. 이 경우 일시적 물량 출회에 따른 주가 하락의 가능성이 존재하며, 인수한 실권주를 일정 기간 보유하더라도 동 인수물량이 잠재매각물량으로 존재하여 주가 상승에는 부담으로 작용할 가능성이 높습니다. 공동대표주관회사 및 인수회사가 최종 실권주를 인수하게 되면 실권주 인수금액의 15%를 추가수수료로 지급하게 되며, 이를 고려 시 공동대표주관회사 및 인수회사의 실권주 매입단가는 일반청약자들보다 15% 낮은 것과 같은 결과가 초래되어 공동대표주관회사 및 인수회사의 실권주 매도단가가 신주의 발행가액보다 낮게 될 가능성이 존재합니다. 투자자께서는 이 점을 반드시 유의하여 주시기 바랍니다.
| 라. 청약 후 추가상장일까지 환금성 제약 및 주가의 급격한 변동에 따른 손실위험 당사의 금번 유상증자로 인한 발행신주는 주금 납입일 이후 코스닥시장에 추가 상장일까지 유동성이 제한될 수 있으며, 추가상장 시점에서 신주발행가액보다 시장의 수준이 낮은 경우 환금성 위험 및 원금 손실의 위험이 있습니다. 본 유상증자 기간동안 주가의 변동이 있을 수 있다는 점, 투자자께서는 유의하여 주시기 바랍니다. |
당사는 코스닥시장 상장법인으로써, 이번 유상증자로 발행되는 신주는 코스닥시장에 상장되어 거래될 예정이므로 유동성과 관계된 심각한 환금성 위험은 존재하지 않습니다. 그러나 유상증자 청약에 참여하여 신주를 배정받을 경우, 신주가 상장되어 매매가 가능할 때까지 납입주금에 대한 유동성의 제약이 있습니다.
그리고 금번 유상증자로 인해 발행되는 신주가 코스닥시장에 추가 상장될 때까지 유상증자로 발행되는 신주의 발행가액 수준의 주가가 유지되지 않을 수 있으며, 당사의 내적인 환경변화 또는 시장전체의 환경 변화 등에 의한 급격한 주가 하락이 발생할 경우, 투자원금에 대한 손실이 발생할수 있습니다. 투자자께서는 유의하여 주시기 바랍니다.
| 마. 경영환경변화 등에 따른 위험 대내외적 경영환경 변화에 따라 당사 실적의 급변동이 있을 경우 투자원금에 대한 손실이 발생할 수 있으므로, 상기 투자위험요소 및 본 증권신고서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 투자자 여러분이 독자적으로 결정해야 함을 유의하시기 바랍니다. |
당사의 주가는 국내외 주식시장 환경 변화와 같은 외부적 요인에 영향을 받아 변동할 가능성이 존재하며, 당사의 외부적인 경영환경 변화에 따라 당사 실적이 악화될 가능성이 높아질 경우 당사의 주가에 부정적인 영향을 미칠 수 있습니다.
본 건 공모 주식을 청약하고자 하는 투자자들은 투자결정을 하기 전에 본 증권신고서의 다른 기재 부분 뿐만 아니라 상기 투자위험요소를 주의 깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 하며, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 상기 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자는 상기 투자위험요소 및 본 신고서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 자신의 독자적인 판단에 의해서 투자하셔야 합니다.
만일 상기 투자위험요소에 기재한 내용 중 부정적인 요소가 현실화될 경우 당사 및 관계회사의 사업, 재무상태, 기타 운영결과에 중대한 부정적 영향을 미칠 수 있으며, 이에 따라 투자자가 금번 공모 과정에서 취득하게 되는 당사 주식의 시장가격이 하락하여 투자금액에 손실이 발생할 수도 있음을 유의하시기 바랍니다.
| 바. 유상증자 일정 변경 가능성에 따른 위험 본 증권신고서는 공시심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. |
「자본시장과 금융투자업에 관한 법률」제120조3항에 의거하여 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 투자자에게 귀속됩니다.
| ※「자본시장과 금융투자업에관한 법률」제120조(신고의 효력발생시기 등) |
|---|
| ① 제119조제1항 및 제2항에 따른 증권의 신고(이하 "증권신고"라 한다)는 그 증권신고서가 금융위원회에 제출되어 수리된 날부터 증권의 종류 또는 거래의 특성 등을 고려하여 총리령으로 정하는 기간이 경과한 날에 그 효력이 발생한다. ② 금융위원회는 증권신고서의 형식을 제대로 갖추지 아니한 경우 또는 그 증권신고서 중 중요사항에 관하여 거짓의 기재 또는 표시가 있거나 중요사항이 기재 또는 표시되지 아니한 경우를 제외하고는 그 수리를 거부하여서는 아니 된다. ③ 제1항의 효력의 발생은 그 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나 정부에서 그 증권의 가치를 보증 또는 승인하는 효력을 가지지 아니한다. ④ 증권의 발행인은 증권신고를 철회하고자 하는 경우에는 그 증권신고서에 기재된 증권의 취득 또는 매수의 청약일 전일까지 철회신고서를 금융위원회에 제출하여야 한다 |
금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서(분기 및 반기보고서 포함) 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있사오니 투자의사를 결정하시는 데 참조하시기 바랍니다.
본 증권신고서는 공시심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행과정에서 일정이 변경될 수도 있으므로 투자자들께서는 투자 시 이러한 점을 감안하시기 바랍니다.
| 사. 유상증자 철회에 따른 위험 유상증자 진행 중에 모집 절차의 진행에 중대한 영향을 미칠만한 사유가 발생할 경우 당사 혹은 공동대표주관회사 및 인수회사의 판단으로 유상증자가 철회될 수 있습니다. 유상증자 납입전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회시점에 따라 권리락으로 인한 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있습니다. 또한, 당사의 자금사용 계획에 따른 자금 조달이 이루어지지 않기 때문에 당사는 단기간 유동성 위험에 직면할 수 있으며, 장기적으로는 당사의 성장을 위해 수립한 경영계획에 차질이 생길 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
금번 주주배정후 실권주 일반공모 유상증자는 공동대표주관회사 및 인수회사의 잔액인수 방식으로 진행됩니다. 유상증자 진행 중에 모집 절차의 진행에 중대한 영향을 미칠만한 사유가 발생할 경우 당사 혹은 공동대표주관회사 및 인수회사의 판단으로 유상증자가 철회될 수 있습니다.
유상증자 납입전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회시점에 따라 권리락으로 인한 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있습니다. 또한, 당사의 자금사용 계획에 따른 자금 조달이 이루어지지 않기 때문에 당사는 단기간 유동성 위험에 직면할 수 있으며, 장기적으로는 당사의 성장을 위해 수립한 경영계획에 차질이 생길 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| 아. 당사의 잘못된 정보 제공 등으로 손해 끼칠 가능성 당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있음을 유의하시기 바랍니다. |
「증권관련 집단소송법」 제12조(소송허가 요건)에 따라 50명 이상의 개인이 발행주식총수의 0.01% 이상 보유할 경우 한 명 이상의 대표 당사자가 상기 50인 이상의 당사자들을 대리하여 회사가 발행한 증권의 거래과정에서 발생한 피해에 대하여 소송을 제기할 수 있습니다.
| 「증권관련 집단소송법」제12조(소송허가 요건) |
|---|
| ① 증권관련 집단소송 사건은 다음 각 호의 요건을 갖추어야 한다. 1. 구성원이 50인 이상이고, 청구의 원인이 된 행위 당시를 기준으로 그 구성원이 보유하고 있는 증권의 합계가 피고 회사의 발행 증권 총수의 1만분의 1 이상일 것 2. 제3조제1항 각 호의 손해배상청구로서 법률상 또는 사실상의 중요한 쟁점이 모든 구성원에게 공통될 것 3. 증권관련집단소송이 총원의 권리 실현이나 이익 보호에 적합하고 효율적인 수단일 것 4. 제9조에 따른 소송허가신청서의 기재사항 및 첨부서류에 흠이 없을 것 ② 증권관련집단소송의 소가 제기된 후 제1항제1호의 요건을 충족하지 못하게 된 경우에도 제소(提訴)의 효력에는 영향이 없다. |
당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있습니다. 본 증권신고서 및 투자설명서에 서 기재된 잘못된 내용, 잘못된 사업보고서의 공시, 내부자거래에 의한 손해배상청구 및 회계부정으로 인한 손해배상 청구 등이 주요한 소송사유에 포함됩니다. 당사는 향후 이와 같은 집단소송의 대상이 되지 않는다고 확신할 수 없으며, 만약 당사에 대하여 집단소송이 제기될 경우 상당한 소송비용이 발생할 수 있습니다.
| 자. 유상증자에 따른 주식가치 하락 및 기재정보 의존에 따른 투자위험 금번 유상증자를 통해 취득한 당사의 주식가치가 하락할 수 있으며, 상기 투자위험요소 및 기타 기재된 정보에만 의존하여, 투자판단을 해서는 안되며 투자자 여러분의 독자적인 판단에 의해야 함을 유의하여 주시기 바랍니다. |
금번 유상증자 실시로 당사의 주식가치가 향후 하락할 수 있으므로 투자자 여러분께서는 이 점 유의하시기 바랍니다.
이 증권신고서의 효력발생은 정부가 증권신고서의 기재사항이 진실 또는 정확하다는것을 인정하거나 이 유가증권의 가치를 보증 또는 승인한 것이 아니며, 기재사항은 청약일 이전에 변경될 수 있으며, 본 건 공모주식을 청약하고자 하는 투자자들은 투자결정을 하기 전에 본 증권신고서의 다른 기재 부분 뿐만 아니라 상기 투자위험요소를 주의 깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 합니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 상기 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 자신의 독자적인 판단에 의해야 합니다.
당사는 상기에 기술된 투자위험요소 외에도 전반적으로 불안정한 경제상황 등에 의하여 직접적으로 또는 간접적으로 영향을 받을 수 있습니다. 당사의 재무제표는 당사의 재무상태에 영향을 미칠 수 있는 경제상황에 대한 경영자의 현재까지의 평가를 반영하고 있으나 그 실제결과는 현재시점에서의 평가와는 상당히 다를 수 있는 만큼, 투자자 여러분께서는 이 점 유의하여 투자에 임하시기 바랍니다.
만일 상기 투자위험요소가 실제로 발생하는 경우 당사의 사업, 재무상태, 기타 운영결과에 부정적 영향을 미칠 수 있으며, 이에 따라 투자자가 금번 공모 과정에서 취득하게 되는 당사 주식의 시장가격이 하락하여 투자금액의 일부 또는 전부를 잃게 될 수도 있습니다. 또한 금번 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 대내외적으로 여러가지 요소들의 영향에 따라 애초에 예측했던 것과 다를 수 있다는 점에 유의해야 합니다.
| 차. 관리감독기준 위반에 따른 위험 최근 상장 기업에 대한 금융감독기관 등의 관리감독기준이 엄격해지고 있는 상황으로 관련 규정을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다. 또한, 2025년 01월 21일, 정부와 유관기관(금융위원회, 금융감독원, 한국거래소, 금융투자협회)은 주식시장의 질적수준 제고를 위한「IPO 및 상장 폐지 제도개선 방안」을 발표하였습니다. 이 중 상장폐지 제도개선 방안은 상장유지 요건을 강화하고, 절차는 효율화함으로써 주식시장 내 저성과 기업을 적시에 퇴출시키고 상장기업의 밸류업을 주요 목적으로 하고 있습니다. 이와 같은 상장폐지 요건이 강화됨에 따라 당사의 영업환경 악화, 재무요건 악화 등을 원인으로 강화된 상장폐지 요건에 해당되어 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있음을 투자자분들은 유의하시기 바랍니다. |
최근 상장 기업에 대한 금융감독기관 등의 관리감독기준이 엄격해지고 있는 상황으로 관련 규정을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다.
특히, 「코스닥시장 상장규정」 제53조(관리종목), 「코스닥시장 상장규정」 제54조(형식적 상장폐지) 및 「코스닥시장 상장규정」 제56조(상장적격성 실질심사에 다른 상장폐지)"에 유의하시기 바랍니다.
자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융감독법규정보시스템(http://law.fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
| [코스닥시장 관리종목 지정요건 및 해당여부 검토] |
| 구 분 | 관리종목 지정(코스닥 상장규정 제53조) | 관리종목지정유예 | 관리종목 지정요건 적용여부 |
회사현황 | ||
|---|---|---|---|---|---|---|
| 해당여부 | 유예기간 | 사업연도 | 금액(백만원) / 비율(%) / 내용 | |||
| (1) 매출액 미달 | 최근 사업연도 30억원 미만 (지주회사는 연결기준) - 이익미실현기업 또는 기술성장기업은 상장후 5년간 미적용 - 기술성장기업 중 A), B), C) 중 어느 하나에 해당하는 제약·바이오기업은 최근 사업연도 미적용 A) 최근 사업연도 말「제약산업 육성 및 지원에 관한 특별법」에 따른 혁신제약기업이 세칙으로 정한 요건을 충족하는 경우 B) 최근 사업연도의 일평균 시가총액 4,000억 이상이며, 그 금액이 현재의 자본금을 초과하는 기업이 세칙으로 정하는 요건을 충족하는 경우 C) 최근 3사엽언도의 매출액 합계 90억 이상이며, 최근 사업연도의 직전 사업연도의 매출액이 30억 이상인 경우 |
- | - | 현재 미해당 | 2024년말 | 매출액 : 7,746백만원 (K-IFRS 별도기준) |
| 2025년 1분기말 | 매출액 : 954백만원 (K-IFRS 별도기준) |
|||||
| (2) 법인세비용차감전 계속사업손실 |
최근 3사업연도중 2사업연도에 각각 10억원 이상이면서 해당 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 있고 최근사업연도에 법인세비용차감전계속사업손실이 있는 경우 - 이익미실현 기업은 상장 후 5년간 미적용 (다만, 상장일부터 상장일이 속한 사업연도의 말일까지의 기간이 3개월 미만인 경우에는 상장일이 속하는 사업연도와 그 이후 5개 사업연도로 한다) - 기술성장기업은 상장후 3년간 미적용(다만, 상장일부터 상장일이 속한 사업연도의 말일까지의 기간이 3개월 미만인 경우에는 상장일이 속하는 사업연도와 그 이후 3개 사업연도로 한다) |
- | - | 2023년이 해당되며 2024년은 미해당, 2025년 해당될 경우 관리종목 지정 |
2023년말 | 세전손실 : (23,137)백만원 자기자본 : 44,517백만원 (자기자본 대비 52.0%) |
| 2024년말 | 세전손실 : (7,083)백만원 자기자본 : 43,182백만원 (자기자본 대비 16.4%) |
|||||
| 2025년 1분기말 | 세전손실 : (4,903)백만원 자기자본 : 38,279백만원 (자기자본 대비 12.8%) |
|||||
| (3) 자본잠식 등 | 최근 사업연도말 현재 자본잠식률이 100분의 50 이상인 경우 | - | - | 현재 미해당 | 2024년말 | 자본금 : 28,027백만원 지배주주지분 : 43,182백만원 자본잠식률 : 해당없음 |
| 2025년 1분기말 | 자본금 : 28,027백만원 지배주주지분 : 38,279백만원 자본잠식률 : 해당없음 |
|||||
| (4)자기자본 미달 | 최근 사업연도말 현재 자기자본이 10억원 미만인 경우 | - | - | 현재 미해당 | 2024년말 | 지배주주지분 : 43,182백만원 |
| 2025년 1분기말 | 지배주주지분 : 38,279백만원 | |||||
| (5) 시가총액 미달 | 보통주 시가총액 40억원미만 30일간 지속 - 천재지변, 시장상황의 급격한 변동 등으로 거래소가 시장 관리를 위하여 필요하다고 인정될 경우 적용배제 가능 |
- | - | 현재 미해당 | 2024년 12월 31일 |
시가총액 : 113,229백만원 |
| 증권신고서 제출일 전일 기준 |
시가총액 : 84,754백만원 |
|||||
| (6) 정기보고서 미제출 | 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않은 경우 | - | - | 현재 미해당 | 현재 기준 | 현재 특이사항 없음 |
| (7) 지배구조 미달 | 최근 사업연도 사업보고서상 A)사외이사의 수가 「상법」 제542조의8의 규정에서 정하는 수에 미달하는 경우 B) 「상법」 제542조의11의 규정에서 정하는 감사위원회를 구성하지 않거나 감사위원회의 구성요건을 충족하지 못하는 경우 *「상법」 제542조의8에 의거 자산총액 1,000억원 미만의 코스닥 상장 벤처기업은 사외이사 선임 의무 면제 **「상법」 제542조의11에 의거 자산총액 2조원 미만의 상장회사는 감사위원회 설치 의무 면제 |
- | - | 현재 미해당 | 2024년말 | 현재 특이사항 없음 |
| (8) 거래량 미달 | 분기월평균거래량이 유동주식수의 1%에 미달 다만, 다음 어느 하나에 해당하는 경우에는 이 호에 적용 받지 않습니다. - 신규상장법인(신규상장일이 속하는 분기에 한정) - 분기의 월평균거래량 1만주 이상(액면가액 5,000원 기준) - 「코스닥시장 업무규정」(이하 “업무규정”이라 한다) 제12조의3제1항에 따른 유동성공급계약이 체결된 경우 - 소액주주가 소유한 보통주식의 총수가 유동주식수의 100분의 20 이상이고, 해당 소액주주의 수가 300명 이상인 경우. |
- | - | 현재 미해당 | 2025년 1분기말 | 소액주주 - 지분율 77.58% - 19,291명 |
| (9) 주식분산 미달 | 소액주주 200인미만 or 소액주주지분 20%미만 - 300인이상의 소액주주가 유동주식수의 10%이상으로서 100만주이상을 소유, 해외증권시장에 상장된 경우는 적용배제 |
- | - | 현재 미해당 | 2025년 1분기말 | 소액주주 - 지분율 77.58% - 19,291명 |
| (10) 회생절차 개시신청 | "채무자 회생 및 파산에 관한 법률" 제34조에 의한 회생 절차개시 신청이 있는 경우 | - | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| (11) 파산신청 | 코스닥시장 상장법인에 대하여 "채무자 회생 및 파산에 관한 법률" 제294조에 의한 파산신청이 있는 경우 | - | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| (12) 기타 | - 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 - 변경·추가상장이 유예된 기간 중에「증권의 발행 및 공시 등에 관한 규정」에 따른 재무관리기준을 위반한 경우 |
- | - | 현재 미해당 | 현재 기준 | 해당사항 없음 |
| 출처)「코스닥시장 상장규정」, 당사 정기보고서 |
| 주1) 상기 도표 중 (1)매출액 미달 요건 관련하여, 별도재무제표를 기준으로 합니다. 그 외 요건은 연결재무제표를 기준으로 합니다. |
| 주2) (2)법인세비용차감전계속사업손실 요건 관련하여, 자기자본은 비지배지분을 제외하지 않은 금액 기준을 적용합니다. (3)자본잠식 등, (4)자기자본 미달 요건 관련하여, 자기자본은 비지배지분을 제외한 지배기업지분금액 기준을 적용합니다. |
또한, 2025년 01월 21일, 정부와 유관기관(금융위원회, 금융감독원, 한국거래소, 금융투자협회)은 주식시장의 질적수준 제고를 위한「IPO 및 상장 폐지 제도개선 방안」을 발표하였습니다. 이 중 상장폐지 제도개선 방안은 상장유지 요건을 강화하고, 절차는 효율화함으로써 주식시장 내 저성과 기업을 적시에 퇴출시키고 상장기업의 밸류업을 주요 목적으로 하고 있습니다. 이와 같은 상장폐지 요건이 강화됨에 따라 당사의 영업환경 악화, 재무요건 악화 등을 원인으로 강화된 상장폐지 요건에 해당되어 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있음을 투자자분들은 유의하시기 바랍니다.
| [IPO 및 상장 폐지 제도개선 방안 및 해당여부 검토] |
| 구 분 | IPO 및 상장 폐지 제도개선 방안 | 상장폐지 지정요건 적용여부 |
회사현황 | |
|---|---|---|---|---|
| 사업연도 | 금액(백만원) / 내용 | |||
| (1) 시가총액 요건 기준 강화 | 정량요건으로서 시장평가 관련 시가총액 기준을 단계적으로 상향하여 코스피 500억원, 코스닥 300억원을 목표로 합니다. - 코스피 : 50억원(현행) → 200억원(2026년) → 300억원(2027년) → 500억원(2028년) - 코스닥 : 40억원(현행) → 150억원(2026년) → 200억원(2027년) → 300억원(2028년) |
현재 미해당 | 2024년 12월 31일 |
시가총액 : 113,229백만원 |
| 증권신고서 제출일 전일 기준 |
시가총액 : 84,754백만원 |
|||
| (2) 매출액 요건 기준 강화 | 정량요건으로서 기업실적 관련 매출액 기준을 단계적으로 상향하여 코스피 300억원(시가총액 1,000원 미만 기업만 적용), 코스닥 100억원(시가총액 600억원 미만 기업만 적용)을 목표로 합니다. - 코스피 : 50억원(현행) → 100억원(2027년) → 200억원(2028년) → 300억원(2029년) - 코스닥 : 30억원(현행) → 50억원(2027년) → 75억원(2028년) → 100억원(2029년) |
현재 미해당 | 2024년말 | 매출액 : 7,746백만원 (K-IFRS 별도기준) |
| 2025년 1분기말 | 매출액 : 954백만원 (K-IFRS 별도기준) |
|||
| (3) 감사의견 미달 요건 기준 강화 | - 2회 연속 감사의결 미달시 즉시 상장폐지 : 감사의견 미달(한정, 부적정, 의견거절)의 경우 2회 연속발생시 즉시 상장폐지되고(회생 ·워크아웃기업에 대해서는 예외인정), 이의신청은 허용되지 않습니다. | 현재 미해당 | 2024년말 | 해당사항 없음 |
| 2023년말 | 해당사항 없음 | |||
| 출처) 금융위원회, 당사 정기보고서 |
상세 내용은 본 증권신고서 "제1부. - III.투자위험요소 - 2.회사위험 - 마. 관리종목 편입 및 상장폐지 가능성에 따른 위험을 참고하여 주시기 바랍니다.
| 카. 재무제표 작성 기준일 이후 재무상황 변동에 따른 위험 본 공시서류 상 재무제표에 관한 사항은 2025년 1분기 재무제표 (K-IFRS 기준) 작성기준일 이후의 변동을 반영하지 않았습니다. 당사는 금번 유상증자를 진행하는 과정에서 투자 의사결정에 중대한 영향을 미칠 것으로 판단되는 변동사항을 향후에도 상세하게 반영하여 공시할 예정입니다. 그럼에도 불구하고, 당사가 중요하지 않다고 판단하여 기재 및 서술을 생략한 사항 중 당사의 기업가치에 영향을 미칠 만한 사건이 없다고 단정할 수는 없어 주기적이고 면밀한 검토가 필요합니다. |
본 공시서류에 기재된 재무제표에 관한 사항과 감사인의 의견에 관한 사항은 2025년 1분기 재무제표 작성기준일 이후의 변동을 반영하지 않았으므로 투자에 유의하시기 바랍니다.
다만, 본 공시서류에 기재된 재무제표의 작성기준일 이후 본 공시서류 제출일 사이에 발생한 것으로 증권신고서에 기재된 사항 이외에 자산, 부채, 현금흐름 또는 손익사항에 중대한 변동을 가져오거나 중요한 영향을 미치는 사항은 없습니다.
당사는 금번 유상증자를 진행하는 과정에서 투자 의사결정에 중대한 영향을 미칠 것으로 판단되는 변동사항을 향후에도 상세하게 반영하여 공시할 예정입니다. 그럼에도 불구하고, 당사가 중요하지 않다고 판단하여 기재 및 서술을 생략한 사항 중 당사의 기업가치에 영향을 미칠 만한 사건이 없다고 단정할 수는 없어 주기적이고 면밀한 검토가 필요합니다. 투자자께서는 이 점 유의하시기 바랍니다.
| 타. 차입공매도 유상증자 참여 제한 관련 금융위원회의 공매도 제도개선 관련 「자본시장과 금융투자업에 관한 법률 시행령」일부개정에 따라, 주권상장법인이 유상증자 계획을 공시한 이후 발행가격 산정을 위한 대상 거래기간의 마지막날(발행가격 산정 기산일)까지, 해당 기업의 주식을 공매도 한 자는 증자참여를 제한하되, 예외적인 경우에만 증자참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 투자자께서는 이 점 유의하시기 바랍니다. |
주권상장법인이 유상증자 계획을 공시한 이후 해당 기업의 주식을 공매도 한 자는 증자참여를 제한하되, 예외적인 경우 증자참여를 허용하고 있습니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 이와 관련 유상증자 참여가 제한되는 공매도 시점과 증자참여가 허용되는 예외사유를 시행령에서 정하도록 위임하고 있습니다.
시행령에 따르면, 유상증자 계획이 공시된 다음 날부터, 발행가격 산정을 위한 대상 거래기간의 마지막날(발행가격 산정 기산일)까지 공매도 한 경우 증자참여가 제한됩니다. (「자본시장과 금융투자업에 관한 법률 시행령」제208조의4제1항)
다만, 다음의 경우 공매도를 통해 발행가격에 부당한 영향을 미쳤다고 보지 않아 증자참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률 시행령」제208조의4제2항).
ⅰ) 마지막 공매도 이후 발행가격 산정 기산일까지 공매도 주문 수량 이상을 증권시장 정규거래시간에 매수(체결일 기준)
ⅱ) 금융위원회가 정하는 기준을 충족한 독립된 거래단위를 운영하는 법인 내에서 공매도를 하지 않은 거래단위가 증자참여
ⅲ) 시장조성 또는 유동성공급을 위한 거래과정에서 공매도
상기 공매도제도 개선 관련 자본시장법 시행령 개정안에 따라, 당사의 주식을 해당 기간 동안 공매도하는 투자자께서는 금번 유상증자 참여가 제한될 수 있음을 유의하시기 바랍니다. 해당 법령과 관련된 자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융법규서비스(http://fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
IV. 인수인의 의견(분석기관의 평가의견)
| 본 장은 「자본시장과 금융투자업에 관한 법률」 제119조 및 제125조, 금융감독원의 '금융투자회사의 기업실사 모범규준'을 참조하여 작성된 공동대표주관회사인 삼성증권㈜ 및 NH투자증권(주)의 내부규정에 따라 본 건 공모 지분증권 인수인이 당해 공모 지분증권에 대한 의견을 기재하고 있는 부분입니다. 따라서 본 장의 작성 주체는 공동대표주관회사인 삼성증권㈜ 및 NH투자증권(주)이며, 발행회사인 (주)강스템바이오텍은 "동사"로 기재하였습니다. 본 장에 기재된 분석의견 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 여러가지 요소들의 영향에 따라 예측했던 것과 다를 수 있다는 점을 유의하시기 바랍니다. |
1. 분석기관
| 구 분 | 증 권 회 사 | |
|---|---|---|
| 회 사 명 | 고 유 번 호 | |
| 공동대표주관회사 | 삼성증권(주) | 00104856 |
| 공동대표주관회사 | NH투자증권(주) | 00120182 |
2. 분석의 개요
공동대표주관회사인 삼성증권(주)과 NH투자증권(주)(이하 "공동대표주관회사"라 합니다.)는 「자본시장과 금융투자업에 관한 법률」제71조 및 동법 시행령 제68조에 의거 공정한 거래질서 확립과 투자자 보호를 위해 다수인을 상대로 한 모집ㆍ매출 등에 관여하는 인수회사로서, 발행인이 제출하는 증권신고서 등에 허위의 기재나 중요한 사항의 누락을 방지하는데 필요한 적절한 주의를 기울였습니다.
공동대표주관회사는 인수 또는 모집ㆍ매출의 주선업무를 수행함에 있어 적절한 주의의무를 다하기 위해 금융감독원이 제정한「금융투자회사의 기업실사(Due Diligence) 모범규준」(이하 "모범규준"이라 한다)의 내용을 내부 규정에 반영하여 2012년 02월 01일부터 제출되는 지분증권, 채무증권 증권신고서를 대상(자산유동화증권 등 제외)으로 기업실사를 의무적으로 수행하도록 규정하고 있습니다.
다만, '모범규준' 제3조제2항에 따라 발행회사의 재무 및 영업현황, 사업 환경, 투자위험, 인수 형태, 신용평가등급 등을 감안하여 강화하거나, 완화할 수 있으며, 동조 제5항에 따르면 금융투자회사의 이사회나 리스크관리위원회의 의사결정을 거쳐 '모범규준'의 내용(실사수준)을 생략하거나 강화 또는 완화 적용할 수 있도록 허용하였는 바, 주관회사는 지분증권의 인수 또는 모집·매출의 주선업무를 수행함에 있어서 지분증권의 특성 및 발행회사의 일정요건 충족여부 등에 따라 기업실사 수준을 완화하여 적용할 수 있도록 규정하고 있습니다.
본 지분증권은 공동대표주관회사인 삼성증권(주)과 NH투자증권(주)의 내부 규정상 기업실사 기준을 적용하여 기업실사 업무를 수행하였습니다.
| 「금융투자회사의 기업실사 모범규준」 제3조(적용범위 등) ① 이 규준은 법 제119조제3항의 규정에 의한 증권신고서 및 법 제122조의 규정에 의한 정정신고서를 제출하는 경우에 적용하며, 영업의 실체가 있는 발행회사가 제출하는 지분증권, 채무증권 증권신고서를 대상으로 하고 자산유동화증권 등은 적용대상에서 제외된다. ② 이 규준은 주간회사가 업무수행 중 참고해야 할 기본적인 지침으로 발행회사의 재무 및 영업 현황, 사업 환경, 투자위험, 인수 형태 등을 감안하여 강화하거나 완화하는 등 탄력적으로 운용할 수 있다. ③ 기업공개의 경우 기업공개 실사절차의 특성을 감안하여 이 규준의 내용중 한국거래소의 상장심사지침 등에서 의무사항으로 규정하고 있는 내용과 중복되는 부분에 대해서는 이를 생략하거나 완화할 수 있다. ④ 채무증권의 경우 i)보증유무, 상환조건(만기, 옵션유무), 특약 등 해당 사채의 특성, ii)법 제119조제2항에서 규정하고 있는 일괄신고서에 의한 발행인지 여부, iii)발행회사가 시행령 제121조제6항의 요건을 충족하고 있는지 여부, iv)해당 사채권에 대한 신용평가등급(외부 및 내부) 등을 감안하여 합리적인 기준에 따라 이 규준을 완화할 수 있다. ⑤ 제2항 내지 제4항에 따라 이 규준을 생략하거나 강화 또는 완화하는 경우에는 이사회나 리스크관리위원회(이하 '리스크관리위원회 등')의 의사결정을 거쳐야 한다. |
3. 기업실사 일정 및 주요 내용
| 일자 | 실사 내용 |
|---|---|
| 2025.04.24 | * 발행회사 방문 - 자금조달 금액, 목적 등 발행회사 의견 청취 - 공시 및 뉴스 등을 통한 발행회사 및 소속 산업 사전조사 - 주요사항 및 일정 체크 - 실사 사전 요청자료 송부 |
| 2025.04.25 ~ 2025.04.29 |
* 발행회사 및 해당 산업 조사 - 실사 사전 요청 자료 송부 - 관련 Q&A 등 * 유상증자 리스크검토 - 발행시장 상황, 자금조달규모 적정성, 공모가액 희망 할인율 |
| 2025.04.30 | * 발행회사 방문 - 공시 및 뉴스 내용 등을 통한 발행회사 및 산업 이해 - 발행회사 및 산업 관련 Q&A - 발행시장 상황, 자금조달 규모 적정성, 최대주주 및 주요주주 청약 참여 등 유상증자 관련 리스크 검토 |
| 2025.05.01 ~ 2025.05.06 |
* 실사 사전 요청 자료 목록 및 Check List 제공 |
| 2025.05.07 | * 현장 방문을 통한 실사 * Due-diligence checklist에 따라 투자위험요소 실사 1) 사업위험관련 실사 - 영위중인 사업의 임상 진행현황 및 기술적 진입 난이도 - 경쟁사 대비 유효성 및 장단점 확인 - 신규 사업에 대한 세부사항 체크 2) 회사위험관련 실사 - 재무관련 위험 등 체크 |
| 2025.05.08 ~ 2025.05.28. |
* 실사 추가 자료 요청 * 발행 세부일정 협의 * 기업실사 관련 Q&A 정리 |
| 2025.05.28 |
* 현장 방문을 통한 실사 * 투자위험요소 세부사항 체크 |
| 2025.05.28 ~ 2025.06.09 |
* 실사 추가자료 요청 * 증권신고서 작성 및 조언 * 이사회의사록 검토/인수계약서 작성 및 검토 * 실사이행보고서 작성 및 증권신고서 검토 |
| 2025.06.17 ~ 2025.06.23 |
* 실사 추가 자료 요청 * (정정) 증권신고서 작성 / 검토 * (정정) 실사이행보고서 작성 및 증권신고서 검토 |
4. 기업실사 참여자
[공동대표주관회사]
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 | 참여기간 | 주요 경력 |
|---|---|---|---|---|---|---|
| 삼성증권(주) | Corporate Finance3팀 | 김준한 | 그룹장 | 기업실사 총괄 | 2025년 05월 08일 ~ 2025년 06월 23일 |
기업금융업무 27년 |
| 삼성증권(주) | Corporate Finance3팀 | 강동진 | 이사 | 기업실사 책임 | 2025년 05월 08일 ~ 2025년 06월 23일 |
기업금융업무 19년 |
| 삼성증권(주) | Corporate Finance3팀 | 홍지연 | 과장 | 기업실사 실무 | 2025년 05월 08일 ~ 2025년 06월 23일 |
기업금융업무 8년 |
| 삼성증권(주) | Corporate Finance3팀 | 김정현 | 대리 | 기업실사 실무 | 2025년 05월 08일 ~ 2025년 06월 23일 |
기업금융업무 2년 |
| 삼성증권(주) | ECM1팀 | 김한룡 | 부장 | 기업실사 실무 | 2025년 05월 08일 ~ 2025년 06월 23일 |
기업금융업무 9년 |
| 삼성증권(주) | ECM1팀 | 이근영 | 대리 | 기업실사 실무 | 2025년 05월 08일 ~ 2025년 06월 23일 |
기업금융업무 2년 |
| NH투자증권 | SME부 | 김기훈 | 이사 | 기업실사 총괄 | 2025년 04월 24일 ~ 2025년 06월 23일 |
기업금융업무 12년 |
| NH투자증권 | SME부 | 노동혁 | 차장 | 기업실사 책임 | 2025년 04월 24일 ~ 2025년 06월 23일 |
기업금융업무 9년 |
| NH투자증권 | SME부 | 김건 | 대리 | 기업실사 실무 | 2025년 04월 24일 ~ 2025년 06월 23일 |
기업금융업무 5년 |
[발행회사]
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 |
|---|---|---|---|---|
| (주)강스템바이오텍 | 경영지원실 | 이계종 | 전무 | 발행업무 총괄 |
| 한성민 | 부장 | IR 담당 및 기업실사 자료 제공 | ||
| 이현아 | 부장 | 기업실사 자료 제공 | ||
| 박미애 | 과장 | 공시 담당 |
5. 기업실사 세부항목 및 점검 결과
- 동 증권신고서에 첨부되어 있는 기업실사 보고서를 참조해 주시기 바랍니다.
6. 종합의견
가. 공동대표주관회사인 삼성증권(주) 및 NH투자증권(주)는 (주)강스템바이오텍이 2025년 06월 10일 이사회에서 결의한 보통주식 38,000,000주에 대한주주배정 후 실권주 일반공모 증자를 잔액인수함에 있어 다음과 같이 평가합니다.
| 긍정적요인 |
▶ 동사는 자체 개발한 다분화능을 가진 줄기세포를 인간 제대혈로부터 고순도(high-purity)로 분리하고, 대량배양(massive culture)하는 기술을 기반으로 동종 제대혈 유래 줄기세포치료제(의약품) 연구개발을 진행하고 있습니다. ▶ 동사의 주요 파이프라인은 (1) 아토피 피부염 치료제(Furestem-AD Inj.) [ 국내 반복투여 제1/2a 변경승인신청 완료, 2025년 하반기 임상 1/2a상 개시 예정], (2) 류마티스관절염 치료제(Furestem-RA Inj.) [2023년 09월 임상2b상 IND 승인 완료, 차후 임상 개시 시기를 결정 후 진행 예정], (3)골관절염 치료제(OSCA) [2025년 3월 임상 2a상 진행중, 2026년 하반기 임상 2b상 진행 예정]입니다. 이 중 동사의 골관절염 치료제인 OSCA의 경우 성공적인 임상 1상 결과를 바탕으로 유영제약과 라이센스-아웃 계약 체결하였으며, 현재 2a상 진행 중에 있습니다.
|
| 부정적요인 | ▶ 동사가 영위하고 있는 바이오 신약이 제품화되기까지 후보물질 선정, 비임상 단계, 임상시험 진행 승인, 임상 1~3상, 품목허가의 단계로 진행되며 장기간의 연구기간이 소요됩니다. 또한, 신약 연구개발을 통하여 가시적인 결과가 나오는 제품의 상용화 단계까지 많은 비용과 시간이 요구되며, 연구개발 과정에서 수많은 변수가 발생할 수 있습니다. 또한, 변수들을 미리 찾아내어 극복하지 못한 경우에 지출했던 연구개발 비용 및 시간 등의 큰 손실을 발생할 수 있습니다. ▶ 동사는 2023년 08월 아토피 피부염 치료제(Furestem-AD Inj.)의 임상3상 통계분석 결과는 EASI-50 평가에서 시험군과 위약 대조군 간 유효성 차이를 입증하지 못하였습니다. 그러나 내부 시뮬레이션을 통해 16주차 이후에는 통계적 유의성 달성 가능성을 확인하였고 특정 연령대의 시험약군에서는 위약군 대비 통계적 유의성 달성을 확인하였습니다. 이에 기존 단회투여에서 반복투여 방식으로 프로토콜을 수정하여 2024년 11월 임상 1/2a상 IND를 변경승인신청하였으나, 식품의약품안전처(MFDS)의 추가 자료보완 요청을 기한 내 회신이 어려울 것으로 판단하여 자진취하 신청을 하였습니다. 그리고 2025년 4월 퓨어스템-에이디주의 반복투여 제1/2a 임상시험계획변경승인신청을 하였으며, 2025년 하반기 임상1/2a상 개시를 계획하고 있습니다. ▶ 동사가 진출하려는 시장에는 국내외 제약회사들도 부작용을 최소화 할 수 있는 다양한 방법으로 치료제를 개발하고 있습니다. 따라서 동사의 연구개발 영역 또는 타겟 질병이 겹치는 잠재적인 경쟁회사의 출현 가능성을 배제 할 수 없으며, 이러한 잠재적 경쟁회사의 연구개발 제품이 시장에 성공적으로 출시될 경우 동사가 장기간 신약 개발에 쓰인 막대한 투자 비용과 시간을 감안할 시 동사의 경영성과 및 재무구조에 부정적인 영향을 미칠 수 있습니다. ▶ 동사는 기술성장특례 적용 기업으로 2015년에 12월에 상장하여 관리종목 지정요건 중 유예 항목들에 대한 적용 기간이 모두 만료되었습니다. 이에 따라 동사가 매출액 미달 요건, 법인세비용차감전계속사업손실 요건 및 자본잠식 요건 등을 충족하지 못할 경우 향후 관리종목으로 지정될 가능성이 있습니다. 동사는 2023년 자기자본의 50%를 초과하는 법인세차감전사업손실이 발생하였습니다. 2024년에는 자기자본의 50%를 초과하는 법인세차감전사업손실이 발행하지 않았으나, 2025년 말에 법인세차감전사업손실이 자기자본의 50%를 초과할 경우 최근 3개 사업연도중 2개 사업연도(2023년, 2025년)의 법인세차감전계속사업손실액이 각 10억원 이상이면서 각 사업연도 말 자기자본의 50%를 초과하는 경우에 해당되어 관리 종목 지정 사유에 해당될 수 있습니다. ▶ 동사는 지속적인 영업적자 및 당기순손실 발생으로 인하여 필요자금을 외부에서 조달하여 사용하고 있기 때문에 적기에 자금조달을 못하거나 실적개선으로 인해 유동성을 확보하지 못한다면 유동성 위험에 노출될 수 있으며, 차입금 만기 연장에 어려움이 발생할 수 있습니다. |
| 자금조달의 필요성 |
▶ 동사는 금번 유상증자를 통해 조달하는 자금을 주요 파이프라인의 국내외 임상진행을 위한 운영자금, 시설자금, 일반 운영자금, 채무상환자금으로 활용할 계획입니다.
|
나. 공동대표주관회사는 (주)강스템바이오텍이 제출한 자료와 객관적으로 정확하고 신뢰할 수 있다고 믿어지는 자료를 중심으로 실사를 수행하였으며, 객관적인 입장에서 공정을 기하기 위하여 최선의 노력을 다하였습니다.
다. 공동대표주관회사는 상기 실사를 통해 제공받는 자료들로부터 도출된 결과나 오류, 누락 등에 대하여 책임지지 않으며, 인간적 또는 기계적, 기타 그 외의 다른 요인에 의한 오류발생 가능성으로 인해 본 평가 내용에 대해 명시적으로 혹은 묵시적으로도 증명이나 서명 또는 보증 및 단언을 할 수 없습니다.
라. (주)강스템바이오텍의 금번 유상증자는 국내외 거시경제 변수 변화로 투자수익에 대한 확실성이 저하될 수 있습니다. 투자자 여러분께서는 상기 검토결과는 물론 동 증권신고서 및 투자설명서에 기재된 동사의 회사 전반에 걸친 현황 및 재무상의 위험과 산업 및 영업상의 위험요인 등을 감안하시어 투자에 유의하시기 바랍니다. 또한, 공동대표주관회사 및 발행회사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 동 증권신고서 및 투자설명서에 기재하지 않은 사항이라 하더라도 동사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자께서는 동 증권신고서 및 투자설명서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 독자적이고도 세밀한 판단에 의해 투자결정을 하시기 바랍니다.
| 2025년 06월 24일 |
| 공동대표주관회사 : 삼성증권 주식회사 |
| 대표이사 박 종 문 |
| 공동대표주관회사 : NH투자증권 주식회사 |
| 대표이사 윤 병 운 |
V. 자금의 사용목적
1. 모집 또는 매출에 의한 자금조달 내역
가. 자금조달금액
| (단위 : 원) |
| 구 분 | 금 액 |
|---|---|
| 모집 또는 매출총액(1) | 49,210,000,000 |
| 발행제비용(2) | 1,025,000,000 |
| 순 수 입 금 [ (1)-(2) ] | 48,185,000,000 |
| 주1) 상기 금액은 예정발행가액을 기준으로 산정한 금액으로 모집가액 확정시 변경될 수 있습니다. |
| 주2) 상기 모집총액은 우선적으로 하단에 기재된 자금의 사용 목적에 따라 사용할 예정입니다. |
| 주3) 발행제비용은 공모금액 및 실권규모에 따라 변경될 수 있으며, 상기 기재 금액은 청약 초과로 인하여 실권이 발생하지 않은 상황을 가정하여 산정되었습니다. 또한 상장수수료는 상장신청일 직전일 주가에 따라 변동될 수 있습니다. |
나. 발행제비용의 내역
| (단위 : 원) |
| 구 분 | 금 액 | 계산근거 |
|---|---|---|
| 발행분담금 | 8,857,800 | 모집총액의 0.018% (10원 미만 절사) |
| 인수수수료 | 639,730,000 | 모집총액의 1.3% |
| 주관수수료 | 246,050,000 | 모집총액의 0.5% |
| 상장수수료 | 5,900,000 | 430만원 + 300억원 초과금액의 10억원당 8만원 (코스닥시장상장규정 시행세칙 별표 14) |
| 등록세 | 76,000,000 | 증자 자본금의 0.4% (지방세법 제28조) |
| 지방교육세 | 15,200,000 | 등록세의 20% (지방세법 제151조) |
| 기타비용 | 33,262,200 | 구주주 청약서, 투자설명서 인쇄 및 발송비 등 |
| 합 계 | 1,025,000,000 | - |
| 주1) 상기 금액은 예정발행가액을 기준으로 산정한 금액으로 모집가액 확정 시 변경될 수 있습니다. |
| 주2) 발행제비용은 공모금액 및 상장신청일 직전일 한국거래소에서 거래되는 당사의 보통주식 종가, 유관기관 정책 등에 따라 변동될 수 있습니다. |
| 주3) 기타비용은 예상금액으로 변동될 수 있습니다. |
| 주4) 발행제비용은 공모금액에서 지급될 예정입니다. |
2. 자금의 사용목적
가. 자금의 사용목적
당사는 금번 유상증자를 통해 조달한 자금을 아래와 같이 사용할 예정입니다.
| (기준일 : | 2025년 06월 09일 | ) | (단위 : 백만원) |
| 시설자금 | 영업양수 자금 |
운영자금 | 채무상환 자금 |
타법인증권 취득자금 |
기타 | 계 |
|---|---|---|---|---|---|---|
| 4,010 | - | 42,775 | 1,400 | - | 1,025 | 49,210 |
| 주1) 상기 금액은 예정발행가액을 기준으로 산정한 금액으로 모집가액 확정 시 변경될 수 있습니다. |
| 주2) 상기 모집총액은 우선적으로 하단에 기재된 자금의 사용 목적에 따라 사용할 예정입니다. |
| 주3) 발행제비용은 공모금액 및 실권규모, 유관기관과의 협의 등에 따라 변경될 수 있으며, 상기 기재 금액은 청약 초과로 인하여 실권이 발생하지 않은 상황을 가정하여 산정되었습니다. 발행제비용은 공모금액에서 지급될 예정이나, 상기 발행제비용 중 일부는 지급시기에 따라 공모자금 외 자체자금으로 집행할 수 있습니다. 해당 비용에 대한 공모자금 미사용액은 운영자금(임상시험비)으로 지출할 예정입니다. |
나. 공모자금 세부 사용목적
당사는 금번 유상증자를 통해 조달된 자금을 골관절염 치료제(OSCA(구.Furestem-OA Kit Inj.)) 및 아토피 피부염 치료제(Furestem-AD Inj.)의 연구개발비(국내 및 해외 임상시험 수행비, 장기추적조사), 당사 배양 지방줄기세포(제2종 재생의료)의 일본재생의료 시장 공급, 국내첨생법 사업 진출 및 오가노이드 연구개발 위한 운영 경비, 그리고 첨단줄기세포 GMP 시설투자, 기타 운영경비 및 채무상환자금으로 사용할 계획입니다. 금번 유상증자 자금 사용의 우선순위는 아래와 같습니다.
| [금번 유상증자 자금사용의 우선순위] |
| (단위 : 원) |
| 우선순위 | 자금용도 | 세부 내용 | 사용(예정)시기 | 금 액 |
|---|---|---|---|---|
| 1 | 운영자금(임상시험비) | 골관절염 치료제(국내 임상) | 2025년 하반기 ~ 2028년 | 14,200,000,000 |
| 골관절염 치료제(해외 임상) | 5,900,000,000 | |||
| 아토피 치료제(장기추적조사) | 2026년 ~ 2028년 | 2,600,000,000 | ||
| 2 | 운영자금(운영경비) | 일본재생의료/국내첨생법 사업 | 2025년 하반기 ~ 2028년 | 5,905,000,000 |
| 오가노이드 연구개발 | 6,340,000,000 | |||
| 시설자금 | GMP 시설투자 | 2026년 ~ 2028년 | 4,010,000,000 | |
| 3 | 운영자금(운영경비) | 기타운영경비 | 2026년 ~ 2028년 | 7,830,000,000 |
| 4 | 채무상환자금 | GMP 시설 취득 용도 차입금 상환 | 2025년 하반기 ~ 2028년 | 1,400,000,000 |
| - | 기타자금 | 발행제비용 | - | 1,025,000,000 |
| 합 계 | 49,210,000,000 | |||
| 주1) 상기 금액은 예정발행가액을 기준으로 산정한 금액으로 모집가액 확정 시 변경될 수 있습니다. |
| 주2) 자금의 사용 시기는 증권신고서 제출일 전일 기준으로 작성되었으며, 향후 실제자금 집행 과정에서 금액 또는 사용시기가 변경될 수 있습니다. |
(1) 운영자금(임상시험비)
| [임상시험에 따른 세부 자금 사용 계획] |
| (단위:백만원) |
| 우선 순위 |
적응증 | 구분 | 구성 | 2023년 증자 잔액 (2025.03.31 기준) |
2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고사항 |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 골관절염 치료제 (OSCA) |
국내임상 2a상 |
임상 기관연구비 | 1,181 | 250 | 500 | 100 | - | 850 | *주요 임상 비용 1. 2a 임상시험 기간(FPI-LPO): 2025. 03-2026. 04 2. 2a 위약군에 대해 1년 시점의 보상투여 관련 비용은 장기추적조사에 포함됨 |
| CRO | 811 | 1,100 | 2,500 | 500 | - | 4,100 | ||||
| 위탁연구개발비 | -834 | 50 | 100 | 100 | - | 250 | ||||
| 인허가 | 63 | 19 | 611 | 178 | 16 | 825 | ||||
| 약물감시 | 157 | - | 932 | 283 | 24 | 1,239 | ||||
| 기타 임상진행비 | 123 | - | 1,253 | 437 | 83 | 1,772 | ||||
| 소계 | 1,501 | 1,419 | 5,896 | 1,598 | 123 | 9,036 | - | |||
| 장기추적조사(K0701-E) | 임상 기관연구비 | -38 | - | - | 300 | 300 | 600 | *주요 비용 1. LTFU 기간(EV1-EV5): ~2031. 3Q (2a 위약군 보상투여 개시 +5년) 2. Scope: 1상 + 2a (위약군 보상투여 포함) - 총 118명 대상 3. 방문시점: 12M/24M/60M |
||
| CRO | 806 | - | - | 1,000 | 1,000 | 2,000 | ||||
| 위탁연구개발비 | 136 | - | - | - | - | - | ||||
| 인허가 | 3 | - | - | 279 | 462 | 741 | ||||
| 약물감시 | 491 | - | - | 212 | 709 | 921 | ||||
| 기타 임상진행비 | 855 | - | - | - | 955 | 955 | ||||
| 소계 | 2,252 | - | - | 1,791 | 3,426 | 5,217 | - | |||
| 해외임상 | GAP분석/RFD | - | 8 | 50 | - | - | 130 | *주요 일정: 1. 융복합제제에 대한 분류 (CAM의 FDA 분류지정): 4Q 2025 2. US preIND Meeting: 3Q/4Q 2026 3. US preIND 보완사항 F/U: 2Q 2027 4. US IND 승인: 3Q/4Q 2027 5. RMAT/BTD 지정: 4Q 2027 *주요 비용: -Pre-IND & IND: 관련 신청 및 F/U에 필요한 CRO 비용 및 부대비용 -RMAT & BTD: 준비 및 지정에 필요한 전체비용 -IP supply: 해외임상시험 수행을 위해 필요한 IP 공급방식/밸리데이션/임대료/물품 등 제반사항의 준비비용 -CMC/Preclinical/Clinical: 해외임상시험 승인을 위해 추가/보완/임상시험 디자인 등의 준비에 필요한 비용 |
||
| Pre-IND | - | 80 | 200 | - | - | 280 | ||||
| IND | - | - | 150 | 150 | - | 300 | ||||
| RMAT | - | - | 50 | 50 | - | 100 | ||||
| BTD | - | - | 50 | 50 | - | 100 | ||||
| IP supply 준비 | - | 50 | 200 | 500 | - | 750 | ||||
| Preclinical | - | - | 200 | 100 | - | 300 | ||||
| CMC | - | - | 300 | 300 | - | 600 | ||||
| Clinical | - | - | 300 | 300 | - | 600 | ||||
| 인허가 | - | 45 | 283 | 291 | - | 619 | ||||
| 약물감시 | - | 68 | 424 | 436 | - | 928 | ||||
| 기타 임상진행비 | - | 91 | 565 | 582 | - | 1,238 | ||||
| 소계 | - | 414 | 2,772 | 2,759 | - | 5,945 | - | |||
| 합계 | 3,752 | 1,833 | 8,668 | 6,147 | 3,549 | 20,198 | - | |||
| 1 | 아토피 피부염 치료제 (Furestem-AD Inj.) |
장기추적조사 | 임상 기관연구비 | -74 | - | 200 | 200 | 200 | 600 | *주요 비용 1. LTFU 기간(EV1-EV5): ~2030 2. Scope: 3상(단회) (위약군 보상투여 포함) - 총 315명 3. 방문시점: 12M/24M/60M |
| CRO | 128 | - | 280 | 300 | 300 | 880 | ||||
| 위탁연구개발비 | -4 | - | - | - | - | - | ||||
| 인허가 | 199 | - | - | 149 | 99 | 248 | ||||
| 약물감시 | 645 | - | - | 228 | 154 | 383 | ||||
| 기타 임상진행비 | 851 | - | - | 278 | 184 | 462 | ||||
| 소계 | 1,745 | - | 480 | 1,155 | 938 | 2,572 | - | |||
| 총합계 | 5,497 | 9,148 | 7,303 | 4,487 | 22,770 | - | ||||
| 출처) 당사 정기보고서 및 당사 제시 |
| 주1) 상기 '비고사항'의 각 임상 및 장기추적조사의 주요 일정은 당사가 목표로 하는 일정이며, 임상 대상 환자모집 난관 등 예상치 못한 상황 발생에 따라 목표와 달리 일정이 지연될 가능성도 존재합니다. |
| 주2) 상기 '2023년 증자 잔액' 합계는 골관절염 치료제(OSCA) 국내임상시험비/장기추적 및 아토피 치료제(퓨어스템-에이디주) 장기추적에 해당하는 잔액만 포함하고 있으며, 나머지 잔액을 포함하고 있지 않습니다. |
상기 임상시험에 따른 세부 자금 계획 시 각 항목별 아래와 같은 비용을 포함하여 산정하였습니다.
| 구분 | 항목 | 내용 |
| 국내임상 및 장기추적조사 |
임상 기관연구비 | 임상 환자 모집에 따른 연구비, 검체 채취 및 임상병리 시험비용, 연구자/부연구자/연구간호사 등의 기본 인건비가 포함되어 있습니다. |
| CRO | 임상시험 수행에 따른 CRO 서비스에 대한 직접비용을 의미하며, 영상의학평가, Lab 분석비용, Lab 검사비용, 임상시험 수행을 위한 시스템(EDC, eCOA 등) 운용 비용 등이 포함되어 있습니다. | |
| 위탁연구개발비 | 위탁연구개발비는 임상시험기간 중 추가로 연구되어야 하는 작용기전 및 생물검정(bioassay)와 같은 비용, 그리고 이제까지 확보한 데이터에 대한 추가분석 및 해석을 위한 자문비용 등이 포함되어 있습니다. | |
| 인허가 | 임상에 필요한 각종 인허가비용과 등록비용 그리고 담당인력의 인건비등이 포함되어 있습니다. | |
| 약물감시 | 임상에 투여하는 약물에 대한 모니터링 비용, 장기추적조사 연차보고 및 안전성 관련 자문비용, 담당인력의 인건비 등이 포함되어 있습니다. | |
| 기타 임상진행비 | 임상과 관련된 논문 및 학회발표, 통계자문 비용, 담당인력의 인건비가 포함되어 있습니다. | |
해외임상 |
GAP분석/RFD | US FDA 관련 신청에 앞서 내부생성 자료에 대한 적합성 및 보완영역 평가 준비에 필요한 비용이 포함되어 있습니다. |
| Pre-IND & IND |
Pre-IND 및 IND의 각 신청 및 F/U에 필요한 각 CRO 비용 및 부대비용(출장 등) 등이 포함되어 있습니다. | |
| RMAT & BTD |
RMAT 및 BTD 각 준비 및 지정에 필요한 전체 비용 등이 포함되어 있습니다. | |
| IP supply 준비 | 해외임상시험 수행을 위해 필요한 IP 공급방식/밸리데이션/임대료/물품 등 제반사항의 준비비용 등이 포함되어 있습니다. | |
| Preclinical | 기존 비임상자료 정리, 번역, gap assessment, 추가 비임상 시험 또는 보완 비임상시험 수행, 후속 단계 IP에 대한 동등성연구 자료 검토 비용 등이 포함되어 있습니다. | |
| CMC | 기존 CMC 자료 정리 및 번역, gap assessment, cell banking 교체에 따른 계획 검토 및 보완, 미국 FDA 관련 규정에 따른 보완 및 수정사항 파악 관련 비용 등이 포함되어 있습니다. | |
| Clinical | 기존 1/2a 임상시험 데이터에 대한 해석, 미국 FDA DMOAD 가이드라인에 맞는 시놉시스 개발, PreIND meeting 관련 질의 및 대응 관련 비용 등이 포함되어 있습니다. | |
| 인허가 | FDA 가이드라인에 맞춰 허가요건을 검토하고 제반 서류 제출, 보완 조율 역할 등과 관련한 비용, 국내 담당인력의 인건비가 포함되어 있습니다. | |
| 약물감시 | 치료제 부작용이나 안정성 문제가 발생할 수 있으므로 임상에 투여하는 약물에 대한 지속한 모니터링이 필요합니다. 이와 관련한 모니터링 비용, 안전성 관련 자문 비용, 국내 담당인력의 인건비가 포함되어 있습니다. | |
| 기타 임상진행비 | 임상 진행에 필요한 물품과 약품 제조비용, 국내 담당인력의 인건비가 포함되어 있습니다. |
(1)-1 골관절염 치료제 (OSCA)
골관절염 치료제(OSCA)는 당사의 핵심 파이프라인으로 임상 1차에서 염증완화 및 연골 재생에서 뛰어난 효능을 확인할 수 있었습니다. 이에 당사는 골관절염 치료제(OSCA) 임상 1상에서 확인된 안전성 및 유효성에 대한 전반적인 평가 결과를 바탕으로 임상 2a상의 규모를 50명에서 108명으로 확대하여 위약 대비 시험약의 효과를 보다 정밀하게 평가할 계획입니다. 임상 2a상은 7개 임상시험기관에서 진행 예정으로 2025년 3월 첫 대상자의 투약을 시작하였으며, 2026년 2분기까지 완료를 목표로 하고 있습니다. 임상 2a상 임상규모를 증가시킨 이유 및 효과로는 1) 위약 대비 시험약의 유효성의 크기 비교에서 통계적 유의성도 확보할 가능성이 있게 되며, 2) 이를 바탕으로 후기 임상전략에 유리한 상황도 도출 가능 할 것으로 판단하였습니다. 즉, 임상 2a상 대상 인원 증원을 통해 위약군 대조를 통한 안전성 및 유효성 결과를 중점 확보하여 2a상 완료 후 바로 3상으로 진행하거나 해외 기술이전으로 빠르게 연결하고자 합니다. 이에 금번 조달 자금 중 14,200백만원은 골관절염 치료제(OSCA)의 국내 임상 시험의 성공적인 수행 및 가치 극대화를 위해 사용될 예정입니다. 이 중 장기추적조사에 소요되는 비용은 약 5,200백만원으로, 세포치료제의 경우 「첨단 재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률」에 의해 임상단계부터 5년까지 장기추적조사를 의무적으로 수행해야하며, 이에 당사는 5년 이상(최소 5년) 진행할 예정이며 시판 제품에 대해서도 장기추적을 시행할 예정입니다
|
| 출처) 당사 제시 |
또한, 골관절염 치료제(OSCA)에 대해 미국 FDA의 첨단재생의료치료제(RMAT) 및 혁신치료제(BTD) 지정 조건에 부합하는 해외 임상시험을 준비할 계획입니다. 관련 신청에 앞서 내부생성 자료에 대한 적합성 및 보완영역 평가인 GAP 분석을 시작으로 2026년 하반기에 pre-IND Meeting 진행, 이후 순차적으로 IND 준비 및 승인, 첨단재생의료치료제(RMAT) 및 혁신치료제(BTD) 준비와 승인을 최종 목표로 하고 있습니다. 이에 금번 조달 자금 중 약 5,900백만원은 골관절염 치료제(OSCA)의 해외 임상 시험 준비 및 수행을 위해 사용할 계획입니다.
(1)-2 아토피 피부염 치료제 (Furestem-AD Inj.)
아토피 피부염 치료제(Furestem-AD Inj.)의 임상3상 통계분석 결과 1차 평가지표인 12주차 시점 위약 대비 시험군과 대조군 간 유효성 차이를 입증하지 못하였으나 내부 시뮬레이션을 통해 16주차 이후에는 통계적 유의성 달성 가능성을 확인하였고 특정 연령대의 시험약군에서는 위약군 대비 통계적 유의성 달성을 확인하였습니다. 이에 기존 단회투여에서 반복투여 방식으로 프로토콜을 수정하여 2024년 11월 임상 1/2a상 IND를 변경 승인신청하였으나, 식품의약품안전처(MFDS)의 추가 자료보완 요청을 기한 내 회신이 어려울 것으로 판단하여 자진취하 신청을 하였습니다. 그리고 2025년 4월 퓨어스템-에이디주의 반복투여 제1/2a 임상시험계획변경승인신청을 하였으며, 2025년 하반기 임상 1/2a상 개시를 계획하고 있습니다. 해당 반복투여 임상 1/2a상은 파트너사를 찾아 컨소시엄을 구성하여 임상 비용 및 장기추적조사 비용을을 부담할 계획입니다. 다만, 「첨단 재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률」에 의해 기존 단회투여 3상에 대한 장기추적조사는 계속 진행 중에 있으며, 금번 조달 자금 중 2,600백만원은 아토피 피부염 치료제(Furestem-AD Inj.)의 해당 장기추적조사를 위해 사용할 계획입니다.
(2) 운영자금(운영경비) 및 시설자금
| [운영자금(운영경비) 사용 계획] |
| (단위:백만원) |
| 우선 순위 |
구분 | 구성 | 2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고 |
|---|---|---|---|---|---|---|---|---|
| 2 | 운영자금(운영경비) | 일본재생의료/국내첨생법 사업 | 600 | 2,000 | 1,650 | 1,655 | 5,905 | - 일본재생의료 공급 및 국내 첨단재생바이오법 개정안 시행에 따른 준비 비용 |
| 운영자금(운영경비) | 오가노이드 연구개발 | 150 | 990 | 2,340 | 2,860 | 6,340 | - 피부 및 췌도 오가노이드 임상 전 연구소의 연구인건비 및 재료비 등의 개발 비용 | |
| 시설자금 | GMP 시설투자 | - | 2,537 | - | 1,473 | 4,010 | - 신규시설 투자 및 기존 노후 시설 개보수 |
|
| 합 계 | 750 | 5,527 | 3,990 | 5,988 | 16,255 | |||
| 출처) 당사 제시 |
(2)-1 일본재생의료/국내첨생법 사업
당사는 일본 재생의료시장 진출을 위해 2024년 일본 후생노동성에 제1종(동종제대혈줄기세포(를 이용한 아토피 피부염 치료)) 및 제2종(자가지방줄기세포) 재생의료 제공계획에 대한 심의 및 승인 절차를 진행하였습니다. 제2종(자가지방줄기세포)의 경우, 특정인정재생의료위원회의 심의를 거쳐 승인을 받고, 2025년 2월 후생노동성 최종 승인까지 완료되었습니다. 현재 일본 내 공급을 위해 동경, 오사카, 나고야 소재의 현지 의료기관과 계약을 완료하였으며, 2025년 하반기부터 환자 수급을 위한 본격적인 영업활동 및 투자를 진행할 계획입니다. 이에 금번 조달 자금 중 2,500백만원은 제2종(자가지방줄기세포)의 일본재생의료 시장 진출 및 공급을 위해 사용할 계획입니다.
한편, 국내 첨단재생바이오법 개정안 시행에 따라 첨단재생의료 기반 바이오 신약의 경우 첨생법에 따른 연구계획 및 치료계획이 승인되는 경우 환자에게 임상 목적이 아닌 치료 목적으로 첨단재생의료 치료를 제공할 수 있게되고, 매출을 발생시킬 수 있게 되었습니다. 따라서 기존 바이오 신약 대비 매출 발생 시점이 앞당겨짐과 동시에 매출 발생 경로 및 가능성이 확대되며, 이를 통해 자체 연구개발 비용을 충당함으로써 전체적인 연구개발 안정성을 증대시킬 수 있게 되었습니다. 당사 주요 파이프라인 치료제의 대상 적응증인 중증아토피와 골관절염은 난치질환에 해당되며, 첨단재생바이오법 개정에 따라 당사의 아토피 피부염 치료제(퓨어스템-에이디 주)와 골관절염 치료제(OSCA)를 조기에 사용할 수 있도록 금번 조달 자금 중 3,405백만원은 협력 의료기관을 통한 해당 파이프라인의 임상 연구 지원, IP 생산 등을 위해 사용할 계획입니다.
| [일본재생의료/국내첨생법 사업 비용 상세 내역] |
| (단위:백만원) |
| 구성 | 2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고 | |
|---|---|---|---|---|---|---|---|
| 일본재생의료 사업 | - 일본내 유통망구축, 공급용 해동기 구매, 해외 공급용 안전재고 확보, 기본 운영 등을 위한 비용 | ||||||
| 해외 유통망 구축 | 150 | 700 | 350 | 350 | 1,550 | ||
| 공급설비(해동기 등)구입/안전재고 확보 | 100 | 200 | 200 | 200 | 700 | ||
| 운영비용 | 50 | 100 | 50 | 50 | 250 | ||
| 소계 | 300 | 1,000 | 600 | 600 | 2,500 | ||
| 국내 첨생법 개정에 따른 사업 | - 국내 첨단재생바이오법 개정안 시행에 따른 임상기관에 대한 연구 지원, IP생산 등을 위한 비용 | ||||||
| 임상연구 지원 | 100 | 200 | 200 | 200 | 700 | ||
| IP생산 | 200 | 800 | 850 | 855 | 2,705 | ||
| 소계 | 300 | 1,000 | 1,050 | 1,055 | 3,405 | ||
| 합 계 | 600 | 2,000 | 1,650 | 1,655 | 5,905 | ||
| 출처) 당사 제시 |
상기 일본재생의료/국내첨생법 사업 비용 자금 계획 시 각 항목별 아래와 같은 비용을 포함하여 산정하였습니다.
| 구분 | 항목 | 내용 |
| 일본재생의료 사업 | 해외 유통망 구축 | 일본 현지 공급을 위해 해외 시술병원을 추가로 섭외하여 실제 투약가능시까지 소요되는 비용으로 병원 섭외 시 소요 비용, 투약 허가 승인, 변경, 실사 대응 등 위한 비용, 모객 관련 마케팅 비용 등이 포함되어 있습니다. |
| 공급설비(해동기 등)구입/안전재고 확보 | 생산한 줄기세포의 해외 시술 병원 공급(운송)을 위한 해동기/디프리저의 구입 비용, 배양을 위한 조직채취, 혈액검사 비용, 안전재고 확보를 위한 세포 보관 비용 등이 포함되어 있습니다. | |
| 운영비용 | 재생의료 사업 컨설팅, 사업 대행, 허가 대행 등과 관련한 비용이 포함되어 있습니다. | |
| 국내 첨생법 개정에 따른 사업 | 임상연구 지원 | 임상연구 실시 기관(대학병원 등)의 당사 치료제를 활용한 임상연구 진행과 관련한 연구 진행 지원, 컨설팅, 신고 서류 준비 등 담당인력의 인건비가 포함되어 있습니다. |
| IP생산 |
임상연구 실시 기관(대학병원 등)의 당사 치료제를 활용한 임상연구 진행과 관련한 IP생산 관련 비용 등이 포함되어 있습니다. |
(2)-2 오가노이드 연구개발
당사는 기타 파이프라인 중 하나로 오가노이드를 연구개발 중에 있습니다. 오가노이드란 장기유사체 혹은 미니 장기라고도 불리며, 당사의 피부 오가노이드 기술은 공기-액체 계면(ALI) 배양을 통해 불필요한 연골 조직의 형성을 억제하여 기존 기술의 한계를 극복하고 실제 피부와 같은 평평한 구조를 형성하여 정상피부와 기능적으로 동등한 피부 오가노이드 플랫폼을 구축하고자 합니다. 최근 선진국 중심으로 동물 임상시험에 대한 규모를 축소 및 최종적으로는 타 시험법으로 완전히 대체하고자 하는 점진적 규제가 진행되는 중이기 때문에 오가노이드는 동물 임상시험 규제에 따른 가장 적합한 대체법 시험물로 잠재적 가능성이 있습니다. 또한, 당사의 오가노이드 기술은 어떠한 세포로도 분화가 가능한 유도만능줄기세포(iPSC) 기반으로 적응 분야를 확대하고 있으며, 현재 모발 오가노이드를 활용한 연구개발도 진행 중에 있습니다. 이에 당사는 오가노이드 R&D 비용으로 2028년까지 6,784백만원의 연구개발비 지출이 필요할 것으로 생각하고 있으며, 이는 2023년 증자 잔액 450백만원과 금번 조달 자금 중 6,340백만원으로 사용할 예정입니다.
| [오가노이드 연구개발 비용 상세 내역] |
| (단위:백만원) |
| 구성 | 2023년 증자 잔액 (2025.03.31 기준) |
2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고 |
|---|---|---|---|---|---|---|---|
| 원재료 구입 | 450 | 350 | 600 | 1,200 | 1,800 | 3,950 | -오가노이드 연구용 원재료 구입 -오가노이드 연구개발 인력 증원 반영 -27년부터 임상 시작 목표로 임상 관련 인허가/약물감시 등 반영 |
| 인건비 | 250 | 389 | 537 | 623 | 1,799 | ||
| 인허가 | - | - | 134 | 96 | 230 | ||
| 약물감시 | - | - | 200 | 144 | 345 | ||
| 기타 임상진행비 | - | - | 267 | 193 | 460 | ||
| 합계 | 450 | 600 | 989 | 2,338 | 2,856 | 6,784 | - |
| 출처) 당사 제시 |
상기 오가노이드 연구개발 비용 자금 계획 시 각 항목별 아래와 같은 비용을 포함하여 산정하였습니다.
| 구분 | 항목 | 내용 |
| 오가노이드 연구개발 |
원재료 구입 | 오가노이드 연구개발을 위한 모낭 오가노이드, iPSC 등의 원재료 구입 비용이 포함되어 있습니다. GMP 오가노이드 공정개발과 관련한 특성분석시험법 및 단계별 제조공정개발비용, scale-up 공정개발비용 등이 포함되어 있습니다. |
| 인건비 | 오가노이드 연구 개발 기존 인력의 인건비, 추가 인력 증원 반영한 인건비가 포함되어 있습니다. | |
| 인허가 | 2027년 임상 1상 목표로 임상 관련 인허가에 필요한 비용으로 임상에 필요한 각종 인허가비용과 등록비용 그리고 담당인력의 인건비 등이 포함되어 있습니다. | |
| 약물감시 | 2027년 임상 1상 목표로 임상 관련 약물감시에 필요한 비용으로 임상에 투여하는 약물에 대한 모니터링 비용, 장기추적조사 연차보고 및 안전성 관련 자문비용, 담당인력의 인건비 등이 포함되어 있습니다. | |
| 기타 임상진행비 | 2027년 임상 1상 목표로 임상과 관련된 논문 및 학회발표, 통계자문 비용, 담당인력의 인건비가 포함되어 있습니다. |
(2)-3 시설자금 (GMP 시설투자)
금번 유상증자로 조달된 자금 중 4,010백만원을 활용하여 GMP 시설 투자에 사용할 예정입니다. 당사가 추진 중인 일본재생의료 사업 및 국내 첨단재생바이오법 개정안에 따른 사업 성장 시 2026년부터 신규시설 투자하여 생산 CAPA를 확대하고, 한편으로는 장비 노후화에 따라 2028년부터 기존 시설 개보수 투자를 진행하고자 합니다. 시설투자에 따른 자금사용의 상세 내역은 아래와 같습니다.
| [GMP 시설투자에 따른 세부 자금 사용 계획] | |
| (단위:백만원) | |
| 우선 순위 |
구분 | 구성 | 2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고사항 | |
|---|---|---|---|---|---|---|---|---|---|
| 2 | 일본재생의료/첨생법 | 신규시설투자 | - 2026년 이후 해당 사업 성장 시 사용 예정 - 제조실4 확장을 통한 재생의료 사업지원 - 생산 CAPA 20lot/월 ->최대 100lot/월 증가 : 제조 배양기 15대등 1090백만원 : 실험 유세포분석기등 1040백만원 |
||||||
| 건물 | - | - | - | - | - | ||||
| 연구기자재 | - |
2,277 | - | - | 2,277 | ||||
| 비품 | - | - | - | - | - | ||||
| 시설장치 | - | 60 | - | - | 60 | ||||
| 기타 | 200 | 200 | |||||||
| 소계 | - | 2,537 | - | - | 2,337 | - | |||
| 장비노후화에 따른 교체 투자 | 기존 시설 개보수 | - 배양기 노후화에 따른 교체투자 (수명주기 10년 도래) - 19년 설비투자된 약 50여대 대체액 반영 |
|||||||
| 건물 | - | - | - | - | - | ||||
| 연구기자재 | - | - | 1,300 | 1,300 | |||||
| 비품 | - | - | - | - | - | ||||
| 시설장치 | - | - | - | - | - | ||||
| 기타 | - | - | - | 173 | 173 | ||||
| 소계 | - | - | - | 1,473 | 1,473 | - | |||
| 합 계 | - | 2,537 | - | 1,473 | 4,010 | - | |||
| 출처) 당사 제시 |
상기 GMP 시설투자 자금 계획 시 각 항목별 아래와 같은 비용을 포함하여 산정하였습니다.
| 구분 | 항목 | 내용 |
| 일본재생의료/국내첨생법 진출에 따른 신규시설투자 | 연구기자재 | 제조실 4 확장을 위한 제조 배양기, 실험용 유세포 분석기 등의 신규 구입 비용 등이 포함되어 있습니다. |
| 시설장치 | ||
| 기타 | 신규 배양기, 유세포 분석기 구입에 따른 설치, 교정 비용 등 기타 비용이 포함되었습니다. | |
| 장비노후화에 따른 기존 시설 개보수 | 연구기자재 | GMP생산 설비 중 수명주기가 도래한 배양기(약 50여대) 교체를 위한 배양기 구입 비용 등이 포함되어 있습니다. |
| 기타 | 배양기 교체에 따른 설치, 교정 비용 등 기타 비용이 포함되었습니다. |
당사 GMP 생산시설의 2024년 기준 줄기세포 배양액 가동률은 47.5%, 세포배양배지 가동률은 약 21~24% 수준이며, 2025년 1분기 기준 줄기세포 배양액 가동률은 64.3%, 세포배양배지 가동률는 0.0%입니다.
| [GMP 생산시설 가동률 추이] |
| 품 목 | 구 분 | 2025년 1분기 | 2024년 | 2023년 | 2022년 | 2021년 |
|---|---|---|---|---|---|---|
|
줄기세포 배양액(주1) (단위: ℓ) |
생산능력 | 600 | 2,400 | 2,400 | 2,400 | 2,400 |
| 생산실적 | 386 | 1,140 | 855 | 188 | 191 | |
| 가 동 률 | 64.3% | 47.5% | 35.6% | 7.8% | 8.0% | |
|
세포배양 배지(주2) (단위: 개) |
생산능력 | 1,500 | 6,000 | 6,000 | 6,000 | 6,000 |
| 생산실적 | 0 | 1,469 | 3,242 | 1,871 | 2,240 | |
| 가 동 률 | 0.0% | 24.5% | 54.0% | 31.2% | 37.3% | |
| 세포배양 배지(주3) (단위: 개) |
생산능력 | 600 | 1,800 | - | - | - |
| 생산실적 | 0 | 379 | - | - | - | |
| 가 동 률 | 0.0% | 21.1% | - | - | - |
| 출처) | 당사 정기보고서 |
| (주1) | 월 200ℓ생산 가능합니다. |
| (주2) | 월 500개 생산 가능합니다. |
| (주3) | 월 200개 생산 가능합니다. |
| (주4) | 2024년 기존 생산 설비를 활용하여 줄기세포 배양 배지(StemVie XF Supplments 제품)를 신규 생산하게 됨에 따라 추가된 내용입니다. |
당사는 현재 당사의 GMP 공장에서 제대혈 유래 줄기세포 배양액, 줄기세포 배양 배지 등을 직접 생산하여 줄기세포 치료제를 제조하여 당사의 주요 파이프라인의 전임상시험 및 임상시험에 사용하고 있습니다. GMP 시설 내에 줄기세포 배양액과 줄기세포 배양 배지 생산을 위한 구획을 구분하여 생산 라인이 가동되어야 하며, 해당 구역들은 당사의 임상 약물 기본 생산 라인이기 때문에 이는 가동률이 낮아도 유지를 해야 하는 구획입니다. 현재 GMP 생산 시설의 가동률이 낮은 편이지만, 상기한 바와 같이 가동률과 별개로 당사 주요 파이프라인의 임상 시험 및 신약개발을 위해 점유되는 구획이 존재하여, 이에 나머지 구역을 개조하여 국내외 재생의료사업 진출을 위한 시설 확충이 필요한 상황입니다.
당사가 금번 GMP시설투자에 사용 예정인 비용은 국내외 재생의료사업을 위한 시설 확충 용도 및 기존시설 노후화에 따른 신규 장비 매입 비용입니다. 현재 당사의 주력 생산시설은 동종줄기세포 생산에 초점이 맞춰져 있으므로 일본 재생의료 사업을 위한 2종(자가지방줄기세포)의 대량 생산설비 구축이 추가로 필요합니다. 2025년은 현재 생산라인을 활용하여 2종(자가지방줄기세포)의 생산량이 가능할 것으로 보이나, 공급이 본격적으로 증가할 것으로 예상되는 2026년부터는 별도 추가 설비 구축을 통해 생산 CAPA를 증설하는 것이 불가피할 것으로 예상되어 금번 자금 사용 목적에 시설투자를 포함하였습니다.
(3) 기타운영경비 (GMP 및 본사 경비)
금번 유상증자로 조달된 자금 중 연구소와 치료제 및 임상약물제조를 담당하는 GMP의 시설관리에 사용되는 전력비, 수수료 등 실험약물제조경비로 약 7,830백만원이 소요될 예정입니다. 이는 GMP 생산, 운영, 본사 운영과 관련하여 직간접적으로 필요한 비용으로 월 평균 250~300백만원 수준으로 집행할 예정입니다.
| [기타운영경비(GMP 및 본사 경비) 비용 상세 내역] |
|
| (단위:백만원) | |
| 구성 | 2025년 하반기 |
2026년 | 2027년 | 2028년 | 합계 | 비고 |
|---|---|---|---|---|---|---|
| 지급수수료 | - | - | 1,720 | 1,806 | 3,526 | - GMP 및 본사 경비: 전력비, 수수료, GMP 실험약물제조를 위한 경비 등 - GMP생산,운영, 본사 운용과 관련한 직간접적으로 필요한 경비 등 |
| 연구기자재와 시설장치 운영비 | - | 504 | 529 | 556 | 1,589 | |
| 수선소모품비 | - | - | 529 | 556 | 1,085 | |
| 세금과공과 | - | - | 132 | 139 | 271 | |
| 관리비 | - | - | 662 | 694 | 1,356 | |
| 합계 | - | 504 | 3,572 | 3,751 | 7,827 | - |
| 출처) 당사 제시 |
(4) 채무상환자금
금번 유상증자로 조달된 자금 중 1,400백만원을 활용하여 부채비율 개선, 금융비용 절감을 위해 시설자금 차입금을 상환할 예정입니다. 당사는 2017년 GMP 시설 및 연구소 취득을 위해 중소기업시설자금을 차입하였으며, 금번 유상자금으로 매반기 200백만씩 분할 상환 중인 해당 차입금 총 1,400백만원을 2028년까지 상환할 예정입니다. 금번 유상증자 자금조달로 차입금 일부를 상환함으로써 이자비용을 절감하고 재무구조 건전성을 확보하고자 합니다. 자금사용의 상세 내역은 아래와 같습니다.
| [상환 예정인 차입금 상세 현황] | |
| (기준일: 2025.06.23) |
(단위: 백만원) |
| 차입처 | 내역 | 최초 대여일 | 만기일 | 이자율 | 잔액 | 상환예정금액 | 상환예정시기 |
|---|---|---|---|---|---|---|---|
| 기업은행 | 중소기업시설자금 | 2017.06.08 | 2032.06.08 | 4.95% | 2,800 | 200 | 2025년 하반기 |
| 2017.06.08 | 2032.06.08 | 4.95% | 2,600 | 400 | 2026년 | ||
| 2017.06.08 | 2032.06.08 | 4.95% | 2,200 | 400 | 2027년 | ||
| 2017.06.08 | 2032.06.08 | 4.95% | 1,800 | 400 | 2028년 | ||
| 합 계 | 1,400 | 1,400 | |||||
| 출처) 당사 제시 |
다. 자금이 계획대로 조달되지 않을 경우의 대응 방안
금번 주주배정 후 실권주 일반공모의 경우 확정발행가액 결정에 따라 최종 조달자금의 변동될 수 있습니다. 자금 사용계획에 대한 우선순위는 상기 기재한 바와 같으며, 금번 주주배정 후 실권주 일반공모를 진행하는 동안 주가 하락에 의하여 유입되는 자금이 감소할 경우 당사의 대응 방안은 다음과 같습니다.
가) 채무상환자금 및 기타운영자금 사용 계획 조정
금번 공모자금이 당사 예상 대비 감소할 경우, 기존 GMP 시설 취득을 목적의 차입금에 대해 만기 연장 모색 또는 회사 보유자금으로 상환할 예정입니다. 또한, 기타운영자금을 절감할 방안을 모색하며, 부족분에 대해서는 자체 보유 자금, 외부 차입 등으로 충당하여 사용 계획을 조정할 예정입니다.
나) 연구개발자금 계획 조정
당사는 효율적인 자금 운용과 연구개발 활동의 최적화를 위해 현재 계획된 다양한 연구 및 사업 진출 중에서 우선 순위를 세밀하게 조정할 예정입니다. 따라서 금번 공모자금이 당사 예상 대비 줄어들 경우, 당사는 골관절염 치료제(OSCA)의 임상연구 프로젝트를 최우선적으로 진행하여 해외 라이센스 아웃을 추진할 예정입니다. 한편, 당사는 계획 중인 일본 재생의료 진출, 국내 첨단재생의료 준비, 오가노이드 연구개발에 대한 우선 순위를 재평가하여, 비용을 절감할 방안을 모색할 예정입니다. 이러한 전략적 조정을 통해, 당사는 제한된 자금을 가장 중요한 연구개발 활동에 효과적으로 할당하고, 장기적으로 회사의 핵심 가치와 성장 잠재력을 높일 수 있을 것으로 기대합니다.
라. 유상증자 진행 배경
당사가 영위하는 신약 개발업은 지속적인 연구개발 비용이 소요되며, 경쟁력 확보를 위해서는 높은 기술력의 파이프라인 확보를 위한 투자가 필수적입니다. 특히, 당사의 주요 파이프라인이 속해있는 아토피 치료제, 골관절염 치료제 등의 분야는 잠재적인 시장 규모가 거대한 만큼, 글로벌 시장에서 치열한 경쟁이 전개되고 있습니다. 이에 따라 당사는 금번 유상증자를 통해 기존 파이프라인의 임상 개발을 더욱 빠르게 추진하여 기술력을 확보하고자 합니다. 동시에, 선제적 투자를 통해 기타 매출처를 확대하고, 자본 건전성을 제고하여 향후 글로벌 시장 내에서 경쟁력을 보유하기 위한 발판을 마련하고자 합니다.
(1) 핵심 파이프라인인 골관절염 치료제(OSCA)의 임상 가속화
당사의 골관절염 치료제(OSCA)는 1상에서 염증 완화 및 연골 재생에서 뛰어난 효과를 입증해내며 2024년 11월 유영제약과 라이센스 아웃 계약을 체결하였습니다. 이후, 세계골관절염학회(OASRI) 등 여러 국제학회에서 성공적인 1상 결과를 발표하며 근본적인 골관절염 치료제(DMOAD)로서의 잠재력을 보여주었습니다. 이로 인해 현재 여러 글로벌 제약사들로부터 OSCA의 기술력에 대한 관심을 받고 있는 상황입니다. 이러한 레퍼런스를 바탕으로 임상 규모를 확대하여 국내 임상 2a상 진행 및 해외임상 등 추가 임상을 진행하여 글로벌 라이센스 아웃을 위한 임상 전략을 수립하는데 있어 최적의 시기로 판단하였습니다.
이러한 핵심 파이프라인의 임상시험은 대규모 자금이 소요되나, 자체 임상 데이터 확보를 통해 신약의 가치를 최대한 높이고, 향후 글로벌 기술이전 시 유리한 협상 위치를 확보하며 파트너사 선택의 폭을 넓히기 위한 필수적인 과정입니다. 당사는 2023년 주주배정 후 실권주 일반공모 유상증자룰 통해 OSCA 임상시험비 약 43.8억원을 확보하였으며 잔액으로 약 37.5억원을 보유 중입니다. 2023년 증자 당시에는 OSCA의 국내임상 1/2a상 및 장기추적조사만을 계획하였지만 현재 당사가 국내 2a 임상 규모 확대 및 해외임상까지 범위를 확대한만큼 2028년까지 예상되는 총 비용은 약 238.5억원으로 증가하였습니다. 이에 따라 기존에 OSCA 임상을 위해 확보한 자금은 현재의 임상 계획을 진행하기에 부족한 수준이며, 추가 재원 확보를 위해 증자를 통한 자금조달을 계획하게 되었습니다. 금번 조달 자금은 이러한 핵심 파이프라인의 임상시험을 계획대로 신속하게 진행하고, 조기에 의미 있는 결과를 도출하여 기업가치를 극대화하는 데 사용될 것입니다.
(2) 줄기세포 치료제의 일본 및 국내(첨생법) 재생의료사업 진출 추진
당사는 안정적인 수익 기반을 확보하기 위해 일본 재생의료 시장 및 국내(첨생법) 재생의료 사업 진출을 계획하고 있습니다. 일본 재생의료시장 진출을 위해 2024년 일본 후생노동성에 제1종(동종제대혈줄기세포) 및 제2종(자가지방줄기세포) 재생의료 제공계획에 대한 심의 및 승인 절차를 진행하였습니다. 제2종(자가지방줄기세포)의 경우, 2025년 2월 후생노동성 최종 승인까지 완료되어 2025년 하반기부터 일본 내 환자 투여를 계획하고 있습니다. 이에 금번 조달 자금의 일부는 일본 현지 환자 수급을 위한 본격적인 영업활동 및 투자를 진행을 위한 운영자금으로 활용될 예정입니다.
한편, 국내 첨단재생바이오법 개정안 시행에 따라 첨단재생의료 임상연구 및 첨단재생의료 치료 제도를 통해 희귀/난치 질환자가 당사의 줄기세포치료제를 조기에 사용할 수 있도록 치료 기회를 확대할 계획을 가지고 있습니다. 당사 주요 파이프라인 치료제의 대상 적응증인 중증아토피와 골관절염은 난치질환에 해당합니다. 금번 조달 자금의 일부는 국내 협력기관과의 협업을 통한 2025년 재생의료 임상연구 계약 개시 및 2026년 임상연구 계획 제출 및 임상연구 시작 등에 활용될 예정이며, 이는 당사의 아토피 피부염 치료제(퓨어스템-에이디 주)와 골관절염 치료제(OSCA) 등의 임상연구데이터를 확보하고 치료제 조기 공급을 통한 수익화 기회 확대의 토대를 마련해 줄 것 입니다.
(3) 기타 파이프라인 연구개발 투자 및 지속 가능한 성장 기반 마련
당사는 기타 파이프라인 중 하나로 오가노이드를 연구개발 중에 있습니다. 특히 당사의 피부 오가노이드 기술의 경우, 공기-액체 계면(ALI) 배양을 통해 불필요한 연골 조직의 형성을 억제하여 실제 피부와 같은 평평한 구조를 완벽 재현하여 다양한 유효물질에 대한 약물 스크리닝 및 효력평가 등에 적용 가능하여, 일부 대형 글로벌 제약사들로부터 관심을 받고 있는 상황입니다. 이러한 파이프라인들의 포트폴리오를 지속적으로 확장하기 위해서는 선제적이고 적극적인 연구개발 투자가 필수적입니다. 이는 단기적인 성과뿐만 아니라 중장기적인 기업 성장의 발판을 마련하는 데 중요한 역할을 할 것입니다.
(4) 실권주 일반공모를 통한 투자자 참여 기회 확대
당사는 주주배정 후 실권주 일반공모 방식을 채택함으로써 기존 주주의 권리를 보호하는 동시에 신규 투자자들에게도 투자 기회를 제공하고자 합니다. 이를 통해 기존 주주들의 지분희석화를 최소화함과 동시에 실권주 일반공모를 통해 다양한 투자자층을 확보하고 기업의 지속 가능한 성장을 위한 기반을 마련할 것입니다.
상기한 바와 같이, 당사는 금번 유상증자를 통해 조달되는 자금을 핵심 파이프라인의 경쟁력 강화, 재생의료 시장 진출 및 추가 성장 동력 확보라는 명확한 목표 하에 투명하고 효율적으로 사용할 계획입니다. 이를 통해 기업가치를 지속적으로 증대시키고, 궁극적으로 주주분들의 이익을 극대화하기 위한 최선의 노력을 다할 것입니다.
당사는 금번 유상증자로 인해 기존 주주들의 지분이 희석될 수 있음을 충분히 인지하고 있으며, 이사회결의시 조달규모 등 정량적인 조건뿐만 아니라, 유상증자의 당위성과 소액주주 등의 유상증자 이해 고려, 주주보호(소통) 방안 등 정성적인 기준도 감안하여 본 유상증자의 목적과 필요성을 논의하였습니다. 당사는 금번 유상증자 자금조달 방안 이외에 다음과 같은 조달 방안들도 함께 검토하였습니다.
1) 회사채 발행
당사는 증권신고서 제출일 현재 공모 회사채 발행을 위한 적격 신용평가기관의 신용등급은 존재하지 않은 상태입니다. 신용평가기관의 등급 평가 방식으로는 정량적 평가(재무분석 : 수익성, 재무건정성, 현금흐름, 성장성 등) 및 정성적 평가(산업전망, 경쟁력, 경영진의 역량, 정부규제 등)과 함께 계량 모델 및 비교분석을 통해 진행되고 있습니다. 이후 신용등급이 확정되어 투자적격 등급 이상(BBB- 이상)의 등급으로 구분될 시 회사채 금융시장에서의 원활한 자금조달이 가능할 것으로 예상한 바, 당사는 공모 회사채 발행을 통한 자금조달은 현재 어려울 것으로 판단하였습니다. 또한, 사모 회사채 발행도 검토하였으나 높은 금리, 짧은 만기, 담보 및 지급보증 요구 등으로 인해 재무적 부담이 과도할 수 있다는 판단하에 실제 발행으로 이어지지 못하였습니다.
2) 주식 관련 사채 발행
주식 관련 사채로는 주식으로 전환될 수 있는 전환사채, 신주인수권 권리를 보유하고 있는 신주인수권부사채, 특정 주식으로 교환할 수 있는 교환사채 등이 존재합니다. 당사는 주식 관련 사채 또한 자금조달의 방안 중 하나로 고려하였으나, 회사의 재무 여건 등을 고려할 때 투자자 모집에 어려움이 있어 선택할 수 없었습니다.
3) 담보 제공을 통한 추가 차입
2025년 1분기 기준 당사 유형자산 중 담보력이 존재한다고 생각되는 토지 및 건물의 총 장부 금액은 약 12,025백만원입니다. 이 중 당사는 토지 및 건물(장부금액 약 11,418백만원)에 대해 8,796백만원 담보 설정하여 6,710백만원을 이미 차입하고 있습니다. 당사는 복수의 금융기관을 통해 현 담보물을 통한 추가 차입 가능 여부를 사전 검토하였으나, 추가 차입 가능성이 매우 낮은 것으로 확인하여 담보 제공을 통한 추가 차입 조달을 선택할 수 없었습니다.
| [2025년 1분기말 유형자산 상세 현황] |
| (단위: 천원) |
| 구 분 | 취득금액 | 감가상각누계액 | 정부보조금 | 장부금액 |
|---|---|---|---|---|
| 토지 | 3,927,206 | - | - | 3,927,206 |
| 건물 | 9,241,382 | (1,143,426) | - | 8,097,956 |
| 시설장치 | 7,998,885 | (3,919,893) | - | 4,078,992 |
| 연구시험용자산 | 7,968,351 | (7,194,122) | (29,906) | 744,323 |
| 비품 | 412,784 | (380,371) | - | 32,413 |
| 합 계 | 29,548,608 | (12,637,812) | (29,906) | 16,880,890 |
| 출처) 당사 정기보고서 |
| [2025년 1분기말 유형자산 담보제공 내역] |
| (단위: 천원) |
| 담보제공자산 | 장부금액 | 담보설정금액 | 담보감정가격 | 관련 계정과목 | 차입금액 | 담보권자 |
|---|---|---|---|---|---|---|
| 토지 | 3,660,774 | 8,796,000 | 11,028,000 | 차입금 | 6,710,000 | 기업은행 |
| 건물 | 7,758,009 |
| 출처) 당사 정기보고서 |
| 주1) 담보제공자산인 토지 및 건물은 글로벌R&D센터줄기세포재생의학연구소(서울 금천구 소재)와 줄기세포GMP센터(경기도 광명시 소재)입니다. |
| 주2) 담보감정가격의 감정일은 2021년입니다. |
또한, 상기 회사채 및 주식 관련 사채 발행과 담보제공을 통한 추가 차입방안의 경우, 금융비용(이자비용) 부담과 함께 수익성 악화가 이루어질 수 있고 부채총계 증가에 따라 재무안정성에 악영향을 줄 수 있는 점 또한 선택되지 않은 사유로 고려되었습니다. 지속적인 영업손실 및 당기순손실에 기인한 당사의 열위한 재무안정성을 고려하였을 때, 유상증자를 통해 자본을 확충하는 경우 차입금 및 부채비율을 보다 안정적으로 관리하여 건실한 재무안정성을 기대할 수 있으며, 추가적인 금융비용 발생을 방지하여 재무적 부담을 완화시킬 수 있을 것이라 판단하였습니다.
이러한 일련의 자금조달 방안 검토 과정을 거쳐, 이사회는 기존 주주에게 신주인수권을 우선적으로 부여하고, 실권주 발생 시 일반 투자자에게도 참여 기회를 제공할 수 있는 주주배정 후 실권주 일반공모 방식의 유상증자를 추진하는 것이 주주 권익 보호와 자금조달 안정성 확보 측면에서 가장 적절하다는 판단에 이르게 되었으며, 이에 대표주관회사와 인수회사의 잔액인수를 조건으로 한 주주배정 후 실권주 일반공모 방식의 유상증자를 최종적으로 결의하였습니다.
마. 주주 권익 보호를 위한 사항
당사는 금번 유상증자로 인해 주주들의 지분이 다소 희석될 수 있음을 충분히 인지하고 있으며, 이에 따라 유상증자 이후의 명확한 비전 제시 등을 통해 지속적으로 주주 소통을 강화할 예정입니다. 금번 유상증자 납입대금을 전략적으로 사용하여 회사의 경쟁력을 강화할 예정이며 이를 통해 기업 가치 상승을 유도하여 중장기적으로 주주 가치를 극대화하도록 노력할 예정입니다.
1) 주주와의 소통 강화 방안
당사는 주주 대상으로 적극적인 IR 활동을 통해 주주 신뢰를 제고하기 위해 노력할 계획입니다. 또한, 당사는 2025년 06월 10일 증권신고서 공시 직후, 금번 주주배정 유상증자 결정과 관련된 주요 내용을 주주들에게 설명하기 위하여 당사 홈페이지 주주 서한을 게재하였습니다.
![이미지: [주주서한]](%EC%A3%BC%EC%A3%BC%EC%84%9C%ED%95%9C.jpg) |
|
[주주서한] |
가) IR자료 및 보도자료 배포를 통한 회사에 대한 이해도 증진
당사는 소액주주의 정보 접근성을 높이고 소통을 활성화하여 주주 권익을 보호하고자 합니다. 구체적으로 당사는 추후 당사 홈페이지에 IR 자료를 즉시 게재하여 주주들이 관련 내용을 신속하게 확인할 수 있도록 할 예정입니다. 더불어, 당사는 유상증자와 관련된 전반적인 내용을 다양한 이해관계자들이 확인할 수 있도록 보도자료를 배포할 예정입니다. 이를 통해 개인, 기관, 외국인 투자자 등 다양한 이해관계자들에게 언론을 통해 당사의 비전과 전략을 정확히 전달할 수 있도록 노력할 계획입니다.
나) 투자설명회(IR) 개최
당사는 공모 유상증자 기간 중 오프라인 투자설명회(IR)를 개최하여 질의응답 세션을 운영하여 당사의 경영전략에 대해 충분히 이해할 수 있도록 진행할 계획입니다. 특히, 당사는 금번 유상증자의 목적 및 회사의 향후 성장 전략 등에 대해 주주분들에게 상세히 설명드리고 의견을 경청하기 위해 증권신고서 공시 익일인 2025년 06월 11일에 첫 번째 투자설명회(IR)를 개최하였습니다. 간담회의 구체적인 시간 및 장소, 참여 방법 등은 2025년 6월 10일 증권신고서 공시 직후 당사 홈페이지 및 공시를 통해 안내하였습니다.
또한, 추가적으로 주주분들의 수요를 조사하여 수도권 외에 지방거점에서도 투자설명회를 개최할 계획이 있습니다. 이를 통해 당사의 파이프라인 임상 현황, 기술이전 현황, 향후 비전 등을 상세히 설명하고 질의응답 시간을 통해 주주분들의 궁금증을 해소하겠습니다.
다) IR응대 전용 라인 강화를 통한 소통 강화
당사는 보다 적극적인 투자자 의사 소통 강화를 위해, 기존에 있는 IR응대 전용 라인을 강화할 계획입니다. IR 응대 전용 이메일 및 유선을 통해 유상증자와 관련한 문의에 신속하고 누락 없이 응대할 수 있도록 하겠습니다. 특히, 소액주주를 포함한 다양한 주주의 의견을 수렴할 수 있도록 당사와 사전 일정 조율 등을 신청한 소액주주에 대해서는 개별적인 대면 미팅 또는 유선 의견청취를 적극 활용하여 실시간 소통을 강화하겠습니다.
2) 주요 기관투자자 대상 IR 진행
주요 기관투자자 대상으로 IR을 진행하여 유상증자의 배경, 목적, 기대 효과와 당사의 중장기 사업전략 등에 대해 상세히 설명을 진행할 예정이며, 증권사 애널리스트 대상으로도 적극적으로 소통하여, 시장 내에 충분한 정보가 전달될 수 있도록 노력할 계획입니다.
당사는 상기와 같이 주주 및 시장과의 적극적인 소통을 통해 회사의 경영 전략 및 본 유상증자의 배경과 필요성을 명확히 전달하는 한편, 본 유상증자와 관련 후속 정보를 지속적으로 제공해 나가겠습니다.
바. 미사용 자금의 운용 계획
당사가 금번 유상증자를 통해 조달한 자금 중 일부 자금은 조달시기와 사용시기가 다소 차이가 생길 수 있습니다. 이에 조달로부터 사용 시까지 미사용 자금에 대해서는 자금 사용시점 및 금리에 따라 적격금융기관의 수시입출금 예금, 정기예금 등 금융상품 또는 A등급 이상의 단기금융상품으로 운용할 예정입니다.
VI. 그 밖에 투자자보호를 위해 필요한 사항
해당사항 없습니다.
제2부 발행인에 관한 사항
I. 회사의 개요
1. 회사의 개요
가. 연결대상 종속회사 개황
1) 연결대상 종속회사 현황(요약)
| (단위 : 사) |
| 구분 | 연결대상회사수 | 주요 종속회사수 |
|||
|---|---|---|---|---|---|
| 기초 | 증가 | 감소 | 기말 | ||
| 상장 | - | - | - | - | - |
| 비상장 | - | - | - | - | - |
| 합계 | - | - | - | - | - |
| ※상세 현황은 '상세표-1. 연결대상 종속회사 현황(상세)' 참조 |
2) 연결대상회사의 변동내용
| 구 분 | 자회사 | 사 유 |
|---|---|---|
| 신규 연결 |
- | - |
| - | - | |
| 연결 제외 |
- | - |
| - | - |
나. 회사의 법적·상업적 명칭
당사의 명칭은 주식회사 강스템바이오텍이고, 영문명은 KANGSTEM BIOTECH CO., LTD. 입니다.
다. 설립일자
당사는 2010년 10월 29일에 줄기세포치료제의 개발, 제조 및 공급 등의 사업 영위를
목적으로 설립되었으며, 2015년 12월 21일 코스닥시장에 주식을 상장하여 매매를
개시하였습니다.
라. 본사의 주소, 전화번호 및 홈페이지
| 주 소 | 서울특별시 강남구 테헤란로 522 홍우빌딩 9층 |
| 전화번호 | 02-888-1590 |
| 홈페이지 | www.kangstem.com |
마. 회사사업 영위의 근거가 되는 법률
당사의 줄기세포치료제 사업 영위의 근거가 되는 법률은 '약사법' 및 '동법 시행령', '의약품 등의 안전에 관한 규칙', '첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률' 등 입니다.
바. 중소기업 등 해당 여부
1) 당사는 중소기업기본법 제2조 및 중소기업기본법 시행령 제3조에 의거 중소기업에 해당합니다.
| 중소기업 해당 여부 | 해당 | |
| 벤처기업 해당 여부 | 해당 | |
| 중견기업 해당 여부 | 미해당 | |
2) 당사는 벤처기업육성에 관한 특별조치법 제25조에 의거, 벤처기업에 해당합니다.
| 인증기관 | 확인유형 | 유효기간 | 발행번호 |
| 신용보증기금 | 연구개발기업 | 2023.02.25~2026.02.24 | 제20230329020028호 |
사. 주요 사업의 내용
당사는 줄기세포치료제의 개발 및 제조를 전문으로 하는 바이오 제약사이며, 영위
하는 목적사업은 다음과 같습니다.
| 목적사업 | 비 고 |
|
1. 세포치료제 개발, 제조, 판매업 2. 의약품 및 의약외품 개발, 제조, 판매업 3. 세포 가공 및 배양 용역업 4. 세포 보관 및 공급업 5. 화장품 제조, 판매 및 수출입업 6. 화장품 원료 제조, 판매 및 수출입업 7. 연구용역사업 8. 제대혈 및 줄기세포 관련 사업 9. 국내외 헬스케어 관련 사업 10. 생명과학과 관련된 컨설팅업 11. 의료기기 제조업, 도·소매업, 수출입업 12. 임신, 출산 및 육아관련 제조업, 도·소매업, 수출입업 13. 전자상거래, 통신판매업 및 이와 관련된 부대사업 일체 14. 부동산 개발, 공급 및 임대업 15. 보험대리업 16. 건강기능식품 제조, 판매 및 수출입업 17. 일반 제품 및 상품 유통업 18. 기타 위에 부대되는 사업 일체 |
- |
※ 상세한 내용은 동 공시서류의 "Ⅱ. 사업의 내용"을 참조하시기 바랍니다.
아. 신용평가에 관한 사항
| 평가일 | 신용평가전문기관명 | 신용등급 | 비고 |
|---|---|---|---|
| 2024년 6월 3일 | SCI 평가정보(주) | bb- | 신용도에는 문제가 없으나, 장래 시장환경 변화에 대한 안정성 면에서 불안한 요소가 있음 |
| 2024년 6월 4일 | 한국평가데이터(주) | bb | - |
* 등급체계 및 정의_SCI 기준
| 기술신용등급 | 정의 |
| AAA | 기술사업의 부실화 가능성이 매우 낮고, 기술경쟁력과 기술사업화 역량을 반영한 기술신용상태가 최고 우량한 수준임. |
| AA | 기술사업의 부실화 가능성이 낮고, 기술경쟁력과 기술사업화 역량을 반영한 기술신용상태가 매우 우량한 수준임 |
| A | 기술사업의 부실화 가능성이 낮고, 기술경쟁력과 기술사업화 역량을 반영한 기술신용상태가 우량한 수준임. |
| BBB | 기술사업의 부실화 가능성이 낮으나, 장래의 시장환경변화에 따라 영향을 받을 가능성이 있음 |
| BB | 기술사업의 부실화 가능성이 낮으나, 장래의 시장환경변화에 따라 안정성 면에서 상당한 변화 요소가 있음 |
| B | 기술사업의 부실화 가능성이 낮으나, 장래의 시장환경변화에 따라 안정성 면에서 불안한 요소가 있음 |
| CCC | 기술사업의 부실화 가능성이 존재함 |
| CC | 기술사업의 부실화 가능성이 높음 |
| C | 기술사업의 부실화 가능성이 매우 높음 |
| D | 현재 채무불이행 상태에 있음 |
| 신용등급 | 정의 |
| aaa | 전반적인 신용도가 매우 우수하며, 장래 환경변화에 대한 안정성이 매우 높은 수준임 |
| aa | 전반적인 신용도가 우수하며, 장래 환경변화에 대한 안정성이 높은 수준임 |
| a | 전반적인 신용도가 우수하나, 장래 환경변화에 대한 안정성이 상위 등급보다는 열위한 수준임 |
| bbb | 전반적인 신용도가 양호한 수준이나, 장래 환경변화에 대한 안정성 면에서 다소 불안한 요소가 있음 |
| bb | 신용도에는 문제가 없으나, 장래 환경변화에 대한 안정성 면에서 불안한 요소가 있음. |
| b | 단기적인 신용도에 문제가 없으나, 환경경변화에 대한 안정성은 낮은 편임 |
| ccc | 신용도가 의문시 되며, 채무불이행 가능성이 있음 |
| cc | 신용상의 위험요소가 많아 채무불이행 가능성이 높음 |
| c | 채무불이행 가능성이 매우 높으며, 신용상태가 불량함 |
| d | 채무불이행 상태임 |
자. 회사의 주권상장(또는 등록ㆍ지정) 및 특례상장에 관한 사항
| 주권상장 (또는 등록ㆍ지정)현황 |
주권상장 (또는 등록ㆍ지정)일자 |
특례상장 유형 |
|---|---|---|
| 코스닥시장 상장 | 2015년 12월 21일 | 기술성장기업의 코스닥시장 상장 |
2. 회사의 연혁
가. 회사의 본점소재지 및 그 변경
| 일 자 | 내 용 | 주 소 |
| 2015년 06월 | 본점이전 | 서울특별시 관악구 관악로 1, 서울대학교 수의과대학 생명공학 연구동 제81동 2층 |
| 2016년 09월 | 본점이전 | 서울특별시 강남구 테헤란로 512 신안빌딩 17층 |
| 2024년 12월 | 본점이전 | 서울특별시 강남구 테헤란로 522 홍우빌딩 9층 |
나. 경영진 및 감사의 중요한 변동
| 변동일자 | 주총종류 | 선임 | 임기만료 또는 해임 |
|
|---|---|---|---|---|
| 신규 | 재선임 | |||
| 2022년 03월 24일 | 정기주총 | - | 기타비상무이사 이상균 기타비상무이사 박용호 |
- |
| 2023년 03월 23일 | 정기주총 | - | 기타비상무이사 최정호 | - |
| 2024년 03월 21일 | 정기주총 | 사내이사 김원균 감사 김재홍 |
사내이사/대표이사 나종천 | 사내이사 배요한 감사 임승원 |
| 2025년 03월 26일 | 정기주총 | 사내이사 이승희 사외이사 안상만 |
- | 기타비상무이사 이상균 기타비상무이사 박용호 |
다. 최대주주의 변동
2023년 11월 07일 기준으로 당사의 최대주주가 '강경선'에서 '주식회사 세종'으로 변경되었습니다. (2025.03.31 기준 총 8,000,000주 / 14.27% 보유)
※ 상세한 내용은 금융감독원 전자공시시스템에 공시된 '최대주주변경'(2023년 11월 8일 공시)를 참조하시기 바랍니다.
라. 상호의 변경
| 일 자 | 변경 전 | 변경 후 |
| 2013년 12월 | 주식회사 강스템홀딩스 | 주식회사 강스템바이오텍 |
마. 회사가 합병등을 한 경우 그 내용
| 일 자 | 합병등의 내용 |
| 2017년 04월 28일 | 세포치료제 양산시설 구축을 목적으로 팅크웨어(주)로부터 경기도 광명시 소하동 1345 소재 토지 및 건물 양수 |
| 2021년 02월 23일 | 라보셀(주)와의 소규모합병 완료 |
바. 회사의 업종 또는 주된 사업의 변화
| 구 분 | 변동 내용 | 비 고 |
| 2013.03.07 정기주주총회 |
- 의약품 및 의외약품 개발, 제조, 판매업 - 회장품 원료 제조, 판매 및 수출입업 - 연구용역사업 - 제대혈 및 줄기세포 관련 사업 - 의료기기 도소매업 - 임신, 출산 및 육아관련 도소매업, 수출입업 - 전자상거래, 통신판매업 및 이와 관련된 부대사업 일체 - 부동산 개발, 공급 및 임대업 - 보험대리업 |
사업목적 추가 |
| 2014.03.28 정기주주총회 |
- 의료기기 제조업, 수출입업 - 임신, 출산 및 육아관련 제조업 |
사업목적 추가 |
| 2021.03.25 정기주주총회 |
- 건강기능식품 제조, 판매 및 수출입업 - 일반 제품 및 상품 유통업 |
사업목적 추가 |
사. 그 밖에 경영활동과 관련된 중요한 사항의 발생내용
1) 주요 연혁
| 일 자 | 내 용 |
| 2014년 05월 | 류마티스관절염 줄기세포치료제, 'Furestem-RA' 임상 1상 승인 (식약처) |
| 2014년 06월 | 기술혁신형중소기업(INNO-BIZ) 인증 (중소기업청) |
| 2014년 09월 | 첨단의료기술개발사업 선정 (보건복지부) |
| 2014년 12월 |
줄기세포치료제 판권 및 공동개발 계약 체결 ((주)대웅제약) 건선 줄기세포치료제(Furestem-CD 적응증 추가)임상 1상 승인 (식약처) 첨단의료기술개발사업 선정 (보건복지부) |
| 2015년 01월 |
줄기세포배양액화장품 공동사업화 계약체결 ((주)코스온) 줄기세포배양액 화장품 'GD11’런칭 |
| 2015년 04월 | 줄기세포 중국사업화 협약 체결 (중국 심양의학원, 대웅제약) |
| 2015년 06월 | 미래산업선도기술개발사업 선정 (산업통상자원부) |
| 2015년 07월 | ISO 9001, ISO 14001 획득 코스닥 특례상장을 위한 기술평가 신청 |
| 2015년 08월 | 미국 Orig3n, iNSC 기술 공동 사업화 계약 체결 첨담의료기술개발사업 선정 (보건복지부) |
| 2015년 12월 | 코스닥 시장 상장 |
| 2016년 02월 | 동화약품, 줄기세포 배양액 사업화 MOU 체결 |
| 2016년 04월 | 안국약품, 건선 줄기세포 치료제 공동개발 계약 체결 |
| 2016년 05월 | 원천기술개발사업 선정 (미래창조과학부) |
| 2016년 07월 | 아토피피부염 줄기세포치료제, 'Furestem-AD' 임상 2b상 승인(식약처) |
| 2016년 10월 | 아시아인을 위한 줄기세포 기반 치료제의 공동연구개발 과제 선정 (미래창조과학부) 2016 년 두뇌역량우수전문기업 (K-BrainPower) 선정 (산업통상자원부) |
| 2017년 03월 | 라비오, 제대혈 줄기세포 배양액 화장품 개발 사업협력 계약 체결 |
| 2017년 04월 | 첨단기술개발사업 선정 (보건복지부) |
| 2017년 07월 | 동화약품, 조인트벤처 '디앤케이코퍼레이션' 설립 |
| 2017년 09월 | 헤라우스, 골관절염 줄기세포 치료제 공동 개발 계약 체결 |
| 2017년 12월 | 아토피피부염 줄기세포치료제, 'Furestem-AD' 임상 3상 변경 승인 (식약처) |
| 2018년 02월 | 류마티스관절염 줄기세포치료제, 'Furestem-RA' 임상 1/2a상 승인 (식약처) |
| 2019년 03월 | SK바이오랜드, 아토피피부염 줄기세포치료제 국내 독점판매권 및 기술전수 계약 체결 (주1) |
| 2020년 04월 | 지플러스생명과학, 세포치료 연구 MOU 체결 |
| 2021년 02월 | 라보셀(주) 소규모 합병 완료 |
| 2021년 05월 | 아토피피부염 줄기세포치료제, '퓨어스템-에이디 주' 임상 3상 승인 (식약처) |
| 2021년 08월 | 골관절염 치료제 1/2a 임상시험 IND신청 |
| 2022년 05월 | 퓨어스템-알에이주(동종제대혈유래중간엽줄기세포)치료제 1/2a상 임상시험 Topline data 발표 |
| 2022년 11월 | 퓨어스템-오에이 키트 주 1/2a 상 임상시험계획(IND) 승인 (식약처) |
| 2023년 01월 | 류마티스관절염 줄기세포치료제, 'Furestem-RA' 임상 2b상 IND 신청 (식약처) |
| 2023년 09월 | 류마티스관절염 줄기세포치료제, 'Furestem-RA' 임상 2b상 IND 승인 (식약처) |
| 2024년 01월 | 특정세포가공물 제조 인정 인증 취득 (일본 후생노동성) |
| 2024년 04월 | '퓨어스템-에이디주' 식품의약품안전처 치료목적 사용승인 |
| 2024년 07월 | '퓨어스템-에이디주' 3상 Topline data 발표 |
| 2024년 11월 | 유영제약, 무릎골관절염치료제(OSCA) 공동개발 및 국내 독점판매권·통상실시권 라이선스 계약 체결 |
| 2024년 12월 | 무릎골관절염치료제(OSCA) 1상 topline data 수령 |
| 2025년 03월 | 무릎골관절염치료제(OSCA) 2a상 환자투약 개시 |
| (주1) 사명 변경 SK바이오랜드→현대바이오랜드 |
3. 자본금 변동사항
가. 자본금 변동추이
| (단위 : 주, 원) |
| 종류 | 구분 | 당분기말 (2025년 3월말) |
15기 (2024년말) |
14기 (2023년말) |
|---|---|---|---|---|
| 보통주 | 발행주식총수 | 56,054,149 | 56,054,149 | 55,937,925 |
| 액면금액 | 500 | 500 | 500 | |
| 자본금 | 28,027,074,500 | 28,027,074,500 | 27,968,962,500 | |
| 우선주 | 발행주식총수 | - | - | 67,499 |
| 액면금액 | - | - | 500 | |
| 자본금 | - | - | 33,749,500 | |
| 기타 | 발행주식총수 | - | - | - |
| 액면금액 | - | - | - | |
| 자본금 | - | - | - | |
| 합계 | 자본금 | 28,027,074,500 | 280,270,745,000 | 28,002,712,000 |
주) 2024년 6월 20일 우선주 67,499주가 보통주 116,224주로 전환되었습니다.
4. 주식의 총수 등
가. 주식의 총수 현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 주, %) |
| 구 분 | 주식의 종류 | 비고 | |||
|---|---|---|---|---|---|
| 보통주 | 우선주 | 합계 | |||
| Ⅰ. 발행할 주식의 총수 | 100,000,000 | - | 100,000,000 | - | |
| Ⅱ. 현재까지 발행한 주식의 총수 | 56,054,149 | 7,697,084 | 63,751,233 | - | |
| Ⅲ. 현재까지 감소한 주식의 총수 | - | 7,697,084 | 7,697,084 | - | |
| 1. 감자 | - | - | - | - | |
| 2. 이익소각 | - | - | - | - | |
| 3. 상환주식의 상환 | - | - | - | - | |
| 4. 기타 | - | 7,697,084 | 7,697,084 | 우선주의 보통주 전환 |
|
| Ⅳ. 발행주식의 총수 (Ⅱ-Ⅲ) | 56,054,149 | - | 56,054,149 | - | |
| Ⅴ. 자기주식수 | - | - | - | - | |
| Ⅵ. 유통주식수 (Ⅳ-Ⅴ) | 56,054,149 | - | 56,054,149 | - | |
| Ⅶ. 자기주식 보유비율 | - | - | - | - | |
5. 정관에 관한 사항
가. 정관 변경 이력
| 정관변경일 | 해당주총명 | 주요변경사항 | 변경이유 |
|---|---|---|---|
| 2019년 03월 21일 | 제9기 정기주주총회 |
- 주식·사채 등의 전자등록에 관한 근거 신설 등 (제8조의2, 제14조, 제15조의2) - 외부감사인의 선임 방법 개정내용 반영 (제55조) - 전환사채 및 신주인수권부사채 액면총액 변경 (제17조, 제 18조) |
- 전자 증권 제도 시행에 따른 변경 - 법령명칭 변경에 따른 자구수정 - 전환사채 신주인수권부사채 사모 발행 한도 확대 |
| 2021년 03월 25일 | 제11기 정기주주총회 |
- 사업목적 추가 (제2조) - 주식 등의 전자등록에 관한 규정 정비 (제8조의 2) - 이익배당기준일 정비 및 동등배당의 근거 명시 (제12조, 제17조, 제57조) - 감사의 선임 (제48조) - 주주명부의 폐쇄 및 기준일 등 관련 조문 정비 (제16조) - 부칙 신설 |
- 사업다각화를 위한 사업의 목적 추가 - 개정된 상법 반영 - 개정된 상법 반영 - 전자투표 도입에 따른 주주총회 결의요건 완화 - 정기주주총회 개최시기의 유연성 확보를 위한 정비 - 시행일 및 감사(위원)의 선임 및 해임에 관한 경과규정 |
나. 사업목적 현황
| 구 분 | 사업목적 | 사업영위 여부 |
|---|---|---|
| 1 | 세포치료제 개발, 제조, 판매업 | 영위 |
| 2 | 의약품 및 의약외품 개발, 제조, 판매업 | 영위 |
| 3 | 세포 가공 및 배양 용역업 | 영위 |
| 4 | 세포 보관 및 공급업 | 영위 |
| 5 | 화장품 제조, 판매 및 수출입업 | 영위 |
| 6 | 화장품 원료 제조, 판매 및 수출입업 | 영위 |
| 7 | 연구용역사업 | 영위 |
| 8 | 제대혈 및 줄기세포 관련 사업 | 영위 |
| 9 | 국내외 헬스케어 관련 사업 | 영위 |
| 10 | 생명과학과 관련된 컨설팅업 | 영위 |
| 11 | 의료기기 제조업, 도·소매업, 수출입업 | 영위 |
| 12 | 임신, 출산 및 육아관련 제조업, 도·소매업, 수출입업 | 미영위 |
| 13 | 전자상거래, 통신판매업 및 이와 관련된 부대사업 일체 | 영위 |
| 14 | 부동산 개발, 공급 및 임대업 | 영위 |
| 15 | 보험대리업 | 미영위 |
| 16 | 건강기능식품 제조, 판매 및 수출입업 | 미영위 |
| 17 | 일반 제품 및 상품 유통업 | 영위 |
| 18 | 기타 위에 부대되는 사업 일체 | 영위 |
다. 정관상 사업목적 변경 내용
- 당사는 공시대상기간 중 정관상 사업목적을 변경한 내용이 없습니다.
II. 사업의 내용
1. 사업의 개요
당사는 2010년에 설립된 줄기세포 치료제 개발 및 제조회사로 당사의 사업부문은 크게 줄기세포 사업, 화장품 사업으로 나눌 수 있습니다.
줄기세포 사업은 자체 개발한 다분화능을 가진 줄기세포를 인간 제대혈로부터 고순도(high-purity)로 분리하고, 대량배양(massive culture)하는 기술을 기반으로 하고 있으며, 주요 파이프라인으로는 퓨어스템-에이디 주(아토피 피부염), 퓨어스템-알에이 주(류마티스 관절염), 오스카(OSCA, 골관절염 치료제, 구.퓨어스템-오에이 키트 주)가 있습니다.
화장품 사업은 당사의 줄기세포 배양액을 기반으로 한 제품을 위주로 판매하고 있으며, 다양한 고객층의 욕구를 만족시키기 위하여 고가부터 중저가의 제품라인업을 형성하였으며, 고정비가 많이 들어가는 오프라인 유통망보다는 다양한 소비층을 만날 수 있는 온라인 유통망을 강화하고 있습니다.
2. 주요 제품 및 서비스
가. 주요 제품, 서비스 등 매출
| (단위 : 백만원, %) |
| 구 분 | 매출 유형 |
품 목 | 2025년 1분기 | 2024년 | 2023년 | 설 명 | |||
|---|---|---|---|---|---|---|---|---|---|
| 매출액 | 비 율 | 매출액 | 비 율 | 매출액 | 비 율 | ||||
| 줄기세포 사업부 | 제 품 | 줄기세포 배양액 | 183 | 19.2 | 430 | 5.6 | 1,023 | 8.1 | 화장품 원료 및 세포배양배지 |
| CDMO | 251 | 26.2 | 1,914 | 24.7 | 404 | 3.2 | 공정개발 및 위탁생산 | ||
| 기 타 | 기타 | 30 | 3.1 | 2,042 | 26.4 | 17 | 0.1 | - | |
| 화장품 사업부 | 제 품 | GD11 | 244 | 25.6 | 1,475 | 19.0 | 2,283 | 18.0 | 줄기세포배양액 화장품 |
| 상 품 | BIO-3 | 247 | 25.8 | 1,799 | 23.2 | 1,833 | 14.4 | 줄기세포배양액 기반 기능성 샴푸 | |
| 기타 | - | - | - | - | 2 | - | - | ||
| 바이오파마 사업부 | 상 품 | 일반의약품 | - | - | 86 | 1.1 | 347 | 2.7 | 일반의약품 |
| 기타 | 기타 | - | - | - | - | 4 | - | 용역, 교정 등 기타매출 | |
| 합 계 | 955 | 100.0 | 7,746 | 100.0 | 5,913 | 100.0 | |||
| 중단영업 (주1) | - | - | - | - | 6,791 | 114.8 | 비임상시험 사업부(주1) | ||
| (주1) | 비임상시험 사업부는 HLB바이오코드(주)(구.(주)크로엔)의 지분 매각으로 연결에서 제외되었습니다. |
3. 원재료 및 생산설비
가. 주요 원재료 매입 현황
| (단위 : 천원) |
| 구 분 | 품 목 | 구분 | 2025년 1분기 |
2024년 | 2023년 | 주요 매입처 |
|---|---|---|---|---|---|---|
| 줄기세포 사업부 |
배지2 | 내수 | 997 | 1,472 | - | 써모피셔 Life |
| 수입 | - | - | - | |||
| 배지3 | 내수 | - | 134,173 | 133,644 | Fujifilm 한국후지필름 |
|
| 수입 | - | - | 135,437 | |||
| 배지4 | 내수 | - | 206,020 | 150,722 | 써모피셔 사이언티픽 솔루션스(유) |
|
| 수입 | - | - | - | |||
| 배지5 | 내수 | - | 189,000 | 94,395 | ||
| 수입 | - | - | - | |||
| 배지6 | 내수 | - | 75,425 | - | Fujifilm 한국후지필름 |
|
| 수입 | - | - | - | |||
| 기타 원재료 |
내수 | 212,651 | 969,184 | 1,060,577 | - | |
| 수입 | - | - | - | |||
| H&B사업부 | 배양액 | 내수 | 3,899 | - | 13,113 | 젠슨리 |
| 수입 | - | - | - | |||
| 합 계 | 내수 | 217,547 | 1,575,274 | 1,452,451 | - | |
| 수입 | - | - | 135,437 | |||
나. 주요 원재료의 가격변동추이
| (단위 : 천원) |
| 주요 원재료 | 구 분 | 2025년 1분기 | 2024년 | 2023년 |
| 배지2 | 내수 | 50 | 49 | - |
| 배지3 | 내수 | - | 67 | 67 |
| 배지4 | 내수 | - | 687 | 685 |
| 배지5 | 내수 | - | 105 | 105 |
| 배지6 | 내수 | - | 108 | - |
다. 기타 주요 매입처 및 공급의 안정성에 관한 사항
당사의 주요 원재료의 매입처는 상기 표와 같으며, 당사와 특수관계에 있는 매입처는없습니다. 또한 해당 매입처와는 공시대상기간 동안 지속적으로 거래를 해오며, 현재까지 공급가와 관련된 문제가 발생한 사례가 없습니다.
라. 생산능력, 생산실적, 가동률
| 구 분 | 품 목 | 구 분 | 2025년 1분기 | 2024년 | 2023년 |
|---|---|---|---|---|---|
| 줄기세포 사업부 |
줄기세포 배양액(주1) (단위: ℓ) |
생산능력 | 600 | 2,400 | 2,400 |
| 생산실적 | 386 | 1,140 | 855 | ||
| 가 동 율 | 64.3% | 47.5% | 35.6% | ||
|
세포배양 배지(주2) (단위: 개) |
생산능력 | 1,500 | 6,000 | 6,000 | |
| 생산실적 | 0 | 1,469 | 3,242 | ||
| 가 동 율 | 0.0% | 24.5% | 54.0% | ||
| 세포배양 배지(주3) (단위: 개) |
생산능력 | 600 | 1,800 | - | |
| 생산실적 | 0 | 379 | - | ||
| 가 동 율 | 0.0% | 21.1% | - |
| (주1) | 월 200ℓ생산 가능합니다. |
| (주2) | 월 500개 생산 가능합니다. |
| (주3) | 월 200개 생산 가능합니다. |
마. 생산설비 현황
| (단위 : 천원) |
| 사업 부분 |
구분 | 2025년 기초 |
당분기 증감 | 당분기 상각 |
2025년 1분기말 |
비 고 | |
|---|---|---|---|---|---|---|---|
| 증가 | 감소 | ||||||
| 줄기 세포 사업부 |
토 지 | 2,832,183 | - | - | - | 2,832,183 | - |
| 건 물 | 6,383,496 | - | - | 45,750 | 6,337,746 | - | |
| 시설장치 | 3,916,264 | - | - | 181,733 | 3,734,531 | - | |
| 연구시험용자산 | 806,546 | 5,000 | - | 252,452 | 559,094 | - | |
| 건설중인자산 | - | - | - | - | - | - | |
| 합 계 | 13,938,489 | 5,000 | - | 479,935 | 13,463,554 | - | |
바. 생산설비 투자계획
- 해당사항 없음 -
4. 매출 및 수주상황
가. 매출실적
| (단위 : 천원) |
| 사업부문 | 품목 |
매출 유형 |
구 분 | 2025년 (제16기 1분기) |
2024년 (제15기) |
2023년 (제14기) |
|
|---|---|---|---|---|---|---|---|
| 줄기세포 사업부 |
줄기세포 치료제 |
제품 | CDMO | 내수 | 250,518 | 1,914,480 | 403,888 |
| 수출 | - | - | - | ||||
| 소계 | 250,518 | 1,914,480 | 403,888 | ||||
|
줄기세포 배양액 |
제품 | 줄기세포 배양액등 |
내수 | 182,760 | 429,676 | 1,023,507 | |
| 수출 | - | - | - | ||||
| 소계 | 182,760 | 429,676 | 1,023,507 | ||||
| 기타기타 | 기술 | OSCA 기술이전 |
내수 | - | 2,000,000 | - | |
| 수출 | - | - | - | ||||
| 소계 | - | 2,000,000 | - | ||||
| 제품 등 | 연구용역 등 | 내수 | 30,000 | 41,637 | 16,540 | ||
| 수출 | - | - | - | ||||
| 소계 | 30,000 | 41,637 | 16,540 | ||||
| 화장품 사업부 |
화장품 | 제품 | GD11 | 내수 | 149,606 | 615,069 | 1,610,028 |
| 수출 | 94,831 | 859,552 | 672,593 | ||||
| 소계 | 244,438 | 1,474,621 | 2,282,621 | ||||
| 상품 | 기타 | 내수 | - | - | 2,201 | ||
| 수출 | - | - | - | ||||
| 소계 | - | - | 2,201 | ||||
| 샴푸 | 상품 | BIO-3 | 내수 | 246,360 | 1,799,377 | 1,832,528 | |
| 수출 | 279 | - | - | ||||
| 소계 | 246,639 | 1,799,377 | 1,832,528 | ||||
| 바이오파마 사업부 |
일반 의약품 |
상품 | 일반의약품 | 내수 | - | 86,033 | 347,172 |
| 수출 | - | - | - | ||||
| 소계 | - | 86,033 | 347,172 | ||||
| 기타 | 기타 | 기타 | 내수 | - | - | 4,211 | |
| 수출 | - | - | - | ||||
| 소계 | - | - | 4,211 | ||||
| 합 계 | 내수 | 859,244 | 6,886,272 | 5,240,075 | |||
| 수출 | 95,111 | 859,552 | 672,593 | ||||
| 소계 | 954,355 | 7,745,824 | 5,912,668 | ||||
| 중 단 영 업 (주1) |
내수 | - | - | 6,791,434 | |||
| 수출 | - | - | - | ||||
| 합계 | - | - | 6,791,434 | ||||
| (주1) | 비임상시험 사업부는 HLB바이오코드(주)(구.(주)크로엔)의 지분 매각으로 연결에서 제외되었습니다. |
나. 판매방법
당사 제품은 고객사와의 계약에 따라 생산되고, 판매방법 및 조건은 고객사와의 계약
시 확정됩니다.
다. 판매전략
당사 제품은 영업(판매)전담부서를 통해 직접 또는 대리점과 거래하고 있습니다. 줄기세포 배양액의 경우, 오랜 업력으로 관련 시장 내 판매 및 영업 인프라를 구축하고 있는 전략적 파트너를 통하여 영업 유지관리 역량 강화와 비용 절감을 실현함과 동시에 수주의 불확실성을 최소화하고 있습니다.
라. 수주현황
| 품목 | 수주 일자 |
납기 | 수주총액 | 기납품액 | 수주잔고 | |||
|---|---|---|---|---|---|---|---|---|
| 수량 | 금액 | 수량 | 금액 | 수량 | 금액 | |||
| - | - | - | - | - | - | - | - | - |
| 합 계 | - | - | - | - | - | - | ||
5. 위험관리 및 파생거래
가. 자본위험관리
당사의 자본관리의 주 목적은 당사의 영업활동을 유지하고 주주가치를 극대화하기 위하여 높은 신용등급과 건전한 자본비율을 유지하기 위한 것입니다. 당사는 자본구조를 경제환경의 변화에 따라 수정하고 있으며, 이를 위하여 배당정책을 수정하거나 자본감소 혹은 신주발행을 검토하도록 하고 있습니다. 한편, 기중 자본관리의 목적, 정책 및 절차에 대한 변경사항은 없습니다.
당사의 당분기말 및 전기말 현재 부채비율은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 부채 | 11,924,801 | 12,804,093 |
| 자본 | 38,278,959 | 43,182,021 |
| 부채비율 | 31.15% | 29.65% |
나. 금융위험관리
당사는 금융상품과 관련하여 시장위험(통화위험, 이자율위험 및 가격위험), 신용위험, 유동성위험과 같은 다양한 금융위험에 노출되어 있습니다. 당사의 위험관리는 당사의 재무적 성과에 영향을 미치는 잠재적 위험을 식별하여 당사가 허용가능한 수준으로 감소, 제거 및 회피하는 것을 그 목적으로 하고 있습니다.
1) 시장위험
당사의 활동은 주로 환율과 이자율의 변동으로 인한 금융위험에 노출되어 있으며 시장위험에 대한 당사의 위험노출정도 또는 위험을 관리하고 측정하는 방식에는 변경이 없습니다.
가. 이자율위험
당사는 변동이자율로 자금을 차입하고 있으며 보유하고 있는 변동이자율부 금융상품의 이자율 변동으로 인하여 이자율 위험에 노출되어 있습니다. 위험회피활동과 관련하여 당사는 이자율 현황과 정의된 위험성향을 적절히 조정하면서 정기적으로 평가하여 최적의 위험회피 전략이 적용되도록 하고 있습니다.
당분기말 현재 각 자산 및 부채에 대한 이자율이 1% 변동시 이자율변동이 법인세비용차감전순손익에 미치는 영향은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 1% 상승시 | 1% 하락시 |
|---|---|---|
| 차입금 | (67,100) | 67,100 |
한편, 당사는 이자율 위험에 대해 다양한 방법의 분석을 수행하고 있습니다. 당사는 이자율변동 위험을 최소화하기 위해 재융자, 기존 차입금의 갱신, 대체적인융자 및 위험회피 등 다양한 방법을 검토하여 당사 입장에서 가장 유리한 자금조달 방안에 대한 의사결정을 수행하고 있습니다.
나. 환율변동위험
당분기말 및 전기말 현재 당사가 보유하고 있는 외화표시 화폐성자산 및 화폐성부채의 장부금액은 다음과 같습니다.
| (원화단위 : 천원, 외화단위 : USD) |
| 구 분 | 통 화 | 당분기말 | 전기말 | ||
|---|---|---|---|---|---|
| 외화금액 | 원화환산금액 | 외화금액 | 원화환산금액 | ||
| 자산 : | |||||
| 현금및현금성자산 | USD | 2,151.47 | 3,155 | 2,151.47 | 3,163 |
보고기간 중 모든 다른 변수가 일정하고 각 외화에 대한 기능통화의 환율이 10% 변동시 환율변동이 당분기손익에 미치는 영향은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 10% 상승시 | 10% 하락시 |
|---|---|---|
| USD | 316 | (316) |
2) 신용위험
신용위험은 보유하고 있는 수취채권 및 확정계약을 포함한 거래처에 대한 신용위험 뿐 아니라 은행, 금융기관 예치금으로부터 발생하고 있습니다. 은행 및 금융기관의 경우, 신용등급이 우수한 금융기관과 거래하고 있으므로 은행 및 금융기관으로부터의 신용위험은 제한적입니다. 일반거래처의 경우 고객의 재무상태, 과거경험 등 기타요소들을 고려하여 신용을 평가하게 됩니다.
① 신용위험에 대한 노출
금융자산의 장부금액은 신용위험에 대한 최대노출정도를 나타냅니다. 당사는 현금및현금성자산을 신용등급이 우수한 금융기관에 예치하고 있어, 금융기관으로부터의 신용위험은 제한적입니다.
당분기말 현재 당사가 보유하고 있는 금융자산의 신용위험에 대한 최대노출금액은 채권의 각 분류별 장부금액입니다.
② 금융자산 손상차손
당분기와 전분기 중 금융자산과 관련하여 발생한 손상차손은 없습니다.
다. 유동성위험관리
당사는 유동성위험을 관리하기 위하여 단기 및 중장기 자금관리계획을 수립하고 현금유출예산과 실제현금유출액을 지속적으로 분석하고 검토하여 금융부채와 금융자산의 만기구조를 대응시키고 있습니다. 당사의 경영진은 영업활동현금흐름과 금융자산의 현금유입으로 금융부채를 상환가능하다고 판단하고 있습니다.
당분기말 및 전기말 현재 당사가 보유하고 있는 비파생 금융자산 및 금융부채의 잔존계약 만기에 따른 만기분석 내역은 다음과 같습니다. 아래 표에 표시된 현금흐름은 원금 및 이자의 현금흐름을 모두 포함하고 있으며, 현재가치로 할인하지 아니한 금액입니다.
(당분기말)
가. 금융자산
| (단위: 천원) |
| 구 분 | 1년미만 | 1년이상 2년미만 | 2년이상 | 합 계 |
|---|---|---|---|---|
| 현금및현금성자산 | 2,165,831 | - | - | 2,165,831 |
| 장단기금융상품 | 15,500,082 | 100,000 | - | 15,600,082 |
| 당기손익-공정가치측정금융자산 | - | - | 2,753,286 | 2,753,286 |
| 매출채권및기타채권 | 1,597,849 | 69,236 | 318,052 | 1,985,137 |
| 합 계 | 19,263,762 | 169,236 | 3,071,338 | 22,504,336 |
나. 금융부채
| (단위: 천원) |
| 구 분 | 1년미만 | 1년이상 2년미만 | 2년이상 | 합 계 |
|---|---|---|---|---|
| 차입금(주1) | 3,916,177 | 911,037 | 2,492,879 | 7,320,093 |
| 매입채무및기타채무(주2) | 1,188,256 | 23,000 | 451,414 | 1,662,670 |
| 리스부채(주3) | 323,072 | 313,862 | 1,952,814 | 2,589,748 |
| 합 계 | 5,427,505 | 1,247,899 | 4,897,107 | 11,572,511 |
| (주1) | 당분기말 현재 예상되는 차입금 이자비용이 포함되어 있습니다. |
| (주2) | 인건비성 미지급비용은 제외한 금액입니다. |
| (주3) | 할인되지 않은 현금흐름을 기초로 작성하였습니다. |
(전기말)
가. 금융자산
| (단위: 천원) |
| 구 분 | 1년미만 | 1년이상 2년미만 | 2년이상 | 합 계 |
|---|---|---|---|---|
| 현금및현금성자산 | 2,766,684 | - | - | 2,766,684 |
| 장단기금융상품 | 15,500,050 | 100,000 | - | 15,600,050 |
| 당기손익-공정가치측정금융자산 | - | - | 2,932,656 | 2,932,656 |
| 매출채권및기타채권 | 5,272,742 | 60,676 | 284,252 | 5,617,670 |
| 합 계 | 23,539,476 | 160,676 | 3,216,908 | 26,917,060 |
나. 금융부채
| (단위: 천원) |
| 구 분 | 1년미만 | 1년이상 2년미만 | 2년이상 | 합 계 |
|---|---|---|---|---|
| 차입금(주1) | 3,974,511 | 930,167 | 2,544,919 | 7,449,597 |
| 매입채무및기타채무(주2) | 1,712,372 | 23,000 | 609,713 | 2,345,085 |
| 리스부채(주3) | 341,028 | 308,601 | 2,001,389 | 2,651,018 |
| 합 계 | 6,027,911 | 1,261,768 | 5,156,021 | 12,445,700 |
| (주1) | 전기말 현재 예상되는 차입금 이자비용이 포함되어 있습니다. |
| (주2) | 인건비성 미지급비용은 제외한 금액입니다. |
| (주3) | 할인되지 않은 현금흐름을 기초로 작성하였습니다. |
한편, 상기 분석은 장부금액을 기초로 당사가 지급하여야 하는 가장 빠른 만기일에 근거하여 작성되었습니다.
라. 파생상품 거래현황
당사는 보고서 작성기준일 현재 외환거래 등과 관련된 위험을 헤지하기 위해 체결한 파생상품 계약은 없으며, 종속회사의 상환전환우선주 발행과 관련된 사항은 재무제표에 대한 주석 15. 차입금을 참조하여 주시기 바랍니다.
6. 주요계약 및 연구개발활동
가. 라이선스아웃(License-out) 계약
1) 라이센스아웃 계약 총괄표
| (단위: 억원) |
| 품목 | 계약상대방 | 대상지역 | 계약체결일 | 계약종료일 | 총 계약금액 | 수취금액 | 진행단계 |
| 퓨어스템 -에이디 주 |
SK바이오랜드(주) (대한민국) *주1) |
국내 | 2019.03.25. | 2024.11.18 | 150 (로열티 별도) |
50 | 국내 3상 종료 국내 1/2a (반복투여)변경신청 *주2) |
| Car-T 기술 (암질환군 한정) |
마루테라퓨틱스(주) (대한민국) |
국내, 국외 |
2021.04.16. | 계약기술 특허존속기간 만료일까지 |
*주3) | *주3) | 기술이전 완료 |
| OSCA(구. 퓨어스템-오에이 키트 주) | (주)유영제약 (대한민국) |
국내 | 2024.11.07 | 품목허가일로부터 10년째 되는 해의 12월 말 | 140 (로열티 별도,임상2b 및 3상 비용 유영제약 부담) |
20 | 국내 1/2a상 진행중 |
| 합 계 | *주3) | *주3) | - | ||||
| *주1) | 사명 변경 SK바이오랜드 → 현대바이오랜드 2024년 11월 18일자로 (주)현대바이오랜드로부터 계약해제 통고를 받아 계약이 해제되었습니다. |
| *주2) | 반복투여 임상으로 2024년 11월 1/2a 임상시험 변경승인 신청하였으며, 2025년 4월 자진취하 하였습니다. 2025년 4월 30일 식약처에 자료를 보완하여 변경승인 신청 하였습니다. |
| *주3) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
2) 품목별 라이선스아웃 계약 세부내용
가) 퓨어스템-에이디 주(아토피 피부염)
| 계약상대방 | - SK바이오랜드(주) (대한민국) *주1) |
| 계약내용 | - 제대혈유래줄기세포치료제(적응증:아토피 피부염)의 국내 독점판매권/통상 실시권 설정 및 기술전수 계약 |
| 대상지역 | - 대한민국 |
| 계약기간 | - 계약체결일 : 2019.03.25. - 계약종료일 : 2024.11.18. |
| 총 계약금 | - 선급기술료 : 150 억원 (경상기술료는 미공개) |
| 수취금액 | - 50 억원 (반환완료 *주3) |
| 계약조건 | - 계약제품에 대한 국내 독점판매권을 현대바이오랜드(구.SK바이오랜드)에 허여함 - 국내 통상실시권 부여 및 기술 전수 - 계약기술 : 당사 보유의 특허권 4건 및 노하우 - 전수시기 : 제품 품목허가 승인 후 현대바이오랜드(구.SK바이오랜드)가 공정 설계 및 투자를 준비하는 시점 - 선급기술료는 총 150억원으로 분할 수령함 1) 계약체결일로부터 15일 이내 50억원 2) 품목허가 후 2년 이내 계약상대방과 협의하에 완제품 협의수량 이상을 연속 생산하고 연속생상된 완제품의 제품공급가 평균값이 vial당 협의된 가격이하가 되는 것을 양사가 확인한 날로부터 90일 이내 20억원 *주2) 3) 현대바이오랜드(SK바이오랜드)가 판매개시 이후 누적판매량이 협의된 수량을 초과한 날로부터 90일 이내 30억원 4) 본 계약에 따라 Know-how 기술전수 요청일로부터 90일 이내 30억원 5) 본 계약에 따라 Know-how 기술전수 종결일로부터 90일 이내 20억원 - 계약제품의 생산은 양사가 공동 협력하며, 당사는 3만 바이알 이내 물량에 대한 제품공급의무를 갖고 있음 |
| 회계처리방법 | - 계약금(Upfront payment) : 라이선스 제공에 대해서는 라이선스 제공과 제품 공급 의무를 단일의 수행의무로 회계처리하며 제품 공급 기간에 걸쳐 수익을 인식하고, 제품의 Know-how 기술이전과 관련 된 수행의무에 대해서는 기술전수가 완료되는 시점에 일시에 수익을 인식 |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 아토피 피부염) - 계약기술 특허는 다음과 같습니다. (1) ZNF281을 발현하는 제대혈 유래 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195호) (2) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량 배양방법(대한민국 특허 등록 제10-1158664호) (3) Isolating Method for Umbilical Cord Blood-Derived Pluripotent Stem Cells Expressing ZNF281(PCT/KR2010/001338) (4) 줄기세포를 유효성분으로 함유하는 면역질환 또는 염증질환의 예방 또는 치료용 조성물(대한민국 특허등록 제10-1512171호) |
| 개발 진행경과 |
- 2013년 퓨어스템-에이디 주 1/2a상 임상시험계획 식약처 승인 - 2015년 1/2a상 임상시험 종료 (2018년 장기추적관찰 종료) - 2017년 3상 임상시험계획 식약처 승인 |
| 기타사항 | 해당 계약에 대하여 (주)현대바이오랜드로부터 2024년 11월 18일 계약해제를 통고 받아 계약이 해제되었습니다. |
| *주1) | 사명 변경 SK바이오랜드 → 현대바이오랜드 |
| *주2) | 2020.12.10 지급조건 변경 |
| *주3) | 2024년 11월 18일 계약해제되었으며, 이에 당사는 ㈜현대바이오랜드로부터 수령한 선급기술료 50억원을 반환하였습니다. 해당 선급기술료는 회계 계정 상 선수수익으로 처리했다가 계약부채로 변경한 후 현대바이오랜드에 반환 후 계약부채에 대한 역분개 처리하였습니다. 이에 관련 분개로 손익에 미치는 영향은 없었습니다. |
나) Cart-T 기술(암질환군 한정)
| 계약상대방 | - 마루테라퓨틱스(주) (대한민국) |
| 계약내용 | - Car-T 기술(암질환군에 한정)에 대한 전용실시권 부여하는 기술이전계약 |
| 대상지역 | - 국내 및 국외 |
| 계약기간 | - 계약체결일 : 2021.04.16. - 계약종료일 : 대상기술 특허 존속기간 만료시까지 |
| 총 계약금 | - *주) |
| 수취금액 | - *주) |
| 계약조건 | * 계약조건은 영업비밀로 자세한 기재는 생략하며, 대략적인 내용은 다음과 같습니다. - 계약금은 ** 원이며 반환의무가 없음 - 1차선정 파이프라인은 두가지로 하며 단계별 기술료는 각각 **원으로 최대 **원 - 향후 제품 생산시 당사에게 CMO생산 위탁 |
| 회계처리방법 | - 계약금 수취액은 계약 조건에 따라 일시에 수익 인식 |
| 대상기술 |
- Car-T 기술(대상 적응증 : 암질환군) |
| 개발 진행경과 |
- 2021년 기술이전 완료 |
| 기타사항 | - |
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
다) OSCA(구. 퓨어스템-오에이 키트 주, 골관절염)
| 계약상대방 | - (주)유영제약 (대한민국) |
| 계약내용 | - 무릎골관절염치료제(OSCA(구. 퓨어스템-오에이 키트 주)) 공동개발 및 국내 독점판매권·통상실시권에 대한 라이선스 계약 체결 |
| 대상지역 | - 국내 |
| 계약기간 | - 계약체결일 : 2024.11.07. - 계약종료일 : 품목허가일로부터 10년째 되는 해의 12월 말 |
| 총 계약금 | - 선급기술료: 140억원 |
| 수취금액 | - 20억원 |
| 계약조건 | - 무릎골관절염치료제(OSCA(구. 퓨어스템-오에이 키트 주))의 공동개발 포함 국내 독점판매권·통상실시권에 대한 라이선스 계약 - 총계약금액 : 140억원 1) 경상기술료 1차 : 20억원 (계약체결시) 2) 경상기술료 2차 : 30억원 (국내 공동개발사 선정시 또는 2026년 말 중 빠른 시점) 3) 경상기술료 3차 : 30억원 (유영제약 또는 공동개발사 첫번째 IND 승인시(2b상 또는 통합 임상 2상)) 4) 경상기술료 4차 : 30억원 (유영제약의 3상 임상 IND 승인시) 5) 경상기술료 5차 : 30억원 (유영제약의 품목허가 취득시) - 로열티 별도지급 (시판 후 12개월 간 발주수량에 따라 합의된 금액 수령) - 조건부 허가로 임상3상 진행시 합의된 금액 수령 |
| 회계처리방법 | - 경상기술료 수취액은 계약 조건에 따라 일시에 수익 인식 |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 아토피 피부염) - 계약기술 특허는 다음과 같습니다. (1) 연골 무세포 파쇄물 및 줄기세포를 포함하는 연골분화 촉진용 복합체 및 그의 용도(대한민국 특허 등록 제10-1901568호) (2)연골 분화능이 증진된 줄기세포의 선별 방법 및 이를 포함하는 세포 치료제(대한민국 특허 출원 제10-2023-0189178호) (3) ZNF281을 발현하는 제대혈 유래만능 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195) (4) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량배양 방법 (대한민국 특허등록 제10-1158664호) |
| 개발 진행경과 | - 2023년 1/2a상 식약처 IND 변경승인 완료 및 임상시험 진행 - 2024년 8월 1/2a상 식약처 IND 변경승인신청, 10월 변경승인 완료 - 2024년 12월 1상 topline data 발표, 1/2a상 식약처 IND 변경승인신청 - 2025년 1월 1/2a상 IND 변경승인 - 2025년 3월 2a상 첫환자 투약 개시 |
| 기타사항 | - |
나. 라이선스인(License-in) 계약
1) 라이센스인 계약 총괄표
| 품목 | 계약상대방 | 대상지역 | 계약체결일 | 계약종료일 | 총 계약금액 | 수취금액 | 진행단계 |
| 피부오가노이드 기술 (아토피피부염 모델) |
서울대학교 산학협력단 |
국내 국외 |
2021.08.30. | 체결일로부터 특허 존속만료일까지 |
*주) | *주) | 기술이전 완료 |
| 인공장기제작 기술 | 서울대학교 산학협력단 |
국내 국외 |
2021.10.01. | 체결일로부터 특허 존속만료일까지 |
*주) | *주) | 기술이전 완료 |
| 모낭 오가노이드 기술 (모낭제작 및 배양기술) |
서울대학교 산학협력단 |
국내 국외 |
2023.12.22 | 체결일로부터 특허 존속만료일 중 가장 늦은 날까지 |
*주) | *주) | 기술이전 완료 |
| UV 손상 피부 오가노이드 기술 |
서울대학교 산학협력단 |
국내 국외 |
2024.02.29 | 체결일로부터 특허 존속만료일 중 가장 늦은 날까지 |
*주) | *주) | 기술이전 완료 |
| 합 계 | *주) | *주) | - | ||||
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
2) 품목별 라이선스인 계약 세부내용
가) 피부오가노이드 기술(아토피피부염 모델)
| 계약상대방 | - 서울대학교 산학협력단(대한민국) |
| 계약내용 | - 피부오가노이드 제조법 및 아토피피부염 모델 개발방법 기술도입 |
| 대상지역 | - 국내 및 국외 |
| 계약기간 | - 계약체결일 : 2021.08.30. - 계약종료일 : 체결일로부터 특허 존속만료일 까지 |
| 총 계약금 | - *주) |
| 수취금액 | - *주) |
| 계약조건 | * 기술이전에 대한 계약조건은 영업비밀로 자세한 기재는 생략하며, 대략적인 내용은 다음과 같습니다. - 기술이전에 대한 강스템바이오텍은 선급금 및 마일스톤은 각 ** 원, ** 원을 서울대에 지급함, 이와 별도로 해당 기술을 사용한 제품 매출액의 ** %를 서울대에게 지급. - 강스템바이오텍이 해당 계약기술을 L/O한 경우 지급받은 금액의 ** %를 서울대에 지급. - L/O와 상관없이 해당 기술을 사용한 상업화의 경우 강스템바이오텍이 서울대에 경상기술료를 지급하는 의무는 유효함. |
| 회계처리방법 | - 자산화 처리 |
| 대상기술 | - 피부오가노이드 제조법 및 아토피피부염 모델 개발방법 특허는 다음과 같습니다. (1) 인간 만능성 줄기세포로 부터 삼차원 공기-액체 계면(Air-liquid interface:ALI)-피부오가노이드 제조법 및 이를 이용한 아토피피부염 모델 개발방법 (대한민국 특허 등록 제10-2020-0136977호) (2) 상기 특허기술을 활용한 서비스 및 중간체원료생산 |
| 개발 진행경과 | - 서울대로 부터 피부오가노이드 제작기술 이전 - 화장품 원료 및 탈모치료 약물 효능 스크리닝 분석법 연구 중 |
| 기타사항 | - |
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
나) 인공장기 제작 기술
| 계약상대방 | - 서울대학교 산학협력단(대한민국) |
| 계약내용 | - 고기능성 인공장기 제작방법에 관한 기술도입 |
| 대상지역 | - 국내 및 국외 |
| 계약기간 | - 계약체결일 : 2021.10.01. - 계약종료일 : 체결일로부터 특허 존속만료일 까지 |
| 총 계약금 | - *주) |
| 수취금액 | - *주) |
| 계약조건 | * 기술이전에 대한 계약조건은 영업비밀로 자세한 기재는 생략하며, 대략적인 내용은 다음과 같습니다. - 기술이전에 대한 강스템바이오텍은 선급금 및 마일스톤은 각 ** 원, ** 원을 서울대에 지급함, 이와 별도로 해당 기술을 사용한 제품 매출액의 ** %를 서울대에게 지급. -강스템바이오텍이 해당 계약기술을 L/O한 경우 지급받은 금액의 ** %를 서울대에 지급. - L/O와 상관없이 해당 기술을 사용한 상업화의 경우 강스템바이오텍이 서울대에 경상기술료를 지급하는 의무는 유효함. |
| 회계처리방법 | - 자산화 처리 |
| 대상기술 | - 고기능성 인공장기 제작방법의 특허는 다음과 같습니다. (1) 관류 가능한 혈관을 포함하는 고기능성 인공 장기 제작방법(대한민국 특허 등록 제10-2020-0150913호) (2) 상기 특허기술을 활용한 서비스 및 중간체 원료생산 |
| 개발 진행경과 |
- 고기능성 인공장기 제작에 사용될 범용적 iPSC 구축 진행 중 |
| 기타사항 | - |
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
다) 모낭 오가노이드 기술 (모낭제작 및 배양기술)
| 계약상대방 | - 서울대학교 산학협력단(대한민국) |
| 계약내용 | - 오가노이드 기반 인간 모낭제작 및 배양기술 도입 |
| 대상지역 | - 국내 및 국외 |
| 계약기간 | - 계약체결일 : 2023.12.22. - 계약종료일 : 체결일로부터 특허 존속만료일 중 가장 늦은 날까지 |
| 총 계약금 | - *주) |
| 수취금액 | - *주) |
| 계약조건 | * 기술이전에 대한 계약조건은 영업비밀로 자세한 기재는 생략하며, 대략적인 내용은 다음과 같습니다. - 기술이전에 대한 강스템바이오텍은 선급금은 ** 원을, 잔금 **원을 서울대에 지급 - 강스템바이오텍이 해당 계약기술을 L/O한 경우 재기술료의 ** %를 서울대에 지급 |
| 회계처리방법 | - 자산화 처리 |
| 대상기술 | - 인간 모발 약물스크리닝 및 모발 이식재를 위한 인간 모낭제작 및 배양기술 (대한민국 특허출원 제10-2023-0034499호) - 피부 오가노이드 기반 모낭의 채취 및 배양기술 - 임상 이식에 적합한 품질관리 기술 |
| 개발 진행경과 |
- 피부 오가노이드 유래 모낭의 순수 분리 및 배양 기술 이전 중 |
| 기타사항 | - |
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
라) UV 손상된 피부 오가노이드 기술
| 계약상대방 | - 서울대학교 산학협력단(대한민국) |
| 계약내용 | - 태양 자외선 노출에 의해 손상된 피부 오가노이드 모델 제작 기술 이전 및 이를 활용한 엑소좀의 치료 효과 |
| 대상지역 | - 국내 및 국외 |
| 계약기간 | - 계약체결일 : 2024.02.29 - 계약종료일 : 체결일로부터 특허 존속만료일 중 가장 늦은 날까지 |
| 총 계약금 | - *주) |
| 수취금액 | - *주) |
| 계약조건 | * 기술이전에 대한 계약조건은 영업비밀로 자세한 기재는 생략하며, 대략적인 내용은 다음과 같습니다. - 기술이전에 대한 강스템바이오텍은 선급금은 ** 원을, 잔금 **원을 서울대에 지급 - 강스템바이오텍이 해당 계약기술을 L/O한 경우 재기술료의 ** %를 서울대에 지급 |
| 회계처리방법 | - 자산화 처리 |
| 대상기술 | - 태양 자외선 노출에 의해 손상된 피부 오가노이드 모델에서의 NF-kb 비활성화를 통한 엑소좀의 치료 효과(대한민국 특허출원 제10-2023-0134662호) - UV 처리를 통한 손상된 피부 오가노이드 모델 제작 기술 - 피부 오가노이드 기반 엑소좀 효력 분석 기술 |
| 개발 진행경과 |
- 피부 오가노이드에 UV 처리 기술 이전 중 |
| 기타사항 | - |
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
다. 공동개발 계약
공시서류 작성기준일 현재 당사가 체결 중인 공동개발계약의 현황은 다음과 같습니다
1) 공동개발계약 총괄표
| (단위: 백만원) |
| 품목 | 계약상대방 | 대상지역 | 계약체결일 | 계약종료일 | 총 계약금액 | 수취금액 | 진행단계 |
| 퓨어스템-알에이 주 퓨어스템-시디 주 |
(주)대웅제약 (대한민국) |
국내외 | 2014.12.29. *주1) |
계약기술 특허존속기간 만료시 | *주2) | *주2) | 퓨어스템-알에이 주 임상 2b상 IND승인 |
| 퓨어스템-오에이 키트 주 |
Heraeus Medical GmbH (독일) |
국내외 | 2017.09.07 | 임상 1/2a상 완료시 | *주2) | *주2) | 국내 임상1/2a상 진행 중 |
| 합 계 | *주2) | *주2) | - | ||||
| *주1) | 2014년 12월 29일에 판권 및 공동개발계약 체결 후 2019년 2월 15일 양사 합의하에 퓨어스템-에이디 주를 적용대상에서 제외하는 추가합의를 체결하였습니다. |
| *주2) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
2) 품목별 공동개발계약 세부내용
가) 퓨어스템-알에이 주, 퓨어스템-시디 주(류마티스관절염, 크론병)
| 계약상대방 | - (주)대웅제약 (대한민국) |
| 계약내용 | - 제대혈유래줄기세포치료제의 개발 및 상업화를 위한 판권 및 공동개발 |
| 대상지역 | - 국내외 |
| 계약기간 | - 계약체결일 : 2014.12.29. (계약변경일 : 2019.02.15.) - 계약종료일 : 계약기술 특허존속기간 만료시 (만료일로부터 1개월전에 계약종료 의사표시하지 않는 경우 동일조건으로 3년단위 자동 연장) |
| 총 계약금 | - *주) |
| 수취금액 | - *주) |
| 계약조건 | * 계약조건은 영업비밀로 자세한 기재는 생략하며, 대략적인 내용은 다음과 같습니다. - 1차 적응증(류마티스관절염,크론병)에 대해 당사와 (주)대웅제약이 단계별 임상 및 공동연구개발 - 후속 적응증 선정 논의 및 이에 대한 공동연구개발 - 계약금액 및 수익 분배는 영업비밀로 기재 생략함. |
| 회계처리방법 | - *주) |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 크론병, 류마티스관절염) - 계약기술 특허는 다음과 같습니다. (1) ZNF281을 발현하는 제대혈 유래 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195호) (2) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량 배양방법(대한민국 특허 등록 제10-1158664호) |
| 개발 진행경과 |
*"퓨어스템-알에이 주"(류마티스 관절염)의 진행경과는 다음과 같습니다. - 2015년 1상(단회투여) 임상시험 종료 - 2018년 1/2a상 반복투여 임상시험(K0202) 식약처 승인 - 2019년 1월 1단계(1상) 대상자 모집완료 |
| 기타사항 | - 2019년 2월 15일 양사 추가합의로 "퓨어스템-에이디 주(아토피 피부염)"를 계약 적용대상에서 제외하였습니다. |
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
나) 퓨어스템-오에이 키트 주 (골관절염)
| 계약상대방 | - Heraeus Medical GmbH (독일) |
| 계약내용 | - 제대혈유래 퇴행성 골관절염 줄기세포치료제를 공동으로 개발 |
| 대상지역 | - 국내외 |
| 계약기간 | - 계약체결일 : 2017.09.07. - 계약종료일 : 임상 1/2a 상 완료시 |
| 총 계약금 | - *주) |
| 수취금액 | - *주) |
| 계약조건 | * 계약조건은 영업비밀로 자세한 기재는 생략하며, 대략적인 내용은 다음과 같습니다. - 당사와 Heraeus는 제대혈유래 퇴행성 골관절염 줄기세포치료제를 공동으로 개발한다. - 임상지역은 대한민국으로 하며 비용은 분담하고 임상 1/2a상 결과에 따라 Heraeus에 라이선스 아웃 또는 글로벌시장에 공동 진출한다. - 금액 및 수익 분배는 영업비밀로 기재 생략함. |
| 회계처리방법 | - *주) |
| 대상기술 | - 제대혈유래 줄기세포를 이용한 세포치료제(대상 적응증 : 퇴행성 골관절염) - 계약기술 특허는 다음과 같습니다. (1) ZNF281을 발현하는 제대혈 유래 줄기세포의 분리방법(대한민국 특허 등록 제10-0950195호) (2) ZNF281을 발현하는 제대혈 유래 줄기세포의 대량 배양방법(대한민국 특허 등록 제10-1158664호) (3) Isolating Method for Umbilical Cord Blood-Derived Pluripotent Stem Cells Expressing ZNF281(PCT/KR2010/001338) |
| 개발 진행경과 | - 2023년 1/2a상 식약처 IND 변경승인 완료 및 임상시험 진행 - 2024년 8월 1/2a상 식약처 IND 변경승인신청, 10월 변경승인 완료 - 2024년 12월 1상 topline data 발표, 1/2a상 식약처 IND 변경승인신청 - 2025년 1월 1/2a상 IND 변경승인 - 2025년 3월 2a상 첫환자 투약 개시 |
| 기타사항 | - |
| *주) | 계약 세부내용의 경우 영업기밀에 해당되어 기재를 생략하였습니다. |
라. 기술제휴계약
- 해당사항 없습니다.
마. 판매계약
- 해당사항 없습니다.
바. 기타계약
- 해당사항 없습니다.
사. 연구개발활동
1) 연구개발활동 개요
당사는 자체 개발한 다분화능을 가진 줄기세포를 인간 제대혈로부터 고순도(high-purity)로 분리하고, 대량배양(massive culture)하는 기술을 기반으로 아토피 피부염, 류마티스관절염, 골관절염 등에 효과적인 동종 제대혈유래 줄기세포치료제(의약품) 개발에 연구 역량을 집중하고 있습니다.
2) 연구개발 조직
가) 연구개발 조직 개요
당사의 연구개발 조직은 임상개발본부 산하 4개팀 줄기세포재생의학연구소 산하 3개팀으로 구성되어 있으며, 각 조직별 업무분장은 다음과 같습니다.
|
본부 |
구성 |
주 요 업 무 |
|
임상개발 본부 |
본부장 |
임상개발 총괄 |
|
임상개발팀 |
치료제별 임상시험 관리 |
|
| 임상전략팀 | 신규 파이프라인 임상전략 및 임상중 및 후 데이터해석 | |
|
RA팀 |
국내외 규제기관 인허가업무 |
|
| 임상안전팀 | 약물 감시 | |
|
연구소 |
연구소장 |
연구소 총괄관리 |
|
연구관리팀 |
연구과제 기획 및 관리업무, 특허등록 관리 업무 등 | |
|
연구1파트 |
임상개발단계 파이프라인 연구 |
|
|
연구2파트 |
세포선별, 제품제형, 생산공정 등에 관한 연구 |
나) 연구개발 인력 현황
공시서류 작성기준일 현재 당사는 박사급 10명(연구소장 포함), 석사급 10명(임상개발본부장 포함) 등 총 26명의 연구인력을 보유하고 있으며, 그 현황은 다음과 같습니다. 당사의 연구소 인력은 의학, 생명공학 및 수의학등을 전공한 줄기세포 전문 연구인력으로 줄기세포 및 줄기세포치료제에 대한 기초연구 및 비임상 연구분야에서 오랜 경험을 바탕으로 최신 연구동향 파악, 비임상 치료효능 및 치료기전에 대한 연구 뿐만 아니라 후속 파이프라인 기반기술 개발을 위한 신기술 발굴, 검증을 수행하고 있습니다.
< 연구개발 인력 현황 (단위: 명) >
|
구 분 |
인 원 |
||||
|
박 사 |
석 사 |
기 타 |
합 계 |
||
|
임상개발본부 |
임상개발팀 |
- | 1 | 1 | 2 |
| 임상전략팀 | 1 | - | - | 1 | |
|
RA팀 |
1 | 1 | - | 2 | |
| 임상안전팀 | - | 1 | 2 | 3 | |
|
연구소 |
연구관리팀 | - | - | 2 | 2 |
| 연구1파트 | 6 | 3 | - | 9 | |
| 연구2파트 | 1 | 3 | 1 | 5 | |
|
합 계 |
9 | 9 | 6 | 24 | |
*주) 연구소장, 임상개발본부장 미포함
다) 핵심 연구인력
당사의 핵심 연구인력은 연구소장 이승희, 연구1파트장 안종찬, 연구2파트장 이송 등 입니다. 연구소장은 줄기세포 분야의 활발한 연구 활동으로 다수의 논문을 출간하였습니다. (아래 주1) 참조)
< 핵심 연구인력 현황 >
|
성명 |
직급 |
담당업무 |
주요경력 |
주요 |
|
이승희 |
연구소장 |
연구총괄 |
해마루 동물병원 인턴수료('06~'07) 인천 노성남 동물병원 진료수의사('07) 서울대학교 수의과대학 석사 ('08~'10) 서울대학교 수의과대학 박사 ('10~'12) |
*주1) |
|
안종찬 |
수석연구원 | 연구1파트장 |
서울대학교 이학박사 ('10) 식품의약품안전평가원 전문연구원('10~'11) 차의과학대학교 의생명과학과 포스닥 ('11~'14) 에이비온(주) 책임연구원 ('15) (주)엑셀세라퓨틱스 책임연구원 ('15~'17) |
*주2) |
| 이송 | 수석연구원 | 연구2파트장 | 고려대학교 의과대학 이학석사('05) 인하대학교 의과대학 의학박사('08) 서울대병원 핵의학과('09~'13) 서울아산병원 의생명연구소('13~'21) |
*주3) |
*주1) 이승희 연구소장의 주요 연구실적은 다음과 같습니다.
[논문]
- Guidelines for Manufacturing and Application of Organoids: Skin (2024)
- LC-MS/MS-based serum proteomics reveals a distinctive signature in a rheumatoid arthritis mouse model after treatment with mesenchymal stem cells (2022)
- Combined Mesenchymal Stem Cells and Cartilage Acellular Matrix Injection Therapy for Osteoarthritis in Goats (2021)
- Immunomodulatory effect of epidermal growth factor secreted by human umbilical cord blood-derived mesenchymal stem cells on atopic dermatitis (2021)
- Pimecrolimus interferes the therapeutic efficacy of human mesenchymal stem cells in atopic dermatitis by regulating NFAT-COX2 signaling (2021)
- Extracellular Vesicles from SOD3-Transduced Stem Cells Exhibit Improved Immunomodulatory Abilities in the Murine Dermatitis Model (2020)
- Effects of conditioned media from human umbilical cord blood-derived mesenchymal stem cells in the skin immune response (2020)
- Therapeutic Effects of Human Umbilical Cord Blood-Derived Mesenchymal Stem Cells Combined with Cartilage Acellular Matrix Mediated Via Bone Morphogenic Protein 6 in a Rabbit Model of Articular Cruciate Ligament Transection (2020)
- TGF-β secreted by human umbilical cord blood-derived mesenchymal stem cells ameliorates atopic dermatitis by inhibiting secretion of TNF-α and IgE, Stem cells (2020)
- Human umbilical cord blood-stem cells direct macrophage polarization and block inflammasome activation to alleviate rheumatoid arthritis, Cell Death Dis (2016)
- DNA methyltransferase inhibition accelerates the immunomodulation and migration of human mesenchymal stem cells. Sci Rep. (2015)
- miR-543 and miR-590-3p regulate human mesenchymal stem cell aging via direct targeting of AIMP3/p18. Age (Dordr). (2014)
[학회발표]
- Practical Cost Reduction Strategies on Mass Production of Stem Cell Therapies, 5th Annual Biologics World Korea (2016)
- Possible application of stem cell and its result, 제6차 대한색소학회 및 제17차 대한코스메틱피부과학회 학술대회 (2016)
*주2) 안종찬 수석연구원의 주요 연구실적은 다음과 같습니다.
[논문]
- Combined Mesenchymal Stem Cells and Cartilage Acellular Matrix Injection Therapy for Osteoarthritis in Goats (2021)
- Human Leukocyte Antigen Class I Pseudo-Homozygous Mesenchymal Stem Cells Derived from Human Induced Pluripotent Stem Cells (2020)
- Therapeutic Effects of Human Umbilical Cord Blood-Derived Mesenchymal Stem Cells Combined with Cartilage Acellular Matrix Mediated Via Bone Morphogenic Protein 6 in a Rabbit Model of Articular Cruciate Ligament Transection (2020)
- AIMP1 down-regulation restores chondrogenic characteristics of dedifferentiated/degenerated chondrocytes by enhancing TGF-β1 signal, Cell Death and Disease (2016)
- Aminoacyl-tRNA synthetase interacting multi-functional protein 1 attenuates liver fibrosis by inhibiting TGFβ signaling, International journal of oncology (2016)
- Transplantation of human Wharton’s jelly-derived mesenchymal stem cells highly expressing TGFβ receptors in a rabbit model of disc degeneration, Stem Cell Res Ther. (2015)
[학회발표]
- 탈분화 연골세포의 기능회복을 위한 유전자 조절 연구, 대한정형외과연구학회 (2014)
*주3) 이송 수석연구원의 주요 연구실적은 다음과 같습니다.
[ 논문 ]
- Continuous Inhibition of Sonic Hedgehog Signaling Leads to Differentiation of Human-Induced Pluripotent Stem Cells into Functional Insulin-Producing β Cells. Lee S, Joo JH, Oh JY, Seo EH, Kim YH, Jun E, Shim IK, Kim SC. Stem cells international. (2021)
- Long-term reversal of diabetes by subcutaneous transplantation of pancreatic islet cells and adipose-derived stem cell sheet using surface-immobilized heparin and engineered collagen scaffold. Kim YH, Ko JH, Lee S, Oh JY, Jeong GS, Park SN, Shim IK, Kim SC. BMJ Open Diabetes Res Care. (2020)
- Enhanced insulin production and reprogramming efficiency of mesenchymal stem cells derived from porcine pancreas using suitable induction medium. Lee S, Moon S, Oh JY, Seo EH, Kim YH, Jun E, Shim IK, Kim SC. Xenotransplantation. (2019)
- Role of High-Mobility Group Box 1 (HMGB1) in Transplantation of Rat Pancreatic Islets. Jeong S, Lee S, Mee-Lee C, Shim IK, Kim SC. Ann Transplant. (2017)
- Mesenchymal Stem Cells Derived from Human Exocrine Pancreas Spontaneously Express Pancreas Progenitor-Cell Markers in a Cell-Passage-Dependent Manner. Lee S, Jeong S, Lee C, Oh J, Kim SC.Stem Cells Int. (2016)
- Adult human pancreas-derived cells expressing stage-specific embryonic antigen 4 differentiate into Sox9-expressing and Ngn3-expressing pancreatic ducts in vivo. Lee S, Lee CM, Kim SC. Stem Cell Res Ther. (2016)
3) 연구개발 비용
당사는 신약 개발 프로젝트가 임상3상 단계에 처음 진입하여 발생한 지출은 무형자산으로 인식하고, 임상3상 단계가 재진입이거나, 이전단계에서 발생한 지출은 당기비용으로 회계처리하고 있습니다.
최근 3년간 연구개발비용은 다음과 같습니다.
가) 연구개발비용 현황
| (단위 : 천원, %) |
|
구분 |
제16기 1분기 | 제15기 | 제14기 | |
|
비용의 성격별 분류 |
원재료 |
109,825 | 725,554 | 917,348 |
|
인건비 |
1,238,206 | 4,481,295 | 4,989,092 | |
|
감가상각비 |
560,263 | 2,168,379 | 2,117,206 | |
|
위탁용역비 |
937,428 | 2,897,969 | 3,573,422 | |
|
기타 |
519,247 | 2,689,190 | 2,961,254 | |
|
연구개발비용 합계 |
3,364,969 | 12,962,387 | 14,558,322 | |
|
회계처리 내역 |
판매비와관리비 |
3,231,117 | 12,143,208 | 14,030,184 |
|
정부보조금 |
133,852 | 819,179 | 528,138 | |
|
연구개발비용 합계 |
3,364,969 | 12,962,387 | 14,558,322 | |
|
연구개발비/매출액 비율 [연구개발비용합계/당기매출액*100] |
352.6 | 167.3 | 114.6 | |
4) 연구개발 실적
가) 연구개발 진행 현황 및 향후계획
공시서류 작성기준일 현재 당사가 연구개발 진행 중인 신약의 현황은 다음과 같으며 모두 당사가 자체 개발한 파이프라인입니다.
(1) 연구개발현황 총괄
< 연구개발 진행 총괄표 >
| 구분 | 품목 |
적응증 |
연구 |
현재 진행단계 |
비고 | |
|
단계(국가) |
승인일 |
|||||
| 바이오 신약 |
퓨어스템-에이디 주 |
아토피피부염 |
2011년 |
임상3상(한국) |
2017년 |
주1) |
| 임상1/2a상(한국) | 2019년 | 주2) | ||||
| 퓨어스템-알에이 주 |
류마티스관절염 |
2012년 |
임상2b상(한국) |
2023년 |
주3) | |
| 퓨어스템-시디 주 |
크론병 |
2012년 |
임상1/2a상(한국) |
2013년 |
주4) | |
|
판상형 건선 |
2013년 |
임상1상(한국) |
2014년 |
주5) | ||
| 퓨어스템-오에이 키트 주 |
골관절염 |
2015년 |
임상 1/2a상(한국) | 2022년 | 주6) | |
| 주1) | 2021년 05월 국내 두번째 3상 승인 완료되어 임상 진행하였으며, 2024년 11월 CSR 결과발표하였습니다. |
| 주2) | 반복투여 임상으로 2024년 11월 1/2a 임상시험 변경승인 신청하였으며, 2025년 4월 자진취하 하였습니다. 2025년 4월 30일 식약처에 자료를 보완하여 변경승인 신청 하였습니다. |
| 주3) | 2023년 9월 2b상 IND 승인을 받았으며, 임상 개시 시기는 2027년 하반기로 예상하고 있습니다. |
| 주4) | 2019년 5월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주5) | 2019년 1월 안전성 평가를 위한 임상1상을 마치고 해당 연구를 종료하였습니다. 현재 구체적인 향후 임상 계획을 갖고 있지 않습니다. |
| 주6) | 2022년 11월 15일 식약처로부터 IND 승인받았으며, 2a 임상시험을 진행 중입니다. |
나) 연구개발 상세내역
(1) 아토피 피부염 치료제(퓨어스템-에이디 주)
| ①구분 |
- 바이오 신약 |
|
②적응증 |
- 중등도 이상의 아토피피부염 |
|
③작용기전 |
- 퓨어스템-에이디 주를 아토피환자에 투여시, TGF-b, PGE2 등 다양한 면역조절인자가 분비되어 비만세포의 활성화 및 탈과립을 억제하고, 그 외에 Th2, Dendritic cell 등 다양한 염증세포의 반응을 조절함으로서 소양감 및 염증증상을 개선하는 효능을 나타냄 |
|
④제품의특성 |
- 세계 최초의 아토피피부염 줄기세포치료제로서, 단일인자에 대한 차단이 아닌, 질환유발과 관련된 면역세포의 반응을 다각적으로 조절함으로서, 부작용이 거의 없으면서 근본적인 치료제로서 역할을 할 수 있는 신개념의 치료제임. |
|
⑤진행경과 |
- 2013년 퓨어스템-에이디 주 1/2a상 임상시험계획 식약처 승인 - 2015년 1/2a상 임상시험 종료 (2018년 장기추적관찰 종료) - 2017년 3상 임상시험계획 식약처 승인 |
|
⑥향후계획 |
- 3상 결과활용 기술수출 진행 - 2a상 임상시험계획서 승인 |
|
⑦경쟁제품 |
- Sanofi Genzyme사의 듀필루맙 등 |
|
⑧관련논문등 |
- Human umbilical cord blood mesenchymal stem cell-derived PGE2 and TGF-β1 alleviate atopic dermatitis by reducing mast cell degranulation. Stem Cells. 2015;33(4):1254-66. - Clinical Trial of Human Umbilical Cord Blood-Derived Stem Cells for the Treatment of Moderate-to- Severe Atopic Dermatitis: Phase I/IIa Studies. Stem Cells. 2017;35(1):248-255 |
|
⑨시장규모 |
- 세계 아토피 치료제 시장은 오는 2030년 276억 8,000달러(37조원) 규모로 성장할 것으로 전망됨 (출처 : Grand View Research) |
|
⑩기타사항 |
- 정부정책과제 수주 4건 1) 아토피 피부염 치료를 위한 제대혈 줄기세포의 실용화 연구(중소기업청) |
(2) 류마티스관절염 치료제(퓨어스템-알에이 주)
| ①구분 |
- 바이오 신약 |
|
②적응증 |
- 중등도 이상의 류마티스관절염 |
|
③작용기전 |
- 퓨어스템-알에이 주를 류마티스 관절염 환자에 투여시, TSG-6, PGE2 등 다양한 면역조절인자가 분비되어 염증성 세포인 M1 phase macrophage의 활성을 억제하고, 항염증성 세포인 M2 phase macrophage의 활성을 촉진하여, 환자의 염증을 억제하고 증상개선효과를 나타냄. |
|
④제품의특성 |
- 세계 최초의 류마티스관절염 줄기세포치료제로서, 단일인자에 대한 차단이 아닌, 질환유발과 관련된 면역세포의 반응을 다각적으로 조절함으로서, 부작용이 거의 없으면서 근본적인 치료제로서 역할을 할 수 있는 신개념의 치료제임. |
|
⑤진행경과 |
- 2014년 퓨어스템-알에이 주 1상 임상시험계획 식약처 승인 - 2015년 1상 임상시험 종료 - 2018년 1/2a상 반복투여 임상시험(K0202) 식약처 승인 - 2021년 4월 대상자 등록 완료 - 2021년 10월 임상종료 - 2021년 12월 K0202 결과 확보 (2022년 5월 임상시험결과보고서 최종화) - 2023년 1월 2b상 IND 승인 신청 - 2023년 9월 2b상 IND 승인 |
|
⑥향후계획 |
- 2b상 임상 개시 준비 |
|
⑦경쟁제품 |
- AbbVie사의 Humira - Johnson & Johnson사의 Remicade - Amgen/Pfizer사의Enbrel 등 |
|
⑧관련논문등 |
- Human umbilical cord blood-stem cells direct macrophage polarization and block inflammasome activation to alleviate rheumatoid arthritis. Cell Death Dis. 2016;7(12):e2524. - Intravenous Infusion of Umbilical Cord Blood-Derived Mesenchymal Stem Cells in Rheumatoid Arthritis: A Phase 1a Clinical Trial. Stem Cells Transl Med. 2018;7(9):636-642. |
|
⑨시장규모 |
- 2019년 류마티스 관절염 치료제 매출이 262억 달러로 2029년까지 연평균 성장률(CAGR) 1% 로 291억 달러까지 완만한 성장을 예상됨. (출처: GlobalData) |
|
⑩기타사항 |
- 정부 정책 과제 수주 1건 제대혈 유래 줄기세포를 이용한 류마티스 관절염 치료제의 상업화 임상 2a상 연구 (보건복지부) |
(3) 크론병 치료제(퓨어스템-시디 주)
| ①구분 |
- 바이오 신약 |
|
②적응증 |
- 중등도 활동성 크론병(염증성 장질환) |
|
③작용기전 |
- 퓨어스템-시디 주를 크론병 환자에 투여시, NOD2 수용체의 활성화를 통해 PGE2 등 다양한 면역조절인자가 분비되어, 항염증성세포인 regulatory T cell의 활성을 촉진하고, Th1/Th17의 활성을 억제하여 염증억제, 조직재생등의 증상개선의 효과를 나타냄. |
|
④제품의특성 |
- 희귀난치성 질환 치료제이며, 해외진출 가능성이 높은 치료제임. 단일인자에 대한 차단이 아닌, 질환유발과 관련된 면역세포의 반응을 다각적으로 조절함으로서, 부작용이 거의 없으면서 근본적인 치료제로서 역할을 할 수 있는 신개념의 치료제임. |
|
⑤진행경과 |
- 2013년 퓨어스템-시디 주 1/2a상 임상시험계획 식약처 승인 |
|
⑥향후계획 |
- 검토 중 |
|
⑦경쟁제품 |
- 존슨앤존슨의 인터류킨 12/23 (IL-12/23) 저해제 '스텔라라(Stelara, ustekinumab)' - 애브비의 IL- 23 저해제 리산키주맙(risankizumab) - 로슈/제넨테크의 에트롤리주맙(etrolizumab) - 다케다의'엔티바이오(Entyvio) 등 |
|
⑧관련논문등 |
- Human umbilical cord blood mesenchymal stem cells reduce colitis in mice by activating NOD2 signaling to COX2. Gastroenterology. 2013;145(6):1392-403.e1-8. |
|
⑨시장규모 |
- 크론병 치료제 시장이 미국, 프랑스, 독일, 이태리, 스페인, 영국, 일본 등 주요7개 국가에서 2029년 126억달러로 추정됨.(출처: GlobalData 2020년) |
|
⑩기타사항 |
- 크론병 중개연구센터 컨소시엄 참여 기업 - 정부정책과제 수주 2건 1) 크론병 치료제 개발을 위한 제대혈유래 줄기세포 상업화 임상연구 (보건복지부) |
(4) 건선 치료제(퓨어스템-시디 주)
| ①구분 |
- 바이오 신약 |
|
②적응증 |
- 중등도 이상의 건선 |
|
③작용기전 |
- 퓨어스템-시디 주를 건선 환자에 투여시, PGE2와 같은 면역조절인자가 분비되어 건선유발에 중요한 역할을 하는 Th17세포를 억제하고, IL-17 과 같은 염증성사이토카인을 억제함으로서, 증상 개선에 대한 효능을 나타냄. |
|
④제품의특성 |
- 세계 최초의 건선 줄기세포치료제로서, 단일인자에 대한 차단이 아닌, 질환유발과 관련된 면역세포의 반응을 다각적으로 조절함으로서, 부작용이 거의 없으면서 근본적인 치료제로서 역할을 할 수 있는 신개념의 치료제임. |
|
⑤진행경과 |
- 2014년 퓨어스템-시디 주 1상 임상시험계획 식약처 승인 |
|
⑥향후계획 |
- 검토 중 |
|
⑦경쟁제품 |
- 얀센의 스텔라라(우스테키누맙) - 노바티스의 코센틱스(세쿠키누맙) - 릴리의 탈츠(이젝키주맙) - 밸리언트의 실리크(브로달루맙) - 존슨앤존슨의 트렘피야(구셀쿠맙) 등 |
|
⑧관련논문등 |
- |
|
⑨시장규모 |
- 건선치료제 글로벌 시장 규모는 2030년 275억 달러로 추정됨 (출처: 메디팜스투데이 2021년) |
|
⑩기타사항 |
- 정부정책과제 수주 1건 1) 제대혈유래 만능줄기세포를 이용한 건선치료를 위한 비임상연구(보건복지부) |
(5) 골관절염 치료제 (퓨어스템-오에이 키트 주)
| ①구분 |
- 바이오 신약 |
|
②적응증 |
- ICRS grade 3 또는 4에 해당하는 무릎골관절염 |
|
③작용기전 |
- 골관절염 환자의 관절강내에 줄기세포와 생체소재를 함께 주입하여, 염증을 억제하면서, 손상된 연골조직의 재생을 유도함. |
|
④제품의특성 |
- 기존의 골관절염 줄기세포치료제의 한계점을 극복할 수 있는 치료제로, 줄기세포와 생체소재를 혼합하여 연골 재생 기능이 탁월한 치료제를 주사제 형태로 개발중에 있음. |
|
⑤진행경과 |
- 2023년 1/2a상 식약처 IND 변경승인 완료 및 임상시험 진행 - 2024년 8월 1/2a상 식약처 IND 변경승인신청, 10월 변경승인 완료 - 2024년 12월 1상 topline data 발표, 1/2a상 식약처 IND 변경승인신청 - 2025년 1월 1/2a상 IND 변경승인 - 2025년 3월 2a상 첫환자 투약 개시 |
|
⑥향후계획 |
- 1상 전체 대상자 영상평가 완료 - 1상 결과 국제학회 발표 - 2a 임상대상자 모집 |
|
⑦경쟁제품 |
- 무릎골관절염 근복적 치료제로 시판승인된 제품 없음. |
|
⑧관련논문등 |
- Therapeutic Effects of Human Umbilical Cord Blood-Derived Mesenchymal Stem Cells Combined with Cartilage Acellular Matrix Mediated Via Bone Morphogenic Protein 6 in a Rabbit Model of Articular Cruciate Ligament Transection 2020 Jun;16(3):596-611 - Combined Mesenchymal Stem Cells and Cartilage Acellular Matrix Injection Therapy for Osteoarthritis in Goats 2022 Feb; 19(1): 177-187 |
|
⑨시장규모 |
- 골관절염 시장은 2032년까지 183억 6000만달러(24조2021억원)으로 성장할 것으로 전망함. (출처 : Precedence Research) |
|
⑩기타사항 |
- 독일Heraeus Medical GmbH 공동개발 계약 체결(2017.09) - 정부 정책과제 수주 1건 차세대 골관절염 줄기세포 치료제 개발을 위한 유효성 안전성 평가 연구 |
다) 연구개발 완료실적
- 해당사항 없습니다. (공시서류 작성기준일 현재 개발이 완료된 신약 없음)
라) 정부출연과제 수행 및 기타 연구 실적
(1) 정부출연과제 수행 실적
|
참여 형태 |
사업명 (시행부처) |
과 제 명 |
사업기간 |
진행 결과 |
|
주관 |
산학연협력기술개발 기업부설연구소지원사업 (중소기업청) |
아토피 피부염 치료를 위한 제대혈 줄기세포의 |
2011.06 ~ |
완료 |
|
주관 |
산학연협력이전기술 사업화촉진지원사업 (서울특별시) |
제대혈 유래 만능줄기세포를 이용한 |
2011.12 ~ |
완료 |
|
주관 |
보건의료연구개발사업 (보건복지부) |
자가면역질환 및 폐색성 동맥질환으로 인한 하지 |
2012.08 ~ 2012.10 |
완료 |
|
세부 |
보건의료연구개발사업 (보건복지부) |
제대혈 유래 만능줄기세포를 이용한 건선 치료를 위한 비임상 연구 |
2012.12 ~ 2014.11 |
완료 |
|
참여 |
생명산업기술개발사업 (농림수산식품부) |
돼지줄기세포 유래 분화세포와 생체지지체 개발 및 |
2012.04 ~ |
종료 |
|
주관 |
부품소재사업 (산업통상자원) |
중간엽 줄기세포의 배양액 첨가물질 개발을 통한 |
2013.10 ~ 2016.09 |
완료 |
|
세부 |
첨단의료기술개발사업 (보건복지부) |
성체줄기세포의 3D 대량배양 기술 개발 및 |
2014.12 ~ 2016.11 |
완료 |
|
주관 |
중소기업제트워크형사업 (중소기업부) |
줄기세포 배양액의 제형개발과 효능평가를 통한 |
2017.04 ~ 2017.10 |
완료 |
|
세부 |
첨단의료기술개발사업 (보건복지부) |
폐색성동맥질환 치료제로서 저산소환경에서 배양한 |
2014.09 ~ 2017.12 |
완료 |
| 주관 |
중소기업제트워크형사업 (중소기업부) |
줄기세포 배양액 화장품 원료와 제형개발 및 병원용 제품개발 |
2017.11~ 2019.11 |
완료 |
|
세부 |
보건의료연구개발사업 (보건복지부) |
면역특성화줄기세포를 이용한 |
2012.05 ~ 2018.03 |
완료 |
|
세부 |
미래산업선도기술개발사업 (산업자원부) |
바이오의약품용 세포배양 시스템 개발 |
2015.06 ~ 2021.05 |
종료 |
|
위탁 |
첨단의료기술개발사업 (보건복지부) |
영장류 기반 장기이식 면역관용 유도를 위한 |
2015.09 ~ 2018.08 |
완료 |
|
세부 |
원천기술개발사업 (과학기술정보통신부) |
유전자 세포치료제 개발을 위한 대량배양법 확립과 |
2016.05 ~ 2021.01 |
종료 |
|
단위 |
신진연구자지원사업 |
AIDS 치료용 유전자 넉아웃 |
2016.08 ~ |
완료 |
|
참여 |
국가간협력기반조성사업 |
아시아인을 위한 신경계 질환 치료용 줄기세포 개발 및 활용 기술 개발 |
2016.10 ~ |
완료 |
|
단위 |
이공학개인기초연구지원사업 |
암세포에서 P53 단백질 안전성 및 항암제 반응성에 |
2016.11 ~ 2018.06 |
완료 |
|
세부 |
첨단의료개발사업 (보건복지부) |
차세대 세포치료제 생산기반 확립 및 |
2016.11 ~ 2019.03 |
종료 |
| 참여 기업 |
선도연구센터사업 (과학기술정보통신부) |
톨유사수용체 기반 질병 연구센터 | 2016.06 ~ 2022.12 |
완료 |
|
주관 |
첨단의료기술개발사업 (보건복지부) |
크론병 치료제 개발을 위한 제대혈 유래 줄기세포의 |
2015.08 ~ 2017.07 |
완료 |
|
주관 |
첨단의료개발사업 (보건복지부) |
제대혈 유래 줄기세포를 이용한 |
2017.04 ~ 2017.12 |
종료 |
|
주관 |
사업화연계기술개발사업 (산업통상자원부) |
제대혈 유래 줄기세포 배양액을 함유한 |
2017.06 ~ 2018.02 |
종료 |
|
세부 |
첨단의료기술개발사업 (보건복지부) |
성체 줄기세포 대량배양용 무혈청 배지 개발 |
2018.04 ~ 2021.12 |
종료 |
| 주관 | 첨단의료기술개발사업 (보건복지부) |
차세대 골관절염 줄기세포 치료제 개발을 위한 유효성 안전성 평가 연구 |
2020.04~ 2022.12 |
종료 |
| 단독 | 첨단의료기술개발사업 (보건복지부) |
제대혈 유래 줄기세포를 이용한 류마티스 관절염 치료제의 상업화 임상 2a상 연구 |
2020.04~ 2023.12 |
종료 (1년 기간연장) |
| 단위 | 이공분야기초연구사업 (과학기술정보통신부) |
인간유도만능줄기세포 유래 조혈모 세포 기반 후천성 면역결핍증 치료기술 확립 |
2020.06~ 2021.02 |
2021.06 과제이관 |
| 주관 | 범부처재생의료기술개발사업 (과학기술정보통신부-보건복지부) |
면역조절능 특화 줄기세포를 이용한 급성호흡곤란증후군 치료제 개발 |
2021.08~ 2024.12 |
종료 |
| 주관 | 이공분야기초연구사업(기본연구) (한국연구재단) |
인체 췌장세포 유래 오가노이드 구축과 분화/ 발생을 통한 맞춤형 당뇨병 치료 개발 플랫폼 연구 |
2020.06~ 2023.02 |
종료 |
| 주관 | 이공분야기초연구사업(중견연구) (한국연구재단) |
B2M 넉아웃 CD24 과발현 면역관용 유도만능줄기세포를 이용한 모낭 이식재 개발 |
2022.09~ 2025.02 |
종료 |
| 공동 | 산업통상자원부 (한국산업기술기획평가원) |
인공지능 기반 세포-생체재료 복합지지체의 최적 설계 및 제조생산기술 개발 |
2024.04~ 2028.12 |
진행중 |
| 주관 | 산업통상자원부 (한국산업기술기획평가원) |
3D 세포 기반 재생치료제의 안정적 보관 및 활용을 위한 신소재 적용 배지·동결보존제 및 탈 LN2급 냉동운송장비·시스템 개발 |
2024.07~ 2028.12 |
진행중 |
| 주관 | 산업통상자원부 (한국산업기술기획평가원) |
3D 세포 기반 재생치료제의 안정적 냉·해동을 위한 다중양쪽성고분자 및 나노전달기술을 이용한 동결보존 신소재 개발 |
2024.07~ 2028.12 |
진행중 |
(2) 기타 연구 실적
- 줄기세포 자동화 대량배양 기술 및 무혈청 배지 개발
|
연구기관 |
강스템바이오텍, 서울대 수의과대학, 삼성서울병원, 성균관대 산학협력단, |
|
기대효과 |
- 정부정책과제 수주 3건 1) 성체줄기세포의 3D 대량배양 기술 개발 및 GMP시설 기반 제조공정 확립 2) 바이오의약품용 세포배양 시스템 개발 (산업자원부) - 3차원 세포배양을 위한 공정 및 시스템 개발 - 제조공정의 자동화 및 최적화를 통한 비용 절감 및 생산성 향상 - 성체 줄기세포 대량배양용 무혈청 배지 개발 - 개발 된 대량배양 자동화 기기 및 무혈청 배지를 활용한 성체 줄기세포 |
| 향후계획 | 대량배양기기의 단계별 제작 및 검증, 무혈청배지 후보군에 대한 검증 |
- 직접분화신경줄기세포 (Directly converted Neural Stem Cells)
|
연구기관 |
강스템바이오텍 |
|
기대효과 |
- 신경 줄기세포를 만드는데 결정적 역할을 수행하는 HMGA2 유도인자 발견 - 논문 게재 4건: Stem Cell Res (2013), Cell Reports (2015), - Retrovirus를 이용한 somatic cell에서 induced neural stem cell의 직접분화 - 인간 체세포(노화된 세포, 혈액세포 가능)에서 직접 분화법(Direct Conver - 미국 Orig3n社와 공동연구 협약 체결 (2015.08) - 퇴행성 신경질환에 대한 약물 스크리닝 및 줄기세포치료제로 개발 기대 |
| 향후계획 | direct conversion 기술을 이용하여 환자 맞춤형 drug screening이 가능한 플랫폼 구축 및 비임상시험을 통한 세포치료제 개발 가능성 확인 |
- 줄기세포 배양액 개발
|
연구기관 |
강스템바이오텍 |
|
주요실적 및 계획 |
- 줄기세포 배양액 원료 개발 및 판매 1) 쎄라덤, 동화약품 등 배양액 공급 계약 2) ㈜코스온과 공동 연구 개발 (GD11 화장품 런칭 및 판매 (2015.01)) - 줄기세포 배양액 내 유효 성분 인자 분석(EGF, FGF, etc) 및 대표적인 인자 - INCI 국제화장품 원료 등록 (5-03-2014-1948) - 피부 내 침투 기전(exosome) 관련 연구 진행 중, BBRC 논문 게재(2017) 2) 제대혈 유래 줄기세포 배양액을 함유한 아토피 기능성 화장품 개발 |
| 향후계획 | 생산공정과 품질을 개선한 2세대 배양액 연구개발 및 제품라인 확대 |
- 면역조절능 특화 줄기세포 ARDS 치료제 개발
|
연구기관 |
강스템바이오텍 |
|
주요실적 및 계획 |
- 세포프라이밍 최적화를 통한 면역조절능 강화 줄기세포주 확립 - 급성 폐손상 온어칩 모델 구축 - ARDS 동물 모델을 통한 비임상 효력 평가, 용량의존성 시험 및 작용기전 연구 - 논문 게재: 2건 Stem Cell Rev Rep. (2017, 2020) - 정부정책과제 수주 1건 1) 면역조절능 특화 줄기세포를 이용한 급성호흡곤란증후군 치료제 개발 (범부처재생의료기술사업단) |
| 향후계획 | - 감염성 질환등으로 부터 유도되는 급성 호흡곤란증후군(ARDS)의 경우 적절 한 치료가 생명 - 현재 관련질환의 치료제는 없는 실정이며, 폐 부전으로 진행시 환자를 사망 하게 함 - 최근 꾸준한 환자의 증가로 관련 치료제 개발이 시급하며, 이런 문제를 해결 하기 위하여 면역조절기능 강화 세포치료제를 제시 |
7. 기타 참고사항
1. 영업개황, 산업분석 외
가. 사업부문별 현황
당사의 사업부문별 현황을 요약하면 아래와 같습니다.
| 구 분 | 주요 사업 내용 |
|---|---|
|
줄기세포 사업 |
줄기세포 치료제 연구개발, 줄기세포 배양액 및 배양배지 공급 |
| 화장품 사업 | 줄기세포 배양액 화장품 제조, 판매 |
| 바이오파마 사업 | 일반의약품(OTC) |
| 비임상시험 사업 (주1) |
의약품, 화학물질, 작물보호제, 동물의약품 등의 효능 및 유해성 평가 |
주1) 당기 중 비임상시험 사업부는 HLB바이오코드(구. ㈜크로엔)의 지분 매각으로 연결에서 제외되었으며, 중단영업으로 재분류하였습니다.
[줄기세포 사업부문]
파이프라인은 다음과 같습니다.
|
사업부문 |
제품명 |
적응증/용도 |
단계 |
판매처 |
| 줄기세포 사업부 |
퓨어스템-에이디 주 |
아토피 피부염 |
임상1/2a상(한국) | *주1) |
| 퓨어스템-알에이 주 |
류마티스관절염 |
임상 2b상(한국) |
(주)대웅제약 |
|
| 퓨어스템-시디 주 |
크론병 |
임상1/2a상(한국) |
(주)대웅제약 |
|
| 판상형 건선 | 임상1상(한국) | - | ||
| 퓨어스템-오에이 키트 주 |
골관절염 | 임상1/2a(한국) | (주)유영제약 |
*주1) 현대바이오랜드(舊 SK바이오랜드)와의 계약이 2024.11.18 해제 되었습니다.
1) 줄기세포 치료제 산업의 특성
가) 재생의약으로서 줄기세포 치료제
재생의약이란 손상된 세포와 조직, 장기를 대체하거나 재생시켜 정상 기능을 복원시키는 의학 분야입니다. 재생의약은 질병의 근본 원인을 해결함으로써 기존의 미충족 영역을 만족시켜주는 새로운 패러다임 입니다. 전 세계적으로 재생의약 기업은 700개 이상 존재하며, 지역별로는 미국(50%이상), 분야별로는 세포치료제 분야(60%)가 산업을 주도하고 있습니다. 재생의약 및 바이오기술의 비약적인 발전과 고령화의 환경적 요인에 따라 향후 관련 산업은 더욱 활성화 될 것으로 전망됩니다.
|
분야 |
세부 내용 |
|
세포치료제 (Cell Therapy) |
- 손상되었거나 질병이 있는 세포/조직을 회복시키기 위해 - 이 세포들은 신약개발과 독성검사 등에 이용됨 |
|
유전자치료제 (Gene Therapy) |
- 질병의 상태를 바꾸도록 처리될 수 있는 변형된 유전자를 |
|
조직공학 (Tissue Engineering) |
- 생물학적 대체 이식재를 개발하는 시장으로 합성물질, |
|
저분자 및 생물의약품 (Small Molecules and Biologics) |
- 세포의 재생적 특성을 회복하기 위하여 이 세포들을 자극할 |
(출처: The New Age of Regenerative Medicine, Frost&Sullivan, 2015.07)
당사의 주력 사업인 줄기세포 치료제는 세포치료제 산업에 속하며 2011년 7월 첫 제품이 출시된 신생 시장으로 현재 도입기에 있으나, 과거의 직접치료방식 및 화학치료의 약물제제나 항원에 대응하는 항체를 형성하는 방법, 시술 등과 달리 질병의 본원적 치료를 통한 향후 확장가능성을 지니고 있어 산업을 이끄는 트렌드로 인정받고 있습니다. 이는 기존 의료 패러다임의 근본적인 변화를 초래하게 되었으며, 특히 급증하는 희귀난치성 질환 치료에 대한 잠재력을 가지고 있다는 점에서 많은 환자들에게 희망이 되고 있을 뿐만 아니라 21세기를 이끌어갈 핵심 의약분야로 부각되고 있습니다.
나) 신약 허가절차 및 규제 환경
신약 개발은 직접적으로 인간의 생명과 건강에 영향을 끼칠 수 있기 때문에 공공성·제도적 규제가 강한 특성을 지니고 있습니다. 신약 허가를 받기 위해서는 비임상시험을 거쳐 임상시험에서 안전성과 유효성을 인정받아야 하며, 이러한 시험을 수행함으로서 신약의 인체 위해성평가를 검증받도록 하고 있습니다.
[신약 개발 과정]
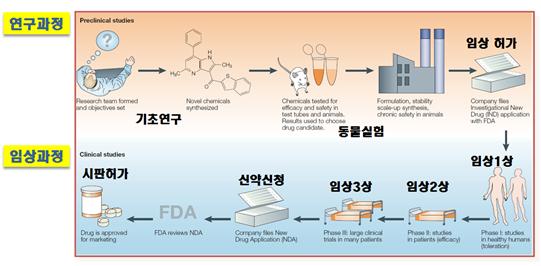 |
|
(출처: Nature Reviews Drug Discovery) |
의약품 개발의 모든 영역은 정부기관이 관리감독하고 있으며, 다른 산업분야에 비해 연구개발에 소요되는 개발기간이 길고 준수해야 하는 제약조건이 많은 반면 진입장벽이 높아, 제품 개발에 성공한 경우 시장 내에서 독점적 지위를 누릴 수 있습니다.
다) 강력한 정부지원
2023년 03월에 발표한 '바이오헬스 글로벌 중심국가 도약을 위한 제3차 제약바이오 산업 육성ㆍ지원 종합계획(2023~2027년)'에 따르면, 글로벌 블록버스터급 신약 창출, 글로벌 수준의 제약바이오 기업 육성, 의약품 수출 2배 달성, 제약바이오 산업 양질 일자리 창출, 임상시험 글로벌 3위 달성을 목표로 설정하였으며, 신약 창출을 위한 R&D 투자 확대, 글로벌 수준의 규제 혁신 및 공급망 인프라 확대 등의 10대 중점 과제를 추진하겠다고 공표하였습니다.
 |
|
바이오헬스 글로벌 중심국가 도약을 위한 제3차 제약바이오 산업 육성 지원 종합계획(2023~2027년) |
| 출처) 보건복지부 |
또한, 2023년 07월 산업통상자원부에서 발표한 '바이오경제 2.0 추진방향'에 따르면, 최근 세포 치료제, 유전자 치료제 등 혁신 바이오의약품이 글로벌 시장을 주도하고 있으며, 신약개발과 제조(위탁생산, CMO)간 분업화가 가속화 되고 있습니다. 또한, 바이오 빅데이터, 디지털 의료기기 등 AI 및 디지털과 바이오간의 융합이 가속화되고 있기 때문에 높은 성장 잠재력을 가지고 있다고 판단되고 있습니다.
 |
|
바이오경제 2.0 추진방향 -1 |
| 출처) 산업통상자원부 |
다만, 이를 뒷받침할 국내 기반은 부족한 상황이기 때문에 미래 유망 바이오 신산업을 본격적으로 육성하기 위해 2030년 바이오경제 생산 100조원, 수출 500억달러 달성을 목표로, 다음과 같이 추진방향을 공표하였습니다.
1) 바이오기업 성장 지원 및 부지, 전력, 상하수도 등의 인프라 지원 등 2030년까지 15.7조원 규모의 투자를 지원할 계획입니다. 이를 통해 바이오의약품 시장의 제조역량 강화를 지원하고, 글로벌 원부자재기업의 국내 투자유치를 통해 바이오 원부자재 국산화율 10%(2027년 달성), 15%(2030년 달성)을 목표하고 있습니다. 또한, 바이오 국가첨단전략산업 특화단지를 조성하여 한국판 보스턴 바이오 클러스터를 육성할 계획입니다.
2) 다양한 바이오신소재 제품 개발 및 원료 기술을 개발할 수 있는 산업을 육성하여 경쟁력을 키우기 위해 지원할 계획이며, 3) 차세대 바이오 연료 기술 개발을 통해 친환경 바이오에너지를 상용화할 수 있는 연구 및 법령 개정을 추진할 계획입니다.
3) AI 및 디지털 전환의 가속화가 심해지고 있는 상황에서, 바이오산업과 AI, ICT 산업과의 융복합을 통해 고부가가치 창출이 가능한 생태계를 조성할 계획입니다.
 |
|
바이오경제 2.0 추진방향 -2 |
| 출처) 산업통상자원부 |
이처럼 제약바이오 산업에 대한 관심도가 증가함에 따라 정부의 우호적인 시장 정책이 다수 도입되고 있지만, 지원 정책이 이루어지지 않거나 향후 정책 기조의 변화에 따라 정부지원이 축소 또는 규제 강화 등의 대외적 변수가 발생될 수 있습니다. 이에 당사는 정책 및 규제 변화에 신속한 대응을 위한 지속적인 모니터링을 항시적으로 진행하고 있지만, 그럼에도 불구하고 국내외 정책 등의 변동 위험이 존재할 가능성이 존재함으로 당사의 줄기세포치료제 연구 개발 사업 전망에도 부정적인 영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
라) 경기변동의 특성
의약품은 크게 전문의의 진단과 처방을 필요로 하는 '전문의약품'과 일반인이 선택
하여 약국에서 구입할 수 있는 '일반의약품'으로 구분되며, 전문의약품에 비하여
일반의약품이 비교적 경기변동이나 날씨, 기후 등의 계절적 요인에 영향을 받는 편이지만, 생명 및 건강과 직접 관련되는 의약품의 특성상 가격이 높아지더라도 비용을
지불하고 구매하려는 속성을 지니고 있어 경기 변동 및 계절적 요인에 따른 민감도가 비교적 낮으며, 비탄력적인 성향을 보입니다.
2) 시장 현황 및 전망
가) 줄기세포 치료제 시장
줄기세포 치료제 시장은 1999년 최초로 기업체 주도의 임상연구가 시작된 이래, 글로벌 줄기세포시장규모는 2022년 137억 840만 달러에서 연평균 14.9%로 성장하여 2030년에는 399억 3,560만 달러규모로 확대 전망됩니다.
| 글로벌 줄기세포 시장 현황 및 전망 (2022~2030) |
| (단위 : 백만달러) |
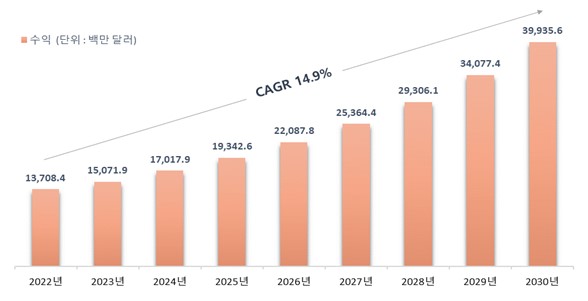 |
|
글로벌 줄기세포 시장 현황 및 전망 |
| 자료: Fortune Business Insights, Stem Cells Global Market Analysis, Insights and Forecast, 2023-2030, 국가생명공학정책연구센터 재가공 |
또한, 아시아-태평양 시장규모는 2022년 기준 약 31억달러로, 중국의 줄기세포 시장 점유율이 35.5%(약 11억 달러, 2022년 기준)으로 아태지역에서 가장 큰 비중을 차지하고 있으며, 그 다음은 일본(21.5%, 약 6억달러), 한국(12.5%, 약3억달러) 순입니다. 한국의 시장규모는 연평균 17.5%로 성장하여 2030년에는 약 13억달러에 이를 것으로 전망됩니다.
|
글로벌 줄기세포 시장 수익현황 및 전망(2022~2026)과 시장 점유율(2022 기준) |
| (단위 : 백만달러) |
|
지역 |
2022년 | 2023년 | 2024년 |
2025년 |
2026년 |
CAGR(%) |
시장 점유율 |
|---|---|---|---|---|---|---|---|
|
북미 |
7,271 | 8,002 | 9,035 | 10,271 | 11,719 | 14.7% |
53.0% |
|
유럽 |
2,506 | 2,726 | 3,071 | 3,471 | 3,932 | 13.8% |
18.0% |
|
아시아 태평양 |
3,101 | 3,443 | 3,905 | 4,474 | 5,172 | 16.8% |
23.0% |
| 남미 | 538 | 585 | 655 | 735 | 826 | 12.9% |
3.9% |
| 중동 및 아프리카 |
291 | 314 | 349 | 390 | 436 | 12.2% |
2.1% |
|
총합 |
13,708 | 15,071 | 17,017 | 19,342 | 22,087 | - |
- |
| 자료 : Fortune Business Insights, Stem Cells Global Market Analysis, Insights and Forecast, 2023-2030, 국가생명공학정책연구센터 재가공 |
줄기세포치료제는 과학적, 의학적 측면 뿐 아니라 사회문화적 측면에서도 커다란 변화를 유도하면서 세계 각국이 줄기세포 분야의 경쟁력을 선점하기 위하여 국가적 역량을 기울이며 연구개발을 진행하고 있습니다. 우리나라 제약산업은 그동안 복제약으로 불리는 제네릭 위주로 성장해왔으나 이제는 국가가 신약개발 지원을 통해 세계 7대 제약강국으로 도약하고자 하는 강한 의지를 보이고 있고, 정부가 줄기세포 연구 강화에 의지를 보인 만큼 난치병 환자를 위한 치료제 개발 속도도 빨라질 것으로 기대됩니다. 줄기세포치료제는 증상의 지연이나 완화에 불과했던 과거의 직접치료방식 및 화학 약물제제, 시술 등과 달리 질병의 근본적인 치료가 가능하여, 기존의 의약품들이 접근하지 못했던 '미충족 의료 수요 (unmet medical needs)'로의 접근을 통한 새로운 시장 창출이 가능할 것으로 기대되며, 이 중 최근 급증하고 있는 난치성 질환에 대한 잠재력을 인정받아 많은 환자들에게 희망이 되고 있습니다.
| [줄기세포치료제 출시 현황] |
| 회사명 | 제품명 | 분류 | 적응증 | 국가 | 허가년월 |
|---|---|---|---|---|---|
| 파미셀 | 하티셀그램-AMI | 자가골수 | 급성심근경색 | 한국 | 2011.07 |
| New York Blood Center | HEMACORD | 제대혈유래 조혈전구세포 (HPC, Cord Blood) |
조혈모세포이식 | 미국 | 2011.11 |
| 메디포스트 | 카티스템 | 동종제대혈 | 무릎연골결손 | 한국 | 2012.01 |
| 안트로젠 | 큐피스템 | 자가지방 | 크론성 누공 | 한국 | 2012.01 |
| Clinimmune Labs, University of Colorado Cord Blood Bank |
HPC, Cord Blood | 제대혈유래 조혈전구세포 (HPC, Cord Blood) |
조혈모세포이식 | 미국 | 2012.05 |
| Osiris Therapeutics | Prochymal | 동종골수 | 이식편대숙주질환 | 캐나다 | 2012.05 |
| 뉴질랜드 | 2012.06 | ||||
| Duke University School of Medicine | DUCORD | 제대혈유래 조혈전구세포 (HPC, Cord Blood) |
조혈모세포이식 | 미국 | 2012.10 |
| SSM Cardinal Glennon Children's Medical Center |
ALLOCORD | 제대혈유래 조혈전구세포 (HPC, Cord Blood) |
조혈모세포이식 | 미국 | 2013.05 |
| LifeSouth Community Blood Center | HPC, Cord Blood | 제대혈유래 조혈전구세포 (HPC, Cord Blood) |
조혈모세포이식 | 미국 | 2013.06 |
| 코아스템켐온 | 뉴로나타-알 | 자가골수 | 루게릭병 | 한국 | 2014.07 |
| Chiesi | Holoclar | 자가각막 | 화상에 의한 각막손상 | 유럽 | 2015.02 |
| JCR | TEMCELL | 동종골수 | 이식편대숙주질환 | 일본 | 2015.09 |
| Bloodworks | HPC, Cord Blood | 제대혈유래 조혈전구세포 (HPC, Cord Blood) |
조혈모세포이식 | 미국 | 2016.01 |
| Cleveland Cord Blood | CLEVECORD | 제대혈유래 조혈전구세포 (HPC, Cord Blood) |
조혈모세포이식 | 미국 | 2016.09 |
| Tigenix | Alofisel | 동종지방 | 크론성 누공 | 유럽 | 2018.03 |
| MD Anderson Cord Blood Bank | HPC, Cord Blood | 제대혈유래 조혈전구세포 (HPC, Cord Blood) |
조혈모세포이식 | 미국 | 2018.06 |
| 니프로 | 스테미락 | 자가골수 | 척수손상 | 일본 | 2018.11 |
| 자료 : 당사 자체 조사 (FDA 및 각 사 홈페이지 참고) |
당사는 그 중 시장성이 가장 높다고 판단되는 자가면역질환을 타겟으로 하고 있으며,
아토피 피부염, 류마티스관절염, 크론병, 골관절염 1차 타겟으로 선정하였습니다.
나) 면역계질환의 시장성
면역제 질환에는 보편적으로 처방되는 스테로이드제제부터 '블록버스터' 의약품으로대표되는 항TNF제제까지 다양한 의약품들이 적용되고 있으나 질병의 근본적인 치료가 아닌 증상 완화 또는 지연 수준의 효능과 일부 부작용 사례로 인하여 새로운 치료법 개발이 절실합니다.
시장조사기관 리서치앤마켓에 따르면 류마티스관절염 등 자가면역질환의 시장 규모는 2022년 2,512억 달러에서 2030년 3,387억 달러로 증가하며, 연평균 3.8%성장하고 있는 시장입니다.
| [자가면역질환 시장 규모 및 전망] |
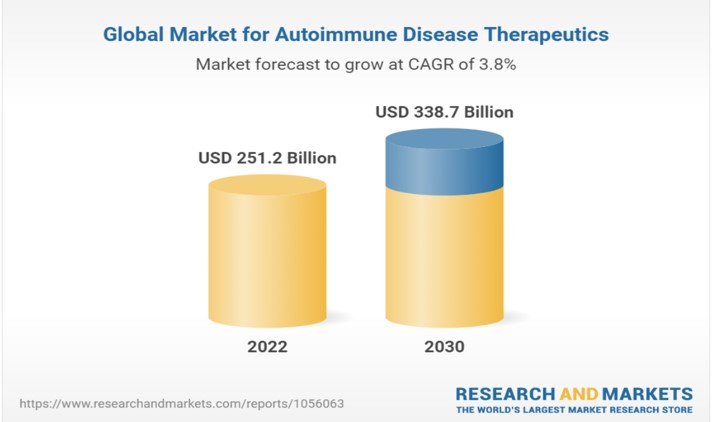 |
|
자가면역질환 치료제 시장 규모 및 전망 |
| 자료 : 리서치앤마켓(Research and Markets), 2024.02 |
국내 역시 의료 및 복지 분야에 있어 자가면역질환에 대한 관심이나 기대가 높습니다. 2014년 한국과학기술정연구원이 국가적 미래상과 사회적 메가트렌드를 기반으로 제시한 보고서에 따르면 바이오분야 뿐만 아니라 모든 기술 분야를 통틀어 미래 유망기술 10가지 중에 자가면역질환 치료기술이 포함되어 있습니다.
[미래유망기술: 자가면역질환 치료기술]
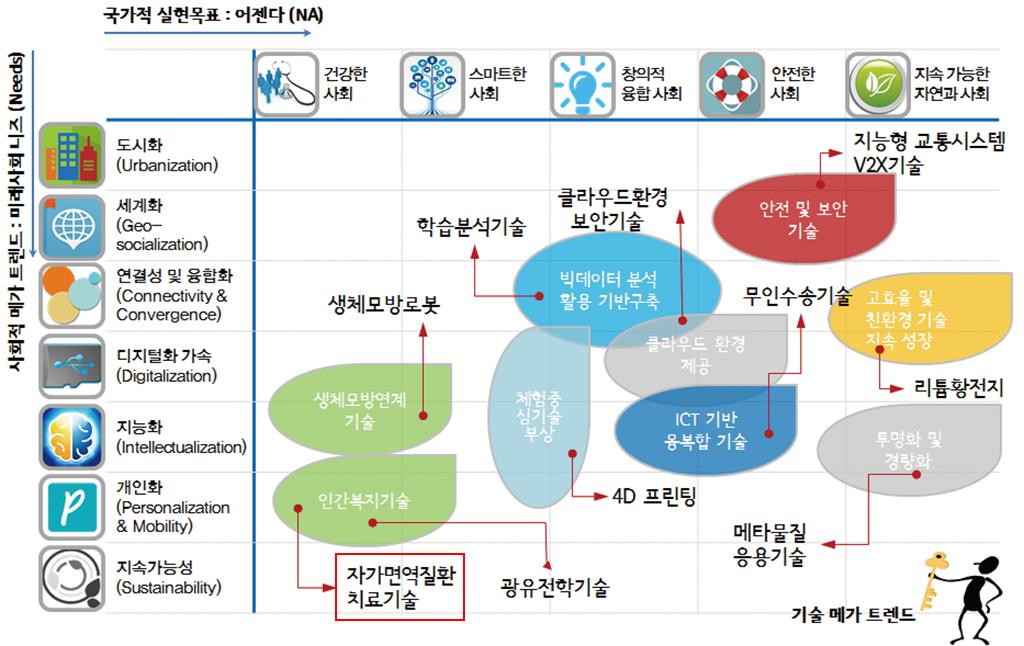 |
|
(출처: 한국과학기술정보연구원, 2014 KISTI 미래유망기술 10선, 2014) |
다) 아토피 피부염 치료제 시장
아토피피부염 치료제의 경우, 전세계 아토피피부염 치료제 시장은 2020년 약 104억 달러에서 연평균 13.1% 수준의 성장을 지속하여 2025년에는 약 193억 달러로 성장할 것으로 전망됩니다.
| [세계 아토피피부염 치료 시장 규모 및 전망] |
| (단위 : 억 달러) |
 |
|
세계 아토피피부염 치료 시장 규모 및 전망 |
| 자료: Market Data Forecast, Atopic Dermatitis Treatment Market, 2020 |
국내 시장만 보았을 때도 아토피피부염은 큰 규모를 나타내고 있습니다. 건강보험심사평가원에 따르면 우리나라 전체 인구대비 아토피피부염 진료실 인원 비중과 절대수치를 보았을 때, 그 수는 약 100만명에 이르며, 소아 및 청소년을 넘어 성인에게도 꾸준히 발생하고 있습니다.
 |
|
연도별 아토피 피부염 환자 증감 추이(단위: 만명) |
| 출처) 건강보험심사평가원, 2020 |
진료실 인원 비중과 상반되게 치료비 규모는 2018년 435억원 규모에서 2022년 1,201억원 규모로 증가하고 있으며, 일시적 증상 완화만 가능한 상태로, 효과적인 치료제에 대한 해법은 아직 없는 상황입니다. 해당 질환은 삶의 질을 급격히 저하시키는 질환으로 전 세계적으로 환자가 꾸준히 발생하고 있어, 당사는 해당 치료제 개발에 매진하고 있습니다.
| [최근 5년 아토피 피부염 질환에 대한 진료환자, 요양급여비 추이] |
| 구 분 |
2018 |
2019 |
2020 |
2021 |
2022 |
5개년 성장률 |
|---|---|---|---|---|---|---|
|
진료환자 (명) |
921,070 |
949,990 |
972,928 |
989,750 |
973,636 |
1.1% |
|
요양급여비 총액 (천원) |
43,562,688 |
45,837,611 |
51,847,661 |
86,472,525 |
120,118,801 |
22.5% |
| 자료: 건강보험심사평가원 보건의료빅데이터개방시스템 |
아직 아토피 피부염의 발병 원인이 정확하게 분석되지 않았음에도 최근 치료비의 증가세에 힘입어 아토피 관련 수많은 제품들이 시중에 출시 되어 있습니다. 아토피 피부염은 면역학적, 유전적, 환경적 요인이 상호작용해 나타나는 대표적인 알러지 질환으로 현재로서는 적절한 치료제가 없기 때문에 병원 치료 외에도 보습제 또는 DIY 천연제품 등 환자 개인마다 다양한 방법으로 관리를 하고 있으며, 이러한 대증요법은 질병의 근본적인 치료보다는 표면적이고 일시적인 증상 완화에 불과합니다. 이에 당사 뿐만 아니라 국내 제약회사들도 부작용을 최소화 할 수 있는 다양한 방법으로 치료제를 개발하고 있습니다.
2018년 3월 사노피아벤티스코리아의 듀피젠트(성분명 두필루맙)가 국내에서 성인 중등증에서 중증 아토피 피부염 치료제로 허가받으면서 새로운 치료 대안으로 제시되었습니다. 2023년에 추가된 소아 치료 적응증을 포함하여 다양한 연령의 중등증에서 중증의 아토피 피부염 환자에게 사용 가능한 주력 치료제로 시장을 선도하고 있습니다. 다만, 듀피젠트가 시장에서 큰 비중을 차지하고 있으나, 매 2주 간격으로 투여를 해야하는 번거로움 등의 단점이 있습니다. 치료효과와 함께 복약 편의성을 높인 신제품 출시 경쟁으로 이러한 아토피 피부염 시장에 국내 제약사들도 앞다퉈 임상에 진입하고 있습니다.
JAK 억제제로 2021년 5월 릴리의 올루미언트(성분명 바리시티닙), 2021년 10월 애브비의 린버크(성분명 유파다시티닙), 2022년 4월 화이자의 시빈코(성분명 아브로시티닙), 2023년 8월 레오파마의 아트랄자(성분명: 트랄로키누맙)이 국내에서 아토피피부염 치료제로 허가를 받으며 새로운 대안을 선택할 수 있게 되었습니다. 다만 자주 복용되어야 한다는 단점이 있습니다.
|
[국내 아토피 치료제 개발 현황] |
| 제약사 | 프로젝트명 | 특징 | 개발단계 |
|---|---|---|---|
| 강스템바이오텍 | Furestem-AD | 제대혈 줄기세포 치료제 | 임상 3상 완료 (단회투여) 임상 1/2a 진행 (반복투여) |
| 큐리언트 | Q301 | 류코트리엔 합성 저해 | 미국 임상 2b상 완료 |
| JW중외제약 | JW1601 | 염증, 가려움증 개선 | 글로벌 2b상 완료 |
| 에스씨엠생명과학 | SCM-AGH | 중등증-중증 아토피피부염 줄기세포 치료제 | 국내 임상 2상 완료 |
| 대웅제약 | DWP212525 | JAK3/TFK 이중 표적 | 전임상 |
| DWP213388 | ITK/BTK 동시 저해 | 미국 임상 1상 진행 | |
| 노바셀 | NCP112 | FPR2 표적 | 국내 1상 완료 |
| 엔지켐생명과학 | EC-18 | 경구투여, 화학합성신약 | 국내 2상 승인 |
| 샤페론 | NuGel | GPCR19 수용체 표적 | 국내 2상, 미국 2상 |
| HK이노엔 | IN-115314 | JAK-1 선택적 억제 | 국내 2상 |
| 출처) 언론사 보도 자료 및 당사 자체 집계(2025.03) |
라) 류마티스관절염 치료제 시장
류마티스관절염 치료제의 경우, 글로벌 류마티스 관절염 시장은 2021년 405억달러 시장으로 예상됩니다. 10년뒤인 2031년은 거의 두배인 725억달러로 성장할 것으로 예상되고 있습니다. 류마티스 관절염은 가장 만성 염증성 골질환으로, 고령의 환자들에게서 높은 유병률을 보이고 있으며 노령화 사회의 지속됨에 따라 환자 수 또한 지속적으로 증가하고 있습니다.
| [Global 류마티스 관절염 시장] |
| (단위 : 백만달러) |
 |
|
Global 류마티스 관절염 시장 |
| 자료: PMR(Persistence Market Research): RA Treatment Market - Global Industry Forecast 2021-2031 |
과거 비스테로이드성 항염제나 스테로이드 제제들이 부작용 등으로 시장에서 외면받은 반면 생물학적 제제들은 비생물학적 항류마티스제제에 대한 반응이 좋지 않았던 환자들의 70% 이상에게서 증상이 호전되어 생물학적제제가 류마티스 관절염 시장을 이끌어 가고 있습니다. 대표적인 생물학제 제제인 종양괴사인자(TNF-α) 억제제는 10년 이상 류마티스관절염 시장을 장악하였으며, TNF-a억제제와 JAK억제제, IL-6억제제가 혼전하는 양상 속에서도 애브비사의 휴미라(TNF-a억제제)는 다수의 적응증 확보와 오랜 투약 경험에서 나오는 안전성 등 강점을 내세우며 국내 시장도 장악하고 있습니다. 다만, 치료 후 약 2년 정도 지나면 내성이 생겨(TNF 억제제에 대한 항체가 생겨) 치료효과를 보이지 않는 것으로 확인되어 TNF-α 억제제를 대체할 만한 치료제의 개발이 요구되고 있는 상황입니다. 이에 최근 새로운 기전으로 작용하는 약물들이 개발되어 당사를 비롯한 제약사들이 류마티스관절염 치료제 TNF-α억제제 시장에 도전하고 있습니다.
| [2020년 글로벌 류마티스 관절염 치료제 시장 Top10 제약사] |
| (단위 : 십억달러) |
| 순위 | 작용기전 | 제품명 | Trade name (Biological name) | 제약사 | 출시 년도 | 매출 (USD) |
|---|---|---|---|---|---|---|
| 1 | TNF-a 억제제 | 휴미라 | Humira® (adalimumab) | 애브비 | 2002 | 20.39 |
| 2 | TNF-α, β 억제제 | 엔브렐 | Enbrel® (etanercept) | 암젠/화이자 | 1998 | 6.37 |
| 3 | CD20 | 리툭산 | Rituxan® (rituximab) | 로슈 | 2006 | 4.52 |
| 4 | TNF-a 억제제 | 레미케이드 | Remicade® (infliximab) | J&J/MSD | 1999 | 4.195 |
| 5 | IL-6 억제제 | 악템라 | Actemra® (tocilizumab) | 로슈 | 2010 | 3.12 |
| 6 | T세포 활성 조절제 | 오렌시아 | Orencia® (abatacept) | BMS | 2005 | 3.2 |
| 7 | TNF-a 억제제 | 심퍼니 | Simponi® (golimumab) | J&J/MSD | 2009 | 2.25 |
| 8 | TNF-a 억제제 | 심지아 | Cimzia® (certolizumab pegol) | UCB | 2009 | 2.1 |
| 9 | JAK 억제제 | 올루미언트 | Olumiant® (baricitinib) | 릴리 | 2020 | 638.9 |
| 10 | IL-1R 억제제 | 키네레트 | Kineret® (anakinra) | 소비 | 2001 | 239 |
| 자료: 각사 Annual Report 및 당사 자체 집계 |
| [류마티스 관절염 치료제 비교] |
|
제품 |
Furestem-RA® |
휴미라 | 레미케이드 | 엔브렐 |
|---|---|---|---|---|
|
구분 |
제대혈 줄기세포 치료제 |
단크론항체 치료제 |
||
|
개발사 |
강스템바이오텍 |
AbbVie |
Johnson & Johnson |
Pfizer |
|
투여주기 |
단회투여 |
2주 1회 |
2주~6주 1회 |
주 1~2회 |
|
부작용 |
면역조절이 이루어지기 |
감염, 결핵, 신경계 이상, 악성종양 및 |
||
|
효과지속성 |
내성없음 |
전체 투여 환자의 1/3 가량이 불응, 지속사용에 따라 효능 저하 발생 |
||
| 자료: 당사 제시 |
마) 크론병 치료제 시장
대표적 염증성 장질환(IBD; Inflammatory Bowel Disease)인 크론병은 현재까지 발생 원인이 밝혀지지 않았으나, 인체를 보호하기 위한 방어체제인 면역계 과민반응으로 인해 염증이 지속돼 장 점막에 손상을 일으키는 것으로 의료계는 추정하고 있습니다. GlobalData의 보고서에 따르면 2012년 글로벌 크론병 시장은 32억 달러 수준으로 향후 10년간 매년 2.8%의 성장률을 보이며 2022년까지 42억 달러까지 성장할 것으로 예상했습니다. 미국, 프랑스 등 주요 10개국을 대상으로 조사한 결과, 미국이 전체 시장의 68%를 장악하고 있으며 캐나다와 일본이 각각 8%, 7%의 점유율로 뒤따르고 있습니다. 향후 오랜 기간 캐나다와 중국, 인도가 시장 성장을 주도할 것으로 내다봤습니다.
전 세계적으로 연간 인구 10만 명 당 0.3명에서 최대 16.5명까지 다양한 유병률을 국가별로 보이고 있으며, 최근 급격히 증가하는 크론병 발병빈도로 인하여 향후 지속적인 시장 성장을 예측했습니다. TNF억제제로 대표되는 기존 치료제들의 잇따른 특허기간 만료로 인하여 신규 파이프라인들의 향후 성장세에 주목하고 있습니다.
환자의 90%는 소장에 염증 및 병변이 생겨 장 절제술을 할 위험이 높고, 수술 환자의 50%는 5년 내 재수술을 하는 등 대표적인 난치성 질환으로 궤양성 대장염과 달리 염증이 입에서 항문까지 위장관 어느 부위라도 발생할 수 있으며, 한번 걸리면 평생 지속하며 합병증을 유발해 사망에 이를 수 있습니다.
3) 시장 경쟁상황
가) 아토피피부염 치료제
1990년대 진입한 치료제 Elidel과 Protopic이 오랜 기간 시장을 장악하고 있어 이들이 커버하지 못하는 심각한 난치 환자에 대한 unmet needs가 더욱 부각되고 있습니다.
아직 아토피 피부염의 발병 원인이 정확하게 분석되지 않았음에도 최근 환자의 증가세와 거대 규모의 시장을 노리고 아토피 관련하여 수많은 제품들이 시중에 출시되어 있습니다. 결국 아토피피부염이라는 질병은 특별한 대체치료제가 존재하지 않고서는 치료제가 아닌, 일반제품들의 경쟁만이 치열해질 뿐이며 치료보다는 상업적인 목적으로 진행됩니다. 스테로이드 제제를 대체할 수 있는 새로운 아토피 치료제가 절실히 요구되며, 미충족 의료 수요를 해결 할 수 있는 줄기세포치료제가 그 대체방법이 될 수 있습니다. 따라서 줄기세포치료제로서 관리가 될 수 있는 중증도 이상의 아토피 피부염을 치료할 수 있을 대체재는 쉽게 출현되지 않을 것으로 예상하고 있습니다.
나) 류마티스관절염 치료제
과거 비스테로이드성 항염제나 스테로이드 제제들이 부작용 등으로 시장에서 외면 받은 반면 생물학적 제제들은 비생물학적 항류마티스제제에 대한 반응이 좋지 않았던 환자들의 70% 이상에게서 증상이 호전되어 생물학적제제가 류마티스 관절염 시장을 이끌어 가고 있습니다. 대표적인 생물학제 제제인 종양괴사인자(TNF-α) 억제제는 10년 이상 류마티스관절염 시장을 장악하였으나 치료 후 약 2년 정도 지나면 내성이 생겨(TNF 억제제에 대한 항체가 생겨) 치료 효과를 보이지 않는 것으로 확인되어 TNF-α 억제제를 대체할 만한 치료제의 개발이 요구되고 있는 상황입니다.
줄기세포치료제는 바이오분야 차세대 시장으로 주목받고 있으며 재생의학의 개념으로 미래의 류마티스 관절염 치료제 시장에서 크게 기대받고 있습니다.
![이미지: [항TNF제제와 신규치료제]](%ED%95%ADtnf.jpg) |
|
[항TNF제제와 신규치료제] |
|
구 분 |
치료제명 |
|
T세포 표적치료제 |
오렌시아 (BMS제약, 2010년 국내허가) |
|
IL-6 저해제(유전자재조합) |
악템라 (로슈, 2012년 국내허가) |
|
야누스 키나아제 억제제 |
젤잔즈 (화이자제약, 2014년 국내허가) |
다) 크론병 치료제
난치성 질환인 크론병을 치료 방법으로는 크게 약물치료와 수술 방법이 있습니다.
약물치료에는 스테로이드제, 항염증제, TNF-α 억제제와 같은 항체 면역억제제 등이 사용되며 약물로 치료가 잘 되지 않거나 합병증이 심한 경우에는 대장절제술 등의 수술을 하는데, 수술을 수차례에 걸쳐 시행하며 만약 반복적으로 소장을 제거하게 되면 영양흡수 장애가 발생하며 일상생활에 상당한 지장을 초래하게 됩니다.
더욱 심각한 경우에는 약 40%에 육박하는 환자들에게서 자살 충동을 느낄 정도로 심각한 질환입니다.
![이미지: [크론병 치료방법 구분]](%ED%81%AC%EB%A1%A0%EB%B3%91%20%EC%B9%98%EB%A3%8C%EB%B0%A9%EB%B2%95.jpg) |
|
[크론병 치료방법 구분] |
보완대체의학 분야의 국제 학술지(Complementary Therapies in Medicine)에 발표된 바에 의하면, 염증성 장질환 진단을 받은 환자의 약 30%가 대체보완요법을 사용한 경험이 있으며, 이 중 대체보완요법의 부작용이 빈번하다고 응답한 환자는 19%, 치료비 부담이 증가했다고 답한 환자비율은 44%였고, 대체보완요법에 대한 신뢰도가 올라갔다고 응답한 환자는 없었습니다. 따라서 현재의 약물치료와 수술을 대체할 만한 적절한 치료방법은 없는 상황이며, 줄기세포 치료제는 크론병을 포함한 희귀·난치성 질병 치료에 있어서 대체 치료가 가능한 시장으로 크게 주목받아 큰 기대를 받고 있습니다.
라) 골관절염 치료제
관절염은 가장 흔한 관절 장애 중에 하나입니다. 노화와 비만(보통 체중을 가진 개인에 비해 비만인 경우 무릎 골관절염에 걸릴 확률이 14배 높음.)은 무릎 골관절염의 가장 흔한 원인이며, 이로 인해 골관절염 환자 수는 지속적으로 증가하고 있습니다. 수년간 혁신이 일어나지 않았던 무릎관절염분야가 최근 급격하게 진전되고 있고, 많은 후보물질들이 활발하게 개발되고 있는 중입니다. 그러나 항체와 같은 물질은 개발에 실패하는 사례가 보고되고 있으며, 골관절염의 통증완화, 기능개선 효과 뿐만 아니라 구조적 질병진행을 억제하거나 회복시키는 근복적인 치료제인 DMOAD(Disease-Modifying Osteoarthritis Drugs)는 여전히 전무한 상태입니다. 골관절염은 진행단계와 환자 상태에 따라 초기, 중기, 말기로 구분되며 초기 단계는 통증치료를 위한 진통소염제, 히알루론신치료제, 물리치료등의 보존적 방법으로 치료하고, 중기단계는 연골재생을 촉진하는 자가세포치료제, 줄기세포 치료제를 이용한 수술적 요법을 적용합니다. 말기단계는 연골 소실로 보행장애증상으로 인공관절 수술을 실시합니다.
연골재생의 촉진 및 통증완화 등 DMOAD로써 수술을 시행하지 않으며, off-the-shelf의 Injection치료법에 대해 절실히 요구되고 있으며, 현재 골관절염치료제로써 DMOAD로써 동종유래줄기세포치료제가 미충족 의료 시장의 해결책이 될 수 있습니다.
4) 회사의 경쟁우위
가) 시장 수요를 충족하는 제품
현재의 시장은 보편적으로 처방되는 스테로이드제부터 '블록버스터' 의약품으로 대표되는 항TNF제제까지 다양한 의약품들이 면역계 질환 치료에 적용되고 있으나 질병의 근본적인 치료가 아닌 증상 완화 또는 지연 수준의 효능과 일부 부작용 사례로 인하여 근본적인 치료를 원하는 '미충족 수요(unmet needs)'가 있습니다.
당사는 이와 같이 치료제 적용에 제약이 있는 시장을 주 타겟으로 하고 있어, 부작용 없이 근본적인 치료가 가능한 새로운 시장 창출이 예상됩니다.
특히 아토피 피부염 치료제의 경우 심각한 난치상태의 수많은 환자 수에도 불구하고, 치료제 요건이 충족되지 않아 아직 시장에서 미개발 영역으로 남아있습니다. 지난
10년동안 아토피 피부염 시장은 큰 변화없이 초기에 진입하였던 치료제(Elidel, Protopic)가 시장을 장악하고 있으나 이는 중등도 이상의 환자들까지 커버하지 못하여 심각한 난치 인구에 대한 치료 수요 충족의 필요성이 강조되고 있습니다.
당사의 '퓨어스템-에이디 주’는 아토피피부염에 대한 'First-in-class' 줄기세포 치료제로서 기존 치료제들이 접근하지 못한 시장을 새롭게 창출할 수 있을 것으로 기대됩니다. 최근 완료된 임상연구 결과 동종제대혈 줄기세포가 지니는 탁월한 면역 조절능을 바탕으로 아토피 중증도지수(SCORAD)가 의미있게 감소함을 확인하였으며, 3개월간 그 효과가 지속됨을 확인하였습니다. 또한 당사의 줄기세포치료제는 간단하고 편리한 투여법(피하주사 또는 정맥주사)을 설정하여 의료인과 환자 모두 에게 편의성을 제공합니다.
나) 누구나 사용이 가능한 동종줄기세포치료제
임상연구가 급증하기 시작한 2010년 이전으로는 자가유래가 우세하였다가 그 이후로는 동종유래의 비율이 크게 증가하였는데 이것은 상업화를 위한 대량생산에는 자가유래 줄기세포보다는 동종유래 줄기세포를 이용하는 것이 더 유리하다는 것에 기인한 것입니다.
[세포기원별 임상개발 현황]
 |
|
(출처: 줄기세포치료제 개발 및 규제 동향 2016, 식품의약처) |
실제 시장에 출시된 세포치료제 매출을 분석해 본 결과, 동종유래 세포치료제가 자가유래 세포치료제에 비하여 보다 높은 상업적 성공 가능성을 보여 왔습니다. 이에 최근 자가유래 세포치료제를 개발하던 회사에서도 점차 동종유래 세포치료제 개발을 위한 연구를 진행하고 있습니다. 당사의 '퓨어스템'은 동종제대혈유래 줄기세포치료제로서 환자 본인의 조직을 채취해야 하는 부담이 없고 출산과정에서 버려지는 medical waste인 제대혈을 채취 즉시 분리 및 배양 공정을 통하여 기성품(off-the-shelf)으로 제조, 치료를 필요로 할 때 언제든지 누구에게나 적용이 가능한 치료제입니다.
다) 우수한 기술력
아토피 피부염을 비롯한 자가면역질환은 그 발병원인이 다양하고 복잡한 대표적인 난치성 질환입니다. 당사는 오랜 연구를 통하여 각 질환별 명확한 치료기전(MoA;
Mechanism of Action)을 규명하여 권위있는 학술지에 소개된 바 있습니다. NOD2 수용체(receptor)가 제대혈유래 줄기세포 내 들어있는 면역인자 중 핵심이 되어 크론병으로 인한 소화기관 염증에 효과가 있음을 규명하여 소화기분야 관련 저널 중 최고 권위를 자랑하는 'Gastroenterology' (IF 16.7)에 소개된 바 있으며, 줄기세포분야 대표적인 저널 'Stem Cells'과 'Nature' 자매지 'Cell Death & Differentiation'에는 아토피 피부염에서 제대혈 줄기세포의 치료기전과 줄기세포의 핵심인자를 규명하였습니다.
당사는 제대혈유래 줄기세포 분리 및 배양에 관한 원천기술을 자체 개발하여 현재 국내외 특허권을 확보하고 있습니다. 하나의 제대혈에서 수백 명의 환자가 치료할 수 있는 대량생산 기술을 갖추고 있으며 이를 장기간 안정적(stable)으로 보관, 유지 관리할 수 있는 생산시스템을 구축하고 있습니다.
라) 산업 인프라 확보
당사는 사업을 영위하기 위한 설비, 인력, 네트워크 등의 인프라가 탄탄하게 구축되어 있습니다. 2019년 완공된 줄기세포GMP센터' '퓨어스템' 임상시험용 의약품을 비롯하여 화장품 원료로 사용되는 줄기세포배양액 과 세포배양배지 등을 생산하고 있으며, 연간 36,000vial 생산가능한 규모로 아토피피부염 치료제 국내 출시에 대비한 양산용 설비입니다. 또한 원천기술 발명에 기여한 전문 연구인력들을 비롯하여, 석박사급 이상의 우수한 인력을 지속적으로 충원하며 know-how를 전수하고 있습니다.
마) 파트너링을 통한 우수한 영업력 및 생산력 확보
당사는 2014년 12월 대웅제약과 줄기세포치료제에 대한 판권 및 공동연구개발 계약을 체결하고 2019년 2월 변경합의를 통하여 대웅제약은 현재 임상개발중인 퓨어스템 2개 제품의 판권을 보유하게 되었습니다. 대웅제약은 국내 제약사 중 3위권의 매출규모를 지닌 대형제약사로 오랜 업력을 바탕으로 특히 전문의약품 분야에 우수한 영업력을 보유하고 있습니다. 또한 후속적응증에 대한 공동연구개발을 진행하면서 당사의 제대혈유래 줄기세포 치료제 상업화에 적극 동참함으로써 단순 제품 유통/판매 이상의 파트너링 관계를 구축해가고 있습니다.
또한 당사는 2024년 11월 유영제약과 무릎골관절염 치료제(OSCA, 구.퓨어스템-오에이 키트 주)의 국내 독점판매권·통상실시권에 대한 라이선스 계약을 체결함에 따라 마일스톤에 따른 임상을 진행할 예정입니다. 당사의 줄기세포 관련 전문기술과 더불어 파트너사의 골관절염 치료제의 임상개발 및 영업 마케팅 경험을 통한 노하우를 활용함으로써 보다 시장 중심적(market-oriented)제품을 개발 하여 시장 성공 가능성을 높일 수 있는 시너지 효과가 기대됩니다.
[화장품 사업부문]
1) 산업의 특성
화장품 산업은 유행에 민감한 전형적인 트렌드 기반의 산업으로 경기변동과도 밀접한 영향을 받습니다. 최근 제약기반의 신규 카테고리 형성 및 고성장 추세에 따라, 제약회사들의 화장품산업 진출 및 효능 중심의 화장품이 급부상되며, 코스메슈티컬(Costmetic 화장품+Pharmaceutical 의약품) 카테고리가 고성장세의 새로운 화장품 트렌드로 주목받고 있습니다. 특히 당사가 보유한 첨단 바이오원료인 제대혈줄기세포배양액 함유 화장품은 대표적인 바이오 코스메슈티컬 화장품으로 인지되고 있습니다.
또한 화장품 산업은 지속 가능한 문화산업으로 성장 및 확장을 거듭하는 고부가가치 산업니다. 초기의 화장품 산업은 대형사 위주의 시장이 형성되어있었으나 OEM 및 ODM 방식의 제조 및 판매가 용이해짐에 따라 진입장벽이 높지 않아 새로운 중소형 브랜드와 제품들이 꾸준히 출시되고 있습니다. 이에 산업 내 경쟁이 치열해지고 있습니다. 또한, 백화점. 브랜드샵과 같은 전통의 오프라인 유통 채널 외에도 멀티브랜드샵, H&B스토어와 같은 신규 오프라인 유통 채널이 생겨남에 따라 소비자의 다양성을 고려한 제품들이 출시되고 있습니다.
최근에는 브랜드 자사온라인몰이나 대형 온라인 쇼핑몰뿐만 아니라 개인 SNS 채널 등을 이용한 온라인 채널이 등장함에 따라 다품종 소량 생산, 급격한 트렌드 대응으로 소비자의 욕구를 만족시키는 브랜드들이 늘어나고 있습니다.
2) 산업의 성장성
2022년 코로나19로 인한 경기 침체로 국내 화장품 생산 실적은 전년대비 18.4% 감소한 13조 원을 기록했습니다.
다만 바이오 및 피부과학을 기반으로 첨단 바이오 원료를 함유한 화장품에 대한 수요는 향후 지속적이며 안정적으로 창출될 것으로 예상되며, 타겟 수요층이 밀집한 판매채널을 확보하고 효율적인 마케팅이 진행된다면, 안정적 내수시장 확보가 가능할 것으로 전망하고 있습니다. 향후 첨단바이오 원료를 함유한 화장품은 내수시장 및 수출 상황 등을 고려하였을 때, 안정적인 성장세를 이어갈 것으로 예상됩니다.
[화장품 산업 현황]
(글로벌)
| 구분 | 2021년 | 2022년 | 2023년(E) | 2024년(E) | 2025년(E) | 2026년(E) |
| 시장규모 (십억 달러) |
430.3 | 463.2 | 508.3 | 549.2 | 590.9 | 635.3 |
| 증가율 (%) |
8.06 | 7.65 | 9.74 | 8.05 | 7.59 | 7.51 |
(출처: 한국보건산업진흥원, 2024)
(국내)
| 구분 | 2018년 | 2019년 | 2020년 | 2021년 | 2022년 | 2023년 |
| 생산금액(조원) | 15.50 | 16.26 | 15.16 | 16.65 | 13.59 | 14.51 |
| 성장률(%) | 14.70 | 4.91 | -6.77 | 9.84 | -18.39 | 6.77 |
(출처: 식약처, 2024 식품의약품 산업동향통계)
3) 경기변동의 특성 및 계절성
화장품은 경기 동향에 민감하게 반응하며 계절에 따라 선호 상품과 수요에 대한 차이가 생깁니다. 이러한 경기 변동 및 계절적 특성을 이용하여 빠르게 변화하는 소비자의 다양한 니즈를 충족시킬수 있는 차별성 있는 제품 개발 및 마케팅이 필요합니다.
4) 시장여건
중소형 화장품 브랜드의 출연으로 시장은 계속적으로 확장되고 있으나 그만큼 경쟁이 심화되고 있습니다. 빠르게 변화하는 트렌드를 따라잡고 초기의 선점이 중요시되어지고 있습니다. 이에 화장품 회사들은 경쟁력 강화를 위해 연구개발을 통한 질적 향상 및 고객 서비스 강화 등의 노력을 이어가고 있습니다.
5) 시장점유율 추이
국내 화장품 시장은 아모레퍼시픽, LG생활건강과 같은 대형사와 토니모리, 클리오 등과 같은 중형사들이 대부분의 시장을 점유하고 있습니다.
당사의 화장품 매출액 추이는 다음과 같습니다.
| 구분 (백만원) | 2021 | 2022 | 2023 | 2024 |
|---|---|---|---|---|
| 매출액 | 3,182 | 4,010 | 4,117 | 3,274 |
2. 그 밖에 투자의사결정에 필요한 사항
가. 지식재산권 현황
당사는 보고서 제출일 현재 총 303건의 지식재산권을 보유하고 있습니다. 줄기세포 사업부문은 특허권은 98건의 등록과 PCT를 포함한 110건의 출원을 합하여 총 208건이 있으며, 상표권은 등록 36건과 1건의 출원이 있습니다. 또한, 화장품 사업무문은 43건의 상표권 등록과 1건의 출원이 있으며, 2건의 디자인권을 보유하고 있습니다.
|
구분 |
국내 |
해외 |
PCT |
합계 |
||
| 줄기세포 사업부문 |
특허권 |
등록 |
34 | 64 | - | 98 |
|
출원 |
23 | 53 | 34 | 110 | ||
| 상표권 |
등록 |
25 | 11 | - | 36 | |
|
출원 |
1 | - | - | 1 | ||
| 디자인권 | 등록 | 5 | 3 | - | 8 | |
| 출원 | - | 4 | - | 4 | ||
| 화장품 사업부문 |
상표권 |
등록 |
24 | 19 | - | 43 |
|
출원 |
- | 1 | - | 1 | ||
| 디자인권 |
등록 |
2 | - | - | 2 | |
|
출원 |
- | - | - | - | ||
|
합계 |
114 | 155 | 34 | 303 | ||
1) 특허권
| 구분 | 내 용 | 권리자 | 국 가 | 출원일 | 등록일 | 적용제품 |
|---|---|---|---|---|---|---|
| 1 | ZNF281을 발현하는 제대혈 유래 만능 줄기세포의 분리방법 |
서울대학교 산학협력단 (전용실시권 : 강스템바이오텍) |
한국 | 2009.03.20 | 2010.03.23 | 줄기세포 분리배양 원천기술 |
| 2 | PCT | 2010.03.03 | 해당없음 | |||
| 3 | 미국 | 2011.09.20 | 2020.03.10 | |||
| 4 | 일본 | 2011.09.20 | 2016.09.28 | |||
| 5 | 일본 (분할 출원) |
2015.01.05 | 2016.11.11 | |||
| 6 | 중국 | 2011.10.14 | 2015.07.22 | |||
| 7 | 유럽 | 2011.10.19 | 2018.12.13 | |||
| 8 | 영국 | 2011.10.19 | 2018.12.13 | |||
| 9 | 독일 | 2011.10.19 | 2018.12.13 | |||
| 10 | 프랑스 | 2011.10.19 | 2018.12.13 | |||
| 11 | 이탈리아 | 2011.10.19 | 2018.12.13 | |||
| 12 | 스페인 | 2011.10.19 | 2018.12.13 | |||
| 13 | 네덜란드 | 2011.10.19 | 2018.12.13 | |||
| 14 | 스위스 | 2011.10.19 | 2018.12.13 | |||
| 15 | 폴란드 | 2011.10.19 | 2018.12.13 | |||
| 16 | 벨기에 | 2011.10.19 | 2018.12.13 | |||
| 17 | 러시아 | 2011.10.18 | 2014.04.10 | |||
| 18 | 말레이시아 | 2011.09.20 | 2017.02.28 | |||
| 19 | 호주 | 2011.10.18 | 2014.10.09 | |||
| 20 | 베트남 | 2011.09.20 | 2018.10.17 | |||
| 21 | 인도 | 2011.10.18 | 2019.01.01 | |||
| 22 | 인도네시아 | 2011.09.20 | 2018.05.15 | |||
| 23 | ZNF281을 발현하는 제대혈 유래 줄기세포의 대량 배양방법 |
서울대학교 산학협력단 (전용실시권 : 강스템바이오텍) |
한국 | 2009.09.14 | 2012.06.14 | 줄기세포 분리배양 원천기술 |
| 24 | 한국(분할) | 2014.04.14 | 2016.05.31 | |||
| 25 | HMGA2를 이용하여 비신경세포로부터 리프로그래밍된 유도신경 줄기 세포를 제조하는 방법 (Method for Producing Reprogrammed Induced Neural Stem Cells from Non-Neuronal Cells Using HMGA2) |
강스템바이오텍/ 서울대학교 산학협력단 |
한국 | 2014.04.04 | 2018.06.18 | 유도신경 줄기세포 |
| 26 | 호주 | 2015.10.19 | 2017.10.16 | |||
| 27 | PCT | 2014.04.04 | 해당없음 | |||
| 28 | 일본 | 2015.10.05 | 2018.03.28 | |||
| 29 | 중국 | 2015.12.04 | 2020.11.10 | |||
| 30 | 미국 | 2015.10.05 | 2022.11.29 | |||
| 31 | NOD2의 아고니스트를 처리한 줄기세포 또는 그 배양물을 포함하는 면역질환 또는 염증질환의 예방 또는 치료용 약학조성물 (Pharmaceutical Composition Comprising Stem Cells Treated with NOD2 Agonist or Culture Thereof for Prevention and Treatment of Immune Disorders and Inflammatory Diseases) |
강스템바이오텍 | 한국 | 2011.08.19 | 2015.01.02 | 아토피 크론병 |
| 32 | PCT | 2011.08.19 | 해당없음 | |||
| 33 | 일본 | 2013.02.22 | 2015.09.11 | |||
| 34 | 중국 | 2013.03.22 | 2016.08.24 | |||
| 35 | 중국(분할) | 2016.02.23 | 2023.11.07 | |||
| 36 | 유럽 | 2013.03.21 | 2019.03.27 | |||
| 37 | 영국 | 2013.03.21 | 2019.02.14 | |||
| 38 | 독일 | 2013.03.21 | 2019.02.14 | |||
| 39 | 프랑스 | 2013.03.21 | 2019.02.14 | |||
| 40 | 이탈리아 | 2013.03.21 | 2019.02.14 | |||
| 41 | 스페인 | 2013.03.21 | 2019.02.14 | |||
| 42 | 스위스 | 2013.03.21 | 2019.02.14 | |||
| 43 | 미국 | 2013.04.09 | 2016.06.29 | |||
| 44 | 미국-CIP | 2016.08.08 | - | |||
| 45 | PI3K/AKT/GSK3 경로를 통해 성체줄기세포의 증식, 다분화능 및 재프로그래밍을 촉진하는 CD49f (CD49f Promoting Proliferation, Multipotency and Reprogramming of Adult Stem Cells through PI3K/AKT/GSK4 Pathway) |
강스템바이오텍 | 한국(분할) | 2018.10.29 | 2020.08.26 | 줄기세포 분리배양 원천기술 |
| 46 | PCT | 2011.02.18 | 해당없음 | |||
| 47 | 미국 | 2012.09.28 | 2015.09.22 | |||
| 48 | 중국 | 2012.10.18 | 2015.06.10 | |||
| 49 | 유럽 | 2012.09.18 | 2021.04.21 | |||
| 50 | 독일 | 2012.09.18 | 2021.04.21 | |||
| 51 | 영국 | 2012.09.18 | 2021.04.21 | |||
| 52 | 프랑스 | 2012.09.18 | 2021.04.21 | |||
| 53 | 말과동물 양수 유래 다분화능 줄기세포 및 그 제조방법 (Equine Amniotic Fluid-Derived Multipotent Stem Cells and a Method for Producing the Same) |
강스템바이오텍 | 한국 | 2011.09.07 | 2014.03.24 | 동물 줄기세포 |
| 54 | PCT | 2011.09.07 | 해당없음 | |||
| 55 | 일본 | 2013.03.07 | 2015.11.06 | |||
| 56 | 미국 | 2013.04.24 | 2016.03.22 | |||
| 57 | 유럽 | 2013.04.04 | 2018.08.15 | |||
| 58 | 영국 | 2013.04.04 | 2018.08.15 | |||
| 59 | 프랑스 | 2013.04.04 | 2018.08.15 | |||
| 60 | 독일 | 2013.04.04 | 2018.08.15 | |||
| 61 | 말과동물 양막-유래 중간엽 줄기세포 (Equine Amniotic Membrane-Derived Mesenshymal Stem Cells) |
강스템바이오텍 | PCT | 2012.11.22 | 해당없음 | 동물 줄기세포 |
| 62 | 한국 | 2011.11.22 | 2018.10.02 | |||
| 63 | 미국 | 2014.05.22 | 2017.05.16 | |||
| 64 | 개과동물 양막-유래 다분화능 줄기세포 (Canine Amniotic Membrane-Derived Multipotent Stem Cells) |
강스템바이오텍 | PCT | 2012.12.06 | 해당없음 | 동물 줄기세포 |
| 65 | 미국 | 2014.06.05 | 2017.09.26 | |||
| 66 | 비만세포 과립을 처리한 줄기세포 또는 그 배양물을 포함하는 면역질환 또는 염증질환의 예방 또는 치료용 약학조성물 |
강스템바이오텍 | 한국 | 2015.09.24 | 2017.08.02 | 아토피 |
| 67 | PCT | 2015.09.24 | 해당없음 | |||
| 68 | GDF11을 포함하는 조성물 및 그의 용도 | 강스템바이오텍 | 한국 | 2016.02.04 | 2017.12.13 | 화장품원료 |
| 69 | 한국(분할) | 2017.09.19 | 2018.08.24 | |||
| 70 | PCT | 2016.12.02 | 해당없음 | |||
| 71 | 망막색소상피 분화 유도용 조성물 | 강스템바이오텍/ 서울대학교 산학협력단 |
한국 | 2015.10.28 | 2019.05.21 | 안과질환 |
| 72 | SOD3를 과발현하는 줄기세포를 유효성분으로 포함하는 염증성 질환의 예방 또는 치료용 조성물 |
강스템바이오텍 | 한국 | 2016.09.19 | 2021.04.21 | 아토피, 건선 |
| 73 | PCT | 2016.09.15 | 해당없음 | |||
| 74 | 미국 | 2018.03.14 | 2023.08.22 | |||
| 75 | 미국(CA) | 2023.06.14 | - | |||
| 76 | 일본 | 2018.03.15 | 2021.12.13 | |||
| 77 | 중국 | 2018.05.14 | 2022.08.02 | |||
| 78 | 퇴행성 뇌질환을 예방, 개선 또는 치료하는 유황의 법제방법 및 상기 방법으로 법제된 유황 | 강스템바이오텍/ 원광대 산학협력단 |
한국 | 2014.10.08 | 2016.07.18 | 신경계질환 |
| 79 | 퇴행성 신경계질환에 유효한 오공을 포함하는 복합약침의 제조방법 및 상기 방법으로 제조 된 복합약침 |
강스템바이오텍/ 원광대 산학협력단 |
한국 | 2014.10.10 | 2016.09.26 | 신경계질환 |
| 80 | 뇌신경세포 보호 기능이 있는 천연물 조성물 및 그를 이용한 건강 음료 |
강스템바이오텍/ 원광대 산학협력단 |
한국 | 2014.10.08 | 2016.11.01 | 신경계질환 |
| 81 | DNA메탈기전달효소 억제제를 처리한 줄기세포 또는 그 배양물을 포함하는 면역질환 또는 염증질환의 예방 또는 치료용 약학조성물 |
강스템바이오텍 | 한국 | 2014.03.06 | 2015.04.24 | 크론병 |
| 82 | 줄기세포를 유효 성분으로 함유하는 면역질환 또는 염증 질환의 예방 또는 치료용 조성물 | 강스템바이오텍 | 한국 | 2013.02.21 | 2015.04.08 | 퓨어스템 |
| 83 | PCT | 2013.02.22 | 해당없음 | |||
| 84 | 피부세포로부터 기능성 인슐린생산 세포의 직접 제조 방법 |
강스템바이오텍/ 서울대학교 산학협력단 |
한국 | 2012.10.24 | 2015.02.02 | 당뇨병 |
| 85 | 제대혈 유래 중간엽 줄기세포의 세포외기질을 유효성분으로 함유하는 암치료용 약제학적 조성물 | 강스템바이오텍 | 한국 | 2012.06.26 | 2014.06.30 | 항암제 |
| 86 | PCT | 2011.01.13 | 해당없음 | |||
| 87 | 성체 줄기세포로부터 췌장 베타 유사세포를 제조하는 방법 |
강스템바이오텍 | 한국 | 2011.02.18 | 2013.11.25 | 당뇨병 |
| 88 | miRNA의 발현 억제를 이용한 성체줄기세포의 노화 억제방법 |
강스템바이오텍 | 한국 | 2011.03.31 | 2013.08.19 | 줄기세포 분리배양 원천기술 |
| 89 | 제대혈 또는 지방조직유래 성체줄기세포를 함유한 항암용 조성물 |
강스템바이오텍 | 한국 | 2009.04.15 | 2013.04.24 | 항암제 |
| 90 | 개의 제대혈, 태반 및 개 태아의 심장 유래 다분화능 성체줄기세포, 그 제조방법 및 이를 함유하는 세포 치료제 |
강스템바이오텍 | 한국 | 2006.05.12 | 2007.12.31 | 동물 줄기세포 |
| 91 | Oct-4, Cripto-1, ABCG2 또는 에스트로겐 수용체를 마커로 이용한 줄기세포 또는 종양줄기세포의 검출방법 및 항암물질의 스크리닝 방법 |
강스템바이오텍 | 한국 | 2006.11.28 | 2008.08.01 | 항암제 |
| 92 | 비신경 세포를 이용한 유도신경줄기세포의 제조방법 |
강스템바이오텍/ 서울대학교 산학협력단 |
한국 | 2016.05.25 | 2017.09.11 | 신경계질환 |
| 93 | PCT | 2016.05.25 | 해당없음 | |||
| 94 | 연골 무세포 파쇄물 및 줄기세포를 포함하는 연골분화 촉진용 복합체 및 그의 용도 | 강스템바이오텍 | 한국 | 2017.07.04 | 2018.09.18 | 퇴행성 관절염 |
| 95 | PCT | 2017.07.04 | 해당없음 | |||
| 96 | 일본 | 2017.07.04 | 2021.08.12 | |||
| 97 | 미국 | 2019.01.04 | - | |||
| 98 | 중국 | 2019.03.01 | - | |||
| 99 | 유럽 | 2019.01.30 | 2022.09.07 | |||
| 100 | 영국 | 2019.01.30 | 2022.09.07 | |||
| 101 | 독일 | 2019.01.30 | 2022.09.07 | |||
| 102 | 프랑스 | 2019.01.30 | 2022.09.07 | |||
| 103 | 이탈리아 | 2019.01.30 | 2022.09.07 | |||
| 104 | 스페인 | 2019.01.30 | 2022.09.07 | |||
| 105 | 네덜란드 | 2019.01.30 | 2022.09.07 | |||
| 106 | 스위스 | 2019.01.30 | 2022.09.07 | |||
| 107 | 터키 | 2019.01.30 | 2022.09.07 | |||
| 108 | 벨기에 | 2019.01.30 | 2022.09.07 | |||
| 109 | Sox2, C-myc을 이용하여 비신경 세포로부터 직접 리프로그래밍 된 유도신경줄기 세포를 제조하는 방법 |
강스템바이오텍 | 한국 | 2018.05.09 | 2020.10.14 | 신경계질환 |
| 110 | PCT | 2019.05.09 | 해당없음 | |||
| 111 | HLA 유전자가 제거된 인간 유도만능줄기세포 유래 중간엽 줄기세포 및 그의 제조방법 | 강스템바이오텍 | 한국 | 2019.05.30 | 2021.09.15 | 이식적합성 치료제개발 |
| 112 | PCT | 2019.05.30 | 해당없음 | |||
| 113 | 유럽 | 2020.12.16 | - | |||
| 114 | 미국 | 2020.11.30 | - | |||
| 115 | 효능이 증진된 줄기세포의 제조방법 | 강스템바이오텍 | PCT | 2020.12.16 | 해당없음 | |
| 116 | 미국 | 2022.06.16 | - | |||
| 117 | 유럽 | 2022.07.11 | - | |||
| 118 | 세포해동기 | 강스템바이오텍/ ㈜아모그린텍 |
한국 | 2021.06.25 | - | 세포치료제 해동기 |
| 119 | PCT | 2022.06.20 | 해당없음 | |||
| 120 | 미국 | 2023.12.25 | - | |||
| 121 | 유럽 | 2023.12.20 | - | |||
| 122 | 세포해동기 및 이의 운전방법 (1) | 한국 | 2021.07.27 | 2024.06.26 | ||
| 123 | 세포해동기 및 이의 운전방법 (2) | 한국 | 2021.07.27 | 2025.01.13 | ||
| 124 | 세포해동기 및 이의 운전방법 (3) | 한국 | 2021.07.27 | 2025.01.13 | ||
| 125 | 세포해동기 | 한국 | 2021.11.05 | - | ||
| 126 | 한국 | 2021.11.05 | - | |||
| 127 | 한국 | 2021.11.05 | - | |||
| 128 | 세포해동기 및 이의 운전방법 | PCT | 2022.06.20 | 해당없음 | ||
| 129 | 미국 | 2023.12.25 | - | |||
| 130 | 유럽 | 2023.12.20 | - | |||
| 131 | 세포해동기 및 이의 운전방법 | PCT | 2022.06.20 | 해당없음 | ||
| 132 | 미국 | 2023.12.25 | - | |||
| 133 | 유럽 | 2023.12.20 | - | |||
| 134 | 세포해동기 및 이의 운전방법 | PCT | 2022.06.20 | 해당없음 | ||
| 135 | 미국 | 2023.12.25 | - | |||
| 136 | 유럽 | 2023.12.20 | - | |||
| 137 | off-the-shelf 줄기세포 및 면역세포, 이를 포함하는 약학적 조성물 |
강스템바이오텍 | 한국 | 2020.01.23 | 2024.06.04 | 혈액암 |
| 138 | PCT | 2021.01.22 | 해당없음 | |||
| 139 | 미국 | 2021.01.22 | - | |||
| 140 | 일본 | 2021.01.22 | - | |||
| 141 | 중국 | 2021.01.22 | - | |||
| 142 | 유럽 | 2021.01.22 | - | |||
| 143 | 주입이 가능한 동물 연골유래 주사제의 제조 방법 및 이의 이용 |
강스템바이오텍 | 한국 | 2021.11.26 | - | 퇴행성 관절염 |
| 144 | PCT | 2021.11.26 | 해당없음 | |||
| 145 | 유럽 | 2023.06.23 | - | |||
| 146 | 미국 | 2023.03.10 | - | |||
| 147 | 중국 | 2023.05.26 | - | |||
| 148 | 일본 | 2023.05.26 | - | |||
| 149 | 일본(분할) | 2025.02.07 | ||||
| 150 | 호주 | 2023.06.27 | - | |||
| 151 | 강스템바이오/에이템즈㈜ | 한국(분할) | 2023.04.10 | - | ||
| 152 | 미국(분할) | 2023.06.13 | - | |||
| 153 | 중국(분할) | 2023.08.04 | - | |||
| 154 | 유럽(분할) | 2023.07.03 | - | |||
| 155 | 칼시뉴린 억제제와 줄기세포를 사용하여 면역질환을 치료하는 방법 |
강스템바이오텍 | 한국 | 2022.08.19 | - | 줄기세포 제조기술 |
| 156 | PCT | 2022.08.19 | 해당없음 | |||
| 157 | 미국 | 2024.02.13 | - | |||
| 158 | 중국 | 2024.03.20 | - | |||
| 159 | 일본 | 2024.02.19 | - | |||
| 160 | 유럽 | 2024.02.27 | - | |||
| 161 | 만능성 줄기세포 유래 피부 오가노이드를 이용한 아토피 피부염 모델 제작 방법 |
강스템바이오텍 | 한국 | 2021.10.20 | 2025.02.04 | 이식적합성 치료제개발 |
| 162 | PCT | 2021.10.21 | 해당없음 | |||
| 163 | 한국(분할) | 2024.09.12 | - | |||
| 164 | 미국 | 2023.04.19 | - | |||
| 165 | 호주 | 2023.04.19 | - | |||
| 166 | 일본 | 2023.04.20 | - | |||
| 167 | 중국 | 2023.04.20 | - | |||
| 168 | 유럽 | 2023.04.21 | - | |||
| 169 | 앱타머를 이용한 고기능성 인공장기 제작 방법 | 강스템바이오텍 | 한국 | 2020.11.12 | - | 이식적합성 치료제개발 |
| 170 | 한국(분할) | 2024.03.20 | - | |||
| 171 | 한국(분할) | 2024.07.02 | - | |||
| 172 | PCT | 2021.07.27 | 해당없음 | |||
| 173 | 유럽 | 2023.03.03 | - | |||
| 174 | 호주 | 2023.02.02 | 2024.09.26 | |||
| 175 | 미국 | 2023.02.03 | - | |||
| 176 | 일본 | 2023.02.06 | - | |||
| 177 | 일본(분할) | 2025.03.05 | ||||
| 178 | 중국 | 2023.02.06 | - | |||
| 179 | 무혈청배지를 이용한 줄기세포 배양 방법 | 강스템바이오텍 | 한국 | 2023.02.27 | - | 줄기세포 제조기술 |
| 180 | PCT | 2023.02.27 | - | |||
| 181 | 미국 | 2024.08.23 | - | |||
| 182 | 유럽 | 2024.09.24 | - | |||
| 183 | 일본 | 2024.08.26 | - | |||
| 184 | 중국 | 2024.08.26 | - | |||
| 185 | 마이크로캐리어를 이용한 줄기세포 배양 방법 | 강스템바이오텍 | 한국 | 2023.02.27 | - | 줄기세포 제조기술 |
| 186 | PCT | 2023.02.27 | 해당없음 | |||
| 187 | 미국 | 2024.08.23 | - | |||
| 188 | 유럽 | 2024.09.24 | - | |||
| 189 | 일본 | 2024.08.26 | - | |||
| 190 | 중국 | 2024.08.26 | - | |||
| 191 | 면역질환 또는 염증질환 치료용 조성물 | 강스템바이오텍 | 한국 | 2019.12.26 | - | |
| 192 | 정적 부유 배양법을 이용한 췌도 오가노이드의 제조방법 |
강스템바이오텍 | 한국 | 2023.10.11 | - | |
| 193 | PCT | 2023.12.20 | 해당없음 | |||
| 194 | 연골 분화능이 증진된 줄기세포의 선별 방법 및 이를 포함하는 세포 치료제 |
강스템바이오텍 | 한국 | 2023.12.22 | - | 줄기세포 제조기술 |
| 195 | PCT | 2023.12.22 | 해당없음 | |||
| 196 | 프라이밍 중간엽 줄기세포를 유효성분으로 포함하는 급성 호흡곤란 증후군 예방 또는 치료용 조성물 | 강스템바이오텍 | 한국 | 2024.11.07 | - | ARDS |
| 197 | 강스템바이오텍 | PCT | 2024.11.07 | 해당없음 | ||
| 198 | 모낭 오가노이드 제작 및 배양방법과 이를 이용한 모발 약물 스크리닝 방법 및 모발 이식 소재 | 강스템바이오텍 | 한국 | 2024.03.18 | - | |
| 199 | PCT | 2024.03.18 | - | |||
| 200 | 액티빈 A를 분비하는 중간엽 줄기세포를 포함하는 M1 대식세포의 활성 또는 분화 억제 및 M2 대식세포로의 분화 유도용 조성물 | 강스템바이오텍 | 한국 | 2025.01.24 | - | |
| 201 | 강스템바이오텍 | PCT | 2025.01.24 | - | ||
| 202 | 피부 손상 오가노이드 모델 및 이를 이용한 약물 스크리닝 방법 |
강스템바이오텍 | 한국 | 2024.10.04 | - | |
| 203 | 강스템바이오텍 | PCT | 2024.10.08 | 해당없음 | ||
| 204 | 강스템바이오텍 | 미국 | 2024.11.28 | - | ||
| 205 | 라파마이신을 함유 약물 전달체가 접합된 줄기세포 및 이의 용도 | 부산대산단, 성균관대산단, 강스템바이오텍 | 한국 | 2024.05.10 | - | |
| 206 | 부산대산단, 성균관대산단, 강스템바이오텍 | 미국 | 2025.02.18 | - | ||
| 207 | 피부 오가노이드를 이용한 의료/미용기기 유효성 평가 모델 및 평가 방법 | 강스템바이오텍 | 한국 | 2024.11.28 | - | |
| 208 | 무릎 골관절염 환자에서 동종 제대혈 유래 중간엽 줄기세포(OSCA)의 관절내 주입을 이용한 1상 연구 | 강스템바이오텍 | 한국 | 2024.11.29 | - |
2) 디자인권
| 구분 | 내 용 | 권리자 | 국 가 | 출원일 | 등록일 | 적용제품 |
| 1 | 실험실용 트레이 | 강스템바이오텍 | 한국 | 2020.03.24 | 2020.11.12 | 퓨어스템 |
| 2 | 바이알병 보관용 박스 | 강스템바이오텍 | 한국 | 2020.03.24 | 2021.01.07 | 퓨어스템 |
| 헤이그 | 2022.09.06 | - | ||||
| 일본 | 2022.08.19 | 2023.10.10 | ||||
| 2023.11.07 | ||||||
| 미국 | 2022.08.19 | 2024.12.17 | ||||
| 독일 | 2022.08.19 | - | ||||
| 영국 | 2022.08.19 | - | ||||
| 싱가포르 | 2022.08.19 | - | ||||
| 베네룩스(벨기에, 네덜란드, 룩셈부르크) | 2022.08.19 | - | ||||
| 3 | 바이알병 보관용 박스 | 강스템바이오텍 | 한국 | 2021.01.15 | 2022.01.18 | 퓨어스템 |
| 4 | 바이알병 보관용 박스(64 셀박스) | 강스템바이오텍 | 한국 | 2020.08.11 | 2021.10.27 | 퓨어스템 |
| 5 | 실험용 플로팅 바이알 랙 | 강스템바이오텍 | 한국 | 2020.08.11 | 2021.06.04 | 퓨어스템 |
III. 재무에 관한 사항
1. 요약재무정보
가. 요약재무정보
| (단위 : 원) |
| 구 분 | 제16기 1분기 | 제15기 | 제14기 |
|---|---|---|---|
| (2025년 3월말) | (2024년 12월말) | (2023년 12월말) | |
| [유동자산] | 23,575,514,872 | 28,528,439,364 | 47,366,035,977 |
| ㆍ현금및현금성자산 | 2,165,830,750 | 2,766,684,203 | 5,855,668,775 |
| ㆍ단기금융상품 | 15,500,082,185 | 15,500,049,761 | 31,504,443,494 |
| ㆍ매출채권 및 기타채권 | 1,597,849,251 | 5,272,741,542 | 4,760,825,000 |
| ㆍ당기법인세자산 | 205,942,890 | 188,795,200 | 206,212,050 |
| ㆍ계약자산 | - | - | 724,251,696 |
| ㆍ재고자산 | 866,948,504 | 858,298,912 | 578,259,711 |
| ㆍ계약이행원가 | 1,541,048,682 | 1,853,184,108 | 2,201,681,606 |
| ㆍ기타자산 | 1,697,812,610 | 2,088,685,638 | 1,534,693,645 |
| [비유동자산] | 26,628,244,919 | 27,457,674,670 | 33,887,005,225 |
| ㆍ장기금융상품 | 100,000,000 | 100,000,000 | 170,000,000 |
| ㆍ당기손익-공정가치측정금융자산 | 2,753,285,654 | 2,932,656,126 | 2,779,723,098 |
| ㆍ장기기타채권 | 262,279,558 | 217,996,184 | 166,317,638 |
| ㆍ종속기업,관계기업및공동기업투자 |
2,538,203,634 | 2,574,302,465 | - |
| ㆍ유형자산 | 16,880,890,626 | 17,413,091,310 | 27,683,603,541 |
| ㆍ무형자산 | 942,109,446 | 975,712,144 | 440,122,143 |
| ㆍ사용권자산 | 1,844,021,797 | 1,886,085,168 | 1,887,899,638 |
| ㆍ기타자산 | 1,307,454,204 | 1,357,831,273 | 759,339,167 |
| 자산총계 | 50,203,759,791 | 55,986,114,034 | 81,253,041,202 |
| [유동부채] | 7,019,154,555 | 7,732,495,470 | 24,199,158,766 |
| [비유동부채] | 4,905,646,602 | 5,071,597,158 | 12,536,332,782 |
| 부채총계 | 11,924,801,157 | 12,804,092,628 | 36,735,491,548 |
| [지배기업의 소유주에게 귀속되는 자본] | 38,278,958,634 | 43,182,021,406 | 48,011,510,083 |
| ㆍ자본금 | 28,027,074,500 | 28,027,074,500 | 28,002,712,000 |
| ㆍ주식발행초과금 | 174,869,357,949 | 174,869,357,949 | 174,894,549,098 |
| ㆍ기타자본항목 | 7,171,627,869 | 7,171,627,869 | 4,468,677,278 |
| ㆍ결손금 | (171,789,101,684) | (166,886,038,912) | (159,354,428,293) |
| [비지배지분] | - | - | (3,493,960,429) |
| 자본총계 | 38,278,958,634 | 43,182,021,406 | 44,517,549,654 |
| 종속·관계·공동기업투자주식의 평가방법 | 지분법 | 지분법 | 지분법 |
| (2025년 1월~3월) | (2024년 1월~12월) | (2023년 1월~12월) | |
| 매출액 | 954,354,847 | 7,745,823,635 | 5,912,667,181 |
| 영업손실 | (4,744,777,675) | (14,842,348,178) | (19,658,231,710) |
| 계속영업당기순손실 | (4,903,062,772) | (7,082,860,546) | (19,306,125,413) |
| 중단영업당기순손실(이익) | - | (907,103,025) | (3,914,979,312) |
| 당기순손실 | (4,903,062,772) | (7,989,963,571) | (23,221,104,725) |
| 지배기업 소유주지분 | (4,903,062,772) | (7,669,438,262) | (21,949,167,960) |
| 계속영업당기순손실 | (4,903,062,772) | (7,082,860,546) | (19,306,125,413) |
| 중단영업당기순손실 | - | (586,577,716) | (2,643,042,547) |
| 비지배지분 | - | (320,525,309) | (1,271,936,765) |
| 기본주당순손실 | (87) | (126) | (476) |
| 연결에 포함된 회사수 | - | - | 1개 |
| (주1) | 상기 재무정보는 한국채택국제회계기준에 따라 작성되었습니다. |
| (주2) | 잠재적 보통주식이 있으나, 희석효과가 존재하지 않아 희석주당손익을 산정하지 않았습니다. |
2. 연결재무제표
해당없음
3. 연결재무제표 주석
해당없음
4. 재무제표
당사는 전기 중 종속회사인 HLB바이오코드(주)의 지분매각으로 연결제외되어 연결재무제표를 작성하지 않았습니다. 당기 재무제표에 포함된 비교표시되는 전기 재무제표는 종속기업에 대한 지배력을 상실하기 전까지 종속기업의 포괄손익 및 현금흐름 등이 포함된 재무제표입니다.
4-1. 재무상태표
|
재무상태표 |
|
제 16 기 1분기말 2025.03.31 현재 |
|
제 15 기말 2024.12.31 현재 |
|
(단위 : 원) |
|
제 16 기 1분기말 |
제 15 기말 |
|
|---|---|---|
|
자산 |
||
|
유동자산 |
23,575,514,872 |
28,528,439,364 |
|
현금및현금성자산 |
2,165,830,750 |
2,766,684,203 |
|
단기금융상품 |
15,500,082,185 |
15,500,049,761 |
|
매출채권 및 기타채권 |
1,597,849,251 |
5,272,741,542 |
|
당기법인세자산 |
205,942,890 |
188,795,200 |
|
재고자산 |
866,948,504 |
858,298,912 |
|
계약이행원가 |
1,541,048,682 |
1,853,184,108 |
|
기타유동자산 |
1,697,812,610 |
2,088,685,638 |
|
비유동자산 |
26,628,244,919 |
27,457,674,670 |
|
장기금융상품 |
100,000,000 |
100,000,000 |
|
당기손익-공정가치측정금융자산 |
2,753,285,654 |
2,932,656,126 |
|
장기기타채권 |
262,279,558 |
217,996,184 |
|
종속기업,관계기업 및 공동기업 투자 |
2,538,203,634 |
2,574,302,465 |
|
유형자산 |
16,880,890,626 |
17,413,091,310 |
|
무형자산 |
942,109,446 |
975,712,144 |
|
사용권자산 |
1,844,021,797 |
1,886,085,168 |
|
기타비유동자산 |
1,307,454,204 |
1,357,831,273 |
|
자산총계 |
50,203,759,791 |
55,986,114,034 |
|
부채 |
||
|
유동부채 |
7,019,154,555 |
7,732,495,470 |
|
매입채무 및 기타채무 |
1,457,736,316 |
1,987,274,140 |
|
차입금 |
3,730,000,000 |
3,730,000,000 |
|
리스부채 |
300,802,071 |
317,689,333 |
|
계약부채 |
1,101,209,588 |
1,266,876,477 |
|
충당부채 |
12,970 |
3,910 |
|
기타부채 |
429,393,610 |
430,651,610 |
|
비유동부채 |
4,905,646,602 |
5,071,597,158 |
|
차입금 |
2,980,000,000 |
2,980,000,000 |
|
리스부채 |
1,419,472,950 |
1,428,288,522 |
|
충당부채 |
31,759,198 |
30,595,327 |
|
기타채무 |
474,414,454 |
632,713,309 |
|
부채총계 |
11,924,801,157 |
12,804,092,628 |
|
자본 |
||
|
자본금 |
28,027,074,500 |
28,027,074,500 |
|
주식발행초과금 |
174,869,357,949 |
174,869,357,949 |
|
기타자본항목 |
7,171,627,869 |
7,171,627,869 |
|
결손금 |
(171,789,101,684) |
(166,886,038,912) |
|
자본총계 |
38,278,958,634 |
43,182,021,406 |
|
자본과부채총계 |
50,203,759,791 |
55,986,114,034 |
4-2. 포괄손익계산서
|
포괄손익계산서 |
|
제 16 기 1분기 2025.01.01 부터 2025.03.31 까지 |
|
제 15 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
(단위 : 원) |
|
제 16 기 1분기 |
제 15 기 1분기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
매출액 |
954,354,847 |
954,354,847 |
1,283,990,966 |
1,283,990,966 |
|
매출원가 |
748,717,513 |
748,717,513 |
754,097,876 |
754,097,876 |
|
매출총이익 |
205,637,334 |
205,637,334 |
529,893,090 |
529,893,090 |
|
판매비와관리비 |
4,950,415,009 |
4,950,415,009 |
4,365,238,314 |
4,365,238,314 |
|
영업손실 |
(4,744,777,675) |
(4,744,777,675) |
(3,835,345,224) |
(3,835,345,224) |
|
기타손익 |
(158,285,097) |
(158,285,097) |
243,587,528 |
243,587,528 |
|
금융수익 |
174,790,312 |
174,790,312 |
435,764,824 |
435,764,824 |
|
금융비용 |
270,238,621 |
270,238,621 |
101,152,938 |
101,152,938 |
|
기타수익 |
20,830,866 |
20,830,866 |
48,183,962 |
48,183,962 |
|
기타비용 |
10,367,624 |
10,367,624 |
2,458,707 |
2,458,707 |
|
관계기업투자손익 |
(73,300,030) |
(73,300,030) |
(136,749,613) |
(136,749,613) |
|
법인세비용차감전순손익 |
(4,903,062,772) |
(4,903,062,772) |
(3,591,757,696) |
(3,591,757,696) |
|
계속영업분기순손실 |
(4,903,062,772) |
(4,903,062,772) |
(3,591,757,696) |
(3,591,757,696) |
|
중단영업분기순손실 |
(580,046,175) |
(580,046,175) |
||
|
분기순손익 |
(4,903,062,772) |
(4,903,062,772) |
(4,171,803,871) |
(4,171,803,871) |
|
지배기업의 소유주지분 |
(4,903,062,772) |
(4,903,062,772) |
(3,967,168,840) |
(3,967,168,840) |
|
계속영업분기순손실 |
(4,903,062,772) |
(4,903,062,772) |
(3,591,757,696) |
(3,591,757,696) |
|
중단영업분기순손실 |
(375,411,144) |
(375,411,144) |
||
|
비지배지분 |
(204,635,031) |
(204,635,031) |
||
|
분기총포괄손익 |
(4,903,062,772) |
(4,903,062,772) |
(4,171,803,871) |
(4,171,803,871) |
|
지배기업의 소유주지분 |
(4,903,062,772) |
(4,903,062,772) |
(3,967,168,840) |
(3,967,168,840) |
|
비지배지분 |
(204,635,031) |
(204,635,031) |
||
|
주당순손익 |
||||
|
계속영업기본주당손실 (단위 : 원) |
(87) |
(87) |
(64) |
(64) |
|
중단영업기본주당손실 (단위 : 원) |
(7) |
(7) |
||
4-3. 자본변동표
|
자본변동표 |
|
제 16 기 1분기 2025.01.01 부터 2025.03.31 까지 |
|
제 15 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
(단위 : 원) |
|
자본 |
|||||||
|---|---|---|---|---|---|---|---|
|
지배기업의 소유주에게 귀속되는 지분 |
비지배지분 |
자본 합계 |
|||||
|
자본금 |
주식발행초과금 |
기타자본항목 |
결손금 |
지배기업의 소유주에게 귀속되는 지분 합계 |
|||
|
2024.01.01 (기초자본) |
28,002,712,000 |
174,894,549,098 |
4,468,677,278 |
(159,354,428,293) |
48,011,510,083 |
(3,493,960,429) |
44,517,549,654 |
|
분기순손익 |
(3,967,168,840) |
(3,967,168,840) |
(204,635,031) |
(4,171,803,871) |
|||
|
확정급여제도의재측정요소 |
(204,351,298) |
(204,351,298) |
(112,469,556) |
(316,820,854) |
|||
|
소유주와의 거래 |
|||||||
|
2024.03.31 (기말자본) |
28,002,712,000 |
174,894,549,098 |
4,468,677,278 |
(163,525,948,431) |
43,839,989,945 |
(3,811,065,016) |
40,028,924,929 |
|
2025.01.01 (기초자본) |
28,002,712,000 |
174,869,357,949 |
7,171,627,869 |
(166,886,038,912) |
43,182,021,406 |
43,182,021,406 |
|
|
분기순손익 |
(4,903,062,772) |
(4,903,062,772) |
(4,903,062,772) |
||||
|
확정급여제도의재측정요소 |
|||||||
|
소유주와의 거래 |
|||||||
|
2025.03.31 (기말자본) |
28,027,074,500 |
174,869,357,949 |
7,171,627,869 |
(171,789,101,684) |
38,278,958,634 |
38,278,958,634 |
|
4-4. 현금흐름표
|
현금흐름표 |
|
제 16 기 1분기 2025.01.01 부터 2025.03.31 까지 |
|
제 15 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
(단위 : 원) |
|
제 16 기 1분기 |
제 15 기 1분기 |
|
|---|---|---|
|
영업활동현금흐름 |
(320,602,320) |
(5,681,229,159) |
|
영업으로부터 창출된 현금흐름 |
(329,595,308) |
(5,654,792,129) |
|
이자의 수취 |
111,357,938 |
138,628,768 |
|
이자의 지급 |
(85,217,260) |
(143,650,178) |
|
법인세 환급(납부) |
(17,147,690) |
(21,415,620) |
|
투자활동현금흐름 |
(195,458,424) |
1,830,640,780 |
|
단기금융상품의 취득 |
(163,251,241) |
(7,099,900,084) |
|
단기금융상품의 처분 |
163,218,817 |
9,599,900,083 |
|
대여금의 증가 |
(450,000,000) |
|
|
유형자산의 취득 |
(163,526,000) |
(320,720,000) |
|
유형자산의 처분 |
7,700,000 |
|
|
임차보증금의 증가 |
(57,460,000) |
(55,268,000) |
|
임차보증금의 감소 |
25,560,000 |
148,928,781 |
|
재무활동현금흐름 |
(84,785,182) |
59,374,920 |
|
차입금의 증가 |
200,000,000 |
|
|
리스상환 |
(84,785,182) |
(140,625,080) |
|
현금및현금성자산의순증가(감소) |
(600,845,926) |
(3,791,213,459) |
|
기초현금및현금성자산 |
2,766,684,203 |
5,855,668,775 |
|
현금및현금성자산의 환율변동효과 |
(7,527) |
123,482 |
|
기말현금및현금성자산 |
2,165,830,750 |
2,064,578,798 |
5. 재무제표 주석
| 제 16 기 1분기 2025년 1월 1일 부터 2025년 03월 31일 까지 |
| 제 15 기 1분기 2024년 1월 1일 부터 2024년 03월 31일 까지 |
| 제 15 기 2024년 1월 1일 부터 2024년 12월 31일 까지 |
| 주식회사 강스템바이오텍 |
1. 회사의 개요
주식회사 강스템바이오텍(이하 "회사")은 제대혈 줄기세포의 연구, 개발 및 세포치료제 개발, 제조 및 판매를 목적으로 2010년 10월 29일에 설립되었습니다. 서울시 강남구 테헤란로 522에 본점 소재지를 두고 있으며, 서울시 금천구 가산디지털1로 84에 연구소와 경기도 광명시 하안로 60 광명SK테크노파크에 공장 소재지를 두고 있습니다. 회사는 2013년 12월 중 주식회사 강스템홀딩스에서 주식회사 강스템바이오텍으로 상호를 변경하였으며, 2015년 12월 중 한국증권업협회 중개시장(KOSDAQ)에 등록하였습니다.
당분기말 현재 회사의 보통주 자본금은 28,027,075천원이며, 최대주주는 주식회사 세종으로 보유주식은 8,000,000주(14.27%)입니다
2. 재무제표 작성기준 및 중요한 회계정책
(1) 분기재무제표 작성기준
당사의 중간재무제표는 '주식회사 등의 외부감사에 관한 법률'에 따라 제정된 한국채택국제회계기준 기업회계기준서 제1034호 '중간재무보고'에 따라 작성되었습니다. 동 요약중간재무제표에 대한 이해를 위해서는 한국채택국제회계기준에 따라 작성된 2024년 12월 31일자로 종료하는 회계연도에 대한 연차개별재무제표를 함께 이용하여야 합니다.
중간재무제표의 작성에 적용된 중요한 회계정책은 아래에서 설명하는 기준서나 해석서의 도입과 관련된 영향을 제외하고는 2024년 12월 31일로 종료하는 회계연도에 대한 연차재무제표 작성시 채택한 회계정책과 동일합니다.
1) 당분기에 새로 도입된 기업회계기준서 및 해석서와 그로 인한 회계정책 변경의 내용은 다음과 같습니다.
- 기업회계기준서 제1021호 '환율변동효과'와 제1101호 '한국채택국제회계기준의 최초채택'(개정) - 교환가능성 결여
동 개정사항은 회계목적상 다른 통화와 교환이 가능하다고 보는 상황에 대해 정의하고, 다른 통화와의 교환가능성 평가, 교환가능성이 결여된 경우 사용할 현물환율 추정 및 공시 요구사항을 명확히 합니다. 해당 기준서의 개정이 재무제표에 미치는 중요한 영향은 없습니다.
2) 제정 또는 공표되었으나 시행일이 도래하지 않아 적용하지 아니한 제·개정 기준서 및 해석서는 다음과 같습니다.
- 기업회계기준서 제1109호 '금융상품'과 제1107호 '금융상품: 공시'(개정) - 금융상품 분류와 측정
동 개정사항은 전자지급시스템을 사용하여 금융부채를 결제할 때의 금융부채의 결제일 전 이행과 관련된 조건, 계약상 현금흐름이 기본대여계약과 일관되는지 평가할 때 고려해야 할 이자 및 우발사건 특성, 비소구 특성을 가진 금융자산, 계약상 연계된 금융상품의 특성을 명확히 합니다. 그리고 기타포괄손익-공정가치로 지정된 지분상품에 대한 투자와 계약상 현금흐름의 시기나 금액을 변경할 수 있는 계약조건에 대한 추가적인 공시 요구사항을 포함합니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도의 개시일 이후 소급적으로 적용되며 조기적용이 허용됩니다.
- 기업회계기준서 제1109호 '금융상품' - 리스부채의 제거 회계처리 및 거래가격의 정의
동 개정사항은 리스부채 제거시 발생하는 차손익을 당기손익으로 인식해야 함을 명확히 하였습니다. 또한 거래가격의 정의를 기업회계기준서 제1115호와 일관되도록 개정하였습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다.
- 기업회계기준서 제1110호 '연결재무제표' - 사실상의 대리인 결정
동 개정사항은 사실상 대리인의 판단과 관련한 기준서 제1110호의 표현을 개정하여 기준서 문단 간의 불일치를 해소하였습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다.
- 기업회계기준서 제1101호 '한국채택국제회계기준의 최초채택' - 위험회피회계 적용
동 개정사항은 위험회피회계의 적용조건을 기업회계기준서 제1109호 '금융상품'의 구체적인 문단을 참조하도록 명시하고 관련 용어를 일치시켰습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다.
- 기업회계기준서 제1107호 '금융상품: 공시' - 제거 손익
동 개정사항은 공정가치 측정과 관련하여 기업회계기준서 제1113호 '공정가치'를 참조하도록 하고 관련 용어를 일치시켰습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다.
- 기업회계기준서 제1007호 - 원가법
동 개정으로 '원가법'이라는 용어를 삭제하고 이를 '원가'로 대체하였습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다.
당사는 상기에 열거된 제ㆍ개정사항이 재무제표에 미치는 영향이 중요하지 않을 것으로 예상하고 있습니다.
3. 중요한 판단과 추정불확실성의 주요 원천
중간재무제표를 작성함에 있어 경영진은 재무제표에 인식되는 금액에 유의적인 영향을 미치는 판단을 하여야 하며(추정과 관련된 사항은 제외), 다른 자료로부터 쉽게 식별할 수 없는 자산과 부채의 장부금액에 대한 추정 및 가정을 하여야 합니다. 추정치와 관련 가정은 과거 경험 및 관련이 있다고 여겨지는 기타 요인에 근거합니다. 또한 실제 결과는 이러한 추정치들과 다를 수도 있습니다.
중간재무제표 작성을 위해 당사 회계정책의 적용과정에서 내린 중요한 판단과 추정불확실성의 주요 원천에 대한 내용은 2024년 12월 31일로 종료하는 회계연도에 대한 연차재무제표와 동일합니다.
4. 부문정보
(1) 보고부문이 수익을 창출하는 제품과 용역의 유형
부문에 자원을 배분하고 부문의 성과를 평가하기 위하여 당사의 최고영업의사결정자에게 보고되는 정보는 각각의 사업의 유형에 초점이 맞추어져 있습니다. 기업회계기준서 제1108호에 따른 당사의 보고부문은 다음과 같습니다.
| 사업부문 | 주요 재화 및 용역 |
|---|---|
| 줄기세포 사업부 | 줄기세포배양액 및 배양배지 |
| 화장품 사업부 | 줄기세포 화장품 |
| 바이오파마 사업부 | 일반의약품(OTC) |
| 비임상 시험 사업부(주1) | 비임상 연구용역 |
| (주1) | 전기 중 비임상시험 사업부는 HLB바이오코드(주)(구.(주)크로엔)의 지분 매각으로 연결에서 제외되었으며, 중단영업으로 재분류하였습니다. |
(2) 당분기 및 전분기 중 당사의 부문별 재무현황은 다음과 같습니다.
| (당분기) | (단위: 천원) |
| 구 분 | 줄기세포 사업부 | 화장품 사업부 | 합 계 |
|---|---|---|---|
| 총부문수익 | 463,278 | 491,077 | 954,355 |
| 부문간수익 | - | - | - |
| 외부고객으로부터의 수익 | 463,278 | 491,077 | 954,355 |
| 부문별 매출총이익 | 17,302 | 188,336 | 205,638 |
| 부문별 영업손익 | (4,575,280) | (169,498) | (4,744,778) |
| (전분기) | (단위: 천원) |
| 구 분 | 계속영업 | 중단영업 | |||
|---|---|---|---|---|---|
| 줄기세포 사업부 | 화장품 사업부 | 바이오파마 사업부 | 합 계 | ||
| 총부문수익 | 146,416 | 1,051,542 | 86,033 | 1,283,991 | 1,635,612 |
| 부문간수익 | - | - | - | - | 3,600 |
| 외부고객으로부터의 수익 | 146,416 | 1,051,542 | 86,033 | 1,283,991 | 1,632,012 |
| 부문별 매출총이익 | 22,803 | 497,856 | 9,234 | 529,893 | 98,378 |
| 부문별 영업손익 | (3,705,833) | (65,560) | (63,951) | (3,835,344) | (472,169) |
(3) 주요고객에 대한 정보
당분기 및 전분기 중 계속영업 관련 당사 수익의 10% 이상을 차지하는 주요 외부고객에 대한 매출액은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 매출액 | 비율 | 매출액 | 비율 | |
| A사 | 364,806 | 38.2% | 510,022 | 39.7% |
5. 사용이 제한된 금융자산
당분기말 및 전기말 현재 사용이 제한된 금융자산의 내역은 다음과 같습니다.
| (단위: 천원) |
| 과 목 | 기관명 | 사용제한의 내용 | 당분기말 | 전기말 |
|---|---|---|---|---|
| 단기금융상품 | 신한은행 | 국책연구과제 | 82 | 50 |
| 장기금융상품(주1) | 신한은행 | 지급보증 | 100,000 | 100,000 |
| 합 계 | 100,082 | 100,050 | ||
| (주1) | 법인카드에 대한 지급보증해당액입니다. |
6. 당기손익-공정가치측정금융자산
당분기말 및 전기말 현재 당기손익-공정가치측정금융자산의 내역은 다음과 같습니다.
| (단위: 천원) |
| 과 목 | 당분기말 | 전기말 |
|---|---|---|
| 비유동 | ||
| 시장성 없는 지분증권 | 500,000 | 500,000 |
| 복합금융상품(주1) | 2,253,286 | 2,432,656 |
| 합 계 | 2,753,286 | 2,932,656 |
| (주1) | 당기손익-공정가치측정금융자산으로 분류한 (주)프리모리스테라퓨틱스 상환전환우선주에서 지분법손실을 반영하였습니다(주석 14 참고). |
7. 매출채권 및 기타채권
(1) 당분기말 및 전기말 현재 매출채권 및 기타채권의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 | ||
|---|---|---|---|---|
| 유동 | 비유동 | 유동 | 비유동 | |
| 매출채권 | 300,515 | - | 517,336 | - |
| 차감: 대손충당금 | (11,506) | - | - | - |
| 매출채권(순액) | 289,009 | - | 517,336 | - |
| 미수금 | 166,040 | - | 3,656,993 | - |
| 차감: 대손충당금 | (6,600) | - | - | - |
| 미수금(순액) | 159,440 | - | 3,656,993 | - |
| 미수수익 | 204,300 | - | 142,852 | - |
| 단기대여금 | 930,000 | - | 930,000 | - |
| 보증금 | 15,100 | 387,288 | 25,560 | 344,928 |
| 차감: 현재가치할인차금 | - | (125,008) | - | (126,932) |
| 보증금(순액) | 15,100 | 262,280 | 25,560 | 217,996 |
| 합 계 | 1,597,849 | 262,280 | 5,272,741 | 217,996 |
(2) 신용위험 및 손실충당금
제품 매출에 대한 평균 신용공여기간은 60일이며, 매출채권에 대해서 이자는 부과되지 아니합니다.
당사는 매출채권에 대해 항상 전체기간 기대신용손실에 해당하는 금액으로 손실충당금을 측정합니다. 매출채권에 대한 기대신용손실은 채무자의 과거 채무불이행 경험 및 차입자 특유의 요인, 일반적인 경제 환경, 보고기간 말에 현재 상황에 대한 평가뿐만 아니라 미래에 상황이 어떻게 변동할 것인지에 대한 평가를 포함한 요소들이 조정된 채무자의 현행 재무상태에 대한 분석을 고려한 충당금 설정률표를 이용하여 산정됩니다. 당사는 과거 경험상 6개월이 경과한 채권은 일반적으로 회수되지 않으므로 6개월이 경과된 모든 채권에 대하여 전액 손실충당금을 인식하고 있습니다. 당분기 중 추정기법이나 중요한 가정의 변경은 없습니다.
1) 당분기말 및 전기말 현재 당사의 충당금 설정률표에 기초한 매출채권의 위험정보의 세부내용은 다음과 같습니다. 당사의 과거 신용손실 경험상 다양한 고객부분이 유의적으로 서로 다른 손실양상을 보이지 아니하므로, 과거의 연체일수에 기초한 충당금 설정률표는 서로 다른 고객군별로 구분하지는 않습니다.
| (당분기말) | (단위: 천원) |
| 구 분 | 연체일수 | ||||
|---|---|---|---|---|---|
| 미연체 | ~30일 | 30~90일 | 90일 초과 | 계 | |
| 총장부금액 | 281,763 | 3,300 | - | 15,453 | 300,516 |
| 전체기간 기대신용손실 | - | - | - | (11,506) | (11,506) |
| 순장부금액 | 281,763 | 3,300 | - | 3,947 | 289,010 |
| (전기말) | (단위: 천원) |
| 구 분 | 연체일수 | ||||
|---|---|---|---|---|---|
| 미연체 | ~30일 | 30~90일 | 90일 초과 | 계 | |
| 총장부금액 | 497,832 | 5,597 | 2,401 | 11,506 | 517,336 |
| 전체기간 기대신용손실 | - | - | - | - | - |
| 순장부금액 | 497,832 | 5,597 | 2,401 | 11,506 | 517,336 |
2) 당분기 및 전분기 중 매출채권 및 기타채권의 손실충당금의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 천원) |
| 구 분 | 비손상채권 | 손상채권 | 계 | |
|---|---|---|---|---|
| 집합평가 대상 | 개별평가 대상 | |||
| 기초금액 | - | - | - | - |
| 손실충당금의 재측정 | - | - | 11,506 | 11,506 |
| 기말금액 | - | - | 11,506 | 11,506 |
| (전분기) | (단위: 천원) |
| 구 분 | 비손상채권 | 손상채권 | 계 | |
|---|---|---|---|---|
| 집합평가 대상 | 개별평가 대상 | |||
| 기초금액 | - | - | 47,818 | 47,818 |
| 회수 | - | - | - | - |
| 손실충당금의 재측정 | - | - | - | - |
| 기말금액 | - | - | 47,818 | 47,818 |
8. 재고자산
당분기말 및 전기말 현재 재고자산의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|
| 취득원가 | 평가손실충당금 | 장부금액 | 취득원가 | 평가손실충당금 | 장부금액 | |
| 상품 | 84,686 | (65,764) | 18,922 | 119,293 | (21,334) | 97,959 |
| 제품 | 775,985 | (136,489) | 639,496 | 703,106 | (151,895) | 551,211 |
| 재공품 | 208,530 | - | 208,530 | 209,129 | - | 209,129 |
| 합 계 | 1,069,201 | (202,253) | 866,948 | 1,031,528 | (173,229) | 858,299 |
당분기 중 비용으로 인식한 재고자산 원가에는 재고자산평가손실 29백만원(전분기: 재고자산평가손실 10백만원)이 포함되어 있습니다.
9. 유형자산
(1) 당분기말 및 전기말 현재 유형자산의 내역은 다음과 같습니다.
| (당분기말) | (단위: 천원) |
| 구 분 | 취득금액 | 감가상각누계액 | 정부보조금 | 장부금액 |
|---|---|---|---|---|
| 토지 | 3,927,206 | - | - | 3,927,206 |
| 건물 | 9,241,382 | (1,143,426) | - | 8,097,956 |
| 시설장치 | 7,998,885 | (3,919,893) | - | 4,078,992 |
| 연구시험용자산 | 7,968,351 | (7,194,122) | (29,906) | 744,323 |
| 비품 | 412,784 | (380,371) | - | 32,413 |
| 합 계 | 29,548,608 | (12,637,812) | (29,906) | 16,880,890 |
| (전기말) | (단위: 천원) |
| 구 분 | 취득금액 | 감가상각누계액 | 정부보조금 | 장부금액 |
|---|---|---|---|---|
| 토지 | 3,927,206 | - | - | 3,927,206 |
| 건물 | 9,241,382 | (1,085,667) | - | 8,155,715 |
| 시설장치 | 8,208,925 | (3,917,064) | - | 4,291,861 |
| 연구시험용자산 | 7,989,114 | (6,946,309) | (35,569) | 1,007,236 |
| 비품 | 414,670 | (383,597) | - | 31,073 |
| 합 계 | 29,781,297 | (12,332,637) | (35,569) | 17,413,091 |
(2) 당분기와 전분기 중 유형자산의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 천원) |
| 구 분 | 기초 | 취득(주1) | 처분 | 감가상각 | 기말 |
|---|---|---|---|---|---|
| 토지 | 3,927,206 | - | - | - | 3,927,206 |
| 건물 | 8,155,715 | - | - | (57,759) | 8,097,956 |
| 시설장치 | 4,291,861 | 1,550 | (566) | (213,853) | 4,078,992 |
| 연구시험용자산 | 1,007,236 | 18,200 | (8) | (281,105) | 744,323 |
| 비품 | 31,073 | 4,800 | (7) | (3,453) | 32,413 |
| 합 계 | 17,413,091 | 24,550 | (581) | (556,170) | 16,880,890 |
| (주1) | 상기 유형자산의 취득과 관련하여 미지급된 11,350천원이 미지급금으로 계상되어 있습니다. |
| (전분기) | (단위: 천원) |
| 구 분 | 기초 | 취득(주1) | 처분 | 감가상각 | 기말 |
|---|---|---|---|---|---|
| 토지 | 8,249,213 | - | - | - | 8,249,213 |
| 건물 | 9,599,684 | - | - | (92,747) | 9,506,937 |
| 시설장치 | 6,650,817 | - | - | (279,663) | 6,371,154 |
| 연구시험용자산 | 2,793,371 | 10,500 | (1) | (370,628) | 2,433,242 |
| 비품 | 73,132 | - | - | (9,859) | 63,273 |
| 차량운반구 | 7,166 | - | - | (597) | 6,569 |
| 건설중인자산 | 310,220 | 238,520 | - | - | 548,740 |
| 합 계 | 27,683,603 | 249,020 | (1) | (753,494) | 27,179,128 |
| (주1) | 상기 유형자산의 취득과 관련하여 미지급된 금액은 없습니다. |
(3) 당분기말 현재 유형자산 담보제공 내역은 다음과 같습니다.
| (단위: 천원) |
| 담보제공자산 | 장부금액 | 담보설정금액 | 관련 계정과목 | 차입금액 | 담보권자 |
|---|---|---|---|---|---|
| 토지 | 3,660,774 | 8,796,000 | 차입금 (주석 16 참조) |
6,710,000 | 기업은행 |
| 건물 | 7,758,009 |
10. 무형자산
(1) 당분기말 및 전기말 현재 무형자산의 구성내역은 다음과 같습니다.
| (당분기말) | (단위: 천원) |
| 구 분 | 취득금액 | 상각누계액 | 장부금액 |
|---|---|---|---|
| 소프트웨어 | 1,120,821 | (413,470) | 707,351 |
| 산업재산권 | 1,955,656 | (1,720,896) | 234,760 |
| 합 계 | 3,076,477 | (2,134,366) | 942,111 |
| (전기말) | (단위: 천원) |
| 구 분 | 취득금액 | 상각누계액 | 장부금액 |
|---|---|---|---|
| 소프트웨어 | 1,120,821 | (370,455) | 750,366 |
| 산업재산권 | 1,930,740 | (1,705,393) | 225,347 |
| 합 계 | 3,051,561 | (2,075,848) | 975,713 |
(2) 당분기와 전분기 중 무형자산의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 천원) |
| 구 분 | 기초 | 취득(주1) | 상각 | 처분 | 기말 |
|---|---|---|---|---|---|
| 소프트웨어 | 750,365 | - | (43,014) | - | 707,351 |
| 산업재산권 | 225,347 | 37,215 | (21,882) | (5,920) | 234,760 |
| 합 계 | 975,712 | 37,215 | (64,896) | (5,920) | 942,111 |
| (주1) | 산업재산권 취득과 관련하여 당분기 이전 지급된 37,215천원이 선급금에서 대체되었습니다. |
| (전분기) | (단위: 천원) |
| 구 분 | 기초 | 취득(주1) | 상각 | 기말 |
|---|---|---|---|---|
| 소프트웨어 | 157,103 | - | (19,676) | 137,427 |
| 산업재산권 | 283,019 | 2,264 | (24,423) | 260,860 |
| 합 계 | 440,122 | 2,264 | (44,099) | 398,287 |
| (주1) | 산업재산권 취득과 관련하여 전분기 이전 지급된 2,264천원이 선급금에서 대체되었습니다. |
11. 기타자산
당분기말 및 전기말 현재 기타자산의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 | ||
|---|---|---|---|---|
| 유동 | 비유동 | 유동 | 비유동 | |
| 선급금 | 1,221,887 | 1,307,454 | 1,204,831 | 1,357,831 |
| 선급비용 | 224,000 | - | 320,000 | - |
| 기타 | 251,926 | - | 563,854 | - |
| 합 계 | 1,697,813 | 1,307,454 | 2,088,685 | 1,357,831 |
12. 리스
(1) 당분기말 및 전기말 현재 리스관련 사용권자산의 장부가액은 다음과 같습니다.
| (당분기말) | (단위: 천원) |
| 구 분 | 건물 | 차량운반구 | 합 계 |
|---|---|---|---|
| 사용권자산 취득가액 | 1,710,999 | 325,040 | 2,036,039 |
| 사용권자산 감가상각누계액 | (57,033) | (134,984) | (192,017) |
| 기말장부금액 | 1,653,966 | 190,056 | 1,844,022 |
| (전기말) | (단위: 천원) |
| 구 분 | 건물 | 차량운반구 | 합 계 |
|---|---|---|---|
| 사용권자산 취득가액 | 4,209,267 | 524,830 | 4,734,097 |
| 사용권자산 감가상각누계액 | (2,512,526) | (335,485) | (2,848,011) |
| 기말장부금액 | 1,696,741 | 189,345 | 1,886,086 |
(2) 당분기 및 전분기 중 사용권자산의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 천원) |
| 구 분 | 건물 | 차량운반구 | 합 계 |
|---|---|---|---|
| 기초금액 | 1,696,741 | 189,345 | 1,886,086 |
| 취득 | - | 60,103 | 60,103 |
| 해지 | - | (39,406) | (39,406) |
| 리스상각비 | (42,775) | (19,986) | (62,761) |
| 기말금액 | 1,653,966 | 190,056 | 1,844,022 |
| (전분기) | (단위: 천원) |
| 구 분 | 건물 | 차량운반구 | 합계 |
|---|---|---|---|
| 기초금액 | 1,690,762 | 197,137 | 1,887,899 |
| 취득 | - | 30,654 | 30,654 |
| 해지 | - | (2,732) | (2,732) |
| 재측정 | (16,062) | - | (16,062) |
| 리스상각비 | (140,443) | (29,330) | (169,773) |
| 기말금액 | 1,534,257 | 195,729 | 1,729,986 |
당사는 건물 및 차량을 리스하였으며, 평균 리스기간은 약 5년 입니다. 사용권자산에 대한 법적 소유권은 리스제공자가 보유하고 있습니다.
당분기 중 건물 및 차량에 대한 리스 중 약 2.09%(전분기: 0.14%)가 계약해지로 종료되었습니다.
(3) 당분기 및 전분기 중 손익으로 인식한 금액은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 사용권자산 감가상각비 | 62,760 | 137,119 |
| 리스부채 이자비용 | 42,778 | 18,917 |
| 복구충당부채 이자비용 | 1,164 | - |
| 단기리스 관련 비용 | 2,500 | 9,480 |
| 소액자산리스 관련 비용 | 3,477 | 4,015 |
| 리스해지 관련 이익 | 4,392 | 152 |
| 리스재측정 관련 이익 | - | 39,496 |
| (주1) | 당분기 및 전분기의 중단영업 관련 손익은 제외한 금액입니다. |
당분기 및 전분기 중 리스로 인한 총 현금유출 금액은 90,762천원과 159,103천원이며, 단기리스 및 소액리스가 포함되어 있습니다.
(4) 당분기 및 전분기 중 리스부채의 변동내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 기초장부금액 | 1,745,978 | 2,083,325 |
| 리스부채 증가 | 60,103 | 30,654 |
| 이자비용 | 42,778 | 23,005 |
| 해지 | (43,798) | (120,509) |
| 재측정 | - | (245,749) |
| 지급 | (84,785) | (140,625) |
| 기말장부금액 | 1,720,276 | 1,630,101 |
(5) 당분기말 및 전기말 현재 리스부채의 만기 분석은 아래와 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 1년이내 | 323,072 | 341,028 |
| 1년 초과 2년 이내 | 313,862 | 308,601 |
| 2년 초과 3년 이내 | 294,956 | 290,208 |
| 3년 초과 4년 이내 | 275,214 | 267,538 |
| 4년 초과 5년 이내 | 243,996 | 243,996 |
| 5년 초과 | 1,138,648 | 1,199,647 |
| 합 계 | 2,589,748 | 2,651,018 |
| (주1) | 동 만기분석은 리스부채에 대한 할인되지 않은 현금흐름을 기초로 작성되었습니다. |
13. 관계기업 및 공동기업
(1) 당분기말 및 전기말 현재 관계기업 및 공동기업에 대한 지분율 현황 및 출자금액은 다음과 같습니다.
| (단위: 천원) |
| 기업명 | 구 분 | 주요영업활동 | 소재지 | 결산월 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|---|---|---|---|
| 지분율(%) | 취득 원가 | 장부 금액 | 지분율(%) | 취득 원가 | 장부 금액 | |||||
| 디앤케이코퍼레이션(주1) | 공동기업 | 화장품 판매 | 대한민국 | 12월 | 50.00% | 1,000,000 | - | 50.00% | 1,000,000 | - |
| (주)블루진(주2) | 관계기업 | 화장품 판매 | 대한민국 | 12월 | 20.00% | 300,000 | - | 20.00% | 300,000 | - |
| (주)프리모리스테라퓨틱스(주3) | 공동기업 | 신약 연구개발 | 대한민국 | 12월 | 64.76% | - | - | 64.76% | - | - |
| HLB바이오코드(주)(주4) | 관계기업 | 비임상 시험용역 | 대한민국 | 12월 | 22.47% | 4,505,517 | 2,538,204 | - | 4,505,517 | 2,574,302 |
| (주1) | 당사가 공동지배력을 보유하고 있는 공동약정은 별도의 회사를 통하여 구조화되었으며, 공동약정의 당사자들이 약정의 자산에 대한 권리와 부채에 대한 의무를 보유한다는 것을 명시하는 합의된 계약상 조건이나 그 밖의 사실과 상황이 존재하지 않습니다. 따라서 공동약정에 대하여 공동지배력을 보유하는 당사자들이 약정의 순자산에 대한 권리를 보유하고 있다고 판단하여 공동기업으로 분류하고 있습니다. 또한 당사는 공동기업에 대한 지분을 지분법으로 회계처리 하고 있습니다. |
| (주2) | 당사가 20%의 지분을 취득하여 재무정책 및 영업정책에 대한 유의적인 영향력을 보유하고 있어 관계기업으로 분류하였습니다. 또한 당사는 해당 관계기업에 대한 지분을 지분법으로 회계처리 하고 있습니다. |
| (주3) | 전기 중 ㈜프리모리스테라퓨틱스 임직원으로부터 추가로 보통주식 27,200주를 무상으로 수증 받아 지분율이 증가하였습니다. 당사는 보통주식 외에 의결권 있는 상환전환우선주 11,765주를 보유하고 있으며 상기 지분율은 상환전환우선주 주식수를 포함한 지분율입니다. |
| (주4) | 전기 중 보유 주식 1,183,676주(64.50%) 중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류하였습니다. 또한 매각 이후 유상증자를 통해 HLB바이오코드(주)의 지분(183,333주)를 추가 취득하였습니다. 이후 HLB바이오코드㈜의 유상증자에 참여하지 않아 지분율이 감소하였습니다. |
(2) 당분기말 및 전기말 중 관계기업 및 공동기업의 변동내역은 다음과 같습니다.
| (당분기말) | (단위: 천원) |
| 구 분 | 기초 | 취득 | 지분법손익 | 당분기말 |
|---|---|---|---|---|
| HLB바이오코드(주) | 2,574,302 | - | (36,098) | 2,538,204 |
| (전기말) | (단위: 천원) |
| 구 분 | 기초 | 취득(주1) | 지분법손익 | 대체(주1)(주2) | 손상 | 전기말 |
|---|---|---|---|---|---|---|
| HLB바이오코드(주) | - | 989,998 | (545,239) | 3,515,519 | (1,385,976) | 2,574,302 |
| (주1) | 전기 중 보유 주식 1,183,676주(64.50%) 중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류하였습니다. 또한 매각 이후 유상증자를 통해 HLB바이오코드(주)의 지분(183,333주)를 추가 취득하였습니다. |
| (주2) | 지배력 상실시 종속기업투자주식처분이익 9,845,033천원이 발생하였습니다. |
(3) 당분기말 및 전기말 현재 관계기업 및 공동기업의 요약 재무상태는 다음과 같습니다.
| (당분기말) | (단위: 천원) |
| 구 분 | 유동자산 | 비유동자산 | 유동부채 | 비유동부채 | 자본 |
|---|---|---|---|---|---|
| 디앤케이코퍼레이션 | 408,280 | 19,563 | 134,171 | 827,416 | (533,743) |
| (주)블루진 | 21,057 | - | 1,797,243 | - | (1,776,186) |
| (주)프리모리스테라퓨틱스 | 156,200 | 182,944 | 2,478,143 | 5,000,200 | (7,139,200) |
| HLB바이오코드(주) | 5,123,374 | 8,913,083 | 9,225,252 | 3,337,216 | 1,473,988 |
| (주1) | 상기 요약 재무상태는 사업결합시 발생한 영업권과 공정가치조정 및 지배기업과의 회계정책 차이조정 등을 반영한 후의 금액이며, 다만 내부거래는 제거하기 전의 금액입니다. |
| (전기말) | (단위: 천원) |
| 구 분 | 유동자산 | 비유동자산 | 유동부채 | 비유동부채 | 자본 |
|---|---|---|---|---|---|
| 디앤케이코퍼레이션 | 380,350 | 20,243 | 131,128 | 827,416 | (557,951) |
| (주)블루진 | 20,326 | - | 1,796,775 | - | (1,776,449) |
| (주)프리모리스테라퓨틱스 | 165,695 | 366,065 | 2,613,312 | 5,000,200 | (7,081,752) |
| HLB바이오코드(주) | 5,867,618 | 9,131,521 | 10,125,333 | 3,270,571 | 1,603,236 |
| (주1) | 상기 요약 재무상태는 사업결합시 발생한 영업권과 공정가치조정 및 지배기업과의 회계정책 차이조정 등을 반영한 후의 금액이며, 다만 내부거래는 제거하기 전의 금액입니다. |
(4) 당분기 및 전분기 중 관계기업 및 공동기업의 요약 경영성과는 다음과 같습니다.
| (당분기) | (단위: 천원) |
| 구 분 | 매출액 | 영업손익 | 당분기순손익 | 기타포괄손익 | 총포괄손익 |
|---|---|---|---|---|---|
| 디앤케이코퍼레이션 | 188,171 | 25,992 | 26,092 | - | 26,092 |
| (주)블루진 | 7,172 | 263 | 264 | - | 264 |
| (주)프리모리스테라퓨틱스 | 124,400 | (81,519) | (57,448) | - | (57,448) |
| HLB바이오코드(주) | 1,659,671 | (138,311) | (160,671) | - | (160,671) |
| (주1) | 상기 요약 경영성과는 사업결합시 발생한 영업권과 공정가치조정 및 지배기업과의 회계정책 차이조정 등을 반영한 후의 금액이며, 다만 내부거래는 제거하기 전의 금액입니다. |
| (전분기) | (단위: 천원) |
| 구 분 | 매출액 | 영업손익 | 당분기순손익 | 기타포괄손익 | 총포괄손익 |
|---|---|---|---|---|---|
| 디앤케이코퍼레이션 | 230,924 | 41,754 | 34,193 | 12,686 | 46,879 |
| (주)블루진 | 3,222 | (409) | (409) | - | (409) |
| (주)프리모리스테라퓨틱스 | 10,000 | (267,610) | (291,204) | - | (291,204) |
| (주1) | 상기 요약 경영성과는 사업결합시 발생한 영업권과 공정가치조정 및 지배기업과의 회계정책 차이조정 등을 반영한 후의 금액이며, 다만 내부거래는 제거하기 전의 금액입니다. |
(5) 당분기말 및 전기말 현재 관계기업 및 공동기업의 순자산에서 관계기업 및 공동기업에 대한 지분의 장부금액으로 조정한 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 | ||||||
|---|---|---|---|---|---|---|---|---|
| 디엔케이코 퍼레이션 |
(주)블루진 | (주)프리모리스 테라퓨틱스 |
HLB바이오 코드(주) |
디엔케이코 퍼레이션 |
(주)블루진 | (주)프리모리스 테라퓨틱스 |
HLB바이오 코드(주) |
|
| 관계기업 및 공동기업 기말 순자산(A) | (533,743) | (1,776,186) | (7,139,200) | 1,473,988 | (557,951) | (1,776,449) | (7,081,752) | 1,603,236 |
| 당사 지분율(B) | 50.00% | 20.00% | 64.76% | 22.47% | 50.00% | 20.00% | 64.76% | 22.47% |
| 순자산 지분금액(A×B) | (266,872) | (355,237) | (4,623,346) | 331,168 | (278,976) | (355,290) | (4,586,143) | 360,207 |
| 누적미반영 지분법손실 | 301,998 | 175,053 | - | - | 315,016 | 175,106 | - | - |
| 투자차액(영업권) | - | - | - | 2,207,036 | - | - | - | 2,214,095 |
| 기타(주1) | - | - | 1,303,160 | - | - | - | 1,265,959 | - |
| 내부거래제거 | (35,126) | 180,184 | 3,320,186 | - | (36,040) | 180,184 | 3,320,184 | - |
| 기말 장부금액 | - | - | - | 2,538,204 | - | - | - | 2,574,302 |
| (주1) | 당기손익-공정가치측정금융자산으로 분류한 (주)프리모리스테라퓨틱스 상환전환우선주에서 지분법손실을 반영하였습니다. |
14. 매입채무 및 기타채무
당분기말 및 전기말 현재 매입채무 및 기타채무의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 유동 | ||
| 매입채무 | 208,693 | 185,842 |
| 미지급금 | 965,683 | 1,511,651 |
| 미지급비용 | 283,361 | 289,781 |
| 소 계 | 1,457,737 | 1,987,274 |
| 비유동 | ||
| 임대보증금 | 23,000 | 23,000 |
| 미지급금 | 451,414 | 609,713 |
| 소 계 | 474,414 | 632,713 |
| 합 계 | 1,932,151 | 2,619,987 |
경영진은 매입채무의 장부금액이 공정가치와 거의 유사하다고 판단하고 있습니다.
15. 차입금
(1) 당분기말 및 전기말 현재 차입금의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 유동 | ||
| 단기차입금 | 3,330,000 | 3,330,000 |
| 유동성장기차입금 | 400,000 | 400,000 |
| 소 계 | 3,730,000 | 3,730,000 |
| 비유동 | ||
| 장기차입금 | 2,980,000 | 2,980,000 |
| 소 계 | 2,980,000 | 2,980,000 |
| 합 계 | 6,710,000 | 6,710,000 |
(2) 당분기말 및 전기말 현재 단기차입금의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 차입처 | 연이자율(%) | 당분기말 | 전기말 |
|---|---|---|---|---|
| 중소기업자금(주1) | 기업은행 | 4.959(여신만료일까지 연 4.959%) | 1,500,000 | 1,500,000 |
| 중소기업시설자금(주1) | 기업은행 | 4.349(3월물 KORIBOR+1.479%) | 1,480,000 | 1,480,000 |
| 중소기업시설자금(주1) | 기업은행 | 4.521(3월물 KORIBOR+1.651%) | 350,000 | 350,000 |
| 합 계 | 3,330,000 | 3,330,000 | ||
| (주1) | 기업은행 차입금과 관련하여 유형자산(장부금액: 11,418,783천원)이 담보(담보설정금액: 8,796,000천원)로 제공되어 있습니다(주석 9 참조). |
(3) 당분기말 및 전기말 현재 장기차입금의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 차입처 | 연이자율(%) | 금 액 | |
|---|---|---|---|---|
| 당분기말 | 전기말 | |||
| 중소기업시설자금(주1) | 기업은행 | 4.945(3월물 KORIBOR+2.065%) | 3,000,000 | 3,000,000 |
| 중소기업시설자금(주1) | 기업은행 | 4.911(여신만료일까지 연 4.911%) | 380,000 | 380,000 |
| 소 계 | 3,380,000 | 3,380,000 | ||
| 유동성대체 | (400,000) | (400,000) | ||
| 합 계 | 2,980,000 | 2,980,000 | ||
| (주1) | 기업은행 차입금과 관련하여 유형자산(장부금액: 11,418,783천원)이 담보(담보설정금액: 8,796,000천원)로 제공되어 있습니다(주석 9 참조). |
(4) 당분기말 및 전기말 현재 장기차입금 등의 연도별 상환계획은 다음과 같습니다.
| (당분기말) | (단위: 천원) |
| 구 분 | 장기차입금 |
|---|---|
| 2025.04.01 ~ 2026.03.31 | 400,000 |
| 2026.04.01 ~ 2027.03.31 | 780,000 |
| 2027.04.01 ~ 2028.03.31 | 400,000 |
| 2028.04.01 ~ 2029.03.31 | 400,000 |
| 2029.04.01 이후 | 1,400,000 |
| 합 계 | 3,380,000 |
| (전기말) | (단위: 천원) |
| 구 분 | 장기차입금 |
|---|---|
| 2025.01.01 ~ 2025.12.31 | 400,000 |
| 2026.01.01 ~ 2026.12.31 | 780,000 |
| 2027.01.01 ~ 2027.12.31 | 400,000 |
| 2028.01.01 ~ 2028.12.31 | 400,000 |
| 2029.01.01 이후 | 1,400,000 |
| 합 계 | 3,380,000 |
16. 충당부채
당분기와 전분기 중 충당부채의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 천원) |
| 구 분 | 기초 | 전입(환입) | 사용 | 당분기말 |
|---|---|---|---|---|
| 복구충당부채 | 30,595 | 1,164 | - | 31,759 |
| 반품충당부채 | 4 | (4) | 13 | 13 |
| 합 계 | 30,599 | 1,160 | 13 | 31,772 |
| (전분기) | (단위: 천원) |
| 구 분 | 기초 | 전입(환입) | 사용 | 전분기말 |
|---|---|---|---|---|
| 하자보수충당부채(주1)(주3) | 96,443 | (39,756) | - | 56,687 |
| 용역계약충당부채(주2)(주3) | 303,421 | (87,676) | - | 215,745 |
| 복구충당부채 | 329,851 | 55 | - | 329,906 |
| 반품충당부채 | 276 | - | - | 276 |
| 장기종업원급여충당부채(주3) | 6,522 | - | - | 6,522 |
| 합 계 | 736,513 | (127,377) | - | 609,136 |
| (주1) | HLB바이이코드㈜(구.(주)크로엔)는 고객에게 제공완료한 용역계약에 대한 보완작업을 위해 소비할 것으로 예상되는 지출을 충당부채로 설정하고 있습니다. |
| (주2) | 용역계약과 관련한 충당부채는 미래손실이 예상되는 용역에 대하여 최선의 추정치를 현재가치로 할인하지 않은 금액입니다. 이러한 추정은 변동될 수 있습니다. |
| (주3) | 전기 중 HLB바이오코드㈜(구.(주)크로엔)의 지분 매각으로 연결에서 제외되었습니다. |
17. 계약자산 및 계약이행원가, 계약부채
당분기말 및 전기말 현재 계약자산 및 계약이행원가, 계약부채의 잔액은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 계약자산 | 계약이행원가 | 계약부채 | |||
|---|---|---|---|---|---|---|
| 당분기말 | 전기말 | 당분기말 | 전기말 | 당분기말 | 전기말 | |
| CDMO(주1) | - | - | 1,541,049 | 1,853,184 | 1,101,210 | 1,266,876 |
| 합 계 | - | - | 1,541,049 | 1,853,184 | 1,101,210 | 1,266,876 |
| (주1) | 계약자산은 CDMO 진행률에 따라 인식되는 회사의 수행의무 이행정도와 고객에게 청구한 대가의 차이로 인해 인식되었습니다. 계약이행원가 및 계약부채는 CDMO 업무진척도 및 기간 안분에 따른 비용인식액 및 고객으로부터 선수취한 금액으로 제품납품시 매출원가 및 매출로 전환 될 예정입니다. |
18. 기타부채
당분기말 및 전기말 현재 기타부채의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 선수수익 | 330,000 | 330,000 |
| 예수금 | 99,394 | 100,632 |
| 선수금 | - | 20 |
| 합 계 | 429,394 | 430,652 |
19. 자본금
(1) 당분기말 및 전기말 현재 자본금에 관한 사항은 다음과 같습니다.
| (단위: 원, 주) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| ①발행할 주식의 총수 | 100,000,000 | 100,000,000 |
| ②1주당 액면금액 | 500 | 500 |
| ③발행한 주식의 수 | 56,054,149 | 56,054,149 |
| 보통주 | 56,054,149 | 56,054,149 |
| 우선주 | - | - |
| ④자본금 | 28,027,074,500 | 28,027,074,500 |
| 보통주자본금 | 28,027,074,500 | 28,027,074,500 |
| 우선주자본금 | - | - |
(2) 당분기와 전분기 중 유통주식수의 변동내역은 없습니다.
| (단위: 주) |
| 구 분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 보통주식수 | 우선주식수 | 보통주식수 | 우선주식수 | |
| 기초 | 56,054,149 | - | 55,937,925 | 67,499 |
| 기말 | 56,054,149 | - | 55,937,925 | 67,499 |
| (주1) | 전기 중 우선주 67,499주가 보통주 116,224주로 전환되었습니다. |
(3) 당분기말 현재 당사가 발행한 전환우선주는 없습니다.
20. 기타불입자본
(1) 당분기말 및 전기말 현재 기타불입자본의 구성내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 주식발행초과금 | 174,869,358 | 174,869,358 |
| 주식선택권 | 2,194,908 | 2,224,860 |
| 기타자본 | 4,976,720 | 4,946,768 |
| 합 계 | 182,040,986 | 182,040,986 |
(2) 당분기와 전분기 중 주식발행초과금의 변동내역은 없습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 기초금액 | 174,869,358 | 174,894,549 |
| 기말금액 | 174,869,358 | 174,894,549 |
(3) 당분기와 전분기 중 주식선택권의 변동내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 기초금액 | 2,224,860 | 2,224,860 |
| 주식매수선택권 권리상실분 대체 | (29,952) | - |
| 기말금액 | 2,194,908 | 2,224,860 |
(4) 당분기와 전분기 중 기타자본의 변동내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 기초금액 | 4,946,768 | 2,243,817 |
| 주식매수선택권 권리상실분 대체 | 29,952 | - |
| 기말금액 | 4,976,720 | 2,243,817 |
21. 결손금
(1) 당분기말 및 전기말 현재 결손금의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 미처리결손금 | (171,789,102) | (166,886,039) |
(2) 당분기 및 전분기 중 결손금의 변동내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 기초금액 | (166,886,039) | (159,354,428) |
| 지배기업 귀속 순손실 | (4,903,063) | (3,967,169) |
| 기말금액 | (171,789,102) | (163,321,597) |
22. 주식기준보상
당사는 설립, 경영 및 기술에 기여하거나 기여할 수 있는 임직원에게 발행주식수의 100분의 15 범위 내에서 주주총회 특별결의에 의하여 주식선택권을 부여할 수 있도록 하고 있으며, 당분기말 현재 부여된 주식선택권은 다음과 같습니다.
(1) 주식선택권의 구성내역
| 결제방식 | 주식결제형 |
|---|---|
| 약정유형 | 10차 |
| 부 여 일 | 2021.03.25 |
| 부여수량 | 689,000주 |
| 전기말 행사가능주식수 | 634,000주 |
| 당분기말 행사가능주식수 | 634,000주 |
| 부여일주식가격 | 7,120원 |
| 행사가격 | 6,123원 |
| 행사가능기간 | 부여일로부터 2년후 5년동안 |
| 가득조건 | 용역제공조건: 2년 |
| (주1) | 8차 주식선택권은 권리행사 만기일 초과로 인해 소멸하였습니다. |
(2) 주식선택권 변동내역
| (단위: 주,원) |
| 구 분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 주식선택권수량 | 가중평균 행사가격 | 주식선택권수량 | 가중평균 행사가격 | |
| 기 초 | 644,000 | 7,713 | 664,000 | 7,713 |
| 부 여 | - | - | - | - |
| 소 멸(주1) | (10,000) | 14,910 | - | - |
| 행 사 | - | - | - | - |
| 기 말 | 634,000 | 7,599 | 644,000 | 7,713 |
| (주1) | 권리행사 만기일 초과로 인해 소멸하였습니다. |
(3) 당분기 및 전분기 중 인식한 주식보상비용은 없습니다.
(4) 당사는 주식선택권의 보상원가를 이항모형을 이용한 공정가치접근법을 적용하여 산정했으며, 보상원가를 산정하기 위한 제반 가정 및 변수는 다음과 같습니다.
| 구 분 | 10차 |
|---|---|
| 부여된 선택권의 가중평균 공정가치 | 3,462원 |
| 부여일의 가중평균 주가 | 7,120원 |
| 주가변동성(주1) | 45.80% |
| 기대만기 | 7 년 |
| 무위험수익률 | 1.70% |
| (주1) | 주가변동성은 유사업종 주가분석에 기초하여 산출한 주식의 연속복리 투자수익률의 표준편차입니다. |
23. 매출
당분기 및 전분기 중 발생한 매출액의 주요 세부 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 한시점에 인식하는 수익 | ||
| 재화의 판매 | 673,837 | 1,160,398 |
| CDMO사업수익 | 236,467 | 1,381 |
| 수수료수익 | 30,000 | 6,437 |
| 소 계 | 940,304 | 1,168,216 |
| 기간에 걸쳐 인식하는 수익 | ||
| CDMO사업수익 | 14,051 | 115,775 |
| 합 계 | 954,355 | 1,283,991 |
| (주1) | 당분기 및 전분기의 중단영업 관련 손익은 제외한 금액입니다. |
24. 판매비와관리비
당분기와 전분기 중 판매비와관리비의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 급여 | 522,091 | 582,812 |
| 퇴직급여 | 95,433 | 80,452 |
| 복리후생비 | 73,394 | 82,342 |
| 경상연구개발비 | 3,231,117 | 2,496,712 |
| 지급수수료 | 760,480 | 766,219 |
| 광고선전비 | 15,378 | 54,593 |
| 감가상각비 | 21,093 | 7,642 |
| 무형자산상각비 | 5,640 | 10,151 |
| 기타 | 225,790 | 284,315 |
| 합 계 | 4,950,416 | 4,365,238 |
| (주1) | 당분기 및 전분기의 중단영업 관련 손익은 제외한 금액입니다. |
25. 금융수익 및 금융비용
(1) 당분기와 전분기 중 금융수익의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 이자수익 | 174,729 | 435,531 |
| 외환차익 | 61 | 111 |
| 외화환산이익 | - | 123 |
| 합 계 | 174,790 | 435,765 |
| (주1) | 당분기 및 전분기의 중단영업 관련 손익은 제외한 금액입니다. |
(2) 당분기와 전분기 중 금융비용의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 이자비용 | 126,996 | 98,740 |
| 외환차손 | 1,066 | 2,413 |
| 외화환산손실 | 8 | - |
| 당기손익-공정가치측정금융자산평가손실 | 142,169 | - |
| 합 계 | 270,239 | 101,153 |
| (주1) | 당분기 및 전분기의 중단영업 관련 손익은 제외한 금액입니다. |
(3) 당분기와 전분기 중 금융비용에 포함된 이자비용의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 장,단기차입금 | 83,054 | 79,823 |
| 리스부채 | 42,778 | 18,917 |
| 복구충당부채 | 1,164 | - |
| 합 계 | 126,996 | 98,740 |
| (주1) | 당분기 및 전분기의 중단영업 관련 손익은 제외한 금액입니다. |
26. 기타수익 및 기타비용
(1) 당분기와 당분기 중 기타수익의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 수입임대료 | 8,520 | 8,520 |
| 리스해지이익 | 4,392 | 152 |
| 리스변경이익 | - | 39,496 |
| 잡이익 | 7,918 | 16 |
| 합 계 | 20,830 | 48,184 |
| (주1) | 당분기 및 전분기의 중단영업 관련 손익은 제외한 금액입니다. |
(2) 당분기와 당분기 중 기타비용의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 무형자산폐기손실 | 5,920 | - |
| 유형자산폐기손실 | 581 | - |
| 잡손실 | 3,867 | 2,459 |
| 합 계 | 10,368 | 2,459 |
| (주1) | 당분기 및 전분기의 중단영업 관련 손익은 제외한 금액입니다. |
27. 비용의 성격별 분류
당분기와 전분기 중 발생한 비용의 성격별 분류 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 재고자산의 변동 | (35,260) | (607,034) |
| 상품 및 원재료 매입액 | 289,864 | 923,764 |
| 종업원급여 | 1,860,970 | 1,810,402 |
| 복리후생비 | 204,021 | 225,606 |
| 여비교통비 | 66,995 | 10,820 |
| 광고선전비 | 15,378 | 54,594 |
| 지급수수료 | 658,073 | 1,082,983 |
| 감가상각비 | 556,170 | 554,622 |
| 무형자산상각비 | 64,898 | 38,196 |
| 리스상각비 | 62,760 | 137,119 |
| 경상연구개발비 | 1,473,022 | 421,861 |
| 기타 | 482,241 | 466,403 |
| 합 계 | 5,699,132 | 5,119,336 |
| (주1) | 당분기 및 전분기의 중단영업 관련 손익은 제외한 금액입니다. |
28. 법인세
(1) 당사는 세무상 결손으로 인하여 당분기 및 전분기 중 법인세부담액이 없으며, 자본에 직접 가감되는 이연법인세도 없습니다.
(2) 이연법인세자산에 대한 미래 실현가능성은 당사의 성과, 전반적인 경제환경과 산업에 대한 전망, 향후 예상수익, 세액공제와 이월결손금의 공제가능기간 등 다양한 요소들을 고려하여 평가합니다.
당사는 주기적으로 이러한 사항들을 검토하고 있으며, 2025년 3월 31일 현재 가산할 일시적인 차이를 초과하는 차감할 일시적차이와 세무상 이월결손금잔액 및 이월세액공제에 대하여 실현가능성이 없다고 판단하여 이연법인세자산을 인식하지 않았습니다.
29. 퇴직급여제도
당사는 확정기여형퇴직급여제도를 시행하고 있습니다. 사외적립자산은 수탁자의 관리하에서 기금 형태로 당사의 자산들로부터 독립적으로 운용되고 있습니다. 종업원들이 확정기여형의 가득조건을 충족하기 전에 퇴사하는 경우에 당사가 지불해야 할 기여금은 상실되는 기여금만큼 감소하게 됩니다.
포괄손익계산서에 인식된 퇴직급여 중 283,670천원(전분기: 191,205천원)은 확정기여형 퇴직급여제도에서 규정하고 있는 비율에 따라 당사가 퇴직급여제도에 납입할 기여금을 나타내고 있습니다.
30. 주당손실
(1) 당분기와 전분기 중 기본주당손익의 내역은 다음과 같습니다.
| (단위: 주,원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 지배기업지분 분기순손익 | (4,903,062,772) | (3,967,168,840) |
| 지배기업지분 귀속 계속영업분기순손익 | (4,903,062,772) | (3,591,757,696) |
| 지배기업지분 귀속 중단영업분기순손익 | - | (375,411,144) |
| 가중평균유통보통주식수 | 56,054,149 | 55,937,925 |
| 계속영업기본주당손실 | (87) | (64) |
| 중단영업기본주당손실 | - | (7) |
(2) 기본주당손익 계산에 사용된 가중평균유통보통주식수는 다음과 같습니다.
| (당분기) | (단위: 주) |
| 일자 | 변동내역 | 발행주식수 | 유통보통주식수 | 가중치 | 가중평균 유통보통주식수 |
|---|---|---|---|---|---|
| 2025-01-01 | 기초 | 56,054,149 | 56,054,149 | 90 | 56,054,149 |
| 합 계 | 56,054,149 | 56,054,149 | 56,054,149 | ||
| (전분기) | (단위: 주) |
| 일자 | 변동내역 | 발행주식수 | 유통보통주식수 | 가중치 | 가중평균 유통보통주식수 |
|---|---|---|---|---|---|
| 2024-01-01 | 기초 | 55,937,925 | 55,937,925 | 91 | 55,937,925 |
| 합 계 | 55,937,925 | 55,937,925 | 55,937,925 | ||
(3) 당분기와 전분기 중 발행된 잠재적 보통주식이 있으나, 당분기순손실 상태이므로 희석주당손익을 산정하지 않았습니다.
31. 현금흐름표
(1) 당분기와 전분기 중 영업으로부터 창출된 현금흐름의 내용은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 분기순손익 | (4,903,063) | (4,171,804) |
| 조정: | ||
| 이자수익 | (174,729) | (435,963) |
| 이자비용 | 126,996 | 221,522 |
| 외화환산이익 | - | (123) |
| 외화환산손실 | 8 | - |
| 당기손익-공정가치측정금융자산평가손실 | 142,169 | - |
| 지분법이익 | - | - |
| 지분법손실 | 73,300 | 136,750 |
| 퇴직급여 | - | 52,901 |
| 하자보수비 | - | (39,756) |
| 용역계약이행비용 | - | (87,676) |
| 유형자산처분손실 | - | 1 |
| 유형자산폐기손실 | 581 | - |
| 무형자산폐기손실 | 5,920 | - |
| 감가상각비 | 556,170 | 753,494 |
| 무형자산상각비 | 64,898 | 44,100 |
| 리스상각비 | 62,760 | 169,772 |
| 대손상각비(환입) | 18,106 | - |
| 재고자산평가손실(환입) | 29,023 | 9,520 |
| 리스해지이익 | (4,392) | (14,688) |
| 리스변경이익 | - | (39,496) |
| 순운전자본의 증감: | ||
| 매출채권의 변동 | 216,821 | (909,230) |
| 기타유동자산의 변동 | 3,881,826 | (244,744) |
| 계약자산의 변동 | - | 56,992 |
| 계약이행원가의 변동 | 312,135 | (599,465) |
| 기타자산의 변동 | 13,162 | (421,647) |
| 재고자산의 변동 | (37,673) | (68,850) |
| 매입채무및기타채무의 변동 | (389,563) | 228,574 |
| 충당부채의 변동 | 1,173 | - |
| 계약부채의 변동 | (165,667) | (185,196) |
| 기타유동부채의 변동 | (1,258) | (109,948) |
| 장기미지급금의 변동 | (158,299) | 168 |
| 영업으로부터 창출된 현금 | (329,596) | (5,654,792) |
(2) 당분기 및 전분기의 현금의 유입과 유출이 없는 중요한 거래내역은 다음과 같습니다.
| (단위: 천원) |
| 내 역 | 당분기 | 전분기 |
|---|---|---|
| 유형자산 미지급금 대체 | 11,350 | - |
| 선급금의 무형자산 대체 | 37,215 | (2,264) |
| 리스회계처리로 인한 사용권자산 변동 | 20,697 | 11,859 |
| 리스회계처리로 인한 리스부채 변동 | 16,304 | 100,354 |
(3) 재무활동에서 발생한 부채의 당분기 및 전분기 중 변동내역은 다음과 같습니다.
| (당분기) | (단위: 천원) |
| 구 분 | 기초 | 재무활동 현금흐름에서 발생한 변동 |
기말 | |||
|---|---|---|---|---|---|---|
| 신규 리스 | 리스 이자비용 |
리스의 변경 등 | ||||
| 금융기관 차입금 | 6,710,000 | - | - | - | - | 6,710,000 |
| 리스부채 | 1,745,978 | (84,785) | 60,103 | 42,778 | (43,798) | 1,720,276 |
| 재무활동으로부터의 총부채 | 8,455,978 | (84,785) | 60,103 | 42,778 | (43,798) | 8,430,276 |
| (전분기) | (단위: 천원) |
| 구 분 | 기초 | 재무활동 현금흐름에서 발생한 변동 |
비현금 변동 | 기말 | |||
|---|---|---|---|---|---|---|---|
| 전환권조정 상각 이자비용 |
신규 리스 | 리스 이자비용 |
리스의 변경 등 | ||||
| 전환사채 | 1,715,956 | - | 12,699 | - | - | - | 1,728,655 |
| 금융기관 차입금 | 9,810,000 | 200,000 | - | - | - | - | 10,010,000 |
| 리스부채 | 2,083,325 | (140,625) | - | 30,654 | 23,005 | (366,258) | 1,630,101 |
| 상환전환우선주부채 | 5,605,045 | - | 41,459 | - | - | - | 5,646,504 |
| 재무활동으로부터의 총부채 | 19,214,326 | 59,375 | 54,158 | 30,654 | 23,005 | (366,258) | 19,015,260 |
32. 금융상품
(1) 자본위험관리
당사의 자본관리의 주 목적은 당사의 영업활동을 유지하고 주주가치를 극대화하기 위하여 높은 신용등급과 건전한 자본비율을 유지하기 위한 것입니다. 당사는 자본구조를 경제환경의 변화에 따라 수정하고 있으며, 이를 위하여 배당정책을 수정하거나 자본감소 혹은 신주발행을 검토하도록 하고 있습니다. 한편, 기중 자본관리의 목적, 정책 및 절차에 대한 변경사항은 없습니다.
당사의 당분기말 및 전기말 현재 부채비율은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 부채 | 11,924,801 | 12,804,093 |
| 자본 | 38,278,959 | 43,182,021 |
| 부채비율 | 31.15% | 29.65% |
(2) 금융위험관리
당사는 금융상품과 관련하여 시장위험(통화위험, 이자율위험 및 가격위험), 신용위험, 유동성위험과 같은 다양한 금융위험에 노출되어 있습니다. 당사의 위험관리는 당사의 재무적 성과에 영향을 미치는 잠재적 위험을 식별하여 당사가 허용가능한 수준으로 감소, 제거 및 회피하는 것을 그 목적으로 하고 있습니다.
1) 시장위험
당사의 활동은 주로 환율과 이자율의 변동으로 인한 금융위험에 노출되어 있으며 시장위험에 대한 당사의 위험노출정도 또는 위험을 관리하고 측정하는 방식에는 변경이 없습니다.
가. 이자율위험
당사는 변동이자율로 자금을 차입하고 있으며 보유하고 있는 변동이자율부 금융상품의 이자율 변동으로 인하여 이자율 위험에 노출되어 있습니다. 위험회피활동과 관련하여 당사는 이자율 현황과 정의된 위험성향을 적절히 조정하면서 정기적으로 평가하여 최적의 위험회피 전략이 적용되도록 하고 있습니다.
당분기말 현재 각 자산 및 부채에 대한 이자율이 1% 변동시 이자율변동이 법인세비용차감전순손익에 미치는 영향은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 1% 상승시 | 1% 하락시 |
|---|---|---|
| 차입금 | (67,100) | 67,100 |
한편, 당사는 이자율 위험에 대해 다양한 방법의 분석을 수행하고 있습니다. 당사는 이자율변동 위험을 최소화하기 위해 재융자, 기존 차입금의 갱신, 대체적인융자 및 위험회피 등 다양한 방법을 검토하여 당사 입장에서 가장 유리한 자금조달 방안에 대한 의사결정을 수행하고 있습니다.
나. 환율변동위험
당분기말 및 전기말 현재 당사가 보유하고 있는 외화표시 화폐성자산 및 화폐성부채의 장부금액은 다음과 같습니다.
| (원화단위 : 천원, 외화단위 : USD) |
| 구 분 | 통 화 | 당분기말 | 전기말 | ||
|---|---|---|---|---|---|
| 외화금액 | 원화환산금액 | 외화금액 | 원화환산금액 | ||
| 자산 : | |||||
| 현금및현금성자산 | USD | 2,151.47 | 3,155 | 2,151.47 | 3,163 |
보고기간 중 모든 다른 변수가 일정하고 각 외화에 대한 기능통화의 환율이 10% 변동시 환율변동이 당분기손익에 미치는 영향은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 10% 상승시 | 10% 하락시 |
|---|---|---|
| USD | 316 | (316) |
2) 신용위험
신용위험은 보유하고 있는 수취채권 및 확정계약을 포함한 거래처에 대한 신용위험 뿐 아니라 은행, 금융기관 예치금으로부터 발생하고 있습니다. 은행 및 금융기관의 경우, 신용등급이 우수한 금융기관과 거래하고 있으므로 은행 및 금융기관으로부터의 신용위험은 제한적입니다. 일반거래처의 경우 고객의 재무상태, 과거경험 등 기타요소들을 고려하여 신용을 평가하게 됩니다.
① 신용위험에 대한 노출
금융자산의 장부금액은 신용위험에 대한 최대노출정도를 나타냅니다. 당사는 현금및현금성자산을 신용등급이 우수한 금융기관에 예치하고 있어, 금융기관으로부터의 신용위험은 제한적입니다.
당분기말 현재 당사가 보유하고 있는 금융자산의 신용위험에 대한 최대노출금액은 채권의 각 분류별 장부금액입니다.
② 금융자산 손상차손
당분기와 전분기 중 금융자산과 관련하여 발생한 손상차손은 없습니다.
3) 유동성위험관리
당사는 유동성위험을 관리하기 위하여 단기 및 중장기 자금관리계획을 수립하고 현금유출예산과 실제현금유출액을 지속적으로 분석하고 검토하여 금융부채와 금융자산의 만기구조를 대응시키고 있습니다. 당사의 경영진은 영업활동현금흐름과 금융자산의 현금유입으로 금융부채를 상환가능하다고 판단하고 있습니다.
당분기말 및 전기말 현재 당사가 보유하고 있는 비파생 금융자산 및 금융부채의 잔존계약 만기에 따른 만기분석 내역은 다음과 같습니다. 아래 표에 표시된 현금흐름은 원금 및 이자의 현금흐름을 모두 포함하고 있으며, 현재가치로 할인하지 아니한 금액입니다.
(당분기말)
가. 금융자산
| (단위: 천원) |
| 구 분 | 1년미만 | 1년이상 2년미만 | 2년이상 | 합 계 |
|---|---|---|---|---|
| 현금및현금성자산 | 2,165,831 | - | - | 2,165,831 |
| 장단기금융상품 | 15,500,082 | 100,000 | - | 15,600,082 |
| 당기손익-공정가치측정금융자산 | - | - | 2,753,286 | 2,753,286 |
| 매출채권및기타채권 | 1,597,849 | 69,236 | 318,052 | 1,985,137 |
| 합 계 | 19,263,762 | 169,236 | 3,071,338 | 22,504,336 |
나. 금융부채
| (단위: 천원) |
| 구 분 | 1년미만 | 1년이상 2년미만 | 2년이상 | 합 계 |
|---|---|---|---|---|
| 차입금(주1) | 3,916,177 | 911,037 | 2,492,879 | 7,320,093 |
| 매입채무및기타채무(주2) | 1,188,256 | 23,000 | 451,414 | 1,662,670 |
| 리스부채(주3) | 323,072 | 313,862 | 1,952,814 | 2,589,748 |
| 합 계 | 5,427,505 | 1,247,899 | 4,897,107 | 11,572,511 |
| (주1) | 당분기말 현재 예상되는 차입금 이자비용이 포함되어 있습니다. |
| (주2) | 인건비성 미지급비용은 제외한 금액입니다. |
| (주3) | 할인되지 않은 현금흐름을 기초로 작성하였습니다. |
(전기말)
가. 금융자산
| (단위: 천원) |
| 구 분 | 1년미만 | 1년이상 2년미만 | 2년이상 | 합 계 |
|---|---|---|---|---|
| 현금및현금성자산 | 2,766,684 | - | - | 2,766,684 |
| 장단기금융상품 | 15,500,050 | 100,000 | - | 15,600,050 |
| 당기손익-공정가치측정금융자산 | - | - | 2,932,656 | 2,932,656 |
| 매출채권및기타채권 | 5,272,742 | 60,676 | 284,252 | 5,617,670 |
| 합 계 | 23,539,476 | 160,676 | 3,216,908 | 26,917,060 |
나. 금융부채
| (단위: 천원) |
| 구 분 | 1년미만 | 1년이상 2년미만 | 2년이상 | 합 계 |
|---|---|---|---|---|
| 차입금(주1) | 3,974,511 | 930,167 | 2,544,919 | 7,449,597 |
| 매입채무및기타채무(주2) | 1,712,372 | 23,000 | 609,713 | 2,345,085 |
| 리스부채(주3) | 341,028 | 308,601 | 2,001,389 | 2,651,018 |
| 합 계 | 6,027,911 | 1,261,768 | 5,156,021 | 12,445,700 |
| (주1) | 전기말 현재 예상되는 차입금 이자비용이 포함되어 있습니다. |
| (주2) | 인건비성 미지급비용은 제외한 금액입니다. |
| (주3) | 할인되지 않은 현금흐름을 기초로 작성하였습니다. |
한편, 상기 분석은 장부금액을 기초로 당사가 지급하여야 하는 가장 빠른 만기일에 근거하여 작성되었습니다.
(3) 범주별 금융상품
1) 당분기말 및 전기말 현재 금융자산의 범주별 장부금액은 다음과 같습니다.
| (단위: 천원) |
| 금융자산 범주 | 계정과목 | 당분기말 | 전기말 |
|---|---|---|---|
| 당기손익-공정가치측정금융자산 | 당기손익-공정가치측정금융자산 | 2,753,286 | 2,932,656 |
| 대여금및수취채권 | 현금및현금성자산 | 2,165,831 | 2,766,684 |
| 단기금융상품 | 15,500,082 | 15,500,050 | |
| 장기금융상품 | 100,000 | 100,000 | |
| 매출채권및기타채권 | 1,597,849 | 5,272,742 | |
| 장기기타채권 | 262,280 | 217,996 | |
| 합 계 | 22,379,328 | 26,790,128 | |
2) 당분기말 및 전기말 현재 금융부채의 범주별 장부금액은 다음과 같습니다.
| (단위: 천원) |
| 금융부채 범주 | 계정과목 | 당분기말 | 전기말 |
|---|---|---|---|
| 상각후원가로 측정하는 금융부채 |
차입금 | 6,710,000 | 6,710,000 |
| 매입채무및기타채무(주1) | 1,662,670 | 2,345,086 | |
| 리스부채 | 1,720,275 | 1,745,978 | |
| 합 계 | 10,092,945 | 10,801,064 | |
| (주1) | 인건비성 미지급비용은 제외한 금액입니다. |
3) 당분기 및 전분기 중 금융자산과 금융부채의 범주별 순손익은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 | ||||
|---|---|---|---|---|---|---|
| 금융수익 | 금융비용 | 금융손익 | 금융수익 | 금융비용 | 금융손익 | |
| 당기손익-공정가치측정금융자산 | - | (142,169) | (142,169) | - | - | - |
| 대여금및수취채권 | 174,790 | (1,073) | 173,717 | 435,765 | (2,413) | 433,352 |
| 상각후원가로 측정하는 금융부채 | - | (126,996) | (126,996) | - | (98,740) | (98,740) |
| 합 계 | 174,790 | (270,238) | (95,448) | 435,765 | (101,153) | 334,612 |
(4) 금융상품의 공정가치
당사는 공정가치로 측정되는 금융상품을 공정가치 측정에 사용된 투입변수에 따라 다음과 같은 공정가치 서열체계로 분류하였습니다.
| (수준1) | 동일한 자산이나 부채에 대한 활성시장에서 공시된 가격(조정되지 않은)을 사용하여 도출되는 공정가치입니다. |
| (수준2) | 수준 1 에 해당되는 공시된 가격을 제외한, 자산이나 부채에 대하여 직접적으로 (가격) 또는 간접적으로(가격으로부터 도출) 관측가능한 투입변수를 사용하여 도출되는 공정가치입니다. |
| (수준3) | 자산이나 부채에 대하여 관측가능한 시장정보에 근거하지 않은 투입변수(관측불가능한 변수)를 사용하는 평가기법으로부터 도출되는 공정가치입니다. |
당분기말 및 전기말 현재 당사의 상기 서열체계에 따른 공정가치 측정치는 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|
| 수준1 | 수준2 | 수준3 | 수준1 | 수준2 | 수준3 | |
| 금융자산: | ||||||
| 당기손익-공정가치측정금융자산 | 608,069 | - | 3,448,377 | 750,238 | - | 3,448,377 |
(5) 당사는 수준 간의 이동을 가져오는 사건이나 상황의 변동이 발생하는 시점에 수준 간의 이동을 인식하고 있으며, 당분기 중 유의적인 이동은 없습니다.
(6) 다음은 수준 2와 수준 3으로 분류되는 주요 금융상품 공정가치측정치에 사용된 가치평가기법과 투입변수에 대한 설명입니다.
| (당분기말) | (단위: 천원) |
| 구 분 | 공정가치 | 수준 | 가치평가기법 | 투입변수 |
|---|---|---|---|---|
| 반복적인 공정가치의 측정치 | ||||
| 금융자산 | ||||
| 당기손익-공정가치측정금융자산 | 1,948,377 | 3 | 이항옵션평가모형 | 주가변동성 79.55% 할인율 2.95% |
| 당기손익-공정가치측정금융자산 | 1,500,000 | 3 | 원가법 | N/A |
| (전기말) | (단위: 천원) |
| 구 분 | 공정가치 | 수준 | 가치평가기법 | 투입변수 |
|---|---|---|---|---|
| 반복적인 공정가치의 측정치 | ||||
| 금융자산 | ||||
| 당기손익-공정가치측정금융자산 | 1,948,377 | 3 | 이항옵션평가모형 | 주가변동성 79.55% 할인율 2.95% |
| 당기손익-공정가치측정금융자산 | 1,500,000 | 3 | 원가법 | N/A |
(7) 금융자산의 재분류 및 양도
당분기 및 전분기 중 목적이나 사용의 변경으로 인하여 재분류된 금융자산은 없으며, 당분기말 및 전기말 현재 양도되었으나 전체가 제거되지 않은 금융자산은 없습니다.
33. 특수관계자 등 거래
(1) 당분기말 및 전기말 현재 당사의 특수관계자 현황은 다음과 같습니다.
| 관 계 | 당분기말 | 전기말 |
|---|---|---|
| 공동기업 및 관계기업 | HLB바이오코드(주)(주2) | HLB바이오코드(주)(주2) |
| (주)디앤케이코퍼레이션 | (주)디앤케이코퍼레이션 | |
| (주)블루진 | (주)블루진 | |
| (주)프리모리스테라퓨틱스 | (주)프리모리스테라퓨틱스 | |
| 기타 특수관계자 | (주)프리모리스인터내셔널(주1) | (주)프리모리스인터내셔널(주1) |
| 마루테라퓨틱스(주1) | 마루테라퓨틱스(주1) | |
| 주요경영진 | 주요경영진 |
| (주1) | 당사에 대한 지배력을 보유하고 있는 개인 등이 지배력을 보유하고 있는 회사입니다. |
| (주2) | 전기 중 사명을 (주)크로엔에서 HLB바이오코드(주)로 변경하였으며, 보유 주식 1,183,676주(64.50%)중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류하였습니다. |
(2) 당분기 및 전분기 중 특수관계자와의 주요 거래 내역은 다음과 같습니다.
| (단위: 천원) |
| 특수관계자 명칭 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 영업수익 등 | 영업비용 등 | 영업수익 등 | 영업비용 등 | |
| HLB바이오코드㈜ | 2,268 | - | - | - |
| (주)프리모리스인터내셔널(주1) | 364,806 | 29,053 | 510,022 | 37,906 |
| (주)프리모리스테라퓨틱스 | 17,280 | 78,117 | 11,826 | 13 |
| 합 계 | 384,354 | 107,170 | 521,848 | 37,919 |
| (주1) | 당사는 특수관계자인 (주)프리모리스인터내셔널과 연간 상품공급계약을 맺고 있습니다. |
(3) 당분기말 및 전기말 현재 특수관계자간 주요 채권ㆍ채무잔액은 다음과 같습니다.
| (단위: 천원) |
| 특수관계자 명칭 | 당분기말 | 전기말 | ||||||
|---|---|---|---|---|---|---|---|---|
| 채권 | 채무 | 채권 | 채무 | |||||
| 매출채권 등 (주1) |
계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | 매출채권 등 (주1) |
계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | |
| HLB바이오코드(주) | 2,268 | - | - | - | - | - | - | - |
| (주)프리모리스인터내셔널 | 172,992 | - | 10,453 | - | 403,923 | - | 14,160 | - |
| (주)프리모리스테라퓨틱스 | 67,555 | - | - | 2,000 | 49,375 | - | - | 2,000 |
| 합 계 | 242,815 | - | 10,453 | 2,000 | 453,298 | - | 14,160 | 2,000 |
| (주1) | 당분기말 채권은 대손충당금 차감전 금액이 기재되어 있습니다. 상기 특수관계자 채권에 설정되어 있는 대손충당금은 18백만원입니다. |
(4) 당분기 중 특수관계에 대한 지분거래내역은 없으며, 전분기 중 특수관계자에 대한 지분거래내역은 다음과 같습니다.
| (전분기) | (단위: 천원) |
| 특수관계자 명칭 | 구 분 | 금액 |
|---|---|---|
| HLB바이오코드㈜ | 보통주 유상증자(주1) | 989,998 |
| (주)프리모리스테라퓨틱스 | 보통주 무상수증(주2) | - |
| (주1) | 전기 중 보통주 유상증자로 183,333주를 취득하였습니다. |
| (주2) | 전기까지 최대주주 및 당사 임원으로부터 프리모리스테라퓨틱스 보통주 87,200주를 무상수증받아, 취득금액은 영(0)입니다. |
(5) 당분기와 전분기 중 특수관계자와의 자금거래내역은 다음과 같습니다.
| (당분기) | (단위: 천원) |
| 특수관계자 명칭 | 구 분 | 기초 | 증가 | 감소 | 기말 |
|---|---|---|---|---|---|
| HLB바이오코드(주) | 대여금 | 200,000 | - | - | 200,000 |
| (주)프리모리스테라퓨틱스 | 대여금 | 730,000 | - | - | 730,000 |
| (주)프리모리스테라퓨틱스 | 상환전환우선주 | 2,000,050 | - | - | 2,000,050 |
| (전분기) | (단위: 천원) |
| 특수관계자 명칭 | 구 분 | 기초 | 증가 | 감소 | 기말 |
|---|---|---|---|---|---|
| (주)프리모리스테라퓨틱스 | 대여금 | - | 450,000 | - | 450,000 |
| (주)프리모리스테라퓨틱스 | 상환전환우선주 | 2,000,050 | - | - | 2,000,050 |
(6) 당분기말 현재 특수관계자에게 제공하거나, 특수관계자로부터 제공받은 담보 및 지급보증은 없습니다.
(7) 지배기업의 주요 경영진에 대한 보상
당사는 기업활동의 계획ㆍ지휘ㆍ통제에 대한 중요한 권한과 책임을 가진 등기이사를 주요 경영진으로 판단하였습니다.
당분기와 전분기 중 지배기업의 주요 경영진에 대한 보상내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 급여 | 170,650 | 171,013 |
| 퇴직급여 | 29,042 | 31,682 |
| 합 계 | 199,692 | 202,695 |
34. 우발부채 및 약정사항
(1) 당분기말 현재 금융기관과의 주요 약정사항은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 금융기관 | 약정금액 | 실행금액 |
|---|---|---|---|
| 시설자본 대출약정 | 기업은행 | 4,000,000 | 3,000,000 |
| 시설자본 대출약정 | 기업은행 | 1,480,000 | 1,480,000 |
| 시설자본 대출약정 | 기업은행 | 350,000 | 350,000 |
| 시설자본 대출약정 | 기업은행 | 380,000 | 380,000 |
| 운영자금 대출약정 | 기업은행 | 1,500,000 | 1,500,000 |
(2) 당분기말 현재 당사가 특수관계자를 제외한 타인으로부터 제공받은 지급보증의 내용은 다음과 같습니다.
| (단위: 천원) |
| 제공받은자 | 보증자 | 보증일 | 보증금액 | 보증내용 |
|---|---|---|---|---|
| (주)지에스리테일 | 서울보증보험 | 2024.11.03~2026.11.02 | 10,000 | 홈쇼핑계약 등에 따른 손해배상금 |
| (주)씨제이이엔엠 | 서울보증보험 | 2023.09.27~2025.09.26 | 40,000 | 홈쇼핑계약 등에 따른 손해배상금 |
(3) 당분기말 현재 당사는 주식회사 대웅제약과 세포치료제에 대한 판권 및 공동개발계약을 체결하고 있으며, 상기 거래와 관련하여 수령한 계약금은 수익을 이연하여 인식합니다.
6. 배당에 관한 사항
가. 회사의 배당정책에 관한 사항
당사는 누적결손에 따른 상법상 배당가능한도 산출이 어려워 과거 배당내역이 없습니다. 이에 별도의 재무지표 산출방법 및 영업이익 기준 배당정책이 마련되어있지 않습니다. 배당수준의 방향성 또한 현재는 없으나, 당사는 안정적인 수익창출을 통한 배당가능재원 확보시, 회사 정관 규정에 의거하여 이익규모 및 미래성장을 위한 투자재원 확보, 기업의 재무구조 건전성 유지 등의 요인을 종합적으로 고려하여 배당정책을 결정할 예정입니다. 또한, 지속적인 주주가치 증대를 위해 핵심사업에 대한 경쟁력 확보와 안정적 수익 창출을 통하여, 주주의 배당요구를 충족시킬 수 있도록 배당을 실시할 계획이며 사업환경, 투자, Cash Flow, 부채비율에 따른 재무구조 개선여부 등을 종합적으로 고려한 잉여현금흐름을 배당재원으로 하여금 그 배당성향을 늘려나가고자 합니다.
나. 배당관련 예측가능성 제공에 관한 사항
1) 정관상 배당절차 개선방안 이행 가부
| 구분 | 현황 및 계획 |
| 정관상 배당액 결정 기관 | 주주총회 |
| 정관상 배당기준일을 배당액 결정 이후로 정할 수 있는지 여부 | 가능 |
| 배당절차 개선방안 이행 관련 향후 계획 | 미정 |
나. 배당액 확정일 및 배당기준일 지정 현황
| 구분 | 결산월 | 배당여부 | 배당액 확정일 |
배당기준일 | 배당 예측가능성 제공여부 |
비고 |
|---|---|---|---|---|---|---|
| 1 | 2024년 12월 | X | - | - | X | - |
| 2 | 2023년 12월 | X | - | - | X | - |
| 3 | 2022년 12월 | X | - | - | X | - |
다. 기타 참고사항(배당 관련 정관의 내용 등)
1) 정관사항
배당과 관련한 회사의 정관내용은 아래와 같습니다.
| 제16조(주주명부의 폐쇄 및 기준일) ① 회사는 의결권을 행사하거나 배당을 받을자 기타 주주 또는 질권자로서 권리를 행사할 자를 정하기 위하여 이사회 결의로 일정한 기간을 정하여 주주명부의 기재변경을 정지하거나 일정한 날에 주주명부에 기재된 주주 또는 질권자를 그 권리를 행사할 주주 또는 질권자로 볼 수있다. ② 회사가 제1항의 기간 또는 날을 정하는 경우 3개월을 경과하지 아니하는 일정한 기간을 정하여 권리에 관한 주주명부의 기재변경을 정지하거나, 3개월내로 정한 날에 주주명부에 기재되어 있는 주주를 그 권리를 행사할 주주로할 수 있다. ③ 회사가 제1항의 기간 또는 날을 정한 때에는 그 기간 또는 날의 2주 전에이를 공고하여야 한다. |
| 제57조(이익배당) ① 이익배당은 금전 또는 금전 외의 재산으로 할 수 있다. ② 이익의 배당을 주식으로 하는 경우 회사가 종류주식을 발행한 때에는 주주총회의 결의로 그와 다른 종류의 주식으로도 할 수 있다. ③ 제1항의 배당은 이사회 결의로 정하는 배당기준일 현재의 주주명부에 기재된 주주 또는 등록된 질권자에게 지급한다. ④ 이익배당은 주주총회의 결의로 정한다. 다만, 제54조제6항에 따라 재무제표를 이사회가 승인하는 경우 이사회 결의로 이익배당을 정한다. ⑤ 제1항의 배당금은 지급개시일로부터 5년 이내에 지급청구를 하지 아니한 때에는 그 청구권을 포기한 것으로 간주하고 이는 회사에 귀속한다. |
2) 주요배당지표
| 구 분 | 주식의 종류 | 당기 | 전기 | 전전기 |
|---|---|---|---|---|
| 제16기 1분기 | 제15기 | 제14기 | ||
| 주당액면가액(원) | 500 | 500 | 500 | |
| (연결)당기순이익(백만원) | -4,903 | -7,990 | -21,949 | |
| (별도)당기순이익(백만원) | - | - | - | |
| (연결)주당순이익(원) | -87 | -126 | -476 | |
| 현금배당금총액(백만원) | - | - | - | |
| 주식배당금총액(백만원) | - | - | - | |
| (연결)현금배당성향(%) | - | - | - | |
| 현금배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주식배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주당 현금배당금(원) | - | - | - | - |
| - | - | - | - | |
| 주당 주식배당(주) | - | - | - | - |
| - | - | - | - | |
3) 과거 배당 이력
| (단위: 회, %) |
| 연속 배당횟수 | 평균 배당수익률 | ||
|---|---|---|---|
| 분기(중간)배당 | 결산배당 | 최근 3년간 | 최근 5년간 |
| - | - | - | - |
-해당사항 없습니다.
7. 증권의 발행을 통한 자금조달에 관한 사항
7-1. 증권의 발행을 통한 자금조달 실적
가. 자본금 변동현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 원, 주) |
| 주식발행 (감소)일자 |
발행(감소) 형태 |
발행(감소)한 주식의 내용 | ||||
|---|---|---|---|---|---|---|
| 종류 | 수량 | 주당 액면가액 |
주당발행 (감소)가액 |
비고 | ||
| 2020년 01월 13일 | 주식매수선택권행사 | 보통주 | 20,000 | 500 | 1,500 | - |
| 2020년 02월 11일 | 주식매수선택권행사 | 보통주 | 110,000 | 500 | 1,500 | - |
| 2020년 08월 21일 | 전환권행사 | 보통주 | 3,423,295 | 500 | 10,370 | 우선주의 보통주 전환 |
| 2020년 08월 28일 | 전환권행사 | 보통주 | 96,431 | 500 | 10,370 | 우선주의 보통주 전환 |
| 2020년 11월 04일 | 전환권행사 | 보통주 | 337,503 | 500 | 10,370 | 우선주의 보통주 전환 |
| 2021년 02월 03일 | 주식매수선택권행사 | 보통주 | 10,000 | 500 | 3,500 | - |
| 2021년 03월 03일 | 주식매수선택권행사 | 보통주 | 10,000 | 500 | 3,500 | - |
| 2021년 03월 22일 | 전환권행사 | 보통주 | 675,022 | 500 | 10,370 | 우선주의 보통주 전환 |
| 2021년 04월 02일 | 주식매수선택권행사 | 보통주 | 30,000 | 500 | 3,500 | - |
| 2021년 10월 22일 | 유상증자(주주배정) | 보통주 | 12,376,237 | 500 | 3,150 | - |
| 2023년 11월 08일 | 유상증자(주주배정) | 보통주 | 18,000,000 | 500 | 1,165 | (주1) |
| 2024년 05월 31일 | 전환권행사 | 보통주 | 116,224 | 500 | 8,604 | 우선주의 보통주 전환 |
| (주1) | 2023년 8월 11일 이사회에서 주주배정 유상증자를 결의하였으며, 2023년 11월 20일 보통주 18,000,000주를 발행하였습니다. |
| [채무증권의 발행 등과 관련된 사항] |
채무증권 발행실적
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 원, %) |
| 발행회사 | 증권종류 | 발행방법 | 발행일자 | 권면(전자등록)총액 | 이자율 | 평가등급 (평가기관) |
만기일 | 상환 여부 |
주관회사 |
|---|---|---|---|---|---|---|---|---|---|
| (주)강스템바이오텍 | 회사채 | 사모 | 2016년 09월 08일 | 30,000 | 표면이자율:0 표면이자율:1 |
- | 2021년 09월 08일 | 상환 | - |
| 합 계 | - | - | - | 30,000 | - | - | - | - | - |
기업어음증권 미상환 잔액
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
1년초과 2년이하 |
2년초과 3년이하 |
3년 초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | |
단기사채 미상환 잔액
| (기준일 : | 2024년 12월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
합 계 | 발행 한도 | 잔여 한도 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
회사채 미상환 잔액
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
신종자본증권 미상환 잔액
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 1년 이하 | 1년초과 5년이하 |
5년초과 10년이하 |
10년초과 15년이하 |
15년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
조건부자본증권 미상환 잔액
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | - | |
7-2. 증권의 발행을 통해 조달된 자금의 사용실적
가. 공모자금의 사용내역
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 증권신고서 등의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
| 주주배정 유상증자 |
1 | 2018년 07월 28일 | 운영자금 | 35,952 | 운영자금 | 35,952 | (주1) |
| 주주배정 유상증자 |
2 | 2021년 10월 21일 | 운영자금 | 38,985 | 운영자금 | 37,781 | (주2) |
| 주주배정 유상증자 |
3 | 2023년 11월 08일 | 운영자금 | 20,970 | 운영자금 | 12,545 | (주3) |
| (주1) | 2018년 유상증자대금 360억원에 대하여 아토피피부염 치료제의 유럽임상비 240억원, 류마티스관절염 치료제의 국내임상비 68억원, 골관절염 국내임상비 8억원으로 계획 및 사용되었습니다. 또한, 공정개발연구를 위해 기기 및 장비 개발, 원재료 구매로 44억원 계획 및 사용되었습니다. |
| (주2) | 2021년 유상증자대금 390억원에 대하여 임상시험비 377억원, 운영경비 13억원으로 계획하였으며, 보고서 작성기준일 현재 임상시험비 365억원, 운영경비 13억원을 사용하였고, 미사용 자금은 예금 보관되어 있습니다. |
| (주3) | 2023년 유상증자대금 210억원에 대하여 임상시험비 107억원, 운영경비 103억원으로 계획하였으며, 보고서 작성기준일 현재 임상시험비 75억, 운영경비 50억원을 사용하였고, 미사용 자금은 예금 보관되어 있습니다. |
나. 사모자금의 사용내역
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 주요사항보고서의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
| 제3자배정 유상증자 |
1 | 2017년 04월 29일 | 운영자금 | 1,400 | 운영자금 | 1,400 | (주1) |
| 제3자배정 유상증자 |
2 | 2019년 07월 12일 | 운영자금 | 48,000 | 운영자금 | 48,000 | (주2) |
| 주1) | 2017년 유상증자대금 14억원에 대하여 연구개발비 7억원, 일반운영비 7억원으로 계획 및 사용하였습니다. |
| (주2) | 2019년 유상증자대금 480억원에 대하여 연구개발비 300억원, 일반운영비 180억원으로 계획 및 사용하였습니다. 연구개발비는 아토피피부염 치료제의 시장확대를 위한 추가 임상개발 및 후속 파이프라인 R&D등에 사용하였습니다. |
다. 미사용자금의 운용내역
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원) |
| 종류 | 운용상품명 | 운용금액 | 계약기간 | 실투자기간 |
|---|---|---|---|---|
| 예ㆍ적금 | 정기예금 | 1,204 | - | - |
| 예ㆍ적금 | 정기예금 | 8,425 | - | - |
| 계 | 9,629 | - | ||
| (주1) | 자금사용시점 도래시 순차적으로 사용할 예정이며, 미사용자금은 보통예금 및 정기예금 등 금융상품에 예치하고 있습니다. |
| (주2) | 정기예금은 3개월~12개월 단위로 운용하고 있습니다. |
8. 기타 재무에 관한 사항
(1) 재무제표를 재작성한 경우 재작성사유, 내용 및 재무제표에 미치는 영향
- 해당사항 없음 -
(2) 합병, 분할, 자산양수도, 영업양수도
- 해당사항 없음 -
(3) 자산유동화와 관련한 자산매각의 회계처리 및 우발채무 등에 관한 사항
| (단위: 천원) |
| 구 분 | 금융기관 | 약정금액 | 실행금액 |
|---|---|---|---|
| 시설자본 대출약정 | 기업은행 | 4,000,000 | 3,000,000 |
| 시설자본 대출약정 | 기업은행 | 1,480,000 | 1,480,000 |
| 시설자본 대출약정 | 기업은행 | 350,000 | 350,000 |
| 시설자본 대출약정 | 기업은행 | 380,000 | 380,000 |
| 운영자금 대출약정 | 기업은행 | 1,500,000 | 1,500,000 |
(2) 당분기말 현재 당사가 특수관계자를 제외한 타인으로부터 제공받은 지급보증의 내용은 다음과 같습니다.
| (단위: 천원) |
| 제공받은자 | 보증자 | 보증일 | 보증금액 | 보증내용 |
|---|---|---|---|---|
| (주)지에스리테일 | 서울보증보험 | 2024.11.03~2026.11.02 | 10,000 | 홈쇼핑계약 등에 따른 손해배상금 |
| (주)씨제이이엔엠 | 서울보증보험 | 2023.09.27~2025.09.26 | 40,000 | 홈쇼핑계약 등에 따른 손해배상금 |
(3) 당분기말 현재 당사는 주식회사 대웅제약과 세포치료제에 대한 판권 및 공동개발계약을 체결하고 있으며, 상기 거래와 관련하여 수령한 계약금은 수익을 이연하여 인식합니다.
4) 기타 재무제표 이용에 유의하여야 할 사항
- 당사는 2018년 2월 1일자로 (주)코스온 합자투자로 더마코스메틱 전문 라보셀 주식회사를 설립, 취득하여 당사에 신규 편입하였으며, 62.5%의 지분을 10억원에 취득하여 지배력을 획득하였습니다만, 2020년 12월 중 잔여지분 37.5%를 추가로 획득 후, 2021년 2월 23일 합병기일을 기준으로 당사에 흡수합병되어 소멸되었습니다.
- 당사는 2017년 4월 28일에 HLB바이오코드(주)(구.(주)크로엔) 지분 1,183,676주(지분율 71.48%)를 27억원에 취득하여 지배력을 획득하고, 당사에 종속회사로 신규 편입하였습니다. 이후 2024년 4월 중, 보유주식 1,183,676주 중 532,654주를 매각하는 등 보유 지분 매각으로 인해 종속회사에 대한 지배력을 상실하여 연결에서 제외하였습니다. 아울러 2024년 5월9일에는 유상증자 참여를 통해 HLB바이오코드(주)의 지분 183,333주를 추가 취득하였습니다.
- 당사는 전기 중 종속회사인 HLB바이오코드㈜(구, ㈜크로엔)의 지분매각으로 연결제외되어 당분기말 현재 연결재무제표 작성대상 종속기업을 보유하고 있지 않습니다. 이에 따라 당사는 연결재무제표와 별도재무제표를 작성하지 않고 개별재무제표만을 작성하였으며, 비교표시되는 제13기(2023년) 재무제표는 연결재무제표입니다.
- 감사보고서상 강조사항과 핵심감사사항
| 구 분 | 강조사항 등 | 핵심감사사항 |
| 제16기 (당기) | 해당사항 없음 | - |
| 제15기 (전기) | 지배력의 상실 | 화장품 사업부 매출의 발생사실 |
| 제14기 (전전기) | 해당사항 없음 | 화장품 사업부 매출의 발생사실 |
나. 대손충당금 설정현황
(1) 당분기말 현재 경과기간별 매출채권 잔액 현황
당분기말 및 전기말 현재 당사의 충당금 설정률표에 기초한 매출채권의 위험정보의 세부내용은 다음과 같습니다. 당사의 과거 신용손실 경험상 다양한 고객부분이 유의적으로 서로 다른 손실양상을 보이지 아니하므로, 과거의 연체일수에 기초한 충당금 설정률표는 서로 다른 고객군별로 구분하지는 않습니다.
| (당분기말) | (단위: 천원) |
| 구 분 | 연체일수 | ||||
|---|---|---|---|---|---|
| 미연체 | ~30일 | 30~90일 | 90일 초과 | 계 | |
| 총장부금액 | 281,763 | 3,300 | - | 15,453 | 300,516 |
| 전체기간 기대신용손실 | - | - | - | (11,506) | (11,506) |
| 순장부금액 | 281,763 | 3,300 | - | 3,947 | 289,010 |
| (전기말) | (단위: 천원) |
| 구 분 | 연체일수 | ||||
|---|---|---|---|---|---|
| 미연체 | ~30일 | 30~90일 | 90일 초과 | 계 | |
| 총장부금액 | 497,832 | 5,597 | 2,401 | 11,506 | 517,336 |
| 전체기간 기대신용손실 | - | - | - | - | - |
| 순장부금액 | 497,832 | 5,597 | 2,401 | 11,506 | 517,336 |
(2) 매출채권 관련 대손충당금(손실충당금) 설정 방침
제품 매출에 대한 평균 신용공여기간은 60일이며, 매출채권에 대해서 이자는 부과되지 아니합니다.
당사는 매출채권에 대해 항상 전체기간 기대신용손실에 해당하는 금액으로 손실충당금을 측정합니다. 매출채권에 대한 기대신용손실은 채무자의 과거 채무불이행 경험 및 차입자 특유의 요인, 일반적인 경제 환경, 보고기간 말에 현재 상황에 대한 평가뿐만 아니라 미래에 상황이 어떻게 변동할 것인지에 대한 평가를 포함한 요소들이 조정된 채무자의 현행 재무상태에 대한 분석을 고려한 충당금 설정률표를 이용하여 산정됩니다. 당사는 과거 경험상 6개월이 경과한 채권은 일반적으로 회수되지 않으므로 6개월이 경과된 모든 채권에 대하여 전액 손실충당금을 인식하고 있습니다. 당분기 중 추정기법이나 중요한 가정의 변경은 없습니다.
다. 재고자산 현황 등
| (단위 : 천원) |
| 사업부문 |
계정과목 |
제16기 | 제15기 | 제14기 |
| 줄기세포 사업 |
제 품 |
511,606 | 384,941 | - |
|
재 공 품 |
208,530 | 209,129 | 73,620 | |
| 계약이행원가 | 1,541,049 | 1,853,184 | 1,670,333 | |
| 소 계 | 2,261,185 | 2,447,254 | 1,743,953 | |
| 화장품 사업부 | 상 품 | 18,922 | 97,959 | 51,997 |
| 제 품 | 127,891 | 166,269 | 375,844 | |
| 소 계 | 146,813 | 264,228 | 427,841 | |
| 바이오파마 사업부 | 상 품 | - | - | 76,799 |
| 소 계 | - | - | 76,799 | |
| 합 계 | 2,407,998 | 2,711,482 | 427,841 | |
|
총자산대비 재고자산 구성비율(%) [재고자산합계÷기말자산총계×100] |
4.80 | 4.74 | 2.77 | |
|
재고자산회전율(회수) [연매출원가÷{(기초재고+기말재고)÷2}] |
0.29 | 0.76 | 5.66 | |
| 중단영업 (주2) |
계약이행원가 | - | - | 531,349 |
| 소 계 | - | - | 531,349 | |
| (주1) | 계약이행원가 포함된 금액입니다. |
| (주2) | 연구용역 사업부는 HLB바이오코드(주)(구.(주)크로엔)의 지분 매각으로 연결에서 제외되었습니다. |
(2) 재고자산의 실사내역
- 연간 1회(1월) 재고 실사
- 회사의 재무상태표일 현재 재고자산과 실사일 현재의 재고자산과의 차이에
대하여 입출고내역 확인절차 수행
- 재고자산 실사시 회사 내부통제시스템에 따라 재고실사를 실시
- 1월 재고실사시 외부감사인 참여, 입회 하에 재고조사 실시
(3) 당분기말 및 전기말 현재 재고자산의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|
| 취득원가 | 평가손실충당금 | 장부금액 | 취득원가 | 평가손실충당금 | 장부금액 | |
| 상품 | 84,686 | (65,764) | 18,922 | 119,293 | (21,334) | 97,959 |
| 제품 | 775,985 | (136,489) | 639,496 | 703,106 | (151,895) | 551,211 |
| 재공품 | 208,530 | - | 208,530 | 209,129 | - | 209,129 |
| 합 계 | 1,069,201 | (202,253) | 866,948 | 1,031,528 | (173,229) | 858,299 |
당분기 중 비용으로 인식한 재고자산 원가에는 재고자산평가손실 29백만원(전분기: 재고자산평가손실환입 10백만원)이 포함되어 있습니다.
라. 공정가치평가 내역
당사는 공정가치로 측정되는 금융상품을 공정가치 측정에 사용된 투입변수에 따라 다음과 같은 공정가치 서열체계로 분류하였습니다.
| (수준1) | 동일한 자산이나 부채에 대한 활성시장에서 공시된 가격(조정되지 않은)을 사용하여 도출되는 공정가치입니다. |
| (수준2) | 수준 1 에 해당되는 공시된 가격을 제외한, 자산이나 부채에 대하여 직접적으로 (가격) 또는 간접적으로(가격으로부터 도출) 관측가능한 투입변수를 사용하여 도출되는 공정가치입니다. |
| (수준3) | 자산이나 부채에 대하여 관측가능한 시장정보에 근거하지 않은 투입변수(관측불가능한 변수)를 사용하는 평가기법으로부터 도출되는 공정가치입니다. |
당분기말 및 전기말 현재 당사의 상기 서열체계에 따른 공정가치 측정치는 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|
| 수준1 | 수준2 | 수준3 | 수준1 | 수준2 | 수준3 | |
| 금융자산: | ||||||
| 당기손익-공정가치측정금융자산 | 608,069 | - | 3,448,377 | 750,238 | - | 3,448,377 |
(5) 당사는 수준 간의 이동을 가져오는 사건이나 상황의 변동이 발생하는 시점에 수준 간의 이동을 인식하고 있으며, 당분기 중 유의적인 이동은 없습니다.
(6) 다음은 수준 2와 수준 3으로 분류되는 주요 금융상품 공정가치측정치에 사용된 가치평가기법과 투입변수에 대한 설명입니다.
| (당기말) | (단위: 천원) |
| 구 분 | 공정가치 | 수준 | 가치평가기법 | 투입변수 |
|---|---|---|---|---|
| 반복적인 공정가치의 측정치 | ||||
| 금융자산 | ||||
| 당기손익-공정가치측정금융자산 | 1,948,377 | 3 | 이항옵션평가모형 | N/A |
| 당기손익-공정가치측정금융자산 | 1,500,000 | 3 | 원가법 | N/A |
| (전기말) | (단위: 천원) |
| 구 분 | 공정가치 | 수준 | 가치평가기법 | 투입변수 |
|---|---|---|---|---|
| 반복적인 공정가치의 측정치 | ||||
| 금융자산 | ||||
| 당기손익-공정가치측정금융자산 | 1,948,377 | 3 | 이항옵션평가모형 | 주가변동성 79.55% 할인율 2.95% |
| 당기손익-공정가치측정금융자산 | 1,500,000 | 3 | 원가법 | N/A |
(7) 금융자산의 재분류 및 양도
당분기 및 전분기 중 목적이나 사용의 변경으로 인하여 재분류된 금융자산은 없으며, 당분기말 및 전기말 현재 양도되었으나 전체가 제거되지 않은 금융자산은 없습니다.
IV. 회계감사인의 감사의견 등
1. 외부감사에 관한 사항
1. 회계감사인의 명칭 및 감사의견(검토의견 포함한다. 이하 이 조에서 같다)을 다음의 표에 따라 기재한다.
회계감사인의 명칭 및 감사의견
| 사업연도 | 구분 | 감사인 | 감사의견 | 의견변형사유 | 계속기업 관련 중요한 불확실성 |
강조사항 | 핵심감사사항 |
|---|---|---|---|---|---|---|---|
| 제16기 (당기) |
감사보고서 | 삼일회계법인 | - | - | - | - | - |
| 연결감사 보고서 |
- | - | - | - | - | - | |
| 제15기 (전기) |
감사보고서 | 안진회계법인 | 적정의견 | 해당없음 | 해당없음 | 지배력의 상실 | 화장품 사업부 매출의 발생사실 |
| 연결감사 보고서 |
- | - | - | - | - | - | |
| 제14기 (전전기) |
감사보고서 | 안진회계법인 | 적정의견 | 해당없음 | 해당없음 | 해당없음 | 화장품 사업부 매출의 발생사실 |
| 연결감사 보고서 |
안진회계법인 | 적정의견 | 해당없음 | 해당없음 | 해당없음 | 화장품 사업부 매출의 발생사실 |
2. 감사용역 체결현황은 다음의 표에 따라 기재한다.
감사용역 체결현황
| (단위 : 백만원, 시간) |
| 사업연도 | 감사인 | 내 용 | 감사계약내역 | 실제수행내역 | ||
|---|---|---|---|---|---|---|
| 보수 | 시간 | 보수 | 시간 | |||
| 제16기(당기) | 삼일회계법인 | - | 169백만원 | 1,340시간 | - | - |
| 제15기(전기) | 안진회계법인 | 별도 및 연결 반기 재무제표 검토 개별 기말 재무제표 감사 |
130백만원 | 1,140시간 | 130백만원 | 1,103시간 |
| 제14기(전전기) | 안진회계법인 | 별도 및 연결 반기 재무제표 검토 별도 및 연결 기말 재무제표 감사 |
125백만원 | 1,140시간 | 125백만원 | 1,134시간 |
3. 회계감사인과의 비감사용역 계약체결 현황은 다음의 표에 따라 기재한다.
| (단위 : 백만원) |
| 사업연도 | 계약체결일 | 용역내용 | 용역수행기간 | 용역보수 | 비고 |
|---|---|---|---|---|---|
| 제16기(당기) | - | - | - | - | - |
| - | - | - | - | - | |
| 제15기(전기) | - | - | - | - | - |
| 제14기(전전기) | - | - | - | - | - |
4. 재무제표 중 이해관계자의 판단에 상당한 영향을 미칠 수 있는 사항에 대해 내부감사기구가 회계감사인과 논의한 결과를 다음의 표에 따라 기재한다.
| 구분 | 일자 | 참석자 | 방식 | 주요 논의 내용 |
|---|---|---|---|---|
| 1 | 2024년 12월 30일 | 회사 : 감사 감사인 : 업무수행이사 |
서면 전달방식 | 감사계약 및 감사계획에 관한 사항 |
| 2 | 2025년 03월 17일 | 회사 : 감사 감사인 : 업무수행이사 |
서면 전달방식 | 감사수행내역 및 감사결과에 관한 사항 |
2. 내부통제에 관한 사항
- 내부통제에 관한 사항은 기업공시서식 작성기준에 따라 분기보고서에 기재하지
않습니다. (사업보고서에 기재 예정)
- 2024년 감사보고서상 내부통제에 이상이 없는것으로 확인되었습니다.
V. 이사회 등 회사의 기관에 관한 사항
1. 이사회에 관한 사항
가. 이사회 구성 개요
당사의 이사회는 주주총회에서 선임된 등기이사로 구성하고 법령 또는 정관에 의한사항, 주주총회로부터 위임 받은 사항, 회사 경영의 기본방침 및 업무집행에 관한 중요사항을 의결하며 이사의 직무집행을 감독하고 있습니다. 이사회에서 선임되는 대표이사는 회사를 대표하고 업무를 총괄하고 있으며, 이사는 대표이사를 보좌하고 이사회에서 정하는 바에 따라 회사의 업무를 분장 집행하며, 대표이사의 유고시에는 정관 및 이사회규정에 정하여진 순서에 따라 그 직무를 대행합니다.
보고서 작성 기준일 현재 당사의 이사회는 5명의 이사(사내이사 3명, 기타비상무이사 1명, 사외이사 1명) 및 감사 1명으로 구성되어 있으며, 각 이사의 주요 이력 및 인적사항은'VIII. 임원 및 직원 등에 관한 사항'을 참조하시기 바랍니다.
나. 사외이사 및 그 변동현황
| (단위 : 명) |
| 이사의 수 | 사외이사 수 | 사외이사 변동현황 | ||
|---|---|---|---|---|
| 선임 | 해임 | 중도퇴임 | ||
| 5 | 1 | 1 | - | - |
주) 2025년 정기주주총회에서 안상만 사외이사가 선임되었습니다.
다. 중요 의결사항
| 회차 |
개최일자 |
의 안 내 용 |
가결 |
사내이사의 성명 | 기타비상무이사의 성명 | 사외이사의 성명 | ||||
| 나종천 (출석률: 100%) |
김원균 (출석률: 100%) |
이승희 (출석률: 100%) |
박용호 (출석률: 75% |
이상균 (출석률: 50%) |
최정호 (출석률: 100%) |
안상만 (출석률: 100%) |
||||
| 찬 반 여 부 | 찬 반 여 부 | |||||||||
| 1 | 2025.01.24 | 1. 제15기 재무제표, 연결재무제표 및 영업보고서 승인의 건 2. 2025년 사업계획 승인의 건 3. ㈜프리모리스테라퓨틱스 합병계약 일부 변경 승인의 건 4. 주주확정 기준일 설정의 건 5. 이사 등과 회사간의 거래승인의 건 ※보고사항 - 내부회계관리제도 운영실태 보고 |
가결 | 찬성 | 찬성 | - | 찬성 | 찬성 | 찬성 | - |
| - | ||||||||||
| 2 | 2025.02.26 | 1. 제15기 정기주주총회 소집 결정의 건 2. 제15기 정기주주총회 회의 목적사항 결정의 건 ※보고사항 - 내부회계관리제도 운영실태 감사의 평가보고 |
가결 | 찬성 | 찬성 | - | 찬성 | 찬성 | 찬성 | - |
| 3 | 2025.03.26 | 1. 이사회 의장 선임의 건 |
가결 | 찬성 | 찬성 | 찬성 | 불참 | 불참 | 찬성 | 찬성 |
| 4 | 2025.03.27 | 1. ㈜프리모리스테라퓨틱스 합병 일정 변경 승인의 건 | 가결 | 찬성 | 찬성 | 찬성 | 찬성 | 불참 | 찬성 | 찬성 |
*주1) 이승희 사내이사, 안상만 사외이사 신규선임(2025.03.26)
박용호, 이상균 기타비상무이사 임기 만료(2025.03.30)
라. 이사회내의 위원회 구성현황과 그 활동내역
- 해당사항 없음 -
마. 이사의 독립성
회사 경영의 중요한 의사 결정과 업무 집행은 이사회의 심의 및 결정을 통하여 이루어지고 있습니다. 또한 당사는 대주주 등의 독단적인 경영과 이로 인한 소액 주주의 이익 침해가 발생하지 않도록 이사회 운영규정을 제정하여 성실히 준수하고 있습니다.
| 구 분 | 성 명 | 담당분야 | 추천인 | 회사와의 거래 | 최대주주 또는 주요주주와의 이해관계 |
임기 | 연임여부 및 회수 |
|---|---|---|---|---|---|---|---|
| 대표이사 | 나종천 | 경영총괄 | 이사회 | 없음 | 없음 | 3년 | 연임 (1회) |
| 사내이사 | 김원균 | 생산총괄 | 이사회 | 없음 | 없음 | 3년 | - |
| 이승희 | 연구총괄 | 이사회 | 없음 | 없음 | 3년 | - | |
| 기타비상무 이사 |
최정호 | - | 이사회 | 없음 | 없음 | 3년 | 연임 (2회) |
| 사외이사 | 안상만 | - | 이사회 | 없음 | 없음 | 3년 | - |
*주1) 최정호 기타비상무이사 2023.03.23 재선임
*주2) 나종천 대표이사 2024.03.21 재선임
바. 사외이사 지원조직 현황
당사는 보고서 작성 기준일 현재 사외이사의 직무수행을 보조하는 별도의 지원조직을 두고 있지 않으며, 이사회 개최 및 주요 경영사항에 대하여 경영지원팀에서 관련 정보를 사전에 제공하고 있습니다.
사. 사외이사 교육 미실시 내역
| 사외이사 교육 실시여부 | 사외이사 교육 미실시 사유 |
|---|---|
| 미실시 | 당사 경영 감독과 자문를 위해 필요한 관련 분야 전문성을 이미 보유하고 있습니다. 또한 필요시 추가 교육을 실시할 예정입니다. |
2. 감사제도에 관한 사항
가. 감사위원회의 설치 여부
- 해당사항 없음 -
나. 감사의 인적사항
| 성 명 | 주요 경력 | 최대주주등과의 이해관계 |
결격요건 여부 |
|---|---|---|---|
| 김재홍 | 한국동물약품기술연구원 원장 (재)한국동물의료정책연구원 원장 행정안전부 정책자문위원회 위원 식약처 중앙약사심사위원회 위원 |
해당사항 없음 |
해당사항 없음 |
다. 감사의 독립성
감사는 회계와 업무를 감사하며 이사회 및 타 부서로부터 독립된 위치에서 업무를
수행하고 있으며, 감사의 감사업무에 필요한 경영정보 접근을 위하여 당사의 정관에
다음과 같은 규정을 두고 있습니다.
|
- 정관 제50조(감사의 직무) |
라. 감사의 주요활동내역
| 회차 | 개최일자 | 의 안 내 용 | 가결 여부 |
감사의 참석여부 |
|---|---|---|---|---|
| 1 | 2025.01.24 | 1. 제15기 재무제표, 연결재무제표 및 영업보고서 승인의 건 2. 2025년 사업계획 승인의 건 3. ㈜프리모리스테라퓨틱스 합병계약 일부 변경 승인의 건 4. 주주확정 기준일 설정의 건 5. 이사 등과 회사간의 거래승인의 건 ※보고사항 - 내부회계관리제도 운영실태 보고 |
가결 | - |
| 2 | 2025.02.26 | 1. 제15기 정기주주총회 소집 결정의 건 2. 제15기 정기주주총회 회의 목적사항 결정의 건 ※보고사항 - 내부회계관리제도 운영실태 감사의 평가보고 |
가결 | 참석 |
| 3 | 2025.03.26 | 1. 이사회 의장 선임의 건 |
가결 | 참석 |
| 4 | 2025.03.27 | 1. ㈜프리모리스테라퓨틱스 합병 일정 변경 승인의 건 | 가결 | - |
*주) 당사 제14기 정기주주총회(2024년 3월 21일 개최)에서 김재홍 감사가 신규선임되었습니다.
마. 감사 교육 미실시 내역
| 감사 교육 실시여부 | 감사 교육 미실시 사유 |
|---|---|
| 미실시 | 당사 업무 감사를 위해 필요한 관련 분야 전문성을 이미 보유하고 있습니다. 또한 필요시 추가 교육을 실시할예정입니다. |
바. 감사 지원조직 현황
당사는 보고서 작성 기준일 현재 감사의 직무수행을 보조하기 위한 별도의 지원조직이 없습니다.
사. 준법지원인 등에 관한 사항
- 해당사항 없음 -
3. 주주총회 등에 관한 사항
가. 투표제도 현황
| (기준일 : | 2025년 03월 31일 | ) |
| 투표제도 종류 | 집중투표제 | 서면투표제 | 전자투표제 |
|---|---|---|---|
| 도입여부 | 배제 | 미도입 | 도입 |
| 실시여부 | - | - | - |
나. 의결권 현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 주식수 | 비고 |
|---|---|---|---|
| 발행주식총수(A) | 보통주 | 56,054,149 | - |
| 우선주 | - | - | |
| 의결권없는 주식수(B) | 보통주 | - | - |
| 우선주 | - | - | |
| 정관에 의하여 의결권 행사가 배제된 주식수(C) | 보통주 | - | - |
| 우선주 | - | - | |
| 기타 법률에 의하여 의결권 행사가 제한된 주식수(D) |
보통주 | - | - |
| 우선주 | - | - | |
| 의결권이 부활된 주식수(E) | 보통주 | - | - |
| 우선주 | - | - | |
| 의결권을 행사할 수 있는 주식수 (F = A - B - C - D + E) |
보통주 | 56,054,149 | - |
| 우선주 | - | - |
다. 소수주주권 행사여부
| 구분 | 행사자 | 안건 | 목적사항 포함여부 |
거부사유 | 진행경과 |
|---|---|---|---|---|---|
| 제14기 정기주주총회 |
소수주주 | 1) 주주총회 목적사항 제안 - 의안 정관 변경의 건(집중투표제의 도입) |
포함 | - | 2024년 1월 26일 제안 접수 2024년 3월 21일 주주총회에서 해당 안건 부결됨 |
| 2) 주주총회 의결권행사 절차 제안 - 전자투표 시행의 건 |
미포함 | 상법 제363조의2 1항, 주주총회 목적사항에 대한 제안이 아닌 주주제안 |
- |
라. 경영권 경쟁
- 당사는 공시대상 기간 중 경영권 경쟁의 사실이 없습니다.
마. 주식사무
| 구분 | 내용 |
|---|---|
| 정관상 신주인수권의 내용 |
① 당회사의 주주는 신주발행에 있어 그가 소유한 주식의 수에 비례하여 ② 회사는 제1항의 규정에도 불구하고 다음 각 호의 어느 하나에 해당하는 1. 발행주식총수의 100분의 50을 초과하지 않는 범위 내에서 「자본 2.「상법」 제542조의3에 따른 주식매수선택권의 행사로 인하여 3. 발행하는 주식총수의 100분의 20 범위 내에서 우리사주조합원에게 4.「근로복지기본법」 제39조의 규정에 의한 우리사주매수선택권의 5. 발행주식총수의 100분의 30을 초과하지 않는 범위 내에서 긴급한 6. 발행주식총수의 100분의 30을 초과하지 않는 범위 내에서 사업상 7. 주권을 코스닥시장에 상장하기 위하여 신주를 모집하거나 인수인에게 ③ 제2항 각 호 중 어느 하나의 규정에 의해 신주를 발행할 경우 발행할 ④ 신주인수권의 포기 또는 상실에 따른 주식과 신주배정에서 발생한 |
| 결산일 | 매년 12월 31일 |
| 정기주주총회 | 매 사업년도 종료 후 3개월 이내 |
| 명의개서 대리인 |
① 한국예탁결제원 ② 주소 : 부산광역시 남구 문현금융로 40 부산국제금융센터 (BIFC) ③ 전화번호 : 1577-6600 |
| 주주의 특전 | 해당사항 없음 |
| 공고게재 | 인터넷 홈페이지 (http://www.kangstem.com) 매일경제신문(전산장애 또는 그 밖의 부득이한 사유로 회사의 인터넷 홈페이지에 공고를 할 수 없는 경우) |
바. 주주총회 의사록 요약
| 주총정보 | 안 건 | 결의내용 | 주요 논의내용 |
|---|---|---|---|
| 제12기 정기주총 (2022.03.24) |
제 1호 의안 : 제12기(2021.01.01.~2021.12.31.) 재무제표 및 연결재무제표 승인의 건 |
가결 | - |
| 제 2호 의안 : 이사 선임의 건 | 가결 | ||
| 제 3호 의안 : 이사 보수한도 승인의 건 | 가결 | ||
| 제 4호 의안 : 감사 보수한도 승인의 건 | 가결 | ||
| 제13기 정기주총 (2023.03.23) |
제 1호 의안 : 제13기(2022.01.01.~2022.12.31.) 재무제표 및 연결재무제표 승인의 건 |
가결 | - |
| 제 2호 의안 : 이사 선임의 건 | 가결 | ||
| 제 3호 의안 : 이사 보수한도 승인의 건 | 가결 | ||
| 제 4호 의안 : 감사 보수한도 승인의 건 | 가결 | ||
| 제14기 정기주총 (2024.03.21) |
제 1호 의안 : 제14기(2023.01.01.~2023.12.31.) 재무제표 및 연결재무제표 승인의 건 |
가결 | [주주제안 안건 설명내용] 집중투표제를 적용하지 않는다고 규정하는 정관은 소수주주들의 이해관계를 배제한다는 점에서 정관 변경을 제안함. |
| 제 2호 의안 : 이사 선임의 건 | 가결 | ||
| 제 3호 의안 : 감사 선임의 건 | 가결 | ||
| 제 4호 의안 : 이사 보수한도 승인의 건 | 가결 | ||
| 제 5호 의안 : 감사 보수한도 승인의 건 | 가결 | ||
| 제 6호 의안 : 정관 일부 변경의 건(주주제안) | 부결 | ||
| 제15기 정기주총 (2025.03.26) |
제 1호 의안 : 제15기(2024.01.01.~2024.12.31.) 재무제표 승인의 건 |
가결 | - |
| 제 2호 의안 : 이사 선임의 건 | 가결 | ||
| 제 3호 의안 : 이사 보수한도 승인의 건 | 가결 | ||
| 제 4호 의안 : 감사 보수한도 승인의 건 | 가결 |
VI. 주주에 관한 사항
1. 최대주주 및 특수관계인의 주식소유 현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 주, %) |
| 성 명 | 관 계 | 주식의 종류 |
소유주식수 및 지분율 | 비고 | |||
|---|---|---|---|---|---|---|---|
| 기 초 | 기 말 | ||||||
| 주식수 | 지분율 | 주식수 | 지분율 | ||||
| 주식회사 세종 | 최대주주 | 보통주 | 8,000,000 | 14.27 | 8,000,000 | 14.27 | - |
| 계 | 보통주 | 8,000,000 | 14.27 | 8,000,000 | 14.27 | - | |
| - | - | - | - | - | - | ||
2. 최대주주의 주요경력 및 개요
가. 최대주주(법인 또는 단체)의 기본정보
| 명 칭 | 출자자수 (명) |
대표이사 (대표조합원) |
업무집행자 (업무집행조합원) |
최대주주 (최대출자자) |
|||
|---|---|---|---|---|---|---|---|
| 성명 | 지분(%) | 성명 | 지분(%) | 성명 | 지분(%) | ||
| 주식회사 세종 | 88 | 김형진 | - | - | - | 김형진외 특수관계자 | 85.85 |
| - | - | - | - | - | - | ||
나. 최대주주(법인 또는 단체)의 최근 결산기 재무현황
| (단위 : 백만원) |
| 구 분 | |
|---|---|
| 법인 또는 단체의 명칭 | ㈜세종 |
| 자산총계 | 550,227 |
| 부채총계 | 256,717 |
| 자본총계 | 293,509 |
| 매출액 | 374,853 |
| 영업이익 | -17,934 |
| 당기순이익 | -35,195 |
* 상기 재무현황은 2024년 말 기준 연결재무제표 기준으로 작성하였습니다.
다. 사업현황 등 회사 경영 안정성에 영향을 미칠 수 있는 주요 내용
(1) 사업현황
주식회사 세종은 기간통신사업자로서 전국 규모의 광통신망을 기반으로 전용회선 임대, 인터넷 전용회선 및 IDC(인터넷데이터센터) 등의 통신서비스 사업을 영위하다 2015년 4월 1일자로 세종텔레콤(주)(구 온세텔레콤)에 통신사업부분을 영업양도하였으며, 서울시 강동구 소재 세종빌딩을 기반으로 한 부동산 임대사업을 영위하고 있습니다.
(2) 최대주주의 변동을 초래할수 있는 특정거래
- 해당사항 없습니다.
3. 최대주주의 최대주주(법인 또는 단체)의 개요
- 해당사항 없습니다.
4. 최대주주 변동내역
최대주주 변동내역
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 주, %) |
| 변동일 | 최대주주명 | 소유주식수 | 지분율 | 변동원인 | 비 고 |
|---|---|---|---|---|---|
| 2023년 11월 07일 | 주식회사 세종 | 6,800,000 | 12.16 | 유상증자 신주 취득(주주배정 유상증자) 및 장내매수 | - |
*주) 2023년 11월 07일 기준으로 당사의 최대주주가 '강경선'에서 '주식회사 세종'으로 변경되었습니다. (상기 소유주식수 및 지분율은 변동일 당시 기준으로 작성하였으며, 2024.12.31 기준 소유주식수는 8,000,000주, 지분율 14.27% 입니다.)
※ 상세한 내용은 금융감독원 전자공시시스템에 공시된 '최대주주변경'(2023년 11월 8일 공시) 및 지분공시를 참조하시기 바랍니다.
5. 주식의 분포현황
가. 주식 소유현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 주) |
| 구분 | 주주명 | 소유주식수 | 지분율(%) | 비고 |
|---|---|---|---|---|
| 5% 이상 주주 | 주식회사 세종 | 8,000,000 | 14.27 | - |
| - | - | - | - | |
| 우리사주조합 | 814 | 0.00 | ||
나. 소액주주 현황
소액주주현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 주) |
| 구 분 | 주주 | 소유주식 | 비 고 | ||||
|---|---|---|---|---|---|---|---|
| 소액 주주수 |
전체 주주수 |
비율 (%) |
소액 주식수 |
총발행 주식수 |
비율 (%) |
||
| 소액주주 | 18,315 | 18,319 | 99.98 | 44,145,222 | 56,054,149 | 78.75 | - |
6. 주가 및 주식 거래실적
| (기준 : 종가, 단위 : 원, 주) |
| 종 류 | '25년 3월 | '25년 2월 | '25년 1월 | '24년 12월 | '24년 11월 | '24년 10월 | ||
|---|---|---|---|---|---|---|---|---|
| 보통주 | 주가 | 최 고 | 2,410 | 2,210 | 2,260 | 2,390 | 2,685 | 2,150 |
| 최 저 | 2,010 | 1,950 | 2,000 | 1,886 | 1,888 | 1,676 | ||
| 평 균 | 2,186 | 2,079 | 2,097 | 2,087 | 2,266 | 1,994 | ||
| 거래량 | 최고(일) | 1,743,725 | 630,696 | 899,151 | 2,236,777 | 22,339,562 | 1,285,343 | |
| 최저(일) | 132,696 | 119,230 | 175,105 | 293,780 | 291,477 | 101,946 | ||
| 월 간 | 9,636,804 | 6,225,449 | 6,258,702 | 12,717,192 | 63,982,706 | 8,198,975 | ||
VII. 임원 및 직원 등에 관한 사항
1. 임원 및 직원 등의 현황
가. 임원 현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 주) |
| 성명 | 성별 | 출생년월 | 직위 | 등기임원 여부 |
상근 여부 |
담당 업무 |
주요경력 | 소유주식수 | 최대주주와의 관계 |
재직기간 | 임기 만료일 |
|
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 의결권 있는 주식 |
의결권 없는 주식 |
|||||||||||
| 나종천 | 남 | 1963년 09월 | 대표이사 | 사내이사 | 상근 | 경영총괄 | 서울대학교 약학 중앙대학교 대학원 약품물리학 박사 건일제약 메디칼본부 본부장 한국쿄와기린 대표이사 사장 강스템바이오텍 대표이사 |
111,729 | - | - | 4년 5개월 | 2027년 03월 24일 |
| 김원균 | 남 | 1967년 02월 | 전무/ 줄기세포GMP센터장 |
사내이사 | 상근 | 생산총괄 | 연세대학교 생물학 한미약품 품질 총괄팀장 코오롱 해외사업개발 부장 플럼라인생명과학 연구개발 이사 강스템바이오텍 줄기세포GMP센터장 |
6,272 | - | - | 8년 1개월 | 2027년 03월 20일 |
| 이승희 | 여 | 1981년 11월 | 상무 /연구소장 |
사내이사 | 상근 | 연구개발 | 서울대학교 수의학 박사 강스템바이오텍 연구부소장/연구기획팀장강스템바이오텍 연구소장 |
19,337 | - | - | 13년 3개월 | 2028년 03월 26일 |
| 최정호 | 남 | 1961년 06월 | 기타비상무이사 | 기타비상무이사 | 비상근 | - | 숭실대 국제경제학과 로젠(주) 대표이사 유진그룹 기초소재 대표이사 |
195,283 | - | - | 11년 1개월 | 2026년 03월 24일 |
| 안상만 | 남 | 1963년 12월 | 사외이사 | 사외이사 | 비상근 | - | 서울대학교 수의과대학 CJ제일제당 제약사업부문 마케팅실장 CJ㈜ 일본사업 운영총괄 및 CJ Japan 대표이사 |
- | - | - | 1개월 | 2028년 03월 26일 |
| 김재홍 | 남 | 1955년 01월 | 감사 | 감사 | 비상근 | 감사 | 서울대 수의학 박사 식약처 중앙약사심의위원회 위원 행정안전부 정책자문위원회 위원 (재)한국동물의료정책연구원 원장 |
- | - | - | 1년 1개월 | 2027년 03월 20일 |
| 이동열 | 남 | 1981년 10월 | 부사장 /H&B사업부문 대표 |
미등기 | 상근 | 기획조정 | Shanghai University of Finance and Economics 강스템바이오텍 전략기획팀장 강스템바이오텍 경영지원본부장 강스템바이오텍 H&B사업부문 대표 |
86,000 | - | - | 14년 5개월 | - |
| 배요한 | 남 | 1968년 12월 | 전무 /임상개발본부장 |
미등기 | 상근 | 임상개발 | 경희대학교 대학원 약물학 BMS제약 APAC RA Associate Director 한국알콘제약 APAC RA Regional RA Director 한국베링거인겔하임 Head of Regulatory Affairs 강스템바이오텍 임상개발본부장 |
36,491 | - | - | 5년 1개월 | - |
| 이계종 | 남 | 1972년 10월 | 전무 /경영지원실장 |
미등기 | 상근 | 경영지원 | 중앙대학교 경영학 Mando America Co. 관리과장 보광그룹 휘닉스소재 재무팀장 (주)포스코ESM 감사 강스템바이오텍 경영지원실장 |
24,116 | - | - | 4년 5개월 | - |
| 어해관 | 남 | 1974년 12월 | 상무 /사업개발본부장 |
미등기 | 상근 | 사업개발 | 중앙대 생명자원공학 차의과대학교 임상약학 석사 ㈜CMG제약 사업개발실장 ㈜알보젠코리아 사업개발 상무이사 |
6,184 | - | - | 2년 1개월 | - |
| 이미혜 | 여 | 1983년 07월 | 상무 /줄기세포GMP부센터장 |
미등기 | 상근 | 생산총괄 | 성균관대학교 약학대학 제약산업학 강스템바이오텍 줄기세포GMP 부센터장 강스템바이오텍 CDMO사업부장 |
35,000 | - | - | 14년 1개월 | - |
| 유연실 | 여 | 1975년 03월 | 이사/ 임상개발팀장 |
미등기 | 상근 | 임상개발 | 서울대학교 약리학 석사 서울대학교 해부학 박사 이화의대 분자의과학교실 연구교수 강스템바이오텍 연구부소장/연구기획팀장 강스템바이오텍 사업개발팀장 |
1,494 | - | - | 7년 11개월 | - |
*주) 상기 임원의 주식소유 현황은 2025년 3월 31일자 기준으로 보고서 제출일 현재 주식 소유현황과 차이가 있을 수 있습니다.
*주) 2025년 3월 30일 이상균, 박용호 기타비상무이사가 임기만료로 퇴임하였습니다.
나. 직원 등 현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원) |
| 직원 | 소속 외 근로자 |
비고 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 사업부문 | 성별 | 직 원 수 | 평 균 근속연수 |
연간급여 총 액 |
1인평균 급여액 |
남 | 여 | 계 | |||||
| 기간의 정함이 없는 근로자 |
기간제 근로자 |
합 계 | |||||||||||
| 전체 | (단시간 근로자) |
전체 | (단시간 근로자) |
||||||||||
| 사무직 | 남 | 9 | - | - | - | 9 | 4.6 | - | - | - | 2 | 2 | - |
| 사무직 | 여 | 15 | - | - | - | 15 | 4.6 | - | - | - | |||
| 연구직 | 남 | 12 | - | - | - | 12 | 3.6 | - | - | - | |||
| 연구직 | 여 | 13 | - | 1 | - | 14 | 4.0 | - | - | - | |||
| 생산직 | 남 | 16 | - | - | - | 16 | 5.0 | - | - | - | |||
| 생산직 | 여 | 23 | - | - | - | 23 | 6.4 | - | - | - | |||
| 성별합계 | 남 | 37 | - | - | - | 37 | 4.5 | 639 | 17 | - | |||
| 성별합계 | 여 | 51 | - | 1 | - | 52 | 5.3 | 703 | 14 | - | |||
| 합 계 | 88 | - | 1 | - | 89 | 4.9 | 1,342 | 15 | - | ||||
| *주1) | 직원수는 2025년 3월 31일 말 재직자기준(등기임원 불포함)이며, 근속연수 단위는 년 입니다. |
| *주2) | 1인 평균 급여액 = 급여 총액 / 직원수 |
| *주3) | 상기 급여에는 주식매수선택권 행사이익이 포함되어 있습니다. |
| *주4) | 직원 현황 표는 미등기임원을 포함하여 작성합니다. |
다. 직원의 육아휴직 등 현황
1) 육아지원제도 사용 현황
| (기준일 : 2025년 3월 31일) | (단위 : 명, %) |
| 구분 | 당기 (16기 1분기) |
전기 (15기) |
전전기 (14기) |
|---|---|---|---|
| 육아휴직 사용자수(남) | 0 | 1 | 2 |
| 육아휴직 사용자수(여) | 1 | 3 | 3 |
| 육아휴직 사용자수(전체) | 1 | 4 | 5 |
| 육아휴직 사용률(남) | - | 100% | 100% |
| 육아휴직 사용률(여) | 100% | 100% | 100% |
| 육아휴직 사용률(전체) | 100% | 100% | 100% |
| 육아휴직 복귀 후 12개월 이상 근속자(남) |
0 | 0 | 1 |
| 육아휴직 복귀 후 12개월 이상 근속자(여) |
0 | 0 | 0 |
| 육아휴직 복귀 후 12개월 이상 근속자(전체) |
0 | 0 | 1 |
| 육아기 단축근무제 사용자 수 | 0 | 2 | 2 |
| 배우자 출산휴가 사용자 수 | 1 | 0 | 1 |
※ 육아휴직 사용률 계산법 산식에 대한 설명
(당해 출산 이후 1년 이내에 육아휴직을 사용한 근로자
/당해 출생일로부터 1년 이내의 자녀가 있는 근로자)
2) 유연근무제도 사용 현황
| (기준일 : 2025년 03월 31일) | (단위 : 명) |
| 구분 | 당기 (16기 1분기) |
전기 (15기) |
전전기 (14기) |
|---|---|---|---|
| 유연근무제 활용 여부 | 활용 | 활용 | 활용 |
| 시차출퇴근제 사용자 수 | 78 | 80 | 93 |
| 선택근무제 사용자 수 | 0 | 0 | 0 |
| 원격근무제(재택근무 포함) 사용자 수 |
0 | 0 | 0 |
라. 미등기임원 보수 현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원) |
| 구 분 | 인원수 | 연간급여 총액 | 1인평균 급여액 | 비고 |
|---|---|---|---|---|
| 미등기임원 | 6 | 242 | 40 | - |
*주1) 미등기임원의 경우 2025년 3월 31일 재직 임원 기준으로 작성함.
2. 임원의 보수 등
| <이사ㆍ감사 전체의 보수현황> |
가. 주주총회 승인금
| (단위 : 백만원) |
| 구 분 | 인원수 | 주주총회 승인금액 | 비고 |
|---|---|---|---|
| 이 사 | 5명 | 2,000 | - |
| 감 사 | 1명 | 200 | - |
나. 보수지급금액
1) 이사ㆍ감사 전체
| (단위 : 백만원) |
| 인원수 | 보수총액 | 1인당 평균보수액 | 비고 |
|---|---|---|---|
| 6 | 171 | 29 | - |
*주1) 1인당 평균보수액은 보수총액을 실지급된 인원수로 나누어 산정하였습니다.
*주2) 상기 급여에는 주식매수선택권 행사이익이 포함되어 있습니다.
*주3) 보고기간 내 퇴임 임원 포함
2) 유형별
| (단위 : 백만원) |
| 구 분 | 인원수 | 보수총액 | 1인당 평균보수액 |
비고 |
|---|---|---|---|---|
| 등기이사 (사외이사, 감사위원회 위원 제외) |
4 | 165 | 41 | - |
| 사외이사 (감사위원회 위원 제외) |
1 | - | - | - |
| 감사위원회 위원 | - | - | - | - |
| 감사 | 1 | 6 | 6 | - |
*주1) 1인당 평균보수액은 보수총액을 실지급된 인원수로 나누어 산정하였습니다.
*주2) 상기 급여에는 주식매수선택권 행사이익이 포함되어 있습니다.
*주3) 보고기간 내 퇴임 임원 포함
3) 보수지급근거
| 구 분 | 지급근거 | 보수체계 및 보수결정시 평가항목 등 |
| 등기이사 | 정관 제39조(이사의 보수와 퇴직금) ① 이사의 보수는 주주총회의 결의로 이를 정한다. ② 이사의 퇴직금의 지급은 주주총회결의를 거친 임원퇴직금지급규정에 의한다. |
당사 "임원 및 임원보수규정"에 따라 주주총회에서 승인 받은 보수총액 범위 내에서 직급과 업무를 고려하여 보수를 결정하고 있습니다. |
| 감사 | 정관 제51조(감사의 보수와 퇴직금) ① 감사의 보수와 퇴직금에 관하여는 제39조의 규정을 준용한다. ② 감사의 보수를 결정하기 위한 의안은 이사의 보수결정을 위한 의안과 구분하여 상정·의결하여야 한다. |
다. 보수지급금액 5억원 이상인 이사·감사의 개인별 보수현황
| <보수지급금액 5억원 이상인 이사ㆍ감사의 개인별 보수현황> |
1) 개인별 보수지급금액
| (단위 : 원) |
| 이름 | 직위 | 보수총액 | 보수총액에 포함되지 않는 보수 |
|---|---|---|---|
| - | - | - | - |
- 당사는 이사 및 감사의 개인별 보수지급액이 5억원 미만이므로 본 항목의 기재를 생략합니다.
2) 산정기준 및 방법
- 해당사항 없음.
라. 보수지급금액 5억원 이상 중 상위 5명의 개인별 보수현황
| <보수지급금액 5억원 이상 중 상위 5명의 개인별 보수현황> |
1) 개인별 보수지급금액
| (단위 : 원) |
| 이름 | 직위 | 보수총액 | 보수총액에 포함되지 않는 보수 |
|---|---|---|---|
| - | - | - | - |
- 당사는 개인별 보수 지급액이 5억원 미만이므로 본 항목의 기재를생략합니다.
2) 산정기준 및 방법
- 해당사항 없음.
<주식매수선택권의 부여 및 행사현황>
<표1>
| (단위 : 원) |
| 구 분 | 부여받은 인원수 |
주식매수선택권의 공정가치 총액 | 비고 |
|---|---|---|---|
| 등기이사 (사외이사, 감사위원회 위원 제외) |
3 | - | - |
| 사외이사 (감사위원회 위원 제외) |
- | - | - |
| 감사위원회 위원 또는 감사 | - | - | - |
| 업무집행지시자 등 | 3 | - | - |
| 계 | 6 | - | - |
| *주1) | 주식매수선택권의 공정가치 총액은 당해 사업연도 손익계산서에 주식매수선택권과 관련하여 비용으로 계상된 금액으로 산출하고 있습니다. |
| *주2) | 당사는 상기 주식선택권의 부여로 인하여 당기 중 인식한 총보상원가는 0원(누적보상원가: 1,622백만원)이며, 잔여보상원가는 0원입니다. 주식선택권의 보상원가는 이항모형을 이용한 공정가치접근법을 적용하여 산정하였습니다. |
<표2>
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 원, 주) |
| 부여 받은자 |
관 계 | 부여일 | 부여방법 | 주식의 종류 |
최초 부여 수량 |
당기변동수량 | 총변동수량 | 기말 미행사수량 |
행사기간 | 행사 가격 |
의무 보유 여부 |
의무 보유 기간 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 행사 | 취소 | 행사 | 취소 | |||||||||||
| 김원균 | 등기임원 | 2018년 03월 23일 | 신주교부 | 보통주 | 10,000 | - | 10,000 | - | 10,000 | - | 2020.03.23 ~2025.03.22 |
12,382 | X | - |
| 나종천 | 등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 100,000 | - | - | - | - | 100,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 김원균 | 등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 60,000 | - | - | - | - | 60,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 이승희 | 등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 50,000 | - | - | - | - | 50,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 배요한 | 미등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 70,000 | - | - | - | - | 70,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 이계종 | 미등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 50,000 | - | - | - | - | 50,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 유연실 | 미등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 25,000 | - | - | - | - | 25,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| OOO 외 14명 | 직원 | 2021년 03월 25일 | 신주교부 | 보통주 | 204,000 | - | - | - | 55,000 | 149,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 노경환 | 계열회사 임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 70,000 | - | - | - | - | 70,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
| 서명관 | - | 2021년 03월 25일 | 신주교부 | 보통주 | 60,000 | - | - | - | - | 60,000 | 2023.03.25 ~2028.03.24 |
6,123 | X | - |
※ 공시서류작성기준일(2025년 3월 31일) 현재 종가 : 2,340 원
VIII. 계열회사 등에 관한 사항
가. 계열회사 현황(요약)
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 사) |
| 기업집단의 명칭 | 계열회사의 수 | ||
|---|---|---|---|
| 상장 | 비상장 | 계 | |
| 강스템바이오텍 | 1 | 6 | 7 |
| ※상세 현황은 '상세표-2. 계열회사 현황(상세)' 참조 |
나. 계통도
| (기준일 : | 2025년 3월 31일 | ) | (단위 : %) |
| 계열회사 | 출자회사 (주1) | |
|---|---|---|
| (주)강스템바이오텍 | (주)프리모리스 인터내셔널 |
|
| (주)디앤케이코퍼레이션 | 50.00 | - |
| (주)블루진 | 20.00 | 13.33 |
| (주)프리모리스테라퓨틱스 | 64.76 | - |
| HLB바이오코드(주)(주2) | 22.47 (주1) | - |
| (주1) | 지분율은 발행주식 총수대비 기준입니다. |
| (주2) | 전기 중 사명을 (주)크로엔에서 HLB바이오코드(주)로 변경하였으며, 보유 주식 1,183,676주(64.50%) 중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류 하였습니다. 또한 매각 이후 유상증자를 통해 HLB바이오코드(주)의 지분(183,333주)를 추가 취득하였습니다. 이후 HLB바이오코드㈜의 유상증자에 참여하지 않아 지분율이 감소하였습니다. |
다. 타법인출자 현황(요약)
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원) |
| 출자 목적 |
출자회사수 | 총 출자금액 | |||||
|---|---|---|---|---|---|---|---|
| 상장 | 비상장 | 계 | 기초 장부 가액 |
증가(감소) | 기말 장부 가액 |
||
| 취득 (처분) |
평가 손익 |
||||||
| 경영참여 | - | 1 | 1 | - | - | - | - |
| 일반투자 | - | 3 | 3 | 5,522 | - | - | 5,522 |
| 단순투자 | - | 2 | 2 | 500 | - | - | 500 |
| 계 | - | 6 | 6 | 6,022 | - | - | 6,022 |
| ※상세 현황은 '상세표-3. 타법인출자 현황(상세)' 참조 |
IX. 대주주 등과의 거래내용
1. 대주주등에 대한 신용공여 등
- 해당사항 없음 -
2. 대주주와의 자산양수도 등
- 해당사항 없음 -
3. 대주주와의 영업거래
- 해당사항 없음 -
4. 대주주 이외의 이해관계자와의 거래
(1) 당분기말 및 전기말 현재 당사의 특수관계자 현황은 다음과 같습니다.
| 관 계 | 당분기말 | 전기말 |
|---|---|---|
| 공동기업 및 관계기업 | HLB바이오코드(주)(주2) | HLB바이오코드(주)(주2) |
| (주)디앤케이코퍼레이션 | (주)디앤케이코퍼레이션 | |
| (주)블루진 | (주)블루진 | |
| (주)프리모리스테라퓨틱스 | (주)프리모리스테라퓨틱스 | |
| 기타 특수관계자 | (주)프리모리스인터내셔널(주1) | (주)프리모리스인터내셔널(주1) |
| 마루테라퓨틱스(주1) | 마루테라퓨틱스(주1) | |
| 주요경영진 | 주요경영진 |
| (주1) | 당사에 대한 지배력을 보유하고 있는 개인 등이 지배력을 보유하고 있는 회사입니다. |
| (주2) | 전기 중 사명을 (주)크로엔에서 HLB바이오코드(주)로 변경하였으며, 보유 주식 1,183,676주(64.50%)중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류하였습니다. |
(2) 당분기 및 전분기 중 특수관계자와의 주요 거래 내역은 다음과 같습니다.
| (단위: 천원) |
| 특수관계자 명칭 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 영업수익 등 | 영업비용 등 | 영업수익 등 | 영업비용 등 | |
| HLB바이오코드㈜ | 2,268 | - | - | - |
| (주)프리모리스인터내셔널(주1) | 364,806 | 29,053 | 510,022 | 37,906 |
| (주)프리모리스테라퓨틱스 | 17,280 | 78,117 | 11,826 | 13 |
| 합 계 | 384,354 | 107,170 | 521,848 | 37,919 |
| (주1) | 당사는 특수관계자인 (주)프리모리스인터내셔널과 연간 상품공급계약을 맺고 있습니다. |
(3) 당분기말 및 전기말 현재 특수관계자간 주요 채권ㆍ채무잔액은 다음과 같습니다.
| (단위: 천원) |
| 특수관계자 명칭 | 당분기말 | 전기말 | ||||||
|---|---|---|---|---|---|---|---|---|
| 채권 | 채무 | 채권 | 채무 | |||||
| 매출채권 등 (주1) |
계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | 매출채권 등 (주1) |
계약자산 및 계약이행원가 |
미지급금 등 | 계약부채 | |
| HLB바이오코드(주) | 2,268 | - | - | - | - | - | - | - |
| (주)프리모리스인터내셔널 | 172,992 | - | 10,453 | - | 403,923 | - | 14,160 | - |
| (주)프리모리스테라퓨틱스 | 67,555 | - | - | 2,000 | 49,375 | - | - | 2,000 |
| 합 계 | 242,815 | - | 10,453 | 2,000 | 453,298 | - | 14,160 | 2,000 |
| (주1) | 당분기말 채권은 대손충당금 차감전 금액이 기재되어 있습니다. 상기 특수관계자 채권에 설정되어 있는 대손충당금은 18백만원입니다. |
(4) 당분기 중 특수관계에 대한 지분거래내역은 없으며, 전분기 중 특수관계자에 대한 지분거래내역은 다음과 같습니다.
| (전분기) | (단위: 천원) |
| 특수관계자 명칭 | 구 분 | 금액 |
|---|---|---|
| HLB바이오코드㈜ | 보통주 유상증자(주1) | 989,998 |
| (주)프리모리스테라퓨틱스 | 보통주 무상수증(주2) | - |
| (주1) | 전기 중 보통주 유상증자로 183,333주를 취득하였습니다. |
| (주2) | 전기까지 최대주주 및 당사 임원으로부터 프리모리스테라퓨틱스 보통주 87,200주를 무상수증받아, 취득금액은 영(0)입니다. |
(5) 당분기와 전분기 중 특수관계자와의 자금거래내역은 다음과 같습니다.
| (당분기) | (단위: 천원) |
| 특수관계자 명칭 | 구 분 | 기초 | 증가 | 감소 | 기말 |
|---|---|---|---|---|---|
| HLB바이오코드(주) | 대여금 | 200,000 | - | - | 200,000 |
| (주)프리모리스테라퓨틱스 | 대여금 | 730,000 | - | - | 730,000 |
| (주)프리모리스테라퓨틱스 | 상환전환우선주 | 2,000,050 | - | - | 2,000,050 |
| (전분기) | (단위: 천원) |
| 특수관계자 명칭 | 구 분 | 기초 | 증가 | 감소 | 기말 |
|---|---|---|---|---|---|
| (주)프리모리스테라퓨틱스 | 대여금 | - | 450,000 | - | 450,000 |
| (주)프리모리스테라퓨틱스 | 상환전환우선주 | 2,000,050 | - | - | 2,000,050 |
(6) 당분기말 현재 특수관계자에게 제공하거나, 특수관계자로부터 제공받은 담보 및 지급보증은 없습니다.
X. 그 밖에 투자자 보호를 위하여 필요한 사항
1. 공시내용 진행 및 변경사항
- 당사가 주요사항보고서 및 한국거래소 공시를 통해 공시한 사항이 공시서류제출일까지 이행이 완료되지 않았거나, 주요내용이 변경되었거나, 또는 신고내용과 다르게 진행된 경우의 상세 내용은 다음과 같습니다.
| 신고일자 | 제목 | 신고내용 | 신고사항의 진행사항 |
| - | - | - | - |
- 해당사항 없음.
2. 우발부채 등에 관한 사항
가. 중요한 소송사건
- 해당사항 없음 -
나. 견질 또는 담보용 어음ㆍ수표 현황
- 해당사항 없음-
다. 채무보증 현황
당분기말 현재 당사가 특수관계자를 위하여 제공하고 있는 담보 및 보증내역은 없습니다.
라. 채무인수약정 현황
- 해당사항 없음 -
마. 그 밖에 우발채무 등
1) 우발채무 등
(1) 당분기말 현재 금융기관과의 주요 약정사항은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 금융기관 | 약정금액 | 실행금액 |
|---|---|---|---|
| 시설자본 대출약정 | 기업은행 | 4,000,000 | 3,000,000 |
| 시설자본 대출약정 | 기업은행 | 1,480,000 | 1,480,000 |
| 시설자본 대출약정 | 기업은행 | 350,000 | 350,000 |
| 시설자본 대출약정 | 기업은행 | 380,000 | 380,000 |
| 운영자금 대출약정 | 기업은행 | 1,500,000 | 1,500,000 |
(2) 당분기말 현재 당사가 특수관계자를 제외한 타인으로부터 제공받은 지급보증의 내용은 다음과 같습니다.
| (단위: 천원) |
| 제공받은자 | 보증자 | 보증일 | 보증금액 | 보증내용 |
|---|---|---|---|---|
| (주)지에스리테일 | 서울보증보험 | 2024.11.03~2026.11.02 | 10,000 | 홈쇼핑계약 등에 따른 손해배상금 |
| (주)씨제이이엔엠 | 서울보증보험 | 2023.09.27~2025.09.26 | 40,000 | 홈쇼핑계약 등에 따른 손해배상금 |
(3) 당분기말 현재 당사는 주식회사 대웅제약과 세포치료제에 대한 판권 및 공동개발계약을 체결하고 있으며, 상기 거래와 관련하여 수령한 계약금은 수익을 이연하여 인식합니다.
2) 관계기업 및 공동기업 지분 손상
(1) 당분기말 및 전기말 현재 관계기업 및 공동기업에 대한 지분율 현황 및 출자금액은 다음과 같습니다.
| (단위: 천원) |
| 기업명 | 구 분 | 주요영업활동 | 소재지 | 결산월 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|---|---|---|---|
| 지분율(%) | 취득 원가 | 장부 금액 | 지분율(%) | 취득 원가 | 장부 금액 | |||||
| 디앤케이코퍼레이션(주1) | 공동기업 | 화장품 판매 | 대한민국 | 12월 | 50.00% | 1,000,000 | - | 50.00% | 1,000,000 | - |
| (주)블루진(주2) | 관계기업 | 화장품 판매 | 대한민국 | 12월 | 20.00% | 300,000 | - | 20.00% | 300,000 | - |
| (주)프리모리스테라퓨틱스(주3) | 공동기업 | 신약 연구개발 | 대한민국 | 12월 | 64.76% | - | - | 64.76% | - | - |
| HLB바이오코드(주)(주4) | 관계기업 | 비임상 시험용역 | 대한민국 | 12월 | 22.47% | 4,505,517 | 2,538,204 | - | 4,505,517 | 2,574,302 |
| (주1) | 당사가 공동지배력을 보유하고 있는 공동약정은 별도의 회사를 통하여 구조화되었으며, 공동약정의 당사자들이 약정의 자산에 대한 권리와 부채에 대한 의무를 보유한다는 것을 명시하는 합의된 계약상 조건이나 그 밖의 사실과 상황이 존재하지 않습니다. 따라서 공동약정에 대하여 공동지배력을 보유하는 당사자들이 약정의 순자산에 대한 권리를 보유하고 있다고 판단하여 공동기업으로 분류하고 있습니다. 또한 당사는 공동기업에 대한 지분을 지분법으로 회계처리 하고 있습니다. |
| (주2) | 당사가 20%의 지분을 취득하여 재무정책 및 영업정책에 대한 유의적인 영향력을 보유하고 있어 관계기업으로 분류하였습니다. 또한 당사는 해당 관계기업에 대한 지분을 지분법으로 회계처리 하고 있습니다. |
| (주3) | 전기 중 ㈜프리모리스테라퓨틱스 임직원으로부터 추가로 보통주식 27,200주를 무상으로 수증 받아 지분율이 증가하였습니다. 당사는 보통주식 외에 의결권 있는 상환전환우선주 11,765주를 보유하고 있으며 상기 지분율은 상환전환우선주 주식수를 포함한 지분율입니다. |
| (주4) | 전기 중 보유 주식 1,183,676주(64.50%) 중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류하였습니다. 또한 매각 이후 유상증자를 통해 HLB바이오코드(주)의 지분(183,333주)를 추가 취득하였습니다. 이후 HLB바이오코드㈜의 유상증자에 참여하지 않아 지분율이 감소하였습니다. |
(2) 당분기말 및 전기말 중 관계기업 및 공동기업의 변동내역은 다음과 같습니다.
| (당분기말) | (단위: 천원) |
| 구 분 | 기초 | 취득 | 지분법손익 | 당분기말 |
|---|---|---|---|---|
| HLB바이오코드(주) | 2,574,302 | - | (36,098) | 2,538,204 |
| (전기말) | (단위: 천원) |
| 구 분 | 기초 | 취득(주1) | 지분법손익 | 대체(주1)(주2) | 손상 | 전기말 |
|---|---|---|---|---|---|---|
| HLB바이오코드(주) | - | 989,998 | (545,239) | 3,515,519 | (1,385,976) | 2,574,302 |
| (주1) | 전기 중 보유 주식 1,183,676주(64.50%) 중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류하였습니다. 또한 매각 이후 유상증자를 통해 HLB바이오코드(주)의 지분(183,333주)를 추가 취득하였습니다. |
| (주2) | 지배력 상실시 종속기업투자주식처분이익 9,845,033천원이 발생하였습니다. |
3. 제재 등과 관련된 사항
- 해당사항 없음
4. 작성기준일 이후 발생한 주요사항 등 기타사항
가. 작성기준일 이후 발생한 주요사항
- 해당사항 없음 -
나.중소기업기준 검토표
 |
|
2024_중소기업검토표_개별_1 |
 |
|
2024_중소기업검토표_개별_2 |
다. 합병등의 사후정보
- 당사는 공시대상기간 중 해당사항이 없습니다.
라. 특례상장기업의 사후정보
1) 특례상장 여부 및 상장일자
- 특례상장 여부 : 기술성장기업의 코스닥시장 상장
- 특례상장 일자 : 2015년 12월 21일
2) 매출액 미달에 대한 관리종목 지정유예 현황
(최근 사업연도 매출액 30억원 미만)
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원) |
| 요건별 회사 현황 | 관리종목 지정요건 해당여부 |
관리종목지정유예 | |||
|---|---|---|---|---|---|
| 사업연도 | 매출금액 | 해당여부 | 사유 | 종료시점 | |
| 2024 | 7,746 | 미해당 | 미해당 | - | 2020년 12월 31일 |
3) 계속사업손실에 대한 관리종목 지정유예 현황
(자기자본 50%이상(10억원 이상에 한함)의 법인세차감전계속사업손실이 최근 3년간 2회 이상 및 최근 사업연도 법인세차감전계속 사업손실 발생)
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원, %) |
| 요건별 회사 현황 | 관리종목 지정요건 해당여부 |
관리종목지정유예 | ||||
|---|---|---|---|---|---|---|
| 사업연도 | 법인세 차감전 계속사업손익(A) |
자기자본금액 (B) |
비율(A/B) | 해당 여부 |
종료 시점 |
|
| 2022년 | -20,215 | 47,260 | -42.8 | 미해당 | 미해당 | 2018년 12월 31일 |
| 2023년 | -23,137 | 44,518 | -52.0 | |||
| 2024년 | -7,083 | 43,182 | -16.4 | |||
XI. 상세표
1. 연결대상 종속회사 현황(상세)
| (단위 : 백만원) |
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| - | - | - | - | - | - | - |
| (주1) | 전기 중 사명을 (주)크로엔에서 HLB바이오코드(주)로 변경하였으며, 보유 주식 1,183,676주(64.50%) 중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류 하였습니다. 또한 매각 이후 유상증자를 통해 HLB바이오코드(주)의 지분(183,333주)를 추가 취득하였습니다. |
2. 계열회사 현황(상세)
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 사) |
| 상장여부 | 회사수 | 기업명 | 법인등록번호 |
|---|---|---|---|
| 상장 | 1 | (주)강스템바이오텍 | 110111-4461002 |
| - | - | ||
| 비상장 | 6 | (주)디앤케이코퍼레이션 | 110111-6473170 |
| (주)블루진 | 110111-6766153 | ||
| (주)마루테라퓨틱스(주1) | 110111-7830452 | ||
| (주)프리모리스인터내셔널(주1) | 110111-6481462 | ||
| (주)프리모리스테라퓨틱스(주2) | 134911-0089581 | ||
| HLB바이오코드(주)(주3) | 110111-4175299 |
| (주1) | 당사에 대한 지배력을 보유하고 있는 개인 등이 지배력을 보유하고 있는 회사입니다. |
| (주2) | 전기까지 최대주주 및 당사 임원으로부터 프리모리스테라퓨틱스 보통주 87,200주를 무상수증받아, 취득금액은 영(0)입니다. |
| (주3) | 전기에 (주)크로엔의 법인명이 HLB바이오코드(주)로 변경되었습니다. |
3. 타법인출자 현황(상세)
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원, 천주, %) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
| HLB바이오코드(주)(주1) | 비상장 | 2017년 04월 29일 | 일반투자 | 2,699 | 834 | 22 | 2,574 | - | - | - | 834 | 22 | 2,574 | 14,036 | -161 |
| (주)디앤케이코퍼레이션 | 비상장 | 2017년 07월 26일 | 경영참가 | 1,000 | 20 | 50 | - | - | - | - | 20 | 50 | - | 428 | 26 |
| (주)지비벤처스 | 비상장 | 2020년 11월 27일 | 단순투자 | 500 | 100 | 6 | 500 | - | - | - | 100 | 6 | 500 | 6,996 | 129 |
| (주)큐라미스 | 비상장 | 2021년 08월 26일 | 단순투자 | 1,000 | 20 | 3 | 1,000 | - | - | - | 20 | 3 | 1,000 | 6,891 | -2,714 |
| (주)블루진 | 비상장 | 2021년 02월 24일 | 일반투자 | - | 6 | 20 | - | - | - | - | 6 | 20 | - | 21 | - |
| (주)프리모리스테라퓨틱스 | 비상장 | 2023년 02월 02일 | 일반투자 | 2,000 | 72 | 65 | 1,948 | - | - | - | 72 | 65 | 1,948 | 339 | -57 |
| 합 계 | - | - | 6,022 | - | - | - | - | - | 6,022 | - | - | ||||
| (주1) | 전기 중 사명을 (주)크로엔에서 HLB바이오코드(주)로 변경하였으며, 보유 주식 1,183,676주(64.50%) 중 532,654주를 매각함에 따라 지배력을 상실하여 관계기업투자주식으로 재분류 하였습니다. 또한 매각 이후 유상증자를 통해 HLB바이오코드(주)의 지분(183,333주)를 추가 취득하였습니다. |
【 전문가의 확인 】
1. 전문가의 확인
- 해당사항 없음 -
2. 전문가와의 이해관계
- 해당사항 없음 -