 |
|
연구개발부서 조직도 |
정 정 신 고 (보고)
| 2025년 05월 08일 |
| 1. 정정대상 공시서류 : | 증권신고서 |
| 2. 정정대상 공시서류의 최초제출일 : | 2025년 03월 28일 |
| [증권신고서 제출 및 정정 연혁] |
| 제출일자 | 문서명 | 비고 |
|---|---|---|
| 2025년 03월 28일 | 증권신고서(지분증권) | 최초 제출 |
| 2025년 04월 11일 | [기재정정]증권신고서(지분증권) | 자진 정정 |
| 2025년 04월 25일 | [기재정정]증권신고서(지분증권) | 자진 정정 |
| 2025년 05월 08일 | [기재정정]증권신고서(지분증권) | 2025년 1분기 분기보고서제출에 따른 정정 |
| 3. 정정사항 |
| 항 목 | 정정요구ㆍ명령 관련 여부 |
정정사유 | 정 정 전 | 정 정 후 |
| ※ 본 '[기재정정]증권신고서'는 기재사항 추가 보완을 위한 자진정정으로, 정정 및 추가 기재된 사항은 '굵은 주황색'을 사용하였으니 참고하시기 바랍니다. ※ 당사는 2025년 1분기 분기보고서를 2025년 05월 08일에 제출하였습니다. 금번 [기재정정]증권신고서는 2025년 1분기 분기보고서 제출에 따른 정정으로써 효력(재)발생예정일은 2025년 05월 23일입니다. 이 과정에서 금융감독원의 추가 심사에 따라 일정이 변경될 수 있습니다. ※ 단순 오탈자/오기재 수정, 띄어쓰기, 단순 일정변경 등 단순 수정의 경우 정오표를 별도로 기재하지 않았습니다. ※ [요약정보 - 1. 핵심투자위험], [요약정보 -2. 모집 또는 매출에 관한 일반사항] 및 [IV. 인수인의 의견(분석기관의 평가의견)]의 정정사항은 본문에 정정사항을반영하였으며, 별도로 정오표를 작성하지 아니하오니 참고하여 주시기 바랍니다. |
||||
| ※ 단순 오탈자/오기재 수정, 띄어쓰기 등 단순 수정의 경우 정오표를 별도로 기재하지 않았습니다. | ||||
| ※ [요약정보 - 1. 핵심투자위험]의 정정사항은 [제1부 모집 또는 매출에 관한 일반사항 - Ⅲ. 투자위험요소]의 정정사항과 동일하여,별도의 정오표를 작성하지 아니하고 본문에 직접 정정하였으니 참고하시기 바랍니다. | ||||
| 제1부 모집 또는 매출에 관한 사항 | ||||
| III. 투자위험요소 | ||||
| 1. 사업위험 | ||||
| 가. 국내외 경기변동에 따른 위험 | 아니오 | 기재정정 | (주1) 정정 전 | (주1) 정정 후 |
| 바. 핵심연구인력 유출 관련 위험 | 아니오 | 2025년 1분기 분기보고서제출에 따른 정정 | (주2) 정정 전 | (주2) 정정 후 |
| 사. 신약 개발 실패 및 연구개발비용 증가에 따른 수익성 악화 위험 | (주3) 정정 전 | (주3) 정정 후 | ||
| 카. 기술도입관련 위험 | (주4) 정정 전 | (주4) 정정 후 | ||
| 2. 회사위험 | ||||
| 가. OCI그룹 기업집단 설정에 따른 위험 | 아니오 | 2025년 1분기 분기보고서제출에 따른 정정 | (주5) 정정 전 | (주5) 정정 후 |
| 나. 수익성 악화 위험 | (주6) 정정 전 | (주6) 정정 후 | ||
| 다. 재무건전성 위험 | (주7) 정정 전 | (주7) 정정 후 | ||
| 라. 자회사 손상차손 관련 위험 | (주8) 정정 전 | (주8) 정정 후 | ||
| 마. 환율변동에 따른 위험 | (주9) 정정 전 | (주9) 정정 후 | ||
| 바. 현금흐름 관련 위험 | (주10) 정정 전 | (주10) 정정 후 | ||
| 사. 연구개발비 증가에 따른 위험 | (주11) 정정 전 | (주11) 정정 후 | ||
| 아. 소송 등 우발부채 관련 위험 | (주12) 정정 전 | (주12) 정정 후 | ||
| 3. 기타위험 | ||||
| 가. 최대주주의 청약 참여율에 따른 지분율 변동 위험 | 아니오 | 2025년 1분기 분기보고서 제출에 따른 정정 | (주13) 정정 전 | (주13) 정정 후 |
| V. 자금의 사용목적 | 아니오 | 2025년 1분기 분기보고서 제출에 따른 정정 | (주14) 정정 전 | (주14) 정정 후 |
| 제2부 발행인에 관한 사항 | ||||
| 제2부 발행인에 관한 사항은 2025년 1분기 분기보고서 제출에 따라 기존 2024년말 기준에서 2025년 1분기말 기준으로 일괄 정정 되었으며 일부 사항은 본 증권신고서 제출일 전영업일 기준으로 반영하였습니다. 정정 내용은 본문을 참고하여 주시기 바라며, 정정 관련 별도 색깔 표시를 생략하였으니 참고하시기 바랍니다. | ||||
(주1) 정정 전
(1) 글로벌 경기 동향
2025년 03월 발표된 경제협력개발기구(OECD)의 '경제전망 중간 보고서(Economic Outlook Interim Report)'에 따르면 세계경제는 2025년 3.1%, 2026년 3.0%의 경제성장이 이루어질 것으로 전망됩니다. 2024년 12월에 발표한 전망치인 2025년 3.3%, 2026년 3.3%와 비교 시 2025년 전망치는 0.2%p, 2026년 전망치는 0.3%p 하향조정 되었습니다.
OECD는 세계 GDP 성장률이 내년까지 점차 둔화될 것으로 예상하고 있으며, 일부 주요 20개국 경제의 무역 장벽이 높아지고 지정학적, 정책적 불확실성이 증가하면서 투자와 가계 지출에 부담이 될 것으로 전망하였습니다. 또한 OECD는 미국과 유럽 간 대서양 동맹 균열로 유럽 국가들 내에서 국방비 지출 증대를 꾀하는 것과 관련해, 국방에 대한 지출 증가는 단기적으로 성장을 뒷받침할 수 있지만, 장기적으로는 재정 압박을 가중할 수 있다고 지적하였습니다.
지정학적 리스크, 보호무역주의 확대 기조 등에 따른 불확실성 확대 등 국내외 경제에 큰 영향을 미칠 수 있는 요인이 상존하고 있는 상황에서, 대외 경제여건 변동성이 확대될 경우 대외 개방도가 높은 한국경제의 특성상 경제성장에 제한이 발생할 가능성이 있을 것으로 예상됩니다. 당사가 영위하는 사업은 경기침체나 금융환경이 불안정할 경우 보유계약이 이탈하는 등 성장이 위축될 수 있으며 이는 당사의 사업과 영업실적, 재무상황에 부정적인 영향을 미칠 가능성이 있습니다.
| [OECD 세계 경제성장 전망] | |
| (단위 : %, %p.) | |
| 구분 | 2024년 | 2025년 | 2026년 | ||||
|---|---|---|---|---|---|---|---|
| 24.12월 (A) |
25.03월 (B) |
조정폭 (B-A) |
24.12월 (C) |
25.03월 (D) |
조정폭 (D-C) |
||
| 전세계 | 3.2 | 3.3 | 3.1 | -0.2 | 3.3 | 3.0 | -0.3 |
| G20 | 3.3 | 3.3 | 3.1 | -0.2 | 3.2 | 2.9 | -0.3 |
| 유로존 | 0.7 | 1.3 | 1.0 | -0.3 | 1.5 | 1.2 | -0.3 |
| 호주 | 1.1 | 1.9 | 1.9 | 0.0 | 2.5 | 1.8 | -0.7 |
| 캐나다 | 1.5 | 2.0 | 0.7 | -1.3 | 2.0 | 0.7 | -1.3 |
| 독일 | -0.2 | 0.7 | 0.4 | -0.3 | 1.2 | 1.1 | -0.1 |
| 프랑스 | 1.1 | 0.9 | 0.8 | -0.1 | 1.0 | 1.0 | 0.0 |
| 이태리 | 0.7 | 0.9 | 0.7 | -0.2 | 1.2 | 0.9 | -0.3 |
| 스페인 | 3.2 | 2.3 | 2.6 | 0.3 | 2.0 | 2.1 | 0.1 |
| 일본 | 0.1 | 1.5 | 1.1 | -0.4 | 0.6 | 0.2 | -0.4 |
| 한국 | 2.1 | 2.1 | 1.5 | -0.6 | 2.1 | 2.2 | 0.1 |
| 멕시코 | 1.5 | 1.2 | -1.3 | -2.5 | 1.6 | -0.6 | -2.2 |
| 튀르키예 | 3.2 | 2.6 | 3.1 | 0.5 | 4.0 | 3.9 | -0.1 |
| 영국 | 0.9 | 1.7 | 1.4 | -0.3 | 1.3 | 1.2 | -0.1 |
| 미국 | 2.8 | 2.4 | 2.2 | -0.2 | 2.1 | 1.6 | -0.5 |
| 아르헨티나 | -1.8 | 3.6 | 5.7 | 2.1 | 3.8 | 4.8 | 1.0 |
| 브라질 | 3.4 | 2.3 | 2.1 | -0.2 | 1.9 | 1.4 | -0.5 |
| 중국 | 5.0 | 4.7 | 4.8 | 0.1 | 4.4 | 4.4 | 0.0 |
| 인도 | 6.3 | 6.9 | 6.4 | -0.5 | 6.8 | 6.6 | -0.2 |
| 인도네시아 | 5.0 | 5.2 | 4.9 | -0.3 | 5.1 | 5.0 | -0.1 |
| 남아공 | 0.6 | 1.5 | 1.6 | 0.1 | 1.7 | 1.7 | 0.0 |
| 출처 : OECD Economic Outlook Interim Report(2025.03) |
(중략)
(주1) 정정 후
(1) 글로벌 경기 동향
국제통화기금(IMF)은 2025년 4월 22일 4월 세계경제전망(World Economic Outlook) 보고서를 발표하였으며, 이번 전망보고서에서는 최근 높은 정책 불확실성을 감안하여 전망 기준일에 따른 기준 전망(reference forecast)과 보완 전망(alternatives)을 함께 제시하였습니다. 기준 전망에서 2025년 4월 4일 기준 반영 가능한 정보를 기반으로 국가별 성장률을 전망하되, 보완 전망을 통해 4월 2일 상호관세 부과 이전 및 4월 9일 상호관세 유예 이후 기준 전망으로 세계 성장률 범위를 추가로 제시하였습니다. 다만, 보완 전망은 지역, 국가별 전망에 대해서는 공개하지 않았습니다.
4월 4일을 기준으로 한 기준 전망에서는 무역긴장 등 글로벌 불확실성을 반영하여 대부분 국가의 성장률 전망을 하향하면서 2025년 세계경제 성장률을 지난 1월 전망 대비 0.5%p. 하향조정한 2.8%로 전망하였습니다.
보완전망에서 4월 2일 상호관세 부과 이전 기준으로는 미국의 2~3월 무역정책, 높은 유가 전망으로 중국, 캐나다, 멕시코의 성장률이 대폭 둔화됨에 따라 2025년 세계경제 성장률을 1월 전망 대비 0.1%p. 하향 조정한 3.2%로 전망하였습니다. 한편, 4월 9일 이후 기준으로는 2025년 상호관세 90일 유예의 효과가 미국과 중국의 성장률 하락으로 상쇄되어 세계경제성장률 2.8%를 전망하였고, 2026년에는 미국과 중국의 손실이 다른 국가의 이득을 넘어섬에 따라 2.9%의 성장률을 전망하였습니다.
| [세계경제성장률 전망] |
| (단위 : %, %p.) |
| 구분 | 2025년 세계 경제 성장률 | 2026년 세계 경제 성장률 |
|---|---|---|
| 2025년 1월 전망 | 3.3% | 3.3% |
| 기준전망(4.4 기준) | 2.8%(-0.5%p.) | 3.0%(-0.3%p.) |
| 보완전망(4.2 이전 기준) | 3.2%(-0.1%p.) | 3.2%(-0.1%p.) |
| 보완전망(4.9 이후 기준) | 2.8%(-0.5%p.) | 2.9%(-0.4%p.) |
| 출처 : IMF World Economic Outlook(세계경제전망)(2025.04) 주) 기준전망 및 보완전망 괄호 내 수치는 2025년 1월 전망치 대비 변동 수치입니다. |
한편, 국가별, 지역별 성장률은 기준전망만 제시하였으며, 선진국 그룹의 2025년 성장률은 지난 1월 전망 대비 0.5%p. 하향 조정된 1.4%로 전망하였습니다. 미국은 정책 불확실성, 무역 긴장, 소비 회복 지연 등으로 성장률 전망치가 대폭 하락 조정되었고, 대부분의 유럽국가와 일본도 하향 조정되었습니다. 한국 성장률의 경우 2025년 1월 전망 대비 1.0%p. 하향 조정된 1.0%로 전망되었습니다.
신흥개도국 그룹의 경우 2025년 성장률은 1월 전망 대비 0.5%p. 하향 조정된 3.7%로 전망되었으며, 특히 중국은 예상보다 견조한 2024년 4분기 실적 및 재정확대에도 불구하고 관세 조치의 부정적 영향으로 2025년 및 2026년 성장률 전망치가 모두 하향 조정되었으며, 멕시코는 2024년말 이후 부진한 경제활동과 더불어 미국의 관세 부과, 지정학적 리스크 및 긴축적 금융환경 등의 영향으로 2025년 성장률이 1월 전망 대비 대폭 하향조정 되었습니다.
국제통화기금(IMF)은 세계경제의 리스크가 하방 요인에 집중되어 있다고 진단하면서, 무역갈등 등 정책 불확실성 확대에 따른 소비·투자 위축, 고금리 및 높은 부채수준으로 인한 재정·통화 정책 여력 부족, 주가 및 시장가격 재조정 가능성 등 금융·외환시장의 높은 변동성 등을 위험 요인으로 제시하였습니다. 다만, 미국 관세 조치 인하와 상호 협상 등이 진전될 경우 세계경제의 상방 조정 요인으로 작용할 수 있다고 언급하였습니다.
국제통화기금(IMF)은 고조된 불확실성과 성장 둔화에 대응하기 위해 예측가능한 무역환경 조성의 필요성을 강조하며 무분별한 산업 보조금을 지양하고 지역, 다자간 무역협정 확대를 통한 무역 분절화 방지 노력이 필요하다고 강조하였습니다. 또한 금융시장 안정과 기대 인플레이션간의 균형을 유지하는 신중한 통화정책과 건전한 재정 운용의 필요성을 언급하고, 자본 변동성 확대에 대응하여 국가별 금융, 외환시장 성숙도에 맞는 적절한 개입 및 건전성 조치를 시행할 것을 권고하였습니다. 그 밖에 중기 성장잠재력 회복을 위한 여성·고령층 노동 참여 제고와 AI, 디지털 기술 투자확대, 규제 정비 등의 노력도 촉구하였습니다.
| [IMF 세계 경제성장 전망] | |
| (단위 : %, %p.) | |
| 구분 | 2024년 | 2025년 | 2026년 | ||||
|---|---|---|---|---|---|---|---|
| 25.01월 (A) |
25.04월 (B) |
조정폭 (B-A) |
25.01월 (C) |
25.04월 (D) |
조정폭 (D-C) |
||
| 세계 | 3.3 | 3.3 | 2.8 | -0.5 | 3.3 | 3.0 | -0.3 |
| 선진국 | 1.8 | 1.9 | 1.4 | -0.5 | 1.8 | 1.5 | -0.3 |
| 미국 | 2.8 | 2.7 | 1.8 | -0.9 | 2.1 | 1.7 | -0.4 |
| 유로존 | 0.8 | 1.0 | 0.8 | -0.2 | 1.4 | 1.2 | -0.2 |
| 독일 | -0.2 | 0.3 | 0.0 | -0.3 | 1.1 | 0.9 | -0.2 |
| 프랑스 | 1.1 | 0.8 | 0.6 | -0.2 | 1.1 | 1.0 | -0.1 |
| 이탈리아 | 0.7 | 0.7 | 0.4 | -0.3 | 0.9 | 0.8 | -0.1 |
| 스페인 | 3.2 | 2.3 | 2.5 | +0.2 | 1.8 | 1.8 | 0.0 |
| 일본 | 0.1 | 1.1 | 0.6 | -0.5 | 0.8 | 0.6 | -0.2 |
| 영국 | 1.1 | 1.6 | 1.1 | -0.5 | 1.5 | 1.4 | -0.1 |
| 캐나다 | 1.5 | 2.0 | 1.4 | -0.6 | 2.0 | 1.6 | -0.4 |
| 한국 | 2.0 | 2.0 | 1.0 | -1.0 | 2.1 | 1.4 | -0.7 |
| 호주 | 1.0 | 2.1 | 1.6 | -0.5 | 2.2 | 1.4 | -0.8 |
| 기타선진국 | 2.2 | 2.1 | 1.8 | -0.3 | 2.3 | 2.0 | -0.3 |
| 신흥개도국 | 4.3 | 4.2 | 3.7 | -0.5 | 4.3 | 3.9 | -0.4 |
| 중국 | 5.0 | 4.6 | 4.0 | -0.6 | 4.5 | 4.0 | -0.5 |
| 멕시코 | 1.5 | 1.4 | -0.3 | -1.7 | 2.0 | 1.4 | -0.6 |
| 출처 : IMF World Economic Outlook(세계경제전망)(2025.04) |
(중략)
(주2) 정정 전
당사가 영위하고 있는 제약업의 특성상 사업의 연구개발 능력은 매우 중요한 요소이며, 지속적인 연구개발을 위해서는 제약분야에 전문성과 노하우를 가진 연구인력을 확보하여야 합니다. 이는 제약 산업내 업체들에 공통적으로 적용되는 사항으로, 우수한 인력을 유치하기 위한 경쟁은 점차 심화되고 있습니다. 인력 유치 경쟁으로 인해 주요 연구 인력의 유출이 발생할 경우 해당 연구 개발과제가 지연되거나 개발전략을 수정해야 할 가능성이 존재하며, 개발비 부담 등으로 당사의 경쟁력 및 성장성이 악화될 수 있습니다.
당사는 당사 내 연구개발본부 산하 허가등록부, 개발부, 연구소 등의 연구개발 조직을 보유 중이며 당사 자회사 또한 연구개발전문 조직의 성격을 보이고 있습니다. 또한 당사와 같은 제약업체는 연구개발에 있어 핵심 인력을 보유하는 것이 주요 경쟁력 이기에 박사급 인력 14명, 석사급 인력 30명 등 총 66명의 연구인력을 보유하고 있으며 기존 인재들에게 적절한 보상을 제공하여 동기부여함과 동시에 향후에도 인재영입을 위해 최선을 다할 계획입니다. 증권신고서 제출일 기준 당사의 연구인력 현황은 다음과 같습니다.
| [당사 연구인력 현황] |
| (단위: 명) |
| 구분 | 박사 | 석사 | 학사 | 기타 | 합계 |
| 부광약품 연구개발 인력 | 4 | 30 | 16 | 1 | 51 |
| Contera Pharma A/S(**) | 9 | - | 5 | - | 14 |
| ProteKt Therapeutics | 1 | - | - | - | 1 |
| 합계(***) | 14 | 30 | 21 | 1 | 66 |
| (자료 : 당사제시) |
당사의 핵심 연구인력은 다음과 같습니다.
| [당사 핵심연구인력 현황] |
| (단위: 명) |
| 직위 | 성명 | 담당업무 | 최종학위 | 주요 경력 |
| 전무 | 김지헌 | 연구개발담당 | 석사 | 前, (주)GC녹십자 사업개발본부 상무 現, 부광약품(주) 연구개발본부 전무 |
| 이사 | 임진희 | 개발담당 | 석사 | 前, 대웅제약 사업개발본부 팀장 現, 부광약품(주) 연구개발본부 이사 |
한편 당사가 개발 성공한 신약 및 진행중인 연구과제에 대한 세부 내용, 당사 연구개발조직도는 아래와 같습니다.
(1) 개발성공신약
| 구분 | 신약명 | 적응증 | 허가년월 | 허가국가/기관명 | 비고 |
| 신약 | 레보비르 | B형 간염치료제 | 2006.11 | 한국/MFDS | 국내 제11호 신약 |
| 개량신약 | 덱시드 | 당뇨병성신경병증 | 2013.11 | 한국/MFDS | - |
| 신약 | 라투다정 | 조현병, 양극성 우울증 | 2023.11 | 한국/MFDS | 국내 8월 출시 |
| (자료 : 당사 사업보고서) |
(2) 진행중인 연구과제
| 연구과제 | 적응증 |
연구 연도 |
진행 경과 | 파트너사/공동개발사 | 개발사 | 비고 | |
| 단계(국가) | 승인년도 | ||||||
| JM-010 | 파킨슨병 환자의 Dyskinesia 치료제 |
2013년 | Phase 1 완료(독일) Phase 2a 완료(남아공) Phase 2 완료(유럽,한국) Phase 2 종료(미국) |
2016년 2015년 2018년 2020년 |
(덴마크) Contera Pharma A/S | (한국) 부광약품(주) (덴마크) Contera Pharma A/S |
- |
| CP-012 | 파킨슨병 환자의 Morning Akinesia (아침무동증) 치료제 |
2013년 | Phase 1a 완료(유럽) Phase 1b 진행(유럽) |
2023년 - |
- | (덴마크) Contera Pharma A/S | - |
| (자료 : 당사 사업보고서) |
- 품목: JM-010
| 적응증 | 파킨슨병 환자의 Dyskinesia 치료제 |
| 작용기전 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 제품의 특성 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 진행경과 |
- 남아공에서 글로벌 임상 전기 2상 (PoC) 완료 (2015년 11월) - 유럽에서 신제형의 Human pharmacokinetic study 완료 (2016년 9월) - 독일/프랑스/스페인 : 임상 2상 승인 완료 및 2019년 4월 임상 개시 모임 진행 |
| 향후계획 | - 임상결과를 바탕으로 활용방안을 검토 중 |
| 경쟁제품 | - |
| 관련논문 등 | - |
| 시장규모 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 기타사항 | 한국에서 개발단계희귀의약품 지정 (2017년 1월) |
| (자료 : 당사 사업보고서) |
- 품목: CP-012
| 적응증 | 파킨슨병 환자의 Morning Akinesia (아침무동증) 치료제 |
| 작용기전 | 개발 초기 단계로 Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 제품의 특성 | 개발 초기 단계로 Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 진행경과 | 유럽 임상 1a상 진행 완료 (2023년 9월) 유럽 임상 1b상 진행 중 |
| 향후계획 | 개발 초기 단계로 예측 불가 |
| 경쟁제품 | - |
| 관련논문 등 | - |
| 시장규모 | 개발 초기 단계로 예측 불가 |
| 기타사항 | - |
| (자료 : 당사 사업보고서) |
| [당사 연구개발 조직도] |
 |
|
연구개발부서 조직도 |
| (자료 : 당사 사업보고서) |
현재 당사는 다양한 신약 및 의약품을 개발중에 있으며, 개발된 의약품을 판매함으로써 사업을 영위하고 있습니다. 따라서 당사의 사업에 있어서 의약품 개발을 위한 연구활동은 매우 중요합니다. 결국 당사의 매출 성장 및 외형확대를 위해서는 우수한 연구개발 인력을 유치해야하고 기존의 인력을 유지해야 합니다.
당사는 인력관리의 중요성을 인지하고 업무 만족도 증진, 회사의 비전 공유, 지속적인 교육을 통한 자기 계발 프로그램 강화, 업무실적에 근거한 인센티브 제도 등 각종 복리후생제도 강화 등을 통해 직원들의 애사심 고취에 힘쓰고 있으며 향후에도 임직원의 다양한 복지 혜택을 확대할 계획입니다.
다만, 이러한 당사의 노력 및 정책에도 불구하고 제약산업의 경쟁심화에 따른 우수인력 스카우트 등에 따라 핵심인력이 경쟁회사 또는 다른 산업분야로 이탈할 수 있으며, 이러한 경우 당사 핵심 기술 노하우의 유출 등은 당사의 경쟁력을 약화시킬 수 있으며 이는 당사 영업활동 및 수익성에 부정적인 영향을 미칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
(주2) 정정 후
당사가 영위하고 있는 제약업의 특성상 사업의 연구개발 능력은 매우 중요한 요소이며, 지속적인 연구개발을 위해서는 제약분야에 전문성과 노하우를 가진 연구인력을 확보하여야 합니다. 이는 제약 산업내 업체들에 공통적으로 적용되는 사항으로, 우수한 인력을 유치하기 위한 경쟁은 점차 심화되고 있습니다. 인력 유치 경쟁으로 인해 주요 연구 인력의 유출이 발생할 경우 해당 연구 개발과제가 지연되거나 개발전략을 수정해야 할 가능성이 존재하며, 개발비 부담 등으로 당사의 경쟁력 및 성장성이 악화될 수 있습니다.
당사는 당사 내 연구개발본부 산하 허가등록부, 개발부, 연구소 등의 연구개발 조직을 보유 중이며 당사 자회사 또한 연구개발전문 조직의 성격을 보이고 있습니다. 또한 당사와 같은 제약업체는 연구개발에 있어 핵심 인력을 보유하는 것이 주요 경쟁력 이기에 박사급 인력 13명, 석사급 인력 30명 등 총 65명의 연구인력을 보유하고 있으며 기존 인재들에게 적절한 보상을 제공하여 동기부여함과 동시에 향후에도 인재영입을 위해 최선을 다할 계획입니다. 증권신고서 제출일 기준 당사의 연구인력 현황은 다음과 같습니다.
| [당사 연구인력 현황] |
| (단위: 명) |
| 구분 | 박사 | 석사 | 학사 | 기타 | 합계 |
| 부광약품(주) 연구소 | 3 | 30 | 15 | 1 | 49 |
| Contera Pharma A/S | 9 | - | 6 | - | 15 |
| ProteKt Therapeutics | 1 | - | - | - | 1 |
| JaguAHR Therapeutics | - | - | - | - | - |
| 합계 | 13 | 30 | 21 | 1 | 65 |
| (자료 : 당사제시) |
당사의 핵심 연구인력은 다음과 같습니다.
| [당사 핵심연구인력 현황] |
| 직위 | 성명 | 담당업무 | 최종학위 | 주요 경력 |
| 전무 | 김지헌 | 연구개발담당 | 석사 | 前, (주)GC녹십자 사업개발본부 상무 現, 부광약품(주) 연구개발본부 전무 |
| 이사 | 임진희 | 개발담당 | 석사 | 前, 대웅제약 사업개발본부 팀장 現, 부광약품(주) 연구개발본부 이사 |
한편 당사가 개발 성공한 신약 및 진행중인 연구과제에 대한 세부 내용, 당사 연구개발조직도는 아래와 같습니다.
(1) 개발성공신약
| 구분 | 신약명 | 적응증 | 허가년월 | 허가국가/기관명 | 비고 |
| 신약 | 레보비르 | B형 간염치료제 | 2006.11 | 한국/MFDS | 국내 제11호 신약 |
| 개량신약 | 덱시드 | 당뇨병성신경병증 | 2013.11 | 한국/MFDS | - |
| 신약 | 라투다정 | 조현병, 양극성 우울증 | 2023.11 | 한국/MFDS | 국내 8월 출시 |
| (출처 : 당사 분기보고서) |
- 신약명 : 레보비르, Levovir(제품명: 레보비르캡슐, Clevudine)
| 구분 | 합성신약 |
| 적응증 | 만성B형 간염치료제 |
| 작용기전 | 바이러스 DNA 합성 억제 |
| 제품의 특성 | 간 조직 내에서 오랜 반감기를 가지므로, 투여 중단 후에도 일정 기간 항바이러스 효과가 지속 |
| 진행 경과 | 2006-11-22 국내 허가 |
| 경쟁 제품 | Lamivudine(GSK), Adefovir dipivoxil(GSK), Entecavir(BMS) |
| 시장규모 | B형간염치료제 국내시장 2,846억원(UBIST, 2023년) |
| 기타사항 | 국산 신약 11호 |
- 신약명 : 덱시드, Dexid(제품명: 덱시드정, R-thioctic acid tromethamine)
| 구분 | 개량신약 |
| 적응증 | 당뇨병성 신경병증 치료제 |
| 작용기전 | 산화 스트레스 감소, 신경 세포 보호 |
| 제품의 특성 | 강력한 항산화제로서 인슐린 감수성을 향상시켜 혈당 조절을 보조하며, 병인치료제로 사용 및 증상치료제와 병용 가능 |
| 진행 경과 | 2013-11-21 국내 허가 |
| 경쟁 제품 | Pregabalin(Pfizer), Gabapentin(Pfizer) |
| 시장규모 | Thioctic acid 국내시장 650억원(IQVIA, 2023년) |
| 기타사항 | 이성질체(Thioctic acid)에서 약효성분만을 분리하여 세계 최초로 개발하여 투여용량 및 부작용 감소 |
- 신약명 : 라투다, Latuda(제품명: 라투다정, Lurasidone hydrochloride)
| 구분 | 합성신약 |
| 적응증 | 조현병 치료제 |
| 작용기전 | D2 receptor antagonist, 5-HT2A, 5-HT7 receptor antagonist |
| 제품의 특성 | 조현병 및 양극성 장애 우울 증상을 빠르고 지속적으로 개선시키며, 이상반응(체중증가)이 감소 |
| 진행 경과 |
국내 가교 3상 임상시험 별도 수행 2023-11-22 국내 허가 |
| 경쟁 제품 | Aripiprazole(Otsuka), Paliperidone(Janssen), Risperidone(Janssen) |
| 시장규모 | 조현병치료제 국내시장 1,904억(IQVIA, 2023년) |
| 기타사항 |
미국, 유럽, 캐나다 일본 등 전세계적으로 장기간 사용 경험과 충분한 노출이 있는 제품 Metabolic side effect가 적어 복약 순응도 및 유지 치료에 효과적 |
(2) 진행중인 연구과제
| 연구과제 | 적응증 |
연구 연도 |
진행 경과 | 파트너사/공동개발사 | 개발사 | 비고 | |
| 단계(국가) | 승인년도 | ||||||
| JM-010 | 파킨슨병 환자의 Dyskinesia 치료제 |
2013년 | Phase 1 완료(독일) Phase 2a 완료(남아공) Phase 2 완료(유럽,한국) Phase 2 종료(미국) |
2016년 2015년 2018년 2020년 |
(덴마크) Contera Pharma A/S | (한국) 부광약품(주) (덴마크) Contera Pharma A/S |
- |
| CP-012 | 파킨슨병 환자의 Morning Akinesia (아침무동증) 치료제 |
2013년 | Phase 1a 완료(유럽) Phase 1b 진행(유럽) |
2023년 - |
- | (덴마크) Contera Pharma A/S | - |
| (출처 : 당사 분기보고서) |
- 품목: JM-010
| 적응증 | 파킨슨병 환자의 Dyskinesia 치료제 |
| 작용기전 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 제품의 특성 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 진행경과 |
- 남아공에서 글로벌 임상 전기 2상 (PoC) 완료 (2015년 11월) - 유럽에서 신제형의 Human pharmacokinetic study 완료 (2016년 9월) - 독일/프랑스/스페인 : 임상 2상 승인 완료 및 2019년 4월 임상 개시 모임 진행 |
| 향후계획 | - 임상결과를 바탕으로 활용방안을 검토 중 |
| 경쟁제품 | - |
| 관련논문 등 | - |
| 시장규모 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 기타사항 | 한국에서 개발단계희귀의약품 지정 (2017년 1월) |
| (자료 : 당사 분기보고서) |
- 품목: CP-012
| 적응증 | 파킨슨병 환자의 Morning Akinesia (아침무동증) 치료제 |
| 작용기전 | 개발 초기 단계로 Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 제품의 특성 | 개발 초기 단계로 Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 진행경과 | 유럽 임상 1a상 진행 완료 (2023년 9월) 유럽 임상 1b상 진행 중 |
| 향후계획 | 개발 초기 단계로 예측 불가 |
| 경쟁제품 | - |
| 관련논문 등 | - |
| 시장규모 | 개발 초기 단계로 예측 불가 |
| 기타사항 | - |
| (자료 : 당사 분기보고서) |
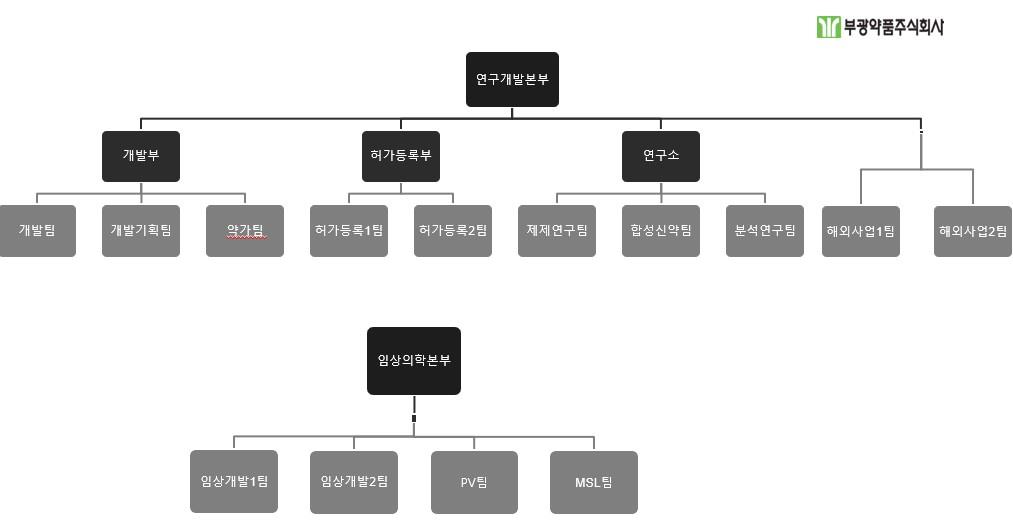
| [당사 연구개발 조직도] |
 |
|
연구개발부서 조직도 |
| (자료 : 당사 분기보고서) |
현재 당사는 다양한 신약 및 의약품을 개발중에 있으며, 개발된 의약품을 판매함으로써 사업을 영위하고 있습니다. 따라서 당사의 사업에 있어서 의약품 개발을 위한 연구활동은 매우 중요합니다. 결국 당사의 매출 성장 및 외형확대를 위해서는 우수한 연구개발 인력을 유치해야하고 기존의 인력을 유지해야 합니다.
당사는 인력관리의 중요성을 인지하고 업무 만족도 증진, 회사의 비전 공유, 지속적인 교육을 통한 자기 계발 프로그램 강화, 업무실적에 근거한 인센티브 제도 등 각종 복리후생제도 강화 등을 통해 직원들의 애사심 고취에 힘쓰고 있으며 향후에도 임직원의 다양한 복지 혜택을 확대할 계획입니다.
다만, 이러한 당사의 노력 및 정책에도 불구하고 제약산업의 경쟁심화에 따른 우수인력 스카우트 등에 따라 핵심인력이 경쟁회사 또는 다른 산업분야로 이탈할 수 있으며, 이러한 경우 당사 핵심 기술 노하우의 유출 등은 당사의 경쟁력을 약화시킬 수 있으며 이는 당사 영업활동 및 수익성에 부정적인 영향을 미칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
(주3) 정정 전
(중략)
당사의 최근 4년간 연결기준 연구개발비용은 다음과 같습니다.
| [당사 연결기준 연구개발비 현황] |
| (단위: 백만원) |
| 구 분 | 2024 | 2023 | 2022 | 2021 | |
|---|---|---|---|---|---|
| 비용의성격별 분류 | 원재료비 | 4,147 | 3,584 | 2,900 | 2,677 |
| 인건비 | 10,537 | 10,021 | 6,565 | 6,919 | |
| 감가상각비 | 1,052 | 587 | 216 | 214 | |
| 위탁용역비 | 9,317 | 14,754 | 12,201 | 12,840 | |
| 기타 | 3,333 | 10,570 | 7,501 | 4,524 | |
| 연구개발비용 합계 | 28,386 | 39,516 | 29,383 | 27,174 | |
| 회계처리내역 | 판매비와 관리비 | 23,430 | 34,551 | 24,274 | 22,465 |
| 제조경비 | 4,956 | 4,965 | 5,108 | 4,709 | |
| 개발비(무형자산) | - | - | - | - | |
| 회계처리금액 계 | 28,386 | 39,516 | 29,382 | 27,174 | |
| 정부보조금 | - | - | - | - | |
| 연구개발비용 합계 | 28,386 | 39,516 | 29,3832 | 27,174 | |
| 연구개발비 / 매출액 비율 | 17.73% | 31.38% | 15.39% | 14.89% | |
| [연구개발비용합계÷당기매출액×100] | |||||
| (자료 : 당사 사업보고서) |
2024년 12월 발표된 한국제약바이오협회 제약바이오산업 데이터북에 따르면, 의약품제조업 및 자연과학 연구개발업을 영위하는 상장사의 2023년 평균 매출액 대비 연구개발비 수준은 12.5%로, 당사는 이보다 높은 수준의 연구개발비를 집행하고 있습니다. 다만, 2023년 JM-010 임상개발로 인해 비경상적으로 높은 규모의 연구개발비중이 집행된 점 고려 시 당사의 평균적인 매출액 대비 연구개발비 비중은 14%~17% 수준으로 연구개발업을 영위하는 상장사 평균 대비 소폭 높은 수준임을 확인할 수 있습니다.
상기와 같이 신약 연구개발을 통하여 가시적인 결과가 나오는 제품의 상용화 단계까지 많은 비용과 시간이 요구되며, 연구개발 과정에서 수많은 변수가 발생할 수 있습니다. 만약 변수들을 미리 찾아내어 극복하지 못한다면, 지출했던 연구개발 비용 및 시간 등의 손실이 발생할 수 있으며 향후 제한적인 국내 시장 등의 한계를 극복하기 위한 연구개발활동이 증가할 수 있습니다. 당사가 진행중인 파이프라인 중 JM-010은 2024년 5월 위약군 대비 통계적으로 유의미한 효과가 나오지 않은 것으로 나타나 임상이 종료된 바 있습니다. 다만, 여러 인종을 대상으로 진행한 해당 임상자체는 종료되었지만 한국인 대상으로는 유효성이 어느정도 확인된 바, 유사 인종(아시아)을 대상으로 임상을 계획중인 기업에게 라이센스 아웃을 검토 중입니다. 실제 당사는 과거 라이센스인한 MLR-1023 관련 2형 당뇨 임상은 종료되었으나 멜리어사가 1형 당뇨로 임상 진행할 목적으로 당사의 MLR-1023 아시아(일본 제외) 권리 및 당사의 제조특허를 포함하여 라이센스 아웃하였으며 당사가 향후 관련 수익의 50%를 수령하는 Benefit sharing agreement를 체결한 바 있습니다.
그럼에도 불구, 연구개발 전략이 계획대로 진행되지 않거나 자금조달에 어려움을 겪어 신약 개발에 실패하거나 지연될 경우 다른 형태로의 라이센스 아웃 가능성은 불확실성이 존재하며, 투입된 연구개발비 회수가 되지 않아 당사의 성장성, 수익성 및 재무안정성에 부정적인 영향을 미칠 수 있으니, 투자자께서는 이 점 유의하시기 바랍니다.
(주3) 정정 후
(중략)
당사의 최근 4년간 연결기준 연구개발비용은 다음과 같습니다.
| [당사 연결기준 연구개발비 현황] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 | |
|---|---|---|---|---|---|---|---|
| 비용의성격별 분류 | 원재료비 | 904 | 695 | 4,147 | 3,584 | 2,900 | 2,677 |
| 인건비 | 3,081 | 2,540 | 10,537 | 10,021 | 6,565 | 6,919 | |
| 감가상각비 | 203 | 181 | 1,052 | 587 | 216 | 214 | |
| 위탁용역비 | 870 | 2,564 | 9,317 | 14,754 | 12,201 | 12,840 | |
| 기타 | 680 | 1,225 | 3,333 | 10,570 | 7,501 | 4,524 | |
| 연구개발비용 합계 | 5,739 | 7,205 | 28,386 | 39,516 | 29,383 | 27,174 | |
| 회계처리내역 | 판매비와 관리비 | 4,452 | 6,056 | 23,430 | 34,551 | 24,274 | 22,465 |
| 제조경비 | 1,287 | 1,149 | 4,956 | 4,965 | 5,108 | 4,709 | |
| 개발비(무형자산) | - | - | - | - | - | - | |
| 회계처리금액 계 | 5,739 | 7,205 | 28,386 | 39,516 | 29,382 | 27,174 | |
| 정부보조금 | - | - | - | - | - | - | |
| 연구개발비용 합계 | 5,739 | 7,205 | 28,386 | 39,516 | 29,3832 | 27,174 | |
| 연구개발비 / 매출액 비율 | 12.00% | 20.95% | 17.73% | 31.38% | 15.39% | 14.89% | |
| [연구개발비용합계÷당기매출액×100] | |||||||
| (자료 : 당사 사업보고서 및 분기보고서) |
2024년 12월 발표된 한국제약바이오협회 제약바이오산업 데이터북에 따르면, 의약품제조업 및 자연과학 연구개발업을 영위하는 상장사의 2023년 평균 매출액 대비 연구개발비 수준은 12.5%로, 당사는 이보다 높은 수준의 연구개발비를 집행하고 있습니다. 다만, 2023년 JM-010 임상개발로 인해 비경상적으로 높은 규모의 연구개발비중이 집행된 점 고려 시 당사의 평균적인 매출액 대비 연구개발비 비중은 14%~17% 수준으로 연구개발업을 영위하는 상장사 평균 대비 소폭 높은 수준임을 확인할 수 있습니다.
상기와 같이 신약 연구개발을 통하여 가시적인 결과가 나오는 제품의 상용화 단계까지 많은 비용과 시간이 요구되며, 연구개발 과정에서 수많은 변수가 발생할 수 있습니다. 만약 변수들을 미리 찾아내어 극복하지 못한다면, 지출했던 연구개발 비용 및 시간 등의 손실이 발생할 수 있으며 향후 제한적인 국내 시장 등의 한계를 극복하기 위한 연구개발활동이 증가할 수 있습니다. 당사가 진행중인 파이프라인 중 JM-010은 2024년 5월 위약군 대비 통계적으로 유의미한 효과가 나오지 않은 것으로 나타나 임상이 종료된 바 있습니다. 다만, 여러 인종을 대상으로 진행한 해당 임상자체는 종료되었지만 한국인 대상으로는 유효성이 어느정도 확인된 바, 유사 인종(아시아)을 대상으로 임상을 계획중인 기업에게 라이센스 아웃을 검토 중입니다. 실제 당사는 과거 라이센스인한 MLR-1023 관련 2형 당뇨 임상은 종료되었으나 멜리어사가 1형 당뇨로 임상 진행할 목적으로 당사의 MLR-1023 아시아(일본 제외) 권리 및 당사의 제조특허를 포함하여 라이센스 아웃하였으며 당사가 향후 관련 수익의 50%를 수령하는 Benefit sharing agreement를 체결한 바 있습니다.
그럼에도 불구, 연구개발 전략이 계획대로 진행되지 않거나 자금조달에 어려움을 겪어 신약 개발에 실패하거나 지연될 경우 다른 형태로의 라이센스 아웃 가능성은 불확실성이 존재하며, 투입된 연구개발비 회수가 되지 않아 당사의 성장성, 수익성 및 재무안정성에 부정적인 영향을 미칠 수 있으니, 투자자께서는 이 점 유의하시기 바랍니다.
(주4) 정정 전
당사는 원료 수입 및 제조/판매, 제품수입 등의 목적으로 다수의 계약을 체결하고 있습니다. 동 계약은 당사의 영업 및 연구개발에 있어 필수적인 요소로 해당 계약이 예상치 못한 변수로 인해 종결되거나 당사에게 불리한 방향으로 변경될 경우 당사 영업환경에 불리하게 작용할 수 있습니다. 특히 당사가 생산 및 판매하는 의약품목의 경우 건강보험평가심사원에서 판매단가를 엄격히 관리하고 있기에 단가 인상에 상방이 존재하며 이 경우 원재료 조달에 있어 불리한 조건이 작용할 시 당사 재무건정성 및 수익성에 악영향을 줄 수 있습니다. 당사의 주요 계약현황은 다음과 같습니다.
| 사업부문 | 계약상대방 | 계약목적 | 대표품목명 | 체결시기 |
| 의약품 및 의약외품 |
Eisai (일본) |
제조/판매 | Selbex (Teprenone) |
2016.07.01 |
| MEDA/Mylan (독일) |
원료수입 | Legalon, Tavex, Alaxyl, Spasmolyt |
1993.12.28 | |
| 원료수입 | Thioctacid, Azeptin, Cormelian, Diurexan |
2003.12.11 | ||
| 제품수입 | Dylastine | 2018.05.25 | ||
| 제품수입 | Sebivo | 2018.10.26 | ||
| Baxter (독일) |
제품수입 | Holoxan Endoxan, Uromitexan |
2013.01.01 | |
| Pierre Fabre (프랑스) |
제품수입 원료수입 |
Navelbine Ixel |
2014.01.01 | |
| Ferrer (스페인) |
제품수입 원료수입 |
Dermofix | 1993.06.02 | |
| 원료수입 | Somazina | 2002.03.04 | ||
| 원료수입 | Nadixa | 2004.05.17 | ||
| 제품수입 |
Repavar Pielato Melagyn |
2016.06.30 | ||
| 제품수입 | Ozanex | 2020.01.10 | ||
|
Ojer (스페인) |
제품수입 | Lipovir | 2018.01.29 | |
| Desitin (독일) |
원료수입 | Orfil | 1978.03.15 | |
| 원료수입 | Timonil | 1994.08.31 | ||
| Sumitomo Pharma Co., Ltd. (일본) |
원료수입 | Lonasen (Blonanserin) | 2005.02.28 | |
| 상표권계약 | Cetapril | 2015.02.27 | ||
| 반제품수입 | Latuda (Lurasidone HCl) | 2017.04.05 | ||
| Sanofi (프랑스) |
라이센스 계약 | Kerlone, Mizollen, Ercefuryl | 2000.05.30 | |
| Eurodrug (네덜란드) |
원료수입 | Fexadin | 1986.07.29 | |
| Asima | 2000.03.24 | |||
| 반제품수입 | Panbesy | 2019.06.01 | ||
| Kalbe International Pte. Ltd. (싱가포르) |
제품수출 | 덱시드정 | 2016.03.03 | |
| Norrizon Sales & Marketing Group Inc. (캐나다) |
의약외품 수출 |
시린메드F, 시린메드 검케어, 안티프라그 캐비티 클리닉 |
2017.02.01 | |
| 연구개발 | Pebean Pharma ApS (덴마크) |
기술도입 | SOL-804 | 2016.06.29 (해지 2024.07.26) |
| Melior Pharmaceuticals, I Inc (미국) |
기술도입 | MLR-1023 | 2013.11.20 | |
| 기술반환, 수익배분 및 이전 |
MLR-1023 | 2023.12.21 | ||
| 공동개발 | Lyn kinase activator | 2017.06.20 | ||
| Contera Pharma A/S (덴마크) |
기술도입 | JM-010 | 2014.12.12 |
| (자료 : 당사 사업보고서) |
당사는 현재 계약을 체결중인 상대방과 우호적인 협력 관계를 유지하고 있으며 이러한 신뢰관계가 향후에도 지속될 것으로 당사는 전망하고 있습니다. 다만 모든 계약에는 불확실성이 존재하며 안정적인 원재료 수급이 절대적으로 중요한 제약 산업에서 예상치 못한 변수로 인해 적절한 원재료 도입에 차질이 생기거나 기술도입/이전 등과 관련하여 분쟁이 발생할 경우 당사의 재무건정성 및 수익성이 악화될 가능성이 존재하는 점 투자자 분들 께서는 유의하시기 바랍니다.
(주4) 정정 후
당사는 원료 수입 및 제조/판매, 제품수입 등의 목적으로 다수의 계약을 체결하고 있습니다. 동 계약은 당사의 영업 및 연구개발에 있어 필수적인 요소로 해당 계약이 예상치 못한 변수로 인해 종결되거나 당사에게 불리한 방향으로 변경될 경우 당사 영업환경에 불리하게 작용할 수 있습니다. 특히 당사가 생산 및 판매하는 의약품목의 경우 건강보험평가심사원에서 판매단가를 엄격히 관리하고 있기에 단가 인상에 상방이 존재하며 이 경우 원재료 조달에 있어 불리한 조건이 작용할 시 당사 재무건정성 및 수익성에 악영향을 줄 수 있습니다. 당사의 주요 계약현황은 다음과 같습니다.
| 사업부문 | 계약 상대방 | 계약목적 | 대표 품목명 | 체결시기 | 진행 단계 |
| 의약품 및 의약외품 |
Eisai (일본) |
제조/판매 | Selbex (Teprenone) |
2016.07.01 | 제조 판매 중 |
| MEDA/Mylan (독일) |
원료 수입 | Legalon, Tavex, Alaxyl, Spasmolyt |
1993.12.28 | 원료 수입/제조 판매 | |
| 원료 수입 | Thioctacid, Azeptin, Cormelian |
2003.12.11 | 원료 수입/제조 판매 | ||
| 제품 수입 | Dylastine | 2018.05.25 | 수입 판매 중 | ||
| 제품 수입 | Sebivo | 2018.10.26 | 수입 판매 중 | ||
| Baxter (독일) |
제품 수입 | Holoxan Endoxan, Uromitexan |
2013.01.01 | 수입 판매 중 | |
| Pierre Fabre (프랑스) |
제품 수입 원료 수입 |
Navelbine Ixel |
2014.01.01 | 수입 판매 중 | |
| Ferrer (스페인) |
제품 수입 원료 수입 |
Dermofix | 1993.06.02 | 제조 판매 중 | |
| 원료 수입 | Somazina | 2002.03.04 | 제조 판매 중 | ||
| 원료 수입 | Nadixa | 2004.05.17 | 제조 판매 중 | ||
| 제품 수입 |
Repavar Pielato Melagyn |
2016.06.30 | 공급 중단 | ||
| 제품 수입 | Ozanex | 2020.01.10 | 제조 판매 중 | ||
|
Ojer (스페인) |
제품 수입 | Lipovir | 2018.01.29 | 개발 논의 중 | |
| Desitin (독일) |
원료 수입 | Orfil | 1978.03.15 | 제조 판매 중 | |
| 원료 수입 | Timonil | 1994.08.31 | 제조 판매 중 | ||
| Sumitomo Pharma Co., Ltd. (일본) |
원료 수입 | Lonasen (Blonanserin) | 2005.02.28 | 제조 판매 중 | |
| 상표권 계약 | Cetapril | 2015.02.27 | 판매 중단 | ||
| 반제품 수입 | Latuda (Lurasidone HCl) | 2017.04.05 | 제조 판매 중 | ||
| Eurodrug (네덜란드) |
원료 수입 | Fexadin | 1986.07.29 | 제조 판매 중 | |
| Asima | 2000.03.24 | 제조 판매 중 | |||
| 반제품 수입 | Panbesy | 2019.06.01 | 반제품 수입 판매 중 | ||
| Kalbe International Pte. Ltd. (싱가포르) |
제품 수출 | 덱시드정 | 2016.03.03 | 제조 판매 중 (완제 수출) |
|
| 연구개발 | Melior Pharmaceuticals, Inc (미국) |
기술 반환, 수익 배분 및 이전 | MLR-1023 | 2023.12.21 | Biodexa에서 임상2a상 진행 중 (캐나다) |
| Contera Pharma A/S (덴마크) |
기술도입 | JM-010 | 2014.12.12 | 임상 2상 종료 (미국) |
| (자료 : 당사 분기보고서) |
당사는 현재 계약을 체결중인 상대방과 우호적인 협력 관계를 유지하고 있으며 이러한 신뢰관계가 향후에도 지속될 것으로 당사는 전망하고 있습니다. 다만 모든 계약에는 불확실성이 존재하며 안정적인 원재료 수급이 절대적으로 중요한 제약 산업에서 예상치 못한 변수로 인해 적절한 원재료 도입에 차질이 생기거나 기술도입/이전 등과 관련하여 분쟁이 발생할 경우 당사의 재무건정성 및 수익성이 악화될 가능성이 존재하는 점 투자자 분들 께서는 유의하시기 바랍니다.
(주5) 정정 전
(중략)
공정거래법 제18조 제2항 제2호에 따르면 지주회사는 자회사 지분율 규제(상장30%, 비상장50% 이상)가 적용되며, 이에 미달하는 자회사 지분을 자회사 지분율 규제 이상으로 추가 취득 또는 처분하여야 합니다. 다만 지주회사로 전환하거나 설립될 당시에 자회사의 주식을 자회사 주식 보유기준 미만으로 소유하고 있는 경우에 한해 지주회사로 전환하거나 설립된 날부터 2년 이내 지분율 요건을 충족할 수 있도록 유예기간을 규정하고 있습니다. 이에 OCI홀딩스는 지주회사 전환일인 2023년 9월 22일 부터 2년이 도래하는 2025년 9월 22일까지 해당 지분율 요건을 충족해야 합니다. 만약 해당 규정을 준수하지 못할 경우 공정거래위원회로부터 공정거래법 제37조 제1항에 따른 주식의 전부 또는 일부의 처분 등의 시정명령 또는 공정거래법 제38조 제3항 제2호에 따라 과징금이 부여될 수 있으며, 이로 인해 당사 최대주주인 OCI홀딩스의 평판 악화 또는 재무적 손실이 발생할 수 있습니다. 다만, 공정거래법 제18조 제6항에 따라 경제 여건의 변화, 주식 처분금지 계약, 사업의 현저한 손실 등의 사유로 주식의 취득이 어려울 경우 공정거래위원회의 승인을 받아 유예기간을 2년 추가로 연장할 수 있습니다. 아울러 금번 유상증자에서 당사 최대주주인 OCI홀딩스가 배정받은 증서 및 2대,3대 주주의 증서까지 매입 후 120% 청약 시 확보하게 될 지분율은 약 16.81%로 당사 최대주주인 OCI홀딩스가 지분율 요건을 충족하기 위해서는 추가 지분매입 및 제3자배정유상증자 등이 수반될 수 있으며 이 경우 당사 주식 가격 변동성이 높아질 수 있으니 투자자 분들께서는 유의하시기 바랍니다.
(중략)
한편 당사는 당사 최대주주인 OCI홀딩스 포함 특수관계인과 다양한 매출 매입활동을 진행하고 있습니다. 당사 외형규모 고려 시 해당 매출 매입금액이 유의적인 수준은 아니나, 향후 특수관계자 거래 규모가 증가할 경우 거래의 적정성에 대해 공정거래위원회 및 세무당국의 조사가 진행될 수 있는 점 참고부탁드립니다.
| [ 당사 특수관계자 현황(자회사) ] |
| 기업명 | 지분율(%) | |
|---|---|---|
| 2024년말 | 2023년말 | |
| Contera Pharma A/S | 99.33 | 74.14 |
| 부광메디카(주) | 100 | 100 |
| 다이나세라퓨틱스(주) | - | 98.84 |
| ProteKt Therapeutics | 97.24 | 97.44 |
| JaguAHR Therapeutics | 75.02 | 65 |
| (자료 : 당사 사업보고서) |
| [당사 특수관계자 현황(기타특수관계자) ] |
| 구 분 | 2024년말 | 2023년말 |
|---|---|---|
| 공동기업 | - | JaguAHR Therapeutics |
| 관계기업 | 덴탈플랫폼투자조합제1호 | 덴탈플랫폼투자조합제1호 |
| - | 에이치 델타 사모투자합자회사 | |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | OCI홀딩스 주식회사 |
| (주)디씨알이 | (주)디씨알이 | |
| 오씨아이드림(주) | 오씨아이드림(주) | |
| OCI(주) | OCI(주) | |
| OCI정보통신(주) | - |
| (자료 : 당사 사업보고서) |
| [당사 특수관계자 매출매입현황(2024년) ] |
| (단위: 원) |
| 구 분 | 기업명 | 2024년 | |
|---|---|---|---|
| 매출 등 | 매입 등 | ||
| 종속기업 | Contera Pharma A/S | 89,255,800 | - |
| 부광메디카(주) | 84,475,334 | 2,591,884,310 | |
| 다이나세라퓨틱스(주) | 15,538,000 | - | |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | 66,552,043 | 34,748,485 |
| (주)디씨알이 | 15,415,355 | - | |
| 오씨아이드림(주) | 17,064,000 | 91,544 | |
| OCI(주) | 24,862,479 | 45,491,982 | |
| OCI정보통신 | - | 277,897,400 | |
| 합 계 | 313,163,011 | 2,950,113,721 | |
| (자료 : 당사 사업보고서) |
| [당사 특수관계자 매출매입현황(2023년)] |
| (단위: 원) |
| 구 분 | 기업명 | 2023년 | |
|---|---|---|---|
| 매출 등 | 매입 등 | ||
| 종속기업 | Contera Pharma A/S | 82,217,651 | - |
| 부광메디카(주) | 39,167,800 | 3,557,332,800 | |
| 다이나세라퓨틱스(주) | 36,162,400 | - | |
| 공동기업 | 비앤오바이오(주) | 3,952,000 | - |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | 94,885,955 | 49,643,306 |
| (주)디씨알이 | 13,179,091 | - | |
| 오씨아이드림(주) | 4,852,900 | 122,448 | |
| OCI(주) | 10,944,631 | 57,905,727 | |
| 합 계 | 285,362,428 | 3,665,004,281 | |
| (자료 : 당사 사업보고서) |
(주5) 정정 후
(중략)
공정거래법 제18조 제2항 제2호에 따르면 지주회사는 자회사 지분율 규제(상장30%, 비상장50% 이상)가 적용되며, 이에 미달하는 자회사 지분을 자회사 지분율 규제 이상으로 추가 취득 또는 처분하여야 합니다. 다만 지주회사로 전환하거나 설립될 당시에 자회사의 주식을 자회사 주식 보유기준 미만으로 소유하고 있는 경우에 한해 지주회사로 전환하거나 설립된 날부터 2년 이내 지분율 요건을 충족할 수 있도록 유예기간을 규정하고 있습니다. 이에 OCI홀딩스는 지주회사 전환일인 2023년 9월 22일부터 2년이 도래하는 2025년 9월 22일까지 해당 지분율 요건을 충족해야 합니다. 만약 해당 규정을 준수하지 못할 경우 공정거래위원회로부터 공정거래법 제37조 제1항에 따른 주식의 전부 또는 일부의 처분 등의 시정명령 또는 공정거래법 제38조 제3항 제2호에 따라 과징금이 부여될 수 있으며, 이로 인해 당사 최대주주인 OCI홀딩스의 평판 악화 또는 재무적 손실이 발생할 수 있습니다. 다만, 공정거래법 제18조 제6항에 따라 경제 여건의 변화, 주식 처분금지 계약, 사업의 현저한 손실 등의 사유로 주식의 취득이 어려울 경우 공정거래위원회의 승인을 받아 유예기간을 2년 추가로 연장할 수 있습니다. 아울러 금번 유상증자에서 당사 최대주주인 OCI홀딩스가 배정받은 증서 및 2대,3대 주주의 증서까지 매입 후 120% 청약 시 확보하게 될 지분율은 약 16.81%로 당사 최대주주인 OCI홀딩스가 지분율 요건을 충족하기 위해서는 추가 지분매입 및 제3자배정유상증자 등이 수반될 수 있습니다. OCI홀딩스(주)가 당사 기존 주주의 신주인수권 증서를 매입하게 될 경우 자본시장법 제173조의3에 따라 신주인수권증서 거래 개시일의 30일 전, 거래계획을 사전 공시할 예정이며 현재 예상되는 사전 공시일은 2025년 05월 30일입니다. 이 경우 당사 주식 가격 변동성이 높아질 수 있으니 투자자 분들께서는 유의하시기 바랍니다.
|
※ 관련법규 <독점규제 및 공정거래에 관한 법률> 제18조(지주회사 등의 행위제한 등) ② 지주회사는 다음 각 호의 어느 하나에 해당하는 행위를 하여서는 아니 된다. 1. 자본총액(대차대조표상의 자산총액에서 부채액을 뺀 금액을 말한다. 이하 같다)의 2배를 초과하는 부채액을 보유하는 행위. 다만, 지주회사로 전환하거나 설립될 당시에 자본총액의 2배를 초과하는 부채액을 보유하고 있을 때에는 지주회사로 전환하거나 설립된 날부터 2년간은 자본총액의 2배를 초과하는 부채액을 보유할 수 있다. 2. 자회사의 주식을 그 자회사 발행주식총수의 100분의 50[자회사가 상장법인인 경우, 주식 소유의 분산요건 등 상장요건이 「자본시장과 금융투자업에 관한 법률」에 따른 증권시장으로서 대통령령으로 정하는 국내 증권시장의 상장요건에 상당하는 것으로 공정거래위원회가 고시하는 국외 증권거래소에 상장된 법인(이하 “국외상장법인”이라 한다)인 경우 또는 공동출자법인인 경우에는 100분의 30으로 하고, 벤처지주회사의 자회사인 경우에는 100분의 20으로 한다. 이하 이 조에서 “자회사주식보유기준”이라 한다] 미만으로 소유하는 행위. 다만, 다음 각 목의 어느 하나에 해당하는 사유로 자회사주식보유기준에 미달하게 된 경우는 제외한다. 가. 지주회사로 전환하거나 설립될 당시에 자회사의 주식을 자회사주식보유기준 미만으로 소유하고 있는 경우로서 지주회사로 전환하거나 설립된 날부터 2년 이내인 경우 ⑥ 제2항제1호 단서, 같은 항 제2호가목, 같은 항 제3호가목, 같은 항 제4호 단서, 같은 항 제5호 단서, 제3항제1호가목, 같은 항 제2호가목, 같은 항 제3호 단서, 제4항제1호 및 제5항제1호를 적용할 때 각 해당 규정의 유예기간은 주식가격의 급격한 변동 등 경제여건의 변화, 주식처분금지계약, 사업의 현저한 손실 또는 그 밖의 사유로 부채액을 감소시키거나 주식의 취득·처분 등이 곤란한 경우 공정거래위원회의 승인을 받아 2년을 연장할 수 있다. 제37조(시정조치 등) 1. 해당 행위의 중지 2. 주식의 전부 또는 일부의 처분 3. 임원의 사임 4. 영업의 양도 5. 채무보증의 취소 6. 시정명령을 받은 사실의 공표 7. 공시의무의 이행 또는 공시내용의 정정 8. 그 밖에 법 위반상태를 시정하기 위하여 필요한 조치 제38조(과징금) ③ 공정거래위원회는 제18조제2항부터 제5항까지, 제20조제2항 또는 제3항의 규정을 위반한 자에게 다음 각 호의 구분에 따른 금액에 100분의 20을 곱한 금액을 초과하지 아니하는 범위에서 과징금을 부과할 수 있다. 1. 제18조제2항제1호를 위반한 경우: 대통령령으로 정하는 재무상태표(이하 이 항에서 “기준재무상태표”라 한다)상 자본총액의 2배를 초과한 부채액 2. 제18조제2항제2호를 위반한 경우: 해당 자회사 주식의 기준재무상태표상 장부가액의 합계액에 다음 각 목의 비율에서 그 자회사 주식의 소유비율을 뺀 비율을 곱한 금액을 그 자회사 주식의 소유비율로 나누어 산출한 금액 가. 해당 자회사가 상장법인 또는 국외상장법인이거나 공동출자법인인 경우에는 100분의 30 나. 벤처지주회사의 자회사인 경우에는 100분의 20 다. 가목 및 나목에 해당하지 아니하는 경우에는 100분의 50 ① 주권상장법인의 임원 또는 주요주주(대통령령으로 정하는 자는 제외한다)가 특정증권등의 매매, 그 밖의 거래(상속ㆍ주식배당 등 대통령령으로 정하는 부득이한 사유로 하는 매매, 그 밖의 거래를 제외한다. 이하 이 조 및 제429조에서 “거래등”이라 한다)를 하려는 때에는 거래목적, 거래가격, 거래수량, 거래기간 등 대통령령으로 정하는 사항(이하 “거래계획”이라 한다)을 그 거래기간의 개시일 전 30일 이상 90일 이내의 대통령령으로 정하는 기간까지 증권선물위원회와 거래소에 각각 보고하여야 한다. 다만, 거래계획의 거래수량 및 거래금액과 그 거래계획의 개시일 기준 과거 6개월간 거래수량 및 거래금액을 합산하여 대통령령으로 정하는 규모 미만인 경우에는 그러하지 아니하다. ② 제1항에 따라 거래계획을 보고한 자(이하 이 조에서 “거래계획 보고자”라 한다)는 그 거래계획을 보고한 때부터 그 거래계획에 따른 거래기간의 종료일까지는 새로운 거래계획을 보고하여서는 아니 된다. ③ 거래계획 보고자는 그 거래계획에 따라 특정증권등의 거래등을 하여야 한다. 다만, 거래 당시의 시장 상황 등을 반영하여 필요한 경우에 한정하여 거래금액의 100분의 30 이하의 비율로서 대통령령으로 정하는 바에 따라 거래계획과 달리 거래등을 할 수 있다. ④ 거래계획 보고자는 사망, 파산, 시장변동성 확대로 과도한 손실이 예상되는 경우 등 대통령령으로 정하는 부득이한 사유가 발생하는 때에는 대통령령으로 정하는 바에 따라 증권선물위원회와 거래소에 보고한 후 그 거래계획을 철회할 수 있다. ⑤ 증권선물위원회와 거래소는 제1항에 따라 보고된 거래계획(제4항에 따라 철회된 경우를 포함한다)을 3년간 갖추어 두고, 인터넷 홈페이지 등을 이용하여 공시하여야 한다. ⑥ 제1항부터 제5항까지에서 규정한 사항 외에 거래계획의 보고 등에 필요한 사항은 대통령령으로 정한다. |
한편 당사는 당사 최대주주인 OCI홀딩스 포함 특수관계인과 다양한 매출 매입활동을 진행하고 있습니다. 당사 외형규모 고려 시 해당 매출 매입금액이 유의적인 수준은 아니나, 향후 특수관계자 거래 규모가 증가할 경우 거래의 적정성에 대해 공정거래위원회 및 세무당국의 조사가 진행될 수 있는 점 참고부탁드립니다.
| [ 당사 특수관계자 현황(자회사) ] |
| 기업명 | 지분율(%) | |
|---|---|---|
| 2025년 1분기말 | 2024년말 | |
| Contera Pharma A/S | 99.33 | 99.33 |
| 부광메디카(주) | 100 | 100 |
| ProteKt Therapeutics | 97.24 | 97.24 |
| JaguAHR Therapeutics | 75.02 | 75.02 |
| (자료 : 당사 사업보고서 및 분기보고서) |
| [당사 특수관계자 현황(기타특수관계자) ] |
| 구 분 | 2025년 1분기말 | 2024년말 |
|---|---|---|
| 공동기업 | - | - |
| 관계기업 | 덴탈플랫폼투자조합제1호 | 덴탈플랫폼투자조합제1호 |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | OCI홀딩스 주식회사 |
| (주)디씨알이 | (주)디씨알이 | |
| 오씨아이드림(주) | 오씨아이드림(주) | |
| OCI(주) | OCI(주) | |
| OCI정보통신 | OCI정보통신(주) |
| (자료 : 당사 사업보고서 및 분기보고서) |
| [당사 특수관계자 매출매입현황(2025년 1분기)] |
| (단위: 원) |
| 구 분 | 기업명 | 2025년 1분기 | |
|---|---|---|---|
| 매출 등 | 매입 등 | ||
| 종속기업 | 부광메디카(주) | 80,069,740 | 331,530,400 |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | 16,646,721 | 5,805,473 |
| (주)디씨알이 | 1,883,182 | - | |
| 오씨아이드림㈜ | 2,486,000 | - | |
| OCI㈜ | 18,014,997 | 19,200,000 | |
| OCI정보통신 | - | 153,965,400 | |
| 합 계 | 119,100,640 | 510,501,273 | |
| (자료 : 당사 분기보고서) |
| [당사 특수관계자 매출매입현황(2024년 1분기)] |
| (단위: 원) |
| 구 분 | 기업명 | 2024년 1분기 | |
|---|---|---|---|
| 매출 등 | 매입 등 | ||
| 종속기업 |
Contera Pharma A/S |
19,989,800 | - |
| 부광메디카(주) | 13,847,214 | 327,211,000 | |
| 다이나세라퓨틱스(주) | 5,904,000 | - | |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | 17,823,292 | 9,333,026 |
| (주)디씨알이 | 5,525,818 | - | |
| 오씨아이드림㈜ | 4,503,000 | 63,908 | |
| OCI㈜ | 9,901,472 | 6,931,982 | |
| 합 계 | 77,494,596 | 343,539,916 | |
| (자료 : 당사 분기보고서) |
(주6) 정정 전
당사는 1960년 10월 17일에 의약품의 제조 및 판매를 목적으로 설립되었습니다. 현재 의약품, 건강기능식품, 의약외품 등을 주요 사업으로 영위하고 있으며, 주요 제품으로는 훼로바, 레가론, 덱시드, 치옥타시드, 씬지로이드 등이 있습니다. 한편, Global Open Innovation 전략의 일환으로 해외 자회사 및 제휴 업체와 협력하여 파킨슨병, 조현병 등 중추신경계(CNS) 질환 치료제와 면역항암제, 신경염증성 질환 치료제 등의 개발도 추진하고 있습니다.
당사의 주요 제품별 매출 현황은 다음과 같습니다.
| [ 당사 제품군별 매출현황 ] |
| (단위: 백만원) |
| 매출 | 품 목 | 구체적용도 | 주요상표등 | 2024 | 2023 | 2022 | 2021 |
| 제품 | 씬지로이드 | 갑상선 부갑상선 호르몬제 | 씬지로이드정 | 10,353 | 7,373 | 6,987 | 8,487 |
| 덱시드정 | 당뇨병성 신경병증 치료제 | 덱시드정 | 10,704 | - | 21,100 | 18,466 | |
| 치옥타시드 | 당뇨병성 신경병증 치료제 | 치옥타시드정 | 10,696 | 5,518 | 11,857 | 12,821 | |
| 훼로바 | 빈혈치료제 | 훼로바유서방정 | 17,415 | 13,424 | 11,801 | 13,586 | |
| 레가론 | 간질환치료제 | 레가론캡슐140 | 13,171 | 4,402 | 17,714 | 15,985 | |
| 타세놀 | 해열,진통,소염제 | 타세놀정 | 6,076 | 8,196 | 9,437 | 9,482 | |
| 헥사메딘액 | 구내염증완화제 | 헥사메딘액 | 3,939 | 4,200 | 5,627 | 4,510 | |
| 오르필 | 간질치료제 | 오르필서방정 | 3,882 | 3,920 | 6,416 | 6,240 | |
| 액시마 | 기관지확장제 | 액시마정 | 4,540 | 3,907 | 4,683 | 4,492 | |
| 플루닐 | 해독제 | 플루닐주사 | - | 3,205 | - | - | |
| 기타 | - | - | 64,434 | 49,680 | 64,102 | 56,971 | |
| 소 계 | - | - | 145,210 | 103,825 | 159,724 | 151,040 | |
| 상품 | 16,993 | 25,510 | 36,991 | 37,385 | |||
| 수출/기타 | 481 | 150 | 217 | 63 | |||
| 단순합계 | 162,684 | 129,485 | 196,932 | 188,488 | |||
| 내부거래제거 | (2,597) | (3,557) | (6,023) | (5,997) | |||
| 매출액 | 160,087 | 125,928 | 190,909 | 182,491 | |||
| (자료 : 당사 사업보고서) |
당사는 매출액 기준 상위 10개 제품을 개별 공시하고 있으며, 이외 제품은 '기타'로 구분하여 표시하고 있습니다. 매출 구성은 제품 매출이 절대적인 비중을 차지하고 있으며, 원가율이 높은 상품 매출은 점진적으로 감소하는 추세를 보이고 있습니다. 이는 수익성 개선을 목표로 상품 비중을 전략적으로 축소하고자 하는 당사의 경영방침에 따른 결과입니다. 또한, 상위 10개 제품군은 연도별로 안정적인 시장 점유율을 유지하고 있으나, 덱시드정은 생산능력 부족에 따른 타 품목 공급부족 해소를 위한 유통재고 관리로 인해 매출이 감소하여 상위 10개 제품에서 제외되었으며, 이에 따라 '기타' 항목으로 분류되어 있습니다.
한편, 당사의 별도 기준 요약손익계산서는 다음과 같습니다.
| [ 당사 요약 별도손익계산서] |
| (단위: 백만원) |
| 구 분 | 2024 | 2023 | 2022 | 2021 |
|---|---|---|---|---|
| 매출액 | 157,607 | 125,176 | 190,339 | 181,631 |
| 매출원가 | 83,886 | 79,039 | 111,793 | 107,184 |
| 매출총이익 | 73,721 | 46,137 | 78,546 | 74,447 |
| 판매비와관리비 | 46,802 | 47,826 | 54,222 | 46,335 |
| 경상연구개발비 | 9,915 | 15,483 | 12,002 | 14,948 |
| 영업이익(손실) | 17,004 | (17,173) | 12,322 | 13,163 |
| 기타수익 | 5,971 | 478 | 619 | 3,763 |
| 기타비용 | 66,441 | 6,514 | 783 | 3,449 |
| 금융수익 | 5,288 | 3,257 | 3,270 | 4,258 |
| 금융비용 | 14,232 | 3,245 | 8,559 | 8,186 |
| 법인세비용차감전순이익(손실) | (52,410) | (23,196) | 6,870 | 9,550 |
| 법인세비용(수익) | 3,200 | (4,103) | 4,828 | 7,112 |
| 당기순이익(손실) | (55,610) | (19,093) | 2,042 | 2,438 |
| 매출총이익율 | 46.78% | 36.86% | 41.27% | 40.99% |
| 경상연구개발비율 | 6.29% | 12.37% | 6.31% | 8.23% |
| 영업이익율 | 10.79% | -13.72% | 6.47% | 7.25% |
| 순이익율 | -35.28% | -15.25% | 1.07% | 1.34% |
| (자료 : 당사 사업보고서) |
당사의 별도 기준 매출액은 2021년 1,816억 원에서 2022년 1,903억 원으로 4.79% 증가하였으나, 2023년에는 1,252억 원으로 34.24% 감소하였습니다. 이는 2023년 당사가 내부 조직을 개편하고 도매상 중심의 유통구조 재정비를 통하여 채권회수에 주력한 결과 매출채권 약 62.2% 감소 하였고, 효율성이 낮은 일부 도매상 정리를 통하여 전체 도매상 수 약 13.5% 감소하는 등 질적 성장을 위한 경영 전략을 추진한 데에 따른 결과입니다. 이 과정에서 제품의 매출 비중이 일시적으로 감소하였으며, 시중 재고 수준이 높은 일부 품목의 출하를 축소함에 따라 전체 매출액이 감소하였습니다. 이에 따라 영업이익도 2022년 123억 원에서 2023년에는 172억 원의 영업손실로 전환되었습니다. 다만, 경영구조 개편의 효과가 2024년부터 본격적으로 나타나면서, 당사의 2024년 매출액은 전년 대비 25.91% 증가한 1,576억 원을 기록하였으며, 영업이익 또한 170억 원으로 흑자 전환에 성공하였습니다. 아울러 공헌이익 기반의 품목 재구성을 통한 매출 구조 개선과 구매원가 절감 전략을 지속적으로 추진한 결과, 2024년 영업이익률은 10.79%를 기록하며 최근 4개년 중 가장 높은 수익성을 달성하였습니다. 한편, 당기순이익은 종속기업 투자주식의 손상차손 반영에 따라 기타비용이 증가함으로써 적자를 기록하였습니다. 손상차손 관련 상세 내용은 회사위험-라. 자회사 손상차손 관련 위험 에서 확인하실 수 있습니다.
당사의 연결 기준 요약손익계산서는 다음과 같습니다.
| [ 당사 요약 연결손익계산서] |
| (단위: 백만원) |
| 구 분 | 2024 | 2023 | 2022 | 2021 |
|---|---|---|---|---|
| 매출액 | 160,087 | 125,928 | 190,909 | 182,491 |
| 매출원가 | 85,744 | 78,855 | 111,481 | 106,733 |
| 매출총이익 | 74,343 | 47,074 | 79,429 | 75,758 |
| 판매비와관리비 | 49,295 | 50,019 | 55,385 | 47,671 |
| 경상연구개발비 | 23,430 | 34,551 | 24,274 | 22,465 |
| 영업이익(손실) | 1,618 | (37,497) | (231) | 5,622 |
| 기타수익 | 10,097 | 2,300 | 569 | 439 |
| 기타비용 | 13,929 | 2,002 | 630 | 185 |
| 금융수익 | 5,680 | 3,846 | 3,450 | 4,265 |
| 금융비용 | 7,077 | 5,315 | 4,249 | 4,992 |
| 지분법이익(손실) | 641 | (901) | 59 | (1,361) |
| 법인세비용차감전순이익(손실) | (2,970) | (39,569) | (1,033) | 3,787 |
| 법인세비용(수익) | 489 | (5,163) | 3,216 | 6,584 |
| 당기순이익(손실) | (3,459) | (34,407) | (4,249) | (2,797) |
| 매출총이익율 | 46.44% | 37.38% | 41.61% | 41.51% |
| 경상연구개발비율 | 14.64% | 27.44% | 12.72% | 12.31% |
| 영업이익율 | 1.01% | -29.78% | -0.12% | 3.08% |
| 순이익율 | -2.16% | -27.32% | -2.23% | -1.53% |
| (자료 : 당사 사업보고서) |
당사의 자회사는 주로 임상시험 등 연구개발 활동을 수행하고 있어, 제한적인 매출만을 창출하고 있습니다. 이에 따라 연결 기준 매출액은 별도 기준 매출액과 유사한 수준을 유지하고 있습니다. 그러나 자회사의 임상개발 비용 등으로 인해 연구개발비가 연간 70억 원에서 190억 원 수준으로 발생하고 있으며, 이로 인해 연결 기준 수익성은 별도 기준에 비해 열위에 있는 모습입니다. 2023년에는 당사의 경영구조 개편에 따른 매출 감소와 더불어 자회사의 JM-010 임상 관련 비용이 크게 증가하면서 375억 원의 영업손실을 기록하였습니다. 다만, 2024년에는 해당 임상이 중단되었고, 전년도 경영구조 개편의 효과가 온전히 반영됨에 따라 영업이익 16억 원을 기록하며 흑자 전환에 성공하였습니다.
당사는 향후 연결 및 별도 기준 모두에서 수익성이 점진적으로 개선될 것으로 전망하고 있으며, 2023년과 같은 대규모 영업손실이 재차 발생할 가능성은 제한적이라고 판단하고 있습니다. 다만, 당사가 속한 제약업종은 식품의약품안전처 등 규제기관의 추가 규제, 임상시험 진행에 따른 추가 연구개발비 발생, 경쟁 제품 출시 등의 예상치 못한 변수에 지속적으로 노출되어 있습니다. 이로 인해 당사의 매출이 감소하거나 수익성이 악화되는 등 영업 환경에 부정적인 영향을 미칠 수 있으므로, 투자자 여러분께서는 이 점을 유의하여 주시기 바랍니다.
(주6) 정정 후
당사는 1960년 10월 17일에 의약품의 제조 및 판매를 목적으로 설립되었습니다. 현재 의약품, 건강기능식품, 의약외품 등을 주요 사업으로 영위하고 있으며, 주요 제품으로는 훼로바, 레가론, 덱시드, 치옥타시드, 씬지로이드 등이 있습니다. 한편, Global Open Innovation 전략의 일환으로 해외 자회사 및 제휴 업체와 협력하여 파킨슨병, 조현병 등 중추신경계(CNS) 질환 치료제와 면역항암제, 신경염증성 질환 치료제 등의 개발도 추진하고 있습니다.
당사의 주요 제품별 매출 현황은 다음과 같습니다.
| [ 당사 제품군별 매출현황 ] |
| (단위: 백만원) |
| 매출 | 품 목 | 구체적용도 | 주요상표등 | 2025년 1분기 |
2024 | 2023 | 2022 | 2021 |
| 제품 | 씬지로이드 | 갑상선 부갑상선 호르몬제 | 씬지로이드정 | 2,168 | 10,353 | 7,373 | 6,987 | 8,487 |
| 덱시드정 | 당뇨병성 신경병증 치료제 | 덱시드정 | 4,423 | 10,704 | - | 21,100 | 18,466 | |
| 치옥타시드 | 당뇨병성 신경병증 치료제 | 치옥타시드정 | 3,317 | 10,696 | 5,518 | 11,857 | 12,821 | |
| 훼로바 | 빈혈치료제 | 훼로바유서방정 | 3,525 | 17,415 | 13,424 | 11,801 | 13,586 | |
| 레가론 | 간질환치료제 | 레가론캡슐140 | 3,548 | 13,171 | 4,402 | 17,714 | 15,985 | |
| 타세놀 | 해열,진통,소염제 | 타세놀정 | 1,958 | 6,076 | 8,196 | 9,437 | 9,482 | |
| 헥사메딘액 | 구내염증완화제 | 헥사메딘액 | 1,109 | 3,939 | 4,200 | 5,627 | 4,510 | |
| 오르필 | 간질치료제 | 오르필서방정 | - | 3,882 | 3,920 | 6,416 | 6,240 | |
| 액시마 | 기관지확장제 | 액시마정 | 1,579 | 4,540 | 3,907 | 4,683 | 4,492 | |
| 플루닐 | 해독제 | 플루닐주사 | - | - | 3,205 | - | - | |
| 기타 | - | - | 19,246 | 64,434 | 49,680 | 64,102 | 56,971 | |
| 소 계 | - | - | 40,873 | 145,210 | 103,825 | 159,724 | 151,040 | |
| 상품 | 7,280 | 16,993 | 25,510 | 36,991 | 37,385 | |||
| 수출/기타 | 44 | 481 | 150 | 217 | 63 | |||
| 단순합계 | 48,197 | 162,684 | 129,485 | 196,932 | 188,488 | |||
| 내부거래제거 | (391) | (2,597) | (3,557) | (6,023) | (5,997) | |||
| 매출액 | 47,806 | 160,087 | 125,928 | 190,909 | 182,491 | |||
| (자료 : 당사 사업보고서 및 분기보고서) |
당사는 매출액 기준 상위 10개 제품을 개별 공시하고 있으며, 이외 제품은 '기타'로 구분하여 표시하고 있습니다. 매출 구성은 제품 매출이 절대적인 비중을 차지하고 있으며, 원가율이 높은 상품 매출은 점진적으로 감소하는 추세를 보이고 있습니다. 이는 수익성 개선을 목표로 상품 비중을 전략적으로 축소하고자 하는 당사의 경영방침에 따른 결과입니다. 또한, 상위 10개 제품군은 연도별로 안정적인 시장 점유율을 유지하고 있으나, 2023년의 덱시드정, 2025년 1분기의 오르필 및 플루닐 등은 생산능력 부족에 따른 타 품목 공급부족 해소를 위한 유통재고 관리로 인해 매출이 감소하여 상위 10개 제품에서 제외되었으며, 이에 따라 '기타' 항목으로 분류되어 있습니다.
한편, 당사의 별도 기준 요약손익계산서는 다음과 같습니다.
| [ 당사 요약 별도손익계산서] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 |
|---|---|---|---|---|---|---|
| 매출액 | 43,850 | 34,029 | 157,607 | 125,176 | 190,339 | 181,631 |
| 매출원가 | 23,292 | 18,554 | 83,886 | 79,039 | 111,793 | 107,184 |
| 매출총이익 | 20,558 | 15,475 | 73,721 | 46,137 | 78,546 | 74,447 |
| 판매비와관리비 | 12,677 | 10,704 | 46,802 | 47,826 | 54,222 | 46,335 |
| 경상연구개발비 | 1,946 | 2,711 | 9,915 | 15,483 | 12,002 | 14,948 |
| 영업이익(손실) | 5,935 | 2,060 | 17,004 | (17,173) | 12,322 | 13,163 |
| 기타수익 | 823 | 93 | 5,971 | 478 | 619 | 3,763 |
| 기타비용 | 83 | 453 | 66,441 | 6,514 | 783 | 3,449 |
| 금융수익 | 1,338 | 1,655 | 5,288 | 3,257 | 3,270 | 4,258 |
| 금융비용 | 5,428 | 953 | 14,232 | 3,245 | 8,559 | 8,186 |
| 법인세비용차감전순이익(손실) | 2,585 | 2,403 | (52,410) | (23,196) | 6,870 | 9,550 |
| 법인세비용(수익) | (208) | 419 | 3,200 | (4,103) | 4,828 | 7,112 |
| 당기순이익(손실) | 2,794 | 1,983 | (55,610) | (19,093) | 2,042 | 2,438 |
| 매출총이익율 | 46.88% | 45.48% | 46.78% | 36.86% | 41.27% | 40.99% |
| 경상연구개발비율 | 4.44% | 7.97% | 6.29% | 12.37% | 6.31% | 8.23% |
| 영업이익율 | 13.53% | 6.05% | 10.79% | -13.72% | 6.47% | 7.25% |
| 순이익율 | 6.37% | 5.83% | -35.28% | -15.25% | 1.07% | 1.34% |
| (자료 : 당사 사업보고서 및 분기보고서) |
당사의 별도 기준 매출액은 2021년 1,816억 원에서 2022년 1,903억 원으로 4.79% 증가하였으나, 2023년에는 1,252억 원으로 34.24% 감소하였습니다. 이는 2023년 당사가 내부 조직을 개편하고 도매상 중심의 유통구조 재정비를 통하여 채권회수에 주력한 결과 매출채권 약 62.2% 감소 하였고, 효율성이 낮은 일부 도매상 정리를 통하여 전체 도매상 수 약 13.5% 감소하는 등 질적 성장을 위한 경영 전략을 추진한 데에 따른 결과입니다. 이 과정에서 제품의 매출 비중이 일시적으로 감소하였으며, 시중 재고 수준이 높은 일부 품목의 출하를 축소함에 따라 전체 매출액이 감소하였습니다. 이에 따라 영업이익도 2022년 123억 원에서 2023년에는 172억 원의 영업손실로 전환되었습니다. 다만, 경영구조 개편의 효과가 2024년부터 본격적으로 나타나면서, 당사의 2024년 매출액은 전년 대비 25.91% 증가한 1,576억 원을 기록하였으며, 영업이익 또한 170억 원으로 흑자 전환에 성공하였습니다. 아울러 공헌이익 기반의 품목 재구성을 통한 매출 구조 개선과 구매원가 절감 전략을 지속적으로 추진한 결과, 2024년 영업이익률은 10.79%를 기록하며 최근 4개년 중 가장 높은 수익성을 달성하였습니다. 한편, 당기순이익은 종속기업 투자주식의 손상차손 반영에 따라 기타비용이 증가함으로써 적자를 기록하였습니다. 손상차손 관련 상세 내용은 회사위험-라. 자회사 손상차손 관련 위험 에서 확인하실 수 있습니다.
2025년 1분기 당사의 별도 기준 매출액은 439억원, 영업이익은 59억원을 기록하며 전년 동기 대비 각각 28.9%, 188.1% 상승하였습니다. 당뇨병성 신경병증 치료제 ‘덱시드’와 ‘치옥타시드’가 전년 동기 대비 234%의 매출 성장을 보이며 실적 반등과 수익성 회복을 이끌었습니다. 또한, 상급종합병원 110개소에서 당사의 항정신병 신약 '라투다정'의 처방이 개시되었고 의원급 의료기관에서도 50%이상 커버리지를 확보하는 등 안정적으로 시장에 안착하며 실적 개선에 기여하였습니다.
당사의 연결 기준 요약손익계산서는 다음과 같습니다.
| [ 당사 요약 연결손익계산서] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 |
|---|---|---|---|---|---|---|
| 매출액 | 47,806 | 34,393 | 160,087 | 125,928 | 190,909 | 182,491 |
| 매출원가 | 26,909 | 18,730 | 85,744 | 78,855 | 111,481 | 106,733 |
| 매출총이익 | 20,897 | 15,664 | 74,343 | 47,074 | 79,429 | 75,758 |
| 판매비와관리비 | 13,431 | 11,236 | 49,295 | 50,019 | 55,385 | 47,671 |
| 경상연구개발비 | 4,452 | 6,056 | 23,430 | 34,551 | 24,274 | 22,465 |
| 영업이익(손실) | 3,014 | (1,628) | 1,618 | (37,497) | (231) | 5,622 |
| 기타수익 | 835 | 54 | 10,097 | 2,300 | 569 | 439 |
| 기타비용 | 115 | 453 | 13,929 | 2,002 | 630 | 185 |
| 금융수익 | 1,377 | 1,792 | 5,680 | 3,846 | 3,450 | 4,265 |
| 금융비용 | 5,434 | 1,629 | 7,077 | 5,315 | 4,249 | 4,992 |
| 지분법이익(손실) | 0 | (261) | 641 | (901) | 59 | (1,361) |
| 법인세비용차감전순이익(손실) | (323) | (2,125) | (2,970) | (39,569) | (1,033) | 3,787 |
| 법인세비용(수익) | 212 | 433 | 489 | (5,163) | 3,216 | 6,584 |
| 당기순이익(손실) | (111) | (2,558) | (3,459) | (34,407) | (4,249) | (2,797) |
| 매출총이익율 | 43.71% | 45.54% | 46.44% | 37.38% | 41.61% | 41.51% |
| 경상연구개발비율 | 9.31% | 17.61% | 14.64% | 27.44% | 12.72% | 12.31% |
| 영업이익율 | 6.31% | -4.73% | 1.01% | -29.78% | -0.12% | 3.08% |
| 순이익율 | -0.23% | -7.44% | -2.16% | -27.32% | -2.23% | -1.53% |
| (자료 : 당사 사업보고서 및 분기보고서) |
당사의 자회사는 주로 임상시험 등 연구개발 활동을 수행하고 있어, 제한적인 매출만을 창출하고 있습니다. 이에 따라 연결 기준 매출액은 별도 기준 매출액과 유사한 수준을 유지하고 있습니다. 그러나 자회사의 임상개발 비용 등으로 인해 연구개발비가 연간 70억 원에서 190억 원 수준으로 발생하고 있으며, 이로 인해 연결 기준 수익성은 별도 기준에 비해 열위에 있는 모습입니다. 2023년에는 당사의 경영구조 개편에 따른 매출 감소와 더불어 자회사의 JM-010 임상 관련 비용이 크게 증가하면서 375억 원의 영업손실을 기록하였습니다. 다만, 2024년에는 해당 임상이 중단되었고, 전년도 경영구조 개편의 효과가 온전히 반영됨에 따라 영업이익 16억 원을 기록하며 흑자 전환에 성공하였습니다.
한편, 2025년 1분기 당사의 연결 기준 매출액은 478억원, 영업이익은 30억원을 기록하며 전년 동기 대비 39%의 매출 성장 및 영업이익 흑자를 달성하였습니다. 그러나 당기순손실 1억원을 기록하며 순이익 흑자 전환에는 실패했는데, 이는 당사가 전략적 파트너로서 출자하여 보유한 TVM Life Science Ventures Vll의 수익증권에 대한 공정가치측정 금융자산 평가손실 42억원을 인식한 것에 기인하였으며, 해당 비용의 경우 일회성 비용에 해당하여 향후 당사의 영업수익성에 미치는 영향은 미미한 것으로 판단됩니다.
당사는 향후 연결 및 별도 기준 모두에서 수익성이 점진적으로 개선될 것으로 전망하고 있으며, 2023년과 같은 대규모 영업손실이 재차 발생할 가능성은 제한적이라고 판단하고 있습니다. 다만, 당사가 속한 제약업종은 식품의약품안전처 등 규제기관의 추가 규제, 임상시험 진행에 따른 추가 연구개발비 발생, 경쟁 제품 출시 등의 예상치 못한 변수에 지속적으로 노출되어 있습니다. 이로 인해 당사의 매출이 감소하거나 수익성이 악화되는 등 영업 환경에 부정적인 영향을 미칠 수 있으므로, 투자자 여러분께서는 이 점을 유의하여 주시기 바랍니다.
(주7) 정정 전
당사의 연결 기준 재무건전성은 타 제약사 대비 상대적으로 우수한 수준을 유지하고 있습니다. 유동비율은 2023년을 제외하고 500% 내외를 기록해 왔으며, 2023년에는 자회사 Contera Pharma A/S에 출자한 에이치델타 사모투자합자회사의 주식매수청구권(Put Option) 행사 기한 도래로 기타유동부채가 증가하면서 유동비율이 일시적으로 260% 수준으로 하락하였습니다. 그럼에도 불구하고, 이는 여전히 양호한 수치로 평가됩니다. 해당 주식매수청구권은 2024년 투자자의 권리 행사에 따라 당사가 인수대가 632억 원에 전량 회수하였고, 이로 인해 2024년 기타유동부채는 크게 감소하며 유동비율은 다시 500% 이상 수준으로 회복되었습니다. 부채비율은 2021년과 2022년에 41~48% 수준을 유지하였으나, 2023년에는 일시적인 영업적자, 신규 차입금 발생, 기타유동부채 증가 등이 복합적으로 작용하면서 83.13%로 상승하였습니다. 그러나 2024년에는 수익성 개선과 함께 기타유동부채가 상환되며, 부채비율은 52.85%로 개선되었습니다.
당사는 한동안 무차입 경영 기조를 유지해 왔으며, 이에 따라 2021년 및 2022년 총차입금의존도는 1% 미만을 기록하였고, 보유 현금이 총차입금을 초과함에 따라 순차입금도 마이너스(-) 상태를 유지하였습니다. 2023년에는 신규 차입이 발생하면서 총차입금의존도가 18.50%로 증가하였고, 2024년에는 기타유동부채 상환에 따른 총자산 감소의 영향으로 21.28%로 소폭 상승하였습니다. 그럼에도 불구하고, 보유 현금이 총차입금을 상회함에 따라 순차입금은 여전히 음(-)의 상태를 유지하고 있습니다. 차입금 실행 및 기타유동부채 상환 등은 모두 당사(별도 기준)에서 발생한 사항으로, 별도 기준 재무안정성 지표 역시 연결 기준과 유사한 흐름을 보이고 있습니다.
당사의 요약 기준 연결재무상태표 및 별도재무상태표는 다음과 같습니다.
| [ 당사 요약 연결재무상태표] |
| (단위: 백만원) |
| 구 분 | 2024 | 2023 | 2022 | 2021 |
| 자산 | 373,180 | 429,017 | 400,929 | 397,417 |
| 유동자산 | 203,739 | 254,179 | 218,741 | 220,095 |
| 비유동자산 | 169,441 | 174,839 | 182,188 | 177,321 |
| 부채 | 129,035 | 194,752 | 129,082 | 117,356 |
| 유동부채 | 35,398 | 97,544 | 44,603 | 36,995 |
| 비유동부채 | 93,637 | 97,208 | 84,479 | 80,361 |
| 자본총계 | 244,145 | 234,265 | 271,847 | 280,061 |
| 총차입금 | 79,424 | 79,387 | 931 | 1,558 |
| 유동리스부채 | 130 | 218 | 243 | 444 |
| 장기차입금 | 79,024 | 78,525 | - | - |
| 비유동리스부채 | 270 | 644 | 688 | 1,114 |
| 현금및현금성자산 | 90,091 | 151,227 | 85,517 | 82,777 |
| 순차입금 | (10,667) | (71,840) | (84,586) | (81,219) |
| 유동비율 | 575.56% | 260.58% | 490.42% | 594.94% |
| 부채비율 | 52.85% | 83.13% | 47.48% | 41.90% |
| 총차입금의존도 | 21.28% | 18.50% | 0.23% | 0.39% |
| 순차입금의존도 | -2.86% | -16.75% | -21.10% | -20.44% |
| (자료 : 당사 사업보고서) |
| [ 당사 요약 별도재무상태표] |
| (단위: 백만원) |
| 구 분 | 2024 | 2023 | 2022 | 2021 |
| 자산 | 370,080 | 460,536 | 420,612 | 406,936 |
| 유동자산 | 190,618 | 232,286 | 192,377 | 186,485 |
| 비유동자산 | 179,462 | 228,250 | 228,235 | 220,451 |
| 부채 | 127,169 | 173,812 | 110,413 | 95,842 |
| 유동부채 | 33,945 | 78,226 | 42,979 | 35,312 |
| 비유동부채 | 93,224 | 95,586 | 67,434 | 60,530 |
| 자본총계 | 242,911 | 286,724 | 310,199 | 311,094 |
| 총차입금 | 79,415 | 79,379 | 878 | 1,399 |
| 유동리스부채 | 130 | 218 | 197 | 365 |
| 장기차입금 | 79,024 | 78,525 | - | - |
| 비유동리스부채 | 261 | 636 | 680 | 1,034 |
| 현금및현금성자산 | 79,680 | 132,380 | 61,821 | 51,442 |
| 순차입금 | (265) | (53,001) | (60,943) | (50,044) |
| 유동비율 | 561.55% | 296.94% | 447.60% | 528.11% |
| 부채비율 | 52.35% | 60.62% | 35.59% | 30.81% |
| 총차입금의존도 | 21.46% | 17.24% | 0.21% | 0.34% |
| 순차입금의존도 | -0.07% | -11.51% | -14.49% | -12.30% |
| (자료 : 당사 사업보고서) |
한편 22년 이후 당사의 순차입금 증가와 영업적자 전환 등의 사유로 인해 당사의 이자보상배율은 악화되는 추세를 보였습니다. 2022년 연결기준 이자보상배율은 -0.13으로 연결영업적자로 인해 마이너스 전환하였으며 2023년의 경우 연결,별도 기준 영업이익이 모두 적자전환함에 따라 이자보상배율은 연결,별도 기준 모두 마이너스 전환 하였습니다. 다만, 경영구조 개편의 효과가 2024년부터 본격적으로 나타나면서, 당사의 별도기준 2024년 매출액은 전년 대비 25.91% 증가한 1,576억 원을 기록하였으며, 영업이익 또한 170억 원으로 흑자 전환에 성공하였습니다. 연결기준 영업이익 또한 16억원으로 흑자전환 함에 따라 당사의 2024년 이자보상배율은 플러스 전환하게 되었습니다. 그러나 2023년의 신규 차입 영향으로 인해, 영업이익이 발생했음에도 불구하고 2024년 이자보상배율은 0.25로 여전히 1 미만의 수준을 보이고 있습니다. 다만, 2025년 이후 라투다정을 중심으로 매출액 및 수익성 개선이 기대되고 있는 상황임에 따라 당사의 이자보상배율은 점진적인 개선 추세를 보일 것으로 전망됩니다.
| [ 당사 연결기준 이자보상배율] |
| (단위: 백만원) |
| 구 분 | 2024년 | 2023년 | 2022년 | 2021년 |
|---|---|---|---|---|
| 영업이익 | 1,618 | -37,497 | -231 | 5,622 |
| 이자비용 | 6,490 | 3,808 | 1,760 | 1,408 |
| 이자보상배율 |
0.25 | -9.85 | -0.13 | 3.99 |
| (자료 : 당사 사업보고서) |
| [ 당사 별도기준 이자보상배율] |
| (단위: 백만원) |
| 구 분 | 2024년 | 2023년 | 2022년 | 2021년 |
|---|---|---|---|---|
| 영업이익 | 17,004 | -17,173 | 12,322 | 13,163 |
| 이자비용 | 4,549 | 1,298 | 162 | 323 |
| 이자보상배율 |
3.74 | -13.23 | 76.07 | 40.76 |
| (자료 : 당사 사업보고서) |
한편, 당사는 2025년 04월 22일 금융감독원 전자공시시스템(http://dart.fss.or.kr)에 2025년 1분기 잠정 영업 실적을 공시하였습니다. 2025년 1분기의 경우 덱시드와 치옥타시드 등 주력 제품군의 매출이 큰 폭으로 증가하였고 라투다가 본격적으로 시장에 진입하며, 별도 기준 전년 동기 대비 28.86%의 매출 성장과 188.16%의 영업이익 성장을 기록하는 등 개선된 실적을 보였습니다. 연결 기준으로는 매출액 478억원을 기록, 5분기 연속 매출 증가를 이어가며 안정적인 성장 흐름을 지속하고 있고, 3분기 연속 영업이익 흑자를 기록하며 수익성 개선에서도 성과를 보였습니다. 자세한 내용은 금융감독원 전자공시시스템(http://dart.fss.or.kr)에 공시된 "연결재무제표기준영업(잠정)실적(공정공시)"를 참고해주시기 바랍니다.
| [연결재무제표기준영업(잠정)실적(공정공시)] |
| (단위: 백만원) |
| ※ 동 정보는 잠정치로서 향후 확정치와는 다를 수 있음. | ||||||
| 1. 연결실적내용 | 단위 : 백만원, % | |||||
| 구분 | 당기실적 | 전기실적 | 전기대비증감율(%) | 전년동기실적 | 전년동기대비증감율(%) | |
| (25.Q1) | (24.Q4) | (24.Q1) | ||||
| 매출액 | 당해실적 | 47,806 | 46,181 | 3.52% | 34,393 | 39.00% |
| 누계실적 | 47,806 | 160,087 | - | 34,393 | 39.00% | |
| 영업이익 | 당해실적 | 3,014 | 1,953 | 54.33% | -1,628 | 흑자전환 |
| 누계실적 | 3,014 | 1,618 | - | -1,628 | 흑자전환 | |
| 법인세비용차감전계속사업이익 | 당해실적 | -323 | -2,096 | 84.59% | -2,125 | 84.80% |
| 누계실적 | -323 | -2,970 | - | -2,125 | 84.80% | |
| 당기순이익 | 당해실적 | -111 | 1,797 | 적자전환 | -2,558 | 95.66% |
| 누계실적 | -111 | -3,459 | - | -2,558 | 95.66% | |
| 지배기업 소유주지분 순이익 | 당해실적 | -69 | 1,848 | 적자전환 | -1,911 | 96.39% |
| 누계실적 | -69 | -2,641 | - | -1,911 | 96.39% | |
| - | - | - | - | - | - | |
| 2. 정보제공내역 | 정보제공자 | 재무지원팀 | ||||
| 정보제공대상자 | 투자자, Analyst 및 기자 등 | |||||
| 정보제공(예정)일시 | 공정공시 후 수시제공 (2025.04.22 Conference Call) |
|||||
| 행사명(장소) | - | |||||
| 3. 연락처(관련부서/전화번호) | 재무지원팀(02-828-8114) | |||||
| 4. 기타 투자판단과 관련한 중요사항 | ||||||
| - 부광약품(주)의 별도(잠정) 실적은 아래와 같습니다. (단위:백만원,%) 당기실적 전기실적 증감율 (2025 Q1 당해) (2024 Q4 당해) (%) 매출액 43,850 44,423 -1.29 영업이익 5,935 5,989 -0.90 법인세비용차감전이익 2,585 -57,042 흑자전환 당기순이익 2,794 -55,852 흑자전환 지배기업소유주지분순이익 2,794 -55,852 흑자전환 - 상기 잠정 영업실적은 한국채택국제회계기준(K-IFRS)에 따라 작성된 잠정 수치로써 외부감사인의 회계 검토를 받지 않은 정보입니다. 이는 투자자들의 편의를 위해 제공되는 정보로서, 실제 실적과는 차이가 발생할 수 있음을 양지하시기 바랍니다. - 상기 실적과 관련된 자료는 4월 22일(화) 오후 당사 홈페이지에 게시할 예정입니다. |
||||||
| ※ 관련공시 | 2025-04-18 기업설명회(IR) 개최(안내공시) | |||||
| (자료 : 금융감독원 전자공시시스템) |
당사의 차입금은 하나은행 및 신한은행으로부터 차입하였으며 만기는 2026년 도래할 예정입니다. 다만, 당사의 보유 현금 규모 및 영업현금흐름 고려 시 해당 차입금 상환에는 무리가 없을 것으로 판단되고 있습니다.
| [ 당사 차입금 현황] |
| (단위: 원) |
| 구 분 | 차입처 | 최종 만기일 | 연이자율(%) | 2024년말 | 2023년말 |
| 원화장기차입금 | 하나은행 | 2026-08-16 | CD91일물 + 1.484 | 30,000,000,000 | 30,000,000,000 |
| 원화장기차입금(*) | 신한은행 | 2026-10-13 | CD91일물 + 1.39 | 50,000,000,000 | 50,000,000,000 |
| 소계 | 80,000,000,000 | 80,000,000,000 | |||
| 유동성 대체 | - | - | |||
| 차감 : 장기차입금할인발행차금 | (975,816,626) | (1,474,872,585) | |||
| 합계 | 79,024,183,374 | 78,525,127,415 | |||
| (자료 : 당사 사업보고서) (*)상기 차입금과 관련하여 유형자산을 담보로 제공하고 있습니다 |
(중략)
(주7) 정정 후
당사의 연결 기준 재무건전성은 타 제약사 대비 상대적으로 우수한 수준을 유지하고 있습니다. 유동비율은 2023년을 제외하고 500% 내외를 기록해 왔으며, 2023년에는 자회사 Contera Pharma A/S에 출자한 에이치델타 사모투자합자회사의 주식매수청구권(Put Option) 행사 기한 도래로 기타유동부채가 증가하면서 유동비율이 일시적으로 260% 수준으로 하락하였습니다. 그럼에도 불구하고, 이는 여전히 양호한 수치로 평가됩니다. 해당 주식매수청구권은 2024년 투자자의 권리 행사에 따라 당사가 인수대가 632억 원에 전량 회수하였고, 이로 인해 2024년 기타유동부채는 크게 감소하며 유동비율은 다시 500% 이상 수준으로 회복되었습니다. 부채비율은 2021년과 2022년에 41~48% 수준을 유지하였으나, 2023년에는 일시적인 영업적자, 신규 차입금 발생, 기타유동부채 증가 등이 복합적으로 작용하면서 83.13%로 상승하였습니다. 그러나 2024년에는 수익성 개선과 함께 기타유동부채가 상환되며, 부채비율은 52.85%로 개선되었습니다. 2025년 1분기말 기준 부채비율은 52.88%로, 2024년 말과 같은 수준을 유지하고 있습니다.
당사는 한동안 무차입 경영 기조를 유지해 왔으며, 이에 따라 2021년 및 2022년 총차입금의존도는 1% 미만을 기록하였고, 보유 현금이 총차입금을 초과함에 따라 순차입금도 마이너스(-) 상태를 유지하였습니다. 2023년에는 신규 차입이 발생하면서 총차입금의존도가 18.50%로 증가하였고, 2024년에는 기타유동부채 상환에 따른 총자산 감소의 영향으로 21.28%로 소폭 상승하였고 2025년 1분기까지 유사한 차입 수준을 유지하고 있습니다. 그럼에도 불구하고, 보유 현금이 총차입금을 상회함에 따라 순차입금은 여전히 음(-)의 상태를 유지하고 있습니다. 차입금 실행 및 기타유동부채 상환 등은 모두 당사(별도 기준)에서 발생한 사항으로, 별도 기준 재무안정성 지표 역시 연결 기준과 유사한 흐름을 보이고 있습니다.
당사의 요약 기준 연결재무상태표 및 별도재무상태표는 다음과 같습니다.
| [ 당사 요약 연결재무상태표] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기말 |
2024 | 2023 | 2022 | 2021 |
| 자산 | 372,643 | 373,180 | 429,017 | 400,929 | 397,417 |
| 유동자산 | 206,464 | 203,739 | 254,179 | 218,741 | 220,095 |
| 비유동자산 | 166,179 | 169,441 | 174,839 | 182,188 | 177,321 |
| 부채 | 128,901 | 129,035 | 194,752 | 129,082 | 117,356 |
| 유동부채 | 35,243 | 35,398 | 97,544 | 44,603 | 36,995 |
| 비유동부채 | 93,658 | 93,637 | 97,208 | 84,479 | 80,361 |
| 자본총계 | 243,742 | 244,145 | 234,265 | 271,847 | 280,061 |
| 총차입금 | 80,159 | 79,424 | 79,387 | 931 | 1,558 |
| 유동리스부채 | 381 | 130 | 218 | 243 | 444 |
| 장기차입금 | 79,135 | 79,024 | 78,525 | - | - |
| 비유동리스부채 | 643 | 270 | 644 | 688 | 1,114 |
| 현금및현금성자산 | 87,813 | 90,091 | 151,227 | 85,517 | 82,777 |
| 순차입금 | (7,655) | (10,667) | (71,840) | (84,586) | (81,219) |
| 유동비율 | 585.83% | 575.56% | 260.58% | 490.42% | 594.94% |
| 부채비율 | 52.88% | 52.85% | 83.13% | 47.48% | 41.90% |
| 총차입금의존도 | 21.51% | 21.28% | 18.50% | 0.23% | 0.39% |
| 순차입금의존도 | -2.05% | -2.86% | -16.75% | -21.10% | -20.44% |
| (자료 : 당사 사업보고서 및 분기보고서) |
| [ 당사 요약 별도재무상태표] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기말 |
2024 | 2023 | 2022 | 2021 |
| 자산 | 372,231 | 370,080 | 460,536 | 420,612 | 406,936 |
| 유동자산 | 196,039 | 190,618 | 232,286 | 192,377 | 186,485 |
| 비유동자산 | 176,192 | 179,462 | 228,250 | 228,235 | 220,451 |
| 부채 | 126,830 | 127,169 | 173,812 | 110,413 | 95,842 |
| 유동부채 | 33,581 | 33,945 | 78,226 | 42,979 | 35,312 |
| 비유동부채 | 93,249 | 93,224 | 95,586 | 67,434 | 60,530 |
| 자본총계 | 245,401 | 242,911 | 286,724 | 310,199 | 311,094 |
| 총차입금 | 80,149 | 79,415 | 79,379 | 878 | 1,399 |
| 유동리스부채 | 381 | 130 | 218 | 197 | 365 |
| 장기차입금 | 79,135 | 79,024 | 78,525 | - | - |
| 비유동리스부채 | 633 | 261 | 636 | 680 | 1,034 |
| 현금및현금성자산 | 80,903 | 79,680 | 132,380 | 61,821 | 51,442 |
| 순차입금 | (754) | (265) | (53,001) | (60,943) | (50,044) |
| 유동비율 | 583.79% | 561.55% | 296.94% | 447.60% | 528.11% |
| 부채비율 | 51.68% | 52.35% | 60.62% | 35.59% | 30.81% |
| 총차입금의존도 | 21.53% | 21.46% | 17.24% | 0.21% | 0.34% |
| 순차입금의존도 | -0.20% | -0.07% | -11.51% | -14.49% | -12.30% |
| (자료 : 당사 사업보고서 및 분기보고서) |
한편 22년 이후 당사의 순차입금 증가와 영업적자 전환 등의 사유로 인해 당사의 이자보상배율은 악화되는 추세를 보였습니다. 2022년 연결기준 이자보상배율은 -0.13으로 연결영업적자로 인해 마이너스 전환하였으며 2023년의 경우 연결,별도 기준 영업이익이 모두 적자전환함에 따라 이자보상배율은 연결,별도 기준 모두 마이너스 전환 하였습니다. 다만, 경영구조 개편의 효과가 2024년부터 본격적으로 나타나면서, 당사의 별도기준 2024년 매출액은 전년 대비 25.91% 증가한 1,576억 원을 기록하였으며, 영업이익 또한 170억 원으로 흑자 전환에 성공하였습니다. 연결기준 영업이익 또한 16억원으로 흑자전환 함에 따라 당사의 2024년 이자보상배율은 플러스 전환하게 되었습니다. 그러나 2023년의 신규 차입 영향으로 인해, 영업이익이 발생했음에도 불구하고 2024년 이자보상배율은 0.25로 여전히 1 미만의 수준을 보이고 있습니다. 다만, 2025년 이후 라투다정을 중심으로 매출액 및 수익성 개선이 기대되고 있는 상황임에 따라 당사의 이자보상배율은 점진적인 개선 추세를 보일 것으로 전망되며, 2025년 1분기 당사의 실적 호조 및 수익성 증가로 연결 기준 영업이익 30억원, 별도 기준 영업이익 59억원을 기록하며 이자보상배율은 연결기준 2.83, 별도기준 5.84를 기록해 전년 동기 대비 실제로 큰 폭 개선되는 모습을 보이고 있습니다.
| [ 당사 연결기준 이자보상배율] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 | 2024년 1분기 | 2024년 | 2023년 | 2022년 | 2021년 |
|---|---|---|---|---|---|---|
| 영업이익 | 3,014 | -1,628 | 1,618 | -37,497 | -231 | 5,622 |
| 이자비용 | 1,064 | 1,537 | 6,490 | 3,808 | 1,760 | 1,408 |
| 이자보상배율 |
2.83 | -1.06 | 0.25 | -9.85 | -0.13 | 3.99 |
| (자료 : 당사 사업보고서 및 분기보고서) |
| [ 당사 별도기준 이자보상배율] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 | 2024년 1분기 | 2024년 | 2023년 | 2022년 | 2021년 |
|---|---|---|---|---|---|---|
| 영업이익 | 5,935 | 2,060 | 17,004 | -17,173 | 12,322 | 13,163 |
| 이자비용 | 1,016 | 1,147 | 4,549 | 1,298 | 162 | 323 |
| 이자보상배율 |
5.84 | 1.80 | 3.74 | -13.23 | 76.07 | 40.76 |
| (자료 : 당사 사업보고서 및 분기보고서) |
(삭제)
당사의 차입금은 하나은행 및 신한은행으로부터 차입하였으며 만기는 2026년 도래할 예정입니다. 다만, 당사의 보유 현금 규모 및 영업현금흐름 고려 시 해당 차입금 상환에는 무리가 없을 것으로 판단되고 있습니다.
| [ 당사 차입금 현황] |
| (단위: 원) |
| 구 분 | 차입처 | 최종 만기일 | 연이자율(%) | 2025년 1분기말 | 2024년말 |
| 원화장기차입금 | 하나은행 | 2026-08-16 | CD91일물 + 1.484 | 30,000,000,000 | 30,000,000,000 |
| 원화장기차입금(*) | 신한은행 | 2026-10-13 | CD91일물+ 1.39 | 50,000,000,000 | 50,000,000,000 |
| 소계 | 80,000,000,000 | 80,000,000,000 | |||
| 유동성 대체 | - | - | |||
| 차감 : 장기차입금할인발행차금 | (864,753,074) | (975,816,626) | |||
| 합계 | 79,135,246,926 | 79,024,183,374 | |||
| (자료 : 당사 분기보고서) (*)상기 차입금과 관련하여 유형자산을 담보로 제공하고 있습니다 |
(중략)
(주8) 정정 전
당사는 당사의 Global Open Innovation 전략의 일환으로 다수 해외계열사를 보유하고 있습니다. 증권신고서 제출일 현재 당사의 지분 투자 회사에 대한 내용 및 지분 취득 히스토리는 다음과 같습니다.
| [당사 연결대상 종속회사 현황] |
| 단위: 백만원 |
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| Contera Pharma A/S |
2010년 07월 09일 (주1) |
DTU Science Park Venlighedsvej 4 2970 Hørsholm Denmark |
의약품 연구 및 개발사업 |
12,523 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
| 부광메디카 (주) |
2015년 06월 17일 (주2) |
서울특별시 동작구 상도로 5(대방동) |
완제 의약품 제조업 및 판매업 |
2,715 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
|
ProteKt Therapeutics |
2015년 01월 01일 (주3) |
Ness Ziona, Israel 2 Ilan Ramon St., Ness Ziona, Israel |
의약품 연구 및 개발사업 |
356 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
|
JaguAHR Therapeutics |
2019년 10월 14일 (주4) |
5 SHENTON WAY, #10-01, UIC BUILDING, SINGAPORE 068808 | 의약품 연구 및 개발사업 |
352 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
| 종속기업 | 소재지 | 지배지분율(%) | 결산월 | 업종 | |
|---|---|---|---|---|---|
| 2024년말 | 2023년말 | ||||
| Contera Pharma A/S | 덴마크 | 99.33 | 74.14 | 12월 | 의약품 연구 및 개발 |
| 부광메디카(주) | 한국 | 100 | 100 | 12월 | 완제 의약품 제조업 및 의약품 도매업 |
| JaguAHR Therapeutics | 싱가포르 | 75.02 | 65.00 | 12월 | 의약품 연구 및 개발 |
| ProteKt Therapeutics | 이스라엘 | 96.53 | 96.73 | 12월 | 의약품 연구 및 개발 |
| (자료 : 당사 사업보고서) (주1) 2014년 11월 24일 부광약품(주)에서 약 34억원을 출자하여 인수(지분율 100%) 2018년 07월 18일 14,000주 약 5.5억원 제3자배정 유상증자(지분율 96.26%) 2019년 07월 15일 10,000주 약 30억원 제3자배정 유상증자(지분율 94.38%) 2020년 07월 22일 40,000주 양도 및 352억원 제3자배정유상증자(지분율71.23%) 2022년 11월 14일 비지배주주의 매도청구권 행사로 인한 10,000주 매수(지분율 72.84%) 2023년 08월 17일 31,250주 약 100억원 유상증자(지분율 74.14%) 2024년 04월 01일 관계회사 에이치델타 사모투자합자회사의 주식매수청구권 행사로 인한 159,380주 매수 (지분율 98.56%) 2024년 08월 27일 413,793주 약 44억원 유상증자 (지분율 99.12%) 2024년 10월 27일 336,700주 약 30억원 유상증자 (지분율 99.33%) (주2) 2015년 06월 17일 부광약품(주)에서 5억원을 출자하여 설립 2015년 10월 17일 약 13억원의 현금출자 2015년 10월 20일 약 127억원 상당의 현물출자 2019년 03월 08일 50억원의 현금출자 2021년 01월 25일 110억원의 유상감자(부광약품(주) 지분율 100%) (주3) 2023년 01월 26일 기존 주주의 주식 3,869,472주를 인수하는 조건의 주주간계약을 체결하여 지배력을 확보함 (부광약품(주)지분율 96.53%) (주4) 2024년 11월 26일 설립 파트너사인 Aslan Pharma가 청산됨에 따라, Aslan Pharma로부터22,050주를 인수하는 계약을 체결하여 지배력을 확보함 (부광약품(주)지분율 75.02%) (주5) 지배회사 자산총액의 10%미만이거나 자산총액이 750억원 미만이므로 주요종속회사에 해당되지 않음 |
| [당사 타법인 출자현황(5% 이상)] |
| 단위: 백만원 |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
| JaguAHR Therapeutics (주1) |
비상장 | 2019.08.16 | 단순 투자 |
5,769 | 143,000 | 65.00 | 5,769 | -143,000 | -5,769 | - | - | - | - | 352 | -93 |
| CytoSite BioPharma Inc 우선주 (주2) |
비상장 | 2018.08.06 | 단순 투자 |
1,720 | 624,973 | 8.54 | 1,720 | - | - | - | 624,973 | 8.54 | 1,720 | 278 | -1,337 |
| 덴탈플랫폼 출자조합제1호(주3) |
비상장 | 2019.05.28 | 단순 투자 |
2,000 | 200 | 50.00 | - | - | - | - | 200 | 50.00 | - | 68 | -2 |
| 에이치 델타 사모투자합자회사 (주4) |
비상장 | 2020.07.22 | 단순 투자 |
10,000 | 10,000 | 18.87 | 10,000 | -10,000 | -10,000 | - | - | - | - | - | - |
| 합 계 | - | - | 17,489 | - | -15,769 | - | - | - | 1,720 | - | - | ||||
| (자료 : 당사 사업보고서) * 최초취득 금액은 총 투자금액을 표시함 (주1) 1. 2021년 04월 28일 28억원 출자로 80,000주 취득. 지분율 65% (이전 45%) 2. 2024년 11월 26일 22,050주 인수로 종속회사로 편입. 지분율 75.02% (이전 65%) (주2) 1. 2018년 08월 06일 약 8.5억 출자로 312,486주 취득 2. 2019년 09월 11일 약 4.5억 출자로 156,243주 취득 3. 2020년 09월 22일 약 8,500만원 출자로 30,636주 취득 4. 2021년 07월 01일 약 3.4억 출자로 125,608주 취득 (주3) 1. 2019년 05월 28일 20억원 출자로 200좌 취득 (주4) 1. 종속기업 Contera Pharma A/S의 유상증자와 관련된 신규 투자 2. 2024년 05월 24일 최종 청산으로 인한 처분완료 |
| [당사 타법인 출자현황(5% 미만)] |
| 단위: 백만원 |
| 구분 | 상장 여부 |
법인명 또는 종목명 |
출자 목적 |
기초잔액 | 증가(감소)내역 | 기말잔액 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 최초 취득 금액 |
수량 | 지 분 율 |
장부 가액 |
취득(처분) | 평가/ 처분 손익 |
수량 | 지 분 율 |
장부 가액 |
비고 | |||||
| 수량 | 금액 | |||||||||||||
| 국외 | 상장 | Zevra Therapeutics, Inc. (구 ACER) (주1) |
단순 투자 |
4,590 | 65,893 | 0.16 | 557 | -65,893 | -642 | 85 | - | - | - | - |
| 국외 | 상장 | Biodexa Pharmaceuticals (주2) | 단순 투자 |
- | - | - | - | 354,428 | 443 | -359 | 14,177 | 2.12 | 84 | - |
| 국외 | 비상장 | Immpact Bio Ltd 우선주 (주3) |
단순 투자 |
7,433 | 429,822 | 2.91 | 4,460 | -429,822 | - | -4,460 | - | - | - | - |
| 국외 | 상장 | Lyell immunopharma (주3) | 단순 투자 |
- | - | - | - | 1,410,071 | 1,801 | -474 | 1,410,071 | 0.48 | 1,327 | - |
| 국외 | 비상장 | 흥국글로벌 사모증권 (주4) (TVM Life Science Ventures Vll) |
단순 투자 |
18,961 | - | - | 8,892 | - | 539 | 520 | - | - | 9,951 | - |
| 국외 | 비상장 | TVM Life Science Innovation II (주5) |
단순 투자 |
2,842 | - | - | 1,868 | - | 723 | 493 | - | - | 3,084 | - |
| 국내 | 비상장 | KDB오픈이노베이션펀드 (주6) | 단순 투자 |
500 | - | 2.37 | 263 | - | - | - | - | 2.37 | 263 | - |
| 합계 | 34,326 | - | - | 16,040 | - | 2,864 | -4,195 | - | - | 14,709 | - | |||
| (자료 : 당사 사업보고서) (주1) 1. 2015년 07월 17일 23억 출자로 306,477주 취득 2. 2016년 04월 15일 23억 출자로 238,095주 취득 3. 2017년 07월 04일 미국 NASDAQ 상장사인 Opexa Therapeutics, Inc. (오펙사 테라퓨틱스 이하, Opexa)와 합병 이사회 결의 4. 2017년 09월 19일 미국 NASDAQ 상장사인 Opexa와 합병 완료됨에 따라 합병 전 지분율 12.89%에서 합병 후 지분율 8.40% 보유 (합병비율 1:10.4). 5. 2017년 12월 1,046,667주 유상증자로 지분율 8.4% (이전 7.3%) 6. 2018년 08월 2,555,555주 유상증자로 지분율 5.4% (이전 7.3%) 7. 2020년 12월 3,137,961주 유상증자로 지분율 4.12% (이전 5.4%) 8. 2023년 10월 중 Zevra Therapeutics, Inc에 합병되었으며,관련 주식은 1:0.121비율로 전환됨 9. 2024년 09월 최종 처분 완료 (주2) 1. 파이프라인 'MLR-1023' 의 판권을 반환하는 대가로 354,428주의 Biodexa Pharmaceuticals 주식을 취득 2. 2024년 10월 중 액면병합으로 1:0.04 비율로 전환됨 (주3) 1. 2021년 07월 07일 11억원 출자로 76,378주 취득 2. 2021년 12월 24일 38억원 출자로 205,558주 취득 3. 2024년 11월 15일 ImmPACT Bio Ltd는 Lyell immunopharma에 합병되었으며, 기존 주식은 현금 2,208백만원과 Lyell immunopharma 주식 1,419,071주로 교환됨 (주4) TVM Capital사가 운용하는 TVM Life Science Ventures Vll에 유한 책임 조합원과 Strategic Partner로서 투자 계약을 체결하고 흥국자산운용 주식회사가 해당 feeder fund의 구성을 위한 신탁계약을 체결함 (주5) TVM Capital사가 운용하는 TVM Life Science Ventures VllI에 유한 책임 조합원으로서 투자 계약을 체결함 (주6) The Turning Point와 GSA PE가 운용하는 펀드이며, 총 약정금액 5억원 중 5억원 납입완료함 |
한편, 2024년말 및 2023년말 기준 당사의 종속기업, 관계기업 및 공동기업 투자주식 현황은 다음과 같습니다.
| [당사 종속기업, 관계기업 및 공동기업 투자주식 현황] |
| (단위: 원) |
| 구 분 | 종 목 | 소재국가 | 2024년말 | 2023년말 | ||
| 지분율(%) | 장부금액 | 지분율(%) | 장부금액 | |||
| 종속기업 | Contera Pharma A/S(*1) | 덴마크 | 99.33 | 10,871,136,907 | 74.14 | 44,461,604,497 |
| 부광메디카(주)(*2) |
대한민국 | 100 | 1,735,689,285 | 100 | 2,682,377,755 | |
| 다이나세라퓨틱스(주)(*3) | 대한민국 | - | - | 98.84 | 8,500,000,000 | |
| ProteKt Therapeutics | 이스라엘 | 97.24 | - | 97.44 | 1,750,826,750 | |
| JaguAHR Therapeutics(*4) | 싱가포르 | 75.02 | 1,428,331,853 | - | - | |
| 소 계 | 14,035,158,045 | 57,394,809,002 | ||||
| 공동기업 | JaguAHR Therapeutics(*4) | 싱가포르 | - | - | 65.00 | 5,768,500,000 |
| 소 계 | - | 5,768,500,000 | ||||
| 관계기업 | 덴탈플랫폼출자조합제1호 | 대한민국 | 50.00 | - | 50.00 | - |
| 에이치 델타 사모투자합자회사(*5) | 대한민국 | - | - | 18.87 | 10,000,000,000 | |
| 소 계 | - | 10,000,000,000 | ||||
| 합 계 | 14,035,158,045 | 73,163,309,002 | ||||
| (자료 : 당사 사업보고서) (*1) 2024년 중 Contera Pharma A/S는 750,493주의 유상증자를 실시하였습니다. (*2) 2024년 중 부광메디카는 738,553주의 유상감자를 진행하였으며, 관련하여 손상차손환입 2,053백만원을 인식하였습니다. (*3) 2024년 중 청산이 완료되었습니다. (*4) JaguAHR Therapeutics의 설립 파트너사인 Aslan Pharma가 청산됨에 따라, Aslan Pharma로부터 22,050주를 인수하고 지배력을 획득하였습니다. (*5) 2024년 중 에이치 델타 사모투자합자회사가 보유한 Contera Pharma A/S 보통주 159,380주를 당사가 양수하였으며, 에이치 델타 사모투자합자회사는 최종 청산 완료되었습니다. |
| [2024년 당사 종속기업, 관계기업 및 공동기업투자주식의 변동내역] |
| (단위: 원) |
| 구 분 | 종속기업 | 공동기업 | 관계기업 | 합 계 |
| 기초금액 | 57,394,809,002 | 5,768,500,000 | 10,000,000,000 | 73,163,309,002 |
| 취득 | 22,227,433,036 | - | - | 22,227,433,036 |
| 손상차손 | (52,102,309,367) | - | - | (52,102,309,367) |
| 유상감자 | (3,000,002,286) | - | - | (3,000,002,286) |
| 처분 | (8,500,000,000) | - | (10,000,000,000) | (18,500,000,000) |
| 지배력변동(*1) | 5,768,500,000 | (5,768,500,000) | - | - |
| 기타(*2) | (7,753,272,340) | - | - | (7,753,272,340) |
| 기말금액 | 14,035,158,045 | - | - | 14,035,158,045 |
| (자료 : 당사 사업보고서) (*1) 2024년 중 공동기업인 JaguAHR Therapeutics의 종속기업 편입으로 인한 변동입니다. (*2) 2024년 중 종속기업인 Contera Pharma A/S와 관련된 주주 간 계약상 조건부대가의 변동을 장부가액에서 차감하였습니다. |
당사는 매 회계연도 말, 종속기업·관계기업·공동기업에 대한 투자주식의 손상징후를 검토하고, 손상검사를 수행하고 있습니다. 투자주식의 회수가능액은 사용가치에 근거하여 산정되며, 미래현금흐름 추정에 따라 결정됩니다. 2024년에는 Contera Pharma A/S의 파이프라인 임상 중단 등의 사유로 인해 종속기업 투자주식 관련 손상차손 521억 원을 인식하였으며, 해당 금액은 당기의 기타비용으로 반영되었습니다.
또한, 당사의 외부 감사인인 안진회계법인은 2024년도 감사에서 종속기업투자주식(Contera Pharma A/S)의 손상검사와 종속기업(ProteKt Therapeutics)과 관련된 무형자산 손상검사를 핵심감사사항(Key Audit Matters)으로 판단하였습니다. 당사는 2024년 12월 31일 기준으로 Contera Pharma A/S 투자주식의 회수가능액을 추정하여 손상검사를 수행하였으며, 그 결과 총 480억 5,800만 원의 손상차손을 인식하였습니다. 해당 회수가능액 평가는 경영진의 유의적인 가정을 바탕으로 하며, 미래현금흐름 추정 과정에서 상당한 불확실성이 수반됩니다. 이에 따라 감사인은 해당 손상평가의 중요성과 경영진 추정의 유의성 등을 종합적으로 고려하여 이를 핵심감사사항으로 기재하였습니다.
한편, 투자주식 손상차손은 현금유출을 수반하지는 않지만, 기타비용으로 인식되어 순이익에는 부정적인 영향을 미칩니다. 향후에도 자회사의 임상 진행 과정에서 불확실성이 현실화될 경우, 추가적인 손상차손 인식이 필요할 수 있으며 이는 당사의 수익성 및 재무건전성뿐만 아니라 신용평가, 대외 평판, 거래처 협상력 등에도 부정적인 영향을 미칠 수 있습니다.따라서 투자자 여러분께서는 당사의 자회사 관련 손상차손 위험을 충분히 인지하신 후, 신중히 투자 의사결정을 내리시기 바랍니다.
(주8) 정정 후
당사는 당사의 Global Open Innovation 전략의 일환으로 다수 해외계열사를 보유하고 있습니다. 증권신고서 제출일 현재 당사의 지분 투자 회사에 대한 내용 및 지분 취득 히스토리는 다음과 같습니다.
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| Contera Pharma A/S |
2010년 07월 09일 (주1) |
DTU Science Park Venlighedsvej 4 |
의약품 연구 및 개발사업 |
12,523 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
| 부광메디카 (주) |
2015년 06월 17일 (주2) |
서울특별시 동작구 상도로 5(대방동) |
완제 의약품 제조업 및 판매업 |
2,715 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
|
ProteKt Therapeutics |
2015년 01월 01일 (주3) |
16 Bar Kochva St., Bnei-Brak, Israel | 의약품 연구 및 개발사업 |
356 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
|
JaguAHR Therapeutics |
2019년 10월 14일 (주4) |
5 SHENTON WAY, #10-01, UIC BUILDING, SINGAPORE 068808 | 의약품 연구 및 개발사업 |
352 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
| 종속기업 | 소재지 | 지배지분율(%) | 결산월 | 업종 | |
|---|---|---|---|---|---|
| 2025년 1분기말 | 2024년말 | ||||
| Contera Pharma A/S | 덴마크 | 99.33 | 99.33 | 12월 | 의약품 연구 및 개발 |
| 부광메디카(주) | 한국 | 100 | 100 | 12월 | 완제 의약품 제조업 및 의약품 도매업 |
| JaguAHR Therapeutics | 싱가포르 | 75.02 | 75.02 | 12월 | 의약품 연구 및 개발 |
| ProteKt Therapeutics | 이스라엘 | 96.53 | 96.53 | 12월 | 의약품 연구 및 개발 |
| (자료 : 당사 사업보고서 및 분기보고서) (주1) 2014년 11월 24일 부광약품(주)에서 약 34억원을 출자하여 인수(지분율 100%) 2018년 07월 18일 14,000주 약 5.5억원 제3자배정 유상증자(지분율 96.26%) 2019년 07월 15일 10,000주 약 30억원 제3자배정 유상증자(지분율 94.38%) 2020년 07월 22일 40,000주 양도 및 352억원 제3자배정유상증자(지분율71.23%) 2022년 11월 14일 비지배주주의 매도청구권 행사로 인한 10,000주 매수(지분율 72.84%) 2023년 08월 17일 31,250주 약 100억원 유상증자(지분율 74.14%) 2024년 04월 01일 관계회사 에이치델타 사모투자합자회사의 주식매수청구권 행사로 인한 159,380주 매수 (지분율 98.56%) 2024년 08월 27일 413,793주 약 44억원 유상증자 (지분율 99.12%) 2024년 10월 27일 336,700주 약 30억원 유상증자 (지분율 99.33%) (주2) 2015년 06월 17일 부광약품(주)에서 5억원을 출자하여 설립 2015년 10월 17일 약 13억원의 현금출자 2015년 10월 20일 약 127억원 상당의 현물출자 2019년 03월 08일 50억원의 현금출자 2021년 01월 25일 110억원의 유상감자(부광약품(주) 지분율 100%) (주3) 2023년 01월 26일 기존 주주의 주식 3,869,472주를 인수하는 조건의 주주간계약을 체결하여 지배력을 확보함 (부광약품(주)지분율 96.53%) (주4) 2024년 11월 26일 설립 파트너사인 Aslan Pharma가 청산됨에 따라, Aslan Pharma로부터22,050주를 인수하는 계약을 체결하여 지배력을 확보함 (부광약품(주)지분율 75.02%) (주5) 지배회사 자산총액의 10%미만이거나 자산총액이 750억원 미만이므로 주요종속회사에 해당되지 않음 |
| [당사 타법인 출자현황(5% 이상)] |
| (단위: 백만원, 주) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
| CytoSite BioPharma Inc 우선주(주1) |
비상장 | 2018.08.06 | 단순 투자 |
1,720 | 624,973 | 8.54 | 1,720 | - | - | - | 624,973 | 8.54 | 1,720 | 278 | -1,337 |
| 덴탈플랫폼 출자조합제1호(주2) |
비상장 | 2019.05.28 | 단순 투자 |
2,000 | 200 | 50.00 | - | - | - | - | 200 | 50.00 | - | 68 | -2 |
| 합 계 | - | - | 1,720 | - | - | - | - | - | 1,720 | - | - | ||||
| (자료 : 당사 분기보고서) * 최초취득 금액은 총 투자금액을 표시함 (주1) 1. 2018년 08월 06일 약 8.5억 출자로 312,486주 취득 2. 2019년 09월 11일 약 4.5억 출자로 156,243주 취득 3. 2020년 09월 22일 약 8,500만원 출자로 30,636주 취득 4. 2021년 07월 01일 약 3.4억 출자로 125,608주 취득 (주2) 1. 2019년 05월 28일 20억원 출자로 200좌 취득 |
| [당사 타법인 출자현황(5% 미만)] |
| (단위: 백만원, 주) |
| 구분 | 상장 여부 |
법인명 또는 종목명 |
출자 목적 |
기초잔액 | 증가(감소)내역 | 기말잔액 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 최초 취득 금액 |
수량 | 지 분 율 |
장부 가액 |
취득(처분) | 평가/ 처분 손익 |
수량 | 지 분 율 |
장부 가액 |
비고 | |||||
| 수량 | 금액 | |||||||||||||
| 국외 | 상장 | Biodexa Pharmaceuticals (주1) | 단순 투자 |
- | 14,177 | 2.12 | 84 | - | - | -57 | 14,177 | 2.12 | 27 | - |
| 국외 | 상장 | Lyell immunopharma (주2) | 단순 투자 |
- | 1,410,071 | 0.48 | 1,327 | - | - | -210 | 1,410,071 | 0.48 | 1,117 | - |
| 국외 | 비상장 | 흥국글로벌 사모증권 (주3) (TVM Life Science Ventures Vll) |
단순 투자 |
18,961 | - | - | 9,951 | - | - | -4,190 | - | - | 5,761 | - |
| 국외 | 비상장 | TVM Life Science Innovation II (주4) |
단순 투자 |
3,201 | - | - | 3,084 | - | 331 | 338 | - | - | 3,753 | - |
| 국내 | 비상장 | KDB오픈이노베이션펀드 (주5) | 단순 투자 |
500 | - | 2.37 | 263 | - | - | - | - | 2.37 | 263 | - |
| 합계 | 22,662 | - | - | 14,709 | - | 331 | -4,119 | - | - | 10,921 | - | |||
| (자료 : 당사 분기보고서) (주1) 1. 파이프라인 'MLR-1023' 의 판권을 반환하는 대가로 354,428주의 Biodexa Pharmaceuticals 주식을 취득 2. 2024년 10월 중 액면병합으로 1:0.04 비율로 전환됨 (주2) 1. 2021년 07월 07일 11억원 출자로 76,378주 취득 2. 2021년 12월 24일 38억원 출자로 205,558주 취득 3. 2024년 11월 15일 ImmPACT Bio Ltd는 Lyell immunopharma에 합병되었으며 기존 주식은 현금 2,208백만원과 Lyell immunopharma 주식 1,419,071주로 교환됨 (주3) TVM Capital사가 운용하는 TVM Life Science Ventures Vll에 유한 책임 조합원과 Strategic Partner로서 투자 계약을 체결하고 흥국자산운용 주식회사가 해당 feeder fund의 구성을 위한 신탁계약을 체결함 (주4) TVM Capital사가 운용하는 TVM Life Science Ventures VllI에 유한 책임 조합으로서 투자 계약을 체결함 (주5) The Turning Point와 GSA PE가 운용하는 펀드이며, 총 약정금액 5억원 중 5억원 납입완료함 |
한편, 증권신고서 제출일 현재 당사의 종속기업, 관계기업 및 공동기업 투자주식 현황은 다음과 같습니다.
| [당사 종속기업, 관계기업 및 공동기업 투자주식 현황] |
| (단위: 원) |
| 구 분 | 종 목 | 소재국가 | 2025년 1분기말 | 2024년말 | ||
| 지분율(%) | 장부금액 | 지분율(%) | 장부금액 | |||
| 종속기업 | Contera Pharma A/S | 덴마크 | 99.33 | 10,871,136,907 | 99.33 | 10,871,136,907 |
| 부광메디카(주) | 대한민국 | 100.00 | 1,735,689,285 | 100.00 | 1,735,689,285 | |
| ProteKt Therapeutics | 이스라엘 | 97.24 | - | 97.24 | - | |
| JaguAHR Therapeutics | 싱가포르 | 75.02 | 1,428,331,853 | 75.02 | 1,428,331,853 | |
| 소 계 | 14,035,158,045 | 14,035,158,045 | ||||
| 관계기업 | 덴탈플랫폼출자조합제1호 | 대한민국 | 50.00 | - | 50.00 | - |
| 소 계 | - | - | ||||
| 합 계 | 14,035,158,045 | 14,035,158,045 | ||||
| (자료 : 당사 분기보고서) |
| [당사 종속기업, 관계기업 및 공동기업투자주식의 변동내역] |
| (단위: 원) |
| 구 분 | 2025년 1분기 | 2024년 1분기 |
| 기초금액 | 14,035,158,045 | 73,163,309,002 |
| 취득 | - | - |
| 손상차손 | - | - |
| 처분 | - | - |
| 기타(*) |
- | 143,153,759 |
| 분기말금액 | 14,035,158,045 | 73,306,462,761 |
| (자료 : 당사 분기보고서) (*) 2024년 1분기 중 종속기업인 Contera Pharma A/S와 관련된 주주 간 계약상 조건부대가의 변동을 장부가액에 가산하였습니다. |
당사는 매 회계연도 말, 종속기업·관계기업·공동기업에 대한 투자주식의 손상징후를 검토하고, 손상검사를 수행하고 있습니다. 투자주식의 회수가능액은 사용가치에 근거하여 산정되며, 미래현금흐름 추정에 따라 결정됩니다. 2024년에는 Contera Pharma A/S의 파이프라인 임상 중단 등의 사유로 인해 종속기업 투자주식 관련 손상차손 521억 원을 인식하였으며, 해당 금액은 당기의 기타비용으로 반영되었습니다.
또한, 당사의 외부 감사인인 안진회계법인은 2024년도 감사에서 종속기업투자주식(Contera Pharma A/S)의 손상검사와 종속기업(ProteKt Therapeutics)과 관련된 무형자산 손상검사를 핵심감사사항(Key Audit Matters)으로 판단하였습니다. 당사는 2024년 12월 31일 기준으로 Contera Pharma A/S 투자주식의 회수가능액을 추정하여 손상검사를 수행하였으며, 그 결과 총 480억 5,800만 원의 손상차손을 인식하였습니다. 해당 회수가능액 평가는 경영진의 유의적인 가정을 바탕으로 하며, 미래현금흐름 추정 과정에서 상당한 불확실성이 수반됩니다. 이에 따라 감사인은 해당 손상평가의 중요성과 경영진 추정의 유의성 등을 종합적으로 고려하여 이를 핵심감사사항으로 기재하였습니다.
한편, 투자주식 손상차손은 현금유출을 수반하지는 않지만, 기타비용으로 인식되어 순이익에는 부정적인 영향을 미칩니다. 향후에도 자회사의 임상 진행 과정에서 불확실성이 현실화될 경우, 추가적인 손상차손 인식이 필요할 수 있으며 이는 당사의 수익성 및 재무건전성뿐만 아니라 신용평가, 대외 평판, 거래처 협상력 등에도 부정적인 영향을 미칠 수 있습니다.따라서 투자자 여러분께서는 당사의 자회사 관련 손상차손 위험을 충분히 인지하신 후, 신중히 투자 의사결정을 내리시기 바랍니다.
(주9) 정정 전
당사는 국제적으로 영업활동을 영위하고 있어 외환위험, 특히 주로 달러 및 유로화와 관련된 환율변동위험에 노출되어 있습니다. 외환위험은 당사가 보유하고 있는 외화표시 금융자산 및 금융부채, 해외사업장에 대한 순투자와 관련하여 발생하고 있습니다. 2024년 현재 다른 모든 변수가 일정하고 달러, 유로화 및 엔화에 대한 원화환율이 10% 변동시 당사의 세후 이익 및 자본에 미치는 영향은 아래 표와 같습니다.
| (단위: 원) |
| 구 분 | 세후 이익에 대한 영향 | 자본에 대한 영향 | |||
| 2024년 | 2023년 | 2024년 | 2023년 | ||
| 유로화/원 | 상승시 | (43,081,939) | (485,346,558) | (43,081,939) | (485,346,558) |
| 하락시 | 43,081,939 | 485,346,558 | 43,081,939 | 485,346,558 | |
| 미국달러/원 | 상승시 | 102,461,088 | 6,795,210 | 102,461,088 | 6,795,210 |
| 하락시 | (102,461,088) | (6,795,210) | (102,461,088) | (6,795,210) | |
| 일본엔화/원 | 상승시 | 9,509,617 | (469,244) | 9,509,617 | (469,244) |
| 하락시 | (9,509,617) | 469,244 | (9,509,617) | 469,244 | |
| (자료 : 당사 사업보고서) |
현재로서 해당 환율변동이 당사의 수익성에 미치는 영향은 미미한 수준으로 판단됩니다. 다만 당사가 대외적으로 표명중인 Global Open Innovation 전략에 따라 당사는 향후에도 다양한 해외 제약회사 및 바이오벤처사와 협업을 진행할 예정입니다.특히, 당사가 현재 임상진행중인 파이프라인을 라이센스아웃 하거나 기존 라이센스아웃한 MLR-1023등과 관련하여 향후 수취하게될 benefit sharing 등은 모두 외화로 결제될 예정이며 당사가 계획중인 수출비중 확대 등이 현실화 될 경우 환율 변동, 특히 미국 달러 변동이 당사에 미치는 영향은 더욱 커질 것으로 전망됩니다.
(중략)
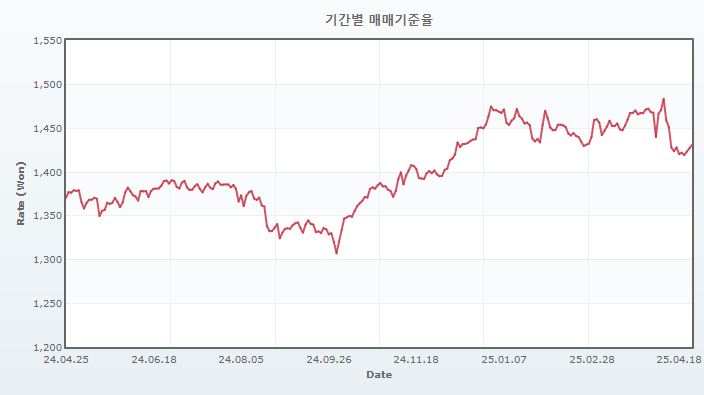
특히 2025년 1월 트럼프 정부 출범으로 인해 글로벌 보호무역 기조 및 정책 불확실성은 더욱 확대되고 있는 상황입니다. 트럼프 대통령은 대선 이전 경선 과정부터 보편관세 도입을 피력하였으며, 2025년 4월 2일 트럼프 정부는 미국과 교역하는 모든 국가에 상호 관세를 부과하기로 발표하였습니다. 먼저, 미국으로 들어오는 모든 수입품에 기본 10% 관세를, 다음으로 미국과 무역 흑자를 내고 있는 약 60여 교역국에는 개별 관세를 부과하기로 결정하였습니다. 한국 26%, 중국 34%, 유럽연합 20%, 일본 24%, 인도 26% 등 각 국가별로 차등을 두어 개별 관세를 부과할 예정이며 기본 관세는 4월 5일부터, 개별 관세는 4월 9일부터 시행하겠다고 발표하였습니다. 한편, 상호관세 부과에 따른 미중 갈등이 격화되며, 4월 9일 트럼프 정부는 중국을 제외한 국가에 대한 상호관세를 90일간 유예하고 해당 기간동안 관세율을 10%로 인하 및 중국에는 125%의 관세를 부과하는 조치(2025년 2월 펜타닐 유입을 문제삼아 중국에 부과한 관세율 20%와 합산하여 미국의 대중국 관세율은 총 145%로 추산)를 발표하였습니다. 하지만, 미국과 중국의 분쟁이 더욱 심화되는 모습을 보이며, 트럼프 정부는 다시금 대중 관세율 인하 가능성을 시사하는 등 실물 및 금융시장 변동성은 여전히 확대된 상황입니다. 이로 인해 미국 자산에 대한 시장 불확실성이 커지며 달러 약세 심리가 자극되고 있고 이는 환율 변동성을 더욱 확대하는 요인이며, 현재 원달러 환율은 1430원대 전후를 등락하고 있습니다. 향후 트럼프 정부의 관세 정책 향방 및 글로벌 자산 투자 심리 변동에 따라 환율 변동성이 크게 확대될 수 있으므로 투자자 분들은 이 점 유의하시기 바랍니다.
 |
|
원달러 환율 추이 |
| (자료 : 서울외국환중개소) |
최근 글로벌 경제 및 정치적 상황의 불확실성, 중동 지정학적 리스크와 함께 트럼프 미국 대통령의 관세 등 예측불가능한 정책 으로 환율 변동성이 크게 확대되는 추세를 보이고 있습니다. 외부적인 요인에 의한 환율 변동은 당사의 수익성에 직간접적인 영향을 미칠 수 있으며 향후 그 영향도가 더욱 높아질 개연성이 존재합니다. 따라서 환율 변동의 불확실성 확대가 당사의 경영성과 및 재무상태에 영향을 미칠 수 있는점 투자자 여러분께서는 참고하시기 바랍니다.
(주9) 정정 후
당사는 국제적으로 영업활동을 영위하고 있어 외환위험, 특히 주로 달러 및 유로화와 관련된 환율변동위험에 노출되어 있습니다. 외환위험은 당사가 보유하고 있는 외화표시 금융자산 및 금융부채, 해외사업장에 대한 순투자와 관련하여 발생하고 있습니다. 2025년 3월 31일 기준 다른 모든 변수가 일정하고 달러, 유로화 및 엔화에 대한 원화환율이 10% 변동시 당사의 세후 이익 및 자본에 미치는 영향은 아래 표와 같습니다.
| (단위: 원) |
| 구 분 | 세후 이익에 대한 영향 | 자본에 대한 영향 | |||
|---|---|---|---|---|---|
| 2025년 1분기 | 2024년 1분기 | 2025년 1분기 | 2024년 1분기 | ||
| 유로화/원 | 상승시 | (60,826,051) | (631,732,059) | (60,826,051) | (631,732,059) |
| 하락시 | 60,826,051 | 631,732,059 | 60,826,051 | 631,732,059 | |
| 미국달러/원 | 상승시 | (53,245,235) | - | (53,245,235) | - |
| 하락시 | 53,245,235 | - | 53,245,235 | - | |
| 일본엔화/원 | 상승시 | (403,818) | - | (403,818) | - |
| 하락시 | 403,818 | - | 403,818 | - | |
| (자료 : 당사 분기보고서) |
현재로서 해당 환율변동이 당사의 수익성에 미치는 영향은 미미한 수준으로 판단됩니다. 다만 당사가 대외적으로 표명중인 Global Open Innovation 전략에 따라 당사는 향후에도 다양한 해외 제약회사 및 바이오벤처사와 협업을 진행할 예정입니다.특히, 당사가 현재 임상진행중인 파이프라인을 라이센스아웃 하거나 기존 라이센스아웃한 MLR-1023등과 관련하여 향후 수취하게될 benefit sharing 등은 모두 외화로 결제될 예정이며 당사가 계획중인 수출비중 확대 등이 현실화 될 경우 환율변동이 당사에 미치는 영향은 더욱 커질 것으로 전망됩니다.
(중략)
특히 2025년 1월 트럼프 정부 출범으로 인해 글로벌 보호무역 기조 및 정책 불확실성은 더욱 확대되고 있는 상황입니다. 트럼프 대통령은 대선 이전 경선 과정부터 보편관세 도입을 피력하였으며, 2025년 4월 2일 트럼프 정부는 미국과 교역하는 모든 국가에 상호 관세를 부과하기로 발표하였습니다. 먼저, 미국으로 들어오는 모든 수입품에 기본 10% 관세를, 다음으로 미국과 무역 흑자를 내고 있는 약 60여 교역국에는 개별 관세를 부과하기로 결정하였습니다. 한국 26%, 중국 34%, 유럽연합 20%, 일본 24%, 인도 26% 등 각 국가별로 차등을 두어 개별 관세를 부과할 예정이며 기본 관세는 4월 5일부터, 개별 관세는 4월 9일부터 시행하겠다고 발표하였습니다.
한편, 상호관세 부과에 따른 미중 갈등이 격화되며, 4월 9일 트럼프 정부는 중국을 제외한 국가에 대한 상호관세를 90일간 유예하고 해당 기간동안 관세율을 10%로 인하 및 중국에는 125%의 관세를 부과하는 조치(2025년 2월 펜타닐 유입을 문제삼아 중국에 부과한 관세율 20%와 합산하여 미국의 대중국 관세율은 총 145%로 추산)를 발표하였습니다. 하지만, 다시금 미중 관세협상에 우호적인 분위기가 감지되며 위안화 가치 상승 기대감이 부각되고 미국과 대만간 협상에 따른 대만달러 통화절상 압력이 제기되는 등 전반적인 아시아 통화에 대한 상승 압력이 확대되며, 환율시장 변동성이 확대된 모습입니다. 이로 인해 현재 원달러 환율은 4월 대비 급락하여 1380원대 전후를 등락하고 있습니다. 향후 트럼프 정부의 관세 정책 향방 및 금융시장 변동에 따라 환율 변동성이 크게 확대될 수 있으므로 투자자 분들은 이 점 유의하시기 바랍니다.
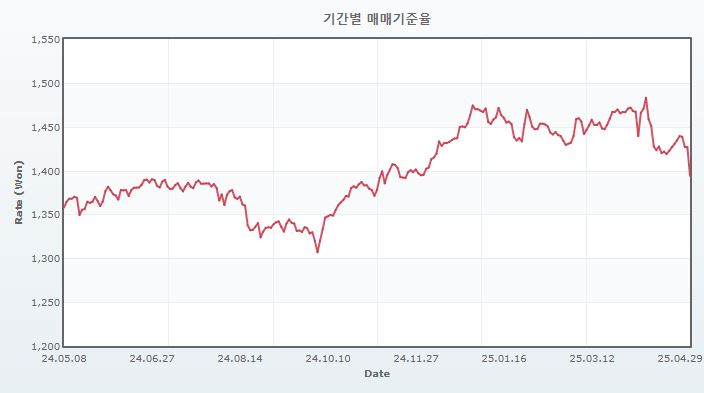 |
|
원달러 환율 추이_2 |
| (자료 : 서울외국환중개소) |
최근 글로벌 경제 및 정치적 상황의 불확실성, 중동 지정학적 리스크와 함께 트럼프 미국 대통령의 관세 등 예측불가능한 정책 으로 환율 변동성이 크게 확대되는 추세를 보이고 있습니다. 외부적인 요인에 의한 환율 변동은 당사의 수익성에 직간접적인 영향을 미칠 수 있으며 향후 그 영향도가 더욱 높아질 개연성이 존재합니다. 따라서 환율 변동의 불확실성 확대가 당사의 경영성과 및 재무상태에 영향을 미칠 수 있는점 투자자 여러분께서는 참고하시기 바랍니다.
(주10) 정정 전
당사는 당뇨병, 간질환 및 중추신경계(CNS) 질환 치료제 시장에서 선도적인 지위를 확보하고 있으며, 인지도가 높은 주요 제품들을 생산·판매하고 있습니다. 이러한 제품을 통해 창출되는 영업현금흐름은 신약 파이프라인 임상, 제제 개발, 연구 등 연구개발 활동에 필요한 운영자금으로 재투자되어 선순환 구조를 이루고 있습니다. 당사는 이와 같은 구조를 기반으로 향후 사업 외형을 지속적으로 확대해 나갈 계획입니다. 따라서 안정적인 현금흐름 확보는 당사의 영업 환경과 성장 전략에 있어 매우 중요한 요소라 할 수 있습니다.
최근 4개년 당사의 현금흐름표는 다음과 같습니다.
| [당사 요약연결현금흐름표] |
| (단위: 백만원) |
| 구 분 | 2024 | 2023 | 2022 | 2021 |
| 영업활동현금흐름 | 34,362 | (9,362) | 16,461 | 26,543 |
| 투자활동현금흐름 | (27,727) | (2,319) | (3,150) | 4,749 |
| 재무활동현금흐름 | (67,651) | 76,839 | (10,398) | (27,484) |
| 환율변동효과 반영전 현금및현금성자산의 순증가(감소) | (61,016) | 65,158 | 2,913 | 3,808 |
| 현금및현금성자산에 대한 환율변동효과 | (120) | 553 | (173) | (321) |
| 현금및현금성자산의 순증가(감소) | (61,136) | 65,710 | 2,740 | 3,486 |
| 기초현금및현금성자산 | 151,227 | 85,517 | 82,777 | 79,291 |
| 기말현금및현금성자산 | 90,091 | 151,227 | 85,517 | 82,777 |
| (자료 : 당사 사업보고서) |
당사는 2021년 및 2022년에 순유입의 영업현금흐름을 기록하였으나, 2023년에는 영업적자 발생으로 인해 영업현금흐름이 마이너스로 전환되었습니다. 다만, 약 800억 원 규모의 신규 차입이 이루어지면서 재무활동현금흐름으로 763억 원이 유입되었고, 이에 따라 2023년 말 현금 및 현금성자산은 전년 대비 증가한 1,512억 원을 기록하였습니다. 2024년에는 2023년에 단행한 경영구조 개선 효과가 온전히 반영되며 영업현금흐름이 344억 원으로 증가하였습니다. 반면, 자회사 Contera Pharma 투자자의 풋옵션 행사로 인해 677억 원이 유출되면서 재무활동현금흐름은 마이너스를 기록하였습니다.
앞으로 당사의 안정적인 영업실적 개선이 지속될 것으로 기대되며, 이에 따라 영업현금흐름도 점진적으로 증가할 것으로 전망됩니다. 당사는 이를 기반으로 신약 개발 등 주요 투자 활동에 자금을 재투자하는 선순환 구조를 구축해 나갈 계획입니다. 다만, 예기치 못한 외부 변수로 인해 2023년과 같은 영업적자가 발생할 경우, 영업현금흐름이 다시 순유출로 전환될 수 있으며, 이는 유동성 부족으로 이어져 추가적인 자금 조달 또는 차입이 필요할 수 있습니다. 제약업체인 당사에게 있어 안정적인 현금흐름 확보는 핵심적인 경영 과제이므로, 투자자 여러분께서는 당사의 현금흐름 추이를 충분히 고려하신 후 투자 의사결정을 해주시기 바랍니다.
(주10) 정정 후
당사는 당뇨병, 간질환 및 중추신경계(CNS) 질환 치료제 시장에서 선도적인 지위를 확보하고 있으며, 인지도가 높은 주요 제품들을 생산·판매하고 있습니다. 이러한 제품을 통해 창출되는 영업현금흐름은 신약 파이프라인 임상, 제제 개발, 연구 등 연구개발 활동에 필요한 운영자금으로 재투자되어 선순환 구조를 이루고 있습니다. 당사는 이와 같은 구조를 기반으로 향후 사업 외형을 지속적으로 확대해 나갈 계획입니다. 따라서 안정적인 현금흐름 확보는 당사의 영업 환경과 성장 전략에 있어 매우 중요한 요소라 할 수 있습니다.
최근 4개년 당사의 현금흐름표는 다음과 같습니다.
| [당사 요약연결현금흐름표] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 |
| 영업활동현금흐름 | 7,244 | 12,745 | 34,362 | (9,362) | 16,461 | 26,543 |
| 투자활동현금흐름 | (8,488) | (946) | (27,727) | (2,319) | (3,150) | 4,749 |
| 재무활동현금흐름 | (995) | (1,136) | (67,651) | 76,839 | (10,398) | (27,484) |
| 환율변동효과 반영전 현금및현금성자산의 순증가(감소) | (2,239) | 10,664 | (61,016) | 65,158 | 2,913 | 3,808 |
| 현금및현금성자산에 대한 환율변동효과 | (39) | 569 | (120) | 553 | (173) | (321) |
| 현금및현금성자산의 순증가(감소) | (2,278) | 11,232 | (61,136) | 65,710 | 2,740 | 3,486 |
| 기초현금및현금성자산 | 90,091 | 151,227 | 151,227 | 85,517 | 82,777 | 79,291 |
| 기말현금및현금성자산 | 87,813 | 162,459 | 90,091 | 151,227 | 85,517 | 82,777 |
| (자료 : 당사 사업보고서 및 분기보고서) |
당사는 2021년 및 2022년에 순유입의 영업현금흐름을 기록하였으나, 2023년에는 영업적자 발생으로 인해 영업현금흐름이 마이너스로 전환되었습니다. 다만, 약 800억 원 규모의 신규 차입이 이루어지면서 재무활동현금흐름으로 763억 원이 유입되었고, 이에 따라 2023년 말 현금 및 현금성자산은 전년 대비 증가한 1,512억 원을 기록하였습니다. 2024년에는 2023년에 단행한 경영구조 개선 효과가 온전히 반영되며 영업현금흐름이 344억 원으로 증가하였습니다. 반면, 자회사 Contera Pharma 투자자의 풋옵션 행사로 인해 677억 원이 유출되면서 재무활동현금흐름은 마이너스를 기록하였습니다. 한편, 2025년 1분기 당사는 기타유동금융자산 증가와 CAPEX 투자 지속 등으로 인한 85억원의 투자활동현금유출과 이자지급에 따른 10억원의 재무활동현금유출이 발생하며 2025년 1분기말 현금 및 현금성 자산은 전년 대비 소폭 하락한 878억원을 기록하였으나, 현금 순유출 규모가 크지 않아 우려할 상황은 아닌 것으로 판단됩니다.
앞으로 당사의 안정적인 영업실적 개선이 지속될 것으로 기대되며, 이에 따라 영업현금흐름도 점진적으로 증가할 것으로 전망됩니다. 당사는 이를 기반으로 신약 개발 등 주요 투자 활동에 자금을 재투자하는 선순환 구조를 구축해 나갈 계획입니다. 다만, 예기치 못한 외부 변수로 인해 2023년과 같은 영업적자가 발생할 경우, 영업현금흐름이 다시 순유출로 전환될 수 있으며, 이는 유동성 부족으로 이어져 추가적인 자금 조달 또는 차입이 필요할 수 있습니다. 제약업체인 당사에게 있어 안정적인 현금흐름 확보는 핵심적인 경영 과제이므로, 투자자 여러분께서는 당사의 현금흐름 추이를 충분히 고려하신 후 투자 의사결정을 해주시기 바랍니다.
(주11) 정정 전
당사는 연구개발본부 산하 허가등록부, 개발부, 연구소 등으로 구성된 내부 연구개발 조직을 보유하고 있으며, 자회사들 또한 연구개발 중심의 전문 조직 체계를 갖추고 있습니다. 제약업의 특성상 연구개발 분야에서 핵심 인재를 확보하는 것이 중요한 경쟁력으로 작용하기 때문에, 당사는 박사급 14명, 석사급 30명을 포함한 총 66명의 연구인력을 확보하고 있습니다. 당사는 우수한 인재들에게 적절한 보상과 동기 부여를 제공함으로써 인력의 안정적 유지에 힘쓰고 있으며, 향후에도 연구개발 경쟁력 강화를 위해 우수 인재 영입에 최선을 다할 계획입니다. 증권신고서 제출일 기준 당사의 연구인력 현황은 다음과 같습니다.
| [당사 연구인력 현황] |
| (단위: 명) |
| 구분 | 박사 | 석사 | 학사 | 기타 | 합계 |
| 부광약품 연구개발인력 | 4 | 30 | 16 | 1 | 51 |
| Contera Pharma A/S | 9 | - | 5 | - | 14 |
| ProteKt Therapeutics | 1 | - | - | - | 1 |
| 합계 | 14 | 30 | 21 | 1 | 66 |
| (자료 : 당사 제시) |
최근 3개년 연구소 소속 인력 변동 현황은 다음과 같습니다.
| [당사 연구 인력 변동 사항] |
| (단위 : 명) |
| 구분 | 직위 | 기초 | 증가 | 감소 | 기말 |
|---|---|---|---|---|---|
| 2022년도 | 부광약품 연구개발인력 | 36 | 25 | 14 | 47 |
| Contera Pharma A/S | 7 | 13 | 1 | 19 | |
| ProteKt Therapeutics | - | - | - | - | |
| 계 | 43 | 38 | 15 | 66 | |
| 2023년도 | 부광약품 연구개발인력 | 47 | 13 | 18 | 42 |
| Contera Pharma A/S | 19 | 3 | 3 | 19 | |
| ProteKt Therapeutics | - | 1 | - | 1 | |
| 계 | 66 | 17 | 21 | 62 | |
| 2024년도 | 부광약품 연구개발인력 | 42 | 19 | 19 | 42 |
| Contera Pharma A/S | 19 | 4 | 9 | 14 | |
| ProteKt Therapeutics | 1 | - | - | 1 | |
| 계 | 62 | 23 | 28 | 57 | |
| 증권신고서 제출일 현재 |
부광약품 연구개발인력 | 42 | 12 | 3 | 51 |
| Contera Pharma A/S | 14 | - | - | 14 | |
| ProteKt Therapeutics | 1 | - | - | 1 | |
| 계 | 57 | 12 | 3 | 66 |
| (출처: 당사 내부자료) |
한편 당사는 특허를 통해 핵심기술에 대한 권리보호 전략을 시행하고 있으나, 핵심 연구 인력의 유출은 당사가 축척해온 기술관련 노하우 등의 기술유출 위험을 내포하고 있습니다. 특히 당사 핵심 연구인력의 유출은 당사의 사업계획 및 주요 임상 진행 계획에 차질을 발생시킬 수 있습니다. 따라서, 핵심 연구개발인력의 동기부여 및 이탈방지 목적으로 핵심 연구개발인력들을 대상으로 성과에 따른 인센티브 등의 금전적 보상을 제공하고, 자유로운 연구 환경과 경력 개발 기회를 지원하고 있습니다. 또한 우수성과 시상, 학회 참여, 유연근무제 도입 등 비금전적 동기요소를 강화하여 핵심 인력의 조직 내 안착을 유도하고 있습니다.
당사의 연결 기준 매출액 대비 연구개발비 비중은 2021년 14.89%, 2022년 15.39%로 유사한 수준을 유지하였으나, 2023년에는 31.38%로 큰 폭 상승하였습니다. 이는 2023년 매출액이 감소한 가운데, JM-010 임상 관련 연구개발비가 대규모로 집행된 데에 기인합니다. 실제 2023년 연결 기준 연구개발비는 395억 원으로, 전년 동기 대비 34.4% 증가하였습니다. 다만 JM-010 임상이 2024년에 종료됨에 따라, 2024년 연결 기준 연구개발비는 284억 원으로 감소하였으며, 매출액 대비 비중 또한 17.73%로 축소되어 2021~2022년 수준으로 회귀하였습니다. 별도 기준 매출액 대비 연구개발비 비중 역시 2023년에는 16.34%로 전년 대비 큰 폭으로 상승하였는데, 이 또한 JM-010 임상개발 비용 집행과 직접적인 관련이 있습니다. 참고로, JM-010의 유럽 임상은 자회사인 Contera Pharma에서, 미국 및 한국 임상은 당사에서 각각 진행하였기에, 당사 별도 및 연결 기준 모두에서 2023년 연구개발비가 증가한 것으로 판단됩니다.
| [당사 연결기준 연구개발비 현황] |
| (단위: 백만원) |
| 구 분 | 2024 | 2023 | 2022 | 2021 | |
|---|---|---|---|---|---|
| 비용의성격별 분류 | 원재료비 | 4,147 | 3,584 | 2,900 | 2,677 |
| 인건비 | 10,537 | 10,021 | 6,565 | 6,919 | |
| 감가상각비 | 1,052 | 587 | 216 | 214 | |
| 위탁용역비 | 9,317 | 14,754 | 12,201 | 12,840 | |
| 기타 | 3,333 | 10,570 | 7,501 | 4,524 | |
| 연구개발비용 합계 | 28,386 | 39,516 | 29,383 | 27,174 | |
| 회계처리내역 | 판매비와 관리비 | 23,430 | 34,551 | 24,274 | 22,465 |
| 제조경비 | 4,956 | 4,965 | 5,108 | 4,709 | |
| 개발비(무형자산) | - | - | - | - | |
| 회계처리금액 계 | 28,386 | 39,516 | 29,382 | 27,174 | |
| 정부보조금 | - | - | - | - | |
| 연구개발비용 합계 | 28,386 | 39,516 | 29,382 | 27,174 | |
| 연구개발비 / 매출액 비율 | 17.73% | 31.38% | 15.39% | 14.89% | |
| [연구개발비용합계÷당기매출액×100] | |||||
| (자료 : 당사 사업보고서) |
| [당사 별도기준 연구개발비 현황] |
| (단위: 백만원) |
| 구 분 | 2024 | 2023 | 2022 | 2021 | |
|---|---|---|---|---|---|
| 비용의성격별 분류 | 원재료비 | 2,727 | 2,620 | 2,773 | 2,406 |
| 인건비 | 6,544 | 6,686 | 6,238 | 6,510 | |
| 감가상각비 | 396 | 301 | 216 | 214 | |
| 위탁용역비 | 3,375 | 8,289 | 6,307 | 9,383 | |
| 기타 | 1,829 | 2,551 | 1,577 | 1,145 | |
| 연구개발비용 합계 | 14,871 | 20,447 | 17,111 | 19,658 | |
| 회계처리내역 | 판매비와 관리비 | 9,915 | 15,482 | 12,003 | 14,949 |
| 제조경비 | 4,956 | 4,965 | 5,108 | 4,709 | |
| 개발비(무형자산) | - | - | - | - | |
| 회계처리금액 계 | 14,872 | 20,447 | 17,111 | 19,658 | |
| 정부보조금 | - | - | - | - | |
| 연구개발비용 합계 | 14,872 | 20,447 | 17,111 | 19,658 | |
| 연구개발비 / 매출액 비율 | 9.44% | 16.34% | 8.99% | 11.84% | |
| [연구개발비용합계÷당기매출액×100] | |||||
| (자료 : 당사 사업보고서) |
당사와 같은 제약업체는 미래 한단계 도약하기 위해서는 연구개발활동이 필수적입니다. 다만 연구개발비가 급격히 증가할 경우 당사 수익성에 영향을 미칠 수 있으며 향후 개발임상이 실패할 시 해당비용은 매몰비용으로 회수에 어려움을 겪게 될 수 있습니다. 투자자분들께서는 이점 참고하시기 바랍니다.
(주11) 정정 후
당사는 연구개발본부 산하 허가등록부, 개발부, 연구소 등으로 구성된 내부 연구개발 조직을 보유하고 있으며, 자회사들 또한 연구개발 중심의 전문 조직 체계를 갖추고 있습니다. 제약업의 특성상 연구개발 분야에서 핵심 인재를 확보하는 것이 중요한 경쟁력으로 작용하기 때문에, 당사는 박사급 13명, 석사급 30명을 포함한 총 65명의 연구인력을 확보하고 있습니다. 당사는 우수한 인재들에게 적절한 보상과 동기 부여를 제공함으로써 인력의 안정적 유지에 힘쓰고 있으며, 향후에도 연구개발 경쟁력 강화를 위해 우수 인재 영입에 최선을 다할 계획입니다. 증권신고서 제출일 기준 당사의 연구인력 현황은 다음과 같습니다.
| [당사 연구인력 현황] |
| (단위: 명) |
| 구분 | 박사 | 석사 | 학사 | 기타 | 합계 |
| 부광약품(주) 연구소 | 3 | 30 | 15 | 1 | 49 |
| Contera Pharma A/S | 9 | - | 6 | - | 15 |
| ProteKt Therapeutics | 1 | - | - | - | 1 |
| JaguAHR Therapeutics | - | - | - | - | - |
| 합계 | 13 | 30 | 21 | 1 | 65 |
| (자료 : 당사 제시) |
최근 3개년 연구소 소속 인력 변동 현황은 다음과 같습니다.
| [당사 연구 인력 변동 사항] |
| (단위 : 명) |
| 구분 | 직위 | 기초 | 증가 | 감소 | 기말 |
|---|---|---|---|---|---|
| 2022년도 | 부광약품 연구개발인력 | 36 | 25 | 14 | 47 |
| Contera Pharma A/S | 7 | 13 | 1 | 19 | |
| ProteKt Therapeutics | - | - | - | - | |
| 계 | 43 | 38 | 15 | 66 | |
| 2023년도 | 부광약품 연구개발인력 | 47 | 13 | 18 | 42 |
| Contera Pharma A/S | 19 | 3 | 3 | 19 | |
| ProteKt Therapeutics | - | 1 | - | 1 | |
| 계 | 66 | 17 | 21 | 62 | |
| 2024년도 | 부광약품 연구개발인력 | 42 | 19 | 19 | 42 |
| Contera Pharma A/S | 19 | 4 | 9 | 14 | |
| ProteKt Therapeutics | 1 | - | - | 1 | |
| 계 | 62 | 23 | 28 | 57 | |
| 증권신고서 제출일 현재 |
부광약품 연구개발인력 | 42 | 12 | 5 | 49 |
| Contera Pharma A/S | 14 | 1 | - | 15 | |
| ProteKt Therapeutics | 1 | - | - | 1 | |
| JaguAHR Therapeutics | - | - | - | - | |
| 계 | 57 | 13 | 5 | 65 |
| (출처: 당사 내부자료) |
한편 당사는 특허를 통해 핵심기술에 대한 권리보호 전략을 시행하고 있으나, 핵심 연구 인력의 유출은 당사가 축척해온 기술관련 노하우 등의 기술유출 위험을 내포하고 있습니다. 특히 당사 핵심 연구인력의 유출은 당사의 사업계획 및 주요 임상 진행 계획에 차질을 발생시킬 수 있습니다. 따라서, 핵심 연구개발인력의 동기부여 및 이탈방지 목적으로 핵심 연구개발인력들을 대상으로 성과에 따른 인센티브 등의 금전적 보상을 제공하고, 자유로운 연구 환경과 경력 개발 기회를 지원하고 있습니다. 또한 우수성과 시상, 학회 참여, 유연근무제 도입 등 비금전적 동기요소를 강화하여 핵심 인력의 조직 내 안착을 유도하고 있습니다.
당사의 연결 기준 매출액 대비 연구개발비 비중은 2021년 14.89%, 2022년 15.39%로 유사한 수준을 유지하였으나, 2023년에는 31.38%로 큰 폭 상승하였습니다. 이는 2023년 매출액이 감소한 가운데, JM-010 임상 관련 연구개발비가 대규모로 집행된 데에 기인합니다. 실제 2023년 연결 기준 연구개발비는 395억 원으로, 전년 동기 대비 34.4% 증가하였습니다. 다만 JM-010 임상이 2024년에 종료됨에 따라, 2024년 연결 기준 연구개발비는 284억 원으로 감소하였으며, 매출액 대비 비중 또한 17.73%로 축소되어 2021~2022년 수준으로 회귀하였습니다. 별도 기준 매출액 대비 연구개발비 비중 역시 2023년에는 16.34%로 전년 대비 큰 폭으로 상승하였는데, 이 또한 JM-010 임상개발 비용 집행과 직접적인 관련이 있습니다. 참고로, JM-010의 유럽 임상은 자회사인 Contera Pharma에서, 미국 및 한국 임상은 당사에서 각각 진행하였기에, 당사 별도 및 연결 기준 모두에서 2023년 연구개발비가 증가한 것으로 판단됩니다. 한편, 2025년 1분기는 JM-010 임상개발 종료 영향으로 연구개발비용이 57억원 수준으로 감소하고 당사 주요 제품의 매출 성장으로 인해 매출이 전년동기대비 급성장하며, 매출액 대비 연구개발비 비중은 12% 수준으로 감소하였습니다. 다만, CP-012, BUK-001 등 후속 파이프라인에 대한 연구개발이 가속화 되며 연구개발비 비중은 예년 수준으로 상승할 것으로 예상됩니다.
| [당사 연결기준 연구개발비 현황] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 | |
|---|---|---|---|---|---|---|---|
| 비용의성격별 분류 | 원재료비 | 904 | 695 | 4,147 | 3,584 | 2,900 | 2,677 |
| 인건비 | 3,081 | 2,540 | 10,537 | 10,021 | 6,565 | 6,919 | |
| 감가상각비 | 203 | 181 | 1,052 | 587 | 216 | 214 | |
| 위탁용역비 | 870 | 2,564 | 9,317 | 14,754 | 12,201 | 12,840 | |
| 기타 | 680 | 1,225 | 3,333 | 10,570 | 7,501 | 4,524 | |
| 연구개발비용 합계 | 5,739 | 7,205 | 28,386 | 39,516 | 29,383 | 27,174 | |
| 회계처리내역 | 판매비와 관리비 | 4,452 | 6,056 | 23,430 | 34,551 | 24,274 | 22,465 |
| 제조경비 | 1,287 | 1,149 | 4,956 | 4,965 | 5,108 | 4,709 | |
| 개발비(무형자산) | - | - | - | - | - | - | |
| 회계처리금액 계 | 5,739 | 7,205 | 28,386 | 39,516 | 29,382 | 27,174 | |
| 정부보조금 | - | - | - | - | - | - | |
| 연구개발비용 합계 | 5,739 | 7,205 | 28,386 | 39,516 | 29,3832 | 27,174 | |
| 연구개발비 / 매출액 비율 | 12.00% | 20.95% | 17.73% | 31.38% | 15.39% | 14.89% | |
| [연구개발비용합계÷당기매출액×100] | |||||||
| (자료 : 당사 사업보고서 및 분기보고서) |
| [당사 별도기준 연구개발비 현황] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 | |
|---|---|---|---|---|---|---|---|
| 비용의성격별 분류 | 원재료비 | 487 | 500 | 2,727 | 2,620 | 2,773 | 2,406 |
| 인건비 | 1,851 | 1,650 | 6,544 | 6,686 | 6,238 | 6,510 | |
| 감가상각비 | 131 | 92 | 396 | 301 | 216 | 214 | |
| 위탁용역비 | 300 | 1,201 | 3,375 | 8,289 | 6,307 | 9,383 | |
| 기타 | 465 | 416 | 1,829 | 2,551 | 1,577 | 1,145 | |
| 연구개발비용 합계 | 3,233 | 3,859 | 14,871 | 20,447 | 17,111 | 19,658 | |
| 회계처리내역 | 판매비와 관리비 | 1,946 | 2,711 | 9,915 | 15,482 | 12,003 | 14,949 |
| 제조경비 | 1,287 | 1,149 | 4,956 | 4,965 | 5,108 | 4,709 | |
| 개발비(무형자산) | - | - | - | - | - | - | |
| 회계처리금액 계 | 3,233 | 3,859 | 14,872 | 20,447 | 17,111 | 19,658 | |
| 정부보조금 | - | - | - | - | - | - | |
| 연구개발비용 합계 | 3,233 | 3,859 | 14,872 | 20,447 | 17,111 | 19,658 | |
| 연구개발비 / 매출액 비율 | 7.37% | 11.34% | 9.44% | 16.34% | 8.99% | 11.84% | |
| [연구개발비용합계÷당기매출액×100] | |||||||
| (자료 : 당사 사업보고서 및 분기보고서) |
당사와 같은 제약업체는 미래 한단계 도약하기 위해서는 연구개발활동이 필수적입니다. 다만 연구개발비가 급격히 증가할 경우 당사 수익성에 영향을 미칠 수 있으며 향후 개발임상이 실패할 시 해당비용은 매몰비용으로 회수에 어려움을 겪게 될 수 있습니다. 투자자분들께서는 이점 참고하시기 바랍니다.
(주12) 정정 전
증권신고서 제출일 현재 당사의 우발부채 현황은 다음과 같습니다.
(1) 당사가 금융기관과 체결하고 있는 약정사항의 내역
| (단위: 원, USD) |
| 금융기관 | 약정사항 | 증권신고서 제출일 | 2023년말 | ||
|---|---|---|---|---|---|
| 한도금액 | 사용금액 | 한도금액 | 사용금액 | ||
| 하나은행 | 일반자금대출 | 30,000,000,000 | 30,000,000,000 | 30,000,000,000 | 30,000,000,000 |
| 수입신용장 | USD 1,000,000 | - | USD 1,000,000 | - | |
| 국민은행 | 일반자금대출 | 30,000,000,000 | - | 40,000,000,000 | - |
| 산업은행 | 일반자금대출 | 10,000,000,000 | - | 10,000,000,000 | - |
| 신한은행 | 일반자금대출 | 50,000,000,000 | 50,000,000,000 | 50,000,000,000 | 50,000,000,000 |
| (자료 : 당사 제시) |
상기 약정 이외에 당사는 국민은행과 기업구매론약정(증권신고서 제출일 현재: 한도 10,000백만원, 2023년말: 한도 10,000백만원)과 신한은행과 전자방식외상매출채권담보대출약정(증권신고서 제출일 현재: 한도 2,500백만원, 2023년말: 한도 2,500백만원)의 공급자금융약정을 체결하고 있습니다.
증권신고서 제출일 현재 매입채무및기타채무 금액 중 공급자금융약정과 관련된 금융부채는 2,449백만원이며, 공급자가 금융기관으로부터 증권신고서 제출일 현재 이미 대금을 수취한 금액은 441백만원입니다.
공급자금융약정에 해당하는 금융부채와 공급자금융약정에 해당하지 않는 금융부채의 지급기일에는 유의적인 차이가 없습니다.
공급자금융약정에 따라 금융기관에게 지급해야 할 금액은 회사의 정상영업주기 내에사용되는 운전자본의 일부로서 매입채무및기타채무와 유사한 성격과 기능을 지니고 있다고 판단하여 이를 매입채무 및 기타채무로 분류하고, 현금흐름표에서 관련 현금흐름을 영업활동현금흐름으로 분류하고 있습니다.
(2) 당사가 타인으로부터 제공받은 지급보증의 내역
| (단위: 원) |
| 금융기관 | 약정사항 | 보증금액 | |
|---|---|---|---|
| 증권신고서 제출일 | 2023년말 | ||
| 서울보증보험 | 납품계약이행보증 | - | 7,000,000 |
| 공탁보증 | 60,000,000 | 111,750,000 | |
| 물품대금보증 | 1,000,000,000 | - | |
| 합 계 | 1,060,000,000 | 118,750,000 | |
| (자료 : 당사 제시) |
(3) 증권신고서 제출일 현재 차입금 등과 관련하여 담보로 제공되어있는 자산내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 제공처 | 내역 | 담보제공자산 | 장부금액 | 설정금액 |
| 유형자산 | 신한은행 | 차입금 담보 | 토지,건물 | 73,543,176,915 | 60,000,000,000 |
| (자료 : 당사 제시) |
(4) 증권신고서 제출 현재 당사가 원고로서 진행 중인 소송은 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소소송 1건, 권리범위확인(특) 3건, 총 4건(2023년말: 1건)입니다. 반면 피고로서 진행중인 소송은 권리범위확인(특) 총 1건(2023년말: 0건)입니다.
| 관할법원 | 원고 | 피고 | 소송의 내용 | 소송가액 | 진행상황 |
| 서울고등법원 | 당사 | 보건복지부장관 | 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소 | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 에치케이이노엔 | 당사 | 권리범위확인(특) | - | 계류중 |
당사가 진행중인 5건의 소송 중 보건복지부장관을 피고로 당사가 제기한 소송은 당사 주요 제품인 레가론에 대한 보험급여 적용 중지에 대한 다툼 입니다. 만약 해당 소송에서 당사가 패소하게 될 경우 레가론에 대한 보헙급여가 중지되어 당사의 향후 레가론 매출 성장에 영향을 줄 수 있습니다. 특허법원에 계류중인 소송 4건은 모두 당사가 개발중인 케이캡 제네릭 관련 특허에 대한 다툼으로, 해당 소송과 동일한 소송이 국내 다수 제네릭 의약품 업체에서 병행 진행되고 있어 당사를 비롯한 이들 회사가 소송 결과에 직접적 영향을 받을 수 있습니다. 당사는 현재까지 케이캡 제네릭 제품을 생산 및 판매하고 있지 않기에 해당 소송에서 부정적인 결과가 나타나더라도 당사의 기존 제품 매출액에 영향을 줄 것으로 판단되진 않습니다. 다만 당사의 향후 매출 성장성에는 영향을 줄 수 있습니다.
(5) 당사는 종속기업인 Contera Pharma A/S와 관련하여 개발 중인 의약품의 허가신청, 시판 승인 및 상용화 조건 달성 여부에 따라 조건부대가를 지급하는 약정을 체결하였습니다. 2024년 중 당사는 해당 의약품의 임상을 중단하였으며, 이에 따라미래에 지불할 가능성이 있는 금액을 0으로 평가하였습니다(2023년말 : 기타금융부채 7,753백만원).
(6) 당사가 증권신고서 제출일 현재 보유 중인 당기손익-공정가치측정 금융자산 중 TVM LifeScience Innovation II SCSP에 대한 투자 약정금액은 총 USD 3,000,000이며, 현재까지 USD 2,623,072에 대한 납입이 완료되었습니다. 잔여금액 USD 376,928은 향후 업무집행사원의 출자이행요청에 따라 추가 납입예정이나, 현재 시점에 그 납입시기를 예상할 수 없습니다.
(7) 당사가 증권신고서 제출일 현재 보유 중인 당기손익-공정가치측정 금융자산 중 KDB오픈이노베이션 제2호에 대한 투자 약정금액은 총 5억원이며, 현재까지 5억원 납입이 완료되었습니다.
(8) 당사는 2020년 중 종속회사인 Contera Pharma A/S(이하 "종속회사")의 출자를 목적으로 설립된 에이치 델타 사모투자합자회사(이하 "투자자")와 주주 간 계약을 체결하였으며, 투자자는 취득한 종속회사의 보통주식 159,380주에 대한 주식매수청구권(Put option)을 보유하게 되었습니다. 투자자는 '기한 내에 종속회사의 적격기업공개(IPO)를 완료하지 못하는 경우 등' 행사 요건을 충족할 경우 당사를 상대로 보유지분 전량에 대해 주식매수청구권을 행사할 수 있으며, 투자자의 풋옵션 행사시 당사는 투자자가 보유한 종속기업 지분 전체에 대해 당사 또는 제3자에게 매도할 것을 청구할 수 있는 권리가 있습니다. 투자자는 당사가 종속기업의 지분을 제3자에게 매각하고자 할 경우, 동일한 조건으로 우선적으로 매도할 수 있는 권리를 보유하고 있습니다. 2024년 중 투자자는 당사를 상대로 Contera Pharma A/S의 보통주식 159,380주에 대한 주식매수청구권(Put option)을 행사하였으며, 당사는 인수대가 63,237백만원에 해당 주식 전량을 취득하고, 관련된 기타유동금융부채 63,237백만원을 제거하였습니다.
(9) 당사는 종속기업인 ProteKt Therapeutics와 관련하여 개발 중인 의약품의 License 관련 판매 및 배당 등의 조건 달성 여부에 따라 조건부대가를 지급하는 약정을 체결하였습니다.
당사는 금융기관과의 약정을 통해 800억원을 차입 중이나 별도 기준 현금을 약 797억원 보유 중이기에 여전히 (-)순차입금을 보이고 있는 상황입니다. 이에 당사의 영업현금흐름 등 고려 시 예상치 못한 긴급한 자금 소요로 인해 한도대가 추가 실행되더라도 대응 가능할 것으로 전망됩니다. 다만 자금 소요 규모가 커지게 될 경우 당사의 재무부담에 영향을 미칠 수 있습니다. 또한 당사가 계류중인 상기 소송사건의 최종결과를 합리적으로 예측할 수 없으므로, 향후 본 소송사건들의 진행 경과에 따라 당사 영업에 부정적으로 작용할 가능성이 존재합니다. 이에, 투자자분들께서는 상기우발채무가 현실화될 경우 당사의 재무상태에 부정적인 영향을 미칠 수 있는점 참고해 주시기 바랍니다.
(주12) 정정 후
증권신고서 제출일 현재 당사의 우발부채 현황은 다음과 같습니다.
(1) 당사가 금융기관과 체결하고 있는 약정사항의 내역
| (단위: 원, USD) |
| 금융기관 | 약정사항 | 증권신고서 제출일 | 2024년말 | ||
|---|---|---|---|---|---|
| 한도금액 | 사용금액 | 한도금액 | 사용금액 | ||
| 하나은행 | 일반자금대출 | 30,000,000,000 | 30,000,000,000 | 30,000,000,000 | 30,000,000,000 |
| 수입신용장 | USD 1,000,000 | - | USD 1,000,000 | - | |
| 국민은행 | 일반자금대출 | 30,000,000,000 | - | 40,000,000,000 | - |
| 산업은행 | 일반자금대출 | 10,000,000,000 | - | 10,000,000,000 | - |
| 신한은행 | 일반자금대출 | 50,000,000,000 | 50,000,000,000 | 50,000,000,000 | 50,000,000,000 |
| (자료 : 당사 제시) |
상기 약정 이외에 당사는 국민은행과 기업구매론약정(증권신고서 제출일 현재: 한도 10,000백만원, 2024년말: 한도 10,000백만원)과 신한은행과 전자방식외상매출채권담보대출약정(증권신고서 제출일 현재: 한도 2,500백만원, 2024년말: 한도 2,500백만원)의 공급자금융약정을 체결하고 있습니다.
증권신고서 제출일 현재 매입채무및기타채무 금액 중 공급자금융약정과 관련된 금융부채는 2,857백만원이며, 공급자가 금융기관으로부터 증권신고서 제출일 현재 이미 대금을 수취한 금액은 315백만원입니다.
공급자금융약정에 해당하는 금융부채와 공급자금융약정에 해당하지 않는 금융부채의 지급기일에는 유의적인 차이가 없습니다.
공급자금융약정에 따라 금융기관에게 지급해야 할 금액은 회사의 정상영업주기 내에사용되는 운전자본의 일부로서 매입채무및기타채무와 유사한 성격과 기능을 지니고 있다고 판단하여 이를 매입채무 및 기타채무로 분류하고, 현금흐름표에서 관련 현금흐름을 영업활동현금흐름으로 분류하고 있습니다.
(2) 당사가 타인으로부터 제공받은 지급보증의 내역
| (단위: 원) |
| 금융기관 | 약정사항 | 보증금액 | |
|---|---|---|---|
| 2025년 1분기말 | 2024년말 | ||
| 서울보증보험 | 공탁보증 | - | 60,000,000 |
| 물품대금보증 | 1,060,000,000 | 1,000,000,000 | |
| 합 계 | 1,060,000,000 | 1,060,000,000 | |
| (자료 : 당사 제시) |
(3) 증권신고서 제출일 현재 차입금 등과 관련하여 담보로 제공되어있는 자산내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 제공처 | 내역 | 담보제공자산 | 장부금액 | 설정금액 |
| 유형자산 | 신한은행 | 차입금 담보 | 토지,건물 | 73,543,176,915 | 60,000,000,000 |
| (자료 : 당사 제시) |
(4) 증권신고서 제출 현재 당사가 원고로서 진행 중인 소송은 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소소송 1건, 권리범위확인(특) 3건, 총 4건(2024년말: 4건)입니다. 또한 회사가 피고로서 진행중인 소송은 권리범위확인(특) 총 1건(2024년말: 1건)으로 소송가액은 없습니다.
| 관할법원 | 원고 | 피고 | 소송의 내용 | 소송가액 | 진행상황 |
| 서울고등법원 | 당사 | 보건복지부장관 | 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소 | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 에치케이이노엔 | 당사 | 권리범위확인(특) | - | 계류중 |
당사가 진행중인 5건의 소송 중 보건복지부장관을 피고로 당사가 제기한 소송은 당사 주요 제품인 레가론에 대한 보험급여 적용 중지에 대한 다툼 입니다. 만약 해당 소송에서 당사가 패소하게 될 경우 레가론에 대한 보헙급여가 중지되어 당사의 향후 레가론 매출 성장에 영향을 줄 수 있습니다. 특허법원에 계류중인 소송 4건은 모두 당사가 개발중인 케이캡 제네릭 관련 특허에 대한 다툼으로, 해당 소송과 동일한 소송이 국내 다수 제네릭 의약품 업체에서 병행 진행되고 있어 당사를 비롯한 이들 회사가 소송 결과에 직접적 영향을 받을 수 있습니다. 당사는 현재까지 케이캡 제네릭 제품을 생산 및 판매하고 있지 않기에 해당 소송에서 부정적인 결과가 나타나더라도 당사의 기존 제품 매출액에 영향을 줄 것으로 판단되진 않습니다. 다만 당사의 향후 매출 성장성에는 영향을 줄 수 있습니다.
(5) 당사는 종속기업인 Contera Pharma A/S와 관련하여 개발 중인 의약품의 허가신청, 시판 승인 및 상용화 조건 달성 여부에 따라 조건부대가를 지급하는 약정을 체결하였습니다. 2024년 중 당사는 해당 의약품의 임상을 중단하였으며, 이에 따라미래에 지불할 가능성이 있는 금액을 0으로 평가하였습니다.
(6) 당사가 증권신고서 제출일 현재 보유 중인 당기손익-공정가치측정 금융자산 중 TVM LifeScience Innovation II SCSP에 대한 투자 약정금액은 총 USD 3,000,000이며, 현재까지 USD 2,848,568에 대한 납입이 완료되었습니다. 잔여금액 USD 151,432은 향후 업무집행사원의 출자이행요청에 따라 추가 납입예정이나, 현재 시점에 그 납입시기를 예상할 수 없습니다.
(7) 당사가 증권신고서 제출일 현재 보유 중인 당기손익-공정가치측정 금융자산 중 KDB오픈이노베이션 제2호에 대한 투자 약정금액은 총 5억원이며, 현재까지 5억원 납입이 완료되었습니다.
(삭제)
(8) 당사는 종속기업인 ProteKt Therapeutics와 관련하여 개발 중인 의약품의 License 관련 판매 및 배당 등의 조건 달성 여부에 따라 조건부대가를 지급하는 약정을 체결하였습니다.
당사는 금융기관과의 약정을 통해 800억원을 차입 중이나 별도 기준 현금을 약 809억원 보유 중이기에 여전히 (-)순차입금을 보이고 있는 상황입니다. 이에 당사의 영업현금흐름 등 고려 시 예상치 못한 긴급한 자금 소요로 인해 한도대가 추가 실행되더라도 대응 가능할 것으로 전망됩니다. 다만 자금 소요 규모가 커지게 될 경우 당사의 재무부담에 영향을 미칠 수 있습니다. 또한 당사가 계류중인 상기 소송사건의 최종결과를 합리적으로 예측할 수 없으므로, 향후 본 소송사건들의 진행 경과에 따라 당사 영업에 부정적으로 작용할 가능성이 존재합니다. 이에, 투자자분들께서는 상기우발채무가 현실화될 경우 당사의 재무상태에 부정적인 영향을 미칠 수 있는점 참고해 주시기 바랍니다.
(주13) 정정 전
증권신고서 제출일 전일 기준 당사 최대주주는 OCI홀딩스(주)(지분율 : 11.32%, 보통주 기준)입니다. 금번 유상증자에 있어서 최대주주인 OCI홀딩스(주)는 신주배정비율에 따라 2,735,416주를 배정받게 될 예정이며 배정받은 신주에 대해 120% 참여를 고려하고 있습니다. 다만 구체적인 참여 규모는 발행가액이 확정된 이후 추후 이사회를 통해 결의할 예정입니다.
한편, 최대주주의 유상증자 참여수준에 따라 최대주주의 지분율이 변동될 수 있습니다. 금번 유상증자는 구주주(보통주+우선주) 1주당 0.3530511453주를 배정받게됨에 따라, 참여수준에 따라 지분율 변동이 클 수 있습니다. 당사의 최대주주 OCI홀딩스(주)의 120% 청약 참여 가정 시, 보통주 기준 지분율은 기존 11.32%에서 11.18%로 소폭 하락할 예정입니다. 한편 당사 2대주주 및 3대주주의 참여 여부는 확정되지 않았으며 참여하지 않을 경우 당사 최대주주인 OCI홀딩스(주)가 증서를 장외 매수하여 120% 청약 하는 방법도 고려할 수 있습니다. 이로 인해 주요주주의 청약 여부 및 이에 따른 당사 최대주주 지분율 변동율은 본 증권신고서 제출일 현재 가늠할 수 없으니 투자자 여러분께서는 이러한 점을 유념해 주시기 바랍니다.
(중략)
(주13) 정정 후
증권신고서 제출일 전일 기준 당사 최대주주는 OCI홀딩스(주)(지분율 : 11.32%, 보통주 기준)입니다. 금번 유상증자에 있어서 최대주주인 OCI홀딩스(주)는 신주배정비율에 따라 2,735,416주를 배정받게 될 예정이며 배정받은 신주에 대해 120% 참여를 고려하고 있습니다. 다만 구체적인 참여 규모는 발행가액이 확정된 이후 추후 이사회를 통해 결의할 예정입니다.
한편, 최대주주의 유상증자 참여수준에 따라 최대주주의 지분율이 변동될 수 있습니다. 금번 유상증자는 구주주(보통주+우선주) 1주당 0.3530511453주를 배정받게됨에 따라, 참여수준에 따라 지분율 변동이 클 수 있습니다. 당사의 최대주주 OCI홀딩스(주)의 120% 청약 참여 가정 시, 보통주 기준 지분율은 기존 11.32%에서 11.18%로 소폭 하락할 예정입니다. 한편 당사 2대주주 및 3대주주의 참여 여부는 확정되지 않았으며 참여하지 않을 경우 당사 최대주주인 OCI홀딩스(주)가 증서를 장외 매수하여 120% 청약 하는 방법도 고려할 수 있습니다. OCI홀딩스(주)가 당사 기존 주주의 신주인수권 증서를 매입하게 될 경우 자본시장법 제173조의3에 따라 신주인수권증서 거래 개시일의 30일 전, 거래계획을 사전 공시할 예정이며 현재 예상되는 사전 공시일은 2025년 05월 30일입니다.이로 인해 주요주주의 청약 여부 및 이에 따른 당사 최대주주 지분율 변동율은 본 증권신고서 제출일 현재 가늠할 수 없으니 투자자 여러분께서는 이러한 점을 유념해 주시기 바랍니다.
(중략)
(주14) 정정 전
(중략)
(1) 시설자금 상세 내역
[1순위: 제조시설 확장 및 생산능력 증대]
현재 당사의 내용고형제 생산시설은 공간적 제약으로 인해 추가 설비 도입이 어려운 상황이며, 이로 인해 생산량 증가에 한계가 있습니다. 이를 해결하기 위해, 기존 완제품 창고를 철거한 후 해당 부지에 제조동을 수평으로 증축하여, 부족한 생산 공간을 확보하고자 합니다.
이번 증축을 통해 기존 제조시설의 활용도를 극대화하고, 연간 생산능력을 현재의 10억 정에서 15억 정 이상으로 확대할 수 있을 것으로 기대됩니다. 이를 통해 증가하는 수요에 대응할 뿐만 아니라, 향후 신제품 개발 시 생산능력 부족으로 인한 기회 손실을 방지할 수 있습니다.
(생산능력 및 생산능력 산출근거)
(1) 생산능력(단위 : 백만원)
|
사업 부문 |
품 목 | 사업소 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|
| 의약품 및 의약외품 | 나정 | 안산공장 | 21,535 | 25,905 | 31,205 |
| 당의정 | 1,253 | 1,177 | 960 | ||
| 필름코팅정 | 59,699 | 72,208 | 96,796 | ||
| 캡슐제 | 18,515 | 27,415 | 35,295 | ||
| 과립제 | 3,898 | 4,184 | 5,240 | ||
| 주사제 | 11,525 | 11,887 | 15,920 | ||
| 내용액제 | 1,641 | 3,451 | 2,608 | ||
| 외용액제 | 3,720 | 5,487 | 6,826 | ||
| 연고제 | 3,969 | 2,506 | 5,837 | ||
| 기타제형 | 75 | 914 | 885 | ||
| 의약외품 | 5,106 | 14,493 | 12,045 | ||
| 합 계 | 130,936 | 169,627 | 213,617 | ||
|
출처 : 당사 제시 1) 산출기준 : 출하가 * 생산량 2) 산출방법 : 평균가동시간 가정 시 생산능력 3) 평균가동시간 |
| 사업부문 | 사업소 |
1일평균 가동시간 |
월평균 가동일수 |
24년 가동일수 |
24년 가동시간 |
|---|---|---|---|---|---|
|
의약품 및 의약외품 |
안산공장 | 8.0 | 20 | 245 | 1,960 |
| 출처 : 당사 제시 |
(2) 생산실적(단위 : 백만원)
| 사업부문 | 품 목 | 사업소 | 2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|
|
의약품 및 의약외품 |
나정 |
안산공장 |
26,704 | 25,646 | 30,893 |
| 당의정 | 1,554 | 1,165 | 950 | ||
| 필름코팅정 | 74,027 | 71,486 | 95,828 | ||
| 캡슐제 | 22,959 | 27,141 | 34,942 | ||
| 과립제 | 4,833 | 4,142 | 5,188 | ||
| 주사제 | 14,291 | 11,768 | 15,761 | ||
| 내용액제 | 2,035 | 3,416 | 2,582 | ||
| 외용액제 | 4,613 | 5,432 | 6,758 | ||
| 연고제 | 4,922 | 2,481 | 5,779 | ||
| 기타제형 | 93 | 905 | 876 | ||
| 의약외품 | 6,331 | 14,348 | 11,925 | ||
| 합 계 | 162,362 | 167,930 | 211,482 |
|
출처 : 당사 제시 1) 산출기준 : 출하가 * 실제 생산량 |
(3) 2024년 가동률(단위 : 시간)
| 사업부문 | 사업소 | 가동가능시간 | 실제가동시간 | 평균가동률 |
|---|---|---|---|---|
| 의약품 및 의약외품 | 안산공장 | 1,960 | 2,426 | 124% |
|
출처 : 당사 제시 ※ 가동가능시간 : 당분기 근무일수 X 8시간 ※ 실제가동시간 : 초과근무를 포함한 분기 실제가동시간 |
(중략)
(주14) 정정 후
(중략)
(1) 시설자금 상세 내역
[1순위: 제조시설 확장 및 생산능력 증대]
현재 당사의 내용고형제 생산시설은 공간적 제약으로 인해 추가 설비 도입이 어려운 상황이며, 이로 인해 생산량 증가에 한계가 있습니다. 이를 해결하기 위해, 기존 완제품 창고를 철거한 후 해당 부지에 제조동을 수평으로 증축하여, 부족한 생산 공간을 확보하고자 합니다.
이번 증축을 통해 기존 제조시설의 활용도를 극대화하고, 연간 생산능력을 현재의 10억 정에서 15억 정 이상으로 확대할 수 있을 것으로 기대됩니다. 이를 통해 증가하는 수요에 대응할 뿐만 아니라, 향후 신제품 개발 시 생산능력 부족으로 인한 기회 손실을 방지할 수 있습니다.
(생산능력 및 생산능력 산출근거)
(1) 생산능력(단위 : 백만원)
|
사업 부문 |
품 목 | 사업소 | 2025년 1분기 |
2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|---|
| 의약품 및 의약외품 | 나정 | 안산공장 | 6,461 | 21,535 | 25,905 | 31,205 |
| 당의정 | 314 | 1,253 | 1,177 | 960 | ||
| 필름코팅정 | 20,345 | 59,699 | 72,208 | 96,796 | ||
| 캡슐제 | 6,440 | 18,515 | 27,415 | 35,295 | ||
| 과립제 | 1,002 | 3,898 | 4,184 | 5,240 | ||
| 주사제 | 340 | 11,525 | 11,887 | 15,920 | ||
| 내용액제 | 376 | 1,641 | 3,451 | 2,608 | ||
| 외용액제 | 873 | 3,720 | 5,487 | 6,826 | ||
| 연고제 | 621 | 3,969 | 2,506 | 5,837 | ||
| 기타제형 | 104 | 75 | 914 | 885 | ||
| 의약외품 | 1,273 | 5,106 | 14,493 | 12,045 | ||
| 합 계 | 38,149 | 130,936 | 169,627 | 213,617 | ||
|
출처 : 당사 제시 1) 산출기준 : 출하가 * 생산량 2) 산출방법 : 평균가동시간 가정 시 생산능력 3) 평균가동시간 |
| 사업부문 | 사업소 |
1일평균 가동시간 |
월평균 가동일수 |
25년 1분기 가동일수 |
25년 분기 가동시간 |
|---|---|---|---|---|---|
|
의약품 및 의약외품 |
안산공장 | 8.0 | 19 | 58 | 464 |
사업부문 |
사업소 |
1일평균 가동시간 |
월평균 가동일수 |
24년 가동일수 |
24년 가동시간 |
|---|---|---|---|---|---|
|
의약품 및 의약외품 |
안산공장 | 8.0 | 20 | 245 | 1,960 |
| 출처 : 당사 제시 |
(2) 생산실적(단위 : 백만원)
| 사업부문 | 품 목 | 사업소 | 2025년 1분기 |
2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|---|
|
의약품 및 의약외품 |
나정 |
안산공장 |
8,012 | 26,704 | 25,646 | 30,893 |
| 당의정 | 389 | 1,554 | 1,165 | 950 | ||
| 필름코팅정 | 25,228 | 74,027 | 71,486 | 95,828 | ||
| 캡슐제 | 7,986 | 22,959 | 27,141 | 34,942 | ||
| 과립제 | 1,243 | 4,833 | 4,142 | 5,188 | ||
| 주사제 | 421 | 14,291 | 11,768 | 15,761 | ||
| 내용액제 | 466 | 2,035 | 3,416 | 2,582 | ||
| 외용액제 | 1,083 | 4,613 | 5,432 | 6,758 | ||
| 연고제 | 770 | 4,922 | 2,481 | 5,779 | ||
| 기타제형 | 129 | 93 | 905 | 876 | ||
| 의약외품 | 1,579 | 6,331 | 14,348 | 11,925 | ||
| 합 계 | 47,306 | 162,362 | 167,930 | 211,482 |
|
출처 : 당사 제시 1) 산출기준 : 출하가 * 실제 생산량 |
(3) 2025년 1분기 및 2024년 가동률(단위 : 시간)
| 사업부문 | 사업소 | 2025년 1분기 가동가능시간 |
2025년 1분기 실제가동시간 |
2025년 1분기 평균가동률 |
|---|---|---|---|---|
| 의약품 및 의약외품 | 안산공장 | 464 | 576 | 124% |
| 사업부문 | 사업소 | 2024년 가동가능시간 |
2024년 실제가동시간 |
2024년 평균가동률 |
|---|---|---|---|---|
| 의약품 및 의약외품 | 안산공장 | 1,960 | 2,426 | 124% |
|
출처 : 당사 제시 ※ 가동가능시간 : 당분기 근무일수 X 8시간 ※ 실제가동시간 : 초과근무를 포함한 분기 실제가동시간 |
(중략)
【 대표이사 등의 확인 】
 |
|
3차정정증권신고서_대표이사등의확인_부광약품 |
증 권 신 고 서
| ( 지 분 증 권 ) |
| [증권신고서 제출 및 정정 연혁] |
| 제출일자 | 문서명 | 비고 |
|---|---|---|
| 2025년 03월 28일 | 증권신고서(지분증권) | 최초 제출 |
| 2025년 04월 11일 | [기재정정]증권신고서(지분증권) | 자진 정정 |
| 2025년 04월 25일 | [기재정정]증권신고서(지분증권) | 자진 정정 |
| 2025년 05월 08일 | [기재정정]증권신고서(지분증권) | 2025년 1분기 분기보고서제출에 따른 정정 |
| 금융위원회 귀중 | 2025년 05월 08일 |
| 회 사 명 : |
부광약품 주식회사 |
| 대 표 이 사 : |
이제영 |
| 본 점 소 재 지 : |
서울특별시 동작구 상도로7(대방동) |
| (전 화) 02 - 828 - 8114 |
|
| (홈페이지) http:// www.bukwang.co.kr |
|
| 작 성 책 임 자 : | (직 책) 재무지원부 상무 (성 명) 김 민 규 |
| (전 화) 02 - 828 - 8114 |
|
| 모집 또는 매출 증권의 종류 및 수 : | 기명식 보통주 30,210,000주 | |
| 모집 또는 매출총액 : | 99,995,100,000 | 원 |
| 증권신고서 및 투자설명서 열람장소 |
| 가. 증권신고서 |
| 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 나. 투자설명서 |
| 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 서면문서 : 부광약품(주) → 서울특별시 동작구 상도로 7(대방동) NH투자증권(주) → 서울특별시 영등포구 여의대로 108 |
【 대표이사 등의 확인 】
 |
|
대표이사등의 확인(0328) |
요약정보
1. 핵심투자위험
| 하단의 핵심투자위험은 증권신고서 본문에 기재된 투자위험요소 중 중요한 항목만을 투자자의 이해도 제고를 위하여 간단ㆍ명료하게 요약한 것입니다. 자세한 투자위험요소는 "본문-제1부 모집 또는 매출에 관한 사항-Ⅲ. 투자위험요소"에 기재되어 있으니 참고하시기 바랍니다. |
| 구 분 | 내 용 |
| 사업위험 | 가. 국내외 경기변동에 따른 위험 당사가 영위하고 있는 완제의약품 제조 및 판매업은 최종 소비재 성격을 보이기에 글로벌 경기 동향 및 국내 경제 동향에 직접적인 영향을 받고 있습니다.주요 기관의 2024년까지의 경제전망에 따르면, 글로벌 경기국면은 코로나19 이후 인플레이션을 거쳐 점차적으로 경기가 회복되고 있는 상황이지만, 이와 동시에 경기 불확실성도 여전히 높게 유지되고 있는 상황입니다. 이러한 거시경제적 요인은 당사가 영위하는 제약 산업 및 전/후방 산업에 영향을 미치며, 글로벌 경기의 경로를 정확히 예측하는 것은 불가능합니다. 경기의 변동성은 당사의 영업실적 및 재무상태에 부정적인 영향을 미칠 수 있으니 투자자께서는 글로벌 경기변동에 대한 상황을 지속적으로 모니터링하시기 바랍니다. 나. 전반적인 제약산업 성장성 둔화 위험 당사가 영위하고 있는 제약산업의 수요 시장은 인구통계학적인 특성에 큰 영향을 받으며, 인구고령화 및 만성질환 증가에 따라 시장 규모가 꾸준히 커지는 특성이 있습니다. 인구구조의 고령화가 심화됨에 따라 건강 유지 및 제약산업에 대한 소비자의 관심과 수요가 커지고 있으며, 이에 따라 국내 의약품 시장규모는 2000년 이후로 계속 증가하고 있으며, 한국제약바이오협회 자료에 따르면 2009년 18조 2,187억원에서 2023년 31조 4,513억원으로 증가하는 모습을 보이며 꾸준한 성장세를 보이고 있습니다.한국이 고령사회로 진입하면서 지속적인 노인인구 증가, 소득증가, 건강에 대한 관심증가 등의 이유로 진료 비용과 의약품 비용을 포함한 의료비용이 증가하고, 이에 따라 국내 제약산업의 매출도 함께 안정적인 성장을 지속 할 것으로 전망됩니다.국내 제약산업은 신약개발을 위한 높은 수준의 R&D 투자, 생산 및 품질관리 경쟁력 확보를 바탕으로 한 이머징마켓 진출, 높은 치료율과 낮은 부작용을 보이는 바이오의약품 개발 등 다양한 노력을 기울이고 있습니다. 그러나 이러한 국내 제약산업 전반의 노력에도 불구하고 전체 제약산업이 위축되거나 시장성장률이 둔화되는 경우, 당사의 매출 또한 크게 저하될 수 있으며, 이는 당사의 사업, 영업성과 및 재무상태에 부정적인 영향을 미칠 가능성이 존재하오니 투자자께서는 이 점 유의하시기 바랍니다. 다. CNS 시장 위축 가능성 관련 위험 당사는 일반의약품, 전문의약품 제조와 별개로 파킨슨병 및 조현병 등 중추신경계(CNS)질환의 미충족 수요를 만족할 수 있는 혁신신약 개발 사업을 주요 사업으로 영위하고 있습니다. 국내 우울증 치료제 시장은 2022년에 3,700억 원 규모였으며, 연평균 3.6% 성장하여 2028년에는 4,600억 원 규모에 달할 것으로 전망되고 있습니다.또한 당사는 중추신경계질환 중 퇴행성 질환인 파킨슨병 치료제 연구개발에도 주력하고 있으며 자회사 콘테라파마를 통해 파킨슨병 치료제인 CP-012 임상을 진행하고 있습니다. 글로벌 시장조사기관 Future Market Insights에 따르면, 글로벌 파킨슨병 치료제 규모는 2024년에 43억 달러 규모에 달할 것으로 전망되며, 이후 연평균 5.1% 성장하여 2034년에는 67억 달러 규모의 시장을 형성할 것으로 전망되고 있습니다. 하지만 현 시점에서 예상치 못한 변수로 인해 향후 우울증 치료제 시장 및 파킨슨병 치료제 시장이 축소될 경우 당사가 현 시판중인 제품 매출 감소로 이어질 뿐만 아니라 임상 진행중인 치료제의 경제성이 하락하여 개발 추진력에 제동이 걸릴 개연성도 존재합니다. 투자자분들께서는 이점 참고하시기 바랍니다. 라. 정부의 의약품 규제 관련 위험 제약산업은 인간의 생명과 보건에 관련한 제품을 생산하는 국민의 건강과 직결된 사업이기 때문에 의약품의 허가, 보험 약가 등재 뿐만 아니라 생산, 유통, 판매에 이르기까지 정부에서 매우 엄격하게 통제, 관리하고 있어 정부정책의 영향을 크게 받고 있습니다.정부는 이러한 기조 하에 건강보험 재정건전화 및 제약산업 선진화를 위해 리베이트 쌍벌제, 일괄 약가인하 등을 시행하는 등 제약산업에 대한 규제를 강화하는 추세이며, 특히 타산업과 달리 정부가 약가를 직접적으로 통제하고 있어 정부의 약가정책이 제약산업내 개별기업의 매출 및 영업수익성에 직접적인 영향을 미치고 있습니다. 제약산업은 국민 건강과 직결되는 특성으로 인해 정부의 엄격한 통제를 받고 있으며, 약가인하, 리베이트 규제, 제조품질 기준 강화 등 정책 변화가 지속될 경우, 당사의 사업환경에도 부정적인 영향을 미칠 수 있습니다. 이에 따라, 투자자께서는 정부 정책 및 규제 강화가 당사의 성장성과 재무 안정성에 영향을 미칠 수 있다는 점을 고려하여 신중히 투자 결정을 내리시기 바랍니다. 마. 지적재산권 침해 등 관련 위험 당사가 영위하고 있는 제약산업은 기술집약적인 산업이며 연구개발성과가 지식재산권 형태로 보호되는 산업입니다. 특허는 산업상 유용한 발명을 한 자가 자신이 이룬 발명의 내용을 공개하는 대가로 일정한 기간 동안 독점적, 배타적 권리를 부여받는 공적 계약의 일종이며, 당사와 같이 제약산업을 영위하는 기업은 핵심 기술 및 제품에 대한 권리를 보호할 수 있는 장치 마련이 필수이기 때문에 특허의 출원 및 등록과 관련제도를 통한 지적재산권의 관리가 중요합니다. 이에 당사 및 당사 주요 자회사는 핵심 기술을 보호하기 위한 특허 출원 및 등록 등으로 지적재산권 침해 관련 위험을 관리하고 있습니다. 그럼에도 불구하고 향후 당사가 보유한 지적재산권을 적절히 보호하지 못하거나 당사가 사용하는 기술과 관련한 지적재산권 관련 분쟁이 발생하는 경우 당사에 대한 신뢰도, 제품 매출에 부정적인 영향을 미쳐 당사의 영업활동 및 수익성이 악화될 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. 바. 핵심연구인력 유출 관련 위험 당사가 영위하고 있는 제약업의 특성상 사업의 연구개발 능력은 매우 중요한 요소이며, 지속적인 연구개발을 위해서는 제약분야에 전문성과 노하우를 가진 연구인력을 확보하여야 합니다. 당사는 당사 내 연구개발본부 산하 허가등록부, 개발부, 연구소 등의 연구개발 조직을 보유 중이며 당사 자회사 또한 연구개발전문 조직의 성격을 보이고 있습니다. 또한 당사와 같은 제약업체는 연구개발에 있어 핵심 인력을 보유하는 것이 주요 경쟁력 이기에 박사급 인력 13명, 석사급 인력 30명 등 총 65명의 연구인력을 보유하고 있으며 기존 인재들에게 적절한 보상을 제공하여 동기부여함과 동시에 향후에도 인재영입을 위해 최선을 다할 계획입니다. 다만, 이러한 당사의 노력 및 정책에도 불구하고 제약산업의 경쟁심화에 따른 우수인력 스카우트 등에 따라 핵심인력이 경쟁회사 또는 다른 산업분야로 이탈할 수 있으며, 이러한 경우 당사 핵심 기술 노하우의 유출 등은 당사의 경쟁력을 약화시킬 수 있으며 이는 당사 영업활동 및 수익성에 부정적인 영향을 미칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. 사. 신약 개발 실패 및 연구개발비용 증가에 따른 수익성 악화 위험 당사가 영위하는 제약산업은 지속적인 연구개발 및 투자의 결과가 기업의 성과와 연결되는 특성을 가지고 있으며, 신제품 및 신약개발을 위해서는 비용 및 시간이 투자되어야 하는 필수 요소를 지니고 있습니다. 신약이 상업화되기까지는 막대한 비용과 시간이 필요합니다. 특히, 임상시험에 진입하여도 최소 8-9년이 소요되며 그에 필요한 비용이 요구됩니다. 또한, 임상시험을 진행한다고 하더라도 시험결과 효능이 부족하거나 안전성 평가에 적합하지 못한 결과가 나올 경우 해당 신약의 연구개발은 중단될 수 있으며, 이러할 경우 당사 및 주요 자회사의 비용 및 시간 투자에도 불구하고 투자비용의 매몰 가능성이 존재합니다.연구개발 전략이 계획대로 진행되지 않거나 자금조달에 어려움을 겪어 신약 개발에 실패하거나 지연될 경우 다른 형태로의 라이센스 아웃 가능성은 불확실성이 존재하며, 투입된 연구개발비 회수가 되지 않아 당사의 성장성, 수익성 및 재무안정성에 부정적인 영향을 미칠 수 있으니, 투자자께서는 이 점 유의하시기 바랍니다. 아. 혁신형 제약기업 제외의 위험 당사는 증권신고서 제출일 현재 기준 혁신형 제약기업으로 인증되어 있습니다. 혁신형 제약기업이 제조한 의약품에 대하여 요양급여 약제의 상한금액 가산 등 대통령령으로 정하는 우대를 제공하도록 하는 조항이 신설되었으며 혁신형 제약기업에 대한 홍보 효과 및 인지도를 제고하기 위해 인증마크 사용 근거 및 벌칙 조항이 마련되었습니다. 하지만 보건복지부는 정부가 공인한 혁신역량 보유 기업이라는 인증 효과로 인해 국내외 투자유치, 기술 및 판매 제휴, 금융기관 자금조달 등의 측면에서 다양한 간접 수혜가 있을 것으로 예상하고 있지만, 국내 중상위권 제약사 대부분이 혁신형 제약기업으로 인증되어 있는 만큼 각 사에 돌아가는 혜택에 따라 차별화가 발생하기는 어려울것으로 판단됩니다. 또한, 3년 뒤 재인증 심사 시 연구개발 투자실적 등에 따라 특별법상 요건을 충족하지 못하여 인증이 연장되지 못할 가능성도 존재합니다. 이 점 투자자께서는 유의하시기 바랍니다. 자. 생산설비 구축에 따른 투자 증가와 재무건정성 훼손 위험 GMP(Good Manufacturing Practice, 우수의약품 제조 및 품질 관리 기준)는 우수한 의약품을 제조하기 위하여 공장에서 원료의 구입부터 제조, 출하 등에 이르는 모든 과정에 필요한 관리기준을 규정한 것으로, 미국 FDA가 1963년 GMP를 제정 및 공표하면서 WHO(세계보건기구)와 각국에서 GMP를 도입하기 시작했습니다. 당사는 국내 제약회사 중 최초로 KGMP시설을 취득한 바 있으며 현재까지 GMP 관련 위반사항 등에 대해 제제를 받은 바 없습니다. 당사는 관련 규정에 의거하여, 품질 관리에 최선을 다하고 있으며 국내 최고의 역량을 갖고 있지만, 새로운 품질 기준 충족을 위한 제약회사들의 설비투자가 과거에 비해 증가하고 있으며 이는 제약회사들의 재무구조에 부담으로 작용할 수 있습니다. 향후에도 생산시설을 규정에 맞게 운영하기 위하여 지속적인 투자가 발생할 수 있으며, 향후 수출 비중이 증가할 경우 각 국가의 제도에 적합한 생산시설 및 제품의 등록이 필요하므로 투자비용이 증가할 수 있습니다. 이는 제약회사의 재무건정성에 부정적 영향을 끼칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. 차. 해외 기술 이전 실패에 따른 위험 당사가 개발하고 있는 파이프라인이 의학적 미충적 수요(medical unmet needs)를 해결할 가능성이 존재한다고 하더라도 각 글로벌 제약사의 이해관계에 따라 기술이전이 이루어지지 않을 가능성이 존재합니다. 예를 들어 특정 글로벌 제약사가 같은 적응증 대상으로 하여 항체 또는 저분자 화합물을 통한 치료제를 개발하고 있는 경우 경쟁 관계에 있는 당사 파이프라인을 확보하고자 하는 수요가 존재하지 않을 수 있습니다. 당사는 임상이 어느정도 진행된 이후 해외 기업을 대상으로 하는 기술이전 계약을 통해 매출을 본격화 할 예정입니다. 그럼에도 불구, 기술이전이 실패할 경우 당사는 추가 임상 개발을 위한 비용을 충당할 수익원을 마련하지 못할 가능성이 있으며 이는 궁극적으로 당사 외부 평판 및 수익성에 악영향을 줄 수 있으므로 투자자 여러분들께서는 이점 유의하시기 바랍니다. 카. 기술도입관련 위험 당사는 원료 수입 및 제조/판매, 제품수입 등의 목적으로 다수의 계약을 체결하고 있습니다. 동 계약은 당사의 영업 및 연구개발에 있어 필수적인 요소로 해당 계약이 예상치 못한 변수로 인해 종결되거나 당사에게 불리한 방향으로 변경될 경우 당사 영업환경에 불리하게 작용할 수 있습니다. 당사는 현재 계약을 체결중인 상대방과 우호적인 협력 관계를 유지하고 있으며 이러한 신뢰관계가 향후에도 지속될 것으로 당사는 전망하고 있습니다. 다만 모든 계약에는 불확실성이 존재하며 안정적인 원재료 수급이 절대적으로 중요한 제약 산업에서 예상치 못한 변수로 인해 적절한 원재료 도입에 차질이 생기거나 기술도입/이전 등과 관련하여 분쟁이 발생할 경우 당사의 재무건정성 및 수익성이 악화될 가능성이 존재하는 점 투자자분들 께서는 유의하시기 바랍니다. 타. 오픈이노베이션 전략에 따른 위험 당사의 R&D 주된 계획은 Global Open innovation을 중심으로 진행하고 있습니다. 이는 천문학적 비용이 투입되는 신약개발을 다양한 회사와의 협업을 통하여 리스크 및 비용을 분산하고 수익 및 향후 임상성공에 따른 benefit을 공유하고자 하는 취지로 신약개발사에서 통상적으로 취하고 있는 R&D 전략 입니다. 이러한 당사 전략으로 인해 당사는 다양한 국가의 규제 변화 및 지원 정책에 따라 영향을 받을 수 있습니다. 따라서 예상치 못한 각 국가의 정책 및 규제변화에 따라 인허가 위험으로 인해 시장이 위축되거나 비우호적인 임상 환경이 조성될 수 있습니다. 또한 환율 이 급등할 경우 당사의 자회사 지원 부담이 증가하는 등, 글로벌 오픈 이노베이션을 통해 다국적 기업과의 협업을 추구하는 당사 전략이 오히려 수익성 악화로 이어질 개연성이 존재합니다. 투자자분들께서는 이점 유의하시기 바랍니다. 파. 주요 경쟁 관련 위험(cmg, 한올바이오파마, 환인제약) 당사는 완제 의약품 제조와 동시에 CNS 질환 치료제 연구개발에 투자를 단행하고 있습니다. 당사와 주요 사업과 유사한 사업을 영위 중인 주요 경쟁사로는 CMG제약과 한올바이오파마가 있습니다. 또한 당사 이외의 CNS 전문 제약업체는 환인제약이 있습니다. 당사의 영업이익율은 2024년 기준 10.79%로 경쟁사인 한올바이오파마 및 CMG제약, 환인제약 대비 우월한 모습을 보이고 있으나 당기순손실 규모가 상대적으로 크게 나타나고 있습니다. 다만 이는 자회사 손상 521억원 등 현금지출을 동반하지 않는 기타영업외비용에 기인한 것으로, 금번 손상차손 조기 인식으로 인해 향후 추가적인 대규모 손상차손을 인식할 가능성은 제한적일 것으로 판단하고 있습니다. 따라서 연구개발비로 환원할 수 있는 영업현금흐름 규모 및 수익성 관점에 있어서 향후 당사는 경쟁사 대비 경쟁력을 보일 것으로 전망됩니다. 다만 향후 CNS 중추신경계 시장 내 당사가 예상하지 못한 신규 경쟁 치료제가 출현하거나 기존 전통적 치료제의 적응증 또는 목표 환자군 확장 등이 발생할 경우, 경쟁 심화에 따라 당사의 영업 및 재무안정성이 악화될 수 있습니다. 따라서 투자자께서는 당사가 연구개발 중인 주요 파이프라인에서 대체재 출시 혹은 경쟁 심화로 인한 수익성이 저하될 수 있다는 사실에 유의하시기 바랍니다. |
| 회사위험 | 가. OCI그룹 기업집단 설정에 따른 위험 당사는 2024년 공정거래위원회에서 지정한 2024년 상호출자금지 기업집단 순위 41위의 OCI 계열사로, OCI그룹은 당사를 포함하여 총 24개의 계열회사로 구성되어 있습니다.OCI그룹은 공정거래법상 대규모기업집단 정책을 적용받으며 해당 정책에서 제시하는 규정을 준수하지 못하거나 관련 공시사항을 이행하지 못하게 될 경우 과징금이 부과될 수 있습니다. 이로 인해 당사 수익성에 영향을 받을 수 있으며 나아가 당사의 외부 평판에도 부정적인 영향을 줄 수 있는 점 투자자분들께서는 유의하시기 바랍니다. 공정거래법상 지주회사는 자회사 지분율 규제(상장30%, 비상장50% 이상)가 적용되며, 이에 미달하는 자회사 지분을 자회사 지분율 규제 이상으로 추가 취득 또는 처분하여야 합니다. 금번 유상증자에서 당사 최대주주인 OCI홀딩스가 배정받은 증서 및 2대,3대 주주의 증서까지 매입 후 120% 청약 시 확보하게 될 지분율은 약 16.81%로 당사 최대주주인 OCI홀딩스가 지분율 요건을 충족하기 위해서는 추가 지분매입 및 제3자배정유상증자 등이 수반될 수 있으며 이 경우 당사 주식 가격 변동성이 높아질 수 있으니 투자자 분들께서는 유의하시기 바랍니다. 한편 당사는 당사 최대주주인 OCI홀딩스 포함 특수관계인과 다양한 매출 매입활동을 진행하고 있습니다. 당사 외형규모 고려 시 해당 매출 매입금액이 유의적인 수준은 아니나, 향후 특수관계자 거래 규모가 증가할 경우 거래의 적정성에 대해 공정거래위원회 및 세무당국의 조사가 진행될 수 있는 점 참고부탁드립니다. 나. 수익성 악화 위험 당사의 별도 기준 매출액은 2021년 1,816억 원에서 2022년 1,903억 원으로 4.79% 증가하였으나, 2023년에는 1,252억 원으로 34.24% 감소하였습니다. 이는 2023년 당사가 내부 조직을 개편하고 도매상 중심의 유통구조를 재정비하는 등 질적 성장을 위한 경영 전략을 추진한 데에 따른 결과입니다. 이에 따라 영업이익도 2022년 123억 원에서 2023년에는 172억 원의 영업손실로 전환되었습니다. 다만, 경영구조 개편의 효과가 2024년부터 본격적으로 나타나면서, 당사의 2024년 매출액은 전년 대비 25.91% 증가한 1,576억 원을 기록하였으며, 영업이익 또한 170억 원으로 흑자 전환에 성공하였습니다. 한편, 2025년 1분기에는 당사의 주요 치료제 제품의 급격한 매출 성장이 나타나며 매출액은 전년 동기 대비 28.9% 증가한 439억원, 영업이익은 188.1% 증가한 59억원을 기록하며 호실적을 나타냈습니다. 연결기준 수익성의 경우 자회사의 임상개발 비용 등으로 인해 연구개발비가 연간 70억 원에서 190억 원 수준으로 발생하고 있으며, 이로 인해 별도 기준에 비해 열위에 있는 모습입니다. 다만,2024년에는 전년도 경영구조 개편의 효과가 온전히 반영됨에 따라 영업이익 16억 원을 기록하며 흑자 전환에 성공하였습니다. 하지만 2025년 1분기에는 일회성 비용이 나타나며 호실적에도 불구하고 연결기준 1억원의 당기순손실을 기록했지만, 당사의 향후 실적에 미치는 영향은 미미할 것으로 판단됩니다. 당사는 향후 연결 및 별도 기준 모두에서 수익성이 점진적으로 개선될 것으로 전망하고 있으며, 2023년과 같은 대규모 영업손실이 재차 발생할 가능성은 제한적이라고 판단하고 있습니다. 다만, 당사가 속한 제약업종은 식품의약품안전처 등 규제기관의 추가 규제, 임상시험 진행에 따른 추가 연구개발비 발생, 경쟁 제품 출시 등의 예상치 못한 변수에 지속적으로 노출되어 있습니다. 이로 인해 당사의 매출이 감소하거나 수익성이 악화되는 등 영업 환경에 부정적인 영향을 미칠 수 있으므로, 투자자 여러분께서는 이 점을 유의하여 주시기 바랍니다. 다. 재무건전성 위험 당사의 연결 기준 재무건전성은 타 제약사 대비 상대적으로 우수한 수준을 유지하고 있습니다. 유동비율은 2023년을 제외하고 500% 내외를 기록해 왔으며, 2023년에는 기타유동부채가 증가하면서 유동비율이 일시적으로 260% 수준으로 하락하였습니다. 다만 2024년 기타유동부채는 크게 감소하며 유동비율은 다시 500% 이상 수준으로 회복되었습니다. 부채비율은 2021년과 2022년에 41~48% 수준을 유지하였으나, 2023년에는 일시적인 영업적자, 신규 차입금 발생, 기타유동부채 증가 등이 복합적으로 작용하면서 83.13%로 상승하였습니다. 그러나 2024년에는 수익성 개선과 함께 기타유동부채가 상환되며, 부채비율은 52.85%로 개선되었고, 2025년 1분기말까지 유사한 수준을 유지하고 있습니다. 2021년 및 2022년 총차입금의존도는 1% 미만을 기록하였고, 보유 현금이 총차입금을 초과함에 따라 순차입금도 마이너스(-) 상태를 유지하였습니다. 2023년에는 신규 차입이 발생하면서 총차입금의존도가 18.50%로 증가하였고, 2024년에는 기타유동부채 상환에 따른 총자산 감소의 영향으로 21.28%로 소폭 상승하였고, 2025년 1분기말에도 동일한 수준을 유지하고 있습니다. 그럼에도 불구하고, 보유 현금이 총차입금을 상회함에 따라 순차입금은 여전히 음(-)의 상태를 유지하고 있습니다. 당사는 2023년 경영 전략 구조 개편 과정에서 영업손실이 발생함에 따라 일시적으로 재무건전성이 다소 약화되었으나, 2024년 영업 정상화와 함께 재무건전성은 개선되었습니다. 한편 22년 이후 당사의 순차입금 증가와 영업적자 전환 등의 사유로 인해 당사의 이자보상배율은 악화되는 추세를 보였습니다.다만, 2025년 이후 라투다정을 중심으로 매출액 및 수익성 개선이 기대되고 있는 상황임에 따라 당사의 이자보상배율은 점진적인 개선 추세를 보일 것으로 전망되며, 2025년 1분기 전년동기대비 급격히 증가된 이자보상배율 수준을 나타내며 실제로 개선되는 모습을 보이고 있습니다. 전반적으로 당사는 타사 대비 우수한 재무구조를 유지하고 있습니다. 다만, 향후 예상치 못한 외부 요인으로 인해 영업실적이 악화될 경우, 재무건전성에도 부정적인 영향이 발생할 수 있는 점을 투자자 여러분께서는 유의해 주시기 바랍니다. 라. 자회사 손상차손 관련 위험 당사는 당사의 Global Open Innovation 전략의 일환으로 다수 해외계열사를 보유하고 있습니다. 당사는 매 회계연도 말, 종속기업·관계기업·공동기업에 대한 투자주식의 손상징후를 검토하고, 손상검사를 수행하고 있습니다. 2024년에는 Contera Pharma A/S의 파이프라인 임상 중단 등의 사유로 인해 종속기업 투자주식 관련 손상차손 521억 원을 인식하였으며, 해당 금액은 당기의 기타비용으로 반영되었습니다. 투자주식 손상차손은 현금유출을 수반하지는 않지만, 기타비용으로 인식되어 순이익에는 부정적인 영향을 미칩니다. 향후에도 자회사의 임상 진행 과정에서 불확실성이 현실화될 경우, 추가적인 손상차손 인식이 필요할 수 있으며 이는 당사의 수익성 및 재무건전성뿐만 아니라 신용평가, 대외 평판, 거래처 협상력 등에도 부정적인 영향을 미칠 수 있습니다.따라서 투자자 여러분께서는 당사의 자회사 관련 손상차손 위험을 충분히 인지하신 후, 신중히 투자 의사결정을 내리시기 바랍니다. 마. 환율변동에 따른 위험 당사는 국제적으로 영업활동을 영위하고 있어 외환위험, 특히 주로 달러 및 유로화와 관련된 환율변동위험에 노출되어 있습니다. 현재로서 해당 환율변동이 당사의 수익성에 미치는 영향은 미미한 수준으로 판단됩니다. 다만 당사가 대외적으로 표명중인 Global Open Innovation 전략에 따라 당사는 향후에도 다양한 해외 제약회사 및 바이오벤처사와 협업을 진행할 예정입니다.특히, 당사가 현재 임상진행중인 파이프라인을 라이센스아웃 하거나 기존 라이센스아웃한 MLR-1023등과 관련하여 향후 수취하게될 benefit sharing 등은 모두 외화로 결제될 예정이며 당사가 계획중인 수출비중 확대 등이 현실화 될 경우 환율 변동이 당사에 미치는 영향은 더욱 커질 것으로 전망됩니다. 최근 글로벌 경제 및 정치적 상황의 불확실성, 중동 지정학적 리스크와 함께 트럼프 미국 대통령의 관세 등 예측불가능한 정책 으로 환율 변동성이 크게 확대되는 추세를 보이고 있습니다. 외부적인 요인에 의한 환율 변동은 당사의 수익성에 직간접적인 영향을 미칠 수 있으며 향후 그 영향도가 더욱 높아질 개연성이 존재합니다. 따라서 환율 변동의 불확실성 확대가 당사의 경영성과 및 재무상태에 영향을 미칠 수 있는점 투자자 여러분께서는 참고하시기 바랍니다. 바. 현금흐름 관련 위험 당사는 당뇨병, 간질환 및 중추신경계(CNS) 질환 치료제 시장에서 선도적인 지위를 확보하고 있으며, 인지도가 높은 주요 제품들을 생산·판매하고 있습니다. 이러한 제품을 통해 창출되는 영업현금흐름은 신약 파이프라인 임상, 제제 개발, 연구 등 연구개발 활동에 필요한 운영자금으로 재투자되어 선순환 구조를 이루고 있습니다. 당사는 이와 같은 구조를 기반으로 향후 사업 외형을 지속적으로 확대해 나갈 계획입니다. 따라서 안정적인 현금흐름 확보는 당사의 영업 환경과 성장 전략에 있어 매우 중요한 요소라 할 수 있습니다. 앞으로 당사의 안정적인 영업실적 개선이 지속될 것으로 기대되며, 이에 따라 영업현금흐름도 점진적으로 증가할 것으로 전망됩니다. 당사는 이를 기반으로 신약 개발 등 주요 투자 활동에 자금을 재투자하는 선순환 구조를 구축해 나갈 계획입니다. 다만, 예기치 못한 외부 변수로 인해 2023년과 같은 영업적자가 발생할 경우, 영업현금흐름이 다시 순유출로 전환될 수 있으며, 이는 유동성 부족으로 이어져 추가적인 자금 조달 또는 차입이 필요할 수 있습니다. 제약업체인 당사에게 있어 안정적인 현금흐름 확보는 핵심적인 경영 과제이므로, 투자자 여러분께서는 당사의 현금흐름 추이를 충분히 고려하신 후 투자 의사결정을 해주시기 바랍니다. 사. 연구개발비 증가에 따른 위험 당사의 연결 기준 매출액 대비 연구개발비 비중은 2021년 14.89%, 2022년 15.39%로 유사한 수준을 유지하였으나, 2023년에는 31.38%로 큰 폭 상승하였습니다. 이는 2023년 매출액이 감소한 가운데, JM-010 임상 관련 연구개발비가 대규모로 집행된 데에 기인합니다. 실제 2023년 연결 기준 연구개발비는 395억 원으로, 전년 동기 대비 34.4% 증가하였습니다. 다만 JM-010 임상이 2024년에 종료됨에 따라, 2024년 연결 기준 연구개발비는 284억 원으로 감소하였으며, 매출액 대비 비중 또한 17.73%로 축소되어 2021~2022년 수준으로 회귀하였습니다. 2025년 1분기 또한 JM-010의 임상중단 영향과 매출 성장으로 인해 매출액 대비 연구개발비 비중이 12% 수준까지 하락하였지만, 이는 당사의 후속 파이프라인 연구개발이 진행되며 예년 수준으로 상승할 것으로 예상됩니다. 당사와 같은 제약업체는 미래 한단계 도약하기 위해서는 연구개발활동이 필수적입니다. 다만 연구개발비가 급격히 증가할 경우 당사 수익성에 영향을 미칠 수 있으며 향후 개발임상이 실패할 시 해당비용은 매몰비용으로 회수에 어려움을 겪게 될 수 있습니다. 투자자분들께서는 이점 참고하시기 바랍니다. 아. 소송 등 우발부채 관련 위험 증권신고서 제출일 현재 당사는 1,200억 및 백만불을 한도로 금융기관과 일반자금대출/수입신용장 약정을 체결하고 있으며 이중 800억원을 사용하고 있습니다. 또한 당사는 원고로 4건, 피고로 1건의 소송에 계류 중입니다. 당사는 금융기관과의 약정을 통해 800억원을 차입 중이나 별도 기준 현금을 약 809억원 보유 중이기에 여전히 (-)순차입금을 보이고 있는 상황입니다. 이에 당사의 영업현금흐름 등 고려 시 예상치 못한 긴급한 자금 소요로 인해 한도대가 추가 실행되더라도 대응 가능할 것으로 전망됩니다. 다만 자금 소요 규모가 커지게 될 경우 당사의 재무부담에 영향을 미칠 수 있습니다. 또한 당사가 계류중인 소송사건의 최종결과를 합리적으로 예측할 수 없으므로, 향후 본 소송사건들의 진행 경과에 따라 당사 영업에 부정적으로 작용할 가능성이 존재합니다. 이에, 투자자분들께서는 상기우발채무가 현실화될 경우 당사의 재무상태에 부정적인 영향을 미칠 수 있는점 참고해 주시기 바랍니다. |
| 기타 투자위험 |
가. 최대주주의 청약 참여율에 따른 지분율 변동 위험 증권신고서 제출일 전일 기준 당사 보통주의 최대주주는 OCI홀딩스(주)(지분율 : 11.32%, 보통주 기준)입니다. 금번 유상증자에 있어서 최대주주인 OCI홀딩스(주)는 신주배정비율에 따라 2,735,416주를 배정받게 될 예정이며 배정받은 신주에 대해 120% 참여를 고려하고 있습니다. 다만 구체적인 참여 규모는 발행가액이 확정된 이후 추후 이사회를 통해 결의할 예정입니다. 한편, 최대주주의 유상증자 참여수준에 따라 최대주주의 지분율이 변동될 수 있습니다. 금번 유상증자는 구주주(보통주+우선주) 1주당 0.3530511453주를 배정받게됨에 따라, 참여수준에 따라 지분율 변동이 클 수 있습니다. 당사의 최대주주 OCI홀딩스(주)의 120% 청약 참여 가정 시, 보통주 기준 지분율은 기존 11.32%에서 11.18%로 소폭 하락할 예정입니다. 한편 당사 2대주주 및 3대주주의 참여 여부는 확정되지 않았으며 참여하지 않을 경우 당사 최대주주인 OCI홀딩스(주)가 증서를 장외 매수하여 120% 청약 하는 방법도 고려할 수 있습니다. 이로 인해 주요주주의 청약 여부 및 이에 따른 당사 최대주주 지분율 변동율은 본 증권신고서 제출일 현재 가늠할 수 없으니 투자자 여러분께서는 이러한 점을 유념해 주시기 바랍니다.
|
2. 모집 또는 매출에 관한 일반사항
| (단위 : 원, 주) |
| 증권의 종류 |
증권수량 | 액면가액 | 모집(매출) 가액 |
모집(매출) 총액 |
모집(매출) 방법 |
|---|---|---|---|---|---|
| 보통주 | 30,210,000 | 500 | 3,310 | 99,995,100,000 | 주주배정후 실권주 일반공모 |
| 인수(주선) 여부 | 지분증권 등 상장을 위한 공모여부 | ||
|---|---|---|---|
| 인수 | 아니오 | 해당없음 | 해당없음 |
| 인수(주선)인 | 증권의 종류 |
인수수량 | 인수금액 | 인수대가 | 인수방법 | |
|---|---|---|---|---|---|---|
| 대표 | NH투자증권 | 보통주 | 30,210,000 | 99,995,100,000 | 인수수수료 : 모집총액의 1.0% | 잔액인수 |
| 청약기일 | 납입기일 | 청약공고일 | 배정공고일 | 배정기준일 |
|---|---|---|---|---|
| 2025년 07월 08일 ~ 2025년 07월 09일 | 2025년 07월 16일 | 2025년 07월 10일 | 2025년 07월 16일 | 2025년 06월 02일 |
| 청약이 금지되는 공매도 거래 기간 | |
|---|---|
| 시작일 | 종료일 |
| 2025년 03월 31일 | 2025년 07월 03일 |
| 자금의 사용목적 | |
|---|---|
| 구 분 | 금 액 |
| 시설자금 | 84,500,000,000 |
| 운영자금 | 15,495,100,000 |
| 발행제비용 | 1,272,163,816 |
| 신주인수권에 관한 사항 | ||
|---|---|---|
| 행사대상증권 | 행사가격 | 행사기간 |
| - | - | - |
| 매출인에 관한 사항 | ||||
|---|---|---|---|---|
| 보유자 | 회사와의 관계 |
매출전 보유증권수 |
매출증권수 | 매출후 보유증권수 |
| - | - | - | - | - |
| 일반청약자 환매청구권 | ||||
|---|---|---|---|---|
| 부여사유 | 행사가능 투자자 | 부여수량 | 행사기간 | 행사가격 |
| - | - | - | - | - |
| 【주요사항보고서】 | 주요사항보고서(유상증자결정)-2025.03.28 |
| 【기 타】 | 1) 금번 부광약품(주) 주주배정후 실권주 일반공모 유상증자의 대표주관회사는 NH투자증권(주) 입니다. 2) 금번 유상증자는 잔액인수방식에 의한 것입니다. 대표주관회사는 주주배정 후 실권주 일반공모 후 최종실권주를 잔액 인수하게 되며, 인수방법 및 인수대가에 대한 자세한 내용은 '제1부 모집 또는 매출에 관한 사항 - Ⅰ. 모집 또는 매출에 관한 일반사항 - 5. 인수 등에 관한 사항'을 참고하여 주시기 바랍니다. 3) 상기 모집가액 및 발행제비용은 예정가액으로 산정된 것으로 향후 변경될 수 있습니다. 확정가액은 구주주 청약일 전 제3거래일(2025년 07월 03일)에 결정될 예정입니다. 4) 상기 청약기일은 구주주의 청약기일이며, 일반공모의 청약기일은 2025년 07월 11일 ~ 2025년 07월 14일(2영업일간)입니다. 일반공모 청약 공고는 2025년 07월 10일에 당사 및 대표주관회사의 인터넷 홈페이지를 통해 게시될 예정입니다. 5) 일반공모 청약은 대표주관회사인 NH투자증권(주)의 본ㆍ지점, 홈페이지 및 HTS/MTS에서 가능합니다. 단, 고위험고수익투자신탁 및 일반청약자에 대하여 배정하여야 할 주식이 총 50,000주(액면가 500원 기준) 이하 이거나 배정하여야 할 주식의 공모금액이 1억원 이하일 경우에는 일반공모 청약을 하지 아니하고, 대표주관회사가 자기계산으로 인수할 수 있습니다. 6) 「자본시장과 금융투자업에 관한 법률」 제180조의4 및 동법 시행령 제208조의4제1항에 의거, 2025년 03월 31일부터 2025년 07월 03일까지 당사의 주식을 공매도 하거나 공매도 주문을위탁한 자는 금번 모집(매출)에 청약할 수 없으며, 이를 위반하여 주식을 취득할 경우 동법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만, 모집(매출)가액의 공정한 가격형성을 저해하지 않는 경우로서 동법 시행령 제208조의4제2항 및 「금융투자업규정」 제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다. 7) 금융감독원에서 본 증권신고서를 심사하는 과정에서 정정명령 조치를 취할 수 있으며, 정정 명령 등에 따라 본 신고서에 기재된 일정이 변경될 수 있습니다. 8) 증권신고서의 효력의 발생은 본 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. 9) 발행제비용은 당사 보유자금으로 지급할 예정입니다. |
제1부 모집 또는 매출에 관한 사항
I. 모집 또는 매출에 관한 일반사항
1. 공모개요
당사는 이사회 결의를 통하여 「자본시장과 금융투자업에 관한 법률」 제165조의6 2항1호에 의거 당사와 NH투자증권(주)(이하 "대표주관회사"라 합니다.) 간에 주주배정후 실권주를 인수하는 계약을 체결하고 사전에 그 실권주를 일반에 공모하기로 하여 기명식 보통주 30,210,000주를 주주배정 후 실권주 일반공모 방식으로 발행하기로 결정하였으며, 동 증권의 개요는 다음과 같습니다.
■ 모집(매출) 정보
| (단위 : 원, 주) |
| 주식의 종류 | 주식의 수 | 액면가액 | 모집(매출)가액 | 모집총액 | 모집(매출)방법 |
|---|---|---|---|---|---|
| 기명식 보통주 | 30,210,000 | 500 | 3,310 | 99,995,100,000 | 주주배정 후 실권주 일반공모 |
| 주1) 최초 이사회 결의일 : 2025년 03월 28일 주2) 1주의 모집가액 및 모집총액은 예정 발행가액 기준으로 한 예정금액이며, 확정되지 않은 금액입니다. |
발행가액은 「증권의 발행 및 공시 등에 관한 규정」 제5-18조 (유상증자의 발행가액 결정)에 의거, 주주배정 증자시 할인율 등이 자율화 되어 자유롭게 산정할 수 있으나, 「(舊)유가증권 발행 및 공시 등에 관한 규정」 제57조를 일부 준용하여 산정할 예정입니다.
■ 예정 발행가액의 산출근거
본 증권신고서의 예정발행가액은 이사회결의일 직전 거래일(2025년 03월 27일)을 기산일로 하여 유가증권시장에서 성립된 거래대금을 거래량으로 나눈 1개월 가중산술평균주가, 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과기산일 종가 중 낮은 금액을 기준주가로 하여 할인율 20%를 적용, 증자비율은 유상증자 주식수/발행주식총수로 계산하여 아래의 산식에 의하여 산정된 발행가액으로 합니다. 단, 할인율 적용에 따른 모집가액이 액면가액(500원) 이하일 경우에는 액면가액을 발행가액으로 하며, 호가 단위 미만은 절상합니다.
| 기준주가(4,500원) X 【 1 - 할인율(20%) 】 | ||
| ▶ 모집예정가액 (3,310원) | = | ---------------------------------------- |
| 1 + 【유상증자비율(44.13%) X 할인율(20%)】 |
| [ 모집예정가액 산정표 (2025.02.28 ~ 2025.03.27) ] | (단위 : 원, 주) |
| 일수 | 일 자 | 종 가 | 거 래 량 | 거래대금 |
|---|---|---|---|---|
| 1 | 2025/03/27 | 4,500 | 107,300 | 485,042,381 |
| 2 | 2025/03/26 | 4,570 | 75,837 | 345,197,520 |
| 3 | 2025/03/25 | 4,570 | 109,596 | 501,461,439 |
| 4 | 2025/03/24 | 4,590 | 86,837 | 401,206,772 |
| 5 | 2025/03/21 | 4,655 | 120,427 | 555,685,342 |
| 6 | 2025/03/20 | 4,660 | 120,170 | 562,224,353 |
| 7 | 2025/03/19 | 4,615 | 99,548 | 461,060,967 |
| 8 | 2025/03/18 | 4,615 | 62,076 | 286,759,224 |
| 9 | 2025/03/17 | 4,610 | 64,649 | 298,783,830 |
| 10 | 2025/03/14 | 4,620 | 73,528 | 339,795,514 |
| 11 | 2025/03/13 | 4,575 | 116,623 | 539,071,833 |
| 12 | 2025/03/12 | 4,675 | 97,647 | 457,745,528 |
| 13 | 2025/03/11 | 4,675 | 89,574 | 413,341,619 |
| 14 | 2025/03/10 | 4,725 | 133,617 | 639,314,685 |
| 15 | 2025/03/07 | 4,715 | 80,842 | 380,534,688 |
| 16 | 2025/03/06 | 4,720 | 59,978 | 282,216,198 |
| 17 | 2025/03/05 | 4,700 | 63,752 | 298,906,039 |
| 18 | 2025/03/04 | 4,670 | 144,987 | 677,697,835 |
| 19 | 2025/02/28 | 4,790 | 122,895 | 587,938,090 |
| 1개월 가중산술평균주가(A) | 4,652.75 | |||
| 1주일 가중산술평균주가(B) | 4,577.21 | |||
| 기산일 종가(C) | 4,500 | |||
| A,B,C의 산술평균(D) | 4,576.65 | [(A)+(B)+(C)]/3 | ||
| 기준주가[Min(C,D)] | 4,500 | (C)와 (D)중 낮은 가액 | ||
| 할인율 | 20% | |||
| 예정발행가액 | 3,310 | 기준주가 X (1- 할인율) 예정발행가 = ──────────── (1 + 증자비율 X 할인율) (단, 호가단위 미만은 절상하며, 액면가 미만인 경우에는 액면가로 합니다.) |
||
■ 공모일정 등에 관한 사항
| [주요일정] |
| 날짜 | 업 무 내 용 | 비고 |
|---|---|---|
| 2025년 03월 28일 | 이사회 결의 | - |
| 2025년 03월 28일 | 증권신고서(예비투자설명서) 제출 | - |
| 2025년 03월 31일 | 신주발행공고 및 신주배정기준일공고 | 당사 인터넷 홈페이지(http://www.bukwang.co.kr) |
| 2025년 05월 28일 | 1차 발행가액 확정 | 신주배정기준일 3거래일전 |
| 2025년 05월 30일 | 권리락 | - |
| 2025년 06월 02일 | 신주배정기준일(주주확정) | - |
| 2025년 06월 16일 | 신주배정 통지 | - |
| 2025년 06월 23일 | 신주인수권증서 상장일 | 5거래일 이상 동안 거래(25.06.23~25.06.27) |
| 2025년 06월 30일 | 신주인수권증서 상장폐지 | 구주주 청약초일 5거래일 전에 상장폐지되어 있어야함 |
| 2025년 07월 03일 | 확정 발행가액 산정 | 구주주 청약초일 3거래일 전 |
| 2025년 07월 04일 | 확정 발행가액 확정 공고 | 당사 인터넷 홈페이지(http://www.bukwang.co.kr) |
| 2025년 07월 08일 | 우리사주조합 청약 | - |
| 2025년 07월 08일~ 2025년 07월 09일 |
구주주 청약 | - |
| 2025년 07월 10일 | 일반공모청약 공고 | 당사 인터넷 홈페이지 (http://www.bukwang.co.kr) NH투자증권㈜ 홈페이지 (http://www.nhqv.com) |
| 2025년 07월 11일~ 2025년 07월 14일 |
일반공모청약 | - |
| 2025년 07월 16일 | 주금납입/환불/배정공고 | - |
| 2025년 07월 28일 | 신주상장 예정일 | - |
| 주1) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정 요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주및 투자자에게 귀속됩니다. 주2) 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
2. 공모방법
[공모방법 : 주주배정후 실권주 일반공모]
| 모집대상 | 주식수 | 비 고 |
|---|---|---|
| 우리사주조합 청약 | 6,042,000주(20.0%) | - 「자본시장과 금융투자업에 관한 법률」 제165조의7제1항제2호 및 「근로복지기본법」 제38조제1항에 따른 배정 - 우리사주조합 청약일 : 2025년 07월 08일(1일간) |
| 구주주 (신주인수권증서 보유자) 청약 |
24,168,000주(80.0%) | - 구주 1주당 신주 배정비율 : 1주당 0.3530511453주 - 신주배정 기준일 : 2025년 06월 02일 - 구주주 청약일 : 2025년 07월 08일 ~ 07월 09일 - 보유한 신주인수권증서의 수량 한도로 청약가능(구주주에게는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율을 곱한 수량만큼의 신주인수권 증서가 배정됨) |
| 초과 청약 | - | - 자본시장과 금융투자업에 관한 법률 제165조의6의 제2항 제2호에 의거 초과청약 - 초과청약비율 : 배정신주(신주인수권증서) 1주당 0.2주 - 신주인수권증서 거래를 통해서 신주인수권증서를 매매시 보유자 기준으로 초과청약 가능 |
| 일반모집 청약 (고위험고수익투자신탁등 청약 포함) |
- | - 구주주 및 초과청약 후 발생하는 단수주 및 실권주에 대해 배정됨 - 일반공모 청약일 : 2025년 07월 11일 ~ 07월 14일 |
| 합 계 | 30,210,000주(100.0%) | - |
| 주1) | 본 건 유상증자는 주주배정후 실권주 일반공모 방식으로 진행되며, 우리사주조합 및 구주주 청약결과 발생하는 실권주 및 단수주는 우선적으로 초과청약자에게 배정되며, 이후 실권이 발생할 경우에 대해서는 일반에게 공모합니다. |
| 주2) | 총 발행예정주식(30,210,000주)의 20%에 해당하는 6,042,000주는 「자본시장과 금융투자업에 관한 법률」 제165조의7(우리사주조합원에 대한 주식의 배정 등에 관한 특례) 제1항 제2호 및 「근로복지기본법」 제38조 제1항에 의거 우리사주조합에 우선 배정합니다. 단, 1주 미만은 절사합니다. |
| 주3) | 금번 유상증자는 보통주 주주에게 배정되며, 배정되는 주식의 종류는 보통주입니다. 구주주의 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식수(보통주)에 1주당 신주배정비율인 0.3530511453주를 곱하여 산정된 배정주식수로 하되, 1주 미만은 절사합니다. |
| 주4) | 신주인수권증서 보유자는 보유한 신주인수권증서 수량의 한도로 증서청약을 할 수 있고, 동 주식수에 초과청약비율(20.0%)를 곱한 수량을 한도로 초과청약 할 수 있습니다. 단, 1주 미만은 절사합니다. ① 청약한도 주식수 = 신주인수권증서청약 한도주식수 + 초과청약한도 주식수 ② 신주인수권증서 청약 한도주식수 = 보유한 신주인수권 증서의 수량 ③ 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 X 초과청약 비율(20.0%) |
| 주5) | 우리사주조합, 구주주 청약(초과청약 포함) 결과 발생한 미청약주식은 다음 각항과 같이 일반에게 공모하되, '증권 인수업무 등에 관한 규정' 제9조 제2항 제3호 내지 제6호에 따라 고위험고수익투자신탁등에 공모주식의 5.0%를 우선배정하고, 나머지 95.0%에 해당하는 주식은 개인투자자 및 기관투자자(집합투자업자 포함)에게 구분 없이 배정합니다. 배정수량 계산시에는 대표주관회사에 청약된 청약 주식수를 모두 합산하여 일반공모 배정분 주식수로 나눈 청약경쟁률에 따라 각 청약자에 배정합니다. ① 1단계: 총 청약물량이 일반공모 배정분 주식수를 초과하는 경우, 각 청약자에 5사 6입을 원칙으로 안분 배정하여 잔여주식이 최소화되도록 합니다. 다만, 고위험고수익투자신탁등에 대한 공모주식 5%와 개인투자자 및 기관투자자(집합투자업자포함)에 대한 공모주식 95%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정합니다. 다만, 한 그룹만 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다. ② 2단계: 1단계 배정 후 최종 잔여주식은 최대청약자부터 순차적으로 1주씩 우선배정하되, 동순위 최대청약자가 최종 잔여주식보다 많은 경우에는 대표주관회사가 무작위 추첨방식을 통하여 배정합니다. |
| 주6) | 일반공모를 거쳐 배정 후에도 미 청약된 잔여주식에 대하여는 대표주관회사가 자기계산으로 잔액인수하기로 합니다. |
| 주7) | 단, 대표주관회사는 「증권 인수업무 등에 관한 규정」 제9조제2항제5호에 의거 고위험고수익투자신탁등 및 개인청약자에 대하여 배정하여야 할 주식이 50,000주(액면가 500원 기준) 이하이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 일반청약자에게 배정하지 아니하고 대표주관회사가 인수비율에 따라 자기 계산으로 인수할 수 있습니다. |
|
※ 「자본시장과 금융투자업에 관한 법률」 제165조의7(우리사주조합원에 대한 주식의 배정 등에 관한 특례) 1. 「외국인투자 촉진법」에 따른 외국인투자기업 중 대통령령으로 정하는 법인이 주식을 발행하는 경우 2. 그 밖에 해당 법인이 우리사주조합원에 대하여 우선배정을 하기 어려운 경우로서 대통령령으로 정하는 경우 ② 우리사주조합원이 소유하는 주식수가 신규로 발행되는 주식과 이미 발행된 주식의 총수의 100분의 20을 초과하는 경우에는 제1항을 적용하지 아니한다. ③ 제165조의6제1항제1호의 방식으로 신주를 발행하는 경우 제1항에 따른 우리사주조합원에 대한 배정분에 대하여는 「상법」 제419조제1항부터 제3항까지의 규정을 적용하지 아니한다. <신설 2013.5.28.> ④ 금융위원회는 제1항에 따른 우리사주조합원에 대한 주식의 배정과 그 주식의 처분 등에 필요한 기준을 정하여 고시할 수 있다. <개정 2013.5.28.> [본조신설 2009.2.3.][제목개정 2013.4.5.] ※ 「자본시장과 금융투자업에 관한 법률 시행령」 제176조의9(우리사주조합원에 대한 주식의 배정 등에 관한 특례의 예외 등) ① 법 제165조의7제1항 각 호 외의 부분 본문에서 "대통령령으로 정하는 주권상장법인"이란 한국거래소가 법 제4조제2항 각 호의 증권의 매매를 위하여 개설한 증권시장으로서 금융위원회가 정하여 고시하는 증권시장(이하 "유가증권시장"이라 한다)에 주권이 상장된 법인을 말한다. <신설 2013. 8. 27.> ② 법 제165조의7제1항 각 호 외의 부분 본문에서 "대통령령으로 정하는 증권시장"이란 유가증권시장을 말한다. <신설 2013. 8. 27.> ③ 법 제165조의7제1항제2호에서 "대통령령으로 정하는 경우"란 다음 각 호의 어느 하나에 해당하는 경우를 말한다. <개정 2010. 12. 7., 2013. 8. 27.> 1. 주권상장법인(유가증권시장에 주권이 상장된 법인을 말한다)이 주식을 모집 또는 매출하는 경우 우리사주조합원(「근로복지기본법」에 따른 우리사주조합의 조합원을 말한다. 이하 이 조에서 같다)의 청약액과 법 제165조의7제1항 각 호 외의 부분 본문에 따라 청약 직전 12개월간 취득한 해당 법인 주식의 취득가액(취득가액이 액면액에 미달하는 경우에는 액면액을 말한다. 이하 이 조에서 같다)을 합산한 금액이 그 법인으로부터 청약 직전 12개월간 지급받은 급여총액(소득세과세대상이 되는 급여액을 말한다)을 초과하는 경우 2. 다음 각 목의 요건을 모두 충족하는 경우 가. 주식의 모집ㆍ매출 규모 및 우리사주조합원의 주금납입능력, 그 밖에 금융위원회가 정하여 고시하는 사유에 비추어 주식총수의 100분의 20까지 우리사주조합원이 청약하기 어려운 경우일 것 나. 「근로복지기본법」에 따른 우리사주조합이 우리사주조합원총회의 의결에 따라 가목의 비율 미만으로 모집하거나 매출하는 주식을 배정받기를 원한다는 의사를 법 제165조의7제1항 각 호 외의 부분 본문에 따른 법인에게 서면으로 표시할 것 다. 법 제165조의7제1항 각 호 외의 부분 본문에 따른 법인이 이 호 나목에 따라 표시된 배정비율에 따라 주식을 배정하는 데 서면으로 동의할 것 ④ 법 제165조의7제2항에 따른 우리사주조합원의 소유주식수는 법 제119조제1항에 따라 증권의 모집 또는 매출에 관한 신고서를 금융위원회에 제출한 날(법 제119조제2항 전단에 따른 일괄신고서를 제출하여 증권의 모집 또는 매출에 관한 신고서를 제출하지 아니하는 경우에는 주주총회 또는 이사회의 결의가 있은 날)의 직전일의 주주명부상 우리사주조합의 대표자 명의로 명의개서된 주식에 따라 산정한다. 다만, 「근로복지기본법」 제43조제1항에 따른 수탁기관(이하 이 항에서 "수탁기관"이라 한다)을 통해서 전자등록(「주식ㆍ사채 등의 전자등록에 관한 법률」 제2조제2호에 따른 전자등록을 말한다. 이하 같다)된 주식의 경우에는 같은 법 제22조제2항에 따른 고객계좌부에 따라 산정하고, 수탁기관이 예탁결제원에 예탁한 주식의 경우에는 법 제310조제1항에 따른 투자자계좌부에 따라 산정한다. <개정 2010. 12. 7., 2013. 8. 27., 2019. 6. 25.> [본조신설 2009. 2. 3.][제목개정 2013. 7. 5.] |
▶ 구주주 1주당 배정비율 산출근거
| A. 보통주식 | 68,454,671주 |
| B. 우선주식 | -주 |
| C. 발행주식총수 (A + B) | 68,454,671주 |
| D. 자기주식 | -주 |
| E. 자기주식을 제외한 발행주식총수 (C - D) | 68,454,671주 |
| F. 유상증자 주식수 | 30,210,000주 |
| G. 증자비율 (F / C) | 44.13% |
| H. 우리사주조합 배정 | 6,042,000주 |
| I. 구주주 배정 (F - H) | 24,168,000주 |
| J. 구주주 1주당 배정비율 (I / E) | 0.3530511453 |
3. 공모가격 결정방법
가. 공모가격 결정방법
「증권의 발행 및 공시 등에 관한 규정」제5-18조에 의거 주주배정 증자 시 가격산정 절차 폐지 및 가격산정의 자율화에 따라 발행가액을 자유롭게 산정할 수 있으나, 시장혼란 우려 및 기존 관행 등으로 「(舊)유가증권 발행 및 공시 등에 관한 규정」 제57조를 일부 준용하여 아래와 같이 산정합니다.
① 예정발행가액 : 예정발행가액은 이사회결의일 전일(2025년 03월 27일)을 기산일로 하여 유가증권시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가, 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액을 기준주가로 하여 할인율 20%를 적용, 증자비율은 유상증자 주식수/발행주식총수로 계산하여 아래의 산식에 의하여 산정된 발행가액(예정발행가액)으로 합니다. 단, 호가단위 미만은 호가단위로 절상하며, 그 가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다.
* 예정발행가액 = [기준주가 × (1-할인율)] / [1+(증자비율 × 할인율)]
② 1차 발행가액 : 1차 발행가액은 신주배정기준일 전 제3거래일(2025년 05월 28일)을 기산일로 하여 각 해당 기간 동안 유가증권시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액을 기준주가로 하여 할인율 20%를 적용, 증자비율은 유상증자 주식수/발행주식총수로 계산하여 아래의 산식에 의하여 산정된 발행가액(1차 발행가액)으로 합니다. 단, 호가단위 미만은 호가단위로 절상하며, 그 가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다.
* 1차 발행가액 = [기준주가 × (1-할인율)] / [1+(증자비율 × 할인율)]
③ 2차 발행가액 : 2차 발행가액은 구주주 청약일 전 제3거래일(2025년 07월 03일)을 기산일로 하여 각 해당 기간 동안 유가증권시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액을 2차 기준주가로 하여 아래의 산식에 따라 결정하며 할인율은 20%를 적용합니다. 단, 호가단위 미만은 호가단위로 절상하며, 그 가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다.
* 2차 발행가액 = 기준주가 × (1-할인율)
④ 확정 발행가액 : 확정 발행가액은 1차 발행가액과 2차 발행가액 중 낮은 가액으로 합니다. 다만 「자본시장과 금융투자업에 관한 법률」 제165조의6 및 「증권의 발행 및 공시 등에 관한 규정」 제5-15조의2에 의거하여 1차 발행가액과 2차 발행가액 중 낮은 가액이 청약일 전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가를 기준주가로 하여 40% 할인율을 적용하여 산정한 가격보다 낮은 경우 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격을 확정발행가액으로 합니다. 단, 호가단위 미만은 호가단위로 절상하며, 그 가액이 액면가액 이하일 경우에는 액면가액을 확정 발행가액으로 합니다.
* 확정 발행가액 = Max{Min[1차 발행가액, 2차 발행가액], 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가의 60%}
※ 일반공모 발행가액은 우리사주조합 및 구주주 청약 시에 적용된 확정 발행가액을 동일하게 적용합니다.
나. 발행 조건 결정 배경
당사는 본 유상증자 규모를 산정함에 있어 자금의 사용목적 뿐만 아니라 증자비율을 함께 고려하여 검토를 진행하였습니다. 이를 바탕으로 이사회에서는 본 건 유상증자 규모의 적정성에 대한 논의를 진행하였습니다.
금번 유상증자는 단순한 재무 비율 개선을 위한 목적이 아닌 미래성장동력 확보를 위한 명확한 투자를 목적으로 하는 당사의 전략적 선택입니다. 증자비율은 기업의 필요 자금 규모와 주주가치 보호의 균형을 고려하여 다양한 비율로 결정될 수 있으나, 증자비율이 과도하게 높을 경우 시장에서 재무 상태에 대한 부정적인 신호로 해석될 가능성이 있어 적정한 수준에서 결정하는 것이 중요합니다. 할인율의 경우 증권의 발행 및 공시 등에 관한 규정에 의거 주주배정후실권주일반공모 유상증자의 경우 40% 이내에서 결정할 수 있으며, 기존주주들의 지분 희석 정도를 감안하여 적정 할인율에 대한 결정이 필요합니다.
이에, 기존 주주의 권익을 보호하면서도 장기적인 기업가치 상승을 기대할 수 있는 발행조건을 결정하기 위해 당사의 이사회는 과거 제약바이오 상장회사의 유사규모(800억~1200억원) 주주배정후실권주일반공모 유상증자 사례 및 대표주관회사인 NH투자증권㈜의 의견을 종합적으로 고려하였습니다.
| [최근 3개년 주주배정 후 실권주 일반공모 유상증자 사례(주1)] |
| (단위 : 억원, 주, %) |
| 회사명 | 자금사용목적(최초) | 이사회 결의일 | 최초공모금액(억원) | 최종발행규모(억원) | 발행 주식수(주) | 증자비율 | 할인율 |
|---|---|---|---|---|---|---|---|
| 현대바이오 | 운영자금 688억 채무상환자금 260억 |
2024/11/15 | 948 | 859 | 8,200,000 | 20.6% | 25.0% |
| 아미코젠 | 시설자금 457억 채무상환자금 500억 |
2023/9/15 | 957 | 703 | 7,700,000 | 39.0% | 20.0% |
| 메드팩토 | 운영자금 1,159억 | 2023/9/12 | 1,159 | 741 | 12,500,000 | 59.3% | 25.0% |
| 박셀바이오 | 시설자금 452억 운영자금 554억 |
2023/8/7 | 1,006 | 718 | 3,938,000 | 25.9% | 25.0% |
| 메디포스트 | 타법인취득자금 1,200억 | 2023/7/25 | 1,200 | 718 | 13,215,859 | 62.9% | 25.0% |
| 제넥신 | 운영자금 1,000억 | 2022/9/26 | 1,000 | 852 | 5,797,102 | 23.1% | 25.0% |
| 아이큐어 | 시설자금 223억 운영자금 100억 채무상환자금 477억 |
2022/9/19 | 800 | 343 | 12,326,650 | 64.9% | 25.0% |
| 오스코텍 | 시설자금 110억 운영자금 1091억 |
2022/8/26 | 1,200 | 886 | 6,400,000 | 20.3% | 20.0% |
| 유틸렉스 | 시설자금 100억 운영자금 866억 |
2022/4/8 | 966 | 516 | 7,000,000 | 40.7% | 20.0% |
| 평균 | 39.6% | 23.3% | |||||
| 출처 : Dart 전자공시시스템 주1) 최초발행규모 800~1200억원 제약바이오 업종 기준 |
과거 사례를 조사한 결과, 평균 증자비율은 39.6%, 평균 할인율은 23.3% 수준으로 파악됩니다. 증자비율의 경우, 자금의 사용목적과 회사의 필요 자금 규모에 따라 20.3% ~ 64.9% 까지 다양한 비율로 결정된 반면, 할인율은 대부분 20% 혹은 25%를 설정하였습니다. 만약, 할인율이 높게 설정될 경우, 동일한 증자규모를 조달하기 위해 더 많은 주식을 발행해야 하므로 주주가치 희석이 더욱 커질 수 있는 반면, 주주가치 희석을 최소화하는 목적으로 할인율을 낮게 설정한다면, 최근 유상증자 시장의 분위기와 당사 주식에 대한 시장의 관심도를 고려해 볼 때, 당초 계획된 청약 수요를 충분히 모집하지 못하게 될 불확실성도 존재하게 됩니다.
당사는 이러한 과거 사례를 기반으로 이사회에서 논의를 진행하였고, 당사의 금번 유상증자는 미래 성장을 위한 시설자금 및 신약연구개발에 우선적으로 사용될 예정으로 시장 평균 대비 낮은 할인율을 설정하더라도 본 증자를 통한 성공적인 자금조달이 가능할 것이라는 대표주관회사의 의견을 반영하여 시장 평균 23.3%보다 낮은 20%를 할인율로 설정하게 되었습니다. 해당 20% 할인율을 적용하여 최초 신고기준 약 천억원 유상증자를 위해 이사회결의일 전 영업일 기준으로 산출한 본 건의 증자비율 역시 시장 평균 39.6%보다 소폭 높은 수준인 44.13%로 주주가치희석을 최소화하면서도 자금조달목적을 효과적으로 달성할 수 있는 발행조건 수준으로 판단하였습니다.
또한 채무상환목적이 아닌 당사의 유상증자 배경 및 사용목적과 유사한 최근 사례 3건(메드팩토, 박셀바이오, 메디포스트)을 살펴보면, 증자비율은 49.4% 수준으로 당사가 설정한 증자비율보다 높게 유상증자를 진행했던 것으로 확인됩니다. 따라서 당사의 자금사용목적과 연계하여 고려한 증자비율은 적절한 수준으로 판단하였습니다.
4. 모집 또는 매출절차 등에 관한 사항
가. 모집 또는 매출조건
| (단위 : 주, 원) |
| 항 목 | 내 용 | |||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 모집 또는 매출주식의 수 | 30,210,000 | |||||||||||||||||||||||||||||||||||||||||||
| 주당 모집가액 또는 매출가액 | 예정가액 | 3,310 | ||||||||||||||||||||||||||||||||||||||||||
| 확정가액 | - | |||||||||||||||||||||||||||||||||||||||||||
| 모집총액 또는 매출총액 | 예정가액 | 99,995,100,000 | ||||||||||||||||||||||||||||||||||||||||||
| 확정가액 | - | |||||||||||||||||||||||||||||||||||||||||||
| 청 약 단 위 |
1) 우리사주조합 : 우리사주조합원의 청약단위는 1주로 하며, 우리사주조합원의 청약한도는 우리사주조합에 배정된 주식수로 합니다.
|
|||||||||||||||||||||||||||||||||||||||||||
| 청약기일 | 우리사주조합 | 개시일 | 2025년 07월 08일 |
| 종료일 | 2025년 07월 08일 | ||
| 구주주 (신주인수권증서 보유자) |
개시일 | 2025년 07월 08일 | |
| 종료일 | 2025년 07월 09일 | ||
| 일반모집 또는 매출 | 개시일 | 2025년 07월 11일 | |
| 종료일 | 2025년 07월 14일 | ||
| 청약 증거금 |
우리사주조합 | 청약금액의 100% | |
| 구주주(신주인수권증서 보유자) | 청약금액의 100% | ||
| 초 과 청 약 | 청약금액의 100% | ||
| 일반모집 또는 매출 | 청약금액의 100% | ||
| 납 입 기 일 / 환 불 일 | 2025년 07월 16일 | ||
| 배당기산일(결산일) | 2025년 01월 01일 | ||
| 주1) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정 요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. 주2) 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
나. 모집 또는 매출의 절차
(1) 공고의 일자 및 방법
| 구 분 | 공고일자 | 공고방법 |
|---|---|---|
| 신주 발행 및 배정기준일(주주확정일) 공고 |
2025년 03월 31일 | 당사 인터넷 홈페이지 (http://www.bukwang.co.kr) |
| 모집가액 확정의 공고 | 2025년 07월 04일 | 당사 인터넷 홈페이지 (http://www.bukwang.co.kr) |
| 실권주 일반공모 청약공고 | 2025년 07월 10일 | 당사 인터넷 홈페이지 (http://www.bukwang.co.kr) NH투자증권㈜ 홈페이지 (http://www.nhqv.com) |
| 실권주 일반공모 배정공고 | 2025년 07월 15일 | 당사 인터넷 홈페이지 (http://www.bukwang.co.kr) NH투자증권㈜ 홈페이지 (http://www.nhqv.com) |
| 주) 청약결과 초과청약금 환불에 대한 통지는 대표주관회사의 홈페이지에 게시함으로써 개별통지에 갈음합니다. |
(2) 청약방법
① 우리사주조합 청약 : 우리사주조합의 청약은 우리사주조합장 명의로 "대표주관회사" NH투자증권 주식회사의 본·지점에서 일괄 청약합니다.
② 구주주 청약(신주인수권증서 보유자 청약) : 구주주 중 주권을 증권회사에 예탁한 일반주주(기존 '실질주주')는 주권을 예탁한 증권회사의 본ㆍ지점 및 대표주관회사의 본ㆍ지점에서 청약할 수 있습니다. 다만, 구주주 중 명의개서대행기관 특별계좌에 주식을 가지고 있는 특별계좌 보유자(기존 '명부주주')는 신주배정통지서를 첨부하여 실명확인증표를 제시한 후 대표주관회사의 본ㆍ지점에서 청약할 수 있습니다. 청약 시에는 소정의 청약서 2통에 필요한 사항을 기입하여 청약증거금과 함께 제출하여야 합니다.
| 2019년 9월 16일 전자증권제도가 시행되어, 주권 상장법인의 상장주식은 전자증권 의무전환대상으로 전자증권제도 시행일에 전자증권으로 일괄 전환되었습니다. 전자증권제도 시행전까지 증권회사에 예탁하고 있는 실질주주 주식은 해당 증권회사 계좌에 전자증권으로 일괄 전환되었으며, 기존 명부주주가 보유한 주식은 명의개서대행기관이 개설하는 특별계좌에 발행되어 소유자별로 관리됩니다. 금번 유상증자시 신주인수권증서는 전자증권으로 발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 "실질주주" 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 "명부주주" 보유주식)에 대하여 배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다. "특별계좌 보유자(기존 "명부주주")"는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후 금번 유상증자 청약 참여 또는 신주인수권증서의 매매가 가능합니다. "특별계좌 보유자(기존 "명부주주")"는 신주인수권증서의 "일반 전자등록계좌(증권회사 계좌)"로 이전 없이 "대표주관회사"의 본ㆍ지점에서 직접 청약하는 방법으로도 금번 유상증자에 청약이 가능합니다. 다만 신주인수권증서의 매매는 명의개서대행기관 내 "특별계좌"에서 "일반 전자등록계좌(증권회사 계좌)"로 신주인수권증서를 이전 신청한 후에만 가능하므로 이 점 유의하시기 바랍니다. |
| 「주식·사채 등의 전자등록에 관한 법률」 제29조(특별계좌의 개설 및 관리) ① 발행인이 제25조부터 제27조까지의 규정에 따라 이미 주권등이 발행된 주식등을 전자등록하는 경우 제25조제1항에 따른 신규 전자등록의 신청을 하기 전에 제27조제1항제2호에 따른 통지를 하지 아니하거나 주권등을 제출하지 아니한 주식등의 소유자 또는 질권자를 위하여 명의개서대행회사, 그 밖에 대통령령으로 정하는 기관(이하 이 조에서 "명의개서대행회사등"이라 한다)에 기준일의 직전 영업일을 기준으로 주주명부등에 기재된 주식등의 소유자 또는 질권자를 명의자로 하는 전자등록계좌(이하 "특별계좌"라 한다)를 개설하여야 한다. ② 제1항에 따라 특별계좌가 개설되는 때에 제22조제2항 또는 제23조제2항에 따라 작성되는 전자등록계좌부(이하 이 조에서 "특별계좌부"라 한다)에 전자등록된 주식등에 대해서는 제30조부터 제32조까지의 규정에 따른 전자등록을 할 수 없다. 다만, 다음 각 호의 어느 하나에 해당하는 경우에는 그러하지 아니하다. 1. 해당 특별계좌의 명의자가 아닌 자가 주식등이 특별계좌부에 전자등록되기 전에 이미 주식등의 소유자 또는 질권자가 된 경우에 그 자가 발행인에게 그 주식등에 관한 권리가 표시된 주권등을 제출(주권등을 제출할 수 없는 경우에는 해당 주권등에 대한 제권판결의 정본·등본을 제출하는 것을 말한다. 이하 제2호 및 제3호에서 같다)하고 그 주식등을 제30조에따라 자기 명의의 전자등록계좌로 계좌간 대체의 전자등록을 하려는 경우(해당 주식등에 질권이 설정된 경우에는 다음 각 목의 어느 하나에 해당하는 경우로 한정한다) 가. 해당 주식등에 설정된 질권이 말소된 경우 나. 해당 주식등의 질권자가 그 주식등을 특별계좌 외의 소유자 명의의 다른 전자등록계좌로 이전하는 것에 동의한 경우 2. 해당 특별계좌의 명의자인 소유자가 발행인에게 전자등록된 주식등에 관한 권리가 표시된 주권등을 제출하고 그 주식등을 제30조에 따라 특별계좌 외의 자기 명의의 다른 전자등록계좌로 이전하려는 경우(해당 주식등에 질권이 설정된 경우에는 제1호 각 목의 어느 하나에 해당하는 경우로 한정한다) 3. 해당 특별계좌의 명의자인 질권자가 발행인에게 주권등을 제출하고 그 주식등을 제30조에 따라 특별계좌 외의 자기 명의의 전자등록계좌로 이전하려는 경우 4. 그 밖에 특별계좌에 전자등록된 주식등의 권리자의 이익을 해칠 우려가 없는 경우로서 대통령령으로 정하는 경우 ③ 누구든지 주식등을 특별계좌로 이전하기 위하여 제30조에 따른 계좌간 대체의 전자등록을 신청할 수 없다. 다만, 제1항에 따라 특별계좌를 개설한 발행인이 대통령령으로 정하는 사유에 따라 신청을 한 경우에는 그러하지 아니하다. ④ 명의개서대행회사등이 발행인을 대행하여 제1항에 따라 특별계좌를 개설하는 경우에는 「금융실명거래 및 비밀보장에 관한 법률」 제3조에도 불구하고 특별계좌부에 소유자 또는질권자로 전자등록될 자의 실지명의를 확인하지 아니할 수 있다. |
③ 초과청약 : 신주인수권증서 청약을 한 자에 한하여 신주인수권증서 청약 한도 주식수의 20%를 추가로 청약할 수 있습니다. 이때, 신주인수권증서 청약 한도주식수의 20%에 해당하는 주식 중 소수점 이하인 주식은 청약할 수 없습니다.
a. 청약한도 주식수 = 신주인수권증서청약 한도주식수 + 초과청약한도 주식수
b. 신주인수권증서청약 한도주식수 = 보유한 신주인수권 증서의 수량
c. 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 * 초과청약 비율(20%)
④ 일반청약자는 “금융실명거래 및 비밀보장에 관한 법률”의 규정에 의한 실명자이어야 하며, 청약사무 취급처에 실명확인증표, 소정의 청약서, 청약증거금을 제시하고 청약합니다. 일반청약자의 청약 시, 각 청약처별로 다중청약은 가능하나, 한 개의 청약처에서 이중청약은 불가능하며, 집합투자기구 중 운용주체가 다른 집합투자기구를 제외한 청약자의 한 개 청약처에 대한 복수청약은 불가능합니다. 고위험고수익투자신탁등은 청약 시, 청약사무 취급처에 「증권의 인수업무 등에 관한규정」 제2조 제18호에 따른 요건을 충족함을 확약하는 서류 및 자산총액이 기재되어 있는 서류를 함께 제출하여야 합니다.
⑤ 청약은 청약주식의 단위에 따라 될 수 있으며 1인당 청약한도를 초과하는 청약부분에 대하여는 청약이 없는 것으로 하고 청약사무 취급처는 그 차액을 납입일까지 당해 청약자에게 반환하며, 이때 받은 날부터의 이자는 지급하지 않습니다.
⑥ 본 유상증자에 청약하고자 하는 투자자(「자본시장과 금융투자업에 관한 법률」 제 9조 제 5항에 규정된 전문투자자 및 「자본시장과 금융투자업에 관한 법률 시행령」 제 132조에 따라 투자설명서의 교부가 면제되는자 제외)는 청약 전 반드시 투자설명서를 교부 받아야 하고, 이를 확인하는 서류에 서명 또는 기명날인하여야 합니다.
⑦ 청약한도
a. 우리사주조합원의 청약단위는 1주로 하며, 우리사주조합원의 청약한도는 우리사주조합에 배정된 주식수로 합니다.
b. 구주주(신주인수권증서 보유자)의 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율인 0.3530511453주를 곱하여 산정된 신주인수권증서(단, 1주 미만은 절사)와 초과청약가능 주식수(보유하고 있는 신주인수권증서 1주당 0.2주를 곱하여 산정된 수, 단 1주 미만은 절사)를 합한 주식수로 합니다(단, 1주 미만은 절사).
c. 일반공모 청약자의 청약한도는 일반공모 총 공모주식 범위 내로 하며, 청약한도를 초과하는 부분에 대해서는 청약이 없는 것으로 간주합니다.
⑧ 기타
a. 일반공모 배정을 함에 있어 이중청약이 있는 경우에는 그 전부를 청약으로 보지 않습니다. 단, 동일한 집합투자기구라도 운용주체(집합투자업자)가 다른 펀드는 제외로 합니다.
b. 일반공모 배정을 함에 있어 1계좌당 청약(배정)한도를 초과하는 청약 부분에 대하여는 청약이 없는 것으로 합니다.
c. 청약자는 금융실명거래 및 비밀보장에 관한 법률에 의거 실명에 의해 청약해야 합니다.
d. 「자본시장과 금융투자업에 관한 법률」제180조의4 및 같은 법 시행령 제208조의4제1항에 따라 2025년 03월 31일부터 2025년 07월 03일까지 공매도를 하거나 공매도 주문을 위탁한 자는 금번 모집(매출)에 청약할 수 없으며, 이를 위반하여 주식을취득할 경우 같은 법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만 모집(매출)가액의 공정한 가격형성을 저해하지 않는 경우로서 같은 법 시행령 제208조의4제2항 및 「금융투자업규정」제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다.
|
※ 예외적으로 모집(매출)에 따른 주식 취득이 허용되는 경우 ① 모집(매출)에 따른 주식 취득이 금지되는 공매도 거래 기간 중에 전체 공매도 주문수량보다 많은 수량의 주식을 가격경쟁에 의한 거래 방식으로 매수한 경우 (매매계약 체결일 기준으로 정규시장의 매매거래시간에 매수한 경우로 한정) ② 한국거래소의 증권시장업무규정 또는 파생상품시장업무규정에서 정한 유동성 공급 및 시장조성 목적을 위해 해당 주식을 공매도하거나 공매도 주문을 위탁한 경우 ③ 동일한 법인 내에서 모집(매출)에 따른 주식 취득 참여가 금지되는 공매도 거래 기간 중 공매도를 하지 않거나 공매도 주문을 위탁하지 않은 독립거래단위(*)가 모집(매출)에 따른 주식을 취득하는 경우- (*)「금융투자업규정」제6-30조 제5항에 따라 의사결정이 독립적이고 상이한 |
(3) 청약취급처
| 청약대상자 | 청약취급처 | 청약일 | |
|---|---|---|---|
| 우리사주조합 | "대표주관회사"의 본ㆍ지점 | 2025년 07월 08일 | |
| 구주주 (신주인수권증서 보유자) |
특별계좌 보유자 (기존 '명부주주') |
"대표주관회사"의 본ㆍ지점 | 2025년 07월 08일 ~ 2025년 07월 09일 |
| 일반주주 (기존 '실질주주') |
1) 주주확정일 현재 부광약품(주)의 주식을 예탁하고 있는 당해 증권회사의 본ㆍ지점 2) "대표주관회사"의 본ㆍ지점 |
||
| 일반공모청약 (고위험고수익투자신탁등 청약 포함) |
"대표주관회사"의 본ㆍ지점 | 2025년 07월 11일 ~ 2025년 07월 14일 |
|
(4) 청약결과 배정방법
① 우리사주조합
총 발행예정주식 30,210,000주의 20%에 해당하는 6,042,000주는 「자본시장과 금융투자업에 관한 법률」제165조의7에 따라 우리사주조합에 우선 배정합니다.
② 구주주 청약 : 신주배정기준일(2025년 06월 02일) 18시 현재 주주명부에 등재된 주주(이하 “구주주”라 한다)에게 본 주식을 1주당 0.3530511453주를 곱하여 산정된 배정주식수(단, 1주 미만은 절사함)로 하고, 배정범위 내에서 청약한 수량만큼 배정합니다.
③ 초과청약에 대한 배정: 우리사주조합 및 구주주(신주인수권증서 보유자) 청약 이후 발생한 실권주가 있는 경우, 실권주를 구주주(신주인수권증서 보유자)가 초과청약(초과청약비율 : 배정 신주 1주당 0.2주)한 주식수에 비례하여 배정하며(단, 초과청약 주식수가 실권주에 미달한 경우 100% 배정), 1주 미만의 주식은 절사하여 배정하지 않습니다.
(i) 청약한도 주식수 = 신주인수권증서청약 한도주식수 + 초과청약 한도주식수
(ii) 신주인수권증서청약 한도주식수 = 보유한 신주인수권 증서의 수량
(iii) 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 X 초과청약 비율(20%)
④ 일반공모 청약 : 상기 우리사주조합, 구주주청약 및 초과청약 결과 발생한 실권주 및 단수주는 "대표주관회사"가 다음 각 호와 같이 일반에게 공모하되, 「증권 인수업무 등에 관한 규정」 제9조제2항제3호에 따라 고위험고수익투자신탁등에 공모주식의 5%를 배정하며, 나머지 95%에 해당하는 주식은 개인청약자 및 기관투자자에게 구분 없이 배정합니다. 고위험고수익투자신탁등에 대한 공모주식 5%와 개인투자자 및 기관투자자에 대한 공모주식 95%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정합니다. 다만,「증권 인수업무 등에 관한 규정」제9조제3항에 따라 어느 한 그룹만 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다.
(i) 일반공모에 관한 배정수량 계산시에는 "대표주관회사""의 "청약물량"(대표주관회사"의 청약처에서 일반공모 방식으로 접수를 받은 청약주식수를 의미하며, "대표주관회사" 에 대하여 개별적으로 산정한 청약주식수를 말한다)에 대해서는 "대표주관회사의 "총청약물량"("대표주관회사"가 일반공모 방식으로 접수를 받은 "청약물량"의 합을 말한다)을 "일반공모 배정분" 주식수로 나눈 통합청약경쟁률에 따라 "대표주관회사" 의 각 청약자에 배정하는 방식(이하 "통합배정"이라 한다)으로 합니다.
(ii) 일반공모에 관한 배정시 "대표주관회사" 의 "총청약물량"이 "일반공모 배정분" 주식수를 초과하는 경우에는 청약경쟁률에 따라 5사6입을 원칙으로 안분 배정하여 잔여주식이 최소화되도록 합니다. 이후 최종 잔여주식은 최대청약자부터 순차적으로 우선 배정하되, 동순위 최대청약자가 최종 잔여 주식보다 많은 경우에는 "대표주관회사"가 무작위 추첨방식을 통하여 배정합니다.
(iii) 일반공모 청약결과 일반공모 총 청약주식수가 일반공모 주식수에 미달하는 경우에는 청약주식수대로 배정하며, 배정결과 발생하는 잔여주식은 "대표주관회사"가 자기의 계산으로 인수합니다.
(iv) 단, "대표주관회사"는 「증권 인수업무 등에 관한 규정」 제9조제2항에 의거 고위험고수익투자신탁등 및 일반청약자에 대하여 배정하여야 할 주식이 50,000주(액면가 500원 기준) 이하이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 일반청약자에게 배정하지 아니하고 자기의 계산으로 인수할 수 있습니다.
(5) 투자설명서 교부에 관한 사항
- 「자본시장과 금융투자업에 관한 법률」 제124조에 의거, 본 주식의 청약에 대한 투자설명서 교부 의무는 부광약품(주) 및 "대표주관회사" 가 부담하며, 금번 유상증자의 청약에 참여하시는 투자자께서는 투자설명서를 의무적으로 교부받으셔야 합니다.
- 금번 유상증자에 청약하고자 하는 투자자께서는 (「자본시장과 금융투자업에 관한 법률」 제9조제5항에 규정된 전문투자자 및 동법 시행령 제132조에 따라 투자설명서의 교부가 면제되는 자 제외) 청약하시기 전 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
- 투자설명서 수령거부 의사표시는 서면, 전화, 전신, 팩스, 전자우편 및 이와 비슷한 전자통신, 그 밖에 금융위원회가 정하여 고시하는 방법으로 가능합니다.
① 투자설명서 교부 방법 및 일시
| 구분 | 교부방법 | 교부일시 |
|---|---|---|
| 우리사주조합 청약자 |
「자본시장과 금융투자업에 관한 법률 시행령」제132조에 의해 투자설명서 교부 면제됨 | 해당사항 없음 |
| 구주주 청약자 |
1),2),3)을 병행 1)우편 송부 2) "대표주관회사" 본ㆍ지점에서 교부 3) "대표주관회사" 홈페이지나 HTS/MTS에서 교부 |
1) 우편송부시 : 구주주청약 초일(2025년 07월 08일) 전 수취 가능 2) "대표주관회사" 본ㆍ지점 3) "대표주관회사" 홈페이지 또는 HTS/MTS 교부 |
| 일반 청약자 (고위험고수익 투자신탁 청약 포함) |
1),2)를 병행 1) "대표주관회사" 본ㆍ지점에서 교부 2) "대표주관회사"의 홈페이지나 HTS/MTS에서 교부 |
1) "대표주관회사"의 본ㆍ지점 : 일반공모 청약 종료일(2025년 07월 14일)까지 2) "대표주관회사"의 홈페이지 또는 HTS/MTS 교부 : 일반공모 청약 종료일(2025년 07월 14일)까지 |
| ※ 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다. |
② 확인절차
a. 우편을 통한 투자설명서 수령시
- 청약하시기 위해 지점을 방문하셨을 경우, 직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
- HTS/MTS를 통한 청약을 원하시는 경우, 청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
- 주주배정 유상증자의 경우 유선청약이 가능합니다. 유선상으로 신분확인을 하신 후, 투자설명서 교부 확인을 해주시고 청약을 진행하여 주시기 바랍니다.
b. 지점 방문을 통한 투자설명서 수령시
직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
c. 홈페이지 또는 HTS/MTS를 통한 교부
청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
③ 기타
a. 금번 유상증자의 경우, 본 증권신고서의 효력발생 이후 주주명부상 주주분들에게 투자설명서를 우편으로 발송할 예정입니다. 우편의 반송 등에 의한 사유로 교부를 받지 못하신 투자자께서는 지점방문을 통해 인쇄물을 받으실 수 있으며, 또한 동일한 내용의 투자설명서를 전자문서의 형태로 NH투자증권(주)의 홈페이지에서 다운로드 받으실 수 있습니다. 다만, 전자문서의 형태로 교부받으실 경우, 「자본시장과 금융투자업에 관한 법률」 제124조 제1항 각호의 요건을 모두 충족해야만 청약이 가능합니다.
b. 구주주 청약시 대표주관회사인 NH투자증권(주) 이외의 증권회사를 이용한 청약 방법
해당 증권회사의 청약방법 및 규정에 의해 청약을 진행하시기 바랍니다. 이 경우에도, 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
※ 투자설명서 교부를 받지 않거나, 수령거부의사를 서면 등의 방법으로 표시하지 않을 경우, 본 유상증자의 청약에 참여할 수 없습니다.
| ※ 관련법규 「자본시장과 금융투자업에 관한 법률」 제9조 (그 밖의 용어의 정의) ⑤ 이 법에서 "전문투자자"란 금융투자상품에 관한 전문성 구비 여부, 소유자산규모 등에 비추어 투자에 따른 위험감수능력이 있는 투자자로서 다음 각 호의 어느 하나에 해당하는 자를 말한다. 다만, 전문투자자 중 대통령령으로 정하는 자가 일반투자자와 같은 대우를 받겠다는 의사를 금융투자업자에게 서면으로 통지하는 경우 금융투자업자는 정당한 사유가 있는 경우를 제외하고는 이에 동의하여야 하며, 금융투자업자가 동의한 경우에는 해당 투자자는 일반투자자로 본다. <개정 2009.2.3> 1. 국가 2. 한국은행 3. 대통령령으로 정하는 금융기관 4. 주권상장법인. 다만, 금융투자업자와 장외파생상품 거래를 하는 경우에는 전문투자자와 같은 대우를 받겠다는 의사를 금융투자업자에게 서면으로 통지하는 경우에 한한다. 5. 그 밖에 대통령령으로 정하는 자 제124조 (정당한 투자설명서의 사용) ① 누구든지 증권신고의 효력이 발생한 증권을 취득하고자 하는 자(전문투자자, 그 밖에 대통령령으로 정하는 자를 제외한다)에게 제123조에 적합한 투자설명서(집합투자증권의 경우 투자자가 제123조에 따른 투자설명서의 교부를 별도로 요청하지 아니하는 경우에는 제2항제3호에 따른 간이투자설명서를 말한다. 이하 이 항 및 제132조에서 같다)를 미리 교부하지 아니하면 그 증권을 취득하게 하거나 매도하여서는 아니 된다. 이 경우 투자설명서가 제436조에 따른 전자문서의 방법에 따르는 때에는 다음 각 호의 요건을 모두 충족하는 때에 이를 교부한 것으로 본다.<개정 2013.5.28> 1. 전자문서에 의하여 투자설명서를 받는 것을 전자문서를 받을 자(이하 "전자문서수신자"라 한다)가 동의할 것 2. 전자문서수신자가 전자문서를 받을 전자전달매체의 종류와 장소를 지정할 것 3. 전자문서수신자가 그 전자문서를 받은 사실이 확인될 것 4. 전자문서의 내용이 서면에 의한 투자설명서의 내용과 동일할 것 「자본시장과 금융투자업에 관한 법률 시행령」 제11조 (증권의 모집·매출) ① 법 제9조제7항 및 제9항에 따라 50인을 산출하는 경우에는 청약의 권유를 하는 날 이전 6개월 이내에 해당 증권과 같은 종류의 증권에 대하여 모집이나 매출에 의하지 아니하고 청약의 권유를 받은 자를 합산한다. 다만, 다음 각 호의 어느 하나에 해당하는 자는 합산 대상자에서 제외한다. <개정 2009.10.1., 2010.12.7., 2013.6.21., 2013.8.27., 2016.6.28., 2016.7.28.> 1. 다음 각 목의 어느 하나에 해당하는 전문가 가. 전문투자자 나. 삭제 <2016.6.28.> 다. 「공인회계사법」에 따른 회계법인 라. 신용평가회사(법 제335조의3에 따라 신용평가업인가를 받은 자를 말한다. 이하 같다) 마. 발행인에게 회계, 자문 등의 용역을 제공하고 있는 공인회계사·감정인·변호사·변리사·세무사 등 공인된 자격증을 가지고 있는 자 바. 그 밖에 발행인의 재무상황이나 사업내용 등을 잘 알 수 있는 전문가로서 금융위원회가 정하여 고시하는 자 2. 다음 각 목의 어느 하나에 해당하는 연고자 가. 발행인의 최대주주[「금융회사의 지배구조에 관한 법률」 제2조제6호가목에 따른 최대주주를 말한다. 이 경우 "금융회사"는 "법인"으로 보고, "발행주식(출자지분을 포함한다. 이하 같다)"은 "발행주식"으로 본다. 이하 같다]와 발행주식 총수의 100분의 5 이상을 소유한 주주 나. 발행인의 임원(「상법」 제401조의2제1항 각 호의 자를 포함한다. 이하 이 호에서 같다) 및 「근로복지기본법」에 따른 우리사주조합원 다. 발행인의 계열회사와 그 임원 라. 발행인이 주권비상장법인(주권을 모집하거나 매출한 실적이 있는 법인은 제외한다)인 경우에는 그 주주 마. 외국 법령에 따라 설립된 외국 기업인 발행인이 종업원의 복지증진을 위한 주식매수제도 등에 따라 국내 계열회사의 임직원에게 해당 외국 기업의 주식을 매각하는 경우에는 그 국내 계열회사의 임직원 바. 발행인이 설립 중인 회사인 경우에는 그 발기인 사. 그 밖에 발행인의 재무상황이나 사업내용 등을 잘 알 수 있는 연고자로서 금융위원회가 정하여 고시하는 자 제132조 (투자설명서의 교부가 면제되는 자) 법 제124조제1항 각 호 외의 부분 전단에서 “대통령령으로 정하는 자”란 다음 각 호의 어느 하나에 해당하는 자를 말한다. <개정 2009. 7. 1., 2013. 6. 21., 2021. 1. 5.> 1. 제11조제1항제1호다목부터 바목까지 및 같은 항 제2호 각 목의 어느 하나에 해당하는 자 1의2. 제11조제2항제2호 및 제3호에 해당하는 자 2. 투자설명서를 받기를 거부한다는 의사를 서면, 전화ㆍ전신ㆍ팩스, 전자우편 및 이와 비슷한 전자통신, 그 밖에 금융위원회가 정하여 고시하는 방법으로 표시한 자 3. 이미 취득한 것과 같은 집합투자증권을 계속하여 추가로 취득하려는 자. 다만, 해당 집합투자증권의 투자설명서의 내용이 직전에 교부한 투자설명서의 내용과 같은 경우만 해당한다. |
(6) 주권 유통에 관한 사항
- 주권유통개시(예정)일: 2025년 07월 28일 (2019년 9월 16일 전자증권제도가 시행됨에 따라 실물 주권의 교부 없이 각 주주의 보유 증권계좌로 상장일에 주식이 등록발행되어 입고되며, 상장일부터 유통이 가능합니다. 단, 유관기관과의 업무 협의 과정에서 상기 일정은 변경될 수 있음을 유의하시기 바랍니다.)
(7) 청약증거금의 대체 및 반환 등에 관한 사항
청약증거금은 청약금액의 100%로 하고, 주금납입기일에 주금납입금으로 대체하며, 청약증거금에 대해서는 무이자로 합니다.
(8) 주금납입장소 : (주)신한은행 보라매역금융센터
다. 신주인수권증서에 관한 사항
| 신주배정기준일 | 신주인수권증서의 매매 금융투자업자 | |
|---|---|---|
| 회사명 | 회사고유번호 | |
| 2025년 06월 02일 | NH투자증권(주) | 00120182 |
(1) 금번과 같이 주주배정방식의 유상증자를 실시할 때, 주주가 소유하고 있는 주식수 비율대로 신주를 인수할 권리인 신주인수권에 대하여 당사는 「자본시장과 금융투자업에 관한 법률」제165의6조제3항 및 「증권의 발행 및 공시 등에 관한 규정」 제5-19조에 의거하여 주주에게 신주인수권증서를 발행합니다.
(2) 금번 유상증자시 신주인수권증서는 전자증권제도 시행일(2019년 09월 16일) 이후에 발행되고 상장될 예정으로 전자증권으로 발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여 배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다.
(3) 신주인수권증서 매매의 중개를 할 증권회사는 대표주관회사인 NH투자증권(주), 로 합니다.
(4) 신주인수권증서 매매 등
① 금번 유상증자시 신주인수권증서는 전자증권제도 시행 이후에 발행되고 상장될 예정으로 실물은 발행 되지 않고 전자증권으로 등록발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여 배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다.
② 신주인수권증서를 매매하고자 하는 주주는 신주인수권증서를 예탁하고 있는 증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자 계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일 내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
(5) 신주인수권증서를 양수한 투자자의 청약방법
신주인수권증서를 증권회사에 예탁하고 있는 양수인은 당해 증권회사 점포 및 대표주관회사인 NH투자증권(주)의 본점 및 지점을 통해 해당 신주인수권증서에 기재되어 있는 수량(초과청약이 있는 경우 초과청약 가능수량이 합산된 수량)만큼 청약할 수 있으며 청약 기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
(6) 신주인수권증서의 상장
당사는 금번 주주배정후 실권주 일반공모 유상증자 관련 신주인수권증서의 상장을 한국거래소에 신청할 예정입니다. 동 신주인수권증서가 상장될 경우 상장기간은 2025년 06월 23일부터 2025년 06월 27일까지 5거래일간으로 예정하고 있으며, 동 기간중 상장된 신주인수권증서를 한국거래소에서 매매할 수 있습니다. 동 신주인수권증서는 2025년 06월 30일에 상장폐지될 예정입니다. (「유가증권시장 상장규정」 제150조 "신규상장"에 따라 5거래일 이상 상장되어야 하며,동 규정 제152조 "신주인수권증서의 상장폐지기준"에 따라 주주청약 개시일 5거래일전에 상장폐지되어야 함)
(7) 신주인수권증서의 거래 관련 추가사항
당사는 금번 유상증자의 신주인수권증서를 상장신청할 예정인 바, 현재까지 관계기관과 협의된 신주인수권증서 상장시의 제반 거래관련 사항은 다음과 같습니다.
① 상장방식 : 전자등록발행된 신주인수권증서 전부를 상장합니다.
② 일반주주의 신주인수권증서 거래
| 구분 | 상장거래방식 | 계좌대체 거래방식 |
|---|---|---|
| 방법 | 주주의 신주인수권증서를 전자등록발행하여 상장합니다. 상장된 신주인수권증서를 장내거래를 통하여 매수하여 증권사 계좌에 보유한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. 주주의 신주인수권증서는 전자등록발행되므로 실물 증서는 발행되지 않습니다. | 신주인수권증서를 매매하고자 하는 기존 실질주주는 위탁증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. |
| 기간 | 2025년 06월 23일부터 2025년 06월 27일까지(5거래일간) 거래 | 신주배정통지일(2025년 06월 16일(예정))부터 신주인수권증서의 상장거래 마지막 날 이후 제2영업일(2025년 07월 01일)까지 거래 |
| 주1) | 상장거래 : 2025년 06월 23일부터 2025년 06월 27일까지(5영업일간) 거래 가능합니다. |
| 주2) |
계좌대체거래 : 신주배정통지일인 2025년 06월 16일(예정)부터 2025년 07월 01일까지 거래 가능합니다. -> 신주인수권증서 상장거래의 마지막 결제일인 2025년 07월 01일까지 계좌대체(장외거래) 가능하며, 동 일자 이후부터는 신주인수권증서의 청약권리 명세를 확정하므로 신주인수권증서의 계좌대체(장외거래)가 제한됩니다. |
| 주3) | 신주인수권증서는 전자등록발행되므로 실물은 발행되지 않습니다. |
③ 특별계좌 소유주(기존 '명부주주')의 신주인수권증서 거래
a. '특별계좌 보유자(기존 '명부주주')'는 명의개서대행기관에 '특별계좌'에서 '일반전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후 금번 유상증자 청약 참여 또는 신주인수권증서의 매매가 가능합니다.
b. '특별계좌 보유자(기존 '명부주주')'는 신주인수권증서의 '일반 전자등록계좌(증권회사 계좌)'로 이전 없이 대표주관회사인 NH투자증권(주)의 본ㆍ지점에서 직접 청약하는 방법으로도 금번 유상증자에 청약이 가능합니다. 다만 신주인수권증서의 매매는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후에만 가능하므로 이 점 유의하시기 바랍니다.
라. 기타 모집 또는 매출에 관한 사항
(1) 본 증권신고서는 공시심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요 내용의 변경시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있으므로 투자자 여러분께서는 투자시 이러한 점을 감안하시기 바랍니다.
(2) 「자본시장과 금융투자업에 관한 법률」제120조 3항에 의거 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다.
(3) 본 증권신고서에 기재된 내용은 신고서 제출일 현재까지 발생된 것으로 본 신고서에 기재된 사항 이외에 자산, 부채, 현금흐름 또는 손익상황에 중대한 변동을 가져오거나 중요한 영향을 미치는 사항은 없습니다. 따라서, 주주 및 투자자가 투자의사를 결정함에 있어 유의하여야 할 사항이 본 증권신고서상에 누락되어 있지 않습니다.
(4) 금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서, 반기보고서, 분기보고서 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있사오니 투자의사를 결정하시는 데 참조하시기 바랍니다.
(5) 본 증권신고서의 예정 모집가액은 확정되어 있는 것은 아니며, 청약일 3거래일 전에 확정 발행가액을 산정함으로써 확정될 예정입니다. 또한, 본 증권신고서의 발행예정금액은 추후 주당 발행가액이 확정되는 내용에 따라 변경될 수 있음을 유의하여 주시기 바랍니다.
5. 인수 등에 관한 사항
[공모방법 : 잔액인수]
| 인수인 | 인수주식 종류 및 수 | 인수대가 | |
|---|---|---|---|
| 대표주관회사 | NH투자증권(주) | 인수주식의 종류 : 기명식 보통주식 인수주식의 수 : 최종 실권주 |
인수수수료 : 모집총액의 1.0% |
| 주1) 최종 실권주 : 우리사주조합, 구주주청약 및 일반공모 후 발생한 배정잔여주 또는 청약미달주식 주2) 모집총액 : 최종 발행가액 × 총 발행주식수 주3) 대표주관회사는 「증권 인수업무 등에 관한 규정」제9조제2항제7호에 의거 고위험고수익투자신탁등 및 일반청약자에 대하여 배정하여야 할 주식이 50,000주(액면가 500원 기준) 이하이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 고위험고수익투자신탁등 및 일반청약자에게 배정하지 아니하고 자기계산으로 인수할 수 있습니다. 주4) 기타 인수에 관한 자세한 사항은 본 증권신고서의 첨부 서류로 공시된 잔액인수계약서를 참조하시기 바랍니다.. |
II. 증권의 주요 권리내용
1. 액면금액
|
※당사의 정관(이하 동일) 제 6 조 (1주의 금액) 이 회사가 발행하는 주식 1주의 금액은 금 오백원으로 한다. |
2. 주식의 발행 및 배정에 관한 사항
|
제 5 조 (발행예정 주식의 총수) 이 회사가 발행할 주식의 총수는 일억 오천만주로 한다. 제 7 조 (주식의 종류) 이 회사가 발행할 주식의 종류는 기명식 보통주식과 기명식 우선주식으로 한다.
1) 이 회사가 발행할 우선주식은 의결권이 없는 것으로 하며, 그 발행주식의 수는 이백만주로 한다. 2) 우선주식에 대하여는 액면금액을 기준으로 하여 년 9%이상에서 발행시에 이사회가 우선배당율을 정한다. 3) 보통주식의 배당율이 우선주식의 배당율을 초과할 경우에는 그 초과분에 대하여 보통주식과 동일한 비율로 참가시켜 배당한다. 4) 우선주식에 대하여 어느 사업년도에 있어서 소정의 배당을 하지 못한 경우에는 누적된 미배당분을 다음 사업년도의 배당시에 우선하여 배당한다. 5) 우선주식에 대하여 소정의 배당을 하지 아니한다는 결의가 있는 경우에는 그 결의가 있는 총회의 다음 총회부터 그 우선적 배당을 한다는 결의가 있는 총회의 종료시까지는 의결권이 있는 것으로 한다. 6) 이 회사가 유상증자 또는 무상증자를 실시하는 경우 우선주식에 대한 신주의 배정은 유상증자의 경우에는 보통주식으로 무상증자의 경우에는 그와 같은 종류의 주식으로 한다. 7) 우선주식의 존속기간은 발행일로부터 5년으로 하고 이 기간 만료와 동시에 보통주식으로 전환된다. 그러나 위 기간중 소정의 배당을 하지 못한 경우에는 소정의 배당을 완료할 때까지 그 기간을 연장한다.
이 회사는 주권 및 신주인수권증서를 발행하는 대신 전자등록기관의 전자등록계좌부에 주식 및 신주인수권증서에 표시되어야 할 권리를 전자등록한다. 가) 주주에게 그가 가진 주식 수에 따라서 신주를 배정하기 위하여 신주인수의 청약을 할 기회를 부여하는 방식 나) 발행주식총수의 100분의 20을 초과하지 않는 범위 내에서 신기술의 도입, 재무구조의 개선 등 회사의 경영상 목적을 달성하기 위하여 필요한 경우 제가호 외의 방법으로 특정한 자(이 회사의 주주를 포함한다)에게 신주를 배정하기 위하여 신주인수의 청약을 할 기회를 부여하는 방식 다) 발행주식총수의 100분의 20을 초과하지 않는 범위 내에서 제가호 외의 방법으로 불특정 다수인(이 회사의 주주를 포함한다)에게 신주인수의 청약을 할 기회를 부여하고 이에 따라 청약을 한 자에 대하여 신주를 배정하는 방식 2) 제1항 제다호의 방식으로 신주를 배정하는 경우에는 이사회의 결의로 다음 각 호의 어느 하나에 해당하는 방식으로 신주를 배정하여야 한다. 가) 신주인수의 청약을 할 기회를 부여하는 자의 유형을 분류하지 아니하고 불특정 다수의 청약자에게 신주를 배정하는 방식 나) 관계 법령에 따라 우리사주조합원에 대하여 신주를 배정하고 청약되지 아니한 주식까지 포함하여 불특정 다수인에게 신주인수의 청약을 할 기회를 부여하는 방식 다) 주주에 대하여 우선적으로 신주인수의 청약을 할 수 있는 기회를 부여하고 청약되지 아니한 주식이 있는 경우 이를 불특정 다수인에게 신주를 배정받을 기회를 부여하는 방식 라) 투자매매업자 또는 투자중개업자가 인수인 또는 주선인으로서 마련한 수요예측 등 관계 법규에서 정하는 합리적인 기준에 따라 특정한 유형의 자에게 신주인수의청약을 할 수 있는 기회를 부여하는 방식 3) 제1항 제나호 및 제다호에 따라 신주를 배정하는 경우 상법 제416조제1호, 제2호, 제2호의2, 제3호 및 제4호에서 정하는 사항을 그 납입기일의 2주 전까지 주주에게 통지하거나 공고하여야 한다. 다만, 자본시장과 금융투자업에 관한 법률 제165조의9에 따라 주요사항보고서를 금융위원회 및 거래소에 공시함으로써 그 통지 및 공고를 갈음할 수 있다. 5) 회사는 신주를 배정하는 경우 그 기일까지 신주인수의 청약을 하지 아니하거나 그 가액을 납입하지 아니한 주식이 발생하는 경우에 그 처리방법은 발행가액의 적정성등 관련 법령에서 정하는 바에 따라 이사회 결의로 정한다. 6) 회사는 신주를 배정하면서 발생하는 단주에 대한 처리방법은 이사회의 결의로 정한다. 제 10 조의 2 (동등배당) 회사는 배당 기준일 현재 발행(전환된 경우를 포함한다)된 동종 주식에 대하여 발행일에 관계 없이 모두 동등하게 배당한다.
1) 이 회사는 임·직원(상법 시행령 제30조에서 정하는 관계회사의 임·직원을 포함한다. 이하 이조에서 같다)에게 발행주식총수의 100분의 15의 범위 내에서 주식매수선택권을 주주총회의 특별결의에 의하여 부여할 수 있다. 다만 발행주식총수의 100분의 1의 범위내에서는 이사회의 결의로 회사의 이사를 제외한 자에 대하여 주식매수선택권을 부여할 수 있다. 이사회 결의로 주식매수선택권을 부여한 경우 회사는 부여 후 처음으로 소집되는 주주총회의 승인을 받아야 한다. 이 경우 주주총회 결의에 의해 부여하는 주식매수선택권은 경영성과목표 또는 시장지수 등에 연동하는 성과연동형으로 할 수 있다. 2) 주식매수선택권을 부여받을 자는 회사의 설립·경영·해외영업 또는 기술혁신 등에 기여하거나 기여할 수 있는 자로 한다. 3) 주식매수선택권의 행사로 교부할 주식(주식매수선택권의 행사가격과 실질가액과의 차액을 현금 또는 자기주식으로 교부하는 경우에는 그 차액의 산정기준이 되는 주식을 말한다)은 제7조의 주식 중 주식매수선택권을 부여하는 주주총회 결의로 정한다. 4) 주식매수선택권을 부여하는 임직원의 수는 재직하는 임직원의 100분의 90을 초과할 수 없고 임원 또는 직원 1인에 대하여 부여하는 주식매수선택권은 발행주식의 100분의 10을 초과할 수 없다. 5) 주식매수선택권을 행사할 주식의 1주당 행사가격은 다음 각호의 가액 이상이어야 한다. 주식매수선택권을 부여한 후 그 행사가격을 조정하는 경우에도 또한 같다. 1. 새로이 주식을 발행하여 교부하는 경우에는 다음 각 목의 가격중 높은 금액 가. 주식매수선택권의 부여일을 기준으로 한 주식의 실질가액 나. 당해 주식의 권면액. 2. 자기주식을 양도하는 경우에는 주식매수선택권 부여일을 기준으로 한 주식의 실질가액 6) 주식매수선택권은 제1항의 결의일로부터 2년이 경과한 날로부터 7년이내에 이를 행사할 수 있다. 7) 주식매수선택권을 부여받은 자는 제1항의 결의일로부터 2년이상 재임 또는 재직하여야 행사할 수 있다. 다만, 주식매수선택권을 부여받은 자가 제1항의 결의일부터 2년내에 사망하거나 기타 본인의 귀책사유가 아닌 사유로 퇴임 또는 퇴직한 경우에는 그 행사기간 동안 주식매수선택권을 행사할 수 있다. 가) 주식매수선택권을 부여받은 임직원이 본인의 의사에 따라 퇴임하거나 퇴직한 경우 나) 주식매수선택권을 부여받은 임직원이 고의 또는 중대한 과실로 회사에 중대한 손해를 입힌 경우 |
3. 의결권에 관한 사항
|
제 24 조 (주주의 의결권) 주주의 의결권은 1주마다 1개로 한다.
이 회사, 모회사 및 자회사 또는 자회사가 다른 회사의 발행주식 총수의 10분의 1을 초과하는 주식을 가지고 있는 경우 그 다른 회사가 가지고 있는 이 회사의 주식은 의결권이 없다.
1) 2이상의 의결권을 가지고 있는 주주가 의결권의 불통일 행사를 하고자 할 때에는 회일의 3일전에 회사에 대하여 서면으로 그 뜻과 이유를 통지하여야 한다. 2) 회사는 주주의 의결권의 불통일 행사를 거부할 수 있다. 그러나 주주가 주식의 신탁을 인수하였거나 기타 타인을 위하여 주식을 가지고 있는 경우에는 그러하지 아니하다.
1) 주주는 대리인으로 하여금, 그 의결권을 행사하게 할 수 있다. 2) 제1항의 대리인은 주주총회 개시전에 그 대리권을 증명하는 서면(위임장)을 제출하여야 한다.
1) 주주는 총회에 출석하지 아니하고 서면에 의하여 의결권을 행사할 수 있다. 2) 회사는 제1항의 경우 총회의 소집통지서를 주주의 의결권 행사에 필요한 서면과 참고자료를 첨부하여야 한다. 3) 서면에 의하여 의결권을 행사하고자 하는 주주는 제2항의 서면에 필요한 사항을 기재하여, 회일의 전일까지 회사에 제출하여야 한다. |
4. 배당에 관한 사항
|
제 45 조의 2 (분기배당) 1) 이 회사는 사업연도 개시일부터 3월, 6월 및 9월 말일부터 45일 이내의 이사회 결의로써 금전으로 자본시장과 금융투자업에 관한 법률 제165조의12에 의한 분기배당을 할 수 있다. 3) 분기배당은 직전결산기의 대차대조표상의 순자산액에서 다음 각호의 금액을 공제한 액을 한도로 한다. (1) 직전결산기의 자본금의 액 (2) 직전결산기까지 적립된 자본준비금과 이익준비금의 합계액 (3) 상법시행령에서 정하는 미실현이익 (4) 직전결산기의 정기주주총회에서 이익배당하기로 정한 금액 (5) 직전결산기까지 정관의 규정 또는 주주총회의 결의에 의하여 특정목적을 위해 적립한 임의준비금 (6) 분기배당에 따라 당해 결산기에 적립하여야 할 이익준비금 (7) 당해 영업년도 중에 분기배당이 있었던 경우 그 금액의 합계 제 46 조 (이익 배당) 1) 이익의 배당은 금전, 주식 및 기타의 재산으로 할 수 있다. 2) 제1항의 배당은 제12조에서 정한 날 현재의 주주명부에 기재된 주주 또는 등록된 질권자에게 지급한다. 제 47 조 (배당금 지급 청구권의 소멸 시효) 1) 배당금의 지급 청구권은 5년간 이를 행사하지 아니하면 소멸 시효가 완성한다. 2) 제1항의 시효의 완성으로 인한 배당금은 이 회사에 귀속한다. |
III. 투자위험요소
1. 사업위험
당사는 1960년 10월 17일 의약품의 제조 및 판매를 목적으로 설립되었습니다. 당사 가 영위하는 주요 사업으로는 의약품, 건강기능식품, 그 외 의약외품 등이 있으며 주요 제품으로는 훼로바, 레가론, 덱시드, 치옥타시드, 씬지로이드 등이 있습니다. 이와 별개로 당사는 당사의 Global open innovation 전략의 일환으로 해외 자회사 및 제휴 업체와 협력하여 파킨슨병 등 중추신경계(CNS) 질환 치료제, 면역항암제, 신경염증성 질환 치료제 개발을 진행하고 있습니다.
[당사 사업 분야]
| 사업부문 | 주요사업영역 | 주요제품 |
|---|---|---|
| 의약품 및 의약외품 | 완제 의약품 및 의약외품 제조업 및 판매업 |
훼로바, 레가론, 덱시드, 치옥타시드, 씬지로이드 타세놀, 액시마, 헥사메딘, 오르필, 딜라스틴 홀록산, 시린메드, 부광탁스, 안티프라그 등 |
| 연구개발 | 의약품 연구 및 개발사업 | CP-012 등 |
| [주요 용어해설] |
| 용어 | 내 용 |
|---|---|
| API |
원료의약품(Active Pharmaceutical Ingredient) 신약 및 제네릭 완제의약품을 제조하기 위한 원재의 총칭 |
| PI | 의약중간체(Pharmaceutical Intermediates), 의약중간체는 복잡한 화학 구조를 갖고 있는 합성 의약품의 주성분을 제조하는데 사용되는 핵심 물질을 뜻 함 |
| 제네릭 | 복제 합성의약품. 특허 만료된 합성의약품을 분석해 복제한 약물을 칭함 |
| CDMO | Contract Development and Manufacturing Organization 의약품 위탁개발 및 위탁생산을 말함 |
| CMC | Chemistry, Manufacturing and Controls, 공정개발 및 품질관리의 전반적인 사항 |
| ETC | Ethical the counter Drug(전문의약품) 의사의 처방이 필요한 의약품 |
| OTC | Over the counter Drug(일반의약품) 의사의 처방 없이 판매가 가능한 의약품 |
| DMF | 원료의약품 신고제도: Drug Master File |
| GMP | 품질이 고도화된 우수의약품을 제조하기 위한 여러 요건을 구체화한 것으로 원료의 입고에서부터 출고에 이르기까지 품질관리의 전반에 지켜야 할 규범(good manufacturing practice) |
| cGMP | 강화된 의약품 제조 및 품질관리기준. 미국 FDA(Food and Drug Administration)가 인정하는 의약품 품질관리 기준으로 국내에서는 '선진GMP'로도 부름 (current good manufacturing practice) |
| 뉴클레오시드 | (nucleoside)염기와 당이 N-클리코시드결합으로 결합된 화합물. 핵산을 구성하는 성분. 핵산은 핵단백질의 비단백 부분으로서 모든 생체 세포 속에 들어 있는 본질적인 성분. 글리코시드결합은 1개의 당분자와 또 다른 1개의 당분자의 탄소 사이 연결이 산소원자에 의해 연계되는 화학적 결합을 뜻함 |
|
올리고 뉴클레오타이드 |
뉴클레오티드 분자가 수 개 내지 십 수 개 결합하여 형성된 중합체. 중합체는 분자가 중합하여 생기는 화합물을 뜻 함 |
| 적응증 | 어떠한 약제나 수술 따위에 의하여 치료 효과가 기대되는 병이나 증상 |
| QA/QC | QA: 품질보증 /QC: 품질관리 |
| 고분자촉매 | 고성능 금속 촉매를 고분자에 고정화시키거나 콜로이드상으로 안정화시켜 사용하는 촉매. 고분자 촉매는 고분자 특유의 기능을 이용한 촉매인데, 높은 선택성(목적하는 화합물이 생성되는 비율)을 가지면서, 단독으로는 사용할 수 없었던 금속 촉매를 고분자와 함께 사용함으로써 사용을 가능하게 한 것 |
| GSK | GlaxoSmithkline, 영국계 다국적 제약회사의 이름 |
| 핵산 | (Nucleic Acid)모든 생물의 세포 속에 들어 있는 고분자 유기물의 한 종류. 유기물은 탄소를 포함하고 있는 물질을 뜻 함 |
| 단량체 | 고분자화합물 또는 화합체를 구성하는 단위가 되는 분자량이 작은 물질 |
| DNA | (deoxyribonucleic acid) 자연에 존재하는 2종류의 핵산 중에서 디옥시리보오스를 가지고 있는 핵산으로, 유전자의 본체를 이룸 |
| RNA | RNA는 핵산의 일종으로, 유전자 본체인 디옥시리보 핵산(DNA)이 가지고 있는 유전정보에 따라 필요한 단백질(protein)을 합성할 때 직접적으로 작용하는 고분자 화합물 |
| 안티센스 (Antisense) |
15~20개의 뉴클레오티드로 이루어진 인공적으로 만든 짧은 DNA |
| siRNA | (작은 간섭 리보핵산) 유전자의 단백질 정보를 갖고 있는 전령 리보핵산(messenger RNA; mRNA)에 염기서열을 특이적으로 결합한 다음, mRNA를 분해해 단백질을 만들지 못하게 하는 기능 |
| miRNA | 마이크로RNA(microRNA, miRNA)는 생물의 유전자 발현을 제어하는 역할을 하는 작은 RNA |
| Phosphoramidite | 뉴클레오티드 합성법의 일종 |
| KGMP | (Korea Good Manufacturing Practice) 한국 우수 의약품 제조기준 |
| KGLP | 비임상시험관리기준 |
| KGCP | 의약품임상시험 관리기준 |
| KDMF | (Korea Drug Master File)원료의약품신고 |
| SFDA | 중국 지방식품의약품 관리국 |
| Thymidine | 생물체 내에 존재하는 결정성 뉴클레오티드 |
| IND | 동물시험까지의 전 임상자료와 임상시험 계획서를 취합하여 임상시험 승인을 신청하는 절차. Investigational New Drug application의 약자 |
| EDQM | 유럽 의약품 품질 위원회. European Directorate for the Quality of Medicines & Healthcare의 약자 |
| PMDA | 일본 의약품의료기기종합기구. Pharmaceuticals and Medical Devices Agency의 약자 |
| SDMS | Scientific Data Management System의 약자, QA/QC, 실험실 정보의 database를 구축하여 실험실의 업무 효율화를 실현하고, 공정, 제품, 출하 등 관련 분야의 생산성 향상을 지원하며 나아가 과학적인 품질관리를 통해 대 고객 신뢰도 향상을 위한 품질 정보 시스템을 뜻함 |
| PCT | 특허협력조약 Patent Cooperation Treaty의 약자. 여러 나라에 동시에 특허 출원을 하는 것은 금전적, 시간적 부담이 큰 경우가 많음을 고려하여 체결한 국제 조약. PCT출원으로 모든 회원국에 특허를 획득할 수 있는 것은 아니나, 출원 단계에서의 편의를 위하여 PCT국제 출원을 하면 모든 회원국에 동시에 출원한 것과 같은 효과를 일단 부여하고 추후에는 실제로 출원할 국가에 대하여만 국내 절차를 밟을 수 있음 |
| Validation | 공정, 시설 또는 시스템이 의도한 대로 적절히 기능하고 있는지를 확인하기 위하여 이들을 체계적으로 조사·검토하여 문서화하는 것이며, "validation되었다" 라는 것은 품질규격에 적합한 제품이 일관되게 제조된다는 것이 증명되어 정식으로승인된 것을 말함. |
| 중추신경계 (CNS) |
두개골에 싸여있는 뇌와 척수를 포함하는 신경계로 말초신경계와 함께 동물의 행동이나 신체 기작을 제어 |
| CSO (Contract Sales Organization) |
의약영업품 판촉업자(CSO, Contract Sales Organization)는 제약사의 매출에 핵심적인 역할 수행. CSO는 제약에 대한 풍부한 지식과 의료기관과의 장기간 관계형성을 바탕으로 제약사를 대신하여 신약을 판매 |
| 유효물질 (hit compound) |
기존의 존재하는 분자들을 대상으로 약물의 효과를 확인하는 스크리닝 실험을 하고 해당 실험에서 기준치 이상의 유효성을 보여준 물질 |
| 선도물질 (lead compund) |
약물 발견에서 치료에 유용할 수 있는 약리학적 또는 생물학적 활성을 갖고 있지만 그럼에도 불구하고 표적에 더 잘 맞도록 변형이 필요한 차선 구조를 가질 수 있는 화합물 |
| 임상시험 허가신청 (Investigational New Drug Application) |
임상시험계획 승인신청(Investigational New Drug Application, 이하 IND)란 사람을 대상으로 특정 의약품을 사용해 임상시험을 할 수 있도록 허가 당국으로부터 공식적인 심사와 승인을 밟는 절차. 한국은 「의약품 임상시험 계획 승인에 관한 규정」에 근거해 식품의약품안전처에서 IND를 주관. 미국은 FDA에서 Investigational New Drug Application, 유럽은 EMA에서 Clinical Trial Application(CTA)라는 이름으로 유사한 제도를 운영 |
| 시판후안정성조사 (PMS : Post-Market Surveillance) |
약사법 및 식약청에서 정한 ‘신약 등의 재심사기준’에 따라 신약 시판 후 4~6년 동안 6백~3천례의 환자에 대해 병원 등에 조사를 의뢰해 자료를 수집, 해당 의약품에 대한 사용경험을 의무적으로 식품의약품안전청에 보고토록 하는 제도. 신약의 상품화 이후 불특정 다수의 환자들을 대상으로 한 광범위한 사용 경험을 통해 얻은 부작용 또는 새로운 효능 등의 자료를 체계적으로 수집·평가해 신약 개발과정에서 발견하지 못한 안전성과 유효성을 확인, 검토를 진행 |
| 아릴 탄화수소수용체(AhR) 길항제 | 아릴탄화수소수용체(Aryl Hydrocarbon Receptor)를 저해하는 약물로, 면역 반응을 활성화시켜 암세포를 공격. kynurenine을 포함한 다양한 리간드와 AhR의 상호작용을 억제하며, 선천과 후천성 면역반응을 모두 조절 |
| CDA (Confidential Disclosure Agreement) |
비밀유지계약(Confidential Disclosure Agreement)을 뜻하며, 연구나 비즈니스를 진행할 때 체결 |
| MTA (Material Transfer Agreement) |
Material Transfer Agreement(물질이전계약서, MTA)는 특정 biological, chemical material을 한 기관에서 다른 기관으로 연구목적으로 송부하는 경우 상호 권리와 의무에 대해 합의하고자 기재. 또는, 라이센싱 계약과 결부 또는 후속하여 진행되기도 함 |
| FDA | Food and Drug Administration, 식품의약국. 미국 식품의약국은 식품이나 의약품, 화장품, 동물약, 장난감 등 소비자가 평소 생활에서 접하는 제품에 대해 그 허가나 위반품 단속을 전문적으로 담당하는 미국의 국가행정조직 |
| EMA | 유럽 의약품 기관 (European Medicines Agency, EMA) 는 의약품의 평가 및 감독을 담당하는 유럽 연합(EU)의 기관. 인간과 수의학적 용도의 의약품에 대한 평가 및 감독을 통해 대중과 동물 건강을 보호하고 증진하는 역할을 함 |
| 마일스톤 | '단계별 기술료’라는 의미의 마일스톤은 국내 제약바이오기업들의 신약 라이선스 계약 시 사용하고 있는 방식. 성공 단계별(전임상 -> 임상 -> 제품화 등)로 대가를 보장하는 것. 기술 수출(라이선스 아웃)을 할때 계약금 외에 개발단계로 발생하는 수수료를 의미 |
| ADME | Absorption(흡수), Distribution(분포), Metabolism(대사), Excretion(배설)의 약어로, 약물이 체내에 투여된 후 여러 주변 조건과 시간의 흐름에 따라 체내에서 이동하며 일어나는 동태를 의미 |
| RMAT | RMAT(Regenerative Medicine Advanced Therapy)는 식품의약국(FDA)이 심각하거나 생명을 위협하는 질환 치료를 위한 약물 후보에 부여하는 지정.RMAT로 지정되면 의학적 미충족 수요를 해결할 수 있는 재생치료제의 개발을 가속화가 목적. 이를 통해 대체 또는 중간 종료 지점을 기반으로 가속 승인을 허용 및 허가 심의 기간을 단축 |
이 외에 추가적으로 당사 주요 사업 관련 용어해설은 하기와 같습니다.
| 용어 | 설명 |
|---|---|
| 신약 (Original) |
화학구조나 본질 조성이 새로운 신물질 또는 신물질을 유효성분으로 함유한 복합제제 의약품 |
| 개량신약 (Super Generic) |
이미 허가(신고)된 의약품에 비해 개량되었거나 의약 기술에 있어 진보성이 있는 의약품 |
| 복제약 (Generic) |
특허만료된 신약(오리지널)을 단순 복제한 의약품 |
| 전문의약품 (ETC: Ethical Drug) |
전문의약품은 적응증, 습관성, 내성, 투여경로의 특성상 의사나 치과의사의 전문적인 진단이 필요한 의약품으로 주사제, 혈압약, 간질약, 항생제 등이 있음 |
| 일반의약품 (OTC: Over-the-counter Drug) |
일반의약품은 오·남용 우려가 적어 의사나 치과의사의 처방없이 사용하여도 부작용이 비교적 작은 의약품으로 일반적인 감기약, 소화제, 비타민제 등이 있음 |
| 리베이트 (Rebate) |
사전적으로 판매자가 구매자로부터 지불 받은 액수의 일부분을 구매자에게 환불하는 행위 및 그 금액을 의미하며, 판매 촉진을 위한 가격할인 전략 |
| GMP (Good Manufacturing Practice) |
의약품의 안정성과 유효성을 품질면에서 보증하는 기본조건으로서의 우수의약품의 제조·품질관리의 기준 |
| 바이오시밀러 (Biosimilar) |
특허가 만료된 오리지널 바이오의약품(biomedicine)을 복제해 동등한 품질로 만든 의약품 |
| 바이오베터 (Biobetter) |
바이오 신약의 효능이나 투여 횟수를 개선한 바이오 의약품으로, 기존 바이오 의약품보다 더 낫다(better)는 의미로 바이오베터라고 불림 |
| 신약 라이선스 계약 (Licensing) |
단일 회사가 신약개발의 전 과정을 수행하는 것이 아니라, 임상 단계별로 역할을 분담해 신약개발의 리스크(risk, 위험도)를 줄이면서도 빠르게 상업화 할 수 있도록 신약 후보물질의 권리 (기술·물질·제품·특허) 등을 도입 또는 이전하는 계약 |
| 라이선스 인 (In-Licensing) |
타사가 보유한 경쟁력 있는 기술·물질·제품·특허 등의 권리를 자사로 들여오는 것 |
| 라이선스 아웃 (Out-Licensing) |
자사가 보유한 기술·물질·제품·특허·노하우 등의 권리를 타사에 허여하는 것 |
| 플랫폼 기술 (Platform Technology) |
기존 의약품에 적용하여 다수의 후보 물질을 도출할 수 있는 기반기술을 의미. 플랫폼 기술은 다양한 질환 분야로 적용할 수 있으며, 끊임없는 기술적 진화와 파급효과를 통해 높은 부가가치를 지닌 수익모델을 확보할 수 있음 |
| 전임상 시험 (Pre-Clinical) |
전임상(비임상) 시험은 새로 개발한 신약후보물질을 사람에게 사용하기 전 동물에게 사용하여 부작용이나 독성, 효과 등을 알아보는 시험임 |
| 임상1상 시험 (Clinical Test - Phase I) |
건강한 사람 20~80명을 대상으로 약물을 안전하게 투여할 수 있는 용량과 인체 내 약물 흡수 정도 등을 평가. 앞서 수행된 전임상 단계에서 독성 시험 등 전임상 시험 결과가 유효한 경우, 시험약을 최초로 사람에 적용하는 단계 |
| 임상2상 시험 (Clinical Test - Phase II) |
100~200명의 소규모 환자들을 대상으로 약물의 약효와 부작용을 평가하고, 유효성을 검증. 단기투약에 따른 흔한 부작용, 약물동태 및 예상 적응증에 대한 효능 효과에 대한 탐색을 위해 실시하는 것으로 대상질환 중 조건에 부합되는 환자를 대상으로 함. 임상3상 시험에 돌입하기 위한 최적용법 용량을 결정하는 단계 |
| 임상3상 시험 (Clinical Test - Phase III) |
신약의 유효성이 어느 정도 확립된 후에 대규모(최소 수백 명에서 수천 명) 환자들을 대상으로 장기 투여시의 안정성 등을 검토하고 확고한 증거를 수집하기 위해 실시. 신약의 유효성이 어느 정도까지 확립된 후에 행해지며 시판허가를 얻기 위한 마지막 단계의 임상시험으로서 비교대조군과 시험처치군을 동시에 설정하여 효능, 효과, 용법, 용량, 사용상의 주의사항 등을 결정. 3상이 성공적으로 끝나면 판매가 가능함 |
| 임상4상 시험 (Clinical Test - Phase IV) |
신약이 시판 사용된 후 장기간의 효능과 안전성에 관한 사항을 평가하기 위한 시험으로, 시판전 제한적인 임상시험에서 파악할 수 없었던 부작용이나 예상하지 못하였던 새로운 적응증을 발견하기 위한 약물역학적인 연구 |
| Regenerative Medicine Advanced Therapy |
FDA가 21세기 치유법에 따라 재생의학 분야 치료제 개발 및 승인을 가속화하기 위해 마련한 특별 지정제도 |
| JPND (Joint Programme Neurodegenerative Disease Research) |
EU에서 신경퇴행성 질환에 대한 치료법을 찾고 조기에 표적 치료를 위한 조기 진단 연구를 목적으로 한 특별 연구계획 |
| 가. 국내외 경기변동에 따른 위험 당사가 영위하고 있는 완제의약품 제조 및 판매업은 최종 소비재 성격을 보이기에 글로벌 경기 동향 및 국내 경제 동향에 직접적인 영향을 받고 있습니다. 주요 기관의 2024년까지의 경제전망에 따르면, 글로벌 경기국면은 코로나19 이후 인플레이션을 거쳐 점차적으로 경기가 회복되고 있는 상황이지만, 이와 동시에 경기 불확실성도 여전히 높게 유지되고 있는 상황입니다. 이러한 거시경제적 요인은 당사가 영위하는 제약 산업 및 전/후방 산업에 영향을 미치며, 글로벌 경기의 경로를 정확히 예측하는 것은 불가능합니다. 경기의 변동성은 당사의 영업실적 및 재무상태에 부정적인 영향을 미칠 수 있으니 투자자께서는 글로벌 경기변동에 대한 상황을 지속적으로 모니터링하시기 바랍니다. |
당사가 영위하고 있는 완제의약품 제조 및 판매업은 최종 소비재 성격을 보이기에 글로벌 경기 동향 및 국내 경제 동향에 직접적인 영향을 받고 있습니다.
(1) 글로벌 경기 동향
국제통화기금(IMF)은 2025년 4월 22일 4월 세계경제전망(World Economic Outlook) 보고서를 발표하였으며, 이번 전망보고서에서는 최근 높은 정책 불확실성을 감안하여 전망 기준일에 따른 기준 전망(reference forecast)과 보완 전망(alternatives)을 함께 제시하였습니다. 기준 전망에서 2025년 4월 4일 기준 반영 가능한 정보를 기반으로 국가별 성장률을 전망하되, 보완 전망을 통해 4월 2일 상호관세 부과 이전 및 4월 9일 상호관세 유예 이후 기준 전망으로 세계 성장률 범위를 추가로 제시하였습니다. 다만, 보완 전망은 지역, 국가별 전망에 대해서는 공개하지 않았습니다.
4월 4일을 기준으로 한 기준 전망에서는 무역긴장 등 글로벌 불확실성을 반영하여 대부분 국가의 성장률 전망을 하향하면서 2025년 세계경제 성장률을 지난 1월 전망 대비 0.5%p. 하향조정한 2.8%로 전망하였습니다.
보완전망에서 4월 2일 상호관세 부과 이전 기준으로는 미국의 2~3월 무역정책, 높은 유가 전망으로 중국, 캐나다, 멕시코의 성장률이 대폭 둔화됨에 따라 2025년 세계경제 성장률을 1월 전망 대비 0.1%p. 하향 조정한 3.2%로 전망하였습니다. 한편, 4월 9일 이후 기준으로는 2025년 상호관세 90일 유예의 효과가 미국과 중국의 성장률 하락으로 상쇄되어 세계경제성장률 2.8%를 전망하였고, 2026년에는 미국과 중국의 손실이 다른 국가의 이득을 넘어섬에 따라 2.9%의 성장률을 전망하였습니다.
| [세계경제성장률 전망] |
| (단위 : %, %p.) |
| 구분 | 2025년 세계 경제 성장률 | 2026년 세계 경제 성장률 |
|---|---|---|
| 2025년 1월 전망 | 3.3% | 3.3% |
| 기준전망(4.4 기준) | 2.8%(-0.5%p.) | 3.0%(-0.3%p.) |
| 보완전망(4.2 이전 기준) | 3.2%(-0.1%p.) | 3.2%(-0.1%p.) |
| 보완전망(4.9 이후 기준) | 2.8%(-0.5%p.) | 2.9%(-0.4%p.) |
| 출처 : IMF World Economic Outlook(세계경제전망)(2025.04) 주) 기준전망 및 보완전망 괄호 내 수치는 2025년 1월 전망치 대비 변동 수치입니다. |
한편, 국가별, 지역별 성장률은 기준전망만 제시하였으며, 선진국 그룹의 2025년 성장률은 지난 1월 전망 대비 0.5%p. 하향 조정된 1.4%로 전망하였습니다. 미국은 정책 불확실성, 무역 긴장, 소비 회복 지연 등으로 성장률 전망치가 대폭 하락 조정되었고, 대부분의 유럽국가와 일본도 하향 조정되었습니다. 한국 성장률의 경우 2025년 1월 전망 대비 1.0%p. 하향 조정된 1.0%로 전망되었습니다.
신흥개도국 그룹의 경우 2025년 성장률은 1월 전망 대비 0.5%p. 하향 조정된 3.7%로 전망되었으며, 특히 중국은 예상보다 견조한 2024년 4분기 실적 및 재정확대에도 불구하고 관세 조치의 부정적 영향으로 2025년 및 2026년 성장률 전망치가 모두 하향 조정되었으며, 멕시코는 2024년말 이후 부진한 경제활동과 더불어 미국의 관세 부과, 지정학적 리스크 및 긴축적 금융환경 등의 영향으로 2025년 성장률이 1월 전망 대비 대폭 하향조정 되었습니다.
국제통화기금(IMF)은 세계경제의 리스크가 하방 요인에 집중되어 있다고 진단하면서, 무역갈등 등 정책 불확실성 확대에 따른 소비·투자 위축, 고금리 및 높은 부채수준으로 인한 재정·통화 정책 여력 부족, 주가 및 시장가격 재조정 가능성 등 금융·외환시장의 높은 변동성 등을 위험 요인으로 제시하였습니다. 다만, 미국 관세 조치 인하와 상호 협상 등이 진전될 경우 세계경제의 상방 조정 요인으로 작용할 수 있다고 언급하였습니다.
국제통화기금(IMF)은 고조된 불확실성과 성장 둔화에 대응하기 위해 예측가능한 무역환경 조성의 필요성을 강조하며 무분별한 산업 보조금을 지양하고 지역, 다자간 무역협정 확대를 통한 무역 분절화 방지 노력이 필요하다고 강조하였습니다. 또한 금융시장 안정과 기대 인플레이션간의 균형을 유지하는 신중한 통화정책과 건전한 재정 운용의 필요성을 언급하고, 자본 변동성 확대에 대응하여 국가별 금융, 외환시장 성숙도에 맞는 적절한 개입 및 건전성 조치를 시행할 것을 권고하였습니다. 그 밖에 중기 성장잠재력 회복을 위한 여성·고령층 노동 참여 제고와 AI, 디지털 기술 투자확대, 규제 정비 등의 노력도 촉구하였습니다.
| [IMF 세계 경제성장 전망] | |
| (단위 : %, %p.) | |
| 구분 | 2024년 | 2025년 | 2026년 | ||||
|---|---|---|---|---|---|---|---|
| 25.01월 (A) |
25.04월 (B) |
조정폭 (B-A) |
25.01월 (C) |
25.04월 (D) |
조정폭 (D-C) |
||
| 세계 | 3.3 | 3.3 | 2.8 | -0.5 | 3.3 | 3.0 | -0.3 |
| 선진국 | 1.8 | 1.9 | 1.4 | -0.5 | 1.8 | 1.5 | -0.3 |
| 미국 | 2.8 | 2.7 | 1.8 | -0.9 | 2.1 | 1.7 | -0.4 |
| 유로존 | 0.8 | 1.0 | 0.8 | -0.2 | 1.4 | 1.2 | -0.2 |
| 독일 | -0.2 | 0.3 | 0.0 | -0.3 | 1.1 | 0.9 | -0.2 |
| 프랑스 | 1.1 | 0.8 | 0.6 | -0.2 | 1.1 | 1.0 | -0.1 |
| 이탈리아 | 0.7 | 0.7 | 0.4 | -0.3 | 0.9 | 0.8 | -0.1 |
| 스페인 | 3.2 | 2.3 | 2.5 | +0.2 | 1.8 | 1.8 | 0.0 |
| 일본 | 0.1 | 1.1 | 0.6 | -0.5 | 0.8 | 0.6 | -0.2 |
| 영국 | 1.1 | 1.6 | 1.1 | -0.5 | 1.5 | 1.4 | -0.1 |
| 캐나다 | 1.5 | 2.0 | 1.4 | -0.6 | 2.0 | 1.6 | -0.4 |
| 한국 | 2.0 | 2.0 | 1.0 | -1.0 | 2.1 | 1.4 | -0.7 |
| 호주 | 1.0 | 2.1 | 1.6 | -0.5 | 2.2 | 1.4 | -0.8 |
| 기타선진국 | 2.2 | 2.1 | 1.8 | -0.3 | 2.3 | 2.0 | -0.3 |
| 신흥개도국 | 4.3 | 4.2 | 3.7 | -0.5 | 4.3 | 3.9 | -0.4 |
| 중국 | 5.0 | 4.6 | 4.0 | -0.6 | 4.5 | 4.0 | -0.5 |
| 멕시코 | 1.5 | 1.4 | -0.3 | -1.7 | 2.0 | 1.4 | -0.6 |
| 출처 : IMF World Economic Outlook(세계경제전망)(2025.04) |
(2) 국내 경기 동향
한국은행이 2025년 02월 발표한 경제전망보고서에 따르면 2025년의 국내 경제 성장률은 내수가 부진한 가운데 수출증가세가 둔화됨에 따라 2024년 11월 전망 대비 0.4%p. 하향 조정된 1.5%로 전망됩니다. 2025년 1분기 중에는 미 관세정책 등 정치 불확실성에 따른 심리 위축, 기후 요인 등의 영향으로 성장이 위축될 전망이며, 2025년 2분기 이후에는 정치 불확실성이 점차 해소되는 가운데 금융여건 완화의 영향도 나타나며 내수는 회복세를 보일 것으로 전망하였습니다. 다만, 수출은 통상환경 악화로 하방압력이 증대될 것으로 전망하였습니다. 2026년의 경우, 통상환경을 둘러싼 불확실성이 존재하나 내수 중심의 회복세를 보이며 성장률 1.8%를 전망하였으며, 이는 2024년 11월 전망과 동일한 수준입니다.
| [한국은행 국내 경제성장 전망] |
| (단위: %) |
| 구분 | 2023년 | 2024년 | 2025년(E) | 2026년(E) | ||||
|---|---|---|---|---|---|---|---|---|
| 상반 | 하반 | 연간 | 상반 | 하반 | 연간 | 연간 | ||
| GDP | 1.4 | 2.8 | 1.3 | 2.0 | 0.8 | 2.2 | 1.5 | 1.8 |
| 민간소비 | 1.8 | 1.0 | 1.3 | 1.1 | 1.0 | 1.7 | 1.4 | 1.8 |
| 건설투자 | 1.5 | 0.4 | -5.5 | -2.7 | -6.7 | 1.1 | -2.8 | 2.5 |
| 설비투자 | 1.1 | -1.8 | 5.3 | 1.8 | 5.7 | -0.2 | 2.6 | 2.0 |
| 지식재산생산물투자 | 1.7 | 1.5 | -0.1 | 0.7 | 2.5 | 4.9 | 3.7 | 3.1 |
| 재화수출 | 2.9 | 8.4 | 4.3 | 6.3 | 0.7 | 1.2 | 0.9 | 0.8 |
| 재화수입 | -0.3 | -1.3 | 3.6 | 1.2 | 2.0 | 0.2 | 1.1 | 1.9 |
| 출처 : 한국은행 경제전망보고서(2025.02) 주) 전년동기대비 성장률 |
부문별로 살펴보면, 민간소비는 심리 위축 등으로 부진한 흐름을 보이고 있으나, 2025년 2분기 이후 정치 불확실성이 줄어들고 금융여건 완화의 영향이 나타나며 점차 회복될 전망입니다. 건설투자는 그간의 수주, 착공 위축 영향으로 작년에 이어 올해도 부진할 전망이며, 설비투자는 2025년 중 반도체장비 투자를 중심으로 완만한 성장세를 나타낼 전망입니다.
지식재산생산물투자는 기술경쟁력 강화를 위한 주요 기업의 연구개발 지속과 정부 연구개발 예산 확대에 힘입어 증가율이 높아질 전망이며, 실질 GDP 기준 재화수출은 예상보다 빠른 미국 통상압력 움직임 등을 감안하면 증가세가 2024년 11월 전망치인 1.5% 대비 0.6%p. 둔화될 것으로 전망하였습니다. 재화수입 또한 내수회복 지연과 수출 증가세 둔화로 2025년 및 2026년 증가율이 2024년 11월 전망치 1.9% 대비 0.8%p. 둔화된 1.1%를 기록할 것으로 전망하였습니다.
정부는 악화된 실물 및 금융 경제를 부양하기 위하여 다양한 통화정책 및 재정정책을내면서, 경제가 안정화되도록 지속적으로 노력하고 있습니다. 하지만 정부의 지속적인 경기 부양 정책에도 불구하고 경기가 악화될 가능성은 존재합니다. 당사가 영위하는 제약사업은 경기회복에 대한 불확실성이 높은 경우에는 소비 감소로 인하여 당사 가 영위하는 일반의약품 매출 감소로 이어질 수 있으며 원재료, 환율 등 수익성에 영향을 미칠 수 있는 지표의 불확실성이 확대되어 장기적으로는 당사의 사업에도 부정적인 영향을 미칠 수 있습니다. 상기 내용을 포함한 국내외의 다양한 요인들로 인해 국내외 경기 회복이 둔화되거나 불확실성의 영향이 커질 경우 당사 및 당사의 주요 자회사의 수익성에 부정적인 영향을 줄 수 있으므로 투자자께서는 이점 유의하시기 바랍니다.
| 나. 전반적인 제약산업 성장성 둔화 위험 당사가 영위하고 있는 제약산업의 수요 시장은 인구통계학적인 특성에 큰 영향을 받으며, 인구고령화 및 만성질환 증가에 따라 시장 규모가 꾸준히 커지는 특성이 있습니다. 인구구조의 고령화가 심화됨에 따라 건강 유지 및 제약산업에 대한 소비자의 관심과 수요가 커지고 있으며, 이에 따라 국내 의약품 시장규모는 2000년 이후로 계속 증가하고 있으며, 한국제약바이오협회 자료에 따르면 2009년 18조 2,187억원에서 2023년 31조 4,513억원으로 증가하는 모습을 보이며 꾸준한 성장세를 보이고 있습니다.한국이 고령사회로 진입하면서 지속적인 노인인구 증가, 소득증가, 건강에 대한 관심증가 등의 이유로 진료 비용과 의약품 비용을 포함한 의료비용이 증가하고, 이에 따라 국내 제약산업의 매출도 함께 안정적인 성장을 지속 할 것으로 전망됩니다.국내 제약산업은 신약개발을 위한 높은 수준의 R&D 투자, 생산 및 품질관리 경쟁력 확보를 바탕으로 한 이머징마켓 진출, 높은 치료율과 낮은 부작용을 보이는 바이오의약품 개발 등 다양한 노력을 기울이고 있습니다. 그러나 이러한 국내 제약산업 전반의 노력에도 불구하고 전체 제약산업이 위축되거나 시장성장률이 둔화되는 경우, 당사의 매출 또한 크게 저하될 수 있으며, 이는 당사의 사업, 영업성과 및 재무상태에 부정적인 영향을 미칠 가능성이 존재하오니 투자자께서는 이 점 유의하시기 바랍니다. |
의약품의 정의는 「약사법」 제2조4호에 따라 사람이나 동물의 질병을 진단, 치료, 경감, 처치 예방 등의 목적으로 사용하는 대한민국약전에 실린 물품으로 의약외품이 아닌 것을 말하며, 제약산업은 의약품을 연구개발ㆍ제조ㆍ가공ㆍ보관 및 유통하는 것과 관련된 산업을 의미합니다.
제약산업은 인간의 생명과 보건에 관련한 고부가가치 산업이자 지식기반 산업으로 원료 및 완제 의약품의 생산과 판매에서부터 신약개발을 위한 연구 등 모든 과정을 포괄하는 첨단 부가가치 산업입니다. 타 업종에 비해 기술 집약도가 높은 편이며 고도의 전문성과 함께 긴 투자기간과 높은 위험을 수반하지만, 글로벌 블록버스터급 신약 개발에 성공할 경우 막대한 고부가가치 창출이 가능하므로 미래 성장산업으로 분류되고 있습니다.
당사가 영위하고 있는 제약산업은 국민 건강 및 질병 치료에 필수적이라는 산업 특성상 경기 순환에 따른 민감도가 높지 않은 산업군입니다. 또한, 제약산업의 수요 시장은 인구통계학적인 특성에 큰 영향을 받으며, 인구고령화 및 만성질환 증가에 따라 시장 규모가 꾸준히 커지는 특성이 있습니다. 인구구조의 고령화가 심화됨에 따라 건강 유지 및 제약산업에 대한 소비자의 관심과 수요가 커지고 있으며, 이에 따라 국내 의약품 시장규모는 2000년 이후로 계속 증가하고 있으며, 한국제약바이오협회 자료에 따르면 2009년 18조 2,187억원에서 2023년 31조 4,513억원으로 증가하는 모습을 보이며 꾸준한 성장세를 보이고 있습니다.
| [국내 의약품 시장현황 2009년~2023년] |
| (단위: 억원, %) |
| 연도 | 생산 | 수출 | 수입 | 무역수지 | 시장규모 | 수입 점유율 |
시장 증가율 |
|---|---|---|---|---|---|---|---|
| 2009 | 147,866 | 17,872 | 52,193 | (34,321) | 182,187 | 28.6 | 6.0 |
| 2010 | 157,098 | 17,810 | 54,184 | (36,374) | 193,472 | 28.0 | 6.2 |
| 2011 | 155,968 | 19,585 | 55,263 | (35,678) | 191,646 | 28.0 | (0.9) |
| 2012 | 157,140 | 23,409 | 58,535 | (35,126) | 192,266 | 30.4 | 0.3 |
| 2013 | 163,761 | 23,306 | 52,789 | (29,483) | 193,244 | 27.3 | 0.5 |
| 2014 | 164,194 | 25,442 | 54,952 | (29,510) | 193,704 | 28.4 | 0.2 |
| 2015 | 169,696 | 33,348 | 56,016 | (22,668) | 192,364 | 29.1 | (0.7) |
| 2016 | 188,061 | 36,209 | 65,404 | (29,195) | 217,256 | 30.1 | 12.9 |
| 2017 | 203,580 | 46,025 | 63,077 | (17,052) | 220,632 | 28.6 | 1.6 |
| 2018 | 221,054 | 51,431 | 71,552 | (20,121) | 231,175 | 30.9 | 4.8 |
| 2019 | 223,132 | 60,581 | 80,549 | (19,968) | 243,100 | 33.1 | 5.2 |
| 2020 | 245,662 | 99,648 | 85,708 | 13,940 | 231,722 | 37.0 | (4.7) |
| 2021 | 254,906 | 113,642 | 112,668 | 974 | 253,932 | 44.4 | 9.6 |
| 2022 | 289,503 | 104,561 | 113,6353 | (9,092) | 298,595 | 38.1 | 17.6 |
| 2023 | 306,303 | 98,851 | 107,061 | (8,210) | 314,513 | 34.0 | 5.3 |
| 주1) 의약품 : 의약품(완제의약품, 마약류, 의료용고압가스 포함)+원료의약품(한약재 포함) |
| 주2) 시장규모 : 생산 - 수출 + 수입 |
| 주3) 수입점유율 : 수입액 / 시장규모 * 100 |
| 주4) 2023년 수출입은 한국은행 원/달러 연평균환율(종가)을 적용해 원화로 환산한 금액임 |
| 출처: 한국제약바이오협회 (2024 제약산업바이오산업DATA BOOK, 2024.12) |
또한 제약산업은 인구변화와 밀접한 관련을 가지고 있습니다. 국내 인구구조는 특히 양적인 팽창속도가 둔화된 가운데 질적인 변화를 보이고 있습니다. 2024년 65세 이상 고령인구는 우리나라 전체 인구의 19.2%인 993만 8천명입니다. 고령인구 비중은 계속 증가하여 2025년에는 20.3%로 초고령 사회로 진입할 것으로 예상됩니다.(전체 인구 중 65세 이상 인구 비중이 14%를 넘으면 '고령사회'로 분류, 20%를 넘으면 초고령사회로 구분) 나아가 2035년에는 29.9%, 2050년에는 40.1%를 넘어설 것으로 전망됩니다. 이처럼 국내 인구 구조가 고령 사회에 진입하는 등 고령화 진행 속도가 빠른 점을 고려할 때, 향후 노인 인구 및 만성 질환자의 증가에 따라 국내 제약 산업의 수요 기반은 견고할 것으로 전망됩니다.
| [65세 이상 인구 추이] | |
| [단위 : 천명] | |
| 구 분 | 2010 | 2020 | 2024 | 2025(E) | 2030(E) | 2035(E) | 2040(E) | 2050(E) | 2060(E) | 2072(E) |
|---|---|---|---|---|---|---|---|---|---|---|
| 총 인구 | 49,554 | 51,836 | 51,751 | 51,685 | 51,306 | 50,825 | 50,059 | 47,107 | 42,302 | 36,222 |
| 65세 이상 | 5,366 | 8,152 | 9,938 | 10,514 | 12,980 | 15,208 | 17,151 | 18,908 | 18,682 | 17,271 |
| 구성비 | 10.8% | 15.7% | 19.2% | 20.3% | 25.3% | 29.9% | 34.3% | 40.1% | 44.2% | 47.7% |
| 주) 구성비 = 고령인구(65세 이상) / 총 인구 X 100 |
| (자료 : 통계청 ( 2024 고령자 통계, 2024.09) |
한국이 고령사회로 진입하면서 지속적인 노인인구 증가, 소득증가, 건강에 대한 관심증가 등의 이유로 진료 비용과 의약품 비용을 포함한 의료비용이 증가하고, 이에 따라 국내 제약산업의 매출도 함께 안정적인 성장을 지속 할 것으로 전망됩니다.
2024년 발표된 건강보험심사평가원 자료에 따르면 2023년 상반기 65세 이상 요양급여비용은 23조 6,764억원으로 전년 반기 대비 19.50% 증가하였습니다. 연간 기준으로는 2019년 34조 9,294억원 수준에서부터 2022년 44조 6,406억원에 이르기까지 증가 양상을 보이고 있으며, 이러한 추세는 고령인구 비중 증가에 따라 향후에도 유지될 것으로 분석되고 있습니다. 지속적인 인구구조의 변화와 의료기술의 발전에 따른 의료이용 증가로 제약산업의 수요기반 역시 안정적인 성장을 지속할 것으로 예상됩니다.
| [노인(65세 이상) 요양급여비용] | ||
|
||
|
특히 약품비를 포함한 국내 의료비 지출은 노인인구 급증과 만성질환 증가 추세가 견고한 성장기반으로 작용하며 꾸준한 증가세를 나타내고 있으며 향후에도 견고한 확대 추세를 이어갈 것으로 예상되고 있습니다. 건강보험심사평가원 진료비 통계지표에 따르면 건강보험 요양급여비용이 2019년부터 2022년까지 꾸준히 증가하는 모습입니다. 2023년 상반기 기준 요양급여비용은 54조 8,836억원으로 전년동기 대비 4.89% 증가하였습니다.
| [건강보험 요양급여비용] | ||
|
|
| (자료 : 건강보험심사평가원, 2023년 상반기 진료비통계지표(2024.01.25)) |
이처럼 고령화 진행속도가 빠른 점, 65세 이상 인구수와 그 진료비가 매년 증가하는 점 등을 고려했을 때, 향후에도 노인인구 및 만성질환자 증가에 따른 의약품의 근원 수요는 견고한 확대 추세를 지속할 것으로 전망됩니다.
그러나 제약산업에 대한 부정적인 환경요인 또한 존재하는 것을 간과할 수 없습니다. 전통적으로 제약산업은 산업정책과 건강보험정책이 상충되는 영역이며, 가치 판단 기준에 따라 '규제'와 '육성 지원'이 중첩된 영역이기 때문입니다. 우리나라 역시 제약산업은 미래성장을 견인할 신성장산업으로서 육성 필요성이 절실한 산업임과 동시에 국민건강증진과 국가보건의료체계의 지속성 확보 차원에서 보험약가규제를 비롯한 정부의 각종 규제가 불가피한 분야로 인식되고 있습니다.
현재 국내 제약산업은 노령인구의 지속적인 증가 및 소득수준의 향상에 힘입어 2000년대 이래로 연평균 10% 내외의 꾸준한 성장을 이루어왔으나, 2010년에 시행된 의약품 리베이트 규제, 2012년 약가인하정책 등 정부의 약가인하 정책시행 의지가 견고함에 따라 산업전체의 성장성이 둔화되었습니다.
다만 COVID-19 기간 동안 관련 처방의약품에 대한 수요가 급격하게 증가됨에 따라 2021년 및 2022년 전망 수준 역시 과거 7개년 수준보다 급격하게 증가하였으며, Evaluate Pharma에 따르면 이러한 성장 기조는 2027년까지 영향을 미칠 것으로 분석되었습니다.
| [처방의약품(prescription drug) 판매현황] |
| (단위: 십억달러) |
| 연도 | 시장 규모 | 전년대비 성장률 |
|---|---|---|
| 2016 | 782 | - |
| 2017 | 801 | 2.43% |
| 2018 | 842 | 5.12% |
| 2019 | 873 | 3.68% |
| 2020 | 890 | 1.95% |
| 2021 | 1,065 | 19.66% |
| 2022 | 1,083 | 1.69% |
| 2023 | 1,053 | -2.77% |
| 2024(E) | 1,118 | 6.17% |
| 2025(E) | 1,205 | 7.78% |
| 2026(E) | 1,294 | 7.39% |
| 2027(E) | 1,398 | 8.04% |
| 2028(E) | 1,509 | 7.94% |
| 2029(E) | 1,621 | 7.42% |
| 2030(E) | 1,743 | 7.53% |
| 출처 : 한국제약바이오협회, 2024 제약바이오산업 DATA BOOK(2024.12) |
| 자료원 : World Preview 2024, Evaluate Pharma |
국내 제약산업은 상기한 국내 및 해외 제약시장의 전반적인 성장률 둔화 추세에 대응하기 위하여 신약개발을 위한 높은 수준의 R&D 투자, 생산 및 품질관리 경쟁력 확보를 바탕으로 한 이머징마켓 진출, 높은 치료율과 낮은 부작용을 보이는 바이오의약품 개발 등 다양한 노력을 기울이고 있습니다.
| [국내 의약품 연구개발비 관련 주요 통계] |
| (단위 : 개, 억원, %) |
| 구분 | 2020 | 2021 | 2022 | 2023 | |
|---|---|---|---|---|---|
| 의약품 제조기업 | 기업 수 | - | - | - | - |
| 매출액 | 335,033 | 399,241 | 419,277 | 422,257 | |
| 연구개발비 | 21,900 | 20,754 | 23,280 | 24,054 | |
| 매출액 대비 비중 | 6.54 | 5.89 | 6.27 | 6.41 | |
| 상장기업 | 기업 수 | 141 | 151 | 156 | 158 |
| 매출액 | 267,018 | 298,734 | 346,644 | 376,917 | |
| 연구개발비 | 32,904 | 35,442 | 43,894 | 47,124 | |
| 매출액 대비 비중 | 12.3 | 11.9 | 12.7 | 12.5 | |
| 혁신형 제약기업 | 기업 수 | 48 | 43 | 43 | 42 |
| 매출액 | 159,186 | 167,459 | 193,559 | 168,524 | |
| 연구개발비 | 22,545 | 21,193 | 25,469 | 24,793 | |
| 매출액 대비 비중 | 14.2 | 12.7 | 13.2 | 14.7 | |
| 주1) 의약품 제조기업 : 한국은행 기업경영분석 |
| 주2) 상장기업: DART 상 의약품 제조업, 자연과학 연구개발업 기준(진단의료기기, 건식, 화장품, 동물용의약품 및 지주사 제외) |
| 주3) 혁신형 제약기업 : 보건복지부 혁신형 제약기업 인증고시 기업 |
| 출처 : 한국제약바이오협회, 2024 제약바이오산업 DATA BOOK(2024.12) |
그러나 이러한 국내 제약산업 전반의 노력에도 불구하고 전체 제약산업이 위축되거나 시장성장률이 둔화되는 경우, 당사의 매출 또한 크게 저하될 수 있으며, 이는 당사의 사업, 영업성과 및 재무상태에 부정적인 영향을 미칠 가능성이 존재하오니 투자자께서는 이 점 유의하시기 바랍니다.
| 다. CNS 시장 위축 가능성 관련 위험 당사는 일반의약품, 전문의약품 제조와 별개로 파킨슨병 및 조현병 등 중추신경계(CNS)질환의 미충족 수요를 만족할 수 있는 혁신신약 개발 사업을 주요 사업으로 영위하고 있습니다. 국내 우울증 치료제 시장은 2022년에 3,700억 원 규모였으며, 연평균 3.6% 성장하여 2028년에는 4,600억 원 규모에 달할 것으로 전망되고 있습니다.또한 당사는 중추신경계질환 중 퇴행성 질환인 파킨슨병 치료제 연구개발에도 주력하고 있으며 자회사 콘테라파마를 통해 파킨슨병 치료제인 CP-012 임상을 진행하고 있습니다. 글로벌 시장조사기관 Future Market Insights에 따르면, 글로벌 파킨슨병 치료제 규모는 2024년에 43억 달러 규모에 달할 것으로 전망되며, 이후 연평균 5.1% 성장하여 2034년에는 67억 달러 규모의 시장을 형성할 것으로 전망되고 있습니다. 하지만 현 시점에서 예상치 못한 변수로 인해 향후 우울증 치료제 시장 및 파킨슨병 치료제 시장이 축소될 경우 당사가 현 시판중인 제품 매출 감소로 이어질 뿐만 아니라 임상 진행중인 치료제의 경제성이 하락하여 개발 추진력에 제동이 걸릴 개연성도 존재합니다. 투자자분들께서는 이점 참고하시기 바랍니다. |
당사는 일반의약품, 전문의약품 제조와 별개로 파킨슨병 및 조현병 등 중추신경계(CNS)질환의 미충족 수요를 만족할 수 있는 혁신신약 개발 사업을 주요 사업으로 영위하고 있습니다. 당사는 일본 스미토모 파마사에서 기존 항전신병 약물의 부작용을 최소화한 조현병/양극성 우울증 치료제 '라투다정'을 License in 하여 국내에서 3상 임상을 진행하였으며 2024년 8월 국내 시장에 출시하였습니다.
라투다정은 국내에서 임상 3상 완료 후 2023년 식품의약품안전처 품목허가 승인을 취득하였으며, 2024년 8월부터 보험급여 시행 및 처방이 이루어지고 있습니다. 현재 국내 56곳의 주요 정신건강의학과 전문병원에서 원내처방이 이루어지고 있으며, 전국 260곳의 정신건강의학과 의원에서도 처방 중 입니다. 2024년 하반기 국내 주요 대학병원 포함 10곳의 종합병원의 약사 심의위원회 통과가 완료되었으며, 전국 주요 상급종합 병원 접수 및 심의도 진행 중인 것으로 확인되었습니다.
정신건강의학과 질환 진단 및 치료에 대한 전반적인 수요 증가, 고령인구 증가로 인한 중추신경계 퇴행성 질환 유병률 증가는 CNS 치료제 시장의 성장을 이끄는 주요 촉진 요인입니다. 한국을 비롯한 다수의 국가에서 정신질환 치료 관련 정부 지원 및 인식 개선이 이루어지고 있으며, 국내에서는 보험급여항목에 CNS약물이 지정되는 등 환자 부담도 완화되는 추세입니다.
조현병, 우울증 등 정신질환이 관리 가능한 질환이라는 사회적 인식 변화로 진단 및 치료가 적극적으로 이루어 지면서 치료제 시장 확장세가 이어지고 있습니다. 2022년 국가정신건강현황보고서에 따르면 정신의료기관에서 조현병으로 진료를 받은 환자는 18만 명이었으나, 세계적으로 조현병의 평생 유병률이 1% 내외로 나타나고 있는점을 고려 시 국내 조현병 환자 수는 약 25만 명에 달할 것으로 추정됩니다. 조현병 환자는 5년 이상의 장기간 지속적인 약물치료가 요구되므로 조현병 치료제 시장은 일정 규모 이상의 수요가 꾸준히 창출되는 시장입니다. 한편, 우울증 치료제 시장은 청년 정신건강 검진 주기의 단축 등 정부의 대국민 정신건강정책 강화에 힘입어 높은 시장성장성을 유지할 것으로 보여지고 있습니다. 우울증 환자는 일반적으로 9개월에서 18개월간 약물치료를 받기에 이러한 장기 투여 권장사항은 우울증의 만성적 특성과 재발 위험을 고려한 것으로, 타 질환 치료제보다 투여기간이 긴 편에 속하고 있습니다. 국내 우울증 치료제 시장은 2022년에 3,700억 원 규모였으며, 연평균 3.6% 성장하여 2028년에는 4,600억 원 규모에 달할 것으로 전망되고 있습니다.
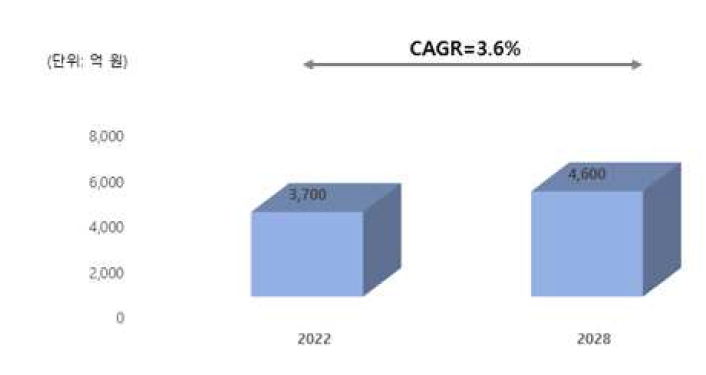 |
|
국내 우울증 시장 전망 |
| 자료: Statista(2023.01) |
또한 당사는 중추신경계질환 중 퇴행성 질환인 파킨슨병 치료제 연구개발에도 주력하고 있으며 자회사 콘테라파마를 통해 파킨슨병 치료제인 CP-012 임상을 진행하고 있습니다. 콘테라파마는 유럽을 중심으로 임상시험을 진행하고 있으며 임상시험에서 긍정적인 결과가 도출될 시 해당 파이프라인의 글로벌 시장 진출 및 License-out을 통한 매출 시현이 가능해질 전망입니다. CP-012는 기존 치료제가 해결하지 못한 아침무동증을 해결해 줄 수 있는 신약으로 주목받고 있습니다. 기존 파킨슨병 표준 치료제 레보도파는 도파민성 약물인데, 환자가 레보도파 투약 후 수면 시 도파민성 약물의 효과가 떨어지는 현상이 발생하며 이를 아침무동증 이라고 합니다. 뇌의 도파민 분비 신경 세포 사멸로 발생하는 파킨슨병은 혈뇌장벽을 통과할 수 있는 도파민 전구체 레보도파를 사용하여 치료 중인데, 레보도파는 반감기가 짧아 야간 투약 후 이른 아침에는 약효가 소진되며 환자는 아침무동증을 겪게 됩니다. 이에 따라 환자는 아침 기상 시 근육이 경직되는 현상을 겪게 되며 50~70%의 파킨슨병 환자들이 아침무동증을 경험하고 있는 것으로 확인됩니다. 콘테라파마가 개발중인 치료제 CP-012는 약물이 특정 부위에서만 방출될 수 있도록 제어하는 지연 방출 특성, 서로 다른 시점에서 약물을 방출하는 시스템인 이중 박동성 방출 특성을 갖춘 제형으로 개발 진행중입니다. 따라서 CP-012의 경우 취침 전 섭취한 후 그 효과가 아침에 나타나게 되는 효용을 검증하는 것으로, 해당 치료제가 현실화될 경우 기존 파킨슨병 치료제의 한계를 극복할 수 있을것으로 전망됩니다. 한편 CP-012는 현재 글로벌 임상 1b상 진행중이며 25년 2분기 중으로 결과가 나올 것으로 전망되고 있습니다.
| [CP-012 개요] |
| 적응증 | 파킨슨병 환자의 Morning Akinesia (아침무동증) 치료제 |
| 작용기전 | 개발 초기 단계로 Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 제품의 특성 | 개발 초기 단계로 Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 진행경과 | 유럽 임상 1a상 진행 완료 (2023년 9월) 유럽 임상 1b상 진행 중 |
| 향후계획 | 개발 초기 단계로 예측 불가 |
| 경쟁제품 | - |
| 관련논문 등 | - |
| 시장규모 | 개발 초기 단계로 예측 불가 |
| 기타사항 | - |
| 자료: 당사 사업보고서 |
글로벌 시장조사기관 Future Market Insights에 따르면, 글로벌 파킨슨병 치료제 규모는 2024년에 43억 달러 규모에 달할 것으로 전망되며, 이후 연평균 5.1% 성장하여 2034년에는 67억 달러 규모의 시장을 형성할 것으로 전망되고 있습니다. 또한 국가생명공학정책연구센터에서 2025년 발간한 바이오인더스트리에 따르면 전 세계적인 고령화 추세로 알츠하이머병, 파킨슨병 등의 신경퇴행성 질환 유병률이 증가함에 따라, 근본적 치료제 개발 및 정밀 치료기술 적용이 시급함을 시사하고 있습니다. 신경퇴행성 질환은 신체적·인지적 기능 저하를 동반하여 삶의 질 저하와 막대한 경제적 부담을 초래하나, 타질환 대비 질병 기전 규명과 치료가 어려운 상황입니다. 또한 신경퇴행성 질환 치료제는 질병 기전에 대한 복잡성, 동물모델 한계, 환자 간 이질성, 평가지표 부족 등의 복합적 요인으로 다른 치료 분야 대비 임상시험 실패율이 높은 편 입니다. 이에 주요 신경퇴행성 질환인 알츠하이머·파킨슨병 치료제 시장은 2023~2030년 동안 두 자릿수의 연평균 성장률로 시장이 급격히 확대될 것으로 전망됩니다. 파킨슨병 치료제 시장도 최근 바이알레브(’24.10) FDA 승인으로 새로운 시장
재편이 기대되며, 알츠하이머병 치료제 시장 대비 작은 규모이나 연평균 성장률 13.3%로 지속 성장하여 2030년 71.7억 달러 형성 전망되고 있습니다. 향후 정밀 신경퇴행성 질환 산업은 유병률 증가, 바이오 기술 및 영상/데이터 분석기술 발전,글로벌 규제기관 필요성 인정, 다양한 파트너십 활성화 등의 성장동인으로 더욱 활성화될 전망입니다.
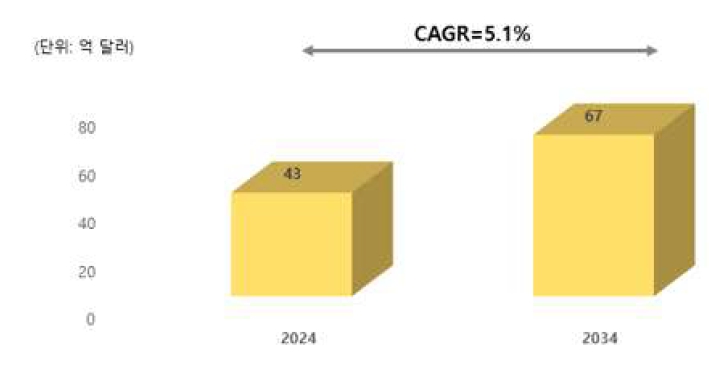 |
|
글로벌 파킨슨병 치료제 성장(future market insight) |
| 자료: Future markte insight(2024.05) |
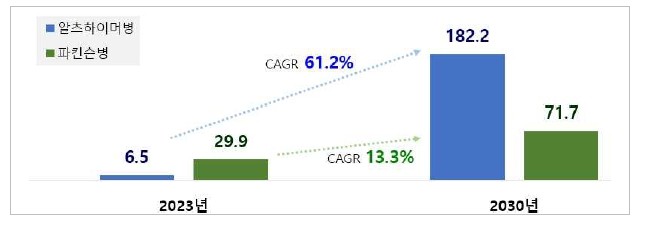 |
|
글로벌 알츠하이머 및 파킨슨병 치료제 시장 규모 전망(단위 억달러) |
| 자료: Frost&Sullivan(2025.01) |
이처럼 당사가 시판중인 우울증 치료제 및 임상 진행중인 파킨슨병 치료제는 향후 (1) 뚜렷한 치료제 부족, (2) 장기간 투여 필요성, (3) 기존 치료제의 한계 등으로 인해 높은 성장성을 보일 것으로 관측됩니다. 또한 당사가 생산하는 대부분의 제품이 의사의 처방이 필요한 전문의약품 임으로 당사는 대형병원을 대상으로 학술마케팅을 진행하고 중추신경계(CNS) 질환 치료제 영업조직의 전문성을 강화하는 등 전방 수요에 대응하기 위한 노력을 기울이고 있습니다. 하지만 현 시점에서 예상치 못한 변수로 인해 향후 우울증 치료제 시장 및 파킨슨병 치료제 시장이 축소될 경우 당사가 현 시판중인 제품 매출 감소로 이어질 뿐만 아니라 임상 진행중인 치료제의 경제성이 하락하여 개발 추진력에 제동이 걸릴 개연성도 존재합니다. 투자자분들께서는 이점 참고하시기 바랍니다.
| 라. 정부의 의약품 규제 관련 위험 제약산업은 인간의 생명과 보건에 관련한 제품을 생산하는 국민의 건강과 직결된 사업이기 때문에 의약품의 허가, 보험 약가 등재 뿐만 아니라 생산, 유통, 판매에 이르기까지 정부에서 매우 엄격하게 통제, 관리하고 있어 정부정책의 영향을 크게 받고 있습니다.정부는 이러한 기조 하에 건강보험 재정건전화 및 제약산업 선진화를 위해 리베이트 쌍벌제, 일괄 약가인하 등을 시행하는 등 제약산업에 대한 규제를 강화하는 추세이며, 특히 타산업과 달리 정부가 약가를 직접적으로 통제하고 있어 정부의 약가정책이 제약산업내 개별기업의 매출 및 영업수익성에 직접적인 영향을 미치고 있습니다. 제약산업은 국민 건강과 직결되는 특성으로 인해 정부의 엄격한 통제를 받고 있으며, 약가인하, 리베이트 규제, 제조품질 기준 강화 등 정책 변화가 지속될 경우, 당사의 사업환경에도 부정적인 영향을 미칠 수 있습니다. 이에 따라, 투자자께서는 정부 정책 및 규제 강화가 당사의 성장성과 재무 안정성에 영향을 미칠 수 있다는 점을 고려하여 신중히 투자 결정을 내리시기 바랍니다. |
제약산업은 인간의 생명과 보건에 관련한 제품을 생산하는 국민의 건강과 직결된 사업이기 때문에 의약품의 허가, 보험 약가 등재 뿐만 아니라 생산, 유통, 판매에 이르기까지 정부에서 매우 엄격하게 통제, 관리하고 있어 정부정책의 영향을 크게 받고 있습니다. 이에 정부는 국내 제약산업이 내수시장에 안주하여 글로벌 경쟁력을 잃을 것을 방지하고 의약품비 부담으로 인해 건강보험 재정건전성이 위협받고 있는 상황을 고려하여 2006년 '약제비 적정화방안'을 시작으로 제약산업 선진화를 추진하였습니다. 주된 골자는 국내 제약사들이 리베이트에 의존하는 기존의 제네릭의약품(복제약) 위주의 영업에서 벗어나 신약개발과 해외수출에 주력하도록 유도하는 것입니다.
정부는 이러한 기조 하에 건강보험 재정건전화 및 제약산업 선진화를 위해 리베이트 쌍벌제, 일괄 약가인하 등을 시행하는 등 제약산업에 대한 규제를 강화하는 추세이며, 특히 타산업과 달리 정부가 약가를 직접적으로 통제하고 있어 정부의 약가정책이 제약산업내 개별기업의 매출 및 영업수익성에 직접적인 영향을 미치고 있습니다. 제약산업과 관련된 정부의 주요 정책 변화와 그에 따른 영향은 아래와 같습니다.
| [정부의 주요 제약산업 규제] |
| 시행년도 | 구분 | 주요내용 | 산업에 미친 영향 |
|---|---|---|---|
| 2000 | 의약분업 | - 의사와 약사의 역할 분리 | - 전문의약품의 처방확대, 전문의약품 중심의 시장성장 |
| 2002 | 약가재평가 제도 도입 | - 정기적으로 가격변동요인을 파악하여 약가조정 - 외국 7개국 약가와 비교하여 약가 조정 |
- 조정수준이 수익성에 미친 영향은 제한적 |
| 2006 | 약제비 적정화 방안 |
- 특허만료 신약의 가격조정 - 제네릭 약가인하 폭 확대 - 선별등재 시스템으로 전환 - 기등재의약품 목록 정비사업 운영 |
- 가격통제와 품목대상의 범위 확대 - 도입 이후 제약기업의 수익성 하락세 - 단계적 가격조정으로 영향은 점진적 양상 |
| - 가격 결정방식이 외국 7개국의 평균값과의 상대비교에 서 보험공단과의 협상에 의한 방식으로 전환 |
- 보험공단의 가격 교섭력이 높아짐 | ||
| 2008 | 제조 및 품질관리기준 개선 | - GMP 규정을 선진국 수준으로 개선 | - 제약기업들의 관련 설비투자 증가 |
| 2009 | 리베이트 약가 연동제 | - 리베이트 적발 품목 보험약가 최고 20% 인하 | - 영업에 대한 정부규제 강화 |
| 2010 | 주) 시장형 실거래가 상환제도 | - 의약품 저가 구매시 의료기관/약국의 이윤인정 | - 처방,조제 약품비 절감 장려금 제도로 전환 |
| 리베이트 쌍벌제 | - 리베이트 받은 사람에 대한 처벌 강화 | - 영업에 대한 정부규제 강화 | |
| 2012 | 약가제도 개편 (일괄약가인하) |
- 기존 계단식 약가 구조를 폐지 - (신규등재의약품) 특허만료 전 오리지널 가격의 53.55%를 부여 - (기등재의약품) 약가를 일괄 인하 |
- 가격조정의 폭과 범위가 매우 큼 - 2012년 제약기업의 수익성이 큰 폭으로 하락함 |
| 2014 | 국민건강보험법 개정 | - 리베이트와 관련된 약제를 건강보험 대상에서 제외 | - 제약업계의 영업방식의 변화 |
| 리베이트 투아웃제 | - 리베이트 금액과 횟수에 따라 급여정지기간 결정 | - 영업사원 인센티브 제도의 조정 등 | |
| 2015 | 의약품 허가-특허권 연계제도 | - 신약 특허권자의 허락 없이 후발주자의 복제약이 판매되지 않도록 함 |
- 신약특허권의 강화 |
| - 단기적으로 국내 제약산업의 매출액 감소 | |||
| 의약품 공급내역 보고 의무화 | - 의약품의 유통현황과 실거래가를 조회 가능 - 공급내역 익일보고원칙 - 바코드사용에 대한 의무화 |
- 유통부문에 대한 정부규제 강화 | |
| 2016 | 의약품 공급내역 보고 의무화 | - 공급내역 익일보고원칙 - 바코드사용에 대한 의무화 제도 |
- 의약품의 유통현황과 실거래가를 조회 가능 |
| 실거래가 약가 인하 | - 시장에서 실제로 거래되는 가격으로 의약품 가격을 인하하는 제도 |
- 전체 평균 1.96% 인하될 예정 - 약가 인하로 연간 1,368억원의 약제비 절감 - 보험제정의 안정화 |
|
| 2017 | 약사법 개정안 시행 | - 경제적 이익 등 제공내역에 관한 지출 보고서 작성 및 보관 의무화 |
- 리베이트에 대한 정부규제 강화 |
| 2019 | 사용량-약가 '유형 다' 연동 협상제 도입 |
- 유형 '다' 협상 대상인 26개사 34개의 품목의 약가를 인하 |
- 의약품 특성에 따라 등재 유형별로 평가 방식 차등화 |
| 2020 | 제네릭 의약품 약가 제도 개편 |
- 자체 생물학적 동등성 시험 실시, 등록된 원료의약품 사용 2개 기준 요건 및 건강보험 등재 순서에 따라 7월부터 제네릭 차등 약가 적용 |
- 무분별한 제네릭 개발 및 생산 방지 - 제네릭 의약품에 대한 품질과 대내외 경쟁력 제고 |
| 2021 | 의약품 공동생동 1+3 제한 | - 동일한 임상(생동)시험자료를 이용한 품목 수 제한 (1+3) |
- 산업의 유통문란과 신약 개발 능력 약화 문제 해소 |
| 2022 | 의약품ㆍ의료기기 리베이트 근절 관련 제도 |
- 영업대행사(CSO) 관리 강화 - 영업대행사(CSO) 지출보고서 작성 제도 관리 강화 |
- 영업대행업체(CSO) 불법 리베이트 처벌 근거 구체화 |
| GMP 원스트라이크 아웃제 | - 의약품 제조ㆍ품질관리기준(GMP) 위반 시 인증 취소 | - 의약품 임의ㆍ불법 제조 사태 방지 | |
| 2023 | 의약품ㆍ의료기기 리베이트 근절 관련 제도 |
- 영업대행사(CSO)의 지출보고서 작성 의무 부과 - 영업대행사(CSO)의 지출보고서 실태조사 및 결과 공표 |
- 영업대행업체(CSO) 불법 리베이트 처벌 근거 구체화 |
| 출처 : 보건복지부 |
| 주1) 시장형실거래가상환제도는 2014년 9월 폐지 |
| 주2) 리베이트 투아웃제 2018년 9월 폐지 |
① 약가 인하 관련 규제
정부는 연간 약제비 지출 규모를 14% 이상 절감하는 내용의 신규 약가 일괄 인하제도를 포함한 '약가제도 개편 및 제약산업 선진화' 방안을 2012년 4월 1일에 시행하였습니다. 새로운 제도는 기존의 계단형 약가제도를 폐지하고 특허만료, 오리지널 및 제네릭의 약가를 일괄 인하하는 방안으로, 주요 내용은 특허만료 의약품에 대해 오리지널 및 제네릭의 약가를 각각 기존의 80%(상한가 대비) 및 68% ~ 53.55%로 일괄 인하하고, 특허 만료 1년 이내 의약품 또한 53.55% 수준으로 상한 가격을 일괄 인하하는 것입니다.
| [변경된 약가 산정 방식] |
|
| (자료 : 보건복지부) |
| [약가제도 주요 개정사항 요약] |
| 구분 | 내용 |
|---|---|
| 계단형 약가제도 폐지 |
특허만료 후 제네릭 등재시 오리지널과 최초 제네릭의 약가인하폭 확대 - 기존 특허만료시 오리지널은 최초가의 80%, 최초 제네릭은 오리지널의 68%, 제네릭은 등재순서 5번째까지 68%, 이후는 최저가의 90%로 체감 - 개정 특허만료 후 1년까지 오리지널은 80%에서 70%, 제네릭은 68%에서 59.5%, 1년 후에는 특허만료 전 오리지널의 53.5%로 일괄 인하 |
| 기등재약 가격조정 | 기등재의약품은 2012년 4월 오리지널의 53.5% 수준으로 상한가격 일괄인하 단, 정책일관성 위하여 동일 최고가 판단시기는 2007년 1월 1일 기준 퇴장방지 의약품과 필수의약품 등은 예외 적용 |
| 동일성분 동일가격 | 생동성 시험 통과한 동일성분 의약품은 동일 상한가격 적용 |
| (자료 : 보건복지부) |
정부의 일괄 약가 인하로 인해 건강보험에 등재된 1만 3,814개 품목 중 47%인 6,506개 품목의 가격이 평균 21% 낮춰졌으며, 이는 전체 약 값이 평균 14% 인하되는 결과를 가져왔습니다. 2013년 7월 한국제약협회가 발표한 '약가 인하 이후 제약산업의 변화' 정책 보고서에 따르면 국내 68개 상장 제약회사들의 2012년 약품비 청구액이 5조 2,914억원으로 전년에 비해 6.8% 감소한 것으로 나타났으며, 2013년 1분기 약품비 청구실적은 1조 2,677억원으로 2012년 동기 대비 12% 줄어든 것으로 나타났습니다.
현재 국내는 단일보험자(국민건강보험공단)에 의한 전국민 건강보험제도를 운영하고 있는 상황으로, 건강보험의 지속가능성 제고와 적정수준의 국민의료비 유지, 불법 리베이트 차단 등의 목표 하에 약가에 대해 정책적 개입이 이루어지고 있습니다. 국내의 약가 사후관리제도는 대내외 보건의료 환경변화에 의하여 수 차례 변화되어, 현재는 실거래가 조사에 의한 약가 인하, 사용량-약가 연동 협상, 급여범위 확대 시 약가인하, 제네릭의약품 등재 시 오리지널의약품의 약가인하 등의 제도가 운영되고 있습니다. 약가는 산업 정책과 보건의료 정책이 상충하여 변동성이 상재해 있는 상황으로, 현재 제네릭 약가 차등제가 시행 예정되어 있는 상황입니다. 이러한 점진적인 약가 인하 정책은 제약산업에서 간과할 수 없는 중요 요인이며, 당사 사업에도 부정적인 영향을 미칠 수 있습니다.
| [약가 인하 정책 추이] |
| 시기 | 인하제도 | 내용 |
|---|---|---|
| 2000년 ~ 2009년 |
실거래가약가인하 (표본조사) |
표본조사(전국 80개 요양기관)를 통해 의약품 청구실태 조사 후 약가인하 |
| 2002년 ~ 2012년 | 약가 재평가 | 최초 상한금액 산정이후 3년마다 7개국 조정 평균가를 조사하여 상한금액 재조정 (인상은 없음) |
| 2007년 ~ 2014년 | 기등재 목록정비 | 2007년 선별등재제도로 전환하면서 기존약재의 경우 20% 약가 인하시 급여등재 유지 |
| 2012년 | 일괄 약가인하 | 상한금액대비 53.55%수준까지 일괄 약가인하 |
| 2016년 ~ |
실거래가약가인하 (전수조사) |
유통정보센터 유통정보를 근거로 가중평가가격 까지 약가 인하 |
| 현행 | 특허만료 약가인하 | 개별약제 특허만료시 1년간 70%, 1년 후 53.55%로 약가인하 |
| 현행 | 사전 약가인하 | 개별약제 급여기준 확대 이전에 협의를 통하여 약가인하 |
| 현행 | 사용량 약가연동 | 개별약제 약가와 사용량을 연계하여 등재 후 사용량이 일정 % 증가할 때 약가 인하 |
| 현행 | 사용(급여) 범위 확대 시 사전 인하 | 연간 3억원 이상 청구금액 증가 예상 품목 대상 상한금액 사전 인하(최대 5%) |
| 현행 (2023.09~ |
약가 차등제 주1) | 기준요건 충족 여부 및 동일제제 수에 따른 약 가 차등산정 |
| 자료 : 보건복지부 주1) 기준 요건은 (1) 자체 생물학적 동등성 시험 수행, (2) 등록된 원료의약품 사용 충족 여부이며, 같은 성분으로 건강보험 급여 목록에 등재된 제네릭이 20개 이상일 시 요건 충족 여부와 관계 없이 약가 인하되어 21번째부터 급여 등재되는 제네릭은 생동성 시험을 직접 수행하고 등록 원료의약품을 사용했어도 더 낮은 가격(최저가의 85%)을 적용 받는 구조임(20개 미만: 38.69~53.55%, 20개 이상: 최저가의 85%) |
2019년에 도입된 사용량-약가 연동 협상제는 해당 약품 매출이 전년보다 크게 늘어 건보 재정에 부담이 된다고 판단되면 건보공단이 제약사와 협상을 통해 약가 일부를 인하하는 제도이며, 2021년 11월 국민건강보험공단은 '20년 4분기 사용량-약가 연동제 협상 모니터링 대상으로 당사의 고혈압 치료제 '카나브' 등 131개 약품 리스트를 공개하였습니다. 전년도 매출(건강보험 청구액)과 당해 판매량을 비교해 당초 공단이 예상했던 것보다 판매량이 늘어난 경우, 사용량-약가 연동제를 적용해 제약사와 약가 인하 협상을 진행하게 됩니다. 사용량-약가 연동제에 따르면 제약사와 공단이 제품 출시 전 협의한 3년치 '건보 예상 청구액'이 있는 경우에는 실제 청구액이 예상 청구액보다 30% 이상 증가할 때 약가 인하 협상 대상이 됩니다. 예상 청구액이 없거나 출시된 지 4년 이상 지난 기존 제품은 당해 청구액이 전년도 청구액보다 60%이상 증가하거나 증가액이 50억원 이상(증가율 10% 이상)인 경우 협상 대상에 포함됩니다.
| [사용량-약가 연동 협상제 개요] |
| 제도 취지 | 건강보험 재정 절감 | |
|---|---|---|
| 적용 대상 | 3년 치 예상 청구액(예상 매출) 있는 경우 | 실 청구액 예상보다 30% 이상 증가 |
| 예상 청구액 없거나 출시 4년 이상 경우 | - 올 청구액 전년보다 60% 이상 증가 - 증가액 50억원 이상(증가율 10% 이상) |
|
| 자료 : 국민건강보험공단 |
또한 정부는 제네릭 품목에 적용되었던 일괄 약가제를 개정하여 차등식 약가제를 2020년 7월부터 시행하였으며, 현재 2가지 기준에 따라 다음과 같이 약가가 차등 산정되고 있습니다.
| [제네릭 의약품 약가제도 개정안] |
| 건강보험 등재 순서 | 기준 요건 | 가격 |
|---|---|---|
| 20개 이내 | 2개 모두 만족 | 원조 의약품 가격의 53.55% |
| 1개 만족 | 53.55%의 85% → 45.52% | |
| 만족 요건 없음 | 45.52%의 85% → 38.69% | |
| 20개 이후 | - | 최저가의 85% |
| 자료 : 보건복지부 |
| 주1) 21번째 제네릭 의약품은 20개 내 제품 최저가의 85%로 산정, 22번째 제네릭은 21번째 제네릭 가격의 85% (단, 기존 제네릭은 기준요건 충족만 적용) |
| 주2) 기준요건 - 효능입증 : 자체 생물학적 동등성 시험 실시('생동') - 원료입증 : 등록된 원료의약품 사용 |
최근에는 외국 약가 비교 재평가 제도가 본격적으로 논의되고 있는 추세입니다. 건강보험에서 약품비 비중은 23~24%를 유지하고 있지만, 약제비는 매년 1조원 이상 폭등하며 건보재정에 큰 부담이 되고 있습니다. 특히 고가신약의 등장으로 건강보험에서 신약의 비중이 높아지면서 정부는 건강보험 재정 건전성에 방점을 두고 정책을 시행하고자 하는 의지를 표명한 바, 자연스레 외국 약가 비교 재평가 추진이 급물살을 타게 되었습니다. 주요 내용으로 특허 만료 의약품 가운데 만성질환 치료제의 가격을 선진국 수준으로 낮춰 재정 절감안을 마련하겠다는 계획으로 확인됩니다.
정부안에 따르면 1년차에는 위장관용약(2043품목), 고혈압치료제(2268품목), 항생제(2156품목)가 재평가 대상이며 2년차에는 고지혈증치료제, 호흡기계용약, 정신신경계용약, 당뇨병용약, 근골격계질환치료제가, 3년차에는 안과, 이비인후과, 치과용약, 진통제, 비뇨생식기관용제, 항혈전제, 피부질환용제, 항암제, 기타 17개 효능군이 재평가 대상으로 확인됩니다.
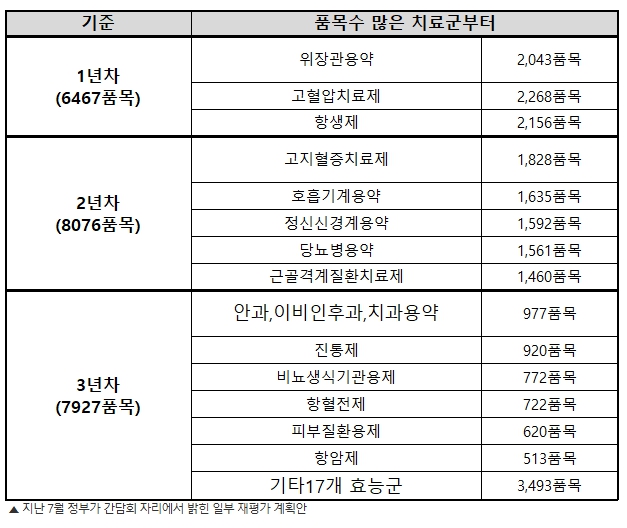 |
|
외국약가비교재평가 대상품목 |
조정기준 금액은 A8국가의 절사 평균가로, 최고·최저 제외한 조정평균가 입니다. 외국 약가 조정 가격 산출은 해당 국가에서 공적으로 급여되거나 이에 준해 급여되는 가격이 기준이 되는 것으로 확인되었습니다. 제약업계는 독일이나 캐나다의 경우 참조가격제도가 시행되는 국가로 공적 급여 가격이 상당히 낮기에 공적급여에 대해 의문을 제기하였으며 독일과 캐나다를 제외한 미국, 일본, 영국, 스위스, 프랑스, 이탈리아 등 6개국만 비교 대상으로 삼자고 건의한 상황입니다.
2024년 11월부터 시작한 관련 민관 간담회는 2024년 7월까지 10차례 진행되었으며 그 결과 정부의 추진의사가 구체적으로 확인된 것으로 나타납니다. 최초 2024년 계획 공고, 2025년 재평가 시작 일정으로 알려져 왔으나 정치적 이슈로 인해 잠시 보류된 것으로 확인됩니다. 그럼에도 불구, 정부의 외국약가 비교 재평가 제도 도입의지가 확고한 만큼 향후 동 제도가 도입될 가능성인 높을 것으로 추정되며 이는 당사의 사업에 부정적인 영향을 미칠 수 있습니다.
이러한 약가 제한 조치 개편 및 시행 현황을 미루어보았을 때 향후에도 정부의 추가적인 약가인하 정책 기조는 지속될 것으로 판단되며, 추가적인 정책 시행 시 당사의 수익성과 영업환경에 추가적인 부담으로 작용할 가능성이 존재합니다.
한편, 2018년 7월 정부는 건강보험료 부과 체계를 개편하여 소득 및 재산이 적은 지역 가입자의 보험료 부담을 줄여주고 고소득자의 보험료를 일부 인상하였습니다. 소득 분포상 저소득층 보험료 인하 총액이 고소득층 보험료 인상 총액보다 크기 때문에 2018년 기준 건강보험료 수입이 약 3,593억원 감소할 것으로 예상되었습니다. 실제 건강보험 재정수지는 해당 개편안 이후 2018년 -0.2조원, 2019년 -2.8조원의 당기적자를 기록하였고, 2020년 -0.4조원, 2021년 +2.8조원을 기록하며 점차 개선되는 모습을 보여왔습니다. 또한 2022년 9월 건강보험료 부담의 형평성을 제고하고, 소득 중심의 공정한 부과를 위한다는 취지로 건강보험료 2단계 부과 체계 개편안을 적용하였습니다.
한편, 2024년 1월 보건복지부는 건강보험 지역 가입자의 재산 및 자동차 보험료 개선 방안의 입법을 예고하였습니다. 법안의 주된 골자는 재산 보험료 산정 시 기본 공제액을 1억원으로 확대하고, 자동차 부과 건강보험료를 폐지하는 것으로 해당 법안은 향후 건강보험료 수입 및 건강보험 재정수지에 부정적인 영향을 미칠 가능성이 있습니다. 만약 이로 인해 건강보험 재정수지 적자가 지속될 시 건강보험 재정 상태의 개선 필요성이 제기되어 추가적인 약가 제한 제도의 강화가 뒤따를 수 있으며, 이는 제약산업의 성장을 제한하는 요소로 작용할 수 있습니다.
| [건강보험 재정 전망] |
| (단위: 억원) |
| 구분 | 2024(E) | 2025(E) | 2026(E) | 2027(E) | 2028(E) |
|---|---|---|---|---|---|
| 총수입 | 988,955 | 1,045,611 | 1,115,354 | 1,183,196 | 1,252,201 |
| 총지출 | 962,553 | 1,040,978 | 1,118,426 | 1,191,091 | 1,268,037 |
| 당기수지 | 26,402 | 4,633 | (3,072) | (7,895) | (15,836) |
| 준비금 | 306,379 | 311,012 | 307,940 | 300,045 | 284,209 |
| 지급가능월수 | 3.8개월 | 3.6개월 | 3.3개월 | 3.0개월 | 2.7개월 |
| 출처: | 보건복지부, 제2차 국민건강보험 종합계획(2024~2028) |
② 리베이트 관련 규제
제약시장은 수요자와 공급자 간의 정보 비대칭이 존재하는 시장입니다. 제약시장에서 수요자는 의약품의 성분 및 효능에 대한 전문지식이 부족한 반면, 공급자는 수요자보다 양질의 정보를 보유하고 있습니다. 따라서 최종 구매자인 일반 소비자가 합리적인 선택을 하는데 제약이 존재합니다. 또한, 전문의약품은 보건당국의 광고 제한 대상으로 규정되어 있어 전문의약품에 대한 일반 소비자의 정보 접근도가 낮습니다. 이와 같은 특징으로 인해 제약시장에서는 수요자와 공급자 간의 정보 비대칭성이 강하게 나타나며, 이로 인해 소비자를 보호할 수 있는 제도적 장치가 필수인 산업입니다.
전문의약품을 선택할 수 있는 권한은 소비자가 아닌 처방 의사에게 있습니다. 제약회사는 전문의약품의 마케팅 및 판매를 의사 또는 의료기관을 중심으로 진행하고 있으며, 전문의약품 선택권이 처방 의사에게 있는 만큼 거래 과정에서 리베이트 행위가 발생할 가능성이 높습니다. 판매 과정에서 리베이트가 발생하면 최종 구매자가 체감하는 약가는 권장 가격보다 높은 수준에서 형성되고, 이는 소비자들의 실질적 피해로 연결됩니다. 따라서, 정부는 제약산업 내 리베이트 근절을 위한 제도적 장치를 지속적으로 마련하고 제약시장을 관리ㆍ감독하고 있으며 관련 규제는 다음과 같습니다.
| [리베이트 관련 규제] |
| 시행시기 | 구분 | 내용 |
|---|---|---|
| 2009 | 리베이트 / 약가 연동제 |
- 리베이트 적발 시 보험약가 최대 20% 인하 - 적발 이후 1년 내 동일행위 반복 시 최대 30% 인하 |
| 2010 | 리베이트 쌍벌제 | - 리베이트 받은 자에 대해서도 형사처벌 규정 신설 |
| 2014 | 리베이트 투아웃제 |
- 리베이트 금액, 지급횟수에 따라 최대 1년 요양급여 정지 - 리베이트 2회 적발 시 해당 품목의 보험목록 삭제 |
| 2017 | 약사법 개정안 시행 | - 경제적 이익 등 제공내역에 관한 지출 보고서 작성 및 보관 의무화 |
| 2022 | 의약품ㆍ의료기기 리베이트 근절 관련 제도 |
- 영업대행사(CSO) 관리 강화 - 영업대행사(CSO) 지출보고서 작성 제도 관리 강화 |
| 2023 | 의약품ㆍ의료기기 리베이트 근절 관련 제도 |
- 영업대행사(CSO)의 지출보고서 작성 의무 부과 - 영업대행사(CSO)의 지출보고서 실태조사 및 결과 공표 |
| 출처 : 보건복지부 |
정부는 2009년 리베이트를 제공한 의약품의 보험 약가를 최고 20% 인하하는 '리베이트 약가연동제'를 실시하였으며, 2010년에는 리베이트를 제공받은 사람에 대한 처벌을 강화하는 '리베이트 쌍벌제'를 도입하였습니다. 2014년 8월부터 시행된 '리베이트 투아웃제'는 리베이트 관련 약제에 대하여 요양급여의 적용을 정지하거나 제외할 수 있도록 하고 있으며, 5년 이내 관련 규정을 두 번 이상 위반 시 제약회사는 해당 요양급여에서 제외될 수 있습니다. 특정 품목에 대한 매출 의존도가 높은 제약회사의 경우, 해당 품목의 적발 시 상당 기간 이익 창출 능력이 저하될 수 있습니다.
| [리베이트 투아웃 급여정지기간] |
| 리베이트 금액 | 급여정지기간 | ||
|---|---|---|---|
| 1회 | 2회 | 3회 | |
| 500만원 미만 | 경고 | 2개월 | 급여제외 |
| 500만원 이상 2,000만원 미만 | 1개월 | 3개월 | |
| 2,000만원 이상 3,500만원 미만 | 2개월 | 4개월 | |
| 3,500만원 이상 5,500만원 미만 | 4개월 | 6개월 | |
| 5,500만원 이상 7,500만원 미만 | 6개월 | 8개월 | |
| 7,500만원 이상 1억원 미만 | 9개월 | 12개월 | |
| 1억원 이상 | 12개월 | 급여제외 | |
| (자료 : 보건복지부) |
또한, 2016년 11월 통과된 '약사법 일부개정 법률안'에서도 리베이트 처벌 수위가 기존 2년 이하의 징역에서 3년으로 강화되었습니다. 실제로 리베이트 적발 시에는 보건복지부 및 식품의약품안전처의 행정처분은 물론, 정부합동 리베이트 전담수사반의 수사를 통해 형사처벌 등이 이루어지고 있으며, 공정거래위원회의 불공정거래 관련 조사, 국세청의 세무조사 등도 함께 진행되고 있습니다. 2018년 1월부터는 경제적 이익 제공에 따른 지출보고서 작성 제도가 시행되어 정부는 제약회사 단위로 제공된 경제적 이익을 체계적으로 관리하고 있습니다.
한편 2018년 9월 기존의 리베이트 투아웃제가 폐지되고 의약품 리베이트를 제공한 약제에 대한 제재처분 변경 및 상향하는 국민건강보험법이 개정되었습니다. 1차 및 2차 위반에 대해서는 각각 약가인하(1차 위반시 최대 20%, 2차 위반시 최대 40%)를 3차 위반 부터는 1년이내 약제 급여정지 처분 등 제약업체의 영업활동을 정지시키는 등 강력한 제재정책을 담고 있습니다. 한편 2019년말 보건당국에 따르면 보건복지부는 제약회사와는 별개로 독자적으로 리베이트를 제공하는 CSO(영업대행업체)에 대한 처벌 대상을 규정하는 등 관련법 개정을 계류하였으며 2021년 7월 개정 약사법에 반영되어 CSO가 리베이트 주체로 추가되었습니다. 이로 인해 약사법,의료법, 의료기기법은 의약품 제조자, 수입자, 도매상 등 의약품 공급자가 의사 등에게 리베이트를 주는 경우에만 처벌하던 기존 규제에서 CSO까지 리베이트 처벌 대상으로 범위가 확되되었습니다.
2022년부터는 의약품 영업대행사(CSO; Contracts Sales Organization)가 의료인 등에게 판매촉진 목적으로 경제적 이익 등을 제공할 시 관련 법령에 따라 처벌하고, 지출보고서 작성 제도를 관리 강화한 '의약품ㆍ의료기기 리베이트 근절 관련 제도'가 시행되었습니다. 또한, 2023년부터는 영업대행사(CSO)에 지출보고서 작성 의무가 부과되고, 작성한 지출보고서에 대한 실태조사 및 결과가 공표되는 등 우회적 불법 리베이트 제공 수단을 차단하고 있습니다.
상기와 같은 리베이트에 관한 정부의 강도 높은 규제는 제약산업 영업환경의 위축으로 이어졌습니다. 한편, 리베이트 규제 강화 추세에 따라 2009년부터 국내 상위 제약회사들의 판매관리비 부담이 큰 폭으로 감소하였습니다. 또한, 2012년 4월 일괄약가 인하제도가 시행되고, 선진화된 마케팅과 영업력으로 과거 리베이트를 통한 업계의 불공정 관행을 극복하려는 상위권 제약회사의 움직임이 나타났으며, 제약회사들의 제네릭을 탈피한 신약개발과 바이오 의약품의 확대를 위한 노력이 지속되고 있습니다. 다만, 품질에 대한 신뢰도와 가격 측면에서 오리지널 제품에 대한 제네릭의 경쟁우위가 높지 않으며, 따라서 마케팅에 대한 의존도가 크게 낮아지기는 어려울 것으로 판단됩니다.
당사는 안전보건경영시스템 및 안전보건 전담조직을 운영하며 종사자를 위한 안전한 사업장 구축(제약업계 최초 ISO45001 인증 기업) 노력을 기울이고 있습니다. 또한 주요 불공정거래정책, 안전보건정책 등 주요정책 공개를 통한 ESG경영 실천의지를 표명하고 있으며 공정거래 자율준수 프로그램을 운영하는 등 윤리경영 내재화를 위한 노력을 기울이고 있습니다.
다만, 당사의 지속적인 내부관리 및 통제 절차에도 불구하고 향후에도 리베이트와 관련한 정부의 엄격한 규제가 지속되고, 당사의 영업활동이 정부 규제에 위배되는 경우 당사의 성장성, 수익성 및 재무안정성에 부정적 영향이 발생할 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
③ GMP(Good Manufacturing Practice; 우수 의약품 제조ㆍ품질관리기준)
GMP(Good Manufacturing Practice, 우수의약품 제조 및 품질관리기준)는 의약품이 일관되게 안전하고 품질에 적합하게 제조되도록 하기 위한 생산 및 품질관리 기준을 의미합니다. 즉, 원료의 입고부터 제조, 포장, 출하에 이르는 모든 과정에서 품질을 보장하기 위한 필수적인 관리 체계입니다. 1963년 미국 FDA의 제정 이후 WHO 및 각국에서 채택되었으며, 우리나라는 「의약품 제조 및 품질관리에 관한 규정」을 통해 국제 기준(PIC/S)을 반영한 GMP 제도를 운영하고 있습니다.
| [GMP 종류별 갱신 주기] |
| 구분 | 승인기관 | 재검토 |
|---|---|---|
|
KGMP (Korea Good |
식품의약품안전처 (한국) |
매 3년 |
|
cGMP (current Good |
미국식품의약국 (Food and DrugAdministration, FDA) |
비정기 |
| 출처 : DART 전자공시시스템 |
당사는 1985년 국내 최초로 KGMP 실시 인가를 받은 이래 식품의약품안전처 등 관계기관이나 규제당국으로부터 GMP 관련 중대한 제재를 받은 사실은 없으며 의약품을 제조, 판매하는 기업으로서, GMP 기준에 부합하는 제조시설 및 품질관리 체계를 갖추고 있으며, 관련 규정에 따라 제조 및 품질관리를 철저히 이행하고 있습니다. 최근, 2022년 11월 약사법 개정에 따라 ‘GMP 원스트라이크 아웃제’가 도입되어, 의약품 임의제조 적발 시 GMP 적합판정이 취소되는 등 규제가 강화되고 있습니다. 향후 GMP 제도의 국제적 기준 강화 또는 관련 법령의 개정에 따라 추가적인 비용 부담 및 설비투자가 발생할 수 있으며, 이에 따라 당사의 영업활동 및 수익성에 영향을 미칠 수 있습니다.
제약산업은 국민 건강과 직결되는 특성으로 인해 정부의 엄격한 통제를 받고 있으며, 약가인하, 리베이트 규제, 제조품질 기준 강화 등 정책 변화가 지속될 경우, 당사의 사업환경에도 부정적인 영향을 미칠 수 있습니다. 이에 따라, 투자자께서는 정부 정책 및 규제 강화가 당사의 성장성과 재무 안정성에 영향을 미칠 수 있다는 점을 고려하여 신중히 투자 결정을 내리시기 바랍니다.
| 마. 지적재산권 침해 등 관련 위험 당사가 영위하고 있는 제약산업은 기술집약적인 산업이며 연구개발성과가 지식재산권 형태로 보호되는 산업입니다. 특허는 산업상 유용한 발명을 한 자가 자신이 이룬 발명의 내용을 공개하는 대가로 일정한 기간 동안 독점적, 배타적 권리를 부여받는 공적 계약의 일종이며, 당사와 같이 제약산업을 영위하는 기업은 핵심 기술 및 제품에 대한 권리를 보호할 수 있는 장치 마련이 필수이기 때문에 특허의 출원 및 등록과 관련제도를 통한 지적재산권의 관리가 중요합니다. 이에 당사 및 당사 주요 자회사는 핵심 기술을 보호하기 위한 특허 출원 및 등록 등으로 지적재산권 침해 관련 위험을 관리하고 있습니다. 그럼에도 불구하고 향후 당사가 보유한 지적재산권을 적절히 보호하지 못하거나 당사가 사용하는 기술과 관련한 지적재산권 관련 분쟁이 발생하는 경우 당사에 대한 신뢰도, 제품 매출에 부정적인 영향을 미쳐 당사의 영업활동 및 수익성이 악화될 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
당사가 영위하고 있는 제약산업은 기술집약적인 산업이며 연구개발성과가 지식재산권 형태로 보호되는 산업입니다. 특허는 산업상 유용한 발명을 한 자가 자신이 이룬 발명의 내용을 공개하는 대가로 일정한 기간 동안 독점적, 배타적 권리를 부여받는 공적 계약의 일종이며, 당사와 같이 제약산업을 영위하는 기업은 핵심 기술 및 제품에 대한 권리를 보호할 수 있는 장치 마련이 필수이기 때문에 특허의 출원 및 등록과 관련제도를 통한 지적재산권의 관리가 중요합니다.
증권신고서 제출 현재 당사가 원고로서 진행 중인 소송은 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소소송 1건, 권리범위확인(특) 3건, 총 4건(2024년말: 4건)입니다. 반면 피고로서 진행중인 소송은 권리범위확인(특) 총 1건(2024년말: 1건)입니다. 신고서 제출일 현재 해당 소송의 최종 결과는 불확실한 바, 투자자께서는 이점 유의하시기 바랍니다.
| 관할법원 | 원고 | 피고 | 소송의 내용 | 소송가액 | 진행상황 |
| 서울고등법원 | 당사 | 보건복지부장관 | 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소 | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 에치케이이노엔 | 당사 | 권리범위확인(특) | - | 계류중 |
이와 별개로 향후 당사가 예상할 수 없는 제3자로부터 당사가 소유하고 있는 특허에 대한 소송 기타 분쟁이 발생할 경우 당사에 대한 신뢰도, 사업개발 및 상업화 이후 제품 매출에 부정적인 영향을 미칠 수 있습니다.
당사 및 당사 주요 자회사는 핵심 기술을 보호하기 위한 특허 출원 및 등록 등으로 지적재산권 침해 관련 위험을 관리하고 있습니다. 그럼에도 불구하고 향후 당사가 보유한 지적재산권을 적절히 보호하지 못하거나 당사가 사용하는 기술과 관련한 지적재산권 관련 분쟁이 발생하는 경우 당사에 대한 신뢰도, 제품 매출에 부정적인 영향을 미쳐 당사의 영업활동 및 수익성이 악화될 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
|
바. 핵심연구인력 유출 관련 위험 |
당사가 영위하고 있는 제약업의 특성상 사업의 연구개발 능력은 매우 중요한 요소이며, 지속적인 연구개발을 위해서는 제약분야에 전문성과 노하우를 가진 연구인력을 확보하여야 합니다. 이는 제약 산업내 업체들에 공통적으로 적용되는 사항으로, 우수한 인력을 유치하기 위한 경쟁은 점차 심화되고 있습니다. 인력 유치 경쟁으로 인해 주요 연구 인력의 유출이 발생할 경우 해당 연구 개발과제가 지연되거나 개발전략을 수정해야 할 가능성이 존재하며, 개발비 부담 등으로 당사의 경쟁력 및 성장성이 악화될 수 있습니다.
당사는 당사 내 연구개발본부 산하 허가등록부, 개발부, 연구소 등의 연구개발 조직을 보유 중이며 당사 자회사 또한 연구개발전문 조직의 성격을 보이고 있습니다. 또한 당사와 같은 제약업체는 연구개발에 있어 핵심 인력을 보유하는 것이 주요 경쟁력 이기에 박사급 인력 13명, 석사급 인력 30명 등 총 65명의 연구인력을 보유하고 있으며 기존 인재들에게 적절한 보상을 제공하여 동기부여함과 동시에 향후에도 인재영입을 위해 최선을 다할 계획입니다. 증권신고서 제출일 기준 당사의 연구인력 현황은 다음과 같습니다.
| [당사 연구인력 현황] |
| (단위: 명) |
| 구분 | 박사 | 석사 | 학사 | 기타 | 합계 |
| 부광약품(주) 연구소 | 3 | 30 | 15 | 1 | 49 |
| Contera Pharma A/S | 9 | - | 6 | - | 15 |
| ProteKt Therapeutics | 1 | - | - | - | 1 |
| JaguAHR Therapeutics | - | - | - | - | - |
| 합계 | 13 | 30 | 21 | 1 | 65 |
| (자료 : 당사제시) |
당사의 핵심 연구인력은 다음과 같습니다.
| [당사 핵심연구인력 현황] |
| 직위 | 성명 | 담당업무 | 최종학위 | 주요 경력 |
| 전무 | 김지헌 | 연구개발담당 | 석사 | 前, (주)GC녹십자 사업개발본부 상무 現, 부광약품(주) 연구개발본부 전무 |
| 이사 | 임진희 | 개발담당 | 석사 | 前, 대웅제약 사업개발본부 팀장 現, 부광약품(주) 연구개발본부 이사 |
한편 당사가 개발 성공한 신약 및 진행중인 연구과제에 대한 세부 내용, 당사 연구개발조직도는 아래와 같습니다.
(1) 개발성공신약
| 구분 | 신약명 | 적응증 | 허가년월 | 허가국가/기관명 | 비고 |
| 신약 | 레보비르 | B형 간염치료제 | 2006.11 | 한국/MFDS | 국내 제11호 신약 |
| 개량신약 | 덱시드 | 당뇨병성신경병증 | 2013.11 | 한국/MFDS | - |
| 신약 | 라투다정 | 조현병, 양극성 우울증 | 2023.11 | 한국/MFDS | 국내 8월 출시 |
| (출처 : 당사 분기보고서) |
- 신약명 : 레보비르, Levovir(제품명: 레보비르캡슐, Clevudine)
| 구분 | 합성신약 |
| 적응증 | 만성B형 간염치료제 |
| 작용기전 | 바이러스 DNA 합성 억제 |
| 제품의 특성 | 간 조직 내에서 오랜 반감기를 가지므로, 투여 중단 후에도 일정 기간 항바이러스 효과가 지속 |
| 진행 경과 | 2006-11-22 국내 허가 |
| 경쟁 제품 | Lamivudine(GSK), Adefovir dipivoxil(GSK), Entecavir(BMS) |
| 시장규모 | B형간염치료제 국내시장 2,846억원(UBIST, 2023년) |
| 기타사항 | 국산 신약 11호 |
- 신약명 : 덱시드, Dexid(제품명: 덱시드정, R-thioctic acid tromethamine)
| 구분 | 개량신약 |
| 적응증 | 당뇨병성 신경병증 치료제 |
| 작용기전 | 산화 스트레스 감소, 신경 세포 보호 |
| 제품의 특성 | 강력한 항산화제로서 인슐린 감수성을 향상시켜 혈당 조절을 보조하며, 병인치료제로 사용 및 증상치료제와 병용 가능 |
| 진행 경과 | 2013-11-21 국내 허가 |
| 경쟁 제품 | Pregabalin(Pfizer), Gabapentin(Pfizer) |
| 시장규모 | Thioctic acid 국내시장 650억원(IQVIA, 2023년) |
| 기타사항 | 이성질체(Thioctic acid)에서 약효성분만을 분리하여 세계 최초로 개발하여 투여용량 및 부작용 감소 |
- 신약명 : 라투다, Latuda(제품명: 라투다정, Lurasidone hydrochloride)
| 구분 | 합성신약 |
| 적응증 | 조현병 치료제 |
| 작용기전 | D2 receptor antagonist, 5-HT2A, 5-HT7 receptor antagonist |
| 제품의 특성 | 조현병 및 양극성 장애 우울 증상을 빠르고 지속적으로 개선시키며, 이상반응(체중증가)이 감소 |
| 진행 경과 |
국내 가교 3상 임상시험 별도 수행 2023-11-22 국내 허가 |
| 경쟁 제품 | Aripiprazole(Otsuka), Paliperidone(Janssen), Risperidone(Janssen) |
| 시장규모 | 조현병치료제 국내시장 1,904억(IQVIA, 2023년) |
| 기타사항 |
미국, 유럽, 캐나다 일본 등 전세계적으로 장기간 사용 경험과 충분한 노출이 있는 제품 Metabolic side effect가 적어 복약 순응도 및 유지 치료에 효과적 |
(2) 진행중인 연구과제
| 연구과제 | 적응증 |
연구 연도 |
진행 경과 | 파트너사/공동개발사 | 개발사 | 비고 | |
| 단계(국가) | 승인년도 | ||||||
| JM-010 | 파킨슨병 환자의 Dyskinesia 치료제 |
2013년 | Phase 1 완료(독일) Phase 2a 완료(남아공) Phase 2 완료(유럽,한국) Phase 2 종료(미국) |
2016년 2015년 2018년 2020년 |
(덴마크) Contera Pharma A/S | (한국) 부광약품(주) (덴마크) Contera Pharma A/S |
- |
| CP-012 | 파킨슨병 환자의 Morning Akinesia (아침무동증) 치료제 |
2013년 | Phase 1a 완료(유럽) Phase 1b 진행(유럽) |
2023년 - |
- | (덴마크) Contera Pharma A/S | - |
| (출처 : 당사 분기보고서) |
- 품목: JM-010
| 적응증 | 파킨슨병 환자의 Dyskinesia 치료제 |
| 작용기전 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 제품의 특성 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 진행경과 |
- 남아공에서 글로벌 임상 전기 2상 (PoC) 완료 (2015년 11월) - 유럽에서 신제형의 Human pharmacokinetic study 완료 (2016년 9월) - 독일/프랑스/스페인 : 임상 2상 승인 완료 및 2019년 4월 임상 개시 모임 진행 |
| 향후계획 | - 임상결과를 바탕으로 활용방안을 검토 중 |
| 경쟁제품 | - |
| 관련논문 등 | - |
| 시장규모 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 기타사항 | 한국에서 개발단계희귀의약품 지정 (2017년 1월) |
| (자료 : 당사 분기보고서) |
- 품목: CP-012
| 적응증 | 파킨슨병 환자의 Morning Akinesia (아침무동증) 치료제 |
| 작용기전 | 개발 초기 단계로 Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 제품의 특성 | 개발 초기 단계로 Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 진행경과 | 유럽 임상 1a상 진행 완료 (2023년 9월) 유럽 임상 1b상 진행 중 |
| 향후계획 | 개발 초기 단계로 예측 불가 |
| 경쟁제품 | - |
| 관련논문 등 | - |
| 시장규모 | 개발 초기 단계로 예측 불가 |
| 기타사항 | - |
| (자료 : 당사 분기보고서) |
| [당사 연구개발 조직도] |
 |
|
연구개발부서 조직도 |
| (자료 : 당사 분기보고서) |
현재 당사는 다양한 신약 및 의약품을 개발중에 있으며, 개발된 의약품을 판매함으로써 사업을 영위하고 있습니다. 따라서 당사의 사업에 있어서 의약품 개발을 위한 연구활동은 매우 중요합니다. 결국 당사의 매출 성장 및 외형확대를 위해서는 우수한 연구개발 인력을 유치해야하고 기존의 인력을 유지해야 합니다.
당사는 인력관리의 중요성을 인지하고 업무 만족도 증진, 회사의 비전 공유, 지속적인 교육을 통한 자기 계발 프로그램 강화, 업무실적에 근거한 인센티브 제도 등 각종 복리후생제도 강화 등을 통해 직원들의 애사심 고취에 힘쓰고 있으며 향후에도 임직원의 다양한 복지 혜택을 확대할 계획입니다.
다만, 이러한 당사의 노력 및 정책에도 불구하고 제약산업의 경쟁심화에 따른 우수인력 스카우트 등에 따라 핵심인력이 경쟁회사 또는 다른 산업분야로 이탈할 수 있으며, 이러한 경우 당사 핵심 기술 노하우의 유출 등은 당사의 경쟁력을 약화시킬 수 있으며 이는 당사 영업활동 및 수익성에 부정적인 영향을 미칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| 사. 신약 개발 실패 및 연구개발비용 증가에 따른 수익성 악화 위험 당사가 영위하는 제약산업은 지속적인 연구개발 및 투자의 결과가 기업의 성과와 연결되는 특성을 가지고 있으며, 신제품 및 신약개발을 위해서는 비용 및 시간이 투자되어야 하는 필수 요소를 지니고 있습니다. 신약이 상업화되기까지는 막대한 비용과 시간이 필요합니다. 특히, 임상시험에 진입하여도 최소 8-9년이 소요되며 그에 필요한 비용이 요구됩니다. 또한, 임상시험을 진행한다고 하더라도 시험결과 효능이 부족하거나 안전성 평가에 적합하지 못한 결과가 나올 경우 해당 신약의 연구개발은 중단될 수 있으며, 이러할 경우 당사 및 주요 자회사의 비용 및 시간 투자에도 불구하고 투자비용의 매몰 가능성이 존재합니다.연구개발 전략이 계획대로 진행되지 않거나 자금조달에 어려움을 겪어 신약 개발에 실패하거나 지연될 경우 다른 형태로의 라이센스 아웃 가능성은 불확실성이 존재하며, 투입된 연구개발비 회수가 되지 않아 당사의 성장성, 수익성 및 재무안정성에 부정적인 영향을 미칠 수 있으니, 투자자께서는 이 점 유의하시기 바랍니다. |
당사가 영위하는 제약산업은 지속적인 연구개발 및 투자의 결과가 기업의 성과와 연결되는 특성을 가지고 있으며, 신제품 및 신약개발을 위해서는 비용 및 시간이 투자되어야 하는 필수 요소를 지니고 있습니다. 신약이 상업화되기까지는 막대한 비용과 시간이 필요합니다. 특히, 임상시험에 진입하여도 최소 8-9년이 소요되며 그에 필요한 비용이 요구됩니다. 또한, 임상시험을 진행한다고 하더라도 시험결과 효능이 부족하거나 안전성 평가에 적합하지 못한 결과가 나올 경우 해당 신약의 연구개발은 중단될 수 있으며, 이러할 경우 당사 및 주요 자회사의 비용 및 시간 투자에도 불구하고 투자비용의 매몰 가능성이 존재합니다.
| [임상시험 구분] |
| 구분 | 목적 | 내용 |
|---|---|---|
| Phase 1 (1상) |
ㆍ안전성 검토 ㆍ내약성 평가 ㆍPK/PD 정의/서술 ㆍ치료효과 추정 |
ㆍ용량-내약성 임상시험 ㆍ안전용량 범위와 부작용 확인 ㆍ체내 약물 동태 검토 ㆍ1a: SAD, 1b: MAD |
| Phase 2 (2상) |
ㆍ단기 유효성/안전성 검토 ㆍ목표 적응증에 대한 탐구 ㆍ후속 시험을 위한 용량 추정 ㆍ치료확증 시험을 위한 시험설계, 평가항목, 평가방법에 대한 근거 제공 |
ㆍ용량-반응 탐색 임상시험 ㆍ소수의 환자에서의 비교적 단기간에 걸친 초기 임상시험 ㆍ2a: 약효확인, 유효용량 검토 ㆍ2b: 약효입증, 유효용량 확인, 유효성 및 안전성의 균형 검토 |
| Phase 3 (3상) |
ㆍ안전성, 유효성 재확인 ㆍ임상적용을 위한 Risk/Benefit의 상대평가 근거제공 ㆍ용량과 반응에 대한 관계 확립 ㆍ효과에 대한 검증 |
ㆍ무작위 배정에 의한 용량-반응 임상시험 ㆍ유효성 확립을 위한 적절하고 잘 통제된 임상시험 ㆍ이환율/사망률을 위한 임상시험 ㆍ충분한 환자에서 유효성 및 안전성 확립 ㆍ대조군을 이용한 비교 임상시험 ㆍ대규모 임상시험 |
| Phase 4 (4상, PMS) |
ㆍ시판 후 안전성 조사 및 추가 임상시험 ㆍ일반 또는 특정 대상군/환경에서 Risk/Benefit에 대한 이해 ㆍ흔하지 않은 이상반응 확인 ㆍ추천되는 용량을 확인 ㆍ모든 시험 디자인이 가능 |
ㆍ장기투여시 부작용 검토 ㆍ안전성 재확립 ㆍ새로운 적응증 등 탐색 연구 ㆍ대조군을 이용한 유효성 임상시험 ㆍ이환율/사망률에 대한 임상시험 ㆍ부가적인 평가 항목에 대한 임상시험 ㆍ약물경제학적 측면의 임상시험 |
| 출처: 한국식품의약처(https://www.mfds.go.kr) | |
| 주1) | 약물의 농도-반응 관계를 PK/PD라고 합니다. PK(Pharmacokinetics 약동학)는 약물의 흡수, 분포, 생체 내 변화 및 배설을 연구합니다. PD(Pharmacodynamics 약력학)는 생체에 대한 약물의 생리학적 및 생화학적 작용과 그 작용 기전, 즉 약물이 일으키는 생체의 반응을 주로 연구함 |
| 주2) | SAD(단회용량상승, single ascending dose) : 단회용량을 투여한 후 안전성과 내약성을 확인함 |
| 주3) | MAD(다중용량 상승, multiple ascending dose) : 반복 투여를 통해 더 높은 용량으로 증량해가면서 최대 내약 용량을 확인함 |
한 개의 신약이 나오기 위해서는 여러 단계를 거치게 되는데, 먼저 신약 후보물질을 도출하기 위한 탐색 과정을 거칩니다. 이 과정에서는 신약의 효능이나 작용기전을 기반으로 신약개발 대상물질을 선정합니다. 유효물질(hit compound), 선도물질(lead compound)을 거쳐 신약 후보물질이 선정되면 후보물질의 안정성과 효과를 확인하기 위해 동물 모델을 대상으로 전임상시험(pre-clinical trial)을 진행합니다. 전임상시험을 통해 후보물질의 효과와 안전성을 검증하면 허가기관에 임상시험 허가신청(IND : Investigational New Drug Application)을 하고, 사람을 대상으로 약물의 효과의 부작용을 확인하는 임상시험(clinical trial)을 수행합니다. 임상시험을 마친 후에는 식약처에 임상시험 결과를 제출하게 되는데, 이를 신약 허가신청(NDA : New Drug Application)이라고 합니다. 신약 허가신청이 정상적으로 이루어지면, 제4상 임상시험으로 분류되는 시판후안전성조사(PMS : Post-Market Surveillance)를 통해 임상시험에서 발견하기 어려웠던 부작용에 대해서 추적 조사를 수행합니다.
임상 1상은 주로 정상인을 대상으로 약물의 독성테스트를 합니다. 소규모(약 20명에서 100명)의 건강한 지원자를 대상으로 시험하는 단계로서 의약품이 사람에게서 안전한지 여부를 확인하는 것을 목적으로 실시되며, 약물의 효과는 평가하지 않고 안전성에 주로 초점을 맞추기 때문에 대부분 성공률이 높습니다. 임상 2상은 인체(환자)를 대상으로 부작용 뿐 아니라 약효를 테스트하는 첫 번째 관문이기 때문에 성공률이 제일 낮을 수밖에 없습니다. 이는 임상시험용 의약품이 기대된 작용기전(mechanism)에 따라 작용되는지 검토하고, 의약품을 사용에 있어서 최적 용량(dose strength)과 투약방법(schedules)을 분석하는 단계입니다.
임상 3상은 임상 2상과 같이 환자를 대상으로 약효와 부작용을 보는 단계이지만, 환자 수가 훨씬 크고 약의 dose(복용량)를 결정하는 단계입니다. 임상 3상은 임상 2상에서 적은 수의 환자를 대상으로 이미 약효와 부작용을 테스트했기 때문에 비교적 성공 확률이 높습니다. 제3상 임상시험은 대규모 환자를 대상으로 하는 시험으로 연구자는 후보의약품의 안전성과 유효성 및 전체적인 benefit-risk 관계에 대한 통계학적으로 유의한 데이터(significant data)를 만들기 위해서 약 1,000명에서 5,000명의 환자를 대상으로 연구가 실시됩니다. 이 단계는 의약품으로서 안전성과 유효성 여부결정의 핵심단계로서 적정한 의약품 사용을 보증하기 위한 다른 의약품과 상호작용 정보 등 표시사항의 기초가 됩니다. 임상시험동안 실생산 규모의 생산계획, 식약청에 품목허가를 받기 위해 필요하고 복잡한 서류준비 등을 위한 품질등에 관한 중요한 연구가 많이 수행됩니다. 유효물질 수준에서 5,000개에서 10,000개의 화합물이 연구개발(R&D)의 파이프라인으로 들어가지만 전임상단계에서 약 250개의 연구를 거쳐 결국 1개의 승인을 받게 되며, 식품의약품안전처에 따르면 이러한 신약개발 과정을 거쳐 환자가 이용할 수 있을 때까지 소요되는 기간과 비용은 약 10년~15년의 연구개발기간과 비용은 800백만달러에서 13억달러($1.3 billion)이상으로 추정하고 있습니다.
2011년부터 2020년까지 Biomedtracker, Pharmapremia가 조사한 바에 따르면 임상 3상 성공률은 약 57.8%입니다. 임상 1상부터 임상 승인(LOA)까지 성공적으로 진입하는데 평균 10.5년이 소요되며, 임상 단계별로는 임상 1상 2.3년, 임상 2상 3.6년, 임상 3상 3.3년, 허가승인단계 1.3년이 각각 소요됩니다.
| [임상 단계별 소요기간] | ||
|
||
| 출처: 한국바이오협회, 2011-2020년 임상 개발 성공률과 기여 요인 분석 |
당사 및 당사 자회사가 연구개발을 진행 중인 신약의 세부내역은 다음과 같습니다.
(1) 개발성공신약
| 구분 | 신약명 | 적응증 | 허가년월 | 허가국가/기관명 | 비고 |
| 신약 | 레보비르 | B형 간염치료제 | 2006.11 | 한국/MFDS | 국내 제11호 신약 |
| 개량신약 | 덱시드 | 당뇨병성신경병증 | 2013.11 | 한국/MFDS | - |
| 신약 | 라투다정 | 조현병, 양극성 우울증 | 2023.11 | 한국/MFDS | 국내 8월 출시 |
| 출처 : 당사 사업보고서 |
(2) 진행중인 연구개발과제
당사는 해외 자회사 포함 다수의 파이프라인을 보유하고 있으며 당사는 임상 2건을 진행하였으나 이중 JM-010이 중단되어 현재 임상이 진행중인 건은 1건 입니다.
 |
|
당사 파이프라인 요약 |
| 출처 : 당사 IR자료 |
- 품목: JM-010
| 적응증 | 파킨슨병 환자의 Dyskinesia 치료제 |
| 작용기전 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 제품의 특성 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 진행경과 |
- 남아공에서 글로벌 임상 전기 2상 (PoC) 완료 (2015년 11월) - 유럽에서 신제형의 Human pharmacokinetic study 완료 (2016년 9월) - 독일/프랑스/스페인 : 임상 2상 승인 완료 및 2019.4월 임상 개시 모임 진행 |
| 향후계획 | 임상결과를 바탕으로 활용방안을 검토 중 |
| 경쟁제품 | - |
| 관련논문 등 | - |
| 시장규모 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 기타사항 | 한국에서 개발단계희귀의약품 지정 (2017년 1월) |
| 출처 : 당사 분기보고서 |
- 품목: CP-012
| 적응증 | 파킨슨병 환자의 Morning Akinesia (아침무동증) 치료제 |
| 작용기전 | 개발 초기 단계로 Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 제품의 특성 | 개발 초기 단계로 Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 진행경과 | 유럽 임상 1a상 진행 완료 (2023년 9월) 유럽 임상 1b상 진행 중 |
| 향후계획 | 개발 초기 단계로 예측 불가 |
| 경쟁제품 | - |
| 관련논문 등 | - |
| 시장규모 | 개발 초기 단계로 예측 불가 |
| 기타사항 | - |
| 출처 : 당사 분기보고서 |
(3) 기타
당사는 글로벌 오픈 이노베이션 전략의 일환으로 다양한 해외(자회사 및 지분투자 포함)사와 협업을 진행하고 있습니다. 이는 천문학적 비용이 투입되는 신약개발을 다양한 회사와의 협업을 통하여 비용, 수익, 리스크 및 향후 임상성공에 따른 benefit을 공유하고자 하는 취지로 신약개발사에서 통상적으로 취하고 있는 R&D 전략 입니다. 그결과 Contera Pharma A/S, ProteKt Therapeutics, JaguAHR Therapeutics를 자회사로 지분 투자 중이며 이외 다양한 글로벌 신약업체에 지분을 투자하고 있습니다.
 |
|
글로벌 이노베이션 전략(요약) |
| 출처 : 당사 IR자료 |
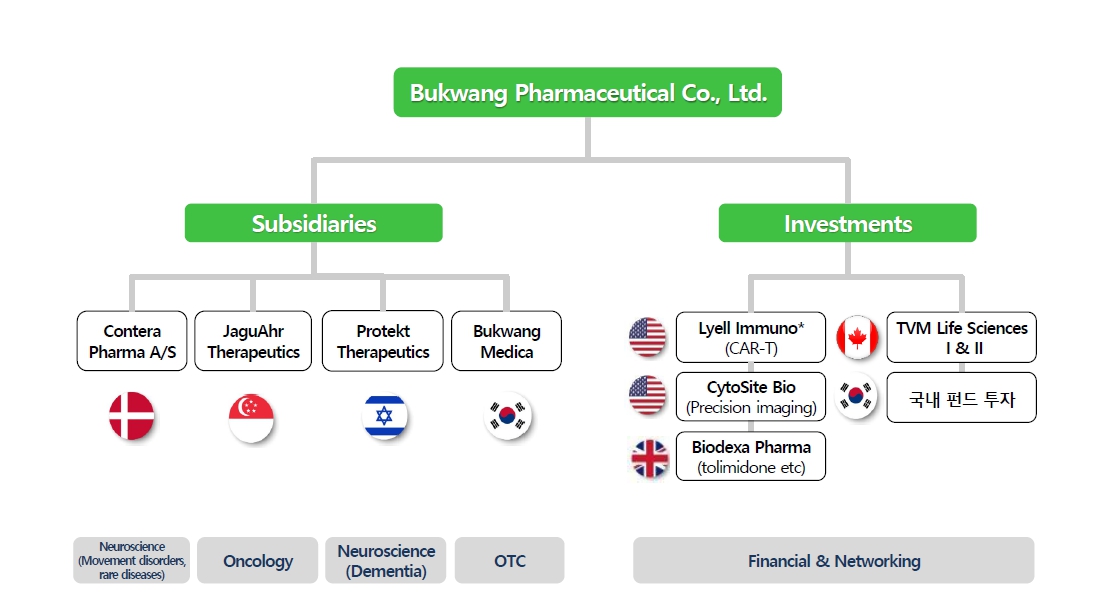 |
|
글로벌 이노베이션 전략에 따른 지분도 |
| 출처 : 당사 IR자료 |
(1) Contera Pharma: Novo Nordisk, Novartis 전직 연구원들에 의해 설립 (Novo A/S, SEED Capital에서 투자)되었으며 CP-012 (파킨슨 아침무동증 치료제) 및 복수 ASO 프로그램 (희귀 유전질환)을 비롯한 신경질환 파이프라인 개발 중심의 연구활동 진행 중입니다. 글로벌 CNS 전문 톱 기업 임원 출신 대표이사 및 임원을 선임하였으며 최첨단 Small molecule, RNA 기반 치료제에 입증된 실적을 가진 연구진으로 연구소를 설립하는 등 성공적인 임상을 추진중에 있습니다. 본 증권신고서 제출일 현재 당사 지분율은 99.33% 입니다.
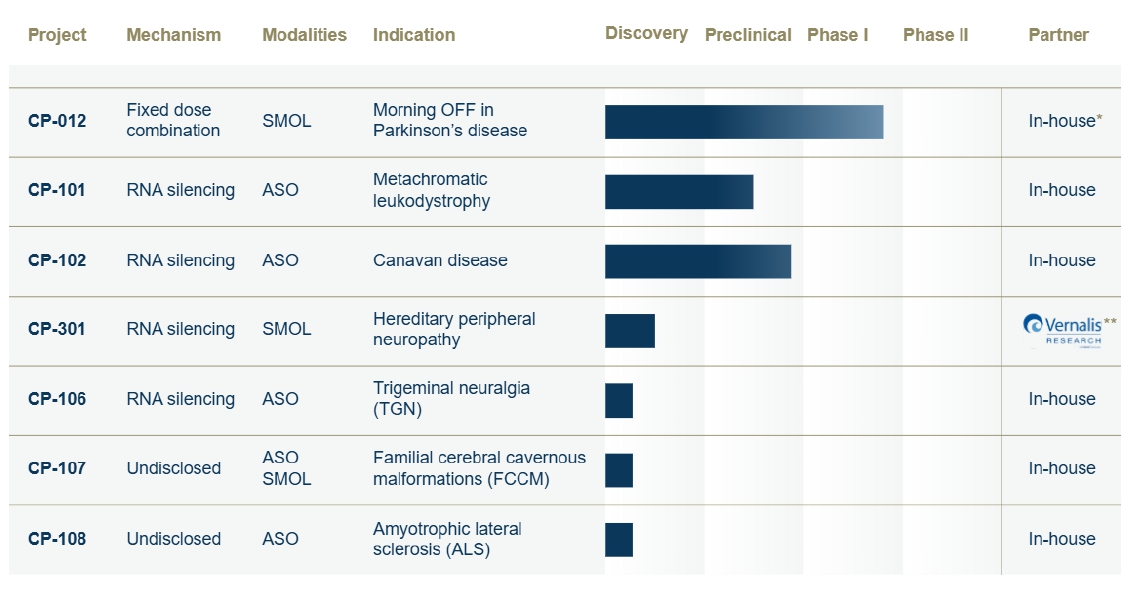 |
|
contera pharma 파이프라인 요약 |
| 출처 : 당사 IR자료 |
(2) JaguAHR Therapeutics: 싱가포르 면역치료 전문 제약사 아슬란 (ASLAN
Pharmaceuticals)과의 합작회사로 JaguAHR Therapeutics는 아슬란으로부터 '아릴탄화수소수용체(AhR) 길항제' 관련 기술 모두를 이전 받아 전세계를 대상으로 고형암을 타겟으로 하는 새로운 면역치료제를 개발하고 있습니다. 본 증권신고서 제출일 현재 당사 지분율은 75.02% 입니다.
(3) Protekt Therapeutics: 신경퇴행 및 신경염증성 질환의 새로운 치료제를 개발하는데 주력하고 있는 이스라엘 소재의 바이오테크 회사로 2019년에 첫 지분 투자 후, 2023년 당사가 인수하였습니다. 본 증권신고서 제출일 현재 당사 지분율은 96.53% 입니다.
당사의 최근 4년간 연결기준 연구개발비용은 다음과 같습니다.
| [당사 연결기준 연구개발비 현황] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 | |
|---|---|---|---|---|---|---|---|
| 비용의성격별 분류 | 원재료비 | 904 | 695 | 4,147 | 3,584 | 2,900 | 2,677 |
| 인건비 | 3,081 | 2,540 | 10,537 | 10,021 | 6,565 | 6,919 | |
| 감가상각비 | 203 | 181 | 1,052 | 587 | 216 | 214 | |
| 위탁용역비 | 870 | 2,564 | 9,317 | 14,754 | 12,201 | 12,840 | |
| 기타 | 680 | 1,225 | 3,333 | 10,570 | 7,501 | 4,524 | |
| 연구개발비용 합계 | 5,739 | 7,205 | 28,386 | 39,516 | 29,383 | 27,174 | |
| 회계처리내역 | 판매비와 관리비 | 4,452 | 6,056 | 23,430 | 34,551 | 24,274 | 22,465 |
| 제조경비 | 1,287 | 1,149 | 4,956 | 4,965 | 5,108 | 4,709 | |
| 개발비(무형자산) | - | - | - | - | - | - | |
| 회계처리금액 계 | 5,739 | 7,205 | 28,386 | 39,516 | 29,382 | 27,174 | |
| 정부보조금 | - | - | - | - | - | - | |
| 연구개발비용 합계 | 5,739 | 7,205 | 28,386 | 39,516 | 29,3832 | 27,174 | |
| 연구개발비 / 매출액 비율 | 12.00% | 20.95% | 17.73% | 31.38% | 15.39% | 14.89% | |
| [연구개발비용합계÷당기매출액×100] | |||||||
| (자료 : 당사 사업보고서 및 분기보고서) |
2024년 12월 발표된 한국제약바이오협회 제약바이오산업 데이터북에 따르면, 의약품제조업 및 자연과학 연구개발업을 영위하는 상장사의 2023년 평균 매출액 대비 연구개발비 수준은 12.5%로, 당사는 이보다 높은 수준의 연구개발비를 집행하고 있습니다. 다만, 2023년 JM-010 임상개발로 인해 비경상적으로 높은 규모의 연구개발비중이 집행된 점 고려 시 당사의 평균적인 매출액 대비 연구개발비 비중은 14%~17% 수준으로 연구개발업을 영위하는 상장사 평균 대비 소폭 높은 수준임을 확인할 수 있습니다.
상기와 같이 신약 연구개발을 통하여 가시적인 결과가 나오는 제품의 상용화 단계까지 많은 비용과 시간이 요구되며, 연구개발 과정에서 수많은 변수가 발생할 수 있습니다. 만약 변수들을 미리 찾아내어 극복하지 못한다면, 지출했던 연구개발 비용 및 시간 등의 손실이 발생할 수 있으며 향후 제한적인 국내 시장 등의 한계를 극복하기 위한 연구개발활동이 증가할 수 있습니다. 당사가 진행중인 파이프라인 중 JM-010은 2024년 5월 위약군 대비 통계적으로 유의미한 효과가 나오지 않은 것으로 나타나 임상이 종료된 바 있습니다. 다만, 여러 인종을 대상으로 진행한 해당 임상자체는 종료되었지만 한국인 대상으로는 유효성이 어느정도 확인된 바, 유사 인종(아시아)을 대상으로 임상을 계획중인 기업에게 라이센스 아웃을 검토 중입니다. 실제 당사는 과거 라이센스인한 MLR-1023 관련 2형 당뇨 임상은 종료되었으나 멜리어사가 1형 당뇨로 임상 진행할 목적으로 당사의 MLR-1023 아시아(일본 제외) 권리 및 당사의 제조특허를 포함하여 라이센스 아웃하였으며 당사가 향후 관련 수익의 50%를 수령하는 Benefit sharing agreement를 체결한 바 있습니다.
그럼에도 불구, 연구개발 전략이 계획대로 진행되지 않거나 자금조달에 어려움을 겪어 신약 개발에 실패하거나 지연될 경우 다른 형태로의 라이센스 아웃 가능성은 불확실성이 존재하며, 투입된 연구개발비 회수가 되지 않아 당사의 성장성, 수익성 및 재무안정성에 부정적인 영향을 미칠 수 있으니, 투자자께서는 이 점 유의하시기 바랍니다.
| 아. 혁신형 제약기업 제외의 위험 당사는 증권신고서 제출일 현재 기준 혁신형 제약기업으로 인증되어 있습니다. 혁신형 제약기업이 제조한 의약품에 대하여 요양급여 약제의 상한금액 가산 등 대통령령으로 정하는 우대를 제공하도록 하는 조항이 신설되었으며 혁신형 제약기업에 대한 홍보 효과 및 인지도를 제고하기 위해 인증마크 사용 근거 및 벌칙 조항이 마련되었습니다. 하지만 보건복지부는 정부가 공인한 혁신역량 보유 기업이라는 인증 효과로 인해 국내외 투자유치, 기술 및 판매 제휴, 금융기관 자금조달 등의 측면에서 다양한 간접 수혜가 있을 것으로 예상하고 있지만, 국내 중상위권 제약사 대부분이 혁신형 제약기업으로 인증되어 있는 만큼 각 사에 돌아가는 혜택에 따라 차별화가 발생하기는 어려울것으로 판단됩니다. 또한, 3년 뒤 재인증 심사 시 연구개발 투자실적 등에 따라 특별법상 요건을 충족하지 못하여 인증이 연장되지 못할 가능성도 존재합니다. 이 점 투자자께서는 유의하시기 바랍니다. |
당사는 증권신고서 제출일 현재 기준 혁신형 제약기업으로 인증되어 있습니다. 보건복지부의 '약가제도 개편 및 제약산업 선진화' 방안에서는 약가인하 이외에도 일정 수준 이상의 R&D 투자를 집행하고 있는 제약사들을 '혁신형 제약기업'으로 선정하여 선별적 약가우대 및 세제혜택, 자금조달 지원 등을 통해 글로벌 신약개발 역량을 강화하는 것을 목표로 삼고 있습니다. 2024년 12월 28일 기준 정부가 인증한 혁신형 제약기업은 총 49개사로, 혁신형 제약기업 선정 기업은 다음과 같습니다.
| [혁신형 제약기업 선정 기업] |
| 구 분 | 기 업 명 |
| 일반제약사(33) | SK바이오사이언스, SK바이오팜, 녹십자, 동구바이오제약, 동국제약, 동아ST, 동화약품, 대웅제약, 대원제약, 대화제약, 메디톡스, 보령, 부광약품, 삼양홀딩스, 셀트리온, 신풍제약, 에스티팜, 에이치케이이노엔, 온코닉테라퓨틱스, 유한양행, 이수앱지스, 일동제약, 태준제약, 파미셀, 한국비엠아이, 한국팜비오, 한독, 한림제약, 한미약품, 한올바이오파마, 현대약품, LG화학, SK케미칼 |
| 바이오 벤처사(12) | 브릿지바이오테라퓨틱스, 비씨월드제약, 알테오젠, 올릭스, 에이비엘바이오, 제넥신, 지아이이노베이션, 코아스템, 큐로셀, 큐리언트, 테고사이언스, 헬릭스미스 |
| 외국계 제약사(4) | 암젠코리아, 한국아스트라제네카, 한국얀센, 한국오츠카 |
| [혁신형 제약기업 인증기준의 세부 평가기준 및 심사항목] |
| 평가기준 | 심사항목 | 평가기준 | 심사항목 |
|
인적ㆍ물적 투입 (37.5) |
연구개발 투자실적 |
기술적ㆍ경제적ㆍ (25) |
의약품 특허 및 기술이전 성과 |
| 연구인력 현황 | 해외진출 성과 | ||
| 연구ㆍ생산 시설 현황 | 우수한 의약품 개발ㆍ보급 성과 | ||
|
연구개발 활동의 혁신성 (25) |
연구개발 비전 및 중장기 추진전략 |
기업의 사회적 책임 및 윤리성, 투명성 (12.5) |
기업의 사회적 책임 및 윤리성 |
| 국내외 대학ㆍ연구소ㆍ기업 등과 제휴ㆍ협력 활동 | |||
| 외부감사 등 경영의 투명성 | |||
| 비임상ㆍ임상 시험 및 후보물질 개발 수행 |
| (자료 : 보건복지부 2024년 12월 28일 기준) |
위의 인증 기준에 따라 인증된 기업에게는 향후 3년간 '제약산업 육성 및 지원에관한 특별법' 등에 따라 국가 R&D 사업 우선 참여, 세제 지원 혜택, 약가 결정시 우대 등의 혜택이 부여될 계획입니다. 또한 보건복지부는 인증 연장 심사를 통하여 인증 전후 제도 운영에 따른 정책 효과 점검 결과, 산업구조 선진화, 글로벌 신약 개발, 해외진출 확대 등 측면에서 일정 부분 성과를 보인 것으로 판단하고 있습니다. 보건복지부는 정부가 공인한 혁신역량 보유 기업이라는 인증효과로 인해 국내외 투자유치, 기술 및 판매 제휴, 금융기관 자금조달 등의 측면에서 다양한 간접 수혜가 있을 것으로 예상하고 있지만, 중상위권 제약사 대부분이 혁신형 제약기업으로 선정된 만큼 각 사에 돌아가는 혜택에 따라 차별화가 발생하기는 어려울 것으로 판단되며, 3년 뒤 재인증 심사시 연구개발 투자실적 등에 따라 특별법상 요건을 충족하지 못하여 인증이 연장되지 못할 가능성도 존재합니다.
| [혁신형 제약기업 지원제도] |
| 지원 사항 | 주요 내용 |
| R&D 우대 |
혁신형 제약기업의 정부 R&D 참여시 가점 부여 - 혁신형 제약기업이 신약 개발 관련 정부 R&D 과제 신청 시, 선정평가에 가산점 부여 * 국가신약개발사업(2% 가산), 범부처재생의료기술개발사업(2점 가산) 등 |
| 세제 지원 |
연구인력개발 비용에 대한 법인세액 공제 * 조세특례제한법 제10조제1항 의약품 품질관리 개선 시설투자비용 세액공제 * 조세특례제한법 제24조 |
| 약가 우대 |
신규등재 제네릭 의약품 및 개량신약복합제 보험약가 우대 * 혁신형제약기업은 68%(일반기업 59.5%)로 최대 5년간 가산 바이오시밀러 보험약가 우대 * 최초등재품목 약가의 70% → 80%로 최대 5년간 10%p 가산 실거래가 약가인하율 30% 또는 50%* 감면 * 해당 연도 R&D 투자액이 500억원 이상 또는 매출액 3,000억원 이상이면서 R&D 투자비율 10% 이상인 혁신형 제약기업의 의약품 사용량-약가 연동제 환급제(3+3년) |
| 규제 완화 |
연구시설 건축시 입지 지역 규제 완화 및 부담금 면제(제약산업법 규정) * 개발 부담금, 교통유발부담금, 대체산림자원조성비, 대체초지조성비 면제 |
| 인허가 지원 |
의약품 우선심사 대상 지정 * 약사법 제35조의4 제2항 제2목 |
| 사업 지원 |
혁신형 제약기업의 글로벌 진출 사업 참여시 가점 부여 - 혁신형 제약기업의 전략적 해외시장 진출 및 글로벌 경쟁력 향상을 위한 지원 사업* 신청 시, 선정평가에 가산점(5점) 부여 * 제약산업 전주기 글로벌 진출 강화 지원 사업, K-블록버스터 미국 진출 지원 사업, 국산 백신ㆍ원부자재ㆍ장비 성능시험 지원 사업 |
| 정책자금 융자 |
제약·바이오기업 대상 대출상품별 우대금리 적용(수출입은행) - 수출촉진자금대출: 수출용 의약품 국내외 임상 2상 이상 프로젝트에 대한 장기 저리의 임상자금 지원 - 수출성장자금대출: 수출실적 보유 중소ㆍ중견기업 앞 수출자금을 과거 수출실적 범위 내에서 일괄 지원(6개월 ~ 3년) - 수입자금대출: 원료의약품 등 국민 생활의 안정, 고용증대 및 수출촉진 등에 기여하는 물품에 대한 수입자금 지원 - 해외사업관련대출: 해외법인 설립 및 인수 등 해외사업을 위한 투자자금 또는 사업자금 대출(이상 수출입은행) |
|
코스닥 상장기업의 |
우수 기술보유 기업 등에 대한 매출액 요건 면제(금융위) - 기술특례ㆍ성장성특례로 진입한 바이오 기업 중 혁신형 제약기업에 대해 매출액 30억 원 요건 면제 |
| (자료 : 보건복지부 2024년 12월 28일 기준) |
혁신형 제약기업이 제조한 의약품에 대하여 요양급여 약제의 상한금액 가산 등 대통령령으로 정하는 우대를 제공하도록 하는 조항이 신설되었으며 혁신형 제약기업에 대한 홍보 효과 및 인지도를 제고하기 위해 인증마크 사용 근거 및 벌칙 조항이 마련되었습니다. 이 조항에는 임상시험 기반 조성을 위하여 관련 제도의 조사 및 연구, 전문인력의 양성 등을 지원하는 임상시험지원센터를 설치 및 운영할 수 있는 근거가 명시됐으며, 혁신형 제약기업 인증 지위승계 절차 기준 등도 개정되었습니다.
또한 미국 무역대표부(USTR)는 2025년 3월 31일 발표한 ‘2025 무역장벽보고서’를 발표하며 한국의 약가 정책과 혁신형 제약기업 인증 기준 투명성 부족이 미국 기업의 시장 진입을 방해하는 원인으로 분석하며 한국의 무역 장벽 개선을 촉구했습니다. 이로 인해 혁신형 제약기업으로 인정되기 위한 요건이 강화될 가능성이 존재합니다.
하지만 보건복지부는 정부가 공인한 혁신역량 보유 기업이라는 인증 효과로 인해 국내외 투자유치, 기술 및 판매 제휴, 금융기관 자금조달 등의 측면에서 다양한 간접 수혜가 있을 것으로 예상하고 있지만, 국내 중상위권 제약사 대부분이 혁신형 제약기업으로 인증되어 있는 만큼 각 사에 돌아가는 혜택에 따라 차별화가 발생하기는 어려울 것으로 판단됩니다. 또한, 3년 뒤 재인증 심사 시 연구개발 투자실적 등에 따라 특별법상 요건을 충족하지 못하여 인증이 연장되지 못할 가능성도 존재합니다. 이 점 투자자께서는 유의하시기 바랍니다.
| 자. 생산설비 구축에 따른 투자 증가와 재무건정성 훼손 위험 GMP(Good Manufacturing Practice, 우수의약품 제조 및 품질 관리 기준)는 우수한 의약품을 제조하기 위하여 공장에서 원료의 구입부터 제조, 출하 등에 이르는 모든 과정에 필요한 관리기준을 규정한 것으로, 미국 FDA가 1963년 GMP를 제정 및 공표하면서 WHO(세계보건기구)와 각국에서 GMP를 도입하기 시작했습니다. 당사는 국내 제약회사 중 최초로 KGMP시설을 취득한 바 있으며 현재까지 GMP 관련 위반사항 등에 대해 제제를 받은 바 없습니다. 당사는 관련 규정에 의거하여, 품질 관리에 최선을 다하고 있으며 국내 최고의 역량을 갖고 있습니다만, 새로운 품질 기준 충족을 위한 제약회사들의 설비투자가 과거에 비해 증가하고 있으며 이는 제약회사들의 재무구조에 부담으로 작용할 수 있습니다. 향후에도 생산시설을 규정에 맞게 운영하기 위하여 지속적인 투자가 발생할 수 있으며, 향후 수출 비중이 증가할 경우 각 국가의 제도에 적합한 생산시설 및 제품의 등록이 필요하므로 투자비용이 증가할 수 있습니다. 이는 제약회사의 재무건정성에 부정적 영향을 끼칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
원료의약품은 원칙적으로 완제의약품에 준하는 허가 및 등록 과정을 거치기 때문에 완제의약품 제조사에게 적용되는 GMP(Good Manufacturing Practice, 우수의약품 제조기준)가 원료의약품 제약사에게도 동일하게 적용됩니다. GMP(Good Manufacturing Practice, 우수의약품 제조 및 품질 관리 기준)는 우수한 의약품을 제조하기 위하여 공장에서 원료의 구입부터 제조, 출하 등에 이르는 모든 과정에 필요한 관리기준을 규정한 것으로, 미국 FDA가 1963년 GMP를 제정 및 공표하면서 WHO(세계보건기구)와 각국에서 GMP를 도입하기 시작했습니다. 우리나라 정부는 1977년에 '우수의약품 제조 관리 기준'을 보건사회부 예규로 공포하고 1978년 'KGMP(Korea GMP) 시행 지침'을 발표하였습니다. 이후 KGMP는 1994년 약사법 시행규칙에 '의약품 제조 및 품질 관리 기준'이 규정되면서 의약품 제조업과 품목 허가의 의무 요건이 되었습니다. 2008년 밸리데이션(Validation), 연간 품질 평가, 변경 관리 등 새로운 규정들이 포함되어 선진국의 GMP와 유사한 수준으로 KGMP가 전면 개정되습니다.
| [정부의 의약품 품질관리 규제] |
| 명 칭 | 주요 내용 |
|---|---|
|
GMP 의무화 |
- GMP는 현대화ㆍ자동화된 제조 시설과 엄격한 공정 관리로 의약품 제조 공정상 발생할 수 있는 인위적인 착오를 없애고 오염을 최소화함으로써 안정성이 높은 고품질의 의약품을 제조 관리운영체계 - 2008년 신약 및 전문의약품, 2009년 일반의약품, 2010년 원료의약품 GMP 의무화 |
|
품목별 밸리데이션 의무화 |
- 밸리데이션은 특정한 공정과 방법ㆍ기계설비ㆍ시스템이 미리 설정돼 있는 판정 기준에 맞는 결과를 일관되게 도출한다는 것을 검증해 문서화하는 제도 - 2008년 1월 신약, 2008년 7월 전문의약품, 2009년 7월 일반의약품, 2010년 1월 원료의약품 및 의약외품 의무화 |
| [의료기기 GMP 참여대상] |
|
| [의료기기 GMP 참여대상] |
한편, 2024년 식품의약품통계연보에 따르면 국내 제약시장에서 생산실적을 보유하고 있는 완제의약품 생산기업은 2023년 기준 403개로 이중 생산액 10억원 미만 업체수가 126개인 바, 시장규모에 비해 참여기업의 수가 다소 과도한 수준으로 보입니다. 이는 과거 제약산업 영위를 위한 설비투자 부담이 타 산업에 비해 크지 않았고 해외 제약사로부터의 도입 품목과 연구개발비 부담이 크지 않은 제네릭 중심의 사업 구성으로 비교적 다수의 기업들이 시장에 참여할 수 있었기 때문입니다.
그러나 상기와 같이 2008년 정부의 GMP(Good Manufacturing Practice, 의약품 제조 및 품질관리기준) 규정 강화에 따라 개별 품목 허가 시 마다 국내외 의약품 제조 현장을 지도 및 점검하는 것이 반드시 요구되기 시작하였습니다. 이에 따라 국내 제약업체들은 각 분류에 적합한 GMP 생산시설을 필수적으로 구비해야 합니다.
위와 같은 국내 GMP 규정의 강화로 인하여 국내 제약회사들은 강화된 GMP 규정에서 요구하는 수준에 맞추어 기존 생산설비를 개선하거나 신규 생산설비를 건설하였습니다. 이러한 설비투자 관련 자금 지출은 국내 주요제약사의 자금 부담으로 작용하였습니다.
한편, 원료의약품 생산ㆍ판매를 위해서는 DMF라고 불리는 원료의약품신고제도(DMF : Drug Master File)의 등록 및 허가가 필요합니다. DMF는 원료 제조 공장의 시설내역, 불순물, 잔류유기용매, 공정관리, 포장재질, 안정성시험자료 등 원료의약품 제조와 품질관리 전반에 관한 자료의 적정성을 평가합니다. 우리나라는 지난 2002년 7월 도입 이후 업계의 준비 기간을 고려해 국민 다소비 성분을 우선 선정해 단계적으로 신고 대상 성분을 확대하고 있으며, 해외 시장 수출을 위해서는 모든 품목에 대해 해당 국가 식약청의 DMF등록과 승인이 필수적입니다. GMP제도 뿐만 아니라 원료의약품신고 제도 또한 설비투자 및 비용 증가 등 국내 주요 제약회사들의 투자 부담으로 작용하고 있습니다.
당사는 국내 제약회사 중 최초로 KGMP시설을 취득한 바 있으며 현재까지 GMP 관련 위반사항 등에 대해 제제를 받은 바 없습니다. 당사는 관련 규정에 의거하여, 품질 관리에 최선을 다하고 있으며 국내 최고의 역량을 갖고 있지만, 새로운 품질 기준 충족을 위한 제약회사들의 설비투자가 과거에 비해 증가하고 있으며 이는 제약회사들의 재무구조에 부담으로 작용할 수 있습니다. 향후에도 생산시설을 규정에 맞게 운영하기 위하여 지속적인 투자가 발생할 수 있으며, 향후 수출 비중이 증가할 경우 각 국가의 제도에 적합한 생산시설 및 제품의 등록이 필요하므로 투자비용이 증가할 수 있습니다. 이는 제약회사의 재무건정성에 부정적 영향을 끼칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
| 차. 해외 기술 이전 실패에 따른 위험 당사가 개발하고 있는 파이프라인이 의학적 미충적 수요(medical unmet needs)를 해결할 가능성이 존재한다고 하더라도 각 글로벌 제약사의 이해관계에 따라 기술이전이 이루어지지 않을 가능성이 존재합니다. 예를 들어 특정 글로벌 제약사가 같은 적응증 대상으로 하여 항체 또는 저분자 화합물을 통한 치료제를 개발하고 있는 경우 경쟁 관계에 있는 당사 파이프라인을 확보하고자 하는 수요가 존재하지 않을 수 있습니다. 당사는 임상이 어느정도 진행된 이후 해외 기업을 대상으로 하는 기술이전 계약을 통해 매출을 본격화 할 예정입니다. 그럼에도 불구, 기술이전이 실패할 경우 당사는 추가 임상 개발을 위한 비용을 충당할 수익원을 마련하지 못할 가능성이 있으며 이는 궁극적으로 당사 외부 평판 및 수익성에 악영향을 줄 수 있으므로 투자자 여러분들께서는 이점 유의하시기 바랍니다. |
해외 기업을 대상으로 한 기술이전의 경우, CDA(Confidential Disclosure Agreement) 및 MTA(Material Transfer Agreement)를 체결한 이 후 계약 조건(Term-Sheet)을 논의하기 까지 상당한 기간이 소요됩니다. 해당 과정에서 경쟁약물의 임상 성공에 의해 기술이전 계약이 성사되지 않을 가능성이 존재합니다. 또한 기술이전이 이루어진 이후에도 임상 결과나 계약 상대방의 자금 현황에 따라 반환되어 전체 계약 규모가 이행되지 않을 수 있습니다. 대형 제약사와의 계약을 추진하는 경우, 협상력의 차이로 인하여 당사가 목표한 선급금(upfront)을 충분히 수령하지 못할 가능성이 존재합니다. 관련하여 선급금을 통해 후속 파이프라인의 개발에 투자할 자금을 확보해야 하는 당사의 사업 모델상 지속적 후보 파이프라인의 발굴에 지연이 생길 위험이 존재합니다.
당사가 개발하고 있는 파이프라인이 의학적 미충적 수요(medical unmet needs)를 해결할 가능성이 존재한다고 하더라도 각 글로벌 제약사의 이해관계에 따라 기술이전이 이루어지지 않을 가능성이 존재합니다. 예를 들어 특정 글로벌 제약사가 같은 적응증 대상으로 하여 항체 또는 저분자 화합물을 통한 치료제를 개발하고 있는 경우 경쟁 관계에 있는 당사 파이프라인을 확보하고자 하는 수요가 존재하지 않을 수 있습니다. 당사가 개발중에 있는 파이프라인과 관련하여 글로벌 제약사들이 공개하지 않은 파이프라인을 독자적으로 개발 중에 있는 경우 기술이전 가능성이 낮아질 수 있습니다.
또한 당사가 개발하고 있는 신약 관련하여 다수의 경쟁회사가 임상을 추가적으로 진행하게 될 경우 경쟁이 심화되어 표준 치료제 기준이 변경될 가능성이 존재합니다. 이 경우 기술 이전에 있어 해외 제약사에서는 글로벌 상업화를 위해 추가적인 임상결과를 요구할 수 있으며 이는 기술이전 지연 사유가 될 수 있습니다.
추가적으로 임상 실패 가능성이 존재한다는 점에서 글로벌 제약사들로의 기술이전에 지연이 발생할 수 있습니다. 당사가 개발중인 파이프라인의 경우 의학적 미충족 수요가 높은 적응증을 대상으로 하고 있습니다. 이는 과거 해당 적응증을 대상으로 하는 글로벌 제약사들의 임상에서 유효성 입증에 실패한 바에 기여합니다. 이러한 경우 글로벌 제약사에서는 임상 실패 관련 위험을 최소화 하기 위해 임상에서의 유효성이 충분히 확인된 경우에만 기술이전을 추진하고자 할 가능성이 존재합니다.
계약 조건에 있어 당사의 경우 후속 파이프라인의 지속적 개발을 위하여 선급금을 높게 받기 위해 협상을 진행할 것으로 예상되며 이는 계약 상대방의 이해관계와 상반될 수 있습니다. 기술 이전 상대방의 협상력에 따라 유효성이 입증된 이후의 마일스톤 비중을 높게 요구 하거나 공동개발 등을 요구할 수 있습니다. 당사 상황, 상대 기업과의 협상력 차이, 대외적 변수 등에 의해 기술이전 조건 협의에 어려움이 발생할 수 있습니다.
지식재산권 관련 사항 역시 기술이전 협상 조건에 영향을 줄 수 있습니다. 기술이전 에 있어 상대 회사에서는 신약개발 이후 최대한 오랜 기간 독적점인 권리를 확보하고자 할 것으로 예상 됩니다. 관련하여 추후 당사가 개발하고자 하는 파이프라인이 앞서 개발완료 후 기술이전을 목표로 하는 파이프라인의 권리범위를 침해할 가능성이 존재하는 경우 해당 협상 과정에서 지연이 발생할 수 있습니다.
기술이전 이후에도 계약된 마일스톤을 모두 수령하기 위해서는 규제기관인 FDA나 EMA로부터의 허가 승인이 있어야 할 것으로 판단됩니다. 규제기관에서 임상 관련 내용에 대하여 불충분하다고 판단할 경우, 추가 임상을 요구하며 허가가 지연될 수 있습니다. 이 경우, 당사가 수취하게 되는 마일스톤 역시 지연될 수 있습니다. 실제로 호주 제약회사 메소블라스트(Mesobalst)가 스테로이드 불응성 급성 이식편대숙주질환 (SR-aGVHD)에 대한 치료제로 개발한 라이온실(Ryoncil, remestemcel-L)의 경우 2020년10월 무작위, 대조임상을 권고함에 따라 자문위원회(ODAC)의 찬성 9표, 반대 1표의 결과에도 불구하고 승인이 거절된 바 있습니다. 이러한 사례와 같이 허가 기관으로부터의 승인이 늦어져 기술이전 이후에도 마일스톤 수령에 차질이 발생할 가능성이 존재합니다.
당사는 임상이 어느정도 진행된 이후 해외 기업을 대상으로 하는 기술이전 계약을 통해 매출을 본격화 할 예정입니다. 그럼에도 불구, 상기 언급된 요인들로 인해 기술이전이 실패할 경우 당사는 추가 임상 개발을 위한 비용을 충당할 수익원을 마련하지 못할 가능성이 있으며 이는 궁극적으로 당사 외부 평판 및 수익성에 악영향을 줄 수 있으므로 투자자 여러분들께서는 이점 유의하시기 바랍니다.
| 카. 기술도입관련 위험 당사는 원료 수입 및 제조/판매, 제품수입 등의 목적으로 다수의 계약을 체결하고 있습니다. 동 계약은 당사의 영업 및 연구개발에 있어 필수적인 요소로 해당 계약이 예상치 못한 변수로 인해 종결되거나 당사에게 불리한 방향으로 변경될 경우 당사 영업환경에 불리하게 작용할 수 있습니다. 당사는 현재 계약을 체결중인 상대방과 우호적인 협력 관계를 유지하고 있으며 이러한 신뢰관계가 향후에도 지속될 것으로 당사는 전망하고 있습니다. 다만 모든 계약에는 불확실성이 존재하며 안정적인 원재료 수급이 절대적으로 중요한 제약 산업에서 예상치 못한 변수로 인해 적절한 원재료 도입에 차질이 생기거나 기술도입/이전 등과 관련하여 분쟁이 발생할 경우 당사의 재무건정성 및 수익성이 악화될 가능성이 존재하는 점 투자자분들 께서는 유의하시기 바랍니다. |
당사는 원료 수입 및 제조/판매, 제품수입 등의 목적으로 다수의 계약을 체결하고 있습니다. 동 계약은 당사의 영업 및 연구개발에 있어 필수적인 요소로 해당 계약이 예상치 못한 변수로 인해 종결되거나 당사에게 불리한 방향으로 변경될 경우 당사 영업환경에 불리하게 작용할 수 있습니다. 특히 당사가 생산 및 판매하는 의약품목의 경우 건강보험평가심사원에서 판매단가를 엄격히 관리하고 있기에 단가 인상에 상방이 존재하며 이 경우 원재료 조달에 있어 불리한 조건이 작용할 시 당사 재무건정성 및 수익성에 악영향을 줄 수 있습니다. 당사의 주요 계약현황은 다음과 같습니다.
| 사업부문 | 계약 상대방 | 계약목적 | 대표 품목명 | 체결시기 | 진행 단계 |
| 의약품 및 의약외품 |
Eisai (일본) |
제조/판매 | Selbex (Teprenone) |
2016.07.01 | 제조 판매 중 |
| MEDA/Mylan (독일) |
원료 수입 | Legalon, Tavex, Alaxyl, Spasmolyt |
1993.12.28 | 원료 수입/제조 판매 | |
| 원료 수입 | Thioctacid, Azeptin, Cormelian |
2003.12.11 | 원료 수입/제조 판매 | ||
| 제품 수입 | Dylastine | 2018.05.25 | 수입 판매 중 | ||
| 제품 수입 | Sebivo | 2018.10.26 | 수입 판매 중 | ||
| Baxter (독일) |
제품 수입 | Holoxan Endoxan, Uromitexan |
2013.01.01 | 수입 판매 중 | |
| Pierre Fabre (프랑스) |
제품 수입 원료 수입 |
Navelbine Ixel |
2014.01.01 | 수입 판매 중 | |
| Ferrer (스페인) |
제품 수입 원료 수입 |
Dermofix | 1993.06.02 | 제조 판매 중 | |
| 원료 수입 | Somazina | 2002.03.04 | 제조 판매 중 | ||
| 원료 수입 | Nadixa | 2004.05.17 | 제조 판매 중 | ||
| 제품 수입 |
Repavar Pielato Melagyn |
2016.06.30 | 공급 중단 | ||
| 제품 수입 | Ozanex | 2020.01.10 | 제조 판매 중 | ||
|
Ojer (스페인) |
제품 수입 | Lipovir | 2018.01.29 | 개발 논의 중 | |
| Desitin (독일) |
원료 수입 | Orfil | 1978.03.15 | 제조 판매 중 | |
| 원료 수입 | Timonil | 1994.08.31 | 제조 판매 중 | ||
| Sumitomo Pharma Co., Ltd. (일본) |
원료 수입 | Lonasen (Blonanserin) | 2005.02.28 | 제조 판매 중 | |
| 상표권 계약 | Cetapril | 2015.02.27 | 판매 중단 | ||
| 반제품 수입 | Latuda (Lurasidone HCl) | 2017.04.05 | 제조 판매 중 | ||
| Eurodrug (네덜란드) |
원료 수입 | Fexadin | 1986.07.29 | 제조 판매 중 | |
| Asima | 2000.03.24 | 제조 판매 중 | |||
| 반제품 수입 | Panbesy | 2019.06.01 | 반제품 수입 판매 중 | ||
| Kalbe International Pte. Ltd. (싱가포르) |
제품 수출 | 덱시드정 | 2016.03.03 | 제조 판매 중 (완제 수출) |
|
| 연구개발 | Melior Pharmaceuticals, Inc (미국) |
기술 반환, 수익 배분 및 이전 | MLR-1023 | 2023.12.21 | Biodexa에서 임상2a상 진행 중 (캐나다) |
| Contera Pharma A/S (덴마크) |
기술도입 | JM-010 | 2014.12.12 | 임상 2상 종료 (미국) |
| (자료 : 당사 분기보고서) |
당사는 현재 계약을 체결중인 상대방과 우호적인 협력 관계를 유지하고 있으며 이러한 신뢰관계가 향후에도 지속될 것으로 당사는 전망하고 있습니다. 다만 모든 계약에는 불확실성이 존재하며 안정적인 원재료 수급이 절대적으로 중요한 제약 산업에서 예상치 못한 변수로 인해 적절한 원재료 도입에 차질이 생기거나 기술도입/이전 등과 관련하여 분쟁이 발생할 경우 당사의 재무건정성 및 수익성이 악화될 가능성이 존재하는 점 투자자 분들 께서는 유의하시기 바랍니다.
|
타. 오픈이노베이션 전략에 따른 위험 |
당사는 IR자료를 통해 투자자분들과 소통한 바와 같이 당사는 R&D 전략을 크게 (1) 신속한 제품 포트폴리오 확보 (2) 당사 Organic R&D 강화, (3) Global Open innovation 전략으로 구분하고 있습니다. 신속한 제품 포트폴리오 확보를 위해 최근 타사의 허가권 3종(치매치료제 RH+ , 당뇨치료제 부디양, 간장용제 레가덱스) 양수 완료하였으며 25년에는 추가 허가권 양수, 공동개발 참여 및 판매협력(co-operation)을 통해 신속한 판매용 제품 확보를 계획입니다. 당사 organic R&D 강화는 크게 신약합성연구와 제제연구로 구분됩니다. 신약합성연구는 비임상 연구장비 도입 및 의약화학연구 강화, Biology 연구인력과 ADME연구인력 확보를 통한 후보물질 검증 역량 강화를 통해 신규 제품군을 확보하는 것을 목적으로 하며 제제연구는 제제 및 분석연구 장비 도입, 장기지속주사제 등 신규제형을 개발하는 것을 목적으로 하고 있습니다. 치옥타시드에서 R/S Form 혼합형태의 주원료에서 R-form만을 추출하여만든 개량신약인 덱시드가 당사 제제연구의 주요 결과물이라고 할 수 있습니다.
다만, 당사의 R&D 주된 계획은 Global Open innovation을 중심으로 진행하고 있습니다. 당사는 기존 제품군에서 안정적인 시장지위를 확보하고 있기에 안정적인 수익성을 시현하고 있습니다. 기존 제품군에서의 안정적인 영업현금흐름을 바탕으로 신약개발을 다양한 해외(자회사 및 지분투자 포함)사와 협업을 진행하고 있습니다. 이는 천문학적 비용이 투입되는 신약개발을 다양한 회사와의 협업을 통하여 리스크 및 비용을 분산하고 수익 및 향후 임상성공에 따른 benefit을 공유하고자 하는 취지로 신약개발사에서 통상적으로 취하고 있는 R&D 전략 입니다. 동사는 JV(조인트벤처) 설립, 리서치 협업, M&A, 지분투자 등을 통해 파이프라인과 사업모델을 확보하는 다양한 형태의 전략을 추진 중이며 미국, 유럽 등 30곳 이상의 글로벌 제약 및 바이오벤처와 파트너십을 구축하고 있고 유망 바이오벤처에 전략적 투자도 진행하고 있습니다. 그 결과 Contera Pharma A/S, ProteKt Therapeutics, JaguAHR Therapeutics를 자회사로 지분 투자 중이며 이외 다양한 글로벌 신약업체에 출자를 진행하고 있습니다. 이를 통해 글로벌 수요가 높은 CNS치료제, 고형암 치료제 중심의 신약 파이프라인을 구축하고자 하고 있습니다. 다만 이러한 당사 전략으로 인해 당사는 다양한 국가의 규제 변화 및 지원 정책에 따라 영향을 받을 수 있습니다.
미국은 주요 규제 기관인 FDA(식품의약국)가 의약품, 의료기기, 생물학적 제제의 안전성과 유효성을 관리합니다. 미국은 신속 승인 제도인 패스트 트랙(Fast Track), 가속 승인(Accelerated Approval) 등 혁신적인 치료제 개발을 지원하는 프로그램을 운영하고 있습니다. 다만 임상시험에서 높은 품질 기준을 요구하며 제조 공정과 품질 관리 강화을 요구하고 있습니다. FDA 승인을 받기 위해서는 광범위한 임상시험 자료와 제품의 안전성 및 유효성에 관한 증거를 제출해야 하며 의약품의 마케팅, 라벨링, 제조 및 유통에 관한 엄격한 기준을 가지고 있습니다. 더불어 미국 정부는 AI, 디지털 치료제 등 혁신 기술에 대한 새로운 규제 프레임워크를 마련하고 있습니다.
유럽은 EMA(유럽의약품청)가 EU 전체에서 통용되는 의약품 허가를 담당하며, 국가별 절차와 통합 절차를 병행합니다. 규제는 주로 정기적 안전성과 효능 데이터를 강조하는 방향에 초점이 맞추어져 있으며, 특히 희귀질환 및 혁신 치료제를 위한 신속 승인 절차를 제공하고 있습니다. 개별 국가도 자체적인 규제 기관을 운영하며, 특히 유럽 경제지역(EEA)의 일원으로서 현지 시장 맞춤 규제를 진행합니다. 또한 EMA 승인을 받은 의약품은 모든 EU 회원국에서 판매가 가능하지만, 가격과 상환 정책은 개별 국가가 결정합니다. 국가별 특징으로 독일은 신약 개발 및 중소기업 지원 강화, 영국은 NHS와 연계한 신속 승인 제도 및 생명과학 육성 및 오스트리아는 동일 성분 조제약 가격 상한제 도입 등이 있습니다.
상기 규제와는 별개로 CNS 중추신경계 분야에 대해서 다양한 글로벌 지원책이 발의되고 있습니다. 북아메리카의 경우 알츠하이머병에 대한 연구자금 및 제도적 지원을 적극적으로 추진하고 있습니다. 2024년 상반기 미국 정부에서는 알츠하이머병/치매 연구를 위한 자금 지원을 확대하고 있습니다. 구체적으로 미국 NIH(국립보건원), NIA(국립노화연구소)의 알츠하이머병/치매 관련 연구를 위해 1억 달러의 추가 예산을 지원하였으며 미국 CDC는 알츠하이머병을 위한 BOLD Act(Building Our Largest Dementia for Alzheimer’s Act)를 통해 3,400만 달러를 추가로 지원하고, 치매 위험 감소, 조기 발견· 진단, 입원 예방, 치매 간병 지원 등 강력한 공중 보건 인프라 구축 의지를 표명하고 있습니다. 그 결과 BlueRock Therapeutics의 파킨슨병 치료제 "베무다네프로셀(bemdaneprocel)’은 재생의학 첨단치료(RMAT) 지정을 받는 등 FDA에서의 정밀의학 기반 치료제 신속 승인을 위한 지원이 강화되는 추세입니다.
유럽의 경우 규제 지원, 연구 협력, 정부 자금, 공공-민간 파트너십을 통해 신경 퇴행성 질환 치료제 개발을 위한 생태계 조성 노력을 기울이고 있습니다. 특히 맞춤형 신경퇴행성 질환 치료제 가속 승인을 위한 규제 지원 및 협력 연구를 장려하고 있으며 유럽의약청(EMA)은 파킨슨병 환자의 삶의 질이나 운동 기능을 개선하거나 알츠하이머병의 아밀로이드 표적 치료제와 같이 신규 경로를 타겟으로 하는 치료제에 대한 신약 가속 승인 및 조건부 허가 고려 중인 것으로 확인됩니다. EU 신경퇴행성 질환 공동 프로그램(JPND)는 대규모 오믹스 데이터 분석을 통해 개인 맞춤형 치료를 위한 약물 표적 및 바이오마커 식별 지원과 증상이 나타나기 전 단계의 질병 메커니즘 연구를 위한 국제적 공모 등을 주도하고 있습니다.
파킨슨 병 등 신경퇴행성 질환 치료제는 질병 기전에 대한 복잡성, 모델 한계, 환자 간 이질성 등의 복합적 요인으로 다른 치료 분야 대비 임상시험 실패율이 높은 편 입니다. 신경계는 매우 복잡하여 신경퇴행성 질환의 병리학적 기전을 전반적으로 이해하는 것이 어렵고, 증상이 나타날 때쯤에는 이미 심각하고 되돌릴 수 없는 신경 손상이 발생한 경우가 다수입니다. 또한 신경퇴행성 질환 치료제 개발을 위한 동물모델은 인간과의 이질성을 잘 반영하지 못해 임상에서 유사한 결과를 도출하는 데 한계점이 존재합니다. 아울러 환자마다 증상 발현과 진행 속도가 달라 임상 시험에서의 적절한 환자 그룹 선정과 연구 결과 해석이 어려운 점도 있습니다. 이로 인해 3상 임상시험 단계에서 대부분 질병이 이미 진행된 상태이기 때문에 시험 성공률이 낮고 치료 효과를 입증하기 어려우며, 질병 진행을 예측하거나 치료 반응을 추적할 수 있는 바이오마커가 부족해 임상 3상에서 치료 유효성을 입증하는 것에 어려움 존재하는 상황입니다.
이로 인해 미국/유럽 등 각 지역에서는 파킨슨병 치료제 개발을 지원하는 다양한 제도가 발휘되거나 논의되는 중이며 이는 당사의 오픈 이노베이션 전략이 유수한 해외 기업과의 협업을 통해 임상에 따른 Risk가 완화되는 반면 지역 특색에 맞는 임상 전략을 가동하여 성공 가능성을 제고하는 등 제약회사에 있어 최적화된 전략임을 보여주고 있습니다. 다만 예상치 못한 각 국가의 정책 및 규제변화에 따라 인허가 위험으로 인해 시장이 위축되거나 비우호적인 임상 환경이 조성될 수 있습니다. 또한 환율 이 급등할 경우 당사의 자회사 지원 부담이 증가하는 등, 글로벌 오픈 이노베이션을 통해 다국적 기업과의 협업을 추구하는 당사 전략이 오히려 수익성 악화로 이어질 개연성이 존재합니다. 투자자분들께서는 이점 유의하시기 바랍니다.
|
파. 주요 경쟁 관련 위험(cmg, 한올바이오파마) |
당사는 완제 의약품 제조와 동시에 CNS 질환 치료제 연구개발에 투자를 단행하고 있습니다. 당사와 주요 사업과 유사한 사업을 영위 중인 주요 경쟁사로는 CMG제약과 한올바이오파마가 있습니다. CMG제약은 ODF(구강용해필름) 제조 특허 기술인 스타필름 테크놀로지를 신약 파이프라인에 적용하며 CNS 질환 치료제, 표적항암제 등의 연구개발을 진행하고 있습니다. 반면 한올바이오파마는 약 160개의 전문의약품, 일반의약품 생산 및 판매에 특화되어 있으나, 최근에는 자가면역질환, 안구질환, 항암제, CNS 질환 분야의 바이오신약 개발에 주력하고 있습니다.
각사별 재무현황은 다음과 같습니다.
| [ 당사 및 경쟁사 별도 손익계산서 현황 ] |
| (단위: 백만원) |
| 구 분 | 2024 | 2023 | 2022 | |
|---|---|---|---|---|
| 당사 | 수익(매출액) | 157,607 | 125,176 | 190,339 |
| 매출원가 | 83,886 | 79,039 | 111,793 | |
| 매출총이익 | 73,721 | 46,137 | 78,546 | |
| 판매비와관리비+연구개발비 | 56,717 | 63,310 | 66,224 | |
| 영업이익(손실) | 17,004 | (17,173) | 12,322 | |
| 당기순이익(손실) | (55,610) | (19,093) | 2,042 | |
| 영업이익율 | 10.79% | -13.72% | 6.47% | |
| 연구개발비율 | 6.29% | 12.37% | 6.31% | |
| 당기순이익율 | -35.28% | -15.25% | 1.07% | |
| 한올바이오파마 | 수익(매출액) | 138,944 | 134,910 | 109,995 |
| 매출원가 | 65,637 | 59,738 | 48,024 | |
| 매출총이익 | 73,306 | 75,172 | 61,971 | |
| 판매비와관리비+연구개발비 | 73,078 | 72,668 | 60,202 | |
| 영업이익(손실) | 228 | 2,504 | 1,770 | |
| 당기순이익(손실) | -1,712 | 3,859 | 546 | |
| 영업이익율 | 0.16% | 1.86% | 1.61% | |
| 연구개발비율 | 26.26% | 24.21% | 19.34% | |
| 당기순이익율 | -1.23% | 2.86% | 0.50% | |
| CMG제약 | 수익(매출액) | 98,149 | 92,743 | 82,197 |
| 매출원가 | 52,759 | 49,507 | 41,296 | |
| 매출총이익 | 45,390 | 43,236 | 40,901 | |
| 판매비와관리비+연구개발비 | 43,981 | 39,958 | 37,920 | |
| 영업이익(손실) | 1,409 | 3,277 | 2,981 | |
| 당기순이익(손실) | 3,162 | 6,658 | -388 | |
| 영업이익율 | 1.44% | 3.53% | 3.63% | |
| 연구개발비율 | 9.66% | 9.14% | 11.07% | |
| 당기순이익율 | 3.22% | 7.18% | -0.47% | |
| (자료 : 각사 사업보고서) |
한편 당사 이외의 CNS 전문 제약업체는 환인제약이 있습니다. 환인제약은 의약품을 제조하여 병원 등에 판매를 주요사업으로 하고 있으며, 회사 전체 매출액 중 80%이상이 정신신경용제 매출이 차지하고 있습니다. 2023년 IMS DATA기준 국내 정신치료 약물시장의 점유율 1위로써 우수한 영업력으로 꾸준한 성장을 이어오고 있습니다. 환인제약 및 당사의 수익성 비교내역은 다음과 같습니다.
| [ 당사 및 경쟁사 별도 손익계산서 현황 ] |
| (단위: 백만원) |
| 구 분 | 2024 | 2023 | 2022 | |
|---|---|---|---|---|
| 당사 | 수익(매출액) | 157,607 | 125,176 | 190,339 |
| 매출원가 | 83,886 | 79,039 | 111,793 | |
| 매출총이익 | 73,721 | 46,137 | 78,546 | |
| 판매비와관리비+연구개발비 | 56,717 | 63,310 | 66,224 | |
| 영업이익(손실) | 17,004 | (17,173) | 12,322 | |
| 당기순이익(손실) | (55,610) | (19,093) | 2,042 | |
| 영업이익율 | 10.79% | -13.72% | 6.47% | |
| 연구개발비율 | 6.29% | 12.37% | 6.31% | |
| 당기순이익율 | -35.28% | -15.25% | 1.07% | |
| 환인제약 | 수익(매출액) | 257,969 | 228,243 | 194,258 |
| 매출원가 | 165,531 | 130,846 | 99,256 | |
| 매출총이익 | 92,438 | 97,396 | 95,002 | |
| 판매비와관리비+연구개발비 | 69,982 | 66,304 | 64,368 | |
| 영업이익(손실) | 22,456 | 31,093 | 30,634 | |
| 당기순이익(손실) | 22,694 | 29,924 | 23,601 | |
| 영업이익율 | 8.71% | 13.62% | 15.77% | |
| 연구개발비율 | 9.10% | 9.50% | 11.30% | |
| 당기순이익율 | 8.80% | 13.11% | 12.15% | |
| (자료 : 각사 사업보고서) |
당사는 영업이익율에 있어 경쟁사인 한올바이오파마 및 CMG제약, 환인제약 대비 우월한 모습을 보이고 있으나 당기순손실 규모가 상대적으로 크게 나타나고 있습니다. 다만 이는 자회사의 JM-010임상 실패로 인한 추정 현금흐름 변동에 따른 사용가치 하락 및 관련 손상차손 521억원 등 현금지출을 동반하지 않는 기타영업외비용에 기인한 것으로, 금번 손상차손 조기 인식으로 인해 향후 추가적인 대규모 손상차손을 인식할 가능성은 제한적일 것으로 판단하고 있습니다. 따라서 연구개발비로 환원할 수 있는 영업현금흐름 규모 및 수익성 관점에 있어서 향후 당사는 경쟁사 대비 경쟁력을 보일 것으로 전망됩니다
당사는 오랜 업황을 통해 축적한 영업노하우 및 기술, 네트워크에 기반하여 조현병 시장 등에 있어 경쟁사 대비하여 선도적인 시장 지위를 확보하고 있는 것으로 확인되고 있습니다. 그럼에도 불구하고, 향후 CNS 중추신경계 시장 내 당사가 예상하지 못한 신규 경쟁 치료제가 출현하거나 기존 전통적 치료제의 적응증 또는 목표 환자군 확장 등이 발생할 경우, 경쟁 심화에 따라 당사의 영업 및 재무안정성이 악화될 수 있습니다. 따라서 투자자께서는 당사가 연구개발 중인 주요 파이프라인에서 대체재 출시 혹은 경쟁 심화로 인한 수익성이 저하될 수 있다는 사실에 유의하시기 바랍니다.
2. 회사위험
| 가. OCI그룹 기업집단 설정에 따른 위험 당사는 2024년 공정거래위원회에서 지정한 2024년 상호출자금지 기업집단 순위 41위의 OCI 계열사로, OCI그룹은 당사를 포함하여 총 24개의 계열회사로 구성되어 있습니다.OCI그룹은 공정거래법상 대규모기업집단 정책을 적용받으며 해당 정책에서 제시하는 규정을 준수하지 못하거나 관련 공시사항을 이행하지 못하게 될 경우 과징금이 부과될 수 있습니다. 이로 인해 당사 수익성에 영향을 받을 수 있으며 나아가 당사의 외부 평판에도 부정적인 영향을 줄 수 있는 점 투자자분들께서는 유의하시기 바랍니다. 공정거래법상 지주회사는 자회사 지분율 규제(상장30%, 비상장50% 이상)가 적용되며, 이에 미달하는 자회사 지분을 자회사 지분율 규제 이상으로 추가 취득 또는 처분하여야 합니다. 금번 유상증자에서 당사 최대주주인 OCI홀딩스가 배정받은 증서 및 2대,3대 주주의 증서까지 매입 후 120% 청약 시 확보하게 될 지분율은 약 16.81%로 당사 최대주주인 OCI홀딩스가 지분율 요건을 충족하기 위해서는 추가 지분매입 및 제3자배정유상증자 등이 수반될 수 있으며 이 경우 당사 주식 가격 변동성이 높아질 수 있으니 투자자 분들께서는 유의하시기 바랍니다. 한편 당사는 당사 최대주주인 OCI홀딩스 포함 특수관계인과 다양한 매출 매입활동을 진행하고 있습니다. 당사 외형규모 고려 시 해당 매출 매입금액이 유의적인 수준은 아니나, 향후 특수관계자 거래 규모가 증가할 경우 거래의 적정성에 대해 공정거래위원회 및 세무당국의 조사가 진행될 수 있는 점 참고부탁드립니다. |
당사는 2024년 공정거래위원회에서 지정한 2024년 상호출자금지 기업집단 순위 41위의 OCI 계열사로, OCI그룹은 당사를 포함하여 총 24개의 계열회사로 구성되어 있습니다.
당사는 2022년 3월 3일 최대주주 변경 공시를 통해 공식적으로 OCI그룹에 편입되었음을 알린 바 있습니다. 구체적으로 기존 당사 주주였던 김상훈 외 8인은 OCI홀딩스 주식회사(구 OCI 주식회사)에 7,730,334주를 양도함에 따라 당사 최대주주는 OCI홀딩스 주식회사(구 OCI주식회사)로 변경되었습니다. OCI그룹은 기존 태양광 및 화학산업 이외 바이오 사업을 미래 성장 동력으로 삼고 있습니다. 이에 당사 지분을 인수하는 등 적극적인 행보를 통해 해당 계획을 구체화 한 것으로 확인됩니다. 본 증권신고서 제출일 기준 OCI홀딩스 주식회사(구 OCI주식회사)의 당사 지분율은 11.32% 이며 최대주주 변경 공시 내역은 다음과 같습니다.
| [최대주주변경 공시(2022.03.03] |
| 1. 변경내용 | 변경전 | 최대주주등 | 김동연 외 11인 | |
| 소유주식수(주) | 15,419,156 | |||
| 소유비율(%) | 21.70 | |||
| 변경후 | 최대주주등 | OCI주식회사 외 3인 | ||
| 소유주식수(주) | 8,383,490 | |||
| 소유비율(%) | 11.70 | |||
| 2. 변경사유 | 최대주주등(김상훈 외 8인)과 OCI주식회사의 주식매매거래에 따른 최대주주 변경 | |||
| 3. 지분인수목적 | 바이오 사업 진출 확대 | |||
| -인수자금 조달방법 | 현금취득 | |||
| -인수후 임원 선ㆍ해임 계획 | - | |||
| 4. 변경일자 | 2022-03-03 | |||
| 5. 변경확인일자 | 2022-03-03 | |||
| 6. 기타 투자판단과 관련한 중요사항 | -최대주주등(김상훈 외 8인)의 소유주식수 7,730,334주를 OCI주식회사가 취득하여 최대주주가 변경됨. - 상기 '4.변경일자' 및 '5.확인일자'는 최대주주 변경을 수반하는 주식매매계약에 따라 2차거래 조건이 완료된 거래종결일 입니다. - 변경후 최대주주인 OCI주식회사의 재무상태는 아래와 같음 (2020년 12월 31일 별도재무제표 기준) 자산총계: 3,368,975,278천원 부채총계: 1,034,656,249천원 자본총계: 2,334,319,029천원 자본금 : 127,246,855천원 |
|||
| ※관련공시 | 2022-02-22 투자판단 관련 주요경영사항 | |||
세부변경내역
| 성명(법인)명 | 관계 | 변경전 | 변경후 | 비고 | ||
| 주식수(주) | 지분율(%) | 주식수(주) | 지분율(%) | |||
| 김상훈 | 변경전 최대주주의 특수관계인 | 4,507,749 | 6.34 | 568,504 | 0.80 | 변경후 최대주주의 특수관계인 (발행회사의 임원) |
| 김은주 | 변경전 최대주주의 특수관계인 | 1,533,698 | 2.16 | 0 | 0 | - |
| 김은미 | 변경전 최대주주의 특수관계인 | 1,661,774 | 2.34 | 0 | 0 | - |
| 김동환 | 변경전 최대주주의 특수관계인 | 274,619 | 0.39 | 0 | 0 | - |
| 김민정 | 변경전 최대주주의 특수관계인 | 71,120 | 0.10 | 0 | 0 | - |
| 이은수 | 변경전 최대주주의 특수관계인 | 61,749 | 0.09 | 0 | 0 | - |
| 이윤수 | 변경전 최대주주의 특수관계인 | 61,822 | 0.09 | 0 | 0 | - |
| 허정윤 | 변경전 최대주주의 특수관계인 | 63,094 | 0.09 | 0 | 0 | - |
| 허소윤 | 변경전 최대주주의 특수관계인 | 63,213 | 0.09 | 0 | 0 | - |
| OCI주식회사 | 변경후 최대주주 | 17,600 | 0.02 | 7,747,934 | 10.90 | - |
| 자료: 전자공시시스템 |
OCI그룹은 2023년 5월 1일 분할기일로 인적분할을 진행함과 동시에 2023년 7월 27일 현물출자 유상증자를 결의하였고 2023년 9월 22일 지주회사 성립 요건을 충족하였습니다. 현물출자 유상증자에 따른 신주는 2023년 10월 13일 상장 완료되었으며 2023년 12월 21일에 지주회사 전환신고에 대한 회신을 접수하였습니다(2023년 9월 22일자로 전환 완료). OCI그룹은 공정거래법상 아래의 대규모기업집단 정책을 적용받으며 해당 정책에서 제시하는 규정을 준수하지 못하거나 관련 공시사항을 이행하지 못하게 될 경우 과징금이 부과될 수 있습니다. 이로 인해 당사 수익성에 영향을 받을 수 있으며 나아가 당사의 외부 평판에도 부정적인 영향을 줄 수 있는 점 투자자분들께서는 유의하시기 바랍니다.
| [대규모기업집단 정책] |
| 구분 | 내용 |
|---|---|
| 계열회사간 제한 | 채무보증제한기업집단에 속하는 회사는 계열회사에 대하여 국내 금융기관으로부터 여신(대출, 지급보증 및 채무인수)과 관련한 채무보증을 할 수 없으며 기존 채무보증은 지정후 2년이내 해소하여야함 |
| 계열회사간의 상호출자 금지 |
상호출자제한기업집단 소속회사(금융·보험회사 포함)는 자기의 주식을 소유하고 있는 동일 기업집단 계열회사의 주식을 취득 또는 소유하는 것이 금지됨 |
| 중소기업창업투자회사의 계열회사주식취득 금지 |
상호출자제한기업집단 소속회사로서 중소기업창업지원법에 의한 중소기업창업투자회사는 국내 계열회사 주식의 취득 또는 소유가 금지됨 |
| 금융, 보험회사의 의결권 제한 | 상호출자제한기업집단 소속회사로서 금융업 또는 보험업을 영위하는 회사는 취득 또는 소유하고 있는 국내계열회사 주식에 대하여 의결권을 행사할 수 없음 |
| 대규모내부거래의 이사회 의결 및 공시 | 상호출자제한기업집단 소속회사는 거래금액이 당해 회사 자본총계 또는 자본금중 큰 금액의 10/100 이상 이거나 100억원 이상인 다음의 대규모내부거래행위시에 이사회의 의결을 거친 후 이를 공시하여야 함(주요내용을 변경하고자하는 때도 동일) |
| 비상장회사등의 중요사항 공시 | - 소유지배구조와 관련된 중요사항 - 경영활동과 관련된 중요한 사항 |
| 기업집단현황공시 | 상호출자제한기업집단 소속회사*는 기업집단의 일반현황, 임원ㆍ이사회현황, 주식소유현황, 특수관계인과의 거래현황 등을 공시 * 직전 사업연도말 자산총액이 100억원 미만인 회사로서 청산 중에 있거나 1년 이상 휴업중인 회사는 제외 |
| 출처: 공정거래위원회 |
공정거래법 제18조 제2항 제2호에 따르면 지주회사는 자회사 지분율 규제(상장30%, 비상장50% 이상)가 적용되며, 이에 미달하는 자회사 지분을 자회사 지분율 규제 이상으로 추가 취득 또는 처분하여야 합니다. 다만 지주회사로 전환하거나 설립될 당시에 자회사의 주식을 자회사 주식 보유기준 미만으로 소유하고 있는 경우에 한해 지주회사로 전환하거나 설립된 날부터 2년 이내 지분율 요건을 충족할 수 있도록 유예기간을 규정하고 있습니다. 이에 OCI홀딩스는 지주회사 전환일인 2023년 9월 22일부터 2년이 도래하는 2025년 9월 22일까지 해당 지분율 요건을 충족해야 합니다. 만약 해당 규정을 준수하지 못할 경우 공정거래위원회로부터 공정거래법 제37조 제1항에 따른 주식의 전부 또는 일부의 처분 등의 시정명령 또는 공정거래법 제38조 제3항 제2호에 따라 과징금이 부여될 수 있으며, 이로 인해 당사 최대주주인 OCI홀딩스의 평판 악화 또는 재무적 손실이 발생할 수 있습니다. 다만, 공정거래법 제18조 제6항에 따라 경제 여건의 변화, 주식 처분금지 계약, 사업의 현저한 손실 등의 사유로 주식의 취득이 어려울 경우 공정거래위원회의 승인을 받아 유예기간을 2년 추가로 연장할 수 있습니다. 아울러 금번 유상증자에서 당사 최대주주인 OCI홀딩스가 배정받은 증서 및 2대,3대 주주의 증서까지 매입 후 120% 청약 시 확보하게 될 지분율은 약 16.81%로 당사 최대주주인 OCI홀딩스가 지분율 요건을 충족하기 위해서는 추가 지분매입 및 제3자배정유상증자 등이 수반될 수 있습니다. OCI홀딩스(주)가 당사 기존 주주의 신주인수권 증서를 매입하게 될 경우 자본시장법 제173조의3에 따라 신주인수권증서 거래 개시일의 30일 전, 거래계획을 사전 공시할 예정이며 현재 예상되는 사전 공시일은 2025년 05월 30일입니다. 이 경우 당사 주식 가격 변동성이 높아질 수 있으니 투자자 분들께서는 유의하시기 바랍니다.
|
※ 관련법규 <독점규제 및 공정거래에 관한 법률> 제18조(지주회사 등의 행위제한 등) ② 지주회사는 다음 각 호의 어느 하나에 해당하는 행위를 하여서는 아니 된다. 1. 자본총액(대차대조표상의 자산총액에서 부채액을 뺀 금액을 말한다. 이하 같다)의 2배를 초과하는 부채액을 보유하는 행위. 다만, 지주회사로 전환하거나 설립될 당시에 자본총액의 2배를 초과하는 부채액을 보유하고 있을 때에는 지주회사로 전환하거나 설립된 날부터 2년간은 자본총액의 2배를 초과하는 부채액을 보유할 수 있다. 2. 자회사의 주식을 그 자회사 발행주식총수의 100분의 50[자회사가 상장법인인 경우, 주식 소유의 분산요건 등 상장요건이 「자본시장과 금융투자업에 관한 법률」에 따른 증권시장으로서 대통령령으로 정하는 국내 증권시장의 상장요건에 상당하는 것으로 공정거래위원회가 고시하는 국외 증권거래소에 상장된 법인(이하 “국외상장법인”이라 한다)인 경우 또는 공동출자법인인 경우에는 100분의 30으로 하고, 벤처지주회사의 자회사인 경우에는 100분의 20으로 한다. 이하 이 조에서 “자회사주식보유기준”이라 한다] 미만으로 소유하는 행위. 다만, 다음 각 목의 어느 하나에 해당하는 사유로 자회사주식보유기준에 미달하게 된 경우는 제외한다. 가. 지주회사로 전환하거나 설립될 당시에 자회사의 주식을 자회사주식보유기준 미만으로 소유하고 있는 경우로서 지주회사로 전환하거나 설립된 날부터 2년 이내인 경우 ⑥ 제2항제1호 단서, 같은 항 제2호가목, 같은 항 제3호가목, 같은 항 제4호 단서, 같은 항 제5호 단서, 제3항제1호가목, 같은 항 제2호가목, 같은 항 제3호 단서, 제4항제1호 및 제5항제1호를 적용할 때 각 해당 규정의 유예기간은 주식가격의 급격한 변동 등 경제여건의 변화, 주식처분금지계약, 사업의 현저한 손실 또는 그 밖의 사유로 부채액을 감소시키거나 주식의 취득·처분 등이 곤란한 경우 공정거래위원회의 승인을 받아 2년을 연장할 수 있다. 제37조(시정조치 등) 1. 해당 행위의 중지 2. 주식의 전부 또는 일부의 처분 3. 임원의 사임 4. 영업의 양도 5. 채무보증의 취소 6. 시정명령을 받은 사실의 공표 7. 공시의무의 이행 또는 공시내용의 정정 8. 그 밖에 법 위반상태를 시정하기 위하여 필요한 조치 제38조(과징금) ③ 공정거래위원회는 제18조제2항부터 제5항까지, 제20조제2항 또는 제3항의 규정을 위반한 자에게 다음 각 호의 구분에 따른 금액에 100분의 20을 곱한 금액을 초과하지 아니하는 범위에서 과징금을 부과할 수 있다. 1. 제18조제2항제1호를 위반한 경우: 대통령령으로 정하는 재무상태표(이하 이 항에서 “기준재무상태표”라 한다)상 자본총액의 2배를 초과한 부채액 2. 제18조제2항제2호를 위반한 경우: 해당 자회사 주식의 기준재무상태표상 장부가액의 합계액에 다음 각 목의 비율에서 그 자회사 주식의 소유비율을 뺀 비율을 곱한 금액을 그 자회사 주식의 소유비율로 나누어 산출한 금액 가. 해당 자회사가 상장법인 또는 국외상장법인이거나 공동출자법인인 경우에는 100분의 30 나. 벤처지주회사의 자회사인 경우에는 100분의 20 다. 가목 및 나목에 해당하지 아니하는 경우에는 100분의 50 ① 주권상장법인의 임원 또는 주요주주(대통령령으로 정하는 자는 제외한다)가 특정증권등의 매매, 그 밖의 거래(상속ㆍ주식배당 등 대통령령으로 정하는 부득이한 사유로 하는 매매, 그 밖의 거래를 제외한다. 이하 이 조 및 제429조에서 “거래등”이라 한다)를 하려는 때에는 거래목적, 거래가격, 거래수량, 거래기간 등 대통령령으로 정하는 사항(이하 “거래계획”이라 한다)을 그 거래기간의 개시일 전 30일 이상 90일 이내의 대통령령으로 정하는 기간까지 증권선물위원회와 거래소에 각각 보고하여야 한다. 다만, 거래계획의 거래수량 및 거래금액과 그 거래계획의 개시일 기준 과거 6개월간 거래수량 및 거래금액을 합산하여 대통령령으로 정하는 규모 미만인 경우에는 그러하지 아니하다. ② 제1항에 따라 거래계획을 보고한 자(이하 이 조에서 “거래계획 보고자”라 한다)는 그 거래계획을 보고한 때부터 그 거래계획에 따른 거래기간의 종료일까지는 새로운 거래계획을 보고하여서는 아니 된다. ③ 거래계획 보고자는 그 거래계획에 따라 특정증권등의 거래등을 하여야 한다. 다만, 거래 당시의 시장 상황 등을 반영하여 필요한 경우에 한정하여 거래금액의 100분의 30 이하의 비율로서 대통령령으로 정하는 바에 따라 거래계획과 달리 거래등을 할 수 있다. ④ 거래계획 보고자는 사망, 파산, 시장변동성 확대로 과도한 손실이 예상되는 경우 등 대통령령으로 정하는 부득이한 사유가 발생하는 때에는 대통령령으로 정하는 바에 따라 증권선물위원회와 거래소에 보고한 후 그 거래계획을 철회할 수 있다. ⑤ 증권선물위원회와 거래소는 제1항에 따라 보고된 거래계획(제4항에 따라 철회된 경우를 포함한다)을 3년간 갖추어 두고, 인터넷 홈페이지 등을 이용하여 공시하여야 한다. ⑥ 제1항부터 제5항까지에서 규정한 사항 외에 거래계획의 보고 등에 필요한 사항은 대통령령으로 정한다. |
한편 당사는 당사 최대주주인 OCI홀딩스 포함 특수관계인과 다양한 매출 매입활동을 진행하고 있습니다. 당사 외형규모 고려 시 해당 매출 매입금액이 유의적인 수준은 아니나, 향후 특수관계자 거래 규모가 증가할 경우 거래의 적정성에 대해 공정거래위원회 및 세무당국의 조사가 진행될 수 있는 점 참고부탁드립니다.
| [ 당사 특수관계자 현황(자회사) ] |
| 기업명 | 지분율(%) | |
|---|---|---|
| 2025년 1분기말 | 2024년말 | |
| Contera Pharma A/S | 99.33 | 99.33 |
| 부광메디카(주) | 100 | 100 |
| ProteKt Therapeutics | 97.24 | 97.24 |
| JaguAHR Therapeutics | 75.02 | 75.02 |
| (자료 : 당사 사업보고서 및 분기보고서) |
| [당사 특수관계자 현황(기타특수관계자) ] |
| 구 분 | 2025년 1분기말 | 2024년말 |
|---|---|---|
| 공동기업 | - | - |
| 관계기업 | 덴탈플랫폼투자조합제1호 | 덴탈플랫폼투자조합제1호 |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | OCI홀딩스 주식회사 |
| (주)디씨알이 | (주)디씨알이 | |
| 오씨아이드림(주) | 오씨아이드림(주) | |
| OCI(주) | OCI(주) | |
| OCI정보통신 | OCI정보통신(주) |
| (자료 : 당사 사업보고서 및 분기보고서) |
| [당사 특수관계자 매출매입현황(2025년 1분기)] |
| (단위: 원) |
| 구 분 | 기업명 | 2025년 1분기 | |
|---|---|---|---|
| 매출 등 | 매입 등 | ||
| 종속기업 | 부광메디카(주) | 80,069,740 | 331,530,400 |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | 16,646,721 | 5,805,473 |
| (주)디씨알이 | 1,883,182 | - | |
| 오씨아이드림㈜ | 2,486,000 | - | |
| OCI㈜ | 18,014,997 | 19,200,000 | |
| OCI정보통신 | - | 153,965,400 | |
| 합 계 | 119,100,640 | 510,501,273 | |
| (자료 : 당사 분기보고서) |
| [당사 특수관계자 매출매입현황(2024년 1분기)] |
| (단위: 원) |
| 구 분 | 기업명 | 2024년 1분기 | |
|---|---|---|---|
| 매출 등 | 매입 등 | ||
| 종속기업 |
Contera Pharma A/S |
19,989,800 | - |
| 부광메디카(주) | 13,847,214 | 327,211,000 | |
| 다이나세라퓨틱스(주) | 5,904,000 | - | |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | 17,823,292 | 9,333,026 |
| (주)디씨알이 | 5,525,818 | - | |
| 오씨아이드림㈜ | 4,503,000 | 63,908 | |
| OCI㈜ | 9,901,472 | 6,931,982 | |
| 합 계 | 77,494,596 | 343,539,916 | |
| (자료 : 당사 분기보고서) |
| 나. 수익성 악화 위험 당사의 별도 기준 매출액은 2021년 1,816억 원에서 2022년 1,903억 원으로 4.79% 증가하였으나, 2023년에는 1,252억 원으로 34.24% 감소하였습니다. 이는 2023년 당사가 내부 조직을 개편하고 도매상 중심의 유통구조를 재정비하는 등 질적 성장을 위한 경영 전략을 추진한 데에 따른 결과입니다. 이에 따라 영업이익도 2022년 123억 원에서 2023년에는 172억 원의 영업손실로 전환되었습니다. 다만, 경영구조 개편의 효과가 2024년부터 본격적으로 나타나면서, 당사의 2024년 매출액은 전년 대비 25.91% 증가한 1,576억 원을 기록하였으며, 영업이익 또한 170억 원으로 흑자 전환에 성공하였습니다. 한편, 2025년 1분기에는 당사의 주요 치료제 제품의 급격한 매출 성장이 나타나며 매출액은 전년 동기 대비 28.9% 증가한 439억원, 영업이익은 188.1% 증가한 59억원을 기록하며 호실적을 나타냈습니다. 연결기준 수익성의 경우 자회사의 임상개발 비용 등으로 인해 연구개발비가 연간 70억 원에서 190억 원 수준으로 발생하고 있으며, 이로 인해 별도 기준에 비해 열위에 있는 모습입니다. 다만, 2024년에는 전년도 경영구조 개편의 효과가 온전히 반영됨에 따라 영업이익 16억 원을 기록하며 흑자 전환에 성공하였습니다. 하지만 2025년 1분기에는 일회성 비용이 나타나며 호실적에도 불구하고 연결기준 1억원의 당기순손실을 기록했지만, 당사의 향후 실적에 미치는 영향은 미미할 것으로 판단됩니다. 당사는 향후 연결 및 별도 기준 모두에서 수익성이 점진적으로 개선될 것으로 전망하고 있으며, 2023년과 같은 대규모 영업손실이 재차 발생할 가능성은 제한적이라고 판단하고 있습니다. 다만, 당사가 속한 제약업종은 식품의약품안전처 등 규제기관의 추가 규제, 임상시험 진행에 따른 추가 연구개발비 발생, 경쟁 제품 출시 등의 예상치 못한 변수에 지속적으로 노출되어 있습니다. 이로 인해 당사의 매출이 감소하거나 수익성이 악화되는 등 영업 환경에 부정적인 영향을 미칠 수 있으므로, 투자자 여러분께서는 이 점을 유의하여 주시기 바랍니다. |
당사는 1960년 10월 17일에 의약품의 제조 및 판매를 목적으로 설립되었습니다. 현재 의약품, 건강기능식품, 의약외품 등을 주요 사업으로 영위하고 있으며, 주요 제품으로는 훼로바, 레가론, 덱시드, 치옥타시드, 씬지로이드 등이 있습니다. 한편, Global Open Innovation 전략의 일환으로 해외 자회사 및 제휴 업체와 협력하여 파킨슨병, 조현병 등 중추신경계(CNS) 질환 치료제와 면역항암제, 신경염증성 질환 치료제 등의 개발도 추진하고 있습니다.
당사의 주요 제품별 매출 현황은 다음과 같습니다.
| [ 당사 제품군별 매출현황 ] |
| (단위: 백만원) |
| 매출 | 품 목 | 구체적용도 | 주요상표등 | 2025년 1분기 |
2024 | 2023 | 2022 | 2021 |
| 제품 | 씬지로이드 | 갑상선 부갑상선 호르몬제 | 씬지로이드정 | 2,168 | 10,353 | 7,373 | 6,987 | 8,487 |
| 덱시드정 | 당뇨병성 신경병증 치료제 | 덱시드정 | 4,423 | 10,704 | - | 21,100 | 18,466 | |
| 치옥타시드 | 당뇨병성 신경병증 치료제 | 치옥타시드정 | 3,317 | 10,696 | 5,518 | 11,857 | 12,821 | |
| 훼로바 | 빈혈치료제 | 훼로바유서방정 | 3,525 | 17,415 | 13,424 | 11,801 | 13,586 | |
| 레가론 | 간질환치료제 | 레가론캡슐140 | 3,548 | 13,171 | 4,402 | 17,714 | 15,985 | |
| 타세놀 | 해열,진통,소염제 | 타세놀정 | 1,958 | 6,076 | 8,196 | 9,437 | 9,482 | |
| 헥사메딘액 | 구내염증완화제 | 헥사메딘액 | 1,109 | 3,939 | 4,200 | 5,627 | 4,510 | |
| 오르필 | 간질치료제 | 오르필서방정 | - | 3,882 | 3,920 | 6,416 | 6,240 | |
| 액시마 | 기관지확장제 | 액시마정 | 1,579 | 4,540 | 3,907 | 4,683 | 4,492 | |
| 플루닐 | 해독제 | 플루닐주사 | - | - | 3,205 | - | - | |
| 기타 | - | - | 19,246 | 64,434 | 49,680 | 64,102 | 56,971 | |
| 소 계 | - | - | 40,873 | 145,210 | 103,825 | 159,724 | 151,040 | |
| 상품 | 7,280 | 16,993 | 25,510 | 36,991 | 37,385 | |||
| 수출/기타 | 44 | 481 | 150 | 217 | 63 | |||
| 단순합계 | 48,197 | 162,684 | 129,485 | 196,932 | 188,488 | |||
| 내부거래제거 | (391) | (2,597) | (3,557) | (6,023) | (5,997) | |||
| 매출액 | 47,806 | 160,087 | 125,928 | 190,909 | 182,491 | |||
| (자료 : 당사 사업보고서 및 분기보고서) |
당사는 매출액 기준 상위 10개 제품을 개별 공시하고 있으며, 이외 제품은 '기타'로 구분하여 표시하고 있습니다. 매출 구성은 제품 매출이 절대적인 비중을 차지하고 있으며, 원가율이 높은 상품 매출은 점진적으로 감소하는 추세를 보이고 있습니다. 이는 수익성 개선을 목표로 상품 비중을 전략적으로 축소하고자 하는 당사의 경영방침에 따른 결과입니다. 또한, 상위 10개 제품군은 연도별로 안정적인 시장 점유율을 유지하고 있으나, 2023년의 덱시드정, 2025년 1분기의 오르필 및 플루닐 등은 생산능력 부족에 따른 타 품목 공급부족 해소를 위한 유통재고 관리로 인해 매출이 감소하여 상위 10개 제품에서 제외되었으며, 이에 따라 '기타' 항목으로 분류되어 있습니다.
한편, 당사의 별도 기준 요약손익계산서는 다음과 같습니다.
| [ 당사 요약 별도손익계산서] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 |
|---|---|---|---|---|---|---|
| 매출액 | 43,850 | 34,029 | 157,607 | 125,176 | 190,339 | 181,631 |
| 매출원가 | 23,292 | 18,554 | 83,886 | 79,039 | 111,793 | 107,184 |
| 매출총이익 | 20,558 | 15,475 | 73,721 | 46,137 | 78,546 | 74,447 |
| 판매비와관리비 | 12,677 | 10,704 | 46,802 | 47,826 | 54,222 | 46,335 |
| 경상연구개발비 | 1,946 | 2,711 | 9,915 | 15,483 | 12,002 | 14,948 |
| 영업이익(손실) | 5,935 | 2,060 | 17,004 | (17,173) | 12,322 | 13,163 |
| 기타수익 | 823 | 93 | 5,971 | 478 | 619 | 3,763 |
| 기타비용 | 83 | 453 | 66,441 | 6,514 | 783 | 3,449 |
| 금융수익 | 1,338 | 1,655 | 5,288 | 3,257 | 3,270 | 4,258 |
| 금융비용 | 5,428 | 953 | 14,232 | 3,245 | 8,559 | 8,186 |
| 법인세비용차감전순이익(손실) | 2,585 | 2,403 | (52,410) | (23,196) | 6,870 | 9,550 |
| 법인세비용(수익) | (208) | 419 | 3,200 | (4,103) | 4,828 | 7,112 |
| 당기순이익(손실) | 2,794 | 1,983 | (55,610) | (19,093) | 2,042 | 2,438 |
| 매출총이익율 | 46.88% | 45.48% | 46.78% | 36.86% | 41.27% | 40.99% |
| 경상연구개발비율 | 4.44% | 7.97% | 6.29% | 12.37% | 6.31% | 8.23% |
| 영업이익율 | 13.53% | 6.05% | 10.79% | -13.72% | 6.47% | 7.25% |
| 순이익율 | 6.37% | 5.83% | -35.28% | -15.25% | 1.07% | 1.34% |
| (자료 : 당사 사업보고서 및 분기보고서) |
당사의 별도 기준 매출액은 2021년 1,816억 원에서 2022년 1,903억 원으로 4.79% 증가하였으나, 2023년에는 1,252억 원으로 34.24% 감소하였습니다. 이는 2023년 당사가 내부 조직을 개편하고 도매상 중심의 유통구조 재정비를 통하여 채권회수에 주력한 결과 매출채권 약 62.2% 감소 하였고, 효율성이 낮은 일부 도매상 정리를 통하여 전체 도매상 수 약 13.5% 감소하는 등 질적 성장을 위한 경영 전략을 추진한 데에 따른 결과입니다. 이 과정에서 제품의 매출 비중이 일시적으로 감소하였으며, 시중 재고 수준이 높은 일부 품목의 출하를 축소함에 따라 전체 매출액이 감소하였습니다. 이에 따라 영업이익도 2022년 123억 원에서 2023년에는 172억 원의 영업손실로 전환되었습니다. 다만, 경영구조 개편의 효과가 2024년부터 본격적으로 나타나면서, 당사의 2024년 매출액은 전년 대비 25.91% 증가한 1,576억 원을 기록하였으며, 영업이익 또한 170억 원으로 흑자 전환에 성공하였습니다. 아울러 공헌이익 기반의 품목 재구성을 통한 매출 구조 개선과 구매원가 절감 전략을 지속적으로 추진한 결과, 2024년 영업이익률은 10.79%를 기록하며 최근 4개년 중 가장 높은 수익성을 달성하였습니다. 한편, 당기순이익은 종속기업 투자주식의 손상차손 반영에 따라 기타비용이 증가함으로써 적자를 기록하였습니다. 손상차손 관련 상세 내용은 회사위험-라. 자회사 손상차손 관련 위험 에서 확인하실 수 있습니다.
2025년 1분기 당사의 별도 기준 매출액은 439억원, 영업이익은 59억원을 기록하며 전년 동기 대비 각각 28.9%, 188.1% 상승하였습니다. 당뇨병성 신경병증 치료제 ‘덱시드’와 ‘치옥타시드’가 전년 동기 대비 234%의 매출 성장을 보이며 실적 반등과 수익성 회복을 이끌었습니다. 또한, 상급종합병원 110개소에서 당사의 항정신병 신약 '라투다정'의 처방이 개시되었고 의원급 의료기관에서도 50%이상 커버리지를 확보하는 등 안정적으로 시장에 안착하며 실적 개선에 기여하였습니다.
당사의 연결 기준 요약손익계산서는 다음과 같습니다.
| [ 당사 요약 연결손익계산서] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 |
|---|---|---|---|---|---|---|
| 매출액 | 47,806 | 34,393 | 160,087 | 125,928 | 190,909 | 182,491 |
| 매출원가 | 26,909 | 18,730 | 85,744 | 78,855 | 111,481 | 106,733 |
| 매출총이익 | 20,897 | 15,664 | 74,343 | 47,074 | 79,429 | 75,758 |
| 판매비와관리비 | 13,431 | 11,236 | 49,295 | 50,019 | 55,385 | 47,671 |
| 경상연구개발비 | 4,452 | 6,056 | 23,430 | 34,551 | 24,274 | 22,465 |
| 영업이익(손실) | 3,014 | (1,628) | 1,618 | (37,497) | (231) | 5,622 |
| 기타수익 | 835 | 54 | 10,097 | 2,300 | 569 | 439 |
| 기타비용 | 115 | 453 | 13,929 | 2,002 | 630 | 185 |
| 금융수익 | 1,377 | 1,792 | 5,680 | 3,846 | 3,450 | 4,265 |
| 금융비용 | 5,434 | 1,629 | 7,077 | 5,315 | 4,249 | 4,992 |
| 지분법이익(손실) | 0 | (261) | 641 | (901) | 59 | (1,361) |
| 법인세비용차감전순이익(손실) | (323) | (2,125) | (2,970) | (39,569) | (1,033) | 3,787 |
| 법인세비용(수익) | 212 | 433 | 489 | (5,163) | 3,216 | 6,584 |
| 당기순이익(손실) | (111) | (2,558) | (3,459) | (34,407) | (4,249) | (2,797) |
| 매출총이익율 | 43.71% | 45.54% | 46.44% | 37.38% | 41.61% | 41.51% |
| 경상연구개발비율 | 9.31% | 17.61% | 14.64% | 27.44% | 12.72% | 12.31% |
| 영업이익율 | 6.31% | -4.73% | 1.01% | -29.78% | -0.12% | 3.08% |
| 순이익율 | -0.23% | -7.44% | -2.16% | -27.32% | -2.23% | -1.53% |
| (자료 : 당사 사업보고서 및 분기보고서) |
당사의 자회사는 주로 임상시험 등 연구개발 활동을 수행하고 있어, 제한적인 매출만을 창출하고 있습니다. 이에 따라 연결 기준 매출액은 별도 기준 매출액과 유사한 수준을 유지하고 있습니다. 그러나 자회사의 임상개발 비용 등으로 인해 연구개발비가 연간 70억 원에서 190억 원 수준으로 발생하고 있으며, 이로 인해 연결 기준 수익성은 별도 기준에 비해 열위에 있는 모습입니다. 2023년에는 당사의 경영구조 개편에 따른 매출 감소와 더불어 자회사의 JM-010 임상 관련 비용이 크게 증가하면서 375억 원의 영업손실을 기록하였습니다. 다만, 2024년에는 해당 임상이 중단되었고, 전년도 경영구조 개편의 효과가 온전히 반영됨에 따라 영업이익 16억 원을 기록하며 흑자 전환에 성공하였습니다.
한편, 2025년 1분기 당사의 연결 기준 매출액은 478억원, 영업이익은 30억원을 기록하며 전년 동기 대비 39%의 매출 성장 및 영업이익 흑자를 달성하였습니다. 그러나 당기순손실 1억원을 기록하며 순이익 흑자 전환에는 실패했는데, 이는 당사가 전략적 파트너로서 출자하여 보유한 TVM Life Science Ventures Vll의 수익증권에 대한 공정가치측정 금융자산 평가손실 42억원을 인식한 것에 기인하였으며, 해당 비용의 경우 일회성 비용에 해당하여 향후 당사의 영업수익성에 미치는 영향은 미미한 것으로 판단됩니다.
당사는 향후 연결 및 별도 기준 모두에서 수익성이 점진적으로 개선될 것으로 전망하고 있으며, 2023년과 같은 대규모 영업손실이 재차 발생할 가능성은 제한적이라고 판단하고 있습니다. 다만, 당사가 속한 제약업종은 식품의약품안전처 등 규제기관의 추가 규제, 임상시험 진행에 따른 추가 연구개발비 발생, 경쟁 제품 출시 등의 예상치 못한 변수에 지속적으로 노출되어 있습니다. 이로 인해 당사의 매출이 감소하거나 수익성이 악화되는 등 영업 환경에 부정적인 영향을 미칠 수 있으므로, 투자자 여러분께서는 이 점을 유의하여 주시기 바랍니다.
| 다. 재무건전성 위험 당사의 연결 기준 재무건전성은 타 제약사 대비 상대적으로 우수한 수준을 유지하고 있습니다. 유동비율은 2023년을 제외하고 500% 내외를 기록해 왔으며, 2023년에는 기타유동부채가 증가하면서 유동비율이 일시적으로 260% 수준으로 하락하였습니다. 다만 2024년 기타유동부채는 크게 감소하며 유동비율은 다시 500% 이상 수준으로 회복되었습니다. 부채비율은 2021년과 2022년에 41~48% 수준을 유지하였으나, 2023년에는 일시적인 영업적자, 신규 차입금 발생, 기타유동부채 증가 등이 복합적으로 작용하면서 83.13%로 상승하였습니다. 그러나 2024년에는 수익성 개선과 함께 기타유동부채가 상환되며, 부채비율은 52.85%로 개선되었고, 2025년 1분기말까지 유사한 수준을 유지하고 있습니다. 2021년 및 2022년 총차입금의존도는 1% 미만을 기록하였고, 보유 현금이 총차입금을 초과함에 따라 순차입금도 마이너스(-) 상태를 유지하였습니다. 2023년에는 신규 차입이 발생하면서 총차입금의존도가 18.50%로 증가하였고, 2024년에는 기타유동부채 상환에 따른 총자산 감소의 영향으로 21.28%로 소폭 상승하였고, 2025년 1분기말에도 동일한 수준을 유지하고 있습니다. 그럼에도 불구하고, 보유 현금이 총차입금을 상회함에 따라 순차입금은 여전히 음(-)의 상태를 유지하고 있습니다. 당사는 2023년 경영 전략 구조 개편 과정에서 영업손실이 발생함에 따라 일시적으로 재무건전성이 다소 약화되었으나, 2024년 영업 정상화와 함께 재무건전성은 개선되었습니다. 한편 22년 이후 당사의 순차입금 증가와 영업적자 전환 등의 사유로 인해 당사의 이자보상배율은 악화되는 추세를 보였습니다.다만, 2025년 이후 라투다정을 중심으로 매출액 및 수익성 개선이 기대되고 있는 상황임에 따라 당사의 이자보상배율은 점진적인 개선 추세를 보일 것으로 전망되며, 2025년 1분기 전년동기대비 급격히 증가된 이자보상배율 수준을 나타내며 실제로 개선되는 모습을 보이고 있습니다. 전반적으로 당사는 타사 대비 우수한 재무구조를 유지하고 있습니다. 다만, 향후 예상치 못한 외부 요인으로 인해 영업실적이 악화될 경우, 재무건전성에도 부정적인 영향이 발생할 수 있는 점을 투자자 여러분께서는 유의해 주시기 바랍니다. |
당사의 연결 기준 재무건전성은 타 제약사 대비 상대적으로 우수한 수준을 유지하고 있습니다. 유동비율은 2023년을 제외하고 500% 내외를 기록해 왔으며, 2023년에는 자회사 Contera Pharma A/S에 출자한 에이치델타 사모투자합자회사의 주식매수청구권(Put Option) 행사 기한 도래로 기타유동부채가 증가하면서 유동비율이 일시적으로 260% 수준으로 하락하였습니다. 그럼에도 불구하고, 이는 여전히 양호한 수치로 평가됩니다. 해당 주식매수청구권은 2024년 투자자의 권리 행사에 따라 당사가 인수대가 632억 원에 전량 회수하였고, 이로 인해 2024년 기타유동부채는 크게 감소하며 유동비율은 다시 500% 이상 수준으로 회복되었습니다. 부채비율은 2021년과 2022년에 41~48% 수준을 유지하였으나, 2023년에는 일시적인 영업적자, 신규 차입금 발생, 기타유동부채 증가 등이 복합적으로 작용하면서 83.13%로 상승하였습니다. 그러나 2024년에는 수익성 개선과 함께 기타유동부채가 상환되며, 부채비율은 52.85%로 개선되었습니다. 2025년 1분기말 기준 부채비율은 52.88%로, 2024년 말과 같은 수준을 유지하고 있습니다.
당사는 한동안 무차입 경영 기조를 유지해 왔으며, 이에 따라 2021년 및 2022년 총차입금의존도는 1% 미만을 기록하였고, 보유 현금이 총차입금을 초과함에 따라 순차입금도 마이너스(-) 상태를 유지하였습니다. 2023년에는 신규 차입이 발생하면서 총차입금의존도가 18.50%로 증가하였고, 2024년에는 기타유동부채 상환에 따른 총자산 감소의 영향으로 21.28%로 소폭 상승하였고 2025년 1분기까지 유사한 차입 수준을 유지하고 있습니다. 그럼에도 불구하고, 보유 현금이 총차입금을 상회함에 따라 순차입금은 여전히 음(-)의 상태를 유지하고 있습니다. 차입금 실행 및 기타유동부채 상환 등은 모두 당사(별도 기준)에서 발생한 사항으로, 별도 기준 재무안정성 지표 역시 연결 기준과 유사한 흐름을 보이고 있습니다.
당사의 요약 기준 연결재무상태표 및 별도재무상태표는 다음과 같습니다.
| [ 당사 요약 연결재무상태표] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기말 |
2024 | 2023 | 2022 | 2021 |
| 자산 | 372,643 | 373,180 | 429,017 | 400,929 | 397,417 |
| 유동자산 | 206,464 | 203,739 | 254,179 | 218,741 | 220,095 |
| 비유동자산 | 166,179 | 169,441 | 174,839 | 182,188 | 177,321 |
| 부채 | 128,901 | 129,035 | 194,752 | 129,082 | 117,356 |
| 유동부채 | 35,243 | 35,398 | 97,544 | 44,603 | 36,995 |
| 비유동부채 | 93,658 | 93,637 | 97,208 | 84,479 | 80,361 |
| 자본총계 | 243,742 | 244,145 | 234,265 | 271,847 | 280,061 |
| 총차입금 | 80,159 | 79,424 | 79,387 | 931 | 1,558 |
| 유동리스부채 | 381 | 130 | 218 | 243 | 444 |
| 장기차입금 | 79,135 | 79,024 | 78,525 | - | - |
| 비유동리스부채 | 643 | 270 | 644 | 688 | 1,114 |
| 현금및현금성자산 | 87,813 | 90,091 | 151,227 | 85,517 | 82,777 |
| 순차입금 | (7,655) | (10,667) | (71,840) | (84,586) | (81,219) |
| 유동비율 | 585.83% | 575.56% | 260.58% | 490.42% | 594.94% |
| 부채비율 | 52.88% | 52.85% | 83.13% | 47.48% | 41.90% |
| 총차입금의존도 | 21.51% | 21.28% | 18.50% | 0.23% | 0.39% |
| 순차입금의존도 | -2.05% | -2.86% | -16.75% | -21.10% | -20.44% |
| (자료 : 당사 사업보고서 및 분기보고서) |
| [ 당사 요약 별도재무상태표] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기말 |
2024 | 2023 | 2022 | 2021 |
| 자산 | 372,231 | 370,080 | 460,536 | 420,612 | 406,936 |
| 유동자산 | 196,039 | 190,618 | 232,286 | 192,377 | 186,485 |
| 비유동자산 | 176,192 | 179,462 | 228,250 | 228,235 | 220,451 |
| 부채 | 126,830 | 127,169 | 173,812 | 110,413 | 95,842 |
| 유동부채 | 33,581 | 33,945 | 78,226 | 42,979 | 35,312 |
| 비유동부채 | 93,249 | 93,224 | 95,586 | 67,434 | 60,530 |
| 자본총계 | 245,401 | 242,911 | 286,724 | 310,199 | 311,094 |
| 총차입금 | 80,149 | 79,415 | 79,379 | 878 | 1,399 |
| 유동리스부채 | 381 | 130 | 218 | 197 | 365 |
| 장기차입금 | 79,135 | 79,024 | 78,525 | - | - |
| 비유동리스부채 | 633 | 261 | 636 | 680 | 1,034 |
| 현금및현금성자산 | 80,903 | 79,680 | 132,380 | 61,821 | 51,442 |
| 순차입금 | (754) | (265) | (53,001) | (60,943) | (50,044) |
| 유동비율 | 583.79% | 561.55% | 296.94% | 447.60% | 528.11% |
| 부채비율 | 51.68% | 52.35% | 60.62% | 35.59% | 30.81% |
| 총차입금의존도 | 21.53% | 21.46% | 17.24% | 0.21% | 0.34% |
| 순차입금의존도 | -0.20% | -0.07% | -11.51% | -14.49% | -12.30% |
| (자료 : 당사 사업보고서 및 분기보고서) |
한편 22년 이후 당사의 순차입금 증가와 영업적자 전환 등의 사유로 인해 당사의 이자보상배율은 악화되는 추세를 보였습니다. 2022년 연결기준 이자보상배율은 -0.13으로 연결영업적자로 인해 마이너스 전환하였으며 2023년의 경우 연결,별도 기준 영업이익이 모두 적자전환함에 따라 이자보상배율은 연결,별도 기준 모두 마이너스 전환 하였습니다. 다만, 경영구조 개편의 효과가 2024년부터 본격적으로 나타나면서, 당사의 별도기준 2024년 매출액은 전년 대비 25.91% 증가한 1,576억 원을 기록하였으며, 영업이익 또한 170억 원으로 흑자 전환에 성공하였습니다. 연결기준 영업이익 또한 16억원으로 흑자전환 함에 따라 당사의 2024년 이자보상배율은 플러스 전환하게 되었습니다. 그러나 2023년의 신규 차입 영향으로 인해, 영업이익이 발생했음에도 불구하고 2024년 이자보상배율은 0.25로 여전히 1 미만의 수준을 보이고 있습니다. 다만, 2025년 이후 라투다정을 중심으로 매출액 및 수익성 개선이 기대되고 있는 상황임에 따라 당사의 이자보상배율은 점진적인 개선 추세를 보일 것으로 전망되며, 2025년 1분기 당사의 실적 호조 및 수익성 증가로 연결 기준 영업이익 30억원, 별도 기준 영업이익 59억원을 기록하며 이자보상배율은 연결기준 2.83, 별도기준 5.84를 기록해 전년 동기 대비 실제로 큰 폭 개선되는 모습을 보이고 있습니다.
| [ 당사 연결기준 이자보상배율] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 | 2024년 1분기 | 2024년 | 2023년 | 2022년 | 2021년 |
|---|---|---|---|---|---|---|
| 영업이익 | 3,014 | -1,628 | 1,618 | -37,497 | -231 | 5,622 |
| 이자비용 | 1,064 | 1,537 | 6,490 | 3,808 | 1,760 | 1,408 |
| 이자보상배율 |
2.83 | -1.06 | 0.25 | -9.85 | -0.13 | 3.99 |
| (자료 : 당사 사업보고서 및 분기보고서) |
| [ 당사 별도기준 이자보상배율] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 | 2024년 1분기 | 2024년 | 2023년 | 2022년 | 2021년 |
|---|---|---|---|---|---|---|
| 영업이익 | 5,935 | 2,060 | 17,004 | -17,173 | 12,322 | 13,163 |
| 이자비용 | 1,016 | 1,147 | 4,549 | 1,298 | 162 | 323 |
| 이자보상배율 |
5.84 | 1.80 | 3.74 | -13.23 | 76.07 | 40.76 |
| (자료 : 당사 사업보고서 및 분기보고서) |
당사의 차입금은 하나은행 및 신한은행으로부터 차입하였으며 만기는 2026년 도래할 예정입니다. 다만, 당사의 보유 현금 규모 및 영업현금흐름 고려 시 해당 차입금 상환에는 무리가 없을 것으로 판단되고 있습니다.
| [ 당사 차입금 현황] |
| (단위: 원) |
| 구 분 | 차입처 | 최종 만기일 | 연이자율(%) | 2025년 1분기말 | 2024년말 |
| 원화장기차입금 | 하나은행 | 2026-08-16 | CD91일물 + 1.484 | 30,000,000,000 | 30,000,000,000 |
| 원화장기차입금(*) | 신한은행 | 2026-10-13 | CD91일물+ 1.39 | 50,000,000,000 | 50,000,000,000 |
| 소계 | 80,000,000,000 | 80,000,000,000 | |||
| 유동성 대체 | - | - | |||
| 차감 : 장기차입금할인발행차금 | (864,753,074) | (975,816,626) | |||
| 합계 | 79,135,246,926 | 79,024,183,374 | |||
| (자료 : 당사 분기보고서) (*)상기 차입금과 관련하여 유형자산을 담보로 제공하고 있습니다 |
또한 당사는 K-IFRS 제1016호에 따라 보유 중인 자산의 실질 가치를 재무제표에 충실히 반영하고자 자산평가방법으로 재평가모형을 적용하고 있으며, 토지에 대한 자산 재평가 용역을 수행하고 있습니다. 토지 자산 재평가 주기와 관련하여, K-IFRS 기준에서는 "공정가치와 장부금액 간 차이가 중요한 경우에는 매년, 차이가 크지 않은 경우에는 3년 이내의 간격으로 재평가를 실시”하도록 규정하고 있습니다. 이에 따라 당사는 3년 주기로 토지 재평가를 실시하고 있으며, 최근 재평가 연도는 2024년으로, 과거에는 2021년 및 2018년에 동일하게 주기적으로 자산 재평가를 진행한 바 있습니다. 본 재평가를 위하여 당사는 대일감정평가법인에 용역을 의뢰하였으며, 2024년12월2일에 용역계약을 체결하고, 동 감정평가법인이 12월20일까지 감정업무를 수행하였습니다. 감정 결과, 기존 929억원으로 평가되었던 토지 자산이 1,133억원으로 재평가되었으며, 평가차액 204억 원은 기타포괄손익누계액으로 계상하였습니다.
| [당사 2024년 유형자산의 변동내역] |
| (단위: 원) |
| 구 분 | 기초순장부가액 | 취득 | 처분 | 기타(*) | 토지재평가 | 감가상각비 | 기말순장부가액 |
| 토지 | 92,875,100,000 | - | - | - | 20,438,400,000 | - | 113,313,500,000 |
| 건물 | 23,735,300,197 | - | - | - | - | (1,692,912,600) | 22,042,387,597 |
| 구축물 | 232,739,888 | 49,000,000 | - | - | - | (59,397,662) | 222,342,226 |
| 기계장치 | 1,247,307,776 | 656,408,266 | (20,000) | - | - | (658,051,586) | 1,245,644,456 |
| 차량운반구 | 76,833,334 | 350,000 | 616,000 | - | - | (35,583,010) | 42,216,324 |
| 공구기구 | 994,536,545 | 717,344,800 | (2,761,319) | - | - | (438,280,428) | 1,270,839,598 |
| 비품 | 1,819,579,180 | 667,871,199 | (968,433) | (14,493,094) | - | (503,019,476) | 1,968,969,376 |
| 건설중인자산 | - | 311,171,100 | - | - | - | - | 311,171,100 |
| 합 계 | 120,981,396,920 | 2,402,145,365 | (3,133,752) | (14,493,094) | 20,438,400,000 | (3,387,244,762) | 140,417,070,677 |
| (자료 : 당사 사업보고서) (*) 기타증감액은 환율변동으로 인한 환산차이로 구성되어 있습니다. |
당사는 2023년 경영 전략 구조 개편 과정에서 영업손실이 발생함에 따라 일시적으로 재무건전성이 다소 약화되었으나, 2024년 영업 정상화와 함께 재무건전성은 개선되었습니다. 전반적으로 당사는 타사 대비 우수한 재무구조를 유지하고 있습니다. 다만, 향후 예상치 못한 외부 요인으로 인해 영업실적이 악화될 경우, 재무건전성에도 부정적인 영향이 발생할 수 있는 점을 투자자 여러분께서는 유의해 주시기 바랍니다.
| 라. 자회사 손상차손 관련 위험 당사는 당사의 Global Open Innovation 전략의 일환으로 다수 해외계열사를 보유하고 있습니다. 당사는 매 회계연도 말, 종속기업·관계기업·공동기업에 대한 투자주식의 손상징후를 검토하고, 손상검사를 수행하고 있습니다. 2024년에는 Contera Pharma A/S의 파이프라인 임상 중단 등의 사유로 인해 종속기업 투자주식 관련 손상차손 521억 원을 인식하였으며, 해당 금액은 당기의 기타비용으로 반영되었습니다. 투자주식 손상차손은 현금유출을 수반하지는 않지만, 기타비용으로 인식되어 순이익에는 부정적인 영향을 미칩니다. 향후에도 자회사의 임상 진행 과정에서 불확실성이 현실화될 경우, 추가적인 손상차손 인식이 필요할 수 있으며 이는 당사의 수익성 및 재무건전성뿐만 아니라 신용평가, 대외 평판, 거래처 협상력 등에도 부정적인 영향을 미칠 수 있습니다.따라서 투자자 여러분께서는 당사의 자회사 관련 손상차손 위험을 충분히 인지하신 후, 신중히 투자 의사결정을 내리시기 바랍니다. |
당사는 당사의 Global Open Innovation 전략의 일환으로 다수 해외계열사를 보유하고 있습니다. 증권신고서 제출일 현재 당사의 지분 투자 회사에 대한 내용 및 지분 취득 히스토리는 다음과 같습니다.
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| Contera Pharma A/S |
2010년 07월 09일 (주1) |
DTU Science Park Venlighedsvej 4 |
의약품 연구 및 개발사업 |
12,523 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
| 부광메디카 (주) |
2015년 06월 17일 (주2) |
서울특별시 동작구 상도로 5(대방동) |
완제 의약품 제조업 및 판매업 |
2,715 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
|
ProteKt Therapeutics |
2015년 01월 01일 (주3) |
16 Bar Kochva St., Bnei-Brak, Israel | 의약품 연구 및 개발사업 |
356 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
|
JaguAHR Therapeutics |
2019년 10월 14일 (주4) |
5 SHENTON WAY, #10-01, UIC BUILDING, SINGAPORE 068808 | 의약품 연구 및 개발사업 |
352 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
| 종속기업 | 소재지 | 지배지분율(%) | 결산월 | 업종 | |
|---|---|---|---|---|---|
| 2025년 1분기말 | 2024년말 | ||||
| Contera Pharma A/S | 덴마크 | 99.33 | 99.33 | 12월 | 의약품 연구 및 개발 |
| 부광메디카(주) | 한국 | 100 | 100 | 12월 | 완제 의약품 제조업 및 의약품 도매업 |
| JaguAHR Therapeutics | 싱가포르 | 75.02 | 75.02 | 12월 | 의약품 연구 및 개발 |
| ProteKt Therapeutics | 이스라엘 | 96.53 | 96.53 | 12월 | 의약품 연구 및 개발 |
| (자료 : 당사 사업보고서 및 분기보고서) (주1) 2014년 11월 24일 부광약품(주)에서 약 34억원을 출자하여 인수(지분율 100%) 2018년 07월 18일 14,000주 약 5.5억원 제3자배정 유상증자(지분율 96.26%) 2019년 07월 15일 10,000주 약 30억원 제3자배정 유상증자(지분율 94.38%) 2020년 07월 22일 40,000주 양도 및 352억원 제3자배정유상증자(지분율71.23%) 2022년 11월 14일 비지배주주의 매도청구권 행사로 인한 10,000주 매수(지분율 72.84%) 2023년 08월 17일 31,250주 약 100억원 유상증자(지분율 74.14%) 2024년 04월 01일 관계회사 에이치델타 사모투자합자회사의 주식매수청구권 행사로 인한 159,380주 매수 (지분율 98.56%) 2024년 08월 27일 413,793주 약 44억원 유상증자 (지분율 99.12%) 2024년 10월 27일 336,700주 약 30억원 유상증자 (지분율 99.33%) (주2) 2015년 06월 17일 부광약품(주)에서 5억원을 출자하여 설립 2015년 10월 17일 약 13억원의 현금출자 2015년 10월 20일 약 127억원 상당의 현물출자 2019년 03월 08일 50억원의 현금출자 2021년 01월 25일 110억원의 유상감자(부광약품(주) 지분율 100%) (주3) 2023년 01월 26일 기존 주주의 주식 3,869,472주를 인수하는 조건의 주주간계약을 체결하여 지배력을 확보함 (부광약품(주)지분율 96.53%) (주4) 2024년 11월 26일 설립 파트너사인 Aslan Pharma가 청산됨에 따라, Aslan Pharma로부터22,050주를 인수하는 계약을 체결하여 지배력을 확보함 (부광약품(주)지분율 75.02%) (주5) 지배회사 자산총액의 10%미만이거나 자산총액이 750억원 미만이므로 주요종속회사에 해당되지 않음 |
| [당사 타법인 출자현황(5% 이상)] |
| (단위: 백만원, 주) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
| CytoSite BioPharma Inc 우선주(주1) |
비상장 | 2018.08.06 | 단순 투자 |
1,720 | 624,973 | 8.54 | 1,720 | - | - | - | 624,973 | 8.54 | 1,720 | 278 | -1,337 |
| 덴탈플랫폼 출자조합제1호(주2) |
비상장 | 2019.05.28 | 단순 투자 |
2,000 | 200 | 50.00 | - | - | - | - | 200 | 50.00 | - | 68 | -2 |
| 합 계 | - | - | 1,720 | - | - | - | - | - | 1,720 | - | - | ||||
| (자료 : 당사 분기보고서) * 최초취득 금액은 총 투자금액을 표시함 (주1) 1. 2018년 08월 06일 약 8.5억 출자로 312,486주 취득 2. 2019년 09월 11일 약 4.5억 출자로 156,243주 취득 3. 2020년 09월 22일 약 8,500만원 출자로 30,636주 취득 4. 2021년 07월 01일 약 3.4억 출자로 125,608주 취득 (주2) 1. 2019년 05월 28일 20억원 출자로 200좌 취득 |
| [당사 타법인 출자현황(5% 미만)] |
| (단위: 백만원, 주) |
| 구분 | 상장 여부 |
법인명 또는 종목명 |
출자 목적 |
기초잔액 | 증가(감소)내역 | 기말잔액 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 최초 취득 금액 |
수량 | 지 분 율 |
장부 가액 |
취득(처분) | 평가/ 처분 손익 |
수량 | 지 분 율 |
장부 가액 |
비고 | |||||
| 수량 | 금액 | |||||||||||||
| 국외 | 상장 | Biodexa Pharmaceuticals (주1) | 단순 투자 |
- | 14,177 | 2.12 | 84 | - | - | -57 | 14,177 | 2.12 | 27 | - |
| 국외 | 상장 | Lyell immunopharma (주2) | 단순 투자 |
- | 1,410,071 | 0.48 | 1,327 | - | - | -210 | 1,410,071 | 0.48 | 1,117 | - |
| 국외 | 비상장 | 흥국글로벌 사모증권 (주3) (TVM Life Science Ventures Vll) |
단순 투자 |
18,961 | - | - | 9,951 | - | - | -4,190 | - | - | 5,761 | - |
| 국외 | 비상장 | TVM Life Science Innovation II (주4) |
단순 투자 |
3,201 | - | - | 3,084 | - | 331 | 338 | - | - | 3,753 | - |
| 국내 | 비상장 | KDB오픈이노베이션펀드 (주5) | 단순 투자 |
500 | - | 2.37 | 263 | - | - | - | - | 2.37 | 263 | - |
| 합계 | 22,662 | - | - | 14,709 | - | 331 | -4,119 | - | - | 10,921 | - | |||
| (자료 : 당사 분기보고서) (주1) 1. 파이프라인 'MLR-1023' 의 판권을 반환하는 대가로 354,428주의 Biodexa Pharmaceuticals 주식을 취득 2. 2024년 10월 중 액면병합으로 1:0.04 비율로 전환됨 (주2) 1. 2021년 07월 07일 11억원 출자로 76,378주 취득 2. 2021년 12월 24일 38억원 출자로 205,558주 취득 3. 2024년 11월 15일 ImmPACT Bio Ltd는 Lyell immunopharma에 합병되었으며 기존 주식은 현금 2,208백만원과 Lyell immunopharma 주식 1,419,071주로 교환됨 (주3) TVM Capital사가 운용하는 TVM Life Science Ventures Vll에 유한 책임 조합원과 Strategic Partner로서 투자 계약을 체결하고 흥국자산운용 주식회사가 해당 feeder fund의 구성을 위한 신탁계약을 체결함 (주4) TVM Capital사가 운용하는 TVM Life Science Ventures VllI에 유한 책임 조합으로서 투자 계약을 체결함 (주5) The Turning Point와 GSA PE가 운용하는 펀드이며, 총 약정금액 5억원 중 5억원 납입완료함 |
한편, 증권신고서 제출일 현재 당사의 종속기업, 관계기업 및 공동기업 투자주식 현황은 다음과 같습니다.
| [당사 종속기업, 관계기업 및 공동기업 투자주식 현황] |
| (단위: 원) |
| 구 분 | 종 목 | 소재국가 | 2025년 1분기말 | 2024년말 | ||
| 지분율(%) | 장부금액 | 지분율(%) | 장부금액 | |||
| 종속기업 | Contera Pharma A/S | 덴마크 | 99.33 | 10,871,136,907 | 99.33 | 10,871,136,907 |
| 부광메디카(주) | 대한민국 | 100.00 | 1,735,689,285 | 100.00 | 1,735,689,285 | |
| ProteKt Therapeutics | 이스라엘 | 97.24 | - | 97.24 | - | |
| JaguAHR Therapeutics | 싱가포르 | 75.02 | 1,428,331,853 | 75.02 | 1,428,331,853 | |
| 소 계 | 14,035,158,045 | 14,035,158,045 | ||||
| 관계기업 | 덴탈플랫폼출자조합제1호 | 대한민국 | 50.00 | - | 50.00 | - |
| 소 계 | - | - | ||||
| 합 계 | 14,035,158,045 | 14,035,158,045 | ||||
| (자료 : 당사 분기보고서) |
| [당사 종속기업, 관계기업 및 공동기업투자주식의 변동내역] |
| (단위: 원) |
| 구 분 | 2025년 1분기 | 2024년 1분기 |
| 기초금액 | 14,035,158,045 | 73,163,309,002 |
| 취득 | - | - |
| 손상차손 | - | - |
| 처분 | - | - |
| 기타(*) |
- | 143,153,759 |
| 분기말금액 | 14,035,158,045 | 73,306,462,761 |
| (자료 : 당사 분기보고서) (*) 2024년 1분기 중 종속기업인 Contera Pharma A/S와 관련된 주주 간 계약상 조건부대가의 변동을 장부가액에 가산하였습니다. |
당사는 매 회계연도 말, 종속기업·관계기업·공동기업에 대한 투자주식의 손상징후를 검토하고, 손상검사를 수행하고 있습니다. 투자주식의 회수가능액은 사용가치에 근거하여 산정되며, 미래현금흐름 추정에 따라 결정됩니다. 2024년에는 Contera Pharma A/S의 파이프라인 임상 중단 등의 사유로 인해 종속기업 투자주식 관련 손상차손 521억 원을 인식하였으며, 해당 금액은 당기의 기타비용으로 반영되었습니다.
또한, 당사의 외부 감사인인 안진회계법인은 2024년도 감사에서 종속기업투자주식(Contera Pharma A/S)의 손상검사와 종속기업(ProteKt Therapeutics)과 관련된 무형자산 손상검사를 핵심감사사항(Key Audit Matters)으로 판단하였습니다. 당사는 2024년 12월 31일 기준으로 Contera Pharma A/S 투자주식의 회수가능액을 추정하여 손상검사를 수행하였으며, 그 결과 총 480억 5,800만 원의 손상차손을 인식하였습니다. 해당 회수가능액 평가는 경영진의 유의적인 가정을 바탕으로 하며, 미래현금흐름 추정 과정에서 상당한 불확실성이 수반됩니다. 이에 따라 감사인은 해당 손상평가의 중요성과 경영진 추정의 유의성 등을 종합적으로 고려하여 이를 핵심감사사항으로 기재하였습니다.
한편, 투자주식 손상차손은 현금유출을 수반하지는 않지만, 기타비용으로 인식되어 순이익에는 부정적인 영향을 미칩니다. 향후에도 자회사의 임상 진행 과정에서 불확실성이 현실화될 경우, 추가적인 손상차손 인식이 필요할 수 있으며 이는 당사의 수익성 및 재무건전성뿐만 아니라 신용평가, 대외 평판, 거래처 협상력 등에도 부정적인 영향을 미칠 수 있습니다.따라서 투자자 여러분께서는 당사의 자회사 관련 손상차손 위험을 충분히 인지하신 후, 신중히 투자 의사결정을 내리시기 바랍니다.
| 마. 환율변동에 따른 위험 당사는 국제적으로 영업활동을 영위하고 있어 외환위험, 특히 주로 달러 및 유로화와 관련된 환율변동위험에 노출되어 있습니다. 현재로서 해당 환율변동이 당사의 수익성에 미치는 영향은 미미한 수준으로 판단됩니다. 다만 당사가 대외적으로 표명중인 Global Open Innovation 전략에 따라 당사는 향후에도 다양한 해외 제약회사 및 바이오벤처사와 협업을 진행할 예정입니다.특히, 당사가 현재 임상진행중인 파이프라인을 라이센스아웃 하거나 기존 라이센스아웃한 MLR-1023등과 관련하여 향후 수취하게될 benefit sharing 등은 모두 외화로 결제될 예정이며 당사가 계획중인 수출비중 확대 등이 현실화 될 경우 환율 변동이 당사에 미치는 영향은 더욱 커질 것으로 전망됩니다. 최근 글로벌 경제 및 정치적 상황의 불확실성, 중동 지정학적 리스크와 함께 트럼프 미국 대통령의 관세 등 예측불가능한 정책 으로 환율 변동성이 크게 확대되는 추세를 보이고 있습니다. 외부적인 요인에 의한 환율 변동은 당사의 수익성에 직간접적인 영향을 미칠 수 있으며 향후 그 영향도가 더욱 높아질 개연성이 존재합니다. 따라서 환율 변동의 불확실성 확대가 당사의 경영성과 및 재무상태에 영향을 미칠 수 있는점 투자자 여러분께서는 참고하시기 바랍니다. |
당사는 국제적으로 영업활동을 영위하고 있어 외환위험, 특히 주로 달러 및 유로화와 관련된 환율변동위험에 노출되어 있습니다. 외환위험은 당사가 보유하고 있는 외화표시 금융자산 및 금융부채, 해외사업장에 대한 순투자와 관련하여 발생하고 있습니다. 2025년 3월 31일 기준 다른 모든 변수가 일정하고 달러, 유로화 및 엔화에 대한 원화환율이 10% 변동시 당사의 세후 이익 및 자본에 미치는 영향은 아래 표와 같습니다.
| (단위: 원) |
| 구 분 | 세후 이익에 대한 영향 | 자본에 대한 영향 | |||
|---|---|---|---|---|---|
| 2025년 1분기 | 2024년 1분기 | 2025년 1분기 | 2024년 1분기 | ||
| 유로화/원 | 상승시 | (60,826,051) | (631,732,059) | (60,826,051) | (631,732,059) |
| 하락시 | 60,826,051 | 631,732,059 | 60,826,051 | 631,732,059 | |
| 미국달러/원 | 상승시 | (53,245,235) | - | (53,245,235) | - |
| 하락시 | 53,245,235 | - | 53,245,235 | - | |
| 일본엔화/원 | 상승시 | (403,818) | - | (403,818) | - |
| 하락시 | 403,818 | - | 403,818 | - | |
| (자료 : 당사 분기보고서) |
현재로서 해당 환율변동이 당사의 수익성에 미치는 영향은 미미한 수준으로 판단됩니다. 다만 당사가 대외적으로 표명중인 Global Open Innovation 전략에 따라 당사는 향후에도 다양한 해외 제약회사 및 바이오벤처사와 협업을 진행할 예정입니다.특히, 당사가 현재 임상진행중인 파이프라인을 라이센스아웃 하거나 기존 라이센스아웃한 MLR-1023등과 관련하여 향후 수취하게될 benefit sharing 등은 모두 외화로 결제될 예정이며 당사가 계획중인 수출비중 확대 등이 현실화 될 경우 환율변동이 당사에 미치는 영향은 더욱 커질 것으로 전망됩니다.
원/달러 환율 추이를 살펴보면, 2019년말 중국에서 발원한 신종 코로나 바이러스는 세계 금융시장에 큰 영향을 미치며 안전자산 선호심리로 인해 환율은 1,200원대 이상으로 급상승하였습니다. 다만, 글로벌 주요국의 빠른 정책적 대응 차원의 경제부양책 실시와 백신 개발에 따른 경제 안정화 기대감으로 원/달러 환율은 지속적으로 하락하는 추이를 보였습니다.
2021년 초에는 장기 금리가 기대 인플레이션 상승 및 미국 경제의 회복 기대감을 반영해 상승하기 시작했고, 외국인의 국내 주식 순매도, 개인 투자자들의 해외투자 확대가 달러 수요를 이끌어 달러/원 환율은 1,130~1,140원 수준으로 상승하였습니다. 6월에는 FOMC 이후 미국에서의 테이퍼링 이슈, 변이 바이러스 출현 및 헝다그룹의 디폴트 가능성 등이 제기되며 안전자산 선호 심리에 따른 달러화 강세 모습을 보였습니다. 2021년 하반기 국제 유가 상승, 미국 국채 금리 상승 등 금융시장 변동성이 확대되고 오미크론 변이 바이러스로 인한 주요국의 확진자수 급증 등으로 인한 불확실성에 따라 1,170원 ~ 1,190원의 박스권을 형성하였습니다.
2022년 들어 미국 등 주요국 인플레이션이 급격하게 상승하는 추세를 나타냈고, 이를 통제하기 위하여 미국 연준은 지속적으로 금리 인상을 단행하였습니다. 한국은행도 2022년 기준금리를 인상하였으나 한-미 금리가 역전되는 등 미국의 강력한 통화 긴축 기조로 달러/원 환율은 지속적으로 상승하였습니다. 특히 2022년 9월에 들어서 달러/원 환율은 글로벌 달러 강세에 따른 수급 쏠림 현상, 위안화 약세 등에 따라 급등하여 13년여만에 가장 높은 수준인 1,400원을 상회하는 수치를 기록하였습니다. 하지만 2022년 10월부터 미국의 금리인상 속도 조절 가능성에 달러인덱스 핵심 통화 중 하나인 유로화와 일본 엔화가 강세를 보이면서 달러인덱스는 안정을 찾기 시작했습니다.
2023년에는 미국 연준의 피벗 기대감, 중국 리오프닝 및 방역 완화 기대감, 미국 소비자물가 둔화 및 연준의 베이비스텝 금리 인상 등이 복합적으로 작용함에 따라 지속적으로 하락하며, 2023년 2월 2일 연저점인 1,216.40원까지 하락하였습니다. 이후 하반기에도 중국 부동산 리스크, 이스라엘-하마스 전쟁 격화 등의 요소로 인한 긴축 장기화 우려가 확산되었고, 10월 말 기준 1,360원대까지 상승하며 연고점을 경신하였습니다. 그러나 11월 및 12월 FOMC를 통해 미국 기준금리 동결이 지속됨에 따라 시장 참여자들이 긴축 사이클 종료를 판단하며 내년 조기 금리인하에 대한 기대감이 커졌고, 원/달러 환율 역시 하락세를 보이며 1,200원대에 재진입하는 등 완만한 내림세가 나타났습니다.
2024년 상반기에는 미국 경기 및 고용지표가 견조한 상황에서 물가 지표 또한 안정화되어 가고 있음을 확인한 연준의 기준금리 인하 기대감에도 미 대선 관련 불확실성과 중동 지정학적 리스크 등으로 위험회피심리가 시장에 작용하여 원/달러 환율은 1,380원대까지 상승하였습니다. 이후 2024년 9월 FOMC에서 기준금리 50bp 인하가 단행됨에 따라 원/달러 환율은 1,300원 초반까지 하락하였으나, 이후 연속적인 경기 호조 지표로 연준의 추가 금리인하 가능성이 하락하고 감세, 금융 규제 완화, 관세 인상 등을 공약으로 발표한 트럼프 대통령의 당선 가능성이 높게 점쳐지며 환율은 약 3주만에 1,380원 수준까지 상승하였습니다. 12월 들어서는 비상계엄 및 탄핵소추안 표결 등으로 불거진 국내 정치리스크와 12월 FOMC에서 2025년도 기준금리 인하 지연 전망에 따른 달러 강세에 2024년 12월 30일 장중 1,470원 선을 웃도는 등 2009년 금융위기 이후 최고 수준에 도달하였습니다. 한편, 2025년 4월 4일 헌법재판소가 대통령 탄핵을 전원일치로 인용하며 계엄사태 이후 존재하던 경제정책 불확실성이 일부 해소되어 탄핵 인용 당일 환율은 1,430원대까지 하락하는 모습을 보였습니다. 다만, 대외 정책 불확실성과 금융시장 변동성 확대에 따른 안전자산 선호가 원화 약세 요인으로 남아 환율의 변동성이 확대될 것으로 예상됩니다.
특히 2025년 1월 트럼프 정부 출범으로 인해 글로벌 보호무역 기조 및 정책 불확실성은 더욱 확대되고 있는 상황입니다. 트럼프 대통령은 대선 이전 경선 과정부터 보편관세 도입을 피력하였으며, 2025년 4월 2일 트럼프 정부는 미국과 교역하는 모든 국가에 상호 관세를 부과하기로 발표하였습니다. 먼저, 미국으로 들어오는 모든 수입품에 기본 10% 관세를, 다음으로 미국과 무역 흑자를 내고 있는 약 60여 교역국에는 개별 관세를 부과하기로 결정하였습니다. 한국 26%, 중국 34%, 유럽연합 20%, 일본 24%, 인도 26% 등 각 국가별로 차등을 두어 개별 관세를 부과할 예정이며 기본 관세는 4월 5일부터, 개별 관세는 4월 9일부터 시행하겠다고 발표하였습니다.
한편, 상호관세 부과에 따른 미중 갈등이 격화되며, 4월 9일 트럼프 정부는 중국을 제외한 국가에 대한 상호관세를 90일간 유예하고 해당 기간동안 관세율을 10%로 인하 및 중국에는 125%의 관세를 부과하는 조치(2025년 2월 펜타닐 유입을 문제삼아 중국에 부과한 관세율 20%와 합산하여 미국의 대중국 관세율은 총 145%로 추산)를 발표하였습니다. 하지만, 다시금 미중 관세협상에 우호적인 분위기가 감지되며 위안화 가치 상승 기대감이 부각되고 미국과 대만간 협상에 따른 대만달러 통화절상 압력이 제기되는 등 전반적인 아시아 통화에 대한 상승 압력이 확대되며, 환율시장 변동성이 확대된 모습입니다. 이로 인해 현재 원달러 환율은 4월 대비 급락하여 1380원대 전후를 등락하고 있습니다. 향후 트럼프 정부의 관세 정책 향방 및 금융시장 변동에 따라 환율 변동성이 크게 확대될 수 있으므로 투자자 분들은 이 점 유의하시기 바랍니다.
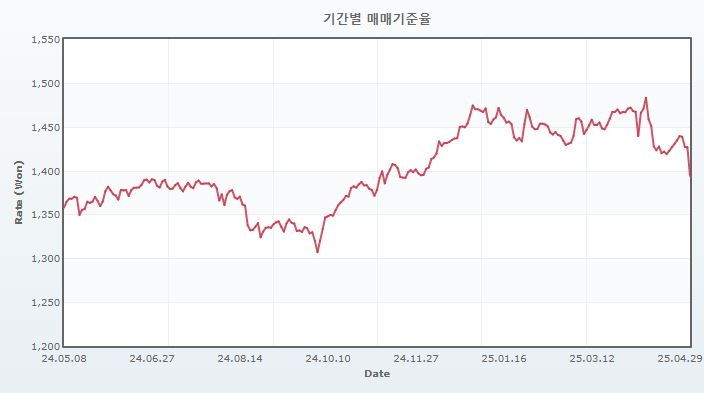 |
|
원달러 환율 추이_1 |
| (자료 : 서울외국환중개소) |
최근 글로벌 경제 및 정치적 상황의 불확실성, 중동 지정학적 리스크와 함께 트럼프 미국 대통령의 관세 등 예측불가능한 정책 으로 환율 변동성이 크게 확대되는 추세를 보이고 있습니다. 외부적인 요인에 의한 환율 변동은 당사의 수익성에 직간접적인 영향을 미칠 수 있으며 향후 그 영향도가 더욱 높아질 개연성이 존재합니다. 따라서 환율 변동의 불확실성 확대가 당사의 경영성과 및 재무상태에 영향을 미칠 수 있는점 투자자 여러분께서는 참고하시기 바랍니다.
| 바. 현금흐름 관련 위험 당사는 당뇨병, 간질환 및 중추신경계(CNS) 질환 치료제 시장에서 선도적인 지위를 확보하고 있으며, 인지도가 높은 주요 제품들을 생산·판매하고 있습니다. 이러한 제품을 통해 창출되는 영업현금흐름은 신약 파이프라인 임상, 제제 개발, 연구 등 연구개발 활동에 필요한 운영자금으로 재투자되어 선순환 구조를 이루고 있습니다. 당사는 이와 같은 구조를 기반으로 향후 사업 외형을 지속적으로 확대해 나갈 계획입니다. 따라서 안정적인 현금흐름 확보는 당사의 영업 환경과 성장 전략에 있어 매우 중요한 요소라 할 수 있습니다. 앞으로 당사의 안정적인 영업실적 개선이 지속될 것으로 기대되며, 이에 따라 영업현금흐름도 점진적으로 증가할 것으로 전망됩니다. 당사는 이를 기반으로 신약 개발 등 주요 투자 활동에 자금을 재투자하는 선순환 구조를 구축해 나갈 계획입니다. 다만, 예기치 못한 외부 변수로 인해 2023년과 같은 영업적자가 발생할 경우, 영업현금흐름이 다시 순유출로 전환될 수 있으며, 이는 유동성 부족으로 이어져 추가적인 자금 조달 또는 차입이 필요할 수 있습니다. 제약업체인 당사에게 있어 안정적인 현금흐름 확보는 핵심적인 경영 과제이므로, 투자자 여러분께서는 당사의 현금흐름 추이를 충분히 고려하신 후 투자 의사결정을 해주시기 바랍니다. |
당사는 당뇨병, 간질환 및 중추신경계(CNS) 질환 치료제 시장에서 선도적인 지위를 확보하고 있으며, 인지도가 높은 주요 제품들을 생산·판매하고 있습니다. 이러한 제품을 통해 창출되는 영업현금흐름은 신약 파이프라인 임상, 제제 개발, 연구 등 연구개발 활동에 필요한 운영자금으로 재투자되어 선순환 구조를 이루고 있습니다. 당사는 이와 같은 구조를 기반으로 향후 사업 외형을 지속적으로 확대해 나갈 계획입니다. 따라서 안정적인 현금흐름 확보는 당사의 영업 환경과 성장 전략에 있어 매우 중요한 요소라 할 수 있습니다.
최근 4개년 당사의 현금흐름표는 다음과 같습니다.
| [당사 요약연결현금흐름표] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 |
| 영업활동현금흐름 | 7,244 | 12,745 | 34,362 | (9,362) | 16,461 | 26,543 |
| 투자활동현금흐름 | (8,488) | (946) | (27,727) | (2,319) | (3,150) | 4,749 |
| 재무활동현금흐름 | (995) | (1,136) | (67,651) | 76,839 | (10,398) | (27,484) |
| 환율변동효과 반영전 현금및현금성자산의 순증가(감소) | (2,239) | 10,664 | (61,016) | 65,158 | 2,913 | 3,808 |
| 현금및현금성자산에 대한 환율변동효과 | (39) | 569 | (120) | 553 | (173) | (321) |
| 현금및현금성자산의 순증가(감소) | (2,278) | 11,232 | (61,136) | 65,710 | 2,740 | 3,486 |
| 기초현금및현금성자산 | 90,091 | 151,227 | 151,227 | 85,517 | 82,777 | 79,291 |
| 기말현금및현금성자산 | 87,813 | 162,459 | 90,091 | 151,227 | 85,517 | 82,777 |
| (자료 : 당사 사업보고서 및 분기보고서) |
당사는 2021년 및 2022년에 순유입의 영업현금흐름을 기록하였으나, 2023년에는 영업적자 발생으로 인해 영업현금흐름이 마이너스로 전환되었습니다. 다만, 약 800억 원 규모의 신규 차입이 이루어지면서 재무활동현금흐름으로 763억 원이 유입되었고, 이에 따라 2023년 말 현금 및 현금성자산은 전년 대비 증가한 1,512억 원을 기록하였습니다. 2024년에는 2023년에 단행한 경영구조 개선 효과가 온전히 반영되며 영업현금흐름이 344억 원으로 증가하였습니다. 반면, 자회사 Contera Pharma 투자자의 풋옵션 행사로 인해 677억 원이 유출되면서 재무활동현금흐름은 마이너스를 기록하였습니다. 한편, 2025년 1분기 당사는 기타유동금융자산 증가와 CAPEX 투자 지속 등으로 인한 85억원의 투자활동현금유출과 이자지급에 따른 10억원의 재무활동현금유출이 발생하며 2025년 1분기말 현금 및 현금성 자산은 전년 대비 소폭 하락한 878억원을 기록하였으나, 현금 순유출 규모가 크지 않아 우려할 상황은 아닌 것으로 판단됩니다.
앞으로 당사의 안정적인 영업실적 개선이 지속될 것으로 기대되며, 이에 따라 영업현금흐름도 점진적으로 증가할 것으로 전망됩니다. 당사는 이를 기반으로 신약 개발 등 주요 투자 활동에 자금을 재투자하는 선순환 구조를 구축해 나갈 계획입니다. 다만, 예기치 못한 외부 변수로 인해 2023년과 같은 영업적자가 발생할 경우, 영업현금흐름이 다시 순유출로 전환될 수 있으며, 이는 유동성 부족으로 이어져 추가적인 자금 조달 또는 차입이 필요할 수 있습니다. 제약업체인 당사에게 있어 안정적인 현금흐름 확보는 핵심적인 경영 과제이므로, 투자자 여러분께서는 당사의 현금흐름 추이를 충분히 고려하신 후 투자 의사결정을 해주시기 바랍니다.
| 사. 연구개발비 증가에 따른 위험 당사의 연결 기준 매출액 대비 연구개발비 비중은 2021년 14.89%, 2022년 15.39%로 유사한 수준을 유지하였으나, 2023년에는 31.38%로 큰 폭 상승하였습니다. 이는 2023년 매출액이 감소한 가운데, JM-010 임상 관련 연구개발비가 대규모로 집행된 데에 기인합니다. 실제 2023년 연결 기준 연구개발비는 395억 원으로, 전년 동기 대비 34.4% 증가하였습니다. 다만 JM-010 임상이 2024년에 종료됨에 따라, 2024년 연결 기준 연구개발비는 284억 원으로 감소하였으며, 매출액 대비 비중 또한 17.73%로 축소되어 2021~2022년 수준으로 회귀하였습니다. 2025년 1분기 또한 JM-010의 임상중단 영향과 매출 성장으로 인해 매출액 대비 연구개발비 비중이 12% 수준까지 하락하였지만, 이는 당사의 후속 파이프라인 연구개발이 진행되며 예년 수준으로 상승할 것으로 예상됩니다. 당사와 같은 제약업체는 미래 한단계 도약하기 위해서는 연구개발활동이 필수적입니다. 다만 연구개발비가 급격히 증가할 경우 당사 수익성에 영향을 미칠 수 있으며 향후 개발임상이 실패할 시 해당비용은 매몰비용으로 회수에 어려움을 겪게 될 수 있습니다. 투자자분들께서는 이점 참고하시기 바랍니다. |
당사는 연구개발본부 산하 허가등록부, 개발부, 연구소 등으로 구성된 내부 연구개발 조직을 보유하고 있으며, 자회사들 또한 연구개발 중심의 전문 조직 체계를 갖추고 있습니다. 제약업의 특성상 연구개발 분야에서 핵심 인재를 확보하는 것이 중요한 경쟁력으로 작용하기 때문에, 당사는 박사급 13명, 석사급 30명을 포함한 총 65명의 연구인력을 확보하고 있습니다. 당사는 우수한 인재들에게 적절한 보상과 동기 부여를 제공함으로써 인력의 안정적 유지에 힘쓰고 있으며, 향후에도 연구개발 경쟁력 강화를 위해 우수 인재 영입에 최선을 다할 계획입니다. 증권신고서 제출일 기준 당사의 연구인력 현황은 다음과 같습니다.
| [당사 연구인력 현황] |
| (단위: 명) |
| 구분 | 박사 | 석사 | 학사 | 기타 | 합계 |
| 부광약품(주) 연구소 | 3 | 30 | 15 | 1 | 49 |
| Contera Pharma A/S | 9 | - | 6 | - | 15 |
| ProteKt Therapeutics | 1 | - | - | - | 1 |
| JaguAHR Therapeutics | - | - | - | - | - |
| 합계 | 13 | 30 | 21 | 1 | 65 |
| (자료 : 당사 제시) |
최근 3개년 연구소 소속 인력 변동 현황은 다음과 같습니다.
| [당사 연구 인력 변동 사항] |
| (단위 : 명) |
| 구분 | 직위 | 기초 | 증가 | 감소 | 기말 |
|---|---|---|---|---|---|
| 2022년도 | 부광약품 연구개발인력 | 36 | 25 | 14 | 47 |
| Contera Pharma A/S | 7 | 13 | 1 | 19 | |
| ProteKt Therapeutics | - | - | - | - | |
| 계 | 43 | 38 | 15 | 66 | |
| 2023년도 | 부광약품 연구개발인력 | 47 | 13 | 18 | 42 |
| Contera Pharma A/S | 19 | 3 | 3 | 19 | |
| ProteKt Therapeutics | - | 1 | - | 1 | |
| 계 | 66 | 17 | 21 | 62 | |
| 2024년도 | 부광약품 연구개발인력 | 42 | 19 | 19 | 42 |
| Contera Pharma A/S | 19 | 4 | 9 | 14 | |
| ProteKt Therapeutics | 1 | - | - | 1 | |
| 계 | 62 | 23 | 28 | 57 | |
| 증권신고서 제출일 현재 |
부광약품 연구개발인력 | 42 | 12 | 5 | 49 |
| Contera Pharma A/S | 14 | 1 | - | 15 | |
| ProteKt Therapeutics | 1 | - | - | 1 | |
| JaguAHR Therapeutics | - | - | - | - | |
| 계 | 57 | 13 | 5 | 65 |
| (출처: 당사 내부자료) |
한편 당사는 특허를 통해 핵심기술에 대한 권리보호 전략을 시행하고 있으나, 핵심 연구 인력의 유출은 당사가 축척해온 기술관련 노하우 등의 기술유출 위험을 내포하고 있습니다. 특히 당사 핵심 연구인력의 유출은 당사의 사업계획 및 주요 임상 진행 계획에 차질을 발생시킬 수 있습니다. 따라서, 핵심 연구개발인력의 동기부여 및 이탈방지 목적으로 핵심 연구개발인력들을 대상으로 성과에 따른 인센티브 등의 금전적 보상을 제공하고, 자유로운 연구 환경과 경력 개발 기회를 지원하고 있습니다. 또한 우수성과 시상, 학회 참여, 유연근무제 도입 등 비금전적 동기요소를 강화하여 핵심 인력의 조직 내 안착을 유도하고 있습니다.
당사의 연결 기준 매출액 대비 연구개발비 비중은 2021년 14.89%, 2022년 15.39%로 유사한 수준을 유지하였으나, 2023년에는 31.38%로 큰 폭 상승하였습니다. 이는 2023년 매출액이 감소한 가운데, JM-010 임상 관련 연구개발비가 대규모로 집행된 데에 기인합니다. 실제 2023년 연결 기준 연구개발비는 395억 원으로, 전년 동기 대비 34.4% 증가하였습니다. 다만 JM-010 임상이 2024년에 종료됨에 따라, 2024년 연결 기준 연구개발비는 284억 원으로 감소하였으며, 매출액 대비 비중 또한 17.73%로 축소되어 2021~2022년 수준으로 회귀하였습니다. 별도 기준 매출액 대비 연구개발비 비중 역시 2023년에는 16.34%로 전년 대비 큰 폭으로 상승하였는데, 이 또한 JM-010 임상개발 비용 집행과 직접적인 관련이 있습니다. 참고로, JM-010의 유럽 임상은 자회사인 Contera Pharma에서, 미국 및 한국 임상은 당사에서 각각 진행하였기에, 당사 별도 및 연결 기준 모두에서 2023년 연구개발비가 증가한 것으로 판단됩니다. 한편, 2025년 1분기는 JM-010 임상개발 종료 영향으로 연구개발비용이 57억원 수준으로 감소하고 당사 주요 제품의 매출 성장으로 인해 매출이 전년동기대비 급성장하며, 매출액 대비 연구개발비 비중은 12% 수준으로 감소하였습니다. 다만, CP-012, BUK-001 등 후속 파이프라인에 대한 연구개발이 가속화 되며 연구개발비 비중은 예년 수준으로 상승할 것으로 예상됩니다.
| [당사 연결기준 연구개발비 현황] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 | |
|---|---|---|---|---|---|---|---|
| 비용의성격별 분류 | 원재료비 | 904 | 695 | 4,147 | 3,584 | 2,900 | 2,677 |
| 인건비 | 3,081 | 2,540 | 10,537 | 10,021 | 6,565 | 6,919 | |
| 감가상각비 | 203 | 181 | 1,052 | 587 | 216 | 214 | |
| 위탁용역비 | 870 | 2,564 | 9,317 | 14,754 | 12,201 | 12,840 | |
| 기타 | 680 | 1,225 | 3,333 | 10,570 | 7,501 | 4,524 | |
| 연구개발비용 합계 | 5,739 | 7,205 | 28,386 | 39,516 | 29,383 | 27,174 | |
| 회계처리내역 | 판매비와 관리비 | 4,452 | 6,056 | 23,430 | 34,551 | 24,274 | 22,465 |
| 제조경비 | 1,287 | 1,149 | 4,956 | 4,965 | 5,108 | 4,709 | |
| 개발비(무형자산) | - | - | - | - | - | - | |
| 회계처리금액 계 | 5,739 | 7,205 | 28,386 | 39,516 | 29,382 | 27,174 | |
| 정부보조금 | - | - | - | - | - | - | |
| 연구개발비용 합계 | 5,739 | 7,205 | 28,386 | 39,516 | 29,3832 | 27,174 | |
| 연구개발비 / 매출액 비율 | 12.00% | 20.95% | 17.73% | 31.38% | 15.39% | 14.89% | |
| [연구개발비용합계÷당기매출액×100] | |||||||
| (자료 : 당사 사업보고서 및 분기보고서) |
| [당사 별도기준 연구개발비 현황] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 | |
|---|---|---|---|---|---|---|---|
| 비용의성격별 분류 | 원재료비 | 487 | 500 | 2,727 | 2,620 | 2,773 | 2,406 |
| 인건비 | 1,851 | 1,650 | 6,544 | 6,686 | 6,238 | 6,510 | |
| 감가상각비 | 131 | 92 | 396 | 301 | 216 | 214 | |
| 위탁용역비 | 300 | 1,201 | 3,375 | 8,289 | 6,307 | 9,383 | |
| 기타 | 465 | 416 | 1,829 | 2,551 | 1,577 | 1,145 | |
| 연구개발비용 합계 | 3,233 | 3,859 | 14,871 | 20,447 | 17,111 | 19,658 | |
| 회계처리내역 | 판매비와 관리비 | 1,946 | 2,711 | 9,915 | 15,482 | 12,003 | 14,949 |
| 제조경비 | 1,287 | 1,149 | 4,956 | 4,965 | 5,108 | 4,709 | |
| 개발비(무형자산) | - | - | - | - | - | - | |
| 회계처리금액 계 | 3,233 | 3,859 | 14,872 | 20,447 | 17,111 | 19,658 | |
| 정부보조금 | - | - | - | - | - | - | |
| 연구개발비용 합계 | 3,233 | 3,859 | 14,872 | 20,447 | 17,111 | 19,658 | |
| 연구개발비 / 매출액 비율 | 7.37% | 11.34% | 9.44% | 16.34% | 8.99% | 11.84% | |
| [연구개발비용합계÷당기매출액×100] | |||||||
| (자료 : 당사 사업보고서 및 분기보고서) |
당사와 같은 제약업체는 미래 한단계 도약하기 위해서는 연구개발활동이 필수적입니다. 다만 연구개발비가 급격히 증가할 경우 당사 수익성에 영향을 미칠 수 있으며 향후 개발임상이 실패할 시 해당비용은 매몰비용으로 회수에 어려움을 겪게 될 수 있습니다. 투자자분들께서는 이점 참고하시기 바랍니다.
| 아. 소송 등 우발부채 관련 위험 증권신고서 제출일 현재 당사는 1,200억 및 백만불을 한도로 금융기관과 일반자금대출/수입신용장 약정을 체결하고 있으며 이중 800억원을 사용하고 있습니다. 또한 당사는 원고로 4건, 피고로 1건의 소송에 계류 중입니다. 당사는 금융기관과의 약정을 통해 800억원을 차입 중이나 별도 기준 현금을 약 809억원 보유 중이기에 여전히 (-)순차입금을 보이고 있는 상황입니다. 이에 당사의 영업현금흐름 등 고려 시 예상치 못한 긴급한 자금 소요로 인해 한도대가 추가 실행되더라도 대응 가능할 것으로 전망됩니다. 다만 자금 소요 규모가 커지게 될 경우 당사의 재무부담에 영향을 미칠 수 있습니다. 또한 당사가 계류중인 소송사건의 최종결과를 합리적으로 예측할 수 없으므로, 향후 본 소송사건들의 진행 경과에 따라 당사 영업에 부정적으로 작용할 가능성이 존재합니다. 이에, 투자자분들께서는 상기우발채무가 현실화될 경우 당사의 재무상태에 부정적인 영향을 미칠 수 있는점 참고해 주시기 바랍니다. |
증권신고서 제출일 현재 당사의 우발부채 현황은 다음과 같습니다.
(1) 당사가 금융기관과 체결하고 있는 약정사항의 내역
| (단위: 원, USD) |
| 금융기관 | 약정사항 | 증권신고서 제출일 | 2024년말 | ||
|---|---|---|---|---|---|
| 한도금액 | 사용금액 | 한도금액 | 사용금액 | ||
| 하나은행 | 일반자금대출 | 30,000,000,000 | 30,000,000,000 | 30,000,000,000 | 30,000,000,000 |
| 수입신용장 | USD 1,000,000 | - | USD 1,000,000 | - | |
| 국민은행 | 일반자금대출 | 30,000,000,000 | - | 40,000,000,000 | - |
| 산업은행 | 일반자금대출 | 10,000,000,000 | - | 10,000,000,000 | - |
| 신한은행 | 일반자금대출 | 50,000,000,000 | 50,000,000,000 | 50,000,000,000 | 50,000,000,000 |
| (자료 : 당사 제시) |
상기 약정 이외에 당사는 국민은행과 기업구매론약정(증권신고서 제출일 현재: 한도 10,000백만원, 2024년말: 한도 10,000백만원)과 신한은행과 전자방식외상매출채권담보대출약정(증권신고서 제출일 현재: 한도 2,500백만원, 2024년말: 한도 2,500백만원)의 공급자금융약정을 체결하고 있습니다.
증권신고서 제출일 현재 매입채무및기타채무 금액 중 공급자금융약정과 관련된 금융부채는 2,857백만원이며, 공급자가 금융기관으로부터 증권신고서 제출일 현재 이미 대금을 수취한 금액은 315백만원입니다.
공급자금융약정에 해당하는 금융부채와 공급자금융약정에 해당하지 않는 금융부채의 지급기일에는 유의적인 차이가 없습니다.
공급자금융약정에 따라 금융기관에게 지급해야 할 금액은 회사의 정상영업주기 내에사용되는 운전자본의 일부로서 매입채무및기타채무와 유사한 성격과 기능을 지니고 있다고 판단하여 이를 매입채무 및 기타채무로 분류하고, 현금흐름표에서 관련 현금흐름을 영업활동현금흐름으로 분류하고 있습니다.
(2) 당사가 타인으로부터 제공받은 지급보증의 내역
| (단위: 원) |
| 금융기관 | 약정사항 | 보증금액 | |
|---|---|---|---|
| 2025년 1분기말 | 2024년말 | ||
| 서울보증보험 | 공탁보증 | - | 60,000,000 |
| 물품대금보증 | 1,060,000,000 | 1,000,000,000 | |
| 합 계 | 1,060,000,000 | 1,060,000,000 | |
| (자료 : 당사 제시) |
(3) 증권신고서 제출일 현재 차입금 등과 관련하여 담보로 제공되어있는 자산내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 제공처 | 내역 | 담보제공자산 | 장부금액 | 설정금액 |
| 유형자산 | 신한은행 | 차입금 담보 | 토지,건물 | 73,543,176,915 | 60,000,000,000 |
| (자료 : 당사 제시) |
(4) 증권신고서 제출 현재 당사가 원고로서 진행 중인 소송은 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소소송 1건, 권리범위확인(특) 3건, 총 4건(2024년말: 4건)입니다. 또한 회사가 피고로서 진행중인 소송은 권리범위확인(특) 총 1건(2024년말: 1건)으로 소송가액은 없습니다.
| 관할법원 | 원고 | 피고 | 소송의 내용 | 소송가액 | 진행상황 |
| 서울고등법원 | 당사 | 보건복지부장관 | 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소 | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 에치케이이노엔 | 당사 | 권리범위확인(특) | - | 계류중 |
당사가 진행중인 5건의 소송 중 보건복지부장관을 피고로 당사가 제기한 소송은 당사 주요 제품인 레가론에 대한 보험급여 적용 중지에 대한 다툼 입니다. 만약 해당 소송에서 당사가 패소하게 될 경우 레가론에 대한 보헙급여가 중지되어 당사의 향후 레가론 매출 성장에 영향을 줄 수 있습니다. 특허법원에 계류중인 소송 4건은 모두 당사가 개발중인 케이캡 제네릭 관련 특허에 대한 다툼으로, 해당 소송과 동일한 소송이 국내 다수 제네릭 의약품 업체에서 병행 진행되고 있어 당사를 비롯한 이들 회사가 소송 결과에 직접적 영향을 받을 수 있습니다. 당사는 현재까지 케이캡 제네릭 제품을 생산 및 판매하고 있지 않기에 해당 소송에서 부정적인 결과가 나타나더라도 당사의 기존 제품 매출액에 영향을 줄 것으로 판단되진 않습니다. 다만 당사의 향후 매출 성장성에는 영향을 줄 수 있습니다.
(5) 당사는 종속기업인 Contera Pharma A/S와 관련하여 개발 중인 의약품의 허가신청, 시판 승인 및 상용화 조건 달성 여부에 따라 조건부대가를 지급하는 약정을 체결하였습니다. 2024년 중 당사는 해당 의약품의 임상을 중단하였으며, 이에 따라미래에 지불할 가능성이 있는 금액을 0으로 평가하였습니다.
(6) 당사가 증권신고서 제출일 현재 보유 중인 당기손익-공정가치측정 금융자산 중 TVM LifeScience Innovation II SCSP에 대한 투자 약정금액은 총 USD 3,000,000이며, 현재까지 USD 2,848,568에 대한 납입이 완료되었습니다. 잔여금액 USD 151,432은 향후 업무집행사원의 출자이행요청에 따라 추가 납입예정이나, 현재 시점에 그 납입시기를 예상할 수 없습니다.
(7) 당사가 증권신고서 제출일 현재 보유 중인 당기손익-공정가치측정 금융자산 중 KDB오픈이노베이션 제2호에 대한 투자 약정금액은 총 5억원이며, 현재까지 5억원 납입이 완료되었습니다.
(8) 당사는 종속기업인 ProteKt Therapeutics와 관련하여 개발 중인 의약품의 License 관련 판매 및 배당 등의 조건 달성 여부에 따라 조건부대가를 지급하는 약정을 체결하였습니다.
당사는 금융기관과의 약정을 통해 800억원을 차입 중이나 별도 기준 현금을 약 809억원 보유 중이기에 여전히 (-)순차입금을 보이고 있는 상황입니다. 이에 당사의 영업현금흐름 등 고려 시 예상치 못한 긴급한 자금 소요로 인해 한도대가 추가 실행되더라도 대응 가능할 것으로 전망됩니다. 다만 자금 소요 규모가 커지게 될 경우 당사의 재무부담에 영향을 미칠 수 있습니다. 또한 당사가 계류중인 상기 소송사건의 최종결과를 합리적으로 예측할 수 없으므로, 향후 본 소송사건들의 진행 경과에 따라 당사 영업에 부정적으로 작용할 가능성이 존재합니다. 이에, 투자자분들께서는 상기우발채무가 현실화될 경우 당사의 재무상태에 부정적인 영향을 미칠 수 있는점 참고해 주시기 바랍니다.
3. 기타위험
|
가. 최대주주의 청약 참여율에 따른 지분율 변동 위험 증권신고서 제출일 전일 기준 당사 보통주의 최대주주는 OCI홀딩스(주)(지분율 : 11.32%, 보통주 기준)입니다. 금번 유상증자에 있어서 최대주주인 OCI홀딩스(주)는 신주배정비율에 따라 2,735,416주를 배정받게 될 예정이며 배정받은 신주에 대해 120% 참여를 고려하고 있습니다. 다만 구체적인 참여 규모는 발행가액이 확정된 이후 추후 이사회를 통해 결의할 예정입니다. 한편, 최대주주의 유상증자 참여수준에 따라 최대주주의 지분율이 변동될 수 있습니다. 금번 유상증자는 구주주(보통주+우선주) 1주당 0.3530511453주를 배정받게됨에 따라, 참여수준에 따라 지분율 변동이 클 수 있습니다. 당사의 최대주주 OCI홀딩스(주)의 120% 청약 참여 가정 시, 보통주 기준 지분율은 기존 11.32%에서 11.18%로 소폭 하락할 예정입니다. 한편 당사 2대주주 및 3대주주의 참여 여부는 확정되지 않았으며 참여하지 않을 경우 당사 최대주주인 OCI홀딩스(주)가 증서를 장외 매수하여 120% 청약 하는 방법도 고려할 수 있습니다. 이로 인해 주요주주의 청약 여부 및 이에 따른 당사 최대주주 지분율 변동율은 본 증권신고서 제출일 현재 가늠할 수 없으니 투자자 여러분께서는 이러한 점을 유념해 주시기 바랍니다. |
증권신고서 제출일 전일 기준 당사 최대주주는 OCI홀딩스(주)(지분율 : 11.32%, 보통주 기준)입니다. 금번 유상증자에 있어서 최대주주인 OCI홀딩스(주)는 신주배정비율에 따라 2,735,416주를 배정받게 될 예정이며 배정받은 신주에 대해 120% 참여를 고려하고 있습니다. 다만 구체적인 참여 규모는 발행가액이 확정된 이후 추후 이사회를 통해 결의할 예정입니다.
한편, 최대주주의 유상증자 참여수준에 따라 최대주주의 지분율이 변동될 수 있습니다. 금번 유상증자는 구주주(보통주+우선주) 1주당 0.3530511453주를 배정받게됨에 따라, 참여수준에 따라 지분율 변동이 클 수 있습니다. 당사의 최대주주 OCI홀딩스(주)의 120% 청약 참여 가정 시, 보통주 기준 지분율은 기존 11.32%에서 11.18%로 소폭 하락할 예정입니다. 한편 당사 2대주주 및 3대주주의 참여 여부는 확정되지 않았으며 참여하지 않을 경우 당사 최대주주인 OCI홀딩스(주)가 증서를 장외 매수하여 120% 청약 하는 방법도 고려할 수 있습니다. OCI홀딩스(주)가 당사 기존 주주의 신주인수권 증서를 매입하게 될 경우 자본시장법 제173조의3에 따라 신주인수권증서 거래 개시일의 30일 전, 거래계획을 사전 공시할 예정이며 현재 예상되는 사전 공시일은 2025년 05월 30일입니다.이로 인해 주요주주의 청약 여부 및 이에 따른 당사 최대주주 지분율 변동율은 본 증권신고서 제출일 현재 가늠할 수 없으니 투자자 여러분께서는 이러한 점을 유념해 주시기 바랍니다.
| [청약참가에 따른 최대주주 및 특수관계인 주식수 및 지분율 변동 예상] | |||
| (기준일 : | 2025년 03월 27일 | ) | (단위 : 주, %) |
| 성 명 | 관 계 | 소유주식수 및 지분율 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 증권신고서 제출일 전일 | 배정받은 증서 100% 참여 시 | 배정받은 증서 120% 참여 시 | 배정받은 증서 및 2대, 3대 주주 증서 장내매수 후 100% 참여시 |
배정받은 증서 및 2대, 3대 주주 증서 장내매수 후 120% 참여시 |
|||||||
| 주식수 | 지분율 | 주식수 | 지분율 | 주식수 | 지분율 | 주식수 | 지분율 | 주식수 | 지분율 | ||
| OCI홀딩스 주식회사 | 최대주주 본인 | 7,747,934 | 11.32 | 10,483,350 | 10.63 | 11,030,434 | 11.18 | 15,109,472 | 15.31 | 16,581,780 | 16.81 |
| 발행주식총수(보통주) | 68,454,671 | 100 | 98,664,671 | 100 | 98,664,671 | 100.00 | 98,664,671 | 100.00 | 98,664,671 | 100.00 | |
| 출처 : 당사 제시 주1) 상기 주식수 및 지분율은 보통주 기준입니다. |
참고로 당사의 최대주주인 OCI홀딩스(주)는 24년 별도 기준 현금및현금성자산 1,523억원을 보유중임에 따라 본 증자 참여에는 무리가 없을 것으로 판단됩니다.
| 나. 신주의 환금성 제약 및 주가 변동에 따른 손실위험 금번 유상증자 청약에 참여하여 신주를 배정받을 경우 신주의 추가상장일까지 환금성에 제약이 있으며, 청약 후 추가상장일 사이에 주가가 하락할 경우 원금에 대한 손해가 발생할 가능성이 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
금번 유상증자 청약에 참여하여 신주를 배정받을 경우 신주의 추가상장일까지 환금성에 제약이 있으며, 청약 후 추가상장일 사이에 주가가 하락할 경우 원금에 대한 손해가 발생할 가능성이 존재합니다. 투자자 여러분께서는 이 점 유의하시기 바랍니다
당사는 유가증권시장 상장법인으로서 이번 유상증자로 발행되는 신주는 유가증권시장에 상장되어 거래될 예정이므로 유동성과 관계된 심각한 환금성 위험은 존재하지 않습니다. 그러나 유상증자 청약에 참여하여 신주를 배정받을 경우, 신주가 상장되어매매가 가능할 때까지 납입주금에 대한 유동성의 제약이 있습니다.
본 유상증자의 자세한 일정은 본 신고서의 '제1부 모집 또는 매출에 관한 사항 - I. 모집 또는 매출에 관한 일반사항 - 1. 공모의 개요'를 참고하시기 바랍니다.
또한 유가증권시장에 추가 상장될 때까지 유상증자로 발행되는 신주의 발행가액 수준의 주가가 유지되지 않을 수 있으며, 당사의 내적인 환경변화 또는 시장전체의 환경 변화 등에 의한 급격한 주가하락이 발생할 경우, 투자원금에 대한 손실이 발생할 수 있습니다.
| 다. 증자방식, 청약절차에 대한 주의 및 주가하락 위험 당사의 금번 유상증자로 인하여 기발행주식총수 68,454,671주의 44.13%에 해당하는 30,210,000주가 추가로 발행 및 상장됩니다. 동 유상증자는 주주배정 후 실권주 일반공모 방식으로 진행되며 초과청약이 가능하므로 증자방식 및 청약절차에 대하여 정확히 이해하고 투자에 임하시기 바라며, 특히, 금번 유상증자의 증자비율은 44.13% 수준이며 신주로 발행되는 주식의 물량 출회 및 주가희석화에 따른 주가 하락의 가능성이 있습니다. 또한 일반공모를 거쳐 배정 후에도 청약이 미달될 경우 "대표주관회사"가 자기계산으로 잔액인수하게 됩니다. 청약 이후 실권주 발생으로 인해 "대표주관회사"가 잔액인수한 물량을 조기에 장내에서 대량 매도할 경우 일시적 물량 출회에 따른 주가 하락의 가능성이 존재하며, 인수한 실권주를 일정 기간 보유하더라도 동 인수물량이 잠재매각물량으로 존재하여 주가 상승에는 부담으로 작용할 가능성이 높습니다. |
당사의 금번 유상증자로 인하여 기발행주식총수 68,454,671주의 44.13%에 해당하는 30,210,000주가 추가로 발행 및 상장됩니다.
| [당사 주가 및 유상증자에 따른 발행주식수 및 가격] |
| 모집예정 주식 종류 | 기명식보통주 | - |
|---|---|---|
| 모집예정주식수 | 30,210,000주 | 보통주 |
| 현재 발행주식총수 | 68,454,671주 | 보통주 |
| 예정발행가액 | 3,310원 | 증자비율 및 할인율 고려 |
| 기산일종가 | 4,500원 | 2025.03.27 종가 |
금번 유상증자에 따른 모집가액은 「(舊)유가증권의 발행 및 공시 등에 대한 규정」 제57조를 일부 준용하여 산출됩니다. 그러나 주식시장의 특성상 향후 주가에 대한 변동성이 있는 관계로 증자에 따른 모집가격 산정시 결정된 1주당 모집가액보다 향후 추가 상장 후 거래 시점의 주가가 낮아져 투자자에게 금전적 손실이 발생할 가능성이 있습니다. 본 유상증자의 모집가액 산출에 대한 자세한 내용은 본 신고서의 '제1부 모집 또는 매출에 관한 사항 - I. 모집 또는 매출에 관한 일반사항 - 3. 공모가격 결정방법'을 참고하시기 바랍니다.
당사는 본 유상증자의 원활한 신주인수권증서 매매를 위하여 5거래일간 신주인수권증서를 상장하여 신주인수권증서를 통한 구주주 청약률을 제고할 계획입니다. 하지만 신주인수권증서의 원활한 매매 및 청약참여를 위한 노력에도 불구하고 신주인수권증서를 통한 청약이 부진하여 대규모 실권이 발생할 경우, 투자심리에 악영향을 끼쳐 일반공모청약에 부정적 영향을 끼칠 수도 있으며 향후 주가하락 가능성도 배제할 수 없습니다.
또한 금번 유상증자로 인해 추가 발행되는 주식은 우선 배정된 우리사주조합 청약분(20.0%)을 제외한 물량 24,168,000주는 보호예수되지 않는 관계로, 일시적인 물량 출회에 따른 주가하락의 가능성이 있습니다. 금번 유상증자에 따른 주권의 상장일은 2025년 07월 28일로 예정되어 있습니다. 금번 유상증자에 따른 모집예정주식 30,210,000주가 향후 유가증권시장에 추가 상장될 경우 유통주식수의 증가로 인하여 주가희석화 위험이 발생할 수 있습니다.
특히 금번 유상증자의 증자비율은 44.13% 수준으로, 향후 유가증권시장에 추가 상장될 경우 주주가치가 희석될 수 있으며, 주가가 급변동하는 등 투자자에게 금전적 손실이 발생할 위험이 존재합니다.
한편, 본 유상증자는 주주배정후 실권주 일반공모 방식으로 진행됨에 따라 일반공모를 거쳐 배정 후에도 미 청약된 잔여주식에 대하여는 "대표주관회사"가 자기계산으로 잔액인수하게 됩니다. 만약 본 유상증자 청약에서 대량 실권이 발생하여 "대표주관회사"가 실권주를 인수하게 될 경우 주가에 어떠한 영향을 미칠지는 예상하기 어렵습니다. "대표주관회사"는 인수리스크 해소 및 손익의 확정을 위하여 인수한 당사 주식을 빠른 시일 내에 장내에서 매각할 수 있으며, 이 경우 단기적으로 당사 주가가 하락할 수 있습니다. "대표주관회사"가 인수한 주식을 일정기간 보유하더라도 동 인수물량이 잠재 매각물량으로 존재하여 주가 상승에 부담으로 작용할 가능성이 높을 것으로 예상됩니다. 투자자 여러분께서는 이 점 유의하시기 바랍니다.
| 라. 주가하락에 따른 발행금액 감소 위험 주식시장의 급격한 상황 악화로 인하여 회사의 금번 유상증자 발행가액이 크게 하락할 경우 당사가 계획했던 자금조달 계획 등에 차질이 발생할 수 있으며, 이러할 경우 당사의 재무적 안정성에 부정적인 영향을 미칠 수 있습니다. 투자자 여러분께서는 이 점 유의하시기 바랍니다. |
금번 유상증자의 확정발행가액은 1차 발행가액, 2차 발행가액 중 낮은 가액으로 결정됩니다. 다만 「자본시장과 금융투자업에 관한 법률」 제165조의6 및 「증권의 발행 및 공시 등에 관한 규정」 제5-15조의2에 의거하여 1차 발행가액, 2차 발행가액 중 낮은가액이 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격보다 낮은 경우, 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격을 확정발행가액으로 합니다. (단, 발행가액이 액면가보다 낮을 경우 액면가를 발행가액으로 합니다.)
일반공모 후 미청약분에 대해서는 그 전부를 "대표주관회사"가 인수하므로 청약 미달에 따른 위험은 없으나, 주가 하락으로 발행가액이 낮아져 당사가 목표로 하는 규모의 자금을조달하지 못할 수도 있습니다. 이 경우, 당사의 재무안정성에 부정적인 영향을 미칠 수 있습니다. 투자자 여러분께서는 이 점 유의하시기 바랍니다.
| 마. 일정 변경 위험 본 증권신고서는 공시심사 과정에서 일부 내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우 감독기관의 정정명령 등에 따라 제반 일정이 지연 또는 연기될 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있습니다. 투자자 여러분께서는 이 점 유의하시기 바랍니다. |
「자본시장과 금융투자업에 관한 법률」 제120조 3항에 의거하여 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 투자자에게 귀속됩니다.
금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서(분기 및 반기보고서 포함) 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있으니 투자의사를 결정하시는 데 참조하시기 바랍니다.
본 증권신고서는 공시심사과정에서 일부 내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우 제반 일정이 지연 또는 연기될 수 있습니다. 또한, 관계기관과의 업무진행과정에서 일정이 변경될 수도 있습니다.
| 바. 분석정보의 한계 및 투자판단 관련 위험 금번 유상증자를 통해 취득한 당사의 주식가치가 하락할 수 있습니다. 본 증권신고서의 효력발생은 정부가 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나 이 유가증권의 가치를 보증 또는 승인한 것이 아니며, 기재사항은 청약일 이전에 변경될 수 있습니다. 또한 금번 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 투자자께서는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안 되며, 다양한 방면에서 신중한 검토를 병행하여 독자적으로 판단하시기 바랍니다. |
상기 서술한 바와 같이, 당사의 주식가치는 금번 유상증자 실시에 따른 전 과정에서 다양한 영향을 받아 하락할 수 있습니다.
본 증권신고서의 효력발생은 정부가 증권신고서의 기재사항이 진실 또는 정확하다는것을 인정하거나 이 유가증권의 가치를 보증 또는 승인한 것이 아니며, 기재사항은 청약일 이전에 변경될 수 있습니다. 본 주식을 청약하고자 하는 투자자께서는 투자결정을 하기 전에 본 증권신고서의 상기 투자위험요소 뿐만 아니라 다른 부분 또한 주의 깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 합니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 상기 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을배제할 수는 없습니다. 따라서 투자자께서는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안 되며, 다양한 방면에서 신중한 검토를 병행하여 독자적으로 판단할 필요가 있습니다.
당사는 상기에 기술된 투자위험요소 외에도 불안정한 경제상황 등에 의하여 직·간접적으로 영향을 받을 수 있습니다. 당사의 재무제표는 당사의 재무상태에 영향을 미칠 수 있는 경제상황에 대한 경영자의 현재까지의 평가를 반영하고 있으나, 실제 결과는 현재시점에서의 평가와는 상당히 다를 수 있는 점을 유의하시기 바랍니다.
만일 상기 투자위험요소가 실제로 발생할 경우, 당사의 사업환경과 재무상태, 기타 운영결과에 부정적인 영향을 미칠 수 있습니다. 이에 따른 주가 하락으로 투자자께서는 금번 공모 과정에서 취득하게 되는 주식의 투자금액의 일부 또는 전부를 잃을 수 있습니다.
또한 금번 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 대내외적으로 여러가지 요소들의 영향에 따라 최초에 예측했던 것과 다를 수 있는 점을 유의하시기 바랍니다.
| 사. 상장기업의 관리감독기준 강화에 따른 위험 최근 상장기업에 대한 관리감독기준이 강화되는 추세이며, 향후 당사가 상장기업 관리감독기준을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다. |
최근 금융감독기관 등의 관리감독기준이 엄격해지고 있는 상황으로 관련 규정을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다.
향후 감독기관으로부터 당사가 현재 파악하지 못한 제재가 부과될 경우 주가하락 및유동성(환금성) 제약 등으로 인해 투자금에 막대한 손실이 발생할 수 있으니 투자자들께서는 관련 규정을 충분히 검토하신 후 투자에 임해주시기 바랍니다.
특히 「유가증권시장 상장규정」 제47조(관리종목지정), 제48조(상장폐지) 및 제49조(상장적격성 실질심사)에 유의하시기 바랍니다. 자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융법규서비스(http://fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
| 아. 집단 소송 제기 위험 당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있습니다. 투자자 여러분께서는 이 점 유의하시기 바랍니다. |
「증권관련 집단소송법」 제12조(소송허가 요건)에 따라 50명 이상의 구성원이 발행주식총수의 0.01% 이상 보유할 경우 한 명 이상의 대표 당사자가 상기 50인 이상의 당사자들을 대리하여 회사가 발행한 증권의 거래과정에서 발생한 피해에 대하여 소송을 제기할 수 있습니다.
증권신고서 및 투자설명서에서 기재된 잘못된 내용, 잘못된 사업보고서의 공시, 내부자거래에 의한 손해배상청구 및 회계부정으로 인한 손해배상 청구 등이 주요한 소송사유에 포함됩니다. 당사는 향후 이와 같은 집단소송의대상이 되지 않는다고 확신할 수 없으며, 만약 당사에 대하여 집단소송이 제기될 경우 상당한 소송비용이 발생할 수 있습니다. 투자자 여러분께서는 이 점 유의하시기 바랍니다.
| 자. 유상증자 철회에 따른 위험 유상증자 진행 과정에서 모집 절차의 진행에 중대한 영향을 미칠만한 사유가 발생하여 당사 혹은 "대표주관회사" 의 판단으로 유상증자가 철회될 수 있습니다. 유상증자 납입 전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회 시점에 따라 권리락에 따른 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있습니다. 투자자 여러분께서는 이 점 유의하시기 바랍니다. |
금번 주주배정 후 실권주 일반공모 유상증자 진행 과정에서 모집 절차의 진행에 중대한 영향을 미칠 만한 사유가 발생하여 당사 혹은 "대표주관회사"의 판단으로 유상증자가 철회될 수 있습니다.
유상증자 납입 전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회 시점에 따라 권리락에 따른 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있음을 투자자 여러분께서는 유의하시기 바랍니다.
| 차. 차입공매도 유상증자 참여 제한 관련 위험 금융위원회의 공매도 제도개선 관련 「자본시장과 금융투자업에 관한 법률 시행령」일부개정에 따라, 주권상장법인이 유상증자 계획을 공시한 이후 발행가격 산정을 위한 대상 거래기간의 마지막날(발행가격 산정 기산일)까지, 해당 기업의 주식을 공매도 한 자는 증자참여를 제한하되, 예외적인 경우에만 증자참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률」제180조의4). |
주권상장법인이 유상증자 계획을 공시한 이후 해당 기업의 주식을 공매도 한 자는 증자참여를 제한하되, 예외적인 경우 증자참여를 허용하고 있습니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 이와 관련 유상증자 참여가 제한되는 공매도 시점과 증자참여가 허용되는 예외사유를 시행령에서 정하도록 위임하고 있습니다.
시행령에 따르면, 유상증자 계획이 공시된 다음 날부터, 발행가격 산정을 위한 대상 거래기간의 마지막날(발행가격 산정 기산일)까지 공매도 한 경우 증자참여가 제한됩니다. (「자본시장과 금융투자업에 관한 법률 시행령」제208조의4 제1항)
다만, 다음의 경우 공매도를 통해 발행가격에 부당한 영향을 미쳤다고 보지 않아 증자참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률 시행령」제208조의4 제2항).
ⅰ) 마지막 공매도 이후 발행가격 산정 기산일까지 공매도 주문 수량 이상을 증권시장 정규거래시간에 매수(체결일 기준)
ⅱ) 금융위원회가 정하는 기준을 충족한 독립된 거래단위를 운영하는 법인 내에서 공매도를 하지 않은 거래단위가 증자참여
ⅲ) 시장조성 또는 유동성공급을 위한 거래과정에서 공매도
상기 공매도제도 개선 관련 자본시장법 시행령 개정안에 따라, 당사의 주식을 해당 기간 동안 공매도하는 투자자께서는 금번 유상증자 참여가 제한될 수 있음을 유의하시기 바랍니다. 해당 법령과 관련된 자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융법규서비스(http://fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
| 카. 개인종합자산관리계좌(ISA) 납입한도에 따른 청약제한 위험 개인종합자산관리계좌(이하 ISA 계좌)는 연간 납입가능한도 제한(연간납입한도 2,000만원, 5년간 최대 1억원까지 납입가능하며 납입한도 이월가능)이 있는 계좌입니다. ISA계좌를 통한 신주인수권증서 보유자 청약시, 투자자별 유상증자 배정주수에 해당하는 청약증거금 납입금액이 ISA계좌 잔여납입한도를 초과할 경우 유상청약이 제한될 수 있으니, 투자자 여러분께서는 이 점 유의하시기 바랍니다. |
개인종합자산관리계좌(이하 ISA 계좌)는 연간 납입가능한도 제한(연간납입한도 2,000만원, 5년간 최대 1억원까지 납입가능하며 납입한도 이월가능)이 있는 계좌입니다. ISA계좌를 통한 신주인수권증서 보유자 청약시, 투자자별 유상증자 배정주수에 해당하는 청약증거금 납입금액이 ISA계좌 잔여납입한도를 초과할 경우 유상청약이 제한될 수 있으니, 투자자 여러분께서는 이 점 유의하시기 바랍니다.
| 타. 유상증자 자금사용목적 관련 위험 당사는 금번 유상증자를 통해 조달할 예정인 약 천억원을 시설자금 및 운영자금으로 사용할 예정입니다. 구체적으로 기존 제조설비 확장 및 설비 도입, 제조설비 신규 취득 등과 관련하여 84,500백만원을 사용할 예정이며 당사 제제개발 등 R&D 운영자금 목적으로 15,495백만원을 집행할 계획입니다. 당사는 당사의 공모규모, 할인율, 증자비율 등에 대해 과거 사례를 기반으로 이사회에서 논의를 진행하였고, 당사의 금번 유상증자는 미래 성장을 위한 시설자금 및 신약연구개발에 우선적으로 사용될 예정으로 시장 평균 대비 낮은 할인율을 설정하더라도 본 증자를 통한 성공적인 자금조달이 가능할 것이라는 대표주관회사의 의견을 반영하여 시장 평균 23.3%보다 낮은 20%를 할인율로 설정하게 되었습니다. 해당 20% 할인율을 적용하여 최초 신고기준 약 천억원 유상증자를 위해 이사회결의일 전 영업일 기준으로 산출한 본 건의 증자비율 역시 시장 평균 39.6%보다 소폭 높은 수준인 44.13%로 주주가치희석을 최소화하면서도 자금조달목적을 효과적으로 달성할 수 있는 발행조건 수준으로 판단하였습니다. 투자자분들 께서는 당사가 본 증자를 통해 조달하고자 자금의 사용목적, 할인율 및 증자비율에 대한 당사 이사회의 결정사항 등을 참고하시기 바랍니다. |
당사는 금번 유상증자를 통해 조달 예정인 자금 약 천억원을 시설자금 및 운영자금으로 사용할 계획이며 아래와 같이 자금을 집행할 계획입니다. 당사는 금번 유상증자를 통하여 조달하는 자금을 본 증권신고서에 기재한 사용목적대로 사용하기 위해 최선의 노력을 다할 것이며 기타 계열사 지원 등을 위한 목적으로는 사용하지 않을 예정입니다. 아울러 매 분기별 공시하는 당사의 정기보고서에 공모자금의 실제 사용내역 및 변동상황에 관하여 성실하게 공시할 예정입니다. 또한, 자금사용시기가 도래하지 않는 금액에 대해서는 국내 제1금융권 등의 안정성이 높은 상품에 예치할 계획이며, 자금의 사용시기가 도래하여 단기간 내에 자금의 사용이 예상되는 경우에는 제1금융권 등의 단기금융상품으로 운용할 계획입니다.
자금의 사용목적
| (기준일 : | 2025년 03월 27일 | ) | (단위 : 백만원) |
| 시설자금 | 영업양수 자금 |
운영자금 | 채무상환 자금 |
타법인증권 취득자금 |
기타 | 계 |
|---|---|---|---|---|---|---|
| 84,500 | - | 15,495 | - | - | - | 99,995 |
당사는 금번 유상증자를 통해 조달할 예정인 약 천억원을 시설자금 및 운영자금으로 사용할 예정입니다. 구체적으로 기존 제조설비 확장 및 설비 도입, 제조설비 신규 취득 등과 관련하여 84,500백만원을 사용할 예정이며 당사 제제개발 등 R&D 운영자금 목적으로 15,495백만원을 집행할 계획입니다. 다만 당사가 영위하는 산업 특성 상 운영자금의 경우 불확실성이 높음에 따라 아래 기재된 우선순위로 자금 사용을 집행하되, 변경될 경우 정정신고를 통해 안내드릴 예정인 점 참고 부탁드립니다.
| [ 자금사용 우선순위] | |
| (단위 : 백만원) | |
| 우선순위 | 자금 용도 | 세부 내용 | 자금의 사용 시기 | 금액 | |
|---|---|---|---|---|---|
| 1 | 시설자금 | 제조시설 확장 및 생산능력 증가 | 기존 생산능력 10억정에서 증축을 통해 15억정으로 생산능력 증대 | '25년 ~ '27년 | 34,000 |
| 최신 생산설비 도입 | 최신의 내용고형제 생산설비 도입 및 공정 효율성 극대화 |
'25년 ~ '27년 | 11,000 | ||
| 자동화 시스템 도입 | 스마트 팩토리 개념을 적용한 자동화 시스템 도입 |
'25년 ~ '28년 1Q | 4,500 | ||
| 제조설비 신규 취득 | 공장 인수 및 신규 제조설비, 영업권 등 무형자산 취득 | '25년 | 35,000 | ||
| 2 | 운영자금 | 신규제제 개발 및 기존제제 개선연구 | 시장 경쟁력이 있는 신제품, 신제형 개발 및 기존제제 개선 |
'25년 ~ '28년 1Q | 13,200 |
| 합성신약 연구 | 당사의 합성신약 연구연략 및 국내외 병원 등과의 협력을 통한 혁신신약 개발 |
'25년 ~ '28년 1Q | 4,330 | ||
| 개발과제 도입 | 외부 업체와의 공동개발, 제제기술이전 등 협력을 통해 제품 개발 | '25년 ~ '28년 1Q | 4,720 | ||
| 적응증 추가 임상연구 | 적응증 추가를 위한 임상연구계획 수립 및 실행 |
'25년 ~ '28년 1Q | 4,193 | ||
| 연구개발 설비투자 | 자체 연구개발 기능 강화를 위해 연구 개발에 필요한 설비확충에 적극 투자 |
'25년 ~ '28년 1Q | 3,689 | ||
| 기타운영자금 | 인건비 및 기타 필수 운영비용 | '25년 ~ '28년 1Q | 15,625 | ||
| 3 | 타법인 취득자금 |
Contera Pharma 출자자금 | Contera Pharma의 CP-012 및 CP-102 연구개발자금 지원을 위한 지분투자 | '25년 ~ '28년 1Q | 90,723 |
| 출처 : 당사 제시 주1) 시설자금중 제조시설 확장이나 설비 도입의 경우 현 시점에서 규모가 어느정도 확정되었으나 제조설비 신규 취득이나 당사가 기재한 R&D 관련 운영자금은 향후 당사가 진행하는 임상 결과에 따라 변동될 가능성이 존재합니다. 이에 본 증자를 통해 조달하는 금액을 상회하는 자금사용목적을 기재하였으며 본 증자를 통해 조달하는 자금을 우선순위에 따라 사용하고 부족분에 대해서는 다른 자금조달(예컨대 한도대 400억원 및 보유현금 100~300억원, 최대주주 대상 3자배정 400~600억원 등) 방안을 통해 조달할 계획입니다. |
※ 공모 규모 및 증자 필요성에 대한 검토
① 미래성장 동력 확보를 위한 생산능력 확장 필요성
당사가 지속적으로 성장하기 위해서는 본업에서의 현금흐름 확장이 필수적입니다. 하지만 당사는 당사 내용고형제제 생산능력의 한계로 당사의 공급량이 시장 수요에 따라가지 못하기에 당사 매출액 성장에 있어서 근본적인 한계에 다다르게 되었습니다. 이에 따라 당사는 시설자금 집행을 통해 생산능력을 확충하여 고질적인 공급부족 문제를 빠른 시일 내에 해소하고자 합니다.
이러한 공급부족 문제는 하나의 영리기업으로서의 이해관계를 넘어서 국민건강 증진의 측면에서도 큰 문제입니다. 당사의 경우 당사가 1년간 생산하는 정제(tablet)에서 퇴장방지의약품이 약 68%를 차지하고 있습니다. 하지만 당사가 겪고 있는 심각한 공급부족 문제로 인해 국민이 반드시 필요로 하는 국가필수의약품과 퇴장방지의약품의 공급에도 큰 차질이 발생하였고 이는 수 차례 언론, 식품의약품안전처, 대한약사회 등 기관에서 이슈가 된 바 있습니다. 당사는 국민건강증진 차원에서도 자금조달을 통한 생산능력 확보가 반드시 필요하다고 판단하게 되었습니다.
당사의 공급 문제는 최근에 당면한 이슈가 아닌 최근 3개년간 지속적으로 논의되어온 이슈 입니다. 이러한 생산설비 확충의 필요성은 이미 수년 전부터 인식하고 있었으나, 2022년과 2023년 연속된 적자와 운영자금 부족, 그리고 800억 원 규모의 차입 등 재무적 제약으로 인해 당장의 운영효율성 개선에 집중이 필요하여 즉각적인 설비 투자나 유상증자 추진은 어려운 상황이었습니다. 특히 2023년에는 영업적자 발생으로 인해 영업현금흐름이 마이너스로 전환되었고 약 800억 원 규모의 신규 차입이 이루어지면서 재무활동현금흐름으로 763억 원이 유입되었지만 2024년 자회사 Contera Pharma 투자자의 풋옵션 행사로 인해 677억 원이 유출되었습니다. 또한 2023~2024년에는 당사가 진행한 JM-010 임상으로 인해 임상개발에 따른 현금 유출이 증가하여 생산설비 확장을 위한 자금 확보가 여의치 않게 되었습니다. 다만 25년 하반기부터 지속적인 신제품 출시가 예정되어 있어 생산설비 부족에 따른 성장 여력 한계가 더욱 시급한 이슈로 부각됨에 따라 더 이상 생산설비 확충 이슈를 미룰 수 없다고 판단하였고 이와 맞물려 2024년 흑자 전환을 계기로 경영이 안정화됨에 따라, 생산 역량 강화와 기업가치 제고를 위하여 유상증자를 결정하였습니다.
당사는 생산능력 확보를 통해 공급부족 문제를 해소할 수 있다면 매출성장의 근본적인 한계요인이 제거되어 매출액 및 수익성 개선으로 이어질 것으로 예상하고 있습니다. 또한 이로 인해 증가되는 현금흐름을 R&D 및 신규제제 개발 등 성장성이 높은 분야에 투자하여 기업의 유기적 성장을 가속화할 수 있는 선순환 구조를 구축할 계획입니다. 궁극적으로 이는 당사의 기업가치 제고 및 배당여력 확대 등 주주환원으로 이어질 것으로 당사는 기대하고 있습니다.
② 자금조달의 필요성
당사는 현재 약 1,200억원 자체 현금을 보유중이나 이를 본 증권신고서에 기재된 자금사용목적 재원으로 활용할 경우 보유 현금은 약 200억원으로 축소됩니다. 이 경우 통제불가능한 외부 변수, 예컨데 (1) 금융권의 차입금 만기 상환 요청(현재 당사는 26년 만기 도래하는 차입금 800억원 보유 중), (2) 건강심사평가원 등 규제기관의 규제 강화로 인한 영업현금흐름 축소, (3) 예상치 못한 연구개발비 증가 등이 발생 시 유동성 부족이 발생하여, 이에 대응하기 위한 추가 조달이 필요하게 됩니다. 또한 당사가 영위하는 의약산업 및 연구개발은 미래 불확실성이 존재하기에 운영자금 목적으로 일정 수준의 현금 보유량을 유지하는 것은 제약회사의 필수적인 경영 전략이라고 할 수 있습니다. 이에, 당사가 본 증권신고서 자금사용목적에 기재된 전략을 실행하기 위해서는 외부 조달이 수반되어야 한다고 할 수 있습니다.
③ 채무증권 및 금융권 조달의 한계
한편, 당사의 경우 업종 특성에 따른 영업현금흐름의 변동성(의약산업 고유 위험, 임상비용 증가 등)으로 인해 일반 제조업에 비해 신용등급이 낮게 평가되어 회사채 등 채무증권을 통한 자금 조달이 용이하지 않은 상황입니다. 또한 2023년 약 800억 규모 신규 차입을 실행할 당시 당사 보유 유형자산을 담보로 제공한 바 있기에 금융권 차입을 위한 추가 담보 제공 여력이 제한적인 상황입니다. 이런 상황에서 추가적인 차입 시 차입이 원할하지 않을 뿐더러, 차입이 가능하더라도 조달비용 상승으로 인해 당사의 재무부담은 가중될 것으로 예상됩니다. 이 경우 당사가 생산능력 확장을 통해 추가로 확보된 영업현금흐름을 재원으로 R&D 등 성장성 높은 분야에 투자하고자 하는 성장전략은 추진력을 잃게 될 우려가 존재합니다.
④ 유상증자의 필요성
결론적으로 당사는 유상증자를 통해 자금을 조달하는 것이 가장 적절한 방향으로 판단하게 되었습니다. 당사가 금번 유상증자를 통해 모집할 자금의 1순위 사용처는 시설자금이며 주로 생산능력 확대 및 제조설비 신규 취득에 사용될 예정입니다. 당사가 시설자금으로 사용할 것으로 예상되는 규모는 약 845억원 수준입니다.
금번 유상증자는 단순한 재무 비율 개선을 위한 목적이 아닌 미래성장동력 확보를 위한 명확한 투자를 목적으로 하는 당사의 전략적 선택입니다. 증자비율은 기업의 필요 자금 규모와 주주가치 보호의 균형을 고려하여 다양한 비율로 결정될 수 있으나, 증자비율이 과도하게 높을 경우 시장에서 재무 상태에 대한 부정적인 신호로 해석될 가능성이 있어 적정한 수준에서 결정하는 것이 중요합니다. 할인율의 경우 증권의 발행 및 공시 등에 관한 규정에 의거 주주배정후실권주일반공모 유상증자의 경우 40% 이내에서 결정할 수 있으며, 기존주주들의 지분 희석 정도를 감안하여 적정 할인율에 대한 결정이 필요합니다.
이에, 기존 주주의 권익을 보호하면서도 장기적인 기업가치 상승을 기대할 수 있는 발행조건을 결정하기 위해 당사의 이사회는 과거 제약바이오 상장회사의 유사규모(800억~1200억원) 주주배정후실권주일반공모 유상증자 사례 및 대표주관회사인 NH투자증권㈜의 의견을 종합적으로 고려하였습니다.
| [최근 3개년 주주배정 후 실권주 일반공모 유상증자 사례(주1)] |
| (단위 : 억원, 주, %) |
| 회사명 | 자금사용목적(최초) | 이사회 결의일 | 최초공모금액(억원) | 최종발행규모(억원) | 발행 주식수(주) | 증자비율 | 할인율 |
|---|---|---|---|---|---|---|---|
| 현대바이오 | 운영자금 688억 채무상환자금 260억 |
2024/11/15 | 948 | 859 | 8,200,000 | 20.6% | 25.0% |
| 아미코젠 | 시설자금 457억 채무상환자금 500억 |
2023/9/15 | 957 | 703 | 7,700,000 | 39.0% | 20.0% |
| 메드팩토 | 운영자금 1,159억 | 2023/9/12 | 1,159 | 741 | 12,500,000 | 59.3% | 25.0% |
| 박셀바이오 | 시설자금 452억 운영자금 554억 |
2023/8/7 | 1,006 | 718 | 3,938,000 | 25.9% | 25.0% |
| 메디포스트 | 타법인취득자금 1,200억 | 2023/7/25 | 1,200 | 718 | 13,215,859 | 62.9% | 25.0% |
| 제넥신 | 운영자금 1,000억 | 2022/9/26 | 1,000 | 852 | 5,797,102 | 23.1% | 25.0% |
| 아이큐어 | 시설자금 223억 운영자금 100억 채무상환자금 477억 |
2022/9/19 | 800 | 343 | 12,326,650 | 64.9% | 25.0% |
| 오스코텍 | 시설자금 110억 운영자금 1091억 |
2022/8/26 | 1,200 | 886 | 6,400,000 | 20.3% | 20.0% |
| 유틸렉스 | 시설자금 100억 운영자금 866억 |
2022/4/8 | 966 | 516 | 7,000,000 | 40.7% | 20.0% |
| 평균 | 39.6% | 23.3% | |||||
| 출처 : Dart 전자공시시스템 주1) 최초발행규모 800~1200억원 제약바이오 업종 기준 |
과거 사례를 조사한 결과, 평균 증자비율은 39.6%, 평균 할인율은 23.3% 수준으로 파악됩니다. 증자비율의 경우, 자금의 사용목적과 회사의 필요 자금 규모에 따라 20.3% ~ 64.9% 까지 다양한 비율로 결정된 반면, 할인율은 대부분 20% 혹은 25%를 설정하였습니다. 만약, 할인율이 높게 설정될 경우, 동일한 증자규모를 조달하기 위해 더 많은 주식을 발행해야 하므로 주주가치 희석이 더욱 커질 수 있는 반면, 주주가치 희석을 최소화하는 목적으로 할인율을 낮게 설정한다면, 최근 유상증자 시장의 분위기와 당사 주식에 대한 시장의 관심도를 고려해 볼 때, 당초 계획된 청약 수요를 충분히 모집하지 못하게 될 불확실성도 존재하게 됩니다.
당사는 이러한 과거 사례를 기반으로 이사회에서 논의를 진행하였고, 당사의 금번 유상증자는 미래 성장을 위한 시설자금 및 신약연구개발에 우선적으로 사용될 예정으로 시장 평균 대비 낮은 할인율을 설정하더라도 본 증자를 통한 성공적인 자금조달이 가능할 것이라는 대표주관회사의 의견을 반영하여 시장 평균 23.3%보다 낮은 20%를 할인율로 설정하게 되었습니다. 해당 20% 할인율을 적용하여 최초 신고기준 약 천억원 유상증자를 위해 이사회결의일 전 영업일 기준으로 산출한 본 건의 증자비율 역시 시장 평균 39.6%보다 소폭 높은 수준인 44.13%로 주주가치희석을 최소화하면서도 자금조달목적을 효과적으로 달성할 수 있는 발행조건 수준으로 판단하였습니다.
또한 채무상환목적이 아닌 당사의 유상증자 배경 및 사용목적과 유사한 최근 사례 3건(메드팩토, 박셀바이오, 메디포스트)을 살펴보면, 증자비율은 49.4% 수준으로 당사가 설정한 증자비율보다 높게 유상증자를 진행했던 것으로 확인됩니다. 따라서 당사의 자금사용목적과 연계하여 고려한 증자비율은 적절한 수준으로 판단하였습니다.
당사는 이와 같은 내용을 이사회를 통해 충분히 논의하였습니다. 구체적으로 3월 28 일 예정된 이사회의 소집을 당사 정관에 따라 이사회 회의 3일전에 각 이사에게 통지하였으며 3월 26일 진행된 주주총회 이후 개최된 이사회에서 각 이사분들에게 관련사항을 설명드렸습니다. 이후 3월 28일 금요일 오전 9시 유상증자 결의를 위한 이사회를 개회하고 참석 이사 5인의 전원 만장일치로 유상증자 안건을 결의하였습니다. 추가로 당사는 할인율 및 증자비율에 대한 적정성에 대해서도 별첨 자료를 작성하여 각 이사분들께 충분히 설명드린 바 있습니다.
투자자분들 께서는 당사가 본 증자를 통해 조달하고자 자금의 사용목적, 할인율 및 증자비율에 대한 당사 이사회의 결정사항 등을 참고하시기 바랍니다.
| 파. 소액주주 보호 관련 위험 당사는 금번 유상증자와 관련하여 주주와의 소통을 강화하고, 기관주주 및 외국인주주, 소액주주 대상으로 본 유상증자 결의일 익영업일인 3월 31일 오후 4시와 4월 22일 오후 2시 30분, 2차례에 걸쳐 투자자들을 대상으로 IR을 진행한 바 있습니다. 해당 IR을 통해 당사의 대표이사는 본 유상증자의 배경, 목적, 기대효과와 당사의 중장기 사업전략 및 경영 목표 등을 상세히 설명하였습니다. 또한 증권사 애널리스트 대상으로도 적극적으로 소통하고 있으며, 시장 내에 충분한 정보가 전달될 수 있도록 노력하고 있습니다. 더불어 당사는 내부적으로 소액주주 전담 상담인력 2명을 구비하여 소액주주분들의 문의사항에 적극 대응 중이며 향후에도 유상증자와 관련한 문의사항, 참여 절차에 대한 안내 등 소액주주가 권리를 행사하는데 불편함이 없도록 도울 예정입니다. 별개로 당사의 최대주주는 최대주주로서의 책임을 다하기 위해 배정받은 신주인수권리를 적극 행사할 예정이며 2대, 3대 주주 또한 자금상황을 고려하여 증자에 참여하거나 참여하지 않을 경우 최대주주가 증서를 장외 매수하여 신주인수권을 행사하는 등 당사의 최대주주 및 주요주주는 책임경영 의지를 표명할 예정입니다. 당사는 상기와 같이 주주 및 시장과의 적극적인 소통을 통해 회사의 경영 전략 및 비전을 명확히 전달하는 한편, 본 유상증자와 관련 후속 정보를 지속적으로 제공해 나갈 예정입니다. 이점 참고해 주시기 바랍니다. |
당사는 금번 유상증자와 관련하여 주주와의 소통을 강화하고, 기관주주 및 외국인주주, 소액주주 대상으로 본 유상증자 결의일 익영업일인 3월 31일 오후 4시와 4월 22일 오후 2시 30분, 2차례에 걸쳐 IR을 진행한 바 있습니다. 해당 IR을 통해 당사의 대표이사는 본 유상증자의 배경, 목적, 기대효과와 당사의 중장기 사업전략 및 경영 목표 등을 상세히 설명하였습니다. 또한 증권사 애널리스트 대상으로도 적극적으로 소통하고 있으며, 시장 내에 충분한 정보가 전달될 수 있도록 노력하고 있습니다.
| [유상증자 주요일정 및 주주보호를 위한 당사의 권익활동 요약] |
 |
|
주요일정 및 주주보호를 위한 권익활동 |
| (자료 : 당사 IR자료) |
이와 함께, 소액주주의 정보 접근성을 높이고 소통을 활성화하여 주주 권익을 보호하고자 합니다. 먼저 유상증자 주요 내용에 대해 주주들이 쉽게 이해할 수 있도록 관련 내용을 PT 형태로 정리하여 당사 홈페이지에 게시하였으며 추가로 증권신고서 제출 이후 회사 홈페이지 내 유상증자의 취지를 담은 대표이사의 서한 및 FAQ 게시 등 관련 정보를 상시 제공하고 있습니다. 더불어 당사는 내부적으로 소액주주 전담 상담인력 2명을 구비하여 소액주주분들의 문의사항에 적극 대응 중이며 향후에도 유상증자와 관련한 문의사항, 참여 절차에 대한 안내 등 소액주주가 권리를 행사하는데 불편함이 없도록 도울 예정입니다. 현재까지 당사에게 접수된 소액주주분들의 문의사항은 본 정정증권신고서 제출일 기준 40건이며 주로 공모일정 및 예정발행가액, 주가변동, OCI홀딩스 및 대주주들의 참여여부, 자금사용목적, 연구개발(R&D) 관련 투자처, 할인율 및 증자비율 선정 배경 등에 대한 내용으로 당사의 "신주배정기준일은 6월 2일이며, 7월 8~9일이 구주주 청약날짜이고, 예정발행가액은 3,310원이지만 확정가액은 7월 3일날 결정됩니다. 대주주들의 참여에 대해서는 저희가 결정하는 문제가 아닌 만큼 확답을 드릴수는 없습니다. OCI홀딩스에서도 이사회 승인을 받아야 하는 사항으로 아직 확정된 것은 없으나 최대 주주의 의무를 다할 것으로 믿고 있습니다."라고 답변드리고 홈페이지에도 질의 응답 게시 및 업데이트를 통하여 적극적으로 안내드리고 있습니다. 아울러 당사가 소액주주분들과 대응하는 과정에서 미진한 부분이 확인될 시 즉각 내부적인 회의를 통해 대응 전략을 구비하여 소액주주분들에게 적절한 안내사항이 전달될 수 있도록 노력하고 있습니다. 앞으로도 소액주주께서 권리를 행사하시는 구주주청약일 전까지 내부 전담 인력을 지속 구비할 예정이며 주주분들의 질의사항에 적절히 대응할 수 있도록 노력할 예정입니다.
당사에 접수된 소액주주의 주요 문의사항 및 당사의 대응은 아래와 같으며, 자세한 사항 및 추가적인 개별 문의는 함께 기재된 당사 IR 이메일 혹은 연락처로 연락주시기 바랍니다.
| 주요 문의 내용 | 당사 답변 |
| 1. 1,200억원 가량 현금을 보유중임에도 불구 유상증자를 통해 자금을 조달하는 사유 | 당사는 현재 약 1,200억원 자체 현금을 보유중이나 이를 본 증권신고서에 기재된 자금사용목적 재원으로 활용할 경우 보유 현금은 약 200억원으로 축소됩니다. 이 경우 통제불가능한 외부 변수, 예컨데 (1) 금융권의 차입금 만기 상환 요청(현재 당사는 26년 만기 도래하는 차입금 800억원 보유 중), (2) 건강심사평가원 등 규제기관의 규제 강화로 인한 영업현금흐름 축소, (3) 예상치 못한 연구개발비 증가 등이 발생 시 유동성 부족이 발생하여, 이에 대응하기 위한 추가 조달이 필요하게 됩니다. 또한 당사가 영위하는 의약산업 및 연구개발은 미래 불확실성이 존재하기에 운영자금 목적으로 일정 수준의 현금 보유량을 유지하는 것은 제약회사의 필수적인 경영 전략이라고 할 수 있습니다. 이에, 당사가 본 증권신고서 자금사용목적에 기재된 전략을 실행하기 위해서는 외부 조달이 수반되어야 한다고 할 수 있습니다. |
| 2. 자금사용목적에 기재된 목적 달성시 예상 효과 | 자금사용목적상 기재된 증축을 통해 당사의 생산능력는 약 50% 이상 증가할 것으로 전망됩니다. 당사는 증가된 생산능력을 현재 계획중인 신제품 생산에 활용할 예정이며 해당 제품군의 수익성(원가율)은 기존 제품 대비 우월한 점, 또한 매출액 증가에도 불구 기존 고정비는 유의적인 증가가 수반되지 않은 소위 "고정비 레버리지효과" 등이 복합적으로 작용하여 당사 매출총이익 및 영업이익 개선에 기여할 것으로 전망됩니다. 궁극적으로 본 생산능력 증축을 통해 약 480억원 매출증가, 175억원 영업이익 증가 및 225억원 EBITDA 증가 효과가 기대되고 있습니다(영업이익율 8.7%에서 14.11%로 개선). |
| 3. OCI홀딩스 및 대주주의 참여 여부 |
해당 사항은 OCI홀딩스의 결정 권한에 속하며, OCI홀딩스 또한 이사회 승인을 거쳐야 하는 사안입니다. 당사는 최대주주로서 OCI홀딩스가 책임을 다할 것이라 믿고 있으며, OCI홀딩스 역시 최대주주의 책임 있는 자세로 최선의 방안을 모색할 것으로 판단하고 있습니다. 다른 대주주들의 참여 여부는 아직 확정되지 않았습니다. 만약 대주주들이 참여하지 않게 될 경우, 최대주주로서 OCI홀딩스가 책임을 다하는 차원에서 적절한 대응 방안을 마련할 것으로 판단하고 있습니다. |
| 4. CAPA 증설은 오랜 기간 논의되어온 이슈인데 지금에서야 의사결정이 진행된 사유 | 당사의 공급 문제는 최근에 당면한 이슈가 아닌 최근 3개년간 지속적으로 논의되어온 이슈 입니다. 이러한 생산설비 확충의 필요성은 이미 수년 전부터 인식하고 있었으나, 2022년과 2023년 연속된 적자와 운영자금 부족, 그리고 800억 원 규모의 차입 등 재무적 제약으로 인해 당장의 운영효율성 개선에 집중이 필요하여 즉각적인 설비 투자나 유상증자 추진은 어려운 상황이었습니다. 특히 2023년에는 영업적자 발생으로 인해 영업현금흐름이 마이너스로 전환되었고 약 800억 원 규모의 신규 차입이 이루어지면서 재무활동현금흐름으로 763억 원이 유입되었지만 2024년 자회사 Contera Pharma 투자자의 풋옵션 행사로 인해 677억 원이 유출되었습니다. 또한 2023~2024년에는 당사가 진행한 JM-010 임상으로 인해 임상개발에 따른 현금 유출이 증가하여 생산설비 확장을 위한 자금 확보가 여의치 않게 되었습니다. 다만 25년 하반기부터 지속적인 신제품 출시가 예정되어 있어 생산설비 부족에 따른 성장 여력 한계가 더욱 시급한 이슈로 부각됨에 따라 더 이상 생산설비 확충 이슈를 미룰 수 없다고 판단하였고 이와 맞물려 2024년 흑자 전환을 계기로 경영이 안정화됨에 따라, 생산 역량 강화와 기업가치 제고를 위하여 유상증자를 결정하였습니다. |
| 5. 유상증자 금액 중 연구개발(R&D) 관련 구체적인 투자처 | 신규 제제 개발 및 기존 제제 개선에 132억 원, 합성 신약 연구에 43억 원, 공동 개발 및 제제 기술 이전 등 개발 과제 도입에 47억 원을 투입할 계획입니다. 또한 라투다 등 기존 제품의 적응증 추가를 위한 임상 연구에는 42억 원, 연구개발 관련 설비 투자에는 약 37억 원이 사용될 예정입니다. 마지막으로 인건비를 포함한 필수 운영 자금 등 기타 운영비로는 156억 원이 투입될 계획입니다. |
| 6. 3월 26일 주주총회 당시 증자계획을 주주들에게 설명하지 않은 경위 | 유상증자 계획은 자본시장법 제174조에 따라 공시 전까지는 미공개 중요정보에 해당하며, 확정되지 않은 계획을 준비 단계에서 언급하는 것은 시장에 혼선을 초래할 우려가 있어 외부 공개하거나 언급하는 것이 불가능합니다. 아울러 금번 주주총회에서는 사외이사 한 분이 퇴임하시고, 새로운 사외이사 및 사내이사 각 한 분이 새로 선임되는 큰 변화가 있었습니다. 유상증자는 이사회 결의를 통해 진행되어야 하므로, 새로운 이사진의 구성 이전에 결의하는 것은 향후 절차상 부담이 될 수 있었습니다. 이에 따라 신임 이사진 선임 후 이사회 결의를 거쳐 유상증자 계획을 확정하게 되었습니다. 아직 확정되지 않은 사안에 대해 주주총회에서 유상증자 관련 답변을 드리지 못한 점, 미공개 중요정보에 해당하는 점을 고려한 불가피한 조치였음을 양해해 주시기 바랍니다. |
| 7. 유상증자가 무산될 가능성 | 주관 증권사와 전액 총액 인수 계약이 되어 있습니다. 만약 기존 주주분들의 참여가 저조하여 실권주가 발생하면, 실권주는 일반 공모 절차로 넘어가서 비주주인 일반 투자자들을 대상으로 공모가 진행됩니다. 일반 공모도 경쟁률이 미달이 되는 경우에는 주관 증권사가 총액 인수 계약에 따라 잔여 물량 전부를 인수하게 됩니다. 따라서 이번 유상증자가 무산될 가능성은 매우 낮다고 볼 수 있습니다. |
| 8. 증자 금액을 1,000억 원으로 결정하고 할인율은 20%, 증자 비율은 44%로 지정한 사유 | 증권신고서에도 기재하였듯, 당사가 필요로 하는 자금 규모는 1,000억 원을 초과합니다. 이 중 1,000억 원을 주주 배정 유상증자를 통해서 모집하고 자금사용 목적에 대해서는 증권신고서에 상세히 적어 기재하였습니다. 할인율 20%와 증자 비율 44%는 유상증자의 다른 사례와 비교해 볼 때 통상적 평균적인 숫자입니다. 할인율 20% 정도는 주주 배정 유상증자에 있어서는 평균치 정도라고 판단합니다. 최근에 2~3년간 있었던 주주 배정 유상증자 증자 비율이 평균이 약 39% 정도입니다. 부광약품의 증자비율 44% 중에 우리 사주 조합에 할당된 걸 제외하면 일반 주주 참여를 가정한 증자 비율은 약 35%입니다. 우리사주조합의 참여 여부는 아직 결정되지 않았으며, 44%라는 비율 역시 다른 유상증자 사례들과 비교해 볼 때 과도하다고 보기 어렵습니다. |
| 9. 어느 생산 설비를 매수할지 결정되었는지 여부 | 현재 2~3개 처의 제약 공장을 검토하고 있고 예비 실사도 거치고 있습니다. 다만, 아직 구체적인 대상이 확정된 것은 아니며, 모두 후보 단계에 있는 상황이기 때문에 현시점에서 특정 대상을 공개하기는 어렵습니다. 현재로서는 CMO 사업을 주력으로 영위하는 공장들을 중심으로 검토 중임을 말씀드릴 수 있습니다. |
| 10. CDMO 사업에 진출하려는 상황에서후발 주자로서 어떤 전략을 마련하고 있는지 여부 | 당사가 추진 중인 CDMO 사업은 바이오 의약품 분야가 아니라 당사가 기존에 강점을 보유하고 있는 합성의약품 및 합성화학 기반 의약품 영역에 집중되어 있습니다.부광약품의 R&D 연구개발 역량과 CMO 사업을 안정적으로 수행하고 있는 공장의 역량을 결합한다면 CDMO 사업의 본격적인 지출이 충분히 가능하다는 판단을 내렸습니다. |
| 11. 증자 전 소액주주 상대 증자 필요성 및 경위에 대해 자세한 설명이 필요하다고 보는데 당사의 입장은? | 유상증자 계획은 공개 전까지는 자본시장법상 미공개 중요정보에 해당하고, 불확정적 계획을 공개 또는 공시하는 것은 시장에 혼란을 초래할 수 있으므로, 확정 전에 이를 외부에 공개하거나 언급하는 것은 불가합니다. 유상증자와 관련하여 이사회 결의와 동시에 주요사항보고서를 공시하였으며, 당사 홈페이지에 대표이사의 유상증자 취지를 담은 서한을 게시하고, 보다 구체적인 내용을 프레젠테이션 자료로 게시하여 제공하였습니다. 또한, 다음 영업일인 3월 31일에는 대표이사가 직접 기관 및 개인 투자자를 포함한 모든 이해관계자를 대상으로 유상증자에 대해 설명하는 자리를 마련하였고, 주주 및 언론 등으로부터 접수된 질의를 정리하여 이에 대한 답변을 FAQ 형태로 홈페이지에 게시하였습니다. 해당 설명회는 웹세미나 방식으로 진행되어 누구나 쉽게 접근할 수 있도록 하였으며, 실시간 질의응답 기회도 충분히 제공하였습니다. 또한, 개인 주주분들의 문의에 신속하고 정확하게 응대하기 위해 전담 인력 2명으로 구성된 콜센터를 운영하고 있습니다. 당사는 본 유상증자에 대해 주주 여러분이 충분한 정보를 접하고 권리행사에 지장이 없도록 최선을 다하고 있으며, 유상증자 절차가 완료될 때까지 이러한 노력을 지속할 예정입니다. |
| 12. 공모일정 및 예정발행가액 | 구주주 청약은 7월 8일부터 9일까지 진행되며, 일반공모 청약에 대한 공고는 7월 10일 당사 인터넷 홈페이지 및 NH투자증권 홈페이지를 통해 게시될 예정입니다. 일반공모 청약은 7월 11일부터 14일까지 진행되며, 최종적으로 신주의 상장 예정일은 7월 28일입니다. 예정 발행가액은 3,310원이며 확정 발행가액은 7월 3일에 산정될 예정입니다. |
당사 IR 연락 정보
E-mail : ir@bukwang.co.kr
Tel : 02-828-8114 (전담콜센터 운영)
내선번호 : 117, 092
별개로 당사의 최대주주는 최대주주로서의 책임을 다하기 위해 배정받은 신주인수권리를 적극 행사할 예정이며 2대, 3대 주주 또한 자금상황을 고려하여 증자에 참여하거나 참여하지 않을 경우 최대주주가 증서를 장외 매수하여 신주인수권을 행사하는 등 당사의 최대주주 및 주요주주는 책임경영 의지를 표명할 예정입니다.
당사는 상기와 같이 주주 및 시장과의 적극적인 소통을 통해 회사의 경영 전략 및 비전을 명확히 전달하는 한편, 본 유상증자와 관련 후속 정보를 지속적으로 제공해 나갈 예정입니다. 이점 참고해 주시기 바랍니다.
IV. 인수인의 의견(분석기관의 평가의견)
1. 분석기관
| 구 분 | 회 사 명 | 고 유 번 호 |
|---|---|---|
| 대표주관회사 | NH투자증권㈜ | 00120182 |
2. 분석의 개요
대표주관회사인 NH투자증권㈜는『자본시장과 금융투자업에 관한 법률』제71조 및 동법 시행령 제68조에 의거 공정한 거래질서 확립과 투자자 보호를 위해 다수인을 상대로 한 모집ㆍ매출 등에 관여하는 인수회사로서, 발행인이 제출하는 증권신고서 등에 허위의 기재나 중요한 사항의 누락을 방지하는데 필요한 적절한 주의를 기울였습니다.
대표주관회사는 인수 또는 모집ㆍ매출의 주선업무를 수행함에 있어 적절한 주의의무를 다하기 위해 금융감독원이 제정한 『금융투자회사의 기업실사(Due Diligence) 모범규준』(이하 '모범규준'이라 한다)의 내용을 내부 규정에 반영하여 2012년 2월 1일부터 제출되는 지분증권, 채무증권 증권신고서를 대상(자산유동화증권 등 제외)으로 기업실사를 의무적으로 수행하도록 규정하고 있습니다.
다만, '모범규준' 제3조 제②항에 따라 발행회사의 재무 및 영업현황, 사업 환경, 투자위험, 인수 형태, 신용평가등급 등을 감안하여 강화하거나, 완화할 수 있으며, 동조제⑤항에 따르면 금융투자회사의 이사회나 리스크관리위원회의 의사결정을 거쳐 '모범규준'의 내용(실사수준)을 생략하거나 강화 또는 완화 적용할 수 있도록 허용하였는 바, 주관회사는 지분증권의 인수 또는 모집·매출의 주선업무를 수행함에 있어서 지분증권의 특성 및 발행회사의 일정요건 충족여부 등에 따라 기업실사 수준을 완화하여 적용할 수 있도록 규정하고 있습니다.
본 지분증권은 대표주관회사인 NH투자증권㈜의 내부 규정상 기업실사 기준을 적용하여 기업실사 업무를 수행하였습니다.
아울러 대표주관회사인 NH투자증권(주)는 본 유상증자를 진행함에 있어 7차례 이상 발행회사인 동사와 대면 미팅을 진행하였으며 사업 및 회사 관련 내용에 대해 사전으로 질의내용을 서면 공유하였으며 관련하여 4회 이상 대면 인터뷰를 진행하였습니다.
| <금융투자회사의 기업실사 모범규준> 제3조(적용범위 등) ① 이 규준은 법 제119조제3항의 규정에 의한 증권신고서 및 법 제122조의 규정에 의한 정정신고서를 제출하는 경우에 적용하며, 영업의 실체가 있는 발행회사가 제출하는 지분증권, 채무증권 증권신고서를 대상으로 하고 자산유동화증권 등은 적용대상에서 제외된다. ② 이 규준은 주간회사가 업무수행 중 참고해야 할 기본적인 지침으로 발행회사의 재무 및 영업 현황, 사업 환경, 투자위험, 인수 형태 등을 감안하여 강화하거나 완화하는 등 탄력적으로 운용할 수 있다. ③ 기업공개의 경우 기업공개 실사절차의 특성을 감안하여 이 규준의 내용중 한국거래소의 상장심사지침 등에서 의무사항으로 규정하고 있는 내용과 중복되는 부분에 대해서는 이를 생략하거나 완화할 수 있다. ④ 채무증권의 경우 i)보증유무, 상환조건(만기, 옵션유무), 특약 등 해당 사채의 특성, ii)법 제119조제2항에서 규정하고 있는 일괄신고서에 의한 발행인지 여부, iii)발행회사가 시행령 제121조제6항의 요건을 충족하고 있는지 여부, iv)해당 사채권에 대한 신용평가등급(외부 및 내부) 등을 감안하여 합리적인 기준에 따라 이 규준을 완화할 수 있다. ⑤ 제2항 내지 제4항에 따라 이 규준을 생략하거나 강화 또는 완화하는 경우에는 이사회나 리스크관리위원회(이하 '리스크관리위원회 등')의 의사결정을 거쳐야 한다. |
3. 기업실사 일정 및 주요 내용
| 일자 | 기업 실사 내용 |
|---|---|
| 2024년 12월 13일 | * 발행회사 방문 - 자금조달 금액 등 발행회사 의견 청취 - 공시 및 뉴스 내용 등을 통한 발행회사 및 소속산업 사전 조사 - 주요 사항 및 일정 체크 - 유상증자 상세 일정 등 업무 협의 - 실사 사전 요청자료 송부 |
| 2025년 01월 02일 ~ 2025년 01월 10일 |
* 발행회사 및 해당 산업 조사 - 실사 사전 요청 자료 목록 및 Check List 제공 - 공시 및 뉴스 내용 등을 통한 발행회사 및 산업 이해 - 관련 Q&A 등 * 유상증자 리스크검토 - 발행시장 상황, 자금조달규모 적정성, 공모가액 희망 할인율 |
| 2025년 01월 13일 ~ 2025년 03월 07일 |
* 현장 방문을 통한 실사(5회 이상) * Due-diligence checklist에 따라 투자위험요소 실사 1) 사업위험관련 실사 - 영위중인 사업 및 신규 사업에 대한 세부사항 등 체크 2) 회사위험관련 실사 - 재무관련 위험 및 우발채무 등의 위험요소 등 체크 3) 기타위험관련 실사 * 투자위험요소 세부사항 체크 - 원장 및 각종 명세서 등의 실제 장부검토 - 주요 계약관련 계약서 및 소송관련 서류 등의 확인 - 각 부서 주요 담당자 인터뷰 * 주요 경영진 면담 - 경영진 평판 리스크 검토 - 향후 사업추진계획 및 발행회사의 비젼 검토 - 책임자 인터뷰를 통한 자금사용목적 확인 |
| 2025년 03월 10일 ~ 2025년 03월 27일 |
* 실사 추가 자료 요청 * 증권신고서 작성 및 조언 * 이사회의사록 검토/인수계약서 체결 * 실사이행보고서 및 증권신고서 작성 / 검토 |
| 2025년 03월 28일 ~ 2025년 05월 07일 |
* 증권신고서 보완 및 정정관련 조언 * 실사 추가 자료 요청 |
4. 기업실사 참여자
| [대표주관회사] |
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 | 참여기간 | 주요경력 |
|---|---|---|---|---|---|---|
| NH투자증권 | General Industry부 | 김영호 | 이사 | 기업실사 총괄 | 2024년 12월 13일 ~ 2025년 05월 07일 |
기업금융업무 15년 |
| NH투자증권 | General Industry부 | 정원식 | 차장 | 기업실사 책임 | 2024년 12월 13일 ~ 2025년 05월 07일 |
기업금융업무 10년 |
| NH투자증권 | General Industry부 | 양희성 | 대리 | 기업실사 실무 | 2024년 12월 13일 ~ 2025년 05월 07일 |
기업금융업무 2년 |
| [발행회사] |
| 소속기관 | 부서 | 성명 | 직 책 | 실사업무분장 |
|---|---|---|---|---|
| 부광약품(주) | 연구개발본부 | 김지헌 | 전무 | 기업실사 자료 제공 |
| 재무지원부 | 김민규 | 상무 | 기업실사 자료 제공 | |
| 생산본부 | 김원섭 | 상무 | 기업실사 자료 제공 | |
| 커뮤니케이션팀 | 최창호 | 부장 | 기업실사 자료 제공 | |
| 재무지원팀 | 이석주 | 팀장 | 기업실사 자료 제공 | |
| 재무지원팀 | 이성희 | 과장 | 기업실사 자료 제공 |
5. 기업실사 세부항목 및 점검 결과
- 동 증권신고서에 첨부되어 있는 기업실사 보고서를 참조해 주시기 바랍니다.
6. 종합 의견
대표주관회사인 NH투자증권㈜는 부광약품㈜가 2025년 03월 28일 이사회에서 결의한 기명식 보통주식 30,210,000주에 대한 주주배정후 실권주 일반공모 유상증자를 잔액인수 함에 있어 다음과 같이 의견을 제시합니다.
가. 부광약품㈜는 의약품의 제조 및 판매를 목적으로 설립되었으며, 주요 사업으로는 의약품, 건강기능식품, 그 외 의약외품 등의 제조 및 판매를 영위하고 있습니다. 주요 제품으로는 훼로바, 레가론, 덱시드, 치옥타시드, 씬지로이드 등이 있습니다. 서울특별시 동작구에 위치한 본사 및 중앙연구소에서 의약품 연구 및 개발사업을 진행하고 있으며, 경기도 안성에 위치한 사업장을 중심으로 하여, 덴마크, 싱가포르 등 국내외 4개의 종속기업을 두고 글로벌 시장 진출을 목표하고 있습니다.
부광약품㈜는 완제 의약품 제조 전문기업으로서, 신규 개발 파이프라인의 수익성, 리스크 등을 종합적으로 고려한 R&D 전략을 수립하고 있으며, 오픈 이노베이션을 통한 연구개발에 특화되어 있습니다. 부광약품㈜가 시판 중인 완제의약품의 대부분은 의사의 처방이 필요한 전문의약품으로, 전국 주요 상급종합병원, 대형병원을 대상으로 영업 활동을 전개하고 있으며, 특히 조현병 및 양극성 우울증 치료제 '라투다정' 등 전문 의약품을 개발 및 판매하며 중추신경계(CNS) 질환 치료제 영업조직의 전문성을 강화하고 있습니다.
다만, 부광약품㈜이 영위하고 있는 제약바이오 산업은 국내외 거시경제의 직ㆍ간접적인 영향을 받고 있으며, 고금리, 고환율, 저성장 등에 따른 글로벌 경기침체로 인해 제약 바이오 산업에 대한 연구개발 투자가 위축되거나 실적이 악화된 바 있습니다. 현재 국내외 경제 불안요인이 완전히 해소되지 않은 상황에서, 제약바이오 산업의 성장성이 저하되거나, 부광약품㈜의 주요 판매 제품이 속한 CNS 시장이 위축되는 등 산업 성장의 불확실성은 잠재적인 위험요인으로 작용하고 있습니다. 이러한 거시경제 및 산업성장 불확실성은 국내외 경기 전반에 걸쳐 영향을 미칠 수 있으며, 동사가 영위하는 사업 및 실적에도 부정적인 요인으로 작용할 수 있습니다.
나. 증권신고서 제출일 현재 부광약품㈜의 최대주주는 OCI홀딩스(주)로 최대주주의 지분율은 보통주 기준으로 11.32%입니다. OCI홀딩스는(주)는 OCI그룹의 지주회사로서, 2023년 5월 1일을 분할기일로 하여 베이직케미컬 사업부문과 카본케미컬 사업부문을 OCI(주)로 인적분할하며 OCI 홀딩스(주)를 출범하고, 같은 해 9월 공개매수 및 현물출자에 의한 유상증자를 통하여 지주회사 요건을 충족하며 2023년 9월 22일 기준으로 지주회사로 전환하였습니다. 한편 최대 주주는 2대주주 및 3대 주주와 현재까지 우호적인 관계를 유지하고 있는 것으로 파악되며, 이들의 지분을 합산할 시 약 30.46%입니다. 2024년 12월 31일 기준 전체 지분 중 67.34%의 지분을 일반소액주주가 보유하고 있으며, 금번 유상증자에 최대주주가 참여를 예정하고 있는 점을 고려 시, 향후 지배구조로 인해 경영권이 불안정해질 수 있는 요소는 보고서 제출일 현재 없는 것으로 판단됩니다.
다. 동사는 타 제약사 대비 상대적으로 우수한 재무비율을 유지하고 있습니다. 연결기준 유동비율은 2023년을 제외하고 500% 내외를 기록해 왔으며, 2023년에는 자회사 주식매수청구권(Put Option) 행사 기한 도래 이슈로 인해 유동비율이 일시적으로 260% 수준으로 하락하였으나, 2024년 해당 이슈 해소로 2024년 유동비율은 다시 500% 이상 수준으로 회복되었습니다. 부채비율은 2021년과 2022년에 41~48% 수준을 유지하였으나, 2023년에는 일시적인 영업적자, 신규 차입금 발생, 기타유동부채 증가 등이 복합적으로 작용하면서 83.13%로 상승하였습니다. 그러나 2024년에는 수익성 개선과 함께 기타유동부채가 상환되며, 부채비율은 52.85%로 개선되었고, 2025년 1분기말 부채비율 또한 52.88%로 유사한 수준을 유지하고 있습니다. 동사는 사업확장 및 매출성장을 위한 신약 연구개발 및 JV설립, 지분투자 등의 투자를 지속하고 있음에도 불구하고, 안정적인 재무지표를 유지하고 있는 등 재무건전성 및 유동성 리스크는 낮은 것으로 판단됩니다.
| 구 분 | 2025년 1분기말 |
2024 | 2023 | 2022 | 2021 |
| 자산 | 372,643 | 373,180 | 429,017 | 400,929 | 397,417 |
| 유동자산 | 206,464 | 203,739 | 254,179 | 218,741 | 220,095 |
| 비유동자산 | 166,179 | 169,441 | 174,839 | 182,188 | 177,321 |
| 부채 | 128,901 | 129,035 | 194,752 | 129,082 | 117,356 |
| 유동부채 | 35,243 | 35,398 | 97,544 | 44,603 | 36,995 |
| 비유동부채 | 93,658 | 93,637 | 97,208 | 84,479 | 80,361 |
| 자본총계 | 243,742 | 244,145 | 234,265 | 271,847 | 280,061 |
| 총차입금 | 80,159 | 79,424 | 79,387 | 931 | 1,558 |
| 유동리스부채 | 381 | 130 | 218 | 243 | 444 |
| 장기차입금 | 79,135 | 79,024 | 78,525 | - | - |
| 비유동리스부채 | 643 | 270 | 644 | 688 | 1,114 |
| 현금및현금성자산 | 87,813 | 90,091 | 151,227 | 85,517 | 82,777 |
| 순차입금 | (7,655) | (10,667) | (71,840) | (84,586) | (81,219) |
| 유동비율 | 585.83% | 575.56% | 260.58% | 490.42% | 594.94% |
| 부채비율 | 52.88% | 52.85% | 83.13% | 47.48% | 41.90% |
| 총차입금의존도 | 21.51% | 21.28% | 18.50% | 0.23% | 0.39% |
| 순차입금의존도 | -2.05% | -2.86% | -16.75% | -21.10% | -20.44% |
| (자료 : 당사 사업보고서 및 분기보고서) |
라. 동사는 2023년 연결기준 2022년 대비 34.04% 감소한 약 1,259원의 매출을 기록하며 급격한 매출 하락을 겪었습니다. 이는 2023년 동사가 내부 조직을 개편하고 도매상 중심의 유통구조를 재정비하는 등 질적 성장을 위한 경영 전략을 추진한 데에 따른 결과이며, 이 과정에서 제품의 매출 비중이 일시적으로 감소하였고 시중 재고 수준이 높은 일부 품목의 출하를 축소함에 따라 전체 매출액이 감소하였습니다. 이에 따라 영업손실도 2022년 2억 원에서 2023년에는 172억원의 영업손실로 손실 규모가 확대되었습니다. 하지만, 2024년부터 경영구조 개편 효과가 나타나며 2024년 연결기준 매출액은 전년 대비 27.13% 증가한 1,601억원을 기록하였고, 영업이익은 16억원을 기록하며 흑자 전환하였습니다. 아울러 공헌이익 기반의 품목 재구성을 통한 매출 구조 개선과 구매원가 절감 전략을 지속적으로 추진한 결과, 2024년 영업이익률은 1.01%를 기록하며 최근 3개년 중 가장 높은 수익성을 달성하였습니다. 2025년 1분기에는 연결 기준 매출액 478억원, 영업이익은 30억원을 기록하며 전년 동기 대비 39%의 매출 성장 및 분기기준 영업이익 흑자를 달성하였습니다. 그러나 당기순손실 1억원을 기록하며 순이익 흑자 전환에는 실패했는데, 주된 원인은 동사가 전략적 파트너로서 출자하여 보유한 TVM Life Science Ventures Vll의 수익증권에 대한 공정가치측정 금융자산 평가손실 42억원을 인식한 것으로, 이는 일회성 비용으로 판단되어 동사의 미래 손익에 추가적인 영향을 미칠 가능성은 미미한 것으로 보입니다. 한편, 최근 동사 제품의 공급부족 현상이 지속되고 있고, 2024년 8월 국내 출시된 신제품 효과 감안 시, 향후 실적 개선이 예상되며, 2023년과 같은 대규모 영업손실이 발생할 가능성은 제한적으로 판단됩니다.
| [ 동사 연결기준 실적 추이] |
| (단위: 백만원) |
| 구 분 | 2025년 1분기 |
2024년 1분기 |
2024 | 2023 | 2022 | 2021 |
|---|---|---|---|---|---|---|
| 매출액 | 47,806 | 34,393 | 160,087 | 125,928 | 190,909 | 182,491 |
| 매출원가 | 26,909 | 18,730 | 85,744 | 78,855 | 111,481 | 106,733 |
| 매출총이익 | 20,897 | 15,664 | 74,343 | 47,074 | 79,429 | 75,758 |
| 판매비와관리비 | 13,431 | 11,236 | 49,295 | 50,019 | 55,385 | 47,671 |
| 경상연구개발비 | 4,452 | 6,056 | 23,430 | 34,551 | 24,274 | 22,465 |
| 영업이익(손실) | 3,014 | (1,628) | 1,618 | (37,497) | (231) | 5,622 |
| 기타수익 | 835 | 54 | 10,097 | 2,300 | 569 | 439 |
| 기타비용 | 115 | 453 | 13,929 | 2,002 | 630 | 185 |
| 금융수익 | 1,377 | 1,792 | 5,680 | 3,846 | 3,450 | 4,265 |
| 금융비용 | 5,434 | 1,629 | 7,077 | 5,315 | 4,249 | 4,992 |
| 지분법이익(손실) | 0 | (261) | 641 | (901) | 59 | (1,361) |
| 법인세비용차감전순이익(손실) | (323) | (2,125) | (2,970) | (39,569) | (1,033) | 3,787 |
| 법인세비용(수익) | 212 | 433 | 489 | (5,163) | 3,216 | 6,584 |
| 당기순이익(손실) | (111) | (2,558) | (3,459) | (34,407) | (4,249) | (2,797) |
| 매출총이익율 | 43.71% | 45.54% | 46.44% | 37.38% | 41.61% | 41.51% |
| 경상연구개발비율 | 9.31% | 17.61% | 14.64% | 27.44% | 12.72% | 12.31% |
| 영업이익율 | 6.31% | -4.73% | 1.01% | -29.78% | -0.12% | 3.08% |
| 순이익율 | -0.23% | -7.44% | -2.16% | -27.32% | -2.23% | -1.53% |
| (자료 : 당사 사업보고서 및 분기보고서) |
마. 동사의 2025년 1분기말 연결기준 매출채권 회전율은 8.13회로 2024년말 5.40회 대비 대폭 개선된 모습을 나타내고 있습니다. 또한, 동사의 연결기준 재고자산은 자산총계의 11.18%를 차지하고 있어 2024년말 11.17% 와 유사한 수준을 유지, 2023년말 13.25% 대비해선 소폭 감소했으며, 동사의 재고자산 규모는 매출 및 사업 확장을 고려하였을 때 과도한 수준은 아닌 것으로 판단하고 있습니다. 동사는 2023년 유통구조 재정비 등 질적 성장을 위한 경영 전략 시행 과정에서 매출이 감소하고 재고가 증가하며 재고자산 회전율이 2022년 2.86회에서 2023년 1.65회로 감소하는 모습을 보였습니다. 다만, 2024년 경영 및 유통구조 개편 효과가 나타나며 매출이 증가하였고, 이에 따른 재고소진으로 재고자산은 2024년 417억으로 감소하고, 재고자산 회전율 또한 1.74회로 소폭 개선되는 모습을 보이고 있습니다. 2025년 1분기에는 동사의 주요 제품군의 매출 급성장 및 라투다정의 시장 안착에 따른 온기 실적 반응에 따라 매출이 전년 동기 대비 39% 급성장하고 이에 따라 매출원가도 전년 동기 대비 43.67% 증가하며 재고자산 회전율은 2.58회로 대폭 증가하는 모습을 보이고 있습니다. 동사의 신제품 효과 반영 및 공급부족 해소에 따른 매출 상승이 실현될 시, 재고자산 회전율 및 회전기간은 추가로 개선될 수 있을 것으로 전망하고 있습니다.
| [동사 연결기준 활동성 지표 추이] | |
| (단위 : 억원, 회) | |
| 구분 | 2025년 1분기 | 2024년 1분기 | 2024년 | 2023년 | 2022년 | 2021년 |
|---|---|---|---|---|---|---|
| 매출액 | 478 | 344 | 1,601 | 1,259 | 1,909 | 1,825 |
| 매출원가 | 269 | 187 | 857 | 789 | 1,115 | 1,067 |
| 자산총계 | 3,726 | 4,225 | 3,732 | 4,290 | 4,009 | 3,974 |
| 자본총계 | 2,437 | 2,326 | 2,441 | 2,343 | 2,718 | 2,801 |
| 재고자산 | 417 | 526 | 417 | 568 | 386 | 393 |
| 매출채권및기타채권 | 235 | 238 | 236 | 357 | 880 | 904 |
| 총자본회전율 | 0.51 | 0.32 | 0.40 | 0.30 | 0.48 | 0.46 |
| 재고자산 회전율 | 2.58 | 1.37 | 1.74 | 1.65 | 2.86 | 2.35 |
| 총자산대비 재고자산 비율 | 11.18% | 12.45% | 11.17% | 13.25% | 9.63% | 9.89% |
| 매출채권 회전율 | 8.13 | 4.63 | 5.40 | 2.04 | 2.14 | 1.88 |
| (출처 : 동사 연도별 사업보고서 및 분기보고서) (주1) 총자본회전율 : 매출액/[(기초 자산총계+기말 자산총계)/2] (주2) 재고자산회전율 : 매출원가/[(기초 재고자산+기말 재고자산)/2] (주3) 매출채권회전율 : 매출액/[(기초 매출채권및기타채권+기말 매출채권및기타채권)/2] (주4) 2025년 1분기 및 2024년 1분기 회전율은 연환산매출액 및 연환산매출원가를 기준으로 계산하였습니다. |
바. 동사는 한동안 무차입 경영 기조를 유지해 왔으며, 이에 따라 2021년 및 2022년 총차입금의존도는 1% 미만을 기록하였고, 보유 현금이 총차입금을 초과함에 따라 순차입금도 마이너스(-) 상태를 유지하였습니다. 2023년에는 신규 차입이 발생하면서 총차입금의존도가 18.50%로 증가하였고, 2024년에는 기타유동부채 상환에 따른 총자산 감소의 영향으로 21.28%로 소폭 상승하였으며, 2025년 1분기까지 유사한 수준을 유지하고 있습니다. 그럼에도 불구하고, 동종 업체와 비교 시 여전히 자산규모 대비 차입금 규모가 낮은 편이며, 보유 현금이 총차입금을 상회함에 따라 순차입금은 여전히 음(-)의 상태를 유지하고 있습니다.
동사의 차입금은 하나은행 및 신한은행으로부터 차입하였으며 만기는 2026년 도래할 예정입니다. 다만, 동사의 보유 현금 규모 및 영업현금흐름 고려 시 해당 차입금 상환에는 무리가 없을 것으로 판단되고 있습니다.
| [차입금 추이(연결기준)] | |
| (단위 : 백만원) | |
| 구 분 | 2025년 1분기말 |
2024 | 2023 | 2022 | 2021 |
| 총차입금 | 80,159 | 79,424 | 79,387 | 931 | 1,558 |
| 유동리스부채 | 381 | 130 | 218 | 243 | 444 |
| 장기차입금 | 79,135 | 79,024 | 78,525 | - | - |
| 비유동리스부채 | 643 | 270 | 644 | 688 | 1,114 |
| 현금및현금성자산 | 87,813 | 90,091 | 151,227 | 85,517 | 82,777 |
| 순차입금 | (7,655) | (10,667) | (71,840) | (84,586) | (81,219) |
| 총차입금의존도 | 21.51% | 21.28% | 18.50% | 0.23% | 0.39% |
| 순차입금의존도 | -2.05% | -2.86% | -16.75% | -21.10% | -20.44% |
| [ 당사 차입금 현황] |
| (단위: 원) |
| 구 분 | 차입처 | 최종 만기일 | 연이자율(%) | 2025년 1분기말 | 2024년말 |
| 원화장기차입금 | 하나은행 | 2026-08-16 | CD91일물 + 1.484 | 30,000,000,000 | 30,000,000,000 |
| 원화장기차입금(*) | 신한은행 | 2026-10-13 | CD91일물+ 1.39 | 50,000,000,000 | 50,000,000,000 |
| 소계 | 80,000,000,000 | 80,000,000,000 | |||
| 유동성 대체 | - | - | |||
| 차감 : 장기차입금할인발행차금 | (864,753,074) | (975,816,626) | |||
| 합계 | 79,135,246,926 | 79,024,183,374 | |||
| (자료 : 당사 분기보고서) (*)상기 차입금과 관련하여 유형자산을 담보로 제공하고 있습니다 |
사. 발행회사의 금번 유상증자로 인하여 기발행주식 총수 68,454,671주(보통주 68,454,671주)의 44.13%에 해당하는 30,210,000주가 추가로 상장됩니다. 금번 유상증자로 인해 추가 발행되는 주식은 전량 물량 출회가 가능하므로, 일시적인 물량출회에 따른 주가하락의 가능성이 있습니다.
아. 대표주관회사인 NH투자증권㈜는 부광약품㈜가 제출한 자료와 대표주관회사가 객관적으로 정확하고 신뢰할 수 있다고 믿어지는 자료를 중심으로 용역을 수행하였으며, 객관적인 입장에서 공정을 기하기 위하여 최선의 노력을 다 하였습니다.
자. 대표주관회사는 상기 실사를 통해 제공받는 자료들로부터 도출된 결과나 오류, 누락 등에 대하여 책임지지 않으며, 인간적 또는 기계적, 기타 그 외의 다른 요인에 의한 오류발생 가능성으로 인해 본 평가 내용에 대해 명시적으로 혹은 묵시적으로도 증명이나 서명 또는 보증 및 단언을 할 수 없습니다.
부광약품㈜의 금번 유상증자는 국내외 거시경제 변수와 사업 특성 등을 고려할 때 투자수익에 대해 증권신고서 제출 시점에서 신뢰성 있는 추측은 불가능합니다. 투자자 여러분께서는 상기 검토결과는 물론 동 증권신고서 및 예비투자설명서에 기재된 회사 전반의 현황 및 재무상의 위험, 산업 및 영업상의 위험요인 등을 감안하시어 투자에 유의하시기 바랍니다. 또한, 대표주관회사 및 발행회사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 동 증권신고서 및 투자설명서에 기재하지 않은 사항이라 하더라도 회사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자께서는 동 증권신고서 및 투자설명서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 독자적이고도 세밀한 판단에 의해 투자결정을 하시기 바랍니다.
| 2025. 05. 08. |
| 대표주관회사 NH투자증권 주식회사 |
| 대표이사 윤 병 운 |
V. 자금의 사용목적
1. 자금 조달 개요
가. 자금조달금액
| (단위 : 원) |
| 구 분 | 금 액 |
|---|---|
| 모집 또는 매출총액(1) | 99,995,100,000 |
| 발행제비용(2) | 1,272,163,816 |
| 순 수 입 금 [ (1)-(2) ] | 98,722,936,184 |
| 주1) 상기 금액은 예정 모집가액을 기준으로 산정한 금액으로 모집가액 확정 시 변경될 수있습니다. 주2) 상기 모집 또는 매출총액은 우선적으로 아래 자금의 사용 목적에 따라 사용하며, 발행제비용은 당사의 자체자금으로 사용할 예정입니다. |
나. 발행제비용의 내역
| (단위 : 원) |
| 구분 | 금액 | 비고 |
|---|---|---|
| 발행분담금 | 17,999,110 | 모집총액의 0.018% (10원 미만 절사) |
| 인수수수료 | 999,951,000 | 인수수수료: 모집총액의 1.0% |
| 신주인수권증서 표준코드발급수수료 | 10,000 | 정액 |
| 상장수수료 | 9,099,706 | 700억 원 초과 ~ 1,000억 원 이하 730만원+700억원 초과금액의 10억원당 6만원 |
| 발행등록수수료 | 500,000 | 1,000주당 300원 (신주인수권증서 및 주권 각 별도, 상한: 50만원) |
| 등록세 | 60,420,000 | 증자 자본금의 0.40% (지방세법 제28조, 10원 미만 절사) |
| 지방교육세 | 12,084,000 | 등록세의 20%(지방세법 제151조, 10원 미만 절사) |
| 기타비용 | 172,100,000 | 투자설명서, 신주배정통지서 인쇄 및 발송비 등 |
| 합계 | 1,272,163,816 | - |
| 주1) 상기 금액은 예정 모집가액을 기준으로 산정한 금액입니다. 주2) 발행제비용은 공모금액 및 상장신청일 직전일 한국거래소에서 거래되는 당사의 보통주식 종가기준으로 산정되며, 유관기관 정책 등에 따라 변동될 수 있습니다. 주3) 상기 등록세에 적용되는 증자 자본금은 [신주발행수 * 액면가액]으로 산출하였습니다. 주4) 기타비용은 예상금액으로 변동될 수 있습니다. 주5) 발행제비용은 당사가 자체적으로 보유한 자금으로 사용할 예정입니다. |
2. 자금의 사용목적
가. 자금의 사용목적
당사는 금번 유상증자를 통해 조달 예정인 자금 약 천억원을 시설자금 및 운영자금으로 사용할 계획이며 아래와 같이 자금을 집행할 계획입니다. 당사는 금번 유상증자를 통하여 조달하는 자금을 본 증권신고서에 기재한 사용목적대로 사용하기 위해 최선의 노력을 다할 것이며 기타 계열사 지원 등을 위한 목적으로는 사용하지 않을 예정입니다. 아울러 매 분기별 공시하는 당사의 정기보고서에 공모자금의 실제 사용내역 및 변동상황에 관하여 성실하게 공시할 예정입니다. 또한, 자금사용시기가 도래하지 않는 금액에 대해서는 국내 제1금융권 등의 안정성이 높은 상품에 예치할 계획이며, 자금의 사용시기가 도래하여 단기간 내에 자금의 사용이 예상되는 경우에는 제1금융권 등의 단기금융상품으로 운용할 계획입니다.
자금의 사용목적
| (기준일 : | 2025년 03월 27일 | ) | (단위 : 백만원) |
| 시설자금 | 영업양수 자금 |
운영자금 | 채무상환 자금 |
타법인증권 취득자금 |
기타 | 계 |
|---|---|---|---|---|---|---|
| 84,500 | - | 15,495 | - | - | - | 99,995 |
나. 자금의 세부 사용내역
당사는 금번 유상증자를 통해 조달할 예정인 약 천억원을 시설자금 및 운영자금으로 사용할 예정입니다. 구체적으로 기존 제조설비 확장 및 설비 도입, 제조설비 신규 취득 등과 관련하여 84,500백만원을 사용할 예정이며 당사 제제개발 등 R&D 운영자금 목적으로 15,495백만원을 집행할 계획입니다. 다만 당사가 영위하는 산업 특성 상 운영자금의 경우 불확실성이 높음에 따라 아래 기재된 우선순위로 자금 사용을 집행하되, 변경될 경우 정정신고를 통해 안내드릴 예정인 점 참고 부탁드립니다.
| [ 자금사용 우선순위] | |
| (단위 : 백만원) | |
| 우선순위 | 자금 용도 | 세부 내용 | 자금의 사용 시기 | 금액 | |
|---|---|---|---|---|---|
| 1 | 시설자금 | 제조시설 확장 및 생산능력 증가 | 기존 생산능력 10억정에서 증축을 통해 15억정으로 생산능력 증대 | '25년 ~ '27년 | 34,000 |
| 최신 생산설비 도입 | 최신의 내용고형제 생산설비 도입 및 공정 효율성 극대화 |
'25년 ~ '27년 | 11,000 | ||
| 자동화 시스템 도입 | 스마트 팩토리 개념을 적용한 자동화 시스템 도입 |
'25년 ~ '28년 1Q | 4,500 | ||
| 제조설비 신규 취득 | 공장 인수 및 신규 제조설비, 영업권 등 무형자산 취득 | '25년 | 35,000 | ||
| 2 | 운영자금 | 신규제제 개발 및 기존제제 개선연구 | 시장 경쟁력이 있는 신제품, 신제형 개발 및 기존제제 개선 |
'25년 ~ '28년 1Q | 13,200 |
| 합성신약 연구 | 당사의 합성신약 연구연략 및 국내외 병원 등과의 협력을 통한 혁신신약 개발 |
'25년 ~ '28년 1Q | 4,330 | ||
| 개발과제 도입 | 외부 업체와의 공동개발, 제제기술이전 등 협력을 통해 제품 개발 | '25년 ~ '28년 1Q | 4,720 | ||
| 적응증 추가 임상연구 | 적응증 추가를 위한 임상연구계획 수립 및 실행 |
'25년 ~ '28년 1Q | 4,193 | ||
| 연구개발 설비투자 | 자체 연구개발 기능 강화를 위해 연구 개발에 필요한 설비확충에 적극 투자 |
'25년 ~ '28년 1Q | 3,689 | ||
| 기타운영자금 | 인건비 및 기타 필수 운영비용 | '25년 ~ '28년 1Q | 15,625 | ||
| 3 | 타법인 취득자금 |
Contera Pharma 출자자금 | Contera Pharma의 CP-012 및 CP-102 연구개발자금 지원을 위한 지분투자 | '25년 ~ '28년 1Q | 90,723 |
| 출처 : 당사 제시 주1) 시설자금중 제조시설 확장이나 설비 도입의 경우 현 시점에서 규모가 어느정도 확정되었으나 제조설비 신규 취득이나 당사가 기재한 R&D 관련 운영자금은 향후 당사가 진행하는 임상 결과에 따라 변동될 가능성이 존재합니다. 이에 본 증자를 통해 조달하는 금액을 상회하는 자금사용목적을 기재하였으며 본 증자를 통해 조달하는 자금을 우선순위에 따라 사용하고 부족분에 대해서는 다른 자금조달(예컨대 한도대 400억원 및 보유현금 100~300억원, 최대주주 대상 3자배정 400~600억원 등) 방안을 통해 조달할 계획입니다. |
당사는 이와 같은 내용을 이사회를 통해 충분히 논의하였습니다. 구체적으로 3월 28 일 예정된 이사회의 소집을 당사 정관에 따라 이사회 회의 3일전에 각 이사에게 통지하였으며 3월 26일 진행된 주주총회 이후 개최된 이사회에서 각 이사분들에게 관련사항을 설명드렸습니다. 이후 3월 28일 금요일 오전 9시 유상증자 결의를 위한 이사회를 개회하고 참석 이사 5인의 전원 만장일치로 유상증자 안건을 결의하였습니다.
※ 공모 규모 및 증자 필요성에 대한 검토
① 미래성장 동력 확보를 위한 생산능력 확장 필요성
당사가 지속적으로 성장하기 위해서는 본업에서의 현금흐름 확장이 필수적입니다. 하지만 당사는 당사 내용고형제제 생산능력의 한계로 당사의 공급량이 시장 수요에 따라가지 못하기에 당사 매출액 성장에 있어서 근본적인 한계에 다다르게 되었습니다. 이에 따라 당사는 시설자금 집행을 통해 생산능력을 확충하여 고질적인 공급부족 문제를 빠른 시일 내에 해소하고자 합니다.
이러한 공급부족 문제는 하나의 영리기업으로서의 이해관계를 넘어서 국민건강 증진의 측면에서도 큰 문제입니다. 당사의 경우 당사가 1년간 생산하는 정제(tablet)에서 퇴장방지의약품이 약 68%를 차지하고 있습니다. 하지만 당사가 겪고 있는 심각한 공급부족 문제로 인해 국민이 반드시 필요로 하는 국가필수의약품과 퇴장방지의약품의 공급에도 큰 차질이 발생하였고 이는 수 차례 언론, 식품의약품안전처, 대한약사회 등 기관에서 이슈가 된 바 있습니다. 당사는 국민건강증진 차원에서도 자금조달을 통한 생산능력 확보가 반드시 필요하다고 판단하게 되었습니다.
당사의 공급 문제는 최근에 당면한 이슈가 아닌 최근 3개년간 지속적으로 논의되어온 이슈 입니다. 이러한 생산설비 확충의 필요성은 이미 수년 전부터 인식하고 있었으나, 2022년과 2023년 연속된 적자와 운영자금 부족, 그리고 800억 원 규모의 차입 등 재무적 제약으로 인해 당장의 운영효율성 개선에 집중이 필요하여 즉각적인 설비 투자나 유상증자 추진은 어려운 상황이었습니다. 특히 2023년에는 영업적자 발생으로 인해 영업현금흐름이 마이너스로 전환되었고 약 800억 원 규모의 신규 차입이 이루어지면서 재무활동현금흐름으로 763억 원이 유입되었지만 2024년 자회사 Contera Pharma 투자자의 풋옵션 행사로 인해 677억 원이 유출되었습니다. 또한 2023~2024년에는 당사가 진행한 JM-010 임상으로 인해 임상개발에 따른 현금 유출이 증가하여 생산설비 확장을 위한 자금 확보가 여의치 않게 되었습니다. 다만 25년 하반기부터 지속적인 신제품 출시가 예정되어 있어 생산설비 부족에 따른 성장 여력 한계가 더욱 시급한 이슈로 부각됨에 따라 더 이상 생산설비 확충 이슈를 미룰 수 없다고 판단하였고 이와 맞물려 2024년 흑자 전환을 계기로 경영이 안정화됨에 따라, 생산 역량 강화와 기업가치 제고를 위하여 유상증자를 결정하였습니다.
당사는 생산능력 확보를 통해 공급부족 문제를 해소할 수 있다면 매출성장의 근본적인 한계요인이 제거되어 매출액 및 수익성 개선으로 이어질 것으로 예상하고 있습니다. 또한 이로 인해 증가되는 현금흐름을 R&D 및 신규제제 개발 등 성장성이 높은 분야에 투자하여 기업의 유기적 성장을 가속화할 수 있는 선순환 구조를 구축할 계획입니다. 궁극적으로 이는 당사의 기업가치 제고 및 배당여력 확대 등 주주환원으로 이어질 것으로 당사는 기대하고 있습니다.
② 자금조달의 필요성
당사는 현재 약 1,200억원 자체 현금을 보유중이나 이를 본 증권신고서에 기재된 자금사용목적 재원으로 활용할 경우 보유 현금은 약 200억원으로 축소됩니다. 이 경우 통제불가능한 외부 변수, 예컨데 (1) 금융권의 차입금 만기 상환 요청(현재 당사는 26년 만기 도래하는 차입금 800억원 보유 중), (2) 건강심사평가원 등 규제기관의 규제 강화로 인한 영업현금흐름 축소, (3) 예상치 못한 연구개발비 증가 등이 발생 시 유동성 부족이 발생하여, 이에 대응하기 위한 추가 조달이 필요하게 됩니다. 또한 당사가 영위하는 의약산업 및 연구개발은 미래 불확실성이 존재하기에 운영자금 목적으로 일정 수준의 현금 보유량을 유지하는 것은 제약회사의 필수적인 경영 전략이라고 할 수 있습니다. 이에, 당사가 본 증권신고서 자금사용목적에 기재된 전략을 실행하기 위해서는 외부 조달이 수반되어야 한다고 할 수 있습니다.
③ 채무증권 및 금융권 조달의 한계
한편, 당사의 경우 업종 특성에 따른 영업현금흐름의 변동성(의약산업 고유 위험, 임상비용 증가 등)으로 인해 일반 제조업에 비해 신용등급이 낮게 평가되어 회사채 등 채무증권을 통한 자금 조달이 용이하지 않은 상황입니다. 또한 2023년 약 800억 규모 신규 차입을 실행할 당시 당사 보유 유형자산을 담보로 제공한 바 있기에 금융권 차입을 위한 추가 담보 제공 여력이 제한적인 상황입니다. 이런 상황에서 추가적인 차입 시 차입이 원할하지 않을 뿐더러, 차입이 가능하더라도 조달비용 상승으로 인해 당사의 재무부담은 가중될 것으로 예상됩니다. 이 경우 당사가 생산능력 확장을 통해 추가로 확보된 영업현금흐름을 재원으로 R&D 등 성장성 높은 분야에 투자하고자 하는 성장전략은 추진력을 잃게 될 우려가 존재합니다.
④ 유상증자의 필요성
결론적으로 당사는 유상증자를 통해 자금을 조달하는 것이 가장 적절한 방향으로 판단하게 되었습니다. 당사가 금번 유상증자를 통해 모집할 자금의 1순위 사용처는 시설자금이며 주로 생산능력 확대 및 제조설비 신규 취득에 사용될 예정입니다. 당사가 시설자금으로 사용할 것으로 예상되는 규모는 약 845억원 수준입니다.
본 증자를 진행하게된 배경과 관련하여 보다 자세한 자금사용목적 내역은 아래 기재된 내용을 참고하여 주시기 바랍니다.
(1) 시설자금 상세 내역
[1순위: 제조시설 확장 및 생산능력 증대]
현재 당사의 내용고형제 생산시설은 공간적 제약으로 인해 추가 설비 도입이 어려운 상황이며, 이로 인해 생산량 증가에 한계가 있습니다. 이를 해결하기 위해, 기존 완제품 창고를 철거한 후 해당 부지에 제조동을 수평으로 증축하여, 부족한 생산 공간을 확보하고자 합니다.
이번 증축을 통해 기존 제조시설의 활용도를 극대화하고, 연간 생산능력을 현재의 10억 정에서 15억 정 이상으로 확대할 수 있을 것으로 기대됩니다. 이를 통해 증가하는 수요에 대응할 뿐만 아니라, 향후 신제품 개발 시 생산능력 부족으로 인한 기회 손실을 방지할 수 있습니다.
(생산능력 및 생산능력 산출근거)
(1) 생산능력(단위 : 백만원)
|
사업 부문 |
품 목 | 사업소 | 2025년 1분기 |
2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|---|
| 의약품 및 의약외품 | 나정 | 안산공장 | 6,461 | 21,535 | 25,905 | 31,205 |
| 당의정 | 314 | 1,253 | 1,177 | 960 | ||
| 필름코팅정 | 20,345 | 59,699 | 72,208 | 96,796 | ||
| 캡슐제 | 6,440 | 18,515 | 27,415 | 35,295 | ||
| 과립제 | 1,002 | 3,898 | 4,184 | 5,240 | ||
| 주사제 | 340 | 11,525 | 11,887 | 15,920 | ||
| 내용액제 | 376 | 1,641 | 3,451 | 2,608 | ||
| 외용액제 | 873 | 3,720 | 5,487 | 6,826 | ||
| 연고제 | 621 | 3,969 | 2,506 | 5,837 | ||
| 기타제형 | 104 | 75 | 914 | 885 | ||
| 의약외품 | 1,273 | 5,106 | 14,493 | 12,045 | ||
| 합 계 | 38,149 | 130,936 | 169,627 | 213,617 | ||
|
출처 : 당사 제시 1) 산출기준 : 출하가 * 생산량 2) 산출방법 : 평균가동시간 가정 시 생산능력 3) 평균가동시간 |
| 사업부문 | 사업소 |
1일평균 가동시간 |
월평균 가동일수 |
25년 1분기 가동일수 |
25년 분기 가동시간 |
|---|---|---|---|---|---|
|
의약품 및 의약외품 |
안산공장 | 8.0 | 19 | 58 | 464 |
사업부문 |
사업소 |
1일평균 가동시간 |
월평균 가동일수 |
24년 가동일수 |
24년 가동시간 |
|---|---|---|---|---|---|
|
의약품 및 의약외품 |
안산공장 | 8.0 | 20 | 245 | 1,960 |
| 출처 : 당사 제시 |
(2) 생산실적(단위 : 백만원)
| 사업부문 | 품 목 | 사업소 | 2025년 1분기 |
2024년 | 2023년 | 2022년 |
|---|---|---|---|---|---|---|
|
의약품 및 의약외품 |
나정 |
안산공장 |
8,012 | 26,704 | 25,646 | 30,893 |
| 당의정 | 389 | 1,554 | 1,165 | 950 | ||
| 필름코팅정 | 25,228 | 74,027 | 71,486 | 95,828 | ||
| 캡슐제 | 7,986 | 22,959 | 27,141 | 34,942 | ||
| 과립제 | 1,243 | 4,833 | 4,142 | 5,188 | ||
| 주사제 | 421 | 14,291 | 11,768 | 15,761 | ||
| 내용액제 | 466 | 2,035 | 3,416 | 2,582 | ||
| 외용액제 | 1,083 | 4,613 | 5,432 | 6,758 | ||
| 연고제 | 770 | 4,922 | 2,481 | 5,779 | ||
| 기타제형 | 129 | 93 | 905 | 876 | ||
| 의약외품 | 1,579 | 6,331 | 14,348 | 11,925 | ||
| 합 계 | 47,306 | 162,362 | 167,930 | 211,482 |
|
출처 : 당사 제시 1) 산출기준 : 출하가 * 실제 생산량 |
(3) 2025년 1분기 및 2024년 가동률(단위 : 시간)
| 사업부문 | 사업소 | 2025년 1분기 가동가능시간 |
2025년 1분기 실제가동시간 |
2025년 1분기 평균가동률 |
|---|---|---|---|---|
| 의약품 및 의약외품 | 안산공장 | 464 | 576 | 124% |
| 사업부문 | 사업소 | 2024년 가동가능시간 |
2024년 실제가동시간 |
2024년 평균가동률 |
|---|---|---|---|---|
| 의약품 및 의약외품 | 안산공장 | 1,960 | 2,426 | 124% |
|
출처 : 당사 제시 ※ 가동가능시간 : 당분기 근무일수 X 8시간 ※ 실제가동시간 : 초과근무를 포함한 분기 실제가동시간 |
이번 증축 과정에서 5층 규모의 제조동을 건설하는 것을 목표로 하고 있으며, 이에 대한 사전 검토 결과 층수 및 최고높이 제한에 대한 별다른 규제가 없는 것으로 확인되었습니다. 따라서, 계획대로 증축이 진행될 경우 기존 대비 약 50% 이상의 생산능력 증가 효과를 기대할 수 있습니다.
| [수평증축 후 조감도] |
 |
|
수평증축 후 예상 조감도 |
| 자료: 당사 제공 |
(4) 건축비 내역
1) 세부 내용 : 공사기간 약 3년(단위 : 백만원)
| 건축면적(평) | 시공비(평당) | 합계 공사비 | 설계, 감리 외 | 합계금액 |
|---|---|---|---|---|
| 2,880 | 11.5 | 33,000 | 1,000 | 34,000 |
| 구분 | 내용 | 사용예정기간 |
총 투자 예정금액 |
금번 유상증자 사용 금액 |
|---|---|---|---|---|
| 건축 | 설계 | 25년4월~26년3월 | 600 | 600 |
| 공사계약금 (30%) | 26년4월~26년6월 | 10,000 | 10,000 | |
| 공사 기성 (40%) | 26년7월~26년9월 | 2,600 | 2,600 | |
| 26년10월~26년12월 | 2,600 | 2,600 | ||
| 27년1월~27년3월 | 2,600 | 2,600 | ||
| 27년4월~27년6월 | 2,600 | 2,600 | ||
| 27년7월~27년9월 | 2,600 | 2,600 | ||
| 공사 잔금 (30%) | 27년10월~27년12월 | 10,400 | 10,400 | |
| 합계 | 34,000 | 34,000 | ||
| 자료: 당사 제공 |
2) 건축내용
| 구분 | 수평 증축 | 기존 제조동 | 합산 | 공장 합산 | 비고 |
|---|---|---|---|---|---|
| 건축면적(㎟) | 1,900 | 5,638 | 11,067 | ||
| 연면적(㎟) | 9,500 | 13,674 | 23,174 | 36,612 | |
| 건폐율(%) | - | - | - | 54% | 법률기준 70% 이하 |
| 연면적(%) | - | - | - | 171% | 법률기준 300% 이하 |
| 자료: 당사 제공 |
[2순위: 최신 생산설비 도입]
증축된 제조동에는 최신의 내용고형제 생산설비를 도입하여 생산 공정의 효율성을 극대화하고, 품질 관리 수준을 향상시킬 계획입니다. 최신 생산설비를 도입함으로써 기존 대비 생산 속도를 향상시키고, 생산 공정에서 발생할 수 있는 품질 이슈를 최소화할 수 있도록 노력할 예정입니다. 또한, 고속 생산이 가능하면서도 균일한 품질을 유지할 수 있는 정제 타정기 및 코팅 설비 등을 적용하여 생산 안정성을 확보할 예정입니다. 도입되는 최신 설비는 국제적인 의약품 제조 기준(GMP)을 준수하며, 이를 통해 제품의 품질 균일성 확보 및 생산 공정의 신뢰성을 높일 수 있습니다. 이와 같은 최신 생산설비 도입을 통해 공정 효율성을 향상시키고, 생산 원가 절감과 더불어 높은 품질의 제품을 안정적으로 공급할 수 있는 체계를 구축하고자 합니다.
[금번 유상증자 자금 중 안산공장 생산투자 현황](단위: 라인, 대, 개, 백만원)
| 시설명 | 내용 | 수량 | 사용예정월 | 총 투자 예정금액 |
금번 유상증자 사용 금액 |
|---|---|---|---|---|---|
| (1)생산설비 | 칭량설비 | 2 | 27년 11월 | 300 | 300 |
| 연합기 | 4 | 28년1월 | 800 | 800 | |
| 건조기 | 6 | 28년 1월 | 720 | 720 | |
| 혼합기 | 2 | 28년 1월 | 300 | 300 | |
| 타정기 | 4 | 28년 2월 | 2,400 | 2,400 | |
| 코팅기 | 3 | 28년 2월 | 1,350 | 1,350 | |
| 선별기 | 3 | 28년 3월 | 1,200 | 1,200 | |
| 병포장라인 | 3 | 28년3월 | 3,600 | 3,600 | |
| 소계 | 10,670 | 10,670 | |||
| (2)시험설비 | 기타(저울 외) | 1 | 27년 10월 | 330 | 330 |
| 합계 | 11,000 | 11,000 | |||
| 자료: 당사 제공 |
[3순위: 자동화 시스템 도입]
당사는 제조 공정의 효율성을 극대화하고 품질 관리를 강화하기 위해 스마트 팩토리 개념을 적용한 자동화 시스템을 도입할 계획입니다. 이를 통해 제조 공정의 자동화율을 높이고, 실시간 모니터링 시스템을 구축하여 생산성 향상과 품질 관리 강화를 동시에 실현하고자 합니다. 최신 자동화 기술을 적용하여 생산 공정을 표준화하고, 인적 개입을 최소화함으로써 공정의 일관성과 안정성을 극대화할 예정입니다. 특히, 자동 계량 및 혼합 시스템, 자동 정제 이송 및 포장 시스템을 도입하여 공정 효율성을 개선하고자 합니다. 생산 공정의 데이터를 실시간으로 수집하고 분석할 수 있는 MES(Manufacturing Execution System) 시스템을 도입하여 설비 가동률을 최적화하고, 문제 발생 시 신속한 대응이 가능한 환경을 구축할 예정입니다. 이를 통해 생산 공정에서 발생할 수 있는 오류를 사전에 방지하고, 보다 체계적인 품질 관리를 실현할 것입니다. 자동화 시스템을 도입함으로써 제조 공정의 변수를 최소화하고, 일관된 품질을 유지할 수 있는 체계를 마련할 것입니다. 이를 통해 불량률을 감소시키고, 생산성을 극대화하여 원가 절감 효과까지 기대할 수 있습니다.
[금번 유상증자 자금 중 안산공장 자동화시스템 투자 현황](단위: 백만원)
| 구분 | 대상 | 사용예정월 |
총 투자 예정 금액 |
금번 유상증자 사용예정금액 |
|---|---|---|---|---|
|
STEP.1 데이터기반 생산관리기반구축 |
공정 주요 설비 및 인자 (설비관리기능도입) |
2026년 1월 | 1,500 | 1,500 |
|
STEP.2 시스템기반 생산성 향상 |
전 제형/공정/설비 확대 전개(생산 관리 기능 도입) |
2028년 12월 | 3,000 | 3,000 |
| 합계 | 4,500 | 4,500 | ||
| 자료: 당사 제공 |
[4순위: 제조설비 신규 취득]
당사가 금번 유상증자를 통해 조달 예정인 자금 35,000백만원은 제조설비와 영업권 취득에 사용할 계획입니다. 이를 통해 당사의 부족한 생산능력을 보완하고 당사가 미래 전략품목군으로 설정한 다수의 품목을 확보하는 것이 주 목적입니다. 부가적으로,향상되는 생산능력과 확보되는 제품을 바탕으로 CDMO사업 진출, 수출 활성화 등의사업 확장을 목표로 하고 있습니다. 이를 위해 당사가 취득 대상으로 설정한 제조설비는 완제 의약품 제조시설(내용고형제)을 보유하고 국내 시장이 큰 순환기, 당뇨, 호흡기, 정신과, 소화기 영역에서 다수 품목의 제조 허가권을 보유하면서 적정한 거래 가격 범위인 제조설비(영업권 포함)입니다. 이 외에 부가적으로 CDMO 사업을 영위하고 있거나 수출사업을 보유한 매물(제조설비 및 영업권)이 있다면 당사와의 시너지 효과를 위해 우선적으로 확보하고자 합니다.
[자금사용 세부내역](단위 : 백만원)
| 구분 | 목적 | 자금사용 시기 | 사용내역 | 금액 |
|---|---|---|---|---|
| 시설자금 | 제조설비 신규 취득 | 25년4월~25년12월 | 공장 인수 및 신규 제조설비, 영업권 등 무형자산 취득 | 35,000 |
| 총 계 | 35,000 | |||
| 자료: 당사 제공 |
(2) 운영자금 상세 내역
당사는 금번 유상증자를 통하여 모집되는 납입자금 15,495백만원을 당사의 Organic R&D, 즉 부광약품 자체의 연구개발 활동에 사용할 계획이며 자금 사용목적 별로 분류하면 신규제제 개발 및 기존제제의 개선연구, 합성신약연구, 외부 개발과제의 도입, 임상개발 및 연구개발을 위한 설비투자입니다. 본 증자를 통해 조달되는 자금을 아래 우선순위에 따라 운영자금으로 사용할 계획입니다.
[R&D 연구개발자금 사용계획](단위: 백만원)
| 구분 | 2025 | 2026 | 2027 | 2028 | 합계 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | ||
| (1) 신규제제 개발 및 기존제제 개선연구 |
365 | 784 | 789 | 1,419 | 1,047 | 820 | 2,038 | 1,334 | 1,231 | 1,324 | 992 | 1,057 | 13,200 |
| (2) 합성신약연구 |
199 | 383 | 382 | 267 | 517 | 567 | 317 | 187 | 187 | 1,037 | 187 | 100 | 4,330 |
| (3) 개발과제 도입 |
1,210 | 100 | 925 | 100 | - | 320 | 450 | 645 | 590 | 230 | 80 | 70 | 4,720 |
| (4) 적응증추가 임상연구 |
5 | 10 | 65 | 463 | 462 | 463 | 462 | 450 | 450 | 450 | 450 | 463 | 4,193 |
| (5) 연구개발 설비투자 |
823 | 123 | 186 | 340 | 360 | 111 | 406 | 500 | 389 | 75 | 196 | 180 | 3,689 |
| 합계 | 2,602 | 1,400 | 2,347 | 2,589 | 2,386 | 2,281 | 3,673 | 3,116 | 2,847 | 3,116 | 1,905 | 1,870 | 30,132 |
[1순위: 신규제제 개발 및 기존제제 개선연구]
당사는 당사 제조처에 대한 시설투자와 제조설비 신규 취득을 통해 확충되는 생산역량을 활용하여 다양한 고부가가치 제품을 생산하고자 하고 이를 실현하기 위해 신제품을 확보하고자 적극적인 투자를 계획하고 있습니다. 당사는 당사 연구소의 약물전달시스템 연구역량을 활용해 환자의 복용 편의성을 증대시키거나 부작용감소 또는 약효증대를 꾀할 수 있는 제어방출제제, 서방제제, 다층정, 장용정 및 장기지속형주사제 등 시장 경쟁력이 있는 새로운 제형개발에 대한 연구를 진행중입니다. 당사는 당사에서 이미 시판중인 약물에 대해서도 생산성과 수익성 향상 및 우수한 품질관리 유지 등을 목적으로 제제 개선, 제조공정 변경, 품질개선 연구를 수행하고 있습니다. 당사는 이러한 신제품 개발 및 기존제제 개선연구 목적으로 2025년 2분기부터 3년간 총 13,200백만원을 사용할 계획입니다.
[당사 신규제제 개발 및 기존제제 개선연구 세부 사용계획]단위: 백만원)
| 구분 | 2025 | 2026 | 2027 | 2028 | 합계 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | ||
| (1) 신규제제 개발 |
178 | 631 | 683 | 756 | 747 | 820 | 1,239 | 1,103 | 1,206 | 1,094 | 740 | 1,057 | 10,254 |
| (2) 제제개선 연구 | 187 | 153 | 106 | 663 | 300 | - | 799 | 231 | 25 | 230 | 252 | - | 2,946 |
| 합계 | 365 | 784 | 789 | 1,419 | 1,047 | 820 | 2,038 | 1,334 | 1,231 | 1,324 | 992 | 1,057 | 13,200 |
| 자료: 당사 제공 (1) 장기지속형 주사제, 복용편의성 개선 서방제제 등의 개량신약 및 제네릭 개발을 위한 연구 (2) 제제개선, 제조 공정변경, 품질개선 등을 위한 제제연구 |
[2순위: 합성신약 연구]
당사는 당사 연구소 합성신약팀의 신약 약물디자인, 약물합성, 공정개선, 약효평가 및 ADME 연구역량과 국내외 병원, 대학 및 협력기관과의 협력을 통해 혁신신약을 개발 중입니다. 당사는 합성신약연구 목적으로 2025년 2분기부터 3년간 총 4,330백만원을 사용할 계획입니다.
| 구분 | 2025 | 2026 | 2027 | 2028 | 합계 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | ||
| (1) BUK-001 | 199 | 196 | 195 | 80 | 330 | 330 | 130 | - | - | 800 | - | - | 2,260 |
| (2) BUK-003 | - | 187 | 187 | 187 | 187 | 237 | 187 | 187 | 187 | 237 | 187 | 100 | 2,070 |
| 합계 | 199 | 383 | 382 | 267 | 517 | 567 | 317 | 187 | 187 | 1,037 | 187 | 100 | 4,330 |
| 자료: 당사 제공 (1) BUK-001 : USP30을 저해하여 미토파지를 활성화함으로써 뇌신경세포를 보호하는 기전의 파킨슨질환 치료제 (2) BUK-003 : 항암제 |
[3순위: 개발과제 도입]
당사는 당사가 판매할 수 있는 제품을 빠르게 확보하기 위해 당사 고유의 연구개발 활동 이외에도 외부 업체와의 공동개발, 제제기술 이전 등 협력을 통해서도 제품을 개발 중입니다. 당사는 외부의 개발과제 도입이나 공동개발 참여 등의 목적으로 2025년 2분기부터 3년간 총 4,720백만원을 사용할 계획입니다.
[당사 개발과제 도입 세부 사용계획](단위: 백만원)
| 구분 | 2025 | 2026 | 2027 | 2028 | 합계 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | ||
| (1) 개발과제 도입 |
1,210 | 100 | 925 | 100 | - | 320 | 450 | 645 | 590 | 230 | 80 | 70 | 4,720 |
| 합계 | 1,210 | 100 | 925 | 100 | - | 320 | 450 | 645 | 590 | 230 | 80 | 70 | 4,720 |
| 자료: 당사 제공 (1) 대상제품 : 파킨슨병 제제, 소화기제제, 고지혈증 개량신약, 고지혈증 복합제 등 |
[4순위: 적응증 추가 임상연구]
당사는 당사가 기존에 발매한 제품의 매출과 Life Cycle을 연장하기 위해 적응증 추가를 위한 임상연구계획을 수립하였습니다. 본 임상연구 추진시 약 5년간 80억원 이상의 자금이 소요될 것으로 예상되며 당사는 유상증자를 통해 확보되는 납입자금에서 총 4,193백만원을 2025년 2분기부터 3년간 본 적응증 추가 임상연구를 위해 사용할 계획입니다.
[당사 임상개발과제 세부 사용계획](단위: 백만원)
| 구분 | 2025 | 2026 | 2027 | 2028 | 합계 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | ||
| ① 적응증 추가를 위한 임상연구 | 5 | 10 | 65 | 463 | 462 | 463 | 462 | 450 | 450 | 450 | 450 | 463 | 4,193 |
| 합계 | 5 | 10 | 65 | 463 | 462 | 463 | 462 | 450 | 450 | 450 | 450 | 463 | 4,193 |
| 자료: 당사 제공 (1) 대상제품 : CNS영역 질환 치료제 |
[5순위: 연구개발 설비투자]
당사는 당사 자체 연구개발 기능 강화를 위해 연구개발에 필요한 설비와 인력 확충에 적극적으로 투자하고 있습니다. 당사가 목적으로 하는 신규제제 개발, 합성신약연구 등을 적시에 수행하기 위해서는 당사 연구소의 설비에 대해서 지속적인 확충과 보완 및 유지보수가 필요합니다. 당사는 2025년 2분기부터 3년간 총 3,689백만원을 제제연구설비, 분석연구설비 및 합성신약연구설비를 확충하거나 보완 및 유지보수하는 목적으로 사용하고자 합니다.
[당사 제제, 분석 및 합성신약연구 장비구입 세부 사용계획](단위: 백만원)
| 구분 | 2025 | 2026 | 2027 | 2028 | 합계 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | ||
| ① 제제/분석연구 설비 | 123 | 123 | 106 | 300 | 360 | 75 | 406 | 200 | 353 | 75 | 196 | 180 | 2,497 |
| ② 합성신약연구 설비 | 700 | 80 | 40 | 36 | 300 | 36 | 1,192 | ||||||
| 합계 | 823 | 123 | 186 | 340 | 360 | 111 | 406 | 500 | 389 | 75 | 196 | 180 | 3,689 |
| 자료: 당사 제공 (1) 제제/분석연구 설비 : 유동층과립기, 3층정타정기, 롤러컴팩터, 캡슐충전기, LC-MS/MS (불순물 분석용), HPLC, 용출기, UPLC 등 (2) 합성신약연구 설비 : LC-MS/MS (혈중흡수/ADME 측정용), MPLC 등 |
[6순위: 기타 운영자금]
[필수운영자금 사용 계획](단위 : 백만원)
| 구분 | 2025 | 2026 | 2027 | 2028 | 합계 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | 2분기 | 3분기 | 4분기 | 1분기 | ||
| ① 인건비 | 1,002 | 1,002 | 1,052 | 1,158 | 1,158 | 1,181 | 1,181 | 1,250 | 1,250 | 1,250 | 1,250 | 1,250 | 13,984 |
| ②PV/PMS/RMP 비용 | 40 | 41 | 33 | 93 | 62 | 23 | 31 | 107 | 43 | 43 | 34 | 108 | 658 |
| 관리비 및 기타 운영자금 | 114 | 123 | 93 | 70 | 53 | 98 | 62 | 72 | 53 | 103 | 68 | 77 | 984 |
| 합계 | 1,157 | 1,165 | 1,178 | 1,321 | 1,273 | 1,302 | 1,274 | 1,429 | 1,346 | 1,396 | 1,352 | 1,435 | 15,625 |
| 자료: 당사 제공 (1) 당사보유 총 54명의 전문 연구개발 인력을 2028년 초 68명까지 점진적으로 증가계획 (2) 관련 법령과 규정에 따라 의약품은 발매 이후에도 지속적으로 안전성과 유효성에대한 관리가 필요. 현재 판매중인 약물과 앞으로 발매될 수종의 제품에 대해서 PV (Pharmacovigilance, 약물감시), PMS (Post-marketing Surveillance, 시판후조사), RMP (Risk Management Plan, 위해성관리계획) 활동 수행 예정 |
(3) 타법인증권 취득자금 상세내역
금번 유상증자를 통해 유입되는 자금을 시설자금 및 운영자금에 우선 집행 한 이후에도 잔여 조달액이 발생하고, 당사 자회사인 Conetra Pharma의 임상결과와 자금조달계획이 예상치 못한 변수로 인해 변경되어 당사의 자금지원이 불가피하게 필요하게 될 경우, 당사의 Contera Pharma 임상지원 목적으로 출자를 단행할 수 있습니다. Contera Pharma는 덴마크 코펜하겐에 위치한 신경질환 치료제 개발사로 파킨슨병 환자의 아침무동증을 적응증으로 하는 CP-012에 대해 영국에서 임상 1b상을 진행 중에 있습니다. Contera Pharma는 2021년부터 자체 RNA 치료제 플랫폼 구축을 시작하였으며, 희귀 신경질환을 적응증으로 내부에서 5건 이상의 신규 후보물질을, 영국 Vernalis 社와의 협력을 통해 1건의 후보물질을 개발하였습니다. 이 중 1건은 IND enabling study 단계에 도달했으며, 개발에 상당한 비용이 필요할 것으로 예상됩니다. Contera Pharma는 RNA 치료제들의 임상시험 진입을 목표로 개발하고 있습니다.
[타법인증권 취득자금-Contera Pharma 출자자금 사용계획](단위 : 백만원)
| 구분 | 2025 | 2026 | 2027 | 2028 | 합계 | ||||||||
| 2분기 |
3분기 |
4분기 |
1분기 |
2분기 |
3분기 |
4분기 |
1분기 |
2분기 |
3분기 |
4분기 |
1분기 |
||
| (1) CP-012 연구개발비 |
525 | 750 | 750 | 5,625 | 5,625 | 5,625 | 5,625 | 5,625 | 5,625 | 5,625 | 5,625 | - | 47,025 |
| (2) CP-102 연구개발비 | 420 | 315 | 1,001 | 1,001 | 1,001 | 1,001 | 1,001 | 1,001 | 2,670 | 2,670 | 2,670 | 2,670 | 17,418 |
| (3) 인건비, 관리비용 등 |
1,950 | 1,500 | 1,500 | 2,370 | 2,370 | 2,370 | 2,370 | 2,370 | 2,370 | 2,370 | 2,370 | 2,370 | 26,280 |
| 합계 | 2,895 | 2,565 | 3,251 | 8,996 | 8,996 | 8,996 | 8,996 | 8,996 | 10,66 | 10,66 | 10,66 | 5,040 | 90,723 |
| 자료: 당사 제공 |
① CP-012 (아침 무동증 치료제)
CP-012는 파킨슨병 환자들의 야간 운동불능과 이른 아침 OFF (약효소실) 증상을 해결하기 위해 특별히 설계된 레보도파와 카르비도파의 독점적 지연방출 제형입니다. 이 제형은 약물이 지연 방출(4-6시간)되며, 맥박성 방출 프로파일을 통해 약효가 점진적으로 발현되도록 설계되었습니다. 이러한 특징은 파킨슨병 환자들이 경험하는 특정 시간대의 증상을 효과적으로 완화할 수 있는 가능성을 가지고 있습니다.Contera Pharma는 개발 초기 단계인 2015년에는 EUROSTAR 보조금 하에 미니정 제형을 개발하였고, 2017년에는 해당 제형의 프로토타입을 완성하고 특허 1건을 출원했습니다. 이후 2022년부터 BDD와 협력하여 CP-012를 개발하였으며, 2023년에는 건강한 자원자를 대상으로 BDD 제형을 이용한 1상 시험을 시작했습니다. 2024년에는 임상 1a 시험을 완료하고, 현재 임상 1b상이 진행중이며 2025년 2분기 결과 확인을 목표로 하고 있습니다. 임상 1b상이 성공적으로 완료되면 임상 2/3상으로의 진행을 계획하고 있습니다. 당사는 2025년 2분기부터 3년간 47,025 백만원의 개발 비용을 사용할 계획입니다.
② CP-102 (카나반병 치료제)
CP-102는 희귀 신경계질환인 카나반병 치료를 위해 설계된 새로운 ASO (Anti-Sense Oligonucleotide) 제제입니다. 이 프로젝트는 Contera의 파이프라인 확장의 일환으로 2021년에 시작되었습니다. Contera Pharma는 2021년 3분기부터 CP-102의 개발을 진행했습니다. 개발 과정에서 2023년 3분기에는 비인간 영장류(NHP)를 대상으로 한 기전 증명(Proof of Mechanism, POM)이 성공적으로 이루어졌습니다. 2024년에는 NHP를 대상으로 한 용량 범위 탐색(Drug Range Finding, DRF) 실험을 시작하여 2025년 비임상 후보물질을 도출하였습니다. CP-102의 주요 장점으로는 ASO가 카나반병과 같은 단일 유전자 질환을 치료하는 데 효과적인 치료법으로 입증되었다는 점, 임상 개선과의 상관관계는 추가적인 검증이 필요하지만 좋은 바이오마커인 뇌척수액(CSF) 내 NAA(N-acetylaspartate) 수치가 존재한다는 점, 그리고 CP-102는 연 3~4회 정도의 주사로 치료가 가능하여 환자에게 부담을 덜 수 있는 장점이 있습니다.
타법인증권 취득에 사용될 자금은 3순위로 우선순위가 낮으며 1순위 및 2순위로 조달할 규모가 본 증자규모를 초과함에 따라 당사가 금번 자금조달을 타법인증권 취득으로 활용할 가능성은 낮을 것으로 판단됩니다. 다만, 예상치 못한 1순위, 2순위 자금사용처 변동으로 인해 타법인증권 취득으로 자금이 사용되게 될 경우 이는 자회사의 CP-012 임상목적 연구개발비로 집행될 예정입니다. 이 경우 당사가 진행한 연구개발 전략이 계획대로 진행되지 않고 신약 개발에 실패하거나 지연될 불확실성이 존재합니다. 유사한 사례로 당사가 과거 임상 진행한 파이프라인 중 JM-010은 2024년 5월 위약군 대비 통계적으로 유의미한 효과가 나오지 않은 것으로 나타나 임상이 종료된 바 있습니다.
다. 자금 집행의 부족한 자금의 재원마련
당사의 금번 신주발행은 주주배정 후 실권주 일반공모 방식으로 진행됨에 따라, 대표주관회사인 NH투자증권(주)는 일반공모 후 발생하는 실권주에 대해 전량 인수하게 됩니다. 그러나, 공모기간 중 당사의 경영실적의 저하 또는 주식시장의 급격한 변동 등에 따라 확정발행가가 예정발행가를 하회할 경우에 모집금액이 예정 모집금액에 미달 될 수 있습니다. 또한 시설자금중 제조시설 확장이나 설비 도입의 경우 현 시점에서 규모가 어느정도 확정되었으나 제조설비 신규 취득이나 당사가 기재한 R&D 관련 운영자금은 향후 당사가 진행하는 임상 결과에 따라 변동될 가능성이 존재합니다. 이에 본 증자를 통해 조달하는 금액(약 천억원)을 상회하는 자금사용목적(이천억원 이상)을 기재하였으며 본 증자를 통해 조달하는 자금을 우선순위에 따라 사용하고 부족분 약 천백억원에 대해서는 다른 자금조달, 예컨대 한도대 400억원 및 보유현금 100~300억원, 최대주주 대상 3자배정 400~600억원 등의 방안을 통해 조달할 계획입니다.
라. 유상증자 배경
[시설자금_제조시설확장, 최신생산설비 도입, 자동화시스템 구축 ]
당사는 제약 산업 내 경쟁력 강화를 위해 지속적인 투자와 혁신을 추진하고 있으며, 이에 따라 제조시설 확충과 생산능력 확대를 위한 전략적 결정을 내렸습니다. 제약산업에서 생산능력은 회사의 최대 매출의 결정지을 수 있는 지표의 하나로 대대적인 성장을 목표로 하고 있는 당사에게 생산능력 확충은 가장 중요한 투자입니다. 특히, 국내 의약품 시장의 변화에 대응 뿐만이 아니라 글로벌 진출을 위한 기준에 부합하고, 최근 지속적으로 발생한 주요 제품의 품절 문제를 근본으로 해결하며, 안정적인 공급 체계를 구축하기 위해 내용고형제 생산설비 확충이 필수적으로 요구되는 상황입니다.
최근 씬지로이드정,액시마정, 파자임정 등 다빈도 의약품의 장기 품절 현상이 지속됨에 따라, 의료기관 및 약국에서 원활한 의약품 공급에 어려움이 발생하고 있으며, 이러한 공급 불안정은 결국 고객의 신뢰를 무너뜨림으로서 회사의 매출에도 부정적인 영향을 미치고 있습니다. 품절로 인해 병/의원 의사들이 당사 의약품을 다른 약품으로 대체를 하게 되고, 신제품을 발매하더라도 품절 우려로 인해 처방을 주저하게 되는 상황이 발생하고 있습니다.
이에 당사는 제조 인프라를 강화하여 생산 차질을 해소하고, 유통 안정성을 높이는 방안을 최우선 과제로 추진하고 있습니다. 제조시설 확장과 생산능력 증대를 통한 근본적 해결 방안을 모색하고 있으며, 관련 시장 뉴스 및 이제영 대표의 인터뷰 내용에서도 밝힌 바와 같이 생산 생산능력 확충 및 공급망 안정화 전략을 체계적으로 추진할 계획입니다.
최근 의약품 공급 불안정에 대한 주요 언론 보도를 살펴보면, 국내 주요 품목들의 지속적인 품절 문제가 제기되고 있으며, 이에 대한 해결책으로 제약사의 생산능력 확장 및 공급망 정비 필요성이 강조되고 있습니다. 이제영 대표 역시 최근 인터뷰에서 생산망 정비 및 생산능력 확장을 핵심 과제로 설정하고 있으며, 제조 인프라 강화와 R&D 전략 재편을 통해 지속 가능한 성장을 도모하고 있음을 밝혔습니다.
현재 당사의 제조시설은 연간 10억 정의 내용고형제 생산이 가능하지만, 증가하는 시장 수요에 따라 이를 초과하는 생산 능력이 요구되고 있습니다. 현 시점에서도 영업 부문에서는 연간 12억 정 이상의 생산량을 필요로 하고 있으나, 기존 제조시설 내 공간 부족과 설비 한계로 인해 이를 충족하기 어려운 실정입니다. 단기 방편으로 생산 외주를 주고 있지만 이 또한 의약품 특성상 허가와 병행하게 되며 품질관리 문제도 있어 쉽게 진행하기 어려운 부분이 있습니다.
중장기적으로 매출기준 2천억원 이하 30~40위의 제약사에서 20위권 이내의 제약사로 발돋움하기 위하여, 지속적인 기존 제품매출 증가와 함께 신제품 발매 및 신규사업 진출을 계획하고 있는 당사에 있어서 생산시설의 확충 및 자동화, 선진화는 반드시 선행되어야 하는 부분입니다.
기존 제품들에 있어서도 단순한 판매량의 증가가 아니라 의료기술의 발달로 인해 의약품의 용량을 다양하게 처방하기를 원하고 있어 고객의 니즈를 충족하기 위하여 기존 제품의 용량 다양화도 추진해야 합니다. 지속가능한 회사의 성장을 위해 향후 발매되는 제품들 특히, 장기처방이 많아 생산능력이 뒷받침되어야 하는 만성질환 분야의 다양한 신제품을 고려할 때 이러한 생산설비 한계로 인한 공급불안정은 반드시 해결되어야 합니다. 또한 고려하고 있는 해외 진출을 비롯한 다양한 사업 영역의 확장에서 직면하게 되는 각종 규제상황에 대응하기 위해서는 최신화된 생산설비와 시스템이 필요합니다.
이에 따라 당사는 기존 제조공장 부지 내에 제조동을 수평 증축하여 생산설비 공간을 확보하고, 최신 생산설비와 자동화 시스템을 도입함으로써 장기 품절 문제를 해소하여 안정적이고 유연한 공급망을 구축하는 데 주력할 계획입니다.
이는 단순히 공급망의 안정화뿐만 아니라, 장기적인 매출 성장과 기업의 지속 가능성을 확보하는 중요한 전략적 투자이며, 이를 통해 시장에서의 신뢰를 회복하고, 원활한 의약품 공급을 통한 공공 보건 기여 및 지속가능한 성장 기반을 마련하겠습니다.
본 증축을 통해 당사의 생산능력는 약 50% 이상 증가할 것으로 전망됩니다. 당사는 증가된 생산능력을 현재 계획중인 신제품 생산에 활용할 예정이며 해당 제품군의 수익성(원가율)은 기존 제품 대비 우월한 점, 또한 매출액 증가에도 불구 기존 고정비는 유의적인 증가가 수반되지 않은 소위 "고정비 레버리지효과" 등이 복합적으로 작용하여 당사 매출총이익 및 영업이익 개선에 기여할 것으로 전망됩니다. 궁극적으로 본 생산능력 증축을 통해 약 480억원 매출증가, 175억원 영업이익 증가 및 225억원 EBITDA 증가 효과가 기대되고 있습니다(영업이익율 8.7%에서 14.11%로 개선).
[시설자금_제조설비 신규 취득]
당사가 본 증자를 통해 조달하는 천억원 중 약 350억원을 외부 제조설비를 신규로 취득하는데 사용할 예정입니다. 이를 통해, 당사는 빠르게 생산능력을 확충하여 고질적인 품절문제를 조기에 안정화할 수 있을 것이며, 기존 안산공장의 시설확장을 통한 추가된 생산능력까지 더하여, 고수익의 신약품목 상업화 뿐만 아니라 이를 연계한 완제의약품 CDMO 사업까지 진출함으로써, 유기적 성장을 지속적으로 추진하고자 합니다.
동 외부 제조설비 신규 취득을 통해 당사가 달성하고자 하는 바는 구체적으로 다음과 같습니다.
(1) 생산역량 조기확보: 당사는 기존 안산 공장의 제조시설 확충을 위한 계획을 진행할 예정이지만, 공사기간은 3년이상 소요되고, 설비가 도입되고 인증을 받을 때까지 또한 추가 기간이 소요됩니다. 당사는 이러한 시간적 제약사항을 외부 제조설비 인수를 통하여 빠르게 해소할 계획입니다.
(2) 고수익 신약품목 상업화 및 CDMO 신규사업 진출: 당사는 추가로 확보되는 생산능력을 바탕으로 과거에는 영위하지 못했던 완제의약품 위탁 개발 생산(CDMO) 사업에 진출할 계획입니다. 당사의 신제품 연구개발 기능을 바탕으로 고수익의 경쟁력 있는 신제품 개발을 추진하고 해당 제품을 인수 제조설비에서 생산하여 [1+3 허가 제도]를 활용한 당사 직접판매 및 3개사 추가 허가권 확보 및 판매를 계획하고 있습니다.
(3) 부가적 영업판매 시너지효과: 당사는 영업권 등 무형자산 인수를 통해 다수의 기승인된 품목 허가권을 단기에 확보하고 빠르게 당사의 전략품목군(순환기, 당뇨, 호흡기, 정신과, 소화기)에 해당하는 포트폴리오를 확보하여 당사가 매출성장 목표를 조기 달성 가능하도록 할 계획입니다. 이를 통하여 시장 수요에 부합하는 품목의 적시 판매 및 공급으로 당사의 추가 수익을 달성 가능한 환경을 구축하고자 합니다. 또한, 취득하는 제조설비에 수출이 가능한 허가와 영업권이 포함되어 있을 경우 이를 적극적으로 활용하여 수출 사업 확대를 계획할 예정입니다.
현재 당사는 해당 설비 취득 관련하여 제한적인 실사를 완료하였으며 취득 의지를 매수자에게 전달한 상황입니다. 이후 상세실사, MOU 체결 등이 예정되어 있으며 향후 진행상황에 대해서는 언론보도, 전자공시, IR을 통해 투자자분들과 적극 소통할 계획입니다. 당사는 제조설비 신규 취득을 통해 당사는 제품군 다변화, 영업 활성화, 신사업 추가에 따른 매출원 다각화 등의 긍정적인 효과가 작용하여 40~100억 수준의 추가 EBITDA가 창출될 것으로 기대하고 있습니다. 다만, 35,000백만원 전후의 투자계획은 현 시점에서 예상되는 계획이며, 향후 집행 시점의 경영환경 등을 고려하여 변경될 가능성이 있으므로 절대적인 계획이 아님을 투자자께서는 인지하시기 바랍니다. 만약 동 시설자금 취득 관련하여 자금사용목적계획에 변경이 발생하거나 취소될 경우 해당 조달액을 차순위 사용목적인 운영자금으로 사용할 예정입니다.
[운영자금, 타법인취득자금]
당사는 자체 R&D 역량 강화와 더불어 오픈이노베이션 전략을 통해 신약개발에 박차를 가하고 있습니다. 당사는 기존 제품군에서 우월한 시장 인지도를 보이고 있으나 향후 수익원 다각화 및 기업가치 증대를 위해서는 연구개발을 통한 파이프라인 강화가 필수적인 상황입니다. 이에, 본 증자를 통해 조달하는 자금 일부를 운영자금(R&D)으로 활용함으로써 현재 계획중인 연구개발활동을 지원하고, 궁극적으로 당사의 기업가치를 증대시킬 계획입니다.
다만, 본 증자를 통해 조달한 자금은 원칙적으로 생산능력 증대 및 당사 매출액&수익성 개선에 직접적인 효과가 있는 시설자금에 우선 사용하며 잔여 조달액을 활용하여 R&D 및 타법인출자 목적으로 사용할 예정입니다. 부족분에 대해서는 다른 조달방안(최대주주 대상 3자배정증자, 추가 차입, 한도대 등)을 통해 확보할 계획입니다.
마. 주주 권익 보호를 위한 사항
당사는 금번 유상증자와 관련하여 주주와의 소통을 강화하고, 기관주주 및 외국인주주, 소액주주 대상으로본 유상증자 결의일 익영업일인 3월 31일 오후 4시와 4월 22일 오후 2시 30분, 2차례에 걸쳐 IR을 진행한 바 있습니다. 해당 IR을 통해 당사의 대표이사는 본 유상증자의 배경, 목적, 기대효과와 당사의 중장기 사업전략 및 경영 목표 등을 상세히 설명하였습니다. 또한 증권사 애널리스트 대상으로도 적극적으로 소통하고 있으며, 시장 내에 충분한 정보가 전달될 수 있도록 노력하고 있습니다.
| [유상증자 주요일정 및 주주보호를 위한 당사의 권익활동 요약] |
 |
|
주요일정 및 주주보호를 위한 권익활동 |
| (자료 : 당사 IR자료) |
이와 함께, 소액주주의 정보 접근성을 높이고 소통을 활성화하여 주주 권익을 보호하고자 합니다. 먼저 유상증자 주요 내용에 대해 주주들이 쉽게 이해할 수 있도록 관련 내용을 PT 형태로 정리하여 당사 홈페이지에 게시하였으며 추가로 증권신고서 제출 이후 회사 홈페이지 내 유상증자의 취지를 담은 대표이사의 서한 및 FAQ 게시 등 관련 정보를 상시 제공하고 있습니다. 더불어 당사는 내부적으로 소액주주 전담 상담인력 2명을 구비하여 소액주주분들의 문의사항에 적극 대응 중이며 향후에도 유상증자와 관련한 문의사항, 참여 절차에 대한 안내 등 소액주주가 권리를 행사하는데 불편함이 없도록 도울 예정입니다. 현재까지 당사에게 접수된 소액주주분들의 문의사항은 본 정정증권신고서 제출일 기준 40건이며 주로 공모일정 및 예정발행가액, 주가변동, OCI홀딩스 및 대주주들의 참여여부, 자금사용목적, 연구개발(R&D) 관련 투자처, 할인율 및 증자비율 선정 배경 등에 대한 내용으로 당사의 "신주배정기준일은 6월 2일이며, 7월 8~9일이 구주주 청약날짜이고, 예정발행가액은 3,310원이지만 확정가액은 7월 3일날 결정됩니다. 대주주들의 참여에 대해서는 저희가 결정하는 문제가 아닌 만큼 확답을 드릴수는 없습니다. OCI홀딩스에서도 이사회 승인을 받아야 하는 사항으로 아직 확정된 것은 없으나 최대 주주의 의무를 다할 것으로 믿고 있습니다."라고 답변드리고 홈페이지에도 질의 응답 게시 및 업데이트를 통하여 적극적으로 안내드리고 있습니다. 아울러 당사가 소액주주분들과 대응하는 과정에서 미진한 부분이 확인될 시 즉각 내부적인 회의를 통해 대응 전략을 구비하여 소액주주분들에게 적절한 안내사항이 전달될 수 있도록 노력하고 있습니다. 앞으로도 소액주주께서 권리를 행사하시는 구주주청약일 전까지 내부 전담 인력을 지속 구비할 예정이며 주주분들의 질의사항에 적절히 대응할 수 있도록 노력할 예정입니다.
당사에 접수된 소액주주의 주요 문의사항 및 당사의 대응은 아래와 같으며, 자세한 사항 및 추가적인 개별 문의는 함께 기재된 당사 IR 이메일 혹은 연락처로 연락주시기 바랍니다.
| 주요 문의 내용 | 당사 답변 |
| 1. 1,200억원 가량 현금을 보유중임에도 불구 유상증자를 통해 자금을 조달하는 사유 | 당사는 현재 약 1,200억원 자체 현금을 보유중이나 이를 본 증권신고서에 기재된 자금사용목적 재원으로 활용할 경우 보유 현금은 약 200억원으로 축소됩니다. 이 경우 통제불가능한 외부 변수, 예컨데 (1) 금융권의 차입금 만기 상환 요청(현재 당사는 26년 만기 도래하는 차입금 800억원 보유 중), (2) 건강심사평가원 등 규제기관의 규제 강화로 인한 영업현금흐름 축소, (3) 예상치 못한 연구개발비 증가 등이 발생 시 유동성 부족이 발생하여, 이에 대응하기 위한 추가 조달이 필요하게 됩니다. 또한 당사가 영위하는 의약산업 및 연구개발은 미래 불확실성이 존재하기에 운영자금 목적으로 일정 수준의 현금 보유량을 유지하는 것은 제약회사의 필수적인 경영 전략이라고 할 수 있습니다. 이에, 당사가 본 증권신고서 자금사용목적에 기재된 전략을 실행하기 위해서는 외부 조달이 수반되어야 한다고 할 수 있습니다. |
| 2. 자금사용목적에 기재된 목적 달성시 예상 효과 | 자금사용목적상 기재된 증축을 통해 당사의 생산능력는 약 50% 이상 증가할 것으로 전망됩니다. 당사는 증가된 생산능력을 현재 계획중인 신제품 생산에 활용할 예정이며 해당 제품군의 수익성(원가율)은 기존 제품 대비 우월한 점, 또한 매출액 증가에도 불구 기존 고정비는 유의적인 증가가 수반되지 않은 소위 "고정비 레버리지효과" 등이 복합적으로 작용하여 당사 매출총이익 및 영업이익 개선에 기여할 것으로 전망됩니다. 궁극적으로 본 생산능력 증축을 통해 약 480억원 매출증가, 175억원 영업이익 증가 및 225억원 EBITDA 증가 효과가 기대되고 있습니다(영업이익율 8.7%에서 14.11%로 개선). |
| 3. OCI홀딩스 및 대주주의 참여 여부 |
해당 사항은 OCI홀딩스의 결정 권한에 속하며, OCI홀딩스 또한 이사회 승인을 거쳐야 하는 사안입니다. 당사는 최대주주로서 OCI홀딩스가 책임을 다할 것이라 믿고 있으며, OCI홀딩스 역시 최대주주의 책임 있는 자세로 최선의 방안을 모색할 것으로 판단하고 있습니다. 다른 대주주들의 참여 여부는 아직 확정되지 않았습니다. 만약 대주주들이 참여하지 않게 될 경우, 최대주주로서 OCI홀딩스가 책임을 다하는 차원에서 적절한 대응 방안을 마련할 것으로 판단하고 있습니다. |
| 4. CAPA 증설은 오랜 기간 논의되어온 이슈인데 지금에서야 의사결정이 진행된 사유 | 당사의 공급 문제는 최근에 당면한 이슈가 아닌 최근 3개년간 지속적으로 논의되어온 이슈 입니다. 이러한 생산설비 확충의 필요성은 이미 수년 전부터 인식하고 있었으나, 2022년과 2023년 연속된 적자와 운영자금 부족, 그리고 800억 원 규모의 차입 등 재무적 제약으로 인해 당장의 운영효율성 개선에 집중이 필요하여 즉각적인 설비 투자나 유상증자 추진은 어려운 상황이었습니다. 특히 2023년에는 영업적자 발생으로 인해 영업현금흐름이 마이너스로 전환되었고 약 800억 원 규모의 신규 차입이 이루어지면서 재무활동현금흐름으로 763억 원이 유입되었지만 2024년 자회사 Contera Pharma 투자자의 풋옵션 행사로 인해 677억 원이 유출되었습니다. 또한 2023~2024년에는 당사가 진행한 JM-010 임상으로 인해 임상개발에 따른 현금 유출이 증가하여 생산설비 확장을 위한 자금 확보가 여의치 않게 되었습니다. 다만 25년 하반기부터 지속적인 신제품 출시가 예정되어 있어 생산설비 부족에 따른 성장 여력 한계가 더욱 시급한 이슈로 부각됨에 따라 더 이상 생산설비 확충 이슈를 미룰 수 없다고 판단하였고 이와 맞물려 2024년 흑자 전환을 계기로 경영이 안정화됨에 따라, 생산 역량 강화와 기업가치 제고를 위하여 유상증자를 결정하였습니다. |
| 5. 유상증자 금액 중 연구개발(R&D) 관련 구체적인 투자처 | 신규 제제 개발 및 기존 제제 개선에 132억 원, 합성 신약 연구에 43억 원, 공동 개발 및 제제 기술 이전 등 개발 과제 도입에 47억 원을 투입할 계획입니다. 또한 라투다 등 기존 제품의 적응증 추가를 위한 임상 연구에는 42억 원, 연구개발 관련 설비 투자에는 약 37억 원이 사용될 예정입니다. 마지막으로 인건비를 포함한 필수 운영 자금 등 기타 운영비로는 156억 원이 투입될 계획입니다. |
| 6. 3월 26일 주주총회 당시 증자계획을 주주들에게 설명하지 않은 경위 | 유상증자 계획은 자본시장법 제174조에 따라 공시 전까지는 미공개 중요정보에 해당하며, 확정되지 않은 계획을 준비 단계에서 언급하는 것은 시장에 혼선을 초래할 우려가 있어 외부 공개하거나 언급하는 것이 불가능합니다. 아울러 금번 주주총회에서는 사외이사 한 분이 퇴임하시고, 새로운 사외이사 및 사내이사 각 한 분이 새로 선임되는 큰 변화가 있었습니다. 유상증자는 이사회 결의를 통해 진행되어야 하므로, 새로운 이사진의 구성 이전에 결의하는 것은 향후 절차상 부담이 될 수 있었습니다. 이에 따라 신임 이사진 선임 후 이사회 결의를 거쳐 유상증자 계획을 확정하게 되었습니다. 아직 확정되지 않은 사안에 대해 주주총회에서 유상증자 관련 답변을 드리지 못한 점, 미공개 중요정보에 해당하는 점을 고려한 불가피한 조치였음을 양해해 주시기 바랍니다. |
| 7. 유상증자가 무산될 가능성 | 주관 증권사와 전액 총액 인수 계약이 되어 있습니다. 만약 기존 주주분들의 참여가 저조하여 실권주가 발생하면, 실권주는 일반 공모 절차로 넘어가서 비주주인 일반 투자자들을 대상으로 공모가 진행됩니다. 일반 공모도 경쟁률이 미달이 되는 경우에는 주관 증권사가 총액 인수 계약에 따라 잔여 물량 전부를 인수하게 됩니다. 따라서 이번 유상증자가 무산될 가능성은 매우 낮다고 볼 수 있습니다. |
| 8. 증자 금액을 1,000억 원으로 결정하고 할인율은 20%, 증자 비율은 44%로 지정한 사유 | 증권신고서에도 기재하였듯, 당사가 필요로 하는 자금 규모는 1,000억 원을 초과합니다. 이 중 1,000억 원을 주주 배정 유상증자를 통해서 모집하고 자금사용 목적에 대해서는 증권신고서에 상세히 적어 기재하였습니다. 할인율 20%와 증자 비율 44%는 유상증자의 다른 사례와 비교해 볼 때 통상적 평균적인 숫자입니다. 할인율 20% 정도는 주주 배정 유상증자에 있어서는 평균치 정도라고 판단합니다. 최근에 2~3년간 있었던 주주 배정 유상증자 증자 비율이 평균이 약 39% 정도입니다. 부광약품의 증자비율 44% 중에 우리 사주 조합에 할당된 걸 제외하면 일반 주주 참여를 가정한 증자 비율은 약 35%입니다. 우리사주조합의 참여 여부는 아직 결정되지 않았으며, 44%라는 비율 역시 다른 유상증자 사례들과 비교해 볼 때 과도하다고 보기 어렵습니다. |
| 9. 어느 생산 설비를 매수할지 결정되었는지 여부 | 현재 2~3개 처의 제약 공장을 검토하고 있고 예비 실사도 거치고 있습니다. 다만, 아직 구체적인 대상이 확정된 것은 아니며, 모두 후보 단계에 있는 상황이기 때문에 현시점에서 특정 대상을 공개하기는 어렵습니다. 현재로서는 CMO 사업을 주력으로 영위하는 공장들을 중심으로 검토 중임을 말씀드릴 수 있습니다. |
| 10. CDMO 사업에 진출하려는 상황에서후발 주자로서 어떤 전략을 마련하고 있는지 여부 | 당사가 추진 중인 CDMO 사업은 바이오 의약품 분야가 아니라 당사가 기존에 강점을 보유하고 있는 합성의약품 및 합성화학 기반 의약품 영역에 집중되어 있습니다.부광약품의 R&D 연구개발 역량과 CMO 사업을 안정적으로 수행하고 있는 공장의 역량을 결합한다면 CDMO 사업의 본격적인 지출이 충분히 가능하다는 판단을 내렸습니다. |
| 11. 증자 전 소액주주 상대 증자 필요성 및 경위에 대해 자세한 설명이 필요하다고 보는데 당사의 입장은? | 유상증자 계획은 공개 전까지는 자본시장법상 미공개 중요정보에 해당하고, 불확정적 계획을 공개 또는 공시하는 것은 시장에 혼란을 초래할 수 있으므로, 확정 전에 이를 외부에 공개하거나 언급하는 것은 불가합니다. 유상증자와 관련하여 이사회 결의와 동시에 주요사항보고서를 공시하였으며, 당사 홈페이지에 대표이사의 유상증자 취지를 담은 서한을 게시하고, 보다 구체적인 내용을 프레젠테이션 자료로 게시하여 제공하였습니다. 또한, 다음 영업일인 3월 31일에는 대표이사가 직접 기관 및 개인 투자자를 포함한 모든 이해관계자를 대상으로 유상증자에 대해 설명하는 자리를 마련하였고, 주주 및 언론 등으로부터 접수된 질의를 정리하여 이에 대한 답변을 FAQ 형태로 홈페이지에 게시하였습니다. 해당 설명회는 웹세미나 방식으로 진행되어 누구나 쉽게 접근할 수 있도록 하였으며, 실시간 질의응답 기회도 충분히 제공하였습니다. 또한, 개인 주주분들의 문의에 신속하고 정확하게 응대하기 위해 전담 인력 2명으로 구성된 콜센터를 운영하고 있습니다. 당사는 본 유상증자에 대해 주주 여러분이 충분한 정보를 접하고 권리행사에 지장이 없도록 최선을 다하고 있으며, 유상증자 절차가 완료될 때까지 이러한 노력을 지속할 예정입니다. |
| 12. 공모일정 및 예정발행가액 | 구주주 청약은 7월 8일부터 9일까지 진행되며, 일반공모 청약에 대한 공고는 7월 10일 당사 인터넷 홈페이지 및 NH투자증권 홈페이지를 통해 게시될 예정입니다. 일반공모 청약은 7월 11일부터 14일까지 진행되며, 최종적으로 신주의 상장 예정일은 7월 28일입니다. 예정 발행가액은 3,310원이며 확정 발행가액은 7월 3일에 산정될 예정입니다. |
당사 IR 연락 정보
E-mail : ir@bukwang.co.kr
Tel : 02-828-8114 (전담콜센터 운영)
내선번호 : 117, 092
별개로 당사의 최대주주는 최대주주로서의 책임을 다하기 위해 배정받은 신주인수권리를 적극 행사할 예정이며 2대, 3대 주주 또한 자금상황을 고려하여 증자에 참여하거나 참여하지 않을 경우 최대주주가 증서를 장외 매수하여 신주인수권을 행사하는 등 당사의 최대주주 및 주요주주는 책임경영 의지를 표명할 예정입니다.
당사는 상기와 같이 주주 및 시장과의 적극적인 소통을 통해 회사의 경영 전략 및 비전을 명확히 전달하는 한편, 본 유상증자와 관련 후속 정보를 지속적으로 제공해 나가겠습니다.
VI. 그 밖에 투자자보호를 위해 필요한 사항
본 건의 경우 시장조성 또는 안정조작에 관한 사항은 해당사항 없습니다.
제2부 발행인에 관한 사항
I. 회사의 개요
1. 회사의 개요
가. 연결대상 종속회사 개황
1. 연결대상 종속회사 개황(연결재무제표를 작성하는 주권상장법인이 사업보고서, 분기ㆍ반기보고서를 제출하는 경우에 한함)
(1) 연결대상 종속회사 현황(요약)
| (단위 : 사) |
| 구분 | 연결대상회사수 | 주요 종속회사수 |
|||
|---|---|---|---|---|---|
| 기초 | 증가 | 감소 | 기말 | ||
| 상장 | - | - | - | - | - |
| 비상장 | 4 | - | - | 4 | - |
| 합계 | 4 | - | - | 4 | - |
가-1. 연결대상회사의 변동내용
1-1. 연결대상회사의 변동내용
| 구 분 | 자회사 | 사 유 |
|---|---|---|
| 신규 연결 |
- | - |
| - | - | |
| 연결 제외 |
- | - |
| - | - |
나. 회사의 법적·상업적 명칭, 본사의 주소 등
| 회사의 명칭 | 부광약품주식회사(Bukwang Pharm.Co.,Ltd.) | |||
| 설립일 | 1960년 10월 17일 | 주권상장일 | 1988년 08월 05일 | |
| 본사소재지 | 서울특별시 동작구 상도로 7(대방동) | |||
| 전화번호 | 02-828-8114 | 홈페이지주소 | http://www.bukwang.co.kr | |
| 주요 사업 | 의약품, 의약외품 제조업 및 판매업 / 연구개발등 생명공학 관련사업 | |||
| 주요 제품 | 덱시드, 레가론, 훼로바, 치옥타시드, 씬지로이드, 타세놀, 액시마, 익셀, 헥사메딘, 딜라스틴, 엔독산, 시린메드, 부광탁스, 안티프라그 등 |
|||
| 종속회사 | Contera Pharma A/S | 비상장 해외 | ||
| 부광메디카(주) | 비상장 국내 | |||
| JaguAHR Therapeutics | 비상장 해외 | |||
| ProteKt Therapeutics | 비상장 해외 | |||
| 관계기업 | 덴탈플랫폼투자조합 1호 | 비상장 국내 | ||
다. 중소기업 해당 여부
중소기업 등 해당 여부
| 중소기업 해당 여부 | 미해당 | |
| 벤처기업 해당 여부 | 미해당 | |
| 중견기업 해당 여부 | 미해당 | |
라. 회사의 주권상장여부 및 특례상장에 관한 사항
| 주권상장 (또는 등록ㆍ지정)현황 |
주권상장 (또는 등록ㆍ지정)일자 |
특례상장 유형 |
|---|---|---|
| 유가증권시장 상장 | 1988년 08월 05일 | 해당사항 없음 |
마. 주요 사업의 내용
부광약품(주)와 연결대상 종속회사의 주요 사업은 의약품 제조 및 판매, 의약품 연구개발등이며, 보다 상세한 내용은 동 공시서류의 'II. 사업의내용'을 참조하시기 바랍니다.
(1) 회사가 영위하는 목적사업
| 상호 | 목 적 사 업 | 비 고 |
|---|---|---|
| 부광약품주식회사 | (1)의약품, 원료의약품, 의약외품 제조업 및 판매업 (2)의약품, 의약외품, 화장품, 의료용구의 소분 및 가공업 (3)식품, 식품 첨가물, 청량음료, 건강식품 제조업 및 판매업 (4)식품, 식품 첨가물, 청량음료, 건강식품의 소분 및 가공업 (5)화장품, 화장용품, 방향제, 방취제 제조업 및 판매업 (6)의료용구, 위생용품, 의료용품, 의료용기기, 세정제 제조업 및 판매업 (7)국내외 수출입업 (8)부동산 임대업 (9)벤처관련사업 (10)생명공학관련사업 |
- |
(2) 연결대상 종속회사가 영위하는 목적사업
| 상호 | 목 적 사 업 | 상장여부 |
|---|---|---|
| Contera Pharma A/S | (1)의약품 연구 및 개발사업 | 비상장 |
| 부광메디카(주) | (1)의약품, 원료의약품, 의약외품 제조업 및 판매업 및 수출입 (2)의약품, 의약외품, 화장품, 의료용구의 소분 및 가공업 (3)식품, 식품첨가물, 청량음료, 건강식품 제조업 및 판매업 (4)식품, 식품첨가물, 청량음료, 건강식품의 소분 및 가공업 (5)도매업 및 소매업 (6)국내외 수출입업 |
비상장 |
| JaguAHR Therapeutics | (1)생명공학 관련 사업 (2)연구실험 개발 사업 |
비상장 |
| ProteKt Therapeutics | (1)의약품 연구 및 개발사업 | 비상장 |
(3) 관계기업 및 공동기업이 영위하는 목적사업
| 상호 | 목 적 사 업 | 상장여부 |
|---|---|---|
| 덴탈플랫폼투자조합1호 | (1)신기술 관련 투자업 | 비상장 |
2. 회사의 연혁
[지배회사의 연혁]
가. 회사의 본점소재지 및 그 변경
- 본점소재지: 서울특별시 동작구 상도로 7(대방동)
(구, 지번주소 : 서울특별시 동작구 대방동 398-1)
나. 경영진의 중요한 변동
| 변동일자 | 주총종류 | 선임 | 임기만료 또는 해임 |
|
|---|---|---|---|---|
| 신규 | 재선임 | |||
| 2025.03.26 | 정기주총 | 사내이사 안미정 사외이사 이상길 |
- | 사외이사 강문성 |
| 2024.04.01 | - | - | - | 사내이사 우기석 (주4) |
| 2024.03.22 | 정기주총 | 사내이사 이제영 사내이사 우기석 |
사외이사 전형수 사외이사 정길영 |
사내이사 이우현 (주3) 사내이사 김선호 |
| 2023.11.17 | - | - | - | 사내이사 유희원 (주2) |
| 2023.03.28 | 정기주총 | 사내이사 서진석(주1) | 사외이사 강문성 | 사내이사 김성준 |
| 2022.03.25 | 정기주총 | 사내이사 이우현 사내이사 김성준 사외이사 전형수 사외이사 정길영 |
사내이사 유희원 | 사내이사 김상훈 사외이사 김상용 사외이사 김범수 |
| 2021.03.19 | 정기주총 | 사내이사 김선호 사외이사 강문성 |
사내이사 김상훈 | - |
(주1) 서진석 사내이사는 2023년 04월 일신상의 사유로 사임하였습니다.
(주2) 유희원 사내이사는 2023년 11월 일신상의 사유로 사임하였습니다.
(주3) 이우현 사내이사는 2024년 03월 22일 사임 후 미등기임원으로 변경되었습니다.(주4) 우기석 사내이사는 2024년 04월 일신상의 사유로 사임하였습니다.
다. 대표이사의 변동
| 취임일 | 퇴임일 | 대표이사명 |
|---|---|---|
| 2024년 03월 22일 | 현재 | 이 제 영 |
| 2024년 03월 22일 | 2024년 04월 01일 | 우 기 석(각자대표) |
| 2022년 03월 25일 | 2024년 03월 22일 | 이 우 현(각자대표) |
| 2022년 03월 25일 | 2023년 11월 17일 | 유 희 원(각자대표) |
*2022년 03월 25일 제62기 정기주주총회 후 개최된 이사회에서 각자대표이사로 변경
*2023년 11월 17일 대표이사 유희원이 일신상의 사유로 사임
*2024년 03월 22일 제64기 정기주주총회 후 개최된 이사회에서 각자대표이사로 변경
*2024년 04월 01일 대표이사 우기석이 일신상의 사유로 사임
라. 최대주주의 변동
| (기준일 : 보고서 제출일 현재) | (단위 : 주,%) |
| 최대주주명 | 최대주주 변동일 결산기말 지분현황 |
소유주식수 | 지분율 | 비 고 |
|---|---|---|---|---|
| OCI홀딩스주식회사 | 2024.03.29 | 7,747,934 | 11.32 | 주식소각에 따른 지분율변동 |
| OCI홀딩스주식회사 | 2023.11.17 | 7,747,934 | 10.90 | 특별관계자 변동(임원퇴임) |
| OCI홀딩스주식회사외 1인 | 2022.03.25 | 7,795,267 | 10.97 | 특별관계자 변동(임원퇴임) |
| OCI홀딩스주식회사외 3인 | 2022.03.03 | 8,383,490 | 11.80 | 장외매도 외 |
| 김동연외 11인 | 2021.06.16 | 15,419,156 | 21.70 | 장내매도 |
| 김동연외 11인 | 2021.03.19 | 17,357,156 | 24.43 | 제28회차 주식배당 |
| 김동연외 11인 | 2020.11.13 | 15.779.237 | 24.34 | 장내매도 |
*작성기준일 이후 변동은 전자공시시스템(http://dart.fss.or.kr)의 주식등의 대량보유상황보고서 및 기타 지분공시 자료등을 참고하십시오.
마. 상호의 변경
| 일 자 | 내 용 |
|---|---|
| 1960.10.17 | 부광상사주식회사 설립 |
| 1962.03.15 | 부광약품공업주식회사로 상호 변경 |
| 2001.05.26 | 부광약품주식회사로 상호 변경 |
바. 경영활동과 관련된 중요한 사항의 발생내용
| 일 자 | 내 용 |
|---|---|
| 2020.04.13 | 자회사 Contera Pharma A/S 한국지사 설립 |
| 2020.06.05 | 자회사 부광메디카(주) 안산 반월공장 매각계약 체결완료 |
| 2020.06.06 | 미다졸람주사 코로나바이러스감염증-19(COVID-19) 마취 진정제 유럽 수출 |
| 2020.07.21 | 자회사 다이나세라퓨틱스(주)의 항암제 후보물질인 'SOL-804' 일본 특허 등록 |
| 2020.07.22 | 자회사 Contera Pharma A/S의 메디치2020의1 사모투자 합자회사로부터 352억원 투자유치 |
| 2021.01.14 | 자회사 다이나세라퓨틱스(주)의 항암제 후보물질인 'SOL-804'유럽, 호주, 멕시코 특허 등록 |
| 2021.04.29 | 자회사 Contera Pharma A/S와 공동 개발중인 운동장애(LID) 치료제 "JM-010" 美FDA 임상 2상 투약 개시 |
| 2021.10.20 | 자회사 다이나세라퓨틱스(주)의 전립선암 치료제 'SOL-804'에 대한 한국식품의약품안전청(KFDA)의 임상1상 시험계획 승인 |
| 2021.11.08 | 자회사 다이나세라퓨틱스(주) 항암제 후보물질인 'SOL-804' 미국 특허등록 결정 |
| 2022.02.25 | 자회사 다이나세라퓨틱스(주)의 전립선암 치료제 'SOL-804'에 대한 한국식품의약품안전청(KFDA)의 임상1상 시험 완료 |
| 2022.07.22 | 조현병 및 양극성장애신약 "Lurasidone"의 3상 임상 시험 결과 발표 |
| 2022.10.31 | 조현병 및 양극성장애신약 "Lurasidone" 품목허가 신청 |
| 2022.11.07 | 파킨슨병 이상운동증치료제 "JM-010" 유럽 2상 임상에 한국 의료기관 추가 |
| 2022.12.19 | 자회사 Contera Pharma A/S 덴마크 본사 DTU 사이언스 파크 이전 및 신규 연구소 개소 |
| 2023.01.26 | 신경퇴행성 질환치료제 개발 이스라엘 회사 ProteKT Theraputics 지분 추가 취득으로 관계기업에서 종속회사로 편입 |
| 2023.04.28 | 파킨슨병 이상운동증치료제 "JM-010" 유럽 2상 임상에 슬로바키아 의료기관 추가 |
| 2023.09.23 | 자회사 Contera Pharma A/S의 파킨슨병 아침무동증 치료제 'CP-012' Phase 1a 임상시험 투약 개시 |
| 2023.11.13 | 조현병 및 양극성장애신약 "Lurasidone" 품목허가 승인 |
| 2024.01.24 | 자회사 Contera Pharma A/S의 파킨슨병 아침무동증 치료제 'CP-012' Phase 1a 임상시험의 개념 증명을 성공적으로 완료 |
| 2024.05.22 | 파킨슨병 이상운동증치료제 "JM-010" 유럽 2상 임상 탑라인 결과 발표 |
| 2024.08.01 | 조현병 및 양극성장애신약 "Lurasidone" (제품명: 라투다정)출시 |
| 2024.11.28 | 자회사 Contera Pharma A/S의 파킨슨병 아침무동증 치료제 'CP-012' 의 phase 1b 임상시험 첫 환자 투약 개시 |
| 2025.03.14 | 자회사 Contera Pharma A/S의 카나반병 치료제 'CP-102', 후보물질 중 CP0014753을 전임상 후보물질로 정식 선정 |
[종속회사의 연혁(Contera Pharma A/S)]
가. 회사의 본점소재지 및 그 변경
- 본점소재지: DTU Science Park Venlighedsvej 4 2970 Hørsholm Denmark
나. 경영진의 중요한 변동
| 변동일자 | 주총종류 | 선임 | 임기만료 또는 해임 |
|
|---|---|---|---|---|
| 신규 | 재선임 | |||
| 2025.04.15 | 정기주총 | 사내이사 안미정 | 사내이사 이우현 사내이사 이제영 사내이사 Thomas N. Sager |
- |
| 2025.02.14 | - | - | - | 사내이사 박수연(주2) |
| 2024.12.01 | 임시주총 | 사내이사 박수연 사내이사 Mahmoud Mahmoudian |
- | - |
| 2024.04.25 | 정기주총 | - | 사내이사 이우현 사내이사 이제영 사내이사 Thomas N. Sager |
- |
| 2024.03.01 | 임시주총 | 사내이사 Paul E.G. Kristjansen | - | - |
| 2023.11.17 | - | - | - | 사내이사 유희원(주1) |
| 2023.07.03 | 임시주총 | 사내이사 이제영 | - | 사내이사 김성준 |
| 2023.03.31 | 정기주총 | - | 사내이사 유희원 사내이사 이우현 사내이사 김성준 사내이사 Thomas N. Sager |
- |
| 2023.02.07 | 임시주총 | - | - | 사내이사 김선호 |
| 2022.07.01 | 임시주총 |
사내이사 이우현 사내이사 Thomas N. Sager |
- | - |
| 2022.03.28 | 정기주총 | 사내이사 김성준 | 사내이사 유희원 사내이사 김선호 |
사내이사 김은주 |
| 2021.04.30 | 임시주총 | 사내이사 김선호 | - | 사내이사 엄정윤 |
| 2021.03.26 | 정기주총 | - | 사내이사 유희원 사내이사 김은주 사내이사 엄정윤 |
- |
| 2020.11.13 | 임시주총 | 사내이사 김은주 | - | 사내이사 김상훈 |
| 2020.03.26 | 정기주총 | - | 사내이사 유희원 사내이사 김상훈 사내이사 엄정윤 |
- |
(주1) 유희원 사내이사는 2023년 11월 일신상의 사유로 사임하였습니다.
(주2) 박수연 사내이사는 2025년 2월 일신상의 사유로 사임하였습니다.
다. 대표이사의 변동
| 취임일 | 퇴임일 | 대표이사명 |
|---|---|---|
| 2020년 12월 01일 | 현재 | Thomas N. Sager |
| 2014년 11월 24일 | 2020년 12월 01일 | John Bondo Hansen |
라. 최대주주의 변동
| (기준일 : 보고서 제출일 현재) | (단위 : 주,%) |
| 최대주주명 | 최대주주 변동일 결산기말 지분현황 |
소유주식수 | 지분율 | 비 고 |
|---|---|---|---|---|
| 부광약품(주) | 2025.04.29 | 1,875,733 | 99.50 | 유상증자 481,927주 |
| 부광약품(주) | 2024.10.25 | 1,393,806 | 99.33 | 유상증자 336,700주 |
| 부광약품(주) | 2024.08.20 | 1,057,106 | 99.12 | 유상증자 413,793주 |
| 부광약품(주) | 2024.04.01 | 643,313 | 98.56 |
매수 159,380주 (양도인 : 에이치델타사모투자합자회사) |
| 부광약품(주) | 2023.08.17 | 483,933 | 74.14 | 유상증자 31,250주 |
| 부광약품(주) | 2022.11.14 | 452,683 | 72.84 |
매수 10,000주 (양도인 : 메디치 중소 선도기업 투자조합 |
| 부광약품(주) | 2020.07.22 | 442,683 | 71.23 | 매도 40,000주 유상증자 110,000주 |
| 부광약품(주) | 2020.06.30 | 482,683 | 94.38 | - |
| 부광약품(주) | 2019.07.09 | 482,683 | 94.38 | 유상증자 10,000주 |
| 부광약품(주) | 2019.02.22 | 482,683 | 96.26 | 무상증자 127,232주 |
| 부광약품(주) | 2018.12.31 | 360,211 | 96.26 | 유상증자 14,000주 |
| 부광약품(주) | 2017.12.31 | 360,211 | 100 | - |
마. 상호의 변경
| 일 자 | 내 용 |
|---|---|
| 2010.07.09 | Concit Pharma ApS 설립 |
| 2013.11.19 | Contera Pharma ApS로 상호변경 |
| 2014.11.24 | Contera Pharma ApS 인수 |
| 2019.02.22 | Contera Pharma A/S로 상호변경 |
바. 경영활동과 관련된 중요한 사항의 발생내용
| 일 자 | 내 용 |
|---|---|
| 2020.01.10 | 운동장애(LID)치료제 "JM-010" 유럽 임상 2상 투약 개시 |
| 2020.04.13 | Contera Pharma A/S 한국지사 설립 |
| 2020.07.22 | 메디치2020의1 사모투자합자회사로부터 352억원 투자유치 |
| 2021.04.29 | 운동장애(LID) 치료제 "JM-010" 美 FDA 임상 2상 투약 개시 |
| 2022.11.07 | 파킨슨병 이상운동증치료제 "JM-010" 유럽 2상 임상에 한국 의료기관 추가 |
| 2022.12.19 | 덴마크 본사 DTU 사이언스 파크 이전 및 신규 연구소 개소 |
| 2023.04.28 | 파킨슨병 이상운동증치료제 "JM-010" 유럽 2상 임상에 슬로바키아 의료기관 추가 |
| 2023.08.27 | 보통주 31,250주 유상증자(100억) |
| 2023.09.23 | 파킨슨병 아침무동증 치료제 "CP-012" phase 1a 임상시험 투약 개시 |
| 2024.05.22 | 파킨슨병 이상운동증치료제 "JM-010" 유럽 2상 임상 탑라인 결과 발표 |
| 2024.08.27 | 보통주 413,793주 유상증자(44억) |
| 2024.10.27 | 보통주 336,700주 유상증자(30억) |
[종속회사의 연혁(부광메디카주식회사)]
가. 회사의 본점소재지 및 그 변경
- 본점소재지: 서울특별시 동작구 상도로 5(대방동)
나. 경영진의 중요한 변동
| 변동일자 | 주총종류 | 선임 | 임기만료 또는 해임 |
|
|---|---|---|---|---|
| 신규 | 재선임 | |||
| 2025.03.27 | 정기주총 | - | 사내이사 이제영 사내이사 박종도 사내이사 장삼순 |
- |
| 2024.08.21 | 임시주총 | 사내이사 박종도 | - | 사내이사 안지영 |
| 2024.03.28 | 정기주총 | 사내이사 안지영 | - | - |
| 2023.12.20 | 임시주총 | 사내이사 장삼순 | - | 사내이사 김지윤 |
| 2023.07.17 | 임시주총 | 사내이사 이제영 | - | 사내이사 김성준 |
| 2022.03.29 | 정기주총 | 사내이사 김지윤 사내이사 김성준 |
사내이사 김선호 | 사내이사 권순일 사내이사 김은주 |
| 2021.03.23 | 정기주총 | - | 사내이사 김은주 | - |
| 2020.03.20 | 정기주총 | - | 사내이사 권순일 | - |
다. 대표이사의 변동
| 취임일 | 퇴임일 | 대표이사명 |
|---|---|---|
| 2023년 12월 20일 | 현재 | 이 제 영 |
| 2022년 03월 29일 | 2023년 12월 20일 | 김 지 윤 |
| 2017년 04월 17일 | 2022년 03월 29일 | 권 순 일 |
라. 최대주주의 변동
| (기준일 : 보고서 제출일 현재) |
(단위 : 주,%) |
| 최대주주명 | 최대주주 변동일 결산기말 지분현황 |
소유주식수 | 지분율 | 비 고 |
|---|---|---|---|---|
| 부광약품(주) | 2024.04.25 | 1,354,087 | 100 | 유상감자 738,553주 |
| 부광약품(주) | 2021.01.25 | 2,092,640 | 100 | 유상감자 2,707,360주 |
| 부광약품(주) | 2020.12.31 | 4,800,000 | 100 | - |
마. 상호의 변경
| 일 자 | 내 용 |
|---|---|
| 2015.06.17 | 부광메디카주식회사 설립 |
바. 경영활동과 관련된 중요한 사항의 발생내용
| 일 자 | 내 용 |
|---|---|
| 2020.08.24 | 안산 반월공장 부지 및 KGMP시설 매각 |
| 2020.12.22 | 보통주 2,707,360주 유상감자(110억) |
| 2024.04.30 | 보통주 738,553주 유상감자(30억) |
[종속회사의 연혁(ProteKt Therapeutics)]
가. 회사의 본점소재지 및 그 변경
- 본점소재지: 16 Bar Kochva St., Bnei-Brak, Israel
나. 경영진의 중요한 변동
| 변동일자 | 주총종류 | 선임 | 임기만료 또는 해임 |
|
|---|---|---|---|---|
| 신규 | 재선임 | |||
| 2023.04.03 | 임시주총 | 사내이사 Riswanto Tan |
- | 사내이사 진혁준 |
| 2023.02.20 | 임시주총 | 사내이사 진혁준 | - | 사내이사 유희원 |
| 2019.11.12 | 임시주총 | 사내이사 유희원 | - | - |
다. 대표이사의 변동
| 취임일 | 퇴임일 | 대표이사명 |
|---|---|---|
| 2015년 01월 01일 | 현재 | Yotam Nisemblat |
라. 최대주주의 변동
| (기준일 : 보고서 제출일 현재) |
(단위 : 주,%) |
| 최대주주명 | 최대주주 변동일 결산기말 지분현황 |
소유주식수 | 지분율 | 비 고 |
|---|---|---|---|---|
| 부광약품(주) | 2023.01.26 | 4,822,004 | 96.53% | - |
마. 상호의 변경
-해당사항 없음
바. 경영활동과 관련된 중요한 사항의 발생내용
| 일 자 | 내 용 |
|---|---|
| 2022.12 | PKR 저해제 신규화합물의 특허 제출 |
| 2023.01 | 부광약품(주)로 최대주주 변경 |
| 2024.06 | 임상 바이오마커 데이터 확보 |
[종속회사의 연혁(JaguAHR Therapeutics]
가. 회사의 본점소재지 및 그 변경
- 본점소재지: 5 SHENTON WAY, #10-01, UIC BUILDING, SINGAPORE
나. 경영진의 중요한 변동
| 변동일자 | 주총종류 | 선임 | 임기만료 또는 해임 |
|
|---|---|---|---|---|
| 신규 | 재선임 | |||
| 2024.12.12 | 임시주총 | 사내이사 Endo Isana | - | 사내이사 Carl Aslan Jason Morton Firth |
| 2024.09.09 | 임시주총 | - | - | 사내이사 Robert John Moore |
| 2024.09.04 | 임시주총 | 사내이사 Riswanto Tan |
- | 사내이사 신지혜 |
| 2024.01.11 | 임시주총 | 사내이사 김지헌 | - | 사내이사 유희원 |
| 2021.05.17 | 임시주총 | 사내이사 신지혜 | - | 사내이사 엄정윤 |
| 2020.05.31 | 임시주총 | 사내이사 Robert John Moore |
- | 사내이사 Mark Thomas Mchale |
다. 대표이사의 변동
| 취임일 | 퇴임일 | 대표이사명 |
|---|---|---|
| - (주1) | - | - |
(주1) 별도의 대표이사를 두지 않고, 주요 의사결정은 이사회 의결권을 통해 이루어짐
라. 최대주주의 변동
| (기준일 : 보고서 제출일 현재) |
(단위 : 주,%) |
| 최대주주명 | 최대주주 변동일 결산기말 지분현황 |
소유주식수 | 지분율 | 비 고 |
|---|---|---|---|---|
| 부광약품(주) | 2024.12.09 | 165,050 | 75.02 | 공동기업 ASLAN으로부터 22,050주 인수 |
| 부광약품(주) | 2021.04.28 | 143,000 | 65.00 | - |
마. 상호의 변경
-해당사항 없음
바. 경영활동과 관련된 중요한 사항의 발생내용
| 일 자 | 내 용 |
|---|---|
| 2019.08 | 면역질환 전문 신약개발사 ASLAN Pharmaceuticals Pte Ltd가 항암신약 연구개발 회사인 JaguAHR Therapeutics 설립 |
| 2019.08 | Ahr 길항제 신규 화합물 특허 제출 |
| 2019.10 | ASLAN과 부광약품(주)이 JaguAHR에 대한 Investment and Joint Venture Agreement를 체결 |
| 2019.10 | 부광약품(주)에 US$2,500,000의 제1차 트랜치 신주 발행 |
| 2021.04 | 부광약품(주)에 US$2,500,000의 제2차 트랜치 신주 발행 |
| 2023.10 | Ahr 길항제 추가 화합물 특허 제출 |
| 2024.12 | 공동기업 ASLAN으로부터 22,050주 인수하여 부광약품(주)의 종속기업으로 편입(지분율 75.02%) |
3. 자본금 변동사항
| (단위 : 원, 주) |
| 종류 | 구분 |
제66기 1분기 (2025년 3월말) |
제65기 (2024년말) |
제64기 (2023년말) |
제63기 (2022년말) |
제62기 (2021년말) |
|---|---|---|---|---|---|---|
| 보통주 | 발행주식총수 | 68,454,671 | 68,454,671 | 71,063,049 | 71,063,049 | 71,063,049 |
| 액면금액 | 500 | 500 | 500 | 500 | 500 | |
| 자본금 | 34,227,335,500 | 34,227,335,500 | 35,531,524,500 | 35,531,524,500 | 35,531,524,500 | |
| 우선주 | 발행주식총수 | - | - | - | - | - |
| 액면금액 | - | - | - | - | - | |
| 자본금 | - | - | - | - | - | |
| 기타 | 발행주식총수 | - | - | - | - | - |
| 액면금액 | - | - | - | - | - | |
| 자본금 | - | - | - | - | - | |
| 합계 | 자본금 | 34,227,335,500 | 34,227,335,500 | 35,531,524,500 | 35,531,524,500 | 35,531,524,500 |
* 발행주식의 액면총액은 34,227백만원으로, 납입자본금 36,402백만원과는 이익소각으로 인하여 상이합니다.
4. 주식의 총수 등
가. 주식의 총수 현황
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 주, %) |
| 구 분 | 주식의 종류 | 비고 | |||
|---|---|---|---|---|---|
| 보통주 | 우선주 | 합계 | |||
| Ⅰ. 발행할 주식의 총수 | 150,000,000 | 2,000,000 | 152,000,000 | - | |
| Ⅱ. 현재까지 발행한 주식의 총수 | 72,803,986 | - | 72,803,986 | - | |
| Ⅲ. 현재까지 감소한 주식의 총수 | 4,349,315 | - | 4,349,315 | - | |
| 1. 감자 | - | - | - | - | |
| 2. 이익소각 | 4,349,315 | - | 4,349,315 | - | |
| 3. 상환주식의 상환 | - | - | - | - | |
| 4. 기타 | - | - | - | - | |
| Ⅳ. 발행주식의 총수 (Ⅱ-Ⅲ) | 68,454,671 | - | 68,454,671 | - | |
| Ⅴ. 자기주식수 | - | - | - | - | |
| Ⅵ. 유통주식수 (Ⅳ-Ⅴ) | 68,454,671 | - | 68,454,671 | - | |
| Ⅶ. 자기주식 보유비율 | - | - | - | - | |
나. 자기주식 취득 및 처분 현황
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 주) |
| 취득방법 | 주식의 종류 | 기초수량 | 변동 수량 | 기말수량 | 비고 | ||||
|---|---|---|---|---|---|---|---|---|---|
| 취득(+) | 처분(-) | 소각(-) | |||||||
| 배당 가능 이익 범위 이내 취득 |
직접 취득 |
장내 직접 취득 |
보통주 | - | - | - | - | - | - |
| 우선주 | - | - | - | - | - | - | |||
| 장외 직접 취득 |
보통주 | - | - | - | - | - | - | ||
| 우선주 | - | - | - | - | - | - | |||
| 공개매수 | 보통주 | - | - | - | - | - | - | ||
| 우선주 | - | - | - | - | - | - | |||
| 소계(a) | 보통주 | - | - | - | - | - | - | ||
| 우선주 | - | - | - | - | - | - | |||
| 신탁 계약에 의한 취득 |
수탁자 보유물량 | 보통주 | - | - | - | - | - | - | |
| 우선주 | - | - | - | - | - | - | |||
| 현물보유물량 | 보통주 | - | - | - | - | - | - | ||
| 우선주 | - | - | - | - | - | - | |||
| 소계(b) | 보통주 | - | - | - | - | - | - | ||
| 우선주 | - | - | - | - | - | - | |||
| 기타 취득(c) | 보통주 | - | - | - | - | - | - | ||
| 우선주 | - | - | - | - | - | - | |||
| 총 계(a+b+c) | 보통주 | - | - | - | - | - | - | ||
| 우선주 | - | - | - | - | - | - | |||
다. 자기주식 직접 취득ㆍ처분 이행현황
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 주, %) |
| 구 분 | 취득(처분)예상기간 | 예정수량 (A) |
이행수량 (B) |
이행률 (B/A) |
결과 보고일 |
|
|---|---|---|---|---|---|---|
| 시작일 | 종료일 | |||||
| 직접 취득 | 2019.05.31 | 2019.08.30 | 3,060,000 | 2,575,314 | 84 | 2019.06.28 |
| 직접 취득 | 2020.01.08 | 2020.04.07 | 1,916,000 | 1,740,937 | 91 | 2020.02.12 |
라. 우리사주조합의 지분현황
(1) 우리사주조합과의 거래내역
해 당 사 항 없 음
(2) 우리사주조합의 의결권행사기준
- 조 합 계 좌 : 조합계정으로 보유되는 자사주의 의결권은 당해 주주총회의 참석주
식수에서 조합계정으로 보유되는 자사주수를 차감한 주식수의
의결 내용에 영향을 미치지 않도록 그 의결권을 행사함.
- 조합원계좌 : 조합원 개인별 계정에 배정된 자사주의 의결권은 근로복지기본법
시행령 제28조에서 정함에 따라 행사함.
(3) 우리사주조합 주식 보유내역
| (2025년 03월 31일 현재) | (단위 : 주) |
| 계좌구분 | 주식의 종류 | 기초잔고 | 기말잔고 |
|---|---|---|---|
| 조합원계좌 | 보통주 | 22,763 | 19,519 |
5. 정관에 관한 사항
가. 정관 변경 이력
| 정관변경일 | 해당주총명 | 주요변경사항 | 변경이유 |
|---|---|---|---|
| 2020년 03월 13일 | 제60기 정기주주총회 | - 수권주식수 조정 - 이사회 소집권자 조문 정비 - 외부감사인 선정 및 공고 방법 변경 - 전자증권 도입에 따른 조문 정비 |
- 전자증권법 시행 - 외감법 개정에 따른 변경 |
| 2021년 03월 19일 | 제61기 정기주주총회 | - 주식매수선택권 부여 주체 관련 조항 변경 - 의결권행사 및 배당기준일 조문 정비 - 감사위원회 위원 선임 방법 변경 |
- 주식매수선택권 상장사 특례규정 반영 - 상법 개정에 따른 변경 |
| 2024년 03월 22일 | 제64기 정기주주총회 | - 이사회내 보상위원회, ESG위원회의 설립 - 사외이사 임기 변경 |
- 이사회의 합리적인 운영 기준 마련 |
| 2025년 03월 26일 | 제65기 정기주주총회 | -발행예정 주식의 총수 변경 -분기배당 기준일 이사회 결의로 지정 가능 -주식의 이익소각 규정 추가 |
-자본 운영 탄력성 및 경영 유연성 확보 -자본시장법 개정 -주식소각 규정 추가 |
나. 사업 목적 현황
| 구 분 | 사업목적 | 사업영위 여부 |
|---|---|---|
| 1 | 의약품, 원료의약품, 의약외품 제조업 및 판매업. | 영위 |
| 2 | 의약품, 의약외품, 화장품, 의료용구의 소분 및 가공업. | 영위 |
| 3 | 식품, 식품 첨가물, 청량음료, 건강식품 제조업 및 판매업 | 영위 |
| 4 | 식품, 식품 첨가물, 청량음료, 건강식품의 소분 및 가공업 | 영위 |
| 5 | 자양, 기호음료, 인삼제품, 다류 제조업 및 판매업. | 미영위 |
| 6 | 광천음료수 제조업 및 판매업. | 미영위 |
| 7 | 화장품, 화장용품, 방향제, 방취제 제조업 및 판매업. | 영위 |
| 8 | 의료용구, 위생용품, 의료용품, 의료용기기, 세정제 제조업 및 판매업. |
영위 |
| 9 | 동물의약품, 농예약품, 화공약품 제조업 및 판매업. | 미영위 |
| 10 | 농축어 사료 및 동 첨가제의 제조업 및 판매업. | 미영위 |
| 11 | 약용작물, 농산물 재배 및 판매업(미곡은 제외). | 미영위 |
| 12 | 각종 유지제품 및 동 가공품의 제조업 및 판매업. | 미영위 |
| 13 | 합성세제, 프라스틱제품의 가공, 제조 및 판매업. | 미영위 |
| 14 | 잡화, 날붙이, 수공구, 일반철물 제조업 및 판매업. | 미영위 |
| 15 | 스포츠용품 제조업 및 판매업. | 미영위 |
| 16 | 레저용품, 가정용 직물제품, 의복악세사리 제조업 및 판매. | 미영위 |
| 17 | 국내외 수출입업. | 영위 |
| 18 | 부동산 임대업. | 영위 |
| 19 | 인터넷 및 전자상거래 관련사업. | 미영위 |
| 20 | 위탁통신판매 및 방문판매업. | 미영위 |
| 21 | 벤처관련사업. | 영위 |
| 22 | 생명공학관련사업. | 영위 |
| 23 | 산업재산권 임대서비스업. | 미영위 |
| 24 | 소프트웨어 개발 및 판매업. | 미영위 |
| 25 | 소프트웨어 및 하드웨어 유지보수 관련사업. | 미영위 |
| 26 | 위 각호에 부대하는 일체의 사업 및 투자. | 미영위 |
II. 사업의 내용
1. 사업의 개요
당사는 1960년 10월 17일 의약품의 제조 및 판매를 목적으로 설립되었습니다. 당사 가 영위하는 주요 사업으로는 의약품, 건강기능식품, 그 외 의약외품 등이 있으며 주요 제품으로는 덱시드, 레가론, 훼로바, 치옥타시드, 씬지로이드 등이 있습니다.
| 사업부문 | 주요 사업영역 | 주요 제품 |
|---|---|---|
| 의약품 및 의약외품 | 완제 의약품 및 의약외품 제조업 및 판매업 |
덱시드, 레가론, 훼로바, 치옥타시드, 씬지로이드 타세놀, 액시마, 익셀, 헥사메딘, 딜라스틴 엔독산, 시린메드, 부광탁스, 안티프라그 등 |
| 연구개발 | 의약품 연구 및 개발사업 | CP-012 등 |
당사의 2025년 1분기 연결기준 매출은 478억원이며, 전년 대비 약 39% 성장하였습니다. 연결기준 영업이익 또한 30억을 기록, 전년도 동분기 대비 흑자전환에 성공하였습니다 .
2. 주요 제품 및 서비스
일부 종속회사는 의약품 연구 개발업을 영위함에 따라 주요 제품을 보유하지 않습니다.
가. 주요 제품 등의 현황
| (단위 : 백만원, %) |
| 사업부문 | 매출 유형 |
품 목 | 구체적용도 | 주요상표등 | 매출액 | 비율 |
|---|---|---|---|---|---|---|
의약품 및 의약외품 |
제품 | 덱시드정 | 당뇨병성 신경병증 치료제 | 덱시드정 | 4,423 | 9 |
| 레가론 | 간질환치료제 | 레가론캡슐140 | 3,548 | 7 | ||
| 훼로바 | 빈혈치료제 | 훼로바유서방정 | 3,525 | 7 | ||
| 치옥타시드 | 당뇨병성 신경병증 치료제 | 치옥타시드정 | 3,317 | 7 | ||
| 씬지로이드 | 갑상선 부갑상선 호르몬제 | 씬지로이드정 | 2,168 | 4 | ||
| 타세놀 | 해열,진통,소염제 | 타세놀정 | 1,958 | 4 | ||
| 액시마 | 기관지확장제 | 액시마정 | 1,579 | 4 | ||
| 익셀 | 정신신경용제 | 익셀캡슐 | 1,288 | 4 | ||
| 헥사메딘액 | 구내염증완화제 | 헥사메딘액 | 1,109 | 2 | ||
| 기타 | - | - | 17,958 | 37 | ||
| 소 계 | - | - | 40,873 | 85 | ||
| 상품 | 딜라스틴 | 이비과용제 | 나잘스프레이 | 789 | 2 | |
| 엔독산 | 항악성종양제 | 엔독산주사 | 253 | 1 | ||
| 홀록산 | 항악성종양제 | 홀록산주 | 249 | - | ||
| 나벨빈 | 비소세포폐암외 항악성종양제 | 나벨빈주사 | 225 | - | ||
| 기타 | - | - | 5,764 | 12 | ||
| 소 계 | - | - | 7,280 | 15 | ||
|
수출/ |
덱시드정 | 당뇨병성 신경병증 치료제 | 덱시드정 | 44 | - | |
| 기타 | - | - | - | |||
| 소 계 | - | - | 44 | - | ||
| 단순합계 | 48,197 | 100 | ||||
| 내부거래 | (391) | - | ||||
| 총 계 | 47,806 | - | ||||
나. 주요 제품 등의 가격변동추이
| (단위 : 원) |
| 사업부문 | 품목 | 규격 | 제66기 1분기 | 제65기 | 제64기 |
|---|---|---|---|---|---|
| 의약품 및 의약외품 |
덱시드정480mg | 100T | 82,800 | 82,800 | 82,900 |
| 레가론캡슐140 | 500C | 120,000 | 120,000 | 120,500 | |
| 훼로바유서방정 | 500T | 46,500 | 46,500 | 46,500 | |
| 치옥타시드HR | 100T | 80,900 | 80,900 | 81,100 | |
| 씬지로이드0.05mg | 500T | 13,000 | 13,000 | 13,000 | |
| 타세놀정500mg | 10T | 880 | 880 | 880 | |
| 액시마정 | 500T | 56,000 | 56,000 | 56,000 |
(1) 산출 기준 : 출하가격
(2) 주요 가격변동원인 : 보험약가 및 보험기준 강화로 인한 변동
3. 원재료 및 생산설비
3.1 주요 원재료 등 현황 및 가격변동 추이
가. 주요 원재료 등의 현황
| (단위 : 백만원, %) |
| 사업부문 | 매입 유형 |
품 목 | 구체적용도 | 매입액 | 비율 | 비 고 |
|---|---|---|---|---|---|---|
| 의약품 및 의약외품 |
원료 | 티옥트산 | 치옥타시드정 | 2,512 | 17% | Mylan Ireland Limited |
| 루라시돈염산염 | 라투다정 | 1,960 | 13% | Sumitomo Pharma | ||
| 알-티옥트산트로메타민염 | 덱시드정 | 1,346 | 9% | 이니스트에스티 | ||
| 독소필린 | 액시마정 | 880 | 6% | EURODRUG LAB. | ||
| 아젤라스틴염산염 | 아젭틴정 | 606 | 4% | MEDA PHARMA GMBH & CO | ||
| 플루마제닐 | 플루닐주사 | 393 | 3% | Wavelength Enterprises LTD | ||
| 트로스퓸염화물 | 스파스몰리트당의정 | 330 | 2% | MADAUSGmbH | ||
| 기타 | - | 4,302 | 28% | - | ||
| 소계 | - | 12,329 | 82% | - | ||
| 재료 | 아기오(스틱) | 아기오과립 | 39 | - | 일신화학공업 | |
| 기타 | - | 939 | 6% | - | ||
| 소계 | - | 978 | 6% | - | ||
| 상품 | 딜라스틴나잘스프레이 | 딜라스틴나잘스프레이 | 1,112 | 7% | Mylan Ireland Limited | |
| 유로미텍산주 | 유로미텍산주 | 243 | 2% | Baxter healthcare PTE | ||
| 엔독산주500mg | 엔독산주 | 152 | 1% | Baxter healthcare PTE | ||
| 쏘팔메토옥타코사놀메가프라임 | 쏘팔메토옥타코사놀메가프라임 | 87 | - | 오름건강 | ||
| 기타 | - | 245 | 2% | - | ||
| 소계 | - | 1,839 | 12% | - | ||
| 합 계 | - | - | - | 15,146 | 100% | - |
나. 주요 원재료 등의 가격변동추이
| (단위 : 원) |
| 사업부문 | 품 목 | 단위 | 제66기 1분기 | 제65기 | 제64기 |
| 의약품 및 의약외품 |
티옥트산 | G | 299 | 291 | 279 |
| 루라시돈염산염 | 정 | 459 | 437 | 443 | |
| 알-티옥트산트로메타민염 | G | 664 | 665 | 666 | |
| 독소필린 | G | 98 | 95 | 92 | |
| 아젤라스틴염산염 | G | 25,154 | 25,154 | 25,154 | |
| 플루마제닐 | G | 2,514,552 | 2,414,000 | 2,448,590 | |
| 트로스퓸염화물 | G | 4,333 | 4,207 | 4,046 |
(1) 산출 기준 : 매입가격
(2) 주요 가격변동원인 : 환율 및 매입가격의 변동
3.2 생산 및 설비에 관한 사항
종속회사는 아직 본격적인 생산활동을 하지 않거나, 의약품 연구 개발업을 영위함에 따라 주요한 생산 및 설비에 대한 사항은 해당되지 않습니다.
가. 생산능력 및 생산능력 산출근거
(1) 생산능력
(단위 : 백만원)
| 사업 부문 |
품 목 | 사업소 | 제66기 1분기 | 제65기 | 제64기 |
| 의약품 및 의약외품 |
나정 | 안산공장 | 6,461 | 21,535 | 25,905 |
| 당의정 | 314 | 1,253 | 1,177 | ||
| 필름코팅정 | 20,345 | 59,699 | 72,208 | ||
| 캡슐제 | 6,440 | 18,515 | 27,415 | ||
| 과립제 | 1,002 | 3,898 | 4,184 | ||
| 주사제 | 340 | 11,525 | 11,887 | ||
| 내용액제 | 376 | 1,641 | 3,451 | ||
| 외용액제 | 873 | 3,720 | 5,487 | ||
| 연고제 | 621 | 3,969 | 2,506 | ||
| 기타제형 | 104 | 75 | 914 | ||
| 의약외품 | 1,273 | 5,106 | 14,493 | ||
| 합 계 | 38,149 | 130,936 | 169,627 | ||
1) 산출 기준 : 출하가 * 생산량(평균가동시간)
(2) 생산능력의 산출근거
(가) 산출 방법 등
1) 산출 기준: 제조 및 충전 기준
2) 산출 방법: 생산실적/가동률
(나) 평균 가동시간
| 사업부문 | 사업소 | 1일평균가동시간 | 월평균가동일수 | 당기 가동일수 | 당기 가동시간 |
|---|---|---|---|---|---|
| 의약품 및 의약외품 | 안산공장 | 8.0 | 19 | 58 | 464 |
나. 생산실적 및 가동률
(1) 생산실적
| (단위 : 백만원) |
| 사업 부문 |
품 목 | 사업소 | 제66기 1분기 | 제65기 | 제64기 |
|---|---|---|---|---|---|
| 의약품 및 의약외품 |
나정 | 안산공장 | 8,012 | 26,704 | 25,646 |
| 당의정 | 389 | 1,554 | 1,165 | ||
| 필름코팅정 | 25,228 | 74,027 | 71,486 | ||
| 캡슐제 | 7,986 | 22,959 | 27,141 | ||
| 과립제 | 1,243 | 4,833 | 4,142 | ||
| 주사제 | 421 | 14,291 | 11,768 | ||
| 내용액제 | 466 | 2,035 | 3,416 | ||
| 외용액제 | 1,083 | 4,613 | 5,432 | ||
| 연고제 | 770 | 4,922 | 2,481 | ||
| 기타제형 | 129 | 93 | 905 | ||
| 의약외품 | 1,579 | 6,331 | 14,348 | ||
| 합 계 | 47,306 | 162,362 | 167,930 | ||
1) 산출 기준: 출하가 * 생산량(실제가동시간)
(2) 당분기의 가동률
| (단위 : 시간) |
| 사업부문 | 사업소 | 가동가능시간 | 실제가동시간 | 평균가동률 |
|---|---|---|---|---|
| 의약품 및 의약외품 | 안산공장 | 464 | 576 | 124% |
- 가동가능시간 : 당분기 근무일수 X 8시간
- 실제가동시간 : 초과근무를 포함한 당분기 실제가동시간
다. 생산설비의 현황 등
(1) 생산설비의 현황
[자산항목 : 토지] (단위 : 백만원)
| 사업 부문 |
사업소 | 소유 형태 |
소재지 | 기초 장부가액 |
증감 | 당기 상각 |
기말 장부가액 |
비고 | |
| 증가 | 감소 | ||||||||
| 의약품 및 의약외품 |
본사 | 자가 | 서울시 | 58,588 | - | 375 | - | 58,213 | - |
| 연구소 | 자가 | 서울시 | 11,107 | - | - | - | 11,107 | - | |
| 기숙사 | 자가 | 안산외 | 463 | - | - | - | 463 | - | |
| 안산공장 | 자가 | 안산시 | 43,155 | - | - | - | 43,155 | - | |
| 연결조정 | - | - | - | - | - | - | |||
| 합 계 | 113,313 | - | 375 | - | 112,938 | - | |||
[자산항목 : 건물] (단위 : 백만원)
| 사업 부문 |
사업소 | 소유 형태 |
소재지 | 기초 장부가액 |
증감 | 당기 상각 |
기말 장부가액 |
비고 | |
| 증가 | 감소 | ||||||||
| 의약품 및 의약외품 |
본사 | 자가 | 서울시 | 995 | - | 42 | 47 | 906 | |
| 연구소 | 자가 | 서울시 | 2,842 | - | - | 44 | 2,798 | - | |
| 안산공장 | 자가 | 안산시 | 18,205 | - | - | 332 | 17,873 | - | |
| 연결조정 | - | - | - | - | - | - | |||
| 합 계 | 22,042 | - | 42 | 423 | 21,577 | - | |||
[자산항목 : 구축물] (단위 : 백만원)
| 사업 부문 |
사업소 | 소유 형태 |
소재지 | 기초 장부가액 |
증감 | 당기 상각 |
기말 장부가액 |
비고 | |
| 증가 | 감소 | ||||||||
| 의약품 및 의약외품 |
본사 | 자가 | 서울시 | 23 | - | - | 4 | 19 | - |
| 연구소 | 자가 | 서울시 | 9 | - | - | 1 | 8 | - | |
| 안산공장 | 자가 | 안산시 | 190 | - | - | 11 | 179 | - | |
| 연결조정 | - | - | - | - | - | - | |||
| 합 계 | 222 | - | - | 16 | 206 | - | |||
[자산항목 : 기계장치] (단위 : 백만원)
| 사업 부문 |
사업소 | 소유 형태 |
소재지 | 기초 장부가액 |
증감 | 당기 상각 |
기말 장부가액 |
비고 | |
| 증가 | 감소 | ||||||||
| 의약품 및 의약외품 |
안산공장 | 자가 | 안산시 | 1,246 | 1,600 | - | 185 | 2,661 | - |
| 연결조정 | - | - | - | - | - | - | |||
| 합 계 | 1,246 | 1,600 | - | 185 | 2,661 | - | |||
[자산항목 : 차량운반구] (단위 : 백만원)
| 사업 부문 |
사업소 | 소유 형태 |
소재지 | 기초 장부가액 |
증감 | 당기 상각 |
기말 장부가액 |
비고 | |
| 증가 | 감소 | ||||||||
| 의약품 및 의약외품 |
본사 | 자가 | 서울시 | 42 | - | 19 | 6 | 17 | - |
| 안산공장 | 자가 | 안산시 | - | - | - | - | - | - | |
| 연구개발 | 콘테라파마 | 자가 | 서울시 | - | - | - | - | - | - |
| 연결조정 | - | - | - | - | - | - | |||
| 합 계 | 42 | - | 19 | 6 | 17 | - | |||
[자산항목 : 공구기구] (단위 : 백만원)
| 사업 부문 |
사업소 | 소유 형태 |
소재지 | 기초 장부가액 |
증감 | 당기 상각 |
기말 장부가액 |
비고 | |
| 증가 | 감소 | ||||||||
| 의약품 및 의약외품 |
연구소 | 자가 | 서울시 | 765 | 423 | - | 82 | 1,106 | - |
| 안산공장 | 자가 | 안산시 | 506 | 13 | - | 65 | 454 | - | |
| 연결조정 | - | - | - | - | - | - | |||
| 합 계 | 1,271 | 436 | - | 147 | 1,560 | - | |||
[자산항목 : 비품] (단위 : 백만원)
| 사업 부문 |
사업소 | 소유 형태 |
소재지 | 기초 장부가액 |
증감 | 당기 상각 |
기말 장부가액 |
비고 | |
| 증가 | 감소 | ||||||||
| 의약품 및 의약외품 |
본사 | 자가 | 서울시 | 424 | 8 | - | 43 | 389 | - |
| 연구소 | 자가 | 서울시 | 47 | 25 | - | 4 | 68 | ||
| 안산공장 | 자가 | 안산시 | 20 | 20 | - | 7 | 33 | - | |
| 메디카본사 | 자가 | 서울시 | - | - | - | - | - | - | |
| 연구개발 | 콘테라파마 | 자가 | 서울시 | 1,479 | 129 | - | 89 | 1,519 | - |
| 연결조정 | - | - | - | - | - | - | |||
| 합 계 | 1,970 | 182 | - | 143 | 2,009 | - | |||
4. 매출 및 수주상황
가. 매출실적
| (단위 : 백만원) |
| 사업 부문 |
매출 유형 |
품 목 |
제66기 1분기 |
제65기 | 제64기 | |
| 의약품 및 의약외품 |
제품 | 덱시드정 | 내 수 | 4,423 | 10,704 | 1,981 |
| 레가론 | 3,548 | 13,171 | 4,402 | |||
| 훼로바 | 3,525 | 17,415 | 13,424 | |||
| 치옥타시드 | 3,317 | 10,696 | 5,518 | |||
| 씬지로이드 | 2,168 | 10,353 | 7,373 | |||
| 타세놀 | 1,958 | 6,076 | 8,196 | |||
| 액시마 | 1,579 | 4,540 | 3,907 | |||
| 익셀 | 1,288 | 2,791 | 1,795 | |||
| 헥사메딘액 | 1,109 | 3,939 | 4,200 | |||
| 기타 | 17,958 | 65,525 | 53,029 | |||
| 제품계 | 40,873 | 145,210 | 103,825 | |||
| 상품 | 딜라스틴 | 내 수 | 789 | 2,571 | 2,025 | |
| 엔독산 | 253 | 1,006 | 979 | |||
| 홀록산 | 249 | 1,114 | 1,154 | |||
| 나벨빈 | 225 | 894 | 1,000 | |||
| 기타 | 5,764 | 11,408 | 20,352 | |||
| 상품계 | 7,280 | 16,993 | 25,510 | |||
| 수출/기술 | 덱시드정 | 수 출 | 44 | 38 | 150 | |
| MLR-1023 | 기 술 | - | 443 | - | ||
| 합 계 | 내 수 | 48,153 | 162,203 | 129,335 | ||
| 수 출 | 44 | 38 | 150 | |||
| 기 술 | - | 443 | - | |||
| 단순합계 | 48,197 | 162,684 | 129,485 | |||
| 내부거래 | (391) | (2,597) | (3,557) | |||
| 총 계 | 47,806 | 160,087 | 125,928 | |||
제66기 1분기(당분기)와 제65기(전기), 제64기(전전기) 매출은 K-IFRS 1115호에 따라작성되었습니다.
나. 판매경로 및 판매방법 등
종속회사 중 Contera Pharma A/S, JaguAHR Therapeutics 및 ProteKt Therapeutics는 연구개발업을 영위하므로 별도의 판매조직이 없습니다.
(1) 판매경로
| 사업부문 | 구분 | 판매경로 | 비고 | |
|---|---|---|---|---|
| 의약품 및 의약외품 |
의약유통 | 약국유통 | 회사 → 약국 | 직거래처 |
| 회사 → 도매상 → 약국 | - | |||
| 병원유통 | 회사 → 병원 | - | ||
| 회사 → 의원 | - | |||
| 회사 → 도매상 → 병원 | - | |||
| 도매유통 | 회사 → 도매상 → 약국 | - | ||
| 회사 → 도매상 → 병원/의원 | - | |||
| 생활용품유통 | 회사 → 대형할인점 | 직거래처 | ||
| 회사 → 대리점 → 소매점 | - | |||
| 회사 → 소매점 | - | |||
| 수출 | 회사 → 해외구매자(MASTR L/C) → 소비자 | - | ||
(2) 판매방법 및 조건
[의약품 및 의약외품 부문]
(가) 내수인 경우 : 병원, 약국, 도매상, 대리점, 소매점, 할인점 등에 현금, 어음,
신용카드, 외상 판매
(나) 수출인 경우 : 취소불능 신용장에 의한 판매(L/C Base)
(3) 판매전략
| 사업부문 | 구분 | 판 매 전 략 |
|---|---|---|
| 의약품 및 의약외품 |
의약품 | - 해외 거래선을 통한 우수한 효능의 신제품 도입 - 오리지널 제품 위주의 제품군 강화 - 기존 오리지널 제품의 개량신약 개발 - 신약개발을 위한 R&D 투자 강화 - 장단기 육성 품목을 선정하여 품목별 육성전략을 수립 - 주요 일반의약품의 브랜드 강화를 위한 광고 및 마케팅 강화 |
| 의약외품 | - 신제품 출시 광고 및 주력 제품 홍보 강화, 판촉사원의 판촉활동 강화 - 소비자 욕구에 맞는 다양한 제품군 형성 - 적정 물량 조절을 통한 가격관리 강화 |
|
| 건강기능식품 | - 다양한 제품군의 형성으로 유아부터 노년층까지의 구매력 촉진 - 양질의 원료를 사용한 고급화된 제품 생산 및 홍보 - 홈쇼핑 등을 통한 다양한 유통망 활용 |
5. 위험관리 및 파생거래
가. 위험관리조직 및 정책
연결회사는 여러 활동으로 인하여 시장위험(외환위험, 이자율위험, 가격위험), 신용위험 및 유동성위험과 같은 다양한 재무 위험에 노출되어 있습니다. 연결회사의 전반적인 위험관리 정책은 금융시장의 변동성에 초점을 맞추고 있으며 재무성과에 미치는 부정적인 영향을 최소화하는데 중점을 두고 있습니다.
위험관리는 이사회에서 승인한 정책에 따라 이루어지고 있습니다. 이사회는 전반적인 위험관리에 대한 문서화된 정책, 외환위험, 이자율 위험, 신용 위험, 파생금융상품과 비파생금융상품의 이용 및 유동성을 초과하는 투자와 같은 특정 분야에 관한 문서화된 정책을 검토하고 승인합니다.
나. 시장위험
(1) 외환위험
연결회사는 국제적으로 영업활동을 영위하고 있어 외환위험, 특히 주로 유로화와 관련된 환율 변동 위험에 노출되어 있습니다. 외환위험은 인식된 자산과 부채, 해외 사업장에 대한 순투자와 관련하여 발생하고 있습니다.
경영진은 연결회사 내의 회사들이 각각의 기능통화에 대한 외환 위험을 관리하도록 하는 정책을 수립하고 있습니다.
보고기간말 현재 다른 모든 변수가 일정하고 달러, 유로화 및 엔화에 대한 원화 환율이 10% 변동시 연결회사의 세후 이익 및 자본에 미치는 영향은 아래 표와 같습니다.
| (단위 : 원) |
| 구 분 | 세후 이익에 대한 영향 | 자본에 대한 영향 | |||
|---|---|---|---|---|---|
| 당분기 | 전분기 | 당분기 | 전분기 | ||
| 유로화/원 | 상승시 | (60,826,051) | (631,732,059) | (60,826,051) | (631,732,059) |
| 하락시 | 60,826,051 | 631,732,059 | 60,826,051 | 631,732,059 | |
| 미국달러/원 | 상승시 | (53,245,235) | - | (53,245,235) | - |
| 하락시 | 53,245,235 | - | 53,245,235 | - | |
| 일본엔화/원 | 상승시 | (403,818) | - | (403,818) | - |
| 하락시 | 403,818 | - | 403,818 | - | |
(2) 이자율위험
이자율위험은 미래의 시장이자율 변동에 따라 예금 또는 차입금 등에서 발생하는 이자수익 및 이자비용이 변동될 위험으로서 이는 주로 변동 금리부 조건의 예금에서 발생하고 있습니다.
보고기간말 현재 다른 모든 변수가 일정하고 이자율의 0.1% 변동시 연결회사의 세후이익 및 자본에 미치는 영향은 아래 표와 같습니다.
| (단위 : 원) |
| 구 분 | 세후 이익에 대한 영향 | 자본에 대한 영향 | ||
|---|---|---|---|---|
| 당분기 | 전분기 | 당분기 | 전분기 | |
| 상승시 | (63,280,000) | (63,280,000) | (63,280,000) | (63,280,000) |
| 하락시 | 63,280,000 | 63,280,000 | 63,280,000 | 63,280,000 |
(3) 가격위험
연결회사는 연결재무상태표상 기타포괄손익-공정가치금융자산 또는 당기손익-공정가치금융자산으로 분류되는 연결회사 보유 지분증권의 가격위험에 노출되어 있습니다.
연결회사가 보유하고 있는 상장주식은 공개시장에서 거래되고 있으며, NASDAQ 주가지수에 속해 있습니다.
보고기간말 현재 다른 모든 변수가 일정하고 주가지수의 10% 변동시 연결회사의 세후이익 및 자본에 미치는 영향은 아래 표와 같습니다.
| (단위: 원) |
|
지수 |
세후 이익에 대한 영향 |
자본에 대한 영향 |
|||
|---|---|---|---|---|---|
| 당분기 | 전분기 | 당분기 | 전분기 | ||
| NASDAQ |
상승시 |
2,170,785 | 40,714,290 | 90,497,747 | 40,714,290 |
|
하락시 |
(2,170,785) | (40,714,290) | (90,497,747) | (40,714,290) | |
당기손익-공정가치 지분증권의 손익은 당기손익에 영향을 미치고 기타포괄손익-공정가치 지분증권의 손익은 자본에 영향을 미칩니다.
6. 주요계약 및 연구개발활동
6.1 주요계약
가. 계약 총괄표
| 사업부문 | 계약 상대방 | 계약목적 | 대표 품목명 | 체결시기 | 진행 단계 |
| 의약품 및 의약외품 |
Eisai (일본) |
제조/판매 | Selbex (Teprenone) |
2016.07.01 | 제조 판매 중 |
| MEDA/Mylan (독일) |
원료 수입 | Legalon, Tavex, Alaxyl, Spasmolyt |
1993.12.28 | 원료 수입/제조 판매 | |
| 원료 수입 | Thioctacid, Azeptin, Cormelian |
2003.12.11 | 원료 수입/제조 판매 | ||
| 제품 수입 | Dylastine | 2018.05.25 | 수입 판매 중 | ||
| 제품 수입 | Sebivo | 2018.10.26 | 수입 판매 중 | ||
| Baxter (독일) |
제품 수입 | Holoxan Endoxan, Uromitexan |
2013.01.01 | 수입 판매 중 | |
| Pierre Fabre (프랑스) |
제품 수입 원료 수입 |
Navelbine Ixel |
2014.01.01 | 수입 판매 중 | |
| Ferrer (스페인) |
제품 수입 원료 수입 |
Dermofix | 1993.06.02 | 제조 판매 중 | |
| 원료 수입 | Somazina | 2002.03.04 | 제조 판매 중 | ||
| 원료 수입 | Nadixa | 2004.05.17 | 제조 판매 중 | ||
| 제품 수입 |
Repavar Pielato Melagyn |
2016.06.30 | 공급 중단 | ||
| 제품 수입 | Ozanex | 2020.01.10 | 제조 판매 중 | ||
|
Ojer (스페인) |
제품 수입 | Lipovir | 2018.01.29 | 개발 논의 중 | |
| Desitin (독일) |
원료 수입 | Orfil | 1978.03.15 | 제조 판매 중 | |
| 원료 수입 | Timonil | 1994.08.31 | 제조 판매 중 | ||
| Sumitomo Pharma Co., Ltd. (일본) |
원료 수입 | Lonasen (Blonanserin) | 2005.02.28 | 제조 판매 중 | |
| 상표권 계약 | Cetapril | 2015.02.27 | 판매 중단 | ||
| 반제품 수입 | Latuda (Lurasidone HCl) | 2017.04.05 | 제조 판매 중 | ||
| Eurodrug (네덜란드) |
원료 수입 | Fexadin | 1986.07.29 | 제조 판매 중 | |
| Asima | 2000.03.24 | 제조 판매 중 | |||
| 반제품 수입 | Panbesy | 2019.06.01 | 반제품 수입 판매 중 | ||
| Kalbe International Pte. Ltd. (싱가포르) |
제품 수출 | 덱시드정 | 2016.03.03 | 제조 판매 중 (완제 수출) |
|
| 연구개발 | Melior Pharmaceuticals, Inc (미국) |
기술 반환, 수익 배분 및 이전 | MLR-1023 | 2023.12.21 | Biodexa에서 임상2a상 진행 중 (캐나다) |
| Contera Pharma A/S (덴마크) |
기술도입 | JM-010 | 2014.12.12 | 임상 2상 종료 (미국) |
나. 라이선스-아웃(License-out) 계약
| 품목 | 계약 상대방 | 대상 지역 및 계약 내용 | 계약 체결일 | 계약 종료일 | 총 계약 금액 | 수취 금액 | 진행 단계 |
|---|---|---|---|---|---|---|---|
| MLR-1023 | Melior Pharmaceuticals I, Inc (미국) Biodexa Pharmaceuticals PLC (영국) |
MLR-1023 아시아(일본 제외)권리 반환 및 1개의 부광약품제조 특허 라이선스 아웃 (전세계) (주1) |
2023.11.22 | - | Melior사 Benefit의 50% |
Biodexa사 주식 141,771,200주 |
임상 2a상 진행 중 |
(주1) 부광약품이 Melior사에 반환 및 라이선스-아웃한 MLR-1023의 권리/특허를 포함하여 Melior사는 Biodexa사에 MLR-1023의 전세계 권리를 라이선스-아웃하는 조건으로 부광약품과 Melior사는 Benefits Sharing Agreement를 체결하였으며 이에 의해 부광약품은 Melior사의 Benefit의 50%를 수령함
(주2) Biodexa사(나스닥 상장) 보통주 기준 141,771,200주이며, 미국주식예탁증서(American Depositary Receipts) 기준으로는 14,177 ADR에 해당
(1) 품목 : MLR-1023
| 계약 상대방 |
Melior Pharmaceuticals I, Inc (미국) Biodexa Pharmaceuticals PLC (영국) |
| 계약 내용 | 2013.11.20 부광약품이 Melior사로 부터 라이선스 인한 MLR-1023의 일본 외 아시아지역의 권리를 반환하고 부광약품의 특허 1건을 Melior에 라이선스 아웃함. |
| 대상 지역 |
기존 Melior 특허: 일본 외 아시아 부광약품 특허: 전세계 |
| 계약기간 |
계약체결일: 2023년 11월 22일 계약종료일: - |
| 총 계약 금액 | Melior사 Benefit의 50% |
| 수취 금액 | Biodexa사 주식 141,771,200주 |
| 계약조건 | 부광약품이 Melior사로부터 라이선스-인한 권리 반환 및 부광약품의 특허를 라이선스 아웃하는 것을 조건으로 향후 MLR-1023에 의한 Melior사 Benefit의 50%를 부광약품이 수령함. |
| 회계처리방법 | License-out 대가로 받은 Biodexa사 주식을 시가 평가(나스닥 상장)하여 매출 인식 |
| 대상 기술 | 대사장애 및 관련 질환 치료제 |
| 개발 진행 경과 |
제2형당뇨병에 대해 Phase 2a 완료(미국, 한국) 제2형당뇨병에 대해 Phase 2b 완료(미국, 한국) 제1형당뇨병에 대해 Phase 2a 진행(캐나다) |
| 기타사항 | - |
다. 라이선스-인(License-in) 계약
| 품목 | 계약 상대방 | 대상 지역 및 계약 내용 | 계약 체결일 | 계약 종료일 | 총 계약 금액 | 진행 단계 |
| JM-010 |
Contera Pharma ApS (덴마크) |
파킨슨병 환자의 Levodopa induced Dyskinesia 치료제 | 2014.12.12 | (주1) | (주1) |
Phase 1 완료(독일) Phase 2 완료(유럽) |
| MLR-1023 (주2) |
Melior Pharmaceuticals I, Inc (미국) |
제2형당뇨병 | 2013.11.20 | 2023.12.21 | (주1) |
Phase 2a 완료(미국, 한국) Phase 2b 완료(미국, 한국) |
(주1) 미기재 내용(계약 종료일, 총 계약 금액, 계약조건, 지급 금액 등)은 영업기밀에
해당되어 계약 상대방과의 협의에 따른 비공개 원칙에 따라 계약 세부내용은 기재하지 않음
(주2) 부광약품이 Melior사로부터 획득한 MLR-0123의 권리를 반환
(자세한 사항은 라이선스 아웃 내용 참조)
(1) 품목: JM-010
| 계약 상대방 | Contera Pharma A/S (덴마크) |
| 계약 내용 | JM-010에 대한 유럽을 제외한 전세계의 개발 및 판매권 보유 |
| 대상 지역 | 유럽을 제외한 전세계 |
| 계약기간 | 계약체결일 : 2014년 12월 12일 |
| 총 계약 금액 | 계약당사자간 합의에 의거 미공개 |
| 수취 금액 | 계약당사자간 합의에 의거 미공개 |
| 계약조건 | 계약당사자간 합의에 의거 미공개 |
| 회계처리방법 | 기술도입비 지급시점에 무형자산으로 인식 |
| 대상 기술 |
파킨슨병 환자의 Dyskinesia 치료제 (적응증 : 파킨슨병 환자의 파킨슨병 치료제 (Levodopa)에 의한 이상운동증(LID)) |
| 개발 진행 경과 |
- 남아공에서 글로벌 임상 전기 2상 (PoC) 완료 (2015년 11월) - 유럽에서 신제형의 Human pharmacokinetic study 완료 (2016년 09월) - 한국에서 개발단계희귀의약품 지정 (2017년 1월) - 독일/프랑스/스페인 : 임상 2상 승인 완료 및 2019.04월 임상 개시 모임 진행 - 미국: 2020.02월 미 FDA 임상 2상 계획 승인 |
| 기타사항 | 임상 결과를 바탕으로 활용 방안 검토 중 |
(2) 품목: MLR-1023
| 계약 상대방 | Melior Pharmaceuticals, Inc (미국) |
| 계약 내용 | MLR-1023에 대한 한국/중국/아시아 지역의 개발 및 판매권 보유 및 Melior사 Benefit의 50% 소유 |
| 대상 지역 | 한국/중국/아시아 지역외 |
| 계약기간 | 계약체결일 : 2013년 11월 20일 계약종료일 : 2023년 12월 21일 |
| 총 계약 금액 | 계약당사자간 합의에 의거 미공개 |
| 수취 금액 | 계약당사자간 합의에 의거 미공개 |
| 계약조건 | 계약당사자간 합의에 의거 미공개 |
| 회계처리방법 | 기술도입비 지급시점에 무형자산으로 인식 |
| 대상 기술 | 당뇨병 (작용기전: LYN-kinase activator (first in class)) |
| 개발 진행 경과 |
- 미국/한국에서 글로벌 임상 전기 2상 완료 - 미국/한국에서 글로벌 임상 후기 2상 완료 |
| 기타사항 | 부광약품이 Melior사로부터 획득한 MLR-1023의 권리를 반환으로 종료 (자세한 사항은 라이선스 아웃 참조) |
6.2 연구개발활동
가. 연구개발활동의 개요
(1) 연구개발 담당 조직
1. 부광약품(주) 기업부설연구소 : 평가연구팀, 합성연구팀, 제제연구팀 외
2. Contera Pharma A/S(연구개발전문)
3. ProteKt Therapeutics(연구개발전문)
4. JaguAHR Therapeutics(연구개발전문)
(2) 연구개발 인력 현황
연결회사는 박사급 13명, 석사급 30명 등 총 65명의 연구인력을 보유하고 있으며, 그 현황은 다음과 같습니다. (단위 : 명)
| 구분 | 박사 | 석사 | 학사 | 기타 | 합계 |
| 부광약품(주) 연구소 | 3 | 30 | 15 | 1 | 49 |
| Contera Pharma A/S | 9 | - | 6 | - | 15 |
| ProteKt Therapeutics | 1 | - | - | - | 1 |
| JaguAHR Therapeutics | - | - | - | - | - |
| 합계 | 13 | 30 | 21 | 1 | 65 |
(3) 핵심 연구인력
당사의 핵심 연구인력은 다음과 같습니다.
| 직위 | 성명 | 담당업무 | 최종학위 | 주요 경력 |
| 전무 | 김지헌 | 개발담당 | 석사 | 前, (주)GC녹십자 사업개발본부 상무 現, 부광약품(주) 연구개발본부 전무 |
| 이사 | 임진희 | 개발담당 | 석사 | 前, 대웅제약 사업개발본부 팀장 現, 부광약품(주) 연구개발본부 이사 |
(4) 연구개발비용
<연결기준 연구개발비용 현황>
(단위 : 원)
|
구 분 |
제66기 1분기 | 제65기 | 제64기 |
비 고 |
|
|
비용의 성격별 분류 |
원재료비 |
904,255,797 | 4,147,001,560 | 3,584,225,496 |
- |
|
인건비 |
3,081,352,109 | 10,537,451,307 | 10,021,442,737 |
- |
|
|
감가상각비 |
203,175,910 | 1,052,256,573 | 587,119,204 |
- |
|
|
위탁용역비 |
870,065,418 | 9,317,154,967 | 14,753,701,202 |
- |
|
|
기타 |
680,072,294 | 3,333,226,500 | 10,569,839,547 |
- |
|
|
연구개발비용 합계 |
5,738,921,528 | 28,387,090,907 | 39,516,328,186 |
- |
|
|
회계처리 내역 |
판매비와 관리비 |
4,451,754,132 | 23,430,643,358 | 34,551,207,828 |
- |
|
제조경비 |
1,287,167,396 | 4,956,447,549 | 4,965,120,358 |
- |
|
|
개발비(무형자산) |
- | - | - |
- |
|
|
회계처리금액 계 |
5,738,921,528 | 28,387,090,907 | 39,516,328,186 |
- |
|
|
정부보조금 |
- | - | - |
- |
|
|
연구개발비용 합계 |
5,738,921,528 | 28,387,090,907 | 39,516,328,186 |
- |
|
|
연구개발비 / 매출액 비율 [연구개발비용합계÷당기매출액×100] |
12.00% | 17.73% | 31.38% |
- |
|
<별도기준 연구개발비용 현황>
(단위 : 원)
|
구 분 |
제66기 1분기 | 제65기 | 제64기 |
비 고 |
|
|
비용의 성격별 분류 |
원재료비 |
487,152,394 | 2,727,252,877 | 2,620,162,397 |
- |
|
인건비 |
1,850,810,322 | 6,544,303,392 | 6,686,333,048 |
- |
|
|
감가상각비 |
130,584,883 | 396,498,209 | 300,949,009 |
- |
|
|
위탁용역비 |
299,623,873 | 3,375,495,160 | 8,289,359,210 |
- |
|
|
기타 |
464,669,148 | 1,828,296,494 | 2,551,413,666 |
- |
|
|
연구개발비용 합계 |
3,232,840,620 | 14,871,846,132 | 20,448,217,330 |
- |
|
|
회계처리 내역 |
판매비와 관리비 |
1,945,673,224 | 9,915,398,583 | 15,483,096,972 |
- |
|
제조경비 |
1,287,167,396 | 4,956,447,549 | 4,965,120,358 |
- |
|
|
개발비(무형자산) |
- | - | - |
- |
|
|
회계처리금액 계 |
3,232,840,620 | 14,871,846,132 | 20,448,217,330 |
- |
|
|
정부보조금 |
- | - | - |
- |
|
|
연구개발비용 합계 |
3,232,840,620 | 14,871,846,132 | 20,448,217,330 |
- |
|
|
연구개발비 / 매출액 비율 [연구개발비용합계÷당기매출액×100] |
7.37% | 9.44% | 16.34% |
- |
|
나. 연구개발 실적
(1) 개발성공신약
| 구분 | 신약명 | 적응증 | 허가년월 | 허가국가/기관명 | 비고 |
| 신약 | 레보비르 | B형 간염치료제 | 2006.11 | 한국/MFDS | 국내 제11호 신약 |
| 개량신약 | 덱시드 | 당뇨병성신경병증 | 2013.11 | 한국/MFDS | - |
| 신약 | 라투다정 | 조현병, 양극성 우울증 | 2023.11 | 한국/MFDS | 국내 8월 출시 |
- 신약명 : 레보비르, Levovir(제품명: 레보비르캡슐, Clevudine)
| 구분 | 합성신약 |
| 적응증 | 만성B형 간염치료제 |
| 작용기전 | 바이러스 DNA 합성 억제 |
| 제품의 특성 | 간 조직 내에서 오랜 반감기를 가지므로, 투여 중단 후에도 일정 기간 항바이러스 효과가 지속 |
| 진행 경과 | 2006-11-22 국내 허가 |
| 경쟁 제품 | Lamivudine(GSK), Adefovir dipivoxil(GSK), Entecavir(BMS) |
| 시장규모 | B형간염치료제 국내시장 2,846억원(UBIST, 2023년) |
| 기타사항 | 국산 신약 11호 |
- 신약명 : 덱시드, Dexid(제품명: 덱시드정, R-thioctic acid tromethamine)
| 구분 | 개량신약 |
| 적응증 | 당뇨병성 신경병증 치료제 |
| 작용기전 | 산화 스트레스 감소, 신경 세포 보호 |
| 제품의 특성 | 강력한 항산화제로서 인슐린 감수성을 향상시켜 혈당 조절을 보조하며, 병인치료제로 사용 및 증상치료제와 병용 가능 |
| 진행 경과 | 2013-11-21 국내 허가 |
| 경쟁 제품 | Pregabalin(Pfizer), Gabapentin(Pfizer) |
| 시장규모 | Thioctic acid 국내시장 650억원(IQVIA, 2023년) |
| 기타사항 | 이성질체(Thioctic acid)에서 약효성분만을 분리하여 세계 최초로 개발하여 투여용량 및 부작용 감소 |
- 신약명 : 라투다, Latuda(제품명: 라투다정, Lurasidone hydrochloride)
| 구분 | 합성신약 |
| 적응증 | 조현병 치료제 |
| 작용기전 | D2 receptor antagonist, 5-HT2A, 5-HT7 receptor antagonist |
| 제품의 특성 | 조현병 및 양극성 장애 우울 증상을 빠르고 지속적으로 개선시키며, 이상반응(체중증가)이 감소 |
| 진행 경과 |
국내 가교 3상 임상시험 별도 수행 2023-11-22 국내 허가 |
| 경쟁 제품 | Aripiprazole(Otsuka), Paliperidone(Janssen), Risperidone(Janssen) |
| 시장규모 | 조현병치료제 국내시장 1,904억(IQVIA, 2023년) |
| 기타사항 |
미국, 유럽, 캐나다 일본 등 전세계적으로 장기간 사용 경험과 충분한 노출이 있는 제품 Metabolic side effect가 적어 복약 순응도 및 유지 치료에 효과적 |
(2) 진행중인 연구과제
| 연구과제 | 적응증 |
연구 연도 |
진행 경과 | 파트너사/공동개발사 | 개발사 | 비고 | |
| 단계(국가) | 승인년도 | ||||||
| JM-010 | 파킨슨병 환자의 Dyskinesia 치료제 |
2013년 | Phase 1 완료(독일) Phase 2a 완료(남아공) Phase 2 완료(유럽,한국) Phase 2 종료(미국) |
2016년 2015년 2018년 2020년 |
(덴마크) Contera Pharma A/S | (한국) 부광약품(주) (덴마크) Contera Pharma A/S |
- |
| CP-012 | 파킨슨병 환자의 Morning Akinesia (아침무동증) 치료제 |
2013년 | Phase 1a 완료(유럽) Phase 1b 진행(유럽) |
2023년 - |
- | (덴마크) Contera Pharma A/S | - |
- 품목: JM-010
| 적응증 | 파킨슨병 환자의 Dyskinesia 치료제 |
| 작용기전 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 제품의 특성 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 진행 경과 |
- 남아공에서 글로벌 임상 전기 2상 (PoC) 완료 (2015년 11월) - 유럽에서 신제형의 Human pharmacokinetic study 완료 (2016년 9월) - 독일/프랑스/스페인 : 임상 2상 승인 완료 및 2019년 4월 임상 개시 모임 진행 |
| 향후 계획 | - 임상결과를 바탕으로 활용방안을 검토 중 |
| 경쟁 제품 | - |
| 관련 논문 등 | - |
| 시장규모 | Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 기타사항 | 한국에서 개발단계희귀의약품 지정 (2017년 1월) |
- 품목: CP-012
| 적응증 | 파킨슨병 환자의 Morning Akinesia (아침무동증) 치료제 |
| 작용기전 | 개발 초기 단계로 Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 제품의 특성 | 개발 초기 단계로 Pipeline 정보 및 전략 등 노출의 우려로 공개 불가 |
| 진행 경과 | 유럽 임상 1a상 진행 완료 (2023년 9월) 유럽 임상 1b상 진행 중 |
| 향후 계획 | 개발 초기 단계로 예측 불가 |
| 경쟁 제품 | - |
| 관련 논문 등 | - |
| 시장규모 | 개발 초기 단계로 예측 불가 |
| 기타사항 | - |
다. 연구개발부서 조직도(2025.03.31 현재)
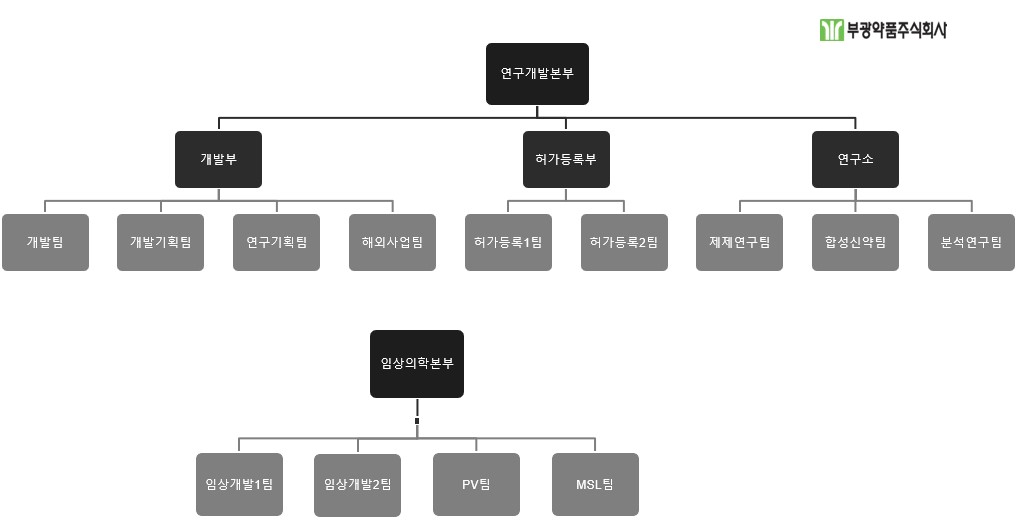 |
|
연구개발조직도 |
7. 기타 참고사항
가. 사업부문별 주요 재무정보
(단위 : 원)
| 당 기 | 매출액 | 영업손익 | 유무형자산 | 감가상각비 및 무형자산상각비 |
| 제약부문 | 48,197,488,268 | 5,946,190,477 | 143,170,918,962 | 186,428,877 |
| 연구개발부문 | - | (3,013,489,090) | 1,519,097,681 | 89,379,235 |
| 연결조정 | (391,050,040) | 81,533,597 | 2,860,232,449 | - |
| 합 계 | 47,806,438,228 | 3,014,234,984 | 147,550,249,092 | 275,808,112 |
(1) 산업의 특성
제약산업은 인간의 생명과 보건에 관련한 고부가가치 산업이자 지식기반 산업으로 원료 및 완제 의약품의 생산과 판매에서부터 신약개발을 위한 연구 등 모든 과정을 포괄하는 첨단 부가가치 산업입니다. 또한 인간의 삶과 직결된 질병을 다루고 있는 사업으로 타 업종 대비 경기변동에 비탄력적인 성향을 보이고 있으며 타 산업에 비해허가, 제조, 유통 단계에서의 직, 간접적인 국가의 규제가 존재하는 사업입니다. 또한타업종에 비해 기술 집약도가 꽤 높은 편이며 미래 성장산업으로 분류되고 있습니다.
최근에는 정밀의학(Precision Medicine), 인공지능(AI) 기반 신약 개발, 지속 가능한 바이오 제조공정 등 다양한 혁신 기술이 접목되면서 산업의 패러다임이 빠르게 변화하고 있습니다.
- 현재 제약산업에서 주목해야 할 4가지 주요 이슈는 아래와 같습니다.
가상의료서비스 (Virtual health delivery)
- 추후 가상의료서비스는 생명과 관련하여 만성 질환으로 고통을 받고 있는 환자 수의 증가, 전 세계적으로 급증하는 인터넷 사용자와 함께 고령화하는 시장 발전에 기여할 것으로 예상됩니다. 이러한 가상의료 서비스로 인하여 장소와 상관없이 실현되는 원격 진료, 치료 서비스로 다양한 문제들을 해결할 수 있습니다. 현재 홈케어 시스템이 잘 도입이 되어있는 스위스는 웨어러블 센서와 기기를 통하여 밀착 모니터링과 원격의료 기술로 담당 의사와 소통을 하며, 필요에 따른 전문간호인력이 직접 방문 진료를 하고 있습니다.
디지털 전환(Digital transformation)
- 제약산업은 스타트업 및 빅테크 회사들과의 협업을 통해 후보물질 발굴부터 임상 시험에 이르는 디지털 솔루션을 공급망 등에 활용하여 신약개발에 들어가는 비용을 절감합니다.
건강형평성(Health equity)
- 건강형평성은 경제 악화 또는 다양한 환경적인 요인들에서부터 영향을 받습니다. 최근 들어 코로나19로 인하여 전세계적으로 고통을 겪었으며 또한 매년 기후변화로 인하여 건강 불평등이 점점 커져가고 있습니다.
지속가능성(Sustainability)
- 지속적으로 변화하는 기후변화로 공중보건 위험의 비용은 2030년까지 매년 20억달러에서 40억달러가 될 것으로 예측됩니다. 이러한 기후변화는 산소와 식량공급 등으로 위험이 이어지며 인류에 큰 정신적 영향을 주며, 탄력적이고 지속이 가능한 의료시스템을 구축할 필요가 있습니다.
(2) 산업의 성장성
- 국내
제약산업은 여러 동향과 요인들에 의해 영향을 받습니다. 고령화 및 만성질환 증가,
보건의료 인프라 개선, 제약 바이오 기술 혁신, 글로벌 제약회사와의 경쟁과 수출 확대, 디지털 헬스케어 증가, 정부 지원 정책, 인공지능과 데이터 분석의 적용으로 인한요인들이 결합하여 국내 제약산업은 새로운 기회와 성장을 앞두고 있습니다. 지속적인 연구 및 혁신, 국제시장 진출은 제약회사의 성장성을 높일 수 있는 기회입니다.
특히, 정부가 바이오를 국가첨단전략산업으로 추가 지정함에 따라 집중 지원과 투자,
적극적인 육성지원이 계획되어 있습니다. 이는 제약바이오산업을 국가 핵심 전략산업으로 집중 육성하겠다는 정부의 의지를 보다 분명히 보여주고 있습니다.
(단위 : 십억원, %)
| 구분 | 의약품총생산 | 제조업GDP | 국내총생산(GDP) | 제조업GDP대비 | GDP대비 |
| 2014 | 18,077 | 422,654 | 1,562,929 | 4.28 | 1.16 |
| 2015 | 18,826 | 441,134 | 1,658,020 | 4.27 | 1.14 |
| 2016 | 20,753 | 458,831 | 1,740,780 | 4.52 | 1.19 |
| 2017 | 21,828 | 494,645 | 1,835,698 | 4.41 | 1.19 |
| 2018 | 22,553 | 504,607 | 1,898,193 | 4.47 | 1.19 |
| 2019 | 23,971 | 485,946 | 1,924,498 | 4.93 | 1.25 |
| 2020 | 28,238 | 479,629 | 1,940,726 | 5.87 | 1.46 |
| 2021 | 27,827 | 527,484 | 2,080,199 | 5.28 | 1.34 |
| 2022 | 31,090 | 554,105 | 2,161,774 | 5.61 | 1.44 |
| 2023 | 32,313 | 543,664 | 2,236,329 | 5.94 | 1.44 |
※ 자료: 2024 식품의약품 통계연보 제26호
- 글로벌
제약회사는 글로벌 산업에서 핵심적인 역할을 하고 있습니다. 제약회사 글로벌 산업의 성장성의 주요 요인은 고령화 인구와 질병 부담 증가, 신약 개발과 기술 혁신, 글로벌 시장 개방, 의료 인프라 개선 및 의료비 지출 증가, 규제 환경의 변화, 파트너십과 인수 합병 활동등이 있습니다. 이러한 요인들로 인하여 제약회사 산업은 계속해서성장하고 변화하고 있습니다. 또한 동시에 경쟁이 치열하며 기술 혁신과 비즈니스 전략이 중요한 역할을 하는 산업입니다.
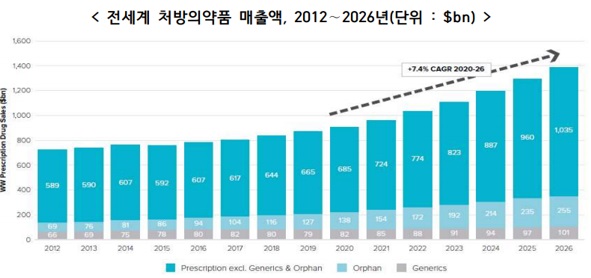 |
|
글로벌 매출추세 |
(3) 경기변동의 특성
[의약품 및 의약외품 부문 & 연구개발 부문]
일반의약품의 경기변동의 특성은 소비자 지출 변동, 의료비용 변동, 신약개발 및 마케팅 등 다양한 요인들이 결합되어 일반의약품 시장의 경기 변동을 형성합니다. 따라서 일반의약품은 일반소비재처럼 경기 변동에 어느정도 민감한 편입니다. 하지만 생활용품 등의 의약외품은 경기변동의 영향을 적게 받고 있습니다.
(4) 계절성
(4-1) [의약품 및 의약외품 부문]
의약품은 제품별로 특성이 다양하므로 계절변화에 따른 비수기, 성수기 구분이 뚜렷하게 나타나는 경우가 있습니다. 이는 특정한 계절이나 시기에 의약품의 수요가 증가하거나 감소하는 것을 의미합니다. 특정한 계절성은 의약품 생산 계획을 수립해야 하는 중요한 측면 중 하나입니다. 계절별 전략을 수립하여 소비자 수요에 효과적으로 대응하는 것이 중요합니다. 의약외품 또한 계절성의 특성이 다양합니다. 계절적 질병
및 증상, 알레르기, 계절적 운동으로 인한 부상 등이 있으며, 이러한 계절적 특성을 이해하고 소비자의 니즈에 신속하게 대응해야 합니다.
(4-2) [연구개발 부문]
계절 변화에 따른 특이사항은 없습니다.
(5) 시장의 안정성
[의약품 및 의약외품 부문 & 연구개발 부문]
식품의약품안전처에 따르면, 2023년 국내의약품 시장규모는 31조 4,513억원을 기록했으며, 전체 제조업 분야 대비 5.64% 수준으로 최근 5년중 가장 큰 비중을 차지했으며, 최근 5년간 연평균 성장률은 8.2%로 같은 기간 국내총생산 성장률(3.8%) 보다 2배 이상 높았습니다.
(6) 경쟁상황
[의약품 및 의약외품 부문 & 연구개발 부문]
제약산업은 다양한 도전과 경쟁에 직면하여 글로벌 의약품 시장에서 경쟁이 치열해질 것으로 예상됩니다. 원인으로는 해외 제약사들의 국내시장 진출에 대한 증가, 수입자본 자유화, 물질특허제 확산, 파이프라인 프로젝트 수용, 한미 FTA 등으로 국제적 압력이 가중되고 있습니다. 국내 제약회사는 이러한 다양한 경쟁 상황에 대응하며, 의료 혁신과 고객만족도를 증진시키는 데에도 노력을 해야 합니다.
(7) 제약바이오기업 매출
(단위 : 억원)
| 구 분 | 2024년 | 2023년 | 2022년 |
| 셀트리온 | 37,092 | 18,734 | 19,375 |
| 삼성바이오로직스 | 34,971 | 29,388 | 24,373 |
| 유한양행 | 20,084 | 18,091 | 17,264 |
| 종근당 | 15,593 | 16,496 | 14,723 |
| 대웅제약 | 12,654 | 12,220 | 11,613 |
| GC녹십자 | 12,760 | 12,098 | 12,449 |
| 한미약품 | 11,141 | 10,969 | 9,820 |
| 광동제약 | 9,748 | 9,171 | 8,505 |
| JW중외제약 | 7,106 | 7,411 | 6,769 |
| 제일약품 | 6,984 | 7,084 | 7,252 |
※ 상기 자료는 전자공시시스템에 공시한 자료를 근거로 작성함(별도 기준)
(8) 회사의 경쟁우위 요소
[의약품 및 의약외품 부문 & 연구개발 부문]
당사는 전국을 대상으로 영업활동을 하고 있으며, 매출 형태별로는 제품매출, 상품매출, 임가공매출, 수출매출, 기술매출로 구분할 수 있습니다. 매출 품목별로는 전문의약품, 일반의약품, 슈퍼나 대형마트 등의 의약외품, 건강기능식품 등으로 구분할 수 있습니다.
- 신약개발
부광약품은 오픈이노베이션을 통한 신약개발을 꾸준히 진행하고 있습니다. 일본 스미토모 파마사에서 도입한 조현병 및 제1형 양극성 장애 우울증 치료제 '라투다'등 다양한 파이프라인에서 의미 있는 성과를 이어 나가고 있습니다.
항정신병 신약 라투다는 국내 판매를 위한 임상 3상이 좋은 결과로 완료되어, 2023년
11월 품목 허가를 승인받았습니다. 새로운 조현병 치료제에 대한 시장 수요를 감안해
신속한 보험 급여 적용이 이루어졌으며, 2024년 8월 1일 자로 의약품 보험급여 적용과 함께 출시되어 처방 판매를 시작했습니다. 2024년 5월에는 대표이사 직속 체제의 CNS 사업본부 신설과 함께 항정신병 신약 라투다의 신속한 시장 투입 및 매출 실현을 통해 CNS 전략 제품군은 전년 대비 42%라는 높을 성장률을 기록했습니다. 새롭게 꾸려진 CNS 사업본부는 양극성 장애 치료제, 항우울제, 조현병 치료제, 불면증 치료제, 뇌전증 치료제 등 정신과 영역과 신경과 영역의 제품을 전반적으로 담당하고 있습니다.
라투다는 기존 비정형 항정신병약물의 부작용인 체중 증가, 혈중 콜레스테롤 및 중성지방 증가, 혈당 증가 등 대사 관련 이상반응의 발생 빈도가 낮아 장기적으로 효과적인 치료가 가능하여 환자들의 삶의 질을 개선시키는 이점이 있습니다. 또한, 라투다는 약물 선택이 매우 제한적인 양극성장애 우울증 환자 및 소아환자에게도 효과적으로 사용할 수 있는 비정형 항정신병 약물로 알려져 있어 조현병 또는 제1형 양극성 장애 우울증 환자들에게 환영받는 치료 옵션이 될 것입니다. 2024년 8월 출시 이후 2025년 3월 말 기준으로 전국 종합병원 101처에서 원내 처방 중이며, 서울대병원, 세브란스병원, 강북삼성병원 등 121처 종합병원에서 약사심의위원회를 통과 완료했습니다. 또한 주요 전문 정신병원에는 81처에서 원내 처방 중이며, 정신과 의원에서는 650처에서 처방 중입니다.
덴마크에 위치한 자회사 콘테라파마에서 임상 시험 진행 중인 파이프라인으로는 CP-012라는 파킨슨병 환자의 아침무동증 치료제가 있습니다. 현재 영국에서 임상1b상을 진행 중에 있으며, 최대 60%의 파킨슨병 환자가 이른 아침의 운동 합병증으로 고통을 받는 것으로 알려져 있으나 현재 마땅한 치료제가 없는 관계로 미충족 수요를 충분히 해결하지 못하는 상황입니다. 이밖에도 콘테라파마는 비임상 단계이지만 카나반병 등 여러가지 희귀질환 파이프라인을 보유하고 있습니다.
카나반병치료제 CP-102는 최근 후보물질 중 CP0014753을 PCC (Pre-Clinical Candidate) 즉 전임상 후보물질로 정식 선정하였고 이에 따라 이 물질을 대상으로 GLP 아급성독성시험 등 후속 실험을 진행할 예정입니다. 콘테라파마는 보유하고 있는 RNA기반 연구 역량을 활용하여 저분자화합물 도출에 관한 연구 플랫폼으로 확장하였으며 이에 따라 저분자화합물 기반의 신규 연구 프로젝트 수종을 진행 중에 있습니다.
또한 임상시험 이전 단계인 파이프라인은 아래와 같습니다.
재규어 테라퓨틱스의 AhR antagonist의 생체효력시험 결과는 금년 하반기 내에 결과를 확인할 수 있을 예정입니다. AhR길항제는 새로운방식의 면역항암제로 글로벌 빅파마 중 일부의 회사에서만 개발을 시작한 분야로, 차별성 및 경쟁력을 갖춘 파이프라인입니다.
프로텍트 테라퓨틱스의 PKR inhibitor는 현재 미국 대학과 희귀신경질환 대상으로 공동연구 진행 중이며, 이와 병행하여 라이선스 아웃 가능성도 탐색 중이기에 결과에 따라 개발 방향을 결정할 예정입니다.
부광약품 자체적으로는 파킨슨병 치료제를 개발 중에 있으며 아주대의료원 정신 및 행동장애 질환 유효성 평가 센터와 공동연구를 시작하는 등 당사의 연구활동을 활성화하고 새로운 연구과제도 검토 중에 있습니다.
부광약품은 글로벌 오픈 이노베이션을 통하여 신약뿐만이 아니라 의료기기, 전자약, AI solution 등 다양한 사업기회를 추구하고 있으며, 자체 R&D 역량 강화를 통해 신약개발과 함께 신속한 신규 제품 포트폴리오를 확보하기 위하여 꾸준히 노력하고 있습니다
(9) 부광약품주식회사 조직도(2025. 03. 31 현재)
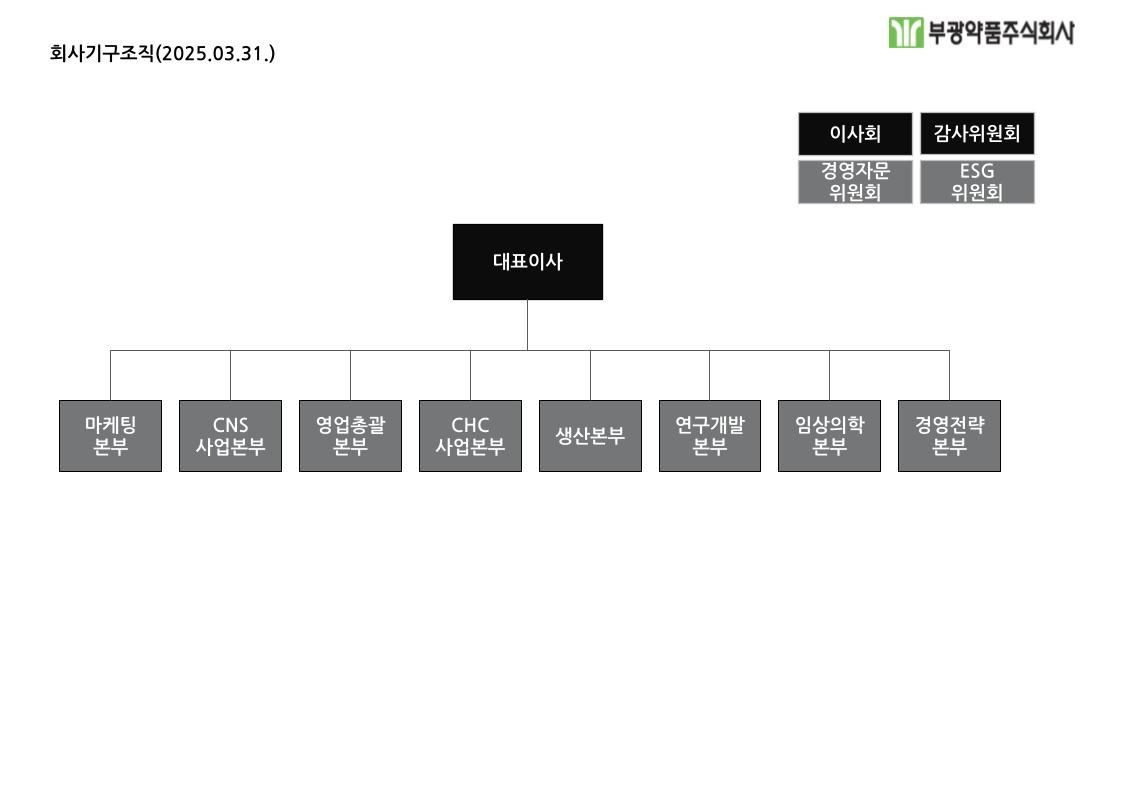 |
|
부광약품 조직도 |
나. 기타 투자의사결정에 필요한 사항
(1) 외부자금조달 요약표
| [국내조달] | (단위 : 백만원) |
| 조 달 원 천 | 기초잔액 | 신규조달 | 상환등감소 | 기말잔액 | 비고 |
| 은 행 | 80,000 | - | - | 80,000 | - |
| 보 험 회 사 | - | - | - | - | - |
| 종합금융회사 | - | - | - | - | - |
| 여신전문금융회사 | - | - | - | - | - |
| 상호저축은행 | - | - | - | - | - |
| 기타금융기관 | - | - | - | - | - |
| 금융기관 합계 | - | - | - | - | - |
| 회사채(공모) | - | - | - | - | - |
| 회사채(사모) | - | - | - | - | - |
| 유 상 증 자(공모) | - | - | - | - | - |
| 유 상 증 자(사모) | - | - | - | - | - |
| 자산유동화(공모) | - | - | - | - | - |
| 자산유동화(사모) | - | - | - | - | - |
| 기 타 | - | - | - | - | - |
| 자본시장 합계 | 80,000 | - | - | 80,000 | - |
| 주주ㆍ임원ㆍ계열회사 차입금 | - | - | - | - | - |
| 기 타 | - | - | - | - | - |
| 총 계 | 80,000 | - | - | 80,000 | - |
(참 고) 당기 중 회사채 총 발행액 : 해 당 사 항 없 음
| [해외조달] | 해 당 사 항 없 음 |
III. 재무에 관한 사항
1. 요약재무정보
가. 연결재무제표
* 표시된 모든 재무정보는 K-IFRS를 적용하여 작성된 (연결)재무제표입니다.
* 제65기 및 제64기 연결재무제표는 외부감사인의 감사(검토)를 받은
재무제표이며, 제66기 1분기 연결재무제표는 외부감사인의 감사(검토)를 받지 않은 재무제표입니다.
| (단위 : 백만원) |
| 구 분 | 제66기 1분기 | 제65기 | 제64기 |
|---|---|---|---|
| (2025년 3월 말) | (2024년 12월 말) | (2023년 12월 말) | |
| [유동자산] | 206,464 | 203,739 | 254,178 |
| ㆍ현금및현금성자산 | 87,813 | 90,091 | 151,227 |
| ㆍ매출채권 | 23,454 | 23,559 | 35,729 |
| ㆍ기타유동금융자산 | 46,571 | 40,994 | 1,647 |
| ㆍ기타유동자산 | 691 | 730 | 1,079 |
| ㆍ유동환불자산 | 5,096 | 5,035 | 6,597 |
| ㆍ재고자산 | 41,667 | 41,667 | 56,832 |
| ㆍ당기법인세자산 | 1,172 | 1,663 | 1,067 |
| [비유동자산] | 166,179 | 169,441 | 174,839 |
| ㆍ당기손익-공정가치 금융자산 | 11,813 | 15,391 | 14,242 |
| ㆍ기타포괄손익-공정가치 금융자산 | 1,117 | 1,327 | 4,460 |
| ㆍ기타비유동금융자산 | 369 | 359 | 1,117 |
| ㆍ유형자산 | 141,161 | 140,417 | 120,981 |
| ㆍ사용권자산 | 1,651 | 1,064 | 1,807 |
| ㆍ무형자산 | 6,389 | 6,275 | 10,056 |
| ㆍ종속기업 및 관계기업투자주식 | 15 | 15 | 12,883 |
| ㆍ순확정급여자산 | 3,664 | 4,593 | 9,293 |
| 자산총계 | 372,643 | 373,180 | 429,017 |
| [유동부채] | 35,243 | 35,398 | 97,544 |
| ㆍ매입채무 | 6,361 | 5,062 | 2,368 |
| ㆍ기타유동금융부채 | 11,185 | 12,216 | 74,555 |
| ㆍ유동환불부채 | 15,035 | 15,198 | 18,464 |
| ㆍ유동리스부채 | 381 | 130 | 218 |
| ㆍ기타유동부채 | 2,183 | 2,792 | 1,582 |
| ㆍ당기법인세부채 | 98 | - | 357 |
| [비유동부채] | 93,658 | 93,637 | 97,208 |
| ㆍ장기차입금 | 79,135 | 79,024 | 78,525 |
| ㆍ기타비유동금융부채 | 425 | 426 | 7,971 |
| ㆍ비유동리스부채 | 643 | 270 | 644 |
| ㆍ이연법인세부채 | 13,455 | 13,917 | 10,068 |
| 부채총계 | 128,901 | 129,035 | 194,752 |
| [지배기업의 소유주지분] | 243,315 | 243,675 | 226,311 |
| ㆍ자본금 | 36,402 | 36,402 | 36,402 |
| ㆍ주식발행초과금 | 2,581 | 2,581 | 2,581 |
| ㆍ기타자본항목 | 37,431 | 37,870 | (38,455) |
| ㆍ이익잉여금 | 166,901 | 166,822 | 225,783 |
| [비지배지분] | 427 | 470 | 7,954 |
| 자본총계 | 243,742 | 244,145 | 234,265 |
| (2025.01.01~ 2025.03.31) |
(2024.01.01~ 2024.12.31) |
(2023.01.01~ 2023.12.31) |
|
| 매출액 | 47,806 | 160,087 | 125,928 |
| 영업이익(손실) | 3,014 | 1,618 | (37,497) |
| 법인세비용차감전순이익(손실) | (323) | (2,970) | (39,569) |
| 연결당기순이익(손실) | (111) | (3,459) | (34,407) |
| 당기순이익(손실)의 귀속 | |||
| 지배기업소유주 | (69) | (2,641) | (31,330) |
| 비지배지분 | (42) | (818) | (3,077) |
| 총포괄손익 | (291) | 9,623 | (37,785) |
| 총포괄손익의 귀속 | |||
| 지배기업소유주지분 | (249) | 10,313 | (34,914) |
| 비지배지분 | (42) | (690) | (2,871) |
| 기본주당순손익(원) | (1) | (39) | (458) |
| 희석주당순손익(원) | (1) | (39) | (458) |
| 연결에 포함된 회사수 | 4 | 4 | 4 |
- 연결대상기업의 변화
| 사업년도 | 연결에 포함된 회사명 | 전기대비 연결에 추가된 회사명 |
전기대비 연결에서 제외된 회사명 |
|---|---|---|---|
| 제 66 기 1분기 | Contera Pharma A/S | - | - |
| 부광메디카(주) | |||
| JaguAHR Therapeutics | |||
| ProteKt Therapeutics | |||
| 제 65 기 | Contera Pharma A/S | JaguAHR Therapeutics | 다이나세라퓨틱스(주) |
| 부광메디카(주) | |||
| JaguAHR Therapeutics | |||
| ProteKt Therapeutics | |||
| 제 64 기 | Contera Pharma A/S | ProteKt Therapeutics | - |
| 부광메디카(주) | |||
| 다이나세라퓨틱스(주) | |||
| ProteKt Therapeutics |
나.재무제표
* 표시된 모든 재무정보는 K-IFRS를 적용하여 작성된 재무제표입니다.
* 제65기 및 제64기 연결재무제표는 외부감사인의 감사(검토)를 받은
재무제표이며, 제66기 1분기 재무제표는 외부감사인의 감사(검토)를 받지 않은재무제표 입니다.
| (단위 : 백만원) |
| 구 분 | 제66기 1분기 | 제65기 | 제64기 |
|---|---|---|---|
| (2025년 3월 말) | (2024년 12월 말) | (2023년 12월 말) | |
| [유동자산] | 196,039 | 190,617 | 232,286 |
| ㆍ현금및현금성자산 | 80,903 | 79,680 | 132,380 |
| ㆍ매출채권 | 21,263 | 22,143 | 35,492 |
| ㆍ기타유동금융자산 | 46,634 | 41,039 | 1,084 |
| ㆍ기타유동자산 | 480 | 387 | 221 |
| ㆍ당기법인세자산 | - | 523 | - |
| ㆍ유동환불자산 | 5,096 | 5,035 | 6,597 |
| ㆍ재고자산 | 41,663 | 41,810 | 56,512 |
| [비유동자산] | 176,191 | 179,462 | 228,250 |
| ㆍ당기손익-공정가치 금융자산 | 12,947 | 16,526 | 17,003 |
| ㆍ기타포괄손익-공정가치 금융자산 | 1,116 | 1,327 | 4,460 |
| ㆍ기타비유동금융자산 | 256 | 245 | 1,022 |
| ㆍ유형자산 | 139,642 | 138,939 | 119,470 |
| ㆍ사용권자산 | 1,010 | 390 | 949 |
| ㆍ무형자산 | 3,527 | 3,413 | 2,902 |
| ㆍ종속기업, 관계기업 및 공동기업투자주식 |
14,035 | 14,035 | 73,163 |
| ㆍ순확정급여자산 | 3,658 | 4,587 | 9,281 |
| 자산총계 | 372,230 | 370,079 | 460,536 |
| [유동부채] | 33,581 | 33,945 | 78,227 |
| ㆍ매입채무 | 6,013 | 4,868 | 2,432 |
| ㆍ기타유동금융부채 | 10,095 | 11,055 | 11,717 |
| ㆍ유동환불부채 | 15,035 | 15,198 | 18,464 |
| ㆍ유동리스부채 | 381 | 130 | 218 |
| ㆍ기타유동부채 | 1,950 | 2,694 | 1,577 |
| ㆍ당기법인세부채 | 107 | - | 382 |
| ㆍ유동파생상품부채 | - | - | 43,437 |
| [비유동부채] | 93,249 | 93,224 | 95,585 |
| ㆍ장기차입금 | 79,135 | 79,024 | 78,525 |
| ㆍ기타비유동금융부채 | 425 | 425 | 7,971 |
| ㆍ비유동리스부채 | 633 | 261 | 636 |
| ㆍ이연법인세부채 | 13,056 | 13,514 | 8,453 |
| 부채총계 | 126,830 | 127,169 | 173,812 |
| ㆍ자본금 | 36,402 | 36,402 | 36,402 |
| ㆍ주식발행초과금 | 2,581 | 2,581 | 2,581 |
| ㆍ기타자본항목 | 49,958 | 50,408 | (17,708) |
| ㆍ이익잉여금 | 156,459 | 153,519 | 265,449 |
| 자본총계 | 245,400 | 242,910 | 286,724 |
|
종속·관계·공동기업 투자주식의 평가방법 |
원가법 | 원가법 | 원가법 |
| (2025.01.01~ 2025.03.31) |
(2024.01.01~ 2024.12.31) |
(2023.01.01~ 2023.12.31) |
|
| 매출액 | 43,850 | 157,607 | 125,176 |
| 영업이익(손실) | 5,935 | 17,004 | (17,173) |
| 법인세비용차감전순이익(손실) | 2,585 | (52,410) | (23,196) |
| 당기순이익(손실) | 2,794 | (55,610) | (19,093) |
| 총포괄손익 | 2,602 | (43,813) | (23,474) |
| 기본주당순손익(원) | 41 | (812) | (279) |
| 희석주당순손익(원) | 41 | (812) | (279) |
2. 연결재무제표
2-1. 연결 재무상태표
|
연결 재무상태표 |
|
제 66 기 1분기말 2025.03.31 현재 |
|
제 65 기말 2024.12.31 현재 |
|
(단위 : 원) |
|
제 66 기 1분기말 |
제 65 기말 |
|
|---|---|---|
|
자산 |
||
|
유동자산 |
206,464,344,289 |
203,739,430,076 |
|
현금및현금성자산 |
87,813,425,211 |
90,091,131,962 |
|
매출채권 |
23,453,671,519 |
23,558,840,664 |
|
기타유동금융자산 |
46,571,100,073 |
40,994,305,512 |
|
기타유동자산 |
691,362,024 |
729,788,247 |
|
유동환불자산 |
5,096,034,069 |
5,034,794,653 |
|
재고자산 |
41,667,177,293 |
41,667,041,774 |
|
당기법인세자산 |
1,171,574,100 |
1,663,527,264 |
|
비유동자산 |
166,179,100,400 |
169,440,881,752 |
|
당기손익-공정가치금융자산 |
11,813,140,836 |
15,391,072,921 |
|
기타포괄손익-공정가치금융자산 |
1,116,649,326 |
1,326,594,797 |
|
기타비유동금융자산 |
369,063,627 |
359,493,896 |
|
유형자산 |
141,160,886,625 |
140,417,070,677 |
|
사용권자산 |
1,651,751,133 |
1,063,671,144 |
|
무형자산 |
6,389,362,467 |
6,275,041,998 |
|
순확정급여자산 |
3,663,673,688 |
4,593,235,777 |
|
관계기업 및 공동기업투자주식 |
14,572,698 |
14,700,542 |
|
자산총계 |
372,643,444,689 |
373,180,311,828 |
|
부채 |
||
|
유동부채 |
35,242,823,152 |
35,398,194,086 |
|
매입채무 |
6,361,471,289 |
5,062,208,013 |
|
기타유동금융부채 |
11,184,617,967 |
12,215,850,152 |
|
기타유동부채 |
2,182,668,576 |
2,791,707,994 |
|
유동환불부채 |
15,035,159,090 |
15,198,233,902 |
|
유동리스부채 |
380,869,869 |
130,194,025 |
|
당기법인세부채 |
98,036,361 |
0 |
|
비유동부채 |
93,658,292,707 |
93,636,537,678 |
|
장기차입금 |
79,135,246,926 |
79,024,183,374 |
|
기타비유동금융부채 |
425,118,311 |
425,118,311 |
|
비유동리스부채 |
642,703,519 |
269,907,950 |
|
이연법인세부채 |
13,455,223,951 |
13,917,328,043 |
|
부채총계 |
128,901,115,859 |
129,034,731,764 |
|
자본 |
||
|
지배기업의 소유지분 |
243,314,893,770 |
243,675,730,043 |
|
자본금 |
36,401,993,000 |
36,401,993,000 |
|
주식발행초과금 |
2,581,379,750 |
2,581,379,750 |
|
기타자본항목 |
37,430,914,727 |
37,869,864,242 |
|
이익잉여금 |
166,900,606,293 |
166,822,493,051 |
|
비지배지분 |
427,435,060 |
469,850,021 |
|
자본총계 |
243,742,328,830 |
244,145,580,064 |
|
자본과부채총계 |
372,643,444,689 |
373,180,311,828 |
2-2. 연결 포괄손익계산서
|
연결 포괄손익계산서 |
|
제 66 기 1분기 2025.01.01 부터 2025.03.31 까지 |
|
제 65 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
(단위 : 원) |
|
제 66 기 1분기 |
제 65 기 1분기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
매출액 |
47,806,438,228 |
47,806,438,228 |
34,393,439,245 |
34,393,439,245 |
|
매출원가 |
26,909,286,016 |
26,909,286,016 |
18,729,677,739 |
18,729,677,739 |
|
매출총이익 |
20,897,152,212 |
20,897,152,212 |
15,663,761,506 |
15,663,761,506 |
|
판매비와관리비 |
13,431,163,096 |
13,431,163,096 |
11,235,648,455 |
11,235,648,455 |
|
경상연구개발비 |
4,451,754,132 |
4,451,754,132 |
6,056,413,596 |
6,056,413,596 |
|
영업이익(손실) |
3,014,234,984 |
3,014,234,984 |
(1,628,300,545) |
(1,628,300,545) |
|
기타수익 |
834,880,563 |
834,880,563 |
53,935,912 |
53,935,912 |
|
기타비용 |
114,951,849 |
114,951,849 |
452,645,264 |
452,645,264 |
|
금융수익 |
1,377,234,387 |
1,377,234,387 |
1,792,414,574 |
1,792,414,574 |
|
금융비용 |
5,433,975,303 |
5,433,975,303 |
1,629,432,392 |
1,629,432,392 |
|
지분법이익(손실) |
(127,844) |
(127,844) |
(261,003,690) |
(261,003,690) |
|
법인세비용차감전순이익 |
(322,705,062) |
(322,705,062) |
(2,125,031,405) |
(2,125,031,405) |
|
법인세비용(수익) |
211,657,631 |
211,657,631 |
433,394,407 |
433,394,407 |
|
분기순이익(손실) |
(111,047,431) |
(111,047,431) |
(2,558,425,812) |
(2,558,425,812) |
|
당기손실의 귀속 |
||||
|
지배기업의 소유주 |
(69,124,001) |
(69,124,001) |
(1,911,483,581) |
(1,911,483,581) |
|
비지배지분 |
(41,923,430) |
(41,923,430) |
(646,942,231) |
(646,942,231) |
|
주당이익 |
||||
|
희석주당이익(손실) (단위 : 원) |
(1) |
(1) |
(28) |
(28) |
|
기본주당이익(손실) (단위 : 원) |
(1) |
(1) |
(28) |
(28) |
|
기타포괄손익 |
(180,026,081) |
(180,026,081) |
497,249,692 |
497,249,692 |
|
당기손익으로 재분류되지 않는항목 |
(191,207,667) |
(191,207,667) |
(114,103,937) |
(114,103,937) |
|
순확정급여자산의 재측정요소 |
(93,439,918) |
(93,439,918) |
(114,103,937) |
(114,103,937) |
|
유형자산재평가손익 |
68,299,119 |
68,299,119 |
0 |
0 |
|
기타포괄손익-공정가치금융자산 평가손익 |
(166,066,868) |
(166,066,868) |
0 |
0 |
|
후속적으로 당기손익으로 재분류되는 항목 |
11,181,586 |
11,181,586 |
611,353,629 |
611,353,629 |
|
해외사업환산손익 |
11,181,586 |
11,181,586 |
611,353,629 |
611,353,629 |
|
총포괄손익 |
(291,073,512) |
(291,073,512) |
(2,061,176,120) |
(2,061,176,120) |
|
포괄손익의 귀속 |
||||
|
지배기업의 소유주 |
(248,658,551) |
(248,658,551) |
(1,571,290,429) |
(1,571,290,429) |
|
비지배지분 |
(42,414,961) |
(42,414,961) |
(489,885,691) |
(489,885,691) |
2-3. 연결 자본변동표
|
연결 자본변동표 |
|
제 66 기 1분기 2025.01.01 부터 2025.03.31 까지 |
|
제 65 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
(단위 : 원) |
|
자본 |
|||||||
|---|---|---|---|---|---|---|---|
|
지배기업의 소유주에게 귀속되는 지분 |
비지배지분 |
자본 합계 |
|||||
|
자본금 |
주식발행초과금 |
기타자본항목 |
이익잉여금 |
지배기업의 소유주에게 귀속되는 지분 합계 |
|||
|
2024.01.01 (기초자본) |
36,401,993,000 |
2,581,379,750 |
(38,455,306,453) |
225,783,289,764 |
226,311,356,061 |
7,953,316,184 |
234,264,672,245 |
|
분기순이익(손실) |
0 |
0 |
0 |
(1,911,483,581) |
(1,911,483,581) |
(646,942,231) |
(2,558,425,812) |
|
순확정급여자산의 재측정요소 |
0 |
0 |
0 |
(114,103,937) |
(114,103,937) |
0 |
(114,103,937) |
|
기타포괄손익-공정가치금융자산 평가손익 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
해외사업환산손익 |
0 |
0 |
824,146,334 |
0 |
824,146,334 |
157,056,539 |
981,202,873 |
|
유형자산재평가손익 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
분기총포괄손익 |
0 |
0 |
824,146,334 |
(2,025,587,518) |
(1,201,441,184) |
(489,885,692) |
(1,691,326,876) |
|
이익소각 |
0 |
0 |
50,784,456,419 |
(50,784,456,419) |
0 |
0 |
0 |
|
소유주와의 거래총액 |
0 |
0 |
50,784,456,419 |
(50,784,456,419) |
0 |
0 |
0 |
|
2024.03.31 (기말자본) |
36,401,993,000 |
2,581,379,750 |
13,153,296,300 |
172,973,245,827 |
225,109,914,877 |
7,463,430,492 |
232,573,345,369 |
|
2025.01.01 (기초자본) |
36,401,993,000 |
2,581,379,750 |
37,869,864,242 |
166,822,493,051 |
243,675,730,043 |
469,850,021 |
244,145,580,064 |
|
분기순이익(손실) |
0 |
0 |
(69,124,001) |
(69,124,001) |
(41,923,430) |
(111,047,431) |
|
|
순확정급여자산의 재측정요소 |
0 |
0 |
(93,439,918) |
(93,439,918) |
0 |
(93,439,918) |
|
|
기타포괄손익-공정가치금융자산 평가손익 |
0 |
(209,945,471) |
0 |
(209,945,471) |
0 |
(209,945,471) |
|
|
해외사업환산손익 |
0 |
11,673,117 |
0 |
11,673,117 |
(491,531) |
11,181,586 |
|
|
유형자산재평가손익 |
0 |
(240,677,161) |
240,677,161 |
0 |
0 |
0 |
|
|
분기총포괄손익 |
0 |
(438,949,515) |
78,113,242 |
(360,836,273) |
(42,414,961) |
(403,251,234) |
|
|
이익소각 |
0 |
0 |
0 |
0 |
0 |
0 |
|
|
소유주와의 거래총액 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
2025.03.31 (기말자본) |
36,401,993,000 |
2,581,379,750 |
37,430,914,727 |
166,900,606,293 |
243,314,893,770 |
427,435,060 |
243,742,328,830 |
2-4. 연결 현금흐름표
|
연결 현금흐름표 |
|
제 66 기 1분기 2025.01.01 부터 2025.03.31 까지 |
|
제 65 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
(단위 : 원) |
|
제 66 기 1분기 |
제 65 기 1분기 |
|
|---|---|---|
|
영업활동현금흐름 |
7,244,497,973 |
12,745,375,842 |
|
분기순이익(손실) |
(111,047,431) |
(2,558,425,812) |
|
조정항목 |
5,426,361,493 |
2,005,998,294 |
|
퇴직급여 |
841,537,525 |
662,434,725 |
|
경상개발비 |
0 |
143,153,759 |
|
법인세비용(수익) |
(211,657,631) |
433,394,407 |
|
감가상각비 |
918,795,392 |
777,382,011 |
|
무형자산상각비 |
87,591,651 |
7,350,482 |
|
사용권자산상각비 |
153,164,292 |
172,746,166 |
|
대손상각비(환입) |
(10,899,336) |
(466,776,665) |
|
재고자산평가손실 |
44,632,967 |
226,041,222 |
|
유형자산처분이익 |
(361,644,406) |
(3,969,312) |
|
유형자산처분손실 |
3,000 |
0 |
|
이자비용 |
1,017,834,745 |
1,537,303,776 |
|
당기손익-공정가치금융자산의 평가이익 |
(337,559,039) |
(343,840,430) |
|
당기손익-공정가치금융자산의 평가손실 |
4,246,789,656 |
41,784,728 |
|
지분법손익 |
127,844 |
261,003,690 |
|
이자수익 |
(1,034,774,822) |
(1,437,884,547) |
|
외화환산이익 |
1,279,793 |
(5,684,396) |
|
외화환산손실 |
71,139,862 |
1,558,678 |
|
순운전자본의 변동 |
773,420,325 |
12,532,330,719 |
|
매출채권의 감소 |
151,056,379 |
11,865,898,610 |
|
기타유동금융자산의 감소(증가) |
(10,228,044) |
(90,779,396) |
|
기타유동자산의 감소(증가) |
50,390,127 |
10,346,968 |
|
재고자산의 감소 |
(118,986,809) |
4,016,046,409 |
|
매입채무의 증가(감소) |
1,193,135,516 |
(60,925,401) |
|
기타유동금융부채의 증가(감소) |
371,511,085 |
(3,937,121,912) |
|
기타유동부채의 증가(감소) |
(609,039,418) |
546,760,888 |
|
순확정급여자산의 증가(감소) |
(30,104,283) |
896,279,054 |
|
환불자산의 감소(증가) |
(61,239,416) |
721,953,719 |
|
환불부채의 증가(감소) |
(163,074,812) |
(1,436,128,220) |
|
이자의 수취 |
751,915,974 |
1,460,865,931 |
|
법인세의 지급 |
403,847,612 |
(695,393,290) |
|
투자활동현금흐름 |
(8,487,911,922) |
(946,149,194) |
|
기타유동금융자산의 감소(증가) |
(5,000,000,000) |
0 |
|
기타비유동금융자산의 감소(증가) |
(4,597,768) |
1,994,323 |
|
기타비유동금융자산의 취득 |
(10,000,000) |
0 |
|
당기손익-공정가치금융자산의 취득 |
(331,298,532) |
(902,641,052) |
|
유형자산의 취득 |
(2,038,903,502) |
(45,502,465) |
|
유형자산의 처분 |
797,500,000 |
0 |
|
무형자산의 취득 |
(1,900,612,120) |
0 |
|
재무활동현금흐름 |
(995,138,304) |
(1,135,551,294) |
|
단기차입금의 감소 |
0 |
(10,000,000,000) |
|
단기차입금의 증가 |
0 |
10,000,000,000 |
|
리스부채의 상환 |
(95,218,750) |
(109,526,132) |
|
이자의 지급 |
(899,919,554) |
(1,026,025,162) |
|
환율변동효과 반영전 현금및현금성자산의 순증가 |
(2,238,552,253) |
10,663,675,354 |
|
현금및현금성자산에 대한 환율변동효과 |
(39,154,498) |
568,571,336 |
|
현금및현금성자산의 순증가 |
(2,277,706,751) |
11,232,246,690 |
|
기초현금및현금성자산 |
90,091,131,962 |
151,227,173,290 |
|
분기말현금및현금성자산 |
87,813,425,211 |
162,459,419,980 |
3. 연결재무제표 주석
| 제 66 기 1분기 : 2025년 1월 1일부터 2025년 3월 31일까지 |
| 제 65 기 1분기 : 2024년 1월 1일부터 2024년 3월 31일까지 |
| 부광약품주식회사와 그 종속기업 |
1. 일반 사항
부광약품주식회사(이하 "회사")와 그 종속기업(이하 회사와 종속기업을 "연결회사")은 의약품 제조 및 판매를 주요 사업으로 하고 있습니다. 연결회사의 본사는 서울시 동작구에 소재하고 있으며 경기도 안산에 공장을 두고 있습니다.
당분기말 현재 자본금은 36,402백만원이며, 주요 주주 현황은 다음과 같습니다.
| 주 주 | 보유 주식 수 | 지분율(%) | 비고 |
|---|---|---|---|
| OCI홀딩스 주식회사 | 7,747,934 | 11.32 | 최대주주 |
| 김동연 | 7,053,266 | 10.30 | - |
| 국민연금공단 | 473,991 | 0.69 | - |
| 기타 | 53,179,480 | 77.69 | - |
| 합 계 | 68,454,671 | 100 |
1.1 종속기업 현황
| 종속기업 | 소재지 | 지배지분율(%) | 결산월 | 업종 | |
| 당분기말 | 전기말 | ||||
| Contera Pharma A/S | 덴마크 | 99.33 | 99.33 | 12월 | 의약품 연구 및 개발 |
| 부광메디카(주) | 대한민국 | 100 | 100 | 12월 | 완제 의약품 제조 및 의약품 도매업 |
| ProteKt Therapeutics | 이스라엘 | 97.24 | 97.24 | 12월 | 의약품 연구 및 개발 |
| JaguAHR Therapeutics | 싱가포르 | 75.02 | 75.02 | 12월 | 의약품 연구 및 개발 |
1.2 종속기업 요약 재무정보
| (단위 : 원) |
| 당분기말 | 자산 | 부채 | 자본 | 매출 | 분기순손익 | 분기총포괄손익 |
| Contera Pharma A/S | 9,363,329,158 | 995,334,110 | 8,367,995,048 | - | (2,847,013,840) | (2,761,599,944) |
| 부광메디카(주) | 3,030,981,300 | 676,109,255 | 2,354,872,045 | 4,347,747,704 | 10,393,184 | 11,154,481 |
| ProteKt Therapeutics | 251,280,522 | 4,765,808,925 | (4,514,528,403) | - | (85,284,216) | (139,746,237) |
| JaguAHR Therapeutics | 246,808,885 | 1,397,320,385 | (1,150,511,500) | - | (82,226,366) | (80,462,176) |
| (단위 : 원) |
| 전기말 | 자산 | 부채 | 자본 | 매출 | 분기순손익 | 분기총포괄손익 |
| Contera Pharma A/S | 12,523,314,397 | 1,393,719,405 | 11,129,594,992 | - | (2,984,510,743) | (2,227,869,358) |
| 부광메디카(주) | 2,715,157,520 | 371,439,956 | 2,343,717,564 | 691,768,623 | (18,335,814) | (18,474,638) |
| 다이나세라퓨틱스(주)(*1) | - | - | - | - | (44,536,771) | (44,536,771) |
| ProteKt Therapeutics | 355,529,643 | 4,730,311,809 | (4,374,782,166) | - | (478,781,351) | (624,069,107) |
| JaguAHR Therapeutics(*2) | 351,629,939 | 1,421,679,263 | (1,070,049,324) | - | - | - |
(*1) 다이나세라퓨틱스㈜의 당기순손익 및 총포괄손익은 청산일까지의 금액입니다.
(*2) JaguAHR Therapeutics의 당기순손익 및 총포괄손익은 지배력 획득일 이후의 금액입니다.
2. 중요한 회계정책
다음은 연결재무제표 작성에 적용된 중요한 회계정책입니다. 이러한 정책은 별도의 언급이 없다면, 표시된 회계기간에 계속적으로 적용됩니다.
2.1 연결재무제표 작성 기준
연결회사의 연결재무제표는 한국채택국제회계기준(이하 기업회계기준)에 따라 작성되었습니다. 한국채택국제회계기준은 국제회계기준위원회("IASB")가 발표한 기준서와 해석서 중 대한민국이 채택한 내용을 의미합니다.
연결재무제표는 다음을 제외하고는 역사적 원가에 기초하여 작성하였습니다.
- 특정 금융자산과 금융부채, 공정가치로 측정하는 특정 유형자산
- 확정급여제도와 공정가치로 측정하는 사외적립자산, 기타장기종업원급여부채
한국채택국제회계기준은 연결재무제표 작성시 중요한 회계추정의 사용을 허용하고 있으며, 회계정책을 적용함에 있어 경영진의 판단을 요구하고 있습니다. 보다 복잡하고 높은 수준의 판단이 필요한 부분이나 중요한 가정 및 추정이 필요한 부분은 주석 3에서 설명하고 있습니다.
2.2 회계정책과 공시의 변경
2.2.1 연결회사가 채택한 제ㆍ개정 기준서 및 해석서
연결회사가 2025년 1월 1일 이후 개시하는 회계기간부터 적용한 제ㆍ개정 기준서 및 해석서는 다음과 같습니다.
(1) 기업회계기준서 제1021호 '환율변동효과' 및 기업회계기준서 제1101호 '한국채택국제회계기준의 최초채택'(개정) - 교환가능성 결여
동 개정사항은 회계목적상 다른 통화와 교환이 가능하다고 보는 상황에 대해 정의하고, 다른 통화와의 교환가능성 평가, 교환가능성이 결여된 경우 사용할 현물환율 추정 및 공시 요구사항을 명확히 합니다. 다른 통화와 교환이 가능하지 않다면 측정일에 현물환율을 추정해야 하며, 관측 가능한 환율을 조정 없이 사용하거나 다른 추정기법을 사용하도록 하고 있습니다. 해당 기준서의 개정으로 인하여 연결재무제표에 미치는 유의적인 영향은 없습니다.
2.2.2 연결회사가 적용하지 않은 제ㆍ개정 기준서 및 해석서
제정 또는 공표되었으나 시행일이 도래하지 않아 적용하지 아니한 제ㆍ개정 기준서 및 해석서는 다음과 같습니다.
(1) 기업회계기준서 제1109호 '금융상품'과 제1107호 '금융상품 : 공시'(개정) - 금융상품 분류와 측정
동 개정사항은 전자지급시스템을 사용하여 금융부채를 결제할 때의 금융부채의 결제일 전 이행과 관련된 조건, 계약상 현금흐름이 기본대여계약과 일관되는지 평가할 때고려해야 할 이자 및 우발사건 특성, 비소구 특성을 가진 금융자산, 계약상 연계된 금융상품의 특성을 명확히 합니다. 그리고 기타포괄손익-공정가치로 지정된 지분상품에 대한 투자와 계약상 현금흐름의 시기나 금액을 변경할 수 있는 계약조건에 대한 추가적인 공시 요구사항을 포함합니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도의 개시일 이후 소급적으로 적용되며 조기적용이 허용됩니다. 연결회사는 동 개정으로 인한 연결재무제표의 영향을 검토 중에 있습니다.
(2) 기업회계기준서 제1109호 '금융상품' - 리스부채의 제거 회계처리 및 거래가격의정의
동 개정사항은 리스부채 제거시 발생하는 차손익을 당기손익으로 인식해야 함을 명확히 하였습니다. 또한 거래가격의 정의를 기업회계기준서 제1115호와 일관되도록 개정하였습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다. 연결회사는 동 개정으로 인한 연결재무제표의 영향을 검토 중에 있습니다.
(3) 기업회계기준서 제1110호 '연결재무제표' - 사실상의 대리인 결정
동 개정사항은 사실상 대리인의 판단과 관련한 기준서 제1110호의 표현을 개정하여 기준서 문단 간의 불일치를 해소하였습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다. 연결회사는 동 개정으로 인한 연결재무제표의 영향을 검토 중에 있습니다.
(4) 기업회계기준서 제1101호 '한국채택국제회계기준의 최초채택' - 위험회피회계 적용
동 개정사항은 위험회피회계의 적용조건을 기업회계기준서 제1109호 '금융상품'의 구체적인 문단을 참조하도록 명시하고 관련 용어를 일치시켰습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다. 연결회사는 동 개정으로 인한 연결재무제표의 영향을 검토 중에 있습니다.
(5) 기업회계기준서 제1107호 '금융상품 : 공시' - 제거 손익
동 개정사항은 공정가치 측정과 관련하여 기업회계기준서 제1113호 '공정가치'를 참조하도록 하고 관련 용어를 일치시켰습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다. 연결회사는 동 개정으로 인한 연결재무제표의 영향을 검토 중에 있습니다.
(6) 기업회계기준서 제1007호 '현금흐름표' - 원가법
동 개정으로 '원가법'이라는 용어를 삭제하고 이를 '원가'로 대체하였습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다. 연결회사는 동 개정으로 인한 연결재무제표의 영향을 검토 중에 있습니다.
2.3 회계정책
분기연결재무제표의 작성에 적용된 유의적 회계정책과 계산방법은 주석 2에서 설명하는 제ㆍ개정 기준서의 적용으로 인한 변경 사항 및 아래 문단에서 설명하는 사항을제외하고는 전기 연결재무제표 작성에 적용된 회계정책이나 계산방법과 동일합니다
.
(1) 법인세비용
중간기간의 법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균연간법인세율, 즉 추정평균연간유효법인세율을 중간기간의 세전이익에 적용하여 계산합니다.
3. 중요한 회계추정 및 가정
연결재무제표 작성에는 미래에 대한 가정 및 추정이 요구되며 경영진은 연결회사의 회계정책을 적용하기 위해 판단이 요구됩니다. 추정 및 가정은 지속적으로 평가되며,과거 경험과 현재의 상황에 비추어 합리적으로 예측가능한 미래의 사건을 고려하여 이루어집니다. 회계추정의 결과가 실제 결과와 동일한 경우는 드물 것이므로 중요한 조정을 유발할 수 있는 유의적인 위험을 내포하고 있습니다.
분기연결재무제표 작성시 사용된 중요한 회계추정 및 가정은 법인세비용을 결정하는데 사용된 추정의 방법을 제외하고는 전기 연결재무제표 작성에 적용된 회계추정 및 가정과 동일합니다.
4. 공정가치
4.1 금융상품 종류별 공정가치
금융상품의 종류별 장부금액 및 공정가치는 다음과 같습니다.
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 | ||
| 장부금액 | 공정가치 | 장부금액 | 공정가치 | |
| 금융자산 | ||||
| 당기손익-공정가치금융자산 | 11,813,140,836 | 11,813,140,836 | 15,391,072,921 | 15,391,072,921 |
| 기타포괄손익-공정가치금융자산 | 1,116,649,326 | 1,116,649,326 | 1,326,594,797 | 1,326,594,797 |
4.2 금융상품 공정가치 서열 체계
공정가치로 측정되는 금융상품은 공정가치 서열체계에 따라 구분되며 정의된 수준들은 다음과 같습니다.
- 측정일에 동일한 자산이나 부채에 대해 접근할 수 있는 활성시장의(조정하지 않은) 공시가격 (수준 1)
- 수준 1의 공시가격 외에 자산이나 부채에 대해 직접적으로나 간접적으로 관측할 수 있는 투입변수 (수준 2)
- 자산이나 부채에 대한 관측할 수 없는 투입변수 (수준 3)
공정가치로 측정되는 금융상품의 공정가치 서열체계 구분은 다음과 같습니다.
| (단위 : 원) |
| 구 분 | 당분기말 | |||
| 수준 1 | 수준 2 | 수준 3 | 합 계 | |
| 공정가치로 측정되는 금융자산 | ||||
| 당기손익-공정가치금융자산 | 27,443,553 | - | 11,785,697,283 | 11,813,140,836 |
| 기타포괄손익-공정가치금융자산 | 1,116,649,326 | - | - | 1,116,649,326 |
| (단위 : 원) |
| 구 분 | 전기말 | |||
| 수준 1 | 수준 2 | 수준 3 | 합 계 | |
| 공정가치로 측정되는 금융자산 | ||||
| 당기손익-공정가치금융자산 | 84,402,770 | - | 15,306,670,151 | 15,391,072,921 |
| 기타포괄손익-공정가치금융자산 | 1,326,594,797 | - | - | 1,326,594,797 |
4.3 반복적인 공정가치 측정치의 서열체계 수준 간 이동
연결회사는 공정가치 서열체계의 수준 간 이동을 보고기간 말에 인식합니다. 당분기 중 반복적인 측정치의 수준 1과 수준 2간의 대체는 없으며, 반복적인 측정치의 수준 3의 변동 내역은 다음과 같습니다.
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 | ||
| 당기손익-공정가치 금융자산 |
기타포괄손익-공정가치 금융자산 |
당기손익-공정가치 금융자산 |
기타포괄손익-공정가치 금융자산 |
|
| 기초금액 | 15,306,670,151 | - | 13,685,034,866 | 4,459,545,887 |
| 연결범위 변동 | - | - | - | - |
| 총손익 | ||||
| 당기손익인식액 | (3,852,271,400) | - | 343,840,430 | - |
| 기타포괄손익인식액 | - | - | - | - |
| 종속회사편입 | - | - | - | |
| 매입금액 | 331,298,532 | - | 902,641,052 | - |
| 매도금액 | - | - | - | |
| 분기말금액 | 11,785,697,283 | - | 14,931,516,348 | 4,459,545,887 |
| (단위 : 원) |
| 구 분 | 기타금융부채 | |
|---|---|---|
| 당분기 | 전분기 | |
| 기초금액 | - | 7,753,272,340 |
| 설정 | - | 143,153,759 |
| 평가손익 | - | - |
| 외화환산 | - | - |
| 분기말금액 | - | 7,896,426,099 |
4.4 가치평가기법 및 투입변수
당분기말 및 전기말 현재 연결회사는 공정가치 서열체계에서 수준 3으로 분류되는 반복적인 공정가치측정치에 대해 다음의 가치평가기법을 사용하고 있습니다.
| (단위 : 원) |
| 구 분 | 당분기말 | ||||
|---|---|---|---|---|---|
| 공정가치 | 수준 | 가치평가기법 |
투입변수 |
수준3 투입변수 범위 |
|
| 당기손익-공정가치금융자산 | |||||
| 시장성없는 지분증권 및 수익증권 | 11,497,015,459 | 3 | 순자산가치법 취득원가법 |
- |
NA |
| 전환사채 | 288,681,824 | 3 | 취득원가법 | - |
NA |
| (단위 : 원) |
| 구 분 | 전기말 | ||||
|---|---|---|---|---|---|
| 공정가치 | 수준 | 가치평가기법 |
투입변수 |
수준3 투입변수 범위 |
|
| 당기손익-공정가치금융자산 | |||||
| 시장성없는 지분증권 및 수익증권 | 15,017,988,327 | 3 | 순자산가치법 취득원가법 |
- |
NA |
| 전환사채 | 288,681,824 | 3 | 취득원가법 | - |
NA |
4.5 수준 3으로 분류된 공정가치 측정치의 가치평가과정
연결회사의 재무부서는 재무보고 목적의 공정가치의 측정을 담당하고 있으며 이러한공정가치 측정치는 수준 3으로 분류되는 공정가치 측정치를 포함하고 있습니다. 연결회사의 재무부서는 공정가치 측정내역 및 결과에 대하여 연결회사의 경영진에게 매 분기 보고하고 있습니다.
4.6 수준 3으로 분류된 반복적인 공정가치 측정치의 민감도 분석
금융상품의 민감도 분석은 통계적 기법을 이용한 관측 불가능한 투입변수의 변동에따른 금융상품의 가치 변동에 기초하여 유리한 변동과 불리한 변동으로 구분하여 이루어집니다. 그리고 공정가치가 두 개 이상의 투입변수에 영향을 받는 경우에는 가장유리하거나 또는 가장 불리한 금액을 바탕으로 산출됩니다.
5. 현금및현금성자산
|
(단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
|
현금 |
1,000,000 | 1,000,000 |
|
보통예금(*) |
9,122,425,211 | 9,551,622,891 |
|
RP |
13,690,000,000 | 20,538,509,071 |
|
정기예금 |
65,000,000,000 | 60,000,000,000 |
|
합 계 |
87,813,425,211 | 90,091,131,962 |
(*) 당분기말 보통예금 중 미결제타점권으로 사용제한이 되어있는 예금은 없습니다.
6. 매출채권
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 매출채권 | 23,580,209,541 | 23,703,786,336 |
| 차감 : 손실충당금 | (126,538,022) | (144,945,672) |
| 매출채권(순액) | 23,453,671,519 | 23,558,840,664 |
7. 환불자산과 환불부채
| (단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
|---|---|---|
| 환불자산 - 예상 고객반품 | 5,096,034,069 | 5,034,794,653 |
|
환불부채 - 반품충당부채 |
14,981,348,880 | 15,143,382,091 |
| 환불부채 - 수금할인 변동대가 | 53,810,210 | 54,851,811 |
8. 기타금융자산
|
(단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
||
|
유동 |
비유동 |
유동 |
비유동 |
|
| 단기금융상품 | 45,000,000,000 | - | 40,000,000,000 | - |
|
미수금 |
688,934,243 | - | 394,105,010 | - |
|
미수수익 |
882,165,830 | - | 600,200,502 | - |
|
장기금융상품(*) |
- | 42,500,000 | - | 42,500,000 |
|
보증금 |
- | 350,122,508 | - | 335,524,740 |
|
현재가치할인차금 |
- | (23,558,881) | - | (18,530,844) |
|
합 계 |
46,571,100,073 | 369,063,627 | 40,994,305,512 | 359,493,896 |
(*) 장기금융상품 중 3백만원은 당좌개설보증금이며, 사용이 제한되어 있습니다.
상각후원가로 측정하는 기타금융자산은 모두 신용위험이 낮은 것으로 판단되며, 따라서 손실충당금은 12개월 기대신용손실로 인식하였습니다. 기타금융자산은 채무불이행 위험이 낮고 단기간 내에 계약상 현금흐름을 지급할 수 있는 발행자의 충분한 능력이 있는 경우 신용위험이 낮은 것으로 간주합니다. 기타금융자산과 관련하여 연결회사가 보유하고 있는 담보는 없습니다.
9. 기타유동자산
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 |
| 선급금 | 272,944,099 | 331,495,303 |
| 선급비용 | 418,417,925 | 398,292,944 |
| 합 계 | 691,362,024 | 729,788,247 |
10. 재고자산
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 상품 | 4,586,213,502 | 5,201,680,441 |
| 제품 | 13,584,272,622 | 13,573,873,054 |
| 재공품 | 8,659,358,642 | 6,960,060,684 |
| 원재료 | 16,090,807,224 | 17,299,121,850 |
| 저장품 | 4,905,778 | 9,788,140 |
| 미착품 | 1,839,236,581 | 1,675,501,694 |
| 평가손실충당금 | (3,097,617,056) | (3,052,984,089) |
| 합 계 | 41,667,177,293 | 41,667,041,774 |
당분기 중 연결회사는 재고자산평가손실 45백만원(전분기 : 226백만원 손실)을 인식하였으며, 손익계산서의 '매출원가'에 가산되었습니다.
11. 당기손익-공정가치금융자산
(1) 당기손익-공정가치금융자산
|
(단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
| 지분상품 | ||
| CytoSite BioPharma Inc. | 1,720,050,057 | 1,720,050,057 |
| Biodexa Pharmaceuticals | 27,443,553 | 84,402,770 |
| 수익증권 | ||
| TVM Life Science Ventures Ⅶ, L.P | 5,760,889,485 | 9,950,719,924 |
| TVM Life Science Innovation II SCSp | 3,752,987,306 | 3,084,129,735 |
| KDB 오픈이노베이션 제2호 | 263,088,611 | 263,088,611 |
| 채무증권 | ||
| CytoSite BioPharma Inc. | 288,681,824 | 288,681,824 |
|
합 계 |
11,813,140,836 | 15,391,072,921 |
(2) 당기손익으로 인식된 금액
|
(단위 : 원) |
|
구 분 |
당분기 |
전분기 |
|
당기손익-공정가치금융자산 평가손익 |
(3,909,230,617) | 302,055,702 |
| 합 계 | (3,909,230,617) | 302,055,702 |
(3) 연결회사는 당기손익-공정가치금융자산에 대한 신용위험에 노출되어 있습니다. 당분기말 현재 연결회사의 관련 최대노출금액은 해당 채무증권의 장부금액(당분기말 : 289백만원, 전기말 : 289백만원)입니다.
12. 기타포괄손익-공정가치금융자산
|
(단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
|
지분상품 |
||
| Lyell immunopharma | 1,116,649,326 | 1,326,594,797 |
|
합 계 |
1,116,649,326 | 1,326,594,797 |
위 지분상품을 처분하는 경우 관련 기타포괄손익누계액은 당기손익으로 재분류되지 않습니다.
13. 유형자산
(1) 유형자산의 내역
|
(단위 : 원) |
|
구 분 |
당분기말 |
||
|
원가 |
상각누계액 |
장부금액 |
|
|
토지 |
112,938,500,000 | - | 112,938,500,000 |
|
건물 |
49,561,818,405 | (27,984,293,779) | 21,577,524,626 |
|
구축물 |
1,821,203,273 | (1,614,527,109) | 206,676,164 |
|
기계장치 |
37,384,556,179 | (34,723,066,054) | 2,661,490,125 |
|
차량운반구 |
998,521,067 | (980,704,838) | 17,816,229 |
|
공구기구 |
6,915,253,717 | (5,355,327,551) | 1,559,926,166 |
|
비품 |
4,518,030,306 | (2,508,358,091) | 2,009,672,215 |
| 건설중인자산 | 189,281,100 | - | 189,281,100 |
|
합 계 |
214,327,164,047 | (73,166,277,422) | 141,160,886,625 |
|
(단위 : 원) |
|
구 분 |
전기말 |
||
|
원가 |
상각누계액 |
장부금액 |
|
| 토지 | 113,313,500,000 | - | 113,313,500,000 |
| 건물 | 49,677,899,587 | (27,635,511,990) | 22,042,387,597 |
| 구축물 | 1,821,203,273 | (1,598,861,047) | 222,342,226 |
| 기계장치 | 37,417,238,048 | (36,171,593,592) | 1,245,644,456 |
| 차량운반구 | 1,045,007,381 | (1,002,791,057) | 42,216,324 |
| 공구기구 | 6,507,361,517 | (5,236,521,919) | 1,270,839,598 |
| 비품 | 4,306,001,596 | (2,337,032,220) | 1,968,969,376 |
| 건설중인자산 | 311,171,100 | - | 311,171,100 |
| 합 계 | 214,399,382,502 | (73,982,311,825) | 140,417,070,677 |
(2) 유형자산의 변동내역
1) 당분기
|
(단위 : 원) |
|
구 분 |
기초순장부가액 | 취득 | 처분 | 감가상각비 | 기타(*) | 분기말순장부가액 |
|
토지 |
113,313,500,000 | - | (375,000,000) | - | - | 112,938,500,000 |
|
건물 |
22,042,387,597 | - | (42,279,723) | (422,583,248) | - | 21,577,524,626 |
|
구축물 |
222,342,226 | - | - | (15,666,062) | - | 206,676,164 |
|
기계장치 |
1,245,644,456 | 1,600,817,491 | (8,000) | (184,963,822) | - | 2,661,490,125 |
|
차량운반구 |
42,216,324 | - | (18,567,871) | (5,832,224) | - | 17,816,229 |
|
공구기구 |
1,270,839,598 | 436,177,000 | (3,000) | (147,087,432) | - | 1,559,926,166 |
|
비품 |
1,968,969,376 | 136,087,406 | - | (142,662,604) | 47,278,037 | 2,009,672,215 |
| 건설중인자산 | 311,171,100 | 129,900,000 | (251,790,000) | - | - | 189,281,100 |
|
합 계 |
140,417,070,677 | 2,302,981,897 | (687,648,594) | (918,795,392) | 47,278,037 | 141,160,886,625 |
(*) 기타증감액은 환율변동으로 인한 환산차이로 구성되어 있습니다.
2) 전분기
|
(단위: 원) |
|
구 분 |
기초순장부가액 | 취득 | 감가상각비 | 기타(*) | 분기말순장부가액 |
|
토지 |
92,875,100,000 | - | - | - | 92,875,100,000 |
|
건물 |
23,735,300,197 | - | (423,228,138) | - | 23,312,072,059 |
|
구축물 |
232,739,888 | - | (14,441,087) | - | 218,298,801 |
|
기계장치 |
1,247,307,776 | - | (188,604,120) | - | 1,058,703,656 |
|
차량운반구 |
76,833,334 | - | (13,185,286) | - | 63,648,048 |
|
공구기구 |
994,536,545 | - | (100,394,418) | - | 894,142,127 |
|
비품 |
1,819,579,180 | 43,707,465 | (37,528,962) | (5,265,838) | 1,820,491,845 |
|
합 계 |
120,981,396,920 | 43,707,465 | (777,382,011) | (5,265,838) | 120,242,456,536 |
(3) 토지의 공정가치 서열체계 구분
|
(단위 : 원) |
|
당분기말 |
수준 1 |
수준 2 |
수준 3 |
합 계 |
|
토지 |
- |
- |
112,938,500,000 | 112,938,500,000 |
|
(단위 : 원) |
|
전기말 |
수준 1 |
수준 2 |
수준 3 |
합 계 |
|
토지 |
- |
- |
113,313,500,000 | 113,313,500,000 |
(4) 토지의 반복적인 측정치의 수준 3의 변동내역
|
(단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
|
기초금액 |
113,313,500,000 | 92,875,100,000 |
| 토지재평가 | - | 20,438,400,000 |
| 처분 | (375,000,000) | - |
|
기말금액 |
112,938,500,000 | 113,313,500,000 |
|
미실현손익(법인세효과 반영후) |
77,345,408,586 | 77,572,776,649 |
(5) 가치평가기법 및 투입변수
|
(단위 : 원) |
|
구 분 |
공정가치 |
수 준 |
가치평가기법 |
투입변수 |
|
토지 |
112,938,500,000 |
3 |
비교표준지 |
공시지가 시점수정요인, |
(6) 감가상각비가 포함되어 있는 계정과목별 금액
|
(단위 : 원) |
|
구 분 |
당분기 |
전분기 |
|
매출원가 |
599,994,048 | 596,561,039 |
|
판매비와관리비 |
188,216,461 | 88,879,717 |
|
경상연구개발비 |
130,584,883 | 91,941,255 |
|
합 계 |
918,795,392 | 777,382,011 |
(7) 보고기간종료일 현재 차입금과 관련하여 연결회사의 유형자산이 담보로 제공되어 있습니다(주석 17, 26 참조).
14. 리스
(1) 연결재무상태표에 인식된 금액
| (단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
|
사용권자산 |
||
|
부동산 |
709,205,488 | 717,313,742 |
|
차량운반구 |
942,545,645 | 346,357,402 |
| 합 계 | 1,651,751,133 | 1,063,671,144 |
| (단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
|
리스부채 |
||
|
유동 |
380,869,869 | 130,194,025 |
|
비유동 |
642,703,519 | 269,907,950 |
| 합 계 | 1,023,573,388 | 400,101,975 |
당분기 중 증가된 사용권자산은 736백만원(전분기: 193백만원)입니다.
(2) 손익계산서에 인식된 금액
| (단위 : 원) |
|
구 분 |
당분기 |
전분기 |
|
사용권자산의 감가상각비 |
||
|
부동산 |
79,854,741 | 133,879,304 |
|
차량운반구 |
73,309,551 | 38,866,862 |
|
합 계 |
153,164,292 | 172,746,166 |
|
리스부채에 대한 이자비용(금융비용에 포함) |
6,960,582 | 9,226,776 |
|
단기리스가 아닌 소액자산 리스료(관리비에 포함) |
63,437,432 | 51,856,207 |
|
리스부채 측정치에 포함되지 않은 변동리스료(관리비에 포함) |
3,200,338 | 1,934,780 |
당분기 중 리스의 총 현금유출은 162백만원(전분기 : 165백만원)입니다.
15. 무형자산
(1) 무형자산의 내역
|
(단위 : 원) |
|
구 분 |
당분기말 |
|||
| 원가 | 상각누계액 | 손상차손누계액 | 장부금액 | |
|
산업재산권 |
738,057,047 | (675,605,035) | - | 62,452,012 |
|
회원권 |
1,090,961,954 | - | (435,014,398) | 655,947,556 |
|
영업권 |
1,322,257,700 | - | (915,640,085) | 406,617,615 |
|
기타의무형자산 |
16,083,105,642 | (131,743,467) | (10,866,414,808) | 5,084,947,367 |
| 소프트웨어 | 216,300,000 | (36,902,083) | - | 179,397,917 |
|
합 계 |
19,450,682,343 | (844,250,585) | (12,217,069,291) | 6,389,362,467 |
|
(단위 : 원) |
|
구 분 |
전기말 |
|||
|
원가 |
상각누계액 |
손상차손누계액 |
장부금액 |
|
|
산업재산권 |
737,444,927 | (669,631,767) | - | 67,813,160 |
|
회원권 |
1,090,961,954 | - | (435,014,398) | 655,947,556 |
|
영업권 |
1,322,257,700 | - | (915,640,085) | 406,617,615 |
| 기타의무형자산 | 17,224,870,352 | (63,589,667) | (12,208,179,518) | 4,953,101,167 |
| 소프트웨어 | 215,000,000 | (23,437,500) | - | 191,562,500 |
|
합 계 |
20,590,534,933 | (756,658,934) | (13,558,834,001) | 6,275,041,998 |
(2) 무형자산의 변동내역
1) 당분기
|
(단위 : 원) |
|
구 분 |
기초 |
취득 |
상각비 |
분기말 |
|
산업재산권 |
67,813,160 | 612,120 | (5,973,268) | 62,452,012 |
|
회원권 |
655,947,556 | - | - | 655,947,556 |
|
영업권 |
406,617,615 | - | - | 406,617,615 |
|
기타의무형자산 |
4,953,101,167 | 200,000,000 | (68,153,800) | 5,084,947,367 |
| 소프트웨어 | 191,562,500 | 1,300,000 | (13,464,583) | 179,397,917 |
|
합 계 |
6,275,041,998 | 201,912,120 | (87,591,651) | 6,389,362,467 |
2) 전분기
|
(단위 : 원) |
|
구 분 |
기초 |
상각비 |
환율변동효과 |
기타(*) |
분기말 |
|
산업재산권 |
89,807,909 | (7,350,482) | - | - | 82,457,427 |
|
회원권 |
699,382,556 | - | - | - | 699,382,556 |
|
영업권 |
878,733,287 | - | 15,817,199 | - | 894,550,486 |
|
기타의무형자산 |
8,388,259,182 | - | 64,559,997 | 141,542,149 | 8,594,361,328 |
|
합 계 |
10,056,182,934 | (7,350,482) | 80,377,196 | 141,542,149 | 10,270,751,797 |
(*) 당분기 중 취득액은 전액 연결범위 변동에 의한 취득입니다. 동 금액은 잠정 금액으로서 측정기간 중 조정될 수 있습니다.
(3) 무형자산상각비가 포함되어 있는 계정과목별 금액
|
(단위 : 원) |
|
구 분 |
당분기 |
전분기 |
|
판매비와관리비 |
87,591,651 | 7,350,482 |
(4) 연구 및 개발활동과 관련하여 지출한 비용
|
(단위 : 원) |
|
구 분 |
당분기 |
전분기 |
|
매출원가 |
||
|
연구비 |
1,287,167,396 | 1,148,570,972 |
|
경상연구개발비 |
||
|
연구비 |
1,718,078,791 | 2,036,760,841 |
|
경상개발비 |
2,733,675,341 | 4,195,673,480 |
|
소 계 |
4,451,754,132 | 6,232,434,321 |
|
합 계 |
5,738,921,528 | 7,381,005,293 |
16. 관계기업 및 공동기업 투자주식
(1) 관계기업 및 공동기업 투자주식현황
| (단위 : 원) |
| 구 분 | 종 목 | 소재국가 | 당분기말 | 전기말 | ||
| 지분율(%) | 장부금액 | 지분율(%) | 장부금액 | |||
| 관계기업 | 덴탈플랫폼투자조합 제1호 | 대한민국 | 50.00 | 14,572,698 | 50.00 | 14,700,542 |
| 합 계 | 14,572,698 | 14,700,542 | ||||
(2) 관계기업 및 공동기업에 대한 투자주식의 변동내역
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 |
| 기초금액 | 14,700,542 | 12,882,667,281 |
| 취득 | - | - |
| 지분법손익 | (127,844) | (261,003,692) |
| 처분 | - | - |
| 종속기업으로 편입 | - | - |
| 분기말금액 | 14,572,698 | 12,621,663,589 |
17. 차입금
| (단위 : 원) |
| 구 분 | 차입처 | 최종 만기일 | 연이자율(%) | 당분기말 | 전기말 |
| 원화장기차입금 | 하나은행 | 2026-08-16 | CD91일물 + 1.484 | 30,000,000,000 | 30,000,000,000 |
| 원화장기차입금(*) | 신한은행 | 2026-10-13 | CD91일물+ 1.39 | 50,000,000,000 | 50,000,000,000 |
| 소계 | 80,000,000,000 | 80,000,000,000 | |||
| 유동성 대체 | - | - | |||
| 차감 : 장기차입금할인발행차금 | (864,753,074) | (975,816,626) | |||
| 합계 | 79,135,246,926 | 79,024,183,374 | |||
(*) 당분기말 현재 상기 차입금과 관련하여 유형자산을 담보로 제공하고 있습니다(주석 13, 26 참조).
18. 순확정급여자산
연결회사는 최종임금기준 확정급여제도를 운영하고 있습니다. 연금의 수준은 종업원의 근무기간 및 최종 임금에 근거하여 산출되며, 연금의 대부분은 기금에 적립되어 외부 전문 신탁사에 의하여 운영되고 있습니다.
(1) 순확정급여자산 산정내역
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 확정급여채무의 현재가치 | 35,260,489,334 | 35,230,954,054 |
| 사외적립자산의 공정가치 | (38,924,163,022) | (39,824,189,831) |
| 재무상태표상 순확정급여자산 | (3,663,673,688) | (4,593,235,777) |
(2) 손익계산서에 반영된 금액
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 3개월 | 누적 | 3개월 | 누적 | |
| 당기근무원가 | 896,418,277 | 896,418,277 | 788,768,895 | 788,768,895 |
| 순이자원가 | (54,880,752) | (54,880,752) | (126,334,170) | (126,334,170) |
| 종업원급여에 포함된 총 비용 | 841,537,525 | 841,537,525 | 662,434,725 | 662,434,725 |
| 매출원가 | 226,997,425 | 226,997,425 | 165,147,281 | 165,147,281 |
| 판매비와관리비 및 연구개발비 | 614,540,100 | 614,540,100 | 497,287,444 | 497,287,444 |
19. 법인세비용
법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균 연간법인세율의 추정에 기초하여 인식하였습니다. 당분기와 전분기 중 법인세차감전순손실이 발생함에따라 평균유효세율을 산정하지 아니하였습니다.
20. 자본금과 주식발행초과금
(1) 자본금의 내역
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 발행할 주식의 총수 | 150,000,000주 | 100,000,000주 |
| 1주당 액면금액 | 500원 | 500원 |
| 발행한 주식의 수 | 68,454,671주 | 68,454,671주 |
| 보통주자본금 | 36,401,993,000원 | 36,401,993,000원 |
연결회사는 2024년 3월 22일 이사회결의에 따라 자기주식 2,608,378주(장부가액 50,784백만원)를 소각하였습니다. 이로 인하여 전기말 및 당분기말 발행주식의 액면총액은 납입자본금과 상이합니다.
(2) 당분기 및 전기 중 자본금과 주식발행초과금의 변동은 없습니다.
21. 기타자본항목
(1) 기타자본항목의 내역
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 |
| 자기주식처분이익 | 23,018,905,016 | 23,018,905,016 |
| 자기주식 | - | - |
| 기타포괄손익-공정가치금융자산 처분손익 | (51,394,485,845) | (51,394,485,845) |
| 기타포괄손익-공정가치금융자산 평가손익 | (585,444,643) | (375,499,172) |
| 해외사업환산손익 | 2,304,941,152 | 2,293,268,035 |
| 주식선택권 | - | - |
| 지분법자본변동 | (109,767,832) | (109,767,832) |
| 유형자산재평가이익 | 77,345,408,586 | 77,586,085,747 |
| 비지배지분과의 주주간계약(주석 26 참조) | (18,359,358,826) | (18,359,358,826) |
| 기타 | 5,210,717,119 | 5,210,717,119 |
| 합 계 | 37,430,914,727 | 37,869,864,242 |
(2) 기타포괄손익누계액의 변동내역
1) 당분기
| (단위 : 원) |
| 구 분 | 기초 | 증감 | 분기말 |
| 기타포괄손익-공정가치금융자산 처분손익 | (51,394,485,845) | - | (51,394,485,845) |
| 기타포괄손익-공정가치금융자산 평가손익 | (375,499,172) | (209,945,471) | (585,444,643) |
|
유형자산재평가손익 |
77,586,085,747 | (240,677,161) | 77,345,408,586 |
| 해외사업환산손익 | 2,293,268,035 | 11,673,117 | 2,304,941,152 |
| 지분법자본변동 | (109,767,832) | - | (109,767,832) |
| 합 계 | 27,999,600,933 | (438,949,515) | 27,560,651,418 |
상기 기타포괄손익누계액의 증감은 법인세 효과가 차감된 후의 금액입니다. 연결회사는 특정 지분상품투자의 공정가치를 기타포괄손익으로 인식하도록 지정하였습니다(주석 12 참조).
2) 전분기
| (단위 : 원) |
| 구 분 | 기초 | 증감 | 분기말 |
| 기타포괄손익-공정가치금융자산 처분손익 | (51,038,416,767) | - | (51,038,416,767) |
| 기타포괄손익-공정가치금융자산 평가손익 | (2,346,328,965) | - | (2,346,328,965) |
|
유형자산재평가손익 |
61,868,956,147 | - | 61,868,956,147 |
| 해외사업환산손익 | 1,084,265,559 | 824,146,334 | 1,908,411,893 |
| 지분법자본변동 | (58,410,555) | - | (58,410,555) |
| 합 계 | 9,510,065,419 | 824,146,334 | 10,334,211,753 |
(3) 자기주식의 변동내역
| (단위 : 주, 원) |
| 구 분 | 당분기 | 전분기 | ||
| 주식수 | 장부금액 | 주식수 | 장부금액 | |
| 기초금액 | - | - | 2,608,378 | 50,784,456,419 |
| 매입 | - | - | - | - |
| 소각 | - | - | 2,608,378 | 50,784,456,419 |
| 기말금액 | - | - | - | - |
22. 주식기준보상
(1) 연결회사는 주주총회 결의에 의거 임직원에게 주식선택권을 부여하였는 바, 주요사항은 다음과 같습니다.
| 구 분 | 내 역 |
|---|---|
| 부여일 | 2018년 3월 16일 |
| 부여주식수 | 130,000주 |
| 부여방법 | 신주교부, 자기주식교부, 차액보상 중 이사회가 결정 |
| 행사가격 | 16,915원 |
| 행사가능기간 | 2020년 3월 16일 ~ 2027년 3월 15일 |
(*) 관련 임직원 퇴직으로 인해 주식매수선택권 부여가 취소되었습니다.
(**) 상기 주식선택권과 관련하여 당분기 중 연결회사가 인식한 주식보상비용은 없습니다.
(2) 연결회사는 상기 주식선택권 외에 종속기업인 Contera Pharma A/S 주식에 대해 주식선택권을 부여하고 있습니다. 이로 인하여 당분기 중 연결회사가 인식한 주식보상비용은 없습니다. (전기 : 주식보상비용 환입 4백만원)
23. 판매비와관리비
|
(단위 : 원) |
|
구 분 |
당분기 |
전분기 |
|
급여 |
6,830,452,158 | 6,345,208,553 |
|
퇴직급여 |
589,318,164 | 477,469,771 |
|
복리후생비 |
525,983,625 | 510,647,207 |
|
회의비 |
112,422,514 | 81,218,459 |
|
여비교통비 |
299,021,615 | 273,341,620 |
|
통신비 |
67,696,799 | 112,215,874 |
|
수도광열비 |
52,375,018 | 50,401,353 |
|
세금과공과 |
240,121,360 | 271,941,025 |
|
지급임차료 |
70,870,569 | 63,324,621 |
|
감가상각비 |
188,216,461 | 88,879,717 |
|
사용권자산상각비 |
108,876,639 | 172,746,166 |
|
수선비 |
37,598,019 | 51,242,578 |
|
보험료 |
65,762,746 | 58,697,858 |
|
접대비 |
71,567,100 | 20,063,048 |
|
교육훈련비 |
78,076,887 | 39,379,208 |
|
광고선전비 |
1,452,529,782 | 1,363,399,581 |
|
견본비 |
2,732,930 | 4,369,982 |
|
도서인쇄비 |
68,238,088 | 57,744,491 |
|
소모품비 |
50,574,769 | 45,144,446 |
|
차량유지비 |
46,354,796 | 12,165,384 |
|
운반및포장비 |
568,569,934 | 408,184,144 |
|
지급수수료 |
1,519,864,377 | 974,891,855 |
|
노무용역비 |
301,931,931 | 206,657,177 |
|
대손상각비(환입) |
(10,899,336) | (466,776,665) |
|
무형자산상각비 |
87,591,651 | 7,350,482 |
|
잡비 |
5,314,500 | 5,740,520 |
|
합 계 |
13,431,163,096 | 11,235,648,455 |
24. 배당금
전기 회계연도에 대한 배당금은 지급하지 않았으며, 당기 회계연도에 대한 배당계획은 없습니다.
25. 영업으로부터 창출된 현금
(1) 영업으로부터 창출된 현금
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 법인세비용차감전순이익(손실) | (322,705,062) | (2,125,031,405) |
| 조정항목: | ||
| 퇴직급여 | 841,537,525 | 662,434,725 |
| 경상개발비 | - | 143,153,759 |
| 감가상각비 | 918,795,392 | 777,382,011 |
| 사용권자산감가상각비 | 153,164,292 | 172,746,166 |
| 무형자산상각비 | 87,591,651 | 7,350,482 |
| 대손상각비(환입) | (10,899,336) | (466,776,665) |
| 재고자산평가손실 | 44,632,967 | 226,041,222 |
| 유형자산처분이익 | (361,644,406) | (3,969,312) |
| 유형자산처분손실 | 3,000 | - |
| 이자비용 | 1,017,834,745 | 1,537,303,776 |
| 당기손익-공정가치금융자산 평가이익 | (337,559,039) | (343,840,430) |
| 당기손익-공정가치금융자산 평가손실 | 4,246,789,656 | 41,784,728 |
| 이자수익 | (1,034,774,822) | (1,437,884,547) |
| 외화환산이익 | 1,279,793 | (5,684,396) |
| 외화환산손실 | 71,139,862 | 1,558,678 |
| 지분법손실(이익) | 127,844 | 261,003,690 |
| 영업활동으로 인한 자산부채의 변동 | ||
| 매출채권의 감소(증가) | 151,056,379 | 11,865,898,610 |
| 기타유동금융자산의 감소(증가) | (10,228,044) | (90,779,396) |
| 기타유동자산의 감소(증가) | 50,390,127 | 10,346,968 |
| 재고자산의 증가(감소) | (118,986,809) | 4,016,046,409 |
| 환불자산의 감소(증가) | (61,239,416) | 721,953,719 |
| 매입채무의 증가(감소) | 1,193,135,516 | (60,925,401) |
| 기타유동금융부채의 증가(감소) | 371,511,085 | (3,937,121,912) |
| 기타유동부채의 증가(감소) | (609,039,418) | 546,760,888 |
| 순확정급여자산의 감소(증가) | (30,104,283) | 896,279,054 |
| 환불부채의 증가(감소) | (163,074,812) | (1,436,128,220) |
| 영업으로부터 창출된 현금 | 6,088,734,387 | 11,979,903,201 |
(2) 현금의 유입ㆍ유출이 없는 거래 중 중요한 사항
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 매출채권의 제각 | 7,539,796 | 31,482 |
| 건설중인자산의 본계정 대체 | 351,790,000 | - |
| 유형자산 취득 미지급금 증감 | 112,288,395 | 39,795,000 |
| 기타비유동금융부채의 증가 | - | 30,112,148 |
(3) 재무활동에서 생기는 부채의 조정내역
| (단위 : 원) |
| 구 분 | 유동 리스부채 | 비유동 리스부채 | 장기차입금 |
| 전기초 | 217,604,354 | 644,168,219 | 78,525,127,415 |
| 현금흐름 | (109,526,132) | - | - |
| 비금융변동(*) | 218,624,074 | (35,371,737) | 102,637,665 |
| 전분기말 | 326,702,296 | 608,796,482 | 78,627,765,080 |
| 당기초 | 130,194,025 | 269,907,950 | 79,024,183,374 |
| 현금흐름 | (364,763,670) | - | - |
| 비금융변동(*) | 615,439,514 | 372,795,569 | 111,063,552 |
| 당분기말 | 380,869,869 | 642,703,519 | 79,135,246,926 |
(*) 비금융변동에는 리스부채에 대한 유동성대체 및 리스계약 변경으로 인한 당기 리스부채 증감 내역이 포함되어 있습니다.
26. 우발상황 및 약정사항
(1) 연결회사가 금융기관과 체결하고 있는 약정사항의 내역
| (단위 : 원, USD) |
| 금융기관 | 약정사항 | 당분기말 | 전기말 | ||
|---|---|---|---|---|---|
| 한도금액 | 사용금액 | 한도금액 | 사용금액 | ||
| 하나은행 | 일반자금대출 | 30,000,000,000 | 30,000,000,000 | 30,000,000,000 | 30,000,000,000 |
| 수입신용장 | USD 1,000,000 | - | USD 1,000,000 | - | |
| 국민은행 | 일반자금대출 | 30,000,000,000 | - | 30,000,000,000 | - |
| 산업은행 | 일반자금대출 | 10,000,000,000 | - | 10,000,000,000 | - |
| 신한은행 | 일반자금대출 | 50,000,000,000 | 50,000,000,000 | 50,000,000,000 | 50,000,000,000 |
상기 약정 이외에 연결회사는 국민은행과 기업구매론약정(당분기말 : 한도 10,000백만원, 전기말 : 한도 10,000백만원)과 신한은행과 전자방식매출채권담보대출약정(당분기말 : 한도 2,500백만원 전기말 : 한도 2,500백만원)을 맺고 있습니다.
당분기말 현재 매입채무및기타채무 금액 중 공급자금융약정과 관련된 금융부채는 2,857백만원이며, 공급자가 금융기관으로부터 당분기말 현재 이미 대금을 수취한 금액은315백만원입니다.
공급자금융약정에 해당하는 금융부채와 공급자금융약정에 해당하지 않는 금융부채의 지급기일에는 유의적인 차이가 없습니다.
공급자금융약정에 따라 금융기관에게 지급해야 할 금액은 회사의 정상영업주기 내에사용되는 운전자본의 일부로서 매입채무및기타채무와 유사한 성격과 기능을 지니고 있다고 판단하여 이를 매입채무및기타채무로 분류하고, 현금흐름표에서 관련현금흐름을 영업활동현금흐름으로 분류하고 있습니다.
(2) 연결회사가 타인으로부터 제공받은 지급보증의 내역
| (단위 : 원) |
| 금융기관 | 약정사항 | 보증금액 | |
|---|---|---|---|
| 당분기말 | 전기말 | ||
| 서울보증보험 | 공탁보증 | - | 60,000,000 |
| 물품대금보증 | 1,060,000,000 | 1,000,000,000 | |
| 합 계 | 1,060,000,000 | 1,060,000,000 | |
(3) 당분기말 현재 차입금 등과 관련하여 담보로 제공되어있는 자산내역은 다음과 같습니다.
| (단위 : 원) |
| 구분 | 제공처 | 내역 | 담보제공자산 | 장부금액 | 설정금액 |
| 유형자산 | 신한은행 | 차입금 담보 | 토지,건물 | 73,453,239,043 | 60,000,000,000 |
(4) 당분기말 현재 연결회사가 원고로서 진행 중인 소송은 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소소송 1건, 권리범위확인(특) 3건, 총 4건(전기말 : 4건)으로 소송가액은 없습니다. 또한 회사가 피고로서 진행중인 소송은 권리범위확인(특) 총 1건(전기말 : 1건)으로 소송가액은 없습니다.
| 관할법원 | 원고 | 피고 | 소송의 내용 | 소송가액 | 진행상황 |
| 서울고등법원 | 당사 | 보건복지부장관 | 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소 | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 에치케이이노엔 | 당사 | 권리범위확인(특) | - | 계류중 |
(5) 연결회사는 종속기업인 Contera Pharma A/S와 관련하여 개발 중인 의약품의 허가신청, 시판 승인 및 상용화 조건 달성 여부에 따라 조건부대가를 지급하는 약정을 체결하였습니다. 전기 중 연결회사는 해당 의약품의 임상을 중단하였으며, 이에 따라미래에 지불할 가능성이 있는 금액을 0으로 평가하였습니다.
(6) 연결회사가 당분기말 현재 보유 중인 당기손익-공정가치측정 금융자산 중 TVM LifeScience Innovation II SCSP에 대한 투자 약정금액은 총 USD 3,000,000이며, 현재까지 USD 2,848,568에 대한 납입이 완료되었습니다. 잔여금액 USD 151,432은 향후 업무집행사원의 출자이행요청에 따라 추가 납입예정이나, 현재 시점에 그 납입시기를 예상할 수 없습니다.
(7) 연결회사가 당분기말 현재 보유 중인 당기손익-공정가치측정 금융자산 중 KDB오픈이노베이션 제2호에 대한 투자 약정금액은 총 5억원이며, 현재까지 5억원 납입이 완료되었습니다.
(8) 연결회사는 종속기업인 ProteKt Therapeutics와 관련하여 개발 중인 의약품의 License 관련 판매 및 배당 등의 조건 달성 여부에 따라 조건부대가를 지급하는 약정을 체결하였습니다.
27. 특수관계자거래
(1) 연결회사와 매출 등 거래 또는 채권ㆍ채무 잔액이 있는 기타특수관계자
|
구 분 |
당분기말 |
전기말 |
|---|---|---|
| 관계기업 | 덴탈플랫폼투자조합제1호 | 덴탈플랫폼투자조합제1호 |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | OCI홀딩스 주식회사 |
| (주)디씨알이 | (주)디씨알이 | |
| 오씨아이드림(주) | 오씨아이드림(주) | |
| OCI(주) | OCI(주) | |
| OCI정보통신 | OCI정보통신 |
(2) 매출 및 매입 등 거래
| (단위 : 원) |
| 구 분 | 기업명 | 당분기 | 전분기 | ||
|---|---|---|---|---|---|
| 매출 등 | 매입 등 | 매출 등 | 매입 등 | ||
| 대규모기업집단 계열회사 |
OCI홀딩스 주식회사 | 16,646,721 | 5,805,473 | 17,823,292 | 9,333,026 |
| (주)디씨알이 | 1,883,182 | - | 5,525,818 | - | |
| 오씨아이드림(주) | 2,486,000 | - | 4,503,000 | 63,908 | |
| OCI(주) | 18,014,997 | 19,200,000 | 9,901,472 | 6,931,982 | |
| OCI정보통신 | - | 153,965,400 | - | - | |
| 합 계 | 39,030,900 | 178,970,873 | 37,753,582 | 16,328,916 | |
(3) 채권ㆍ채무의 주요 잔액
| (단위 : 원) |
| 구 분 | 기업명 | 당분기말 | ||
|---|---|---|---|---|
| 채권 | 채무 | |||
| 기타채권 | 매입채무 | 기타채무 | ||
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | 6,763,735 | - | 930,875 |
| 오씨아이드림(주) | 784,300 | - | - | |
| OCI(주) | 12,142,232 | 10,560,000 | - | |
| OCI정보통신 | - | - | 12,685,310 | |
| 합 계 | 19,690,267 | 10,560,000 | 13,616,185 | |
| (단위 : 원) |
| 구 분 | 기업명 | 전기말 | ||
|---|---|---|---|---|
| 채권 | 채무 | |||
| 기타채권 | 매입채무 | 기타채무 | ||
| 대규모기업집단 계열회사 |
OCI홀딩스 주식회사 | 968,542 | - | 1,235,664 |
| 오씨아이드림(주) | 1,725,350 | - | - | |
| OCI(주) | - | - | 16,896,000 | |
| OCI정보통신 | - | - | 10,964,800 | |
| 합 계 | 2,693,892 | 0 | 29,096,464 | |
(4) 특수관계자와의 자금 거래
| (단위 : 원) |
| 구 분 | 기업명 | 당분기 | |||
|---|---|---|---|---|---|
| 현금출자 | 유상감자 | 현금배당 | 기타 | ||
| 주요 경영진 등 | - | - | - | - | |
| 합 계 | - | - | - | - | |
| (단위 : 원) |
| 구 분 | 기업명 | 전분기 | |||
|---|---|---|---|---|---|
| 현금출자 | 유상감자 | 현금배당 | 기타 | ||
| 주요 경영진 등 | - | - | - | - | |
| 합 계 | - | - | - | - | |
(5) 주요 경영진에 대한 보상내역
주요 경영진은 등기이사, 미등기이사(상무)와 감사위원회 위원을 포함하고 있습니 다. 종업원 용역의 대가로서 주요 경영진에게 지급되었거나 지급된 보상금액은 다음과 같습니다.
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 단기종업원 급여 | 1,270,980,712 | 1,005,810,033 |
| 퇴직급여 | 46,184,288 | 27,488,289 |
| 합 계 | 1,317,165,000 | 1,033,298,322 |
28. 영업부문 정보
(1) 영업부문에 대한 일반 정보
연결회사의 영업부문은 '의약품 제조 및 판매 부문'과 '의약품 연구 및 개발 부문'으로 구성되어 있습니다. 연결회사는 각 사업부문에 배분될 자원에 대한 의사결정 및 성과평가를 위하여 최고경영진이 주기적으로 검토하는 내부자료에 기초하여 사업부문을 구분하였습니다.
(2) 보고부문 정보
| (단위 : 원) |
| 당분기 | 매출액 | 영업손익 | 유무형자산 |
감가상각비 및 무형자산상각비 |
|---|---|---|---|---|
| 제약부문 | 48,197,488,268 | 5,946,190,477 | 143,170,918,962 | 917,007,808 |
| 연구개발부문 | - | (3,013,489,090) | 1,519,097,681 | 89,379,235 |
| 연결조정 | (391,050,040) | 81,533,597 | 2,860,232,449 | - |
| 합 계 | 47,806,438,228 | 3,014,234,984 | 147,550,249,092 | 1,006,387,043 |
| (단위 : 원) |
| 전분기 | 매출액 | 영업손익 | 유무형자산 |
감가상각비 및 무형자산상각비 |
|---|---|---|---|---|
| 제약부문 | 34,720,650,245 | 2,030,613,859 | 121,600,938,644 | 783,550,607 |
| 연구개발부문 | - | (3,586,709,296) | 2,875,442,002 | 1,181,886 |
| 연결조정 | (327,211,000) | (72,205,108) | 6,036,776,996 | - |
| 합 계 | 34,393,439,245 | (1,628,300,545) | 130,513,157,642 | 784,732,493 |
(3) 연결회사 매출의 상세내역
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 상품매출액 | 6,948,156,419 | 3,281,335,642 |
| 제품매출액 | 40,813,814,309 | 31,112,103,603 |
| 기술매출액 | - | - |
| 수출매출액 | 44,467,500 | - |
| 합 계 | 47,806,438,228 | 34,393,439,245 |
(4) 지역별 매출의 구성
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 국 내 | 47,761,970,728 | 34,393,439,245 |
| 해 외 | 44,467,500 | - |
| 합 계 | 47,806,438,228 | 34,393,439,245 |
(5) 주요 고객에 대한 정보
당분기와 전분기 중 연결회사 매출액의 10% 이상을 차지하는 단일의 외부고객과 관련된 정보는 다음과 같습니다.
| (단위 : 원) |
| 구 분 | 매출액 | 관련 보고 부문 | |
|---|---|---|---|
| 당분기 | 전분기 | ||
| 고객 A | 5,224,521,168 | 3,804,134,675 | 제약 부문 |
4. 재무제표
4-1. 재무상태표
|
재무상태표 |
|
제 66 기 1분기말 2025.03.31 현재 |
|
제 65 기말 2024.12.31 현재 |
|
(단위 : 원) |
|
제 66 기 1분기말 |
제 65 기말 |
|
|---|---|---|
|
자산 |
||
|
유동자산 |
196,039,043,504 |
190,617,729,403 |
|
현금및현금성자산 |
80,902,755,251 |
79,680,401,227 |
|
매출채권 |
21,263,368,603 |
22,143,109,107 |
|
기타유동금융자산 |
46,633,631,082 |
41,038,954,432 |
|
기타유동자산 |
480,389,190 |
387,031,000 |
|
유동환불자산 |
5,096,034,069 |
5,034,794,653 |
|
당기법인세자산 |
0 |
522,988,225 |
|
재고자산 |
41,662,865,309 |
41,810,450,759 |
|
비유동자산 |
176,191,693,178 |
179,462,244,706 |
|
당기손익-공정가치금융자산 |
12,947,665,836 |
16,525,597,921 |
|
기타포괄손익-공정가치금융자산 |
1,116,649,326 |
1,326,594,797 |
|
기타비유동금융자산 |
255,875,427 |
245,743,689 |
|
유형자산 |
139,641,779,944 |
138,938,913,374 |
|
사용권자산 |
1,010,161,189 |
389,930,991 |
|
무형자산 |
3,526,895,903 |
3,413,080,165 |
|
순확정급여자산 |
3,657,507,508 |
4,587,225,724 |
|
관계기업 및 공동기업투자주식 |
14,035,158,045 |
14,035,158,045 |
|
자산총계 |
372,230,736,682 |
370,079,974,109 |
|
부채 |
||
|
유동부채 |
33,580,681,783 |
33,944,891,577 |
|
매입채무 |
6,012,426,311 |
4,868,207,208 |
|
기타유동금융부채 |
10,095,265,274 |
11,054,598,372 |
|
기타유동부채 |
1,949,938,283 |
2,693,658,070 |
|
유동환불부채 |
15,035,159,090 |
15,198,233,902 |
|
유동리스부채 |
380,869,869 |
130,194,025 |
|
당기법인세부채 |
107,022,956 |
0 |
|
비유동부채 |
93,249,490,443 |
93,224,082,111 |
|
장기차입금 |
79,135,246,926 |
79,024,183,374 |
|
비유동리스부채 |
633,069,583 |
260,737,555 |
|
이연법인세부채 |
13,056,055,623 |
13,514,042,871 |
|
기타비유동금융부채 |
425,118,311 |
425,118,311 |
|
부채총계 |
126,830,172,226 |
127,168,973,688 |
|
자본 |
||
|
자본금 |
36,401,993,000 |
36,401,993,000 |
|
주식발행초과금 |
2,581,379,750 |
2,581,379,750 |
|
기타자본항목 |
49,958,014,713 |
50,408,637,345 |
|
이익잉여금 |
156,459,176,993 |
153,518,990,326 |
|
자본총계 |
245,400,564,456 |
242,911,000,421 |
|
자본과부채총계 |
372,230,736,682 |
370,079,974,109 |
4-2. 포괄손익계산서
|
포괄손익계산서 |
|
제 66 기 1분기 2025.01.01 부터 2025.03.31 까지 |
|
제 65 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
(단위 : 원) |
|
제 66 기 1분기 |
제 65 기 1분기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
매출액 |
43,849,740,564 |
43,849,740,564 |
34,028,881,622 |
34,028,881,622 |
|
매출원가 |
23,291,986,716 |
23,291,986,716 |
18,554,027,029 |
18,554,027,029 |
|
매출총이익 |
20,557,753,848 |
20,557,753,848 |
15,474,854,593 |
15,474,854,593 |
|
판매비와관리비 |
12,677,459,452 |
12,677,459,452 |
10,704,394,494 |
10,704,394,494 |
|
경상연구개발비 |
1,945,673,224 |
1,945,673,224 |
2,710,830,771 |
2,710,830,771 |
|
영업이익 |
5,934,621,172 |
5,934,621,172 |
2,059,629,328 |
2,059,629,328 |
|
기타수익 |
823,156,006 |
823,156,006 |
93,324,812 |
93,324,812 |
|
기타비용 |
82,851,648 |
82,851,648 |
452,654,502 |
452,654,502 |
|
금융수익 |
1,337,995,991 |
1,337,995,991 |
1,655,475,943 |
1,655,475,943 |
|
금융비용 |
5,427,673,788 |
5,427,673,788 |
953,136,326 |
953,136,326 |
|
법인세비용차감전순이익 |
2,585,247,733 |
2,585,247,733 |
2,402,639,255 |
2,402,639,255 |
|
법인세비용(수익) |
(208,462,988) |
(208,462,988) |
419,265,239 |
419,265,239 |
|
분기순이익(손실) |
2,793,710,721 |
2,793,710,721 |
1,983,374,016 |
1,983,374,016 |
|
주당이익 |
||||
|
보통주기본주당이익 (단위 : 원) |
41 |
41 |
29 |
29 |
|
보통주희석주당이익 (단위 : 원) |
41 |
41 |
29 |
29 |
|
기타포괄손익 |
(191,968,964) |
(191,968,964) |
(113,965,113) |
(113,965,113) |
|
당기손익으로 재분류되지 않는항목 |
(191,968,964) |
(191,968,964) |
(113,965,113) |
(113,965,113) |
|
순확정급여자산의 재측정요소 |
(94,201,215) |
(94,201,215) |
(113,965,113) |
(113,965,113) |
|
기타포괄손익-공정가치금융자산평가손익 |
(166,066,868) |
(166,066,868) |
0 |
0 |
|
기타포괄손익-공정가치금융자산처분손익 |
0 |
0 |
0 |
0 |
|
유형자산재평가손익 |
68,299,119 |
68,299,119 |
0 |
0 |
|
총포괄손익 |
2,601,741,757 |
2,601,741,757 |
1,869,408,903 |
1,869,408,903 |
4-3. 자본변동표
|
자본변동표 |
|
제 66 기 1분기 2025.01.01 부터 2025.03.31 까지 |
|
제 65 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
(단위 : 원) |
|
자본 |
|||||
|---|---|---|---|---|---|
|
자본금 |
주식발행초과금 |
기타자본항목 |
이익잉여금 |
자본 합계 |
|
|
2024.01.01 (기초자본) |
36,401,993,000 |
2,581,379,750 |
(17,707,709,389) |
265,448,585,448 |
286,724,248,809 |
|
총포괄손익 |
0 |
0 |
0 |
1,869,408,903 |
1,869,408,903 |
|
분기순이익(손실) |
0 |
0 |
0 |
1,983,374,016 |
1,983,374,016 |
|
순확정급여자산의 재측정요소 |
0 |
0 |
0 |
(113,965,113) |
(113,965,113) |
|
기타포괄손익-공정가치금융자산 평가손익 |
0 |
0 |
0 |
0 |
0 |
|
유형자산재평가손익 |
0 |
0 |
0 |
0 |
0 |
|
분기총포괄손익 |
0 |
0 |
0 |
1,869,408,903 |
1,869,408,903 |
|
자기주식의 소각 |
0 |
0 |
50,784,456,419 |
(50,784,456,419) |
0 |
|
소유주와의 거래총액 |
0 |
0 |
50,784,456,419 |
(50,784,456,419) |
0 |
|
2024.03.31 (기말자본) |
36,401,993,000 |
2,581,379,750 |
33,076,747,030 |
216,533,537,932 |
288,593,657,712 |
|
2025.01.01 (기초자본) |
36,401,993,000 |
2,581,379,750 |
50,408,637,345 |
153,518,990,326 |
242,911,000,421 |
|
총포괄손익 |
0 |
0 |
(450,622,632) |
2,940,186,667 |
2,489,564,035 |
|
분기순이익(손실) |
0 |
0 |
0 |
2,793,710,721 |
2,793,710,721 |
|
순확정급여자산의 재측정요소 |
0 |
0 |
0 |
(94,201,215) |
(94,201,215) |
|
기타포괄손익-공정가치금융자산 평가손익 |
0 |
0 |
(209,945,471) |
0 |
(209,945,471) |
|
유형자산재평가손익 |
0 |
0 |
(240,677,161) |
240,677,161 |
0 |
|
분기총포괄손익 |
0 |
0 |
(450,622,632) |
2,940,186,667 |
2,489,564,035 |
|
자기주식의 소각 |
0 |
0 |
0 |
0 |
0 |
|
소유주와의 거래총액 |
0 |
0 |
0 |
0 |
0 |
|
2025.03.31 (기말자본) |
36,401,993,000 |
2,581,379,750 |
49,958,014,713 |
156,459,176,993 |
245,400,564,456 |
4-4. 현금흐름표
|
현금흐름표 |
|
제 66 기 1분기 2025.01.01 부터 2025.03.31 까지 |
|
제 65 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
(단위 : 원) |
|
제 66 기 1분기 |
제 65 기 1분기 |
|
|---|---|---|
|
영업활동현금흐름 |
10,614,857,104 |
16,364,440,635 |
|
분기순이익(손실) |
2,793,710,721 |
1,983,374,016 |
|
조정항목 |
5,311,983,591 |
991,645,423 |
|
급여 |
0 |
419,265,239 |
|
법인세비용(수익) |
(208,462,988) |
114,915,253 |
|
퇴직급여 |
840,731,203 |
660,589,122 |
|
감가상각비 |
829,416,157 |
776,040,498 |
|
무형자산상각비 |
87,484,262 |
7,274,449 |
|
사용권자산상각비 |
91,906,074 |
0 |
|
대손상각비(환입) |
(10,899,336) |
(466,776,665) |
|
파생상품평가손실(이익) |
0 |
(278,675,984) |
|
유형자산처분이익 |
(361,644,406) |
(3,969,312) |
|
유형자산처분손실 |
3,000 |
0 |
|
이자비용 |
1,015,548,556 |
1,147,283,640 |
|
이자수익 |
(997,102,377) |
(1,309,831,731) |
|
당기손익-공정가치금융자산의 평가이익 |
(337,559,039) |
(343,840,430) |
|
당기손익-공정가치금융자산의 평가손실 |
4,246,789,656 |
41,784,728 |
|
외화환산이익 |
0 |
(13,284) |
|
외화환산손실 |
71,139,862 |
1,558,678 |
|
재고자산평가손실 |
44,632,967 |
226,041,222 |
|
순운전자본의 변동 |
1,388,811,693 |
12,751,033,841 |
|
매출채권의 감소 |
890,639,840 |
12,507,172,474 |
|
기타유동금융자산의 감소(증가) |
(313,441,890) |
(190,954,374) |
|
기타유동자산의 감소(증가) |
(93,358,190) |
(209,027,724) |
|
재고자산의 감소 |
102,952,483 |
4,179,847,919 |
|
매입채무의 증가(감소) |
1,073,079,241 |
(641,343,481) |
|
기타유동금융부채의 증가(감소) |
727,078,507 |
(3,628,245,845) |
|
기타유동부채의 증가(감소) |
(743,719,787) |
551,480,319 |
|
순확정급여자산의 증가(감소) |
(30,104,283) |
896,279,054 |
|
환불자산의 감소(증가) |
(61,239,416) |
721,953,719 |
|
환불부채의 증가(감소) |
(163,074,812) |
(1,436,128,220) |
|
이자의 수취 |
714,974,097 |
1,325,570,515 |
|
법인세의 지급 |
405,377,002 |
(687,183,160) |
|
투자활동현금흐름 |
(8,399,651,458) |
(1,952,455,352) |
|
기타유동금융자산의 감소(증가) |
(5,000,000,000) |
0 |
|
기타비유동금융자산의 감소(증가) |
(10,000,000) |
4,000,000 |
|
당기손익-공정가치금융자산의 취득 |
(331,298,532) |
(1,943,126,352) |
|
유형자산의 취득 |
(1,955,852,926) |
(13,329,000) |
|
유형자산의 처분 |
797,500,000 |
0 |
|
무형자산의 취득 |
(1,900,000,000) |
0 |
|
재무활동현금흐름 |
(992,851,622) |
(1,145,287,617) |
|
단기차입금의 증가 |
0 |
10,000,000,000 |
|
단기차입금의 감소 |
0 |
(10,000,000,000) |
|
리스부채의 상환 |
(95,218,750) |
(109,770,680) |
|
이자의 지급 |
(897,632,872) |
(1,035,516,937) |
|
환율변동효과 반영전 현금및현금성자산의 순증가 |
1,222,354,024 |
13,266,697,666 |
|
현금및현금성자산에 대한 환율변동효과 |
0 |
13,284 |
|
현금및현금성자산의 순증가 |
1,222,354,024 |
13,266,710,950 |
|
기초현금및현금성자산 |
79,680,401,227 |
132,379,945,401 |
|
분기말현금및현금성자산 |
80,902,755,251 |
145,646,656,351 |
5. 재무제표 주석
| 제 66 기 1분기 : 2025년 1월 1일부터 2025년 3월 31일까지 |
| 제 65 기 1분기 : 2024년 1월 1일부터 2024년 3월 31일까지 |
| 부광약품주식회사 |
1. 일반 사항
부광약품주식회사(이하 "회사")는 1960년 10월 17일에 설립되어, 1988년 8월 5일에 주식을 한국거래소가 개설하는 유가증권시장에 상장하였습니다. 회사는 의약품 제조 및 판매를 주요 사업으로 하고 있습니다. 회사의 본사는 서울시 동작구에 소재하고 있으며 경기도 안산에 공장을 두고 있습니다.
당분기말 현재 자본금은 36,402백만원이며, 주요 주주 현황은 다음과 같습니다.
| 주 주 | 보유 주식 수 | 지분율(%) | 비고 |
|---|---|---|---|
| OCI홀딩스 주식회사 | 7,747,934 | 11.32 | 최대주주 |
| 김동연 | 7,053,266 | 10.30 | - |
| 국민연금공단 | 473,991 | 0.69 | - |
| 기타 | 53,179,480 | 77.69 | - |
| 합 계 | 68,454,671 | 100 |
2. 중요한 회계정책
다음은 재무제표 작성에 적용된 주요한 회계정책입니다. 이러한 정책은 별도의 언급이 없다면, 표시된 회계기간에 계속적으로 적용됩니다.
2.1 재무제표 작성 기준
회사의 재무제표는 한국채택국제회계기준(이하 기업회계기준)에 따라 작성되었습니다. 한국채택국제회계기준은 국제회계기준위원회("IASB")가 발표한 기준서와 해석서중 대한민국이 채택한 내용을 의미합니다.
재무제표는 다음을 제외하고는 역사적 원가에 기초하여 작성하였습니다.
- 특정 금융자산과 금융부채(파생상품 포함), 공정가치로 측정하는 특정 유형자산
- 확정급여제도와 공정가치로 측정하는 사외적립자산, 기타장기종업원급여부채
한국채택국제회계기준은 재무제표 작성시 중요한 회계추정의 사용을 허용하고 있으며, 회계정책을 적용함에 있어 경영진의 판단을 요구하고 있습니다. 보다 복잡하고 높은 수준의 판단이 필요한 부분이나 중요한 가정 및 추정이 필요한 부분은 주석 3에서 설명하고 있습니다.
2.2 회계정책과 공시의 변경
2.2.1 회사가 채택한 제ㆍ개정 기준서 및 해석서
회사가 2025년 1월 1일 이후 개시하는 회계기간부터 적용한 제ㆍ개정 기준서 및 해석서는 다음과 같습니다.
(1) 기업회계기준서 제1021호 '환율변동효과' 및 기업회계기준서 제1101호 '한국채택국제회계기준의 최초채택'(개정) - 교환가능성 결여
동 개정사항은 회계목적상 다른 통화와 교환이 가능하다고 보는 상황에 대해 정의하고, 다른 통화와의 교환가능성 평가, 교환가능성이 결여된 경우 사용할 현물환율 추정 및 공시 요구사항을 명확히 합니다. 다른 통화와 교환이 가능하지 않다면 측정일에 현물환율을 추정해야 하며, 관측 가능한 환율을 조정 없이 사용하거나 다른 추정기법을 사용하도록 하고 있습니다. 해당 기준서의 개정으로 인하여 재무제표에 미치는 유의적인 영향은 없습니다.
2.2.2 회사가 적용하지 않은 제ㆍ개정 기준서 및 해석서
제정 또는 공표되었으나 시행일이 도래하지 않아 적용하지 아니한 제ㆍ개정 기준서 및 해석서는 다음과 같습니다.
(1) 기업회계기준서 제1109호 '금융상품'과 제1107호 '금융상품 : 공시'(개정) - 금융상품 분류와 측정
동 개정사항은 전자지급시스템을 사용하여 금융부채를 결제할 때의 금융부채의 결제일 전 이행과 관련된 조건, 계약상 현금흐름이 기본대여계약과 일관되는지 평가할 때고려해야 할 이자 및 우발사건 특성, 비소구 특성을 가진 금융자산, 계약상 연계된 금융상품의 특성을 명확히 합니다. 그리고 기타포괄손익-공정가치로 지정된 지분상품에 대한 투자와 계약상 현금흐름의 시기나 금액을 변경할 수 있는 계약조건에 대한 추가적인 공시 요구사항을 포함합니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도의 개시일 이후 소급적으로 적용되며 조기적용이 허용됩니다. 회사는 동 개정으로 인한 재무제표의 영향을 검토 중에 있습니다.
(2) 기업회계기준서 제1109호 '금융상품' - 리스부채의 제거 회계처리 및 거래가격의 정의
동 개정사항은 리스부채 제거시 발생하는 차손익을 당기손익으로 인식해야 함을 명확히 하였습니다. 또한 거래가격의 정의를 기업회계기준서 제1115호와 일관되도록 개정하였습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다. 회사는 동 개정으로 인한 재무제표의 영향을 검토 중에 있습니다.
(3) 기업회계기준서 제1110호 '연결재무제표' - 사실상의 대리인 결정
동 개정사항은 사실상 대리인의 판단과 관련한 기준서 제1110호의 표현을 개정하여 기준서 문단 간의 불일치를 해소하였습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다. 회사는 동 개정으로 인한 재무제표의 영향을 검토 중에 있습니다.
(4) 기업회계기준서 제1101호 '한국채택국제회계기준의 최초채택' - 위험회피회계 적용
동 개정사항은 위험회피회계의 적용조건을 기업회계기준서 제1109호 '금융상품' 의구체적인 문단을 참조하도록 명시하고 관련 용어를 일치시켰습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다. 회사는 동 개정으로 인한 재무제표의 영향을 검토 중에 있습니다.
(5) 기업회계기준서 제1107호 '금융상품' : 공시 - 제거 손익
동 개정사항은 공정가치 측정과 관련하여 기업회계기준서 제1113호 '공정가치'를 참조하도록 하고 관련 용어를 일치시켰습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다. 회사는 동 개정으로 인한 재무제표의 영향을 검토 중에 있습니다.
(6) 기업회계기준서 제1007호 '현금흐름표' - 원가법
동 개정으로 '원가법'이라는 용어를 삭제하고 이를 '원가'로 대체하였습니다. 동 개정사항은 2026년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기적용이 허용됩니다. 회사는 동 개정으로 인한 재무제표의 영향을 검토 중에 있습니다.
2.3 회계정책
분기재무제표의 작성에 적용된 유의적 회계정책과 계산방법은 주석 2에서 설명하는 제ㆍ개정 기준서의 적용으로 인한 변경 사항 및 아래 문단에서 설명하는 사항을 제외하고는 전기 재무제표 작성에 적용된 회계정책이나 계산방법과 동일합니다.
(1) 법인세비용
중간기간의 법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균연간법인세율, 즉 추정평균연간유효법인세율을 중간기간의 세전이익에 적용하여 계산합니다.
3. 중요한 회계추정 및 가정
재무제표 작성에는 미래에 대한 가정 및 추정이 요구되며 경영진은 회사의 회계정책을 적용하기 위해 판단이 요구됩니다. 추정 및 가정은 지속적으로 평가되며, 과거 경험과 현재의 상황에 비추어 합리적으로 예측가능한 미래의 사건을 고려하여 이루어집니다. 회계추정의 결과가 실제 결과와 동일한 경우는 드물 것이므로 중요한 조정을유발할 수 있는 유의적인 위험을 내포하고 있습니다.
분기재무제표 작성시 사용된 중요한 회계추정 및 가정은 법인세비용을 결정하는데 사용된 추정의 방법을 제외하고는 전기 재무제표 작성에 적용된 회계추정 및 가정과 동일합니다.
4. 공정가치
4.1 금융상품 종류별 공정가치
금융상품의 종류별 장부금액 및 공정가치는 다음과 같습니다.
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 | ||
| 장부금액 | 공정가치 | 장부금액 | 공정가치 | |
| 금융자산 | ||||
| 당기손익-공정가치금융자산 | 12,947,665,836 | 12,947,665,836 | 16,525,597,921 | 16,525,597,921 |
| 기타포괄손익-공정가치금융자산 | 1,116,649,326 | 1,116,649,326 | 1,326,594,797 | 1,326,594,797 |
상기 외 금융자산과 금융부채는 장부금액이 공정가치의 합리적인 근사치이므로 공정가치 공시에서 제외하였습니다.
4.2 금융상품 공정가치 서열 체계
공정가치로 측정되는 금융상품은 공정가치 서열체계에 따라 구분되며 정의된 수준들은 다음과 같습니다.
- 측정일에 동일한 자산이나 부채에 대해 접근할 수 있는 활성시장의(조정하지 않은) 공시가격(수준 1)
- 수준 1의 공시가격 외에 자산이나 부채에 대해 직접적으로나 간접적으로 관측할 수 있는 투입변수(수준 2)
- 자산이나 부채에 대한 관측할 수 없는 투입변수(수준 3)
공정가치로 측정되는 금융상품의 공정가치 서열체계 구분은 다음과 같습니다.
| (단위 : 원) |
| 구 분 | 당분기말 | |||
| 수준 1 | 수준 2 | 수준 3 | 합 계 | |
| 공정가치로 측정되는 금융자산 | ||||
| 당기손익-공정가치금융자산 | 27,443,553 | - | 12,920,222,283 | 12,947,665,836 |
| 기타포괄손익-공정가치금융자산 | 1,116,649,326 | - | - | 1,116,649,326 |
| (단위 : 원) |
| 구 분 | 전기말 | |||
| 수준 1 | 수준 2 | 수준 3 | 합 계 | |
| 공정가치로 측정되는 금융자산 | ||||
| 당기손익-공정가치금융자산 | 84,402,770 | - | 16,441,195,151 | 16,525,597,921 |
| 기타포괄손익-공정가치금융자산 | 1,326,594,797 | - | - | 1,326,594,797 |
4.3 반복적인 공정가치 측정치의 서열체계 수준 간 이동
회사는 공정가치 서열체계의 수준 간 이동을 보고기간 말에 인식합니다. 당분기 중 반복적인 측정치의 수준 1과 수준 2간의 대체는 없으며, 반복적인 측정치의 수준 3의변동 내역은 다음과 같습니다.
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 | ||
| 당기손익-공정가치 금융자산 |
기타포괄손익-공정가치 금융자산 |
당기손익-공정가치 금융자산 |
기타포괄손익-공정가치 금융자산 |
|
| 기초금액 | 16,441,195,151 | - | 16,446,643,666 | 4,459,545,887 |
| 총손익 | ||||
| 당기손익인식액 | (3,852,271,400) | - | 343,840,430 | - |
| 기타포괄손익인식액 | - | - | - | - |
| 매입금액 | 331,298,532 | - | 1,943,126,353 | - |
| 매도금액 | - | - | - | |
| 분기말금액 | 12,920,222,283 | - | 18,733,610,449 | 4,459,545,887 |
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 | ||
| 기타금융부채 | 파생상품부채 | 기타금융부채 | 파생상품부채 | |
| 기초금액 | - | - | 7,753,272,340 | 43,437,065,805 |
| 설정(환입) | - | - | 143,153,759 | - |
| 상환 | - | - | - | - |
| 평가손익 | - | - | - | (278,675,984) |
| 외화환산 | - | - | - | - |
| 분기말금액 | - | - | 7,896,426,099 | 43,158,389,821 |
4.4 가치평가기법 및 투입변수
당분기말 및 전기말 현재 회사는 공정가치 서열체계에서 수준 3으로 분류되는 반복적인 공정가치 측정치에 대해 다음의 가치평가기법을 사용하고 있습니다.
| (단위 : 원) |
| 구 분 | 당분기말 | ||||
|---|---|---|---|---|---|
| 공정가치 | 수준 | 가치평가기법 |
투입변수 |
수준3 투입변수 범위 |
|
| 당기손익-공정가치금융자산 | |||||
| 시장성없는 지분증권 및 수익증권 | 11,497,015,459 | 3 | 순자산가치법 취득원가법 |
- |
NA |
| 전환사채 등 | 1,423,206,824 | 3 | 취득원가법 | - | NA |
| (단위 : 원) |
| 구 분 | 전기말 | ||||
|---|---|---|---|---|---|
| 공정가치 | 수준 | 가치평가기법 |
투입변수 |
수준3 투입변수 범위 |
|
| 당기손익-공정가치금융자산 | |||||
| 시장성없는 지분증권 및 수익증권 | 15,017,988,327 | 3 | 순자산가치법 취득원가법 |
- |
NA |
| 전환사채 등 | 1,423,206,824 | 3 | 취득원가법 | - | NA |
4.5 수준 3으로 분류된 공정가치 측정치의 가치평가과정
회사의 재무부서는 재무보고 목적의 공정가치의 측정을 담당하고 있으며 이러한 공정가치 측정치는 수준 3으로 분류되는 공정가치 측정치를 포함하고 있습니다. 회사의 재무부서는 공정가치 측정 내역 및 결과에 대하여 회사의 경영진에게 매 분기 보고하고 있습니다.
4.6 수준 3으로 분류된 반복적인 공정가치 측정치의 민감도 분석
금융상품의 민감도 분석은 통계적 기법을 이용한 관측 불가능한 투입변수의 변동에 따른 금융상품의 가치 변동에 기초하여 유리한 변동과 불리한 변동으로 구분하여 이루어집니다. 그리고 공정가치가 두 개 이상의 투입변수에 영향을 받는 경우에는 가장 유리하거나 또는 가장 불리한 금액을 바탕으로 산출됩니다.
5. 현금및현금성자산
|
(단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
|
현금 |
1,000,000 | 1,000,000 |
|
보통예금(*) |
2,901,755,251 | 154,371,338 |
|
RP |
13,000,000,000 | 19,525,029,889 |
|
정기예금 |
65,000,000,000 | 60,000,000,000 |
|
합 계 |
80,902,755,251 | 79,680,401,227 |
(*) 당분기말 보통예금 중 미결제타점권으로 사용제한이 되어있는 예금은 없습니다.
6. 매출채권
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 매출채권 | 21,389,906,625 | 22,288,054,779 |
| 차감 : 손실충당금 | (126,538,022) | (144,945,672) |
| 매출채권(순액) | 21,263,368,603 | 22,143,109,107 |
7. 환불자산과 환불부채
| (단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
|---|---|---|
| 환불자산 - 예상 고객반품 | 5,096,034,069 | 5,034,794,653 |
|
환불부채 - 반품충당부채 |
14,981,348,880 | 15,143,382,091 |
| 환불부채 - 수금할인 변동대가 | 53,810,210 | 54,851,811 |
8. 기타금융자산
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 | ||
|---|---|---|---|---|
| 유동 | 비유동 | 유동 | 비유동 | |
| 단기금융상품 | 45,000,000,000 | - | 40,000,000,000 | - |
| 미수금 | 752,195,820 | 438,753,930 | - | |
| 미수수익 | 881,435,262 | - | 600,200,502 | - |
| 장기금융상품(*) | - | 42,500,000 | - | 42,500,000 |
| 보증금 | - | 217,314,219 | - | 207,314,219 |
| 현재가치할인차금 | - | (3,938,792) | - | (4,070,530) |
| 합 계 | 46,633,631,082 | 255,875,427 | 41,038,954,432 | 245,743,689 |
(*) 장기금융상품 중 3백만원은 당좌개설보증금이며, 사용이 제한되어 있습니다.
상각후원가로 측정하는 기타금융자산은 모두 신용위험이 낮은 것으로 판단되며, 따라서 손실충당금은 12개월 기대신용손실로 인식하였습니다. 기타금융자산은 채무불이행 위험이 낮고 단기간 내에 계약상 현금흐름을 지급할 수 있는 발행자의 충분한 능력이 있는 경우 신용위험이 낮은 것으로 간주합니다. 기타금융자산과 관련하여 회사가 보유하고 있는 담보는 없습니다.
9. 기타유동자산
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 |
| 선급금 | 83,735,342 | 3,271,520 |
| 선급비용 | 396,653,848 | 383,759,480 |
| 합 계 | 480,389,190 | 387,031,000 |
10. 재고자산
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 상품 | 4,578,613,211 | 5,343,562,799 |
| 제품 | 13,587,560,929 | 13,575,399,681 |
| 재공품 | 8,659,358,642 | 6,960,060,684 |
| 원재료 | 16,090,807,224 | 17,299,121,850 |
| 저장품 | 4,905,778 | 9,788,140 |
| 미착품 | 1,839,236,581 | 1,675,501,694 |
| 평가손실충당금 | (3,097,617,056) | (3,052,984,089) |
| 합 계 | 41,662,865,309 | 41,810,450,759 |
당분기 중 회사는 재고자산평가손실 45백만원(전분기 : 226백만원 손실)을 인식하였으며, 손익계산서의 '매출원가'에 가산되었습니다.
11. 당기손익-공정가치금융자산
(1) 당기손익-공정가치금융자산
|
(단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
| 지분상품 | ||
| CytoSite BioPharma Inc. | 1,720,050,057 | 1,720,050,057 |
| Biodexa Pharmaceuticals | 27,443,553 | 84,402,770 |
| 수익증권 | ||
| TVM Life Science Ventures Ⅶ, L.P | 5,760,889,485 | 9,950,719,924 |
| TVM Life Science Innovation II SCSp | 3,752,987,306 | 3,084,129,735 |
| KDB 오픈이노베이션 제2호 | 263,088,611 | 263,088,611 |
| 채무증권 | ||
| JaguAHR Therapeutics | 1,134,525,000 | 1,134,525,000 |
| CytoSite BioPharma Inc. | 288,681,824 | 288,681,824 |
|
합 계 |
12,947,665,836 | 16,525,597,921 |
(2) 당기손익으로 인식된 금액
|
(단위 : 원) |
|
구 분 |
당분기 |
전분기 |
| 당기손익-공정가치금융자산 평가손익 | (3,909,230,617) | 302,055,702 |
| 합 계 | (3,909,230,617) | 302,055,702 |
(3) 회사는 당기손익-공정가치금융자산에 대한 신용위험에 노출되어 있습니다. 당분기말 현재 회사의 관련 최대노출금액은 해당 채무증권의 장부금액(당분기말: 1,423백만원, 전기말: 1,423백만원)입니다.
12. 기타포괄손익-공정가치금융자산
|
(단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
|
지분상품 |
||
| Lyell immunopharma | 1,116,649,326 | 1,326,594,797 |
|
합 계 |
1,116,649,326 | 1,326,594,797 |
위 지분상품을 처분하는 경우 관련 기타포괄손익누계액은 당기손익으로 재분류되지 않습니다.
13. 유형자산
(1) 유형자산의 내역
|
(단위 : 원) |
|
구 분 |
당분기말 |
||
|
원가 |
상각누계액 |
장부금액 |
|
|
토지 |
112,938,500,000 | - | 112,938,500,000 |
|
건물 |
49,561,818,405 | (27,984,293,779) | 21,577,524,626 |
|
구축물 |
1,821,203,273 | (1,614,527,109) | 206,676,164 |
|
기계장치 |
37,384,556,179 | (34,723,066,054) | 2,661,490,125 |
|
차량운반구 |
998,521,067 | (980,704,838) | 17,816,229 |
|
공구기구 |
6,915,253,717 | (5,355,327,551) | 1,559,926,166 |
|
비품 |
2,187,385,562 | (1,696,820,028) | 490,565,534 |
| 건설중인자산 | 189,281,100 | - | 189,281,100 |
|
합 계 |
211,996,519,303 | (72,354,739,359) | 139,641,779,944 |
|
(단위 : 원) |
|
구 분 |
전기말 |
||
|
원가 |
상각누계액 |
장부금액 |
|
| 토지 | 113,313,500,000 | - | 113,313,500,000 |
| 건물 | 49,677,899,587 | (27,635,511,990) | 22,042,387,597 |
| 구축물 | 1,821,203,273 | (1,598,861,047) | 222,342,226 |
| 기계장치 | 37,417,238,048 | (36,171,593,592) | 1,245,644,456 |
| 차량운반구 | 1,045,007,381 | (1,002,791,057) | 42,216,324 |
| 공구기구 | 6,507,361,517 | (5,236,521,919) | 1,270,839,598 |
| 비품 | 2,134,348,732 | (1,643,536,659) | 490,812,073 |
| 건설중인자산 | 311,171,100 | - | 311,171,100 |
| 합 계 | 212,227,729,638 | (73,288,816,264) | 138,938,913,374 |
(2) 유형자산의 변동내역
1) 당분기
|
(단위 : 원) |
|
구 분 |
기초순장부가액 |
취득 |
처분 | 감가상각비 |
분기말순장부가액 |
|
토지 |
113,313,500,000 | - | (375,000,000) | - | 112,938,500,000 |
|
건물 |
22,042,387,597 | - | (42,279,723) | (422,583,248) | 21,577,524,626 |
|
구축물 |
222,342,226 | - | - | (15,666,062) | 206,676,164 |
|
기계장치 |
1,245,644,456 | 1,600,817,491 | (8,000) | (184,963,822) | 2,661,490,125 |
|
차량운반구 |
42,216,324 | - | (18,567,871) | (5,832,224) | 17,816,229 |
|
공구기구 |
1,270,839,598 | 436,177,000 | (3,000) | (147,087,432) | 1,559,926,166 |
|
비품 |
490,812,073 | 53,036,830 | - | (53,283,369) | 490,565,534 |
| 건설중인자산 | 311,171,100 | 129,900,000 | (251,790,000) | - | 189,281,100 |
|
합 계 |
138,938,913,374 | 2,219,931,321 | (687,648,594) | (829,416,157) | 139,641,779,944 |
2) 전분기
|
(단위 : 원) |
|
구 분 |
기초순장부가액 |
취득 |
감가상각비 |
분기말순장부가액 |
|
토지 |
92,875,100,000 | - | - | 92,875,100,000 |
|
건물 |
23,735,300,197 | - | (423,228,138) | 23,312,072,059 |
|
구축물 |
232,739,888 | - | (14,441,087) | 218,298,801 |
|
기계장치 |
1,247,307,776 | - | (188,604,120) | 1,058,703,656 |
|
차량운반구 |
77,452,334 | - | (13,185,286) | 64,267,048 |
|
공구기구 |
991,783,226 | - | (100,394,418) | 891,388,808 |
|
비품 |
310,567,569 | 11,534,000 | (36,187,449) | 285,914,120 |
|
합 계 |
119,470,250,990 | 11,534,000 | (776,040,498) | 118,705,744,492 |
(3) 토지의 공정가치 서열체계 구분
|
(단위 : 원) |
|
당분기말 |
수준 1 |
수준 2 |
수준 3 |
합 계 |
|
토지 |
- |
- |
112,938,500,000 | 112,938,500,000 |
|
(단위 : 원) |
|
전기말 |
수준 1 |
수준 2 |
수준 3 |
합 계 |
|
토지 |
- |
- |
113,313,500,000 |
113,313,500,000 |
(4) 토지의 반복적인 측정치의 수준 3의 변동내역
|
(단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
|
기초금액 |
113,313,500,000 | 92,875,100,000 |
| 토지재평가 | - | 20,438,400,000 |
| 처분 | (375,000,000) | - |
|
기말금액 |
112,938,500,000 | 113,313,500,000 |
|
미실현손익(법인세효과 반영후) |
77,345,408,586 | 77,572,776,649 |
(5) 가치평가기법 및 투입변수
|
(단위 : 원) |
|
구 분 |
공정가치 |
수 준 |
가치평가기법 |
투입변수 |
|
토지 |
112,938,500,000 |
3 |
비교표준지 |
공시지가 시점수정요인, |
(6) 감가상각비가 포함되어 있는 계정과목별 금액
|
(단위 : 원) |
|
구 분 |
당분기 |
전분기 |
|
매출원가 |
599,994,048 | 596,561,039 |
|
판매비와관리비 |
98,837,226 | 87,538,204 |
|
경상연구개발비 |
130,584,883 | 91,941,255 |
|
합 계 |
829,416,157 | 776,040,498 |
(7) 보고기간종료일 현재 차입금과 관련하여 회사의 유형자산이 담보로 제공되어 있습니다(주석 17, 26 참조).
14. 리스
(1) 재무상태표에 인식된 금액
| (단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
|
사용권자산 |
||
|
부동산 |
67,615,544 | 43,573,589 |
|
차량운반구 |
942,545,645 | 346,357,402 |
|
합 계 |
1,010,161,189 | 389,930,991 |
| (단위 : 원) |
|
구 분 |
당분기말 |
전기말 |
|
리스부채 |
||
|
유동 |
380,869,869 | 130,194,025 |
|
비유동 |
633,069,583 | 260,737,555 |
| 합 계 | 1,013,939,452 | 390,931,580 |
당분기 중 증가된 사용권자산은 712백만원(전분기: 178백만원)입니다.
(2) 손익계산서에 인식된 금액
| (단위 : 원) |
|
구 분 |
당분기 |
전분기 |
|
사용권자산의 감가상각비 |
||
|
부동산 |
18,596,523 | 76,048,391 |
|
차량운반구 |
73,309,551 | 38,866,862 |
|
합 계 |
91,906,074 | 114,915,253 |
|
리스부채에 대한 이자비용(금융비용에 포함) |
6,852,132 | 9,129,038 |
|
단기리스가 아닌 소액자산 리스료(관리비에 포함) |
63,437,432 | 51,856,207 |
|
리스부채 측정치에 포함되지 않은 변동리스료(관리비에 포함) |
3,200,338 | 1,934,780 |
당분기 중 리스의 총 현금유출은 162백만원(전분기 : 165백만원)입니다.
15. 무형자산
(1) 무형자산의 내역
|
(단위 : 원) |
|
구 분 |
당분기말 |
|||
|
원가 |
상각누계액 |
손상차손누계액 |
장부금액 |
|
|
산업재산권 |
733,761,487 | (673,543,590) | - | 60,217,897 |
|
회원권 |
1,090,961,954 | - | (435,014,398) | 655,947,556 |
|
기타의무형자산 |
8,105,398,850 | (131,743,467) | (5,342,322,850) | 2,631,332,533 |
| 소프트웨어 | 216,300,000 | (36,902,083) | - | 179,397,917 |
|
합 계 |
10,146,422,291 | (842,189,140) | (5,777,337,248) | 3,526,895,903 |
|
(단위 : 원) |
|
구 분 |
전기말 |
|||
|
원가 |
상각누계액 |
손상차손누계액 |
장부금액 |
|
| 산업재산권 | 733,761,487 | (667,677,711) | - | 66,083,776 |
| 회원권 | 1,090,961,954 | - | (435,014,398) | 655,947,556 |
| 기타의무형자산 | 7,905,398,850 | (63,589,667) | (5,342,322,850) | 2,499,486,333 |
| 소프트웨어 | 215,000,000 | (23,437,500) | - | 191,562,500 |
| 합 계 | 9,945,122,291 | (754,704,878) | (5,777,337,248) | 3,413,080,165 |
(2) 무형자산의 변동내역
1) 당분기
|
(단위 : 원) |
|
구 분 |
기초 |
취득 | 상각비 |
분기말 |
|
산업재산권 |
66,083,776 | - | (5,865,879) | 60,217,897 |
|
회원권 |
655,947,556 | - | 655,947,556 | |
|
기타의무형자산 |
2,499,486,333 | 200,000,000 | (68,153,800) | 2,631,332,533 |
| 소프트웨어 | 191,562,500 | 1,300,000 | (13,464,583) | 179,397,917 |
|
합 계 |
3,413,080,165 | 201,300,000 | (87,484,262) | 3,526,895,903 |
2) 전분기
|
(단위 : 원) |
|
구 분 |
기초 |
상각비 |
분기말 |
|
산업재산권 |
88,411,162 | (7,274,449) | 81,136,713 |
|
회원권 |
699,382,556 | - | 699,382,556 |
|
기타의무형자산 |
2,113,395,860 | - | 2,113,395,860 |
|
합 계 |
2,901,189,578 | (7,274,449) | 2,893,915,129 |
(3) 무형자산상각비가 포함되어 있는 계정과목별 금액
|
(단위 : 원) |
|
구 분 |
당분기 |
전분기 |
|
판매비와관리비 |
87,484,262 | 7,274,449 |
(4) 연구 및 개발활동과 관련하여 지출한 비용
|
(단위 : 원) |
|
구 분 |
당분기 |
전분기 |
|
매출원가 |
||
|
연구비 |
1,287,167,396 | 1,148,570,972 |
|
경상연구개발비 |
||
|
연구비 |
1,060,102,954 | 933,175,349 |
|
경상개발비 |
885,570,270 | 1,777,655,422 |
|
소 계 |
1,945,673,224 | 2,710,830,771 |
|
합 계 |
3,232,840,620 | 3,859,401,743 |
16. 종속기업, 관계기업 및 공동기업 투자주식
(1) 종속기업, 관계기업 및 공동기업 투자주식현황
| (단위 : 원) |
| 구 분 | 종 목 | 소재국가 | 당분기말 | 전기말 | ||
| 지분율(%) | 장부금액 | 지분율(%) | 장부금액 | |||
| 종속기업 | Contera Pharma A/S | 덴마크 | 99.33 | 10,871,136,907 | 99.33 | 10,871,136,907 |
| 부광메디카(주) | 대한민국 | 100.00 | 1,735,689,285 | 100.00 | 1,735,689,285 | |
| ProteKt Therapeutics | 이스라엘 | 97.24 | - | 97.24 | - | |
| JaguAHR Therapeutics | 싱가포르 | 75.02 | 1,428,331,853 | 75.02 | 1,428,331,853 | |
| 소 계 | 14,035,158,045 | 14,035,158,045 | ||||
| 관계기업 | 덴탈플랫폼출자조합제1호 | 대한민국 | 50.00 | - | 50.00 | - |
| 소 계 | - | - | ||||
| 합 계 | 14,035,158,045 | 14,035,158,045 | ||||
(2) 종속기업, 관계기업 및 공동기업투자주식의 변동내역
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 |
| 기초금액 | 14,035,158,045 | 73,163,309,002 |
| 취득 | - | - |
| 손상차손 | - | - |
| 처분 | - | - |
| 기타(*) |
- | 143,153,759 |
| 분기말금액 | 14,035,158,045 | 73,306,462,761 |
(*) 전분기 중 종속기업인 Contera Pharma A/S와 관련된 주주 간 계약상 조건부대가의 변동을 장부가액에 가산하였습니다.
17. 차입금
| (단위 : 원) |
| 구 분 | 차입처 | 최종 만기일 | 연이자율(%) | 당분기말 | 전기말 |
| 원화장기차입금 | 하나은행 | 2026-08-16 | CD91일물 + 1.484 | 30,000,000,000 | 30,000,000,000 |
| 원화장기차입금(*) | 신한은행 | 2026-10-13 | CD91일물+ 1.39 | 50,000,000,000 | 50,000,000,000 |
| 소계 | 80,000,000,000 | 80,000,000,000 | |||
| 유동성 대체 | - | - | |||
| 차감 : 장기차입금할인발행차금 | (864,753,074) | (975,816,626) | |||
| 합계 | 79,135,246,926 | 79,024,183,374 | |||
(*) 당분기말 현재 상기 차입금과 관련하여 유형자산을 담보로 제공하고 있습니다(주석 13, 26 참조).
18. 순확정급여자산
회사는 최종임금기준 확정급여제도를 운영하고 있습니다. 연금의 수준은 종업원의 근무기간 및 최종 임금에 근거하여 산출되며, 연금의 대부분은 기금에 적립되어 외부전문 신탁사에 의해 운영되고 있습니다.
(1) 순확정급여자산 산정내역
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 확정급여채무의 현재가치 | 35,258,132,296 | 35,228,506,830 |
| 사외적립자산의 공정가치 | (38,915,639,804) | (39,815,732,554) |
| 재무상태표상 순확정급여자산 | (3,657,507,508) | (4,587,225,724) |
(2) 손익계산서에 반영된 금액
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 3개월 | 누적 | 3개월 | 누적 | |
| 당기근무원가 | 895,548,550 | 895,548,550 | 786,750,333 | 786,750,333 |
| 순이자원가 | (54,817,347) | (54,817,347) | (126,161,211) | (126,161,211) |
| 종업원급여에 포함된 총 비용 | 840,731,203 | 840,731,203 | 660,589,122 | 660,589,122 |
| 매출원가 | 226,997,425 | 226,997,425 | 165,147,281 | 165,147,281 |
| 판매비와관리비 및 연구개발비 | 613,733,778 | 613,733,778 | 495,441,841 | 495,441,841 |
19. 법인세비용
법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균 연간법인세율의 추정에 기초하여 인식하였습니다. 당분기와 전분기 중 법인세차감전순손실이 발생함에따라 평균유효세율을 산정하지 아니하였습니다.
20. 자본금과 주식발행초과금
(1) 자본금의 내역
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 발행할 주식의 총수 | 150,000,000주 | 100,000,000주 |
| 1주당 액면금액 | 500원 | 500원 |
| 발행한 주식의 수 | 68,454,671주 | 68,454,671주 |
| 보통주자본금 | 36,401,993,000원 | 36,401,993,000원 |
회사는 2020년 및 2024년 자기주식을 소각하여, 전기말 및 당기말 발행주식의 액면총액은 납입자본금과 상이합니다.
(2) 당분기 및 전기 중 자본금과 주식발행초과금의 변동은 없습니다.
21. 기타자본항목
(1) 기타자본항목의 내역
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 |
| 자기주식처분이익 | 23,018,905,016 | 23,018,905,016 |
| 자기주식 | - | |
| 기타포괄손익-공정가치금융자산처분손익 | (51,394,485,845) | (51,394,485,845) |
| 기타포괄손익-공정가치금융자산평가손익 | (585,444,643) | (375,499,172) |
| 유형자산재평가손익 | 77,345,408,586 | 77,586,085,747 |
| 기타 | 1,573,631,599 | 1,573,631,599 |
| 합 계 | 49,958,014,713 | 50,408,637,345 |
(2) 기타포괄손익누계액의 변동내역
1) 당분기
| (단위 : 원) |
| 구 분 | 기초 | 증감 | 분기말 |
| 기타포괄손익-공정가치금융자산 처분손익 | (51,394,485,845) | - | (51,394,485,845) |
| 기타포괄손익-공정가치금융자산 평가손익 | (375,499,172) | (209,945,471) | (585,444,643) |
|
유형자산재평가손익 |
77,586,085,747 | (240,677,161) | 77,345,408,586 |
| 합 계 | 25,816,100,730 | (450,622,632) | 25,365,478,098 |
상기 기타포괄손익누계액의 증감은 법인세 효과가 차감된 후의 금액입니다. 회사는 특정 지분상품투자의 공정가치를 기타포괄손익으로 인식하도록 지정하였습니다(주석 12 참조).
2) 전분기
| (단위 : 원) |
| 구 분 | 기초 | 증감 | 기말 |
| 기타포괄손익-공정가치금융자산 처분손익 | (51,038,416,767) | - | (51,038,416,767) |
| 기타포괄손익-공정가치금융자산 평가손익 | (2,346,328,965) | - | (2,346,328,965) |
|
유형자산재평가손익 |
61,868,956,147 | - | 61,868,956,147 |
| 합 계 | 8,484,210,415 | - | 8,484,210,415 |
(3) 자기주식의 변동내역
| (단위 : 주, 원) |
| 구 분 | 당분기 | 전분기 | ||
| 주식수 | 장부금액 | 주식수 | 장부금액 | |
| 기초금액 | - | - | 2,608,378 | 50,784,456,419 |
| 매입 | - | - | - | - |
| 소각 | - | - | 2,608,378 | 50,784,456,419 |
| 기말금액 | - | - | - | - |
22. 주식기준보상
(1) 회사는 주주총회 결의에 의거 임직원에게 주식선택권을 부여하였는 바, 주요사항은 다음과 같습니다.
| 구 분 | 내 역 |
|---|---|
| 부여일 | 2018년 3월 16일 |
| 부여 주식 수 | 130,000주 |
| 부여 방법 | 신주교부, 자기주식교부, 차액보상 중 이사회가 결정 |
| 행사가격 | 16,915원 |
| 행사 가능 기간 | 2020년 3월 16일 ~ 2027년 3월 15일 |
(*) 관련 임직원 퇴직으로 인해 주식매수선택권 부여가 취소되었습니다.
(**) 상기 주식선택권과 관련하여 당분기 중 회사가 인식한 주식보상비용은 없습니다.
23. 판매비와관리비
|
(단위 : 원) |
|
구 분 |
당분기 |
전분기 |
|
급여 |
6,801,692,458 | 6,288,897,296 |
|
퇴직급여 |
588,511,842 | 475,624,168 |
|
복리후생비 |
525,198,595 | 506,327,979 |
|
회의비 |
89,822,214 | 70,428,798 |
|
여비교통비 |
219,996,410 | 237,597,879 |
|
통신비 |
48,609,017 | 56,211,200 |
|
수도광열비 |
52,375,018 | 50,401,353 |
|
세금과공과 |
239,356,430 | 269,619,925 |
|
지급임차료 |
37,200,066 | 35,455,108 |
|
감가상각비 |
98,837,226 | 87,538,204 |
|
사용권자산감가상각비 |
47,618,421 | 114,915,253 |
|
수선비 |
35,350,084 | 33,308,000 |
|
보험료 |
44,109,454 | 45,870,922 |
|
접대비 |
71,189,062 | 17,268,734 |
|
교육훈련비 |
78,076,887 | 39,299,208 |
|
광고선전비 |
1,390,906,334 | 1,283,949,842 |
|
견본비 |
2,732,930 | 4,369,982 |
|
도서인쇄비 |
12,132,859 | 10,738,981 |
|
소모품비 |
49,128,423 | 43,363,602 |
|
차량유지비 |
20,661,713 | 12,165,384 |
|
운반및포장비 |
550,082,053 | 407,085,417 |
|
지급수수료 |
1,316,046,181 | 879,272,924 |
|
노무용역비 |
275,926,349 | 188,446,031 |
|
대손상각비(환입) |
(10,899,336) | (466,776,665) |
|
무형자산상각비 |
87,484,262 | 7,274,449 |
|
잡비 |
5,314,500 | 5,740,520 |
|
합 계 |
12,677,459,452 | 10,704,394,494 |
24. 배당금
전기 회계연도에 대한 배당금은 지급하지 않았으며, 당기 회계연도에 대한 배당계획은 없습니다.
25. 영업으로부터 창출된 현금
(1) 영업으로부터 창출된 현금
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 법인세비용차감전순이익 | 2,585,247,733 | 2,402,639,255 |
| 조정항목: | ||
| 퇴직급여 | 840,731,203 | 660,589,122 |
| 감가상각비 | 829,416,157 | 776,040,498 |
| 사용권자산상각비 | 91,906,074 | 114,915,253 |
| 무형자산상각비 | 87,484,262 | 7,274,449 |
| 대손상각비(환입) | (10,899,336) | (466,776,665) |
| 재고자산평가손실(환입) | 44,632,967 | 226,041,222 |
| 파생상품평가손실 | - | (278,675,984) |
| 유형자산처분이익 | (361,644,406) | (3,969,312) |
| 유형자산처분손실 | 3,000 | - |
| 이자비용 | 1,015,548,556 | 1,147,283,640 |
| 당기손익-공정가치금융자산 평가이익 | (337,559,039) | (343,840,430) |
| 당기손익-공정가치금융자산 평가손실 | 4,246,789,656 | 41,784,728 |
| 이자수익 | (997,102,377) | (1,309,831,731) |
| 외화환산이익 | - | (13,284) |
| 외화환산손실 | 71,139,862 | 1,558,678 |
| 영업활동으로 인한 자산부채의 변동 | ||
| 매출채권의 감소(증가) | 890,639,840 | 12,507,172,474 |
| 기타유동금융자산의 감소(증가) | (313,441,890) | (190,954,374) |
| 기타유동자산의 감소(증가) | (93,358,190) | (209,027,724) |
| 재고자산의 감소(증가) | 102,952,483 | 4,179,847,919 |
| 환불자산의 감소(증가) | (61,239,416) | 721,953,719 |
| 매입채무의 증가(감소) | 1,073,079,241 | (641,343,481) |
| 기타유동금융부채의 증가(감소) | 727,078,507 | (3,628,245,845) |
| 기타유동부채의 증가(감소) | (743,719,787) | 551,480,319 |
| 순확정급여자산의 감소(증가) | (30,104,283) | 896,279,054 |
| 환불부채의 증가(감소) | (163,074,812) | (1,436,128,220) |
| 영업으로부터 창출된 현금 | 9,494,506,005 | 15,726,053,280 |
(2) 현금의 유입ㆍ유출이 없는 거래 중 중요한 사항
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 매출채권의 제각 | 7,539,796 | 31,482 |
| 건설중인자산의 본계정 대체 | 351,790,000 | - |
| 종속기업투자주식의 증가 | - | 143,153,759 |
| 유형자산 취득 미지급금 증감 | 112,288,395 | 39,795,000 |
| 기타비유동금융부채의 증가 | - | 30,112,148 |
(3) 재무활동에서 생기는 부채의 조정내역
| (단위 : 원) |
| 구 분 | 유동 리스부채 | 비유동 리스부채 | 장기차입금 |
|---|---|---|---|
| 전기초 | 217,604,354 | 635,999,355 | 78,525,127,415 |
| 현금흐름 | (109,770,680) | - | - |
| 비금융변동(*) | 218,868,622 | (35,616,285) | 102,637,665 |
| 전분기말 | 326,702,296 | 600,383,070 | 78,627,765,080 |
| 당기초 | 130,194,025 | 260,737,555 | 79,024,183,374 |
| 현금흐름 | (364,763,670) | - | - |
| 비금융변동(*) | 615,439,514 | 372,332,028 | 111,063,552 |
| 당분기말 | 380,869,869 | 633,069,583 | 79,135,246,926 |
(*) 비금융변동에는 리스부채에 대한 유동성대체 및 리스계약 변경으로 인한 당기 리스부채 증감 내역이 포함되어 있습니다.
26. 우발상황 및 약정사항
(1) 회사가 금융기관과 체결하고 있는 약정사항의 내역
| (단위 : 원, USD) |
| 금융기관 | 약정사항 | 당분기말 | 전기말 | ||
|---|---|---|---|---|---|
| 한도금액 | 사용금액 | 한도금액 | 사용금액 | ||
| 하나은행 | 일반자금대출 | 30,000,000,000 | 30,000,000,000 | 30,000,000,000 | 30,000,000,000 |
| 수입신용장 | USD 1,000,000 | - | USD 1,000,000 | - | |
| 국민은행 | 일반자금대출 | 30,000,000,000 | - | 30,000,000,000 | - |
| 산업은행 | 일반자금대출 | 10,000,000,000 | - | 10,000,000,000 | - |
| 신한은행 | 일반자금대출 | 50,000,000,000 | 50,000,000,000 | 50,000,000,000 | 50,000,000,000 |
상기 약정 이외에 회사는 국민은행과 기업구매론약정(당분기말 : 한도 10,000백만원,전기말 : 한도 10,000백만원)과 신한은행과 전자방식매출채권담보대출약정(당분기 : 한도 2,500백만원 전기말 : 한도 2,500백만원)을 맺고 있습니다.
당분기말 현재 매입채무및기타채무 금액 중 공급자금융약정과 관련된 금융부채는 2,857백만원이며, 공급자가 금융기관으로부터 당분기말 현재 이미 대금을 수취한 금액은 315백만원입니다.
공급자금융약정에 해당하는 금융부채와 공급자금융약정에 해당하지 않는 금융부채의 지급기일에는 유의적인 차이가 없습니다.
공급자금융약정에 따라 금융기관에게 지급해야 할 금액은 회사의 정상영업주기 내에사용되는 운전자본의 일부로서 매입채무및기타채무와 유사한 성격과 기능을 지니고 있다고 판단하여 이를 매입채무및기타채무로 분류하고, 현금흐름표에서 관련현금흐름을 영업활동현금흐름으로 분류하고 있습니다.
(2) 회사가 타인으로부터 제공받는 지급보증의 내역
| (단위 : 원) |
| 금융기관 | 약정사항 | 보증금액 | |
|---|---|---|---|
| 당분기말 | 전기말 | ||
| 서울보증보험 | 공탁보증 | - | 60,000,000 |
| 합 계 | - | 60,000,000 | |
(3) 당분기말 현재 차입금 등과 관련하여 담보로 제공되어있는 자산내역은 다음과 같습니다.
| (단위 : 원) |
| 구분 | 제공처 | 내역 | 담보제공자산 | 장부금액 | 설정금액 |
| 유형자산 | 신한은행 | 차입금 담보 | 토지,건물 | 73,453,239,043 | 60,000,000,000 |
(4) 당분기말 현재 회사가 원고로서 진행 중인 소송은 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소소송 1건, 권리범위확인(특) 3건, 총 4건(전기말 : 4건)으로 소송가액은 없습니다. 또한 회사가 피고로서 진행중인 소송은 권리범위확인(특) 총 1건(전기말 : 1건)으로 소송가액은 없습니다.
| 관할법원 | 원고 | 피고 | 소송의 내용 | 소송가액 | 진행상황 |
| 서울고등법원 | 당사 | 보건복지부장관 | 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소 | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 에치케이이노엔 | 당사 | 권리범위확인(특) | - | 계류중 |
(5) 회사는 종속기업인 Contera Pharma A/S와 관련하여 개발 중인 의약품의 허가신청, 시판 승인 및 상용화 조건 달성 여부에 따라 조건부대가를 지급하는 약정을 체결하였습니다. 전기 중 회사는 해당 의약품의 임상을 중단하였으며, 이에 따라 미래에 지불할 가능성이 있는 금액을 0으로 평가하였습니다.
(6) 회사가 당분기말 현재 보유 중인 당기손익-공정가치측정 금융자산 중 TVM Life Science Innovation II SCSP에 대한 투자 약정금액은 총 USD 3,000,000이며, 현재까지 USD 2,848,568에 대한 납입이 완료되었습니다. 잔여금액 USD 151,432은 향후 업무집행사원의 출자이행요청에 따라 추가 납입예정이나, 현재 시점에 그 납입시기를 예상할 수 없습니다.
(7) 회사가 당분기말 현재 보유 중인 당기손익-공정가치측정 금융자산 중 KDB오픈이노베이션 제2호에 대한 투자 약정금액은 총 5억원이며, 현재까지 5억원 납입이 완료되었습니다.
(8) 회사는 종속기업인 ProteKt Therapeutics와 관련하여 개발 중인 의약품의 License 관련 판매 및 배당 등의 조건 달성 여부에 따라 조건부대가를 지급하는 약정을 체결하였습니다.
(9) 회사는 종속기업인 ProteKt Therapeutics와 자금조달약정을 통한 조건부지분인수계약을 체결하였습니다. 회사는 ProteKt Therapeutics로부터 미래에 주식 또는 현금을 받을 권리가 있습니다. 회사는 상기 약정과 관련하여 당기손익-공정가치금융자산을 인식하였으나, 전기 중 평가손실 4,145백만원이 발생하여 당분기말 현재 잔액이 없습니다.
(10) 회사는 종속기업인 JaguAHR Therapeutics와 자금조달약정을 통한 조건부 지분인수계약을 체결하였습니다. 회사는 JaguAHR Therapeutics로부터 미래에 주식 또는현금을 받을 권리가 있습니다. 당분기말 현재 회사는 상기 약정과 관련하여 당기손익-공정가치금융자산 1,135백만원(전기말 : 1,135백만원)을 계상하고 있습니다.
27. 특수관계자거래
(1) 종속기업 현황
| 기업명 | 지분율(%) | |
|---|---|---|
| 당분기말 | 전기말 | |
| Contera Pharma A/S | 99.33 | 99.33 |
| 부광메디카(주) | 100 | 100 |
| ProteKt Therapeutics | 97.24 | 97.24 |
| JaguAHR Therapeutics | 75.02 | 75.02 |
(2) 회사와 매출 등 거래 또는 채권ㆍ채무 잔액이 있는 기타특수관계자
|
구 분 |
당분기말 |
전기말 |
|---|---|---|
| 관계기업 | 덴탈플랫폼투자조합제1호 | 덴탈플랫폼투자조합제1호 |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | OCI홀딩스 주식회사 |
| (주)디씨알이 | (주)디씨알이 | |
| 오씨아이드림㈜ | 오씨아이드림㈜ | |
| OCI㈜ | OCI㈜ | |
| OCI정보통신 | OCI정보통신 |
(3) 매출 및 매입 등 거래
| (단위 : 원) |
| 구 분 | 기업명 | 당분기 | |
|---|---|---|---|
| 매출 등 | 매입 등 | ||
| 종속기업 | 부광메디카(주) | 80,069,740 | 331,530,400 |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | 16,646,721 | 5,805,473 |
| (주)디씨알이 | 1,883,182 | - | |
| 오씨아이드림㈜ | 2,486,000 | - | |
| OCI㈜ | 18,014,997 | 19,200,000 | |
| OCI정보통신 | - | 153,965,400 | |
| 합 계 | 119,100,640 | 510,501,273 | |
| (단위 : 원) |
| 구 분 | 기업명 | 전분기 | |
|---|---|---|---|
| 매출 등 | 매입 등 | ||
| 종속기업 |
Contera Pharma A/S |
19,989,800 | - |
| 부광메디카(주) | 13,847,214 | 327,211,000 | |
| 다이나세라퓨틱스(주) | 5,904,000 | - | |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | 17,823,292 | 9,333,026 |
| (주)디씨알이 | 5,525,818 | - | |
| 오씨아이드림㈜ | 4,503,000 | 63,908 | |
| OCI㈜ | 9,901,472 | 6,931,982 | |
| 합 계 | 77,494,596 | 343,539,916 | |
(4) 채권ㆍ채무의 주요 잔액
| (단위 : 원) |
| 구 분 | 기업명 | 당분기말 | ||
|---|---|---|---|---|
| 채권 | 채무 | |||
| 기타채권 | 매입채무 | 기타채무 | ||
| 종속기업 | 부광메디카(주) | 17,655,110 | 121,456,940 | 30,000,000 |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | 6,761,735 | - | 930,875 |
| 오씨아이드림㈜ | 784,300 | - | - | |
| OCI㈜ | 12,142,232 | 10,560,000 | - | |
| OCI정보통신 | - | - | 12,685,310 | |
| 합 계 | 37,343,377 | 132,016,940 | 43,616,185 | |
| (단위 : 원) |
| 구 분 | 기업명 | 전기말 | ||
|---|---|---|---|---|
| 채권 | 채무 | |||
| 기타채권 | 매입채무 | 기타채무 | ||
| 종속기업 | Contera Pharma A/S | 23,465,400 | - | 342,435,220 |
| 부광메디카(주) | 18,132,400 | 238,904,490 | 30,000,000 | |
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | 968,542 | - | 1,235,664 |
| 오씨아이드림㈜ | 1,725,350 | - | - | |
| OCI㈜ | - | 16,896,000 | - | |
| OCI정보통신 | - | - | 10,964,800 | |
| 합 계 | 44,291,692 | 255,800,490 | 384,635,684 | |
(5) 특수관계자와의 자금 거래
| (단위 : 원) |
| 구 분 | 기업명 | 당분기 | |||
|---|---|---|---|---|---|
| 현금출자 | 유상감자 | 현금배당 | 기타 | ||
| 주요 경영진 등 | - | - | - | - | |
| 합 계 | - | - | - | 0 | |
| (단위 : 원) |
| 구 분 | 기업명 | 전분기 | |||
|---|---|---|---|---|---|
| 현금출자 | 유상감자 | 현금배당 | 기타 | ||
| 종속기업 | ProteKt Therapeutics | - | - | - | 1,040,485,300 |
| 주요 경영진 등 | - | - | - | - | |
| 합 계 | - | - | - | 1,040,485,300 | |
(6) 주요 경영진에 대한 보상내역
주요 경영진은 등기이사, 미등기이사(상무)와 감사위원회 위원을 포함하고 있습니 다. 종업원 용역의 대가로서 주요 경영진에게 지급되었거나 지급된 보상금액은 다음과 같습니다.
| (단위 : 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 단기종업원 급여 | 1,259,979,712 | 938,875,700 |
| 퇴직급여 | 46,184,288 | 27,488,289 |
| 합 계 | 1,306,164,000 | 966,363,989 |
6. 배당에 관한 사항
가. 배당에 관한 사항
(1) 회사의 배당정책에 관한 사항
회사는 매사업연도 이익규모와 상법상 배당가능이익에 따라 차기 사업연도의 사업 계획 및 자금 소요계획을 종합적으로 감안하여 이익 규모에 따른 과거연도 배당성향 및 배당금을 기준으로 매 사업연도의 결산 결과에 따라 배당액을 결정합니다.
배당수준 및 자사주 매입 소각 계획 등의 향후 방향성은 급변하는 대내외 경제 변수 등에 따라 그 변동성이 매우 클 것으로 예상되며, 보고서 제출일 현재 그 방향성에 대한 예측가능성은 매우 낮습니다. 배당 결정시 사용되는 근거는 상법 제462조(이익의 배당)에 따른 배당가능이익 한도이며, 그외 잉여현금흐름 등의 별도 재무지표는 사용하지 않고 있습니다.
(2) 배당관련 예측가능성 제공에 관한 사항
(가) 정관상 배당절차 개선방안 이행 가부
| 구분 | 현황 및 계획 |
| 정관상 배당액 결정 기관 | 이사회,주주총회 |
| 정관상 배당기준일을 배당액 결정 이후로 정할 수 있는지 여부 | 제65기 주주총회(25.03.26)를 통해 정관개정하여 제66기 분기배당부터 적용 가능 |
| 배당절차 개선방안 이행 관련 향후 계획 | 25년 주주총회에서 분기배당관련 정관 개정 예정 |
(나) 배당액 확정일 및 배당기준일 지정 현황
| 구분 | 결산월 | 배당여부 | 배당액 확정일 |
배당기준일 | 배당 예측가능성 제공여부 |
비고 |
|---|---|---|---|---|---|---|
| 63기 결산배당 | 2022년 12월 | X | - | 2022년 12월 31일 | X | - |
| 64기 결산배당 | 2023년 12월 | X | - | 2023년 12월 31일 | X | - |
| 65기 결산배당 | 2024년 12월 | X | - | 2024년 12월 31일 | X | - |
(3) 기타 참고사항(배당 관련 정관의 내용 등)
정관의 배당관련 조항
- 배당에 관한 사항은 당사 정관 제45조의2(분기배당) 및 제46조(이익배당)에 따름
※ 제45조의2 (분기배당)
1) 이 회사는 사업연도 개시일부터 3월, 6월 및 9월 말일 현재의 주주에게 자본시
장과 금융투자업에 관한 법률 제165조의12에 의한 분기배당을 할 수 있다.
분기배당은 금전으로 한다.
2) 제1항의 분기배당은 이사회의 결의로 하되, 그 결의는 제1항의 각 기준일 이후
45일 내에 하여야 한다.
- 중략 -
※ 제46조 (이익배당)
1) 이익의 배당은 금전, 주식 및 기타의 재산으로 할 수 있다.
2) 제1항의 배당은 매 결산기 말 현재의 주주명부에 기재된 주주 또는 등록된 질권
자에게 지급한다.
※ 제47조 (배당금 지급 청구권의 소멸 시효)
1) 배당금의 지급 청구권은 5년간 이를 행사하지 아니하면 소멸 시효가 완성한다.
2) 제1항의 시효의 완성으로 인한 배당금은 이 회사에 귀속한다.
나. 최근 3사업연도 배당에 관한 사항
| 구 분 | 주식의 종류 | 당기 | 전기 | 전전기 |
|---|---|---|---|---|
| 제66기 1분기 | 제65기 | 제64기 | ||
| 주당액면가액(원) | 500 | 500 | 500 | |
| (연결)당기순이익(백만원) | -111 | -3,459 | -34,407 | |
| (별도)당기순이익(백만원) | 2,794 | -55,610 | 19,093 | |
| (연결)주당순이익(원) | -1 | -39 | -458 | |
| 현금배당금총액(백만원) | - | - | - | |
| 주식배당금총액(백만원) | - | - | - | |
| (연결)현금배당성향(%) | - | - | - | |
| 현금배당수익률(%) | 보통주 | - | - | - |
| 우선주 | - | - | - | |
| 주식배당수익률(%) | 보통주 | - | - | - |
| 우선주 | - | - | - | |
| 주당 현금배당금(원) | 보통주 | - | - | - |
| 우선주 | - | - | - | |
| 주당 주식배당(주) | 보통주 | - | - | - |
| 우선주 | - | - | - | |
| 구 분 | 제66기 1분기 | 제65기 | 제64기 | |
|---|---|---|---|---|
| 액면배당률(%) | 현금 | - | - | - |
| 주식 | - | - | - | |
| (개별)현금배당성향(%) | - | - | - | |
(주1) 주식배당수익률의 산정
= [{배당락 직후 주식의 종가+(1주당 배당주식수*배당락 직후 주식의 종가)}
/과거 1주일간 배당부 종가의 평균]-1
(주2) 현금배당수익률의 산정
= 1주당 현금배당금/과거 1주일간 배당부 종가의 평균
(주3) 배당성향의 산정(%) = 현금배당총액/당기순이익*100
다. 과거배당이력
| (단위: 회, %) |
| 연속 배당횟수 | 평균 배당수익률 | ||
|---|---|---|---|
| 분기(중간)배당 | 결산배당 | 최근 3년간 | 최근 5년간 |
| - | - | - | 0.152 |
(주1) 연속 배당 횟수는 1999년(제40기)부터 매년 발생된 현금 결산배당을 기준으로 작성하였습니다.
(주2) 평균 배당수익률은 현금배당과 주식배당수익률을 합산하여 작성하였습니다.
7. 증권의 발행을 통한 자금조달에 관한 사항
7-1. 증권의 발행을 통한 자금조달 실적
| [지분증권의 발행 등과 관련된 사항] |
증자(감자)현황
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 원, 주) |
| 주식발행 (감소)일자 |
발행(감소) 형태 |
발행(감소)한 주식의 내용 | ||||
|---|---|---|---|---|---|---|
| 종류 | 수량 | 주당 액면가액 |
주당발행 (감소)가액 |
비고 | ||
| 2024.03.29 | - | 보통주 | 2,608,378 | 500 | 500 | 이익소각 (주6) |
| 2021.03.19 | 주식배당 | 보통주 | 6,225,071 | 500 | 500 | 제28회차 주식배당 (주5) |
| 2020.03.13 | 주식배당 | 보통주 | 3,047,548 | 500 | 500 | 제27회차 주식배당 (주4) |
| 2020.02.13 | - | 보통주 | 1,740,937 | 500 | - | 이익소각 (주3) |
| 2019.03.15 | 주식배당 | 보통주 | 14,661,084 | 500 | 500 | 제26회차 주식배당 (주2) |
| 2018.03.16 | 주식배당 | 보통주 | 4,305,799 | 500 | 500 | 제25회차 주식배당 (주1) |
(주1) 2018년 03월 16일 개최된 제58기 정기주주총회에서 주식배당 10%를 결의함에 따라 배당 주식총수 4,305,799주, 배당 후 총 발행 주식총수 48,870,283주, 배당 후 자본금 총액 24,435,141,500원입니다.
(주2) 2019년 03월 15일 개최된 제59기 정기주주총회에서 주식배당 30%를 결의함에 따라 배당 주식총수 14,661,084주, 배당 후 총 발행 주식총수 63,531,367주, 배당 후 자본금 총액 31,765,683,500원입니다.
(주3) 2020년 02월 12일 개최된 이사회에서 자기주식 1,740,937주에 대한 이익소각을결의함에 따라 소각 후 총 발행 주식총수 61,790,430주, 소각 후 자본금 총액 31,765,683,500원입니다.
(주4) 2020년 03월 13일 개최된 제60기 정기주주총회에서 주식배당 5%를 결의함에 따라 배당 주식총수 3,047,548주, 배당 후 총 발행 주식총수 64,837,978주, 배당 후 자본금 총액 33,289,457,500원입니다.
(주5) 2021년 03월 19일 개최된 제61기 정기주주총회에서 주식배당 10%를 결의함에따라 배당 주식총수 6,225,071주, 배당 후 총 발행 주식총수 71,063,049주, 배당 후 자본금 총액 36,401,993,000원입니다.
(주6) 2024년 03월 22일 개최된 이사회에서 자기주식 2,608,378주에 대한 이익소각을결의함에 따라 소각 후 총 발행 주식총수 68,454,671주, 소각 후 자본금 총액 36,401,993,000원입니다
(나) 자본금 변동현황
| (단위 : 주, 원, %) |
| 주식발행 (감소) 일자 |
발행(감소) 형태 | 증가(감소)한 주식의 내용 | 증(감)자 후 자본금 |
신주의 배정방법 |
증자 비율 |
|||
|---|---|---|---|---|---|---|---|---|
| 종류 | 수량 | 주 당 액면가액 |
주 당 발행가액 |
|||||
| 60.10.17 | 설립자본금 | 보통주 | 18,494 | 1,000 | 1,000 | 18,494,000 | 발기설립 | - |
| 75.03.25 | 유상증자 | 보통주 | 21,506 | 1,000 | 1,000 | 40,000,000 | 주주배정 | 116 |
| 75.04.23 | 유상증자 | 보통주 | 20,000 | 1,000 | 1,000 | 60,000,000 | 주주배정 | 50 |
| 75.08.16 | 유상증자 | 보통주 | 20,000 | 1,000 | 1,000 | 80,000,000 | 주주배정 | 33 |
| 75.12.02 | 유상증자 | 보통주 | 20,000 | 1,000 | 1,000 | 100,000,000 | 주주배정 | 25 |
| 79.03.20 | 유상증자 | 보통주 | 300,000 | 1,000 | 1,000 | 400,000,000 | 주주배정 | 300 |
| 80.09.24 | 유상증자 | 보통주 | 100,000 | 1,000 | 1,000 | 500,000,000 | 주주배정 | 25 |
| 80.09.26 | 유상증자 | 보통주 | 250,000 | 1,000 | 1,000 | 750,000,000 | 주주배정 | 50 |
| 81.09.25 | 유상증자 | 보통주 | 200,000 | 1,000 | 1,000 | 950,000,000 | 주주배정 | 27 |
| 85.02.08 | 유상증자 | 보통주 | 50,000 | 1,000 | 1,000 | 1,000,000,000 | 주주배정 | 5.2 |
| 86.10.02 | 무상증자 | 보통주 | 900,000 | 1,000 | 1,000 | 1,900,000,000 | 주주배정 | 90 |
| 87.02.07 | 액면병합 | 보통주 | 380,000 | 5,000 | 5,000 | 1,900,000,000 | - | - |
| 88.04.18 | 무상증자 | 보통주 | 620,000 | 5,000 | 5,000 | 5,000,000,000 | 주주배정 | 163 |
| 88.07.16 | 유상증자 | 보통주 | 200,000 | 5,000 | 9,500 | 6,000,000,000 | 일반공모 | 20 |
| 90.05.26 | 주식배당 | 보통주 | 72,000 | 5,000 | 5,000 | 6,360,000,000 | 주주배정 | 6 |
| 92.05.28 | 주식배당 | 보통주 | 63,600 | 5,000 | 5,000 | 6,678,000,000 | 주주배정 | 5 |
| 93.05.27 | 주식배당 | 보통주 | 64,400 | 5,000 | 5,000 | 7,000,000,000 | 주주배정 | 4.8 |
| 94.05.28 | 주식배당 | 보통주 | 70,000 | 5,000 | 5,000 | 7,350,000,000 | 주주배정 | 5 |
| 95.05.27 | 주식배당 | 보통주 | 70,000 | 5,000 | 5,000 | 7,700,000,000 | 주주배정 | 4.8 |
| 96.05.30 | 주식배당 | 보통주 | 80,000 | 5,000 | 5,000 | 8,100,000,000 | 주주배정 | 5.2 |
| 98.05.30 | 주식배당 | 보통주 | 324,000 | 5,000 | 5,000 | 9,720,000,000 | 주주배정 | 20 |
| 98.07.11 | 액면분할 | 보통주 | 19,440,000 | 500 | 500 | 9,720,000,000 | - | - |
| 99.05.29 | 주식배당 | 보통주 | 1,944,000 | 500 | 500 | 10,692,000,000 | 주주배정 | 10 |
| 00.05.27 | 주식배당 | 보통주 | 1,028,850 | 500 | 500 | 11,206,425,000 | 주주배정 | 5 |
| 04.09.30 | 무상증자 | 보통주 | 2,160,350 | 500 | 500 | 12,286,600,000 | 주주배정 | 10 |
| 07.05.25 | 주식배당 | 보통주 | 1,186,260 | 500 | 500 | 12,879,730,000 | 주주배정 | 5 |
| 08.05.30 | 주식배당 | 보통주 | 1,285,765 | 500 | 500 | 13,522,612,500 | 주주배정 | 5 |
| 12.03.16 | 주식배당 | 보통주 | 1,299,375 | 500 | 500 | 14,172,300,000 | 주주배정 | 5 |
| 13.03.15 | 주식배당 | 보통주 | 1,342,721 | 500 | 500 | 14,843,660,500 | 주주배정 | 5 |
| 14.03.14 | 주식배당 | 보통주 | 1,409,690 | 500 | 500 | 15,548,505,500 | 주주배정 | 5 |
| 15.03.20 | 주식배당 | 보통주 | 2,960,018 | 500 | 500 | 17,028,514,500 | 주주배정 | 10 |
| 15.10.23 | 주식매수선택권행사 | 보통주 | 32,500 | 500 | 16,580 | 17,044,764,500 | - | 0.1 |
| 16.03.18 | 주식배당 | 보통주 | 3,258,992 | 500 | 500 | 18,674,260,500 | 주주배정 | 10 |
| 16.12.06 | 주식매수선택권행사 | 보통주 | 39,000 | 500 | 16,580 | 18,693,760,500 | - | 0.1 |
| 17.03.17 | 주식배당 | 보통주 | 7,176,963 | 500 | 500 | 22,282,242,000 | 주주배정 | 20 |
| 18.03.16 | 주식배당 | 보통주 | 4,305,799 | 500 | 500 | 24,435,141,500 | 주주배정 | 10 |
| 19.03.15 | 주식배당 | 보통주 | 14,661,084 | 500 | 500 | 31,765,683,500 | 주주배정 | 30 |
| 20.02.13 | 이익소각 | 보통주 | -1,740,937 | 500 | - | 31,765,683,500 | - | - |
| 20.03.13 | 주식배당 | 보통주 | 3,047,548 | 500 | 500 | 33,289,457,500 | 주주배정 | 5 |
| 21.03.19 | 주식배당 | 보통주 | 6,225,071 | 500 | 500 | 36,401,993,000 | 주주배정 | 10 |
| 24.03.29 | 이익소각 | 보통주 | -2,608,378 | 500 | - | 36,401,993,000 | - | - |
| [채무증권의 발행 등과 관련된 사항] |
채무증권 발행실적
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 원, %) |
| 발행회사 | 증권종류 | 발행방법 | 발행일자 | 권면(전자등록)총액 | 이자율 | 평가등급 (평가기관) |
만기일 | 상환 여부 |
주관회사 |
|---|---|---|---|---|---|---|---|---|---|
| - | - | - | - | - | - | - | - | - | - |
| - | - | - | - | - | - | - | - | - | - |
| 합 계 | - | - | - | - | - | - | - | - | - |
기업어음증권 미상환 잔액
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
1년초과 2년이하 |
2년초과 3년이하 |
3년 초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | |
단기사채 미상환 잔액
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
합 계 | 발행 한도 | 잔여 한도 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
회사채 미상환 잔액
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
신종자본증권 미상환 잔액
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 5년이하 |
5년초과 10년이하 |
10년초과 15년이하 |
15년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
조건부자본증권 미상환 잔액
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | - | |
7-2. 증권의 발행을 통해 조달된 자금의 사용실적
해 당 사 항 없 음
8. 기타 재무에 관한 사항
가. 재무제표 재작성 등 유의사항
회사는 2011년 4월 1일 이후에 개시하는 연차보고기간부터 국제회계기준을 채택하여 제정한 한국채택국제회계기준을 적용하고 있으며, 첨부된 재무제표는 연결재무제표입니다. 한국채택국제회계기준은 국제회계기준위원회(IASB)가 발표한 기준서, 개정서, 해석서 중 대한민국이 채택한 내용을 의미합니다. 기업회계기준서 제1101호에 따른 한국기업회계기준(과거회계기준)에서 한국채택국제회계기준으로의 전환일은 2010년 4월 1일입니다.
한국채택국제회계기준은 재무제표 작성시 중요한 회계추정의 사용을 허용하고 있으며, 회계정책을 적용함에 있어 경영진의 판단을 요구하고 있습니다. 보다 복잡하고 높은 수준의 판단이 요구되는 부분이나 중요한 가정 및 추정이 요구되는 부분은 "연결재무제표에 대한 주석3"에서 설명하고 있습니다.
당기 연결재무제표는 보고기간말인 2025년 03월 31일 현재 유효하거나 조기 도입한 한국채택국제회계기준에 따라 작성되었습니다.
- 합병, 분할, 자산양수도, 영업양수도
당사는 2024년 03월 22일 자회사 Contera Pharma A/S의 보통주 159,380주에 관한 취득에 대한 타법인 주식 및 출자증권 양수결정에 대한 주요사항 보고서를 제출하였으며, 2024년 04월 01일 최종 양수도대금 지급 및 주식 이전이 완료되어 합병등 종료보고서를 제출하였습니다.
본 지분 양수 관련 상세 내용은 2024년 03월 22일 최초 공시된 주요사항보고서(타법인주식 및 출자증권 양수결정)를 참고하시기 바랍니다.
| 구 분 | 일 자 | 비 고 |
| 외부평가기간 | 2024년 03월 05일 ~ 2024년 03월 21일 | 지안회계법인 |
| 이사회결의일 | 2024년 03월 22일 | - |
| 주요사항보고서 제출일 | 2024년 03월 22일 | - |
| 매매 체결일 | 2024년 04월 01일 | - |
| 거래완료일 | 2024년 04월 01일 | - |
나. 기타 계정재분류 사항
해 당 사 항 없 음
다. 연결 및 별도재무제표로의 전환
당사는 제55기 이후 재무제표는 연결기준으로 작성되었으며, 제55기 이전의 재무제표는 개별재무제표입니다. 또한 회사는 한국채택국제회계기준에 따라 2013년 1월 1일 별도재무제표로 전환되었습니다. 별도재무제표로의 전환에 따라 관계기업 투자는원가법으로 측정하고 있습니다.
종속기업, 공동기업 및 관계기업 투자는 직접적인 지분투자에 근거하여 원가로 측정하고 있으며, 다만 한국채택국제회계기준으로의 전환일 시점에는 전환일 시점의 과거 회계기준에 따른 장부금액을 간주원가로 사용하였습니다. 또한, 종속기업, 공동기업 및 관계기업으로부터 수취하는 배당금은 배당에 대한 권리가 확정되는 시점에 당기손익으로 인식하고 있습니다.
라. 외부감사인의 감사 여부
2025년 03월 31일 현재의 연결재무제표 및 재무제표는 외부감사인의 감사(검토)를 받지 않은 재무제표이며, 비교표시된 2024년 12월 31일과 2023년 12월 31일 현재의연결재무제표 및 재무제표는 외부감사인의 감사(검토)를 받은 재무제표입니다.
마. 선택가능한 회계처리 대안중 연결회사가 선택한 회계처리방법
유,무형자산의 후속측정 방법으로 한국채택국제회계기준에서는 원가모형과 재평가모형을 규정하고 있습니다. 연결회사는 토지에 대해서는 재평가모형을 적용하고, 그외 유,무형자산에 대해서는 원가법을 적용하고 있습니다. 또한, 연결회사는 확정급여제도에서 발생하는 보험수리적손익을 발생한 기간의 기타포괄손익으로 인식하고 즉시 이익잉여금으로 대체하며, 그 이후의 기간에 당기손익으로 재분류하지 않고 있습니다.
바. 재무제표의 작성 기준 및 유의적인 회계정책
"3.연결재무제표 주석 2" 및 "5.재무제표 주석 2"을 참조하시기 바랍니다.
사. 추정불확실성의 주요 원천(유의적인 회계적 추정과 가정)
"3.연결재무제표 주석 3" 및 "5.재무제표 주석 3"을 참조하시기 바랍니다.
아. 대손충당금 설정현황(연결기준)
(1) 최근 3사업연도의 계정과목별 대손충당금 설정내역
| (단위 : 원) |
| 구 분 | 계정과목 | 채권 총액 | 대손충당금 | 대손충당금 설정률 |
|---|---|---|---|---|
|
제66기 |
매출채권 | 23,580,209,541 | 126,538,022 | 0.5% |
| 미수금 | 688,934,243 | - | 0.0% | |
| 선급금 | 272,944,099 | - | 0.0% | |
| 소계 | 24,542,087,883 | 126,538,022 | 0.5% | |
| 제65기 | 매출채권 | 23,703,786,336 | 144,945,672 | 0.6% |
| 미수금 | 394,105,010 | - | 0.0% | |
| 선급금 | 331,495,303 | - | 0.0% | |
| 소계 | 24,429,386,649 | 144,945,672 | 0.6% | |
| 제64기 | 매출채권 | 36,475,332,304 | 746,055,351 | 2.0% |
| 미수금 | 901,226,734 | - | 0.0% | |
| 선급금 | 912,039,460 | - | 0.0% | |
| 소계 | 38,288,598,498 | 746,055,351 | 2.0% |
(2) 최근 3사업연도의 대손충당금 변동현황
| (단위 : 원) |
| 구 분 | 제66기 1분기 | 제65기 | 제64기 |
|---|---|---|---|
| 1. 기초 대손충당금 잔액합계 | 144,945,672 | 746,055,351 | 5,812,916,317 |
| 2. 순대손처리액(①-②±③) | (7,508,314) | (46,564,760) | (170,335,870) |
| ① 대손처리액(상각채권액) | (7,539,796) | (46,690,688) | (262,151,225) |
| ② 상각채권회수액 | 31,482 | 125,928 | 91,815,355 |
| 3. 대손상각비 계상(환입)액 | (10,899,336) | (554,544,919) | (4,896,525,096) |
| 4. 기말 대손충당금 잔액합계 | 126,538,022 | 144,945,672 | 746,055,351 |
(3) 매출채권 관련 대손충당금 설정 방침
연결회사는 미래 전망 정보에 근거하여 매출채권에 대한 기대 신용손실을 주기적으로 평가하고 있습니다. 이러한 신용위험을 관리하기 위하여 고객과 거래 상대방의 재무 상태와 과거 경험 및 기타 요소들을 종합적으로 고려하여 주기적으로 재무 신용도를 평가하고 있으며, 고객과 거래상대방 각각에 대한 신용 한도를 설정하고 있습니다. 당사의 매출채권과 기타자산(미수금, 선급금) 등에 대한 평균 회수기간은 3개월~6개월이 소요되며, 당사는 평균적으로 정상 회수 기일을 경과한 채권에 대하여 연체채권으로 관리하고 있습니다. 당사는 개별적으로 파악된 손상 채권을 제외한 연체채권에 대해서 집합 평가를 통하여 손상차손을 인식하고 있습니다. 또한, 당사는 과거 경험에 따라 채권 발생일로부터 3년이 경과한 매출채권은 일반적으로 회수되지 않으므로 전액 손상 채권으로 분류하고 있습니다. 대손금의 해당 여부를 판단하는 대손처리기준은 법인세법 시행령 제61조제2항 각호와 같습니다.
기타자산 중 미수금 및 선급금 등은 과거 대손 경험이 없으며, 대부분 담보 등의 채권확보가 되었으므로 대손충당금을 설정하지 않았습니다.
(가) 당기 대손예상액 및 대손충당금 설정 내역
| (단위 : 원) |
| 구 분 | 당분기말 | 전기말 |
| 연체되지 않은 채권 | 23,034,475,973 | 21,649,178,866 |
| 6개월 이하 연체 | 386,243,328 | 497,829,298 |
| 6개월 초과 연체 | 92,394,208 | 53,562,684 |
| 1년 초과 연체 | 64,685,648 | 87,483,931 |
| 소계 | 23,580,209,541 | 23,703,786,336 |
| 손상채권 | (126,538,022) | (144,945,672) |
| 합계 | 23,453,671,519 | 23,558,840,664 |
매출채권에 대해 전체 기간 기대신용손실을 손실충당금으로 인식하는 간편법을 적용합니다. 기대신용손실을 측정하기 위해 매출채권은 신용위험 특성과 경과일을 기준으로 구분하였습니다.
자. 재고자산의 보유 및 실사내역 등 (연결기준)
(1) 최근 3사업연도의 재고자산의 사업부문별 보유현황
| (단위 : 원) |
| 사업부문 | 계정과목 | 제66기 1분기 | 제65기 | 제64기 |
|---|---|---|---|---|
| 의약품 및 의약외품 |
상 품 | 3,792,057,919 | 4,429,024,882 | 6,396,505,146 |
| 제 품 | 12,367,335,335 | 12,446,198,077 | 16,831,157,664 | |
| 재 공 품 | 8,659,358,642 | 6,960,060,684 | 8,690,440,542 | |
| 원 재 료 | 15,004,283,038 | 16,146,468,297 | 22,426,287,094 | |
| 저 장 품 | 4,905,778 | 9,788,140 | 4,591,534 | |
| 미 착 품 | 1,839,236,581 | 1,675,501,694 | 2,482,856,039 | |
| 합 계 | 41,667,177,293 | 41,667,041,774 | 56,831,838,019 | |
| 총자산대비 재고자산 구성비율(%) [재고자산÷기말자산총계×100] |
11.18% | 11.17% | 13.25% | |
| 재고자산회전율(회수) [연환산 매출원가÷{(기초재고+기말재고)÷2}] |
2.58회 | 1.74회 | 1.65회 |
|
(2) 재고자산의 실사내역 등
연결회사는 감사인의 입회하에 재고자산 실사를 실시하였으며, 재고자산 실사장소, 실사일자 및 실사입회자의 내역은 다음과 같습니다.
(가) 최근 재고자산 실사장소, 실사일자 및 실사입회자
| 법인명 | 실사장소 | 실사일자 | 실사입회자 |
| 부광약품(주) | 안산공장 | 2025년 1월 2일 | 안진회계법인 |
| 평택 위탁창고 | 2025년 1월 2일 | 안진회계법인 |
(나) 재고자산 평가현황
| (2025년 03월 31일) | (단위 : 원) |
|
| (2024년 12월 31일) | (단위 : 원) |
| 계정과목 | 취득원가 | 보유금액 | 당기재고자산 평가충당금 |
기말잔액 | 비 고 |
|---|---|---|---|---|---|
| 상 품 | 5,201,680,441 | 5,201,680,441 | (772,655,559) | 4,429,024,882 | - |
| 제 품 | 13,573,873,054 | 13,573,873,054 | (1,127,674,977) | 12,446,198,077 | - |
| 재 공 품 | 6,960,060,684 | 6,960,060,684 | - | 6,960,060,684 | - |
| 원 재 료 | 17,299,121,850 | 17,299,121,850 | (1,152,653,553) | 16,146,468,297 | - |
| 저 장 품 | 9,788,140 | 9,788,140 | - | 9,788,140 | - |
| 미 착 품 | 1,675,501,694 | 1,675,501,694 | - | 1,675,501,694 | - |
| 합 계 | 44,720,025,863 | 44,720,025,863 | (3,052,984,089) | 41,667,041,774 | - |
차. 금융상품 공정가치 평가에 관한 사항
금융상품의 공정가치와 그 평가 방법은 "3. 연결재무제표 주석"의 "4. 공정가치" 항목을 참조하시기 바랍니다.
카. 유형자산 공정가치 평가에 관한 사항
(1) 토지의 공시지가
당분기와 전분기말 현재 연결회사가 보유하고 있는 토지의 공시지가 내역은 다음과 같습니다.
| (단위 : 원) |
| 지역 | 소재지 | 장부가액 | 공시지가 | ||
|---|---|---|---|---|---|
| 당분기말 | 전분기말 | 당분기말 | 전분기말 | ||
| 서울 본사 | 서울 동작구 상도로 7 | 69,694,250,000 | 56,313,300,000 | 31,261,240,620 | 31,004,795,380 |
| 안산공장 | 경기도 안산시 단원구 능안로 47외 | 43,244,250,000 | 36,242,800,000 | 23,475,450,000 | 23,207,747,500 |
| 기타 | 제주특별자치도 제주시 국기로 14 | - | 319,000,000 | - | 266,844,200 |
| 합계 | 112,938,500,000 | 92,875,100,000 | 54,736,690,620 | 54,479,387,080 | |
(2) 유형자산 장부가액의 변동
당분기와 전분기 중 유형자산의 변동내용은 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 기초순장부가액 | 취득 | 처분 | 기타증감액(*) | 감가상각비 | 당기말순장부가액 |
|---|---|---|---|---|---|---|
|
토지 |
113,313,500,000 | - | (375,000,000) | - | - | 112,938,500,000 |
|
건물 |
22,042,387,597 | - | (42,279,723) | (422,583,248) | - | 21,577,524,626 |
|
구축물 |
222,342,226 | - | - | (15,666,062) | - | 206,676,164 |
|
기계장치 |
1,245,644,456 | 1,600,817,491 | (8,000) | (184,963,822) | - | 2,661,490,125 |
|
차량운반구 |
42,216,324 | - | (18,567,871) | (5,832,224) | - | 17,816,229 |
|
공구기구 |
1,270,839,598 | 436,177,000 | (3,000) | (147,087,432) | - | 1,559,926,166 |
|
비품 |
1,968,969,376 | 136,087,406 | - | (142,662,604) | 47,278,037 | 2,009,672,215 |
| 건설중인자산 | 311,171,100 | 129,900,000 | (251,790,000) | 0 | - | 189,281,100 |
|
합 계 |
140,417,070,677 | 2,302,981,897 | (687,648,594) | (918,795,392) | 47,278,037 | 141,160,886,625 |
(*) 기타증감액은 환율변동으로 인한 환산차이로 구성되어 있습니다.
| (전분기) | (단위: 원) |
| 구 분 | 기초순장부가액 | 취득 | 처분 | 기타증감액(*) | 감가상각비 | 전기말 순장부가액 |
|---|---|---|---|---|---|---|
| 토 지 | 92,875,100,000 | - | - | - | - | 92,875,100,000 |
| 건 물 | 23,735,300,197 | - | - | - | (423,228,138) |
23,312,072,059 |
| 구축물 | 232,739,888 | - | - | - | (14,441,087) |
218,298,801 |
| 기계장치 | 1,247,307,776 | - | - | - | (188,604,120) |
1,058,703,656 |
| 차량운반구 | 76,833,334 | - | - | - | (13,185,286) | 63,648,048 |
| 공구기구 | 994,536,545 | - | - | - | (100,394,418) |
894,142,127 |
| 비 품 | 1,819,579,180 | 43,707,465 | - | (5,265,838) | (37,528,962) |
1,820,491,845 |
| 합 계 | 120,981,396,920 | 43,707,465 | - | (5,265,838) | (777,382,011) | 120,242,456,536 |
(*) 기타증감액은 환율변동으로 인한 환산차이로 구성되어 있습니다.
(3) 유형자산 공정가치 평가
연결회사의 토지는 2024년 12월 31일(서울특별시 동작구 및 안산시 단원구 소재 토지)을 기준일로 하여 독립된 평가 기관에 의하여 재평가되었습니다. 평가는 비교표 준지공시지가를 기준하여 평가한 금액과 독립적인 제3자와의 거래 조건에 따른 거래사례비교법에 의해 평가한 금액에 근거하여 수행되었습니다. 이연법인세를 차감한 후의 재평가잉여금 77,345백만원은 기타포괄손익으로 인식하고 자본항목 중 기타자본항목으로 표시하고 있으며, 동 금액은 주주에 대한 배당금의 재원으로 사용할 수 없습니다. 토지를 역사적 원가로 인식하는 장부가액은 없습니다.
IV. 회계감사인의 감사의견 등
1. 외부감사에 관한 사항
가. 회계감사인의 명칭 및 감사의견 등
| 사업연도 | 구분 | 감사인 | 감사의견 | 의견변형사유 | 계속기업 관련 중요한 불확실성 |
강조사항 | 핵심감사사항 |
|---|---|---|---|---|---|---|---|
| 제66기 1분기 (당기) |
감사보고서 | 삼일회계법인 | - | - | - | - | - |
| 연결감사 보고서 |
삼일회계법인 | - | - | - | - | - | |
| 제65기 (전기) |
감사보고서 | 안진회계법인 | 적정의견 | - | - | - | 종속기업투자주식(Contera Pharma A/S) 손상 검사 |
| 연결감사 보고서 |
안진회계법인 | 적정의견 | - | - | - | 종속기업(ProteKt Therapeutics)과 관련한 무형자산 손상 검사 | |
| 제64기 (전전기) |
감사보고서 | 안진회계법인 | 적정의견 | - | - | - | 종속기업투자주식(Contera Pharma A/S) 손상 검사 |
| 연결감사 보고서 |
안진회계법인 | 적정의견 | - | - | - | 종속기업(Contera Pharma A/S)과 관련한 무형자산 손상 검사 |
나. 회계감사용역 체결현황
| (단위 : 백만원, 시간) |
| 사업연도 | 감사인 | 내 용 | 감사계약내역 | 실제수행내역 | ||
|---|---|---|---|---|---|---|
| 보수 | 시간 | 보수 | 시간 | |||
| 제66기(당기) | 삼일회계법인 | 연결재무제표 및 별도재무제표에 대한 결산,반기,중간감사,재고실사,내부회계관리제도 감사에 관한 사항 |
165 | 1,750 | - | - |
| 제65기(전기) | 안진회계법인 | 연결재무제표 및 별도재무제표에 대한 결산,반기,중간감사,재고실사,내부회계관리제도 감사에 관한 사항 |
320 | 2,710 | 338 | 2,606 |
| 제64기(전전기) | 안진회계법인 | 연결재무제표 및 별도재무제표에 대한 결산,반기,중간감사,재고실사,내부회계관리제도 감사에 관한 사항 |
320 | 2,600 | 338 | 2,606 |
-감사 소요기간
| 사업연도 | 연간 감사 | 분반기 검토 | ||
|---|---|---|---|---|
| 기 간 | 일수 | 기 간 | 일수 | |
| 제66기 (당기) |
- | - | - | - |
| 제65기 (전기) |
25.02.03~25.02.14 | 10일간 | 24.07.22~24.08.02 | 10일간 |
| 제64기 (전전기) |
24.02.08~24.02.23 | 10일간 | 23.07.24~23.08.04 | 10일간 |
다. 회계감사인의 변경
| 사업연도 | 감사인 | 비고 |
| 제66기 | 삼일회계법인 | 외감법에 따라 제66기와 연속하는 2개 사업연도에 대하여 삼일회계법인과 계약함. |
| 제63기 | 안진회계법인 | 외감범 제11조 제1항 및 제2항등에 의거 금융감독원으로부터 외부감사인 지정 통보를 받아 제63기와 연속하는 2개 사업연도에 대하여 안진회계법인과 계약함. |
| 제62기 | 삼일회계법인 | 외감법에 따라 제62기와 연속하는 2개 사업연도에 대하여 삼일회계법인과 재계약함. |
라. 회계감사인과의 비감사용역 계약체결 현황
| 사업연도 | 계약체결일 | 용역내용 | 용역수행기간 | 용역보수 | 비고 |
|---|---|---|---|---|---|
| 제66기(당기) | - |
- | - | - | - |
| 제65기(전기) | 2024.07.23 2024.04.18 |
공시효율화 솔루션 공급계약 혁신형제약기업 연차보고 제출관련 합의된절차 수행 |
2024.08.05~2027.08.04 2024.04.18~2024.04.23 |
20,000,000 2,000,000 |
- |
| 제64기(전전기) | 2023.12.15 2023.08.09 2023.05.01 2023.05.23 |
세무자문 용역 업무 제출관련 합의된절차 수행 |
2024.01.04~2024.03.27 2023.08.09~2023.10.11 2023.05.01~2024.04.30 2023.05.23~2023.05.31 |
- 88,000,000 6,000,000 2,000,000 |
- |
마. 내부감사기구와의 커뮤니케이션
| 구분 | 일자 | 참석자 | 방식 | 주요 논의 내용 |
|---|---|---|---|---|
| 1 | 2024.04.03 | 회사측 : 감사위원회 3인 감사인측 : 업무수행이사, 담당회계사 등 3인 |
대면회의 | 지배기구와의 필수 커뮤니케이션 사항, 전반감사계획 등 |
| 2 | 2024.10.22 | 회사측 : 감사위원회 3인 감사인측 : 업무수행이사, 담당회계사 등 3인 |
대면회의 |
감사계획단계의 유의적 위험 및 핵심감사사항, 전반감사계획 등 |
| 3 | 2025.02.27 | 회사측 : 감사위원회 3인 감사인측 : 업무수행이사, 담당회계사 등 3인 |
대면회의 | 2024년 재무제표감사 업무 수행 결과보고 |
2. 내부통제에 관한 사항
가. 내부통제
당사의 내부감시장치는 다음과 같으며 그 기능은 다음과 같습니다.
- 이사회 : 이사의 직무 집행을 감독합니다.
- 감사위원회 : 이사의 직무 집행을 감사합니다. 이를 위하여 이사에 대하여 영업에
관한 보고를 요구하거나 회사의 업무상태와 재산상태를 조사합니다.
- 내부감사부서 : 각 부서의 업무를 감사합니다. 이를 위하여 일상감사, 정기감사, 수
시감사, 특별감사, 시재감사를 수행합니다.
- 기타의 내부감시장치 : 감사위원회는 직무를 수행하기 위하여 필요한 때에는 자회
사에 대하여 영업의 보고를 요구하거나 자회사의 업무상태와 재산상태를 조사합니
다. 보고서 제출기준일 현재 내부감시장치는 효과적으로 작동되고 있으며, 감사
결과 지적사항 등은 없습니다.
나. 내부회계관리제도
대상기간 중 대표이사, 내부회계관리자 및 회계감사인이 내부회계관리제도에 대한 문제점 또는 중요한 개선방안 등의 지적사항은 없습니다.
3. 연결대상 종속회사 감사
당분기말 현재 종속회사들의 감사인은 아래와 같습니다.
| 종속회사 | 감사인 |
| Contera Pharma A/S | PKF Munkebo Eriksen Funch |
| 부광메디카주식회사 | 삼영회계법인 |
| ProteKt Therapeutics | Brightman Almagor Zohar & Co.(주1) |
| JaguAHR Therapeutics | Forvis Mazars |
(주1) A Firm in the Deloitte Global Network
V. 이사회 등 회사의 기관에 관한 사항
1. 이사회에 관한 사항
가. 이사회의 구성 개요
당사의 이사회는 사내이사 2명, 사외이사 3명 총 5명으로 구성되어 있으며, 사내이사안미정이 이사회 의장을 맡고 있습니다.
(1) 이사회내 위원회
당사는 정관 제 35조의 3에 따라 다음의 위원회를 구성하고 있습니다.
정관 제 35 조의 3 (위원회)
1) 이 회사는 이사회내 다음의 위원회를 둔다.
가) 감사위원회
나) 보상위원회
다) ESG위원회
라) 기타 이사회가 필요하다고 인정하는 위원회
※ 감사위원회는 "VI.이사회 등 회사의 기관에 관한 사항"의 "2. 감사제도에
관한 사항"을 참고하시기 바랍니다.
※ 보상위원회와 ESG위원회는 2024년 03월 22일 개최된 제64기 정기주주총회
결의를 통한 정관 변경으로 신설되었으며, 보고서 제출일 현재 구성되어 있지 않습니다.
(2) 이사후보의 인적사항에 관한 주총 전 공시여부 및 주주의 추천여부 공시 및
주총 소집통지서로 인적사항 공개
(3) 이사회 구성원 현황
(기준일: 2025년 03월 31일)
| 직 명 (상근여부) |
성 명 | 주요 경력 | 담당업무 | 최대주주등과의 이해관계 |
대내외 교육 참여현황 |
|---|---|---|---|---|---|
| 사내이사 회장 (상 근) |
안미정 | 前,특허청 심판관 前,산업부 R/D 전략기획단 MD 前,메디포스트(주) 사외이사/감사위원 前,제넥신 사외이사/감사위원 前,(주)SL바이젠 대표이사 前, OCI홀딩스(주) 사외이사/이사회의장 現, 연세대학교 신소재공학과 겸임교수 現, 특허법인 지평 대표변리사 |
경영전반 | 최대주주인 법인의 계열회사 사내이사 |
- |
| 사내이사 대표이사 사장 (상 근) |
이제영 | 前,OCI㈜ 법무부, 감사실 전무 前,OCI홀딩스 법무실 전무 |
경영전반 | 최대주주인 법인의 계열회사 사내이사 |
- |
| 사외이사 (비 상 근) |
정길영 |
前, 감사원 감사위원 現,명지대학교 미래융합대학 |
감사위원회 위원장 |
최대주주인 법인의 계열회사 사외이사/감사위원 |
- |
| 사외이사 (비 상 근) |
전형수 | 前,서울지방국세청장 現,김앤장 법률사무소 고문 |
감사위원회 위원 | 최대주주인 법인의 계열회사 사외이사/감사위원 |
|
| 사외이사 (비 상 근) |
이상길 | 前,연세암병원 식도암 센터장 前,연세암병원 위암 센터장 現,연세의료원 대외협력처 처장 現,연세의료원 세브란스병원 교수 |
감사위원회 위원 | 최대주주인 법인의 계열회사 사외이사/감사위원 |
(4) 사외이사 변동현황
| (단위 : 명) |
| 이사의 수 | 사외이사 수 | 사외이사 변동현황 | ||
|---|---|---|---|---|
| 선임 | 해임 | 중도퇴임 | ||
| 5 | 3 | 1 | - | - |
* 선임은 당기 중 신규선임만 기재하였으며, 재선임은 기재 생략하였습니다.
나. 중요의결사항 등
(1) 이사회 운영규정의 주요 내용
1) 이사회의 결의는 이사 과반수의 출석과 출석이사의 과반수로 한다.
다만 상법 제397조의2(회사의 기회 및 자산의 유용 금지) 및 제398조(이사등과
회사 간의 거래)에 해당하는 사안에 대한 이사회 결의는 이사 3분의 2 이상의 수
로 한다.
2) 이사회는 이사의 전부 또는 일부가 직접 회의에 출석하지 아니하고 모든 이사가
음성을 동시에 송.수신하는 통신 수단에 의하여 참가하는 것을 허용할 수 있다.
이 경우 당해 이사는 이사회에 직접 출석한 것으로 본다.
3) 이사회의 의결에 관하여 특별한 이해관계가 있는 자는 의결권을 행사하지
못한다.
4) 이사회의 의사에 관하여는 의사록을 작성하여야 한다.
5) 의사록에는 의사의 안건, 경과요령, 그 결과, 반대하는 자와 그 반대 이유를 기재
하고 출석한 이사가 기명 날인 또는 서명하여야 한다.
(2) 이사회의 중요의결사항
(기준일: 보고서 제출일 현재)
| 회차 | 개최일자 | 의안내용 | 가결 여부 |
비고 |
|---|---|---|---|---|
| 1 | 2025.02.06 | 1. 제65기 연결 및 별도 재무제표 및 영업보고서 승인의 건 |
가결 | - |
| 2. 산업안전보건법에 따른 안전보건관리계획서 승인의 건 |
가결 | - | ||
| 2 | 2025.02.27 | 1. 제65기 정기주주총회 소집 및 전자투표제도 도입의 건 | 가결 | - |
| 2. 미등기임원 (재)선임의 건 | 가결 | - | ||
| 3. ESG현황 및 계획 승인의 건 | 가결 | - | ||
| 3 | 2025.03.26 | 1. 등기이사 개별보수 한도 결정 건 | 가결 | - |
| 2. 이사회 의장 선임의 건 | 가결 | - | ||
| 3. 회장 선임의 건 | 가결 | - | ||
| 4. 고문 선임의 건 | 가결 | - | ||
| 5. 임원 인사규정 개정의 건 | 가결 | - | ||
| 4 | 2025.03.28 | 1. 유상증자 결의의 건 | 가결 | - |
| 5 | 2025.04.22 | 1. 임원 인사규정 개정의 건 | 가결 | - |
| 2. 이사회 규정 개정의 건 | 가결 | - |
(3) 이사회에서의 이사의 주요활동내역
| 회차 | 개최일자 | 의안내용 | 이사의 성명 | |||||
|---|---|---|---|---|---|---|---|---|
| 안미정 (출석률: 100%) |
이제영 (출석률: 100%) |
강문성 (출석률: 100%) |
정길영 (출석률: 100%) |
전형수 (출석률: 100%) |
이상길 (출석률: 100%) |
|||
| 찬 반 여 부 | ||||||||
| 1 | 2025.02.06 | 1. 제65기 연결 및 별도 재무제표 및 영업보고서 승인의 건 | 해당없음 | 찬성 | 찬성 | 찬성 | 찬성 | 해당없음 |
| 2. 산업안전보건법에 따른 안전보건관리계획서 승인의 건 |
해당없음 | 찬성 | 찬성 | 찬성 | 찬성 | 해당없음 | ||
| 2 | 2025.02.27 | 1. 제65기 정기주주총회 소집 및 전자투표제도 도입의 건 | 해당없음 | 찬성 | 찬성 | 찬성 | 찬성 | 해당없음 |
| 2. 미등기임원 (재)선임의 건 | 해당없음 | 찬성 | 찬성 | 찬성 | 찬성 | 해당없음 | ||
| 3. ESG현황 및 계획 승인의 건 | 해당없음 | 찬성 | 찬성 | 찬성 | 찬성 | 해당없음 | ||
| 3 | 2025.03.26 | 1. 등기이사 개별보수 한도 결정 건 | 찬성 | 찬성 | 해당사항 없음 (임기만료) |
찬성 | 찬성 | 찬성 |
| 2. 이사회 의장 선임의 건 | 찬성 | 찬성 | 해당사항 없음 (임기만료) |
찬성 | 찬성 | 찬성 | ||
| 3. 회장 선임의 건 | 찬성 | 찬성 | 해당사항 없음 (임기만료) |
찬성 | 찬성 | 찬성 | ||
| 4. 고문 선임의 건 | 찬성 | 찬성 | 해당사항 없음 (임기만료) |
찬성 | 찬성 | 찬성 | ||
| 5. 임원 인사규정 개정의 건 | 찬성 | 찬성 | 해당사항 없음 (임기만료) |
찬성 | 찬성 | 찬성 | ||
| 4 | 2025.03.28 | 1. 유상증자 결의의 건 | 찬성 | 찬성 | 해당사항 없음 (임기만료) |
찬성 | 찬성 | 찬성 |
다. 이사회내 위원회
(1) 감사위원회 : 세부사항은 "2. 감사제도에 관한 사항" 참조
라. 이사의 독립성
| (기준일: 보고서 제출일 현재) |
| 성 명 | 직명 | 임기 | 선임배경 | 추천인 | 활동분야 | 회사와의 거래 |
최대주주 또는 주요주주와의 관계 |
|---|---|---|---|---|---|---|---|
| 안 미 정 | 사내이사 | 2025.03~2028.03 (신임) |
경영 전반 운영 경험 및 전문성 | 이사회 | 이사회 및 전사 경영 전반 | 없음 | 최대주주인 법인의 계열회사 사내이사 |
| 이 제 영 | 사내이사 | 2024.03~2027.03 (신임) |
경영 전반 운영 경험 및 전문성 | 이사회 | 이사회 및 전사 경영 전반 | 없음 | 최대주주인 법인의 계열회사 사내이사 |
| 정 길 영 | 사외이사 | 2024.03~2027.03 (연임 1회) |
감사 분야 전문가로서 경험과 지식을 갖추고 있음 |
이사회 | 이사회 및 감사위원회 | 없음 | 최대주주인 법인의 계열회사 사외이사/ 감사위원 |
| 전 형 수 | 사외이사 | 2024.03~2027.03 (연임 1회) |
조세 분야 전문가로서 경험과 지식을 갖추고 있음 |
이사회 | 이사회 및 감사위원회 | 없음 | 최대주주인 법인의 계열회사 사외이사/ 감사위원 |
| 이 상 길 | 사외이사 | 2025.03~2028.03 (신임) |
의학 분야 전문가로서 경험과 지식을 갖추고 있음 |
이사회 | 이사회 및 감사위원회 | 없음 | 최대주주인 법인의 계열회사 사외이사/ 감사위원 |
마. 사외이사의 전문성
| 부서명 | 직원수 | 직위 | 주요활동내역(2025년) |
|---|---|---|---|
| 총무팀 | 7명 | 부서장1인, 팀장1인,팀원5인 |
1. 사외이사 직무수행에 필요한 요청사항에 대한 지원 등의 업무 수행 2. 이사회 개최 지원 및 기타 이슈사항 수시 보고 |
| 재무지원팀 | 9명 | 임원1인, 팀장1인,팀원7인 |
바. 사외이사 교육실시 현황
| 교육일자 | 교육실시주체 | 참석 사외이사 | 불참시 사유 | 주요 교육내용 |
|---|---|---|---|---|
| 2021년 10월 14일 | 전략기획부 | 강문성, 김범수, 김상용 | - | 상장회사 내부회계관리제도 감사(검토)등 의견 현황과 시사점(주1) |
| 2022년 04월 29일 | 전략기획부 | 강문성, 전형수, 정길영 | - | 이사회와 감사위원회 모범규준 교육(주3) |
| 2022년 07월 27일 | 안전보건경영팀 | 강문성, 전형수, 정길영 | - | 중대재해처벌법 및 안전보건경영 법률교육(주2) |
| 2022년 10월 25일 | 딜로이트 안진 | 강문성, 전형수, 정길영 | - | 금융감독원 23년 중점심사 회계이슈(주2) |
| 2022년 12월 16일 | 삼정KPMG | 강문성, 전형수, 정길영 | - | 2022년도 내부회계관리제도 교육(주3) |
| 2023년 11월 01일 | 삼정KPMG | 강문성, 전형수, 정길영 | - | 2023년도 내부회계관리제도 교육(주3) |
| 2024년 05월 21일 | 삼정KPMG | 강문성, 전형수, 정길영 | - | 감사위원회 교육 프로그램(주2) |
| 2024년 10월 17일 | 삼정KPMG | 강문성, 전형수, 정길영 | - | 2024년도 내부회계관리제도 교육(주3) |
(주1) 교육자료를 사전 배포하고, 주요 사항에 대해 유선 및 서면으로 실시함.
(주2) 교육자료를 사전 배포하고, 관련부서 담당자가 대면교육을 실시함.
(주3) 외부교육기관의 동영상 강의 교육을 실시함.
2. 감사제도에 관한 사항
가. 감사기구 관련 사항
(1) 감사위원회(감사) 설치여부, 구성방법 등
2009년 5월 29일 개최된 제49기 정기주주총회에서 기존 상근감사제도에서 상법상 감사위원회 제도로 변경하여 시행하고 있음.
- 감사위원회의 구성
1) 이 회사는 감사에 갈음하여 정관 제35조의3의 규정에 의한 감사위원회를 둔다.
2) 감사위원회는 3인 이상의 이사로 구성하며, 위원의 3분의 2 이상은 사외이사
이어야 한다. 이 경우 사외이사가 아닌 위원은 상법 제542조의10
제2항의 요건을 갖추어야 한다.
3) 사외이사인 감사위원회 위원의 선임에는 의결권 있는 발행 주식총수의
100분의 3을 초과하는 수의 주식을 가진 주주는 그 초과하는 주식에
대하여는 의결권을 행사하지 못한다.
4) 사외이사가 아닌 감사위원회 위원을 선임하거나 해임할 때에는 의결권을
행사할 최대주주와 그 특수관계인, 최대주주 또는 그 특수관계인의 계산
으로 주식을 보유하는 자, 최대주주 또는 그 특수관계인에게 의결권을
위임한 자가 소유하는 의결권 있는 주식의 합계가 의결권 있는 발행주식
총수의 100분의 3을 초과하는 경우 그 주주는 그 초과하는 주식에 관하여
의결권을 행사하지 못한다.
5) 감사위원회는 그 결의로 위원회를 대표할 자를 선정하여야 한다. 이 경우
위원장은 사외이사이어야 한다.
- 감사위원회의 직무
1) 감사위원회는 이 회사의 회계와 업무를 감사한다.
2) 감사위원회는 이사회에 출석하여 의견을 진술할 수 있다.
3) 감사위원회는 필요하면 회의의 목적사항과 소집 이유를 서면에 적어 이사
(소집권자가 있는 경우에 소집권자를 말한다. 이하 같다.)에게 제출하여
이사회 소집을 청구할 수 있다.
4) 제2항의 청구를 하였는데도 이사가 지체 없이 이사회를 소집하지 아니하면
그 청구한 감사위원회가 이사회를 소집할 수 있다.
5) 감사위원회는 회의의 목적사항과 소집의 이유를 기재한 서면을 이사회에
제출하여 임시총회의 소집을 청구할 수 있다.
6) 감사위원회는 그 직무를 수행하기 위하여 필요한 때에는 자회사에 대하여
영업의 보고를 요구할 수 있다. 이 경우 자회사가 지체 없이 보고를 하지
아니할 때 또는 그 보고의 내용을 확인할 필요가 있는 때에는 자회사의
업무와 재산상태를 조사할 수 있다.
7) 감사위원회는 외부감사인을 선정한다.
8) 감사위원회는 제1항 내지 제7항 외에 이사회가 위임한 사항을 처리한다.
9) 감사위원회 결의에 대하여 이사회는 재결의 할 수 없다.
10) 감사위원회는 회사의 비용으로 전문가의 도움을 구할 수 있다.
- 감사위원회의 감사록
감사위원회는 감사에 관하여 감사록을 작성하여야 하며, 감사록에는 감사의
실시요령과 그 결과를 기재하고 감사를 실시한 감사위원회 위원이 기명날인
또는 서명하여야 한다.
(2) 감사위원회의 감사업무에 필요한 경영정보접근을 위한 내부장치 마련 여부
내부감사업무 전담부서를 운영하여 감사에 필요한 정보의 수집 및 보고가
체계적으로 이루어질 수 있도록 하고 있음.
(3) 감사위원회 위원의 인적사항
| 성명 | 사외이사 여부 |
경력 | 회계ㆍ재무전문가 관련 | ||
|---|---|---|---|---|---|
| 해당 여부 | 전문가 유형 | 관련 경력 | |||
| 정길영 | 예 |
前, 감사원 감사위원 現,명지대학교 미래융합대학 |
- | - | - |
| 전형수 | 예 | 前,서울지방국세청장 現,김앤장 법률사무소 고문 |
예 | 4호 유형 (금융기관·정부·증권유관기관 등 경력자) |
대전지방국세청장('00~'03) 재정경제부 국세심판원장('03~'04) 서울지방국세청장('04~'05) |
| 이상길 | 예 | 前,연세암병원 식도암 센터장 前,연세암병원 위암 센터장 現, 연세의료원 대외협력처 처장 現, 연세의료원 세브란스병원 교수 |
- | - | - |
※ 전문가 유형은 기업공시서식 작성 기준 및「상법 시행령」제37조 제2항에 따른 회계ㆍ재무전문가 유형입니다.
ㆍ2호 유형 : 회계ㆍ재무 분야 관련 석사학위 이상 학위 취득자로서 연구기관 또는 대학에서 회계 또는 재무 관련 분야의 연구원이나 조교수 이상으로 근무한 경력이 모두5년 이상인지 여부
ㆍ4호 유형 : 금융기관·정부·증권유관기관 등에서 회계·재무관련 업무 또는 이에 대한 감독 업무를 근무한 경력이 모두 5년 이상인지 여부
나. 감사위원회의 주요 활동내역
(1) 감사위원회 활동내역
| (기준일: 보고서 제출일 현재) |
| 회차 | 개최일자 | 의안내용 | 가결 여부 |
강문성 (출석률: 100%) |
전형수 (출석률: 100%) |
정길영 (출석률: 100%) |
이상길 (출석률: 100%) |
|---|---|---|---|---|---|---|---|
| 1 | 2025.02.06 | 1. 2024년 영업실적 및 재무제표 보고 | (주1) | 참석 | 참석 | 참석 | 해당사항 없음 |
| 2. 2025년도 업무감사 일정계획(안) 승인의 건 | 가결 | 찬성 | 찬성 | 찬성 | 해당사항 없음 |
||
| 3. 외부감사인 선임의 건 | 가결 | 찬성 | 찬성 | 찬성 | 해당사항 없음 |
||
| 2 | 2025.02.27 | 1. 2024년 4분기 내부감사 업무보고 | (주1) | 참석 | 참석 | 참석 | 해당사항 없음 |
| 2. 외부감사인과 지배기구와의 커뮤니케이션 보고 |
(주1) | 참석 | 참석 | 참석 | 해당사항 없음 |
||
| 3. 제65기 재무제표, 연결재무제표 및 영업보고서 승인의 건 |
가결 | 찬성 | 찬성 | 찬성 | 해당사항 없음 |
||
| 4. 제65기 감사보고서 채택의 건 | 가결 | 찬성 | 찬성 | 찬성 | 해당사항 없음 |
||
| 5. 제65기 내부회계관리제도 평가보고서 채택의 건 | 가결 | 찬성 | 찬성 | 찬성 | 해당사항 없음 |
||
| 6. 제65기 내부감시장치 가동현황에 대한 평가 의견서 채택의 건 |
가결 | 찬성 | 찬성 | 찬성 | 해당사항 없음 |
||
| 3 | 2025.03.26 | 1. 감사위원회 위원장 선임의 건 | 가결 | 해당사항 없음 |
찬성 | 찬성 | 찬성 |
| 4 | 2025.04.22 | 1. 2025년 1분기 영업 실적 보고 | (주1) | 해당사항 없음 |
참석 | 참석 | 참석 |
| 2. 2025년 1분기 내부감사 업무 보고 | (주1) | 해당사항 없음 |
참석 | 참석 | 참석 |
(주1) 의안사항이 아닌 감사위원회 보고사항
다. 감사위원회 교육 실시 현황
| 교육일자 | 교육실시주체 | 참석 감사위원 | 불참시 사유 | 주요 교육내용 |
|---|---|---|---|---|
| 2021년 10월 14일 | 재무회계팀 | 강문성, 김범수, 김상용 | - | 상장회사 내부회계관리제도 감사(검토)등 의견 현황과 시사점(주1) |
| 2022년 04월 29일 | 재무회계팀 | 강문성, 전형수, 정길영 | - | 이사회와 감사위원회 모범규준 교육(주2) |
| 2022년 07월 27일 | 안전보건경영팀 | 강문성, 전형수, 정길영 | - | 중대재해처벌법 및 안전보건경영 법률교육(주2) |
| 2022년 10월 25일 | 딜로이트 안진 | 강문성, 전형수, 정길영 | - | 금융감독원 23년 중점심사 회계이슈(주2) |
| 2022년 12월 16일 | 삼정KPMG | 강문성, 전형수, 정길영 | - | 2022년도 내부회계관리제도 교육(주3) |
| 2023년 11월 01일 | 삼정KPMG | 강문성, 전형수, 정길영 | - | 2023년도 내부회계관리제도 교육(주3) |
| 2024년 05월 21일 | 삼정KPMG | 강문성, 전형수, 정길영 | - | 감사위원회 교육 프로그램 (주2) |
| 2024년 10월 17일 | 삼정KPMG | 강문성, 전형수, 정길영 | - | 2024년도 내부회계관리제도 교육(주3) |
(주1) 교육자료를 사전 배포하고, 주요 사항에 대해 유선 및 서면으로 실시함.
(주2) 교육자료를 사전 배포하고, 관련부서 담당자가 대면교육을 실시함.
(주3) 외부교육기관의 동영상 강의 교육을 실시함
라. 감사위원회 지원 조직 현황
| 부서(팀)명 | 직원수(명) | 직위(근속연수) | 주요 활동내역 |
|---|---|---|---|
| 감사팀 | 3 | 팀장1인,팀원2인(34년) | 감사위원회 개최 지원 및 감사에 필요한 정보의 수집 및 보고 |
| 총무팀 | 7 | 부서장1인, 팀장1인,팀원5인(20년) |
감사위원회 개최 지원 및 감사에 필요한 정보의 수집 및 보고 |
| 재무지원팀 | 9 | 임원1인, 팀장1인,팀원7인(11년) |
감사위원회 개최 지원 및 감사에 필요한 정보의 수집 및 보고 |
마. 준법지원인 등 지원 조직 현황
해 당 사 항 없 음
3. 주주총회 등에 관한 사항
가. 투표제도 현황
| (기준일 : | 2025년 03월 31일 | ) |
| 투표제도 종류 | 집중투표제 | 서면투표제 | 전자투표제 |
|---|---|---|---|
| 도입여부 | 배제 | 도입 | 도입 |
| 실시여부 | 미실시 | 실시 | 실시 |
나. 소수주주권의 행사 여부
당사는 공시대상 기간 중 소수주주권이 행사되지 않았습니다.
다. 경영권 경쟁
당사는 공시대상 기간 중 경영권 경쟁이 발생하지 않았습니다.
라. 의결권 현황
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 주식수 | 비고 |
|---|---|---|---|
| 발행주식총수(A) | 보통주 | 68,454,671 | - |
| 우선주 | - | - | |
| 의결권없는 주식수(B) | 보통주 | - | - |
| 우선주 | - | - | |
| 정관에 의하여 의결권 행사가 배제된 주식수(C) | 보통주 | - | - |
| 우선주 | - | - | |
| 기타 법률에 의하여 의결권 행사가 제한된 주식수(D) |
보통주 | - | - |
| 우선주 | - | - | |
| 의결권이 부활된 주식수(E) | 보통주 | - | - |
| 우선주 | - | - | |
| 의결권을 행사할 수 있는 주식수 (F = A - B - C - D + E) |
보통주 | 68,454,671 | - |
| 우선주 | - | - |
마. 주식사무
| 정관상 신주인수권의 내용 |
- 우리회사 정관 제10조「주식의 발행 및 배정」 1. 주주에게 그가 가진 주식 수에 따라서 신주를 배정하기 2. 발행주식총수의 100분의 20을 초과하지 않는 범위 내에 ② 제1항 제3호의 방식으로 신주를 배정하는 경우에는 이사회 의 결의로 다음 각 호의 어느 하나에 해당하는 방식으로 신주 를 배정하여야 한다. 1. 신주인수의 청약을 할 기회를 부여하는 자의 유형을 분 2. 관계 법령에 따라 우리사주조합원에 대하여 신주를 배정 하고 청약되지 아니한 주식까지 포함하여 불특정 다수인 에게 신주인수의 청약을 할 기회를 부여하는 방식 3. 주주에 대하여 우선적으로 신주인수의 청약을 할 수 있 는 기회를 부여하고 청약되지 아니한 주식이 있는 경우, 이를 불특정 다수인에게 신주를 배정받을 기회를 부여하 는 방식 4. 투자매매업자 또는 투자중개업자가 인수인 또는 주선인 으로서 마련한 수요예측 등 관계 법규에서 정하는 합리적 인 기준에 따라 특정한 유형의 자에게 신주인수의 청약을 할 수 있는 기회를 부여하는 방식 ③ 제1항 제2호 및 제3호에 따라 신주를 배정하는 경우 상법 제 416조제1호, 제2호, 제2호의2, 제3호 및 제4호에서 정하는 사항을 그 납입기일의 2주 전까지 주주에게 통지하거나 공고 하여야 한다. 다만, 자본시장과 금융투자업에 관한 법률 제1 65조의9에 따라 주요사항보고서를 금융위원회 및 거래소에 공시함으로써 그 통지 및 공고를 갈음할 수 있다. ④ 제1항 각호의 어느 하나의 방식에 의해 신주를 발행할 경우 에는 발행할 주식의 종류와 수 및 발행가격 등은 이사회의 결 의로 정한다. ⑤ 회사는 신주를 배정하는 경우 그 기일까지 신주인수의 청약 을 하지 아니하거나 그 가액을 납입하지 아니한 주식이 발생 하는 경우에 그 처리방법은 발행가액의 적정성등 관련 법령 에서 정하는 바에 따라 이사회 결의로 정한다. ⑥ 회사는 신주를 배정하면서 발생하는 단주에 대한 처리방법은 이사회의 결의로 정한다. ⑦ 회사는 제1항 제1호에 따라 신주를 배정하는 경우에는 주권 |
||
| 결 산 일 | 12월 31일 | 정기주주총회 | 2~3월 중 |
| 주주명부폐쇄시기 | 당사 정관 제 12조(주주명부 기준일) 준용 | ||
| 명의개서대리인 | (주)국민은행 증권대행부 | ||
| 주주의 특전 | 없 음 | 공고게재 | www.bukwang.co.kr |
바. 주주총회 의사록 요약
| 주총일자 | 안 건 | 결 의 내 용 | 비 고 |
| 제65기 정기 주주총회 (25.03.26) |
제1호 의안 : 제64기(2024.01.01~2024.12.31) 재무제표 및 연결재무제표 승인의 건 제2호 의안 : 정관변경의 건 제3호 의안 : 이사 선임의 건 사내이사 안미정 선임의 건 제4호 의안 : 감사위원 선임의 건 감사위원 이상길 선임의 건 제5호 의안 : 이사 보수한도 승인의 건 |
원안대로 승인함 원안대로 승인함 원안대로 승인함 원안대로 승인함 원안대로 승인함(한도액25억원) |
- |
| 제64기 정기 주주총회 (24.03.22) |
제1호 의안 : 제64기(2023.01.01~2023.12.31) 재무제표 및 연결재무제표 승인의 건 제2호 의안 : 정관변경의 건 제3호 의안 : 이사 선임의 건 3-1호 의안 : 사내이사 우기석 선임의 건 3-2호 의안 : 사내이사 이제영 선임의 건 3-3호 의안 : 사외이사 전형수 선임의 건 사외이사 정길영 선임의 건 제4호 의안 : 감사위원 선임의 건 4-1호 의안 : 감사위원 전형수 선임의 건 4-2호 의안 : 감사위원 정길영 선임의 건 제5호 의안 : 이사 보수한도 승인의 건 |
원안대로 승인함 원안대로 승인함 원안대로 승인함 원안대로 승인함 원안대로 승인함 원안대로 승인함 원안대로 승인함 원안대로 승인함 원안대로 승인함(한도액25억원) |
- |
| 제63기 정기 주주총회 (23.03.28) |
제1호 의안 : 제63기(2022.01.01~2022.12.31) 재무제표 및 연결재무제표 승인의 건 제2호 의안 : 사내이사 서진석 선임의 건 제3호 의안 : 감사위원회 위원이 되는 사외이사 강문성 선임의 건 제4호 의안 : 이사 보수한도 승인의 건 |
원안대로 승인함 원안대로 승인함 원안대로 승인함 원안대로 승인함(한도액25억원) |
- |
VI. 주주에 관한 사항
1. 최대주주 및 특수관계인의 주식소유 현황
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 주, %) |
| 성 명 | 관 계 | 주식의 종류 |
소유주식수 및 지분율 | 비고 | |||
|---|---|---|---|---|---|---|---|
| 기 초 | 기 말 | ||||||
| 주식수 | 지분율 | 주식수 | 지분율 | ||||
| OCI홀딩스 주식회사 |
본인 | 보통주 | 7,747,934 | 11.32 | 7,747,934 | 11.32 | - |
| 계 | 보통주 | 7,747,934 | 11.32 | 7,747,934 | 11.32 | - | |
| 우선주 | - | - | - | - | - | ||
* 상기 소유주식수는 보고서 제출일 현재 금융감독원 전자공시시스템에 최종 공시된 주식등의 대량보유상황보고서 및 기타 지분공시 자료를 기준으로 작성함.
가. 당사가 보유하고 있는 자기주식의 내역
| (보고서 제출일 현재) | (단위 : 주, %) |
| 주식의 종류 |
소유주식수(지분율) | 변동원인 | |||||
|---|---|---|---|---|---|---|---|
| 기 초 | 증 가 | 감 소 | 기 말 | ||||
| 주식수 | 지분율 | 주식수 | 주식수 | 주식수 | 지분율 | ||
| 보통주 | - | - | - | - | - | - | - |
나. 최대주주의 주요경력
(1) 최대주주(법인 또는 단체)의 기본정보
| 명 칭 | 출자자수 (명) |
대표이사 (대표조합원) |
업무집행자 (업무집행조합원) |
최대주주 (최대출자자) |
|||
|---|---|---|---|---|---|---|---|
| 성명 | 지분(%) | 성명 | 지분(%) | 성명 | 지분(%) | ||
| OCI 홀딩스 주식회사 |
61,822 | 이우현 | 7.00 | - | - | 이화영 | 7.68 |
* 출자자 수는 최근 주주명부 폐쇄일인 2024년 12월 31일자 기준 전체 주주의 수를 기재하였습니다.
* 업무집행자는 대표이사와 동일하여 기재하지 않았습니다.
* 상기 최대주주의 주식소유현황은 2024년 12월 31일 기준으로 작성되었으며, 사업보고서 공시일 현재의 현황은 OCI 홀딩스(주)의 사업보고서를 참고하시기 바랍니다.
(2) 최대주주(법인 또는 단체)의 최근 결산기 재무현황
| (단위 : 백만원) |
| 구 분 | |
|---|---|
| 법인 또는 단체의 명칭 | 오씨아이홀딩스㈜ |
| 자산 총계 | 8,093,655 |
| 부채 총계 | 3,258,113 |
| 자본 총계 | 4,835,541 |
| 매출액 | 3,577,383 |
| 영업이익 | 101,528 |
| 당기순이익 | 113,724 |
※ 상기 금액은 2024년말 연결재무제표 기준입니다.
(3) 사업현황 등 회사 경영 안정성에 영향을 미칠 수 있는 주요 내용
- 해당사항 없음
다. 최대주주의 최대주주(법인 또는 단체)의 개요
- 해당사항 없음
2. 최근5년간 최대주주의 변동현황
최대주주 변동내역
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 주, %) |
| 변동일 | 최대주주명 | 소유주식수 | 지분율 | 변동원인 | 비 고 |
|---|---|---|---|---|---|
| 2024년 03월 29일 | OCI홀딩스주식회사 | 7,747,934 | 11.32 | 자기주식소각 | - |
| 2024년 01월 05일 | OCI홀딩스주식회사 | 7,747,934 | 10.90 | 특별관계자 변동 (임원퇴임) |
- |
| 2022년 03월 25일 | OCI홀딩스주식회사외 1인 | 7,795,267 | 10.97 | 특별관계자 변동 (임원퇴임) |
- |
| 2022년 03월 03일 | OCI홀딩스주식회사외 3인 | 8,383,490 | 11.80 | 장외매도 외 | - |
| 2021년 06월 16일 | 김동연외 11인 | 15,419,156 | 21.70 | 장내매도 | - |
| 2021년 03월 19일 | 김동연외 11인 | 17,357,156 | 24.43 | 주식배당 | - |
| 2020년 03월 13일 | 김동연외 11인 | 16,349,237 | 25.22 | 주식배당 외 | - |
* 작성기준일 이후 변동은 전자공시시스템(http://dart.fss.or.kr)의 주식등의 대량보유상황보고서 및 기타 지분공시 자료 등을 참고하십시오.
3. 주주 및 주식의 분포
가. 5%이상 주주의 주식 소유현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 주) |
| 구분 | 주주명 | 소유주식수 | 지분율(%) | 비고 |
|---|---|---|---|---|
| 5% 이상 주주 | OCI홀딩스 주식회사 | 7,747,934 | 11.32 | - |
| 김동연 | 7,053,266 | 10.30 | - | |
| 정창수 | 6,050,000 | 8.84 | - | |
| 우리사주조합 | 19,519 | 0.03 | - | |
* 상기 소유주식수와 지분율은 보고서 제출일 현재 금융감독원 전자공시시스템에 최종 공시된 주식등의 대량보유상황보고서 및 기타 지분공시 자료를 기준으로 작성함.
나. 소액주주 현황
소액주주현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 주) |
| 구 분 | 주주 | 소유주식 | 비 고 | ||||
|---|---|---|---|---|---|---|---|
| 소액 주주수 |
전체 주주수 |
비율 (%) |
소액 주식수 |
총발행 주식수 |
비율 (%) |
||
| 소액주주 | 67,382 | 67,386 | 99.99 | 46,098,314 | 68,454,671 | 67.34 | - |
4. 주가 및 주식 거래실적
가. 국내증권시장
| (단위 : 원, 주) |
| 종 류 | 3월 | 2월 | 1월 | 12월 | 11월 | 10월 | |
|---|---|---|---|---|---|---|---|
| 보통주 | 최 고 | 4,870 | 5,160 | 5,150 | 4,870 | 5,700 | 5,240 |
| 최 저 | 3,785 | 4,535 | 4,530 | 4,070 | 4,255 | 4,800 | |
| 월간거래량 | 3,015,339 | 2,576,263 | 1,663,905 | 3,006,047 | 9,203,746 | 2,388,410 | |
VII. 임원 및 직원 등에 관한 사항
1. 임원 및 직원 등의 현황
가. 임원 현황
(1) 등기임원 현황
| (기준일 : | 보고서 제출일 현재 | ) | (단위 : 주) |
| 성명 | 성별 | 출생년월 | 직위 | 등기임원 여부 |
상근 여부 |
담당 업무 |
주요경력 | 소유주식수 | 최대주주와의 관계 |
재직기간 | 임기 만료일 |
|
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 의결권 있는 주식 |
의결권 없는 주식 |
|||||||||||
| 안미정 | 여 | 1961.11 | 회장 | 사내이사 | 상근 | 경영전반 | 前,특허청 심판관 前,OCI홀딩스(주)사외이사/이사회의 現, 특허법인 지평 대표변리사 |
- | - | 최대주주인 법인의 계열회사 사내이사 |
- | 2028.03.25 |
| 이제영 | 남 | 1974.01 | 대표이사 사장 |
사내이사 | 상근 | 경영전반 | 前,OCI㈜ 법무부, 감사실 전무 前,OCI홀딩스 법무실 전무 |
- | - | 최대주주인 법인의 계열회사 사내이사 |
1년 | 2027.03.22 |
| 전형수 | 남 | 1953.04 | 사외이사 | 사외이사 | 비상근 | 감사위원회 위원 |
前,서울지방국세청장 現,김앤장 법률사무소 고문 |
- | - | 최대주주인 법인의 계열회사 사외이사/ 감사위원 |
3년 | 2027.03.22 |
| 정길영 | 남 | 1962.06 | 사외이사 | 사외이사 | 비상근 | 감사위원회 위원 |
前,감사원 감사위원 現,명지대학교 미래융합대학 |
- | - | 최대주주인 법인의 계열회사 사외이사/ 감사위원 |
3년 | 2027.03.22 |
| 이상길 | 남 | 1969.02 | 사외이사 | 사외이사 | 비상근 | 감사위원회 위원 |
前,연세암병원 위암 센터장 現, 연세의료원 대외협력처 처장 現, 연세의료원 세브란스병원 교수 |
- | - | 최대주주인 법인의 계열회사 사외이사/ 감사위원 |
- | 2028.03.25 |
* 작성기준일 이후 변동은 전자공시시스템(http://dart.fss.or.kr)의 주식등의
대량보유상황보고서 및 기타 지분공시 자료등을 참고하십시오.
* 등기임원의 임기만료일은 주총결의로 인한 임기만료일입니다.
(2) 미등기임원 현황
| (기준일 : 보고서 제출일 현재) |
| 성명 | 성별 | 출생년월 | 직위 | 상근 여부 |
담당 업무 |
주요경력 | 소유주식수 | 최대주주와의 관계 |
재직기간 | |
|---|---|---|---|---|---|---|---|---|---|---|
|
의결권 주식 |
의결권 주식 |
|||||||||
| 정창수 | 남 | 1936년 12월 | 부회장 | 상근 | 경영자문 | 現,부광약품(주) 부회장 | 6,050,000 | - | - | 51년 |
| 김성수 | 남 | 1973년 04월 | 부사장 | 상근 | 사업총괄 | 前, EY한영 감사담당 파트너 現,부광약품(주) 경영전략본부 본부장 |
- | - | - | 1년 |
| 김지헌 | 남 | 1976년 03월 | 전무 | 상근 | 개발담당 | 前,GC녹십자 사업개발본부 상무 現,부광약품(주) 연구개발본부 본부장 |
- | - | - | 1년 |
| 권순일 | 남 | 1969년 01월 | 상무 | 상근 | 영업관리/ 안전관리/ 인사담당 |
前,부광약품(주) 병원사업부 이사 現,부광약품(주)CHC사업본부 부서장 |
1,651 | - | - | 24년 |
| 김민규 | 남 | 1972년 12월 | 상무 | 상근 | 재무회계 담당 |
前,부광약품(주) 전략기획부 부서장 現,부광약품(주) 재무지원부 부서장 |
- | - | - | 24년 |
| 박종도 | 남 | 1972년 05월 | 상무 | 상근 | 영업총괄 | 前,부광약품(주) 수도권본부장 이사 現,부광약품(주) 영업총괄본부 본부장 |
- | - | - | 24년 |
| 김원섭 | 남 | 1975년 01월 | 상무 | 상근 | 생산담당 | 前,부광약품(주) 생산부 이사 現,부광약품(주) 생산본부 본부장 |
- | - | - | 4년 |
| 김경민 | 남 | 1977년 02월 | 상무 | 상근 | CNS사업 담당 |
前,한독 Marketing Director 現,부광약품(주) CNS사업본부 본부장 |
- | - | - | 1년 |
| 장삼순 | 남 | 1970년 06월 | 상무 | 상근 | 경영기획/ 공장관리 담당 |
前,OCI Compliance1팀 부장 現,부광약품(주) 경영기획부, 공장관리부부서장 |
- | - | - | 1년 |
(3) 임원의 겸직현황
| (기준일 : 보고서 제출일 현재) |
| 겸직임원 | 겸직회사 | 비고 | |||
| 성명 | 직위 | 회사명 | 직위 | 담당업무 | |
| 이제영 | 대표이사 | Contera Pharma A/S | Members of the Board of Director | - | - |
| 부광메디카(주) | 대표이사 | 경영전반 | - | ||
| 김지헌 | 전무 | JaguAHR Therapeutics | Members of the Board of Director | 경영전반 | 미등기임원 |
| 박종도 | 상무 | 부광메디카(주) | 사내이사 | - | 미등기임원 |
| 장삼순 | 상무 | 부광메디카(주) | 사내이사 | - | 미등기임원 |
*사외이사의 경우 모두 감사위원을 겸직하고 있습니다.
나. 직원 현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 원) |
| 직원 | 소속 외 근로자 |
비고 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 사업부문 | 성별 | 직 원 수 | 평 균 근속연수 |
연간급여 총 액 |
1인평균 급여액 |
남 | 여 | 계 | |||||
| 기간의 정함이 없는 근로자 |
기간제 근로자 |
합 계 | |||||||||||
| 전체 | (단시간 근로자) |
전체 | (단시간 근로자) |
||||||||||
| 전체 | 남 | 415 | - | 4 | - | 419 | 12.6 | 7,989,797,538 | 19,068,729 | 12 | 19 | 31 | - |
| 전체 | 여 | 191 | - | 1 | - | 192 | 6.6 | 2,411,196,056 | 12,558,313 | - | |||
| 합 계 | 606 | - | 5 | - | 611 | 10.7 | 10,400,993,594 | 17,022,903 | - | ||||
* 등기임원 보수는 제외되어 있으며, 미등기임원 보수는 포함되어 있습니다.
* 연간급여총액은 당기 전직원의 소득세법 제20조, 제21조에 따른 급여, 상여,
기타소득을 포함한 금액이며, 퇴직급여 및 퇴직급여충당금은 제외되었습니다.
* 1인평균급여액은 기준일 현재의 직원수에 연간급여총액을 나눈 금액입니다.
(1) 육아지원제도 사용 현황
(단위 : 명, %)
| 구분 | 당분기(66기) | 전기(65기) | 전전기(64기) |
|---|---|---|---|
| 육아휴직 사용자수(남) | - | - | 1 |
| 육아휴직 사용자수(여) | 6 | 8 | 3 |
| 육아휴직 사용자수(전체) | 6 | 8 | 4 |
| 육아휴직 사용률(남) | - | - | 0.2% |
| 육아휴직 사용률(여) | 3.1% | 4.3% | 1.5% |
| 육아휴직 사용률(전체) | 1.0% | 1.4% | 0.7% |
| 육아휴직 복귀 후 12개월 이상 근속자(남) |
- | - | 1 |
| 육아휴직 복귀 후 12개월 이상 근속자(여) |
3 | 1 | 3 |
| 육아휴직 복귀 후 12개월 이상 근속자(전체) |
3 | 1 | 4 |
| 육아기 단축근무제 사용자 수 | - | 1 | 2 |
| 배우자 출산휴가 사용자 수 | 1 | 13 | 8 |
(2) 유연근무제도 사용 현황
(단위 : 명, %)
| 구분 | 당분기(66기) | 전기(65기) | 전전기(64기) |
|---|---|---|---|
| 유연근무제 활용 여부 | 활용 | 활용 | 활용 |
| 시차출퇴근제 사용자 수 | 144 | 126 | - |
| 선택근무제 사용자 수 | - | - | - |
| 원격근무제(재택근무 포함) 사용자 수 |
- | - | - |
다. 미등기임원 보수 현황
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 원) |
| 구 분 | 인원수 | 연간급여 총액 | 1인평균 급여액 | 비고 |
|---|---|---|---|---|
| 미등기임원 | 9 | 505,538,642 | 56,170,960 | - |
2. 임원의 보수 등
가. 이사(사외이사 포함) 및 감사위원회 위원(감사)의 보수현황
| <이사ㆍ감사 전체의 보수현황> |
(1) 주주총회 승인금액
| (단위 : 원) |
| 구 분 | 인원수 | 주주총회 승인금액 | 비고 |
|---|---|---|---|
| 사내이사 | 2 | - | - |
| 사외이사 | 3 | - | - |
| 합계 | 5 | 2,500,000,000 | - |
※ 인원수는 주주총회 승인일 기준입니다.
(2) 보수지급금액
(2)-1. 이사ㆍ감사 전체
| (단위 : 원) |
| 인원수 | 보수총액 | 1인당 평균보수액 | 비고 |
|---|---|---|---|
| 6 | 86,001,000 | 14,333,500 | - |
※ 인원수는 당 사업연도 총 재직인원 기준입니다.
(2)-2. 유형별
| (단위 : 원) |
| 구 분 | 인원수 | 보수총액 | 1인당 평균보수액 |
비고 |
|---|---|---|---|---|
| 등기이사 (사외이사, 감사위원회 위원 제외) |
2 | 50,001,000 | 25,000,500 | 사내이사 |
| 사외이사 (감사위원회 위원 제외) |
- | - | - | - |
| 감사위원회 위원 | 4 | 36,000,000 | 9,000,000 | 사외이사포함 |
| 감사 | - | - | - | - |
※ 인원수는 당 사업연도 총 재직인원 기준입니다.
나. 이사ㆍ감사의 개인별 보수현황
| <보수지급금액 5억원 이상인 이사ㆍ감사의 개인별 보수현황> |
(1) 개인별 보수지급금액
| (단위 : 원) |
| 이름 | 직위 | 보수총액 | 보수총액에 포함되지 않는 보수 |
|---|---|---|---|
| - | - | - | - |
(2) 산정기준 및 방법
해 당 사 항 없 음
다. 보수지급금액 5억원 이상 중 상위 5명의 개인별 보수현황
| <보수지급금액 5억원 이상 중 상위 5명의 개인별 보수현황> |
(1) 개인별 보수지급금액
| (단위 : 원) |
| 이름 | 직위 | 보수총액 | 보수총액에 포함되지 않는 보수 |
|---|---|---|---|
| 이우현 | 회장 | 575,001,000 | - |
(2) 산정기준 및 방법
| (단위 : 원) |
| 이름 | 보수의 종류 | 총액 | 산정기준 및 방법 | |
|---|---|---|---|---|
| 이우현 | 근로소득 | 급여 | 575,001,000 | - 임원처우규정에 따라 직급(회장), 업무의 성격, 업무 수행경과등을 고려하여 산정된 2024년 기본급의 12분의1에 해당하는 금액을 매월 균등 지급 |
| 상여 | - | - | ||
| 주식매수선택권 행사이익 |
- | - | ||
| 기타 근로소득 | - | - | ||
| 퇴직소득 | - | - | ||
| 기타소득 | - | - | ||
라. 주식매수선택권의 부여 및 행사현황
※ 2018년 주식매수선택권이 부여된 바 있으나, 해당 공시기준일 현재 전원 퇴사 및 권리 소멸로 인해 기재하지 않았습니다.
마. 개인별 주식매수선택권의 부여 및 행사현황
해당사항 없음.
바. 임원배상책임보험 가입 현황
[2024년 12월 31일 현재] (단위 : 원)
| 보험의 명칭 | 보험료납입액 | 부보(보상) 한도 |
비 고 | |
| 당기 납입액 | 누적납입액 (당기분 포함) |
|||
| 임원배상책임보험 | 4,771,000 | 218,124,300 | 2,000,000,000 | 2024.07.03~2025.07.02 보험료는 연간금액임 |
VIII. 계열회사 등에 관한 사항
1. 계열회사에 관한 사항
가. 계열회사 현황(요약)
(1) 회사가 속해있는 기업집단
지배회사는 독점규제 및 공정거래에 관한 법률에 의해 OCI홀딩스 주식회사 대표이사인 이우현을 동일인으로 하는 오씨아이 기업집단에 속해 있습니다. 공시서류작성기준일 현재 소속 계열회사의 현황은 아래와 같습니다. 기업집단에 속해있는 기업들의 기업명, 업종 등 상세 내용은 상세표를 참조하여 주시기 바랍니다.
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 사) |
| 기업집단의 명칭 | 계열회사의 수 | ||
|---|---|---|---|
| 상장 | 비상장 | 계 | |
| 오씨아이 기업집단 | 7 | 17 | 24 |
(2) 계통도
공시서류제출일 전일 기준, 오씨아이 기업집단의 주요 계통도는 아래와 같습니다.
| 출자자 피출자자 |
오씨아이 홀딩스(주) |
오씨아이(주) | (주)디씨알이 | (주)유니드 | (주)유니드 글로벌상사 |
(주)유니드 비티플러스 |
에스지씨 에너지(주) |
에스지씨 이앤씨(주) |
부광약품(주) |
|---|---|---|---|---|---|---|---|---|---|
| 오씨아이홀딩스(주) | *0.57% | - | - | 0.58% | - | - | - | - | - |
| 오씨아이(주) | 44.97% | - | - | - | - | - | - | - | - |
| (주)디씨알이 | 100.00% | - | - | - | - | - | - | - | - |
| (주)디씨알이대우제1호 위탁관리부동산투자회사 |
- | - | 29.36% | - | - | - | - | - | - |
| (주)새한리싸이클 | 100.00% | ||||||||
| 오씨아이페로(주) | 50.00% | - | - | - | - | - | - | - | - |
| 오씨아이에스이(주) | 100.00% | - | - | - | - | - | - | - | - |
| 오씨아이드림(주) | - | 100.00% | - | - | - | - | - | - | - |
| 오씨아이스페셜티(주) | 100.00% | - | - | - | - | - | - | - | - |
| 오씨아이정보통신(주) | 100.00% | - | - | - | - | - | - | - | - |
| 오씨아이파워(주) | 100.00% | - | - | - | - | - | - | - | - |
| 행복도시태양광발전소(주) | 40.00% | - | - | - | - | - | - | - | - |
| (주)유니드 | - | - | - | *1.90% | 25.06% | - | - | - | - |
| (주)유니드비티플러스 | - | - | - | 1.78% | 25.06% | *3.69% | - | - | - |
| 에스지씨에너지(주) | - | - | - | 5.68% | - | - | *0.01% | - | - |
| 에스지씨이앤씨(주) | - | - | - | - | - | - | 26.85% | *0.22% | - |
| 에스지씨그린파워(주) | - | - | - | - | - | - | 95.00% | - | - |
| 에스지씨디벨롭먼트(주) | - | - | - | - | - | - | 100.00% | - | - |
| 에스지씨솔루션(주) | - | - | - | - | - | - | 100.00% | - | - |
| 에스지씨파트너스(주) | - | - | - | - | - | - | 100.00% | - | - |
| 웨스트사이드로지스틱스(주) | - | - | - | - | - | - | 51.00% | 49.00% | - |
| 부광약품(주) | 11.32% | - | - | - | - | - | - | - | - |
| 부광메디카(주) | - | - | - | - | - | - | - | - | 100.00% |
*자기주식
(3) 임원의 겸직현황
| (기준일 : 보고서 제출일 현재) |
| 겸직임원 | 겸직회사 | 비고 | |||
| 성명 | 직위 | 회사명 | 직위 | 담당업무 | |
| 이제영 | 대표이사 | Contera Pharma A/S | Members of the Board of Director | - | - |
| 부광메디카(주) | 대표이사 | 경영전반 | - | ||
| 김지헌 | 전무 | JaguAHR Therapeutics | Members of the Board of Director | 경영전반 | 미등기임원 |
| 박종도 | 상무 | 부광메디카(주) | 사내이사 | - | 미등기임원 |
| 장삼순 | 상무 | 부광메디카(주) | 사내이사 | - | 미등기임원 |
*사외이사의 경우 모두 감사위원을 겸직하고 있습니다.
나. 타법인출자 현황(요약)
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 원) |
| 출자 목적 |
출자회사수 | 총 출자금액 | |||||
|---|---|---|---|---|---|---|---|
| 상장 | 비상장 | 계 | 기초 장부 가액 |
증가(감소) | 기말 장부 가액 |
||
| 취득 (처분) |
평가 손익 |
||||||
| 경영참여 | - | - | - | - | - | - | - |
| 일반투자 | - | - | - | - | - | - | - |
| 단순투자 | 2 | 5 | 7 | 16,429 | 331 | -4,119 | 12,639 |
| 계 | 2 | 5 | 7 | 16,429 | 331 | -4,119 | 12,639 |
IX. 대주주 등과의 거래내용
1. 대주주 등에 대한 신용공여 등
해 당 사 항 없 음
2. 대주주와의 자산양수도 등
해 당 사 항 없 음
3. 대주주와의 영업거래
해 당 사 항 없 음
4. 대주주 이외의 이해관계자와의 거래
가. 출자 및 출자지분 처분내역
| (단위 : 백만원) |
| 성명 (법인명) |
관계 | 출자 및 출자지분 처분내역 | 비 고 | |||||
|---|---|---|---|---|---|---|---|---|
| 출자지분의 종류 | 거 래 내 역 | |||||||
| 기 초 | 증 가 | 감 소 | 평가/ 처분 손익 |
기말 | ||||
| Contera Pharma A/S | 종속기업 | 보통주 | 10,871 | - | - | - | 10,871 | 연결 |
| 부광메디카(주) | 종속기업 | 보통주 | 1,736 | - | - | - | 1,736 | 연결 |
| ProteKt Therapeutics | 종속기업 | 보통주 | - | - | - | - | - | 연결 |
| JaguAHR Therapeutics | 종속기업 | 보통주 | 1,428 | - | - | - | 1,428 | 연결 |
| 종속기업 소계 | 14,035 | - | - | - | 14,035 | - | ||
| 덴탈플랫폼출자조합제1호 | 관계기업 | 지분증권 | - | - | - | - | - | - |
| 관계기업 소계 | - | - | - | - | - | - | ||
| Biodexa Pharmaceuticals | - | 보통주 | 84 | - | - | (57) | 27 | - |
| CytoSite BioPharma Inc | - | 우선주 | 1,720 | - | - | - | 1,720 | - |
| Lyell immunopharma | - | 보통주 | 1,327 | - | - | (210) | 1,117 | - |
| 흥국글로벌사모증권 TVM Life Science Ventures Vll |
- | 지분증권 | 9,951 | - | - | (4,190) | 5,761 | - |
| TVM Life Science Innovation II | - | 지분증권 | 3,084 | 331 | - | 338 | 3,753 | - |
| KDB오픈이노베이션펀드 | - | 지분증권 | 263 | - | - | - | 263 | - |
| 기타 소계 | 16,429 | 331 | - | (4,119) | 12,641 | - | ||
| 합 계 | 30,464 | 331 | - | (4,119) | 26,676 | - | ||
나. 기타 대주주등과의 거래내역
(1) 당분기말 현재 회사와 특수관계에 있는 주요 기업의 개요
| 구 분 | 특수관계자의 명칭 |
|---|---|
| 종속기업 | Contera Pharma A/S |
| 종속기업 | 부광메디카(주) |
| 종속기업 | ProteKt Therapeutics |
| 종속기업 | JaguAHR Therapeutics |
| 관계기업 | 덴탈플랫폼투자조합제1호 |
| 대규모기업집단계열회사 | 오씨아이홀딩스㈜ |
| 대규모기업집단계열회사 | (주)디씨알이 |
| 대규모기업집단계열회사 | 오씨아이드림㈜ |
| 대규모기업집단계열회사 | OCI㈜ |
| 대규모기업집단계열회사 | OCI정보통신 |
(2) 매출 및 매입 등 거래
| (단위: 원) |
| 구 분 | 기업명 | 당분기 | 전분기 | ||
|---|---|---|---|---|---|
| 매출 등 | 매입 등 | 매출 등 | 매입 등 | ||
| 대규모기업집단 계열회사 |
오씨아이홀딩스㈜ | 16,646,721 | 5,805,473 | 17,823,292 | 9,333,026 |
| (주)디씨알이 | 1,883,182 | - | 5,525,818 | - | |
| 오씨아이드림㈜ | 2,486,000 | - | 4,503,000 | 63,908 | |
| OCI㈜ | 18,014,997 | 19,200,000 | 9,901,472 | 6,931,982 | |
| OCI정보통신 | - | 153,965,400 | - | - | |
| 합 계 | 39,030,900 | 178,970,873 | 37,753,582 | 16,328,916 | |
(3) 채권ㆍ채무의 주요 잔액
| (단위: 원) |
| 구 분 | 기업명 | 당분기말 | ||
|---|---|---|---|---|
| 채권 | 채무 | |||
| 기타채권 | 매입채무 | 기타채무 | ||
| 대규모기업집단계열회사 | OCI홀딩스 주식회사 | 6,763,735 | - | 930,875 |
| 오씨아이드림(주) | 784,300 | - | - | |
| OCI(주) | 12,142,232 | 10,560,000 | - | |
| OCI정보통신 | - | - | 12,685,310 | |
| 합 계 | 19,690,267 | 10,560,000 | 13,616,185 | |
| (단위: 원) |
| 구 분 | 기업명 | 전기말 | |
|---|---|---|---|
| 채권 | 채무 | ||
| 기타채권 | 기타채무 | ||
| 대규모기업집단계열회사 | 오씨아이홀딩스㈜ |
968,542 | 1,235,664 |
| 오씨아이드림㈜ | 1,725,350 | - | |
| OCI㈜ | - | 16,896,000 | |
| OCI 정보통신 | - | 10,964,800 | |
| 합 계 | 2,693,892 | 29,096,464 | |
(4) 특수관계자와의 자금 거래
| (단위: 원) |
| 구 분 | 기업명 | 당분기 | |
|---|---|---|---|
| 청산배당 | 기타금융부채상환 | ||
| 주요 경영진 등 | - | - | |
| (단위: 원) |
| 구 분 | 기업명 | 전분기 | |
|---|---|---|---|
| 청산배당 | 기타(*) | ||
| 주요 경영진 등 | - | - | |
(5) 주요 경영진에 대한 보상내역
주요 경영진은 등기이사, 미등기이사(상무)와 감사위원회 위원을 포함하고 있습니 다. 종업원 용역의 대가로서 주요 경영진에게 지급되었거나 지급된 보상금액은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 단기종업원급여 | 1,270,980,712 | 1,005,810,033 |
| 퇴직급여 | 46,184,288 | 27,488,289 |
| 합 계 | 1,317,165,000 | 1,033,298,322 |
X. 그 밖에 투자자 보호를 위하여 필요한 사항
1. 공시내용 진행 및 변경사항
해 당 사 항 없 음
2. 우발부채 등에 관한 사항
(1) 연결회사가 금융기관과 체결하고 있는 약정사항의 내역
| (단위: 원, USD) |
| 금융기관 | 약정사항 | 당분기말 | 전기말 | ||
|---|---|---|---|---|---|
| 한도금액 | 사용금액 | 한도금액 | 사용금액 | ||
| 하나은행 | 일반자금대출 | 30,000,000,000 | 30,000,000,000 | 30,000,000,000 | 30,000,000,000 |
| 수입신용장 | USD 1,000,000 | - | USD 1,000,000 | - | |
| 국민은행 | 일반자금대출 | 30,000,000,000 | - | 30,000,000,000 | - |
| 산업은행 | 일반자금대출 | 10,000,000,000 | - | 10,000,000,000 | - |
| 신한은행 | 일반자금대출 | 50,000,000,000 | 50,000,000,000 | 50,000,000,000 | 50,000,000,000 |
상기 약정 이외에 연결회사는 국민은행과 기업구매론약정(당분기말: 한도 10,000백만원, 전기말: 한도 10,000백만원)과 신한은행과 전자방식매출채권담보대출약정(당분기말: 한도 2,500백만원 전기말: 한도 2,500백만원)을 맺고 있습니다.
당분기말 현재 매입채무및기타채무 금액 중 공급자금융약정과 관련된 금융부채는 2,857백만원이며, 공급자가 금융기관으로부터 당분기말 현재 이미 대금을 수취한 금액은 315백만원입니다.
공급자금융약정에 해당하는 금융부채와 공급자금융약정에 해당하지 않는 금융부채의 지급기일에는 유의적인 차이가 없습니다.
공급자금융약정에 따라 금융기관에게 지급해야 할 금액은 회사의 정상영업주기 내에사용되는 운전자본의 일부로서 매입채무및기타채무와 유사한 성격과 기능을 지니고 있다고 판단하여 이를 매입채무및기타채무로 분류하고, 현금흐름표에서 관련현금흐름을 영업활동현금흐름으로 분류하고 있습니다.
(2) 연결회사가 타인으로부터 제공받은 지급보증의 내역
| (단위: 원) |
| 금융기관 | 약정사항 | 보증금액 | |
|---|---|---|---|
| 당분기말 | 전기말 | ||
| 서울보증보험 | 공탁보증 | - | 60,000,000 |
| 물품대금보증 | 1,060,000,000 | 1,000,000,000 | |
| 합 계 | 1,060,000,000 | 1,060,000,000 | |
(3) 당분기말 현재 차입금 등과 관련하여 담보로 제공되어있는 자산내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 제공처 | 내역 | 담보제공자산 | 장부금액 | 설정금액 |
| 유형자산 | 신한은행 | 차입금 담보 | 토지,건물 | 73,453,239,043 | 60,000,000,000 |
(4) 당분기말 현재 연결회사가 원고로서 진행 중인 소송은 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소소송 1건, 권리범위확인(특) 3건, 총 4건(전기말: 4건)으로 소송가액은 없습니다. 또한 회사가 피고로서 진행중인 소송은 권리범위확인(특) 총 1건(전기말: 1건)으로 소송가액은 없습니다.
| 관할법원 | 원고 | 피고 | 소송의 내용 | 소송가액 | 진행상황 |
| 서울고등법원 | 당사 | 보건복지부장관 | 약제 급여 목록 및 급여 상한금액표 일부개정 고시 취소 | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 당사 | 라퀼리아 파마 인코포레이티드 | 권리범위확인(특) | - | 계류중 |
| 특허법원 | 에치케이이노엔 | 당사 | 권리범위확인(특) | - | 계류중 |
(5) 연결회사는 종속기업인 Contera Pharma A/S와 관련하여 개발 중인 의약품의 허가신청, 시판 승인 및 상용화 조건 달성 여부에 따라 조건부대가를 지급하는 약정을 체결하였습니다. 전기 중 연결회사는 해당 의약품의 임상을 중단하였으며, 이에 따라
미래에 지불할 가능성이 있는 금액을 0으로 평가하였습니다.
(6) 연결회사가 당분기말 현재 보유 중인 당기손익-공정가치측정 금융자산 중 TVM LifeScience Innovation II SCSP에 대한 투자 약정금액은 총 USD 3,000,000이며, 현재까지 USD 2,848,568에 대한 납입이 완료되었습니다. 잔여금액 USD 151,432은 향후 업무집행사원의 출자이행요청에 따라 추가 납입예정이나, 현재 시점에 그 납입시기를 예상할 수 없습니다.
(7) 연결회사가 당분기말 현재 보유 중인 당기손익-공정가치측정 금융자산 중 KDB오픈이노베이션 제2호에 대한 투자 약정금액은 총 5억원이며, 현재까지 5억원 납입이 완료되었습니다.
(8) 연결회사는 종속기업인 ProteKt Therapeutics와 관련하여 개발 중인 의약품의 License 관련 판매 및 배당 등의 조건 달성 여부에 따라 조건부대가를 지급하는 약정을 체결하였습니다.
3. 제재 등과 관련된 사항
가. 제재현황
해 당 사 항 없 음
나. 한국거래소 등으로부터 받은 제재
해 당 사 항 없 음
다. 단기매매차익의 발생 및 반환에 관한 사항
해 당 사 항 없 음
4. 작성기준일 이후 발생한 주요사항 등 기타사항
해 당 사 항 없 음
5. 공모자금 및 사모자금의 사용내역
해 당 사 항 없 음
6. 합병전후의 재무사항 비교표
합병 등의 사후정보
당사는 2024년 03월 22일 자회사 Contera Pharma A/S의 보통주 159,380주에 관한 취득에 대한 타법인 주식 및 출자증권 양수결정에 대한 주요사항 보고서를 제출하였으며, 2024년 04월 01일 최종 양수도대금 지급 및 주식 이전이 완료되어 합병등 종료보고서를 제출하였습니다.
1) 자산양수도 자산내역 및 금액
| 구 분 | 내 용 | 비 고 |
| 양수 대상자산 | Contera Pharma A/S 보통주 | - |
| 양수 주식수 | 159,380주 | - |
| 양수금액(원) | 63,237,230,752원 | 현금 지급 |
| 양도인 | 에이치델타사모투자합자회사 | - |
2) 양수내역
| 구 분 | 내 용 |
| 거래상대방 | 에이치델타사모투자합자회사 |
| 양수 주식 내역 | Contera Pharma A/S 159,380주 |
| 양수금액(원) | 63,237,230,752원 |
3) 진행경과 및 일정
| 구 분 | 일 자 | 비 고 |
| 외부평가기간 | 2024년 03월 05일 ~ 2024년 03월 21일 | 지안회계법인 |
| 이사회결의일 | 2024년 03월 22일 | - |
| 주요사항보고서 제출일 | 2024년 03월 22일 | - |
| 매매 체결일 | 2024년 04월 01일 | - |
| 거래완료일 | 2024년 04월 01일 | - |
4) 합병전후의 요약재무상황
| (단위: K USD) |
| 대상회사 | 계정과목 | 예측 | 실적 | 비고 | ||||
| 1차연도 | 2차연도 | 1차연도 | 2차연도 | |||||
| 실적 | 괴리율 | 실적 | 괴리율 | |||||
| Contera Pharma A/S | 매출액 | 30 | 30 | - | - | - | - | - |
| 영업이익 | (7,775) | (11,430) | (10,596) | 36.3 | - | - | - | |
| 당기순이익 | (7,775) | (11,430) | (9,786) | 25.9 | - | - | - | |
주1) 1차연도는 2024년이고, 2차연도는 2025년입니다.
주2) 재무사항 예측치는 외부평가기관의 평가의견서 자료입니다.
주3) 1차연도 예측대비 마일스톤 매출 미발생 및 CP-012 임상비용 증가 등으로 연구개발비가 예측대비 과다 발생해 괴리율이 10%이상 발생하였습니다.
7. 공개매수신고 등에 관한 사항
해 당 사 항 없 음
8. 견질 또는 담보용 어음ㆍ수표 현황
해 당 사 항 없 음
XI. 상세표
1. 연결대상 종속회사 현황(상세)
| (단위 : 백만원) |
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| Contera Pharma A/S |
2010년 07월 09일 (주1) |
DTU Science Park Venlighedsvej 4 |
의약품 연구 및 개발사업 |
12,523 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
| 부광메디카 (주) |
2015년 06월 17일 (주2) |
서울특별시 동작구 상도로 5(대방동) |
완제 의약품 제조업 및 판매업 |
2,715 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
|
ProteKt Therapeutics |
2015년 01월 01일 (주3) |
16 Bar Kochva St., Bnei-Brak, Israel |
의약품 연구 및 개발사업 |
356 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
|
JaguAHR Therapeutics |
2019년 10월 14일 (주4) |
5 SHENTON WAY, #10-01, UIC BUILDING, SINGAPORE 068808 | 의약품 연구 및 개발사업 |
352 | 기업 의결권의 과반수 소유 (K-IFRS 1110호) |
해당없음 (주5) |
| 종속기업 | 소재지 | 지배지분율(%) | 결산월 | 업종 | |
|---|---|---|---|---|---|
| 당분기말 | 전기말 | ||||
| Contera Pharma A/S | 덴마크 | 99.33 | 99.33 | 12월 | 의약품 연구 및 개발 |
| 부광메디카(주) | 한국 | 100 | 100 | 12월 | 완제 의약품 제조업 및 의약품 도매업 |
| JaguAHR Therapeutics | 싱가포르 | 75.02 | 75.02 | 12월 | 의약품 연구 및 개발 |
| ProteKt Therapeutics | 이스라엘 | 96.53 | 96.53 | 12월 | 의약품 연구 및 개발 |
(주1) 2014년 11월 24일 부광약품(주)에서 약 34억원을 출자하여 인수(지분율 100%) 2018년 07월 18일 14,000주 약 5.5억원 제3자배정 유상증자(지분율 96.26%)
2019년 07월 15일 10,000주 약 30억원 제3자배정 유상증자(지분율 94.38%)
2020년 07월 22일 40,000주 양도 및 352억원 제3자배정유상증자(지분율71.23%)
2022년 11월 14일 비지배주주의 매도청구권 행사로 인한 10,000주 매수
(지분율 72.84%)
2023년 08월 17일 31,250주 약 100억원 유상증자(지분율 74.14%)
2024년 04월 01일 관계회사 에이치델타 사모투자합자회사의
주식매수청구권 행사로 인한 159,380주 매수(지분율 98.56%)
2024년 08월 27일 413,793주 약 44억원 유상증자(지분율 99.12%)
2024년 10월 27일 336,700주 약 30억원 유상증자(지분율 99.33%)
(주2) 2015년 06월 17일 부광약품(주)에서 5억원을 출자하여 설립
2015년 10월 17일 약 13억원의 현금출자
2015년 10월 20일 약 127억원 상당의 현물출자
2019년 03월 08일 50억원의 현금출자
2021년 01월 25일 110억원의 유상감자(부광약품(주) 지분율 100%)
(주3) 2023년 01월 26일 기존 주주의 주식 3,869,472주를 인수하는 조건의 주주간계약을 체결하여 지배력을 확보함(부광약품(주)지분율 96.53%)
(주4) 2024년 11월 26일 설립 파트너사인 Aslan Pharma가 청산됨에 따라, Aslan Pharma로부터 22,050주를 인수하는 계약을 체결하여 지배력을 확보함(부광약품(주)지분율 75.02%)
(주5) 지배회사 자산총액의 10%미만이거나 자산총액이 750억원 미만이므로 주요종속회사에 해당되지 않음
2. 계열회사 현황(상세)
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 사) |
| 상장여부 | 회사수 | 기업명 | 법인등록번호 |
|---|---|---|---|
| 상장 | 7 | 오씨아이홀딩스㈜ | 174611-0000981 |
| 오씨아이㈜ | 110111-8626793 | ||
| ㈜유니드 | 110111-0275069 | ||
| 에스지씨에너지㈜ | 110111-0079817 | ||
| 에스지씨이앤씨㈜ | 110111-0327555 | ||
| 부광약품㈜ | 110111-0030405 | ||
| ㈜유니드비티플러스 | 110111-8466280 | ||
| 비상장 | 17 | (주)디씨알이 | 120111-0464149 |
| (주)디씨알이대우제1호 위탁관리부동산투자회사 |
110111-9019666 | ||
| (주)새한리싸이클 | 134611-0061866 | ||
| (주)유니드글로벌상사 | 110111-1072159 | ||
| 부광메디카(주) | 110111-5755199 | ||
| 에스지씨그린파워(주) | 211111-0042698 | ||
| 에스지씨디벨롭먼트(주) | 211111-0033639 | ||
| 에스지씨솔루션(주) | 110111-7669736 | ||
| 에스지씨파트너스(주) | 110111-8124242 | ||
| 오씨아이드림(주) | 110111-7198024 | ||
| 오씨아이스페셜티(주) | 161511-0108609 | ||
| 오씨아이에스이(주) | 211111-0035867 | ||
| 오씨아이파워(주) | 110111-4984137 | ||
| 오씨아이페로(주) | 110111-2410233 | ||
| 오씨아이정보통신(주) | 110111-1443780 | ||
| 웨스트사이드로지스틱스(주) | 211111-0080606 | ||
| 행복도시태양광발전소(주) | 131111-0336311 |
3. 타법인출자 현황(상세)
가. 타법인 출자현황(5% 이상)
| (기준일 : | 2025년 03월 31일 | ) | (단위 : 백만원, 주, %) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
| CytoSite BioPharma Inc 우선주(주1) |
비상장 | 2018.08.06 | 단순 투자 |
1,720 | 624,973 | 8.54 | 1,720 | - | - | - | 624,973 | 8.54 | 1,720 | 278 | -1,337 |
| 덴탈플랫폼 출자조합제1호(주2) |
비상장 | 2019.05.28 | 단순 투자 |
2,000 | 200 | 50.00 | - | - | - | - | 200 | 50.00 | - | 68 | -2 |
| 합 계 | - | - | 1,720 | - | - | - | - | - | 1,720 | - | - | ||||
* 최초 취득금액은 총 투자금액을 표시함
(주1) 1. 2018년 08월 06일 약 8.5억 출자로 312,486주 취득
2. 2019년 09월 11일 약 4.5억 출자로 156,243주 취득
3. 2020년 09월 22일 약 8,500만원 출자로 30,636주 취득
4. 2021년 07월 01일 약 3.4억 출자로 125,608주 취득
(주2) 1. 2019년 05월 28일 20억원 출자로 200좌 취득
나. 5%미만 타법인 출자현황
| (2025년 03월 31일 현재) | (단위 : 주, 백만원, %) |
| 구분 | 상장 여부 |
법인명 또는 종목명 |
출자 목적 |
기초잔액 | 증가(감소)내역 | 기말잔액 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 최초 취득 금액 |
수량 | 지 분 율 |
장부 가액 |
취득(처분) | 평가/ 처분 손익 |
수량 | 지 분 율 |
장부 가액 |
비고 | |||||
| 수량 | 금액 | |||||||||||||
| 국외 | 상장 | Biodexa Pharmaceuticals (주1) | 단순 투자 |
- | 14,177 | 2.12 | 84 | - | - | -57 | 14,177 | 2.12 | 27 | - |
| 국외 | 상장 | Lyell immunopharma (주2) | 단순 투자 |
- | 1,410,071 | 0.48 | 1,327 | - | - | -210 | 1,410,071 | 0.48 | 1,117 | - |
| 국외 | 비상장 | 흥국글로벌 사모증권 (주3) (TVM Life Science Ventures Vll) |
단순 투자 |
18,961 | - | - | 9,951 | - | - | -4,190 | - | - | 5,761 | - |
| 국외 | 비상장 | TVM Life Science Innovation II (주4) |
단순 투자 |
3,201 | - | - | 3,084 | - | 331 | 338 | - | - | 3,753 | - |
| 국내 | 비상장 | KDB오픈이노베이션펀드 (주5) | 단순 투자 |
500 | - | 2.37 | 263 | - | - | - | - | 2.37 | 263 | - |
| 합계 | 22,662 | - | - | 14,709 | - | 331 | -4,119 | - | - | 10,921 | - | |||
(주1) 1. 파이프라인 'MLR-1023' 의 판권을 반환하는 대가로 354,428주의
Biodexa Pharmaceuticals 주식을 취득
2. 2024년 10월 중 액면병합으로 1:0.04 비율로 전환됨
(주2) 1. 2021년 07월 07일 11억원 출자로 76,378주 취득
2. 2021년 12월 24일 38억원 출자로 205,558주 취득
3. 2024년 11월 15일 ImmPACT Bio Ltd는 Lyell immunopharma에 합병되었으며 기존 주식은 현금 2,208백만원과 Lyell immunopharma 주식 1,419,071주로 교 환됨
(주3) TVM Capital사가 운용하는 TVM Life Science Ventures Vll에 유한 책임 조합원
과 Strategic Partner로서 투자 계약을 체결하고 흥국자산운용 주식회사가
해당 feeder fund의 구성을 위한 신탁계약을 체결함
(주4) TVM Capital사가 운용하는 TVM Life Science Ventures VllI에 유한 책임 조합
으로서 투자 계약을 체결함
(주5) The Turning Point와 GSA PE가 운용하는 펀드이며, 총 약정금액 5억원 중
5억원 납입완료함
【 전문가의 확인 】
1. 전문가의 확인
해 당 사 항 없 음
2. 전문가와의 이해관계
해 당 사 항 없 음