 |
|
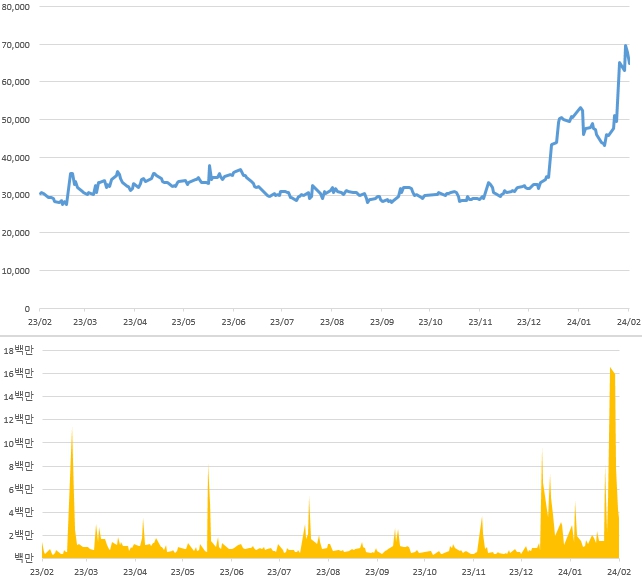
에이치엘비 최근 1개년 주가 추이 |
정 정 신 고 (보고)
| 2024년 05월 23일 |
1. 정정대상 공시서류 : 증권신고서
2. 정정대상 공시서류의 최초제출일 : 2024년 03월 21일
3. 정정사항
| 항 목 | 정정요구ㆍ명령 관련 여부 |
정정사유 | 정 정 전 | 정 정 후 |
|---|---|---|---|---|
| ※ 단순 오타 및 표현 수정 등은 별도의 색깔표시 없이 정정하였습니다. ※ 요약정보 관련해서는 본문의 정정사항을 반영하였으며, 정오표를 별도로 기재하지 않았습니다. ※ 금번 정정사항은 기재사항 추가 및 보완을 위한 기재정정으로, 정정사항 확인의 편의를 위해 정정사항은 '굵은 보라색 글씨체'를 사용하여 기재하였습니다. |
||||
| 제 1부 모집 또는 매출에 관한 사항 | ||||
| III. 투자위험요소 - 1. 사업위험 | ||||
| 라. 신약개발의 낮은 성공가능성 및 수익성 위험 | 아니요 | 기재정정 | (주1) 정정 전 | (주1) 정정 후 |
| III. 투자위험요소 - 2. 회사위험 | ||||
| 마. 특수관계자와의 거래에 따른 위험 | 아니요 | 기재정정 | (주2) 정정 전 | (주2) 정정 후 |
| 바. 우발채무 및 소송관련 위험 | (주3) 정정 전 | (주3) 정정 후 | ||
| 차. 에이치엘비 주식회사 주가 변동에 따른 손익 변동 위험 | (주4) 정정 전 | (주4) 정정 후 | ||
| III. 투자위험요소 - 3. 기타위험 | ||||
| 차. 재무제표 작성 기준일 이후 재무상황 변동에 따른 위험 | 아니요 | 기재정정 | (주5) 정정 전 | (주5) 정정 후 |
| IV. 인수인의 의견(분석기관의 평가의견) | (주6) 정정 전 | (주6) 정정 후 | ||
| V. 자금의 사용목적 | (주7) 정정 전 | (주7) 정정 후 | ||
| 제 2부 발행인에 관한 사항 | ||||
| I. 회사의 개요 - 1. 회사의 개요 | 아니요 | 기재정정 | (주8) 정정 전 | (주8) 정정 후 |
| II. 사업의 내용 - 1. 사업의 개요 | (주9) 정정 전 | (주9) 정정 후 | ||
| II. 사업의 내용 - 6. 주요계약 및 연구개발활동 | (주10) 정정 전 | (주10) 정정 후 | ||
| II. 사업의 내용 - 7. 기타 참고사항 | (주11) 정정 전 | (주11) 정정 후 | ||
(주1) 정정 전
(전략)
당사는 현재 자체적으로 3개의 항암 신약 물질에 대한 국내 전용실시권을 보유하고 있으며, 당사가 본 공시서류 제출일 전일 기준 99.30%의 지분을 보유한 종속회사 에이치엘비셀(주)는 바이오인공간, 지혈제(생분해성 의료용 접착제 또는 실란트 조성물), 인간 세포외기질의 3개 분야에서 파이프라인을 구축하고 있습니다. 또한 계열회사인 Elevar Therapeutics("Elevar")는 표적항암제 리보세라닙(Rivoceranib, 舊 Apatinib Mesylate) 관련 라이센스 인(License-in) 계약을 체결하였습니다. 리보세라닙의 경우 위암 말기 치료제 임상 3상을 완료하여 미국식품의약국(FDA)에 NDA 준비중이며, 타 암종으로의 적응증 확대를 위한 단독 및 병용 임상을 지속적으로 진행하고 있습니다. 또한 리보세라닙과 캄렐리주맙(Camrelizumab) 병용요법 간암 1차 치료제는 2023년 5월 미국 FDA에 NDA Submission 완료한 상태이며, 파이로티닙의 경우 비소세포폐암과 전이성 유방암은 임상3상을 진행중에 있습니다.
(중략)
| [연구개발 진행 총괄표] |
|
구 분 |
품 목 |
적응증 |
임상시작일 |
현재 진행단계 |
임상주도 기업 | ||||
|---|---|---|---|---|---|---|---|---|---|
|
단계(국가) |
승인일 |
비 고 | 회사명 | 비고 | |||||
|
화학합성 |
신약 |
리보세라닙 (Rivoceranib) [Elevar Therapeutics, Inc.주도 글로벌 임상 포함] |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안정성평가 완료 | Elevar | Rivoceranib 전용실시권 도입 후 자체 개발 |
|
위암 (3차/4차 단일요법) |
2017년 |
임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
Elevar | Rivoceranib 전용실시권 도입 후 자체 개발 | |||
|
위암 (1차 병용요법) |
2021년 |
임상2상 |
2021년 09월 (임상2상 승인일) |
임상 진행 중 | HLB생명과학 | Rivoceranib 한국 내 전용실시권 도입 후 개발 |
|||
|
간암 (1차 병용요법) |
2019년 |
임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
임상 종료 22년 9월 초록 발표 (1차 평가 지표 만족) 23년 5월 미국 FDA에 NDA Submission 완료 |
Elevar | 항서제약과 공동개발 | |||
|
선양낭성암종 (1/2차 단일요법) |
2020년 |
임상2상 |
2020년 4월 (임상2상 개시일) |
임상 2상 종료 6월 초록 발표, |
Elevar HLB생명과학 |
Rivoceranib 전용실시권 도입 후 자체 개발 |
|||
|
위암 (2차 병용요법) |
2018년 |
임상2상 |
2018년 10월 (임상1상 개시일) |
임상 종료 22년 결과 발표 |
HLB생명과학 | Rivoceranib 전용실시권 도입 후 자체 개발 |
|||
|
대장암 (3차 병용요법) |
2019년 |
임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 종료 |
Elevar | Rivoceranib 전용실시권 도입 후 자체 개발 |
|||
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상 진행 중 (농림축산검역본부) |
HLB생명과학 | Rivoceranib 한국 내 전용실시권 도입 후 자체 개발 |
|||
| 파이로티닙 (Pyrotinib) |
전이성 유방암 | 2023년 | 임상3상 (한국) |
2023년 03월 (임상계획 승인) |
임상3상 진행 중 | HLB생명과학 | Pyrotinib 한국 내 전용실시권 도입 후 자체 개발 |
||
| 비소세포폐암 | 2020년 | 임상3상 (전세계 13개국) |
2020년 (임상계획 승인) |
임상3상 진행 중 | 항서제약 | Pyrotinib 한국 내 전용실시권 도입 후 자체 개발 |
|||
|
HLS221-N01 G2M 억제제 |
폐암 유방암 대장암 췌장암 |
- |
비임상시험 단계 |
- |
비임상평가 진행 중 |
HLB생명과학 |
특허권 도입 후 자체 개발 | ||
|
HLS222-N01 Cannabinoids derivatives |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
HLB생명과학 |
네오켄바이오와 공동연구 | ||
|
HLS232-N01 CDK 억제제 |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
HLB생명과학 |
LDC와 공동연구 | ||
|
HLS231-G01 의료용 대마 |
뇌전증 | - | 탐색 단계 | - | 제형 연구 중 | HLB생명과학 R&D |
- | ||
|
바이오 |
신약 |
바이오인공간 |
급성간부전 |
2001년 |
임상 2b상 |
2017년 임상 2a 완료 |
자체 개발 |
HLB셀 | - |
|
의료기기 |
지혈제 |
조직/장기 출혈 |
2015년 |
확증임상시험 |
2021년 임상계획 승인 |
확증임상 진행 중 |
HLB셀 | UI-DDS 연구소 글로벌 권리 도입 후 자체 개발 |
|
| 연구용 재료 | 인체 세포 외 기질 (Hutrigel®-RU) |
줄기세포, 오가노이드 배양 기질 | N/A | 연구개발완료 | N/A | 제품판매 준비 중 |
HLB셀 | 자체 개발 | |
| 의료기기 | 인체 세포 외 기질 (Hutrigel®-MU) |
피부, 신경, 심근 등 상처 치유 및 조직 재생 |
N/A | 연구개발 중 | N/A | GMP-compliant , 비임상 유효성평가 준비 중 |
HLB셀 | 자체 개발 | |
|
의료기기 |
인체 세포 외 기질 (Hutrigel®-AU) |
의료용/미용용 기능성 제품 |
N/A |
연구개발 중 |
N/A |
제형화 및 생체 외 |
HLB셀 HLB제약 |
자체 개발 | |
(중략)
Elevar는 리보세라닙 위암 말기 단독치료제를 목적으로 하는 3상 임상시험 완료 후 데이터를 확정하여 2019년 10월 미국 FDA와 Pre-NDA 미팅을 하였으며, 그 결과를 바탕으로 최종 Data분석 및 적절한 허가 전략을 수립한 후, 신약허가를 신청할 계획입니다. 리보세라닙은 위암에 대해 희귀의약품으로 지정(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국)됨에 따라 임상종료 후 시판허가에 대한 신속화, 수수료 감면 등의 혜택과 더불어 이후 최소 8년(2029년까지)에서 최대 13년(2034년까지)동안 독점 판매할 수 있습니다. 특히, 위암에 대해서는 중국에서 항서제약이 임상 3상을 종료 후 시판허가를 득하여 현재 중국에서 판매되고 있습니다. 현재 당사는 특허기간 등을 고려하여 리보세라닙 단독 요법 보다는 캄렐리주맙 병용요법에 집중하고 있습니다. 리보세라닙과 캄렐리주맙 병용요법의 간암 1차 치료제 경우, 2023년 5월 NDA(신약 허가신청)를 신청하였으며, 7월 NDA 본심사가 개시되었습니다. 2023년 8월 리보세라닙 공장실사 및 12월 캄렐리주맙 공장실사까지 완료했으며, 2024년 5월 리보세라닙과 캄렐리주맙 병용요법 FDA 신약 허가 관련 결과를 기다리고 있는 상황입니다. FDA 신약 승인 허가가 난다면, 당사는 국내에서 리보세라닙과 캄렐리주맙 병용요법 임상 및 시판 허가 관련 식품의약품안전처로부터 승인 요청을 연내에 진행할 계획입니다.
| [계열회사 Elevar의 신약 후보물질 개발 추진 현황(리보세라닙)] |
| 구 분 |
개발제품 |
적응증 |
개발현황 및 향후 계획 |
|---|---|---|---|
| 신약개발 | 리보세라닙 (Rivoceranib, 구Apatinib Mesylate) |
표적항암제 |
1) 위암 3/4차 치료제: 단독 요법으로 글로벌 임상 3상 종료 및 조건부 품목허가 및 임상 3상 계획수립 2) 위암 2차 치료제: 파클리탁셀과 병용으로 임상 1/2상 종료 3) 선양낭성암 1,2차 치료제: 단독요법으로 미국, 한국에서 임상 2상 연구 종료, 한국 조건부 품목허가 신청 및 자진 취하 4) 간암 1차 치료제: 항서제약의 캄렐리주맙과 병용으로 글로벌 13개국 임상 3상종료, 2022년 9월 ESMO에서 임상 결과 공개(1차 평가지표 만족), 23년 5월 미국 FDA에 NDA Submission 완료. 미국 NDA 대응 및 상업화 전략 수립, 한국 NDA 신청전략 수립 및 NDA 신청 계획 5) 대장암 3차 치료제: 타이호제약의 론서프와 병용으로 미국, 한국에서 임상 1b/2상 중 1b상 종료 |
| 출처: 당사 제공 자료 |
(중략)
또한, 당사는 상기 언급한 파이프라인의 제품 개발을 위한 연구개발 및 임상을 위해 지속적인 노력을 쏟고 있습니다. 하지만 임상시험이 성공하고 제품이 시판되더라도,경쟁사 제품이 당사 제품보다 더욱 빨리 시판되거나, 관련 시장을 먼저 선점할 경우 추후 당사의 연구개발 성과가 상대적으로 저평가 될 수 있습니다.
당사가 개발 중인 항암치료제, 의료용 접착제 및 실란트 조성물 등의 경우 당사 외에도 다수의 제약회사들이 개발을 진행 중에 있으며, 개발단계가 당사보다 앞서 있거나 이미 시판중인 제품을 보유한 회사들도 존재합니다. 따라서 당사 제품의 개발이 성공적으로 완료되어 시장에 출시되더라도 기 출시된 타 제품 대비 차별성이 크지 않을 경우 교체 수요 저하로 매출 확대에 어려움이 존재할 수 있으며, 당사 제품보다 효능이 뛰어난 의약품이 출시될 경우 당사 제품에 대한 수요가 감소할 수 있습니다. 또한, 당사가 주력하고 있는 파이프라인보다 경쟁신약의 연구개발 단계가 선행되거나, 경쟁신약의 효능이 당사 개발 신약보다 뛰어나다고 판명되는 등 관련 경쟁에서 당사가 뒤처질 경우, 당사의 파이프라인 상에서 발생되는 매출이 적어지거나 발생하지 않을 가능성이 있으며, 이는 기존에 신약 개발에 투자한 당사의 수익성에 부정적인 영향을 끼칠 수 있습니다. 특히 당사의 경우 FDA 판매승인을 통한 간암 대상 리보세라닙과 캄렐리주맙 병용요법의 상용화를 앞두고 있는 상황에서 FDA 판매 승인 허가가 기존 예상되는 시점 대비 지연될 경우 당사 및 당사 관계회사의 수익성과 주가에 부정적으로 작용할 가능성이 있으니 투자자께서는 유의하시기 바랍니다.
(주1) 정정 후
(전략)
당사는 현재 자체적으로 3개의 항암 신약 물질에 대한 국내 전용실시권을 보유하고 있으며, 당사가 본 공시서류 제출일 전일 기준 99.30%의 지분을 보유한 종속회사 에이치엘비셀(주)는 바이오인공간, 지혈제(생분해성 의료용 접착제 또는 실란트 조성물), 인간 세포외기질의 3개 분야에서 파이프라인을 구축하고 있습니다. 또한 계열회사인 Elevar Therapeutics("Elevar")는 표적항암제 리보세라닙(Rivoceranib, 舊 Apatinib Mesylate) 관련 라이센스 인(License-in) 계약을 체결하였습니다. 리보세라닙의 경우 위암 말기 치료제 임상 3상을 완료하여 미국식품의약국(FDA)에 NDA 준비중이며, 타 암종으로의 적응증 확대를 위한 단독 및 병용 임상을 지속적으로 진행하고 있습니다. 또한 리보세라닙과 캄렐리주맙(Camrelizumab) 병용요법 간암 1차 치료제는 2023년 5월 미국 FDA에 NDA Submission 완료하였으며, 2024년 5월 17일 FDA로부터 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL(보완요구서한, Complete Response Letter) 수령하였습니다. 파이로티닙의 경우 비소세포폐암과 전이성 유방암은 임상3상을 진행중에 있습니다.
(중략)
| [연구개발 진행 총괄표] |
|
구 분 |
품 목 |
적응증 |
임상시작일 |
현재 진행단계 |
임상주도 기업 | ||||
|---|---|---|---|---|---|---|---|---|---|
|
단계(국가) |
승인일 |
비 고 | 회사명 | 비고 | |||||
|
화학합성 |
신약 |
리보세라닙 (Rivoceranib) [Elevar Therapeutics, Inc.주도 글로벌 임상 포함] |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안정성평가 완료 | Elevar | Rivoceranib 전용실시권 도입 후 자체 개발 |
|
위암 (3차/4차 단일요법) |
2017년 |
임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
Elevar | Rivoceranib 전용실시권 도입 후 자체 개발 | |||
|
위암 (1차 병용요법) |
2021년 |
임상2상 |
2021년 09월 (임상2상 승인일) |
임상 진행 중 | HLB생명과학 | Rivoceranib 한국 내 전용실시권 도입 후 개발 |
|||
|
간암 (1차 병용요법) |
2019년 |
임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
- 임상 종료, 22년 9월 초록 발표(1차 평가 지표 만족) - 23년 5월 미국 FDA에 NDA Submission 완료 - 24년 5월 미국 FDA 수정 보완 요구(CRL 수령) |
Elevar | 항서제약과 공동개발 | |||
|
선양낭성암종 (1/2차 단일요법) |
2020년 |
임상2상 |
2020년 4월 (임상2상 개시일) |
임상 2상 종료 6월 초록 발표, |
Elevar HLB생명과학 |
Rivoceranib 전용실시권 도입 후 자체 개발 |
|||
|
위암 (2차 병용요법) |
2018년 |
임상2상 |
2018년 10월 (임상1상 개시일) |
임상 종료 22년 결과 발표 |
HLB생명과학 | Rivoceranib 전용실시권 도입 후 자체 개발 |
|||
|
대장암 (3차 병용요법) |
2019년 |
임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 종료 |
Elevar | Rivoceranib 전용실시권 도입 후 자체 개발 |
|||
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상 진행 중 (농림축산검역본부) |
HLB생명과학 | Rivoceranib 한국 내 전용실시권 도입 후 자체 개발 |
|||
| 파이로티닙 (Pyrotinib) |
전이성 유방암 | 2023년 | 임상3상 (한국) |
2023년 03월 (임상계획 승인) |
임상3상 진행 중 | HLB생명과학 | Pyrotinib 한국 내 전용실시권 도입 후 자체 개발 |
||
| 비소세포폐암 | 2020년 | 임상3상 (전세계 13개국) |
2020년 (임상계획 승인) |
임상3상 진행 중 | 항서제약 | Pyrotinib 한국 내 전용실시권 도입 후 자체 개발 |
|||
|
HLS221-N01 G2M 억제제 |
폐암 유방암 대장암 췌장암 |
- |
비임상시험 단계 |
- |
비임상평가 진행 중 |
HLB생명과학 |
특허권 도입 후 자체 개발 | ||
|
HLS222-N01 Cannabinoids derivatives |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
HLB생명과학 |
네오켄바이오와 공동연구 | ||
|
HLS232-N01 CDK 억제제 |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
HLB생명과학 |
LDC와 공동연구 | ||
|
HLS231-G01 의료용 대마 |
뇌전증 | - | 탐색 단계 | - | 제형 연구 중 | HLB생명과학 R&D |
- | ||
|
바이오 |
신약 |
바이오인공간 |
급성간부전 |
2001년 |
임상 2b상 |
2017년 임상 2a 완료 |
자체 개발 |
HLB셀 | - |
|
의료기기 |
지혈제 |
조직/장기 출혈 |
2015년 |
확증임상시험 |
2021년 임상계획 승인 |
확증임상 진행 중 |
HLB셀 | UI-DDS 연구소 글로벌 권리 도입 후 자체 개발 |
|
| 연구용 재료 | 인체 세포 외 기질 (Hutrigel®-RU) |
줄기세포, 오가노이드 배양 기질 | N/A | 연구개발완료 | N/A | 제품판매 준비 중 |
HLB셀 | 자체 개발 | |
| 의료기기 | 인체 세포 외 기질 (Hutrigel®-MU) |
피부, 신경, 심근 등 상처 치유 및 조직 재생 |
N/A | 연구개발 중 | N/A | GMP-compliant , 비임상 유효성평가 준비 중 |
HLB셀 | 자체 개발 | |
|
의료기기 |
인체 세포 외 기질 (Hutrigel®-AU) |
의료용/미용용 기능성 제품 |
N/A |
연구개발 중 |
N/A |
제형화 및 생체 외 |
HLB셀 HLB제약 |
자체 개발 | |
(중략)
Elevar는 리보세라닙 위암 말기 단독치료제를 목적으로 하는 3상 임상시험 완료 후 데이터를 확정하여 2019년 10월 미국 FDA와 Pre-NDA 미팅을 하였으며, 그 결과를 바탕으로 최종 Data분석 및 적절한 허가 전략을 수립한 후, 신약허가를 신청할 계획입니다. 리보세라닙은 위암에 대해 희귀의약품으로 지정(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국)됨에 따라 임상종료 후 시판허가에 대한 신속화, 수수료 감면 등의 혜택과 더불어 이후 최소 8년(2029년까지)에서 최대 13년(2034년까지)동안 독점 판매할 수 있습니다. 특히, 위암에 대해서는 중국에서 항서제약이 임상 3상을 종료 후 시판허가를 득하여 현재 중국에서 판매되고 있습니다. 현재 당사는 특허기간 등을 고려하여 리보세라닙 단독 요법 보다는 캄렐리주맙 병용요법에 집중하고 있습니다. 리보세라닙(HLB)과 캄렐리주맙(항서제약) 병용요법의 간암 1차 치료제 경우, 2023년 5월 NDA(신약 허가신청)를 신청하였으며, 7월 NDA 본심사가 개시되었습니다. 2023년 8월 리보세라닙 공장실사 및 12월 캄렐리주맙 공장실사까지 완료하였으나, 2024년 5월 미국 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL(보완요구서한, Complete Response Letter) 수령하였습니다. CRL 통한 요구 사항은 1) 병용투여 약물인 캄렐리주맙(항서제약)의 CMC(의약품 생산시설 실사) 진행 후 항서제약이 보완한 사항에 대해 일부 미비한 점에 대한 보완 2) 미국 FDA가 BIMO Inspection(임상사이트 실사)를 여행제한으로 인해 완료하지 못했다는 내용입니다. 계열회사 Elevar Therapeutics, Inc.는 상기 두가지 보완사항에 대해 항서제약과 긴밀히 협의하여 이에 대해 신속히 보완하고 FDA 재승인 신청할 예정이며, 재승인 신청 후 최장 6개월 이내 FDA는 승인여부를 결정하게 됩니다.
| [계열회사 Elevar의 신약 후보물질 개발 추진 현황(리보세라닙)] |
| 구 분 |
개발제품 |
적응증 |
개발현황 및 향후 계획 |
|---|---|---|---|
| 신약개발 | 리보세라닙 (Rivoceranib, 구Apatinib Mesylate) |
표적항암제 |
1) 위암 3/4차 치료제: 단독 요법으로 글로벌 임상 3상 종료 및 조건부 품목허가 및 임상 3상 계획수립 2) 위암 2차 치료제: 파클리탁셀과 병용으로 임상 1/2상 종료 3) 선양낭성암 1,2차 치료제: 단독요법으로 미국, 한국에서 임상 2상 연구 종료, 한국 조건부 품목허가 신청 및 자진 취하 4) 간암 1차 치료제: 항서제약의 캄렐리주맙과 병용으로 글로벌 13개국 임상 3상종료, 2022년 9월 ESMO에서 임상 결과 공개(1차 평가지표 만족), 2023년 5월 미국 FDA에 NDA Submission 완료, 2024년 5월 미국 FDA로부터 CRL(보완요구서한) 수령 5) 대장암 3차 치료제: 타이호제약의 론서프와 병용으로 미국, 한국에서 임상 1b/2상 중 1b상 종료 |
| 출처: 당사 제공 자료 |
(중략)
또한, 당사는 상기 언급한 파이프라인의 제품 개발을 위한 연구개발 및 임상을 위해 지속적인 노력을 쏟고 있습니다. 하지만 임상시험이 성공하고 제품이 시판되더라도,경쟁사 제품이 당사 제품보다 더욱 빨리 시판되거나, 관련 시장을 먼저 선점할 경우 추후 당사의 연구개발 성과가 상대적으로 저평가 될 수 있습니다.
당사가 개발 중인 항암치료제, 의료용 접착제 및 실란트 조성물 등의 경우 당사 외에도 다수의 제약회사들이 개발을 진행 중에 있으며, 개발단계가 당사보다 앞서 있거나 이미 시판중인 제품을 보유한 회사들도 존재합니다. 따라서 당사 제품의 개발이 성공적으로 완료되어 시장에 출시되더라도 기 출시된 타 제품 대비 차별성이 크지 않을 경우 교체 수요 저하로 매출 확대에 어려움이 존재할 수 있으며, 당사 제품보다 효능이 뛰어난 의약품이 출시될 경우 당사 제품에 대한 수요가 감소할 수 있습니다. 또한, 당사가 주력하고 있는 파이프라인보다 경쟁신약의 연구개발 단계가 선행되거나, 경쟁신약의 효능이 당사 개발 신약보다 뛰어나다고 판명되는 등 관련 경쟁에서 당사가 뒤처질 경우, 당사의 파이프라인 상에서 발생되는 매출이 적어지거나 발생하지 않을 가능성이 있으며, 이는 기존에 신약 개발에 투자한 당사의 수익성에 부정적인 영향을 끼칠 수 있습니다. 특히 당사의 경우 최대주주인 에이치엘비가 리보세라닙과 캄렐리주맙 병용요법 관련하여 2024년 5월 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL(보완요구서한)을 수령하였습니다. 이와 관련하여 항서제약의 CMC(의약품 생산시설 실사) 보완 및 BIMO Inspection(임상사이트 실사) 완료 시기에 대한 불확실성이 있습니다. 또한 당사는 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있어 FDA 재승인 신청 후 판매승인 시점이 지연될 경우 당사 및 당사 관계회사의 수익성과 주가에도 부정적으로 작용할 가능성이 있으니 투자자께서는 유의하시기 바랍니다.
(주2) 정정 전
(전략)
한편 당사의 특수관계자 바다중공업은 에이치엘비의 종속회사인 에이치엘비이앤지의 종속회사이며, 바다중공업 기타채권 중 당사의 종속회사 에이치엘비셀로부터 받은 대여금 및 이자 비용 800백만원을 상환하였습니다. 또한 HLB그룹에서 설립한 에이치벨류에셋에 부동산 투자를 위해 50억원을 출자하였습니다.
| [특수관계자와의 자금 거래 내역] |
| (단위: 천원) |
| 구 분 | 회사명 | 자금 대여(차입) 거래 | 금융수익(원가) | 현금 출자 등 | |
|---|---|---|---|---|---|
| 대여(차입) | 회수(상환) | 이자수익 | |||
| 관계기업 | 에이치벨류에셋 | - | - | - | 5,000,000 |
| 소계 | - | - | - | 5,000,000 | |
| 기타의 특수관계자 | 에이치엘비아이알밤제1호투자조합 | - | - | - | 800,000 |
| 바다중공업㈜ | - | (800,000) | 3,125 | - | |
| 임직원 | - | (1,500) | - | - | |
| 소계 | - | (801,500) | 3,125 | 800,000 | |
| 합계 | - | (801,500) | 3,125 | 5,800,000 | |
| 출처 : 당사 분기보고서 |
(후략)
(주2) 정정 후
(전략)
또한 당사는 종속회사 HLB에너지가 현재 진행중인 부산 구평동 소각시설 증설사업 프로젝트 금융 자금 대출 420억원에 대해 2024년 05월 23일 채무보증 및 담보제공을 결정하였으며, 이는 타인에 대한 담보제공 결정 공시(2024.05.23)로 공시되었습니다. HLB에너지는 담보대출 중 환경부 환경정책자금 명목으로 하나은행으로부터의 200억원 및 하나은행 150억원, 하나캐피탈 70억원의 일반대출까지 총 420억원의 대출을 진행하였으며, 자세한 내용은 아래와 같습니다.
| [HLB에너지 소각로 증설 대출금액] |
|
구분
|
내용 | 차입처 | 금액(억원) | 금리(%) |
만기
|
비고 |
|---|---|---|---|---|---|---|
| 담보대출 | 환경정책자금 | 하나은행 |
200
|
2.44(변동) | 2033년 09월 30일 | 환경부 분기별 금리 고시 |
| 일반 | 하나은행 |
150
|
7.10(변동) | 최초 인출일 ~ 36개월 경과 |
- | |
| 하나캐피탈 | 70 | 7.10(고정) | - | |||
|
합계
|
- | - | 420 | - | - | - |
| 출처: 당사 제공 자료 |
대출에 대한 당사가 보유한 HLB에너지 보통주식 전부가 근질권 설정을 통해 담보제공되며, 본건 사업 관련 당사의 책임준공확약, 대출약정상 피담보채무에 대한 당사의 연대보증, 출자약정을 통한 자금보충약정을 제공합니다.
| [HLB에너지 대출 담보내역] |
| 구분 | 내용 | 담보설정액(억원) | 장부가액(억원) |
|---|---|---|---|
| HLB생명과학 보유 지분 |
HLB에너지 보통주식 2,302,099주 |
대출약정금액 420억원의 120% |
302억원 |
| 출처: 당사 제공 자료 |
한편 당사의 특수관계자 바다중공업은 에이치엘비의 종속회사인 에이치엘비이앤지의 종속회사이며, 바다중공업 기타채권 중 당사의 종속회사 에이치엘비셀로부터 받은 대여금 및 이자 비용 800백만원을 상환하였습니다. 또한 HLB그룹에서 설립한 에이치벨류에셋에 부동산 투자를 위해 50억원을 출자하였습니다.
(후략)
(주3) 정정 전
(전략)
증권신고서 제출일 현재 계류 중인 소송 사건에 대해서는 소송의 결과를 합리적으로 예측할 수 없으며, 당사가 피고로 진행 중인 사건과 관련해서 최종적으로 패소 시 청구액에 상당하는 금액의 손실이 발생할 수 있습니다.
당사는 담보 및 보증제공으로 인한 우발부채와 소송으로 인한 우발부채가 존재합니다. 당사가 제공한 담보 및 보증과 관련하여 우발부채가 현실화되거나 당사가 소송에서 패소함에 따라 추가적인 대손충당 등이 발생할 경우 당사 재무에 부정적인 영향을 줄 수 있습니다. 투자 판단 시 당사의 담보 및 보증 제공과 관련한 우발부채 현황 및 소송의 현황을 확인하고 이로 인한 우발부채의 현실화 가능성에 주의하시기 바랍니다.
(주3) 정정 후
(전략)
증권신고서 제출일 현재 계류 중인 소송 사건에 대해서는 소송의 결과를 합리적으로 예측할 수 없으며, 당사가 피고로 진행 중인 사건과 관련해서 최종적으로 패소 시 청구액에 상당하는 금액의 손실이 발생할 수 있습니다.
또한 당사는 ESCO(Energy Service Company, 에너지절약전문기업)사업을 통해 경험한 소각플랜트 수행실적을 바탕으로 부산 소재의 산업용 폐기물 중간처분업체를 인수하여 정상화 작업을 위한 EPC(Engineering(설계), Procurement(조달), Construction(건설))사업을 진행하고 있습니다. 현재 부산권역에 산업용 폐기물 중간 처분 업체는 당사의 종속회사인 HLB에너지를 포함하여 2곳 밖에 존재하지 않은 상태입니다. 그러나 부산 산업단지 10여개 연차별 준공으로 인한 사업장 폐기물 증가가 예상되며, 매년 매립량은 감소하고 소각량은 증가하고 있는 추세입니다. 이에 당사의 종속회사인 HLB에너지는 기존 부산 사하구에 보유하고 있는 소각로 증설을 통해 일 48톤의 소각 용량을 90톤까지 증가시킴으로써 산업폐기물을 처리할 수 있는 가동률을 높여 매출 확대 및 수익성 개선을 계획하였습니다.
| [소각로 증설 계획] |
| 일정 | 내용 |
|---|---|
| 2023년 4월 12일 | 건축허가 완료 |
| 2023년 6월 | 실시설계 완료 |
| 2023년 7월 | 시공사 선정, 계약 |
| 2023년 12월 | 공사착공 |
| 2024년 12월 | 준공 및 시운전 |
| 출처: 당사 제공 자료 |
당사는 종속회사 HLB에너지가 현재 진행중인 부산 구평동 소각시설 증설사업 프로젝트 금융 자금 대출 420억원에 대해 2024년 05월 23일 채무보증 및 담보제공을 결정하였으며, 이는 타인에 대한 담보제공 결정 공시(2024.05.23)로 공시되었습니다. HLB에너지는 담보대출 중 환경부 환경정책자금 명목으로 하나은행으로부터의 200억원 및 하나은행 150억원, 하나캐피탈 70억원의 일반대출까지 총 420억원의 대출을 진행하였으며, 자세한 내용은 아래와 같습니다.
| [HLB에너지 소각로 증설 대출금액] |
|
구분
|
내용 | 차입처 | 금액(억원) | 금리(%) |
만기
|
비고 |
|---|---|---|---|---|---|---|
| 담보대출 | 환경정책자금 | 하나은행 |
200
|
2.44(변동) | 2033년09월30일 | 환경부 분기별 금리 고시 |
| 일반 | 하나은행 |
150
|
7.10(변동) | 최초 인출일 ~ 36개월 경과 |
- | |
| 하나캐피탈 | 70 | 7.10(고정) | - | |||
|
합계
|
- | - | 420 | - | - | - |
| 출처: 당사 제공 자료 |
대출에 대한 당사가 보유한 HLB에너지 보통주식 전부가 근질권 설정을 통해 담보제공되며, 본건 사업 관련 당사의 책임준공확약, 대출약정상 피담보채무에 대한 당사의 연대보증, 출자약정을 통한 자금보충약정을 제공합니다.
| [HLB에너지 대출 담보내역] |
| 구분 | 내용 | 담보설정액(억원) | 장부가액(억원) |
|---|---|---|---|
| HLB생명과학 보유 지분 |
HLB에너지 보통주식 2,302,099주 |
대출약정금액 420억원의 120% |
302억원 |
| 출처: 당사 제공 자료 |
당사는 담보 및 보증제공으로 인한 우발부채와 소송가능성 등으로 인한 우발부채가 상기와 같이 존재합니다. 당사가 제공한 담보 및 보증과 관련하여 우발부채가 현실화되거나 제기될 수 있는 소송에서 당사가 패소함에 따라 추가적인 대손충당 등이 발생할 경우 당사 재무에 부정적인 영향을 줄 수 있습니다. 투자 판단 시 당사의 담보 및 보증 제공과 관련한 우발부채 현황 및 소송의 현황을 확인하고 이로 인한 우발부채의 현실화 가능성에 주의하시기 바랍니다.
(주4) 정정 전
당사는 2024년 1분기말 기준 최대주주인 에이치엘비 주식회사의 주식 1,933,601주를 보유하고 있으며, 해당 보유분은 매분기 공정가치 평가를 통해 공정가치 측정 금융자산 평가손익 계정으로 금융수익 및 금융원가로 계상되고 있습니다. 매분기말일의 에이치엘비 보통주 종가를 기준으로 평가를 진행하며, 전분기 대비 주가가 상승 할 경우, 평가 이익으로 인식하고, 전분기 대비 주가가 하락 할 경우, 평가 손실로 인식하게 됩니다. 실제로, 당사는 에이치엘비 주식회사의 주가 상승으로 인해 2024년 1분기 당기손익-공정가치 측정 금융자산평가이익으로 19,848백만원을 금융수익으로 계상 하였습니다.
| [에이치엘비 최근 1개년 주가 추이] |
 |
|
에이치엘비 최근 1개년 주가 추이 |
| 출처: KRX/정보데이터시스템 |
에이치엘비 주식회사의 주식은 최근 1개년간 최저 27,565원, 최고 69,800원을 기록하였으며, 최근 리보세라닙(Rivoceranib)과 캄렐리주맙(Camrelizumab) 병용요법의 간암 1차 치료제의 FDA(미국 식품의약국) 판매승인을 통한 상용화를 앞두고 상대적으로 큰 변동성을 보였습니다. 따라서, 에이치엘비의 주가가 하락할 경우, 당사의 금융자산평가손실이 발생하여 당사의 당기순이익에 부정적인 영향을 미칠 수 있습니다. 투자자께서는 이 점 인지하시어 투자의사 결정하시기 바랍니다.
또한 리보세라닙(Rivoceranib)과 캄렐리주맙(Camrelizumab) 병용요법의 간암 1차 치료제의 FDA(미국 식품의약국) 판매승인을 통한 상용화를 앞두고 있는 상황에서 FDA 판매 승인 허가가 기존 예상되는 시점 대비 지연될 경우 당사 및 당사 관계회사의 수익성과 주가에 부정적으로 작용할 가능성이 있습니다. 리보세라닙과 캄렐리주맙 병용요법은 2019년부터 2022년까지 13개국 121개 병원에서 543명 시험대상자를 상대로 진행한 임상 3상 시험 결과, 전체 생존기간(mOS)은 22.1개월로 간암 1차 치료제들 중 최장 환자 생존기간을 기록했으며, 그 밖에 주요 지표에서는 무진행 생존기간(mPFS) 5.6개월, 객관적 반응률(ORR) 33.1%, 질병 조절률(DCR) 78.3% 등 우수한 결과치를 기록했습니다.
| [리보세라닙과 캄렐리주맙 임상 3상 결과] |
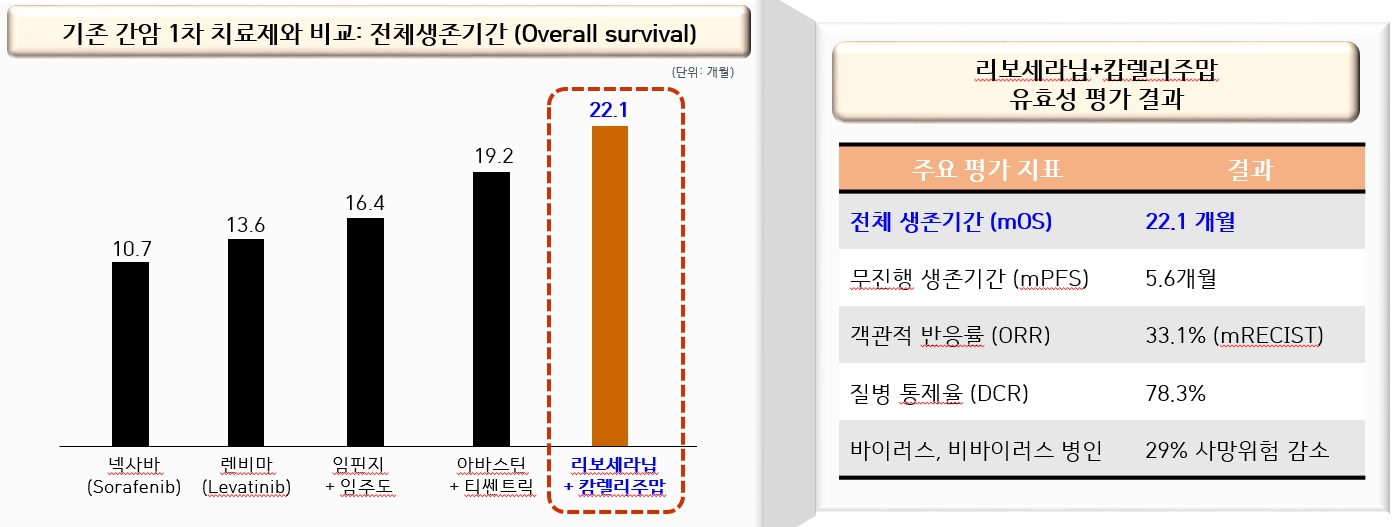 |
|
리보세라닙과 캄렐리주맙 유효성 평가 결과 |
| 출처: 당사 제공 자료(HLB IR 자료) |
이를 바탕으로 2023년 5월 NDA(신약 허가신청)를 신청하였으며, 7월 NDA 본심사가 개시되었습니다. 2023년 8월 리보세라닙 공장실사 및 12월 캄렐리주맙 공장실사까지 완료했으며, 2024년 5월 리보세라닙과 캄렐리주맙 병용요법 FDA 신약 허가 관련 결과를 기다리고 있는 상황입니다.
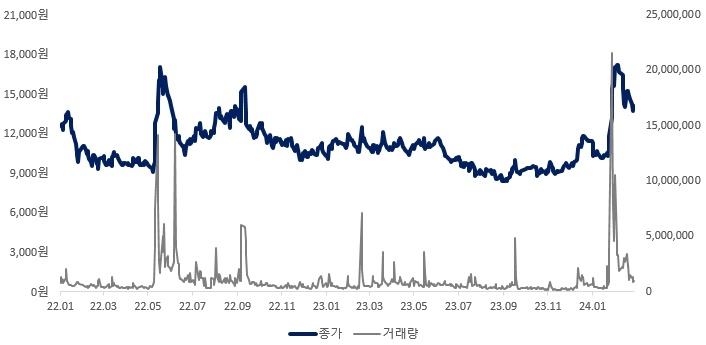
당사는 2018년 8월 14일에 리보세라닙 관련 부광약품(주)에 인정되는 계약상 지위, 권리 및 의무 일체를 취득하여 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있습니다. 이에 따라 에이치엘비의 리보세라닙 영향은 당사의 수익성과 주가에도 영향을 미치고 있습니다. 당사의 최근 2개년 주가 추이를 살펴보면, 2022년 5월 12일 에이치엘비는 리보세라닙과 캄렐리주맙을 병용한 간암 1차 치료제 관련 글로벌 임상 3상의 1차 유효성 지표가 모두 충족돼 통계적 유의성이 확보되었음을 발표했고, 이에 12일 9,868원이었던 당사의 주가는 13일 30% 오른 12,538원으로 마감했습니다. 또한 프랑스 파리 유럽암학회에서 임상 3상 최종 결과 발표가 열리기 하루 전인 2022년 9월 8일 주가는 전일 보다 17% 오른 15,159원으로 마감했습니다. 그리고 2024년 1월 에이치엘비의 리보세라닙과 캄렐리주맙 병용 간암 1차 치료제 관련 기업설명회 및 기사 등으로 이슈화 되면서 당사의 주가는 상승 기류를 보였습니다.
| [에이치엘비생명과학 최근 주가 추이] |
 |
|
에이치엘비생명과학 주가 변동 추이('22.01~'24.02) |
| 출처: KRX/정보데이터시스템 |
2022년 1월 3일부터 2024년 2월 29일까지 당사의 주가 최저는 8,380원, 최고는 17,200원을 기록하며, 상대적으로 큰 변동성을 보였습니다. 이는 최대주주인 에이치엘비의 리보세라닙과 캄렐리주맙 병용요법 간암 1차 치료제의 영향이 크며, FDA 판매승인을 통한 간암 대상 리보세라닙과 캄렐리주맙 병용요법의 상용화를 앞두고 있는 상황에서 FDA 판매 승인 허가가 기존 예상되는 시점 대비 지연될 경우 당사 및 당사 관계회사의 수익성과 주가에 부정적으로 작용할 가능성이 있으니 투자자께서는 이 점 유의하시기 바랍니다.
(주4) 정정 후
당사는 2024년 1분기말 기준 최대주주인 에이치엘비 주식회사의 주식 1,933,601주를 보유하고 있으며, 해당 보유분은 매분기 공정가치 평가를 통해 공정가치 측정 금융자산 평가손익 계정으로 금융수익 및 금융원가로 계상되고 있습니다. 매분기말일의 에이치엘비 보통주 종가를 기준으로 평가를 진행하며, 전분기 대비 주가가 상승 할 경우, 평가 이익으로 인식하고, 전분기 대비 주가가 하락 할 경우, 평가 손실로 인식하게 됩니다. 실제로, 당사는 에이치엘비 주식회사의 주가 상승으로 인해 2024년 1분기 당기손익-공정가치 측정 금융자산평가이익으로 19,848백만원을 금융수익으로 계상 하였습니다.
| [에이치엘비 최근 1개년 주가 추이] |
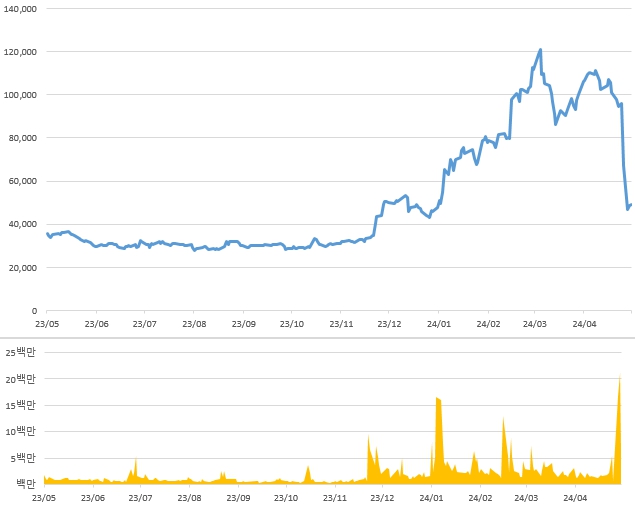 |
|
에이치엘비 최근 1개년 주가 추이 |
| 출처: KRX/정보데이터시스템 |
에이치엘비 주식회사의 주식은 최근 1개년간(2023년 05월 23일부터 2024년 5월 22일까지) 최저 28,050원, 최고 120,800원을 기록하였으며, 이는 리보세라닙(Rivoceranib)과 캄렐리주맙(Camrelizumab) 병용요법의 간암 1차 치료제의 FDA(미국 식품의약국) 결과를 앞두고 상대적으로 큰 변동성을 보였습니다. 따라서, 에이치엘비의 주가가 하락할 경우, 당사의 금융자산평가손실이 발생하여 당사의 당기순이익에 부정적인 영향을 미칠 수 있습니다. 투자자께서는 이 점 인지하시어 투자의사 결정하시기 바랍니다.
(삭제) 리보세라닙과 캄렐리주맙 병용요법은 2019년부터 2022년까지 13개국 121개 병원에서 543명 시험대상자를 상대로 진행한 임상 3상 시험 결과, 전체 생존기간(mOS)은 22.1개월로 간암 1차 치료제들 중 최장 환자 생존기간을 기록했으며, 그 밖에 주요 지표에서는 무진행 생존기간(mPFS) 5.6개월, 객관적 반응률(ORR) 33.1%, 질병 조절률(DCR) 78.3% 등 우수한 결과치를 기록했습니다.
| [리보세라닙과 캄렐리주맙 임상 3상 결과] |
 |
|
리보세라닙과 캄렐리주맙 유효성 평가 결과 |
| 출처: 당사 제공 자료(HLB IR 자료) |
이를 바탕으로 2023년 5월 NDA(신약 허가신청)를 신청하였으며, 7월 NDA 본심사가 개시되었습니다. 2023년 8월 리보세라닙 공장실사 및 12월 캄렐리주맙 공장실사까지 완료하였으나, 2024년 5월 미국 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL(보완요구서한, Complete Response Letter) 수령하였습니다. CRL 통한 요구 사항은 1) 병용투여 약물인 캄렐리주맙(항서제약)의 CMC(의약품 생산시설 실사) 진행 후 항서제약이 보완한 사항에 대해 일부 미비한 점에 대한 보완 2) 미국 FDA가 BIMO Inspection(임상사이트 실사)를 여행제한으로 인해 완료하지 못했다는 내용입니다. 계열회사 Elevar Therapeutics, Inc.는 상기 두가지 보완사항에 대해 항서제약과 긴밀히 협의하여 이에 대해 신속히 보완하고 FDA 재승인 신청할 예정이며, 재승인 신청 후 최장 6개월 이내 FDA는 승인여부를 결정하게 됩니다.
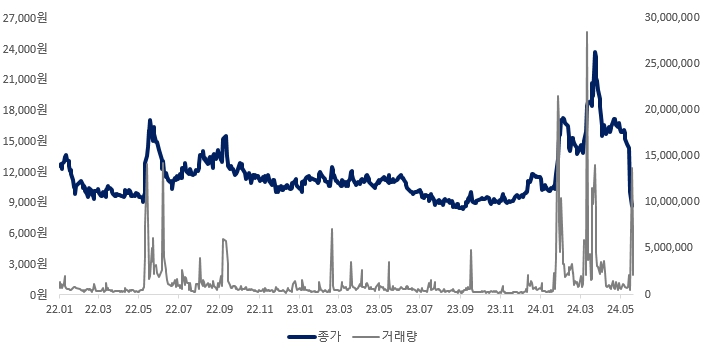
당사는 2018년 8월 14일에 리보세라닙 관련 부광약품(주)에 인정되는 계약상 지위, 권리 및 의무 일체를 취득하여 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있습니다. 이에 따라 에이치엘비의 리보세라닙 영향은 당사의 수익성과 주가에도 영향을 미치고 있습니다. 당사의 2022년 1월 3일부터 2024년 5월 22일까지의 주가 추이를 살펴보면, 2022년 5월 12일 에이치엘비는 리보세라닙과 캄렐리주맙을 병용한 간암 1차 치료제 관련 글로벌 임상 3상의 1차 유효성 지표가 모두 충족돼 통계적 유의성이 확보되었음을 발표했고, 이에 12일 9,868원이었던 당사의 주가는 13일 30% 오른 12,538원으로 마감했습니다. 또한 프랑스 파리 유럽암학회에서 임상 3상 최종 결과 발표가 열리기 하루 전인 2022년 9월 8일 주가는 전일 보다 17% 오른 15,159원으로 마감했습니다. 그리고 2024년 3월 25일 에이치엘비의 리보세라닙과 캄렐리주맙 병용 간암 1차 치료제 FDA 승인 기대로 인해 23,680원까지 오르며 최근 2개년 중 최고 주가를 기록했습니다. 하지만 2024년 5월 17일 에이치엘비가 FDA로부터 리보세라닙과 캄렐리주맙을 병용한 간암 1차 치료제 CRL을 수령하자, 당사의 주가는 전일 대비 29.98% 감소한 8,630원을 기록했습니다.
| [에이치엘비생명과학 최근 주가 추이] |
 |
|
에이치엘비생명과학 주가 변동 추이('22.01~'24.05) |
| 출처: KRX/정보데이터시스템 |
2022년 1월 3일부터 2024년 5월 22일까지 당사의 주가는 최저 8,380원, 최고 23,680원을 기록하며, 큰 변동성을 보였습니다. 이는 최대주주인 에이치엘비의 리보세라닙과 캄렐리주맙 병용요법 간암 1차 치료제의 영향이 큰 상황에서 2024년 5월 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL을 수령하였습니다. 이와 관련하여 항서제약의 CMC(의약품 생산시설 실사) 보완 및 BIMO Inspection(임상사이트 실사) 완료 시기에 대한 불확실성이 있습니다. 또한 당사는 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있어 FDA 재승인 신청 후 판매승인 시점이 지연될 경우 당사 및 당사 관계회사의 수익성과 주가에도 부정적으로 작용할 가능성이 있으니 투자자께서는 유의하시기 바랍니다.
(주5) 정정 전
본 공시서류에 기재된 재무제표에 관한 사항과 감사인의 의견에 관한 사항은 2023년 12월 31일 재무제표 작성기준일 이후의 변동을 반영하지 않았으므로 투자에 유의하시기 바랍니다.
다만, 본 공시서류에 기재된 재무제표의 작성기준일 이후 본 공시서류 제출일 사이에 발생한 것으로 본 공시서류에 기재된 사항 이외에 자산, 부채, 현금흐름 또는 손익사항에 중대한 변동을 가져오거나 중요한 영향을 미치는 사항은 없습니다.
(후략)
(주5) 정정 전
본 공시서류에 기재된 재무제표에 관한 사항과 감사인의 의견에 관한 사항은 2024년 1분기 재무제표 작성기준일 이후의 변동을 반영하지 않았으므로 투자에 유의하시기 바랍니다.
다만, 본 공시서류에 기재된 재무제표의 작성기준일 이후 본 공시서류 제출일 사이에 발생한 것으로 본 공시서류에 기재된 사항 이외에 자산, 부채, 현금흐름 또는 손익사항에 중대한 변동을 가져오거나 중요한 영향을 미치는 사항은 없습니다.
(후략)
(주6) 정정 전
(전략)
3. 기업실사 일정 및 주요 내용
| 일자 | 실사내용 |
| 2024.02.06 ~ 2024.02.23 |
* 발행회사 초도 방문 - 발행회사의 유상증자 의사 확인 - 자금조달 희망금액 등 발행회사 의견 청취 * 발행회사의 유상증자 방식결정 협의 * 유상증자 일정 협의 및 확정 * 유상증자를 위한 사전 준비사항 및 진행절차 설명 - 발행가 산정 및 세부일정 설명 * 세부 증자관련 논의 - 유상증자 방식 결정 및 대주주 증자 참여 논의 * 유상증자 진행에 대한 질의/응답 * 실사 사전요청자료 송부 |
| 2024.02.24 ~ 2024.03.08 |
* 증자리스크 검토 - 발행시장 상황, 자금조달규모 적정성, 공모가액 희망 할인율 * 발행사와의 협의 - 발행가액 산정방식, 발행일정, 발행규모, 인수수수료 협의 * 기업실사 진행 및 추가자료 요청 - 기업실사 관련 자료요청 및 절차에 대한 설명 - 기업실사 관련 Q&A * 이사회 등 상법 절차 및 정관 등 검토 * 투자위험요소 실사 1) 사업위험관련 실사 - 기존사업 및 신규사업에 대한 세부사항 등 체크 2) 회사위험관련 실사 - 재무관련 위험 및 우발채무 등의 위험요소 등 체크 3) 기타위험관련 실사 - 주가 희석화관련 위험 등 체크 * 담당자 인터뷰 - 회사개요, 사업의 내용, 주요 재무적 이슈 확인 - 자금사용 계획 파악 - 향후 사업추진계획 및 발행회사의 비전 검토 |
| 2024.03.09 ~ 2024.03.21 |
* 증권신고서 작성 및 조언 * 이사회의사록 등 검토 * 인수계약서 작성 및 체결 * 증권신고서 인수인의 의견 완료 * 첨부서류 등 검토 * 증권신고서 업데이트 |
| 2024.03.22 ~ 2024.05.13 |
* 금융감독원의 정정요구제출에 따른 증권신고서 작성 가이드 및 추가자료 작성 |
4. 기업실사 참여자
| [대표주관회사] |
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 | 참여기간 | 주요 경력 |
| 한국투자증권(주) | IB2본부 | 김성열 | 본부장 | 기업실사 총괄 | 2024년 02월 06일 ~ 2024년 05월 13일 |
기업금융업무 등 28년 |
| ECM1부 | 김현서 | 이사 | 기업실사 책임 | 2024년 02월 06일 ~ 2024년 05월 13일 |
기업금융업무 등 22년 | |
| ECM1부 | 박상욱 | 팀장 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 13일 |
기업금융업무 등 14년 | |
| ECM1부 | 정인묵 | 과장 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 13일 |
기업금융업무 등 7년 | |
| ECM1부 | 임주형 | 대리 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 13일 |
기업금융업무 등 4년 | |
| ECM1부 | 구찬웅 | 주임 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 13일 |
기업금융업무 등 1년 | |
| 케이비증권(주) | SME금융부 | 이경재 | 이사 | 기업실사 총괄 | 2024년 02월 06일 ~ 2024년 05월 13일 |
기업금융업무 등 24년 |
| SME금융부 | 김자환 | 이사 | 기업실사 책임 | 2024년 02월 06일 ~ 2024년 05월 13일 |
기업금융업무 등 23년 | |
| SME금융부 | 이형준 | 팀장 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 13일 |
기업금융업무 등 9년 | |
| SME금융부 | 박진혁 | 대리 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 13일 |
기업금융업무 등 6년 | |
| SME금융부 | 박성윤 | 주임 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 13일 |
기업금융업무 등 2년 |
| [발행회사] |
| 소속 | 부서 | 성명 | 직급 | 담당업무 |
| 에이치엘비생명과학(주) | 경영전략본부 | 이근식 | 상무이사 | 발행업무 총괄 |
| 경영기획팀 | 안동환 | 과장 | 발행업무 |
5. 기업실사 세부 항목 및 점검 결과
- 동 증권신고서에 첨부되어 있는 기업실사 보고서를 참조해 주시기 바랍니다.
6. 종합의견
가. 공동대표주관회사인 한국투자증권(주) 및 케이비증권(주)는 에이치엘비생명과확(주)가 2024년 03월 21일 이사회에서 결의한 보통주식 11,005,125주에 대한 주주배정 후 실권주 일반공모 증자를 잔액인수함에 있어 에이치엘비생명과학(주)에 대하여 다음과 같이 평가합니다.
| 긍정적요인 | ▶ 전 세계 글로벌 체외 진단(IVD) 시장은 2021년 982억 달러에서 연평균 성장률 2.9%로 증가하여, 2026년에는 1,131억 달러에 이를 것으로 전망됩니다. COVID-19로 인해 글로벌 체외 진단 시장은 급격하게 성장하였으며, 기존 또는 신규 감염 질병 진단을 위한 차세대 체외 진단의 R&D 확장으로 앞으로도 성장 추세는 꾸준히 이어질 것으로 예상됩니다. 동사는 150여 종의 제품개발 성과의 근간인 기술력과 품질 시스템을 바탕으로 의료기기 분야를 비롯한 다양한 품목군을 개발, 연구 중에 있으며 전사적 품질 경영 시스템 운영을 통해 안정성, 유효성 및 GMP, ISO13485 기준의 품질이 확보된 제품을 생산하고 있습니다. 이에 따라 높은 수익률을 달성할 가능성이 있습니다. ▶ 세계 의약품 시장은 고령화에 따른 만성 질환자 수의 증가, 소득 수준 향상에 따라 의약품 시장의 성장이 급격하게 이루어지고 있는 중국, 인도, 중남미 등의 제약 신흥 국가들의 의료비 지출증가 등으로 시장 규모는 역대 최대치를 경신했습니다. 동사의 종속회사 HLB셀은 바이오의약품 및 생체적합성 의료기기 개발 기술을 중심으로 ①바이오인공간 ②지혈제 ③인체세포외기질 3개 분야의 주요 파이프라인을 갖고 있으며, 관련 특허 등을 활용하여 연구, 개발 중에 있습니다. 또한 동사의 계열회사 Elevar Therapeutics,Inc.의 Rivoceranib(구. Apatinib Mesylate)는 위암(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국), 간암 (2021년 11월 미국식품의약국), 선양낭성암 (2021년 2월 미국식품의약국) 대상으로 희귀의약품 지정을 받아 임상종료 후 시판허가에 대한 심사의 신속화, 수수료 감면 등의 혜택과 최소 8년(2029년)에서 최대 13년(2034년) 동안 독점 판매할 수 있습니다. 동사의 계열회사 HLB생명과학R&D는 2022년 4월 1일 신약개발 전문성 강화를 위해 설립되었습니다.현재, 항암 파이프라인 신규 구축을 위해 초기 비임상 단계 물질을 도입(G2M Project)하였으며 한국을 포함한 글로벌 주요 국가에 대한 특허권과 물질의 생산, 판매 그리고 향후 기술이전에 대한 권리 등의 일체의 권리를 확보했습니다. ▶ 2022년 전체 의약품 유통금액은 88.9조원으로 전년대비 10.2%(8.2조원)증가하였으며, 최근 3년간 연평균 7.8%증가('20년 약 75.9조원, '21년 약 80.6조원, '22년 약 88.9조원)한 것으로 나타났습니다. 2022년 의약품 유통금액 88.9조원은 중 49.2조원('21년도 42조)은 도매상 유통금액으로 전체 시장의 55.3%를 차지하고 있습니다. 동사의 종속회사 신화어드밴스는 무차입경영의 우수한 재무상태와 풍부한 유동성을 보유하고 있으며, 20여년 이상 수행하며 다져진 영업력을 바탕으로 신규거래처를 꾸준히 확보하였습니다. 자사 영업 조직과 물류센터를 통한 안정적 매출과 함께 제약업체 및 도매업체와의 전략적 제휴로 품목 및 가격 경쟁력에 우위를 선점하였습니다. 향후 지역 인구 및 소득, 물류 효율성, 주변 상권 및 원외 시장 분석 등의 데이터를 활용하여 표적시장 선정을 통해 안정적인 성장을 이룰 것입니다. |
| 부정적요인 | ▶ 연구개발을 통한 신약 개발은 일반적으로 막대한 연구개발비와 장기에 걸친 투자 및 연구기간이 소요되며, 신약 개발에 성공한다 하더라도 기투자된 금액과 시간을 상쇄할 수 있을 정도의 수익 창출이 가능할지 여부는 불확실합니다. ▶ 동사는 최근 4개년 영업손실 및 당기순손실 구조가 지속 되고 있습니다. 2020년 약 558억원, 2021년 약 493억원, 2022년 약 544억원, 2023년 약 59억원의 당기순손실을 기록했습니다.향후 경쟁 심화로 인한 의약품 유통 사업 매출 감소, 바이오 사업 임상시험 지연 및 비용 증가 등으로 인해 당사의 수익은 더욱 악화될 수 있습니다. ▶ 동사의 주요 재무안정성 지표 추이를 살펴보면, 연결기준 부채비율은 2020년말 13.7%, 2021년말 9.8%, 2022년말 74.4% 2023년말 83.2% 로 계속해서 증가하였습니다. 향후에도 계속되는 영업실적의 부진, 임상 지연 등으로 인한 바이오 사업 매출 미실현 등에 따른 투자 등에 따라 차입금이 증가할 가능성이 존재하며, 지속적으로 차입을 할 경우 당사의 재무안정성이 악화될 가능성이 존재합니다. ▶ 동사는 2020년을 제외하고 최근 지속적으로 영업활동현금유출이 발생하고 있습니다. 2020년 약 2,010백만원으로 영업활동현금유입이 발생하였으나, 2021년 약 14,084백만원, 2022년 약 29,744백만원, 2023년 약 10,016백만원의 영업활동현금유출을 기록했습니다. 동사의 영업활동현금흐름 유출의 주된 원인은 실적부진이며 영업활동현금흐름과 투자활동현금흐름의 유출을 재무활동(외부차입 등)을 통하여 충당하고 있습니다. 그러나 바이오사업 매출 실현 지연으로 인한 영업활동현금 유출 지속 및 국내 경기의 악화, 금융시장의 부진 등으로 재무활동현금 유입이 원활하지 못할 경우 당사는 유동성 압박에 시달릴 수 있습니다. ▶ 동사는 현재 신규사업 진출을 위한 타법인 인수로 재무구조가 크게 변동하고 있으며 이에 따라 재무안정성 지표 또한 같이 변동하고 있습니다. 이처럼 동사의 영업상황과 더불어 신규사업 진출을 위한 투자가 지속될 경우 재무안정성이 악화될 수 있습니다. ▶동사는 최대주주인 에이치비엘비(주)의 주가의 영향을 많이 받고 있습니다.에이치엘비(주) 리보세라닙(Rivoceranib)과 캄렐리주맙(Camrelizumab) 병용요법 간암 1차 치료제의 FDA(미국 식품의약국) 판매승인을 통한 상용화를 앞두고 있는 상황입니다. 동사는 2018년 8월 14일에 리보세라닙 관련 부광약품(주)에 인정되는 계약상 지위, 권리 및 의무 일체를 취득하여 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있습니다. 이에 따라 에이치엘비의 리보세라닙 영향은 동사의 수익성과 주가에도 영향을 미치고 있습니다. FDA 판매 승인 허가가 기존 예상되는 시점 대비 지연될 경우 동사 및 동사 관계회사의 수익성과 주가에 부정적으로 작용할 가능성이 있습니다. |
| 자금조달의 필요성 |
▶ 동사는 금번 유상증자를 통해 조달하는 자금을 시설자금, 운영자금, 채무상환자금 및 기타자금으로 활용할 계획입니다. ▶ 금번 유상증자를 통해 조달한 자금의 세부사용 내역은 "Ⅴ. 자금의 사용목적"을 참고하시기 바랍니다. |
(후략)
(주6) 정정 후
(전략)
3. 기업실사 일정 및 주요 내용
| 일자 | 실사내용 |
| 2024.02.06 ~ 2024.02.23 |
* 발행회사 초도 방문 - 발행회사의 유상증자 의사 확인 - 자금조달 희망금액 등 발행회사 의견 청취 * 발행회사의 유상증자 방식결정 협의 * 유상증자 일정 협의 및 확정 * 유상증자를 위한 사전 준비사항 및 진행절차 설명 - 발행가 산정 및 세부일정 설명 * 세부 증자관련 논의 - 유상증자 방식 결정 및 대주주 증자 참여 논의 * 유상증자 진행에 대한 질의/응답 * 실사 사전요청자료 송부 |
| 2024.02.24 ~ 2024.03.08 |
* 증자리스크 검토 - 발행시장 상황, 자금조달규모 적정성, 공모가액 희망 할인율 * 발행사와의 협의 - 발행가액 산정방식, 발행일정, 발행규모, 인수수수료 협의 * 기업실사 진행 및 추가자료 요청 - 기업실사 관련 자료요청 및 절차에 대한 설명 - 기업실사 관련 Q&A * 이사회 등 상법 절차 및 정관 등 검토 * 투자위험요소 실사 1) 사업위험관련 실사 - 기존사업 및 신규사업에 대한 세부사항 등 체크 2) 회사위험관련 실사 - 재무관련 위험 및 우발채무 등의 위험요소 등 체크 3) 기타위험관련 실사 - 주가 희석화관련 위험 등 체크 * 담당자 인터뷰 - 회사개요, 사업의 내용, 주요 재무적 이슈 확인 - 자금사용 계획 파악 - 향후 사업추진계획 및 발행회사의 비전 검토 |
| 2024.03.09 ~ 2024.03.21 |
* 증권신고서 작성 및 조언 * 이사회의사록 등 검토 * 인수계약서 작성 및 체결 * 증권신고서 인수인의 의견 완료 * 첨부서류 등 검토 * 증권신고서 업데이트 |
| 2024.03.22 ~ 2024.05.23 |
* 금융감독원의 정정요구제출에 따른 증권신고서 작성 가이드 및 추가자료 작성 |
4. 기업실사 참여자
| [대표주관회사] |
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 | 참여기간 | 주요 경력 |
| 한국투자증권(주) | IB2본부 | 김성열 | 본부장 | 기업실사 총괄 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 28년 |
| ECM1부 | 김현서 | 이사 | 기업실사 책임 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 22년 | |
| ECM1부 | 박상욱 | 팀장 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 14년 | |
| ECM1부 | 정인묵 | 과장 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 7년 | |
| ECM1부 | 임주형 | 대리 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 4년 | |
| ECM1부 | 구찬웅 | 주임 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 1년 | |
| 케이비증권(주) | SME금융부 | 이경재 | 이사 | 기업실사 총괄 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 24년 |
| SME금융부 | 김자환 | 이사 | 기업실사 책임 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 23년 | |
| SME금융부 | 이형준 | 팀장 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 9년 | |
| SME금융부 | 박진혁 | 대리 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 6년 | |
| SME금융부 | 박성윤 | 주임 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 2년 |
| [발행회사] |
| 소속 | 부서 | 성명 | 직급 | 담당업무 |
| 에이치엘비생명과학(주) | 경영전략본부 | 이근식 | 상무이사 | 발행업무 총괄 |
| 경영기획팀 | 안동환 | 과장 | 발행업무 |
5. 기업실사 세부 항목 및 점검 결과
- 동 증권신고서에 첨부되어 있는 기업실사 보고서를 참조해 주시기 바랍니다.
6. 종합의견
가. 공동대표주관회사인 한국투자증권(주) 및 케이비증권(주)는 에이치엘비생명과확(주)가 2024년 03월 21일 이사회에서 결의한 보통주식 11,005,125주에 대한 주주배정 후 실권주 일반공모 증자를 잔액인수함에 있어 에이치엘비생명과학(주)에 대하여 다음과 같이 평가합니다.
| 긍정적요인 | ▶ 전 세계 글로벌 체외 진단(IVD) 시장은 2021년 982억 달러에서 연평균 성장률 2.9%로 증가하여, 2026년에는 1,131억 달러에 이를 것으로 전망됩니다. COVID-19로 인해 글로벌 체외 진단 시장은 급격하게 성장하였으며, 기존 또는 신규 감염 질병 진단을 위한 차세대 체외 진단의 R&D 확장으로 앞으로도 성장 추세는 꾸준히 이어질 것으로 예상됩니다. 동사는 150여 종의 제품개발 성과의 근간인 기술력과 품질 시스템을 바탕으로 의료기기 분야를 비롯한 다양한 품목군을 개발, 연구 중에 있으며 전사적 품질 경영 시스템 운영을 통해 안정성, 유효성 및 GMP, ISO13485 기준의 품질이 확보된 제품을 생산하고 있습니다. 이에 따라 높은 수익률을 달성할 가능성이 있습니다. ▶ 세계 의약품 시장은 고령화에 따른 만성 질환자 수의 증가, 소득 수준 향상에 따라 의약품 시장의 성장이 급격하게 이루어지고 있는 중국, 인도, 중남미 등의 제약 신흥 국가들의 의료비 지출증가 등으로 시장 규모는 역대 최대치를 경신했습니다. 동사의 종속회사 HLB셀은 바이오의약품 및 생체적합성 의료기기 개발 기술을 중심으로 ①바이오인공간 ②지혈제 ③인체세포외기질 3개 분야의 주요 파이프라인을 갖고 있으며, 관련 특허 등을 활용하여 연구, 개발 중에 있습니다. 또한 동사의 계열회사 Elevar Therapeutics,Inc.의 Rivoceranib(구. Apatinib Mesylate)는 위암(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국), 간암 (2021년 11월 미국식품의약국), 선양낭성암 (2021년 2월 미국식품의약국) 대상으로 희귀의약품 지정을 받아 임상종료 후 시판허가에 대한 심사의 신속화, 수수료 감면 등의 혜택과 최소 8년(2029년)에서 최대 13년(2034년) 동안 독점 판매할 수 있습니다. 동사의 계열회사 HLB생명과학R&D는 2022년 4월 1일 신약개발 전문성 강화를 위해 설립되었습니다.현재, 항암 파이프라인 신규 구축을 위해 초기 비임상 단계 물질을 도입(G2M Project)하였으며 한국을 포함한 글로벌 주요 국가에 대한 특허권과 물질의 생산, 판매 그리고 향후 기술이전에 대한 권리 등의 일체의 권리를 확보했습니다. ▶ 2022년 전체 의약품 유통금액은 88.9조원으로 전년대비 10.2%(8.2조원)증가하였으며, 최근 3년간 연평균 7.8%증가('20년 약 75.9조원, '21년 약 80.6조원, '22년 약 88.9조원)한 것으로 나타났습니다. 2022년 의약품 유통금액 88.9조원은 중 49.2조원('21년도 42조)은 도매상 유통금액으로 전체 시장의 55.3%를 차지하고 있습니다. 동사의 종속회사 신화어드밴스는 무차입경영의 우수한 재무상태와 풍부한 유동성을 보유하고 있으며, 20여년 이상 수행하며 다져진 영업력을 바탕으로 신규거래처를 꾸준히 확보하였습니다. 자사 영업 조직과 물류센터를 통한 안정적 매출과 함께 제약업체 및 도매업체와의 전략적 제휴로 품목 및 가격 경쟁력에 우위를 선점하였습니다. 향후 지역 인구 및 소득, 물류 효율성, 주변 상권 및 원외 시장 분석 등의 데이터를 활용하여 표적시장 선정을 통해 안정적인 성장을 이룰 것입니다. |
| 부정적요인 | ▶ 연구개발을 통한 신약 개발은 일반적으로 막대한 연구개발비와 장기에 걸친 투자 및 연구기간이 소요되며, 신약 개발에 성공한다 하더라도 기투자된 금액과 시간을 상쇄할 수 있을 정도의 수익 창출이 가능할지 여부는 불확실합니다. ▶ 동사는 최근 4개년 영업손실 및 당기순손실 구조가 지속 되고 있습니다. 2020년 약 558억원, 2021년 약 493억원, 2022년 약 544억원, 2023년 약 59억원의 당기순손실을 기록했습니다.향후 경쟁 심화로 인한 의약품 유통 사업 매출 감소, 바이오 사업 임상시험 지연 및 비용 증가 등으로 인해 당사의 수익은 더욱 악화될 수 있습니다. ▶ 동사의 주요 재무안정성 지표 추이를 살펴보면, 연결기준 부채비율은 2020년말 13.7%, 2021년말 9.8%, 2022년말 74.4% 2023년말 83.2% 로 계속해서 증가하였습니다. 향후에도 계속되는 영업실적의 부진, 임상 지연 등으로 인한 바이오 사업 매출 미실현 등에 따른 투자 등에 따라 차입금이 증가할 가능성이 존재하며, 지속적으로 차입을 할 경우 당사의 재무안정성이 악화될 가능성이 존재합니다. ▶ 동사는 2020년을 제외하고 최근 지속적으로 영업활동현금유출이 발생하고 있습니다. 2020년 약 2,010백만원으로 영업활동현금유입이 발생하였으나, 2021년 약 14,084백만원, 2022년 약 29,744백만원, 2023년 약 10,016백만원의 영업활동현금유출을 기록했습니다. 동사의 영업활동현금흐름 유출의 주된 원인은 실적부진이며 영업활동현금흐름과 투자활동현금흐름의 유출을 재무활동(외부차입 등)을 통하여 충당하고 있습니다. 그러나 바이오사업 매출 실현 지연으로 인한 영업활동현금 유출 지속 및 국내 경기의 악화, 금융시장의 부진 등으로 재무활동현금 유입이 원활하지 못할 경우 당사는 유동성 압박에 시달릴 수 있습니다. ▶ 동사는 현재 신규사업 진출을 위한 타법인 인수로 재무구조가 크게 변동하고 있으며 이에 따라 재무안정성 지표 또한 같이 변동하고 있습니다. 이처럼 동사의 영업상황과 더불어 신규사업 진출을 위한 투자가 지속될 경우 재무안정성이 악화될 수 있습니다. ▶동사는 최대주주인 에이치비엘비(주)의 주가의 영향을 많이 받고 있습니다.에이치엘비 주가에는 리보세라닙과 캄렐리주맙 병용요법 간암 1차 치료제가 미치는 영향이 큰 상황에서 2024년 5월 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL을 수령하였습니다. 이와 관련하여 항서제약의 CMC(의약품 생산시설 실사) 보완 및 BIMO Inspection(임상사이트 실사) 완료 시기에 대한 불확실성이 있습니다. 또한 동사는 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있어 FDA 재승인 신청 후 판매승인 시점이 지연될 경우 동사 및 동사 관계회사의 수익성과 주가에도 부정적으로 작용할 가능성이 있습니다. |
| 자금조달의 필요성 |
▶ 동사는 금번 유상증자를 통해 조달하는 자금을 시설자금, 운영자금, 채무상환자금 및 기타자금으로 활용할 계획입니다. ▶ 금번 유상증자를 통해 조달한 자금의 세부사용 내역은 "Ⅴ. 자금의 사용목적"을 참고하시기 바랍니다. |
(후략)
(주7) 정정 전
(전략)
※ 파이프라인 개발현황
현재 당사 및 종속기업이 보유한 파이프라인 연구개발 진행 중인 연구개발(Elevar Therapeutics, Inc.주도 글로벌 임상 포함) 현황은 다음과 같습니다.
 |
|
파이프라인 개발현황 |
|
품 목 |
적응증 |
임상시작일 |
현재 진행단계 |
||
|---|---|---|---|---|---|
|
단계(국가) |
승인일 |
비 고 | |||
| 리보세라닙 (Rivoceranib) [Elevar Therapeutics, Inc.주도 글로벌 임상 포함] |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안정성평가 완료 |
|
위암 (3차/4차 단일요법) |
2017년 |
임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
|
|
위암 (1차 병용요법) |
2021년 |
임상2상 |
2021년 09월 (임상2상 승인일) |
임상 진행 중 | |
|
간암 (1차 병용요법) |
2019년 |
임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
임상 종료 22년 9월 초록 발표 (1차 평가 지표 만족) 23년 5월 미국 FDA에 NDA Submission 완료 |
|
|
선양낭성암종 (1/2차 단일요법) |
2020년 |
임상2상 |
2020년 4월 (임상2상 개시일) |
임상 2상 종료 6월 초록 발표 |
|
|
위암 (2차 병용요법) |
2018년 |
임상2상 |
2018년 10월 (임상1상 개시일) |
임상 종료 22년 결과 발표 |
|
|
대장암 (3차 병용요법) |
2019년 |
임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 종료 |
|
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상 진행 중 (농림축산검역본부) |
|
| 파이로티닙 (Pyrotinib) |
전이성 유방암 | 2023년 | 임상3상 (한국) |
2023년 03월 (임상계획 승인) |
임상3상 진행 중 |
| 비소세포폐암 | 2020년 | 임상3상 (전세계 13개국) |
2020년 (임상계획 승인) |
임상3상 진행 중 | |
|
HLS221-N01 G2M 억제제 |
폐암 유방암 대장암 췌장암 |
- |
비임상시험 단계 |
- |
비임상평가 진행 중 |
|
HLS222-N01 Cannabinoids derivatives |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
|
HLS232-N01 CDK 억제제 |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
|
HLS231-G01 의료용 대마 |
뇌전증 | - | 탐색 단계 | - | 제형 연구 중 |
| 출처: 당사 제공 자료 |
(후략)
(주7) 정정 후
(전략)
※ 파이프라인 개발현황
현재 당사 및 종속기업이 보유한 파이프라인 연구개발 진행 중인 연구개발(Elevar Therapeutics, Inc.주도 글로벌 임상 포함) 현황은 다음과 같습니다.
 |
|
파이프라인 개발현황 |
|
품 목 |
적응증 |
임상시작일 |
현재 진행단계 |
||
|---|---|---|---|---|---|
|
단계(국가) |
승인일 |
비 고 | |||
| 리보세라닙 (Rivoceranib) [Elevar Therapeutics, Inc.주도 글로벌 임상 포함] |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안정성평가 완료 |
|
위암 (3차/4차 단일요법) |
2017년 |
임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
|
|
위암 (1차 병용요법) |
2021년 |
임상2상 |
2021년 09월 (임상2상 승인일) |
임상 진행 중 | |
|
간암 (1차 병용요법) |
2019년 |
임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
- 임상 종료, 22년 9월 초록 발표(1차 평가 지표 만족) - 23년 5월 미국 FDA에 NDA Submission 완료 - 24년 5월 미국 FDA 수정 보완 요구(CRL 수령) |
|
|
선양낭성암종 (1/2차 단일요법) |
2020년 |
임상2상 |
2020년 4월 (임상2상 개시일) |
임상 2상 종료 6월 초록 발표 |
|
|
위암 (2차 병용요법) |
2018년 |
임상2상 |
2018년 10월 (임상1상 개시일) |
임상 종료 22년 결과 발표 |
|
|
대장암 (3차 병용요법) |
2019년 |
임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 종료 |
|
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상 진행 중 (농림축산검역본부) |
|
| 파이로티닙 (Pyrotinib) |
전이성 유방암 | 2023년 | 임상3상 (한국) |
2023년 03월 (임상계획 승인) |
임상3상 진행 중 |
| 비소세포폐암 | 2020년 | 임상3상 (전세계 13개국) |
2020년 (임상계획 승인) |
임상3상 진행 중 | |
|
HLS221-N01 G2M 억제제 |
폐암 유방암 대장암 췌장암 |
- |
비임상시험 단계 |
- |
비임상평가 진행 중 |
|
HLS222-N01 Cannabinoids derivatives |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
|
HLS232-N01 CDK 억제제 |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
|
HLS231-G01 의료용 대마 |
뇌전증 | - | 탐색 단계 | - | 제형 연구 중 |
| 출처: 당사 제공 자료 |
(후략)
(주8) 정정 전
(전략)
또한, 당사 및 종속회사 HLB생명과학R&D는 현재 자체적으로 표적항암제 리보세라닙(Rivoceranib), 파이로티닙(Pyrotinib) 및 G2M Project 3개의 항암신약 물질에 대한 국내 전용실시권을 보유하고 있으며, 이외 다수의 관계회사에서 바이오 사업을 진행하고 있습니다.
당사의 종속회사 HLB셀은 바이오인공간, 지혈제, 인간 세포외기질 분야에서 파이프라인을 구축하고 있습니다.
계열회사 Elevar therapeutics는 리보세라닙의 글로벌 간암 임상 3상을 완료하여 미국 식품의약국(FDA)에 NDA 신청을 완료하였습니다.
각 사업부문별 주요 제품과 매출비중은 다음과 같습니다.
[부문별 주요제품]
| 사업부문 | 주요제품 | 2024년 당분기 매출비중 |
| 메디케어사업 | 체외진단의료기기 및 기타 의료용기기 제조,판매업 | 16.89% |
| 의료기기사업 | 일회용 주사기 제조,판매업 | 8.42% |
| 의약품유통사업 | 의약품도매업 및 기타 판매업 | 70.51% |
| 에너지사업 | 신재생에너지 시설 건설업 | 4.18% |
| 합 계 | 100.00% | |
기타 자세한 사항은 동 보고서의「II. 사업의 내용」을 참조하시기 바랍니다.
(후략)
(주8) 정정 후
(전략)
또한, 당사 및 종속회사 HLB생명과학R&D는 현재 자체적으로 표적항암제 리보세라닙(Rivoceranib), 파이로티닙(Pyrotinib) 및 G2M Project 3개의 항암신약 물질에 대한 국내 전용실시권을 보유하고 있으며, 이외 다수의 관계회사에서 바이오 사업을 진행하고 있습니다.
당사의 종속회사 HLB셀은 바이오인공간, 지혈제, 인간 세포외기질 분야에서 파이프라인을 구축하고 있습니다.
계열회사 Elevar therapeutics는 리보세라닙의 글로벌 간암 임상 3상을 완료하여 미국 식품의약국(FDA)에 NDA 신청을 완료하였으며, 2024년 5월 FDA로부터 보완요구서한(CRL)을 수령하였습니다.
각 사업부문별 주요 제품과 매출비중은 다음과 같습니다.
[부문별 주요제품]
| 사업부문 | 주요제품 | 2024년 당분기 매출비중 |
| 메디케어사업 | 체외진단의료기기 및 기타 의료용기기 제조,판매업 | 16.89% |
| 의료기기사업 | 일회용 주사기 제조,판매업 | 8.42% |
| 의약품유통사업 | 의약품도매업 및 기타 판매업 | 70.51% |
| 에너지사업 | 신재생에너지 시설 건설업 | 4.18% |
| 합 계 | 100.00% | |
기타 자세한 사항은 동 보고서의「II. 사업의 내용」을 참조하시기 바랍니다.
(후략)
(주9) 정정 전
(전략)
나. 바이오사업부문
당사 및 종속회사 HLB생명과학R&D는 현재 자체적으로 표적항암제 리보세라닙(Rivoceranib), 파이로티닙(Pyrotinib) 및 G2M Project 3개의 항암신약 물질에 대한 국내 전용실시권을 보유하고 있으며, 이외 다수의 관계회사에서 바이오 사업을 진행하고 있습니다.
당사의 종속회사 HLB셀은 바이오인공간, 지혈제, 인간 세포외기질 분야에서 파이프라인을 구축하고 있습니다.
계열회사 Elevar therapeutics는 리보세라닙의 글로벌 간암 임상 3상을 완료하여 미국식품의약국(FDA)에 NDA 신청을 완료하였습니다.
(후략)
(주9) 정정 후
(전략)
나. 바이오사업부문
당사 및 종속회사 HLB생명과학R&D는 현재 자체적으로 표적항암제 리보세라닙(Rivoceranib), 파이로티닙(Pyrotinib) 및 G2M Project 3개의 항암신약 물질에 대한 국내 전용실시권을 보유하고 있으며, 이외 다수의 관계회사에서 바이오 사업을 진행하고 있습니다.
당사의 종속회사 HLB셀은 바이오인공간, 지혈제, 인간 세포외기질 분야에서 파이프라인을 구축하고 있습니다.
계열회사 Elevar therapeutics는 리보세라닙의 글로벌 간암 임상 3상을 완료하여 미국식품의약국(FDA)에 NDA 신청을 완료하였으며, 2024년 5월 FDA로부터 보완요구서한(CRL)을 수령하였습니다.
(후략)
(주10) 정정 전
(전략)
라. 연구개발실적
※ 연구개발 진행 현황 및 향후계획
본 보고서 제출기준일 현재 당사 및 종속기업이 보유한 파이프라인 연구개발 진행 중인 연구개발(Elevar Therapeutics, Inc.주도 글로벌 임상 포함) 현황은 다음과 같습니다.
| [연구개발 진행 총괄표] (주1) 연구개발 진행 총괄표는 분기보고서 제출일 기준으로 작성하였습니다. 주2) 통상적 통계적으로 유효성을 만족하는 수준의 임상데이터 수집이 완료되면 임상결과를 발표하나, 이는 임상의 완전한 종료를 뜻하는 바는 아닙니다. 모든 임상 참여 환자의 데이터가 축적된 후 임상결과보고서(CSR) 작성이 완료되면 공식적으로 임상시험이 종료됩니다. |
|
구 분 |
품 목 |
적응증 |
임상시작일 |
현재 진행단계 |
임상주도 기업 | ||||
|
단계(국가) |
승인일 |
비 고 | 회사명 | 비고 | |||||
|
화학합성 |
신약 |
리보세라닙 (Rivoceranib) [Elevar Therapeutics, Inc.주도 글로벌 임상 포함] |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안정성평가 완료 | Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|
위암 (3차/4차 단일요법) |
2017년 |
임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 | |||
|
위암 (1차 병용요법) |
2021년 |
임상2상 |
2021년 09월 (임상2상 승인일) |
임상 진행 중 | HLB생명과학 | Rivoceranib 한국 내 전용실시권 L/I 후 개발 |
|||
|
간암 (1차 병용요법) |
2019년 |
임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
임상 종료 22년 9월 초록 발표 (1차 평가 지표 만족) 23년 5월 미국 FDA에 NDA Submission 완료 |
Elevar | 항서제약과 공동개발 | |||
|
선양낭성암종 (1/2차 단일요법) |
2020년 |
임상2상 |
2020년 4월 (임상2상 개시일) |
임상 2상 종료 6월 초록 발표 |
Elevar HLB생명과학 |
Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
|
위암 (2차 병용요법) |
2018년 |
임상2상 |
2018년 10월 (임상1상 개시일) |
임상 종료 22년 결과 발표 |
HLB생명과학 | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
|
대장암 (3차 병용요법) |
2019년 |
임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 종료 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상 진행 중 (농림축산검역본부) |
HLB생명과학 | Rivoceranib 한국 내 전용실시권 L/I 후 자체 개발 |
|||
| 파이로티닙 (Pyrotinib) |
전이성 유방암 | 2023년 | 임상3상 (한국) |
2023년 03월 (임상계획 승인) |
임상3상 진행 중 | HLB생명과학 | Pyrotinib 한국 내 전용실시권 L/I 후 자체 개발 |
||
| 비소세포폐암 | 2020년 | 임상3상 (전세계 13개국) |
2020년 (임상계획 승인) |
임상3상 진행 중 | 항서제약 | Pyrotinib 한국 내 전용실시권 L/I 후 자체 개발 |
|||
|
HLS221-N01 G2M 억제제 |
폐암 유방암 대장암 췌장암 |
- |
비임상시험 단계 |
- |
비임상평가 진행 중 |
HLB생명과학 |
특허권 L/I 후 자체 개발 | ||
|
HLS222-N01 Cannabinoids derivatives |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
HLB생명과학 |
네오켄바이오와 공동연구 | ||
|
HLS232-N01 CDK 억제제 |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
HLB생명과학 |
LDC와 공동연구 | ||
|
HLS231-G01 의료용 대마 |
뇌전증 | - | 탐색 단계 | - | 제형 연구 중 | HLB생명과학 R&D |
- | ||
|
바이오 |
신약 |
바이오인공간 |
급성간부전 |
2001년 |
임상 2b상 |
2017년 임상 2a 완료 |
자체 개발 |
HLB셀 | - |
|
의료기기 |
지혈제 |
조직/장기 출혈 |
2015년 |
확증임상시험 |
2021년 임상계획 승인 |
확증임상 진행 중 |
HLB셀 | UI-DDS 연구소 글로벌 권리 L/I 후 자체 개발 |
|
| 연구용 재료 | 인체 세포 외 기질 (Hutrigel®-RU) |
줄기세포, 오가노이드 배양 기질 | N/A | 연구개발완료 | N/A | 제품판매 준비 중 |
HLB셀 | 자체 개발 | |
| 의료기기 | 인체 세포 외 기질 (Hutrigel®-MU) |
피부, 신경, 심근 등 상처 치유 및 조직 재생 |
N/A | 연구개발 중 | N/A | GMP-compliant , 비임상 유효성평가 준비 중 |
HLB셀 | 자체 개발 | |
|
의료기기 |
인체 세포 외 기질 (Hutrigel®-AU) |
의료용/미용용 기능성 제품 |
N/A |
연구개발 중 |
N/A |
제형화 및 생체 외 |
HLB셀 HLB제약 |
자체 개발 | |
|
주1) 당사는 2018년 8월 14일에 리보세라닙(아파티닙) 관련 부광약품에 인정되는 계약상 지위, 권리 및 의무 일체를 취득하여 연구개발을 진행하고 있습니다. (2018.8.14 공시 참조)
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1)품 목 : 리보세라닙(Rivoceranib)
| 구 분 | 화학합성의약품 |
| 적응증 | 위암 3/4차 치료제(Rivoceranib 단독), 위암 2차 치료제(파클리탁셀 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독), 간암 1차 치료제(항서제약 캄렐리주맙 병용), 대장암 3차 치료제(타이호제약 론서프 병용) |
| 작용기전 | 신생혈관억제, VEGFR2-TKI |
| 제품의특성 | 혈관내피세포성장인자수용체2(VEGFR-2)를 타켓으로 암 조직의 신생혈관 성장을 억제하고, 암세포의 증식억제와 면역세포의 정상화를 유도하는 경구용 표적 항암제입니다. |
| 진행경과 | 위암 3/4차 치료제: 단독 요법으로 글로벌 임상 3상 종료 위암 2차 치료제: 파클리탁셀과 병용으로 임상 1/2상 종료 선양낭성암 1,2차 치료제: 단독요법으로 미국, 한국에서 임상 2상 연구 종료, 한국 조건부 품목허가 신청 완료 (23년 2월), 식약처 보완요청에 따라 자진취하 (23년 12월) 간암 1차 치료제: 항서제약의 캄렐리주맙과 병용으로 글로벌 13개국 임상 3상종료, 2022년 9월 ESMO에서 임상 결과 공개(1차 평가지표 만족), 23년 5월 미국 FDA에 NDA Submission 완료 대장암 3차 치료제: 타이호제약의 론서프와 병용으로 미국, 한국에서 임상 1b/2상 중 1b상 종료 |
| 향후계획 | 위암 3/4차 치료제(Rivoceranib 단독): 조건부 품목허가 및 임상 3상 계획수립 간암 1차 치료제(항서제약 캄렐리주맙 병용) : 미국 NDA 대응 및 상업화 전략 수립, 한국 NDA 신청전략 수립 및 NDA 신청 계획 적응증 확대 계획 캄렐리주맙과 병용 임상 계획 및 전략 수립 선낭암: 식약처 보완요청 자료 확보 후 품목허가 재신청 계획 |
| 경쟁제품 | 선양낭성암 1,2차 치료제: 표준치료제 없음(Off-label)로 치료 진행 간암 1차 치료제: 넥세바, 렌비마, 아바스틴, 티센트릭 |
|
관련논문등 |
선양낭성암 (선낭암) 중국 선낭암 임상 2상: 2021년 Therapeutic Advances in Medical Oncology 13 미국, 한국 선낭암 임상 2상 결과: 2022년 미국암학회 발표, 2023년 11월 Clinical Cancer Research 발표 간암 중국 간암 임상 2상: 2021년 Clin Cancer Res 15:27(4) 글로벌 간암 1차 치료제(항서제약 캄렐리주맙 병용) 임상 3상 결과: 2022년 9월 ESMO (유럽암학회)에서 공개 (1차 평가지표 만족) |
| 시장규모 | 선낭암 치료제 글로벌시장: 표준치료제가 없고 발병률이 낮아 글로벌 시장 규모 추산이 어려움 간암 치료제 글로벌시장: 2023년 8억1060만 달러 (약 1조 538억원)에서 2028년에는 12억5200만달러(약 1조 6275억원)로 성장 예상 ※시장규모 관련 출처 선낭암 데이터 - DataM Intelligence "Adenoid Cystic Carcinoma Market Size, Share, Industry, Forecast and Outlook (2023-2030)" (2023.09) 간암 데이터 - Market Data Forecast "Global Liver Cancer Therapeutics Market Size, Share, Trends, COVID-19 Impact & Growth Analysis Report - Segmented By Type, Therapeutics, End-User & Region - Industry Forecast (2023 to 2028)" (2023.03) |
| 기타사항 | 특허 및 권리 보유 현황 - 리보세라닙의 물질특허: HLB - 글로벌 전용실시권: Elevar - 한국 전용실시권: HLB생명과학 - 중국 전용실시권: 중국 항서제약 항서제약에서 2014년 위암 3차 치료제로 중국 내 시판허가를 득한 후 현재까지 꾸준한 매출 성장 유지 중입니다. 2015년 매출 약 450억에서 2018년 2,800억까지 매출 성장을 보여줘, 약효와 안전성을 입증하였습니다. 2021년 부터 간암 2차 치료제로 적응증을 확대하여, 중국 내 매출 확대가 기대됩니다. |
(후략)
(주10) 정정 후
(전략)
라. 연구개발실적
※ 연구개발 진행 현황 및 향후계획
본 보고서 제출기준일 현재 당사 및 종속기업이 보유한 파이프라인 연구개발 진행 중인 연구개발(Elevar Therapeutics, Inc.주도 글로벌 임상 포함) 현황은 다음과 같습니다.
| [연구개발 진행 총괄표] (주1) 연구개발 진행 총괄표는 분기보고서 제출일 기준으로 작성하였습니다. 주2) 통상적 통계적으로 유효성을 만족하는 수준의 임상데이터 수집이 완료되면 임상결과를 발표하나, 이는 임상의 완전한 종료를 뜻하는 바는 아닙니다. 모든 임상 참여 환자의 데이터가 축적된 후 임상결과보고서(CSR) 작성이 완료되면 공식적으로 임상시험이 종료됩니다. |
|
구 분 |
품 목 |
적응증 |
임상시작일 |
현재 진행단계 |
임상주도 기업 | ||||
|
단계(국가) |
승인일 |
비 고 | 회사명 | 비고 | |||||
|
화학합성 |
신약 |
리보세라닙 (Rivoceranib) [Elevar Therapeutics, Inc.주도 글로벌 임상 포함] |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안정성평가 완료 | Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|
위암 (3차/4차 단일요법) |
2017년 |
임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 | |||
|
위암 (1차 병용요법) |
2021년 |
임상2상 |
2021년 09월 (임상2상 승인일) |
임상 진행 중 | HLB생명과학 | Rivoceranib 한국 내 전용실시권 L/I 후 개발 |
|||
|
간암 (1차 병용요법) |
2019년 |
임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
- 임상 종료, 22년 9월 초록 발표(1차 평가 지표 만족) - 23년 5월 미국 FDA에 NDA Submission 완료 - 24년 5월 미국 FDA 수정 보완 요구(CRL 수령) |
Elevar | 항서제약과 공동개발 | |||
|
선양낭성암종 (1/2차 단일요법) |
2020년 |
임상2상 |
2020년 4월 (임상2상 개시일) |
임상 2상 종료 6월 초록 발표 |
Elevar HLB생명과학 |
Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
|
위암 (2차 병용요법) |
2018년 |
임상2상 |
2018년 10월 (임상1상 개시일) |
임상 종료 22년 결과 발표 |
HLB생명과학 | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
|
대장암 (3차 병용요법) |
2019년 |
임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 종료 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상 진행 중 (농림축산검역본부) |
HLB생명과학 | Rivoceranib 한국 내 전용실시권 L/I 후 자체 개발 |
|||
| 파이로티닙 (Pyrotinib) |
전이성 유방암 | 2023년 | 임상3상 (한국) |
2023년 03월 (임상계획 승인) |
임상3상 진행 중 | HLB생명과학 | Pyrotinib 한국 내 전용실시권 L/I 후 자체 개발 |
||
| 비소세포폐암 | 2020년 | 임상3상 (전세계 13개국) |
2020년 (임상계획 승인) |
임상3상 진행 중 | 항서제약 | Pyrotinib 한국 내 전용실시권 L/I 후 자체 개발 |
|||
|
HLS221-N01 G2M 억제제 |
폐암 유방암 대장암 췌장암 |
- |
비임상시험 단계 |
- |
비임상평가 진행 중 |
HLB생명과학 |
특허권 L/I 후 자체 개발 | ||
|
HLS222-N01 Cannabinoids derivatives |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
HLB생명과학 |
네오켄바이오와 공동연구 | ||
|
HLS232-N01 CDK 억제제 |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
HLB생명과학 |
LDC와 공동연구 | ||
|
HLS231-G01 의료용 대마 |
뇌전증 | - | 탐색 단계 | - | 제형 연구 중 | HLB생명과학 R&D |
- | ||
|
바이오 |
신약 |
바이오인공간 |
급성간부전 |
2001년 |
임상 2b상 |
2017년 임상 2a 완료 |
자체 개발 |
HLB셀 | - |
|
의료기기 |
지혈제 |
조직/장기 출혈 |
2015년 |
확증임상시험 |
2021년 임상계획 승인 |
확증임상 진행 중 |
HLB셀 | UI-DDS 연구소 글로벌 권리 L/I 후 자체 개발 |
|
| 연구용 재료 | 인체 세포 외 기질 (Hutrigel®-RU) |
줄기세포, 오가노이드 배양 기질 | N/A | 연구개발완료 | N/A | 제품판매 준비 중 |
HLB셀 | 자체 개발 | |
| 의료기기 | 인체 세포 외 기질 (Hutrigel®-MU) |
피부, 신경, 심근 등 상처 치유 및 조직 재생 |
N/A | 연구개발 중 | N/A | GMP-compliant , 비임상 유효성평가 준비 중 |
HLB셀 | 자체 개발 | |
|
의료기기 |
인체 세포 외 기질 (Hutrigel®-AU) |
의료용/미용용 기능성 제품 |
N/A |
연구개발 중 |
N/A |
제형화 및 생체 외 |
HLB셀 HLB제약 |
자체 개발 | |
|
주1) 당사는 2018년 8월 14일에 리보세라닙(아파티닙) 관련 부광약품에 인정되는 계약상 지위, 권리 및 의무 일체를 취득하여 연구개발을 진행하고 있습니다. (2018.8.14 공시 참조)
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1)품 목 : 리보세라닙(Rivoceranib)
| 구 분 | 화학합성의약품 |
| 적응증 | 위암 3/4차 치료제(Rivoceranib 단독), 위암 2차 치료제(파클리탁셀 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독), 간암 1차 치료제(항서제약 캄렐리주맙 병용), 대장암 3차 치료제(타이호제약 론서프 병용) |
| 작용기전 | 신생혈관억제, VEGFR2-TKI |
| 제품의특성 | 혈관내피세포성장인자수용체2(VEGFR-2)를 타켓으로 암 조직의 신생혈관 성장을 억제하고, 암세포의 증식억제와 면역세포의 정상화를 유도하는 경구용 표적 항암제입니다. |
| 진행경과 | 위암 3/4차 치료제: 단독 요법으로 글로벌 임상 3상 종료 위암 2차 치료제: 파클리탁셀과 병용으로 임상 1/2상 종료 선양낭성암 1,2차 치료제: 단독요법으로 미국, 한국에서 임상 2상 연구 종료, 한국 조건부 품목허가 신청 완료 (23년 2월), 식약처 보완요청에 따라 자진취하 (23년 12월) 간암 1차 치료제: 항서제약의 캄렐리주맙과 병용으로 글로벌 13개국 임상 3상종료, 22년 9월 ESMO에서 임상 결과 공개(1차 평가지표 만족), 23년 5월 미국 FDA에 NDA Submission 완료, 24년 5월 미국 FDA로부터 CRL(보완요구서한) 수령 대장암 3차 치료제: 타이호제약의 론서프와 병용으로 미국, 한국에서 임상 1b/2상 중 1b상 종료 |
| 향후계획 | 위암 3/4차 치료제(Rivoceranib 단독): 조건부 품목허가 및 임상 3상 계획수립 간암 1차 치료제(항서제약 캄렐리주맙 병용): FDA 재승인 신청 적응증 확대 계획 선낭암: 식약처 보완요청 자료 확보 후 품목허가 재신청 계획 |
| 경쟁제품 | 선양낭성암 1,2차 치료제: 표준치료제 없음(Off-label)로 치료 진행 간암 1차 치료제: 넥세바, 렌비마, 아바스틴, 티센트릭 |
|
관련논문등 |
선양낭성암 (선낭암) 중국 선낭암 임상 2상: 2021년 Therapeutic Advances in Medical Oncology 13 미국, 한국 선낭암 임상 2상 결과: 2022년 미국암학회 발표, 2023년 11월 Clinical Cancer Research 발표 간암 중국 간암 임상 2상: 2021년 Clin Cancer Res 15:27(4) 글로벌 간암 1차 치료제(항서제약 캄렐리주맙 병용) 임상 3상 결과: 2022년 9월 ESMO (유럽암학회)에서 공개 (1차 평가지표 만족) |
| 시장규모 | 선낭암 치료제 글로벌시장: 표준치료제가 없고 발병률이 낮아 글로벌 시장 규모 추산이 어려움 간암 치료제 글로벌시장: 2023년 8억1060만 달러 (약 1조 538억원)에서 2028년에는 12억5200만달러(약 1조 6275억원)로 성장 예상 ※시장규모 관련 출처 선낭암 데이터 - DataM Intelligence "Adenoid Cystic Carcinoma Market Size, Share, Industry, Forecast and Outlook (2023-2030)" (2023.09) 간암 데이터 - Market Data Forecast "Global Liver Cancer Therapeutics Market Size, Share, Trends, COVID-19 Impact & Growth Analysis Report - Segmented By Type, Therapeutics, End-User & Region - Industry Forecast (2023 to 2028)" (2023.03) |
| 기타사항 | 특허 및 권리 보유 현황 - 리보세라닙의 물질특허: HLB - 글로벌 전용실시권: Elevar - 한국 전용실시권: HLB생명과학 - 중국 전용실시권: 중국 항서제약 항서제약에서 2014년 위암 3차 치료제로 중국 내 시판허가를 득한 후 현재까지 꾸준한 매출 성장 유지 중입니다. 2015년 매출 약 450억에서 2018년 2,800억까지 매출 성장을 보여줘, 약효와 안전성을 입증하였습니다. 2021년 부터 간암 2차 치료제로 적응증을 확대하여, 중국 내 매출 확대가 기대됩니다. |
(후략)
(주11) 정정 전
(전략)
(2) 계열회사의 관한 사항 : Elevar Therapeutics, Inc.(구. HLB USA, Inc.)
Elevar Therapeutics,Inc.는 2005년 7월 신약개발 컨설팅 회사로 설립되어 2007년 12월 Rivoceranib(구. Apatinib Mesylate) 표적항암제 라이센스 취득 계약 체결(Advenchen Laboratories, Inc., CA, USA)로 중국을 제외한 세계 판권을 취득하여 독자적인 바이오사업을 시작하였습니다. 본 Rivoceranib(구. Apatinib Mesylate)는 위암(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국), 간암 (2021년 11월 미국식품의약국), 선양낭성암 (2021년 2월 미국식품의약국) 대상으로 희귀의약품 지정을 받아 임상종료 후 시판허가에 대한 심사의 신속화, 수수료 감면 등의 혜택과 최소 8년(2029년)에서 최대 13년(2034년) 동안 독점 판매할 수 있습니다.
2011년 11월 US FDA로부터 다국가(미국/한국) 1/2a 임상시험을 위한 IND 승인을 받아 표적항암제 리보세라닙(구. Apatinib Mesylate)은 다국가(미국/한국) 1/2상 임상시험을 종료하였고, 2017년 표준치료법으로 2차 치료제 이상에서 치료에 실패한 진행성 또는 전이성 환자를 대상으로 글로벌(미국, 유럽, 한국, 일본, 대만 등 12개국) 3상 임상시험을 완료하였습니다. 그 이후 적응증 확대를 위해 간암 1차, 선양낭성암의글로벌 임상을 추진하였고, 최근 두 임상 모두 환자 모집을 완료했습니다. 선양낭성암은 현재까지 표준치료제가 전무한 희귀암으로, 글로벌 최초 대규모 2상 임상을 진행하여 그 결과를 2022년 6월 미국 암학회(ASCO)에서 발표한 바 있습니다. 표준치료제가 없는 희귀암의 의료미충족수요가 높은 암종으로 First in Class를 기대하고 있습니다. 그리고 간암 1차 치료제 글로벌 임상은 항서제약에서 개발한 PD-1 면역항암제 캄렐리주맙과 리보세라닙의 병용으로 실시되었으며, 글로벌 543명의 임상 환자를 모집하였고, 2022년 ESMO에서 그 결과를 발표했습니다. 통상적으로 임상 결과의 유효성을 입증하는 1차 평가지표는 적응증, 치료방식, 대조군 등에 따라 다르게 이루어집니다. 당사가 진행한 간암 1차 치료제 글로벌 3상 임상(항서제약 캄렐리주맙 병용)의 경우 기존 1차 치료제인 소라페닙을 대조군으로 하여 OS와 PFS를 1차 평가지표로 하여 진행되었습니다. mOS의 경우 대조군인 소라페닙 대비 6.9개월 긴 22.1개월을 기록했고, mPFS는 대조군 대비 1.9개월 증가한 5.6개월을 기록해(통계적 유의성 확보) 1차 평가지표의 유효성을 만족했습니다. 회사는 임상 데이터를 면밀히 분석해 적절한 허가 전략을 수립한 후 신약허가를 신청할 계획입니다. 그 밖에도, 대장암(Colorectal cancer) 3차 치료제, 위암(Gastric cancer) 2차 치료제에 대해서 임상시험중에 있습니다. 대장암 3차 치료제는 타이호제약의 론서프(Lonsurf)와 병용으로 임상 1/2상을, 위암 2차 치료제는 파클리탁셀(Paclitaxel)과 병용요법으로 임상 1/2상을 진행 중입니다. 그리고 미국 서던 캘리포니아 암센터에서 육종(Sarcoma)에 대해서 BMS의 면역항암제 옵디보(Nivolumab)의 병용임상시험을 종료하였습니다.
(후략)
(주11) 정정 후
(전략)
(2) 계열회사의 관한 사항 : Elevar Therapeutics, Inc.(구. HLB USA, Inc.)
Elevar Therapeutics,Inc.는 2005년 7월 신약개발 컨설팅 회사로 설립되어 2007년 12월 Rivoceranib(구. Apatinib Mesylate) 표적항암제 라이센스 취득 계약 체결(Advenchen Laboratories, Inc., CA, USA)로 중국을 제외한 세계 판권을 취득하여 독자적인 바이오사업을 시작하였습니다. 본 Rivoceranib(구. Apatinib Mesylate)는 위암(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국), 간암 (2021년 11월 미국식품의약국), 선양낭성암 (2021년 2월 미국식품의약국) 대상으로 희귀의약품 지정을 받아 임상종료 후 시판허가에 대한 심사의 신속화, 수수료 감면 등의 혜택과 최소 8년(2029년)에서 최대 13년(2034년) 동안 독점 판매할 수 있습니다.
2011년 11월 US FDA로부터 다국가(미국/한국) 1/2a 임상시험을 위한 IND 승인을 받아 표적항암제 리보세라닙(구. Apatinib Mesylate)은 다국가(미국/한국) 1/2상 임상시험을 종료하였고, 2017년 표준치료법으로 2차 치료제 이상에서 치료에 실패한 진행성 또는 전이성 환자를 대상으로 글로벌(미국, 유럽, 한국, 일본, 대만 등 12개국) 3상 임상시험을 완료하였습니다. 그 이후 적응증 확대를 위해 간암 1차, 선양낭성암의글로벌 임상을 추진하였고, 최근 두 임상 모두 환자 모집을 완료했습니다. 선양낭성암은 현재까지 표준치료제가 전무한 희귀암으로, 글로벌 최초 대규모 2상 임상을 진행하여 그 결과를 2022년 6월 미국 암학회(ASCO)에서 발표한 바 있습니다. 표준치료제가 없는 희귀암의 의료미충족수요가 높은 암종으로 First in Class를 기대하고 있습니다. 그리고 간암 1차 치료제 글로벌 임상은 항서제약에서 개발한 PD-1 면역항암제 캄렐리주맙과 리보세라닙의 병용으로 실시되었으며, 글로벌 543명의 임상 환자를 모집하였고, 2022년 ESMO에서 그 결과를 발표했습니다. 통상적으로 임상 결과의 유효성을 입증하는 1차 평가지표는 적응증, 치료방식, 대조군 등에 따라 다르게 이루어집니다. 당사가 진행한 간암 1차 치료제 글로벌 3상 임상(항서제약 캄렐리주맙 병용)의 경우 기존 1차 치료제인 소라페닙을 대조군으로 하여 OS와 PFS를 1차 평가지표로 하여 진행되었습니다. mOS의 경우 대조군인 소라페닙 대비 6.9개월 긴 22.1개월을 기록했고, mPFS는 대조군 대비 1.9개월 증가한 5.6개월을 기록해(통계적 유의성 확보) 1차 평가지표의 유효성을 만족했습니다. 이에 회사는 2023년 5월 FDA에 NDA(시판승인허가)를 신청하였으며, 2024년 5월 FDA로부터 CRL(보완요구서한)을 수령하였습니다. 그 밖에도, 대장암(Colorectal cancer) 3차 치료제, 위암(Gastric cancer) 2차 치료제에 대해서 임상시험중에 있습니다. 대장암 3차 치료제는 타이호제약의 론서프(Lonsurf)와 병용으로 임상 1/2상을, 위암 2차 치료제는 파클리탁셀(Paclitaxel)과 병용요법으로 임상 1/2상을 진행 중입니다. 그리고 미국 서던 캘리포니아 암센터에서 육종(Sarcoma)에 대해서 BMS의 면역항암제 옵디보(Nivolumab)의 병용임상시험을 종료하였습니다.
(후략)
【 대표이사 등의 확인 】
 |
|
HLB생명과학_대표이사등의확인서 |
증 권 신 고 서
| ( 지 분 증 권 ) |
| [증권신고서 제출 및 정정 연혁] |
| 제출일자 | 문서명 | 비고 |
|---|---|---|
| 2024년 03월 21일 | 증권신고서(지분증권) | 최초제출 |
| 2024년 04월 04일 | [기재정정] 증권신고서(지분증권) | 기재정정(파란색) |
| 2024년 04월 19일 | [기재정정] 증권신고서(지분증권) | 기재정정(빨간색) |
| 2024년 05월 08일 | [발행조건확정] 증권신고서(지분증권) | 1차 발행가액 확정(초록색) |
| 2024년 05월 13일 | [기재정정] 증권신고서(지분증권) | 1분기 분기보고서 제출에 따른 기재정정(주황색) |
| 2024년 05월 23일 | [기재정정] 증권신고서(지분증권) | 기재정정(보라색) |
| 금융위원회 귀중 | 2024 년 05 월 23 일 |
| 회 사 명 : |
에이치엘비생명과학 주식회사 |
| 대 표 이 사 : |
남상우, 한용해 |
| 본 점 소 재 지 : |
경기도 화성시 동탄첨단산업1로 51-9, 8층 (영천동, 엠타워지식산업센터) |
| (전 화) 02-2627-6700 | |
| (홈페이지) http://www.hlb-ls.com | |
| 작 성 책 임 자 : | (직 책) 경영관리본부장 (성 명) 이근식 |
| (전 화) 02-2627-6700 | |
| 모집 또는 매출 증권의 종류 및 수 : | 기명식 보통주 11,005,125주 | |
| 모집 또는 매출총액 : | 130,850,936,250 | 원 |
| 증권신고서 및 투자설명서 열람장소 |
| 가. 증권신고서 |
| 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 나. 투자설명서 |
| 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 서면문서 : 에이치엘비생명과학(주) → 경기도 화성시 동탄첨단산업1로 51-9, 8층(영천동,엠타워지식산업센터) |
| 한국투자증권(주) → 서울특별시 영등포구 의사당대로 88 케이비증권(주) → 서울특별시 영등포구 여의나루로 50 |
【 대표이사 등의 확인 】
 |
|
대표이사등의확인서 |
요약정보
1. 핵심투자위험
| 하단의 핵심투자위험은 증권신고서 본문에 기재된 투자위험요소 중 중요한 항목만을 투자자의 이해도 제고를 위하여 간단ㆍ명료하게 요약한 것입니다. 자세한 투자위험요소는 "본문-제1부 모집 또는 매출에 관한 사항-Ⅲ. 투자위험요소"에 기재되어 있으니 참고하시기 바랍니다. |
| 구 분 | 내 용 |
| 사업위험 |
가. 국내외 경기 변동에 따른 사업환경 악화 위험 자. 제약 산업의 성장 둔화 위험 제약산업은 인구의 고령화 및 소득증가에 따른 1인당 약제비가 증가하여 꾸준한 성장을 이어왔습니다. 하지만 정부의 리베이트 규제 강화, 일괄 약가인하 등 비우호적인 영업환경이 지속됨에 따라 최근 성장성이 둔화된 추세를 보이고 있습니다. 이에 따라 국내 제약산업은 높은 수준의 R&D 투자, 이머징 마켓으로의 진출, 신규 바이오 의약품 개발 등 다양한 노력을 기울이고 있습니다. 그러나 이러한 전반의 노력에도 불구하고 당사가 영위하는 사업의 전방산업인 전체 제약산업이 위축되거나 시장성장률이 둔화되는 경우 의약품 유통업을 영위하는 당사의 영업 성과 및 재무 상태에 부정적인 영향을 끼칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
| 회사위험 | 가. 매출액 및 수익성 저하 위험 당사는 구성품 개발 및 완제품 위탁 생산하는 메디케어사업, 주사기 제조 및 판매하는 의료기기사업, 종속회사 에이치엘비셀(주)가 영위하는 바이오 신약 및 의료기기를 개발하는 바이오 개발 사업, 종속회사 (주)신화어드밴스가 영위하는 의약품 유통 사업, 종속회사 에이치엘비에너지(주)가 영위하는 신재생에너지 사업으로 구성된 에너지사업까지 크게 5가지 부문으로 매출이 구성됩니다. 당사는 2022년 10월 체외 진단의료기기 및 기타 의료용기기 제조, 판매 기업인 에임(주)와 의료기기 및 의료소모품 생산, 판매 업체인 에임텍(주)를 흡수합병 함으로써 체외진단키드 등 의료기기 산업에 진출하였습니다. 이에 따라 2022년 기준, 전기 대비 86% 증가한 약 996억원(연결기준)의 매출을 달성하였으며, 2023년에는 약 980억을 기록했습니다. 2023년말 기준 사업별 매출액은 메디케어사업부문이 약 250억원으로 25.46%, 의료기기사업부문이 약 44억원으로 4.47%, 의약품유통사업이 약 634억원으로 64.71%, 에너지 사업부문이 약 53억원으로 5.36%의 매출액을 기록했습니다. 특히 2023년 7월 의료기기사업부 확대를 위하여 일회용 주사기 제조업을 영위하고 있는 화진메다칼(주)를 인수하여 약 44억원의 매출을 기록했습니다. 2022년과 2023년은 신규사업 확장을 통해 매출액 개선을 보였으며, 2023년말 기준 당사는 59억원의 당기순손실 기록했습니다. 2024년 1분기 메디케어사업부문이 약 40억원으로 16.9%, 의료기기사업부문이 약 20억원으로 8.4%, 의약품유통사업부문이 168억원으로 70.5%, 에너지사업부문이 약 10억원으로 4.2%의 매출을 기록했습니다. 또한 당사는 상대적으로 영업외수익 및 영업외비용이 수익성에서 큰 비중을 차지하고 있습니다. 그 중 매년 금융수익 및 금융원가의 변동폭에 따라, 당기순이익 및 당기순손실을 시현하고 있습니다. 단, 이는 주로 당사가 보유하고 있는 에이치엘비 주식회사 및 공제조합 지분 평가에 의한 금융자산 평가손익에 의한 것으로 향후에도 당사가 보유한 금융자산의 평가손익에 따라 당사의 수익성이 변동 될 위험이 있습니다. 투자자 여러분께서는 이 점 각별히 유의하시기 바랍니다. 나. 재무안정성 악화 가능성에 따른 위험 당사의 주요 재무안정성 지표 추이를 살펴보면, 연결기준 부채비율은 2020년말 13.7%, 2021년말 9.8%, 2022년말 74.4% 2023년말 83.2% 로 계속해서 증가하였습니다. 이는 신규사업 확장 및 운영자금 확보를 위해 2022년 신주인수권부사채 1,000억원, 전환사채 450억원을 발행, 2023년 전환사채 83억원 발행함으로써 부채비율이 증가했습니다. 이에 따라 총차입금이 꾸준히 증가 추세를 보이면서 차입금의존도 역시 2020년 3.3%를 기록 이후 지속적으로 증가하여 2023년 39.0%를 기록하고 있습니다. 2024년 1분기에는 제10회차 전환사채 2024.03.29 기준, 미상환사채 잔액 모두 전환청구와 제9회차 신주인수권부사채의 지속적인 전환 및 당사가 보유하고 있는 HLB(주) 보통주의 주가의 상승으로 인해 자본총계 약 4,328억원을 기록하며 부채비율 45.45% 및 차입금의존도 27.3%를 기록했습니다. 제10회차 전환사채 2024.03.29 기준, 미상환사채 잔액 모두 전환청구 하였으며, 제9회차 신주인수권부사채는 신주배정기준일(2024.05.10) 기준, 약 804억원은 만기 상 장기차입금으로 분류되어 있으나, 최초 조기상환일 기준 실질만기가 2024년중에 도래하기 때문에 단기적 상환부담이 존재하는 상황입니다. 향후에도 계속되는 영업실적의 부진, 임상 지연 등으로 인한 바이오 사업 매출 미실현 등에 따른 투자 등에 따라 차입금이 증가할 가능성이 존재하며, 지속적으로 차입을 할 경우 당사의 재무안정성이 악화될 가능성이 존재합니다. 투자자 분들께서는 이 점 유의하시기 바랍니다. 다. 유동성 악화에 따른 위험 당사는 2020년을 제외하고 최근 지속적으로 영업활동현금유출이 발생하고 있습니다. 2020년 약 2,010백만원으로 영업활동현금유입이 발생하였으나, 2021년 약 14,084백만원, 2022년 약 29,744백만원, 2023년 약 10,016백만원, 2024년 1분기 약 5,465백만원의 영업활동현금유출을 기록했습니다. 당사의 영업활동현금흐름 유출의 주된 원인은 실적부진이며 영업활동현금흐름과 투자활동현금흐름의 유출을 재무활동(외부차입 등)을 통하여 충당하고 있습니다. 2020년, 2021년 음(-)의 재무활동현금흐름을 기록했으나, 2022년, 2023년 양(+)의 재무활동현금흐름을 기록했습니다. 2022년 제9회 신주인수권부사채 1,000억 및 제10회 전환사채 450억 발행과 에임(주) 및 에임텍(주)를 흡수합병 함으로써 102,096백만원의 순재무활동현금흐름을 기록했습니다. 2023년에는 제11회 전환사채 83억 발행 및 단기차입금 증가로 약 7,710백만원의 재무활동현금흐름을 기록했으며, 2024년 1분기에는 제9회차 신주인수권부사채의 청구에 따라 58,803백만원의 재무활동현금흐름을 기록했습니다. 현재까지 투자활동을 통한 현금 유입으로 유동성을 확보하였으나, 바이오사업 매출 실현 지연으로 인한 영업활동현금 유출 지속 및 국내 경기의 악화, 금융시장의 부진 등으로 재무활동현금 유입이 원활하지 못할 경우 당사는 유동성 압박에 시달릴 수 있습니다. 투자자 분들께서는 이 점 유의하시기 바랍니다. 라. 신사업 진출을 위한 타법인 출자에 따른 위험 당사는 기업 전반의 손익 개선 및 신성장동력확보를 위해 2013년말부터 사업 다각화를 진행하여 왔고, 이 과정에서 주식양수도 등을 통하여 계열회사 지분을 지속적으로 취득하였습니다. 당사 종속기업의 손익은 당사 연결재무제표의 손익에 직접 영향을 미치며2024년 1분기 기준, 연결대상 종속회사인 (주)신화어드밴스, 에이치엘비셀(주), 에이치엘비에너지(주), 에이치엘비생명과학알엔 디(주), 에이치엘비솔루션(주)는 관련 손익이 직접 연결제무제표에 계상되었습니다. 그 외 에이치엘비제약(주) 같은 관계기업의 손익도 그 지분율만큼 지분법손익에 따라 영업외손익으로 인식하여 당사의 연결재무제표에 영향을 미칩니다. 당사는 2022년 5월 31일 조용호 외 1인과 자산양수도 계약을 체결하고, 에임의 주식 100,000주(지분율 : 100.00%)를 양수하였으며, 2023년 7월 3일 HLB테라퓨틱스와 자산양수도 계약을 체결하고, 화진메디칼의 주식 863,500주(지분율 : 100.00%)를 양수하였습니다. 향후 당사의 종속 및 관계회사를 통한 시너지 효과 및 수익성 회복이 이루어지지 않고 당사가 투자한 종속기업 및 관계기업의 경영 악화로 인하여 해당회사들의 손실이 발생된다면, 당사의 손익에 부정적인 영향을 줄 수 있으며 당사의 재무건전성 역시 악화될 수 있습니다. 투자자 여러분께서는 이 점을 유의하시기 바랍니다. 마. 특수관계자와의 거래에 따른 위험 당사는 HLB바이오스텝(주)이 2022년 1월에 발행한 제1회 무기명식 무보증 전환사채 약 10,243백만원을 보유하고 있습니다. 또한 당사의 최대주주인 HLB(주)는 당사가 2022년 6월 발행한 제9회 무기명식 이권부 무보증 분리형 신주인수권부사채 19,603백만원을 보유하고 있습니다. 또한 당사의 특수관계자 바다중공업은 에이치엘비의 종속회사인 에이치엘비이앤지의 종속회사이며, 바다중공업 기타채권 중 당사의 종속회사 에이치엘비셀로부터 받은 대여금 및 이자 비용 800백만원을 상환하였습니다. 또한 HLB그룹에서 설립한 에이치벨류에셋에 부동산 투자를 위해 50억원을 출자하였습니다. 당사는 이사회 결의 등 적법절차를 준수하고 당사의 피해 또는 특수관계자에 대한 부당한 이익제공에 해당하지 않도록 특수관계자와의 거래를 진행하고 있습니다. 그러나 특수관계자와의 거래 발생 시 거래 조건 등이 제3자와의 거래와 비교하여 적정성이 유지되지 않을 경우 당사의 주주가 향유하여야 할 이익이 특수관계자 측에 전가될 위험이 있습니다. 또한 특수관계자에 대한 채권 규모가 증가할수록 현금흐름 및 재무구조에는 부정적으로 작용할 가능성이 있습니다. 투자자분들께서는 이 점 유의하여 주시기 바랍니다. 바. 우발채무 및 소송관련 위험 2024년 1분기 기준 당사는 종속회사인 에이치엘비에너지(주)의 소각로 증축과 관련하여 기업은행으로부터 차입한 차입금에 대한 60억원 후순위 담보제공과 48억원 지급보증을 제공하였습니다. 당사는 견질 제공한 어음 및 수표의 내역은 없으며, 연결회사 및 그 종속회사의 차입금 등과 관련하여 금융기관에 유형자산, 금융자산 및 투자부동산을 담보로 제공하고 있으며, 총 장부금액은 약 298,022백만원입니다. 2024년 1분기 기준 당사는 현재 총 4건의 소송을 진행 중에 있습니다. 당사가 피고로 계류중인 소송은 2건으로 소송금액 총 2,343백만원이며 원고로 계류중인 소송은 2건으로 소송금액은 10,055백만원입니다. 증권신고서 제출일 현재 계류 중인 소송 사건에 대해서는 소송의 결과를 합리적으로 예측할 수 없으며, 당사가 피고로 진행 중인 사건과 관련해서 최종적으로 패소 시 청구액에 상당하는 금액의 손실이 발생할 수 있습니다. 당사는 담보 및 보증제공으로 인한 우발부채와 소송으로 인한 우발부채가 존재합니다. 당사가 제공한 담보 및 보증과 관련하여 우발부채가 현실화되거나 당사가 소송에서 패소함에 따라 추가적인 대손충당 등이 발생할 경우 당사 재무에 부정적인 영향을 줄 수 있습니다. 투자 판단 시 당사의 담보 및 보증 제공과 관련한 우발부채 현황 및 소송의 현황을 확인하고 이로 인한 우발부채의 현실화 가능성에 주의하시기 바랍니다. 사. 경영권 안정성에 대한 위험 당사의 현재 최대주주인 에이치엘비(주)는 2015년 10월 23일 7,462,687주(25,000,001,450원)의 제3자배정 유상증자 중에서 2,089,553주(9.49%)를 취득하여 최대주주가 되었습니다. 최대주주 지분율은 전환권 행사 등을 통해 증가하였고, 신주배정기준일 기준 총 발행주식수는 107,650,759주이며, 최대주주인 에이치엘비(주)는 발행주식총수의 18.29%인 19,688,685주를 보유하고 있습니다. 금번 유상증자를 통해 발행 예정인 주식은 11,005,125주이며, 당사 최대주주인 에이치엘비(주)는 2,014,080주를 배정 받을 예정입니다. 당사 최대주주인 에이치엘비(주)는 50% 청약에 참여할 예정이며, 배정주식의 50% 수준의 청약률을 가정할 경우 예상 청약 주식수는 1,007,040주입니다. 최대주주는 금번 유상증자 청약자금을 자체보유 현금으로 집행할 예정입니다. 다만, 증자 진행 과정에서 주가 상승으로 인해 예정발행가액 대비 확정발행가액이 변동될 경우 최대주주의 청약자금 부담 증가로 인하여 청약 주식수와 금액에 일부 변동이 발생할 수 있습니다. 또한 현재 미상환 신주인수권부사채 및 전환사채가 보통주로 전환될 경우 기존주주들의 지분희석이 발생하게 되며, 최대주주 에이치엘비(주)의 지분율 또한 희석될 수 있습니다. 9BW의 발행 당시 인수계약서 상 '행사가격의 조정' 관련 조항과 11CB 및 12CB의 발행 당시 인수계약서 상 '전환가액의 조정' 관련 조항에 따라, 금번 유상증자 이후 행사가격 및 전환가액이 조정될 예정입니다. 이에 따라 금번 주주배정후 실권주 일반공모 유상증자에 따라 전환 및 행사가액이 조정된 이후 최대주주가 배정물량의 50%를 청약을 하고 전환 및 행사가능 주식수 전량이 전환 청구될 경우 당사 최대주주 지분율은 18.16%로 본 공시서류 제출일 전일 지분율 대비 0.13%p. 감소할 예정입니다. 유상증자 이후 지분율 하락에도 에이치엘비(주)는 당사 최대주주로서의 지위를 유지할 예정이나, 이와 같은 지분율 감소는 최대주주의 경영권 등에 부정적인 영향을 미칠 수 있습니다. 또한 예기치 못한 상황으로 인한 청약실패 가능성이 상존하고 있으며, 청약참여율이 당초 계획대비 낮아질 경우 상기와 같은 경영권 위험이 대두될 가능성이 있으니 투자자께서는 투자 판단시 이점 유의하시기 바랍니다. 아. 종속회사 관련 위험 당사는 5개의 연결대상 종속회사를 보유하고 있으며, 주요 연결대상 종속회사로는 (주)신화어드밴스, 에이치비셀(주), 에이치엘비에너지(주) 및 에이치엘비솔루션(주)가 있습니다. 에이치엘비셀(주)는 바이오인공간, 지혈제, 인간 세포외기질을 연구 개발하는 회사로 해당 제품에 대한 본격적인 매출이 실현되지 않았으며, 2021년까지의 매출은 임상 컨설팅 등의 용역제공에 따른 매출이였습니다. 그러나 에이치엘비셀(주)는 2022년 10월 의료기기 및 의료소모품 생산, 판매 기업인 에임텍(주)을 흡수합병 함으로써 2020년 89백만원, 2021년 13백만원에서 2022년 1,166백만원, 2023년 1,407백만원으로 매출액 증가를 기록했습니다. 그러나 연구개발에 따른 인건비 등 비용이 발생함에 따라 영업이익은 계속해서 영업손실을 기록했습니다. 종속기업인 주식회사 신화어드밴스는 의약품 유통업을 영위하는 업체로서, 당사는 2016년 8월 3일 종속기업의 주식 100%를 취득하였습니다. (주)신화어드밴스는 2020년 매출액 75,059백만원을 기록하였으나 이후 감소하여 2021년 37,734백만원, 2022년 54,058백만원, 2023년 63,4177백만원 및2024년 1분기 16,849백만원을 기록하였습니다. 영업이익 또한 2020년 106백만원에서 2024년 1분기 -249백만원을 기록하며 영업손실을 보이고 있으며, 당기순이익 역시 2020년 179백만원에서 2024년 1분기 -86백만원의 당기순손실로 감소하였습니다. 종속기업인 에이치엘비에너지(주)는 폐기물 처리업을 영위하는 업체로서 당사는 2019년 5월 에이치엘비에너지(주)의 지분 100%를 취득하였습니다. 에이치엘비에너지(주)의 매출액은 2020년 3,080백만원, 2021년 3,761백만원, 2022년 4,266백만원, 2023년 3,487백만원 및 2024년 1분기 999백만원을 기록하였습니다. 2022년을 제외하고는 영업손실을 기록했으며, 당기순손실의 경우 2023년까지 계속해서 손실을 기록하기는 했지만, 2020년 1,022백만원에서 2023년 370백만원으로 손실의 폭이 감소하였습니다. 수익성 악화, 영업환경 악화 등 예상치 못한 이슈발생으로 인하여 종속회사의 실적 악화로 이어질 수 있으며, 이는 당사의 연결기준 재무에 악영향을 끼칠 수 있으므로 연결대상 종속회사에 대한 지속적인 모니터링이 필요하오니 투자자 여러분께서는 유의하시기 바랍니다. 자. 회계처리 관련 제재 리스크 당사는 금융감독원으로부터 제21기(2018.1.1 ~ 2018.12.31)부터 제22기(2019.1.1 ~ 2019.12.31)까지의 연결재무제표 등에 대한 심사결과 지적된 회계처리 기준 위반사항 등에 대하여 수정권고를 제시받았습니다. 금융감독원은 당사의 18년말 에이치엘비셀(주) 관련 영업권과 관련하여, 연결기준 15,125백만원 및 별도기준 8,858백만원을 18년 및 19년 재무제표에서 각각 과대 및 과소계상한 것으로 판단하였습니다. 당사는 2018년 영업권 손상평가보고서가 당시 이용가능한 최신 자료를 모두 반영하지 못하였다는 금융감독원의 수정권고를 수용하되 회계기준서에 근거한 최선의 합리적 추정치를 산출하여 재무제표를 수정하는 것이 타당하다고 판단하여 소명서를 제출하였습니다. 당사는 수정권고를 수용하여 2021년 12월 10일 수정 권고 내용이 반영된 제21기 및 제22기 재무제표를 전자공시시스템에 재공시하였습니다. 위법동기를 직무상 주의의무를 현저히 결하였다고 인정할 수 있는 경우 등에 해당하지 않아 과실로 판단되었고 경고 조치로 마무리되었습니다. 투자자께서는 이 점 인지하시어 투자의사결정하시기 바랍니다. 차. 에이치엘비 주식회사 주가 변동에 따른 손익 변동 위험 당사는 2024년 1분기말 기준 최대주주인 에이치엘비 주식회사의 주식 1,933,601주를 보유하고 있으며, 해당 보유분은 매분기 공정가치 평가를 통해 공정가치 측정 금융자산 평가손익 계정으로 금융수익 및 금융원가로 계상되고 있습니다. 따라서, 에이치엘비의 주가가 하락할 경우, 당사의 금융자산평가손실이 발생하여 당사의 당기순이익에 부정적인 영향을 미칠 수 있습니다. 에이치엘비 주가에는 리보세라닙과 캄렐리주맙 병용요법 간암 1차 치료제가 미치는 영향이 큰 상황에서 2024년 5월 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL을 수령하였습니다. 이와 관련하여 항서제약의 CMC(의약품 생산시설 실사) 보완 및 BIMO Inspection(임상사이트 실사) 완료 시기에 대한 불확실성이 있습니다. 또한 당사는 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있어 FDA 재승인 신청 후 판매승인 시점이 지연될 경우 당사 및 당사 관계회사의 수익성과 주가에도 부정적으로 작용할 가능성이 있으니 투자자께서는 유의하시기 바랍니다. |
| 기타 투자위험 |
가. 신주의 환금성 제약 및 주가 변동에 따른 손실 위험 라. 공시서류 정정에 따른 일정 변경 위험
본 공시서류는 공시심사 과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있습니다. 마. 분석정보의 한계 및 투자판단 관련 위험 금번 유상증자를 통해 취득한 당사의 주식가치가 하락할 수 있습니다. 본 공시서류의 효력발생은 정부가 공시서류의 기재사항이 진실 또는 정확하다는 것을 인정하거나 이 유가증권의 가치를 보증 또는 승인한 것이 아니며, 기재사항은 청약일 이전에 변경될 수 있습니다. 또한 금번 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 투자자께서는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안 되며, 다양한 방면에서 신중한 검토를 병행하여 독자적으로 판단하시기 바랍니다. 바. 집단 소송 제기 위험 당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있으니 이 점 유의하시기 바랍니다. 자. 차입공매도 유상증자 참여 제한 관련 위험
금융위원회의 공매도 제도개선 관련 「자본시장과 금융투자업에 관한 법률과 시행령」이 개정되어 2021년 4월 6일부터 시행됨에 따라, 주권상장법인이 유상증자 계획을 공시한 이후 발행가격 산정을 위한 대상 거래기간의 마지막 날(발행가격 산정 기산일)까지, 해당 기업의 주식을 공매도 한 자는 증자 참여를 제한하되, 예외적인 경우에만 증자 참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 상기 사항을 위반 시 과징금 등의 제재 조치를 받을 수 있으니, 투자자께서는 이 점 유의하시기 바랍니다. 차. 재무제표 작성 기준일 이후 재무상황 변동에 따른 위험
본 공시서류 상 재무제표에 관한 사항은 2024년 1분기 재무제표 (K-IFRS 기준) 작성기준일 이후의 변동을 반영하지 않았습니다. 당사는 금번 유상증자를 진행하는 과정에서 투자 의사결정에 중대한 영향을 미칠 것으로 판단되는 변동사항을 향후에도 상세하게 반영하여 공시할 예정입니다. 그럼에도 불구하고, 당사가 중요하지 않다고 판단하여 기재 및 서술을 생략한 사항 중 당사의 기업가치에 영향을 미칠 만한 사건이 없다고 단정할 수는 없어 주기적이고 면밀한 검토가 필요합니다. 카. 개인종합자산관리계좌(ISA) 납입한도에 따른 청약제한 위험
개인종합자산관리계좌(이하 ISA 계좌)는 연간 납입가능한도 제한(연간납입한도 2,000만원, 5년간 최대 1억원까지 납입가능하며 납입한도 이월가능)이 있는 계좌입니다. ISA 계좌를 통한 신주인수권증서 보유자 청약시, 투자자별 유상증자 배정주수에 해당하는 청약증거금 납입금액이 ISA계좌 잔여납입한도를 초과할 경우 유상청약이 제한될 수 있으니, 투자자께서는 이 점 유의하시기 바랍니다. 타. 기타 투자자 유의사항
당사의 대내외적 경영환경 변화에 따라 당사 실적의 급변동이 있을 경우, 투자원금에 대한 손실이 발생할 수 있으므로, 상기 투자위험요소 및 본 공시서류에 기재된 정보에만 의존하여 투자 판단을 해서는 안되며, 투자자 여러분의 독자적인 판단에 의해야 함을 유의하시어 투자에 임하시기 바랍니다. |
2. 모집 또는 매출에 관한 일반사항
| (단위 : 원, 주) |
| 증권의 종류 |
증권수량 | 액면가액 | 모집(매출) 가액 |
모집(매출) 총액 |
모집(매출) 방법 |
|---|---|---|---|---|---|
| 보통주 | 11,005,125 | 500 | 11,890 | 130,850,936,250 | 주주배정후 실권주 일반공모 |
| 인수(주선) 여부 | 지분증권 등 상장을 위한 공모여부 | ||
|---|---|---|---|
| 인수 | 아니오 | 해당없음 | 해당없음 |
| 인수(주선)인 | 증권의 종류 |
인수수량 | 인수금액 | 인수대가 | 인수방법 | |
|---|---|---|---|---|---|---|
| 대표 | 한국투자증권 | 보통주 | 8,070,425 | 95,957,353,250 | 대표주관수수료: 모집총액의 0.2% 인수수수료 : 모집총액의 0.8% 中 15분의 11 실권수수료 : 잔액인수금액의 16.0% |
잔액인수 |
| 대표 | 케이비증권 | 보통주 | 2,934,700 | 34,893,583,000 | 인수수수료 : 모집총액의 0.8% 中 15분의 4 실권수수료 : 잔액인수금액의 16.0% |
잔액인수 |
| 청약기일 | 납입기일 | 청약공고일 | 배정공고일 | 배정기준일 |
|---|---|---|---|---|
| 2024년 06월 14일 ~ 2024년 06월 17일 | 2024년 06월 24일 | 2024년 06월 18일 | 2024년 06월 24일 | 2024년 05월 10일 |
| 청약이 금지되는 공매도 거래 기간 | |
|---|---|
| 시작일 | 종료일 |
| 2024년 03월 22일 | 2024년 06월 11일 |
| 자금의 사용목적 | |
|---|---|
| 구 분 | 금 액 |
| 채무상환자금 | 98,145,000,000 |
| 시설자금 | 6,000,000,000 |
| 운영자금 | 25,205,936,250 |
| 기타 | 1,500,000,000 |
| 발행제비용 | 1,422,534,823 |
| 신주인수권에 관한 사항 | ||
|---|---|---|
| 행사대상증권 | 행사가격 | 행사기간 |
| - | - | - |
| 매출인에 관한 사항 | ||||
|---|---|---|---|---|
| 보유자 | 회사와의 관계 |
매출전 보유증권수 |
매출증권수 | 매출후 보유증권수 |
| - | - | - | - | - |
| 일반청약자 환매청구권 | ||||
|---|---|---|---|---|
| 부여사유 | 행사가능 투자자 | 부여수량 | 행사기간 | 행사가격 |
| - | - | - | - | - |
| 【주요사항보고서】 | [정정] 주요사항보고서(유상증자결정)-2024.05.08 |
| 【기 타】 | 1) 금번 HLB생명과학의 주주배정후 실권주 일반공모 유상증자의 공동대표주관회사는 한국투자증권(주)과 케이비증권(주)입니다. 2) 금번 유상증자는 잔액인수방식에 의한 것입니다. 공동대표주관회사는 주주배정후 실권주 일반공모 후 최종실권주를 잔액인수하게 되며, 인수방법 및 인수대가에 대한 자세한 내용은 '제1부 모집 또는 매출에 관한 사항 - Ⅰ. 모집 또는 매출에 관한 일반사항 - 5. 인수 등에 관한 사항'을 참고하여 주시기 바랍니다. 3) 상기 모집가액 및 발행제비용은 1차발행가액으로 산정된 것으로 향후 변경될 수 있습니다. 확정가액은 구주주 청약 초일 전 제3거래일에 결정될 예정입니다. 4) 상기 청약기일은 구주주의 청약기일이며, 일반공모의 청약기일은 2024년 06월 19일 ~ 2024년 06월 20일(2영업일간)입니다. 일반공모 청약 공고는 2024년 06월 18일에 당사, 공동대표주관회사의 인터넷 홈페이지를 통해 게시될 예정입니다. 5) 일반공모 청약은 공동대표주관회사인 한국투자증권(주)과 케이비증권(주)의 본ㆍ지점, 홈페이지 및 HTS에서 가능합니다. 단, 구주주 청약 결과 발생한 실권주 및 단수주가 총 50,000주(액면가 500원 기준) 이하 이거나 배정하여야 할 주식의 공모금액이 1억원 이하일 경우에는 일반공모 청약을 하지 아니하고, 공동대표주관회사가 자기계산으로 인수할 수 있습니다. 6) 「자본시장과 금융투자업에 관한 법률」 제180조의4 및 동법 시행령 제208조의4제1항에 의거, 2024년 03월 22일부터 2024년 06월 11일까지 당사의 주식을 공매도 하거나 공매도 주문을 위탁한 자는 금번 모집(매출)에 청약할 수 없으며, 이를 위반하여 주식을 취득할 경우 동법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만, 모집(매출)가액의 공정한 가격형성을 저해하지 않는 경우로서 동법 시행령 제208조의4제2항 및 「금융투자업규정」 제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다. 7) 금융감독원에서 본 증권신고서를 심사하는 과정에서 정정명령 조치를 취할 수 있으며, 정정 명령 등에 따라 본 신고서에 기재된 일정이 변경될 수 있습니다. 8) 증권신고서의 효력의 발생은 본 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. |
제1부 모집 또는 매출에 관한 사항
I. 모집 또는 매출에 관한 일반사항
1. 공모개요
당사는 이사회 결의를 통하여 「자본시장과 금융투자업에 관한 법률」 제165조의6 제2항제1호에 의거 당사와 한국투자증권(주) 및 케이비증권(주)(이하 "공동대표주관회사"라 합니다.) 간에 주주배정후 실권주 일반공모에 대한 잔액인수계약을 체결하고 사전에 그 실권주를 일반에 공모하기로 하여 보통주 11,005,125주를 주주배정후 실권주 일반공모 방식으로 발행하기로 결정하였으며, 동 증권의 개요는 다음과 같습니다.
| (단위 :원, 주) |
| 증권의 종류 | 증권수량 | 액면가액 | 모집(매출)가액 | 모집(매출)총액 | 모집(매출) 방법 |
|---|---|---|---|---|---|
| 보통주 | 11,005,125 | 500 | 11,890 | 130,850,936,250 | 주주배정후 실권주 일반공모 |
| 주1) 이사회 결의일 : 2024년 03월 21일 주2) 1주의 모집가액 및 모집총액은 1차 발행가액 기준으로 한 예정금액이며, 확정되지 않은 금액입니다. |
발행가액은 「증권의 발행 및 공시 등에 관한 규정」 제5-18조에 의거 주주배정 증자시가격산정 절차 폐지 및 가격산정의 자율화에 따라 발행가격을 자유롭게 산정할 수 있으나, 시장혼란 우려 및 기존 관행 등으로 (舊) 「유가증권의 발행 및 공시등에 관한 규정」 제57조의 방식을 일부 준용하여 'Ⅰ. 모집 또는 매출에 관한 일반사항의 3. 공모가격 결정방법'에 기재된 바와 같이 산정할 예정입니다.
■ 1차 발행가액 산출 근거
본 공시서류의 1차 발행가액은 신주배정기준일 전 3거래일(2024년 05월 07일)을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액을 기준주가로 하여 할인율 25%를 적용, 아래의 산식에 의하여 산정된 발행가액으로 합니다. 단, 할인율 적용에 따른 모집가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다. (단, 호가단위 미만은 절상함)
※ 1차 발행가액 = [기준주가 * (1- 할인율) ] / [ 1 + ( 증자비율 * 할인율 )]
상기 방법에 따라 산정된 발행가액은 1차발행가액이며, 구주주 청약일전 3거래일에 확정발행가액이 결정될 예정입니다.
| [1차 발행가액 산정표] |
| 기산일 : 2024년 05월 07일 |
(단위: 원, 주) |
| 일자 | 종가 | 가중산술평균주가 | 거래량 | 거래대금 |
|---|---|---|---|---|
| 2024-05-07 | 16,250 | 16,685 | 1,171,161 | 19,540,982,430 |
| 2024-05-03 | 16,250 | 16,303 | 657,294 | 10,715,793,180 |
| 2024-05-02 | 16,580 | 17,085 | 736,554 | 12,584,305,250 |
| 2024-04-30 | 17,210 | 17,162 | 1,219,659 | 20,932,281,170 |
| 2024-04-29 | 16,800 | 16,753 | 521,535 | 8,737,120,480 |
| 2024-04-26 | 16,950 | 16,941 | 1,318,555 | 22,337,108,900 |
| 2024-04-25 | 17,480 | 17,594 | 750,794 | 13,209,780,630 |
| 2024-04-24 | 17,600 | 17,501 | 613,594 | 10,738,598,550 |
| 2024-04-23 | 17,550 | 17,499 | 765,431 | 13,394,428,780 |
| 2024-04-22 | 17,310 | 17,410 | 1,484,144 | 25,838,314,450 |
| 2024-04-19 | 16,750 | 16,451 | 664,509 | 10,931,984,200 |
| 2024-04-18 | 16,680 | 16,569 | 563,603 | 9,338,310,150 |
| 2024-04-17 | 16,270 | 16,332 | 924,358 | 15,096,841,090 |
| 2024-04-16 | 16,700 | 16,479 | 708,552 | 11,676,522,980 |
| 2024-04-15 | 16,790 | 16,514 | 1,022,483 | 16,885,537,830 |
| 2024-04-12 | 16,280 | 16,151 | 785,616 | 12,688,307,940 |
| 2024-04-11 | 16,100 | 16,376 | 912,394 | 14,941,193,660 |
| 2024-04-09 | 16,500 | 16,912 | 2,429,860 | 41,093,223,920 |
| 2024-04-08 | 17,000 | 16,739 | 3,619,964 | 60,593,835,760 |
| 1개월 거래량 가중산술평균주가 (A) | 16,832 | - | ||
| 1주일 거래량 가중산술평균주가 (B) | 16,702 | - | ||
| 기산일 종가(C) | 16,250 | - | ||
| (A),(B),(C)의 산술 평균 (D) | 16,595 | (A+B+C)/3 | ||
| 기준주가 (E) | 16,250 | (C와 D중 낮은가액) | ||
| 할인율 (F) | 25.0% | - | ||
| 증자비율 (G) | 10.22% | - | ||
| 1차 발행가액 (호가단위 미만은 호가단위로 절상,액면가액 이하일 경우 액면가액을발행가액으로 함) |
11,890 | 기준주가 × (1-할인율) / (1+유상증자비율 × 할인율 ) |
||
■ 공모일정 등에 관한 사항
당사는 2024년 03월 21일 이사회를 통해 유상증자 결의를 하였으며, 세부 일정은 다음과 같습니다
| [주요일정] |
| 날짜 | 업 무 내 용 | 비고 |
|---|---|---|
| 2024년 03월 21일 | 이사회결의 | 주요사항보고서 제출 |
| 2024년 03월 21일 | 증권신고서(예비투자설명서) 제출 | - |
| 2024년 03월 22일 | 신주발행공고 및 기준일 공고 | 당사 인터넷 홈페이지 (http://www.hlb-ls.com) |
| 2024년 05월 07일 | 1차 발행가액 확정 | 신주배정기준일 전 제3거래일 |
| 2024년 05월 09일 | 권리락 | 신주배정기준일 전 제1거래일 |
| 2024년 05월 10일 | 유상증자 신주배정기준일(주주확정) | - |
| 2024년 05월 22일 | 신주배정 통지 | - |
| 2024년 05월 29일 ~ 2024년 06월 04일 |
신주인수권증서 상장 및 거래 기간 | 5거래일 이상 동안 거래 |
| 2024년 06월 05일 | 신주인수권증서 상장폐지 | 신주인수권증서 상장폐지일과 구주주청약 초일 사이 5거래일 확보 |
| 2024년 06월 11일 | 확정 발행가액 산정 | 구주주 청약초일 3거래일 전 |
| 2024년 06월 12일 | 확정 발행가액 확정 공고 | 당사 인터넷 홈페이지 (http://www.hlb-ls.com) |
| 2024년 06월 14일 ~ 2024년 06월 17일 |
구주주 청약 | - |
| 2024년 06월 18일 | 일반공모청약 공고 | 당사 인터넷 홈페이지 (http://www.hlb-ls.com) 한국투자증권 홈페이지(http://www.truefriend.com) 케이비증권 홈페이지(http://www.kbsec.com) |
| 2024년 06월 19일 ~ 2024년 06월 20일 |
일반공모청약 | - |
| 2024년 06월 24일 | 주금납입/환불/배정공고 | - |
| 2024년 07월 08일 | 유상증자 신주상장 예정일 | - |
|
주1) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. |
2. 공모방법
| [공모방법 : 주주배정후 실권주 일반공모] |
| 모 집 대 상 | 주식수 | 비 고 |
|---|---|---|
| 구주주 청약 (신주인수권증서 보유자 청약) |
11,005,125주 (100%) |
- 구주 1주당 신주 배정비율 : 1주당 0.1022963299주 - 신주배정기준일 : 2024년 05월 10일 - 구주주 청약일 : 2024년 06월 14일 ~ 2024년 06월 17일 (2영업일간) - 보유한 신주인수권증서의 수량 한도로 청약가능(구주주에게는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율을 곱한 수량만큼의 신주인수권 증서가 배정됨) |
| 초과 청약 | - | - 「자본시장과 금융투자업에 관한 법률」 제165조의6 제2항제2호에 의거 초과청약 - 초과청약비율 : 배정신주(신주인수권증서) 1주당 0.2 - 신주인수권증서 거래를 통해서 신주인수권증서를 매매시 보유자 기준으로 초과청약 가능 |
| 일반모집 청약 (고위험고수익투자신탁등, 벤처기업투자신탁 청약 포함) |
- | - 구주주 청약 후 발생하는 단수주 및 실권주에 대해 배정됨 - 일반공모 청약일 : 2024년 06월 19일 ~ 2024년 06월 20일(2영업일간) |
| 합 계 | 11,005,125주 (100%) |
- |
|
주1) 본 건 유상증자는 주주배정후 실권주 일반공모 방식으로 진행되며, 구주주 청약결과 발생하는 실권주 및 단수주는 우선적으로 초과청약자에게 배정되며, 이후 실권이 발생할 경우에 대해서는 일반에게 공모합니다. ① 모집(매출)에 따른 주식 취득이 금지되는 공매도 거래 기간 중에 전체 공매도 주문수량보다 많은 수량의 주식을 가격경쟁에 의한 거래 방식으로 매수한 경우 (매매계약 체결일 기준으로 정규시장의 매매거래시간에 매수한 경우로 한정) ② 한국거래소의 증권시장업무규정 또는 파생상품시장업무규정에서 정한 유동성 공급 및 시장조성 목적을 위해 해당 주식을 공매도하거나 공매도 주문을 위탁한 경우 ③ 동일한 법인 내에서 모집(매출)에 따른 주식 취득 참여가 금지되는 공매도 거래 기간 중 공매도를 하지 않거나 공매도 주문을 위탁하지 않은 독립거래단위*가 모집(매출)에 따른 주식을 취득하는 경우 * 금융투자업규정 제6-30조 제5항에 따라 의사결정이 독립적이고 상이한 증권계좌를 사용하는 등의 요건을 갖춘 거래단위 |
▶ 구주주 1주당 배정비율 산출근거
| 구분 | 상세내역 |
|---|---|
| A. 보통주식 | 107,650,759 |
| B. 우선주식 | - |
| C. 발행주식총수 (A + B) | 107,650,759 |
| D. 자기주식 + 자기주식신탁 | 69,920 |
| E. 자기주식을 제외한 발행주식총수 (C - D) | 107,580,839 |
| F. 유상증자 주식수 | 11,005,125 |
| G. 증자비율 (F / C) | 10.22% |
| H. 우리사주조합 배정주식수 (F X 0%) | - |
| I. 구주주 배정주식수 ((F-H) | 11,005,125 |
| J. 구주주 1주당 배정주식수 (I/E) | 0.1022963299 |
| 주1) 신주배정기준일 전 주식관련사채 및 종류주식의 권리행사, 주식매수선택권의 행사 등으로 구주주 1주당 배정비율이 변경될 수 있습니다. 주2) 제9회차 신주인수권부사채 권리행사에 따라 기발행주식수 및 배정비율은 지속적으로 변경될 수 있으며, 확정 기발행주식수 및 배정비율은 신주배정기준일 익일 증권신고서 정정 공시를 통해 반영할 예정입니다. |
3. 공모가격 결정방법
■ 확정 발행가액 산정
「증권의발행및공시등에관한규정」 제5-18조 (유상증자의 발행가액 결정)에 의거, 주주배정 및 주주우선공모증자시 할인율 등이 자율화 되어 발행가는 자유롭게 산정할 수 있으나, 시장혼란 우려 및 기존 관행 등으로 (舊)「유가증권발행및공시등에관한 규정」 제 57조의 방식을 일부 준용하여 발행가액을 산정합니다.
① 1차 발행가액 산정 : 신주배정기준일전 제 3거래일을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액을 기준주가로 하여 할인율 25%를 적용,다음의 산식에 의하여 산정된 발행가액을 1차 발행가액으로 합니다. 단, 호가단위 미만은 절상하며, 1주당 발행가액이 액면가 미만일 경우에는 액면가로 합니다.
기준주가 ×【 1 - 할인율(25%)】 |
||
| ▶ 1차 발행가액 | = | ------------------------------------- |
1 + 【증자비율 × 할인율(25%)】 |
② 2차 발행가액 산정 : 2차발행가액은 구주주 청약일전 제 3거래일을 기산일로 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액에 동일한 할인율(25%)을 적용하여 다음의 산식에 의하여 산정한 발행가액으로 합니다.
단, 호가단위 미만은 절상하며, 1주당 발행가액이 액면가 미만일 경우에는 액면가로 합니다.
▶ 2차 발행가액 = 기준주가 ×【1 - 할인율(25%)】
③ 확정 발행가액 산정 : 확정발행가액은 ① 의 1차발행가액과 ② 의 2차발행가액 중 낮은 가액으로 합니다. 단, 「자본시장과 금융투자업에관한법률」 제165조의6 및 「증권의 발행 및 공시에 관한 규정」제5-15조의2의 산출근거에 의거, 청약일 전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가를 기준주가로 할인율 40% 적용하여 산정한 가액이 ① 의 1차발행가액과 ② 의 2차발행가액 중 낮은 가액을 초과하는 경우 동 금액을 확정 발행가액으로 합니다. (단, 호가단위 미만은 절상함)
▶ 확정 발행가액 = Max{Min[1차 발행가액, 2차 발행가액], 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가의 60%}
④ 모집가액 확정공시에 관한 사항 : 1차 발행가액은 신주배정기준일 전 제3거래일(2024년 05월 07일)에 결정되어 2024년 05월 08일에 금융감독원 전자공시시스템에 공시될 예정이며, 확정 발행가액은 구주주청약일전 제3거래일(2024년 06월 11일)에 결정되어 2024년 06월 12일에 금융감독원 전자공시시스템에 공시될 예정이며, 정관에서 정한 당사 인터넷 홈페이지(http://www.hlb-ls.com)에 공고하여 개별통지에 갈음할 예정입니다. 확정 발행가액 결정에 따라 정정 신고서(증권발행조건확정)가 금융감독원 전자공시시스템에 공시 됩니다.
※ 일반공모 발행가액은 구주주 청약시에 적용된 확정 발행가액을 동일하게 적용합니다.
4. 모집 또는 매출절차 등에 관한 사항
가. 모집 또는 매출조건
| (단위 : 주, 원) |
| 항 목 | 내 용 | |||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 모집 또는 매출주식의 수 | 11,005,125 | |||||||||||||||||||||||||||||||||||
| 주당 모집가액 또는 매출가액 |
예정가액 | 11,890 | ||||||||||||||||||||||||||||||||||
| 확정가액 | - | |||||||||||||||||||||||||||||||||||
| 모집총액 또는 매출총액 |
예정가액 | 130,850,936,250 | ||||||||||||||||||||||||||||||||||
| 확정가액 | - | |||||||||||||||||||||||||||||||||||
| 청 약 단 위 |
(1) "구주주"의 청약단위는 10주로 하며, 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식수에 신주배정비율("주주 배정분"에 해당하는 주식수를 자기주식을 제외한 발행주식 총수로 나눈 비율을 말하며, 자기주식과 발행주식총수는 신주배정기준일 현재의 주식수를 말한다)을 곱하여 산정된 배정주식수로 합니다. 다만, 신주배정기준일 전 주식관련사채 및 종류주식의 권리행사, 주식매수선택권의 행사 등으로 1주당 배정비율이 변경될 수 있습니다.(단, 1주 미만은 절사합니다). 제9회차 신주인수권부사채 권리행사에 따라 배정비율은 지속적으로 변경될 수 있으며, 확정 배정비율은 신주배정기준일 익일 증권신고서 정정 공시를 통해 반영할 예정입니다.
|
|||||||||||||||||||||||||||||||||||
| 청약기일 | 구주주 (신주인수권증서 보유자) |
개시일 | 2024년 06월 14일 | |||||||||||||||||||||||||||||||||
| 종료일 | 2024년 06월 17일 | |||||||||||||||||||||||||||||||||||
| 일반모집 또는 매출 | 개시일 | 2024년 06일 19일 | ||||||||||||||||||||||||||||||||||
| 종료일 | 2024년 06월 20일 | |||||||||||||||||||||||||||||||||||
| 청약 증거금 |
구주주(신주인수권증서 보유자) | 청약금액의 100% | ||||||||||||||||||||||||||||||||||
| 초 과 청 약 | 청약금액의 100% | |||||||||||||||||||||||||||||||||||
| 일반모집 또는 매출 | 청약금액의 100% | |||||||||||||||||||||||||||||||||||
| 납 입 기 일 | 2024년 06월 24일 | |||||||||||||||||||||||||||||||||||
| 배당기산일(결산일) | 2024년 01월 01일 | |||||||||||||||||||||||||||||||||||
| 주1) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정 요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. 주2) 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
나. 모집 또는 매출의 절차
(1) 공고의 일자 및 방법
| 구 분 | 공고일자 | 공고방법 |
|---|---|---|
| 신주발행공고 및 배정기준일(주주확정일) 공고 |
2024년 03월 22일 | 당사 인터넷 홈페이지 (http://www.hlb-ls.com) |
| 모집가액 확정의 공고 | 2024년 06월 12일 | 당사 인터넷 홈페이지 (http://www.hlb-ls.com) |
| 실권주 일반공모 청약공고 | 2024년 06월 18일 | 당사 인터넷 홈페이지 (http://www.hlb-ls.com) 한국투자증권(주) 홈페이지 (http://www.truefriend.com) 케이비증권(주) 홈페이지 (http://www.kbsec.com) |
| 실권주 일반공모 배정공고 | 2024년 06월 24일 | 한국투자증권(주) 홈페이지 (http://www.truefriend.com) 케이비증권(주) 홈페이지 (http://www.kbsec.com) |
| 주1) 청약결과 초과청약금 환불에 대한 통지는 공동대표주관회사 홈페이지에 게시함으로써 개별통지에 갈음합니다. 주2) 전산장애 또는 그 밖의 부득이한 사유로 회사의 인터넷 홈페이지(http://www.hlb-ls.com)에 공고를 할 수 없는 때에는 서울특별시에서 발행되는 일간 한국경제신문에 게재할 예정입니다. |
(2) 청약방법
① 구주주 청약(신주인수권증서 보유자 청약) : 구주주 중 주권을 증권회사에 예탁한 주주(기존 "실질주주". 이하 "일반주주"라 합니다.)는 주권을 예탁한 증권회사의 본·지점 및 공동대표주관회사의 본ㆍ지점에서 청약할 수 있습니다. 다만, 구주주 중 명의개서대행기관 특별계좌에 주식을 가지고 있는 주주(기존 "명부주주". 이하 "특별계좌 보유자"라 합니다.)는 신주배정통지서를 첨부하여 실명확인증표를 제시한 후 공동대표주관회사의 본ㆍ지점에서 청약할 수 있습니다. 청약 시에는 소정의 청약서 2통에 필요한 사항을 기입하여 청약증거금과 함께 제출하여야 합니다.
| 2019년 09월 16일 전자증권제도가 시행되며, 주권 상장법인의 상장주식은 전자증권 의무전환대상으로 전자증권제도 시행일에 전자증권으로 일괄전환됩니다. 전자증권제도 시행전까지 증권회사에 예탁하고 있는 실질주주 주식은 해당 증권회사 계좌에 전자증권으로 일괄 전환되며, 기존 명부주주가 보유한 주식은 명의개서대행기관이 개설하는 특별계좌에 발행되어 소유자별로 관리됩니다. 금번 유상증자시 신주인수권증서는 전자증권제도 시행일 이후에 발행되고 상장될 예정으로 전자증권으로 발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다. '특별계좌 보유자(기존 '명부주주')'는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후 금번 유상증자 청약 참여또는 신주인수권증서의 매매가 가능합니다. '특별계좌 보유자(기존 '명부주주')'는 신주인수권증서의 '일반 전자등록계좌(증권회사 계좌)'로 이전 없이 공동대표주관회사인 한국투자증권(주)과 케이비증권(주)의 본ㆍ지점에서 직접 청약하는 방법으로도 금번 유상증자에 청약이 가능합니다. 다만 신주인수권증서의 매매는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후에만 가능하므로 이 점 유의하시기 바랍니다. |
|
「주식ㆍ사채 등의 전자등록에 관한 법률」 |
② 초과청약 : 신주인수권증서 청약을 한자에 한하여 신주인수권증서 청약 한도 주식수의 20%를 추가로 청약할 수 있습니다. 이때, 신주인수권증서 청약 한도주식수의 20%에 해당하는 주식 중 소수점 이하인 주식은 청약할 수 없습니다.
a. 청약한도 주식수 = 신주인수권증서청약 한도주식수 + 초과청약한도 주식수
b. 신주인수권증서청약 한도주식수 = 보유한 신주인수권 증서의 수량
c. 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 * 초과청약 비율(20%)
③ 일반공모 청약: 고위험고수익투자신탁등, 벤처기업투자신탁 및 일반청약자는「금융실명거래 및 비밀보장에 관한 법률」의 규정에 의한 실명자이어야 하며, 청약사무 취급처에 실명확인증표를 제시하고 청약합니다. 고위험고수익투자신탁등, 벤처기업투자신탁 및 일반청약자의 청약 시, 한 개의 청약처에서 이중청약은 불가능합니다. 또한 고위험고수익투자신탁등은 청약 시, 청약사무 취급처에 「증권 인수업무 등에 관한 규정」 제2조 제18호에 따른 요건을 충족함을 확약하는 서류 및 자산총액이 기재되어 있는 서류를 함께 제출하여야 합니다. 벤처기업투자신탁은 청약 시, 청약사무 취급처에 「증권 인수업무 등에 관한 규정」 제2조 제20호에 따른 요건을 충족하고, 제9조제10항에 따른 확약서 및 자산총액이 기재되어 있는 서류를 함께 제출하여야 합니다.
④ 청약은 청약주식의 단위에 따라 할 수 있으며 1인당 청약한도를 초과하는 청약부분에 대하여는 청약이 없는 것으로 하고, 청약사무취급처는 그 차액을 납입일에 당해 청약자에게 반환하며, 이때 받은 날부터의 이자는 지급하지 않습니다.
⑤ 본 유상증자에 청약하고자 하는 투자자(「자본시장과 금융투자업에 관한 법률」 제9조 제5항에 규정된 전문투자자 및 「자본시장과 금융투자업에 관한 법률 시행령」 제132조에 따라 투자설명서의 교부가 면제되는자 제외)는 청약 전 반드시 투자설명서를 교부 받아야 하고, 이를 확인하는 서류에 서명 또는 기명날인하여야 합니다.
⑥ 청약한도
a. 구주주의 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율인 0.1022963299주를 곱하여 산정된 신주인수권증서(단, 1주 미만은 절사)와 초과청약가능 주식수(보유하고 있는 신주인수권증서 1주당 0.2주를 곱하여 산정된 수, 단 1주 미만은 절사)를 합한 주식수로 하되, 신주배정기준일 전 주식관련사채 및 종류주식의 권리행사, 주식매수선택권의 행사 등으로 구주주의 1주당 배정비율은 변경될 수 있습니다. 제9회차 신주인수권부사채 권리행사에 따라 배정비율은 지속적으로 변경될 수 있으며, 확정 배정비율은 신주배정기준일 익일 증권신고서 정정 공시를 통해 반영할 예정입니다.
b. 일반공모 청약자의 청약한도는 일반공모 총 공모주식 100% 범위 내로 하며, 청약한도를 초과하는 부분에 대해서는 청약이 없는 것으로 간주합니다.
⑦ 기타
a. 일반공모 배정을 함에 있어 이중청약이 있는 경우에는 그 청약자의 청약 전부를 청약하지 아니한 것으로 봅니다. 단, 구주주가 신주배정비율에 따라 배정받은 주식을 청약한 후 일반공모에 참여하는 경우에는 금지되는 이중청약이 있는 경우로 보지 않습니다. 단, 동일한 집합투자기구라도 운용주체(집합투자업자)가 다른 경우는 예외로 합니다.
b. 1인당 청약한도를 초과하는 청약부분에 대하여는 청약이 없는 것으로 합니다.
c. 청약자는 '금융실명거래 및 비밀보장에 관한 법률'에 의거 실지 명의에 의해 청약해야 합니다.
d. 「자본시장과 금융투자업에 관한 법률」 제180조의4 및 같은 법 시행령 제208조의4 제1항에 따라 2024년 03월 22일부터 2024년 06월 11일까지 공매도를 하거나 공매도 주문을 위탁한 자는 금번 모집(매출)에 청약할 수 없으며, 이를 위반하여 주식을 취득할 경우 같은 법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만 모집(매출)가액의 공정한 가격형성을 저해하지 않는 경우로서 같은 법 시행령 제208조의4제2항 및 「금융투자업규정」 제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다.
|
※ 예외적으로 모집(매출)에 따른 주식 취득이 허용되는 경우 ① 모집(매출)에 따른 주식 취득이 금지되는 공매도 거래 기간 중에 전체 공매도 주문수량보다 많은 수량의 주식을 가격경쟁에 의한 거래 방식으로 매수한 경우 (매매계약 체결일 기준으로 정규시장의 매매거래시간에 매수한 경우로 한정) ② 한국거래소의 증권시장업무규정 또는 파생상품시장업무규정에서 정한 유동성 공급 및 시장조성 목적을 위해 해당 주식을 공매도하거나 공매도 주문을 위탁한 경우 ③ 동일한 법인 내에서 모집(매출)에 따른 주식 취득 참여가 금지되는 공매도 거래 기간 중 공매도를 하지 않거나 공매도 주문을 위탁하지 않은 독립거래단위(*)가 모집(매출)에 따른 주식을 취득하는 경우 (*) 「금융투자업규정」 제6-30조 제5항에 따라 의사결정이 독립적이고 상이한 증권계좌를 사용하는 등의 요건을 갖춘 거래단위 |
(3) 청약취급처
| 청약대상자 | 청약취급처 | 청약일 | |
|---|---|---|---|
| 구주주 (신주인수권증서 보유자) |
특별계좌 보유자 (기존 '명부주주') |
1) 한국투자증권(주)의 본ㆍ지점 2) 케이비증권(주)의 본ㆍ지점 |
2024년 06월 14일 ~ 2024년 06월 17일 |
| 일반주주 (기존 '실질주주') |
1) 주주확정일 현재 주식회사 에이치엘비생명과학의 주식을 예탁하고 있는 당해 증권회사 본ㆍ지점 2) 한국투자증권(주)의 본ㆍ지점 3) 케이비증권(주)의 본ㆍ지점 |
||
| 일반공모청약 (고위험고수익투자신탁등 및 벤처기업투자신탁청약 포함) |
1) 한국투자증권(주)의 본ㆍ지점 2) 케이비증권(주)의 본ㆍ지점 |
2024년 06월 19일 ~ 2024년 06월 20일 |
|
(4) 청약결과 배정방법
1) 구주주(신주인수권증서 보유자) 청약 : '신주배정기준일' 18:00 현재 주주명부에 등재된 주주(이하 "구주주"라 한다)에게 본 주식을 1주당 0.1022963299주를 곱하여 산정된 배정주식수(단, 1주 미만은 절사함)로 하고, 배정범위 내에서 청약한 수량만큼 배정합니다. 단, 신주배정기준일 전 주식관련사채 및 종류주식의 권리행사, 주식매수선택권의 행사 등으로 1주당 배정주식수가 변경될 수 있습니다.
2) 초과청약 : 구주주(신주인수권증서 보유자) 청약 이후 발생한 실권주가 있는 경우, 실권주를 구주주(신주인수권증서 보유자)가 초과청약(초과청약비율 : 배정 신주 1주당 0.2주)한 주식수에 비례하여 배정하며, 1주 미만의 주식은 절사하여 배정하지 않습니다. (단, 초과청약 주식수가 실권주에 미달한 경우 100% 배정)
(i) 청약한도 주식수 = 신주인수권증서청약 한도주식수 + 초과청약한도 주식수
(ii) 신주인수권증서청약 한도주식수 = 보유한 신주인수권 증서의 수량
(iii) 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 x 초과청약 비율(20%)
3) 일반공모 청약 : 상기 구주주 청약 및 초과청약 결과 발생한 실권주 및 단수주(이하 "일반공모 배정분"이라 한다)는 "공동대표주관회사"가 다음 각호와 같이 일반에게 공모하되, 「증권 인수업무 등에 관한 규정」 제9조 제2항 제3호에 따라 고위험고수익투자신탁등에 공모주식의 10%를 배정하고, 「증권 인수업무 등에 관한 규정」 제9조 제2항 제4호에 따라 벤처기업투자신탁에 공모주식의 25%를 배정한다. 나머지 65%에 해당하는 주식은 개인청약자 및 기관투자자(집합투자업자 포함)에게 구분 없이 배정한다. 고위험고수익투자신탁등에 대한 공모주식 10%와 벤처기업투자신탁에 공모주식의 25%와 개인투자자 및 기관투자자에 대한 공모주식 65%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정한다. 다만, 어떤 그룹에 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정한다.
(i) 일반공모에 관한 배정수량 계산시“공동대표주관회사”의“청약물량”(“공동대표주관회사”의 각 청약처에서 일반공모 방식으로 접수를 받은 청약주식수를 의미하며, “공동대표주관회사”에 대하여 개별적으로 산정한 청약주식수를 말한다)에 대해서는“공동대표주관회사”의“총청약물량”(“공동대표주관회사”가 일반공모 방식으로 접수를 받은“청약물량”의 합을 말한다)을“일반공모 배정분” 주식수로 나눈 통합청약경쟁률에 따라“공동대표주관회사”의 각 청약자에 배정하는 방식(이하“통합배정”이라 한다)으로 한다.
(ii) 일반공모 청약결과 일반공모 총 청약자의 청약주식수가 일반공모 배정분을 초과하는 경우에는 청약경쟁률에 따라5사6입을 원칙으로 안분 배정하여 잔여주식이 최소화되도록 한다. 이후 최종 잔여주식은 최대청약자부터 순차적으로 우선 배정하되, 동순위 최고청약자가 최종 잔여 주식보다 많은 경우에는 “공동대표주관회사”가 합리적으로 판단하여 배정한다.
(iii) 일반공모 청약결과 일반공모 총 청약자의 청약주식수가 일반공모 배정분에 미달하는 경우에는 청약주식수대로 배정한다. 배정결과 발생하는 잔여주식은“공동대표주관회사”가 제2조 제3항에 따라 인수한다. 단, “공동대표주관회사” 중 “청약초과회사”(“청약물량”이“인수한도 의무주식수”를 초과하는 회사를 말한다)가 있는 경우, “초과청약물량” (“청약초과회사”의 “청약물량”에서 “인수한도 의무주식수”를 차감한 주식수를 의미하되, 0이상으로 한다)을“청약미달회사” (“청약물량”이 “인수한도 의무주식수”보다 적은 회사를 말한다)에게 배분하여 산정한다.
(iv) 단, “공동대표주관회사”는 “증권 인수업무 등에 관한 규정” 제9조 제2항에 의거 고위험고수익투자신탁등, 벤처기업투자신탁 및 일반청약자에 대하여 배정하여야 할 주식이 50,000주 이하(액면가500원 기준)이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 청약자에게 배정하지 아니할 수 있다. 이 경우 “공동대표주관회사”가 잔여주식을 자기 계산으로 인수한다.
(5) 투자설명서 교부에 관한 사항
- 「자본시장과 금융투자업에 관한 법률」 제124조에 의거, 본 주식의 청약에 대한 투자설명서 교부 의무는 에이치엘비생명과학(주), 공동대표주관회사인 한국투자증권(주)와 케이비증권(주)가 부담하며, 금번 유상증자의 청약에 참여하시는 투자자께서는 투자설명서를 의무적으로 교부받으셔야 합니다.
- 금번 유상증자에 청약하고자 하는 투자자께서는 (「자본시장과 금융투자업에 관한 법률」 제9조 제5항에 규정된 전문투자자 및 「자본시장과 금융투자업에 관한 법률 시행령」 제132조에 따라 투자설명서의 교부가 면제되는 자 제외) 청약하시기 전 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
- 투자설명서 수령거부 의사 표시는 서면, 전화ㆍ전신ㆍFAX, 전자우편 및 이와 비슷한 전자통신으로만 하여야 합니다.
① 투자설명서 교부 방법 및 일시
| 구분 | 교부방법 | 교부일시 |
|---|---|---|
|
구주주 청약자 |
1),2),3)을 병행 1) 등기우편 송부 2) "공동대표주관회사"의 본ㆍ지점 교부 3) "공동대표주관회사"의 홈페이지나 HTS, MTS에서 교부 |
1) 우편송부시 : 구주주청약초일인 2024년 06월 14일 전 수취 가능 2) "공동대표주관회사"의 본ㆍ지점 : 청약종료일 (2024년 06월 17일)까지 3) "공동대표주관회사”의 홈페이지 또는 HTS, MTS 교부 |
|
일반 청약자 |
1), 2)를 병행 1) "공동대표주관회사"의 본ㆍ지점에서 교부 2) "공동대표주관회사"의 홈페이지나 HTS, MTS 에서 교부 |
1) "공동대표주관회사"의 본ㆍ지점 2) "공동대표주관회사"의 홈페이지 또는 HTS, MTS 교부 |
| ※ 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다. |
② 확인절차
a. 우편을 통한 투자설명서 수령시
- 청약하시기 위해 지점을 방문하셨을 경우, 직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
- HTS 또는 MTS를 통한 청약을 원하시는 경우, 청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
- 주주배정 유상증자 경우 유선청약이 가능합니다. 유선상으로 신분확인을 하신 후, 투자설명서 교부 확인을 해주시고 청약을 진행하여 주시기 바랍니다.
b. 지점 방문을 통한 투자설명서 수령시
직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
c. 홈페이지, HTS 또는 MTS를 통한 교부
청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
③ 기타
a. 금번 유상증자의 경우, 본 증권신고서의 효력발생 이후 주주명부상 주주에게 투자설명서를 우편으로 발송할 예정입니다. 우편의 반송 등에 의한 사유로 교부를 받지 못하신 투자자께서는, 한국투자증권(주) 및 케이비증권(주)의 본ㆍ지점 방문을 통해 인쇄물을 받으실 수 있으며, 또한 동일한 내용의 투자설명서를 전자문서의 형태로 한국투자증권(주)의 홈페이지에서 다운로드 받으실 수 있습니다. 한편, 일반공모 청약시 투자자께서는 공동대표주관회사에 방문하여 투자설명서 인쇄물을 수령하시거나 공동대표주관회사의 홈페이지에서 동일한 내용의 투자설명서를 전자문서의 형태로 다운로드 받으시는 2가지 방법으로 투자설명서를 교부받으실 수 있습니다. 다만, 전자문서의 형태로 교부 받으실 경우, 「자본시장과 금융투자업에 관한 법률」 제124조 제1항 각호의 요건을 모두 충족해야만 청약이 가능합니다.
b. 구주주 청약시 공동대표주관회사 이외의 증권회사를 이용한 청약 방법
- 해당 증권회사의 청약방법 및 규정에 의해 청약을 진행하시기 바랍니다. 이 경우에도, 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
※ 투자설명서 교부를 받지 않거나, 수령거부의사를 서면 등의 방법으로 표시하지 않을 경우, 본 유상증자의 청약에 참여할 수 없습니다.
|
※ 관련법규 「자본시장과 금융투자업에 관한 법률」 1. 국가 2. 한국은행 3. 대통령령으로 정하는 금융기관 4. 주권상장법인. 다만, 금융투자업자와 장외파생상품 거래를 하는 경우에는 전문투자자와 같은 대우를 받겠다는 의사를 금융투자업자에게 서면으로 통지하는 경우에 한한다. 5. 그 밖에 대통령령으로 정하는 자
1. 전자문서에 의하여 투자설명서를 받는 것을 전자문서를 받을 자(이하 "전자문서수신자"라 한다)가 동의할 것 2. 전자문서수신자가 전자문서를 받을 전자전달매체의 종류와 장소를 지정할 것 3. 전자문서수신자가 그 전자문서를 받은 사실이 확인될 것 4. 전자문서의 내용이 서면에 의한 투자설명서의 내용과 동일할 것 ② 누구든지 증권신고의 대상이 되는 증권의 모집 또는 매출, 그 밖의 거래를 위하여 청약의 권유 등을 하고자 하는 경우에는 다음 각 호의 어느 하나에 해당하는 방법에 따라야 한다. 1. 제120조제1항에 따라 증권신고의 효력이 발생한 후 투자설명서를 사용하는 방법 2. 제120조제1항에 따라 증권신고서가 수리된 후 신고의 효력이 발생하기 전에 발행인이 대통령령으로 정하는 방법에 따라 작성한 예비투자설명서(신고의 효력이 발생되지 아니한 사실을 덧붙여 적은 투자설명서를 말한다. 이하 같다)를 사용하는 방법 3. 제120조제1항에 따라 증권신고서가 수리된 후 신문ㆍ방송ㆍ잡지 등을 이용한 광고, 안내문ㆍ홍보전단 또는 전자전달매체를 통하여 발행인이 대통령령으로 정하는 방법에 따라 작성한 간이투자설명서(투자설명서에 기재하여야 할 사항 중 그 일부를 생략하거나 중요한 사항만을 발췌하여 기재 또는 표시한 문서, 전자문서, 그 밖에 이에 준하는 기재 또는 표시를 말한다. 이하 같다)를 사용하는 방법 ③ 집합투자증권의 경우 제2항에도 불구하고 간이투자설명서를 사용할 수 있다. 다만, 투자자가 제123조에 따른 투자설명서의 사용을 별도로 요청하는 경우에는 그러하지 아니하다. <신설 2013. 5. 28.> ④ 제1항 및 제3항에 따라 집합투자증권의 간이투자설명서를 교부하거나 사용하는 경우에는 투자자에게 제123조에 따른 투자설명서를 별도로 요청할 수 있음을 알려야 한다. <신설 2013. 5. 28.>
1. 다음 각 목의 어느 하나에 해당하는 전문가 가. 전문투자자 나. 삭제 <2016. 6. 28.> 다. 「공인회계사법」에 따른 회계법인 라. 신용평가회사(법 제335조의3에 따라 신용평가업인가를 받은 자를 말한다. 이하 같다) 마. 발행인에게 회계, 자문 등의 용역을 제공하고 있는 공인회계사ㆍ감정인ㆍ변호사ㆍ변리사ㆍ세무사 등 공인된 자격증을 가지고 있는 자 바. 그 밖에 발행인의 재무상황이나 사업내용 등을 잘 알 수 있는 전문가로서 금융위원회가 정하여 고시하는 자 2. 다음 각 목의 어느 하나에 해당하는 연고자 가. 발행인의 최대주주[「금융회사의 지배구조에 관한 법률」 제2조제6호가목에 따른 최대주주를 말한다. 이 경우 "금융회사"는 "법인"으로 보고, "발행주식(출자지분을 포함한다. 이하 같다)"은 "발행주식"으로 본다. 이하 같다]와 발행주식 총수의 100분의 5 이상을 소유한 주주 나. 발행인의 임원(「상법」 제401조의2제1항 각 호의 자를 포함한다. 이하 이 호에서 같다) 및 「근로복지기본법」에 따른 우리사주조합원 다. 발행인의 계열회사와 그 임원 라. 발행인이 주권비상장법인(주권을 모집하거나 매출한 실적이 있는 법인은 제외한다)인 경우에는 그 주주 마. 외국 법령에 따라 설립된 외국 기업인 발행인이 종업원의 복지증진을 위한 주식매수제도 등에 따라 국내 계열회사의 임직원에게 해당 외국 기업의 주식을 매각하는 경우에는 그 국내 계열회사의 임직원 바. 발행인이 설립 중인 회사인 경우에는 그 발기인 사. 그 밖에 발행인의 재무상황이나 사업내용 등을 잘 알 수 있는 연고자로서 금융위원회가 정하여 고시하는 자 제132조(투자설명서의 교부가 면제되는 자) 1. 제11조제1항제1호다목부터 바목까지 및 같은 항 제2호 각 목의 어느 하나에 해당하는 자 1의2. 제11조제2항제2호 및 제3호에 해당하는 자 2. 투자설명서를 받기를 거부한다는 의사를 서면, 전화ㆍ전신ㆍ팩스, 전자우편 및 이와 비슷한 전자통신, 그 밖에 금융위원회가 정하여 고시하는 방법으로 표시한 자 3. 이미 취득한 것과 같은 집합투자증권을 계속하여 추가로 취득하려는 자. 다만, 해당 집합투자증권의 투자설명서의 내용이 직전에 교부한 투자설명서의 내용과 같은 경우만 해당한다. |
(6) 주권 유통에 관한 사항
- 주권유통개시(예정)일: 2024년 07월 08일(유상증자 신주) (2019년 9월 16일 전자증권제도가 시행됨에 따라 실물 주권의 교부 없이 등록발행되어 각 주주의 보유 증권계좌로 상장일에 입고되며, 상장일부터 유통이 가능합니다. 단, 유관기관과의 업무 협의 과정에서 상기 일정은 변경될 수 있음을 유의하시기 바랍니다.)
(7) 청약증거금의 대체 및 반환 등에 관한 사항
- 청약증거금은 청약금액의 100%로 하고, 주금납입기일에 주금납입금으로 대체하며, 청약증거금에 대해서는 무이자로 합니다. 일반공모 총 청약주식수(기관투자자 포함)가 일반공모주식수를 초과하여 청약증거금이 발생한 경우, 그 초과 청약증거금은 2024년 06월 24일부터 해당 청약사무 취급처에서 환불합니다.
(8) 주금납입장소 : 하나은행 구로디지털금융센터
다. 신주인수권증서에 관한 사항
| 신주배정기준일 | 신주인수권증서의 매매 금융투자업자 | |
|---|---|---|
| 회사명 | 회사고유번호 | |
| 2024년 05월 10일 | 한국투자증권(주) | 00160144 |
| 케이비증권(주) | 00164876 | |
(1) 금번과 같이 주주배정방식의 유상증자를 실시할 때, 주주가 소유하고 있는 주식수 비율대로 신주를 인수할 권리인 신주인수권에 대하여 당사는 「자본시장과 금융투자업에 관한 법률」 제165의 6조 3항 및 「증권의발행및공시등에관한규정」 제5-19조에 의거하여 주주에게 신주인수권증서를 발행합니다.
(2) 금번 유상증자시 신주인수권증서는 전자증권제도 시행일(2019년 09월 16일) 이후에 발행되고 상장될 예정으로 전자증권으로 발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여 배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다.
(3) 신주인수권증서 매매의 중개를 할 증권회사는 공동대표주관회사인 한국투자증권(주)과 케이비증권(주)로 합니다.
(4) 신주인수권증서 매매 등
① 금번 유상증자시 신주인수권증서는 전자증권제도 시행 이후에 발행되고 상장될 예정으로 실물은 발행 되지 않고 전자증권으로 등록발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여 배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다.
② 신주인수권증서를 매매하고자 하는 주주는 신주인수권증서를 예탁하고 있는 증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자 계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일 내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
(5) 신주인수권증서를 양수한 투자자의 청약방법
신주인수권증서를 증권회사에 예탁하고 있는 양수인은 당해 증권회사 점포 및 한국투자증권(주)과 케이비증권(주)의 본ㆍ지점을 통해 해당 신주인수권증서에 기재되어 있는 수량(초과청약이 있는 경우 초과청약 가능수량이 합산된 수량)만큼 청약할 수 있으며 청약 기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
(6) 신주인수권증서의 상장
당사는 금번 주주배정후 실권주 일반공모 유상증자 관련 신주인수권증서의 상장을 한국거래소에 신청할 예정입니다. 동 신주인수권증서가 상장될 경우 상장기간은 2024년 05월 29일부터 2024년 06월 04일까지 5거래일간으로 예정하고 있으며, 동 기간중 상장된 신주인수권증서를 한국거래소에서 매매할 수 있습니다. 동 신주인수권증서는 2024년 06월 05일에 상장폐지될 예정입니다. 「코스닥시장 상장규정」 제83조(신주인수권증권 및 신주인수권증서의 신규상장)에 따라 5거래일 이상 상장되어야 하며, 동 규정 제85조(신주인수권증권 및 신주인수권증서의 상장폐지)에 따라 신주청약 개시일 5거래일전에 상장폐지되어야 합니다.
|
※ 관련법령 제165조의6(주식의 발행 및 배정 등에 관한 특례) ③ 주권상장법인은 제1항제1호의 방식으로 신주를 배정하는 경우 「상법」 제416조제5호 및 제6호에도 불구하고 주주에게 신주인수권증서를 발행하여야 한다. 이 경우 주주 등의 이익 보호, 공정한 시장질서 유지의 필요성 등을 고려하여 대통령령으로 정하는 방법에 따라 신주인수권증서가 유통될 수 있도록 하여야 한다. 제176조의8(주식의 발행 및 배정에 관한 방법 등) ④ 법 제165조의6제3항 후단에서 "대통령령으로 정하는 방법"이란 다음 각 호의 어느 하나에 해당하는 방법을 말한다. 1. 증권시장에 상장하는 방법 2. 둘 이상의 금융투자업자(주권상장법인과 계열회사의 관계에 있지 아니한 투자매매업자 또는 투자중개업자를 말한다)를 통하여 신주인수권증서의 매매 또는 그 중개ㆍ주선이나 대리업무가 이루어지도록 하는 방법. 이 경우 매매 또는 그 중개ㆍ주선이나 대리업무에 관하여 필요한 세부사항은 금융위원회가 정하여 고시한다.
제83조(신주인수권증권 및 신주인수권증서의 신규상장) ② 신주인수권증권을 신규상장하려면 다음 각 호의 심사요건을 모두 충족하여야 한다. 1. 신주인수권증권의 발행회사의 주식(외국주식예탁증권을 포함한다. 이하 이 장에서 같다)이 코스닥시장에 상장되어 있을 것 2. 신주인수권증권의 발행회사의 상장 주식이 상장신청일 현재 이 규정에 따른 관리종목으로 지정되지 않고, 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유에 해당되지 않을 것 3. 신주인수권증권의 발행총수가 1만 증권 이상일 것. 이 경우 해당 증권의 목적인 신주가 액면주식인 경우에는 액면가액 5,000원을 기준으로 한다. 4. 신주인수권증권의 잔존 권리행사기간이 상장신청일 현재 1년 이상일 것 5. 신주인수권부사채권이 모집 또는 매출로 발행되었을 것. 다만, 주주에게 해당 사채권의 인수권이 주어진 경우에는 그러하지 아니하다. ③ 신주인수권증서를 신규상장하려면 다음 각 호의 심사요건을 모두 충족하여야 한다. 1. 신주인수권증서의 발행회사의 주식이 코스닥시장에 상장되어 있을 것 2. 신주인수권증서의 발행회사의 상장 주식이 상장신청일 현재 이 규정에 따른 관리종목으로 지정되지 않고, 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유에 해당되지 않을 것 3. 신주인수권의 양도를 허용하고, 신주인수권을 갖는 모든 주주에게 신주인수권증서를 발행하였을 것 4. 신주인수권증서의 발행총수가 1만 증서 이상일 것. 이 경우 해당 증서의 목적인 신주가 액면주식인 경우에는 액면가액 5,000원을 기준으로 한다. 5. 신주인수권증서의 거래 가능 기간이 5일(매매거래일을 기준으로 한다) 이상일 것 제85조(신주인수권증권 및 신주인수권증서의 상장폐지) 1. 신주인수권증권의 목적인 주식이 관리종목으로 지정되거나, 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 2. 신주인수권증권의 목적인 주식에 대한 상장폐지 신청으로 해당 주식이 상장폐지되는 경우 3. 신주인수권 행사기간이 만료되거나 행사가 완료된 경우 4. 그 밖에 공익 실현과 투자자 보호를 위하여 거래소가 신주인수권증권의 상장폐지가 필요하다고 인정하는 경우 ② 거래소는 신주인수권증서가 다음 각 호의 어느 하나에 해당하는 경우 해당 신주인수권증서의 상장을 폐지한다. 1. 신주인수권증서의 목적인 주식이 관리종목으로 지정되거나, 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 2. 신주인수권증서의 목적인 주식에 대한 상장폐지 신청으로 해당 주식이 상장폐지되는 경우 3. 신주 청약 개시일의 5일(매매거래일을 기준으로 한다) 전이 된 경우. 다만, 신주인수권증서의 유통상황을 고려하여 세칙으로 정하는 경우에는 그 기간 전으로 한다. 4. 그 밖에 공익 실현과 투자자 보호를 위하여 거래소가 신주인수권증서의 상장폐지가 필요하다고 인정하는 경우 |
(7) 신주인수권증서의 거래 관련 추가사항
당사는 금번 유상증자의 신주인수권증서를 상장신청할 예정인 바, 현재까지 관계기관과 협의된 신주인수권증서 상장시의 제반 거래관련 사항은 다음과 같습니다.
① 상장방식 : 전자등록발행된 신주인수권증서 전부를 상장합니다.
② 일반주주의 신주인수권증서 거래
| 구분 | 상장거래방식 | 계좌대체 거래방식 |
|---|---|---|
| 방법 | 주주의 신주인수권증서를 전자등록발행하여 상장합니다. 상장된 신주인수권증서를 장내거래를 통하여 매수하여 증권사 계좌에 보유한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. 주주의 신주인수권증서는 전자등록발행되므로 실물 증서는 발행되지 않습니다. | 신주인수권증서를 매매하고자 하는 기존 실질주주는 위탁증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. |
| 기간 | 2024년 05월 29일부터 2024년 06월 04일까지(5거래일간) 거래 | 신주배정통지일(2024년 05월 22일(예정))부터 신주인수권증서의 상장거래 마지막 날 이후 제2거래일(2024년 06월 07일)까지 거래 |
| 주1) | 상장거래 : 2024년 05월 29일부터 2024년 06월 04일까지(5거래일간) 거래 가능합니다. |
| 주2) | 계좌대체거래 : 신주배정통지일인 2024년 05월 22일(예정)부터 2024년 06월 07일까지 거래 가능합니다. → 신주인수권증서 상장거래의 결제일인 2024년 06월 07일까지 계좌대체(장외거래) 가능하며, 동일 이후부터는 신주인수권증서의 청약권리 명세를 확정하므로 신주인수권증서의 계좌대체(장외거래)가 제한됩니다. |
| 주3) | 신주인수권증서는 전자등록발행되므로 실물은 발행되지 않습니다. |
③ 특별계좌 소유주(기존 '명부주주')의 신주인수권증서 거래
a. '특별계좌 보유자(기존 '명부주주')'는 명의개서대행기관에 '특별계좌'에서 '일반전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후 금번 유상증자 청약 참여 또는 신주인수권증서의 매매가 가능합니다.
b. '특별계좌 보유자(기존 '명부주주')'는 신주인수권증서의 '일반 전자등록계좌(증권회사 계좌)'로 이전 없이 공동대표주관회사의 본ㆍ지점에서 직접 청약하는 방법으로도 금번 유상증자에 청약이 가능합니다. 다만 신주인수권증서의 매매는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후에만 가능하므로 이 점 유의하시기 바랍니다.
라. 기타 모집 또는 매출에 관한 사항
(1) 본 증권신고서는 공시심사 과정에서 일부 내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요 내용의 변경시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있으므로 투자자 여러분께서는 투자 시 이러한 점을 감안하시기 바랍니다.
(2) 「자본시장과 금융투자업에 관한 법률」 제120조 3항에 의거 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다.
(3) 본 증권신고서에 기재된 내용은 신고서 제출일 현재까지 발생된 것으로 본 신고서에 기재된 사항 이외에 자산, 부채, 현금흐름 또는 손익상황에 중대한 변동을 가져오거나 중요한 영향을 미치는 사항은 없습니다. 따라서, 주주 및 투자자가 투자의사를 결정함에 있어 유의하여야 할 사항이 본 증권신고서상에 누락되어 있지 않습니다.
(4) 금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서, 반기보고서, 분기보고서 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있사오니 투자의사를 결정하시는 데 참조하시기 바랍니다.
(5) 본 증권신고서의 예정 모집가액은 확정되어 있는 것은 아니며, 청약일 3거래일 전에 확정 발행가액을 산정함으로써 확정될 예정입니다. 또한, 본 증권신고서의 발행예정금액은 추후 주당 발행가액이 확정되는 내용에 따라 변경될 수 있음을 유의하여 주시기 바랍니다.
5. 인수 등에 관한 사항
| [인수방법: 잔액인수] |
| 인수인 | 인수주식 종류 및 수 | 인수대가 | |
|---|---|---|---|
| 공동 대표주관회사 | 한국투자증권(주) | 인수주식의 종류: 보통주 인수주식의 수: 인수한도 의무주식수 X 인수비율(15분의 11) |
- 대표주관수수료: 모집총액의 0.2% - 인수수수료 : 모집총액의 0.8% 中 15분의 11 - 실권수수료 : 잔액인수금액의 16.0% |
| 케이비증권(주) | 인수주식의 종류: 보통주 인수주식의 수: 인수한도 의무주식수 X 인수비율(15분의 4) |
- 인수수수료 : 모집총액의 0.8% 中 15분의 4 - 실권수수료 : 잔액인수금액의 16.0% |
|
| 주1) 잔여주식총수: 구주주청약 및 일반공모 후 발생한 배정잔여주 또는 청약미달주식 주2) 모집총액 : 최종 발행가액 X 총 발행주식수 주3) 상기 일반공모를 거친 후에도 미청약된 잔여주식에 대하여는 공동대표주관회사가 인수계약서 상 인수의무주식수를 한도로 하여 인수의무주식수만큼 자기 책임 하에 인수하기로 합니다. |
II. 증권의 주요 권리내용
1. 액면금액 : 기명식 보통주 1주당 500원
|
※ 당사의 정관 (이하 동일) 회사가 발행하는 주식 일주의 금액은 500원으로 한다. |
2. 주식에 관한 사항
|
제5조(발행예정주식의 총수) ① 회사는 이익배당 및 주식의 상환에 관한 종류주식(이하 이 조에서 “종류주식”이라 한다)을 발행할 수 있다. ② 제 5 조의 발행예정주식총수 중 종류주식의 발행한도는 보통주식의 50% 이내로 한다. ③ 종류주식에 대하여는 의결권이 있고 우선배당한다. 종류주식에 대한 우선배당은 1 주의 금액을 기준으로 연 1% 이상 10% 이내에서 발행시에 이사회가 정한 배당률에 따라 현금으로 지급한다. ④ 종류주식에 대하여 제 3 항에 따른 배당을 하고 보통주식에 대하여 종류주식의 배당률과 동률의 배당을 한 후, 잔여배당가능이익이 있으면 보통주식과 종류주식에 대하여 동등한 비율로 배당한다. ⑤ 종류주식에 대하여 제 3 항에 따른 배당을 하지 못한 사업연도가 있는 경우에는 미배당분을 누적하여 다음 사업연도의 배당시에 우선하여 배당한다. ⑥ 회사는 이사회 결의로 종류주식을 상환할 수 있다. ⑦ 주주는 회사에 대하여 종류주식의 상환을 청구할 수 있다. ⑧ 상환가액은 발행가액에 발행가액의 10%를 넘지 않는 범위내에서 발행시 이사회에서 정한 금액을 더한 가액으로 한다. 다만, 상환가액을 조정하려는 경우 이사회에서 조정할 수 있다는 뜻, 조정사유, 조정방법 등을 정하여야 한다. ⑨ 상환기간(또는 상환청구 기간)은 종류주식의 발행 후 1 월이 경과한 날로부터 만기일 전일까지 이사회 결의로 정한다. ⑩ 회사는 주식의 취득의 대가로 현금 이외의 유가증권이나(다른 종류의 주식은 제외한다) 그 밖의 자산을 교부할 수 있다.
① 회사는 이익배당 및 주식의 전환에 관한 종류주식(이하 이 조에서 “종류주식”이라 한다)을 발행할 수 있다. ② 제 5 조의 발행예정주식총수 중 종류주식의 발행한도는 보통주식의 50% 이내로 한다. ③ 종류주식에 대하여는 의결권이 있고 우선배당한다. 종류주식에 대한 우선배당은 1 주의 금액을 기준으로 연 1% 이상 10% 이내에서 발행시에 이사회가 정한 배당률에 따라 현금으로 지급한다. ④ 종류주식에 대하여 제 3 항에 따른 배당을 하고 보통주식에 대하여 종류주식의 배당률과 동률의 배당을 한 후, 잔여배당가능이익이 있으면 보통주식과 종류주식에 대하여 동등한 비율로 배당한다. ⑤ 종류주식에 대하여 제 3 항에 따른 배당을 하지 못한 사업연도가 있는 경우에는 미배당분을 누적하여 다음 사업연도의 배당시에 우선하여 배당한다. ⑥ 종류주식의 주주는 회사에 대하여 전환을 청구할 수 있다. 전환을 청구할 수 있는 기간은 1 년 이상 만기일 이내에서 발행시 이사회결의로 정한다. 다만, 전환기간내에 전환권이 행사되지 아니하면, 전환기간 만료일에 전환된 것으로 본다. ⑦ 회사는 발행일로부터 1 년이 경과한 후 다음 각 호의 어느 하나에 해당하는 경우 종류주식을 전환할 수 있다. 1. 전환청구기간에 투자자가 전환 청구를 한 경우 2. 전환에 관한 종류주식의 청구기간이 만료되었을 경우 ⑧ 제 7 항 또는 제 8 항의 전환으로 인하여 발행할 주식은 보통주식으로 하고, 그 전환비율은 종류주식 1 주 당 전환으로 인하여 발행하는 주식 1 주로 한다. ⑨ 제 7 항 또는 제 8 항에 따라 발행되는 신주에 대한 이익의 배당에 관하여는 제 13 조를 준용한다. 제10조(주권의종류)(삭제2016. 03. 29) 제15조(주식의소각) 회사는 이사회의 결의에 의하여 회사가 보유하는 자기주식을 소각할 수 있다. |
3. 의결권에 관한 사항
|
제28조(주주의의결권) 주주의 의결권은 1 주마다 1 개로 한다. 제 29 조 (상호주에 대한 의결권 제한) 회사, 회사와 회사의 자회사 또는 회사의 자회사가 다른 회사의 발행주식총수의 10 분의 1 을 초과하는 주식을 가지고 있는 경우 그 다른 회사가 가지고 있는 이 회사의 주식은 의결권이 없다. 제30조(의결권의불통일행사) ① 2 이상의 의결권을 가지고 있는 주주가 의결권의 불통일행사를 하고자 할 때에는 회일의 3 일전에 회사에 대하여 서면 또는 전자문서로 그 뜻과 이유를 통지하여야 한다. ② 회사는 주주의 의결권의 불통일행사를 거부할 수 있다. 그러나 주주가 주식의 신탁을 인수 하였거나 기타 타인을 위하여 주식을 가지고 있는 경우에는 그러하지 아니하다. 제31조(의결권의대리행사) ① 주주는 대리인으로 하여금 그 의결권을 행사하게 할 수 있다. ② 제 1 항의 대리인은 주주총회 개시전에 그 대리권을 증명하는 서면(위임장)을 제출하여야 한다. |
4. 신주인수권에 관한 사항
|
제11조(신주인수권) ① 회사의 주주는 신주발행에 있어서 그가 소유한 주식수에 비례하여 신주의 배정을 받을 권리를 가진다. ② 제 1 항의 규정에 불구하고 다음 각호의 경우에는 주주 외의 자에게 신주를 배정할 수 있다. 1. 주주우선공모의 방식으로 신주를 발행하는 경우 2. 발행할 주식총수의 범위 내에서 자본시장과 금융투자업에 관한 법률 제 165 조의 6 에 따라 일반공모증자 방식으로 신주를 발행하는 경우 3. 자본시장과 금융투자업에 관한 법률 제 165 조의 7 의 규정에 의하여 우리사주조합 원에게 신주를 우선배정하는 경우 4. 상법 제 340 조의 2 및 제 542 조의 3 의 규정에 의하여 주식매수선택권의 행사로 인하여 신주를 발행하는 경우 5. 발행주식총수의 100 분의 100 을 초과하지 않는 범위 내에서 경영상 필요로 주식예탁증서(DR) 발행에 따라 신주를 발행하는 경우 6. 발행주식총수의 100 분의 100 을 초과하지 않는 범위 내에서 경영상 필요로 외국인 투자촉진법에 의한 외국인투자를 위하여 신주를 발행하는 경우 7. 발행할 주식총수의 범위 내에서 재무구조 개선, 기술도입, 사업제휴, 신규사업 추진 및 긴급한 자금조달 등 회사의 경영상 목적을 달성하기 위하여 국내외 금융기관, 기관투자자, 전문투자자 및 기타 이사회에서 정한 자에게 신주를 발행하는 경우 8. 근로복지기본법 제 39 조의 규정에 따라 우리사주매수선택권 행사로 인하여 신주를 발행하는 경우 ③ 제 2 항의 각 호 중 어느 하나의 규정에 의해 신주를 발행할 경우 발행할 주식의 종류와 수 및 발행가격 등은 이사회 결의로 정한다. ④ 주주가 신주인수권을 포기 또는 상실하거나 신주배정에서 단주가 발생하는 경우에 그 처리 방법은 이사회 결의로 정한다. |
5. 배당에 관한 사항
|
제14조(신주의 동등배당) 회사가 정한 배당기준일 전에 유상증자, 무상증자 및 주식배당에 의하여 발행한 주식에 대하여는 동등배당한다. 제9조 (이익배당및주식의상환에관한종류주식) ① 회사는 이익배당 및 주식의 상환에 관한 종류주식(이하 이 조에서 “종류주식”이라 한다)을 발행할 수 있다. ② 제 5 조의 발행예정주식총수 중 종류주식의 발행한도는 보통주식의 50% 이내로 한다. ③ 종류주식에 대하여는 의결권이 있고 우선배당한다. 종류주식에 대한 우선배당은 1 주의 금액을 기준으로 연 1% 이상 10% 이내에서 발행시에 이사회가 정한 배당률에 따라 현금으로 지급한다. ④ 종류주식에 대하여 제 3 항에 따른 배당을 하고 보통주식에 대하여 종류주식의 배당률과 동률의 배당을 한 후, 잔여배당가능이익이 있으면 보통주식과 종류주식에 대하여 동등한 비율로 배당한다. ⑤ 종류주식에 대하여 제 3 항에 따른 배당을 하지 못한 사업연도가 있는 경우에는 미배당분을 누적하여 다음 사업연도의 배당시에 우선하여 배당한다. ⑥ 회사는 이사회 결의로 종류주식을 상환할 수 있다. ⑦ 주주는 회사에 대하여 종류주식의 상환을 청구할 수 있다. ⑧ 상환가액은 발행가액에 발행가액의 10%를 넘지 않는 범위내에서 발행시 이사회에서 정한 금액을 더한 가액으로 한다. 다만, 상환가액을 조정하려는 경우 이사회에서 조정할 수 있다는 뜻, 조정사유, 조정방법 등을 정하여야 한다. ⑨ 상환기간(또는 상환청구 기간)은 종류주식의 발행 후 1 월이 경과한 날로부터 만기일 전일까지 이사회 결의로 정한다. ⑩ 회사는 주식의 취득의 대가로 현금 이외의 유가증권이나(다른 종류의 주식은 제외한다) 그 밖의 자산을 교부할 수 있다.
① 회사는 이익배당 및 주식의 전환에 관한 종류주식(이하 이 조에서 “종류주식”이라 한다)을 발행할 수 있다. ② 제 5 조의 발행예정주식총수 중 종류주식의 발행한도는 보통주식의 50% 이내로 한다. ③ 종류주식에 대하여는 의결권이 있고 우선배당한다. 종류주식에 대한 우선배당은 1 주의 금액을 기준으로 연 1% 이상 10% 이내에서 발행시에 이사회가 정한 배당률에 따라 현금으로 지급한다. ④ 종류주식에 대하여 제 3 항에 따른 배당을 하고 보통주식에 대하여 종류주식의 배당률과 동률의 배당을 한 후, 잔여배당가능이익이 있으면 보통주식과 종류주식에 대하여 동등한 비율로 배당한다. ⑤ 종류주식에 대하여 제 3 항에 따른 배당을 하지 못한 사업연도가 있는 경우에는 미배당분을 누적하여 다음 사업연도의 배당시에 우선하여 배당한다. ⑥ 종류주식의 주주는 회사에 대하여 전환을 청구할 수 있다. 전환을 청구할 수 있는 기간은 1 년 이상 만기일 이내에서 발행시 이사회결의로 정한다. 다만, 전환기간내에 전환권이 행사되지 아니하면, 전환기간 만료일에 전환된 것으로 본다. ⑦ 회사는 발행일로부터 1 년이 경과한 후 다음 각 호의 어느 하나에 해당하는 경우 종류주식을 전환할 수 있다. 1. 전환청구기간에 투자자가 전환 청구를 한 경우 2. 전환에 관한 종류주식의 청구기간이 만료되었을 경우 ⑧ 제 7 항 또는 제 8 항의 전환으로 인하여 발행할 주식은 보통주식으로 하고, 그 전환비율은 종류주식 1 주 당 전환으로 인하여 발행하는 주식 1 주로 한다. ⑨ 제 7 항 또는 제 8 항에 따라 발행되는 신주에 대한 이익의 배당에 관하여는 제 13 조를 준용한다. |
III. 투자위험요소
1. 사업위험
| 가. 국내외 경기 변동에 따른 사업환경 악화 위험 국제통화기금(IMF)이 2024년 01월 발표한 "World Economic Outlook"에 따르면, 2023년 세계 경제성장률 전망치는 2023년 10월의 전망치인 3.0%보다 0.1%p 증가한 3.1%를, 2024년 성장률은 0.2%p 상향조정하여 3.1%로 전망하였습니다. IMF에 따르면 2024년 경제 성장률 전망치는 주요 중앙은행의 고금리 지속, 높은 부채 부담, 낮은 기본 생산성 등에도 불구하고 미국과 대형 신흥시장 및 개발도상국의 예상보다 큰 회복력과 중국의 재정지원, 인플레이션률 하락 등으로 인해 지난 10월 전망보다 상승했다고 밝혔습니다. 또한 한국은행은 2024년 2월 경제전망보고서를 통해 국내 경제성장률을 2024년 2.1%로 전망하였습니다. 이는 지난 2023년 11월 전망치와 동일한 수치입니다. 국내경제는 소비, 건설투자 등 내수 회복 모멘텀이 약화된 반면 수출이 예상보다 양호함에 따라 완만한 개선흐름을 이어갈 것으로 전망합니다. 또한, 대외적으로 주요국의 통화정책 기조 변화, 국제 유가 흐름, 중국 경제 향방, 지정학적 리스크 증가 등 다양한 불확실성이 상존하고 있어 지속적인 모니터링이 필요할 것으로 판단됩니다. 당사의 주력 상품인 의약품은 경기변동에 직접적인 영향을 받는 일반 소비재에 해당되지 않는 바, 급격한 경기 악화에 대한 부정적인 영향은 상대적으로 제한적일 것으로 판단됩니다. 그럼에도 불구하고 거시경제상황의 둔화는 당사 제품에 대한 수요를 감소시키는 요인으로 작용할 수 있으며, 경기 둔화로 인하여 증시의 변동성이 높아질 시, 상장 이후 당사의 주가 역시 높은 변동성을 보일 가능성이 존재합니다. |
(1) 글로벌 경기 동향
국제통화기금(IMF)이 2024년 01월 발표한 World Economic Outlook(세계경제전망보고서)에 따르면, 세계경제성장률 전망치는 2024년 3.1%, 2025년 3.2%로 발표되었습니다. 이는 지난 2023년 10월 전망치인 2024년 2.9%, 2025년 3.2%와 비교 시 2024년 전망치는 +0.2%p 상향하였고, 2025년 전망치는 동일한 수치입니다. IMF는 미국과 몇 개의 큰 신흥시장 및 개발도상국에서 나타난 예상보다 강한 회복력과 중국의 재정 지원을 상향 조정의 이유로 들었으며, 인플레이션 완화와 꾸준한 성장 덕분에 경기가 경착륙할 가능성이 멀어졌다고 평가하였습니다. 그 외에도 통화정책 완화와 지나친 긴축 기조 유지 모두를 경계해 통화정책 완화 시기에 대한 적절한 시점 설정이 중요하다고 권고하였으며, 미래 충격에 대응하기 위한 재정여력 확충, 구조개혁을 통한 중장기 생산성 향상 및 기후변화 대응 등을 강조하였습니다. 2024년 01월 IMF가 제시한 세계 경제성장률 전망치는 다음과 같습니다.
| [국제통화기금 세계 경제성장 전망] |
| (단위 : %, %p.) |
|
구분 |
2023년 |
2024년(E) |
2025년(E) | ||||
|---|---|---|---|---|---|---|---|
| 23.10월 (A) |
24.01월 (B) |
조정폭 (B-A) |
23.10월 (C) |
24.01월 (D) |
조정폭 (D-C) |
||
|
세계 |
3.1 | 2.9 | 3.1 | 0.2 | 3.2 | 3.2 | 0.0 |
|
선진국 |
1.6 | 1.4 | 1.5 | 0.1 | 1.8 | 1.8 | 0.0 |
|
미국 |
2.5 | 1.5 | 2.1 | 0.6 | 1.8 | 1.7 | -0.1 |
|
유로존 |
0.5 | 1.2 | 0.9 | -0.3 | 1.8 | 1.7 | -0.1 |
|
독일 |
-0.3 | 0.9 | 0.5 | -0.4 | 2.0 | 1.6 | -0.4 |
|
프랑스 |
0.8 | 1.3 | 1.0 | -0.3 | 1.8 | 1.7 | -0.1 |
|
이탈리아 |
0.7 | 0.7 | 0.7 | 0.0 | 1.0 | 1.1 | 0.1 |
|
스페인 |
2.4 | 1.7 | 1.5 | -0.2 | 2.1 | 2.1 | 0.0 |
|
일본 |
1.9 | 1.0 | 0.9 | -0.1 | 0.6 | 0.8 | 0.2 |
|
영국 |
0.5 | 0.6 | 0.6 | 0.0 | 2.0 | 1.6 | -0.4 |
|
캐나다 |
1.1 | 1.6 | 1.4 | -0.2 | 2.4 | 2.3 | -0.1 |
|
기타 선진국 |
1.7 | 2.2 | 2.1 | -0.1 | 2.3 | 2.5 | 0.2 |
|
한국 |
1.4 | 2.2 | 2.3 | 0.1 | 2.3 | 2.3 | 0.0 |
|
신흥개도국 |
4.1 | 4.0 | 4.1 | 0.1 | 4.1 | 4.2 | 0.1 |
|
중국 |
5.2 | 4.2 | 4.6 | 0.4 | 4.1 | 4.1 | 0.0 |
|
인도 |
6.7 | 6.3 | 6.5 | 0.2 | 6.3 | 6.5 | 0.2 |
|
러시아 |
3.0 | 1.1 | 2.6 | 1.5 | 1.0 | 1.1 | 0.1 |
|
브라질 |
3.1 | 1.5 | 1.7 | 0.2 | 1.9 | 1.9 | 0.0 |
|
멕시코 |
3.4 | 2.1 | 2.7 | 0.6 | 1.5 | 1.5 | 0.0 |
|
사우디 |
-1.1 | 4.0 | 2.7 | -1.3 | 4.2 | 5.5 | 1.3 |
|
남아공 |
0.6 | 1.8 | 1.0 | -0.8 | 1.6 | 1.3 | -0.3 |
| 출처 : IMF World Economic Outlook (2024.01) |
상기 IMF의 전망은 2024년 01월 발표된 것으로, 이후 개최된 01월 미국 연방준비위원회 FOMC 성명서에서 추가 인상을 시사하던 문구를 삭제하고 기준금리의 조정 가능성을 고려하는 문구를 추가함에 따라 시장참여자들의 금리인하 사이클 진입에 대한 기대감이 더욱 커졌습니다. 다만, 물가 안정화에 자신감을 가질 수 있는 데이터가 더 필요함을 지속 강조한 바, 2분기 물가 데이터 확인이 중요할 것으로 사료됩니다. 또한, 금리 수준과는 별개로 전쟁의 지속, 제조업의 부진, 국내 PF 이슈 지속 등 국내외 경기침체가 해소되고 있지 않은 상황으로 경기 동향에 대한 지속적인 모니터링이 필요할 것으로 사료됩니다.
(2) 국내 경기 동향
한국은행은 2024년 2월 경제전망보고서를 통해 국내 경제성장률을 2024년 2.1%로 전망하였습니다. 이는 지난 2023년 11월 전망치와 동일한 수치입니다. 국내경제는 소비, 건설투자 등 내수 회복 모멘텀이 약화된 반면 수출이 예상보다 양호함에 따라 완만한 개선흐름을 이어갈 것으로 전망합니다. 또한, 대외적으로 주요국의 통화정책 기조 변화, 국제 유가 흐름, 중국 경제 향방, 지정학적 리스크 증가 등 다양한 불확실성이 상존하고 있어 지속적인 모니터링이 필요할 것으로 판단됩니다. 2024년 2월 한국은행이 제시한 국내 경제성장률 전망치는 다음과 같습니다.
| [한국은행 국내 경제성장률 전망치] |
| (단위: %) |
|
구분 |
2022년 |
2023년 |
2024년(E) |
2025년(E) |
||||
|---|---|---|---|---|---|---|---|---|
|
연간 |
상반기 |
하반기 |
연간 |
상반기 |
하반기 |
연간 |
연간 |
|
|
GDP성장률(%) |
2.6 |
0.9 |
1.8 |
1.4 |
2.2 |
2.0 |
2.1 |
2.3 |
|
민간소비 |
4.1 |
3.1 |
0.6 | 1.8 |
1.1 |
2.0 |
1.6 |
2.3 |
|
설비투자 |
-0.9 |
5.3 |
-4.0 |
0.5 |
2.6 |
5.7 |
4.2 |
3.7 |
|
지식재산생산물투자 |
5.0 |
2.9 |
0.3 |
1.6 |
1.5 |
2.8 |
2.2 |
3.3 |
|
건설투자 |
-2.8 |
1.8 |
1.0 |
1.4 |
-2.4 |
-2.9 |
-2.6 |
-1.0 |
|
재화수출 |
3.6 |
-0.9 |
6.6 |
2.9 |
6.0 |
3.2 |
4.5 |
3.6 |
|
재화수입 |
4.3 |
1.9 |
-3.0 |
-0.6 |
0.1 |
5.4 |
2.7 |
3.1 |
| 자료: | 한국은행 경제전망보고서(2024.02) |
국내 경기는 소비 회복 모멘텀의 약화에도 불구하고 IT 부문의 수출이 증가하면서 완만한 회복세를 보일 것으로 예상됩니다. 각 항목별로 살펴보면 민간소비의 경우 회복 모멘텀이 약화되고 있으며, 건설투자는 최근 부진이 두드러진 모습으로 부동산 PF 관련 불확실성이 상존하고 있습니다. 그러나 수출이 반도체 경기 반등, 양호한 미국 성장세 등으로 예상보다 빠른 증가세를 보이고 있습니다. 2024년에도 반도체 경기 회복, 신성장산업 관련 주요국 투자 확대 등으로 수출과 설비투자 부문을 중심으로 개선될 것으로 전망됩니다.
특히 설비투자의 경우 2023년 중 글로벌 제조업경기 부진, 자금조달 비용 상승 등으로 인해 상반기 성장률 5.3%에서 하반기 성장률 -4.0%로 급격히 악화되었습니다. 그러나 최근 이연되었던 항공기 투자 확대 등으로 부진이 다소 완화되고 있으며, 향후 IT 경기 회복이 본격화되면서 반도체 기업들의 첨단 공정 투자 확대, 비IT 부문 중에서도 전기차, 이차전지, 바이오 등 친환경·신성장 분야를 중심으로 투자가 개선되면서 점차 회복될 것으로 전망됩니다.
코로나19 이후 각국 정부 및 중앙은행은 적극적인 정책 대응을 통해 경기회복을 도모하고 있으며, 이에 따라 서비스 소비 등 민간소비가 회복되고 있는 상황입니다. 그러나 이와 동시에 중국 성장세 약화, 러시아-우크라이나 전쟁 등의 지정학적 리스크증대와 더불어 고금리 환경 지속으로 금융 불안정성이 확대되고 있습니다. 글로벌 경기가 단기적으로 회복되는 추세이기는 하나, 여전히 위험요인이 상존하고 있는 상황으로 국내·외 경기가 크게 둔화되거나 침체가 지속될 가능성을 배제할 수 없습니다.
다만, 당사의 주력 상품인 의약품은 경기변동에 직접적인 영향을 받는 일반 소비재에 해당되지 않는 바, 급격한 경기 악화에 대한 부정적인 영향은 상대적으로 제한적일 것으로 판단됩니다. 그럼에도 불구하고 거시경제상황의 둔화는 당사 제품에 대한 수요를 감소시키는 요인으로 작용할 수 있으며,경기 둔화로 인하여 증시의 변동성이 높아질 시, 상장 이후 당사의 주가 역시 높은 변동성을 보일 가능성이 존재합니다.
|
나. 진단 시장 성장성 정체에 따른 위험 |
당사는 2022년 10월 1일 에임과 합병하여 체외진단키트 등 의료기기사업에 진출함으로써 Malaria, HIV, Covid-19, Influenza 등 항원 및 항체 기반의 Immunoassay Rapid POCT 진단 시약의 주요 구성품을 개발하였으며, 다수의 기술 및 디자인 특허를 보유하고 있습니다. 주요 고객사는 Abbott, SD BIOSENSOR 등 이며, 특히 Covid Ag 신속진단 키트 관련하여 Roche, SD BIOSENSOR, Abbott의 OEM 및 TPM(Third Party Manufacturing)을 진행하고 있습니다. 당사의 제품/상품 구성내역은 아래와 같습니다.
| [당사의 제품/상품 구성] |
| 매출유형 | 품목카테고리 | 용도 | 주요상표 |
|---|---|---|---|
| 제품 | 체외 진단 (Covid) | Covid-19 진단 | Standard Q, Panbio 외 |
| 체외 진단 (Non-Covid) | Malaria 외 진단 | Mini Tip 외 | |
| 기타 제품 | 일반 사출 외 | - | |
| 체외 진단 (Covid) | Covid-19 진단 | Standard Q, Panbio 외 | |
| 체외 진단 (Non-Covid) | Malaria 외 진단 | Mini Tip 외 | |
| 상품 | 체외 진단 (Covid) | Covid-19 진단 | Standard Q, Panbio 외 |
| 체외 진단 (Non-Covid) | Malaria 외 진단 | Ezi-Tube, Capillary Tube 외 | |
| 기타 제품 | 화장품 용기 외 | Standard Q, Panbio 외 | |
| 체외 진단 (Non-Covid) | Malaria 외 진단 | Ezi-Tube, Capillary Tube 외 | |
| 기타 제품 | 일반 사출 외 | - |
| 자료: 당사 자료 제공 |
인체를 진단하는 방식에는 크게 내시경, MRI와 같이 몸속을 들여다보고 진단하는 체내 진단과 인체로부터 채취된 물질을 기반으로 몸 밖에서 진단하는 체외진단으로 구분됩니다. 그 중 체외진단은 질병의 진단과 예후, 건강상태 파악, 치료효과 판정, 예방 등의 목적으로 혈액과 침 등 인체에서 유래한 물질을 이용해 몸 밖에서 신속하게 질병을 진단하는 방식입니다.
| [진단방법의 종류] |
| 구분 | 세부내용 |
|---|---|
| 체내진단 | 내시경을 직접 활용하거나 방사선, 초음파 등 매개체를 활용하여 얻은 체내 영상 Data를 바탕으로 질병의 유무 및 경중을 판단하는 진단방법. |
| 체외진단 | 인체로부터 채취한 다양한 검체에 대해 생화학적 반응을 활용하여 얻은 Data를 바탕으로 질병의 유무 및 경중을 판단하는 진단방법 |
| 출처: 식품의약품안전처, 식의약 R&D 이슈보고서 |
체외진단 의료기기는 다음 어느 하나에 해당되는 제품을 의미합니다.
| 체외진단의료기기법 제2조 1항 |
|---|
|
1. “체외진단의료기기”란 사람이나 동물로부터 유래하는 검체를 체외에서 검사하기 위하여 단독 또는 조합하여 사용되는 시약, 대조ㆍ보정 물질, 기구ㆍ기계ㆍ장치, 소프트웨어 등 「의료기기법」 제2조제1항에 따른 의료기기로서 다음 각 목의 어느 하나에 해당하는 제품을 말한다. 가. 생리학적 또는 병리학적 상태를 진단할 목적으로 사용되는 제품 나. 질병의 소인(素因)을 판단하거나 질병의 예후를 관찰하기 위한 목적으로 사용되는 제품 다. 선천적인 장애에 대한 정보 제공을 목적으로 사용되는 제품 라. 혈액, 조직 등을 다른 사람에게 수혈하거나 이식하고자 할 때 안전성 및 적합성 판단에 필요한 정보 제공을 목적으로 사용되는 제품 마. 치료 반응 및 치료 결과를 예측하기 위한 목적으로 사용되는 제품 바. 치료 방법을 결정하거나 치료 효과 또는 부작용을 모니터링하기 위한 목적으로 사용되는 제품 |
체외진단(IVD) 검사는 그 결과를 토대로 환자의 치료 및 약물처방의 방향을 결정하는 중요한 역할을 하며 환자 치료의 필수적이고 전문화된 요소로 자리매김하고 있습니다. 개인 맞춤 치료를 제공하는 현대의 정밀 의학 분야에서 체외진단(IVD) 검사는 그 중요도가 점점 증폭되고 있는 상황입니다. 한편, 의료서비스 분야에서 환자의 접근성이 큰 화두가 된 만큼 현장진단검사(POCT)에 대한 요구도가 증폭되고 있는 상황입니다. 이러한 시장의 요구에 따라, 체외진단(IVD) 시장은 Point of Care(POC) 검사 장치에 대한 수요 증가, 공공 및 민간 진단 센터의 증가, 미세유체의 진단, 바이오칩 및 나노 바이오 기술의 도입, 최소 침습성 및 비침습성 진단 장치의 수요 증가 등에 의해 더욱 성장하고 있습니다. 이와 같은 요인으로 세계 체외진단(IVD) 시장은 2021년 982억 달러에서 연평균 성장률 2.9%로 증가하여, 2026년에는 1,131억 달러에 이를 것으로 전망됩니다. COVID-19로 인해 글로벌 체외 진단 시장은 급격하게 성장하였으며, 기존 또는 신규 감염 질병 진단을 위한 차세대 체외 진단의 R&D 확장으로 앞으로도 성장 추세는 꾸준히 이어질 것으로 예상됩니다.
| [글로벌 체외진단시장 성장 추세] |
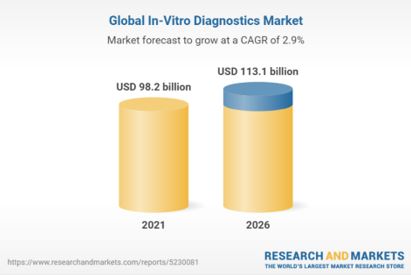 |
|
글로벌 체외진단 시장 |
| 출처: Research & Markets - In-Vitro Diagnostics/IVD Market by Product and Service ,Technology ,Application (Diabetes, Oncology, Cardiology, Nephrology, Infectious Disease, End User - Global Forecast to 2026 (2022.05) |
이처럼 글로벌 체외진단 시장은 다양한 질환 발생 및 이에 따른 진단 수요 증가, 기술의 발전 등으로 인하여 지속적인 성장이 예상되고 있습니다. 그럼에도 불구하고, 당사가 예상하지 못한 체외진단 시장의 트렌드 변화, 체외진단 수요 감소, 판매단가 하락 등으로 인하여 체외진단 시장 성장이 둔화될 경우 당사의 매출에 부정적인 영향을 미칠 수 있습니다. 이 점 투자자께서는 유의하시기 바랍니다.
|
다. COVID-19 종식에 따른 메디케어사업 진단 제품 매출 감소 위험 |
2020년부터 코로나 질병 확산에 따라 코로나 체외진단 관련 매출이 2022년까지 가파르게 증가하였으며, 동시에 당사가 영위하는 체외진단 제품의 매출 또한 지속적으로 성장하는 모습을 보여주었습니다. 다만 최근 코로나 종식이 다가오고 일상생활화 됨에 따라 당사 매출액은 급감하는 추이를 보이고 있습니다. 당사의 제품/상품별 매출 상세내역은 아래와 같습니다.
| [매출 상세 내역] |
| (단위 : 백만원, %) |
| 매출유형 | 품목카테고리 | 용도 | 주요상표 | 2024년 1분기 | 2023년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 매출액 | 비중 | 매출액 | 비중 | 매출액 | 비중 | 매출액 | 비중 | 매출액 | 비중 | 매출액 | 비중 | ||||
| 제품 | 체외 진단 (Covid) | Covid-19 진단 | Standard Q, Panbio 외 | 531 | 15.77% | 7,789 | 75.74% | 6,351 | 33.8% | 80,566 | 43.1% | 65,064 | 39.0% | 41,132 | 42.6% |
| 체외 진단 (Non-Covid) | Malaria 외 진단 | Mini Tip 외 | 1,261 | 37.45% | 1,378 | 13.40% | 6,497 | 34.5% | 29,865 | 16.0% | 22,577 | 13.5% | 3,115 | 3.2% | |
| 기타 제품 | 일반 사출 외 | - | 276 | 8.20% | 84 | 0.82% | 410 | 2.2% | 46 | 0.1% | 4 | 0.0% | - | - | |
| 체외 진단 (Covid) | Covid-19 진단 | Standard Q, Panbio 외 | - | - | - | - | - | - | - | - | 87 | 0.1% | - | - | |
| 체외 진단 (Non-Covid) | Malaria 외 진단 | Mini Tip 외 | - | - | - | - | - | - | - | - | 6 | 0.0% | 133 | 0.1% | |
| 상품 | 체외 진단 (Covid) | Covid-19 진단 | Standard Q, Panbio 외 | 1 | 0.03% | - | - | 1 | 0.0% | 2,042 | 1.1% | 2,916 | 1.7% | 3,711 | 3.8% |
| 체외 진단 (Non-Covid) | Malaria 외 진단 | Ezi-Tube, Capillary Tube 외 | 1,265 | 37.57% | 991 | 9.64% | 5,172 | 27.5% | 72,484 | 38.8% | 74,752 | 44.8% | 48,152 | 49.9% | |
| 기타 제품 | 화장품 용기 외 | Standard Q, Panbio 외 | 19 | 0.56% | - | - | 216 | 1.1% | 469 | 0.3% | 273 | 0.2% | 198 | 0.2% | |
| 체외 진단 (Non-Covid) | Malaria 외 진단 | Ezi-Tube, Capillary Tube 외 | - | - | - | - | - | - | - | - | 930 | 0.6% | 6 | 0.0% | |
| 기타 제품 | 일반 사출 외 | - | 2 | 0.06% | 42 | 0.41% | - | - | - | - | 2 | - | - | - | |
| 기타 (용역, 임대 등) | 기타 | - | 12 | 0.36% | - | - | 163 | 0.9% | 1,559 | 0.8% | 260 | 0.2% | 97 | 0.1% | |
| 총합계 | 3,367 | 100.0% | 10,284 | 100.0% | 18,810 | 100.0% | 187,032 | 100.0% | 166,874 | 100.0% | 96,544 | 100.0% | |||
| 출처: 당사 자료 제공 |
신종 코로나바이러스감염증은 2019년 12월 1일 발견된 후 감염 확산세가 전세계로 확대되었으며, 현재까지도 일일 신규 확진자가 지속적으로 발생하고 있습니다. 코로나 확진자는 2022년 2월 이후 급격한 증가세를 보이며 가파르게 증가하는 추이를 보였습니다. 다만 이에 대한 기저효과로 2023년 들어서는 코로나 누진 확진자수가 완만한 증가세를 보이고 있습니다.
|
국내 코로나 확진자 추이 |
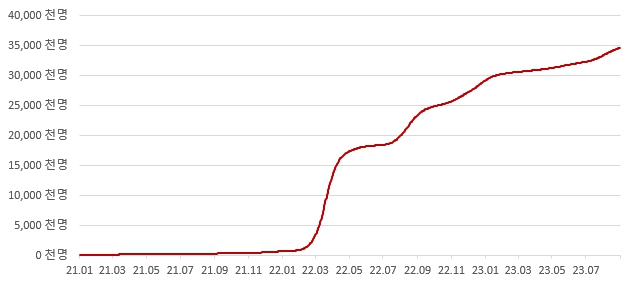 |
|
국내 코로나 확진자 누적 |
| 주) 2021년1월1일 부터 2023년 8월31까지의 국내 코로나 누적 확진자(23.08.31 누적 확진자 수: 34,572,554명) |
| 출처: 질병관리청 |
최근에는 코로나 팬데믹 종식 가능성이 제기된 상황이며, 코로나가 일상생활의 일부분으로 받아들여짐에 따라 향후 진단키트에 대한 수요는 더욱 감소할 개연성이 존재합니다. 이에 따라 당사의 코로나 관련 체외진단 제품 매출이 큰 폭으로 감소할 가능성이 존재하며 이로 인해 당사의 재무실적에 악영향을 미칠 수 있습니다. 투자자께서는 이 점 유의하여 주시기 바랍니다.
| 라. 신약개발의 낮은 성공가능성 및 수익성 위험 일반적으로 신약개발은 후보물질 선정, 물리화학 및 생물학적 분석연구, 비임상 및 임상 1상~3상, 품목허가의 단계를 거쳐 시장에 출시되며, 통상 약 10~15년 정도의 오랜 기간이 소요됩니다. 이 중 임상 시험에만 보통 6년 이상의 시간이 소요되며, 비임상 단계에서 안전성 및 효능이 검증되었음에도 불구하고 각 임상 단계에서 부작용이나 낮은 효능 등 예상치 못한 결과로 인하여 의약품 개발에 실패할 위험이 상존합니다. 이렇듯 신약연구개발 사업은 대표적인 '고위험 고수익형' 사업으로 당사 뿐 아니라 신약개발 업종을 영위하는 회사들에게는 필연적인 실패 위험이 있습니다. 새로운 의약품이 개발되어 소비자에게 전달되기까지는 많은 비용과 노력이 필요하며, 시판으로 이어질 확률은 10,000분의 1 정도로 낮은 편입니다. 당사는 현재 자체적으로 3개의 항암 신약 물질에 대한 국내 전용실시권을 보유하고 있으며, 당사가 본 공시서류 제출일 전일 기준 99.30%의 지분을 보유한 종속회사 에이치엘비셀(주)는 바이오인공간, 지혈제(생분해성 의료용 접착제 또는 실란트 조성물), 인간 세포외기질의 3개 분야에서 파이프라인을 구축하고 있습니다. 또한 계열회사 Elevar Therapeutics, Inc.(구,HLB USA, Inc.)의 리보세라닙과 캄렐리주맙 병용요법의 간암 1차 치료제 경우, 2023년 5월 NDA(신약 허가신청)를 신청하였으며, 7월 NDA 본심사가 개시되었습니다. 2023년 8월 리보세라닙 공장실사 및 12월 캄렐리주맙 공장실사까지 완료하였으나, 2024년 5월 미국 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL(보완요구서한, Complete Response Letter) 수령하였습니다. CRL 통한 요구 사항은 1) 병용투여 약물인 캄렐리주맙(항서제약)의 CMC(의약품 생산시설 실사) 진행 후 항서제약이 보완한 사항에 대해 일부 미비한 점에 대한 보완 2) 미국 FDA가 BIMO Inspection(임상사이트 실사)를 여행제한으로 인해 완료하지 못했다는 내용입니다. 계열회사 Elevar Therapeutics, Inc.는 상기 두가지 보완사항에 대해 항서제약과 긴밀히 협의하여 이에 대해 신속히 보완하고 FDA 재승인 신청할 예정이며, 재승인 신청 후 최장 6개월 이내 FDA는 승인여부를 결정하게 됩니다. 이와 같이 각 단계별 임상 및 FDA 승인 지연 등의 가능성은 항상 존재합니다. 또한 당사가 주력하고 있는 파이프라인보다 경쟁신약의 연구개발 단계가 선행되거나, 경쟁신약의 효능이 당사 개발 신약보다 뛰어나다고 판명되는 등 관련 경쟁에서 당사가 뒤처질 경우, 당사의 파이프라인 상에서 발생되는 매출이 적어지거나 발생하지 않을 가능성이 있으며, 이는 기존에 신약 개발에 투자한 당사의 수익성에 부정적인 영향을 끼칠 수 있으니 이 점 투자자께서는 유의하시기 바랍니다. |
[주요 용어 설명]
|
용 어 |
설 명 |
|---|---|
|
의약품 |
사람, 동물의 질병 진단, 치료, 예방목적으로 사용되는 물품으로 기구,기계 장치가 아닌 것 |
|
바이오의약품 |
사람이나 다른 생물체에서 유래된 세포, 조직, 호르몬 등을 이용해 유전자 재조합 또는 세포 배양기술을 통해 개발한 의약품 |
|
신약 |
화학구조나 본질 조성이 전혀 새로운 신물질의약품 또는 신물질을 유효성분으로 함유한 복합제제 의약품 |
|
의료기기 |
사람 또는 동물에게 단독 또는 조합하여 사용되는 기구, 기계, 장치, 재료 또는 이와 유사한 제품으로서 질병의 진단, 치료 또는 예방의 목적으로 사용되거나, 구조 또는 기능의 검사, 대체 또는 변형의 목적으로 사용되는 제품 등을 말함. |
|
FDA |
미국에서 식품과 의약품의 인허가를 주관하는 정부 기관. 1931년 설립되었으며, 의약품의 인허가 및 규제, 화장품, 식품 그리고 의료 기기 등에 대한 허가와 규제를 담당하고 있음. 국내에는 이와 유사한 기관으로 식품의약품안전처가 있음. |
|
파이프라인(Pipeline) |
신약 개발 계획을 뜻하는 말로 주로 연구 개발 단계에 있는 품목을 말함 |
|
마일스톤 |
신약 라이선스 계약은 대부분 마일스톤 방식으로 이루어지며, 계약 체결 후 받는 <계약금>, 개발 단계별 성취도에 따라 받는 <단계별 기술료>로 구성됨. 제품 상용화 이후에는 마일스톤과 별개로 판매액 일정비율의 <로열티>를 받음. 마일스톤의 단계별 기술료 세부내역은 치열한 시장 경쟁 상황 등을 고려해 계약 당사자들간 협의에 따라 통상적으로 비공개로 함. ① 확정된 계약금 - 계약 체결 직후 또는 일정기간 내에 받게되는 금액. ② 단계별 기술료 - 전임상 → 임상 → 허가신청 → 허가완료 등 개발 단계별로 성공시에 받게 되는 금액. 개발 종료 시점까지 수년에 걸쳐 나누어 받게 되며, 도중에 여건이 나빠지거나 임상에 실패하여 더 이상 개발하지 않을 경우 일정 금액을 받지 못할 수 있음. ③ 로열티 - 기술 이전으로 생산된 제품의 매출에 따라 받게 되는 금액. 대개 로열티는 매출액 대비 비율로 책정되는데, 로열티를 어느 정도로 할 것인가는 당사자의 협의에 의하는 문제로서 일률적인 기준은 없음. |
|
IND |
Investigational New Drug Application, 임상시험계획신청, 동물실험에서 의약품의 효과와 독성을 확인한 후에 사람에게 임상시험을 하기위해 진행하는 절차. 의사의 엄중한 감시 아래 투약하고, 여러 단계의 임상을 통해서 유효성과 안전성이 최종 확인되면 NDA 신청하게됨 |
|
NDA |
New Drug Application, 신약허가신청, 연구개발부터 동물시험까지 비임상시험결과와 인체를 대상으로 하는 임상시험결과 및 제조까지를 종합하여 식품의약품안전처에 의약품허가를 신청하는 절차 |
|
세포독성 |
물질이 세포의 효소, 구조를 이루는 성분에 영향을 미쳐 세포를 죽일 수 있는 경우 또는 세포의 염색체나 유전자(즉, DNA)의 변형을 유발하는 것 |
|
안전성 |
신약후보물질이 사람이 복용하였을 때 독성이나 심각한 부작용이 없음을 입증하기 위해 실험동물을 통한 안전성 시험이 필수임. |
|
생물학적 안전성 평가 |
원재료 특성분석, 생물학적 안전성 시험 성적서, 관련 문헌 및 임상 보고 등을 통한 종합적인 생물학적 안전성 평가로, 인체에 접촉되는 모든 의료기기에 적용될 정도로 의료기기의 안전성 확보에 절대적인 영향을 미침 |
|
안정성 |
의약품 또는 의료기기가 실제로 취급되는 상황을 생각하여 빛, 열, 온도, pH 등의 영향에 얼마나 안정한가를 알아보는 시험. 약물 또는 화합물이 화학변화를 쉽게 일으키지 않거나 반응속도가 느려 일정 기간동안 일정한 상태를 유지하는 성질 |
|
비임상시험 |
사람을 대상으로 하지 않는 생의학 시험으로 동물에서의 독성과 유효성 시험임 |
|
임상 1상 |
비임상시험(동물을 상대로 한 실험)을 거친 신약을 사람에서 처음으로 평가하는 과정. 비교적 제한된 수의 대상자(약 20-80명)에게 투여되며 약의 종류에 따라 다르지만 대개 건강한 성인을 대상으로 진행함. 안전성을 검토하여 안전용량의 범위를 확인하게 됨. 또한 약물의 체내에서의 흡수, 분포, 대사, 배설에 대한 자료를 수집함 |
|
임상 2상a |
임상시험에 사용되는 의약품의 안전성과 유효성을 증명하기 위하여 해당약물의 약동, 약력, 약리, 임상적 효과를 확인하고 이상반응 등을 평가하기 위하여 사람을 대상으로 실시하는 시험 또는 연구로 사람을 피시험자로 하는 것이기 때문에 윤리적인 배려와 함께 과학적인 방법으로 진행됨 |
|
임상 2상b |
임상 2a의 결과에 따라 설계된 용량을 가지고 다시 환자에 투여, 어느 만큼의 용량이 가장 효과가 있을지 적정 투여 용량의 범위를 정하는 과정 |
|
임상 3상 |
제 2상 임상시험에서 확인된 사항들을 종합적으로 판단하여 유용성이 인정될 때 대상질환 중 조건에 부합되는 다수 환자를 대상으로 효능효과, 용법용량, 사용상의 주의사항 등 전반적인 안전성, 유효성을 확인하여 의약품으로서의 유용성을 결정하는 시험 |
| 전용실시권 | 당사자가 권한을 가지고 임상 진행, 허가 승인, 상업화를 추진 할 수 있음을 의미 |
당사는 현재 자체적으로 3개의 항암 신약 물질에 대한 국내 전용실시권을 보유하고 있으며, 당사가 본 공시서류 제출일 전일 기준 99.30%의 지분을 보유한 종속회사 에이치엘비셀(주)는 바이오인공간, 지혈제(생분해성 의료용 접착제 또는 실란트 조성물), 인간 세포외기질의 3개 분야에서 파이프라인을 구축하고 있습니다. 또한 계열회사인 Elevar Therapeutics("Elevar")는 표적항암제 리보세라닙(Rivoceranib, 舊 Apatinib Mesylate) 관련 라이센스 인(License-in) 계약을 체결하였습니다. 리보세라닙의 경우 위암 말기 치료제 임상 3상을 완료하여 미국식품의약국(FDA)에 NDA 준비중이며, 타 암종으로의 적응증 확대를 위한 단독 및 병용 임상을 지속적으로 진행하고 있습니다. 또한 리보세라닙과 캄렐리주맙(Camrelizumab) 병용요법 간암 1차 치료제는 2023년 5월 미국 FDA에 NDA Submission 완료하였으며, 2024년 5월 17일 FDA로부터 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL(보완요구서한, Complete Response Letter) 수령하였습니다. 파이로티닙의 경우 비소세포폐암과 전이성 유방암은 임상3상을 진행중에 있습니다.
신약(New Drug)은 기존 약물에 모방이나 개량 합성에 의한 것이 아닌, 기존약물의 부작용과 현저한 기능 개선이 포함되어야 하며, 화학합성, 미생물·배양조직세포로부터 유전자재조합을 이용한 생산, 천연물 추출 등의 신물질 탐색 작업, 비임상시험, 임상시험 등을 거쳐 제조 승인을 받은 의약품 입니다. 신약은 제조방식에 따라 합성의약품과 바이오의약품으로 나눌 수 있습니다. 합성의약품은 화학반응을 이용해서 제조하는 저분자 의약품을 뜻하며, 바이오의약품은 세포의 생물학적 반응을 이용해 서 만드는 고분자 단백질 의약품을 의미합니다. 최근 언론에서 흔히 접하는 바이오시밀러라고 하는 것은 바이오의약품의 복제약을 의미합니다.
한 개의 신약이 나오기 위해서는 여러 단계를 거치게 되는데, 먼저 신약 후보물질을 도출하기 위한 탐색 과정을 거칩니다. 이 과정에서는 신약의 효능이나 작용기전을 기반으로 신약개발 대상 물질을 선정합니다. 유효물질(Hit), 선도물질(Lead)을 거쳐 신약 후보물질이 선정되면 후보물질의 안정성과 효과를 확인하기 위해 동물 모델을 대상으로 비임상시험(Pre-Clinical trial)을 진행합니다. 비임상시험을 통해 후보물질의 효과와 안전성을 검증하면 식약처에 임상시험 승인신청 (IND : Investigational New Drug Application)을 하고, 사람을 대상으로 약물의 효과와 부작용을 확인하는 임상시험(Clinical Trial)을 수행합니다. 목표한 임상시험 결과를 얻게된 경우에는 모든 관련자료를 모아서 식약처에 제출하게 되는데, 이를 신약 허가신청(NDA : New Drug Application) 이라고 합니다. 신약 허가 신청이 정상적으로 이루어지면, 제4상 임상시험으로 분류되는 시판후안전성조사(PMS : Post Market Surveillance)를 통해 임상시험에서 발견되지 않았던 광범위한 부작용에 대해서 추적 조사를 수행 합니다.
| [신약개발 단계별 특징] |
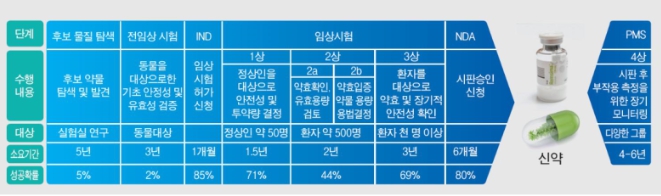 |
|
신약개발 단계별 특징 |
| 출처: 한국신약개발연구조합. 식품의약안전처, 디지털타임즈 기사, Pri-med care.org 홈페이지 등. 한국바이오경제연구센터 재구성 |
임상시험에 대한 구분은 「약사법」시행규칙에서 정의하고 있으며, "임상시험"이라 함은 의약품의 안정성과 유효성을 증명하기 위하여 사람을 대상으로 해당 약물의 약동ㆍ약력ㆍ약리ㆍ임상적 효과를 확인하고 이상반응을 조사하는 시험을 말합니다. 임상시험은 시판 허가 전의 3단계(1상, 2상, 3상)와 시판 후 임상시험(PMS)을 포함하여 총 4단계로 구분합니다.
| [임상시험 구분] |
| 구분 | 목적 | 내용 |
|---|---|---|
| Phase 1 (1상) |
ㆍ안전성 검토 ㆍ내약성 평가 ㆍPK/PD 정의/서술 ㆍ치료효과 추정 |
ㆍ용량-내약성 임상시험 ㆍ안전용량 범위와 부작용 확인 ㆍ체내 약물 동태 검토 ㆍ1a: SAD, 1b: MAD |
| Phase 2 (2상) |
ㆍ단기 유효성/안전성 검토 ㆍ목표 적응증에 대한 탐구 ㆍ후속 시험을 위한 용량 추정 ㆍ치료확증 시험을 위한 시험설계, 평가항목, 평가방법에 대한 근거 제공 |
ㆍ용량-반응 탐색 임상시험 ㆍ소수의 환자에서의 비교적 단기간에 걸친 초기 임상시험 ㆍ2a: 약효확인, 유효용량 검토 ㆍ2b: 약효입증, 유효용량 확인, 유효성 및 안전성의 균형 검토 |
| Phase 3 (3상) |
ㆍ안전성, 유효성 재확인 ㆍ임상적용을 위한 Risk/Benefit의 상대평가 근거제공 ㆍ용량과 반응에 대한 관계 확립 ㆍ효과에 대한 검증 |
ㆍ무작위 배정에 의한 용량-반응 임상시험 ㆍ유효성 확립을 위한 적절하고 잘 통제된 임상시험 ㆍ이환율/사망률을 위한 임상시험 ㆍ충분한 환자에서 유효성 및 안전성 확립 ㆍ대조군을 이용한 비교 임상시험 ㆍ대규모 임상시험 |
| Phase 4 (4상, PMS) |
ㆍ시판 후 안전성 조사 및 추가 임상시험 ㆍ일반 또는 특정 대상군/환경에서 Risk/Benefit에 대한 이해 ㆍ흔하지 않은 이상반응 확인 ㆍ추천되는 용량을 확인 ㆍ모든 시험 디자인이 가능 |
ㆍ장기투여시 부작용 검토 ㆍ안전성 재확립 ㆍ새로운 적응증 등 탐색 연구 ㆍ대조군을 이용한 유효성 임상시험 ㆍ이환율/사망률에 대한 임상시험 ㆍ부가적인 평가 항목에 대한 임상시험 ㆍ약물경제학적 측면의 임상시험 |
| 주1) 약물의 농도-반응 관계를 PK/PD라고 합니다. PK(Pharmacokinetics 약동학)는 약물의 흡수, 분포, 생체 내 변화 및 배설을 연구합니다. PD(Pharmacodynamics 약력학)는 생체에 대한 약물의 생리학적 및 생화학적 작용과 그 작용 기전, 즉 약물이 일으키는 생체의 반응을 주로 연구함 주2) SAD(단회용량상승, single ascending dose) : 단회용량을 투여한 후 안전성과 내약성을 확인함 주3) MAD(다중용량 상승, multiple ascending dose) : 반복 투여를 통해 더 높은 용량으로 증량해가면서 최대 내약 용량을 확인함 |
일반적으로 신약개발은 후보물질 선정, 물리화학 및 생물학적 분석연구, 비임상 및 임상 1상~3상, 품목허가의 단계를 거쳐 시장에 출시되며, 통상 약 10~15년 정도의 오랜 기간이 소요됩니다. 이 중 임상 시험에만 보통 6년 이상의 시간이 소요되며, 비임상 단계에서 안전성 및 효능이 검증되었음에도 불구하고 각 임상 단계에서 부작용 등 예상치 못한 결과로 인하여 의약품 개발에 실패할 위험이 상존합니다. 신약 후보물질을 탐색하고, 유효성을 갖는 물질을 개발하기까지도 낮은 성공률을 보이지만, 임상 단계에 진입하여 최종 신약 등록을 마치는 데에도 성공 확률은 높지 않습니다.
이렇듯 신약연구개발 사업은 대표적인 '고위험 고수익형' 사업으로 당사 뿐 아니라 신약개발 업종을 영위하는 회사들에게는 필연적인 실패 위험이 있습니다. 임상단계의 높은 불확실성 뿐만 아니라 승인을 받은 경우에도 상업적인 성공으로 직결되지 않아, 마일스톤 달성 후 추가 자금이 유입되지 않을 가능성도 존재합니다. 따라서 막대한 투자 비용을 줄이고 위험을 감소시키기 위한 목적으로 일부 회사들은 개발 초기부터 국내외 제약사들과 공동 연구개발을 하거나 License-out(라이센스 아웃, 기술이전)을 통하여 연구개발비 부담을 줄이고 사업화 가능성을 높이는 전략을 취하고 있습니다. 당사 및 당사의 계열회사의 경우에도 타겟 시장에 따라 직접 판매 또는 기술이전을 목표로 신약개발에 집중하고 있으나, 임상 연구개발이 지연되거나 라이센스 아웃에 따른 수익이 실현되지 않을 경우 당사의 향후 사업계획에 차질이 발생할 수 있습니다.
FDA(Food and Drug Administration)는 미국의 식품의약국으로 미국에서 생산 및 유통, 판매되는 모든 종류의 의약품에서부터 의료기기, 화장품, 식품 등의 품목에 대 해 통제, 관리, 승인을 하는 기관입니다. FDA는 의약품 등에 대해 전세계에서 가장 엄격하고 신중하게 관리 및 승인하는 기관으로 FDA 에서 승인된 신약은 매우 안전 하고 뛰어난 약효를 가진 신약으로 인정을 받기 때문에 사실상 전세계 어디에서나 특별한 절차 없이 출시가 가능하게 됩니다.
FDA에서의 임상 단계별 성공 가능성을 추정하기 위해서, 2011년부터 2020년까지 과거 10년간 FDA에서 임상을 수행했거나 진행중인 자료를 조사해보면 여러 특징적인 사실들이 보여집니다. 모든 임상들에 대해 임상 1상에서 신약승인까지의 신약 승인 성공률은 평균 7.9%입니다. 임상 1상 통과 가능성은 52.0%이고, 임상 2상은 각 임상 단계별로 가장 낮은 28.9%입니다. 일반적으로 임상 2상은 개념 증명(입증)을 환자를 대상으로 시험하는 첫 번째 단계임으로, 기업이 고가의 대규모 임상 3상 연구로의 진입 여부를 결정해야 하는 중요한 지점입니다. 임상 3상의 경우 57.8%, 신약 승인 단계인 NDA/BLA는 가장 높은 90.6%의 성공률을 기록하였습니다..
| [FDA 임상 시 각 단계별 성공 가능성] |
 |
|
FDA 임상 시 각 단계별 성공 가능성 |
| 주) NDA - New Drug Application , 합성 의약품의 신약승인 단계 BLA- Biologic License Application, 바이오 의약품의 신약승인 단계 출처: Clinical Development Success Rates and Contributing Factors 2011-2020 |
종양질환의 경우 의약품 시장에서 가장 큰 부문을 차지하는 질환이지만, 임상 1상부터 허가승인까지의 성공률은 5.3%로 가장 낮은 성공률을 기록하였습니다. 2016년에 발표된 보고서와 비교하면 이전의 5.1% 대비 소폭 증가한 수치입니다. 그러나 여전히 종양질환의 허가승인 성공률은 모든 적응증의 평균 성공률인 7.9%에 비해 낮은 수준입니다.
| [주요 질환 군별 FDA 임상 성공 가능성 (임상 1상~신약승인)] |
 |
|
주요 질환 군별 fda 임상 성공 가능성(임상 1상~신약승인) |
| 주) Hematology - 혈액질환 / Metabolic - 대사질환 / Infectious disease - 감염질환 / Other - 기타질환 / Ophthalmology - 안질환 / Autoimmune - 자가면역질환 / Allergy - 알레르기질환 / Gastroenterology - 소화기질환 / Respiratory - 호흡기질환 Psychiatry - 정신질환 / Endocrine - 내분비 질환 / Neurology - 신경질환 Oncology - 종양질환 / Cardiovascular - 심혈관질환 / Urology - 비뇨기질환 출처: Clinical Development Success Rates and Contributing Factors 2011-2020 |
| [각 질환의 FDA 임상 단계별 허가승인 가능성] |
| (단위 : %) |
| 구분 | 임상 1상~ 신약승인 |
임상 2상~ 신약승인 |
임상 3상~ 신약승인 |
NDA/BLA~ 신약승인 |
|
|---|---|---|---|---|---|
| 혈액질환 | Hematology | 23.9 | 34.4 | 71.5 | 93.1 |
| 대사질환 | Metabolic | 15.5 | 25.0 | 55.7 | 87.5 |
| 감염질환 | Infectious disease | 13.2 | 22.8 | 59.4 | 92.9 |
| 기타 | Others | 13.0 | 20.5 | 53.0 | 88.4 |
| 안질환 | Ophthalmology | 11.9 | 16.6 | 46.7 | 91.1 |
| 자가면역질환 | Autoimmune | 10.7 | 19.3 | 61.4 | 94.1 |
| 알레르기질환 | Allergy | 10.3 | 18.3 | 64.7 | 100.0 |
| 소화기질환 | Gastroenterology | 8.3 | 17.8 | 51.9 | 90.9 |
| 호흡기질환 | Respiratory | 7.5 | 13.5 | 61.6 | 95.6 |
| 정신질환 | Psychiatry | 7.3 | 13.8 | 51.4 | 91.2 |
| 내분비질환 | Endocrine | 6.6 | 15.2 | 57.1 | 86.3 |
| 신경질환 | Neurology | 5.9 | 12.3 | 46.0 | 86.7 |
| 종양질환 | Oncology | 5.3 | 10.8 | 43.9 | 92.0 |
| 심혈관질환 | Cardiovascular | 4.8 | 9.6 | 45.6 | 82.5 |
| 비뇨기질환 | Urology | 3.6 | 8.8 | 58.6 | 84.6 |
| 모든 적응증 | All indications | 7.9 | 15.1 | 52.4 | 90.6 |
| 주) 기타 - 피부질환, 신장질환, 임산부질환, 류마티스질환, 이비인후질환, 구강질환, 정형외과질환 포함 출처: Clinical Development Success Rates and Contributing Factors 2011-2020 |
2011~2020년 간 임상 1상에서 허가승인까지의 평균 소요시간은 10.5년으로, 이에 임상 과정 시간 증가에 따른 리스크는 기업에게 위험요소로 작용하고 있습니다. 항암제 개발기간의 경우 임상기간은 10.3년으로 전체 평균과 비슷하나 다른 질환군과 다르게 임상 1상이 길고 품목 허가 신청기간이 짧은 편입니다.
앞서 상술한 바와 같이 바이오의약품 제품 개발에 있어 각 단계별 제품 실패 가능성이 존재하며, 이는 신약을 연구개발하는 회사들에게는 공통적으로 적용되는 부분입니다. 당사는 현재 자체적으로 3개의 항암 신약 물질에 대한 국내 전용실시권을 보유하고 있으며, 당사가 99.30%의 지분을 보유한 종속회사 에이치엘비셀(주)는 바이오인공간, 지혈제(생분해성 의료용 접착제 또는 실란트 조성물), 인간 세포외기질의 3개 분야에서 파이프라인을 구축하고 있습니다.
공시서류 제출기준일 현재 당사 및 종속기업이 보유한 파이프라인 연구개발 진행 중인 연구개발(Elevar Therapeutics, Inc.주도 글로벌 임상 포함) 현황은 다음과 같습니다.
| [연구개발 진행 총괄표] |
|
구 분 |
품 목 |
적응증 |
임상시작일 |
현재 진행단계 |
임상주도 기업 | ||||
|---|---|---|---|---|---|---|---|---|---|
|
단계(국가) |
승인일 |
비 고 | 회사명 | 비고 | |||||
|
화학합성 |
신약 |
리보세라닙 (Rivoceranib) [Elevar Therapeutics, Inc.주도 글로벌 임상 포함] |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안정성평가 완료 | Elevar | Rivoceranib 전용실시권 도입 후 자체 개발 |
|
위암 (3차/4차 단일요법) |
2017년 |
임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
Elevar | Rivoceranib 전용실시권 도입 후 자체 개발 | |||
|
위암 (1차 병용요법) |
2021년 |
임상2상 |
2021년 09월 (임상2상 승인일) |
임상 진행 중 | HLB생명과학 | Rivoceranib 한국 내 전용실시권 도입 후 개발 |
|||
|
간암 (1차 병용요법) |
2019년 |
임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
- 임상 종료, 22년 9월 초록 발표(1차 평가 지표 만족) - 23년 5월 미국 FDA에 NDA Submission 완료 - 24년 5월 미국 FDA 수정 보완 요구(CRL 수령) |
Elevar | 항서제약과 공동개발 | |||
|
선양낭성암종 (1/2차 단일요법) |
2020년 |
임상2상 |
2020년 4월 (임상2상 개시일) |
임상 2상 종료 6월 초록 발표, |
Elevar HLB생명과학 |
Rivoceranib 전용실시권 도입 후 자체 개발 |
|||
|
위암 (2차 병용요법) |
2018년 |
임상2상 |
2018년 10월 (임상1상 개시일) |
임상 종료 22년 결과 발표 |
HLB생명과학 | Rivoceranib 전용실시권 도입 후 자체 개발 |
|||
|
대장암 (3차 병용요법) |
2019년 |
임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 종료 |
Elevar | Rivoceranib 전용실시권 도입 후 자체 개발 |
|||
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상 진행 중 (농림축산검역본부) |
HLB생명과학 | Rivoceranib 한국 내 전용실시권 도입 후 자체 개발 |
|||
| 파이로티닙 (Pyrotinib) |
전이성 유방암 | 2023년 | 임상3상 (한국) |
2023년 03월 (임상계획 승인) |
임상3상 진행 중 | HLB생명과학 | Pyrotinib 한국 내 전용실시권 도입 후 자체 개발 |
||
| 비소세포폐암 | 2020년 | 임상3상 (전세계 13개국) |
2020년 (임상계획 승인) |
임상3상 진행 중 | 항서제약 | Pyrotinib 한국 내 전용실시권 도입 후 자체 개발 |
|||
|
HLS221-N01 G2M 억제제 |
폐암 유방암 대장암 췌장암 |
- |
비임상시험 단계 |
- |
비임상평가 진행 중 |
HLB생명과학 |
특허권 도입 후 자체 개발 | ||
|
HLS222-N01 Cannabinoids derivatives |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
HLB생명과학 |
네오켄바이오와 공동연구 | ||
|
HLS232-N01 CDK 억제제 |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
HLB생명과학 |
LDC와 공동연구 | ||
|
HLS231-G01 의료용 대마 |
뇌전증 | - | 탐색 단계 | - | 제형 연구 중 | HLB생명과학 R&D |
- | ||
|
바이오 |
신약 |
바이오인공간 |
급성간부전 |
2001년 |
임상 2b상 |
2017년 임상 2a 완료 |
자체 개발 |
HLB셀 | - |
|
의료기기 |
지혈제 |
조직/장기 출혈 |
2015년 |
확증임상시험 |
2021년 임상계획 승인 |
확증임상 진행 중 |
HLB셀 | UI-DDS 연구소 글로벌 권리 도입 후 자체 개발 |
|
| 연구용 재료 | 인체 세포 외 기질 (Hutrigel®-RU) |
줄기세포, 오가노이드 배양 기질 | N/A | 연구개발완료 | N/A | 제품판매 준비 중 |
HLB셀 | 자체 개발 | |
| 의료기기 | 인체 세포 외 기질 (Hutrigel®-MU) |
피부, 신경, 심근 등 상처 치유 및 조직 재생 |
N/A | 연구개발 중 | N/A | GMP-compliant , 비임상 유효성평가 준비 중 |
HLB셀 | 자체 개발 | |
|
의료기기 |
인체 세포 외 기질 (Hutrigel®-AU) |
의료용/미용용 기능성 제품 |
N/A |
연구개발 중 |
N/A |
제형화 및 생체 외 |
HLB셀 HLB제약 |
자체 개발 | |
|
주1) 당사는 2018년 8월 14일에 리보세라닙(아파티닙) 관련 부광약품에 인정되는 계약상 지위, 권리 및 의무 일체를 취득하여 연구개발을 진행하고 있습니다. (2018.8.14 공시 참조)
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(1) Rivoceranib(리보세라닙)
당사는 HLB(주)의 자회사인 LSK BioPartners, Inc.(現 Elevar Therapeutics)이 2009년 부광약품(주)에 양도한 리보세라닙의 권리와 관련하여 2018년 8월 14일에 부광약품(주)으로 부터 계약상 지위, 권리 및 의무 일체를 취득하여 연구개발을 진행중에 있으며, 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있습니다. 계약 상세 내역은 하기와 같습니다.
| [[리보세라닙(Rivoceranib) 계약정리] |
|
계약상대방 |
부광약품, Elevar Therapeutics, Inc.(구,HLB USA, Inc.) |
|
계약내용 |
Rivoceranib에 대한 한국 내 독점 개발, 판권 및 일본, 유럽에 대한 수익 지분(14.5%) 허여 |
|
대상지역 |
대한민국, 일본, 유럽 |
|
계약기간 |
유효특허의 만료일까지 (2029년 6월 예상) |
|
총계약금액 |
총 447억원 |
|
지급금액 |
총 401억 7천만원 |
|
계약조건 |
1) 부광과 Elevar Therapeutics, Inc.(구,HLB USA, Inc.)(*)간의 계약조건 그대로 양도양수 (한국내 독점개발, 판매권 및 유럽, 일본에 대한 수익 지분) |
| 회계처리 | 매수금액 및 개발 마일스톤 401억 7천만원은 반환의무 및 조건이 없고 관련하여 수행할 추가적인 의무가 존재하지 않아 신약연구개발 라이선스 자산으로 인식함. |
| 대상기술 | 경구용 제품이며, 광범위하게 적용되는 항암제로 진행형 고형암(위암, 대장암, 간세포암, 폐암(비소세포암), 유방암, 중피종, 신세포암, 신경내분비종양)에서 신생혈관 억제, 직접적인 항종양 효과, 면역세포의 활성화를 통해 항암효과가 있음. |
|
기타사항 |
Elevar Therapeutics, Inc. 는 2009년 12월 부광약품㈜에게 리보세라닙의 한국 판권을 양도하는 조건으로 리보세라닙 공동개발을 하였으며, 이후 부광약품㈜은 2018년 08월 한국 판권에 대한 모든 권리 및 의무를 HLB생명과학으로 400억원에 양도하였습니다. (2018.8.14 공시 참조) |
당사의 계열회사인 Elevar Therapeutics("Elevar")는 리보세라닙에 대하여 중국,한국을 제외한 세계 판권을 보유하고 있습니다.(한국판권은 당사가 보유함)
| [계열회사 Elevar의 Pipeline 현황] |
| 품목명 | 적응증 | 특징 |
|---|---|---|
| 리보세라닙 (Rivoceranib) |
위암 간암 대장암 선양낭성암 |
1. 특징 - Oral : 경구용 제품으로 낮은 생산단가 2. 임상시험 현황 - 위암 말기 : 단독요법 - 간암 1차 : 캄렐리주맙과 병용요법 - 대장암 3차 : 론서프와 병용요법 - 위암 2차 : 파클리탁셀과 병용요법 - 선양낭성암 : 단독요법 |
| 출처: 당사 제공 자료 |
Elevar는 리보세라닙 위암 말기 단독치료제를 목적으로 하는 3상 임상시험 완료 후 데이터를 확정하여 2019년 10월 미국 FDA와 Pre-NDA 미팅을 하였으며, 그 결과를 바탕으로 최종 Data분석 및 적절한 허가 전략을 수립한 후, 신약허가를 신청할 계획입니다. 리보세라닙은 위암에 대해 희귀의약품으로 지정(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국)됨에 따라 임상종료 후 시판허가에 대한 신속화, 수수료 감면 등의 혜택과 더불어 이후 최소 8년(2029년까지)에서 최대 13년(2034년까지)동안 독점 판매할 수 있습니다. 특히, 위암에 대해서는 중국에서 항서제약이 임상 3상을 종료 후 시판허가를 득하여 현재 중국에서 판매되고 있습니다. 현재 당사는 특허기간 등을 고려하여 리보세라닙 단독 요법 보다는 캄렐리주맙 병용요법에 집중하고 있습니다. 리보세라닙(HLB)과 캄렐리주맙(항서제약) 병용요법의 간암 1차 치료제 경우, 2023년 5월 NDA(신약 허가신청)를 신청하였으며, 7월 NDA 본심사가 개시되었습니다. 2023년 8월 리보세라닙 공장실사 및 12월 캄렐리주맙 공장실사까지 완료하였으나, 2024년 5월 미국 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL(보완요구서한, Complete Response Letter) 수령하였습니다. CRL 통한 요구 사항은 1) 병용투여 약물인 캄렐리주맙(항서제약)의 CMC(의약품 생산시설 실사) 진행 후 항서제약이 보완한 사항에 대해 일부 미비한 점에 대한 보완 2) 미국 FDA가 BIMO Inspection(임상사이트 실사)를 여행제한으로 인해 완료하지 못했다는 내용입니다. 계열회사 Elevar Therapeutics, Inc.는 상기 두가지 보완사항에 대해 항서제약과 긴밀히 협의하여 이에 대해 신속히 보완하고 FDA 재승인 신청할 예정이며, 재승인 신청 후 최장 6개월 이내 FDA는 승인여부를 결정하게 됩니다.
| [계열회사 Elevar의 신약 후보물질 개발 추진 현황(리보세라닙)] |
| 구 분 |
개발제품 |
적응증 |
개발현황 및 향후 계획 |
|---|---|---|---|
| 신약개발 | 리보세라닙 (Rivoceranib, 구Apatinib Mesylate) |
표적항암제 |
1) 위암 3/4차 치료제: 단독 요법으로 글로벌 임상 3상 종료 및 조건부 품목허가 및 임상 3상 계획수립 2) 위암 2차 치료제: 파클리탁셀과 병용으로 임상 1/2상 종료 3) 선양낭성암 1,2차 치료제: 단독요법으로 미국, 한국에서 임상 2상 연구 종료, 한국 조건부 품목허가 신청 및 자진 취하 4) 간암 1차 치료제: 항서제약의 캄렐리주맙과 병용으로 글로벌 13개국 임상 3상종료, 2022년 9월 ESMO에서 임상 결과 공개(1차 평가지표 만족), 2023년 5월 미국 FDA에 NDA Submission 완료, 2024년 5월 미국 FDA로부터 CRL(보완요구서한) 수령 5) 대장암 3차 치료제: 타이호제약의 론서프와 병용으로 미국, 한국에서 임상 1b/2상 중 1b상 종료 |
| 출처: 당사 제공 자료 |
(2) Pyrotinib(파이로티닙)
Pyrotinib은 중국 항서제약에서 개발한 HER 1/2/4을 표적으로 하는 경구용 항암제로서 유방암 및 비소세포 폐암을 포함한 HER2의 과발현 혹은 돌연변이를 가지고 있는 고형암에 유효한 약물이며 국내 전용실시권을 보유하고 있습니다. Pyrotinib에 대한 당사 주요 계약은 다음과 같습니다.
| [파이로티닙(Pyrotinib) 계약 정리] |
|
계약상대방 |
항서제약 (Jiangsu Hengrui Medicine Co., Ltd., 중국) |
|
계약내용 |
파이로티닙(Pyrotinib)의 개발, 허가, 판매에 대한 국내 독점권한 및 생산에 대한 선택적 권한 허여 (API 생산 미포함) |
|
대상지역 |
대한민국 |
|
계약기간 |
계약체결일: 2020.09.28 계약종료일: 비용지급 만료 시까지 |
|
총계약금액 |
4,929백만원, 로열티는 별도 |
|
지급금액 |
<환수 불가능 금액> |
|
계약조건 |
계약금(Upfront Payment): 1,995백만원 - 지급조건: 계약 체결 시 마일스톤(Milestone): 로열티(Royalty): |
| 회계처리방법 | 계약금 1,995백만원은 반환의무 및 조건이 없고 관련하여 수행할 추가적인 의무가 존재하지 않아 신약연구개발 라이선스 자산으로 인식함. |
| 대상기술 | EGFR, HER2, HER4를 특이적으로 억제하는 표적항암제이며, 주요 적응증은 HER2(+) 전이성 유방암 또는 HER2 변이성 (엑손20 삽입) 비소세포폐암을 포함한 다양한 암종이 될 수 있음. |
|
기타사항 |
- |
| 출처: 당사 제공 자료 |
| [파이로티닙(Pyrotinib의 개요] |
|
중국 CNDA 조건부 승인일 |
2018년 08월 22일 |
|---|---|
|
- EGFR (EGFR, HER2, HER3, HER4) 신호 전달 활성은 암세포에 있어서 성장과 분열, 전이를 일으키는 주요 원인으로 알려져 있음. - 특히, 15%-20%의 유방암 환자들은 HER2 수용체의 증가가 나타나고 있으며 매우 공격적인 성향을 띔. - 비소세포 폐암에서는 2-3% 정도 HER2 돌연변이가 나타나고 있음. 이에 HER2를 표적하는 다양한 시도가 진행되고 있음. - 현재 해당 기전을 억제하는 약물들은 출시되어 있지만 부작용이 크거나 항암제 저항성이 생기는 현상이 일어남. 또한 충분한 OS(전체 생존 기간)를 달성하고 있지 못함. - Pyrotinib은 EGFR, HER2, HER4 모두를 억제하는 약물로서 하위 기전인 PI3K /AKT 및 MAPK의 신호 전달 기전을 차단하여 암세포의 증식, 분열, 생존을 억제하는 항암제임. - 기존 약물 대비 부작용이 적으며 효력이 동등하거나 우월함 - 중국에서는 임상 2상의 결과를 통해 조건부 허가 및 판매를 승인하였음 - 현재 전이성 HER2 양성 유방암에 대한 중국 내 임상3상 시험이 완료되었음 - 당사에서 2020년 9월 28일에 도입 계약을 체결하였으며 국내 가교 임상 시험 진행을 기획하고 있음 |
|
| 출처: 당사 내부 자료 |
Epidermal growth factor receptor (EGFR) family는 EGFR (ErbB-1, HER1]), HER2 (ErbB2), HER3 (ErbB3)와 HER4 (ErbB)로 구성되며 모두 tyrosine kinase 활성을 갖고 있습니다. 각각의EGFR family는 특정 라이간드의 결합을 통해 활성화되며 이는 PI3'K-AKT 및 RAS-MAPK 경로의 하위 신호 전달을 통해 세포의 성장 등을 조절합니다. 하지만 몇몇 암종에서 EGFR family는 특정 부위의 돌연변이 혹은 과발현을 통해 라이간드 결합 없이도 스스로 높은 활성을 유지하게 되고 이를 통해 암세포의 성장, 전이 및항암제 내성을 획득합니다.
|
[암세포에서 HER2 신호 전달 경로] |
||
|---|---|---|
|
HER2는 알려진 어떤 리간드에도 직접 결합하지 않는 것으로 알려져 있습니다. HER2 매개 신호 경로의 활성화는 리간드-활성화된 EGFR 또는 HER3를 이용한 이형이합체화 활성화된 HER2는 리간드가 결합한 다른 EGFR family 중 하나와의 상호 작용을 통해 EGFR과 유사한 하위 신호 전달을 시작합니다. 모든 EGFR 쌍 중에서 HER2 / HER3 이형이합체는 PI3K의 p85 서브 유닛과 HER3의 결합을 통해 PI3K/AKT 신호 전달을 강력하게 활성화 시키며 동시에 RAS-RAF-MAP 신호전달을 통해서도 하위 신호 전달을 활성화 시킵니다. HER2의 과발현은 주로 HER2 유전자 증폭에 기인하며, HER2 돌연변이 또한 HER2 신호 전달 과정의 활성화를 초래합니다. 이러한 HER2 과발현 및 돌연변이는 유방, 위, 폐, 방광 및 자궁내막암에서 보고되었습니다.
|
특히 유방암 환자의 15-20%가 HER2의 과발현을 가지고 있으며, 비소세포 폐암(NSCLC)에서는 HER2 돌연변이 (exon 20에 12 염기 쌍의 프레임 삽입)가 2%-3% 정도 발생하는 것으로 알려져 있습니다. 이러한 과발현 혹은 돌연변이는 좀 더 공격적인 암 진행과 관련이 있습니다. 유방암 및 비소세포 폐암 환자의 임상 결과는 주로 항HER2 항체 및 그 유도체를 포함한 HER2 표적 치료법의 개발로 크게 향상되었습니다. 특히 Tyrosine kinase inhibitors (TKIs)와 trastuzumab-emtansine과 같은 항체-약물 결합체는 지금까지 많은 연구가 진행되었습니다. 하지만 이러한 항암제들에 대해 저항이 생기는 현상이 나타나고 있기 때문에 현재 결과를 개선하고 저항을 극복하기 위해 추가 항암제가 더 개발되어야 합니다.
|
[HER2 신호 전달 경로 관련 주요 항암제 개발 현황] |
|
개발명 |
표적/제형 |
회사명 |
|---|---|---|
|
Trastuzumab |
HER2 |
Roche |
|
Pertuzumab |
HER2 |
Roche |
|
Trastuzumab-emtansine |
HER2 |
Roche |
|
Lapatinib |
HER1/2 |
Novartis |
|
Neratinib |
HER1/2/4 |
Puma Biotechnology |
|
Tucatinib |
HER2/3 |
Seattle Genetics |
| 출처 : 당사 내부자료 |
Pyrotinib은 중국 항서제약에서 개발한 HER 1/2/4을 표적으로 하는 경구용 항암제로서 유방암 및 비소세포 폐암을 포함한 HER2의 과발현 혹은 돌연변이를 가지고 있는 고형암에 유효한 약물입니다. Pyrotinib은 이미 안트라시클라인 또는 탁산 화학요법으로 치료한 환자에서 HER2 양성, 전이성 유방암 치료를 위해 카페시타빈과 함께 병용하는 항암제로서 2018년 8월에 중국식약처 (CFDA)로부터 조건부 승인을 받은 후 2020년 7월에 정식 승인을 받았습니다. 또한, HER2 양성 유방암을 대상으로 현재 Trastuzumab/Docetaxel과 병용요법에 대한 임상시험도 진행 중에 있습니다. 당사는 전이성 HER2 양성 유방암과 초기 및 국소 진행성HER2 양성 유방암에 대해 허가 신청을 위한 3상 임상 시험을 진행할 예정입니다.
유방암과 별도로 Pyrotinib에 대해 HER2 변이성(엑손20 삽입) 비소세포폐암(NSCLC)을 대상으로 하는 글로벌 임상3상 시험이 진행중이며, 한국에서는 2020년 12월에 식약처로부터 IND 승인을 받아 서울아산병원, 분당서울대병원, 삼성서울병원, 연세대 세브란스병원, 고려대병원 등 국내 7개 병원에서 비소세포폐암 환자를 대상으로 Docetaxel 대비 Pyrotinib의 유효성과 안전성을 비교하는 임상 시험이 진행되고 있습니다.
최근의 연구 결과들을 보면 HER2를 표적으로 하는 항체 또는 저분자 약물은 HER2 양성 유방암을 뚜렷하게 개선하고 있습니다. 이러한 HER2 표적 치료제에는 항 HER2 항체 (trastuzumab and pertuzumab), 항체-약물 결합체(ado-trastuzumab emtansine) 및 저분자 저해제 (Lapatinib, Neratinib, Afatinib, Tucatinib) 등이 있습니다. 하지만 이러한 치료제는 각각 저항성 기전에 의한 항암 효과 감소 및 인체에 대한 부작용 문제를 갖고 있습니다. 당사는 Pyrotinib이 기존 항암제들이 갖는 한계점을 극복할 수 있는 새로운 대안 치료제라고 판단하고 있습니다.
(3) 바이오인공간, 지혈제 (의료용 접착제, 실란트)
당사가 99.30%의 지분을 보유한 종속회사 에이치엘비셀(주)는 바이오인공간, 지혈제(생분해성 의료용 접착제 또는 실란트 조성물), 인간 세포외기질의 3개 분야에서 파이프라인을 구축하고 있으며, 바이오인공간 및 지혈제에의 특성은 다음과 같습니다.
| 품목명 | 특징 |
|---|---|
| 바이오인공간 (LifeLiver system) |
- 간 기능이 손실된 간부전환자의 간 기능을 체외에서 대신하여 주는 국내 최초 '세포치료제 + 의료기기(4등급)' 복합제품 형태의 첨단 세포치료제 - 간부전환자는 LifeLiver system을 통해 손상된 간이 재생, 회복될 때까지 또는 간 이식을 받기 전까지 생명을 연장할 수 있음 - LifeLiver system은 간 손상으로 제거하지 못한 체내 독소로 인하여 발생하는 뇌병증을 감소 시킴으로써 간 이식 이후 예후 기대 |
| 생분해성 의료용 접착제, 실란트 (BleeFix®) |
- 외과 수술용 체내 흡수성 지혈제품 (의료기기 4등급) - 수술과정이나 부상으로 인한 조직 손상 및 출혈에 조직접착/지혈을 목적으로 한 제품으로 수일내에 체내에 흡수되어 기존 제품대비 우수한 접착력과 지혈능력 보유 |
|
인체 세포 외 기질 (Hutrigel®) |
- 인간 정상세포를 체외에서 배양하여 생산한 단백질 혼합체 - 상피, 신경세포 등의 성장, 이동, 분화 등에 영향을 미치는 구조 단백질인 기저막 성분을 함유 - 연구용 제품 및 의료용 제품으로 개발할 예정임 |
| 출처: 당사 내부자료 |
| [바이오인 품목 설명] |
|
구 분 |
바이오 신약(세포치료제) |
|
적응증 |
급성 간부전(Acute hepatic failure) |
|
작용기전 |
바이오인공간은 무균돼지의 간세포를 최적의 간기능을 유지하는 형태로 배양하는 생물반응기를 사용하여 신장투석과 유사한 체외순환의 형태로 환자의 혈액내 독성물질을 제거하고 유용한 물질을 분비하도록 하여 간부전 환자의 간기능을 보조함으로써 생명을 연장하는 것을 목적으로 함 |
|
제품의특성 |
1) 충분한 양의 간세포 - 기존 바이오인공간과 비교하여 가장 많은 양의 신선한 간세포를 적용 2) 간세포 구형 응집체(구상체) 사용 - 간세포 구상체는 환자 혈장 접촉 조건에서 단일 간세포보다 월등히 높은 간기능을 더 오래 유지함 3) 미세캡슐화로 면역장벽과 넓은 표면적 제공 - 간세포 구상체를 직경 1 mm의 칼슘-알긴산 미세캡슐화를 통해 면역세포와 항체로 인한 간세포 손상을 방지하고, 기존 중공사막 반응기 보다 약 50% 증대된 접촉 표면적을 제공 |
|
진행경과 |
- 2017년 12월 임상시험 1/2a상 종료 - 임상시험 2b 진행 중(시작일: 2019.03.29) |
|
향후계획 |
- 현재 임상시험 2b상 진행 중으로 임상 2b 종료 후 품목허가 진행 예정임. |
|
경쟁제품 |
- 국내 유일한 바이오인공간 개발 제품임 |
|
관련논문 등 |
- Functional Evaluation of a Bioartificial Liver Support System Using Immobilized Hepatocyte Spheroids in a Porcine Model of Acute Liver Failure, Sci Rep, 2017 - Effect of fulminant hepatic failure porcine plasma supplemented with essential components on encapsulated rat hepatocyte spheroids, Transplant Proc, 2012 - Potentiality of immobilized pig hepatocyte spheroids in bioartificial liver system,Transplant Proc, 2012 - Current Status of Development of Bioartificial Liver Systems for the Treatment of Acute Liver Failure, Tissue Eng Regen Med, 2008 |
|
시장규모 |
- 2016년도 국내: 1,500억원(기술보증기금 2017.03.09) - 2034년도 국내: 3,145억원(기술보증기금 2017.03.09) - 2016년도 미국/유럽: 120억달러(Vital therapies Inc. 2016.8) |
| 출처: 당사 내부자료 |
바이오인공간은 생물학적 요소가 완전히 배제된 형태인 『인공간(Artificial Liver)』의 한계를 극복하기 위해 생체 조직이나 세포와 결합한 "하이브리드형"의 인공장기를 "Bio-Artificial Liver", 즉 "바이오인공간"으로 구분하여 명명합니다.
바이오인공간의 대상환자는 일주일 내로 간이식을 받지 않으면 생명을 유지할 수 없는 환자가 대부분으로 기증간이 발생하여 간이식을 받을 수 있을 때까지 생명을 연장하고 또한 간이식을 받더라도 간부전에 동반되는 뇌병증 등의 후유증을 예방하여 간이식의 예후를 향상시키기 위한 Bridge(다리) 역할을 합니다.
간기능이 손실된 간부전환자의 간기능을 체외에서 대신하여 주는 국내 최초 '세포치료제 + 의료기기(4등급)' 복합제품 형태의 첨단 바이오의약품(세포치료제)이며, 삼성서울병원과 함께 개발한 바이오인공간의 "급성 간부전 환자에서 바이오인공간(체외순환형생인공간)의 안전성을 평가하고 유효성을 탐색하기 위한 1/2a 임상시험"을 2017년 3월에 종료하고, 임상보고서를 제출하였습니다. 2015년 3월 식품의약품안전처로부터 "개발단계 희귀의약품"으로 지정 고시되었고, 2018년 11월 임상 2b IND 승인 후 2019년 3월 임상시험이 개시되어 현재 임상시험을 진행 중에 있습니다.
| [생분해성 의료용 접착제 또는 실란트 조성물 품목 설명] |
|
구 분 |
의료기기 |
|
적응증 |
조직/장기 출혈, 창상 |
|
작용기전 |
파우더형태의 제품으로 수액과 만나면 겔화되어 창상 보호 및 물리적 압박에 의한 지혈 |
|
제품의특성 |
생체유래 물질인 글라코사미노글라이칸(glycosaminoglycan, GAG)를 기반으로 하여 만든 파우더 형태의 제품으로 장기/조직 손상부위 및 출혈부위에 분사하여 조직 접착 및 지혈 작용을 하고, 창상 부위를 보호할 수 있는 의료기기임 |
|
진행경과 |
- 본 기술에 대해 2015년 11월 (재) 유타 인하 디디에스 및 신의료기술개발 |
|
향후계획 |
- 확증임상시험 대상자수 조정 재승인(2022.01.14) - 확증임상시험 완료 후 품목허가 예정 |
|
경쟁제품 |
지혈 단백질인 피브리노겐을 사용하는 제품인 Tisseel(다림바이오텍), Tachosil(현대약품), Floseal(Baxter) 등이 있음 ※ 객관적인 자료출처를 통한 경쟁제품 간 시장점유율 비교가 불가능하여 기재를 생략합니다. (자료 구매에 1천만원 가량 소요됨) |
|
관련논문 등 |
- Evaluation of anti-hemorrhagic efficiency of a highly adhesive powder in a swine model, 2017년 한국화생방방어학회 학술대회 - 생체모방고분자를 이용한 신속지혈제 개발에 관한 연구, 2017년 한국군사과학기술학회 |
|
시장규모 |
- IMS 데이트에 따르면, 국내 수술용 국소 지혈제 시장은 2015년 513억여원으로 연평균 10%이상 성장하고 있음 - MedMarket Diligence에 따르면, 세계 의료용 지혈제 시장 규모 역시 2015년 72억 달러로 연평균 12%의 성장이 예상됨 |
|
정부보조금 |
- 지혈제 개발과 관련하여 2016년 민군겸용기술개발사업의 참여기관으로 선정되어 총 33억원을 지원받음(2016년 ~ 2021년) - '범부처의료기기연구개발사업(R&D) / 의료기기 사업화 역량 강화'에 선정되어 연구비 8.3억원 지원 중(2022년 ~ 2024년) |
| 출처: 당사 내부자료 |
또한, 생분해성 의료용 접착제 또는 실란트 조성물 기술은 파우더 형태의 체내용 흡수성 지혈제, 조직접착제 및 창상피복재 용도로, 일회용 디바이스(device) 내에 담겨있는 파우더를 장기의 조직이나 혈관 출혈 부위에 분사하는 제품입니다. 사전혼합 및 준비가 되어 있어 사용 전 별도의 절차가 필요 없고 적용(출혈, 장기/조직손상)부위에 즉각적으로 사용 가능하고, 생체물질 기반이므로 체내에 흡수되는 제품입니다. 생분해성 의료용 접착제 또는 실란트 BleeFix®는 최근 의료용 조직 접착제에서 요구되는 사항인 무독성, 생분해성, 사용 및 보관의 편리성, 빠르고 강한 접착력, 유착방지 효과 등에 대해 만족하는 제품입니다. HLB셀은 2016년 민군겸용기술개발사업에 선정되어 임상시험용 제품 개발을 완료하고, 2019년 6월부터 간절제 수술 환자를 대상으로 탐색임상시험을 진행하여 2020년 7월 완료하고 2021년 8월부터 확증임상시험을 진행 중에 있습니다.
신약개발은 시간과 노력에 비해 성공확률이 낮기 때문에 높은 위험 부담이 있음에도 불구하고, 성공 시 창출되는 높은 경제적 가치를 고려했을 때 매력적인 산업일 수 있습니다. 하지만 새로운 의약품이 개발되어 소비자에게 전달되기까지는 오랜 기간과 많은 비용 및 노력이 필요하며, 초기 개발 단계에서 실제 시판으로 이어질 확률은 10,000분의 1 정도로 낮은 편입니다. 따라서 당사에서 진행 중인 신약개발 역시 높은 실패위험 속에 진행되고 있습니다.
또한, 당사는 상기 언급한 파이프라인의 제품 개발을 위한 연구개발 및 임상을 위해 지속적인 노력을 쏟고 있습니다. 하지만 임상시험이 성공하고 제품이 시판되더라도,경쟁사 제품이 당사 제품보다 더욱 빨리 시판되거나, 관련 시장을 먼저 선점할 경우 추후 당사의 연구개발 성과가 상대적으로 저평가 될 수 있습니다.
당사가 개발 중인 항암치료제, 의료용 접착제 및 실란트 조성물 등의 경우 당사 외에도 다수의 제약회사들이 개발을 진행 중에 있으며, 개발단계가 당사보다 앞서 있거나 이미 시판중인 제품을 보유한 회사들도 존재합니다. 따라서 당사 제품의 개발이 성공적으로 완료되어 시장에 출시되더라도 기 출시된 타 제품 대비 차별성이 크지 않을 경우 교체 수요 저하로 매출 확대에 어려움이 존재할 수 있으며, 당사 제품보다 효능이 뛰어난 의약품이 출시될 경우 당사 제품에 대한 수요가 감소할 수 있습니다. 또한, 당사가 주력하고 있는 파이프라인보다 경쟁신약의 연구개발 단계가 선행되거나, 경쟁신약의 효능이 당사 개발 신약보다 뛰어나다고 판명되는 등 관련 경쟁에서 당사가 뒤처질 경우, 당사의 파이프라인 상에서 발생되는 매출이 적어지거나 발생하지 않을 가능성이 있으며, 이는 기존에 신약 개발에 투자한 당사의 수익성에 부정적인 영향을 끼칠 수 있습니다. 특히 당사의 경우 최대주주인 에이치엘비가 리보세라닙과 캄렐리주맙 병용요법 관련하여 2024년 5월 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL(보완요구서한)을 수령하였습니다. 이와 관련하여 항서제약의 CMC(의약품 생산시설 실사) 보완 및 BIMO Inspection(임상사이트 실사) 완료 시기에 대한 불확실성이 있습니다. 또한 당사는 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있어 FDA 재승인 신청 후 판매승인 시점이 지연될 경우 당사 및 당사 관계회사의 수익성과 주가에도 부정적으로 작용할 가능성이 있으니 투자자께서는 유의하시기 바랍니다.
|
마. 정부정책 및 규제에 관한 위험 제약산업은 인간의 생명 및 건강과 직결되는 의약품을 개발ㆍ제조ㆍ판매하는 산업으로, 제품의 개발ㆍ제조, 임상시험, 인ㆍ허가, 유통ㆍ판매에 이르기까지 전 과정에 걸쳐 각 국가의 규제 당국이 제시하는 엄격한 규정과 절차를 따라야 합니다. 당사는 내부에 담당 인력과 외부 전문가들을 통하여 국내 및 해외 제약 산업 정책 및 규제 환경을 지속적으로 모니터링하고 있으며, 각국의 규제 당국과의 소통을 통해 정책 및 규제 환경의 변화에 효과적으로 대비하기 위해 최선의 노력을 다하고 있습니다. 그러나 실제 효율적인 정책 지원이 이루어지지 않거나, 세부 과제 추진에 어려움이 생길 수 있으며, 관련 법규의 제정 및 개정 단계, 예산 확보 등에 난항이 발생할 수 있습니다. 또한 해당 정책의 기대효과가 감소되는 경우 정책 기조의 변화로 정부 지원이 축소될 수 있으며, 조건부 허가와 같은 규제 완화에 대한 실효성이 크지 않을 경우, 규제 완화의 범위가 축소될 수 있습니다. 이러한 정부의 우호적인 정책 및 규제 완화의 변동 가능성은 당사의 사업에 부정적인 영향을 끼칠 수 있습니다. |
제약산업은 인간의 생명 및 건강과 직결되는 의약품을 개발ㆍ제조ㆍ판매하는 산업으로, 제품의 개발 및 제조, 임상시험, 인허가, 유통 및 판매에 이르기까지 전 과정에 걸쳐 각 국가의 규제 당국이 제시하는 엄격한 규정과 절차를 따라야 합니다. 제약 및 신약개발 사업과 관련된 국내 법률 중 당사의 사업과 밀접하게 연관된 법률로는 식품의약품안전처 및 보건복지부 소관의「약사법」이 대표적이며, 그 외 보건복지부 소관의 「국민건강보험법」, 「생명윤리 및 안전에 관한 법률」, 「제약산업 육성 및 지원에 관한 특별법', 「희귀질환관리법」, 「첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률」과 식품의약품안전처 소관의 「실험동물에 관한 법률」 등이 있습니다.
특히, 「약사법」 하위 시행령/시행규칙 중 의약품 등의 안전에 관한 규칙, 의약품 등의 제조업 및 수입자의 시설기준령 시행규칙, 생물학적 제제 등의 제조ㆍ판매관리 규칙, 동물용 의약품등 취급규칙 등과 이의 하위 규정을 준수해야 합니다. 이에 따라, 신약 후보물질의 발굴에서부터 동물을 대상으로 하는 비임상시험, 인체를 대상으로 하는 임상시험, 품목허가에 이르기 까지 임상 승인에 관한 규정, 의약품의 약리 및 독성, 안정성 시험 기준, 임상시험 실시기관 지정에 관한 규정, 품목허가ㆍ심사 등의 규정 등을 반드시 준수하여 진행해야 합니다. 또한 제조 및 판매 단계에서도 제조소 시설 기준, 제조 및 품질관리 규정, 포장 및 공급에 관한 규정, 표시 등에 관한 규정을 준수해야 하며, 사후에도 정기적으로 규제기관으로부터 제품 생산 공정 및 품질관리 전반에 대한 실사 및 관리, 감독을 받게 됩니다. 이러한 규제 및 검증을 통해 제약산업의 선진화 정책을 시현할 수 있지만, 각종 규제 및 절차, 검증 강화로 인한 부담이 높아지는 경우, 당사의 사업에 부정적인 영향을 미칠 수 있습니다.
국내는 단일보험자(국민건강보험공단)에 의한 전국민 건강보험제도를 운영하고 있는 상황으로, 건강보험의 지속가능성 제고와 적정수준의 국민의료비 유지, 불법 리베이트 차단 등의 목표 하에 약가에 대해 정책적 개입이 이루어지고 있습니다. 국내의 약가 사후관리제도는 대내외 보건의료 환경변화에 의하여 수 차례 변화되어, 현재는 실거래가 조사에 의한 약가 인하, 사용량-약가 연동 협상, 급여범위 확대 시 약가인하, 제네릭의약품 등재 시 오리지널의약품의 약가인하 등의 제도가 운영되고 있습니다. 약가는 산업 정책과 보건의료 정책이 상충하여 변동성이 상재해 있는 상황으로, 현재 제네릭 약가 차등제가 시행 예정되어 있는 상황입니다. 이러한 점진적인 약가 인하 정책은 제약산업에서 간과할 수 없는 중요 요인이며, 당사의 사업에도 부정적인 영향을 미칠 수 있습니다.
| [약가 인하 정책 추이] |
|
시기 |
인하제도 |
내용 |
|---|---|---|
|
2000년 ~ 2009년 |
실거래가약가인하 (표본조사) |
표본조사(전국 80개 요양기관)를 통해 의약품 청구 실태 조사 후 약가인하 |
| 2002년 ~ 2012년 |
약가 재평가 |
최초 상한금액 산정이후 3년마다 7개국 조정 평균가를 |
| 2007년 ~ 2014년 |
기등재 목록정비 |
2007년 선별등재제도로 전환하면서 기존약재의 경우 20% |
| 2012년 |
일괄 약가인하 |
상한금액대비 53.55% 수준까지 일괄 약가인하 |
| 2016년 ~ |
실거래가약가인하 (전수조사) |
유통정보센터 유통정보를 근거로 가중평가가격 까지 약가 인하 |
|
현행 |
특허만료 약가인하 |
개별약제 특허만료시 1년간 70%, 1년 후 53.55%로 약가인하 |
|
현행 |
사전 약가인하 |
개별약제 급여기준 확대 이전에 협의를 통하여 약가인하 |
|
현행 |
사용량 약가연동 |
개별약제 약가와 사용량을 연계하여 등재 후 사용량이 일정 % 증가할 때 약가 인하 |
| 자료 : 보건복지부 |
국내의 식품의약품안전처는 희귀의약품이나 항암제, 일부 세포치료제(자가연골세포치료제, 자가피부세포치료제)에 대해 신속한 출시를 허용하는 목적으로 1997년부터 조건부허가제도를 도입하여 식약처 예규로 운영해 왔으며, 2016년부터는 생명을 위협하는 질환 또는 중증의 비가역질환을 대상으로 치료적 탐색(2상) 임상 시험의 허가 요건과 그 결과를 충족하는 세포치료제의 경우에도 조건부 허가를 신청할 수 있도록 세포치료제 조건부 허가 범위를 확대하여 운영하고 있는 상황입니다. 이에 따라 해당 운영 가이드라인 및 요건에 부합하는 세포치료제는 추후 임상 3상(치료적 확증) 시험 자료를 제출하는 조건으로, 임상 2상(치료적 탐색) 시험 자료만으로 우선 허가받아 시판할 수 있게 되었습니다.
「생명윤리법」등에 산재한 바이오의약품 관련 규제를 일원화하며, 신속허가제도 도입 및 안전관리체계를 구축하는 것이 핵심입니다. 본 법이 시행되면 재생의료 임상연구가 가능해져 의료기술의 기술경쟁력을 제고하여 희귀ㆍ난치 질환자에게 새로운 치료 기회를 제공할 수 있을 뿐만 아니라, 품목허가 검증 체계를 첨단바이오의약품 특성에 맞게 재편하여 맞춤형 심사, 우선 심사, 조건부 허가 등의 혜택이 가능할 것으로 기대됩니다.
[미국 관련 규제 당국 규제 관련]
미국 FDA는 인체 및 동물용 의약품, 생약 제제, 의료기기, 국가 식량 공급, 화장품, 방사선 제품의 안전성, 유효성 및 안전을 보장함으로써 공중보건을 보호하는 기관입니다. FDA는 식품 및 의약품의 유효성을 확보하고 자국민에게 보다 안전하고 비용부담이 적은 제품의 공급을 추진하며, 국민 건강 유지 및 개선을 위해 의약품과 식품 사용에 필요한 정확하고 과학적 기반을 가진 정보를 얻을 수 있도록 도움으로써 공중보건을 증진시키고 있습니다.
임상시험을 위해서는 임상시험계획승인 신청(Investigational New Drug application, IND)를 통과하여야 하며, 판매용 및 연구용(비판매용) 두가지 범주가 있고, 다음과 같은 세가지 신청 유형이 있습니다.
| [미국 임상시험계획 승인 신청] |
| 구 분 | 내 용 |
|---|---|
| 연구자 임상시험계획 승인신청 | 해당 신청은 임상시험을 개시하고 수행하는 의사가 제출하며, 의사의 직접적인 지시 하에 시험용 의약품이 투여 또는 조제됩니다. 의사는 미허가 의약품 또는 새로운 적응증이나 새로운 환자군에 대한 허가 의약품에 대한 시험을 제안하기 위해 연구용 임상시험계획 승인신청을 제출할 수 있습니다. |
| 응급상황 사용 임상시험계획 승인신청 | 해당 신청은 미국 식품의약품청이 『연방규정집』312.23조 또는 312.34조에 따른 임상시험계획 승인을 위한 시간이 허용되지 않는 상황에서의 시험약의 사용을 허가할 수 있도록 합니다. 또한 기존의 시험 계획 조건을 충족시키기 못하는 환자를 대상으로 또는 허가된 시험 계획서가 존재하지 않을 경우에 사용될 수 있습니다. |
| 치료목적 임상시험계획 승인신청 | 해당 신청은 임상 시험이 수행되고 미국 식품의약품청의 검토가 진행 중일 때, 임상 시험에서 중증 또는 즉각적으로 생명을 위협할 수 있는 증상에 대한 전망을 보이는 시험약을 위해 제출됩니다. 중증질환의 경우 임상 3상 중이거나 또는 모든 임상시험들이 완료된 의약품을 본 항에 따른 치료용 사용이 가능합니다. 즉각적으로 생명을 위협할 수 있는 질환의 경우, 임상 3상 이전이라 하더라도, 통상 임상 2상 이전이 아니라면 해당 의약품을 본 항에 따른 치료용으로 사용 가능할 수 있습니다. |
| 출처 : 식품의약품 안전처(미국 의약품 허가 제도, 2016.06.30) |
이후, 신약 허가신청(New Drug Application, NDA)은 미국 FDA가 미국에서 신약 판매 허가를 승인 받기 위해 의약품 의뢰자가 취하는 공식 단계로, 신약 허가신청은 의약품이 어떻게 체내에서 작용하고 어떻게 제조되는지에 대한 정보를 포함하여 모든 동물 및 인체 데이터와 그 분석을 포함합니다. 신약 허가신청 절차는 아래와 같은 단계를 따릅니다.
| [미국 신약 허가 신청 결과] |
| 구 분 | 내 용 |
|---|---|
| 신약 허가신청 사전회의(Pre-NDA Meeting) | - |
| 신약 허가신청서 제출 및 심사 | - 신약 허가가 신청되면 식품의약품청은 해당 신청이 정식으로 제출되어 심사 받을 수 있도록 할지 결정하는 60일의 기간이 주어집니다. 미국 식품의약품청은 완전하지 않은 신청에 대한 정식 제출을 거절할 수 있습니다. - 신약 허가신청이 정식 제출되면, 식품의약품청 심사팀(의사, 화학자, 통계학자, 미생물학자, 약리학자, 다른 전문가들)은 의뢰자가 제출한 시험이, 제안된 용법에서 해당 의약품이 안전하고 유효성이 있음을 나타내는지 평가합니다. 어떤 의약품도 절대적으로 안전하지 않으며 모든 의약품은 부작용이 있으나, “안전하다”라는 의미는 의약품의 유익성이 알려진 위해성을 상회한다는 뜻입니다. - 심사팀은 시험결과를 검토하고, 시험방법 또는 분석의 취약점과 같은 가능한 문제들에 대해 검토합니다. 심사자들은 의뢰자의 결과 및 결론에 동의할지 여부를 결정하거나, 결정을 내리기 위해 필요한 추가 정보가 필요한지 여부를 결정합니다. - 각 심사자는 신청에 대한 결론과 권고사항을 포함한 서면 평가서를 준비합니다. 이러한 평가는 이후 신청 종류에 따라 팀장, 부서장, 실장의 검토를 거칩니다. |
| 의약품 표시기재사항에 대한 심사 | 식품의약품청은 의약품 표시기재사항에 아래 정보가 포함되었는지 여부를 심사합니다. (1) 적응증, 용량, 투여 경로 및 방법, 투여 횟수 및 기간, 관련 경고문, 위험, 금기사항, 부작용, 주의사항 등 사용법에 대한 적절한 정보로서 의약품을 투여하는 법률상 허가된 의료인이 해당 의약품을 안전하게 사용할 수 있고, 광고되거나 표현된 모든 증상을 포함하여 본래 목적에 따라 사용될 수 있도록 하는 자료 (2) 라벨 및 표시기재사항 또는 의약품이 조제된 포장 내 표시된 의약품의 성분과 관련한 정보 |
| 실태조사 | 시설 등에 대한 실태조사는 식품의약품청이 수행하며, 미국의 의약품 제조 및 품질관리기준(GMP)을 따릅니다. |
| 의약품 허가 | - |
| 출처 : 식품의약품 안전처(미국 의약품 허가 제도, 2016.06.30) |
당사는 내부에 담당 인력과 외부 전문가들을 통하여 국내 및 해외 제약 산업 정책 및 규제 환경을 지속적으로 모니터링하고 있으며, 각국의 규제 당국과의 소통을 통해 정책 및 규제 환경의 변화에 효과적으로 대비하기 위해 최선의 노력을 다하고 있습니다. 그러나 상기 언급된 제약 및 신약개발 산업에 대한 우호적인 정책 기조 및 지원 계획, 규제 완화 노력에도 불구하고, 실제 효율적인 정책 지원이 이루어지지 않거나, 세부과제 추진에 어려움이 생길 수 있으며, 관련 법규의 제정 및 개정 단계, 예산 확보 등에 난항이 발생할 수 있습니다. 또한 해당 정책의 기대효과가 감소되는 경우 정책 기조의 변화로 정부 지원이 축소될 수 있으며, 조건부 허가와 같은 규제 완화에 대한 실효성이 크지 않을 경우, 규제 완화의 범위가 축소될 수 있습니다. 이러한 정부의 우호적인 정책 및 규제 완화의 변동 가능성은 당사의 사업에 부정적인 영향을 끼칠 수 있습니다.
| 바. 신약 연구개발의 전략 수립 실패에 따른 위험 연구개발을 통한 신약 개발은 일반적으로 막대한 연구개발비와 장기간에 걸친 투자 및 연구기간이 소요되며, 신약 개발에 성공한다 하더라도 기투자된 금액과 시간을 상쇄할 수 있을 정도의 수익 창출이 가능할지 여부는 불확실합니다. 또한 내외부적인 요인으로 인하여 개발이 지연되거나 추가적인 비용 지출이 요구될 경우도 존재합니다. 따라서 연결대상 종속회사의 연구개발 계획이 실패하거나, 장기적인 연구개발 전략과 사업계획, 그리고 그에 맞는 자금운용계획을 적정하게 수립하지 못할 경우 당사의 수익성 및 재무안정성에 부정적인 영향이 있을 수 있습니다. |
국내 제약업계는 연구개발을 통한 신약 개발보다는 의약품 수요의 꾸준한 증가와 의약분업 시행 이후 전문의약품 시장의 고성장을 배경으로 제네릭 위주의 제품 포트폴리오와 영업력을 통해 안정적인 성장세를 시현해 왔습니다. 하지만 산업의 성장둔화에 대비하여 대형 제약사를 중심으로 신약개발 및 해외진출을 위한 투자를 확대하고 있으며 다국적 임상과 해외 제약사와의 제휴도 증가하고 있습니다.
글로벌 제약사 매출액 및 R&D 투자 현황을 살펴보면 2021년 평균 R&D투자비율은 20%, 2022년 18.7%를 보이고 있으며, 국내 제약는 2021년 평균 16.6%, 2022년 17.3%를 기록하고 있습니다. 국내·외 제약사 모두 비슷한 수준의 R&D투자비율을 보이고 있으며 꾸준히 신약 연구개발을 위해 노력하고 있음을 보여주고 있습니다.
| [상위 10개 글로벌 제약사 매출액 및 R&D 투자 현황] |
| (단위: $million, %) |
| 순위 | 제약회사 | 2022년 | 2021년 | ||||
|---|---|---|---|---|---|---|---|
| 매출액 | 연구개발비 | R&D투자비율 | 매출액 | 연구개발비 | R&D투자비율 | ||
| 1 | Roche | 66,206 | 14,710 | 22.0 | 71,400 | 16,100 | 23.0 |
| 2 | Johnson & Johnson | 94,940 | 14,600 | 15.4 | 93,800 | 14,700 | 16.0 |
| 3 | Merch & Co | 59,280 | 13,550 | 23.0 | 48,700 | 12,200 | 25.0 |
| 4 | Pfizer | 100,330 | 11,430 | 11.4 | 81,300 | 13,800 | 17.0 |
| 5 | Novartis | 50,550 | 10,000 | 20.0 | 51,600 | 9,000 | 17.0 |
| 6 | AstraZeneca | 44,350 | 9,760 | 22.0 | 37,400 | 9,700 | 26.0 |
| 7 | Bristol Myers Squibb | 46,160 | 9,510 | 21.0 | 46,400 | 11,300 | 24.0 |
| 8 | Eli Lilly | 28,540 | 7,190 | 25.0 | 28,300 | 7,000 | 25.0 |
| 9 | Sanofi | 45,220 | 7,060 | 16.0 | 40,872 | 5,790 | 14.0 |
| 10 | AbbVie | 58,050 | 6,510 | 11.2 | 56,200 | 7,100 | 13.0 |
| 출처: 2022 제약바이오산업 DATABOOK (2022.12) |
| [상위 10개 국내 제약사 매출액 및 R&D 투자 현황] |
| (단위: 억원, %) |
| 순위 | 제약회사 | 2022년 | 2021년 | ||||
|---|---|---|---|---|---|---|---|
| 매출액 | 연구개발비 | R&D투자비율 | 매출액 | 연구개발비 | R&D투자비율 | ||
| 1 | 셀트리온 | 23,839 | 4,122 | 17.3 | 18,934 | 3,979 | 21.0 |
| 2 | 삼성바이오로직스 | 30,012 | 2,682 | 8.9 | 15,680 | 919 | 5.9 |
| 3 | GC녹십자 | 17,113 | 2,076 | 12.1 | 15,378 | 1,550 | 10.1 |
| 4 | 대웅제약 | 12,800 | 2,005 | 15.7 | 11,529 | 1,673 | 14.5 |
| 5 | 종근당 | 14,883 | 1,801 | 12.1 | 13,435 | 1,634 | 12.2 |
| 6 | 유한양행 | 17,758 | 1,800 | 10.1 | 16,878 | 1,782 | 10.6 |
| 7 | 한미약품 | 13,315 | 1,747 | 13.1 | 12,031 | 1,607 | 13.4 |
| 8 | 일동제약 | 6,377 | 1,250 | 19.6 | 5,601 | 1,081 | 19.3 |
| 9 | SK바이오팜 | 2,461 | 1,228 | 49.9 | 4,186 | 1,145 | 27.4 |
| 10 | 동아에스티 | 6,353 | 886 | 13.9 | 5,932 | 1857 | 31.3 |
| 출처: 2022 제약바이오산업 DATABOOK (2022.12), 전자공시시스템 사업보고서 |
국내 상위 제약사의 경우에도 외형 및 R&D 투자 규모에서 글로벌 제약사와 비교할 때 열위한 수준이며, 신약개발을 둘러싼 높은 불확실성도 신약개발을 통한 사업구조 전환을 어렵게 만드는 요인입니다. 하지만 정부의 정책이 차별성 낮은 제네릭중심의 산업구도를 R&D에 기반한 신약개발로 유도하는 방향으로 전개되고 있으며, 정부 규제가 제약사의 영업성과에 미치는 직접적인 영향을 고려할 때 R&D 투자확대를 통한 신약개발과 해외진출은 약가인하 등 규제로 인한 영향을 최소화하고 미래의 성장 잠재력을 확보하기 위한 필요조건입니다.
연구개발을 통한 신약 개발은 일반적으로 막대한 연구개발비와 장기에 걸친 투자 및연구기간이 소요되며, 신약 개발에 성공한다 하더라도 기투자된 금액과 시간을 상쇄할 수 있을 정도의 수익 창출이 가능할지 여부는 불확실합니다. 또한 내외부적인 요인으로 인하여 개발이 지연되거나 추가적인 비용 지출이 요구될 경우도 존재합니다. 따라서 당사 및 당사계열회사의 연구개발 계획이 실패하거나, 장기적인 연구개발 전략과 사업계획, 그리고 그에 맞는 자금운용계획을 적정하게 수립하지 못할 경우 당사의 수익성 및 재무안정성에 부정적인 영향이 있을 수 있습니다.
| 사. 지적재산권 분쟁 관련 위험 바이오의약품 산업은 특허의 확보가 사업의 핵심 성공 요인으로, 특허를 확보하지 못할 경우 원천적으로 사업이 불가능하거나 특허 소유자로부터 기술이전을 받아야 합니다. 당사는 보유 특허에 대한 보호 강화를 위해 특허보호와 관련된 국내외 정책 동향 및 법률적 사항 등을 확인 하는 등 당사의 지식재산권 보호를 위한 노력을 최대한 기울이고 있습니다. 다만, 향후 당사가 보유한 지적재산권을 적절히 보호하지 못하거나, 라이센스 계약 등에 있어서 당사의 지적재산권 관련 분쟁이 발생하는 경우 당사의 경쟁력은 약화될 수 있으며 이는 당사의 영업 및 손익에 부정적인 영향을 미칠 수 있습니다. |
바이오의약품 산업은 특허의 확보가 사업의 핵심 성공 요인으로, 특허를 확보하지 못할 경우 원천적으로 사업이 불가능하거나 특허 소유자로부터 기술이전을 받아야 합니다. 특허가 가장 중요한 경쟁요소이기 때문에 많은 바이오의약품 개발 회사와 제약사들은 특허기간을 최대한 보호하기 위한 다양한 전략 및 정책을 도입하고 있으며, 제품화 이후 특허 보호기간을 연장하기 위한 전략으로 공정 특허, 제법 특허 등의 방법을 활용하고 있습니다. 이에 따라 당사 역시 바이오의약품 개발을 위한 핵심 기술을 확보하고 이에 대해 국내외 특허를 등록 또는 출원하였습니다. 특허를 등록 또는 출원한 제품에 대하여는 제반 권리 및 판매에 관한 유효성을 특허로 보호 받기 때문에 특허존속기간 동안 배타적인 권리를 통해 진입장벽을 형성할 수 있습니다. 당사가 보유한 특허권 및 전용실시권의 내역은 다음과 같습니다.
| [분야별/단계별 특허출원 내역] |
|
주요과제명 |
유형별 |
국내 진행단계 |
PCT |
해외 (국가별진입) |
||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
방법 |
용도 |
물질 특허 |
기타 |
계 |
출원 | 심사 | 등록 | 계 | 출원 | 심사 | 등록 | 계 | ||
| 리보세라닙 |
- | - | 2 | - | 2 | - | - | 2 | 2 | - | 1 | - | 45 | 46 |
| 파이로티닙 |
- | - | 3 | - | 3 | - | - | 3 | 3 | - | - | - | - | - |
| G2M 물질
|
1 | 2 | 3 | 1 | 2 | 3 | 3 | - | 15 | 15 | ||||
| 간세포치료제 |
1 | - | - | - | 1 | - | - | 1 | 1 | - | - | - | - | - |
|
기타세포치료제 (μMatricel) |
1 | - | - | - | 1 | - | - | 1 | 1 | 1 | - | - | 3 | 3 |
|
기타의료기기 (Hutrigel) |
2 | - | - | - | 2 | - | 2 | - | 2 | 2 | - | - | - | - |
| 바이오인공간 |
6 | - | - | - | 6 | - | - | 6 | 6 | 4 | 1 | - | 8 | 9 |
| 조직접착, 지혈 및 창상피복재 |
- | - | - | 2 | 2 | - | - | 2 | 2 | 1 | - | - | 12 | 12 |
| 합 계 |
10 | 1 | 7 | 2 | 20 | 1 | 2 | 17 | 20 | 11 | 2 | - | 83 | 85 |
| (주1) '유형별' 특허는 패밀리 특허당 1건으로 판단하였습니다. 출처: 당사 분기보고서 |
| [특허권 현황] |
| 파이프라인 | 명칭 | 국가 | 상태 | 권리자 | 출원일 | 등록일 | 등록번호 |
| G2M 물질 | 신규한 4-(아릴)-N-(2-알콕시티에노[3,2-b]피라진-3-일)-피페라진-1-카복스아미드 유도체 및 이의 항증식 효과 | 대한민국 | 등록 | HLB생명과학 R&D | 2015-12-03 | 2017-04-10 | 제 1727412 호 |
| G2M 물질 | Substituted thieno[3,2-b]pyrazines for inhibiting cancer cell proliferation and inducing cancer cell apoptosis | 미국 | 등록 | HLB생명과학 R&D | 2015-12-03 | 2018-08-28 | US 10059721 |
| G2M 물질 | 신규한4-(아릴) -N-(2-알콕시 티에노[3,2-b]피라진-3-일)-피페라진-1-카르복사마이드 유도체 및 그 항증식 효과 | 일본 | 등록 | HLB생명과학 R&D | 2015-12-03 | 2018-06-08 | JP 6349464 |
| G2M 물질 | Substituted thieno[3,2-b]pyrazines for inhibiting cancer cell proliferation and inducing cancer cell apoptosis | 유럽 5개국 |
등록 | HLB생명과학 R&D | 2015-12-03 | 2019-08-14 | EP 3231800 |
| G2M 물질 | 신규한 4-(아릴)-N-(3-알콕시퓨로[2,3-b]피라진-2-일)-피페라진-1-카복스아미드 유도체 및 이의 항증식 효과 | 대한민국 | 등록 | HLB생명과학 R&D | 2017-06-08 | 2018-06-22 | 제 1872645 호 |
| G2M 물질 | 4-(aryl)-N-(3-alkoxyfuro[2,3-b]pyrazin-2-yl)-piperazine-1-carboxamide derivative and antiproliferative effect thereof | 미국 | 등록 | HLB생명과학 R&D | 2017-06-09 | 2020-10-13 | US 10800788 |
| G2M 물질 | 신규한4-(아릴) -N-(3-알콕시 프로[2,3-b]피라진-2-일)-피페라진-1-카르복사미드 유도체 및 그 항증식 효과 | 일본 | 등록 | HLB생명과학 R&D | 2017-06-09 | 2020-04-30 | JP 6698180 |
| G2M 물질 | NOVEL 4-(ARYL)-N-(3-ALKOXYFURO[2,3-B]PYRAZIN-2-YL)-PIPERAZINE-1-CARBOXAMIDE DERIVATIVE AND ANTIPROLIFERATIVE EFFECT THEREOF | 중국 | 등록 | HLB생명과학 R&D | 2017-06-09 | 2021-05-28 | CN 109641915 |
| G2M 물질 | NOVEL 4-(ARYL)-N-(3-ALKOXYFURO[2,3-B]PYRAZIN-2-YL)-PIPERAZINE-1-CARBOXAMIDE DERIVATIVE AND ANTIPROLIFERATIVE EFFECT THEREOF | 유럽 4개국 |
등록 | HLB생명과학 R&D | 2017-06-09 | 2021-05-28 | EP E052987 |
| G2M 물질 | NOVEL 4-(ARYL)-N-(3-ALKOXYFURO[2,3-B]PYRAZIN-2-YL)-PIPERAZINE-1-CARBOXAMIDE DERIVATIVE AND ANTIPROLIFERATIVE EFFECT THEREOF | 인도 | 등록 | HLB생명과학 R&D | 2017-06-09 | 2020-11-27 | IN 351819 |
| 기타세포치료제 | 모낭유도 능력이 있는 모유두 조직의 제조방법 | 대한민국 | 등록 | 동국대학교 산학협력단 | 2004-11-29 | 2006-08-22 | 제 0616752 호 |
| 기타세포치료제 | Method for the preparation of a dermal papilla tissue having hair follicle inductive potency | 미국 | 등록 | HLB셀 (구. 라이프코드) 박정극 |
2005-11-29 | 2009-12-22 | US 7635589 |
| 기타세포치료제 | Method for the preparation of a dermal papilla tissue having hair follicle inductive potency | 영국 | 등록 | HLB셀 (구. 라이프코드) 박정극 |
2005-11-29 | 2008-09-17 | GB 1819810 |
| 기타세포치료제 | Method for the preparation of a dermal papilla tissue having hair follicle inductive potency | 중국 | 등록 | HLB셀 (구. 라이프코드) 박정극 |
2005-11-29 | 2010-12-15 | CN 101068920 |
| 바이오인공간 | 담체의 표면에 세포를 고정화하는 방법 | 대한민국 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2005-06-27 | 2007-01-31 | 제 0679729 호 |
| 바이오인공간 | 겔 비드 충전형 생물반응기를 이용한 생인공 간 시스템 | 대한민국 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2007-03-30 | 2009-02-20 | 제 0886003 호 |
| 바이오인공간 | Bioartificial liver system using bioreactor packed with gel beads | 미국 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-03-28 | 2012-12-11 | US 8329457 |
| 바이오인공간 | Bioartificial liver system using bioreactor packed with gel beads | 캐나다 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-03-28 | 2013-02-26 | CA 2681798 |
| 바이오인공간 | Bioartificial liver system using bioreactor packed with gel beads | 독일 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-03-28 | 2012-01-26 | DE 11-2008-000814 |
| 바이오인공간 | Bioartificial liver system using bioreactor packed with gel beads | 영국 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-03-28 | 2011-09-21 | GB002462946 |
| 바이오인공간 | Bioartificial liver system using bioreactor packed with gel beads | 인도 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-03-28 | 2018-05-28 | IN 297164 |
| 바이오인공간 | Bioartificial liver system using bioreactor packed with gel beads | 중국 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-03-28 | 2012-08-22 | CN 101668494 |
| 바이오인공간 | 일체형 무균 캡슐 제조장치 | 대한민국 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2007-10-05 | 2009-06-08 | 제 0902781 호 |
| 바이오인공간 | Apparatus and method of manufacturing aseptic capsules | 캐나다 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-10-01 | 2014-11-18 | CA 2701598 |
| 바이오인공간 | Apparatus and method of manufacturing aseptic capsules | 독일 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-10-01 | 2017-06-08 | DE 11-2008-002671 |
| 간세포치료제 | 간세포의 제조방법 및 이로부터 제조된 간세포 | 대한민국 | 등록 | HLB셀 (구. 라이프리버) 동국대학교 |
2010-07-15 | 2013-01-22 | 제 1227047 호 |
| 바이오인공간 | 복막 순환 장치 및 이를 이용한 바이오인공 간 시스템 | 대한민국 | 등록 | HLB셀 (구. 라이프리버) 삼성생명공익재단 |
2016-03-07 | 2018-12-17 | 제 1931854 호 |
| 바이오인공간 | 간세포 및 캡슐화한 간세포 구상체의 동결 보존을 위한 동결보존용 무혈청 용액 및 이를 이용한 동결보존법 | 대한민국 | 등록 | HLB셀 (구. 라이프리버) 삼성생명공익재단 |
2018-11-29 | 2020-08-21 | 제 2148998 호 |
| 조직접착, 지혈 및 창상피복재 | 분사량 조절이 가능한 분말 분사장치 | 대한민국 | 등록 | HLB셀 | 2018-04-18 | 2020-02-10 | 제 207779 호 |
| 출처: 당사 내부자료 |
| [전용실시권 현황] |
| 파이프라인 | 명칭 | 국가 | 상태 | 권리자 | 출원일 | 등록일 | 에이치엘비셀(주)가 보유한 실시권 내용 |
보유기간 (계약일~만기일) |
비고 | 등록번호 |
|---|---|---|---|---|---|---|---|---|---|---|
| 리보세라닙 | 혈관신생 억제제로서의 6환 아미노-아미드 유도체 | 대한민국 | 등록 | HLB | 2004-06-04 | 2012-06-15 | "계약기술” 및 "계약지적재산권"에 관한 한국 전용실시권 | 2018년8월14일부터 2024년6월4일까지 |
보유기간 만료일 : 특허존속기간 만료일 | 제 1159034호 |
| 리보세라닙 | Six membered amino-amide derivatives an angiogenisis inhibitors | 미국 | 등록 | HLB | 2004-06-04 | 2006-10-31 | "계약기술” 및 "계약지적재산권"에 관한 통상실시권 | 2021년01월06일부터 2024년10월08일까지 |
보유기간 만료일 : 특허존속기간 만료일 | US 7129252 |
| 리보세라닙 | 혈관신생 억제제로서의 6환 아미노-아미드 유도체 | 일본 | 등록 | HLB | 2004-06-04 | 2012-07-27 | "계약기술” 및 "계약지적재산권"에 관한 통상실시권 | 2020년11월11일부터 2024년06월04일까지 |
보유기간 만료일 : 특허존속기간 만료일 | JP 5046643 |
| 리보세라닙 | Six membered amino-amide derivatives an angiogenisis inhibitors | 캐나다 | 등록 | HLB | 2004-06-04 | 2012-01-24 | "계약기술” 및 "계약지적재산권"에 관한 통상실시권 | 2021년02월01일부터 2024년06월04일까지 |
보유기간 만료일 : 특허존속기간 만료일 | CA 2568608 |
| 리보세라닙 | Six membered amino-amide derivatives an angiogenisis inhibitors | 유럽 27개국 |
등록 | HLB | 2004-06-04 | 2014-06-25 | "계약기술” 및 "계약지적재산권"에 관한 통상실시권 | 2021년02월24일부터 2024년06월04일까지 |
보유기간 만료일 : 특허존속기간 만료일 | EP 1633712 |
| 리보세라닙 |
N-[4-(1-사이아노사이클로펜틸)페닐]-2-(4-피리딜메틸)아미노-3-피리딘카복스아마이드의 염 | 대한민국 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 | 2009-06-11 | 2016-11-02 | "계약기술” 및 "계약지적재산권"에 관한 한국 전용실시권 | 2018년08월14일부터 2029년06월11일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
제 1674227 호 |
| 리보세라닙 |
Salts of N-[4-(1-cyanocyclopentyl)phenyl]-2-(4-pyridylmethyl)amino-3-pyridinecarboxamide | 미국 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 | 2009-06-11 | 2013-01-29 | "계약기술” 및 "계약지적재산권"에 관한 전용실시권 | 2018년08월14일부터 2029년06월11일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
US 8362256 |
| 리보세라닙 |
N-[4-(1-사이아노사이클로펜틸)페닐]-2-(4-피리딜메틸)아미노-3-피리딘카복스아마이드의 염 | 일본 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 | 2009-06-11 | 2014-11-21 | "계약기술” 및 "계약지적재산권"에 관한 전용실시권 | 2018년08월14일부터 2028년09월16일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
JP 5649132 |
| 리보세라닙 |
N-4-(1-cyan cyclopentyl) phenyl-2-(4-picolyl) amidogen-3-pyridinecarboxamide salt | 중국 홍콩 |
등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드, 상하이 헨그루이 파마수티컬 컴퍼니 리미티드 |
2008-09-16 | 2012-12-26 | "계약기술” 및 "계약지적재산권"에 관한 전용실시권 | 2018년08월14일부터 2028년09월16일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
CN 101676267 HK 1141514 |
| 리보세라닙 |
N-4-(1-cyan cyclopentyl) phenyl-2-(4-picolyl) amidogen-3-pyridinecarboxamide salt | 캐나다 호주 남아공 러시아 베트남 |
등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 | 2009-06-11 | 2016-05-24 2014-02-13 - 2013-11-27 |
"계약기술” 및 "계약지적재산권"에 관한 전용실시권 | 2018년08월14일부터 2029년06월11일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
CA 2736664 AU 2009295168 ZA 201101891 RU 0002499796 VN 1-0014320-000 |
| 리보세라닙 |
Salt of n-[4-(1-cyanocyclopentyl)phenyl]-2-(4-pyridinemethyl)amino-3-pyridinecarboxamide | 대만 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 | 2009-12-17 | 2014-12-01 | "계약기술” 및 "계약지적재산권"에 관한 전용실시권 | 2018년08월14일부터 2029년12월16일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
TW I462738 |
| 리보세라닙 |
THE SALTS OF N-(4-(1-CYANOCYCLOPENTYL)PHENYL)-2-(4-PYRIDYL METHYL)AMINO-3-PYRIDINECARBOXAMIDE | 유럽3개국 | 등록 | 지양수 헨그루이 메디스 컴퍼니 리미티드 |
2009-06-11 | 2014-03-12 | "계약기술” 및 "계약지적재산권"에 관한 전용실시권 |
2018년08월14일부터 2029년06월11일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
EP 2327697 |
| 파이로티닙 | 6-아미노 퀴나졸린 또는 3-시아노 퀴놀린 유도체, 그 제조 방법 및 약학적 용도 | 대한민국 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 상하이 헨그루이 파마수티컬 컴퍼니 리미티드 |
2010-08-26 | 2017-05-15 | "계약기술” 및 "계약지적재산권"에 관한 한국 전용실시권 |
2020년09월28일부터 2030년08월26일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
제 1738191 호 |
| 파이로티닙 | (이)-엔-[4-[[3-클로로-4-(2-피리딜메톡시)페닐]아미노]-3-시아노-7-에톡시-6-퀴놀릴]-3-[(2알)-1-메틸피롤리딘-2-일]프로프-2-엔아미드의 약학적으로 허용 가능한 염, 그의 제조 방법, 및 그의 의학적 용도 | 대한민국 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 상하이 헨그루이 파마수티컬 컴퍼니 리미티드 |
2012-02-10 | 2018-06-21 | "계약기술” 및 "계약지적재산권"에 관한 한국 전용실시권 |
2020년09월28일부터 2030년02월10일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
제 1871889 호 |
| 파이로티닙 | 타이로신 키나제 억제제 다이말리에이트의 결정형 아이 및 그의 제조 방법 | 대한민국 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 |
2013-06-04 | 2020-02-11 | "계약기술” 및 "계약지적재산권"에 관한 한국 전용실시권 |
2020년09월28일부터 2033년06월04일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
제 2078077 호 |
| 바이오인공간 | 간세포 동결 보존용 무혈청 용액 및 이를 이용한 간세포 동결 보존방법 | 대한민국 | 등록 | 사회복지법인 삼성생명공익재단 | 2013-05-08 | 2015-01-05 | "계약기술” 및 "계약지적재산권"에 관한 한국 전용실시권 |
2015년01월05일부터 2033년05월08일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
제 1480987 호 |
| 조직접착, 지혈 및 창상피복재 |
생분해성 의료용 접착제 또는 실란트조성물 | 대한민국 | 등록 | (재)유타 인하 디디에스 및 신의료기술개발 공동연구소 | 2014-07-15 | 2016-10-04 | "계약기술”및 "계약지적재산권"에 관한 기술이전 및 전세계 전용 실시권 | 2015년11월5일부터 2034년7월15일까지 |
보유기간: 출원일로부터 20년간 | 제 1664444호 |
| 조직접착, 지혈 및 창상피복재 |
생분해성 의료용 접착제 또는 실란트조성물 | 멕시코 인도 유럽 러시아 중국 |
등록 | (재)유타 인하 디디에스 및 신의료기술개발 공동연구소 | 2016-06-10 2016-06-13 2016-06-16 2016-07-13 2016-06-13 |
2019-05-29 2020-07-28 2018-12-12 2018-06-15 2020-10-16 |
"계약기술” 및 "계약지적재산권"에 관한 기술이전 및 전세계 전용 실시권 | 2015년11월5일부터 2034년7월15일까지 |
보유기간: 출원일로부터 20년간 | MX 366143 IN 342623 EP 3081236 RU 2657836 CN 106061518 |
| 조직접착, 지혈 및 창상피복재 |
생분해성 의료용 접착제 또는 실란트조성물 | 미국 | 등록 | (재)유타 인하 디디에스 및 신의료기술개발 공동연구소 | 2016-06-07 | 2017-10-18 | "계약기술” 및 "계약지적재산권"에 관한 기술이전 및 전세계 전용 실시권 | 2015년11월5일부터 2034년7월15일까지 |
보유기간: 출원일로부터 20년간 | US 10105465 |
| 조직접착, 지혈 및 창상피복재 |
생분해성 의료용 접착제 또는 실란트조성물 | 일본 | 등록 | (재)유타 인하 디디에스 및 신의료기술개발 공동연구소 | 2016-06-10 | 2017-09-15 | "계약기술” 및 "계약지적재산권"에 관한 기술이전 및 전세계 전용 실시권 | 2015년11월5일부터 2034년7월15일까지 |
보유기간: 출원일로부터 20년간 | JP 6207745 |
| 조직접착, 지혈 및 창상피복재 |
생분해성 의료용 접착제 또는 실란트조성물 | 호주 | 등록 | (재)유타 인하 디디에스 및 신의료기술개발 공동연구소 | 2016-06-24 | 2017-08-17 | "계약기술” 및 "계약지적재산권"에 관한 기술이전 및 전세계 전용 실시권 | 2015년11월5일부터 2034년7월15일까지 |
보유기간: 출원일로부터 20년간 | AU 2014360958 |
| 조직접착, 지혈 및 창상피복재 |
생분해성 의료용 접착제 또는 실란트조성물 | 캐나다 | 등록 | (재)유타 인하 디디에스 및 신의료기술개발 공동연구소 | 2016-06-09 | 2017-11-21 | "계약기술” 및 "계약지적재산권"에 관한 기술이전 및 전세계 전용 실시권 | 2015년11월5일부터 2034년7월15일까지 |
보유기간: 출원일로부터 20년간 | 제 2933271호 |
|
(주1) 계약기술 : "계약제품"의 설계,제조,사용과 관련하여 “갑”에 의해 개발되었거나 기타 일반적으로 사용되고 있는 것으로서 “갑”이 알고 있는 모든 기술적 지식,노하우, 자료 및 정보를 의미하며,지적재산권의 등록 여부를 불문한다. (주2) 계약지적재산권 : "계약제품"과 관련하여 “갑”에 의해 현재 소유중이거나 또는 소유하게 될, 그리고 “계약제품”의 제조에 사용 또는 적용되고 본 계약기간 동안에 라이센스 관리 또는 설정할 수 있는 특허, 실용신안, 출원에 관한 모든 권한을 의미한다. |
바이오의약품 개발사업은 각 개발사들이 보유한 특화된 기술 및 제품화 능력에 의하여 성패가 결정되는 기술지향형 산업입니다. 또한 여러 관련 분야의 지식과 기술을 토대로 신약 개발이 가능한 첨단 기술 및 지식 집약 산업입니다. 다른 제품에 비하여 개발 비용이 막대한 반면 복제는 상대적으로 쉽기 때문에 특허에 의한 보호가 결정적인 중요성을 가지고 있습니다. 또한 임상 및 승인 기간 때문에 실질특허기간이 감소되는 문제가 발생하게 되고 의료비 부담으로 인한 사회적 비용을 줄이기 위해서는 특허 기간을 적정선에서 제한하고 제네릭 생산을 용이하게 하는 것도 필요합니다.
당사(연결대상 종속회사 및 계열회사 포함)는 보유 특허에 대한 보호 강화를 위해 특허보호와 관련된 국내외 정책 동향 및 법률적 사항 등을 확인 하는 등 당사의 지식재산권 보호를 위한 노력을 최대한 기울이고 있습니다. 다만, 향후 당사가 보유한 지적재산권을 적절히 보호하지 못하거나 당사가 사용하는 기술과 관련한 지적재산권 관련 분쟁이 발생하는 경우 당사의 경쟁력은 약화될 수 있으며 이는 당사의 영업 및 손익에 부정적인 영향을 미칠 수 있습니다.
|
아. 핵심 연구인력 이탈 위험 |
당사가 속한 산업은 고부가가치 산업으로 오랜 연구기간이 필요하고 높은 기술력이 필요합니다. 이에 핵심 연구인력의 능력이 매우 중요하고 지속적으로 우수한 인재를 유치하는 것이 회사의 성과를 결정하는 주요한 요인이며, 핵심 연구인력의 이탈은 경영활동에 부정적인 영향을 미칠 수 있습니다.
당사의 연구개발 조직 구성은 HLB생명과학 R&D의 바이오사업본부 산하 5개팀과 신약연구소, 종속회사인 HLB셀의 의학연구소 산하 4개팀과 QA팀으로 구성되어 있으며, 그 현황은 다음과 같습니다.
| <연구개발 조직 구성> |
|
회사명 |
부서 |
팀 |
주요 업무 |
|---|---|---|---|
| HLB생명과학R&D | 바이오사업본부 | 신약연구소 | - 항암제 연구개발 |
| 사업개발팀 | - 라이센싱 (IN/OUT) 관련 재반 활동 | ||
| IP팀 | - 특허 관리 | ||
| 오픈이노베이션팀 | - 국내외 우수 기술 검토 및 도입 타당성 분석 | ||
| 임상개발팀 | - 리보세라닙, 파이로티닙 등 임상관련 연구개발 | ||
| R&D기획팀 | - 신규과제 기획, 의료용대마/동물함암제 연구개발 | ||
|
HLB셀 |
의학연구소 |
공정개발팀 |
- 인간 세포외기질, 지혈제 공정개발 |
|
세포/의료기기팀 |
- 세포치료제 연구개발 |
||
|
분석연구팀 |
- 기준 및 시험법 확립 - Method validation |
||
| 개발전략팀 |
- 파이프라인 개발전략 수립 및 사업화 |
||
| QA팀 | - 임상시험용 의약품, 의료기기 품질 보증 | ||
| 출처: 당사 내부자료 |
당사의 연구개발전문인력은 증권신고서 제출일 현재, 종속회사인 HLB생명과학R&D는 박사급 12명, 석사급 8명 등 총 25명의 연구인력을 보유하고 있으며, 종속회사인 HLB셀은 박사급 4명, 석사급 6명 등 총 17명의 연구인력을 보유하고 있으며, 그 현황은 다음과 같습니다.
| <연구개발 인력 현황> |
|
회사명 |
팀 |
인 원(단위 : 명) |
||||
|---|---|---|---|---|---|---|
|
박 사 |
석 사 |
기 타 |
합 계 |
|||
| HLB생명과학R&D | 대표이사 | 1 | - | - | 1 | |
| 부사장 | 1 | - | - | 1 | ||
| 바이오사업 |
신약연구소 | 4 | 4 | - | 8 | |
| 사업개발팀 | - | - | 1 | 1 | ||
|
오픈이노베이션팀 |
3 | - | - | 3 | ||
|
임상개발팀 |
- | 3 | 3 | 6 | ||
|
R&D기획팀 |
2 | - | - | 2 | ||
| 바이오지원실 |
IP팀 |
- | 1 | 1 | 2 | |
| 지원팀 | 1 | - | - | 1 | ||
| HLB셀 | 대표이사 | 1 | - | - | 1 | |
| 의학연구소 | 의학연구소 | 1 | - | - | 1 | |
| 공정개발팀 | 1 | - | 4 | 5 | ||
| 세포/의료기기팀 | - | 3 | - | 3 | ||
| 분석연구팀 | - | 1 | 2 | 3 | ||
| 개발전략팀 | 1 | 1 | - | 2 | ||
| QA팀 | - | 1 | 1 | 2 | ||
| 합 계 | 16 | 14 | 12 | 42 | ||
| 출처: 당사 제공 자료 |
종속회사인 HLB생명과학R&D 및 HLB셀의 핵심 연구인력은 아래와 같습니다.
| <핵심 연구인력 현황> |
|
회사명 |
직 위 |
성 명 |
담당업무 |
주요 경력 |
주요 연구실적 |
|---|---|---|---|---|---|
| HLB생명과학R&D | 소장 | 강희범 | 연구개발 |
고려대학교 약리학 박사 전) 서울아산병원 연구교수 전) 비에스티 부소장 현) HLB생명과학R&D 신약연구소 부소장 |
[학술 발표] 1. AACR(2019) Abstract B002: Discovery of selective and potent EGFR kinase inhibitors for exon20 insertion mutations. 2. Immune-Stimulating Effects of Dendropanax morbiferusBranch Extract via Improving Nitric Oxide and Cytokines in Raw264. 7 Macrophages.(2017).한국식품영양과학회한국식품영양과학회 학술대회발표집, p10326 - 326 3. Porphyra tenera extracts enhance immune stimulation activity via increasing cytokines in mouse primary splenocytes and RAW264. 7 macrophages.(2016).한국식품영양과학회 학술대회발표집, p502-502. 1. Catechol inhibits epidermal growth factor-induced epithelial-to-mesenchymal transition and stem cell-like properties in hepatocellular carcinoma cells. Sci Rep. 2020 May6;10(1):7620. Co-author:IF (4.52) 2. Inositol-triphosphate 3-kinase B confers cisplatin resistance by regulating NOX4-dependent redox balance. J Clin Invest. 2019 May 13;129(6):2431-2445 Co-author;IF (12.282) |
| HLB셀 |
대표이사 |
이두훈 |
사업총괄 |
동국대학교 공학 박사 전) 동국대학교 의생명공학과 겸임교수 |
[저서] Bioartificial Liver. Fundamentals of Tissue Engineering and Regenerative Medicine, Meyer, U.; Meyer, Eds., Springer [논문] 1. Hepatocyte Isolation, Culture, and Its Clinical Applications, 외 2건 (국내) 2. Functional Evaluation of a Bioartificial Liver Support System Using Immobilized Hepatocyte Spheroids in a Porcine Model of Acute Liver Failure 외 21건 (국외) |
| 연구소장 | 윤희훈 | 연구총괄 |
동국대학교 생물화학공학 박사 전) 동국대 의생명공학과 연구초빙교수 전) HLB셀 의학연구소 현) HLB셀 의학연구소장 |
[저서] Human Amniotic Epithelial Stem Cells in A Manual for Primary Human Cell Culture (편저) [논문] In vitro hepatic differentiation of umbilical cord-derived mesenchymal stem cell (Process Biochemistry) 외 42건 |
| 출처: 당사 내부자료 |
일반적으로 업계 연구 인력들의 특성이 학계나 국가 연구원 등에서 근무하는 것을 선호하고 있으며, 개인적인 학업 증진을 위한 해외유학 등의 사유로 핵심연구 인력의 이탈이 발생할 수 있습니다. 특히 제약산업의 경쟁심화에 따른 당사 우수인력의 스카우트는 당사가 사업을 영위함에 있어 큰 문제가 될 수 있습니다. 또한, 핵심인력 이탈과 함께 당사의 주요 기술이 유출될 경우, 당사의 경쟁력이 악화될 수 있으며, 지속적인 성장에 부정적인 영향을 끼칠 수 있습니다. 투자자분들께서는 이 점 유의하시기 바랍니다.
|
자. 제약 산업의 성장 둔화 위험 제약산업은 인구의 고령화 및 소득증가에 따른 1인당 약제비가 증가하여 꾸준한 성장을 이어왔습니다. 하지만 정부의 리베이트 규제 강화, 일괄 약가인하 등 비우호적인 영업환경이 지속됨에 따라 최근 성장성이 둔화된 추세를 보이고 있습니다. 이에 따라 국내 제약산업은 높은 수준의 R&D 투자, 이머징 마켓으로의 진출, 신규 바이오 의약품 개발 등 다양한 노력을 기울이고 있습니다. 그러나 이러한 전반의 노력에도 불구하고 당사가 영위하는 사업의 전방산업인 전체 제약산업이 위축되거나 시장성장률이 둔화되는 경우 의약품 유통업을 영위하는 당사의 영업 성과 및 재무 상태에 부정적인 영향을 끼칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
당사는 신규 바이오사업 강화를 위해 의약품 도매업을 영위하는 주식회사 신화어드밴스를 양수하기로 결정하여 주원재 외 3명의 양도인과 2016년 8월 3일 주식양수도 계약을 체결하고 양도인의 지분 100.00%를 현금 33억원(제4회 기명식 무보증 사모 전환사채 발행 자금 중 일부)과 제3회 기명식 무보증 사모 전환사채 37억원을 발행하여 총 거래금액 70억원에 양수하였습니다.
국내 의약품 산업은 인구고령화를 비롯하여 소득수준의 향상, 성인병 및 만성질환의 증가 등의 환경변화에 힘입어 꾸준히 성장하여 왔습니다. 2017년 22조 632억원이었던 국내 의약품시장은 2022년 29조 8,595억원 규모로 성장하며 연평균 5.17%의 꾸준한 성장세를 보여주고 있습니다.
| [국내의약품 시장규모] |
| (단위 : 억원, %) |
|
구분 |
2017년 |
2018년 |
2019년 |
2020년 |
2021년 |
2022년 |
전년 대비 성장률 |
CAGR ('17~'22) |
|---|---|---|---|---|---|---|---|---|
|
생산 |
203,580 | 211,054 | 223,132 | 245,662 | 254,906 | 289,503 | 13.57% | 6.04% |
|
수출 |
46,025 | 51,431 | 60,581 | 99,648 | 113,642 | 104,561 | -7.99% | 14.66% |
|
수입 |
63,077 | 71,552 | 80,549 | 85,708 | 112,668 | 113,653 | 0.87% | 10.31% |
|
시장규모 |
220,632 | 231,175 | 243,100 | 231,722 | 253,932 | 298,595 | 17.59% | 5.17% |
| 주) 시장규모: 생산 - 수출 + 수입 |
| 출처: 제약바이오산업 DATABOOK(2022), 식품의약품안전처 |
국내 의약품시장의 경우 인구 고령화 및 만성질환 증가 등의 영향으로 판매되는 의약품의 종류와 사용량이 지속적으로 증가하고 있습니다. 만성질환으로 병원을 찾는 인구 수의 증가는 의약 산업 매출 성장에 긍정적으로 작용할 전망이며, 특히 국내 의약품 시장의 경우 일반의약품 대비 전문의약품이 품목수와 금액 측면에서 훨씬 더 높은 점유율을 확보하고 있는 것으로 확인됩니다. 금액 기준으로 2022년 전문의약품의 생산실적은 전체 24.69조원 중에서 21.18조원을 생산했고, 일반의약품은 3.51조원을 생산하며 각각 85.77%와 14.23%를 차지하였습니다.
| [연도별 일반/전문의약품 생산실적] |
| (단위: 단위: 개, 억원, %) |
|
구분 |
일반의약품 |
전문의약품 |
총계 |
||||
|---|---|---|---|---|---|---|---|
|
품목수 |
생산액 |
비중 |
품목수 |
생산액 |
비중 |
||
|
2017년 |
5,650 |
28,535 |
16.57% |
13,982 |
143,646 |
83.43% |
172,181 |
|
2018년 |
5,334 |
28,467 |
15.67% |
14,597 |
153,248 |
84.33% |
181,715 |
|
2019년 |
5,474 |
31,087 |
15.99% |
15,618 |
163,385 |
84.01% |
194,472 |
|
2020년 |
5,365 |
33,699 |
16.37% |
16,197 |
172,173 |
83.63% |
205,872 |
|
2021년 |
4,875 |
30,851 |
14.16% |
15,909 |
187,099 |
85.84% |
217,950 |
|
2022년 |
4,944 |
35,143 |
14.23% |
16,361 |
211,791 |
85.77% |
246,934 |
| 자료: 건강보험심사평가원 |
이밖에도 제약산업은 인구의 변화와 밀접하게 연관되어 있습니다. 건강 유지와 질병 치료를 목적으로 하는 제품의 특성상 인구 수 증가 및 의약품 지출이 큰 노령 인구의 증가는 제약 산업의 외형 성장과 맞물려 있는데, 생활수준 향상과 의료기술 발달로 우리나라를 비롯한 세계 여러 나라에서 인구 고령화가 나타나고 있습니다.
우리나라의 65세 이상 인구 비중인 고령화율을 살펴보면 2021년에 17.5%를 넘어 이미 고령사회로 진입했고, 이 추세는 더욱 심화되어 2025년경에는 25.5%, 2040년도에는 46.4%를 기록할 것으로 전망되고 있습니다.
| [65세 이상 인구 추이] |
| (단위 : 천명, %) |
|
구분 |
2023년 |
2025년(E) |
2030년(E) |
2035년(E) |
2040년(E) |
|---|---|---|---|---|---|
|
총인구 |
51,558 |
51,448 |
51,199 |
50,869 |
50,193 |
|
65세 이상 |
9,500 |
10,585 |
13,056 |
15,289 |
17,245 |
|
구성비 |
18.4% |
20.6% |
25.5% |
30.1% |
34.4% |
| 출처: 통계청, 고령자 통계(2023) |
이처럼 고령화 진행속도가 빠른 점, 65세 이상 인구수와 그 진료비가 매년 증가하는 점 등을 고려했을 때, 향후에도 노인인구 및 만성질환자 증가에 따른 의약품의 근원 수요는 견고한 확대 추세를 지속할 것으로 전망됩니다. 그러나 제약산업에 대한 부정적인 환경요인 또한 존재하는 것을 간과할 수 없습니다.
현재 국내 제약산업은 노령인구의 지속적인 증가 및 소득수준의 향상에 힘입어 2000년대 이래로 연평균 10% 내외의 꾸준한 성장을 이루어왔으나, 2010년에 시행된 의약품 리베이트 규제, 2012년 약가인하정책 등 정부의 약가인하 정책시행 의지가 견고함에 따라 산업전체의 성장성이 둔화되고 있으며, 향후 현재 수준의 성장률의 지속여부는 장담할 수 없습니다. 국내 제약산업은 상기한 국내 및 해외 제약시장의 전반적인 성장률 둔화 추세에 대응하기 위하여 높은 수준의 R&D 투자, 생산 및 품질관리경쟁력 확보를 바탕으로 한 이머징마켓 진출, 높은 치료율과 낮은 부작용을 보이는 신규 바이오의약품 개발 등 다양한 노력을 기울이고 있습니다. 그러나 이러한 전반의 노력에도 불구하고 당사의 연결종속회사 (주)신화어드밴스가 영위하고 있는 의약품도매업의 수익성 역시 국내 제약시장의 성장성과 밀접한 관련을 보이고 있으며, 국내 제약시장의 전반적인 성장성이 저하될 경우 향후 당사의 매출과 수익성에 부정적 영향을 미칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| 차. 제약유통 경쟁 관련 위험 국내 의약품 도매유통 시장의 특징으로는 과도한 경쟁 및 대형 도매업체의 집중도 증가를 꼽을 수 있습니다. 도매업체의 수는 2010년 1,716개에서 2022년 3,433개로 증가하였으며, 2022년을 기준으로 매출액 1,000억원 이상 규모의 도매업체는 76개소로 전체 도매업체의 2.3%에 해당하지만 이들이 요양기관에 공급하는 금액은 약 27.4조원으로 전체 도매상 공급금액의 61.9%를 차지하고 있습니다. 이러한 상황속에서 당사의 연결종속회사 (주)신화어드밴스의 수익성은 꾸준함을 보이고 있습니다. 주식회사 신화어드밴스는 2016년 4분기부터 당사의 연결기준 손익계산서에 실적이 반영되고 있으며, 당사의 연결기준 손익계산서에서 주식회사 신화어드밴스의 매출비중은 2021년 70.54%, 2022년 54.28%, 2023년 64.71%, 2024년 1분기 70.51%로 매우 높은 비중을 차지하고 있어 주식회사 신화어드밴스의 매출 및 수익성은 당사의 연결기준 실적에 직접적으로 영향을 미치고 있습니다. 향후 국내외 제약유통업체 간의 경쟁이 더욱 치열해지거나 신규 기업이 시장에 진입할 경우 주식회사 신화어드밴스의 시장점유율이 축소되거나 가격 경쟁이 심화될 수 있으며, 이 경우 당사의 매출 및 수익성에 부정적인 영향을 미치게 되오니 투자자 여러분께서는 이 점을 유의하시어 투자에 임해주시기 바랍니다. |
주식회사 신화어드밴스는 2007년 11월 19일 의약품 유통업 및 관련사업 등을 주 사업목적으로 설립하였습니다. 국,공립병원에 의약품을 납품하고 있으며, 특히 유한양행, 동아에스티, 제일약품, 대웅제약, 한미약품, 종근당, 일동제약, 보령제약, SK케미칼 등 국내 상위권 제약사와 한국다이이찌산쿄(Daiichi Sankyo Korea), 비아트리스코리아(Viatris), 노바티스(Novartis), MSD, 아스트라 제네카(Astra Zeneca), 오츠카제약(Otsuka) 등 유수의 외국계 제약사와 거래 관계를 맺고 있습니다.
의약품도매의 기능은 「약사법」제44조 제2항 제2호와 제45조에 의거하여 제약사는 연구개발 및 제조에만 전념할 수 있도록 의약품물류를 비롯한 유통전반을 책임지는 것이라고 할 수 있습니다.
| 「약사법」 |
|---|
|
제44조(의약품 판매) ②제1항에도 불구하고 다음 각 호의 어느 하나에 해당하는 자는 의약품을 판매하거나 판매할 목적으로 의약품을 취득할 수 있다. <개정 2012.5.14., 2016.12.2.> 1. 제91조에 따라 설립된 한국희귀·필수의약품센터 1의2. 제44조의2에 따라 등록한 안전상비의약품 판매자(제44조의2제1항에 따른 안전상비의약품을 판매하는 경우만 해당한다) 2. 제45조에 따라 허가를 받은 한약업사 및 의약품 도매상 |
|
제45조(의약품 판매업의 허가) ② 제1항에 따라 허가를 받으려는 한약업사 또는 의약품 도매상은 다음 각 호의 구분과 같이 시설을 갖추어야 한다. <개정 2011.3.30., 2014.3.18., 2015.1.28.> 1. 한약업사는 영업소와 그 밖에 대통령령으로 정하는 기준에 맞는 시설 2. 의약품 도매상은 영업소와 창고 및 그 밖에 대통령령으로 정하는 기준에 맞는 시설. 이 경우 창고의 면적은 165제곱미터 이상이어야 한다. 다만, 수입의약품·시약·원료의약품만을 취급하는 경우에는 창고의 면적이 66제곱미터 이상이어야 하고, 동물용의약품만을 취급하는 경우에는 창고의 면적이 33제곱미터 이상이어야 하며, 한약·의료용고압가스 및 방사성의약품만을 취급하는 경우에는 창고의 면적기준을 적용하지 아니한다. ③제1항에 따른 한약업사는 보건복지부령이 정하는 지역에 한정하여 대통령령으로 정하는 한약업사시험에 합격한 자에게 허가한다. <개정 2008.2.29., 2010.1.18.> ④제1항에 따라 허가를 받은 한약업사는 환자가 요구하면 기존 한약서에 실린 처방 또는 한의사의 처방전에 따라 한약을 혼합 판매할 수 있다. ⑤제1항에 따라 허가를 받은 의약품 도매상은 약사를 두고 업무를 관리하게 하여야 하며, 한약 도매상은 다음 각 호의 어느 하나에 해당하는 자를 두고 업무를 관리하게 하여야 한다. 다만, 의약품 도매상 자신이 약사로서 업무를 직접 관리하거나, 한약 도매상이 다음 각 호의 어느 하나에 해당한 자로서 업무를 직접 관리하는 경우에는 그러하지 아니하다. <개정 2008.2.29., 2010.1.18.> 1. 약사 2. 한약사 3. 한약업사 4. 보건복지부장관이 인정하는 대학의 한약 관련 학과를 졸업한 자 ⑥ 의약품 도매상 및 한약 도매상은 제5항에 따라 업무를 관리하는 자를 두려는 경우에는 보건복지부령으로 정하는 바에 따라 시장·군수·구청장에게 신고하여야 한다. <신설 2011.6.7.> ⑦제1항에 따른 허가의 기준, 조건 및 관리에 필요한 사항은 보건복지부령으로 정한다. <개정 2008.2.29., 2010.1.18., 2011.6.7.> ⑧ 제5항에도 불구하고 보건복지부령으로 정하는 요건을 갖춘 다른 의약품 도매상에 의약품의 보관·배송 등 유통관리 업무를 위탁하는 경우에는 제5항에 따른 업무관리자를 두지 아니할 수 있다. 다만, 이 경우 해당 유통관리 업무를 위탁받는 자는 보건복지부령으로 정하는 바에 따라 제5항에 따른 업무관리자를 두어야 한다. <신설 2015.12.29.> |
한국의 의약품 도매유통 시장은 지속적으로 성장하는 모습을 보이고 있습니다. 2010년도 이후 도매상 허가기준 완화가 이루어져 의약품 유통업체의 수가 급증하였습니다. 2022년에는 3,433개에 이른 것으로 나타나고 있습니다.
| [의약품 도매상 현황] |
| (단위:개수 |
 |
|
의약품 도매상 현황 |
| 출처: 완제의약품 유통정보통계집(2009~2022) |
의약품 시장의 대형 도매업체의 집중도는 더욱 높아지고 있습니다. 2022년을 기준으로 매출액 1,000억원 이상 규모의 도매업체는 76개소로 전체 도매업체의 2.3%에 해당하지만 이들이 요양기관에 공급하는 금액은 약 27.4조원으로 전체 도매상 공급금액의 61.9%를 차지하고 있습니다. 이는 규모가 큰 도매 업체 일수록 더 많은 품목을 공급하고, 가격 경쟁력 및 영업 커버리지 역량에 있어 소규모 도매 업체들보다 높은 경쟁력을 가지고 있기 때문입니다.
| [매출액 1,000억원 이상 도매상 비중 추이] |
 |
|
매출액 1,000억원 이상 도매상 비중 추이 |
| 출처: 완제의약품 유통정보통계집(2022) |
국내 의약품의 거래 구조 특징으로는 제조ㆍ수입사와 요양기관 간의 직거래가 감소하고, 제조ㆍ수입사에서 도매를 거쳐 요양기관으로 유통되는 도매유통 거래가 증가하고 있습니다. 의약품 도매상 간 거래 증가에 따른 유통마진 증가는 약품비 청구가격의 상승 요인으로 작용하여 건강보험재정에 악영향을 줄 수 있다는 우려가 있는 상태입니다.
| [국내 의약품 유통의 특성] |
| 도매유통의 특성 |
- 도매거래는 물류비용이 추가된다는 단점이 있지만 직거래와 비교할 때 통합 및 전문화된 물류를 제공하여 거래효율성을 증가시킬 수 있는 장점이 있음 - 요양기관은 도매거래를 통해 다양한 의약품을 안정적으로 공급받을 수 있으며 제약사는 재고부담, 물류비용, 판매촉진비, 인건비 등의 부담을 줄일 수 있음 |
| 일반 재화 유통과의 차별성 |
- 의약품은 사적재화인 동시에 공적재화로써의 특성을 가짐 - 의약품의 유통은 유효성, 안전성, 편의성 등이 확보되어야 함 - 의약품은 개발 및 제조(생산), 유통, 판매, 투약(소비)에 이르는 전 단계에서 정부의 제도적 규제의 대상이 됨 - 의약품은 소량의 다품종 상품이 다빈도로 거래됨 |
| 의약품 유통 구조 | - 제약업체와 도매업체의 수가 과도하게 많으며 영세 업체가 난립하고 있음 - 여러 단계의 도매를 거치는 도매가 증가하고 있음 - 외국에 비해 대형 도매업체의 비율이 현저하게 낮아 규모의 경제를 실현하지 못하고 있으며 의약품 유통 시스템의 분배 효율성이 떨어짐 |
| 의약품 도매유통 마진 |
- 업체의 마진은 매출총이익(매출액과 매출원가의 차이)을 의미하며 여기에는 순이익, 법인세, 판매관리비, 영업외비용이 포함됨 - 의약품 유통 마진은 의약품의 특성, 제조사의 특성, 요양기관과의 관계, 도매상의 기능 등에 의해 다양하게 영향을 받음 - 의약품 유통 마진은 업체의 이익뿐만 아니라 개별 의약품의 유통 단가 차액과도 혼재되어 사용되고 있음 - 의약품 유통 마진에 관한 성행 연구조사 대상과 마진에 대한 정의가 상이하고 매축액에 의약품 외의 이익이 반영되어 있을 수 있어 정보가 제한적임 |
| 출처: 의약품 도매상 유통 현황 및 비용구조 등 실태조사, 2015.12(건강보험심사평가원) |
의약품 도매업체의 의약품 유통 규모를 살펴보면 2022년 기준 자사 제품을 판매하는 제조/수입사가 전체 도매상으로 공급하는 의약품 금액은 27.7조원이며 요양기관에 직접 공급하는 금액은 3.3조원이었습니다. 도매상과 도매상 간 거래과정에서의 공급금액은 23.8조원으로 1차 도매상이 최초로 공급받는 금액 27.7조원의 89.5%로 나타났습니다.
| [의약품 유통단계별 공급금액 (2022년 기준)] |
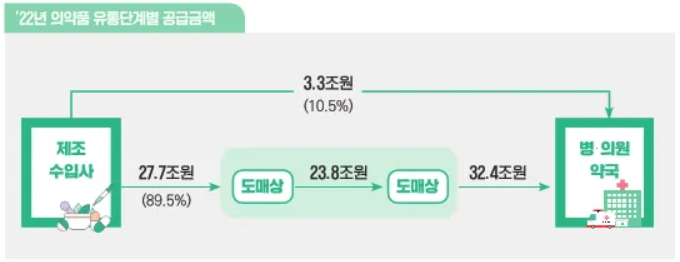 |
|
의약품 유통단계별 공급금액 |
| 출처: 완제의약품 유통정보 통계집, 2022 (건강보험심사평가원) |
| [연도별 유통단계별 의약품 공급금액] |
| (단위 : 억원) |
| 구 분 | 2020년 | 2021년 | 2022년 |
|---|---|---|---|
| 제조/수입 -> 요양기관 | 27,872 | 28,578 | 32,685 |
| 제조/수입 -> 도매상 | 235,830 | 248,405 | 277,356 |
| 도매상 -> 도매상 | 209,298 | 224,868 | 238,269 |
| 도매상 -> 요양기관 | 275,606 | 293,330 | 323,513 |
| 주) 제조/수입 -> 요양기관 : 자사제품을 공급한 제주/수입사가 요양기관에 공급한 경우 제조/수입 -> 도매상 : 자사제품을 공급한 제조/수입사가 도매상에 공급한 경우 도매상 -> 도매상 : 도매상 및 타사제품을 공급한 제조/수입사가 도매상에 공급한 경우 도매상 -> 요양기관 : 도매상 및 타사제품을 공급산 제조/수입사가 요양기관에 공급한 경우 |
| 출처: 2022 완제의약품 유통정보 통계집 |
주식회사 신화어드밴스가 영위하는 의약품도매사업의 특성은 제약업체와 요양기관을 위해 재고유지 및 품목보유와 다품목 소량판매 등의 기능을 수행함으로서 의약품의 수요와 공급 결합, 의약품의 유통비용을 절약, 요양기관에 의약품 구색갖춤 서비스를 제공하고 있습니다.
의약품 도매업을 수행하기 위해서는 영업소의 소재지를 관할하는 시장, 군수, 구청장의 허가를 받아야 하며, 허가를 얻기 위해 의약품 도매업체는 영업소와 창고 및 그 밖의 시설을 갖추고 일정 규모 이상의 자본을 가지고 약사를 두어 업무를 관리하게 하여합니다. 그러나 도매업 허가의 주요 요소인 창고 및 자본금 등은 모니터링 기전이 없이 도매업 허가 당시에만 검토의 대상이 되며, 특히 창고는 위탁운영이 가능하다는 한계가 있어 도매업의 진입장벽은 매우 낮다고 판단됩니다. 앞서 언급한 바와 같이 국내 의약품 도매유통기업은 지속적으로 증가하고 있고 도매상의 난립과 과다경쟁에 따른 효율성 저하 그리고 제도적, 시장 경제적 과점 환경요인으로 관련 업계의 수익성에 큰 영향을 미치고 있습니다.
당사의 종속회사인 주식회사 신화어드밴스는 오랜 업력을 바탕으로 의약품유통사업을 수행하며 다져진 영업력을 바탕으로 신규거래처를 꾸준히 확보하여 왔습니다. 또한 기업의 영업 조직을 통한 촉진 전략과 함께 제약업체 및 도매업체와의 전략적 제휴로 품목 경쟁력을 도모하였습니다. 이에 따라 향후 지역 인구 및 소득, 물류 효율성, 주변 상권 및 원외 시장 분석을 토대로 한 시장 표적 선정을 통해 안정적인 성장을 지향하고 있습니다. 주식회사 신화어드밴스는 2016년 4분기부터 당사의 연결기준 손익계산서에 실적이 반영되고 있으며, 당사의 연결기준 손익계산서에서 주식회사 신화어드밴스의 매출비중은 2021년 70.54%, 2022년 54.28%, 2023년 64.71%, 2024년 1분기 70.51%로 매우 높은 비중을 차지하고 있어 주식회사 신화어드밴스의 매출 및 수익성은 당사의 연결기준 실적에 직접적으로 영향을 미치고 있습니다.
| [당사 및 종속회사 매출현황] |
| (단위 : 백만원,%) |
| 구분 | 매출액 | |||||||||||
| 2024년 1분기 | 2023년 1분기 | 2023년 | 2022년 | 2021년 | ||||||||
| 금액 | 비중 | 금액 | 비중 | 금액 | 비중 | 금액 | 비중 | 금액 | 비중 | |||
| 메디케어사업 | HLB생명과학 | 제품매출 | 2,120 | 8.87 | 9,270 | 29.74 | 13,272 | 13.54 | 16,777 | 16.85 | - | - |
| 상품매출 | 1,530 | 6.40 | 6,045 | 19.40 | 10,776 | 11.00 | 15,508 | 15.57 | - | - | ||
| 용역매출 | - | - | - | - | - | - | 2,141 | 2.15 | - | - | ||
| 임대매출 | 387 | 1.62 | - | - | 897 | 0.92 | 258 | 0.26 | - | - | ||
| 기타매출 | - | - | 115 | 0.37 | - | - | 94 | 0.09 | - | - | ||
| HLB셀 | 제품매출 | - | - | 1 | 0.01 | 3 | 0.00 | 64 | 0.06 | - | - | |
| 상품매출 | - | - | - | - | - | - | 160 | 0.16 | - | - | ||
| 바이오 개발 사업 | HLB셀 | 용역 매출 | - | - | 18 | 0.05 | - | - | 93 | 0.09 | 13 | 0.02 |
| HLB생명과학 R&D | 용역 매출 | - | - | - | - | - | - | 18 | 0.02 | - | - | |
| 의료기기사업 | 화진메디칼 | 제품매출 | 1,940 | 8.12 | - | - | 4,268 | 4.36 | - | - | - | - |
| 상품매출 | 70 | 0.29 | - | - | 106 | 0.11 | - | - | - | - | ||
| 의약품유통사업 | 신화어드밴스 | 상품 매출 | 16,849 | 70.51 | 14,817 | 47.54 | 63,412 | 64.71 | 54,058 | 54.28 | 37,734 | 70.54 |
| 에너지사업 | HLB솔루션(*) | ESCO(에너지 절약) | - | - | - | - | - | - | 1,824 | 1.83 | 1,213 | 2.27 |
| 신재생에너지(태양광 및 지열) | - | - | 54 | 0.17 | 1,362 | 1.39 | 4,062 | 4.09 | 10,107 | 18.89 | ||
| 임대매출 | - | - | 6 | 0.02 | - | - | 260 | 0.26 | 500 | 0.94 | ||
| 기타매출 | - | - | 2 | 0.01 | 406 | 0.41 | 8 | 0.01 | 45 | 0.08 | ||
| HLB에너지 | 용역매출 | 999 | 4.18 | 838 | 2.69 | 3,487 | 3.56 | 4,266 | 4.28 | 3,761 | 7.03 | |
| 의령태양광1호 | 태양광 전력매출 | - | - | - | - | - | - | - | - | 120 | 0.23 | |
| 합 계 | 23,895 | 100.00 | 31,166 | 100.00 | 97,990 | 100.00 | 99,591 | 100.00 | 53,494 | 100.00 | ||
| (*) 2023년 9월 18일 에너지사업부 회사분할 결정하였으며, 2024년 1월 1일 분할신설회사 HLB솔루션을 설립하였습니다. 출처: 당사 분기보고서 |
향후 국내외 제약유통업체 간의 경쟁이 치열해지거나 신규 기업이 시장에 진입할 경우 주식회사 신화어드밴스의 시장점유율이 축소되거나 가격 경쟁이 심화될 수 있으며, 이 경우 당사의 매출 및 수익성에 부정적인 영향을 미치게 되오니 투자자 여러분께서는 이 점을 유의하시어 투자에 임해주시기 바랍니다.
| 카. 신재생에너지사업 관련 위험 에이치엘비솔루션(주)는 신재생에너지사업(태양광발전사업 포함)을 영위하고 있으며 신재생에너지 사업 역시 기본적으로 국가 정책에 큰 영향을 받습니다. 또한 신재생에너지사업으로 폐기물 등을 재생시켜 고형연료(SRF:Solid Refuse Fuel), 바이오에너지연료[목재칩(Wood Chip Fuel(WCF)), 목재펠릿(Wood Pellet)] 등을 소각하여 열에너지 및 전기에너지를 생산하는 재생에너지 소각발전 사업을 영위하고 있습니다. 신재생에너지 사업의 매출은 경제상황, 유가, 주력 대체자원 및 정부정책의 변화 등에 영향을 받으며 이는 에이치엘비솔루션(주)의 수익성 및 실적에 부정적인 영향을 미칠 수 있습니다. 투자자 여러분께서는 이 점을 유의하시고 투자에 임해주시기 바랍니다. |
한국수출입은행 해외경제연구소에 따르면 2022년 5.5GW를 정점으로 국내 태양광 설치량이 감소하고 있으며, 2023년 국내 태양광 시장은 전년 대비 15% 감소한 2.7GW가 설치될 것으며 예상하며, 2030년까지 연간 2.5~3.0GW 내외의 수요가 발생할 것으로 전망하고 있습니다. 국내 태양광 설치량은 2030년 신재생에너지 비중을 21.6%로 하향 조정, 신재생에너지 공급의무화(RPS) 제도 폐지 및 경매제도 도입, 전력도매가격(SMP) 상한 고정 등 정부정책 변경에 따라 정체될 것으로 예상하고 있습니다.
| [국내 태양광 기업들의 실적동향] |
| (단위: 억원) |
| 업체 | 2020년 | 2021년 | 2022년 | 2022년 1분기 | 2023년 1분기 | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| 매출 | 영업 이익 |
매출 | 영업 이익 |
매출 | 영업 이익 |
매출 | 영업 이익 |
매출 | 영업 이익 |
|
| OCI | 8,520 | -77 | 13,330 | 4,870 | 8,651 | 895 | 1,948 | 109 | 2,180 | 87 |
| 한화솔루션 태양광산업 |
37,023 | 1,904 | 35,685 | -3,285 | 55,685 | 3,501 | 9,206 | -1,142 | 13,661 | 2,450 |
| 현대에너지 솔루션 |
3,944 | 88 | 5,932 | 95 | 9,848 | 902 | 1,761 | 77 | 1,408 | 80 |
| 신성이엔지 RE사업부 |
1,183 | -84 | 1,041 | -130 | 1,196 | 47 | 291 | 6 | 200 | 15 |
| 출처: 한국수출입은행 해외경제연구소 |
2023년 세계 태양광 설치량은 Big2(중국 및 미국) 지역의 양호한 수요 및 개도국 시장 의 빠른 성장으로 연초 전망치(320~340GW)보다 20GW 이상 더 설치될 전망되며, 2027년 이전에 연간 태양광 수요 500GW가 가능할 것으로 전망됩니다.
에이치엘비솔루션(주)는 신재생에너지사업(태양광발전사업 포함)을 영위하고 있으며 신재생에너지 사업 역시 기본적으로 국가 정책에 큰 영향을 받습니다. 태양광발전 및 신재생에너지에 대한 관심이 대두되면서 세계 각국은 정부 차원에서 집중 육성하려는 움직임 역시 나타나고 있습니다. 다만, 태양광발전사업은 각 프로젝트가 장기성(약 20년) 사업으로 수익성 판단 시 장기간에 대한 비용 및 수익성 추정이 필요하나 기술력의 개발 등으로 인한 투자비용의 감소추이 및 매전단가 예측과 관련하여 불확실성이 존재합니다. 따라서 투자시점에서 수익성 판단에 따라 투자된 사업이 실제 운영과정에서 수익성이 변동될 수 있으며 수익성이 기대를 하회하거나 운영손실이 발생할 가능성이 존재합니다.
또한 에이치엘비솔루션(주)는 신재생에너지사업으로 폐기물 등을 재생시켜 고형연료(SRF:Solid Refuse Fuel), 바이오에너지연료[목재칩(Wood Chip Fuel(WCF)), 목재펠릿(Wood Pellet)] 등을 소각하여 열에너지 및 전기에너지를 생산하는 재생에너지 소각발전 사업을 영위하고 있습니다. 이는 국내 현 신재생에너지사업의 30% 이상을 차지하고 있는 부문으로 상대적으로 경제성이 높아 태양광, 수력, 풍력보다는 공급의무발전사들이 선호하는 발전형태입니다. 그러나 고형연료(SRF), 바이오에너지연료(목재칩, 목재펠릿) 등은 경제성 문제와 함께 소각시 발생하는 분진 및 미세먼지 관련 환경문제가 제기되고 있어 환경규제 강화 관련 사업리스크가 존재합니다. 이에 따라 제한적 내용인 혼소비율, 대기배출인허가 항목 등은 법적 범위 내에서 사업성 검토 하고 추진함으로서 환경문제 관련 사업리스크를 최소화할 필요성이 있습니다.
| [신재생에너지사업(태양광 발전사업 위주) 위험요소] |
| 구분 | 내용 |
|---|---|
| 1 | 태양광 발전은 무엇보다 일조량을 음영 없이 많이 받는 것이 핵심이며, 이러한 일조량을 좌우하는 것이 바로 지형임. 험한 산지가 많은 한국의 특성상 태양광 발전을 위한 부지를 조성하기 위해 땅을 최대한 평탄하게 하기위한 토목공사가 반드시 수반되어야 함. 이러한 과정에서 발생하는 부대비용이 상당하다는 점과 환경적인 측면에서 이러한 부지조성을 위한 개발로 산림의 훼손을 고려할 때, 애로사항이 있음. |
| 2 | 전력공기업의 자체적 신재생에너지 설비 증대에 따른 급격한 REC 하락, 태풍으로 인한 시설물 파괴, 인버터 고장, 지속적인 설비에 대한 감가상각 발생함. |
| 3 | 신재생에너지 발전사업은 바람, 태양광 등 자연자원을 활용하는 것이기에, 사업자가 통제할 수 없는 자원임. 즉, 바람의 풍량 및 풍향, 태양의 일사량의 경우 기후환경에 따라 매우 유동적인 특징을 가지고 있어 그 크기를 정확히 예상할 수 없는 특징을 가지고 있기 때문에 예상밖의 저조한 발전량을 가져올 수 있는 위험이 항상 내재되어 있음. |
이처럼 신재생에너지 사업의 매출은 경제상황, 유가, 주력 대체자원 및 정부정책의 변화 등에 영향을 받으며 이는 에이치엘비솔루션(주)의 수익성 및 실적에 부정적인 영향을 미칠 수 있습니다. 투자자 여러분께서는 이 점을 유의하시고 투자에 임해주시기 바랍니다.
2. 회사위험
| [투자자 주의사항] |
|---|
| ■ 본 증권신고서는 당사의 영업활동 및 재무에 대해 보다 정확하고 실체적인 정보전달을 위해 연결기준으로 작성되었으며, 별도기준 재무제표는 [제2부 발행인에 관한 사항] 및 감사보고서 등을 참조하시기 바랍니다. |
당사와 연결대상 종속회사의 사업부문별 현황은 다음과 같습니다.
| 회 사 명 | 사업부문 | 사업영역 |
|---|---|---|
| HLB생명과학 HLB셀 |
메디케어사업 부문 |
1. 체외 진단용 의료기기 개발/제조 2. 구성품 개발 및 완제품 위탁 생산(OEM/ODM) 3. 시약, 기자재 및 소모품 공급 4. 제품설계 및 금형 제작 5. 플라스틱 사출/제조 |
| HLB셀 HLB생명과학R&D |
바이오개발사업 부문 | 1. 체외순환형 바이오인공간 2. 지혈제 개발 3. 신약개발사업 4. 의약품 연구개발 및 판매업 5. 연구개발 용역업 및 서비스 |
| HLB생명과학 | 의료기기사업 부문 | 1. 일회용 주사기 제조, 판매업 2. 의료용구 제조, 판매업 3. 의료용구 유통판매(수입포함) |
| 신화어드밴스 | 의약품유통사업 부문 | 의약품 유통업 |
| HLB솔루션 HLB에너지 |
에너지사업 부문 | 1. 태양광 EPC 사업 2. 폐기물 소각열 관련사업 |
| 주1) 당사는 2023년 9월 18일 실시한 이사회 결의를 통해 단순 물적분할로 2024년 01월 01일부 에너지 사업부문을 분할신설회사인 에이치엘비솔루션(주)로 포괄 승계하였습니다. |
| [요약 연결재무정보] |
| (단위 : 백만원) |
| 구 분 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 자산총계 | 629,554 | 423,500 | 411,790 | 270,780 | 327,197 |
| - 유동자산 | 229,728 | 147,043 | 160,776 | 156,822 | 181,329 |
| - 비유동자산 | 399,825 | 276,457 | 251,051 | 113,977 | 145,868 |
| 부채총계 | 196,711 | 192,288 | 175,724 | 24,188 | 39,453 |
| - 유동부채 | 144,796 | 135,457 | 26,785 | 13,536 | 17,865 |
| - 비유동부채 | 51,915 | 56,831 | 148,939 | 10,652 | 21,587 |
| 자본총계 | 432,843 | 231,213 | 236,067 | 246,611 | 287,744 |
| - 자본금 | 54,274 | 51,407 | 48,831 | 48,223 | 24,009 |
| 매출액 | 23,894 | 97,990 | 99,591 | 53,494 | 91,797 |
| 매출총이익 | 254 | (749) | (3,046) | (5,537) | 2,326 |
| 영업이익(손실) | (5,647) | (24,533) | (20,161) | (18,480) | (8,067) |
| 당기순이익(손실) | 145,390 | (5,913) | (54,360) | (49,292) | (55,836) |
| 출처 : 당사 각 사업년도 분기보고서 및 사업보고서 |
| 가. 매출액 및 수익성 저하 위험 당사는 구성품 개발 및 완제품 위탁 생산하는 메디케어사업, 주사기 제조 및 판매하는 의료기기사업, 종속회사 에이치엘비셀(주)가 영위하는 바이오 신약 및 의료기기를 개발하는 바이오 개발 사업, 종속회사 (주)신화어드밴스가 영위하는 의약품 유통 사업, 종속회사 에이치엘비에너지(주)가 영위하는 신재생에너지 사업으로 구성된 에너지사업까지 크게 5가지 부문으로 매출이 구성됩니다. 당사는 2022년 10월 체외 진단의료기기 및 기타 의료용기기 제조, 판매 기업인 에임(주)와 의료기기 및 의료소모품 생산, 판매 업체인 에임텍(주)를 흡수합병 함으로써 체외진단키드 등 의료기기 산업에 진출하였습니다. 이에 따라 2022년 기준, 전기 대비 86% 증가한 약 996억원(연결기준)의 매출을 달성하였으며, 2023년에는 약 980억을 기록했습니다. 2023년말 기준 사업별 매출액은 메디케어사업부문이 약 250억원으로 25.46%, 의료기기사업부문이 약 44억원으로 4.47%, 의약품유통사업이 약 634억원으로 64.71%, 에너지 사업부문이 약 53억원으로 5.36%의 매출액을 기록했습니다. 특히 2023년 7월 의료기기사업부 확대를 위하여 일회용 주사기 제조업을 영위하고 있는 화진메다칼(주)를 인수하여 약 44억원의 매출을 기록했습니다. 2022년과 2023년은 신규사업 확장을 통해 매출액 개선을 보였으며, 2023년말 기준 당사는 59억원의 당기순손실 기록했습니다. 2024년 1분기 메디케어사업부문이 약 40억원으로 16.9%, 의료기기사업부문이 약 20억원으로 8.4%, 의약품유통사업부문이 168억원으로 70.5%, 에너지사업부문이 약 10억원으로 4.2%의 매출을 기록했습니다. 또한 당사는 상대적으로 영업외수익 및 영업외비용이 수익성에서 큰 비중을 차지하고 있습니다. 그 중 매년 금융수익 및 금융원가의 변동폭에 따라, 당기순이익 및 당기순손실을 시현하고 있습니다. 단, 이는 주로 당사가 보유하고 있는 에이치엘비 주식회사 및 공제조합 지분 평가에 의한 금융자산 평가손익에 의한 것으로 향후에도 당사가 보유한 금융자산의 평가손익에 따라 당사의 수익성이 변동 될 위험이 있습니다. 투자자 여러분께서는 이 점 각별히 유의하시기 바랍니다. |
당사는 구성품 개발 및 완제품 위탁 생산하는 메디케어사업, 주사기 제조 및 판매하는 의료기기사업, 종속회사 에이치엘비셀(주)가 영위하는 바이오 신약 및 의료기기를 개발하는 바이오 개발 사업, 종속회사 (주)신화어드밴스가 영위하는 의약품 유통 사업, 종속회사 에이치엘비에너지(주)가 영위하는 신재생에너지 사업으로 구성된 에너지사업까지 크게 5가지 부문으로 매출이 구성되어 있습니다.
| [당사 및 종속회사 매출현황] |
| (단위 : 백만원,%) |
| 구분 | 매출액 | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2024년 1분기 | 2023년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 | |||||||||
| 금액 | 비중 | 금액 | 비중 | 금액 | 비중 | 금액 | 비중 | 금액 | 비중 | 금액 | 비중 | |||
| 메디케어사업 | HLB생명과학 | 제품매출 | 2,120 | 8.87 | 9,270 | 29.74 | 13,272 | 13.54 | 16,777 | 16.85 | - | - | - | - |
| 상품매출 | 1,530 | 6.40 | 6,045 | 19.40 | 10,776 | 11.00 | 15,508 | 15.57 | - | - | - | - | ||
| 용역매출 | - | - | - | - | - | - | 2,141 | 2.15 | - | - | - | - | ||
| 임대매출 | 387 | 1.62 | - | - | 897 | 0.92 | 258 | 0.26 | - | - | - | - | ||
| 기타매출 | - | - | 115 | 0.37 | - | - | 94 | 0.09 | - | - | - | - | ||
| HLB셀 | 제품매출 | - | - | 1 | 0.01 | 3 | 0.00 | 64 | 0.06 | - | - | - | - | |
| 상품매출 | - | - | - | - | - | - | 160 | 0.16 | - | - | - | - | ||
| 바이오 개발 사업 | HLB셀 | 용역 매출 | - | - | 18 | 0.05 | - | - | 93 | 0.09 | 13 | 0.02 | 7 | 0.01 |
| HLB생명과학 R&D | 용역 매출 | - | - | - | - | - | - | 18 | 0.02 | - | - | - | - | |
| 의료기기사업 | 화진메디칼 | 제품매출 | 1,940 | 8.12 | - | - | 4,268 | 4.36 | - | - | - | - | - | - |
| 상품매출 | 70 | 0.29 | - | - | 106 | 0.11 | - | - | - | - | - | - | ||
| 의약품유통사업 | 신화어드밴스 | 상품 매출 | 16,849 | 70.51 | 14,817 | 47.54 | 63,412 | 64.71 | 54,058 | 54.28 | 37,734 | 70.54 | 75,059 | 81.77 |
| 에너지사업 | HLB솔루션 | ESCO(에너지 절약) | - | - | - | - | - | - | 1,824 | 1.83 | 1,213 | 2.27 | 643 | 0.70 |
| 신재생에너지(태양광 및 지열) | - | - | 54 | 0.17 | 1,362 | 1.39 | 4,062 | 4.09 | 10,107 | 18.89 | 12,230 | 13.32 | ||
| 임대매출 | - | - | 6 | 0.02 | - | - | 260 | 0.26 | 500 | 0.94 | 346 | 0.38 | ||
| 기타매출 | - | - | 2 | 0.01 | 406 | 0.41 | 8 | 0.01 | 45 | 0.08 | 55 | 0.06 | ||
| HLB에너지 | 용역매출 | 999 | 4.18 | 838 | 2.69 | 3,487 | 3.56 | 4,266 | 4.28 | 3,761 | 7.03 | 3,080 | 3.36 | |
| 의령태양광1호 | 태양광 전력매출 | - | - | - | - | - | - | - | - | 120 | 0.23 | 14 | 0.02 | |
| 케이오쏠라 등 3개 회사 | 태양광 전력매출 | - | - | - | - | - | - | - | - | - | - | 363 | 0.40 | |
| 합 계 | 23,895 | 100.00 | 31,166 | 100.00 | 97,990 | 100.00 | 99,591 | 100.00 | 53,494 | 100.00 | 91,797 | 100.00 | ||
| 주1) 당사는 2021년 8월 25일 실시한 이사회 결의에 의하여 종속기업인 (주)아이오쏠라, (주)엠오쏠라, (주)케이오쏠라 3사는 청산되었습니다. 주2) 당사는 2021년 8월 26일 종속기업인 의령태양광1호㈜의 태양광발전소와 관련된 모든 자산을 1,870,000천원에 매각하는 계약을 체결하였으며, 2021년 10월 29일 행정절차가 완료되어 거래 종결되었습니다. 주3) 당사는 2023년 7월 3일 화진메디칼 지분 100% 를 인수하였고 2023년 10월 1일 합병하여 의료기기사업부로 편입하였습니다. 주4) 2023년 9월 18일 에너지사업부 회사분할 결정하였으며, 2024년 1월 1일 분할신설회사 HLB솔루션을 설립하였습니다. 출처: 당사 각 사업년도 분기보고서 및 사업보고서 |
당사는 2022년 10월 체외 진단의료기기 및 기타 의료용기기 제조, 판매 기업인 에임(주)와 의료기기 및 의료소모품 생산, 판매 업체인 에임텍(주)를 흡수합병 함으로써 체외진단키드 등 의료기기 산업에 진출하였습니다. 이에 따라 당사는 2022년 기준, 전기 대비 86% 증가한 약 996억원(연결기준)의 매출을 달성하였습니다. 에너지사업 부문은 전기 대비 34% 감소한 약 104억원, 의약품 유통 부문은 전기 대비 43% 증가한 약 540억원, 에임(주)과 에임텍(주)을 인수 및 합병을 통해 신설된 메디케어사업부문은 약 350억원의 매출을 달성하였습니다. 2023년에는 메디케어사업부문이 약 250억원으로 25.46%, 의료기기사업부문이 약 44억원으로 4.47%, 의약품유통사업이 약 634억원으로 64.71%, 에너지 사업부문이 약 53억원으로 5.36%의 매출액을 기록했습니다. 특히 2023년 7월 의료기기사업부 확대를 위하여 일회용 주사기 제조업을 영위하고 있는 화진메다칼(주)를 인수하여 약 44억원의 매출을 기록했습니다. 하지만 ESCO 사업의 경우 산업의 역성장 및 경쟁심화로 인해 매출이 점차 감소하였습니다. 따라서 당사는 바이오, 메디케어, 의료기기 등 의료용품 및 기타 의약관련제품 제조 사업부문을 주력 사업으로 경영 자원을 집중하고자, 2023년 9월 실시한 이사회 결의에 의해 단순 물적분할로 에너지 사업부문을 2024년 01월 01일부로 분할신설회사인 에이치엘비솔루션(주)로 포괄 승계하여 이 사업부문에 전문화된 사업역량을 강화하고자 하였습니다. 2024년 1분기 메디케어사업부문이 약 40억원으로 16.9%, 의료기기사업부문이 약 20억원으로 8.4%, 의약품유통사업부문이 168억원으로 70.5%, 에너지사업부문이 약 10억원으로 4.2%의 매출을 기록했습니다.
연결기준 당사 주요 수익성 관련 지표는 아래와 같습니다.
| [주요 영업수익성 추이(연결기준)] |
| (단위 : 백만원) |
| 구 분 | 2024년 1분기 | 2023년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|---|
| 매출액 | 23,894 | 31,166 | 97,990 | 99,591 | 53,494 | 91,797 |
| 매출원가 | 23,640 | 28,898 | 98,739 | 102,638 | 59,031 | 89,470 |
| 판매비관리비 | 5,900 | 5,090 | 23,784 | 17,115 | 12,943 | 10,393 |
| 영업이익(손실) | (5,647) | (2,822) | (24,533) | (20,161) | (18,480) | (8,067) |
| 영업이익(손실)률 | -23.63 | -9.05% | -25.04% | -20.24% | -34.55% | -8.79% |
| 금융수익 | 155,198 | 20,249 | 86,364 | 1,452 | 1,147 | 3,239 |
| 금융원가 | 5,839 | 4,919 | 28,161 | 32,902 | 26,765 | 23,395 |
| 당기순이익(손실) | 145,390 | 13,688 | (5,913) | (54,360) | (49,292) | (55,836) |
| 당기순이익(손실)률 | 608.48% | 43.92% | -6.03% | -54.58% | -92.14% | -60.83% |
| 출처: 당사 각 사업년도 반기보고서 및 사업보고서 |
당사는 최근 4개년 영업손실 및 당기순손실 구조가 지속 되고 있습니다. 2020년 약 558억원, 2021년 약 493억원, 2022년 약 544억원, 2023년 약 59억원의 당기순손실을 기록했습니다. 매출액을 살펴보면, 2021년은 2020년도 대비 ESCO(에너지 절약) 사업, 신재생에너지(태양광 및 지열) 등 매출액이 증가하였으나, 매출 비중의 약 70% 이상을 차지하는 종속회사 신화어드밴스가 영위하는 의약품 유통 사업이 2020년 약 751억원에서 2021년 약 377억원 매출액을 기록하며, 약 373억원(-49.73%) 감소한 것이 매출액 감소의 주요 원인이 되었습니다. 2022년에는 에임(주)과 에임텍(주)을 인수 및 합병을 통해 메디케어사업부문이 신규 추가됨으로써 약 350억원의 매출액 달성이 당사 매출액 상승의 주된 요인으로 작용으며, 2023년에는 화진메디칼(주)를 인수, 합병함으로써 의료기기사업부문의 신규 매출을 창출했습니다. 2024년 1분기에는 당사가 보유하고 있는 HLB(주) 보통주 1,933,601주가 2023년 12월 28일 기준 50,700원에서 2024년 3월 29일 기준 105,200원으로 107.5% 상승함에 따라 금융수익 약 1,552억원에 기인하며 당기순이익률 607.5%를 기록했습니다.
결국 당사 연결 실체의 매출액 변화는 신규사업 확장과 종속회사 신화어드밴스의 영업부진에 기인했습니다. 특히 2021년 신화어드밴스의 의약품 유통 사업 부문 매출 및 영업이익의 감소 사유는 1) 국공립병원 대상 입찰 성과 부진, 2) 제약사 저마진 정책, 3) 일련번호 제도 도입 등 의약품 유통 규제 강화 4) 반품 불용재고 문제로 인한 물류 유통 비용 증가 등이 있습니다. 의료법인들은 의약품 공급회사의 수익을 재단 법인 또는 병원으로 종속시키고자 조인트벤처(Joint venture)를 설립하여 의약품 유통 사업에 직접 참여를 하는 추세였으며, 이러한 환경 변화로 주요 매출처인 아주대병원, 차병원도 조인트벤처를 설립을 하게 되었고 신화어드밴스는 조인트벤처에 동참하지 못하여 지속적인 공급을 하지 못하게 된 것이 직접적인 원인이 되었습니다. 주요 거래처의 공급을 하지 못하게 됨으로 인하여, 관계 제약사들이 품목 할인율을 변경하거나 직거래 공급을 중단하게 되어 도매 매출과 기타 요양기관으로 공급되던 매출이 급감하게 된 원인도 있었습니다. 하지만 이후에 신화어드밴스는 오랜 기간 동안 의약품유통사업을 수행하며 다져진 영업력을 바탕으로 신규거래처 확보를 위해 꾸준히 노력하고, 자사 영업조직, 물류센터와 함께 제약업체 및 도매업체와의 전략적 제휴로 품목 및 가격 경쟁력에 우위를 선점하고, 지역 인구 및 소득, 물류 효율성, 주변 상권 및 원외 시장 분석 등의 데이터를 활용하여 표적시장 선정을 통해 안정적인 성장을 이루기 위해 노력함으로써 2022년 매출액 약 540억원으로 2021년 대비 43% 증가하였고 2023년 약 634억원을 기록했습니다.
당사는 상대적으로 영업외수익 및 영업외비용이 수익성에서 큰 비중을 차지하고 있습니다. 그 중 매년 금융수익 및 금융원가의 변동폭에 따라, 당기순이익 및 당기순손실을 시현하고 있습니다. 당사의 금융수익 및 원가는 주로 당사가 보유하고 있는 에이치엘비 주식회사의 보통주 및 공제조합 지분 평가에 의한 금융자산 평가손익에 의한 것으로 매분기 평가 결과에 따라 손익이 결정 됩니다.
| [주요 공정가치측정 금융자산 평가손익 현황] |
| (단위 : 주, 좌, 원) |
| 분류 | 구분 | 2022년 3분기 시가(평가액) |
2022년 3분기 장부가액 [A] |
2022년 4분기 시가(평가액) |
2022년 4분기 장부가액 [B] |
2022년 4분기 평가손익 증감액 [B-A] |
2023년 1분기 시가(평가액) |
2023년 1분기 장부가액 [C] |
2023년 1분기 평가손익 증감액 [C-B] |
|---|---|---|---|---|---|---|---|---|---|
| 공정가치평가 (유동금융자산) |
에이치엘비(주) 보통주 | 42,850 | 95,445,975,400 | 28,400 | 69,547,311,600 | (25,898,663,800) | 34,750 | 85,097,502,750 | 15,550,191,150 |
| 공정가치평가 (비유동금융자산) |
전기공사공제조합 | 352,773 | 70,554,600 | 352,773 | 70,554,600 | - | 353,871 | 70,774,200 | 219,600 |
| 기계설비건설공제조합 | 1,012,780 | 880,105,820 | 1,012,780 | 880,105,820 | - | 1,058,970 | 920,244,930 | 40,139,110 | |
| 엔지니어링공제조합 | 777,173 | 1,546,574,270 | 777,173 | 1,546,574,270 | - | 811,705 | 1,615,292,950 | 68,718,680 | |
| 합계 | - | 97,943,210,090 | - | 72,044,546,290 | (25,898,663,800) | - | 87,703,814,830 | 15,659,268,540 | |
| 분류 | 구분 | 2023년 2분기 시가(평가액) |
2023년 2분기 장부가액 [D] |
2023년 2분기 평가손익 증감액 [D-C] |
2023년 3분기 시가(평가액) |
2023년 3분기 장부가액 [E] |
2023년 3분기 평가손익 증감액 [E-D] |
|---|---|---|---|---|---|---|---|
| 공정가치평가 (유동금융자산) |
에이치엘비(주) 보통주 | 32,500 | 81,736,265,000 | (3,361,237,750) | 30,000 | 80,453,940,000 | (1,282,325,000) |
| 공정가치평가 (비유동금융자산) |
전기공사공제조합 | 355,501 | 71,100,200 | 326,000 | 356,295 | 71,259,000 | 158,800 |
| 기계설비건설공제조합 | 1,058,970 | 920,244,930 | - | 1,058,970 | 920,244,930 | - | |
| 엔지니어링공제조합 | 811,705 | 1,615,292,950 | - | 811,705 | 1,615,292,950 | - | |
| 합계 | - | 84,342,903,080 | (3,360,911,750) | - | 83,060,736,880 | (1,282,166,200) | |
| 분류 | 구분 | 2023년 4분기 시가(평가액) |
2023년 4분기 장부가액 [F] |
2023년 4분기 평가손익 증감액 [F-E] |
2024년 1분기 시가(평가액) |
2024년 1분기 장부가액 [G] |
2024년 1분기 평가손익 증감액 [G-F] |
|---|---|---|---|---|---|---|---|
| 공정가치평가 (유동금융자산) |
에이치엘비(주) 보통주 | 50,700 | 135,967,158,600 | 55,513,218,600 | 105,200 | 203,414,825,200 | 67,447,666,600 |
| 공정가치평가 (비유동금융자산) |
전기공사공제조합 | 356,295 | 71,259,000 | - | 356,295 | 71,259,000 | - |
| 기계설비건설공제조합 | 1,058,970 | 920,244,930 | - | - | - | - | |
| 엔지니어링공제조합 | 811,705 | 1,615,292,950 | - | 811,705 | 1,693,700,940 | 78,407,990 | |
| 합계 | - | 138,573,955,480 | 55,513,218,600 | - | 205,179,785,140 | 67,526,074,590 | |
| 주1) 에이치엘비(주) 보통주는 각 분기말 종가를 적용하여 시가 평가함 주2) 공제조합 평가액은 각 분기말 외부 평가를 통해 평가함 출처: 당사 내부자료 |
또한, 산정된 평가 손익은 전기 평가 손익 대비 손실 환입 및 이익 계상이 결정 됩니다. 2024년 1분기 기준 공정가치 측정 금융자산평가이익은 약 19,782백만원을 기록하였으며, 최근 3개년 당사의 공정가치 측정 금융자산 평가 손익 추이는 하기와 같습니다.
| [최근 4개년 공정가치 측정 금융자산 평가 손익 추이] |
| (단위 : 백만원) |
| 구 분 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 공정가치 측정 금융자산평가이익 | 19,848 | 73,874 | 126 |
632 |
92 |
| 공정가치 측정 금융자산평가손실 | 66 | 815 | 20,636 |
25,504 |
11,129 |
| 손익 합계 | 19,782 | 73,059 | (20,510) | (24,872) | (11,037) |
| 주1) 연결기준으로 작성되었으며 HLB셀의 HLB 보통주 평가이익 반영 출처: 당사 각 사업년도 분기보고서 및 사업보고서 |
상기와 같이, 당사의 금융수익 및 금융원가는 보유 금융자산의 평가손익에 따라 변동성이 있습니다. 따라서 당사가 안정적인 매출액을 바탕으로 영업이익을 지속적으로 시현 하지 못하는 한, 당사의 수익성이 악화 될 위험이 있습니다.
당사는 영업실적 부진 및 바이오사업 확장에 따른 비용 증가로 인해 2020년부터 계속해서 영업손실을 기록하였으며, 당사의 매출회복 및 적자구조 탈피를 위해 전사적으로 노력하고 있습니다. 의약품 유통 사업의 경우 대형 도매/약국 거래의 초단기확대, 신규 병원 확보 활동 강화, 입찰병원 진입 기회 조기 확보 등을 통해 기존사업의 매출확대와 총판 사업 확보, 비급여 시장 진입, 메디컬 약국 신규 확대 등을 통한 매출 확대를 계획하고 있습니다. 또한 기업 합병을 통한 메디케어사업부문과 의료기기사업부의 신규 매출을 통해 매출액 개선에 노력을 가하고 있습니다. 바이오 개발 사업 부문에서는 당사가 권리를 보유한 리보세라닙, 파이로티닙 등 신약물질의 임상 통과 등을 통해 매출 실현을 기대할 수 있습니다. 그러나 이와 같은 노력에도 불구하고 경쟁 심화로 인한 의약품 유통 사업 매출 감소, 바이오 사업 임상시험 지연 및 비용 증가 등으로 인해 당사의 수익은 더욱 악화될 수 있습니다. 투자자 여러분께서는 이 점 각별히 유의하시기 바랍니다.
| 나. 재무안정성 악화 가능성에 따른 위험 당사의 주요 재무안정성 지표 추이를 살펴보면, 연결기준 부채비율은 2020년말 13.7%, 2021년말 9.8%, 2022년말 74.4% 2023년말 83.2% 로 계속해서 증가하였습니다. 이는 신규사업 확장 및 운영자금 확보를 위해 2022년 신주인수권부사채 1,000억원, 전환사채 450억원을 발행, 2023년 전환사채 83억원 발행함으로써 부채비율이 증가했습니다. 이에 따라 총차입금이 꾸준히 증가 추세를 보이면서 차입금의존도 역시 2020년 3.3%를 기록 이후 지속적으로 증가하여 2023년 39.0%를 기록하고 있습니다. 2024년 1분기에는 제10회차 전환사채 2024.03.29 기준, 미상환사채 잔액 모두 전환청구와 제9회차 신주인수권부사채의 지속적인 전환 및 당사가 보유하고 있는 HLB(주) 보통주의 주가의 상승으로 인해 자본총계 약 4,328억원을 기록하며 부채비율 45.45% 및 차입금의존도 27.3%를 기록했습니다. 제10회차 전환사채 2024.03.29 기준, 미상환사채 잔액 모두 전환청구 하였으며, 제9회차 신주인수권부사채는 신주배정기준일(2024.05.10) 기준, 약 804억원은 만기 상 장기차입금으로 분류되어 있으나, 최초 조기상환일 기준 실질만기가 2024년중에 도래하기 때문에 단기적 상환부담이 존재하는 상황입니다. 향후에도 계속되는 영업실적의 부진, 임상 지연 등으로 인한 바이오 사업 매출 미실현 등에 따른 투자 등에 따라 차입금이 증가할 가능성이 존재하며, 지속적으로 차입을 할 경우 당사의 재무안정성이 악화될 가능성이 존재합니다. 투자자 분들께서는 이 점 유의하시기 바랍니다. |
당사의 연결기준 재무안정성 지표 추이는 다음과 같습니다.
| [연결기준 주요 재무안정성 지표 추이] |
| (단위: 백만원) |
| 구분 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 자산총계 | 629,554 | 423,500 | 411,790 | 270,799 | 327,197 |
| 부채총계 | 196,711 | 192,288 | 175,724 | 24,188 | 39,453 |
| 자본총계 | 432,843 | 231,213 | 236,067 | 246,612 | 287,744 |
| 부채비율 | 45.45% | 83.16% | 74.44% | 9.81% | 13.71% |
| 총차입금 | 171,563 | 165,231 | 144,496 | 3,500 | 10,734 |
| 차입금의존도 | 27.3% | 39.0% | 35.1% | 1.3% | 3.3% |
| 출처: 당사 각 사업년도 분기보고서 및 사업보고서 |
당사의 주요 재무안정성 지표 추이를 살펴보면, 연결기준 부채비율은 2020년 13.7%, 2021년 9.8%, 2022년 74.4% 및 2023년 83.2% 로 2021년 이후로 계속 증가하였습니다. 이는 신규사업 확장 및 운영자금 확보를 위해 신주인수권부사채 및 전환사채를 발행이 부채비율 증가에 기인했습니다. 이에 따라 총차입금이 꾸준히 증가 추세를 보이며 차입금의존도 역시 2020년 3.3%를 기록한 이후 지속적으로 증가하여 2023년 39.0%를 기록했습니다. 2024년 1분기에는 제10회차 전환사채 2024.03.29 기준, 미상환사채 잔액 모두 전환청구와 제9회차 신주인수권부사채의 지속적인 전환 및 당사가 보유하고 있는 HLB(주) 보통주의 주가의 상승으로 인해 자본총계 약 4,328억원을 기록하며 부채비율 45.45% 및 차입금의존도 27.3%를 기록했습니다.
| [연결기준 당사 차입금 현황 및 추이] |
| (단위: 백만원) |
| 구분 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 총차입금 | 171,563 | 165,231 | 144,496 | 3,500 | 10,734 |
| 현금및현금성자산 | 55,569 | 16,769 | 30,978 | 31,254 | 37,157 |
| 순차입금 | 115,994 | 148,462 | 113,518 | (27,754) | (26,423) |
| 출처: 당사 각 사업년도 분기보고서 및 사업보고서 |
당사의 연결기준 총차입금은 2020년말 약 10,734백만원, 2021년말 3,500백만원, 2022년말 약 144,496백만원, 2023년 약 165,231백만원 및 2024년 1분기 171,563백만원을 기록하였습니다. 유동성차입금은 은행 차입금으로 평균 5.3% 금리로 사용중에 있습니다. 비유동차입금으로는 2022년 체외진단의료기기 및 기타 의료용기기 제조, 판매 기업인 에임(주)과 의료기기 및 의료소모품 생산, 판매 기업인 에임텍(주)를 흡수합병함에 따라 신규사업 확장 및 운영자금 확보를 위해 발행된 제9회차 신주인수권부사채 1,000억원, 10회차 전환사채 450억원, 2023년 11회차 전환사채 83억원 등이 해당합니다. 총차입금 중 장기차입금이 큰 비중을 차지하고 있으며, 이는 주로 전환사채 및 신주인수권부사채 발행에 따른 장기차입금 증가에 기인했습니다.
| [2022~2023년 당사 전환사채, 신주인수권부사채 발행내역] |
| (단위: 백만원) |
|
구분 |
회차 |
납입일 |
최초 조기상환일 |
만기일 |
사용용도 |
조달금액 |
미상환잔액 |
|---|---|---|---|---|---|---|---|
|
사모 |
제10회 전환사채 |
2022-07-01 |
2024-07-01 |
2027-07-01 |
타법인 증권 취득자금 |
45,000 |
- |
|
제11회 전환사채 |
2023-07-04 |
2025-07-04 |
2028-07-04 |
운영자금 |
8,300 |
8,300 |
|
| 제12회 전환사채 | 2023-11-07 | 2025-07-07 | 2027-07-01 | 채무상환자금 | 28,800 | 28,800 | |
|
공모 |
제9회 신주인수권부사채 |
2022-06-15 |
2024-06-15 |
2025-06-15 |
운영자금 및 |
100,000 |
80,374 |
| 합 계 | 182,100 | 117,474 | |||||
| 주1) 미상환 잔액은 신주배정기준일(2024.05.10) 기준 주2) 제10회차 전환사채 2024.03.29 기준, 미상환사채 잔액 모두 전환청구 하였습니다. |
당사는 현금및현금성자산을 규모 대비 차입금 규모가 큰 편이며 지속적으로 차입을 할 경우 당사의 재무안정성이 악화될 가능성이 존재합니다. 투자자 분들께서는 이 점 유의하시기 바랍니다.
당사의 2023년말과 2024년 1분기의 연결기준 장·단기차입금 세부내역 및 차입금 상환계획은 아래와 같습니다.
| [당사 단기차입금 내역] |
| (단위 : 천원) |
| 구분 | 차입처 | 이자율(%) | 만기일 | 2024년 1분기 | 2023년말 |
|---|---|---|---|---|---|
| 시설자금 | 우리은행 | 5.96 | 2025-03-20 | 1,150,000 | 1,150,000 |
| 시설자금 | 국민은행 | 5.14 | 2024-08-16 | 5,000,000 | 5,000,000 |
| 시설자금 | 국민은행 | 5.14 | 2024-08-20 | 4,070,000 | 4,070,000 |
| 주식담보대출 | 한국투자증권 | 4.5 | 2025-01-30 | 20,000,000 | - |
| 소 계 | 30,220,000 | 10,220,000 | |||
| 차감 : 현재가치할인차금 | (334,074) | - | |||
| 차감잔액 | 29,885,926 | 10,220,000 | |||
| 출처 : 당사 분기보고서 |
| [당사 장기차입금 내역] |
| (단위 : 천원) |
| 구분 | 차입처 | 이자율(%) | 만기일 | 2024년 1분기 | 2023년말 |
|---|---|---|---|---|---|
| 시설자금 | 국민은행 | 4.98 | 2025-01-16 | 1,560,000 | 1,560,000 |
| 시설자금 | 우리은행 | 5.36 | 2025-03-31 | 4,800,000 | 4,800,000 |
| 온렌딩대출 | 하나은행 | 4.96 | 2030-03-15 | 3,000,000 | 3,125,000 |
| 시설자금 | 산업은행 | 4.21 | 2032-01-17 | 10,000,000 | 10,000,000 |
| 시설자금 | 국민은행 | 4.83 | 2024-08-20 | 5,000,000 | 5,000,000 |
| 시설자금 | 국민은행 | 3.8 | 2024-09-30 | 1,560,000 | 1,560,000 |
| 시설자금대출 | 기업은행 | 4.545 | 2028-09-30 | 50,000 | 50,000 |
| 시설자금대출 | 기업은행 | 2.32 | 2033-09-30 | 3,750,000 | 2,520,000 |
| 소 계 | 29,720,000 | 28,615,000 | |||
| 차감 : 유동성대체 | (13,420,000) | (7,060,000) | |||
| 차감잔액 | 16,300,000 | 21,555,000 | |||
| 출처 : 당사 분기보고서 |
| [당사 차입금 상환 계획] |
| (단위: 천원) |
| 구 분 | 금액 |
| 1년 이내 | 33,480,000 |
| 1년 초과 2년 이내 | 133,383,115 |
| 2년 초과 3년 이내 | 1,928,560 |
| 3년 초과 4년 이내 | 1,928,560 |
| 4년 초과 5년 이내 | 1,928,560 |
| 5년 초과 | 5,267,820 |
| 합 계 | 177,916,615 |
| - 상환스케줄 금액은 장기차입금의 상환 예정 금액과 전환사채 및 신주인수권부사채의 권면총액에 상환할증금이 가산된 금액으로 구성되어있습니다. 한편 전환사채는 최초 조기상환일인에 모두 상환되고, 신주인수권부사채는 최초 조기상환일인 2024년 6월 15일에 모두 상환되는 것으로 가정하였습니다. - 2024년 만기 도래하는 차입금과 관련하여 내부적인 자금계획을 수립 중이며, 해당 계획은 시장상황에 따라 변동할 수 있습니다. - 공시작성기준일 현재 당사의 주요 사업을 위한 일반적 지출 외 특이사항은 없습니다. 당사 및 연결회사는 지속가능한 수익을 추구함과 동시에 안정적인 유동성 확보를 위해 균형적인 자금조달 및 지출을 실행할 예정입니다. |
| 출처 : 당사 사업보고서 |
제10회차 전환사채 2024.03.29 기준, 미상환사채 잔액 모두 전환청구 하였으며, 제9회차 신주인수권부사채는 신주배정기준일(2024.05.10) 기준, 약 804억원은 만기 상 장기차입금으로 분류되어 있으나, 최초 조기상환일 기준 실질만기가 2024년중에 도래하기 때문에 단기적 상환부담이 존재하는 상황입니다. 향후에도 계속되는 영업실적의 부진, 임상 지연 등으로 인한 바이오 사업 매출 미실현 등에 따른 투자 등에 따라 차입금이 증가할 가능성이 존재하며, 지속적으로 차입을 할 경우 당사의 재무안정성이 악화될 가능성이 존재합니다. 투자자 분들께서는 이 점 유의하시기 바랍니다.
| 다. 유동성 악화에 따른 위험 당사는 2020년을 제외하고 최근 지속적으로 영업활동현금유출이 발생하고 있습니다. 2020년 약 2,010백만원으로 영업활동현금유입이 발생하였으나, 2021년 약 14,084백만원, 2022년 약 29,744백만원, 2023년 약 10,016백만원, 2024년 1분기 약 5,465백만원의 영업활동현금유출을 기록했습니다. 당사의 영업활동현금흐름 유출의 주된 원인은 실적부진이며 영업활동현금흐름과 투자활동현금흐름의 유출을 재무활동(외부차입 등)을 통하여 충당하고 있습니다. 2020년, 2021년 음(-)의 재무활동현금흐름을 기록했으나, 2022년, 2023년 양(+)의 재무활동현금흐름을 기록했습니다. 2022년 제9회 신주인수권부사채 1,000억 및 제10회 전환사채 450억 발행과 에임(주) 및 에임텍(주)를 흡수합병 함으로써 102,096백만원의 순재무활동현금흐름을 기록했습니다. 2023년에는 제11회 전환사채 83억 발행 및 단기차입금 증가로 약 7,710백만원의 재무활동현금흐름을 기록했으며, 2024년 1분기에는 제9회차 신주인수권부사채의 청구에 따라 58,803백만원의 재무활동현금흐름을 기록했습니다. 현재까지 투자활동을 통한 현금 유입으로 유동성을 확보하였으나, 바이오사업 매출 실현 지연으로 인한 영업활동현금 유출 지속 및 국내 경기의 악화, 금융시장의 부진 등으로 재무활동현금 유입이 원활하지 못할 경우 당사는 유동성 압박에 시달릴 수 있습니다. 투자자 분들께서는 이 점 유의하시기 바랍니다. |
당사는 2020년을 제외하고 최근 지속적으로 영업활동현금유출이 발생하고 있습니다. 2020년 약 2,010백만원으로 영업활동현금유입이 발생하였으나, 2021년 약 14,084백만원, 2022년 약 29,744백만원, 2023년 약 10,016백만원, 2024년 1분기 약 5,465백만원의 영업활동현금유출을 기록했습니다. 당사의 영업활동현금흐름 유출의 주된원인은 실적부진입니다. 2020년 약 558억원, 2021년 약 493억원, 2022년 약 544억원 및 2023년 약 59억원의 당기순손실을 기록했습니다. 이는 당사의 의약품 유통 사업의 저마진 거래처로 인한 높은 매출원가율, 바이오개발사업의 매출 대비 높은 비용으로 기인된 것으로 판단됩니다. 2024년 1분기에는 당사가 보유하고 있는 HLB(주) 보통주의 주가의 상승으로 인해 당기순이익 145,527백만원 기록하며 영업활동현금흐름 또한 2023년말 대비 개선되었습니다.
| [영업활동현금흐름 상세내역] |
| (단위: 백만원) |
| 구 분 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 영업활동현금흐름 | (5,465) |
(10,016) |
(29,744) | (14,084) | 2,010 |
| 당기순이익(손실) | 145,527 |
(6,553) |
(54,360) | (49,292) | (55,836) |
| 비현금항목 조정 | (149,665) |
(8,589) |
38,516 | 33,698 | 51,594 |
| 운전자본의 변동 | (1,177) |
5,761 |
(13,241) | 602 | 4,930 |
| 이자수익 수취 | 241 |
1,389 |
1,147 | 589 | 1,859 |
| 배당금수취(영업) | - | - | 9 | - | - |
| 이자비용 지급 | (453) |
(2,728) |
(675) | (251) | (324) |
| 법인세납부(환급) | 62 | 704 | (1,140) | 569 | (214) |
| 출처: 당사 각 사업년도 분기보고서 및 사업보고서 |
당사의 투자활동현금흐름의 경우 2020년, 2021년 현금유입을 기록했지만, 2022년, 2023년, 2024년 1분기 현금유출을 기록했습니다. 2020년에는 단/장기 금융상품 처분으로 약 88,711백만원의 현금유입을 기록하였으나, 에이치엘비제약(주) 지분 인수 및 파이로티닙 한국 독점 라이선스 도입계약 등으로 인해 약 62백만원의 순투자활동현금흐름을 기록했습니다. 2022년에는 체외 진단의료기기 및 기타 의료용기기 제조, 판매 기업인 에임(주)과 의료기기 및 의료소모품 생산, 판매 기업인 에임텍(주)를 10월 흡수합병하고, 에이치엘비제약(주) 전환사채 매입 등을 통해 약 72,643백만원의 현금유출을 기록했습니다. 2023년에는 당기손익-공정가치측정금융자산의 처분 및 유형자산의 취득으로 약 8,883백만원의 현금유출을 기록했습니다. 또한 2024년 1분기에는 단기금융상품의 취득 및 당기손익-공정가치측정금융자산의 취득으로 약 14,540백만원의 현금유출을 기록했습니다.
| [투자활동현금흐름 상세내역] |
| (단위: 백만원) |
| 구 분 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 투자활동현금흐름 | (14,540) | (8,883) | (72,643) | 8,822 | 62 |
| 단기금융상품의 처분 | 1,859 | 13,916 | 33,934 | 15,405 | 51,046 |
| 장기금융상품의 처분 | - | - | 324 | - | 37,665 |
| 당기손익-공정가치측정금융자산의 처분 | 2,441 | 28,454 | 5,000 | - | 1,564 |
| 기타포괄손익-공정가치측정금융자산의 처분 | - | - | - | 250 | 250 |
| 상각후원가 측정 금융자산의 처분 | - | - | - | 1,579 | - |
| 단기대여금의 감소 | - | 491 | 7,445 | 6,368 | |
| 장기대여금의 감소 | - | 16 | 126 | 136 | 50 |
| 유형자산의 처분 | 15 | 6,652 | 833 | 94 | 50 |
| 투자부동산의 처분 | - | - | - | 3,432 | - |
| 무형자산의 처분 | - | 1,231 | 9 | 208 | - |
| 매각예정비유동자산의 처분 | - | - | 6,846 | 1,870 | 6,090 |
| 종속기업 및 관계기업투자의 처분 | - | (972) | - | 12,690 | - |
| 금융리스채권의 감소 | - | - | 179 | - | - |
| 임차보증금의 감소 | 8 | 714 | 603 | 316 | 329 |
| 기타보증금의 감소 | - | - | - | - | - |
| 단기금융상품의 취득 | (8,051) | (11,046) | (20,674) | (21,521) | (46,388) |
| 장기금융상품의 취득 | - | - | (9) | - | (402) |
| 당기손익-공정가치측정금융자산의 취득 | (5,215) | (12,085) | (30,672) | (1,043) | (6,611) |
| 상각후원가측정금융자산의 취득 | - | - | - | (28) | - |
| 단기대여금의 증가 | - | - | (3,985) | (5) | (7,480) |
| 장기대여금의 증가 | - | - | (30) | - | (10) |
| 유형자산의 취득 | (4,514) | (20,618) | (10,601) | (2,356) | (8,410) |
| 투자부동산의 취득 | - | - | (76) | (65) | - |
| 무형자산의 취득 | (33) | (904) | (1,053) | (254) | (12,398) |
| 종속기업 및 관계기업투자의 취득 | (600) | (14,057) | (17,214) | (1,620) | (21,323) |
| 사업결합으로인한현금유출 | (449) | - | (43,184) | - | - |
| 임차보증금의 증가 | - | (675) | (424) | (266) | (329) |
| 기타보증금의 증가 | - | - | -21 | - | - |
| 출처: 당사 각 사업년도 분기보고서 및 사업보고서 |
당사는 2020년, 2021년 음(-)의 재무활동현금흐름을 기록했으나, 2022년, 2023년, 2024년 1분기에는 양(+)의 재무활동현금흐름을 기록했습니다. 2022년 제9회 신주인수권부사채 1,000억 및 제10회 전환사채 450억 발행과 에임(주) 및 에임텍(주)를 흡수합병 함으로써 약 102,096백만원의 순재무활동현금흐름을 기록했습니다. 2023년에는 제11회 전환사채 83억 발행 및 단기차입금 증가로 약 7,710백만원의 재무활동현금흐름을 기록했으며, 2024년 1분기에는 제9회차 신주인수권부사채의 청구에 따라 58,803백만원의 재무활동현금흐름을 기록했습니다.
| [재무활동현금흐름 상세내역] |
| (단위: 백만원) |
| 구 분 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 재무활동현금흐름 | 58,803 | 4,786 | 102,096 | (641) | (1,684) |
| 단기차입금의 증가 | 24,600 | 7,710 | 7,400 | 1,000 | - |
| 장기차입금의 증가 | 1,230 | 2,570 | 180 | - | 3,500 |
| 신주인수권부사채의 증가 | - | - | 98,580 | - | - |
| 단기차입금의 상환 | - | (5,000) | (4,000) | (1,000) | (868) |
| 유동성장기차입금의 상환 | (125) | - | (6) | - | (3,900) |
| 신주인수권부사채의 청구 | 34,552 | - | - | - | - |
| 금융리스부채의 감소 | (242) | (1,428) | (1,316) | (633) | (498) |
| 기타 | (1,212) | 934 | 1,259 | (7) | 82 |
| 출처: 당사 각 사업년도 분기보고서 및 사업보고서 |
당사는 영업활동현금흐름과 투자활동현금흐름의 유출을 재무활동(외부차입 등)을 통하여 충당하고 있습니다. 그러나 바이오사업 매출 실현 지연으로 인한 영업활동현금 유출 지속 및 국내 경기의 악화, 금융시장의 부진 등으로 재무활동현금 유입이 원활하지 못할 경우 당사는 유동성 압박에 시달릴 수 있습니다. 투자자 분들께서는 이 점 유의하시기 바랍니다.
| [현금흐름표 요약] |
| (단위 : 백만원) |
| 구분 | 2024년1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 영업활동현금흐름 | (5,465) | (10,016) | (29,744) | (14,084) | 2,010 |
| 투자활동현금흐름 | (14,540) | (8,883) | (72,643) | 8,822 | 62 |
| 재무활동현금흐름 | 58,804 | 4,786 | 102,096 | (641) | (1,684) |
| 현금및현금성자산의순증가(감소) | 38,798 | (14,113) | (291) | (5,903) | 388 |
| 기초현금및현금성자산 | 16,769 | 30,978 | 31,254 | 37,157 | 36,769 |
| 기말현금및현금성자산 | 55,569 | 16,769 | 30,978 | 31,254 | 37,157 |
| 출처: 당사 각 사업년도 분기보고서 및 사업보고서 |
한편, 당사가 2024년 1분기 연결기준 보유하고 있는 매출채권잔액은 약 143억원이며, 향후 거래처의 경영사정에 따라 회수실적이 변경될 수 있어 주기적으로 점검할 예정입니다.
| [매출채권잔액 현황] |
| (단위: 천원) |
| 구분 | 정상채권 | 3개월 이하 | 3개월 초과 ~ 6개월 이하 |
6개월 초과 | 대손확정 | 합계 |
|---|---|---|---|---|---|---|
| 기대 손실률 | 0.05% | 0.01% | 5.31% | 49.62% | 100.00% | 6.29% |
| 총 장부금액 | 12,381,110 | 936,778 | 45,189 | 13,410 | 0 | 13,376,487 |
| 매출채권 | 12,387,837 | 936,899 | 47,721 | 26,619 | 875,335 | 14,274,411 |
| 손실충당금 | (6,727) | (121) | (2,532) | (13,208) | (875,335) | (897,924) |
| 출처: 당사 분기보고서 |
또한 당사의 유동비율은 계속해서 100%를 상회하고 있습니다. 2020년 1,015.0%, 2021년 1,158.6%으로 매우 높은 수준을 기록한 후, 지속적으로 하락하여 2023년 108.6% 및 2024년 1분기 158.7% 수준을 기록하고 있는데, 이는 단기차입금 및 유동성 장기차입금의 증가에 따른 유동부채 증가에 기인합니다. 이자보상배율은 모두 음(-)의 값을 기록하고 있으며, 이는 영업이익 적자에 따른 결과입니다. 이자보상배율이 1배 미만인 경우 영업활동에서 창출한 이익으로는 금융비용을 지불할 수 없을 정도로 채무상환능력이 취약하다는 것을 의미합니다. 따라서 향후에도 현재와 같은 추세가 지속될 경우 당사의 채권상환 능력에 의문이 제기될 수 있으며, 이로 인해 신용대출이 어려워질 경우 당사의 유동성에 부정적인 영향을 미칠 수 있습니다.
당사의 총차입금은 2024년 1분기 연결기준 약 1,716억원으로 2020년말 총차입금 약 107억원을 기록한 이후 큰 폭으로 증가했습니다. 이로 인해 차입금의존도 또한 2020년말 3.28%에서 증가하여 2024년 1분기 27.3%을 기록했습니다. 지속적인 신사업 진출에 따른 자금조달, 영업환경의 악화, 매출채권 회수의 지연 등이 발생하여 대규모 현금 지출이 발생하거나 유동성 부채가 증가하게 될 경우 당사의 유동성은 악화될 수 있습니다.
| [차입금 및 유동성 지표] |
| (단위: 백만원, %) |
|
구 분 |
2024년 1분기 |
2023년 |
2022년 |
2021년 |
2020년 |
|---|---|---|---|---|---|
| 이자보상배율 | (0.5) | (1.1) | (2.0) | (3.8) | (14.7) |
|
총차입금 |
171,563 | 165,231 |
144,496 |
3,500 |
10,734 |
|
유동비율 |
158.66% |
108.55% |
600.26% |
1,158.55% |
1,015.00% |
|
부채비율 |
45.45% | 83.16% |
74.44% |
9.81% |
13.71% |
|
차입금의존도 |
27.25% |
39.02% |
35.08% |
1.29% |
3.28% |
| 출처: 당사 각 사업년도 분기보고서 및 사업보고서 |
당사는 유동성 위험 최소화를 위해 자금수지계획 수립을 통한 자금 유출입 관리, 이번 유상증자 추진 등 다양한 노력을 기울이고 있으나 이것이 유동성 위험을 근본적으로 제거할 수는 없습니다. 당사는 이와 같은 유동성 위험을 최소화하기 위해 매년 자금수지계획을 수립하고 현금유출예산과 실제 현금유출액을 지속적으로 관리하려는 노력을 기울이고 있습니다. 그러나 국내외 경제의 불확실성 증대, 당사가 영위하는 산업의 지속적인 영업환경 악화, 금융기관의 차입금 상환 압력 및 매출채권 회수지연 등 현재로서는 예측할 수 없는 다양한 요인에 의해 당사가 유동성 부족에 처할 가능성이 존재하오니, 투자자 여러분께서는 이 점을 유의하시기 바랍니다.
| 라. 신사업 진출을 위한 타법인 출자에 따른 위험 당사는 기업 전반의 손익 개선 및 신성장동력확보를 위해 2013년말부터 사업 다각화를 진행하여 왔고, 이 과정에서 주식양수도 등을 통하여 계열회사 지분을 지속적으로 취득하였습니다. 당사 종속기업의 손익은 당사 연결재무제표의 손익에 직접 영향을 미치며, '2024년 1분기 기준, 연결대상 종속회사인 (주)신화어드밴스, 에이치엘비셀(주), 에이치엘비에너지(주), 에이치엘비생명과학알엔디(주), 에이치엘비솔루션(주)는 관련 손익이 직접 연결제무제표에 계상되었습니다. 그 외 에이치엘비제약(주) 같은 관계기업의 손익도 그 지분율만큼 지분법손익에 따라 영업외손익으로 인식하여 당사의 연결재무제표에 영향을 미칩니다. 당사는 2022년 5월 31일 조용호 외 1인과 자산양수도 계약을 체결하고, 에임의 주식 100,000주(지분율 : 100.00%)를 양수하였으며, 2023년 7월 3일 HLB테라퓨틱스와 자산양수도 계약을 체결하고, 화진메디칼의 주식 863,500주(지분율 : 100.00%)를 양수하였습니다. 향후 당사의 종속 및 관계회사를 통한 시너지 효과 및 수익성 회복이 이루어지지 않고 당사가 투자한 종속기업 및 관계기업의 경영 악화로 인하여 해당회사들의 손실이 발생된다면, 당사의 손익에 부정적인 영향을 줄 수 있으며 당사의 재무건전성 역시 악화될 수 있습니다. 투자자 여러분께서는 이 점을 유의하시기 바랍니다. |
당사는 기업 전반의 손익 개선 및 신성장동력확보를 위해 2013년말부터 사업 다각화를 진행하여 왔고, 이 과정에서 주식양수도 등을 통하여 계열회사 지분을 지속적으로 취득하였습니다. 당사 타법인출자 현황은 다음과 같습니다.
| [타법인출자 현황] |
| (단위: 백만원, 주, %) |
| 법인명 | 상장여부 | 최초취득일자 | 출자목적 | 최초취득금액 | 2024년 1분기말 | ||
|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부가액 | |||||
| ㈜두산포천에너지 | 비상장 | 2008.11.03 | 단순투자 | 40 | 8,000 | 20.0 | 0 |
| ㈜엘에스케이인베스트먼트 | 비상장 | 2016.04.06 | 단순투자 | 1,500 | 90,000 | 9.0 | 450 |
| ㈜신화어드밴스 | 비상장 | 2016.08.03 | 경영참여 | 7,000 | 304,546 | 100.0 | 22,623 |
| 에이치엘비셀㈜ | 비상장 | 2018.03.21 | 경영참여 | 79,487 | 32,610,666 | 99.3 | 52,909 |
| 에이치엘비에너지㈜ | 비상장 | 2019.05.29 | 경영참여 | 1,880 | 1,475,000 | 100.0 | 27,638 |
| 에이치엘비제약㈜ | 상장 | 2020.09.11 | 경영참여 | 14,033 | 4,322,044 | 13.61 | 29,559 |
| 에이치엘비㈜ | 상장 | 2020.06.05 | 단순투자 | 4,395 | 1,933,601 | 1.5 | 203,415 |
| 에이치엘비생명과학알앤디㈜ | 비상장 | 2022.04.01 | 경영참여 | 1,000 | 20,000,000 | 100.0 | 5,991 |
| 에이치엘비아이 알밤 제1호 투자조합 | 비상장 | 2022.07.05 | 단순투자 | 1,000 | 1,000 | 18.0 | 1,800 |
| 에이치엘비이노베이션㈜ | 상장 | 2023.03.13 | 경영참여 | 2,000 | 2,074,688 | 2.2 | 12,946 |
| 에이치엘비사이언스㈜ | 상장 | 2023.09.30 | 경영참여 | 6,000 | 3,365,165 | 19.5 | 6,000 |
| 에이치엘비솔루션㈜ | 비상장 | 2024.01.01 | 경영참여 | 1,200 | 40,000 | 100 | 1,200 |
| 합 계 | 66,224,710 | - | 364,531 | ||||
| 출처: 당사 내부자료 |
1) (주)두산포천에너지
| 구분 | 내용 |
| 출자배경 | 폐기물 소각장 증설 공사를 위한 특수목적법인 설립 |
| 출자목적 | 단순투자 |
| 주요사업 | 소각설비 설치 사업 |
| 23년 이익 및 손실 발생 사유 | - |
| 추가 출자 계획 | 없음 |
2) (주)엘에스케이인베스트먼트
| 구분 | 내용 |
| 출자배경 | 투자조합의 조합원 참여를 통한 주주가치 제고 |
| 출자목적 | 단순투자 |
| 주요사업 | 투자조합 |
| 23년 이익 및 손실 발생 사유 | 영업성과 증가 |
| 추가 출자 계획 | 없음 |
3) (주)신화어드밴스
| 구분 | 내용 |
| 출자배경 | 의약품 유통업 사업 진출 |
| 출자목적 | 경영참여 |
| 주요사업 | 의약품 유통업 |
| 23년 이익 및 손실 발생 사유 | 시설비용 증가 및 매출 감소 |
| 추가 출자 계획 | 없음 |
4) 에이치엘비셀(주)
| 구분 | 내용 |
| 출자배경 | 바이오 사업 진출 |
| 출자목적 | 경영참여 |
| 주요사업 | 바이오의약품 개발 |
| 23년 이익 및 손실 발생 사유 | 보유주식 평가액 증가 |
| 추가 출자 계획 | 없음 |
5) 에이치엘비에너지(주)
| 구분 | 내용 |
| 출자배경 | 기존사업 매출 확대 및 수익성 개선 |
| 출자목적 | 경영참여 |
| 주요사업 | 산업 폐기물 처리 |
| 23년 이익 및 손실 발생 사유 | 소각로 투자비용 증가 |
| 추가 출자 계획 | 없음 |
6) 에이치엘비제약(주)
| 구분 | 내용 |
| 출자배경 | 당사와의 시너지 및 기업가치 극대화 |
| 출자목적 | 경영참여 |
| 주요사업 | 완제의약품과 원료의약품의 개발 및 제조 |
| 23년 이익 및 손실 발생 사유 | 건강기능식품 론칭에 따른 판관비 증가 |
| 추가 출자 계획 | 없음 |
7) 에이치엘비(주)
| 구분 | 내용 |
| 출자배경 | 삼각합병 절차 수행에 따른 소멸법인의 LSK BioPartners, Inc.보통주 325,010주처분대가 |
| 출자목적 | 단순투자 |
| 주요사업 | 합성수지선 건조업 |
| 23년 이익 및 손실 발생 사유 | 헬스케어사업부 매출감소 및 종속회사 손상에 따른 손실 증가 |
| 추가 출자 계획 | 없음 |
8) 에이치엘비생명과학알앤디(주)
| 구분 | 내용 |
| 출자배경 | R&D 전문성 강화 |
| 출자목적 | 경영참여 |
| 주요사업 | 신약개발사업 및 연구개발 용역업 |
| 23년 이익 및 손실 발생 사유 | 연구개발비 |
| 추가 출자 계획 | 24년도 추가 출자 70억원 진행 예정 |
9) 에이치엘비 알밤 제1호 투자조합
| 구분 | 내용 |
| 출자배경 | 사업 다각화 |
| 출자목적 | 의료용 대마 사업 진출을 위한 투자조합의 조합원 참여 |
| 주요사업 | 투자조합 |
| 23년 이익 및 손실 발생 사유 | 영업성과 증가 |
| 추가 출자 계획 | 없음 |
10) 에이치엘비이노베이션(주)
| 구분 | 내용 |
| 출자배경 | 당사와의 시너지 및 기업가치 극대화 |
| 출자목적 | 경영참여 |
| 주요사업 | 반도체 리드프레임, 유전자 치료제 연구 및 개발 |
| 23년 이익 및 손실 발생 사유 | 매출액 감소 및 BIO사업 신규 진출에 따른 R&D비용 증가 |
| 추가 출자 계획 | 없음 |
11) 에이치엘비사이언스(주)
| 구분 | 내용 |
| 출자배경 | 당사와의 시너지 및 기업가치 극대화 |
| 출자목적 | 지분 출자를 통한 기업가치 극대화 및 PIPE-LINE 확대 |
| 주요사업 | 의약품 연구개발 |
| 23년 이익 및 손실 발생 사유 | 연구개발비 |
| 추가 출자 계획 | 없음 |
12) 에이치엘비솔루션(주)
| 구분 | 내용 |
| 출자배경 | 당사와의 시너지 및 기업가치 극대화 |
| 출자목적 | 경영참여 |
| 주요사업 | 에너지 |
| 23년 이익 및 손실 발생 사유 | - |
| 추가 출자 계획 | 없음 |
당사 종속기업의 손익은 당사 연결재무제표의 손익에 직접 영향을 미치며, 연결대상 종속회사인 (주)신화어드밴스, 에이치엘비셀(주), 에이치엘비에너지(주), 에이치엘비생명과학알앤디(주), 에이치엘비솔루션(주)는 관련 손익이 직접 연결제무제표에 계상되었습니다. 그 외 에이치엘비제약(주) 같은 관계기업의 손익도 그 지분율만큼 지분법손익에 따라 영업외손익으로 인식하여 당사의 연결재무제표에 영향을 미칩니다.
| [관계회사 지분법평가 내역] |
| (단위: 천원) |
| 회사명 | 2023년말 | 취득 | 지분법손익 | 지분법자본변동 | 지분법 이익잉여금변동 |
처분 | 2024년 1분기 |
| ㈜두산포천에너지 | - | - | - | - | - | 2,042,915 | 2,042,915 |
| 에이치엘비제약㈜ | 27,990,911 | - | -229,408 | 1,841,270 | -5,817 | - | 29,596,956 |
| ㈜엘에스케이인베스트먼트 | 3,267,111 | - | 65,410 | -6,188 | - | - | 3,326,333 |
| 노마드 제2호 조합 | - | - | - | - | - | - | - |
| 에이치엘비사이언스㈜ | 5,951,252 | - | -614,042 | 433,096 | 2,762 | 25,479 | 5,798,547 |
| 에이치벨류에셋 | - | 600,000 | -41,998 | - | - | - | 558,002 |
| 합계 | 37,209,274 | 600,000 | -820,038 | 2,268,178 | -3,055 | 2,068,394 | 41,322,753 |
| 출처: 당사 제공 자료 |
한편 당사는 2022년 5월 31일 조용호 외 1인과 자산양수도 계약을 체결하고, 에임의 주식 100,000주(지분율 : 100.00%)를 양수하였으며, 자산양수도 가액은 97,900백만원입니다.
| [양수도주식수 및 양수도가액] |
| (단위 : 주, 천원) |
| 양도인 | 양수주식수 | 양수가액 | 양수대금 지급방법 | 비 고 |
| 조용호 | 64,000 | 62,656,000 | 당사는 본 거래대금 62,656,000천원을 양도인에 지급하여야 하나, 당사가 거래상대방에게 지급해야 할 HLB생명과학 제10회 무기명식 무보증 사모 전환사채의 사채납입대금 28,800,000천원을 상호 상계처리하기로 함에 따라 실제 현금 유출액은 33,856,000천원 입니다. | - |
| 문영주 | 36,000 | 35,244,000 | 당사는 본 거래대금 35,244,000천원을 양도인에 지급하여야 하나, 당사가 거래상대방에게 지급해야 할 HLB생명과학 제10회 무기명식 무보증 사모 전환사채의 사채납입대금 16,200,000천원을 상호 상계처리하기로 함에 따라 실제 현금 유출액은 19,044,000천원 입니다. | - |
| 합 계 | 100,000 | 97,900,000 | - | - |
| [에임 자산양수도 주요일정] |
| 구분 | 일자 |
| 외부평가계약체결일 | 2022년 5월 11일 |
| 평가기간 | 2022년 5월 11일 ~ 2022년 5월 31일 |
| 이사회결의일 | 2022년 5월 31일 |
| 자산양수도 계약일 | 2022년 5월 31일 |
| 자산양수도 거래종결일 | 2022년 7월 1일 |
당사는 본 자산양수도를 통하여 에임의 주식을 전량을 취득함으로써 재무구조 개선 및 안정적인 현금흐름 확보를 기대하고 있습니다. 총 양수가액은 97,900백만원이며, 거래대금 지급형태는 현금 52,900백만원 및 전환사채 45,000백만원 대용납입(상계)입니다. 기타 자산양수도에 대한 자세한 사항은 주요사항보고서(2022.05.31, 2022.06.29) 공시를 참조하시기 바랍니다.
이후 당사는 안정적인 수익창출을 통한 재무안정성 구축 및 향후 예정된 바이오 사업과의 시너지극대화를 위해 2022년 10월 1일 에임와 합병하였습니다.
| [합병 당사회사의 개요] |
|
합병 후 존속회사 |
회사명 |
HLB생명과학 |
|
본점소재지 |
경기도 화성시 동탄첨단산업1로 51-9 | |
|
대표이사 |
남상우, 한용해 |
|
|
상장 여부 |
코스닥 상장법인 |
|
합병 후 소멸회사 |
회사명 |
에임 |
|
본점소재지 |
경기도 수원시 영통구 신원로 88 | |
|
대표이사 |
조용호 | |
|
상장 여부 |
비상장법인 |
| [에임 합병 주요일정] |
|
구분 |
날짜 |
비고 |
|
|
합병 이사회 결의일 |
2022-07-18 |
- |
|
|
주요사항보고서 제출 |
2022-07-18 |
- |
|
|
주주확정기준일 공고 |
2022-08-04 |
- |
|
|
합병 계약 체결일 |
2022-07-21 |
- |
|
|
주주확정기준일 |
2022-08-04 |
- |
|
|
소규모합병 공고 |
2022-08-04 |
- |
|
|
주주명부 폐쇄기간 |
2022-08-05 ~ |
- |
|
|
합병반대의사 통지 접수기간 |
시작일 |
2022-08-04 |
- |
|
종료일 |
2022-08-18. |
||
|
합병승인 이사회 |
2022-08-24 |
주주총회 갈음 |
|
|
채권자 이의제출 공고 |
2022-08-26 |
- |
|
|
채권자 이의제출 기간 |
시작일 |
2022-08-26 |
- |
|
종료일 |
2022-09-26 | ||
|
합병기일 |
2022-10-01. |
- |
|
|
합병 종료보고 총회 |
2022-10-04 |
이사회 보고 |
|
|
합병 종료보고 공고 |
2022-10-04 |
- |
|
|
합병 등기 |
2022-10-07 |
- |
|
당사는 에임의 발행주식을 100% 소유하여 합병신주를 발행하지 않는 무증자 합병으로 진행되었으며, 합병 완료 후 당사의 주주변경은 없습니다. 본 합병은 상법 제527조의3에 근거하여 소규모 합병에 해당되며, 합병승인은 이사회승인으로서 갈음됩니다. 기타 합병에 대한 자세한 사항은 회사합병 결정(2022.07.18) 및 합병 등 종료보고서(2022.10.04) 공시를 참조하시기 바랍니다.
또한 당사는 2023년 7월 3일 HLB테라퓨틱스와 자산양수도 계약을 체결하고, 화진메디칼의 주식 863,500주(지분율 : 100.00%)를 양수하였으며, 자산양수도 가액은 8,300백만원입니다.
| [양수도주식수 및 양수도가액] |
| (단위 : 주, 천원) |
| 양도인 | 양수주식수 | 양수가액 | 양수대금 지급방법 | 비 고 |
| HLB테라퓨틱스 | 863,500 | 8,300,000 | 현금지급 |
| [화진메디칼 자산양수도 주요일정] |
| 구분 | 일자 |
| 외부평가계약체결일 | 2023년 5월 22일 |
| 평가기간 | 2023년 5월 22일 ~ 2023년 6월 21일 |
| 이사회결의일 | 2023년 6월 29일 |
| 자산양수도 계약일 | 2023년 6월 29일 |
| 자산양수도 거래종결일 | 2022년 7월 3일 |
당사는 본 자산양수도를 통하여 화진메디칼의 주식을 전량을 취득함으로써 재무구조 개선 및 안정적인 현금흐름 확보를 기대하고 있습니다. 총 양수가액은 8,300백만원이며, 거래대금 지급형태는 전액 8,300백만원 현금납입 입니다. 기타 자산양수도에 대한 자세한 사항은 주요사항보고서(2023.07.18, 2023.09.27) 공시를 참조하시기 바랍니다.
이후 당사는 안정적인 수익창출을 통한 재무안정성 구축 및 향후 예정된 바이오 사업과의 시너지극대화를 위해 2023년 10월 1일 화진메디칼과 합병하였습니다.
| [합병 당사회사의 개요] |
|
합병 후 존속회사 |
회사명 |
HLB생명과학 |
|
본점소재지 |
경기도 화성시 동탄첨단산업1로 51-9 | |
|
대표이사 |
남상우, 한용해 |
|
|
상장 여부 |
코스닥 상장법인 |
|
합병 후 소멸회사 |
회사명 |
화진메디칼 |
|
본점소재지 |
충청남도 천안시 동남구 성남면 성심원길 20 | |
|
대표이사 |
이우준 | |
|
상장 여부 |
비상장법인 |
| [화진메디칼 합병 주요일정] |
|
구분 |
날짜 |
비고 |
|
|
합병 이사회 결의일 |
2023-07-18 |
- |
|
|
주요사항보고서 제출 |
2023-07-18 |
- |
|
|
주주확정기준일 공고 |
2023-08-04 |
- |
|
|
합병 계약 체결일 |
2023-07-21 |
- |
|
|
주주확정기준일 |
2023-08-04 |
- |
|
|
소규모합병 공고 |
2023-08-04 |
- |
|
|
주주명부 폐쇄기간 |
2023-08-05 ~ |
- |
|
|
합병반대의사 통지 접수기간 |
시작일 |
2023-08-04 |
- |
|
종료일 |
2023-08-18. |
||
|
합병승인 이사회 |
2023-08-24 |
주주총회 갈음 |
|
|
채권자 이의제출 공고 |
2023-08-25 |
- |
|
|
채권자 이의제출 기간 |
시작일 |
2023-08-25 |
- |
|
종료일 |
2023-09-25 | ||
|
합병기일 |
2023-10-01. |
- |
|
|
합병 종료보고 총회 |
2023-10-04 |
이사회 보고 |
|
|
합병 종료보고 공고 |
2023-10-04 |
- |
|
|
합병 등기 |
2023-10-06 |
- |
|
당사는 화진메디칼 발행주식을 100% 소유하여 합병신주를 발행하지 않는 무증자 합병으로 진행되었으며, 합병 완료 후 당사의 주주변경은 없습니다. 본 합병은 상법 제527조의3에 근거하여 소규모 합병에 해당되며, 합병승인은 이사회승인으로서 갈음됩니다. 기타 합병에 대한 자세한 사항은 회사합병 결정(2023.07.18) 및 합병 등 종료보고서(2023.10.04) 공시를 참조하시기 바랍니다.
향후 당사의 종속 및 관계회사를 통한 시너지 효과 및 수익성 회복이 이루어지지 않고 당사가 투자한 종속기업 및 관계기업의 경영 악화로 인하여 해당회사들의 손실이 발생된다면, 당사의 손익에 부정적인 영향을 줄 수 있으며 당사의 재무건전성 역시 악화될 수 있습니다. 투자자 여러분께서는 이 점을 유의하시기 바랍니다.
| 마. 특수관계자와의 거래에 따른 위험 당사는 HLB바이오스텝(주)이 2022년 1월에 발행한 제1회 무기명식 무보증 전환사채 약 10,243백만원을 보유하고 있습니다. 또한 당사의 최대주주인 HLB(주)는 당사가 2022년 6월 발행한 제9회 무기명식 이권부 무보증 분리형 신주인수권부사채 19,603백만원을 보유하고 있습니다. 또한 당사의 특수관계자 바다중공업은 에이치엘비의 종속회사인 에이치엘비이앤지의 종속회사이며, 바다중공업 기타채권 중 당사의 종속회사 에이치엘비셀로부터 받은 대여금 및 이자 비용 800백만원을 상환하였습니다. 또한 HLB그룹에서 설립한 에이치벨류에셋에 부동산 투자를 위해 50억원을 출자하였습니다. 당사는 이사회 결의 등 적법절차를 준수하고 당사의 피해 또는 특수관계자에 대한 부당한 이익제공에 해당하지 않도록 특수관계자와의 거래를 진행하고 있습니다. 그러나 특수관계자와의 거래 발생 시 거래 조건 등이 제3자와의 거래와 비교하여 적정성이 유지되지 않을 경우 당사의 주주가 향유하여야 할 이익이 특수관계자 측에 전가될 위험이 있습니다. 또한 특수관계자에 대한 채권 규모가 증가할수록 현금흐름 및 재무구조에는 부정적으로 작용할 가능성이 있습니다. 투자자분들께서는 이 점 유의하여 주시기 바랍니다. |
당사의 특수관계자 현황은 다음과 같습니다.
| 구분 | 회사명 |
|---|---|
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ |
| 관계기업 | 에이치엘비제약㈜ |
| ㈜엘에스케이인베스트먼트 | |
| 에이치벨류에셋(주1) | |
| ㈜두산포천에너지 | |
| 에이치엘비사이언스㈜ | |
| 기타특수관계자 | 에이치엘비글로벌㈜ |
| 에이치엘비일렉㈜ | |
| 에이치엘비아이 알밤 제1호 투자조합 | |
| 에이치엘비네트웍스㈜ | |
| Elevar Therapeutics, Inc. | |
| Immunomic Therapeutics, Inc. | |
| 에이치엘비바이오스텝㈜ | |
| ㈜펭귄오션레저 | |
| 에이치엘비생활건강㈜ | |
| ㈜프레시코 | |
| ㈜코아바이오 | |
| 에포케㈜ | |
| 에이치엘비테라퓨틱스㈜ | |
| 바다중공업㈜ | |
| 현대요트㈜ | |
| ㈜노터스 | |
| 에이치엘비에프앤비㈜ | |
| 에이치엘비파나진㈜ | |
| 브이에스팜㈜ | |
| 에이치엘비이노베이션㈜ | |
| 임직원 |
| (주1) 당분기 중 신규로 편입되었습니다. |
당사는 당사의 최대주주인 에이치엘비(주)와 임대차 계약을 맺은 상태입니다. 이로 인한 관리비 발생으로 인해 매입거래 약 31백만원이 발생하였습니다. 당사는 바다중공업(주)에 대해 2020년 발생한 1,380백만의 대여금을 보유하고 있으며, 이후 추가적인 차입은 발생하지 않았습니다. 또한, 당사는 기타 특수관계회사 HLB바이오스텝(주)이 2022년 1월 발행한 제1회 무기명식 무보증 전환사채 약 10,815백만원을 보유하고 있습니다. 이와 같이 최근 4년 동안 당사는 자금 대여처가 원리금을 미상환함에도 불구하고 추가 자금대여를 한 경우는 없었으나, 향후 특수관계자의 경영 환경이 악화되거나 지배구조 등의 변동에 따라 특수관계가 해소될 경우 대여금 회수가 지연될 가능성을 배재할 수 없습니다.
| [특수관계자와의 주요 거래내역] |
| (단위: 천원) |
| 구분 | 회사명 | 매출 등 | 매입 등 | |||
|---|---|---|---|---|---|---|
| 매출 | 이자수익 | 기타 | 임차료 | 기타 | ||
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ | 128,971 | - | - | 31,460 | 30,508 |
| 관계기업 | 에이치엘비제약㈜ | 8,924 | - | - | - | - |
| 에이치엘비사이언스㈜ | 6,913 | - | - | - | - | |
| 소계 | 15,837 | - | - | - | - | |
| 기타의 특수관계자 | Elevar Therapeutics, Inc. | - | - | - | - | 54,604 |
| ㈜프레시코 | - | - | - | - | 1,084 | |
| 에이치엘비글로벌㈜ | 3,000 | - | - | - | - | |
| ㈜펭귄오션레져 | - | - | - | - | 6,470 | |
| 에이치엘비바이오스텝㈜ | 420 | - | - | - | 54,543 | |
| 에이치엘비에프앤비㈜ | - | - | - | - | 15,312 | |
| 에포케㈜ | - | - | - | - | 12,740 | |
| 바다중공업 | - | 3,125 | - | - | - | |
| 브이에스팜㈜ | 40,128 | - | - | - | - | |
| 임직원 | - | - | 376 | - | - | |
| 소계 | 43,548 | 3,125 | 376 | - | 144,753 | |
| 합계 | 188,356 | 3,125 | 376 | 31,460 | 175,261 | |
| 출처 : 당사 분기보고서 |
특수관계자와의 채권의 경우, 당사는 HLB바이오스텝(주)이 2022년 1월에 발행한 제1회 무기명식 무보증 전환사채 약 10,243백만원을 보유하고 있습니다. 또한 당사의 최대주주인 HLB(주)는 당사가 2022년 6월 발행한 제9회 무기명식 이권부 무보증 분리형 신주인수권부사채 19,603백만원을 보유하고 있으며, 동 신주인수권부사의 사채권자는 발행일(2022년 6월 15일)부터 24개월이 경과하는 날(2024년 6월 15일)부터 신주인수권부사채의 만기일까지 신주인수권부사채의 조기상환을 청구할 수 있는 권리를 보유하고 있습니다. 이와 같이 최근 4년 동안 당사는 자금 대여처가 원리금을 미상환함에도 불구하고 추가 자금대여를 한 경우는 없었으나, 향후 특수관계자의 경영 환경이 악화되거나 지배구조 등의 변동에 따라 특수관계가 해소될 경우 대여금 회수가 지연될 가능성을 배재할 수 없습니다.
| [특수관계자와의 채권 및 채무 잔액] |
| (단위: 천원) |
| 구분 | 회사명 | 채권 등 | 채무 등 | |||
|---|---|---|---|---|---|---|
| 매출채권 | 기타채권 | 전환사채 (주1) |
기타채무 | 신주인수권부사채 (주2) |
||
| 유의적인 영향력을행사하는 기업 | 에이치엘비㈜ | - | 5,742 | - | 4,787 | 19,603,370 |
| 관계기업 | 에이치엘비제약㈜ | - | 3,707 | - | 40,000 | - |
| ㈜두산포천에너지(주4) |
- | 505,804 | - | - | - | |
| 에이치엘비사이언스㈜ | - | 658 | - | 25,000 | - | |
| 소계 | - | 510,169 | - | 65,000 | - | |
| 기타의 특수관계자 | 에이치엘비테라퓨틱스㈜(주5) |
- | - | - | 8,300,000 | - |
| Elevar Therapeutics, Inc. | - | - | - | 87,640 | - | |
| ㈜프레시코 | - | - | - | 712 | - | |
| 에이치엘비글로벌㈜ | - | 1,100 | - | - | - | |
| 에이치엘비바이오스텝㈜ | 139 | - | 10,242,854 | - | - | |
| ㈜펭귄오션레저 | - | 6,750 | - | - | - | |
| 브이에스팜㈜ | 20,659 | - | - | - | - | |
| 임직원 | - | 36,000 | - | - | - | |
| 소계 | 20,798 | 43,850 | 10,242,854 | 8,388,352 | - | |
| 합계 | 20,798 | 559,761 | 10,242,854 | 8,458,139 | 19,603,370 | |
| (주1) 공정가치평가 후 금액입니다. (주2) 신주인수권부사채 채무 잔액은 액면금액입니다. (주3) 특수관계자와의 채권 및 채무 잔액 대부분은 에이치엘비 그룹에서 발생한 그룹 공동비용에 기인하며, 별도 내용 설명이 필요한 경우 아래 주석에 기재하였습니다. (주4) 회사는 해당 대여금에 대하여 전액 대손충당금을 설정하였습니다. (주5) 특수관계자 HLB테라퓨틱스 기타채무는 당사가 2023년 7월에 발행한 11회차 전환사채입니다. |
| 출처 : 당사 분기보고서 |
또한 당사는 종속회사 HLB에너지가 현재 진행중인 부산 구평동 소각시설 증설사업 프로젝트 금융 자금 대출 420억원에 대해 2024년 05월 23일 채무보증 및 담보제공을 결정하였으며, 이는 타인에 대한 담보제공 결정 공시(2024.05.23)로 공시되었습니다. HLB에너지는 담보대출 중 환경부 환경정책자금 명목으로 하나은행으로부터의 200억원 및 하나은행 150억원, 하나캐피탈 70억원의 일반대출까지 총 420억원의 대출을 진행하였으며, 자세한 내용은 아래와 같습니다.
| [HLB에너지 소각로 증설 대출금액] |
|
구분
|
내용 | 차입처 | 금액(억원) | 금리(%) |
만기
|
비고 |
|---|---|---|---|---|---|---|
| 담보대출 | 환경정책자금 | 하나은행 |
200
|
2.44(변동) | 2033년 09월 30일 | 환경부 분기별 금리 고시 |
| 일반 | 하나은행 |
150
|
7.10(변동) | 최초 인출일 ~ 36개월 경과 |
- | |
| 하나캐피탈 | 70 | 7.10(고정) | - | |||
|
합계
|
- | - | 420 | - | - | - |
| 출처: 당사 제공 자료 |
대출에 대한 당사가 보유한 HLB에너지 보통주식 전부가 근질권 설정을 통해 담보제공되며, 본건 사업 관련 당사의 책임준공확약, 대출약정상 피담보채무에 대한 당사의 연대보증, 출자약정을 통한 자금보충약정을 제공합니다.
| [HLB에너지 대출 담보내역] |
| 구분 | 내용 | 담보설정액(억원) | 장부가액(억원) |
|---|---|---|---|
| HLB생명과학 보유 지분 |
HLB에너지 보통주식 2,302,099주 |
대출약정금액 420억원의 120% |
302억원 |
| 출처: 당사 제공 자료 |
한편 당사의 특수관계자 바다중공업은 에이치엘비의 종속회사인 에이치엘비이앤지의 종속회사이며, 바다중공업 기타채권 중 당사의 종속회사 에이치엘비셀로부터 받은 대여금 및 이자 비용 800백만원을 상환하였습니다. 또한 HLB그룹에서 설립한 에이치벨류에셋에 부동산 투자를 위해 50억원을 출자하였습니다.
| [특수관계자와의 자금 거래 내역] |
| (단위: 천원) |
| 구 분 | 회사명 | 자금 대여(차입) 거래 | 금융수익(원가) | 현금 출자 등 | |
|---|---|---|---|---|---|
| 대여(차입) | 회수(상환) | 이자수익 | |||
| 관계기업 | 에이치벨류에셋 | - | - | - | 5,000,000 |
| 소계 | - | - | - | 5,000,000 | |
| 기타의 특수관계자 | 에이치엘비아이알밤제1호투자조합 | - | - | - | 800,000 |
| 바다중공업㈜ | - | (800,000) | 3,125 | - | |
| 임직원 | - | (1,500) | - | - | |
| 소계 | - | (801,500) | 3,125 | 800,000 | |
| 합계 | - | (801,500) | 3,125 | 5,800,000 | |
| 출처 : 당사 분기보고서 |
당사는 이사회 결의 등 적법절차를 준수하고 당사의 피해 또는 특수관계자에 대한 부당한 이익제공에 해당하지 않도록 특수관계자와의 거래를 진행하고 있습니다. 그러나 특수관계자와의 거래 발생 시 거래 조건 등이 제3자와의 거래와 비교하여 적정성이 유지되지 않을 경우 당사의 주주가 향유하여야 할 이익이 특수관계자 측에 전가될 위험이 있습니다. 또한 특수관계자에 대한 채권 규모가 증가할수록 현금흐름 및 재무구조에는 부정적으로 작용할 가능성이 있으니, 투자자분들께서는 투자 판단 시 이 점 유의하여 주시기 바랍니다.
| 바. 우발채무 및 소송관련 위험 2024년 1분기 기준 당사는 종속회사인 에이치엘비에너지(주)의 소각로 증축과 관련하여 기업은행으로부터 차입한 차입금에 대한 60억원 후순위 담보제공과 48억원 지급보증을 제공하였습니다. 당사는 견질 제공한 어음 및 수표의 내역은 없으며, 연결회사 및 그 종속회사의 차입금 등과 관련하여 금융기관에 유형자산, 금융자산 및 투자부동산을 담보로 제공하고 있으며, 총 장부금액은 약 298,022백만원입니다. 2024년 1분기 기준 당사는 현재 총 4건의 소송을 진행 중에 있습니다. 당사가 피고로 계류중인 소송은 2건으로 소송금액 총 2,343백만원이며 원고로 계류중인 소송은 2건으로 소송금액은 10,055백만원입니다. 증권신고서 제출일 현재 계류 중인 소송 사건에 대해서는 소송의 결과를 합리적으로 예측할 수 없으며, 당사가 피고로 진행 중인 사건과 관련해서 최종적으로 패소 시 청구액에 상당하는 금액의 손실이 발생할 수 있습니다. 당사는 담보 및 보증제공으로 인한 우발부채와 소송으로 인한 우발부채가 존재합니다. 당사가 제공한 담보 및 보증과 관련하여 우발부채가 현실화되거나 당사가 소송에서 패소함에 따라 추가적인 대손충당 등이 발생할 경우 당사 재무에 부정적인 영향을 줄 수 있습니다. 투자 판단 시 당사의 담보 및 보증 제공과 관련한 우발부채 현황 및 소송의 현황을 확인하고 이로 인한 우발부채의 현실화 가능성에 주의하시기 바랍니다. |
2024년 1분기 기준 당사는 종속회사인 에이치엘비에너지(주)의 소각로 증축과 관련하여 기업은행으로부터 차입한 차입금에 대한 60억원 후순위 담보제공과 48억원 지급보증을 제공하였습니다.
| [채무보증 현황] |
| (단위: 천원) |
| 구분 | 회사명 | 보증처 | 이사회 결의일 | 판단근거 | 내용 | 지급보증금액 | 보증기간 | |
| 기초 (2024.01.01) |
기준일 (2024.03.31) |
|||||||
| 종속기업 | 에이치엘비에너지 | 기업은행 | 2023-12-15 | 이사회 결의 | 부동산 담보제공 | - | 6,000,000 | 2023.12.15 ~ 채무 상환시 |
| 신용 연대보증 | 4,800,000 | |||||||
| 합 계 | - | 10,800,000 | ||||||
| 출처: 당사 분기보고서 |
(삭제)
당사는 견질 제공한 어음 및 수표의 내역은 없습니다. 연결회사 및 그 종속회사의 차입금 등과 관련하여 금융기관에 유형자산, 금융자산 및 투자부동산을 담보로 제공하고 있으며, 총 장부금액은 약 298,022백만원으로 자세한 내역은 아래와 같습니다.
| [담보제공자산 내역] |
| (단위: 천원) |
| 구분 | 장부가액 | 담보설정액 | 관련계정 | 관련금액 | 제공처 |
|---|---|---|---|---|---|
| 토지 및 건물 | 4,768,018 | 4,200,000 | 차입금 | 3,000,000 | 하나은행 |
| 토지 및 건물 | 15,560,511 | 10,884,000 | 차입금 | 9,070,000 | 국민은행 |
| 토지 및 건물 | 24,285,155 | 9,744,000 | 차입금 | 8,120,000 | 국민은행 |
| 토지 및 건물 | 955,260 | 3,222,000 | 차입금 | 1,150,000 | 우리은행 |
| 토지 및 건물 | 11,609,857 | 5,760,000 | 차입금 | 4,800,000 | 우리은행 |
| 토지 및 건물 | 14,360,238 | 12,000,000 | 차입금 | 10,000,000 | 산업은행 |
| 정기예금 | 6,040,000 | 6,303,158 | 기타금융자산 | 6,040,000 | 우리은행 |
| 정기예금 | 3,900,000 | 4,290,000 | 기타금융자산 | 3,900,000 | 기업은행 |
| 정기예금 | 120,000 | 120,000 | 기타금융자산 | 120,000 | 서울보증보험 |
| 토지 | 8,324,397 | 22,8000,000 | 장기차입금 | 3,800,000 | 한국투자증권 |
| 건물 | 589,226 | 장기차입금 | 기업은행 | ||
| 구축물 | 432,795 | 장기차입금 | 기업은행 | ||
| 기계장치 | 3,662,359 | 장기차입금 | 기업은행 | ||
| 주식 | 203,414,825 | 20,000,000 | 차입금 | 20,000,000 | 기업은행 |
| 합 계 | 298,022,641 | 99,323,158 | - | 70,000,000 | - |
| (주1) 에포케㈜ (특수관계자)가 한국투자증권으로부터 차입한 차입금에 대한 연대보증인으로서, 연결회사가 보유하고 있는 MMF 금융자산 (장부금액: 15억원)에 대한 질권이 설정되어있습니다. (채권최고액: 10억원). |
| 출처: 당사 분기보고서 |
2024년 1분기 기준 당사는 현재 총 4건의 소송을 진행 중에 있습니다. 당사가 피고로 계류중인 소송은 2건으로 소송금액 총 2,343백만원입니다. 당사는 당사는 현대로오텍 및 주원전력으로부터 공사대금 청구에 따라 각각 소송금액 약 15억, 9억원의 소송절차가 진행중에 있습니다.
| [연결회사가 피고인 소송사건] |
| (단위: 천원) |
| 원고 | 계류 법원 | 소송 금액 | 소송 내용 | 진행 상황 |
|---|---|---|---|---|
| 현대로오텍 | 광주지방법원 | 1,458,874 | 공사대금 청구 | 소송절차로 이행 |
| 주원전력 | 전주지방법원 | 883,872 | 공사대금 청구 | 소송절차로 이행 |
| 합계 | 2,342,746 | - | - | |
| 출처: 당사 분기보고서 |
한편 당사가 원고로 계류중인 소송은 2건으로 소송금액은 10,055백만원입니다. 당사는 2019년 4월 엔에이치투자증권(주)를 통해 판매되었던 옵티머스자산운용 펀드에 100억원을 위탁하였으나, 사기적 부정거래행위 및 불완전판매 요소가 발견되어 부당이득금 반환 청구소송을 진행 중입니다. 이에 당시 대표이사는 최종 의사결정권자로서 엔에이치투자증권 투자 관련 회사측 손실이 발생할 경우 손실액 전액을 본인이 보유한 HLB(주) 주식으로 충당하기 위해서 법무법인에 HLB(주) 주식을 위탁하는 계약을 체결하였습니다. 또한, 당사는 2023년 5월 11일자로 반정동 공장 임차인 박승규와의 임대차 계약 종료 이후 발생한 명도소송을 진행 중입니다. 당사는 계약 종료에 대한 내용증명 발송 및 매각 등 사유로 이전을 요청하였습니다. 그러나, 피고 박승규는 이를 거부하며 현재 9개월치 임대료 (4,500만원) 및 5개월치 전기세 연체중(600만원)으로 확인되어 당사가 연체금액 납부를 요구하고 있으나 피고인은 연기하고 있습니다. 또한 기존 당사 원고, 피고 엘케이쏠라테크 공사대금 청구관련 소송 진행 중 이였으나, 2024년 1월 1일 당사 에너지사업부 회사분할하여 종속회사인 HLB솔루션으로 관련 소송 승계되어 소송 진행중입니다. 해당 사건은 현재 공사대금 채권 가압류 이의 신청 심문종결 후 소송비용액확정 사건으로 2024년 3월 18일에 일부인용 결정 되었습니다.
| [연결회사가 원고인 소송사건] |
| (단위: 천원) |
| 피고 | 계류 법원 | 소송 금액 | 소송 내용 | 진행 상황 |
|---|---|---|---|---|
| 엔에이치투자증권 | 서울남부지방법원 | 10,000,000 | 부당이득금반환청구 | 1심 진행중 |
| 박승규(탑스코리아) | 수원지방법원 | 55,000 | 명도소송 | 판결선고 |
| 합계 | 10,055,000 | - | - | |
| 출처: 당사 분기보고서 |
증권신고서 제출일 현재 계류 중인 소송 사건에 대해서는 소송의 결과를 합리적으로 예측할 수 없으며, 당사가 피고로 진행 중인 사건과 관련해서 최종적으로 패소 시 청구액에 상당하는 금액의 손실이 발생할 수 있습니다.
또한 당사는 ESCO(Energy Service Company, 에너지절약전문기업)사업을 통해 경험한 소각플랜트 수행실적을 바탕으로 부산 소재의 산업용 폐기물 중간처분업체를 인수하여 정상화 작업을 위한 EPC(Engineering(설계), Procurement(조달), Construction(건설))사업을 진행하고 있습니다. 현재 부산권역에 산업용 폐기물 중간 처분 업체는 당사의 종속회사인 HLB에너지를 포함하여 2곳 밖에 존재하지 않은 상태입니다. 그러나 부산 산업단지 10여개 연차별 준공으로 인한 사업장 폐기물 증가가 예상되며, 매년 매립량은 감소하고 소각량은 증가하고 있는 추세입니다. 이에 당사의 종속회사인 HLB에너지는 기존 부산 사하구에 보유하고 있는 소각로 증설을 통해 일 48톤의 소각 용량을 90톤까지 증가시킴으로써 산업폐기물을 처리할 수 있는 가동률을 높여 매출 확대 및 수익성 개선을 계획하였습니다.
| [소각로 증설 계획] |
| 일정 | 내용 |
|---|---|
| 2023년 4월 12일 | 건축허가 완료 |
| 2023년 6월 | 실시설계 완료 |
| 2023년 7월 | 시공사 선정, 계약 |
| 2023년 12월 | 공사착공 |
| 2024년 12월 | 준공 및 시운전 |
| 출처: 당사 제공 자료 |
당사는 종속회사 HLB에너지가 현재 진행중인 부산 구평동 소각시설 증설사업 프로젝트 금융 자금 대출 420억원에 대해 2024년 05월 23일 채무보증 및 담보제공을 결정하였으며, 이는 타인에 대한 담보제공 결정 공시(2024.05.23)로 공시되었습니다. HLB에너지는 담보대출 중 환경부 환경정책자금 명목으로 하나은행으로부터의 200억원 및 하나은행 150억원, 하나캐피탈 70억원의 일반대출까지 총 420억원의 대출을 진행하였으며, 자세한 내용은 아래와 같습니다.
| [HLB에너지 소각로 증설 대출금액] |
|
구분
|
내용 | 차입처 | 금액(억원) | 금리(%) |
만기
|
비고 |
|---|---|---|---|---|---|---|
| 담보대출 | 환경정책자금 | 하나은행 |
200
|
2.44(변동) | 2033년09월30일 | 환경부 분기별 금리 고시 |
| 일반 | 하나은행 |
150
|
7.10(변동) | 최초 인출일 ~ 36개월 경과 |
- | |
| 하나캐피탈 | 70 | 7.10(고정) | - | |||
|
합계
|
- | - | 420 | - | - | - |
| 출처: 당사 제공 자료 |
대출에 대한 당사가 보유한 HLB에너지 보통주식 전부가 근질권 설정을 통해 담보제공되며, 본건 사업 관련 당사의 책임준공확약, 대출약정상 피담보채무에 대한 당사의 연대보증, 출자약정을 통한 자금보충약정을 제공합니다.
| [HLB에너지 대출 담보내역] |
| 구분 | 내용 | 담보설정액(억원) | 장부가액(억원) |
|---|---|---|---|
| HLB생명과학 보유 지분 |
HLB에너지 보통주식 2,302,099주 |
대출약정금액 420억원의 120% |
302억원 |
| 출처: 당사 제공 자료 |
당사는 담보 및 보증제공으로 인한 우발부채와 소송가능성 등으로 인한 우발부채가 상기와 같이 존재합니다. 당사가 제공한 담보 및 보증과 관련하여 우발부채가 현실화되거나 제기될 수 있는 소송에서 당사가 패소함에 따라 추가적인 대손충당 등이 발생할 경우 당사 재무에 부정적인 영향을 줄 수 있습니다. 투자 판단 시 당사의 담보 및 보증 제공과 관련한 우발부채 현황 및 소송의 현황을 확인하고 이로 인한 우발부채의 현실화 가능성에 주의하시기 바랍니다.
| 사. 경영권 안정성에 대한 위험 당사의 현재 최대주주인 에이치엘비(주)는 2015년 10월 23일 7,462,687주(25,000,001,450원)의 제3자배정 유상증자 중에서 2,089,553주(9.49%)를 취득하여 최대주주가 되었습니다. 최대주주 지분율은 전환권 행사 등을 통해 증가하였고, 신주배정기준일 기준 총 발행주식수는 107,650,759주이며, 최대주주인 에이치엘비(주)는 발행주식총수의 18.29%인 19,688,685주를 보유하고 있습니다. 금번 유상증자를 통해 발행 예정인 주식은 11,005,125주이며, 당사 최대주주인 에이치엘비(주)는 2,014,080주를 배정 받을 예정입니다. 당사 최대주주인 에이치엘비(주)는 50% 청약에 참여할 예정이며, 배정주식의 50% 수준의 청약률을 가정할 경우 예상 청약 주식수는 1,007,040주입니다. 최대주주는 금번 유상증자 청약자금을 자체보유 현금으로 집행할 예정입니다. 다만, 증자 진행 과정에서 주가 상승으로 인해 예정발행가액 대비 확정발행가액이 변동될 경우 최대주주의 청약자금 부담 증가로 인하여 청약 주식수와 금액에 일부 변동이 발생할 수 있습니다. 또한 현재 미상환 신주인수권부사채 및 전환사채가 보통주로 전환될 경우 기존주주들의 지분희석이 발생하게 되며, 최대주주 에이치엘비(주)의 지분율 또한 희석될 수 있습니다. 9BW의 발행 당시 인수계약서 상 '행사가격의 조정' 관련 조항과 11CB 및 12CB의 발행 당시 인수계약서 상 '전환가액의 조정' 관련 조항에 따라, 금번 유상증자 이후 행사가격 및 전환가액이 조정될 예정입니다. 이에 따라 금번 주주배정후 실권주 일반공모 유상증자에 따라 전환 및 행사가액이 조정된 이후 최대주주가 배정물량의 50%를 청약을 하고 전환 및 행사가능 주식수 전량이 전환 청구될 경우 당사 최대주주 지분율은 18.16%로 본 공시서류 제출일 전일 지분율 대비 0.13%p. 감소할 예정입니다. 유상증자 이후 지분율 하락에도 에이치엘비(주)는 당사 최대주주로서의 지위를 유지할 예정이나, 이와 같은 지분율 감소는 최대주주의 경영권 등에 부정적인 영향을 미칠 수 있습니다. 또한 예기치 못한 상황으로 인한 청약실패 가능성이 상존하고 있으며, 청약참여율이 당초 계획대비 낮아질 경우 상기와 같은 경영권 위험이 대두될 가능성이 있으니 투자자께서는 투자 판단시 이점 유의하시기 바랍니다. |
당사의 현재 최대주주인 에이치엘비(주)는 2015년 10월 23일 7,462,687주(25,000,001,450원)의 제3자배정 유상증자 중에서 2,089,553주(9.49%)를 취득하여 최대주주가 되었습니다. 최대주주 지분율은 전환권 행사 등을 통해 증가하였고, 신주배정기준일(2024년 5월 10일) 기준 총 발행주식수는 107,650,759주이며, 최대주주인 에이치엘비(주)는 발행주식총수의 18.29%인 19,688,685주를 보유하고 있습니다. 금번 유상증자를 통해 발행 예정인 주식은 11,005,125주이며, 당사 최대주주인 에이치엘비(주)는 2,014,080주를 배정 받을 예정입니다. 에이치엘비(주)는 배정주식의 50%를 청약할 예정이며, 청약에 필요한 예상자금은 자체 보유 현금을 통해 집행할 예정입니다. 이에 따라 금번 유상증자 이후 당사 최대주주의 예상 지분율은 17.44%로 신주배정기준일 기준 지분율 대비 0.85%p. 감소할 것으로 예상됩니다.
| [최대주주 및 특수관계인 주식소유 현황] | |||
| (기준일 : | 2024년 05월 10일 | ) | (단위 : 주, %) |
| 성 명 | 관 계 | 주식의 종류 |
소유주식수 및 지분율 | 비고 | |||
|---|---|---|---|---|---|---|---|
| 2023년말 | 2024년 05월 10일 | ||||||
| 주식수 | 지분율 | 주식수 | 지분율 | ||||
| HLB | 본인 | 보통주 | 19,688,685 | 19.33 | 19,688,685 | 18.29 | - |
| 계 | 보통주 | 19,688,685 | 19.33 | 19,688,685 | 18.29 | - | |
| - | - | - | - | - | - | ||
| 출처: 당사 제공 자료 |
전술한 바와 같이 당사 최대주주인 에이치엘비(주)는 50% 청약에 참여할 예정이며, 배정주식의 50% 수준의 청약률을 가정할 경우 예상 청약 주식수는 1,007,040주입니다. 또한 이에 따른 예상 필요 청약 자금은 약 119.7억원입니다. 최대주주는 금번 유상증자 청약자금을 자체보유 현금으로 집행할 예정입니다. 다만, 증자 진행 과정에서 주가 상승으로 인해 예정발행가액 대비 확정발행가액이 변동될 경우 최대주주의 청약자금 부담 증가로 인하여 청약 주식수와 금액에 일부 변동이 발생할 수 있습니다.
금번 유상증자 후 상기 청약 참여율을 적용했을 때, 당사의 최대주주 지분율은 17.44%로 예상되며 이는 신주배정기준일 기준 지분율 대비 0.85%p 하락한 수치입니다. 유상증자 이후 지분율 하락에도 에이치엘비(주)는 당사 최대주주로서의 지위를 유지할 예정이나, 이와 같은 지분율 감소는 최대주주의 경영권 등에 부정적인 영향을 미칠 수 있습니다. 또한 전술 한바와 같이 예기치 못한 상황으로 인한 청약실패 가능성이 상존하고 있으며, 청약참여율이 당초 계획대비 낮아질 경우 상기와 같은 경영권 위험이 대두될 가능성이 있으니 투자자께서는 투자 판단시 이점 유의하시기 바랍니다.
| [최대주주 지분율 변동 시뮬레이션 : 유상증자] | |
| (기준일 : 2024년 05월 10일) | (단위: 주, %) |
| 성 명 | 주식의 종류 |
유상증자 전 | 배정 주식수 (예정) |
청약 참여 주식수(예정) |
유상증자 후(예정) | ||
| 주식수 | 지분율 | 주식수 | 지분율 | ||||
| 에이치엘비(주) | 의결권 있는 주식 | 19,688,685 | 18.29 | 2,014,080 | 1,007,040 | 20,695,725 | 17.44 |
| 주1) 최대주주 청약 참여 주식수는 배정주식수의 50%입니다.(1주 미만 단수주 절사) |
한편 당사는 2022년 6월 '제9회 무기명식 이권부 무보증 공모 분리형 신주인수권부사채(이하 '9BW')'를 발행한 이력이 있으며, 해당 9BW는 신주배정일기준일 기준 약 804억원이 미상환 신주인수권부사채로 남아있습니다. 신주인수권부사채는 신주인수권 보유자의 신주인수권 행사청구에 따라 당사의 보통주가 추가로 발행되는 옵션(신주인수권)이 부여된 주식연계채권이며, 신주배정일기준일 기준 9BW 미상환 잔액에 대한 신주인수권 행사청구가 가능한 주식는 3,773,143주(행사가액:8,889원), 유상증자 반영 후 행사가능 주식 수 3,868,450주(행사가액:8,670원)입니다.
또한, 당사는 에임(주)의 주식양수도에 따른 양수도 대금 지급을 위해 에임(주)의 주주인 조용호, 문영주를 대상으로 450억원 규모의 '제10회 무기명식 이권부 무보증 사모 전환사채(이하 '10CB')'를 발행한 이력과, 의료기기 사업 확대를 위한 연구 개발비 및 홍보비, 관리비를 위해 83억원 규모의 '제11회 무기명식 이권부 무보증 사모 전환사채(이하 '11CB')를 발행한 이력이 있으며, 채무상환자금으로 288억원 규모의 '제12회 무기명식 무보증 사모 전환사채(이하 '12CB')를 발행했었습니다. 제10회차 전환사채는 2024년 3월 29일 미상환사채 잔액 모두 전환청구 되었습니다. 11CB 및 12CB는 신주배정일기준일 기준 371억원이 미상환 전환사채로 남아있습니다. 전환사채는 투자자의 전환청구에 따라 당사 보통주가 추가로 발행되는 옵션(전환권)이 부여된 주식연계채권이며, 신주배정일기준일 기준 11CB 및 12CB 미상환 잔액에 대한 전환청구로 인한 전환가능 주식은 총 3,817,788주(전환가액: 11CB 10,204원, 12CB 9,586), 유상증자 반영 후 전환가능 주식 수는 3,914,383주(전환가액: 11CB 9,950원, 12CB 9,350원)입니다.
다음은 당사 미상환 신주인수권부사채 및 전환사채 중 당사 보통주가 추가 발행될 수 있는 옵션이 부여된 주식연계채권에 대한 상세 내역입니다.
| [미상환 신주인수권부사채 발행현황] | |||
| (기준일 : | 2024년 05월 10일 | ) | (단위 : 원, 주) |
| 종류\구분 | 회차 | 발행일 | 만기일 | 권면(전자등록)총액 | 행사대상 주식의 종류 |
신주인수권 행사가능기간 | 행사조건 | 미상환사채 | 미행사 신주인수권 |
비고 | |
| 행사비율(%) | 행사가액 | 권면(전자등록)총액 | 행사가능주식수 | ||||||||
| 무기명식 이권부 무보증 공모 분리형 신주인수권부사채 |
9 | 2022.06.15 | 2025.06.15 | 100,000,000,000 | 기명식 보통주 |
2022.07.15~2025.05.15 | 100 | 8,889 | 80,373,782,388 | 3,773,143 | - |
| 합 계 | - | - | - | 100,000,000,000 | - | - | - | - | 80,373,782,388 | 3,773,143 | - |
| 출처: 당사 제공자료 |
| [미상환 전환사채 발행현황] | |||
| (기준일 : | 2024년 05월 10일 | ) | (단위 : 원, 주) |
| 종류\구분 | 회차 | 발행일 | 만기일 | 권면(전자등록)총액 | 전환대상 주식의 종류 |
전환청구가능기간 | 전환조건 | 미상환사채 | 비고 | ||
| 전환비율 (%) |
전환가액 | 권면(전자등록)총액 | 전환가능주식수 | ||||||||
| 무기명식 이권부 무보증 사모 전환사채 |
10 | 2022.07.01 | 2027.07.01 | 45,000,000,000 | 기명식 보통주 |
2023.07.01~2027.06.01 | 100 | 11,434 | - | - | (*) |
| 무기명식 이권부 무보증 사모 전환사채 |
11 | 2023.07.07 | 2028.07.07 | 8,300,000,000 | 기명식 보통주 |
2024.07.07~2028.06.07 | 100 | 10,204 | 8,300,000,000 | 813,407 | - |
| 무기명식 이권부 무보증 사모 전환사채 | 12 | 2023.11.07 | 2026.11.07 | 28,800,000,000 | 기명식 보통주 |
2024.11.07~2026.10.06 | 100 | 9,586 | 28,800,000,000 | 3,004,381 | |
| 합 계 | - | - | - | 53,300,000,000 | - | - | - | - | 37,100,000,000 | 3,817,788 | - |
| 출처: 당사 제공자료 (*) 제10회차 전환사채 2024.03.29 기준, 미상환사채 잔액 모두 전환청구 하였습니다. |
| [당사 9BW 인수계약서 일부] |
|
1)본 사채를 소유한 자가 신주인수권 행사를 하기 전에 발행회사가 아래 (i) 또는 (ii)의 발행 당시 시가를 하회하는 발행가액으로 (i) 유상증자, 주식배당 및 준비금의 자본전입 등을 함으로써 주식을 발행하거나 또는 (ii) 신주인수권 또는 신주인수권이나 신주전환권이 부착된 회사채의 발행 등으로 신주인수권을 부여하는 증권을 발행하는 경우에는 아래와 같이 행사가액을 조정한다. 본 사유에 따른 행사가액의 조정일은 (i) 유상증자, 주식배당, 준비금의 자본전입 등으로 인한 신주의 발행일로 하며, (ii)의 경우 해당 증권의 발행일로 한다. A: 기발행주식수 B: 신발행주식수 C: 1주당 발행가격 D: 시가 |
| [당사 10CB, 11CB 및 12CB 인수계약서 일부] |
|
1)본 사채권을 소유한 자가 전환청구를 하기 전에 발행회사가 시가를 하회하는 발행가액으로 유상증자, 주식배당 및 준비금의 자본전입 등을 함으로써 주식을 발행하거나 또는 시가를 하회하는 전환가액 또는 행사가액으로 전환사채 또는 신주인수권부사채를 발행(당해 유상신주 또는 주식연계사채 발행 후 사후적으로 전환가액 또는 행사가액이 인수인의 주당 전환가액보다 하향 조정되는 경우 포함)하는 경우에는 아래와 같이 전환가격을 조정한다. 단, 유,무상증자를 병행 실시하는 경우, 유상증자의 1주당 발행가액이 조정 전 전환가액을 상회하는 때에는 유상증자에 의한 신발행주식수는 전환가액 조정에 적용하지 아니하고, 무상증자에 의한 신발행주식수만 적용한다. A: 기발행주식수 B: 신발행주식수 C: 1주당 발행가격 D: 시가 다만, 위 산식 중 "기발행주식수"는 당해 조정사유가 발생하기 직전일 현재의 발행주식 총수로 하며, 전환사채 또는 신주인수권부사채를 발행할 경우 "신발행주식수"는 당해 사채 발행 시 전환가액으로 전부 주식으로 전환되거나 당해 사채 발행 시 행사가액으로 신주인수권이 전부 행사될 경우 발행될 주식의 수로 한다. 또한, 위 산식 중 "1주당 발행가격"은 주식분할, 무상증자, 주식배당의 경우에는 영(0)으로 하고, 전환사채 또는 신주인수권부사채를 발행할 경우에는 당해 사채 발행 시 전환가액 또는 행사가액으로 하며, 위 산식에서 "시가"라 함은 발행가격 산정의 기준이 되는 기준주가(증권의발행및공시등에관한규정 제5-18조에서 정하는 기준주가) 또는 권리락주가(유상증자 이외의 경우에는 조정사유 발생 전일을 기산일로 하여 계산한 기준주가)로 한다. 2) 합병, 자본의 감소, 주식분할 및 병합 등에 의하여 전환가액의 조정이 필요한 경우에는 그 사유 발생 직전에 본 사채가 보통주식으로 전환되었다면 받을 수 있었던 주식 수를 산출할 수 있는 가액으로 본 사채의 전환가액을 조정한다. 단, 본 항에 따른 조정사유 중 감자 및 주식병합의 경우에 있어서는, 감자 및 주식병합 등을 위한 주주총회 결의일 전일을 기산일로 하여 증권의 발행 및 공시 등 에 관한 규정 제5-22조 제1항 본문의 규정에 의하여 산정한 가액이 액면가액 미만이면서 기산일 전에 전환가액을 액면가액으로 이미 조정한 경우(전환가액을 액면가액 미만으로 조정할 수 있는 경우는 제외한다)에는 조정 후 전환가액은 산정가액을 기준으로 감자 및 주식병합 등으로 인한 조정비율만큼 상향 조정한 가액 이상으로 조정한다. 회사는 전환사채 보유자의 권리에 불리한 영향을 미치게 되는 방식으로 합병, 분할 및 영업양수도를 하여서는 아니되며, 계속하여 상장을 유지할 의무를 부담한다. |
9BW의 발행 당시 인수계약서 상 '행사가격의 조정' 관련 조항과 11CB 및 12CB의 발행 당시 인수계약서 상 '전환가액의 조정' 관련 조항에 따라, 금번 유상증자 이후 행사가격 및 전환가액이 조정될 예정이며, 이 경우 행사 및 전환가능 주식수는 상기 산식에 따라 기존 7,590,931주에서 191,902주 늘어난 7,782,833주로 변경될 예정입니다. 신주배정일기준일 기준 전환 및 행사가격 대비 주식의 시가가 높은 내가격(ITM, In The Money) 상태로 이는 투자자의 전환 및 행사 청구에 따른 신주발행 가능성은 높은 상태이며, 상기 조정 관련 조항에 따라 본 주주배정 후 실권주 일반공모 유상증자 확정발행가액 결정 이후에도 전환 및 행사 가격은 내가격 상태로 전환 및 행사 청구의 가능성은 높다고 판단됩니다. 이에 전환 및 행사가능 주식수 전량이 전환 청구될 경우 기존주주들의 지분희석이 발생하게 되며, 최대주주 에이치엘비(주)의 지분율 또한 희석될 수 있습니다. 또한 9BW의 미상환사채는 신주배정일기준일 기준, 약 804억원으로 만기 상 장기차입금으로 분류되어 있으나, 최초 조기상환일 기준 실질만기가 2024년중에 도래하기 때문에 단기적 상환부담이 존재하는 상황입니다.
한편, 신주배정일기준일 기준 당사의 최대주주인 에이치엘비(주)는 앞서 기술한 9BW 196억원을 취득하였습니다. 9BW의 발행 당시 인수계약서 상 '행사가격의 조정' 관련 조항에 따라, 금번 유상증자 이후 행사가격 및 전환가액이 조정될 예정이며, 이 경우 당사의 최대주주인 에이치엘비(주)가 보유한 9BW의 행사가능 주식수는 상기 산식에 따라 기존 2,205,352주에서 55,706주 늘어난 2,261,058주로 변경될 예정입니다.
| [에이치엘비(주) 보유 9BW 내역] |
| 발행회사 및 사채명 | 에이치엘비생명과학㈜ 제9회 무기명식 이권부 무보증 분리형 신주인수권부사채 |
| 취득금액 | 19,603,370,000원 |
| 사채만기일 | 2025년 6월 15일 |
| 전환(행사)가액 (원/주) | 8,889 |
| 전환(행사)청구 시작일 | 2022년 7월 15일 |
| 전환(행사)청구 종료일 | 2025년 5월 15일 |
| 전환(행사)에 따라 발행할 주식 | 2,205,352주 |
| 옵션에 관한 사항 | 조기상환(Put Option): 본 사채의 발행일로부터 24개월이 경과하는 날로부터 3개월에 해당하는 날에 본 사채 금액의 전부 또는 일부에 대하여 조기상환 청구 가능. |
| 기타 | "신주인수권증권"과 "신주인수권이 분리된 채권"이 각각 상장되어 유통되는 분리형 신주인수권부사채임. |
| 출처: 에이치엘비(주) 분기보고서 |
따라서 금번 주주배정후 실권주 일반공모 유상증자에 따라 전환 및 행사가액이 조정된 이후, 최대주주가 배정물량의 50%를 청약을 하고 전환 및 행사가능 주식수 전량이 전환 청구될 경우 당사 최대주주 지분율은 18.16%로 본 공시서류 제출일 전일 지분율 대비 0.13%p. 감소할 예정입니다.
| [최대주주 지분율 변동 시뮬레이션 : 유상증자 + 9BW 행사청구 + 11CB, 12CB 전환청구] | |
| (기준일 : 2024년 05월 10일) | (단위: 주, %) |
| 성 명 | 주식의 종류 |
유상증자 전 |
배정 주식 수 (예정) |
청약 참여 주식수(예정) |
최대주주 보유 9BW 행사(예정) |
유상증자 및 전환/행사청구 후(예정) | ||
|---|---|---|---|---|---|---|---|---|
| 주식수 | 지분율 | 주식수 | 지분율 | |||||
| 에이치엘비(주) | 의결권 있는 주식 | 19,688,685 | 18.29 | 2,014,080 | 1,007,040 | 2,261,058 | 22,956,783 | 18.16 |
| 주1) 1차발행가액 기준. 최종적으로 실제 전환사채의 조정 전환가액은 확정발행가액으로 결정될 예정 |
상기 최대주주의 지분율 변화 시뮬레이션은 증권신고서 제출일 현재 1차발행가액 11,890원을 기준으로 산출하였으며, 향후 최종 발행가액이 확정됨에 따라서 최대주주 지분율 희석 정도가 변동될 수 있습니다. 최종발행가액이 하락할 경우, 최대주주의 지분율 희석은 제한적일 것으로 판단되나, 최종발행가액이 상승할 경우, 최대주주의 청약 및 납입 부담이 증가하여 참여 수량이 축소할 가능성이 있으며, 이 경우 지분율 희석 효과는 커질 것으로 판단됩니다. 이처럼, 금번 유상증자에 따라 현 최대주주의 지분율 하락, 경영권과 관련한 위험이 잠재되어 있으며, 그밖에 예상치 못한 경영권 혼란 가중 가능성도 있을 수 있으니, 투자자께서는 이점 유의하시기 바랍니다.
| 아. 종속회사 관련 위험 당사는 5개의 연결대상 종속회사를 보유하고 있으며, 주요 연결대상 종속회사로는 (주)신화어드밴스, 에이치비셀(주), 에이치엘비에너지(주) 및 에이치엘비솔루션(주)가 있습니다. 에이치엘비셀(주)는 바이오인공간, 지혈제, 인간 세포외기질을 연구 개발하는 회사로 해당 제품에 대한 본격적인 매출이 실현되지 않았으며, 2021년까지의 매출은 임상 컨설팅 등의 용역제공에 따른 매출이였습니다. 그러나 에이치엘비셀(주)는 2022년 10월 의료기기 및 의료소모품 생산, 판매 기업인 에임텍(주)을 흡수합병 함으로써 2020년 89백만원, 2021년 13백만원에서 2022년 1,166백만원, 2023년 1,407백만원으로 매출액 증가를 기록했습니다. 그러나 연구개발에 따른 인건비 등 비용이 발생함에 따라 영업이익은 계속해서 영업손실을 기록했습니다. 종속기업인 주식회사 신화어드밴스는 의약품 유통업을 영위하는 업체로서, 당사는 2016년 8월 3일 종속기업의 주식 100%를 취득하였습니다. (주)신화어드밴스는 2020년 매출액 75,059백만원을 기록하였으나 이후 감소하여 2021년 37,734백만원, 2022년 54,058백만원, 2023년 63,4177백만원 및2024년 1분기 16,849백만원을 기록하였습니다. 영업이익 또한 2020년 106백만원에서 2024년 1분기 -249백만원을 기록하며 영업손실을 보이고 있으며, 당기순이익 역시 2020년 179백만원에서 2024년 1분기 -86백만원의 당기순손실로 감소하였습니다. 종속기업인 에이치엘비에너지(주)는 폐기물 처리업을 영위하는 업체로서 당사는 2019년 5월 에이치엘비에너지(주)의 지분 100%를 취득하였습니다. 에이치엘비에너지(주)의 매출액은 2020년 3,080백만원, 2021년 3,761백만원, 2022년 4,266백만원, 2023년 3,487백만원 및 2024년 1분기 999백만원을 기록하였습니다. 2022년을 제외하고는 영업손실을 기록했으며, 당기순손실의 경우 2023년까지 계속해서 손실을 기록하기는 했지만, 2020년 1,022백만원에서 2023년 370백만원으로 손실의 폭이 감소하였습니다. 수익성 악화, 영업환경 악화 등 예상치 못한 이슈발생으로 인하여 종속회사의 실적 악화로 이어질 수 있으며, 이는 당사의 연결기준 재무에 악영향을 끼칠 수 있으므로 연결대상 종속회사에 대한 지속적인 모니터링이 필요하오니 투자자 여러분께서는 유의하시기 바랍니다. |
| [연결대상 종속회사 현황] |
| (단위 : 백만원) |
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| HLB셀 | 2009.09.16 | 경기도 화성시 동탄첨단산업로 | 바이오의약품 개발 | 38,250 | 의결권의 과반수이상 보유 (기업회계기준서 제1110호) |
미해당 |
| 신화어드밴스 | 2007.11.19 | 서울시 영등포구 선유로 | 의약품 유통업 | 25,679 | 의결권의 과반수이상 보유 (기업회계기준서 제1110호) |
미해당 |
| HLB에너지 | 1997.06.27 | 부산광역시 사하구 감천항로 | 폐기물 소각열 관련사업 |
17,296 | 의결권의 과반수이상 보유 (기업회계기준서 제1110호) |
미해당 |
| HLB생명과학R&D | 2022.04.01 | 경기도 화성시 동탄첨단산업로 | 신약개발사업 | 4,434 | 의결권의 과반수이상 보유 (기업회계기준서 제1110호) |
미해당 |
| HLB솔루션 | 2024.01.01 | 경기도 화성시 동탄첨단산업로 | 에너지 | 4,519 | 의결권의 과반수이상 보유 (기업회계기준서 제1110호) |
미해당 |
| 주1) 당사는 2023년 9월 18일 실시한 이사회 결의를 통해 단순 물적분할로 2024년 01월 01일부로 에너지 사업부문을 분할신설회사인 에이치엘비솔루션(주)로 포괄 승계하였습니다. 주2) 당사는 2023년 7월 3일 화진메디칼 지분 100% 를 인수하였고 2023년 10월 1일 합병하여 의료기기사업부로 편입하였습니다. |
| 출처: 당사 내부자료 |
당사는 5개의 연결대상 종속회사를 보유하고 있으며, 주요 연결대상 종속회사로는 (주)신화어드밴스, 에이치비셀(주), 에이치엘비에너지(주) 및 에이치엘비솔루션(주)가 있습니다. 당사는 바이오, 메디케어, 의료기기 등 의료용품 및 기타 의약관련제품 제조 사업부문을 주력 사업으로 경영 자원을 집중하고자, 2023년 9월 실시한 이사회 결의에 의해 단순 물적분할로 에너지 사업부문을 2024년 01월 01일부로 분할신설회사인 에이치엘비솔루션(주)로 포괄 승계하여 이 사업부문에 전문화된 사업역량을 강화하고자 하였습니다.
| [2024년 1분기 당사 종속기업의 실적] |
| (단위: %, 천원) |
| 회사명 | HLB셀 | 신화어드밴스 | HLB에너지 | HLB생명과학R&D | HLB솔루션 |
| 구분 | 종속기업 | 종속기업 | 종속기업 | 종속기업 | 종속기업 |
| 지분율 | 99.30% | 100% | 100% | 100% | 100% |
| 자산 | 91,408 | 25,620 | 30,525 | 5,178 | 3,587 |
| 부채 | 744 | 3,083 | 10,420 | 612 | 2,438 |
| 자본 | 90,664 | 22,537 | 20,104 | 4,566 | 1,149 |
| 매출 | 247 | 16,849 | 999 | 120 | 0 |
| 당기순이익(손실) | 42,010 | -86 | 9 | -1,409 | -51 |
| 출처: 당사 내부자료 |
■ 에이치엘비셀(주)
종속기업인 에이치엘비셀(주)는 화성시 영천동에 소재하고 있는 체외순환형 바이오인공간개발업을 영위하는 업체로서 당사는 2018년 3월 21일 종속기업의 주식 97.95%를 취득하였습니다. 이후 지분을 지속 취득하여 증권신고서 제출일 현재 지분율은 99.30% 입니다.
에이치엘비셀(주)는 바이오인공간, 지혈제, 인간 세포외기질을 연구 개발하는 회사로 해당 제품에 대한 본격적인 매출이 실현되지 않았으며, 2021년까지의 매출은 임상 컨설팅 등의 용역제공에 따른 매출이였습니다. 그러나 에이치엘비셀(주)는 2022년 10월 의료기기 및 의료소모품 생산, 판매 기업인 에임텍(주)을 흡수합병 함으로써 2020년 89백만원, 2021년 13백만원에서 2022년 1,166백만원, 2023년 1,407백만원으로 매출액 증가를 기록했습니다. 그러나 연구개발에 따른 인건비 등 비용이 발생함에 따라 영업이익은 계속해서 영업손실을 기록했습니다. 당기순이익의 경우 2020년 5,430백만원, 2021년 10,940백만원, 2022년 232백만원 당기순손실을 기록했으나, 2023년 및 2024년 1분기 지속적으로 증가한 금융자산 평가이익 등의 영업외이익으로 인해 각각 18,511백만원, 42,009백만원의 당기순이익을 기록했습니다.
| [에이치엘비셀(주) 요약재무정보] |
| (단위: 백만원) |
| 계 정 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 유동자산 | 86,984 | 45,633 | 30,038 | 35,353 | 46,938 |
| 비유동자산 | 4,424 | 4,505 | 8,213 | 2,761 | 1,958 |
| 자산총계 | 91,408 | 50,138 | 38,251 | 38,114 | 48,896 |
| 유동부채 | 448 | 1,204 | 9,504 | 379 | 306 |
| 비유동부채 | 296 | 279 | 1,018 | 677 | 539 |
| 부채총계 | 744 | 1,483 | 10,522 | 1,056 | 845 |
| 자본금 | 17,234 | 17,234 | 16,425 | 16,425 | 16,425 |
| 이익잉여금 | 35,774 | (6,263) | (24,715) | (15,332) | (9,215) |
| 자본총계 | 90,664 | 48,655 | 27,729 | 37,058 | 48,051 |
| 매출액 | 247 | 1,407 | 1,166 | 13 | 89 |
| 매출총이익 | (75) | (160) | 18 | 13 | 89 |
| 영업이익 | (897) | (2,923) | (3,386) | (2,790) | (2,276) |
| 금융자산 평가이익 | 42,750 | 23,392 | - | 502 | - |
| 당기순이익 | 42,009 | 18,511 | (232) | (10,940) | (5,430) |
| 출처: 당사 내부자료 |
에이치엘비셀(주)의 유동비율은 높은 유동자산의 비중으로 인해 매우 높은 수준을 유지하고 있으며, 부채비율의 경우 낮은 금액의 부채에 따라 2024년 1분기 0.8%로 낮은 수치를 기록하였습니다. 에이치엘비셀(주)는 개발 중인 바이오 제품의 본격적인 매출 실현이 발생하지 않았지만, 2022년 10월 에임텍(주)를 흡수합병 함으로써 수익성 및 재무상태가 개선되었습니다.
| [에이치엘비셀(주) 주요 재무 비율] |
| (단위: %) |
| 구분 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 유동비율 | 19,418.3% | 3,790.1% | 316.1% | 9,328.0% | 15,339.2% |
| 부채비율 | 0.80% | 3.0% | 37.9% | 2.8% | 1.8% |
| 영업이익률 | -363.12% | -207.7% | -290.4% | -21,461.5% | -2,557.3% |
| 순이익률 | 17,001.9% | 1,315.6% | -19.9% | -84,153.8% | -6,101.1% |
| 출처: 당사 내부자료 |
■ (주)신화어드밴스
종속기업인 주식회사 신화어드밴스는 서울특별시 영등포구에 소재하고 있는 의약품 유통업을 영위하는 업체로서, 당사는 2016년 8월 3일 종속기업의 주식 100%를 취득하였습니다. 당사는 바이오 산업에 진출을 하였으며, 시너지 효과를 위해 의약품 유통업체인 (주)신화어드밴스를 인수하였습니다.
(주)신화어드밴스는 2020년 매출액 75,059백만원을 기록하였으나 이후 감소하여 2021년 37,734백만원, 2022년 54,058백만원, 2023년 63,4177백만원 및 2024년 1분기 16,849백만원을 기록하였습니다. 영업이익 또한 2020년 106백만원에서 2024년 1분기 -249백만원을 기록하며 영업손실을 보이고 있으며, 당기순이익 역시 2020년 179백만원에서 2024년 1분기 -86백만원의 당기순손실로 감소하였습니다. 이러한 (주)신화어드밴스의 수익성 악화는 역마진 거래처 등 거래 중단으로 인한 매출 감소에 기인하며, 기존 사업의 매출 확대 및 신규 거래처 확보 등을 통해 수익성 회복하려 노력하고 있습니다.
| [(주)신화어드밴스 요약재무제표] |
| (단위: 백만원) |
| 계 정 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 유동자산 | 24,905 | 24,336 | 24,891 | 24,872 | 23,567 |
| 비유동자산 | 715 | 724 | 788 | 791 | 3,404 |
| 자산총계 | 25,620 | 25,060 | 25,679 | 25,663 | 26,971 |
| 유동부채 | 3,017 | 2,369 | 2,790 | 2,272 | 2,901 |
| 비유동부채 | 66 | 69 | 46 | 23 | 51 |
| 부채총계 | 3,083 | 2,438 | 2,836 | 2,295 | 2,952 |
| 자본금 | 1,523 | 1,523 | 1,523 | 1,523 | 1,523 |
| 이익잉여금 | 5,223 | 5,308 | 5,529 | 6,054 | 6,703 |
| 자본총계 | 22,537 | 22,623 | 22,843 | 23,368 | 24,019 |
| 매출액 | 16,849 | 63,417 | 54,058 | 37,734 | 75,059 |
| 매출총이익 | 279 | 1,148 | 790 | 710 | 2,248 |
| 영업이익 | (249) | (771) | (891) | (969) | 106 |
| 당기순이익 | (86) | (221) | (525) | (649) | 179 |
| 출처: 당사 내부자료 |
(주)신화어드밴스의 유동비율은 2020년 812.4%를 기록한 후 2021년 1,094.7%, 2022년 892.2%, 2023년 1,027.3%, 2024년 1분기 825.5%로 증가하였습니다. (주)신화어드밴스는 도매업의 특성상 매입채무가 다량으로 발생하며, 이에 따라 부채비율이 높은 특성을 보입니다. 영업이익률 및 순이익률의 경우 마진율이 낮은 의약품 유통 사업 특성상 낮은 수준을 유지하고 있으며, 2020년 외에는 영업손실과 당기순손실을 기록하였습니다. 당사 및 (주)신화어드밴스는 지속적으로 재무비율을 개선하기 위해 노력하고 있으나 낮은 수익성 및 영업환경에 대한 부적절한 대응으로 실적이 악화될 경우 재무비율이 악화될 수 있습니다.
| [(주)신화어드밴스 주요 재무 비율] |
| (단위: %) |
| 구 분 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 유동비율 | 825.5% | 1,027.3% | 892.2% | 1,094.7% | 812.4% |
| 부채비율 | 13.7% | 10.8% | 12.4% | 9.8% | 12.3% |
| 영업이익률 | -1.5% | -1.2% | -1.6% | -2.6% | 0.1% |
| 순이익률 | -0.5% | -0.3% | -1.0% | -1.7% | 0.2% |
| 출처: 당사 내부자료 |
■ 에이치엘비에너지(주)
종속기업인 에이치엘비에너지(주)는 부산시 사하구에 소재하고 있는 폐기물 처리업을 영위하는 업체로서 당사는 2019년 5월 에이치엘비에너지(주)의 지분 100%를 취득하였습니다.
에이치엘비에너지(주)의 매출액은 2020년 3,080백만원, 2021년 3,761백만원, 2022년 4,266백만원, 2023년 3,487백만원 및 2024년 1분기 999백만원을 기록하였습니다. 2022년을 제외하고는 영업손실을 기록했으며, 당기순손실의 경우 2023년까지 계속해서 손실을 기록하기는 했지만, 2020년 1,022백만원에서 2023년 370백만원으로 손실의 폭이 감소하였습니다. 당사는 2023년 09월 18일 이사회결의를 통해 바이오, 메디케어, 의료기기 등 의료용품 및 기타 의약관련제품 제조 사업부문을 주력 사업으로 경영 자원을 집중하고자, 에너지사업부문을 2024년 01월 01일부로 단순물적분할을 통해 분할신설회사인 에이치엘비솔루션으로 포괄 승계하였습니다.
| [에이치엘비에너지(주) 요약재무정보] |
| (단위: 백만원) |
| 계 정 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 유동자산 | 4,887 | 2,584 | 1,794 | 1,273 | 1,632 |
| 비유동자산 | 25,636 | 21,730 | 15,502 | 16,277 | 15,727 |
| 자산총계 | 30,523 | 24,314 | 17,296 | 17,550 | 17,359 |
| 유동부채 | 6,253 | 1,298 | 6,359 | 6,402 | 5,719 |
| 비유동부채 | 4,167 | 2,921 | 208 | 450 | 913 |
| 부채총계 | 10,420 | 4,219 | 6,567 | 6,852 | 6,632 |
| 자본금 | 2,302 | 2,302 | 14,750 | 14,750 | 14,750 |
| 이익잉여금 | 10 | (11,697) | (11,498) | (10,905) | |
| 자본총계 | 20,102 | 20,095 | 10,729 | 10,698 | 10,727 |
| 매출액 | 999 | 3,487 | 4,266 | 3,761 | 3,080 |
| 매출총이익 | 158 | (379) | 526 | 315 | 37 |
| 영업이익 | (13) | (1,075) | 23 | (310) | (474) |
| 당기순이익 | 7 | (370) | (232) | (596) | (1,022) |
| 출처: 당사 내부자료 |
에이치엘비에너지(주)의 유동비율은 2020년 28.5%, 2021년 19.9%, 2022년 28.2를 기록한 뒤 2023년 199.1%, 2024년 1분기 78.2%를 기록하며 급격히 증가하였습니다. 부채비율의 경우에는 2020년 61.8%, 2021년 64.0%, 2022년 61.2%을 기록한 이후에 2023년 21.0%로 감소하였지만 2024년 1분기 51.8%로 다시 증가하였습니다. 순이익률은 2023년까지 계속해서 적자로 인해 음(-)의 값을 기록하고 있으며, 2022년 영업이익률과 순이익률 모두 개선되는 모습을 보였으나, 2023년 -30.8% 영업이익률과 -10.6% 순이익률을 기록했습니다. 2024년 1분기에는 영업이익률 -1.3% 및 순이익률 0.7%를 기록하며 다시 개선되는 모습을 보이고 있습니다.
| [에이치엘비에너지(주) 주요 재무 비율] |
| (단위: %) |
| 구 분 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 유동비율 | 78.2% | 199.1% | 28.2% | 19.9% | 28.5% |
| 부채비율 | 51.8% | 21.0% | 61.2% | 64.0% | 61.8% |
| 영업이익률 | -1.3% | -30.8% | 0.5% | -8.2% | -15.4% |
| 순이익률 | 0.7% | -10.6% | -5.4% | -15.8% | -33.2% |
| 출처: 당사 내부자료 |
수익성 악화, 영업환경 악화 등 예상치 못한 이슈발생으로 인하여 종속회사의 실적 악화로 이어질 수 있으며, 이는 당사의 연결기준 재무에 악영향을 끼칠 수 있으므로 연결대상 종속회사에 대한 지속적인 모니터링이 필요하오니 투자자 여러분께서는 유의하시기 바랍니다.
| 자. 회계처리 관련 제재 리스크 당사는 금융감독원으로부터 제21기(2018.1.1 ~ 2018.12.31)부터 제22기(2019.1.1 ~ 2019.12.31)까지의 연결재무제표 등에 대한 심사결과 지적된 회계처리 기준 위반사항 등에 대하여 수정권고를 제시받았습니다. 금융감독원은 당사의 18년말 에이치엘비셀(주) 관련 영업권과 관련하여, 연결기준 15,125백만원 및 별도기준 8,858백만원을 18년 및 19년 재무제표에서 각각 과대 및 과소계상한 것으로 판단하였습니다. 당사는 2018년 영업권 손상평가보고서가 당시 이용가능한 최신 자료를 모두 반영하지 못하였다는 금융감독원의 수정권고를 수용하되 회계기준서에 근거한 최선의 합리적 추정치를 산출하여 재무제표를 수정하는 것이 타당하다고 판단하여 소명서를 제출하였습니다. 당사는 수정권고를 수용하여 2021년 12월 10일 수정 권고 내용이 반영된 제21기 및 제22기 재무제표를 전자공시시스템에 재공시하였습니다. 위법동기를 직무상 주의의무를 현저히 결하였다고 인정할 수 있는 경우 등에 해당하지 않아 과실로 판단되었고 경고 조치로 마무리되었습니다. 투자자께서는 이 점 인지하시어 투자의사결정하시기 바랍니다. |
당사는 금융감독원으로부터 제21기(2018.1.1 ~ 2018.12.31)부터 제22기(2019.1.1 ~ 2019.12.31)까지의 연결재무제표 등에 대한 심사결과 지적된 회계처리 기준 위반사항 등에 대하여 수정권고를 제시받았습니다. 금융감독원은 당사가 18년말 에이치엘비셀(주) 관련 영업권 등의 손상을 소홀히하여, 연결기준 15,125백만원 및 별도기준 8,858백만원을 18년 및 19년 재무제표에서 각각 과대 및 과소계상한 것으로 판단하였습니다.
| [당사 연결재무제표 주요 수정내역] |
| (단위: 백만원) |
|
구 분 |
수정 전 | 수정 후 | ||
| 제22기 |
제21기 |
제22기 |
제21기 |
|
|
매출액 |
114,019 |
102,476 |
114,019 |
102,476 |
|
영업이익(손실) |
(4,479) |
(7,963) |
(4,479) |
(7,963) |
|
영업외손익 |
(2,082) |
4,693 |
13,043 |
(10,432) |
|
당기순이익(손실) |
(7,563) |
(3,299) |
7,562 |
(18,424) |
|
유동자산 |
223,667 |
239,086 |
223,667 |
239,086 |
|
비유동자산 |
181,268 |
147,169 |
181,268 |
132,044 |
|
자산총계 |
404,935 |
386,255 |
404,935 |
371,130 |
|
유동부채 |
39,845 |
48,639 |
39,845 |
48,639 |
|
비유동부채 |
30,666 |
116,378 |
30,666 |
116,378 |
|
부채총계 |
70,510 |
165,016 |
70,510 |
165,016 |
|
자본금 |
24,002 |
18,623 |
24,002 |
18,623 |
|
자본총계 |
334,425 |
221,239 |
334,425 |
206,114 |
| 주1) 연결기준 수치 주2) 수정된 부분 굵은 글씨체 표시 |
| 출처: 당사 2018년, 2019년 사업보고서 |
| [당사 별도재무제표 주요 수정내역] |
| (단위: 백만원) |
| 구 분 | 수정 전 | 수정 후 | ||
| 제22기 | 제21기 | 제22기 | 제21기 | |
| 매출액 | 12,431 | 4,271 | 12,431 | 4,271 |
| 영업이익(손실) | 657 | -6,491 | 657 | -6,491 |
| 영업외손익 | 1,049 | 6,038 | 9,907 | -2,820 |
| 당기순이익(손실) | 1,706 | -453 | 10,564 | -9,311 |
| 유동자산 | 121,512 | 200,596 | 121,512 | 200,596 |
| 비유동자산 | 250,980 | 141,055 | 250,980 | 132,197 |
| 자산총계 | 372,492 | 341,650 | 372,492 | 332,793 |
| 유동부채 | 10,222 | 23,638 | 10,222 | 23,638 |
| 비유동부채 | 16,753 | 97,696 | 16,753 | 97,696 |
| 부채총계 | 26,975 | 121,334 | 26,975 | 121,334 |
| 자본금 | 24,002 | 18,623 | 24,002 | 18,623 |
| 자본총계 | 345,517 | 220,316 | 345,517 | 211,459 |
| 주1) 별도기준 수치 주2) 수정된 부분 굵은 글씨체 표시 |
| 출처: 당사 2018년, 2019년 사업보고서 |
당사는 2018년 영업권 손상평가보고서가 당시 이용가능한 최신 자료를 모두 반영하지 못하였다는 금융감독원의 수정권고를 수용하되 회계기준서에 근거한 최선의 합리적 추정치를 산출하여 재무제표를 수정하는 것이 타당하다고 판단하여 소명서를 제출하였습니다. 당사는 소명서를 통해 2018년말의 경우 평가보고서상 추정된 사용가치보다 실제 상황이 훨씬 우호적이었고 손상을 인식할 만한 객관적인 상황이나 정황이 전혀 없었다는 점을 설명하였습니다.
당사는 수정권고를 수용하여 2021년 12월 10일 수정 권고 내용이 반영된 제21기 및 제22기 재무제표를 전자공시시스템에 재공시하였습니다. 심사 조치의 중요도는 2단계였으나, 위법동기를 직무상 주의의무를 현저히 결하였다고 인정할 수 있는 경우 등에 해당하지 않아 과실로 판단하였고 경고 조치로 마무리되었습니다. 투자자께서는 이 점 인지하시어 투자의사결정하시기 바랍니다.
| 차. 에이치엘비 주식회사 주가 변동에 따른 손익 변동 위험 당사는 2024년 1분기말 기준 최대주주인 에이치엘비 주식회사의 주식 1,933,601주를 보유하고 있으며, 해당 보유분은 매분기 공정가치 평가를 통해 공정가치 측정 금융자산 평가손익 계정으로 금융수익 및 금융원가로 계상되고 있습니다. 따라서, 에이치엘비의 주가가 하락할 경우, 당사의 금융자산평가손실이 발생하여 당사의 당기순이익에 부정적인 영향을 미칠 수 있습니다. 에이치엘비 주가에는 리보세라닙과 캄렐리주맙 병용요법 간암 1차 치료제가 미치는 영향이 큰 상황에서 2024년 5월 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL을 수령하였습니다. 이와 관련하여 항서제약의 CMC(의약품 생산시설 실사) 보완 및 BIMO Inspection(임상사이트 실사) 완료 시기에 대한 불확실성이 있습니다. 또한 당사는 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있어 FDA 재승인 신청 후 판매승인 시점이 지연될 경우 당사 및 당사 관계회사의 수익성과 주가에도 부정적으로 작용할 가능성이 있으니 투자자께서는 유의하시기 바랍니다. |
당사는
2024년 1분기말 기준 최대주주인 에이치엘비 주식회사의 주식
1,933,601주
를 보유하고 있으며, 해당 보유분은 매분기 공정가치 평가를 통해 공정가치 측정 금융자산 평가손익 계정으로 금융수익 및 금융원가로 계상되고 있습니다. 매분기말일의 에이치엘비 보통주 종가를 기준으로 평가를 진행하며, 전분기 대비 주가가 상승 할 경우, 평가 이익으로 인식하고, 전분기 대비 주가가 하락 할 경우, 평가 손실로 인식하게 됩니다.
실제로, 당사는 에이치엘비 주식회사의 주가 상승으로 인해 2024년 1분기 당기손익-공정가치 측정 금융자산평가이익으로 19,848백만원을 금융수익으로 계상 하였습니다.
| [에이치엘비 최근 1개년 주가 추이] |
 |
|
에이치엘비 최근 1개년 주가 추이 |
| 출처: KRX/정보데이터시스템 |
에이치엘비 주식회사의 주식은 최근 1개년간(2023년 05월 23일부터 2024년 5월 22일까지) 최저 28,050원, 최고 120,800원을 기록하였으며, 이는 리보세라닙(Rivoceranib)과 캄렐리주맙(Camrelizumab) 병용요법의 간암 1차 치료제의 FDA(미국 식품의약국) 결과를 앞두고 상대적으로 큰 변동성을 보였습니다. 따라서, 에이치엘비의 주가가 하락할 경우, 당사의 금융자산평가손실이 발생하여 당사의 당기순이익에 부정적인 영향을 미칠 수 있습니다. 투자자께서는 이 점 인지하시어 투자의사 결정하시기 바랍니다.
(삭제) 리보세라닙과 캄렐리주맙 병용요법은 2019년부터 2022년까지 13개국 121개 병원에서 543명 시험대상자를 상대로 진행한 임상 3상 시험 결과, 전체 생존기간(mOS)은 22.1개월로 간암 1차 치료제들 중 최장 환자 생존기간을 기록했으며, 그 밖에 주요 지표에서는 무진행 생존기간(mPFS) 5.6개월, 객관적 반응률(ORR) 33.1%, 질병 조절률(DCR) 78.3% 등 우수한 결과치를 기록했습니다.
| [리보세라닙과 캄렐리주맙 임상 3상 결과] |
 |
|
리보세라닙과 캄렐리주맙 유효성 평가 결과 |
| 출처: 당사 제공 자료(HLB IR 자료) |
이를 바탕으로 2023년 5월 NDA(신약 허가신청)를 신청하였으며, 7월 NDA 본심사가 개시되었습니다. 2023년 8월 리보세라닙 공장실사 및 12월 캄렐리주맙 공장실사까지 완료하였으나, 2024년 5월 미국 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL(보완요구서한, Complete Response Letter) 수령하였습니다. CRL 통한 요구 사항은 1) 병용투여 약물인 캄렐리주맙(항서제약)의 CMC(의약품 생산시설 실사) 진행 후 항서제약이 보완한 사항에 대해 일부 미비한 점에 대한 보완 2) 미국 FDA가 BIMO Inspection(임상사이트 실사)를 여행제한으로 인해 완료하지 못했다는 내용입니다. 계열회사 Elevar Therapeutics, Inc.는 상기 두가지 보완사항에 대해 항서제약과 긴밀히 협의하여 이에 대해 신속히 보완하고 FDA 재승인 신청할 예정이며, 재승인 신청 후 최장 6개월 이내 FDA는 승인여부를 결정하게 됩니다.
당사는 2018년 8월 14일에 리보세라닙 관련 부광약품(주)에 인정되는 계약상 지위, 권리 및 의무 일체를 취득하여 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있습니다. 이에 따라 에이치엘비의 리보세라닙 영향은 당사의 수익성과 주가에도 영향을 미치고 있습니다. 당사의 2022년 1월 3일부터 2024년 5월 22일까지의 주가 추이를 살펴보면, 2022년 5월 12일 에이치엘비는 리보세라닙과 캄렐리주맙을 병용한 간암 1차 치료제 관련 글로벌 임상 3상의 1차 유효성 지표가 모두 충족돼 통계적 유의성이 확보되었음을 발표했고, 이에 12일 9,868원이었던 당사의 주가는 13일 30% 오른 12,538원으로 마감했습니다. 또한 프랑스 파리 유럽암학회에서 임상 3상 최종 결과 발표가 열리기 하루 전인 2022년 9월 8일 주가는 전일 보다 17% 오른 15,159원으로 마감했습니다. 그리고 2024년 3월 25일 에이치엘비의 리보세라닙과 캄렐리주맙 병용 간암 1차 치료제 FDA 승인 기대로 인해 23,680원까지 오르며 최근 2개년 중 최고 주가를 기록했습니다. 하지만 2024년 5월 17일 에이치엘비가 FDA로부터 리보세라닙과 캄렐리주맙을 병용한 간암 1차 치료제 CRL을 수령하자, 당사의 주가는 전일 대비 29.98% 감소한 8,630원을 기록했습니다.
| [에이치엘비생명과학 최근 주가 추이] |
 |
|
에이치엘비생명과학 주가 변동 추이('22.01~'24.05) |
| 출처: KRX/정보데이터시스템 |
2022년 1월 3일부터 2024년 5월 22일까지 당사의 주가는 최저 8,380원, 최고 23,680원을 기록하며, 큰 변동성을 보였습니다. 이는 최대주주인 에이치엘비의 리보세라닙과 캄렐리주맙 병용요법 간암 1차 치료제의 영향이 큰 상황에서 2024년 5월 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL을 수령하였습니다. 이와 관련하여 항서제약의 CMC(의약품 생산시설 실사) 보완 및 BIMO Inspection(임상사이트 실사) 완료 시기에 대한 불확실성이 있습니다. 또한 당사는 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있어 FDA 재승인 신청 후 판매승인 시점이 지연될 경우 당사 및 당사 관계회사의 수익성과 주가에도 부정적으로 작용할 가능성이 있으니 투자자께서는 유의하시기 바랍니다.
3. 기타위험
| 가. 신주의 환금성 제약 및 주가 변동에 따른 손실 위험 금번 유상증자 청약에 참여하여 신주를 배정받을 경우 신주의 추가상장일까지 환금성에 제약이 있으며, 청약 후 추가상장일 사이에 주가가 하락할 경우 원금에 대한 손해가 발생할 가능성이 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
금번 유상증자 청약에 참여하여 신주를 배정받을 경우 신주의 추가상장일까지 환금성에 제약이 있으며, 청약 후 추가상장일 사이에 주가가 하락할 경우 원금에 대한 손해가 발생할 가능성이 존재합니다. 투자자께서는 이 점 유의하시기 바랍니다.
당사는 코스닥시장 상장법인으로서 이번 유상증자로 발행되는 신주는 코스닥시장에 상장되어 거래될 예정이므로 유동성과 관계된 심각한 환금성 위험은 존재하지 않습니다. 그러나 유상증자 청약에 참여하여 신주를 배정받을 경우, 신주가 상장되어 매매가 가능할 때까지 납입주금에 대한 유동성의 제약이 있습니다.
본 유상증자의 자세한 일정은 본 신고서의 '제1부 모집 또는 매출에 관한 사항 - I. 모집 또는 매출에 관한 일반사항 - 1. 공모의 개요'를 참고하시기 바랍니다.
또한 코스닥시장에 추가 상장될 때까지 유상증자로 발행되는 신주의 발행가액 수준의 주가가 유지되지 않을 수 있으며, 당사의 내적인 환경변화 또는 시장전체의 환경 변화 등에 의한 급격한 주가하락이 발생할 경우, 투자원금에 대한 손실이 발생할 수 있는 점 투자자께서는 유의하시기 바랍니다.
| 나. 증자방식, 청약절차에 대한 주의 및 주가 하락 위험 당사의 금번 유상증자로 인하여 신주배정기준일 기준, 기발행주식총수 107,650,759의 10.22%에 해당하는 11,005,125주가 추가로 발행될 예정입니다. 본 유상증자는 주주배정 후 실권주 일반공모 방식으로 진행됨에 따라 일반공모를 거쳐 배정 후에도 미 청약된 잔여주식에 대해서는 대표주관회사가 자기계산으로 잔액인수하게 됩니다. 만약 본 유상증자 청약에서 대량 실권이 발생하여 대표주관회사가 실권주를 인수하게 될 경우 주가에 어떠한 영향을 미칠지는 예상하기 어렵습니다. 다만, 대표주관회사가 당사 주식 인수 후 수익을 확정하기 위해 빠른 시일 내에 인수한 주식을 장내에서 매각하게 된다면 단기적으로 당사 주가에 악영향을 미칠 수 있으며, 대표주관회사가 인수한 주식을 일정 기간 보유하더라도 동 인수 물량이 잠재 매각 물량으로 존재하여 주가 상승에 부담으로 작용할 가능성이 있습니다. 대표주관회사가 최종 실권주를 인수할 경우, 당사는 실권주 인수금액의 16.0%를 추가수수료로 지급하게 됩니다. 이를 고려할 때, 대표주관회사의 실권주 매입단가는 일반청약자들 보다 16.0% 낮은 것과 같은 결과가 초래되어 인수 물량을 단기간에 처분하게 될 소지가 높을 것으로 예상되며 일시적으로 대규모 물량이 출회하여 주가가 하락할 가능성이 있습니다. 실질적으로 유상증자 청약자 및 대표주관회사는 신주상장 2영업일 전부터 입고예정 주식의 매도가 가능합니다. 투자자 여러분께서는 이 점에 유의하시어 투자에 임하시기 바랍니다. |
당사의 금번 유상증자로 인하여 신주배정기준일 기준, 기발행주식총수 107,650,759주의 10.22%에 해당하는 11,005,125주가 추가로 발행될 예정입니다.
| [당사 주가 및 유상증자에 따른 발행주식수 및 가격] |
| 모집예정 주식 종류 | 기명식보통주 | 비 고 |
| 모집예정주식수 | 11,005,125주 | - |
| 현재 발행주식총수 | 107,650,759주 |
- |
| 1차 발행가액 | 11,890원 | 증자비율 및 할인율 고려 |
| 기산일 종가 | 16,250원 | 2024.05.07 종가 |
금번 유상증자에 따른 모집가액은 (舊)「유가증권의 발행 및 공시등에 대한 규정」 제57조를 일부 준용하여 산출됩니다. 그러나 주식시장의 특성상 향후 주가에 대한 변동성이 있는 관계로 증자에 따른 모집가격 산정시 결정된 1주당 모집가액보다 향후 추가 상장 후 거래 시점의 주가가 낮아져 투자자에게 금전적 손실이 발생할 가능성이 있습니다.
당사는 본 유상증자의 원활한 신주인수권증서 매매를 위하여 5거래일간 신주인수권증서를 상장하여 신주인수권증서를 통한 구주주 청약률을 제고할 계획입니다. 하지만 신주인수권증서의 원활한 매매 및 청약참여를 위한 노력에도 불구하고 신주인수권증서를 통한 청약이 부진하여 대규모 실권이 발생할 경우, 투자심리에 악영향을 끼쳐 일반공모청약에 부정적 영향을 끼칠 수도 있으며 향후 주가하락 가능성도 배제할 수 없습니다.
또한 금번 유상증자로 인해 추가 발행되는 주식은 보호예수되지 않는 관계로, 일시적인 물량 출회에 따른 주가하락의 가능성이 있습니다. 금번 유상증자에 따른 주권의 상장일은 2024년 06월 26일로 예정되어 있습니다. 금번 유상증자에 따른 모집예정주식 11,005,125주가 향후 코스닥시장에 추가 상장될 경우 유통주식수의 증가로 인하여 주가희석화 위험이 발생할 수 있습니다.
특히 금번 주주배정 후 실권주 일반공모의 경우 10.22%의 증자비율로 실권이 발생할 확률과 추가 유통주식수 상장에 따른 주가희석화 위험이 있습니다. 2020년 이후 증자비율 90% 이상의 주주배정 후 실권주 일반공모는 총 12건이며, 실권이 발생한 유상증자는 와이오엠, 미코바이오메드 2건입니다. 또한 총 12건 중 8건이 예정발행가액 대비 확정발행가액이 감소하였습니다. 최근 3개년 증자비율 90% 이상의 주주배정 후 실권주 일반공모 유상증자 동향은 다음과 같습니다.
| [유상증자 동향] |
| 법인명 | 증자비율 | 예정발행가 | 확정발행가 | 발행가증감율 | 구주주 청약율 | 일반 경쟁률 |
| 엔케이물산 | 90% | 635 | 458 | ▼27.87% | 97.0% | 419.83 : 1 |
| 대한항공 | 99% | 14,400 | 19,100 | ▲32.64% | 104.9% | 518.26 : 1 |
| 해성옵틱스 | 96% | 784 | 705 | ▼10.08% | 108.7% | 0.00 : 1 |
| 에어부산 | 136% | 2,235 | 2,030 | ▼9.17% | 105.4% | 0.00 : 1 |
| 에이티세미콘 | 107% | 1,835 | 1,875 | ▲2.18% | 92.6% | 82.95 : 1 |
| 현대두산인프라코어 | 145% | 6,950 | 5,980 | ▼13.96% | 100.2% | 2,486.03 : 1 |
| 아이윈플러스 | 99% | 713 | 493 | ▼30.86% | 104.3% | 0.00 : 1 |
| KC코트렐 | 97% | 1,930 | 1,610 | ▼16.58% | 93.2% | 17.94 : 1 |
| 와이오엠 | 122% | 910 | 936 | ▲2.86% | 77.7% | 0.21 : 1 |
| 젠큐릭스 | 93% | 4,325 | 3,925 | ▼9.25% | 84.5% | 273.93 : 1 |
| CJ CGV | 156.5% | 7,630 | 5,560 | ▼27.13% | 89.4% | 75.67 : 1 |
| 미코바이오메드 | 98.3% | 2,670 | 2,705 | ▲1.31% | 62.8% | 0.14 : 1 |
| 출처: 당사 제시 자료 |
한편, 본 유상증자는 주주배정 후 실권주 일반공모 방식으로 진행됨에 따라 일반공모를 거쳐 배정 후에도 미 청약된 잔여주식에 대하여는 대표주관회사가 자기계산으로 잔액인수하게 됩니다. 만약 본 유상증자 청약에서 대량 실권이 발생하여 대표주관회사가 실권주를 인수하게 될 경우 주가에 어떠한 영향을 미칠지는 예상하기 어렵습니다. 다만, 대표주관회사가 당사 주식 인수 후 수익을 확정하기 위해 빠른 시일 내에 인수한 주식을 장내에서 매각하게 된다면 단기적으로 당사 주가에 악영향을 미칠 수 있으며, 대표주관회사가 인수한 주식을 일정 기간 보유하더라도 동 인수 물량이 잠재 매각 물량으로 존재하여 주가 상승에 부담으로 작용할 가능성이 있습니다.
대표주관회사가 최종 실권주를 인수할 경우, 당사는 실권주 인수금액의 16.0%를 추가수수료로 지급하게 됩니다. 이를 고려할 때, 대표주관회사의 실권주 매입단가는 일반청약자들 보다 16.0% 낮은 것과 같은 결과가 초래되어 인수 물량을 단기간에 처분하게 될 소지가 높을 것으로 예상되며 일시적으로 대규모 물량이 출회하여 주가가 하락할 가능성이 있습니다. 실질적으로 유상증자 청약자 및 대표주관회사는 신주상장 2영업일 전부터 입고예정 주식의 매도가 가능합니다. 투자자 여러분께서는 이 점에 유의하시어 투자에 임하시기 바랍니다.
|
다. 주가하락에 따른 발행금액 감소 위험
|
금번 유상증자의 확정발행가액은 1차 발행가액과 2차 발행가액 중 낮은 가액으로 결정됩니다. 다만 「자본시장과 금융투자업에 관한 법률」 제165조의6 및 「증권의 발행 및 공시 등에 관한 규정」 제5-15조의2에 의거하여 1차 발행가액과 2차 발행가액 중 낮은가액이 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격보다 낮은 경우 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격을 확정발행가액으로 합니다. (단, 발행가액이 액면가보다 낮을 경우 액면가를 발행가액으로 합니다.)
일반공모 후 미청약분에 대해서는 그 전부를 대표주관회사가 인수하므로 청약 미달에 따른 위험은 없으나, 주가 하락으로 발행가액이 낮아져 당사가 목표로 하는 규모의 자금을 조달하지 못할 수도 있습니다. 이 경우, 당사의 재무안정성이 부정적인 영향을 받을 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
|
라. 공시서류 정정에 따른 일정 변경 위험
본 공시서류는 공시심사 과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있습니다. |
「자본시장과 금융투자업에 관한 법률」 제120조 3항에 의거하여 본 공시서류의 효력의 발생은 공시서류의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 투자자에게 귀속됩니다.
금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서(분기 및 반기보고서 포함) 및 감사보고서 등 기타 정기 공시사항과 수시 공시사항 등이 전자공시되어 있사오니 투자 의사를 결정하시는 데 본 공시서류 참조하시기 바랍니다.
본 공시서류는 공시 심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행과정에서 일정이 변경될 수도 있으므로 투자자들께서는 투자시 이러한 점을 감안하시기 바랍니다.
|
마. 분석정보의 한계 및 투자판단 관련 위험 금번 유상증자를 통해 취득한 당사의 주식가치가 하락할 수 있습니다. 본 공시서류의 효력발생은 정부가 공시서류의 기재사항이 진실 또는 정확하다는 것을 인정하거나 이 유가증권의 가치를 보증 또는 승인한 것이 아니며, 기재사항은 청약일 이전에 변경될 수 있습니다. 또한 금번 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 투자자께서는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안 되며, 다양한 방면에서 신중한 검토를 병행하여 독자적으로 판단하시기 바랍니다. |
상기 서술한 바와 같이, 당사의 주식가치는 금번 유상증자 실시에 따른 전 과정에서 다양한 영향을 받아 하락할 수 있습니다.
본 공시서류의 효력발생은 정부가 공시서류의 기재사항이 진실 또는 정확하다는것을 인정하거나 이 유가증권의 가치를 보증 또는 승인한 것이 아니며, 기재사항은 청약일 이전에 변경될 수 있습니다. 본 주식을 청약하고자 하는 투자자께서는 투자결정을 하기 전에 본 공시서류의 상기 투자위험요소 뿐만 아니라 다른 부분 또한 주의 깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 합니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 상기 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없습니다. 따라서 투자자께서는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안 되며, 다양한 방면에서 신중한 검토를 병행하여 독자적으로 판단할 필요가 있습니다.
당사는 상기에 기술된 투자위험요소 외에도 불안정한 경제상황 등에 의하여 직·간접적으로 영향을 받을 수 있습니다. 당사의 재무제표는 당사의 재무상태에 영향을 미칠 수 있는 경제상황에 대한 경영자의 현재까지의 평가를 반영하고 있으나, 실제 결과는 현재시점에서의 평가와는 상당히 다를 수 있는 점을 유의하시기 바랍니다.
만일 상기 투자위험요소가 실제로 발생할 경우, 당사의 사업환경과 재무상태, 기타 운영결과에 부정적인 영향을 미칠 수 있습니다. 이에 따른 주가 하락으로 투자자께서는 금번 공모 과정에서 취득하게 되는 주식의 투자금액의 일부 또는 전부를 잃을 수 있습니다.
또한 금번 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 대내외적으로 여러가지 요소들의 영향에 따라 최초에 예측했던 것과 다를 수 있는 점을 유의하시기 바랍니다.
|
바. 집단 소송 제기 위험 당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있으니 이 점 유의하시기 바랍니다. |
「증권관련 집단소송법」 제12조(소송허가 요건)에 따라 50명 이상의 개인이 발행주식총수의 0.01% 이상 보유할 경우 한 명 이상의 대표 당사자가 상기 50인 이상의 당사자들을 대리하여 회사가 발행한 증권의 거래과정에서 발생한 피해에 대하여 소송을 제기할 수 있습니다.
공시서류에서 기재된 잘못된 내용, 잘못된 사업보고서의 공시, 내부자거래에 의한 손해배상청구 및 회계부정으로 인한 손해배상 청구 등이 주요한 소송사유에 포함됩니다. 당사는 향후 이와 같은 집단소송의대상이 되지 않는다고 확신할 수 없으며, 만약 당사에 대하여 집단소송이 제기될 경우 상당한 소송비용이 발생할 수 있음을 유의하시기 바랍니다.
|
사. 유상증자 철회에 따른 위험
|
금번 주주배정 후 실권주 일반공모 유상증자 진행 과정에서 모집 절차의 진행에 중대한 영향을 미칠 만한 사유가 발생하여 당사 혹은 대표주관회사의 판단으로 유상증자가 철회될 수 있습니다.
유상증자 납입 전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회 시점에 따라 권리락에 따른 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있음을 투자자께서는 유의하시기 바랍니다.
|
아. 금융감독기관의 규제 강화에 따른 위험
|
최근 금융감독기관 등의 상장기업에 대한 관리감독기준은 투자자보호 차원에서 엄격해지고 있는 상황이며, 회사가 관련 규정을 위반할 경우 회사 및 회사가 발행한 주식에 대해 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다.
당사는 현재 주권매매정지, 상장폐지, 관리종목 등의 사유에는 해당하지 않지만, 향후 감독기관으로부터 당사가 현재 파악하지 못한 제재가 부과될 경우 주가하락 및 유동성(환금성) 제약 등으로 인해 투자금에 막대한 손실이 발생할 수 있으니 투자자들께서는 관련 규정을 충분히 검토하신 후 투자에 임해주시기 바랍니다.
특히 코스닥시장상장규정 제53조(관리종목), 코스닥시장상장규정 제54조(형식적 상장폐지) 및 제56조(상장적격성 실질심사에 따른 상장폐지) 등의 규정사항에 해당되어 관리종목 지정 및 상장폐지 등이 발생할 위험에 유의하시기 바랍니다.
자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융법규서비스(http://fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
|
자. 차입공매도 유상증자 참여 제한 관련 위험
금융위원회의 공매도 제도개선 관련 「자본시장과 금융투자업에 관한 법률과 시행령」이 개정되어 2021년 4월 6일부터 시행됨에 따라, 주권상장법인이 유상증자 계획을 공시한 이후 발행가격 산정을 위한 대상 거래기간의 마지막 날(발행가격 산정 기산일)까지, 해당 기업의 주식을 공매도 한 자는 증자 참여를 제한하되, 예외적인 경우에만 증자 참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 상기 사항을 위반 시 과징금 등의 제재 조치를 받을 수 있으니, 투자자께서는 이 점 유의하시기 바랍니다. |
주권상장법인이 유상증자 계획을 공시한 이후 해당 기업의 주식을 공매도 한 자는 증자참여를 제한하되, 예외적인 경우 증자참여를 허용하고 있습니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 이와 관련 유상증자 참여가 제한되는 공매도 시점과 증자참여가 허용되는 예외사유를 시행령에서 정하도록 위임하고 있습니다.
시행령에 따르면, 유상증자 계획이 공시된 다음날부터, 발행가격 산정을 위한 대상 거래기간의 마지막날(발행가격 산정 기산일)까지 공매도 한 경우 증자참여가 제한됩니다 (「자본시장과 금융투자업에 관한 법률 시행령」제208조의4 제1항)
다만, 다음의 경우 공매도를 통해 발행가격에 부당한 영향을 미쳤다고 보지 않아 증자참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률 시행령」제208조의4 제2항「금융투자업규정」제6-34조)
ⅰ) 마지막 공매도 이후 발행가격 산정 기산일까지 공매도 주문 수량 이상을 증권시장 정규거래시간에 매수(체결일 기준)
ⅱ) 금융위원회가 정하는 기준을 충족한 독립된 거래단위를 운영하는 법인 내에서 공매도를 하지 않은 거래단위가 증자참여
ⅲ) 시장조성 또는 유동성공급을 위한 거래과정에서 공매도
상기 공매도제도 개선 관련 자본시장법 시행령 시행에 따라, 당사의 주식을 해당 기간 동안 공매도하는 투자자께서는 금번 유상증자 참여가 제한될 수 있음을 유의하시기 바랍니다. 해당 법령과 관련된 자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융법규서비스(http://fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
|
차. 재무제표 작성 기준일 이후 재무상황 변동에 따른 위험
본 공시서류 상 재무제표에 관한 사항은 2024년 1분기 재무제표 (K-IFRS 기준) 작성기준일 이후의 변동을 반영하지 않았습니다. 당사는 금번 유상증자를 진행하는 과정에서 투자 의사결정에 중대한 영향을 미칠 것으로 판단되는 변동사항을 향후에도 상세하게 반영하여 공시할 예정입니다. 그럼에도 불구하고, 당사가 중요하지 않다고 판단하여 기재 및 서술을 생략한 사항 중 당사의 기업가치에 영향을 미칠 만한 사건이 없다고 단정할 수는 없어 주기적이고 면밀한 검토가 필요합니다. |
본 공시서류에 기재된 재무제표에 관한 사항과 감사인의 의견에 관한 사항은 2024년 1분기 재무제표 작성기준일 이후의 변동을 반영하지 않았으므로 투자에 유의하시기 바랍니다.
다만, 본 공시서류에 기재된 재무제표의 작성기준일 이후 본 공시서류 제출일 사이에 발생한 것으로 본 공시서류에 기재된 사항 이외에 자산, 부채, 현금흐름 또는 손익사항에 중대한 변동을 가져오거나 중요한 영향을 미치는 사항은 없습니다.
당사는 금번 유상증자를 진행하는 과정에서 투자 의사결정에 중대한 영향을 미칠 것으로 판단되는 변동사항을 향후에도 상세하게 반영하여 공시할 예정입니다. 그럼에도 불구하고, 당사가 중요하지 않다고 판단하여 기재 및 서술을 생략한 사항 중 당사의 기업가치에 영향을 미칠 만한 사건이 없다고 단정할 수는 없어 주기적이고 면밀한 검토가 필요합니다. 투자자께서는 이 점 유의하시기 바랍니다.
|
카. 개인종합자산관리계좌(ISA) 납입한도에 따른 청약제한 위험
개인종합자산관리계좌(이하 ISA 계좌)는 연간 납입가능한도 제한(연간납입한도 2,000만원, 5년간 최대 1억원까지 납입가능하며 납입한도 이월가능)이 있는 계좌입니다. ISA 계좌를 통한 신주인수권증서 보유자 청약시, 투자자별 유상증자 배정주수에 해당하는 청약증거금 납입금액이 ISA계좌 잔여납입한도를 초과할 경우 유상청약이 제한될 수 있으니, 투자자께서는 이 점 유의하시기 바랍니다. |
개인종합자산관리계좌(이하 ISA 계좌)는 연간 납입가능한도 제한(연간납입한도 2,000만원, 5년간 최대 1억원까지 납입가능하며 납입한도 이월가능)이 있는 계좌입니다. ISA계좌를 통한 신주인수권증서 보유자 청약시, 투자자별 유상증자 배정주수에 해당하는 청약증거금 납입금액이 ISA 계좌 잔여납입한도를 초과할 경우 유상청약이 제한될 수 있으니, 투자자께서는 이 점 유의하시기 바랍니다.
|
타. 기타 투자자 유의사항
당사의 대내외적 경영환경 변화에 따라 당사 실적의 급변동이 있을 경우, 투자원금에 대한 손실이 발생할 수 있으므로, 상기 투자위험요소 및 본 공시서류에 기재된 정보에만 의존하여 투자 판단을 해서는 안되며, 투자자 여러분의 독자적인 판단에 의해야 함을 유의하시어 투자에 임하시기 바랍니다. |
(1) 금번 유상증자 실시로 당사의 주식가치가 향후 하락할 수 있으므로 투자자 여러분들께서는 이 점을 유의하여 주시기 바랍니다.
(2)「자본시장과 금융투자업에 관한 법률」제120조 제3항에 의거하여 본 공시서류의 효력의 발생은 공시서류의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 투자자에게 귀속됩니다.
(3) 본 공시서류의 공시심사 과정에서 기재사항은 청약일 이전에 변경될 수 있고, 일부 내용은 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 시에는 본 공시서류상의 일정에 차질을 가져올 수 있습니다. 또한 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있습니다.
(4) 본 건 공모주식을 청약하고자 하는 투자자들은 투자결정을 하기 전에 본 공시서류의 다른 기재 부분 뿐만 아니라 상기 투자위험요소를 주의 깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 합니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 상기 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 자신의 독자적인 판단에 의해야 합니다.
(5) 당사는 상기에 기술된 투자위험요소 외에도 전반적으로 불안정한 경제상황 등에 의하여 직접적으로 또는 간접적으로 영향을 받을 수 있습니다. 당사의 재무제표는 당사의 재무상태에 영향을 미칠 수 있는 경제상황에 대한 경영자의 현재까지의 평가를 반영하고 있으나, 그 실제결과는 현재시점에서의 평가와는 상당히 다를 수 있는 만큼, 투자자 여러분께서는 이 점을 유의하여 투자에 임하시기 바랍니다.
(6) 만일 상기 투자위험요소가 실제로 발생하는 경우 당사의 사업, 재무상태, 기타 운영결과에 중대한 부정적 영향을 미칠 수 있으며, 이에 따라 투자자가 금번 공모 과정에서 취득하게 되는 당사 주식의 시장가격이 하락하여 투자금액의 일부 또는 전부를 잃게 될 수도 있습니다.
(7) 본건 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 대내외적으로 여러가지 요소들의 영향에 따라 애초에 예측했던 것과 다를 수 있다는 점에 유의해야 합니다.
(8) 금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서(분기 및 반기보고서 포함) 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있으니 투자의사를 결정하시는 데 참조하시기 바랍니다.
이와 같이, 본 건 유상증자를 통해 취득한 당사의 주식 가치는 하락할 수 있으며, 본 공시서류에서 제시된 투자위험요소 및 기타 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 투자자 여러분의 독자적인 판단에 의해야 함을 다시 한번 유의하여 주시기 바랍니다.
| ※ 상기 제반사항을 고려하시어 투자자 제위의 현명한 판단을 바랍니다. 투자자는 본건 공모주식에의 투자 여부를 결정함에 있어서 필요한 경우 스스로 별도의 독립된 자문을 받아야 하며, 이에 따른 투자의 결과에 대하여는 투자자가 책임을 부담합니다. |
IV. 인수인의 의견(분석기관의 평가의견)
| 본 장은 「자본시장과 금융투자업에 관한 법률」 제119조 및 제125조, 금융감독원의 '금융투자회사의 기업실사 모범규준'에 따라 본건 공모 지분증권 인수인이 당해 공모 지분증권에 대한 의견을 기재하고 있는 부분입니다. 따라서 본 장의 작성 주체는 공동대표주관회사인 한국투자증권(주) 및 케이비증권(주)이며, 발행회사인 에이치엘비생명과학(주)는 "동사"로 기재였습니다. 본 장에 기재된 분석의견 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 여러가지 요소들의 영향에 따라 예측했던 것과 다를 수 있다는 점을 유의하시기 바랍니다. |
1. 분석기관
| 구 분 | 증 권 회 사 | |
| 회 사 명 | 고 유 번 호 | |
| 공동대표주관회사 | 한국투자증권(주) | 00160144 |
| 공동대표주관회사 | 케이비증권(주) | 00164876 |
2. 분석의 개요
공동대표주관회사인 및 한국투자증권(주) 및 케이비증권(주)(이하 "공동대표주관회사"라 합니다.)는「자본시장과 금융투자업에 관한 법률」제71조 및 동법 시행령 제68조에 의거 공정한 거래질서 확립과 투자자 보호를 위해 다수인을 상대로 한 모집·매출 등에 관여하는 인수회사로서, 발행인이 제출하는 증권신고서 등에 허위의 기재나 중요한 사항의 누락을 방지하는데 필요한 적절한 주의를 기울였습니다.
공동대표주관회사는 인수 또는 모집·매출의 주선업무를 수행함에 있어 적절한 주의의무를 다하기 위해 금융감독원이 제정한 '금융투자회사의 기업실사(Due Diligence) 모범규준'(이하 "모범규준"이라 한다)의 내용을 내부 규정에 반영하여 2012년 2월 1일부터 제출되는 지분증권, 채무증권 증권신고서를 대상(자산유동화증권 등 제외)으로 기업실사를 의무적으로 수행하도록 규정하고 있습니다.
다만, '모범규준' 제3조 제②항에 따라 발행회사의 재무 및 영업현황, 사업 환경, 투자위험, 인수 형태, 신용평가등급 등을 감안하여 강화하거나, 완화할 수 있으며, 동조 제⑤항에 따르면 금융투자회사의 이사회나 리스크관리위원회의 의사결정을 거쳐 '모범규준'의 내용(실사수준)을 생략하거나 강화 또는 완화 적용할 수 있도록 허용하였는 바, 주관회사는 지분증권의 인수 또는 모집·매출의 주선업무를 수행함에 있어서 지분증권의 특성 및 발행회사의 일정요건 충족여부 등에 따라 기업실사 수준을 완화하여 적용할 수 있도록 규정하고 있습니다.
본 지분증권은 공동대표주관회사의 내부 규정상 기업실사 기준을 적용하여 기업실사 업무를 수행하였습니다.
| 「금융투자회사의 기업실사 모범규준」 제3조(적용범위 등) ①이 규준은 법 제119조제3항의 규정에 의한 증권신고서 및 법 제122조의 규정에 의한 정정신고서를 제출하는 경우에 적용하며, 영업의 실체가 있는 발행회사가 제출하는 지분증권, 채무증권 증권신고서를 대상으로 하고 자산유동화증권 등은 적용대상에서 제외된다. ②이 규준은 주간회사가 업무수행 중 참고해야 할 기본적인 지침으로 발행회사의 재무 및 영업 현황, 사업 환경, 투자위험, 인수 형태 등을 감안하여 강화하거나 완화하는 등 탄력적으로 운용할 수 있다. ③기업공개의 경우 기업공개 실사절차의 특성을 감안하여 이 규준의 내용중 한국거래소의 상장심사지침 등에서 의무사항으로 규정하고 있는 내용과 중복되는 부분에 대해서는 이를 생략하거나 완화할 수 있다. ④채무증권의 경우 i)보증유무, 상환조건(만기, 옵션유무), 특약 등 해당 사채의 특성, ii)법 제119조제2항에서 규정하고 있는 일괄신고서에 의한 발행인지 여부, iii)발행회사가 시행령 제121조제6항의 요건을 충족하고 있는지 여부, iv)해당 사채권에 대한 신용평가등급(외부 및 내부) 등을 감안하여 합리적인 기준에 따라 이 규준을 완화할 수 있다. ⑤제2항 내지 제4항에 따라 이 규준을 생략하거나 강화 또는 완화하는 경우에는 이사회나 리스크관리위원회(이하 ‘리스크관리위원회 등’)의 의사결정을 거쳐야 한다. |
분석의견의 상세한 내용은 동 증권신고서에 첨부되어 있는 기업실사 부분을 참고하시기 바랍니다.
3. 기업실사 일정 및 주요 내용
| 일자 | 실사내용 |
| 2024.02.06 ~ 2024.02.23 |
* 발행회사 초도 방문 - 발행회사의 유상증자 의사 확인 - 자금조달 희망금액 등 발행회사 의견 청취 * 발행회사의 유상증자 방식결정 협의 * 유상증자 일정 협의 및 확정 * 유상증자를 위한 사전 준비사항 및 진행절차 설명 - 발행가 산정 및 세부일정 설명 * 세부 증자관련 논의 - 유상증자 방식 결정 및 대주주 증자 참여 논의 * 유상증자 진행에 대한 질의/응답 * 실사 사전요청자료 송부 |
| 2024.02.24 ~ 2024.03.08 |
* 증자리스크 검토 - 발행시장 상황, 자금조달규모 적정성, 공모가액 희망 할인율 * 발행사와의 협의 - 발행가액 산정방식, 발행일정, 발행규모, 인수수수료 협의 * 기업실사 진행 및 추가자료 요청 - 기업실사 관련 자료요청 및 절차에 대한 설명 - 기업실사 관련 Q&A * 이사회 등 상법 절차 및 정관 등 검토 * 투자위험요소 실사 1) 사업위험관련 실사 - 기존사업 및 신규사업에 대한 세부사항 등 체크 2) 회사위험관련 실사 - 재무관련 위험 및 우발채무 등의 위험요소 등 체크 3) 기타위험관련 실사 - 주가 희석화관련 위험 등 체크 * 담당자 인터뷰 - 회사개요, 사업의 내용, 주요 재무적 이슈 확인 - 자금사용 계획 파악 - 향후 사업추진계획 및 발행회사의 비전 검토 |
| 2024.03.09 ~ 2024.03.21 |
* 증권신고서 작성 및 조언 * 이사회의사록 등 검토 * 인수계약서 작성 및 체결 * 증권신고서 인수인의 의견 완료 * 첨부서류 등 검토 * 증권신고서 업데이트 |
| 2024.03.22 ~ 2024.05.23 |
* 금융감독원의 정정요구제출에 따른 증권신고서 작성 가이드 및 추가자료 작성 |
4. 기업실사 참여자
| [대표주관회사] |
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 | 참여기간 | 주요 경력 |
| 한국투자증권(주) | IB2본부 | 김성열 | 본부장 | 기업실사 총괄 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 28년 |
| ECM1부 | 김현서 | 이사 | 기업실사 책임 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 22년 | |
| ECM1부 | 박상욱 | 팀장 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 14년 | |
| ECM1부 | 정인묵 | 과장 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 7년 | |
| ECM1부 | 임주형 | 대리 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 4년 | |
| ECM1부 | 구찬웅 | 주임 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 1년 | |
| 케이비증권(주) | SME금융부 | 이경재 | 이사 | 기업실사 총괄 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 24년 |
| SME금융부 | 김자환 | 이사 | 기업실사 책임 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 23년 | |
| SME금융부 | 이형준 | 팀장 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 9년 | |
| SME금융부 | 박진혁 | 대리 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 6년 | |
| SME금융부 | 박성윤 | 주임 | 기업실사 실무 | 2024년 02월 06일 ~ 2024년 05월 23일 |
기업금융업무 등 2년 |
| [발행회사] |
| 소속 | 부서 | 성명 | 직급 | 담당업무 |
| 에이치엘비생명과학(주) | 경영전략본부 | 이근식 | 상무이사 | 발행업무 총괄 |
| 경영기획팀 | 안동환 | 과장 | 발행업무 |
5. 기업실사 세부 항목 및 점검 결과
- 동 증권신고서에 첨부되어 있는 기업실사 보고서를 참조해 주시기 바랍니다.
6. 종합의견
가. 공동대표주관회사인 한국투자증권(주) 및 케이비증권(주)는 에이치엘비생명과확(주)가 2024년 03월 21일 이사회에서 결의한 보통주식 11,005,125주에 대한 주주배정 후 실권주 일반공모 증자를 잔액인수함에 있어 에이치엘비생명과학(주)에 대하여 다음과 같이 평가합니다.
| 긍정적요인 | ▶ 전 세계 글로벌 체외 진단(IVD) 시장은 2021년 982억 달러에서 연평균 성장률 2.9%로 증가하여, 2026년에는 1,131억 달러에 이를 것으로 전망됩니다. COVID-19로 인해 글로벌 체외 진단 시장은 급격하게 성장하였으며, 기존 또는 신규 감염 질병 진단을 위한 차세대 체외 진단의 R&D 확장으로 앞으로도 성장 추세는 꾸준히 이어질 것으로 예상됩니다. 동사는 150여 종의 제품개발 성과의 근간인 기술력과 품질 시스템을 바탕으로 의료기기 분야를 비롯한 다양한 품목군을 개발, 연구 중에 있으며 전사적 품질 경영 시스템 운영을 통해 안정성, 유효성 및 GMP, ISO13485 기준의 품질이 확보된 제품을 생산하고 있습니다. 이에 따라 높은 수익률을 달성할 가능성이 있습니다. ▶ 세계 의약품 시장은 고령화에 따른 만성 질환자 수의 증가, 소득 수준 향상에 따라 의약품 시장의 성장이 급격하게 이루어지고 있는 중국, 인도, 중남미 등의 제약 신흥 국가들의 의료비 지출증가 등으로 시장 규모는 역대 최대치를 경신했습니다. 동사의 종속회사 HLB셀은 바이오의약품 및 생체적합성 의료기기 개발 기술을 중심으로 ①바이오인공간 ②지혈제 ③인체세포외기질 3개 분야의 주요 파이프라인을 갖고 있으며, 관련 특허 등을 활용하여 연구, 개발 중에 있습니다. 또한 동사의 계열회사 Elevar Therapeutics,Inc.의 Rivoceranib(구. Apatinib Mesylate)는 위암(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국), 간암 (2021년 11월 미국식품의약국), 선양낭성암 (2021년 2월 미국식품의약국) 대상으로 희귀의약품 지정을 받아 임상종료 후 시판허가에 대한 심사의 신속화, 수수료 감면 등의 혜택과 최소 8년(2029년)에서 최대 13년(2034년) 동안 독점 판매할 수 있습니다. 동사의 계열회사 HLB생명과학R&D는 2022년 4월 1일 신약개발 전문성 강화를 위해 설립되었습니다.현재, 항암 파이프라인 신규 구축을 위해 초기 비임상 단계 물질을 도입(G2M Project)하였으며 한국을 포함한 글로벌 주요 국가에 대한 특허권과 물질의 생산, 판매 그리고 향후 기술이전에 대한 권리 등의 일체의 권리를 확보했습니다. ▶ 2022년 전체 의약품 유통금액은 88.9조원으로 전년대비 10.2%(8.2조원)증가하였으며, 최근 3년간 연평균 7.8%증가('20년 약 75.9조원, '21년 약 80.6조원, '22년 약 88.9조원)한 것으로 나타났습니다. 2022년 의약품 유통금액 88.9조원은 중 49.2조원('21년도 42조)은 도매상 유통금액으로 전체 시장의 55.3%를 차지하고 있습니다. 동사의 종속회사 신화어드밴스는 무차입경영의 우수한 재무상태와 풍부한 유동성을 보유하고 있으며, 20여년 이상 수행하며 다져진 영업력을 바탕으로 신규거래처를 꾸준히 확보하였습니다. 자사 영업 조직과 물류센터를 통한 안정적 매출과 함께 제약업체 및 도매업체와의 전략적 제휴로 품목 및 가격 경쟁력에 우위를 선점하였습니다. 향후 지역 인구 및 소득, 물류 효율성, 주변 상권 및 원외 시장 분석 등의 데이터를 활용하여 표적시장 선정을 통해 안정적인 성장을 이룰 것입니다. |
| 부정적요인 | ▶ 연구개발을 통한 신약 개발은 일반적으로 막대한 연구개발비와 장기에 걸친 투자 및 연구기간이 소요되며, 신약 개발에 성공한다 하더라도 기투자된 금액과 시간을 상쇄할 수 있을 정도의 수익 창출이 가능할지 여부는 불확실합니다. ▶ 동사는 최근 4개년 영업손실 및 당기순손실 구조가 지속 되고 있습니다. 2020년 약 558억원, 2021년 약 493억원, 2022년 약 544억원, 2023년 약 59억원의 당기순손실을 기록했습니다.향후 경쟁 심화로 인한 의약품 유통 사업 매출 감소, 바이오 사업 임상시험 지연 및 비용 증가 등으로 인해 당사의 수익은 더욱 악화될 수 있습니다. ▶ 동사의 주요 재무안정성 지표 추이를 살펴보면, 연결기준 부채비율은 2020년말 13.7%, 2021년말 9.8%, 2022년말 74.4% 2023년말 83.2% 로 계속해서 증가하였습니다. 향후에도 계속되는 영업실적의 부진, 임상 지연 등으로 인한 바이오 사업 매출 미실현 등에 따른 투자 등에 따라 차입금이 증가할 가능성이 존재하며, 지속적으로 차입을 할 경우 당사의 재무안정성이 악화될 가능성이 존재합니다. ▶ 동사는 2020년을 제외하고 최근 지속적으로 영업활동현금유출이 발생하고 있습니다. 2020년 약 2,010백만원으로 영업활동현금유입이 발생하였으나, 2021년 약 14,084백만원, 2022년 약 29,744백만원, 2023년 약 10,016백만원의 영업활동현금유출을 기록했습니다. 동사의 영업활동현금흐름 유출의 주된 원인은 실적부진이며 영업활동현금흐름과 투자활동현금흐름의 유출을 재무활동(외부차입 등)을 통하여 충당하고 있습니다. 그러나 바이오사업 매출 실현 지연으로 인한 영업활동현금 유출 지속 및 국내 경기의 악화, 금융시장의 부진 등으로 재무활동현금 유입이 원활하지 못할 경우 당사는 유동성 압박에 시달릴 수 있습니다. ▶ 동사는 현재 신규사업 진출을 위한 타법인 인수로 재무구조가 크게 변동하고 있으며 이에 따라 재무안정성 지표 또한 같이 변동하고 있습니다. 이처럼 동사의 영업상황과 더불어 신규사업 진출을 위한 투자가 지속될 경우 재무안정성이 악화될 수 있습니다. ▶동사는 최대주주인 에이치비엘비(주)의 주가의 영향을 많이 받고 있습니다.에이치엘비 주가에는 리보세라닙과 캄렐리주맙 병용요법 간암 1차 치료제가 미치는 영향이 큰 상황에서 2024년 5월 FDA로부터 일부 미비한 사항에 대해 수정 또는 보완을 요청하는 CRL을 수령하였습니다. 이와 관련하여 항서제약의 CMC(의약품 생산시설 실사) 보완 및 BIMO Inspection(임상사이트 실사) 완료 시기에 대한 불확실성이 있습니다. 또한 동사는 리보세라닙에 대한 국내 전용실시권과 일본, 유럽에 대한 수익 지분(14.5%)을 보유하고 있어 FDA 재승인 신청 후 판매승인 시점이 지연될 경우 동사 및 동사 관계회사의 수익성과 주가에도 부정적으로 작용할 가능성이 있습니다. |
| 자금조달의 필요성 |
▶ 동사는 금번 유상증자를 통해 조달하는 자금을 시설자금, 운영자금, 채무상환자금 및 기타자금으로 활용할 계획입니다. ▶ 금번 유상증자를 통해 조달한 자금의 세부사용 내역은 "Ⅴ. 자금의 사용목적"을 참고하시기 바랍니다. |
나. 공동대표주관회사는 에이치엘비생명과학(주)가 제출한 자료와 객관적으로 정확하고 신뢰할 수 있다고 믿어지는 자료를 중심으로 실사를 수행하였으며, 객관적인 입장에서 공정을 기하기 위하여 최선의 노력을 다하였습니다.
다. 공동대표주관회사는 상기 실사를 통해 제공받는 자료들로부터 도출된 결과나 오류, 누락 등에 대하여 책임지지 않으며, 인간적 또는 기계적, 기타 그 외의 다른 요인에 의한 오류발생 가능성으로 인해 본 평가 내용에 대해 명시적으로 혹은 묵시적으로도 증명이나 서명 또는 보증 및 단언을 할 수 없습니다.
라. 동사의 금번 유상증자는 국내외 거시경제 변수 변화로 투자수익에 대한 확실성이 저하될 수 있습니다. 투자자 여러분께서는 상기 검토결과는 물론 동 증권신고서 및 투자설명서에 기재된 동사의 회사 전반에 걸친 현황 및 재무상의 위험과 산업 및 영업상의 위험요인 등을 감안하시어 투자에 유의하시기 바랍니다.
또한, 공동대표주관회사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 동 증권신고서 및 투자설명서에 기재하지 않은 사항이라 하더라도 동사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자께서는 동 증권신고서 및 투자설명서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 독자적이고도 세밀한 판단에 의해 투자결정을 하시기 바랍니다.
| 2024년 05월 23일 |
| 공동대표주관회사 : 한국투자증권 주식회사 |
| 대표이사 김 성 환 |
| 공동대표주관회사 : 케이비증권 주식회사 |
| 대표이사 김 성 현 |
V. 자금의 사용목적
1. 모집 또는 매출에 의한 자금조달 내역
가. 자금조달금액
| (단위 : 원) |
| 구 분 | 금 액 |
|---|---|
| 모집 또는 매출총액(주1) | 130,850,936,250 |
| 발행제비용(주2) | 1,422,534,823 |
| 순 수 입 금 [ (1)-(2) ] | 129,428,401,427 |
| 주1) | 상기 금액은 1차발행가액을 기준으로 산정한 금액으로 모집가액 확정시 변경될 수 있습니다. |
| 주2) | 상기 모집총액은 우선적으로 하단에 기재된 자금의 사용 목적에 따라 사용할 예정입니다. |
| 주3) | 발행제비용은 공모금액 및 실권규모에 따라 변경될 수 있으며, 상기 기재 금액은 청약 초과로 인하여 실권이 발생하지 않은 상황을 가정하여 산정되었습니다. 또한 상장수수료는 상장신청일 직전일 주가에 따라 변동될 수 있습니다. |
나. 발행제비용의 내역
| (단위 : 원) |
| 구분 | 금액 | 비고 |
|---|---|---|
| 발행분담금 | 23,553,160 | 모집총액의 0.018% (10원 미만 절사) |
| 대표주관수수료 | 261,701,873 | |
| 인수수수료 | 1,046,807,490 | 기본수수료: 최종 모집금액의 0.8% 실권수수료: 16.0%(실권수수료 미포함) |
| 표준코드발급수수료 | 10,000 | 신주인수권증서(R) 건당 10,000원 |
| 보통주 추가상장수수료 |
13,050,000 | 910만원+1,000억원 초과금액의 10억원당 5만원(코스닥시장상장규정 시행세칙 별표 14) |
| 주식발행등록수수료 (신주인수권 및 주권) |
1,000,000 | 1,000주당 300원 (주식 및 신주인수권증서 각각 별도 징수, 수수료 건당 상한 50만원 및 하한 4천원)(주식·사채 등의 전자등록업무규정 시행세칙 별표) |
| 등록면허세 | 22,010,250 | 증자 자본금의 0.40% (지방세법 제28조, 10원 미만 절사) |
| 지방교육세 | 4,402,050 | 등록면허세의 20%(지방세법 제151조, 10원 미만 절사) |
| 기타비용 | 50,000,000 | 투자설명서, 통지서 인쇄 및 발송비 등 |
| 합계 | 1,422,534,823 | - |
| 주1) | 상기 금액은 1차발행가액을 기준으로 산정한 금액입니다. |
| 주2) | 발행제비용은 공모금액 및 상장신청일 직전일 한국거래소에서 거래되는 당사의 보통주식 종가, 유관기관 정책 등에 따라 변동될 수 있습니다. |
| 주3) | 기타비용은 예상금액으로 변동될 수 있습니다. |
2. 자금의 사용목적
가. 자금의 사용목적
당사는 금번 유상증자를 통해 조달하는 자금을 1) 시설자금, 2) 운영자금, 3) 채무상환자금 및 4) 기타 자금으로 사용할 계획이며, 공모자금의 세부 사용 계획은 아래와 같습니다.
| (기준일 : | 2024년 05월 07일 | ) | (단위 : 원) |
| 시설자금 | 영업양수 자금 |
운영자금 | 채무상환 자금 |
타법인증권 취득자금 |
기타 | 계 |
|---|---|---|---|---|---|---|
| 6,000,000,000 | - | 25,205,936,250 | 98,145,000,000 | - | 1,500,000,000 | 130,850,936,250 |
| 주1) 상기 금액은 1차발행가액을 기준으로 산정한 금액으로 모집가액 확정시 변경될 수 있습니다. |
| 주2) 금번 발행과 관련된 발행제비용은 당사의 자체자금으로 충당할 예정입니다. |
| 주3) 부족자금은 당사 자체자금을 활용할 예정입니다 |
나. 자금의 세부 사용내역
| [유상증자 자금사용의 개요] |
| (단위 : 백만원) |
| 구분 | 적요 | 사용(예정) 시기 | 합계 | 우선순위 | ||||
|---|---|---|---|---|---|---|---|---|
| 2024년 | 2025년 | |||||||
| 운영자금 | R&D | 바이오 사업부 | 임상 | 리보세라닙 | 2,200 | 4,400 | 6,600 | 2 |
| 비임상 | G2M | 750 | 800 | 1,550 | ||||
| CDK | 2,700 | 2,300 | 5,000 | |||||
| 칸나비노이드 | 150 | 350 | 500 | |||||
| 의료용대마 | 160 | 200 | 360 | |||||
| 리보세라닙 | 150 | 150 | 300 | |||||
| 신사업개발 | 신규물질 도입 | 3,000 | 5,000 | 8,000 | ||||
| 특허비용 | 연구자 임상 | 60 | 150 | 210 | ||||
| 연구개발비 | 재료비, 인건비 등 판관비 | 723 | 1,963 | 2,686 | ||||
| 운영 | 메디케어/ 의료기기사업부 |
메디케어 및 의료기기사업부 원재료 | - | - | - | |||
| 메디케어사업부 | 메디서플라이 유통사업 운영 | - | - | - | ||||
| 전체 사업부 | 급여, 지급수수료 등 판관비 | - | - | - | ||||
| 운영자금 합계 | 9,893 | 15,313 | 25,206 | |||||
| 채무상환자금 | 단기차입금 | 천안공장 담보 | 1,150 | - | 1,150 | 1 | ||
| 진위공장 담보 | 9,070 | - | 9,070 | |||||
| 장기차입금 | 안성2공장 담보 | 4,800 | - | 4,800 | ||||
| 통탄엠타워 담보 | 3,125 | - | 3,125 | |||||
| 주식담보대출 | 한국투자증권 | 20,000 | - | 20,000 | ||||
| 제9회차 신주인수권부사채 | 신주인수권부사채 조기상환 | 60,000 | - | 60,000 | ||||
| 채무상환자금 합계 | 98,145 | - | 98,145 | |||||
| 시설자금 | HLB에너지(종속) | 소각로 증설 | 5,431 | 569 | 6,000 | 3 | ||
| 시설자금 합계 | 5,431 | 569 | 6,000 | |||||
| 기타 | 수수료 | 1,500 | - | 1,500 | - | |||
| 총 합 계 | 114,969 | 15,882 | 130,851 | |||||
| 출처: 당사 제공 자료 |
(1) 운영자금
당사는 금번 유상증자 자금 중 약 252억원을 운영자금으로 바이오사업부의 파이프라인 임상비용, 신사업 개발 및 특허비용 등으로 R&D 투자에 사용할 예정입니다. 당사의 바이오개발사업부는 상기 운영자금을 바탕으로 향후 리보세라닙 임상비용 및 신규 항암제 발굴 중심으로 운영할 계획 중에 있습니다. 바이오개발사업부의 운영자금 상세 사용 예정 내역은 하기와 같습니다.
| [바이오개발사업 R&D 자금 사용 계획] |
| (단위 : 백만원) |
| 구분 | 단계 | 사용(예정) 시기 | 합 계 | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 2024년 | 2025년 | |||||||||
| 3Q | 4Q | 1Q | 2Q | 3Q | 4Q | |||||
| 임상 | 리보세라닙 | 간암 (1차 병용요법) |
품목허가 | 75 | 75 | 75 | 75 | 300 | ||
| 선양낭성암종 (1/2차 단일요법) |
품목허가 | 50 | 50 | 25 | 25 | 25 | 25 | 200 | ||
| 적응증 추가 임상 | 임상 | - | - | - | 1,000 | 1,000 | 1,000 | 3,000 | ||
| 동물용항암제 | 임상 | 275 | 275 | 10 | 210 | 70 | 260 | 1,100 | ||
| 연주주 주도 임상 | 임상 | 700 | 700 | 150 | 150 | 150 | 150 | 2,000 | ||
| 소 계 | 1,100 | 1,100 | 260 | 1,460 | 1,245 | 1,435 | 6,600 | |||
| 비임상 | G2M | 독성시험, IND 진입 등 |
탐색 | 375 | 375 | 200 | 200 | 200 | 200 | 1,550 |
| CDK | 약물 스크리닝 등 | 탐색 | 900 | 1,800 | 170 | 170 | 170 | 1,790 | 5,000 | |
| 칸나비노이드 | 약물 스크리닝 등 | 탐색 | 75 | 75 | 85 | 85 | 90 | 90 | 500 | |
| 의료용 대마 | 시생산, 동등성 평가 등 |
제형연구 | 60 | 100 | - | 100 | - | 100 | 360 | |
| 리보세라닙 | 병용 약물 탐색 | 탐색 | - | 150 | - | - | 150 | - | 300 | |
| 소 계 | 1,410 | 2,500 | 455 | 555 | 610 | 2,180 | 7,710 | |||
| 기타 | 신사업개발 | 신규물질도입 | - | 1,000 | 2,000 | - | 2,000 | - | 3,000 | 8,000 |
| 특허비용 | 특허출원 및 유지비용 |
- | 40 | 20 | 20 | 20 | 40 | 70 | 210 | |
| 연구개발비 | 재료비, 인건비 등 | - | 216 | 636 | 253 | 276 | 365 | 940 | 2,686 | |
| 소 계 | 1,256 | 2,656 | 273 | 2,296 | 405 | 4,010 | 10,896 | |||
| 합 계 | 3,766 | 6,256 | 988 | 4,311 | 2,260 | 7,625 | 25,206 | |||
| 출처: 당사 제공 자료 |
당사는 우수한 제약/바이오 인력과 신약개발 관련 글로벌 네트워크를 갖추었습니다. "글로벌 종합 신약 플랫폼"을 기반으로 신약 개발 선도 기업으로 성장할계획입니다. 증권신고서 제출일 현재 당사가 연구개발 진행 중인 파이프라인 현황은 아래와 같습니다.
※ 파이프라인 개발현황
현재 당사 및 종속기업이 보유한 파이프라인 연구개발 진행 중인 연구개발(Elevar Therapeutics, Inc.주도 글로벌 임상 포함) 현황은 다음과 같습니다.
 |
|
파이프라인 개발현황 |
|
품 목 |
적응증 |
임상시작일 |
현재 진행단계 |
||
|---|---|---|---|---|---|
|
단계(국가) |
승인일 |
비 고 | |||
| 리보세라닙 (Rivoceranib) [Elevar Therapeutics, Inc.주도 글로벌 임상 포함] |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안정성평가 완료 |
|
위암 (3차/4차 단일요법) |
2017년 |
임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
|
|
위암 (1차 병용요법) |
2021년 |
임상2상 |
2021년 09월 (임상2상 승인일) |
임상 진행 중 | |
|
간암 (1차 병용요법) |
2019년 |
임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
- 임상 종료, 22년 9월 초록 발표(1차 평가 지표 만족) - 23년 5월 미국 FDA에 NDA Submission 완료 - 24년 5월 미국 FDA 수정 보완 요구(CRL 수령) |
|
|
선양낭성암종 (1/2차 단일요법) |
2020년 |
임상2상 |
2020년 4월 (임상2상 개시일) |
임상 2상 종료 6월 초록 발표 |
|
|
위암 (2차 병용요법) |
2018년 |
임상2상 |
2018년 10월 (임상1상 개시일) |
임상 종료 22년 결과 발표 |
|
|
대장암 (3차 병용요법) |
2019년 |
임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 종료 |
|
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상 진행 중 (농림축산검역본부) |
|
| 파이로티닙 (Pyrotinib) |
전이성 유방암 | 2023년 | 임상3상 (한국) |
2023년 03월 (임상계획 승인) |
임상3상 진행 중 |
| 비소세포폐암 | 2020년 | 임상3상 (전세계 13개국) |
2020년 (임상계획 승인) |
임상3상 진행 중 | |
|
HLS221-N01 G2M 억제제 |
폐암 유방암 대장암 췌장암 |
- |
비임상시험 단계 |
- |
비임상평가 진행 중 |
|
HLS222-N01 Cannabinoids derivatives |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
|
HLS232-N01 CDK 억제제 |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
|
HLS231-G01 의료용 대마 |
뇌전증 | - | 탐색 단계 | - | 제형 연구 중 |
| 출처: 당사 제공 자료 |
(삭제)
(2) 채무상환자금 상세 내역
당사의 연결기준 전체 차입금 규모는 2021년 35억원, 2022년 1,445억원, 2023년 1,652억원, 2024년 1분기 1,716억원을 기록하며 최근 큰폭으로 증가했습니다. 이는 신규사업 확장 및 운영자금 확보를 위한 전환사채, 신주인권부사채 발행이 기인했습니다. 이에 따라 차입금의존도 또한 2021년 1.3%에서 2022년 35.1%, 2023년 39.0%, 2024년 1분기 27.3%로 상승했습니다. 이와 같이 차입금 증가가 계속될 경우 유동성을 포함해 당사 재무 안정성에 일부 부담으로 작용할 수 있는 가능성이 존재하여 당사는 금번 유상증자 조달 자금 중 약 981억원을 차입금을 상환하는데 사용할 계획입니다.
| [연결기준 주요 재무안정성 지표 추이] |
| (단위: 백만원) |
| 구분 | 2024년 1분기 | 2023년 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|---|
| 자산총계 | 629,554 | 423,764 | 411,790 | 270,799 | 327,197 |
| 부채총계 | 196,711 | 192,551 | 175,724 | 24,188 | 39,453 |
| 자본총계 | 432,843 | 231,213 | 236,067 | 246,612 | 287,744 |
| 부채비율 | 45.45% | 83.28% | 74.44% | 9.81% | 13.71% |
| 총차입금 | 171,563 | 165,231 | 144,496 | 3,500 | 10,734 |
| 차입금의존도 | 27.3% | 39.0% | 35.1% | 1.3% | 3.3% |
| 출처: 당사 각 사업년도 및 분기 보고서 |
당사는 금번 유상증자 납입 자금 중 채무상환자금으로 1) 제9회 신주인수권부사채 상환자금, 2) 주식담보대출 상환자금, 3) 은행 차입금 상환자금으로 자금을 사용할 예정입니다. 제9회 신주인수권부사채의 미상환잔액은 신주배정기준일 기준 약 804억원으로 최초 조기상환일은 2024년 6월 15일입니다. 이는 금번 유상증자 자금 납입 전 상환 요청 금액에 대해서는 브릿지론으로 상환하고 금번 유상증자 자금으로 브릿지론을 상환할 예정입니다. 당사의 미상환 전환사채 및 신주인수권부사채 발행현황은 아래와 같습니다.
| [당사 미상환 전환사채 및 신주인수권부사채 내역] |
| (단위 : 백만원) |
|
구분 |
회차 |
납입일 |
최초 조기상환일 |
만기일 |
사용용도 |
조달금액 |
미상환잔액 |
|---|---|---|---|---|---|---|---|
|
사모 |
제10회 전환사채 |
2022-07-01 |
2024-07-01 |
2027-07-01 |
타법인 증권 취득자금 |
45,000 |
- |
|
제11회 전환사채 |
2023-07-04 |
2025-07-04 |
2028-07-04 |
운영자금 |
8,300 |
8,300 |
|
| 제12회 전환사채 | 2023-11-07 | 2025-07-07 | 2027-07-01 | 채무상환자금 | 28,800 | 28,800 | |
|
공모 |
제9회 신주인수권부사채 |
2022-06-15 |
2024-06-15 |
2025-06-15 |
운영자금 및 |
100,000 |
80,374 |
| 합 계 | 182,100 | 117,474 | |||||
| 주1) 미상환 잔액은 신주배정기준일(2024.05.10) 기준 주2) 제10회차 전환사채 2024.03.29 기준, 미상환사채 잔액 모두 전환청구 하였습니다. |
당사는 한국투자증권으로부터 2024년 1월 30일 HLB(주) 보통주 792,394주를 담보로 200억원을 대출 받았으며, 이는 금번 유상증자를 통해 200억원 모두 상환 예정입니다.
| [주식담보대출 내역] |
| 구분 | 대출기관 | 대출실행일 | 대출만기일 | 대출금액 | 대출금리 | 담보주식 |
|---|---|---|---|---|---|---|
| 주식담보대출 | 한국투자증권 | 2024-01-30 | 2025-01-30 | 200억원 | 4.50% | HLB㈜ 보통주 792,394주(담보비율: 250%) |
| 출처: 당사 제공 자료 |
당사가 은행으로부터 차입한 차입금 상세 내역은 아래와 같습니다.
| [당사 연결기준 단기차입금 상세 내역] |
| (단위 : 천원) |
| 구분 | 차입처 | 이자율(%) | 만기일 | 2024년 1분기 | 2023년말 |
|---|---|---|---|---|---|
| 시설자금 | 우리은행 | 5.96 | 2025-03-20 | 1,150,000 | 1,150,000 |
| 시설자금 | 국민은행 | 5.14 | 2024-08-16 | 5,000,000 | 5,000,000 |
| 시설자금 | 국민은행 | 5.14 | 2024-08-20 | 4,070,000 | 4,070,000 |
| 주식담보대출 | 한국투자증권 | 4.5 | 2025-01-30 | 20,000,000 | - |
| 소 계 | 30,220,000 | 10,220,000 | |||
| 차감 : 현재가치할인차금 | (334,074) | - | |||
| 차감잔액 | 29,885,926 | 10,220,000 | |||
| 출처 : 당사 분기보고서 |
| [당사 연결기준 장기차입금 상세 내역] |
| (단위 : 천원) |
| 구분 | 차입처 | 이자율(%) | 만기일 | 2024년 1분기 | 2023년말 |
|---|---|---|---|---|---|
| 시설자금 | 국민은행 | 4.98 | 2025-01-16 | 1,560,000 | 1,560,000 |
| 시설자금 | 우리은행 | 5.36 | 2025-03-31 | 4,800,000 | 4,800,000 |
| 온렌딩대출 | 하나은행 | 4.96 | 2030-03-15 | 3,000,000 | 3,125,000 |
| 시설자금 | 산업은행 | 4.21 | 2032-01-17 | 10,000,000 | 10,000,000 |
| 시설자금 | 국민은행 | 4.83 | 2024-08-20 | 5,000,000 | 5,000,000 |
| 시설자금 | 국민은행 | 3.8 | 2024-09-30 | 1,560,000 | 1,560,000 |
| 시설자금대출 | 기업은행 | 4.545 | 2028-09-30 | 50,000 | 50,000 |
| 시설자금대출 | 기업은행 | 2.32 | 2033-09-30 | 3,750,000 | 2,520,000 |
| 소 계 | 29,720,000 | 28,615,000 | |||
| 차감 : 유동성대체 | (13,420,000) | (7,060,000) | |||
| 차감잔액 | 16,300,000 | 21,555,000 | |||
| 출처 : 당사 분기보고서 |
당사는 금번 유상증자를 통해 은행 차입금 중 만기 및 금리를 고려하여 아래와 같이 상환 예정입니다.
| [은행 차입금 상환 세부내역] |
| (단위 : 백만원) |
| 구분 | 담보자산 | 제공처(은행) | 사용예정 시기 | 금액 |
|---|---|---|---|---|
| 단기차입금 | 천안공장 | 우리은행 | 2024년 9월 | 1,150 |
| 단기차입금 | 진위공장 | 국민은행 | 2024년 8월 | 5,000 |
| 단기차입금 | 진위공장 | 국민은행 | 2024년 8월 | 4,070 |
| 장기차입금 | 통탄엠타워 | 하나은행 | 2024년 3월 | 3,125 |
| 장기차입금 | 안성2공장 | 우리은행 | 2025년 3월 | 4,800 |
| 합 계 | 18,145 | |||
| 출처: 당사 제공 자료 |
당사는 상기 차입금에 대하여 금번 유상증자 자금으로 상환할 순위를 다음과 같이 정하고 있습니다. 다만, 금리변동 및 상환연장 등 사용조건의 유불리에 따라 실제 우선순위는 변동될 수 있습니다.
| [차입금에 대한 상환우선순위] |
| (단위: 백만원) |
| 금융기관 | 대출명 | 만기일 | 한 도 | 사용액 | 상 환 | 사용예정 시기 | 상환우선순위 |
|---|---|---|---|---|---|---|---|
| 국민은행 | 기업일반시설자금대출 | 2024-08-20 | 4,070 | 4,070 | 4,070 | 2024년 8월 | 6 |
| KB모아드림론[기술창조기업] | 2024-08-16 | 5,000 | 5,000 | 5,000 | 2024년 8월 | 5 | |
| 우리은행 | 기업운전일반자금대출 | 2024-03-20 | 1,150 | 1,150 | 1,150 | 2024년 9월 | 3 |
| 기업시설일반대출 | 2025-03-31 | 4,800 | 4,800 | 4,800 | 2024년 3월 | 4 | |
| 하나은행 | 온랜딩대출 | 2030-03-15 | 3,500 | 3,125 | 3,125 | 2025년 3월 | 7 |
| 한국투자증권 | 주식담보대출 | 2025-01-30 | 20,000 | 20,000 | 20,000 | 2024년 7월 | 2 |
| 제9회차 신주인수권부사채 | 2025-06-15 | 100,000 | 18,519 | 60,000 | 2024년 7월 | 1 | |
| 합 계 | 138,520 | 56,664 | 98,145 | - | - | ||
| 주1) 제9회차 신주인수권부사채의 최초 조기상환일은 2024년 6월 15일로 금번 유상증자 자금 납입 전일로 예상되어, 자금 납입 전 상환 요청 금액에 대해서는 브릿지론으로 상환하고 금번 유상증자 자금으로 브릿지론을 상환할 예정입니다. |
| 출처: 당사 제공 자료 |
당사가 계획한 바와 같이 금번 유상증자를 통해 약 1,500억원의 자금을 조달하고, 그 중 차입금 상환을 위해 약 981억원의 자금을 사용할 시, 당사의 차입금의존도는 약 15.8% 수준으로 개선 될 것으로 판단됩니다.
(3) 시설자금 상세 내역
당사는 ESCO사업을 통해 경험한 소각플랜트 수행실적을 바탕으로 부산 소재의 산업용 폐기물 중간처분업체를 인수하여 정상화 작업을 위한 EPC사업을 진행하고 있으며, 부산권역에 산업용 폐기물 중간 처분 업체는 당사의 종속회사인 HLB에너지를 포함하여 2곳 밖에 존재하지 않은 상태입니다. 그러나 부산 산업단지 10여개 연차별 준공으로 인한 사업장 폐기물 증가가 예상되며, 매년 매립량은 감소하고 소각량은 증가하고 있는 추세입니다. 이에 당사의 종속회사인 HLB에너지는 기존 부산 사하구에 보유하고 있는 소각로 증설을 통해 일 48톤의 소각 용량을 90톤까지 증가시킴으로써 산업폐기물을 처리할 수 있는 가동률을 높여 매출 확대 및 수익성 개선을 계획하였습니다.
| [소각로 증설 계획] |
| 일정 | 내용 |
|---|---|
| 2023년 4월 12일 | 건축허가 완료 |
| 2023년 6월 | 실시설계 완료 |
| 2023년 7월 | 시공사 선정, 계약 |
| 2023년 12월 | 공사착공 |
| 2024년 12월 | 준공 및 시운전 |
| 출처: 당사 제공 자료 |
소각로 증설 예상 공사비는 본공사비 300억원, 스팀관로공사 70억원, 주민편의시설 20억원, 기타 10억원으로 총 400억원이며, 금번 유상증자 자금 중 60억을 공사비로 사용 예정입니다. 상세내역으로는 토목 및 건축 공사 비용으로 393백만원, 소각로 시설 공사 비용으로 4,835백만원, 스팀배관 공사 비용으로 620백만원, 주민편의시설 등 공사 비용으로 152백만원 사용 예정입니다.
| [시설 자금 상세내역] |
| (단위: 백만원) |
| 구분 | 상세 내역 | 사용 예정시기 | 합계 | |
|---|---|---|---|---|
| '24년 | '25년 | |||
| 공사비 | 토목, 건축 공사(도급계약) | 273 | 120 | 393 |
| 공사비 | 소각로시설(도급계약) | 4,549 | 286 | 4,835 |
| 공사비 | 스팀배관공사(도급계약) | 550 | 70 | 620 |
| 기타 | 주민편의시설 등 | 59 | 93 | 152 |
| 합계 | 5,431 | 569 | 6,000 | |
| 출처: 당사 제공 자료 |
(4) 기타자금 상세 내역
당사는 금번 주주배정후 실권주 일반공모 유상증자를 통해 조달할 자금 중 일부인 15억원을 대표주관회사인 한국투자증권 주식회사와 케이비증권 주식회사에 지급할 대표주관수수료 및 인수수수료로 사용할 예정입니다.
VI. 그 밖에 투자자보호를 위해 필요한 사항
본 건의 경우 시장조성 또는 안정조작에 관한 사항은 해당사항 없습니다.
제2부 발행인에 관한 사항
I. 회사의 개요
1. 회사의 개요
가. 회사의 법적, 상업적 명칭
당사의 명칭은 "에이치엘비생명과학 주식회사"라고 표기합니다. 또한, 영문으로는 "HLB Life Science Co., Ltd."라고 표기합니다. 단, 약식으로 표기할 경우 "HLB생명과학"이라고 표기합니다.
나. 설립일자 및 존속기간
당사는 1998년 07월 24일에 설립되었으며, 2008년 11월 25일자로 코스닥시장 상장을 승인받아 매매가 개시되었습니다. 2015년 12월 11일에 "에이치엘비생명과학 주식회사"로 상호를 변경하였습니다.
다. 본사의 주소, 전화번호, 홈페이지 주소
| 본사주소 | 경기도 화성시 동탄첨단산업1로 51-9, 8층 (영천동,엠타워지식산업센터) |
| 전화번호 | 02-2627-6700 |
| 홈페이지 | http://www.hlb-ls.com |
라. 주요사업의 내용
당사와 그 종속기업들은 메디케어사업, 바이오사업, 의료기기사업, 의약품유통사업, 에너지사업 부문으로 총 5개 사업부문으로 이루어져 있으며, 당사는 체외 진단용 의료기기 개발 및 제조, 의약외품의 구성품 개발 및 완제품 위탁생산을 하는 메디케어사업을 주사업으로 하고 있습니다.
당사와 종속기업의 주요 사업내용은 아래와 같습니다.
| 회 사 명 | 사업부문 | 사업영역 |
| HLB생명과학 HLB셀 |
메디케어사업 부문 |
1. 체외 진단용 의료기기 개발/제조 2. 구성품 개발 및 완제품 위탁 생산(OEM/ODM) 3. 시약, 기자재 및 소모품 공급 4. 제품설계 및 금형 제작 5. 플라스틱 사출/제조 |
| HLB셀 HLB생명과학R&D |
바이오개발사업 부문 | 1. 체외순환형 바이오인공간 2. 지혈제 개발 3. 신약개발사업 4. 의약품 연구개발 및 판매업 5. 연구개발 용역업 및 서비스 |
| HLB생명과학 | 의료기기사업 부문 | 1. 일회용 주사기 제조, 판매업 2. 의료용구 제조, 판매업 3. 의료용구 유통판매(수입포함) |
| 신화어드밴스 | 의약품유통사업 부문 | 의약품 유통업 |
| HLB솔루션 HLB에너지 |
에너지사업 부문 | 1. 태양광 EPC 사업 2. 폐기물 소각열 관련사업 |
또한, 당사 및 종속회사 HLB생명과학R&D는 현재 자체적으로 표적항암제 리보세라닙(Rivoceranib), 파이로티닙(Pyrotinib) 및 G2M Project 3개의 항암신약 물질에 대한 국내 전용실시권을 보유하고 있으며, 이외 다수의 관계회사에서 바이오 사업을 진행하고 있습니다.
당사의 종속회사 HLB셀은 바이오인공간, 지혈제, 인간 세포외기질 분야에서 파이프라인을 구축하고 있습니다.
계열회사 Elevar therapeutics는 리보세라닙의 글로벌 간암 임상 3상을 완료하여 미국 식품의약국(FDA)에 NDA 신청을 완료하였으며, 2024년 5월 FDA로부터 보완요구서한(CRL)을 수령하였습니다.
각 사업부문별 주요 제품과 매출비중은 다음과 같습니다.
[부문별 주요제품]
| 사업부문 | 주요제품 | 2024년 당분기 매출비중 |
| 메디케어사업 | 체외진단의료기기 및 기타 의료용기기 제조,판매업 | 16.89% |
| 의료기기사업 | 일회용 주사기 제조,판매업 | 8.42% |
| 의약품유통사업 | 의약품도매업 및 기타 판매업 | 70.51% |
| 에너지사업 | 신재생에너지 시설 건설업 | 4.18% |
| 합 계 | 100.00% | |
기타 자세한 사항은 동 보고서의「II. 사업의 내용」을 참조하시기 바랍니다.
마. 중소기업 등 해당 여부
| 중소기업 해당 여부 | 해당 | |
| 벤처기업 해당 여부 | 해당 | |
| 중견기업 해당 여부 | 미해당 | |
(*) 당사는「중소기업기본법」제2조에 따른 중소기업 입니다.
바. 회사의 주권상장(또는 등록ㆍ지정) 및 특례상장에 관한 사항
| 주권상장 (또는 등록ㆍ지정)현황 |
주권상장 (또는 등록ㆍ지정)일자 |
특례상장 유형 |
|---|---|---|
| 코스닥시장 상장 | 2008년 11월 25일 | 해당사항 없음 |
사. 신용평가에 관한 사항
| 평가일 | 평가대상 증권등 |
평가대상증권의 신용등급 | 평가회사 (신용평가등급범위) |
평가구분 |
| 2020.04.13 | - | BB- | 나이스디앤비 (AAA~D) |
정기평가 |
| 2021.04.13 | - | BB- | 나이스디앤비 (AAA~D) |
정기평가 |
| 2022.04.05 | 제9회 무보증사채 | B | 한국기업평가 (AAA~D) |
본평가 |
| 2022.04.05 | 제9회 무보증사채 | B | 나이스디앤비 (AAA~D) |
본평가 |
| 2022.04.29 | - | BB- | 나이스디앤비 (AAA~D) |
정기평가 |
| 2023.06.28 | 제9회 무보증사채 | B | 한국기업평가 (AAA~D) |
본평가 |
| 2023.06.30 | 제9회 무보증사채 | B | 나이스디앤비 (AAA~D) |
본평가 |
[참고] 국내 신용평가사 (NICE신용평가, 한국기업평가) 등급 정의
| 신용등급 | 등급의 정의 |
| AAA | 원리금 지급확실성이 최고 수준임 |
| AA | 원리금 지급확실성이 매우 높지만, AAA등급에 비하여 다소 낮은 요소가 있음 |
| A | 원리금 지급확실성이 높지만, 장래의 환경변화에 따라 다소 영향을 받을 가능성이 있음 |
| BBB | 원리금 지급확실성이 있지만, 장래의 환경변화에 따라 저하될 가능성이 내포되어 있음 |
| BB | 원리금 지급능력에 당면문제는 없으나, 장래의 안정성면에서는 투기적인 요소가 내포되어 있음 |
| B | 원리금 지급능력이 부족하여 투기적임 |
| CCC | 원리금의 채무불이행이 발생할 위험요소가 내포되어 있음 |
| CC | 원리금의 채무불이행이 발생할 가능성이 높음 |
| C | 원리금의 채무불이행이 발생할 가능성이 지극히 높음 |
| D | 현재 채무불이행 상태에 있음 |
2. 회사의 연혁
가. 주요 연혁
- HLB생명과학
| 연월 | 주요 내용 |
| 1998.08. | (주)에너지솔루션즈 법인설립 |
| 2008.11. | 코스닥(KOSDAQ) 상장 |
| 2018.03. | 라이프리버(주) 지분 인수, 바이오사업 확장 지점 이전(경기도 평택시 → 경기도 군포시) |
| 2018.08. | 경구용 표적항암제 리보세라닙의 국내전용실시권 및 일본/유럽 지역 일부 수익 권리 양수 |
| 2019.06. | 대표이사 변경(김하용 → 진양곤) |
| 2020.03. | 본점 이전(경기도 성남시 → 경기도 화성시) 대표이사 변경(진양곤 → 각자 대표이사 진양곤, 남상우) |
| 2020.09. | HLB제약 지분 인수, 제약제조시설 확보 |
| 2020.09. | 파이로티닙(Pyrotinib)의 한국 독점 라이선스 도입 |
| 2020.12. | 파이로티닙(Pyrotinib)의 HER2 변이성(엑손20 삽입) 비소세포폐암 제3상 임상시험 계획 승인 |
| 2021.01. | 재발 및 난치성 유잉육종(Ewing Sarcoma) 제 1상 임상시험 계획 승인 |
| 2021.03. | 신약연구소 설립(경기도 동탄) |
| 2021.03. | 무상증자 실시(자본금 : 23,545백만원, 주식수 47,090,453주) |
| 2021.09. | 이전 치료력이 없는 진행성 또는 전이성 위암(GC) 및 위식도 접합부암(GEJ) 환자를 대상으로 캄렐리주맙(SHR-1210)+카페시타빈/옥살리플라틴 병용투여 후 리보세라닙(아파티닙)+캄렐리주맙(SHR-1210) 투여에 대한무작위배정, 공개, 다기관, 제2상 임상시험 계획(IND) 승인 |
| 2022.03. | 리보세라닙(Rivoceranib)의 반려견 유선암 치료제 개발을 위한 허가용 임상시험 계획(IND) 승인 |
| 2022.03. | 대표이사 변경 (각자 대표이사 진양곤, 남상우 → 각자 대표이사 남상우, 한용해) |
| 2022.07. | 에임 지분 인수, 사업다각화 |
| 2022.07. | HER2 양성 전이성 또는 재발성 유방암 환자에서 라파티닙+ 카페시타빈 병용 투여 대비 파이로티닙 + 카페시타빈 병용 투여시의 유효성 및 안전성을 평가하기 위한 무작위배정, 활성대조, 공개, 다기관, 제3상 가교 임상시험계획(IND) 신청 |
| 2022.10. | 에임 합병 완료 |
| 2022.11. | 리보세라닙(Rivoceranib)의 전이성 또는 재발성 선양낭성암 국내 개발단계 희귀의약품 지정 |
| 2023.02. | 리보세라닙(Rivoceranib) 전이성 또는 재발성 선양낭성암 식품의약품안전처 국내 조건부 품목허가 신청 |
| 2023.03. | HER2 양성 전이성 또는 재발성 유방암 환자에서 라파티닙+ 카페시타빈 병용 투여 대비 파이로티닙 + 카페시타빈 병용 투여시의 유효성 및 안전성을 평가하기 위한 무작위배정, 활성대조, 공개, 다기관, 제 3상 임상시험계획(IND) 승인 |
| 2023.07. | 화진메디칼 지분 인수, 의료기기사업 확대 |
| 2023.10 | 화진메디칼 합병 완료 |
| 2024.01 | 회사분할 (분할신설회사 : 에이치엘비솔루션 주식회사) |
나. 회사의 본점소재지 및 그 변경
| 연월 | 본점소재지 |
| 2019.09. | 경기도 성남시 분당구 판교로 228번길 15, 3동 10층 (삼평동, 판교세븐벤처밸리 1단지) |
| 2020.03. | 경기도 화성시 동탄첨단산업1로 51-9, 8층 (영천동,엠타워지식산업센터) |
다. 경영진 및 감사의 중요한 변동
| 변동일자 | 주총종류 | 선임 | 임기만료 또는 해임 |
|
|---|---|---|---|---|
| 신규 | 재선임 | |||
| 2020년 03월 26일 | 정기주총 | 사내이사 남상우 사내이사 이근식 사내이사 장인근 사외이사 정승면 상근감사 김영현 |
- | - |
| 2021년 03월 31일 | 정기주총 | 사내이사 이을규 사내이사 백윤기 사외이사 최수자 |
사내이사 진양곤 | - |
| 2022년 03월 31일 | 정기주총 | 사내이사 한용해 | - | - |
| 2023년 03월 31일 | 정기주총 | 사외이사 김윤 | 사내이사 남상우 사내이사 장인근 상근감사 김영현 |
- |
| 2024년 03월 28일 | 정기주총 | 사내이사 이근식 사외이사 심연섭 사외이사 송세빈 |
사내이사 진양곤 | - |
| (*1) 2021년 06월 15일 이을규 사내이사는 일신상의 사유로 사임하였습니다. (*2) 2022년 03월 31일 백윤기 사내이사, 이근식 사내이사는 일신상의 사유로 사임하였습니다. (*3) 2022년 05월 20일 정승면 사외이사가 일신상의 사유로 사임하였습니다. (*4) 2024년 03월 28일 장인근 사내이사, 김윤 사외이사는 일신상의 이유로 사임하였습니다. |
라. 회사가 합병 등을 한 경우 그 내용
| 연월 | 내용 |
| 2019.11. | 삼각합병 동의에 따른 LSK BioPartners, Inc. 주식 처분 및 HLB 주식 취득완료 |
| 2022.07. | 에임 자산(주식)양수완료 |
| 2022.10. | 에임 합병완료 |
| 2023.07 | 화진메디칼 지분인수완료 |
| 2023.10 | 화진메디칼 합병완료 |
마. 그 밖에 경영활동과 관련된 중요한 사항의 발생내용
- 해당사항 없습니다.
바. 회사의 업종 또는 주된 사업의 변화
- 2022년 10월, 에임을 합병하여 메디케어사업부로 편입하였고 관련 사업으로 의료용품 및 의약 관련 제품 제조업을 추가하였습니다.
- 2023년 5월, 기존 엔지니어링 및 관련 기술 서비스업 중심에서 의료용품 및 기타 의약 관련 제품 제조업 주업종 변경하였습니다.
※ 상세내용은 Ⅰ. 회사의 개요 - 5. 정관에 관한 사항 참고 바랍니다.
3. 자본금 변동사항
※ 자본금 변동추이
| (단위 : 원, 주) |
| 종류 | 구분 | 27기 (2024년 당분기말) |
26기 (2023년말) |
25기 (2022년말) |
24기 (2021년말) |
23기 (2020년말) |
|---|---|---|---|---|---|---|
| 보통주 | 발행주식총수 | 107,600,282 | 101,866,689 | 96,714,952 | 95,498,081 | 47,070,453 |
| 액면금액 | 500 | 500 | 500 | 500 | 500 | |
| 자본금 | 54,273,709,000 | 51,406,912,500 | 48,831,044,000 | 48,222,608,500 | 24,008,794,500 | |
| 우선주 | 발행주식총수 | - | - | - | - | - |
| 액면금액 | - | - | - | - | - | |
| 자본금 | - | - | - | - | - | |
| 기타 | 발행주식총수 | - | - | - | - | - |
| 액면금액 | - | - | - | - | - | |
| 자본금 | - | - | - | - | - | |
| 합계 | 자본금 | 54,273,709,000 | 51,406,912,500 | 48,831,044,000 | 48,222,608,500 | 24,008,794,500 |
4. 주식의 총수 등
※ 주식의 총수 현황
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 비고 | |||
|---|---|---|---|---|---|
| 보통주 | 우선주 | 합계 | |||
| Ⅰ. 발행할 주식의 총수 | 300,000,000 | - | 300,000,000 | - | |
| Ⅱ. 현재까지 발행한 주식의 총수 | 107,600,282 | - | 107,600,282 | - | |
| Ⅲ. 현재까지 감소한 주식의 총수 | - | - | - | - | |
| 1. 감자 | - | - | - | - | |
| 2. 이익소각 | - | - | - | - | |
| 3. 상환주식의 상환 | - | - | - | - | |
| 4. 기타 | - | - | - | - | |
| Ⅳ. 발행주식의 총수 (Ⅱ-Ⅲ) | 107,600,282 | - | 107,600,282 | - | |
| Ⅴ. 자기주식수 | 69,920 | - | 69,920 | - | |
| Ⅵ. 유통주식수 (Ⅳ-Ⅴ) | 107,530,362 | - | 107,530,362 | - | |
※ 자기주식 취득 및 처분 현황
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 주) |
| 취득방법 | 주식의 종류 | 기초수량 | 변동 수량 | 기말수량 | 비고 | ||||
|---|---|---|---|---|---|---|---|---|---|
| 취득(+) | 처분(-) | 소각(-) | |||||||
| 배당 가능 이익 범위 이내 취득 |
직접 취득 |
장내 직접 취득 |
- | - | - | - | - | - | - |
| - | - | - | - | - | - | - | |||
| 장외 직접 취득 |
- | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 공개매수 | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 소계(a) | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 신탁 계약에 의한 취득 |
수탁자 보유물량 | - | - | - | - | - | - | - | |
| - | - | - | - | - | - | - | |||
| 현물보유물량 | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 소계(b) | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 기타 취득(c) | 보통주 | 69,920 | - | - | - | 69,920 | - | ||
| - | - | - | - | - | - | - | |||
| 총 계(a+b+c) | 보통주 | 69,920 | - | - | - | 69,920 | - | ||
| - | - | - | - | - | - | - | |||
5. 정관에 관한 사항
가. 정관 변경 이력
| 정관변경일 | 해당주총명 | 주요변경사항 | 변경이유 |
|---|---|---|---|
| 2020년 03월 26일 | 제 22기 정기주주총회 |
- 제2조: 목적 - 제3조: 본점의 소재지 및 지점 등의 설치 - 제34조: 이사의 수 - 제40조: 이사회 - 제40조의2: 이사회의 의장 - 제40조의3: 이사회의 소집 |
- 사업영역확대 - 본점소재지 변경 - 사외이사 규정 신설 - 이사회 의장제도 도입을 위한 근거 마련 |
| 2022년 03월 31일 | 제 24기 정기주주총회 |
- 제8조: 주식의 종류 및 주식 등의 전자등록 - 제14조: 신주의 동등배당 - 제19조: 전환사채의 발행 - 제20조: 신주인수권부사채의 발행 - 제22조: 소집시기 - 제32조: 주주총회의 결의방법 - 제39조: 이사의 보수와 퇴직금 - 제47조: 감사의 선임·해임 - 제57조: 이익배당 |
- 비상장사채 등 의무등록 대상이 아닌 주식등에 대해서는 전자 등록을 하지 않을 수 있도록 함 - 동등배당 원칙을 명시 - 전환사채 발행한도 증액 - 신주인수권부사채 발행한도 증액 - 정기주주총회 개최시기의 유연성을 확보 - 적대적 인수합병 방어를 위한 조항 신설 - 감사선임에 관한 조문 정비 - 기준일 제도 운영상의 편의성을 제고 |
| 2023년 03월 31일 | 제 25기 정기주주총회 |
- 제1조: 상호 - 제2조: 목적 - 제32조: 주주총회의 결의방법 - 제39조: 이사의 보수와 퇴직금 - 제39조의 2: 이사의 책임감경 |
- HLB 사용 명시 - 사업영역 확대 - 정상적 인수합병을 방해할 수 있는 제도의 삭제 - 이사의 책임감경 규정 재정비(상법 제400조 준용) |
나. 사업목적 현황
1. 사업목적 추가 사항
| 구 분 | 사업목적 | 사업영위 여부 |
|---|---|---|
| 1 | 에너지절약관련 엔지니어링 서비스업 | 영위 |
| 2 | 전기, 전자 공조 냉.온방 및 통신관련 엔지니어링 서비스업 | 미영위 |
| 3 | 전기공급, 제어장치, 전동기, 발전기 및 전기변환장치 제조업 | 미영위 |
| 4 | 상기관련 수출입업 | 미영위 |
| 5 | 에너지절약관련 전자상거래 및 인터넷 용역 서비스업 | 미영위 |
| 6 | 기계설비 공사업 | 영위 |
| 7 | 전문소방 공사업 | 미영위 |
| 8 | 자동제어 공사업 | 미영위 |
| 9 | 일반전기 공사업 | 미영위 |
| 10 | 냉난방기기 제조 및 도.소매 | 미영위 |
| 11 | 시설유지보수 점검업 | 미영위 |
| 12 | 태양에너지. 풍력 및 지열관련 사업 | 영위 |
| 13 | 폐기물 소각열 관련사업 | 영위 |
| 14 | 바이오 에너지 관련사업 | 미영위 |
| 15 | 에너지진단사업 | 영위 |
| 16 | 해외건설산업 | 미영위 |
| 17 | 조명기기 제조 및 도·소매 | 미영위 |
| 18 | 정보통신 공사업 | 미영위 |
| 19 | 산업·환경설비 공사업 | 영위 |
| 20 | 기술자문, 엔지니어링, 컨설팅 용역 서비스업 | 영위 |
| 21 | 프로그램, 시스템개발, 판매, 용역서비스업 | 미영위 |
| 22 | 소프트웨어 자문, 개발, 판매, 용역 서비스업 | 미영위 |
| 23 | 지리정보시스템관련 용역업 | 미영위 |
| 24 | 수치지도 제작업 | 미영위 |
| 25 | 문서 및 도면관리를 위한 씨디 제작 용역업 | 미영위 |
| 26 | 씨디 토탈 및 영상 제조 용역업 | 미영위 |
| 27 | 컴퓨터그래픽, 애니메이션, 캐드, 스캐닝 용역 서비스업 | 미영위 |
| 28 | 부동산임대업 | 영위 |
| 29 | 환경전문공사업 | 영위 |
| 30 | 컴퓨터관련 서비스사업 | 미영위 |
| 31 | 패키지소프트웨어 개발 공급사업 | 미영위 |
| 32 | 정보통신시스템 기술개발, 생산 및 판매 | 미영위 |
| 33 | 정보보호시스템 기술개발, 생산 및 판매 | 미영위 |
| 34 | 정보보호서비스 및 컨설팅 | 미영위 |
| 35 | 네트워크관리 서비스개발 및 판매, 운영 | 미영위 |
| 36 | 통신공사업 | 미영위 |
| 37 | 기상사업 | 미영위 |
| 38 | 시스템 통합 구축사업 | 미영위 |
| 39 | 위 각호에 관련된 무역업 | 미영위 |
| 40 | 지능형전력망 서비스제공사업 | 미영위 |
| 41 | 산업용 우드펠렛 보일러의 제조 및 판매 | 미영위 |
| 42 | 우드펠렛의 도소매, 수출입 | 미영위 |
| 43 | 고형연료제품(에쓰알에프)의 제조 및 수출입, 도소매 | 미영위 |
| 44 | 열 및 증기(스팀)공급사업 | 영위 |
| 45 | 전력판매사업 | 미영위 |
| 46 | 인공간 제조 및 인공간 판매업 | 영위 |
| 47 | 의료기기 및 용품의 제조, 판매업 | 영위 |
| 48 | 장기, 혈액, 적출물 관련 사업 및 연구 | 영위 |
| 49 | 의약품 원료개발, 생산 및 판매업 | 영위 |
| 50 | 저온 냉동 관련사업 | 미영위 |
| 51 | 의료관련 자문업 및 연구 | 미영위 |
| 52 | 사업경영 및 관리자문업 | 미영위 |
| 53 | 헬스케어사업 | 영위 |
| 54 | 의료기기 및 의약품 수출입업 | 영위 |
| 55 | 건강기능식품 제조 및 판매업 | 미영위 |
| 56 | 식품소분 판매업 | 미영위 |
| 57 | 연구용 식약재료(냉동으로 보관한 동물간세포, 배양배지, 플레이트 세트) 판매업 | 영위 |
| 58 | 간독성 및 약물대사 시험서비스업 | 영위 |
| 59 | 의약품 도소매업 | 영위 |
| 60 | 의약품 수출입업 | 영위 |
| 61 | 의약품 유통업 | 영위 |
| 62 | 전자상거래업 | 미영위 |
| 63 | 병의원관리 및 컨설팅업 | 미영위 |
| 64 | 의료기기 유통, 도,소매업 | 영위 |
| 65 | 생명공학을 이용한 의약품 연구, 개발 및 상품화, 판매업 | 영위 |
| 66 | 생명공학 관련 신기술 연구, 개발 및 상품화, 판매업 | 영위 |
| 67 | 위 연구개발에 따른 국내외서의 지적재산권 획득 및 이전 | 영위 |
| 68 | 신약특허 기술이전 및 이에 따른 로열티 획득 사업 | 영위 |
| 69 | 신약개발 사업 | 영위 |
| 70 | 유전자 검사 및 신약개발을 위한 약효검색, 발굴 및 분석 서비스업 | 영위 |
| 71 | 연구개발 용역업 및 서비스업 | 영위 |
| 72 | 각종 기술이전 사업 | 영위 |
| 73 | 의약품 및 건강기능식품 제조를 위한 기계장치 개발 및 판매업 | 미영위 |
| 74 | 의약품 및 건강기능식품 제조를 위한 기계장치 수출입업 | 미영위 |
| 75 | 의약품 및 건강기능식품 제조를 위한 기계장치 무역 및 무역대리업 | 미영위 |
| 76 | 의약품 및 건강기능식품 제조를 위한 기계장치 유통업 | 미영위 |
| 77 | 국민건강진흥사업 | 영위 |
| 78 | 의약품 소분 및 판매업 | 미영위 |
| 79 | 의약 부의품 제조 및 판매업 | 영위 |
| 80 | 동물용 의약품 제조 및 판매업 | 미영위 |
| 81 | 건강보조식품 제조 및 판매업 | 미영위 |
| 82 | 위 각호에 관련된 부대사업일체 | 영위 |
| 83 | 연구용 시약, 연구용 소모품 제조/판매 및 관련업 | 영위 |
| 84 | 실험용 동물 도소매 및 관련업 | 미영위 |
| 85 | 플라스틱 사출품 제조 유통 및 관련업 | 영위 |
| 86 | 기타 도급업 | 미영위 |
| 87 | 포장용 플라스틱 제품 제조업 및 관련업 | 영위 |
| 88 | 일회용 주사기 제조 및 도/소매업 및 수출입업 | 영위 |
| 89 | 의료용구 제조 및 도/소매업 및 수출입업 | 영위 |
2. 사업목적 변경 내용
| 구분 | 변경일 | 사업목적 | |
|---|---|---|---|
| 변경 전 | 변경 후 | ||
| 추가 | 2023.03.31 | - |
83. 연구용 시약, 연구용 소모품 제조/판매 및 관련업 |
1) 변경 사유
당사는 이사회 및 경영진 방침에 따라 글로벌 제약/바이오 회사로 성장하기 위하여 신약개발, 의료기기 등 제약/바이오 사업 부문 역량을 강화하고 있으며 이러한 목표의 일환으로 의료용품 및 의약 관련 제품 제조업을 영위 중인 에임을 2022.10.01 합병하여 메디케어사업부로 편입하였고 관련 사업을 추가하여 영위 및 추진하고 있습니다. (관련 사항은 2022년 7월 18일 공시된 '회사합병 결정' 및 2022년 10월 4일 공시된 '합병등종료보고서'를 참고하시기 바랍니다.)
메디케어사업부 편입 이후 2022년도말 별도 기준 매출액 비중은 기존 건축 기술, 엔지니어링 및 관련 기술 서비스업 중심에서 의료용품 및 기타 의약 관련 제품 제조업중심으로 빠르게 재편되었습니다. 이를 바탕으로 제약/바이오 전문기업으로 탈바꿈하기 위하여 2023년 05월 02일 정기심사를 통하여 의료용품 및 기타 의약 관련 제품제조업으로 업종변경을 완료하였습니다. (관련 사항은 2023년 4월 28일 공시된 '업종변경'을 참고하시기 바랍니다.)
(*) 2023년 사업연도말 매출비중 (별도기준)
| (단위 : 억원 / %) |
|
구 분 |
2023년 | |
| 매출 | 비율 | |
|
의료용품 및 기타 의약관련제품제조업 |
264 | 89.7 |
| 건축 기술, 엔지니어링 및 관련 기술 서비스업 | 14 | 4.6 |
|
부동산 임대 및 공급업 |
13 | 4.3 |
|
기타 사업지원 서비스업 |
4 | 1.4 |
|
합 계 |
294 | 100 |
3. 정관상 사업목적 추가 현황표
| 구 분 | 사업목적 | 추가일자 |
|---|---|---|
| 추가 |
연구용 시약, 연구용 소모품 제조/판매 및 관련업 |
2023.03.31 |
| 추가 | 실험용 동물 도소매 및 관련업 | 2023.03.31 |
| 추가 | 플라스틱 사출품 제조 유통 및 관련업 | 2023.03.31 |
| 추가 | 기타 도급업 | 2023.03.31 |
| 추가 | 포장용 플라스틱 제품 제조업 및 관련업 | 2023.03.31 |
| 추가 | 일회용 주사기 제조 및 도/소매업 및 수출입업 | 2023.03.31 |
| 추가 | 의료용구 제조 및 도/소매업 및 수출입업 | 2023.03.31 |
[사업부문별 사업목적 추가사항]
| 사업부 구분 | 사업목적 | 추진현황 |
| 메디케어사업부 | 연구용 시약, 연구용 소모품 제조/판매 및 관련업 플라스틱 사출품 제조 유통 및 관련업 포장용 플라스틱 제품 제조업 및 관련업 의료용구 제조 및 도/소매업 및 수출입업 |
영위 |
| 의료기기사업부 | 일회용 주사기 제조 및 도/소매업 및 수출입업 의료용구 제조 및 도/소매업 및 수출입업 |
영위 |
| 기타 | 실험용 동물 도소매 및 관련업 기타 도급업 |
미추진 |
□ 메디케어사업부
(1) 그 사업 분야 및 진출 목적
당사는 글로벌 제약/바이오 기업으로 역량 강화를 위하여 메디케어사업을 추진하고 있습니다. 주로 연구용 시약, 연구용 소모품 제조 및 판매업 등을 영위하고 있으며, 금형을 통한 플라스틱 사출 성형 및 패키징 기술을 기반으로 COVID-19 등의 체외 진단기기의 선도 기업인 Roche, SD BIOSENSOR, Abboatt 등의 구성품 개발부터 완제품 위탁 생산 (OEM/ODM) 및 TPM (Third Party Manufacturing)을 주된 사업으로 운영하고 있습니다.
(2) 시장의 주요 특성ㆍ규모 및 성장성
체외진단은 인체의 혈액, 소변 등으로부터 유래하는 검체를 체외에서 건강 및 질병관리에 필요한 정보를 얻기 위해 실시하는 의료적 행위입니다. 이에, 체외진단 산업은 시약, 기기, 소모품, 소프트웨어 등 검사와 관여되는 일체의 제품 개발 및 제조와 관련되며 아래와 같은 특징을 갖고 있습니다.
| 특징 | 내용 |
| 성장성이 높은 산업 | 인구 고령화, 맞춤의료, 질병 예측 수요의 증가로 빠른 성장 예상 |
| 고부가가치를 창출하는 지식산업 | 무형가치의 투입으로 고부가가치의 창출의 첨단 지식산업 |
| 정부 규제 사업 | 체외진단 제품의 생산, 임상시험, 유통 및 판매 등 정부 규제 |
| 융복합기술 기반 산업 | 바이오기술과 광학, 전기전자, 기계공학, 화학 및 의학이 합쳐진 전형적인 융복합기술을 기반으로 하는 산업 |
| 경기변동의 영향이 적은 산업 | 인간의 생명 및 건강과 관련되어 있어 경기변동에 따른 영향 미미 |
(출처 : 식품의약품안전평가원)
헬스케어 패러다임은 예방, 진단, 사후관리 중심으로 변화하고 있습니다. COVID-19의 경우 짧은 기간 급격하게 헬스케어 분야의 패러다임 변화를 잘 보여주고 있으며 최근 질병 진단의 패러다임이 예방의학으로 변화되는 추세에 맞춰 진단의학에 대한 수요가 증가하면서 체외진단 시장은 지속적으로 성장할 것으로 전망됩니다.
전 세계 글로벌 체외 진단(IVD) 시장은 2021년 982억 달러에서 연평균 성장률 2.9%로 증가하여, 2026년에는 1,131억 달러에 이를 것으로 전망됩니다. COVID-19로 인해 글로벌 체외 진단 시장은 급격하게 성장하였으며, 기존 또는 신규 감염 질병 진단을 위한 차세대 체외 진단의 R&D 확장으로 앞으로도 성장 추세는 꾸준히 이어질 것으로 예상됩니다. (출처 : Research & Markets - In-Vitro Diagnostics/IVD Market by Product and Service ,Technology ,Application (Diabetes, Oncology, Cardiology, Nephrology, Infectious Disease, End User - Global Forecast to 2026 (2022.05))
(3) 신규사업과 관련된 투자 및 예상 자금소요액
당사는 메디케어사업을 추진하기 위하여 에임을 2022년 07월 21일 979억원에 100% 지분 인수하였습니다. 이 중 529억원은 당사 보유 현금으로 납입하였으며, 나머지 450억원은 전환사채를 발행하여 대용 납입하였습니다.
(4) 사업 추진현황
- 조직 및 인력구성 현황_경영기획팀 작성
당분기 기준 메디케어사업부는 1개 사업부, 1개 본부, 1개소, 6개 부문, 10개팀으로 구성되어 있으며 인원은 64명입니다.
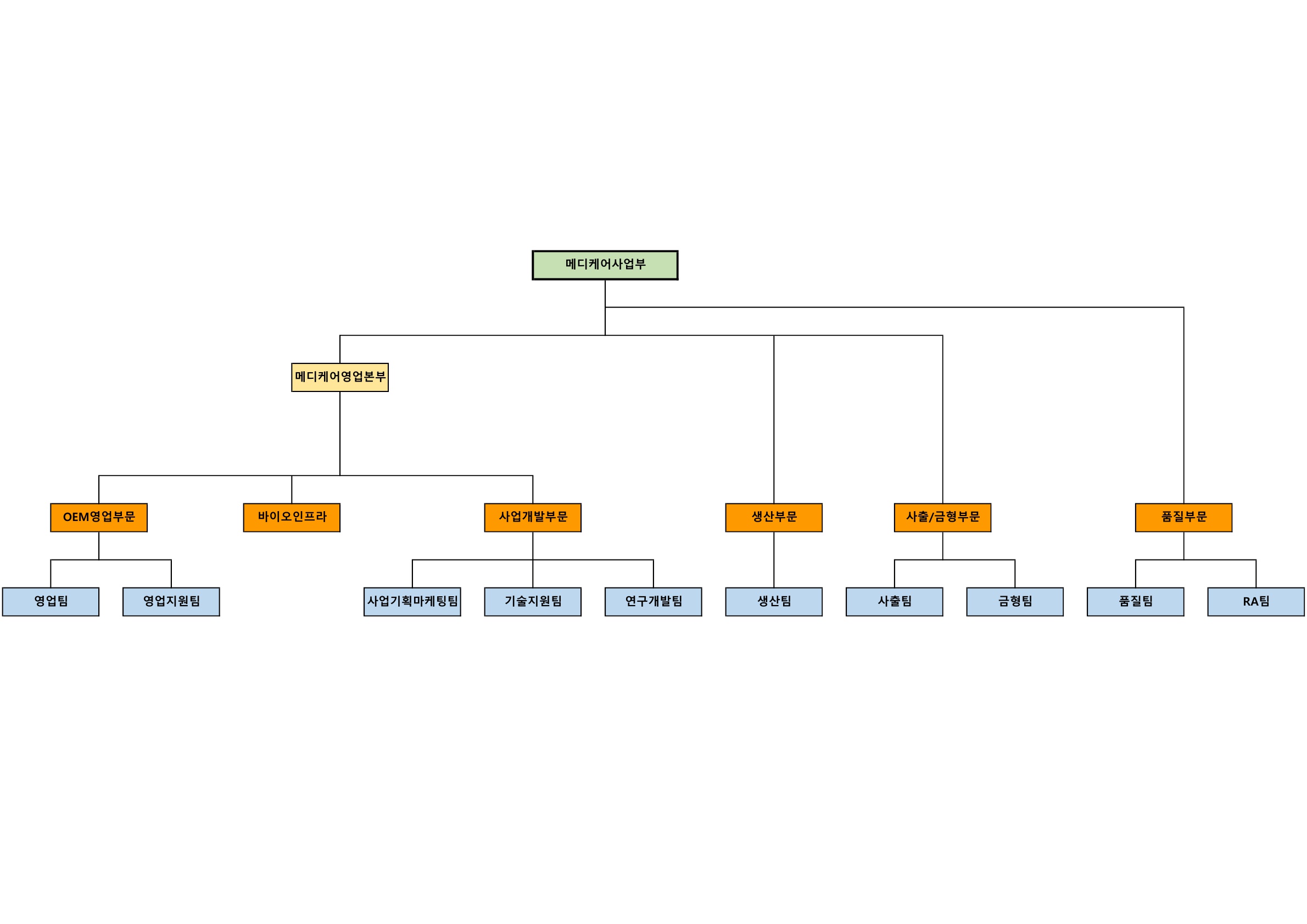 |
|
메디케어사업부 조직도 |
- 연구개발활동 내역
당사는 COVID-19 관련 검체 테스트기 외에도 NON COVID 등 다양한 체외진단제품으로 확대하기 위하여 연구개발을 진행하고 있습니다.
- 매출발생 내역
당사는 COVID-19 관련 검체 테스트기 어셈블리, 진단 소모품 제조 및 의료 소모품등의 제품을 생산 및 판매하고 있으며 최근 사업연도말(2023년) 연결 기준 매출 249억원을 달성하였습니다.
(5) 기존 사업과의 연관성
의료용품 및 의약 관련 제품 제조업을 영위 중인 에임을 2022년 10월 01일 합병하여메디케어사업부로 편입하여 기존 건축 기술, 엔지니어링 및 관련 기술 서비스업에서 의료용품 및 기타 의약 관련 제품 제조업으로 주업종 변경하였습니다. 따라서 기존 사업과의 연관성은 크지 않습니다.
(6) 주요 위험
메디케어사업부는 면역화학진단키트 등을 제조 및 판매하고 있는 체외진단 산업의 OEM 및 TPM(Third Party Manufacturing)을 진행하고 있어 해당 전방 산업 기업의 제품에 대한 수요가 당사 매출 실적에 큰 영향을 주고 있습니다.
□ 의료기기사업부
(1) 그 사업 분야 및 진출 목적
당사는 메디케어사업 외에 사업의 다각화를 통한 안정적인 현금 창출을 위하여 의료기기사업을 추진할 예정이며 해당 사업은 주사기, 주사기침류 등 일회용 주사기를 주요 제품으로 생산 및 판매할 예정입니다.
(2) 시장의 주요 특성ㆍ규모 및 성장성
주사기 시장은 고령사회가 본격화되면서 점진적으로 확대되고 있으며, 주사기 및 주삿바늘과 같이 위생ㆍ보건상의 이유로 재사용이 어려운 제품의 특성으로 출하량이 계속 증가할 것으로 전망됩니다.
주사기의 사용량은 일반적으로 사용되는 다른 의료 용품보다 1.5배가 높으며, 기술적인 발전과 함께 다양한 산업 및 지역에서 여러 용도로 확장되고 있습니다. 주사기의 디자인과 기능 개선, 안전성 향상, 자동화 기술의 도입 등이 이루어지고 있으며, 의료 및 생명과학 분야에서 핵심적인 역할을 수행합니다. 세계 주사기 시장은 2022년 178.9억 달러로 추정되며 연평균 4.2%의 성장률로 2032년 270억 달러에 이를 것으로 전망됩니다.
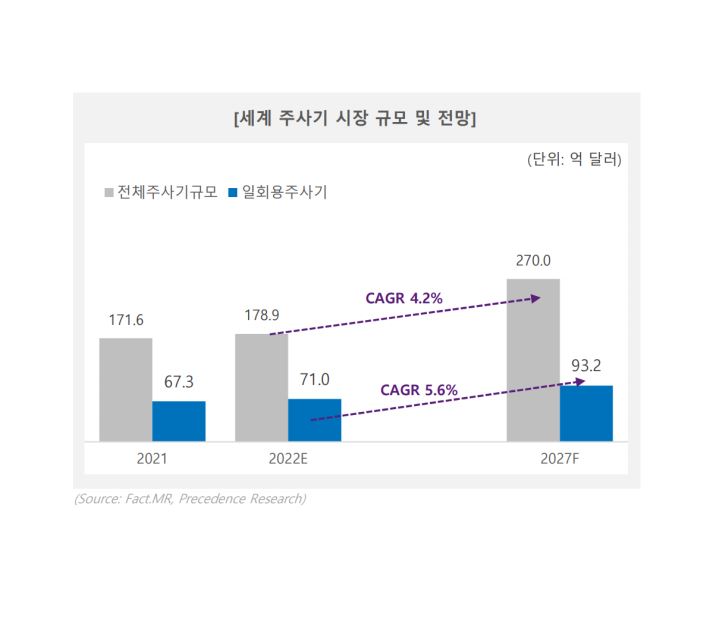 |
|
세계 주사기 시장 규모 및 전망 |
(3) 신규사업과 관련된 투자 및 예상 자금소요액
당사는 의료기기사업을 영위하기 위하여 화진메디칼을 2023년 07월 03일 83억원에 100% 지분 인수하였으며 전액 당사가 보유한 현금으로 대금 납입 완료하였습니다. 또한, 금년도 해당사업 영위를 위해 약 60억원의 신규투자를 집행할 예정입니다.
(4) 사업 추진현황
의료기기사업부는 해당 사업을 확대하기 위하여 2023년 07월 03일 관련 일회용 주사기 제조업을 영위하고 있는 화진메디칼을 인수하여 연결 종속회사로 편입한 이후, 합병 절차를 완료하여 2023년 10월 1일자로 당사 의료기기사업부로 편입 완료하였습니다. (관련 사항은 2023년 10월 4일 공시된 '합병등종료보고서'를 참고하시기 바랍니다.)
- 조직 및 인력구성 현황_경영기획팀 작성
당분기 기준 의료기기사업부는 1개 사업본부, 2개 부문, 6개 팀으로 구성되어 있으며 인원은 64명입니다.
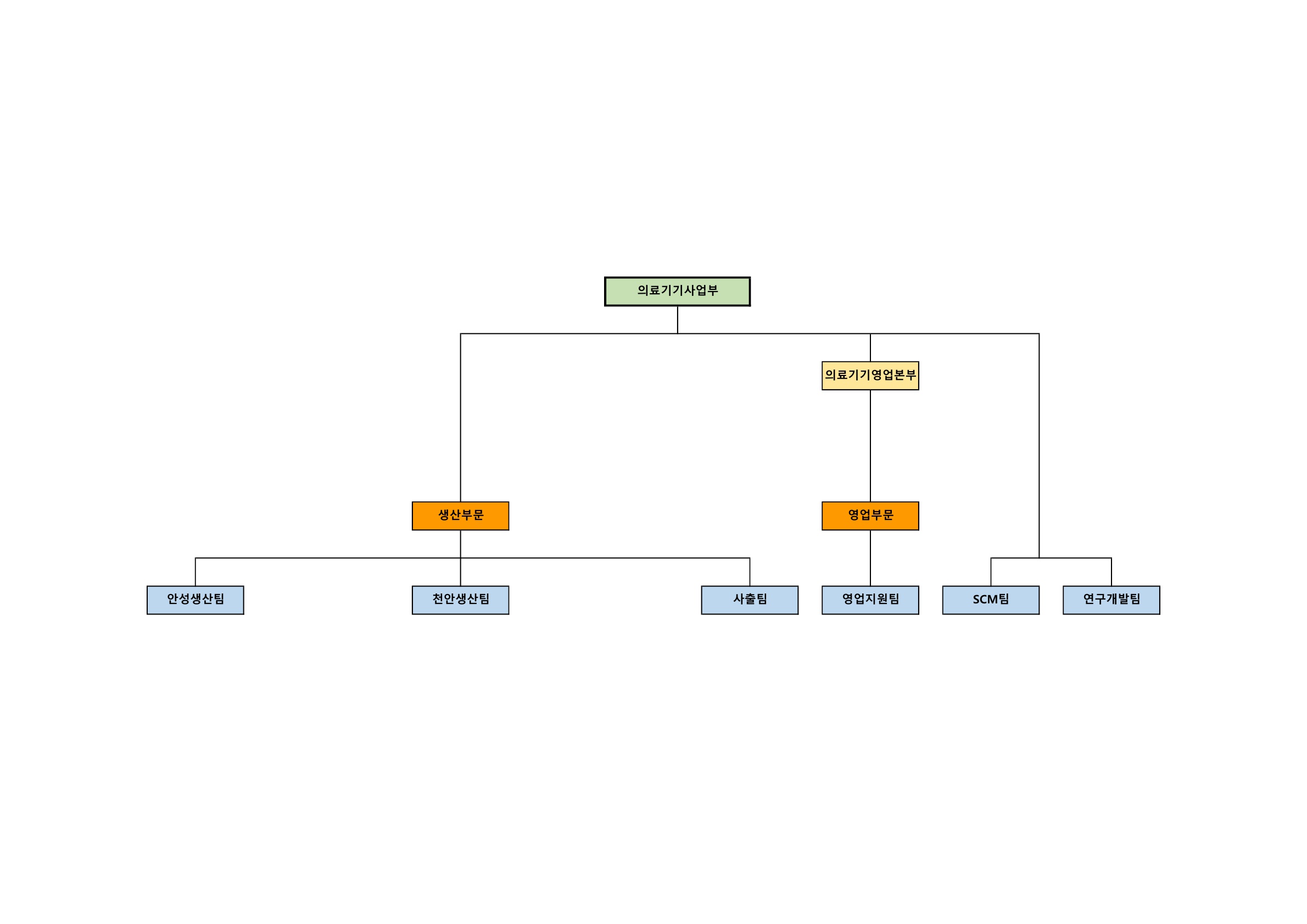 |
|
의료기기사업부 조직도 |
- 연구개발활동 내역
일회용 주사기 외에 다양한 특수 목적 주사기 등을 개발 진행 중에 있습니다.
- 매출발생 내역
화진메디칼은 소프젝(Sofjec)이라는 브랜드로 주사기, 주사침류 등의 제품을 생산 및판매하고 있으며 최근 사업연도말(2023년) 기준 매출 44억원을 달성하였습니다
(5) 기존 사업과의 연관성
해당사항 없습니다.
(6) 주요 위험
일반적인 제약산업과 마찬가지로 해당 산업은 국민의 건강과 직접적으로 연관된 산업으로 타 사업과 비교하여 경기변동 및 계절성 등에 비하여 민감도가 낮으며 필수재적인 재화 성격으로 경기방어적인 특징을 갖고 있어 위험도가 낮은 편입니다.
(7) 향후 추진계획
의료기기사업부 편입 후 추가 생산 CAPA 확보를 위하여 신규 공장 설비 셋업 및 생산 준비를 진행 중에 있으며 매출 증대를 위하여 일회용 주사기 외 특수 목적 주사기 등 판매 품목을 확대할 예정입니다.
□ 기타
실험용 동물 도소매 및 기타 도급업 관련 사업은 당사 주업종 사업에 집중하기 위해 현재 추진중에 있지 않으며 향후 추진 계획에 대하여도 내부 검토 중에 있습니다.
II. 사업의 내용
1. 사업의 개요
연결회사는 메디케어사업, 바이오개발사업, 의료기기사업,의약품유통사업, 에너지사업 부문으로 총 5개 사업부문 체제로 운영되고 있습니다. 각 사업부문별 주요 사업영역은 다음과 같습니다.
|
회 사 명 |
사업부문 |
사업영역 |
| HLB생명과학 HLB셀 |
메디케어사업 부문 |
1. 체외 진단용 의료기기 개발/제조 2. 구성품 개발 및 완제품 위탁 생산(OEM/ODM) 3. 시약, 기자재 및 소모품 공급 4. 제품설계 및 금형 제작 5. 플라스틱 사출/제조 |
| HLB셀 HLB생명과학R&D |
바이오개발사업 부문 | 1. 체외순환형 바이오인공간 2. 지혈제 개발 3. 신약개발사업 4. 의약품 연구개발 및 판매업 5. 연구개발 용역업 및 서비스 |
| HLB생명과학 | 의료기기사업 부문 | 1. 일회용 주사기 제조, 판매업 2. 의료용구 제조, 판매업 3. 의료용구 유통판매(수입포함) |
| 신화어드밴스 | 의약품유통사업 부문 | 의약품 유통업 |
| HLB솔루션 HLB에너지 |
에너지사업 부문 | 1. 태양광 EPC 사업 2. 폐기물 소각열 관련사업 |
가. 메디케어사업부문
당사는 Medical & Healthcare 시장을 선도하는 기업에서부터 신규 기업까지 관련 산업의 모든 기업들이 빠르게 변화하는 글로벌 산업에 발맞추어 진화할 수 있도록, 구성품 개발부터 완제품 위탁 생산 (OEM/ODM)에 최적화된 솔루션을 제공하고 있습니다. 또한 연구소, 의료시설 및 제조사에서 사용되는 시약, 기자재 및 소모품까지 최적화된 사업 기반을 바탕으로 Total-Solution을 제공합니다. 의료기기 분야에서 Malaria, HIV, Covid-19, Influenza 등 항원 및 항체 기반의 Immunoassay Rapid POCT 진단 시약의 주요 구성품을 개발하였으며, 다수의 기술 및 디자인 특허를 보유하고 있습니다. 주요 고객사는 Abbott, SD BIOSENSOR 등 이며, 특히 Covid Ag 신속진단 키트 관련하여 Roche, SD BIOSENSOR, Abbott의 OEM 및 TPM(Third Party Manufacturing)을 진행하고 있습니다.
지난 RDT 사업을 통한 Project 개발, 플라스틱 사출, 임가공 Ass’y 등의 제조 및 품질 보증 노하우를 통해 시장에 한 발 더 나아가 전자, 화장품, 제약, 요식업 등의 시장에 OEM / ODM Project를 확장하며, 당 사업부 자체 인적 인프라를 이용한 외주 Validation consulting, Quality Management Consulting 등의 영역에도 발 들일 수 있게 되었습니다. 이는 헬스케어 산업에 중요시 되고 있는 Qualification, CSV, Process/Method/Cleaning validation 등에 대한 기술 노하우 및 고객 만족 서비스를 바탕으로 의료시장의 품질 및 제조 경쟁력의 향상을 통해 기업과 더 나아가 인류의 더 나은 삶에 기여합니다.
또한, 다채로운 케이스의 개발 노하우를 이용, 철저한 시장 분석을 통한 B2C Item(유아, 실버 케어 등) 개발 중에 있습니다.
나. 바이오사업부문
당사 및 종속회사 HLB생명과학R&D는 현재 자체적으로 표적항암제 리보세라닙(Rivoceranib), 파이로티닙(Pyrotinib) 및 G2M Project 3개의 항암신약 물질에 대한 국내 전용실시권을 보유하고 있으며, 이외 다수의 관계회사에서 바이오 사업을 진행하고 있습니다.
당사의 종속회사 HLB셀은 바이오인공간, 지혈제, 인간 세포외기질 분야에서 파이프라인을 구축하고 있습니다.
계열회사 Elevar therapeutics는 리보세라닙의 글로벌 간암 임상 3상을 완료하여 미국식품의약국(FDA)에 NDA 신청을 완료하였으며, 2024년 5월 FDA로부터 보완요구서한(CRL)을 수령하였습니다.
다. 의료기기사업부문
HLB생명과학은 2023년 10월 4일자로 화진메디칼 합병을 완료하였습니다. 구. 화진메디칼은 1993년 설립된 의료기기전문회사로서, 소프젝(Sofjec)이라는 브랜드로 주사기, 주사침류 등을 생산하고 있습니다. 2023년 2월 미국 FDA로부터 일회용주사기, 주사침, 필터주사기 등에 대한 미국 내 판매허가를 획득했습니다. 현재 해당 주사기 제품들은 국내 대형병원, 대학병원, 중소병원 및 동물병원 등에 대량 납품하고 있으며 국내 외 미국, 사우디, 베트남, 몽골 등으로 수출하고 있습니다. 특히 일회용주사기 외통 끝부분이 기존에 Luer Slip 타입에 더하여 Luer Lock 타입 설비를 새롭게 갖춤으로써 늘어나는 Luer Lock 타입 주사기의 수요에 충분히 대응할 수 있게 되었습니다.
라. 의약품유통사업 부문
당사는 신규사업 부분에 대한 투자의 일환으로 2016년 8월 5일 신화어드밴스 지분 132,000주를 100% 인수하여 의약품 유통 사업분야의 첫걸음을 떼었습니다.
신화어드밴스는 2007년 11월 19일 의약품 유통업 및 관련사업 등을 주 사업목적으로 설립하였습니다. 국,공립병원에 의약품을 납품하고 있으며, 특히 유한양행, 동아에스티, 제일약품, 대웅제약, 한미약품, 종근당, 일동제약, 보령제약, SK케미칼 등 국내 상위권 제약사와 화이자(Pfizer), 글락소스미스클라인(GSK), 노바티스(Novartis), 사노피(Sanofi-Aventis), MSD, 아스트라 제네카(Astra Zeneca), 베링거 잉겔하임(Boehringer-ingelheim), 오츠카제약(Otsuka) 등 유수의 외국계제약사와 거래 관계를 맺고 있습니다.
마. 에너지사업 부문
당사는 신재생에너지 사업과 관련하여 2006년 정부의 발전차액제도 시행에 따라 2008년 9월까지 6.1MW를 준공하였을 뿐 아니라 2010년부터 에너지관리공단의 Green Home 100만호 사업, 서울시 주택보급사업에 태양광, 지열 시스템 설치 사업에 참여하였습니다. 또한, 당사는 ESCO사업을 통해 경험한 소각플랜트 수행실적을 바탕으로 부산 소재의 산업용 폐기물 중간처분업체를 인수하여 정상화 작업을 위한 EPC사업을 진행하고 있으며, 부산권역에 산업용 폐기물 중간 처분 업체는 당사의 종속회사인 HLB에너지를 포함하여 2곳 밖에 존재하지 못한 상황이므로 설비 재구축 후 고단가의 산업폐기물을 처리할 수 있는 고정거래선을 확보하고 가동률을 높여 매출 확대 및 수익성을 개선할 예정입니다. 또한 폐기물 처리의 부산물인 스팀을 판매하는 사업과 발전 설비를 가동하는 등 추가 수익을 계획하고 있습니다.
바. 매출 및 수주상황
당사는 거래처별 수익인식 회계처리(재화 인도기준) 방식으로 매출인식을 하고 있으며, 당분기는 23,804백만원(전분기 31,166백만원 동기대비 23.6% 감소)의 매출을 달성하였습니다.
본 사업의 개요에 요약된 내용의 세부사항 및 포함되지 않은 내용 등은 "II. 사업의 내용"의 "2. 주요 제품 및 서비스"부터 "7. 기타 참고사항"까지의 항목에 상세히 기재되어 있으며 이를 참고하여 주시기 바랍니다.
2. 주요 제품 및 서비스
당사 및 종속회사의 주요 제품 및 서비스 현황은 다음과 같습니다.
가. 매출현황
| (기준일 : 2024년 03월 31일) | (단위 : 백만원,%) |
| 구 분 | 매출액 | 비 율 | ||
| 메디케어 사업 | HLB생명과학 | 제품매출 | 2,120 | 8.87 |
| 상품매출 | 1,530 | 6.40 | ||
| 기타매출 | 387 | 1.62 | ||
| 의료기기사업 | HLB생명과학 | 제품매출 | 1,940 | 8.12 |
| 상품매출 | 70 | 0.29 | ||
| 의약품 유통 사업 | 신화어드밴스 | 상품매출 | 16,849 | 70.51 |
| 에너지사업 | HLB에너지 | 용역매출 | 999 | 4.18 |
| 합 계 | 23,895 | 100.00 | ||
3. 원재료 및 생산설비
당사 및 종속회사의 원재료 및 생산설비 현황은 다음과 같습니다.
가. HLB생명과학 원재료 및 생산/설비
(1) 주요 원재료 현황
| (단위: 백만원) |
| 주요매입처 | 품목 | 매입액 | 비율(%) | 특수관계여부 | 독과점정도 | 비고 |
| (주)범석화학 | 사출원료 | 304 | 23.34 | - | - | - |
| ㈜부영흥산 | 사출원료 | 237 | 18.22 | - | - | - |
| ㈜영우코퍼레이션 | 주사기 Needle | 201 | 15.41 | - | - | - |
| 기타 | 주사기 생산외 | 560 | 43.03 | - | - | - |
| 합 계 | 1,302 | 100.00 | - | - | - | |
| ※ 주요 원재료 가격 변동 추이 당사 제품의 원재료 등은 종류가 매우 다양하고 세부 사양과 가격이 상이합니다. 또한 지속적으로 신규 제품을 개발하고 원재료 등을 교체하며 제품을 개선해 가고 있어 원재료의 가격변동 추이를 산출할 만한 자료가 부족하고 거래처 및 경쟁사에 누출될 경우 당사의 사업경쟁력에 영향을 미칠 수 있어 원재료 가격변동 추이의 기재를 생략합니다. |
(2) 생산 및 설비
- 주요 생산능력, 생산실적, 가동률
| (단위: 백만개) |
| 사업부문 | 품목 | 소재지 | 2024년 당분기 | 2023년 | 2022년 | ||||||
| 생산능력 | 생산실적 | 가동률 | 생산능력 | 생산실적 | 가동률 | 생산능력 | 생산실적 | 가동률 | |||
| 메디케어사업 | 사출품 화장품용기 등 |
안성 | 20 | 10 | 50% | 230 | 77 | 33% | - | - | - |
| 의료기기사업 | 주사기 | 안성 | 41 | 11 | 27% | 44 | 22 | 49% | |||
| 천안 | 42 | 19 | 44% | 42 | 14 | 33% | - | - | - | ||
| 주1) 생산능력 산출근거 시간(1H) ÷Cycle Time ×cvt수X 일 생산시간(23) X 월 생산일(22) |
- 생산설비에 관한 현황
| 사업장 | 소재지 | 구분 |
|
안성1사업장 |
경기 안성시 공도읍 용두리 443-9 |
보유 |
|
안성2사업장 |
경기 안성시 공도읍 용두리 453-4 |
보유 |
| 천안 사업장 | 충청남도 천안시 동남구 성남면 성심원길 20 | 보유 |
- 생산설비 등의 현황
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 백만원) |
| 구 분 | 기 초 | 취 득 | 처 분 | 감가상각비 | 기 타 | 기 말 |
| 토지 | 12,509 | - | - | - | - | 12,509 |
| 건물 | 17,585 | - | - | (118) | - | 17,467 |
| 구축물 | 68 | - | - | (3) | - | 65 |
| 차량운반구 | 71 | 4 | - | (10) | - | 65 |
| 공구와기구 | 1,748 | 67 | - | (132) | - | 1,683 |
| 비품 | 599 | 7 | - | (57) | (2) | 547 |
| 기계장치 | 10,062 | 103 | (18) | (316) | 230 | 10,061 |
| 시설장치 | 1,649 | 21 | - | (88) | (8) | 1,574 |
| 건설중인자산 | 394 | 219 | - | - | (230) | 383 |
| 합 계 | 44,685 | 421 | (18) | (724) | (10) | 44,354 |
- 시설투자 현황
2024년 당분기 중 신사업 및 신축투자에 21백만원을 사용하였습니다. 기투자된 시설을 활용하여 시장상황에 맞춰 탄력적으로 대응할 예정이며, 사출품 및 의료용품의 중장기적 경쟁력 확보를 위한 투자에 자금을 집행할 계획입니다.
|
[2024년 당분기말 부문별 시설투자금액] |
(단위 : 백만원) |
|
구 분 |
구 분 |
내 용 |
대상자산 |
투자액 |
비 고 |
|
메디케어사업 |
의료용품 |
신ㆍ증설, 보완 등 |
설비 및 기구 | 7 | - |
| 기타 | 신ㆍ증설, 보완 등 | 건물,시설 및 기계 | 22 | - | |
| 의료기기사업 | 의료용품 |
신ㆍ증설, 보완 등 |
설비 및 기구 | - | - |
| 기타 | 신ㆍ증설, 보완 등 | 건물,시설 및 기계 | - | - | |
| 합 계 | 29 | - | |||
나. HLB셀 원재료 및 생산/설비
1) 주요 원재료 현황
| (단위: 백만원) |
| 주요매입처 | 품목 | 매입액 | 비율(%) | 특수관계여부 | 독과점정도 | 비고 |
| 범석화학 | PP(SJ-170) 외 | 43 | 100 | - | - | - |
| ※ 주요 원재료 가격 변동 추이 당사 제품의 원재료 등은 종류가 매우 다양하고 세부 사양과 가격이 상이합니다. 또한 지속적으로 신규 제품을 개발하고 원재료 등을 교체하며 제품을 개선해 가고 있어 원재료의 가격변동 추이를 산출할 만한 자료가 부족하고 거래처 및 경쟁사에 누출될 경우 당사의 사업경쟁력에 영향을 미칠 수 있어 원재료 가격변동 추이의 기재를 생략합니다. |
- 주요 생산능력, 생산실적, 가동률
| (단위: 백만개) |
| 사업부문 | 품목 | 소재지 | 2024년 당분기 | 2023년 | 2022년 | ||||||
| 생산능력 | 생산실적 | 가동률 | 생산능력 | 생산실적 | 가동률 | 생산능력 | 생산실적 | 가동률 | |||
|
사출품 |
BOTTLE 검사용 디바이스 기타 플라스틱 사출물 등 |
안성 |
25 | 16 | 64% | 149 | 106 | 71% | 108 | 6 | 6% |
| 주1) 생산능력 산출근거 시간(1H) ÷Cycle Time ×cvt수X 일 생산시간(23) X 월 생산일(22) |
- 생산설비에 관한 현황
| 사업장 | 소재지 | 구분 |
| 안성지점 | 경기도 안성시 용머리큰길 104 | 임차 |
- 생산설비 등의 현황
| (기준일 : | 2024년 03월 31일) | (단위 : 백만원) |
| 구 분 | 기 초 | 취 득 | 처 분 | 감가상각비 | 손상 | 연결범위조정 | 환율변동효과 | 기 말 |
| 기계장치 | 1,502 | 3 | - | (577) | - | - | - | 929 |
| 차량운반구 | 25 | - | - | (10) | - | - | - | 15 |
| 시설장치 | 10 | - | - | - | - | - | - | 9 |
| 사용권자산 | 49 | - | - | (41) | - | - | - | 8 |
| 합 계 | 1,586 | 3 | - | (629) | - | - | - | 960 |
다. 신화어드밴스 주요 상품 매입현황
| (기준일 : 2024년 03월 31일) | (단위 : 백만원) |
| 사업부문 | 매입유형 | 품목 | 구체적용도 | 매입액 | 비 고 |
| 의약품유통 | 상품 | 의약품 | 의약품판매 | 1,290 | - |
4. 매출 및 수주상황
당사 및 종속회사의 매출 및 수주상황은 다음과 같습니다.
가. 매출실적
| (기준일 : 2024년 03월 31일) | (단위 : 백만원,%) |
| 구분 | 매출액 | |||||||
| 2024년 당분기 | 2023년 | 2022년 | ||||||
| 금액 | 비중 | 금액 | 비중 | 금액 | 비중 | |||
| 메디케어사업 | HLB생명과학 | 제품매출 | 2,120 | 8.87 | 13,272 | 13.54 | 16,777 | 16.85 |
| 상품매출 | 1,530 | 6.40 | 10,776 | 11.00 | 15,508 | 15.57 | ||
| 용역매출 | - | - | - | - | 2,141 | 2.15 | ||
| 임대매출 | 387 | 1.62 | 897 | 0.92 | 258 | 0.26 | ||
| 기타매출 | - | - | - | - | 94 | 0.09 | ||
| HLB셀 | 제품매출 | - | - | 3 | 0.00 | 64 | 0.06 | |
| 상품매출 | - | - | - | - | 160 | 0.16 | ||
| 바이오 개발 사업 | HLB셀 | 용역 매출 | - | - | - | - | 93 | 0.09 |
| HLB생명과학 R&D | 용역 매출 | - | - | - | - | 18 | 0.02 | |
| 의료기기사업 | HLB생명과학 | 제품매출 | 1,940 | 8.12 | 4,268 | 4.36 | - | - |
| 상품매출 | 70 | 0.29 | 106 | 0.11 | - | - | ||
| 의약품유통사업 | 신화어드밴스 | 상품 매출 | 16,849 | 70.51 | 63,412 | 64.71 | 54,058 | 54.28 |
| 에너지사업 | HLB솔루션(*) | ESCO(에너지 절약) | - | - | - | - | 1,824 | 1.83 |
| 신재생에너지(태양광 및 지열) | - | - | 1,362 | 1.39 | 4,062 | 4.09 | ||
| 임대매출 | - | - | - | - | 260 | 0.26 | ||
| 기타매출 | - | - | 406 | 0.41 | 8 | 0.01 | ||
| HLB에너지 | 용역매출 | 999 | 4.18 | 3,487 | 3.56 | 4,266 | 4.28 | |
| 합 계 | 23,895 | 100.00 | 97,990 | 100.00 | 99,591 | 100.00 | ||
| (*) 2023년 9월 18일 에너지사업부 회사분할 결정하였으며, 2024년 1월 1일 분할신설회사 HLB솔루션을 설립하였습니다. |
나. 영업 및 판매전략 등
(1) 영업전략
메디케어 사업
- 당사는 품질 경영 시스템을 기반으로 지속적인 제품의 품질 개선을 지향하고 있으며, R&D 조직과 시설, 장비에 대한 공격적인 투자를 통해 새로운 제품들을 꾸준히 개발하고 있습니다. 그 결과 150여 종에 달하는 개발 성과를 성공적으로 이뤄냈으며 다수의 기술 특허와 디자인 특허를 출원하였습니다.
- COVID-19 Pandemic에서 OEM/ODM 기술력으로 Global Market Leader들과의 협업을 진행하였으며 긴급한 상황 속에서도 대량 생산과 고품질을 유지하여 국내외 COVID-19 진단산업에 많은 기여를 하였습니다.
- 단기 매출 성과를 위해 Bio-infra 사업 부문에서는 국내/외 제조사로부터 상품을 사입 하여, 전국 딜러 망 이용 및 직접 영업을 통해 매출을 이루며, 국내 굴지의 기업 및 대학, 연구소 시험 소모품 및 시약 공급 계약 체결을 하고 있습니다.
- 기존의 RDT 시장에서의 영업, 제조, 품질 보증 및 인허가 노하우를 통하여 전자/요식업/화장품/제약 등의 신규 시장에 대한 OEM / ODM 개발 Project를 진행하며, 중/장기적인 Cash cow의 역할을 할 수 있는 사업을 목표로 합니다. 또한, 제조 GMP 승인 및 Roche 감사 등의 자체적인 품질/인허가 대응 노하우를 통해 Validation consulting을 진행중에 있으며, Quality management consulting 사업 시작 예정에 있습니다.
- 지속 다변화의 최종 소비자를 위한 B2C 사업 중 유아, 실버케어를 위한 제품의 지속적인 개발 및 런칭을 계획하며, 실행 중에 있습니다.
(2) 판매전략
① 의약품유통 사업
|
사업목표 및 전략 |
전략 과제 |
- 의약품 및 진료재료 유통 시장 확대 |
|
전략 방침 |
- 요양기관 등 신규 거래선 확보 |
|
|
세부 목표 및 전략 |
1) 종합병원 및 세미병원 신규 진입 |
|
② 메디케어 사업
|
사업목표 및 전략 |
전략 과제 |
- 자사개발품 시장진출 및 위탁생산 확대 |
|
전략 방침 |
- 자사개발품 카테고리 확장 - 해외시장 마케팅 강화 및 자사개발품 홍보 - 위탁생산 제조원가 절감 - 영업전략본부를 통한 위탁생산 및 판매/수주 촉진 |
|
|
세부 목표 및 전략 |
1) 국내/외 시장조사 - 국내/외 체외진단 기업 분석 - 글로벌 IVD 동향 분석 - R&D 방향 설정 및 Needs에 따른 개발 2) 국가별 타겟 제품 선정 - 국가/지역별 감염, 진단 현황 분석 - 마케팅 채널별 주력상품 별도 선정 3) 대량 생산/제조능력 강화 - 생산 공정별 검토 및 개선을 통한 제조원가 절감 - 엔지니어링 강화를 통한 공정 자동화 4) 신규거래처 발굴 및 거래처 영업 강화 - 국내/외 위탁생산 및 제조능력 강조 홍보물 제작 - 학술마케팅 지원을 통한 전문성 및 영업력 강화 |
|
③ 의료기기 사업
| 사업목표 및 전략 | 전략 과제 | - 제조기술 및 노하우를 바탕으로 고객만족 실현 |
| 전략 방침 |
- 국내외 유통망 확장 - 영업 & 마케팅 능력 강화 |
|
| 세부 목표 및 전략 |
- 품목다변화를 통한 국내,외 영업확장 - 생산 전문성강화 및 효율성 극대화 - 산.학협력을 통한 혁신제품개발 확대 - 임상적/학술적 영업 & 마케팅 활동강화 - 품질향상을 통한 경쟁력 강화 - 공급의 안정성 제고 - SCM 서비스 확대 |
|
라. 향후 수주 및 영업계획
- 회사 정책상 비공개 진행
5. 위험관리 및 파생거래
연결회사의 주요 금융부채는 차입금과 매입채무및기타채무로 구성되어 있으며, 이러한 금융부채는 영업활동을 위한 자금을 조달하기 위해 발생하였습니다. 또한, 연결회사는 영업활동에서 발생하는 현금, 예금, 단기예치금, 매출채권, 기타채권, 매도가능금융자산 등을 보유하고 있습니다.
연결회사의 금융상품에서 발생할 수 있는 주요 위험은 시장위험, 신용위험 및 유동성위험입니다. 연결회사의 경영진은 위험관리를 감독하고 있으며, 감독업무 수행 시 아래에서 설명하는 바와 같이 각 위험별 관리정책 부합 여부를 검토하고 있습니다.
가. 시장위험
시장위험은 시장가격의 변화로 인하여 금융상품의 미래현금흐름에 대한 공정가치가 변동될 위험입니다. 시장위험은 환율변동위험, 이자율위험 및 기타 가격위험의 세가지 유형의 위험으로 구성되어 있습니다. 시장위험에 영향을 받는 주요 금융상품은 차입금,예금 및 매도가능금융자산입니다.
다음의 민감도 분석은 당분기말 및 전기말과 관련되어 있으며 분석대상 변수 외에 다른사항은 모두 동일하다고 가정하였습니다.
(1) 이자율 위험
이자율위험은 시장이자율의 변동으로 인하여 금융상품의 공정가치나 미래현금흐름이 변동할 위험입니다. 연결회사는 변동이자부 장기차입금과 관련된 시장이자율 변동위험에 노출되어 있습니다. 당분기말 및 전기말 현재 이자율변동위험에 노출된 변동이자부 차입금의 장부금액은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 |
| 변동이자부차입금 | 59,940,000 | 38,835,000 |
아래의 표는 차입금에 대해 합리적인 범위내에서 가능한 이자율변동이 미치는 효과에 대한 민감도 분석결과입니다. 다른 모든 변수가 일정하다고 가정할 때 연결회사의당기순손익은 변동이자부차입금으로 인해 다음과 같은 영향을 받습니다.
| (단위: 천원) |
| 구 분 | 당분기 | 전기 | ||
| 100bp 상승 | 100bp 하락 | 100bp 상승 | 100bp 하락 | |
| 변동이자부차입금 | (474,125) | 474,125 | (307,185) | 307,185 |
(2) 환율변동위험
환율변동위험은 환율변동으로 인하여 금융상품의 미래현금흐름에 대한 공정가치가 변동될 위험입니다. 연결회사가 수익이나 비용이 연결회사의 기능통화와 다른 통화로 발생하는 영업활동으로 인해 환율변동위험에 노출되어 있습니다. 당분기말 및 전기말 현재 연결회사의 외화자산 및 부채의 내역은 다음과 같습니다.
| (외화단위: USD,EUR,CNY,SEK / 원화단위: 천원) |
| 구 분 | 화폐단위 | 당분기말 | 전기말 | ||
| 외화 | 원화 | 외화 | 원화 | ||
| 화폐성 외화자산 | USD | 140,527.07 | 189,262 | 2,824,560.68 | 3,641,989 |
| EUR | - | - | 0.62 | 1 | |
| 화폐성 외화부채 | USD | 76,882.50 | 103,545 | 115,368.92 | 148,757 |
| CNY | 83,953.20 | 15,594 | 101,779.00 | 18,406 | |
당분기말 및 전기말 현재 다른 모든 변수가 일정하고 주요 외화에 대한 원화환율이 10% 변동 시 상기 자산부채 등으로부터 발생하는 환산손익이 당기순손익에 미칠 영향은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 | ||
| 10% 상승시 | 10% 하락시 | 10% 상승시 | 10% 하락시 | |
| 화폐성 외화자산 | 1,497 | (1,497) | 288,081 | (288,081) |
| 화폐성 외화부채 | (942) | 942 | (13,223) | 13,223 |
(3) 기타가격위험
기타 가격위험은 이자율위험이나 환위험 이외의 시장가격의 변동으로 인하여 금융상품의 공정가치나 현금흐름이 변동할 위험입니다. 연결회사는 당기손익-공정가치 측정 금융자산과 기타포괄손익-공정가치 측정 금융자산의 가격변동위험에 노출되어 있습니다. 당분기말 및 전기말 현재 시장성 있는 금융자산 및 금융부채의 내역은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 |
| 시장성 있는 지분증권 | 224,701,420 | 143,387,678 |
당분기말 및 전기말 현재 다른 모든 변수가 일정하고 상기 자산부채의 공정가치가 10% 변동할 경우에 향후 1년간의 총포괄손익에 미칠 영향은 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 | ||
| 10% 상승시 | 10% 하락시 | 10% 상승시 | 10% 하락시 | |
| 당기손익-공정가치 측정 금융자산 | 17,773,882 | (17,773,882) | 11,341,965 | (11,341,965) |
나. 신용위험
신용위험은 거래상대방이 의무를 이행하지 않아 재무손실이 발생할 위험입니다. 연결회사는 영업활동과 재무활동에서 신용위험에 노출되어 있습니다.
(1) 금융자산
금융자산의 장부금액은 신용위험에 대한 최대 노출정도를 나타내고 있습니다. 당분기말과 전기말 현재 연결회사의 신용위험에 대한 최대 노출정도는 다음과 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 |
| 매출채권 | 12,975,102 | 11,457,320 |
| 장기매출채권 | - | - |
| 유동-당기손익-공정가치측정금융자산 | 92,041,018 | 50,793,156 |
| 비유동-당기손익-공정가치측정금융자산 | 224,701,420 | 108,477,906 |
| 비유동-기타포괄손익-공정가치측정금융자산 | 225,253 | 225,253 |
| 기타유동금융자산 | 2,491,406 | 4,379,886 |
| 기타비유동금융자산 | 534,927 | 554,697 |
| 합 계 | 332,969,126 | 175,888,218 |
연결회사는 상기 채권에 대해 매 보고기간말에 개별적 또는 집합적으로 손상여부를 검토하고 있습니다.
연결회사는 매출채권 및 기타채권, 기타금융자산에 대해 발생할 것으로 예상되는 손실에 대해 충당금을 설정하고 있습니다. 연결회사는 개별분석 및 과거의 대손경험률에 의한 추산액에 근거하여 충당금을 설정하고 있습니다.
(2) 기타자산
현금, 단ㆍ장기예금 등으로 구성되는 연결회사의 기타자산으로부터 발생하는 신용위험은 거래상대방의 부도 등으로 발생합니다. 이러한 경우 연결회사의 신용위험 노출정도는 최대 해당 금융상품 장부금액과 동일한 금액이 될 것입니다. 한편, 연결회사는 신한은행 등의 금융기관에 현금및현금성자산 등을 예치하고 있으며, 신용등급이 우수한 금융기관과 거래하고 있으므로 금융기관으로부터의 신용위험은 제한적입니다.
(3) 유동성위험
유동성위험은 만기까지 모든 금융계약상의 약정사항들을 이행할 수 있도록 자금을 조달하지 못할 위험입니다.
연결회사는 당좌차월, 은행차입금, 사채 등을 사용하여 자금조달의 연속성과 유연성간의 조화를 유지하는 것을 목적으로 하고 있습니다.
당분기말 및 전기말 현재 할인되지 않은 계약상 현금흐름에 근거하여 작성된 금융부채의 만기정보는 다음과 같습니다.
| <당분기말> | (단위: 천원) |
| 구 분 | 1년 이하 | 1년 이상 | 합 계 |
| 매입채무 | 6,199,116 | - | 6,199,116 |
| 미지급금 | 2,977,812 | 286,427 | 3,264,240 |
| 미지급비용 | 385,383 | - | 385,383 |
| 임대보증금 | 85,000 | 740,000 | 825,000 |
| 단기차입금 | 30,220,000 | 30,220,000 | |
| 장기차입금 | - | 16,300,000 | 16,300,000 |
| 전환사채 | - | 37,100,000 | 37,100,000 |
| 신주인수권부사채 | 80,600,569 | - | 80,600,569 |
| 금융리스부채 | 774,939 | 280,798 | 1,055,736 |
| 합 계 | 121,242,820 | 54,707,225 | 175,950,045 |
| <전기말> | (단위: 천원) |
| 구 분 | 1년 이하 | 1년 이상 | 합 계 |
| 매입채무 | 5,160,179 | - | 5,160,179 |
| 미지급금 | 4,367,951 | 262,983 | 4,630,934 |
| 미지급비용 | 422,547 | - | 422,547 |
| 임대보증금 | 70,000 | 740,000 | 810,000 |
| 단기차입금 | 10,528,910 | - | 10,528,910 |
| 장기차입금 | 7,751,408 | 26,859,329 | 34,610,737 |
| 전환사채 | 16,526,851 | 37,267,461 | 53,794,312 |
| 신주인수권부사채 | 87,857,303 | - | 87,857,303 |
| 금융리스부채 | 1,017,049 | 543,201 | 1,560,250 |
| 합 계 | 133,702,198 | 65,672,974 | 199,375,172 |
다. 자본위험관리
자본관리의 주 목적은 연결회사의 영업활동을 유지하고 주주가치를 극대화하기 위하여 높은 신용등급과 건전한 자본비율을 유지하기 위한 것입니다.
연결회사는 자본구조를 경제환경의 변화에 따라 수정하고 있으며, 동일 산업의 다른 기업과 마찬가지로 자본조정 후 부채비율에 기초하여 자본을 관리합니다. 이 비율은 순부채를 조정자본으로 나누어 계산합니다. 순부채는 부채총계(재무상태표에 표시된것)에서 현금및현금성자산을 차감하여 계산합니다.
한편, 기중 자본관리의 목적, 정책 및 절차에 대한 어떠한 사항도 변경되지 않았습니다.
당분기말 및 전기말 현재 부채비율은 아래와 같습니다.
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 |
| 부채총계 | 196,710,904 | 192,287,513 |
| 차감: 현금및현금성자산 | (55,569,341) | (16,768,575) |
| 순부채 | 141,141,563 | 175,518,938 |
| 자본총계 | 432,842,765 | 231,212,934 |
| 부채비율(%) | 32.61 | 75.91 |
라. 파생상품 등에 관한 사항
(1) 파생상품계약 체결 현황
당사는 이자율위험을 관리하기 위하여 이자율스왑의 파생상품계약을 체결하고 있습니다.
파생상품은 최초 인식시 계약일의 공정가치로 측정하고 있으며, 후속적으로 매 보고기간 말의 공정가치로 재측정하고 있습니다. 파생상품을 위험회피수단으로 지정하지않거나 위험회피에 효과적이지 않다면 파생상품의 공정가치변동으로 인한 평가손익은 즉시 당기손익으로 인식하고 있습니다. 파생상품을 위험회피수단으로 지정하고 위험회피에 효과적이라면 당기손익의 인식시점은 위험회피관계의 특성에 따라 좌우됩니다.
공정가치가 정(+)의 값을 갖는 파생상품은 금융자산으로 인식하며, 부(-)의 값을 갖는파생상품을 금융부채로 인식하고 있습니다. 법적으로 집행가능한 상계권리가 없거나상계할 의도가 없다면 재무상태표상 파생상품은 상계하지 아니합니다. 파생상품은 파생상품의 잔여만기가 12개월을 초과하고 12개월 이내에 실현되거나 결제되지 않는 경우에는 비유동자산 또는 비유동부채로 분류하고 있습니다. 기타 파생상품은 유동자산 또는 유동부채로 표시하고 있습니다.
(2) 리스크관리에 관한 사항
- 당사의 환위험 노출 등에 있어 리스크 관리는 환차익의 실현이 아닌 환차손위험의 제거이며, 당사는 사업특성상 외환거래가 빈번하지 않은 관계로 경영기획팀에서 환율의 변동 추이와 회사의 자금상황을 고려하여 선물환 등의 헷징방법을 다각적으로 검토하여 리스크 관리를 하고 있으나, 리스크 관리만을 전담하는 별도의 조직은 구성되어 있지 않습니다.
6. 주요계약 및 연구개발활동
□ 주요계약 현황
| <라이센스인 계약 총괄표> (단위: 백만원) |
| 대상회사 |
품 목 |
계약상대방 |
대상지역 |
계약체결일 |
계약종료일 |
총계약금액 |
지급금액 |
|
HLB생명과학 |
리보세라닙 (Rivoceranib) |
부광약품 |
대한민국, |
2018.08.14 |
유효특허만료일까지 |
44,697 |
40,167 |
| HLB생명과학 | 파이로티닙 (Pyrotinib) |
항서제약 Jiangsu Hengrui Medicine Co., Ltd., (CHN) |
대한민국 | 2020.09.28 | 항서제약에 비용 지급 만료시점까지 |
4,929 | 1,995 |
| HLB셀 |
생분해성 의료용 접착제 |
(재) 유타 인하 디디에스 및 |
전세계 |
2015.11.05 |
2034.07.15 |
550 |
350 |
| HLB생명과학 R&D | G2M Project |
엘에스케이엔알디오 |
대한민국, 미국일본, 영국 프랑스, 독일 폴란드, 헝가리중국, 인도 |
2022.01.17 | 엘에스케이엔알디오에 계약금 전액 지급 만료시점까지 | 130 | 130 |
| HLB생명과학 R&D | CDK inhibitor |
Lead Discovery Center GmbH (LDC) |
전세계 | 2023.08.01 | - | 비공개 | 비공개 |
|
합 계 |
50,306 | 42,642 | |||||
1) 품 목 : 리보세라닙(Rivoceranib)
|
계약상대방 |
부광약품, Elevar Therapeutics, Inc.(구,HLB USA, Inc.) |
|
계약내용 |
Rivoceranib에 대한 한국 내 독점 개발, 판권 및 일본, 유럽에 대한 수익 지분(14.5%) 허여 |
|
대상지역 |
대한민국, 일본, 유럽 |
|
계약기간 |
유효특허의 만료일까지 (2029년 6월 예상) |
|
총계약금액 |
총 447억원 |
|
지급금액 |
총 401억 7천만원 |
|
계약조건 |
1) 부광과 Elevar Therapeutics, Inc.(구,HLB USA, Inc.)(*)간의 계약조건 그대로 양도양수 (한국내 독점개발, 판매권 및 유럽, 일본에 대한 수익 지분) |
| 회계처리 | 매수금액 및 개발 마일스톤 401억 7천만원은 반환의무 및 조건이 없고 관련하여 수행할 추가적인 의무가 존재하지 않아 신약연구개발 라이선스 자산으로 인식함. |
| 대상기술 | 경구용 제품이며, 광범위하게 적용되는 항암제로 진행형 고형암(위암, 대장암, 간세포암, 폐암(비소세포암), 유방암, 중피종, 신세포암, 신경내분비종양)에서 신생혈관 억제, 직접적인 항종양 효과, 면역세포의 활성화를 통해 항암효과가 있음. |
|
기타사항 |
Elevar Therapeutics, Inc. 는 2009년 12월 부광약품㈜에게 리보세라닙의 한국 판권을 양도하는 조건으로 리보세라닙 공동개발을 하였으며, 이후 부광약품㈜은 2018년 08월 한국 판권에 대한 모든 권리 및 의무를 HLB생명과학으로 400억원에 양도하였습니다. (2018.8.14 공시 참조) |
2) 품 목 : 생분해성 의료용 접착제 또는 실란트 조성물
|
계약상대방 |
(재) 유타 인하 디디에스 및 신의료기술개발 공동연구소 |
|
계약내용 |
(재) 유타 인하 디디에스 및 신의료기술개발 공동연구소는 생분해성 의료용 접착제 또는 실란트 조성물의 계약지적재산권에 대한 기술이전 및 전세계 전용 실시권을 제공한다. |
|
대상지역 |
전 세계 |
|
계약기간 |
계약체결일: 2015.11.05 계약종료일: 지적재산권 만료 시까지(2034.07.15) |
|
총계약금액 |
550백만원, 로열티는 별도 |
|
지급금액 |
<환수 불가능 금액> 계약금(Upfront Payment): 350백만원, 2015년 11월 지급 |
|
계약조건 |
계약금(Upfront Payment): 350백만원 - 지급조건: 계약 체결 시 마일스톤(Milestone): 비공개 로열티(Royalty): 비공개 |
|
회계처리방법 |
해당 파이프라인의 비용은 경상연구개발비로 인식하고, 국책과제 참여부분은 국고보조금으로 인식 |
|
대상기술 |
생분해성 의료용 접착제 또는 실란트 조성물에 관한 기술로 수술용 지혈제, 창상피복재, 지혈작용과 창상피복을 촉진시키는 약물 혹은 치료효능을 향상시킬 수 있는 기능을 가진 구성성분을 추가하여 개발된 수술용 지혈제 및 창상피복재에 대한 것으로 치과용과 내시경용은 제외한다. |
|
기타사항 |
- |
3) 품 목 : 파이로티닙(Pyrotinib)
|
계약상대방 |
항서제약 (Jiangsu Hengrui Medicine Co., Ltd., 중국) |
|
계약내용 |
파이로티닙(Pyrotinib)의 개발, 허가, 판매에 대한 국내 독점권한 및 생산에 대한 선택적 권한 허여 (API 생산 미포함) |
|
대상지역 |
대한민국 |
|
계약기간 |
계약체결일: 2020.09.28 계약종료일: 비용지급 만료 시까지 |
|
총계약금액 |
4,929백만원, 로열티는 별도 |
|
지급금액 |
<환수 불가능 금액> |
|
계약조건 |
계약금(Upfront Payment): 1,995백만원 - 지급조건: 계약 체결 시 마일스톤(Milestone): 로열티(Royalty): |
| 회계처리방법 | 계약금 1,995백만원은 반환의무 및 조건이 없고 관련하여 수행할 추가적인 의무가 존재하지 않아 신약연구개발 라이선스 자산으로 인식함. |
| 대상기술 | EGFR, HER2, HER4를 특이적으로 억제하는 표적항암제이며, 주요 적응증은 HER2(+) 전이성 유방암 또는 HER2 변이성 (엑손20 삽입) 비소세포폐암을 포함한 다양한 암종이 될 수 있음. |
|
기타사항 |
- |
4) 품 목 : G2M Project
|
계약상대방 |
엘에스케이엔알디오(LSK NRDO) |
|
계약내용 |
세포주기 관련 신규 항암 후보 물질 및 관련 특허 일체와 국내외 권리를 양도 받음 |
|
대상지역 |
대한민국, 미국, 일본, 영국, 프랑스, 독일, 중국, 인도, 폴란드, 헝가리 |
|
계약기간 |
계약체결일: 2022.01.17 계약종료일: 계약금 전액 지급 만료시점까지 |
|
총계약금액 |
130백만원 |
|
지급금액 |
<환수 불가능 금액> 계약금(Upfront Payment): 30백만원, 2022년 2월 지급 |
|
계약조건 |
계약금(Upfront Payment): 30백만원 - 지급조건: 계약 체결 시 잔금 : 100백만원 - 지급조건 : 양도대상 자산이 완전히 양도 이전이 완료된 시점 |
| 회계처리 | 계약금 30백만원은 반환의무 및 조건이 없고 관련하여 수행할 추가적인 의무가 존재하지 않아 신약연구개발 라이선스 자산으로 인식함. |
| 대상기술 | - Cell cycle에 관련되는 신호를 모듈레이션하여 항암효과를 나타냄 - c-jun 및 FBW7 단백질을 포함하는 새로운 메커니즘 |
|
기타사항 |
- |
5) 품 목 : CDK inhibitor
|
계약상대방 |
Lead Discovery Center GmbH |
|
계약내용 |
CDK inhibitor의 개발 및 상업화에 대한 전세계 독점 권한 |
|
대상지역 |
전 세계 |
|
계약기간 |
계약체결일: 2023.08.01 계약종료일: - |
|
총계약금액 |
비공개, 로열티 별도 |
|
지급금액 |
<환수 불가능 금액> 계약금(Upfront Payment): 비공개 |
|
계약조건 |
계약금(Upfront Payment): 비공개 (지급조건: 계약 체결 시) 마일스톤(Milestone): 비공개 로열티(Royalty): 비공개 |
|
회계처리방법 |
계약금은 반환의무 및 조건이 없고 관련하여 수행할 추가적인 의무가 존재하지 않아 신약연구개발 라이선스 자산으로 인식함. |
|
대상기술 |
세포주기 조절 관여 및 암 단백질의 전사를 촉진하는 Cyclin-Dependent Kinase 저해제이며, 주요 적응증은 HER2(-) 전이성 유방암 또는 비소세포폐암, 난소암, 위암을 포함한 다양한 암종이 될 수 있음. |
|
기타사항 |
- |
□ 연구개발활동 현황
가. 연구개발활동의 개요
당사의 종속회사인 HLB생명과학 R&D 및 HLB셀의 연구개발조직은 항암제 신약, 바이오의약품(세포치료제), 의료기기에 대한 연구개발을 진행하고 있습니다. 그동안 신약을 연구개발해 오면서 축적된 기술력과 노하우를 바탕으로 글로벌 협업을 통해 새로운 파이프라인을 추가해가고 있으며 회사의 가치를 높이고 있습니다.
나. 연구개발 담당조직
1) 연구개발 조직 개요
당사의 연구개발조직은 HLB생명과학 R&D의 바이오사업본부 산하 5개팀과 신약연구소, 종속회사인 HLB셀의 의학연구소 산하 4개팀과 QA팀으로 구성되어 있으며, 그 현황은 다음과 같습니다.
| <연구개발 조직 구성> |
|
회사명 |
부서 |
팀 |
주요 업무 |
| HLB생명과학R&D | 바이오사업본부 | 신약연구소 | - 항암제 연구개발 |
| 사업개발팀 | - 라이센싱 (IN/OUT) 관련 제반 활동 | ||
| 오픈이노베이션팀 | - 국내외 우수 기술 검토 및 도입 타당성 분석 | ||
| 임상개발팀 | - 리보세라닙, 파이로티닙 등 임상관련 연구개발 | ||
| R&D기획팀 | - 신규과제 기획, 의료용대마/동물항암제 연구개발 | ||
| 바이오지원실 | IP팀 | - 특허 등 지적재산권에 대한 동향 분석, 관리, 전략 수립 | |
| 지원팀 | - 각종 기술 검토 | ||
|
HLB셀 |
의학연구소 |
공정개발팀 |
- 인간 세포외기질, 지혈제 공정개발 |
|
세포/의료기기팀 |
- 세포치료제 연구개발 |
||
|
분석연구팀 |
- 기준 및 시험법 확립 - Method validation |
||
| 개발전략팀 |
- 파이프라인 개발전략 수립 및 사업화 |
||
| QA팀 | - 임상시험용 의약품, 의료기기 품질 보증 | ||
<HLB생명과학R&D>
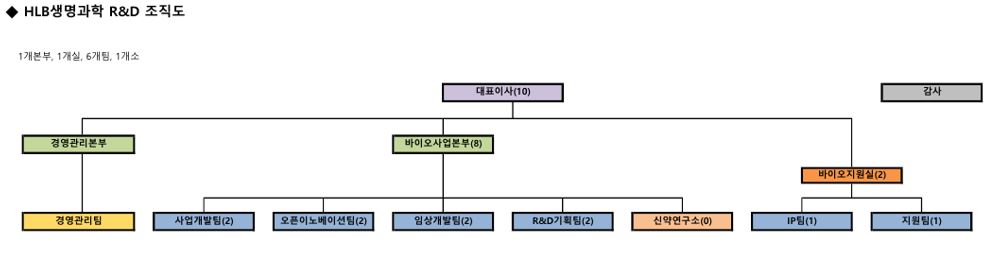 |
|
연구개발 조직도 |
<HLB셀>
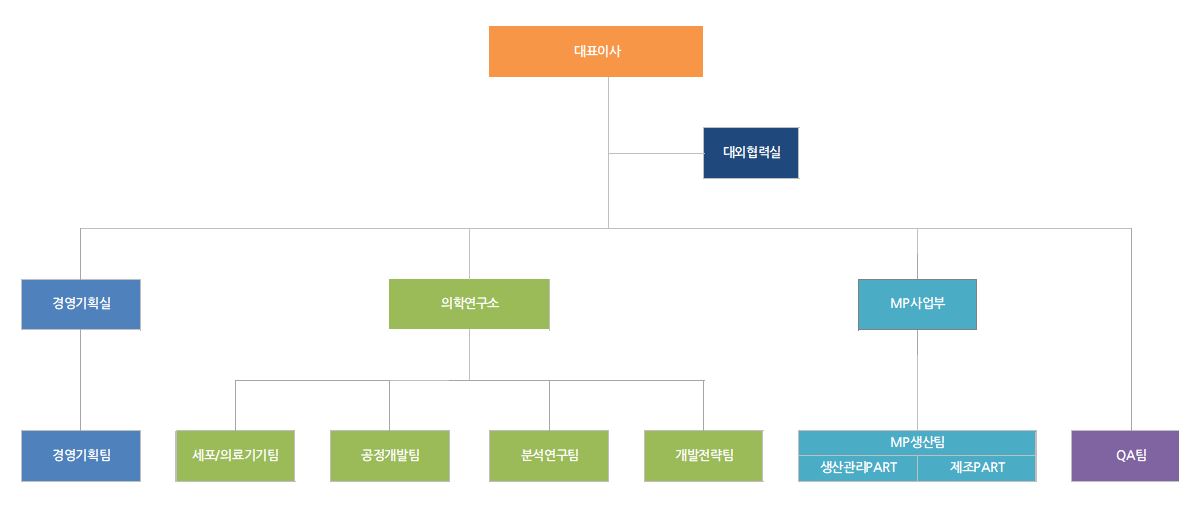 |
|
연구개발조직도 |
2) 연구개발 인력 현황
본 보고서 작성기준일 현재, 종속회사인 HLB생명과학R&D는 박사급 12명, 석사급 8명 등 총 25명의 연구인력을 보유하고 있으며, 종속회사인 HLB셀은 박사급 4명, 석사급 6명 등 총 17명의 연구인력을 보유하고 있으며, 그 현황은 다음과 같습니다.
| <연구개발 인력 현황> |
|
회사명 |
팀 |
인 원(단위 : 명) |
||||
|
박 사 |
석 사 |
기 타 |
합 계 |
|||
| HLB생명과학R&D | 대표이사 | 1 | - | - | 1 | |
| 부사장 | 1 | - | - | 1 | ||
| 바이오사업 |
신약연구소 |
4 |
4 |
- |
8 |
|
|
사업개발팀 |
- |
- |
1 |
1 |
||
|
오픈이노베이션팀 |
3 |
- |
- |
3 |
||
|
임상개발팀 |
- |
3 |
3 |
6 |
||
|
R&D기획팀 |
2 |
- |
- |
2 |
||
| 바이오지원실 | IP팀 | - | 1 | 1 | 2 | |
| 지원팀 | 1 | - | - | 1 | ||
| HLB셀 | 대표이사 | 1 | - | - | 1 | |
|
의학연구소 |
의학연구소 | 1 | - | - | 1 | |
| 공정개발팀 | 1 | - | 4 | 5 | ||
|
세포/의료기기팀 |
- | 3 | - | 3 | ||
|
분석연구팀 |
- | 1 | 2 | 3 | ||
| 개발전략팀 | 1 | 1 | - | 2 | ||
| QA팀 | - | 1 | 1 | 2 | ||
| 합 계 | 16 | 14 | 12 | 42 | ||
3) 핵심 연구인력
종속회사인 HLB생명과학R&D 및 HLB셀의 핵심 연구인력은 아래와 같습니다.
| <핵심 연구인력 현황> |
|
회사명 |
직 위 |
성 명 |
담당업무 |
주요 경력 |
주요 연구실적 |
| HLB생명과학R&D | 소장 | 강희범 | 연구개발 |
고려대학교 약리학 박사 전) 서울아산병원 연구교수 전) 티움바이오 수석연구원 전) 보로노이 수석연구원 전) 비에스티 소장 현) HLB생명과학R&D 신약연구소 소장 |
[학술 발표] 1. AACR(2019) Abstract B002: Discovery of selective and potent EGFR kinase inhibitors for exon20 insertion mutations. 2. Immune-Stimulating Effects of Dendropanax morbiferusBranch Extract via Improving Nitric Oxide and Cytokines in Raw264. 7 Macrophages.(2017).한국식품영양과학회한국식품영양과학회 학술대회발표집, p10326 - 326 3. Porphyra tenera extracts enhance immune stimulation activity via increasing cytokines in mouse primary splenocytes and RAW264. 7 macrophages.(2016).한국식품영양과학회 학술대회발표집, p502-502. 1. Catechol inhibits epidermal growth factor-induced epithelial-to-mesenchymal transition and stem cell-like properties in hepatocellular carcinoma cells. Sci Rep. 2020 May6;10(1):7620. Co-author:IF (4.52) 2. Inositol-triphosphate 3-kinase B confers cisplatin resistance by regulating NOX4-dependent redox balance. J Clin Invest. 2019 May 13;129(6):2431-2445 Co-author;IF (12.282) |
| HLB셀 |
대표이사 |
이두훈 |
사업총괄 |
동국대학교 공학 박사 전) 동국대학교 의생명공학과 겸임교수 |
[저서] Bioartificial Liver. Fundamentals of Tissue Engineering and Regenerative Medicine, Meyer, U.; Meyer, Eds., Springer [논문] 1. Hepatocyte Isolation, Culture, and Its Clinical Applications, 외 2건 (국내) 2. Functional Evaluation of a Bioartificial Liver Support System Using Immobilized Hepatocyte Spheroids in a Porcine Model of Acute Liver Failure 외 21건 (국외) |
| 연구소장 | 윤희훈 | 연구총괄 |
동국대학교 생물화학공학 박사 전) 동국대 의생명공학과 연구초빙교수 전) HLB셀 의학연구소 현) HLB셀 의학연구소장 |
[저서] Human Amniotic Epithelial Stem Cells in A Manual for Primary Human Cell Culture (편저) [논문] In vitro hepatic differentiation of umbilical cord-derived mesenchymal stem cell (Process Biochemistry) 외 42건 |
다. 연구개발비용
당사 및 종속회사의 최근 3년간 연구개발비용은 다음과 같습니다.
| <연구개발비용 현황 (연결 기준)> |
| (단위: 천원, %) |
|
구 분 |
당분기 |
전기 |
전전기 |
|
|
비용의 성격별 분류 |
재료비 | 547,977 | 1,191,767 | 1,009,110 |
| 인건비 | 393,139 | 1,454,786 | 1,298,109 | |
| 일반경비 | 436,336 | 2,807,937 | 2,042,002 | |
|
연구개발비용 합계 |
1,377,452 | 5,454,490 | 4,349,221 | |
|
(정부보조금) |
0 | - | - | |
|
보조금 차감 후 금액 |
1,377,452 | 5,454,490 | 4,349,221 | |
|
회계처리 내역 |
판매비와 관리비 |
1,377,452 | 5,454,490 | 4,349,221 |
|
제조경비 |
- | - | - | |
|
개발비(무형자산) |
- | - | - | |
|
회계처리금액 계 |
1,377,452 | 5,454,490 | 4,349,221 | |
|
연구개발비 / 매출액 비율 [연구개발비용합계÷당기매출액×100] |
5.79 | 5.57 | 4.37 | |
| (*) 연구개발비용은 발생액 기준이며, 정부과제로 받은 판관비가 포함되었고 판관비 상각액을 포함 |
| <연구개발비용 현황 (별도 기준)> |
|
(단위 : 천원, %) |
|
구 분 |
당분기 |
전기 |
전전기 |
|
|
비용의 성격별 분류 |
재료비 | - | - | 104,255 |
| 인건비 | - | - | 86,278 | |
| 일반경비 | 34,177 | 963,341 | 1,030,705 | |
|
연구개발비용 합계 |
34,177 | 963,341 | 1,221,238 | |
|
(정부보조금) |
- | - | - | |
|
보조금 차감 후 금액 |
34,177 | 963,341 | 1,221,238 | |
|
회계처리 내역 |
판매비와 관리비 |
34,177 | 963,341 | 1,221,238 |
|
제조경비 |
- | - | - | |
|
개발비(무형자산) |
- | - | - | |
|
회계처리금액 계 |
34,177 | 963,341 | 1,221,238 | |
|
연구개발비 / 매출액 비율 [연구개발비용합계÷당기매출액×100] |
0.14 | 3.26 | 5.91 | |
라. 연구개발실적
※ 연구개발 진행 현황 및 향후계획
본 보고서 제출기준일 현재 당사 및 종속기업이 보유한 파이프라인 연구개발 진행 중인 연구개발(Elevar Therapeutics, Inc.주도 글로벌 임상 포함) 현황은 다음과 같습니다.
| [연구개발 진행 총괄표] (주1) 연구개발 진행 총괄표는 분기보고서 제출일 기준으로 작성하였습니다. 주2) 통상적 통계적으로 유효성을 만족하는 수준의 임상데이터 수집이 완료되면 임상결과를 발표하나, 이는 임상의 완전한 종료를 뜻하는 바는 아닙니다. 모든 임상 참여 환자의 데이터가 축적된 후 임상결과보고서(CSR) 작성이 완료되면 공식적으로 임상시험이 종료됩니다. |
|
구 분 |
품 목 |
적응증 |
임상시작일 |
현재 진행단계 |
임상주도 기업 | ||||
|
단계(국가) |
승인일 |
비 고 | 회사명 | 비고 | |||||
|
화학합성 |
신약 |
리보세라닙 (Rivoceranib) [Elevar Therapeutics, Inc.주도 글로벌 임상 포함] |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안정성평가 완료 | Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|
위암 (3차/4차 단일요법) |
2017년 |
임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 | |||
|
위암 (1차 병용요법) |
2021년 |
임상2상 |
2021년 09월 (임상2상 승인일) |
임상 진행 중 | HLB생명과학 | Rivoceranib 한국 내 전용실시권 L/I 후 개발 |
|||
|
간암 (1차 병용요법) |
2019년 |
임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
- 임상 종료, 22년 9월 초록 발표(1차 평가 지표 만족) - 23년 5월 미국 FDA에 NDA Submission 완료 - 24년 5월 미국 FDA 수정 보완 요구(CRL 수령) |
Elevar | 항서제약과 공동개발 | |||
|
선양낭성암종 (1/2차 단일요법) |
2020년 |
임상2상 |
2020년 4월 (임상2상 개시일) |
임상 2상 종료 6월 초록 발표 |
Elevar HLB생명과학 |
Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
|
위암 (2차 병용요법) |
2018년 |
임상2상 |
2018년 10월 (임상1상 개시일) |
임상 종료 22년 결과 발표 |
HLB생명과학 | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
|
대장암 (3차 병용요법) |
2019년 |
임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 종료 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상 진행 중 (농림축산검역본부) |
HLB생명과학 | Rivoceranib 한국 내 전용실시권 L/I 후 자체 개발 |
|||
| 파이로티닙 (Pyrotinib) |
전이성 유방암 | 2023년 | 임상3상 (한국) |
2023년 03월 (임상계획 승인) |
임상3상 진행 중 | HLB생명과학 | Pyrotinib 한국 내 전용실시권 L/I 후 자체 개발 |
||
| 비소세포폐암 | 2020년 | 임상3상 (전세계 13개국) |
2020년 (임상계획 승인) |
임상3상 진행 중 | 항서제약 | Pyrotinib 한국 내 전용실시권 L/I 후 자체 개발 |
|||
|
HLS221-N01 G2M 억제제 |
폐암 유방암 대장암 췌장암 |
- |
비임상시험 단계 |
- |
비임상평가 진행 중 |
HLB생명과학 |
특허권 L/I 후 자체 개발 | ||
|
HLS222-N01 Cannabinoids derivatives |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
HLB생명과학 |
네오켄바이오와 공동연구 | ||
|
HLS232-N01 CDK 억제제 |
고형암 |
- |
탐색 단계 |
- |
후보물질 도출 중 |
HLB생명과학 |
LDC와 공동연구 | ||
|
HLS231-G01 의료용 대마 |
뇌전증 | - | 탐색 단계 | - | 제형 연구 중 | HLB생명과학 R&D |
- | ||
|
바이오 |
신약 |
바이오인공간 |
급성간부전 |
2001년 |
임상 2b상 |
2017년 임상 2a 완료 |
자체 개발 |
HLB셀 | - |
|
의료기기 |
지혈제 |
조직/장기 출혈 |
2015년 |
확증임상시험 |
2021년 임상계획 승인 |
확증임상 진행 중 |
HLB셀 | UI-DDS 연구소 글로벌 권리 L/I 후 자체 개발 |
|
| 연구용 재료 | 인체 세포 외 기질 (Hutrigel®-RU) |
줄기세포, 오가노이드 배양 기질 | N/A | 연구개발완료 | N/A | 제품판매 준비 중 |
HLB셀 | 자체 개발 | |
| 의료기기 | 인체 세포 외 기질 (Hutrigel®-MU) |
피부, 신경, 심근 등 상처 치유 및 조직 재생 |
N/A | 연구개발 중 | N/A | GMP-compliant , 비임상 유효성평가 준비 중 |
HLB셀 | 자체 개발 | |
|
의료기기 |
인체 세포 외 기질 (Hutrigel®-AU) |
의료용/미용용 기능성 제품 |
N/A |
연구개발 중 |
N/A |
제형화 및 생체 외 |
HLB셀 HLB제약 |
자체 개발 | |
|
주1) 당사는 2018년 8월 14일에 리보세라닙(아파티닙) 관련 부광약품에 인정되는 계약상 지위, 권리 및 의무 일체를 취득하여 연구개발을 진행하고 있습니다. (2018.8.14 공시 참조)
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1)품 목 : 리보세라닙(Rivoceranib)
| 구 분 | 화학합성의약품 |
| 적응증 | 위암 3/4차 치료제(Rivoceranib 단독), 위암 2차 치료제(파클리탁셀 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독), 간암 1차 치료제(항서제약 캄렐리주맙 병용), 대장암 3차 치료제(타이호제약 론서프 병용) |
| 작용기전 | 신생혈관억제, VEGFR2-TKI |
| 제품의특성 | 혈관내피세포성장인자수용체2(VEGFR-2)를 타켓으로 암 조직의 신생혈관 성장을 억제하고, 암세포의 증식억제와 면역세포의 정상화를 유도하는 경구용 표적 항암제입니다. |
| 진행경과 | 위암 3/4차 치료제: 단독 요법으로 글로벌 임상 3상 종료 위암 2차 치료제: 파클리탁셀과 병용으로 임상 1/2상 종료 선양낭성암 1,2차 치료제: 단독요법으로 미국, 한국에서 임상 2상 연구 종료, 한국 조건부 품목허가 신청 완료 (23년 2월), 식약처 보완요청에 따라 자진취하 (23년 12월) 간암 1차 치료제: 항서제약의 캄렐리주맙과 병용으로 글로벌 13개국 임상 3상종료, 22년 9월 ESMO에서 임상 결과 공개(1차 평가지표 만족), 23년 5월 미국 FDA에 NDA Submission 완료, 24년 5월 미국 FDA로부터 CRL(보완요구서한) 수령 대장암 3차 치료제: 타이호제약의 론서프와 병용으로 미국, 한국에서 임상 1b/2상 중 1b상 종료 |
| 향후계획 | 위암 3/4차 치료제(Rivoceranib 단독): 조건부 품목허가 및 임상 3상 계획수립 간암 1차 치료제(항서제약 캄렐리주맙 병용): FDA 재승인 신청 적응증 확대 계획 선낭암: 식약처 보완요청 자료 확보 후 품목허가 재신청 계획 |
| 경쟁제품 | 선양낭성암 1,2차 치료제: 표준치료제 없음(Off-label)로 치료 진행 간암 1차 치료제: 넥세바, 렌비마, 아바스틴, 티센트릭 |
|
관련논문등 |
선양낭성암 (선낭암) 중국 선낭암 임상 2상: 2021년 Therapeutic Advances in Medical Oncology 13 미국, 한국 선낭암 임상 2상 결과: 2022년 미국암학회 발표, 2023년 11월 Clinical Cancer Research 발표 간암 중국 간암 임상 2상: 2021년 Clin Cancer Res 15:27(4) 글로벌 간암 1차 치료제(항서제약 캄렐리주맙 병용) 임상 3상 결과: 2022년 9월 ESMO (유럽암학회)에서 공개 (1차 평가지표 만족) |
| 시장규모 | 선낭암 치료제 글로벌시장: 표준치료제가 없고 발병률이 낮아 글로벌 시장 규모 추산이 어려움 간암 치료제 글로벌시장: 2023년 8억1060만 달러 (약 1조 538억원)에서 2028년에는 12억5200만달러(약 1조 6275억원)로 성장 예상 ※시장규모 관련 출처 선낭암 데이터 - DataM Intelligence "Adenoid Cystic Carcinoma Market Size, Share, Industry, Forecast and Outlook (2023-2030)" (2023.09) 간암 데이터 - Market Data Forecast "Global Liver Cancer Therapeutics Market Size, Share, Trends, COVID-19 Impact & Growth Analysis Report - Segmented By Type, Therapeutics, End-User & Region - Industry Forecast (2023 to 2028)" (2023.03) |
| 기타사항 | 특허 및 권리 보유 현황 - 리보세라닙의 물질특허: HLB - 글로벌 전용실시권: Elevar - 한국 전용실시권: HLB생명과학 - 중국 전용실시권: 중국 항서제약 항서제약에서 2014년 위암 3차 치료제로 중국 내 시판허가를 득한 후 현재까지 꾸준한 매출 성장 유지 중입니다. 2015년 매출 약 450억에서 2018년 2,800억까지 매출 성장을 보여줘, 약효와 안전성을 입증하였습니다. 2021년 부터 간암 2차 치료제로 적응증을 확대하여, 중국 내 매출 확대가 기대됩니다. |
2)품 목 : 파이로티닙(Pyrotinib)
|
구 분 |
화학 합성 신약 | |||||||||||||||||||||
|
적응증 |
1) HER2 양성 전이성 또는 재발성 유방암 환자 2) HER2 exon20 돌연변이 비소세포폐암(NSCLC) |
|||||||||||||||||||||
|
작용기전 |
- EGFR (EGFR, HER2, HER3, HER4) 신호 전달 활성은 암세포에 있어서 성장과 분열, 전이를 일으키는 주요 원인으로 알려져 있음. - 특히, 15%-20%의 유방암 환자들은 HER2 수용체의 증가가 나타나고 있으며 매우 공격적인 성향을 띔. 비소세포폐암에서는 2-3% HER2 돌연변이가 나타나고 있음. - Pyrotinib은 EGFR, HER2, HER4 모두를 억제하는 약물로 하위 기전인 PI3K /AKT 및 MAPK의 신호 전달 기전을 차단하여 암세포의 증식, 분열, 생존을 억제하는 항암제임 |
|||||||||||||||||||||
|
제품의 특성 |
- Pyrotinib은 small molecule의 표적항암제로서 HER2 양성 고형암에 특이적으로 암세포 사멸을 유도함 - 해당 기전을 억제하는 약물들은 출시되어 있지만 부작용이 크거나 항암제 저항성이 생기는 현상이 일어남. 또한 충분한 생존 기간 연장 효과를 나타내지 못함. |
|||||||||||||||||||||
|
진행경과 |
[적응증: 전이성유방암] - 2021. 4Q 식약처와 pyrotinib의 국내 시판 가능에 대한 사전 검토 진행 - 2022. 3Q 임상시험계획 IND 제출 [적응증: 비소세포폐암] - 2020. 07 다국가, 다기관 임상시험에 한국 참여, 국내 IND 신청 (2020.07.24.) - 2020. 12 IND승인 (2020.12.22.) - 2021. 4Q 국내 연구 참여 기관 확대 - 2022. 1Q 국내 모집 목표 대상자 수 확대 - 2022. 4Q 시험 대상자 모집 완료 및 투약 진행 중 |
|||||||||||||||||||||
|
향후계획 |
- 전이성 HER2 양성 유방암의 허가 신청을 위한 임상 시험을 진행 예정임 - 유방암과 별도로 Pyrotinib에 대해 HER2 변이성(엑손20 삽입) 비소세포폐암(NSCLC)을 대상으로 하는 글로벌 임상3상 시험을 진행중이며, 향후 임상결과 확보 및 검토 후 한국 내 제품 허가를 목표로 함 [적응증: 전이성유방암] - 2027년 허가 목표 [적응증: 비소세포폐암] - 2027년 허가 목표 |
|||||||||||||||||||||
|
경쟁제품 |
[HER2 신호 전달 경로 관련 주요 항암제 개발 현황]
|
|||||||||||||||||||||
|
관련논문 등 |
논문 1) Dalpiciclib Combined With Pyrotinib and Letrozole in Women With HER2-Positive, Hormone Receptor-Positive Metastatic Breast Cancer (LORDSHIPS): A Phase Ib Study. Front Oncol. 2022 Mar 7;12:775081 2) Pyrotinib plus capecitabine for patients with human epidermal growth factor receptor 2-positive breast cancer and brain metastases (PERMEATE): a multicentre, single-arm, two-cohort, phase 2 trial. Lancet Oncol. 2022 Mar;23(3):353-361. 3) Consensus for HER2 alterations testing in non-small-cell lung cancer. ESMO Open. 2022 Feb;7(1):100395. 4) Neoadjuvant pyrotinib plus trastuzumab and nab-paclitaxel for HER2-positive early or locally advanced breast cancer: an exploratory phase II trial. Gland Surg. 2022 Jan;11(1):216-225. 5) Population pharmacokinetic modeling of pyrotinib in patients with HER2-positive advanced or metastatic breast cancer. Eur J Pharm Sci. 2021 Apr 1;159:105729. 6) Pyrotinib plus capecitabine versus lapatinib plus capecitabine for the treatment of HER2-positive metastatic breast cancer (PHOEBE): a multicentre, open-label, randomised, controlled, phase 3 trial. Lancet Oncol. 2021 Mar;22(3):351-360. 7) Molecular subtyping and genomic profiling expand precision medicine in refractory metastatic triple-negative breast cancer: the FUTURE trial. Cell Res. 2021 Feb;31(2):178-186. 8) Pyrotinib in HER2-Mutant Advanced Lung Adenocarcinoma After Platinum-Based Chemotherapy: A Multicenter, Open-Label, Single-Arm, Phase II Study. J Clin Oncol. 2020 Aug 20;38(24):2753-2761. 9) Pyrotinib combined with CDK4/6 inhibitor in HER2-positive metastatic gastric cancer: A promising strategy from AVATAR mouse to patients. Clin Transl Med. 2020 Aug;10(4):e148 10) Pyrotinib with trastuzumab and aromatase inhibitors as first-line treatment for HER2 positive and hormone receptor positive metastatic or locally advanced breast cancer: study protocol of a randomized controlled trial. BMC Cancer. 2020 Jul 13;20(1):653. 11) Pyrotinib or Lapatinib Combined With Capecitabine in HER2-Positive Metastatic Breast Cancer With Prior Taxanes, Anthracyclines, and/or Trastuzumab: A Randomized, Phase II Study. J Clin Oncol. 2019 Oct 10;37(29):2610-2619. 12) Safety, Efficacy, and Biomarker Analysis of Pyrotinib in Combination with Capecitabine in HER2-Positive Metastatic Breast Cancer Patients: A Phase I Clinical Trial. Clin Cancer Res. 2019 Sep 1;25(17):5212-5220. 13) Metabolism and disposition of pyrotinib in healthy male volunteers: covalent binding with human plasma protein. Acta Pharmacol Sin. 2019 Jul;40(7):980-988. 14) HER2 exon 20 insertions in non-small-cell lung cancer are sensitive to the irreversible pan-HER receptor tyrosine kinase inhibitor pyrotinib. Ann Oncol. 2019 Mar 1;30(3):447-455. 15) Discovery and development of pyrotinib: A novel irreversible EGFR/HER2 dual tyrosine kinase inhibitor with favorable safety profiles for the treatment of breast cancer. Eur J Pharm Sci. 2017 Dec 15;110:51-61. 16) Metabolic characterization of pyrotinib in humans by ultra-performance liquid chromatography/quadrupole time-of-flight mass spectrometry. J Chromatogr B Analyt Technol Biomed Life Sci. 2016 Oct 15;1033-1034:117-127. 학회발표 1) Pyrotinib combined with capecitabine as first-line therapy for HER2-positive metastatic breast cancer: A pooled analysis of three randomized controlled trials. 2020 ASCO Virtual Scientific Program DOI:10.1200/JCO.2020.38.15_suppl.e13022 Abstract #e13022 2) Updated overall survival (OS) results from the phase 3 PHOEBE trial of pyrotinib versus lapatinib in combination with capecitabine in patients with HER2-positive metastatic breast cancer.#GS3-02. San Antonio Breast Cancer Symposium 2021 3) 2020 ASCO #1003 Pyrotinib or lapatinib plus capecitabine for HER2+ metastatic breast cancer (PHOEBE): A randomized phase III trial. First Author: Binghe Xu, National Cancer Center/Cancer Hospital, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing, China 4) 2020 ASCO #1048 Pyrotinib plus capecitabine for HER2-positive, trastuzumab-resistant metastatic breast cancer: A pooled analysis of three randomized controlled trials. 5) 2020 ASCO #3510 Safety and efficacy of pyrotinib in patients with NSCLC and other advanced solid tumors with activating HER2 alterations: A phase I basket trial. F 6) 2021 ASCO #572 Pyrotinib as neoadjuvant therapy for HER2+ breast cancer: A multicenter, randomized, controlled, phase II trial. 7) 2021 ASCO #1034 Cyclin-dependent kinase 4/6 (CDK4/6) inhibitor SHR6390 combined with pyrotinib and letrozole in patients with human epidermal growth factor receptor 2-positive (HER2+), hormone receptor positive (HR+) metastatic breast cancer (MBC): Phase Ib study results. 8) 2021 ASCO #1036 Pyrotinib plus capecitabine for HER2-positive metastatic breast cancer patients with brain metastases (PERMEATE): A multicenter, single-arm phase II study. 9) 2021 ASCO #9034 Efficacy and safety of pan-ErbB inhibitor pyrotinib combined with antiangiogenic agent apatinib for HER2-mutant or amplified metastatic NSCLC: A phase II clinical study. |
|||||||||||||||||||||
|
시장규모 |
- 진행성 및 전이성 유방암 시장 HER2(+) 진행성 및 전이성 유방암 2차 치료제 국내 예상 시장규모는 2026년 약 540억원, 2031년 약 660억원으로 연평균4-5 %로 성장할 것으로 추정됨 - NSCLC 폐암 시장 HER2(+) Exon2 NSCLC 치료제 국내 예상 시장규모는 2026년 약 160억, 2031년 약 280억원으로 연평균 2-5 %로 성장할 것으로 추정됨 ※ 참고: 2019년도 건강보험심사 평가원, 2018년도 국가암등록사업 연례보고서 |
3) 품 목 : 바이오인공간
|
구 분 |
바이오 신약(세포치료제) |
|
적응증 |
급성 간부전(Acute hepatic failure) |
|
작용기전 |
바이오인공간은 무균돼지의 간세포를 최적의 간기능을 유지하는 형태로 배양하는 생물반응기를 사용하여 신장투석과 유사한 체외순환의 형태로 환자의 혈액내 독성물질을 제거하고 유용한 물질을 분비하도록 하여 간부전 환자의 간기능을 보조함으로써 생명을 연장하는 것을 목적으로 함 |
|
제품의특성 |
1) 충분한 양의 간세포 - 기존 바이오인공간과 비교하여 가장 많은 양의 신선한 간세포를 적용 2) 간세포 구형 응집체(구상체) 사용 - 간세포 구상체는 환자 혈장 접촉 조건에서 단일 간세포보다 월등히 높은 간기능을 더 오래 유지함 3) 미세캡슐화로 면역장벽과 넓은 표면적 제공 - 간세포 구상체를 직경 1 mm의 칼슘-알긴산 미세캡슐화를 통해 면역세포와 항체로 인한 간세포 손상을 방지하고, 기존 중공사막 반응기 보다 약 50% 증대된 접촉 표면적을 제공 |
|
진행경과 |
- 2017년 12월 임상시험 1/2a상 종료 - 임상시험 2b 진행 중(시작일: 2019.03.29) |
|
향후계획 |
- 현재 임상시험 2b상 진행 중으로 임상 2b 종료 후 품목허가 진행 예정임. |
|
경쟁제품 |
- 국내 유일한 바이오인공간 개발 제품임 |
|
관련논문 등 |
- Functional Evaluation of a Bioartificial Liver Support System Using Immobilized Hepatocyte Spheroids in a Porcine Model of Acute Liver Failure, Sci Rep, 2017 - Effect of fulminant hepatic failure porcine plasma supplemented with essential components on encapsulated rat hepatocyte spheroids, Transplant Proc, 2012 - Potentiality of immobilized pig hepatocyte spheroids in bioartificial liver system,Transplant Proc, 2012 - Current Status of Development of Bioartificial Liver Systems for the Treatment of Acute Liver Failure, Tissue Eng Regen Med, 2008 |
|
시장규모 |
- 2016년도 국내: 1,500억원(기술보증기금 2017.03.09) - 2034년도 국내: 3,145억원(기술보증기금 2017.03.09) - 2016년도 미국/유럽: 120억달러(Vital therapies Inc. 2016.8) |
4) 품 목 : 생분해성 의료용 접착제 또는 실란트 조성물
|
구 분 |
의료기기 |
|
적응증 |
조직/장기 출혈, 창상 |
|
작용기전 |
파우더형태의 제품으로 수액과 만나면 겔화되어 창상 보호 및 물리적 압박에 의한 지혈 |
|
제품의특성 |
생체유래 물질인 글라코사미노글라이칸(glycosaminoglycan, GAG)을 기반으로 하여 만든 파우더 형태의 제품으로 장기/조직 손상부위 및 출혈부위에 분사하여 조직 접착 및 지혈 작용을 하고, 창상 부위를 보호할 수 있는 의료기기임 |
|
진행경과 |
- 본 기술에 대해 2015년 11월 (재) 유타 인하 디디에스 및 신의료기술개발 - 탐색임상시험용 비임상시험 완료 |
|
향후계획 |
- 확증임상시험 대상자수 조정 재승인(2022.01.14) - 확증임상시험 완료 후 품목허가 예정 |
|
경쟁제품 |
지혈 단백질인 피브리노겐을 사용하는 제품인 Tisseel(다림바이오텍), Tachosil(현대약품), Floseal(Baxter) 등이 있음 |
|
관련논문 등 |
- Evaluation of anti-hemorrhagic efficiency of a highly adhesive powder in a swine model, - 생체모방고분자를 이용한 신속지혈제 개발에 관한 연구, 2017년 한국군사과학기술학회 |
|
시장규모 |
- IMS 데이터에 따르면, 국내 수술용 국소 지혈제 시장은 2015년 513억여원으로 연평균 10%이상 성장하고 있음 - MedMarket Diligence에 따르면, 세계 의료용 지혈제 시장 규모 역시 2015년 72억 달러로 연평균 12%의 성장이 예상됨 |
|
정부보조금 |
- 지혈제 개발과 관련하여 2016년 민군겸용기술개발사업의 참여기관으로 선정되어 총 33억원을 지원받음(2016년 ~ 2021년) - '범부처의료기기연구개발사업(R&D) / 의료기기 사업화 역량 강화'에 선정되어 연구비 8.3억원 지원 중(2022년 ~ 2024년) |
5) 품 목 : G2M Project
|
구분 |
화학 합성 신약 |
|
적응증 |
폐암, 유방암, 대장암, 췌장암 등 각종 고형암종 대상 |
|
작용기전 |
세포분열 주기 중 G2기→M기의 진행을 방해함으로써 세포분열을 억제, 암세포의 성장을 저해하고 사멸을 유도 |
|
제품의 특성 |
- 세포주기(Cell cycle)에 관련된 신호를 조절해 암세포 증식을 저해 - 항암제 내성 암에서 효과를 보임 |
|
진행경과 |
비임상 진행 중 |
|
향후계획 |
비임상 독성 profile 확보 |
|
경쟁제품 |
개발초기 단계로 작용기전에 의한 경쟁제품을 특정하기 어려움 |
|
관련논문등 |
개발초기 단계로 관련논문 등 사례가 없음 |
|
시장규모 |
개발초기 비임상 단계로 시장규모 예상이 어려움 ※ 객관적인 자료출처를 통한 경쟁제품 간 시장점유율 비교가 불가능하여 기재를 생략합니다. |
|
기타사항 |
- |
6) 품 목 : 인간 세포 외 기질
|
구 분 |
인체 세포 외 기질(Hutrigel®-RU) |
|
적응증 |
줄기세포, 오가노이드 배양 재료 |
|
작용기전 |
라미닌 등 기저막 성분의 세포외기질을 통한 세포 성장, 증식, 분화 |
|
제품의특성 |
동물 및 종양 유래가 아닌 인체세포 대량배양을 이용하여 제조한 무이종, 정상 기저막 세포외기질 |
|
진행경과 |
연구용 재료여서 인허가 필요하지 않음 연구실 규모 제조공정 수립 완료 현재 양산제조공정 수립 및 양산이관 중 |
|
향후계획 |
2024년도 2분기에 제품 출시 예정 마케팅/영업 활동 예정 마케팅 목적 데이터 확보를 위한 위탁연구 추진 예정 |
|
경쟁제품 |
마우스 종양 유래 기저막 세포외기질: Matrigel (Corning 사), Geltrex (Thermo Fisher 사), Cultrex (Biotechne 사): 돼지 정상조직 유래 세포외기질: Regenix (Cellartgen 사) |
|
관련논문 등 |
없음 |
|
시장규모 |
Matrigel 제품군의 글로벌 시장규모는 2023년도 1,102억원, 2029년도 2,112억원으로 CAGR 11.45% 으로 예상됨 (Global Matrigel Market Insights, Forecast to 2029; QY Research 2023) |
|
정부보조금 |
2022년도에 중소기업 기술혁신개발사업에 선정되어 2023년까지 3.6억원을 지원받았고, 당해년도에 1.2억원을 지원받을 예정 |
7) 품목 : Cannabinoids derivatives
|
구분 |
화학 합성 신약 |
|
적응증 |
고형암종 대상 |
|
작용기전 |
스크리닝을 통해 작용기전 규명 중 |
|
제품의 특성 |
고형암의 성장을 저해. (세포의 성장 억제 분석을 통해 최적 암종 탐색 중) |
|
진행경과 |
후보물질 도출 중 |
|
향후계획 |
- 후보 물질 선별 - 비임상 독성 profile 확보 |
|
경쟁제품 |
개발초기 단계로 경쟁제품을 특정하기 어려움 |
|
관련논문등 |
개발초기 단계로 관련논문 등 사례가 없음 |
|
시장규모 |
개발초기 단계로 시장규모 예상이 어려움 ※ 객관적인 자료출처를 통한 경쟁제품 간 시장점유율 비교가 불가능하여 기재를 생략합니다. |
|
기타사항 |
- |
8) 품목 : CDK inhibitor
|
구분 |
화학 합성 신약 |
|
적응증 |
고형암종 대상 |
|
작용기전 |
CDK 인산화 효소 억제 |
|
제품의 특성 |
고형암의 성장을 저해 |
|
진행경과 |
후보물질 도출 중 |
|
향후계획 |
- 후보 물질 선별 - 비임상 독성 profile 확보 |
|
경쟁제품 |
개발초기 단계로 경쟁제품을 특정하기 어려움 |
|
관련논문등 |
개발초기 단계로 관련논문 등 사례가 없음 |
|
시장규모 |
개발초기 단계로 시장규모 예상이 어려움 ※ 객관적인 자료출처를 통한 경쟁제품 간 시장점유율 비교가 불가능하여 기재를 생략합니다. |
|
기타사항 |
- |
마. 정부출연과제 수행 실적
| 지원기관 | 계약명 |
개발기간 |
취득권리/인증제 | 개발과제 및 내용 | 비고 |
| 산업통상자원부 방위사업청 |
생체모방 고분자 신속 지혈제 개발 (총 5개년 중 5년차) |
2016.6.26 ~ 2021.6.25 |
- | □ 민 ·군겸용기술 개발사업 | 세부연구기관 |
| 산업통상자원부 | Off-the-shelf 바이오인공간 사업화 |
2017.7.1~ 2020.10.31 |
임상진입 | □ 유망바이오IP사업화촉진 | 주관연구기관 |
|
범부처 |
범부처의료기기연구개발사업(R&D) / 의료기기 사업화 역량 강화 |
2022.4.1 ~ 2024.12.31 |
- |
□ 흡수성체내용지혈용품(BleeFix®) 확증임상시험 및 국내 품목허가 |
주관연구기관 |
|
중소벤처기업부 |
중소기업기술혁신개발사업 |
2022.7.1 ~ 2024.06.30 |
- |
□ 인체 세포배양 유래 세포외기질 사업화 |
주관연구기관 |
7. 기타 참고사항
[ 메디케어사업 부문 ]
① 산업의 특성 등
□ 산업의 특성
(1)체외진단 의료기기
체외진단은 혈액, 객담, 타액, 분뇨, 체액 등 인체로부터 채취한 대상물을 이용하여 몸 밖에서 신속하게 질병 등을 진단하는 기술로 세부적인 분류로는 면역화학진단, 분자진단, 현장진단, 혈액진단, 임상미생물학적진단, 조직병리진단, 지혈진단, 자가혈당측정으로 나눠집니다. 최근 신종질병(Covid-19)의 출현 및 감염 질병의 유행과 인구고령화의 가속으로 인해 수요가 급격하게 증가하고 있으며, 기존의 치료 중심에서 예측 및 예방으로 변화하는 의료 패러다임에 있어 중요성이 점차 강조되고 있습니다.
(2)의료기기 산업분야의 아웃소싱 (OEM/ODM)
과거 아웃소싱 활동이 매우 적었던 의료기기 산업은 최근 전 세계적인 규제 강화와 경쟁 심화 및 신시장 기회 확대에 따라 아웃소싱을 통한 제조가 증가하고 있으며, 설비투자에 대한 부담 감소, 생산체제 구축 시간 단축을 통한 제조원가 절감 등의 강점으로 전반적인 시장 수요가 증가하고 있습니다.
□ 산업의 성장성
(1)글로벌 체외진단 시장
전 세계 글로벌 체외 진단(IVD) 시장은 2021년 982억 달러에서 연평균 성장률 2.9%로 증가하여, 2026년에는 1,131억 달러에 이를 것으로 전망됩니다. COVID-19로 인해 글로벌 체외 진단 시장은 급격하게 성장하였으며, 기존 또는 신규 감염 질병 진단을 위한 차세대 체외 진단의 R&D 확장으로 앞으로도 성장 추세는 꾸준히 이어질 것으로 예상됩니다.
 |
|
글로벌 체외진단 시장 |
출처 : Research & Markets - In-Vitro Diagnostics/IVD Market by Product and Service ,Technology ,Application (Diabetes, Oncology, Cardiology, Nephrology, Infectious Disease, End User - Global Forecast to 2026 (2022.05)
(2) 글로벌 의료기기 아웃소싱 시장
전 세계 글로벌 의료기기 아웃소싱 시장은 2022년 1,174.7억 달러에서 연평균 성장률 12.1%로 증가하여 2030년에는 2,929.3억 달러에 이를 것으로 전망됩니다. 아웃소싱 시장은 CM(Contract Manufacturing), 품질보증, 법규 컨설팅, 제품설계&개발, 제품시험&멸균, 제품구현 등으로 이뤄져 있으며, CM의 경우 가장 큰 점유율을 차지하고 있습니다.
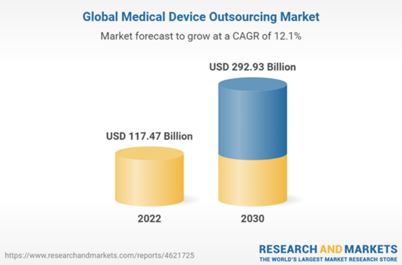 |
|
글로벌 의료기기 아웃소싱 시장 |
출처 : Medical Device Outsourcing Market Size, Share & Trends Analysis Report by Application (Cardiology, General & Plastic Surgery, IVD), by Service (Contract Manufacturing, Quality Assurance), by Region, and Segment Forecasts, 2022-203 (2022.02)
□ 경기변동의 특성
일반적인 제조업의 특성상 대외적인 환경 변화에 의한 경기 변동에 영향을 받고 있습니다. 하지만, 의약외품 및 체외진단 의료기기 시장의 경우, 기업 및 정부 조직간의 거래 관계인 B2B 및 B2G 계약의 점유율이 높기 때문에 해당 경기 변동에 따른 리스크는 상대적으로 미비합니다.
② 국내외 시장여건
세계적인 고령화 추세, 건강에 대한 관심 고조 및 웰빙에 대한 사회적 분위기 확산, 주요 국가들의 보건 의료 정책 등으로 인한 의료 서비스 수요 증가, 감염성 질환을 포함한 질병의 증가, 치료에서 예방 및 진단으로의 의료 트렌드 변화 등의 요인으로 향후 지속적이며 예측 가능한 성장이 예상됩니다. 주기적으로 발생하는 감염성 질환 진단 제품, 지속적인 진단 수요가 있는 제품, 높은 정확도를 확보하고 있는 제품들의 경우, 꾸준한 제품 개발을 통해 정확도를 높이고 있으며 그에 더해 진단장비를 활용하여 편의성을 확보하는 등의 영향으로 체외 진단 제품의 라이프 사이클은 장기화되고 있는 추세입니다.
③ 회사의 경쟁우위 요소
150여 종의 제품개발 성과의 근간인 기술력과 품질 시스템을 바탕으로 의료기기 분야를 비롯한 다양한 품목군을 개발, 연구 중에 있으며 전사적 품질 경영 시스템 운영을 통해 안정성, 유효성 및 GMP, ISO13485 기준의 품질이 확보된 제품을 생산하고 있습니다.
금형 팀은 금형을 제작, 관리, 보전하여 신뢰성 있는 제품 생산을 직접적으로 지원합니다. 보다 정밀한 금형 제작을 위해 지속적으로 선진기술을 도입하여 우수한 품질의 제품을 생산합니다. 아울러 제작된 금형의 상태 유지를 위하여 금형별 보전(Mainternance) 업무를 진행하고, 통계적 공정관리를 운영함으로써 잠재적 고장 유형을 개선 진행하고 있습니다.
의료기기 및 생활용품 등 플라스틱 소재로 사출품을 생산하며, 원자재 공급 및 사출물을 생산하는 사출 공정, 제품을 검사하는 검사/포장 공정, 포장된 제품을 출하하는 출하 공정으로 나누어 원활한 생산 및 출하가 이뤄질 수 있도록 합니다. 고객의 다양한 요청에 따라 플라스틱 사출 성형품을 생산하고 공급합니다.
어셈블리 서비스를 제공하여 시간을 보다 효율적으로 배분하고, 생산효율을 증대시키며, 포장, 조립, 분주 및 인쇄 등 다양한 프로젝트를 진행해 품목별로 적합한 솔루션을 제공합니다. ISO13485 : 2016 인증, 통제된 제조 공간, 당사의 리소스 및 숙련된 생산팀은 높은 생산성을 기반으로 대량 프로젝트를 처리할 수 있습니다.
[특허권 현황]
| 구분 | 명칭 | 국가 | 상태 | 권리자 | 실제권리보유내역 | 출원일 | 등록일 | 등록번호 |
| (권리비율) | ||||||||
| 체외진단 의료기기 | 혈액 채취용구 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2013.08.08 | 2013.10.01 | 제30-0711266호 |
| 체외진단 의료기기 | 혈액 채취용구 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2013.08.08 | 2013.10.01 | 제30-0711266호의 유사 제 01호 |
| 체외진단 의료기기 | 혈액 채취용 주사기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2013.04.03 | 2014.04.02 | 제30-0737697호 |
| 체외진단 의료기기 | 혈액 채취용 주사기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2013.04.03 | 2014.04.02 | 제30-0737697호의 유사 제01호 |
| 체외진단 의료기기 | 일회용 액체 포장용기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2015.08.26 | 2015.10.24 | 제30-0822478호 |
| 체외진단 의료기기 | 일회용 액체 앰플 (DISPOSABLE AMPULE FOR LIQUID) |
대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2016.04.11 | 2018.08.07 | 제10-1888122호 |
| 체외진단 의료기기 | 일회용 액체 포장용기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2016.04.05 | 2017.01.10 | 제30-0890513호 |
| 체외진단 의료기기 | 일회용 액체 포장용기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2016.04.05 | 2017.01.10 | 제30-0890511호 |
| 체외진단 의료기기 | 비침투형 혈액 채취 디바이스 (NON-PENETRATING TYPE BLOOD COLLECTION DEVICE) |
대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2017.11.28 | 2019.12.20 | 제10-2059956호 |
| 체외진단 의료기기 | 모세관 튜브 사이즈 적응형 혈액 채취 디바이스 (BLOOD COLLECTION DEVICE ADAPTIVE TO SIZE OF CAPILLARY TUBE) |
대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2018.11.13 | 2021.02.26 | 제10 - 2223629호 |
| 체외진단 의료기기 | 혈액 채취기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2019.10.14 | 2020.06.02 | 제30 - 1061718호 |
| 체외진단 의료기기 | 일회용 검체 용해 용기 (DISPOSABLE BOTTLE FOR DISSOLVING SAMPLE) |
대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2019.04.19 | 2021.03.24 | 제10 - 2233904 호 |
| 체외진단 의료기기 | 혈액 수집 유니트 (UNIT FOR COLLECTING BLOOD) |
대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2019.07.15 | 2020.12.16 | 제10 -2194252호 |
| 체외진단 의료기기 | 혈액 수집과 배출을 위한 유니트 (UNIT FOR COLLECTING AND EJECTING BLOOD) |
대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2019.10.04 | 2021.06.09 | 제10 -2265307호 |
| 체외진단 의료기기 | Mini tip (50ul)/비침투형 혈액 채취 디바이스 | 중국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2019.11.12 | 2020.08.18 | CN 211270781 U |
| 체외진단 의료기기 | 타액 수집기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2021.02.10 | 2022.01.20 | 제30-1148273호 |
| 체외진단 의료기기 | 타액 수집기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2021.02.10 | 2022.01.20 | 제30-1148274호 |
| 체외진단 의료기기 | 일회용 액체 포장용기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2021.03.19 | 2021.04.08 | 제30-1104470호 |
| 체외진단 의료기기 | 일회용 액체 포장용기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2021.03.19 | 2021.08.03 | 제30-1122440호 |
| 체외진단 의료기기 | 일회용 액체 포장용기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2021.03.19 | 2021.04.08 | 제30-1104471호 |
| 체외진단 의료기기 | 일회용 액체 포장용기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2021.03.19 | 2021.08.03 | 제30-1122441호 |
| 체외진단 의료기기 | 일회용 액체 포장용기 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2021.03.19 | 2021.04.08 | 제30-1104472호 |
| 체외진단 의료기기 | 시험관 | 대한민국 | 등록 | HLB생명과학 | HLB생명과학 (100%) | 2021.03.29 | 2022.06.02 | 제30-1167213호 |
[ 바이오사업 부문 ]
① 산업의 특성 등
□ 산업의 특성
의약산업은 신약개발을 위한 연구에서부터 원료 및 완제의약품의 생산과 판매 등 모든 과정을 포괄하는 첨단 부가가치산업으로 기술 집약도가 높고 신제품 개발 여부에 따라 높은 부가가치를 창출할 수 있는 미래 성장산업입니다. 원료의약을 포함한 의약산업은 고도의 기술력과 품질관리 능력이 필요한 산업의 특성상 진입이 쉽지 않고, 원료의약의 경우 허가된 완제 의약품 생산업체로만 매출이 제한되어 기술과 품질의 우위를 점한 제품의 경우 사업 경쟁력에서 유리한 지위를 갖는 특징이 있습니다.
□ 규제와 지원
신약 연구개발 과정은 정부의 각종 규제로 엄격한 안전성과 유효성 검증을 받아야 합니다. 특히 개발단계는 연구단계에서 선정된 신약 후보물질의 동물과 사람에 대한 안전성과 유효성(약효)을 검증하는 과정입니다. 일반적으로 신약 연구개발 전 과정에서 소요되는 비용의 85%이상을 개발단계에서 사용합니다. 그리고 모든 자료는 허가기관에 제출해야 하고, 까다로운 정부의 규제와 지침을 잘 지켜야 합니다. 제약사업은 신약 후보물질의 안전성과 유효성을 확인하기 위하여 정부에서 많은 단계의 예비실험과 자료 심사 절차를 요구하고 있습니다. 또한, 각 단계마다 실험 수행 시 엄수해야 할 규정을 제정하여 실험자료의 질적 수준과 자료의 일관성을 확보하도록 하고 있습니다. 또한, 정부는 신약 연구개발의 중요성을 감안하여 전임상, 임상 단계에 있는 과제들에 대한 연구비 지원을 지속적으로 확대하고 있습니다. 특히, 바이오 신약, 장기사업을 차세대 성장동력 산업으로 지정하고 미래창조과학부, 교육부, 농림축산식품부, 산업통상자원부 그리고 보건복지부가 협력하여 계획을 수립, 시행하고 있습니다.
□ 경쟁요소
국내 의약산업은 인구 고령화에 따른 만성질환 및 QOL(Quality of Life, 삶의 질 개선)의약품 수요의 증가와 특허만료에 따른 제네릭의약품 시장의 성장, 정부의 중증 질환에 대한 급여 확대, 블록버스터 품목의 집중마케팅 등으로 정책적 악재가 극복되어 매출증가 및 수익성 개선이 지속되고 있습니다. 신약개발은 차별화된 R&D 경쟁력 및 고도의 기술개발을 위해 10~15년의 오랜 기간과 대규모투자를 필요로 합니다. 신약의 성공확률이 낮아 오리지날 의약품에서 강점을 가진 다국적 제약사들이 대부분 강세를 나타내고 있습니다. 한편, 국내의 거대기업들도 원료의약품, 신약개발 및 바이오 의약품 등에 진출하여 투자를 계속하고 있어 의약품시장의 경쟁은 더욱 치열한 상황입니다. 최근 국내 제약사들도 지속적인 R&D 투자의 결실로 다국적 제약사와 기술이전계약 등 신약개발에 대한 모멘텀이 활발하게 이루어지고 있어, 향후 국내 제약사들 간의 R&D 투자 확대로 한층 경쟁이 격화될 것입니다.
□ 자원조달의 특성
공급업체와의 협력관계 구축 등으로 인해 안정적으로 원료 공급이 가능하며, 일부 수입 원료 또한, 국내 업체로의 전환이 가능한 상황입니다. 기술집약적 산업 특성상 전문 지식의 노동력이 중요하며 국내 인력 수급은 안정적입니다.
□ 바이오의약품의 분류와 현황
바이오의약품은 사람이나 다른 생물체에서 유래하는 단백질, 유전자, 세포 등을 원료또는 재료로 하여 유전자재조합, 세포융합, 세포배양 등 생명체 관련 바이오기술을 활용하여 약효를 가진 새로운 물질이나 호르몬 ·항체 등과 같이 원래 생명체 내에 존재하는 물질을 생산하여 질병의 예방 및 치료를 목적으로 제조하는 의약품을 말합니다.
【바이오의약품의 분류】
| 구분 | 유전자재조합 단백질 |
세포치료제 | 유전자치료제 | 생물학적 제제 | |
| 혈액제제 | 백신 | ||||
| 유효성분 | 유전자조작 기술을 이 용하여 제조하는 펩타이드, 또는 단백질 |
체외에서 배양 ·증식선별 ·조작한 살아있는 세포 | 질병치료를 목적으로 하는 유전물질 | 혈액을 원료로 하는 혈액성분제재와 혈액분획제제 | 감염병 ·일반질환의예방등을 목적으로 하는 단백질 또는 미생물체 |
| 종류 | 성장호르몬, 인슐린, 항암제, 자가면역 질환 치료제 | 체세포치료제, 줄기세포치료제 |
DNA백신 | 적혈구, 혈소판, 혈장, 알부민등 |
인플루엔자백신, 폐렴구균백신 |
<자료 : 한국바이오의약품협회, 식약처, KDB산업은행 (2015.6.1)>
바이오의약품은 일반적으로 합성의약품에 비해 분자량이 크고, 복잡한 구조를 가지고 있으며, 생물체를 이용하여 복잡한 제조공정을 거쳐야 하므로, 변화에 민감하고 특히 오염 및 불순물관리에 유의해야 하는 단점이 있으나, 고유의 독성이 낮고 작용기전이 명확하여 난치성 및 만성질환에 뛰어난 효과를 보입니다.
바이오의약품은 백신과 혈액제제 등으로 일컬어지는 1세대 Biologics를 시작으로 유전자 조작 및 세포배양기술을 도입한 재조합의약품과 세포배양의약품 그리고 최근에는 세포융합기술 및 정보기술 등을 접목한 단클론 항체, 유전자치료제, 세포치료제, DNA 백신 등과 같은 첨단바이오의약품으로 발전되고 있습니다.
정부는 미래유망신기술(6T) 중 BT분야에 바이오제약, 의료기기, 고부가 식품, 글로벌헬스케어 등의 분야를 신성장 동력분야로 선정하고, 다양한 지원정책을 마련하여 바이오의약품에 대한 투자를 확대하고 있습니다.
| 구분 | 촉진요인 | 저해요인 |
| 정책 | ·바이오제약분야를 국가 신성장 동력분야로 선정 ·'혁신형 제약기업 인증제도'의 시행으로 국내 제약기 업의 혁신형 바이오의약품 개발수요 증가 ·의료비 절감 정책 추진 예상에 따른 바이오 시밀러관 련 산업의 정책적 지원수요 증가 |
·기술개발에 소요되는 고비용 및 인체실험 관련 규제가 바이오의약품 연구를 저해 ·정부 내 일원화되지 않은 허가절차 문제 ·국가연구개발사업의 중복투자 영역 및 공백분야 발생 |
| 경제 | ·OECD는 20세기 후반부터 생명공학과 바이오 기술을 앞세운 바이오 경제가 본격화하고 있다고 분석 ·기술 혁신과 소득 증대로 인해 개별 맞춤의료 및 고급 의료에 대한 수요가 급격히 증가 |
·의약품 산업의 고도화로 신물질 개발이 한계에 이르러 연구개발 투자 규모 대비 효용성이 감소 ·개발도상국 제품에 대한 안전성, 유효성 및 생산공정 기 준의 점진적 강화로 인한 진입장벽 심화 |
| 종류 | ·전 세계의 인구 고령화로 인해 의약품의 수요 증가 ·의료비 급증에 따라 저비용 다효능의 천연물의 가치 재평가 ·바이오제약분야의 기업들은 특허만료로 인한 타격을 상쇄시키기 위하여, 파이프라인 구축 등 차세대 의약 품을 준비 중 |
·소형화, 개체화로 대표되는 바이오 경제 패러다임의 변 화문제 ·생체 자원의 확보 문제 및 자원 확보 과정에서의 윤리적 문제 ·세계시장 진출을 위한 천연물의약품의 과학화, 표준화, 규격화 |
| 기술 | ·높은 임상실험 성공율, 개발초기 타겟 발굴, 활성대사 체와 관련 독성의 부재 ·질병관련 유전자 발현 양상 및 정체 확인에 대한 유전 자 정보축적 ·개량기술을 통한 신규 항체, 신규 단백질의약품 개발 활발 |
·관련시장의 미성숙으로 인한 연구개발의 초기단계 정체 ·바이오시밀러 관련 기술 및 분석은 복잡한 기술이해도 를 요구 ·바이오시밀러에 대한 안전성 문제가 아직 불확실 |
자료 : 2013 중소기업 기술로드맵 수립사업 최종보고서, 중소기업청
② 산업의 성장성
□ 바이오의약품 시장전망
세계 의약품 시장은 고령화에 따른 만성 질환자 수의 증가, 소득 수준 향상에 따라 의약품 시장의 성장이 급격하게 이루어지고 있는 중국, 인도, 중남미 등의 제약 신흥 국가들의 의료비 지출증가 등으로 시장 규모는 역대 최대치를 경신했습니다. 2021년 세계 의약품 시장 규모는 전년(1.1조 달러) 대비 9.4% 증가한 1.2조 달러에 달했습니다. (출처 : QuintilesIMS, 제약바이오협회) 또한, 합성의약품은 블록버스터 품목의 특허만료, 제네릭시장 확대, R&D 생산성 저하 등으로 시장비중이 축소되고 있는 반면, 바이오의약품은 높은 유효성과 안전성, 난치성 질병 치료제 개발 등으로 비중이 확대되어 글로벌 바이오의약품 시장은 2022년 3,440억 달러에서 2026년 5,050억 달러로 연평균 10.1%의 높은 성장세를 보이며 확대될 것으로 전망합니다. (출처 : Frost&Sullivan, 한국보건산업진흥원) 이중 차세대 바이오의약품으로 꼽히는 세포치료제는 기존 바이오신약 및 바이오시밀러 또는 바이오베터와는 완전히 다른 새로운 약으로서, 현재 국내외 규제기관에서 첨단제제로 분류하여 심사하고 있으며, 시장주기에서 매우 초기에 속하지만 가능성 면에서는 매우 잠재력이 큰 분야라고 할 수 있습니다.
세포치료제는 세포와 조직의 기능을 복원하기 위해 살아있는 자가, 동종, 이종세포를체외에서 배양 증식, 선별 등 여러 가지 방법으로 생물학적 특성을 변화시켜 치료에 이용하는 의약품을 뜻하며, 연골세포치료제, 항암세포치료제, 줄기세포치료제, 면역세포치료제 등이 속합니다. 세포 자체를 약으로 활용하므로 환자로부터 분리한 세포를 특정 성질을 갖도록 처리한 후 다시 주입하는 경우가 많아 맞춤형 의약품으로 불리기도 합니다. 또한 기존의 제제가 단일 또는 특정 기전을 타깃으로 하기 때문에 다양한 원인에 의해 발병하고 병리기전이 복합적으로 결합되어 있는 퇴행성질환이나 면역질환에 좋은 효과를 보이지 못하고 있는 반면, 세포치료제는 질환에 복합적으로 작용하는 기전을 가지고 있어 난치성 질환에 대한 차세대 치료제로서 기대를 받고 있습니다.
바이오의약품 허가 및 심사기준 재정비를 통한 산업 지원 정책이 마련되어 자가유래 세포치료제의 경우 연구자 임상의 상업화 진입이 가능하도록 하고 조직 타이핑 자료를 면제하도록 심사기준을 변경하는 등 허가 승인 발판이 마련되었습니다.
또한 세포치료제의 경우, 현재까지 태동기 상태로서 원천기술 확보와 기술선점이 가능해 임상 시험 진입 시 국제 경쟁력 우위 선점이 가능할 것이라 예상됩니다.
③ 회사의 경쟁우위 요소
(1) 종속회사의 관한 사항 : HLB셀
HLB셀은 바이오의약품 및 생체적합성 의료기기 개발 기술을 중심으로 ①바이오인공간 ②지혈제 ③인체세포외기질 3개 분야의 주요 파이프라인을 갖고 있으며, 관련 특허 등을 활용하여 연구, 개발 중에 있습니다
급성 간부전환자의 간기능을 보조하여 간이식 대기기간 동안 생명을 연장할 목적의 바이오인공간을 개발하여 현재 2b 상 임상시험을 진행 중입니다
바이오인공간은 생물학적 요소가 완전히 배제된 형태인 『인공간(Artificial Liver)』의 한계를 극복하기 위해 생체 조직이나 세포와 결합한 "하이브리드형"의 인공장기를 "Bio-Artificial Liver", 즉 "바이오인공간"으로 구분하여 명명합니다.
바이오인공간의 대상환자는 일주일 내로 간이식을 받지 않으면 생명을 유지할 수 없는 환자가 대부분으로 기증간이 발생하여 간이식을 받을 수 있을 때까지 생명을 연장하고 또한 간이식을 받더라도 간부전에 동반되는 뇌병증 등의 후유증을 예방하여 간이식의 예후를 향상시키기 위한 Bridge(다리) 역할을 합니다.
간기능이 손실된 간부전환자의 간기능을 체외에서 대신하여 주는 국내 최초 '세포치료제 + 의료기기(4등급)' 복합제품 형태의 첨단 바이오의약품(세포치료제)이며, 삼성서울병원과 함께 개발한 바이오인공간의 "급성 간부전 환자에서 바이오인공간(체외순환형생인공간)의 안전성을 평가하고 유효성을 탐색하기 위한 1/2a 임상시험"을 2017년 3월에 종료하고, 임상보고서를 제출하였습니다. 2015년 3월 식품의약품안전처로부터 "개발단계 희귀의약품"으로 지정 고시되었고, 2018년 11월 임상 2b IND 승인 후 2019년 3월 임상시험이 개시되어 현재 임상시험을 진행 중에 있습니다.
또한, 생분해성 의료용 접착제 또는 실란트 조성물 기술은 파우더 형태의 체내용 흡수성 지혈제, 조직접착제 및 창상피복재 용도로, 일회용 디바이스(device) 내에 담겨있는 파우더를 장기의 조직이나 혈관 출혈 부위에 분사하는 제품입니다. 사전혼합 및 준비가 되어 있어 사용 전 별도의 절차가 필요 없고 적용(출혈, 장기/조직손상)부위에 즉각적으로 사용 가능하고, 생체물질 기반이므로 체내에 흡수되는 제품입니다. 생분해성 의료용 접착제 또는 실란트 BleeFix®는 최근 의료용 조직 접착제에서 요구되는 사항인 무독성, 생분해성, 사용 및 보관의 편리성, 빠르고 강한 접착력, 유착방지 효과 등에 대해 만족하는 제품입니다. HLB셀은 2016년 민군겸용기술개발사업에 선정되어 임상시험용 제품 개발을 완료하고, 2019년 6월부터 간절제 수술 환자를 대상으로 탐색임상시험을 진행하여 2020년 7월 완료하고 2021년 8월부터 확증임상시험을 진행 중에 있습니다.
인간 세포외기질은 인간 정상세포를 체외에서 배양하여 생산한 세포외기질로 세포의 성장, 이동, 분화 등에 깊게 영향을 미치는 단백질 혼합체입니다. 특히, 기저막 성분으로 분류되는 단백질들을 함유하고 있어 상피, 신경 재생 및 혈관화 향상에 크게 기여할 것으로 판단하고 있습니다. 2023년 연구용 제품 출시 예정이며, 의료용 제품의 경우 GMP-순응 제조공정 수립, 동물시험 예비유효성 평가 등을 실시할 예정입니다.
* Pipe Line 현황
| 품목명 | 특징 |
| 바이오인공간 (LifeLiver system) |
- 간 기능이 손실된 간부전환자의 간 기능을 체외에서 대신하여 주는 국내 최초 '세포치료제 + 의료기기(4등급)' 복합제품 형태의 첨단 세포치료제 - 간부전환자는 LifeLiver system을 통해 손상된 간이 재생, 회복될 때까지 또는 간 이식을 받기 전까지 생명을 연장할 수 있음 - LifeLiver system은 간 손상으로 제거하지 못한 체내 독소로 인하여 발생하는 뇌병증을 감소 시킴으로써 간 이식 이후 예후 기대 |
| 생분해성 의료용 접착제, 실란트 (BleeFix®) |
- 외과 수술용 체내 흡수성 지혈제품 (의료기기 4등급) - 수술과정이나 부상으로 인한 조직 손상 및 출혈에 조직접착/지혈을 목적으로 한 제품으로 수일내에 체내에 흡수되어 기존 제품대비 우수한 접착력과 지혈능력 보유 |
|
인체 세포 외 기질 (Hutrigel®) |
- 인간 정상세포를 체외에서 배양하여 생산한 단백질 혼합체 - 상피, 신경세포 등의 성장, 이동, 분화 등에 영향을 미치는 구조 단백질인 기저막 성분을 함유 - 연구용 제품 및 의료용 제품으로 개발할 예정임 |
(2) 계열회사의 관한 사항 : Elevar Therapeutics, Inc.(구. HLB USA, Inc.)
Elevar Therapeutics,Inc.는 2005년 7월 신약개발 컨설팅 회사로 설립되어 2007년 12월 Rivoceranib(구. Apatinib Mesylate) 표적항암제 라이센스 취득 계약 체결(Advenchen Laboratories, Inc., CA, USA)로 중국을 제외한 세계 판권을 취득하여 독자적인 바이오사업을 시작하였습니다. 본 Rivoceranib(구. Apatinib Mesylate)는 위암(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국), 간암 (2021년 11월 미국식품의약국), 선양낭성암 (2021년 2월 미국식품의약국) 대상으로 희귀의약품 지정을 받아 임상종료 후 시판허가에 대한 심사의 신속화, 수수료 감면 등의 혜택과 최소 8년(2029년)에서 최대 13년(2034년) 동안 독점 판매할 수 있습니다.
2011년 11월 US FDA로부터 다국가(미국/한국) 1/2a 임상시험을 위한 IND 승인을 받아 표적항암제 리보세라닙(구. Apatinib Mesylate)은 다국가(미국/한국) 1/2상 임상시험을 종료하였고, 2017년 표준치료법으로 2차 치료제 이상에서 치료에 실패한 진행성 또는 전이성 환자를 대상으로 글로벌(미국, 유럽, 한국, 일본, 대만 등 12개국) 3상 임상시험을 완료하였습니다. 그 이후 적응증 확대를 위해 간암 1차, 선양낭성암의글로벌 임상을 추진하였고, 최근 두 임상 모두 환자 모집을 완료했습니다. 선양낭성암은 현재까지 표준치료제가 전무한 희귀암으로, 글로벌 최초 대규모 2상 임상을 진행하여 그 결과를 2022년 6월 미국 암학회(ASCO)에서 발표한 바 있습니다. 표준치료제가 없는 희귀암의 의료미충족수요가 높은 암종으로 First in Class를 기대하고 있습니다. 그리고 간암 1차 치료제 글로벌 임상은 항서제약에서 개발한 PD-1 면역항암제 캄렐리주맙과 리보세라닙의 병용으로 실시되었으며, 글로벌 543명의 임상 환자를 모집하였고, 2022년 ESMO에서 그 결과를 발표했습니다. 통상적으로 임상 결과의 유효성을 입증하는 1차 평가지표는 적응증, 치료방식, 대조군 등에 따라 다르게 이루어집니다. 당사가 진행한 간암 1차 치료제 글로벌 3상 임상(항서제약 캄렐리주맙 병용)의 경우 기존 1차 치료제인 소라페닙을 대조군으로 하여 OS와 PFS를 1차 평가지표로 하여 진행되었습니다. mOS의 경우 대조군인 소라페닙 대비 6.9개월 긴 22.1개월을 기록했고, mPFS는 대조군 대비 1.9개월 증가한 5.6개월을 기록해(통계적 유의성 확보) 1차 평가지표의 유효성을 만족했습니다. 이에 회사는 2023년 5월 FDA에 NDA(시판승인허가)를 신청하였으며, 2024년 5월 FDA로부터 CRL(보완요구서한)을 수령하였습니다. 그 밖에도, 대장암(Colorectal cancer) 3차 치료제, 위암(Gastric cancer) 2차 치료제에 대해서 임상시험중에 있습니다. 대장암 3차 치료제는 타이호제약의 론서프(Lonsurf)와 병용으로 임상 1/2상을, 위암 2차 치료제는 파클리탁셀(Paclitaxel)과 병용요법으로 임상 1/2상을 진행 중입니다. 그리고 미국 서던 캘리포니아 암센터에서 육종(Sarcoma)에 대해서 BMS의 면역항암제 옵디보(Nivolumab)의 병용임상시험을 종료하였습니다.
2020년 3월 아필리아(Apealea) 라이센스를 스웨덴 비베스토(Vivesto, 舊 Oasmia)로부터 러시아, 북유럽과 동유럽 일부 국가를 제외한 세계 판권을 취득하였습니다. 아필리아는 파클리탁셀(paclitaxel)의 3세대 개량 신약으로 Vivesto의 독점 기술 플랫폼인 'XR17'을 사용하여 개발된 항암제로, 주입 전에 사전 처치가 필요가 없고, 주사제 주입 시간이 짧아 환자의 편의성을 증대시키면서 부작용을 최소화했습니다. 유럽에서 난소암 2차 치료제로 카보플라틴(carboplatin)과 병용으로 허가받았습니다. 2022년 5월 독일을 시작으로 본격적인 마케팅 활동을 시작하였으며, 점진적으로 시판국을 넓혀나갈 계획입니다.
※ Pipeline 현황
|
품목명 |
적응증 |
특징 및 임상현황 |
|
리보세라닙 |
위암 간암 대장암 선양낭성암 |
1. 특징 - Oral : 경구용 제품으로 낮은 생산단가 2. 임상시험 현황 - 위암 말기 : 단독요법 - 간암 1차 : 캄렐리주맙과 병용요법 - 대장암 3차 : 론서프와 병용요법 - 위암 2차 : 파클리탁셀과 병용요법 - 선양낭성암 : 단독요법 |
|
아필리아 (Apealea) |
난소암 |
1. 특징 - 파클리탁셀의 개량신약(주사제) - 기존 파클리탁셀과 달리 전처치가 필요없고, 가용화제인 크레모포어 2. 개발현황 - 유럽에서 난소암 2차 치료제로 카보플라틴과 병용요법으로 허가 |
(3) 계열회사의 관한 사항 : HLB생명과학R&D
HLB생명과학R&D는 2022년 4월 1일 신약개발 전문성 강화를 위해 설립되었습니다.현재, 항암 파이프라인 신규 구축을 위해 초기 비임상 단계 물질을 도입(G2M Project)하였으며 한국을 포함한 글로벌 주요 국가에 대한 특허권과 물질의 생산, 판매 그리고 향후 기술이전에 대한 권리 등의 일체의 권리를 확보했습니다. 신규 항암물질은 세포주기에 관여하는 신호를 조절해 암세포의 증식을 저해하는 기전입니다. 세포주기는 모세포가 두 개의 딸세포로 분열해 유전물질을 물려줄 때까지의 세포 일생을 의미합니다. 그리고 세포들은 보통 4단계(G1기→S기→G2기→M기) 주기를 반복하며 세포분열을 진행합니다. 신규 항암물질은 세포분열 주기 중 G2기→M기의 진행을 방해함으로써 세포분열을 억제, 암세포의 성장을 저해하고 사멸을 유도합니다. 향후 해당 후보물질을 폐암, 유방암, 대장암, 췌장암 등 각종 고형암종을 대상으로 in vitro / in vivo 유효성 평가와 독성시험을 진행 후 임상후보물질로 개발할 계획입니다.
* Pipeline 현황
|
품목명 |
적응증 |
특징 및 진행 현황 |
| G2M Project | 폐암 유방암 대장암 췌장암 |
1.특징 - 세포주기(Cell cycle)에 관련된 신호를 조절해 암세포 증식을 저해 - 항암제 내성 암에서 효과를 보임 2. 진행 현황 - 암종별 유효성 평가를 진행 - 항암제 물성 개선 화합물 합성 중 - 기전 심화 탐색을 위한 mRNA array 분석 진행 - 항암제 내성 암세포 구축 및 내성 암세포에서의 유효성 평가 |
| CDK | 유방암 난소암 |
1.특징
- CDK 인산화 효소를 저해하여 암세포 증식 저해
- BRCA 돌연변이 암세포에 효과를 보임
- PARP 저해제와 시너지 효과를 보임 2. 진행 현황
- 암종별 유효성 평가 진행 중
- 선도물질 화합물 합성 중 |
| Cannabinoid |
대장암 위암 |
1.특징
- CB1, CB2 저해하여 암세포 증식 저해
- AKT관련 시그널에 효과를 보임 2. 진행 현황
- 암종별 유효성 평가 진행 중
- 선도물질 화합물 합성 중
- 항암효과평가 동물실험 진행예정 |
(4) 신규한 기전의 항암 신약 물질 국내 전용실시권 - HLB생명과학
당사는 2020년 9월 28일 항서제약(Jiangsu Hengrui Medicine Co., Ltd., 중국)으로부터 '파이로티닙(Pyrotinib)' 의 국내전용실시권(Sublicense) 계약을 체결하였습니다.
국내 전용실시권의 보유는 당사가 권한을 가지고 국내에서 임상 진행, 허가 승인, 상업화를 추진할 수 있음을 의미합니다. 후보물질에 대한 자세한 사항은 다음과 같습니다.
□ 파이로티닙(Pyrotinib)
| [항서제약(Jiangsu Hengrui Medicine Co., Ltd.회사 개요] |
|
구분 |
내용 |
|
설립년도 |
1997 년 |
|
본점소재지 |
중화인민공화국 장쑤성 롄윈강시 |
|
주요 사업 |
항암약품과 수술약품 연구 및 생산 |
|
주요 파이프라인 |
항암제, 마취제, 조영제, 항염증제, 심혈관 치료 약물 |
|
주요 구성원 |
쑨퍄오양 (회장) |
출처 : 당사 내부 자료
| [파이로티닙(Pyrotinib의 개요] |
|
중국 CNDA 조건부 승인일 |
2018년 08월 22일 |
|---|---|
|
- EGFR (EGFR, HER2, HER3, HER4) 신호 전달 활성은 암세포에 있어서 성장과 분열, 전이를 일으키는 주요 원인으로 알려져 있음. - 특히, 15%-20%의 유방암 환자들은 HER2 수용체의 증가가 나타나고 있으며 매우 공격적인 성향을 띔 - 비소세포 폐암에서는 2-3% 정도 HER2 돌연변이가 나타나고 있음. 이에 HER2를 표적하는 다양한 시도가 진행되고 있음 - 현재 해당 기전을 억제하는 약물들은 출시되어 있지만 부작용이 크거나 항암제 저항성이 생기는 현상이 일어남. 또한 충분한 OS(전체 생존 기간)를 달성하고 있지 못함 - Pyrotinib은 EGFR, HER2, HER4 모두를 억제하는 약물로서 하위 기전인 PI3K /AKT 및 MAPK의 신호 전달 기전을 차단하여 암세포의 증식, 분열, 생존을 억제하는 항암제임 - 기존 약물 대비 부작용이 적으며 효력이 동등하거나 우월함 - 중국에서는 임상 2상의 결과를 통해 조건부 허가 및 판매를 승인하였음 - 현재 전이성 HER2 양성 유방암에 대한 중국 내 임상 3상 시험이 완료되었음 - 당사에서 2020년 9월 28일에 도입 계약을 체결하였으며 국내 3상 임상 시험 진행을 기획하고 있음 |
|
출처 : 당사 내부 자료
Epidermal growth factor receptor (EGFR) family는 EGFR (ErbB-1, HER1]), HER2 (ErbB2), HER3 (ErbB3)와 HER4 (ErbB)로 구성되며 모두 tyrosine kinase 활성을 갖고 있습니다. 각각의 EGFR family는 특정 라이간드의 결합을 통해 활성화되며 이는 PI3'K-AKT 및 RAS-MAPK 경로의 하위 신호 전달을 통해 세포의 성장 등을 조절합니다. 하지만 몇몇 암종에서 EGFR family는 특정 부위의 돌연변이 혹은 과발현을 통해 라이간드 결합 없이도 스스로 높은 활성을 유지하게 되고 이를 통해 암세포의 성장, 전이 및 항암제 내성을 획득합니다.
|
[암세포에서 HER2 신호 전달 경로] |
||
|---|---|---|
|
HER2는 알려진 어떤 리간드에도 직접 결합하지 않는 것으로 알려져 있습니다. HER2 매개 신호 경로의 활성화는 리간드-활성화된 EGFR 또는 HER3를 이용한 이형이합체화 또는 HER2 자체가 과발현으로 존재할 때 동종이합체화에 의해 발생합니다. 활성화된 HER2는 리간드가 결합한 다른 EGFR family 중 하나와의 상호 작용을 통해 EGFR과 유사한 하위 신호 전달을 시작합니다. 모든 EGFR 쌍 중에서 HER2 / HER3 이형이합체는 PI3K의 p85 서브 유닛과 HER3의 결합을 통해 PI3K/AKT 신호 전달을 강력하게 활성화시키며 동시에 RAS-RAF-MAP 신호전달을 통해서도 하위 신호 전달을 활성화시킵니다. HER2의 과발현은 주로 HER2 유전자 증폭에 기인하며, HER2 돌연변이 또한 HER2 신호 전달 과정의 활성화를 초래합니다. 이러한 HER2 과발현 및 돌연변이는 유방, 위, 폐, 방광 및 자궁내막암에서 보고되었습니다.
|
특히 유방암 환자의 15-20%가 HER2의 과발현을 가지고 있으며, 비소세포 폐암 (NSCLC)에서는 HER2 돌연변이 (exon 20에 12 염기 쌍의 프레임 삽입)가 2%-3% 정도 발생하는 것으로 알려져 있습니다. 이러한 과발현 혹은 돌연변이는 좀 더 공격적인 암 진행과 관련이 있습니다. 유방암 및 비소세포 폐암 환자의 임상 결과는 주로 항HER2 항체 및 그 유도체를 포함한 HER2 표적 치료법의 개발로 크게 향상되었습니다. 특히 Tyrosine kinase inhibitors (TKIs)와 trastuzumab-emtansine과 같은 항체-약물 결합체는 지금까지 많은 연구가 진행되었습니다. 하지만 이러한 항암제들에 대해 저항이 생기는 현상이 나타나고 있기 때문에 현재 결과를 개선하고 저항을 극복하기 위해 추가 항암제가 더 개발되어야 합니다.
|
[HER2 신호 전달 경로 관련 주요 항암제 개발 현황] |
|
개발명 |
표적/제형 |
회사명 |
|
Trastuzumab |
HER2 |
Roche |
|
Pertuzumab |
HER2 |
Roche |
|
Trastuzumab-emtansine |
HER2 |
Roche |
|
Lapatinib |
HER1/2 |
Novartis |
|
Neratinib |
HER1/2/4 |
Puma Biotechnology |
|
Tucatinib |
HER2/3 |
Seattle Genetics |
출처 : 당사 내부 자료
Pyrotinib은 중국 항서제약에서 개발한 HER 1/2/4을 표적으로 하는 경구용 항암제로서 유방암 및 비소세포 폐암을 포함한 HER2의 과발현 혹은 돌연변이를 가지고 있는 고형암에 유효한 약물입니다. Pyrotinib은 이미 안트라시클라인 또는 탁산 화학요법으로 치료한 환자에서 HER2 양성, 전이성 유방암 치료를 위해 카페시타빈과 함께 병용하는 항암제로서 2018년 8월에 중국식약처 (CFDA)로부터 조건부 승인을 받은 후 2020년 7월에 정식 승인을 받았습니다. 또한, HER2 양성 유방암을 대상으로 현재 Trastuzumab/Docetaxel과 병용요법에 대한 임상시험도 진행 중에 있습니다. 당사는 전이성 HER2 양성 유방암과 초기 및 국소 진행성HER2 양성 유방암에 대해 허가 신청을 위한 3상 임상 시험을 진행할 예정입니다.
유방암과 별도로 Pyrotinib에 대해 HER2 변이성(엑손20 삽입) 비소세포폐암(NSCLC)을 대상으로 하는 글로벌 임상3상 시험이 진행중이며, 한국에서는 2020년 12월에 식약처로부터 IND 승인을 받아 서울아산병원, 분당서울대병원, 삼성서울병원, 연세대 세브란스병원, 고려대병원 등 국내 7개 병원에서 비소세포폐암 환자를 대상으로 Docetaxel 대비 Pyrotinib의 유효성과 안전성을 비교하는 임상 시험이 진행되고 있습니다.
최근의 연구 결과들을 보면 HER2를 표적으로 하는 항체 또는 저분자 약물은 HER2 양성 유방암을 뚜렷하게 개선하고 있습니다. 이러한 HER2 표적 치료제에는 항 HER2 항체 (trastuzumab and pertuzumab), 항체-약물 결합체(ado-trastuzumab emtansine) 및 저분자 저해제 (Lapatinib, Neratinib, Afatinib, Tucatinib) 등이 있습니다. 하지만 이러한 치료제는 각각 저항성 기전에 의한 항암 효과 감소 및 인체에 대한 부작용 문제를 갖고 있습니다. 당사는 Pyrotinib이 기존 항암제들이 갖는 한계점을 극복할 수 있는 새로운 대안 치료제라고 판단하고 있습니다.
④ 사업과 관련된 중요한 지적재산권(특허권) 등
| [분야별/단계별 특허출원 내역] |
|
주요과제명 |
유형별 |
국내 진행단계 |
PCT |
해외 (국가별진입) |
||||||||||
|
방법특허 |
용도특허 |
물질특허 |
기타 |
계 |
출원 | 심사 | 등록 | 계 | 출원 | 심사 | 등록 | 계 | ||
| 리보세라닙 | - | - | 2 | - | 2 | - | - | 2 | 2 | - | 1 | - | 45 | 46 |
| 파이로티닙 | - | - | 3 | - | 3 | - | - | 3 | 3 | - | - | - | - | - |
| G2M 물질 | - | 1 | 2 | - | 3 | 1 | - | 2 | 3 | 3 | - | - | 15 | 15 |
| 간세포치료제 | 1 | - | - | - | 1 | - | - | 1 | 1 | - | - | - | - | - |
| 기타세포치료제 ( μMatricel) |
1 | - | - | - | 1 | - | - | 1 | 1 | 1 | - | - | 3 | 3 |
| 기타의료기기 (Hutrigel) |
2 | - | - | - | 2 | - | 2 | - | 2 | 2 | - | - | - | - |
| 바이오인공간 | 6 | - | - | - | 6 | - | - | 6 | 6 | 4 | 1 | - | 8 | 9 |
| 조직접착, 지혈 및 창상피복재 |
- | - | - | 2 | 2 | - | - | 2 | 2 | 1 | - | - | 12 | 12 |
|
합 계 |
10 | 1 | 7 | 2 | 20 | 1 | 2 | 17 | 20 | 11 | 2 | - | 83 | 85 |
출처: 당사 내부자료
| (*) '유형별' 특허는 패밀리 특허당 1건으로 판단하였습니다. |
| [특허권 현황] |
| 파이프라인 | 명칭 | 국가 | 상태 | 권리자 | 출원일 | 등록일 | 등록번호 |
| G2M 물질 | 신규한 4-(아릴)-N-(2-알콕시티에노[3,2-b]피라진-3-일)-피페라진-1-카복스아미드 유도체 및 이의 항증식 효과 | 대한민국 | 등록 | HLB생명과학 R&D | 2015-12-03 | 2017-04-10 | 제 1727412 호 |
| G2M 물질 | Substituted thieno[3,2-b]pyrazines for inhibiting cancer cell proliferation and inducing cancer cell apoptosis | 미국 | 등록 | HLB생명과학 R&D | 2015-12-03 | 2018-08-28 | US 10059721 |
| G2M 물질 | 신규한4-(아릴) -N-(2-알콕시 티에노[3,2-b]피라진-3-일)-피페라진-1-카르복사마이드 유도체 및 그 항증식 효과 | 일본 | 등록 | HLB생명과학 R&D | 2015-12-03 | 2018-06-08 | JP 6349464 |
| G2M 물질 | Substituted thieno[3,2-b]pyrazines for inhibiting cancer cell proliferation and inducing cancer cell apoptosis | 유럽 5개국 |
등록 | HLB생명과학 R&D | 2015-12-03 | 2019-08-14 | EP 3231800 |
| G2M 물질 | 신규한 4-(아릴)-N-(3-알콕시퓨로[2,3-b]피라진-2-일)-피페라진-1-카복스아미드 유도체 및 이의 항증식 효과 | 대한민국 | 등록 | HLB생명과학 R&D | 2017-06-08 | 2018-06-22 | 제 1872645 호 |
| G2M 물질 | 4-(aryl)-N-(3-alkoxyfuro[2,3-b]pyrazin-2-yl)-piperazine-1-carboxamide derivative and antiproliferative effect thereof | 미국 | 등록 | HLB생명과학 R&D | 2017-06-09 | 2020-10-13 | US 10800788 |
| G2M 물질 | 신규한4-(아릴) -N-(3-알콕시 프로[2,3-b]피라진-2-일)-피페라진-1-카르복사미드 유도체 및 그 항증식 효과 | 일본 | 등록 | HLB생명과학 R&D | 2017-06-09 | 2020-04-30 | JP 6698180 |
| G2M 물질 | NOVEL 4-(ARYL)-N-(3-ALKOXYFURO[2,3-B]PYRAZIN-2-YL)-PIPERAZINE-1-CARBOXAMIDE DERIVATIVE AND ANTIPROLIFERATIVE EFFECT THEREOF | 중국 | 등록 | HLB생명과학 R&D | 2017-06-09 | 2021-05-28 | CN 109641915 |
| G2M 물질 | NOVEL 4-(ARYL)-N-(3-ALKOXYFURO[2,3-B]PYRAZIN-2-YL)-PIPERAZINE-1-CARBOXAMIDE DERIVATIVE AND ANTIPROLIFERATIVE EFFECT THEREOF | 유럽 4개국 |
등록 | HLB생명과학 R&D | 2017-06-09 | 2021-05-28 | EP E052987 |
| G2M 물질 | NOVEL 4-(ARYL)-N-(3-ALKOXYFURO[2,3-B]PYRAZIN-2-YL)-PIPERAZINE-1-CARBOXAMIDE DERIVATIVE AND ANTIPROLIFERATIVE EFFECT THEREOF | 인도 | 등록 | HLB생명과학 R&D | 2017-06-09 | 2020-11-27 | IN 351819 |
| 기타세포치료제 | 모낭유도 능력이 있는 모유두 조직의 제조방법 | 대한민국 | 등록 | 동국대학교 산학협력단 | 2004-11-29 | 2006-08-22 | 제 0616752 호 |
| 기타세포치료제 | Method for the preparation of a dermal papilla tissue having hair follicle inductive potency | 미국 | 등록 | HLB셀 (구. 라이프코드) 박정극 |
2005-11-29 | 2009-12-22 | US 7635589 |
| 기타세포치료제 | Method for the preparation of a dermal papilla tissue having hair follicle inductive potency | 영국 | 등록 | HLB셀 (구. 라이프코드) 박정극 |
2005-11-29 | 2008-09-17 | GB 1819810 |
| 기타세포치료제 | Method for the preparation of a dermal papilla tissue having hair follicle inductive potency | 중국 | 등록 | HLB셀 (구. 라이프코드) 박정극 |
2005-11-29 | 2010-12-15 | CN 101068920 |
| 바이오인공간 | 담체의 표면에 세포를 고정화하는 방법 | 대한민국 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2005-06-27 | 2007-01-31 | 제 0679729 호 |
| 바이오인공간 | 겔 비드 충전형 생물반응기를 이용한 생인공 간 시스템 | 대한민국 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2007-03-30 | 2009-02-20 | 제 0886003 호 |
| 바이오인공간 | Bioartificial liver system using bioreactor packed with gel beads | 미국 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-03-28 | 2012-12-11 | US 8329457 |
| 바이오인공간 | Bioartificial liver system using bioreactor packed with gel beads | 캐나다 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-03-28 | 2013-02-26 | CA 2681798 |
| 바이오인공간 | Bioartificial liver system using bioreactor packed with gel beads | 독일 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-03-28 | 2012-01-26 | DE 11-2008-000814 |
| 바이오인공간 | Bioartificial liver system using bioreactor packed with gel beads | 영국 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-03-28 | 2011-09-21 | GB002462946 |
| 바이오인공간 | Bioartificial liver system using bioreactor packed with gel beads | 인도 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-03-28 | 2018-05-28 | IN 297164 |
| 바이오인공간 | Bioartificial liver system using bioreactor packed with gel beads | 중국 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-03-28 | 2012-08-22 | CN 101668494 |
| 바이오인공간 | 일체형 무균 캡슐 제조장치 | 대한민국 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2007-10-05 | 2009-06-08 | 제 0902781 호 |
| 바이오인공간 | Apparatus and method of manufacturing aseptic capsules | 캐나다 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-10-01 | 2014-11-18 | CA 2701598 |
| 바이오인공간 | Apparatus and method of manufacturing aseptic capsules | 독일 | 등록 | HLB셀 (구. 라이프코드) 동국대학교 (박정극) 삼성생명재단 (이석구) 김성구 |
2008-10-01 | 2017-06-08 | DE 11-2008-002671 |
| 간세포치료제 | 간세포의 제조방법 및 이로부터 제조된 간세포 | 대한민국 | 등록 | HLB셀 (구. 라이프리버) 동국대학교 |
2010-07-15 | 2013-01-22 | 제 1227047 호 |
| 바이오인공간 | 복막 순환 장치 및 이를 이용한 바이오인공 간 시스템 | 대한민국 | 등록 | HLB셀 (구. 라이프리버) 삼성생명공익재단 |
2016-03-07 | 2018-12-17 | 제 1931854 호 |
| 바이오인공간 | 간세포 및 캡슐화한 간세포 구상체의 동결 보존을 위한 동결보존용 무혈청 용액 및 이를 이용한 동결보존법 | 대한민국 | 등록 | HLB셀 (구. 라이프리버) 삼성생명공익재단 |
2018-11-29 | 2020-08-21 | 제 2148998 호 |
| 조직접착, 지혈 및 창상피복재 | 분사량 조절이 가능한 분말 분사장치 | 대한민국 | 등록 | HLB셀 | 2018-04-18 | 2020-02-10 | 제 207779 호 |
| [전용실시권 현황] |
| 파이프라인 | 명칭 | 국가 | 상태 | 권리자 | 출원일 | 등록일 | 보유한 전용실시권 내용 | 보유기간 (계약일~만기일) |
비고 | 등록번호 |
| 리보세라닙 | 혈관신생 억제제로서의 6환 아미노-아미드 유도체 | 대한민국 | 등록 | HLB | 2004-06-04 | 2012-06-15 | "계약기술” 및 "계약지적재산권"에 관한 한국 전용실시권 | 2018년8월14일부터 2024년6월4일까지 |
보유기간 만료일 : 특허존속기간 만료일 | 제 1159034호 |
| 리보세라닙 | Six membered amino-amide derivatives an angiogenisis inhibitors | 미국 | 등록 | HLB | 2004-06-04 | 2006-10-31 | "계약기술” 및 "계약지적재산권"에 관한 통상실시권 | 2021년01월06일부터 2024년10월08일까지 |
보유기간 만료일 : 특허존속기간 만료일 | US 7129252 |
| 리보세라닙 | 혈관신생 억제제로서의 6환 아미노-아미드 유도체 | 일본 | 등록 | HLB | 2004-06-04 | 2012-07-27 | "계약기술” 및 "계약지적재산권"에 관한 통상실시권 | 2020년11월11일부터 2024년06월04일까지 |
보유기간 만료일 : 특허존속기간 만료일 | JP 5046643 |
| 리보세라닙 | Six membered amino-amide derivatives an angiogenisis inhibitors | 캐나다 | 등록 | HLB | 2004-06-04 | 2012-01-24 | "계약기술” 및 "계약지적재산권"에 관한 통상실시권 | 2021년02월01일부터 2024년06월04일까지 |
보유기간 만료일 : 특허존속기간 만료일 | CA 2568608 |
| 리보세라닙 | Six membered amino-amide derivatives an angiogenisis inhibitors | 유럽 27개국 |
등록 | HLB | 2004-06-04 | 2014-06-25 | "계약기술” 및 "계약지적재산권"에 관한 통상실시권 | 2021년02월24일부터 2024년06월04일까지 |
보유기간 만료일 : 특허존속기간 만료일 | EP 1633712 |
| 리보세라닙 |
N-[4-(1-사이아노사이클로펜틸)페닐]-2-(4-피리딜메틸)아미노-3-피리딘카복스아마이드의 염 | 대한민국 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 | 2009-06-11 | 2016-11-02 | "계약기술” 및 "계약지적재산권"에 관한 한국 전용실시권 | 2018년08월14일부터 2029년06월11일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
제 1674227 호 |
| 리보세라닙 |
Salts of N-[4-(1-cyanocyclopentyl)phenyl]-2-(4-pyridylmethyl)amino-3-pyridinecarboxamide | 미국 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 | 2009-06-11 | 2013-01-29 | "계약기술” 및 "계약지적재산권"에 관한 전용실시권 | 2018년08월14일부터 2029년06월11일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
US 8362256 |
| 리보세라닙 |
N-[4-(1-사이아노사이클로펜틸)페닐]-2-(4-피리딜메틸)아미노-3-피리딘카복스아마이드의 염 | 일본 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 | 2009-06-11 | 2014-11-21 | "계약기술” 및 "계약지적재산권"에 관한 전용실시권 | 2018년08월14일부터 2028년09월16일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
JP 5649132 |
| 리보세라닙 |
N-4-(1-cyan cyclopentyl) phenyl-2-(4-picolyl) amidogen-3-pyridinecarboxamide salt | 중국 홍콩 |
등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드, 상하이 헨그루이 파마수티컬 컴퍼니 리미티드 |
2008-09-16 | 2012-12-26 | "계약기술” 및 "계약지적재산권"에 관한 전용실시권 | 2018년08월14일부터 2028년09월16일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
CN 101676267 HK 1141514 |
| 리보세라닙 |
N-4-(1-cyan cyclopentyl) phenyl-2-(4-picolyl) amidogen-3-pyridinecarboxamide salt | 캐나다 호주 남아공 러시아 베트남 |
등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 | 2009-06-11 | 2016-05-24 2014-02-13 - 2013-11-27 |
"계약기술” 및 "계약지적재산권"에 관한 전용실시권 | 2018년08월14일부터 2029년06월11일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
CA 2736664 AU 2009295168 ZA 201101891 RU 0002499796 VN 1-0014320-000 |
| 리보세라닙 |
Salt of n-[4-(1-cyanocyclopentyl)phenyl]-2-(4-pyridinemethyl)amino-3-pyridinecarboxamide | 대만 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 | 2009-12-17 | 2014-12-01 | "계약기술” 및 "계약지적재산권"에 관한 전용실시권 | 2018년08월14일부터 2029년12월16일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
TW I462738 |
| 리보세라닙 |
THE SALTS OF N-(4-(1-CYANOCYCLOPENTYL)PHENYL)-2-(4-PYRIDYL METHYL)AMINO-3-PYRIDINECARBOXAMIDE | 유럽3개국 | 등록 | 지양수 헨그루이 메디스 컴퍼니 리미티드 |
2009-06-11 | 2014-03-12 | "계약기술” 및 "계약지적재산권"에 관한 전용실시권 |
2018년08월14일부터 2029년06월11일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
EP 2327697 |
| 파이로티닙 | 6-아미노 퀴나졸린 또는 3-시아노 퀴놀린 유도체, 그 제조 방법 및 약학적 용도 | 대한민국 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 상하이 헨그루이 파마수티컬 컴퍼니 리미티드 |
2010-08-26 | 2017-05-15 | "계약기술” 및 "계약지적재산권"에 관한 한국 전용실시권 |
2020년09월28일부터 2030년08월26일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
제 1738191 호 |
| 파이로티닙 | (이)-엔-[4-[[3-클로로-4-(2-피리딜메톡시)페닐]아미노]-3-시아노-7-에톡시-6-퀴놀릴]-3-[(2알)-1-메틸피롤리딘-2-일]프로프-2-엔아미드의 약학적으로 허용 가능한 염, 그의 제조 방법, 및 그의 의학적 용도 | 대한민국 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 상하이 헨그루이 파마수티컬 컴퍼니 리미티드 |
2012-02-10 | 2018-06-21 | "계약기술” 및 "계약지적재산권"에 관한 한국 전용실시권 |
2020년09월28일부터 2030년02월10일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
제 1871889 호 |
| 파이로티닙 | 타이로신 키나제 억제제 다이말리에이트의 결정형 아이 및 그의 제조 방법 | 대한민국 | 등록 |
지양수 헨그루이 메디스 컴퍼니 리미티드 |
2013-06-04 | 2020-02-11 | "계약기술” 및 "계약지적재산권"에 관한 한국 전용실시권 |
2020년09월28일부터 2033년06월04일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
제 2078077 호 |
| 바이오인공간 | 간세포 동결 보존용 무혈청 용액 및 이를 이용한 간세포 동결 보존방법 | 대한민국 | 등록 | 사회복지법인 삼성생명공익재단 | 2013-05-08 | 2015-01-05 | "계약기술” 및 "계약지적재산권"에 관한 한국 전용실시권 |
2015년01월05일부터 2033년05월08일까지 |
보유기간 만료일 : 특허존속기간 만료일 |
제 1480987 호 |
| 조직접착, 지혈 및 창상피복재 |
생분해성 의료용 접착제 또는 실란트조성물 | 대한민국 | 등록 | (재)유타 인하 디디에스 및 신의료기술개발 공동연구소 | 2014-07-15 | 2016-10-04 | "계약기술”및 "계약지적재산권"에 관한 기술이전 및 전세계 전용 실시권 | 2015년11월5일부터 2034년7월15일까지 |
보유기간: 출원일로부터 20년간 | 제 1664444호 |
| 조직접착, 지혈 및 창상피복재 |
생분해성 의료용 접착제 또는 실란트조성물 | 멕시코 인도 유럽 러시아 중국 |
등록 | (재)유타 인하 디디에스 및 신의료기술개발 공동연구소 | 2016-06-10 2016-06-13 2016-06-16 2016-07-13 2016-06-13 |
2019-05-29 2020-07-28 2018-12-12 2018-06-15 2020-10-16 |
"계약기술” 및 "계약지적재산권"에 관한 기술이전 및 전세계 전용 실시권 | 2015년11월5일부터 2034년7월15일까지 |
보유기간: 출원일로부터 20년간 | MX 366143 IN 342623 EP 3081236 RU 2657836 CN 106061518 |
| 조직접착, 지혈 및 창상피복재 |
생분해성 의료용 접착제 또는 실란트조성물 | 미국 | 등록 | (재)유타 인하 디디에스 및 신의료기술개발 공동연구소 | 2016-06-07 | 2017-10-18 | "계약기술” 및 "계약지적재산권"에 관한 기술이전 및 전세계 전용 실시권 | 2015년11월5일부터 2034년7월15일까지 |
보유기간: 출원일로부터 20년간 | US 10105465 |
| 조직접착, 지혈 및 창상피복재 |
생분해성 의료용 접착제 또는 실란트조성물 | 일본 | 등록 | (재)유타 인하 디디에스 및 신의료기술개발 공동연구소 | 2016-06-10 | 2017-09-15 | "계약기술” 및 "계약지적재산권"에 관한 기술이전 및 전세계 전용 실시권 | 2015년11월5일부터 2034년7월15일까지 |
보유기간: 출원일로부터 20년간 | JP 6207745 |
| 조직접착, 지혈 및 창상피복재 |
생분해성 의료용 접착제 또는 실란트조성물 | 호주 | 등록 | (재)유타 인하 디디에스 및 신의료기술개발 공동연구소 | 2016-06-24 | 2017-08-17 | "계약기술” 및 "계약지적재산권"에 관한 기술이전 및 전세계 전용 실시권 | 2015년11월5일부터 2034년7월15일까지 |
보유기간: 출원일로부터 20년간 | AU 2014360958 |
| 조직접착, 지혈 및 창상피복재 |
생분해성 의료용 접착제 또는 실란트조성물 | 캐나다 | 등록 | (재)유타 인하 디디에스 및 신의료기술개발 공동연구소 | 2016-06-09 | 2017-11-21 | "계약기술” 및 "계약지적재산권"에 관한 기술이전 및 전세계 전용 실시권 | 2015년11월5일부터 2034년7월15일까지 |
보유기간: 출원일로부터 20년간 | 제 2933271호 |
|
(*1) 계약기술 : "계약제품"의 설계,제조,사용과 관련하여 “갑”에 의해 개발되었거나 기타 일반적으로 사용되고 있는 것으로서 “갑”이 알고 있는 모든 기술적 지식,노하우, 자료 및 정보를 의미하며,지적재산권의 등록 여부를 불문한다. (*2) 계약지적재산권 : "계약제품"과 관련하여 “갑”에 의해 현재 소유중이거나 또는 소유하게 될, 그리고 “계약제품”의 제조에 사용 또는 적용되고 본 계약기간 동안에 라이센스 관리 또는 설정할 수 있는 특허, 실용신안, 출원에 관한 모든 권한을 의미한다. |
[의료기기사업 부문]
① 산업의 특성 등
□ 산업의 특성
주사기에 대한 전 세계 수요의 증가는 COVID-19와 같은 전염병 증가, 의료비 지출 증가, 정부 지원 정책, 만성 질환 및 전염병 증가에 기인하며 아래표와 같은 특징을 가지고 있습니다.
| 특징 | 내용 |
| 제품의 다양성 | 의료기기는 주사기 등 소모품, 기초의료용품, MRI, CT, 의료용 로봇 및 수술기기 등 광범위한 기기와 장비를 포괄하며, 기술발전에 따라 점차 다양화 되는 추세 |
| 다품종 소량생산 | 의료기기 제품 종류는 수천 가지가 넘고, 품목당 생산 수량도 10만대를 초과하는 품목의 거의 없을 정도로 대표적인 다품종 소량 생산 사업임 |
| 정보와의 밀접성 | 의료기산업은 인간의 생명과 보건에 관련된 제품을 생산하는 산업으로 국민의 건강증진 및 건강권 확보 등에 직간접적 영향을 받기 때문에 정부의 인허가 등 규제가 필요함 |
| 한정된 수요처 | 의료기기는 의료진단과 치료에 전문성을 가진 병원이 주요 수요처이며, 건강 및 보건과 관련되므로 제품의 안정성, 신뢰성을 우선적으로 고려함 |
| 지속적 투자필요 | 개발 제품의 시장 규모가 작고 수명주기가 짧아 연구개발에 대한 지속적인 투자가 요구되는 산업 |
(출처: 한국보건산업진흥원)
□ 경기변동의 특성
일반적인 제약산업과 마찬가지로 해당 산업은 국민의 건강과 직접적으로 연관된 산업으로 타 사업과 비교하여 경기변동 및 계절성 등에 비하여 민감도가 낮으며 필수재적인 재화 성격으로 경기방어적인 특징을 갖고 있어 위험도가 낮은 편입니다.
② 국내외 시장여건
주사기 시장은 고령사회가 본격화되면서 점진적으로 확대되고 있으며, 주사기 및 주삿바늘과 같이 위생, 보건상의 이유 등 제품 고유의 특성으로 출하량이 계속 증가할 것으로 전망되며 국내 의료기기 기업들도 제품의 품질과 기술력에서 우수성을 인정 받아 선진 국가들과 긴밀한 협력을 통해 글로벌 시장에서의 입지를 다지고 있습니다.
1) 세계 주사기 산업 동향 및 전망
주사기의 사용량은 일반적으로 사용되는 다른 의료용품보다 1.5배 높으며, 기술적인 발전과 함께 다양한 산업 및 지역에서 여러 용도로 확장되고 있습니다. 주사기의 디자인과 기능 개선, 안정성 향상, 자동화 기술의 도입 등이 이루어지고 있으며, 의료 및 생명과학 분야에서 핵심적인 역할을 수행하고 있습니다. 세계 주사기 시장은 2022년 178.9억 만 달러로 추정되며 연평균 4.2%의 성장률로 2032년 270억 달러에 이를 것으로 전망됩니다.
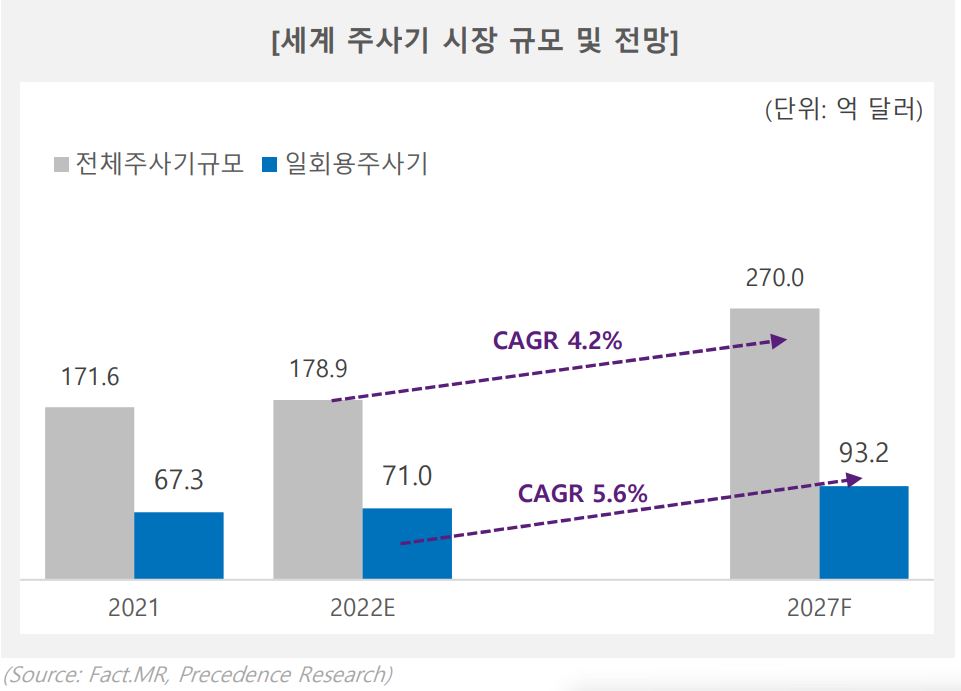 |
|
세계주사기 시장의 규모 |
2) 국내 주사기 산업 동향 및 전망
국내 의료기기 생산 품목군 중 하나인 '주사기 및 주사침류'는 2020년대 들어 코로나 여파로 생산규모가 크게 늘어나기 시작했습니다. 2021년 주사기 및 주사침류 생산액은 8,090억원으로 2020년 대비 17.9% 성장했고, 생산 품목군 중 6.28%를 차지하며 5위를 기록했습니다. 주사기 및 주사침류의 수출실적은 2021년 1억 9,700만 달러로 전년대비 24.7% 상승한 것으로 나타났습니다.
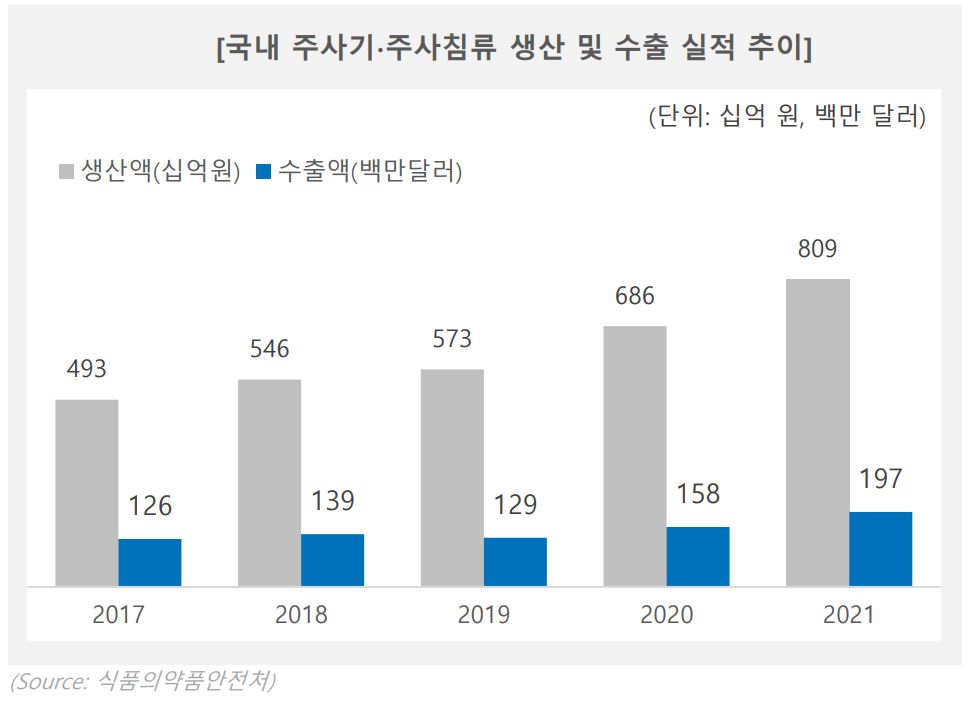 |
|
국내 주사기주사침류 생산 및 실적 추이 |
③ 회사의 경쟁우위 요소
의료기기 제조 20여 년 업력의 제조기술 및 노하우를 보유하고 있으며 특히 '소프젝(Sofjec)'이라는 브랜드로 주사기, 주사침류 등을 주력 제품으로 생산 중에 있습니다. 국내 식품의약품안전처(MFDS), GMP 등 의료기기 품목허가를 보유하고 있으며 다년간 대형병원(서울아산병원, 강남성모병원 외), 중소병원 및 동물 병원 등에 납품하여 기업의 인지도와 제품의 신뢰도를 쌓아왔습니다. 또한, 국내뿐만 아니라 미국, 사우디, 베트남 몽골 등으로 수출하고 있으며 2021년 8월 미국 의료기기 유통 전문 업체 ‘AMTC’를 통해 소프젝에 대한 판매허가를 받았고, 2023년 2월 미국 FDA로부터 일회용주사기, 주사침, 필터주사기 등에 대한 미국 내 판매허가를 획득하였습니다.
[특허권 현황]
| 구분 | 명칭 | 국가 | 상태 | 권리자 | 실제권리보유내역 | 출원일 | 등록일 | 등록번호 |
| (권리비율) | ||||||||
|
특허 |
교체형 수액 정량 주입기 |
대한민국 |
등록 |
HLB생명과학 | HLB생명과학 |
2015.05.19 |
2016.01.25 |
제10-1589982호 |
|
상표 |
FREE TRADE TAMDAT |
대한민국 |
등록 |
HLB생명과학 | HLB생명과학 |
2012.01.30 |
2013.02.13 |
제40-0969236호 |
|
상표 |
FREEDOM EAGLE |
대한민국 |
등록 |
HLB생명과학 | HLB생명과학 |
2012.01.30 |
2013.05.14 |
제40-0969230호 |
|
상표 |
Sofcare |
대한민국 |
등록 |
HLB생명과학 | HLB생명과학 |
2020.01.17 |
2022.03.02 |
제40-1839138호 |
|
상표 |
Sofcare Animal |
대한민국 |
등록 |
HLB생명과학 | HLB생명과학 |
2020.01.17 |
2022.03.02 |
제40-1839141호 |
|
상표 |
Sofjec |
대한민국 |
등록 |
HLB생명과학 | HLB생명과학 |
2005.04.22 |
2006.01.17 |
제40-0647647호 |
[의약품유통사업 부문]
① 산업의 특성 등
□ 산업의 특성
의약품 유통업은 다수의 제약회사에서 다품종 의약품을 대량 구매하여 병원에 납품하는 업종을 의미합니다. 의약품 유통업체들은 유통구조를 단순화함으로써 제약사의 재고 부담을 덜어주고, 제약사 영업활동에 따른 인건비 및 판촉비의 과다지출을 억제해주는 역할을 하고 있습니다. 또한, 약제비 상승 문제를 해소하여 구매사에게 합리적인 가격에 의약품을 제공합니다.
□ 산업의 성장성
2022
년 전체 의약품 유통금액은 88.9조원으로 전년대비 10.2%(8.2조원)증가하였으며, 최근 3년간 연평균 7.8%증가('20년 약 75.9조원, '21년 약 80.6조원, '22년 약 88.9조원)한 것으로 나타났습니다. 2022년 의약품 유통금액 88.9조원은 중 49.2조원('21년도 42조)은 도매상 유통금액으로 전체 시장의 55.3%를 차지하고 있습니다
.(
출처: '22년완제의약품유통정보통계집발췌, 2023.06, 건강보험심사평가원).
이렇듯 현재까지 의약품 유통업 시장은 매년 꾸준한 성장을 보여왔으며, 앞으로도 성장 추세는 지속될 것으로 판단됩니다. 국내 의료비 증가속도는 국민소득 증가율을 상회하여 빠르게 증가하고 있으며, 2023년 기준 국내 인구의 기대수명은 83.6년으로 OECD 국가 평균 기대수명 80.3년을 상회하고 있습니다
.(
출처: OECD 보건통계자료일부(2023), 보건복지부)
즉, 국내 의료비 증가 속도와 빠른 고령화 사회 진입 속도에 비추어 보았을 때, 의약품 및 의료용품 시장은 지속적으로 성장할 것으로 보고 있습니다.
□ 경기변동의 특성
국민건강과 직접적으로 연관된 의약품은 특성상 경기 방어적인 성격을 갖고 있습니다. 일반의약품의 경우 일반적인 경기변동이나 계절적 경기변동에 다소 영향을 받는 편이며, 전문의약품은 상대적으로 경기변동에 덜 민감한 특성을 가지고 있습니다.
② 국내외 시장여건
22
년말 기준 우리나라 의약품을 공급하는 업체수는 약 3,987개소로, 도매상 3,503개소(87.9%), 제조사 298개소(7.5%), 수입사 186개소(4.6%) 로 전체 업체의 도매상 비중이 가장 높습니다.
해외 의약품 유통시장에 비하여 국내 의약품 유통시장은 중소형 업체들이 난립해있는 상황입니다. 그러나 해외사례에 비추어 볼 때, 점차 국내시장도 대형화 및 집중화될 전망입니다. 미국의 의약품 유통업체는 1970년 144개사에서 현재 20여개사로 통합되었으며, 이 중 상위 4개사의 매출이 전체 의약품 유통매출의 약 90%를 차지할 정도로 거대화되어 있습니다. 일본의 경우 정부 정책 및 과다 경쟁에 따른 이익 저하 등의 이유로, 의약품 유통업체가 1988년 418개에서 2006년 134개로 그 수가 줄어들었습니다. 해외 추세와 같이 국내도 일부 업체들을 중심으로 점차 의약품 유통시장의 통합화가 진행될 것으로 예상됩니다.
상기의 경쟁요소로 인하여 제약사와 의료기관, 조제약국 등은 변화에 적응하기 위해 규모를 확대해 왔습니다. 2022
년 상위유통업체(500억 이상 7.1%)가 시장점유율 약 78.6%을 기록하는 등 과점시장의 형태를 취하고 있습니다.
【최근 3개년 매출규모별 시장점유율】
| (단위 : 개사, %) |
| 구 분 | 매출규모 | 1000억이상 | 500억-1000억미만 | 100억-500억미만 | 100억미만 | 계 |
|
2022년 |
업체수 |
177
|
98 | 525 | 3,063 | 3,863 |
|
업체수점유율 |
4.6
|
2.5 | 13.6 | 79.3 | 100.0
|
|
|
시장점유율 |
71.0
|
7.6
|
12.9 | 8.5 | 100.0
|
|
| 2021년 | 업체수 |
76 |
38 |
391 |
2,773 |
3,278 |
| 업체수점유율 |
2.3 |
1.2 |
11.9 |
84.4 |
100.0 |
|
| 시장점유율 |
60.9 |
6.0 |
18.5 |
14.6 |
100.0 |
|
| 2020년 | 업체수 | 74 | 45 | 364 | 2,625 | 3,108 |
| 업체수점유율 | 2.5 | 1.4 | 11.7 | 84.4 | 100.0 | |
| 시장점유율 | 60.3 | 7.5 | 17.7 | 14.5 | 100.0 |
출처 : 의약품관리종합정보센터, 건강보험심사평가원 '2022' 완제의약품 유통정보 통계집 일부 발췌
2022년 기준 공급업체별로 요양기관에 공급한 내역의 분포도를 살펴보면 도매상은 약국 64.7% > 종합병원급 23.4% > 병원급 등 12.5% 공급으로 약국의 비중이 높으며 제조사 및 수입사도 마찬가지로 약국의 공급 비중이 가장 높게 차지하였습니다. 반면, 종합병원급의 공급 비중은 제조,수입사 4.1% 공급에 비해 도매상의 비중은 23.4% 로 더 높은 비중을 차지하고 있습니다. 이러한 통계를 보면 제조사 및 수입사들의 도매상을 통한 거래는 점차 증대할 것으로 보여집니다.
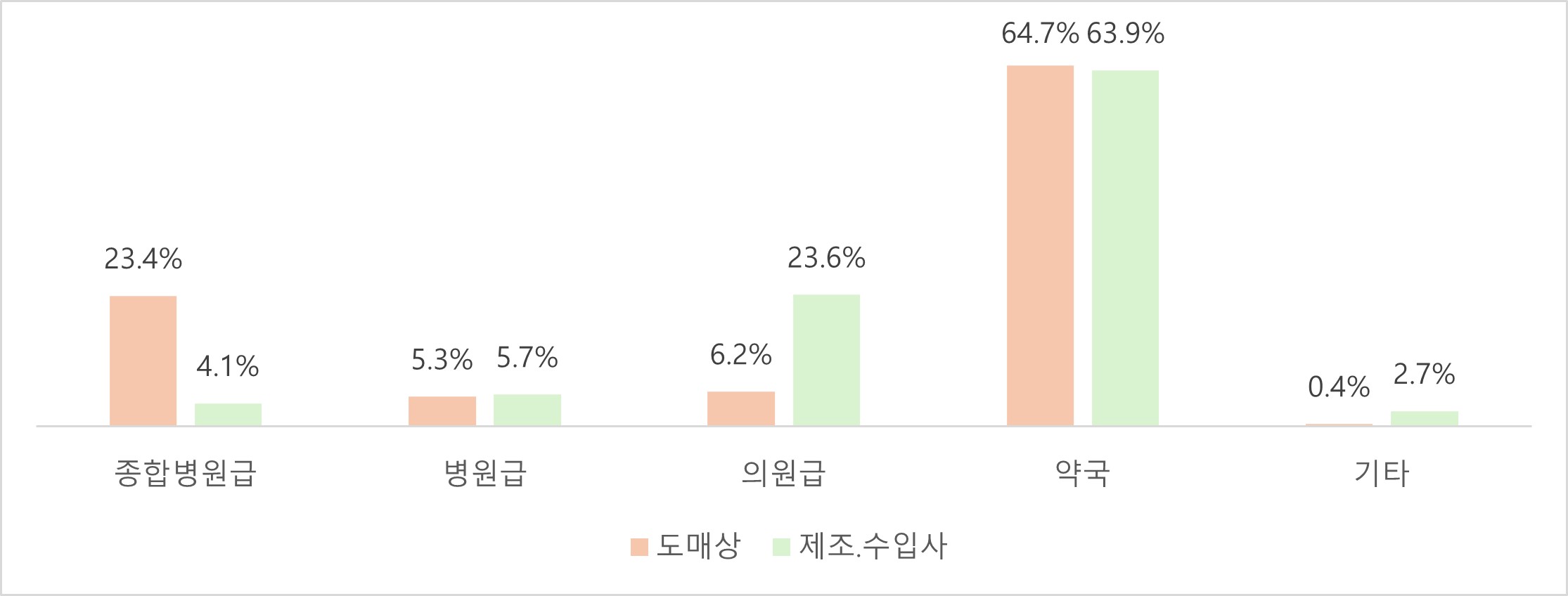 |
|
2022년 공급업체별 요양기관 종별 공급금액 비율 |
③ 회사의 경쟁우위 요소
신화어드밴스는 무차입경영의 우수한 재무상태와 풍부한 유동성을 보유하고 있으며, 20여년 이상 수행하며 다져진 영업력을 바탕으로 신규거래처를 꾸준히 확보하였습니다. 자사 영업 조직과 물류센터를 통한 안정적 매출과 함께 제약업체 및 도매업체와의 전략적 제휴로 품목 및 가격 경쟁력에 우위를 선점하였습니다. 향후 지역 인구 및 소득, 물류 효율성, 주변 상권 및 원외 시장 분석 등의 데이터를 활용하여 표적시장 선정을 통해 안정적인 성장을 이룰 것입니다.
[에너지사업 부문]
① 산업의 특성 등
□ 산업의 특성
태양광 및 폐기물에너지와 같은 신재생에너지 산업은 점차 고갈되는 화석연료의 대체연료 및 에너지 회수와 관련된 친환경 정책의 영향을 받으며, 폐기물 처분사업의 경우 폐기물 발생량에 직접 관련이 있는 산업으로 경제 및 산업규모에 영향을 받는 특징이 있습니다. 전 세계 신재생에너지 시장은 자원 고갈과 친환경 에너지원에 대한 지속적 수요 창출로 매년 성장하고 있습니다. 또한, 정부는 2012년부터 시행중인 공급의무화제도(RPS)를 통해 신재생에너지 확대를 도모하고 있습니다. 공급의무비율은 2012년 2.0%부터 점진적으로 상승하여 2023년 10%로 확대되며, 2021년에는 9.0%가 부과되고 있습니다. 공급의무자들은 RPS 이행을 위해 공급인증서(REC)를 확보해야하며, 신재생에너지원에 따라 REC 가중치는 상이합니다.
□ 경기변동의 특성
EPC사업은 일반 경제활동에 많은 영향을 받고 있기 때문에 거시경제지표들과 유기적인 관계를 맺고 있으며 산업구조 및 경제환경의 변화와 정부의 정책 등 복합적인 요인에 의하여 변동됩니다. 그 중 EPC사업은 특히, 정부자금에 대한 의존율이 높기 때문에 정부 정책 등에 따라 크게 영향을 받고 있습니다. 또한 파이낸싱 방식을 이용하기에 금융기관의 담보 및 보증 요구 등 정책변화에 따라 수익성 및 수주물량이 크게 좌우되고 있습니다.
□ 산업의 성장성
한국에너지공단에 따르면, 국내 신재생에너지 생산량은 2005년 이후 연평균 10%씩 증가하여 2017년 1,561만toe를 기록하였으며, 전체 1차 에너지 생산량의 5.2%를 차지하고 있습니다. 또한, 2017년 신재생에너지 발전량은 46,619GWh로 2005년 이후 연평균 23%씩 증가하였으며, 전체 발전량의 8.1%를 차지하고 있습니다. 2017년 국내 신재생에너지 설비용량은 15.7GW이며, 이중 태양광이 37%로 최대를 차지하고, 뒤를 이어 폐기물 24%, 바이오 15%, 수력 11%, 풍력 7%, 기타 5% 순으로 보급되어 있습니다. 2017년 한 해 동안 설치된 용량은 2.1GW이며, 이중 태양광(1.4GW)과 바이오(487MW)가 전체 설치량의 88%를 점유, 2017년 발전량으로는 폐기물이 51%로 절반이상을 차지하고 있으며, 바이오 16%, 태양광 15%, 수력 6%, 풍력 5%, 기타 7% 순입니다. 설비용량으로는 태양광이 5.8GW로 가장 많이 보급되었으며, 실제 발전량은 폐기물이 최대인 상황입니다..
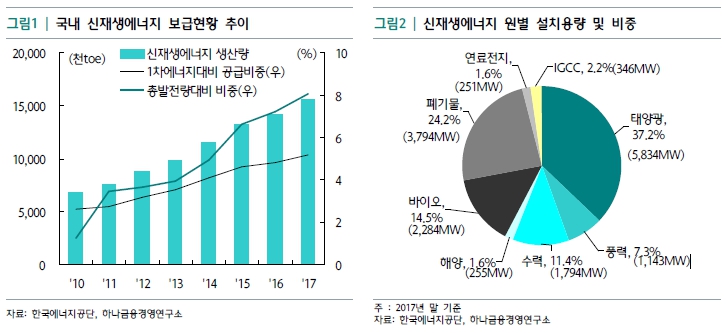 |
|
국내 신재생에너지 현황 |
정부는 전력계통의 안정성, 국내 보급여건, 재생에너지 잠재량 등을 고려하여 2030년까지 총 발전량의 20%를 신재생에너지로 달성하는 것을 목표로 설정하여, 2018~2030년간 정부재정 18조원을 포함 약 92조원을 투자하여 48.7GW의 신재생에너지 발전설비를 신규 건설할 계획입니다.
핵심 발전원을 현재 폐기물, 바이오에서 태양광, 풍력으로 변경해 나가고자 하며, 신규 설비의 63%인 30.8GW를 태양광으로, 34%인 16.5GW를 풍력으로 구성할 예정이며, 기간에 따라 단기(2018~2022) 12.4GW, 중장기(2023~2030) 36.3GW로 나누어 발전설비 구축할 예정입니다. 이를 위해 계획입지제도 등을 실시하여 대형 프로젝트를 지원하고, 농업진흥지역 외 농지, 염해간척지 등에 태양광을 보급하는 농가 태양광 사업을 확대하고 국민 수용성 확보를 위해 소규모 태양광 발전에 대해 한국형 FIT 제도를 실시하고 있습니다.
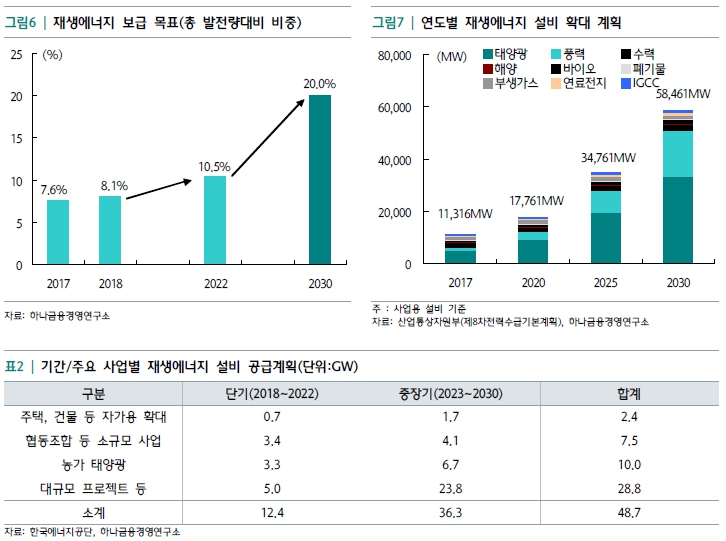 |
|
국내 신재생에너지 현황_2 |
② 회사의 경쟁우위 요소
당사는 전문적이고 다양한 실적으로 에너지 진단을 수행하며 EPC 투자사업에서 가장 까다로운 자금조달 단계에서도 다년간의 수행실적을 통해 검증된 업계 최고의 신속 정확한 서비스를 제공하고 있습니다.
III. 재무에 관한 사항
1. 요약재무정보
가. 에이치엘비생명과학 주식회사와 그종속기업
| (단위 : 천원) |
| 구 분 | 제27(당)분기 (2024년 1분기) |
제26(전)기 (2023년) |
제25(전전)기 (2022년) |
|---|---|---|---|
| [유동자산] | 229,728,203 | 147,043,191 | 160,775,696 |
| ㆍ현금및현금성자산 | 55,569,341 | 16,768,575 | 30,978,386 |
| ㆍ단기금융상품 | 12,991,000 | 10,100,000 | 11,801,548 |
| ㆍ당기손익-공정가치 측정 금융자산 | 92,041,018 | 50,793,156 | 88,661,009 |
| ㆍ매출채권 | 12,975,102 | 11,457,320 | 12,750,927 |
| ㆍ기타채권 | 2,491,406 | 4,379,886 | 3,998,261 |
| ㆍ재고자산 | 5,237,968 | 5,266,832 | 10,867,379 |
| ㆍ기타유동자산 | 48,354,021 | 48,277,422 | 619,254 |
| ㆍ당기법인세자산 | 68,347 | - | 1,098,932 |
| [비유동자산] | 399,825,466 | 276,457,256 | 251,014,675 |
| ㆍ장기금융상품 | 141,496 | 125,500 | 125,500 |
| ㆍ장기매출채권 | - | - | 143,546 |
| ㆍ장기기타채권 | 534,926 | 554,697 | 1,944,822 |
| ㆍ장기선급비용 | - | - | 163,294 |
| ㆍ당기손익-공정가치측정금융자산 | 224,701,420 | 108,477,905 | 3,185,071 |
| ㆍ기타포괄손익-공정가치측정금융자산 | 225,253 | 225,253 | 329,538 |
| ㆍ관계기업투자 | 41,322,754 | 37,209,275 | 41,108,621 |
| ㆍ유형자산 | 75,031,428 | 71,565,811 | 89,404,925 |
| ㆍ투자부동산 | 1,139,162 | 1,145,512 | 20,494,288 |
| ㆍ사용권자산 | 1,033,291 | 1,352,492 | 2,683,871 |
| ㆍ무형자산 | 55,695,736 | 55,800,811 | 91,431,199 |
| 자산총계 | 629,553,669 | 423,500,447 | 411,790,371 |
| [유동부채] | 144,795,739 | 135,456,990 | 26,784,511 |
| [비유동부채] | 51,915,165 | 56,830,524 | 148,939,211 |
| 부채총계 | 196,710,904 | 192,287,514 | 175,723,722 |
| [지배기업 소유주지분] | 432,134,156 | 230,796,723 | 234,724,951 |
| ㆍ자본금 | 54,273,709 | 51,406,913 | 48,831,044 |
| ㆍ기타불입자본 | 173,685,498 | 122,577,398 | 194,843,995 |
| ㆍ자본조정 | (8,297,174) | (8,297,174) | (5,644,345) |
| ㆍ기타자본구성요소 | 56,947,165 | 54,679,023 | 37,657,640 |
| ㆍ이익잉여금(결손금) | 155,524,958 | 10,430,563 | (40,963,383) |
| [비지배지분] | 708,609 | 416,210 | 1,341,698 |
| 자본총계 | 432,842,765 | 231,212,933 | 236,066,649 |
| 관계기업투자주식의 평가방법 | 지분법 | 지분법 | 지분법 |
| 기간 | (2024.01.01∼2024.03.31) | (2023.01.01∼2023.12.31) | (2022.01.01∼2022.12.31) |
| 매출액 | 23,894,368 | 97,990,441 | 99,591,376 |
| 영업이익(손실) | (5,646,641) | (24,532,796) | (20,161,282) |
| 당기순이익(손실) | 145,389,881 | (5,913,047) | (54,359,670) |
| ㆍ지배기업 소유주지분 | 145,097,449 | (5,983,400) | (54,277,435) |
| ㆍ비지배지분 | 292,432 | 70,353 | (82,235) |
| 당기총포괄이익(손실) | 147,655,004 | (5,831,638) | (54,169,450) |
| ㆍ지배기업 소유주지분 | 147,363,176 | (5,901,420) | (54,088,279) |
| ㆍ비지배지분 | 291,828 | 69,782 | (81,171) |
| ㆍ기본주당손익(손실)(단위:원) | 1,394 | (58) | (565) |
| ㆍ희석주당손익(손실)(단위:원) | 1,394 | (58) | (565) |
| 연결에 포함된 회사수 | 5 | 7 | 6 |
| 상기 연결재무정보는 한국채택국제회계기준(K-IFRS)에 따라 작성되었습니다. 한편, 연결실체는 제21기(2018년 1월 1일)부터 기업회계기준서 제1119호 '금융상품'과 제1115호 '고객과의 계약에서 생기는 수익'을 최초 적용하였습니다. |
나. 연결대상 종속기업 변동현황
| 사업연도 | 연결에 포함된 회사 | 연결에 추가된 회사 | 연결에서 제외된 회사 |
|---|---|---|---|
| 제27기 당분기 | 에이치엘비셀㈜ ㈜신화어드밴스 에이치엘비에너지㈜ 에이치엘비생명과학알앤디㈜ 에이치엘비솔루션㈜ |
에이치엘비솔루션㈜(*) | - |
| 제26기 | 에이치엘비셀㈜ ㈜신화어드밴스 에이치엘비엘이디㈜ 에이치엘비에너지㈜ 에이치엘비생명과학알앤디㈜ HLBI알밤제1호투자조합 ㈜화진메디칼(*1) |
㈜화진메디칼 | 에이치엘비엘이디㈜ HLBI알밤제1호투자조합 ㈜화진메디칼 |
| 제25기 | 에이치엘비셀㈜ ㈜신화어드밴스 에이치엘비엘이디㈜ 에이치엘비에너지㈜ 에이치엘비생명과학알앤디㈜ HLBI알밤제1호투자조합 |
에이치엘비생명과학알앤디㈜ HLBI알밤제1호투자조합 에임㈜ 에임텍㈜ |
의령태양광1호㈜ 에임㈜ 에임텍㈜ |
(*) 당분기 중 물적분할 완료하였습니다.
다. 에이치엘비생명과학 주식회사
| (단위 : 천원) |
| 구 분 | 제27(당)분기 (2024년 1분기) |
제26(전)기 (2023년) |
제25(전전)기 (2022년) |
|---|---|---|---|
| [유동자산] | 113,360,240 | 73,779,673 | 116,410,319 |
| ㆍ현금및현금성자산 | 40,363,246 | 5,956,212 | 22,093,002 |
| ㆍ단기금융상품 | 1,000 | 10,000 | 3,711,548 |
| ㆍ당기손익-공정가치 측정 금융자산 | 10,242,854 | 10,242,854 | 68,694,215 |
| ㆍ매출채권 | 5,748,107 | 5,187,922 | 6,991,581 |
| ㆍ기타채권 | 6,388,859 | 1,863,048 | 5,375,044 |
| ㆍ재고자산 | 2,385,041 | 2,305,275 | 8,072,794 |
| ㆍ기타유동자산 | 48,211,034 | 48,214,362 | 456,667 |
| ㆍ당기법인세자산 | 20,099 | - | 1,015,466 |
| [비유동자산] | 459,860,877 | 341,186,025 | 288,793,252 |
| ㆍ장기매출채권 | 0 | - | 143,546 |
| ㆍ장기기타채권 | 233,853 | 245,660 | 1,766,182 |
| ㆍ기타비유동자산 | 0 | - | 163,294 |
| ㆍ당기손익-공정가치측정금융자산 | 222,665,163 | 108,217,679 | 2,841,720 |
| ㆍ기타포괄손익-공정가치측정금융자산 | 200,002 | 200,002 | 304,288 |
| ㆍ종속기업 및 관계기업투자 | 146,969,703 | 142,169,703 | 125,902,600 |
| ㆍ유형자산 | 44,353,281 | 44,684,503 | 63,300,667 |
| ㆍ투자부동산 | 4,266,136 | 4,289,758 | 28,269,719 |
| ㆍ사용권자산 | 471,925 | 674,370 | 1,786,243 |
| ㆍ무형자산 | 40,700,814 | 40,704,350 | 64,314,993 |
| 자산총계 | 573,221,117 | 414,965,698 | 405,203,571 |
| [유동부채] | 137,599,979 | 131,084,884 | 22,078,492 |
| [비유동부채] | 44,329,039 | 50,468,336 | 142,896,790 |
| 부채총계 | 181,929,018 | 181,553,220 | 164,975,282 |
| ㆍ자본금 | 54,273,709 | 51,406,913 | 48,831,044 |
| ㆍ기타불입자본 | 173,685,498 | 122,577,398 | 194,843,995 |
| ㆍ자본조정 | (680,039) | (679,971) | (2,478,063) |
| ㆍ기타자본구성요소 | 45,452,765 | 45,452,766 | 28,066,414 |
| ㆍ이익잉여금(결손금) | 118,560,166 | 14,655,371 | (29,035,101) |
| 자본총계 | 391,292,099 | 233,412,478 | 240,228,289 |
| 종속 및 관계기업 투자주식의 평가방법 | 원가법 | 원가법 | 원가법 |
| 기간 | (2024.01.01∼2024.03.31) | (2023.01.01∼2023.12.31) | (2022.01.01∼2022.12.31) |
| 매출액 | 6,086,470 | 29,493,646 | 20,651,553 |
| 영업이익(손실) | (2,695,080) | (14,731,958) | (9,757,015) |
| 당기순이익(손실) | 103,904,795 | (13,809,528) | (57,603,820) |
| 총포괄손익(손실) | 103,904,795 | (13,809,528) | (57,574,311) |
| ㆍ기본주당손익(손실)(단위:원) | 996 | (136) | (600) |
| ㆍ희석주당손익(손실)(단위:원) | 996 | (136) | (600) |
| 상기 별도재무정보는 한국채택국제회계기준(K-IFRS)에 따라 작성되었습니다. 한편, 연결실체는 제21기(2018년 1월 1일)부터 기업회계기준서 제1119호 '금융상품'과 제1115호 '고객과의 계약에서 생기는 수익'을 최초 적용하였습니다. |
2. 연결재무제표
2-1. 연결 재무상태표
|
연결 재무상태표 |
|
제 27 기 1분기말 2024.03.31 현재 |
|
제 26 기말 2023.12.31 현재 |
|
(단위 : 원) |
|
제 27 기 1분기말 |
제 26 기말 |
|
|---|---|---|
|
자산 |
||
|
유동자산 |
229,728,203,591 |
147,043,191,219 |
|
현금및현금성자산 |
55,569,341,424 |
16,768,574,597 |
|
매출채권 |
12,975,102,428 |
11,457,319,700 |
|
공정가치측정금융자산 |
92,041,017,871 |
50,793,156,023 |
|
기타유동금융자산 |
15,482,405,791 |
14,479,885,678 |
|
재고자산 |
5,237,967,596 |
5,266,832,007 |
|
기타유동자산 |
771,198,174 |
694,600,107 |
|
당기법인세자산 |
68,347,200 |
0 |
|
매각예정비유동자산 |
47,582,823,107 |
47,582,823,107 |
|
비유동자산 |
399,825,465,850 |
276,457,256,338 |
|
장기매출채권 |
0 |
0 |
|
공정가치측정금융자산 |
224,926,672,282 |
108,703,158,021 |
|
기타비유동금융자산 |
676,422,400 |
680,197,154 |
|
기타비유동자산 |
0 |
0 |
|
종속기업및관계기업투자주식 |
41,322,753,940 |
37,209,274,627 |
|
유형자산 |
75,031,428,386 |
71,565,810,967 |
|
투자부동산 |
1,139,162,069 |
1,145,512,376 |
|
무형자산 |
55,695,735,965 |
55,800,811,262 |
|
사용권자산 |
1,033,290,808 |
1,352,491,931 |
|
자산총계 |
629,553,669,441 |
423,500,447,557 |
|
부채 |
||
|
유동부채 |
144,795,738,539 |
135,456,989,572 |
|
매입채무 |
6,199,116,409 |
5,160,179,449 |
|
리스부채 |
763,569,805 |
922,333,520 |
|
단기차입금 |
29,885,926,464 |
10,220,000,000 |
|
유동성장기차입금 |
13,420,000,000 |
7,060,000,000 |
|
기타유동금융부채 |
3,448,195,141 |
4,860,497,679 |
|
유동성사채 |
81,008,586,931 |
96,541,148,375 |
|
기타유동부채 |
2,241,984,879 |
3,108,393,766 |
|
충당부채 |
28,278,830 |
29,846,753 |
|
당기법인세부채 |
7,800,080,080 |
7,554,590,030 |
|
비유동부채 |
51,915,165,569 |
56,830,523,697 |
|
파생상품부채 |
23,822,228 |
33,229,382 |
|
리스부채 |
271,357,781 |
424,014,817 |
|
장기차입금 |
16,300,000,000 |
21,555,000,000 |
|
사채 |
30,948,429,659 |
29,855,004,141 |
|
기타비유동금융부채 |
1,026,427,333 |
1,002,982,596 |
|
비유동충당부채 |
0 |
0 |
|
순확정급여부채 |
369,214,656 |
615,572,286 |
|
이연법인세부채 |
2,975,913,912 |
3,344,720,475 |
|
부채총계 |
196,710,904,108 |
192,287,513,269 |
|
자본 |
||
|
지배기업 소유주지분 |
432,134,155,738 |
230,796,723,443 |
|
자본금 |
54,273,709,000 |
51,406,912,500 |
|
주식발행초과금 |
173,685,497,651 |
122,577,398,479 |
|
기타자본구성요소 |
36,585,921,241 |
36,585,989,927 |
|
기타포괄손익누계액 |
12,064,069,731 |
9,795,859,404 |
|
이익잉여금(결손금) |
155,524,958,115 |
10,430,563,133 |
|
비지배지분 |
708,609,595 |
416,210,845 |
|
자본총계 |
432,842,765,333 |
231,212,934,288 |
|
자본과부채총계 |
629,553,669,441 |
423,500,447,557 |
2-2. 연결 포괄손익계산서
|
연결 포괄손익계산서 |
|
제 27 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
제 26 기 1분기 2023.01.01 부터 2023.03.31 까지 |
|
(단위 : 원) |
|
제 27 기 1분기 |
제 26 기 1분기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
매출액 |
23,894,368,063 |
23,894,368,063 |
31,166,194,280 |
31,166,194,280 |
|
매출원가 |
23,640,827,860 |
23,640,827,860 |
28,898,206,824 |
28,898,206,824 |
|
매출총이익 |
253,540,203 |
253,540,203 |
2,267,987,456 |
2,267,987,456 |
|
판매비와관리비 |
5,900,181,335 |
5,900,181,335 |
5,090,333,378 |
5,090,333,378 |
|
영업이익(손실) |
(5,646,641,132) |
(5,646,641,132) |
(2,822,345,922) |
(2,822,345,922) |
|
금융수익 |
155,198,444,980 |
155,198,444,980 |
20,249,366,901 |
20,249,366,901 |
|
금융원가 |
5,839,008,096 |
5,839,008,096 |
4,919,990,806 |
4,919,990,806 |
|
기타수익 |
2,136,801,732 |
2,136,801,732 |
143,662,829 |
143,662,829 |
|
기타비용 |
23,850,634 |
23,850,634 |
156,075,542 |
156,075,542 |
|
지분법손익 |
(820,037,650) |
(820,037,650) |
182,194,182 |
182,194,182 |
|
법인세비용차감전순이익(손실) |
145,005,709,200 |
145,005,709,200 |
12,676,811,642 |
12,676,811,642 |
|
법인세비용(수익) |
384,171,771 |
384,171,771 |
1,011,192,788 |
1,011,192,788 |
|
연결당기순이익(손실) |
145,389,880,971 |
145,389,880,971 |
13,688,004,430 |
13,688,004,430 |
|
순이익(손실)귀속 |
||||
|
지배기업의 소유주지분 |
145,097,449,387 |
145,097,449,387 |
13,659,258,741 |
13,659,258,741 |
|
비지배주주지분 |
292,431,584 |
292,431,584 |
28,745,689 |
28,745,689 |
|
기타포괄손익 |
2,265,123,088 |
2,265,123,088 |
(87,114,556) |
(87,114,556) |
|
후속적으로 당기손익으로 재분류되지 않는 항목 |
(3,054,405) |
(3,054,405) |
1,823,080 |
1,823,080 |
|
확정급여제도의 재측정요소 |
1,823,080 |
1,823,080 |
||
|
지분법이익잉여금변동 |
(3,054,405) |
(3,054,405) |
||
|
기타포괄손익-공정가치측정자산 평가손익 |
0 |
|||
|
기타포괄손익-공정가치측정자산 처분손익 |
0 |
|||
|
후속적으로 당기손익으로 재분류되는 항목 |
2,268,177,493 |
2,268,177,493 |
(88,937,636) |
(88,937,636) |
|
지분법자본변동 |
2,268,177,493 |
2,268,177,493 |
(88,937,636) |
(88,937,636) |
|
당기총포괄손익 |
147,655,004,059 |
147,655,004,059 |
13,600,889,874 |
13,600,889,874 |
|
총 포괄손익의 귀속 |
||||
|
지배기업 소유주지분 |
147,363,176,119 |
147,363,176,119 |
13,572,072,257 |
13,572,072,257 |
|
비지배주주지분 |
291,827,940 |
291,827,940 |
28,817,617 |
28,817,617 |
|
주당이익 |
||||
|
기본주당이익(손실) (단위 : 원) |
1,394 |
1,394 |
142 |
142 |
|
희석주당이익(손실) (단위 : 원) |
1,394 |
1,394 |
142 |
142 |
2-3. 연결 자본변동표
|
연결 자본변동표 |
|
제 27 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
제 26 기 1분기 2023.01.01 부터 2023.03.31 까지 |
|
(단위 : 원) |
|
자본 |
||||||||
|---|---|---|---|---|---|---|---|---|
|
지배기업소유주지분 |
비지배지분 |
자본 합계 |
||||||
|
자본금 |
주식발행초과금 |
기타자본구성요소 |
기타포괄손익누계액 |
이익잉여금(결손금) |
지배기업소유주지분 합계 |
|||
|
2023.01.01 (기초자본) |
48,831,044,000 |
181,375,478,936 |
35,890,585,001 |
9,591,225,414 |
(40,963,382,699) |
234,724,950,652 |
1,341,698,215 |
236,066,648,867 |
|
결손금 보전 |
0 |
(60,000,000,000) |
60,000,000,000 |
|||||
|
총포괄손익 |
||||||||
|
연결당기순이익(손실) |
0 |
0 |
0 |
0 |
13,659,258,741 |
13,659,258,741 |
28,745,689 |
13,688,004,430 |
|
확정급여제도의 재측정요소 |
0 |
0 |
0 |
0 |
1,823,080 |
1,823,080 |
0 |
1,823,080 |
|
지분법자본변동 |
0 |
0 |
0 |
(88,937,636) |
0 |
(88,937,636) |
71,928 |
(88,865,708) |
|
지분법이익잉여금변동 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
총포괄손익 합계 |
0 |
0 |
0 |
(88,937,636) |
13,661,081,821 |
13,572,144,185 |
28,817,617 |
13,600,961,802 |
|
자본에 직접 인식된 주주와의 거래 |
||||||||
|
주식배당 |
0 |
0 |
2,500,000,000 |
0 |
(2,500,000,000) |
0 |
0 |
0 |
|
전환사채의 전환 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
신주인수권부사채의 전환 |
10,911,000 |
175,718,085 |
0 |
0 |
0 |
186,629,085 |
0 |
186,629,085 |
|
2023.03.31 (기말자본) |
48,841,955,000 |
121,551,197,021 |
38,390,585,001 |
9,502,287,778 |
30,197,699,122 |
248,483,723,922 |
1,370,515,832 |
249,854,239,754 |
|
2024.01.01 (기초자본) |
51,406,912,500 |
122,577,398,479 |
36,585,989,927 |
9,795,859,404 |
10,430,563,133 |
230,796,723,443 |
416,210,845 |
231,212,934,288 |
|
결손금 보전 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
총포괄손익 |
||||||||
|
연결당기순이익(손실) |
0 |
0 |
0 |
0 |
145,097,449,387 |
145,097,449,387 |
292,431,584 |
145,389,880,971 |
|
확정급여제도의 재측정요소 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
지분법자본변동 |
0 |
0 |
0 |
2,268,210,327 |
0 |
2,268,210,327 |
(32,834) |
2,268,177,493 |
|
지분법이익잉여금변동 |
0 |
0 |
0 |
0 |
(3,054,405) |
(3,054,405) |
0 |
(3,054,405) |
|
총포괄손익 합계 |
0 |
0 |
0 |
2,268,210,327 |
145,094,394,982 |
147,362,605,309 |
292,398,750 |
147,655,004,059 |
|
자본에 직접 인식된 주주와의 거래 |
||||||||
|
주식배당 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
전환사채의 전환 |
708,410,500 |
14,970,500,059 |
(68,686) |
0 |
0 |
15,678,841,873 |
0 |
15,678,841,873 |
|
신주인수권부사채의 전환 |
2,158,386,000 |
36,137,599,113 |
0 |
0 |
0 |
38,295,985,113 |
0 |
38,295,985,113 |
|
2024.03.31 (기말자본) |
54,273,709,000 |
173,685,497,651 |
36,585,921,241 |
12,064,069,731 |
155,524,958,115 |
432,134,155,738 |
708,609,595 |
432,842,765,333 |
2-4. 연결 현금흐름표
|
연결 현금흐름표 |
|
제 27 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
제 26 기 1분기 2023.01.01 부터 2023.03.31 까지 |
|
(단위 : 원) |
|
제 27 기 1분기 |
제 26 기 1분기 |
|
|---|---|---|
|
영업활동으로 인한 현금흐름 |
(5,465,334,085) |
3,549,152,688 |
|
영업으로부터 창출된 현금흐름 |
(5,315,125,016) |
2,778,415,388 |
|
이자의 수취 |
240,757,451 |
290,201,450 |
|
이자의 지급 |
(452,929,230) |
(445,947,572) |
|
배당금수령 |
0 |
0 |
|
법인세 환급(납부) |
61,962,710 |
926,483,422 |
|
투자활동으로 인한 현금흐름 |
(14,540,077,757) |
(4,265,325,543) |
|
당기손익-공정가치 측정 금융자산의 취득 |
(5,214,715,069) |
(2,023,816,301) |
|
당기손익-공정가치 측정 금융자산의 처분 |
2,440,789,010 |
10,002,599 |
|
상각후원가 측정 금융자산의 취득 |
0 |
0 |
|
상각후원가 측정 금융자산의 처분 |
0 |
0 |
|
기타포괄손익-공정가치측정금융자산의 처분 |
0 |
0 |
|
기타유동금융자산의 증가 |
(8,051,222,000) |
(3,267,924,890) |
|
기타유동금융자산의 감소 |
1,858,792,000 |
4,294,264,529 |
|
기타비유동금융자산의 증가 |
0 |
0 |
|
기타비유동금융자산의 감소 |
7,580,000 |
0 |
|
종속기업 및 관계기업투자의 취득 |
600,000,000 |
0 |
|
종속기업 및 관계기업투자의 처분 |
0 |
0 |
|
유형자산의 취득 |
(4,514,398,858) |
(3,400,972,244) |
|
유형자산의 처분 |
14,909,250 |
39,420,000 |
|
투자부동산의 취득 |
0 |
0 |
|
투자부동산의 처분 |
0 |
0 |
|
무형자산의 취득 |
(32,741,968) |
(121,626,483) |
|
무형자산의 처분 |
0 |
140,000,000 |
|
매각예정비유동자산의 처분 |
0 |
0 |
|
사업분할 |
(449,070,122) |
0 |
|
종속기업 취득에 따른 순현금흐름 |
0 |
0 |
|
종속기업 처분에 따른 순현금흐름 |
0 |
0 |
|
금융리스채권의 감소 |
0 |
65,327,247 |
|
재무활동으로 인한 현금흐름 |
58,803,599,459 |
111,193,294 |
|
단기차입금의 증가 |
24,600,000,000 |
650,000,000 |
|
단기차입금의 감소 |
0 |
0 |
|
장기차입금의 증가 |
1,230,000,000 |
0 |
|
장기차입금의 감소 |
(125,000,000) |
(3,050,000) |
|
정부보조금의 수취 |
0 |
0 |
|
전환사채의 발행 |
0 |
0 |
|
전환사채의 청구 |
0 |
0 |
|
주식선택권행사로 인한 현금유입 |
0 |
0 |
|
신주인수권부사채의 발행 |
0 |
(15,382,720) |
|
신주인수권부사채의 청구 |
34,551,569,459 |
6,821,621 |
|
리스부채의 감소 |
(256,314,544) |
(527,195,607) |
|
유상증자 |
(1,211,586,770) |
0 |
|
자기주식의 취득 |
(68,686) |
0 |
|
임대보증금의 증가 |
15,000,000 |
0 |
|
현금및현금성자산의 증가(감소) |
38,798,187,617 |
(604,979,561) |
|
기초현금및현금성자산 |
16,768,574,597 |
30,978,386,499 |
|
현금및현금성자산의 환율변동효과 |
2,579,210 |
115,246 |
|
당기말현금및현금성자산 |
55,569,341,424 |
30,373,522,184 |
3. 연결재무제표 주석
1. 일반사항
기업회계기준서 제1110호 '연결재무제표'에 의한 지배회사인 에이치엘비생명과학 주식회사(이하 "지배기업")와 5개의 종속기업(이하 지배기업과 그 종속기업을 일괄하여 "연결실체")의 일반적인 사항은 다음과 같습니다.
1.1 지배기업의 개요
지배기업은 1998년 7월 24일에 에너지 절약 관련 엔지니어링 서비스업을 위한 진단,설계, 시공 등을 목적으로 설립되어, 에너지절약 사업, 태양광발전소 건설 및 의료기기사업 등을 영위하고 있습니다. 지배기업은 2008년에 보통주를 한국거래소가 개설하는 코스닥시장에 상장하였습니다.
지배기업의 납입자본금은 54,274백만원이며, 당분기말 현재 최대 주주는 에이치엘비 주식회사(지분율 : 18.3%)입니다.
1.2 종속기업 현황
<당분기말>
| (단위: 천원, 주) |
| 회사명 | 업종 | 자본금 | 보유주식수 | 지분율(%) | 소재지 | 결산일 |
|---|---|---|---|---|---|---|
| ㈜신화어드밴스 | 도매업 | 1,522,730 | 304,546 | 100 | 대한민국 | 12월 31일 |
| 에이치엘비셀㈜ | 제조업 | 17,233,691 | 34,227,742 | 99.3 | 대한민국 | 12월 31일 |
| 에이치엘비에너지㈜ | 제조업 | 2,302,099 | 2,302,099 | 100 | 대한민국 | 12월 31일 |
| 에이치엘비생명과학R&D㈜ | 서비스 | 13,000,000 | 26,000,000 | 100 | 대한민국 | 12월 31일 |
| 에이치엘비솔루션㈜ | 제조업 | 200,000 | 40,000 | 100 | 대한민국 | 12월 31일 |
<전기말>
| (단위: 천원, 주) |
| 회사명 | 업종 | 자본금 | 보유주식수 | 지분율(%) | 소재지 | 결산일 |
|---|---|---|---|---|---|---|
| ㈜신화어드밴스 | 도매업 | 1,522,730 | 304,546 | 100 | 대한민국 | 12월 31일 |
| 에이치엘비셀㈜ | 서비스업 | 17,233,691 | 34,227,742 | 99.3 | 대한민국 | 12월 31일 |
| 에이치엘비에너지㈜ | 제조업 | 2,302,099 | 2,302,099 | 100 | 대한민국 | 12월 31일 |
| 에이치엘비생명과학R&D㈜ | 서비스 | 10,000,000 | 20,000,000 | 100 | 대한민국 | 12월 31일 |
1.3 종속기업 관련 주요 재무정보 요약
<당분기말 및 당분기>
| (단위: 천원) |
| 회사명 | 당분기말 | 당분기 | ||||
|---|---|---|---|---|---|---|
| 자산 | 부채 | 자본 | 매출액 | 분기순손익 | 총포괄손익 | |
| ㈜신화어드밴스 | 25,620,174 | 3,083,201 | 22,536,974 | 16,848,632 | (85,785) | (85,785) |
| 에이치엘비셀㈜ | 91,453,495 | 743,992 | 90,709,503 | 247,085 | 42,058,886 | 42,054,163 |
| 에이치엘비에너지㈜ | 30,522,589 | 10,420,222 | 20,102,367 | 998,755 | 7,403 | 7,403 |
| 에이치엘비생명과학R&D㈜ | 5,178,382 | 612,682 | 4,565,699 | 119,851 | (1,409,600) | (1,409,600) |
| 에이치엘비솔루션㈜ | 3,586,749 | 2,438,009 | 1,148,740 | - | (51,260) | (51,260) |
<전분기말 및 전분기>
| (단위: 천원) |
| 회사명 | 전분기말 | 전분기 | ||||
|---|---|---|---|---|---|---|
| 자산 | 부채 | 자본 | 매출액 | 분기순손익 | 총포괄손익 | |
| ㈜신화어드밴스 | 25,905,138 | 3,230,217 | 22,674,921 | 14,821,839 | (168,550) | (168,550) |
| 에이치엘비셀㈜ | 42,929,015 | 10,267,260 | 32,661,755 | 524,165 | 4,923,368 | 4,923,368 |
| 에이치엘비엘이디㈜ | - | - | - | - | 1,152,456 | 1,152,456 |
| 에이치엘비에너지㈜ | 16,946,506 | 6,633,129 | 10,313,377 | 838,114 | (415,706) | (415,706) |
| 에이치엘비생명과학R&D㈜ | 3,357,030 | 651,595 | 2,705,435 | 41,556 | (818,354) | (816,531) |
| HLBI 알밤 제1호 투자조합 | 1,972,265 | - | 1,972,265 | - | (11,833) | (11,833) |
당분기 및 전분기 종속기업의 요약 재무현황은 내부거래가 제거되지 않은 재무현황입니다.
1.4. 연결대상범위의 변동
| 구분 | 기업명 | 사유 |
|---|---|---|
| 신규연결 | 에이치엘비솔루션㈜ | 물적분할 |
2. 중요한 회계정책
2.1 재무제표 작성기준
연결회사의 2024년 3월 31일로 종료하는 3개월 보고기간에 대한 요약분기연결재무제표는 기업회계기준서 제1034호 '중간재무보고'에 따라 작성되었습니다. 이 중간재무제표는 연차재무제표에 기재되는 사항이 모두 포함되지 않았으므로 전기말 연차재무제표와 함께 이해해야 합니다.
2.1.1 연결회사가 채택한 제ㆍ개정 기준서 및 해석서
연결회사는 2024년 1월 1일로 개시하는 회계기간부터 다음의 제ㆍ개정 기준서 및 해석서를 신규로 적용하였습니다.
(1) 기업회계기준서 제1001호 '재무제표 표시' 개정 - 부채의 유동/비유동 분류, 약정사항이 있는 비유동부채
보고기간말 현재 존재하는 실질적인 권리에 따라 유동 또는 비유동으로 분류되며, 부채의 결제를 연기할 수 있는 권리의 행사가능성이나 경영진의 기대는 고려하지 않습 니다. 또한, 부채의 결제에 자기지분상품의 이전도 포함되나, 복합금융상품에서 자기지분상품으로 결제하는 옵션이 지분상품의 정의를 충족하여 부채와 분리하여 인식된경우는 제외됩니다. 또한, 기업이 보고기간말 후에 준수해야하는 약정은 보고기간말에 해당 부채의 분류에 영향을 미치지 않으며, 보고기간 이후 12개월 이내 약정사항을 준수해야하는 부채가 보고기간말 현재 비유동부채로 분류된 경우 보고기간 이후 12개월 이내 부채가 상환될 수 있는 위험에 관한 정보를 공시해야 합니다. 해당 기준서의 개정이 재무제표에 미치는 중요한 영향은 없습니다.
(2) 기업회계기준서 제1007호 '현금흐름표', 기업회계기준서 제1107호 '금융상품: 공시' 개정 - 공급자금융약정에 대한 정보 공시
공급자금융약정을 적용하는 경우, 재무제표이용자가 공급자금융약정이 기업의 부채와 현금흐름 그리고 유동성위험 익스포저에 미치는 영향을 평가할 수 있도록 공급자금융약정에 대한 정보를 공시해야 합니다. 이 개정내용을 최초로 적용하는 회계연도 내 중간보고기간에는 해당 내용을 공시할 필요가 없다는 경과규정에 따라 중간재무제표에 미치는 영향이 없습니다.
(3) 기업회계기준서 제1116호 ‘리스’ 개정 - 판매후리스에서 생기는 리스부채
판매후리스에서 생기는 리스부채를 후속적으로 측정할 때 판매자-리스이용자가 보유하는 사용권 관련 손익을 인식하지 않는 방식으로 리스료나 수정리스료를 산정합니다. 해당 기준서의 제정이 재무제표에 미치는 중요한 영향은 없습니다.
(4) 기업회계기준서 제1001호 ‘재무제표 표시’ 개정 - '가상자산 공시’
가상자산을 보유하는 경우, 가상자산을 고객을 대신하여 보유하는 경우, 가상자산을 발행한 경우의 추가 공시사항을 규정하고 있습니다. 해당 기준서의 개정이 재무제표에 미치는 중요한 영향은 없습니다.
2.1.2 연결회사가 적용하지 않은 제ㆍ개정 기준서 및 해석서
제정 또는 공표되었으나 시행일이 도래하지 않아 적용하지 아니한 제ㆍ개정 기준서 및 해석서는 다음과 같습니다.
(1) 기업회계기준서 제1021호 ‘환율변동효과’와 기업회계기준서 제1101호 ‘한국채택국제회계기준의 최초채택’ 개정 - 교환가능성 결여
통화의 교환가능성을 평가하고 다른 통화와 교환이 가능하지 않다면 현물환율을 추정하며 관련 정보를 공시하도록 하고 있습니다. 동 개정사항은 2025 년 1 월 1 일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 해당 기준서의 개정이 재무제표에 미치는 중요한 영향은 없습니다.
2.2 법인세비용
중간기간의 법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균연간법인세율, 즉 추정평균연간유효법인세율을 중간기간의 세전이익에 적용하여 계산합니다.
3. 중요한 회계추정 및 가정
연결회사는 미래에 대하여 추정 및 가정을 하고 있습니다. 추정 및 가정은 지속적으로 평가되며, 과거 경험과 현재의 상황에서 합리적으로 예측가능한 미래의 사건과 같은 다른 요소들을 고려하여 이루어집니다. 이러한 회계추정은 실제 결과와 다를 수도있습니다.
요약분기재무제표 작성시 사용된 중요한 회계추정 및 가정은 법인세비용을 결정하는데 사용된 추정의 방법을 제외하고는 전기 연결재무제표 작성시 적용된 회계추정 및 가정과 동일합니다.
4. 공정가치
당분기 중 연결회사의 금융자산과 금융부채의 공정가치에 영향을 미치는 사업환경 및 경제적인 환경의 유의적인 변동은 없습니다.
4.1 금융상품 종류별 공정가치
연결회사의 금융상품 중 상각후원가로 측정하는 금융자산 및 금융부채는 장부금액과공정가치의 차이가 유의적이지 않으며, 기타 금융상품은 장부금액과 공정가치가 일치합니다.
4.2 공정가치 서열체계
공정가치로 계상되거나 공시되는 모든 금융상품은 다음의 세 가지 공정가치 서열체계 수준으로 분류됩니다.
| - | 활성시장의 (조정되지 않은)공시가격을 이용하여 측정한 공정가치 (수준 1) |
| - | 직접적으로 또는 간접적으로 관측가능한 투입변수를 이용하여 측정한 공정가치 (수준 2) |
| - | 관측가능하지 않은 투입변수를 이용하여 측정한 공정가치 (수준3) |
공정가치로 측정되는 금융상품의 공정가치 서열체계 구분
<당분기말>
| (단위: 천원) |
| 구 분 | 수준1 | 수준2 | 수준3 | 합 계 |
|---|---|---|---|---|
| 금융자산 | ||||
| 당기손익-공정가치 측정 금융자산 | ||||
| 지분증권 | 297,992,550 | - | 104,285 | 298,096,835 |
| 채무증권 | - | - | - | - |
| 복합금융상품 | - | - | 14,642,854 | 14,642,854 |
| 출자금 | - | - | 3,630,915 | 3,630,915 |
| 저축성보험 | - | 371,833 | - | 371,833 |
| 기타포괄손익-공정가치 측정 금융자산 | ||||
| 지분증권 | - | - | 225,253 | 225,253 |
| 금융부채 | ||||
| 당기손익-공정가치 측정 금융부채 | ||||
| 파생상품부채 | - | 23,822 | - | 23,822 |
<전기말>
| (단위: 천원) |
| 구 분 | 수준1 | 수준2 | 수준3 | 합 계 |
|---|---|---|---|---|
| 금융자산 | ||||
| 당기손익-공정가치 측정 금융자산 | ||||
| 지분증권 | 143,387,678 | - | 104,285 | 143,491,963 |
| 채무증권 | - | 1,512,161 | - | 1,512,161 |
| 복합금융상품 | - | - | 10,242,854 | 10,242,854 |
| 출자금 | - | - | 3,668,384 | 3,668,384 |
| 저축성보험 | - | 355,699 | - | 355,699 |
| 기타포괄손익-공정가치 측정 금융자산 | ||||
| 지분증권 | - | - | 225,253 | 225,253 |
| 금융부채 | ||||
| 당기손익-공정가치 측정 금융부채 | ||||
| 파생상품부채 | - | 33,229 | - | 33,229 |
4.3 반복적인 공정가치 측정치의 서열체계 수준간 이동
연결회사는 공정가치 서열체계의 수준 간 이동을 보고기간말에 인식합니다.
4.4 반복적인 측정치의 수준3의 변동 내역
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 기초 | 14,240,775 | 21,439,090 |
| 취득 | 5,200,000 | 23,817 |
| 평가 | 78,540 | 147,039 |
| 처분 | (916,009) | (10,003) |
| 기말 | 18,603,306 | 21,599,943 |
4.5 가치평가기법 및 투입변수
<당분기말>
| (단위: 천원) |
| 구 분 | 공정가치 | 가치평가기법 | 수준 | 투입변수 | 투입변수 범위 |
|---|---|---|---|---|---|
| HLB바이오스텝㈜ 제1회 무기명식 무보증 전환사채 | 10,242,854 | 이항모형 | 3 | 위험할인율 | 7.94% ~ 12.82% |
| 주 변동성 | 5.16% | ||||
| 무위험할인율 | 3.16% ~ 3.39% | ||||
| 기계설비건설공제조합 | 4,368 | 순자산가치평가법 | 3 | - | - |
| 엔지니어링공제조합 | 1,693,701 | 순자산가치평가법 | 3 | - | - |
| 전기공사공제조합 | 71,259 | 순자산가치평가법 | 3 | - | - |
| HLBI 알밤 제1호 투자조합 | 1,800,000 | 순자산가치평가법 | 3 | - | - |
| 백년약속 | 80,240 | 순자산가치평가법 | 3 | - | - |
| 참다운창조교육 | 24,045 | 순자산가치평가법 | 3 | - | - |
| 에이치벨류에셋 | 4,400,000 | 순자산가치평가법 | 3 | - | - |
| 매일방송 | 200,003 | 순자산가치평가법 | 3 | - | - |
| 저축성보험 | 371,833 | 순자산가치평가법 | 2 | - | - |
| ㈜차케어스 | 25,250 | 순자산가치평가법 | 3 | - | - |
| 한국자원순환에너지공제조합 | 61,588 | 순자산가치평가법 | 3 | - | - |
<전기말>
| (단위: 천원) |
| 구분 | 공정가치 | 가치평가기법 | 수준 | 투입변수 | 투입변수 범위 |
|---|---|---|---|---|---|
| HLB바이오스텝㈜ 제1회 무기명식 무보증 전환사채 |
10,242,854 | 이항모형 | 수준 3 | 위험할인율 | 7.94% ~ 12.82% |
| 주 변동성 | 5.16% | ||||
| 무위험할인율 | 3.16% ~ 3.39% | ||||
| HLBI 알밤 제1호 투자조합 | 1,000,000 | 순자산가치평가법 | 수준 3 | - | - |
| 엔지니어링공제조합 | 1,615,293 | 순자산가치평가법 | 수준 3 | - | - |
| 기계설비건설공제조합 | 920,245 | 순자산가치평가법 | 수준 3 | - | - |
| 전기공사공제조합 | 71,259 | 순자산가치평가법 | 수준 3 | - | - |
| 매일방송 | 200,003 | 순자산가치평가법 | 수준 3 | - | - |
| 백년약속 | 80,240 | 순자산가치평가법 | 수준 3 | - | - |
| 참다운창조교육 | 24,045 | 순자산가치평가법 | 수준 3 | - | - |
| ㈜차케어스 | 25,250 | 순자산가치평가법 | 수준 3 | - | - |
| 한국자원순환에너지공제조합 | 61,588 | 순자산가치평가법 | 수준 3 | - | - |
| 삼성스마트MMF법인제1호_C | 1,512,161 | 현재가치법 | 수준 2 | - | - |
| 저축성보험 | 355,699 | 순자산가치평가법 | 수준 2 | - | - |
4.6 수준 3으로 분류된 공정가치 측정치의 가치평가과정
연결회사의 재무부서는 재무보고 목적의 공정가치의 측정을 담당하고 있으며 이러한공정가치 측정치는 수준 3으로 분류되는 공정가치 측정치를 포함하고 있습니다. 연결회사의 재무부서는 공정가치 측정내역 및 결과에 대하여 당사의 경영진에게 매 분기 보고하고 있습니다.
4.7 수준 3으로 분류된 반복적인 공정가치 측정치의 민감도 분석
금융상품의 민감도 분석은 통계적 기법을 이용한 관측 불가능한 투입변수의 변동에따른 금융상품의 가치 변동에 기초하여 유리한 변동과 불리한 변동으로 구분하여 이루어집니다. 그리고 공정가치가 두 개 이상의 투입변수에 영향을 받는 경우에는 가장유리하거나 또는 가장 불리한 금액을 바탕으로 산출됩니다. 민감도 분석대상으로 수준3으로 분류되는 금융상품 중 해당 공정가치 변동이 당기손익으로 인식되는 파생상품이 있고, 공정가치 변동이 당기손익 혹은 기타포괄손익으로 인식되는 지분상품과 채무상품 등이 있습니다.
5. 공정가치 측정 금융자산
5.1 공정가치 측정 금융자산의 내역
| (단위: 천원) |
| 구분 | 당분기말 | 전기말 |
|---|---|---|
| 당기손익-공정가치 측정 금융자산 | ||
| 시장성 있는 지분증권 | 297,992,550 | 143,387,678 |
| 시장성 없는 지분증권 | 104,285 | 104,285 |
| 복합금융상품 | 14,642,854 | 10,242,854 |
| 채무증권 | - | 1,512,161 |
| 출자금 | 3,630,915 | 3,668,384 |
| 저축성보험 | 371,833 | 355,699 |
| 소계 | 316,742,437 | 159,271,061 |
| 기타포괄손익-공정가치 측정 금융자산 | ||
| 시장성 없는 지분증권 | 225,253 | 225,253 |
| 합계 | 316,967,690 | 159,496,314 |
5.2 당기손익-공정가치 측정 금융자산의 내역
| (단위: 천원) |
| 구분 | 종목 | 당분기말 | 전기말 |
|---|---|---|---|
| 시장성 있는 지분증권 |
HLB | 282,125,150 | 135,967,159 |
| HLB이노베이션 | 12,946,053 | 6,473,027 | |
| HLB테라퓨틱스 | 2,921,348 | 947,493 | |
| 시장성 없는 지분증권 |
백년약속 | 80,240 | 80,240 |
| 참다운창조교육 | 24,045 | 24,045 | |
| 출자금 | 엔지니어링공제조합 | 1,693,701 | 1,615,293 |
| 기계설비건설공제조합 | 4,368 | 920,245 | |
| 전기공사공제조합 | 71,259 | 71,259 | |
| HLBI 알밤 제1호 투자조합 | 1,800,000 | 1,000,000 | |
| 한국자원순환에너지공제조합 | 61,588 | 61,588 | |
| 복합금융상품 | HLB바이오스텝 | 10,242,854 | 10,242,854 |
| 에이치벨류에셋 | 4,400,000 | - | |
| 채무증권 | 삼성스마트MMF법인제1호 | - | 1,512,161 |
| 저축성보험 | 삼성생명보험 | 205,341 | 198,639 |
| 메리츠화재해상보험 | 166,492 | 157,060 | |
| 합계 | 316,742,439 | 159,271,063 | |
5.3 당기손익-공정가치 측정 금융자산의 변동 내역
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 기초 | 159,271,062 | 21,109,552 |
| 취득 | 5,214,715 | 23,817 |
| 평가손익 | 154,684,831 | 147,039 |
| 처분 | (2,428,170) | (10,003) |
| 기말 | 316,742,438 | 21,270,405 |
6. 기타금융자산
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 | ||
|---|---|---|---|---|
| 유동 | 비유동 | 유동 | 비유동 | |
| 금융기관예치금(*1) | 12,991,000 | 141,496 | 10,100,000 | 125,500 |
| 대여금 | 92,080 | 629,242 | 892,080 | 630,742 |
| 손실충당금 | (80,880) | (505,804) | (80,880) | (505,804) |
| 미수금 | 2,838,067 | 62,400 | 3,136,866 | 62,400 |
| 손실충당금 | (956,492) | (62,400) | (956,492) | (62,400) |
| 미수수익 | 272,327 | - | 190,358 | - |
| 임차보증금 | 342,758 | 483,871 | 1,222,793 | 514,736 |
| 현재가치할인차금 | (16,454) | (72,482) | (24,839) | (85,077) |
| 기타보증금 | - | 100 | - | 100 |
| 합 계 | 15,482,406 | 676,423 | 14,479,886 | 680,197 |
| (*1) 단기금융상품 중 100억은 엔에이치투자증권㈜의 사기적 부정거래 행위 및 불완전판매로 인하여 부당이득금 반환 청구 소송중인 상품으로 당사는 단기금융상품 전액에 대해서 대손충당금을 설정하고 있으며, 당사의 등기임원은 본 사건과 관련하여 발생가능한 손실을 보전하기위하여 당사의 등기임원이 보유한 에이치엘비(주)의 주식을법무법인에 위탁하는 계약을 체결하였습니다. |
보고기간말 현재 전액 대손을 설정한 금융자산 외 기타금융자산은 신용위험이 유의적으로 증가하지 않아 손실충당금은 12개월 기대신용손실로 인식하였습니다.
7. 재고자산
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|
| 취득원가 | 평가손실충당금 | 장부금액 | 취득원가 | 평가손실충당금 | 장부금액 | |
| 상품 | 3,168,578 | (70,628) | 3,097,950 | 3,317,088 | (91,374) | 3,225,714 |
| 원재료 | 1,164,828 | (287,696) | 877,132 | 1,986,174 | (894,716) | 1,091,458 |
| 재공품 | 599,555 | (222,693) | 376,862 | 391,359 | (252,947) | 138,411 |
| 제품 | 1,379,269 | (493,246) | 886,023 | 1,099,357 | (288,109) | 811,248 |
| 합 계 | 6,312,230 | (1,074,263) | 5,237,967 | 6,793,978 | (1,527,146) | 5,266,831 |
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 매출원가: | ||
| 재고자산평가손실(환입) | (452,883) | 514,593 |
| 비용으로 인식된 재고자산 원가 | 18,578,094 | 19,603,907 |
8. 관계기업투자
8.1 관계기업투자주식의 상세내역
| (단위: 천원) |
| 회사명 | 소재지 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|---|
| 지분율(%) | 취득원가 | 장부금액 | 지분율(%) | 취득원가 | 장부금액 | ||
| 관계기업투자 | |||||||
| 에이치엘비제약㈜ | 대한민국 | 13.61 | 29,559,250 | 31,639,872 | 14.26 | 29,559,250 | 27,990,911 |
| ㈜엘에스케이인베스트먼트 | 대한민국 | 38 | 1,900,000 | 3,326,333 | 38 | 1,900,000 | 3,267,111 |
| 에이치엘비사이언스㈜ | 대한민국 | 20.51 | 6,000,092 | 5,798,548 | 20.62 | 6,000,092 | 5,951,252 |
| ㈜에이치밸류에셋(*1) | 대한민국 | 20 | 600,000 | 558,002 | - | - | - |
| ㈜두산포천에너지 | 대한민국 | - | - | - | 20 | 40,000 | - |
| 합 계 | - | 38,059,342 | 41,322,755 | - | 37,499,342 | 37,209,274 | |
| (*1) 당분기 중 취득하였습니다. |
8.2 관계기업투자의 변동 내역
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 기초 순장부금액 | 37,209,275 | 41,108,621 |
| 취득 | 600,000 | - |
| 손익 중 지분 | (820,038) | 182,194 |
| 기타포괄손익 중 지분 | 2,268,177 | (88,866) |
| 기타 | 2,065,339 | 63,210 |
| 분기말 순장부금액 | 41,322,753 | 41,265,159 |
9. 유형자산
9.1 유형자산의 내역
| (단위: 천원) |
| 구분 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|
| 원가 | 상각누계액(주1) | 장부금액 | 원가 | 상각누계액(주1) | 장부금액 | |
| 토지 | 21,471,089 | - | 21,471,089 | 21,471,089 | - | 21,471,089 |
| 건물 | 22,534,071 | (1,988,607) | 20,545,464 | 22,534,071 | (1,844,038) | 20,690,032 |
| 구축물 | 686,733 | (188,567) | 498,166 | 686,733 | (183,038) | 503,695 |
| 차량운반구 | 737,001 | (492,680) | 244,321 | 755,771 | (484,456) | 271,315 |
| 공구와기구 | 3,631,466 | (1,920,032) | 1,711,434 | 3,561,616 | (1,784,597) | 1,777,019 |
| 비품 | 1,914,397 | (1,261,338) | 653,059 | 1,899,233 | (1,189,138) | 710,095 |
| 기계장치 | 33,328,217 | (18,252,271) | 15,075,946 | 33,002,745 | (17,704,303) | 15,298,442 |
| 시설장치 | 5,507,667 | (3,294,747) | 2,212,920 | 5,486,467 | (3,114,783) | 2,371,684 |
| 건설중인자산 | 12,619,032 | - | 12,619,032 | 8,472,439 | - | 8,472,439 |
| 합계 | 102,429,673 | (27,398,242) | 75,031,431 | 97,870,164 | (26,304,353) | 71,565,810 |
(주1) 손상차손누계액을 합산한 금액입니다.
9.2 유형자산의 변동 내역
<당분기>
| (단위: 천원) |
| 구분 | 기초 | 취득 및 자본적 지출 |
처분 및 폐기 | 감가상각비 | 손상차손 | 대체 | 연결범위변동 | 기말 |
|---|---|---|---|---|---|---|---|---|
| 토지 | 21,471,089 | - | - | - | - | - | - | 21,471,089 |
| 건물 | 20,690,032 | - | - | (144,568) | - | - | - | 20,545,464 |
| 구축물 | 503,695 | - | - | (5,529) | - | - | - | 498,166 |
| 차량운반구 | 271,315 | 3,730 | (1) | (30,723) | - | - | - | 244,321 |
| 공구와기구 | 1,777,018 | 69,850 | - | (135,434) | - | - | - | 1,711,434 |
| 비품 | 710,095 | 15,164 | - | (72,200) | - | - | - | 653,059 |
| 기계장치 | 15,298,443 | 119,620 | (17,871) | (554,746) | - | 230,500 | - | 15,075,946 |
| 시설장치 | 2,371,684 | 21,200 | - | (179,964) | - | - | - | 2,212,920 |
| 건설중인자산 | 8,472,439 | 4,377,093 | - | - | - | (230,500) | - | 12,619,032 |
| 합계 | 71,565,810 | 4,606,657 | (17,872) | (1,123,164) | - | - | - | 75,031,431 |
<전분기>
| (단위: 천원) |
| 구분 | 기초 | 취득 및 자본적 지출 |
처분 및 폐기 | 감가상각비 | 손상차손 | 대체 | 연결범위변동 | 기말 |
|---|---|---|---|---|---|---|---|---|
| 토지 | 29,579,761 | - | - | - | - | - | - | 29,579,761 |
| 건물 | 18,623,823 | 34,170 | - | (129,846) | - | 688,000 | - | 19,216,147 |
| 구축물 | 448,067 | - | - | (3,054) | - | - | - | 445,013 |
| 차량운반구 | 199,585 | 98,345 | (1) | (25,032) | - | - | - | 272,897 |
| 공구와기구 | 1,815,704 | - | - | (116,035) | - | - | - | 1,699,669 |
| 비품 | 941,151 | 19,399 | (20,742) | (72,209) | - | - | - | 867,599 |
| 기계장치 | 16,168,715 | 21,807 | (690,560) | (538,806) | 660,560 | - | - | 15,621,716 |
| 시설장치 | 2,986,626 | 25,000 | (41,383) | (163,498) | - | - | - | 2,806,745 |
| 임차점포시설물 | 251,459 | - | - | (58,029) | - | - | - | 193,430 |
| 건설중인자산 | 18,390,035 | 4,715,278 | - | - | - | (688,000) | - | 22,417,313 |
| 합계 | 89,404,926 | 4,913,999 | (752,686) | (1,106,509) | 660,560 | - | - | 93,120,290 |
9.3 당분기말 현재 유형자산 중 일부가 관련 부채에 대한 담보로 제공되어 있습니다(주석 19 참조).
9.4 당분기 중 차입원가를 자본화하여 건설중인자산으로 계상한 금액은 34,148천원(전분기: 121,856천원)입니다.
10. 사용권자산 및 리스부채
10.1 사용권자산 및 리스부채의 변동내역
<당분기>
| (단위: 천원) |
| 구분 | 사용권자산 | 리스부채 | ||
|---|---|---|---|---|
| 건물 | 기타 | 합계 | ||
| 기초 | 86,072 | 1,266,420 | 1,352,492 | 1,346,348 |
| 취득 | - | 144,214 | 144,214 | 135,024 |
| 감가상각 | (65,752) | (188,311) | (254,063) | - |
| 리스부채의 상환 | - | - | - | (273,110) |
| 이자비용 | - | - | - | 30,833 |
| 리스변경 및 계약종료 등 | (95,548) | (113,804) | (209,352) | (204,168) |
| 기말 | (75,228) | 1,108,519 | 1,033,291 | 1,034,927 |
<전분기>
| (단위: 천원) |
| 구분 | 사용권자산 | 리스부채 | ||
|---|---|---|---|---|
| 건물 | 기타 | 합계 | ||
| 기초 | 1,316,809 | 1,367,062 | 2,683,871 | 2,977,307 |
| 취득 | 100,866 | 235,445 | 336,311 | 303,385 |
| 감가상각 | 36,830 | (459,778) | (422,948) | - |
| 리스부채의 상환 | - | - | - | (594,920) |
| 이자비용 | - | - | - | 67,724 |
| 리스변경 및 계약종료 등 | (144,466) | (329) | (144,795) | (139,661) |
| 기말 | 1,310,039 | 1,142,400 | 2,452,439 | 2,613,835 |
10.2 손익계산서에 인식된 금액
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 사용권자산상각비 | 254,063 | 422,948 |
| 리스료 - 단기 리스 | 76,910 | 103,960 |
| 리스료 - 소액 기초자산 리스 | 13,433 | 27,289 |
| 금융리스해지이익 | 13,335 | 6,006 |
| 금융리스해지손실 | 3,610 | - |
| 리스부채 이자비용 | 30,833 | 88,239 |
10.3 리스로 인한 현금유출액
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 리스부채의 지급 | 273,110 | 594,920 |
| 리스료 - 단기 리스 | 76,910 | 103,960 |
| 리스료 - 소액 기초자산 리스 | 13,433 | 27,289 |
| 합계 | 363,453 | 726,169 |
11. 무형자산
11.1 무형자산의 내역
| (단위: 천원) |
| 구분 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|
| 원가 | 상각누계액(주1) | 장부금액 | 원가 | 상각누계액(주1) | 장부금액 | |
| 영업권 | 24,239,334 | (22,467,221) | 1,772,113 | 24,239,334 | (22,467,221) | 1,772,113 |
| 고객관계 | 3,708,850 | (1,608,576) | 2,100,274 | 5,059,277 | (2,858,991) | 2,200,287 |
| 회원권 | 2,214,237 | (9,985) | 2,204,252 | 2,214,237 | (9,986) | 2,204,252 |
| 소프트웨어 | 213,518 | (76,406) | 137,112 | 152,799 | (8,471) | 144,328 |
| 특허권 | 221,332 | (53,381) | 167,951 | 191,590 | (49,860) | 141,731 |
| 상표권 | 22,533 | (7,023) | 15,510 | 22,533 | (5,896) | 16,637 |
| 라이선스 | 35,057,161 | 1 | 35,057,162 | 34,979,691 | - | 34,979,691 |
| 디자인권 | 5,268 | (2,729) | 2,539 | 5,268 | (2,465) | 2,802 |
| 허가권 | 2,002,046 | (1,935,311) | 66,735 | 2,002,046 | (1,835,209) | 166,837 |
| 개발비 | 288,939 | (288,939) | - | 312,922 | (312,922) | - |
| 기술가치 | 37,033,686 | (22,861,598) | 14,172,088 | 37,033,686 | (22,861,599) | 14,172,088 |
| 기타의무형자산 | 14,614 | (14,612) | 2 | 14,614 | (14,567) | 47 |
| 합계 | 105,021,518 | (49,325,780) | 55,695,738 | 106,227,996 | (50,427,185) | 55,800,811 |
(주1) 손상차손누계액을 합산한 금액입니다.
11.2 무형자산 변동 내역
<당분기>
| (단위: 천원) |
| 구분 | 기초 | 취득 및 자본적 지출 |
처분 및 폐기 | 감가상각비 | 손상차손 | 대체 | 연결범위변동 | 기말 |
|---|---|---|---|---|---|---|---|---|
| 영업권 | 1,772,113 | - | - | - | - | - | - | 1,772,113 |
| 고객관계 | 2,200,287 | - | - | (100,013) | - | - | - | 2,100,274 |
| 회원권 | 2,204,252 | - | - | - | - | - | - | 2,204,252 |
| 소프트웨어 | 144,328 | 3,000 | - | (10,216) | - | - | - | 137,112 |
| 특허권 | 141,731 | 29,742 | - | (3,522) | - | - | - | 167,951 |
| 상표권 | 16,637 | - | - | (1,127) | - | - | - | 15,510 |
| 라이선스 | 34,979,691 | 77,471 | - | - | - | - | - | 35,057,162 |
| 디자인권 | 2,802 | - | - | (263) | - | - | - | 2,539 |
| 허가권 | 166,837 | - | - | (100,102) | - | - | - | 66,735 |
| 기술가치 | 14,172,088 | - | - | - | - | - | - | 14,172,088 |
| 기타의무형자산 | 47 | - | - | (45) | - | - | - | 2 |
| 합계 | 55,800,813 | 110,213 | - | (215,288) | - | - | - | 55,695,738 |
<전분기>
| (단위: 천원) |
| 구분 | 기초 | 취득 및 자본적 지출 |
처분 및 폐기 | 감가상각비 | 손상차손 | 대체 | 연결범위변동 | 기말 |
|---|---|---|---|---|---|---|---|---|
| 영업권 | 21,924,795 | - | - | - | - | - | - | 21,924,795 |
| 고객관계 | 7,324,461 | - | - | (281,710) | - | - | - | 7,042,751 |
| 회원권 | 2,857,252 | - | - | - | - | - | - | 2,857,252 |
| 소프트웨어 | 84,865 | - | - | (5,091) | - | - | - | 79,774 |
| 특허권 | 26,699 | 1,129 | - | (2,785) | - | - | - | 25,043 |
| 상표권 | 10,352 | 2,316 | - | (682) | - | - | - | 11,986 |
| 라이선스 | 34,693,787 | - | - | - | - | - | - | 34,693,787 |
| 디자인권 | - | - | - | (263) | - | - | - | (263) |
| 허가권 | 567,246 | - | - | (100,102) | - | - | - | 467,144 |
| 개발비 | - | - | - | - | - | - | - | - |
| 기술가치 | 23,903,075 | - | - | - | - | - | - | 23,903,075 |
| 기타의무형자산 | 38,667 | 118,182 | - | (8,152) | - | - | - | 148,697 |
| 합계 | 91,431,199 | 121,627 | - | (398,785) | - | - | - | 91,154,041 |
12. 투자부동산
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 기초 순장부금액 | 1,145,512 | 20,494,288 |
| 감가상각비 | (6,350) | (33,839) |
| 분기말금액 | 1,139,162 | 20,460,449 |
당분기말 현재 회사의 일부 투자부동산은 차입금에 대하여 담보로 제공되어 있습니다(주석 19.1 참조).
13. 차입부채
13.1 차입부채의 내역
| (단위: 천원) |
| 구 분 | 당분기말 | 전기말 | ||
|---|---|---|---|---|
| 유동 | 비유동 | 유동 | 비유동 | |
| 단기차입금 | 29,885,926 | - | 10,220,000 | - |
| 장기차입금 | 13,420,000 | 16,300,000 | 7,060,000 | 21,555,000 |
| 전환사채 | - | 30,948,430 | 15,158,535 | 29,855,004 |
| 신주인수권부사채 | 81,008,587 | - | 81,382,614 | |
| 합 계 | 124,314,513 | 47,248,430 | 113,821,149 | 51,410,004 |
13.2 단기차입금의 상세 내역
| (단위: 천원) |
| 구분 | 차입처 | 이자율(%) | 만기일 | 당분기말 | 전기말 |
|---|---|---|---|---|---|
| 시설자금 | 우리은행 | 5.96 | 2025-03-20 | 1,150,000 | 1,150,000 |
| 시설자금 | 국민은행 | 5.14 | 2024-08-16 | 5,000,000 | 5,000,000 |
| 시설자금 | 국민은행 | 5.14 | 2024-08-20 | 4,070,000 | 4,070,000 |
| 주식담보대출 | 한국투자증권 | 4.5 | 2025-01-30 | 20,000,000 | - |
| 소 계 | 30,220,000 | 10,220,000 | |||
| 차감 : 현재가치할인차금 | (334,074) | - | |||
| 차감잔액 | 29,885,926 | 10,220,000 | |||
13.3 장기차입금의 상세 내역
| (단위: 천원) |
| 구분 | 차입처 | 이자율(%) | 만기일 | 당분기말 | 전기말 |
|---|---|---|---|---|---|
| 시설자금 | 국민은행 | 4.98 | 2025-01-16 | 1,560,000 | 1,560,000 |
| 시설자금 | 우리은행 | 5.36 | 2025-03-31 | 4,800,000 | 4,800,000 |
| 온렌딩대출 | 하나은행 | 4.96 | 2030-03-15 | 3,000,000 | 3,125,000 |
| 시설자금 | 산업은행 | 4.21 | 2032-01-17 | 10,000,000 | 10,000,000 |
| 시설자금 | 국민은행 | 4.83 | 2024-08-20 | 5,000,000 | 5,000,000 |
| 시설자금 | 국민은행 | 3.8 | 2024-09-30 | 1,560,000 | 1,560,000 |
| 시설자금대출 | 기업은행 | 4.545 | 2028-09-30 | 50,000 | 50,000 |
| 시설자금대출 | 기업은행 | 2.32 | 2033-09-30 | 3,750,000 | 2,520,000 |
| 소 계 | 29,720,000 | 28,615,000 | |||
| 차감 : 유동성대체 | (13,420,000) | (7,060,000) | |||
| 차감잔액 | 16,300,000 | 21,555,000 | |||
13.4 전환사채의 상세 내역
| (단위: 천원) |
| 차입내용 | 발행일 | 만기일 | 이자율(%) | 당분기말 | 전기말 |
|---|---|---|---|---|---|
| 제10회 무기명식 무보증 사모 전환사채 | 2022-07-01 | 2027-07-01 | - | - | 16,200,000 |
| 제11회 무기명식 무보증 사모 전환사채 | 2023-07-07 | 2028-07-07 | - | 8,300,000 | 8,300,000 |
| 제12회 무기명식 무보증 사모 전환사채 | 2023-11-07 | 2026-11-07 | 2 | 28,800,000 | 28,800,000 |
| 상환할증금 | 167,461 | 494,312 | |||
| 전환권조정 | (6,319,031) | (8,780,773) | |||
| 사채잔액 | 30,948,430 | 45,013,539 | |||
| 차감 : 유동성대체 | - | (15,158,535) | |||
| 차감잔액 | 30,948,430 | 29,855,004 | |||
13.5 전환사채의 주요 발행조건
| 구 분 | 내 용 |
|---|---|
| 사채의 명칭 | 제10회 무기명식 무보증 사모 전환사채 |
| 권면총액 | 16,200,000,000 원 |
| 발행회사 | 에이치엘비생명과학㈜ |
| 발행가액 | 권면금액의 100% |
| 만기일 | 2027-07-01 |
| 보장수익률 | 1.00% |
| 유효이자율 | 17.41% |
| 원금상환방법(주1) | 만기일시상환 - 사채만기일에 미행사 사채권면총액에 대하여는 원금의 105.1206%의 금액을 일시상환함 |
| 조기상환청구(Put Option) | 발행일로부터 2년 경과 및 그 이후 3개월마다 조기상환청구가 가능함 |
| 매도청구권 (Call Option) (주2) | 발행회사 또는 제3자가 사채에 관하여 콜옵션 보유 |
| 전환가액 | 11,434원 |
| 전환가능 주식수(주3) | 0주 |
| 행사(전환)에 따라 발행할 주식의 종류 | 에이치엘비생명과학㈜ 기명식 보통주 |
| 행사(전환청구)기간 | 2023년 07월 01일부터 2027년 06월 01일까지 |
| 신주의 배당기산일 | 행사일이 속하는 사업연도의 개시일 |
| (주1) 회사는 제10회차 전환사채의 전환사채금 450억원의 일부인 288억원을 조기 상환함에 따라 조기 상환된 288억원 전액을 대환하여 제12회차 전환사채의 인수대금으로 납입을 결정하였습니다. |
| (주2) 회사는 전기 중 회사 또는 회사가 지정하는 제3자에게 매도청구권(Call Option)을 부여하는 조건의 제10회 무기명식 무보증 사모 전환사채를 발행하였습니다. 회사는 동 전환사채 발행시 매도청구권을 특수관계자인 에포케㈜에게 부여하였으며, 동 매도청구권과 관련하여 발행시 매도청구권의 공정가치 2,309,652천원을 파생상품거래손실로 인식하였습니다. |
| (주3) 당분기말 모두 전환되었습니다. |
| 구 분 | 내 용 |
|---|---|
| 사채의 명칭 | 제11회 무기명식 무보증 사모 전환사채 |
| 권면총액 | 8,300,000,000 원 |
| 발행회사 | 에이치엘비생명과학㈜ |
| 발행가액 | 권면금액의 100% |
| 만기일 | 2028-07-07 |
| 보장수익률 | 1.00% |
| 유효이자율 | 16.72% |
| 원금상환방법 | 만기일시상환 - 사채만기일에 미행사 사채권면총액에 대하여는 원금의 105.1206%의 금액을 일시상환함 |
| 조기상환청구(Put Option) | 발행일로부터 2년 경과 및 그 이후 3개월마다 조기상환청구가 가능함 |
| 전환가액 | 10,204원 |
| 전환가능 주식수 | 813,406주 |
| 행사(전환)에 따라 발행할 주식의 종류 | 에이치엘비생명과학㈜ 기명식 보통주 |
| 행사(전환청구)기간 | 2024년 07월 07일부터 2028년 06월 07일까지 |
| 신주의 배당기산일 | 행사일이 속하는 사업연도의 개시일 |
| 구분 | 내용 |
|---|---|
| 사채의 명칭 | 제12회 무기명식 무보증 사모 전환사채 |
| 권면총액 | 28,800,000,000 원 |
| 발행회사 | 에이치엘비생명과학㈜ |
| 발행가액 | 권면금액의 100% |
| 만기일 | 2026-11-07 |
| 보장수익률 | 2.00% |
| 유효이자율 | 16.40% |
| 원금상환방법 | 만기일시상환 - 사채만기일에 미행사 사채권면총액에 대하여는 원금의 100%의 금액을 일시상환함 |
| 조기상환청구 (Put Option) | 발행일로부터 1년 8개월 경과 및 그 이후 3개월마다 조기상환청구가 가능함 |
| 전환가액 | 9,586원 |
| 조정 후 전환가능주식수 | 3,004,381주 |
| 행사(전환)에 따라 발행할 주식의 종류 | 에이치엘비생명과학㈜ 기명식 보통주 |
| 행사(전환청구)기간 | 2024년 11월 07일부터 2026년 10월 07일까지 |
| 신주의 배당기산일 | 행사일이 속하는 사업연도의 개시일 |
13.6 신주인수권부사채 상세 내역
| (단위: 천원) |
| 구 분 | 발행일 | 만기일 | 이자율(%) | 당분기말 | 전기말 |
|---|---|---|---|---|---|
| 제9회 무기명식 이권부 무보증 공모 분리형 신주인수권부사채 |
2022-06-15 | 2025-06-15 | - | 80,600,569 | 84,420,786 |
| 상환할증금 | (2,872,990) | 3,436,517 | |||
| 신주인수권조정 | 3,281,007 | (6,474,690) | |||
| 사채잔액 | 81,008,586 | 81,382,614 | |||
| 차감 : 유동성대체 | (81,008,586) | (81,382,614) | |||
| 차감잔액 | - | - | |||
13.7 신주인수권부사채의 주요 발행조건
| 구 분 | 내 용 |
|---|---|
| 사채의 명칭 | 제9회 무기명식 이권부 무보증 공모 분리형 신주인수권부사채 |
| 권면총액 | 100,000,000,000 원 |
| 발행회사 | 에이치엘비생명과학㈜ |
| 발행가액 | 권면금액의 100% |
| 만기일 | 2025-06-15 |
| 보장수익률 | 2.00% |
| 유효이자율 | 16.89% |
| 원금상환방법 | 만기일시상환 - 사채만기일에 미행사 사채권면총액에 대하여는 원금의 106.1677%의 금액을 일시상환함 |
| 조기상환청구(Put Option) | 발행일로부터 2년 경과 및 그 이후 3개월마다 조기상환청구가 가능함 |
| 행사가액(*1) | 8,889원 |
| 행사가능 주식수(*1) | 3,813,744 주 |
| 행사(전환)에 따라 발행할 주식의 종류 | 에이치엘비생명과학㈜ 기명식 보통주 |
| 행사(전환청구)기간 | 2022년 07월 15일부터 2025년 05월 15일까지 |
| 신주의 배당기산일 | 행사일이 속하는 사업연도의 개시일 |
| (*1) 보고서 작성일 현재 행사가액은 10,209원에서 8,889원으로 변경되었습니다. |
14. 자본금 및 주식발행초과금
14.1 자본금의 내역
| (단위: 원, 주) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 회사가 발행할 주식의 총 수 | 300,000,000 | 300,000,000 |
| 1주당 금액 | 500 | 500 |
| 발행한 주식의 수 | ||
| 보통주 | 107,560,274 | 101,826,681 |
| 보통주자본금 | 54,273,709,000 | 51,406,912,500 |
14.2 납입자본금의 변동내역
| (단위: 천원, 주) |
| 구 분 | 유통주식수 | 자본금 | 주식발행초과금 |
|---|---|---|---|
| 전기초 | 96,714,952 | 48,831,044 | 181,375,479 |
| 이익잉여금 전입 | - | - | (60,000,000) |
| 신주인수권부사채 전환 | 5,021,822 | 10,911 | 175,718 |
| 전분기말 | 101,736,774 | 48,841,955 | 121,551,197 |
| 당기초 | 101,826,681 | 51,406,913 | 122,577,398 |
| 전환사채 전환 | 1,416,821 | 708,411 | 14,970,500 |
| 신주인수권부사채 전환 | 4,316,772 | 2,158,386 | 36,137,599 |
| 당분기말 | 107,560,274 | 54,273,710 | 173,685,497 |
전기 이전 상환청구된 947,136주의 상환전환우선주를 상환 후 이익소각함에 따라 총발행주식수의 액면총액이 보통주자본금과 일치하지 않습니다.
15. 고객과의 계약에서 생기는 수익
15.1 수익으로 인식한 금액
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 고객과의 계약에서 생기는 수익 | 23,632,393 | 31,160,210 |
| 기타 원천으로부터의 수익 : 임대 수익 | 261,975 | 5,984 |
| 합 계 | 23,894,368 | 31,166,194 |
15.2 고객과의 계약에서 생기는 수익의 구분
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 고객과의 계약에서 생기는 수익 | ||
| 건설업 및 엔지니어링 | - | 54,000 |
| 상품 및 제품매출 | 22,508,794 | 30,133,261 |
| 용역매출 | 998,755 | 855,779 |
| 기타매출 | 124,844 | 117,170 |
| 합 계 | 23,632,393 | 31,160,210 |
| 지리적시장 | ||
| 국내 | 23,538,987 | 31,120,094 |
| 국외 | 93,406 | 40,116 |
| 합 계 | 23,632,393 | 31,160,210 |
| 수익인식 시기 | ||
| 한 시점에 인식 | 23,632,393 | 31,106,210 |
| 기간에 걸쳐 인식 | - | 54,000 |
| 합 계 | 23,632,393 | 31,160,210 |
16. 비용의 성격별 분류
16.1 비용(매출원가 및 판매비와 관리비)의 성격별 분류
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 재고자산의 변동 | 28,864 | 3,165,970 |
| 원재료 및 상품매입액 | 18,549,230 | 16,437,937 |
| 종업원급여 | 4,375,151 | 3,608,852 |
| 감가상각비 및 무형자산상각비 | 1,598,868 | 1,962,082 |
| 지급수수료 | 1,707,547 | 1,486,031 |
| 기타 | 3,281,349 | 7,327,668 |
| 합 계 | 29,541,009 | 33,988,540 |
16.2 종업원 급여 비용
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 급여 | 3,613,357 | 2,845,969 |
| 퇴직급여 | 195,329 | 344,089 |
| 복리후생비 | 566,465 | 418,794 |
| 합 계 | 4,375,151 | 3,608,852 |
17. 판매비와관리비
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 임직원급여 | 1,969,938 | 1,693,664 |
| 퇴직급여 | 228,825 | 210,727 |
| 복리후생비 | 302,334 | 230,839 |
| 여비교통비 | 83,608 | 43,913 |
| 접대비 | 151,993 | 160,204 |
| 통신비 | 8,621 | 8,027 |
| 세금과공과금 | 96,011 | 21,233 |
| 감가상각비 | 382,297 | 270,043 |
| 지급임차료 | 119,291 | 3,433 |
| 보험료 | 37,603 | 41,147 |
| 차량유지비 | 36,303 | 44,838 |
| 교육훈련비 | 10,474 | 3,039 |
| 도서인쇄비 | 3,287 | 3,164 |
| 협회비 | 6,300 | 7,877 |
| 소모품비 | 28,505 | 29,341 |
| 지급수수료 | 906,666 | 1,049,977 |
| 광고선전비 | 22,157 | 29,372 |
| 건물관리비 | 79,310 | 33,392 |
| 무형자산상각비 | 114,711 | 298,209 |
| 전력비 | 264 | - |
| 수선비 | 41 | - |
| 운반비 | 121,704 | 91,600 |
| 대손상각비(환입) | 6,009 | (73,234) |
| 경상연구개발비 | 1,183,931 | 889,528 |
| 합 계 | 5,900,183 | 5,090,333 |
18. 법인세비용
법인세비용은 당분기 중 발생한 이연법인세 미인식효과 등을 제외하였을 때 전체 회계연도에 대해서 예상되는 최선의 가중평균 연간 유효 법인세율의 추정에 기초하여 인식하였습니다.
19. 우발사항 및 약정사항
19.1 금융기관과 체결하고 있는 약정사항
| (단위: 천원) |
| 금융기관명 | 차입종별 | 당분기말 | 전기말 | ||
|---|---|---|---|---|---|
| 약정금액 | 실행금액 | 약정금액 | 실행금액 | ||
| 하나은행 | 기업시설자금대출 | 3,500,000 | 3,000,000 | 3,500,000 | 3,125,000 |
| 국민은행 | 시설자금 대출 | 17,190,000 | 17,190,000 | 17,190,000 | 17,190,000 |
| 우리은행 | 기업운전일반자금대출 | 1,150,000 | 1,150,000 | 1,150,000 | 1,150,000 |
| 우리은행 | 시설자금 대출 | 4,800,000 | 4,800,000 | 4,800,000 | 4,800,000 |
| 산업은행 | 시설자금 대출 | 10,000,000 | 10,000,000 | 10,000,000 | 10,000,000 |
| 한국투자증권 | 주식담보대출 | 20,000,000 | 20,000,000 | - | - |
| 우리은행 | 원화지급보증 | 6,040,000 | 5,680,000 | 3,040,000 | 2,200,000 |
| 기업은행 | 원화지급보증 | 4,000,000 | 2,980,000 | 4,000,000 | 3,450,000 |
| 기업은행 | 중소기업 시설자금 (ESG) |
4,000,000 | 50,000 | 4,000,000 | 50,000 |
| 기업은행 | 오염방지자금 (환경정책) |
10,000,000 | 3,750,000 | 10,000,000 | 2,520,000 |
| 기업은행 | 시설설치자금 (환경정책) |
10,000,000 | - | - | - |
| 합계 | 90,680,000 | 68,600,000 | 57,680,000 | 44,485,000 | |
19.2 담보제공내역
| (단위: 천원) |
| 구분 | 장부가액 | 담보설정액 | 관련계정 | 관련금액 | 제공처 |
|---|---|---|---|---|---|
| 토지 및 건물 | 4,768,018 | 4,200,000 | 차입금 | 3,000,000 | 하나은행 |
| 토지 및 건물 | 15,560,511 | 10,884,000 | 차입금 | 9,070,000 | 국민은행 |
| 토지 및 건물 | 24,285,155 | 9,744,000 | 차입금 | 8,120,000 | 국민은행 |
| 토지 및 건물 | 955,260 | 3,222,000 | 차입금 | 1,150,000 | 우리은행 |
| 토지 및 건물 | 11,609,857 | 5,760,000 | 차입금 | 4,800,000 | 우리은행 |
| 토지 및 건물 | 14,360,238 | 12,000,000 | 차입금 | 10,000,000 | 산업은행 |
| 정기예금 | 6,040,000 | 6,303,158 | 기타금융자산 | 6,040,000 | 우리은행 |
| 정기예금 | 3,900,000 | 4,290,000 | 기타금융자산 | 3,900,000 | 기업은행 |
| 정기예금 | 120,000 | 120,000 | 기타금융자산 | 120,000 | 서울보증보험 |
| 토지 | 8,324,397 | 22,800,000 | 장기차입금 | 3,800,000 | 기업은행 |
| 건물 | 589,226 | 장기차입금 | 기업은행 | ||
| 구축물 | 432,795 | 장기차입금 | 기업은행 | ||
| 기계장치 | 3,662,359 | 장기차입금 | 기업은행 | ||
| 주식 | 203,414,825 | 20,000,000 | 차입금 | 20,000,000 | 한국투자증권 |
| 합 계 | 298,022,641 | 99,323,158 | 70,000,000 |
19.3 전기 중 에이치엘비에너지㈜의 소각로 증축과 관련하여 기업은행으로부터 차입한 차입금에 대한 60억원 후순위 담보제공과 48억원 지급보증을 제공하였습니다.
19.4 계류중인 중요한 소송사건
(1) 회사가 피고인 사건
| (단위: 천원) |
| 원고 | 계류 법원 | 소송 금액 | 소송 내용 | 진행 상황 |
|---|---|---|---|---|
| 현대로오텍 | 광주지방법원 | 1,458,874 | 공사대금 청구 | 소송절차로 이행 |
| 주원전력 | 전주지방법원 | 883,872 | 공사대금 청구 | 소송절차로 이행 |
(2) 회사가 원고인 사건
| (단위: 천원) |
| 피고 | 계류 법원 | 소송 금액 | 소송 내용 | 진행 상황 |
|---|---|---|---|---|
| 엔에이치투자증권㈜(주1) | 서울남부지방법원 | 10,000,000 | 부당이득금반환청구 | 1심 진행중 |
| 박승규 (탑스코리아)(주2) | 수원지방법원 | 55,000 | 명도소송 | 판결선고 |
(주1) 회사가 펀드투자를 위해 엔에이치투자증권㈜에 최초 예치한 금액이나. 사기적 부정거래행위 및 불완전판매 요소가 발견되어 부당이득금 반환 청구소송을 진행 중입니다. 회사의 등기임원은 본 사건과관련하여 발생가능한 손실을 보전하기 위하여 회사의 등기임원이 보유한 에이치엘비㈜의 주식을 법무법인에 위탁하는 계약을 체결하였습니다.
(주2) 회사는 본 사건의 판결에 대해 2024년 1월 18일자로 승소하여 판결 확정되었습니다.
※ 기존 당사 원고, 피고 엘케이쏠라테크 공사대금 청구관련 소송 진행 중 이였으나, 2024년 1월 1일 당사 에너지사업부 회사분할하여 종속회사인 HLB솔루션으로 관련 소송 승계되어 소송 진행중입니다. 해당 사건은 현재 공사대금 채권 가압류 이의 신청 심문종결 후 소송비용액확정 사건으로 2024년 3월 18일에 일부인용 결정 되었습니다.
당분기말 현재 계류중인 소송사건에 대해서는 소송의 결과를 합리적으로 예측할 수 없으며, 보고기간 후 발생한 중요한 소송사건은 없습니다.
19.5 회사는 중국의 항서제약으로 부터 EGFR, HER2, HER4를 특이적으로 억제하는표적항암제와 관련하여 파이로티닙의 한국 독점 라이센스를 2020년 9월에 19.1억원을지급하고 획득하였습니다. 이와 관련하여 적응증 승인 및 확대와 관련 완제품의 판매로 인한 수익 발생 시 기술이전대가의 일정비율을 항서제약에 지급해야 하는 약정을 맺고 있습니다.
19.6 회사는 Elevar Therapeutics, lnc.와 리보세라닙의 한국내 독점개발, 판매권 및 유럽, 일본에 대한 수익 지분을 무형자산으로 인식하였습니다. 이와 관련하여 회사는 FDA(정식명칭 기재)의 승인 및 리보세라닙의 적응증 범위 확대 및 관련 완제품 판매로 인한 수익 발생 시 판매액의 일정비율을 Elevar Therapeutics, lnc.에 지급해야 하는 약정을 맺고 있습니다.
20. 특수관계자
20.1 특수관계자 현황
| 구 분 | 회사명 |
|---|---|
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ |
| 관계기업 | 에이치엘비제약㈜ |
| 에이치벨류에셋(주1) | |
| ㈜두산포천에너지 | |
| 에이치엘비사이언스㈜ | |
| 에이치엘비인베스트먼트㈜ | |
| 기타의 특수관계자 | 에이치엘비글로벌㈜ |
| 에이치엘비일렉㈜ | |
| 에이치엘비아이 알밤 제1호 투자조합 | |
| 에이치엘비네트웍스㈜ | |
| Elevar Therapeutics, Inc. | |
| Immunomic Therapeutics, Inc. | |
| 에이치엘비바이오스텝㈜ | |
| ㈜펭귄오션레저 | |
| 에이치엘비생활건강㈜ | |
| ㈜프레시코 | |
| ㈜코아바이오 | |
| 에포케㈜ | |
| 에이치엘비테라퓨틱스㈜ | |
| 바다중공업㈜ | |
| 현대요트㈜ | |
| ㈜노터스 | |
| 에이치엘비에프앤비㈜ | |
| 에이치엘비파나진㈜ | |
| 브이에스팜㈜ | |
| 에이치엘비이노베이션㈜ | |
| 임직원 |
(주1) 당분기 중 신규로 편입되었습니다.
20.2 특수관계자와의 주요 거래내역
<당분기>
| (단위: 천원) |
| 구 분 | 회사명 | 매출 등 | 매입 등 | |||
|---|---|---|---|---|---|---|
| 매출 | 이자수익 | 기타 | 임차료 | 기타 | ||
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ | 128,971 | - | - | 31,460 | 30,508 |
| 관계기업 | 에이치엘비제약㈜ | 8,924 | - | - | - | - |
| 에이치엘비사이언스㈜ | 6,913 | - | - | - | - | |
| 소 계 | 15,837 | - | - | - | - | |
| 기타의 특수관계자 | Elevar Therapeutics, Inc. | - | - | - | - | 54,604 |
| ㈜프레시코 | - | - | - | - | 1,084 | |
| 에이치엘비글로벌㈜ | 3,000 | - | - | - | - | |
| ㈜펭귄오션레져 | - | - | - | - | 6,470 | |
| 에이치엘비바이오스텝㈜ | 420 | - | - | - | 54,543 | |
| 에이치엘비에프앤비㈜ | - | - | - | - | 15,312 | |
| 에포케㈜ | - | - | - | - | 12,740 | |
| 바다중공업 | - | 3,125 | - | - | - | |
| 브이에스팜㈜ | 40,128 | - | - | - | - | |
| 임직원 | - | - | 376 | - | - | |
| 소 계 | 43,548 | 3,125 | 376 | - | 144,753 | |
| 합계 | 188,356 | 3,125 | 376 | 31,460 | 175,261 | |
<전분기>
| (단위: 천원) |
| 구 분 | 회사명 | 매출 등 | 매입 등 | ||||
|---|---|---|---|---|---|---|---|
| 공사매출 | 임대매출 | 이자수익 | 기타 | 임차료 | 기타 | ||
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ | 54,000 | 84,300 | - | 72,936 | 57,510 | 27,643 |
| 관계기업 | 에이치엘비제약(주) | - | 5,100 | - | (386) | - | - |
| 기타의 특수관계자 | Elevar Therapeutics, Inc. | - | - | - | - | - | 10,583 |
| Immunomic Therapeutics, Inc. | - | 1,330 | - | - | - | - | |
| 에이치엘비생활건강㈜ | - | - | - | - | - | 292 | |
| ㈜프레시코 | - | - | - | - | - | 2,751 | |
| 에이치엘비글로벌㈜ | - | - | - | 300 | - | - | |
| 에이치엘비사이언스㈜ | - | 3,000 | - | 1,063 | - | - | |
| ㈜펭귄오션레져 | - | - | - | - | - | 14,610 | |
| 에이치엘비인베스트먼트㈜ | - | - | - | - | - | 9,863 | |
| 바다중공업㈜ | - | - | 10,939 | - | - | - | |
| 에이치엘비바이오스텝㈜ | - | - | - | - | - | 46,550 | |
| 임직원 | - | - | 530 | - | 10,200 | - | |
| 소 계 | - | 4,330 | 11,469 | 1,363 | 10,200 | 84,649 | |
| 합 계 | 54,000 | 93,730 | 11,469 | 73,913 | 67,710 | 112,292 | |
20.3 특수관계자에 대한 채권ㆍ채무의 주요 내역
<당분기말>
| (단위: 천원) |
| 구 분 | 회사명 | 채권 등 | 채무 등 | |||
|---|---|---|---|---|---|---|
| 매출채권 | 기타채권 | 전환사채(주1) | 기타채무 | 신주인수권부사채(주2) | ||
| 유의적인 영향력을행사하는 기업 | 에이치엘비㈜ | - | 5,742 | - | 4,787 | 19,603,370 |
| 관계기업 | 에이치엘비제약㈜ | - | 3,707 | - | 40,000 | - |
| ㈜두산포천에너지(주3) | - | 505,804 | - | - | - | |
| 에이치엘비사이언스㈜ | - | 658 | - | 25,000 | - | |
| 소 계 | - | 510,169 | - | 65,000 | - | |
| 기타의 특수관계자 | 에이치엘비테라퓨틱스㈜ | - | - | - | 8,300,000 | - |
| Elevar Therapeutics, Inc. | - | - | - | 87,640 | - | |
| ㈜프레시코 | - | - | - | 712 | - | |
| 에이치엘비글로벌㈜ | - | 1,100 | - | - | - | |
| 에이치엘비바이오스텝㈜ | 139 | - | 10,242,854 | - | - | |
| ㈜펭귄오션레져 | - | 6,750 | - | - | - | |
| 브이에스팜㈜ | 20,659 | - | - | - | - | |
| 임직원 | - | 36,000 | - | - | - | |
| 소 계 | 20,798 | 43,850 | 10,242,854 | 8,388,352 | - | |
| 합계 | 20,798 | 559,761 | 10,242,854 | 8,458,139 | 19,603,370 | |
(주1) 공정가치평가 후 금액입니다.
(주2) 신주인수권부사채 채무 잔액은 액면금액입니다.
(주3) 회사는 해당 대여금에 대하여 전액 대손충당금을 설정하였습니다.
<전기말>
| (단위: 천원) |
| 구 분 | 회사명 | 채권 등 | 채무 등 | |||
|---|---|---|---|---|---|---|
| 매출채권 | 기타채권 | 전환사채(주1) | 기타채무 | 신주인수권부사채(주2) | ||
| 유의적인 영향력을행사하는 기업 | 에이치엘비㈜ | - | 239,319 | - | 793,321 | 19,603,370 |
| 관계기업 | 에이치엘비제약㈜ | - | 77,155 | - | 46,810 | - |
| ㈜두산포천에너지(주3) | - | 505,804 | - | - | - | |
| 에이치엘비사이언스㈜ | - | 2,756 | - | 13,143 | - | |
| 소계 | - | 585,715 | - | 59,954 | - | |
| 기타의 특수관계자 | 에이치엘비테라퓨틱스㈜ | - | 98,392 | - | 8,314,300 | - |
| Elevar Therapeutics, Inc. | - | - | - | 369,693 | - | |
| 에이치엘비생활건강㈜ | - | 1,216 | - | - | - | |
| ㈜프레시코 | - | 5,505 | - | 160 | - | |
| 에이치엘비글로벌㈜ | - | 49,862 | - | 7,951 | - | |
| 바다중공업㈜ | - | 823,179 | - | - | - | |
| ㈜펭귄오션레저 | - | 292 | - | - | - | |
| 에이치엘비바이오스텝㈜ | - | 85,809 | 10,815,389 | 30 | - | |
| 에이치엘비에프앤비㈜ | - | 18,234 | - | - | - | |
| 현대요트㈜ | - | 1,327 | - | - | - | |
| ㈜코아바이오 | - | 2,578 | - | - | - | |
| 에이치엘비네트웍스㈜ | - | 5,063 | - | 22,754 | - | |
| 에포케㈜ | - | 9,981 | - | 12,597 | - | |
| 에이치엘비파나진㈜ | - | 7,290 | - | - | - | |
| 에이치엘비이노베이션㈜ | - | 38,352 | - | - | - | |
| 에이치엘비인베스트먼트㈜ | - | 4,276 | - | - | - | |
| ㈜펭귄오션레져 | - | 202 | - | - | - | |
| 브이에스팜㈜ | 22,205 | - | - | - | - | |
| 임직원 | - | 45,000 | - | - | - | |
| 소계 | 22,205 | 1,196,557 | 10,815,389 | 8,727,486 | - | |
| 합계 | 22,205 | 2,021,591 | 10,815,389 | 9,580,761 | 19,603,370 | |
(주1) 공정가치평가 후 금액입니다.
(주2) 신주인수권부사채 채무 잔액은 액면금액입니다.
(주3) 연결회사는 해당 대여금에 대하여 전액 대손충당금을 설정하였습니다.
20.4 특수관계자와의 자금거래 내역
<당분기>
| (단위: 천원) |
| 구 분 | 회사명 | 자금 대여(차입) 거래 | 금융수익(원가) | 현금 출자 등 | |
|---|---|---|---|---|---|
| 대여(차입) | 회수(상환) | 이자수익 | |||
| 관계기업 | 에이치벨류에셋 | - | - | - | 5,000,000 |
| 소계 | - | - | - | 5,000,000 | |
| 기타의 특수관계자 | 에이치엘비아이알밤제1호투자조합 | - | - | - | 800,000 |
| 바다중공업㈜ | - | (800,000) | 3,125 | - | |
| 임직원 | - | (1,500) | - | - | |
| 소계 | - | (801,500) | 3,125 | 800,000 | |
| 합계 | - | (801,500) | 3,125 | 5,800,000 | |
<전분기>
| (단위: 천원) |
| 구 분 | 회사명 | 자금 대여(차입) | 리스부채 | 유상증자 | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 기초 대여금 (차입금) |
대여 (차입) |
회수 (상환) |
기말대여금 (차입금) |
기초 리스부채 |
이자비용 | 리스부채 상환 |
기말 리스부채 |
|||
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ | - | - | - | - | 393,837 | 9,077 | (64,200) | 338,714 | - |
| 관계기업 | ㈜두산포천에너지 | 505,804 | - | - | 505,804 | - | - | - | - | - |
| 기타의 특수관계자 | 바다중공업㈜ | 1,000,000 | - | (200,000) | 800,000 | - | - | - | - | - |
| 에이치엘비 이노베이션㈜ | - | - | - | - | - | - | - | - | 1,999,999 | |
| 임직원 | 33,083 | - | (2,750) | 30,333 | - | - | - | - | - | |
| 소 계 | 1,033,083 | - | (202,750) | 830,333 | - | - | - | - | - | |
| 합 계 | 1,538,887 | - | (202,750) | 1,336,137 | - | - | - | - | 1,999,999 | |
20.5 주요 경영진에 대한 보상
연결회사는 기업 활동의 계획ㆍ운영ㆍ통제에 대하여 중요한 권한과 책임을 가진 등기임원, 비등기임원, 내부감사 책임자 및 각 사업부문장 등을 주요 경영진으로 판단하였으며, 당기 및 전기 중 주요 경영진에 대한 보상을 위해 지급한 금액은 다음과 같습니다.
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 단기종업원급여 | 567,993 | 458,392 |
| 퇴직급여 | 497,493 | 67,193 |
| 합계 | 1,065,486 | 525,585 |
20.6 특수관계자와의 기타 유의적인 거래 및 약정사항
(1) 연결회사는 전기 중 제9회 무기명식 무보증 공모 분리형 신주인수권부사채를 발행하였으며, 연결회사에 유의적인 영향력을 행사하는 회사인 에이치엘비㈜가 공모에참여하여 액면가 기준 19,603,370천원을 취득하였습니다. 동 신주인수권부사의 사채권자는 발행일(2022년 6월 15일)부터 24개월이 경과하는 날(2024년 6월 15일)부터 신주인수권부사채의 만기일까지 신주인수권부사채의 조기상환을 청구할 수 있는 권리를 보유하고 있습니다.
20.7 현재 특수관계자에게 제공한 담보 및 보증 등
| 특수관계 구분 | 특수관계자명 | 담보제공 및 보증금액 | 보증 제공처 | 비고 |
|---|---|---|---|---|
| 기타의 특수관계자 | 에포케㈜ | 1,000,000,000 | 한국투자증권㈜ | 연대보증 |
에포케㈜ (특수관계자)가 한국투자증권으로부터 차입한 차입금에 대한 연대보증인으로서, ㈜신화어드밴스가 한국투자증권에 보유하고 있는 MMF 금융자산 (장부금액: 15억원)에 대한 질권이 설정되었습니다(채권최고액: 10억원).
21. 영업부문
21.1 당사의 영업부문 및 사업의 내용
| 구 분 | 사업의 내용 |
|---|---|
| 건설업 및 엔지니어링 | ESCO사업 및 신재생에너지 시설 건설업 |
| 바이오개발 | 체외순환형 바이오인공간 개발업 |
| 의약품 유통 | 의약품도매업 및 기타 판매업 |
| 메디케어 | 체외진단의료기기 및 기타 의료용기기 제조,판매업 |
| 기타 | 수수료매출 및 건물 임대 등 |
21.2 영업부문별 정보
<당분기>
| (단위: 천원) |
| 구 분 | 건설업 및 엔지니어링 |
바이오개발 | 의약품 유통 | 메디케어 사업부 |
기타 | 합 계 |
|---|---|---|---|---|---|---|
| 총매출액 | - | - | 16,848,632 | 5,933,151 | 1,608,532 | 24,390,315 |
| 내부매출액 | - | - | - | (248,716) | (247,231) | (495,947) |
| 순매출액 | - | - | 16,848,632 | 5,684,435 | 1,361,302 | 23,894,369 |
| 영업이익(손실) | (132,962) | - | (248,811) | (2,478,777) | (2,648,778) | (5,509,328) |
<전분기>
| (단위: 천원) |
| 구 분 | 건설업 및 엔지니어링 |
바이오개발 | 의약품 유통 | 메디케어 사업부 |
기타 | 합 계 |
|---|---|---|---|---|---|---|
| 총매출액 | 54,000 | 61,556 | 14,821,839 | 15,819,350 | 1,210,333 | 31,967,078 |
| 내부매출액 | - | - | (4,676) | (503,252) | (292,956) | (800,884) |
| 순매출액 | 54,000 | 61,556 | 14,817,163 | 15,316,098 | 917,377 | 31,166,194 |
| 영업이익(손실) | (1,859,413) | (1,509,924) | (239,610) | 910,541 | (123,940) | (2,822,346) |
22. 현금흐름표
22.1 영업으로부터 창출된 현금흐름 내역
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 당기순이익 | 145,389,881 | 13,688,004 |
| 조정: | ||
| 법인세비용 | (384,172) | (1,011,193) |
| 이자비용 | 5,814,563 | 4,848,475 |
| 퇴직급여 | 60,662 | 66,053 |
| 장기근속포상 | - | 514 |
| 감가상각비 | 1,123,167 | 1,106,508 |
| 사용권자산상각비 | 254,063 | 422,948 |
| 투자부동산상각비 | 6,350 | 33,839 |
| 무형자산상각비 | 215,288 | 398,787 |
| 외화환산손실 | 2,034 | 1,547 |
| 대손상각비 | 6,009 | (73,234) |
| 하자보수비 | - | 49 |
| 금융리스해지손실 | 3,610 | - |
| 당기손익-공정가치 측정 금융자산 평가손실 | 77 | 66,128 |
| 재고자산평가손실(환입) | (452,883) | 514,593 |
| 유형자산처분손실 | 13,871 | - |
| 유형자산폐기손실 | - | 54,009 |
| 잡손실 | 3,631 | - |
| 지분법손실 | 885,447 | 1,415 |
| 이자수익 | (344,355) | (388,839) |
| 외화환산이익 | (4,158) | (2,008) |
| 기타의대손충당금환입 | - | (9,600) |
| 당기손익-공정가치 측정 금융자산 평가이익 | (154,694,523) | (19,848,976) |
| 당기손익-공정가치 측정 금융자산 처분이익 | (3,004) | - |
| 파생상품평가이익 | (9,407) | - |
| 유형자산처분이익 | (10,908) | (1,303) |
| 하자보수충당금환입 | (1,568) | - |
| 지분법이익 | (65,410) | (183,609) |
| 환불부채충당금환입 | (189) | - |
| 잡이익 | (1,470) | - |
| 종속기업처분이익 | - | (56,268) |
| 관계기업처분이익 | (2,068,394) | (63,210) |
| 금융리스해지이익 | (13,335) | (6,006) |
| 운전자본의 변동: | ||
| 매출채권 | (1,346,841) | 5,243,968 |
| 기타유동금융자산 | 1,041,886 | 378,293 |
| 기타유동자산 | (215,828) | (1,010,985) |
| 재고자산 | 481,747 | 2,635,799 |
| 매입채무 | 1,101,417 | (1,699,249) |
| 기타유동금융부채 | (1,123,944) | (2,353,009) |
| 기타비유동금융부채 | 23,445 | - |
| 기타유동부채 | (1,034,503) | 18,695 |
| 기타비유동부채 | - | 8,931 |
| 순확정급여부채 | (8,420) | (2,651) |
| 합 계 | (5,356,164) | 2,778,415 |
22.2 현금의 유입과 유출이 없는 중요한 거래의 내역
| (단위: 천원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 건설중인자산 본계정 대체 | 230,500 | 688,000 |
| 당기 취득 유형자산 미지급금 대체 | 58,110 | 1,391,170 |
| 무형자산 취득 관련 선수금 변동 | - | 140,000 |
| 주식발행초과금의 결손금 보전 | - | 60,000,000 |
| 퇴직급여의 전환 | 370,611 | - |
| 장기차입금의 유동성 대체 | 6,485,000 | 125,000 |
23.3 재무활동현금흐름에서 생기는 부채의 조정내역
<당분기>
| (단위: 천원) |
| 구 분 | 기초 | 증가 | 재무활동 현금흐름 | 상각 | 대체 | 전환 | 기타 | 기말 |
|---|---|---|---|---|---|---|---|---|
| 단기차입금 | 10,220,000 | - | 19,600,000 | 65,926 | - | - | - | 29,885,926 |
| 유동성장기차입금 | 7,060,000 | - | (125,000) | - | 6,485,000 | - | - | 13,420,000 |
| 장기차입금 | 21,555,000 | - | 1,230,000 | - | (6,485,000) | - | - | 16,300,000 |
| 전환사채 | 45,013,539 | - | - | 1,622,099 | - | (15,687,208) | - | 30,948,430 |
| 신주인수권부사채 | 81,382,614 | - | 34,551,569 | 3,409,125 | - | (38,334,722) | - | 81,008,586 |
| 금융리스부채 | 1,346,348 | 135,024 | (242,277) | - | - | - | (204,168) | 1,034,927 |
| 합 계 | 166,577,501 | 135,024 | 55,014,292 | 5,097,150 | - | (54,021,930) | (204,168) | 172,597,869 |
<전분기>
| (단위: 천원) |
| 구 분 | 기초 | 증가 | 재무활동 현금흐름 | 상각 | 대체 | 전환 | 기타 | 기말 |
|---|---|---|---|---|---|---|---|---|
| 단기차입금 | 7,920,000 | - | 650,000 | - | 1,560,000 | - | - | 10,130,000 |
| 유동성장기차입금 | 387,200 | - | (3,050) | - | 125,000 | - | - | 509,150 |
| 장기차입금 | 30,854,650 | - | - | - | (1,685,000) | - | - | 29,169,650 |
| 전환사채 | 35,423,163 | - | - | 1,542,226 | - | - | - | 36,965,389 |
| 신주인수권부사채 | 69,911,050 | - | 6,822 | 2,950,189 | - | (248,164) | 46,152 | 72,666,049 |
| 금융리스부채 | 2,977,307 | 303,385 | (594,920) | 67,724 | - | - | (139,661) | 613,813 |
| 합 계 | 147,473,370 | 303,385 | 58,852 | 4,560,139 | - | (248,164) | (93,509) | 152,054,074 |
23. 매각예정비유동자산
| (단위: 천원) |
| 구분 | 당분기말 | 전기말 |
|---|---|---|
| 투자부동산(건물) | 25,526,489 | 25,526,489 |
| 투자부동산(토지) | 22,056,334 | 22,056,334 |
| 합 계 | 47,582,823 | 47,582,823 |
4. 재무제표
4-1. 재무상태표
|
재무상태표 |
|
제 27 기 1분기말 2024.03.31 현재 |
|
제 26 기말 2023.12.31 현재 |
|
(단위 : 원) |
|
제 27 기 1분기말 |
제 26 기말 |
|
|---|---|---|
|
자산 |
||
|
유동자산 |
113,360,240,711 |
73,779,672,546 |
|
현금및현금성자산 |
40,363,246,230 |
5,956,211,886 |
|
매출채권 |
5,748,107,162 |
5,187,922,466 |
|
당기손익-공정가치 측정 금융자산 |
10,242,853,602 |
10,242,853,602 |
|
기타유동금융자산 |
6,389,859,173 |
1,873,047,595 |
|
재고자산 |
2,385,041,471 |
2,305,275,099 |
|
기타유동자산 |
628,211,316 |
631,538,791 |
|
당기법인세자산 |
20,098,650 |
0 |
|
매각예정비유동자산 |
47,582,823,107 |
47,582,823,107 |
|
비유동자산 |
459,860,876,742 |
341,186,025,403 |
|
장기매출채권 |
0 |
0 |
|
당기손익-공정가치 측정 금융자산 |
222,665,163,320 |
108,217,679,140 |
|
기타포괄손익-공정가치 측정 비유동금융자산 |
200,002,500 |
200,002,500 |
|
기타비유동금융자산 |
233,851,862 |
245,659,998 |
|
기타비유동자산 |
0 |
0 |
|
종속기업 및 관계기업투자 |
146,969,702,810 |
142,169,702,810 |
|
유형자산 |
44,353,281,440 |
44,684,503,067 |
|
투자부동산 |
4,266,136,066 |
4,289,757,628 |
|
무형자산 |
40,700,814,208 |
40,704,349,971 |
|
사용권자산 |
471,924,536 |
674,370,289 |
|
자산총계 |
573,221,117,453 |
414,965,697,949 |
|
부채 |
||
|
유동부채 |
137,599,978,849 |
131,084,884,097 |
|
매입채무 |
1,232,001,728 |
3,249,845,456 |
|
리스부채 |
372,958,818 |
487,189,246 |
|
단기차입금 |
29,885,926,464 |
10,220,000,000 |
|
유동성장기차입금 |
13,420,000,000 |
7,060,000,000 |
|
유동성사채 |
81,008,586,931 |
96,541,148,375 |
|
기타유동금융부채 |
1,908,506,200 |
3,639,779,426 |
|
기타유동부채 |
1,971,918,628 |
2,172,174,901 |
|
충당부채 |
0 |
29,846,753 |
|
당기법인세부채 |
7,800,080,080 |
7,684,899,940 |
|
비유동부채 |
44,329,039,259 |
50,468,336,348 |
|
파생상품부채 |
23,822,228 |
33,229,382 |
|
리스부채 |
116,787,372 |
204,114,914 |
|
장기차입금 |
12,500,000,000 |
18,985,000,000 |
|
사채 |
30,948,429,659 |
29,855,004,141 |
|
기타비유동금융부채 |
740,000,000 |
740,000,000 |
|
비유동충당부채 |
0 |
0 |
|
순확정급여부채 |
0 |
303,102,728 |
|
이연법인세부채 |
0 |
347,885,183 |
|
부채총계 |
181,929,018,108 |
181,553,220,445 |
|
자본 |
||
|
자본금 |
54,273,709,000 |
51,406,912,500 |
|
주식발행초과금 |
173,685,497,651 |
122,577,398,479 |
|
기타자본구성요소 |
44,772,726,880 |
44,772,795,566 |
|
이익잉여금(결손금) |
118,560,165,814 |
14,655,370,959 |
|
자본총계 |
391,292,099,345 |
233,412,477,504 |
|
자본과부채총계 |
573,221,117,453 |
414,965,697,949 |
4-2. 포괄손익계산서
|
포괄손익계산서 |
|
제 27 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
제 26 기 1분기 2023.01.01 부터 2023.03.31 까지 |
|
(단위 : 원) |
|
제 27 기 1분기 |
제 26 기 1분기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
매출액 |
6,086,469,777 |
6,086,469,777 |
15,741,404,695 |
15,741,404,695 |
|
매출원가 |
6,108,222,513 |
6,108,222,513 |
13,227,796,339 |
13,227,796,339 |
|
매출총이익(손실) |
(21,752,736) |
(21,752,736) |
2,513,608,356 |
2,513,608,356 |
|
판매비와관리비 |
2,673,327,081 |
2,673,327,081 |
3,071,105,735 |
3,071,105,735 |
|
영업이익(손실) |
(2,695,079,817) |
(2,695,079,817) |
(557,497,379) |
(557,497,379) |
|
금융수익 |
112,052,722,870 |
112,052,722,870 |
14,397,636,108 |
14,397,636,108 |
|
금융원가 |
5,822,800,315 |
5,822,800,315 |
4,864,509,382 |
4,864,509,382 |
|
기타수익 |
29,374,240 |
29,374,240 |
35,346,851 |
35,346,851 |
|
기타비용 |
22,672,514 |
22,672,514 |
71,447,918 |
71,447,918 |
|
법인세비용차감전순이익(손실) |
103,541,544,464 |
103,541,544,464 |
8,939,528,280 |
8,939,528,280 |
|
법인세비용(수익) |
363,250,391 |
363,250,391 |
965,801,087 |
965,801,087 |
|
연결당기순이익(손실) |
103,904,794,855 |
103,904,794,855 |
9,905,329,367 |
9,905,329,367 |
|
기타포괄손익 |
0 |
0 |
0 |
0 |
|
후속적으로 당기손익으로 재분류되지 않는 항목 |
||||
|
확정급여제도의 재측정요소 |
0 |
0 |
0 |
0 |
|
당기총포괄손익 |
103,904,794,855 |
103,904,794,855 |
9,905,329,367 |
9,905,329,367 |
|
주당이익 |
||||
|
기본주당이익(손실) (단위 : 원) |
996 |
996 |
(102.00) |
(102) |
|
희석주당이익(손실) (단위 : 원) |
996 |
996 |
(102.00) |
(102) |
4-3. 자본변동표
|
자본변동표 |
|
제 27 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
제 26 기 1분기 2023.01.01 부터 2023.03.31 까지 |
|
(단위 : 원) |
|
자본 |
|||||
|---|---|---|---|---|---|
|
자본금 |
주식발행초과금 |
기타자본구성요소 |
이익잉여금(결손금) |
자본 합계 |
|
|
2023.01.01 (기초자본) |
48,831,044,000 |
181,375,478,936 |
39,056,867,553 |
(29,035,100,845) |
240,228,289,644 |
|
결손금 보전 |
0 |
(60,000,000,000) |
0 |
60,000,000,000 |
0 |
|
연결당기순이익(손실) |
0 |
0 |
0 |
9,905,329,367 |
9,905,329,367 |
|
자본에 직접 인식된 주주와의 거래 |
|||||
|
주식배당 |
0 |
0 |
2,500,000,000 |
(2,500,000,000) |
0 |
|
전환사채의 전환 |
0 |
0 |
0 |
0 |
0 |
|
신주인수권부사채의 발행 |
0 |
191,100,805 |
0 |
0 |
191,100,805 |
|
신주인수권부사채의 전환 |
10,911,000 |
(15,382,720) |
0 |
0 |
(4,471,720) |
|
2023.03.31 (기말자본) |
48,841,955,000 |
121,551,197,021 |
41,556,867,553 |
38,370,228,522 |
250,320,248,096 |
|
2024.01.01 (기초자본) |
51,406,912,500 |
122,577,398,479 |
44,772,795,566 |
14,655,370,959 |
233,412,477,504 |
|
결손금 보전 |
0 |
0 |
0 |
0 |
0 |
|
연결당기순이익(손실) |
0 |
0 |
0 |
103,904,794,855 |
103,904,794,855 |
|
자본에 직접 인식된 주주와의 거래 |
|||||
|
주식배당 |
0 |
0 |
0 |
0 |
0 |
|
전환사채의 전환 |
708,410,500 |
14,970,500,059 |
(68,686) |
0 |
15,678,841,873 |
|
신주인수권부사채의 발행 |
0 |
0 |
0 |
0 |
0 |
|
신주인수권부사채의 전환 |
2,158,386,000 |
36,137,599,113 |
0 |
0 |
38,295,985,113 |
|
2024.03.31 (기말자본) |
54,273,709,000 |
173,685,497,651 |
44,772,726,880 |
118,560,165,814 |
391,292,099,345 |
4-4. 현금흐름표
|
현금흐름표 |
|
제 27 기 1분기 2024.01.01 부터 2024.03.31 까지 |
|
제 26 기 1분기 2023.01.01 부터 2023.03.31 까지 |
|
(단위 : 원) |
|
제 27 기 1분기 |
제 26 기 1분기 |
|
|---|---|---|
|
영업활동으로 인한 현금흐름 |
(4,644,201,712) |
5,240,786,468 |
|
영업으로부터 창출된 현금 |
(4,317,978,584) |
4,420,319,405 |
|
이자의 수취 |
130,889,800 |
240,490,912 |
|
이자의 지급 |
(437,014,278) |
(435,490,355) |
|
배당금수령 |
0 |
0 |
|
법인세 환급(납부) |
(20,098,650) |
1,015,466,506 |
|
투자활동으로 인한 현금흐름 |
(14,969,230,090) |
(4,097,767,969) |
|
당기손익-공정가치 측정 금융자산의 취득 |
(5,200,000,000) |
(2,009,101,232) |
|
당기손익-공정가치 측정 금융자산의 처분 |
0 |
10,002,599 |
|
기타유동금융자산의 증가 |
(5,043,000,000) |
(3,253,424,890) |
|
기타유동금융자산의 감소 |
908,792,000 |
4,008,864,529 |
|
기타비유동금융자산의 증가 |
0 |
0 |
|
기타비유동금융자산의 감소 |
7,580,000 |
0 |
|
종속기업 및 관계기업투자의 취득 |
(4,800,000,000) |
0 |
|
종속기업 및 관계기업투자의 처분 |
0 |
15,247,780 |
|
유형자산의 취득 |
(366,290,000) |
(3,162,559,336) |
|
유형자산의 처분 |
4,000,000 |
39,420,000 |
|
투자부동산의 취득 |
0 |
0 |
|
투자부동산의 처분 |
0 |
0 |
|
무형자산의 취득 |
(31,241,968) |
(3,444,666) |
|
무형자산의 처분 |
0 |
140,000,000 |
|
매각예정비유동자산의 처분 |
0 |
0 |
|
사업분할 |
(449,070,122) |
0 |
|
금융리스채권의 감소 |
0 |
117,227,247 |
|
재무활동으로 인한 현금흐름 |
54,017,886,936 |
214,965,648 |
|
리스부채의 감소 |
(141,613,837) |
(426,473,253) |
|
단기차입금의 증가 |
19,600,000,000 |
650,000,000 |
|
단기차입금의 감소 |
0 |
0 |
|
장기차입금의 감소 |
(125,000,000) |
0 |
|
전환사채의 발행 |
0 |
0 |
|
전환사채의 감소 |
0 |
0 |
|
신주인수권부사채의 발행 |
0 |
(15,382,720) |
|
신주인수권부사채의 청구 |
34,551,569,459 |
6,821,621 |
|
주식선택권행사로 인한 현금유입 |
0 |
0 |
|
자기주식의 취득 |
(68,686) |
0 |
|
임대보증금의 증가 |
133,000,000 |
|
|
현금및현금성자산의 증가(감소) |
34,404,455,134 |
1,357,984,147 |
|
기초현금및현금성자산 |
5,956,211,886 |
22,093,001,838 |
|
현금및현금성자산에 대한 환율변동효과 |
2,579,210 |
115,246 |
|
당기말현금및현금성자산 |
40,363,246,230 |
23,451,101,231 |
5. 재무제표 주석
1. 일반사항
에이치엘비생명과학 주식회사(이하 '회사')는 1998년 7월 24일에 에너지 절약 관련 엔지니어링 서비스업을 위한 진단,설계, 시공 등을 목적으로 설립되어, ESCO(Energy Service Company) 사업 등을 영위하고 있습니다. 회사는 2008년에 보통주를 한국거래소가 개설하는 코스닥시장에 상장하였습니다.
또한, 회사는 2022년 10월 1일 에임(주)와 합병하여 체외진단키트 등 의료기기사업에 진출하였습니다.
회사의 납입자본금은 54,274백만원이며, 당분기말 현재 최대 주주는 에이치엘비 주식회사(지분율 : 18.30%)입니다.
2. 재무제표 작성기준 및 중요한 회계정책
2.1 재무제표 작성기준
회사의 2024년 3월 31일로 종료하는 3개월 보고기간에 대한 요약분기재무제표는 기업회계기준서 제1034호 '중간재무보고'에 따라 작성되었습니다.
이 중간재무제표는 연차재무제표에 기재되는 사항이 모두 포함되지 않았으므로 전기말 연차재무제표와 함께 이해해야 합니다.
2.1.1 회사가 채택한 제ㆍ개정 기준서 및 해석서
회사는 2024년 1월 1일로 개시하는 회계기간부터 다음의 제ㆍ개정 기준서 및 해석서를 신규로 적용하였습니다.
(1) 기업회계기준서 제1001호 '재무제표 표시' 개정 - 부채의 유동/비유동 분류, 약정사항이 있는 비유동부채
보고기간말 현재 존재하는 실질적인 권리에 따라 유동 또는 비유동으로 분류되며, 부채의 결제를 연기할 수 있는 권리의 행사가능성이나 경영진의 기대는 고려하지 않습 니다. 또한, 부채의 결제에 자기지분상품의 이전도 포함되나, 복합금융상품에서 자기 지분상품으로 결제하는 옵션이 지분상품의 정의를 충족하여 부채와 분리하여 인식된 경우는 제외됩니다. 또한, 기업이 보고기간말 후에 준수해야하는 약정은 보고기간말에 해당 부채의 분류에 영향을 미치지 않으며, 보고기간 이후 12개월 이내 약정사항을 준수해야하는 부채가 보고기간말 현재 비유동부채로 분류된 경우 보고기간 이후 12개월 이내 부채가 상환될 수 있는 위험에 관한 정보를 공시해야 합니다. 해당 기준서의 개정이 재무제표에 미치는 중요한 영향은 없습니다.
(2) 기업회계기준서 제1007호 '현금흐름표', 기업회계기준서 제1107호 '금융상품: 공시' 개정 - 공급자금융약정에 대한 정보 공시
공급자금융약정을 적용하는 경우, 재무제표이용자가 공급자금융약정이 기업의 부채와 현금흐름 그리고 유동성위험 익스포저에 미치는 영향을 평가할 수 있도록 공급자금융약정에 대한 정보를 공시해야 합니다. 이 개정내용을 최초로 적용하는 회계연도 내 중간보고기간에는 해당 내용을 공시할 필요가 없다는 경과규정에 따라 중간재무제표에 미치는 영향이 없습니다.
(3) 기업회계기준서 제1116호 ‘리스’ 개정 - 판매후리스에서 생기는 리스부채
판매후리스에서 생기는 리스부채를 후속적으로 측정할 때 판매자-리스이용자가 보유하는 사용권 관련 손익을 인식하지 않는 방식으로 리스료나 수정리스료를 산정합니다. 해당 기준서의 제정이 재무제표에 미치는 중요한 영향은 없습니다.
(4) 기업회계기준서 제1001호 ‘재무제표 표시’ 개정 - '가상자산 공시’
가상자산을 보유하는 경우, 가상자산을 고객을 대신하여 보유하는 경우, 가상자산을 발행한 경우의 추가 공시사항을 규정하고 있습니다. 해당 기준서의 개정이 재무제표에 미치는 중요한 영향은 없습니다.
2.1.2 회사가 적용하지 않은 제ㆍ개정 기준서 및 해석서
제정 또는 공표되었으나 시행일이 도래하지 않아 적용하지 아니한 제ㆍ개정 기준서 및 해석서는 다음과 같습니다.
(1) 기업회계기준서 제1021호 ‘환율변동효과’와 기업회계기준서 제1101호 ‘한국채택국제회계기준의 최초채택’ 개정 - 교환가능성 결여
통화의 교환가능성을 평가하고 다른 통화와 교환이 가능하지 않다면 현물환율을 추정하며 관련 정보를 공시하도록 하고 있습니다. 동 개정사항은 2025 년 1 월 1 일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 해당 기준서의 개정이 재무제표에 미치는 중요한 영향은 없습니다.
2.2 법인세비용
중간기간의 법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균연간법인세율, 즉 추정평균연간유효법인세율을 중간기간의 세전이익에 적용하여 계산합니다.
3. 중요한 회계추정 및 가정
회사는 미래에 대하여 추정 및 가정을 하고 있습니다. 추정 및 가정은 지속적으로 평가되며, 과거 경험과 현재의 상황에서 합리적으로 예측가능한 미래의 사건과 같은 다른 요소들을 고려하여 이루어집니다. 이러한 회계추정은 실제 결과와 다를 수도있습니다.
글로벌 시장상황이 시장의 신뢰와 소비자의 소비형태에 영향을 미쳤지만, 회사는 지속적인 제품 혁신과 최근 Complete Office Furniture Limited의 인수를 통해 수익을 창출할 수 있는 여력이 충분합니다. 회사는 기후 관련 및 그 밖의 사업위험에 대한 익스포저를 검토하였으나 당분기말 현재 회사의 재무실적이나 재무상태에 영향을 미칠 수 있는 위험은 식별되지 않았습니다. 회사는 기존 차입금의 약정사항을 충족할 수 있도록 충분한 자금여력을 보유하고 있으며, 영업활동과 지속적인 투자를 뒷받침할 충분한 운전자본 및 자금조달약정을 통한 미사용 자금한도를 보유하고 있습니다.
요약분기재무제표 작성시 사용된 중요한 회계추정 및 가정은 법인세비용을 결정하는데 사용된 추정의 방법을 제외하고는 전기 재무제표 작성에 적용된 회계추정 및 가정과 동일합니다.
4. 공정가치
4.1 금융상품 종류별 공정가치
회사의 금융상품 중 상각후원가로 측정하는 금융자산과 금융부채는 장부금액과 공정가치의 차이가 유의적이지 않으며, 기타 금융상품은 장부금액과 공정가치가 일치합니다.
4.2 공정가치 서열체계
공정가치로 측정되거나 공정가치가 공시되는 항목은 공정가치 서열체계에 따라 구분하며, 정의된 수준들은 다음과 같습니다.
| 구분 | 투입변수의 유의성 |
|---|---|
| 수준 1 | 동일한 자산이나 부채에 대한 활성시장의 공시가격 |
| 수준 2 | 직접적으로 또는 간접적으로 관측가능한 자산이나 부채에 대한 투입변수 |
| 수준 3 | 관측가능한 시장자료에 기초하지 않은 자산이나 부채에 대한 투입변수 |
4.3 공정가치로 측정되는 금융상품의 공정가치 서열체계 구분
<당분기말>
| (단위: 천원) |
| 구분 | 수준 1 | 수준 2 | 수준 3 | 합계 |
|---|---|---|---|---|
| 금융자산 | ||||
| 당기손익-공정가치 측정 금융자산 | ||||
| 지분증권 | 216,360,878 | - | 104,285 | 216,465,163 |
| 복합금융상품 | - | - | 14,642,854 | 14,642,854 |
| 출자금 | - | - | 1,800,000 | 1,800,000 |
| 기타포괄손익-공정가치 측정 금융자산 | ||||
| 지분증권 | - | - | 200,002 | 200,002 |
| 금융부채 | ||||
| 당기손익-공정가치 측정 금융부채 | ||||
| 파생상품부채 | - | 23,822 | - | 23,822 |
<전기말>
| (단위: 천원) |
| 구분 | 수준1 | 수준2 | 수준3 | 합계 |
|---|---|---|---|---|
| 금융자산 | ||||
| 당기손익-공정가치 측정 금융자산 | ||||
| 지분증권 | 104,506,597 | - | 104,285 | 104,610,882 |
| 복합금융상품 | - | - | 10,242,854 | 10,242,854 |
| 출자금 | - | - | 3,606,797 | 3,606,797 |
| 기타포괄손익-공정가치 측정 금융자산 | ||||
| 지분증권 | - | - | 200,002 | 200,002 |
| 금융부채 | ||||
| 당기손익-공정가치 측정 금융부채 | ||||
| 파생상품부채 | - | 33,229 | - | 33,229 |
4.4 반복적인 공정가치 측정치의 서열체계 수준 간 이동
회사는 공정가치 서열체계의 수준 간 이동을 보고기간말에 인식합니다. 당분기말 현재 회사의 반복적인 측정치의 수준1과 수준2 사이의 이동 내역은 존재하지 않습니다.
4.5 반복적인 측정치의 수준 3의 변동 내역
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 기초 | 14,153,938 | 28,700,000 |
| 취득 | 5,200,000 | - |
| 평가 | - | (3,693,845) |
| 대체(주1) | (2,606,797) | - |
| 기말 | 16,747,141 | 25,006,155 |
(주1) 당분기 중 에너지 사업부를 물적분할하였으며, 사업분할을 통해 승계한 금액입니다.
4.6 가치평가기법 및 투입변수
수준 2와 수준 3으로 분류되는 금융상품의 가치평가기법 및 투입변수
<당분기말>
| (단위: 천원) |
| 구분 | 공정가치 | 가치평가기법 | 수준 | 투입변수 | 투입변수 범위 |
|---|---|---|---|---|---|
| HLB바이오스텝 제1회 무기명식 무보증 전환사채 | 10,242,854 | 이항모형 | 수준 3 | 위험할인율 | 7.94% ~ 12.82% |
| 주 변동성 | 5.16% | ||||
| 무위험할인율 | 3.16% ~ 3.39% | ||||
| HLBI 알밤 제1호 투자조합 | 1,800,000 | 원가법 | 수준3 | - | - |
<전기말>
| (단위: 천원) |
| 구분 | 공정가치 | 가치평가기법 | 수준 | 투입변수 | 투입변수 범위 |
|---|---|---|---|---|---|
| HLB바이오스텝 제1회 무기명식 무보증 전환사채 | 10,242,854 | 이항모형 | 수준 3 | 위험할인율 | 7.94% ~ 12.82% |
| 주 변동성 | 5.16% | ||||
| 무위험할인율 | 3.16% ~ 3.39% | ||||
| 기계설비건설공제조합 | 920,245 | 순자산가치평가법 | 수준3 | - | - |
| 엔지니어링공제조합 | 1,615,293 | 순자산가치평가법 | 수준3 | - | - |
| 전기공사공제조합 | 71,259 | 순자산가치평가법 | 수준3 | - | - |
| HLBI 알밤 제1호 투자조합 | 1,000,000 | 원가법 | 수준3 | - | - |
회사의 재무부서는 재무보고 목적의 공정가치의 측정을 담당하고 있으며 이러한 공정가치 측정치는 수준 3으로 분류되는 공정가치 측정치를 포함하고 있습니다. 회사의 재무부서는 공정가치 측정내역 및 결과에 대하여 회사의 경영진에게 매 분기 보고하고 있습니다.
4.7 수준 3으로 분류된 반복적인 공정가치 측정치의 민감도 분석
금융상품의 민감도 분석은 통계적 기법을 이용한 관측 불가능한 투입변수의 변동에따른 금융상품의 가치 변동에 기초하여 유리한 변동과 불리한 변동으로 구분하여 이루어집니다. 그리고 공정가치가 두 개 이상의 투입변수에 영향을 받는 경우에는 가장유리하거나 또는 가장 불리한 금액을 바탕으로 산출됩니다. 민감도 분석대상으로 수준3으로 분류되는 금융상품 중 해당 공정가치 변동이 당기손익으로 인식되는 파생상품이 있고, 공정가치 변동이 당기손익 혹은 기타포괄손익으로 인식되는 지분상품과 채무상품 등이 있습니다.
5. 공정가치 측정 금융자산
5.1 공정가치 측정 금융자산의 내역
| (단위: 천원) |
| 구분 | 당분기말 | 전기말 |
|---|---|---|
| 당기손익-공정가치 측정 금융자산 | ||
| 시장성 있는 지분증권 | 216,360,878 | 104,506,597 |
| 시장성 없는 지분증권 | 104,285 | 104,285 |
| 복합금융상품 | 14,642,854 | 10,242,854 |
| 출자금 | 1,800,000 | 3,606,797 |
| 소계 | 232,908,017 | 118,460,533 |
| 기타포괄손익-공정가치 측정 금융자산 | ||
| 시장성 없는 지분증권 | 200,002 | 200,002 |
| 합계 | 233,108,019 | 118,660,535 |
5.2 당기손익-공정가치 측정 금융자산의 내역
| (단위: 천원) |
| 구분 | 종목 | 당분기말 | 전기말 |
|---|---|---|---|
| 시장성 있는 지분증권 |
HLB | 203,414,825 | 98,033,570 |
| HLB이노베이션 | 12,946,053 | 6,473,027 | |
| 시장성 없는 지분증권 |
백년약속 | 80,240 | 80,240 |
| 참다운창조교육 | 24,045 | 24,045 | |
| 출자금 | 엔지니어링공제조합 | - | 1,615,293 |
| 기계설비건설공제조합 | - | 920,245 | |
| 전기공사공제조합 | - | 71,259 | |
| HLBI 알밤 제1호 투자조합 | 1,800,000 | 1,000,000 | |
| 복합금융상품 | HLB바이오스텝 | 10,242,854 | 10,242,854 |
| 에이치벨류에셋 | 4,400,000 | - | |
| 합계 | 232,908,017 | 118,460,533 | |
5.3 당기손익-공정가치 측정 금융자산의 변동 내역
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 기초 | 118,460,533 | 71,535,935 |
| 취득 | 5,200,000 | 2,009,101 |
| 평가손익 | 111,854,281 | 14,065,822 |
| 처분 | - | (10,003) |
| 대체(주1) | (2,606,797) | - |
| 기말 | 232,908,017 | 87,600,855 |
(주1) 당분기 중 에너지 사업부를 물적분할하였으며, 사업분할을 통해 승계한 금액입니다.
6. 기타금융자산
6.1 기타금융자산 내역
| (단위: 천원) |
| 구분 | 당분기말 | 전기말 | ||
|---|---|---|---|---|
| 유동 | 비유동 | 유동 | 비유동 | |
| 금융기관예치금(주1) | 1,000 | 15,996 | 10,000 | - |
| 대여금 | 5,086,880 | 609,242 | 86,880 | 610,742 |
| 손실충당금 | (80,880) | (505,804) | (80,880) | (505,804) |
| 미수금 | 1,088,144 | 62,400 | 1,675,543 | 62,400 |
| 손실충당금 | (41,765) | (62,400) | (956,492) | (62,400) |
| 미수수익 | 31,626 | - | 139 | - |
| 임차보증금 | 323,536 | 128,754 | 1,161,793 | 159,619 |
| 현재가치할인차금 | (18,682) | (14,336) | (23,935) | (18,897) |
| 합계 | 6,389,859 | 233,852 | 1,873,048 | 245,660 |
(주1) 단기금융상품 중 100억은 엔에이치투자증권㈜의 사기적 부정거래 행위 및 불완전판매로 인하여 부당이득금 반환 청구 소송중인 상품으로 회사는 단기금융상품 전액에 대해서 대손충당금을 설정하고 있으며, 회사의 등기임원은 본 사건과 관련하여 발생가능한 손실을 보전하기 위하여 회사의 등기임원이 보유한 에이치엘비(주)의 주식을 법무법인에 위탁하는 계약을 체결하였습니다.
7. 재고자산
7.1 재고자산의 내역
| (단위: 천원) |
| 구분 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|
| 취득원가 | 평가손실충당금 | 장부금액 | 취득원가 | 평가손실충당금 | 장부금액 | |
| 상품 | 432,316 | (70,628) | 361,688 | 502,708 | (91,374) | 411,334 |
| 원재료 | 1,114,025 | (287,696) | 826,329 | 1,933,999 | (894,716) | 1,039,283 |
| 재공품 | 599,555 | (222,693) | 376,862 | 391,358 | (252,947) | 138,411 |
| 제품 | 1,313,408 | (493,246) | 820,162 | 1,004,356 | (288,109) | 716,247 |
| 합계 | 3,459,304 | (1,074,263) | 2,385,041 | 3,832,421 | (1,527,146) | 2,305,275 |
7.2 재고자산 관련 원가
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 매출원가: | ||
| 재고자산평가손실(환입) | (452,883) | (514,593) |
| 비용으로 인식된 재고자산 원가 | 2,344,654 | 5,291,275 |
8. 종속기업 및 관계기업투자
8.1 종속기업 및 관계기업투자의 내역
| (단위: 천원) |
| 구분 | 소재지 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|---|
| 지분율(%) | 취득원가 | 장부금액 | 지분율(%) | 취득원가 | 장부금액 | ||
| 종속기업투자 | |||||||
| ㈜신화어드밴스 | 대한민국 | 100.00 | 24,625,692 | 22,622,758 | 100.00 | 24,625,692 | 22,622,758 |
| HLB셀㈜ | 대한민국 | 99.30 | 120,613,509 | 52,908,843 | 99.30 | 120,613,509 | 52,908,843 |
| HLB솔루션㈜(주1) | 대한민국 | 100.00 | 1,200,000 | 1,200,000 | - | - | - |
| HLB에너지㈜ | 대한민국 | 100.00 | 27,638,046 | 27,638,046 | 100.00 | 27,638,046 | 27,638,046 |
| HLB생명과학알앤디㈜ | 대한민국 | 100.00 | 13,000,000 | 5,990,713 | 100.00 | 10,000,000 | 2,990,713 |
| 소계 | 187,077,247 | 110,360,360 | 182,877,247 | 106,160,360 | |||
| 관계기업투자 | |||||||
| 에이치엘비제약㈜ | 대한민국 | 14.60 | 29,559,250 | 29,559,250 | 14.60 | 29,559,250 | 29,559,250 |
| ㈜엘에스케이인베스트먼트 | 대한민국 | 9.00 | 450,000 | 450,000 | 9.00 | 450,000 | 450,000 |
| 에이치벨류에셋 | 대한민국 | 20.00 | 600,000 | 600,000 | - | - | - |
| HLB사이언스㈜ | 대한민국 | 20.62 | 6,000,093 | 6,000,093 | 20.62 | 6,000,093 | 6,000,093 |
| ㈜두산포천에너지 | 대한민국 | 20.00 | 40,000 | - | 20.00 | 40,000 | - |
| 소계 | 36,649,343 | 36,609,343 | 36,049,343 | 36,009,343 | |||
| 합계 | 223,726,590 | 146,969,703 | 218,926,590 | 142,169,703 | |||
(주1) 당분기 중 에너지 사업부를 물적분할하여 신규 편입되었습니다.
8.2 종속기업 및 관계기업투자의 변동 내역
<당분기>
| (단위: 천원) |
| 구분 | 기초 | 취득 | 기말 |
|---|---|---|---|
| 종속기업투자 | |||
| ㈜신화어드밴스 | 22,622,758 | - | 22,622,758 |
| HLB셀㈜ | 52,908,843 | - | 52,908,843 |
| HLB에너지㈜ | 27,638,046 | - | 27,638,046 |
| HLB생명과학알앤디㈜ | 2,990,713 | 3,000,000 | 5,990,713 |
| HLB솔루션㈜ | - | 1,200,000 | 1,200,000 |
| 소계 | 106,160,360 | 4,200,000 | 110,360,360 |
| 관계기업투자 | |||
| 에이치엘비제약㈜ | 29,559,250 | - | 29,559,250 |
| ㈜엘에스케이인베스트먼트 | 450,000 | - | 450,000 |
| 에이치벨류에셋 | - | 600,000 | 600,000 |
| HLB사이언스㈜ | 6,000,093 | - | 6,000,093 |
| 소계 | 36,009,343 | 600,000 | 36,609,343 |
| 합계 | 142,169,703 | 4,800,000 | 146,969,703 |
<전분기>
| (단위: 천원) |
| 구분 | 기초 | 취득 | 기말 |
|---|---|---|---|
| 종속기업투자 | |||
| ㈜신화어드밴스 | 23,711,297 | - | 23,711,297 |
| HLB셀㈜ | 50,408,843 | - | 50,408,843 |
| HLB에너지㈜ | 15,056,500 | - | 15,056,500 |
| HLB생명과학알앤디㈜ | 4,028,478 | - | 4,028,478 |
| HLBI알밤제1호투자조합 | 1,000,000 | - | 1,000,000 |
| 소계 | 94,205,118 | - | 94,205,118 |
| 관계기업투자 | |||
| 에이치엘비제약㈜ | 21,096,983 | - | 21,096,983 |
| ㈜엘에스케이인베스트먼트 | 450,000 | - | 450,000 |
| 노마드제2호조합 | 10,150,500 | - | 10,150,500 |
| 소계 | 31,697,483 | - | 31,697,483 |
| 합계 | 125,902,601 | - | 125,902,601 |
8.3 당분기말 현재 시장성이 있는 관계기업투자의 시장가격
| (단위: 천원) |
| 구분 | 주당 공정가치 | 주식수 | 시장가격 |
|---|---|---|---|
| HLB제약 | 36,800원 | 4,322,044주 | 159,051,219 |
| HLB사이언스 | 4,345원 | 3,365,165주 | 14,621,642 |
9. 유형자산
9.1 유형자산의 내역
| (단위: 천원) |
| 구분 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|
| 원가 | 상각누계액(주1) | 장부금액 | 원가 | 상각누계액(주1) | 장부금액 | |
| 토지 | 12,509,021 | - | 12,509,021 | 12,509,021 | - | 12,509,021 |
| 건물 | 18,919,833 | (1,452,900) | 17,466,933 | 18,919,833 | (1,334,666) | 17,585,167 |
| 차량운반구 | 247,042 | (181,794) | 65,248 | 243,312 | (172,569) | 70,743 |
| 공구와기구 | 2,798,685 | (1,115,858) | 1,682,827 | 3,501,562 | (1,753,479) | 1,748,083 |
| 비품 | 1,370,535 | (823,669) | 546,866 | 1,375,271 | (776,106) | 599,165 |
| 기계장치 | 17,838,698 | (7,777,062) | 10,061,636 | 17,529,178 | (7,467,348) | 10,061,830 |
| 기타유형자산 | 3,962,802 | (2,323,652) | 1,639,150 | 4,036,203 | (2,319,309) | 1,716,894 |
| 건설중인자산 | 381,600 | - | 381,600 | 393,600 | - | 393,600 |
| 합계 | 58,028,216 | (13,674,935) | 44,353,281 | 58,507,980 | (13,823,477) | 44,684,503 |
(주1) 손상차손누계액을 합산한 금액입니다.
9.2 유형자산의 변동 내역
<당분기>
| (단위: 천원) |
| 구분 | 기초 | 취득 및 자본적 지출 |
처분 및 폐기 | 감가상각비 | 대체 | 사업분할(주1) | 기말 |
|---|---|---|---|---|---|---|---|
| 토지 | 12,509,021 | - | - | - | - | - | 12,509,021 |
| 건물 | 17,585,167 | - | - | (118,234) | - | - | 17,466,933 |
| 구축물 | 67,846 | - | - | (2,475) | - | - | 65,371 |
| 차량운반구 | 70,743 | 3,730 | - | (9,225) | - | - | 65,248 |
| 공구와기구 | 1,748,083 | 67,050 | - | (132,292) | - | (14) | 1,682,827 |
| 비품 | 599,164 | 7,250 | - | (57,228) | - | (2,321) | 546,865 |
| 기계장치 | 10,061,830 | 103,670 | (17,871) | (316,493) | 230,500 | - | 10,061,636 |
| 시설장치 | 1,649,048 | 21,200 | - | (88,251) | - | (8,217) | 1,573,780 |
| 건설중인자산 | 393,600 | 218,500 | - | - | (230,500) | - | 381,600 |
| 합계 | 44,684,502 | 421,400 | (17,871) | (724,198) | - | (10,552) | 44,353,281 |
(주1) 당분기 중 에너지 사업부를 물적분할하였으며, 사업분할을 통해 승계한 금액입니다.
<전분기>
| (단위: 천원) |
| 구분 | 기초 | 취득 및 자본적 지출 |
처분 및 폐기 | 감가상각비 | 손상차손 | 대체 | 기타 | 기말 |
|---|---|---|---|---|---|---|---|---|
| 토지 | 17,681,413 | - | - | - | - | - | - | 17,681,413 |
| 건물 | 13,787,796 | 34,170 | - | (93,035) | - | 688,000 | - | 14,416,931 |
| 차량운반구 | 112,575 | - | (1) | (12,117) | - | - | - | 100,457 |
| 공구와기구 | 1,776,990 | - | - | (113,128) | - | - | - | 1,663,862 |
| 비품 | 791,177 | 12,468 | (20,742) | (57,095) | - | - | - | 725,808 |
| 기계장치 | 9,620,372 | - | (690,560) | (269,376) | 660,560 | - | - | 9,320,996 |
| 시설장치 | 1,972,932 | 25,000 | (41,383) | (84,290) | - | - | - | 1,872,259 |
| 임차점포시설물 | 251,459 | - | - | (58,029) | - | - | - | 193,430 |
| 건설중인자산 | 17,305,953 | 4,484,842 | - | - | - | (688,000) | 100,519 | 21,203,314 |
| 합계 | 63,300,667 | 4,556,480 | (752,686) | (687,070) | 660,560 | - | 100,519 | 67,178,470 |
9.3 당분기말 현재 유형자산 중 일부가 관련 부채에 대한 담보로 제공되어 있습니다(주석 21 참조).
9.4 당분기 중 차입원가를 자본화하여 건설중인자산으로 계상한 금액은 없습니다(전분기: 101백만원). 전분기 중 차입원가를 산정하기 위하여 사용된 차입금 자본화 이자율은 1.36% 입니다.
10. 투자부동산
10.1 투자부동산의 내역
| (단위: 천원) |
| 구분 | 당분기말 | 전기말 |
|---|---|---|
| 토지 | 872,436 | 872,436 |
| 건물 | 3,779,451 | 3,779,451 |
| 감가상각누계액 | (385,751) | (362,129) |
| 합계 | 4,266,136 | 4,289,758 |
11. 무형자산
11.1 무형자산의 내역
| (단위: 천원) |
| 구분 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|
| 원가 | 상각누계액(주1) | 장부금액 | 원가 | 상각누계액(주1) | 장부금액 | |
| 영업권 | 20,760,785 | (19,298,262) | 1,462,523 | 20,760,785 | (19,298,262) | 1,462,523 |
| 고객관계 | 3,708,850 | (1,608,576) | 2,100,274 | 3,708,850 | (1,508,563) | 2,200,287 |
| 회원권 | 2,214,238 | (9,986) | 2,204,252 | 2,214,238 | (9,986) | 2,204,252 |
| 소프트웨어 | 175,205 | (68,166) | 107,039 | 173,705 | (59,952) | 113,753 |
| 특허권 | 102,481 | (53,030) | 49,451 | 72,739 | (49,533) | 23,206 |
| 상표권 | 4,312 | (834) | 3,478 | 4,312 | (619) | 3,693 |
| 라이선스 | 34,771,257 | - | 34,771,257 | 34,693,787 | - | 34,693,787 |
| 디자인권 | 5,267 | (2,729) | 2,538 | 5,267 | (2,465) | 2,802 |
| 개발비 | 288,939 | (288,939) | - | 288,939 | (288,939) | - |
| 기타의무형자산 | 14,614 | (14,612) | 2 | 14,614 | (14,567) | 47 |
| 합계 | 62,045,948 | (21,345,134) | 40,700,814 | 61,937,236 | (21,232,886) | 40,704,350 |
(주1) 손상차손누계액을 합산한 금액입니다.
11.2 무형자산 변동 내역
<당분기>
| (단위: 천원) |
| 구분 | 기초 | 취득 및 자본적 지출 |
감가상각비 | 기말 |
|---|---|---|---|---|
| 영업권 | 1,462,523 | - | - | 1,462,523 |
| 고객관계 | 2,200,287 | - | (100,013) | 2,100,274 |
| 회원권 | 2,204,252 | - | - | 2,204,252 |
| 소프트웨어 | 113,753 | 1,500 | (8,214) | 107,039 |
| 특허권 | 23,206 | 29,742 | (3,497) | 49,451 |
| 상표권 | 3,693 | - | (215) | 3,478 |
| 라이선스 | 34,693,787 | 77,470 | - | 34,771,257 |
| 디자인권 | 2,802 | - | (264) | 2,538 |
| 기타의무형자산 | 47 | - | (45) | 2 |
| 합계 | 40,704,350 | 108,712 | (112,248) | 40,700,814 |
<전분기>
| (단위: 천원) |
| 구분 | 기초 | 취득 및 자본적 지출 |
감가상각비 | 기말 |
|---|---|---|---|---|
| 영업권 | 19,298,262 | - | - | 19,298,262 |
| 고객관계 | 7,324,461 | - | (281,710) | 7,042,751 |
| 회원권 | 2,857,252 | - | - | 2,857,252 |
| 소프트웨어 | 76,303 | - | (4,456) | 71,847 |
| 특허권 | 26,261 | 1,129 | (2,762) | 24,628 |
| 상표권 | - | 2,316 | (39) | 2,277 |
| 라이선스 | 34,693,787 | - | - | 34,693,787 |
| 디자인권 | 3,856 | - | (263) | 3,593 |
| 기타의무형자산 | 34,811 | - | (2,243) | 32,568 |
| 합계 | 64,314,993 | 3,445 | (291,473) | 64,026,965 |
12. 사용권자산 및 리스부채
12.1 사용권자산 및 리스부채의 변동내역
<당분기>
| (단위: 천원) |
| 구분 | 사용권자산 | 리스부채 | ||
|---|---|---|---|---|
| 건물 | 기타 | 합계 | ||
| 기초 | 61,762 | 612,608 | 674,370 | 691,304 |
| 취득 | - | - | - | - |
| 감가상각 | (92,283) | (52,604) | (144,887) | - |
| 리스부채의 상환 | - | - | - | (155,651) |
| 이자비용 | - | - | - | 14,038 |
| 리스변경 및 계약종료 등 | 2,858 | (47,590) | (44,732) | (44,560) |
| 사업분할(주1) | - | (12,827) | (12,827) | (15,385) |
| 기말 | (27,663) | 499,587 | 471,924 | 489,746 |
(주1) 당분기 중 에너지 사업부를 물적분할하였으며, 사업분할을 통해 승계한 금액입니다.
<전분기>
| (단위: 천원) |
| 구분 | 사용권자산 | 리스부채 | ||
|---|---|---|---|---|
| 건물 | 기타 | 합계 | ||
| 기초 | 1,287,075 | 499,168 | 1,786,243 | 2,442,585 |
| 취득 | 100,866 | 108,006 | 208,872 | 186,609 |
| 감가상각 | (57,936) | (300,636) | (358,572) | - |
| 리스부채의 상환 | - | - | - | (482,042) |
| 이자비용 | - | - | - | 55,569 |
| 리스변경 및 계약종료 등 | (90,998) | - | (90,998) | (86,058) |
| 기말 | 1,239,007 | 306,538 | 1,545,545 | 2,116,663 |
12.2 손익계산서에 인식된 금액
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 사용권자산상각비 | (144,887) | (358,572) |
| 리스료 - 단기 리스 | (75,141) | (103,960) |
| 리스료 - 소액 기초자산 리스 | (13,433) | (27,289) |
| 금융리스해지이익 | 8,253 | 2,065 |
| 금융리스해지손실 | (3,610) | - |
| 리스부채 이자비용 | (14,038) | (55,569) |
12.3 리스로 인한 현금유출액
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 리스부채의 지급 | 155,651 | 482,042 |
| 리스료 - 단기 리스 | 75,141 | 103,960 |
| 리스료 - 소액 기초자산 리스 | 13,433 | 27,289 |
| 합계 | 244,225 | 613,291 |
13. 차입금 및 사채
13.1 단기차입금의 내역
| (단위: 천원) |
| 구분 | 차입처 | 이자율(%) | 만기일 | 당분기말 | 전기말 |
|---|---|---|---|---|---|
| 시설자금 | 우리은행 | 5.96 | 2025-03-20 | 1,150,000 | 1,150,000 |
| 시설자금 | 국민은행 | 5.14 | 2024-08-16 | 5,000,000 | 5,000,000 |
| 시설자금 | 국민은행 | 5.14 | 2024-08-20 | 4,070,000 | 4,070,000 |
| 주식담보대출 | 한국투자증권 | 4.5 | 2025-01-30 | 20,000,000 | - |
| 소 계 | 30,220,000 | 10,220,000 | |||
| 차감 : 현재가치할인차금 | (334,074) | - | |||
| 차감잔액 | 29,885,926 | 10,220,000 | |||
13.2 장기차입금의 내역
| (단위: 천원) |
| 구분 | 차입처 | 이자율(%) | 만기일 | 당분기말 | 전기말 |
|---|---|---|---|---|---|
| 시설자금 | 국민은행 | 4.98 | 2025-01-16 | 1,560,000 | 1,560,000 |
| 시설자금 | 우리은행 | 5.36 | 2025-03-31 | 4,800,000 | 4,800,000 |
| 온렌딩대출 | 하나은행 | 4.96 | 2030-03-15 | 3,000,000 | 3,125,000 |
| 시설자금 | 산업은행 | 4.21 | 2032-01-17 | 10,000,000 | 10,000,000 |
| 시설자금 | 국민은행 | 4.83 | 2024-08-20 | 5,000,000 | 5,000,000 |
| 시설자금 | 국민은행 | 3.8 | 2024-09-30 | 1,560,000 | 1,560,000 |
| 소계 | 25,920,000 | 26,045,000 | |||
| 차감 : 유동성대체 | (13,420,000) | (7,060,000) | |||
| 차감잔액 | 12,500,000 | 18,985,000 | |||
13.3 전환사채의 내역
| (단위: 천원) |
| 차입내용 | 발행일 | 만기일 | 이자율(%) | 당분기말 | 전기말 |
|---|---|---|---|---|---|
| 제10회 무기명식 무보증 사모 전환사채 | 2022-07-01 | 2027-07-01 | - | - | 16,200,000 |
| 제11회 무기명식 무보증 사모 전환사채 | 2023-07-07 | 2028-07-07 | - | 8,300,000 | 8,300,000 |
| 제12회 무기명식 무보증 사모 전환사채 | 2023-11-07 | 2026-11-07 | 2.0 | 28,800,000 | 28,800,000 |
| 상환할증금 | 167,461 | 494,312 | |||
| 전환권조정 | (6,319,031) | (8,780,773) | |||
| 사채잔액 | 30,948,430 | 45,013,539 | |||
| 차감 : 유동성대체 | - | (15,158,535) | |||
| 차감잔액 | 30,948,430 | 29,855,004 | |||
(1) 전환사채의 주요 발행조건
| 구분 | 내용 |
|---|---|
| 사채의 명칭 | 제10회 무기명식 무보증 사모 전환사채 |
| 권면총액(주1) | 16,200,000,000 원 |
| 발행회사 | 에이치엘비생명과학㈜ |
| 발행가액 | 권면금액의 100% |
| 만기일 | 2027-07-01 |
| 보장수익률 | 1.00% |
| 유효이자율 | 17.41% |
| 원금상환방법 | 만기일시상환 - 사채만기일에 미행사 사채권면총액에 대하여는 원금의 105.1206%의 금액을 일시상환함 |
| 조기상환청구 (Put Option) | 발행일로부터 2년 경과 및 그 이후 3개월마다 조기상환청구가 가능함 |
| 매도청구권 (Call Option) (주2) | 발행회사 또는 제3자가 사채에 관하여 콜옵션 보유 |
| 전환가액 | 11,434원 |
| 조정 후 전환가능주식수(주3) | - |
| 행사(전환)에 따라 발행할 주식의 종류 | 에이치엘비생명과학㈜ 기명식 보통주 |
| 행사(전환청구)기간 | 2023년 07월 01일부터 2027년 06월 01일까지 |
| 신주의 배당기산일 | 행사일이 속하는 사업연도의 개시일 |
(주1) 회사는 제10회차 전환사채의 전환사채금 450억원의 일부인 288억원을 조기 상환함에 따라 조기 상환된 288억원 전액을 대환하여 제12회차 전환사채의 인수대금으로 납입을 결정하였습니다.
(주2) 회사는 전기 중 회사 또는 회사가 지정하는 제3자에게 매도청구권(Call Option)을 부여하는 조건의 제10회 무기명식 무보증 사모 전환사채를 발행하였습니다. 회사는 동 전환사채 발행시 매도청구권을 특수관계자인 에포케㈜에게 부여하였으며, 동 매도청구권과 관련하여 발행시 매도청구권의 공정가치 2,309,652천원을 파생상품거래손실로 인식하였습니다.
(주3) 당분기말 모두 전환되었습니다.
| 구분 | 내용 |
|---|---|
| 사채의 명칭 | 제11회 무기명식 무보증 사모 전환사채 |
| 권면총액 | 8,300,000,000 원 |
| 발행회사 | 에이치엘비생명과학㈜ |
| 발행가액 | 권면금액의 100% |
| 만기일 | 2028-07-07 |
| 보장수익률 | 1.00% |
| 유효이자율 | 16.72% |
| 원금상환방법 | 만기일시상환 - 사채만기일에 미행사 사채권면총액에 대하여는 원금의 105.1206%의 금액을 일시상환함 |
| 조기상환청구 (Put Option) | 발행일로부터 2년 경과 및 그 이후 3개월마다 조기상환청구가 가능함 |
| 전환가액 | 10,204원 |
| 조정 후 전환가능주식수 | 813,407주 |
| 행사(전환)에 따라 발행할 주식의 종류 | 에이치엘비생명과학㈜ 기명식 보통주 |
| 행사(전환청구)기간 | 2024년 07월 07일부터 2028년 06월 07일까지 |
| 신주의 배당기산일 | 행사일이 속하는 사업연도의 개시일 |
| 구분 | 내용 |
|---|---|
| 사채의 명칭 | 제12회 무기명식 무보증 사모 전환사채 |
| 권면총액 | 28,800,000,000 원 |
| 발행회사 | 에이치엘비생명과학㈜ |
| 발행가액 | 권면금액의 100% |
| 만기일 | 2026-11-07 |
| 보장수익률 | 2.00% |
| 유효이자율 | 16.40% |
| 원금상환방법 | 만기일시상환 - 사채만기일에 미행사 사채권면총액에 대하여는 원금의 100%의 금액을 일시상환함 |
| 조기상환청구 (Put Option) | 발행일로부터 1년 8개월 경과 및 그 이후 3개월마다 조기상환청구가 가능함 |
| 전환가액 | 9,586원 |
| 조정 후 전환가능주식수 | 3,004,381주 |
| 행사(전환)에 따라 발행할 주식의 종류 | 에이치엘비생명과학㈜ 기명식 보통주 |
| 행사(전환청구)기간 | 2024년 11월 07일부터 2026년 10월 07일까지 |
| 신주의 배당기산일 | 행사일이 속하는 사업연도의 개시일 |
13.4 신주인수권부사채의 내역
| (단위: 천원) |
| 차입내용 | 발행일 | 만기일 | 이자율(%) | 당분기말 | 전기말 |
|---|---|---|---|---|---|
| 제9회 무기명식 이권부 무보증 공모 분리형 신주인수권부사채 |
2022-06-15 | 2025-06-15 | - | 80,600,569 | 84,420,786 |
| 상환할증금 | 3,281,008 | 3,436,517 | |||
| 전환권조정 | (2,872,990) | (6,474,690) | |||
| 사채잔액 | 81,008,587 | 81,382,613 | |||
| 차감 : 유동성대체 | (81,008,587) | (81,382,613) | |||
| 차감잔액 | - | - | |||
(1) 신주인수권부사채의 주요 발행조건
| 구분 | 내용 |
|---|---|
| 사채의 명칭 | 제9회 무기명식 이권부 무보증 공모 분리형 신주인수권부사채 |
| 권면총액 | 100,000,000,000 원 |
| 발행회사 | 에이치엘비생명과학㈜ |
| 발행가액 | 권면금액의 100% |
| 만기일 | 2025-06-15 |
| 보장수익률 | 2.00% |
| 유효이자율 | 16.89% |
| 원금상환방법 | 만기일시상환 - 사채만기일에 미행사 사채권면총액에 대하여는 원금의 106.1677%의 금액을 일시상환함 |
| 조기상환청구(Put Option) | 발행일로부터 2년 경과 및 그 이후 3개월마다 조기상환청구가 가능함 |
| 행사가액(주1) | 8,889원 |
| 행사가능 주식수 | 3,813,744주 |
| 행사(전환)에 따라 발행할 주식의 종류 | 에이치엘비생명과학㈜ 기명식 보통주 |
| 행사(전환청구)기간 | 2022년 07월 15일부터 2025년 05월 15일까지 |
| 신주의 배당기산일 | 행사일이 속하는 사업연도의 개시일 |
14. 법인세비용
법인세비용은 당분기 중 발생한 이연법인세 미인식효과 등을 제외하였을 때 전체 회계연도에 대해서 예상되는 최선의 가중평균 연간 유효 법인세율의 추정에 기초하여 인식하였습니다.
15. 자본금 및 주식발행초과금
15.1 자본금의 내역
| (단위: 원, 주) |
| 구분 | 당분기말 | 전기말 |
|---|---|---|
| 회사가 발행할 주식의 총 수 | 300,000,000 | 300,000,000 |
| 1주당 금액 | 500 | 500 |
| 발행한 보통주식의 수 | 107,560,274 | 101,826,681 |
| 보통주자본금(주1) | 54,273,709,000 | 51,406,912,500 |
(주1) 전기 이전 상환청구된 947,136주의 상환전환우선주를 상환 후 이익소각함에 따라 총발행주식수의 액면총액이 보통주자본금과 일치하지 않습니다. 또한 에너지사업부 물적분할에 따른 주식매수청구권 40,008주를 자기주식으로 인식함에 따라 총발행주식수의 액면총액이 보통주자본금과 일치하지 않습니다.
15.2 납입자본금의 변동내역
| (단위: 천원, 주) |
| 구 분 | 유통주식수 | 자본금 | 주식발행초과금 |
|---|---|---|---|
| 전기초 | 96,714,952 | 48,831,044 | 181,375,479 |
| 이익잉여금 전입 | - | - | (60,000,000) |
| 신주인수권부사채 전환 | 21,822 | 10,911 | 175,718 |
| 전분기말 | 96,736,774 | 48,841,955 | 121,551,197 |
| 당기초 | 101,826,681 | 51,406,913 | 122,577,398 |
| 전환사채 전환 | 1,416,821 | 708,410 | 14,970,500 |
| 신주인수권부사채 전환 | 4,316,772 | 2,158,386 | 36,137,600 |
| 당분기말 | 107,560,274 | 54,273,709 | 173,685,498 |
16. 고객과의 계약에서 생기는 수익
16.1 수익으로 인식한 금액
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 고객과의 계약에서 생기는 수익 | 5,755,789 | 15,510,129 |
| 기타 원천으로부터의 수익 : 임대 수익 | 330,681 | 231,276 |
| 합계 | 6,086,470 | 15,741,405 |
16.2 고객과의 계약에서 생기는 수익의 구분
| (단위: 천원) |
| 구분 | 당분기 | 전분기 | |||||
|---|---|---|---|---|---|---|---|
| 메디케어 사업부 |
기타 | 합계 | 건설업 및 엔지니어링 |
메디케어 사업부 |
기타 | 합계 | |
| 주요 제품/용역 | |||||||
| 제품매출 | 4,059,993 | - | 4,059,993 | - | 9,269,614 | - | 9,269,614 |
| 건설매출 | - | - | - | 54,000 | - | - | 54,000 |
| 상품매출 | 1,601,801 | - | 1,601,801 | - | 6,045,572 | - | 6,045,572 |
| 용역매출 | - | 55,262 | 55,262 | - | - | 20,398 | 20,398 |
| 기타매출 | 24,272 | 14,461 | 38,733 | - | - | 120,545 | 120,545 |
| 합계 | 5,686,066 | 69,723 | 5,755,789 | 54,000 | 15,315,186 | 140,943 | 15,510,129 |
| 지리적시장 | |||||||
| 국내 | 5,662,383 | - | 5,662,383 | 54,000 | 15,275,070 | 140,943 | 15,470,013 |
| 기타 | 93,406 | - | 93,406 | - | 40,116 | - | 40,116 |
| 합계 | 5,755,789 | - | 5,755,789 | 54,000 | 15,315,186 | 140,943 | 15,510,129 |
| 수익인식 시기 | |||||||
| 한 시점에 인식 | 5,686,066 | 69,723 | 5,755,789 | - | 15,315,186 | 140,943 | 15,456,129 |
| 기간에 걸쳐 인식 | - | - | - | 54,000 | - | - | 54,000 |
| 합계 | 5,686,066 | 69,723 | 5,755,789 | 54,000 | 15,315,186 | 140,943 | 15,510,129 |
16.3 고객과의 계약과 관련된 자산과 부채
| (단위: 천원) |
| 구분 | 당분기말 | 전기말 |
|---|---|---|
| 계약자산 - 미청구공사 | 18,306 | 7,014 |
| 계약부채 - 하자보수충당부채 | - | 29,847 |
| 계약부채 - 환불부채 | 1,282 | 1,471 |
16.4 계약부채와 관련하여 인식한 수익
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 계약부채 - 환불부채 | 189 | 4,325 |
16.5 나머지 수행의무(이행되지 않거나 부분적으로 미이행된)에 배분된 거래가격
| (단위: 천원) |
| 구분 | 당분기 | 전기 |
|---|---|---|
| 1년 이내 | 1,282 | 1,471 |
17. 판매비와관리비
| (단위: 천원) |
| 구분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 3개월 | 누적 | 3개월 | 누적 | |
| 임직원급여 | 1,096,184 | 1,096,184 | 1,033,593 | 1,033,593 |
| 퇴직급여 | 167,658 | 167,658 | 182,601 | 182,601 |
| 복리후생비 | 194,362 | 194,362 | 151,627 | 151,627 |
| 여비교통비 | 22,782 | 22,782 | 20,244 | 20,244 |
| 접대비 | 48,229 | 48,229 | 42,361 | 42,361 |
| 통신비 | 3,637 | 3,637 | 3,960 | 3,960 |
| 세금과공과금 | 77,836 | 77,836 | 8,886 | 8,886 |
| 감가상각비 | 209,215 | 209,215 | 212,803 | 212,803 |
| 지급임차료 | 114,087 | 114,087 | 5,603 | 5,603 |
| 보험료 | 21,889 | 21,889 | 19,820 | 19,820 |
| 차량유지비 | 16,832 | 16,832 | 22,681 | 22,681 |
| 교육훈련비 | 5,062 | 5,062 | 425 | 425 |
| 도서인쇄비 | 1,396 | 1,396 | 1,664 | 1,664 |
| 협회비 | 6,300 | 6,300 | 7,877 | 7,877 |
| 소모품비 | 17,272 | 17,272 | 20,247 | 20,247 |
| 지급수수료 | 357,713 | 357,713 | 812,199 | 812,199 |
| 광고선전비 | 15,557 | 15,557 | 12,809 | 12,809 |
| 건물관리비 | 66,376 | 66,376 | 20,518 | 20,518 |
| 무형자산상각비 | 112,248 | 112,248 | 291,473 | 291,473 |
| 운반비 | 102,386 | 102,386 | 90,045 | 90,045 |
| 대손상각비(환입) | 6,009 | 6,009 | (73,234) | (73,234) |
| 경상연구개발비 | 10,297 | 10,297 | 182,904 | 182,904 |
| 합계 | 2,673,327 | 2,673,327 | 3,071,106 | 3,071,106 |
18. 비용의 성격별 분류
| (단위: 천원) |
| 구분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 3개월 | 누적 | 3개월 | 누적 | |
| 재고자산의 변동 | 79,766 | 79,766 | 3,151,454 | 3,151,454 |
| 원재료 및 상품매입액 | 2,264,888 | 2,264,888 | 2,139,821 | 2,139,821 |
| 급여 | 2,107,489 | 2,107,489 | 1,605,644 | 1,605,644 |
| 퇴직급여 | 69,780 | 69,780 | 265,761 | 265,761 |
| 복리후생비 | 383,654 | 383,654 | 272,670 | 272,670 |
| 여비교통비 | 34,322 | 34,322 | 32,533 | 32,533 |
| 접대비 | 48,767 | 48,767 | 42,360 | 42,360 |
| 통신비 | 4,081 | 4,081 | 4,581 | 4,581 |
| 세금과공과금 | 78,006 | 78,006 | 9,083 | 9,083 |
| 감가상각비 | 724,199 | 724,199 | 687,070 | 687,070 |
| 사용권자산상각비 | 144,887 | 144,887 | 358,572 | 358,572 |
| 투자부동산상각비 | 23,622 | 23,622 | 61,586 | 61,586 |
| 무형자산상각비 | 112,248 | 112,248 | 291,473 | 291,473 |
| 지급임차료 | 123,627 | 123,627 | 130,315 | 130,315 |
| 수도광열비 | 7,024 | 7,024 | 20,006 | 20,006 |
| 전력비 | 224,907 | 224,907 | 211,237 | 211,237 |
| 보험료 | 43,934 | 43,934 | 37,735 | 37,735 |
| 차량유지비 | 21,383 | 21,383 | 25,401 | 25,401 |
| 교육훈련비 | 5,360 | 5,360 | 620 | 620 |
| 도서인쇄비 | 3,978 | 3,978 | 1,749 | 1,749 |
| 협회비 | 6,300 | 6,300 | 7,877 | 7,877 |
| 소모품비 | 492,195 | 492,195 | 94,537 | 94,537 |
| 지급수수료 | 543,214 | 543,214 | 1,045,593 | 1,045,593 |
| 외주가공비 | 1,008,861 | 1,008,861 | 5,577,166 | 5,577,166 |
| 광고선전비 | 15,557 | 15,557 | 12,809 | 12,809 |
| 건물관리비 | 66,376 | 66,376 | 20,518 | 20,518 |
| 수선비 | 34,012 | 34,012 | 1,400 | 1,400 |
| 운반비 | 103,104 | 103,104 | 91,462 | 91,462 |
| 하자보수비 | - | - | 49 | 49 |
| 대손상각비 | 6,009 | 6,009 | (73,234) | (73,234) |
| 기타 | - | - | 171,054 | 171,054 |
| 합계 | 8,781,550 | 8,781,550 | 16,298,902 | 16,298,902 |
19. 현금흐름표
19.1 영업으로부터 창출된 현금
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 당분기순이익(손실) | 103,904,795 | 9,905,329 |
| 조정: | ||
| 법인세비용 | (363,250) | (965,801) |
| 이자비용 | 5,801,236 | 4,859,355 |
| 이자수익 | (171,007) | (324,268) |
| 감가상각비 | 724,199 | 687,070 |
| 투자부동산상각비 | 23,622 | 61,586 |
| 무형자산상각비 | 112,248 | 291,473 |
| 사용권자산상각비 | 144,887 | 358,572 |
| 외화환산손실 | 2,034 | 1,547 |
| 외화환산이익 | (4,158) | (2,008) |
| 대손상각비 | 6,009 | (73,234) |
| 기타의대손충당금환입 | - | (9,600) |
| 하자보수비 | - | 49 |
| 재고자산평가손실 | (452,883) | 514,593 |
| 당기손익-공정가치 측정 금융자산 평가이익 | (111,854,281) | (14,065,822) |
| 유형자산처분손실 | 13,871 | - |
| 유형자산폐기손실 | - | 54,009 |
| 유형자산처분이익 | - | (1,303) |
| 종속기업처분이익 | - | (15,248) |
| 파생상품평가이익 | (9,407) | - |
| 잡손실 | 3,630 | - |
| 잡이익 | (1,470) | - |
| 금융리스해지손실 | 3,609 | - |
| 금융리스해지이익 | (8,254) | (2,065) |
| 환불부채충당금환입 | (189) | - |
| 운전자본의 변동: | ||
| 매출채권 | (713,369) | 5,210,392 |
| 기타유동금융자산 | (356,165) | 258,077 |
| 재고자산 | 373,116 | 2,636,861 |
| 기타유동자산 | (107,393) | (974,552) |
| 매입채무 | 441,815 | (1,823,864) |
| 기타유동금융부채 | (1,446,024) | (2,165,542) |
| 기타유동부채 | (380,696) | 4,713 |
| 퇴직급여부채 | (4,504) | - |
| 합계 | (4,317,979) | 4,420,319 |
19.2 현금의 유입과 유출이 없는 거래 중 중요한 사항
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 건설중인자산의 본계정 대체 | 230,500 | 688,000 |
| 매출채권 및 기타금융자산의 제각 | 3,880 | - |
| 금융리스부채의 해지 | 51,028 | - |
| 퇴직급여의 전환 | 370,611 | - |
| 당기 취득 유형자산 미지급금 대체 | 55,110 | 1,393,920 |
| 당기 취득 무형자산 미지급금 대체 | 77,471 | - |
| 장기차입금의 유동성 대체 | 6,485,000 | 125,000 |
19.3 재무활동에서 생기는 부채의 변동
<당기>
| (단위: 천원) |
| 구분 | 기초 | 재무활동 현금흐름 |
상각 | 대체 | 전환 | 기타 | 사업분할 | 기말 |
|---|---|---|---|---|---|---|---|---|
| 리스부채 | 691,304 | (141,614) | - | - | - | (44,560) | (15,384) | 489,746 |
| 단기차입금 | 10,220,000 | 19,600,000 | 65,926 | - | - | - | - | 29,885,926 |
| 유동성장기차입금 | 7,060,000 | (125,000) | - | 6,485,000 | - | - | - | 13,420,000 |
| 장기차입금 | 18,985,000 | - | - | (6,485,000) | - | - | - | 12,500,000 |
| 전환사채 | 45,013,539 | - | 1,622,099 | - | (15,687,208) | - | - | 30,948,430 |
| 신주인수권부사채 | 81,382,614 | 34,551,569 | 3,409,126 | - | (38,334,722) | - | - | 81,008,587 |
<전분기>
| (단위: 천원) |
| 구분 | 기초 | 증가 | 재무활동 현금흐름 |
상각 | 대체 | 전환 | 기타 | 기말 |
|---|---|---|---|---|---|---|---|---|
| 단기차입금 | 7,920,000 | - | 650,000 | - | 1,560,000 | - | - | 10,130,000 |
| 유동성장기차입금 | 375,000 | - | - | - | 125,000 | - | - | 500,000 |
| 유동성금융리스부채 | 1,784,542 | 97,174 | (195,193) | 28,618 | (66,206) | - | - | 1,648,935 |
| 장기차입금 | 30,815,000 | - | - | - | (1,685,000) | - | - | 29,130,000 |
| 전환사채 | 35,423,163 | - | - | 1,542,226 | - | - | - | 36,965,389 |
| 신주인수권부사채 | 69,911,050 | - | 6,822 | 2,950,189 | - | (248,164) | 46,152 | 72,666,049 |
| 금융리스부채 | 658,042 | 89,435 | (286,849) | 26,951 | 66,206 | - | (86,057) | 467,728 |
20. 특수관계자
20.1 특수관계자 현황
| 구분 | 회사명 |
|---|---|
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ |
| 종속기업 | ㈜신화어드밴스 |
| 에이치엘비셀㈜ | |
| 에이치엘비엘이디㈜(주1) | |
| 에이치엘비솔루션㈜(주2) | |
| 에이치엘비에너지㈜ | |
| 에이치엘비생명과학R&D㈜ | |
| 관계기업 | 에이치엘비제약㈜ |
| 에이치벨류에셋(주3) | |
| ㈜두산포천에너지 | |
| 에이치엘비사이언스㈜ | |
| 에이치엘비인베스트먼트㈜ | |
| 기타의 특수관계자 | 에이치엘비글로벌㈜ |
| ㈜화진메디스 | |
| 에이치엘비일렉㈜ | |
| 에이치엘비아이 알밤 제1호 투자조합 | |
| 에이치엘비네트웍스㈜ | |
| Elevar Therapeutics, Inc. | |
| Immunomic Therapeutics, Inc. | |
| 에이치엘비바이오스텝㈜ | |
| ㈜펭귄오션레저 | |
| 에이치엘비생활건강㈜ | |
| ㈜프레시코 | |
| ㈜코아바이오 | |
| 에포케㈜ | |
| 에이치엘비테라퓨틱스㈜ | |
| ㈜킵코 | |
| 바다중공업㈜ | |
| 현대요트㈜ | |
| ㈜노터스 | |
| 에이치엘비에프앤비㈜ | |
| 에이치엘비파나진㈜ | |
| 브이에스팜㈜ | |
| 에이치엘비이노베이션㈜ | |
| 임직원 |
(주1) 전기 중 청산하였습니다.
(주2) 당분기 중 에너지 사업부를 물적분할하여 신규 편입되었습니다.
(주3) 당분기 중 HLB그룹 및 계열사 통합 사옥 마련을 위한 SPC 출자를 완료하여 신규로 편입되었습니다.
20.2 특수관계자와의 주요 거래내역
<당분기>
| (단위: 천원) |
| 구분 | 회사명 | 매출 등 | 매입 등 | ||
|---|---|---|---|---|---|
| 매출 | 이자수익 | 임차료 | 기타 | ||
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ | 128,971 | - | 31,460 | 30,466 |
| 종속기업 | 에이치엘비셀㈜ | 45,999 | - | - | 247,085 |
| 에이치엘비에너지㈜ | - | 16,967 | - | - | |
| 에이치엘비생명과학R&D㈜ | 65,917 | - | - | 114,141 | |
| 에이치엘비솔루션㈜ | 17,095 | - | - | - | |
| 소 계 | 129,011 | 16,967 | - | 361,226 | |
| 관계기업 | 에이치엘비제약㈜ | 8,924 | - | - | - |
| 에이치엘비사이언스㈜ | 6,913 | - | - | - | |
| 소 계 | 15,837 | - | - | - | |
| 기타의 특수관계자 | Elevar Therapeutics, Inc. | - | - | - | 54,604 |
| ㈜프레시코 | - | - | - | 291 | |
| 에이치엘비글로벌㈜ | 3,000 | - | - | - | |
| ㈜펭귄오션레져 | - | - | - | 4,252 | |
| 에이치엘비바이오스텝㈜ | 420 | - | - | - | |
| 에이치엘비에프앤비㈜ | - | - | - | 13,254 | |
| 임직원 | - | 376 | - | - | |
| 소 계 | 3,420 | 376 | - | 72,401 | |
| 합계 | 277,239 | 17,343 | 31,460 | 464,093 | |
<전분기>
| (단위: 천원) |
| 구분 | 회사명 | 매출 등 | 매입 등 | ||||
|---|---|---|---|---|---|---|---|
| 공사매출 | 임대매출 | 이자수익 | 기타 | 임차료 | 기타 | ||
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ | 54,000 | 84,300 | - | 36,936 | 57,510 | 27,604 |
| 종속기업 | 에이치엘비셀㈜ | - | 74,336 | 28,356 | 3,374 | - | 503,344 |
| 에이치엘비생명과학R&D㈜ | - | 58,110 | - | 20,398 | - | 41,153 | |
| 소 계 | - | 132,446 | 28,356 | 23,772 | - | 544,497 | |
| 관계기업 | 에이치엘비제약㈜ | - | 5,100 | - | 1,186 | - | - |
| 기타의 특수관계자 | Elevar Therapeutics, Inc. | - | - | - | - | - | 10,583 |
| Immunomic Therapeutics, Inc. | - | 1,330 | - | - | - | - | |
| 에이치엘비생활건강㈜ | - | - | - | - | - | 292 | |
| ㈜프레시코 | - | - | - | - | - | 2,751 | |
| 에이치엘비글로벌㈜ | - | - | - | 300 | - | - | |
| ㈜펭귄오션레져 | - | - | - | - | - | 634 | |
| 에이치엘비사이언스㈜ | - | 3,000 | - | 547 | - | - | |
| 임직원 | - | - | 530 | - | 10,200 | - | |
| 소 계 | - | 4,330 | 530 | 847 | 10,200 | 14,260 | |
| 합계 | 54,000 | 226,176 | 28,886 | 62,741 | 67,710 | 586,361 | |
20.3 특수관계자에 대한 채권ㆍ채무의 주요 내역
<당분기말>
| (단위: 천원) |
| 구분 | 회사명 | 채권 등 | 채무 등 | ||
|---|---|---|---|---|---|
| 기타채권 | 전환사채(주1) | 기타채무 | 신주인수권부사채(주2) | ||
| 유의적인 영향력을행사하는 기업 | 에이치엘비㈜ | 5,742 | - | 4,787 | 19,603,370 |
| 종속기업 | 에이치엘비에너지㈜ | 16,967 | - | - | - |
| 에이치엘비셀㈜ | 8,989 | - | 304,025 | - | |
| 에이치엘비솔루션㈜ | 18,275 | - | 8,000 | - | |
| 에이치엘비생명과학R&D㈜ | 44,652 | - | 235,791 | - | |
| 소 계 | 88,883 | - | 547,816 | - | |
| 관계기업 | 에이치엘비제약㈜ | 3,707 | - | 40,000 | - |
| ㈜두산포천에너지(주3) | 505,804 | - | - | - | |
| 에이치엘비사이언스㈜ | 658 | - | 25,000 | - | |
| 소 계 | 510,169 | - | 65,000 | - | |
| 기타의 특수관계자 | 에이치엘비테라퓨틱스㈜ | - | - | 8,300,000 | - |
| Elevar Therapeutics, Inc. | - | - | 87,640 | - | |
| ㈜프레시코 | - | - | 320 | - | |
| 에이치엘비글로벌㈜ | 1,100 | - | - | - | |
| 에이치엘비바이오스텝㈜ | 139 | 10,242,854 | - | - | |
| 임직원 | 16,000 | - | - | - | |
| 소 계 | 17,239 | 10,242,854 | 8,387,960 | - | |
| 합계 | 622,033 | 10,242,854 | 9,005,563 | 19,603,370 | |
(주1) 공정가치평가 후 금액입니다.
(주2) 신주인수권부사채 채무 잔액은 액면금액입니다.
(주3) 회사는 해당 대여금에 대하여 전액 대손충당금을 설정하였습니다.
<전기말>
| (단위: 천원) |
| 구분 | 회사명 | 채권 등 | 채무 등 | ||
|---|---|---|---|---|---|
| 기타채권 | 전환사채(주1) | 기타채무 | 신주인수권부사채(주2) | ||
| 유의적인 영향력을행사하는 기업 | 에이치엘비㈜ | 239,319 | - | 793,321 | 19,603,370 |
| 종속기업 | ㈜신화어드밴스 | 4,824 | - | - | - |
| 에이치엘비셀㈜ | 16,435 | - | 586,345 | - | |
| 에이치엘비에너지㈜ | 3,249 | - | 15,000 | - | |
| 에이치엘비생명과학R&D㈜ | 91,314 | - | 210,631 | - | |
| 소 계 | 115,822 | - | 811,976 | - | |
| 관계기업 | 에이치엘비제약㈜ | 29,784 | - | 46,810 | - |
| ㈜두산포천에너지(주3) | 505,804 | - | - | - | |
| 에이치엘비사이언스㈜ | 1,163 | - | 13,143 | - | |
| 소 계 | 536,751 | - | 59,953 | - | |
| 기타의 특수관계자 | 에이치엘비테라퓨틱스㈜ | 36,919 | - | 8,311,961 | - |
| Elevar Therapeutics, Inc. | - | - | 369,693 | - | |
| 에이치엘비생활건강㈜ | 484 | - | - | - | |
| ㈜프레시코 | 4,967 | - | - | - | |
| 에이치엘비글로벌㈜ | 19,917 | - | - | - | |
| 바다중공업㈜ | 4,933 | - | - | - | |
| 에이치엘비바이오스텝㈜ | 30,940 | 10,815,389 | - | - | |
| 에이치엘비에프앤비㈜ | 16,151 | - | - | - | |
| 현대요트㈜ | 1,327 | - | - | - | |
| ㈜코아바이오 | 2,578 | - | - | - | |
| 에이치엘비네트웍스㈜ | 2,016 | - | 19,032 | - | |
| 에포케㈜ | 3,974 | - | 10,536 | - | |
| 에이치엘비파나진㈜ | 2,736 | - | - | - | |
| 에이치엘비이노베이션㈜ | 14,391 | - | - | - | |
| 에이치엘비인베스트먼트㈜ | 1,702 | - | - | - | |
| ㈜펭귄오션레져 | 182 | - | - | - | |
| 임직원 | 25,000 | - | - | - | |
| 소 계 | 168,217 | 10,815,389 | 8,711,222 | - | |
| 합계 | 1,060,109 | 10,815,389 | 10,376,472 | 19,603,370 | |
(주1) 공정가치평가 후 금액입니다.
(주2) 신주인수권부사채 채무 잔액은 액면금액입니다.
(주3) 회사는 해당 대여금에 대하여 전액 대손충당금을 설정하였습니다.
20.4 특수관계자와의 자금거래 내역
<당분기>
| (단위: 천원) |
| 구분 | 회사명 | 자금 대여(차입) 거래 | 유상증자 | 현금 출자 등 | |
|---|---|---|---|---|---|
| 대여(차입) | 회수(상환) | ||||
| 종속기업 | 에이치엘비솔루션㈜(주1) | - | - | - | 1,200,000 |
| 에이치엘비에너지㈜ | 5,000,000 | - | - | - | |
| 에이치엘비생명과학R&D㈜ | - | - | 3,000,000 | - | |
| 소계 | 5,000,000 | - | 3,000,000 | 1,200,000 | |
| 관계기업 | 에이치벨류에셋(주2) | - | - | - | 5,000,000 |
| 기타의 특수관계자 | 에이치엘비아이알밤제1호투자조합 | - | - | - | 800,000 |
| 임직원 | - | 1,500 | - | - | |
| 소계 | - | 1,500 | - | 800,000 | |
| 합계 | 5,000,000 | 1,500 | 3,000,000 | 7,000,000 | |
(주1) 당분기 에너지 사업부를 물적분할하여 보통주 40,000주를 취득하였습니다.
(주2) 당분기 중 보통주 6억, 상환우선주 44억을 출자하였습니다.
<전분기>
| (단위: 천원) |
| 구분 | 회사명 | 자금 대여(차입) | 리스부채 | 유상증자 | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 기초 | 회수(상환) | 기타 | 기말 | 기초 | 이자비용 | 상환 | 기말 | |||
| 유의적인 영향력을 행사하는 기업 |
에이치엘비㈜ | - | - | - | - | 393,837 | 9,077 | (64,200) | 338,714 | - |
| 종속기업 | 에이치엘비셀㈜ | 2,500,000 | - | - | 2,500,000 | - | - | - | - | - |
| 에이치엘비엘이디㈜ | 1,038,000 | - | (1,038,000) | - | - | - | - | - | - | |
| 에이치엘비에너지㈜ | - | - | - | - | - | - | - | - | - | |
| 에이치엘비생명과학R&D㈜ | - | - | - | - | - | - | - | - | - | |
| 소계 | 3,538,000 | - | (1,038,000) | 2,500,000 | - | - | - | - | - | |
| 관계기업 | ㈜두산포천에너지 | 505,804 | - | - | 505,804 | - | - | - | - | - |
| 에이치엘비사이언스㈜ | - | - | - | - | - | - | - | - | - | |
| 소계 | 505,804 | - | - | 505,804 | - | - | - | - | - | |
| 기타의 특수관계자 | 임직원 | 33,084 | (2,750) | - | 30,334 | - | - | - | - | - |
| 에이치엘비이노베이션㈜(주1) | - | - | - | - | - | - | - | - | 1,999,999 | |
| 소계 | 33,084 | (2,750) | - | 30,334 | - | - | - | - | 1,999,999 | |
| 합계 | 4,076,888 | (2,750) | (1,038,000) | 3,036,138 | 393,837 | 9,077 | (64,200) | 338,714 | 1,999,999 | |
(주1) 전분기 중 에이치엘비이노베이션㈜(구. 피에스엠씨)의 신주를 취득하였습니다.
20.5 주요 경영진에 대한 보상
회사는 기업 활동의 계획ㆍ운영ㆍ통제에 대하여 중요한 권한과 책임을 가진 등기임원, 비등기임원, 내부감사 책임자 및 각 사업부문장 등을 주요 경영진으로 판단하였으며, 당기 및 전기 중 주요 경영진에 대한 보상을 위해 지급한 금액은 다음과 같습니다.
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 단기종업원급여 | 473,993 | 458,392 |
| 퇴직급여 | 79,423 | 67,193 |
| 합계 | 553,416 | 525,585 |
20.6 특수관계자와의 기타 유의적인 거래 및 약정사항
(1) 회사는 전기 중 제9회 무기명식 무보증 공모 분리형 신주인수권부사채를 발행하였으며, 회사에 유의적인 영향력을 행사하는 회사인 에이치엘비㈜가 공모에 참여하여 액면가 기준 19,603,370천원을 취득하였습니다. 동 신주인수권부사의 사채권자는 발행일(2022년 6월 15일)부터 24개월이 경과하는 날(2024년 6월 15일)부터 신주인수권부사채의 만기일까지 신주인수권부사채의 조기상환을 청구할 수 있는 권리를 보유하고 있습니다.
(2) 회사는 전기 중 회사 또는 회사가 지정하는 제3자에게 매도청구권(Call Option)을부여하는 조건의 제10회 무기명식 무보증 사모 전환사채를 발행하였습니다. 회사는동 전환사채 발행시 매도청구권을 특수관계자인 에포케㈜에게 부여하였으며, 동 매도청구권과 관련하여 발행시 매도청구권의 공정가치 2,309,652천원을 파생상품거래손실로 인식하였습니다.
21. 우발사항 및 약정사항
21.1 금융기관과 체결하고 있는 약정사항
| (단위: 천원) |
| 금융기관명 | 차입종별 | 당분기말 | 전기말 | ||
|---|---|---|---|---|---|
| 약정금액 | 실행금액 | 약정금액 | 실행금액 | ||
| 하나은행 | 기업시설자금대출 | 3,500,000 | 3,000,000 | 3,500,000 | 3,125,000 |
| 국민은행 | 시설자금 대출 | 17,190,000 | 17,190,000 | 17,190,000 | 17,190,000 |
| 우리은행 | 기업운전일반자금대출 | 1,150,000 | 1,150,000 | 1,150,000 | 1,150,000 |
| 우리은행 | 시설자금 대출 | 4,800,000 | 4,800,000 | 4,800,000 | 4,800,000 |
| 산업은행 | 시설자금 대출 | 10,000,000 | 10,000,000 | 10,000,000 | 10,000,000 |
| 한국투자증권 | 주식담보대출 | 20,000,000 | 20,000,000 | - | - |
| 합계 | 56,640,000 | 56,140,000 | 36,640,000 | 36,265,000 | |
21.2 담보제공내역
| (단위: 천원) |
| 구분 | 장부가액 | 담보설정액 | 관련계정 | 관련금액 | 제공처 |
|---|---|---|---|---|---|
| 토지 및 건물 | 4,768,018 | 4,200,000 | 차입금 | 3,000,000 | 하나은행 |
| 토지 및 건물 | 15,560,511 | 10,884,000 | 차입금 | 9,070,000 | 국민은행 |
| 토지 및 건물 | 24,285,155 | 9,744,000 | 차입금 | 8,120,000 | 국민은행 |
| 토지 및 건물 | 955,260 | 3,222,000 | 차입금 | 1,150,000 | 우리은행 |
| 토지 및 건물 | 11,609,857 | 5,760,000 | 차입금 | 4,800,000 | 우리은행 |
| 토지 및 건물 | 14,360,238 | 12,000,000 | 차입금 | 10,000,000 | 산업은행 |
| 주식 | 203,414,824 | 20,000,000 | 차입금 | 20,000,000 | 한국투자증권 |
| 합 계 | 274,953,863 | 65,810,000 | 56,140,000 |
21.3 전기 중 에이치엘비에너지㈜의 소각로 증축과 관련하여 기업은행으로부터 차입한 차입금에 대한 60억원 후순위 담보제공과 48억원 지급보증을 제공하였습니다.
21.4 계류중인 중요한 소송사건
(1) 회사가 피고인 사건
| (단위: 천원) |
| 원고 | 계류 법원 | 소송 금액 | 소송 내용 | 진행 상황 |
|---|---|---|---|---|
| 현대로오텍 | 광주지방법원 | 1,458,874 | 공사대금 청구 | 소송절차로 이행 |
| 주원전력 | 전주지방법원 | 883,872 | 공사대금 청구 | 소송절차로 이행 |
(2) 회사가 원고인 사건
| (단위: 천원) |
| 피고 | 계류 법원 | 소송 금액 | 소송 내용 | 진행 상황 |
|---|---|---|---|---|
| 엔에이치투자증권㈜(주1) | 서울남부지방법원 | 10,000,000 | 부당이득금반환청구 | 1심 진행중 |
| 박승규 (탑스코리아)(주2) | 수원지방법원 | 55,000 | 명도소송 | 판결선고 |
(주1) 회사가 펀드투자를 위해 엔에이치투자증권㈜에 최초 예치한 금액이나. 사기적 부정거래행위 및 불완전판매 요소가 발견되어 부당이득금 반환 청구소송을 진행 중입니다. 회사의 등기임원은 본 사건과관련하여 발생가능한 손실을 보전하기 위하여 회사의 등기임원이 보유한 에이치엘비㈜의 주식을 법무법인에 위탁하는 계약을 체결하였습니다.
(주2) 회사는 본 사건의 판결에 대해 2024년 1월 18일자로 승소하여 판결 확정되었습니다.
※ 기존 당사 원고, 피고 엘케이쏠라테크 공사대금 청구관련 소송 진행 중 이였으나, 2024년 1월 1일 당사 에너지사업부 회사분할하여 종속회사인 HLB솔루션으로 관련 소송 승계되어 소송 진행중입니다. 해당 사건은 현재 공사대금 채권 가압류 이의 신청 심문종결 후 소송비용액확정 사건으로 2024년 3월 18일에 일부인용 결정 되었습니다.
당분기말 현재 계류중인 소송사건에 대해서는 소송의 결과를 합리적으로 예측할 수 없으며, 보고기간 후 발생한 중요한 소송사건은 없습니다.
21.5 회사는 중국의 항서제약으로 부터 EGFR, HER2, HER4를 특이적으로 억제하는표적항암제와 관련하여 파이로티닙의 한국 독점 라이센스를 2020년 9월에 22.1억원을지급하고 획득하였습니다. 이와 관련하여 적응증 승인 및 확대와 관련 완제품의 판매로 인한 수익 발생 시 기술이전대가의 일정비율을 항서제약에 지급해야 하는 약정을 맺고 있습니다.
21.6 회사는 Elevar Therapeutics, lnc.와 리보세라닙의 한국내 독점개발, 판매권 및 유럽, 일본에 대한 수익 지분을 무형자산으로 인식하였습니다. 이와 관련하여 회사는 FDA(정식명칭 기재)의 승인 및 리보세라닙의 적응증 범위 확대 및 관련 완제품 판매로 인한 수익 발생 시 판매액의 일정비율을 Elevar Therapeutics, lnc.에 지급해야 하는 약정을 맺고 있습니다.
21.7 회사는 2019년 LSK BioPartners, Inc.주식 325,010주(보유주식 전량)를 처분하고, Earn-out 조건으로 LSK BioPartners, Inc.에서 진행 중인 리보세라닙의 최초 암 적응증에 대해 NDA 신청시점 및 NDA 승인시점에 각 USD 3,893,151.12씩 총USD 7,786,302.24을 추가로 지급받을수 있는 약정을 체결하였습니다. 회사는 전기 중 LSK BioPartners, Inc.에서 간암3차치료제의 NDA 신청이 완료됨에 따라 USD 3,893,151.12를 수령하였습니다.
22. 매각예정비유동자산
| (단위: 천원) |
| 구분 | 금액 |
|---|---|
| 투자부동산(건물) | 25,526,489 |
| 투자부동산(토지) | 22,056,334 |
| 합계 | 47,582,823 |
6. 배당에 관한 사항
주요배당지표
| 구 분 | 주식의 종류 | 당기 | 전기 | 전전기 |
|---|---|---|---|---|
| 제27기 당분기 | 제26기 | 제25기 | ||
| 주당액면가액(원) | 500 | 500 | 500 | |
| (연결)당기순이익(백만원) | 145,390 | -5,913 | -54,359 | |
| (별도)당기순이익(백만원) | 103,905 | -13,810 | -57,604 | |
| (연결)주당순이익(원) | 1,394 | -58 | -565 | |
| 현금배당금총액(백만원) | - | - | - | |
| 주식배당금총액(백만원) | - | - | 2,500 | |
| (연결)현금배당성향(%) | - | - | - | |
| 현금배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주식배당수익률(%) | - | - | - | -0.63 |
| - | - | - | - | |
| 주당 현금배당금(원) | - | - | - | - |
| - | - | - | - | |
| 주당 주식배당(주) | 보통주 | - | - | 0.0516983 |
| - | - | - | - | |
과거 배당 이력
| (단위: 회, %) |
| 연속 배당횟수 | 평균 배당수익률 | ||
|---|---|---|---|
| 분기(중간)배당 | 결산배당 | 최근 3년간 | 최근 5년간 |
| - | - | -0.21 | -0.13 |
7. 증권의 발행을 통한 자금조달에 관한 사항
7-1. 증권의 발행을 통한 자금조달 실적
| [지분증권의 발행 등과 관련된 사항] |
가. 증자(감자)현황
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 원, 주) |
| 주식발행 (감소)일자 |
발행(감소) 형태 |
발행(감소)한 주식의 내용 | ||||
|---|---|---|---|---|---|---|
| 종류 | 수량 | 주당 액면가액 |
주당발행 (감소)가액 |
비고 | ||
| 2022.07.15 | 신주인수권행사 | 보통주 | 348,300 | 500 | 11,925 | - |
| 2022.07.18 | 신주인수권행사 | 보통주 | 181,414 | 500 | 11,925 | - |
| 2022.07.19 | 신주인수권행사 | 보통주 | 93,417 | 500 | 11,925 | - |
| 2022.07.20 | 신주인수권행사 | 보통주 | 73,398 | 500 | 11,925 | - |
| 2022.07.21 | 신주인수권행사 | 보통주 | 29,912 | 500 | 11,925 | - |
| 2022.07.22 | 신주인수권행사 | 보통주 | 25,254 | 500 | 11,925 | - |
| 2022.07.25 | 신주인수권행사 | 보통주 | 7,622 | 500 | 11,925 | - |
| 2022.07.26 | 신주인수권행사 | 보통주 | 14,559 | 500 | 11,925 | - |
| 2022.07.27 | 신주인수권행사 | 보통주 | 10,102 | 500 | 11,925 | - |
| 2022.07.28 | 신주인수권행사 | 보통주 | 18,125 | 500 | 11,925 | - |
| 2022.07.29 | 신주인수권행사 | 보통주 | 23,405 | 500 | 11,925 | - |
| 2022.08.01 | 신주인수권행사 | 보통주 | 16,876 | 500 | 11,925 | - |
| 2022.08.02 | 신주인수권행사 | 보통주 | 11,778 | 500 | 11,925 | - |
| 2022.08.03 | 신주인수권행사 | 보통주 | 9,591 | 500 | 11,925 | - |
| 2022.08.04 | 신주인수권행사 | 보통주 | 31,122 | 500 | 11,925 | - |
| 2022.08.05 | 신주인수권행사 | 보통주 | 34,892 | 500 | 11,925 | - |
| 2022.08.08 | 신주인수권행사 | 보통주 | 20,970 | 500 | 11,925 | - |
| 2022.08.09 | 신주인수권행사 | 보통주 | 27,979 | 500 | 11,925 | - |
| 2022.08.10 | 신주인수권행사 | 보통주 | 20,332 | 500 | 11,925 | - |
| 2022.08.11 | 신주인수권행사 | 보통주 | 13,919 | 500 | 11,925 | - |
| 2022.08.12 | 신주인수권행사 | 보통주 | 11,825 | 500 | 11,925 | - |
| 2022.08.16 | 신주인수권행사 | 보통주 | 5,803 | 500 | 11,925 | - |
| 2022.08.17 | 신주인수권행사 | 보통주 | 2,932 | 500 | 11,925 | - |
| 2022.08.18 | 신주인수권행사 | 보통주 | 6,357 | 500 | 11,925 | - |
| 2022.08.19 | 신주인수권행사 | 보통주 | 6,494 | 500 | 11,925 | - |
| 2022.08.22 | 신주인수권행사 | 보통주 | 8,270 | 500 | 11,925 | - |
| 2022.08.23 | 신주인수권행사 | 보통주 | 9,501 | 500 | 11,925 | - |
| 2022.08.24 | 신주인수권행사 | 보통주 | 5,141 | 500 | 11,925 | - |
| 2022.08.25 | 신주인수권행사 | 보통주 | 11,573 | 500 | 11,925 | - |
| 2022.08.26 | 신주인수권행사 | 보통주 | 12,237 | 500 | 11,925 | - |
| 2022.08.29 | 신주인수권행사 | 보통주 | 3,790 | 500 | 11,925 | - |
| 2022.08.30 | 신주인수권행사 | 보통주 | 2,714 | 500 | 11,925 | - |
| 2022.08.31 | 신주인수권행사 | 보통주 | 2,406 | 500 | 11,925 | - |
| 2022.09.01 | 신주인수권행사 | 보통주 | 4,541 | 500 | 11,925 | - |
| 2022.09.02 | 신주인수권행사 | 보통주 | 1,878 | 500 | 11,925 | - |
| 2022.09.05 | 신주인수권행사 | 보통주 | 2,243 | 500 | 11,925 | - |
| 2022.09.06 | 신주인수권행사 | 보통주 | 1,533 | 500 | 11,925 | - |
| 2022.09.07 | 신주인수권행사 | 보통주 | 1,004 | 500 | 11,925 | - |
| 2022.09.08 | 신주인수권행사 | 보통주 | 2,093 | 500 | 11,925 | - |
| 2022.09.13 | 신주인수권행사 | 보통주 | 11,982 | 500 | 11,925 | - |
| 2022.09.14 | 신주인수권행사 | 보통주 | 10,852 | 500 | 11,925 | - |
| 2022.09.15 | 신주인수권행사 | 보통주 | 712 | 500 | 11,925 | - |
| 2022.09.16 | 신주인수권행사 | 보통주 | 10,572 | 500 | 11,925 | - |
| 2022.09.19 | 신주인수권행사 | 보통주 | 2,002 | 500 | 11,925 | - |
| 2022.09.20 | 신주인수권행사 | 보통주 | 2,983 | 500 | 11,925 | - |
| 2022.09.21 | 신주인수권행사 | 보통주 | 3,089 | 500 | 11,925 | - |
| 2022.09.22 | 신주인수권행사 | 보통주 | 674 | 500 | 11,925 | - |
| 2022.09.23 | 신주인수권행사 | 보통주 | 2,084 | 500 | 11,925 | - |
| 2022.09.26 | 신주인수권행사 | 보통주 | 1,323 | 500 | 11,925 | - |
| 2022.09.27 | 신주인수권행사 | 보통주 | 610 | 500 | 11,925 | - |
| 2022.09.28 | 신주인수권행사 | 보통주 | 477 | 500 | 11,925 | - |
| 2022.09.29 | 신주인수권행사 | 보통주 | 451 | 500 | 11,925 | - |
| 2022.09.30 | 신주인수권행사 | 보통주 | 84 | 500 | 11,925 | - |
| 2022.10.04 | 신주인수권행사 | 보통주 | 1,113 | 500 | 11,925 | - |
| 2022.10.05 | 신주인수권행사 | 보통주 | 2,053 | 500 | 11,925 | - |
| 2022.10.06 | 신주인수권행사 | 보통주 | 423 | 500 | 11,925 | - |
| 2022.10.07 | 신주인수권행사 | 보통주 | 730 | 500 | 11,925 | - |
| 2022.10.11 | 신주인수권행사 | 보통주 | 13 | 500 | 11,925 | - |
| 2022.10.12 | 신주인수권행사 | 보통주 | 976 | 500 | 11,925 | - |
| 2022.10.13 | 신주인수권행사 | 보통주 | 51 | 500 | 11,925 | - |
| 2022.10.14 | 신주인수권행사 | 보통주 | 296 | 500 | 11,925 | - |
| 2022.10.17 | 신주인수권행사 | 보통주 | 147 | 500 | 11,925 | - |
| 2022.10.18 | 신주인수권행사 | 보통주 | 282 | 500 | 11,925 | - |
| 2022.10.19 | 신주인수권행사 | 보통주 | 29 | 500 | 11,925 | - |
| 2022.10.20 | 신주인수권행사 | 보통주 | 21 | 500 | 11,925 | - |
| 2022.10.24 | 신주인수권행사 | 보통주 | 1,082 | 500 | 11,925 | - |
| 2022.10.25 | 신주인수권행사 | 보통주 | 48 | 500 | 11,925 | - |
| 2022.10.26 | 신주인수권행사 | 보통주 | 426 | 500 | 11,925 | - |
| 2022.10.27 | 신주인수권행사 | 보통주 | 122 | 500 | 11,925 | - |
| 2022.10.28 | 신주인수권행사 | 보통주 | 543 | 500 | 11,925 | - |
| 2022.10.31 | 신주인수권행사 | 보통주 | 1,040 | 500 | 11,925 | - |
| 2022.11.01 | 신주인수권행사 | 보통주 | 511 | 500 | 11,925 | - |
| 2022.11.02 | 신주인수권행사 | 보통주 | 15 | 500 | 11,925 | - |
| 2022.11.03 | 신주인수권행사 | 보통주 | 23 | 500 | 11,925 | - |
| 2022.11.04 | 신주인수권행사 | 보통주 | 1,199 | 500 | 11,925 | - |
| 2022.11.08 | 신주인수권행사 | 보통주 | 1,860 | 500 | 11,925 | - |
| 2022.11.09 | 신주인수권행사 | 보통주 | 97 | 500 | 11,925 | - |
| 2022.11.10 | 신주인수권행사 | 보통주 | 962 | 500 | 11,925 | - |
| 2022.11.11 | 신주인수권행사 | 보통주 | 596 | 500 | 11,925 | - |
| 2022.11.14 | 신주인수권행사 | 보통주 | 9 | 500 | 11,925 | - |
| 2022.11.15 | 신주인수권행사 | 보통주 | 319 | 500 | 11,925 | - |
| 2022.11.16 | 신주인수권행사 | 보통주 | 2,063 | 500 | 11,925 | - |
| 2022.11.17 | 신주인수권행사 | 보통주 | 477 | 500 | 11,925 | - |
| 2022.11.18 | 신주인수권행사 | 보통주 | 217 | 500 | 11,925 | - |
| 2022.11.21 | 신주인수권행사 | 보통주 | 58 | 500 | 11,925 | - |
| 2022.11.22 | 신주인수권행사 | 보통주 | 14 | 500 | 11,925 | - |
| 2022.11.23 | 신주인수권행사 | 보통주 | 122 | 500 | 11,925 | - |
| 2022.11.24 | 신주인수권행사 | 보통주 | 240 | 500 | 11,925 | - |
| 2022.11.25 | 신주인수권행사 | 보통주 | 1,264 | 500 | 11,925 | - |
| 2022.11.28 | 신주인수권행사 | 보통주 | 1,247 | 500 | 11,925 | - |
| 2022.11.29 | 신주인수권행사 | 보통주 | 324 | 500 | 11,925 | - |
| 2022.11.30 | 신주인수권행사 | 보통주 | 1,979 | 500 | 11,925 | - |
| 2022.12.01 | 신주인수권행사 | 보통주 | 1,171 | 500 | 11,925 | - |
| 2022.12.02 | 신주인수권행사 | 보통주 | 274 | 500 | 11,925 | - |
| 2022.12.06 | 신주인수권행사 | 보통주 | 39 | 500 | 11,925 | - |
| 2022.12.08 | 신주인수권행사 | 보통주 | 144 | 500 | 11,925 | - |
| 2022.12.09 | 신주인수권행사 | 보통주 | 701 | 500 | 11,925 | - |
| 2022.12.15 | 신주인수권행사 | 보통주 | 112 | 500 | 11,104 | - |
| 2022.12.16 | 신주인수권행사 | 보통주 | 8,188 | 500 | 11,104 | - |
| 2022.12.19 | 신주인수권행사 | 보통주 | 7,634 | 500 | 11,104 | - |
| 2022.12.20 | 신주인수권행사 | 보통주 | 1,000 | 500 | 11,104 | - |
| 2022.12.21 | 신주인수권행사 | 보통주 | 2,453 | 500 | 11,104 | - |
| 2022.12.22 | 신주인수권행사 | 보통주 | 1,310 | 500 | 11,104 | - |
| 2022.12.23 | 신주인수권행사 | 보통주 | 1,429 | 500 | 11,104 | - |
| 2022.12.26 | 신주인수권행사 | 보통주 | 1,526 | 500 | 11,104 | - |
| 2022.12.27 | 신주인수권행사 | 보통주 | 4,503 | 500 | 11,104 | - |
| 2022.12.28 | 신주인수권행사 | 보통주 | 199 | 500 | 11,104 | - |
| 2023.01.02 | 신주인수권행사 | 보통주 | 8 | 500 | 11,104 | - |
| 2023.01.04 | 신주인수권행사 | 보통주 | 211 | 500 | 11,104 | - |
| 2023.01.05 | 신주인수권행사 | 보통주 | 21 | 500 | 11,104 | - |
| 2023.01.09 | 신주인수권행사 | 보통주 | 224 | 500 | 11,104 | - |
| 2023.01.10 | 신주인수권행사 | 보통주 | 140 | 500 | 11,104 | - |
| 2023.01.11 | 신주인수권행사 | 보통주 | 782 | 500 | 11,104 | - |
| 2023.01.12 | 신주인수권행사 | 보통주 | 291 | 500 | 11,104 | - |
| 2023.01.13 | 신주인수권행사 | 보통주 | 9 | 500 | 11,104 | - |
| 2023.01.16 | 신주인수권행사 | 보통주 | 153 | 500 | 11,104 | - |
| 2023.01.18 | 신주인수권행사 | 보통주 | 560 | 500 | 11,104 | - |
| 2023.01.19 | 신주인수권행사 | 보통주 | 10 | 500 | 11,104 | - |
| 2023.01.25 | 신주인수권행사 | 보통주 | 46 | 500 | 11,104 | - |
| 2023.01.27 | 신주인수권행사 | 보통주 | 729 | 500 | 11,104 | - |
| 2023.01.30 | 신주인수권행사 | 보통주 | 183 | 500 | 11,104 | - |
| 2023.02.01 | 신주인수권행사 | 보통주 | 420 | 500 | 11,104 | - |
| 2023.02.02 | 신주인수권행사 | 보통주 | 18 | 500 | 11,104 | - |
| 2023.02.03 | 신주인수권행사 | 보통주 | 86 | 500 | 11,104 | - |
| 2023.02.06 | 신주인수권행사 | 보통주 | 223 | 500 | 11,104 | - |
| 2023.02.07 | 신주인수권행사 | 보통주 | 187 | 500 | 11,104 | - |
| 2023.02.09 | 신주인수권행사 | 보통주 | 97 | 500 | 11,104 | - |
| 2023.02.10 | 신주인수권행사 | 보통주 | 155 | 500 | 11,104 | - |
| 2023.02.13 | 신주인수권행사 | 보통주 | 1,204 | 500 | 11,104 | - |
| 2023.02.15 | 신주인수권행사 | 보통주 | 57 | 500 | 11,104 | - |
| 2023.02.16 | 신주인수권행사 | 보통주 | 346 | 500 | 11,104 | - |
| 2023.02.20 | 신주인수권행사 | 보통주 | 535 | 500 | 11,104 | - |
| 2023.02.21 | 신주인수권행사 | 보통주 | 1,367 | 500 | 11,104 | - |
| 2023.02.22 | 신주인수권행사 | 보통주 | 898 | 500 | 11,104 | - |
| 2023.02.23 | 신주인수권행사 | 보통주 | 1,083 | 500 | 11,104 | - |
| 2023.02.24 | 신주인수권행사 | 보통주 | 625 | 500 | 11,104 | - |
| 2023.02.27 | 신주인수권행사 | 보통주 | 10 | 500 | 11,104 | - |
| 2023.02.28 | 신주인수권행사 | 보통주 | 50 | 500 | 11,104 | - |
| 2023.03.03 | 신주인수권행사 | 보통주 | 245 | 500 | 11,104 | - |
| 2023.03.06 | 신주인수권행사 | 보통주 | 29 | 500 | 11,104 | - |
| 2023.03.07 | 신주인수권행사 | 보통주 | 47 | 500 | 11,104 | - |
| 2023.03.08 | 신주인수권행사 | 보통주 | 411 | 500 | 11,104 | - |
| 2023.03.09 | 신주인수권행사 | 보통주 | 86 | 500 | 11,104 | - |
| 2023.03.10 | 신주인수권행사 | 보통주 | 171 | 500 | 11,104 | - |
| 2023.03.13 | 신주인수권행사 | 보통주 | 208 | 500 | 11,104 | - |
| 2023.03.14 | 신주인수권행사 | 보통주 | 148 | 500 | 11,104 | - |
| 2023.03.16 | 신주인수권행사 | 보통주 | 155 | 500 | 10,736 | - |
| 2023.03.20 | 신주인수권행사 | 보통주 | 1,257 | 500 | 10,736 | - |
| 2023.03.21 | 신주인수권행사 | 보통주 | 2,009 | 500 | 10,736 | - |
| 2023.03.22 | 신주인수권행사 | 보통주 | 1,590 | 500 | 10,736 | - |
| 2023.03.23 | 신주인수권행사 | 보통주 | 1,710 | 500 | 10,736 | - |
| 2023.03.24 | 신주인수권행사 | 보통주 | 512 | 500 | 10,736 | - |
| 2023.03.27 | 신주인수권행사 | 보통주 | 1,287 | 500 | 10,736 | - |
| 2023.03.28 | 신주인수권행사 | 보통주 | 388 | 500 | 10,736 | - |
| 2023.03.30 | 신주인수권행사 | 보통주 | 778 | 500 | 10,736 | - |
| 2023.03.31 | 신주인수권행사 | 보통주 | 63 | 500 | 10,736 | - |
| 2023.03.31 | 주식배당 | 보통주 | 5,000,000 | 500 | 10,780 | - |
| 2023.04.03 | 신주인수권행사 | 보통주 | 166 | 500 | 10,209 | - |
| 2023.04.04 | 신주인수권행사 | 보통주 | 159 | 500 | 10,209 | - |
| 2023.04.05 | 신주인수권행사 | 보통주 | 200 | 500 | 10,209 | - |
| 2023.04.07 | 신주인수권행사 | 보통주 | 342 | 500 | 10,209 | - |
| 2023.04.10 | 신주인수권행사 | 보통주 | 179 | 500 | 10,209 | - |
| 2023.04.11 | 신주인수권행사 | 보통주 | 354 | 500 | 10,209 | - |
| 2023.04.12 | 신주인수권행사 | 보통주 | 61 | 500 | 10,209 | - |
| 2023.04.13 | 신주인수권행사 | 보통주 | 1,820 | 500 | 10,209 | - |
| 2023.04.14 | 신주인수권행사 | 보통주 | 1,385 | 500 | 10,209 | - |
| 2023.04.17 | 신주인수권행사 | 보통주 | 527 | 500 | 10,209 | - |
| 2023.04.19 | 신주인수권행사 | 보통주 | 163 | 500 | 10,209 | - |
| 2023.04.20 | 신주인수권행사 | 보통주 | 168 | 500 | 10,209 | - |
| 2023.04.21 | 신주인수권행사 | 보통주 | 460 | 500 | 10,209 | - |
| 2023.04.24 | 신주인수권행사 | 보통주 | 9 | 500 | 10,209 | - |
| 2023.04.25 | 신주인수권행사 | 보통주 | 777 | 500 | 10,209 | - |
| 2023.04.26 | 신주인수권행사 | 보통주 | 162 | 500 | 10,209 | - |
| 2023.04.27 | 신주인수권행사 | 보통주 | 191 | 500 | 10,209 | - |
| 2023.04.28 | 신주인수권행사 | 보통주 | 150 | 500 | 10,209 | - |
| 2023.05.02 | 신주인수권행사 | 보통주 | 2,426 | 500 | 10,209 | - |
| 2023.05.03 | 신주인수권행사 | 보통주 | 1,602 | 500 | 10,209 | - |
| 2023.05.08 | 신주인수권행사 | 보통주 | 617 | 500 | 10,209 | - |
| 2023.05.09 | 신주인수권행사 | 보통주 | 113 | 500 | 10,209 | - |
| 2023.05.10 | 신주인수권행사 | 보통주 | 776 | 500 | 10,209 | - |
| 2023.05.11 | 신주인수권행사 | 보통주 | 2,828 | 500 | 10,209 | - |
| 2023.05.12 | 신주인수권행사 | 보통주 | 9,300 | 500 | 10,209 | - |
| 2023.05.15 | 신주인수권행사 | 보통주 | 10,120 | 500 | 10,209 | - |
| 2023.05.16 | 신주인수권행사 | 보통주 | 2,653 | 500 | 10,209 | - |
| 2023.05.17 | 신주인수권행사 | 보통주 | 5,125 | 500 | 10,209 | - |
| 2023.05.18 | 신주인수권행사 | 보통주 | 2,011 | 500 | 10,209 | - |
| 2023.05.19 | 신주인수권행사 | 보통주 | 840 | 500 | 10,209 | - |
| 2023.05.22 | 신주인수권행사 | 보통주 | 1,926 | 500 | 10,209 | - |
| 2023.05.23 | 신주인수권행사 | 보통주 | 1,913 | 500 | 10,209 | - |
| 2023.05.24 | 신주인수권행사 | 보통주 | 805 | 500 | 10,209 | - |
| 2023.05.25 | 신주인수권행사 | 보통주 | 81 | 500 | 10,209 | - |
| 2023.05.26 | 신주인수권행사 | 보통주 | 1,104 | 500 | 10,209 | - |
| 2023.05.30 | 신주인수권행사 | 보통주 | 563 | 500 | 10,209 | - |
| 2023.05.31 | 신주인수권행사 | 보통주 | 1,591 | 500 | 10,209 | - |
| 2023.06.01 | 신주인수권행사 | 보통주 | 59 | 500 | 10,209 | - |
| 2023.06.02 | 신주인수권행사 | 보통주 | 1,045 | 500 | 10,209 | - |
| 2023.06.05 | 신주인수권행사 | 보통주 | 2,458 | 500 | 10,209 | - |
| 2023.06.07 | 신주인수권행사 | 보통주 | 1,168 | 500 | 10,209 | - |
| 2023.06.08 | 신주인수권행사 | 보통주 | 742 | 500 | 10,209 | - |
| 2023.06.09 | 신주인수권행사 | 보통주 | 572 | 500 | 10,209 | - |
| 2023.06.12 | 신주인수권행사 | 보통주 | 46 | 500 | 10,209 | - |
| 2023.06.19 | 신주인수권행사 | 보통주 | 266 | 500 | 10,209 | - |
| 2023.06.20 | 신주인수권행사 | 보통주 | 101 | 500 | 10,209 | - |
| 2023.06.21 | 신주인수권행사 | 보통주 | 29 | 500 | 10,209 | - |
| 2023.06.28 | 신주인수권행사 | 보통주 | 262 | 500 | 10,209 | - |
| 2023.06.29 | 신주인수권행사 | 보통주 | 532 | 500 | 10,209 | - |
| 2023.07.06 | 신주인수권행사 | 보통주 | 224 | 500 | 10,209 | - |
| 2023.07.13 | 신주인수권행사 | 보통주 | 1,202 | 500 | 10,209 | - |
| 2023.07.17 | 신주인수권행사 | 보통주 | 98 | 500 | 10,209 | - |
| 2023.07.19 | 신주인수권행사 | 보통주 | 156 | 500 | 10,209 | - |
| 2023.07.21 | 신주인수권행사 | 보통주 | 753 | 500 | 10,209 | - |
| 2023.07.24 | 신주인수권행사 | 보통주 | 1 | 500 | 10,209 | - |
| 2023.07.27 | 신주인수권행사 | 보통주 | 375 | 500 | 10,209 | - |
| 2023.08.11 | 신주인수권행사 | 보통주 | 3,293 | 500 | 10,209 | - |
| 2023.08.14 | 신주인수권행사 | 보통주 | 189 | 500 | 10,209 | - |
| 2023.08.16 | 신주인수권행사 | 보통주 | 11 | 500 | 10,209 | - |
| 2023.08.18 | 신주인수권행사 | 보통주 | 1,134 | 500 | 10,209 | - |
| 2023.08.24 | 신주인수권행사 | 보통주 | 59 | 500 | 10,209 | - |
| 2023.08.29 | 신주인수권행사 | 보통주 | 245 | 500 | 10,209 | - |
| 2023.08.31 | 신주인수권행사 | 보통주 | 219 | 500 | 10,209 | - |
| 2023.09.04 | 신주인수권행사 | 보통주 | 122 | 500 | 10,209 | - |
| 2023.09.06 | 신주인수권행사 | 보통주 | 123 | 500 | 10,209 | - |
| 2023.09.08 | 신주인수권행사 | 보통주 | 21 | 500 | 10,209 | - |
| 2023.09.15 | 신주인수권행사 | 보통주 | 352 | 500 | 8,889 | - |
| 2023.09.18 | 신주인수권행사 | 보통주 | 1,915 | 500 | 8,889 | - |
| 2023.09.19 | 신주인수권행사 | 보통주 | 1,274 | 500 | 8,889 | - |
| 2023.09.20 | 신주인수권행사 | 보통주 | 1,601 | 500 | 8,889 | - |
| 2023.09.21 | 신주인수권행사 | 보통주 | 148 | 500 | 8,889 | - |
| 2023.09.27 | 신주인수권행사 | 보통주 | 55 | 500 | 8,889 | - |
| 2023.10.06 | 신주인수권행사 | 보통주 | 1,014 | 500 | 8,889 | - |
| 2023.10.10 | 신주인수권행사 | 보통주 | 215 | 500 | 8,889 | - |
| 2023.10.11 | 신주인수권행사 | 보통주 | 173 | 500 | 8,889 | - |
| 2023.10.12 | 신주인수권행사 | 보통주 | 5 | 500 | 8,889 | - |
| 2023.10.17 | 신주인수권행사 | 보통주 | 66 | 500 | 8,889 | - |
| 2023.10.18 | 신주인수권행사 | 보통주 | 48 | 500 | 8,889 | - |
| 2023.10.19 | 신주인수권행사 | 보통주 | 126 | 500 | 8,889 | - |
| 2023.10.20 | 신주인수권행사 | 보통주 | 73 | 500 | 8,889 | - |
| 2023.10.23 | 신주인수권행사 | 보통주 | 33 | 500 | 8,889 | - |
| 2023.10.24 | 신주인수권행사 | 보통주 | 207 | 500 | 8,889 | - |
| 2023.11.02 | 신주인수권행사 | 보통주 | 645 | 500 | 8,889 | - |
| 2023.11.06 | 신주인수권행사 | 보통주 | 68 | 500 | 8,889 | - |
| 2023.11.07 | 신주인수권행사 | 보통주 | 982 | 500 | 8,889 | - |
| 2023.11.08 | 신주인수권행사 | 보통주 | 658 | 500 | 8,889 | - |
| 2023.11.09 | 신주인수권행사 | 보통주 | 6 | 500 | 8,889 | - |
| 2023.11.13 | 신주인수권행사 | 보통주 | 274 | 500 | 8,889 | - |
| 2023.11.15 | 신주인수권행사 | 보통주 | 6,095 | 500 | 8,889 | - |
| 2023.11.16 | 신주인수권행사 | 보통주 | 348 | 500 | 8,889 | - |
| 2023.11.17 | 신주인수권행사 | 보통주 | 352 | 500 | 8,889 | - |
| 2023.11.23 | 신주인수권행사 | 보통주 | 643 | 500 | 8,889 | - |
| 2023.11.24 | 신주인수권행사 | 보통주 | 284 | 500 | 8,889 | - |
| 2023.11.27 | 신주인수권행사 | 보통주 | 1,362 | 500 | 8,889 | - |
| 2023.11.28 | 신주인수권행사 | 보통주 | 3,826 | 500 | 8,889 | - |
| 2023.11.30 | 신주인수권행사 | 보통주 | 168 | 500 | 8,889 | - |
| 2023.12.01 | 신주인수권행사 | 보통주 | 44 | 500 | 8,889 | - |
| 2023.12.04 | 신주인수권행사 | 보통주 | 65 | 500 | 8,889 | - |
| 2023.12.05 | 신주인수권행사 | 보통주 | 272 | 500 | 8,889 | - |
| 2023.12.06 | 신주인수권행사 | 보통주 | 367 | 500 | 8,889 | - |
| 2023.12.07 | 신주인수권행사 | 보통주 | 145 | 500 | 8,889 | - |
| 2023.12.08 | 신주인수권행사 | 보통주 | 6 | 500 | 8,889 | - |
| 2023.12.11 | 신주인수권행사 | 보통주 | 2,833 | 500 | 8,889 | - |
| 2023.12.12 | 신주인수권행사 | 보통주 | 1,265 | 500 | 8,889 | - |
| 2023.12.13 | 신주인수권행사 | 보통주 | 4,510 | 500 | 8,889 | - |
| 2023.12.14 | 신주인수권행사 | 보통주 | 1,406 | 500 | 8,889 | - |
| 2023.12.15 | 신주인수권행사 | 보통주 | 8,287 | 500 | 8,889 | - |
| 2023.12.18 | 신주인수권행사 | 보통주 | 3,321 | 500 | 8,889 | - |
| 2023.12.19 | 신주인수권행사 | 보통주 | 3,531 | 500 | 8,889 | - |
| 2023.12.20 | 신주인수권행사 | 보통주 | 2,899 | 500 | 8,889 | - |
| 2023.12.21 | 신주인수권행사 | 보통주 | 2,694 | 500 | 8,889 | - |
| 2023.12.22 | 신주인수권행사 | 보통주 | 2,954 | 500 | 8,889 | - |
| 2023.12.26 | 신주인수권행사 | 보통주 | 1,903 | 500 | 8,889 | - |
| 2023.12.27 | 신주인수권행사 | 보통주 | 444 | 500 | 8,889 | - |
| 2023.12.28 | 신주인수권행사 | 보통주 | 378 | 500 | 8,889 | - |
| 2023.12.29 | 신주인수권행사 | 보통주 | 403 | 500 | 8,889 | - |
| 2024.01.02 | 신주인수권행사 | 보통주 | 20 | 500 | 8,889 | - |
| 2024.01.03 | 신주인수권행사 | 보통주 | 1,396 | 500 | 8,889 | - |
| 2024.01.04 | 신주인수권행사 | 보통주 | 5,866 | 500 | 8,889 | - |
| 2024.01.05 | 신주인수권행사 | 보통주 | 4,762 | 500 | 8,889 | - |
| 2024.01.08 | 신주인수권행사 | 보통주 | 2,052 | 500 | 8,889 | - |
| 2024.01.09 | 신주인수권행사 | 보통주 | 23,647 | 500 | 8,889 | - |
| 2024.01.10 | 신주인수권행사 | 보통주 | 840 | 500 | 8,889 | - |
| 2024.01.11 | 신주인수권행사 | 보통주 | 2,767 | 500 | 8,889 | - |
| 2024.01.12 | 신주인수권행사 | 보통주 | 1,236 | 500 | 8,889 | - |
| 2024.01.15 | 신주인수권행사 | 보통주 | 304 | 500 | 8,889 | - |
| 2024.01.16 | 신주인수권행사 | 보통주 | 964 | 500 | 8,889 | - |
| 2024.01.17 | 신주인수권행사 | 보통주 | 444 | 500 | 8,889 | - |
| 2024.01.22 | 신주인수권행사 | 보통주 | 42 | 500 | 8,889 | - |
| 2024.01.23 | 신주인수권행사 | 보통주 | 596 | 500 | 8,889 | - |
| 2024.01.24 | 신주인수권행사 | 보통주 | 702 | 500 | 8,889 | - |
| 2024.01.25 | 신주인수권행사 | 보통주 | 352 | 500 | 8,889 | - |
| 2024.01.26 | 신주인수권행사 | 보통주 | 726 | 500 | 8,889 | - |
| 2024.01.29 | 신주인수권행사 | 보통주 | 216,236 | 500 | 8,889 | - |
| 2024.01.30 | 신주인수권행사 | 보통주 | 522,912 | 500 | 8,889 | - |
| 2024.01.31 | 전환권행사 | 보통주 | 918,314 | 500 | 11,434 | - |
| 2024.01.31 | 신주인수권행사 | 보통주 | 324,862 | 500 | 8,889 | - |
| 2024.02.01 | 신주인수권행사 | 보통주 | 35,570 | 500 | 8,889 | - |
| 2024.02.02 | 신주인수권행사 | 보통주 | 30,185 | 500 | 8,889 | - |
| 2024.02.05 | 신주인수권행사 | 보통주 | 36,506 | 500 | 8,889 | - |
| 2024.02.06 | 신주인수권행사 | 보통주 | 45,478 | 500 | 8,889 | - |
| 2024.02.07 | 신주인수권행사 | 보통주 | 62,256 | 500 | 8,889 | - |
| 2024.02.08 | 신주인수권행사 | 보통주 | 27,374 | 500 | 8,889 | - |
| 2024.02.13 | 신주인수권행사 | 보통주 | 46,409 | 500 | 8,889 | - |
| 2024.02.14 | 신주인수권행사 | 보통주 | 834,664 | 500 | 8,889 | - |
| 2024.02.15 | 신주인수권행사 | 보통주 | 351,259 | 500 | 8,889 | - |
| 2024.02.16 | 신주인수권행사 | 보통주 | 14,746 | 500 | 8,889 | - |
| 2024.02.19 | 신주인수권행사 | 보통주 | 8,425 | 500 | 8,889 | - |
| 2024.02.20 | 신주인수권행사 | 보통주 | 9,400 | 500 | 8,889 | - |
| 2024.02.21 | 신주인수권행사 | 보통주 | 9,008 | 500 | 8,889 | - |
| 2024.02.22 | 신주인수권행사 | 보통주 | 12,832 | 500 | 8,889 | - |
| 2024.02.23 | 신주인수권행사 | 보통주 | 5,098 | 500 | 8,889 | - |
| 2024.02.26 | 신주인수권행사 | 보통주 | 6,509 | 500 | 8,889 | - |
| 2024.02.26 | 전환권행사 | 보통주 | 20,990 | 500 | 11,434 | - |
| 2024.02.27 | 신주인수권행사 | 보통주 | 605,534 | 500 | 8,889 | - |
| 2024.02.28 | 신주인수권행사 | 보통주 | 14,084 | 500 | 8,889 | - |
| 2024.02.29 | 신주인수권행사 | 보통주 | 52,402 | 500 | 8,889 | - |
| 2024.03.04 | 신주인수권행사 | 보통주 | 10,065 | 500 | 8,889 | - |
| 2024.03.05 | 신주인수권행사 | 보통주 | 1,245 | 500 | 8,889 | - |
| 2024.03.06 | 신주인수권행사 | 보통주 | 1,044 | 500 | 8,889 | - |
| 2024.03.07 | 신주인수권행사 | 보통주 | 1,695 | 500 | 8,889 | - |
| 2024.03.08 | 신주인수권행사 | 보통주 | 1,431 | 500 | 8,889 | - |
| 2024.03.11 | 신주인수권행사 | 보통주 | 6,079 | 500 | 8,889 | - |
| 2024.03.12 | 신주인수권행사 | 보통주 | 22,489 | 500 | 8,889 | - |
| 2024.03.13 | 신주인수권행사 | 보통주 | 103,908 | 500 | 8,889 | - |
| 2024.03.14 | 신주인수권행사 | 보통주 | 78,643 | 500 | 8,889 | - |
| 2024.03.15 | 신주인수권행사 | 보통주 | 544,290 | 500 | 8,889 | - |
| 2024.03.18 | 신주인수권행사 | 보통주 | 23,058 | 500 | 8,889 | - |
| 2024.03.19 | 신주인수권행사 | 보통주 | 11,766 | 500 | 8,889 | - |
| 2024.03.20 | 신주인수권행사 | 보통주 | 25,145 | 500 | 8,889 | - |
| 2024.03.21 | 신주인수권행사 | 보통주 | 5,206 | 500 | 8,889 | - |
| 2024.03.22 | 신주인수권행사 | 보통주 | 9,687 | 500 | 8,889 | - |
| 2024.03.25 | 신주인수권행사 | 보통주 | 19,968 | 500 | 8,889 | - |
| 2024.03.26 | 신주인수권행사 | 보통주 | 22,762 | 500 | 8,889 | - |
| 2024.03.27 | 신주인수권행사 | 보통주 | 15,709 | 500 | 8,889 | - |
| 2024.03.28 | 신주인수권행사 | 보통주 | 11,604 | 500 | 8,889 | - |
| 2024.03.28 | 전환권행사 | 보통주 | 302,606 | 500 | 11,434 | - |
| 2024.03.29 | 신주인수권행사 | 보통주 | 82,513 | 500 | 8,889 | - |
| 2024.03.29 | 전환권행사 | 보통주 | 174,917 | 500 | 11,434 | - |
나. 미상환 전환사채 등 발행현황
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 원, 주) |
| 종류\구분 | 회차 | 발행일 | 만기일 | 권면(전자등록)총액 | 전환대상 주식의 종류 |
전환청구가능기간 | 전환조건 | 미상환사채 | 비고 | ||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 전환비율 (%) |
전환가액 | 권면(전자등록)총액 | 전환가능주식수 | ||||||||
| 무기명식 이권부 무보증 사모 전환사채 | 12 | 2023.11.07 | 2026.11.07 | 28,800,000,000 | 기명식 보통주 |
2024.11.07~2026.10.06 | 100 | 9,586 | 28,800,000,000 | 3,004,381 | - |
| 무기명식 이권부 무보증 사모 전환사채 |
11 | 2023.07.07 | 2028.07.07 | 8,300,000,000 | 기명식 보통주 |
2024.07.07~2028.06.07 | 100 | 10,204 | 8,300,000,000 | 813,406 | - |
| 합 계 | - | - | - | 37,100,000,000 | - | - | - | - | 37,100,000,000 | 3,817,787 | - |
다. 미상환 신주인수권부사채 등 발행현황
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 원, 주) |
| 종류\구분 | 회차 | 발행일 | 만기일 | 권면(전자등록)총액 | 행사대상 주식의 종류 |
신주인수권 행사가능기간 | 행사조건 | 미상환 사채 |
미행사 신주 인수권 |
비고 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 행사비율 (%) |
행사가액 | 권면(전자등록)총액 | 행사가능주식수 | ||||||||
| 무기명식 이권부 무보증 공모 분리형 신주인수권부사채 |
9 | 2022.06.15 | 2025.06.15 | 100,000,000,000 | 기명식 보통주 |
2022.07.15~2025.05.15 | 134 | 8,889 | 80,600,569,485 | 3,813,744 | - |
| 합 계 | - | - | - | 100,000,000,000 | - | - | - | - | 80,600,569,485 | 3,813,744 | - |
| [채무증권의 발행 등과 관련된 사항] |
라. 채무증권 발행실적
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 백만원, %) |
| 발행회사 | 증권종류 | 발행방법 | 발행일자 | 권면(전자등록)총액 | 이자율 | 평가등급 (평가기관) |
만기일 | 상환 여부 |
주관회사 |
|---|---|---|---|---|---|---|---|---|---|
| - | - | - | - | - | - | - | - | - | - |
| 합 계 | - | - | - | - | - | - | - | - | - |
마. 기업어음증권 미상환 잔액
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
1년초과 2년이하 |
2년초과 3년이하 |
3년 초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | |
바. 단기사채 미상환 잔액
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
합 계 | 발행 한도 | 잔여 한도 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
사. 회사채 미상환 잔액
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | 80,600 | - | - | - | - | - | 80,600 |
| 사모 | - | - | 28,800 | - | 8,300 | - | - | 37,100 | |
| 합계 | - | 80,600 | 28,800 | - | 8,300 | - | - | 117,700 | |
아. 신종자본증권 미상환 잔액
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 1년 이하 | 1년초과 5년이하 |
5년초과 10년이하 |
10년초과 15년이하 |
15년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
자. 조건부자본증권 미상환 잔액
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | - | |
차. 사채관리계약 주요내용 및 충족여부 등_재무회계팀 작성
| (작성기준일 : | 2024년 03월 31일 | ) | (단위 : 백만원, %) |
| 채권명 | 발행일 | 만기일 | 발행액 | 사채관리 계약체결일 |
사채관리회사 |
|---|---|---|---|---|---|
| 제9회 무기명식 이권부 무보증 공모 분리형 신주인수권부사채 |
2022.06.15 | 2025.06.15 | 100,000 | 2022.04.14 | DB금융투자 |
| (이행현황기준일 : | 2024년 03월 31일 | ) |
| 재무비율 유지현황 | 계약내용 | 부채비율 300% 이하 (연결기준) |
| 이행현황 | 이행 (76.03%) | |
| 담보권설정 제한현황 | 계약내용 | 자기자본의 300% 이하 (연결기준) |
| 이행현황 | 이행 (24.88%) | |
| 자산처분 제한현황 | 계약내용 | 자산총계의 100% 이하 (연결기준) |
| 이행현황 | 이행 (1.65%) | |
| 지배구조변경 제한현황 | 계약내용 | 최대주주 "HLB" 유지 |
| 이행현황 | 이행 (최대주주 "HLB" 유지) | |
| 이행상황보고서 제출현황 | 이행현황 | 본 보고서 제출일로부터 30일 이내 제출예정 |
| * 이행현황기준일은 이행현황 판단 시 적용한 회계감사인의 감사의견(확인 및 의견표시)이 표명된 가장 최근의 재무제표의 작성기준일이며, 지배구조변경 제한현황은 공시서류작성기준일임. |
7-2. 증권의 발행을 통해 조달된 자금의 사용실적
가. 공모자금의 사용내역_재무회계팀 작성
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 증권신고서 등의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
| 주주배정 유상증자 |
- | 2018.10.23 | 운영자금 : 75,000 1. 바이오파이프라인 구축 (40,000) 2. 바이오파이프라인 구축 (35,000) 기타자금 : 45,099 1. 신규확보 파이프라인 임상 비용 등 (15,099) 2. 제약제조시설 인수 등 (30,000) (시설 보유 타법인 지분 인수 포함) 시설자금 : 27,993 1. 사옥매입 (27,993) |
148,092 | 운영자금 : 75,000 1. 바이오파이프라인 구축 (40,000) 2. 사채상환 (35,000) 기타자금 : 45,099 1. 사채상환 (15,099) 2. 제약제조시설 인수 (27,783) (시설 보유 타법인 지분 인수 포함) 3. 바이오파이프라인 구축 (2,217) 시설자금 : 27,993 1. 사옥매입 등 (27,993) |
148,092 | (*1) |
| 분리형 신주인수권부사채 |
- | 2022.06.15 | 운영자금 : 40,000 1. 바이오사업 (25,000) 2. 에너지사업 (15,000) 타법인증권취득자금 : 60,000 1. 타법인증권취득자금 (60,000) |
100,000 | 운영자금 : 40,000 1. 바이오사업 (25,501) 2. 에너지사업 (11,368) 3. 메디케어사업 (3,131) 타법인증권취득자금 : 60,000 1. 타법인증권취득자금 (60,000) |
100,000 | - |
| (*1) 본 보고서 작성기준을 현재 운영자금 75,000백만원, 기타자금 45,099백만원, 시설자금 23,845백만원이 사용되었으며, 총 미사용금액 4,148백만원은 자금사용 계획에 맞추어 사용될 예정입니다. |
나. 사모자금의 사용내역_재무회계팀 작성
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 주요사항보고서의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
| 무기명식 무보증 사모 전환사채 | 10 | 2022.07.01 | 타법인주식취득 : 45,000 | 45,000 | 타법인주식취득 : 45,000 | 45,000 | - |
| 무기명식 무보증 사모 전환사채 | 11 | 2023.07.07 | 운영자금 : 8,300 | 8,300 | 운영자금 :8,300 1. 바이오사업 (3,300) 2. 메디케어사업 (5,000) |
8,300 | - |
| 무기명식 무보증 사모 전환사채 | 12 | 2023.11.07 | 채무상환자금 : 28,800 | 28,800 | 채무상환자금 : 28,800 |
28,800 | (*) |
| (*) 2022.07.01 발행한 HLB생명과학 주식회사 제10회차 전환사채의 전환사채금 450억원의 일부인 288억원을 조기 상환함에 따라 조기 상환 된 288억원 전액을 대환하여 12회차 전환사채 인수대금으로 납입하였습니다. |
다. 미사용자금의 운용내역_재무회계팀 작성
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 백만원) |
| 종류 | 운용상품명 | 운용금액 | 계약기간 | 실투자기간 |
|---|---|---|---|---|
| 예ㆍ적금 | 정기적금 | 1 | 2024.03 ~ 2025.03 | 12개월 |
| 예ㆍ적금 | 수시입출금 | 2,147 | - | - |
| - | 펀드예치금 | 2,000 | - | 3년 11개월 |
| 계 | 4,148 | - | ||
8. 기타 재무에 관한 사항
가. 재무제표 재작성 등 유의사항
(1) 합병등의 사후정보
- 본 보고서 항목중 "XI.그 밖에 투자자 보호를 위하여 필요한 사항 => 3.제재현황
등 그 밖의 사항 => 마.합병등의 사후정보" 를 참조하시기 바랍니다.
(2) 연결대상범위의 변동
- 당분기 중 연결대상범위의 변동 내역은 다음과 같습니다.
| 구 분 | 종속회사 | 사 유 |
|---|---|---|
| 신규연결 | 에이치엘비솔루션(주) | 물적분할 |
(3) 기타 재무제표 이용에 유의하여야 할 사항
- 연결 및 별도 감사보고서상 강조사항 및 핵심 감사 사항 등은 사업보고서 "V. 회계감사인의 감사의견 등 1. 외부감사에 관한 사항" 을 참고하시기 바랍니다.
나. 대손충당금 설정현황
(1) 최근 3사업연도의 계정과목별 대손충당금 설정내역
| (기준일 : 2024년 03월 31일) | (단위 : 천원, % ) |
| 구분 | 계정과목 | 채권총액 | 대손충당금 | 대손충당금설정율 | 채권잔액 |
| 제27기 (당분기) |
매출채권 | 14,274,411 | (1,299,309) | 9.10 | 12,975,102 |
| 단기대여금 | 92,080 | (80,880) | 87.84 | 11,200 | |
| 미수수익 | 272,327 | 0 | - | 272,327 | |
| 미수금 | 2,838,067 | (956,492) | 33.70 | 1,881,574 | |
| 선급금 | 702,471 | (483,476) | 68.83 | 218,995 | |
| 미청구공사 | 18,894 | 0 | - | 18,894 | |
| 장기대여금 | 629,242 | (505,804) | 80.38 | 123,438 | |
| 장기미수금 | 62,400 | (62,400) | 100.00 | 0 | |
| 합계 | 18,827,492 | (3,388,362) | 18.00 | 15,501,531 | |
| 제26기 (전기) |
매출채권 | 12,069,814 | (1,297,180) | 10.75 | 10,772,634 |
| 단기대여금 | 892,080 | (80,880) | 9.07 | 811,200 | |
| 미수수익 | 190,358 | - | - | 190,358 | |
| 미수금 | 3,136,866 | (956,492) | 30.49 | 2,180,374 | |
| 선급금 | 722,325 | (483,476) | 66.93 | 238,849 | |
| 미청구공사 | 7,014 | - | - | 7,014 | |
| 장기대여금 | 630,742 | (505,804) | 80.19 | 124,938 | |
| 장기미수금 | 62,400 | (62,400) | 100.00 | 0 | |
| 합계 | 17,711,600 | (3,386,233) | 19.12 | 14,325,367 | |
| 제25기 (전전기) |
매출채권 | 14,236,064 | (1,481,688) | 10.41 | 12,754,376 |
| 단기대여금 | 1,383,204 | (369,921) | 26.74 | 1,013,283 | |
| 미수수익 | 190,778 | 0 | - | 190,778 | |
| 미수금 | 2,150,119 | (224,518) | 10.44 | 1,925,600 | |
| 선급금 | 838,745 | (428,476) | 51.09 | 410,269 | |
| 미청구공사 | 588 | 0 | - | 588 | |
| 장기매출채권 | 149,014 | - | - | 149,014 | |
| 장기대여금 | 646,742 | (505,804) | 78.21 | 140,938 | |
| 합계 | 19,595,254 | (3,010,407) | 15.36 | 16,584,847 |
(2) 최근 3사업연도의 대손충당금 변동현황
| (단위 : 천원) |
| 구 분 | 제26기 (당기) |
제25기 (전기) |
제24기 (전전기) |
| 1. 기초금액 | 3,386,233 | 3,010,407 | 3,261,135 |
| 2. 순대손처리액 | - | (512,781) | (304,330) |
| 3. 대손상각비 계상(환입)액 | 2,129 | 884,725 | (121,682) |
| 4. 종속기업 변동으로 인한 증감 | - | 3,880 | 175,283 |
| 5. 기말금액 | 3,388,362 | 3,386,232 | 3,010,407 |
(3) 매출채권관련 대손충당금 설정방침
연결실체는 재무상태표일 현재 매출채권의 대손충당금 설정비율은 연령분석과 과거의 대손경험율을 토대로 다음과 같은 기준으로 설정하고 있습니다.
재무상태표일 현재 매출채권 잔액중 재무상태표일 이후에 회수된 금액 및 담보권이 설정되어 있는 채권은 설정대상에서 제외하고, 개별분석 및 과거의 대손경험율을 토대로 하여 대손충당금으로 설정하고 있습니다.
(4) 당기 현재 경과기간별 매출채권잔액 현황
| (단위 : 천원) |
| 구분 | 정상채권 | 3개월 이하 | 3개월 초과 ~ 6개월 이하 |
6개월 초과 | 대손확정 | 합계 |
|---|---|---|---|---|---|---|
| 기대 손실률 | 0.05% | 0.01% | 5.31% | 49.62% | 100.00% | 6.29% |
| 총 장부금액 | 12,381,110 | 936,778 | 45,189 | 13,410 | 0 | 13,376,487 |
| 매출채권 | 12,387,837 | 936,899 | 47,721 | 26,619 | 875,335 | 14,274,411 |
| 손실충당금 | (6,727) | (121) | (2,532) | (13,208) | (875,335) | (897,924) |
다. 재고자산의 현황 등
(1) 최근 3사업연도의 재고자산의 사업부문별 보유현황
| (단위 : 천원, %) |
| 사업부문 | 계정과목 | 제27기 (당분기) |
제26기 (전기) |
제25기 (전전기) |
| (주)신화어드밴스 | 상품 | 2,736,262 | 2,816,056 | 2,440,452 |
| 총자산대비 재고자산 구성비율(%) [재고자산합계÷기말자산총계×100] |
10.68 | 11.24 | 9.50 | |
| 재고자산회전율(회수) [연환산 매출원가÷{(기초재고+기말재고)÷2}] |
23.87 | 23.69 | 25.31 | |
| 에이치엘비생명과학 (메디케어) |
상품 | 432,316 | 502,708 | 5,025,269 |
| 제품 | 1,313,408 | 1,004,356 | 817,287 | |
| 원재료 | 1,114,025 | 1,933,999 | 1,434,560 | |
| 재공품 | 599,555 | 391,359 | 795,678 | |
| 소계 | 3,459,305 | 3,832,421 | 8,072,794 | |
| 총자산대비 재고자산 구성비율(%) [재고자산합계÷기말자산총계×100] |
0.60 | 0.92 | 7.52 | |
| 재고자산회전율(회수) [연환산 매출원가÷{(기초재고+기말재고)÷2}] |
2.64 | 5.00 | 1.97 | |
| 에이치엘비셀(주) (메디케어) |
원재료 | 50,803 | 52,175 | 54,169 |
| 제품 | 65,861 | 95,001 | 299,964 | |
| 소계 | 116,664 | 147,176 | 354,133 | |
| 총자산대비 재고자산 구성비율(%) [재고자산합계÷기말자산총계×100] |
0.13 | 0.29 | 0.93 | |
| 재고자산회전율(회수) [연환산 매출원가÷{(기초재고+기말재고)÷2}] |
4.18 | 6.25 | 6.38 | |
(2) 재고자산의 실사내역 등
연결실체는 재고자산에 대하여 분기별 서면실사와 분기 및 반기, 결산기 실물 실사를실시하고 있습니다.
(3) 장기체화 재고 등 현황
재고자산의 시가가 취득원가보다 하락한 경우 저가법 등을 사용하여 재고자산의 장부금액을 결정하고 있으며, 2023년 기말 현재 재고자산에 대한 평가내역은 다음과 같습니다.
| (기준일 : 2023년 12월 31일) | (단위 : 천원) |
| 구 분 | 취득원가 | 평가충당금 | 장부금액 | 비 고 |
|---|---|---|---|---|
| 원재료 | 1,164,828 | (287,696) | 877,132 | - |
| 재공품 | 599,555 | (222,693) | 376,862 | - |
| 제품 | 1,379,269 | (493,246) | 886,022 | - |
| 상품 | 3,168,578 | (70,628) | 3,097,950 | - |
| 합계 | 6,312,231 | (1,074,263) | 5,237,968 | - |
라. 공정가치평가 내역
공시대상기간 중 금융상품의 공정가치와 그 평가방법은『Ⅲ. 재무에 관한 사항』중 연결재무제표 주석 [5. 공정가치], [6. 기타금융자산] 등의 내용을 참조하시기 바랍니다.
마. 진행률적용 수주계약 현황
2024년 분기말 현재 당사 재무제표에 중요한 영향을 미치는 장기공급계약 수주거래는 없습니다.
IV. 회계감사인의 감사의견 등
1. 외부감사에 관한 사항
가. 회계감사인의 명칭 및 감사의견
(1) 감사인의 연결 감사의견
| 사업연도 | 감사인 | 감사의견 | 강조사항 등 | 핵심감사사항 |
|---|---|---|---|---|
| 제27기(당분기) | 삼정회계법인 | 해당사항 없음 | - | - |
| 제26기(전기) | 한영회계법인 | 적정 | 해당사항 없음 | 영업권 및 비한정내용연수무형자산 손상평가 |
| 제25기(전전기) | 우리회계법인 | 적정 | 해당사항 없음 | 영업권 손상검토 |
(2) 감사인의 별도 감사의견
| 사업연도 | 감사인 | 감사의견 | 강조사항 등 | 핵심감사사항 |
|---|---|---|---|---|
| 제27기(당분기) | 삼정회계법인 | 해당사항 없음 | - | - |
| 제26기(전기) | 한영회계법인 | 적정 | 해당사항 없음 | 영업권 및 비한정내용연수무형자산 손상평가 |
| 제25기(전전기) | 우리회계법인 | 적정 | 해당사함 없음 | 영업권 손상검토 |
나. 감사용역 체결현황
| (단위 : 천원, VAT제외) |
| 사업연도 | 감사인 | 내 용 | 감사계약내역 | 실제수행내역 | ||
|---|---|---|---|---|---|---|
| 보수 | 시간 | 보수 | 시간 | |||
| 제27기(당분기) | 삼정회계법인 | 연결 및 별도 회계감사 및 분반기검토, 내부회계관리제도 감사 |
260,000 | 2,600 | - | - |
| 제26기(전기) | 한영회계법인 | 연결 및 별도 회계감사 및 분반기검토, 내부회계관리제도 감사 |
400,000 | 2,874 | 400,000 | 3,173 |
| 제25기(전전기) | 우리회계법인 | 연결 및 별도 회계감사 및 분반기검토, 내부회계관리제도 감사 |
365,000 | 2,631 | 365,000 | 2,688 |
다. 회계감사인과의 비감사용역 계약체결 현황
| 사업연도 | 계약체결일 | 용역내용 | 용역수행기간 | 용역보수 | 비고 |
|---|---|---|---|---|---|
| 제26기(당기) | - | - | - | - | - |
| - | - | - | - | - | |
| 제25기(전기) | - | - | - | - | - |
| - | - | - | - | - | |
| 제24기(전전기) | - | - | - | - | - |
| - | - | - | - | - |
라. 내부감사기구가 회계감사인과 논의한 결과
| 구분 | 일자 | 참석자 | 방식 | 주요 논의 내용 |
|---|---|---|---|---|
| 1 | 2024년 03월 08일 | [감사인: 한영회계법인] 이유창 회계사(파트너), 이원재 회계사 [HLB생명과학] 김영현 감사, 이대호 부사장, 이근식 상무 |
대면회의 |
기말감사결과 내부회계관리제도감사결과에 대한 사항 및 핵심감사사항에 대한 논의 |
| 2 | 2023년 08월 04일 | [감사인: 한영회계법인] 이유창 회계사(파트너), 이원재 회계사 [HLB생명과학] 김영현 감사, 이대호 부사장, 이근식 상무 |
대면회의 | 반기검토결과 |
| 3 | 2023년 03월 13일 | [감사인: 우리회계법인] 류선영 회계사(파트너), 송우헌 회계사 [HLB생명과학] 김영현 감사, 이대호 부사장, 김경배 상무 |
대면회의 | 기말감사결과 내부회계관리제도감사결과에 대한 사항 및 핵심감사사항에 대한 논의 |
| 4 | 2022년 12월 02일 | [감사인: 우리회계법인] 류선영 회계사(파트너), 송우헌 회계사 [HLB생명과학] 김영현 감사, 이대호 부사장, 김대용 이사 |
대면회의 | 중간감사결과 및 기말감사계획 핵심감사사항에 대한논의 |
| 5 | 2022년 08월 06일 | [감사인: 우리회계법인] 류선영 회계사(파트너), 송우헌 회계사 [HLB생명과학] 김영현 감사, 이대호 부사장, 김대용 이사 |
대면회의 | 반기검토결과 |
| 6 | 2022년 02월 16일 | [감사인: 우리회계법인] 류선영 회계사(파트너), 송우헌 회계사 [HLB생명과학] 김영현 감사, 백윤기 부사장, 김대용 이사 |
대면회의 | 기말감사결과 및 내부회계관리제도 검토결과에 대한 사항 |
| 7 | 2021년 12월 03일 | [감사인: 우리회계법인] 류선영 회계사(파트너), 송우헌 회계사 [HLB생명과학] 김영현 감사, 백윤기 부사장, 김대용 이사 |
대면회의 | 중간감사결과 및 기말감사계획등 |
| 8 | 2021년 07월 30일 | [감사인: 우리회계법인] 류선영 회계사(파트너), 송우헌 회계사 [HLB생명과학] 김영현 감사, 백윤기 부사장, 김대용 이사 |
대면회의 | 반기검토결과 |
| 9 | 2021년 02월 17일 | [감사인: 우리회계법인] 류선영 회계사(파트너), 송우헌 회계사 [HLB생명과학] 김영현 감사, 백윤기 부사장, 김대용 부장 |
대면회의 | 기말감사결과 및 내부회계관리제도 검토결과에 대한 사항 |
2. 내부통제에 관한 사항
가. 내부통제
회사의 감사는 회사의 내부통제의 유효성에 대하여 감사하며, 당사의 내부감시장치는 효과적으로 가동되고 있습니다.
나. 내부회계관리제도
당사는 신뢰할 수 있는 회계정보의 작성 및 공시를 위하여 내부회계관리제도를 운영하고 있습니다. 대표이사는 내부회계관리제도의 관리 및 운영을 책임지고 내부회계 관리제도의 효율적인 관리 및 운영을 위하여 내부회계관리자를 지정하도록 하고 있으며, 내부회계관리자는 내부회계관리제도의 운영을 총괄하고, 회계정보의 작성 및 공시, 회계정보의 전산처리 등에 관한 사항을 통제하며 이를 확인, 감독하고 있습니다. 또한, 내부회계관리자는 내부회계관리제도의 정비와 운영을 총괄하고, 연 1회의 이사회 및 감사위원회에 이 규정에 따른 운영실태에 관한 보고와 당사 조직관리 부서의 협조를 거친 후, 회계정보의 작성 및 공시를 담당하는 부서에 대한 적절하고 효율적인 업무분장을 수행하고 있습니다.
다. 내부회계관리제도의 문제점 또는 개선방안 등
- 해당사항 없습니다.
라. 회계감사인의 내부회계관리제도에 대한 감사 또는 검토의견
| 사업연도 | 회계감사인 | 검토의견 |
| 제26기 (전기) |
한영회계법인 |
우리는 2023년 12월 31일 현재 「내부회계관리제도 설계 및 운영 개념체계」에 근거한 HLB생명과학 (이하 "회사")의 내부회계관리제도를 감사하였습니다. 우리의 의견으로는 회사의 내부회계관리제도는 2023년 12월 31일 현재「내부회계관리제도 설계 및 운영 개념체계」에 따라 중요성의 관점에서 효과적으로 설계 및 운영되고 있습니다. |
| 제25기 (전전기) |
우리회계법인 |
우리는 2022년 12월 31일 현재 「내부회계관리제도 설계 및 운영 개념체계」에 근거한 HLB생명과학 (이하 "회사")의 내부회계관리제도를 감사하였습니다. 우리의 의견으로는 회사의 내부회계관리제도는 2022년 12월 31일 현재「내부회계관리제도 설계 및 운영 개념체계」에 따라 중요성의 관점에서 효과적으로 설계 및 운영되고 있습니다. |
V. 이사회 등 회사의 기관에 관한 사항
1. 이사회에 관한 사항
가. 이사회의 구성 개요
| (기준일 : 2024년 03월 31일) |
| 구 분 | 성 명 | 비 고 | |
| HLB생명과학 이사회 (6명) | 사내이사 (4명) | 진양곤 | 이사회의장 |
| 남상우 | 대표이사 | ||
| 한용해 | 대표이사 | ||
| 이근식 | - | ||
| 사외이사 (2명) | 심연섭 | - | |
| 송세빈 | - | ||
1) 이사회 구성 개요
보고서 작성 기준일 현재, 당사의 이사회는 사내이사 4인 (진양곤, 남상우, 한용해, 이근식), 사외이사 2인 (심연섭, 송세빈) 총 6인의 이사로 구성되어 있습니다. 이사회내에 별도의 위원회는 없습니다.(Ⅷ.임원 및 직원 등에 관한 사항, 1. 임원 및 직원 등의 현황 참조)
2) 이사회 의장에 관한 사항
이사회 의장은 당사 정관 제26조에 의거, 진양곤 사내이사가 겸직하고 있습니다. 이사회 의장은 이사회의 소집과 안건의 주재를 담당한다는 점에서 이사회 안건, 운영 등에 대하여 이해도가 높은 이사가 의장으로 적합하다고 볼 수 있습니다. 이에 따라, 당사의 이사회에 부의되는 각종 현안을 가장 잘 파악하고 있는 진양곤 사내이사가 이사회 의장 직무를 수행하기에 가장 적합하다고 판단되어 이사들의 의결을 거쳐 이사회 의장으로 선임하였습니다.
3) 사외이사 및 그 변동현황
| (단위 : 명) |
| 이사의 수 | 사외이사 수 | 사외이사 변동현황 | ||
|---|---|---|---|---|
| 선임 | 해임 | 중도퇴임 | ||
| 4 | 2 | 2 | - | 1 |
나. 이사회의 중요의결사항 등
| (기준일 : 2024년 03월 31일) |
| 회차 | 개최일자 | 의안내용 | 가결여부 | 사내이사 | 사외이사 | |||||||
| 진양곤 (출석률: 100%) |
남상우 (출석률: 100%) |
한용해 (출석률:100%) |
장인근 (출석률 :100%) |
이근식 (출석률: 100%) |
최수자 (출석률: 100%) |
김윤 (출석률:100%) |
심연섭 (출석률: 100%) |
송세빈 (출석률: 100%) |
||||
| 찬 반 여 부 | ||||||||||||
| 1 | 2024-01-02 | 분할계획서 변경의 건 | 가결 | 찬성 | 찬성 | 찬성 | 찬성 | - | 찬성 | 찬성 | - | - |
| 2 | 2024-01-02 | 회사분할종료 보고 주주총회 갈음의 건 | 가결 | 찬성 | 찬성 | 찬성 | 찬성 | - | 찬성 | 찬성 | - | - |
| 3 | 2024-01-30 | 자금 차입 결정의 건 | 가결 | 찬성 | 찬성 | 찬성 | 찬성 | - | 찬성 | 찬성 | - | - |
| 4 | 2024-02-13 | 제26기 재무제표(2023년) 확정의 건 | 가결 | 찬성 | 찬성 | 찬성 | 찬성 | - | 찬성 | 찬성 | - | - |
| 5 | 2024-02-27 | 제26기 정기주주총회 소집의 건 | 가결 | 찬성 | 찬성 | 찬성 | 찬성 | - | 찬성 | 찬성 | - | - |
| 6 | 2024-03-04 | 자회사(HLB에너지) 대여금 지급 및 자회사(HLB생명과학R&D) 추가 출자의 건 |
가결 | 찬성 | 찬성 | 찬성 | 찬성 | - | 찬성 | 찬성 | - | - |
| 7 | 2024-03-13 | 내부회계관리제도 운영실태의 보고의 건 내부회계관리제도 운영평가 보고의 건 |
가결 | 찬성 | 찬성 | 찬성 | 찬성 | - | 찬성 | 찬성 | - | - |
| 8 | 2024-03-14 | 우리은행 차입금 연장의 건 | 가결 | 찬성 | 찬성 | 찬성 | 찬성 | - | 찬성 | 찬성 | - | - |
| 9 | 2024-03-20 | 제26기 재무제표(2023년) 정정 확정의 건 | 가결 | 찬성 | 찬성 | 찬성 | 찬성 | - | 찬성 | 찬성 | - | - |
| 10 | 2024-03-21 | 주주배정 실권주 일반공모 유상증자 결의의 건 | 가결 | 찬성 | 찬성 | 찬성 | 찬성 | - | 찬성 | 찬성 | - | - |
| (*1) 사내이사 장인근, 사외이사 김윤은 2024년 03월 28일 일신상의 이유로 사임하였습니다. |
| (*2) 사외이사 최수자는 2024년 03월 31일 임기 만료 되였습니다. |
| (*3) 사내이사 이근식, 사외이사 심연섭, 송세빈은 2024년 03월 28일 개최한 정기주주총회를 통해 신규 선임되었습니다. |
1) 사외이사 현황
| (기준일 : 2024년 03월 31일) |
| 성명 | 생년월일 | 주요경력 | 최대주주등과의 이해관계 |
결격요건여부 | 비고 |
| 심연섭 | 1975-03 | 현) (주)맑은기술 대표이사 전) HLB글로벌 사외이사 |
- | - | - |
| 송세빈 | 1962-05 | 현) 법무법인(유) 화우 파트너 변호사 전) (주)이마트 법무실장 |
- | - | - |
2) 사외이사의 지원 조직 현황_경영기획팀 작성
| 팀명 | 직원수 | 직위(근속연수) | 주요 활동내역 |
| 경영전략본부 | 11 | 이사1명, 부장1명, 차장3명, 과장1명, 대리3명, 사원2명 (평균2.0년) |
이사회 운영 및 사외이사 직무수행 지원 |
3) 사외이사 교육 미실시 내역
| 사외이사 교육 실시여부 | 사외이사 교육 미실시 사유 |
|---|---|
| 미실시 | 사외이사의 경력과 전문성을 고려한 바, 당사의 사외이사로 충분한 자격을 갖추었기에 교육을 실시하지 않았으나, 업무수행 관련 교육이 필요할 경우 진행할 예정입니다. |
4) 이사회에서의 사외이사의 주요활동내역
| (기준일 : 2024년 03월 31일) |
| 회차 | 개최일자 | 의안내용 | 사외이사 | |||
| 최수자 (출석률: 100%) |
김윤 (출석률: 100%) |
심연섭 (출석률: 100%) |
송세빈 (출석률: 100%) |
|||
| 찬 반 여 부 | ||||||
| 1 | 2024-01-02 | 분할계획서 변경의 건 | 참석(찬성) | 참석(찬성) | - | - |
| 2 | 2024-01-02 | 회사분할종료 보고 주주총회 갈음의 건 | 참석(찬성) | 참석(찬성) | - | - |
| 3 | 2024-01-30 | 자금 차입 결정의 건 | 참석(찬성) | 참석(찬성) | - | - |
| 4 | 2024-02-13 | 제26기 재무제표(2023년) 확정의 건 | 참석(찬성) | 참석(찬성) | - | - |
| 5 | 2024-02-27 | 제26기 정기주주총회 소집의 건 | 참석(찬성) | 참석(찬성) | - | - |
| 6 | 2024-03-04 | 자회사(HLB에너지) 대여금 지급 및 자회사(HLB생명과학R&D) 추가 출자의 건 |
참석(찬성) | 참석(찬성) | - | - |
| 7 | 2024-03-13 | 내부회계관리제도 운영실태의 보고의 건 내부회계관리제도 운영평가 보고의 건 |
참석(찬성) | 참석(찬성) | - | - |
| 8 | 2024-03-14 | 우리은행 차입금 연장의 건 | 참석(찬성) | 참석(찬성) | - | - |
| 9 | 2024-03-20 | 제26기 재무제표(2023년) 정정 확정의 건 | 참석(찬성) | 참석(찬성) | - | - |
| 10 | 2024-03-21 | 주주배정 실권주 일반공모 유상증자 결의의 건 | 참석(찬성) | 참석(찬성) | - | - |
(*1) 사외이사 최수자는 2024년 03월 31일 임기만료 되었습니다.
(*2) 사외이사 김윤은 2024년 03월 28일 일신상의 이유로 사임하였습니다.
(*3) 사외이사 심연섭,송세빈은 2024년 03월 28일 개최한 정기주주총회를 통해 신규 선임되었습니다.
다. 이사회내의 위원회
- 해당사항 없습니다.
라. 이사의 독립성
1) 이사회의 권한 내용
이사는 대표이사를 보좌하고 이사회에서 정하는 바에 따라 회사의 업무를 분장, 집행하고 있습니다. 각 이사의 주요 이력 및 담당업무는 「VIII. 임원 및 직원 등에 관한 사항」을 참조하시기 바랍니다.
※ 상기 내용 이외, 법령, 정관 및 주주총회의 결의에 의해 이사회의 결의사항으로 하여야 할 사항과 대표이사가 특히 의결할 필요가 있다고 인정하는 사항
2) 이사회의 결의에 대한 독립성
정관상 이사회의 결의에 관한 특별한 이해관계가 있는 경우, 결의권 제한사항을
규정하고 있습니다.
| 정관 제 41 조(이사회의 결의방법) |
|---|
|
제41조(이사회의 결의방법) |
3) 이사회 구성에 관한 독립성
회사 경영의 중요한 의사 결정과 업무 진행은 이사회의 심의 및 결정을 통하여 이루어지고 있습니다. 또한 동사는 대주주 등의 독단적인 경영과 이로 인한 소액주주의 이익 침해가 발생하지 않도록 이사회 운영규정을 제정하여 성실히 준수하고 있습니다. 보고서 작성기준일 현재 이사회의 구성은 아래와 같습니다.
| (기준일 : 2024년 03월 31일) |
| 성명 | 추천인 | 직 위 | 담당업무 | 회사와의 거래 관계 |
최대주주와의 관계 |
임기 | 연임 여부 |
연임 횟수 |
비 고 |
| 진양곤 | 이사회 | 회장 | 이사회의장 | - | 임원 | 2027.03.28 | O | 2회 | - |
| 남상우 | 이사회 | 대표이사 | 각자 대표이사 (경영총괄) |
- | 계열회사 임원 | 2026.03.31 | O | 1회 | - |
| 한용해 | 이사회 | 대표이사 | 각자 대표이사 (바이오총괄) |
- | 계열회사 임원 | 2025.03.31 | X | - | - |
| 이근식 | 이사회 | 사내이사 | 경영관리 | - | 계열회사 임원 | 2027.03.28 | X | - | (*) |
| 심연섭 | 이사회 | 사외이사 | 경영고문 | - | - | 2027.03.28 | X | - | (*) |
| 송세빈 | 이사회 | 사외이사 | 경영고문 | - | - | 2027.03.28 | X | - | (*) |
| (*) 사내이사 이근식, 사외이사 심연섭, 송세빈은 2024년 03월 28일 개최한 정기주주총회를 통해 신규 선임되었습니다. |
2. 감사제도에 관한 사항
가. 감사위원회
| 감사 및 감사위원회 설치 여부 | 미설치 |
| 감사운영기준 | 정관 제46 조 내지 제52조의 감사에 관한 규정 |
| 감사규정내용 | [제40조 ~ 제45조] 당사는 1인 이상의 감사를 둘 수 있으며, 현재 1인의 상근감사를 두고 있습니다.감사는 회사의 회계 업무를 감사하며, 상법상 정해진 일체의 권한을 보유하고, 이사회에 출석하여 의견을 진술하거나, 임시 주주총회 소집을 요구할 수도 있습니다. 아울러 직무상 필요한 영업의 보고나, 회사의 재산상태 등을 조사할 수 있습니다. |
| 감사수행 | 회계 및 업무에 대한 감사업무를 수행하는데 이사회에 참석하여 독립적으로 이사의 업무를 감독할 수 있으며, 그 직무를 수행하기 위하여 필요한 때에는 영업의 보고를 요구할 수 있습니다. 당사는 감사업무에 필요한 회사정보가 효율적으로 수행되고, 공시될 수 있도록 내부회계관리규정을 운영 중에 있습니다. |
나. 감사
1) 감사의 인적사항
| 성 명 | 주 요 경 력 | 재임기간 | 겸직현황(재임년수) |
| 김영현 | 전) 삼일회계법인 31년 근무 전) 중앙일보 (사)위스타트운동본부 감사 현) 새만금 투자유치 자문위원 |
3년 | 해당사항 없음 |
2) 감사의 독립성
당사의 감사는 회사와의 거래, 최대주주 또는 주요주주와의 관계 등 기타 이해관계 가 없으며, 「상법」과 당사의 정관에서 정한 바에 따라 감사로서의 권한과 의무를 수행하고 있으며 구체적인 내용은 아래와 같습니다.
| 정관 제50조(감사의 직무) |
|
① 감사는 회사의 회계와 업무를 감사한다. ② 감사는 회의의 목적사항과 소집의 이유를 기재한 서면을 이사회에 제출하여 임시 ③ 감사는 그 직무를 수행하기 위하여 필요한 때에는 자회사에 대하여 영업의 보고를 ④ 감사는 재임 중 뿐만 아니라 퇴임 후에도 직무상 취득한 회사의 영업상 비밀을 누설 |
3) 감사의 주요활동내역
| (기준일 : 2024년 03월 31일) |
| 회차 | 개최일자 | 의안내용 | 감사의 성명 |
| 김영현 (출석률 : 100%) |
|||
| 1 | 2024-01-02 | 분할계획서 변경의 건 | 참석 |
| 2 | 2024-01-02 | 회사분할종료 보고 주주총회 갈음의 건 | 참석 |
| 3 | 2024-01-30 | 자금 차입 결정의 건 | 참석 |
| 4 | 2024-02-13 | 제26기 재무제표(2023년) 확정의 건 | 참석 |
| 5 | 2024-02-27 | 제26기 정기주주총회 소집의 건 | 참석 |
| 6 | 2024-03-04 | 자회사(HLB에너지) 대여금 지급 및 자회사(HLB생명과학R&D) 추가 출자의 건 |
참석 |
| 7 | 2024-03-13 | 내부회계관리제도 운영실태의 보고의 건 내부회계관리제도 운영평가 보고의 건 |
참석 |
| 8 | 2024-03-14 | 우리은행 차입금 연장의 건 | 참석 |
| 9 | 2024-03-20 | 제26기 재무제표(2023년) 정정 확정의 건 | 참석 |
| 10 | 2024-03-21 | 주주배정 실권주 일반공모 유상증자 결의의 건 | 참석 |
4)감사 교육 미실시 내역
| 감사 교육 실시여부 | 감사 교육 미실시 사유 |
|---|---|
| 미실시 | 감사의 경력과 전문성을 고려한 바, 당사의 감사로 충분한 자격을 갖추었기에 교육을 실시하지 않았으나, 업무수행 관련 교육이 필요할 경우 진행할 예정입니다. |
5) 감사 지원조직 현황_경영기획팀 작성
| 부서(팀)명 | 직원수(명) | 직위(근속연수) | 주요 활동내역 |
|---|---|---|---|
| 경영전략본부 | 11 | 이사1명, 부장1명, 차장3명, 과장1명, 대리3명, 사원2명 (평균2.0년) |
이사회 운영 및 감사 직무 수행 지원 |
3. 주주총회 등에 관한 사항
가. 집중투표제, 서면투표제, 또는 전자투표제의 채택
당사 이사회는 제19기 정기주주총회부터 의결권 행사에 있어 주주의 편의를 제고하기 위하여 「상법」제368조의4에 따른 전자투표제도와「자본시장과 금융투자업에 관한 법률 시행령」제160조 제5호에 따른 전자위임장 권유제도를 주주총회에서 활용하기로 결의하였습니다.
당사는 주주총회 소집공고 시 전자적 방법으로 의결권을 행사할 수 있다는 내용을 공고하고 있으며, 제 25기 정기주주총회의 관리업무를 삼성증권에 위탁하였습니다. 한편, 당사는 집중투표제 및 서면투표제를 채택하고 있지 않습니다.
나. 투표제도 현황
| (기준일 : | 2024년 03월 31일 | ) |
| 투표제도 종류 | 집중투표제 | 서면투표제 | 전자투표제 |
|---|---|---|---|
| 도입여부 | 배제 | 도입 | 도입 |
| 실시여부 | - | - | 제26기 정기주주총회 실시 |
다. 소수주주권 행사여부
- 해당사항 없습니다.
라. 경영권 경쟁
- 해당사항 없습니다.
마. 의결권 현황
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 주식수 | 비고 |
|---|---|---|---|
| 발행주식총수(A) | 보통주식 | 107,600,282 | - |
| 종류주식 | - | - | |
| 의결권없는 주식수(B) | 보통주식 | 69,920 | - |
| 종류주식 | - | - | |
| 정관에 의하여 의결권 행사가 배제된 주식수(C) | - | - | - |
| - | - | - | |
| 기타 법률에 의하여 의결권 행사가 제한된 주식수(D) |
- | - | - |
| - | - | - | |
| 의결권이 부활된 주식수(E) | - | - | - |
| - | - | - | |
| 의결권을 행사할 수 있는 주식수 (F = A - B - C - D + E) |
보통주식 | 107,530,362 | - |
| 종류주식 | - | - |
바. 주식사무에 관한 사항
| 신주인수권의 내용 |
회사 정관 제11조 (신주인수권) ① 회사의 주주는 신주발행에 있어서 그가 소유한 주식수에 비례하여 신주의 배정을 받을 권리를 가진다. ② 제1항의 규정에 불구하고 다음 각호의 경우에는 주주 외의 자에게 신주를 배정할 수 있다. 1. 주주우선공모의 방식으로 신주를 발행하는 경우 5. 발행주식총수의 100분의 100을 초과하지 않는 범위 내에서 경영상필요로 주식예탁증서 발행에 따라 신주를 발행하는 경우 6. 발행주식총수의 100분의 100을 초과하지 않는 범위 내에서 사업상 중요한 기술도입, 연구개발, 생산, 판매, 자본제휴, 재무구조개선을 위하여 그 상대방에게 신주를 발행하는 경우 7. 주권을 유가증권거래소나 코스닥시장에 상장하기 위하여 신주를 모집하거나 모집을 위하여 인수인에게 인수하게 하는 경우 ③ 제2항의 각 호 중 어느 하나의 규정에 의해 신주를 발행할 경우 발행할 주식의 종류와 수 및 발행가격 등은 이사회의결의로 정한다. ④ 주주가 신주인수권을 포기 또는 상실하거나 신주배정에서 단주가 발생하는 경우에 그 처리 방법은 이사회 결의로 정한다. |
||
| 결산일 | 매년 12월 31일 | 정기주주총회일 | 3월 이내 |
| 주주명부폐쇄시기 | 매년 1월 1일부터 1월 7일까지 (7일간) | ||
| 명의개서대리인 | 하나은행 증권대행부 | ||
| 주주에 대한 특전 | 특이사항 없음 | ||
| 공고방법 | 회사의 공고는 회사의 인터넷 홈페이지(www.hlb-ls.com)에 한다. 다만, 전산장애 또는 그 밖의 부득이한 사유로 회사의 인터넷 홈페이지에 공고를 할 수 없는 때에는 서울특별시 내에서 발행되는 한국경제신문에 게재한다. | ||
VI. 주주에 관한 사항
가. 최대주주 및 특수관계인의 주식소유 현황
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 주, %) |
| 성 명 | 관 계 | 주식의 종류 |
소유주식수 및 지분율 | 비고 | |||
|---|---|---|---|---|---|---|---|
| 기 초 | 기 말 | ||||||
| 주식수 | 지분율 | 주식수 | 지분율 | ||||
| HLB | 본인 | 보통주 | 19,688,685 | 19.33 | 19,688,685 | 18.30 | - |
| 계 | 보통주 | 19,688,685 | 19.33 | 19,688,685 | 18.30 | - | |
| - | - | - | - | - | - | ||
※ 상기 지분율 산정 근거
- 기초 발행주식 총수 : 101,866,689주(2023/12/31 기준)
- 당분기말 발행주식 총수 : 107,600,282주(2024/03/31 기준)
주) 지분율은 소수 셋째자리에서 반올림한 수치
나. 최대주주의 주요경력 및 개요
(1) 최대주주(법인 또는 단체)의 기본정보
| 명 칭 | 출자자수 (명) |
대표이사 (대표조합원) |
업무집행자 (업무집행조합원) |
최대주주 (최대출자자) |
|||
|---|---|---|---|---|---|---|---|
| 성명 | 지분(%) | 성명 | 지분(%) | 성명 | 지분(%) | ||
| HLB | 134,871 | 진양곤 | 7.30 | - | - | 진양곤 | 7.30 |
| 백윤기 | - | - | - | - | - | ||
(*1) 지분율 및 출자자수(주주수)는 보통주 기준
(*2) 상기 출자자수 및 지분율은 최근 주주명부 폐쇄일인 2023년 12월 31일 기준이며, 지분율은 최대주주와 특수관계인이 소유하고 있는 주식을 합산하여 기재하였습니다.
(2) 법인 또는 단체의 대표이사, 업무집행자, 최대주주의 변동내역
| 변동일 | 대표이사 (대표조합원) |
업무집행자 (업무집행조합원) |
최대주주 (최대출자자) |
|||
|---|---|---|---|---|---|---|
| 성명 | 지분(%) | 성명 | 지분(%) | 성명 | 지분(%) | |
| 2019년 03월 27일 | 김하용 | 0.19 | - | - | 진양곤 | 15.81 |
| 2019년 03월 27일 | 김성철 | 1.42 | - | - | 진양곤 | 15.81 |
| 2019년 06월 10일 | 진양곤 | 15.6 | - | - | 진양곤 | 15.6 |
(3) 최대주주(법인 또는 단체)의 최근 결산기 재무현황
| (단위 : 백만원) |
| 구 분 | |
|---|---|
| 법인 또는 단체의 명칭 | HLB |
| 자산총계 | 751,722 |
| 부채총계 | 169,475 |
| 자본총계 | 582,246 |
| 매출액 | 42,900 |
| 영업이익 | -125,024 |
| 당기순이익 | -206,042 |
(*) 상기 재무현황은 최근 결산기인 2023년 12월 31일 기준이며, 연결기준 재무현황입니다.
(4) 사업현황 등 회사 경영 안정성에 영향을 미칠 수 있는 주요 내용
- 해당사항 없습니다.
(5) 최대주주의 최대주주(법인 또는 단체)의 개요
당사 최대주주인 HLB는 1985년 10월 18일에 설립되어 1996년 07월 27일자로 코스닥시장에 상장(종목코드 028300) 된 후 현재까지 상장을 유지하고 있습니다. 보고서 작성 기준일 체외진단의료기기 등을 제조, 판매하는 체외진단 의료기기 및 의약외품 사업과 특수선박 및 GRP/ GRE PIPE를 제조 및 판매하는 사업을 영위하고 있습니다. 연결대상 종속회사는 총 5개 사이며, 이중 주요 종속회사인 Elevar Therapeutics, Inc.와 Immunomic Therapeutics,Inc.는 바이오연구개발사업을 영위하고 있습니다.
다. 최대주주 변동내역
- 최근 3년간 최대주주 변동내역 없음
라. 주식 소유현황
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 주) |
| 구분 | 주주명 | 소유주식수 | 지분율(%) | 비고 |
|---|---|---|---|---|
| 5% 이상 주주 | HLB | 19,688,685 | 18.30 | |
| - | - | - | - | |
| 우리사주조합 | - | - | - | |
마. 소액주주현황
| (기준일 : | 2023년 12월 31일 | ) | (단위 : 주) |
| 구 분 | 주주 | 소유주식 | 비 고 | ||||
|---|---|---|---|---|---|---|---|
| 소액 주주수 |
전체 주주수 |
비율 (%) |
소액 주식수 |
총발행 주식수 |
비율 (%) |
||
| 소액주주 | 60,854 | 60,856 | 99.99 | 82,178,004 | 101,866,689 | 80.67 | - |
| (*) 상기 출자자수 및 지분율은 최근 사업연도말 주주명부 폐쇄일인 2023년 12월 31일 기준입니다. |
바. 주가 및 주식거래실적
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 원, 주) |
| 종 류 | 23년 10월 | 23년 11월 | 23년 12월 | 24년 01월 | 24년 02월 | 24년 03월 | ||
| 보통주 | 주가 | 최 고 | 9,500 | 9,800 | 11,790 | 15,800 | 17,200 | 24,300 |
| 최 저 | 8,410 | 8,790 | 9,400 | 10,120 | 13,730 | 14,190 | ||
| 평균 | 9,211 | 9,316 | 10,615 | 11,125 | 15,361 | 18,677 | ||
| 거래량 | 최고(일) | 431,010 | 909,046 | 2,090,298 | 21,557,515 | 10,486,035 | 28,428,253 | |
| 최저(일) | 171,730 | 128,953 | 168,009 | 264,161 | 859,666 | 869,185 | ||
| 월간거래량 | 289,969 | 253,537 | 718,533 | 2,829,556 | 2,798,015 | 6,108,616 | ||
(*) 상기 자료는 한국거래소(www.krx.co.kr) 종목정보를 참조 하였습니다.
VII. 임원 및 직원 등에 관한 사항
1. 임원 및 직원 등의 현황
가. 등기임원 현황
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 주) |
| 성명 | 성별 | 출생년월 | 직위 | 등기임원 여부 |
상근 여부 |
담당 업무 |
주요경력 | 소유주식수 | 최대주주와의 관계 |
재직기간 | 임기 만료일 |
|
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 의결권 있는 주식 |
의결권 없는 주식 |
|||||||||||
| 진양곤 | 남 | 1966년 01월 | 회장 | 사내이사 | 상근 | 이사회의장 | 연세대학교 경제학 대학원 졸업(1993.02) 현) HLB 대표이사 현) HLB제약 이사 현) HLB글로벌 이사 |
- | - | 임원 | 8년 2개월 | 2027년 03월 28일 |
| 남상우 | 남 | 1957년 10월 | 대표이사 | 사내이사 | 상근 | 각자 대표이사 (경영총괄) |
연세대학교 경영대학원 졸업(2003.02) 전) HLB 대표이사/사장 (2009.01~2012.01) 현) HLB일렉 대표이사 현) HLB생명과학 대표이사 |
- | - | 계열회사 임원 | 4년 2개월 | 2026년 03월 31일 |
| 한용해 | 남 | 1962년 05월 | 대표이사 | 사내이사 | 상근 | 각자 대표이사 (바이오총괄) |
서울대학교 약제학 대학원 졸업(1995.02) 전) 대웅제약 연구본부장 (2016.12 ~ 2018.02) 전) CJ헬스케어 Innovation 센터장 (2018.07 ~ 2019.12) 현) HLB생명과학 대표이사 |
- | - | 계열회사 임원 | 4년 2개월 | 2025년 03월 31일 |
| 이근식 | 남 | 1973년 06월 | 사내이사 | 사내이사 | 상근 | 경영관리 | 현) HLB생명과학 경영전략본부 상무 전) HLB제약 경영관리 상무 (2020.10 ~ 2023.08) |
- | - | 계열회사 임원 | 0년 8개월 | 2027년 03월 28일 |
| 심연섭 | 남 | 1975년 03월 | 사외이사 | 사외이사 | 비상근 | 경영고문 | 현) (주)맑은기술 대표이사 전) HLB글로벌 사외이사 |
- | - | 계열회사 임원 | 0년 0개월 | 2027년 03월 28일 |
| 송세빈 | 남 | 1962년 05월 | 사외이사 | 사외이사 | 비상근 | 경영고문 | 현) 법무법인(유) 화우 파트너변호사 전) (주)이마트 법무실장 (2016.06 ~ 2019.12) |
- | - | 계열회사 임원 | 0년 0개월 | 2027년 03월 28일 |
| 김영현 | 남 | 1958년 11월 | 감사 | 감사 | 상근 | 상임감사 | 홍익대학교 경영대학원 졸업(2001.01) 전) 삼일회계법인 31년 근무 (1985.01 ~ 2016.06) 전) 중앙일보 (사)위스타트운동본부 감사 (2006.03 ~ 2017.01) 현) 새만금 투자유치 자문위원 |
- | - | 계열회사 임원 | 3년 11개월 | 2026년 03월 31일 |
나. 미등기임원 현황
| (기준일 : | 2024년 03월 31일 | ) |
| 성명 | 성별 | 출생년월 | 직위 | 상근 여부 |
담당 업무 |
주요경력 | 최대주주와의 관계 |
재직기간 |
| 조용호 | 남 | 1980.01 | 사장 | 상근 | 메디케어 사업총괄 |
전) 에임 대표이사 (2010.07 ~ 2022.09) 현) HLB생명과학 메디케어사업부 총괄 |
계열회사 임원 | 1년 6개월 |
|
김연태 |
여 |
1964.05 |
부사장 |
상근 |
바이오총괄 |
전) 분당차병원 임상시험센터 부센터장 (2013.06 ~ 2014.05) 전) 한국오츠카제약 임상개발부문장 전무 (2014.06 ~ 2023.08) 현) HLB생명과학 바이오사업부 총괄 |
계열회사 임원 |
0년 7개월 |
| 이광희 | 남 | 1962.04 | 부사장 | 상근 | 의료기기 사업총괄 |
전) (주)화진메디칼 사장 (2021.01.01 ~ 2023.9.30) 현) HLB생명과학 의료기기사업부 총괄 |
계열회사 임원 | 0년 6개월 |
| 이웅호 | 남 | 1988.04 | 이사 | 상근 | 메디케어 OEM영업부문 |
전) 에임 영업이사 (2013.06 ~ 2022.09) 현) HLB생명과학 메디케어케어사업부 OEM영업부문 부문장 |
계열회사 임원 | 1년 6개월 |
| 김지호 | 남 | 1982.02 | 이사 | 상근 | 메디케어 사업개발부문 |
전) 한국헤보트진단 구매담당 (2012.09 ~ 2022.02) 전) 티유브이슈드 코리아 Medical & Health Services (2022.03 ~ 2022.05) 현) HLB생명과학 메디케어사업부 사업개발부문 부문장 |
계열회사 임원 | 1년 6개월 |
| 유춘성 | 남 | 1966.05 | 상무 | 상근 | 의료기기 사업본부 |
전) Ansell Korea, Head of Sales & Business Development (2012.07 ~ 2019.05) 전) ㈜메디메스터 영업&마케팅 전무이사 (2019.07 ~ 2023.09) 현) HLB생명과학 의료기기사업부 사업본부장 |
계열회사 임원 | 0년 6개월 |
| 최승호 | 남 | 1980.07 | 이사 | 상근 | 경영관리부문 | 전) 넥스트사이언스 기획담당 (2019.07 ~ 2021.03) 현) HLB생명과학 경영관리부문 부문장 |
계열회사 임원 | 3년 0개월 |
다. 직원 등 현황_경영기획팀 작성
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 천원) |
| 직원 | 소속 외 근로자 |
비고 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 사업부문 | 성별 | 직 원 수 | 평 균 근속연수 |
연간급여 총 액 |
1인평균 급여액 |
남 | 여 | 계 | |||||
| 기간의 정함이 없는 근로자 |
기간제 근로자 |
합 계 | |||||||||||
| 전체 | (단시간 근로자) |
전체 | (단시간 근로자) |
||||||||||
|
바이오사업
|
여 |
1 |
0 |
1 |
0 |
2 |
0.7 |
56,360 |
28,180 |
- | - | - | - |
|
메디케어사업
|
남 |
44 |
0 |
3 |
0 |
47 |
2.3 |
712,629 |
15,162 |
- | |||
|
메디케어사업
|
여 |
20 |
0 |
3 |
0 |
23 |
1.9 |
170,713 |
7,422 |
- | |||
|
의료기기사업
|
남 |
31 |
0 |
1 |
0 |
32 |
0.6 |
387,155 |
12,099 |
- | |||
|
의료기기사업
|
여 |
33 |
0 |
3 |
0 |
36 |
0.5 |
221,059 |
6,141 |
- | |||
|
경영관리
|
남 |
8 |
0 |
0 |
1 |
8 |
2.5 |
140,416 |
17,552 |
- | |||
|
경영관리
|
여 |
5 |
0 |
0 |
1 |
5 |
0.8 |
56,731 |
11,346 |
- | |||
| 합 계 |
142 |
0 |
11 |
2 |
153 |
- |
1,745,062 |
11,406 |
- | ||||
라. 미등기임원 보수 현황_경영기획팀 작성
| (기준일 : | 2024년 03월 31일 | ) | (단위 : 천원) |
| 구 분 | 인원수 | 연간급여 총액 | 1인평균 급여액 | 비고 |
|---|---|---|---|---|
| 미등기임원 | 7 | 233,629 | 33,376 | - |
2. 임원의 보수 등
| <이사ㆍ감사 전체의 보수현황> |
가. 주주총회 승인금액
| (단위 : 천원) |
| 구 분 | 인원수 | 주주총회 승인금액 | 비고 |
|---|---|---|---|
| 이사 | 6 | 1,500,000 | - |
| 감사 | 1 | 150,000 | - |
나. 보수지급금액_경영기획팀 작성
2-1. 이사ㆍ감사 전체
| (단위 : 천원) |
| 인원수 | 보수총액 | 1인당 평균보수액 | 비고 |
|---|---|---|---|
| 9 | 345,610 | 49,308 | - |
(*) 상기 보수액에는 2024년 3월 28일 사임한 사외이사 김윤, 사외이사 최수자 보수가 포함되어 있습니다.
2-2. 유형별
| (단위 : 천원) |
| 구 분 | 인원수 | 보수총액 | 1인당 평균보수액 |
비고 |
|---|---|---|---|---|
| 등기이사 (사외이사, 감사위원회 위원 제외) |
4 | 307,440 | 76,860 | - |
| 사외이사 (감사위원회 위원 제외) |
4 | 12,360 | 6,180 | - |
| 감사위원회 위원 | - | - | - | - |
| 감사 | 1 | 25,360 | 25,360 | - |
(*) 상기 보수액에는 2024년 3월 28일 사임한 사외이사 김윤, 사외이사 최수자 보수가 포함되어 있습니다.
| <보수지급금액 5억원 이상인 이사ㆍ감사의 개인별 보수현황> |
다. 개인별 보수지급금액
| (단위 : 원) |
| 이름 | 직위 | 보수총액 | 보수총액에 포함되지 않는 보수 |
|---|---|---|---|
| - | - | - | - |
※ 이사 및 감사에게 지급한 개인별 보수가 5억원 이상인 경우가 없습니다.
1) 산정기준 및 방법
- 해당사항 없습니다.
| (단위 : 백만원) |
| 이름 | 보수의 종류 | 총액 | 산정기준 및 방법 | |
|---|---|---|---|---|
| - | 근로소득 | 급여 | - | - |
| 상여 | - | - | ||
| 주식매수선택권 행사이익 |
- | - | ||
| 기타 근로소득 | - | - | ||
| 퇴직소득 | - | - | ||
| 기타소득 | - | - | ||
| <보수지급금액 5억원 이상 중 상위 5명의 개인별 보수현황> |
라. 개인별 보수지급금액
| (단위 : 백만원) |
| 이름 | 직위 | 보수총액 | 보수총액에 포함되지 않는 보수 |
|---|---|---|---|
| - | - | - | - |
※ 보수지급액이 5억원 이상인 상위 5명의 보수현황은 없습니다.
1) 산정기준 및 방법
| (단위 : 백만원) |
| 이름 | 보수의 종류 | 총액 | 산정기준 및 방법 | |
|---|---|---|---|---|
| - | 근로소득 | 급여 | - | - |
| 상여 | - | - | ||
| 주식매수선택권 행사이익 |
- | - | ||
| 기타 근로소득 | - | - | ||
| 퇴직소득 | - | - | ||
| 기타소득 | - | - | ||
마. 주식매수선택권의 부여 및 행사현황
- 해당사항 없습니다.
VIII. 계열회사 등에 관한 사항
가. 계열회사 현황(요약)
| (기준일 : | 2023년 12월 31일 | ) | (단위 : 사) |
| 기업집단의 명칭 | 계열회사의 수 | ||
|---|---|---|---|
| 상장 | 비상장 | 계 | |
| HLB그룹 | 9 | 35 | 44 |
| ※상세 현황은 '상세표-2. 계열회사 현황(상세)' 참조 |
나. 타법인출자 현황(요약)
| (기준일 : | 2023년 12월 31일 | ) | (단위 : 백만원) |
| 출자 목적 |
출자회사수 | 총 출자금액 | |||||
|---|---|---|---|---|---|---|---|
| 상장 | 비상장 | 계 | 기초 장부 가액 |
증가(감소) | 기말 장부 가액 |
||
| 취득 (처분) |
평가 손익 |
||||||
| 경영참여 | 3 | 5 | 8 | 114,301 | 35,544 | -1,654 | 148,191 |
| 일반투자 | - | - | - | - | - | - | - |
| 단순투자 | 1 | 3 | 4 | 55,289 | -1,651 | 45,846 | 99,484 |
| 계 | 4 | 8 | 12 | 169,590 | 33,893 | 44,192 | 247,675 |
| ※상세 현황은 '상세표-3. 타법인출자 현황(상세)' 참조 |
IX. 대주주 등과의 거래내용
가. 특수관계자 현황
| 구 분 | 회사명 |
|---|---|
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ |
| 관계기업 | 에이치엘비제약㈜ |
| 에이치벨류에셋(주1) | |
| ㈜두산포천에너지 | |
| 에이치엘비사이언스㈜ | |
| 에이치엘비인베스트먼트㈜ | |
| 기타의 특수관계자 | 에이치엘비글로벌㈜ |
| 에이치엘비일렉㈜ | |
| 에이치엘비아이 알밤 제1호 투자조합 | |
| 에이치엘비네트웍스㈜ | |
| Elevar Therapeutics, Inc. | |
| Immunomic Therapeutics, Inc. | |
| 에이치엘비바이오스텝㈜ | |
| ㈜펭귄오션레저 | |
| 에이치엘비생활건강㈜ | |
| ㈜프레시코 | |
| ㈜코아바이오 | |
| 에포케㈜ | |
| 에이치엘비테라퓨틱스㈜ | |
| 바다중공업㈜ | |
| 현대요트㈜ | |
| ㈜노터스 | |
| 에이치엘비에프앤비㈜ | |
| 에이치엘비파나진㈜ | |
| 브이에스팜㈜ | |
| 에이치엘비이노베이션㈜ | |
| 임직원 |
(주1) 당분기 중 신규로 편입되었습니다.
나. 특수관계자와의 주요 거래내역
<당분기>
| (단위: 천원) |
| 구 분 | 회사명 | 매출 등 | 매입 등 | |||
|---|---|---|---|---|---|---|
| 매출 | 이자수익 | 기타 | 임차료 | 기타 | ||
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ | 128,971 | - | - | 31,460 | 30,508 |
| 관계기업 | 에이치엘비제약㈜ | 8,924 | - | - | - | - |
| 에이치엘비사이언스㈜ | 6,913 | - | - | - | - | |
| 소 계 | 15,837 | - | - | - | - | |
| 기타의 특수관계자 | Elevar Therapeutics, Inc. | - | - | - | - | 54,604 |
| ㈜프레시코 | - | - | - | - | 1,084 | |
| 에이치엘비글로벌㈜ | 3,000 | - | - | - | - | |
| ㈜펭귄오션레져 | - | - | - | - | 6,470 | |
| 에이치엘비바이오스텝㈜ | 420 | - | - | - | 54,543 | |
| 에이치엘비에프앤비㈜ | - | - | - | - | 15,312 | |
| 에포케㈜ | - | - | - | - | 12,740 | |
| 바다중공업 | - | 3,125 | - | - | - | |
| 브이에스팜㈜ | 40,128 | - | - | - | - | |
| 임직원 | - | - | 376 | - | - | |
| 소 계 | 43,548 | 3,125 | 376 | - | 144,753 | |
| 합계 | 188,356 | 3,125 | 376 | 31,460 | 175,261 | |
<전분기>
| (단위: 천원) |
| 구 분 | 회사명 | 매출 등 | 매입 등 | ||||
|---|---|---|---|---|---|---|---|
| 공사매출 | 임대매출 | 이자수익 | 기타 | 임차료 | 기타 | ||
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ | 54,000 | 84,300 | - | 72,936 | 57,510 | 27,643 |
| 관계기업 | 에이치엘비제약(주) | - | 5,100 | - | (386) | - | - |
| 기타의 특수관계자 | Elevar Therapeutics, Inc. | - | - | - | - | - | 10,583 |
| Immunomic Therapeutics, Inc. | - | 1,330 | - | - | - | - | |
| 에이치엘비생활건강㈜ | - | - | - | - | - | 292 | |
| ㈜프레시코 | - | - | - | - | - | 2,751 | |
| 에이치엘비글로벌㈜ | - | - | - | 300 | - | - | |
| 에이치엘비사이언스㈜ | - | 3,000 | - | 1,063 | - | - | |
| ㈜펭귄오션레져 | - | - | - | - | - | 14,610 | |
| 에이치엘비인베스트먼트㈜ | - | - | - | - | - | 9,863 | |
| 바다중공업㈜ | - | - | 10,939 | - | - | - | |
| 에이치엘비바이오스텝㈜ | - | - | - | - | - | 46,550 | |
| 임직원 | - | - | 530 | - | 10,200 | - | |
| 소 계 | - | 4,330 | 11,469 | 1,363 | 10,200 | 84,649 | |
| 합 계 | 54,000 | 93,730 | 11,469 | 73,913 | 67,710 | 112,292 | |
다. 특수관계자에 대한 채권ㆍ채무의 주요 내역
<당분기말>
| (단위: 천원) |
| 구 분 | 회사명 | 채권 등 | 채무 등 | |||
|---|---|---|---|---|---|---|
| 매출채권 | 기타채권 | 전환사채(주1) | 기타채무 | 신주인수권부사채(주2) | ||
| 유의적인 영향력을행사하는 기업 | 에이치엘비㈜ | - | 5,742 | - | 4,787 | 19,603,370 |
| 관계기업 | 에이치엘비제약㈜ | - | 3,707 | - | 40,000 | - |
| ㈜두산포천에너지(주3) | - | 505,804 | - | - | - | |
| 에이치엘비사이언스㈜ | - | 658 | - | 25,000 | - | |
| 소 계 | - | 510,169 | - | 65,000 | - | |
| 기타의 특수관계자 | 에이치엘비테라퓨틱스㈜ | - | - | - | 8,300,000 | - |
| Elevar Therapeutics, Inc. | - | - | - | 87,640 | - | |
| ㈜프레시코 | - | - | - | 712 | - | |
| 에이치엘비글로벌㈜ | - | 1,100 | - | - | - | |
| 에이치엘비바이오스텝㈜ | 139 | - | 10,242,854 | - | - | |
| ㈜펭귄오션레져 | - | 6,750 | - | - | - | |
| 브이에스팜㈜ | 20,659 | - | - | - | - | |
| 임직원 | - | 36,000 | - | - | - | |
| 소 계 | 20,798 | 43,850 | 10,242,854 | 8,388,352 | - | |
| 합계 | 20,798 | 559,761 | 10,242,854 | 8,458,139 | 19,603,370 | |
(주1) 공정가치평가 후 금액입니다.
(주2) 신주인수권부사채 채무 잔액은 액면금액입니다.
(주3) 회사는 해당 대여금에 대하여 전액 대손충당금을 설정하였습니다.
<전기말>
| (단위: 천원) |
| 구 분 | 회사명 | 채권 등 | 채무 등 | |||
|---|---|---|---|---|---|---|
| 매출채권 | 기타채권 | 전환사채(주1) | 기타채무 | 신주인수권부사채(주2) | ||
| 유의적인 영향력을행사하는 기업 | 에이치엘비㈜ | - | 239,319 | - | 793,321 | 19,603,370 |
| 관계기업 | 에이치엘비제약㈜ | - | 77,155 | - | 46,810 | - |
| ㈜두산포천에너지(주3) | - | 505,804 | - | - | - | |
| 에이치엘비사이언스㈜ | - | 2,756 | - | 13,143 | - | |
| 소계 | - | 585,715 | - | 59,954 | - | |
| 기타의 특수관계자 | 에이치엘비테라퓨틱스㈜ | - | 98,392 | - | 8,314,300 | - |
| Elevar Therapeutics, Inc. | - | - | - | 369,693 | - | |
| 에이치엘비생활건강㈜ | - | 1,216 | - | - | - | |
| ㈜프레시코 | - | 5,505 | - | 160 | - | |
| 에이치엘비글로벌㈜ | - | 49,862 | - | 7,951 | - | |
| 바다중공업㈜ | - | 823,179 | - | - | - | |
| ㈜펭귄오션레저 | - | 292 | - | - | - | |
| 에이치엘비바이오스텝㈜ | - | 85,809 | 10,815,389 | 30 | - | |
| 에이치엘비에프앤비㈜ | - | 18,234 | - | - | - | |
| 현대요트㈜ | - | 1,327 | - | - | - | |
| ㈜코아바이오 | - | 2,578 | - | - | - | |
| 에이치엘비네트웍스㈜ | - | 5,063 | - | 22,754 | - | |
| 에포케㈜ | - | 9,981 | - | 12,597 | - | |
| 에이치엘비파나진㈜ | - | 7,290 | - | - | - | |
| 에이치엘비이노베이션㈜ | - | 38,352 | - | - | - | |
| 에이치엘비인베스트먼트㈜ | - | 4,276 | - | - | - | |
| ㈜펭귄오션레져 | - | 202 | - | - | - | |
| 브이에스팜㈜ | 22,205 | - | - | - | - | |
| 임직원 | - | 45,000 | - | - | - | |
| 소계 | 22,205 | 1,196,557 | 10,815,389 | 8,727,486 | - | |
| 합계 | 22,205 | 2,021,591 | 10,815,389 | 9,580,761 | 19,603,370 | |
(주1) 공정가치평가 후 금액입니다.
(주2) 신주인수권부사채 채무 잔액은 액면금액입니다.
(주3) 연결회사는 해당 대여금에 대하여 전액 대손충당금을 설정하였습니다.
라. 특수관계자와의 자금거래 내역
<당분기>
| (단위: 천원) |
| 구 분 | 회사명 | 자금 대여(차입) 거래 | 금융수익(원가) | 현금 출자 등 | |
|---|---|---|---|---|---|
| 대여(차입) | 회수(상환) | 이자수익 | |||
| 관계기업 | 에이치벨류에셋 | - | - | - | 5,000,000 |
| 소계 | - | - | - | 5,000,000 | |
| 기타의 특수관계자 | 에이치엘비아이알밤제1호투자조합 | - | - | - | 800,000 |
| 바다중공업㈜ | - | (800,000) | 3,125 | - | |
| 임직원 | - | (1,500) | - | - | |
| 소계 | - | (801,500) | 3,125 | 800,000 | |
| 합계 | - | (801,500) | 3,125 | 5,800,000 | |
<전분기>
| (단위: 천원) |
| 구 분 | 회사명 | 자금 대여(차입) | 리스부채 | 유상증자 | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 기초 대여금 (차입금) |
대여 (차입) |
회수 (상환) |
기말대여금 (차입금) |
기초 리스부채 |
이자비용 | 리스부채 상환 |
기말 리스부채 |
|||
| 유의적인 영향력을 행사하는 기업 | 에이치엘비㈜ | - | - | - | - | 393,837 | 9,077 | (64,200) | 338,714 | - |
| 관계기업 | ㈜두산포천에너지 | 505,804 | - | - | 505,804 | - | - | - | - | - |
| 기타의 특수관계자 | 바다중공업㈜ | 1,000,000 | - | (200,000) | 800,000 | - | - | - | - | - |
| 에이치엘비 이노베이션㈜ | - | - | - | - | - | - | - | - | 1,999,999 | |
| 임직원 | 33,083 | - | (2,750) | 30,333 | - | - | - | - | - | |
| 소 계 | 1,033,083 | - | (202,750) | 830,333 | - | - | - | - | - | |
| 합 계 | 1,538,887 | - | (202,750) | 1,336,137 | - | - | - | - | 1,999,999 | |
마. 주요 경영진에 대한 보상
연결회사는 기업 활동의 계획ㆍ운영ㆍ통제에 대하여 중요한 권한과 책임을 가진 등기임원, 비등기임원, 내부감사 책임자 및 각 사업부문장 등을 주요 경영진으로 판단하였으며, 당기 및 전기 중 주요 경영진에 대한 보상을 위해 지급한 금액은 다음과 같습니다.
| (단위: 천원) |
| 구분 | 당분기 | 전분기 |
|---|---|---|
| 단기종업원급여 | 567,993 | 458,392 |
| 퇴직급여 | 497,493 | 67,193 |
| 합계 | 1,065,486 | 525,585 |
바. 특수관계자와의 기타 유의적인 거래 및 약정사항
(1) 연결회사는 전기 중 제9회 무기명식 무보증 공모 분리형 신주인수권부사채를 발행하였으며, 연결회사에 유의적인 영향력을 행사하는 회사인 에이치엘비㈜가 공모에참여하여 액면가 기준 19,603,370천원을 취득하였습니다. 동 신주인수권부사의 사채권자는 발행일(2022년 6월 15일)부터 24개월이 경과하는 날(2024년 6월 15일)부터 신주인수권부사채의 만기일까지 신주인수권부사채의 조기상환을 청구할 수 있는 권리를 보유하고 있습니다.
사. 현재 특수관계자에게 제공한 담보 및 보증 등
| 특수관계 구분 | 특수관계자명 | 담보제공 및 보증금액 | 보증 제공처 | 비고 |
|---|---|---|---|---|
| 기타의 특수관계자 | 에포케㈜ | 1,000,000,000 | 한국투자증권㈜ | 연대보증 |
에포케㈜ (특수관계자)가 한국투자증권으로부터 차입한 차입금에 대한 연대보증인으로서, ㈜신화어드밴스가 한국투자증권에 보유하고 있는 MMF 금융자산 (장부금액: 15억원)에 대한 질권이 설정되었습니다(채권최고액: 10억원).
(2) 연결회사는 전기 중 회사 또는 회사가 지정하는 제3자에게 매도청구권(Call Option)을 부여하는 조건의 제10회 무기명식 무보증 사모 전환사채를 발행하였습니다. 연결회사는 동 전환사채 발행시 매도청구권을 특수관계자인 에포케㈜에게 부여하였으며, 동 매도청구권과 관련하여 발행시 매도청구권의 공정가치 2,309,652천원을 파생상품거래손실로 인식하였습니다.
X. 그 밖에 투자자 보호를 위하여 필요한 사항
1. 공시내용 진행 및 변경사항
| 신고일자 | 제 목 | 신 고 내 용 (최종) | 신고사항의 진행 상황 |
| 2024년 03월 22일 | - 주요사항보고서(유상증자결정) - 증권신고서(지분증권) |
1. 신주의 종류와 수 : 보통주 11,005,125주 (액면가 500원) 2. 자금조달의 목적 : 시설자금 60억원 / 운영자금 444억원 / 채무상환자금 981억원 / 기타자금 15억원 3. 증자방식 : 주주배정후 실권주 일반공모 4. 예정발행가 : 13,630원 * 확정 예정일 : 2024년 06월 11일 5. 신주배정기준일 : 2024년 05월 10일 6. 쳥약예정일(구주주) : 2024년 06월 14일, 17일 7. 납입일 : 2024년 06월 24일 8. 대표주관회사 : 한국투자증권(주), 케이비증권(주) 9. 이사회결의일: 2024년 03월 21일 |
진행중 |
| 2024년 04월 04일 | - [정정] 증권신고서(지분증권) | 제 1부 모집 또는 매출에 관한 일반사항 기재 정정 | |
| 2024년 04월 19일 | - [정정] 증권신고서(지분증권) | 제 1부 모집 또는 매출에 관한 일반사항 기재 정정 | |
| 2024년 04월 22일 | - 투자설명서 | 증권신고서 효력 발생에 따른 투자설명서 제출 | |
| 2024년 05월 08일 | - 유상증자 1차발행가액결정 - [정정] 주요사항보고서(유상증자결정) - [정정] 증권신고서(지분증권) - [정정] 투자설명서 |
유상증자 1차 발항가액 결정에 따른 제출 |
| (*) 당사는 2024년 3월 21일에 유상증자 발행을 결정하였습니다. 기타 자세한 사항은 2024년 3월 21일에 공시한 주요사항보고서, 2024년 04월 19일 제출한 [정정] 증권신고서 및 2024년 04월 22일 제출한 투자설명서 참고하시기 바랍니다. |
2. 우발부채 등에 관한 사항
가. 중요한 소송사건
(1) 회사가 피고인 사건
| (단위: 천원) |
| 원고 | 계류 법원 | 소송 금액 | 소송 내용 | 진행 상황 |
|---|---|---|---|---|
| 현대로오텍 | 광주지방법원 | 1,458,874 | 공사대금 청구 | 소송절차로 이행 |
| 주원전력 | 전주지방법원 | 883,872 | 공사대금 청구 | 소송절차로 이행 |
(2) 회사가 원고인 사건
| (단위: 천원) |
| 피고 | 계류 법원 | 소송 금액 | 소송 내용 | 진행 상황 |
|---|---|---|---|---|
| 엔에이치투자증권㈜(주1) | 서울남부지방법원 | 10,000,000 | 부당이득금반환청구 | 1심 진행중 |
| 박승규 (탑스코리아)(주2) | 수원지방법원 | 55,000 | 명도소송 | 판결선고 |
|
(주1) 회사가 펀드투자를 위해 엔에이치투자증권㈜에 최초 예치한 금액이나. 사기적 부정거래행위 및 불완전판매 요소가 발견되어 부당이득금 반환 청구소송을 진행 중입니다. 회사의 등기임원은 본 사건과관련하여 발생가능한 손실을 보전하기 위하여 회사의 등기임원이 보유한 에이치엘비㈜의 주식을 법무법인에 위탁하는 계약을 체결하였습니다. (주2) 회사는 본 사건의 판결에 대해 2024년 1월 18일자로 승소하여 판결 확정되었습니다. ※ 기존 당사 원고, 피고 엘케이쏠라테크 공사대금 청구관련 소송 진행 중 이였으나, 2024년 1월 1일 당사 에너지사업부 회사분할하여 종속회사인 HLB솔루션으로 관련 소송 승계되어 소송 진행중입니다. 해당 사건은 현재 공사대금 채권 가압류 이의 신청 심문종결 후 소송비용액확정 사건으로 2024년 3월 18일에 일부인용 결정 되었습니다. |
당분기말 현재 계류중인 소송사건에 대해서는 소송의 결과를 합리적으로 예측할 수 없으며, 보고기간 후 발생한 중요한 소송사건은 없습니다.
나. 견질 또는 담보용 어음ㆍ수표현황
- 해당사항 없습니다.
다. 채무보증 현황
- 종속회사인 에이치엘비에너지㈜의 소각로 증축과 관련하여 기업은행으로부터 차입한 차입금에 대한 60억원 후순위 담보제공과 48억원 지급보증을 제공하였습니다.
| (단위: 천원) |
| 구분 | 회사명 | 보증처 | 이사회 결의일 | 판단근거 | 내용 | 지급보증금액 | 보증기간 | |
| 기초 (2024.01.01) |
기준일 (2024.03.31) |
|||||||
| 종속기업 | 에이치엘비에너지 | 기업은행 | 2023-12-15 | 이사회 결의 | 부동산 담보제공 | 6,000,000 | 6,000,000 | 2023.12.15 ~ 채무 상환시 |
| 신용 연대보증 | 4,800,000 | 4,800,000 | ||||||
| 합 계 | 10,800,000 | 10,800,000 | ||||||
라. 채무인수약정
- 해당사항 없습니다.
마. 그 밖의 우발채무 등
- 금융기관과 체결하고 있는 약정사항
| (단위: 천원) |
| 금융기관명 | 차입종 | 당분기말 | 전기말 | ||
|---|---|---|---|---|---|
| 약정금액 | 실행금액 | 약정금액 | 실행금액 | ||
| 하나은행 | 기업시설자금대출 | 3,500,000 | 3,000,000 | 3,500,000 | 3,125,000 |
| 국민은행 | 시설자금 대출 | 17,190,000 | 17,190,000 | 17,190,000 | 17,190,000 |
| 우리은행 | 기업운전일반자금대출 | 1,150,000 | 1,150,000 | 1,150,000 | 1,150,000 |
| 우리은행 | 시설자금 대출 | 4,800,000 | 4,800,000 | 4,800,000 | 4,800,000 |
| 산업은행 | 시설자금 대출 | 10,000,000 | 10,000,000 | 10,000,000 | 10,000,000 |
| 한국투자증권 | 주식담보대출 | 20,000,000 | 20,000,000 | - | - |
| 우리은행 | 원화지급보증 | 6,040,000 | 5,680,000 | 3,040,000 | 2,200,000 |
| 기업은행 | 원화지급보증 | 4,000,000 | 2,980,000 | 4,000,000 | 3,450,000 |
| 기업은행 | 중소기업 시설자금 (ESG) |
4,000,000 | 50,000 | 4,000,000 | 50,000 |
| 기업은행 | 오염방지자금 (환경정책) |
10,000,000 | 3,750,000 | 10,000,000 | 2,520,000 |
| 기업은행 | 시설설치자금 (환경정책) |
10,000,000 | - | - | - |
| 합계 | 90,680,000 | 68,600,000 | 57,680,000 | 44,485,000 | |
- 담보제공내역
| (단위: 천원) |
| 구분 | 장부가액 | 담보설정액 | 관련계정 | 관련금액 | 제공처 |
|---|---|---|---|---|---|
| 토지 및 건물 | 4,768,018 | 4,200,000 | 차입금 | 3,000,000 | 하나은행 |
| 토지 및 건물 | 15,560,511 | 10,884,000 | 차입금 | 9,070,000 | 국민은행 |
| 토지 및 건물 | 24,285,155 | 9,744,000 | 차입금 | 8,120,000 | 국민은행 |
| 토지 및 건물 | 955,260 | 3,222,000 | 차입금 | 1,150,000 | 우리은행 |
| 토지 및 건물 | 11,609,857 | 5,760,000 | 차입금 | 4,800,000 | 우리은행 |
| 토지 및 건물 | 14,360,238 | 12,000,000 | 차입금 | 10,000,000 | 산업은행 |
| 정기예금 | 6,040,000 | 6,303,158 | 기타금융자산 | 6,040,000 | 우리은행 |
| 정기예금 | 3,900,000 | 4,290,000 | 기타금융자산 | 3,900,000 | 기업은행 |
| 정기예금 | 120,000 | 120,000 | 기타금융자산 | 120,000 | 서울보증보험 |
| 토지 | 8,324,397 | 22,8000,000 | 장기차입금 | 3,800,000 | 한국투자증권 |
| 건물 | 589,226 | 장기차입금 | 기업은행 | ||
| 구축물 | 432,795 | 장기차입금 | 기업은행 | ||
| 기계장치 | 3,662,359 | 장기차입금 | 기업은행 | ||
| 주식 | 203,414,825 | 20,000,000 | 차입금 | 20,000,000 | 기업은행 |
| 합 계 | 298,022,641 | 99,323,158 | - | 70,000,000 | - |
| (주1) 에포케㈜ (특수관계자)가 한국투자증권으로부터 차입한 차입금에 대한 연대보증인으로서, 연결회사가 보유하고 있는 MMF 금융자산 (장부금액: 15억원)에 대한 질권이 설정되어있습니다. (채권최고액: 10억원). |
- 당사는 중국의 항서제약으로 부터 EGFR, HER2, HER4를 특이적으로 억제하는 표적항암제와 관련하여 파이로티닙의 한국 독점 라이센스를 2020년 9월에 22.1억원을 지급하고 획득하였습니다. 이와 관련하여 적응증 승인 및 확대와 관련 완제품의 판매로 인한 수익 발생 시 기술이전 대가의 일정 비율을 항서 제약에 지급해야 하는 약정을 맺고 있습니다.
- 당사는 Elevar Therapeutics, lnc.와 리보세라닙의 한국내 독점개발, 판매권 및 유럽, 일본에 대한 수익 지분을 무형자산으로 인식하였습니다. 이와 관련하여 당사는 FDA(정식명칭 기재)의 승인 및 리보세라닙의 적응증 범위 확대 및 관련 완제품 판매로 인한 수익 발생 시 판매액의 일정비율을 Elevar Therapeutics, lnc.에 지급해야 하는 약정을 맺고 있습니다.
3. 제재 등과 관련된 사항
- 해당사항 없습니다.
4. 작성기준일 이후 발생한 주요사항 등 기타사항
가. 작성기준일 이후 발생한 주요사항
- 해당사항 없습니다.
나. 외국지주회사의 자회사 현황
- 해당사항 없습니다.
다. 중소기업 등 기준검토표
 |
|
중소기업등 기준검토표 |
라. 합병등의 사후정보
< 중요한 자산양수도_에임>
(1) 자산양수도 배경
당사는 2022년 5월 31일 조용호 외 1인과 자산양수도 계약을 체결하고, 에임의 주식 100,000주(지분율 : 100.00%)를 양수하였으며, 자산양수도 가액은 97,900백만원입니다.
(2) 양수도주식수 및 양수도가액
| (단위 : 주, 천원) |
| 양도인 | 양수주식수 | 양수가액 | 양수대금 지급방법 | 비 고 |
| 조용호 | 64,000 | 62,656,000 | 당사는 본 거래대금 62,656,000천원을 양도인에 지급하여야 하나, 당사가 거래상대방에게 지급해야 할 HLB생명과학 제10회 무기명식 무보증 사모 전환사채의 사채납입대금 28,800,000천원을 상호 상계처리하기로 함에 따라 실제 현금 유출액은 33,856,000천원 입니다. | - |
| 문영주 | 36,000 | 35,244,000 | 당사는 본 거래대금 35,244,000천원을 양도인에 지급하여야 하나, 당사가 거래상대방에게 지급해야 할 HLB생명과학 제10회 무기명식 무보증 사모 전환사채의 사채납입대금 16,200,000천원을 상호 상계처리하기로 함에 따라 실제 현금 유출액은 19,044,000천원 입니다. | - |
| 합 계 | 100,000 | 97,900,000 | - | - |
※ 양도가액은 주당 979,000원을 적용하여 산출하였습니다.
(3) 자산양수도 주요일정
| 구분 | 일자 |
| 외부평가계약체결일 | 2022년 5월 11일 |
| 평가기간 | 2022년 5월 11일 ~ 2022년 5월 31일 |
| 이사회결의일 | 2022년 5월 31일 |
| 자산양수도 계약일 | 2022년 5월 31일 |
| 자산양수도 거래종결일 | 2022년 7월 1일 |
(4) 회사에 미치는 중요영향 등
당사는 본 자산양수도를 통하여 에임의 주식을 전량을 취득함으로써 재무구조 개선 및 안정적인 현금흐름 확보를 기대하고 있습니다. 총 양수가액은 97,900백만원이며, 거래대금 지급형태는 현금 52,900백만원 및 전환사채 45,000백만원 대용납입(상계)입니다.
※ 기타 자산양수도에 대한 자세한 사항은 주요사항보고서(2022.05.31, 2022.06.29) 공시를 참조하시기 바랍니다.
<회사 합병결정_에임>
(1) 합병 배경
당사는 안정적인 수익창출을 통한 재무안정성 구축 및 향후 예정된 바이오 사업과의 시너지극대화를 위해 2022년 10월 1일 에임와 합병하였습니다.
(2) 합병 당사회사의 개요
|
합병 후 존속회사 |
회사명 |
HLB생명과학 |
|
본점소재지 |
경기도 화성시 동탄첨단산업1로 51-9 | |
|
대표이사 |
남상우, 한용해 |
|
|
상장 여부 |
코스닥 상장법인 |
|
합병 후 소멸회사 |
회사명 |
에임 |
|
본점소재지 |
경기도 수원시 영통구 신원로 88 | |
|
대표이사 |
조용호 | |
|
상장 여부 |
비상장법인 |
(3) 합병 주요일정
|
구분 |
날짜 |
비고 |
|
|
합병 이사회 결의일 |
2022-07-18 |
- |
|
|
주요사항보고서 제출 |
2022-07-18 |
- |
|
|
주주확정기준일 공고 |
2022-08-04 |
- |
|
|
합병 계약 체결일 |
2022-07-21 |
- |
|
|
주주확정기준일 |
2022-08-04 |
- |
|
|
소규모합병 공고 |
2022-08-04 |
- |
|
|
주주명부 폐쇄기간 |
2022-08-05 ~ |
- |
|
|
합병반대의사 통지 접수기간 |
시작일 |
2022-08-04 |
- |
|
종료일 |
2022-08-18. |
||
|
합병승인 이사회 |
2022-08-24 |
주주총회 갈음 |
|
|
채권자 이의제출 공고 |
2022-08-26 |
- |
|
|
채권자 이의제출 기간 |
시작일 |
2022-08-26 |
- |
|
종료일 |
2022-09-26 | ||
|
합병기일 |
2022-10-01. |
- |
|
|
합병 종료보고 총회 |
2022-10-04 |
이사회 보고 |
|
|
합병 종료보고 공고 |
2022-10-04 |
- |
|
|
합병 등기 |
2022-10-07 |
- |
|
(4) 회사에 미치는 중요영향 등
당사는 에임의 발행주식을 100% 소유하여 합병신주를 발행하지 않는 무증자 합병으로 진행되었으며, 합병 완료 후 당사의 주주변경은 없습니다.
본 합병은 상법 제527조의3에 근거하여 소규모 합병에 해당되며, 합병승인은 이사회승인으로서 갈음됩니다.
※ 기타 합병에 대한 자세한 사항은 회사합병 결정(2022.07.18) 및 합병 등 종료보고서(2022.10.04) 공시를 참조하시기 바랍니다.
(5) 합병등 전후의 재무사항 비교표
* 합병등(합병, 중요한 영업ㆍ자산양수도, 주식의 포괄적교환ㆍ이전, 분할)
| (단위 : 백만원) |
| 대상회사 | 계정과목 | 예측 | 실적 | 비고 | ||||
|---|---|---|---|---|---|---|---|---|
| 1차연도 | 2차연도 | 1차연도 | 2차연도 | |||||
| 실적 | 괴리율 | 실적 | 괴리율 | |||||
| 에이치엘비생명과학(주) | 매출액 | 126,815 | 124,514 | 25,198 | 80 | - | - | - |
| 영업이익 | 26,279 | 25,566 | -7,296 | 128 | - | - | - | |
| 당기순이익 | - | - | - | - | - | - | - | |
| (*1) 상기 예측치는 소규모합병 당시 외부평가기관의 평가의견서 상의 2023년(1차연도) 및 2024년(2차연도) 수치를 기재하였습니다. 해당 평가는 현금흐름할인법(DCF)을 적용하였고, 해당 평가의견서에는 영업이익에 대한 법인세 추청치는 존재하나 당기순이익에 대한 추정은 제외되어 있습니다. (*2) 에임(주) 합병 후 당사 메디케어사업부로 편입되어 상기 예측치 및 실적은 메디케어사업부 경영실적 기준으로 작성하였습니다. (*3) COVID-19 엔더믹으로 인해 당사의 주력 제품인 COVID-19 진단기기의 매출 감소 및 원가 상승 등으로 실적 괴리율이 발생하였습니다. |
< 중요한 자산양수도_화진메디칼>
(1) 자산양수도 배경
당사는 2023년 7월 3일 HLB테라퓨틱스와 자산양수도 계약을 체결하고, 화진메디칼의 주식 863,500주(지분율 : 100.00%)를 양수하였으며, 자산양수도 가액은 8,300백만원입니다.
(2) 양수도주식수 및 양수도가액
| (단위 : 주, 천원) |
| 양도인 | 양수주식수 | 양수가액 | 양수대금 지급방법 | 비 고 |
| HLB테라퓨틱스 | 863,500 | 8,300,000 | 현금지급 |
※ 양도가액은 주당 979,000원을 적용하여 산출하였습니다.
(3) 자산양수도 주요일정
| 구분 | 일자 |
| 외부평가계약체결일 | 2023년 5월 22일 |
| 평가기간 | 2023년 5월 22일 ~ 2023년 6월 21일 |
| 이사회결의일 | 2023년 6월 29일 |
| 자산양수도 계약일 | 2023년 6월 29일 |
| 자산양수도 거래종결일 | 2022년 7월 3일 |
(4) 회사에 미치는 중요영향 등
당사는 본 자산양수도를 통하여 화진메디칼의 주식을 전량을 취득함으로써 재무구조 개선 및 안정적인 현금흐름 확보를 기대하고 있습니다. 총 양수가액은 8,300백만원이며, 거래대금 지급형태는 전액 8,300백만원 현금납입 입니다.
※ 기타 자산양수도에 대한 자세한 사항은 주요사항보고서(2023.07.18, 2023.09.27) 공시를 참조하시기 바랍니다.
<회사 합병결정_화진메디칼>
(1) 합병 배경
당사는 안정적인 수익창출을 통한 재무안정성 구축 및 향후 예정된 바이오 사업과의 시너지극대화를 위해 2023년 10월 1일 화진메디칼과 합병하였습니다.
(2) 합병 당사회사의 개요
|
합병 후 존속회사 |
회사명 |
HLB생명과학 |
|
본점소재지 |
경기도 화성시 동탄첨단산업1로 51-9 | |
|
대표이사 |
남상우, 한용해 |
|
|
상장 여부 |
코스닥 상장법인 |
|
합병 후 소멸회사 |
회사명 |
화진메디칼 |
|
본점소재지 |
충청남도 천안시 동남구 성남면 성심원길 20 | |
|
대표이사 |
이우준 | |
|
상장 여부 |
비상장법인 |
(3) 합병 주요일정
|
구분 |
날짜 |
비고 |
|
|
합병 이사회 결의일 |
2023-07-18 |
- |
|
|
주요사항보고서 제출 |
2023-07-18 |
- |
|
|
주주확정기준일 공고 |
2023-08-04 |
- |
|
|
합병 계약 체결일 |
2023-07-21 |
- |
|
|
주주확정기준일 |
2023-08-04 |
- |
|
|
소규모합병 공고 |
2023-08-04 |
- |
|
|
주주명부 폐쇄기간 |
2023-08-05 ~ |
- |
|
|
합병반대의사 통지 접수기간 |
시작일 |
2023-08-04 |
- |
|
종료일 |
2023-08-18. |
||
|
합병승인 이사회 |
2023-08-24 |
주주총회 갈음 |
|
|
채권자 이의제출 공고 |
2023-08-25 |
- |
|
|
채권자 이의제출 기간 |
시작일 |
2023-08-25 |
- |
|
종료일 |
2023-09-25 | ||
|
합병기일 |
2023-10-01. |
- |
|
|
합병 종료보고 총회 |
2023-10-04 |
이사회 보고 |
|
|
합병 종료보고 공고 |
2023-10-04 |
- |
|
|
합병 등기 |
2023-10-06 |
- |
|
(4) 회사에 미치는 중요영향 등
당사는 화진메디칼 발행주식을 100% 소유하여 합병신주를 발행하지 않는 무증자 합병으로 진행되었으며, 합병 완료 후 당사의 주주변경은 없습니다.
본 합병은 상법 제527조의3에 근거하여 소규모 합병에 해당되며, 합병승인은 이사회승인으로서 갈음됩니다.
※ 기타 합병에 대한 자세한 사항은 회사합병 결정(2023.07.18) 및 합병 등 종료보고서(2023.10.04) 공시를 참조하시기 바랍니다.
(5) 합병등 전후의 재무사항 비교표
* 합병등(합병, 중요한 영업ㆍ자산양수도, 주식의 포괄적교환ㆍ이전, 분할)
| (단위 : 백만원) |
| 대상회사 | 계정과목 | 예측 | 실적 | 비고 | ||||
|---|---|---|---|---|---|---|---|---|
| 1차연도 | 2차연도 | 1차연도 | 2차연도 | |||||
| 실적 | 괴리율 | 실적 | 괴리율 | |||||
| 화진 메디칼 |
매출액 | 11,888 | 15,134 | - | - | - | - | - |
| 영업이익 | 216 | 932 | - | - | - | - | - | |
| 당기순이익 | - | - | - | - | - | - | - | |
| (*) 상기 예측치는 소규모합병 당시 외부평가기관의 평가의견서 상의 2024년(1차연도) 및 2025년(2차연도) 수치를 기재하였습니다. 해당 평가는 현금흐름할인법(DCF)을 적용하였고, 해당 평가의견서에는 영업이익에 대한 법인세 추청치는 존재하나 당기순이익에 대한 추정은 제외되어 있습니다. |
XI. 상세표
1. 연결대상 종속회사 현황(상세)
기업공시서식작성기준에 따라 분기보고서의 본 항목 기재 생략하였으며, 관련 내용은 2024.03.20에 제출된 사업보고서(2023.12)를 참고하시기 바랍니다.
| (기준일 : | 2023년 12월 31일 | ) | (단위 : 백만원) |
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| HLB셀 | 2009.09.16 | 경기도 화성시 동탄첨단산업로 | 바이오의약품 개발 | 38,250 | 의결권의 과반수이상 보유 (기업회계기준서 제1110호) |
미해당 |
| 신화어드밴스 | 2007.11.19 | 서울시 영등포구 선유로 | 의약품 유통업 | 25,679 | 의결권의 과반수이상 보유 (기업회계기준서 제1110호) |
미해당 |
| HLB에너지 | 1997.06.27 | 부산광역시 사하구 감천항로 | 폐기물 소각열 관련사업 |
17,296 | 의결권의 과반수이상 보유 (기업회계기준서 제1110호) |
미해당 |
| HLB생명과학R&D | 2022.04.01 | 경기도 화성시 동탄첨단산업로 | 신약개발사업 | 4,434 | 의결권의 과반수이상 보유 (기업회계기준서 제1110호) |
미해당 |
2. 계열회사 현황(상세)
기업공시서식작성기준에 따라 분기보고서의 본 항목 기재 생략하였으며, 관련 내용은 2024.03.20에 제출된 사업보고서(2023.12)를 참고하시기 바랍니다.
가. 계열회사 현황(지배회사 기준)
| (기준일 : | 2023년 12월 31일 | ) | (단위 : 사) |
| 상장여부 | 회사수 | 기업명 | 법인등록번호 |
|---|---|---|---|
| 상장 |
9 |
HLB |
170111-0021600 |
|
HLB생명과학 |
110111-1568885 |
||
|
HLB글로벌 |
144911-0000072 |
||
|
HLB제약 |
110111-1538391 |
||
|
HLB사이언스 |
110111-6042363 |
||
|
HLB테라퓨틱스 |
160111-0099451 |
||
|
HLB바이오스텝(구.노터스) |
284211-0063231 |
||
|
HLB이노베이션(구.피에스엠씨) |
110111-0234312 |
||
|
HLB파나진(구.파나진) |
170111-0007098 |
||
| 비상장 | 35 |
Elevar Therpeutics, Inc. |
- |
|
Immunomic Therapeutics, Inc. |
- |
||
|
바다중공업 |
180111-0288654 |
||
|
바다엔지니어링 |
195511-0230907 |
||
|
현대요트 |
230111-0143435 |
||
|
현대앤코스모스요팅 |
110111-5137868 |
||
|
HLB셀 |
131311-0092331 |
||
|
엘에스케이인베스트먼트 |
110111-6028595 |
||
|
HLB인베스트먼트 |
110111-7902657 |
||
|
HLB일렉 |
284911-0134898 |
||
|
HLB네트웍스 |
230111-0155076 |
||
|
HLBN Singapore, Ltd. |
- |
||
|
신화어드밴스 |
110111-3790113 |
||
|
HLB에너지 |
180111-0235332 |
||
|
HLB생명과학R&D |
134811-0680620 |
||
|
펭귄오션레저 |
230111-0222320 |
||
|
HLB생활건강 |
110111-3920108 |
||
|
프레시코 |
161311-0037563 |
||
|
코아바이오 |
110111-5989128 |
||
|
에포케 |
110111-5998111 |
||
|
VerismoTherapeutics, Inc. |
- |
||
|
고션 |
205411-0015431 |
||
|
지트리파마슈티컬 |
131111-0379709 |
||
|
REGENTREE |
- |
||
|
OBLATO |
- |
||
|
HLB Shanghai Co., Ltd
|
- |
||
|
새론바이오 |
135211-0033010 |
||
|
브이에스팜 |
110111-4752542 |
||
|
베리스모테라퓨틱스 아시아 |
110111-8164199 |
||
|
대해선박기술(구.디에이치) |
180111-1111490 |
||
|
HLB이엔지 |
230111-0392678 |
||
|
HLB에프앤비 |
110111-8570784 |
||
|
퍼플리쉬 |
110111-7207495 |
||
|
모던파파스 |
110111-8247804 |
||
|
더롬다이어트 |
110111-8542220 |
나. 계열회사 간의 계통도(지배회사 기준)
| (기준일 : 2023년 12월 31일) | (단위 : %) |
|
피출자사 |
상장 여부 |
출자사 |
|||||||||||||||
|
HLB |
HLB 생명과학 |
HLB셀 |
HLB 글로벌 |
HLB 네트웍스 |
프레시코 |
에포케 (*13) |
HLB제약 |
현대앤 |
HLB 테라퓨틱스 |
바다 중공업 |
HLB 바이오스텝 |
Verismo Therapeutics,Inc. |
HLB |
HLB 이엔지 |
HLB 이노베이션 |
||
|
HLB |
상장 |
0.20 |
1.49 |
0.57 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
Elevar Therapeutics, Inc. |
비상장 |
99.98 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
Immunomic Therapeutics,Inc. |
비상장 |
40.99 |
- |
- |
3.63 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
HLB생명과학 |
상장 |
19.33 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
현대요트 |
비상장 |
- |
- |
- |
- |
- |
- |
- |
- |
17.32 |
- |
- |
- |
- |
- |
39.43 |
- |
|
현대앤 코스모스요팅 |
비상장 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
17.24 |
- |
|
바다중공업 |
비상장 |
- |
- |
- |
- |
1.45 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
90.11 |
- |
|
고션 |
비상장 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
18.76 |
- |
|
HLB셀 |
비상장 |
- |
99.30 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
엘에스케이 인베스트먼트 |
비상장 |
- |
9.00 |
29.00 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
HLB네트웍스 |
비상장 |
- |
- |
- |
- |
- |
- |
75.19 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
신화어드밴스 |
비상장 |
- |
100.00 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
HLB에너지 |
비상장 |
- |
100.00 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
HLB생활건강 |
비상장 |
- |
- |
- |
100.00 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
HLB사이언스(*1) |
상장 |
- |
20.62 |
- |
36.19 |
- |
- |
- |
- |
- |
- |
- |
7.99 |
- |
- |
- |
- |
|
프레시코 |
비상장 |
- |
- |
- |
92.46 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
코아바이오 |
비상장 |
- |
- |
- |
- |
- |
55.52 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
HLB제약 |
상장 |
- |
14.26 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
- |
|
Verismo TherapeuticsInc.(*2) |
비상장 |
13.01 |
- |
- |
- |
- |
- |
- |
19.35 |
- |
- |
- |
- |
- |
- |
- |
18.50 |
|
HLB인베스트먼트(*3) |
비상장 |
100.00 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
HLB테라퓨틱스(*4) |
상장 |
5.46 |
- |
0.29 |
4.38 |
- |
- |
1.46 |
1.46 |
0.29 |
0.44 |
- |
- |
- |
0.29 |
- |
- |
|
지트리파마슈티컬(*5) |
비상장 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
100.00 |
- |
- |
- |
- |
- |
- |
|
REGENTREE(*6) |
비상장 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
61.50 |
- |
- |
- |
- |
- |
- |
|
OBLATO(*7) |
비상장 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
100.00 |
- |
- |
- |
- |
- |
- |
|
HLB바이오스텝 (구.노터스)(*8) |
상장 |
16.09 |
- |
- |
- |
- |
- |
- |
- |
- |
2.04 |
- |
- |
- |
- |
- |
- |
|
브에이스팜(*9) |
비상장 |
- |
- |
- |
- |
|
|
- |
- |
- |
- |
- |
66.20 |
- |
- |
- |
- |
|
새론바이오(*10) |
비상장 |
- |
- |
- |
- |
|
|
- |
- |
- |
- |
- |
60.00 |
- |
- |
- |
- |
|
바다엔지니어링 |
비상장 |
- |
- |
- |
- |
|
|
- |
- |
- |
- |
100.00 |
- |
- |
- |
- |
- |
|
HLB Shanghai(*11) |
비상장 |
100.00 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
베리스모테라퓨틱스 아시아(*12) |
비상장 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
62.00 |
- |
- |
- |
|
HLB일렉 |
비상장 |
- |
- |
- |
- |
10.00 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
|
HLB생명과학R&D(*14) |
비상장 |
- |
100.00 |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
- |
| (*1) |
2020년 4월, HLB사이언스는 코넥스시장에 상장되었습니다. |
| (*2) |
2021년 4월, 신규 Pipeline 확보를 통한 지속적인 미래 기업가치의 극대화를 위해 2020년 6월에 설립된 미국 벤처기업 Verismo Therapeutics, Inc. 에 5백만불을 투자하였습니다. |
| (*3) |
2021년 5월, 바이오와 헬스케어 등의 분야의 신기술사업자에 대한 투자 및 융자 등신기술사업 금융업을 통한 기업가치 극대화를 위해 HLB인베스트먼트의 보통주 600,000주를 30억원에 취득하였으며,2021년 11월, 보통주 1,400,000주를 70억원에 추가 취득하였습니다. |
| (*4) |
2021년 11월, 지분취득을 통한 바이오 사업과의 시너지 극대화와 기업가치극대화를 위해 HLB테라퓨틱스 보통주 530,899주를 약 50억에 취득하였습니다.2023년 1월, HLB테라퓨틱스의 Pipeline 임상비용 지원 등의 목적으로 제3자배정 유상증자에 참여하여 보통주 115만주를 약 130억원에 취득하였습니다. |
| (*5) |
2021년 11월, 지트리파마슈티컬은 HLB테라퓨틱스의 지분 100% 자회사로서 계열회사로 편입되었습니다 |
| (*6) |
2021년 11월, REGENTREE는 HLB테라퓨틱스의 지분 61.5% 자회사로서 계열회사로 편입되었습니다. |
| (*7) |
2021년 11월, OBLATO는 HLB테라퓨틱스의 지분 100% 자회사로서 계열회사로 편입되었습니다. |
| (*8) |
2022
년
3
월
,
지분취득을 통한 신규사업진출 및 기존사업과의 시너지 극대화를 위해
HLB
바이오스텝
(
구
.
노터스
)
보통주
1,405,648
주를 약
562
억에 취득하였습니다
. |
| (*9) |
2022년 3월, 브이에스팜은 노터스의 지분 66.2% 자회사로서 계열회사로 편입되었습니다. |
| (*10) |
2022년 3월, 새론바이오는 노터스의 지분 60.0% 자회사로서 계열회사로 편입되었습니다. |
| (*11) |
2022
년
2
월
,
리보세라닙 중국 로열티 수령 및 향후 중국사업진출을 위해
HLB Shanghai Co.,Ltd(
구
. Hyundai Lifeboats Shanghai Co., Ltd)
의 지분
100%
를 약
1.1
백만불에 취득하였습니다
. |
| (*12) |
2022년 1월, 베리스모테라퓨틱스아시아는 Verismo Therapeutics, Inc의 지분 62.0% 자회사로서 계열회사로 편입되었습니다. |
| (*13) |
2021년 7월, 에포케는 HLB파워로부터 HLB네트웍스의 지분 75.19%를 취득하였습니다. |
| (*14) |
2022년 4월, HLB생명과학R&D는 HLB생명과학의 100% 자회사로서 계열회사로 편입되었습니다. |
| (*15) |
2022
년
10
월
,
선박설계 전문업체인 대해선박기술
(
구
.
디에이치
)
의 지분
70%
을 취득하였습니다
. |
| (*16) |
2023
년
3
월
,
기업가치 극대화를 위해
HLB
이노베이션
(
구
.
피에스엠씨
)
의 보통주
16,985,477
주를 약
200
억원에 취득하였습니다
. |
| (*17) |
2023년 5월, HLB이엔지는 당사의 선박사업부 물적분할에 따라 설립된 분할신설회사입니다. |
| (*18) |
2023년 3월, HLB에프앤비는 HLB네트웍스의 리테일사업부 물적분할에 따라 설립되었습니다. |
| (*19) |
2023년 8월, 기업가치 극대화를 위해 PNA 유전자 진단제품 개발 및 제조 판매사인 HLB파나진(구. 파나진)의 보통주3,842,743주를 약130억원에 취득하였습니다 |
| (*20) |
2023년 7월, 티아이코퍼레이션의 자회사 퍼플리쉬, 모던파파스,더롬다이어트는 HLB글로벌과의 흡수합병을 통해 계열회사로 편입되었습니다. |
다. 계열회사간 (당사)임원 겸직 현황
| (기준일 : 2023년 12월 31일) |
| 구분 | 진양곤 | 남상우 | 한용해 | 장인근 | 최수자 | 김윤 | 김영현 |
| HLB | 대표이사 (상근) |
- | - | - | - | - | - |
| HLB생명과학 | 의장 (상근) |
대표이사 (상근) |
대표이사 (상근) |
이사 (상근) |
이사 (비상근) |
- | 감사 (상근) |
| HLB일렉 | 이사 (비상근) |
대표이사 (상근) |
- | - | - | - | - |
| Immunomic Theraceutics Inc. | 이사 (비상근) |
- | - | - | - | - | - |
| Elevar Therapeutics,Inc | 의장 (비상근) |
- | - | 이사 (비상근) |
- | - | - |
| HLB글로벌 | 이사 (비상근) |
- | - | - | - | - | - |
| HLB셀 | 이사 (비상근) |
- | - | - | - | - | - |
| 신화어드밴스 | - | 이사 (비상근) |
- | - | - | - | - |
| HLB제약 | 이사 (비상근) |
이사 (비상근) |
- | 이사 (비상근) |
- | - | - |
| 엘에스케이인베스트먼트 | 이사 (비상근) |
- | - | - | - | - | - |
| HLB네트웍스 | 이사 (비상근) |
- | - | - | - | - | - |
| 바다중공업 | 이사 (비상근) |
- | - | - | - | - | - |
| HLB사이언스 | 이사 (비상근) |
- | - | - | - | - | - |
| 프레시코 | 이사 (비상근) |
이사 (비상근) |
- | - | - | - | - |
| 코아바이오 | 이사 (비상근) |
이사 (비상근) |
- | - | - | - | - |
| 에포케 | 이사 (비상근) |
- | - | - | - | - | - |
| HLB인베스트먼트 | 이사 (비상근) |
- | - | - | - | - | - |
| HLB테라퓨틱스 | 이사 (비상근) |
- | - | - | - | - | - |
| Hyundai Lifeboats Singapore Pte. Ltd |
이사 (비상근) |
- | - | - | - | - | - |
| HLB바이오스텝(구.노터스) | 이사 (비상근) |
- | - | - | - | - | - |
| Hyundai Lifeboats Shanghai Co.,Ltd |
감사 (비상근) |
- | - | - | - | - | - |
|
HLBN Singapore Pte. Ltd |
이사(비상근) |
- | - | - | - | - | - |
| HLB생명과학R&D | 이사 (비상근) |
- | 대표이사 (상근) |
- | - | - | - |
| 베리스모테라퓨틱스 아시아 | 이사 (비상근) |
- | - | - | - | - | - |
| HLB이노베이션 (구.피에스엠씨) |
이사 (비상근) |
- | - | - | - | - | - |
|
HLB파나진(구.파나진) |
이사(비상근) |
- | - | 대표이사 (상근) |
- | - | - |
3. 타법인출자 현황(상세)
기업공시서식작성기준에 따라 분기보고서의 본 항목 기재 생략하였으며, 관련 내용은 2024.03.20에 제출된 사업보고서(2023.12)를 참고하시기 바랍니다.
| (기준일 : | 2023년 12월 31일 | ) | (단위 : 백만원, 주, %) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
| 두산포천에너지 | 비상장 | 2008.11.03 | 단순투자 | 40 | 8,000 | 20.0 | - | - | - | - | 8,000 | 20.0 | - | - | - |
| 엘에스케이인베스트먼트 | 비상장 | 2016.04.06 | 단순투자 | 1,500 | 90,000 | 9.0 | 450 | - | - | - | 90,000 | 9.0 | 450 | 7,188 | 2,211 |
| 신화어드밴스 | 비상장 | 2016.08.03 | 경영참여 | 7,000 | 304,546 | 100.0 | 23,711 | - | - | - | 304,546 | 100.0 | 23,712 | 25,679 | -525 |
| HLB셀 | 비상장 | 2018.03.21 | 경영참여 | 79,487 | 32,610,666 | 99.3 | 50,409 | 1,617,076 | 2,500 | - | 34,227,742 | 99.3 | 52,909 | 38,250 | -9,447 |
| HLB에너지 | 비상장 | 2019.05.29 | 경영참여 | 1,880 | 1,475,000 | 100.0 | 15,056 | 827,099 | 12,582 | - | 2,302,099 | 100.0 | 27,638 | 17,296 | -231 |
| HLB제약 | 상장 | 2020.09.11 | 경영참여 | 14,033 | 3,574,549 | 12.8 | 21,097 | 747,495 | 8,462 | - | 3,574,549 | 12.8 | 29,559 | 142,850 | -11,104 |
| HLB | 상장 | 2020.06.05 | 단순투자 | 4,395 | 1,538,312 | 1.3 | 43,688 | 303,213 | - | 16,162 | 1,841,525 | 1.3 | 59,850 | 1,147,905 | 10,325 |
| HLB생명과학R&D | 비상장 | 2022.04.01 | 경영참여 | 1,000 | 12,000,000 | 100.0 | 4,028 | - | - | - | 12,000,000 | 100.0 | 4,028 | 4,434 | -2,455 |
| 노마드제2호투자조합 | 비상장 | 2022.07.01 | 단순투자 | 10,151 | 10,100 | 18.5 | 10,151 | - | - | - | 10,100 | 18.5 | 10,151 | 66,663 | 11,789 |
| HLBI알밤제1호투자조합 | 비상장 | 2022.07.05 | 단순투자 | 1,000 | 1,000 | 83.3 | 1,000 | - | - | - | 1,000 | 18.5 | 1,000 | 1,994 | -16 |
| HLB이노베이션 | 상장 | 2023.03.13 | 경영참여 | 2,000 | - | - | - | 2,074,688 | 2,000 | 5,336 | 2,074,688 | 3.1 | 7,336 | 38,728 | 13,684 |
| HLB사이언스 | 상장 | 2023.09.30 | 경영참여 | - | - | - | - | 3,365,165 | 6,000 | 203 | 3,365,165 | 20.62 | 6,203 | 5,076 | -4,769 |
| 화진메디칼 | 비상장 | 2023.07.03 | 경영참여 | - | - | - | - | 863,500 | 8,351 | - | 863,500 | 100.00 | 8,351 | 8,292 | 183 |
| 합 계 | - | - | 169,590 | - | 41,580 | 12,023 | - | - | 223,194 | 1,504,355 | 9,645 | ||||
【 전문가의 확인 】
1. 전문가의 확인
해당사항 없습니다.
2. 전문가와의 이해관계
- 해당사항 없습니다.