 |
|
글로벌 체외진단 산업 3대 트렌드 |
주주총회소집공고
| 2024 년 3 월 13 일 | ||
| 회 사 명 : | 주식회사 유투바이오 | |
| 대 표 이 사 : | 김진태 | |
| 본 점 소 재 지 : | 서울시 송파구 오금로 489, 4층 (거여동) | |
| (전 화)1577-1338 | ||
| (홈페이지)http://u2bio.com | ||
| 작 성 책 임 자 : | (직 책)상무 | (성 명)김지원 |
| (전 화)070-4492-2727 | ||
주주총회 소집공고
| (제15기 정기 주주총회) |
주식회사 유투바이오 주주 귀하
주주님의 건승과 댁내의 평안을 기원합니다.
당사는 상법 제363조와 정관 제17조에 의거하여 제15기 정기주주총회를 다음과 같이 개최하고자 하오니 참석하여 주시기 바랍니다.
또한, 의결권 있는 발행주식총수의 100분의 1이하의 주식을 소유한 소액주주에 대해서는 상법 제542조의 4 및 당사 정관 제17조에 의거 본 공고로 소집 통지를 갈음하오니 이점 양지하여 주시기 바랍니다.
- 아 래 -
1. 일 시 : 2024년 3월 28일(목) 오전 9시
2. 장 소 : 서울특별시 송파구 오금로 489, 4층 당사 대회의실
3. 회의목적사항
가. 보고 사항 : ① 감사보고 ② 영업보고 ③ 내부회계관리제도 운영실태보고
나. 부의 안건
제 1 호 의안 : 제 15 기(2023.01.01~2023.12.31) 재무제표 승인의 건
제 2 호 의안 : 제 15 기(2023년) 현금배당 결정의 건
제 3 호 의안 : 정관 일부 변경의 건
- 제3-1호 의안 : 목적사업의 추가 (정관 제 2 조)
- 제3-2호 의안 : 주식 전자등록(정관 제 8 조의 4)
- 제3-3호 의안 : 이사 정원 수 변경 (정관 제 24 조)
- 제3-4호 의안 : 기타 수정 (부칙)
제 4 호 의안 : 이사 선임의 건
- 제4-1호 의안 : 사내이사 김진태 선임의 건
- 제4-2호 의안 : 사내이사 김지원 선임의 건
- 제4-3호 의안 : 기타비상무이사 박영수 선임의 건
제 5 호 의안 : 감사 김현석 선임의 건
제 6 호 의안 : 이사 보수한도 승인의 건(한도금액 20억원)
제 7 호 의안 : 감사 보수한도 승인의 건(한도금액 5억원)
4. 경영참고사항 비치
- 상법 제542조의 4의 3항에 의거 경영참고사항은 당사 본점과 명의개서대행기관(국민은행 증권대행부)에 비치하였으며, 금융위원회 및 한국거래소에 전자공시하여 조회가 가능하오니 참고하시기 바랍니다.
5. 실질주주의 의결권 행사에 관한 사항
- 이번 당사 정기주주총회에는 한국예탁결제원이 주주님들의 의결권을 행사할 수 없습니다. 따라서 주주님들께서는 한국예탁결제원에 의결권행사에 관한 의사표시를 통지하실 필요가 없으며, 종전과 같이 주주총회에 참석하여 의결권을 직접 행사하시거나 또는 위임장에 의거 의결권을 간접 행사하실 수 있습니다.
6. 주주총회 참석시 준비물
- 직접행사 : 주총참석장, 신분증(주민등록증, 운전면허증 또는 여권)
- 대리행사 : 주총참석장, 위임장(주주와 대리인의 인적사항 기재, 날인)
대리인의 신분증
- 주주총회시 참석 주주님들께 별도의 기념품을 지급하지 아니하오니 이점 널리 양해하여 주시기 바랍니다.
2024년 3월 13일
서울시 송파구 오금로 489, 4층 (거여동)
주식회사 유투바이오
대표이사 김 진 태 (직인생략)
[별첨1] 주주총회 참석장
주주총회 참석장
본인은 주식회사 유투바이오 제 15 기 정기주주총회에 주주로서 참석합니다.
(주주총회참석자는 다음 사항을 기재하여 주주총회일에 제출하여 주시기 바랍니다.)
--- 다 음 ---
|
실 질 주 주 참 석 자 |
|||
|
성 명 |
( 인 ) |
법인:사업자등록번호 개인:생년월일 |
|
|
주 소 |
|
||
|
보유주식수 |
주 |
|
|
|
참석 구분 |
주주직접참석 ( ) 대리인 참석 ( ) |
대리참석자 와의 관계 |
|
|
※ 아래 사항은 대리참석 위임시 작성하여 주시기 바랍니다. (대리 참석자 위임장) 본인은 주식회사 유투바이오 제15기 정기주주총회에 주주로서 대리참석자를 아래와 같이 지정하여 본인을 대신하여 주주총회 결의 및 기타 사항에 대하여 전권을 위임합니다. 2024 년 3월 일 주주 ( 인 ) |
|||
|
대 리 참 석 자 |
|||
|
성 명 |
(인) |
법인:사업자등록번호 개인:생년월일 |
|
|
주 소 |
|
||
|
관 계 |
|
||
※ 지참물
1) 본 인 : 주총참석장, 신분증
2) 대리인 : 주총참석장, 위임장(주주와 대리인의 인적사항기재, 인감날인), 대리인 신분증
I. 사외이사 등의 활동내역과 보수에 관한 사항
1. 사외이사 등의 활동내역
가. 이사회 출석률 및 이사회 의안에 대한 찬반여부
| 회차 | 개최일자 | 의안내용 | 사외이사 등의 성명 | |
|---|---|---|---|---|
| 김희찬 (출석률: 92%) |
이상원 (출석률: 85%) |
|||
| 찬 반 여 부 | ||||
| 1 | 2023-02-09 | 준비금 자본전입(무상증자) 승인의 건 | 찬성 | 찬성 |
| 2 | 2023-02-16 | 제14기 외부감사전 사전 제시 재무제표 보고의 건 | 찬성 | 찬성 |
| 3 | 2023-03-14 | 제14기 정기주주총회 소집에 관한 건 | 찬성 | 찬성 |
| 4 | 2023-04-11 | 코스닥시장 상장 동의의 건 | 찬성 | 찬성 |
| 5 | 2023-04-25 | 제15기 1분기 재무제표(안) 보고의 건 | 찬성 | 찬성 |
| 6 | 2023-08-10 | 제15기 2분기 재무제표(안) 보고의 건 | 찬성 | 찬성 |
| 7 | 2023-09-06 | 코스닥시장 상장을 위한 신주발행 승인의 건 | 찬성 | 찬성 |
| 8 | 2023-10-26 | 코넥스시장 상장 폐지 및 코스닥시장 상장 결의의 건 | 찬성 | 찬성 |
| 9 | 2023-11-09 | 제15기 3분기 재무제표(안) 보고의 건 | 찬성 | 불참 |
| 10 | 2023-12-14 | 주주명부폐쇄기간 및 기준일 설정의 건 | 찬성 | 찬성 |
| 11 | 2023-12-14 | 배당 기준일 설정의 건 | 찬성 | 찬성 |
| 12 | 2024-01-30 | 제15기 외부감사전 사전 제시 재무제표 보고의 건 | 불참 | 불참 |
| 13 | 2024-02-15 | 제15기 정기주주총회 소집에 관한 건 | 찬성 | 찬성 |
나. 이사회내 위원회에서의 사외이사 등의 활동내역
| 위원회명 | 구성원 | 활 동 내 역 | ||
|---|---|---|---|---|
| 개최일자 | 의안내용 | 가결여부 | ||
| - | - | - | - | - |
당사의 이사회 내에는 별도의 위원회가 없습니다.
2. 사외이사 등의 보수현황
| (단위 : 원) |
| 구 분 | 인원수 | 주총승인금액 | 지급총액 | 1인당 평균 지급액 |
비 고 |
|---|---|---|---|---|---|
| 사외이사 | 2 | 2,000,000,000 | 48,000,000 | 24,000,000 | - |
II. 최대주주등과의 거래내역에 관한 사항
1. 단일 거래규모가 일정규모이상인 거래
| (단위 : 억원) |
| 거래종류 | 거래상대방 (회사와의 관계) |
거래기간 | 거래금액 | 비율(%) |
|---|---|---|---|---|
| - | - | - | - | - |
2. 해당 사업연도중에 특정인과 해당 거래를 포함한 거래총액이 일정규모이상인 거래
| (단위 : 억원) |
| 거래상대방 (회사와의 관계) |
거래종류 | 거래기간 | 거래금액 | 비율(%) |
|---|---|---|---|---|
| - | - | - | - | - |
III. 경영참고사항
1. 사업의 개요
가. 업계의 현황
(1) 산업의 특성
(가) 체외진단검사서비스
글로벌 체외진단산업은 시장 성장성 측면에서 1)인구 고령화 및 만성질환 유병률 증가, 2)신기술발전으로 인한 새로운 시장 개화에 따라 꾸준하게 성장하는 산업이며, 이익 비중이 높은 고부가가치 산업입니다. 또한 경쟁구조 측면에서 1)인수합병에 따른 소수 업체의 과점구조, 2)각국의 의료기기에 대한 규제산업의 특징을 가지고 있습니다.
체외진단제품 및 검사서비스 시장의 주요 고객은 의료기관 및 대학/연구소, 유통회사입니다. 당사의 주 거래처는 의료기관과 연구소로 체외진단검사 서비스 및 연구용역서비스를 제공하고 있습니다.
체외진단 산업의 최근 트렌드는 1)탈중앙화, 2)정밀의료 기반 신기술 발전, 3)IT/디지털 헬스케어 융합을 꼽을 수 있는데 기존 진단검사는 의료현장에서 채취된 검체를 대형 검사소로 보내 한번에 검사를 진행하는 중앙집중식이 일반적이었습니다. 그러나 개발도상국에서는 인프라 구축이 쉽지 않고 심혈관 질환 등 신속한 결과가 필요한 질병에는 중앙집중식진단검사 방식이 효율적이지 않습니다.
현장진단(Point of Care)은 의료 현장에서 소형 장비를 통해 검사를 진행하고 바로 검사 결과를 얻을 수 있는 방식을 의미하며 현재는 개발도상국뿐 아니라 미국, 유럽 등 선진국에서도 현장검사가 보편화되고 있습니다. 도입 초기에는 신뢰도 문제로 활용성이 적었으나, 최근 기술의 발전으로 비숙련 검사자가 수행해도 오류가 없도록 개발되고 있습니다.
또한 유전체분석 기술의 발전으로 진단에 소요되는 비용과 시간이 단축되면서 유전적 질병 발생 확률을 조기에 진단하거나 혈액으로 암을 진단하는 방식이 등장하였습니다. 특히NGS기반 개인유전체 분석과 액체생검은 높은 성장성을 보일 것으로 전망됩니다. 마지막으로 IT/디지털 헬스케어 융합입니다. 인공지능 기술을 진단 영역에 도입하고자 하는 시도가 계속되고 있으며, 원격진료 제도화 논의가 시작되면서 웨어러블 장비 등을 이용하여 비대면으로 환자의 질병 유무를 판단하고 적합한 치료법을 제시하는 실시간 진단(Realtime Diagnosis)기술이 부각되고 있습니다.
 |
|
글로벌 체외진단 산업 3대 트렌드 |
| 출처: 의료기기: 체외진단 산업의 중장기적 성장성에 주목, 대신증권 2022.05.23 |
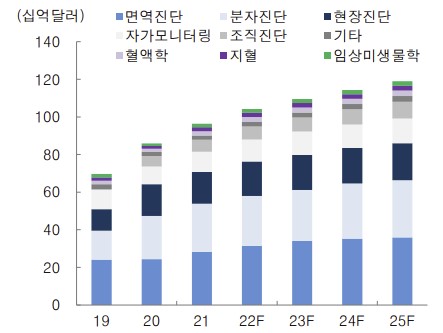
Frost&Sullivan의 2021.09월 시장보고서에 따르면 글로벌 체외진단 시장 매출은 2019년 752억 달러에서 2025년 1,188억 달러로 연평균 7.9% 성장할 것으로 전망되고 있습니다. 팬데믹 영향으로 2020년 체외진단시장 규모가 2019년 대비 59.3% 성장하였는데 COVID-19 효과를 제외하더라도 1)인구 고령화 및 만성질환 유병률 증가, 2)신기술 발전으로 인한 새로운 시장 개화 등의 구조적 이유로 꾸준히 성장하는 시장이며 이익 비중이 높은 고부가가치 산업입니다.
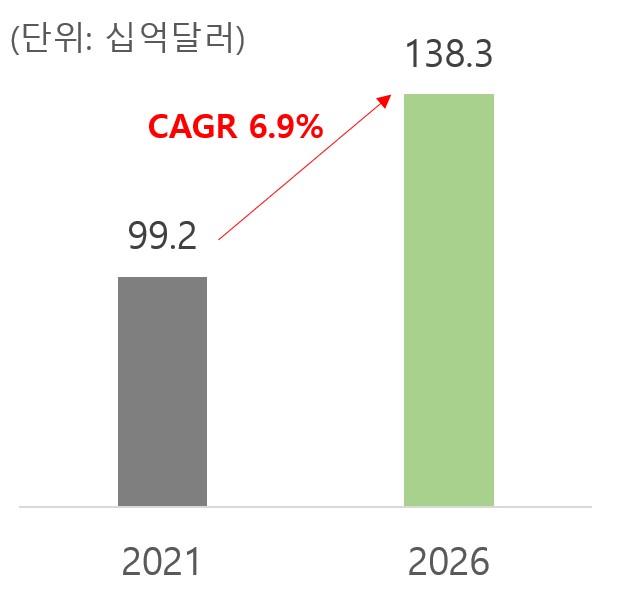
임상화학 및 면역분석 시장은 심장, 종양 분석 등의 영역에서 높은 성장이 기대되며 2020년 244억 달러에서 2025년 359억 3천만 달러로 연평균 8% 성장이 예상됩니다. 분자진단시장은 COVID-19에 대한 PCR사용 핵산 기반 테스트 수용 증가를 토대로 2020년 229억 4천만 달러에서 2025년 304억 2천만 달러로 연평균 5.8% 성장이 예상되며, 현장진단 시장은 디지털 현장테스트로의 전환, 감영성 질병검사, 임신검사 등의 수요 증가를 바탕으로 2020년 169억 2천만 달러에서 2025년 196억 2천만 달러로 연평균 3.0% 성장이 예상됩니다.
 |
|
글로벌 체외진단 시장 규모 |
| 출처: Frost Sullivan 2021.09, 대신증권리서치센터 |
 |
|
체외진단 방식별 시장규모 추이 |
| 출처: Frost Sullivan 2021.09, 대신증권리서치센터 |
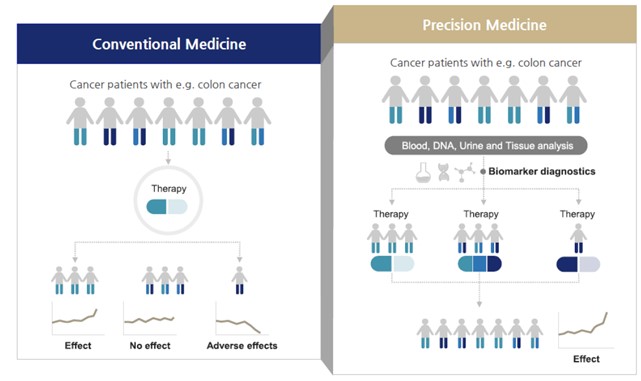
진단산업의 성장근거 중 하나는 아직 미충족 수요가 높은 부분이 존재하며, 기술의 발전으로 이를 해결하는 새로운 방법이 개발되고 있다는 것입니다. 학계에서 인정받은 새로운 기술들이 산업계로 들어오면서 기존 시장 규모를 키우거나(동반진단, 액체생검), 완정히 새로운 시장을 창출해 낼 수 있는데(DTC, 개인유전체 분석), 차세대 진단 기술은 기존 진단 방법에 생명공학과 관련된 여러 기술(DNA 시퀀싱, CRISPR 유전자 가위, 인공지능)을 융합하여 정확도와 정밀도를 크게 향상시키고, 환자 개인 정보에 기반한 맞춤 의료를 가능하게 합니다.
 |
|
정밀의료 패러다임 전환 |
| 출처: 마크로젠, 대신증권리서치센터 |
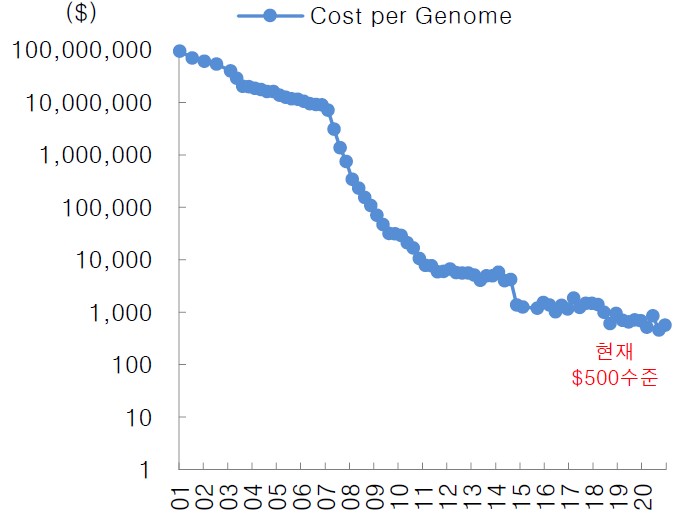
최초의 인간 게놈 분석은 3조원의 비용과 13년의 시간이 걸렸으나(2003년, 휴먼게놈 프로젝트) 기술의 발전으로 이제는 500달러의 비용과 15분의 시간으로 크게 단축되었습니다. 이는 차세대염기서열 분석법(NGS, Next-Generation Sequencing)의 상용화에 기인합니다. NGS는 DNA를 조각내 복제한 뒤 한번에 여러 염기서열을 읽어들이는 병렬적 방법으로 1세대 염기서열 분석법(직렬적 방법) 대비 효율적입니다. 시퀀싱 서비스는 크게 1)연구용 시장, 2)임상 시장, 3)상업용 시장으로 나뉘는데 연구용 시장은 생명공학 및 의학 연구에 필요한 유전체 분석 섭시의 위ㆍ수탁 사업이며 1세대 시퀀싱 서비스(Standard Sequencing, Difficult Template Sequnecing), 2세대 NGS서비스(Whole Genome Sequencing, Transciptome Sequencing)등 연구자의 요구에 맞춰 알맞은 유전체 분석 서비를 제공합니다. 정부기관이나 학계의 의뢰를 받아 진행되기 때문에 안정적인 매출이 기대되고, 신뢰성 및 비용 효율성이 중요한 분야입니다. 임상 시장은 병원이나 신약개발을 하는 제약사에 유전체 분석 서비스를 제공하는 것이며 관련 분야로는 비침습산전진단검사(NIPT), 유전성 암 예측검사, 동반진단, 액체생검 등이 있습니다. 검사 건수가 누적될수록 환자 유전체 데이터를 확보할 수 있기 때문에 다양한 사업기회 요인이 존재합니다.
2016년 미국 유전체 분석 업체 23앤드미는 서비스를 통해 얻은 유전자 정보 라이브러리 데이터를 글로벌 빅파마인 GSK에 판매하는 계약을 체결하기도 하였습니다. 임상 시장에서 가장 주목할 만한 부분은 암 진단으로, 최근에는 혈액 내 유전체를 분석하여 암을 진단하는 액체생검(Liquid Biospy)이 주목받고 있습니다.
상업용 시장은 일반인 대상 헬스케어 서비스로 파트너사(보험사, 핀테크)의 마케팅을 지원하기 위해 요구에 맞춰 유전자검사 키트를 개발/판매하는 B2B 모델과 소비자에게 직접 유전체 분석 서비스를 제공하는 B2C모델이 있습니다. 비록 규제의 한계로 서비스 제공이 자유롭지 않지만, 최근에는 병원이나 의사를 거치지 않고 제품이나 서비스를 제공하는 DTC(Direct to Consumer) 개인유전체 분석 모델이 각광받고 있습니다.
 |
|
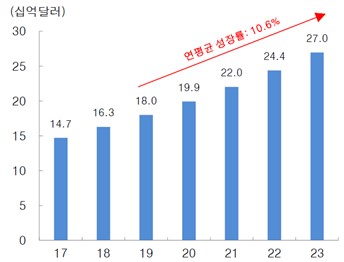
글로벌 유전체 산업 시장규모 |
| 출처: Frost&Sullivan, NH, 대신증권리서치센터 |
 |
|
DNA 시퀀싱 비용 감소 |
| 출처: Frost&Sullivan, NH, 대신증권리서치센터 |
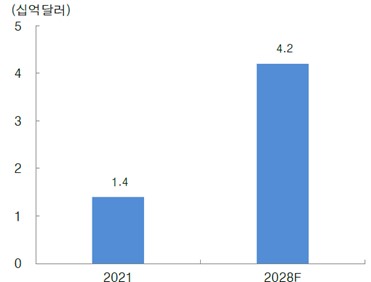
개인유전체 분석 서비스는 개인의 유전정보를 분석해 질병 위험을 예측하거나 생활습관 개선을 돕는 맞춤형 헬스케어 서비스이며 의료기관용 서비스와 소비자직접의뢰(DTC)라고 불리는 비의료기관 서비스로 구분됩니다. 글로벌DTC 유전체분석 시장은 2021년 14억 달러에서 2028년 42억 달러로 연평균 15.3% 성장할 것으로 전망되며, 이는 검사비용 감소로 인한 접근성 증대, 각 국의 규제 완화 효과 등에 기인합니다.
 |
|
DTC 유전체분석 산업 시장규모 |
| 출처: Global Market Insight, theDNAgeek, 대신증권리서치센터 |
(나) 의료IT솔루션
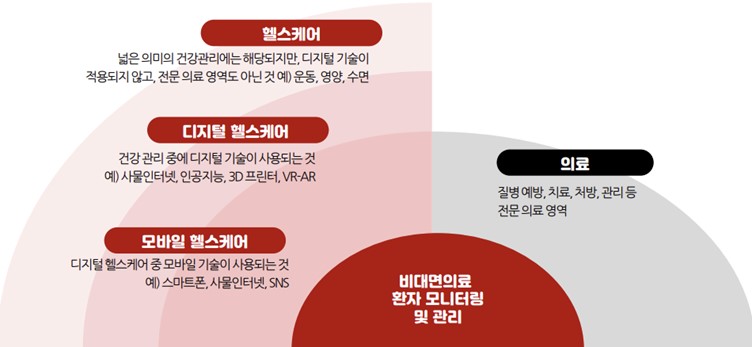
당사가 영위하는 의료IT솔루션 서비스는 광의로 디지털 헬스케어 산업에 속하며 디지털헬스케어는 질병의 진단, 치료와 함께 건강의 유지 및 증진까지 포괄하는 의미로 국내/외에서 광범위하게 사용중입니다. “ICT(Information and Communication Technologies)기술을 활용한 건강관리 서비스”로 의료/비의료 서비스를 포괄합니다. 기존 의료시스템이 환자의 치료에만 초점을 맞춘 사후적 대응 및 관리였다면, 디지털헬스케어는 치료뿐만 아니라 미래에측을 통한 질병예방까지, 환자 개개인의 고유한 특성에 적합한 맞춤의학을 제공하는 것을 목표로 지향하고 있습니다.
 |
|
디지털헬스케어 산업 범위 |
| 출처: 한국과학기술정보연구원, 한국IR협의회 기업리서치센터 22.02.10 |
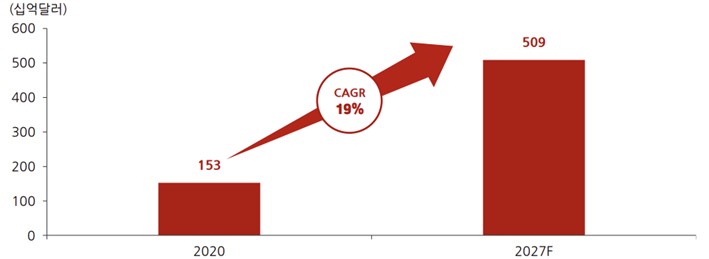
한국보건산업진흥원이 GIA(2020)자료를 인용해 발표한 글로벌 디지털 헬스케어 산업시장 매출규모는 2020년 1,525억 달러로 추정하였고 2027년까지 연평균 19% 성장하여 2027년 5,089억 달러가 될 것으로 전망하였습니다. 이 같은 빠른 성장 근거로는 1)고령화 시대로의 진입, 2)5G 상용화, 3)Covid-19 팬데믹 등을 꼽았습니다.
 |
|
글로벌 디지털 헬스케어 시장 현황과 성장 전망 |
| 출처: Global Industry, 한국IR협의회 기업리서치센터 22.02.10 |
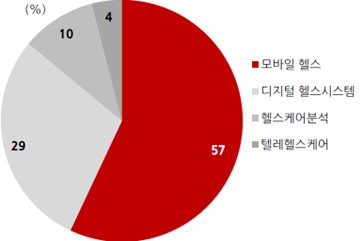
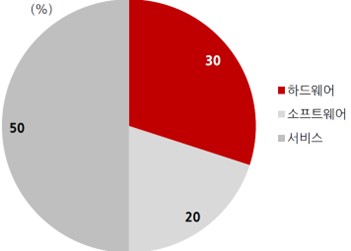
분야별로는 모바일 헬스와 디지털헬스시스템이 각각 57%, 29%로 높은 비중을 차지하고 있으며 구성 요소별로는 하드웨어, 소프트웨어, 서비스가 각각 30%, 20%, 50% 비중을 차지하고 있습니다.
| [글로벌 디지털 헬스산업 내 분야별 비중(2020)] |
 |
|
글로벌 디지털 헬스산업 내 분야별 비중 |
| 출처: 한국보건산업진흥원, 대신증권리서치센 |
| [글로벌 디지털 헬스산업 내 구성요소별 비중(2020)] |
 |
|
글로벌 디지털 헬스사업 내 구성요소별 비중 |
| 출처: 한국보건산업진흥원, 대신증권리서치센터 |
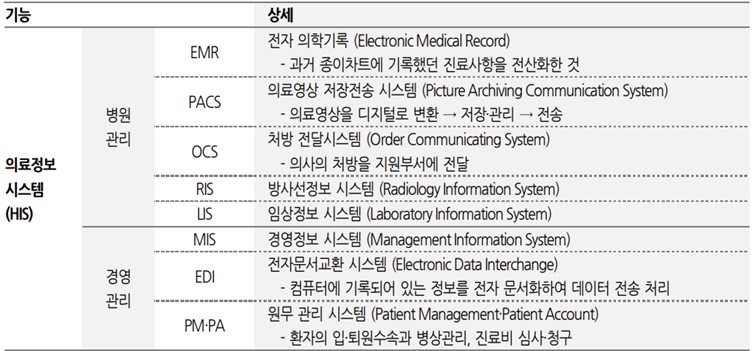
디지털 헬스케어는 건광관련 서비스와 의료IT가 융합된 종합 의료서비스인데 정보통신산업진흥원에 따르면 의료정보시스템은 디지털 헬스케어의 한 분야입니다. IT분야의 전문 리서치 기업인 Gartner는 의료정보시스템이 환자, 헬스케어기업, 의료기관들에게 디지털헬스케어 생태계의 중심이 되는 플랫폼으로 진화할 것이라 예상했습니다. 특히 현재는 기능, 고객규모, 지리적 시장을 중심으로 파편화된 의료정보시스템 시장이 장기적으로 기술력 있는 대형벤더(Vender) 중심으로 재편될 것으로 전망하였습니다. 의료정보시스템(HIS)의 핵심적 기능은 전자의학기록(EMR, Electronic Medical Record)으로 국내에서는 HIS와 EMR을 동일한 개념으로 사용하고 있습니다.
 |
|
의료정보시스템 구성 |
| 출처: 한국과학기술정보연구원, PwC, 한국IR협의회 기업리서치센터 22.02.10 |
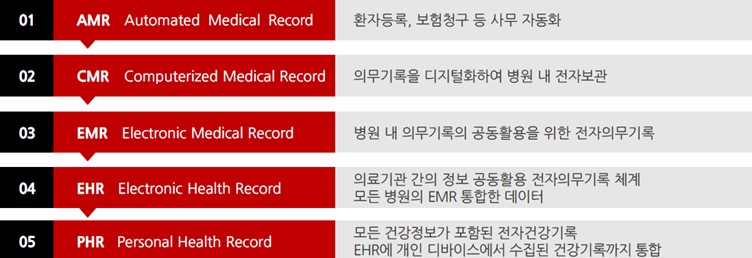
EMR은 5단계의 발전단계를 거치는데, 한국은 현재 3단계(EMR, 병원 내 의무기록의 공동활용을 위해 전자의무 기록단계)에서 4단계(EHR, Electronic Health Record, 의료기관 간 정보 공동활용 전자의무기록 체계) 사이에 위치해 있으며 3단계에 가깝습니다.
 |
|
EMR 발전 5단계 |
| 출처: 심평원, PwC, 한국IR협의회 기업리서치센터 22.02.10 |
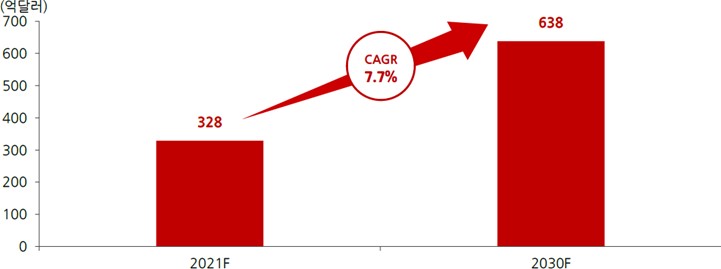
시장조사업체인 MordorIntelligence에 따르면, 2020년 글로벌 EHR(Electronic Health Records)시장은 305억 달러로 추정되며 이 시장은 2021년부터 2030년까지 연평균 7.7% 성장해, 2030년 638억 달러 규모로 성장할 것으로 전망됩니다.
 |
|
글로벌 EHR 시장 성장 전망 |
| 출처: Mordorintelligence, 한국IR협의회 기업리서치센터 22.02.10 |
원격의료(Telemedicine)는 디지털헬스케어의 한 분야로 의료수요자와 의료공급자 사이에 원거리에서 ICT기술을 활용하여 의료서비스를 제공하는 것입니다. 즉 환자가 병의원을 직접 방문하지 않고 정보통신기술을 이용해 적절한 진료, 처방, 모니터링을 하는 것을 의미합니다. 원격의료는 1)서비스의 제공대상에 따라 ‘의사-의사’, ‘의사-환자’, 2)종류에 따라 ‘원격진료’, ‘원격모니터링’,’원격수술’등으로 나눌 수 있는데 국내에서는 의료인 간 의료 행위에 국한되어 있었으나 Covid-19 방역대책 일부로 2020년 2월 24일부터 전화상담과 대리처방을 한시적으로 허용하였습니다.
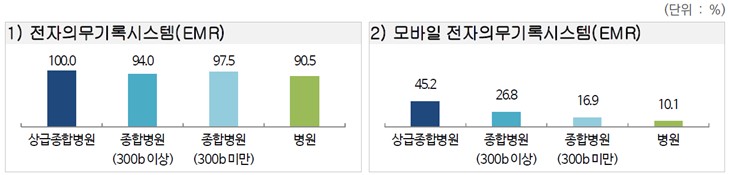
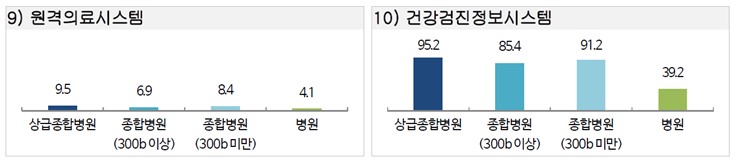
한국보건의료정보원 ‘2020년 보건의료정보화 실태조사’에 따르면 국내 전자의무기록시스템 도입률은 상급종합병원 100%, 종합병원 96%, 병원 90.5%순으로 도입율이 높으며 모바일 전자의무기록시스템의 도입률은 상급종합병원 45.2%, 종합병원 21.1%, 병원 10.1%의 도입률로 전자의무기록시스템 대비 현저히 낮아 향후 성장 잠재력이 높은 분야로 꼽힙니다. 원격의료시스템은 상급종합병원 9.5%, 종합병원 7.8%, 병원 4.1%로 큰 차이 없이 의료기관 전체적으로 도입률이 낮으며 건강검진정보시스템의 도입률은 상급종합병원 95.2%, 종합병원 88.7%로 높으편이나 병원은 39.2%로 도입률이 상대적으로 저조합니다.
 |
|
국내 의료기관별 의료정보시스템 도입 여부_1 |
 |
|
국내 의료기관별 의료정보시스템 도입 여부_2 |
| 출처: 한국보건의료정보원 '2020년 보건의료정보화 실태조사' |
(2) 산업의 성장성
(가) 체외진단검사서비스
체외진단(IVD : In vitro Diagnostics) 시장은 경제상황이나 산업의 많은 어려움 속에서도 지속적으로 성장하고 있으며, 'IMS Health, IMS Health Market Prognosis(2013)'에 따르면 체외진단 시장의 성장률은 7.3%로 제약시장 성장률 5.3%보다 빠른 속도로 성장하고 있습니다. IVD 시장은 기술 변화 주기가 빠르게 변화하는 분야로 프로스트 앤 설리번 한국 지사가 발표한 '세계 체외진단(IVD : In Vitro Diagnostics) 시장 분석 보고서(Analysis of the Global In Vitro Diagnostics Market(2014))'에 따르면, 2013년 해당 시장 수익은 472억 7천만 달러에서 2017년에는 626억 3천만 달러에 달할 것으로 예상하고 있습니다.
매출액 상위 분야는 면역화학 199.5억 달러, 자가혈당 측정 85.2억 달러, 현장진단 의료기기 63.4억 달러이며, 성장률 상위분야는 분자진단, 현장진단 의료기기, 지혈진단 분야순으로 분석되었습니다.
또한 경기침체로 미국·유럽 시장은 위축되었으나, 아시아·태평양 지역은 신흥시장으로 떠오르고 있습니다. 글로벌 체외진단 시장은 매우 세분화되어 있으며, 상위 3개 기업이 전체 시장규모의 46.8%를 차지하고 있습니다.
분자진단이란 병원균 및 병원체의 DNA, RNA를 검출하는 방법으로 2012년 시장규모는 50억달러 규모로 전체 체외진단(IVD) 시장의 11%를 점유하고 있습니다. 2017년 90.7억달러로 연평균 12.6%의 성장을 보일 것으로 전망되며, 감염병 진단에 가장 높은 활용도를 보이고 있습니다. 성장단계에 있는 국가들인 중국, 인도, 한국 등에서 임상시험 및 분석 수요가 증가하면서 해당제품의 수요가 증가하고 있는 상황이며, 진단의 정확도가 높은 반면 고비용의 단점을 지니고 있습니다. Top 3 기업의 시장점유율은 51.2%이지만, Roche Diagnostics가 전체시장의 25.2%로 높은 시장점유를 보이고 있습니다. 분자진단 시장은 IVD 시장에서 가장 빠르게 제품의 변화를 보이고 있는 시장입니다.
(나) 의료IT솔루션
2015년 시장 성장세는 빠르게 성장할 것으로 전망하며 전년 대비 약 8.1%의 성장률을 보이며 490억 달러에 달할 것으로 예상됩니다. 특히, 아시아-태평양 지역에서 신축 건물 조성과 보강된 제조 설비에 따라 시장규모가 약 8~9%의 높은 성장률을 보일 것으로 전망됩니다
(3) 경기변동의 특성
(가) 체외진단검사서비스
① 경기변동 및 계절성
의료기기는 다른 산업과 비교하여 상대적으로 경기변동이나 계절적 요인에 비탄력적인 특징을 나타내고 있습니다. 계절적 요인에 따른 부분은 특정 시기에 급격히 발생하는 인플루엔자에 대한 진단 수요나 여름철 발생할 수 있는 모기 매개질환에 대한 진단 수요 등 특정 시기에 수요가 증가할 수 있는 경우는 있으나 전반적으로 다른 산업 대비 계절적 요인이나 경기변동에 민감하다고 할 수 없습니다. 특히 세계적인 고령화 추세, 건강에 대한 관심 고조 및 웰빙에 대한 사회적 분위기 확산, 주요 국가들의 보건 의료 정책 등으로 인한 의료서비스 수요 증가, 감염성 질환을 포함한 질병의 증가, 치료에서 예방 및 진단으로의 의료 트렌드 변화 등의 요인으로 향후 지속적이며 예측 가능한 성장이 예상됩니다.
② 라이프사이클
체외진단 제품은 의약품 및 신약들과 비교해서도 라이프사이클이 짧지 않으며, 새롭게 개발되는 진단 기술, 진단장비 등에 대해서도 지적재산권을 통해 보호받고 있습니다. 또한 산업 내 범용으로 사용되고 있는 체외진단 기술 및 제품들 역시 진단 대상 질환, 제품의 정확도 등에 따라 라이프사이클은 상이하며, 주기적으로 발생하는 감염성 질환 진단 제품, 지속적인 진단 수요가 있는 제품, 높은 정확도를 확보하고 있는 제품들의 경우 라이프사이클이 보다 긴 특징을 보이고 있습니다. 아울러 지속적인 제품 개발을 통해 정확도를 높이고 있으며 진단장비를 활용하여 정확도 및 진단 편의성을 확보하는 등의 영향으로 체외진단 제품의 라이프사이클은 장기화되고 있는 추세입니다.
(나) 의료IT솔루션
① 경기변동 및 계절성
의료 서비스 수준에 대한 소비자의 관심 증대, 의료 패러다임의 변화 등 의료서비스에 대한 관심이 증대되는 한편 국민소득의 증대와 평균수명이 늘어나면서 개인들의 의료소비는 점점 증가하고 있습니다. 이에 따라 의료기관의 서비스 경쟁은 더욱 치열해지고 있으며, 의료정보시스템은 의료기관의 필수적인 요소로 자리 잡고 있습니다. 따라서 의료정보시스템 관련사업은 그 특성상 타 사업분야에 비해서는 경기변동에 영향을 적게 받는 사업입니다.
의료정보시스템 신규 도입 프로젝트는 평균적으로 1년 이상의 기간이 소요되고, 해당기간 동안 꾸준하게 인력이 투입되며, 당사의 매출인식 기준은 프로젝트 진행률을 기준으로 하고 있어 계절적 요인에 의해 매출 등이 영향을 받지 않습니다. 의료정보시스템 운영의 경우에도 365일 동일한 품질로 운영되어야 하는 특성상 계절적 요인은 없다고 볼 수 있습니다. 의료정보시스템 신규 발주 시기도 특별히 계절에 영향을 받지 않습니다.
② 라이프사이클
의료IT솔루션 중 EMR 등 병원에서 주로 사용되는 의료정보시스템은 도입 후 특정 주기 없이 지속적으로 사용하고 있어 제품 주기가 긴 편에 속합니다. 다만 개인화된 의료서비스 정보 제공에 따라 당사 제품의 주요 소비자인 병의원들은 EMR과 연동되는 부가적인 소프트웨어 도입을 하게 되며 DTC 체외진단제품의 성장에 따라 해당 영역을 담당하는 IT솔루션의 성장성 또한 더욱 높아질 것으로 전망되고 있습니다.
(4) 경쟁요소
(가) 체외진단검사서비스
a. 글로벌 체외진단검사 업체
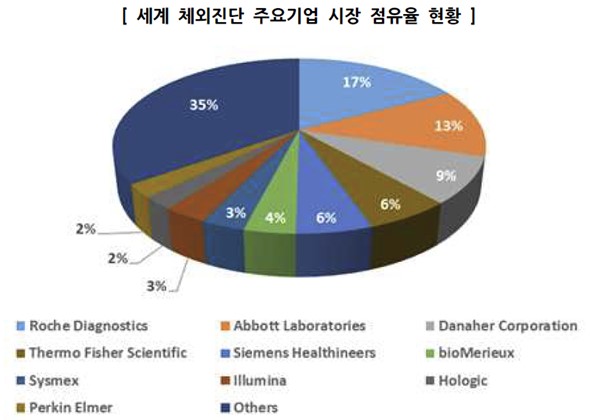
체외진단 시장은 글로벌 업체에 의해 주도되는 시장이라고 말할 수 있습니다. 체외진단시장 상위 3개사가 전체 시장의 39%를 차지하여 높은 진입장벽이 존재합니다. 세계 분자/면역진단시장은 스위스의 Roche Diagnostics가 가장 높은 점유율을 보이고 있으며, Abbott Laboratories, Danaher Corporation, Siemens Healthineers, Thermo Fischer Scientific, Johnson & Johnson 등의 업체가 경쟁하고 있습니다. 2020년 기준 글로벌 Top 10 기업의 총 매출액은 560.19억달러로 글로벌 시장의 65.2%를 차지하고 있으며 글로벌 상위 20개 기업의 글로벌 시장 점유율은 78.8%에 달합니다. 로슈진단의 글로벌 시장 점유율은 17.3%로 선두를 지키고 있으며, 애보트와 다나허가 각각 점유율 2위와 3위를 차지하고 있습니다.
분자/면역 진단 시장은 일부 자가측정용 기기를 제외하고 대부분 의료산업에 종사하는 전문가용으로 한정되어 있어 제품의 안전성과 신뢰성을 중시합니다.
 |
|
세계 체외진단 주요기업 시장 점유율 현황 |
| 출처: Global In Vitro Diagnostics Market Outlook 2021, Frost&Sullivan 2021.09 |
① 애보트
세계적으로 선도적인 의료 기업 중 하나로, 다양한 건강 문제를 관리하기 위한 의약품, 정보, 획기적인 기술을 제공하는 다양한 사업을 영위하고 있으며 주로 진단 솔루션 및 서비스, 의료기기, 영양제품, 기성 의약품 등 다양한 제품 및 서비스를 제공하고 있습니다.
 |
|
애보트 주요 제품 및 서비스 |
| 출처: Allied Market Research, Global In-Vitro Diagnostics Market, 2021 |
② 다나허
산업 및 소비자 제품, 서비스의 설계, 제조 및 마케팅을 위한 제품 및 서비스를 제공하는 기업으로, 생명과학, 환경, 진단, 치과 등 4개 사업 부문을 통해 다양한 제품과 서비스를 제공하고 있습니다. 자회사인 Beckman Coulter, Inc(미국)을 통해 체외진단 제품과 서비스를 제공하고 있습니다.
 |
|
다나허 주요 제품 및 서비스 |
| 출처: Allied Market Research, Global In-Vitro Diagnostics Market, 2021 |
b. 국내 체외진단검사 업체
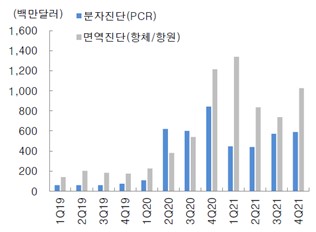
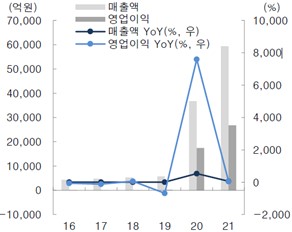
기존 국내 제약/바이오섹터에서는 체외진단보다는 치료관련 기업들이 주목받아 왔으나, COVID-19 팬데믹 이후 진단 섹터가 주목을 받기 시작했으며 국내 체외진단기업들은 팬데믹 시작과 동시에 빠르게 PCR 분자진단 및 면역진단 COVID-19 키트를 개발, 전세계에 수출하였습니다. 관세청 통관 데이터에 의하면 분자진단 키트(HS Code:3822.00)와 면역진단 키트(HS Code:3002.15)의 2021년 수출액은 `19년 대비 각각 8.1배(20.5억달러), 5.6배(39.4달러)로 증가하였으며, 주요 진단 9개 기업의 합산 매출액은 `19년 5,438억원에서 `20년과 `21년 각각 3조 6,755억원, 5조 9,424억원으로 증가하였습니다. COVID-19 진단키트는 마진율이 평균 70%에 달하기 때문에 영업이익 개선폭도 매우 컸는데, 합산 영업이익은 `19년 227억원에서 `20년과 `21년 각각 1조 7,460억원, 2조 6,799억원으로 증가하였습니다.
 |
|
국내 진단키트 수출액 추이(분기별) |
| 출처: 관세청, Quantiwise, 대신증권 |
 |
|
주요 국내 진단기업 매출액, 영업이익 |
| 출처: 관세청, Quantiwise, 대신증권 |
①씨젠
씨젠은 2000년 설립 후 2010년 9월 코스닥 시장에 상장되었으며 분자진단에 사용되는 시약 및 장비 제조/판매 사업을 영위하고 있습니다. 원하는 유전자만 증폭시켜 질병의 원인을 다양하게 분석할 수 있는 멀티플렉스 유전자 증폭 시약 및 분석 원천기술을 보유하고 있습니다. 유럽을 중심으로 아메리카, 중동 등지에 해외 법인을 설립하여 글로벌 네트워크를 구축, 60여개국에 분자진단 제품을 공급하고 있습니다. 동사는 분자진단 분야에서 세계적인 수준의 기술력을 보유하고 있으며 다양한 질병을 한 번에 분석할 수 있는 멀티플렉스 진단 관련 원천 기술을 보유하고 있습니다.
 |
|
씨젠 주요 제품 및 서비스 |
| 출처: 씨젠, 대신증권 |
②마크로젠
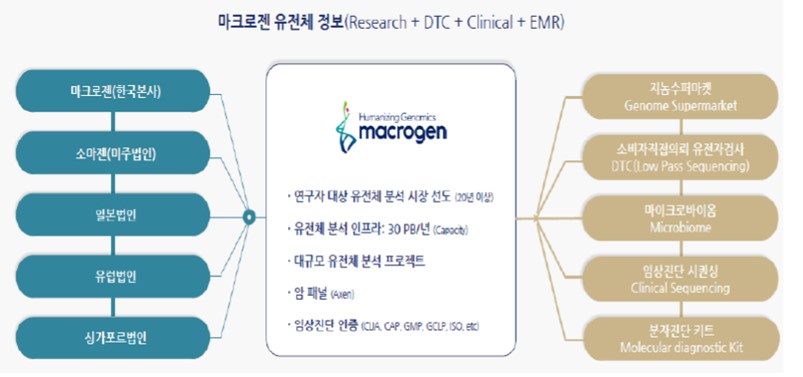
동사는 1997년 설립, 2000년 2월 코스닥 시장에 상장되었으며 유전체 분석 용역 서비스로 세계 5위 수준의 유전체 분석 설비를 보유하고 있으며 시퀀싱 서비스 기술력을 가지고 있습니다. 20년 이상 업력에 기반한 유전체 분석 노하우를 기반으로 전세계 다양한 고객에게 분석서비스를 제공하고 있습니다. 주요 사업영역은 유전체 분석(CES, NGS), 올리고합성, 마이크로어레이 등 유전체 연구에 활용되는 제품이나 서비스입니다. 동사는 유전체 분석 리처시 분야 국내 1위 업체로 150개국에 18,000여개 기관 및 기업에 유전체 분석 서비스를 제공하고 있으며 `22년 사업부별 매출비중은 DNA 시퀀싱 82.3%, 마이크로어레이 5%, 생체조작쥐 2.2%, 올리고 합성 7% 등으로 구성되어 있습니다.
 |
|
마크로젠 주요 제품 및 서비스 |
| 출처: 마크로젠, 대신증권 |
③EDGC
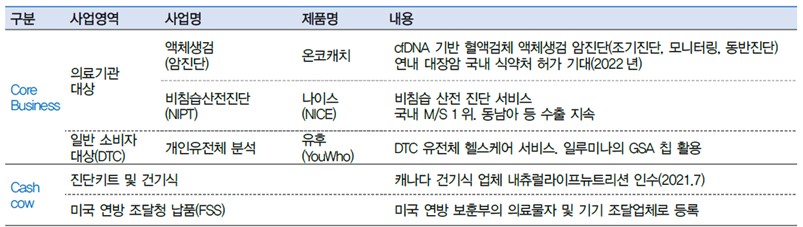
EDGC는 유전체분석 상업 서비스를 제공하기 위한 클리닉 랩으로 국내 진단 위수탁기관인 이원의료재단과 미국 NGS업체 Diagnomics가 2013년 합작 설립하였으며 2018년 코스닥시장에 상장하였습니다. 동사의 주요 사업영역은 혈액기반 액체생검, 비침습산전검사(NIPT), 개인유전체분석(PGS) G헬스케어 서비스가 있으며 액체생검 암 조기진단 서비스에 경쟁력을 가지고 있습니다.
 |
|
EDGC 주요 제품 및 서비스 |
| 출처: EDGC, 대신증권 |
(나) 의료IT솔루션
국내 의료정보시스템 시장은 상급종합 병원의 경우 소수 업체가 제품 공급하고 있으며 중소형병원과 약국 대상으로는 유비케어, 비트컴퓨터 등이 관련 제품을 출시해 판매하고 있습니다.
① 이지케어텍
이지케어텍은 2001년 서울대학교 전산팀에서 분사해서 설립된 회사로 주로 종합병원을 대상으로 구축형 의료정보시스템을 납품 후 관리서비스를 제공하며 중소형병원에는 클라우드형 의료정보시스템을 제공합니다.
② 유비케어
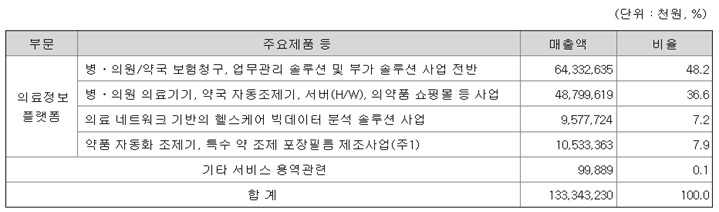
유비케어는 GC녹십자 그룹 계열사로서 1993년 국내 최초로 병의원 의료정보시스템(EMR) ‘의사랑’을 출시했으며 주요 영위사업으로는 EMR솔루션, 유통, 제약데이터, 제조사업이 있습니다. 동사는 전국 25,700여 병ㆍ의원/약국 (17,700여 개의 병원ㆍ의원, 8,000여개의 약국)과 38개에 이르는 전국 법인 대리점을 포함한 국내 최대 의료 네트워크를 보유하고 있으며 EMR 및 다양한 부가 솔루션을 제공하고 있습니다. 유통사업부문은 디지털 방사선 장비 등 다양한 ‘의료기기’부터 의약품/의료 소모품을 온라인으로 쉽게 주문할 수 있는 ‘모소몰닷컴’을 비롯하여 의약품 자동조제기인 ‘유팜오토팩’, 약국 전용 온ㆍ오프라인 통합 주문 온라인 쇼핑몰 ‘유팜몰’ 등 요양기관 운영을 효율적으로 돕는 맞춤형 유통 솔루션을 제공하고 있습니다. 또한 제약사와 증권사를 대상으로 요양기관 기반의 헬스케어 빅데이터를 수집ㆍ분석하여 제공하고 있습니다.
 |
|
유비케어 사업부문별 매출비중 |
| 출처: DART |
③ 비트컴퓨터
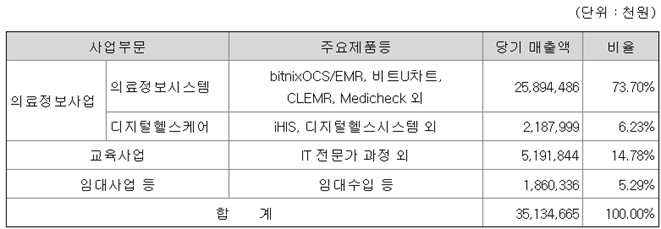
비트컴퓨터는 ‘의료정보사업’, ‘디지털헬스케어사업’ 등을 영위하고 있으며 ‘의료정보사업’의 경우 1~3차 의료기관과 약국에 의료정보시스템을 개발 및 공급하고 있습니다. 중대형 병원에는 오랜 시간 시장에서 검증된 솔루션인 통합의료정보시스템 bitnixHIS로, 중소형 병원과 전문병원은 기존의 구축형 통합의료정보시스템 bitnitHIB와 함께 구독형 방식인 클라우드 기반의 클레머(CLMER) 서비스를 제공중입니다. 요양병원은 bitnixSilver와 클라우드 기반의 bitnixCloud를 공급하고 있으며 의원급 의료기관은 전자차트 프로그램인 비트U차트를 시작으로 비트A차트와 국내 최초의 클라우드 기반 PHR플랫폼 ‘비트플러스’를 제공하고 있습니다. ‘디지털헬스케어사업’은 의료정보 분야의 경험과 기술력을 기반으로 다수의 의료기관을 고객으로 확보하고 있습니다.
 |
|
비트컴퓨터 주요 제품 및 매출 비중 |
| 출처: DART |
(5) 관련 법령 또는 정부의 규제
(가) 체외진단검사 서비스
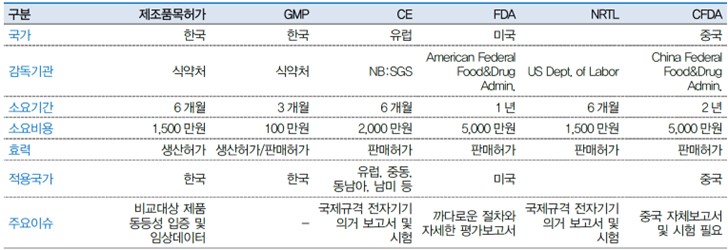
각 국가는 인체에 미치는 위험도에 따라 의료기기를 등급으로 나누어 관리하고 있습니다. 체외진단은 의료기기의 일종으로 성능이나 안정성에 대한 품질이 확보되어야 하기 때문에 국내외 규제기관의 기준에 따른 규제를 받고 있습니다. 제품의 임상시험부터 보험 등재까지 기간은 수개월에서 길게는 2~3년까지 소요되며 규제기관의 허가를 확보한 후 시장에 진입할 수 있기 때문에 판매하고자 하는 국가의 규제기관이 정한 허가 심사 규정을 준수해야 합니다.
 |
|
주요 국가별 체외진단산업 인허가 제도 |
| 출처: 에스디바이오센서 사업보고서, 대신증권리서치센터 |
당사가 영위하는 체외진단기기 및 의료IT솔루션 산업은 제품에 대한 허가 및 의료정보데이터에 포함한 개인정보보호를 위한 다양한 법적 규제를 받고 있습니다. 체외진단의료기기 관련해서 당사가 적용 받고 있는 각종 규제는 다음과 같습니다.
| 구분 | 내용 |
|
체외진단의료기기법 [법률 제16433호] |
사람이나 동물로부터 유래하는 검체를 체외에서 검사하기 위하여 단독 또는 조합하여 사용되는 시약, 대조ㆍ보정 물질, 기구ㆍ기계ㆍ장치, 소프트웨어 등 「의료기기법」에 따른 의료기기로서 다음 각 목의 어느 하나에 해당하는 체외진단의료기기 제품의 제조·수입 및 판매 등에 관한 사항을 규정함으로써 의료기기의 효율적인 관리를 도모하고 국민보건 향상에 기여하기 위해 제정한 법령입니다.
② 질병의 소인(素因)을 판단하거나 질병의 예후를 관찰하기 위한 목적으로 사용되는 제품 ③ 선천적인 장애에 대한 정보 제공을 목적으로 사용되는 제품 ④ 혈액, 조직 등을 다른 사람에게 수혈하거나 이식하고자 할 때 안전성 및 적합성 판단에 필요한 정보 제공을 목적으로 사용되는 제품 ⑤ 치료 반응 및 치료 결과를 예측하기 위한 목적으로 사용되는 제품 ⑥ 치료 방법을 결정하거나 치료 효과 또는 부작용을 모니터링하기 위한 목적으로 사용되는 제품
|
|
의료기기법 [법률 제18319호] |
사람이나 동물에게 단독 또는 조합하여 사용되는 기구·기계·장치·재료 또는 이와 유사한 제품으로서 다음의 어느 하나에 해당하는 의료기기 제품의 제조·수입 및 판매 등에 관한 사항을 규정함으로써 의료기기의 효율적인 관리를 도모하고 국민보건 향상에 기여하기 위해 제정한 법령입니다.
② 상해(傷害) 또는 장애를 진단·치료·경감 또는 보정할 목적으로 사용되는 제품 ③ 구조 또는 기능을 검사·대체 또는 변형할 목적으로 사용되는 제품 ④ 임신을 조절할 목적으로 사용되는 제품
|
|
폐기물관리법 [법률 제19126호] |
본 법령은 폐기물의 발생을 최대한 억제하고 발생한 폐기물을 친환경적으로 처리함으로써 환경보전과 국민생활의 질적 향상 이바지를 목적으로 합니다. 당사는 당사에서 판매하는 체외진단의료기기들의 제조 과정에서 발생하는 일반 및 의료 폐기물 처리에 있어서 본 규정을 철저히 준수하고 있습니다. |
|
생명윤리 및 안전에 관한 법률 [법률 제17783호] |
본 법령은 인간과 인체유래물 등을 연구하거나, 배아나 유전자 등을 취급할 때 인간의 존엄과 가치를 침해하거나 인체에 위해(危害)를 끼치는 것을 방지함으로써 생명윤리 및 안전을 확보하고 국민의 건강과 삶의 질 향상에 이바지함을 목적으로 합니다. 당사에서 판매하는 체외진단의료기기들의 연구 및 개발 과정에서 필요한 인체유래물에 대해서는 본 법령 제42조 인체유래물 채취 시 동의, 잔여검체의 제공 및 잔여검체의 관리 세부 규정에 따라 철저히 취급하고 있습니다. |
|
개인정보 보호법 [법률 제16930호] |
개인정보 보호법은 당사자의 동의 없는 개인정보 수집 및 활용하거나 제3자에게 제공하는 것을 금지하는 등 개인정보보호를 강화한 내용을 담아 제정한 법률입니다. 이 법은 개인정보의 수집ㆍ유출ㆍ오용ㆍ남용으로부터 사생활의 비밀 등을 보호함으로써 국민의 권리와 이익을 증진하고, 나아가 개인의 존엄과 가치를 구현하기 위하여 개인정보 처리에 관한 사항을 규정함을 목적으로 하는데, 당사의 경우 사내 임직원뿐만 아니라 영업활동을 통한 국내외 대리점, 병원, 보건소 및 개인용혈당측정기 구매자에 해당하는 일반 사용자 등으로부터 수집된 정보가 그 대상이 되며, 이와 같은 개인정보가 본 법령에 따라 철저히 보호될 수 있도록 준수하고 있습니다. |
|
체외진단의료기기 제조 및 품질관리 기준 [식약처고시 제2021-31호] |
「의료기기산업 육성 및 혁신 의료기기 지원법」제정(법률 제16405호, 2019.4.30 공포, 2020.5.1 시행)으로 혁신의료기기로 지정을 받은 의료기기소프트웨어에 대한 적합성인정등 심사에 대한 세부사항을 마련하고, 「체외진단의료기기법」제정(법률 제16433호, 2019.4.30 공포, 2020.5.1 시행)에 따라 체외진단의료기기 관련 적합성인정등 심사에 대한 사항은 이 고시에서 삭제하고 별도로 규정하는 한편, 제조·수입 허가 취소 등의 사유가 발생한 경우에는 제조·수입업자가 해당 적합 인증서를 반납할 수 있도록 하는 등 의료기기 제조 및 품질관리 업무에 적정을 기하고자 함에 목적을 두고 있습니다. 당사는 본 기준에 따라 품질관리기준 적합성 인증을 받고 있습니다. |
|
ISO13485 Medical devices - Quality management systems Requirements for regulatory purposes |
ISO 13485은 현재 전 세계 대부분의 의료기기 법규에 부합하는 품질경영시스템 관련 규격으로, 이에 따라 의료기기 제조업체, 위탁 제조업체, 서비스 제공 업체 및 유통 업체 등 다양한 형태의 조직에 적용되는 품질 인증입니다. 이는 전 세계 가장 많은 나라에서 신뢰하는 품질경영시스템에 대한 요구사항으로, 의료기기 수출을 위한 주요 국가에서 통용이 되는 규격임에 따라 당사는 본 규격에 따른 품질시스템을 구축하고 매년 이에 대한 심사를 통해 인증을 유지하여 전 세계 제품 수출, 판매가 가능하게 됩니다. |
국내에서는 위해성에 따라 1~4등급 분류 후 위해성이 낮은 1등급의 경우 한국의료기기안전정보원에 신고로 별도의 신청기술문서 심사가 불필요합니다. 2등급 인증에 해당되는 품목은 시험검사기관 또는 기술문서심사기관을 통해 시험성적서 혹은 기술문서적합통지서를 수령한 후 한국의료기기안전정보원을 통해 인증서를 발급받게 되며 2등급 허가품목은 임상자료를 구비하여 식품의약품안전처로부터 허가증을 발급받아야 하며 3~4등급의 경우도 심사 및 임상적 성능시험을 통해 식품안전처로부터 허가증을 발급 받아야합니다.
[국내 체외진단의료기기 등급 분류]
| 위해성 | 등급 | 종류 |
|---|---|---|
| 낮음 | 1등급 | 균동정 배지, 유전자 추출시약 등 |
| 낮음 | 2등급 | 임신진단, 헬리코박터 파이로리 검사 등 |
| 중등 | 3등급 | 인플루엔자 감염진단 시약, 종양검사 시약 등 |
| 높음 | 4등급 | 수혈용 HIV, HBV, HCV, 선별 시약, 혈액혈 판정 시약 등 |
| 출처: 식품의약품안전처, 대신증권리서치센터 |
미국 FDA는 의료기기를 약 17,800개의 종류로 분류해 놓고 있으며, 이를 패널(Panel)이라 명명하는 16개의 의료 전문분야 카테고리로 재구성해 놓고 있습니다. 이 같이 다양한 의료기기 종류에 포함되는 품목들은 1976년 연방식품, 의약품 및 화장품 법의 의료기기법 개정 이후로 크게 세가지 등급으로 분류되기 시작하였으며 이 세가지 등급은 다양한 종류의 의료기기들의 안전성과 효과성을 확인, 규제하기 위한 목적으로 만들어졌습니다.
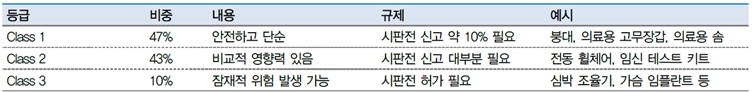
1등급에 속하는 의료기기들은 사용자에 대해 최소한의 위해요인을 가지고 있는 기기들로 의료기기 위험등급 2, 3보다 간단한 디자인이며 품목으로는 관장키트와 압박붕대 등이 있습니다. 47%의 의료기기가 이 카테고리에 포함되며 이 중 95%가 규제절차에서 면제됩니다.
2등급 기기들은 43%의 비중을 차지하고 있으며 시판전 대부분 신고가 필요하며 전동휠체어, 임신 테스트기 등의 품목이 있습니다.
3등급 의료기기의 경우 일반적으로 생명을 유지하거나 보존하기 위해 설치, 사용되거나 또는 의도치 않은 질병 및 상해 유발 등 예측되지 않는 잠재 위험을 가지고 있는 최고 등급의 품목입니다. 1~3등급 의료기기 모두에 적용되는 일반규제(General Control)의 경우는 1)공장시설등록(Establishment Registration, FDA 2891), 2)의료기기 리스팅(Medical Device Listing, FDA 2892), 3)의료기기 표시사항(Labeling)제출, 4)시판 전 신고서인 510(k)제출 및 5)품질시스템(QSR)확인사항 제출이 있습니다. 특별규제(Special Conntrol)의 경우는 2등급의 의료기기에 보통 적용되며 전등급에 동일하게 적용되는 일반규제에 대한 사항들을 충족한 이후 추가적인 서류들을 제출해야 하며 이들 서류는 1)특별표시사항 표기, 2)해당 품목에 대한 사용자 모니터링 결과 3)제품에 대한 상세한 사용설명서 제공 4)시판 후 감시 등을 포함합니다. 여기에 PMA(시판 전 승인)은 위험 등급 3에 해당하는 의료기기들로 일반규제 내용들을 충족한 이후에도 1)임상실험을 통한 임상자료, 2)비임상 실험을 통한 동물실험자료를 제출해야 하며, 3)공장 등 생산시설 설비에 대해 Cgmp(Current Good Manufacturig Practices)심사를 받아야 합니다.
 |
|
미국 FDA 의료기기 등급 분류 |
| 출처: FDA, 한국보건산업진흥원, 대신증권리서치센터 |
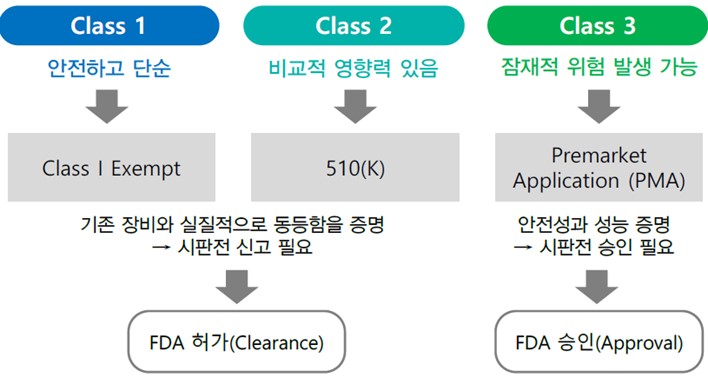
미국 FDA의 의료기기 인허가 프로세스는 안전하고 단순한 기기의 경우 신고서를 심사하여 본질적 동등성 여부를 판단하며 본질적으로 동등하다고 판단하면 시판전 신고를 허가하는 통지문인 SE(Substantially Equivalent)Letter를 신청기업에 송부하며 신청기업은 해당 SE Letter를 수령 후 미국시장에서 상업적으로 판매할 수 있습니다. 반면 FDA가 신고품목이 기허가 의료기기와 본질적으로 동등하지 않다고 판단하는 경우는 시판 전 신고를 불허하는 공문인 NSE(Not-substantianlly equivalent) Letter를 신청기업에게 제공하며 불허공문을 받은 신청기업은 510(k)를 재작성해 제출할 수 있습니다. 3등급에 해당하는 사람의 생명과 건강에 위협이 될 수 있는 위험성을 가지는 의료기기는 시판 전 승인(Premarket Approval, PMA)을 받아야 하며 일반적으로 PMA 절차에서는 해당 품목의 효과성을 증명할 수 있는 자료 및 이를 뒷받침하는 임상실험(Clinical Trial)이 필요하므로 시판 전 신고와는 비교하기 어려울 정도로 비용과 시간이 많이 소요됩니다.
 |
|
미국 FDA 의료기기 인허가 프로세스 |
| 출처: FDA, 대신증권리서치센터 |
(나) 의료IT솔루션
국내에서 의료데이터는 ‘개인정보보호법’ 뿐 아니라 ‘보건의료기본법’, ‘생명윤리 및 안전에 관한 법률’, ‘의료법’, ‘국민건강보험법’, ‘보건의료기술 진흥법’ 등의 적용을 받고 있습니다. 의료기관에서 생성, 이용되는 환자의 개인정보는 의료행위 과정에 필요한 환자의 인적 정보인 성명, 주민등록번호, 연락처, 환자등록번호, 진료카드번호, 건강보험증번호, 아이디, 비밀번호 등과 의학적 배경정보인 유전자 정보, 환자의 건강상태, 신체적 특징, 병력(가족력), 체력, 유전정보, 신용카드 정보 등이 있습니다. 이러한 환자의 개인정보는 의료건강 외에 여러 정보를 포함하고 있어 가장 민감한 정보로서 높은 수준의 보호조치가 필요한 정보에 속하며 보호되는 정보에는 정보시스템에 저장된 정보뿐 아니라 모든 유형의 개인정보를 포함하고 있어 종이문서 또는 구두로 전달되는 정보까지 보호대상으로 하고 있습니다.
| 구분 | 내용 |
|
개인정보보호법 |
제2조(정의)이법에서 사용하는 용어의 뜻은 다음과 같다 1. ‘개인정보’란 살아 있는 개인에 관한 정보로서 다음 각 목의 어느 하나에 해당하는 정보를 말한다 가. 성명, 주민등록번호 및 영상 등을 통하여 개인을 알아볼 수 있는 정보 나. 해당 정보만으로는 특정 개인을 알아볼 수 없더라도 다른 정보와 쉽게 결합하여 알아볼 수 있는 정보, 이 경우 쉽게 결합할 수 있는지 여부는 다른 정보의 입수 가능성 등 개인을 알아보는데 소요되는 시간, 비용, 기술 등을 합리적으로 고려하여야 한다. 다. 가목 또는 나목을 제1호의 2에 따라 가명처리함으로써 원래의 상태로 복원하기 위한 추가 정보의 사용ㆍ결합 없이는 특정 개인을 알아 볼 수 없는 정보(이하”가명정보”라 한다) |
의료기관에서 처리되는 환자의 개인정보의 종류, 성격, 형식 등에 대하여 의료법에서는 특별한 규정을 두고 있지 않으며, ‘보건의료기본법’에서 보건의료정보에 관련하여 정의하고 있습니다. 제3조1호는 보건의료에 관하여 “국민의 건강을 보호ㆍ증진하기 위하여 국가ㆍ지방자치단체ㆍ보건의료기관 또는 보건의료인등이 행하는 모든 활동”이라고 정의하면서 “보건의료에 관련한 지식 또는 부호, 숫자, 문자, 음성, 음향, 영상 등으로 표현된 모든 종류의 자료”를 보건의료정보라고 규정하고 있습니다. 이를 의료법에 적용하면 의료기관이나 의료인이 행하는 모든 활용에 관한 지식, 부호, 숫자, 문자, 음성, 음향 등으로 표현된 모든 자료를 말하며, 의료법의 적용을 받는 진료기록부, 간호기록부, 조산기록부, 처방전, 진단서 등에 작성ㆍ보관된 정보를 말합니다. 의료법에서의 환자 개인정보에 관한 규정으로 제19조 정보 누설금지, 제21조의2 진료기록의 송부 등, 제23조 전자의무기록, 제23조의3 진료정보 침해사고의 통지, 제23조의4 진료정보 침해사고의 예방 및 대응 등이 있으며 의료법 제19조 1항은 의료인이나 의료기관 종사자가 관련 업무에 종사하면서 알게 된 정보, 제23조제3항은 전자의무기록에 저장된 개인정보, 제23조의3 및 제23조4는 전자의무기록에 저장된 진료정보를 누설, 유출, 변조, 훼손 등 행위를 금지하고 있으며 보호주체에 대한 용어를 각 조항에서 다르게 사용하고 있습니다.
| 구분 | 내용 |
|
보건의료기본법 |
제3조(정의) 이 법에서 사용하는 용어의 뜻은 다음과 같다 1. “보건의료”란 국민의 건강을 보호ㆍ증진하기 위하여 국가ㆍ지방자치단체ㆍ보건의료기관 또는 보건의료인 등이 행하는 모든 활동을 말한다 2.”보건의료서비스”란 국민의 건강을 보호ㆍ증진하기 위하여 보건의료인이 행하는 모든 활동을 말한다. 3. “보건의료인”이란 보건의료 관계법령에서 정하는 바에 따라 자격ㆍ면허 등을 취득하거나 보건의료서비스에 종사하는 것이 허용된 자를 말한다. 4. “보건의료기관”이란 보건의료인이 공중 또는 특정 다수인을 위하여 보건의료서비스를 행하는 보건기관, 의료기관, 약국, 그밖의 대통령영으로 정하는 기관을 말한다. 5. “공공보건의료기관”이란 국가ㆍ지방자치단체 그 밖의 공공단체가 설립, 운영하는 보건의료기관을 말한다. 6.”보건의료정보”란 보건의료와 관련한 지식 또는 부호ㆍ숫자ㆍ문자ㆍ음성ㆍ음향ㆍ영상 등으로 표현된 모든 종류의 자료를 말한다 |
|
의료법 |
제19조(정보누설금지) ①의료인이나 의료기관 종사는 이 법이나 다른 법령에 특별히 규정된 경우 외에는 의료ㆍ조산 또는 간호업무나 제17조에 따른 진단서ㆍ검안서ㆍ증명서 작성ㆍ교부 업무, 제18조에 따른 처방전 작성ㆍ교부업무, 제21조에 따른 진료기록 열람ㆍ사본 교부 업무, 제22조 2항에 따른 진료기록부 등 보존 업무 및 제23조에 따른 전자의무기록 작성ㆍ보관, 관리 업무를 하면서 알게 된 다른 사람의 정보를 누설하거나 발표하지 못한다 ②제58조제2항에 따라 의료기관 인증에 관한 업무에 종사하는 자 또는 종사하였던 자는 그 업무를 하면서 알게 된 정보를 다른 사람에게 누설하거나 부당한 목적으로 사용하여서는 아니 된다. 제21조2(진료기록의 송부 등) ① 의료인 또는 의료기관의 장은 다른 의료인 또는 의료기관의장응로부터 제22조 또는 제23조에 따른 진료기록의 내용 확인이나 진료기록의 사본 및 환자의 진료경과에 대한 소견 등을 송부 또는 전송할 것을 요청 받은 경우 해당 환자나 환자 보호자의 동의를 받아 그 요청에 응하여야 한다. 다만, 해당 환자의의식이 없거나 응급환자인 경우 또는 환자의 보호자가 없어 동의를 받을 수 없는 경우에는 환자나 환자 보호자의 동의 없이 송부 또는 전송할 수 있다. …중략… ⑧누구든지 정당한 사유 없이 진료기록전송지원시스템에 저장된 정보를 누출, 변조 또는 훼손하여서는 아니 된다. ⑨진료기록전송지원시스템의 구축, 운영에 관하여 이 법에서 규정된 것을 제외하고는 ‘개인정보보호법’을 따른다. 제23조(전자의무기록) ③누구든지 정당한 사유 없이 전자의무기록에 저장된 개인 정보를 탐지하거나 누출ㆍ 변조 또는 훼손하여서는 아니된다. |
나. 회사의 현황
(1) 영업개황 및 사업부문의 구분
(가) 영업개황
당사는 본 보고서 제출일 현재까지 주요 매출사업으로 일반진단 및 분자진단검사서비스인 체외진단검사서비스 사업과 건강검진/의료기관용 EMR 연동SW로 대표되는 의료IT솔루션서비스 사업으로 구분할 수 있으며 그 외 검체를 보유한 협력의료기관과의 협업을 통한 제약임상, 마이크로바이옴을 신성장동력사업으로 추진하고 있습니다.
당사는 전국에 분포한 직영점 1곳, 대리점 19곳을 통해 병의원으로부터 혈액, 소변 등의 검체를 수거하여 협력의료기관을 통해 분석 후 그 결과를 당사가 개발한 SW를 통해 의료기관에 전달합니다.
의료IT서비스사업은 건강검진솔루션, 진단검사솔루션, PHR서비스, 클라우드서비스로 구성되어 있으며 각 분야별로 전문화된 SW를 고객사에 공급하고 있습니다.
신규로 추진하고 있는 제약임상의 경우 체외진단의료기기 임상에서 쌓은 노하우와 검체를 보유한 협력의료기관과의 협업에서 발생하는 검체 경쟁력을 활용하여 전개할 예정입니다. 개인 맞춤형 건강관리 솔루션은 장내 미생물 분석 및 유산균 추천에 관한 사업으로, 향후 당사의 주요 매출원이 될 것으로 기대하고 있습니다.
[주요 사업분야]
|
구분 |
대분류 |
소분류 |
사업내용 |
|
체외진단검사서비스 |
일반진단검사 |
임상화학 | - 단백질, 탄수화물, 대사산물, 세포등의 검사를 통해 면역혈청악, 혈액학, 뇨 및 미생물학, 병리학 등의 진단 검사 정보를 제공 - 내과, 비뇨기과, 산부인과 등 병의원으로부터 체외진단 검사를 의뢰받아 검체를 수거하고 운송하며 협력의료기관을 통하여 검사를 수행 |
|
면역혈청 |
|||
| 진단혈액 | |||
| 요경검미생물 | |||
| 분자진단검사 |
분자진단검사 코로나 진단검사 |
- 혈액, 소변, 체액, 조직 등의 환자의 검체에서 추출한 DNA 혹은 RNA를 이용하여 감염질환검사 및 유전질환 검사 정보를 제공 - 내과, 비뇨기과, 산부인과 등 병의원으로부터 체외진단 검사를 의뢰받아 검체를 수거하고 운송하며 협력의료기관을 통하여 검사를 수행 |
|
|
비의료건강검사 |
- 개인 건강 관리를 위한 검사 및 솔루션을 제공 |
||
| 체외진단의료기기 | - 신속하고 정확한 질병진단을 위한 체외진단의료기기 개발 | ||
|
의료IT솔루션 |
의료IT솔루션 |
건강검진 솔루션 |
- 디지털 헬스케어의 한 분야로 병원 내 행정, 의료 등 활동을 지원, 관리하기 위한 시스템과 그외 병의원에서 필요로 하는 IT 서비스를 제공 |
|
진단검사 솔루션 |
|||
| PHR 서비스 | |||
| 신사업 | 신사업 |
임상시험서비스 |
- 의약품 허가를 위한 의약품 임상시험서비스 및 건강기능식품허가를 위한 세포면역 성능시험서비스 제공 |
| 개인 맞춤형 건강관리 솔루션 | - NGS 기반 장내미생물분석을 통한 개인 맞춤형 건강관리솔루션 제공 |
(나) 공시대상 사업부문의 구분
|
대분류 |
소분류 |
제품설명 |
|
일반진단검사 |
임상화학 |
내과, 비뇨기과, 산부인과 등 병의원으로부터 체외진단 검사를 의뢰받아 검체를 수거하고 운송하며 협력의료기관을 통하여 검사를 수행하고 있습니다. |
|
면역혈청 |
항원-항체 반응을 이용하여 알레르기질환, 내분비질환, 자가면역질환 외 바이러스 및 세균 등각종 감염질환을 진단하기 위해 혈청학적 검사 등을 실시하고 있습니다. 항원항체, 자가면역관련질환, 비타민, 내분비호르몬, 알러지, 간염 및 바이러스, 잠복결핵 등의 검사 정보를 제공하며, 25-OH Vitamin D, CK-MB, 알러지, CA19-9, Mycoplasma, 잠복결핵 검사 등 약90종의 검사를 진행하고 있습니다. |
|
|
진단혈액 |
빈혈, 혈액 종양 등 혈액 질환의 필수적인 검사를 수행하고 있으며, 혈액 응고 및 수혈 관련 검사를 수행합니다. 또한 당뇨병 관리 지표인 Hemoglobin A1c 등의 검사를 수행하고 있으며 NGSP Level 1을 유지하여 정확한 검사결과 검증합니다. WBC, RBC, HbA1c, ESR 등 약 30종의 검사를 진행하고 있습니다. |
|
|
요경검미생물 |
(요경검) 소변을 검사하여 대사 산물, 세포 등을 검출하여 신장 및 요로계 질환을 비롯하여 내분비, 산-염기 대사이상 등의 질환을 모니터링하고 감시함에 있어 유용한 정보를 제공합니다. 전자동 요분석기를 통해 잠혈, 빌리루빈, 유로빌리노겐, 케톤, 단백질, 아질산염, 포도당, pH, 비중, 백혈구 등의 검사결과와 이미지 분석 장비를 이용한 요세포의 반정량 요침사 결과를 제공합니다. | |
| (미생물) 감염이 의심되어 의뢰된 다양한 임상 검체(소변, 대변, 체액, 농 등)에서 원인이 되는 병원체를 분리, 동정합니다. 분리된 균주는 CLSI (Clinical and Laboratory Standards Institute) 지침에 따라 적절한 항생제를 선택하여 감수성 검사를 시행하고 있습니다. 항생제 감수성 검사는 MIC와 Disk 방법으로 시행하며 약제의 감수성과 내성 여부를 보고하여 적절한 치료를 지원합니다. | ||
|
분자진단검사 |
분자진단검사 |
내과, 비뇨기과, 산부인과 등 병의원으로부터 체외진단 검사를 의뢰받아 검체를 수거하고 운송하며 협력의료기관을 통하여 검사를 수행하고 있습니다. |
|
비의료건강검사 |
개인 건강 관리를 위한 검사 및 솔루션을 제공하는 것으로서 질병의 진단 및 치료의 영역에 속하지 않으며 현재 본인의 건강 상태를 참고할 수 있는 정보를 제공하는 서비스로, 장내미생물 유전체 분석 서비스를 제공하고 있습니다. 장내미생물 유전체 분석 서비스는 사람의 대변검체에서 핵산을 추출하고 NGS 기술을 이용하여 미생물 군집의 유전체를 분석합니다. |
|
| 체외진단의료기기 | (U2PlexTM Alpha-Thalassemia Diagnostics Kit) 알파 지중해빈혈 진단에 사용되며, 비정상적 혈구 생성으로 인해 용혈성 빈혈, 비장 종대 및 뼈의 이상 등의 증상이 나타나는 상염색체 열성 유전 질환을 진단할 수 있습니다. 또한, 이 키트는 알파 지중해빈혈의 주요 원인이 되는 9개의 돌연변이를 확인할 수 있고, 동형 또는 이형 접합체를 구별하여 유전 상담에 활용이 가능합니다. |
|
| (U2PlexTMQ COVID-19 Fast Real-time PCR Kit) 사람의 비인두 및 구인두 혼합액과 객담을 검체로 Covid-19 바이러스의 유전자를 검출할 수 있습니다. 키트는 적혈구 추출물, 인공 염색체 및 RT-PCR 시약 등이 들어있는 리액션 믹스와 함께 제공되며, 바이러스 유전자를 포함하는 샘플에서 RNA를 추출한 후, 추출물을 키트에 추가하여 증폭 및 검출을 수행할 수 있습니다. 검사 결과는 약 45분 이내에 제공되며, 이 제품은 COVID-19의 신속한 진단에 유용합니다. |
||
|
의료IT솔루션 |
건강검진 솔루션 |
(U2Check) |
|
(U2e-문진) 수검자 입장에서는 병원 방문 전 충분한 시간을 가지고 문진을 작성하기에, 자신의 상태에 대하여 더욱 면밀히 살펴본 내용을 작성할 수 있게 됩니다. 또한 지면상의 한계로 인해 설명하기 어려웠던 내용을 상세하게 표현해 줄 수 있어 환자들이 문진내용에 대해 정확히 이해하고 문진을 작성할 수 있습니다. 또한 병원 방문 당일 대기시간을 줄일 수 있습니다. 검진기관에서는 수검자들의 대기시간이 줄어 접수 후 바로 검진을 시작시켜 대기 공간의 복잡함을 해소하고, 면밀히 작성된 문진을 토대로 환자의 건강상태에 대한 상세한 상담이 가능해 집니다. 또한 문진내용이 검진시스템으로 연동되기에 수작업으로 옮겨 적는 과정이 없어져 훨씬 빠르고 정확히 문진 업무를 처리할 수 있습니다. |
||
| (U2CA) U2CA는 퇴실 체크리스트에 따라 퇴실이 가능한 수검자를 선별하여 간편하고 빠른 퇴실을 도와주는 퇴실관리 솔루션입니다. 본 프로그램을 통해 보다 정확한 결과지 수령 정보를 작성할 수 있습니다. 수납과 퇴실 프로세스에 있어 무결제, 유결제 퇴실자를 분리해 퇴실 프로세스를 최적화하였으며, 수납 대기 공간의 과밀화를 방지합니다. 퇴실 업무 처리 방식도 탁월하게 개선하여 퇴실 시 휴먼에러를 방지하고, 신속한 퇴실 처리로 대기자 수를 감소시킵니다. U2CA는 병원이 설정한 조건에 따라 수납 여부 및 미완료 검사 등을 파악하여 퇴실이 가능한 수검자를 자동으로 선정해줍니다. VIP, 퇴실 가능자, 퇴실 불가자, 퇴실 완료자에 따라 색상을 구분하여 퇴실 현황 파악이 가능합니다. 퇴실 시 필요한 주차등록 연계 및 각종 편의 기능을 제공하여 고객 경험을 한층 끌어올렸습니다. |
||
| (U2Sign) U2Sign은 진료기록 인증 전자서명 솔루션입니다. 의료법에 따라 전자의무기록의 전자서명 수요가 증가하게 되어 해당 솔루션을 개발했습니다. 전자 서명 모듈과 타임스템프 서비스를 이용한 위 변조 검증 시스템을 통해 의료문서의 진위성을 보장합니다. |
||
|
진단검사 솔루션 |
(Lab2Gene) 임상병리검사 서비스를 기반으로 한 자동입력시스템으로 검사 의뢰부터 완료된 검사 결과를 EMR과 연동하는 전 과정이 자동화된 IT서비스입니다. 다양한 EMR과 연동되어 EMR의 검사 오더만으로 손쉽게 검사의뢰가 가능합니다. 환자별, 항목별, 기간별 검색 등 다양한 검색 기능을 제공합니다. Lab2Gene의 Smart Report System은 인터넷이 연결된 PC나 장치를 통해 어느 곳에서나 검사 결과 열람이 가능하게 합니다. 검사 결과에 대한 EMR 자동입력 기능이 존재하며, 검사 결과의 출력이 쉽고 자료에 대한 여러 파일 형태로 변환할 수 있으며, 검사 진행 상황을 모니터링 할 수 있습니다. |
|
| (U2Gateway) 의료기관에서 사용하는 진단장비와 EMR과의 연동을 통해 검사결과 입력의 오류를 최소화하고, 환자정보를 포함한 정보의 중복입력을 방지하는 의료기관 솔루션입니다. U2Gateway는 장비와 호스트 컴퓨터 간의 통신 인터페이스를 구현하는 프로그램으로써 Serial Communication 및 Ethernet 등의 표준 통신 프로토콜을 사용하여 장비와 호스트 컴퓨터 간의 데이터 통신을 제공합니다. 이를 통해 진단검사장비를 제어하고 데이터를 수집 및 분석하여 검사결과 관리에 편의성을 제공하고 있으며 EMR과의 양방향 연동을 통해 신속하고 정확하게 검사결과를 보고 할 수 있도록 하여 검사기관의 업무 편의성과 효율성을 보장하고 있습니다. |
||
| (U2LIS) U2LIS는 검사실에서 사용되는 임상정보 시스템으로, 당사가 자체적으로 개발한 LIS(Laboratory Information System)시스템입니다. U2LIS는 검사실의 업무 프로세스를 효율화하고 품질관리를 강화하여 환자진료와 의료서비스의 품질을 향상시키는데 기여하는 시스템이며, 선진적인 IT 기술과 임상병리실 운영 전문가의 지식과 노하우가 결합된 결과물로써, 현대 의료환경에서 필요로 하는 다양한 요구사항을 충족하기 위해 개발된 LIS 솔루션입니다. U2LIS는 사용자 친화적인 인터페이스와 다양한 기능을 제공하며, 연속적인 기술 개발과 업데이트가 가능하여 최신 트렌드와 요구사항에 부합합니다. |
||
| (U2SmartQC) U2SmartQC는 검사기관의 내부정도관리를 자동화하여 검사업무의 효율성을 높여주는 솔루션입니다. 우선, 내부정도관리란 검사기관이 수행하는 검사 과정의 정확성, 신뢰성, 일관성 등을 유지하고 향상시키기 위한 일련의 절차와 활동을 말합니다. 이는 검사기관이 정확하고 신뢰성 있는 검사결과를 제공할 수 있도록 하기 위한 중요한 요소입니다. U2SmartQC는 이러한 활동을 자동화하고 편의성을 제공하기 위해 다양한 기능을 제공하고 있으며 당사 자체 솔루션과의 완벽한 호환성을 이루고 있습니다. 자체개발 솔루션인 U2Gateway와의 Interface를 통한 QC결과 입력 자동화, 검사결과 신뢰성을 측정하는 정도관리 지표, 학부 별 특성에 맞는 출력물 관리 등 정도관리에 필요한 다양한 기능을 제공함으로써 검사업무의 효율성과 신뢰성을 높이는데 주력하고 있습니다. |
||
| PHR 서비스 |
(U2Mobile) Prime/Pro 버전은 특정 병원만을 위한 병원 전용 모바일 앱 서비스로 해당 병원만이 이용할 수 있도록 설계되어 있습니다. Standard 버전과는 다르게, 병원 로고와 이미지를 포함한 메인화면을 비롯하여, 병원에 대한 정보를 확인할 수 있으며, 예약, 자가측정 결과 관리 등 추가적인 서비스가 함께 포함되어 있습니다. SMART 버전은 규모가 큰 병원을 대상으로 하는 병원 전용 앱으로, 병원의 OCS와 직접 연계하여 병원의 의료행정 전반적인 서비스를 모두 이용할 수 있는 버전입니다. 진료예약, 접수, 수납은 물론, 환경에 따라서 위치기반 서비스, 대기번호표 발급, 실손보험 청구 및 제증명 발급 등의 기능도 추가될 수 있습니다. |
|
|
신사업 |
임상시험서비스 |
당사는 검사 전문 수탁 서비스 기업으로 협업의료기관과 협력하여 임상검사 질 관리와 검체 검사 프로세스의 축적된 기술을 기반으로 연구의 다양성, 특이성을 고려한 연구 과제별 시스템을 구축하여 보건의료 전반에 걸쳐 있는 연구과제를 수행하고 있습니다. 현재는 체외진단의료기기에 대한 연구임상, 허가임상, 수탁임상등의 영역에서 당사가 검체관리, 전체적인 시스템 셋업, 검체보관, 일반관리등의 업무를 수행하고 협업의료기관에서 검사업무를 수행합니다. 이러한 협업 하에 제약임상서비스로 영역을 확대하고자 하며 당사의 주요 주주인 일동제약과 관련된 사업을 2023년 내에 구체화할 계획입니다. |
| 개인 맞춤형 건강관리 솔루션 | (U2Biome) U2Biome은 차세대 염기 서열 분석 기술을 활용한 장내미생물 분석 서비스와 이를 연계한 맞춤형 프로바이오틱스 제품을 추천하고 제공하는 통합 패키지 서비스입니다. 개인 맞춤형 건강관리 솔루션으로서 장내 미생물의 다양성과 유익균 및 유해균의 균형도, 장내 유산균 분포, 6가지 건강 지표에 기반한 전반적인 장내 환경 분석 결과를 확인할 수 있습니다. 장 건강관리를 위한 올바른 식습관, 생활습관 등의 솔루션도 함께 운영하여 고객에게 차별화된 헬스케어 서비스를 제공합니다. |
(2) 시장점유율
(가) 체외진단 서비스
세계 체외진단(IVD)시장을 비롯해 국내 체외진단(IVD)시장의 규모는 지속적으로 확대되고 있으며, 국내 시장은 공식적인 통계자료가 존재하지 않으나, 프로스트 앤 설리번 한국 지사가 발표한 '세계 체외진단(IVD : In Vitro Diagnostics) 시장 분석 보고서(Analysis of the Global In Vitro Diagnostics Market finds the market)'에 따르면, 2014년 해당 시장 수익은 505억 6천만 달러로 2017년에는 626억 3천만 달러에 달할 것으로 예측하고 있습니다. IMF에서 발표한 2014년 G20의 GDP 총액 중 국내 GDP 비율 2.42%를 통해 전세계 대비 비율을 약 2%로 판단시, 전세계에서 차지하는 국내 GDP 비율에 따라 국내 시장 규모를 추정해 보면, 2014년 국내 체외진단 시장은 약 1조 1,123억원(환율 1,100원 가정)으로 예상됩니다. 따라서 2014년을 기준으로 2023년 당사의 시장점유율은 약 2.77%로 추정됩니다. 그 외 분자진단 서비스 및 제품 시장은 시장이 형성되는 시기로 신뢰성 있는 자료가 존재하지 않는 상황입니다.
(단위 : 억원, %)
|
국내 시장 규모 |
당사 매출액 |
점유율 |
|
11,123 |
308 |
2.77 |
(나) 의료IT솔루션
국내 시장규모는 통계자료로 존재하지 않으나, 보건복지부의 국가시행 검진의 통계자료와 당사의 고객현황을 통해 추정할 수 있습니다. 국내 건강검진 소프트웨어 산업은 아름누리, 다인소프트 등 건강검진 소프트웨어를 전문적으로 개발하여 판매하는 중소기업과 중외정보기술, 메트로소프트, 엔지테크 등 진료와 청구를 위한 전자의무기록을 개발하는 회사가 건강검진 소프트웨어를 함께 판매하는 중소기업으로 구분할 수 있습니다.
(3) 시장의 특성
(가) 체외진단 시장
체외진단 시장은 생명공학정책연구센터가 발행하는 '바이오인더스트리' 2015년 3월호에 실린 '글로벌 체외진단 시장현황 및 전망' 자료에 따르면 2013년 시장규모 472억 달러 규모로 파악되며, 연평균 7.3%의 성장세로 2017년 620억 달러 규모로 성장할 것으로 전망되고 있습니다. 이처럼 경제상황이나 산업불황속에서도 제약시장보다 빠른 속도로 성장하고 있습니다. 전세계적인 인구고령화 및 IVD 진단 치료법을 이용하는 인구가 증가할 것으로 예상됩니다.또한 저렴해지는 IVD검사 가격으로 인해 보다 많은 사람들이 in vitro 진단을 받을 가능성이 있으며, 질환 치료에서 질환 예방(disease prevention) 및 건강보건 증진(health promotion) 차원의 트렌드로 변화하고 있습니다.
(나) 의료IT솔루션
컴퓨터와 네트워크 기술을 바탕으로 하는 IT기술은 비약적인 발전과 함께 스마트폰 보급 트렌드에 따라 기업간의 정보화뿐 아니라, 개인의 정보화 욕구증진으로 인한 IT기술이 접목되고 있습니다. 의료복지, 특히 예방형 건강검진의 분야도 예외는 아니어서 IT기술을 접목하여 건강검진을 받는 수검자에게 맞춤형 정보제공 등의 욕구가 증가되고 있습니다. 고령화와 개인 건강에 대한 관심은 증가하면서 의료서비스 시장은 점차 커지고 있으며, 의료기술과 IT기술 발달이 u-Health 시장의 기폭제가 되고 있습니다. 국내 대규모 의료기관이 환자정보와 진료기록 등을 전산화하고 있는 케이스가 크게 증가하고 있는 등 시장의 매력도 또한 높으며, 유비쿼터스 사회 구현이 현실적인 서비스로 각광받고 있습니다.
(4) 신규사업 등의 내용 및 전망
|
구분 |
사업내용 |
기대효과 |
| 제약임상서비스 (CRO) |
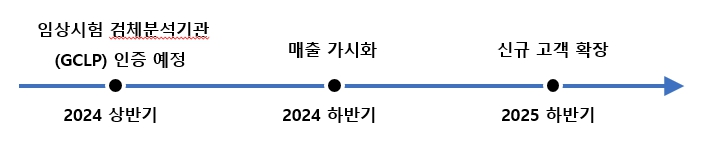
당사는 검사 전문 수탁 서비스 기업으로 협업의료기관과 협력하여 임상검사 질 관리와 검체 검사 프로세스의 축적된 기술을 기반으로 연구의 다양성, 특이성을 고려한 연구 과제별 시스템을 구축하여 보건의료 전반에 걸쳐 있는 연구과제를 수행하고 있습니다. 현재는 체외진단의료기기에 대한 연구임상, 허가임상, 수탁임상등의 영역에서 당사가 검체관리, 전체적인 시스템 셋업, 검체보관, 일반관리등의 업무를 수행하고 협업의료기관에서 검사업무를 수행합니다. 이러한 협업 하에 제약임상서비스로 영역을 확대하고자 하며 당사의 주요 주주인 일동제약과 관련된 사업을 2024년 내에 구체화할 계획입니다. |
IT솔루션(e-CRF와 LIS연동 및 모바일어플리케이션 서비스제공) 및 배송모니터링 전담조직 제공 등으로 제약임상 서비스 차별화를 꾀할 예정입니다. 다수의 학회와 세미나 참여를 통한 가망고객 pool을 확장하고, 다양한 제약사와 MOU 및 글로벌 제약임상도 수행하여 매출성장이 기대됩니다. |
|
U2Biome |
U2Biome은 차세대 염기 서열 분석 기술을 활용한 장내미생물 분석 서비스와 이를 연계한 맞춤형 프로바이오틱스 제품을 추천하고 제공하는 통합 패키지 서비스입니다. 개인 맞춤형 건강관리 솔루션으로서 장내 미생물의 다양성과 유익균 및 유해균의 균형도, 장내 유산균 분포, 6가지 건강 지표에 기반한 전반적인 장내 환경 분석 결과를 확인할 수 있습니다. 장 건강관리를 위한 올바른 식습관, 생활습관 등의 솔루션도 함께 운영하여 고객에게 차별화된 헬스케어 서비스를 제공합니다. |
당사는 U2Biome의 브랜드 홍보를 위해 구체적이고 지속적인 홍보를 진행하고 있으며 소비자 인지도 상승에 따른 매출성장이 기대됩니다. 또한 2023년 2분기 이후부터 U2Biome bebe 런칭을 통해 아기들의 장건강에 높은 관심과 소비력을 가지고 있는 소비자 층을 집중적으로 공략해 왔습니다. |
 |
|
임상서비스 사업계획 |
| 출처: 당사 제공 |
 |
|
U2Biome 경쟁력 |
 |
|
U2Biome 브랜드 영상 광고 |
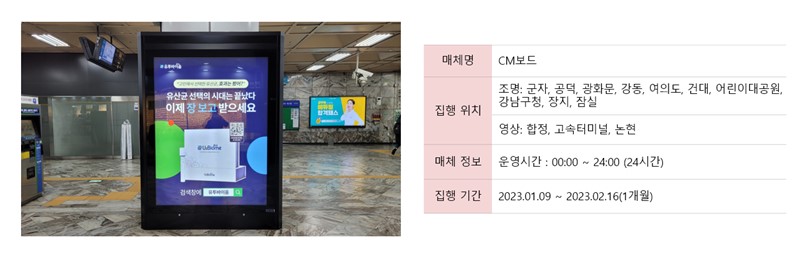 |
|
지하철 CM보드 광고 집행 |
 |
|
버스 외부광고 집행 |
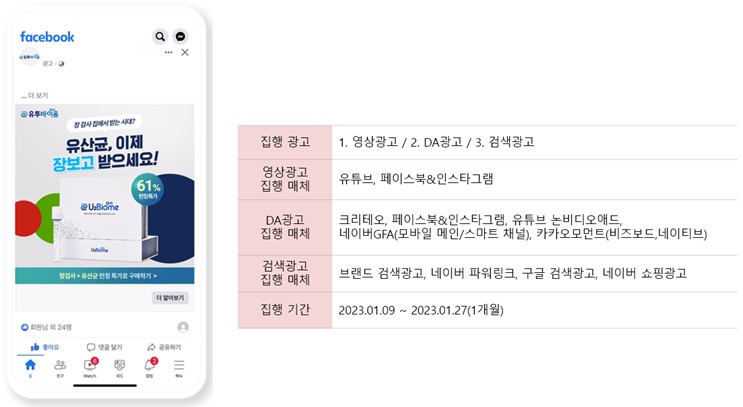 |
|
디지털광고 집행 |
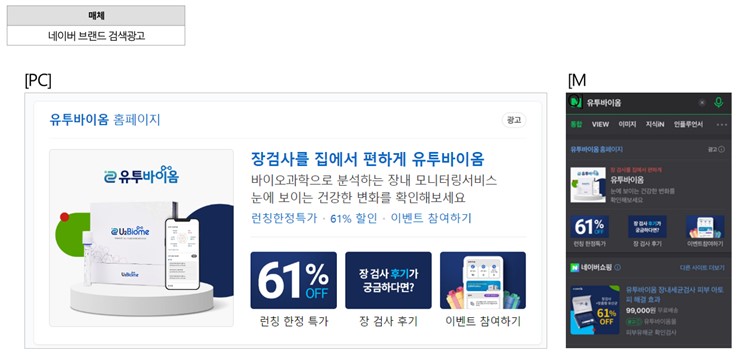 |
|
네이버 브랜드 광고 |
 |
|
U2Biome Bebe 제품 라인업 |
| 출처: 당사 제공 |
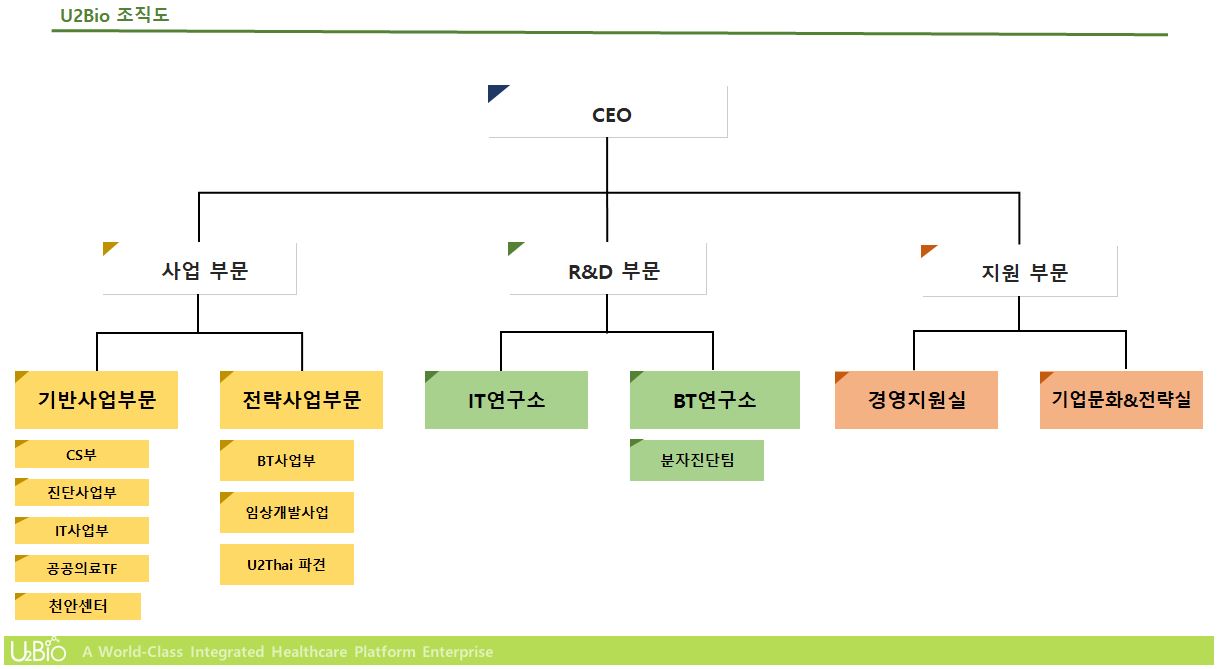
(5) 조직도
 |
|
조직도 |
2. 주주총회 목적사항별 기재사항
□ 재무제표의 승인
가. 해당 사업연도의 영업상황의 개요
⇒ Ⅲ. 경영참고사항 中 '1. 사업의 개요' 참조
나. 해당 사업연도의 대차대조표(재무상태표)ㆍ손익계산서(포괄손익계산서)ㆍ이익잉여금처분계산서(안) 또는 결손금처리계산서(안)
- 재무상태표
<재 무 상 태 표>
| 제 15 기 당기 : 2023년 1월 1일 부터 2023년 12월 31일까지 |
| 제 14 기 전기 : 2022년 1월 1일 부터 2022년 12월 31일까지 |
| (단위 : 원) |
| 과 목 | 제 15(당) 기 | 제 14(전) 기 |
|---|---|---|
| 자 산 | ||
| Ⅰ. 유동자산 | 45,172,071,715 | 47,873,266,416 |
| 현금및현금성자산 | 35,290,495,063 | 1,432,761,631 |
| 단기금융상품 | 1,501,389,879 | 35,488,682,191 |
| 매출채권 | 7,300,485,082 | 9,935,343,159 |
| 기타금융자산 | 90,757,655 | 247,228,481 |
| 기타자산 | 206,141,853 | 73,669,245 |
| 재고자산 | 782,802,183 | 695,581,709 |
| Ⅱ. 비유동자산 | 4,027,319,404 | 3,155,101,285 |
| 유형자산 | 1,548,977,032 | 1,870,682,392 |
| 무형자산 | 729,932,195 | 172,870,000 |
| 기타금융자산 | 466,945,015 | 496,411,958 |
| 이연법인세자산 | 1,281,465,162 | 615,136,935 |
| 자 산 총 계 | 49,199,391,119 | 51,028,367,701 |
| 부 채 | ||
| Ⅰ. 유동부채 | 8,003,148,264 | 14,634,472,896 |
| 매입채무 | 3,710,706,148 | 4,656,022,827 |
| 기타금융부채 | 3,797,639,377 | 6,681,897,229 |
| 기타부채 | 176,045,240 | 174,279,265 |
| 당기법인세부채 | - | 2,662,002,322 |
| 리스부채 | 260,307,299 | 416,950,953 |
| 충당부채 | 58,450,200 | 43,320,300 |
| Ⅱ. 비유동부채 | 3,204,832,646 | 2,549,731,744 |
| 기타금융부채 | 30,046,132 | 26,276,648 |
| 충당부채 | - | 26,604,300 |
| 순확정급여부채 | 2,982,828,215 | 2,392,214,281 |
| 리스부채 | 191,958,299 | 104,636,515 |
| 부 채 총 계 | 11,207,980,910 | 17,184,204,640 |
| 자 본 | ||
| Ⅰ. 자본금 | 5,643,598,000 | 1,262,755,000 |
| Ⅱ. 자본잉여금 | 13,934,571,030 | 13,426,383,670 |
| Ⅲ. 기타포괄손익누계액 | (8,655,062) | (8,655,062) |
| Ⅳ. 이익잉여금 | 18,421,896,241 | 19,163,679,453 |
| 자 본 총 계 | 37,991,410,209 | 33,844,163,061 |
| 부 채 및 자 본 총 계 | 49,199,391,119 | 51,028,367,701 |
- 포괄손익계산서
<포 괄 손 익 계 산 서>
| 제 15 기 당기 : 2023년 1월 1일 부터 2023년 12월 31일까지 |
| 제 14 기 전기 : 2022년 1월 1일 부터 2022년 12월 31일까지 |
| (단위 : 원) |
| 과 목 | 제 15(당) 기 | 제 14(전) 기 |
|---|---|---|
| 매출액 | 30,792,036,515 | 69,013,134,090 |
| 매출원가 | 22,573,470,725 | 42,374,374,436 |
| 매출총이익 | 8,218,565,790 | 26,638,759,654 |
| 판매비와관리비 | 9,556,558,016 | 10,930,963,398 |
| 영업이익 | (1,337,992,226) | 15,707,796,256 |
| 금융수익 | 1,365,000,253 | 590,301,593 |
| 금융비용 | 40,355,630 | 93,374,619 |
| 기타수익 | 153,788,378 | 29,021,482 |
| 기타비용 | 102,288,904 | 167,991,613 |
| 법인세비용차감전순이익(손실) | 38,151,871 | 16,065,753,099 |
| 법인세비용(수익) | (607,743,406) | 2,905,758,253 |
| 당기순이익(손실) | 645,895,277 | 13,159,994,846 |
| 기타포괄손익 : | (124,923,489) | (81,826,806) |
| 후속적으로 당기손익으로 재분류되는 항목 | ||
| 지분법자본변동 | - | - |
| 후속적으로 당기손익으로 재분류되지 않는 항목 | ||
| 순확정급여부채의 재측정요소 | (124,923,489) | (81,826,806) |
| 총포괄이익(손실) | 520,971,788 | 13,078,168,040 |
| 주당순이익 | ||
| 기본주당순이익 | 63 | 1,303 |
- 이익잉여금처분계산서(안)
<이익잉여금처분계산서>
| 제 15 기 당기 : 2023년 1월 1일 부터 2023년 12월 31일 까지 |
| 제 14 기 전기 : 2022년 1월 1일 부터 2022년 12월 31일 까지 |
| (단위 : 원) |
| 과 목 | 제 15(당) 기 | 제 14(전) 기 | ||
|---|---|---|---|---|
| Ⅰ.미처분이익잉여금(미처리결손금) | 18,219,855,441 | 19,087,914,153 | ||
| 1. 전기이월결손금 | 17,698,883,653 | 6,009,746,113 | ||
| 2. 순확정급여부채의 재측정요소 | (124,923,489) | (81,826,806) | ||
| 3. 당기순이익 | 645,895,277 | 13,159,994,846 | ||
| Ⅱ. 이익잉여금처분액(결손금처리액) | - | (372,477,468) | - | (1,389,030,500) |
| 1.자본잉여금 | - | - | ||
| 2.이익준비금 | 33,861,588 | 126,275,500 | ||
| 3.현금배당 | 338,615,880 | 1,262,755,000 | ||
| Ⅲ. 차기이월미처리결손금 | 17,847,377,973 | 17,698,883,653 | ||
※ 당기의 이익잉여금처분계산서는 2024년 3월 28일 당사 제15기 정기주주총회에서 최종 확정 및 승인될 예정 입니다.
- 자본변동표
<자본변동표>
| 제 15 기 당기 : 2023년 1월 1일 부터 2023년 12월 31일 까지 |
| 제 14 기 전기 : 2022년 1월 1일 부터 2022년 12월 31일 까지 |
| (단위 : 원) |
| 과 목 | 자 본 금 | 자본잉여금 | 기타포괄손익 누계액 |
이익잉여금 | 총 계 |
|---|---|---|---|---|---|
| 2022.01.01(전기초) | 1,262,755,000 | 13,426,383,670 | (8,655,062) | 6,843,164,413 | 21,523,648,021 |
| 총포괄손익 | |||||
| 당기순이익 | - | - | - | 13,159,994,846 | 13,159,994,846 |
| 확정급여채무의 재측정 | - | - | - | (81,826,806) | (81,826,806) |
| 소유주와의 거래 | |||||
| 배당금의 지급 | - | - | - | (757,653,000) | (757,653,000) |
| 2022.12.31(전기말) | 1,262,755,000 | 13,426,383,670 | (8,655,062) | 19,163,679,453 | 33,844,163,061 |
| 2023.01.01(당기초) | 1,262,755,000 | 13,426,383,670 | (8,655,062) | 19,163,679,453 | 33,844,163,061 |
| 총포괄손익 | |||||
| 당기순이익 | - | - | - | 645,895,277 | 645,895,277 |
| 확정급여채무의 재측정 | - | - | - | (124,923,489) | (124,923,489) |
| 소유주와의 거래 | |||||
| 유상증자 | 592,578,000 | 4,315,950,030 | - | - | 4,908,528,030 |
| 무상증자 | 3,788,265,000 | (3,807,762,670) | - | - | (19,497,670) |
| 배당금의 지급 | - | - | - | (1,262,755,000) | (1,262,755,000) |
| 2023.12.31(당기말) | 5,643,598,000 | 13,934,571,030 | (8,655,062) | 18,421,896,241 | 37,991,410,209 |
- 현금흐름표
<현금흐름표>
| 제 15 기 당기 : 2023년 1월 1일 부터 2023년 12월 31일 까지 |
| 제 14 기 전기 : 2022년 1월 1일 부터 2022년 12월 31일 까지 |
| (단위 : 원) |
| 과 목 | 제15(당)기 | 제14(전)기 |
|---|---|---|
| Ⅰ. 영업활동으로 인한 현금흐름 | (2,554,600,355) | 24,405,910,002 |
| 영업으로부터 창출된 현금흐름(주34) | (1,107,723,635) | 24,351,092,154 |
| 이자의 수취 | 1,479,069,919 | 283,452,585 |
| 이자의 지급 | (36,318,787) | (38,440,453) |
| 법인세의 납부 | (2,889,627,852) | (190,194,284) |
| Ⅱ. 투자활동으로 인한 현금흐름 | 33,204,855,440 | (36,686,482,325) |
| 1. 투자활동으로 인한 현금유입액 | 41,162,034,682 | 7,363,562,194 |
| 보증금의 회수 | 50,000,000 | 373,280,000 |
| 단기투자자산의 처분 | 40,966,580,137 | 6,990,282,194 |
| 무형자산의 처분 | 145,454,545 | - |
| 2. 투자활동으로 인한 현금유출액 | (7,957,179,242) | (44,050,044,519) |
| 단기투자자산의 증가 | (6,979,287,825) | (42,467,945,209) |
| 유형자산의 취득 | (214,432,780) | (967,099,310) |
| 무형자산의 취득 | (763,458,637) | (175,000,000) |
| 보증금의 증가 | - | (440,000,000) |
| Ⅲ. 재무활동으로 인한 현금흐름 | 3,207,478,347 | (2,771,337,300) |
| 1. 재무활동으로 인한 현금유입액 | 5,214,686,400 | - |
| 유상증자 | 5,214,686,400 | - |
| 2. 재무활동으로 인한 현금유출액 | (2,007,208,053) | (2,771,337,300) |
| 단기차입금의 상환 | - | (700,000,000) |
| 유동성장기부채의 상환 | - | (900,000,000) |
| 리스부채의 상환 | (418,797,013) | (413,684,300) |
| 배당금의 지급 | (1,262,755,000) | (757,653,000) |
| 신주발행비용 | (325,656,040) | - |
| Ⅳ. 현금및현금성자산의 순증가 (Ⅰ+Ⅱ+Ⅲ) | 33,857,733,432 | (15,051,909,623) |
| Ⅴ. 기초 현금및현금성자산 | 1,432,761,631 | 16,484,671,254 |
| Ⅵ. 기말 현금및현금성자산 | 35,290,495,063 | 1,432,761,631 |
- 재무제표에 대한 공시
- 외부감사인의 감사 의견과 주석을 포함한 최종 재무제표는 추후 전자공시시스템(http://dart.fss.or.kr) 및 당사 홈페이지(http://www.u2bio.com)에 공시 예정인 당사의 감사보고서를 참조하시기 바랍니다.
- 최근 2사업연도의 배당에 관한 사항
- 해당사항 없음
□ 정관의 변경
가. 집중투표 배제를 위한 정관의 변경 또는 그 배제된 정관의 변경
| 변경전 내용 | 변경후 내용 | 변경의 목적 |
|---|---|---|
| - | - | 해당사항 없음 |
나. 그 외의 정관변경에 관한 건
| 변경전 내용 | 변경후 내용 | 변경의 목적 |
|---|---|---|
|
제2조 (목적) 당회사는 다음 사업을 경영함을 목적으로 한다.
1.~22. <
생략>
23. <
신설>
|
제2조 (목적) 당회사는 다음 사업을 경영함을 목적으로 한다.
1.~22. <
좌동>
23.
부동산 임대업
|
목적사업 추가
|
|
<
신설>
|
제8조의4(주식 및 신주인수권증서에 표시되어야 할 권리의 전자등록)
이 회사는 주권 및 신주인수권증서를 발행하는 대신 전자등록기관의 전자등록계좌부에 주식 및 신주인수권증서에 표시되어야 할 권리를 전자등록한다.
|
발행 주식 및 신주인수권증서에 표시되어야 할 권리에 대한 전자등록 의무화에 따른 관련 근거 신설
|
|
제24조 (이사와 감사의 원수)
당 회사의 이사는 7인이하, 감사는 2인이하로 한다.
|
제24조 (이사와 감사의 원수) 당 회사의 이사는 8인이하, 감사는 2인이하로 한다.
|
이사 정원 수 변경
|
|
부칙
1.~7. <
생략>
8.
이 정관은 2022년 3월 29일부터 시행한다.
|
부칙
1.~7. <
생략>
8.
이 정관은 2022년 3월 29일부터 시행한다.
9.
이 정관은 2024년 3월 28일부터 시행한다.
|
정관 일부 변경에 따른
부칙 변경
|
※ 기타 참고사항
- 해당사항 없음
□ 이사의 선임
가. 후보자의 성명ㆍ생년월일ㆍ추천인ㆍ최대주주와의 관계ㆍ사외이사후보자 등 여부
| 후보자성명 | 생년월일 | 사외이사 후보자여부 |
감사위원회 위원인 이사 분리선출 여부 |
최대주주와의 관계 | 추천인 |
|---|---|---|---|---|---|
| 김진태 | 1964.09.24 | 사내이사 | 해당사항 없음 | 해당사항 없음 | 이사회 |
| 김지원 | 1971.12.29 | 사내이사 | 해당사항 없음 | 해당사항 없음 | 이사회 |
| 박영수 | 1954.12.07 | 기타비상무이사 | 해당사항 없음 | 최대주주의 임원 | 이사회 |
| 총 ( 3 ) 명 | |||||
나. 후보자의 주된직업ㆍ세부경력ㆍ해당법인과의 최근3년간 거래내역
| 후보자성명 | 주된직업 | 세부경력 | 해당법인과의 최근3년간 거래내역 |
|
|---|---|---|---|---|
| 기간 | 내용 | |||
| 김진태 | 現 유투바이오 대표이사 | 1989.03 ~ 2008.02 | 서울대 공과대학 전기컴퓨터공학과 박사 | 해당사항 없음 |
| 1989.03 ~ 1991.02 | 서울대 공과대학 제어계측공학과 박사 수료 | |||
| 1987.03 ~ 1989.02 | 서울대 공과대학 제어계측공학과 석사 | |||
| 1983.03 ~ 1987.02 | 서울대 공과대학 제어계측공학과 학사 | |||
| 1994.12 ~ 2009.10 | 前 (주)유비케어 대표이사 | |||
| 1999.06 ~ 2006.02 | 前 코스닥상장법인협의회 이사 | |||
| 2002.01 ~ 2005.12 | 前 대한의료정보학회 부회장 | |||
| 2009.11 ~ 현재 | 現 (주)유투바이오 대표이사 | |||
| 김지원 | 現 유투바이오 기업문화전략실 상무 |
1990.03 ~ 1995.02 | 아주대학교 수학과 학사 | 해당사항 없음 |
| 2017.03 ~ 2018.08 | 가톨릭대학교 의료경영정보학과 석사 | |||
| 2005.01 ~ 2010.05 | 前 (주)유비케어 EMR S/W 실장 | |||
| 2000.10 ~ 2004.12 | 前 (주)유비케어 EMR S/W 팀장 | |||
| 2010.06 ~ 현재 | 現 (주)유투바이오 기업문화전략실 상무 | |||
| 박영수 | 現 (주)엔디에스 감사 | 1979 | 고려대학교 경영학과 졸업 | 해당사항 없음 |
| 1989 | 고려대학교 경영 대학원 석사 | |||
| 1999 ~ 2002 | 前 하와이 은행 동북아지역본부장 | |||
| 2002 ~ 2010 | 前 포티스 은행 서울 대표 | |||
| 2017 ~ 현재 | 現 (주)엔디에스 감사 | |||
다. 후보자의 체납사실 여부ㆍ부실기업 경영진 여부ㆍ법령상 결격 사유 유무
| 후보자성명 | 체납사실 여부 | 부실기업 경영진 여부 | 법령상 결격 사유 유무 |
|---|---|---|---|
| 김진태 | 없음 | 없음 | 없음 |
| 김지원 | 없음 | 없음 | 없음 |
| 박영수 | 없음 | 없음 | 없음 |
라. 후보자의 직무수행계획(사외이사 선임의 경우에 한함)
| 해당사항 없음 |
마. 후보자에 대한 이사회의 추천 사유
| [김진태 사내이사 후보자] (주)유비케어와 (주)유투바이오의 창업자로 헬스케어 사업분야에 대한 오랜 경험과 노하우, 폭넓은 네트워크를 보유하고 있습니다. 지난 임기 중에는 코로나 유행에 따른 기회를 포착하고 적극적인 경영으로 회사의 성장에 매우 크게 기여 하였으며, 코스닥시장에 상장 시킴으로서 명실상부한 BT&IT 컨버전스 기업으로 자리매김 하도록 하였습니다. 김진태 후보자는 앞으로도 다년간 축적된 경영 역량과 통찰력을 기반으로 지속가능한 성장을 추구할 수 있을 것으로 판단되어 추천하였습니다. [김지원 사내이사 후보자] 지난 임기 중에 IT연구소장과 기업문화&전략실장을 역임하여 회사의 안정적인 성장에 기여하고 미래 비전을 향한 도전을 이끌었으며, 현재 (주)유투바이오의 인사 및 전략담당 임원으로서 풍부한 경험과 전문성, 그리고 관련 산업분야에 대한 통찰력을 바탕으로 경영 상의 의사결정이 효과적으로이루어질 수 있도록 기여할 것으로 판단되어 추천하였습니다. [박영수 기타비상무이사 후보자] 박영수 기타비상무이사 후보자는 하와이 은행 및 포티스 은행에서 다년간 근무하였으며,현재는 (주)엔디에스에서 상근감사직을 맡고 있습니다. 해당 분야의 풍부한 경험과 전문지식을 토대로 다양한 조언과 회사의 안정적인 재무구조 유지에 기여할 것으로 판단되어 추천하였습니다. |
확인서
 |
|
후보자 확인서(사내이사)_김진태 |
 |
|
후보자 확인서(사내이사)_김지원 |
 |
|
후보자 확인서(기타비상무이사)_박영수 |
※ 기타 참고사항
- 해당사항 없음
□ 감사의 선임
<감사후보자가 예정되어 있는 경우>
가. 후보자의 성명ㆍ생년월일ㆍ추천인ㆍ최대주주와의 관계
| 후보자성명 | 생년월일 | 최대주주와의 관계 | 추천인 |
|---|---|---|---|
| 김현석 | 1973.06.22 | 해당사항 없음 | 이사회 |
| 총 ( 1 ) 명 | |||
나. 후보자의 주된직업ㆍ세부경력ㆍ해당법인과의 최근3년간 거래내역
| 후보자성명 | 주된직업 | 세부경력 | 해당법인과의 최근3년간 거래내역 |
|
|---|---|---|---|---|
| 기간 | 내용 | |||
| 김현석 | 現 (주)바이오비스타 사장 | 1996.03 ~ 2000.08 | 연세대학교 경영학과 학사 | 해당사항 없음 |
| 2000.07 ~ 2001.08 | 前 베어링포인트㈜ Consultant | |||
| 2001.09 ~ 2016.02 | 前 ㈜행남자기 전무이사 | |||
| 2006.02 ~ 현재 | 現 ㈜바이오비스타 사장 | |||
다. 후보자의 체납사실 여부ㆍ부실기업 경영진 여부ㆍ법령상 결격 사유 유무
| 후보자성명 | 체납사실 여부 | 부실기업 경영진 여부 | 법령상 결격 사유 유무 |
|---|---|---|---|
| 김현석 | 없음 | 없음 | 없음 |
라. 후보자에 대한 이사회의 추천 사유
| 베어링포인트(주)의 Consultant를 역임하고 (주)행남자기 전무이사 역임 경력 등을 토대로 다양한 업무 지식과 전문성을 보유하고 있으며, 지난 임기 중 회사의 회계와 내부통제 및 내부회계관리제도 운영 점검 등 감사가 수행하여야 할 역할에 대해 객관적으로 수행하였습니다. 앞으로도 윤리의식과 공정성을 바탕으로 회사와 경영진으로부터 독립된 자격으로 감사의 역할을 수행하기에 충분한 역량을 갖추고 있다고 판단됩니다. |
확인서
 |
|
후보자 확인서(감사)_김현석 |
<감사후보자가 예정되지 아니한 경우>
| 선임 예정 감사의 수 | -(명) |
※ 기타 참고사항
- 해당사항 없음
□ 이사의 보수한도 승인
가. 이사의 수ㆍ보수총액 내지 최고 한도액
(당 기)
| 이사의 수 (사외이사수) | 8명 ( 2 명 ) |
| 보수총액 또는 최고한도액 | 2,000,000,000원 |
※ 이사의 수는 제15기 정기주주총회 목적사항인 이사의 선임 제4-3호 의안 박영수 기타비상무이사 후보자를 포함하였습니다.
(전 기)
| 이사의 수 (사외이사수) | 7명 ( 2 명 ) |
| 실제 지급된 보수총액 | 797,433,121원 |
| 최고한도액 | 2,000,000,000원 |
※ 기타 참고사항
- 해당사항 없음
□ 감사의 보수한도 승인
가. 감사의 수ㆍ보수총액 내지 최고 한도액
(당 기)
| 감사의 수 | 1명 |
| 보수총액 또는 최고한도액 | 500,000,000원 |
(전 기)
| 감사의 수 | 1명 |
| 실제 지급된 보수총액 | 24,000,000원 |
| 최고한도액 | 500,000,000원 |
※ 기타 참고사항
- 해당사항 없음
IV. 사업보고서 및 감사보고서 첨부
가. 제출 개요
| 제출(예정)일 | 사업보고서 등 통지 등 방식 |
|---|---|
| 2024년 03월 20일 | 1주전 회사 홈페이지 게재 |
나. 사업보고서 및 감사보고서 첨부
당사는 상법 시행령 제31조(주주총회의 소집공고) 제4항 제4호에 의거하여 2024년 3월 20일 사업보고서 및 감사보고서를 전자공시시스템(http://dart.fss.or.kr)에 공시하고, 당사 홈페이지(http://www.u2bio.com)에 게재할 예정입니다.
사업보고서는 향후 주주총회 이후 변경되거나 오기 등이 있는 경우 수정될 수 있으며, 이 경우 전자공시시스템(http://dart.fss.or.kr)에 정정보고서를 공시할 예정이므로 이를 참조하시기 바랍니다.
※ 참고사항
|
- 주주총회 개최(예정)일 : 2024년 3월 28일(목) 오전 9시 |