 |
|
2023.11.14_대표이사의 확인 |
분 기 보 고 서
(제 08 기)
| 사업연도 | 2023년 01월 01일 | 부터 |
| 2023년 09월 30일 | 까지 |
| 금융위원회 | |
| 한국거래소 귀중 | 2023년 11월 14일 |
| 제출대상법인 유형 : | 주권상장법인 |
| 면제사유발생 : | 해당사항 없음 |
| 회 사 명 : | 주식회사 큐라클 |
| 대 표 이 사 : | 유재현 |
| 본 점 소 재 지 : | 서울특별시 서초구 효령로 23-1(방배동) |
| (전 화)02-3487-0077 | |
| (홈페이지) http://www.curacle.com | |
| 작 성 책 임 자 : | (직 책) 이사 (성 명) 황용 |
| (전 화) 070-4193-4067 | |
【 대표이사 등의 확인 】
 |
|
2023.11.14_대표이사의 확인 |
I. 회사의 개요
1. 회사의 개요
1. 연결대상 종속회사 개황(연결재무제표를 작성하는 주권상장법인이 사업보고서, 분기ㆍ반기보고서를 제출하는 경우에 한함)
연결대상 종속회사 현황(요약)
| (단위 : 사) |
| 구분 | 연결대상회사수 | 주요 종속회사수 |
|||
|---|---|---|---|---|---|
| 기초 | 증가 | 감소 | 기말 | ||
| 상장 | - | - | - | - | - |
| 비상장 | - | - | - | - | - |
| 합계 | - | - | - | - | - |
| ※상세 현황은 '상세표-1. 연결대상 종속회사 현황(상세)' 참조 |
1-1. 연결대상회사의 변동내용
| 구 분 | 자회사 | 사 유 |
|---|---|---|
| 신규 연결 |
- | - |
| - | - | |
| 연결 제외 |
- | - |
| - | -- |
2. 회사의 법적ㆍ상업적 명칭
당사의 명칭은 "주식회사 큐라클"이며, 영문명은 "curacle co.,ltd."입니다.
3. 설립일자
당사의 설립일은 2016년 05월 12일 입니다.
4. 본사의 주소, 전화번호, 홈페이지 주소
| 구분 | 내용 |
|---|---|
| 본사 주소 | 서울특별시 서초구 효령로 23-1 |
| 전화번호 | 02-3487-0077 |
| 홈페이지 | www.curacle.com |
5. 중소기업 등 해당 여부
| 중소기업 해당 여부 | 해당 | |
| 벤처기업 해당 여부 | 해당 | |
| 중견기업 해당 여부 | 미해당 | |
6. 대한민국에 대리인이 있는 경우에는 이름(대표자), 주소 및 연락처
보고서 작성기준일 현재 해당사항이 없습니다.
7. 주요 사업의 내용 및 향후 추진하려는 신규사업에 관한 간략한 설명
당사는 고령화에 따른 난치성 혈관 및 대사성질환의 혁신적인 치료제 연구/개발업을 주력사업으로 영위하고 있습니다. 기타 자세한 사항은 「Ⅱ. 사업의 내용」을 참조하시기 바랍니다.
8. 당사의 정관에 기재된 목적 사업은 다음과 같습니다.
| 사업목적 | 비고 |
|---|---|
|
1. 의약품, 의약외품 개발, 제조, 판매업 2. 의료기기, 기자재 개발, 제조, 판매업 3. 건강식품, 건강기능 및 보조식품 개발, 제조, 판매업 4. 식품 및 화장품 개발, 제조, 판매업 5. 농축산약품, 화공약품 개발, 제조, 판매업 6. 화장품 및 화장품 원료, 신변잡화 개발, 제조, 판매업 7. 의료기기, 미용기기, 미용제품, 의료장비, 헬스용품 개발, 제조, 판매업 8. 위 각호와 관련된 도소매, 유통, 임가공, 서비스업 9. 위 각호와 관련된 무역(수출입) 및 무역중개업 10. 부동산임대 및 전대업 11. 동물 의약품/의약외품 개발 제조, 판매업 12. 위 각호와 관련된 부대사업 일체 |
- |
9. 신용평가에 관한 사항
보고서 작성기준일 현재 해당사항이 없습니다.
10. 회사의 주권상장(또는 등록ㆍ지정)여부 및 특례상장에 관한 사항
| 주권상장 (또는 등록ㆍ지정)여부 |
주권상장 (또는 등록ㆍ지정)일자 |
특례상장 등 여부 |
특례상장 등 적용법규 |
|---|---|---|---|
| 코스닥시장 | 2021년 07월 22일 | 기술성장기업 특례상장 | 코스닥시장 상장규정 제7조 2항 |
2. 회사의 연혁
1. 회사의 본점소재지 및 그 변경
| 일자 | 본점소재지 |
|---|---|
| 2016.05.12 | 서울시 강남구 밤고개로1길 10, 912호 (수서동, 현대벤처빌) |
| 2016.11.18 | 경기도 성남시 분당구 판교로 253, 비동 801호 (삼평동, 판교이노밸리) |
| 2018.10.10 | 경기도 성남시 분당구 판교로 255번길 9-22, 512호 (삼평동, 우림더블유시티) |
| 2019.09.27 |
경기도 성남시 수정구 창업로 54, 608, 609, 610, 611호 (시흥동, 엘에이치 판교 제2테크노밸리 기업성장센터) |
| 2022.04.15 | 서울특별시 서초구 효령로 23-1(방배동, 큐라클빌딩) |
2. 경영진 및 감사의 중요한 변동
경영진 및 감사의 중요한 변동
| 변동일자 | 주총종류 | 선임 | 임기만료 또는 해임 |
|
|---|---|---|---|---|
| 신규 | 재선임 | |||
| 2019.03.22 | 정기주총 | 사내이사 김영명 | 사내이사 권영근 대표이사 박광락 감사 김활년 |
사내이사 이인규 |
| 2019.07.24 | 임시주총 | 사내이사 김명화 | - | - |
| 2019.07.24 | - | 사내이사 김명화 대표이사 취임 | - | - |
| 2019.12.24 | - | 기타비상무이사 김영명 기타비상무이사 권영근 |
- | - |
| 2020.03.30 | 정기주총 | 사외이사 추연성 | - | - |
| 2021.01.05 | 임시주총 | 사외이사 최동훈 | - | - |
| 2021.03.29 | 정기주총 | 기타비상무이사 추연성 감사 고민석 |
- | 사외이사 추연성 감사 김활년 |
| 2021.09.30 | - | - | - | 대표이사 김명화 |
| 2021.11.26 | 임시주총 | 사내이사 유재현 | - | 대표이사 박광락 |
| 2021.11.26 | - | 사내이사 유재현 대표이사 취임 사외이사 조상헌 |
- | - |
| 2022.03.30 | 정기주총 | - | 기타비상무이사 김영명 기타비상무이사 권영근 |
- |
| 2022.07.22 | 임시주총 | 감사 서규영 | - | 감사 고민석 |
3. 최대주주의 변동
보고서 작성기준일 현재 해당사항이 없습니다.
4. 상호의 변경
보고서 작성기준일 현재 해당사항이 없습니다.
5. 회사가 화의, 회사정리절차 그 밖에 이에 준하는 절차를 밟은 적이 있거나 현재 진행 중인 경우 그 내용과 결과
보고서 작성기준일 현재 해당사항이 없습니다.
6. 회사가 합병 등을 한 경우 그 내용
보고서 작성기준일 현재 해당사항이 없습니다.
7. 회사의 업종 또는 주된 사업의 변화
보고서 작성기준일 현재 해당사항이 없습니다.
8. 그 밖에 경영활동과 관련된 중요한 사항의 발생내용
|
일자 |
주요 연혁 |
|---|---|
|
2019.01 |
신약연구소 이전 (대전시 한국화학연구원) |
|
2019.04 |
CU06 (혈관내피기능장애) 기술도입계약 체결 (연세대학교) |
|
2019.05 |
CU01 (당뇨병성 신증) 임상 2a상 IND 식약처 승인 |
|
2019.06 |
Covance(UK)와 연구협약 체결 (CU06 global GLP 시험 관련) |
|
액면분할(5,000원 →500원)후 빌행주식총수 4,848,980주 |
|
|
2019.08 |
IPO 대표주관사 계약 체결 (삼성증권) |
|
2019.10 |
본사이전 (경기도 판교제2테크노밸리 기업성장센터) |
|
Patheon (cGMP, USA)와 협약 체결 |
|
|
2019.10 |
3차 유상증자(3자배정) : 561,291주 / 증자 후 자본금 2,705백만원 |
|
2019.12 |
CU03 (습성 황반변성) 임상 2a상 IND 식약처 승인 |
|
2020.01 |
중앙연구소 설립 (판교제2테크노밸리 기업성장센터) |
|
2020.03 |
유한화학(cGMP)과 계약 체결 (미국 임상용 DS생산 관련) |
|
2020.04 |
중소벤처기업부 연구기반활용사업(연구집중형) 선정 |
|
CU06 보건복지부 제약사업 전주기 글로벌 진출 강화 지원사업 과제 선정 |
|
|
2020.06 |
LS Pharma 와의 연구협약 체결(제제연구) |
|
2020.08 |
CU01 (당뇨병성 신증) 임상2a상 시험대상자 모집 완료 |
|
CU03(습성 황반변성) 임상2a상 내약성 평가완료. 추가환자 60명 모집 |
|
|
2020.10 |
전자증권제도 도입 |
| CU06 (혈관내피기능장애) 미국 임상용 DP 생산완료 (cGMP) | |
|
4차 유상증자 : 149,213주 / 증자 후 자본금 2,780백만원 |
|
|
2020.11 |
연세대학교 연구협약 체결 및 산학협력 바이오랩 개설 |
|
이노비즈 인증 (중소벤처기업부 인증번호 : 200605-01197) |
|
|
스톡옵션 행사 : 98,500주 / 증자 후 자본금 2,829백만원 |
|
|
2020.12 |
연세대 세브란스병원과 신약 연구개발 및 학술활동 연구협약 체결 |
|
2차 무상증자 : 5,657,984주 / 증자 후 자본금 5,658백만원 |
|
|
2021.01 |
CU06-RE, 임상1상 미국 IND 신청 |
|
고려대 약학대학 및 약과학연구소와의 혁신 신약개발 연구협약 체결 |
|
|
2021.03 |
CU06-RE, 임상 1상 미국 IND 승인 |
|
CU01, 임상2a상 국내 완료 |
|
| 기술특례상장을 위한 기술성 평가 통과 (등급:AA. A) | |
| 2021.07 | 코스닥시장 상장 |
| 2021.09 | CU01 (당뇨병성 신증) 임상3상 국내 IND 신청 |
| 2021.10 | CU06 (당뇨병성 황반부종 및 습성 황반변성 치료제) 기술이전 계약 체결 |
| 2021.11 | 유재현 단독 대표이사 취임 |
| 2022.01 | 바이오연구소 설립 |
| 2022.04 | 본사이전 (서울 서초구 효령로 23-1 큐라클빌딩) |
| 2022.06 | CU06 임상1상 결과 보고서 확보 |
| 2022.07 | CU01(당뇨병성 신증), 임상2b상 IND 승인 |
| 2022.09 | CU06 (당뇨병성 황반부종), 임상2a상 미국 IND 승인 |
| 2022.11 | 연구개발유형 벤처기업 인증 획득 |
| 2022.12 | 산업통상자원부 첨단기술제품 확인인증 획득 |
|
2023.04 |
서울대학교 약학대학 임상약학 연구실과 학술교류 및 공동연구 수행을 위한 업무협약(MOU) 체결 |
|
2023.05 |
CU104(궤양성 대장염), 임상2상 미국 IND 제출 |
|
2023.06 |
항체치료제 개발기업 맵틱스와 글로벌 신약 공동 연구개발 및 사업화를 위한 업무협약(MOU) 체결 |
|
2023.06 |
CU104(궤양성 대장염), 임상2상 미국 IND 승인 |
|
2023.06 |
CU06 (당뇨병성 황반부종), 미국 임상2a상 시험대상자 모집 완료 |
|
2023.06 |
반려동물신약개발사업단과 동물용 의약품 신약개발을 위한 업무협약(MOU) 체결 |
|
2023.07 |
인공지능 기반 신약발굴 기업 스탠다임과 글로벌 신약 공동 연구개발 및 사업화를 위한 업무협약(MOU) 체결 |
|
2023.07 |
CU104(궤양성 대장염), 임상2상 유럽 IND 제출 |
| 2023.08 | 궤양성 대장염 및 면역 항암 병용 치료 후보물질 국내 임상1b상 신청 |
3. 자본금 변동사항
당사는 기업공시서식 작성기준에 따른 소규모기업에 해당하여 '자본금 변동사항' 을 기재하지 아니합니다.
4. 주식의 총수 등
주식의 총수 현황
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 비고 | |||
|---|---|---|---|---|---|
| 보통주 | 우선주 | 합계 | |||
| Ⅰ. 발행할 주식의 총수 | 50,000,000 | - | 50,000,000 | - | |
| Ⅱ. 현재까지 발행한 주식의 총수 | 13,855,342 | - | 13,855,342 | - | |
| Ⅲ. 현재까지 감소한 주식의 총수 | - | - | - | - | |
| 1. 감자 | - | - | - | - | |
| 2. 이익소각 | - | - | - | - | |
| 3. 상환주식의 상환 | - | - | - | - | |
| 4. 기타 | - | - | - | - | |
| Ⅳ. 발행주식의 총수 (Ⅱ-Ⅲ) | 13,855,342 | - | 13,855,342 | - | |
| Ⅴ. 자기주식수 | - | - | - | - | |
| Ⅵ. 유통주식수 (Ⅳ-Ⅴ) | 13,855,342 | - | 13,855,342 | - | |
5. 정관에 관한 사항
당기에 변동사항이 없으며, 기업공시서식 작성기준에 따라 본 항목을 기재하지 않습니다. 관련 내용은 2023년 03월 22일에 제출된 사업보고서를 참조하시기 바랍니다.
사업목적 현황
| 구 분 | 사업목적 | 사업영위 여부 |
|---|---|---|
| 1 | 의약품, 의약외품 개발, 제조, 판매업 | 영위 |
| 2 | 의료기기, 기자재 개발, 제조, 판매업 | 미영위 |
| 3 | 건강식품, 건강기능 및 보조식품 개발, 제조, 판매업 | 미영위 |
| 4 | 식품 및 화장품 개발, 제조, 판매업 | 미영위 |
| 5 | 농축산약품, 화공약품 개발, 제조, 판매업 | 미영위 |
| 6 | 화장품 및 화장품 원료, 신변잡화 개발, 제조, 판매업 | 미영위 |
| 7 | 의료기기, 미용기기, 미용제품, 의료장비, 헬스용품 개발, 제조, 판매업 | 미영위 |
| 8 | 위 각호와 관련된 도소매, 유통, 임가공, 서비스업 | 미영위 |
| 9 | 위 각호와 관련된 무역(수출입) 및 무역중개업 | 미영위 |
| 10 | 부동산임대 및 전대업 | 미영위 |
| 11 | 동물 의약품/의약외품 개발 제조, 판매업 | 영위 |
| 12 | 위 각호와 관련된 부대사업 일체 | 미영위 |
II. 사업의 내용
1. 사업의 개요
당사는 플랫폼 기술을 기반으로 모세혈관 기능장애에 기인하는 난치성 혈관질환치료제를 연구/개발하는 바이오 벤처기업으로 고령화에 따른 난치성 혈관 및 대사성질환의 혁신적인 치료제 개발을 목표로 미충족 의료 수요(Unmet Medical Needs)가 높고 시장의 지속적인 성장세를 보이는 연령 관련 혈관 질환, 만성 질환, 대사성 질환 및 암 질환 등을 핵심 연구개발 분야로 정하고 핵심 파이프라인을 구축하여 연구/개발을 진행하고 있습니다.
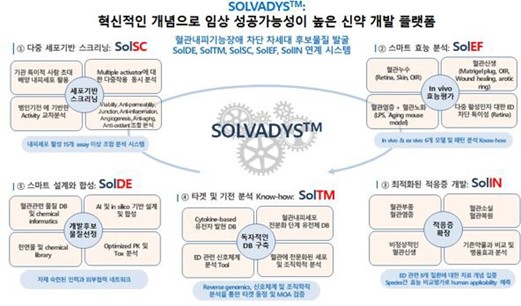 |
|
솔바디스 플랫폼 |
당사는 세계 최초로 혈관내피기능장애 차단제(Endothelial Dysfunction Blocker, ED Blocker) 개발에 특화된 신개념 플랫폼 기술인 SOLVADYS® 를 활용하여 혈관누수 및 염증 차단을 특징으로 하는 ED Blocker 물질, CU06-1004를 개발하였습니다. CU06-1004는 2021년 10월에 기술수출을 통해 아시아를 제외한 전세계 지역에 대한 판권을 떼아오픈이노베이션(Thea Open Innovation)에 이전하였습니다. 떼아오픈이노베이션에 이전한 판권은 당뇨 황반부종 및 습성 황반변성에 국한되며, 그 외의 적응증에 대한 권리는 당사가 소유하고 있습니다. CU06은 2022년 6월 건강인을 대상으로 임상1상을 완료하고, 9월 미국 FDA로 부터 당뇨병성 황반부종에 대한 임상2a상 IND를 승인 받았으며, 미국에서 임상시험을 진행 하고 있습니다. 또한 대표적인 ED 질환 중 하나인 당뇨병성 신증치료제 CU01은 2023년 1월 임상 2b상 시험을 개시했으며, 경구용 궤양성대장염 치료제 CU104는 2023년 6월 미국 FDA로부터 임상2상 IND를 승인을 받았으며, 현재 유럽 3개국의 임상2상 IND 승인을 기다리고 있습니다.
 |
|
파이프라인1 |
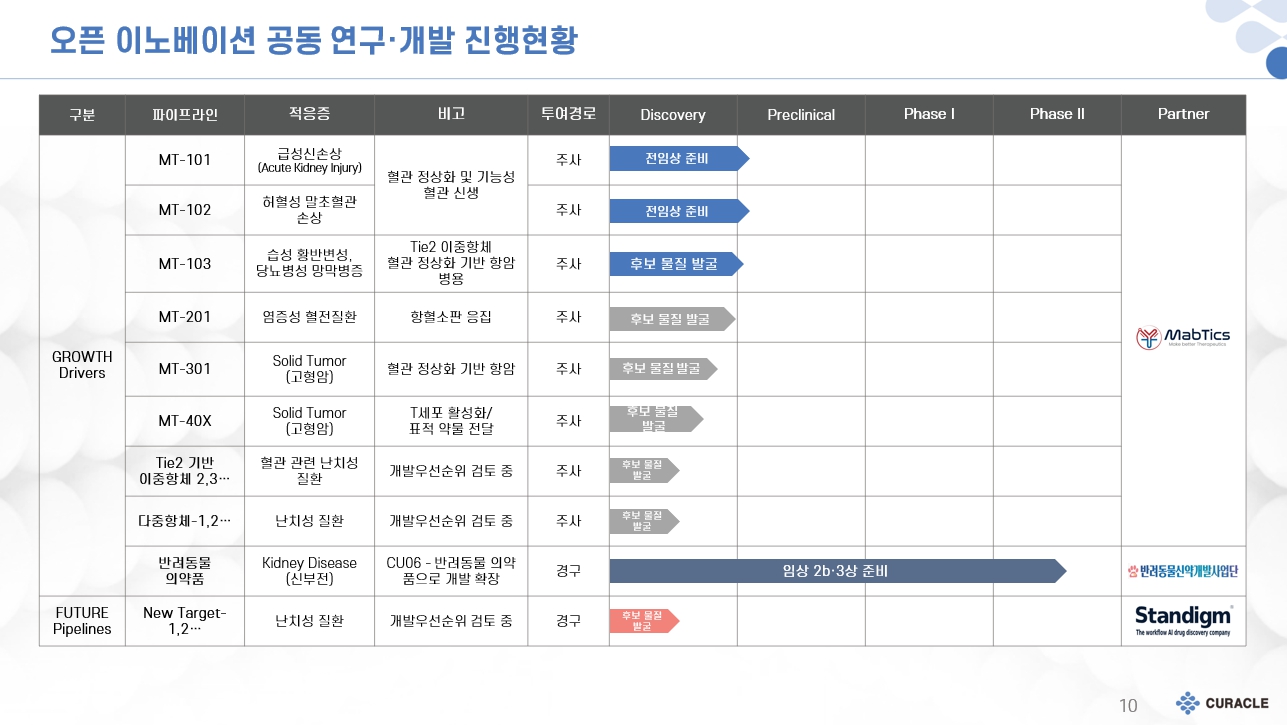 |
|
파이프라인2 |
2. 주요 제품 및 서비스
가.주요 제품 등의 현황
당사는 혈관내피기능장애 차단제 개발의 혁신 플랫폼 기술인 SOLVADYS® 플랫폼 기술을 이용한 First-in-Class 신약후보물질을 개발하고 파트너사와의 공동연구 또는 기술이전을 사업화 모델로 하고 있어 제품 판매에 대한 매출은 존재하지 아니합니다. 다만, 라이선스 계약에 따른 초기 기술료(Upfront), 개별 단계별 마일스톤(Milestone), 판매액에 대한 로열티와 임상연구비용 및 제반비용 등을 수익으로 인식하고 있습니다. 당사는 2021년 10월 떼아 오픈이노베이션에 기술 이전한 CU06에 대하여 계약금(Upfront)을 수령하였습니다.
| (단위: 백만원) |
|
품목 |
매출액 (비율) |
제품설명 |
|---|---|---|
|
CU06 |
9,022 (100%) |
□ 망막 질환의 하나인 당뇨병성 황반부종 치료제로서 전임상에서 보여준 신생혈관 생성 억제 효과는 유리체강내주사제(아일리아)의 전임상 연구 결과와 비교해 볼 때 동등 이상의 효능을 보임. |
|
CU01 |
- |
□Nrf2 활성 및 TGF-β/Smad3 억제를 통해 당뇨병성 신증을 치료할 수 있는 새로운 작용 기전의 First-in-Class 혁신신약임 |
| CU03 (경구용) |
- | □경구용 습성 황반변성 치료제이며 글로벌 최초의 천연물 신약으로서 높은 인체 안전성이 특징□기존 안구내주사제와의 병용으로 주사투여의 횟수 감소와 동시에 황반변성치료 효과의 시너지를 기대할 수 있음 |
|
CU104 |
- |
□경구용 궤양성 대장염 치료제이며 전임상 동물 질환 모델에서 시판약과 비교해 볼 때 동등 이상의 효능을 보임. |
3. 원재료 및 생산설비
가.원재료 매입에 관한 사항
당사의 주요 영업활동은 신약연구개발로서 제품 제조를 위한 별도의 원재료에 대한 매입은 없습니다.
나.생산설비에 관한 사항
당사의 주요 영업활동은 신약연구개발로서 제품 제조를 위한 별도의 생산 및 생산 설비에 관 하여는 해당사항이 없습니다. 비임상 및 임상약 생산은 위탁생산전문업체(CMO, Contract and Manufacturing Organization)가 업무를 수행하고 있습니다.
4. 매출 및 수주상황
가.매출실적
당사는 기술이전을 통한 신약 개발을 주요 사업 모델로 하고 있으며, 2021년에 Thea Open Innovation과 당뇨병성 황반부종 및 습성 황반변성 치료제 CU06-RE에 대한 아시아 지역을 제외한 기술이전 계약을 체결하였습니다. 본 계약에 따라, 당사는 CU06의 임상2상 시험, 비임상 시험 및 CMC(Chemistry, Manufacturing and Controls)에 필요한 외주 용역 비용의 보상을 받을 뿐만 아니라, 이 과정을 수행하는 데 소요되는 큐라클 전문 인력의 인건비 및 간접비용 등 서비스 비용도 Thea Open Innovation으로부터 지급받아 이를 모두 수익으로 인식하고 있습니다.
| (단위: 백만원) |
| 매출유형 | 품목 | 제8기 3분기 | 제7기 | 제6기 |
|---|---|---|---|---|
|
용역매출 |
CU06 |
9,022 |
3,583 |
6,255 |
|
합 계 |
9,022 |
3,583 |
6,255 |
|
나.판매경로 및 판매방법
(1) 판매조직
당사는 신약후보물질을 개발하여 기술이전을 목표로 하고 있으며 이를 위한 조직으로 사업개발본부를 운영하고 있습니다. 미국 및 북미시장은 BIO USA 및 각 북미학회 지회 Conference 참가 및 Business meeting을 통하여 다수의 글로벌 제약사 및 사업기회가 있는 회사들과 라이선스 아웃에 대한 접촉을 하고 있으며, 아시아 및 유럽은 Bio China, Bio Japan, Bio Europe 등의 Conference 참가 및 SM SINO사와 계약을 맺고 활발히 진행하고 있습니다. 또한, 국내 Major 제약회사들과 지속적으로 접촉하는 등 다방면으로 사업기회를 찾고 있습니다.
(2) 판매전략
당사는 신약개발을 전문으로하는 바이오벤처 기업이며, 비즈니스 모델은 SOLVADYS® 플랫폼을 통해 개발한 차세대 혈관관련질환 치료제와 더불어 난치성 질환에 대한 혁신적인 신약 파이프라인으로 글로벌 제약사와의 전략적 기술제휴를 통한 기술료매출 및 수익 창출입니다.
글로벌 제약사와의 라이선스 아웃 추진은 해외 컨퍼런스, 파트너사와의 네트워크를 통해 상호 정보교환으로 착수되며 기본적인 프로세스는 '파트너링 미팅 → NCD 자료공개 → CDA 체결 → 지속적인 정보공유 → MTA 계약 → Term sheet 작성 → Due diligence → 라이선스 계약' 단계로 구성되어 있습니다. 당사는 이미 라이선스 대상 기술 및 파이프라인에 대하 여 다수의 글로벌 제약사와 CDA 계약을 체결하고 '지속적인 정보공유' 단계로 파트너사의 Unmet needs에 대해 지속적으로 연구결과를 업데이트하며 소통하고 있습니다.
다.수주상황
당사의 주요 영업활동은 신약연구개발로서 수주 산업이 아니므로 해당사항이 없습니다.
5. 위험관리 및 파생거래
가.시장위험과 위험관리
당사는 금리위험, 가격위험, 환위험 등 다양한 시장위험에 노출되어 있습니다. 이러한 위험 요소들을 관리하기 위하여 각각의 위험요인에 대해 면밀하게 모니터링하고 대응하는 위험관 리 정책을 운용하고 있으며, 이에 대한 자세한 사항은「III. 재무에 관한 사항 → 5. 재무제표 주석」을 참조하시기 바랍니다.
나.파생상품 및 풋백옵션 등 거래현황
당사는 보고서 작성기준일 현재 해당사항이 없습니다.
6. 주요계약 및 연구개발활동
가.경영상의 주요계약
(1) 라이선스 아웃(License out) 계약
보고서 작성기준일 현재 당사가 체결 중인 주요 라이선스 아웃 계약의 현황은 다음과 같습니다.
|
품목 |
계약 상대방 |
대상 지역 |
계약 체결일 |
계약 종료일 |
계약금액 |
수취금액 |
진행 단계 |
|---|---|---|---|---|---|---|---|
|
CU06- RE |
Thea Open Innovation (떼아오픈이노베이션) |
아시아제외 전세계 |
2021.10.27 |
각 나라별 상업화 시점부터 10년 |
US$163,500,000 |
US$6,000,000 |
미국 임상2a상 진행중 |
■ 품목: CU06
|
계약상대방 |
Thea Open Innovation (떼아오픈이노베이션, 프랑스) |
|
계약내용 |
떼아오픈이노베이션이 CU06-RE에 대한 독점권 권리를 갖고 임상시험, 허가, 상업화를 진행 |
|
대상지역 |
아시아를 제외한 전세계 지역 |
|
계약기간 |
계약체결일 : 2021.10.27 |
|
총계약금액 |
US$163,500,000, 로열티는 매출액의 8% 별도 수취 |
|
수취금액 |
반환 의무가 없는 계약금(Upfront) : US$6,000,000 (2021.11.10) |
|
계약조건 |
계약금(Upfront): US$6,000,000 마일스톤(Milestone) : US$157,500,000 경상기술료(Royalty) : 매출액의 8% |
|
회계처리방법 |
계약금은 2021년~2022년 동안 분할하여 수익 인식 |
|
대상기술 |
당뇨병성 황반부종 및 습성 황반변성 치료제 |
|
개발진행경과 |
2022.06 미국 임상1상 완료 (당뇨병성 황반부종/습성 황반변성) 2022.08 미국 임상2a상 IND 신청 (당뇨병성 황반부종) 2022.09 미국 임상2a상 IND 승인 (당뇨병성 황반부종) 2023.06 미국 임상2a상 대상자 등록 완료(당뇨병성 황반부종) 2023.08 한국 임상1b상 IND 신청 (당뇨병성 황반부종 등) |
|
기타사항 |
□ 상기 마일스톤은 임상 성공시, 적응증 및 지역에 따른 허가시, 매출에 따른 목표 달성시 수령 하며, 계약금과 각 단계별로 수령하는 마일스톤과 로열티는 반환 의무가 없음. □ 당사는 FDA 1상까지의 비용을 부담하며, 2상 진입시부터는 떼아오픈이노베이션에서 비용을 부담합니다. 기존 계약에 추가하여 비임상 비용도 떼아오픈이노베이션에서 부담함. |
(2) 라이선스 인(License in) 계약
|
품목 |
계약상대방 |
대상지역 |
계약체결일 |
계약종료일 |
계약의 목적 및 내용 |
총계약금액 |
지급금액 |
진행단계 |
비고 |
|---|---|---|---|---|---|---|---|---|---|
|
CU06 |
연세대학교 산학협력단(한국) |
전세계 |
2019.04.12 |
2030.10.29 |
특허기술 양도 |
주1) |
주1) |
임상 2a상(미국) 진행중 |
경상기술료 별도 |
|
CU01 |
경북대학교 산학협력단, 경북대학교병원(한국) |
전세계 |
2017.02.01 |
2033.02.13 |
특허기술 양도 |
주1) |
주1) |
임상 2b상(한국) 진행중 |
경상기술료 별도 |
|
CU03 |
한국한의학연구원(한국) |
전세계 |
2017.03.21 |
특허권 만료일 (2035.05.21) 또는 제품출시후 10년 중 더 늦은 기간 |
특허기술 실시계약 (전용실시권) |
주1) |
주1) |
임상 2a상(한국) 완료 |
경상기술료 별도 |
|
CU05 |
연세대학교 산학협력단(한국) |
전세계 |
2017.02.03 |
2035.06.29 |
특허기술 양도 |
주1) |
주1) |
후보물질 최적화 진행중 |
경상기술료 별도 |
|
합계 |
- |
- |
- |
- |
|||||
주1) 계약 세부 내용의 경우 영업기밀에 해당하므로 기재하지 않았습니다. 자료: ㈜큐라클
■ 품목 : CU06
|
계약상대방 |
연세대학교 산학협력단 |
|
계약내용 |
특허 양수도 계약에 따라 큐라클이 신약후보물질 CU06-1004 물질특허권리를 양도 받고 임상시험, 허가, 생산, 상업화를 진행 |
|
대상지역 |
전세계 |
|
계약기간 |
계약체결일 (2019.04.12) ~ 2030.10.29 |
|
총 계약금액 |
양사 합의에 의해 계약 규모 미공개 |
|
지급금액 |
양사 합의에 의해 계약 규모 미공개 |
|
계약조건 |
매출 발생에 대한 로열티 수취 |
|
회계처리방법 |
기술료는 향후 발생 시 인식 |
|
대상기술 |
신규 혈관누출 차단제,당뇨병성 황반부종 치료제 |
|
개발 진행경과 |
임상2a상 진행 중 (미국) |
|
기타사항 |
- |
자료: ㈜큐라클
■ 품목 : CU01
|
계약상대방 |
경북대학교 산학협력단, 경북대학교병원 |
|
계약내용 |
특허 양수도 계약에 따라 CU01 용도 특허권리를 양도 받고 임상시험, 허가, 생산, 상업화를 진행 |
|
대상지역 |
전세계 |
|
계약기간 |
계약체결일 (2017.02.01) ~ 2033.02.13 |
|
총 계약금액 |
양사 합의에 의해 계약 규모 미공개 |
|
지급금액 |
양사 합의에 의해 계약 규모 미공개 |
|
계약조건 |
매출 발생에 대한 로열티 수취 |
|
회계처리방법 |
기술료는 향후 발생 시 인식 |
|
대상기술 |
만성 신장 질환 포함 당뇨병성 신증 치료제 |
|
개발 진행경과 |
임상2b상 진행 중(한국) |
|
기타사항 |
- |
자료: ㈜큐라클
■ 품목 : CU03
|
계약상대방 |
한국한의학연구원 |
|
계약내용 |
특허 전용실시권 계약에 따라 독점권 물질 특허 권리를 양도 받고 임상시험, 허가, 생산, 상업화를 진행 |
|
대상지역 |
전세계 |
|
계약기간 |
계약체결일 (2017.03.21) ~ 특허권 만료일(2035.05.21) 또는 제품출시후 10년 중 더 늦은 기간 |
|
총 계약금액 |
양사 합의에 의해 계약 규모 미공개 |
|
지급금액 |
양사 합의에 의해 계약 규모 미공개 |
|
계약조건 |
매출 발생에 대한 로열티 수취 |
|
회계처리방법 |
기술료는 향후 발생 시 인식 |
|
대상기술 |
습성 황반변성 치료제 및 당뇨망막병증 치료제 |
|
개발 진행경과 |
임상2a상 완료(한국) |
|
기타사항 |
- |
자료: ㈜큐라클
■ 품목 : CU05
|
계약상대방 |
연세대학교 산학협력단 |
|
계약내용 |
특허 양수도 계약에 따라 용도 특허권리를 양도 받고 비임상 후보물질 도출연구 진행 |
|
대상지역 |
전세계 |
|
계약기간 |
계약체결일 (2017.02.03) ~ 2035.06.29 |
|
총 계약금액 |
양사 합의에 의해 계약 규모 미공개 |
|
지급금액 |
양사 합의에 의해 계약 규모 미공개 |
|
계약조건 |
매출 발생에 대한 로열티 수취 |
|
회계처리방법 |
기술료는 향후 발생 시 인식 |
|
대상기술 |
항암제(췌장암, 대장암, 삼중음성유방암 등) |
|
개발 진행경과 |
후보물질 최적화 중 |
|
기타사항 |
- |
자료: ㈜큐라클
(3) 공동 연구개발 계약
|
품목 |
계약 상대방 (국적) |
계약체결일 |
계약종료일 |
계약의 목적 및 내용 |
계약금액 |
지급방법 |
진행경과 |
비고 |
|---|---|---|---|---|---|---|---|---|
|
CU02 |
광주과학기술원(한국), 경북대학교(한국), 한국과학기술원(한국) |
2017.08.25 |
2038.08.24 |
공동 연구개발 |
주1) |
주1) |
후보물질 도출 |
경상기술료 별도 |
자료: ㈜큐라클
■ 품목 : CU02
|
계약상대방 |
광주과학기술원, 경북대학교, 한국과학기술연구원 |
|
계약내용 |
공동 연구개발 계약에 따라 CU02의 후보물질 도출연구 공동 진행 |
|
대상지역 |
전세계 |
|
계약기간 |
계약체결일 (2017.08.25)~ 2038.08.24 |
|
총 계약금액 |
양사 합의에 의해 계약 규모 미공개 |
|
지급금액 |
양사 합의에 의해 계약 규모 미공개 |
|
계약조건 |
매출 발생에 대한 로열티 수취 |
|
회계처리방법 |
기술료는 향후 발생 시 인식 |
|
대상기술 |
비알콜성 지방간염 치료제 |
|
개발 진행경과 |
후보물질 최적화 중 |
|
기타사항 |
- |
자료: ㈜큐라클
나. 연구개발 활동
(1) 연구개발 활동의 개요
당사는 플랫폼 기술을 기반으로 모세혈관 기능장애에 기인하는 난치성 혈관질환치료제를 연 구 개발하는 바이오 벤처기업으로 고령화에. 따른 난치성 혈관 및 대사성질환의 혁신적인 치료제 개발을 목표로 하고 있습니다.
(2) 연구개발 담당 조직
가) 연구개발 조직 구성
보고서 작성기준일 현재 당사는 박사급 9명, 석사급 9명 등 총 22명의 연구인력을 보유하고 있으며 각 조직별 주요 역할은 아래와 같습니다.
|
조직 |
역할 |
|---|---|
|
신약연구본부 |
- 전임상 후보물질 개발, 합성 공정 개발 - 공정 지표 물질 및 방사성 표지 물질 (Stable isotope) 합성 |
|
임상개발본부 |
- 임상시험 전략 수립 및 임상개발 수행 - 임상 인허가 관리 |
|
연구개발본부 |
- 임상 DS/DP개발 및 생산, GLP 시험 관리, 지식재산권 관리 - 대사체 분석 연구, 후보물질 분석 연구 및 MV 시험 |
|
바이오연구본부 |
- 기전 및 in vitro/ in vivo 효능 시험 |
나) 연구개발 인력 구성
|
구분 |
박사 |
석사 |
학사 |
합계 |
|---|---|---|---|---|
|
신약연구본부 |
5 |
2 |
0 |
7 |
|
임상개발본부 |
0 |
4 |
2 |
6 |
|
연구개발본부 |
1 |
1 |
2 |
4 |
|
바이오연구본부 |
3 |
2 |
0 |
5 |
|
계 |
9 |
9 |
4 |
22 |
다) 주요 연구개발 인력
|
직위 |
성명 |
담당업무 |
주요경력 |
주요 연구실적 |
|---|---|---|---|---|
| 이사회의장 |
권영근 |
기전 및 효력연구 자문 |
미국 State University of New York at Buffalo, 이학박사(생화학) |
-신규 혈관 누출 차단제 개발 (기술이전) |
|
사외이사 |
최동훈 |
임상개발 및 중개 연구 자문 |
연세대학교 의과대학, 의학박사(M.D) - 연세대 의과대학 교수 ('99~현재) - 세브란스병원 심혈관제품유효성평가센터 부센터장 ('10~'16) |
- 대한 심장학회 학술이사/기초과학연구회 회장 |
|
기타 |
추연성 |
해외사업 |
미국 Univ. Illinois at Chicago 약학박사 - LG화학 바이오텍연구소 책임연구원 ('96~'00) - ㈜스탠다임, ㈜바이오에스파트너즈, ㈜진메디신 등 |
- LG생명과학 합성신약(신규 퀴놀론계항균제) 한국 최초 美 FDA 승인 획득 - LG생명과학 바이오의약품(인간성장호르몬) 한국 최초 유럽 EMEA / 美 FDA 승인 획득 - LG생명과학 신약/신제품 (신규 당뇨병치료제, 골관절염치료제, 진통소염제) 출시 - 美 훽스트메리엔루셀 신규 항구토제 美 FDA 승인 획득 |
|
기타 |
김영명 |
연구개발자문 |
미국 Utah 주립대학교, 이학박사(생화학) - 강원대 우수연구센터장 ('01~현재) |
- 황반 및 당뇨성 망막질환 치료제 개발 |
|
상무이사 |
이원일 |
전임상 후보물질 및 |
서울대학교, 약학박사 -C&C 신약연구소 책임연구원('01~'15) -젬백스앤카엘 연구개발본부 이사('15~'16) -제일약품 신약연구부 책임연구원('16~'17) -대원제약 신약연구부 이사('17~'22) |
-제2형 당뇨병, 고지혈증 치료제 및 항암제 개발 -소염진통제, 제2형 당뇨병 치료제의 신규염/공결정을 이용한 개량신약 개발 -GnRH 길항제의 process development 및 임상시험을 위한 API 합성 -역류성식도염 치료제, 진통제, 항암제 개발 -펩타이드 백신 및 약물 개발 -유방암 치료제 개발 -통풍 치료제 개발 -아토피 피부염 치료제 개발 -COPD치료제 개발(PDE4 inhibitor) -당뇨병 치료제 개발(SGLT2 inhibitor) |
|
이사 |
김판경 |
임상 개발, |
경북대학교, 의학 석사 -LG 생명과학 Clinical study leader ('10.08~'14.05) |
-국내신약 제미글로 임상개발 및 품목허가 -글로벌신약 롤론티스 임상개발 -다수의 신약, 개량신약 임상개발 및 품목허가 -글로벌 라이센싱 아웃 2건 |
| 이사 /본부장 |
표정인 | DS/DP 생산 및 품질관리, 조제물 및 생체시료 분석 연구 | 연세대학교, 이학박사(의약화학) -한국과학기술연구원(KIST) 연구원('03-06~'14.12) -삼육대학교 특임교수/비전임('11.09~'14.07) -iNtRON Biotechnology 신약연구 팀장('15.01~'17.07) |
-CMC 총괄: 국내 2a상(2건), 2b상(1건), 미국 1상(1건), 2a상(1건) -파키슨병 치료제 개발: Pyrazolopyrimidine -Calcium channel blocker 개발: Oxo & thioxoquinaxoline carboxamides -천연물 유래의 생리활성물질 개발: Xanthorrhizol, Vitamin D3 전합성 -약물전달 기술개발: nanoparticle(polymeric, liposome), BNCT modulater(Nucleoside, Inositol, Folic acid complex) -Generic drug 개발: 항히스타민제, 과민성 방광증상 치료제, 당뇨병 치료제(DPP-4) -발효균주를 이용한 빈혈 치료제 개발: eHeme -산업용 소재개발(효소촉매 고정화 및 반응): 생체 고분자, Carbohydrate -특허출원 국내외 77건 |
(3) 연구개발 비용
당사는 연구 및 임상개발 등에 소요되는 모든 비용을 당기 비용으로 회계처리하고 있습니다.
[연구개발비 현황]
| (단위 : 백만원) |
|
구분 |
2023년 |
2022년 (제7기) |
2021년 (제6기) |
|
|---|---|---|---|---|
|
연구개발비용 총계 |
11,722 |
11,375 |
10,040 |
|
|
회계처리내역 |
회계처리금액 |
11,722 |
11,648 |
10,148 |
|
정부보조금 |
- |
(273) |
(108) |
|
|
연구개발비용 합계 |
11,722 |
11,375 |
10,040 |
|
|
연구개발비/매출액 비율 |
129.93% |
317.4%. |
160.5% |
|
(4) 연구개발 실적
가. 연구개발 진행현황 및 향후계획
[연구개발 진행 총괄표]
|
구분 |
품목 |
적응증 |
현재 진행단계 (국가) |
비고 |
|
|---|---|---|---|---|---|
|
혁신신약 |
화학 |
CU06 |
당뇨병성 황반부종 |
임상2a상 진행중 (미국) |
2022.09 (임상2a상 IND 승인) |
|
CU06 |
습성 황반변성 |
임상1상 완료 (미국) |
CU06 적응증 확장 |
||
|
CU104 |
궤양성 대장염 |
임상2상 IND 승인 (미국) |
|||
|
CU106 |
면역항암제 병용 |
임상1상 완료 (미국) |
|||
|
화학합성 |
CU01 |
당뇨병성 신증 |
임상2b상 진행중 (한국) |
2022.07 (임상2b상 IND 승인) |
|
|
천연물 |
CU03 |
습성 황반변성 |
임상2a상 완료 (한국) |
2019.12 (임상2a상 IND 승인) |
|
■ 품목 : CU06
|
구분 |
화학합성 신약(경구용) |
|
적응증 |
당뇨병성 황반부종 |
|
작용기전 |
- 혈관내피세포의 actin 구조 변형을 통해 내피세포 연접을 안정화 - 혈관내피세포 NF-kB 염증신호체계 차단 - 혈관내피세포의 생존율 향진 및 보호 효과 |
|
제품의 특성 |
[경구용 당뇨병성 황반부종 치료] - 당뇨병성 황반부종은 망막 혈관 장벽의 파괴 및 염증을 동반하며 비정상적 혈관 신생으로 진행하여 혈관내피기능장애를 차단하는 것이 중요한 치료 타깃임. - 전임상단계에서 보여준 신생혈관생성억제 효과는 유리체강내 주사제 (아일리아)의 전임상 연구 결과와 비교해 볼 때 동등 이상의 효능을 보임 |
|
진행경과 |
- 2021.01 미국 FDA 임상1상 IND 신청 - 2021.02 미국 FDA 임상1상 IND 승인 - 2021.03 임상시험 개시 후, 7월에 첫 투여 실시함 - 2022.03 마지막시험대상자의 마지막 방문 완료 - 2022.08 미국 FDA 임상2a상 IND 신청 - 2022.09 미국 FDA 임상2a상 IND 승인 - 2023.06 미국 임상2a상 대상자 등록 완료 - 2023.08 한국 임상1b상 IND 신청(당뇨병성 황반부종 등) |
|
향후계획 |
- 1상을 마친 후 다양한 난치성 질환 (급성 폐손상, 급성 심근경색, 뇌졸중, 궤양성 대장염, 유전성 혈관부종, 면역항암제 병용요법)을 목표로 하여 적응증 확장을 준비 하고 있음 |
|
경쟁제품 |
- 현재 시장에 출시되어 있는 경구용 당뇨병성 황반부종 치료제 없음. - 레이저 치료(국/격자/범안저광응고술) 또는 스테로이드 유리 체강내 주사 및 Anti-VEGF 주사제가 치료에 사용되고 있으며, 대표적인 제품은 Anti-VEGF 주사제 인 Lucentis(ranibizumab), Avastin(bevacizumab), Eylea (aflibercept) 등이 90%의 시장 점유율을 차지하고 있으며, 연평균 6%의 증가가 예상됨 |
|
관련논문 등 |
Sac-1004, a novel vascular leakage blocker, enhances endothelial barrier through the cAMP/Rac/cortactin pathway. Biochem Biophys Res Commun. 435(3): 420-427 (2013)를 통한 기전규명 등 다수 적응증 확장 논문/학회 발표 진행 |
|
글로벌 시장규모 |
2017년도 27억 달러에서 2025년 32억 달러(CAGR: 3.30%)로 성장예측 |
| 기타사항 | - |
■ 품목 : CU01
|
구분 |
화학합성 신약(경구용) |
|
적응증 |
당뇨병성 신증 |
|
작용기전 |
Nrf2 활성(Nuclear factor erythroid-2-related factor 2, 항산화 유전자의 유도발 현에 영향을 주는 대표적인 전사인자)과 TGF-β(전환성장인자 베타, Transforming growth factor-beta)/Smad3(전환성장인자의 수용체에 작용하는 단백질) 억제 기 전의 First-in-Class 약제로 항산화 및 섬유화 억제 작용을 갖고 있어 신섬유증 및 신섬유증을 수반하는 만성신장질환 환자의 예방 및 치료 |
|
제품의 특성 |
[당뇨병성 신증의 근본적인 치료] - 당뇨병성 신증은 혈역학적 요인과 당뇨 및 고혈압 등과 관련된 대사성 요인에 의하여 발생하며, 여기에는 각종 세포내 신호전달 경로와 TGF-β 등의 여러 사이토카인이 작용함. - CU01은 디메틸푸마레이트(DMF)의 Nrf2 활성 및 TGF-β/Smad3 억제를 통한 신 장 섬유화를 치료할 수 있는 새로운 작용 기전의 First-in-Class 혁신 신약임. - 미국 Biogen 사의 블록버스터 의약품(다발성 경화증 치료제 Tecfidera, 2019 Peak Sales;제네릭 출시 이전 4,433 Million US$ / 2021 Sales 486.5 Million US$)의 주성분 디메틸푸마레이트를 Drug Repositioning 방법을 이용하여 당뇨병성 신증 치료제로 개발하였음. |
|
진행경과 |
- 2019.05 식품의약품안전처 임상2a상 IND 승인 - 2019.09 첫 환자 투여 - 2020.08 안전성자료모니터링위원회(DSMB)에서 안전성 중간분석 회의 결과, CU01의 안전성 이슈가 없으므로 임상시험 지속 권고 받음. - 2021.03 국내에서 진행한 임상 2a 상 임상시험결과보고서(CSR) 발행됨 - 알부민뇨가 나타나는 제2형 당뇨병성 신증 (Diabetic Nephropathy) 환자 39명을 대상으로 CU01-1001 또는 위약을 12주간 투여한 결과 CU01-1001 투여군에서 ACR 개선에 효과 확인. - 신기능 개선에 주요 지표가 되는 사구체 여과율 (estimated Glomerular Filtration Rate)의 통계적으로 유의한 증가를 관찰함 [임상 2a시험 → 유효성/안전성 확인] -2022.07 식품의약품안전처 임상 2b상 IND 승인 -2023.02 임상 2b상 대상자 등록 진행 |
|
향후계획 |
-후기 임상 진입 전략 수립 |
|
경쟁제품 |
- 현재 당뇨병성 신증 치료제는 고혈압 및 당뇨병 치료제가 주로 사용되고 있으며, 섬유화 진행을 억제하는 경쟁 약물은 없음. - 고혈압 치료제: Cozaar(Losartan Potassium), Micardis(Telmisartan) - 당뇨병 치료제: Ozempic(semaglutide), Trulicity(dulaglutide) |
|
관련논문 등 |
Dimethylfumarate Attenuates Renal Fibrosis via NF-E2-Related Factor 2- Mediated Inhibition of Transforming Growth Factor-β/Smad3 Signaling, PLoS One 2012, 7(10):e45870를 통한 기전규명 등 다수 논문/학회 발표 진행 |
|
글로벌 시장규모 |
2022년 1,011 Million US$ (CAGR : 1.23%) (출처:Global Data) |
|
기타사항 |
- |
■ 품목 : CU03
|
구분 |
천연물 신약(경구용) |
|
적응증 |
습성 황반변성 |
|
작용기전 |
항산화, 항염증, 항신생혈관 및 항투과성 |
|
제품의 특성 |
- 경구용 천연물 신약으로 안전하고 효과적인 천연 약재인 계지와 목단피가 주성분 - 경구투여로 기존 유리체강내 주사 치료제가 갖는 부작용을 줄이고, 황반변성 치료에 큰 효과를 나타낼 수 있는 것이 동물실험에서 확인됨. - 기존 anti-VEGF 주사제와 병용 사용하여 치료 효율을 높일 수 있는 장점이 있고, - 약리 활성 연구를 통해 항염증/항신생혈관/항과투과성/항산화효과 등이 검증함 |
|
진행경과 |
[임상2a시험 진행] - 2019.12 식품의약품안전처 IND 승인 - 2020.09 내약성 평가완료 - 마지막 대상자의 마지막 방문 완료 - 2022.01 국내에서 진행한 임상 2a상 임상시험결과보고서(CSR) 발행됨 -비임상시험(26주 반복투여 독성시험) 완료 |
|
향후계획 |
- 후기 임상 진입 전략수립 |
|
경쟁제품 |
- 현재 시장에 출시되어 있는 경구용 황반변성 치료제 없음. - 레이저 치료 (국/격자/범안저광응고술) 또는 스테로이드 유리체강내 주사 및 Anti-VEGF 주사제가 치료에 사용되고 있음 - 대표적인 제품은 anti-VEGF 주사제인 Lucentis(ranibizumab), Avastin(bevacizumab), Eylea (aflibercept) 등이 90%의 시장 점유율을 차지하고 있으며, 연평균 6%의 증가가 예상됨 |
|
관련논문 등 |
Extract of Moutan radicis cortex and Cinnamomi ramulus ameliorates laser- induced choroidal neovascularization in Brown-Norway rats, Phytomedicine, 심 사中를 통해 CNV 동물모델 효능을 논문/학회 발표함 |
|
글로벌 시장규모 |
2017년 63억 달러에서 2025년 88억 달러(CAGR: 3.8%)로 성장예측 |
|
기타사항 |
- |
나. 계획 중인 후속 프로젝트
당사는 보고서 작성기준일 현재 임상연구 중인 프로젝트와 함께 계획중인 후속 프로젝트는 아래와 같습니다. 다만 당사의 사업 전략에 따라 연구 개발 계획의 변동이 발생할 수 있습니다.
[계획 중인 후속 프로젝트 총괄표]
|
구분 |
품목 |
적응증 |
현재 진행단계 |
비고 |
|
|---|---|---|---|---|---|
|
화학합성 |
신약 |
CU04 |
Oncology(차세대 항암제) |
선도물질 탐색 |
자체연구 |
|
화학합성 |
신약 |
CU05 |
Oncology(차세대 항암제) |
후보물질 도출 |
공동연구 |
|
연고 |
신약 |
CU301 |
Psoriasis(건선) |
전임상 단계 |
자체연구 |
|
화학합성 |
신약 |
CU71-R01 |
차세대 혈관내피기능장애 차단제 |
후보물질 도출 |
자체연구 |
(주1) 당분기 중 파이프라인 명칭이 기존 CU07에서 CU71-R01로 변경되었습니다.
다. 보유 기술에 대한 연구실적(논문 및 학회 발표)
- CU06 핵심기술에 대한 논문 14편 및 학회 발표 25건(주저자: 연세대 권영근 교수)
- CU01 핵심기술에 대한 논문 4편 및 학회 발표 2건(주저자: 경북대 의대 이인규 교수)
- CU03 핵심기술에 대한 논문 1편 및 학회 발표 1건 (주저자: 한국한의학연구원 김진숙 박사)
- CU05 핵심기술에 대한 논문 1편 및 학회 발표 5건 (주저자: 연세대 권영근 교수)
[논문발표 목록]
| 구분 | 논문제목 | 게재정보 | 비고 |
|---|---|---|---|
| CU06 | CU06-1004 alleviates vascular hyperpermeability in a murine model of hereditary angioedema by protecting the endothelium | Allergy (2023) | 유전성 혈관부종 모델에서 효과규명 |
| Long-term administration of CU06-1004 ameliorates cerebrovascular aging and BBB injury in aging mouse model | Fluids Barriers CNS. 1;20(1):9 (2023) | 노화 모델에서 효과규명 | |
| Oral administration of CU06-1004 attenuates vascular permeability and stabilizes neovascularization in retinal vascular diseases | Eur J Pharmacol. 15; 939:175427 (2023) | 망막혈관질환 모델에서 효과규명 | |
| CU06-1004 modulates the adenosine monophosphate (AMP)-associated protein kinase (AMPK) signaling pathway and inhibits lipogenesis in 3T3-L1 adipocytes and high-fat diet-induced obese mice | Life Sci. 1; 296:120440 (2022) | 비만모델에서 효과 규명 | |
| CU06-1004 enhances vascular integrity and improves cardiac remodeling by suppressing edema and inflammation in myocardial ischemia-reperfusion injury | Exp Mol Med. 54(1):23-34 (2022) | 심근경색 모델에서 효과 규명 | |
| CU06-1004-inducedvascular normalization improves immunotherapy by modulating tumor microenviroment via cytotoxic T cell. | Front. Immunol. 11; 620166 (2021) | 종양 미세환경 개선 효과 규명 | |
| The endothelial dysfunction blocker CU06-1004 ameliorates choline-deficient L-amino acid diet-induced non-alcoholic steatohepatitis in mice | PLoS One. 15(12):e0243497(2020) | 비알코올성 지방간 모델에서 효과 규명 | |
| CU06-1004 Alleviates Experimental Colitis by Modulating Colonic Vessel Dysfunction | Front Pharmacol. 15;11:571266(2020) | 대장염 모델에서 효과 규명 | |
| CU06-1004 (endothelial dysfunction blocker) ameliorates astrocyte end-feet swelling by stabilizing endothelial cell junctions in cerebral ischemia/reperfusion injury | J Mol Med (Berl). | 뇌졸중 모델에서 효과 및 기전 규명 | |
| Sac-1004, a vascular leakage blocker, reduces cerebral ischemia-reperfusion injury by suppressing blood-brain barrier disruption and inflammation | J Neuroinflammation. | 뇌졸중 모델에서 효과 규명 | |
| Sac-1004, a Pseudo-Sugar Derivative of Cholesterol, Restores Erectile Function through Reconstruction of Nonleaky and Functional Cavernous Angiogenesis in the Streptozotocin Induced Diabetic Mouse | J Urol. 195(6): 1936-46 (2016) | 당뇨 마우스에서 발기기능 효과 규명 | |
| Direct endothelial junction restoration results in significant tumor vascular normalization and metastasis inhibition in mice | Oncotarget. 5(9): 2761-77 (2014) | 종양 혈관 정상화 효과 규명 | |
| Combined effect of vascular-leakage-blocker Sac-1004 and antiangiogenic drug sunitinib on tumor angiogenesis | Biochem Biophys Res Commun. 450(4): 1320-6 (2014) | 항암제와의 병용투여 효과 규명 | |
| Sac-1004, a novel vascular leakage blocker, enhances endothelial barrier through the cAMP/Rac/cortactin pathway. | Biochem Biophys Res Commun. 435(3): 420-427 (2013) | 기전 규명 | |
| CU01 | Dimethylfumarate Attenuates Renal Fibrosis via NF-E2-Related Factor 2-Mediated Inhibition of Transforming Growth Factor-β/Smad3 Signaling | PLoS One 2012, | Renal fibrosis 감소효능 |
| Dimethylfumarate suppresses adipogenic differentiation in 3T3-L1 preadipocytes through inhibition of STAT3 activity | PLoS One 2013, 18;8(4):e61411 | Adipocytes 분화 억제 효능 | |
| Activation of Nrf2 by dimethyl fumarate improves vascular calcification | Vascul Pharmacol. | Vascular calcification 억제 효능 | |
| Dimethylfumarate attenuates restenosis after acute vascular injury by cell-specific and Nrf2-dependent mechanisms | Redox Biol 2014 | Vascular restenosis 감소효능 | |
| CU03 | Extract of Moutan radicis cortex and Cinnamomi ramulus ameliorates laser-induced choroidal neovascularization in Brown-Norway rats | Phytomedicine,심사中 | CNV 동물모델 효능 |
| CU05 | AMIGO2, a novel membrane anchor of PDK1, controls cell survival and angiogenesis via Akt activation | J Cell Biol. 211(3): 619-37 (2015) | 기전 규명 |
(5) 연구개발 완료 실적
당사는 보고서 작성기준일 현재 연구개발 완료 실적이 없습니다.
(6) 연구활동 및 판매 중단 현황
당사는 보고서 작성기준일 현재 연구활동 및 판매 중단 현황이 없습니다.
(7) 기타 연구개발 실적
[당사 국책과제 현황]
(단위: 백만원)
|
기술구분 |
사업명 (시행부처) |
과제명 |
사업기간 |
총 지원금 (당사 부담금) |
참여 형태 |
현황 |
|---|---|---|---|---|---|---|
|
- |
- |
- |
- |
- |
- |
- |
7. 기타 참고사항
가. 지적재산권 보유 현황
당사는 파이프라인의 시장 진입장벽을 확보하기 위하여 특허권 보유전략 및 관리체계를 확립하였고, 핵심특허의 지역적 실효성 평가를 통해 플랫폼 및 파이프라인에 대한 다양한 특허 출원 및 등록으로 광범위한 지적재산권을 확보하고 있습니다. 현재 당사의 지적재산권 현황은 다음과 같습니다.
|
특허 (전용실시권) |
등록 |
30 (4) |
상표권 |
등록 |
13 |
|
출원 |
44 (3) |
출원 |
- |
|
CU06 |
CU01 |
CU03 (전용실시권) |
CU02 |
CU05 |
|||||
|---|---|---|---|---|---|---|---|---|---|
|
등록 |
출원 |
등록 |
출원 |
등록 |
출원 |
등록 |
출원 |
등록 |
출원 |
|
15 |
23 |
9 |
16 |
(4) |
2(4) |
4 |
1 |
2 |
2 |
| 번호 | 구분 | 내용 | 출원인 | 권리자 | 출원 | 등록 | 적용 | 출원국 | 비고 |
|---|---|---|---|---|---|---|---|---|---|
| 1 | 특허권 | 신규 혈관누출 차단제 | 연세대 산학협력단 외 1곳 | (주)큐라클 | 2012.04.26 | 2014.11.18 | CU06 | 미국 | 특허 양수도 |
| 2 | 2010.10.29 | 2015.02.27 | 일본 | ||||||
| 3 | 2010.10.29 | 2016.05.04 | 유럽 | ||||||
| 4 | 2010.10.29 | 2015.02.18 | 중국 | ||||||
| 5 | 2010.10.29 | - | PCT | ||||||
| 6 | 특허권 | 신규 혈관누출 차단제 | 연세대 산학협력단 | ㈜큐라클 | 2011.12.29 | 2014.01.10 | 한국 | 특허 양수도 | |
| 7 | 2012.12.28 | 2016.05.31 | 미국 | ||||||
| 8 | 2012.12.28 | - | PCT | ||||||
| 9 | 특허권 | 면역항암 보조제 | 연세대 산학협력단, ㈜큐라클 |
연세대 산학 협력단, ㈜큐라클 |
2020.04.23 | 2022.09.20 | 한국 | 공동 출원 | |
| 10 | 2020.04.23 | - | PCT | ||||||
| 11 | 2021.09.15 | - | 미국 | ||||||
| 12 | 2021.09.07 | - | 유럽 | ||||||
| 13 | 2021.10.28 | - | 일본 | ||||||
| 14 | 2021.09.27 | - | 중국 | ||||||
| 15 | 특허권 | 지방간 질환의 예방 또는 치료를 위한 약학적 조성물 | 연세대 산학협력단, ㈜큐라클 |
- | 2020.07.03 | - | 한국 | 공동 출원 | |
| 16 | 2021.06.24 | - | PCT | ||||||
| 17 | 특허권 | 신규 혈관누출 차단제의 고수율 제조방법 | ㈜큐라클 | ㈜큐라클 | 2019.12.13 | 2020.06.12 | 한국 | 단독 출원 | |
| 18 | 2020.07.28 | - | PCT | ||||||
| 19 | 2020.11.24 | 2022.09.27 | 미국 | ||||||
| 20 | 2020.11.25 | - | 인도 | ||||||
| 21 | 2020.12.01 | 2023.06.07 | 유럽 | ||||||
| 22 | 2020.12.01 | 2022.08.02 | 일본 | ||||||
| 23 | 2020.12.10 | 2022.08.05 | 중국 | ||||||
| 24 | 특허권 | 혈관 누출 차단제 화합물의 신규 결정형 | ㈜큐라클 | ㈜큐라클 | 2020.05.04 | 2021.02.26 | 한국 | 단독 출원 |
|
| 25 | 2020.10.05 | - | PCT | ||||||
| 26 | 2021.04.22 | - | 아르헨티나 | ||||||
| 27 | 2021.07.07 | - | 미국 | ||||||
| 28 | 2021.07.07 | - | 유럽 | ||||||
| 29 | 2021.07.05 | - | 인도 | ||||||
| 30 | 2021.07.23 | - | 중국 | ||||||
| 31 | 2021.07.20 | 2023.02.03 | 일본 | ||||||
| 32 | 2021.10.11 | - | 브라질 | ||||||
| 33 | 2021.10.06 | 2023.01.03 | 캐나다 | ||||||
| 34 | 2021.10.29 | - | 러시아 | ||||||
| 35 | 2021.10.05 | - | 호주 | ||||||
| 36 | 2021.11.12 | - | 멕시코 | ||||||
| 37 | 2021.11.15 | - | 사우디아라비아 | ||||||
| 38 | 2022.04.24 | - | 이스라엘 | ||||||
| 39 | 특허권 | 디메틸푸마레이트를 유효성분으로 포함 하는 신섬유증의 예방 또는 치료용 | 경북대 산학 협력단 외 1곳 | ㈜큐라클 | 2013.02.13 | 2014.03.24 | CU01 | 한국 | 특허 양수도 |
| 40 | 2013.02.20 | - | PCT | ||||||
| 41 | 2013.02.20 | 2017.08.08 | 미국 | ||||||
| 42 | 특허권 | 디메틸푸마르산염을 함유한 장용성정제 조성물 | ㈜큐라클 | ㈜큐라클 | 2020.05.21 | 2020.12.24 | CU01 | 한국 | 단독 출원 |
| 43 | 2020.05.21 | - | PCT | ||||||
| 44 | 2021.09.20 | - | 미국 | ||||||
| 45 | 2021.09.27 | - | 유럽 | ||||||
| 46 | 2021.09.28 | 2023.02.09 | 일본 | ||||||
| 47 | 2021.09.27 | - | 중국 | ||||||
| 48 | 2021.09.22 | - | 인도 | ||||||
| 49 | 2021.10.01 | 2022.08.09 | 캐나다 | ||||||
| 50 | 2021.09.16 | 2022.10.04 | 브라질 | ||||||
| 51 | 2021.10.11 | 2022.10.07 | 멕시코 | ||||||
| 52 | 2021.11.29 | - | 사우디아라비아 | ||||||
| 53 | 2021.10.20 | - | 필리핀 | ||||||
| 54 | 2021.09.23 | - | 태국 | ||||||
| 55 | 2021.09.10 | - | 베트남 | ||||||
| 56 | 2021.12.07 | 2022.10.20 | 호주 | ||||||
| 57 | 2021.12.23 | - | 인도네시아 | ||||||
| 58 | 2021.12.29 | 2023.01.28 | 러시아 | ||||||
| 59 | 특허권 | 모노메틸푸마레이트를 유효성분으로 포함하는 장기 섬유증의 예방 또 는 치료용 약학적 조성물 |
㈜큐라클 | ㈜큐라클 | 2020.11.27 | - | 한국 | 단독 출원 | |
| 60 | 2021.08.25 | - | PCT | ||||||
| 61 | 특허권 | 특정 약동학적 매개변수를 나타내는 디메틸푸마 레이트 를 유효성분으로 함유한 약학적 조성물 | ㈜큐라클 | - | 2021.03.25 | - | 한국 | 단독 출원 | |
| 62 | 2021.03.24 | - | PCT | ||||||
| 63 | 2022.08.10 | - | 미국 | ||||||
| 64 | 특허권 | 천연 혼합 추출물을 유효성분으로 함유 하는 '당뇨합병증 및 혈관부종 예방 또는 치료용 약학적 조성물 |
한국한의학 연구원 | 한국한의학 연구원 | 2015.05.21 | 2016.10.27 | CU03 | 한국 | 전용 실시권 |
| 65 | 2015.05.21 | - | PCT | ||||||
| 66 | 2015.05.21 | 2021.12.07 | 미국 | ||||||
| 67 | 2015.05.21 | 2021.01.13 | 유럽 | ||||||
| 68 | 2015.05.21 | - | 중국 | ||||||
| 69 | 2021.05.19 | - | 중국 | ||||||
| 70 | 2023.04.10 | - | 중국 | ||||||
| 71 | 2016.08.26 | 2021.03.24 | 한국 | ||||||
| 72 | 계지 및 목단피 혼합추 출물을 유효성분으로 함유한 정제 및 이의 특정 투여요량에 의한 치료를 위한 조성물 |
㈜큐라클 | - | 2022.12.29 | - | 한국 | 단독 출원 | ||
| 73 | 2022.12.30 | - | PCT | ||||||
| 74 | 특허권 | 신규한 트립토판 수산화 효소 저해제 및 이를 포함하는 약학 조성물 |
광주과학기술원 산학협력단, KAIST 산학협력단 | 광주과학기술원 산학협력단, KAIST 산학협력단, |
2018.08.24 | 2020.03.05 | CU02 | 한국 | 공동 출원 |
| 75 | 2018.08.24 | - | PCT | ||||||
| 76 | 2020.02.24 | 2022.08.09 | 미국 | ||||||
| 77 | 2020.03.24 | 2022.07.20 | 유럽 | ||||||
| 78 | 경북대 산학협력단, ㈜큐라클 |
경북대 산학협력단, ㈜큐라클 |
2020.04.23 | 2022.11.29 | 중국 | ||||
| 79 | 특허권 | AMIGO2와 3-포스포이 노시티드- 의존 키나아 제1의 결합 억제용 데코 이펩타이드 |
㈜큐라클 | ㈜큐라클 | 2015.06.29 | 2017.09.21 | CU05 | 한국 | 특허 양수도 |
| 80 | 2016.06.28 | 2018.11.13 | 미국 | ||||||
| 81 | 특허권 | 신규한 카바졸 유도체 및 이를 유효 성분으로 포함하는 암의 예방 또 는 치료용 약학적 조성물 |
㈜큐라클 | ㈜큐라클 | 2021.11.10 | - | 한국 | 단독 출원 | |
| 82 | 특허권 | 2021.11.10 | - | PCT | |||||
| 83 | 상표 특허 | Solvadys | ㈜큐라클 | ㈜큐라클 | 2019.11.04 | 2021.02.08 | CU06 | 한국 | 단독 출원 |
| 84 | 솔바디스 | 2019.11.04 | 2021.02.01 | 한국 | |||||
| 85 | Healvasc | 2019.11.04 | 2021.02.08 | 한국 | |||||
| 86 | 힐바스크 | 2019.11.04 | 2021.02.08 | 한국 | |||||
| 87 | Vesaegis | 2019.11.04 | 2021.02.01 | 한국 | |||||
| 88 | 베세지스 | 2019.11.04 | 2021.02.08 | 한국 | |||||
| 89 | Dnitier | 2022.01.27 | 2023.07.10 | CU01 | 한국 | ||||
| 90 | 디니티어 | 2022.01.27 | 2023.07.10 | 한국 | |||||
| 91 | Qunef | 2022.01.27 | 2023.07.10 | 한국 | |||||
| 92 | 큐네프 | 2022.01.27 | 2023.07.10 | 한국 | |||||
| 93 | CURACLE | 2019.09.11 | 2020.10.21 | 기타 | 한국 | ||||
| 94 | THE CURACLE | 2019.09.11 | 2020.10.21 | 한국 | |||||
| 95 | 큐라클 | 2019.09.11 | 2020.10.21 | 한국 |
나. 영업에 영향을 미치는 법률 또는 제규정
의약품의 제품 개발에서 의약품이 판매되기 위해서는 신약후보물질의 발굴에서부터 동물을 대상으로 하는 비임상시험, 인체를 대상으로 하는 임상 1상부터 3상 시험, 신약 판매 허가라는 각 단계를 모두 거쳐야 합니다. 모든 단계에서 한국을 포함한 각 국가는 엄격히 허가 및 규제기관을 통해 통제되고 있으며, 본 사업과 밀접하게 연관된 국내외 규제는 『약사법』, 『의약품 등의 안전에 관한 규칙』, 『생명윤리 및 안전에 관한 법률』, 『국민건강보험법』, 『독점규제 및 공정거래에 관한 법률』, 『The Food, Drug and Cosmetic Act, the Code of Federal Regulations』 등의 법령과 미국(FDA), 유럽 (EMEA) 및 일본 (PMDA) 등의 선진국의 규제가 매우 엄격합니다. 이에 당사는 연구개발 초기단계부터 관련국에 규격에 맞게 모든 자료를 준비하고 있고 해외 컨설턴트와 지속적으로 협업하여 진행하고 있습니다.
다. 산업의 특성
(1) 산업의 특성
제약산업(Pharmaceutical Industry)은 「약사법」제2조제4호와 「제약산업 육성 및 지원에 관한 특별법」제2조에는 의약품을 연구개발ㆍ제조ㆍ가공ㆍ보관 및 유통하는 것과 관련된 산업으로 정의되어 있습니다. 전 세계적으로 고령화로 인한 뇌/심혈관 질환, 난치성 및 만성 질환 환자 규모는 증가하여 제약산업은 꾸준히 성장하고 있습니다. 제약산업은 인간의 생명과 보건에 관련된 제품을 개발하고 생산하는 첨단산업으로서 우수한 의약품 개발과 접근성 제고를 통해 질병으로 인한 사회적 비용 감소 등 국민 건강증진 및 건강권 확보와 직결된 산업입니다.
(2) 의약품의 분류
의약품은 제조방식에 따라 화학합성으로 제조되는 합성의약품, 천연물로부터 약효를 가진주성분을 함유하는 천연물의약품, 생물학적 제제로서 재조합 단백질, 백신, 혈액제제를 포함하는 생물학적 반응을 이용하여 제조하는 바이오의약품으로 분류되며, 「약사법」제2조제10항에 따라 일반의약품(Over the Counter Drug, OTC)과 전문의약품(Ethical the Counter Drug, ETC)으로 구분됩니다.
| [의약품의 분류] |
| 의약품 구분 | 내용 | |
|---|---|---|
| 제조방식 | 합성의약품 | 실험실에서 유기화학에 기반하여 합성에 의해 인위적으로 만들어진 저분자 화합물 의약품 |
| 천연물의약품 | 약용식물 등 이미 존재하는 천연물로부터 약효를 가진 성분만을 분리 정제하여 만든 의약품 | |
| 바이오의약품 | 생물체(미생물, 동식물 세포 등)를 활용하여 바이오기술을 응용하여 만들어진 의약품 | |
| 의사 처방유무 | 전문 의약품 | 일반의약품이 아닌 의약품을 말하는 것으로, 약리작용 또는 적응증으로 볼 때, 의사의 전문적인 진단과 지시·감독에 따라 사용되어야 하는 의약품 (Ethical the Counter Drug, ETC) |
| 일반 의약품 | 의약품의 제형과 약리작용상 인체에 미치는 부작용이 비교적 적거나, 오용·남용의 우려가 적고 의사나 치과의사의 처방 없이 사용하더라도 안전성 및 유효성을 기대할 수 있는 의약품(Over the Counter Drug, OTC) | |
당사는 난치성 혈관질환의 First-in-Class 혁신신약으로 합성의약품(CU06-RE, CU01)과 천연물의약품(CU03)의 연구 개발을 진행하고 있으며, 해당 파이프라인들은 약리작용 또는 적응증으로 볼 때, 의사의 전문적인 진단과 지시/감독에 따라 사용하는 전문의약품(ETC)으로 분류됩니다.
(3) 산업의 특성
당사가 추진 중인 사업은 제약 및 바이오산업에 속해 있으며, 동 산업의 특성은 다음과 같습니다.
- 각 국가별 식품의약국의 규정 준수 필요
신약은 기존 약물의 유효성 혹은 안전성 측면에서 현저한 개선이 포함되어야 하며, 신물질 탐색 작업, 비임상 시험, 임상시험, 허가 신청 (NDA) 등을 거쳐 제조 승인 및 시판허가를 받은 의약품을 말합니다. 한 개의 신약이 나오기 위해서는 여러 단계를 수행해야 합니다. 첫 번째로 신약 후보물질을 도출하기 위한 탐색 과정에서 신약의 효능이나 작용기전을 기반으로 신약개발 대상 품질을 선정합니다. 유효물질, 선도물질을 거쳐 신약 후보물질이 선정되면 후보물질의 안전성과 효과를 확인하기 위해 동물 모델을 대상으로 비임상시험을 진행합니다. 비임상시험을 통해 후보물질의 효과와 안전성이 검증되면 식약처에 임상시험 허가신청 (IND)을 하고, 사람을 대상으로 약물의 효과 및 부작용을 확인하는 임상시험 (Clinical Trial)을 수행합니다. 임상시험을 완료한 후에는 식약처에 임상시험 결과를 제출하게 되는데, 이를 신약 허가신청(NDA) 이라고 합니다. 신약 허가 신청이 정상적으로 이루어지면, 제4상 임상시험으로 분류되는 시판 후 안전성 조사(PMS)를 통해 임상시험에서 발견하기 어려웠던 부작용에 대해서 추적 조사를 수행합니다. 이처럼 새로운 의약품이 개발되어 소비자에게 전달되기까지는 높은 비용과 노력이 필요하며, 시판으로 이어질 확률은 10,000분의 1 정도로 낮은 편입니다. 이렇게 성공 가능성이 낮지만, 성공했을 경우 특허법, 각 국가별 약사법 등으로 독점적 시장 보호가 가능하고 막대한 경제적 가치를 창출할 수 있기 때문에 글로벌 시장에 도전하는 신약개발은 여전히 매력적인 사업입니다.
- 다양한 정책에 따른 높은 진입장벽 존재
신약개발 산업은 높은 기술력과 천문학적인 개발비용, 국가별 허가 당국의 시판 승인 등 진입장벽이 상당히 높은 편입니다. 또한 특허법, 의약품 특허존속기간 연장제도, 희귀의약품 지정제도, 의약품 자료 독점권 제도 등 신약 개발사에 혜택을 주는 다양한 보호 제도가 있어 제네릭사의 시장 진입을 제한하고 있습니다.
- 국내 의약품 시장의 글로벌 성장성
글로벌 제약산업 시장 조사기관인 IQVIA가 발표한 리포트에 따르면 2021년 글로벌 제약산업 시장 규모는 1조 4,003억 달러를 형성하고 있으며 이후 연평균 4.1%로 성장하여 2025년에는 1조 6,420억 달러에 달할 것으로 예상됩니다. 대한민국의 제약산업 시장 규모는 2021년 179억 달러에서 글로벌 성장보다 빠른 연평균 5.8%의 성장을 통해 2025년에는 224억 달러를 형성할 것으로 예상됩니다.
2021년 기준으로 대한민국의 제약산업 시장 규모는 글로벌 전체 시장 규모의 1.27%를 차지하고 있으며 국내 제약기업과 바이오벤처가 다국적기업과의 기술 제휴 또는 라이선스 아웃 등을 통해 글로벌 파트너사와 임상 개발을 진행하여 경험과 노하우를 습득하면서 고도화되고 있어 향후 글로벌 성장성 대비 높은 성장성을 보이며 시장이 확대될 것으로 보입니다.
- 고부가가치 산업
제약산업은 다른 어떤 산업보다도 기술과 자본이 집약된 '고부가가치 지식산업'으로, 개발된 의약품의 제조원가 자체는 매우 낮지만, 장기적인 R&D 투자를 통한 신약개발 여부가 성패를 좌우하는 특성을 가집니다. 글로벌 신약개발 시 평균 1조 원에서 2조 원에 이르는 개발비용과 10~15년의 개발기간이 소요되며, 더욱이 신약개발 성공확률은 5,000분의 1에 불과한 것으로 알려져 있습니다. 후보물질 발굴 단계에서 5,000~10,000개의 화합물이 R&D 파이프라인으로 들어간 이후 전임상단계에서 약 250여 개의 연구를 거쳐 임상단계에서 2~5개가량만 남게 되며, 이중 1개만이 최종 판매허가를 받고 상용화됩니다.
신약 하나를 개발하기 위해서는 장기간에 걸친 R&D 과정에서 막대한 자본과 인력의 지속적인 투입이 수반되지만 성공을 확신할 수 없습니다. 그러나, 이른바 '죽음의 계곡'을 넘어 신약 개발에 성공하게 되면, 확실한 시장 우위를 점하며 그동안의 R&D에 투자한 것 이상의 많은 이익을 회수할 수 있습니다. 다국적 제약사 화이자에서 출시한 '비아그라(성분 실데나필)'는 임상 실패 이후 신약 재창출 과정을 통해 큰 성공을 거둔 사례입니다. 실데나필은 협심증 치료를 목표로 개발된 약물이었지만, 임상 실패 이후 발기부전 치료제로 재탄생했습니다. '20세기 최고의 발명품'으로 불리는 비아그라는 1998년 5월 출시 이후 단 3개월 만에 4억 달러(약 4,700억 원) 규모, 지난 20년 간 연간 평균 18억 달러(약 2조 1,300억 원) 규모의 매출을 기록하여 대표적인 블록버스터급 의약품으로 알려져 있습니다. 같은 회사에서 출시한 고지혈증 치료제 '리피토’는 2010년 무려 127억 달러의 매출을 기록하였는데, 이는 '자동차 100만 대 수출' 수익보다도 높은 수준입니다.
- 주력 기술제품의 산업의 연혁
당뇨병은 췌장에서 분비되는 인슐린이 부족하거나 우리 몸에서 제대로 작용하지 못하여 혈액 속의 혈당이 에너지로 이용되지 않고 혈액 속에 축적되어 고혈당 증상과 이로 인한 합병증을 나타내는 질환입니다. 2017년에는 전세계적으로 당뇨 환자가 4억 5천 1백만 명(18세~99세) 발병했고 2045년경에는 6억 9천 3백만 명으로 증가할 것으로 예상되고 있으며, 당뇨 의약품 시장 또한 폭발적으로 증가하여 2026년경에는 950 ~ 1020억 달러(107 ~ 115조원)에 이를 것으로 추정되고 있습니다. 이와 같이 당뇨병 환자의 증가와 함께 고령인구 증가로 당뇨합병증 시장 또한 높은 성장성이 예상되어 글로벌제약사들이 치료제 개발을 위해 많은 투자를 진행하고 있습니다.
합병증은 크게 혈관 합병증과 신경 합병증으로 나눌 수 있으며, 혈관 합병증은 다시 대혈관 손상과 미세혈관 손상으로 나눌 수 있습니다. 대혈관이 손상되면 협심증, 동맥경화, 심근경색, 뇌졸중이 발병하고 미세혈관이 손상되면 망막병증, 신장병, 신경병, 족부궤양 등의 다양한 합병증이 나타날 수 있습니다. 그리고 신경 합병증은 말초신경장애와 자율신경장애로 나누어 집니다.
혈관 합병증의 원인은 아직까지 확실히 밝혀져 있지 않으나 대혈관 손상의 경우 고혈합, 고지혈증이 동반되면서 복합적인 원인에 의해 발생하는 것으로 알려져 있습니다. 또한 제2형 당뇨병 환자에서는 비만과 관상동맥질환 등이 위험인자로 작용함으로써 고혈당의 치료와 더불어 이들 질환의 치료가 동시에 이루어져야 합병증의 진행을 막을 수 있습니다.
미세혈관 합병증 중 하나인 당뇨병성 신증은 당뇨환자의 주요 사망요인으로 아주 서서히 진행되기 때문에 초기에는 검사로도 식별이 어려우며 환자에 따라 다르나 대개 15년 정도 지난 후에 단백뇨 증상이 나타나게 됩니다. 처음에는 단백뇨로 인해 부종이 발생하고 더욱 진행이 되면 노폐물이 신장에서 배설되지 않음으로써 만성 신부전증으로 결국 요독증에 빠지게 됩니다. 당뇨병성 신증 치료제 중 신장 섬유화를 치료하는 전문치료제는 없으며, 질환의 원인이 될 수 있는 혈당과 혈압을 관리하는 치료제가 처방되고 있습니다. 60세 이상 당뇨병 환자 중 75%가 당뇨병성 신증 환자임을 고려할 때 전문치료제의 개발이 절실하다고 하겠습니다.
또한 미세혈관 합병증 하나인 당뇨황반부종도 당뇨병 환자에서 20년 유병 기간 후 약 30~50%정도 발생하는데, 25세 이후의 시력상실 질병 중 가장 많은 원인이 되고 있습니다. 그러나 모든 환자가 시력이 상실되는 것이 아니라 적극적으로 혈당을 조절하고 자주 검사하여 조기에 발견하면 예방할 수 있으며 그 진행속도 또한 늦출 수 있습니다. 최근에는 치료를 위해 혈관내피성장인자(VEGF) 저해제인 아일리아 혹은 루센티스를 유리체강 내에 주사(intravitreal injection)하여 치료제가 사용되고 있습니다. 다만, 2019년도 Scientific reports 에 의하면 이 약물에 불응성을 나타내는 환자가 41% 정도이고 약가는 각각 1,940달러/vial, 1,575달러/vial 로 상당히 고가여서 환자 및 국가 보험 재정에 부담을 주고 있어 높은 효능, 경제성, 투여방식 편의성 등의 측면을 개선할 수 있는 신약 개발이 필요한 상황입니다.
황반변성은 시력에 중요한 역할을 담당하는 망막중심부 신경조직인 황반이 노화, 염증 등으로 기능이 떨어지는 질환을 말하며 국내 65세 이상의 노인인구에서 실명을 일으키는 주요 원인으로 알려져 있습니다. 2017년 황반변성 환자는 70억 세계 인구의 약 8.3%인 5천800만명 이상으로 추정되고 있으며 2020년에는 환자수가 약 2억 명, 2040년경에는 약 3억명에 육박할 것으로 예측되고 있습니다. 당뇨황반부종도 동일하게 혈관 내피성장인자(VEGF) 저해제인 아일리아나 루센티스가 치료제로 사용되고 있으며 노령인구의 중가의 함께 황반변성 치료제 시장도 크게 성장할 것으로 예상됩니다.
(4) 산업의 전망
- 글로벌 제약시장 전망
글로벌 전문의약품(ETC) 시장은 지속적으로 성장해왔습니다. 전세계 전문의약품 매출액은 2020년 9,040억 달러(약 1,073조 원)에서 연평균 7.4%씩 성장해 2026년에는 1조 3,903억 달러(약 1,650조 원) 규모가 될 전망입니다. 이는 지난 2012∼2019년 처방의약품 매출액 연평균 성장률이 2.7%에 그친 것과 비교할 때 매우 빠른 성장세를 볼 수 있습니다.
|
자료: EvaluatePharma, World Preview 2020, outlook to 2026
생명공학정책 연구센터, 글로벌 제약산업 2020년 프리뷰 및 2026년 전망
인구증가 및 고령화, 만성질환 증가, 규제장벽 완화, 맞춤형 치료제, 희귀병 치료제 등의 성장 요인(Market Drivers)에 따라 미국 FDA에서 최근 10년간(2013~2022년) 승인된 화학합성신약은 428건으로 이는 과거 10년(2010~2019년) 289건에 비해 48% 증가되었습니다. 미국 FDA의 산업 친화적(industry-friendly) 입장은 유지 될 것으로 전망되며, 미국 FDA가 채택한 입장은 전세계 제약시장에 대한 투자심리를 결정하는 데 중요한 역할을 합니다.
|
자료: FDA CDER, New Drug Therapy Approval 2022, 2023.01
또한, 전세계적으로 신약 개발 기간 단축을 통한 효율성 제고를 위해 플랫폼 기술 도입이 늘어나고 있습니다. 전통적인 신약 탐색 과정에서 통상 약물 후보물질을 찾을 때까지 소요되는 시간과 비용을 플랫폼 기술을 활용함으로써 절감하려는 시도가 이루어지고 있습니다. 당사 또한 신개념 SOLVADYS® 플랫폼 기술을 이용하여 유효물질을 효율적으로 발굴하기 위한 초기 단계 연구개발을 적극적으로 진행하고 있으며 이 플랫폼을 통하여 신약개발기간을 효율적으로 단축시키고 실패를 줄일 수 있을 것으로 기대 하고 있습니다.
(5) 경기변동의 특성
- 라이프사이클
일반적으로 의약품은 관련된 특허의 존속기간(선출원 후 20년)이 만료될 때까지 독점적인 판매가 가능하며, 또한 국가별로 자료 및 시장독점권(Data & Market Exclusivity) 제도에 의하여 미국인 경우 신약 승인 후 5년간의 자료독점권을 그리고 유럽의 경우 자료독점권 8년에 시장독점권 2년을 추가로 부여하고, 희귀의약품으로 지정된 경우 미국은 7년 , 유럽은 11년간의 시장 독점권을 주는 것을 허용하는 등 다양한 제도를 통하여 독점적 판매권을 보장받을 수 있습니다.
당사는 신개념 SOLVADYS® 플랫폼 기술을 이용하여 난치성 혈관질환의 First-in-Class 혁신신약을 개발하고 있으며 각 파이프라인별로 물질, 용도(적응증/용법 용량). 조성물(제제, 병용투여), 결정형 및 제법 등 연구단계별 다양한 특허를 출원, 등록하는 evergreening 전략을 사용하여 특허의 존속기간을 연장하고 있습니다. 또한 특허존속기간 연장제도 (최장 5년 추가)로 대부분 제품이 2045년까지 특허보호를 받을 수 있어 제품 판매 후 13 ~ 17년간 시장 진입장벽이 존재할 것으로 예상합니다.
- 경기변동 및 계절성
일반적으로 의약품은 크게 전문의약품(ETC)과 일반의약품(OTC)으로 분류됩니다. 전문의약품은 의사의 진단과 처방을 통해 약 복용이 엄격히 관리되어야 하는 의약품을 의미하며, 일반의약품은 안전성과 유효성이 충분히 인정되어 약사나 소비자가 임의로 선택할 수 있는 의약품을 의미합니다. 당사가 개발중인 파이프라인은 모두 전문의약품 분야에 속하며, 의학적 미충족 수요가 큰 영역이라 경기 변동에 거의 영향을 받지 않습니다.
삶의 질 향상과 수명연장에 대한 요구가 높아지고 있고 GDP 수준 향상과 전세계적으로 고령화 사회가 확산됨에 따라 만성질환과 치매 같은 문제가 사회적 이슈로 대두되고 있어 이러한 추세로 인해 의약품 산업은 지속적이고 안정적인 증가가 예상됩니다. 한편, 의약품 산업의 특성상 국가별 의료 정책이나 약가 정책에 따라 변동성이 있을 수 있으나 당사가 개발중인 First-in-Class 혁신 신약의 경우 약가 결정에 이점이 있어 상대적으로 높고 안정적인 수익을 창출할 것으로 기대됩니다.
앞서 설명한 바와 같이 당사가 개발중인 파이프라인은 모두 전문의약품 분야에 속하며, 당뇨합병증은 만성 질환이고 같은 유전적 또는 생활 환경 요인에 따라 발생되는 질환으로 날씨와 기후에 의한 계절적 요인에는 거의 영향을 받지 않습니다. 이와는 달리 일반의약품의 경우 소비자 선택으로 경기변동이나 기후에 의한 계절적 영향이 다소 있는 편입니다. 또한 인플루엔자나 전염성 질환 관련 의약품의 경우 계절, 환경적 요인에 따라 영향을 받을 수 있습니다.
- 대체재 현황
당사에서 개발하고 있는 신약은 전문의약품(ETC)이며 의사의 진단과 처방에 의해서만 약을 구입할 수 있도록 제도적으로 엄격히 관리보호되고 있으며, 모든 단계에서 한국을 포함한 각 국가는 엄격히 허가 및 규제기관을 통해 통제되고 있으며 각 국가에서 설정한 기준에 의해 허가절차를 거쳐 승인을 받아야만 출시할 수 있습니다. 동일한 목표시장에 대해 경쟁제품이 있을 수 있으나 경쟁제품 상호 간에 제품의 약효와 안전성이 완전히 일치하는 신약은 존재할 수 없습니다.
연구단계별 다양한 특허를 출원, 등록하는 evergreening 전략을 사용하여 특허의 존속기간을 연장하고 있습니다. 다만, 특허기간이 만료된 이후에는 다수의 복제약(제네릭/바이오시밀러)이 출시되어 오리지널 의약품이 경쟁력을 잃고 대체될 수 있겠으나, 특허 만료 이후에도 오리지널 제품에 대한 수요가 일정 부분 지속적으로 존재하는 현상이 있습니다
라. 회사 경쟁상의 특징
- 당뇨병성 황반부종 치료제
글로벌 시장 조사 전문기관인 Global Market Insights 2016에 따르면 당뇨병성 황반부종 및 습성 황반변성 치료제는 anti-VEGF 주사제인 Eylea, Lucentis, Avastin 등이 90%의 시장 점유율을 차지하고 있으며, 연평균 6%의 증가가 예상됩니다.
| [시판되고 있는 anti-VEGF, Steroid 유리체강내 주사제] |
|
제품명 |
제약사 |
2019년 매출 | 가격 | 비고 |
|---|---|---|---|---|
|
Lucentis (ranibizumab) |
Novartis |
전세계 매출 4조 6천억원 |
824,513~941,098원 | 시장에 주사제외에 경구제가 존재하지 않고, Endothelial dysfunction을 차단 하는 약물 역시 존재하지 않기에, First-in-class & Oral agent로 시장 진입 가능 |
|
Avastin (bevacizumab) |
Roche |
전세계 매출 7조 5천억원 |
330,387~346,320원 | |
|
Eylea (aflibercept) |
Regeneron/Bayer |
전세계 매출 8조 3천억원 |
751,493~851,788원 |
자료: ㈜큐라클
하지만, anti-VEGF 안구내 주사제는 모두 병증이 많이 진행된 후에 처방되어 진단 초기 경증의 환자에게는 투약의 제한이 있습니다. 당뇨환자 중 당뇨황반부종 진단 후 첫해에 치료(anti-VEGF 항체, Laser치료, corticosteroid 및 병용 치료 등)를 받고 있는 환자는 40% 미만으로 60% 환자가 약물투여를 제대로 받지 못하는 것으로 알려져 있습니다. 이에 진단받은 후 많은 환자는 병의 진행을 악화시키고 있다고 볼 수 있어 환자에게 복용편의성이 높은 적절한 경구치료제가 개발된다면 환자의 삶의 질을 향상시킬 뿐만 아니라 엄청난 시장을 확보할 것으로 기대하고 있습니다.
CU06-RE는 anti-VEGF 주사제와 비교하여 당뇨황반부종 및 습성 황반변성과 같은 다양한원인 인자에 기인되는 혈관 손상 및 누수를 치료할 수 있는 최적의 치료제입니다. 또한 경구 투여에 의한 복용편의성으로 만성질환인 당뇨황반부종 및 습성 황반변성 치료제로 개발된다면 글로벌 시장에서 충분히 경쟁력이 있습니다.
현재 세계적 제약기업 및 신약벤처들이 아래 다양한 타깃의 당뇨황반부종 치료제 개발에 집중하고 있습니다.
| ▶ 유리체강내 주사제: | VEGF 외에 Tissue-protective receptor, Corticosteroid, c-Raf kinase, Plasma kallikrein, PIGF, pan RGD integrin 타깃 |
| ▶ 점안제: | Bradykinin receptor B1, Plasma kallikrein 타깃 |
| ▶ 경구제: | Steroid ethisterone, C-Kit, Plasma kallikrein 타깃 |
대표적인 혈관내피세포 타겟 치료제는 anti-VEGF 중화 항체로 주로 항암 및 망막 혈관질환 치료제로 사용되고 있습니다. 망막 혈관질환 치료제의 경우, 전세계 시장규모가 년간 150억 달러를 상회함에도 불구하고 안구내 주사의 불편함과 2019년도 Scientific reports 에 의하면 41% 의 불응 환자로 인하여 치료의 한계가 있어 대체 치료제가 절실하게 필요한 상황입니다 (자료: Scientific reports, 9(1), 10952)
- 당뇨병성 신증 치료제
현재 당뇨병성 신증 치료제는 고혈압 및 당뇨병 치료제가 주로 사용되고 있습니다.
안지오텐신 전환효소억제제(angiotensin converting enzyme inhibitor), 안지오텐신II 수용체 차단제(angiotensin II receptor blocker) 등 고혈압 치료제가 있습니다.
J&J사의 Canagliflozin(Invokana), AstraZeneca/Mitsubishi Tanabe의 Dapagliflozin이 SGLT-2 억제제(Sodium Glucose Co-Transporter 2, 신장에서 포도당이 재흡수되는 것을 억제하여 소변으로 포도. 당이 배출되도록 하는 기전)인 당뇨병 치료제로 당뇨병성 신증 치료제로서 허가 받고 사용되고 있습니다.
| [시판되고 있는 고혈압 및 당뇨병치료제] |
|
제품명 |
제약사 |
2019년 매출 | 가격 | 비고 |
|---|---|---|---|---|
| Cozaar (Losartan Potassium) |
Boehringer Ingelheim |
1조원 | 416~585원 | 당뇨병성 신증 환자에게 보조치료제로 쓰임 |
| Micardis (Telmisartan) |
MSD | 6,500억원 | 481원 | |
| Ozempic (semaglutide) |
Novo nordisk |
3조 8천억원 | TBD | 직접적인 경쟁관계 약물은 아님 |
| Trulicity (dulaglutide) |
Lilly | 5조 6천억원 | 19,811 ~ 32,129원 |
자료: ㈜큐라클
만성 신섬유증 치료제로 섬유화 진행을 억제하는 시장에 나온 경쟁 약물은 없습니다. CU01은 Nrf2 활성과 TGF-β/Smad3 억제 기전의 First-in-Class 약제로 항산화 및 섬유화 억제 작용을 갖고 있어 신섬유증 및 신섬유증을 수반하는 만성신장질환 환자의 예방 및 치료에 사용될 수 있고 발 빠른 국내 출시를 목표로 후기임상을 준비하고 있습니다.
당사의 CU01은 물질특허가 없는 블록버스터 의약품이며 약물의 안전성이 확보된 Tecfidera의 주성분인 DMF를 신약재창출 방법으로 재평가하여 Nrf2 활성제 및 TGF-β/Smad3 억제 기전으로 당뇨병성 신증 모델에서 우수한 효능을 보였고, 당사가 국내에서 진행한 임상 2a상 시험에서 유효성, 안전성 및 내약성을 확보하였습니다.
- 습성 황반변성 치료제
글로벌 시장 조사 전문기관인 Global Market Insights 2016에 따르면 습성 황반변성치료제 시장도 anti-VEGF 제제가 90%를 차지하고 있으며, 연평균 6%의 증가가 예상됩니다.
| [시판되고 있는 anti-VEGF, Steroid 유리체강내 주사제] |
|
제품명 |
제약사 |
2019년 매출 | 가격 | 비고 |
|---|---|---|---|---|
|
Lucentis (ranibizumab) |
Novartis |
전세계 매출 4조 6천억원 |
824,513~941,098원 | 시장에 주사제외에 경구제가 존재하지 않고, Endothelial dysfunction을 차단 하는 약물 역시 존재하지 않기에, First-in-class & Oral agent로 시장 진입 가능 |
|
Avastin (bevacizumab) |
Roche |
전세계 매출 7조 5천억원 |
330,387~346,320원 | |
|
Eylea (aflibercept) |
Regeneron/Bayer |
전세계 매출 8조 3천억원 |
751,493~851,788원 |
자료: ㈜큐라클
경구제로는 growth factor 저해제, kinase 저해제, 활성산소를 제거하는 항산화제, DNA lygase 등의 저분자 물질로 주로 단일 타깃을 저해하는 물질이 개발되고 있고 현재 시장에 나온 제품은 없습니다.
천연물 신약인 CU03는 만성 난치성 질환의 다양한 병인에 의하여 발병되는 습성 황반변성의 경구용 치료제로 환자에게 복용 편의성 및 안전성을 제공하여 장기적 투여가 가능하고 기존의 주사제와 차별성이 있습니다. 당사는 천연물의 multi-component and multi-target (다중 성분과 다중 타깃)의 작용 원리로 다양한 인자가 원인이 되는 만성질환의 치료제 CU03를 개발하고 특허의 특허연장 전략으로 천연물 중 성분함량, 임상시험에 의한 용량, 추가 적응증 확보 등을 기반으로 특허를 출원하여 특허권리 확보 및 권리기간 연장을 할 계획입니다. 새로운 개념의 경구용 혈관내피기능장애 치료제는 전 세계적으로 당사가 유일하고 신약개발의 특성상 글로벌 제약사가 단기간 내에 진입하기는 어려울 것으로 봅니다.
마. 용어해설
당사가 영위하는 사업의 내용을 이해하기 위하여 개념 정리가 필요한 용어에 대한 해설은 다음과 같습니다.
| [주요 용어 정리] |
|
용어 |
해설 |
|---|---|
|
당뇨합병증 |
당뇨병이 발생하여 췌장에서 분비되는 인슐린이 부족하거나 우리 몸에서 제대로 작용하지 못하여 혈액 속의 혈당이 에너지로 이용되지 않고 혈액 속에 축적되어 고혈당증상과 이로 인한 합병증을 나타내는 질환입니다. |
|
당뇨병성 신증 |
미세혈관에 발생하는 당뇨 합병증으로 신장이 손상되어 단백뇨와 부종, 고혈압이 동반되고 노폐물이 신장에서 배설되지 않음으로써 만성신부전으로 진행되는 질환입니다. |
|
당뇨병성 황반부종 |
당뇨병으로 인하여 안구의 모세혈관의 파괴로 인하여 시각 세포가 손상되어 시력상실을 일으키는 질환입니다. |
| 당뇨망막병증 (DR; Diabetic Retionopathy) |
당뇨병에 의한 발생하며 고혈당으로 인하여 일어나는 말초 순환장애로 인하여 망막에 발생하는 합병증입니다. |
| 망막색소상피 박리 (PED; Pigment epithelial Detachment) |
망막의 10개층 중에 가장 아래층을 구성하는 1개 층으로 유일하게 색소를 지니고 있어 망막색소상피로 불리며, 망막색소상피가 그 아래의 맥락막으로부터 떨어지는 현상을 망막색소상피 박리라고 합니다. |
| 맥락망신생혈관 (CNV; Choroidal Neovascularization) |
망상색소상피 박리로 생긴 공간에서 신생혈관이 자라나 맥락막신생혈관이 되며 우리 눈의 망막중에서 특히 중요한 황분부에 삼출물, 출혈 등을 일으켜서 중심시력에 영향을 주는 현상을 황반변성이라고 합니다. |
| 습성 황반변성 (wet AMD; wet Age-related macular degeneration) |
삼출성-연령관련 황반 변성, 시력에 매우 중요한 역할을 하는 황반에 나이가 들면서 드루젠(drusen), 망막 색소상피 위축(retinal pigment epithelial atrophy), 맥락막 신생혈관(choroidal neovascularization) 등 변화가 생겨 시력상실을 초래하는 질환입니다. |
|
생체 이용률 (Bioavailability) |
투여된 약물이 변화되지 않은 형태로 전신 순환혈에 도달하는 정도이며 주로 경구투여 시의 흡수정도를 의미하며, 약물의 화학적 형태, 제형, 투여경로, 위장관내 안정도, 초회통과효과 등에 영향을 받습니다. |
|
신약후보물질 |
질병과 관련된 단백질(약물 타겟)의 기능을 조절하는 물질을 찾은 후 동물, 독성, 약물 체내동태 등을 평가하여 임상 개발 가치가 있는 물질로 선정하는 일련의 과정을 의미합니다. |
|
신약허가신청 (NDA; new drug application) |
합성의약품에 대한 신약승인 신청서를 의미합니다. 바이오의약품의 경우는 BLA(Biologic License Application)라고 합니다. |
|
임상시험 |
임상시험용 의약품의 안전성과 유효성을 증명할 목적으로 해당 약물의 약동 · 약력 · 약리 · 임상적 효과를 확인하고 이상반응을 조사하기 위하여 사람을 대상으로 실시하는 시험 또는 연구를 총칭하는 것이며, 임상1상, 임상2상 (임상2a 와 임상2b를 구분하여 진행할 수도 있음), 임상3상 크게 3단계로 구분하여 운영되고 있습니다. |
|
임상1상 |
건강한 사람을 대상으로 약물을 안전하게 부여할 수 있는 용량과 인체 내 약물흡수 정도 등을 평가합니다. 앞서 수행된 전임상 단계에서 독성시험 등 전임상시험 결과가 유효한 경우, 시험약을 최초로 사람에 적용하는 단계입니다. 건강한 지원자 또는 약물군에 따른 적응환자를 대상으로 부작용 및 약물의 체내동태 등 안전성 확인에 중점을 두고 있습니다. |
|
임상2상 |
소규모 환자들을 대상으로 약물의 약효와 부작용을 평가하고, 유효성을 검증하는 단계입니다. 단기투약에 따른 흔한 부작용, 약물동태 및 예상적응증에 대한 효능 효과에 대한 탐색을 위해 실시하는 것으로 대상질환 중 조건에 부합되는 환자를 대상으로 합니다. 임상3상 시험에 진입하기 위해 적응증과 최적용법 용량을 결정하는 단계입니다. |
|
임상2a상 (Pilot study) |
약효확인, 작용시간 및 유효용량 검토하는 단계로 효과의 증거를 찾는 것이 목적입니다. 반드시 허가기관이 인정하는 변수를 사용하지 않아도 되며, 설계측면에서 여러 디자인 사용이 가능하고, 피험자 수도 통계적 검정력에 의해 결정하지만 디자인에 따라 현실적 이유를 반영하여 결정됩니다. |
|
임상2b상 (Pivotal study) |
약효 입증, 용량-반응양상 검토, 최적의 용량 및 용법 결정하는 단계로 임상3상과 함께 허가의 핵심이 되는 단계입니다. 허가기관에서 인정하는 검증된 변수만을 사용해야 하고, 임상시험 디자인은 주로 평행군 시험으로 설계되며, 환자 수는 통계적 검정을 통해 결정됩니다. |
|
임상3상 |
신약의 유효성이 어느 정도 확립된 후에 대규모(최소 수백 명에서 수천 명) 환자들의 자료를 식약처에 제출하여 승인을 받아야 판매가 가능합니다. |
|
임상4상(PMS) (시판 후 안전성, 유효성 조사) |
신약이 시판 사용된 후 장기간의 효능과 안전성에 관한 사항을 평가하기 위한 시험으로, 시판 전 제한적인 임상시험에서 파악할 수 없었던 부작용이나 예상하지 못하였던 새로운 적응증을 발견하기 위한 약물역학적인 연구가 실시되는데 이것을 시판 후 조사(Post Market Surveillance)라고 합니다. |
|
유효성 |
의약품 등이 그 적응증에 대해서 효능 및 효과를 갖는 것 또는 그 정도를 의미합니다. |
|
안전성 |
의약품의 독성을 판단하는 것으로 그 사용용량과 투여방식에 있어 인체에 유해하지 않다는 것 또는 그 정도를 의미합니다. |
|
의약품 자료 독점권 |
데이터 독점권은 신약을 처음 개발한 혁신적인 회사를 보호하는 제도로 제네릭 또는 바이오시밀러를 개발하는 회사가 일정기간 동안 원개발사의 안전성, 유효성 자료 즉, 임상자료를 인용하지 못하도록 하는 제도입니다. 이럴 경우 후속개발자가 원개발사의 데이터 인용없이 의약품 허가를 받기 위해서는 임상을 수행해야 하기 때문에 경제적, 시간적 부담이 따르게 됩니다. 따라서 이 제도는 의약품 원개발사에게 유리한 제도입니다. |
|
작용기전 (MOA; Mode of Action) |
의약품이 효능을 나타내는 원리 및 치료 효능과 화학적 작용의 과정을 의미합니다. |
|
전임상시험 |
새로 개발한 신약후보물질을 사람에게 사용하기 전에 동물에게 사용하여 부작용이나 독성, 효과 등을 알아보는 시험입니다. 약물이 체내에 어떻게 흡수되어 분포되고 배설되는가를 연구하는 체내동태 연구와 약효약리 연구가 수행됩니다. 그 후 동물실험을 통해 시험약이 지니는 부작용 및 독성을 검색하는 안전성 평가를 진행하는 단계입니다. |
|
제형 |
약품을 인체에 투여하는 사용 목적이나 용도에 맞게 적절한 형태로 만든 물질을 의미합니다. (예: 정제, 캡슐제, 액제, 크림제, 주사제) |
|
적응증 |
어떠한 약제나 수술 등에 의하여 치료효과가 기대되는 질병이나 증상을 의미합니다. 의약품의 적응증은 회사가 어떤 약을 허가 받기 위해 여러 효능시험과 성적서와 관련 논문, 안전성 자료 등을 종합하여 식품의약품 안전처에 제출하면 승인된 부분에 한해서 적응증으로 사용할 수 있습니다. |
| 최종당화산물 (AGEs;advanced glycation end products) |
당화(Glycation)는 우리 몸, 피부 등에 있는 단백질(콜라겐, 엘라스틴), 핵산(DNA), 지질 등에 당(포도당glucose, 과당fructose)이 효소작용 없이( 비효소반응) 공유 결합하여 단백질(콜라겐, 엘라스틴), 핵산(nucleotides), 지질의 물성이 변하는 현상을 말하며 이때 생성되는 당화산물(AGE, advanced glycation end product) 은 축적되어 노화 및 질병(당뇨합병증, 동맥경화)의 유발 과정에 깊이 관여한다는 것이 알려있습니다. |
|
체내동태 (Pharmacokinetics, PK) |
생체 내 투여된 약물은 흡수되어 작용부위에 도달해 약효를 발현하고 생체 내에 분포합니다. 그리고 간 등에서 분해(대사)되고 뇨중으로 배설되어 생체로부터 소실됩니다. 이러한 약물의 생체 내 이행과 변화의 과정을 약물의 체내동태라고 합니다. |
|
합성의약품 신약 |
화학적 합성에 의하여 생산되는 의약품으로 바이오의약품과 비교 시 QC 관리가 용이하고 생산단가가 저렴한 것이 특징입니다. |
| 혈액-뇌 장벽 (BBB; Blood-Brain Barrier) |
뇌-혈관장벽은 뇌와 혈액을 보다 격리시키는 혈관 장벽으로 높은 선택적 투과성을 갖고 있어 뇌를 포함한 중추신경계의 조절기능을 세균 등과 같은 혈액으로 운반될 수 있는 병원체와 혈액 내의 잠재적인 위험 물질로부터 격리시키는 역할을 합니다. 또한, 생체항상성을 조절하고 뇌기능에 필수적인 물질들을 선택적으로 뇌속으로 전달하는 기능을 합니다. |
|
혈관 투여(IV) (Intravenous Injection) |
치료제를 정맥주사를 통해 주입하는 방법을 의미합니다. |
| ALI (acute lung injury) |
급성폐손상을 의미합니다. |
| Amigo2-PDK1 | Amigo2의 세포질 도메인과 PDK-1의 PH 도메인과의 결합을 의미합니다. |
| Ang-2 (Angiopoietin-2) |
신생혈관의 혈관성장인자를 의미합니다. |
| ARDS (Acute respiratory distress syndrome) |
급성호흡곤란증후군을 의미합니다. |
|
CDA |
기밀 공개 계약을 의미하며 독점정보를 보호하고 당사자들이 일정기간 동안 정보를 기말로 유지하도록 구속하는 법적 계약입니다. |
|
CRO: 임상시험수탁기관 |
제약회사가 신약개발에 드는 비용을 절감하기 위해 임상시험 연구를 아웃소싱하는 기관으로 임상시험수탁기관은 신약개발 단계에서 제약사의 의뢰를 받아 임상시험 진행의 설계, 컨설팅, 모니터링, 데이터 관리, 허가 대행 등의 업무를 대행해 주는 기관을 말합니다. |
|
CMO: 위탁제조기관 (Contract Manufacturing Organization ) |
위탁 받은 제품을 생산해 주는 기업으로 바이오, 제약부문에서 주로 사용되는 용어입니다. 의약품 대량생산시설을 갖추고 있지 않거나 생산역량이 부족할 때 경영효율화를 위하여 바이오·제약 기업은 CMO를 활용함으로써 공장 건설에 필요한 초기투자 비용을 아끼고 생산원가를 낮출 수 있습니다. |
| CNV (Choroidal Neovascularization) |
안구내 맥락막 신생혈관을 의미합니다. |
| cGMP (Current Good Manufacturing Practice) |
강화된 의약품 제조 및 품질관리기준으로 미국 FDA가 인정하는 의약품 품질관리 기준입니다. |
|
Drug Repositioning (신약재창출) |
기존에 나와 있는 약물이 다른 질환에 쓰일 수 있게 하는 것으로, ‘약물 재창출’이라고 합니다. 이는 이미 출시된 약의 새로운 기전을 찾아 새로운 증상에 대해 쓰일 수 있도록 개발을 진행하는 전략입니다. |
| DMF (Dimethyl Fumarate) |
푸마린산에 메틸에스터기가 붙은 물질을 의미합니다. |
|
FDA |
미국의 식품의약국이며 미국 내에서 생산되는 식품·의약품·화장품 뿐만 아니라 수입품과 일부 수출품의 효능과 안전성을 주로 관리하고 있습니다. 또한 FDA는 전세계적으로 가장 엄격하고 신중한 시판승인 결정을 내리는 것으로 유명하기 때문에 세계적으로 공신력을 인정받고 있습니다. 참고로 한국 식약처는 MFDS, 중국 식약처는 CFDA 라고 합니다. |
|
EMA |
유럽연합(EU)을 통해 설립된 유럽식약청이며, 유럽연합(EU) 소속 국가들의 의약품관련 규제를 맞추고 관리·감독하는 기관입니다. 의약품 시판승인과 관련하여 미국의 FDA와 비슷한 수준의 엄격한 기준을 가지고 있으며 그 공신력 또한 인정받고 있습니다. |
|
First-in-Class 신약 (혁신 신약) |
기존에 치료제가 없는 질병을 고치는 신약이거나 특정 질환에 사용되는 약품이 있지만 기존의 약물과 비교 시 효능, 독성 면이 개선된 약물을 의미합니다. 질병을 일으키는 단백질을 밝혀내고 이를 치유하는 최적의 물질을 찾아 동물실험을 하는 전임상, 안전성과 약효를 검증하는 임상 1·2·3상 단계를 거쳐 각국의 식약처에서 의약품으로 승인받은 신약을 의미합니다. |
|
GLP: 우수 실험실 관리기준 |
의약품, 화장품 등의 안전성 평가를 위해 실시하는 각종 독성 시험의 신뢰성을 보증하기 위한 기준으로 '비임상시험 관리 기준’ 또는 '우수 실험실 운영기준' 이라고도 합니다. 식약처로부터 적격성을 승인 받아야 GLP기관의 자격이 부여됩니다. |
|
GCP: 임상시험 실시 기준 |
인체를 대상으로 하는 시험의 안전성 및 유효성 검증 절차를 규정하는 기준으로 시험결과에 대한 신뢰성 뿐만 아니라 시험 대상자의 인권보호 등 임상시험이 윤리적인 배려 하에 과학적으로 시행되도록 국가가 정한 기준을 말합니다. |
|
GMP: 우수의약품 제조관리기준 |
의약품의 안정성과 유효성을 확보하기 위해 준수해야 하는 우수 의약품의 제조 관리 기준, 우리나라의 KGMP, 미국의 cGMP(Current Good Manufacturing Practice)와 유럽 EU GMP(또는 who GMP) 등 국가별 GMP규정을 두고 운영하고 있으며, 식약처의 실사 및 정기적 관리보고를 통해 적격성을 승인받아야 자격이 부여 됩니다. |
|
IVT 주사 (Intravitreal Injection) |
안구 내 약물 전달을 위해 유리체 내에 약물을 직접 주사하는 방법을 의미합니다. |
| I/R injury (ischemia-reperfusion injury) |
허혈/재관류 손상. 막힌 혈관을 재관류할 때 허혈조직으로의 혈류 회복과 산소화로 더 많은 조직 손상을 초래하는 현상입니다. |
| IBD (Inflammatory bowel disease) |
만성염증성 장염을 의미합니다. 발병의 원인은 불명확하며 궤양성대장염과 크론병이 있습니다. |
|
IND 신청: 임상시험계획 승인 신청 (IND; Investigational New Drug application) |
인체를 대상으로 한 안전성·유효성 자료 수집을 목적으로 해당 의약품을 사용하여 임상시험을 실시하고자 하는 자가 식약처에 승인을 신청하는 과정으로 신약개발의 경우 반드시 허가당국의 승인이 있어야 진행할 수 있습니다. |
|
MTA |
물질이전계약을 의미하며 수신자가 자신의 연구목적으로 사용하려는 경우 두 조직간이 유형연구자료 혹은 물질을 이전하기 위해 체결하는 계약입니다. |
|
MFDS (한국 식품의약품안전처, |
식품과 의약품에 관해 임상실험이나 안전검증 등을 하여 국민들의 건강에 유익하거나 유해한 식품, 의약품을 분류, 고시, 단속하는 등의 업무를 수행합니다. |
| NASH (Non-alcoholic steatohepatitis) |
비알콜성지방간염을 의미합니다. |
| Nrf2 (Nuclear factor erythroid 2-related factor 2) |
다양한 항산화 유전자들을 증가시킴으로써 세포 방어 기전에 중요한 역할을 담당하는 물질입니다. |
|
NCD 자료공개 |
기밀이 아닌 데이터의 자료공개를 의미합니다. |
|
NDA |
비공개 계약을 의미합니다. |
| SGLT2 (Sodium glucose co-transporter 2) |
나트륨 / 포도당 공동 수송체 2를 의미하며, 신세뇨관에서 포도당이 재흡수되어 혈류 내로 들어가는데 이용됩니다. |
| TGF-β (전환성장인자 베타, Transforming growth factor-beta) |
상피세포와 조혈세포의 성장, 이동, 분화 및 사멸 등을 조절하여 세포의 성장과 고사를 통한 생물의 항상성 유지에 기본이 되는 세포 성장인자이며, 당뇨 병성 신증에서 TGF-β에 의해 활성화되어 혈관간세포가 콜라겐을 형성하는데 중요한 역할을 하는 것으로 알려져 있습니다. |
| TNF-α (tumor necrosis factor alpha) |
염증반응에 포함되고 급성기 반응의 구성원인 사이토카인입니다. TNF-α는 주로 활성화된 대식세포에 의해 분비되는데, 보조 T 세포, 자연살해세포, 그리고 손상된 뉴런 등의 다양한 세포에서도 분비됩니다. |
| TPH1 (Tryptophan Hydroxylase 1) |
혈관수축작용을 하는 물질인 세로토닌을 합성하는데 관여하는 효소입니다. |
| VEGF (vascular endothelial) |
혈관내피세포에 특이적으로 작용하여 세포 증식이나 혈관신생을 촉진하는 당단백입니다. |
III. 재무에 관한 사항
1. 요약재무정보
당사는 기업공시서식 작성기준에 따른 소규모기업에 해당하여 '요약재무정보' 를 기재하지 아니합니다. 다음의 재무제표 본문을 참고하시기 바랍니다.
2. 연결재무제표
당사는 보고서 작성기준일 현재 해당사항이 없습니다.
3. 연결재무제표 주석
당사는 보고서 작성기준일 현재 해당사항이 없습니다.
4. 재무제표
4-1. 재무상태표
|
재무상태표 |
|
제 8 기 3분기말 2023.09.30 현재 |
|
제 7 기말 2022.12.31 현재 |
|
(단위 : 원) |
|
제 8 기 3분기말 |
제 7 기말 |
|
|---|---|---|
|
자산 |
||
|
유동자산 |
48,674,118,015 |
33,406,557,981 |
|
현금및현금성자산 |
11,529,957,430 |
8,510,611,529 |
|
단기금융상품 |
28,000,000,000 |
20,000,000,000 |
|
매출채권 |
3,181,284,848 |
888,710,035 |
|
기타투자자산 |
2,992,831,699 |
3,073,466,867 |
|
기타유동금융자산 |
275,397,503 |
220,978,801 |
|
기타유동자산 |
1,095,866,132 |
563,470,010 |
|
계약자산 |
1,598,780,403 |
149,320,739 |
|
비유동자산 |
23,822,096,075 |
22,250,914,726 |
|
유형자산 |
20,722,682,386 |
21,021,608,835 |
|
무형자산 |
337,472,959 |
321,619,982 |
|
사용권자산 |
116,984,872 |
150,162,088 |
|
기타비유동투자자산 |
1,300,864,000 |
300,160,000 |
|
기타비유동금융자산 |
25,689,251 |
50,374,936 |
|
기타비유동자산 |
466,481,449 |
406,988,885 |
|
순확정급여자산 |
||
|
파생상품금융자산 |
851,921,158 |
|
|
자산총계 |
72,496,214,090 |
55,657,472,707 |
|
부채 |
||
|
유동부채 |
1,537,095,893 |
1,370,678,057 |
|
유동 리스부채 |
76,541,962 |
44,043,015 |
|
기타 유동부채 |
45,964,080 |
67,833,320 |
|
기타유동금융부채 |
1,414,589,851 |
1,258,801,722 |
|
비유동부채 |
23,298,783,328 |
8,116,067,674 |
|
장기차입금 |
8,000,000,000 |
8,000,000,000 |
|
전환사채 |
8,966,844,139 |
|
|
순확정급여부채 |
163,627,974 |
9,348,328 |
|
비유동 리스부채 |
41,573,606 |
106,719,346 |
|
파생상품금융부채 |
6,126,737,609 |
|
|
부채총계 |
24,835,879,221 |
9,486,745,731 |
|
자본 |
||
|
자본금 |
6,927,671,000 |
6,922,984,000 |
|
보통주자본금 |
6,927,671,000 |
6,922,984,000 |
|
자본잉여금 |
101,359,651,614 |
101,263,129,602 |
|
주식발행초과금 |
101,359,651,614 |
101,263,129,602 |
|
기타자본구성요소 |
9,905,666,780 |
2,597,450,326 |
|
주식선택권 |
3,841,712,547 |
2,597,450,326 |
|
전환권대가 |
6,063,954,233 |
|
|
이익잉여금(결손금) |
(70,532,654,525) |
(64,612,836,952) |
|
미처분이익잉여금(미처리결손금) |
(70,532,654,525) |
(64,612,836,952) |
|
자본총계 |
47,660,334,869 |
46,170,726,976 |
|
자본과부채총계 |
72,496,214,090 |
55,657,472,707 |
4-2. 포괄손익계산서
|
포괄손익계산서 |
|
제 8 기 3분기 2023.01.01 부터 2023.09.30 까지 |
|
제 7 기 3분기 2022.01.01 부터 2022.09.30 까지 |
|
(단위 : 원) |
|
제 8 기 3분기 |
제 7 기 3분기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
영업수익 |
2,265,810,125 |
9,021,888,345 |
873,400,880 |
2,544,237,804 |
|
영업비용 |
5,701,726,715 |
15,242,779,934 |
2,842,399,380 |
10,354,937,777 |
|
영업이익(손실) |
(3,435,916,590) |
(6,220,891,589) |
(1,968,998,500) |
(7,810,699,973) |
|
기타수익 |
17,376,060 |
75,637,223 |
589,459 |
8,795,580 |
|
기타비용 |
358,889 |
2,703,502 |
737,624 |
57,805,923 |
|
금융수익 |
491,111,711 |
1,102,717,518 |
649,208,340 |
1,340,659,091 |
|
금융비용 |
580,578,652 |
872,603,518 |
72,766,534 |
206,459,860 |
|
법인세비용차감전순이익(손실) |
(3,508,366,360) |
(5,917,843,868) |
(1,392,704,859) |
(6,725,511,085) |
|
법인세비용(수익) |
||||
|
당기순이익(손실) |
(3,508,366,360) |
(5,917,843,868) |
(1,392,704,859) |
(6,725,511,085) |
|
기타포괄손익 |
(174,836) |
(1,973,705) |
(3,678,271) |
(10,626,322) |
|
당기손익으로 재분류되지 않는항목(세후기타포괄손익) |
(174,836) |
(1,973,705) |
(3,678,271) |
(10,626,322) |
|
확정급여제도의 재측정손익(세후기타포괄손익) |
(174,836) |
(1,973,705) |
(3,678,271) |
(10,626,322) |
|
당기손익으로 재분류될 수 있는 항목(세후기타포괄손익) |
||||
|
총포괄손익 |
(3,508,541,196) |
(5,919,817,573) |
(1,396,383,130) |
(6,736,137,407) |
|
주당이익 |
||||
|
기본주당이익(손실) (단위 : 원) |
(253) |
(427) |
(101.00) |
(489.00) |
|
희석주당이익(손실) (단위 : 원) |
||||
4-3. 자본변동표
|
자본변동표 |
|
제 8 기 3분기 2023.01.01 부터 2023.09.30 까지 |
|
제 7 기 3분기 2022.01.01 부터 2022.09.30 까지 |
|
(단위 : 원) |
|
자본 |
|||||
|---|---|---|---|---|---|
|
자본금 |
자본잉여금 |
기타자본구성요소 |
이익잉여금 |
자본 합계 |
|
|
2022.01.01 (기초자본) |
6,843,734,000 |
99,848,101,817 |
1,649,973,752 |
(53,325,056,573) |
55,016,752,996 |
|
당기순이익(손실) |
(6,725,511,085) |
(6,725,511,085) |
|||
|
기타포괄손익 |
(10,626,322) |
(10,626,322) |
|||
|
주식선택권 부여 |
|||||
|
주식선택권 행사 |
51,250,000 |
986,780,448 |
687,739,216 |
1,725,769,664 |
|
|
전환사채 발행 |
|||||
|
주식기준보상거래에 따른 증가(감소), 지분 |
|||||
|
2022.09.30 (기말자본) |
6,894,984,000 |
100,834,882,265 |
2,337,712,968 |
(60,061,193,980) |
50,006,385,253 |
|
2023.01.01 (기초자본) |
6,922,984,000 |
101,263,129,602 |
2,597,450,326 |
(64,612,836,952) |
46,170,726,976 |
|
당기순이익(손실) |
(5,917,843,868) |
(5,917,843,868) |
|||
|
기타포괄손익 |
(1,973,705) |
(1,973,705) |
|||
|
주식선택권 부여 |
1,289,192,433 |
1,289,192,433 |
|||
|
주식선택권 행사 |
4,687,000 |
96,522,012 |
(44,930,212) |
(56,278,800) |
|
|
전환사채 발행 |
6,063,954,233 |
6,063,954,233 |
|||
|
주식기준보상거래에 따른 증가(감소), 지분 |
|||||
|
2023.09.30 (기말자본) |
6,927,671,000 |
101,359,651,614 |
9,905,666,780 |
(70,532,654,525) |
47,660,334,869 |
4-4. 현금흐름표
|
현금흐름표 |
|
제 8 기 3분기 2023.01.01 부터 2023.09.30 까지 |
|
제 7 기 3분기 2022.01.01 부터 2022.09.30 까지 |
|
(단위 : 원) |
|
제 8 기 3분기 |
제 7 기 3분기 |
|
|---|---|---|
|
영업활동현금흐름 |
(8,050,063,346) |
(2,492,315,167) |
|
영업활동으로부터 창출된 현금흐름 |
(8,370,451,251) |
(2,648,141,505) |
|
이자수취 |
642,146,682 |
405,528,097 |
|
이자지급(영업) |
(288,383,557) |
(194,919,449) |
|
법인세환급(납부) |
(33,375,220) |
(54,782,310) |
|
투자활동현금흐름 |
(9,027,321,790) |
(2,809,465,294) |
|
투자활동으로 인한 현금유입액 |
56,126,990,693 |
25,346,635,573 |
|
임차보증금의 감소 |
13,980,000 |
245,086,800 |
|
당기손익공정가치측정 금융자산의 감소 |
7,101,228,874 |
25,037,100,000 |
|
상각후원가측정 금융자산의 감소 |
25,726,962 |
|
|
장단기금융상품의 감소 |
49,000,000,000 |
31,552,741 |
|
유형자산의 처분 |
11,781,819 |
7,139,070 |
|
기타보증금의 감소 |
30,000 |
|
|
투자활동으로 인한 현금유출액 |
(65,154,312,483) |
(28,156,100,867) |
|
임차보증금의 증가 |
(20,026,000) |
|
|
당기손익공정가치측정금융자산의 증가 |
(7,000,000,000) |
(24,994,508,850) |
|
기타포괄손익공정가치측정금융자산의 증가 |
(1,000,704,000) |
|
|
장단기금융상품의 증가 |
(57,000,000,000) |
(1,623,917) |
|
유형자산의 취득 |
(82,042,364) |
(3,052,773,783) |
|
기타보증금의 증가 |
(860,000) |
|
|
무형자산의 취득 |
(9,000,000) |
(86,308,317) |
|
장기선급금의 증가 |
(62,566,119) |
|
|
재무활동현금흐름 |
19,818,457,980 |
486,229,500 |
|
재무활동으로 인한 현금유입액 |
56,278,800 |
547,075,400 |
|
상환기술료 관련 보조금 수령액 |
||
|
주식선택권의 행사 |
56,278,800 |
547,075,400 |
|
재무활동으로 인한 현금유출액 |
19,762,179,180 |
(60,845,900) |
|
리스부채의 상환 |
(37,500,820) |
(60,845,900) |
|
전환사채의 발행 |
19,799,680,000 |
|
|
현금및현금성자산의순증가(감소) |
2,741,072,844 |
(4,815,550,961) |
|
외화표시현금및현금성자산의 환율변동효과 |
278,273,057 |
814,459,603 |
|
기초현금및현금성자산 |
8,510,611,529 |
10,441,591,400 |
|
기말현금및현금성자산 |
11,529,957,430 |
6,440,500,042 |
5. 재무제표 주석
주석
| 제 8 (당)기 3분기 2023년 09월 30일 현재 |
| 제 7 (전)기 3분기 2022년 09월 30일 현재 |
| 주식회사 큐라클 |
1. 일반사항
주식회사 큐라클(이하 "당사"라고 함)은 2016년 5월 12일 설립되어, 의학 및 약학 연구개발업을 주요 사업으로 영위하고 있으며, 2021년 7월 22일자로 코스닥시장에 주식을 상장한 공개법인입니다. 당사의 본점은 서울특별시 서초구 효령로 23-1(방배동,큐라클빌딩)에 소재하고 있으며, 대표이사는 유재현입니다.
당분기말 현재 당사의 주요 주주 현황은 다음과 같습니다.
| 주주명 | 보통주 | |
|---|---|---|
| 주식수(주) | 지분율(%) | |
| 권영근 | 1,809,047 | 13.06 |
| 이인규 | 1,053,780 | 7.61 |
| 김태윤 | 470,880 | 3.40 |
| 박광락 | 425,800 | 3.07 |
| 장덕수 | 343,605 | 2.48 |
| 김명화 | 215,357 | 1.55 |
| 넥시드-어니스트 제1호 투자조합 | 152,716 | 1.10 |
| 스마트혁신산업단지 제1호 투자조합 | 151,420 | 1.09 |
| 기타주주 | 9,232,737 | 66.64 |
| 합계 | 13,855,342 | 100.00 |
2. 중요한 회계정책
당사의 분기재무제표는 한국채택국제회계기준(이하 "기업회계기준")에 따라 작성되는 요약중간재무제표입니다. 동 재무제표는 기업회계기준서 제1034호 '중간재무보고'에 따라 작성되었으며, 연차재무제표에서 요구되는 정보에 비하여 적은 정보를 포함하고 있습니다. 선별적 주석은 직전 연차보고기간말 후 발생한 회사의 재무상태와 경영성과의 변동을 이해하는데 유의적인 거래나 사건에 대한 설명을 포함하고 있습니다.
분기재무제표는 매 보고기간말에 공정가치로 측정되는 금융자산 및 금융부채를 제외하고는 역사적 원가에 기초하여 작성하였습니다.
기업회계기준은 중간재무제표 작성시 중요한 회계추정의 사용을 허용하고 있으며, 회계정책을 적용함에 있어 경영진의 판단을 요구하고 있습니다. 보다 복잡하고 높은 수준의 판단이 필요한 부분이나 중요한 가정 및 추정이 필요한 부분은 주석 3에서 설명하고 있습니다.
2023년 1월 1일부터 시행되는 회계기준이 있으나, 그 기준들은 당사의 재무제표에 중요한 영향을 미치지 않으며, 이를 제외하고는 중간재무제표의 작성에 적용된 유의적 회계정책은 2022년 12월 31일로 종료하는 회계연도에 대한 연차재무제표 작성시채택한 회계정책과 동일합니다.
3. 중요한 회계추정 및 가정
중간재무제표 작성에는 미래에 대한 가정 및 추정이 요구되며 경영진은 당사의 회계정책을 적용하기 위해 판단이 요구됩니다. 추정 및 가정은 지속적으로 평가되며, 과거 경험과 현재의 상황에 비추어 합리적으로 예측가능한 미래의 사건을 고려하여 이루어집니다. 회계추정의 결과가 실제 결과와 동일한 경우는 드물 것이므로 중요한 조정을 유발할 수 있는 유의적인 위험을 내포하고 있습니다.
분기재무제표 작성을 위한 당사의 회계정책 적용과 추정 금액에 대한 경영진의 판단은 2022년 12월 31일로 종료하는 회계연도의 연차재무제표와 동일한 회계정책과 추정의 근거를 사용하였습니다.
4. 원가기준 투입법 적용 계약
(1) 당분기 및 전기의 계약잔액 및 영업수익 등의 내역은 다음과 같습니다.
① 당분기
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 |
기초 계약잔액 |
증감액 |
영업수익 |
분기말 계약잔액(*) |
| CU06-RE 임상시험 | - | 3,441,676 | 3,441,676 | - |
| CU06-RE 비임상시험 | - | 5,580,212 | 5,580,212 | - |
| 합 계 | - | 9,021,888 | 9,021,888 | - |
② 전기
| (단위: 천원) | ||||
|---|---|---|---|---|
| 전기 |
기초 계약잔액 |
증감액 |
영업수익 |
기말 계약잔액(*) |
| CU06-RE 임상시험 | 850,715 | 2,732,144 | 3,582,859 | - |
(*) 임상 2상 및 비임상 시험 용역 제공 수행의무를 통해 수행의무 결과를 합리적으로측정할 수없는 상황에서 투입되는 원가만큼 회수가 가능할 것으로 예상하고 있기 때문에, 계약잔액이 존재하지 않습니다.
(2) 당분기말 및 전기말 현재 진행중인 용역(보고기간 중 완료된 용역 포함)과 관련된 누적원가 등의 내역은 다음과 같습니다.
① 당분기말
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 누적원가 | 누적손익 | 계약자산 | 계약부채 |
| CU06-RE 임상시험 | 7,123,912 | 131,227 | 586,300 | - |
| CU06-RE 비임상시험(*) | 5,580,212 | - | 1,011,591 | - |
| 합 계 | 12,704,124 | 131,227 | 1,597,891 | - |
(*) Thea Open Innovation과의 기술이전계약을 비임상시험에 대한 비용까지 보전 받는 것으로 변경함에 따라 2022년도 이전까지 발생한 비용을 포함하고 있습니다.
② 전기말
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 누적원가 | 누적손익 | 계약자산 | 계약부채 |
| CU06-RE 임상시험 | 3,682,236 | 131,227 | 149,321 | - |
(3) 당분기 및 전기의 계약수익금액이 전기 매출액의 5% 이상인 수행의무별 정보는 다음과 같습니다.
① 당분기
| (단위: 천원) | |||||||
|---|---|---|---|---|---|---|---|
| 구분 | 수행의무 | 계약일 | 이행종료시점 | 진행률 | 계약수익 | 계약자산 | 계약부채 |
| CU06-RE | 임상 2상 시험 | 2021-10 | 2023년 이후 | (*) | 3,441,676 | 586,300 | - |
| 비임상 시험 | 2023-03 | 2023년 이후 | (*) | 5,580,212 | 1,011,591 | - | |
| 합계 | 9,021,888 | 1,597,891 | - | ||||
② 전기
| (단위: 천원) | |||||||
|---|---|---|---|---|---|---|---|
| 구분 | 수행의무 | 계약일 | 이행종료시점 | 진행률 | 계약수익 | 계약자산 | 계약부채 |
| CU06-RE 임상시험 |
임상 1상 시험 | 2021-10 | 2022년 | 100% | 850,715 | - | - |
| 임상 2상 시험 | 2021-10 | 2023년 이후 | (*) | 2,732,144 | 149,321 | - | |
| 합계 | 3,582,859 | 149,321 | - | ||||
(*) 당분기말 및 전기말 현재 임상 2상 및 비임상 시험 용역에 대한 수행의무의 결과를 합리적으로 측정할 수 없으나, 수행의무를 이행하는 동안에 드는 원가는 회수될 것으로 예상하여 발생원가의 범위에서 수익을 인식하고 있습니다.
5. 금융상품 공정가치
(1) 금융상품 종류별 공정가치
당분기말 및 전기말 현재 금융상품의 종류별 장부금액 및 공정가치는 다음과 같습니다.
|
(단위: 천원) |
||||
|
구분 |
당분기말 |
전기말 |
||
|
장부금액 |
공정가치 |
장부금액 |
공정가치 |
|
|
금융자산 |
||||
| 현금및현금성자산(*) | 11,529,957 | 11,529,957 | 8,510,612 | 8,510,612 |
| 매출채권(*) | 3,181,285 | 3,181,285 | 888,710 | 888,710 |
| 단기금융상품(*) | 28,000,000 | 28,000,000 | 20,000,000 | 20,000,000 |
| 당기손익공정가치측정금융자산 | 2,992,832 | 2,992,832 | 3,073,467 | 3,073,467 |
| 기타포괄손익공정가치측정금융자산 | 1,300,864 | 1,300,864 | 300,160 | 300,160 |
| 기타금융자산(*) | 301,087 | 301,087 | 271,354 | 271,354 |
| 파생상품자산 | 851,921 | 851,921 | - | - |
|
합계 |
48,157,946 | 48,157,946 | 33,044,303 | 33,044,303 |
|
금융부채 |
||||
| 전환사채 | 8,966,844 | 8,966,844 | - | - |
| 기타금융부채(*) | 1,414,590 | 1,414,590 | 1,258,802 | 1,258,802 |
| 리스부채(*) | 118,116 | 118,116 | 150,762 | 150,762 |
| 장기차입금(*) | 8,000,000 | 8,000,000 | 8,000,000 | 8,000,000 |
| 파생상품부채 | 6,126,738 | 6,126,738 | - | - |
|
합계 |
24,626,288 | 24,626,288 | 9,409,564 | 9,409,564 |
(*) 상각후원가로 측정되는 금융자산 및 금융부채로서 장부금액은 공정가치의 합리적인 근사치입니다.
(2) 공정가치 서열체계
공정가치로 측정되는 금융상품은 공정가치 서열체계에 따라 구분되며 정의된 수준들은 다음과 같습니다.
- 수준 1: 측정일에 동일한 자산이나 부채에 대한 접근가능한 활성시장의 조정되지 않은 공시가격
- 수준 2: 수준 1의 공시가격 이외에 자산이나 부채에 대해 직접적으로 또는 간접적으로 관측가능한 투입변수
- 수준 3: 자산이나 부채에 대한 관측가능하지 않은 투입변수
당분기말 및 전기말 현재 공정가치로 측정되는 금융상품의 공정가치 서열체계 구분은 다음과같습니다.
| (단위: 천원) | ||||
| 당분기말 | 수준 1 | 수준 2 | 수준 3 | 합계 |
| 금융자산 | ||||
| 당기손익공정가치측정금융자산 | - | 2,992,832 | - | 2,992,832 |
| 기타포괄손익공정가치측정금융자산 | - | - | 1,300,864 | 1,300,864 |
| 파생상품자산 | - | - | 851,921 | 851,921 |
| 금융부채 | ||||
| 파생상품부채 | - | - | 6,126,738 | 6,126,738 |
|
(단위: 천원) |
||||
|
전기말 |
수준 1 |
수준 2 |
수준 3 |
합계 |
| 금융자산 | ||||
| 당기손익공정가치측정금융자산 | - | 3,073,467 | - | 3,073,467 |
| 기타포괄손익공정가치측정금융자산 | - | - | 300,160 | 300,160 |
(3) 반복적인 공정가치 측정치의 서열체계 수준 간 이동
당사는 공정가치 서열체계의 수준 간 이동을 보고기간말에 인식하며 각 공정가치 서열체계의 수준 간 이동 내역은 없습니다.
(4) 반복적인 측정치의 수준 3의 변동 내역
당분기 및 전기의 반복적인 측정치의 수준 3의 변동 내역은 다음과 같습니다.
|
(단위: 천원) |
||||
|---|---|---|---|---|
|
구분 |
당분기 |
전기 |
||
| 기타포괄손익 공정가치측정금융자산 |
파생상품자산 | 파생상품부채 | 기타포괄손익 공정가치측정금융자산 |
|
|
기초금액 |
300,160 | - | - | - |
| 취득 | 1,000,704 | 851,921 | 6,126,738 | 300,160 |
|
평가이익(손실) 인식액 |
- | - | - | - |
|
기말금액 |
1,300,864 | 851,921 | 6,126,738 | 300,160 |
(5) 가치평가기법 및 투입변수
① 당분기말 및 전기말 현재 재무상태표에서 공정가치로 측정되는 자산,부채 중 공정가치 서열체계 수준 2로 분류된 항목의 가치평가기법과 투입변수는 다음과 같습니다.
| (단위: 천원) | |||||
| 당분기말 | 공정가치 | 수준 | 가치평가기법 | 투입변수 | 투입변수 범위 |
| 당기손익공정가치측정금융자산 | |||||
| 수익증권 및 펀드 | 2,992,832 | 2 | 시장접근법 | 기초자산가격 | - |
| (단위: 천원) | |||||
| 전기말 | 공정가치 | 수준 | 가치평가기법 | 투입변수 | 투입변수 범위 |
| 당기손익공정가치측정금융자산 | |||||
| 수익증권 및 펀드 | 3,073,467 | 2 | 시장접근법 | 기초자산가격 | - |
② 당분기말 및 전기말 현재 재무상태표에서 공정가치로 측정되는 자산, 부채 중 공정가치 서열체계 수준 3으로 분류된 항목의 가치평가기법과 투입변수는 다음과 같습니다.
| (단위: 천원) | |||||
| 당분기말 | 공정가치 | 수준 | 가치평가기법 | 투입변수 | 투입변수 범위 |
| 당기손익공정가치측정금융자산 | |||||
| 파생상품자산 | 851,921 | 3 | 이항모형 | 할인율 | 3.49% ~ 3.63% |
| 주가변동성 | 40.61% | ||||
| 기타포괄손익공정가치측정금융자산 | |||||
| 비상장주식 | 1,300,864 | 3 | 원가접근법 | 기초자산가격 | - |
| 당기손익공정가치측정금융부채 | |||||
| 파생상품부채 | 6,126,738 | 3 | 이항모형 | 할인율 | 3.49% ~ 3.63% |
| 주가변동성 | 40.61% | ||||
| (단위: 천원) | |||||
| 전기말 | 공정가치 | 수준 | 가치평가기법 | 투입변수 | 투입변수 범위 |
| 기타포괄손익공정가치측정금융자산 | |||||
| 비상장주식 | 300,160 | 3 | 원가접근법 | 기초자산가격 | - |
(6) 수준 3으로 분류된 공정가치 측정치의 가치평가과정
당사는 재무보고 목적의 공정가치 측정을 담당하는 담당자가 있으며, 이러한 공정가치 측정치는 수준 3으로 분류되는 공정가치 측정치를 포함하고 있습니다. 공정가치 측정 담당자는 당사의 재무담당이사와 감사에 직접 보고하며 매기 보고일정에 맞추어 공정가치 평가과정 및 그 결과에 대해 재무담당이사 및 감사와 협의합니다.
6. 범주별 금융상품
(1) 당분기말 및 전기말 현재 금융자산 내역은 다음과 같습니다.
|
(단위: 천원) |
||||
|
구분 |
당분기말 |
전기말 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
|
상각후원가측정금융자산 |
||||
|
현금및현금성자산 |
11,529,957 | - | 8,510,612 | - |
| 매출채권 | 3,181,285 | - | 888,710 | - |
|
장단기금융상품 |
28,000,000 | - | 20,000,000 | - |
|
기타금융자산 |
275,398 | 25,689 | 220,979 | 50,375 |
|
소계 |
42,986,640 | 25,689 | 29,620,301 | 50,375 |
| 당기손익공정가치측정금융자산 | ||||
| 기타투자자산 | 2,992,832 | - | 3,073,467 | - |
| 파생상품자산 | - | 851,921 | - | - |
| 소계 | 2,992,832 | 851,921 | 3,073,467 | - |
| 기타포괄손익공정가치측정금융자산 | ||||
| 기타투자자산 | - | 1,300,864 | - | 300,160 |
|
합계 |
45,979,472 | 2,178,474 | 32,693,768 | 350,535 |
(2) 당분기말 및 전기말 현재 금융부채 내역은 다음과 같습니다.
|
(단위: 천원) |
||||
|
구분 |
당분기말 |
전기말 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
|
상각후원가측정금융부채 |
||||
|
차입금 |
- | 8,000,000 | - | 8,000,000 |
| 전환사채 | - | 8,966,844 | - | - |
| 리스부채 | 76,542 | 41,574 | 44,043 | 106,719 |
|
기타금융부채 |
1,414,590 | - | 1,258,802 | - |
| 소계 | 1,491,132 | 17,008,418 | 1,302,845 | 8,106,719 |
| 당기손익공정가치측정금융부채 | ||||
| 파생상품부채 | - | 6,126,738 | - | - |
|
합계 |
1,491,132 | 23,135,156 | 1,302,845 | 8,106,719 |
(3) 당분기 및 전분기의 금융상품 범주별 순손익 정보는 다음과 같습니다.
|
(단위: 천원) |
||||
|
구분 |
당분기 |
전분기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
|
당기손익공정가치측정금융자산 |
||||
| 평가이익 | 2,605 | 14,028 | 1,800 | 20,300 |
| 평가손실 | (9,773) | (9,773) | (300) | (3,700) |
| 처분이익 | 88 | 16,339 | 35,657 | 35,657 |
|
상각후원가측정금융자산 |
||||
| 이자수익 | 283,967 | 606,998 | 83,488 | 313,947 |
| 외화환산이익 | 172,250 | 306,248 | 469,835 | 814,460 |
| 외환차익 | 27,899 | 125,638 | 149,841 | 154,535 |
| 외화환산손실 | 22,322 | (2,627) | - | - |
|
상각후원가측정금융부채 |
||||
| 이자비용 | (552,614) | (779,670) | (76,124) | (201,827) |
| 잡이익(임차료 할인) | - | - | (302) | 4,998 |
| 외환차손 | (42,646) | (80,533) | (432) | (933) |
| 외화환산손실 | 2,133 | - | (4,089) | - |
| 외환차익 | 3,486 | 23,547 | (89,406) | - |
| 외화환산이익 | 815 | 815 | (2,006) | 1,760 |
7. 사용제한 금융상품
당분기말 및 전기말 현재 사용이 제한된 금융상품은 다음과 같습니다.
| (단위: 천원) | ||
| 구분 | 당분기말 | 전기말 |
| 보통예금(*) | 1 | 1 |
(*) 정부로부터 수령한 연구개발비 보조금으로 연구개발비 용도로 사용이 제한되어 있습니다(주석8 참조).
8. 정부보조금
(1) 당분기말 현재 개발과제 등과 관련하여 수령한 정부보조금은 없습니다.
(2) 당분기말 및 전기말 현재 정부보조금의 미사용잔액은 없습니다.
(3) 당분기의 정부보조금 변동내역은 없습니다.
(4) 전분기의 정부보조금 변동내역은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구분 | 기초금액 | 수령금액 | 사용금액 | 기말금액 | |
| 자산취득 | 비용보전 등 | ||||
| 바이오의료기술개발사업 | - | 113,689 | - | (113,689) | - |
| 고경력연구인력채용지원사업 | 45,745 | - | - | (33,247) | 12,498 |
| 합계 | 45,745 | 113,689 | - | (146,936) | 12,498 |
9. 유형자산
(1) 당분기 및 전분기의 유형자산 변동 내역은 다음과 같습니다.
① 당분기
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구분 | 기초 | 취득 | 처분 | 감가상각비 | 기타(*) | 분기말 |
| 토지 | 16,379,631 | - | - | - | - | 16,379,631 |
| 건물 | 3,023,789 | - | - | (57,780) | - | 2,966,009 |
| 기계장치 | 1,324,310 | 19,350 | (359) | (279,645) | 102,500 | 1,166,156 |
| (정부보조금) | (8,361) | - | - | 3,447 | - | (4,914) |
| 비품 | 239,500 | 7,492 | - | (45,315) | - | 201,677 |
| 차량운반구 | - | - | (13,721) | (232) | 13,953 | - |
| 리스개량자산 | 2,240 | - | - | (1,317) | - | 923 |
| 건설중인자산 | 60,500 | 55,200 | - | - | (102,500) | 13,200 |
| 합계 | 21,021,609 | 82,042 | (14,080) | (380,842) | 13,953 | 20,722,682 |
(*) 건설중인자산의 본계정대체 및 선급금에서 대체된 13,953천원으로 구성되어 있습니다.
② 전분기
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구분 | 기초 | 취득 | 처분 | 감가상각비 | 기타(*) | 분기말 |
| 토지 | 16,379,631 | - | - | - | - | 16,379,631 |
| 건물 | - | 3,000 | - | (31,978) | 3,078,569 | 3,049,591 |
| 기계장치 | 562,463 | 149,053 | (17,442) | (151,358) | 609,539 | 1,152,255 |
| (정부보조금) | (14,583) | - | 1,324 | 3,714 | - | (9,545) |
| 시설장치 | 47,139 | - | (40,439) | (6,700) | - | - |
| 비품 | 51,787 | 142,922 | (4,001) | (20,994) | 67,780 | 237,494 |
| 리스개량자산 | 2,853 | - | - | (458) | - | 2,395 |
| 건설중인자산 | 1,025,589 | 2,757,799 | - | - | (3,755,888) | 27,500 |
| 합계 | 18,054,879 | 3,052,774 | (60,558) | (207,774) | - | 20,839,321 |
(*) 건설중인자산의 본계정대체로 구성되어 있습니다.
(2) 당분기말 현재 유형자산 담보제공내역은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구분 | 장부금액 | 담보설정금액 | 관련 계정과목 | 관련 차입금 | 담보권자 |
| 토지 | 16,379,631 | 9,600,000 | 차입금 (주석12) |
8,000,000 | 하나은행 |
| 건물 | 2,966,009 | ||||
10. 무형자산
당분기 및 전분기의 무형자산 변동 내역은 다음과 같습니다.
① 당분기
|
(단위: 천원) |
|||||
|---|---|---|---|---|---|
|
구분 |
기초 |
취득 |
상각비 |
대체(*) |
분기말 |
| 특허권 | 90,279 | - | (24,013) | 71,505 | 137,771 |
| 전용실시권 | 129,876 | - | (31,392) | - | 98,484 |
| 소프트웨어 | 27,784 | 9,000 | (7,866) | - | 28,918 |
| 상표권 | 5,681 | - | (1,381) | - | 4,300 |
| 회원권 | 68,000 | - | - | - | 68,000 |
| 합계 | 321,620 | 9,000 | (64,652) | 71,505 | 337,473 |
(*) 장기선급금에서 대체된 금액입니다.
② 전분기
|
(단위: 천원) |
||||
|
구분 |
기초 |
취득 |
상각비 |
분기말 |
| 특허권 | 42,113 | 35,969 | (11,308) | 66,774 |
| 전용실시권 | 101,345 | 45,839 | (25,856) | 121,328 |
| 소프트웨어 | 32,424 | 4,500 | (6,705) | 30,219 |
| 상표권 | 7,524 | - | (1,382) | 6,142 |
| 회원권 | 68,000 | - | - | 68,000 |
| 합계 | 251,406 | 86,308 | (45,251) | 292,463 |
11. 리스
당사가 리스이용자인 경우의 리스에 대한 정보는 다음과 같습니다.
(1) 당분기 및 전분기의 사용권자산 변동 내역은 다음과 같습니다.
① 당분기
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구분 | 기초 | 취득 | 처분 | 감가상각비 | 분기말 |
| 차량운반구 | 150,162 | - | - | (33,177) | 116,985 |
② 전분기
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구분 | 기초 | 취득 | 처분 | 감가상각비 | 분기말 |
| 건물 | 57,516 | - | (2,934) | (54,582) | - |
| 차량운반구 | 178,248 | - | - | (38,604) | 139,644 |
| 합계 | 235,764 | - | (2,934) | (93,186) | 139,644 |
(2) 재무상태표에 인식된 금액
당분기말 및 전기말 현재 리스와 관련해 재무상태표에 인식된 금액은 다음과 같습니다.
① 사용권자산
|
(단위: 천원) |
||
|
구분 |
당분기말 |
전기말 |
| 사용권자산 | ||
|
차량운반구 |
116,985 | 150,162 |
② 리스부채
|
(단위: 천원) |
||
|
구분 |
당분기말 |
전기말 |
|
리스부채 |
||
|
유동 |
76,542 | 44,043 |
|
비유동 |
41,574 | 106,719 |
|
합계 |
118,116 | 150,762 |
당분기 및 전분기 중 증가된 사용권자산은 없습니다.
(3) 포괄손익계산서에 인식된 금액
당분기 및 전분기 중 리스와 관련해서 포괄손익계산서에 인식된 금액은 다음과 같습니다.
|
(단위: 천원) |
||||
|---|---|---|---|---|
|
구분 |
당분기 |
전분기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
|
사용권자산의 감가상각비 |
||||
|
건물 |
- | - | - | 54,583 |
|
차량운반구 |
9,024 | 33,177 | 15,876 | 41,538 |
|
합계 |
9,024 | 33,177 | 15,876 | 96,121 |
|
리스부채에 대한 이자비용 |
2,073 | 4,854 | 1,297 | 4,501 |
|
단기리스가 아닌 소액자산리스료 |
3,264 | 9,634 | 1,968 | 4,096 |
|
리스부채 측정치에 포함되지 않은 변동리스료 |
- | - | 3,889 | 18,957 |
당분기 및 전분기 중 선급리스료를 포함한 리스의 총 현금유출은 각각 37,501천원 및 60,846천원입니다.
12. 차입금
(1) 당분기말 및 전기말 현재 차입금의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당분기말 | 전기말 |
| 장기차입금 | 8,000,000 | 8,000,000 |
상기 차입금과 관련하여 유형자산이 담보로 제공되어 있습니다(주석9 참조).
(2) 당분기말 및 전기말 현재 차입금의 상세내역은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 차입처 | 만기일 | 연이자율(%) | 당분기말 | 전기말 |
| 원화대출 | 하나은행 | 2024-12-29 | CD(3M)+1.64% |
8,000,000 | 8,000,000 |
(3) 당분기말 현재 장기차입금의 상환일정은 다음과 같습니다.
| (단위: 천원) | |
|---|---|
| 상환연도 | 상환금액 |
| 1년 이내 | - |
| 2년 이내 | 8,000,000 |
| 합계 | 8,000,000 |
13. 전환사채
(1) 당분기말 현재 전환사채의 내역은 다음과 같습니다.
| (단위 : 천원) | |||||
|---|---|---|---|---|---|
| 종 류 | 발행일 | 만기일 | 액면이자율 | 보장수익률 | 당분기말 |
| 제1회차 무기명식 무보증 사모 전환사채 |
2023-06-28 | 2028-06-28 | 0.0% | 3.0% | 20,000,000 |
| 사채상환할증금 | 3,223,680 | ||||
| 전환권조정 | (14,256,836) | ||||
| 가감 계 | 8,966,844 | ||||
(2) 당분기말 현재 발행된 전환사채의 발행조건은 다음과 같습니다.
| 구 분 | 내 역 |
|---|---|
| 종류 | 제1회차 무기명식 무보증 사모 전환사채 |
| 사채의 권면총액 | 20,000,000천원 |
| 사채의 발행가액 | 사채권면금액의 100% |
| 발행일 | 2023년 06월 28일 |
| 만기일 | 2028년 06월 28일 |
| 표면이자율 | 연 0.0% |
| 만기보장수익률 | 연 3.0% |
| 이자지급조건 및 기한 | 표면이자율이 0%로 별도의 이자지급기일 없음 |
| 원금상환방법 | 만기까지 보유하고 있는 "본 사채"의 전자등록금액에 대하여는 만기일에 전자등록금액의 116.1184%에 해당하는 금액을 일시 상환함 |
| 전환가격의 조정 | 시가를 하회하는 가격으로 주식 등을 발행하는 경우, 전환가격을 조정함 |
| 옵션에 관한 사항 | 1. 조기상환청구권(Put Option)에 관한 사항 발행일로부터 24개월이 되는 날 및 이후 매3개월에 해당되는 날에 원금의 전부 또는 일부를 조기상환 할 것을 청구할 수 있다. 2. 매도청구권(Call Option)에 관한 사항 발행일로부터 12개월이 되는날로부터 24개월이 되는날까지 매3개월이 되는 날마다 전환사채 액면금액의 20%인 40억원까지 발행회사 또는 발행회사가 지정하는 제3자에게 매도하도록 청구할 수 있다. |
| 전환조건 | (1) 전환가격 : 10,567 원 |
| (2) 전환청구기간 : 2024년 6월 28일부터 2028년 6월 28일까지 | |
| (3) 전환비율 : 100% | |
| (4) 전환대상 유가증권 : 주식회사 큐라클 기명식 보통주 |
(3) 당분기말 현재 전환사채 발행과 관련하여 인식한 파생상품 내역은 다음과 같습니다.
| (단위:천원) | ||
|---|---|---|
| 구 분 | 당분기말 | |
| 유동 | 비유동 | |
| 파생상품자산 | - | 851,921 |
| 파생상품부채 | - | 6,126,738 |
당사는 전환사채 발행과 관련하여 약정된 매도청구권(발행자의 콜옵션)과 조기상환청구권(사채권자의 풋옵션)을 해당 전환사채의 최초 발행시점에 별도의 파생상품으로 보아 각각 파생상품자산 및 파생상품부채로 인식하였습니다.
(4) 당사가 발행한 전환사채에 시가하락에 따른 전환가액 조정약정이 존재하지만, 금융감독원 질의회신 '회제이-00094'에 의거하여 전환권대가를 자본으로 인식하였으며, 동 회계처리는 '주식회사 등의 외부감사에 관한 법률' 제 13조 제1항 제 1호의 한국채택국제회계기준에 한하여 효력이 있습니다.
14. 퇴직급여
(1) 당분기 및 전분기의 포괄손익계산서에 반영된 금액은 다음과 같습니다.
|
(단위: 천원) |
||||
|---|---|---|---|---|
|
구분 |
당분기 |
전분기 |
||
| 3개월 | 누적 | 3개월 | 누적 | |
| 당기근무원가 | 57,098 | 180,303 | 61,879 | 185,634 |
| 순이자원가 | 238 | 379 | 13,728 | 12,942 |
| 종업원급여에 포함된 총 비용 | 57,336 | 180,682 | 75,607 | 198,576 |
(2) 당분기말 및 전기말 현재 순확정급여부채(자산) 금액의 산정내역은 다음과 같습니다.
|
(단위: 천원) |
||
|---|---|---|
|
구분 |
당분기말 |
전기말 |
|
확정급여채무의 현재가치 |
579,035 | 596,643 |
|
사외적립자산의 공정가치 |
(415,407) | (587,295) |
|
재무상태표상 순확정급여부채 |
163,628 | 9,348 |
15. 충당부채
(1) 당분기 중 충당부채 변동내역은 없습니다.
(2) 전분기의 충당부채 변동내역은 다음과 같습니다.
|
(단위: 천원) |
||||
|
구분 |
기초 |
증가 |
감소 |
기말 |
|
복구충당부채 |
42,000 | - | (42,000) | - |
16. 기타자산 및 기타부채
당분기말 및 전기말 현재 기타자산 및 기타부채 내역은 아래와 같습니다.
|
(단위: 천원) |
||||
|
구분 |
당분기말 |
전기말 |
||
| 유동 | 비유동 | 유동 | 비유동 | |
| 기타자산 | ||||
| 선급금 | 628,609 | 376,897 | - | 406,989 |
| 선급비용 | 155,975 | 89,584 | 312,658 | - |
| 당기법인세자산 | 109,671 | - | 76,295 | - |
| 부가세대급금 | 201,612 | - | 174,517 | - |
| 합계 | 1,095,867 | 466,481 | 563,470 | 406,989 |
| 기타부채 | ||||
| 예수금 | 45,964 | - | 67,833 | - |
17. 법인세비용 및 이연법인세
법인세비용은 당기법인세비용에서 과거기간 당기법인세에 대하여 당기에 인식한 조정사항, 일시적차이의 발생과 소멸로 인한 이연법인세비용(수익) 및 당기손익 이외로인식되는 항목과 관련된 법인세비용을 조정하여 산출하였습니다. 당분기 및 전분기는 법인세비용이 존재하지 않습니다.
18. 자본금과 자본잉여금
(1) 당사가 발행할 주식의 총수는 50,000,000주이고, 발행한 주식수는 보통주식 13,855,342주(전기말: 13,845,968주)이며 1주당 액면금액은 500원입니다.
(2) 당분기 및 전기의 자본금 및 자본잉여금 변동은 다음과 같습니다.
| (단위: 주, 천원) | |||
|---|---|---|---|
| 구분 | 주식수 | 자본금 | 주식발행초과금 |
| 전기초 | 13,687,468 | 6,843,734 | 99,848,102 |
| 2022-04-11 주식선택권 행사 | 98,500 | 49,250 | 945,746 |
| 2022-06-17 주식선택권 행사 | 4,000 | 2,000 | 41,034 |
| 2022-11-30 주식선택권 행사 | 56,000 | 28,000 | 428,248 |
| 전기말 | 13,845,968 | 6,922,984 | 101,263,130 |
| 당기초 | 13,845,968 | 6,922,984 | 101,263,130 |
| 2023-01-13 주식선택권 행사 | 2,000 | 1,000 | 20,081 |
| 2023-06-15 주식선택권 행사 | 7,374 | 3,687 | 76,441 |
| 당분기말 | 13,855,342 | 6,927,671 | 101,359,652 |
19. 기타자본구성요소
당분기말 및 전기말 현재 기타자본구성요소의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당분기말 | 전기말 |
| 주식선택권 | 3,841,713 | 2,597,450 |
| 전환권대가 | 6,063,954 | - |
| 합계 | 9,905,667 | 2,597,450 |
20. 결손금
당분기말 및 전기말 현재 결손금의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당분기말 | 전기말 |
| 미처리결손금 | (70,532,655) | (64,612,837) |
21. 주식기준보상
(1) 당사는 주주총회 결의에 의거하여 당사의 임직원에게 주식선택권을 부여하였으며, 보고기간말 현재 그 주요 내용은 다음과 같습니다.
| (단위: 주, 원) | ||||||
|---|---|---|---|---|---|---|
| 구분 | 부여방법 | 잔여 부여수량(*) |
가득기간 | 만기일 | 행사가격(*) | 부여일 공정가치(*) |
| 3-1차 - 2019년 6월 30일 부여 | 주식교부형 | 20,000 | 2.0년 | 2026-07-13 | 3,384 | 4,782 |
| 4차 - 2020년 3월 31일 부여 | 주식교부형 | 28,626 | 2.0년 | 2027-04-01 | 6,200 | 4,793 |
| 5-1차 - 2021년 1월 5일 부여 | 주식교부형 | 20,000 | 2.0년 | 2028-01-05 | 7,750 | 11,061 |
| 5-2차 - 2021년 1월 5일 부여 | 주식교부형 | 10,000 | 2.0년 | 2028-01-05 | 10,720 | 10,669 |
| 6-1차 - 2021년 3월 29일 부여 | 주식교부형 | 100,000 | 2.0년 | 2028-03-29 | 8,500 | 10,700 |
| 6-2차 - 2021년 3월 29일 부여 | 주식교부형 | 4,000 | 2.0년 | 2028-03-29 | 10,720 | 10,376 |
| 7차 - 2022년 3월 30일 부여 | 주식교부형 | 135,000 | 2.0년 | 2029-03-29 | 21,500 | 18,999 |
| 8차 - 2022년 11월 16일 부여 | 주식교부형 | 45,000 | 2.0년 | 2029-11-15 | 12,700 | 9,985 |
| 9차 - 2023년 3월 30일 부여 | 주식교부형 | 30,000 | 2.0년 | 2030-03-29 | 11,100 | 7,646 |
(*) 당사는 2020년 12월 12일 100% 무상증자를 실시함에 따라 주식선택권 부여수량,행사가격 및 부여일 공정가치를 조정하였습니다.
주식선택권은 행사시점에 당사의 주식으로 전환되며, 종업원이 주식선택권을 부여받을 때 지급하였거나 지급할 금액은 없습니다. 주식선택권은 배당에 대한 권리나 의결권을 가지지 않으며, 가득일로부터 만기일까지의 기간 동안 행사될 수 있습니다.
(2) 당분기 및 전기의 주식선택권 변동은 다음과 같습니다.
| (단위: 주) | ||
|---|---|---|
| 구분 | 당분기 | 전기 |
| 기초 잔여주식 | 417,000 | 374,500 |
| 기중 부여수량 | 30,000 | 225,000 |
| 기중 권리상실분 | (45,000) | (24,000) |
| 기중 행사분 | (9,374) | (158,500) |
| 기말 잔여주식 | 392,626 | 417,000 |
당분기말 현재 유효한 주식선택권의 가중평균 잔여만기는 5년이며, 가중평균 행사가격은 13,256원입니다.
(3) 당사는 부여된 주식선택권의 보상원가를 이항모형을 이용한 공정가치접근법을 적용하여 산정했으며, 보상원가를 산정하기 위한 제반 가정 및 변수는 다음과 같습니다.
| 구분 | 3-1차 | 4차 | 5-1차 | 5-2차 | 6-1차 | 6-2차 | 7차 | 8차 | 9차 |
|---|---|---|---|---|---|---|---|---|---|
| 주식선택권 공정가치 | 4,782원 | 4,793원 | 11,061원 | 10,669원 | 10,700원 | 10,376원 | 18,999원 | 9,985원 | 7,646원 |
| 주가 | 7,172원 | 7,514원 | 13,218원 | 13,218원 | 13,218원 | 13,218원 | 24,200원 | 12,900원 | 10,620원 |
| 무위험이자율 | 1.54% | 1.22% | 1.50% | 1.50% | 1.73% | 1.73% | 2.90% | 3.84% | 3.26% |
| 연환산 예상주가변동성 | 43.82% | 61.79% | 91.25% | 91.25% | 85.88% | 85.88% | 86.26% | 85.15% | 77.26% |
(4) 당분기 및 전분기의 비용으로 인식된 주식기준보상은 각각 1,289,192천원 및 1,178,694천원이며 전액 주식결제형 주식기준보상과 관련된 비용입니다.
22. 영업수익
(1) 수익의 구성
당분기 중 당사의 영업수익은 프랑스 소재 기업인 Thea Open Innovation과 체결한 기술이전계약에서 발생하였습니다(주석30 참조).
(2) 당분기 및 전분기의 영업수익 인식 시기에 대한 구분은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당분기 | 전분기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 기간에 걸쳐 이행 | 2,265,810 | 9,021,888 | 873,401 | 2,544,238 |
(3) 당사가 당분기 및 전기 중 고객과의 계약과 관련하여 인식한 자산, 부채는 다음과 같습니다.
① 당분기
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 기초 | 증가 | 감소 | 분기말 |
| 계약자산 | 149,321 | 8,848,186 | 7,398,727 | 1,598,780 |
② 전기
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 기초 | 증가 | 감소 | 기말 |
| 계약자산 | 35,267 | 2,732,143 | 2,618,089 | 149,321 |
| 계약부채 | 850,715 | - | 850,715 | - |
(4) 당분기 중 당사 영업수익의 10%이상을 차지하는 주요 고객은 1개 거래처로 영업수익은 9,021,888천원입니다.
23. 영업비용
당분기 및 전분기의 영업비용 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 당분기 | 전분기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 종업원 급여 | 841,891 | 2,565,926 | 865,297 | 2,340,841 |
| 퇴직급여 | 57,336 | 180,682 | 61,484 | 184,453 |
| 복리후생비 | 91,031 | 244,613 | 54,299 | 153,154 |
| 주식보상비용 | 401,735 | 1,289,192 | 505,710 | 1,178,694 |
| 여비교통비 | 28,664 | 235,935 | 59,077 | 151,591 |
| 접대비 | 34,916 | 108,379 | 30,755 | 77,842 |
| 세금과공과 | 86,495 | 236,982 | 98,846 | 321,180 |
| 감가상각비 | 137,718 | 414,020 | 101,011 | 300,960 |
| 지급임차료 | 3,263 | 9,633 | 2,746 | 7,402 |
| 보험료 | 5,152 | 20,674 | 8,824 | 24,693 |
| 차량유지비 | 3,889 | 12,580 | 2,882 | 10,394 |
| 소모품비 | 100,992 | 341,728 | 217,398 | 334,931 |
| 지급수수료 | 129,530 | 624,672 | 261,185 | 881,169 |
| 광고선전비 | 15,995 | 69,836 | 32,223 | 57,126 |
| 건물관리비 | 30,179 | 85,175 | 19,358 | 52,660 |
| 무형자산상각비 | 22,148 | 64,652 | 16,632 | 45,252 |
| 위탁용역연구비 | 3,660,673 | 8,591,459 | 468,833 | 4,142,192 |
| 전력비 | 18,613 | 48,919 | 12,122 | 20,373 |
| 기타 | 31,507 | 97,723 | 23,718 | 70,031 |
| 합계 | 5,701,727 | 15,242,780 | 2,842,400 | 10,354,938 |
24. 기타수익 및 기타비용
당분기 및 전분기의 기타수익 및 기타비용 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 당분기 | 전분기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 기타수익 | ||||
| 잡이익 | 17,376 | 75,637 | 590 | 8,209 |
| 유형자산처분이익 | - | - | - | 587 |
| 합계 | 17,376 | 75,637 | 590 | 8,796 |
| 기타비용 | ||||
| 유형자산처분손실 | 359 | 2,298 | - | 56,940 |
| 잡손실 | - | 406 | 738 | 866 |
| 합계 | 359 | 2,704 | 738 | 57,806 |
25. 금융수익 및 금융비용
당분기 및 전분기의 금융수익 및 금융비용 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 당분기 | 전분기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 금융수익 | ||||
| 이자수익 | 283,967 | 606,998 | 83,488 | 313,947 |
| 당기손익공정가치측정금융자산처분이익 | 88 | 16,339 | 35,657 | 35,657 |
| 당기손익공정가치측정금융자산평가이익 | 2,606 | 14,028 | 1,800 | 20,300 |
| 외화환산이익 | 165,887 | 307,063 | 467,829 | 816,220 |
| 외환차익 | 38,564 | 158,290 | 60,434 | 154,535 |
| 합계 | 491,112 | 1,102,718 | 649,208 | 1,340,659 |
| 금융비용 | ||||
| 이자비용 | 552,614 | 779,670 | 76,124 | 201,827 |
| 당기손익공정가치측정금융자산평가손실 | 9,773 | 9,773 | 300 | 3,700 |
| 외화환산손실 | (24,455) | 2,627 | (4,089) | - |
| 외환차손 | 42,646 | 80,533 | 432 | 933 |
| 합계 | 580,578 | 872,603 | 72,767 | 206,460 |
26. 현금흐름표
(1) 보고기간 중 영업활동으로부터 창출된 현금흐름은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당분기 | 전분기 |
| 분기순손실 | (5,917,844) | (6,725,511) |
| 조정 | 1,847,854 | 784,213 |
| 감가상각비 | 379,526 | 300,960 |
| 무형자산상각비 | 64,652 | 45,251 |
| 사용권자산상각비 | 34,494 | - |
| 이자비용 | 779,670 | 201,827 |
| 주식보상비용 | 1,289,192 | 1,178,694 |
| 당기손익-공정가치측정 금융자산평가손실 | 9,773 | 3,700 |
| 외화환산손실 | 2,627 | - |
| 유형자산처분손실 | 2,298 | 56,940 |
| 당기손익-공정가치측정 금융자산처분이익 | (16,339) | (35,657) |
| 이자수익 | (607,780) | (313,947) |
| 외화환산이익 | (314,241) | (812,699) |
| 당기손익-공정가치측정 금융자산평가이익 | (14,028) | (20,300) |
| 퇴직급여 | 180,682 | 184,453 |
| 지급수수료 | 57,328 | - |
| 유형자산처분이익 | - | (587) |
| 잡이익 | - | (4,998) |
| 잡손실 | - | 576 |
| 영업활동으로 인한 자산 부채의 변동 | (4,300,461) | 3,293,156 |
| 매출채권 | 5,134,128 | - |
| 미수금 | (93,999) | (16,636) |
| 계약자산 | (8,841,009) | (838,135) |
| 선급금 | (629,270) | - |
| 선급비용 | 179,124 | 41,988 |
| 부가세대급금 | (27,095) | 179,097 |
| 장기선급비용 | (90,872) | - |
| 예수금 | (21,869) | (4,345) |
| 단기금융상품 | - | 5,000,000 |
| 장기선급금 | - | (28,663) |
| 미지급금 | 243,929 | 416,202 |
| 미지급비용 | (141,432) | (725,357) |
| 퇴직금지급 | (201,556) | (209,324) |
| 사외적립자산 | 189,460 | 404,291 |
| 선수수익 | - | (33,247) |
| 계약부채 | - | (850,715) |
| 유동복구충당부채 | - | (42,000) |
| 영업활동으로부터 창출된 현금흐름 | (8,370,451) | (2,648,142) |
(2) 현금의 유출ㆍ입이 없는 거래 중 중요한 사항은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당분기 | 전분기 |
| 건설중인자산의 본계정대체 | 102,500 | 3,755,888 |
| 장기선급금의 무형자산 대체 | 71,505 | - |
| 계약자산의 매출채권 대체 | 7,398,727 | - |
27. 우발부채와 약정사항
(1) 당분기말 현재 당사가 피소되어 계류중인 소송사건은 없습니다.
(2) 당분기말 현재 당사는 서울보증보험에 반려동물의약품 실용화 기술노하우에 대한 기술료 지급과 관련한 지급보증보험(부보금액: 16,500천원) 및 도시가스 사용료 납부와 관련한 지급보증보험(부보금액: 4,200천원)을 가입하고 있습니다.
(3) 당분기말 현재 금융기관과 체결한 약정한도는 다음과 같습니다.
| (단위: 천원) | ||
| 구분 | 금융기관 | 약정한도 |
| 시설대출 | 하나은행 | 8,000,000 |
28. 연구개발관련 약정사항
(1) 당분기말 현재 당사가 타기관과 공동연구를 진행 중인 계약 현황은 다음과 같습니다.
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 품목 | 계약상대방 | 계약체결일 | 계약종료일 | 총계약금액 | 기지급금액 | 미지급액 |
| 후보물질 효능 및 기전분석 연구 | 연세대산학협력단 | 2022-10-25 | 2024-02-28 | 206,000 | 206,000 | - |
(2) 당분기말 현재 당사가 진행중인 연구개발 현황 및 각 파이프라인별 개발 진행단계는 다음과 같습니다.
| 구분 | 품 목 | 적응증 | 연구시작일 | 현재 진행단계 | ||
|---|---|---|---|---|---|---|
| 단계(국가) | 승인일 | |||||
| 화학합성 | 신약 개발 | CU01 | 당뇨병성 신증 | 2016년 | 임상 2b상(한국) | 2022년7월 |
| CU02 | 비알콜성 지방간염 | 2017년 | 후보물질 최적화 중 | - | ||
| CU03 | 습성 황반변성 | 2016년 | 임상 2a상(한국) 종료 | 2019년12월 | ||
| CU04 | 면역항암 | 2017년 | 선도물질 탐색 중 | - | ||
| CU05 | 폐암 | 2017년 | 후보물질 최적화 중 | - | ||
| CU06 | 혈관손상과 관련된 다양한 질환 | 2017년 | 임상 2a상(미국) | 2022년9월 | ||
| CU71-R01(*) | 차세대 혈관내피기능장애차단제 | 2023년 | 유효물질 탐색 중 | - | ||
(*) 당분기 중 파이프라인 명칭이 기존 CU07에서 CU71-R01로 변경되었습니다.
(3) 보고기간 중 파이프라인별로 발생한 경상연구개발비 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 당분기 | 전분기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| CU01 | 139,479 | 1,041,585 | 258,274 | 362,137 |
| CU02 | - | 301 | 7,142 | 17,250 |
| CU03 | 1,121 | 267,345 | (22,794) | 627,231 |
| CU04 | 47,025 | 269,220 | 25,552 | 81,606 |
| CU05 | 252 | 363 | 20,604 | 43,587 |
| CU06 | 3,628,925 | 7,271,879 | 290,339 | 3,412,789 |
| CU71-R01(*) |
28,083 | 81,289 | - | - |
| 기타공통비 | 775,976 | 2,790,272 | 1,068,109 | 2,757,968 |
| 합계 | 4,620,861 | 11,722,254 | 1,647,226 | 7,302,568 |
(*) 당분기 중 파이프라인 명칭이 기존 CU07에서 CU71-R01로 변경되었습니다.
29. 특수관계자거래
(1) 당분기 및 전분기 중 특수관계자에 대한 수익 및 비용 거래 내역은 없습니다.
(2) 당분기말 및 전기말 현재 특수관계자에 대한 채무 금액은 없습니다.
(3) 당분기 및 전분기 중 특수관계자에 대한 자금거래 내역은 없습니다.
(4) 주요 경영진에 대한 보상
주요 경영진은 등기 및 비등기임원에 해당하며, 종업원 용역의 대가로서 주요 경영진에게 지급됐거나 지급될 보상금액은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 당분기 | 전분기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 급여 및 기타 단기종업원 급여 | 388,400 | 1,225,008 | 481,535 | 1,348,834 |
| 퇴직 급여 | 31,965 | 95,895 | 31,904 | 95,713 |
| 주식기준보상 | 401,733 | 1,284,120 | 497,276 | 1,163,462 |
| 합 계 | 822,098 | 2,605,023 | 1,010,715 | 2,608,009 |
(5) 지급보증 및 담보제공 내역
당사가 특수관계자로부터 제공받거나 특수관계자에게 제공한 지급보증 및 담보제공 내역은 없습니다.
30. 기술이전계약
(1) 당사는2021년10월27일자로 프랑스에 소재한 Thea Open Innovation과 당뇨병성 황반부종 및 습성 황반변성 치료제CU06-RE에 대한 기술이전 계약을 체결하였으며, 반환조건 없는 계약금(Upfront payment) USD 6,000,000과 관련된 수행의무를 식별하였습니다. 반환조건 없는 계약금(Upfront payment) USD 6,000,000과 관련된 수행의무는 2022년 중 이행이 완료되었으며, 이에 따라 전기 중 수익인식이 완료되었습니다.
당사가 2021년 10월 27일자로 Thea Open Innovation과 체결한 당뇨병성 황반부종 및 습성 황반변성 치료제 CU06-RE 기술이전 계약에는 임상2상 시험 비용을 보전 받는 조건이 포함되어 있으며, 이에 따라 당사는 임상2상 시험 용역 제공에 대한 수행의무를 식별하였으며, 2023년 3월 6일자로 Thea Open Innovation과의 기술이전 계약을 비임상시험에 대한 비용까지 보전 받는 것으로 변경함에 따라 비임상시험 용역 제공에 대한 수행의무를 당기 중 추가로 식별하였습니다.
한편, 당사는 향후 임상2상 시험 성공 및 규제당국의 허가 등 일정요건을 달성하는 경우 최대USD 157,500,000 규모의 마일스톤 금액을 수령할 수 있으며, 고객이 인식하는 해당 기술과 관련된 순매출액의 일정 부분을 로열티로 수령할 수 있습니다.
(2) 기술이전계약과 관련된 불확실성 및 기타사항
당사의 향후 마일스톤 및 로열티 수익은 임상시험, 관계당국의 허가 등 개발의 성공 여부에 따라 달라질 수 있으므로 발생가능성에 불확실성이 내포되어 있습니다.
6. 배당에 관한 사항
당기에 변동사항이 없으며, 기업공시서식 작성기준에 따라 본 항목을 기재하지 않습니다. 관련 내용은 2023년 03월 22일에 제출된 사업보고서를 참조하시기를 바랍니다.
7. 증권의 발행을 통한 자금조달에 관한 사항
7-1. 증권의 발행을 통한 자금조달 실적
| [지분증권의 발행 등과 관련된 사항] |
1. 증자(감자)현황
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 원, 주) |
| 주식발행 (감소)일자 |
발행(감소) 형태 |
발행(감소)한 주식의 내용 | ||||
|---|---|---|---|---|---|---|
| 종류 | 수량 | 주당 액면가액 |
주당발행 (감소)가액 |
비고 | ||
| 2016.05.12 | - | 보통주 | 20,000 | 5,000 | 5,000 | 설립자본금 |
| 2016.09.12 | 유상증자(제3자배정) | 보통주 | 2,408 | 5,000 | 415,000 | - |
| 2016.09.30 | 유상증자(제3자배정) | 보통주 | 1,204 | 5,000 | 415,000 | - |
| 2016.10.13 | 유상증자(제3자배정) | 보통주 | 481 | 5,000 | 415,000 | - |
| 2017.06.07 | 무상증자 | 보통주 | 330,435 | 5,000 | - | 1주당 13.715주 배정 |
| 2018.07.14 | 유상증자(제3자배정) | 우선주 | 11,820 | 5,000 | 84,600 | - |
| 2018.07.18 | 유상증자(제3자배정) | 우선주 | 11,820 | 5,000 | 84,600 | - |
| 2018.08.29 | 유상증자(제3자배정) | 우선주 | 12,170 | 5,000 | 84,600 | - |
| 2018.09.21 | 유상증자(제3자배정) | 우선주 | 23,640 | 5,000 | 84,600 | - |
| 2018.10.06 | 유상증자(제3자배정) | 우선주 | 41,370 | 5,000 | 84,600 | - |
| 2018.10.27 | 유상증자(제3자배정) | 우선주 | 11,820 | 5,000 | 84,600 | - |
| 2018.11.30 | 유상증자(제3자배정) | 우선주 | 17,730 | 5,000 | 84,600 | - |
| 2019.10.26 | 유상증자(제3자배정) | 우선주 | 258,065 | 500 | 15,500 | 주1) |
| 2019.10.30 | 유상증자(제3자배정) | 우선주 | 109,678 | 500 | 15,500 | - |
| 2019.11.30 | 유상증자(제3자배정) | 우선주 | 129,032 | 500 | 15,500 | - |
| 2019.12.13 | 유상증자(제3자배정) | 우선주 | 64,516 | 500 | 15,500 | - |
| 2020.10.31 | 유상증자(제3자배정) | 보통주 | 149,213 | 500 | 26,800 | - |
| 2020.11.02 | 주식매수선택권행사 | 보통주 | 2,500 | 500 | 2,820 | - |
| 2020.11.02 | 주식매수선택권행사 | 보통주 | 96,000 | 500 | 500 | - |
| 2020.11.16 | 전환권행사 | 보통주 | 40,000 | 500 | - | 전환상환우선주 보통주전환 |
| 2020.12.01 | 전환권행사 | 보통주 | 40,000 | 500 | - | 전환상환우선주 보통주전환 |
| 2020.12.12 | 무상증자 | 보통주 | 3,872,993 | 500 | - | 1주당 1주 배정 |
| 2020.12.12 | 무상증자 | 우선주 | 1,784,991 | 500 | - | 1주당 1주 배정 |
| 2020.12.23 | 전환권행사 | 보통주 | 365,432 | 500 | - | 전환상환우선주 보통주전환 |
| 2020.12.24 | 전환권행사 | 보통주 | 1,229,474 | 500 | - | 전환상환우선주 보통주전환 |
| 2020.12.28 | 전환권행사 | 보통주 | 803,432 | 500 | - | 전환상환우선주 보통주전환 |
| 2020.12.29 | 전환권행사 | 보통주 | 548,148 | 500 | - | 전환상환우선주 보통주전환 |
| 2020.12.30 | 전환권행사 | 보통주 | 258,064 | 500 | - | 전환상환우선주 보통주전환 |
| 2021.01.07 | 전환권행사 | 보통주 | 365,432 | 500 | - | 전환상환우선주 보통주전환 |
| 2021.07.19 | 유상증자(일반공모) | 보통주 | 2,040,000 | 500 | 25,000 | 신규상장 |
| 2021.09.02 | 주식매수선택권행사 | 보통주 | 53,000 | 500 | 500 | - |
| 2021.09.02 | 주식매수선택권행사 | 보통주 | 154,000 | 500 | 3,384 | - |
| 2021.09.02 | 주식매수선택권행사 | 보통주 | 20,000 | 500 | 1,410 | - |
| 2021.12.06 | 주식매수선택권행사 | 보통주 | 11,000 | 500 | 500 | - |
| 2021.12.06 | 주식매수선택권행사 | 보통주 | 43,500 | 500 | 3,384 | - |
| 2021.12.06 | 주식매수선택권행사 | 보통주 | 50,000 | 500 | 500 | - |
| 2022.04.11 | 주식매수선택권행사 | 보통주 | 30,500 | 500 | 3,384 | - |
| 2022.04.11 | 주식매수선택권행사 | 보통주 | 68,000 | 500 | 6,200 | - |
| 2022.06.17 | 주식매수선택권행사 | 보통주 | 4,000 | 500 | 6,200 | - |
| 2022.11.30 | 주식매수선택권행사 | 보통주 | 56,000 | 500 | 3,384 | - |
| 2023.01.13 | 주식매수선택권행사 | 보통주 | 2,000 | 500 | 6,200 | - |
| 2023.06.14 | 주식매수선택권행사 | 보통주 | 7,374 | 500 | 6,200 | - |
미상환 전환사채 발행현황
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 원, 주) |
| 종류\구분 | 회차 | 발행일 | 만기일 | 권면(전자등록)총액 | 전환대상 주식의 종류 |
전환청구가능기간 | 전환조건 | 미상환사채 | 비고 | ||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 전환비율 (%) |
전환가액 | 권면(전자등록)총액 | 전환가능주식수 | ||||||||
|
무기명식 이권부 무보증 사모 전환사채 |
1회차 |
2023.06.28 | 2028.06.28 |
20,000,000,000 |
보통주 |
24.06.28~28.05.28 |
100 |
10,567 |
20,000,000,000 |
1,892,684 |
주1) |
| 합 계 | - | - | - |
20,000,000,000 |
- |
- |
- |
- |
20,000,000,000 |
1,892,684 |
- |
주1) Put Option에 관한 사항: 본 사채의 사채권자는 본 사채의 발행일로부터 24개월이 되는 2025년 06월 28일 및 이후 매 3개월에 해당되는 날(이하"조기상환일"이라 한다.)에 조기상환청구 전자등록금액의 원금에 해당하는 금액의 전부 또는 일부를 조기상환율에 따라 조기상환을 청구할 수 있다. 단, 조기상환지급일이 영업일이 아닌 경우에는 그 다음 영업일에 상 환하고 조기상환지급일 이후의 이자는 계산하지 아니한다.
| [채무증권의 발행 등과 관련된 사항] |
채무증권 발행실적
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 원, %) |
| 발행회사 | 증권종류 | 발행방법 | 발행일자 | 권면(전자등록)총액 | 이자율 | 평가등급 (평가기관) |
만기일 | 상환 여부 |
주관회사 |
|---|---|---|---|---|---|---|---|---|---|
|
주식회사 큐라클 |
회사채 | 사모 | 2023년 06월 28일 |
20,000,000,000 |
표면:0% 만기:3% |
- |
2028년 06월 28일 |
부 |
NH투자증권 |
| 합 계 | - | - | - |
20,000,000,000 |
- |
- |
- |
- |
- |
기업어음증권 미상환 잔액
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
1년초과 2년이하 |
2년초과 3년이하 |
3년 초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | |
단기사채 미상환 잔액
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
합 계 | 발행 한도 | 잔여 한도 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
회사채 미상환 잔액
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 |
20,000,000,000 |
- |
- |
- |
- |
- |
- |
20,000,000,000 |
|
| 합계 |
20,000,000,000 |
- |
- |
- |
- |
- |
- |
20,000,000,000 |
|
신종자본증권 미상환 잔액
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 5년이하 |
5년초과 10년이하 |
10년초과 15년이하 |
15년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 |
- |
- |
- |
- |
- |
- |
- |
- |
| 사모 |
- |
- |
- |
- |
- |
- |
- |
- |
|
| 합계 |
- |
- |
- |
- |
- |
- |
- |
- |
|
조건부자본증권 미상환 잔액
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | - | |
7-2. 증권의 발행을 통해 조달된 자금의 사용실적
가. 공모자금의 사용내역
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 증권신고서 등의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
|
코스닥시장 상장 |
- |
2021.07.16 |
시설자금 |
11,082 |
시설자금 |
11,082 |
주1) |
|
코스닥시장 상장 |
- |
2021.07.16 |
연구개발자금 |
37,028 |
연구개발자금 |
21,763 |
주2) |
(주1) 증권신고서 제출 당시 기재한 자금사용 계획에 따라 유형자산 취득(수수료 및 세금 등 부대비용 포함)을 위해 동 자금을 사용하였습니다.
(주2) 미사용잔액은 다. 미사용자금의운용내역에 기재하였습니다.
나. 사모자금의 사용내역
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 주요사항보고서의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
|
유상증자 |
1회 |
2018.07.14 |
운영 및 연구개발자금 |
1,000 |
운영 및 연구개발자금 |
1,000 |
- |
|
유상증자 |
2회 |
2018.07.18 |
운영 및 연구개발자금 |
1,000 |
운영 및 연구개발자금 |
1,000 |
- |
|
유상증자 |
3회 |
2018.08.29 |
운영 및 연구개발자금 |
1,030 |
운영 및 연구개발자금 |
1,030 |
- |
|
유상증자 |
4회 |
2018.09.21 |
운영 및 연구개발자금 |
2,000 |
운영 및 연구개발자금 |
2,000 |
- |
|
유상증자 |
5회 |
2018.10.06 |
운영 및 연구개발자금 |
3,500 |
운영 및 연구개발자금 |
3,500 |
- |
|
유상증자 |
6회 |
2018.10.27 |
운영 및 연구개발자금 |
1,000 |
운영 및 연구개발자금 |
1,000 |
- |
|
유상증자 |
7회 |
2018.11.30 |
운영 및 연구개발자금 |
1,500 |
운영 및 연구개발자금 |
1,500 |
- |
|
유상증자 |
8회 |
2019.10.26 |
운영 및 연구개발자금 |
4,000 |
운영 및 연구개발자금 |
4,000 |
- |
|
유상증자 |
9회 |
2019.10.30 |
운영 및 연구개발자금 |
1,700 |
운영 및 연구개발자금 |
1,700 |
- |
|
유상증자 |
10회 |
2019.11.30 |
운영 및 연구개발자금 |
2,000 |
운영 및 연구개발자금 |
2,000 |
- |
|
유상증자 |
11회 |
2019.12.13 |
운영 및 연구개발자금 |
1,000 |
운영 및 연구개발자금 |
1,000 |
- |
|
유상증자 |
12회 |
2020.10.31 |
운영 및 연구개발자금 |
3,999 |
운영 및 연구개발자금 |
3,999 |
- |
|
유상증자 |
13회 |
2020.11.02 |
운영 및 연구개발자금 |
55 |
운영 및 연구개발자금 |
55 |
- |
|
전환사채 |
1회 |
2023.07.03 |
운영 및 연구개발자금 |
20,000 |
운영 및 연구개발자금 |
- |
(주1),(주2) |
(주1) 보고서 작성기준일 현재 자금사용 계획과 실제 자금사용 현황의 차액은 상기와같으며 미사용자금은 안정성이 높은정기예금 및 보통예금에 예치하여 운용하고 있습니다.
(주2) 1회 전환사채: 제1회 무기명식 무보증 사모 전환사채
다. 미사용자금의 운용내역
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 백만원) |
| 종류 | 금융상품명 | 운용금액 | 계약기간 | 실투자기간 |
|---|---|---|---|---|
| 예ㆍ적금 |
정기예금 (우리은행) |
5,000 |
2023년 07월 ~ 2024년 01월 |
3개월 |
| 예ㆍ적금 |
정기예금 (하나은행) |
3,000 |
2023년 07월 ~ 2024년 01월 |
3개월 |
| 예ㆍ적금 |
정기예금 (우리은행) |
2,000 |
2023년 08월 ~ 2024년 02월 |
2개월 |
| 예ㆍ적금 |
정기예금 (하나은행) |
3,000 |
2023년 08월 ~ 2024년 02월 |
2개월 |
| 예ㆍ적금 |
정기예금 (삼성증권) |
5,000 |
2023년 07월 ~ 2024년 01월 |
3개월 |
| 예ㆍ적금 |
정기예금 (NH증권) |
2,000 |
2023년 07월 ~ 2024년 01월 |
3개월 |
| 예ㆍ적금 |
정기예금 (NH증권) |
5,000 |
2023년 08월 ~ 2024년 02월 |
2개월 |
| 예ㆍ적금 |
정기예금 (NH증권) |
3,000 |
2023년 08월 ~ 2024년 02월 |
2개월 |
| 예ㆍ적금 |
다원하이일드 사모투자신탁 제1호 |
3,000 |
- |
3개월 |
| 예ㆍ적금 |
CMA (삼성증권) |
4,048 |
- |
1개월 |
| 예ㆍ적금 |
보통예금 (우리은행) |
73 |
- |
- |
| 예ㆍ적금 |
보통예금 (하나은행) |
107 |
- |
- |
| 예ㆍ적금 |
보통예금 (기업은행) |
37 |
- |
- |
| 계 |
35,265 |
- | ||
8. 기타 재무에 관한 사항
당기에 변동사항이 없으며, 기업공시서식 작성기준에 따라 본 항목을 기재하지 않습니다. 관련 내용은 2023년 03월 22일에 제출된 사업보고서를 참고하시기 바랍니다.
IV. 이사의 경영진단 및 분석의견
기업공시서식 작성기준에 따라 본 항목을 기재하지 않습니다.
V. 회계감사인의 감사의견 등
1. 외부감사에 관한 사항
당 분기에 변동사항이 없으며 기업공시서식 작성기준에 따라 본 항목을 기재하지 않습니다. 관련 내용은 2023.08.11에 제출된 사업보고서를 참고하시기 바랍니다.
2. 내부통제에 관한 사항
당 분기에 변동사항이 없으며 기업공시서식 작성기준에 따라 본 항목을 기재하지 않습니다. 관련 내용은 2023.08.11에 제출된 사업보고서를 참고하시기 바랍니다.
VI. 이사회 등 회사의 기관에 관한 사항
1. 이사회에 관한 사항
기업공시서식 작성기준에 따라 본 항목을 기재하지 않습니다. 관련 내용은 2023.08.11에 제출된 사업보고서를 참고하시기 바랍니다.
2. 감사제도에 관한 사항
기업공시서식 작성기준에 따라 본 항목을 기재하지 않습니다. 관련 내용은 2023.08.11에 제출된 사업보고서를 참고하시기 바랍니다.
3. 주주총회 등에 관한 사항
기업공시서식 작성기준에 따라 본 항목을 기재하지 않습니다. 관련 내용은 2023.08.11에 제출된 사업보고서를 참고하시기 바랍니다.
VII. 주주에 관한 사항
가. 최대주주 및 특수관계인의 주식소유 현황
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 주, %) |
| 성 명 | 관 계 | 주식의 종류 |
소유주식수 및 지분율 | 비고 | |||
|---|---|---|---|---|---|---|---|
| 기 초 | 기 말 | ||||||
| 주식수 | 지분율 | 주식수 | 지분율 | ||||
| 권영근 | 최대주주 | 보통주 | 1,809,047 | 13.07 | 1,809,047 | 13.06 | - |
| 김영명 | 등기임원 | 보통주 | 40,000 | 0.29 | 40,000 | 0.29 | - |
| 곽현정 | 미등기임원 | 보통주 | 50,000 | 0.36 | 50,000 | 0.36 | - |
| 표정인 | 미등기임원 | 보통주 | 10,000 | 0.07 | 10,000 | 0.07 | - |
| 황용 | 미등기임원 | 보통주 | 18,000 | 0.13 | 18,000 | 0.13 | - |
| 계 | 보통주 | 1,927,047 | 13.92 | 1,927,047 | 13.91 | - | |
| 우선주 | - | - | - | - | - | ||
(주1) 기초의 발행주식 총수는 13,845,968주 입니다.
(주2) 기말의 발행주식 총수는 13,855,342주입니다.
(주3) 김명화 : 2023년 6월 말일자로 퇴사하여, 특수관계인 주식소유 현황에서 제외됨
나. 최대주주의 주요경력 및 개요
| 명 칭 | 직 책 | 학력 및 경력 |
|---|---|---|
| 권영근 | 이사회의장 | 서울대학교 화학교육과 학사 State University of New York at Buffalo, 이학 석/박사(생화학) 연세대학교 생화학과 교수 ('04~현재) 연세대학교 생명시스템대학 학장 ('20~'22.01) (주)큐라클 ('16~현재) |
다. 최대주주의 최대주주(법인 또는 단체)의 개요
당사는 설립이후 현재까지 최대주주 변동내역이 없습니다.
라. 주식 소유현황
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 주) |
| 구분 | 주주명 | 소유주식수 | 지분율(%) | 비고 |
|---|---|---|---|---|
| 5% 이상 주주 | 권영근 | 1,809,047 | 13.06 | - |
| 이인규 | 1,053,780 | 7.61 | - | |
| 우리사주조합 | 2,862,827 | 20.67 | - | |
마. 소액주주현황
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 주) |
| 구 분 | 주주 | 소유주식 | 비 고 | ||||
|---|---|---|---|---|---|---|---|
| 소액 주주수 |
전체 주주수 |
비율 (%) |
소액 주식수 |
총발행 주식수 |
비율 (%) |
||
| 소액주주 | 34,912 | 34,920 | 99.98 | 9,232,737 | 13,855,342 | 66.64 | - |
VIII. 임원 및 직원 등에 관한 사항
1. 임원 및 직원 등의 현황
가. 임원 현황
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 주) |
| 성명 | 성별 | 출생년월 | 직위 | 등기임원 여부 |
상근 여부 |
담당 업무 |
주요경력 | 소유주식수 | 최대주주와의 관계 |
재직기간 | 임기 만료일 |
|
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 의결권 있는 주식 |
의결권 없는 주식 |
|||||||||||
| 유재현 | 남 | 1972.08 | 대표이사 | 사내이사 | 상근 | 총괄 | 서울대학교 약학 학사 한국얀센 Immunology사업부 총괄이사('11~'14) 한국얀센 Specialty사업부 총괄상무('14~'18) 얀센북아시아 Specialty사업부 총괄전무('18~'20) (주)큐라클 대표이사 ('21.11~현재) |
- | - | - | 1년 11개월 | 2024.11.26 |
| 권영근 | 남 | 1964.04 | 이사회 의장 |
기타비상무이사 | 비상근 | 이사회 의장 |
State University of New York at Buffalo 생화학 박사 연세대학교 생화학과 교수('04.03~현재) (주)큐라클 이사회의장('16.05~현재) |
1,809,047 | - | 본인 | 7년 5개월 | 2025.03.30 |
| 김영명 | 남 | 1956.05 | 기타 비상무 이사 |
기타비상무이사 | 비상근 | 기타 비상무 이사 |
미국 Utah 주립대학교 생화학 박사 강원대학교 의학과 교수('97.03~현재) 강원대학교 혈관연구센터장('01.01~현재) (주)큐라클 기타비상무이사('19.03~현재) |
40,000 | - | - | 4년 7개월 | 2025.03.30 |
| 추연성 | 남 | 1956.03 | 기타 비상무 이사 |
사외이사 | 비상근 | 기타 비상무 이사 |
미국 Univ Illinois at Chicago 약학 박사 LG생명과학 부사장 및 고문('00.07~'18.03) (주)바이오파트너즈 대표이사('19.07~현재) (주)큐라클 기타비상무이사('20.03~현재) |
- | - | - | 3년 7개월 | 2024.03.29 |
| 최동훈 | 남 | 1963.06 | 사외 이사 |
사외이사 | 비상근 | 사외 이사 |
연세대학교 의학 박사 연세대학교 내과학교실 교수('10.03~현재) 용인세브란스병원 병원장('19.03~현재) (주)큐라클 사외이사('21.01~현재) |
- | - | - | 2년 9개월 | 2024.03.29 |
| 조상헌 | 남 | 1959.12 | 사외 이사 |
사외이사 | 비상근 | 사외 이사 |
서울대학교 내과학 박사 서울대학교 내과학교실 교수('92~현재) 서울대학교병원 알레르기내과교수('93~현재) (주)큐라클 사외이사('21.11~현재) |
- | - | - | 1년 11개월 | 2024.11.26 |
| 서규영 | 남 | 1966.12 | 감사 | 감사 | 비상근 | 감사 | 금융감독원 기업공시제도실 금융투자국 부국장('15~'17) 금융감독원 공보국장, 인재교육원실장, 자산운용검사국장, 인적자원개발실 국장('17~'21) 금융채권자조정위원회 사무국장('22.03~현재) (주)큐라클 감사('22.07~현재) |
- | - | 1년 3개월 | 2025.07.22 | |
| 김정한 | 남 | 1974.04 | 상무 이사 |
미등기 | 상근 | 사업 개발 총괄 |
University of california,Berkeley, Marketing&Global business MBA 동화약품 BD, Global&ETC Marketing 총괄임원 ('12.12~'20.09) (주)큐라클 사업개발본부 본부장('21.04~현재) |
- | - | - | 2년 6개월 | - |
| 최재진 | 남 | 1969.02 | 상무 이사 |
미등기 | 상근 | 전략 기획 총괄 |
서강대학교 마케팅 석사 한독 Commercial Excellence 부서장 ('15.05~19.05) 아이큐비아코리아 Strategic Consultant ('20.12~21.12) (주)큐라클 상무이사 ('21.12~현재) |
- | - | - | 1년 10개월 | - |
| 이원일 | 남 | 1975.09 | 상무 이사 |
미등기 | 상근 | 신약&바이오 연구소 총괄 |
서울대학교 약학박사 C&C신약연구소 신약연구 책임연구원('01.01~'15.01) 젬백스앤카엘 연구개발 이사('15.02~'16.07) 제일약품 신약연구 책임연구원('16.08~'17.06) (주)대원제약 신약연구 이사('17.06~'22.07) (주)큐라클 신약연구본부 상무('22.08~현재) |
- | - | - | 1년 2개월 | - |
| 곽현정 | 여 | 1971.01 | 이사 | 미등기 | 상근 | 전임상 후보물질 발굴 |
충남대학교, 화학과 이학박사 (주)SK 바이오팜 사업부 책임연구원('00.08~'10.12) 한국화학연구원 선임연구원('11.02~'16.11) (주)큐라클 신약연구소 이사('17.03~'22.04) (주)큐라클 전락기획실 이사('22.05~현재) |
50,000 | - | - | 6년 7개월 | - |
| 표정인 | 남 | 1977.11 | 이사 | 미등기 | 상근 | 중앙 연구소 총괄 |
연세대학교, 이학박사(의약화학) 한국과학기술연구원(KIST) 연구원('03.06~'14.12) 삼육대학교 특임교수/비전임('11.09~'14.07) iNtRON Biotechnology 신약연구 팀장('15.01~'17.07) (주)큐라클 연구개발본부 수석연구원('17.08~'20.11) (주)큐라클 연구개발본부 이사('20.12~현재) |
10,000 | - | - | 6년 2개월 | - |
| 황용 | 남 | 1971.08 | 이사 | 미등기 | 상근 | 경영 관리 총괄 |
서해대학교 경영학 학사 (주)네온테크 경영지원총괄('06.11~'19.06) (주)큐라클 경영관리본부 이사('19.07~현재) |
18,000 | - | - | 4년 3개월 | - |
| 김판경 | 여 | 1980.03 | 이사 | 미등기 | 상근 | 임상 개발 총괄 |
경북대학교, 의학 석사 한미약품 임상팀장('14.05~'17.04) 현대약품 임상팀장('17.04~'19.03) 유영제약 임상팀장('20.06~'22.05) (주)큐라클 임상개발본부 이사('22.05~현재) |
- | - | - | 1년 5개월 | - |
나. 직원 등 현황
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 백만원) |
| 직원 | 소속 외 근로자 |
비고 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 사업부문 | 성별 | 직 원 수 | 평 균 근속연수 |
연간급여 총 액 |
1인평균 급여액 |
남 | 여 | 계 | |||||
| 기간의 정함이 없는 근로자 |
기간제 근로자 |
합 계 | |||||||||||
| 전체 | (단시간 근로자) |
전체 | (단시간 근로자) |
||||||||||
|
연구/관리 |
남 |
17 |
- |
- |
- |
17 |
2.3 |
1,160 |
68 |
- |
- |
- |
- |
|
연구/관리 |
여 |
18 |
- |
- |
- |
18 |
2.6 |
797 |
44 |
- |
|||
| 합 계 |
35 |
- |
- |
- |
35 |
2.4 |
1,957 |
56 |
- |
||||
다. 미등기임원 보수 현황
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 백만원) |
| 구 분 | 인원수 | 연간급여 총액 | 1인평균 급여액 | 비고 |
|---|---|---|---|---|
| 미등기임원 |
7 |
703 |
100 |
- |
주1) 인원수는 보고서 작성기준일 현재 재직중인 미등기임원의 수입니다.
주2) 연간급여 총액은 2023년 1월 1일부터 보고서 작성기준일까지의 누계금액입니다. 주3) 1인 평균 급여액은 급여 총액을 인원수로 나누어 산출하였습니다.
2. 임원의 보수 등
기업공시서식 작성기준에 따라 본 항목을 기재하지 않습니다. 관 련 내용은 2023년 08월 11일에 제출된 반기보고서를 참조하시기를 바랍니다.
IX. 계열회사 등에 관한 사항
가. 계열회사 현황(요약)
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 사) |
| 기업집단의 명칭 | 계열회사의 수 | ||
|---|---|---|---|
| 상장 | 비상장 | 계 | |
| - | - | - | - |
| ※상세 현황은 '상세표-2. 계열회사 현황(상세)' 참조 |
나. 타법인출자 현황(요약)
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 원) |
| 출자 목적 |
출자회사수 | 총 출자금액 | |||||
|---|---|---|---|---|---|---|---|
| 상장 | 비상장 | 계 | 기초 장부 가액 |
증가(감소) | 기말 장부 가액 |
||
| 취득 (처분) |
평가 손익 |
||||||
| 경영참여 | - | - | - | - | - | - | - |
| 일반투자 | - | - | - | - | - | - | - |
| 단순투자 | - | - | - | - | - | - | - |
| 계 | - | - | - | - | - | - | - |
| ※상세 현황은 '상세표-3. 타법인출자 현황(상세)' 참조 |
X. 대주주 등과의 거래내용
기업공시서식 작성기준에 따라 본 항목을 기재하지 않습니다. 관련 내용은 2023년 03월 22일에 제출된 사업보고서를 참조하시기를 바랍니다.
XI. 그 밖에 투자자 보호를 위하여 필요한 사항
1. 공시내용 진행 및 변경사항
당사는 보고서 작성기준일 현재 주요사항보고서 및 한국거래소 공시를 통해 공시한 사항이 공시서류제출일까지 이행이 완료되지 않았거나 주요내용이 변경된 사실이 없습니다.
2. 우발부채 등에 관한 사항
당사는 보고서 작성기준일 현재 해당사항이 없습니다.
3. 제재 등과 관련된 사항
당사는 보고서 작성기준일 현재 해당사항이 없습니다.
4. 작성기준일 이후 발생한 주요사항 등 기타사항
가. 작성기준일 이후 발생한 주요사항
해당사항 없음.
나. 중소기업기준 검토표
당사는 기업공시서식 작성기준에 따라, 분/반기보고서의 본 항목을 기재하지 않습니다.
다. 합병등 사후정보
당사는 보고서 작성기준일 현재 해당사항이 없습니다.
라. 보호예수 현황
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 주) |
| 주식의 종류 | 예수주식수 | 예수일 | 반환예정일 | 보호예수기간 | 보호예수사유 | 총발행주식수 |
|---|---|---|---|---|---|---|
|
보통주 |
1,731,428 |
2021.07.22 | 2022.07.22 |
상장일로부터 1년 |
한국거래소 상장규정에 따른 보호예수 |
13,855,342 |
|
보통주 |
2,883,067 |
2021.07.22 | 2024.07.22 |
상장일로부터 3년 |
한국거래소 상장규정에 따른 보호예수 |
13,855,342 |
마. 상장기업의 재무사항 비교표
| (기준 재무제표 : | 개별 | ) | (상장일 : | 2021년 07월 22일 | , 인수인 : | 삼성증권 | ) | (단위 : 백만원) |
| 추정대상 | 계정과목 | 예측치 | 실적치 | 괴리율 |
|---|---|---|---|---|
| 2021년 | 매출액 |
- |
6,255 |
- |
| 영업이익 |
-17,255 |
-6,870 |
60 | |
| 당기순이익 |
-17,079 |
-6,678 |
61 | |
| 2022년 | 매출액 |
16,128 |
3,583 |
78 |
| 영업이익 |
-3,032 |
-11,982 |
-295 | |
| 당기순이익 |
-2,784 |
-11,406 |
-310 | |
| 2023년 | 매출액 |
31,146 |
- |
- |
| 영업이익 |
2,837 |
- |
- | |
| 당기순이익 |
3,057 |
- |
- |
주1) 예측치는 상장시 증권신고서에 기재된 수치입니다
주2) 2021년 10월 떼아오픈이노베이션에 기술 이전한 CU06에 대하여 계약금(upfront)을 수령하여 예측치 대비 매출액이 발생하였습니다.
주3)인력 증가 및 연구개발비 증가의 영향으로 영업비용이 증가하였습니다
바. 특례상장기업 관리종목 지정유예 현황
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 백만원, %) |
| 관리종목 지정요건 | 요건별 회사 현황 | 관리종목 지정요건 해당여부 |
관리종목지정유예 | |||
|---|---|---|---|---|---|---|
| 항목 | 사업연도 | 금액/비율 | 해당 여부 |
종료 시점 |
||
| 최근 사업연도말 매출액 30억원 미만 |
최근 사업연도말 매출액(별도) | 2022년 | 3,582 | 미해당 | 해당 | 2025년 12월 31일 |
| 최근 4사업연도 연속 영업손실 발생 | 최근 4사업연도 각 영업손익 (별도) |
2022년 |
-11,982 |
해당 | 해당 | - |
| 2021년 |
-6,870 |
|||||
| 2020년 |
-7,853 |
|||||
| 2019년 |
-5,734 |
|||||
| 자기자본 50%이상(10억원 이상에 한함)의 법인세차감전계속사업손실이 최근 3년간 2회 이상 및 최근 사업연도 법인세차감전계속사업손실 발생 | 최근 3사업연도 각 자기자본 대비 법인세차감전 계속사업손익 비율(연결) |
2022년 |
-24.7 | 미해당 | 해당 | 2023년 12월 31일 |
| 2021년 | -12.14 | |||||
| 2020년 | -425.3 | |||||
주1) 당사는 기술성장기업으로 2021년 07월 22일 코스닥 시장에 상장하였습니다.
주2) 매출액 요건의 경우, 신규상장일이 속하는 사업연도를 포함하는 연속하는 5개 사업연도(상장 일부터 상장일이 속한 사엽연도의 말일까지의 기간이 3월미만인 경우에는 그 다음 사업연도)까지 지정 유예되며, 2026년부터 대상이 됩니다.
주3) 기술성장기업의 경우에는 영업손실과 관련한 관리종목규정을 적용받지 않습니 다.
주4) 법인세비용차감전계속사업손실 요건은 신규상장일이 속하는 사업연도를 포함 한 연속 하는 3개 사업연도 동안 해당 요건을 적용받지 않게 됩니다. 2024년부터 해 당 요건을 적용 받게 될 예정입니다.
주5) 당사의 2022년 법인세차감전계속사업손실은 11,405,592,529 이며, 2021년 법인세차감전계속사업손실은 6,677,788,863원 이며, 2020년은 28,609,794,407원입니다.
XII. 상세표
1. 연결대상 종속회사 현황(상세)
당사는 보고서 작성기준일 현재 해당사항이 없습니다.
| ☞ 본문 위치로 이동 |
| (단위 : 원) |
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| - | - | - | - | - | - | - |
| - | - | - | - | - | - | - |
| - | - | - | - | - | - | - |
2. 계열회사 현황(상세)
| ☞ 본문 위치로 이동 |
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 사) |
| 상장여부 | 회사수 | 기업명 | 법인등록번호 |
|---|---|---|---|
| 상장 | - | - | - |
| - | - | ||
| 비상장 | - | - | - |
| - | - |
3. 타법인출자 현황(상세)
| ☞ 본문 위치로 이동 |
| (기준일 : | 2023년 09월 30일 | ) | (단위 : 원, 주, %) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
| - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - |
| - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - |
| 합 계 | - | - | - | - | - | - | - | - | - | - | - | ||||
(주1) 당사는 소규모기업에 해당하므로 타법인 출자현황을 기재하지 아니하고 있습니다.
【 전문가의 확인 】
1. 전문가의 확인
당사는 보고서 작성기준일 현재 해당사항이 없습니다.
2. 전문가와의 이해관계
당사는 보고서 작성기준일 현재 해당사항이 없습니다.