 |
|
대표이사확인서_20231030_1 |
정 정 신 고 (보고)
| 2023년 10월 30일 |
1. 정정대상 공시서류 : 투자설명서
2. 정정대상 공시서류의 최초제출일 : 2023년 09월 06일
3. 정정사유 : 최대주주 및 특수관계인 구주매각에 따른 기재정정
4. 정정사항
| 항 목 | 정 정 전 | 정 정 후 |
|---|---|---|
| 금번 정정신고서는 발행가액 확정에 따른 정정사항으로, 본문에 정정된 사항은 공통적으로 요약정보에 반영되었습니다. 금번 정정사항은 '굵은 붉은색 글씨체'를 사용하여 기재하였습니다. |
||
| 공통 정정사항 | 모집(매출)총액: 93,921,300,000원 모집(매출)가액: 23,850원 |
모집(매출)총액: 71,789,740,000원 모집(매출)가액: 18,230원 |
| 요약정보 - 2. 모집 또는 매출에 관한 일반사항 | (주1) 정정 전 | (주1) 정정 후 |
| 제1부 모집 또는 매출에 관한 사항 - I. 모집 또는 매출에 관한 일반사항 | ||
| 1. 공모개요 | (주2) 정정 전 | (주2) 정정 후 |
| 4. 모집 또는 매출절차 등에 관한 사항 | (주3) 정정 전 | (주3) 정정 후 |
| 제1부 모집 또는 매출에 관한 사항 - III. 투자위험요소 | ||
| 2. 회사위험 - 라. | (주4) 정정 전 | (주4) 정정 후 |
| 제1부 모집 또는 매출에 관한 사항 - V. 자금의 사용목적 | (주5) 정정 전 | (주5) 정정 후 |
(주1) 정정 전
2. 모집 또는 매출에 관한 일반사항
| (단위 : 원, 주) |
| 증권의 종류 |
증권수량 | 액면가액 | 모집(매출) 가액 |
모집(매출) 총액 |
모집(매출) 방법 |
|---|---|---|---|---|---|
| 보통주 | 3,938,000 | 500 | 23,850 | 93,921,300,000 | 주주배정후 실권주 일반공모 |
| 인수(주선) 여부 | 지분증권 등 상장을 위한 공모여부 | ||
|---|---|---|---|
| 인수 | 아니오 | 해당없음 | 해당없음 |
| 인수(주선)인 | 증권의 종류 |
인수수량 | 인수금액 | 인수대가 | 인수방법 | |
|---|---|---|---|---|---|---|
| 대표 | 한국투자증권 | 보통주 | 3,150,400 | 75,137,040,000 | - 인수수수료: 모집총액의 80.0% × 1.3% - 실권수수료: 잔액인수금액의 15.0% |
잔액인수 |
| 대표 | 신한투자증권 | 보통주 | 787,600 | 18,784,260,000 | - 인수수수료: 모집총액의 20.0% × 1.3% - 실권수수료: 잔액인수금액의 15.0% |
잔액인수 |
| 청약기일 | 납입기일 | 청약공고일 | 배정공고일 | 배정기준일 |
|---|---|---|---|---|
| 2023년 11월 01일 ~ 2023년 11월 02일 | 2023년 11월 09일 | 2023년 11월 03일 | 2023년 11월 09일 | 2023년 09월 21일 |
| 청약이 금지되는 공매도 거래 기간 | |
|---|---|
| 시작일 | 종료일 |
| 2023년 08월 08일 | 2023년 10월 27일 |
| 자금의 사용목적 | |
|---|---|
| 구 분 | 금 액 |
| 시설자금 | 45,192,000,000 |
| 운영자금 | 48,729,300,000 |
| 발행제비용 | 1,470,963,530 |
| 신주인수권에 관한 사항 | ||
|---|---|---|
| 행사대상증권 | 행사가격 | 행사기간 |
| - | - | - |
| 매출인에 관한 사항 | ||||
|---|---|---|---|---|
| 보유자 | 회사와의 관계 |
매출전 보유증권수 |
매출증권수 | 매출후 보유증권수 |
| - | - | - | - | - |
| 일반청약자 환매청구권 | ||||
|---|---|---|---|---|
| 부여사유 | 행사가능 투자자 | 부여수량 | 행사기간 | 행사가격 |
| - | - | - | - | - |
(후략)
(주1) 정정 후
2. 모집 또는 매출에 관한 일반사항
| (단위 : 원, 주) |
| 증권의 종류 |
증권수량 | 액면가액 | 모집(매출) 가액 |
모집(매출) 총액 |
모집(매출) 방법 |
|---|---|---|---|---|---|
| 보통주 | 3,938,000 | 500 | 18,230 | 71,789,740,000 | 주주배정후 실권주 일반공모 |
| 인수(주선) 여부 | 지분증권 등 상장을 위한 공모여부 | ||
|---|---|---|---|
| 인수 | 아니오 | 해당없음 | 해당없음 |
| 인수(주선)인 | 증권의 종류 |
인수수량 | 인수금액 | 인수대가 | 인수방법 | |
|---|---|---|---|---|---|---|
| 대표 | 한국투자증권 | 보통주 | 3,150,400 | 57,431,792,000 | - 인수수수료: 모집총액의 80.0% × 1.3% - 실권수수료: 잔액인수금액의 15.0% |
잔액인수 |
| 대표 | 신한투자증권 | 보통주 | 787,600 | 14,357,948,000 | - 인수수수료: 모집총액의 20.0% × 1.3% - 실권수수료: 잔액인수금액의 15.0% |
잔액인수 |
| 청약기일 | 납입기일 | 청약공고일 | 배정공고일 | 배정기준일 |
|---|---|---|---|---|
| 2023년 11월 01일 ~ 2023년 11월 02일 | 2023년 11월 09일 | 2023년 11월 03일 | 2023년 11월 09일 | 2023년 09월 21일 |
| 청약이 금지되는 공매도 거래 기간 | |
|---|---|
| 시작일 | 종료일 |
| 2023년 08월 08일 | 2023년 10월 27일 |
| 자금의 사용목적 | |
|---|---|
| 구 분 | 금 액 |
| 시설자금 | 45,192,000,000 |
| 운영자금 | 26,597,740,000 |
| 발행제비용 | 1,179,389,570 |
| 신주인수권에 관한 사항 | ||
|---|---|---|
| 행사대상증권 | 행사가격 | 행사기간 |
| - | - | - |
| 매출인에 관한 사항 | ||||
|---|---|---|---|---|
| 보유자 | 회사와의 관계 |
매출전 보유증권수 |
매출증권수 | 매출후 보유증권수 |
| - | - | - | - | - |
| 일반청약자 환매청구권 | ||||
|---|---|---|---|---|
| 부여사유 | 행사가능 투자자 | 부여수량 | 행사기간 | 행사가격 |
| - | - | - | - | - |
(후략)
(주2) 정정 전
1. 공모개요
당사는 이사회 결의를 통하여 '자본시장과 금융투자업에 관한 법률' 제165조의6 제2항1호에 의거 한국투자증권(주) 및 신한투자증권(주)와 주주배정후 실권주 일반공모에 대한 잔액인수 계약을 체결하고 사전에 그 실권주를 일반에 공모하기로 하여 보통주 3,938,000주를 주주배정후 실권주 일반공모 방식으로 발행하기로 결정하였으며, 동 증권의 개요는 다음과 같습니다.
| (단위 :원, 주) |
| 증권의 종류 | 증권수량 | 액면가액 | 모집(매출)가액 | 모집(매출)총액 | 모집(매출) 방법 |
|---|---|---|---|---|---|
| 보통주 | 3,938,000 | 500 | 23,850 | 93,921,300,000 | 주주배정후 실권주 일반공모 |
| 주1) 이사회 결의일 : 2023년 08월 07일 주2) 1주의 모집가액 및 모집총액은 예정 발행가액 기준으로 한 예정금액이며, 확정되지 않은 금액입니다. |
발행가액은 '증권의 발행 및 공시 등에 관한 규정' 제5-18조에 의거 주주배정 증자시가격산정 절차 폐지 및 가격산정의 자율화에 따라 발행가격을 자유롭게 산정할 수 있으나, 시장혼란 우려 및 기존 관행 등으로 (舊) '유가증권의 발행 및 공시등에 관한 규정' 제57조의 방식을 일부 준용하여 Ⅰ. 모집 또는 매출에 관한 일반사항의 3. 공모가격 결정방법에 기재된 바와 같이 산정할 예정입니다.
■ 모집예정가액의 산출근거
본 증권신고서의 예정 모집가액은 이사회 결의일 전일(2023년 08월 04일)을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액을 기준주가로 하여 할인율 25%를 적용, 아래의 산식에 의하여 산정된 발행가액으로 합니다. 단, 할인율 적용에 따른 모집가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다. (단, 호가단위 미만은 절상함)
※ 예정발행가액 = [기준주가 * (1- 할인율) ] / [ 1 + ( 증자비율 * 할인율 ) ]
상기 방법에 따라 산정된 예정발행가액은 참고용이며, 청약일전 3거래일에 확정발행가액을 공시할 예정입니다.
| [예정 발행가액 산정표] |
| 기산일 : 2023년 09월 18일 |
(단위: 원, 주) |
| 일자 | 종가 | 거래량 | 거래대금 |
|---|---|---|---|
| 2023/08/21 | 30,250 | 89,629 | 2,747,569,650 |
| 2023/08/22 | 30,650 | 77,910 | 2,373,483,900 |
| 2023/08/23 | 30,100 | 90,646 | 2,742,215,300 |
| 2023/08/24 | 30,500 | 78,432 | 2,402,063,100 |
| 2023/08/25 | 30,400 | 60,125 | 1,824,987,100 |
| 2023/08/28 | 30,700 | 61,037 | 1,861,150,900 |
| 2023/08/29 | 31,700 | 127,757 | 4,011,818,800 |
| 2023/08/30 | 41,200 | 2,662,025 | 99,230,240,200 |
| 2023/08/31 | 42,000 | 6,742,718 | 296,080,117,850 |
| 2023/09/01 | 43,200 | 4,647,898 | 206,742,335,250 |
| 2023/09/04 | 43,200 | 940,731 | 40,913,925,100 |
| 2023/09/05 | 41,250 | 1,088,470 | 45,318,588,850 |
| 2023/09/06 | 41,950 | 1,009,801 | 42,409,836,150 |
| 2023/09/07 | 42,300 | 3,445,259 | 145,231,906,800 |
| 2023/09/08 | 39,300 | 796,232 | 31,870,323,050 |
| 2023/09/11 | 44,250 | 2,820,787 | 120,357,801,350 |
| 2023/09/12 | 43,000 | 11,276,406 | 547,844,550,200 |
| 2023/09/13 | 37,550 | 2,487,093 | 100,858,203,400 |
| 2023/09/14 | 36,000 | 1,283,632 | 46,449,952,900 |
| 2023/09/15 | 35,400 | 636,700 | 22,828,857,100 |
| 2023/09/18 | 33,850 | 639,930 | 22,086,529,150 |
| 1개월 거래량 가중산술평균주가 (A) | 43,498 | - | |
| 1주일 거래량 가중산술평균주가 (B) | 45,337 | - | |
| 기산일 종가(C) | 33,850 | - | |
| (A),(B),(C)의 산술 평균 (D) | 40,895 | (A+B+C)/3 | |
| 기준주가 (E) | 33,850 | (C와 D중 낮은가액) | |
| 할인율 (F) | 25% | - | |
| 증자비율 (G) | 25.87% | - | |
| 예정발행가액 (호가단위 미만은 호가단위로 절상, 액면가액 이하일 경우 액면가액을 발행가액으로 함) |
23,850 | 기준주가 × (1-할인율) / (1+유상증자비율 × 할인율 ) |
|
(후략)
(주2) 정정 후
1. 공모개요
당사는 이사회 결의를 통하여 '자본시장과 금융투자업에 관한 법률' 제165조의6 제2항1호에 의거 한국투자증권(주) 및 신한투자증권(주)와 주주배정후 실권주 일반공모에 대한 잔액인수 계약을 체결하고 사전에 그 실권주를 일반에 공모하기로 하여 보통주 3,938,000주를 주주배정후 실권주 일반공모 방식으로 발행하기로 결정하였으며, 동 증권의 개요는 다음과 같습니다.
| (단위 :원, 주) |
| 증권의 종류 | 증권수량 | 액면가액 | 모집(매출)가액 | 모집(매출)총액 | 모집(매출) 방법 |
|---|---|---|---|---|---|
| 보통주 | 3,938,000 | 500 | 18,230 | 71,789,740,000 | 주주배정후 실권주 일반공모 |
| 주1) 이사회 결의일 : 2023년 08월 07일 주2) 1주의 모집가액 및 모집총액은 확정 발행가액 기준으로 산정된 금액입니다. |
발행가액은 '증권의 발행 및 공시 등에 관한 규정' 제5-18조에 의거 주주배정 증자시가격산정 절차 폐지 및 가격산정의 자율화에 따라 발행가격을 자유롭게 산정할 수 있으나, 시장혼란 우려 및 기존 관행 등으로 (舊) '유가증권의 발행 및 공시등에 관한 규정' 제57조의 방식을 일부 준용하여 Ⅰ. 모집 또는 매출에 관한 일반사항의 3. 공모가격 결정방법에 기재된 바와 같이 산정할 예정입니다.
■ 모집가액의 산출근거
본 증권신고서의 1차 발행가액은 신주배정기준일 전 3거래일(2023년 09월 18일)을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액을 기준주가로 하여 할인율 25%를 적용, 아래의 산식에 의하여 산정된 발행가액으로 합니다. 단, 할인율 적용에 따른 모집가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다. (단, 호가단위 미만은 절상함)
※ 1차발행가액 = [기준주가 * (1- 할인율) ] / [ 1 + ( 증자비율 * 할인율 ) ]
상기 방법에 따라 산정된 1차발행가액은 참고용이며, 청약일전 3거래일에 확정발행가액을 공시할 예정입니다.
| [예정 발행가액 산정표] |
| 기산일 : 2023년 09월 18일 |
(단위: 원, 주) |
| 일자 | 종가 | 거래량 | 거래대금 |
|---|---|---|---|
| 2023/08/21 | 30,250 | 89,629 | 2,747,569,650 |
| 2023/08/22 | 30,650 | 77,910 | 2,373,483,900 |
| 2023/08/23 | 30,100 | 90,646 | 2,742,215,300 |
| 2023/08/24 | 30,500 | 78,432 | 2,402,063,100 |
| 2023/08/25 | 30,400 | 60,125 | 1,824,987,100 |
| 2023/08/28 | 30,700 | 61,037 | 1,861,150,900 |
| 2023/08/29 | 31,700 | 127,757 | 4,011,818,800 |
| 2023/08/30 | 41,200 | 2,662,025 | 99,230,240,200 |
| 2023/08/31 | 42,000 | 6,742,718 | 296,080,117,850 |
| 2023/09/01 | 43,200 | 4,647,898 | 206,742,335,250 |
| 2023/09/04 | 43,200 | 940,731 | 40,913,925,100 |
| 2023/09/05 | 41,250 | 1,088,470 | 45,318,588,850 |
| 2023/09/06 | 41,950 | 1,009,801 | 42,409,836,150 |
| 2023/09/07 | 42,300 | 3,445,259 | 145,231,906,800 |
| 2023/09/08 | 39,300 | 796,232 | 31,870,323,050 |
| 2023/09/11 | 44,250 | 2,820,787 | 120,357,801,350 |
| 2023/09/12 | 43,000 | 11,276,406 | 547,844,550,200 |
| 2023/09/13 | 37,550 | 2,487,093 | 100,858,203,400 |
| 2023/09/14 | 36,000 | 1,283,632 | 46,449,952,900 |
| 2023/09/15 | 35,400 | 636,700 | 22,828,857,100 |
| 2023/09/18 | 33,850 | 639,930 | 22,086,529,150 |
| 1개월 거래량 가중산술평균주가 (A) | 43,498 | - | |
| 1주일 거래량 가중산술평균주가 (B) | 45,337 | - | |
| 기산일 종가(C) | 33,850 | - | |
| (A),(B),(C)의 산술 평균 (D) | 40,895 | (A+B+C)/3 | |
| 기준주가 (E) | 33,850 | (C와 D중 낮은가액) | |
| 할인율 (F) | 25% | - | |
| 증자비율 (G) | 25.87% | - | |
| 예정발행가액 (호가단위 미만은 호가단위로 절상, 액면가액 이하일 경우 액면가액을 발행가액으로 함) |
23,850 | 기준주가 × (1-할인율) / (1+유상증자비율 × 할인율 ) |
|
■ 2차 발행가액의 산출근거
본 증권신고서의 2차 발행가액은 구주주 청약 초일 전 3거래일(2023년 10월 27일)을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액을 기준주가로 하여 할인율 25%를 적용, 아래의 산식에 의하여 산정된 발행가액(2차 발행가액)으로 합니다. 단, 할인율 적용에 따른 모집가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다. (단, 호가단위 미만은 절상함)
※ 2차 발행가액 = 기준주가 * (1- 할인율)
| [2차 발행가액 산정표] |
| 기산일 : 2023년 10월 27일 |
(단위: 원, 주) |
| 일자 | 종가 | 거래량 | 거래대금 |
|---|---|---|---|
| 2023/10/23 | 24,950 | 140,184 | 3,551,327,950 |
| 2023/10/24 | 25,950 | 483,053 | 12,698,594,000 |
| 2023/10/25 | 25,150 | 164,807 | 4,163,956,000 |
| 2023/10/26 | 24,050 | 232,503 | 5,597,100,850 |
| 2023/10/27 | 24,300 | 263,624 | 6,470,065,150 |
| 1주일 거래량 가중산술평균주가 (A) | 25,302 | - | |
| 기산일 종가(B) | 24,300 | - | |
| (A),(B)산술 평균 (C) | 24,801 | (A+B)/2 | |
| 기준주가 (D) | 24,300 | (C와 D중 낮은가액) | |
| 할인율 | 25% | - | |
| 2차 발행가액 (호가단위 미만은 호가단위로 절상, 액면가액 이하일 경우 액면가액을 발행가액으로 함) |
18,230 | 기준주가 × (1-할인율) | |
(후략)
(주3) 정정 전
4. 모집 또는 매출절차 등에 관한 사항
가. 모집 또는 매출조건
| (단위 : 주, 원) |
| 항 목 | 내 용 | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 모집 또는 매출주식의 수 | 3,938,000 | ||||||||||||||||||||||||||||||||
| 주당 모집가액 또는 매출가액 |
예정가액 | 23,850 | |||||||||||||||||||||||||||||||
| 확정가액 | - | ||||||||||||||||||||||||||||||||
| 모집총액 또는 매출총액 |
예정가액 | 93,921,300,000 | |||||||||||||||||||||||||||||||
| 확정가액 | - | ||||||||||||||||||||||||||||||||
| 청 약 단 위 |
(1) "구주주"의 청약단위는 1주로 하며, 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식수에 신주배정비율("주주 배정분"에 해당하는 주식수를 자기주식을 제외한 발행주식 총수로 나눈 비율을 말하며, 자기주식과 발행주식총수는 신주배정기준일 현재의 주식수를 말한다)을 곱하여 산정된 배정주식수로 합니다. 다만, 신주배정기준일 현재 신주배정비율은 자기주식 변동으로 인하여 변경될 수 있습니다(단, 1주 미만은 절사한다).
|
||||||||||||||||||||||||||||||||
| 청약기일 | 구주주 (신주인수권증서 보유자) |
개시일 | 2023년 11월 01일 | ||||||||||||||||||||||||||||||
| 종료일 | 2023년 11월 02일 | ||||||||||||||||||||||||||||||||
| 일반모집 또는 매출 | 개시일 | 2023년 11일 06일 | |||||||||||||||||||||||||||||||
| 종료일 | 2023년 11월 07일 | ||||||||||||||||||||||||||||||||
| 청약 증거금 |
구주주(신주인수권증서 보유자) | 청약금액의 100% | |||||||||||||||||||||||||||||||
| 초 과 청 약 | 청약금액의 100% | ||||||||||||||||||||||||||||||||
| 일반모집 또는 매출 | 청약금액의 100% | ||||||||||||||||||||||||||||||||
| 납 입 기 일 | 2023년 11월 09일 | ||||||||||||||||||||||||||||||||
| 배당기산일(결산일) | 2023년 1월 1일 | ||||||||||||||||||||||||||||||||
| 주1) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정 요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. 주2) 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
(후략)
(주3) 정정 후
4. 모집 또는 매출절차 등에 관한 사항
가. 모집 또는 매출조건
| (단위 : 주, 원) |
| 항 목 | 내 용 | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 모집 또는 매출주식의 수 | 3,938,000 | ||||||||||||||||||||||||||||||||
| 주당 모집가액 또는 매출가액 |
예정가액 | - | |||||||||||||||||||||||||||||||
| 확정가액 | 18,230 |
||||||||||||||||||||||||||||||||
| 모집총액 또는 매출총액 |
예정가액 | - | |||||||||||||||||||||||||||||||
| 확정가액 | 71,789,740,000 |
||||||||||||||||||||||||||||||||
| 청 약 단 위 |
(1) "구주주"의 청약단위는 1주로 하며, 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식수에 신주배정비율("주주 배정분"에 해당하는 주식수를 자기주식을 제외한 발행주식 총수로 나눈 비율을 말하며, 자기주식과 발행주식총수는 신주배정기준일 현재의 주식수를 말한다)을 곱하여 산정된 배정주식수로 합니다. 다만, 신주배정기준일 현재 신주배정비율은 자기주식 변동으로 인하여 변경될 수 있습니다(단, 1주 미만은 절사한다).
|
||||||||||||||||||||||||||||||||
| 청약기일 | 구주주 (신주인수권증서 보유자) |
개시일 | 2023년 11월 01일 | ||||||||||||||||||||||||||||||
| 종료일 | 2023년 11월 02일 | ||||||||||||||||||||||||||||||||
| 일반모집 또는 매출 | 개시일 | 2023년 11일 06일 | |||||||||||||||||||||||||||||||
| 종료일 | 2023년 11월 07일 | ||||||||||||||||||||||||||||||||
| 청약 증거금 |
구주주(신주인수권증서 보유자) | 청약금액의 100% | |||||||||||||||||||||||||||||||
| 초 과 청 약 | 청약금액의 100% | ||||||||||||||||||||||||||||||||
| 일반모집 또는 매출 | 청약금액의 100% | ||||||||||||||||||||||||||||||||
| 납 입 기 일 | 2023년 11월 09일 | ||||||||||||||||||||||||||||||||
| 배당기산일(결산일) | 2023년 1월 1일 | ||||||||||||||||||||||||||||||||
| 주1) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정 요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. 주2) 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
(후략)
(주4) 정정 전
(전략)
당사 최대주주인 이제중 대표이사 및 사내이사 1인(이준행)은 30% 수준으로 청약에 참여할 예정이며, 30% 참여 가정 시 청약 주식 수는 각각 152,094주, 114,706주입니다. 증권신고서 제출일 기준 예정발행가액에 따른 상기 2인의 예상 필요 청약 자금은 각각 36.3억원, 27.4억원 입니다.
(후략)
(주4) 정정 후
(전략)
당사 최대주주인 이제중 대표이사 및 사내이사 1인(이준행)은 30% 수준으로 청약에 참여할 예정이며, 30% 참여 가정 시 청약 주식 수는 각각 152,094주, 114,706주입니다. 증권신고서 제출일 기준 예정발행가액에 따른 상기 2인의 예상 필요 청약 자금은 각각 29.3억원, 21.2억원 입니다.
(후략)
(주5) 정정 전
1. 모집 또는 매출에 의한 자금조달 내역
가. 자금조달금액
|
(단위: 원) |
|
구 분 |
금 액 |
|---|---|
|
모집 또는 매출총액(1) |
93,921,300,000 |
|
발행제비용(2) |
1,470,963,530 |
|
순 수 입 금 [ (1)-(2) ] |
92,450,336,470 |
| 주1) | 상기 금액은 예정발행가액을 기준으로 산정한 금액으로 모집가액 확정시 변경될 수 있습니다. |
| 주2) | 상기 모집총액은 우선적으로 하단에 기재된 자금의 사용 목적에 따라 사용할 예정입니다. |
| 주3) | 발행제비용은 공모금액 및 실권규모에 따라 변경될 수 있으며, 상기 기재 금액은 청약 초과로 인하여 실권이 발생하지 않은 상황을 가정하여 산정되었습니다. 또한 상장수수료는 상장신청일 직전일 주가에 따라 변동될 수 있습니다. |
나. 발행제비용의 내역
|
(단위: 원) |
|
구 분 |
금 액 |
지급일자 |
계산근거 |
|---|---|---|---|
|
발행분담금 |
16,905,830 |
신고서제출일 |
모집총액의 0.018%(10원 미만 절사) |
|
인수수수료 |
1,220,976,900 |
납입일익일 |
인수수수료 1.3% |
| 표준코드발급수수료 | 10,000 | 표준코드발급 신청일 | 신주인수권증서 건당 10,000원 |
|
상장수수료 |
8,740,000 |
신주상장일 |
910만원 + 1,000억원 초과금액의 10억원당 5만원 (코스닥시장상장규정 시행세칙 별표 14) |
| 주식발행등록수수료 | 1,000,000 | - | 1,000주당 300원(주식 및 신주인수권증서 각각 별도 징수, 수수료 건당 상한 50만원 및 하한 4천원) (주식·사채 등의 전자등록업무규정 시행세칙 별표 |
|
등록세 |
7,876,000 |
등기일 |
증자 자본금의 0.4% |
|
교육세 |
1,575,200 |
등기일 |
등록세의 20% |
|
기타비용 |
213,879,600 |
- |
투자설명서 인쇄 및 발송비, 표준코드발급비용 등 |
|
합 계 |
1,470,963,530 |
- |
- |
| 주1) | 상기 금액은 예정 모집가액을 기준으로 산정한 금액입니다. |
| 주2) | 발행제비용은 공모금액 및 상장신청일 직전일 한국거래소에서 거래되는 당사의 보통주식 종가, 유관기관 정책 등에 따라 변동될 수 있습니다. |
| 주3) | 기타비용은 예상금액으로 변동될 수 있습니다. |
2. 자금의 사용목적
가. 자금의 사용목적
당사가 금번 보통주 유상증자를 통해 조달 예정인 자금은 운영자금 및 시설자금으로 사용할 계획입니다.
| (기준일 : | 2023년 09월 19일 | ) | (단위 : 백만원) |
| 시설자금 | 영업양수 자금 |
운영자금 | 채무상환 자금 |
타법인증권 취득자금 |
기타 | 계 |
|---|---|---|---|---|---|---|
| 45,192 | - | 48,729 | - | - | - | 93,921 |
(후략)
(주5) 정정 후
1. 모집 또는 매출에 의한 자금조달 내역
가. 자금조달금액
|
(단위: 원) |
|
구 분 |
금 액 |
|---|---|
|
모집 또는 매출총액(1) |
71,789,740,000 |
|
발행제비용(2) |
1,179,389,570 |
|
순 수 입 금 [ (1)-(2) ] |
70,610,350,430 |
| 주1) | 상기 금액은 확정발행가액을 기준으로 산정한 금액입니다 |
| 주2) | 상기 모집총액은 우선적으로 하단에 기재된 자금의 사용 목적에 따라 사용할 예정입니다. |
| 주3) | 발행제비용은 공모금액 및 실권규모에 따라 변경될 수 있으며, 상기 기재 금액은 청약 초과로 인하여 실권이 발생하지 않은 상황을 가정하여 산정되었습니다. 또한 상장수수료는 상장신청일 직전일 주가에 따라 변동될 수 있습니다. |
나. 발행제비용의 내역
|
(단위: 원) |
|
구 분 |
금 액 |
지급일자 |
계산근거 |
|---|---|---|---|
|
발행분담금 |
12,922,150 |
신고서제출일 |
모집총액의 0.018%(10원 미만 절사) |
|
인수수수료 |
933,266,620 |
납입일익일 |
인수수수료 1.3% |
| 표준코드발급수수료 | 10,000 | 표준코드발급 신청일 | 신주인수권증서 건당 10,000원 |
|
상장수수료 |
8,860,000 |
신주상장일 |
730만원 + 700억원 초과금액의 10억원당 6만원 (코스닥시장상장규정 시행세칙 별표 14) |
| 주식발행등록수수료 | 1,000,000 | - | 1,000주당 300원(주식 및 신주인수권증서 각각 별도 징수, 수수료 건당 상한 50만원 및 하한 4천원) (주식·사채 등의 전자등록업무규정 시행세칙 별표 |
|
등록세 |
7,876,000 |
등기일 |
증자 자본금의 0.4% |
|
교육세 |
1,575,200 |
등기일 |
등록세의 20% |
|
기타비용 |
213,879,600 |
- |
투자설명서 인쇄 및 발송비, 표준코드발급비용 등 |
|
합 계 |
1,179,389,570 |
- |
- |
| 주1) | 상기 금액은 확정 발행가액을 기준으로 산정한 금액입니다. |
| 주2) | 발행제비용은 공모금액 및 상장신청일 직전일 한국거래소에서 거래되는 당사의 보통주식 종가, 유관기관 정책 등에 따라 변동될 수 있습니다. |
| 주3) | 기타비용은 예상금액으로 변동될 수 있습니다. |
2. 자금의 사용목적
가. 자금의 사용목적
당사가 금번 보통주 유상증자를 통해 조달 예정인 자금은 운영자금 및 시설자금으로 사용할 계획입니다.
| (기준일 : | 2023년 10월 30일 | ) | (단위 : 백만원) |
| 시설자금 | 영업양수 자금 |
운영자금 | 채무상환 자금 |
타법인증권 취득자금 |
기타 | 계 |
|---|---|---|---|---|---|---|
| 45,192 | - | 26,598 | - | - | - | 71,790 |
(후략)
투 자 설 명 서
2023년 10월 30일 |
|
| 주식회사 박셀바이오 | |
| 기명식 보통주 3,938,000주 | |
| 71,789,740,000원 | |
| 1. 증권신고의 효력발생일 : |
2023년 09월 06일 |
| 2. 모집가액 : |
18,230원 |
| 3. 청약기간 : |
구주주 : 2023년 11월 01일 ~ 2023년 11월 02일 일반공모 : 2023년 11월 06일 ~ 2023년 11월 07일 |
| 4. 납입기일 : |
2023년 11월 09일 |
| 5. 증권신고서 및 투자설명서의 열람장소 |
|
| 가. 증권신고서 : |
전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 나. 일괄신고 추가서류 : |
해당사항 없음 |
| 다. 투자설명서 : | 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 서면문서 : (주)박셀바이오 - 전라남도 화순군 화순읍 산단길 12-55 한국투자증권(주) - 서울특별시 영등포구 의사당대로 88 신한투자증권(주) - 서울특별시 영등포구 여의대로 70 |
|
| 6. 안정조작 또는 시장조성에 관한 사항 | |
| 해당사항없음 | |
| 이 투자설명서에 대한 증권신고의 효력발생은 정부가 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나 이 증권의 가치를 보증 또는 승인한 것이 아니며, 이 투자설명서의 기재사항은 청약일 전에 정정될 수 있음을 유의하시기 바랍니다. |
| 한국투자증권(주) 신한투자증권(주) |
【 대표이사 등의 확인 】
 |
|
대표이사확인서_20231030_1 |
【 본 문 】
요약정보
1. 핵심투자위험
| 하단의 핵심투자위험은 증권신고서 본문에 기재된 투자위험요소 중 중요한 항목만을 투자자의 이해도 제고를 위하여 간단ㆍ명료하게 요약한 것입니다. 자세한 투자위험요소는 "본문-제1부 모집 또는 매출에 관한 사항-Ⅲ. 투자위험요소"에 기재되어 있으니 참고하시기 바랍니다. |
| 구 분 | 내 용 |
| 사업위험 |
가. 국내외 거시경제 침체 및 불확실성 관련 위험 그러나, 신약 개발 과정은 후보물질의 유효성과 안전성을 평가하고 이에 대한 근거를 마련하기 위한 중요한 과정으로 관련 규정과 절차를 반드시 준수해야합니다. 먼저, 타겟 질환에 대해 약리적인 효과가 있을 것으로 예상되는 후보물질 탐색 및 발굴을 시작으로, 동물을 대상으로 하는 전임상 연구(preclinical study)와 사람을 대상으로 하는 임상 연구(clinical study)를 통해 후보물질의 안전성과 유효성에 대한 검증을 분석하여, 최종적으로 규제 당국으로부터 의약품 품목 허가를 받아야 합니다. 이와같이 신약 연구개발을 통하여 가시적인 결과가 나오는 제품의 상용화 단계까지 많은 비용과 시간이 요구되며, 연구개발 과정에서 수많은 변수가 발생할 수 있습니다. 또한, 변수들을 미리 찾아내어 극복하지 못한 경우에 지출했던 연구개발 비용 및 시간 등의 큰 손실을 발생할 수 있으므로 투자자 여러분들께서는 이 점 유의하시기 바랍니다. 당사가 영위하고 있는 바이오사업부문 증권신고서 및 회사 IR자료 등 관련 자료를 참고하더라도 합리적인 투자의사 결정하기에는 고도의 전문적 식견이 필요하며, 관련 산업 및 기술을 정확히 이해하기에는 한계가 있으므로 투자자 여러분께서는 이 점 유의하여 주시기 바랍니다. 다. 새로운 치료 요법 등장에 따른 시장 환경 변화 위험 이 같은 문제를 극복하기 위하여 2010년대 들어서는 면역항암제가 본격적으로 개발 적용되기 시작하였습니다. 면역항암제는 암세포가 획득한 면역억제 또는 면역회피 기전을 극복하기 위하여 면역체계의 종양 인지 능력 또는 파괴 능력을 회복 또는 강화시키는 기전의 약제로, 면역체계의 특이성, 기억력, 적응력을 증강시킴으로써 항암효과를 나타냅니다. 면역관문억제제를 필두로 한 다수의 면역항암제에 관한 임상연구 및 시판 후 증례를 통해, 1세대 화학항암제, 2세대 표적항암제와 달리, 장기간 효과 지속, 장기 생존가능, 폭넓은 항암효과 및 낮은 부작용 등의 특성을 보여주고 있어, 기존 항암치료의 패러다임을 바꾸며, 암 표준치료 중의 하나로 자리매김하고 있습니다. 라. 경쟁 면역항암제 개발에 따른 경쟁 심화 위험
바. 핵심연구인력 유출 위험 신약 개발사업은 후보물질 발굴, 비임상시험, 임상시험, 허가, 생산 및 마케팅 등 전 단계에 걸쳐 전문인력을 필요로 합니다. 특히 기존 의약품으로 치료가 어려웠던 난치성 질환에 대하여 의학적 미충족 수요를 충족시킬 수 있는 first-in-class 신약을 개발하거나 글로벌 시장가치가 매우 높은 블록버스터급 신약을 개발하기 위해서는 해당 분야에 지식과 경험을 갖춘 우수한 전문인력을 확보하는 것이 중요하며, 각 분야별 전문인력의 확보 여부는 곧 당사와 같은 연구개발 벤처기업의 경쟁력으로 직결됩니다. 당사는 지식과 경험이 풍부한 전문인력의 확보가 신약 연구개발 사업의 핵심 경쟁력이라는 사실을 인지하고 우수한 전문 인력을 영입하고자 기존 조직원들의 역량을 최대한으로 끌어올리기 위해 다양한 지원을 아끼지 않고 있습니다. 아. 기술이전 지연 및 실패 위험 당사의 항암 면역플랫폼 파이프라인에 따라 자사제품별 타겟하고 있는 질환의 발병률, 유병률을 고려 후 시장성 분석을 통해 지역을 구분하여 다른 나라에 L/O를 진행 예정입니다. 하지만 당사의 이러한 노력에도 불구하고 글로벌 기술이전 거래 건수 및 규모의 감소, 제약/바이오 시장의 수요 감소, 글로벌 제약사들의 사업전략 변동 등의 이유로 인해 기술이전이 예상보다 지연되거나 실패하는 경우 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
차. 기술이전 파트너사 관련 위험 신약 파이프라인의 기술이전이 성공하면, 일반적으로 기술이전의 대가로 초기 계약금을 수령하게 되며, 이 후 임상단계 또는 허가단계 성공시마다의 마일스톤, 신약 발매 후 매출액의 일정 비율에 대한 로열티, 특정 금액 이상의 매출 발생시 판매 마일스톤 등을 수취하게 됩니다. 증권신고서 제출일 현재 당사의 유효한 기술 라이선스 아웃 계약은 없습니다. 그러나 추후 기술 이전에 성공하더라도, 해당 기술이전 계약에서 목표하는 기간 내에 일정 수준의 마일스톤 실적을 충족시키지 못하거나, 해당 계약에서 규정한 계약 해제 및 해지 사유 등의 발생 시, 기 지급받은 초기 계약금의 경우 계약 조건에 따라 일부 또는 전부를 반환해야 하는 의무가 있을 수 있으며, 기 계약금을 제외한 나머지 마일스톤 및 로열티 금액 등을 추가로 수령할 수 없을 가능성이 존재합니다. 또한 기술 도입한 파트너사의 임상 수행 능력 및 파트너사 내부적인 사정 등으로 임상 진행을 연기 또는 중단해야 하는 가능성도 존재하며, 이에 따라 해당 계약이 중도에 해지되거나 계약 금액이 하향 조정될 가능성도 있습니다. 제품 출시 후에도 해당 지역에서 계획한 정도의 수익이 창출되지 않아 로열티 수입이 확보되지 아니하는 경우에는 당사의 기대 수익 또한 감소할 가능성이 있습니다. 이처럼 기술 이전 자체가 가지는 한계로 인하여 당사가 통제할 수 없는 파트너사의 역량에 따라 당사의 재무 성과가 변동될 위험이 있으니 투자자께서는 이 점 유의하시기 바랍니다. 카. 업무 위탁기관 관련 위험 당사와 같이 신약 개발사업을 영위하고 있는 다수의 바이오벤처 업체는 신약개발의 효율성을 높이고 리스크를 감소시키기 위한 전략으로, 임상시험 전문수탁기관(Contract Research Organization, CRO)을 대상으로 비임상시험 및 임상시험을 위탁 진행하거나, 의약품 생산 전문대행기관(Contract Manufacturing Organization, CMO)을 대상으로 임상시험에 필요한 원료 및 완제 생산을 위탁 진행하고 있습니다. 당사는 GMP 생산시설을 보유하여 면역세포치료제를 자체 생산하고 있으나, 이에 대한 임상시험은 환자의 안전, 임상시험의 품질보증 및 관리, 규제기관 관점에서의 임상시험 결과물의 타당성, 객관성 확보 등을 위한 목적으로 CRO 업체에 위탁 진행하고 있습니다. 당사는 CRO에 대하여 지속적으로 관리 및 모니터링하고 있으며, 예상치 못한 사고의 발생에 즉각 대처할 수 있도록 만반의 준비를 갖추기 위해 노력하고 있습니다. 한편, 동물용 항암면역치료제인 박스루킨-15의 대량 생산은 동물 의약품 생산이 가능한 업체를 CMO로 선정하여 위탁 생산할 계획이며, 당사는 이와 관련하여 제품의 표준서 및 관련정보를 제공하고, 원부자재를 공급하며, 제품의 최종 출하 판정 및 승인을 담당할 예정입니다. 하지만 당사의 이러한 노력에도 불구하고 CMO 및 CRO 기관 자체의 사정으로 인한 의도하지 않은 결과가 발생할 수 있습니다. 소속 직원 재배치, 수탁업무 수행능력 부족, 계약상 의무 미준수, 관련 규정 및 절차 미준수, 인력의 파업, 재정적 위기로 인한 파산 등의 상황이 발생할 수 있습니다. 특히, CMO의 경우 제조 공장 강제 폐쇄, 자연 재해, 인공 재해, 규정 미준수, 품질 저하 등으로 인한 생산 일정 지연 또는 생산 중단 상황이 발생할 수 있고, CRO의 경우 임상 결과 분석의 오류 및 임상 결과 도출 지연, 임상시험 과정에서 발생한 부작용에 대한 미흡한 대처 등이 발생할 수 있습니다. 이와 같이 업무위탁 기관을 활용할 경우 당사가 통제할 수 없는 위험요소들로 인하여 당사의 신약 개발 일정이 지연되거나 연구 결과에 부정적인 영향을 미칠 수 있으며, 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. 타. 생산 및 생산관련 투자에 따른 위험 당사는 설립 초기인 2011년도부터 녹십자 EM 및 전남생물의약연구센터 등과 함께 세포치료제 전용의 우수의약품 제조 및 품질관리 기준(GMP, Good Manufacturing Practice) 적합 시설에 관한 설계 작업에 착수하여, 2012년 7월 준공 완료하였습니다. 당사 GMP생산시설의 총 면적은 409 ㎡로, Vax-NK 전용 배양실, 원자재 및 제품보관소, 기계실 등으로 구획되어 있습니다. 2012년 11월 Vax-DC/MM의 시험생산을 시작으로, 현재는 임상연구를 위한 Vax-NK 플랫폼에대해 제1,2 제조소 모두를 가동하고있으며, CAR-T,CAR-NK, CAR-MIL은 비임상단계로 추후 신사옥이 건설되기 전까지 JBRC 내 GMP시설을 임차하여 임상용 치료제를 생산할 계획입니다. 그러나 당사의 제품은 환자의 자가유래 면역세포로서, 대상 암환자의 병기 및 전신상태, 기 적용된 항암약물요법 등에 따라, 백혈구 분반술 시행이 어려운 상황이 발생할 수 있으며, 분리된 말초혈액단핵구 내 면역세포의 수가 유효한 수준 이하일 가능성이 있습니다. 또한 자연재해, 인공재해 등으로 인하여 제조 공장이 멸실되거나, 제조인력이 파업을 하거나, 제조 및 품질관리 기준이 갑작스럽게 대폭 강화되어 제조공정의 개선이 필요하여 생산라인이 마비되는 등 예측하기 어려운 문제들이 발생할 경우, 당사의 제품 상업화 또는 임상개발에 부정적인 영향을 미칠 수 있습니다. 또한 GMP제조 시설의 상각비가 지속적으로 발생함에도 불구하고, 매출 시현이 지연될 경우 당사의 손익이 악화될 가능성이 존재하며 현금 확보가 제한되어 향후 임상 진행 등의 측면에서 제약을 받을 가능성이 존재하오니 투자자께서는 이 점 유의하여 주시기 바랍니다. |
| 회사위험 |
가. 성장성 및 수익성 감소에 따른 위험
라. 최대주주 및 특수관계인 지분희석 및 경영권 관련 위험
사. 정부 연구개발 과제 수행 관련 위험 당사는 설립 이래 총 8건의 정부과제를 성공적으로 수행 완료하였으며, 현재 2건의 정부 과제에 대해서도 특이사항 없이 진행 중에 있습니다. 당사는 이와 같은 정부과제의 성공적인 수행 및 진행을 통해 당사 연구개발에 필요한 자금 중 상당 부분을 충당하여 왔습니다. 따라서 당사는 향후에도 사업과 관련된 정부 출연 연구개발 과제에 적극적으로 지원할 예정입니다. 정부과제 수행에 따른 목적이탈 사항의 부존재와 합법적인 이행시 상환위험은 존재하지 않습니다.
아. 분쟁에 따른 우발채무 등에 관한 위험 차. 내부회계관리제도 및 내부통제 관련 위험 당사는 상장 이전 2018년에 내부회계관리제도를 조기 도입하여 내부통제시스템을 강화하였으며, 삼덕회계법인의 컨설팅 용역을 통해 내부회계관리시스템 구축과 함께 2019년 1월 1일 내부회계관리규정을 제정하였습니다. 증권신고서 제출일 현재 내부회계관리제도를 운영하기 위한 조직이 구축되어 있으며, 외부감사인이 운영 실태를 보고한 사항은 존재하지 않습니다. 당사는 내부회계관리제도를 철저히 운영하여 외부 감사인의 내부회계관리제도에 대한 검토의견을 받을 계획입니다. 종합적으로 당사는 내부통제를 위한 규정 및 조직을 구축하고 있으며, 우발상황 등이 발생하지 않도록 상시 모니터링을 통해 내부통제 강화를 위하여 상당한 노력을 기울이며 대비하고 있습니다. 그럼에도 불구하고, 내부회계관리조직이 적절하게 운영되지 않거나 혹은 외부감사인의 내부회계관리 운영실태를 감사한 결과 중요한 취약점이 발견될 시 각종 제재사항에 해당할 수 있습니다. 투자자 여러분께서는 공시된 당사의 내부회계관리 운영실태를 충분히 확인하시고 투자에 임해주시기 바랍니다. |
| 기타 투자위험 | 가. 환금성 제약 및 주가 변동에 따른 손실 위험 금번 유상증자 청약에 참여하여 신주를 배정받을 경우 신주의 추가상장일까지 환금성에 제약이 있으며, 청약 후 추가상장일 사이에 주가가 하락할 경우 원금에 대한 손해가 발생할 가능성이 있으니 투자자께서는 이 점 유의하시기 바랍니다. 나. 주가하락에 따른 발행금액 감소 위험 주식시장의 급격한 상황 악화로 인하여 회사의 금번 유상증자 발행가액이 크게 하락할 경우 당사가 계획했던 자금조달 계획 등에 차질이 발생할 수 있으며, 이러할 경우 당사의 재무적 안정성은 부정적인 영향을 받을 수 있으니 이 점 유의하시기 바랍니다. 다. 증권신고서 정정에 따른 일정 변경 위험 본 증권신고서는 공시심사 과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있습니다. 라. 분석정보의 한계 및 투자판단 관련 위험 금번 유상증자를 통해 취득한 당사의 주식가치가 하락할 수 있습니다. 본 증권신고서의 효력발생은 정부가 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나 이 유가증권의 가치를 보증 또는 승인한 것이 아니며, 기재사항은 청약일 이전에 변경될 수 있습니다. 또한 금번 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 투자자께서는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안 되며, 다양한 방면에서 신중한 검토를 병행하여 독자적으로 판단하시기 바랍니다. 마. 당사의 잘못된 정보 제공 등으로 손해 끼칠 가능성 당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있으니 이 점 유의하시기 바랍니다. 바. 유상증자 철회에 따른 위험 유상증자 진행 과정에서 모집 절차의 진행에 중대한 영향을 미칠만한 사유가 발생하여 당사 혹은 공동대표주관회사의 판단으로 유상증자가 철회될 수 있습니다. 유상증자 납입 전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회 시점에 따라 권리락에 따른 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있음을 투자자께서는 유의하시기 바랍니다. 사. 금융감독기관의 규제 강화에 따른 위험 최근 상장기업에 대한 관리감독기준이 강화되는 추세이며, 향후 당사가 상장기업 관리 감독기준을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지 실질심사, 상장폐지, 불성실법인 지정에 따른 벌금 및 벌점 부과 등의 조치가 취해질 수 있습니다. 향후 감독기관으로부터 당사가 현재 파악하지 못한 제재가 부과될 경우 주가하락 및 유동성(환금성)제약 등으로 인해 투자금에 막대한 손실이 발생할 수 있으니, 투자자께서는 이점 유의하시기 바랍니다. 아. 차입공매도 유상증자 참여 제한 관련 위험 「자본시장과 금융투자업에 관한 법률 시행령」일부 개정령에 따라, 주권상장법인이 유상증자 계획을 공시한 이후 발행가격 산정을 위한 대상 거래기간의 마지막 날(발행가격 산정 기산일)까지, 해당 기업의 주식을 공매도 한 자는 증자 참여를 제한하되, 예외적인 경우에만 증자 참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 투자자께서는 이 점 유의하시기 바랍니다. 자. 개인종합자산관리계좌(ISA 납입한도에 따른 청약제한 위험 개인종합자산관리계좌(이하 ISA 계좌)는 연간 납입가능한도 제한(연간납입한도 2,000만원, 5년간 최대 1억원까지 납입가능하며 납입한도 이월가능)이 있는 계좌입니다. ISA계좌를 통한 신주인수권증서 보유자 청약시, 투자자별 유상증자 배정주수에 해당하는 청약증거금 납입금액이 ISA계좌 잔여납입한도를 초과할 경우 유상청약이 제한될 수 있으니, 투자자께서는 이 점 유의하시기바랍니다. 차. 기타 투자자 유의사항 당사의 대내외적 경영환경 변화에 따라 당사 실적의 급변동이 있을 경우, 투자원금에 대한 손실이 발생할 수 있으므로, 상기 투자위험요소 및 본 증권신고서에 기재된 정보에만 의존하여 투자 판단을 해서는 안되며, 투자자 여러분의 독자적인 판단에 의해야 함을 유의하시어 투자에 임하시기 바랍니다. 카. 신주 물량 출회에 따른 주가 하락 가능성 주식시장의 특성상 향후 주가에 대한 변동성이 있는 관계로 증자에 따른 모집가격 산정 시 결정된 1주당 모집가액보다 향후 추가 상장 후 거래 시점의 주가가 낮아져 투자자에게 금전적 손실을 끼칠 가능성이 있습니다. 또한 금번 유상증자로 인해 추가 발행되는 신주는 보호예수되지 않으므로 신주 상장 직후 주식의 물량 출회 및 주가희석화에 따른 주가하락의 가능성이 있는 점 유의하시기 바랍니다. 타. 주가의 높은 변동성에 따른 시장조치 관련 위험 당사의 최근 1년 주가를 검토하였을 때, 2022년 07월부터 2023년 08월 중순까지 크게 세가지 이슈로 주가가 급등락하였습니다. '22년 7월 Vax-NK/HCC 데이터 발표와 함께 급등하였고, '22년 8월 Vax-DC 임상연구 조기종료로 급락한 바 있으며, '23년 4월 Vax-NK 진행성 간암 환자 대상 치료목적 사용 승인과 함께 급등하였습니다. 한국거래소는 시장감시규정 및 그 시행세칙에 의거하여 주가상승률, 거래 회전율 및 주가 변동성 등이 과도할 경우 투자주의종목 및 투자경고종목을 지정하고 있습니다. 이에 따라 당사는 2022년 07월부터 2023년 08월 중순까지 코스닥시장 업무규정 제 조의 2와 같은 규정 시행세칙 제8조의 5에 따른 공매도 과열종목, 업무규정 제23조의 2와 같은 규정 시행세칙 28조의 3에 따른 단기과열종목 지정예고를 받은 바 있습니다 예고일부터 10거래일 이내 주가 상승률, 거래 회전율 및 주가 변동성과 관련하여 다음의 요건에 모두 해당하고, 해당일의 종가가 직전 거래일 종가 및 지정예고일 전일 종가 대비 상승한 경우에는 그 직후 매매거래일부터 단기과열종목에 지정됩니다. 당사는 신약 개발을 사업으로 영위하는 회사로 임상 결과에 따라 주가가 급등락할 수 있는 가능성이 상대적으로 높은 편입니다. 이에 따라 투자경고종목 지정 가능성이 타 산업군 대비 높을 수 있습니다. 실제로 당사는 상장 직후 임상진행상황 발표에 따라 주가가 급등락하여 2020년초부터 2021년까지 다수의 시장조치를 받은 이력이 있습니다. 투자경고종목 지정 후 실제 매매거래정지 조치가 취해져 해당 종목의 환금성이 제한될 가능성도 존재하므로 투자자께서는 이 점 유의하시기 바랍니다. 파. 공모자금 사용 관련 위험 당사는 금번 공모 유상증자 이전 2020년 9월 IPO를 통해 공모자금을 모집한 바 있습니다. 해당 자금은 약 293억원으로, 파이프라인 연구개발 및 임상 시험에 약 185억원, 운영자금 98억원 그리고 시설자금 97억원이 쓰일 계획이었습니다. 그러나 당사는 2023년 반기보고서 기준 2022년까지 사용 예정이었던 공모자금 293억원 중 135억원을 사용하였습니다. 일부 임상연구 진행이 지연되고, 파이프라인 변경 등의 사유로 공모자금이 IPO당시의 예상한 것보다 미진하게 사용되었습니다. 당사는 금번 유상증자를 통해 잔존한 공모자금과 새로 유입될 공모자금을 바탕으로 'V. 자금의 사용목적'에 기재한 바와 같이 사업계획을 구상하고 있습니다. 그러나 IPO 공모대금이 계획과 다르게 사용된 바와 같이 임상중단 및 지연, 임상위수탁 및 제조관련 비용 증가, 연구 및 운영 인력 모집 관련 어려움 등 당사의 사업계획과 다른 이벤트가 발생할 경우 증권신고서에 기재한 바와 상이하게 자금이 사용될 가능성이 존재합니다. 또한 당사 경영진은 금번 공모를 통해 조달한 공모자금을 투자자가 동의하지 않을 수 있는 또는 당사 주주에게 유리한 수익이 발생하지 않는 방식으로 사용할 수 있습니다. 이에 투자자께서는 주의하시기 바랍니다. |
2. 모집 또는 매출에 관한 일반사항
| (단위 : 원, 주) |
| 증권의 종류 |
증권수량 | 액면가액 | 모집(매출) 가액 |
모집(매출) 총액 |
모집(매출) 방법 |
|---|---|---|---|---|---|
| 보통주 | 3,938,000 | 500 | 18,230 | 71,789,740,000 | 주주배정후 실권주 일반공모 |
| 인수(주선) 여부 | 지분증권 등 상장을 위한 공모여부 | ||
|---|---|---|---|
| 인수 | 아니오 | 해당없음 | 해당없음 |
| 인수(주선)인 | 증권의 종류 |
인수수량 | 인수금액 | 인수대가 | 인수방법 | |
|---|---|---|---|---|---|---|
| 대표 | 한국투자증권 | 보통주 | 3,150,400 | 57,431,792,000 | - 인수수수료: 모집총액의 80.0% × 1.3% - 실권수수료: 잔액인수금액의 15.0% |
잔액인수 |
| 대표 | 신한투자증권 | 보통주 | 787,600 | 14,357,948,000 | - 인수수수료: 모집총액의 20.0% × 1.3% - 실권수수료: 잔액인수금액의 15.0% |
잔액인수 |
| 청약기일 | 납입기일 | 청약공고일 | 배정공고일 | 배정기준일 |
|---|---|---|---|---|
| 2023년 11월 01일 ~ 2023년 11월 02일 | 2023년 11월 09일 | 2023년 11월 03일 | 2023년 11월 09일 | 2023년 09월 21일 |
| 청약이 금지되는 공매도 거래 기간 | |
|---|---|
| 시작일 | 종료일 |
| 2023년 08월 08일 | 2023년 10월 27일 |
| 자금의 사용목적 | |
|---|---|
| 구 분 | 금 액 |
| 시설자금 | 45,192,000,000 |
| 운영자금 | 26,597,740,000 |
| 발행제비용 | 1,179,389,570 |
| 신주인수권에 관한 사항 | ||
|---|---|---|
| 행사대상증권 | 행사가격 | 행사기간 |
| - | - | - |
| 매출인에 관한 사항 | ||||
|---|---|---|---|---|
| 보유자 | 회사와의 관계 |
매출전 보유증권수 |
매출증권수 | 매출후 보유증권수 |
| - | - | - | - | - |
| 일반청약자 환매청구권 | ||||
|---|---|---|---|---|
| 부여사유 | 행사가능 투자자 | 부여수량 | 행사기간 | 행사가격 |
| - | - | - | - | - |
| 【주요사항보고서】 | [정정] 주요사항보고서(유무상증자결정) - 2023.10.30 |
| 【기 타】 | 1) 금번 (주)박셀바이오의 주주배정후 실권주 일반공모 유상증자의 공동대표주관회사는 한국투자증권(주), 신한투자증권(주) 입니다. 2) 금번 유상증자는 잔액인수방식에 의한 것입니다. 공동대표주관회사는 주주배정후 실권주 일반공모 후 최종실권주를 잔액인수하게 되며, 인수방법 및 인수대가에 대한 자세한 내용은 '제1부 모집 또는 매출에 관한 사항 - Ⅰ. 모집 또는 매출에 관한 일반사항 - 5. 인수 등에 관한 사항'을 참고하여 주시기 바랍니다. 공동대표주관회사 한국투자증권(주)와 신한투자증권(주)는 투자매매ㆍ중개업자로서 증권의 발행ㆍ인수에 대한 청약의 권유, 청약, 청약의 승낙 및 자본시장법 상의 증권 인수업무를 수행합니다. 3) 상기 모집가액 및 발행제비용은 예정가액으로 산정된 것으로 향후 변경될 수 있습니다. 확정가액은 구주주 청약 초일 전 제3거래일에 결정될 예정입니다. 4) 상기 청약기일은 구주주의 청약기일이며, 일반공모의 청약기일은 2023년 11월 06일 ~ 2023년 11월 07일(2영업일간)입니다. 일반공모 청약 공고는 2023년 11월 03일에 당사, 공동대표주관회사의 인터넷 홈페이지를 통해 게시될 예정입니다. 5) 일반공모 청약은 공동대표주관회사인 한국투자증권(주)와 신한투자증권(주)의 본ㆍ지점, 홈페이지 및 HTS에서 가능합니다. 단, 구주주 청약 결과 발생한 실권주 및 단수주가 총 50,000주(액면가 500원 기준) 이하 이거나 배정하여야 할 주식의 공모금액이 1억원 이하일 경우에는 일반공모 청약을 하지 아니하고, 공동대표주관회사가 자기계산으로 인수할 수 있습니다. 6) 「자본시장과 금융투자업에 관한 법률」 제180조의4 및 동법 시행령 제208조의4제1항에 의거, 2023년 08월 08일부터 2023년 10월 27일까지 당사의 주식을 공매도 하거나 공매도 주문을 위탁한 자는 금번 모집(매출)에 청약할 수 없으며, 이를 위반하여 주식을 취득할 경우 동법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만, 모집(매출)가액의 공정한 가격형성을 저해하지 않는 경우로서 동법 시행령 제208조의4제2항 및 「금융투자업규정」 제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다. 7) 금융감독원에서 본 증권신고서를 심사하는 과정에서 정정명령 조치를 취할 수 있으며, 정정 명령 등에 따라 본 신고서에 기재된 일정이 변경될 수 있습니다. 8) 증권신고서의 효력의 발생은 본 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. |
제1부 모집 또는 매출에 관한 사항
I. 모집 또는 매출에 관한 일반사항
1. 공모개요
당사는 이사회 결의를 통하여 '자본시장과 금융투자업에 관한 법률' 제165조의6 제2항1호에 의거 한국투자증권(주) 및 신한투자증권(주)와 주주배정후 실권주 일반공모에 대한 잔액인수 계약을 체결하고 사전에 그 실권주를 일반에 공모하기로 하여 보통주 3,938,000주를 주주배정후 실권주 일반공모 방식으로 발행하기로 결정하였으며, 동 증권의 개요는 다음과 같습니다.
| (단위 :원, 주) |
| 증권의 종류 | 증권수량 | 액면가액 | 모집(매출)가액 | 모집(매출)총액 | 모집(매출) 방법 |
|---|---|---|---|---|---|
| 보통주 | 3,938,000 | 500 | 18,230 | 71,789,740,000 | 주주배정후 실권주 일반공모 |
| 주1) 이사회 결의일 : 2023년 08월 07일 주2) 1주의 모집가액 및 모집총액은 확정 발행가액 기준으로 산정된 금액입니다. |
발행가액은 '증권의 발행 및 공시 등에 관한 규정' 제5-18조에 의거 주주배정 증자시가격산정 절차 폐지 및 가격산정의 자율화에 따라 발행가격을 자유롭게 산정할 수 있으나, 시장혼란 우려 및 기존 관행 등으로 (舊) '유가증권의 발행 및 공시등에 관한 규정' 제57조의 방식을 일부 준용하여 Ⅰ. 모집 또는 매출에 관한 일반사항의 3. 공모가격 결정방법에 기재된 바와 같이 산정할 예정입니다.
■ 모집가액의 산출근거
본 증권신고서의 1차 발행가액은 신주배정기준일 전 3거래일(2023년 09월 18일)을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액을 기준주가로 하여 할인율 25%를 적용, 아래의 산식에 의하여 산정된 발행가액으로 합니다. 단, 할인율 적용에 따른 모집가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다. (단, 호가단위 미만은 절상함)
※ 1차발행가액 = [기준주가 * (1- 할인율) ] / [ 1 + ( 증자비율 * 할인율 ) ]
상기 방법에 따라 산정된 1차발행가액은 참고용이며, 청약일전 3거래일에 확정발행가액을 공시할 예정입니다.
| [예정 발행가액 산정표] |
| 기산일 : 2023년 09월 18일 |
(단위: 원, 주) |
| 일자 | 종가 | 거래량 | 거래대금 |
|---|---|---|---|
| 2023/08/21 | 30,250 | 89,629 | 2,747,569,650 |
| 2023/08/22 | 30,650 | 77,910 | 2,373,483,900 |
| 2023/08/23 | 30,100 | 90,646 | 2,742,215,300 |
| 2023/08/24 | 30,500 | 78,432 | 2,402,063,100 |
| 2023/08/25 | 30,400 | 60,125 | 1,824,987,100 |
| 2023/08/28 | 30,700 | 61,037 | 1,861,150,900 |
| 2023/08/29 | 31,700 | 127,757 | 4,011,818,800 |
| 2023/08/30 | 41,200 | 2,662,025 | 99,230,240,200 |
| 2023/08/31 | 42,000 | 6,742,718 | 296,080,117,850 |
| 2023/09/01 | 43,200 | 4,647,898 | 206,742,335,250 |
| 2023/09/04 | 43,200 | 940,731 | 40,913,925,100 |
| 2023/09/05 | 41,250 | 1,088,470 | 45,318,588,850 |
| 2023/09/06 | 41,950 | 1,009,801 | 42,409,836,150 |
| 2023/09/07 | 42,300 | 3,445,259 | 145,231,906,800 |
| 2023/09/08 | 39,300 | 796,232 | 31,870,323,050 |
| 2023/09/11 | 44,250 | 2,820,787 | 120,357,801,350 |
| 2023/09/12 | 43,000 | 11,276,406 | 547,844,550,200 |
| 2023/09/13 | 37,550 | 2,487,093 | 100,858,203,400 |
| 2023/09/14 | 36,000 | 1,283,632 | 46,449,952,900 |
| 2023/09/15 | 35,400 | 636,700 | 22,828,857,100 |
| 2023/09/18 | 33,850 | 639,930 | 22,086,529,150 |
| 1개월 거래량 가중산술평균주가 (A) | 43,498 | - | |
| 1주일 거래량 가중산술평균주가 (B) | 45,337 | - | |
| 기산일 종가(C) | 33,850 | - | |
| (A),(B),(C)의 산술 평균 (D) | 40,895 | (A+B+C)/3 | |
| 기준주가 (E) | 33,850 | (C와 D중 낮은가액) | |
| 할인율 (F) | 25% | - | |
| 증자비율 (G) | 25.87% | - | |
| 예정발행가액 (호가단위 미만은 호가단위로 절상, 액면가액 이하일 경우 액면가액을 발행가액으로 함) |
23,850 | 기준주가 × (1-할인율) / (1+유상증자비율 × 할인율 ) |
|
■ 2차 발행가액의 산출근거
본 증권신고서의 2차 발행가액은 구주주 청약 초일 전 3거래일(2023년 10월 27일)을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액을 기준주가로 하여 할인율 25%를 적용, 아래의 산식에 의하여 산정된 발행가액(2차 발행가액)으로 합니다. 단, 할인율 적용에 따른 모집가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다. (단, 호가단위 미만은 절상함)
※ 2차 발행가액 = 기준주가 * (1- 할인율)
| [2차 발행가액 산정표] |
| 기산일 : 2023년 10월 27일 |
(단위: 원, 주) |
| 일자 | 종가 | 거래량 | 거래대금 |
|---|---|---|---|
| 2023/10/23 | 24,950 | 140,184 | 3,551,327,950 |
| 2023/10/24 | 25,950 | 483,053 | 12,698,594,000 |
| 2023/10/25 | 25,150 | 164,807 | 4,163,956,000 |
| 2023/10/26 | 24,050 | 232,503 | 5,597,100,850 |
| 2023/10/27 | 24,300 | 263,624 | 6,470,065,150 |
| 1주일 거래량 가중산술평균주가 (A) | 25,302 | - | |
| 기산일 종가(B) | 24,300 | - | |
| (A),(B)산술 평균 (C) | 24,801 | (A+B)/2 | |
| 기준주가 (D) | 24,300 | (C와 D중 낮은가액) | |
| 할인율 | 25% | - | |
| 2차 발행가액 (호가단위 미만은 호가단위로 절상, 액면가액 이하일 경우 액면가액을 발행가액으로 함) |
18,230 | 기준주가 × (1-할인율) | |
■ 공모일정 등에 관한 사항
당사는 2023년 08월 07일 이사회를 통해 유상증자 결의를 하였으며, 세부 일정은 다음과 같습니다.
| [주요일정] |
| 날짜 | 업 무 내 용 | 비고 |
|---|---|---|
| 2023년 08월 07일 | 이사회 결의 | 주요사항보고서 제출 |
| 2023년 08월 07일 | 증권신고서(예비투자설명서) 제출 | - |
| 2023년 08월 08일 | 신주발행공고 및 기준일 공고 | 당사 인터넷 홈페이지 (www.vaxcell-bio.com) |
| 2023년 09월 18일 | 1차 발행가액 확정 | 신주배정기준일 전 제3거래일 |
| 2023년 09월 20일 | 권리락 | 신주배정기준일 전 제1거래일 |
| 2023년 09월 21일 | 신주배정기준일(주주확정) | - |
| 2023년 10월 06일 | 신주배정 통지 | - |
| 2023년 10월 17일 ~ 2023년 10월 23일 |
신주인수권증서 상장 및 거래 기간 | 5거래일 이상 동안 거래 |
| 2023년 10월 24일 | 신주인수권증서 상장폐지 | 구주주 청약초일 5거래일 전 폐지 |
| 2023년 10월 27일 | 확정 발행가액 산정 | 구주주 청약초일 3거래일 전 |
| 2023년 10월 30일 | 확정 발행가액 확정 공고 | 당사 인터넷 홈페이지 (www.vaxcell-bio.com) |
| 2023년 11월 01일 ~ 2023년 11월 02일 |
구주주 청약 | - |
| 2023년 11월 03일 | 일반공모청약 공고 | 당사 인터넷 홈페이지 (www.vaxcell-bio.com) 한국투자증권 홈페이지 (securities.koreainvestment.com) 신한투자증권 홈페이지 (www.shinhansec.com) |
| 2023년 11월 06일 ~ 2023년 11월 07일 |
일반공모청약 | - |
| 2023년 11월 09일 | 주금납입/환불/배정공고 | - |
| 2023년 11월 23일 | 신주상장 예정일 | - |
|
주1) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. |
■ 무상증자에 관한 사항
당사는 2023년 08월 07일에 개최된 이사회에서 무상증자를 결의하였으며, 유상증자 납입일(2023년 11월 09일)의 2영업일 후인 2023년 11월 13일을 무상증자 신주배정기준일로 하여, 유상증자 후 주주명부에 기재된 주주(자기주식 제외)에 대하여 소유주식 1주당 0.2주의 비율로 신주를 무상으로 배정하는 증자를 시행할 예정입니다. 금번 유상증자로 인해 발행되는 신주의 경우에도 자동적으로 무상증자에 참여하여 신주를 받을 수 있는 권리가 발생하게 됩니다.
1) 신주의 재원 : 주식발행초과금
2) 단주 처리방법 : 신주의 상장 초일 종가를 기준으로 현금 지급함
3) 무상증자에 관한 기타사항은 이사회를 통해 대표이사에게 위임되었으며, 상기 일정은 유관 기관과의 협의를 통해 변경될 수 있음.(본 무상증자는 유상증자 청약자도 무상증자를 받을 수 있도록 진행되고 있습니다. 만약, 유상증자 일정이 변경되면, 본 무상증자의 일정 또한 변경될 수 있습니다.)
[무상증자 개요]
| 구분 | 내용 |
|---|---|
| 무상증자 신주배정 기준일 | 2023년 11월 13일 |
| 무상증자 신주의 주당 발행가액 | 500원 |
| 무상증자 신주의 종류와 수 | 보통주 3,832,200주 |
| 1주당 신주배정 수 | 0.2주 |
| 무상증자 신주의 재원 | 주식발행초과금 |
| 무상증자 신주권 유통 예정일 | 2023년 11월 30일 |
| 무상증자 신주상장 예정일 | 2023년 11월 30일 |
| 주1) 무상증자 신주의 수는 현재까지 발행한 주식의 총수에서 자기주식을 제외한 유통주식수에 금번 유무상증자 이사회 결의시 결의한 유상증자 주식수를 더한 주식수에 0.2를 곱한 주식수 입니다.(단수주 미만 절사) |
2. 공모방법
| [공모방법 : 주주배정후 실권주 일반공모] |
| 모 집 대 상 | 주식수 | 비 고 |
| 구주주 청약 (신주인수권증서 보유자 청약) |
3,938,000주 (100.00%) |
- 구주 1주당 신주 배정비율 : 1주당 0.2586875123주 - 신주배정 기준일 : 2023년 09월 21일 - 구주주 청약일 : 2023년 11월 01일 ~ 2023년 11월 02일 (2일간) - 보유한 신주인수권증서의 수량 한도로 청약가능(구주주에게는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율을 곱한 수량만큼의 신주인수권 증서가 배정됨) |
| 초과 청약 | - | - 「자본시장과 금융투자업에 관한 법률」 제165조의6 제2항제2호에 의거 초과청약 - 초과청약비율 : 배정신주(신주인수권증서) 1주당 0.2 - 신주인수권증서 거래를 통해서 신주인수권증서를 매매시 보유자 기준으로 초과청약 가능 |
| 일반모집 청약 (고위험고수익투자신탁, 벤처기업투자신탁 청약 포함) |
- | - 구주주 청약 후 발생하는 단수주 및 실권주에 대해 배정됨 |
| 합 계 | 3,938,000주 (100.00%) |
- |
|
주1) 본 건 유상증자는 주주배정후 실권주 일반공모 방식으로 진행되며, 구주주 청약결과 발생하는 실권주 및 단수주는 우선적으로 초과청약자에게 배정되며, 이후 실권이 발생할 경우에 대해서는 일반에게 공모합니다. ※ 예외적으로 모집(매출)에 따른 주식 취득이 허용되는 경우 ① 모집(매출)에 따른 주식 취득이 금지되는 공매도 거래 기간 중에 전체 공매도 주문수량보다 많은 수량의 주식을 가격경쟁에 의한 거래 방식으로 매수한 경우 (매매계약 체결일 기준으로 정규시장의 매매거래시간에 매수한 경우로 한정) ② 한국거래소의 증권시장업무규정 또는 파생상품시장업무규정에서 정한 유동성 공급 및 시장조성 목적을 위해 해당 주식을 공매도하거나 공매도 주문을 위탁한 경우 ③ 동일한 법인 내에서 모집(매출)에 따른 주식 취득 참여가 금지되는 공매도 거래 기간 중 공매도를 하지 않거나 공매도 주문을 위탁하지 않은 독립거래단위*가 모집(매출)에 따른 주식을 취득하는 경우 * 금융투자업규정 제6-30조 제5항에 따라 의사결정이 독립적이고 상이한 증권계좌를 사용하는 등의 요건을 갖춘 거래단위 |
▶ 구주주 1주당 배정비율 산출근거
| A. 보통주식 | 15,223,000 |
| B. 우선주식 | - |
| C. 발행주식총수 (A + B) | 15,223,000 |
| D. 자기주식 + 자기주식신탁 | - |
| E. 자기주식을 제외한 발행주식총수 (C - D) | 15,223,000 |
| F. 유상증자 주식수 | 3,938,000 |
| G. 증자비율 (F / C) | 0.2586875123 |
| H. 구주주 1주당 배정비율 (F/ E) | 0.2586875123 |
3. 공모가격 결정방법
■ 확정 발행가액 산정
「증권의발행및공시등에관한규정」 제5-18조 (유상증자의 발행가액 결정)에 의거, 주주배정 증자 시 할인율 등이 자율화 되어 발행가는 자유롭게 산정할 수 있으나, 시장혼란 우려 및 기존 관행 등으로 (舊)「유가증권발행및공시등에관한 규정」 제 57조의 방식을 일부 준용하여 발행가액을 산정합니다.
① 1차 발행가액 산정 : 신주배정기준일전 제 3거래일을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액을 기준주가로 하여 할인율 25%를 적용, 다음의 산식에 의하여 산정된 발행가액을 1차 발행가액으로 합니다. 단, 호가단위 미만은 절상하며, 1주당 발행가액이 액면가 미만일 경우에는 액면가로 합니다.
| 기준주가 ×【 1 - 할인율(25%)】 | ||
| ▶ 1차 발행가액 | = | ------------------------------------- |
| 1 + 【증자비율 × 할인율(25%)】 |
② 2차 발행가액 산정 : 2차발행가액은 구주주 청약일전 제 3거래일을 기산일로 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1주일 가중산술평균주가 및 기산일 종가를 산술평균하여 산정한 가액과 기산일 종가 중 낮은 금액에 동일한 할인율(25%)을 적용하여 다음의 산식에 의하여 산정한 발행가액으로 합니다. 단, 호가단위 미만은 절상하며, 1주당 발행가액이 액면가 미만일 경우에는 액면가로 합니다.
▶ 2차 발행가액 = 기준주가 ×【1 - 할인율(25%)】
③ 확정 발행가액 산정 : 확정발행가액은 ① 의 1차발행가액과 ② 의 2차발행가액 중 낮은 가액으로 합니다. 단, 「자본시장과 금융투자업에관한법률」 제165조의6 및 「증권의 발행 및 공시에 관한 규정」제5-15조의2의 산출근거에 의거, 청약일 전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가를 기준주가로 할인율 40% 적용하여 산정한 가액이 ① 의 1차발행가액과 ② 의 2차발행가액 중 낮은 가액을 초과하는 경우 동 금액을 확정 발행가액으로 합니다. (단, 호가단위 미만은 절상함)
▶ 확정 발행가액 = Max{Min[1차 발행가액, 2차 발행가액], 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가의 60%}
④ 모집가액 확정공시에 관한 사항 : 1차 발행가액은 신주배정기준일전 제3거래일(2023년 09월 18일)에 결정되어 2023년 09월 19일에 금융감독원 전자공시시스템에 공시될 예정이며, 확정 발행가액은 구주주청약일전 제3거래일(2023년 10월 27일)에 결정되어 2023년 10월 30일에 금융감독원 전자공시시스템에 공시될 예정이며, 정관에서 정한 당사 인터넷 홈페이지(www.vaxcell-bio.com)에 공고하여 개별통지에 갈음할 예정입니다. 확정 발행가액 결정에 따라 정정 신고서(증권발행조건확정)가 금융감독원 전자공시시스템에 공시 됩니다.
※ 일반공모 발행가액은 구주주 청약시에 적용된 확정 발행가액을 동일하게 적용합니다.
4. 모집 또는 매출절차 등에 관한 사항
가. 모집 또는 매출조건
| (단위 : 주, 원) |
| 항 목 | 내 용 | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 모집 또는 매출주식의 수 | 3,938,000 | ||||||||||||||||||||||||||||||||
| 주당 모집가액 또는 매출가액 |
예정가액 | - | |||||||||||||||||||||||||||||||
| 확정가액 | 18,230 |
||||||||||||||||||||||||||||||||
| 모집총액 또는 매출총액 |
예정가액 | - | |||||||||||||||||||||||||||||||
| 확정가액 | 71,789,740,000 |
||||||||||||||||||||||||||||||||
| 청 약 단 위 |
(1) "구주주"의 청약단위는 1주로 하며, 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식수에 신주배정비율("주주 배정분"에 해당하는 주식수를 자기주식을 제외한 발행주식 총수로 나눈 비율을 말하며, 자기주식과 발행주식총수는 신주배정기준일 현재의 주식수를 말한다)을 곱하여 산정된 배정주식수로 합니다. 다만, 신주배정기준일 현재 신주배정비율은 자기주식 변동으로 인하여 변경될 수 있습니다(단, 1주 미만은 절사한다).
|
||||||||||||||||||||||||||||||||
| 청약기일 | 구주주 (신주인수권증서 보유자) |
개시일 | 2023년 11월 01일 | ||||||||||||||||||||||||||||||
| 종료일 | 2023년 11월 02일 | ||||||||||||||||||||||||||||||||
| 일반모집 또는 매출 | 개시일 | 2023년 11일 06일 | |||||||||||||||||||||||||||||||
| 종료일 | 2023년 11월 07일 | ||||||||||||||||||||||||||||||||
| 청약 증거금 |
구주주(신주인수권증서 보유자) | 청약금액의 100% | |||||||||||||||||||||||||||||||
| 초 과 청 약 | 청약금액의 100% | ||||||||||||||||||||||||||||||||
| 일반모집 또는 매출 | 청약금액의 100% | ||||||||||||||||||||||||||||||||
| 납 입 기 일 | 2023년 11월 09일 | ||||||||||||||||||||||||||||||||
| 배당기산일(결산일) | 2023년 1월 1일 | ||||||||||||||||||||||||||||||||
| 주1) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정 요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. 주2) 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
나. 모집 또는 매출의 절차
(1) 공고의 일자 및 방법
| 구 분 | 공고일자 | 공고방법 |
|---|---|---|
| 신주발행공고 및 배정기준일(주주확정일) 공고 |
2023년 08월 08일 | 당사 인터넷 홈페이지 (www.vaxcell-bio.com) |
| 모집가액 확정의 공고 | 2023년 10월 30일 | 당사 인터넷 홈페이지 (www.vaxcell-bio.com) |
| 실권주 일반공모 청약공고 | 2023년 11월 03일 | 당사 인터넷 홈페이지 (www.vaxcell-bio.com) 한국투자증권(주) 홈페이지 (securities.koreainvestment.com) 신한투자증권(주) 홈페이지 (www.shinhansec.com) |
| 실권주 일반공모 배정공고 | 2023년 11월 09일 | 한국투자증권(주) 홈페이지 (securities.koreainvestment.com) 신한투자증권(주) 홈페이지 (www.shinhansec.com) |
| 주1) 청약결과 초과청약금 환불에 대한 통지는 공동대표주관회사 홈페이지에 게시함으로써 개별통지에 갈음합니다. 주2) 전산장애 또는 그 밖의 부득이한 사유로 회사의 인터넷 홈페이지(www.vaxcell-bio.com)에 공고를 할 수 없는 때에는, 광주광역시에서 발행되는 일간 광주일보에 게재하며, 기타 부득이한 사유로 일간 광주일보에 게재할 수 없는 경우에는 서울특별시에서 발행되는 일간 한국경제신문에 게재합니다. |
(2) 청약방법
① 구주주 청약(신주인수권증서 보유자 청약) : 구주주 중 주권을 증권회사에 예탁한 주주(기존 "실질주주". 이하 "일반주주"라 합니다.)는 주권을 예탁한 증권회사의 본ㆍ지점 및 공동대표주관회사의 본ㆍ지점에서 청약할 수 있습니다. 다만, 구주주 중 명의개서대행기관 특별계좌에 주식을 가지고 있는 주주(기존 "명부주주". 이하 "특별계좌 보유자"라 합니다.)는 신주배정통지서를 첨부하여 실명확인증표를 제시한 후 공동대표주관회사의 본ㆍ지점에서 청약할 수 있습니다. 청약 시에는 소정의 청약서 2통에 필요한 사항을 기입하여 청약증거금과 함께 제출하여야 합니다.
| 2019년 09월 16일 전자증권제도가 시행되며, 주권 상장법인의 상장주식은 전자증권 의무전환대상으로 전자증권제도 시행일에 전자증권으로 일괄전환됩니다. 전자증권제도 시행전까지 증권회사에 예탁하고 있는 실질주주 주식은 해당 증권회사 계좌에 전자증권으로 일괄 전환되며, 기존 명부주주가 보유한 주식은 명의개서대행기관이 개설하는 특별계좌에 발행되어 소유자별로 관리됩니다. 금번 유상증자시 신주인수권증서는 전자증권제도 시행일 이후에 발행되고 상장될 예정으로 전자증권으로 발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다. '특별계좌 보유자(기존 '명부주주')'는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후 금번 유상증자 청약 참여또는 신주인수권증서의 매매가 가능합니다. '특별계좌 보유자(기존 '명부주주')'는 신주인수권증서의 '일반 전자등록계좌(증권회사 계좌)'로 이전 없이 공동대표주관회사인 한국투자증권(주)와 신한투자증권(주)의 본ㆍ지점에서 직접 청약하는 방법으로도 금번 유상증자에 청약이 가능합니다. 다만 신주인수권증서의 매매는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후에만 가능하므로 이 점 유의하시기 바랍니다. |
|
「주식ㆍ사채 등의 전자등록에 관한 법률」 |
② 초과청약 : 신주인수권증서 청약을 한자에 한하여 신주인수권증서 청약 한도 주식수의 20%를 추가로 청약할 수 있습니다. 이때, 신주인수권증서 청약 한도주식수의 20%에 해당하는 주식 중 소수점 이하인 주식은 청약할 수 없습니다.
a. 청약한도 주식수 = 신주인수권증서청약 한도주식수 + 초과청약한도 주식수
b. 신주인수권증서청약 한도주식수 = 보유한 신주인수권 증서의 수량
c. 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 * 초과청약 비율(20%)
③ 일반공모 청약: 고위험고수익투자신탁, 벤처기업투자신탁 및 일반청약자는「금융실명거래 및 비밀보장에 관한 법률」의 규정에 의한 실명자이어야 하며, 청약사무 취급처에 실명확인증표를 제시하고 청약합니다. 고위험고수익투자신탁, 벤처기업투자신탁 및 일반청약자의 청약 시, 각 청약처별 다중청약은 가능하나, 한 개의 청약처에서 이중청약은 불가능하며, 집합투자기구 중 운용주체가 다른 집합투자기구를 제외한 청약자의 한 개의 청약처에 대한 복수청약은 불가능합니다. 또한 고위험고수익투자신탁은 청약 시, 청약사무 취급처에 「증권 인수업무 등에 관한 규정」 제2조제18호에 따른 요건을 충족함을 확약하는 서류 및 자산총액이 기재되어 있는 서류를 함께 제출하여야 합니다. 벤처기업투자신탁은 청약 시, 청약사무 취급처에 「증권 인수업무 등에 관한 규정」 제2조제20호에 따른 요건을 충족하고, 제9조제10항에 따른 확약서 및 자산총액이 기재되어 있는 서류를 함께 제출하여야 합니다.
④ 청약은 청약주식의 단위에 따라 할 수 있으며 1인당 청약한도를 초과하는 청약부분에 대하여는 청약이 없는 것으로 하고, 청약사무취급처는 그 차액을 납입일에 당해 청약자에게 반환하며, 이때 받은 날부터의 이자는 지급하지 않습니다.
⑤ 본 유상증자에 청약하고자 하는 투자자(「자본시장과 금융투자업에 관한 법률」 제9조 제5항에 규정된 전문투자자 및 「자본시장과 금융투자업에 관한 법률 시행령」 제132조에 따라 투자설명서의 교부가 면제되는자 제외)는 청약 전 반드시 투자설명서를 교부 받아야 하고, 이를 확인하는 서류에 서명 또는 기명날인하여야 합니다.
⑥ 청약한도
a. 구주주의 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율인 0.2586875123주를 곱하여 산정된 신주인수권증서(단, 1주 미만은 절사)와 초과청약가능 주식수(보유하고 있는 신주인수권증서 1주당 0.2주를 곱하여 산정된 수, 단 1주 미만은 절사)를 합한 주식수로 하되, 자기주식, 자사주신탁, 주식관련사채의 권리행사 등의 변동으로 인하여 구주주의 1주당 배정 비율은 변동될 수 있습니다.
b. 일반공모 청약자의 청약한도는 일반공모 총 공모주식 100% 범위 내로 하며, 청약한도를 초과하는 부분에 대해서는 청약이 없는 것으로 간주합니다.
⑦ 기타
a. 일반공모 배정을 함에 있어 이중청약이 있는 경우에는 그 청약자의 청약 전부를 청약하지 아니한 것으로 봅니다. 단, 구주주가 신주배정비율에 따라 배정받은 주식을 청약한 후 일반공모에 참여하는 경우에는 금지되는 이중청약이 있는 경우로 보지 않습니다. 단, 동일한 집합투자기구라도 운용주체(집합투자업자)가 다른 경우는 예외로 합니다.
b. 1인당 청약한도를 초과하는 청약부분에 대하여는 청약이 없는 것으로 합니다.
c. 청약자는 「금융실명거래 및 비밀보장에 관한 법률」에 의거 실지 명의에 의해 청약해야 합니다.
d. 자본시장과 금융투자업에 관한 법률」 제180조의4 및 같은 법 시행령 제208조의4제1항에 따라 2023년 08월 08일부터 2023년 10월 27일까지 공매도를 하거나 공매도 주문을 위탁한 자는 금번 모집(매출)에 청약할 수 없으며, 이를 위반하여 주식을 취득할 경우 같은 법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만 모집(매출)가액의 공정한 가격형성을 저해하지 않는 경우로서 같은 법 시행령 제208조의4제2항 및 「금융투자업규정」 제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다.
|
※ 예외적으로 모집(매출)에 따른 주식 취득이 허용되는 경우 ① 모집(매출)에 따른 주식 취득이 금지되는 공매도 거래 기간 중에 전체 공매도 주문수량보다 많은 수량의 주식을 가격경쟁에 의한 거래 방식으로 매수한 경우 (매매계약 체결일 기준으로 정규시장의 매매거래시간에 매수한 경우로 한정) ② 한국거래소의 증권시장업무규정 또는 파생상품시장업무규정에서 정한 유동성 공급 및 시장조성 목적을 위해 해당 주식을 공매도하거나 공매도 주문을 위탁한 경우 ③ 동일한 법인 내에서 모집(매출)에 따른 주식 취득 참여가 금지되는 공매도 거래 기간 중 공매도를 하지 않거나 공매도 주문을 위탁하지 않은 독립거래단위(*)가 모집(매출)에 따른 주식을 취득하는 경우 (*) 금융투자업규정 제6-30조 제5항에 따라 의사결정이 독립적이고 상이한 |
(3) 청약취급처
| 청약대상자 | 청약취급처 | 청약일 | |
|---|---|---|---|
| 구주주 (신주인수권증서 보유자) |
특별계좌 보유자 (기존 '명부주주') |
한국투자증권(주), 신한투자증권(주)의 본ㆍ지점 | 2023년 11월 01일 ~ 2023년 11월 02일 |
| 일반주주 (기존 '실질주주') |
1) 주주확정일 현재 주식회사 박셀바이오의 주식을 예탁하고 있는 당해 증권회사 본ㆍ지점 2) 한국투자증권(주), 신한투자증권(주) 본ㆍ지점 |
||
| 일반공모청약 (고위험고수익투자신탁 및 벤처기업투자신탁청약 포함) |
한국투자증권(주) 및 신한투자증권(주) 본ㆍ지점 | 2023년 11월 06일 ~ 2023년 11월 07일 |
|
(4) 청약결과 배정방법
① 구주주(신주인수권증서 보유자) 청약 : '신주배정기준일' 18:00 현재 주주명부에 등재된 주주(이하 "구주주"라 한다)에게 본 주식을 1주당 0.2586875123주를 곱하여 산정된 배정주식수(단, 1주 미만은 절사함)로 하고, 배정범위 내에서 청약한 수량만큼 배정합니다. 단, 신주배정기준일 전 주식관련사채 및 종류주식의 권리행사, 주식매수선택권의 행사 등으로 1주당 배정주식수가 변경될 수 있습니다.
② 초과청약 : 구주주(신주인수권증서 보유자) 청약 이후 발생한 실권주가 있는 경우, 실권주를 구주주(신주인수권증서 보유자)가 초과청약(초과청약비율 : 배정 신주 1주당 0.2주)한 주식수에 비례하여 배정하며, 1주 미만의 주식은 절사하여 배정하지 않습니다. (단, 초과청약 주식수가 실권주에 미달한 경우 100% 배정)
(i) 청약한도 주식수 = 신주인수권증서청약 한도주식수 + 초과청약한도 주식수
(ii) 신주인수권증서청약 한도주식수 = 보유한 신주인수권 증서의 수량
(iii) 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 x 초과청약 비율(20%)
③ 일반공모 청약 : 상기 구주주 청약 및 초과청약 결과 발생한 실권주 및 단수주(이하 "일반공모 배정분"이라 한다)는 "공동대표주관회사"가 다음 각호와 같이 일반에게 공모하되, 「증권 인수업무 등에 관한 규정」 제9조 제2항 제3호에 따라 고위험고수익투자신탁에 공모주식의 5%를 배정하고, 「증권 인수업무 등에 관한 규정」 제9조 제2항 제4호에 따라 벤처기업투자신탁에 공모주식의 30%를 배정합니다. 나머지 65%에 해당하는 주식은 개인청약자 및 기관투자자(집합투자업자 포함)에게 구분 없이 배정합니다. 고위험고수익투자신탁에 대한 공모주식 5%와 벤처기업투자신탁에 공모주식의 30%와 개인투자자 및 기관투자자에 대한 공모주식 65%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정합니다. 다만, 어떤 그룹에 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다.
(i) 일반공모에 관한 배정수량 계산 시에는 "공동대표주관회사"의 "청약물량" ("공동대표주관회사"의 각 청약처에서 일반공모 방식으로 접수를 받은 청약주식수를 의미하며, "공동대표주관회사"에 대하여 개별적으로 산정한 청약주식수를 말한다)에 대해서는 "공동대표주관회사"의 "총청약물량" ("공동대표주관회사"가 일반공모 방식으로 접수를 받은 "청약물량"의 합을 말한다)을 "일반공모 배정분" 주식수로 나눈 통합청약경쟁률에 따라 "공동대표주관회사"의 각 청약자에 배정하는 방식(이하 "통합배정"이라 한다)으로 합니다.
(ii) 일반공모에 관한 배정 시 "공동대표주관회사"의 "총청약물량"이 "일반공모 배정분" 주식수를 초과하는 경우에는 청약경쟁률에 따라 5사6입을 원칙으로 안분 배정하여 잔여주식이 최소화되도록 합니다. 다만, 고위험고수익투자신탁에 대한 공모주식 5%와 벤처기업투자신탁에 공모주식의 30%와 개인투자자 및 기관투자자(집합투자업자포함)에 대한 공모주식 65%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정합니다. 다만, 어떤 그룹에 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다. 이후 최종 잔여주식은 최대청약자부터 순차적으로 우선 배정하되, 동순위 최대청약자가 최종 잔여 주식보다 많은 경우에는 "공동대표주관회사"가 무작위 추첨방식을 통하여 배정합니다.
(iii) "공동대표주관회사"의 "총청약물량"이 "일반공모 배정분" 주식수에 미달하는 경우, "공동대표주관회사"는 "개별인수 의무주식수"를 각각 자기의 계산으로 인수합니다. "잔액인수계약서" 제2조제5항에 따라 "청약미달회사"("청약물량"이 "인수한도 의무주식수"보다 적은 회사를 말한다)의 "개별인수 의무주식수"는 "잔액인수계약서" 제2조제5항에 따른 "공동대표주관회사"의 인수비율로 나누어 산정하며, "청약미달회사"의 인수책임을 면하게 된 주식수는 "청약초과회사"("청약물량"이 "인수한도 의무주식수"를 초과하는 회사를 말한다)의 "초과청약물량"("청약물량"에서 "인수한도 의무주식수"를 차감한 주식수를 의미하되, 0 이상으로 한다)을 "청약미달회사"에게 배분하여 산정합니다.
(iv) 단, "공동대표주관회사"와 "인수회사"는「증권 인수업무 등에 관한 규정」 제9조 제2항에 의거 고위험고수익투자신탁등 및 일반청약자에 대하여 배정하여야 할 주식이 50,000주(액면가 500원 기준) 이하 이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 고위험고수익투자신탁등 및 일반청약자에게 배정하지 아니할 수 있습니다..
(5) 투자설명서 교부에 관한 사항
- 「자본시장과 금융투자업에 관한 법률」 제124조에 의거, 본 주식의 청약에 대한 투자설명서 교부 의무는 (주)박셀바이오, 공동대표주관회사인 한국투자증권(주), 신한투자증권(주)가 부담하며, 금번 유상증자의 청약에 참여하시는 투자자께서는 투자설명서를 의무적으로 교부받으셔야 합니다.
- 금번 유상증자에 청약하고자 하는 투자자께서는 (「자본시장과 금융투자업에 관한 법률」 제9조제5항에 규정된 전문투자자 및 「자본시장과 금융투자업에 관한 법률 시행령」 제132조에 따라 투자설명서의 교부가 면제되는 자 제외) 청약하시기 전 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
- 투자설명서 수령거부 의사 표시는 서면, 전화ㆍ전신ㆍFAX, 전자우편 및 이와 비슷한 전자통신으로만 하여야 합니다.
① 투자설명서 교부 방법 및 일시
| 구분 | 교부방법 | 교부일시 |
|---|---|---|
|
구주주 청약자 |
1),2),3)을 병행 1) 등기우편 송부 2) "공동대표주관회사"의 본지점 교부 3) "공동대표주관회사"의 홈페이지나 HTS, MTS에서 교부 |
1) 우편송부시 : 구주주청약초일인 2023년 11월 01일 전 수취 가능 2) "공동대표주관회사"의 본지점 : 청약종료일 (2023년 11월 02일)까지 3) "공동대표주관회사"의 홈페이지 또는 HTS, MTS 교부 |
|
일반 청약자 |
1), 2)를 병행 1) "공동대표주관회사"의 본지점에서 교부 2) "공동대표주관회사"의 홈페이지나 HTS, MTS 에서 교부 |
1) "공동대표주관회사"의 본지점 2) "공동대표주관회사"의 홈페이지 또는 HTS, MTS 교부 |
| ※ 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다. |
② 확인절차
a. 우편을 통한 투자설명서 수령시
- 청약하시기 위해 지점을 방문하셨을 경우, 직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
- HTS 또는 MTS를 통한 청약을 원하시는 경우, 청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
- 주주배정 유상증자 경우 유선청약이 가능합니다. 유선상으로 신분확인을 하신 후, 투자설명서 교부 확인을 해주시고 청약을 진행하여 주시기 바랍니다.
b. 지점 방문을 통한 투자설명서 수령시
직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
c. 홈페이지, HTS 또는 MTS를 통한 교부
청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
③ 기타
a. 금번 유상증자의 경우, 본 증권신고서의 효력발생 이후 주주명부상 주주에게 투자설명서를 우편으로 발송할 예정입니다. 우편의 반송 등에 의한 사유로 교부를 받지 못하신 투자자께서는, "공동대표주관회사"의 본ㆍ지점 방문을 통해 인쇄물을 받으실 수 있으며, 또한 동일한 내용의 투자설명서를 전자문서의 형태로 "공동대표주관회사"의 홈페이지에서 다운로드 받으실 수 있습니다. 한편, 일반공모 청약시 투자자께서는 "공동대표주관회사"에 방문하여 투자설명서 인쇄물을 수령하시거나 "공동대표주관회사"의 홈페이지에서 동일한 내용의 투자설명서를 전자문서의 형태로 다운로드 받으시는 2가지 방법으로 투자설명서를 교부받으실 수 있습니다. 다만, 전자문서의 형태로 교부 받으실 경우, 「자본시장과 금융투자업에 관한 법률」 제124조제1항 각호의 요건을 모두 충족해야만 청약이 가능합니다.
b. 구주주 청약시 공동대표주관회사 이외의 증권회사를 이용한 청약 방법
- 해당 증권회사의 청약방법 및 규정에 의해 청약을 진행하시기 바랍니다. 이 경우에도, 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
※ 투자설명서 교부를 받지 않거나, 수령거부의사를 서면 등의 방법으로 표시하지 않을 경우, 본 유상증자의 청약에 참여할 수 없습니다.
|
※ 관련법규 「자본시장과 금융투자업에 관한 법률」 1. 국가 2. 한국은행 3. 대통령령으로 정하는 금융기관 4. 주권상장법인. 다만, 금융투자업자와 장외파생상품 거래를 하는 경우에는 전문투자자와 같은 대우를 받겠다는 의사를 금융투자업자에게 서면으로 통지하는 경우에 한한다. 5. 그 밖에 대통령령으로 정하는 자
1. 전자문서에 의하여 투자설명서를 받는 것을 전자문서를 받을 자(이하 "전자문서수신자"라 한다)가 동의할 것 2. 전자문서수신자가 전자문서를 받을 전자전달매체의 종류와 장소를 지정할 것 3. 전자문서수신자가 그 전자문서를 받은 사실이 확인될 것 4. 전자문서의 내용이 서면에 의한 투자설명서의 내용과 동일할 것 ② 누구든지 증권신고의 대상이 되는 증권의 모집 또는 매출, 그 밖의 거래를 위하여 청약의 권유 등을 하고자 하는 경우에는 다음 각 호의 어느 하나에 해당하는 방법에 따라야 한다. 1. 제120조제1항에 따라 증권신고의 효력이 발생한 후 투자설명서를 사용하는 방법 2. 제120조제1항에 따라 증권신고서가 수리된 후 신고의 효력이 발생하기 전에 발행인이 대통령령으로 정하는 방법에 따라 작성한 예비투자설명서(신고의 효력이 발생되지 아니한 사실을 덧붙여 적은 투자설명서를 말한다. 이하 같다)를 사용하는 방법 3. 제120조제1항에 따라 증권신고서가 수리된 후 신문ㆍ방송ㆍ잡지 등을 이용한 광고, 안내문ㆍ홍보전단 또는 전자전달매체를 통하여 발행인이 대통령령으로 정하는 방법에 따라 작성한 간이투자설명서(투자설명서에 기재하여야 할 사항 중 그 일부를 생략하거나 중요한 사항만을 발췌하여 기재 또는 표시한 문서, 전자문서, 그 밖에 이에 준하는 기재 또는 표시를 말한다. 이하 같다)를 사용하는 방법 ③ 집합투자증권의 경우 제2항에도 불구하고 간이투자설명서를 사용할 수 있다. 다만, 투자자가 제123조에 따른 투자설명서의 사용을 별도로 요청하는 경우에는 그러하지 아니하다. <신설 2013. 5. 28.> ④ 제1항 및 제3항에 따라 집합투자증권의 간이투자설명서를 교부하거나 사용하는 경우에는 투자자에게 제123조에 따른 투자설명서를 별도로 요청할 수 있음을 알려야 한다. <신설 2013. 5. 28.>
1. 다음 각 목의 어느 하나에 해당하는 전문가 가. 전문투자자 나. 삭제 <2016. 6. 28.> 다. 「공인회계사법」에 따른 회계법인 라. 신용평가회사(법 제335조의3에 따라 신용평가업인가를 받은 자를 말한다. 이하 같다) 마. 발행인에게 회계, 자문 등의 용역을 제공하고 있는 공인회계사ㆍ감정인ㆍ변호사ㆍ변리사ㆍ세무사 등 공인된 자격증을 가지고 있는 자 바. 그 밖에 발행인의 재무상황이나 사업내용 등을 잘 알 수 있는 전문가로서 금융위원회가 정하여 고시하는 자 2. 다음 각 목의 어느 하나에 해당하는 연고자 가. 발행인의 최대주주[「금융회사의 지배구조에 관한 법률」 제2조제6호가목에 따른 최대주주를 말한다. 이 경우 "금융회사"는 "법인"으로 보고, "발행주식(출자지분을 포함한다. 이하 같다)"은 "발행주식"으로 본다. 이하 같다]와 발행주식 총수의 100분의 5 이상을 소유한 주주 나. 발행인의 임원(「상법」 제401조의2제1항 각 호의 자를 포함한다. 이하 이 호에서 같다) 및 「근로복지기본법」에 따른 우리사주조합원 다. 발행인의 계열회사와 그 임원 라. 발행인이 주권비상장법인(주권을 모집하거나 매출한 실적이 있는 법인은 제외한다)인 경우에는 그 주주 마. 외국 법령에 따라 설립된 외국 기업인 발행인이 종업원의 복지증진을 위한 주식매수제도 등에 따라 국내 계열회사의 임직원에게 해당 외국 기업의 주식을 매각하는 경우에는 그 국내 계열회사의 임직원 바. 발행인이 설립 중인 회사인 경우에는 그 발기인 사. 그 밖에 발행인의 재무상황이나 사업내용 등을 잘 알 수 있는 연고자로서 금융위원회가 정하여 고시하는 자 제132조(투자설명서의 교부가 면제되는 자) 1. 제11조제1항제1호다목부터 바목까지 및 같은 항 제2호 각 목의 어느 하나에 해당하는 자 1의2. 제11조제2항제2호 및 제3호에 해당하는 자 2. 투자설명서를 받기를 거부한다는 의사를 서면, 전화ㆍ전신ㆍ팩스, 전자우편 및 이와 비슷한 전자통신, 그 밖에 금융위원회가 정하여 고시하는 방법으로 표시한 자 3. 이미 취득한 것과 같은 집합투자증권을 계속하여 추가로 취득하려는 자. 다만, 해당 집합투자증권의 투자설명서의 내용이 직전에 교부한 투자설명서의 내용과 같은 경우만 해당한다. |
(6) 주권 유통에 관한 사항
- 주권유통개시(예정)일: 2023년 11월 23일 (2019년 9월 16일 전자증권제도가 시행됨에 따라 실물 주권의 교부 없이 각 주주의 보유 증권계좌로 상장일에 주식이 등록발행되어 입고되며, 상장일부터 유통이 가능합니다. 단, 유관기관과의 업무 협의 과정에서 상기 일정은 변경될 수 있음을 유의하시기 바랍니다.)
(7) 청약증거금의 대체 및 반환 등에 관한 사항
- 청약증거금은 청약금액의 100%로 하고, 주금납입기일에 주금납입금으로 대체하며, 청약증거금에 대해서는 무이자로 합니다. 일반공모 총 청약주식수(기관투자자 포함)가 일반공모주식수를 초과하여 청약증거금이 발생한 경우, 그 초과 청약증거금은 2023년 11월 09일부터 해당 청약사무 취급처에서 환불합니다.
(8) 주금납입장소 : 광주은행 화순전대병원출장소
다. 신주인수권증서에 관한 사항
| 신주배정기준일 | 신주인수권증서의 매매 금융투자업자 | |
|---|---|---|
| 회사명 | 회사고유번호 | |
| 2023년 09월 21일 | 한국투자증권(주) | 00160144 |
| 2023년 09월 21일 | 신한투자증권(주) | 00138321 |
(1) 금번과 같이 주주배정방식의 유상증자를 실시할 때, 주주가 소유하고 있는 주식수 비율대로 신주를 인수할 권리인 신주인수권에 대하여 당사는 「자본시장과 금융투자업에 관한 법률」 제165의6조3항 및 「증권의 발행 및 공시 등에 관한 규정」 제5-19조에 의거하여 주주에게 신주인수권증서를 발행합니다.
(2) 금번 유상증자시 신주인수권증서는 전자증권제도 시행일(2019년 09월 16일) 이후에 발행되고 상장될 예정으로 전자증권으로 발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여 배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다.
(3) 신주인수권증서 매매의 중개를 할 증권회사는 공동대표주관회사인 한국투자증권(주)과 신한투자증권(주)로 합니다.
(4) 신주인수권증서 매매 등
① 금번 유상증자시 신주인수권증서는 전자증권제도 시행 이후에 발행되고 상장될 예정으로 실물은 발행 되지 않고 전자증권으로 등록발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여 배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다.
② 신주인수권증서를 매매하고자 하는 주주는 신주인수권증서를 예탁하고 있는 증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자 계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일 내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
(5) 신주인수권증서를 양수한 투자자의 청약방법
신주인수권증서를 증권회사에 예탁하고 있는 양수인은 당해 증권회사 점포 및 한국투자증권(주), 신한투자증권(주)의 본ㆍ지점을 통해 해당 신주인수권증서에 기재되어 있는 수량(초과청약이 있는 경우 초과청약 가능수량이 합산된 수량)만큼 청약할 수 있으며 청약 기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
(6) 신주인수권증서의 상장
당사는 금번 주주배정후 실권주 일반공모 유상증자 관련 신주인수권증서의 상장을 한국거래소에 신청할 예정입니다. 동 신주인수권증서가 상장될 경우 상장기간은 2023년 10월 17일부터 2023년 10월 23일까지 5거래일간으로 예정하고 있으며, 동 기간중 상장된 신주인수권증서를 한국거래소에서 매매할 수 있습니다. 동 신주인수권증서는 2023년 10월 24일에 상장폐지될 예정입니다. 「코스닥시장 상장규정」 제83조(신주인수권증권 및 신주인수권증서의 신규상장)에 따라 5거래일 이상 상장되어야 하며, 동 규정 제85조(신주인수권증권 및 신주인수권증서의 상장폐지)에 따라 신주청약 개시일 5거래일전에 상장폐지되어야 함)
|
※ 관련법령 제165조의6(주식의 발행 및 배정 등에 관한 특례) ③ 주권상장법인은 제1항제1호의 방식으로 신주를 배정하는 경우 「상법」 제416조제5호 및 제6호에도 불구하고 주주에게 신주인수권증서를 발행하여야 한다. 이 경우 주주 등의 이익 보호, 공정한 시장질서 유지의 필요성 등을 고려하여 대통령령으로 정하는 방법에 따라 신주인수권증서가 유통될 수 있도록 하여야 한다. 제176조의8(주식의 발행 및 배정에 관한 방법 등) ④ 법 제165조의6제3항 후단에서 "대통령령으로 정하는 방법"이란 다음 각 호의 어느 하나에 해당하는 방법을 말한다. 1. 증권시장에 상장하는 방법 2. 둘 이상의 금융투자업자(주권상장법인과 계열회사의 관계에 있지 아니한 투자매매업자 또는 투자중개업자를 말한다)를 통하여 신주인수권증서의 매매 또는 그 중개ㆍ주선이나 대리업무가 이루어지도록 하는 방법. 이 경우 매매 또는 그 중개ㆍ주선이나 대리업무에 관하여 필요한 세부사항은 금융위원회가 정하여 고시한다.
제83조(신주인수권증권 및 신주인수권증서의 신규상장) ② 신주인수권증권을 신규상장하려면 다음 각 호의 심사요건을 모두 충족하여야 한다. 1. 신주인수권증권의 발행회사의 주식(외국주식예탁증권을 포함한다. 이하 이 장에서 같다)이 코스닥시장에 상장되어 있을 것 2. 신주인수권증권의 발행회사의 상장 주식이 상장신청일 현재 이 규정에 따른 관리종목으로 지정되지 않고, 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유에 해당되지 않을 것 3. 신주인수권증권의 발행총수가 1만 증권 이상일 것. 이 경우 해당 증권의 목적인 신주가 액면주식인 경우에는 액면가액 5,000원을 기준으로 한다. 4. 신주인수권증권의 잔존 권리행사기간이 상장신청일 현재 1년 이상일 것 5. 신주인수권부사채권이 모집 또는 매출로 발행되었을 것. 다만, 주주에게 해당 사채권의 인수권이 주어진 경우에는 그러하지 아니하다. ③ 신주인수권증서를 신규상장하려면 다음 각 호의 심사요건을 모두 충족하여야 한다. 1. 신주인수권증서의 발행회사의 주식이 코스닥시장에 상장되어 있을 것 2. 신주인수권증서의 발행회사의 상장 주식이 상장신청일 현재 이 규정에 따른 관리종목으로 지정되지 않고, 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유에 해당되지 않을 것 3. 신주인수권의 양도를 허용하고, 신주인수권을 갖는 모든 주주에게 신주인수권증서를 발행하였을 것 4. 신주인수권증서의 발행총수가 1만 증서 이상일 것. 이 경우 해당 증서의 목적인 신주가 액면주식인 경우에는 액면가액 5,000원을 기준으로 한다. 5. 신주인수권증서의 거래 가능 기간이 5일(매매거래일을 기준으로 한다) 이상일 것 제85조(신주인수권증권 및 신주인수권증서의 상장폐지) 1. 신주인수권증권의 목적인 주식이 관리종목으로 지정되거나, 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 2. 신주인수권증권의 목적인 주식에 대한 상장폐지 신청으로 해당 주식이 상장폐지되는 경우 3. 신주인수권 행사기간이 만료되거나 행사가 완료된 경우 4. 그 밖에 공익 실현과 투자자 보호를 위하여 거래소가 신주인수권증권의 상장폐지가 필요하다고 인정하는 경우 ② 거래소는 신주인수권증서가 다음 각 호의 어느 하나에 해당하는 경우 해당 신주인수권증서의 상장을 폐지한다. 1. 신주인수권증서의 목적인 주식이 관리종목으로 지정되거나, 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 2. 신주인수권증서의 목적인 주식에 대한 상장폐지 신청으로 해당 주식이 상장폐지되는 경우 3. 신주 청약 개시일의 5일(매매거래일을 기준으로 한다) 전이 된 경우. 다만, 신주인수권증서의 유통상황을 고려하여 세칙으로 정하는 경우에는 그 기간 전으로 한다. 4. 그 밖에 공익 실현과 투자자 보호를 위하여 거래소가 신주인수권증서의 상장폐지가 필요하다고 인정하는 경우 |
(7) 신주인수권증서의 거래 관련 추가사항
당사는 금번 유상증자의 신주인수권증서를 상장신청할 예정인 바, 현재까지 관계기관과 협의된 신주인수권증서 상장시의 제반 거래관련 사항은 다음과 같습니다.
① 상장방식 : 전자등록발행된 신주인수권증서 전부를 상장합니다.
② 일반주주의 신주인수권증서 거래
| 구분 | 상장거래방식 | 계좌대체 거래방식 |
|---|---|---|
| 방법 | 주주의 신주인수권증서를 전자등록발행하여 상장합니다. 상장된 신주인수권증서를 장내거래를 통하여 매수하여 증권사 계좌에 보유한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. 주주의 신주인수권증서는 전자등록발행되므로 실물 증서는 발행되지 않습니다. | 신주인수권증서를 매매하고자 하는 기존 실질주주는 위탁증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. |
| 기간 | 2023년 10월 17일부터 2023년 10월 23일까지(5거래일간) 거래 | 신주배정통지일(2023년 10월 06일(예정))부터 신주인수권증서의 상장거래 마지막 날 이후 제2영업일(2023년 10월 25일)까지 거래 |
| 주1) | 상장거래 : 2023년 10월 17일부터 2023년 10월 23일까지(5영업일간) 거래 가능합니다. |
| 주2) |
계좌대체거래 : 신주배정통지일인 2023년 10월 06일(예정)부터 2023년 10월 25일까지 거래 가능합니다. -> 신주인수권증서 상장거래의 결제일인 2023년 10월 25일까지 계좌대체(장외거래) 가능하며, 동일 이후부터는 신주인수권증서의 청약권리 명세를 확정하므로 신주인수권증서의 계좌대체(장외거래)가 제한됩니다. |
| 주3) | 신주인수권증서는 전자등록발행되므로 실물은 발행되지 않습니다. |
③ 특별계좌 소유주(기존 '명부주주')의 신주인수권증서 거래
a. '특별계좌 보유자(기존 '명부주주')'는 명의개서대행기관에 '특별계좌'에서 '일반전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후 금번 유상증자 청약 참여 또는 신주인수권증서의 매매가 가능합니다.
b. '특별계좌 보유자(기존 '명부주주')'는 신주인수권증서의 '일반 전자등록계좌(증권회사 계좌)'로 이전 없이 공동대표주관회사의 본ㆍ지점에서 직접 청약하는 방법으로도 금번 유상증자에 청약이 가능합니다. 다만 신주인수권증서의 매매는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후에만 가능하므로 이 점 유의하시기 바랍니다.
라. 기타 모집 또는 매출에 관한 사항
(1) 본 증권신고서는 공시심사 과정에서 일부 내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요 내용의 변경시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있으므로 투자자 여러분께서는 투자 시 이러한 점을 감안하시기 바랍니다.
(2) 「자본시장과 금융투자업에 관한 법률」 제120조 3항에 의거 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다.
(3) 본 증권신고서에 기재된 내용은 신고서 제출일 현재까지 발생된 것으로 본 신고서에 기재된 사항 이외에 자산, 부채, 현금흐름 또는 손익상황에 중대한 변동을 가져오거나 중요한 영향을 미치는 사항은 없습니다. 따라서, 주주 및 투자자가 투자의사를 결정함에 있어 유의하여야 할 사항이 본 증권신고서상에 누락되어 있지 않습니다.
(4) 금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서, 반기보고서, 분기보고서 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있사오니 투자의사를 결정하시는 데 참조하시기 바랍니다.
(5) 본 증권신고서의 예정 모집가액은 확정되어 있는 것은 아니며, 청약일 3거래일 전에 확정 발행가액을 산정함으로써 확정될 예정입니다. 또한, 본 증권신고서의 발행예정금액은 추후 주당 발행가액이 확정되는 내용에 따라 변경될 수 있음을 유의하여 주시기 바랍니다.
5. 인수 등에 관한 사항
| [인수방법: 잔액인수] |
| 인수인 | 인수주식 종류 및 수 | 인수대가 | |
|---|---|---|---|
| 공동대표주관회사 | 한국투자증권(주) | 인수주식의 종류: 기명식 보통주식 인수주식의 수: 인수한도 의무주식수 X 80% |
- 인수수수료: 모집총액의 1.3% 中 80.0% - 추가수수료: 잔액인수금액의 15.0% |
| 공동대표주관회사 | 신한투자증권(주) | 인수주식의 종류: 기명식 보통주식 인수주식의 수: 인수한도 의무주식수 X 20% |
- 인수수수료: 모집총액의 1.3% 中 20.0% - 추가수수료: 잔액인수금액의 15.0% |
| 주1) 모집총액 : 최종 발행가액 × 총 발행주식수 주2) 인수한도 의무주식수는 일반공모 실시 전 수량 기준이며, 실제 인수인별 잔액인수 수량은 인수인별로 집계된 일반공모 청약 수량에 따라 변동될 수 있습니다. 일반공모를 거쳐 배정 후에도 미 청약된 잔여주식 또는 청약 미달주식에 대하여는 공동대표주관회사가 자기계산으로 잔액인수하기로 합니다. |
II. 증권의 주요 권리내용
1. 액면금액 : 기명식 보통주 1주당 500원
|
※ 당사의 정관 (이하 동일) 본 회사가 발행하는 주식 1주의 금액은 500원으로 한다. |
2. 주식에 관한 사항
|
제5조(발행예정주식총수) 제7조(1주의 금액) 본 회사가 발행하는 주식 1주의 금액은 500원으로 한다. 제8조(주식 등의 전자등록) 회사는 「주식·사채 등의 전자등록에 관한 법률」 제2조 제1호에 따른 주식 등을 발행하는 경우에는 전자등록기관의 전자등록계좌부에 주식 등을 전자등록 하여야 한다. 제9조(주식의 종류) ① 본 회사가 발행할 주식의 종류는 보통주식과 종류주식으로 한다. ② 회사가 발행하는 종류주식은 이익배당에 관한 우선주식, 의결권 배제 또는 제한에 관한 주식, 상환주식, 전환주식 및 이들의 전부 또는 일부를 혼합한 주식으로 한다. ③ 회사가 발행할 주권의 종류는 1주권, 5주권, 10주권, 50주권, 100주권, 500주권, 1,000주권, 10,000주권의 8종으로 한다. 다만, 「주식·사채등의 전자등록에 관한 법률」에 따라 전자등록계좌부에 주식 등을 전자등록하는 경우에는 동 조항의 적용을 배제한다. |
3. 의결권에 관한 사항
|
제26조(주주의 의결권) 주주의 의결권은 1주마다 1개로 한다. 제27조(상호주에 대한 의결권 제한) 회사, 회사와 회사의 자회사 또는 회사의 자회사가 다른 회사의 발행주식총수의 10분의 1을 초과하는 주식을 가지고 있는 경우, 그 다른 회사가 가지고 있는 이 회사의 주식은 의결권이 없다. 제28조(의결권의 불통일행사) ① 2 이상의 의결권을 가지고 있는 주주가 의결권의 불통일행사를 하고자 할 때에는 회일의 3일전에 회사에 대하여 서면 또는 전자문서로 그 뜻과 이유를 통지하여야 한다. ② 회사는 주주의 의결권의 불통일행사를 거부할 수 있다. 그러나 주주가 주식의 신탁을 인수하였거나 기타 타인을 위하여 주식을 가지고 있는 경우에는 그러하지 아니하다. 제29조(의결권의 행사) ① 주주는 총회에 출석하지 아니하고 서면에 의하여 의결권을 행사할 수 있다. ② 서면에 의하여 의결권을 행사하고자 하는 주주는 의결권행사에 관한 서면에 필요한 사항을 기재하여, 회일의 전일까지 회사에 제출하여야 한다. ③ 주주는 대리인으로 하여금 그 의결권을 행사하게 할 수 있으며, 이 경우 대리인은 주주총회 개시 전에 그 대리권을 증명하는 서면(위임장)을 제출하여야 한다. |
4. 신주인수권에 관한 사항
|
제10조(신주인수권) ① 당 회사의 주주는 신주발행에 있어서 그가 소유한 주식의 수에 비례하여 신주의 배정을 받을 권리를 갖는다. ② 회사는 제1항의 규정에도 불구하고 다음 각 호의 어느 하나에 해당하는 경우 이사회의 결의로 주주 외의 자에게 신주를 배정할 수 있다. 1. 발행주식총수의 100분의 30을 초과하지 않는 범위 내에서 「자본시장과 금융투자업에 관한 법률」 제165조의6에 따라 일반공모증자 방식으로 신주를 발행하는 경우 2. 「상법」 제340조의 2 및 제542조의3에 따른 주식매수선택권의 행사로 인하여 신주를 발행하는 경우 3. 발행하는 주식총수의 100분의 20 범위 내에서 우리사주조합원에게 주식을 우선배정하는 경우 4. 근로복지기본법 제39조의 규정에 의한 우리사주매수선택권의 행사로 인하여 신주를 발행하는 경우 5. 발행주식총수의 100분의 30을 초과하지 않는 범위 내에서 긴급한 자금조달을 위하여 국내외 금융기관 또는 기관투자자에게 신주를 발행하는 경우 6. 발행주식총수의 100분의 20을 초과하지 않는 범위 내에서 사업상 중요한 기술도입, 연구개발, 생산, 판매, 자본제휴, 재무구조의 개선 등 회사의 경영상 목적을 달성하기 위하여 그 상대방에게 신주를 발행하는 경우 7. 주권을 한국거래소에 상장하기 위하여 신주를 모집하거나 인수인에게 인수하게 하는 경우 8. 증권 인수업무 등에 관한 규정 제10조의2(신주인수권)에 의거하여 신주를 발행하는 경우 ③ 제2항 각 호 중 어느 하나의 규정에 의해 신주를 발행할 경우 발행할 주식의 종류와 수 및 발행가격 등은 이사회의 결의로 정한다. ④ 신주인수권의 포기 또는 상실에 따른 주식과 신주배정에서 발생한 단주에 대한 처리방법은 이사회의 결의로 정한다. |
5. 배당에 관한 사항
|
제12조(신주의 배당기산일) 회사가 유상증자, 무상증자 및 주식배당에 의하여 발행한 신주에 대한 이익의 배당에 관하여는 신주를 발행한 때가 속하는 영업연도의 직전영업연도말에 발행된 것으로 본다. 제9조(주식의 종류) ① 본 회사가 발행할 주식의 종류는 보통주식과 종류주식으로 한다. ② 회사가 발행하는 종류주식은 이익배당에 관한 우선주식, 의결권 배제 또는 제한에 관한 주식, 상환주식, 전환주식 및 이들의 전부 또는 일부를 혼합한 주식으로 한다. ③ 회사가 발행할 주권의 종류는 1주권, 5주권, 10주권, 50주권, 100주권, 500주권, 1,000주권, 10,000주권의 8종으로 한다. 다만, 「주식·사채등의 전자등록에 관한 법률」에 따라 전자등록계좌부에 주식 등을 전자등록하는 경우에는 동 조항의 적용을 배제한다. 제9조의 2(우선주식) ① 본 회사가 발행할 우선주식은 이익배당우선주식으로 하며, 그 발행 주식의 수는 발행주식총수의 2분의 1 범위 내에서 이사회 결의로 정한다 ② 이익배당우선주식에 대하여는 액면금액 또는 1주당 발행금액을 기준으로 발행시에 이사회가 정한 우선 비율에 따른 금액을 현금 또는 현물로 우선 배당한다. ③ 보통주식의 배당률이 이익배당우선주식의 배당률을 초과할 경우 그 초과분에 대하여 참가적 또는 비참가적인 것으로 할 수 있다. ④ 이익배당우선주식에 대하여 어느 사업연도에 있어서 소정의 배당을 하지 못한 경우에는 누적된 미배당분에 대하여 다음 사업연도의 배당 시에 누적적 또는 비누적적인 것으로 할 수 있다. ⑤ 본 회사가 유상증자, 무상증자 또는 주식배당을 실시하는 경우 이익배당우선주식에 대한 신주의 배정은 유상증자 및 주식배당의 경우에는 이사회 결의에 따라 그와 같은 종류의 주식 또는 그와 다른 종류의 주식으로 할 수 있으며 무상증자의 경우에는 그와 같은 종류의 주식으로 한다. ⑥ 본 회사는 이익배당우선주식의 발행 시 이사회 결의로 존속기간 및 동 기간 만료와 동시에 전환될 주식의 종류를 정할 수 있다. ⑦ 존속기간 만료일까지 소정의 배당을 하지 못한 경우에는 소정의 배당을 완료할 때까지 그 기간을 연장하는 것으로 이사회 결의로 정할 수 있다. ⑧ 위 제7항의 경우 전환으로 인하여 발행할 주식에 대한 이익의 배당에 관하여 제12조의 규정의 준용 여부는 이익배당우선주식 발행 시 이사회 결의로 정한다. 제9조의 3(의결권배제주식) ① 본 회사는 이사회 결의로 발행주식총수의 2분의1 범위 내에서 관련 법령상 허용되는 한도까지 의결권이 배제되는 주식을 발행할 수 있다. ② 본 회사가 유상증자, 무상증자 또는 주식배당을 실시하는 경우 의결권배제주식에 대한 신주의 배정은 유상증자 및 주식배당의 경우에는 이사회 결의에 따라 그와 같은 종류의 주식 또는 그와 다른 종류의 주식으로 할 수 있으며 무상증자의 경우에는 그와 같은 종류의 주식으로 한다. ③ 이익배당우선주식을 제1항의 의결권이 배제되는 주식으로 발행하는 경우, 이사회는 동 이익배당우선주식에 대하여 소정의 배당을 하지 아니한다는 결의가 있는 경우 그 결의가 있는 총회의 다음 총회부터 그 우선적 배당을 한다는 결의가 있는 총회의 종료 시까지 의결권이 있는 것으로 정할 수 있다. 제54조(이익배당) ① 이익의 배당은 금전 또는 금전 외의 재산으로 할 수 있다. ② 이익의 배당을 주식으로 하는 경우 회사가 종류 주식을 발행한 때에는 주주총회의 결의로 그와 다른 종류의 주식으로도 할 수 있다. ③ 제1항의 배당은 매결산기말 현재의 주주명부에 기재된 주주 또는 등록된 질권자에게 지급한다. ④ 이익배당은 주주총회의 결의로 정한다. |
III. 투자위험요소
| 【투자자 유의사항】 |
|---|
| ■ 금번 유상증자를 청약하고자 하는 투자자들은 투자결정을 하기전에 증권신고서의 다른 기재 부분 뿐만 아니라 특히 아래 기재된 투자위험요소를 주의깊게 검토한 후 이를 고려하여 최종적인 투자판단을 하시기 바랍니다. ■ 당사는 본 증권신고서를 통하여 청약 전에 투자자께서 숙지하셔야 하는 부분에 대하여 성실히 기재하고자 노력하고 있습니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 아래 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수 없으므로, 투자자는 아래 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 투자자 자신의 독자적이고도 세밀한 판단에 의해야 합니다. 따라서 증권신고서에 기재된 사항은 투자 판단 시 참고 자료로 활용하실 것을 권고드리며, 투자자의 투자 판단에 대한 결과는 투자자 본인에게 귀속됨을 다시 한번 알려드립니다. ■ 만일, 아래 기재한 투자위험요소가 실제로 발생하는 경우, 당사의 사업, 재무상태, 기타 영업활동에 중대한 부정적 영향을 미칠 수 있으며, 이에 따라 투자자가 금번 공모과정에서 취득하게 되는 당사 주식의 시장가격이 하락하여 투자금액의 일부 또는 전부를 잃게 될 수도 있음을 유의하시기 바랍니다. ■ 2009년 2월 4일 부로 시행된 『자본시장과 금융투자업에 관한 법률』제124조에 의거 누구든지 증권신고의 효력이 발생한 증권을 취득하고자 하는 자 (전문투자자, 그밖에 대통령령으로 정하는 자를 제외함) 에게 적합한 투자설명서를 미리 교부하지 아니하면 그 증권을 취득하게 하거나 매도하여서는 안됩니다. 다만, 『자본시장과 금융투자업에 관한 법률 시행령』제132조에 의거하여 투자설명서를 받기를 거부한다는 의사를 서면으로 표시한 자는 투자설명서의 교부없이 청약이 가능합니다. ■ 본 공시서류의 기재사항은 투자 결정을 위한 참고사항일 뿐이며, 투자에 대한 모든 손익 및 투자책임은 투자자 본인에게 귀속됨을 다시 한 번 말씀드립니다. |
1. 사업위험
주식회사 박셀바이오는 2010년 2월에 항암면역치료제를 연구ㆍ개발하는 목적으로 설립되었으며 2020년 9월 코스닥 시장에 상장하였습니다. 현재는 자연살해세포 치료제(Vax-NK)의 임상2a상 연구 및 CAR-T의 전임상 연구, CAR-NK 연구개발과 박스루킨-15의 임상연구에 매진하고 있으며, 향후에는 현재의 파이프라인을 더욱 확장하여 강력한 면역치료와 다른 항암요법을 병합하는 새로운 항암치료법을 창출함으로써 세계 항암치료제 시장의 프론티어로 발전하고자 하는 비전을 가지고 있습니다.
[주요용어]
|
구분 |
내용 |
|
간세포암종 |
간세포(hepatocyte)에서 유래한 악성 신생물, 즉 간암. 전체 간암 중, 80% 이상을 차지함. |
|
진행성 간세포암종 |
간세포암종 중, 수술 또는 여타의 기존 치료에도 불구하고 재발되거나 치료에 반응하지 않는 것 |
|
수정된 고형 종양 반응평가기준 |
고형암 중, 간암에 대해 특이적으로 치료에 대한 반응을컴퓨터단층촬영(CT scan)을 통하여 평가하는 기준. 통상 고형암에 대한 치료 반응은 RECIST 기준 1.1에 의거함. 그러나 간세포암의 경우, RECIST 기준에 따라 평가할 때에 오차가 많이 발생하는 까닭에 기존의 RECIST 평가법을 교정 내지는 수정한 mRECIST 기준에 따라 평가함. 특이점으로는 조영제 투여 전/후를 비교하여 동맥조영증강 시기 등을 모두 고려하여 치료의 반응 여부를 평가함. |
|
완전반응 |
전체 표적병변에 대해 종양 내 동맥의 조영증강이 전혀 관찰되지 않은 경우(mRECIST 기준); 표적병변이 전체적으로 관찰되지 않은 경우(RECIST 기준) |
|
부분반응 |
관찰되는 표적병변 직경의 합이(동맥조영증강 시) 기준점 대비 최소 30% 감소한 경우 |
|
안정성 병변 |
부분반응도 진행성 병변도 아닌 경우. 즉, 부분반응으로판정할 정도의 종양의 감소는 가져오지 않았으나, 종양의증식은 유의미하게 억제되어 질환이 안정적으로 유지되는 경우 |
|
진행성 병변 |
치료가 시작된 이후로 관찰되는 표적병변 직경의 합(동맥조영증강 시)이 최소 20% 이상 증가한 경우(mRECIST기준) |
|
객관적 반응률 |
치료 관찰 종료시점에서 완전반응과 부분반응의 합. 즉,객관적으로 종양이 특정 치료에 반응하여 완전히 사라지거나 유의미하게 감소된 경우의 합 |
|
질병조절율 |
치료 관찰 종료시점에서 완전반응과 부분반응, 안전성 병변의 합. 즉, 종양이 특정 치료에 반응하여 완전히 사라지거나 유의미하게 감소되었거나 성장이 억제되어 안정적으로 유지된 경우의 합 |
|
생존분석 |
특정 치료 후, 대상자의 생존기간을 분석한 것 |
|
전체 생존기간 |
특정 치료 후, 전체 대상자의 전체 생존기간을 통계적으로 분석한 것. 통상 중앙 값(50 퍼센타일)에 해당하는 중앙 생존기간(median overall survival, mOS)를 표기함. |
|
질환 진행까지의 기간 |
mOS 분석에 너무 오랜 기간이 걸리는 까닭에 치료 후 재발까지 걸리는 기간을 대리마커(surrogate marker)로 산정하여 생존분석을 진행함. 주로 재발이 잦거나 재발까지의 기간이 오래 걸리는 다발골수종 등의 혈액암 등의 판정에 이용 |
|
무진행 생존기간 |
TTP와 유사한 개념. 경우에 따라서는 둘을 혼용하기도 함. 주로 재발까지의 기간이 짧은 고형암 등의 생존 분석에 주로 이용함. |
|
다발(성)골수종 |
혈액암의 일종으로 항체를 생산하는 형질세포에 발생하는 악성 병변 |
|
재발성/불응성 다발골수종 |
다발골수종의 일차 치료선택인 골수이식을 할 수 없거나 시행 후에도 반응을 하지 않거나 재발한 다발골수종 |
|
B 림프구 |
항체를 생성하여 체액성 적응면역을 담당하는 세포. 감염 또는 악성 질환을 일으키는 항원 자극에 반응하여 성숙된 후, 항체를 형성하는 형질세포로 성숙화 됨. |
|
형질세포 |
B 림프구로부터 분화되어 체액성 적응면역을 담당하는 항체를 생산하는 세포 |
|
임상적 이득률 |
국제 골수종 연구회 (international myeloma working group, IMWG)에서 정한 기준에 의거 최소 반응(minimal response, MR) 이상의 치료 반응을 거둔 합계 |
|
최소 반응 |
다발골수종 치료에서 혈청 M-단백이 25-49% 감소를 보이고, 24 시간 뇨단백이 50-89%감소를 보이는 경우 |
|
면역학적 반응률 |
면역치료 후, 항종양 면역반응검사를 평가지표로 활용하여 면역학적 반응 여부를 백분율로 환산한 값. 통상 환자의 말초혈액 중 T세포를 분리하여 항원 특이적 T세포의 증식 능력과 감마인터페론(IFN-γ) 분비능 분석과 각종 항종양 싸이토카인의 농도를 측정하여 판정함. |
|
간동맥내 주입 화학요법 |
간세포암종 치료의 한 방법으로 간세포암종에 분지하는간동맥에 도관(카테터, catheter)을 거치시키고 이를 통해 직접 고농도의 항암화학요법제를 투여하여 암의 사멸을 유도하는 치료법 |
|
경동맥화학색전술 |
간세포암종 치료의 한 방법으로 간세포암종에 공급하는동맥을 통해 소량의 항암화학요법제 투여와 동시에 해당 혈관색전을 유도하여(혈관을 응고물질로 막아) 종양의 영양 공급을 차단하여 암의 사멸을 유도하는 치료법 |
|
자연살해세포 |
선천면역을 담당하는 세포의 일종. 바이러스 감염이나 악성 종양의 발생에서 중요한 1차 방어를 형성하는 역할을 함. 암세포치료제 개발 시 주요 표적 면역세포 중의 하나. |
|
수지상세포 |
항원제시세포 중 가장 전문적인 역할을 하는 세포. 선천면역과 적응면역의 가교 역할을 하여 감염이나 종양 등에대하여 항원특이적 면역반응의 개시를 매개하는 세포 |
|
자가유래세포 입양 도입 |
환자 자신의 세포에 대하여 체외 배양 등을 통해 선택 및증폭 과정 등을 거쳐 다시 환자에게 투여하여 치료적 효과를 꾀하는 치료법. 지금까지 자연살해세포 또는 암항원특이적 T세포, 줄기세포 등의 치료적 이용에 적용되고있음. |
|
사이토카인 |
신체 내의 세포, 특히 면역세포 사이에서 신호전달을 위하여 생성하고 분비하는 일련의 과정을 매개하는 단백질.각 사이토카인은 특정 세포군에 의해 생산되며, 작동하는 표적세포도 특화되어 있음. |
|
체외 세포 증폭 |
특정 종류의 세포를 몸 밖으로 분리하여 신체 외부에서 증폭하는 일련의 공정. |
|
인터루킨-15 |
사이토카인의 일종. 주로 수지상세포나 혈액단구(monocyte), 상피세포(epithelial cell) 등에서 생산되어 분비됨. 주요 표적세포는 항암 면역능에 중요한 역할을 하는 자연살해세포나 세포독성 T세포 등임. |
|
림프종 |
혈구세포의 일종인 림프구에 발생하는 악성종양. 즉, 림프구에 발생하는 암. |
|
유선(젖샘) 종양 |
포유동물 유방의 젖샘에 발생하는 악성종양 |
| 골수침윤림프구 (Marrow Infiltrating Lymphocytes) |
골수에 있는 항원 경험을 한 T세포 |
| 출처: 당사 정기보고서 |
| 가. 국내외 거시경제 침체 및 불확실성 관련 위험 한국은행에서는 2023년 02월 발표한 경제전망보고서를 통해 2023년 국내 경제성장률이 2022년 2.6% 대비 낮은 1.6%의 성장률을 보일 것으로 예측하였습니다. 또한, IMF(국제통화기금)에서는 2023년 04월 발표한 세계경제전망 자료를 통해 2023년 세계경제성장률을 직전 전망치(2023년 01월) 2.9% 대비 0.1% 낮은 2.8%로 전망하였습니다. 지난해 발발한 러-우 전쟁이 여전히 지속되고 있으며, 경제분절화 심화, 인플레이션 등 불안요인이 세계경제성장률 전망치 하락의 주요 원인으로 작용하였습니다. 한편, 실리콘밸리은행 및 크레딧스위스 사태 등의 금융시장 불안요인이 완전히 해소되지 않고 있으며, 이 외에도 지나치게 높은 공공ㆍ민간부채 수준, 신흥국 및 개도국 그룹 중심으로 나타나는 신용 스프레드 상승 등이 세계경제성장의 잠재적인 위험요인으로 작용하고 있습니다. 이러한 거시경제 불확실성은 국내외 경기 전반에 걸쳐 영향을 미칠 수 있는 요인으로, 당사가 영위하는 사업 및 재무실적에 부정적인 요인으로 작용할 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
① 국내 경기 동향
한국은행에서는 2023년 02월 발표한 경제전망보고서를 통해 2023년 국내 경제성장률이 2022년 2.6% 대비 낮은 1.6%의 성장률을 보일 것으로 예측하였습니다. 국내경제는 2023년 상반기에는 1.1% 수준으로 낮은 성장률을 보이겠으나 2023년 하반기 부터는 대외 불확실성이 줄어들면서 부진이 점차 완화될 것으로 예상하였습니다. 민간소비는 소득여건 개선과 일상회복 지속 등으로 완만한 회복세를 이어갈 전망이지만 그 속도는 점차 둔화될 전망입니다. 설비투자는 향후 글로벌 수요둔화와 자본조달비용 상승으로 위축될 것으로 예상되며, 건설투자는 주택수요 둔화와 정부 SOC예산 감소로 부진한 흐름을 이어갈 전망입니다. 상품수출은 중국과 IT품목을 중심으로 글로벌 수입수요가 약화되면서 부진할 것으로 예측되었습니다.
| [한국은행 국내 주요 거시경제지표 전망] |
| (단위: %) |
| 구분 | 2022년 | 2023년(E) | 2024년 (E) |
||||
|---|---|---|---|---|---|---|---|
| 상반기 | 하반기 | 연간 | 상반기 | 하반기 | 연간 | 연간 | |
| GDP | 3.0 | 2.2 | 2.6 | 1.1 | 2.0 | 1.6 | 2.4 |
| 민간소비 | 4.1 | 4.6 | 4.4 | 3.3 | 1.3 | 2.3 | 2.4 |
| 설비투자 | -6.4 | 5.4 | -0.7 | 3.2 | -8.9 | -3.1 | 3.6 |
| 지식재산생산물투자 | 4.6 | 5.0 | 4.8 | 3.6 | 3.5 | 3.5 | 3.5 |
| 건설투자 | -4.5 | -2.6 | -3.5 | 0.1 | -1.5 | -0.7 | 0.4 |
| 상품수출 | 6.0 | 0.3 | 3.1 | -4.0 | 5.0 | 0.5 | 3.4 |
| 상품수입 | 5.3 | 3.9 | 4.6 | -0.4 | -0.1 | -0.2 | 3.1 |
| 자료 : 한국은행 경제전망보고서 |
② 글로벌 경기 동향
IMF(국제통화기금)에서는 2023년 04월 발표한 세계경제전망 자료를 통해 2023년 세계경제성장률을 직전 전망치(2023년 01월) 2.9% 대비 0.1% 낮은 2.8%로 전망하였습니다. 지난해 발발한 러-우 전쟁이 여전히 지속되고 있으며, 경제분절화 심화, 인플레이션 등 불안요인이 세계경제성장률 전망치 하락의 주요 원인으로 작용하였습니다.
한국의 경우 2023년 경제성장률 전망치는 1.5%로 직전 전망치(2023년 1월) 1.7% 대비 0.2%p 하향 조정되었으며, 2024년에는 2.4% 경제성장률을 달성할 것으로 전망되었습니다. 대외수요 감소, 무역수지 악화, 내수 위축, 주택시장 둔화 등을 하향조정의 배경으로 설명하였습니다. 추가로 러시아-우크라이나 전쟁을 필두로 국가간 외교 마찰 및 무역 갈등이 잦아지고 있으며 그 과정에서 농산물, 에너지 자원을 중심으로 글로벌 공급망 위기가 발생하고 있습니다. 전쟁 및 서방 국가간 외교 갈등 장기화 시 경제성장률 전망 역시 추가 하향될 가능성이 존재하는 상황입니다.
| [국제통화기금(IMF) 경제성장률 전망치] |
| (단위 : %, %p) |
| 구분 | 2022년 | 2023년(E) | 2024년(E) | ||||
|---|---|---|---|---|---|---|---|
| 2023년 1월 | 2023년 4월 | 조정폭 | 2023년 1월 | 2023년 4월 | 조정폭 | ||
| (A) | (B) | (B-A) | (C) | (D) | (D-C) | ||
| 세계 | 3.4 | 2.9 | 2.8 | -0.1 | 3.2 | 3.1 | -0.1 |
| 선진국 | 2.7 |
1.2 |
1.3 |
0.1 |
1.4 |
1.4 |
- |
| 미국 | 2.1 |
1.4 |
1.6 |
0.2 |
1.0 |
1.1 |
0.1 |
| 유로존 | 3.5 |
0.7 |
0.8 |
0.1 |
1.6 |
1.4 |
-0.2 |
| 일본 |
1.1 |
1.8 |
1.3 |
-0.5 |
0.9 |
1.0 |
0.1 |
| 영국 |
4.0 |
-0.6 |
-0.3 |
0.3 |
0.9 |
1.0 |
0.1 |
| 캐나다 |
3.4 |
1.5 |
1.5 |
- |
1.5 |
1.5 |
- |
| 신흥국 | 4.0 |
4.0 |
3.9 |
-0.1 |
4.2 |
4.2 |
- |
| 러시아 | -2.1 |
0.3 |
0.7 |
0.4 |
2.1 |
1.3 |
-0.8 |
| 중국 | 3.0 |
5.2 |
- |
4.5 |
4.5 |
- |
- |
| 인도 | 6.8 |
5.9 |
-0.2 |
6.8 |
6.3 |
-0.5 |
- |
| 한국 | 2.6 |
1.7 |
1.5 |
-0.2 |
2.6 |
2.4 |
-0.2 |
| 자료 : World Economic Outlook |
또한, 2023년 3월 17일 경제협력기구(OECD)는 OECD 중간 경제전망(OECD Interim Economic Outlook)을 통해 러시아-우크라이나 전쟁, COVID-19 재확산, 주요국 통화긴축 영향 등으로 세계 경제의 회복세 둔화 및 물가상승 압력이 지속될 것으로 전망하였습니다. 2022년 세계 경제 성장률은 3.2%였으며, 2023년 세계 경제성장률은 지난 전망치(2022년 11월) 대비 0.4%p 상향 조정된 2.6%로 전망하였습니다.
인플레이션은 세계경제 성장 둔화, 에너지 및 식품 가격 안정, 주요국 통화긴축 효과 등으로 점차 둔화되겠으나 대부분 G20 국가의 경우 내년에도 연간으로는 여전히 목표치를 크게 상회할 것으로 전망하였습니다. 향후 성장 및 인플레이션 전망 경로상 상하방 리스크가 이전보다 균형을 이루고 있으나 아직은 하방리스크가 다소 우세한 것으로 평가하였습니다.
| [경제협력기구(OECD) 경제성장률 전망치] |
| (단위 : %, %p) |
| 구 분 | 2022년 | 2023년(E) | 2024년(E) | ||||
|---|---|---|---|---|---|---|---|
| 2022년11월 | 2023년 03월 | 조정폭 | 2022년11월 | 2023년 03월 | 조정폭 | ||
| 전세계 | 3.2 | 2.2 | 2.6 | 0.4 | 2.7 | 2.9 | 0.2 |
| 유로존 | 3.5 | 0.5 | 0.8 | 0.3 | 1.4 | 1.5 | 0.1 |
| G20 | 3.1 | 2.2 | 2.6 | 0.4 | 2.7 | 2.9 | 0.2 |
| - 호주 | 3.6 | 1.9 | 1.8 | -0.1 | 1.6 | 1.5 | -0.1 |
| - 캐나다 | 3.4 | 1.0 | 1.1 | 0.1 | 1.3 | 1.4 | 0.1 |
| - 독일 | 1.9 | -0.3 | 0.3 | 0.6 | 1.5 | 1.7 | 0.2 |
| - 프랑스 | 2.6 | 0.6 | 0.7 | 0.1 | 1.2 | 1.3 | 0.1 |
| - 이탈리아 | 3.8 | 0.2 | 0.6 | 0.4 | 1.0 | 1.0 | 0.0 |
| - 스페인 | 5.5 | 1.3 | 1.7 | 0.4 | 1.7 | 1.7 | 0.0 |
| - 일본 | 1.0 | 1.8 | 1.4 | -0.4 | 0.9 | 1.1 | 0.2 |
| - 한국 | 2.6 | 1.8 | 1.6 | -0.2 | 1.9 | 2.3 | 0.4 |
| - 멕시코 | 3.0 | 1.6 | 1.8 | 0.2 | 2.1 | 2.1 | 0.0 |
| - 터키 | 5.6 | 3.0 | 2.8 | -0.2 | 3.4 | 3.8 | 0.4 |
| - 영국 | 4.0 | -0.4 | -0.2 | 0.2 | 0.2 | 0.9 | 0.7 |
| - 미국 | 2.1 | 0.5 | 1.5 | 1.0 | 1.0 | 0.9 | -0.1 |
| - 아르헨티나 | 5.6 | 0.5 | 0.1 | -0.4 | 1.8 | 1.8 | 0.0 |
| - 브라질 | 3.0 | 1.2 | 1.0 | -0.2 | 1.4 | 1.1 | -0.3 |
| - 중국 | 3.0 | 4.6 | 5.3 | 0.7 | 4.1 | 4.9 | 0.8 |
| - 인도 | 6.9 | 5.7 | 5.9 | 0.2 | 6.9 | 7.1 | 0.2 |
| - 인도네시아 | 5.3 | 4.7 | 4.7 | 0.0 | 5.1 | 5.1 | 0.0 |
| - 러시아 | -2.1 | -5.6 | -2.5 | 3.1 | -0.2 | -0.5 | -0.3 |
| - 사우디 | 8.7 | 5.0 | 2.6 | -2.4 | 3.5 | 3.7 | 0.2 |
| - 남아공 | 2.0 | 1.1 | 0.6 | -0.5 | 1.6 | 0.9 | -0.7 |
| 자료 : OECD Interim Economic Outlook |
한편, 실리콘밸리은행 및 크레딧스위스 사태 등의 금융시장 불안요인이 완전히 해소되지 않고 있으며, 이 외에도 지나치게 높은 공공ㆍ민간부채 수준, 신흥국 및 개도국 그룹 중심으로 나타나는 신용 스프레드 상승 등이 세계경제성장의 잠재적인 위험요인으로 작용하고 있습니다. 이러한 거시경제 불확실성은 국내외 경기 전반에 걸쳐 영향을 미칠 수 있는 요인으로, 당사가 영위하는 사업 및 재무실적에 부정적인 요인으로 작용할 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
|
나. 신약개발 특성에 따른 위험 그러나, 신약 개발 과정은 후보물질의 유효성과 안전성을 평가하고 이에 대한 근거를 마련하기 위한 중요한 과정으로 관련 규정과 절차를 반드시 준수해야합니다. 먼저, 타겟 질환에 대해 약리적인 효과가 있을 것으로 예상되는 후보물질 탐색 및 발굴을 시작으로, 동물을 대상으로 하는 전임상 연구(preclinical study)와 사람을 대상으로 하는 임상 연구(clinical study)를 통해 후보물질의 안전성과 유효성에 대한 검증을 분석하여, 최종적으로 규제 당국으로부터 의약품 품목 허가를 받아야 합니다. 이와같이 신약 연구개발을 통하여 가시적인 결과가 나오는 제품의 상용화 단계까지 많은 비용과 시간이 요구되며, 연구개발 과정에서 수많은 변수가 발생할 수 있습니다. 또한, 변수들을 미리 찾아내어 극복하지 못한 경우에 지출했던 연구개발 비용 및 시간 등의 큰 손실을 발생할 수 있으므로 투자자 여러분들께서는 이 점 유의하시기 바랍니다. 당사가 영위하고 있는 바이오사업부문 증권신고서 및 회사 IR자료 등 관련 자료를 참고하더라도 합리적인 투자의사 결정하기에는 고도의 전문적 식견이 필요하며, 관련 산업 및 기술을 정확히 이해하기에는 한계가 있으므로 투자자 여러분께서는 이 점 유의하여 주시기 바랍니다. |
신약개발 사업은 사업화에 성공 시 통상적으로 특허권에 의해 일정기간 동안 독점권으로 보호받게 되며, 시판 승인 후 일정기간 동안 독점 판매기간을 인정받을 수도 있습니다. 대부분의 국가에서 특허 존속기간은 출원 후 20년이며, 특허의 존속기간과 관계없이 신약의 경우, 미국은 시판 승인 후 5년 이상의 시장독점권, EU는 10년의 시장독점권, 국내은 6년의 시장독점권을 보장받을 수 있습니다. 이처럼 특허권 및 독점판매권(시장독점권)을 통해 일정기간 배타적 수익을 보장받을 수 있기 때문에 글로벌 블록버스터급 신약 개발에 성공 시 막대한 수익을 창출할 수 있는 고부가가치 사업입니다.
그러나, 신약 개발 과정은 후보물질의 유효성과 안전성을 평가하고 이에 대한 근거를 마련하기 위한 중요한 과정으로 관련 규정과 절차를 반드시 준수해야합니다. 먼저, 타겟 질환에 대해 약리적인 효과가 있을 것으로 예상되는 후보물질 탐색 및 발굴을 시작으로, 동물을 대상으로 하는 전임상 연구(preclinical study)와 사람을 대상으로 하는 임상 연구(clinical study)를 통해 후보물질의 안전성과 유효성에 대한 검증을 분석하여, 최종적으로 규제 당국으로부터 의약품 품목 허가를 받아야 합니다.
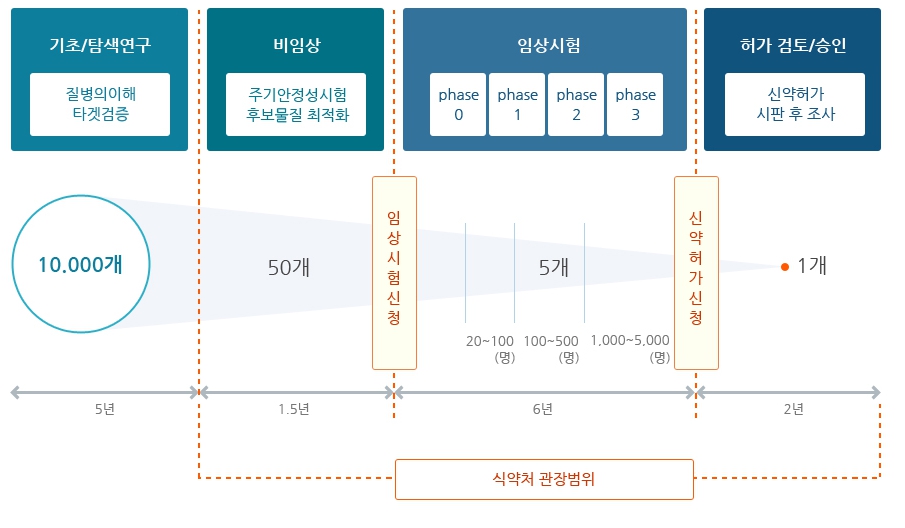
특히, 일반인 또는 환자를 대상으로 하는 임상시험을 진행하고자 할 때에는 효능과 안전성에 대한 각 국가의 정부규제가 엄격하여, 임상시험 이전 단계부터 엄격한 규제에 의해 축적된 다양한 데이터를 각 국가의 규제 당국에 제출하여야 합니다. 기본적으로 임상 1상(임상약리시험) 및 임상 2상(치료적 탐색시험), 임상 3상(치료적 확증시험)의 연구를 진행하게 되며, 임상시험 계획 승인(IND)을 통과하여 임상시험을 진행 중인 경우에도 심각한 부작용 등이 보고되는 경우에는 규제 당국에 의해 임상시험이 중단되거나 철회될 수 있습니다. 또한, 임상시험을 성공적으로 마치고 신약허가신청(NDA) 심사를 통과하여 시판 허가를 받아 신약을 생산 및 판매하는 과정에서도 규제 당국의 엄격한 규정을 따라야 하며, 약물을 시판한 이후에도 부작용을 추적하여 검토하는 제4상 임상 연구를 진행해야 합니다. 이처럼 신약개발 사업은 고수익을 창출할 수 있지만, 오랜 시간과 막대한 비용을 투자하더라도 최종 제품으로의 성공확률이 매우 낮은, 대표적인 High Risk, High Return, Long Term Investment 사업입니다.
| [신약 개발 과정] |
 |
|
신약 개발 과정 |
| 출처: 의약품안전나라 의약품통합정보시스템 |
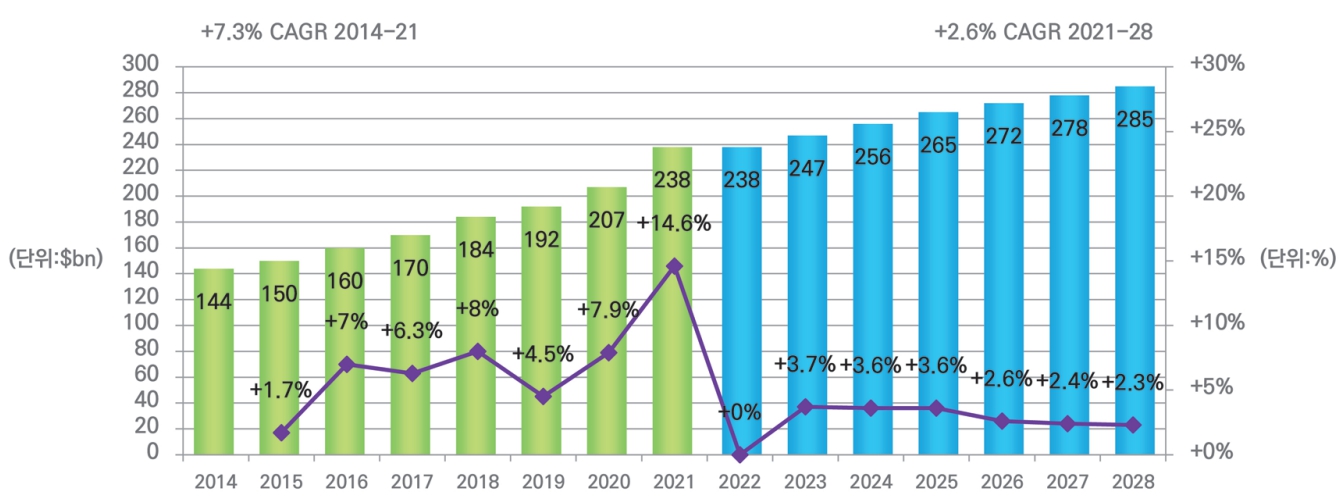
신약개발 과정에 소요되는 기간 및 비용 분석에 관하여 분석기관마다 편차는 있으나, 일반적으로 신약후보물질이 초기 연구 및 임상시험을 거쳐 출시되기까지 보통 10~15년 정도가 소요되는 것으로 알려져 있습니다. 또한 Evaluate Pharma World Preview 2022에 따르면 전 세계 제약 R&D 비용은 2014년 1,440억달러에서 꾸준히 상승하여 2022년 2,380억달러, 2028년에는 2,850억달러가 소요될 것으로 예상하였습니다.
| [전 세계 제약 R&D 비용 추이] |
 |
|
글로벌 r&d 비용 추이 |
| 출처: 2022 제약바이오산업 Databook |
이러한 시간적, 재정적 막대한 투자에도 불구하고, 신약개발의 최종 성공률은 다소 낮은 수준입니다. IQVIA Institute(2022) 보고서에 따르면, 2010년부터 2021년까지 FDA 임상 파이프라인을 대상으로 조사된 임상의 성공률은 평균 13.1%로 나타났습니다.
| [연도별 임상 단계별 이행성공률 및 임상 성공률 추이(2010~2021, FDA)] |
|
| 출처: Global Trends in R&D 2022, IQVIA Institute, 2022.02 |
증권신고서 제출일 현재, 당사 파이프라인의 연구개발 정도는 아래와 같습니다.
| [당사 파이프라인 적응증 및 진행단계] |
|
구분 |
품목 |
적응증 |
현재 진행단계 |
비고 |
|
|---|---|---|---|---|---|
|
단계(국가) |
승인년도 |
||||
|
항암제 |
Vax-NK |
진행성 간세포암 |
임상2a상(한국) |
2018년 |
Vax-NK + HAIC(5-FU/시스플라틴) 병용요법 |
|
진행성 췌장암 |
임상2a상 신청 |
- |
식품의약품안전처 임상시험계획 변경신청 (적응증 추가) |
||
|
소세포폐암 |
임상연구 승인 |
- |
첨단재생의료 임상연구계획 승인 (연구자임상) |
||
|
항암제 |
Vax-CAR (CAR-T, CAR-NK, CAR-MIL) |
MSLN, EphA2 발현 난치성 고형암 |
비임상 |
- |
소동물 종양모델에서 효능시험 진행중 |
|
PD-L1 발현 난치성 고형암 |
비임상 |
- |
소동물 종양모델에서 효능시험 진행중 |
||
|
BCMA 발현 난치성 다발골수종 |
비임상 |
- |
임상시험을 위한 생산공정 확립 중 | ||
|
동물용 |
박스루킨-15 |
개의 악성종양 |
임상시험(한국) |
- |
농림축산검역본부 임상시험 진행 후 품목허가 재신청 예정 |
| 주) 당사는 2022년 08월 24일 연구개발의 타당성과 투자대비 사업성에 대한 판단 하에 Vax-DC 플랫폼의 연구개발을 조기 종료하고, 대체재로 골수침윤T림프구를 확장 배양한 CAR-MIL 치료제 개발을 본격화하기로 결정하였습니다. 출처: 당사 제시 |
당사 파이프라인 세부 내역은 아래와 같습니다.
(가) Vax-NK
|
구분 |
항암제(바이오 신약) |
|
적응증 |
진행성 간세포암(HAIC와의 병용 치료) 진행성 췌장암(mFOLFIRINOX 요법과 병용 치료) 소세포폐암(아테졸리주맙과 병용 투여) |
|
M제품설명 |
- Vax-NK는 백혈구분반술을 통해 대상환자의 말초혈액단핵구를 추출하여 자연살해(NK)세포를 분리 후, 방사선조사영양세포주 및 싸이토카인 칵테일에 의한 자극을 통하여 2주 동안 배양하여 제조하는 자가유래 NK세포 기반의 면역세포치료제임. |
|
제품의 특성 |
- 영양세포주와 낮은 농도 사이토카인를 이용한 NK세포의 증폭률(평균 300배 증폭) 및 순도(평균 85% 이상) 극대화 - 진행성 췌장암은 예후가 좋지 않고 워낙 발견이 늦은 경우가 많기 때문에 수술 가능한 환자는 전체 환자의 12.5%에 불과하며 췌장암에 특어적으로 작용하여 허가받은 면역항암제가 없는 실정이며, 표준치료인mOLFIRINOX 요법과 Vax-NK 병용 투여 시 우수한 효과를 보일 것이라 기대함 - 소세포 폐암은 암세포의 성장이 아주 빠르며 초기 단계에서도 전이가 쉽게 일어나는 암으로 예후가 좋지 않은 암종으로 알려져 있으며 5년 생존율도 5~10%로 매우 낮기 때문에 미충족 의료수요가 높은 암종임. 아테졸리주맙과 Vax-NK 병용 투여한 비임상 시험에서 높은 종양억제 효과를 확인했으며, 높은 항암효과를 가진 치료제가 될 것으로 기대함 |
|
진행경과 |
- 11명의 진행성 간세포암 환자 대상 임상 1상 완료 - 진행성 췌장암은 식약처에 적응증 추가를 위한 Vax-NK 임상시험계획변경 승인(임상2a상) 신청 완료 (2023.07.31) - 소세포폐암 대상 첨단재생의료 임상연구계획 승인(연구자임상) |
|
향후계획 |
- 진행성 간세포암 임상 2a상 완료 후 임상 2b상 또는 임상3상 진입 예정 - 진행성 췌장암 임상2a상 승인 후 실시 예정 (신청완료) - 소세포폐암 첨단재생의료 임상연구 실시 예정(승인완료) |
|
유사경쟁제품 |
- 간세포암에 대한 항암면역세포치료제로는 녹십자셀의 이뮨셀엘씨주(2007년 국내 조건부품목허가, 2012년 임상3상완료)가 있음. 그러나 이뮨셀엘씨주는 간세포암 제거술(수술, 고주파절제술, 경피적 에탄올 주입술) 후 종양제거가 확인된 환자에서 보조요법으로 사용되고 있으며, 주세포군은 활성화 T-림프구와 싸이토카인 유도 살해세포(Cytokine induced killer cell, CIK cell)로, NK세포를 기반으로 하는 Vax-NK와는 차이점이 있어 상호 배타적인 경쟁제품으로 특정하기 어려움. |
|
시장규모 |
시장형성 초기 단계이므로, 목표 시장을 특정하기 어려움. |
나) Vax-CAR-T/-NK (MSLN, EphA2)
|
구분 |
항암제(바이오 신약) |
|
적응증 |
MSLN, EphA2 발현 난치성 고형암 |
|
제품 설명 |
- CAR-T/-NK의 작용기전은 환자유래 T세포 또는 NK세포에 인위적으로 도입된 항원 특이적 키메라 항원 수용체(chimeric antigen receptor, CAR)에 의해 선택적으로 표적암을 사멸시킴. |
|
제품의 특성 |
- CAR-T/-NK 세포는 특정항원에 결합하는 CAR를 T/NK 세포에 도입하므로, MHC 분자의 도움 없이도 특정 암을 직접 인지하여 T세포 또는 NK세포의 선택적 살상능을 높임. |
|
진행경과 |
- 다양한 고형암 세포주(CAPAN2, OVCAR3, AsPC1)를 대상으로 한 in vitro 효능 시험에서 암세포 살상능을 확인함 |
|
향후계획 |
GLP수준의 비임상 독성 시험 및 기전 연구를 진행 후, 임상시험에 진입할 계획 |
|
유사경쟁 |
- CAR-T세포 치료제로는 노바티스사의 킴리아와 길리어드사의 예스카르타, 테카터스, BMS사의 브레얀지, 아벡마 그리고 J&J의 카빅티가 혈액암을 대상으로 시판되었음. |
|
시장규모 |
시장형성 초기 단계이므로, 목표 시장을 특정하기 어려움. |
다) Vax-CAR-T/-NK (PD-L1)
|
구분 |
항암제(바이오 신약) |
|
적응증 |
PD-L1 발현 난치성 고형암 |
|
제품 설명 |
- CAR-T/-NK의 작용기전은 환자유래 T세포 또는 NK세포에 인위적으로 도입된 항원 특이적 키메라 항원 수용체(chimeric antigen receptor, CAR)에 의해 선택적으로 표적암을 사멸시킴. |
|
제품의 특성 |
- CAR-T/-NK 세포는 특정 항원에 결합하는 CAR(anti-PD-L1)를 T/NK세포에 도입하므로, MHC 분자의 도움 없이도 특정 암을 직접 인지하여 T세포 또는 NK세포의 선택적 살상능을 높임. |
|
진행경과 |
- 다양한 고형암 세포주를 대상으로 한 in vitro 효능 시험에서 암세포 살상능을 확인함 |
|
향후계획 |
GLP수준의 비임상 독성 시험 및 기전 연구를 진행 후, 임상시험에 진입할 계획 |
|
유사경쟁 |
- CAR-T세포 치료제로는 노바티스사의 킴리아와 길리어드사의 예스카르타, 테카터스, BMS사의 브레얀지, 아벡마 그리고 J&J의 카빅티가 혈액암을 대상으로 시판되었음. |
|
시장규모 |
시장형성 초기 단계이므로, 목표 시장을 특정하기 어려움. |
라) Vax-CAR-T (BCMA)
|
구분 |
항암제 (바이오 신약) |
|
적응증 |
재발성/불응성 다발골수종 |
|
제품 설명 |
- B-cell maturation antigen (BCMA)를 표적으로 인식하는 항체를 T 세포에 도입하여 제조되며, 이 항체는 BCMA를 발현하는 다발골수종 세포를 선택적으로 인식하고 결합하는 선택적 암세포 파괴 능력을 가짐 - BCMA를 인식하는 항체를 도입한 T 세포를 대량 제조하며, 이렇게 제조된 CAR-T 세포는 BCMA를 발현하는 다발골수종 세포를 인식하고 결합함으로써 다양한 면역 반응 메커니즘을 발동함 - 활성화된 Vax-CAR-T 세포는 세포독성 작용, 사멸 프로그램을 유도하는 신호 분자의 분비, 면역 세포의 파괴를 돕는 다른 면역 세포와의 상호작용 등을 통해 암세포에 대한 파괴 작용을 수행함 |
|
제품의 특성 |
- BCMA CAR-T는 B-cell maturation antigen (BCMA)를 표적으로 하는 항체를 T 세포에 도입하여 제작되며, 이로 인해 BCMA를 발현하는 다발골수종 세포만을 선택적으로 인식하고 표적으로 함 - BCMA CAR-T는 제조된 T 세포가 항원 표적을 인식한 후 암세포를 파괴하는 능력을 가지며, 제조된 CAR-T 세포는 혈액 순환 속에서 암세포를 탐색하고 파괴하는 지속적인 활동을 수행함 - BCMA CAR-T는 환자 자체의 T 세포를 추출하여 제조되며, 이를 통해 개인의 면역 시스템과 유전자 프로필에 기반한 최적화된 맞춤형 치료를 제공함 |
|
진행경과 |
- Vax-CAR-T의 생산공정을 확립하는 중 |
|
향후계획 |
- GLP수준의 비임상 독성 시험 및 기전 연구를 진행 후, 임상시험에 진입할 계획 |
|
유사경쟁 |
- Janssen의 Carvykti는 한국에서 허가를 받았지만 아직 상용화 단계에 도달하지 않았음. - BMS(Bristol-Myers Squibb)의 Abecma는 한국에서는 아직 허가를 받지 않은 상황임. |
|
시장규모 |
- 시장형성 초기 단계이므로, 목표 시장을 특정하기 어려움. |
마) Vax-CAR-MIL (BCMA)
|
구분 |
항암제(바이오 신약) |
|
적응증 |
재발성 불응성 다발골수종 |
|
제품 설명 |
- MIL은 "말초혈액"에서 분리하여 개발되는 CAR-T, TCR-T, 종양침윤림프구(TIL) 등의 면역세포치료제와는 달리 ‘골수’에서 분리했다는 점에서 차이점을 보이며 골수 미세환경의 독특한 생물학적 특성 때문에 기억T세포가 풍부해 항암효과 및 지속성을 향상시킬 수 있음 - 다수의 암 항원에 대한 특이성을 가져 항원 손실에 의한 재발을 막을 수 있고 다양한 암 유형에 적용 가능함 - CAR 단일사슬 변수 단편 항체(scFV)와 결합하여 암세포 살상능이 더 증폭시킴 |
|
제품의 특성 |
- CAR-MIL은 환자의 골수에서 유래한 골수침윤림프구(MIL)과 당사의 CAR와 결합시켜 다발골수종에 매우 특이적이고 암세포 살상능이 매우 높을 것으로 기대됨 |
|
진행경과 |
- 다발골수종 세포를 대상으로 한 in vitro 효능 시험에서 높은 암세포 살상능을 확인함 |
|
향후계획 |
- GLP 수준 비임상 독성 시험과 공정개발을 확립한 후 임상시험에 진입할 계획 |
|
유사경쟁 |
- CAR-T세포 치료제로는 아베크마(Abecma, BMS, 2021년 FDA승인)와 카비티(CARVYKTI, J&J, 2022년 FDA승인)의 두 가지 제품이 재발성 불응성 다발골수종에 승인되었으며 처방되고 있음. 그러나 아직 한국시장에는 진입하지 못함 |
|
시장규모 |
- 시장형성 초기 단계이므로, 목표 시장을 특정하기 어려움. |
바). 박스루킨-15
|
구분 |
반려견 항암병용(보조)치료제 |
|
적응증 |
개의 악성종양(유선종양, 림프종 등) |
|
제품 설명 |
- 개 인터루킨-15 유전자를 기반으로 한 재조합 단백질로 동물용 항암면역증강제임. |
|
제품의 특성 |
- 반려견 전용 면역증강제(개의 유전체 정보를 바탕으로 한 설계 및 개발) - 항암화학효법과 병용 시 다양한 암종에 대한 높은 치료 효과를 보임 |
|
진행경과 |
- 랫드 및 비글견 대상 비임상 독성시험 완료(한국화학융합시험연구원 헬스케어연구소) - 21년 09월 품목허가 보완서류 제출 - 21년 11월 2차 보완요청 [시험군의 충분한 확보를 통한 통계적 유의성 확보 필요] - 21년 12월 품목허가 철회 [시험기관 추가 및 제품 생산 등 준비 중] - 국내 동물의약품 제약사와 생산 및 유통 협약 체결 - 전국 50여개의 동물병원을 대상으로 임상시험 진행 중 |
|
향후계획 |
- KVGMP 시설 위탁생산업체를 통한 대량생산 및 판매 |
|
유사경쟁제품 |
아직까지 동물 전용 항암면역치료제로 승인된 사례는 없음. |
|
시장규모 |
시장형성 초기 단계이므로, 목표 시장을 특정하기 어려움. |
당사는 증권신고서 제출일 현재, 모든 파이프라인이 연구개발 단계로 임상 연구를 진행하고 있으며, 박스루킨-15 품목의 경우 2021년 12월 농림축산검역본부 품목허가 신청을 철회하고, 2023년 8월 기준 유선종양 연구 대상 환견 60마리를 등록 완료하여 주사제 투여 및 모니터링 중이며, 데이터 정리 후 품목 허가를 신청할 계획입니다.
| [당사의 연구개발비용] |
| (단위: 백만원) |
|
구 분 |
2023년도 반기 |
2022년도 | 2021년도 | 2020년도 | |
|---|---|---|---|---|---|
|
자산 처리 |
원재료비 |
- | - | - | - |
|
인건비 |
- | - | - | - | |
|
감가상각비 |
- | - | - | - | |
|
위탁용역비 |
- | - | - | - | |
|
기타 경비 |
- | - | - | - | |
|
소 계 |
- | - | - | - | |
|
비용 |
제조원가 |
- | - | - | - |
|
판관비(*) |
2,016 | 2,062 | 1,800 | 1,340 | |
|
소계 |
2,016 | 2,062 | 1,800 | 1,340 | |
|
(정부보조금) |
- | - | - | - | |
|
보조금 차감 후 금액 |
2,016 | 2,062 | 1,800 | 1,340 | |
|
합계 |
2,016 | 2,062 | 1,800 | 1,340 | |
| 주) 연구개발비용은 전액 판관비로 계상되어 있으며, 정부보조금은 별도의 수익으로 처리하고 있습니다. 출처: 당사 정기보고서 |
당사는 코스닥시장 상장 제약사로서 제한된 연구개발비 내에서 실질적인 수익 창출 기여도를 높이기 위한 의약품 개발에 집중하고 있습니다. 당사의 임상단계를 거치고 있는 파이프라인은 추가적인 연구개발이 필요하며 이에 따라, 향후 연구개발활동이 확대될 것으로 예상됩니다. 하지만, 현재까지 연구개발에 대한 성과가 큰 수익으로 연결되지 않아 계속적인 영업적자를 기록하고 있습니다.
이와같이 신약 연구개발을 통하여 가시적인 결과가 나오는 제품의 상용화 단계까지 많은 비용과 시간이 요구되며, 연구개발 과정에서 수많은 변수가 발생할 수 있습니다. 또한, 변수들을 미리 찾아내어 극복하지 못한 경우에 지출했던 연구개발 비용 및 시간 등의 큰 손실을 발생할 수 있으므로 투자자 여러분들께서는 이 점 유의하시기 바랍니다. 당사가 영위하고 있는 바이오사업부문 증권신고서 및 회사 IR자료 등 관련 자료를 참고하더라도 합리적인 투자의사 결정하기에는 고도의 전문적 식견이 필요하며, 관련 산업 및 기술을 정확히 이해하기에는 한계가 있으므로 투자자 여러분께서는 이 점 유의하여 주시기 바랍니다.
|
다. 새로운 치료 요법 등장에 따른 시장 환경 변화 위험 이 같은 문제를 극복하기 위하여 2010년대 들어서는 면역항암제가 본격적으로 개발 적용되기 시작하였습니다. 면역항암제는 암세포가 획득한 면역억제 또는 면역회피 기전을 극복하기 위하여 면역체계의 종양 인지 능력 또는 파괴 능력을 회복 또는 강화시키는 기전의 약제로, 면역체계의 특이성, 기억력, 적응력을 증강시킴으로써 항암효과를 나타냅니다. 면역관문억제제를 필두로 한 다수의 면역항암제에 관한 임상연구 및 시판 후 증례를 통해, 1세대 화학항암제, 2세대 표적항암제와 달리, 장기간 효과 지속, 장기 생존가능, 폭넓은 항암효과 및 낮은 부작용 등의 특성을 보여주고 있어, 기존 항암치료의 패러다임을 바꾸며, 암 표준치료 중의 하나로 자리매김하고 있습니다. |
암의 치료 요법으로는 외과적 수술, 방사선 치료, 약물 치료 등이 시행되고 있습니다. 약물 치료 중1세대 항암제는 화학항암제로, 이는 세포독성 화학물질을 처리하여 정상 세포에 비해 세포분화 및 증식 속도가 빠른 암세포를 사멸시키는 기전의 치료제 입니다. 그러나 암세포 뿐만 아니라 정상세포까지도 공격해 심각한 부작용을 유발하는 단점이 있습니다. 2000년대 들어 사용된 2세대 표적 항암제는 암세포에 나타나는 특정 단백질이나 특정 유전자 변화에 작용하여 암의 성장과 분화에 관여하는 신호전달을 차단하는 기전의 항암제로, 화학항암제 대비 치료율이 향상되고 부작용이 개선되었습니다. 그러나 표적 대상이 제한적이어서 같은 암종이라도 표적 인자가 발현되지 않으면 사용이 제한적이며, 표적 유전자가 밝혀지지 않은 암종에 대한 적용의 어려움, 암세포의 돌연변이로 인한 약제 내성 등으로 한계가 있는 상황입니다.
이 같은 문제를 극복하기 위하여 2010년대 들어서는 면역항암제가 본격적으로 개발 적용되기 시작하였습니다. 면역항암제는 암세포가 획득한 면역억제 또는 면역회피 기전을 극복하기 위하여 면역체계의 종양 인지 능력 또는 파괴 능력을 회복 또는 강화시키는 기전의 약제로, 면역체계의 특이성, 기억력, 적응력을 증강시킴으로써 항암효과를 나타냅니다. 면역관문억제제를 필두로 한 다수의 면역항암제에 관한 임상연구 및 시판 후 증례를 통해, 1세대 화학항암제, 2세대 표적항암제와 달리, 장기간 효과 지속, 장기 생존가능, 폭넓은 항암효과 및 낮은 부작용 등의 특성을 보여주고 있어, 기존 항암치료의 패러다임을 바꾸며, 암 표준치료 중의 하나로 자리매김하고 있습니다.
| [세대별 항암제 종류 및 특징] |
|
구분 |
특징 |
|
|
1세대 (1950년대~) |
화학항암제 |
- 약물을 이용하여 암세포를 죽이는 전신치료 방법 |
|
2세대 (2000년대~) |
표적항암제 |
- 암세포나 암조직에만 많이 발현되는 특정 단백질이나 유전자 변화를 표적으로 삼아 암의 성장과 암의 발생에 관여하는 활동을 방해하는 치료방법 - 암세포만을 식별해 공격하는 장점이 있지만, 유전자 변이를 가진 환자에만 사용할 수 있어 다양한 암치료가 불가능 |
|
3세대 (2010년대~) |
면역항암제 |
- 인체 면역세포를 활성화시켜 암세포를 사멸시키는 방법 |
| 출처: 약학정보원 및 업계자료 취합 |
| [각 세대별 항암제의 원리] |
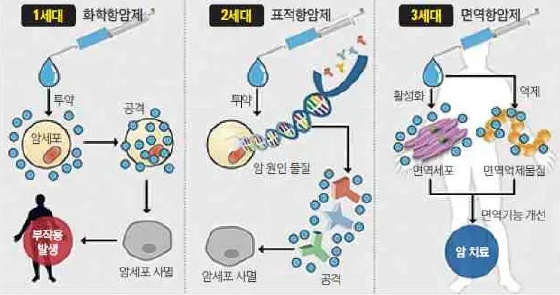 |
|
각 세대별 항암제의 원리 |
| 출처: 표적치료에대한 이해(2016.10), 삼성서울병원 |
다만, 면역항암제 역시 일부 면역관문조절과 같은 특정 바이오마커의 발현율에 따라 치료의 반응률이 차이가 나는 한계점이 있어, 단독요법 외에도 다양한 항암기전을 가지는 치료제들과의 병용요법이 시도되고 있으며, 장기 생존(혹은 완치)을 가능하게 하는 우수한 병용 임상연구 및 시판 후 증례를 통해 현재 다수의 면역항암제 병용요법이 1차 치료제로 승인되어 적용되고 있습니다.
| [항암제 종류별 생존곡선 비교] |
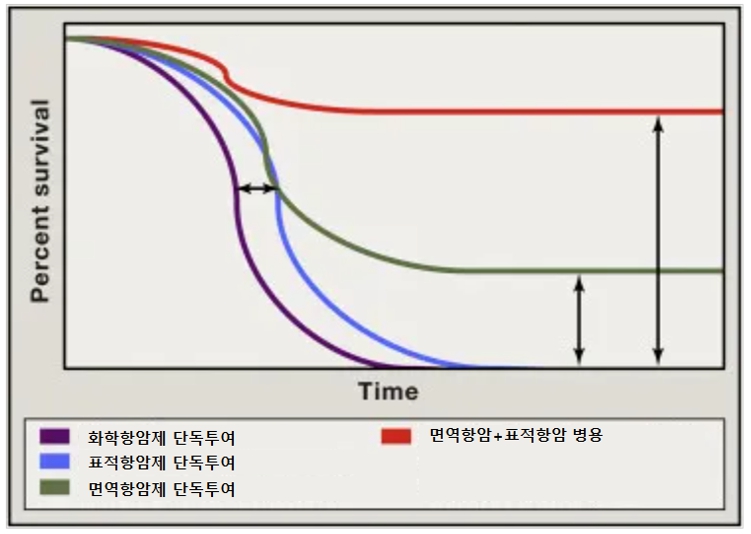 |
|
항암제 종류별 생존곡선 비교 |
| 출처: P. Sharma, J.P. Allison, Cell, 2015, 161, 205-214, 당사 재구성 |
2011년 면역관문억제제인 BMS사의 여보이(Yervoy, 성분명: Ipilimumab)의 승인을 시작으로 면역항암제의 연구 및 임상 적용이 본격적으로 진행되었으며, 현재 면역관문억제제(여보이, 키트루다, 옵디보, 티센트릭, 임핀지, 바벤시오 등)를 중심으로, 면역세포치료제(예스카타, 킴리아 등)와 항암바이러스치료제(임리직 등) 등이 다수 허가돼 판매되고 있습니다. 이 중 키트루다, 옵디보, 티센트릭, 임핀지, 여보이 등 주요 10개 면역항암제 제품의 2020년 글로벌 총 매출은 307억 달러 규모로 조사되었습니다. 특히, MSD의 '키트루다'는 암의 종류에 상관없는 바이오마커를 기반으로 한 치료제로, 흑색종을 대상으로 최초 승인을 획득한 이래 비소세포페암, 두경부암, 호지킨 림프종, 방광암 등 다양한 암 적응증에 대부분 1차 치료제로 승인되면서, 2019년 처음으로 단일품목 매출 100억달러를 넘었으며, 항암제를 넘어서 글로벌 의약품 매출 1위 품목이 되었습니다. EvaluatePharma 자료에 따르면, 키트루다는 2026년 270억 달러의 매출로 여전히 글로벌 매출1위 품목에 이름을 올릴 것으로 예상되고 있습니다.
| [주요 10개 글로벌 면역항암제의 2020년 매출 실적 및 2026년 예상 매출] |
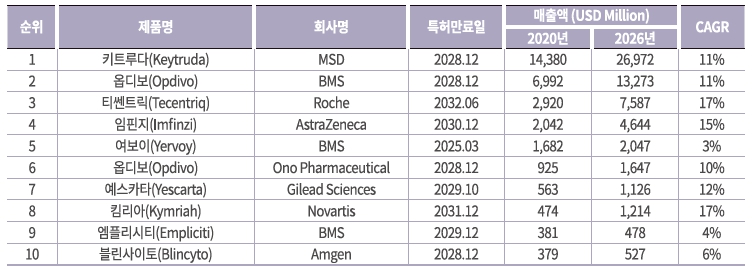 |
|
주요 글로벌 면역항암제의 매출 실적 및 예상 매출 |
| 출처: KPBMA 한국제약바이오협회, EvaluatePharma |
이처럼 글로벌 면역항암제 시장은 키트루다, 옵디보, 티센트릭, 임핀지 등 면역관문억제제들의 적응증 확대, 킴리아, 예스카타 등 CAR-T 치료제의 출시, 병용요법 및 수술 전ㆍ후 보조요법으로 적용 방식 확대, 신규 면역항암제의 출시 등으로 인해 지속적으로 고성장할 것으로 전망됩니다. FutureWise Market Research 자료에 따르면 글로벌 면역항암제 시장 규모는 인구 증가와 고령화에 따른 질병 유병률 증가, 기존 치료법의 한계를 개선하는 치료방식, 이에 따른 해당 시장에 대한 관심 및 R&D 활동의 증가로 2020년 746억 달러에서 연 평균 11.8% 성장(2021-2027)하여 2027년에는 1,595억 달러에 이를 것으로 전망됩니다.
| [글로벌 면역항암제 시장 현황 및 전망(단위: 십억달러)] |
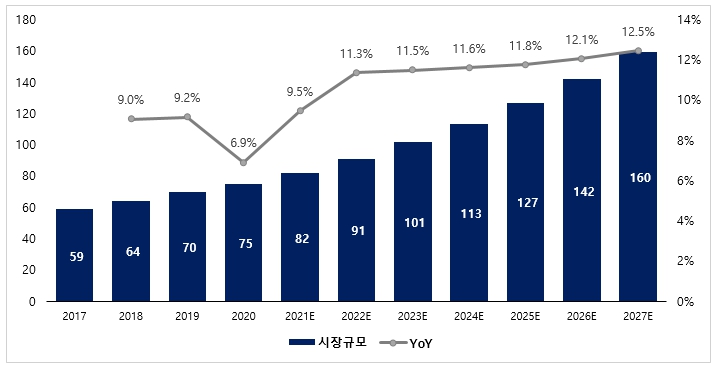 |
|
글로벌 면역항암제 시장 현황 및 전망 |
| 출처: FutureWise Market Research, 2021 |
이러한 면역항암제의 본격적인 시장 확대는 그 간의 지속적인 면역항암제 연구개발 노력에 따른 것으로 해석할 수 있으며, 동시에 최근의 면역항암제 연구개발 동향을 파악함으로서 향후의 시장 동향도 전망할 수 있습니다. Nature Reviews Drug Discovery 논문에 따르면, 글로벌 면역항암제의 전임상 및 임상(승인 포함) 파이프라인은 2017년 2,030개에서 2020년 4,720개로 3년새 233% 증가하였습니다. 특히 면역항암제 중에서도 연구개발 파이프라인의 가장 두드러진 성장을 보인 계열은 세포치료제 부문으로, 2017년 이래 1,192개의 파이프라인이 증가하여, 2019년 1,597개의 면역세포치료제 파이프라인이 연구개발 단계에 있는 것으로 조사되었습니다.
| [글로벌 면역항암제 종류별 파이프라인 현황] |
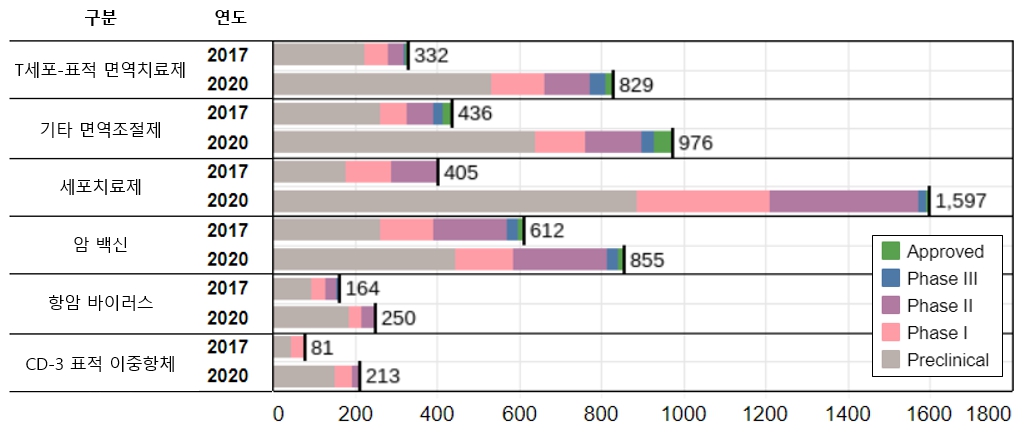 |
|
글로벌 면역항암제 종류별 파이프라인 현황 |
| 출처: J. Tang et al., Nature Reviews Drug Discovery, 2019, 18, 899-900. (당사 재구성) |
이처럼 항암 치료제 분야는 면역항암제로 패러다임 전환이 이뤄지고 있습니다. 그 중에서도 현재는 면역관문억제제가 면역항암제 시장을 견인하고 있는 상황이나, 2017년 CAR-T세포 치료제의 승인 및 본격적인 적용을 시작으로 다양한 세포 치료제에 대한 연구개발이 활발히 진행되고 있습니다.
당사는 면역세포를 이용한 항암제를 연구개발하고 있는 바이오 벤처회사로, 이 같은 글로벌 항암제 개발 트렌드에 부합하는 연구개발을 수행하고 있습니다. 또한 면역세포 종류 및 특성을 고려한 생산 플랫폼 기술을 바탕으로 다양한 암종을 대상으로 적응증 확대가 가능하며, 기존 항암제 및 당사 면역세포치료제 간의 병용요법을 통한 보완 및 확장이 가능합니다. 또한 환자 개인의 면역세포를 활용하는 측면에서 기존의 암 치료법을 개선하고, 개인맞춤형 암 치료 시대를 열 수 있는 잠재력이 높은 기술로 기대되고 있습니다.
그러나, 이러한 당사의 기술 수준에도 불구하고, 새로운 치료법의 등장, 시장 환경의 변화 등으로 글로벌 트렌드에 부합하지 않게 되는 경우, 당사의 사업계획 및 수익창출 등에 부정적인 영향을 미칠 수 있으므로 투자자께서는 이 점 유의하여 주시기 바랍니다.
|
라. 경쟁 면역항암제 개발에 따른 경쟁 심화 위험 또한 과거에는 암 치료를 위해 한가지 항암제만 처방하던 단일요법(Monotherapy)이 주류였으나 현재는 두 가지 또는 그 이상의 항암제를 동시에 혹은 순차적으로 처방하여 암을 치료하는 병용 요법(Combination Therapy)으로 패러다임이 변화하였습니다. 상호 보완적인 작용기전을 가지는 항암제를 동시에 혹은 순차적으로 처방할 경우 시너지 효과가 극대화되어 더욱 우수한 치료 효과를 나타내기 때문입니다. 이에 따라 다수의 바이오 제약사들은 면역항암제와 기존 항암제 혹은 면역항암제들 사이의 최적 조합의 병용요법 개발을 위하여 수많은 연구 및 개발을 진행하고 있습니다. Nature Reviews Drug Discovery(2020) 논문 분석에 따르면, 2019년 기준 활성화 상태인 면역관문억제제의 임상시험은 2975개로 확인되었습니다. 제품별로는 키트루다(펨브롤리주맙)와 옵디보(니볼루맙)의 임상연구가 전체 임상시험의 56%를 차지했으며, 유형별로는 단일요법 보다는 병용요법 연구가 전체 임상시험의 76%를 차지했습니다. |
현재 항암제 신약 개발의 주요 트렌드는 암 종에 무관한 바이오마커(생체지표) 기반의 항암제 개발 및 병용 요법입니다. 과거에도 특정 암에서 효능이 있는 환자군을 세밀하게 나누는 바이오마커를 기반으로 하는 항암제들은 있었으나, 최근에는 암의 종류에 상관없는 바이오마커 기반의 항암제가 승인 및 개발되고 있습니다. 대표적인 예가 PD-1이라는 면역관문 억제기전을 가진 면역항암제인 '키트루다'로, 2017년 현미부수체불안정성(microsatellite instability-high, MSI-H) 또는 DNA복제실수교정결핍(mismatch repair deficient, dMMR)라는 바이오마커를 가진 고형 종양에 대해 허가를 받으면서, 종양 유형에 무관한 바이오마커 기반 최초의 암 치료제로서, 현재 다수의 암종에 1차 치료제로 적용되고 있습니다. 이 같은 암종에 구분 없는 항암제 개발에 따라, 경쟁 관계에 있어서 동일 질환 내 경쟁관계 보다는 동일 작용기전 내 경쟁관계가 중요한 요소가 되었습니다.
또한 과거에는 암 치료를 위해 한가지 항암제만 처방하던 단일요법(Monotherapy)이 주류였으나 현재는 두 가지 또는 그 이상의 항암제를 동시에 혹은 순차적으로 처방하여 암을 치료하는 병용 요법(Combination Therapy)으로 패러다임이 변화하였습니다. 상호 보완적인 작용기전을 가지는 항암제를 동시에 혹은 순차적으로 처방할 경우 시너지 효과가 극대화되어 더욱 우수한 치료 효과를 나타내기 때문입니다. 이에 따라 다수의 바이오 제약사들은 면역항암제와 기존 항암제 혹은 면역항암제들 사이의 최적 조합의 병용요법 개발을 위하여 수많은 연구 및 개발을 진행하고 있습니다.
Nature Reviews Drug Discovery(2020) 논문 분석에 따르면, 2019년 기준 활성화 상태인 면역관문억제제의 임상시험은 2975개로 확인되었습니다. 제품별로는 키트루다(펨브롤리주맙)와 옵디보(니볼루맙)의 임상연구가 전체 임상시험의 56%를 차지했으며, 유형별로는 단일요법 보다는 병용요법 연구가 전체 임상시험의 76%를 차지했습니다. 병용요법 연구로는 서로 다른 기전의 면역관문억제제간 병용연구를 비롯하여, 항암화학요법, 표적항암요법, 방사선요법 등과의 병용연구가 진행되고 있습니다.
| [주요 면역항암제(면역관문억제제) 임상연구 동향] |
|
| * 출처: J. Tang et al., Nature Reviews Drug Discovery 2020, 19, 163-164 |
이처럼 현재 면역항암제 분야의 글로벌 제약회사들은 면역관문억제제를 중심으로 다양한 암종에 대한 대규모 임상 실험과 병용 처방을 통해 빠르게 시장을 선점해가고 있는 상황입니다. 따라서 당사는 치열한 경쟁이 진행중인 면역관문억제제 분야 대신, 당사의 축적된 세포치료제 노하우를 바탕으로 선천면역과 관련된 NK세포, 적응면역과 관련된 T세포의 효능을 강화시킨 CAR-T세포, 세포 간 신호전달 역할을 수행하는 싸이토카인 등을 기반으로 하는 다양한 면역계 레벨의 접근방식을 고려하여 당사만의 면역항암제 파이프라인을 전략적으로 계획하였습니다.
당사가 연구를 집중하고 있는 CAR-T세포 치료제는 환자에서 유래된 T세포를 채집하여, 인위적으로 특이적 키메라 항원 수용체를 도입해 선택적으로 암을 강력하게 살상시키는 기능을 높여서 만들어진 치료제로 기존 항암제보다 치료효과가 매우 높다는 장점이 있습니다.
NK세포치료제는 면역세포치료제의 일종으로 면역세포인 NK세포를 대량 배양하여 환자에게 투여해 환자의 선천면역을 강화하여 암을 치료하는 방식입니다. 이는 특정한 항원없이도 비정상 세포를 감지하고 직접 살상하는 NK세포의 특성을 이용한 것이기 때문에 다양한 암종에 적용이 가능할 것으로 보이며, 부작용이 기존치료법 대비 거의 없다는 장점을 가지고 있습니다.
싸이토카인을(IL-15) 기반으로 한 반려견 항암제 역시 면역치료제입니다. 기존에는 암 환견 전용 면역항암제가 없었기 때문에 사람에 이용되는 항암제를 사용하여 치료효율이 낮고 부작용이 발생하는 경우가 있었으나, 해당 파이프라인은 반려견의 유전체 정보를 바탕으로 설계되어 치료효과가 높을 것으로 기대하고 있습니다.
그리고, 당사의 파이프라인 역시 단독 요법 보다는 기존 화학항암제, 표적항암제와의 병용요법, 다른 타겟의 면역항암제와의 상호보완적인 병용요법을 통해 독성 문제 해결, 재발율 감소, 전체 생존율의 증대 등의 시너지 효과를 기대하고 있습니다. 따라서 기존의 시장 내 주력제품들은 당사의 제품과 경쟁관계가 아닌 협력관계에 있으며, 병용 처방을 통해 상호보완적인 시너지 효과를 발휘할 것으로 기대하고 있습니다.
당사의 Vax-NK/HCC는 간암 대상 HAIC라는 약물투여방식을 병용하는 차별성을 가지고 있으며, 특히 NK세포는 일부 국가에서 조건부 허가를 받은 제품은 있지만, 글로벌 수준에서 아직 본격적으로 처방되고 있는 제품이 없는 상황으로, 유의미한 임상 결과를 바탕으로 성공적인 시장진입 시 경쟁력을 갖출 수 있을 것으로 기대됩니다.
한편, 당사의 파이프라인 중 Vax-CAR 세포치료제와 관련하여, 현재 전세계적으로 시판이 허용된 6종의 CAR-T 치료제인 노바티스사의 킴리아와 길리아드사의 예스카르타, 테카터스, BMS사의 브레얀지, 아벡마 그리고 J&J의 카빅티는 모두 혈액암과 관련된 치료제로 앞선 네개는 급성림프구성백혈병(acute lymphoblastic leukemia)에 대한 anti-CD19, 아벡마와 카빅티는 다발골수종(BCMA) CAR-T 치료제입니다. 또한 이외에도 머지 않은 미래에 출시될 것으로 예측되는 또 다른 종류의 CAR-T 치료제들 역시 혈액암을 적응증으로 하는 CAR-T 치료제이며, 국내에서도 큐로셀, 앱클론 등의 회사에서 난치성 림프종을 대상으로 임상연구를 진행하고 있습니다. 이에 당사는 유병자수가 많고 미충족 의료 수요가 높은 또 다른 혈액암인 다발골수종과 난치성 고형암을 적응증으로 선택하였으며, 2023년 부터 중국 센랑바이오와 공동연구개발 협약을 체결하여 다발골수종에 대한 CAR-T, CAR-MIL 치료제 개발을 수행 하고 있습니다. 당사는 이러한 연구개발의 성과로 지난 2021년 monobody 기반 CAR-T 세포치료제에 대한 특허를 출원하고 2022년 국제 PCT 출원을 완료하였으며, 2021년부터 공동연구를 진행하고 있는 와이바이오로직스와 고형암을 타 겟으로 한 anti PD-L1 CAR-T 세포치료제에 대한 특허를 2022년 3월 공동출원하여 지난 3월 국제 PCT 출원을 완료하였습니다.
마지막으로 당사는 반려견용 면역항암제 박스루킨-15를 개발하고 있습니다. 이는 면역체계를 활성화하는 물질인 인터루킨-15를 이용한 치료제로, 이미 임상학적으로 유효한 것으로 알려진 사이토카인 면역항암 후보물질을 선택하였습니다. 아직까지 동물용 면역항암제로 출시된 제품은 없는 상황으로, 당사는 최초의 동물용 면역항암제 개발로 반려동물용 항암제 시장을 선도하려는 차별화 전략을 보유하고 있습니다.
농림축산검역본부의 품목허가를 득한 뒤 바로 시판할 수 있도록 대한수의사회, 한국동물병원협회 등과의 네트워크를 적극 활용할 계획이며 이미 MOU를 맺은 바 있는 (주)케어사이드, (주)씨티씨바이오를 통한 마케팅을 함께 추진할 예정입니다.
특히 당사가 추구하는 NK세포, CAR-T 세포 등 세포치료제 연구개발사업은 기존의 의약품과는 차별화된 새로운 방식의 치료제인 신개념 치료제에 해당합니다. 세포치료제 연구개발을 위해서는 세포의 분리 및 배양 기술, 유전학, 단백질학 등 다양한 생명공학 기술의 노하우를 필요로 하므로, 타 제약 및 바이오 업체의 진입장벽이 높은 편이며, 비교적 성장 초기 단계이므로 독자 기술 확보를 통해 고부가가치 창출이 가능할 것으로 기대합니다.
하지만, 당사는 2022년 08월 24일 기존 파이프라인이었던 Vax-DC의 임상시험 연구개발의 조기종료를 발표하였습니다. 최근 재발성/불응성 다발골수종 치료제 분야가 다양한 기전의 신약과 세포치료제 (CAR-T)의 도입으로 급속한 발전을 이루어 중앙 생존기간과 치료 반응률이 계속 높아지고 있으며, 최근 임상 연구를 진행한 일부 치료제의 경우 80%이상의 높은 반응률을 기록하는 등 해당 분야의 경쟁이 치열해지고 있어 연구 개발의 타당성과 투자대비 사업성이 낮아졌다고 판단했기 때문입니다.
VAX-DC는 자가 골수종세포를 자외선으로 조사시켜 만들어진 Dying tumor cell(종양세포 사멸체)를 종양항원으로 부가시킨 다발골수종 환자 유래의 자가 수지상세포 치료제이며, 환자의 체내에 투여하였을 때 T세포와 상호작용을 하면서 교육을 통해 항원-특이적인 Cytotoxic T lymphocyte(CTLs) 만들어 종양세포를 제거하는 간접적인 치료방법이었습니다.
이에 비하여 당사에서 신규로 도입한 BCMA-CAR-T, BCMA-CAR-MILs 은직접 암세포를 공격하는 강력한 치료제라 할 수 있습니다.
BCMA-CAR-MILs의 경우 MIL(골수침윤림프구) 내에 수많은 종양항원을 인식하고 기억하는 기억T세포를 다량 함유하고 있어서 체내에서 장기 생존이 가능한 효과적인 치료요법이며, BCMA CAR scFV와 결합하여 더욱더 강력한 효과를 보일 수 있다는 점을 비임상으로 통해서 입증하였습니다.
이는 기존의 BCMA-CAR-T 치료제의 한계인 높은 재발율을 극복할 수 있을 것이라 예상하고 있습니다.
이에따라 Vax-DC 플랫폼은 재발성/불응성 다발골수종을 임상 1/2a상에서 77.8%의 높은 면역학적 반응률을 보이는 등 유의미한 결과를 얻어 2019년 임상 2a상을 승인받았지만, 급격한 발전을 이루고 있는 다발골수종 시장에서 Vax-DC 치료제를 고수하기보다는 주력 파이프라인에 연구 인력을 재배치하기로 결정하였습니다. 기존 주력 파이프라인인 Vax-NK/HCC에 보다 집중하고, 기존 Vax-DC 치료제보다 진보된 다발골수종 치료제인 CAR-MIL 개발을 본격화하는 등 선택과 집중을 강화할 예정입니다.
이와 같이, 면역세포치료제 시장의 높은 시장성을 보고 다수의 제약사들이 임상을 확대하여 속도를 내고 있다는 점은 당사 사업에 위협 요인으로 작용할 수 있습니다. 해당 경쟁 파이프라인이 당사 제품의 임상속도보다 앞서 임상에 성공하여 시장에 진입할 경우, 당사 면역세포치료제 파이프라인의 시장 경쟁력이 약화될 수 있으며, 이는 제품 판매 및 기술 이전에 부정적인 영향을 미칠 수 있습니다. 이 경우, 당사의 수익성 및 재무상태에 부정적인 영향을 미칠 수 있으므로 투자자께서는 유의하여 주시기 바랍니다.
| 마. 예방의학 및 조기진단에 따른 시장 감소 위험성 전 세계적인 고령화로 인해 당사의 사업분야인 항암제 시장은 지속적인 성장이 전망되고 있습니다. 하지만 조기 진단을 통한 빠른 치료로 완치율이 향상되고, 건강에 대한 관심이 높아짐에 따라 예방을 위한 운동 및 식습관 개선으로 암 발생률이 낮아지고 있습니다. 특히 간암의 경우에는 국내 간암의 주요 원인인 B형간염의 예방접종사업 확대와 B형간염 및 C형간염에 대한 항바이러스 치료의 효과로 1999년 이후 간암 발생률이 지속적으로 낮아지고 있습니다. 또한 「암관리법」 제 11조(암검진사업), 동법 시행령 제 6조(암검진사업의 범위)부터 제8조(암검진사업 대상 암의 종류ㆍ 검진주기 등)까지 및 동법 시행규칙 제 4조, 「국민건강보험법」제 52조 및 동법 시행령 제25조, 「의료급여법」 제 14조의 규정에 근거하여 보건복지부는 암의 치료율을 높이고 암으로 안한 사망률을 줄이기 위하여 암을 조기에 발견하는 검진사업(암검진사업)을 시행하고 있습니다. 이처럼 조기진단 및 예방의학에 대한 인식 변화에 따른 발병률 감소, 완치율 향상 등으로 당사가 개발 중인 면역항암제 시장 규모의 감소가 발생할 경우 당사의 향후 수익에 부정적인 영향을 미칠 수 있으니 투자자분들 께서는 이점 유의하여 주시기 바랍니다. |
전 세계적인 고령화로 인해 당사의 사업분야인 항암제 시장은 지속적인 성장이 전망되고 있습니다. 하지만 조기 진단을 통한 빠른 치료로 완치율이 향상되고, 건강에 대한 관심이 높아짐에 따라 예방을 위한 운동 및 식습관 개선으로 암 발생률이 낮아지고 있습니다. 특히 간암의 경우에는 국내 간암의 주요 원인인 B형간염의 예방접종사업 확대와 B형간염 및 C형간염에 대한 항바이러스 치료의 효과로 1999년 이후 간암 발생률이 지속적으로 낮아지고 있습니다. 보건복지부 통계자료에 따르면 1999년 10만 명 당 간암 발생자는 52.4명이었으나, 2020년에는 29.5명으로 집계되어 간암 발생률은 감소 추세를 보이고 있습니다. 주요 암종별 발생률은 다음과 같습니다.
| [주요 암종별 발생률(남녀 전체) 추이] |
| (단위: 명/10만 명) |
| 구분 | 위 | 직장 | 간 | 폐 | 유방 | 자궁경부 | 전립선 | 갑상선 |
|---|---|---|---|---|---|---|---|---|
| 1999 | 86 | 20.4 | 52.4 | 59.8 | 17.2 | 14.2 | 7.4 | 9.8 |
| 2010 | 84.4 | 32.7 | 44.2 | 62.9 | 33.2 | 9.5 | 24.3 | 79.8 |
| 2015 | 67.8 | 26.4 | 36.7 | 59 | 40.2 | 7.7 | 24.9 | 51.4 |
| 2019 | 59.8 | 24.2 | 31.7 | 61.3 | 49.3 | 6.5 | 34.5 | 60.6 |
| 2020 | 51.9 | 22.9 | 29.5 | 56.4 | 48.5 | 5.8 | 32.7 | 56.8 |
| 주1) 발생률(incidence rate): 일정기간동안 한 인구 집단 내에서 어떤 질병이 새로 발생한 환자의 수 주2) 발생률은 각 연령군에 해당하는 표준인구의 비율을 가중치로 주어 산출한 가중평균발생률(연령표준화발생률) 출처: 보건복지부 |
한편 암종별 상대생존율은 지속적으로 증가하고 있습니다. 국내 '93년~'95년 기간별 암의 상대생존율은 42.9%에 불과했으나 '16년~'20년에는 상대생존율이 71.5%까지 증가하며 28.6% 증가하였습니다. 당사 치료제의 주요 적응증인 간암의 경우에는 '93년~'95년 상대생존율이 11.8%에서 '16~'20년 38.7%까지 증가하였습니다. 주요 암종 5년 상대생존율 추이는 다음과 같습니다.
| [주요 암종 5년 상대생존율 추이(남녀 전체)] |
| (단위: %, %p) |
|
발생 순위 |
암종 |
발생기간 |
증감 |
|||||
|---|---|---|---|---|---|---|---|---|
| '93년~'95년 | '96년~00년 |
'01년~'05년 |
'06년~'10년 |
'15년~'19년 |
'16년~'20년 | |||
| 모든 암 | 42.9 | 45.2 | 54.1 | 65.5 | 70.7 | 71.5 | 28.6 | |
| 1 | 갑상선 | 94.5 | 95 | 98.4 | 100 | 100.2 | 100 | 5.5 |
| 2 | 폐 | 12.5 | 13.7 | 16.6 | 20.3 | 27.6 | 36.8 | 24.3 |
| 3 | 대장 | 56.2 | 58.9 | 66.9 | 73.9 | 76.1 | 74.3 | 18.1 |
| 4 | 위 | 43.9 | 47.3 | 58 | 68.4 | 75.9 | 78 | 34.1 |
| 5 | 유방 | 79.2 | 83.6 | 88.7 | 91.2 | 92.8 | 93.8 | 14.5 |
| 6 | 전립선 | 59.1 | 69.4 | 81 | 92 | 94.2 | 95.2 | 36.1 |
| 7 | 간 | 11.8 | 14.1 | 20.5 | 28.3 | 34.4 | 38.7 | 26.9 |
| 8 | 췌장 | 10.6 | 8.7 | 8.4 | 8.6 | 10.9 | 15.2 | 4.6 |
| 9 | 담낭 및 기타담도 | 18.7 | 20.7 | 23.1 | 26.9 | 28.8 | 29 | 10.4 |
| 10 | 신장 | 64.2 | 67 | 73.7 | 78.6 | 82.6 | 85.7 | 21.4 |
| 주) 증감의 경우 '93년~'95년 대비 '16년~'20년 암발생자의 생존률 차이 출처: 보건복지부 |
또한 「암관리법」 제 11조(암검진사업), 동법 시행령 제 6조(암검진사업의 범위)부터 제8조(암검진사업 대상 암의 종류ㆍ 검진주기 등)까지 및 동법 시행규칙 제 4조, 「국민건강보험법」제 52조 및 동법 시행령 제25조, 「의료급여법」 제 14조의 규정에 근거하여 보건복지부는 암의 치료율을 높이고 암으로 안한 사망률을 줄이기 위하여 암을 조기에 발견하는 검진사업(암검진사업)을 시행하고 있습니다.
| [암검진사업 관련 법령] |
|---|
|
「암관리법」 제11조(암검진사업) ② 암검진사업의 범위, 대상자, 암의 종류ㆍ검진주기, 연령 기준 등에 관하여 필요한 사항은 대통령령으로 정한다. 이 경우 보건복지부장관은 암의 발생률, 생존율, 사망률 등 암 통계 및 치료에 관한 자료를 고려하여 암검진사업의 대상자, 암의 종류ㆍ검진주기 등을 정하여야 한다. ③ 암의 검진 방법 및 절차 등에 관하여 필요한 사항은 보건복지부령으로 정한다. ④ 보건복지부장관은 암검진을 받는 사람 중 「의료급여법」에 따른 의료급여수급자 및 대통령령으로 정하는 건강보험가입자에 대하여는 예산 또는 「국민건강증진법」에 따른 국민건강증진기금(이하 “국민건강증진기금”이라 한다)에서 그 비용의 전부 또는 일부를 지원할 수 있다. 1. 암검진의 기준 연구 및 질 관리 2. 암검진 대상자 중 해당 연도 내 암검진을 받을 사람(이하 “수검 예정자”라 한다)의 선정 및 통보 3. 수검 예정자에 대한 검사 및 진단 4. 법 제11조제4항에 따른 검진비 지원 5. 암검진에 관한 교육 및 홍보 6. 암검진에 관한 정보시스템의 개발 및 관리 7. 그 밖에 암검진사업과 관련하여 보건복지부장관이 필요하다고 인정하는 사업 「암관리법 시행령」 제7조(암검진사업의 대상자 등) 1. 「국민건강보험법」 제5조에 따른 건강보험가입자 및 피부양자 2. 「의료급여법」에 따른 의료급여수급자 ② 법 제11조제4항에서 “대통령령으로 정하는 건강보험가입자”란 「국민건강보험법」 제69조에 따른 월별 보험료액 등을 기준으로 하여 보건복지부장관이 정하여 고시하는 사람을 말한다.
① 법 제11조제2항에 따른 암검진사업의 대상이 되는 암의 종류는 다음 각 호와 같다. 1. 위암 2. 간암 3. 대장암 4. 유방암 5. 자궁경부암 6. 폐암 ② 암의 종류별 검진주기와 연령 기준 등은 별표 1과 같다. |
| 출처: 국가법령정보센터 |
암검진사업은 1999년부터 의료급여수급권자를 대상으로 위암, 유방암, 자궁경부암 등 3종에 대한 검진을 실시하였으며, 2003년 간암, 2004년 대장암, 2019년 폐암이 추가되고 2021년에는 암검진비용 지원 대상자가 보험료부과기준이 직장가입자 100,000원, 지역가입자 94,000원 이하인 자가 추가되어 암검진사업 대상 범위가 확대되었습니다.
| [국가암검진 프로그램 검진대상 및 방법] |
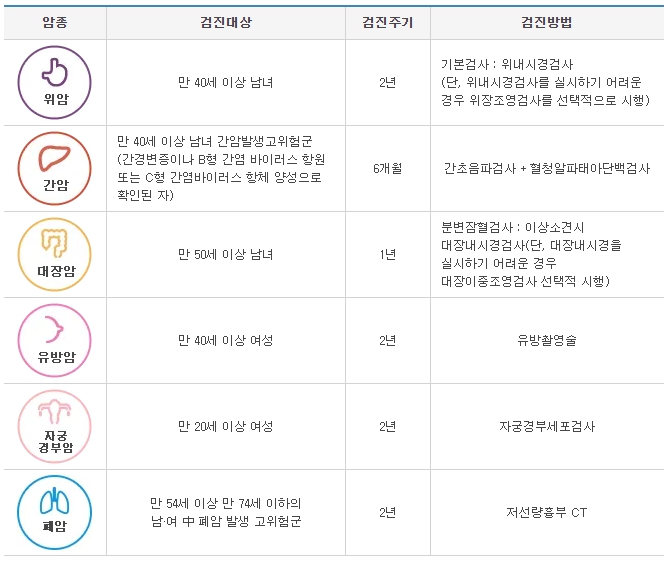 |
|
국가암검진 프로그램 검진대상 및 방법 |
국가 암검진을 통하여 암검진을 받은 수검자는 2013년 9,525천명에서 2022년 14,184천명으로 증가하였으며 간암의 경우에는 2013년 267천명에서 2022년 344천명으로 증가하였습니다. 특히 간암의 경우 2022년 기준 국가 암검진 사업에 포함된 암종 중 수검률 72.5%로 가장 높은 수검률을 보이고 있습니다. 수검자수와 수검률 추이는 다음과 같습니다.
| [국내 암 조기검진 수검자 수] |
| (단위: 천명, %) |
| 구 분 | 2013 | 2014 | 2015 | 2016 | 2017 | 2018 | 2019 | 2020 | 2021 | 2022 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 전체 | 수검자수 | 9,525 | 10,327 | 11,230 | 12,012 | 12,424 | 12,942 | 13,897 | 11,925 | 14,076 | 14,184 |
| 수검률 | 37.4 | 48.4 | 50.1 | 51.5 | 52.7 | 55.0 | 55.6 | 49.2 | 55.1 | 54.9 | |
| 위암 | 수검자수 | 3,079 | 3,332 | 3,568 | 3,758 | 3,801 | 3,922 | 4,189 | 3,559 | 4,268 | 4,338 |
| 수검률 | 43.7 | 55.0 | 56.9 | 59.0 | 59.9 | 61.9 | 62.2 | 55.4 | 62.6 | 62.3 | |
| 간암 | 수검자수 | 267 | 309 | 341 | 245 | 241 | 287 | 309 | 293 | 342 | 344 |
| 수검률 | 44.2 | 59.6 | 60.3 | 66.4 | 68.7 | 71.9 | 73.1 | 68.4 | 72.9 | 72.5 | |
| 대장암 | 수검자수 | 2,465 | 2,593 | 2,891 | 3,105 | 3,327 | 3,557 | 3,755 | 3,190 | 3,642 | 3,687 |
| 수검률 | 27.0 | 34.9 | 36.8 | 38.6 | 40.2 | 43.0 | 43.0 | 36.9 | 40.3 | 40.4 | |
| 유방암 | 수검자수 | 1,822 | 1,966 | 2,099 | 2,202 | 2,243 | 2,287 | 2,454 | 2,072 | 2,517 | 2,518 |
| 수검률 | 48.6 | 60.4 | 61.8 | 63.8 | 64.5 | 65.8 | 66.0 | 58.5 | 65.9 | 65.4 | |
| 자궁경부암 | 수검자수 | 1,892 | 2,127 | 2,331 | 2,702 | 2,812 | 2,889 | 3,141 | 2,756 | 3,239 | 3,213 |
| 수검률 | 38.5 | 52.1 | 53.9 | 52.8 | 54.6 | 57.3 | 59.8 | 54.8 | 61.7 | 61.0 | |
| 폐암 | 수검자수 | 0 | 0 | 0 | 0 | 0 | 0 | 49 | 55 | 69 | 84 |
| 수검률 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 33.1 | 36.6 | 47.9 | 52.6 | |
| 주1) 2019년부터 폐암 검진대상자 및 수검자 포함 주2) 대상자: 의료급여수급자 + 건강보험 가입자 하위 50% 주3) 수검률: 국가 암검진 사업에 포함된 6대 암종별 대상자 중 국가 암검진 사업을 통하여 암검진을 받은 암종별 수검자의 백분율 출처: e-나라지표 |
이처럼 조기진단 및 예방의학에 대한 인식 변화에 따른 발병률 감소, 완치율 향상 등으로 당사가 개발 중인 면역항암제 시장 규모의 감소가 발생할 경우 당사의 향후 수익에 부정적인 영향을 미칠 수 있으니 투자자분들 께서는 이점 유의하여 주시기 바랍니다.
|
바. 핵심연구인력 유출 위험 신약 개발사업은 후보물질 발굴, 비임상시험, 임상시험, 허가, 생산 및 마케팅 등 전 단계에 걸쳐 전문인력을 필요로 합니다. 특히 기존 의약품으로 치료가 어려웠던 난치성 질환에 대하여 의학적 미충족 수요를 충족시킬 수 있는 first-in-class 신약을 개발하거나 글로벌 시장가치가 매우 높은 블록버스터급 신약을 개발하기 위해서는 해당 분야에 지식과 경험을 갖춘 우수한 전문인력을 확보하는 것이 중요하며, 각 분야별 전문인력의 확보 여부는 곧 당사와 같은 연구개발 벤처기업의 경쟁력으로 직결됩니다. 당사는 지식과 경험이 풍부한 전문인력의 확보가 신약 연구개발 사업의 핵심 경쟁력이라는 사실을 인지하고 우수한 전문 인력을 영입하고자 기존 조직원들의 역량을 최대한으로 끌어올리기 위해 다양한 지원을 아끼지 않고 있습니다. |
신약 개발사업은 후보물질 발굴, 비임상시험, 임상시험, 허가, 생산 및 마케팅 등 전 단계에 걸쳐 전문인력을 필요로 합니다. 특히 기존 의약품으로 치료가 어려웠던 난치성 질환에 대하여 의학적 미충족 수요를 충족시킬 수 있는 first-in-class 신약을 개발하거나 글로벌 시장가치가 매우 높은 블록버스터급 신약을 개발하기 위해서는 해당 분야에 지식과 경험을 갖춘 우수한 전문인력을 확보하는 것이 중요하며, 각 분야별 전문인력의 확보 여부는 곧 당사와 같은 연구개발 벤처기업의 경쟁력으로 직결됩니다.
당사는 지식과 경험이 풍부한 전문인력의 확보가 신약 연구개발 사업의 핵심 경쟁력이라는 사실을 인지하고 우수한 전문 인력을 영입하고자 기존 조직원들의 역량을 최대한으로 끌어올리기 위해 다양한 지원을 아끼지 않고 있습니다. 당사의 현재 연구개발 조직도 및 인력 현황은 다음과 같습니다.
 |
|
박셀바이오 연구개발 담당조직 |
| [당사의 주요 연구개발 조직 구성] |
|
연구소 |
주요 업무 |
|
기업부설연구소 |
- Vax-CARs 플랫폼 개발연구 - 차세대 박스루킨-15 연구 - Monobody 플랫폼 개발 연구 |
| 공정개발실 | - 차세대 Vax-NK 공정개발 연구 - 박스루킨-15 효율 및 생산성 개선 연구 - 차세대 박스루킨-15 연구 - Vax-CAR-T 의 공정개발 연구 및 Vax-CAR-MIL의 연구개발 |
|
|
|
| 출처: 당사 정기보고서 |
| [연구개발인력 현황] |
|
구분 |
인원 (명) |
|||
|---|---|---|---|---|
|
박사 |
석사 |
기타 |
합계 |
|
|
기술연구소 |
2 | 2 | 3 | 7 |
|
임상연구실 |
1 | 1 | 2 | 4 |
|
공정개발실 |
1 | 2 | 2 | 5 |
|
동물의약품실 |
2 | 0 | 2 | 4 |
|
기타 핵심 연구 인력 |
6 | 2 | 0 | 8 |
|
계 |
12 | 7 | 9 | 28 |
| 기준일 : 증권신고서 제출 전 영업일 |
| [연구개발인력 3개년 추이] |
| 2020년 | 2021년 | 2022년 | 2023년 반기 |
|
|
기술연구소 |
7 | 8 | 8 | 7 |
|
임상연구실 |
1 | 4 | 3 | 4 |
|
공정개발실 |
- | - | 3 | 5 |
|
동물의약품실 |
- | 1 | 3 | 4 |
|
기타 핵심 연구 인력 |
5 | 5 | 6 | 8 |
| 계 (명) | 13 | 18 | 23 | 28 |
| 출처 : 당사 정기보고서 |
증권신고서 제출일 현재 당사의 임직원 수는 56명이며, 그 중 28명이 당사의 연구개발인력입니다. 당사의 이제중 대표이사는 수석의학자로서 경영 뿐만 아니라 임상/제조 부문을 총괄하며 당사의 핵심 임상연구를 이끌고 있습니다.
연구소는 이준행 CSO와 연구소장인 김미화 소장을 중심으로 연구 업무를 총괄하고 있습니다. 이제중 대표이사, 이준행 사내이사, 배우균 이사, 김상기 이사 등 4명의 교수급 인력과 공정개발실 Vo Manh Coung 부장, 기술연구소 김미화 소장과 백민우 수석 연구원, 제조소 장윤영 소장, 임상연구실 하선아 실장, 품질실 심재웅 실장, 동물의약품실 이재일 실장 등 8명의 박사급 실무 인력들을 주요 핵심 연구개발 인력으로 확보하고 있습니다. 이들 주요 핵심 연구인력은 다년간의 업계 경험을 통해 상당한 전문성을 갖춘 인력으로 동사는 해당 인력들을 적극 활용하여 기존 사업을 안정적으로 수행함과 동시에 회사를 성장시키기 위한 노력을 지속하고 있습니다. 당사의 주요연구 인력 현황은 아래와 같습니다.
| [당사의 핵심 연구개발인력 현황] |
|
직책명 |
성 명 (출생년) |
담당업무 |
약 력 |
|
대표이사(CEO/CMO) |
이제중 |
총괄 |
99.02 전남대학교 의과대학 혈액종양학 박사 99.05~03.07 화순전남대학교병원 임상교수 00.07~01.01 일본 동경 국립암센터 방문연구원 06.03~07.12 미국 피츠버그대학교 암연구소 방문교수 10.02~19.06 ㈜박셀바이오 대표이사 (설립) 15.01~17.12 한국다발골수종연구회 위원장 03.07~전남의대/현재 화순전남대학교병원 혈액종양내과 교수 08.12~현재 화순전남대학교병원 암면역치료연구센터장 21.02~현재 ㈜박셀바이오 대표이사 |
|
사내이사 (CSO) |
이준행 |
기술연구소 총괄 (연구) |
92.02 전남대학교 의과대학 미생물학 박사 17.05~19.04 대한기초의학협의회 부회장 19.06~19.11 ㈜박셀바이오 대표이사 93.08~현재 전남대학교 의과대학 교수 17.01~현재 (재)백신글로벌산업화기반 구축사업단 선임이사 21.01~현재 ㈜박셀바이오 연구총괄 및 사내이사 |
|
이사 |
배우균 |
연구개발 |
11.03 전남대학교 의학박사 |
| 이사 (비등기/상근) |
김상기 (1960년) |
연구개발 (공정개발) |
93.08 전남대학교 수의학과 05.09~ 현재 화순전남대학교 병원 암면역세포치료연구센터 06.02~ 현재 공주대학교 산업과학대학 특수동물학과 교수 23.03~ 현재 (주)박셀바이오 공정개발실장 |
|
이사 (비등기/상근) |
하선아 (1971년) |
연구개발 (임상) |
02.02 미주리주립대학교 박사 (세포생물학) 02.08~04.04 가톨릭의과대학교 연구교수 04.06~06.04 Riken Institute (Yokohama) 박사후 연구원 (면역학) 06.05~18.01 가톨릭의과대 연구교수/기진싸이언스 겸직 17.04~18.01 서울대의과대학 (임상기획) 18.02~18.09 ㈜헤링스 (임상기획) 18.10~21.05 ㈜퓨쳐메디신 (임상/전임상 총괄) |
|
이사 (비등기/상근) |
김미화 |
기술연구소 총괄 |
03.02 전남대학교 의학 박사(병리학) 03.03~07.03 조선대학교 의과대학 약리학교실 계약교수 07.04~09.04 조선대학교 단백질소재연구센터 (ERC) 전임강사 09.05~12.02 조선대학교 한국인유전자손상연구센터 (KDRRC) 연구교수 12.05~14.02 전남대학교 치의학과 미네랄장애연구센터 (MRC) 연구교수 14.10~15.08 미국 텍사스 주립대 의과대학 약리학과 박사후 연구원 15.09~17.03 미국 텍사스 주립대 의과대학 생명과학과 연구원 17.04~20.08 미국 텍사스 주립대 의과대학 생물의학부 조교수 |
|
이사 (비등기/상근) |
이재일 |
연구개발 |
94.03 전남대학교 수의학 박사 |
|
이사 (비등기/상근) |
장윤영 |
연구개발 |
13.08 전남대학교 분자의과학협동과정 박사 02.02~03.07 조선대학교 유전공학 분자세포생물학 실험실 연구보조 03.08~04.02 전남대학교 치과대학 구강병리학교실 연구원 06.02~08.09 JB줄기세포연구소 동물실험팀장 08.11~10.08 암면역치료연구센터 연구원 13.01~현재 ㈜박셀바이오 제조소장 |
|
부 장 |
심재웅 |
연구개발 |
13.08 전남대학교 분자의과학 이학박사 13.09~15.07 전남대학교 알레르기내과 연구원 15.08~17.10 화순전남대병원 의생명연구원 연구교수 17.12~현재 ㈜박셀바이오 품질관리실장 |
|
부 장 |
Vo Manh Cuong (1983년) |
연구개발 (공정개발) |
11.03~16.02 전남대학교 분자의학과 석사, 박사 16.03~19.02 화순전남대병원 혈액종양내과 박사후 연구원 19.03~22.12 화순전남대병원 혈액종양내과 연구교수 22.12~현재 ㈜박셀바이오 공정개발실 |
|
수석연구원 |
백민우 (1978년) |
연구개발 (연구) |
06.03~10.08 전남대학교 생명과학기술학과 박사 10.09~12.01 한국기초과학지원연구원(KBSI) 박사후 연구원 12.02~13.03 전남대학교 치과대학 생체광물화질환 연구센터 연구교수 13.04~16.03 전남대학교 생명과학기술학과 박사후 연구원 16.04~17.08 텍사스대학교 UTRGV 의과대학 박사후 연구원 17.09~21.03 미네소타대학교 약학과 박사후 연구원 18.09~21.03 미네소타대학교 연구기기연구실 관리자 21.05~22.11 충북대학교 노화연구소 초빙 부교수 22.12~현재 ㈜박셀바이오 기술연구소 수석연구원 |
| 출처: 당사 제공 |
당사는 지속적인 인력 투자를 통해 목표기간 내 임상 성공 및 연구개발의 완전성 실현을 이루고자 계획하고 있으며 인력관리의 중요성을 인지하고 업무 만족도 증진, 회사의 비전 공유, 지속적인 자기 개발 기회 부여, 업무실적에 근거한 인센티브제도 등 각종 복리후생제도 강화 등을 통해 직원들의 애사심 고취에 힘쓰고 있으며 향후에도 임직원의 다양한 복지 혜택을 확대할 계획입니다.
당사는 연구인력 및 주요 직원들에 대해 사기진작 및 보상과 함께 장기근속 유도로 이탈을 방지하기 위하여 주식매수선택권을 부여하고 있습니다. 당사가 현재까지 부여한 주식매수선택권은 다음과 같습니다.
| [당사의 주식매수선택권 부여 현황] |
| (단위 : 원, 주) |
| 부여 받은자 |
관 계 | 부여일 | 부여방법 | 주식의 종류 |
최초 부여 수량 |
당기변동수량 | 총변동수량 | 기말 미행사수량 |
행사기간 | 행사 가격 |
의무 보유 여부 |
의무 보유 기간 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 행사 | 취소 | 행사 | 취소 | |||||||||||
| 김미화 | 미등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 4,500 | - | - | - | - | 4,500 | 23.03.25 ~ 28.03.24 | 118,712 | X | - |
| 하선아 | 미등기임원 | 2022년 02월 07일 | 신주교부 | 보통주 | 4,500 | - | - | - | - | 4,500 | 24.02.07 ~ 29.02.06 | 42,274 | X | - |
| OOO | 미등기임원 | 2022년 07월 15일 | 신주교부 | 보통주 | 4,500 | - | - | - | - | 4,500 | 24.07.15 ~ 29.07.14 | 41,940 | X | - |
| OOO | 미등기임원 | 2023년 02월 23일 | 신주교부 | 보통주 | 6,000 | - | - | - | - | 6,000 | 25.02.23 ~ 30.02.22 | 36,185 | X | - |
| OOO | 미등기임원 | 2023년 02월 23일 | 신주교부 | 보통주 | 5,000 | - | - | - | - | 5,000 | 25.02.23 ~ 30.02.22 | 36,185 | X | - |
| OOO | 미등기임원 | 2023년 02월 23일 | 신주교부 | 보통주 | 5,000 | - | - | - | - | 5,000 | 25.02.23 ~ 30.02.22 | 36,185 | X | - |
| 출처: 당사 정기보고서 |
항암면역치료제 시장은 세계적으로 중소규모부터 대규모 제약회사들까지 다양한 기이 앞다투어 연구를 하고 있기에 당사와 같은 벤처기업이 전문성이 있는 우수한 인력을 확보하는 것은 어려우며 나아가 핵심인력을 유지하고 유출을 방지하는 것 또한 매우 어려운 일입니다. 이러한 특성으로 인하여 당사의 노력에도 불구하고 당사의 핵심인력이 해외 및 국내의 경쟁회사로 유출되는 경우, 당사의 경쟁적 지위를 약화시킬 수 있습니다. 또한 당사의 첨단 신약을 이해하고 기여할만한 대체인력을 찾고 교육/훈련하는 과정에서 많은 비용이 소요되어 당사의 수익성과 안정성에 부정적인 영향을 미칠 수 있으니 이 점 투자자께서는 유의하여 주시기 바랍니다.
|
사. 지적재산권 침해에 따른 위험 |
당사와 같은 연구개발기업은 특허의 출원 및 등록과 관련제도를 통한 지적재산권의 관리가 중요하며 핵심 기술 및 제품에 대한 권리를 보호할 수 있는 장치를 마련하는 것이 필요합니다. 특허의 출원은 특허법인을 통한 사전 조사를 바탕으로 진행되며, 신규성을확인하고 연구개발을 통해 진보성을 확보 후 출원을 하는 방식으로 진행하여 특허 등록이 거절될 확률을 최소화하고 있습니다.
당사는 개별적으로 등록한 특허 이외에 PCT제도를 활용하여 전 세계 거의 모든 국가에서 출원할 수 있도록 하고 있습니다. PCT (Patent Cooperation Treaty: 특허협력조약)는 150개 이상의 체결국들간의 국제조약으로 개별적으로 다수의 국내 또는 해외 특허출원을 하는 대신 한번의 “국제출원(PCT)”를 함으로써, 정해진 기간내에 많은 국가에 출원을 할 수 있도록 하는 제도입니다.
특허는 특허독립(속지주의)의 원칙상 각 국에서 직접 출원을 하여 그 나라의 특허권 등을 취득하여야만 해당국에서 독점 배타적 권리를 확보할 수 있습니다. 이러한 1국 1특허의 원칙 때문에 해외에서의 특허권 획득을 위해서는 별도의 해외출원이 필요하며, 해외출원을 하는 방법으로 PCT 국제출원을 이용하는 경우가 많습니다.
PCT에 의한 출원방법은 국적국 또는 거주국의 특허청(수리관청)에 하나의 PCT출원서를 제출하고, 우선권의 기초가 되는 출원일로부터 30개월내에 특허획득을 원하는 국가로의 국내단계에 진입하여 해당 국가 특허청에서 특허 심사를 받게 되는데 이때 PCT국제출원의 출원일이 지정국가에서 출원일로 인정받을 수 있게 됩니다.
|
[PCT 출원 설명] |
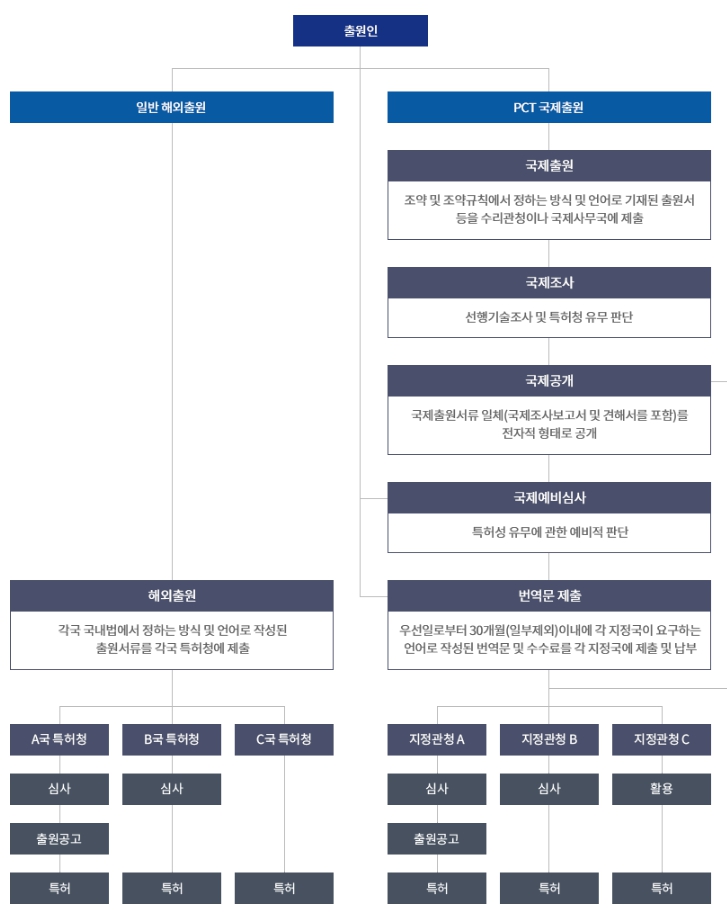 |
|
PCT 국제출원절차와 일반해외 출원절차 비교도 |
| 출처: 특허청 |
증권신고서 제출일 현재 국내외 총 10건의 지적재산권을 보유하고 있으며, 당사가 보유한 특허의 세부 내역은 아래와 같습니다
| [당사의 지적재산권 현황] |
| No. |
명칭 |
출원국 |
특허권자 |
등록번호 |
등록일 |
|---|---|---|---|---|---|
| 1 |
암-고환 항원을 포함하는 한국 난치성 다발골수종 예방 또는 치료용 세포 면역치료제 조성물 및 그 제조방법 |
대한민국 |
전남대학교 산학협력단/ (주)박셀바이오 |
10-1756073 PCT/KR2016/011178 |
2017.07.04 |
| 2 |
개 인터루킨-15 체외 증폭용 프라미어 세트, 이의 용도 및 이를 이용한 재조합 개 인터루킨-15 제조방법 |
대한민국 |
(주)박셀바이오 |
10-1440915 |
2014.09.05 |
| 3 |
수지상세포의 이동성 증진 및 수지상세포에 의해 제조된 세포독성 T세포의 세포살상능 증진방법 |
대한민국 |
전남대학교 산학협력단 |
10-1117186 |
2012.02.09 |
| 4 |
수지상세포의 이동성 증진 및 수지상세포에 의해 제조된 세포독성 T세포의 세포살상능 증진방법 |
대한민국 |
전남대학교 산학협력단 |
10-1083404 |
2011.11.08 |
| 5 |
수지상세포의 성숙화 유도용 조성물 |
대한민국 |
전남대학교 산학협력단 |
10-0997753 |
2010.11.25 |
| 6 |
OX40L을 발현하는 배양보조세포 및 이를 이용한 자연살해세포 배양 방법 |
대한민국 |
(주)박셀바이오 |
10-2227155 PCT/KR2019/006463 |
2021.03.08 |
| 7 |
인간 피브로넥틴 도메인 III 기본 골격의 신규 인간 EphA2 특이적 결합 단백질 및 그의 용도 |
대한민국 |
전남대학교 산학협력단 |
10-1636882 |
2016.06.30 |
| 8 |
모노바디 기반 키메라 항원 수용체 및 이를 포함하는 면역 세포 |
대한민국 |
㈜박셀바이오 |
10-2021-0067276 PCT/KR2022/007379 |
2021.05.25. PCT 출원2022.05.24. |
| 9 |
배양보조세포를 포함하는 자연살해세포 증식용 조성물 |
대한민국 |
㈜박셀바이오/ |
10-2021-0070778 PCT/KR2022/007782 |
2021.06.01. PCT 출원 2022.05.31 |
| 10 |
PD-L1 특이적 키메라 항원 수용체 및 이를 포함하는 면역세포 |
대한민국 |
㈜박셀바이오/ |
10-2022-0029633 |
2022.03.08 |
| 출처: 당사 정기보고서 |
현재 당사가 보유한 특허들은 설립 초기 공동설립자 등이 개발하여 전남대학교 산학협력단이 보유하던 특허를 전용실시권 형태로 기술이전 받은 특허들과 전남대학교 산학협력단과의 공동출원/등록 특허, 그리고 정부출연연구소, 대학교 등 외부 연구자들과의 협력 연구를 통한 공동출원 및 기술양수 특허 등으로 구성되어 있습니다. 전남대학교 산학협력단과 삼성서울병원 및 서울대학교 산학협력단에서 전용실시를 부여 받은 특허들의 전용실시 기한은 해당 특허가 만료되는 시기와 같습니다.
당사는 특허법, 약사법 등에서 인정되는 제도를 기반으로 당사의 독점적인 판매기간 확보를 통한 당사 경쟁력 확보할 수 있을 뿐만 아니라, 경쟁제품 시장 진입 지연을 위하여 특허권 존속기간 연장제도, 희귀의약품 지정제도 등의 전략을 적극적으로 활용할 예정입니다. 또한, 당사는 보유하고 있는 기술에 대하여 향후 공동연구개발 추진, 라이선스 아웃, 경쟁회사의 유사 기술개발 방어 및 진입장벽 구축 등을 위해 지적재산권 확보 및 보호 전략을 수립하고 있습니다.
당사는 당사의 지적재산권 보호를 위해 종합법률사무소에서 비정기적으로 종합적인 자문을 받고 있으며 그 외에 국제특허법률사무소를 통해 특허현황조사 및 특허작성 전략에 대한 논의를 진행하고 있습니다.
그럼에도 불구하고, 향후 제3자에 의하여 당사가 보유하고 있는 특허권에 대한 소송 또는 기타 분쟁이 발생할 가능성을 배제할 수 없으며, 임상시험 또는 제품 상용화에 실패하여 특허 연장을 하지 못할 경우, 특허가 만료되어 동일 기반 기술의 경쟁 제품이 개발될 수 있음에 따라 당사의 손익에 부정적인 영향을 미칠 수 있습니다.
|
아. 기술이전 지연 및 실패 위험 당사의 항암 면역플랫폼 파이프라인에 따라 자사제품별 타겟하고 있는 질환의 발병률, 유병률을 고려 후 시장성 분석을 통해 지역을 구분하여 다른 나라에 L/O를 진행 예정입니다. 하지만 당사의 이러한 노력에도 불구하고 글로벌 기술이전 거래 건수 및 규모의 감소, 제약/바이오 시장의 수요 감소, 글로벌 제약사들의 사업전략 변동 등의 이유로 인해 기술이전이 예상보다 지연되거나 실패하는 경우 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
당사와 같은 바이오벤처는 신약 개발사업이 태생적으로 부담하고 있는 낮은 임상성공률, 대규모 개발비용, 오랜 개발기간에 따른 리스크를 국내외 대형 제약사와 분산하기 위하여 자체제조 및 판매와 더불어 글로벌 바이오제약회사 혹은 해외 파트너 회사로의 기술이전(L/O)함으로써 조기에 수익을 시현하는 것을 기본적 수익모델로 삼고 있습니다. 국내외 대형 제약사 또한 대규모 개발비용을 감수하고 성공확률이 높은 약제로의 선택과 집중을 통해 최상의 결과를 얻고자 사내 연구개발에만 의존하지 않고 외부에서 신약 개발의 기회를 찾는 오픈 이노베이션(open innovation) 전략을 적극적으로 추진하는 추세에 있습니다.
하기 내용은 당사에서 진행 중인 오픈 이노베이션 전략 현황입니다.
| [오픈 이노베이션 전략 현황] |
| 와이바이오로직스 | 디알큐어 | Sanlang Bio (중국) |
|---|---|---|
| PD-L1 CAR scFV 도입으로 난치성 고형암 타겟으로 비임상 시험 진행 |
효능은 오래 지속되며 부작용은 적은 차세대 박스루킨 서방형 제제 개발 중 |
BCMA-CAR-T 공정개발 중이며 2024년 임상시험 진입을 목표로 진행/ BCMA-CAR-MIL 비임상 진행 중 |
| 출처 : 당사 제공 |
글로벌 신약 개발 시 평균 1조~2조 원 상당의 개발 비용과 평균 10~15년 정도의 장기간의 개발기간 소요됩니다. 신약개발은 크게 후보물질 탐색, 前임상, 임상시험 단계로 구분되는데, 임상 단계는 6~7년이 걸리고, 전문역량과 고비용이 요구되는 단계로 전체 신약개발 비용의 약 70% 소요됩니다.
의약품 산업은 연구개발에서부터 신약개발 성공과 제품 상용화 생산에 이르기까지 높은 R&D 비용과 10년 이상의 기간이 소요되는 기술, 자본집약적 산업입니다.
딜로이트가 발간한 Measuring the return from pharmaceutical innovation 2022 보고서에 따르면 글로벌 제약기업들은 2013년부터 2022년까지 R&D 생산성이 감소세를 보이고 있습니다. 자료에 따르면 2013년 글로벌 제약기업들의 IRR은 6.5% 수준이었으나 2022년 IRR은 1.2%에 불과하고, 이 중 증가하고 있는 R&D 비용은 IRR 4.4%p의 감소 효과를 발생시켰다고 합니다. 실제로 2010년에 평균 850억달러를 R&D비용으로 지출한 기업군들은 2022년 평균 1,390억달러를 지출한 것으로 나타났습니다.
| [글로벌 제약기업 IRR추이] |
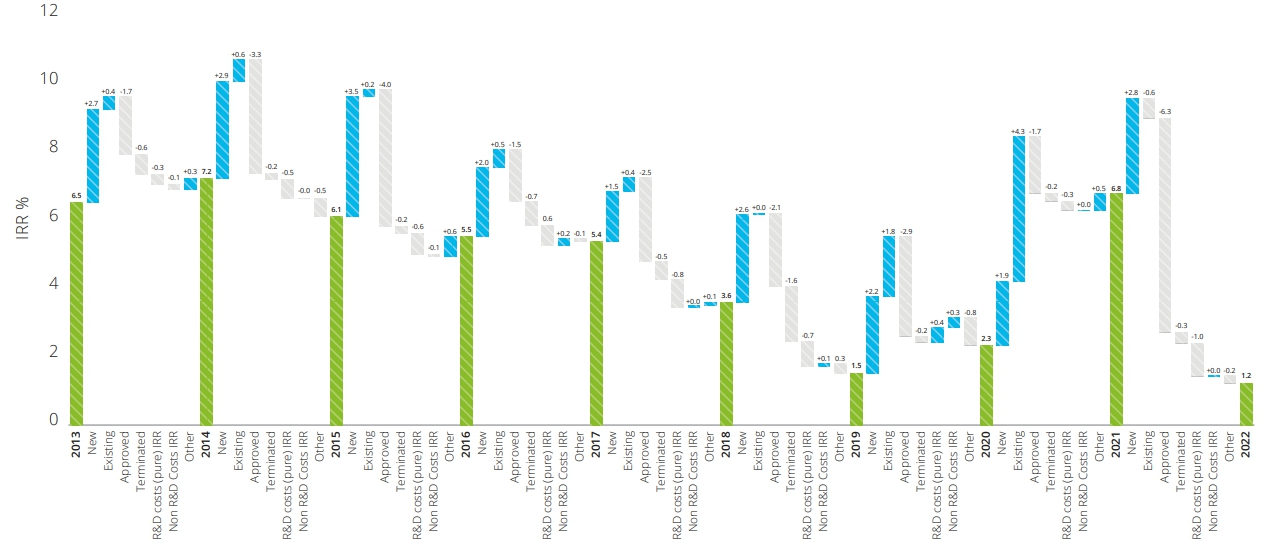 |
|
글로벌 제약기업 irr추이 |
| (출처 : 딜로이트, Measuring the return from pharmaceutical innovation 2022) |
같은 기간동안 글로벌 제약 기업들의 평균 R&D비용(물질 발견에서 출시까지)은 2013년 약 13억달러에서 2022년 약 23억달러로 증가하였습니다. 또한 파이프라인 별 예상 피크 판매액은 2013년 약 5.2억달러에서 2023년 약 3.9억달러로 감소하는 추세를 보이고 있습니다. 이와 같은 트렌드에 따라 최근 R&D 투자 효율성 하락으로 글로벌 제약기업들의 R&D 지출액 증가율 둔화되고 있습니다.
| [글로벌 제약 기업들의 평균 R&D비용(물질 발견에서 출시까지)] |
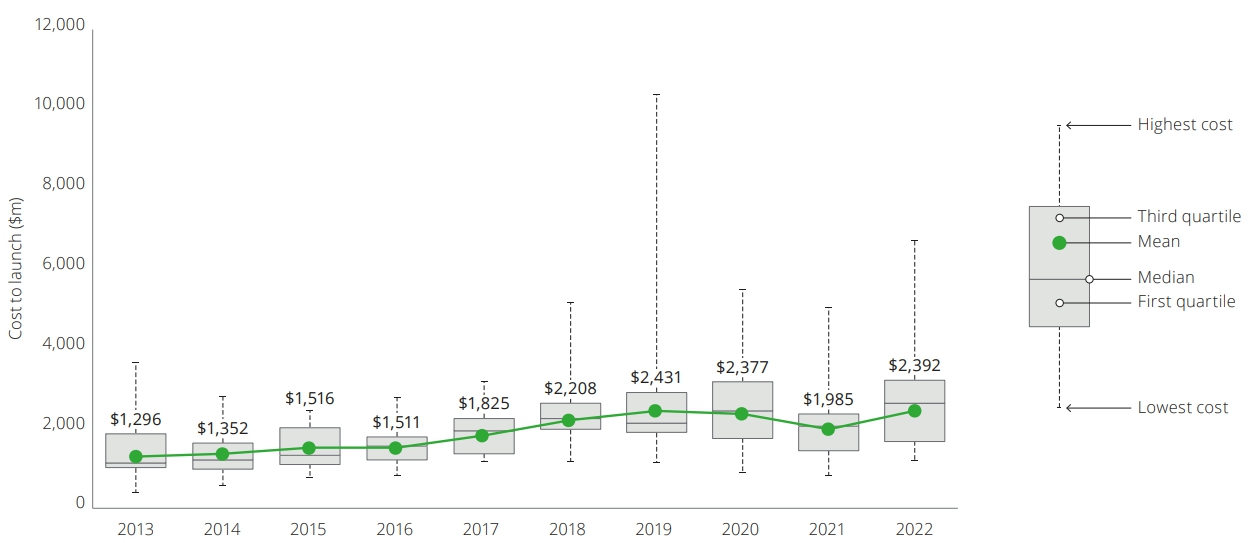 |
|
글로벌 제약 기업들의 평균 r&d비용(물질 발견에서 출시까지) |
| (출처 : 딜로이트, Measuring the return from pharmaceutical innovation 2022) |
| [글로벌 제약 기업 R&D 지출 총액] |
 |
|
r&d 지출 총액 |
| (출처 : 딜로이트, Measuring the return from pharmaceutical innovation 2022) |
한편, 2022년 2월 Biotechnology Innovation Organization(BIO) 발간 'The State of Innovation in Antibacterial Therapeutics'에 따르면 2011년부터 2021년 3분기까지 10년 동안 전세계 제약ㆍ바이오 벤처회사의 라이선스 아웃 딜(계약금 규모 1천만 달러 이상)을 분석한 결과 거래건수는 2011년 109건에서 2020년 238건, 2021년 3분기 195건으로 증가하였고, 계약금(upfront) 규모는 2011년 34억달러에서 2020년 162억달러, 2021년 3분기 73억달러로 증가하였습니다.
해당 기간 라이선스 아웃 딜 중 매년 발생하는 건수 중 평균 55.3%가 전임상 단계에서 체결되었습니다. 전임상 단계에서 발생하는 라이선스 아웃 계약금(upfront) 총 규모는 평균 23억달러이며 이는 매해 발생하는 계약금의 평균 37.7% 비중입니다. 이에 더해 라이선스 아웃 딜 총 규모(계약금, 임상/허가/세일즈 마일스톤 등 모든 금전적 보상의 합산금액) 기준 전임상 단계에서 발생하는 금액은 평균 422억달러이며, 매해 발생하는 금액 대비 평균 58.5%입니다. 상기 사실로 미루어 볼 때 신약 후보물질의 안전성과 효능이 임상 단계에서 입증되기 전이라고 하더라도 그 잠재력만으로도 높은 가치를 인정받을 수 있음을 알 수 있습니다.
| [제약ㆍ바이오 벤처회사의 라이선스 아웃 딜 현황 (임상단계별)] |
| (단위 : 건, 십억달러) |
|
구분 |
2011년 |
2012년 |
2013년 |
2014년 |
2015년 |
||||||||||
| 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | |
|
전임상 |
65 |
1.6 |
13.1 | 50 |
0.6 |
13.6 | 63 |
1.3 |
15.1 | 69 |
1.6 |
16.8 | 79 |
2.4 |
29.7 |
|
임상1상 |
10 |
0.2 |
4.1 | 13 |
0.2 |
2.7 | 14 |
0.5 |
8 | 16 |
0.5 |
3.3 | 16 |
1.8 |
8.6 |
|
임상2상 |
21 |
0.6 |
6.3 | 22 |
0.9 |
5.4 | 21 |
0.5 |
4.2 | 26 |
1.3 |
10 | 31 |
1.8 |
13 |
|
임상3상 |
13 |
1 |
5.2 | 13 |
0.5 |
3.4 | 10 |
0.2 |
1.7 | 18 |
2.2 |
9.6 | 19 |
1 |
4.9 |
|
합계 |
109 | 3.4 | 28.7 | 98 | 2.2 | 25.1 | 108 | 2.5 | 29 | 129 | 5.6 | 39.7 | 145 | 7 | 56.2 |
|
구분 |
2016년 |
2017년 |
2018년 |
2019년 | 2020년 | 2021년 3분기 | ||||||||||||
| 건수 | 계약금 | 총규모 | 건수 | 계약금 | 총규모 | 건수 | 계약금 | 총규모 | 건수 | 계약금 | 총규모 | 건수 | 계약금 | 총규모 | 건수 | 계약금 | 총규모 | |
|
전임상 |
78 |
2.6 |
47 | 78 |
1.9 |
38 | 111 |
3.7 |
62.4 | 107 | 2.9 | 64.1 | 134 | 4.7 | 105.3 | 95 | 1.8 | 59 |
|
임상1상 |
9 |
0 |
1.5 | 22 |
0.7 |
10.9 | 18 |
0.4 |
6 | 14 | 0.5 | 7.7 | 24 | 2.3 | 12.4 | 18 | 0.4 | 5.1 |
|
임상2상 |
22 |
0.6 |
6.8 | 24 |
1.2 |
5.8 | 33 |
1.8 |
18.6 | 32 | 3.7 | 15.7 | 38 | 4.3 | 18 | 41 | 2.8 | 18.1 |
|
임상3상 |
20 |
0.6 |
3.7 | 33 |
0.7 |
5.6 | 29 |
3.5 |
11.7 | 33 | 6 | 18.4 | 42 | 4.9 | 18.3 | 41 | 2.3 | 13.5 |
|
합계 |
129 | 3.8 | 59 | 157 | 4.5 | 60.3 | 191 | 9.4 | 98.7 | 186 | 13.1 | 105.9 | 238 | 16.2 | 154 | 195 | 7.3 | 95.7 |
| 출처) Emerging Therapeutic Company Investment and Deal Trends(BIO, 2022) |
| 주) 라이선스 아웃 딜 계약금 규모 1천만 달러 이상 |
또한, 한국제약바이오협회가 Evaluate Pharma DB를 이용해 면역항암제로만 한정지어 2018년 1월 1일부터 2021년 8월 20일까지 면역항암제 개발단계별 거래 비중을 분석한 결과, 비임상 단계의 파이프라인 거래 횟수가 40%를 차지하며 가장 높은 비중을 보이며, 임상1상(22%), 임상2상(20%) 순으로 거래 비중이 높은 바, 면역항암제 시장에서도 임상 초기 단계의 파이프라인의 잠재력이 높게 평가받음을 알 수 있습니다.
| [면역항암제 시장 개발단계별 거래 비중] |
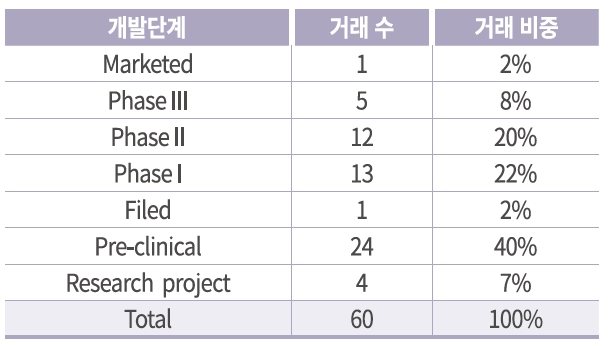 |
|
면역항암제 시장 개발단계별 거래 비중 |
| 출처: KPBMA 한국제약바이오협회 |
한편, 2022년 국내 제약바이오기업의 기술수출 현황은 다음과 같습니다.
| [2022 국내 제약바이오기업 기술수출 현황] |
| 순번 | 개발사 | 계약상대(국가) | 제품/적응증/기술 | 계약규모(억원) |
|---|---|---|---|---|
| 1 | 지씨셀 | 리바라(인도) | 이문셀엘씨(면역항암제) | 비공개 |
| 2 | 에이비엘바이오 | 사노피(프랑스) | ABL301(퇴행성뇌질환) | 12,720 |
| 3 | 종근당바이오 | 큐티아테라퓨틱스(중국) | Tyemvers(보툴리눔 톡신) | 83 |
| 4 | 이수앱지스 | NPO페트로박스팜(러시아) | 파바갈(파브리병) | 비공개 |
| 5 | 노벨티노빌리티 | 발렌자바이오(미국) | NN2802(자가면역질환) | 8,778 |
| 6 | 제넥신 | KGBIO(인도네시아) | GX-E4(지속성 빈혈) | 159 |
| 7 | 코오롱생명과항 | 주니퍼바이로로직스(싱가포르) | TG-C(골관절염) | 7,234 |
| 8 | SK바이오팜 | 유로파마(브라질) | 세노바메이트(뇌전증) | 810 |
| 9 | 티움바이오 | 한소제약(중국) | TU2670(자궁내막증) | 2,208 |
| 10 | 보로노이 | 메티스 테라퓨틱스(미국) | 고형암치료신약 후보물질 | 6,680 |
| 11 | 동아에스티 | 뉴로보 파마슈티컬(미국) | 당뇨 및 NASH(DA-1241) 비만 및 NASH(DA-1726) |
4,715 |
| 12 | 올리패스 | 반다제약(미국) | Olipass PNA플랫폼 (희귀질환/면역항암제) |
43 |
| 13 | 동아에스티 | 폴리파마(튀르키예) | DA-3880(다베포이틴 알파) (빈혈치료제) |
비공개 |
| 출처: KPBMA 한국제약바이오협회, 언론보도 종합 |
2022년에는 13건의 기술수출이 이루어졌으며, 계약금 규모는 전체 4조 3,430억원(비공개 제외)을 기록했습니다. 다양한 적응증에 대한 치료제들이 수출이 되었으며, 이중 지씨셀, 보로노이는 당사가 연구하고 있는 항암제 기술수출에 성공하였습니다.
앞서 기재한 바와 같이 당사가 주력하고 있는 항암면역치료제 시장은 새로운 치료제에 대한 의약적 요구가 높고, 시장의 관심이 주목되어 있는 분야로, 일반적인 경우와 비교하여 신약개발의 초기단계라고 할 수 있는 후보물질 도출 혹은 전임상 단계에서도 활발한 기술이전 및 기업합병이 일어나고 있습니다. 따라서 기술의 주요 수요자인 글로벌제약사들의 기술도입(in-licensing) 건수나 계약규모가 빠른 성장을 하고 있고 이러한 추세는 향후 더욱 가속화될 것으로 판단됩니다.
당사의 항암 면역플랫폼 파이프라인에 따라 자사제품별 타겟하고 있는 질환의 발병률, 유병률을 고려 후 시장성 분석을 통해 지역을 구분하여 다른 나라에 L/O를 진행 예정입니다.
예를 들어, 당사의 간세포암종 적응증을 타겟으로 하는 Vax-NK/HCC의 경우 통계적으로 아시아에서 전세계의 간세포암종 중, 75% 차지하므로 L/O시 아시아 시장을 우선대상으로 진행할 계획이며, 다발골수종을 타겟으로 하는 당사의 Vax-CAR-MILs은 유럽 및 미국지역에서 세번째로 흔한 혈액암으로 높은 수요가 확인되어 L/O 계획시 우선 고려하고 있는 시장입니다.
또한, 당사는 신약 L/O은 제약바이오, 의료계 전문가 네트워크를 통하여 선별적으로 추진중에 있으며 Vax-NK 플랫폼, Vax-CAR 플랫폼 연구개발/임상시험 결과를 바탕으로 국내 외 학회 및 유관 제약바이오 파트너사와 미팅을 통하여 각 적합한 회사와의 협상을 진행할 예정입니다.
박스루킨-15는 해외 L/O는 동물의약품 전문 글로벌제약사와 및 국내 외전문 파트너와 접촉 중에 있으며 박스루킨-15는 '세계 최초의 반려견 항암면역치료제'이기에 많은 회사에서 관심을 가지고 있으며 이외 반려동물 전용 기능성 액상사료에 대한 개발 진행 중이며 향후 회사의 이윤 창출에 시너지가 있을 것이라 사료됩니다.
하지만 당사의 이러한 노력에도 불구하고 글로벌 기술이전 거래 건수 및 규모의 감소, 제약/바이오 시장의 수요 감소, 글로벌 제약사들의 사업전략 변동 등의 이유로 인해 기술이전이 예상보다 지연되거나 실패하는 경우 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| 자. 정부 정책 및 규제 변화에 따른 위험 제약산업은 인간의 생명 및 건강과 직결되는 의약품을 개발ㆍ제조ㆍ판매하는 산업으로, 제품의 개발ㆍ제조, 임상시험, 인ㆍ허가, 유통ㆍ판매에 이르기까지 전 과정에 걸쳐 각 국가의 규제 당국이 제시하는 엄격한 규정과 절차를 따라야 합니다. 특히, '약사법' 하위 시행령/시행규칙 중 의약품 등의 안전에 관한 규칙, 의약품 등의 제조업 및 수입자의 시설기준령 시행규칙, 생물학적 제제 등의 제조ㆍ판매관리 규칙, 동물용 의약품등 취급규칙 등과 이의 하위 규정을 준수해야 합니다. 또한, 국내의 약가 사후관리제도는 대내외 보건의료 환경변화에 의하여 수 차례 변화되어, 현재는 실거래가 조사에 의한 약가 인하, 사용량-약가 연동 협상, 급여범위 확대 시 약가인하, 제네릭의약품 등재 시 오리지널의약품의 약가인하 등의 제도가 운영되고 있습니다. 이러한 약가 인하 정책은 제약산업에서 간과할 수 없는 중요 요인이며, 당사의 사업에도 부정적인 영향을 미칠 수 있습니다. 당사는 내부에 의학 전문가(혈액종양내과 교수 2인), 수의학 전문가 (수의사 4인) 및 과학자(다수의 박사연구원)를 보유하고 있으며, 외부 전문가인 대학병원 암전공 임상교수, 대학병원 수의대교수, 국내외에서 기초연구를 수행하고 있는 유망한 교수들과 자문 계약을 통하여 기초 연구개발(차세대 박스루킨의 개발, CAR-T세포/-NK세포/-MIL의 개발, ADC-NK의 개발 등) 및 임상연구(임상연구의 대상 질환의 설정, 프로토콜의 개발, 임상연구의 수행 등)의 준비 및 진행을 수행하고 있습니다. 또한 국내 및 해외 제약 산업 정책 및 규제 환경을 지속적으로 모니터링하고 있으며, 각국의 규제 당국과의 소통을 통해 정책 및 규제 환경의 변화에 효과적으로 대비하기 위해 최선의 노력을 다하고 있습니다. 그럼에도 불구하고 국내를 포함한 주요 국가에서의 제약 산업 관련 정책이 비우호적 분위기로 전환되거나 규제가 강화되는 경우, 당사의 사업에 부정적인 영향을 미칠 수 있습니다. 한편, 국내를 비롯한 미국, 유럽 등 글로벌 선진국에서는 제약ㆍ바이오 산업을 국민의 건강을 증진하고 일자리와 고부가가치를 창출하는 핵심 기간산업이자 미래 신성장 동력 산업으로 인지하고, 제약·바이오 산업에 대한 우호적 정책을 펼치고 있는 상황입니다. 국내 정부의 경우, 2013년부터 '제약산업육성ㆍ지원 시행계획'을 수립하여 세부 과제를 추진해오고 있으며, 2019년에는 '바이오헬스 산업 혁신전략'을 발표하였습니다. 이러한 정부 방침에 지방자치단체들도 바이오 산업을 지역 역점산업으로 육성하기 위해 노력하고 있습니다. 이에 더불어, 신약 R&D 및 인허가에 소요되는 막대한 비용 부담을 줄일 수 있도록 다양한 규제장벽을 완화하는 정책을 적극적으로 펼치고 있습니다. 국내 식품의약품안전처는 희귀의약품이나 항암제, 세포치료제에 대해 신속한 출시를 허용하는 목적으로 조건부허가제도를 운영하고 있으며, 2020년 8월부터 시행되고 있는 '첨단재생의료법'을 통해 품목허가 검증 체계를 첨단바이오의약품 특성에 맞게 재편하여 맞춤형 심사, 우선 심사, 조건부 허가 등의 혜택이 가능할 것으로 기대됩니다. 그러나 상기 언급된 제약 및 신약개발 산업에 대한 우호적인 정책 기조 및 지원 계획, 규제 완화 노력에도 불구하고, 실제 효율적인 정책 지원이 이루어지지 않거나, 세부과제 추진에 어려움이 생길 수 있으며, 관련 법규의 제정 및 개정 단계, 예산 확보 등에 난항이 발생할 수 있습니다. 또한 해당 정책의 기대효과가 감소되는 경우 정책 기조의 변화로 정부 지원이 축소될 수 있으며, 조건부 허가와 같은 규제 완화에 대한 실효성이 크지 않을 경우, 규제 완화의 범위가 축소될 수 있습니다. 이러한 정부의 우호적인 정책 및 규제 완화의 변동 가능성은 당사의 사업에 부정적인 영향을 끼칠 수 있습니다. |
제약산업은 인간의 생명 및 건강과 직결되는 의약품을 개발ㆍ제조ㆍ판매하는 산업으로, 제품의 개발 및 제조, 임상시험, 인허가, 유통 및 판매에 이르기까지 전 과정에 걸쳐 각 국가의 규제 당국이 제시하는 엄격한 규정과 절차를 따라야 합니다. 제약 및 신약개발 사업과 관련된 국내 법률 중 당사의 사업과 밀접하게 연관된 법률로는 식품의약품안전처 및 보건복지부 소관의 '약사법'이 대표적이며, 그 외 보건복지부 소관의 '국민건강보험법', '생명윤리 및 안전에 관한 법률', '제약산업 육성 및 지원에 관한 특별법', '희귀질환관리법', '첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률'과 식품의약품안전처 소관의 '실험동물에 관한 법률' 등이 있습니다.
특히, '약사법' 하위 시행령/시행규칙 중 의약품 등의 안전에 관한 규칙, 의약품 등의 제조업 및 수입자의 시설기준령 시행규칙, 생물학적 제제 등의 제조ㆍ판매관리 규칙, 동물용 의약품등 취급규칙 등과 이의 하위 규정을 준수해야 합니다. 이에 따라, 신약 후보물질의 발굴에서부터 동물을 대상으로 하는 비임상시험, 인체를 대상으로 하는 임상시험, 품목허가에 이르기 까지 임상 승인에 관한 규정, 의약품의 약리 및 독성, 안정성 시험 기준, 임상시험 실시기관 지정에 관한 규정, 품목허가ㆍ심사 등의 규정 등을 반드시 준수하여 진행해야 합니다. 또한 제조 및 판매 단계에서도 제조소 시설 기준, 제조 및 품질관리 규정, 포장 및 공급에 관한 규정, 표시 등에 관한 규정을 준수해야 하며, 사후에도 정기적으로 규제기관으로부터 제품 생산 공정 및 품질관리 전반에 대한 실사 및 관리, 감독을 받게 됩니다. 이러한 규제 및 검증을 통해 제약산업의 선진화 정책을 시현할 수 있지만, 각종 규제 및 절차, 검증 강화로 인한 부담이 높아지는 경우, 당사의 사업에 부정적인 영향을 미칠 수 있습니다.
| [의약품 등의 안전에 관한 규칙] |
|---|
|
제2조(의약품등의 제조업 허가ㆍ신고 등) 제9조(안전성ㆍ유효성에 관한 자료) 1. 기원 또는 발견 및 개발 경위에 관한 자료 2. 구조결정, 물리화학적 성질에 관한 자료 3. 안정성에 관한 자료 4. 독성에 관한 자료 5. 약리작용에 관한 자료 6. 임상시험성적에 관한 자료 7. 외국의 사용현황 등에 관한 자료 8. 국내 유사제품과의 비교검토 및 해당 의약품등의 특성에 관한 자료 제10조(기준 및 시험방법에 관한 자료) ② 제1항에 따라 기준 및 시험방법에 관한 자료를 제출하려는 자는 심사대상물품(식품의약품안전처장이 품질검사를 위하여 특별히 필요하다고 인정하는 경우에만 해당한다)을 식품의약품안전처장에게 제출하여야 한다. |
| 출처: 국가법령정보센터 |
또한, 국내는 단일보험자(국민건강보험공단)에 의한 전국민 건강보험제도를 운영하고 있는 상황으로, 건강보험의 지속가능성 제고와 적정수준의 국민의료비 유지, 불법 리베이트 차단 등의 목표 하에 약가에 대해 정책적 개입이 이루어지고 있습니다. 국내의 약가 사후관리제도는 대내외 보건의료 환경변화에 의하여 수 차례 변화되어, 현재는 실거래가 조사에 의한 약가 인하, 사용량-약가 연동 협상, 급여범위 확대 시 약가인하, 제네릭의약품 등재 시 오리지널의약품의 약가인하 등의 제도가 운영되고 있습니다. 약가는 산업 정책과 보건의료 정책이 상충하여 변동성이 상존해 있는 상황으로, 현재 제네릭 약가 차등제가 시행 예정되어 있는 상황입니다. 이러한 점진적인 약가 인하 정책은 제약산업에서 간과할 수 없는 중요 요인이며, 당사의 사업에도 부정적인 영향을 미칠 수 있습니다.
| [약가 인하 정책 추이] |
|
시기 |
인하제도 |
내용 |
|
2000년 ~ 2009년 |
실거래가약가인하 (표본조사) |
표본조사(전국 80개 요양기관)를 통해 의약품 청구 실태 조사 후 약가인하 |
| 2002년 ~ 2012년 |
약가 재평가 |
최초 상한금액 산정이후 3년마다 7개국 조정 평균가를 |
| 2007년 ~ 2014년 |
기등재 목록정비 |
2007년 선별등재제도로 전환하면서 기존약재의 경우 20% |
| 2012년 |
일괄 약가인하 |
상한금액대비 53.55%수준까지 일괄 약가인하 |
| 2016년 ~ |
실거래가약가인하 (전수조사) |
유통정보센터 유통정보를 근거로 가중평가가격 까지 약가 인하 |
|
현행 |
특허만료 약가인하 |
개별약제 특허만료시 1년간 70%, 1년 후 53.55%로 약가인하 |
|
현행 |
사전 약가인하 |
개별약제 급여기준 확대 이전에 협의를 통하여 약가인하 |
|
현행 |
사용량 약가연동 |
개별약제 약가와 사용량을 연계하여 등재 후 사용량이 일정 % 증가할 때 약가 인하 |
| 출처: 언론보도 종합 |
당사는 내부에 의학 전문가(혈액종양내과 교수 2인), 수의학 전문가 (수의사 4인) 및 과학자(다수의 박사연구원)를 보유하고 있으며, 외부 전문가인 대학병원 암전공 임상교수, 대학병원 수의대교수, 국내외에서 기초연구를 수행하고 있는 유망한 교수들과 자문 계약을 통하여 기초 연구개발(차세대 박스루킨의 개발, CAR-T세포/-NK세포/-MIL의 개발, ADC-NK의 개발 등) 및 임상연구(임상연구의 대상 질환의 설정, 프로토콜의 개발, 임상연구의 수행 등)의 준비 및 진행을 수행하고 있습니다. 또한 국내 및 해외 제약 산업 정책 및 규제 환경을 지속적으로 모니터링하고 있으며, 각국의 규제 당국과의 소통을 통해 정책 및 규제 환경의 변화에 효과적으로 대비하기 위해 최선의 노력을 다하고 있습니다. 그럼에도 불구하고 국내를 포함한 주요 국가에서의 제약 산업 관련 정책이 비우호적 분위기로 전환되거나 규제가 강화되는 경우, 당사의 사업에 부정적인 영향을 미칠 수 있습니다.
한편, 국내를 비롯한 미국, 유럽 등 글로벌 선진국에서는 제약·바이오 산업을 국민의 건강을 증진하고 일자리와 고부가가치를 창출하는 핵심 기간산업이자 미래 신성장 동력 산업으로 인지하고, 제약ㆍ바이오 산업에 대한 우호적 정책을 펼치고 있는 상황입니다.
미국정부의 경우 국가 생명공학 및 바이오제조 이니셔티브(NBBI), 미국의 국가안보각서 및 바이오방어 전략 등을 통해서 생명 공학 및 제조를 위한 연방 투자확대, 기술혁신을 위한 안정적인 데이터 환경 조성 및 미국 바이오 제조 역량 강화를 위한 규제 간소화와 인재 육성 투자 등을 과제로 삼고 제약·바이오 산업을 체계적인 국가 전략을 바탕으로 육성시키고 있습니다.
| [국가 바이오기술 및 바이오제조 행정명령 주요 내용] |
 |
|
국가 바이오기술 및 바이오제조 행정명령 주요 내용 |
| 출처: 코트라, '미국의 바이오제약 산업 육성 정책과 시사점' |
국내 정부의 경우, 한-미 FTA 발효, 약가제도 개편 등 제약산업의 환경 악화로 2012년 제약산업 육성대책 마련 필요성이 제기되었으며, 제약산업 발전기반 조성 및 국제 경쟁력 강화를 촉진하기 위하여, 2012년 '제약산업 육성 및 지원에 관한 특별법'을 시행하였습니다. 이에 따라 2013년부터 5년 단위의 제약산업육성ㆍ지원 종합계획과 1년 단위의 제약산업육성ㆍ지원 시행계획을 수립ㆍ시행하여 세부 과제를 추진하고 있습니다.
| [제3차 제약바이오산업 육성·지원 5개년 종합계획] |
 |
|
제3차 제약바이오산업 육성지원 5개년 종합계획 발표 |
| 출처: 보건복지부 |
또한 국내 정부는 2019년 5월, 바이오헬스 분야 기술개발, 인허가, 생산, 시장출시 등 전주기에 걸쳐 단계별 지원내용을 담고 있는 '바이오헬스 산업 혁신전략'을 발표하였습니다. 이러한 정부 방침에 지방자치단체들도 바이오 산업을 지역 역점산업으로 육성하기 위해 노력하고 있습니다.
국내 및 미국, 유럽 등 글로벌 선진국은 제약사들의 신약 R&D 및 인허가에 소요되는 막대한 비용 부담을 줄일 수 있도록 다양한 규제장벽을 완화하는 정책을 적극적으로 펼치고 있습니다. 대표적으로, 의학적 미충족 수요에 부응할 가능성이 있는 제약/바이오 기술들을 위중한 상태에 있는 환자들에게 신속하게 전달할 기회를 제공하기 위해 조건부 신속허가를 제도적으로 정착하려는 노력이 진행되고 있습니다. 미국은 가속 승인(Accelerated Approval) 제도를 통해 기존의 치료 요법으로는 해결되지 않는 중증질환을 대상으로 하는 치료제의 경우 대리 평가변수(surrogate endpoint)를 이용한 연구결과로 조기에 승인해주는 제도를 운영하고 있으며, 유럽은 미충족 의료수요를 충족하는 일부 의약품에 대해 시판 후 임상적 확증시험 이행을 조건으로 조기 허가하는 조건부허가(Conditional marketing authorization)와 임상적 확증시험이 어려운 희귀 질환을 대상으로 하는 예외적 허가(Marketing authorization under exceptional circumstances) 등의 제도가 시행되고 있습니다. 일본은 생명을 위협하거나 중증의 질환을 대상으로 하는 세포치료제를 포함하는 '재생의료 등 제품'에 대하여 조건 기한부 허가 제도를 운영하고 있습니다.
국내의 식품의약품안전처 역시 희귀의약품이나 항암제, 일부 세포치료제(자가연골세포치료제, 자가피부세포치료제)에 대해 신속한 출시를 허용하는 목적으로 1997년부터 조건부허가제도를 도입하여 식약처 예규로 운영해 왔으며, 2016년부터는 생명을 위협하는 질환 또는 중증의 비가역질환을 대상으로 치료적 탐색(2상) 임상 시험의 허가 요건과 그 결과를 충족하는 세포치료제의 경우에도 조건부 허가를 신청할 수 있도록 세포치료제 조건부 허가 범위를 확대하여 운영하고 있는 상황입니다. 이에 따라 해당 운영 가이드라인 및 요건에 부합하는 세포치료제는 추후 임상 3상(치료적 확증) 시험 자료를 제출하는 조건으로, 임상 2상(치료적 탐색) 시험 자료만으로 우선 허가받아 시판할 수 있게 되었습니다.
이에 더불어, 최근에는 재생의료 임상연구실시 및 첨단바이오의약품 패스트트랙을 골자로 하는 '첨단재생의료법(첨단재생의료 및 첨단바이오의약품의 안전ㆍ지원에 관한 법률)'이 국회 본회의를 통과하여 2020년 8월부터 시행되고 있습니다. 첨단바이오의약품은 세포치료제, 유전자체료제, 조직공학제제 등 살아있는 세포ㆍ조직 또는 유전자를 원료로 제조한 의약품을 의미합니다. 첨단재생의료법은 첨단재생의료의 안전성 확보 체계 및 기술 혁신ㆍ실용화 방안을 마련하고, 약사법, 생명윤리법 등에 산재한 바이오의약품 관련 규제를 일원화하며, 신속허가제도 도입 및 안전관리체계를 구축하는 것이 핵심입니다. 본 법을 통해 재생의료 임상연구가 가능해져 의료기술의 기술경쟁력을 제고하여 희귀ㆍ난치 질환자에게 새로운 치료 기회를 제공할 수 있을 뿐만 아니라, 품목허가 검증 체계를 첨단바이오의약품 특성에 맞게 재편하여 맞춤형 심사, 우선 심사, 조건부 허가 등의 혜택이 가능할 것으로 기대됩니다.
상기 언급된 제약 및 신약개발 산업에 대한 우호적인 정책 기조 및 지원 계획, 규제 완화 노력에도 불구하고, 실제 효율적인 정책 지원이 이루어지지 않거나, 세부과제 추진에 어려움이 생길 수 있으며, 관련 법규의 제정 및 개정 단계, 예산 확보 등에 난항이 발생할 수 있습니다. 또한 해당 정책의 기대효과가 감소되는 경우 정책 기조의 변화로 정부 지원이 축소될 수 있으며, 조건부 허가와 같은 규제 완화에 대한 실효성이 크지 않을 경우, 규제 완화의 범위가 축소될 수 있습니다. 이러한 정부의 우호적인 정책 및 규제 완화의 변동 가능성은 당사의 사업에 부정적인 영향을 끼칠 수 있습니다.
|
차. 기술이전 파트너사 관련 위험 신약 파이프라인의 기술이전이 성공하면, 일반적으로 기술이전의 대가로 초기 계약금을 수령하게 되며, 이 후 임상단계 또는 허가단계 성공시마다의 마일스톤, 신약 발매 후 매출액의 일정 비율에 대한 로열티, 특정 금액 이상의 매출 발생시 판매 마일스톤 등을 수취하게 됩니다. 증권신고서 제출일 현재 당사의 유효한 기술 라이선스 아웃 계약은 없습니다. 그러나 추후 기술 이전에 성공하더라도, 해당 기술이전 계약에서 목표하는 기간 내에 일정 수준의 마일스톤 실적을 충족시키지 못하거나, 해당 계약에서 규정한 계약 해제 및 해지 사유 등의 발생 시, 기 지급받은 초기 계약금의 경우 계약 조건에 따라 일부 또는 전부를 반환해야 하는 의무가 있을 수 있으며, 기 계약금을 제외한 나머지 마일스톤 및 로열티 금액 등을 추가로 수령할 수 없을 가능성이 존재합니다. 또한 기술 도입한 파트너사의 임상 수행 능력 및 파트너사 내부적인 사정 등으로 임상 진행을 연기 또는 중단해야 하는 가능성도 존재하며, 이에 따라 해당 계약이 중도에 해지되거나 계약 금액이 하향 조정될 가능성도 있습니다. 제품 출시 후에도 해당 지역에서 계획한 정도의 수익이 창출되지 않아 로열티 수입이 확보되지 아니하는 경우에는 당사의 기대 수익 또한 감소할 가능성이 있습니다. 이처럼 기술 이전 자체가 가지는 한계로 인하여 당사가 통제할 수 없는 파트너사의 역량에 따라 당사의 재무 성과가 변동될 위험이 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
신약 파이프라인의 기술이전이 성공하면, 일반적으로 기술이전의 대가로 초기 계약금을 수령하게 되며, 이 후 임상단계 또는 허가단계 성공시마다의 마일스톤, 신약 발매 후 매출액의 일정 비율에 대한 로열티, 특정 금액 이상의 매출 발생시 판매 마일스톤 등을 수취하게 됩니다.
| [라이선스 계약 수익구조] |
| 구분 | 내용 | |
|---|---|---|
| 총계약금액 | 계약금 | 계약 체결 직후 또는 일정기간 내에 받게 되는 금액 |
| 마일스톤 | 전임상, 임상, 허가신청, 허가완료 등 개발 단계별로 성공시 받게 되는 금액 | |
| 로열티 | 기술 이전으로 생산된 제품의 매출에 따라 받게 되는 금액 (통상 매출액 대비 비율로 책정) |
|
증권신고서 제출일 현재 당사의 유효한 기술 라이선스 아웃 계약은 없습니다. 그러나 추후 기술 이전에 성공하더라도, 해당 기술이전 계약에서 목표하는 기간 내에 일정 수준의 마일스톤 실적을 충족시키지 못하거나, 해당 계약에서 규정한 계약 해제 및 해지 사유 등의 발생 시, 기 지급받은 초기 계약금의 경우 계약 조건에 따라 일부 또는 전부를 반환해야 하는 의무가 있을 수 있으며, 기 계약금을 제외한 나머지 마일스톤 및 로열티 금액 등을 추가로 수령할 수 없을 가능성이 존재합니다. 또한 기술 도입한 파트너사의 임상 수행 능력 및 파트너사 내부적인 사정 등으로 임상 진행을 연기 또는 중단해야 하는 가능성도 존재하며, 이에 따라 해당 계약이 중도에 해지되거나 계약 금액이 하향 조정될 가능성도 있습니다. 제품 출시 후에도 해당 지역에서 계획한 정도의 수익이 창출되지 않아 로열티 수입이 확보되지 아니하는 경우에는 당사의 기대 수익 또한 감소할 가능성이 있습니다.
이와 같은 위험을 감소시키기 위하여 당사는 소수 제품의 개발에 치중하기 보다는 당사의 면역세포 플랫폼 기술을 활용하여 파이프라인을 확대하는 전략을 취하고 있습니다. 당사는 향후 다수 파이프라인의 기술이전을 통하여 해외 임상 비용에 투입에 대한 위험을 줄이고 파트너사의 성공적인 개발에 따른 로열티 수익을 수취할 계획입니다. 다만 당사의 이러한 노력에도 불구하고, 기술 이전 자체가 가지는 한계로 인하여 당사가 통제할 수 없는 파트너사의 역량에 따라 당사의 재무 성과가 변동될 위험이 있으니 투자자께서는 이 점 유의하시기 바랍니다.
|
카. 업무 위탁기관 관련 위험 당사와 같이 신약 개발사업을 영위하고 있는 다수의 바이오벤처 업체는 신약개발의 효율성을 높이고 리스크를 감소시키기 위한 전략으로, 임상시험 전문수탁기관(Contract Research Organization, CRO)을 대상으로 비임상시험 및 임상시험을 위탁 진행하거나, 의약품 생산 전문대행기관(Contract Manufacturing Organization, CMO)을 대상으로 임상시험에 필요한 원료 및 완제 생산을 위탁 진행하고 있습니다. 당사는 GMP 생산시설을 보유하여 면역세포치료제를 자체 생산하고 있으나, 이에 대한 임상시험은 환자의 안전, 임상시험의 품질보증 및 관리, 규제기관 관점에서의 임상시험 결과물의 타당성, 객관성 확보 등을 위한 목적으로 CRO 업체에 위탁 진행하고 있습니다. 당사는 CRO에 대하여 지속적으로 관리 및 모니터링하고 있으며, 예상치 못한 사고의 발생에 즉각 대처할 수 있도록 만반의 준비를 갖추기 위해 노력하고 있습니다. 한편, 동물용 항암면역치료제인 박스루킨-15의 대량 생산은 동물 의약품 생산이 가능한 업체를 CMO로 선정하여 위탁 생산할 계획이며, 당사는 이와 관련하여 제품의 표준서 및 관련정보를 제공하고, 원부자재를 공급하며, 제품의 최종 출하 판정 및 승인을 담당할 예정입니다. 하지만 당사의 이러한 노력에도 불구하고 CMO 및 CRO 기관 자체의 사정으로 인한 의도하지 않은 결과가 발생할 수 있습니다. 소속 직원 재배치, 수탁업무 수행능력 부족, 계약상 의무 미준수, 관련 규정 및 절차 미준수, 인력의 파업, 재정적 위기로 인한 파산 등의 상황이 발생할 수 있습니다. 특히, CMO의 경우 제조 공장 강제 폐쇄, 자연 재해, 인공 재해, 규정 미준수, 품질 저하 등으로 인한 생산 일정 지연 또는 생산 중단 상황이 발생할 수 있고, CRO의 경우 임상 결과 분석의 오류 및 임상 결과 도출 지연, 임상시험 과정에서 발생한 부작용에 대한 미흡한 대처 등이 발생할 수 있습니다. 이와 같이 업무위탁 기관을 활용할 경우 당사가 통제할 수 없는 위험요소들로 인하여 당사의 신약 개발 일정이 지연되거나 연구 결과에 부정적인 영향을 미칠 수 있으며, 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. |
당사와 같이 신약 개발사업을 영위하고 있는 다수의 바이오벤처 업체는 신약개발의 효율성을 높이고 리스크를 감소시키기 위한 전략으로, GLP(Good Laboratory Practice) 및 GCP(Good Clinical Practice) 허가를 받은 임상시험 전문수탁기관(Contract Research Organization, CRO)을 대상으로 비임상시험 및 임상시험을 위탁 진행하거나, GMP(Good Manufacturing Practice) 허가를 받은 의약품 생산 전문대행기관(Contract Manufacturing Organization, CMO)을 대상으로 임상시험에 필요한 원료 및 완제 생산을 위탁 진행하고 있습니다.
먼저, 면역세포치료제 플랫폼과 관련하여, 당사는 자체 GMP 시설을 보유하여 현재 임상 및 응급임상용 Vax-NK 세포치료제를 표준화된 절차에 따라 생산하고 있습니다.
| [당사 GMP 시설 개요] |
| (단위: batch) |
| 제품 품목명 | 구 분 | 2023년도 상반기 | 2022년도 | 2021년도 | |||
|---|---|---|---|---|---|---|---|
| 수량 | 금액 | 수량 | 금액 | 수량 | 금액 | ||
| Vax-NK (제1제조소) |
생산능력 | 81 | - | 81 | - | - | - |
| 생산실적 | 9 | - | 19 | - | - | - | |
| 가 동 율 | 11.11% | 23.46% | - | ||||
| 기말재고 | - | - | - | - | - | - | |
| Vax-NK (제2제조소) |
생산능력 | 81 | - | 81 | - | 81 | - |
| 생산실적 | 6 | - | 14 | - | 18 | - | |
| 가 동 율 | 7.4% | 17.28% | 22.22% | ||||
| 기말재고 | - | - | - | - | - | - | |
| 주) 당사는 2022년 08월 24일 연구개발의 타당성과 투자대비 사업성에 대한 판단 하에 Vax-DC 플랫폼의 연구개발을 조기 종료하는 것으로 결정하였습니다 출처: 당사 정기보고서 |
그러나, 면역세포치료제의 임상시험은 환자의 안전, 임상시험의 품질보증 및 관리, 규제기관 관점에서의 임상시험 결과물의 타당성, 객관성 확보 등을 위한 목적으로 CRO 업체에 위탁 진행하고 있습니다. 당사는 현재 국내 주요 CRO 업체 중 하나인 ㈜씨엔알리서치와 전략적 업무협약을 맺어 간세포암을 대상으로 하는 Vax-NK의 임상 2a상 시험을 안전하고 효율적이며 공정하게 진행하고 있습니다.
당사는 이제중 대표이사 겸 수석의학자를 중심으로 CRO에 대하여 지속적으로 관리 및 모니터링하고 있으며, 예상치 못한 사고의 발생에 즉각 대처할 수 있도록 만반의 준비를 갖추기 위해 노력하고 있습니다. 한편, 동물용 항암면역치료제인 박스루킨-15의 대량 생산은 동물 의약품 생산이 가능한 업체를 CMO로 선정하여 위탁 생산할 계획이며, 현재 임상시험용 의약품 또는 관련업체에서 제조하고 있습니다. 당사는 이와 관련하여 제품의 표준서 및 관련 정보를 제공하고, 원부자재를 공급하며, 제품의 최종 출하 판정 및 승인을 담당할 예정입니다.
하지만 당사의 이러한 노력에도 불구하고 생산 및 임상시험 업무를 위탁 수행중인 CMO 및 CRO 기관 자체의 사정으로 인한 의도하지 않은 결과가 발생할 수 있습니다. 위탁 수행 업체 공통적으로는 소속 직원 재배치, 수탁업무 수행능력 부족, 계약상 의무 미준수, 관련 규정 및 절차 미준수, 인력의 파업, 재정적 위기로 인한 파산 등의 상황이 발생할 수 있습니다. 또한, CMO의 경우 제조 공장 강제 폐쇄, 자연 재해, 인공 재해, 규정 미준수, 품질 저하 등으로 인한 생산 일정 지연 또는 생산 중단 상황이 발생할 수 있고, CRO의 경우 임상 결과 분석의 오류 및 임상 결과 도출 지연, 임상시험 과정에서 발생한 부작용에 대한 미흡한 대처 등이 발생할 수 있습니다. 이러한 일이 발생하여 또 다른 위탁 수행 업체와 계약하게 되는 경우 임상시험 또는 제조공정의 반복 수행으로 인한 추가적인 비용, 기간 연장이 요구되며, 이에 따른 상용화 시기가 지연될 수 있습니다. 이와 같이 업무위탁 기관을 활용할 경우 당사가 통제할 수 없는 위험요소들로 인하여 당사의 신약 개발 일정이 지연되거나 연구 결과에 부정적인 영향을 미칠 수 있으며, 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다.
|
타. 생산 및 생산관련 투자에 따른 위험 당사는 설립 초기인 2011년도부터 녹십자 EM 및 전남생물의약연구센터 등과 함께 세포치료제 전용의 우수의약품 제조 및 품질관리 기준(GMP, Good Manufacturing Practice) 적합 시설에 관한 설계 작업에 착수하여, 2012년 7월 준공 완료하였습니다. 당사 GMP생산시설의 총 면적은 409 ㎡로, Vax-NK 전용 배양실, 원자재 및 제품보관소, 기계실 등으로 구획되어 있습니다. 2012년 11월 Vax-DC/MM의 시험생산을 시작으로, 현재는 임상연구를 위한 Vax-NK 플랫폼에대해 제1,2 제조소 모두를 가동하고있으며, CAR-T,CAR-NK, CAR-MIL은 비임상단계로 추후 신사옥이 건설되기 전까지 JBRC 내 GMP시설을 임차하여 임상용 치료제를 생산할 계획입니다. 그러나 당사의 제품은 환자의 자가유래 면역세포로서, 대상 암환자의 병기 및 전신상태, 기 적용된 항암약물요법 등에 따라, 백혈구 분반술 시행이 어려운 상황이 발생할 수 있으며, 분리된 말초혈액단핵구 내 면역세포의 수가 유효한 수준 이하일 가능성이 있습니다. 또한 자연재해, 인공재해 등으로 인하여 제조 공장이 멸실되거나, 제조인력이 파업을 하거나, 제조 및 품질관리 기준이 갑작스럽게 대폭 강화되어 제조공정의 개선이 필요하여 생산라인이 마비되는 등 예측하기 어려운 문제들이 발생할 경우, 당사의 제품 상업화 또는 임상개발에 부정적인 영향을 미칠 수 있습니다. 또한 GMP제조 시설의 상각비가 지속적으로 발생함에도 불구하고, 매출 시현이 지연될 경우 당사의 손익이 악화될 가능성이 존재하며 현금 확보가 제한되어 향후 임상 진행 등의 측면에서 제약을 받을 가능성이 존재하오니 투자자께서는 이 점 유의하여 주시기 바랍니다. |
당사는 설립 초기인 2011년도부터 녹십자 EM 및 전남생물의약연구센터 등과 함께 세포치료제 전용의 우수의약품 제조 및 품질관리 기준(GMP, Good Manufacturing Practice) 적합 시설에 관한 설계 작업에 착수하여, 2012년 7월 준공 완료하였습니다. 당사 GMP생산시설의 총 면적은 409 ㎡로, Vax-NK 전용 배양실, 원자재 및 제품보관소, 기계실 등으로 구획되어 있습니다. 2012년 11월 Vax-DC/MM의 시험생산을 시작으로, 현재는 임상연구를 위한 Vax-NK 플랫폼에대해 제1,2 제조소 모두를 가동하고있으며, CAR-T, CAR-NK, CAR-MIL은 비임상단계로 추후 신사옥이 건설되기 전까지 JBRC 내 GMP시설을 임차하여 임상용 치료제를 생산할 계획입니다.
당사의 GMP시설은 생물의약품 중에서도 세포치료제, 그리고 임상시험용 의약품 제조와 관련된 규정인 '의약품 등의 안전에 관한 규칙' (별표1. 의약품 제조 및 품질관리기준, 별표 1의 2. 원료의약품 제조 및 품질관리기준, 별표 4의 2. 임상시험용 의약품 제조 및 품질관리기준 등)을 준수하고 있습니다. 다만, 해당 연구개발 파이프라인이 조건부판매 승인 신청 단계에 접어들기 전에 시판단계와 동일한 GMP규정에 대한 실사를 받아야 하는 상황으로, 이에 대비하기 위하여 당사는 현재 자체적으로 품목허가에 준하는 GMP 규정에 맞게 GMP시설을 운용, 관리하고 있습니다.
특히, 세포치료제는 최종 멸균이 불가능하므로 공정에서의 무균성이 매우 중요하며, 작업자에 의한 수작업이 많이 요구됩니다. 또한 소규모 생산 또는 환자별 맞춤 제조 등 고유의 제품 특성 때문에 타 의약품 대비 안정성 시험 실시, 보관검체의 보관량 및 기간, 최종 품질검사 완료 후 출고 조건 조항 등을 각별히 고려하여야 합니다. 이러한 점에서 당사는 설립 초기부터 항암면역세포치료제의 생산 및 품질관리, GMP 운영에 대한 노하우를 확보하는 등 생산 측면에서의 경쟁력을 보유하고 있습니다.
당사의 제품은 자가유래 면역세포로서, Vax-NK 세포치료제 제조를 위해서는, 병원에서 환자로부터 백혈구 분반술(leukapheresis)을 통해 말초혈액을 채취 후 당사의 세포치료제 GMP 제조소로 이송하여, 밀도구배 원심분리법을 통해 말초혈액단핵구(peripheral blood mononuclear cell, PBMC)를 분리해내어 제조하게 됩니다. 그러나 대상 암환자의 병기 및 전신상태, 기 적용된 항암약물요법 등에 따라, 백혈구 분반술 시행이 어려운 상황이 발생할 수 있으며, 분리된 말초혈액단핵구 내 면역세포의 수가 유효한 수준 이하일 가능성이 있습니다.
CAR-T, CAR-NK, CAR-MIL 또한 당사에서 개발하는 세포치료제로써 자가세포유래로 환자의 혈액 T세포나 NK세포 또는 골수의 MIL세포를 이용하여 제조합니다. 대다수의 환자에서는 당사의 제조 기술력에 의해서 품질시험 기준에 합격할 수 있는 세포치료제의 제조가 가능하지만, 타 개발사와 마찬가지로 환자의 면역세포가 극히 적게 포함되어 있거나, 그 기능이 현저히 떨어져 있는 소수의 환자에서 세포치료제의 제조가 어려운 경우도 발생할 수 있습니다.
또한 자연재해, 인공재해 등으로 인하여 제조 공장이 멸실되거나, 제조인력이 파업을 하거나, 제조 및 품질관리 기준이 갑작스럽게 대폭 강화되어 제조공정의 개선이 필요하여 생산라인이 마비되는 등 예측하기 어려운 문제들이 발생할 경우, 당사의 제품 상업화 또는 임상개발에 부정적인 영향을 미칠 수 있습니다. 또한 GMP 제조 시설의 상각비가 지속적으로 발생함에도 불구하고, 매출 시현이 지연될 경우 당사의 손익이 악화될 가능성이 존재하며 현금 확보가 제한되어 향후 임상 진행 등의 측면에서 제약을 받을 가능성이 존재하오니 투자자께서는 이 점 유의하여 주시기 바랍니다.
2. 회사위험
| [투자자 주의사항] |
| ■ 당사는 연결대상 종속기업이 존재하지 않는 바. 본 증권신고서는 별도 재무제표를 기준으로 작성하였습니다. 투자자분들께서는 이점 유의하여주시기 바랍니다. ■ 회사위험에는 당사의 주요 재무적 위험요소들이 기재되어 있습니다. 투자자분들의 이해 편의를 위하여, 당사의 최근 3개년간 주요 재무사항 총괄표를 요약 기재하였으니, 투자 판단에 참고하여 주시기 바랍니다. |
|
[주요 재무상황 총괄표] |
| (단위: 백만원, 배) |
| 항목 | 2023년 반기 | 2022년 | 2021년 | 2020년 | 비 고 |
|---|---|---|---|---|---|
| 외부감사인 | - | 신한회계법인 | 신한회계법인 | 신한회계법인 | - |
| 감사의견 | - | 적정 | 적정 | 적정 | - |
| 강조사항 등 | - | 해당사항 없음 | 해당사항 없음 | 해당사항 없음 | - |
| 자산총계 | 20,075 | 24,163 | 31,276 | 35,498 | - |
| 유동자산 | 16,747 | 20,898 | 28,197 | 19,186 | - |
| 비유동자산 | 3,328 | 3,265 | 3,079 | 16,311 | - |
| 부채총계 | 1,378 | 836 | 1,196 | 830 | - |
| 유동부채 | 488 | 307 | 392 | 594 | - |
| 비유동부채 | 890 | 529 | 804 | 236 | - |
| 자본총계 | 18,696 | 23,327 | 30,080 | 34,667 | - |
| 자본금 | 7,612 | 7,612 | 7,612 | 3,762 | - |
| 매출액 | 0 | 0 | 0 | 0 | - |
| 판매관리비 | 5,269 | 8,213 | 5,904 | 4,255 | - |
| 영업이익 | (5,269) | (8,213) | (5,904) | (4,255) | - |
| 당기순이익 | (4,737) | (6,825) | (4,763) | (3,984) | - |
| 영업현금흐름 | (4,455) | (6,045) | (4,662) | (3,303) | - |
| 투자현금흐름 | (4,931) | 4,333 | (3,237) | (20,049) | - |
| 재무현금흐름 | (72) | (208) | 305 | 29,180 | - |
| 기초현금 | 390 | 2,309 | 9,903 | 4,074 | - |
| 기말현금 | 793 | 390 | 2,309 | 9,903 | - |
| 영업이익률 | 매출 미시현 | 매출 미시현 | 매출 미시현 | 매출 미시현 | 영업이익 ÷ 매출액 |
| EBITDA이익률 | 매출 미시현 | 매출 미시현 | 매출 미시현 | 매출 미시현 | EBITDA ÷ 매출액 |
| 당기순이익률 | 매출 미시현 | 매출 미시현 | 매출 미시현 | 매출 미시현 | 당기순이익 ÷ 매출액 |
| ROA | -42.8% | -24.6% | -14.3% | -17.5% | 당기순이익 ÷ 자산총계 |
| ROE | -45.1% | -25.6% | -14.7% | -18.2% | 당기순이익 ÷ 자본총계 |
| 매출액 성장률 | 매출 미시현 | 매출 미시현 | 매출 미시현 | 매출 미시현 | - |
| 영업이익 성장률 | 적자지속 | 적자지속 | 적자지속 | 적자지속 | - |
| 당기순이익 성장률 | 적자지속 | 적자지속 | 적자지속 | 적자지속 | - |
| 자산총계 성장률 | -27.5% | -22.7% | -11.9% | 253.7% | - |
| 이자보상비율 | -265.3 | -492.4 | -219.5 | -121.9 | 영업이익 ÷ 이자비용 |
| 부채비율 | 7.4% | 3.6% | 4.0% | 2.4% | 부채총계 ÷ 자본총계 |
| 유동비율 | 3429.3% | 6806.4% | 7187.7% | 3229.0% | 유동자산 ÷ 유동부채 |
| 총차입금 | 336 | 105 | 220 | 339 | - |
| 총차입금 의존도 | 1.7% | 0.4% | 0.7% | 1.0% | 총차입금 ÷ 자산총계 |
주) 2023년 분기 ROA, ROE는 단순 연환산수치를 사용하였으며, 자산/자본 총계는
((해당 기 + 전년 말)/2)를 사용하였습니다.
|
가. 성장성 및 수익성 감소에 따른 위험 당사는 항암면역치료제 전문기업으로서, 항암면역치료제 개발과 관련하여 연구개발 단계에서부터 임상 단계에 이르기까지 사업화 전주기에 걸쳐 신약 개발 사업을 진행하고 있으며, 향후에는 현재의 파이프라인을 더욱 확장하여 강력한 면역치료와 다른 항암요법을 병합하는 새로운 항암치료법을 창출함으로써 세계 항암치료제 시장의 프론티어로 발전하고자 하는 비전을 가지고 있습니다. 그러나, 당사는 아직 본격적인 신약 출시의 이전 단계 연구개발을 진행하고 있는 상황으로, 매출시현을 하지 못하여 지속적인 적자를 보이고 있습니다. |
당사는 항암면역치료제 전문기업으로서, 항암면역치료제 개발과 관련하여 연구개발 단계에서부터 임상 단계에 이르기까지 사업화 전주기에 걸쳐 신약 개발 사업을 진행하고 있으며, 향후에는 현재의 파이프라인을 더욱 확장하여 강력한 면역치료와 다른 항암요법을 병합하는 새로운 항암치료법을 창출함으로써 세계 항암치료제 시장의 프론티어로 발전하고자 하는 비전을 가지고 있습니다.
그러나, 당사는 아직 본격적인 신약 출시의 이전 단계 연구개발을 진행하고 있는 상황으로, 매출시현을 하지 못하여 지속적인 적자를 보이고 있습니다. 당사의 최근 손익 현황은 다음과 같습니다.
| [손익계산서 주요계정 및 수익성 추이] |
| (단위 : 백만원) |
| 구분 | 2023년 반기 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|
| Ⅰ.매출액 | - | - | - | |
| Ⅱ.매출원가 | - | - | - | |
| Ⅲ.매출총이익 | - | - | - | |
| Ⅳ.판매관리비 | 5,269 | 8,213 | 5,904 | 4,255 |
| Ⅴ.영업이익(손실) | (5,269) | (8,213) | (5,904) | (4,255) |
| Ⅵ.금융수익 | 457 | 422 | 322 | 110 |
| Ⅶ.금융원가 | 30 | 17 | 27 | 35 |
| Ⅷ.기타수익 | 126 | 1,010 | 869 | 227 |
| Ⅸ.기타비용 | 20 | 27 | 23 | 31 |
| XⅡ.당기순이익(손실) | (4,737) | (6,825) | (4,763) | (3,984) |
| 출처: 당사 정기보고서 |
이와 같이 당사는 사업이 본격적인 궤도에 진입하지 못한 관계로 현재까지 매출규모가 제한적이며 과거 실적 성장률을 토대로 회사의 잠재성장성을 판단하는데 한계가 있습니다. 또한 지속적으로 상승하고 있는 판매비와관리비으로 인해 영업손실과 당기순손실을 시현하고 있습니다. 연도별 영업비용의 성격별 분류는 아래와 같습니다.
| [판매비와관리비 세부 내역] |
| (단위: 백만원) |
| 구분 | 2023년 반기 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|
| 급여 | 1,071 | 2,405 | 1,788 | 1,231 |
| 퇴직급여 | 126 | 252 | 134 | 142 |
| 인력개발비 | 5 | 12 | 11 | 10 |
| 복리후생비 | 138 | 724 | 172 | 132 |
| 여비교통비 | 31 | 53 | 26 | 40 |
| 접대비 | 40 | 32 | 17 | 24 |
| 통신비 | 3 | 5 | 4 | 4 |
| 수도광열비 | 1 | 1 | 1 | 1 |
| 전력비 | 24 | 61 | 67 | 52 |
| 세금과공과금 | 8 | 17 | 7 | 0 |
| 감가상각비 | 135 | 270 | 232 | 172 |
| 무형자산상각비 | 27 | 41 | 25 | 14 |
| 지급임차료 | 26 | 27 | 29 | 13 |
| 보험료 | 1 | 5 | 11 | 3 |
| 차량유지비 | 2 | 16 | 19 | 5 |
| 경상연구개발비 | 2,016 | 2,062 | 1,800 | 1,340 |
| 운반비 | 0 | 0 | 1 | - |
| 교육훈련비 | 1 | 7 | 1 | 1 |
| 도서인쇄비 | 6 | 6 | 10 | 13 |
| 회의비 | 1 | 3 | 4 | - |
| 사무용품비 | 1 | 0 | 3 | 4 |
| 소모품비 | 263 | 316 | 364 | 143 |
| 지급수수료 | 1,220 | 1,794 | 1,106 | 748 |
| 광고선전비 | 7 | 38 | 2 | 20 |
| 건물관리비 | 15 | 20 | 18 | 12 |
| 주식보상비용 | 97 | 38 | 47 | 132 |
| 협회비 | 3 | 5 | 7 | - |
| 합 계 | 5,269 | 8,213 | 5,904 | 4,255 |
| 출처: 당사 정기보고서 |
당사의 판매비와관리비가 증가하는 주요 원인은 무형자산 인식요건을 충족하지 못한 경상연구개발비, 파이프라인이 확대되는 과정에서 증가한 연구인력으로 인한 임직원 인건비, 지급수수료 등이 있습니다. 지급수수료의 경우 임상시험연구비, 시험분석료, 임상연구 위탁 수수료 등 임상연구 진행 과정에서 발행하는 수수료가 포함되어있어 당사 파이프라인이 확대되는 과정에서 증가하는 추세를 보이고 있습니다.
비용의 성격별 분류 내역은 다음과 같습니다.
| [비용의 성격별 분류내역] |
| (단위: 백만원) |
| 구분 | 2023년 상반기 |
비율 | 2022년 | 비율 | 2021년 | 비율 | 2020년 | 비율 |
|---|---|---|---|---|---|---|---|---|
| 종업원급여 | 1,910 | 36.3% | 3,190 | 38.8% | 2,419 | 41.0% | 1,703 | 40.0% |
| 감가상각비 | 267 | 5.1% | 559 | 6.8% | 521 | 8.8% | 475 | 11.2% |
| 경상연구개발비 | 1,134 | 21.5% | 1,155 | 14.1% | 942 | 16.0% | 680 | 16.0% |
| 기타 | 1,958 | 37.2% | 3,309 | 40.3% | 2,022 | 34.3% | 1,397 | 32.8% |
| 합 계 | 5,269 | 100.0% | 8,213 | 100.0% | 5,904 | 100.0% | 4,255 | 100.0% |
| 출처: 당사 정기보고서 |
| [임직원 수 추이] |
| 2020년 | 2021년 | 2022년 | 2023년 반기 |
|
|---|---|---|---|---|
|
기술연구소 |
7 | 8 | 8 | 7 |
|
임상연구실 |
1 | 4 | 3 | 4 |
|
공정개발실 |
- | - | 3 | 5 |
|
동물의약품실 |
- | 1 | 3 | 4 |
|
기타 핵심 연구 인력 |
5 | 5 | 6 | 8 |
| 계 | 13 | 18 | 23 | 28 |
| 출처: 당사 정기보고서 |
임직원 수가 2020년 25명에서 2023년 반기 53명으로 증가하는 추세를 반영하여 종업원 급여의 규모는 매년 증가하고 있으며 가장 큰 비중을 차지하고 있습니다.
비용 중 가장 큰 비중을 차지하는 종업원급여의 경우 2023년 반기 기준 전체 비용에서 36.3%를 차지하였으며, 2022년 38.8%, 2021년 41.0%, 2020년 40.0%를 기록하였습니다. 경상연구개발비의 경우에는 2023년 반기 21.5%를 기록, 2022년 14.1%, 2021년 16.0%, 2020년 16.0%를 기록하였습니다.
당사는 당사 파이프라인 대상 적응증 환자들이 매년 증가하고 있고, 필요한 경우 당사 파이프라인에 대한 다양한 분석을 통해 경쟁 제품 대비 개선된 효능을 파악하고 있으며, 기존에 고형암에 적용되지 않던 CAR기반 치료제를 개발하고 있어 향후 당사 파이프라인들이 제품화 되었을 때의 높은 시장성에 대해 긍정적으로 판단하고 있습니다. 국내외 대형 제약사와의 License-Out 계약 및 제품화에 성공할 시 매출확대 및 흑자전환이 가능할 것으로 판단하고 있습니다. 당사는 보유 파이프라인의 조속한 기술이전과 제품출시를 통해 매출시현을 계획하고 있으나 주요 파이프라인의 임상계획이 지연 혹은 중단되거나, 유의미한 수준의 License-Out 계약 체결에 실패하는 경우 당사의 매출성장 및 이익률 개선에 악영향이 발생할 수 있습니다. 투자자께서는 이점 유의하여 주시기 바랍니다.
| 나. 재무안정성 관련 위험 당사가 개발하고 있는 항암면역치료제는 후보물질발굴부터 임상 진행, 품목허가까지 대규모의 자금이 소요되는 사업입니다. 당사는 원활한 연구개발의 진행을 위해 설립 초기부터 여러 차례 증자를 통해 자금을 조달하였으며 이를 통해 재무안정성을 개선하고자 노력하였습니다. 다만, 핵심 파이프라인의 제품매출이 발생하기 전까지 영업활동으로 인한 현금흐름이 지속적으로 적자를 기록할 것으로 예상되며, 기술이전 계약 및 제품 판매 시점이 예상보다 지연되거나 연구개발비가 증가하게 될 경우 재무안정성 및 유동성이 악화될 수 있으니 투자자께서는 이 점을 유의하시기 바랍니다. |
당사가 개발하고 있는 항암면역치료제는 후보물질발굴부터 임상 진행, 품목허가까지 대규모의 자금이 소요되는 사업입니다. 당사는 원활한 연구개발의 진행을 위해 설립 초기부터 여러 차례 증자를 통해 자금을 조달하였으며 이를 통해 재무안정성을 개선하고자 노력하였습니다. 당사의 최근 재무안정성 지표 추이는 다음과 같습니다.
| [당사의 재무안정성 지표 추이] |
| (단위: 백만원, %) |
| 구분 | 2023년 반기 | 2022년 | 2021년 | 2020년 | 업종평균 |
|---|---|---|---|---|---|
| 자산총계 | 20,075 | 24,163 | 31,276 | 35,498 | - |
| 유동자산 | 16,747 | 20,898 | 28,197 | 19,186 | - |
| 비유동자산 | 3,328 | 3,265 | 3,079 | 16,311 | - |
| 부채총계 | 1,378 | 836 | 1,196 | 830 | - |
| 유동부채 | 488 | 307 | 392 | 594 | - |
| 비유동부채 | 890 | 529 | 804 | 236 | - |
| 자본총계 | 18,696 | 23,327 | 30,080 | 34,667 | - |
| 부채비율 | 7.4% | 3.6% | 4.0% | 2.4% | 70.4% |
| 유동비율 | 3429.3% | 6806.4% | 7187.7% | 3229.0% | 180.6% |
| 총차입금 | 336 | 105 | 220 | 339 | - |
| 총차입금 의존도 | 1.7% | 0.4% | 0.7% | 1.0% | 22.5% |
| 주) 업종평균은 한국은행이 발간한 2021년 기업경영분석 C21(의료용 물질 및 의약품 중 중소기업) 기준 출처: 당사 정기보고서 |
2020년에는 코스닥 시장 상장을 통해 296억원 규모의 공모금액을 조달하며 재무안정성이 크게 개선되었습니다. 이로 인해 부채비율은 2020년 2.4%을 기록하였으며, 2021년에는 4.0%, 2022년에는 3.6%, 2023년 반기에는 7.4% 기록하여 매년 적자를 기록하여 자본이 감소해 부채비율이 증가하고 있으나, 업종 평균 70.86% 대비 부채비율은 낮은 수준입니다.
한편, 당사의 차입금은 리스부채로만 구성되어 있으며 2023년 반기 3.4억원, 2020년 1.05억원, 2021년 2.2억원, 2020년 3.39억원. 차입금을 자산총계로 나눈 값인 차입금 의존도는 2023년 반기 1.7%, 2022년 0.4%, 2021년 0.7%, 2020년 1.0%, 2019년 4.6%인 바, 업종 평균 20.53% 대비 낮은 수준입니다.
다만, 핵심 파이프라인의 제품매출이 발생하기 전까지 영업활동으로 인한 현금흐름이 지속적으로 적자를 기록할 것으로 예상되며, 기술이전 계약 및 제품 판매 시점이 예상보다 지연되거나 연구개발비가 증가하게 될 경우 재무안정성 및 유동성이 악화될 수 있습니다.
| [연구개발비 현황] |
| (단위: 천원) |
|
구 분 |
2023년 반기 | 2022년 | 2021년 | 2020년 | |
|---|---|---|---|---|---|
|
자산 처리 |
원재료비 |
- | - | - | - |
|
인건비 |
- | - | - | - | |
|
감가상각비 |
- | - | - | - | |
|
위탁용역비 |
- | - | - | - | |
|
기타 경비 |
- | - | - | - | |
|
소 계 |
- | - | - | - | |
|
비용 |
제조원가 |
- | - | - | - |
|
판관비(*) |
2,016 | 2,062 | 1,800 | 1,340 | |
|
소계 |
2,016 | 2,062 | 1,800 | 1,340 | |
|
(정부보조금) |
- | - | - | - | |
|
보조금 차감 후 금액 |
2,016 | 2,062 | 1,800 | 1,340 | |
|
합계 |
2,016 | 2,062 | 1,800 | 1,340 | |
| 출처: 당사 정기보고서 |
또한, 상기 표와 같이 당사는 연구개발비를 전액 비용으로 처리하고 있습니다. 2023년 반기 20.16억원을 비용으로 처리하였으며, 2022년 20.62억원, 2021년 18억원, 2020년 13.4억원을 차례로 비용으로 처리하였습니다. 연구개발비의 지속적인 증가는 당사의 재무 안전성에 악영향을 미칠 것으로 판단되오니, 투자자께서는 이 점을 유의하시기 바랍니다.
| 다. 영업현금흐름 및 유동성 관련 위험 당사는 지속적인 연구개발 활동으로 인해 음(-)의 영업활동현금흐름을 보이고 있으며,이를 재무활동현금흐름을 통하여 충당하고 있는 상황입니다. 당사는 항암면역치료제를 개발하고 있으며, 이에 따라 매년 대규모 연구개발비가 발생하고 있습니다. 향후 임상 파이프라인 및 임상 단계 진전에 따라 더 많은 연구개발비가 투입될 예정이며 이에 따라 영업비용 또한 확대될 것으로 보입니다. 비록 금번 주주배정 후 실권주 일반공모 유상증자를 통하여 재무활동현금이 유입될 예정이나, 보유 파이프라인의 라이센스 아웃 및 영업활동 전반에 대한 모니터링이 필요하다고 판단되며, 지속적으로 영업 성과에 부정적인 영향으로 음(-)의 영업활동현금흐름이 발생할 경우 장기적으로 회사의 현금흐름에 문제가 발생할 소지가 있습니다. |
당사는 지속적인 연구개발 활동으로 인해 음(-)의 영업활동현금흐름을 보이고 있으며, 이러한 음(-)의 영업활동현금흐름을 대체적으로 IPO 공모 등으로 인한 재무활동현금흐름을 통해 충당하고 있는 상황이며, 2023년 반기 기준 당사는 8억원의 현금 및 현금성자산과 150억원의 단기금융상품을 보유하고 있습니다. 당사의 최근 3년간 요약 현금흐름 추이는 다음과 같습니다.
| [당사의 3개년 요약현금흐름 추이] |
| (단위: 백만원) |
| 구 분 | 2023년 반기 | 2022년 | 2021년 | 2020년 |
|---|---|---|---|---|
| 영업활동현금흐름 | -4,455 | -6,045 | -4,662 | -3,303 |
| 투자활동현금흐름 | 4,931 | 4,333 | -3,237 | -20,049 |
| 재무활동현금흐름 | -72 | -208 | 305 | 29,180 |
| 현금의 증가(감소) | 404 | -1,919 | -7,594 | 5,828 |
| 기초의 현금 | 390 | 2,309 | 9,903 | 4,074 |
| 기말의 현금 | 793 | 390 | 2,309 | 9,903 |
| 출처: 당사 정기보고서 |
당사는 항암면역치료제를 연구ㆍ개발하는 바이오텍 회사로 이에 따라 향후 임상 파이프라인 및 임상 단계 진전에 따라 더 많은 연구개발비가 투입될 예정이며 판매비와관리비 또한 확대될 것으로 보입니다. 당사는 매년 연구개발비용 등 대규모 순 현금 소요가 발생하고 있고, 이를 외부자금 조달 및 금융자산의 처분 등을 통해 충당하고 있습니다. 금번 유상증자를 통해 유입된 자금을 당사는 연구개발비, 시설자금, 운영자금에 사용할 예정입니다. 자세한 내용은 'V. 자금의 사용목적'을 참고하시기 바랍니다.
당사는 현금흐름 및 유동성에 대하여 지속적으로 모니터링하면서 유동성 이슈가 발생하지 않도록 대응하고 있으나, 최근 3년간 지속적으로 현금흐름 지표가 악화되어 왔으며, 영업 실적이 개선되지 않아 음(-)의 영업활동현금흐름이 계속 발생할 경우 유동성 리스크가 부각될 위험이 있습니다. 때문에 보유 파이프라인의 라이센스 아웃 및 영업활동 전반에 대한 모니터링이 필요하다고 판단되며, 지속적으로 영업 성과에 부정적인 영향으로 음(-)의 영업활동현금흐름이 발생할 경우 장기적으로 회사의 현금흐름에 문제가 발생할 소지가 있습니다. 투자자께서는 회사의 현금흐름 및 유동성 관련 위험요인을 면밀히 검토하시고 투자에 임해주시기 바랍니다.
| 라. 최대주주 및 특수관계인 지분희석 및 경영권 관련 위험 당사의 최대주주는 이제중 대표이사로 1,959,820주(지분율 12.87%) 보유하고 있으며, 사내이사 이준행(연구총괄)은 1,478,060주(지분율 9.71%)를 보유하고 있습니다, 이외 특수관계인은 1,043,987주(지분율 6.86%)를 보유하고 있습니다. 최대주주 및 특수관계인 합산시에는 4,481,867주(지분율 29.44%)를 보유중에 있습니다. 금번 유상증자의 총 공모 주식수는 3,938,000주이며, 당사 최대주주 및 2대주주와 기타 특수관계인들은 각각 506,980주, 382,355주, 270,066주를 배정 받을 것으로 예상됩니다. 당사의 최대주주인 이제중 대표이사 및 사내이사 이준행은 배정주식수의 약 30% 수준에 대해 청약할 예정입니다. 당사 최대주주인 이제중 대표이사 및 사내이사 1인(이준행)은 30% 수준으로 청약에 참여할 예정이며, 30% 참여 가정 시 청약 주식 수는 각각 152,094주, 114,706주입니다. 증권신고서 제출일 기준 예정발행가액에 따른 상기 2인의 예상 필요 청약 자금은 각각 29.3억원, 21.2억원 입니다. 다만, 최대주주 이제중 및 2대주주인 이준행은 금번 유상증자 청약자금 마련을 위해 2023년 09월 26일 블록딜(장외대량매매) 방식으로 보유 주식 일부를 매각 완료하였습니다. 주당 매각가액은 2023년 09월 25일 종가에 할인율 10.0%를 적용한 25,515원입니다. 최대주주 이제중은 본 공시서류 제출일 전일 기준 보유주식 1,959,820주에서 170,000주를 매각하였으며, 2대주주 이준행은 보유주식 1,478,060주에서 130,000주를 매각하였습니다. 이에따라 각각의 지분율은 11.76%, 8.86%로 하락하였습니다. 아울러 청약에 참여하지 않는 배정물량의 70%에 해당하는 신주인수권증서 또한 매각하여 청약대금으로써 활용할 계획입니다. 구주 및 신주인수권증서 매각에 따라, 금번 유상증자 후 당사의 최대주주 및 2대주주의 지분율은 각각 10.13%, 7.63%로 예상되며 이는 본 공시서류 전출일 전일 기준 지분율 대비 각각 1.63%p. 및 1.23%p. 하락한 수치입니다. 아울러 보수적인 가정을 위해 기타 특수관계인들은 전량 미청약을 가정 시 유상증자 후 지분율이 5.45%로 -1.41%p 하락하게 됩니다. 금번 유상증자 및 구주매각에 따라 당사 최대주주 및 특수관계인의 지분율은 전술한 바와 같이 하락할 수 있으며, 이는 당사 최대주주의 경영권 등에 부정적인 영향을 미칠 수 있습니다. 이처럼 유상증자 진행 과정 중 최대주주 등의 블록딜이 예정되어 있으니 투자자께서는 투자 판단시 이점 유의하시기 바랍니다. |
당사의 최대주주는 이제중 대표이사로 1,959,820주(지분율 12.87%) 보유하고 있으며, 사내이사 이준행(연구총괄)은 1,478,060주(지분율 9.71%)를 보유하고 있습니다, 이외 특수관계인은 1,043,987주(지분율 6.86%)를 보유하고 있습니다. 최대주주 및 특수관계인 합산시에는 4,481,867주(지분율 29.44%)를 보유중에 있습니다. 금번 유상증자의 총 공모 주식수는 3,938,000주이며, 당사 최대주주 및 2대주주와 기타 특수관계인들은 각각 506,980주, 382,355주, 270,066주를 배정 받을 것으로 예상됩니다. 당사의 최대주주인 이제중 대표이사 및 사내이사 이준행은 배정주식수의 약 30% 수준에 대해 청약할 예정입니다.
당사 최대주주인 이제중 대표이사 및 사내이사 1인(이준행)은 30% 수준으로 청약에 참여할 예정이며, 30% 참여 가정 시 청약 주식 수는 각각 152,094주, 114,706주입니다. 증권신고서 제출일 기준 예정발행가액에 따른 상기 2인의 예상 필요 청약 자금은 각각 29.3억원, 21.2억원 입니다.
다만, 최대주주 이제중 및 2대주주인 이준행은 금번 유상증자 청약자금 마련을 위해 2023년 09월 26일 블록딜(장외대량매매) 방식으로 보유 주식 일부를 매각 완료하였습니다. 주당 매각가액은 2023년 09월 25일 종가에 할인율 10.0%를 적용한 25,515원입니다. 최대주주 이제중은 본 공시서류 제출일 전일 기준 보유주식 1,959,820주에서 170,000주를 매각하였으며, 2대주주 이준행은 보유주식 1,478,060주에서 130,000주를 매각하였습니다. 이에따라 각각의 지분율은 11.76%, 8.86%로 하락하였습니다. 아울러 청약에 참여하지 않는 배정물량의 70%에 해당하는 신주인수권증서 또한 매각하여 청약대금으로써 활용할 계획입니다.
향후 증자 진행 과정에서 주가 상승으로 인해 예정발행가액 대비 확정발행가액이 변동될 경우 최대주주 및 2대주주의 청약자금 부담 증가로 인하여 청약 주식수와 금액에 일부 변동이 발생할 수 있으며, 예기치 못한 상황으로 인한 청약 실패 가능성도 배제할 수 없으니 투자자께서는 투자판단시 이점 유의하시기 바랍니다.
구주 및 신주인수권증서 매각에 따라, 금번 유상증자 후 당사의 최대주주 및 2대주주의 지분율은 각각 10.13%, 7.63%로 예상되며 이는 본 공시서류 전출일 전일 기준 지분율 대비 각각 1.63%p. 및 1.23%p. 하락한 수치입니다. 아울러 보수적인 가정을 위해 기타 특수관계인들은 전량 미청약을 가정 시 유상증자 후 지분율이 5.45%로 -1.41%p 하락하게 됩니다. 금번 유상증자에 따라 당사 최대주주 및 특수관계인의 지분율은 전술한 바와 같이 하락할 수 있으며, 이는 당사 최대주주의 경영권 등에 부정적인 영향을 미칠 수 있습니다, 투자자께서는 투자 판단시 이점 유의하시기 바랍니다.
| [최대주주 및 주요 특수관계자 지분율 변동 시뮬레이션(구주매각 후 유상증자 전)] | |
| (기준일 : 증권신고서 제출일 전일) | (단위 : 주) |
| 성 명 | 주식의 종류 |
구주매각 전 | 매각 주식수 | 구주매각 후 | |||
|---|---|---|---|---|---|---|---|
| 주식수 | 지분율(%) | 주식수 | 지분율(%) | 지분율 변동(%p.) | |||
| 이제중 | 의결권 있는 주식 | 1,959,820 | 12.87% | 170,000 | 1,789,820 | 11.76% | -1.11% |
| 이준행 | 1,478,060 | 9.71% | 130,000 | 1,348,060 | 8.86% | -0.85% | |
| 주1) 지분율 변동은 본 공시서류 제출일 전일 기준 지분율 대비입니다. |
| 자료 : 당사 제시 |
| [최대주주 및 주요 특수관계자 지분율 변동 시뮬레이션(구주매각 및 유상증자 후)] | |
| (기준일 : 증권신고서 제출일 전일) | (단위 : 주) |
| 성 명 | 주식의 종류 |
구주매각 후 유상증자 전 | 배정 주식수 | 청약 참여 주식수(예정) |
구주매각 및 유상증자 후(예정) | |||
|---|---|---|---|---|---|---|---|---|
| 주식수 | 지분율(%) | 주식수 | 지분율(%) | 지분율 변동(%p.) | ||||
| 이제중 | 의결권 있는 주식 | 1,789,820 | 11.76% | 506,980 | 152,094 | 1,941,914 | 10.13% | -1.63% |
| 이준행 | 1,348,060 | 8.86% | 382,355 | 114,706 | 1,462,766 | 7.63% | -1.23% | |
| 박기원 외 30명 (기타특수관계인) |
1,043,987 | 6.86% | 270,066 | 0 | 1,043,987 | 5.45% | -1.41% | |
| 주1) 최대주주 및 2대주주의 청약 참여 주식수는 배정주식수의 30%이며, 1주 미만 단수주 절사 |
| 주2) 지분율 변동은 본 공시서류 제출일 전일 기준 지분율 대비입니다. |
| 자료 : 당사제시 |
당사는 상장 당시 안정적인 경영권을 확보하기 위해 최대주주등 5인 및 박기원 외 3인 등 총 9인이 의결권공동보유약정을 체결하였습니다. 상장 당시 의결권 공동보유약정 체결 현황은 다음과 같습니다.
| [상장 당시 의결권 공동보유약정 체결 현황] |
| (단위: 주, %) |
| 구분 | 주주명 | 관계 | 상장 당시 기준 | 비고 | |
|---|---|---|---|---|---|
| 소유주식수 | 지분율 | ||||
| 약정주주 및 대상주식 | 이제중 | 최대주주 본인 | 979,910 | 13.03% | 상장일로부터 3년간 의무보유 |
| 이준행 | 공동대표이사 | 739,030 | 9.82% | ||
| 이제완 | 친인척 | 227,950 | 3.03% | 상장일로부터 1년간 의무보유 |
|
| 이미영 | 친인척 | 111,620 | 1.48% | ||
| KO BYOUNGWE | 친인척 | 5,360 | 0.07% | ||
| 박기원 | 타인 | 149,090 | 1.98% | ||
| 안옥선 | 타인 | 111,620 | 1.48% | ||
| 이미란 | 타인 | 28,200 | 0.37% | ||
| 이시은 | 타인 | 10,000 | 0.13% | ||
| 소계 | 2,362,780 | 31.41% | - | ||
| 약정기간 | 코스닥시장 상장일로부터 2년 간 | ||||
| 약정내용 | 약정기간 동안 청구회사 이준행 사내이사와 의결권 공동 행사, 지분 매각시 이준행 사내이사에게 우선매수권 부여 |
||||
| 주) 상기 주식수와 지분율은 상장 당시 기준으로, 무상증자 등의 효과를 반영하지 않은 수치입니다. 출처: 당사 증권신고서(2020.08.31) |
의결권공동보유 약정주주들은 코스닥 상장일(2020년 09월 22일)로부터 2년 동안 당사가 개최하는 주주총회에서 의결권을 행사함에 있어 주주총회일 전까지 이준행 사내이사와 합의를 마치고 의결권을 공동으로 행사하며, 동 기간 내에 보유 주식을 매도할 경우 이준행 사내이사가 우선매수권을 행사할 수 있습니다. 의결권 공동보유약정은 종료일은 2022년 09월 22일로 증권신고서 제출일 기준 해당 약정은 종료 되었습니다. 이에 따라 최대주주 2인을 제외한 공동의결계약인의 주식 매도 시 우선매수권을 행사할 수 없어 특수관계인 지분율의 하락 우려가 있습니다.
한편, 당사가 임직원에게 부여한 주식매수선택권 중 미행사수량은 29,500주 입니다. 해당 미행사 주식매수선택권은 보고서 제출일 전일 현재 발행주식총수의 0.19% 해당하는 수준으로, 발행주식총수에 비해 현저히 적은 수량이나 행사할 경우 주식 희석에 따라 최대주주 지분율이 소폭 하락할 수 있습니다.
| [당사의 주식매수선택권 부여 현황] |
| (단위 : 원, 주) |
| 성명 | 관 계 | 부여일 | 주식의종류 | 최초부여수량 | 잔여수량 | 행사기간 | 행사가격 |
| 김미화 | 미등기임원 | 2021년 03월 25일 | 보통주식 | 4,500 | 4,500 | 23.03.25 ~ 28.03.24 | 118,712 |
| 하선아 | 미등기임원 | 2022년 02월 07일 | 보통주식 | 4,500 | 4,500 | 24.02.07 ~ 29.02.06 | 42,274 |
| OOO | 미등기임원 | 2022년 07월 15일 | 보통주식 | 4,500 | 4,500 | 24.07.15 ~ 29.07.14 | 41,940 |
| OOO | 미등기임원 | 2023년 02월 23일 | 보통주식 | 6,000 | 6,000 | 25.02.23 ~ 30.02.22 | 36,185 |
| OOO | 미등기임원 | 2023년 02월 23일 | 보통주식 | 5,000 | 5,000 | 25.02.23 ~ 30.02.22 | 36,185 |
| OOO | 미등기임원 | 2023년 02월 23일 | 보통주식 | 5,000 | 5,000 | 25.02.23 ~ 30.02.22 | 36,185 |
| 합계 | 29,500 | 29,500 | - | ||||
| 출처: 당사 정기보고서 |
상기와 같이 당사는 금번 유상증자나 주식매수선택권 행사로 인해 희석이 발생하여 최대주주의 지분율이 하락할 수 있고, 의결권 공동보유약정기간 만료로 인해 특수관계인을 포함한 지분율 또한 하락할 수 있습니다. 이로 인해 적대적 M&A 등의 경영권 분쟁이 발생할 수 있으니 투자자께서는 이점 유의하시기 바랍니다.
| 마. 관리종목 지정 및 상장폐지 위험 당사는 기술성장특례 적용 기업으로서 2개 기관(기술보증기금, 이크레더블)으로부터 각각 A, BBB 등급을 받아 2020년 09월 22일 코스닥시장에 상장하였습니다. 다만, 당사는 보유 파이프라인의 비임상 및 임상시험의 진행으로 인원확충에 따른 인건비 증가, 연구개발비용 증가로 설립 이후 현재까지 지속적으로 적자를 기록하고 있습니다. 지속적인 신약후보물질의 발굴과 보유 파이프라인의 적응증 증가를 위하여 많은 비임상 및 임상시험을 준비하고 있으며 이에 따라 관련비용도 증가하여 이러한 추세는 일정기간 지속될 것으로 예상합니다. 당사는 향후 대규모의 법인세차감전사업손실이 발생하거나 2025 사업연도에 매출을 시현하지 못할 경우, 감사인의 검토의견(감사의견 포함)이 부적정, 의견거절 및 감사범위제한으로 인한 한정으로 나오는 등의 사유가 발생하면 관리종목으로 지정될 수 있습니다. 관리종목으로 지정될 경우 중요 사유 발생시마다 한국거래소는 일정기간 매매거래정지 명령을 발동할 수 있습니다. 이외에도 주식의 미수나 신용거래가 금지되며, 미수나 신용거래의 증거금이 되는 대용유가증권으로도 사용할 수 없습니다. 투자자께서는 관리종목 지정에 따른 위험을 인지하시고 투자에 임하시기 바랍니다. 또한, 이러한 관리종목 지정사유 확인 당일 코스닥시장에서의 거래는 정지됩니다. 이를 기한 내에 해결하지 못한다면 코스닥시장 상장폐지 사유에 해당하여, 당사 주식은 향후 장내에서 거래가 이루어지지 못할 수 있습니다. 투자자 여러분들께서는 당사의 주식이 상장폐지될 경우, 투자금액을 회수하지 못하게 될 수도 있는 점을 반드시 유의하여 주시기 바랍니다. |
당사는 기술성장특례 적용 기업으로서 2개 기관(기술보증기금, 이크레더블)으로부터 각각 A, BBB 등급을 받아 2020년 09월 22일 코스닥시장에 상장하였습니다. 다만, 당사는 보유 파이프라인의 비임상 및 임상시험의 진행으로 인원확충에 따른 인건비 증가, 연구개발비용 증가로 설립 이후 현재까지 지속적으로 적자를 기록하고 있습니다. 지속적인 신약후보물질의 발굴과 보유 파이프라인의 적응증 증가를 위하여 많은 비임상 및 임상시험을 준비하고 있으며 이에 따라 관련비용도 증가하여 이러한 추세는 일정기간 지속될 것으로 예상합니다.
코스닥 관리종목 지정요건과 당사의 해당 여부는 다음과 같습니다
| [코스닥시장 관리종목 지정요건 및 해당여부 검토] |
| 구 분 | 관리종목 지정(코스닥 상장규정 제53조) | 회사현황 | 관리종목 지정요건 |
관리종목지정유예 | ||
| 사업연도 | 금액(백만원) /비율(%) /내용 |
해당여부 | 해당여부 | 종료시점 | ||
| 1) 매출액 미달(별도) | 최근 사업연도 30억원 미만 (지주회사는 연결기준) - 이익미실현기업 또는 기술성장기업은 상장후 5년간 미적용 - 기술성장기업 중 A), B), C) 중 어느 하나에 해당하는 제약·바이오기업은 최근 사업연도 미적용 A) 최근 사업연도 말「제약산업 육성 및 지원에 관한 특별법」에 따른 혁신제약기업이 세칙으로 정한 요건을 충족하는 경우 B) 최근 사업연도의 일평균 시가총액 4,000억 이상이며, 그 금액이 현재의 자본금을 초과하는 기업이 세칙으로 정하는 요건을 충족하는 경우 C) 최근 3사엽언도의 매출액 합계 90억 이상이며, 최근 사업연도의 직전 사업연도의 매출액이 30억 이상인 경우 |
2022년 (별도) |
- | 해당가능 | 해당 | 2024년 12월 31일 |
| 2) 법인세비용차감전 계속사업손실(연결) | 최근 3사업연도중 2사업연도에 각각 당해 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 있고 최근사업연도에 법인세비용차감전계속사업손실이 있는 경우 - 이익미실현 기업은 상장 후 5년간 미적용 - 기술성장기업은 상장후 3년간 미적용 |
2022년 (별도) |
-6,825 / 29.3% | 미해당 | 해당 | 2022년 12월 31일 |
| 2021년 (별도) |
-4,763 / 15.8% | |||||
| 2020년 (별도) |
-3,984 / 11.5% | |||||
| 3) 자본잠식 등(연결) | 반기말 또는 사업연도 말을 기준으로 다음의 어느 하나에 해당하는 경우 A) 최근 반기말 또는 사업연도말을 기준으로 자본잠식률 50%이상 B) 최근 반기말 또는 사업연도말을 기준으로 자기자본 10억원 미만 C) 감사보고서 감사(검토)의견이 부적정 또는 의견 거절이거나 감사범위제한으로 인한 한정인 경우 D) 반기보고서 법정제출기한 다음날부터 10일 이내에 반기검토(감사)보고서를 제출하지 아니한 경우 |
2022년말 (별도) |
A) 자본잠식상태가 아님 B) 자기자본: 23,327 C) 감사의견 적정 D) 2023.03.15. 제출 |
미해당 | - | - |
| 4) 시가총액 미달 | 보통주 시가총액 40억원미만 30일간 지속 -천재지변, 시장상황의 급격한 변동 등으로 거래소가 시장 관리를 위하여 필요하다고 인정될 경우 적용배제 가능 |
현재 기준 | 시가총액 요건 충족 | 미해당 | - | - |
| 5) 정기보고서 미제출 | 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않은 경우 | 2023년 2022년 |
반기보고서 제출일 2023년 8월 14일 분기보고서 제출일 2023년 05월 12일, 사업보고서 제출일 2023년 03월 15일 |
미해당 | - | - |
| 6) 지배구조 미달 | 최근 사업연도 사업보고서상 A)사외이사의 수가 법에서 정하는 수에 미달 B)법에서 정하는 감사위원회를 구성하지 않거나 구성요건을 충족하지 아니하는 경우 *「상법」 제542조의8에 의거 자산총액 1,000억원 미만의 코스닥 상장 벤처기업은 사외이사 선임 의무 면제 **「상법」 제542조의11에 의거 자산총액 2조원 미만의 상장회사는 감사위원회 설치 의무 면제 |
2022년 | 2022년(별도) 기준 자산총액 242억원 사외이사 선임 및 감사위원회 설치 의무 면제 |
미해당 | - | - |
| 7) 거래량 미달 | 분기월평균거래량이 유동주식수의 1%에 미달 - 신규상장법인(신규상장일이 속하는 분기에 한정), 월평균거래량 1만주 이상(액면가액 5,000원 기준), 법에 따른 유동성공급계약 체결, 소액주주 300인이상이 20%이상 지분 보유 등은 적용배제 |
2022년말 | 소액주주 지분율 68.53%소액주주수 101,658명 | 미해당 | - | - |
| 8) 주식분산 미달 | 소액주주200인미만 or 소액주주지분 20%미만 - 300인이상의 소액주주가 유동주식수의 10%이상으로서 100만주이상을 소유, 해외증권시장에 상장된 경우는 적용배제 |
2022년말 | 소액주주 지분율 70.32%소액주주수 88,380명 | 미해당 | - | - |
| 9) 회생절차 개시신청 |
"채무자 회생 및 파산에 관한 법률" 제34조에 의한 회생 절차개시 신청이 있는 경우 | 신고서 제출일기준 |
해당사항 없음 | 미해당 | - | - |
| 10) 파산신청 | 코스닥시장 상장법인에 대하여 "채무자 회생 및 파산에 관한 법률" 제294조에 의한 파산신청이 있는 경우 | 신고서 제출일기준 |
해당사항 없음 | 미해당 | - | - |
| 11) 기타 | - 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 - 변경·추가상장이 유예된 기간 중에「증권의 발행 및 공시 등에 관한 규정」에 따른 재무관리기준을 위반한 경우 |
신고서 제출일기준 |
해당사항 없음 | 미해당 | - | - |
| 출처: 당사 정기보고서 |
(1) 매출액 미달 여부 검토
| [매출액 미달 여부 검토] | |
| (K-IFRS, 별도) | (단위 : 백만원) |
| 구분 | 2022년 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
| 매출액 | - | - | - | - |
| 출처: 당사 정기보고서 |
코스닥시장 상장규정 제53조 1항 1호에 따라 최근 사업연도의 매출액이 30억 미만일 경우 관리종목으로 지정되게 됩니다. 당사는 최근 4개년간 매출이 발생하지 않아 매출액 미달 에 관리종목 지정이 가능하나, 코스닥시장 상장규정 제53조 1항 1호 가목을 적용받아 매출액 미달에 따른 관리종목 지정은 2024년 12월 31일까지 지정 유예를 받습니다. 따라서 지정 유예가 종료되는 2025년부터 라이선스 아웃 실패 등의 사유로 당사의 매출이 관리종목 지정 요건에 미달할 경우, 관리종목 지정 가능성이 있음을 투자자분들께서는 이 점 유의하여 주시기 바랍니다.
(2) 법인세차감전계속사업손실 발생 여부 검토
| [법인세차감전계속사업손실 발생 여부 검토] | |
| (K-IFRS, 별도) | (단위 : 백만원) |
| 구분 | 2022년 | 2021년 | 2020년 |
| 법인세비용차감전순손실 | (6,825) | (4,763) | (3,984) |
| 자기자본 | 23,327 | 30,080 | 34,667 |
| 법인세비용차감전순손실/자기자본 | 29.3% | 15.8% | 11.5% |
주) 당사는 연결대상 종속법인이 존재하지 않는 바, 연결재무제표 기준 검토사항임에도 별도재무제표 값으로 계산하였습니다.
코스닥시장 상장규정 제53조 1항 2호에 따라 최근 3사업연도 중 2사업연도에 각각 당해 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 있고 최근 사업연도에 법인세비용차감전계속사업손실이 있는 경우 관리종목으로 지정되게 됩니다.
당사는 최근 3사업연도(2019년~2021년) 중 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 발생한 적이 없으며(2019년 13.8%, 2020년 11.5%, 2021년 15.8%), 코스닥시장 상장규정 제53조 1항 2호 나목을 적용받아 법인세비용차감전계손사업손실에 따른 관리종목 지정은 2022년 12월 31일까지 지정 유예를 받습니다. 이에 따라 당사는 해당 항목에 따른 관리종목 지정 사유에 해당하지 않습니다.
(3) 자본잠식 여부 검토
| [자본잠식 여부 검토] | |
| (K-IFRS, 별도) | (단위 : 백만원) |
| 구분 | 2022년 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
| 자기자본(별도) | 23,327 | 30,080 | 34,667 | 9,071 |
| 자본금(별도) | 7,612 | 7,612 | 3,762 | 3,254 |
| 자본잠식여부(별도) | - | - | - | - |
| 감사의견 | 적정 | 적정 | 적정 | 적정 |
| 출처: 당사 정기보고서 |
주) 당사는 연결대상 종속법인이 존재하지 않는 바, 연결재무제표 기준 검토사항임에도 별도재무제표 값으로 계산하였습니다.
코스닥시장 상장규정 제53조 1항 4호에 따라 반기말 또는 사업연도 말을 기준으로 다음의 어느 하나에 해당하는 경우 A) 최근 반기말 또는 사업연도말을 기준으로 자본잠식률 50%이상 / B) 최근 반기말 또는 사업연도말을 기준으로 자기자본 10억원 미만 / C) 반기보고서 감사(검토)의견이 부적정 또는 의견 거절이거나 감사범위제한으로 인한 한정인 경우 / D) 반기보고서 법정제출기한 다음날부터 10일 이내에 반기검토(감사)보고서를 제출하지 아니한 경우 관리종목으로 지정됩니다.
당사는 A) 최근 반기말(2022년 말) 자본잠식상태가 아니고, B) 최근 반기말(2022년 말) 자기자본이 약 233억원으로 10억원 이상이며, C) 최근 반기보고서(2022년 말) 검토의견이 부적정 또는 의견 거절이거나 감사범위제한으로 인한 한정에 해당되지 않으며, D) 최근 반기보고서(2022년 말) 제출일이 2023년 03월 15일로 법정제출기한 내에 제출하였습니다. 이에 따라 당사는 자본잠식 요건에 의한 관리종목 지정요건에 해당하지 않습니다.
(4) 시가총액 미달여부 검토
| [시가총액 미달여부 검토] |
| 구분 | 시가총액(최고) | 시가총액(최저) | 시가총액(평균) |
|---|---|---|---|
| 2023년 2분기 | 1조 641억원 | 5,301억원 | 6,389억원 |
| 출처: KRX 정보데이터시스템 |
코스닥시장 상장규정 제53조 1항 5호에 따라 보통주 시가총액 40억원미만 30일간 지속되는 경우 관리종목으로 지정됩니다.
당사의 2023년 2분기 시가총액은 최고 1조 641억원, 최저 5,301억원, 평균 6,389억원으로 시가총액 40억원 미만을 기록한 바가 없어 관리종목 지정요건에 해당하지 않습니다.
(5) 정기보고서 미제출 여부 검토
코스닥시장 상장규정 제53조 1항 6호에 따라 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않은 경우 관리종목으로 지정됩니다.
당사는 2023년 8월 14일 반기보고서를, 2023년 5월 12일 분기보고서를, 2023년 3월 15일에 사업보고서를 제출함에 따라 법정제출기한 내에 제출한 바, 관리종목 지정요건에 해당하지 않습니다.
(6) 지배구조 미달 여부 검토
코스닥시장 상장규정 제53조 1항 7호에 따라 최근 사업연도 사업보고서상 A)사외이사의 수가 법에서 정하는 수에 미달 B) 법에서 정하는 감사위원회를 구성하지 않거나 구성요건을 충족하지 아니하는 경우 관리종목으로 지정됩니다.
최근 사업연도말(2022년) 당사의 자산총액은 242억원이며 자산총액 1,000억원에 미달하는 벤처기업으로, 「상법 시행령」제34조1항1호에 따라 이사 총수의 4 분의 1 명 이상을 사외이사로 하는 요건에 해당하지 않으며, 감사위원회 요건 및 상근감사를 1명 이상 두어야 하는 요건에 해당하지 않습니다.
A) 당사는 최근 사업연도말(2022년) 기준 사내이사 2명, 사외이사 1명로 이사회가 구성되어 있습니다. B) 당사는 감사위원회를 별도로 설치하고 있지 아니하며, 비상근 감사 1인이 감사업무를 수행하고 있습니다. 당사는 지배구조 미달 요건에 의한 관리종목 지정요건에 해당하지 않습니다.
(7) 거래량 미달 여부 검토
코스닥시장 상장규정 제53조 1항 8호에 따라 분기월평균거래량이 유동주식수의 1%에 미달하는 경우 관리종목으로 지정됩니다. 다만, 다음 어느 하나에 해당하는 경우에는 이 호에 적용 받지 않습니다. 가) 신규 신규상장법인의 경우. 다만, 신규상장일이 속하는 분기에 한정하는 경우, 나) 분기의 월평균거래량이 1만주 이상인 경우. 이 경우 보통주식 상장법인이 액면주식을 발행한 때에는 액면가액 5,000원을 기준, 다) 세칙으로 정하는 소액주주가 소유한 보통주식의 총수가 유동주식수의 100분의 20 이상이고, 해당 소액주주의 수가 300명 이상인 경우. 이 경우 소액주주가 소유한 주식 수와 소액주주의 수는 최근 사업연도 말을 기준으로 하되, 최근 사업연도 말 이후 주주명부를 폐쇄한 경우에는 그 폐쇄시점 현재를 기준으로 거래소에 제출한 주주명부 및 「주식·사채 등의 전자등록에 관한 법률」에 따른 소유자명세를 기준으로 하는 경우입니다.
| 단위 : 원, 주 |
| 종 류 | 2023년 4월 | 2023년 5월 | 2023년 6월 | 2023년 7월 | |
|---|---|---|---|---|---|
| 보 통 주 | 최 고 | 69,900 | 41,800 | 40,800 | 38,100 |
| 최 저 | 40,000 | 38,950 | 34,850 | 33,000 | |
| 평 균 | 48,300 | 40,115 | 37,511 | 35,738 | |
| 월 거래량 (최고) | 9,070,618 | 798,222 | 347,444 | 1,178,360 | |
| 월 거래량 (최저) | 630,776 | 118,080 | 71,859 | 101,517 | |
| 월간 총 거래수량 | 50,397,817 | 5,936,206 | 3,339,266 | 6,861,827 | |
(8) 주식분산 미달 여부 검토
코스닥시장 상장규정 제53조 1항 9호에 따라 최근 사업연도말 소액주주가 200인 미만이거나 소액주주지분이 20% 미만일 경우 관리종목으로 지정됩니다.
당사는 2022년 말 기준 소액주주 지분율 70.32%, 소액주주 수 88,380명임에 따라 주식분산 미달에 따른 관리종목 지정 요건에 해당되지 않습니다.
(11) 기타사항
코스닥시장 상장규정 제53조 1항 10호에서 13호까지에 따라 회생절차개시신청, 파산신청, 상장폐지사유발생, 재무관리기준 위반 요건에 해당하는 경우 관리종목으로 지정됩니다.
당사는 증권신고서 제출일 현재 동 관리종목지정요건에 해당하지 않습니다.
당사는 향후 대규모의 법인세차감전사업손실이 발생하거나 2025 사업연도에 매출을 시현하지 못할 경우, 감사인의 검토의견(감사의견 포함)이 부적정, 의견거절 및 감사범위제한으로 인한 한정으로 나오는 등의 사유가 발생하면 관리종목으로 지정될 수 있습니다. 관리종목으로 지정될 경우 중요 사유 발생시마다 한국거래소는 일정기간 매매거래정지 명령을 발동할 수 있습니다. 이외에도 주식의 미수나 신용거래가 금지되며, 미수나 신용거래의 증거금이 되는 대용유가증권으로도 사용할 수 없습니다. 투자자께서는 관리종목 지정에 따른 위험을 인지하시고 투자에 임하시기 바랍니다.
또한, 이러한 관리종목 지정사유 확인 당일 코스닥시장에서의 거래는 정지됩니다. 이를 기한 내에 해결하지 못한다면 코스닥시장 상장폐지 사유에 해당하여, 당사 주식은 향후 장내에서 거래가 이루어지지 못할 수 있습니다. 투자자 여러분들께서는 당사의 주식이 상장폐지될 경우, 투자금액을 회수하지 못하게 될 수도 있는 점을 반드시 유의하여 주시기 바랍니다.
| 바. 임상결과에 따른 기업가치 급등락 위험 업종 특성상 당사의 기업가치는 통상적으로 개발중인 파이프라인의 사업가치에 따라 결정됩니다. 이에 따라 제약/바이오 기업들의 주가는 통상적으로 개발중인 파이프라인의 임상실험 진행 및 결과 발표에 따라 영향을 받고 있습니다. 당사는 2021년 12월 당사의 동물용의약품 파이프라인인 박스루킨-15주의 임상시험 중 통계적 유의성 확인 필요성이 제기되어 품목허가 신청을 자진 철회한 바 있으며, 추가 연구를 진행하여 차후 품목허가를 재신청할 것을 공시하였습니다. 상기공시는 2021년 12월 15일 장마감 이후 공시되었으며, 해당 공시 다음날 주가는 전일 종가 대비 26.77% 하락하는 등 당사의 주가는 2개월에 걸쳐 크게 하락하였습니다. 또한, 당사는 2022년 08월 24일 당사 파이프라인 Vax-DC의 임상 2상 연구개발 조기종료를 공시한 바 있습니다. 타사들의 더욱 진보된 신약 병용요법이 개발되어 연구개발의 타당성과 투자대비 사업성이 낮을 것이라는 판단 하에 임상을 조기종료한 것으로, 당사의 주력 플랫폼 개발부문으로 핵심 연구인력을 재배치하기로 결정하였습니다. 해당 공시는 장 마감이후 공시되어 시간 외 거래에서 하한가를 기록하였으나, 공시 다음날 주가는 소폭 회복하여 공시일 익일 종가는 전일 대비 5.06% 하락으로 마감하였습니다. 당사는 기존 Vax-DC 다발골수종 치료제를 대신하여, 화순전남대학교병원 암면역치료연구센터에서 다발골수종을 대상으로 확립한 CAR-MIL 치료제 개발을 본격화하기로 결정하였으며, 화순전남대학교병원 암면역치료연구센터와 업무협약을 체결하고 MIL 관련 연구 내용과 그를 이용한 다발골수종 치료법을 2개의 국제학회(국제다발골수종학회 연례 모임(International Myeloma Society Annual Meeting) / 대한조혈모세포이식학회 국제학술대회(ICBMT 2022)) 를 통해 발표하였습니다. 또한, 다발골수종에 특이성이 높은BCMA항원을 도입하여 2024년 임상연구 진입을 목표로 BCMA-CAR-T세포 치료제에 대한 공정개발을 수행하고 있을 뿐만 아니라 후속으로BCMA-CAR-MIL 치료제도 개발 중입니다. 또한, 당사는 2023년 07월 31일 당사 파이프라인 Vax-NK/HCC에 진행성 췌장암 적응증을 추가하여 임상 2a상 변경승인 신청을 하였습니다. 기존에 정기보고서에서 기재했던 바와 같이 mFOLFIRINOX 요법과 병용 치료하여 비임상시험이 완료되었던 파이프라인이며 약 20명을 대상, 무진행 생존기간을 1차 지표로 활용하여 진행하고자 합니다. 해당 공시는 적응증 추가 신청에 관련된 내용으로 주가에 급등락을 발생시키지는 않았으나, 향후 임상 진행 과정에서 중단 또는 성공등의 사유가 발생 시에는 주가 급등락이 이루어질 수 있습니다. 임상시험 약물이 의약품으로 최종 허가받을 확률은 통계적으로 약 10% 수준에 불과합니다. 임상시험 및 품목허가 과정에서 기대에 상응하지 못하는 결과가 나올 수 있으며, 이에 따라 당사가 상업화 계획을 변경하거나 포기할 수 있는 가능성도 상존합니다. 투자자는 수시공시 및 사업보고서 등을 통해 공시된 투자 위험을 종합적으로 고려하여 신중히 투자하시기 바랍니다. |
업종 특성상 당사의 기업가치는 통상적으로 개발중인 파이프라인의 사업가치에 따라 결정됩니다. 이에 따라 제약/바이오 기업들의 주가는 통상적으로 개발중인 파이프라인의 임상실험 진행 및 결과 발표에 따라 영향을 받고 있습니다.
당사는 2021년 12월 당사의 동물용의약품 파이프라인인 박스루킨-15주의 임상시험 중 통계적 유의성 확인 필요성이 제기되어 품목허가 신청을 자진 철회한 바 있으며, 추가 연구를 진행하여 차후 품목허가를 재신청할 것을 공시하였습니다.
당사는 품목허가 신청 자진 철회 이후 연구를 지속하고 있으며, 향후 품목허가 신청 등, 공시사유 발생시 즉시 한국거래소/금융감독원을 통해 전자공시를 진행하겠습니다.
상세 공시 내역은 아래와 같습니다.
| [당사의 투자판단 관련 주요 경영사항 공시(2021.12.15)] |
| 1. 제목 | 동물용의약품 제조품목(박스루킨-15주)허가 신청 철회 | |
| 2. 주요내용 | 1) 2018년 01월 농림축산검역본부의 승인을 받아 진행한 임상시험에서 환견에 대해 안전성과 유효성을 확인하였으나 금번 기술검토결과 통계적 유의성 확인의 필요성이 제기되어 금일 품목허가 신청을 자진 철회하였음. 2) 앞으로 기존 임상시험과 동일하게 림프종 또는 고형암에 이환된 환견 및 대조군에 대한 추가 연구를 진행하여 품목허가를 재신청할 계획임. 3) 기존 임상 연구기관인 전남대학교, 전북대학교에 국립경상대학교 등을 포함한 시험기관을 추가 확보하여 임상시험을 진행할 예정임. |
|
| 3. 사실발생(확인)일 | 2021-12-15 | |
| 4. 결정일 | 2021-12-15 | |
| - 사외이사 참석여부 | 참석(명) | 2 |
| 불참(명) | 0 | |
| - 감사(사외이사가 아닌 감사위원) 참석여부 | 참석 | |
| 5. 기타 투자판단과 관련한 중요사항 | ||
| -기술검토 결과에 대한 보완사항 준비하여 차후 재신청할 예정입니다. | ||
| ※ 관련공시 | - | |
| 출처: 당사 공시내역, 투자판단 주요 경영사항(2021.12.15) |
상기공시는 2021년 12월 15일 장마감 이후 공시되었으며, 해당 공시 다음날 주가는 전일 종가 대비 26.77% 하락하는 등 당사의 주가는 2개월에 걸쳐 크게 하락하였습니다. 박스루킨-15 품목 허가 신청 철회 이후 2개월간 당사의 주가 추이는 다음과 같습니다.
| [박스루킨-15 품목 허가 신청 철회 이후 2개월간 당사의 주가 추이] |
| 일자 | 종가 | 등락률 | 시가총액 |
| 2021-12-15 | 69,100원 | 1.92% | 1조 519억원 |
| 2021-12-16 | 50,600원 | -26.77% | 7,703억원 |
| 2021-12-17 | 46,400원 | -8.30% | 7,063억원 |
| 2021-12-20 | 44,600원 | -3.88% | 6,789억원 |
| 2021-12-21 | 43,150원 | -3.25% | 6,569억원 |
| 2021-12-22 | 44,550원 | 3.24% | 6,782억원 |
| 2021-12-23 | 42,600원 | -4.38% | 6,485억원 |
| 2021-12-24 | 43,300원 | 1.64% | 6,592억원 |
| 2021-12-27 | 44,000원 | 1.62% | 6,698억원 |
| 2021-12-28 | 44,050원 | 0.11% | 6,706억원 |
| 2021-12-29 | 44,500원 | 1.02% | 6,774억원 |
| 2021-12-30 | 43,400원 | -2.47% | 6,607억원 |
| 2022-01-03 | 43,400원 | 0.00% | 6,607억원 |
| 2022-01-04 | 42,850원 | -1.27% | 6,523억원 |
| 2022-01-05 | 41,400원 | -3.38% | 6,302억원 |
| 2022-01-06 | 39,850원 | -3.74% | 6,066억원 |
| 2022-01-07 | 41,300원 | 3.64% | 6,287억원 |
| 2022-01-10 | 40,300원 | -2.42% | 6,135억원 |
| 2022-01-11 | 40,000원 | -0.74% | 6,089억원 |
| 2022-01-12 | 40,750원 | 1.88% | 6,203억원 |
| 2022-01-13 | 39,650원 | -2.70% | 6,036억원 |
| 2022-01-14 | 38,150원 | -3.78% | 5,808억원 |
| 2022-01-17 | 38,250원 | 0.26% | 5,823억원 |
| 2022-01-18 | 37,400원 | -2.22% | 5,693억원 |
| 2022-01-19 | 37,200원 | -0.53% | 5,663억원 |
| 2022-01-20 | 38,150원 | 2.55% | 5,808억원 |
| 2022-01-21 | 38,200원 | 0.13% | 5,815억원 |
| 2022-01-24 | 35,700원 | -6.54% | 5,435억원 |
| 2022-01-25 | 33,850원 | -5.18% | 5,153억원 |
| 2022-01-26 | 34,050원 | 0.59% | 5,183억원 |
| 2022-01-27 | 31,950원 | -6.17% | 4,864억원 |
| 2022-01-28 | 34,250원 | 7.20% | 5,214억원 |
| 2022-02-03 | 36,500원 | 6.57% | 5,556억원 |
| 2022-02-04 | 35,900원 | -1.64% | 5,465억원 |
| 2022-02-07 | 35,100원 | -2.23% | 5,343억원 |
| 2022-02-08 | 35,050원 | -0.14% | 5,336억원 |
| 2022-02-09 | 35,750원 | 2.00% | 5,442억원 |
| 2022-02-10 | 34,450원 | -3.64% | 5,244억원 |
| 2022-02-11 | 33,450원 | -2.90% | 5,092억원 |
| 2022-02-14 | 32,950원 | -1.49% | 5,016억원 |
| 2022-02-15 | 31,900원 | -3.19% | 4,856억원 |
출처: KRX 정보데이터시스템
당사는 시험군 추가 확보가 필요하다는 검역본부의 의견을 받아들여 2021년 12월 박스루킨-15 품목허가 신청을 철회하고 추가 임상연구에 돌입하였으며, 2022년 02월, 빠른 품목 허가 및 출시를 위해 동물의약품 임상연구계획서 변경 승인을 받아 임상연구기관으로 경상국립대학교를 추가하는 등 임상을 활발히 진행하고 있습니다.
또한, 당사는 2022년 08월 24일 당사 파이프라인 Vax-DC의 임상 2상 연구개발 조기종료를 공시한 바 있습니다. 타사들의 더욱 진보된 신약 병용요법이 개발되어 연구개발의 타당성과 투자대비 사업성이 낮을 것이라는 판단 하에 임상을 조기종료한 것으로, 당사의 주력 플랫폼 개발부문으로 핵심 연구인력을 재배치하기로 결정하였습니다.
상세 공시 내역은 아래와 같습니다.
| [당사의 투자판단 관련 주요 경영사항 공시(2022.08.24)] |
| 1. 제목 | 임상시험 연구개발 조기종료의 건 (수지상세포와 레날리도마이드/덱사메타손 병합요법 또는 레날리도마이드/덱사메타손 병합요법을 비교하는 무작위 임상 2상 연구) |
|
| 2. 주요내용 | 1. 임상시험 제목 : 수지상세포와 레날리도마이드/덱사메타손 병합요법 또는 레날리도마이드/덱사메타손 병합요법을 비교하는 무작위 임상 2상 연구 (이하 "Vax-DC") 2. 임상시험 단계 : 임상 2a/b 상 3. 대상 질환명 : 재발성 또는 불응성 다발골수종 4. 임상시험 승인일(승인처) : 2017-08-14 (2b상, 식품의약품안전처) : 2019-04-05 (2a상, 식품의약품안전처) 5. 주요내용 : 재발성/불응성 다발골수종을 대상으로 하는 대표적인 혈액암을 치료하기 위해 당사는 2017년 임상시험 승인받아 Vax-DC/MM 플렛폼을 보유하였으며 1/2a상 임상에서 77.8%라는 높은 면역학적 반응률을 보이는 등 좋은 결과를 얻었습니다. : 그러나 최근 타사들의 더욱 진보된 신약 병용요법이 개발되어 당사의 임상진행결과 보다 더 우수한 연구결과가 발표되며 발매 허가를 얻고 있는 상황입니다. : 당사는 현재기준 연구개발의 타당성과 투자대비 사업성에 대한 판단 하에 Vax-DC 플렛폼의 연구개발을 조기종료 하는 것으로 결정합니다. |
|
| 3. 사실발생(확인)일 | 2022-08-24 | |
| 4. 결정일 | 2022-08-24 | |
| - 사외이사 참석여부 |
참석(명) | 0 |
| 불참(명) | 0 | |
| - 감사(사외이사가 아닌 감사위원) 참석여부 | - | |
| 5. 기타 투자판단과 관련한 중요사항 | ||
| : 본 조기종료로 당사가 보유한 우수한 연구인력을 주력플렛폼 개발부문으로 전환하여 자연살해세포치료제 (VaxNK/HCC 등)와 Vax-DC플렛폼을 대체하는 Vax-CAR치료제 플렛폼에 집중하는 것이 수익성이 더 높다고 판단합니다. : 본 임상시험 승인은 상장일(2020.09.22.) 전 발생하여 관련 공시사항은 없습니다. |
||
| ※ 관련공시 | - | |
상기 공시는 장 마감이후 공시되어 시간 외 거래에서 하한가를 기록하였으나, 공시 다음날 주가는 소폭 회복하여 공시일 익일 종가는 전일 대비 5.06% 하락으로 마감하였습니다.Vax-DC의 임상 2상 연구개발 조기종료를 공시 이후 2개월간 당사의 주가 추이는 다음과 같습니다.
| [Vax-DC의 임상 2상 연구개발 조기종료 이후 2개월간 당사의 주가 추이] |
| 일자 | 종가 | 등락률 | 시가총액 |
| 2022/08/25 | 82,600 | -5.06 | 1조 2,574억원 |
| 2022/08/26 | 79,500 | -3.75 | 1조 2,102억원 |
| 2022/08/29 | 74,200 | -6.67 | 1조 1,295억원 |
| 2022/08/30 | 74,800 | 0.81 | 1조 1,387억원 |
| 2022/08/31 | 71,200 | -4.81 | 1조 0,839억원 |
| 2022/09/01 | 59,700 | -16.15 | 9,088억원 |
| 2022/09/02 | 60,700 | 1.68 | 9,240억원 |
| 2022/09/05 | 55,300 | -8.90 | 8,418억원 |
| 2022/09/06 | 53,700 | -2.89 | 8,175억원 |
| 2022/09/07 | 52,300 | -2.61 | 7,962억원 |
| 2022/09/08 | 52,200 | -0.19 | 7,946억원 |
| 2022/09/13 | 54,400 | 4.21 | 8,281억원 |
| 2022/09/14 | 50,600 | -6.99 | 7,703억원 |
| 2022/09/15 | 46,950 | -7.21 | 7,147억원 |
| 2022/09/16 | 45,500 | -3.09 | 6,926억원 |
| 2022/09/19 | 43,750 | -3.85 | 6,660억원 |
| 2022/09/20 | 44,100 | 0.80 | 6,713억원 |
| 2022/09/21 | 43,500 | -1.36 | 6,622억원 |
| 2022/09/22 | 42,600 | -2.07 | 6,485억원 |
| 2022/09/23 | 41,100 | -3.52 | 6,257억원 |
| 2022/09/26 | 40,250 | -2.07 | 6,127억원 |
| 2022/09/27 | 40,850 | 1.49 | 6,219억원 |
| 2022/09/28 | 39,300 | -3.79 | 5,983억원 |
| 2022/09/29 | 40,400 | 2.80 | 6,150억원 |
| 2022/09/30 | 40,300 | -0.25 | 6,135억원 |
| 2022/10/04 | 42,500 | 5.46 | 6,470억원 |
| 2022/10/05 | 39,950 | -6.00 | 6,082억원 |
| 2022/10/06 | 41,550 | 4.01 | 6,325억원 |
| 2022/10/07 | 40,150 | -3.37 | 6,112억원 |
| 2022/10/11 | 37,700 | -6.10 | 5,739억원 |
| 2022/10/12 | 38,000 | 0.80 | 5,785억원 |
| 2022/10/13 | 37,050 | -2.50 | 5,640억원 |
| 2022/10/14 | 38,950 | 5.13 | 5,929억원 |
| 2022/10/17 | 38,900 | -0.13 | 5,922억원 |
| 2022/10/18 | 40,200 | 3.34 | 6,120억원 |
| 2022/10/19 | 38,600 | -3.98 | 5,876억원 |
| 2022/10/20 | 37,100 | -3.89 | 5,648억원 |
| 2022/10/21 | 36,450 | -1.75 | 5,549억원 |
| 2022/10/24 | 37,400 | 2.61 | 5,693억원 |
| 2022-02-14 | 32,950원 | -1.49% | 5,016억원 |
| 2022-02-15 | 31,900원 | -3.19% | 4,856억원 |
출처: KRX 정보데이터시스템
당사는 기존 Vax-DC 다발골수종 치료제를 대신하여, 화순전남대학교병원 암면역치료연구센터에서 다발골수종을 대상으로 확립한 CAR-MIL 치료제 개발을 본격화하기로 결정하였으며, 화순전남대학교병원 암면역치료연구센터와 업무협약을 체결하고 MIL 관련 연구 내용과 그를 이용한 다발골수종 치료법을 2개의 국제학회(국제다발골수종학회 연례 모임(International Myeloma Society Annual Meeting) / 대한조혈모세포이식학회 국제학술대회(ICBMT 2022)) 를 통해 발표하였습니다. 또한, 다발골수종에 특이성이 높은BCMA항원을 도입하여 2024년 임상연구 진입을 목표로 BCMA-CAR-T세포 치료제에 대한 공정개발을 수행하고 있을 뿐만 아니라 후속으로BCMA-CAR-MIL 치료제도 개발 중입니다.
또한, 당사는 2023년 07월 31일 당사 파이프라인 Vax-NK/HCC에 진행성 췌장암 적응증을 추가하여 임상 2a상 변경승인 신청을 하였습니다. 기존에 정기보고서에서 기재했던 바와 같이 mFOLFIRINOX 요법과 병용 치료하여 비임상시험이 완료되었던 파이프라인이며 약 20명을 대상, 무진행 생존기간을 1차 지표로 활용하여 진행하고자 합니다. 해당 공시는 적응증 추가 신청에 관련된 내용으로 주가에 급등락을 발생시키지는 않았으나, 향후 임상 진행 과정에서 중단 또는 성공등의 사유가 발생 시에는 주가 급등락이 이루어질 수 있습니다.
| [당사의 투자판단 관련 주요 경영사항 공시(2023.07.31)] |
| 1. 제목 | 진행성 췌장암 환자에서 자연살해세포와 mFOLFIRINOX 병합치료의 임상 2a상 연구 | |
| 2. 주요내용 | 1) 임상시험명칭 | 진행성 췌장암 환자에서 자연살해세포와 mFOLFIRINOX 병합치료의 임상 2a상 연구 |
| 2) 임상시험단계 | 2a상 | |
| 3) 임상시험승인기관 | 식품의약품안전처 | |
| 4) 임상시험실시국가 | 대한민국 | |
| 5) 임상시험실시기관 | - 가톨릭대학교 서울성모병원 - 화순전남대학교병원 - 분당서울대병원 - 분당차병원 |
|
| 6) 대상질환 | 진행성 췌장암 | |
| 7) 변경승인신청일 | 2023-07-31 | |
| 8) 등록번호 | 30786 | |
| 9) 임상시험 목적 | 이전에 화학요법으로 치료받은 적인 없는 진행성 췌장암 환자에 대해 1차 치료법으로 Vax-NK/HCC와 mFOLFIRINOX 병합요법의 유효성 및 안전성을 평가하기 위함입니다. | |
| 10) 임상시험 방법 | 본 임상시험은 mFOLFIRINOX, Vax-NK/HCC 투여 후 유효성 및 안전성을 평가하기 위한 다기관, 공개, 단일군 2a상 임상시험입니다. 1) 스크리닝 및 Vax-NK/HCC 제조: 스크리닝 과정동안에 선정된 대상자의 경우 백혈구분반술(leukapheresis)을 통해 임상시험용 의약품인 Vax-NK/HCC를 제조합니다. 2) mFOLFIRINOX 단독투여: mFOLFIRINOX(옥살리플라틴+이리노테칸+류코보린+5-플루오로우라실)는 Visit 3에 시작하여 질병의 진행(PD) 또는 수용 불가능한 독성(unacceptable toxicity)이 있을 때까지 투여되며, 1주기는 2주로 구성됩니다. 3) mFOLFIRINOX, Vax-NK/HCC 병용투여: Vax-NK/HCC는 Visit 4에 시작하여 총 3주기(2, 4, 6주기)까지 투여된다. 1주기당 매일 1회 총 3일 동안 투여되며, 1주기는 4주로 구성됩니다. |
|
| 11) 1차 지표 | 무진행 생존기간 (progression free survival, PFS) |
|
| 12) 1차 지표 통계분석방법 | 무진행 생존기간(PFS)는 첫 mFOLFIRINOX 투여 시작 날짜로부터 기록으로 입증된 객관적인 질병의 진행(PD)까지의 일수로 정의하며, Kaplan-Meier 분석법(Kaplan-Meier method)을 이용하여 그래프를 제시하고, 중앙값에 도달한 경우, 그 값과 양측 95% 신뢰구간을 제시한다. | |
| 13) 임상시험기간 | 식품의약품안전처 또는 임상시험심사위원회 승인일로부터 약 24개월 (단, 시험대상자 등록 속도에 따라 연장될 수 있음) |
|
| 14) 목표 시험대상자 수 | 약 20명 | |
| 3. 변경신청 사유 | 임상시험추가 (사유: 새로운 적응증 추가) | |
| 4. 사실발생(확인)일 | 2023-07-31 | |
| 5. 기타 투자판단과 관련한 중요사항 | ||
| - 상기 사실발생(확인)일은 한국 식품의약품안전처(MFDS)에 임상시험계획 변경승인신청 (IND)을 한 날짜입니다. - 추후 임상시험계획 승인 시 관련 공시를 즉시 제출하겠습니다. - 본 공시 내용은 향후 당사의 보도자료 및 IR 자료로 사용될 예정입니다. |
||
| ※ 관련 공시 | - | |
| [Vax-NK/HCC 적응증 추가 승인신청 공시 이후 2주간 당사의 주가 추이] |
| 일자 | 종가 | 등락률 | 시가총액 |
|---|---|---|---|
| 2023/08/01 | 38,300 | 5.08 | 5,830억원 |
| 2023/08/02 | 35,600 | -7.05 | 5,419억원 |
| 2023/08/03 | 36,850 | 3.51 | 5,610억원 |
| 2023/08/04 | 36,200 | -1.76 | 5,511억원 |
| 2023/08/07 | 34,900 | -3.59 | 5,313억원 |
| 2023/08/08 | 28,250 | -19.05 | 4,300억원 |
| 2023/08/09 | 31,850 | 12.74 | 4,849억원 |
| 2023/08/10 | 31,650 | -0.63 | 4,818억원 |
| 2023/08/11 | 31,850 | 0.63 | 4,849억원 |
| 2023/08/14 | 30,800 | -3.30 | 4,689억원 |
출처: KRX 정보데이터시스템
당사의 이러한 노력에도 불구하고 임상시험 약물이 의약품으로 최종 허가받을 확률은 통계적으로 약 10% 수준에 불과합니다. 임상시험 및 품목허가 과정에서 기대에 상응하지 못하는 결과가 나올 수 있으며, 이에 따라 당사가 상업화 계획을 변경하거나 포기할 수 있는 가능성도 상존합니다. 투자자는 수시공시 및 사업보고서 등을 통해 공시된 투자 위험을 종합적으로 고려하여 신중히 투자하시기 바랍니다.
특히 이와 같이 임상의 진행 중 경과가 당사 기업가치와 주가에 중요한 영향을 끼치고 있기에 투자자께서는 이점 유의하시기 바랍니다.
|
사. 정부 연구개발 과제 수행 관련 위험 당사는 설립 이래 총 8건의 정부과제를 성공적으로 수행 완료하였으며, 현재 2건의 정부 과제에 대해서도 특이사항 없이 진행 중에 있습니다. 당사는 이와 같은 정부과제의 성공적인 수행 및 진행을 통해 당사 연구개발에 필요한 자금 중 상당 부분을 충당하여 왔습니다. 따라서 당사는 향후에도 사업과 관련된 정부 출연 연구개발 과제에 적극적으로 지원할 예정입니다. 정부과제 수행에 따른 목적이탈 사항의 부존재와 합법적인 이행시 상환위험은 존재하지 않습니다.
|
당사는 설립 이래 총 8건의 정부과제를 성공적으로 수행 완료 하였으며, 현재 진행중인 2건의 정부 과제에 대해서도 특이사항 없이 진행 중에 있습니다. 당사는 이와 같은 정부과제의 성공적인 수행 및 진행을 통해 당사 연구개발에 필요한 자금 중 상당 부분을 충당하여 왔습니다. 따라서 당사는 향후에도 사업과 관련된 정부 출연 연구개발 과제에 적극적으로 지원할 예정입니다. 정부과제 수행에 따른 목적이탈 사항의 부존재와 합법적인 이행시 상환위험은 존재하지 않습니다.
| [당사 정부과제 수행 실적 현황] |
| (단위: 천원) |
|
해당 파이프라인 |
구분 |
사업명 |
과제명 |
주관부처 |
연구기간 |
사업비총액 |
성과 |
과제 |
|
Vax-NK |
중앙정부 |
사업화연계 |
간암치료제로써 Vax-NK/HCC의 안전성 및 항암효과 평가 |
산업통상 |
2016.07.01 |
1,995,620 |
임상2상 |
보통 |
|
중앙정부 |
창업성장 |
간암치료용 자연살해세포치료제 (Vax-NK)의 안전성 및 유효성 평가 |
중소기업청 |
2014.05.22 |
206,000 |
비임상 시험 |
성공 |
|
|
Vax-DC |
지방정부 |
지역수요맞춤형 |
다발골수종 특이 재조합 종양항원을 이용한 자가 수지상세포 항암백신의 안정성 평가 |
(재)전남 |
2018.06.01 |
202,500 |
장기보존시험 |
성공 |
|
지방정부 |
지역산업 |
항암백신으로서 강력한 자가 수지상세포치료제인 Vax-DC의 안전성 및 유효성 평가 |
한국산업 |
2011.04.01 |
480,000 |
임상1/2a상 |
성공 |
|
|
지방정부 |
전남생물산업 |
Vax-DC의 품질관리 시험법 확립 |
전남생물산업 |
2012.03.14 |
37,500 |
Vax-DC완제품 |
완료 |
|
|
지방정부 |
전남생물산업 |
혈액암 치료를 위한 강력한 자가수지상 세포치료제 개발 |
전남생물산업 |
2011.04.04 |
34,500 |
세포치료제 개발 전략 수립 |
완료 |
|
|
Vax-DC 및 |
중앙정부 |
예비기술창업자 |
혈액암을 치료하기 위한 차세대 강력한 암면역세포치료제 개발 |
전남대학교 |
2010.03.10 |
70,000 |
비임상(효력시험) |
성공 |
|
박스루킨15 |
중앙정부 |
기술혁신 |
재조합 단백질 IL-15를 이용한 동물용 항암면역증강제 개발 |
중소기업청 |
2016.09.01 |
800,000 |
비임상/임상시험 완료 |
성공 |
|
Vax-NK 및 Vax-CAR |
중앙정부 지원과제 |
바이오·의료기술개발 |
면역치료 혁신센터 |
과학기술 정보통신부 |
2020.06.01 |
47,375,000 (23,000,000) |
진행중 |
진행중 |
|
동물용 의약품 |
중앙정부 지원과제 |
반려동물전주기산업화기술개발사업 |
항암 면역치료를 위한 개 키메라항원수용체-자연살해세포(CAR-NK cells) 치료제 및 개발 |
농림축산식품부 |
2022.04.01 |
3,331,500 (3,000,000) |
진행중 |
진행중 |
| 출처: 당사 정기보고서 (주1) 본 정부과제는 당사 파이프라인에 산입되기 전의 기초연구단계로 공주대학교와 공동연구를 진행하고 있습니다. |
특히, 당사는 과학기술정보통신부가 공모하여 전남대학교가 주관기관으로 선정된 '면역치료 혁신 플랫폼 구축'과제의 제3세부 '실용화 연구단'의 책임기업으로서, 해당 연구과제에서 임상개발을 이끄는 역할을 맡아 연구비를 지원받고 있으며, 차세대 파이프라인 개발의 추가 동력 확보와 면역치료 분야 선도 기업이라는 이미지 제고 및 홍보 효과를 누릴 수 있을 것으로 기대하고 있습니다. 연구개발이 시작된 2020년부터 2023년 상반기까지 해당 연구개발비 사용실적은 다음과 같습니다.
| [<면역치료 실용화 연구단> 연구개발비 사용실적 현황] |
| (단위: 천원) |
| 연도 | 정부출연금 | 민간부담금 | 합계 | ||||
|---|---|---|---|---|---|---|---|
| 현금 | 현물 | 현금 | 현물 | 현금 | 현물 | 합계 | |
| 2020년 | 520,000 | - | 17,400 | 156,600 | 537,400 | 156,600 | 694,000 |
| 2021년 | 570,000 | - | 19,000 | 171,000 | 589,000 | 171,000 | 760,000 |
| 2022년 | 1,100,000 | - | 31,670 | 322,530 | 1,131,670 | 322,539 | 1,454,200 |
| 2023년 상반기 |
1,150,000 | - | 16,000 | 144,000 | 1,166,000 | 144,000 | 1,310,000 |
| 주) 민간부담금은 당사가 부담하는 재원입니다. 주) 현물의 경우 당사 기존 보유 자산으로 원재료, 시약, 참여연구원 인건비 등으로 계상하였습니다. |
또한 지난 2022년 04월, 농림축산식품부의 반려동물전주기산업화기술개발사업에 공주대학교 산학협력단이 주관기관으로 선정된 '항암 면역치료를 위한 개 키메라항원수용체-자연살해세포(CAR-NK cells) 치료제 및 개 면역관문저해제(immune-checkpoint inhibitor) 개발' 과제에 공동연구개발기관의 역할로 연구를 수행하고 있습니다. 해당 연구과제를 통해 차세대 반려동물 전용 항암면역치료 플랫폼을 확장시킬 수 있으며, 유례없는 반려동물용 CAR-NK 개발을 통해 항암면역치료 개발 전문회사로서 입지를 다질 수 있을 것으로 기대합니다.
하지만 향후 당사의 신약개발 파이프라인에 대한 국책과제 추가 선정의 불확실성, 현재 진행중인 과제의 실패에 따른 과제 참여의 제한, 정부의 정책 변화에 따른 국고보조금의 감소 등은 지속적으로 자금이 투입되어야 하는 당사의 연구개발활동에 부정적인 영향을 미칠 수 있습니다. 특히, 현행 제도 상 정부 출연 연구개발 과제는 최종 목표달성에 실패하더라도 성실 수행을 입증할 수 있는 경우에는 제제 조치를 면제 받을 수 있으나, 불성실 수행으로 연구개발의 결과가 극히 불량하여 최종 평가 시 실패 과제로 결정된 경우에는 정부로부터 받은 지원금의 전부 혹은 일부의 환수 또는 향후 정부출연과제 참여 제한의 제제 조치가 가해질 수 있음을 투자판단에 참고하시기 바랍니다.
| 아. 분쟁에 따른 우발채무 등에 관한 위험 당사는 증권신고서 작성기준일 현재 당사의 영업에 중대한 영향을 미치는 소송 등의 분쟁 사항은 없습니다. 하지만 향후 당사의 연구개발 파이프라인이 확대되고, 임상 단계가 고도화 및 기술 이전 계약 등이 본격적으로 협의될 경우, 다양한 이해관계자들 간 권리 분쟁 등이 발생할 가능성을 배제할 수 없습니다. 이 경우, 당사 기술과 관련된 특허권 분쟁, 핵심인력 유출입, 임직원 및 관련자가 당사에 중대한 손해를 입히는 경우 등과 관련된 다양한 종류의 분쟁 또는 소송이 발생할 수 있습니다. 법률 분쟁은 통상적으로 장기간에 걸쳐 진행되며, 사안에 따라 매우 큰 규모의 분쟁이 될 경우 큰 규모의 소송비용이 발생할 수 있습니다. 당사는 법률위반으로 인한 리스크를 회피하고자 내부회계관리제도를 운영중이며, 2023년 이후 외부감사인이 아닌 회계법인 등 전문기관을 통하여 법률검토/자문을 진행할 계획을 가지고 있습니다. 다만, 소송이나 분쟁, 예상치 못한 법률적 리스크가 발생할 경우 당사의 영업 및 재무구조에 부정적인 영향을 미칠 수 있으므로 투자자께서는 이 점 유의하시고 투자에 임하시길 바랍니다. |
당사는 증권신고서 작성기준일 현재 당사의 영업에 중대한 영향을 미치는 소송 등의 분쟁 사항은 없습니다. 하지만 향후 당사의 연구개발 파이프라인이 확대되고, 임상 단계가 고도화 및 기술 이전 계약 등이 본격적으로 협의될 경우, 다양한 이해관계자들 간 권리 분쟁 등이 발생할 가능성을 배제할 수 없습니다. 이 경우, 당사 기술과 관련된 특허권 분쟁, 핵심인력 유출입, 임직원 및 관련자가 당사에 중대한 손해를 입히는 경우 등과 관련된 다양한 종류의 분쟁 또는 소송이 발생할 수 있습니다.
법률 분쟁은 통상적으로 장기간에 걸쳐 진행되며, 사안에 따라 매우 큰 규모의 분쟁이 될 경우 큰 규모의 소송비용이 발생할 수 있습니다. 당사는 법률위반으로 인한 리스크를 회피하고자 내부회계관리제도를 운영중이며, 2023년 이후 외부감사인이 아닌 회계법인 등 전문기관을 통하여 법률검토/자문을 진행할 계획을 가지고 있습니다. 다만, 소송이나 분쟁, 예상치 못한 법률적 리스크가 발생할 경우 당사의 영업 및 재무구조에 부정적인 영향을 미칠 수 있으므로 투자자께서는 이 점 유의하시고 투자에 임하시길 바랍니다.
| 자. IPO 당시 추정 손익과 실제 손익과의 차이 관련 위험 당사의 2020년 기업공개 당시 당사가 제출한 증권신고서에 기재된 추정 손익계산서에 따르면, 매출은 2021년부터 시현하여 2021년 매출액 2,711백만원, 2022년 12,687백만원, 2023년 15,538백만원, 2024년 88,185원을 기록, 영업이익은 2020년 -7,223백만원, 2021년 -10,740백만원, 2022년 -317백만원, 2023년 -2,580백만원, 2024년 58,923백만원을 기록, 당기순이익은 2020년 -7,136백만원, 2021년 -10,420백만원, 2022년 -109백만원, 2023년 -2,360백만원, 2024년 52,150백만원을 기록할 것으로 예상하였습니다. 2021년~2022년 매출 예상치에는 Vax-DC, NK+DC, CAR-T, mCAR-T의 미국 기술이전 기술료와 박스루킨-15의 판매매출이 산정되어 있습니다. 이 중 박스루킨-15의 경우 품목허가 과정에서 통계적 유의성 확인의 필요성이 제기되어 자친철회 후 추가연구를 진행하고 있으며 2023년 중으로 추가연구를 마무리하고 2024년에 제품 판매계획을 가지고 있습니다. Vax-DC와 NK+DC의 경우 당사의 파이프라인 전략 수정으로 Vax-DC 파이프라인은 중단하고 VAX-CARs 파이프라인 개발에 집중하고 있습니다. 또한 VAX-CAR-T 및 VAX-mCAR-T의 경우 현재 비임상 진행으로 매출 계획이 지연되었습니다. 이에 따라 2,711백만원과 12,687백만원 규모의 매출이 발생할 것이라고 예상했던 2021년과 2022년에는 매출을 시현하지 못하였습니다. 2021년~2022년 매출 예상치에는 Vax-DC, NK+DC, CAR-T, mCAR-T의 미국 기술이전 기술료와 박스루킨-15의 판매매출이 산정되어 있습니다. 이 중 2021년 매출이 발생할 것으로 예상했던 동물용의약품 박스루킨-15의 경우, 2020년 하반기에 품목허가를 접수하였고 2021년 초에 품목허가 승인과 동시에 국내 제품 출시 계획을 하고 있었습니다. 그러나 예상치 못하게 검역본부와의 협의 과정에서, 품목허가 신청을 자진철회하고 추가적인 임상연구를 수행하게 되어 박스루킨-15의 출시 시점이 미뤄지게 되었습니다. 박스루킨-15는 반려동물 전용 항암면역치료제로 검역본부에서도 전례가 없는 케이스였기 때문에, 임상시험 계획서를 승인받는 과정에서도 충분히 논의를 거쳐서 진행한 바 있습니다. 그러나 점차 반려동물에 대한 산업의 관심도가 높아지면서, 검역본부에서도 식약처의 기준에 따라 관련 규정이 더욱 까다로워 지는 등의 변화가 있었습니다. 최초 임상시험계획 승인 당시에는 15마리 이상의 환견 수로 승인받았고, 해당 마리 수에 대한 데이터로 품목허가를 신청하였으나, 당사가 품목허가를 신청한 시기에는 검역본부 판단에 모수가 부족하다는 의견을 전달받았고 통계적 유의성을 확보하기 위하여 추가 연구를 진행하라는 사항을 포함해 몇 가지 보완사항이 발생하였습니다. 결국 추가적인 임상시험을 진행해야 하는 까닭에, 예상 출시 시점이 미루어져 예상했던 매출 계획이 지연되었습니다. 현재는 유선종양 대조군 포함 60마리, 림프종 대조군 포함 60마리로 총 120마리에 대한 임상시험을 진행하고 있으며, 유선종양 대상 연구는 최종 투여가 마무리되고 모니터링 중에 있습니다. 연내 모니터링 및 분석을 마치고 품목허가를 재신청할 계획입니다. Vax-DC와 NK+DC의 경우 당사의 파이프라인 전략 수정으로 Vax-DC 파이프라인은 중단하고 VAX-CARs 파이프라인 개발에 집중하고 있습니다. 본 증권신고서 사업위험 라. 에 기재한 바와 같이 VAX-CARs의 연구개발에 집중하는 것이 투자 대비 효율성 제고에 도움이 될 것이라고 판단하였기 때문입니다. 이에따라 DC 파이프라인 관련된 예상 매출은 시현하지 못하였습니다. 또한 VAX-CAR-T 및 VAX-mCAR-T의 경우 현재 비임상 진행으로 매출 계획이 지연되었습니다. 이에 따라 2,711백만원과 12,687백만원 규모의 매출이 발생할 것이라고 예상했던 2021년과 2022년에는 매출을 시현하지 못하였습니다. 이와 더불어 당사는 IPO신고서 제출 당시 Vax-NK에 대한 타임라인을 '22년~'24 년 2b상으로 제시하였습니다. 그러나 증권신고서 제출일 현재 Vax-NK는 2a상을 진행중이며, 과거에 예상했던 Vax-NK관련 매출 역시 지연될 가능성이 높습니다. Vax-NK 관련 타임라인이 지연된 사유는 다음과 같으며, 임상연구 진행 현황은 다음과 같습니다. 첫 환자는 20년 초에 등록되었으나, 임상시험계획서에 기재된대로 환자를 선정하는데는 까다로운 기준이 정해져 있기에 모든 진행성간암 환자가 임상 시험 대상자가 될 수 없었고, 대상자 선정 과정에서 환자가 선정대상에서 탈락될 가능성 등이 있어 계획한 일정보다 더디게 진행되었습니다. Vax-NK/HCC는 임상1상과 달리 임상2a상에서는 '공고요법'을 추가하면서 1주기 투여 4주 후 2주기로 한 번 더 주입하는 방식으로 디자인을 변경하였습니다. 이 과정에서 식약처와 논의한 결과, 처음 3명의 환자에 대한 안전성 심의 위원회를 거친 뒤 남은 임상시험을 진행하기로 결정하였습니다. 그리고 안전성 심의 위원회가 통과(21년 06월)된 후, 본격적으로 임상시험에 속도를 내기 위하여 기존 임상시험 실시기관 2곳에 3곳을 추가하여 총 5개 기관에서 임상시험을 진행하였으며 안전성을 한 번 더 입증하여 각 연구자분들께서 더욱 더 적극적으로 연구에 참여하게 되었습니다. 2022년 9월, 12명의 환자에 대한 데이터를 바탕으로 예비연구결과를 발표하였으며, 2023년 8월 기준 17번째 환자에 대한 임상시험용 의약품 투여를 완료하고 모니터링 중에 있습니다. 임상2a상은 17번째 환자를 마지막으로 임상시험 참여자 모집을 완료하고자 하며, 향후 예정된 종료를 위한 절차를 진행할 예정입니다. 상기와 같이 당사는 기업공개를 위한 공모 당시 당사의 적정주가를 도출하기 위해 제시한 당사의 추정손익과 현재 영업을 통해 달성한 실현 손익 간 괴리를 보이고 있습니다. 이는 당사와 같이 신약개발에 특화 된 바이오벤처 기업 특성상 개발하고 있는 신약 등 파이프라인에 대한 성공 가능성 및 라이선스 아웃 계약 가능성을 합리적으로 예상하는데는 제약이 존재함을 시사합니다. 투자자께서는 이 점 유의하시기 바랍니다. |
당사의 2020년 기업공개 당시 당사가 제출한 증권신고서에 기재된 추정 손익계산서에 따르면, 매출은 2021년부터 시현하여 2021년 매출액 2,711백만원, 2022년 12,687백만원, 2023년 15,538백만원, 2024년 88,185원을 기록, 영업이익은 2020년 -7,223백만원, 2021년 -10,740백만원, 2022년 -317백만원, 2023년 -2,580백만원, 2024년 58,923백만원을 기록, 당기순이익은 2020년 -7,136백만원, 2021년 -10,420백만원, 2022년 -109백만원, 2023년 -2,360백만원, 2024년 52,150백만원을 기록할 것으로 예상하였습니다. 기업공개 당시 추정한 5개년 손익계산서의 세부 내역은 다음과 같습니다.
| [기업공개(IPO)당시 2020년~2024년 추정 손익계산서] |
| (단위: 백만원) |
| 구분 | 2020년(E) | 2021년(E) | 2022년(E) | 2023년(E) | 2024년(E) |
| (제11기) | (제12기) | (제13기) | (제14기) | (제15기) | |
| 매출액 | - | 2,711 | 12,687 | 15,538 | 88,185 |
| 매출원가 | - | - | - | 2,584 | 12,097 |
| 매출총이익 | - | 2,711 | 12,687 | 12,954 | 76,088 |
| 판매비와관리비 | 7,223 | 13,451 | 13,003 | 15,533 | 17,165 |
| 영업이익(손실) | (7,223) | (10,740) | (317) | (2,580) | 58,923 |
| 영업외수익 | 87 | 320 | 208 | 220 | 194 |
| 영업외비용 | - | - | - | - | - |
| 법인세비용차감전순이익(손실) | (7,136) | (10,420) | (109) | (2,360) | 59,117 |
| 법인세비용 | - | - | - | - | 6,967 |
| 당기순이익(손실) | (7,136) | (10,420) | (109) | (2,360) | 52,150 |
| 출처: 당사 정정 증권신고서(2020.08.31) |
당사는 항암면역치료제를 연구개발하는 기업으로서, 각 파이프라인 별 사업 계획을 기초로 하여 기업공개(IPO) 당시 추정 매출액을 자체 제조 및 판매에 따른 제품매출과 글로벌 제약사로의 기술이전(라이선스 아웃)에 따른 기술료 수익으로 구분하여 추정하였습니다. 상장 당시 당사의 파이프라인 연구개발 현황 및 계획과 매출액 추정 세부내역은 다음과 같습니다.
| [기업공개(IPO) 당시 파이프라인 연구개발 현황 및 계획] |
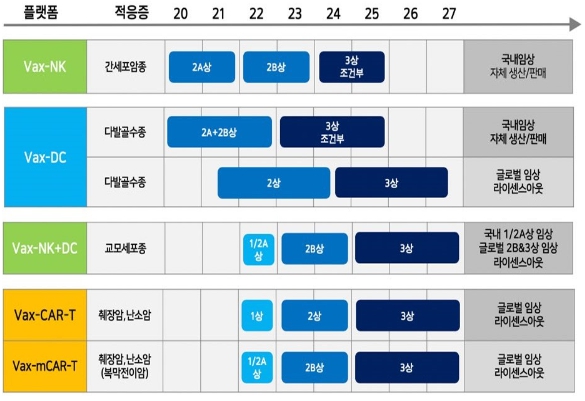 |
|
출처: 당사 정정 증권신고서(2020.08.31) |
| 출처: 당사 정정 증권신고서(2020.08.31) |
| [기업공개(IPO) 당시 2020년 ~ 2024년 매출액 추정 세부내역] |
| (단위: 백만원) |
| 구분 | 파이프라인명 | 적응증 | 지역 | 2020년(E) | 2021년(E) | 2022년(E) | 2023년(E) | 2024년(E) |
| 제품매출 | Vax-NK | 간세포암 | 국내 | - | - | - | - | 26,733 |
| Vax-DC | 다발골수종 | 국내 | - | - | - | 8,468 | 16,581 | |
| 기술료수익 | Vax-DC | 다발골수종 | 미국 | - | 2,661 | - | - | 5,323 |
| Vax-NK+DC | 교모세포종 | 미국 | - | - | 2,759 | 1,830 | 10,169 | |
| Vax-CAR-T | 췌장암 난소암 |
미국 | - | - | 1,362 | - | 2,725 | |
| Vax-mCAR-T | 췌장암 난소암 |
미국 | - | - | 7,593 | 1,592 | 18,823 | |
| 박스루킨-15 | 반려견의 암 | 국내 | - | 49 | 207 | 617 | 1,209 | |
| 반려견의 암 | 미국 | - | - | 766 | 3,030 | 6,622 | ||
| 합계 | - | 2,711 | 12,687 | 15,538 | 88,185 | |||
| 출처: 당사 정정 증권신고서(2020.08.31) |
1. 제품매출 추정
IPO 당시 당사의 제품매출은 아래와 같은 방식으로 추정하였습니다.
먼저, 각 파이프라인 적응증의 연도별 국내 환자수를 추정한 후, 회사가 설정한 시장점유율 목표치를 적용하여 목표 환자수를 산출하였습니다. 그리고, 목표 환자수에 환자 1인당 치료제 판매가격을 곱한 후, 연도별 임상 성공확률을 적용하여 매출액을 추정하였습니다. 또한, Vax-NK 자연살해세포 항암면역치료제 플랫폼과 Vax-DC 수지상세포 항암면역치료제 플랫폼은 국내에서 직접 생산하고 판매하는 것을 목표로 하였으며, 국내 임상2상 종료 후 3상조건부판매승인을 받는 것을 가정하였습니다.
1-1) Vax-NK 제품매출
Vax-NK 파이프라인은 2023년에 임상2b상을 종료한 후, 2024년에 3상조건부판매승인을 받아 제품매출이 발생하는 것을 가정하였습니다. Vax-NK의 연도별 매출액 추정의 세부 내용은 아래와 같습니다.
| [기업공개(IPO) 당시 Vax-NK의 연도별 매출액 추정 세부 내용] |
| (단위: 명, 백만원) |
| 구분 | 2020년(E) | 2021년(E) | 2022년(E) | 2023년(E) | 2024년(E) | 비고 |
| 임상단계 | 임상 2a상 | 임상 2a상 | 임상 2b상 | 임상 2b상 | 임상 3상 | - |
| 시장점유율 | - | - | - | - | 2.00% | - |
| 간암 환자수(A) | 65,591 | 67,938 | 70,370 | 72,889 | 75,498 | CAGR 3.58%적용 |
| 간세포암 환자수(B) | 49,062 | 50,818 | 52,637 | 54,521 | 56,473 | B=Ax74.8% |
| 재발환자수(C) | 34,343 | 35,572 | 36,846 | 38,165 | 39,531 | C=Ax70% |
| 목표환자수(D) | - | - | - | - | 790 | D=Cx시장점유율 |
| 매출액(E) | - | - | - | - | 26,733 | E=Dx8천만원x임상성공확률 |
| 출처: 당사 정정 증권신고서(2020.08.31) |
주1) 시장점유율은 점유율 목표치를 10%로 설정하고, 2024년부터 점유율이 단계적으로 증가하여 2029년에 목표치를 달성하는 것으로 가정하였습니다. 제품 출시 첫해인 2024년은 환자수 약 800명에 해당하는 2%의 시장점유율을 가정하였습니다.
주2) 국내 간세포암 환자수는 '보건의료빅데이터개방시스템'에서 산출한 2014년부터 2019년까지의 국내 간암환자수의 연평균성장률(3.58%)을 바탕으로 2020년~2024년까지의 국내 간암환자수를 추정한 후, '대한간학회지(제11권 제4호, 2005년)'에서 발췌한 국내 간암환자수 대비 간세포암환자수의 비율인 74.8%를 적용하여 산출하였습니다.
주3) 'The New England Journal of Medicine'에 게재된 'Article(Recurrence of Hepatocellular Carcinoma)'에서 발췌한 간세포암의 재발률 70%를 적용하여 간세포암 재발환자수를 목표환자수로 설정하였습니다.
주4) 환자 1인당 치료제 판매가격은 현재 간암에 대해 항암보조치료용으로 품목허가를 받아 판매중인 이뮨셀-엘씨의 가격(1회 투여 가격 약 500만원, 16회 투여)을 참고하여 8,000만원(환자 1인당 총 10회 주사 시의 판매가격)으로 가정하였습니다.
주5) 단계별 누적 임상성공확률은 아래와 같은 항암제의 임상 성공확률을 토대로 계산하여 적용하였습니다. Vax-NK의 경우 3상조건부판매승인을 허가 받는 시점(2024년)의 누적 임상성공확률은 42.3% x 54.7% x 82.8% = 19.2%를 적용하였습니다.
| 구분 | 임상1상 → 2상 |
임상2상 → 3상 |
임상3상 → NDA/BLA 신청 |
NDA/BLA 신청 → NDA/BLA 승인 |
임상1상 → NDA/BLA 승인 |
| 단계별 성공확률 | 68.9% | 42.3% | 54.7% | 82.8% | 13.2% |
출처: Nature Biotechnology, 2014, 32, 40-51
1-2) Vax-DC 제품매출
Vax-DC 파이프라인은 2022년에 임상2상(2a 및 2b)을 종료한 후, 2023년에 3상조건부판매승인을 받아 제품매출이 발생하는 것을 가정하였습니다. Vax-DC의 연도별 매출액 추정의 세부 내용은 아래와 같습니다.
| [기업공개(IPO) 당시 Vax-DC의 연도별 매출액 추정 세부 내용] |
| (단위: 명, 백만원) |
| 구분 | 2020년(E) | 2021년(E) | 2022년(E) | 2023년(E) | 2024년(E) | 비고 |
| 임상단계(예상) | 임상2상* | 임상2상* | 임상2상* | 임상 3상 | 임상 3상 | - |
| 시장점유율 | - | - | - | 2.00% | 3.60% | - |
| 다발골수종 환자수(A) | 8,750 | 9,504 | 10,323 | 11,212 | 12,178 | CAGR 8.62%적용 |
| 재발환자수(B) | 6,445 | 7,000 | 7,603 | 8,258 | 8,970 | B=Ax80% |
| 재재발환자수(C) | 4,744 | 5,156 | 5,600 | 6,083 | 6,607 | C=전년도 재발환자수X80% |
| 목표환자수(D) | - | - | - | 286 | 560 | D=(B+C)x시장점유율 |
| 매출액(E) | - | - | - | 8,468 | 16,581 | E=Dx7천만원x임상성공확률 |
(*) 임상2상(임상2a 및 임상2b)
| 출처: 당사 정정 증권신고서(2020.08.31) |
주1) 시장점유율은 점유율 목표치를 10%로 설정하고 2023년부터 점유율이 단계적으로 증가하여 2028년에 목표치를 달성하는 것으로 가정하였습니다. 제품 출시 첫해인 2023년은 환자수 약 300명에 해당하는 2%의 시장점유율을 가정하였습니다.
주2) 국내 다발골수종 환자수는 '보건의료빅데이터개방시스템'에서 산출한 2014년부터 2019년까지의 국내 다발골수종 환자수의 연평균성장률(8.62%)을 바탕으로 2020년~2024년까지의 환자수를 추정하였습니다.
주3) 다발골수종의 재발률은 거의 대부분 재발(incurable)하지만 20%의 생존율을 보이는 점('Leukemia 2010, 24, 623-628'에서 발췌)과 일부 환자가 치료에서 이탈하는 경우를 감안하여 80%로 가정하였으며, 치료후에도 재발이 반복되는 다발골수종의 특성을 반영하여 재재발환자수(전년도 재발환자수의 80%)를 목표 환자수에 추가하였습니다.
주4) 환자 1인당 치료제 판매가격은 '건강보험정책심의위원회의 가이드라인(고시단가 기준 1년간 사용 약가 합산액은 1인당 GDP의 2배수 이하로 한다)'을 참고하여 2019년 한국 1인당 GDP의 2배수(31,791$ X 2 = 73,119천원, 1$ = 1,150원 가정) 대비 소폭 하회하는 금액인 7,000만원(환자 1인당 총 6회 주사 시의 판매가격)으로 가정하였습니다.
주5) 단계별 누적 임상성공확률은 아래와 같은 항암제의 임상 성공확률을 토대로 계산하여 적용하였습니다. Vax-DC의 경우 3상조건부판매승인을 허가 받는 시점(2023년)의 누적 임상성공확률은 42.3% x 54.7% x 82.8% = 19.2%를 적용하였습니다.
| 구분 | 임상1상 → 2상 |
임상2상 → 3상 |
임상3상 → NDA/BLA 신청 |
NDA/BLA 신청 → NDA/BLA 승인 |
임상1상 → NDA/BLA 승인 |
| 단계별 성공확률 | 68.9% | 42.3% | 54.7% | 82.8% | 13.2% |
출처: Nature Biotechnology, 2014, 32, 40-51
2. 기술료 수익 추정
2-1) 라이선스 아웃
당사는 Vax-DC, Vax-NK+DC 병용투여, Vax-CAR 시리즈 파이프라인에 대해 미국시장을 대상으로 한 라이선스아웃을 목표로 하였으며, 각 파이프라인은 FDA의 희귀의약품 지정(Orphan Drug Designation, ODD) 또는 첨단 재생의학 치료제(Regenerative Medicine Advanced Therapy, RMAT) 지정 제도를 활용하여 우선 심사(Priority Review) 및 가속 승인(Accelerated Approval)을 통해 심사기간 단축 및 조기에 로열티 수익을 시현하는 것을 가정하였습니다.
먼저 Vax-DC는 국내 임상2a상 데이터를 토대로 2021년에 미국시장을 대상으로 한 라이선스 아웃을 가정하였습니다. 또한, Vax-NK와 Vax-DC 플랫폼을 병용하여 대표적인 난치성 고형암 중 하나인 교모세포종으로 적응증을 확대할 계획을 가졌으며, 국내에서 임상1/2a상을 진행한 후, 이를 바탕으로 2022년 말에 미국시장을 대상으로 한 라이선스아웃을 목표로 삼았습니다. 마지막으로, 췌장암, 난소암 등의 고형암에서 주로 발현하는 암특이 단백질인 EphA2와 메소텔린(mesothelin, MSLN)을 타겟으로 한 Vax-mCAR-T/EphA2와 Vax-CAR-T/MSLN의 2개의 Vax-CAR 시리즈 파이프라인을 통해 2021년에 두 파이프라인의 비임상 연구결과를 마무리 짓고, 2022년에 전임상 단계에서 미국시장을 대상으로 한 라이선스아웃을 가정하였습니다.
위의 내용을 바탕으로 IPO 당시 파이프라인별 라이선스아웃 계획 및 추정 기술료 수익의 상세내역은 아래와 같습니다.
| [기업공개(IPO) 당시 파이프라인별 라이선스아웃 계획 및 추정 기술료 수익 상세내역] |
| (단위: 백만원) |
| 파이프라인 | 적응증 | 지역 | L/O 예상시점 | 구분 | 2020년(E) | 2021년(E) | 2022년(E) | 2023년(E) | 2024년(E) |
| Vax-DC | 다발골수종 | 미국 | 2021년 | 임상단계 | 국내 임상2상* |
국내 임상2상* |
미국 임상2상 |
미국 임상2상 |
미국 임상 3상 |
| Upfront fee & Milestone | - | 2,661 | - | - | 5,323 | ||||
| Royalty | - | - | - | - | - | ||||
| Vax-NK+DC | 교모세포종 | 미국 | 2022년 | 임상단계 | - | 국내 전임상 |
국내 임상1/2a상 |
미국 임상2b상 |
미국 임상2b상 |
| Upfront fee & Milestone | - | - | 2,759 | - | 5,518 | ||||
| Royalty | - | - | - | 1,830 | 4,651 | ||||
| Vax-CAR-T | 췌장암 난소암 |
미국 | 2022년 | 임상단계 | - | 국내 전임상 |
미국 임상1상 |
미국 임상2상 |
미국 임상2상 |
| Upfront fee & Milestone | - | - | 1,362 | - | 2,725 | ||||
| Royalty | - | - | - | - | - | ||||
| Vax-mCAR-T | 췌장암 난소암 |
미국 | 2022년 | 임상단계 | - | 국내 전임상 |
미국 임상1/2a상 |
미국 임상2b상 |
미국 임상2b상 |
| Upfront fee & Milestone | - | - | 7,593 | - | 15,185 | ||||
| Royalty | - | - | - | 1,592 | 3,638 |
* 임상2상(임상2a 및 임상2b)
| 주1) | 원/달러 환율은 2020년 7월말 기준 최근 3개년(2017.08.01~2020.07.31) 외국환거래소 매매기준율 평균이 1,145원임을 감안하여, 보수적으로 1,100원으로 가정하였습니다. |
| 출처: 당사 정정 증권신고서(2020.08.31) |
파이프라인의 라이선스 아웃에 따른 기술료 수익을 추정하는 방법으로는 rNPV(risk-adjusted Net Present Value) 평가 방법을 사용했습니다.
rNPV는 현금흐름할인법(Discounted Cash Flows)에 연도별 현금흐름에서 발생할 수 있는 위험 가능성(임상성공률)을 적용한 후, 미래의 현금흐름을 할인율(WACC) 값으로 현가 할인하여 현재가치로 변환한 '위험 조정 미래 예상 현금흐름'입니다. 동 평가방법은 약물 개발에 따르는 임상성공률 등의 불확실한 요소들에 대한 위험 가중치를 투입 변수로 활용함으로써, 개발 과정에 임상 단계라는 과정을 반드시 통과해야만 상용화가 가능한 약물개발과정의 특수성을 반영한 평가 방법입니다.
각 파이프라인의 기술료 수익은 'Upfront fee, Milestone, Sales Royalty'로 구성되며, 각 파이프라인의 라이선스아웃 거래금액을 추정했던 과정은 아래와 같습니다.
|
구분 |
내용 |
비고 |
|
사업가치(A) |
파이프라인별 순현금흐름 추정(rNPV) |
- |
|
기술료 비율(B) |
동사의 파이프라인 중 Vax-NK+DC 병용, Vax-CAR 시리즈가 각각 임상1/2a상 및 전임상 단계에서 기술이전을 가정하고 있는 점과 기술이전 파트너사와의 협상과정에서 거래가치가 조정될 수 있는 불확실성을 감안하여 보수적으로 20%를 적용함 |
- |
|
총 거래가치(C) |
사업가치 X 기술료 비율 |
(C) = (A) X (B) |
|
Sales Royalty(D) |
추정기간 동안 동사가 수령 가능한 Sales Royalty를 의미하며, 최근 독일 Medigene사의 DC수지상세포 백신의 라이선스아웃 Royalty Rate가 낮은 두 자리수(low double digit)였던 점을 참고하여 10%를 가정함 |
- |
|
거래금액(E) |
'총 거래가치 - Sales Royalty'로 Upfront fee와 Milestone으로 구성됨 |
(E) = (C) - (D) |
| 출처: 당사 정정 증권신고서(2020.08.31) |
각 파이프라인의 rNPV 추정 시에 적용했던 주요 가정의 내용은 아래와 같습니다.
|
구분 |
가정내용 |
비고 |
|
추정연도 |
2020년 ~ 2033년 |
- |
|
매출 |
파이프라인별 목표환자수를 추정한 후, 목표시장점유율과 환자 1인당 예상 치료제가격을 적용하여 산정함 |
- |
|
목표환자수 |
파이프라인별 적응증의 특성을 감안하여 추정함 |
주1) |
|
목표시장점유율 |
주2) |
|
|
환자 1인당 예상 치료제가격 |
||
|
비용 |
매출원가 + R&D Cost + 기타 판관비(Other SG&A Expense) |
|
|
매출원가 |
전세계 전문의약품 매출액 기준 2018년 Top 10 글로벌 대형제약사 최근 3개년 매출액 대비 매출원가 평균치 29.0%를 적용함 (EvaluatePharma 2018, Factset) |
- |
|
R&D Cost |
파이프라인별 판매 개시연도 이전까지 Licensee가 부담하는 임상비용 적용. 적응증별 임상단계별 임상시험 환자수 및 환자당 비용을 고려하여 추정 |
주3) |
|
기타 판관비 |
전세계 전문의약품 매출액 기준 2018년 Top 10 글로벌 대형제약사 최근 3개년 매출액 대비 R&D Cost 제외 판관비 평균치 24.7%를 적용함 (EvaluatePharma 2018, Factset) |
- |
|
세전이익 |
매출 - 비용 |
- |
|
법인세비용 |
법인세율 20% 적용 |
- |
|
현금흐름 |
세전이익 - 법인세비용 |
- |
|
임상성공률 |
Nature Biotechnology에서 발췌한 단계별 임상성공률 수치를 적용함 |
주4) |
|
Risk-adjusted Cash Flows |
연도별 현금흐름 × 임상성공률 |
- |
|
WACC |
2019년 매출액 기준 상위 10개 글로벌 대형제약사의 최근 3개년 가중평균자본비용(WACC)의 평균치를 참고하여 보수적으로 9%를 적용함 |
주5) |
|
rNPV |
연도별 Risk-adjusted Cash Flows를 WACC으로 현가화한 NPV |
- |
* 현금흐름 추정 시, 현금의 유출이 없는 회계적 비용(유/무형자산 감가상각비)의 가산은 보수적인 관점에서 고려하지 않았습니다.
| 출처: 당사 정정 증권신고서(2020.08.31) |
주1) 연도별 파이프라인별 적응증의 목표 환자수는 아래와 같이 가정하였습니다.
| (단위: 명) |
| 파이프라인 | 적응증 | 구분 | 2020년(E) | 2021년(E) | 2022년(E) | 2023년(E) | 2024년(E) | 비고 |
| Vax-DC | 다발골수종 | 다발골수종 환자수(A) | 27,192 | 27,795 | 28,412 | 29,043 | 29,687 | CAGR 2.22%적용 |
| 재발환자수(B) | 21,262 | 21,754 | 22,236 | 22,730 | 23,234 | B=Ax80% | ||
| 재재발환자수(C) | 16,616 | 17,010 | 17,403 | 17,789 | 18,184 | C=전년도 재발환자수X80% | ||
| 목표환자수(D) | 37,878 | 38,764 | 39,639 | 40,519 | 41,418 | D=B+C | ||
| Vax-NK+DC | 교모세포종 | 뇌암환자수(A) | 24,969 | 25,326 | 25,688 | 26,055 | 26,427 | CAGR 1.43%적용 |
| 교모세포종 환자수(B) | 10,604 | 10,756 | 10,910 | 11,066 | 11,224 | B=Ax42% | ||
| 재발환자수(C) (Vax-NK 투여환자수) |
9,927 | 10,074 | 10,218 | 10,365 | 10,513 | C=전년도 교모세포종 환자수x95% | ||
| Vax-DC 투여환자수(D) | 6,618 | 6,716 | 6,812 | 6,910 | 7,009 | D=Cx66.67% | ||
| Vax-CAR | 췌장암 난소암 |
췌장암환자수(A) | 53,241 | 54,454 | 55,694 | 56,963 | 58,260 | CAGR 2.28%적용 |
| 난소암환자수(B) | 25,264 | 25,643 | 26,029 | 26,419 | 26,816 | CAGR 1.50%적용 | ||
| 목표환자수(C) | 48,599 | 49,701 | 50,827 | 51,980 | 53,158 | C=Ax90%+Bx2.7% |
| 출처: 당사 정정 증권신고서(2020.08.31) |
각 파이프라인별 적응증의 목표 환자수 도출을 위해 사용했던 주요 가정의 내용은 아래와 같습니다.
|
파이프라인 |
적응증 |
가정내용 |
|
Vax-DC |
다발골수종 |
- Global Cancer Observatory(GCO)에서 발췌한 2020년과 2025년의 미국의 다발골수종 예상 환자수를 토대로 연평균성장률을 산출한 후, 이를 적용하여 2020년~2024년까지의 환자수를 추정함 - 다발골수종의 재발률80%를 적용하여 연도별 재발환자수를 산출함 - 재발이 반복되는 다발골수종의 특성을 반영하여 전년도 재발환자수의 80%를 재재발환자수로 산출하여 목표 환자수에 추가함 |
|
Vax-NK+DC |
교모세포종 |
- Global Cancer Observatory(GCO)에서 발췌한 2020년과 2025년의 미국의 뇌암(Brain Tumor) 예상 환자수를 토대로 연평균성장률을 산출한 후, 이를 적용하여 2020년~2024년의 뇌암 환자수를 추정 - Glioblastoma(Steven De Vleeschouwer, 2017)에서 발췌한 미국 전체인구 대비 교모세포종 환자수 데이터(10만명당 3.19명)를 토대로 미국 뇌암 환자수 대비 교모세포종 환자수의 비율(약 42%)을 구한 후, 이를 적용하여 2020년~2024년의 미국 교모세포종 환자수를 추정함 - 교모세포종 환자의 대부분이 재발하는 점을 감안하여 전년도 교모세포종 환자수에 재발률 95%를 적용하여 교모세포종 재발환자수를 산출함 - Vax-NK 투여 후 교모세포종 재발환자수 중 3분의 1이 이탈한다고 가정하여 Vax-NK투여 환자수의 66.6%만을 Vax-DC의 투여환자수로 가정함 |
|
Vax-CAR 시리즈 |
췌장암 |
- Global Cancer Observatory(GCO)에서 발췌한 2020년과 2025년의 미국의 췌장암 및 난소암 예상 환자수를 토대로 연평균성장률을 산출한 후, 이를 적용하여 2020년~2024년까지의 환자수를 추정함 - 국립암센터의 보도자료에서 발췌한 미국의 췌장암 5년 생존율 9%를 참고하여 췌장암 전체환자수의 90%를 목표환자수(생존 가능성이 희박한 말기암 환자)로 가정함 - OCRA(Ovarian Cancer Research Alliance) 웹사이트에서 발췌한 난소암 각 스테이지별 재발률을 토대로 난소암 전체환자수의 2.7%를 목표환자수(생존 가능성이 희박한 말기암 환자)로 가정함 |
| 출처: 당사 정정 증권신고서(2020.08.31) |
주2) 각 파이프라인의 목표시장점유율 및 환자 1인당 치료제 가격은 아래와 같이 가정하였습니다.
| (단위: USD) |
|
파이프라인명 |
목표시장 점유율 |
환자 1인당 |
가정내용 |
|
Vax-DC |
10% (2029년) |
99,000 |
- 환자1인당 치료제 가격은 수지상세포 기반 항암백신인 프로벤지의 가격(1회당 약 65,000USD, 3회 투여 시 약 195,000USD, Drugs.com에서 발췌)을 참고하였으며, 프로벤지의 실패원인 중 하나가 높은 약제가격이었던 점을 감안하여 동사의 Vax-DC의 가격은 99,000USD로 가정함 - 시장점유율 목표치를 10%로 설정하고, 2024년부터 점유율이 단계적으로 증가하여 2029년에 목표치를 달성하는 것으로 가정함. 매출 추정기간에 포함되는 2024년의 예상 시장점유율은 0.2%로 가정함 |
|
Vax-NK+DC 병용 |
30% (2028년) |
Vax-NK 50,000 Vax-DC 100,000 |
- 환자1인당 치료제 가격은 경쟁약품인 bevacizumab(상품명 아바스틴)의 가격 150,000USD(몸무게 70kg인 환자가 2주에 1회씩 1년간 아바스틴을 주사한다고 가정, 단위가격은 Drugs.com에서 발췌)를 참고하여 가정함 - 시장점유율 목표치를 30%로 설정하고, 2023년부터 점유율이 단계적으로 증가하여 2028년에 목표치를 달성하는 것으로 가정함. 매출 추정기간에 포함되는 2023년과 2024년의 예상 시장점유율은 각각 2%와 5%로 가정함 |
|
Vax-CAR-T |
3% (2031년) |
200,000 |
- 환자1인당 치료제 가격은 현재 시장 내 MSLN을 타겟으로한 CAR-T 치료제의 임상시험이 매우 활발하고, 동사가 후발주자로서 시장에 참여하는 점을 감안하여 시판중인 CAR-T 세포치료제인 킴리아의 가격 475,000USD(Drugs.com에서 발췌)대비 할인한 200,000USD로 가정함 - 시장점유율 목표치를 3%로 설정하고, 2025년부터 점유율이 단계적으로 증가하여 2031년에 목표치를 달성하는 것으로 가정함. |
|
Vax-mCAR-T |
5% (2032년) |
500,000 |
- 환자 1인당 치료제 가격은 동사의 Vax-mCAR-T가 모노바디를 활용한 first-in-class인 점을 감안하여 시판이 허가된 CAR-T세포치료제인 킴리아의 가격 475,000USD(Drugs.com에서 발췌)대비 소폭 상승한 500,000USD로 가정함 - 시장점유율 목표치를 5%로 설정하고, 2023년부터 점유율이 단계적으로 증가하여 2032년에 목표치를 달성하는 것으로 가정함. 매출 추정기간에 포함되는 2023년과 2024년의 예상 시장점유율은 각각 0.1%와 0.2%로 가정함 |
| 출처: 당사 정정 증권신고서(2020.08.31) |
주3) 임상비용은 각 임상단계별 환자수에 회사에서 추정하고 있는 환자 1인당 평균 임상비용(Vax-DC $200,000, Vax-NK+DC 병용 $300,000, Vax-CAR 시리즈 $450,000)을 적용하여 산출하였습니다. 각 파이프라인별 연도별 임상시험 환자수는 회사가 추정하고 있는 예상치를 근거로 하였으며, NDA 관련 비용은 미국 IGEAHUB 자료의 FDA NDA/BLA Review Phase의 비용을 준용하여 2백만 USD로 가정하였습니다.
주4) 단계별 누적 임상성공확률은 아래와 같은 항암제의 임상 성공확률을 토대로 계산하여 적용하였습니다.
| 구분 | 임상1상 → 2상 |
임상2상 → 3상 |
임상3상 → NDA/BLA 신청 |
NDA/BLA 신청 → NDA/BLA 승인 |
임상1상 → NDA/BLA 승인 |
| 단계별 성공확률 | 68.9% | 42.3% | 54.7% | 82.8% | 13.2% |
출처: Nature Biotechnology, 2014, 32, 40-51
주5) 2019년 매출액 기준 상위 10개 글로벌 대형제약사의 최근 3개년 가중평균자본비용(WACC) 평균치는 아래와 같습니다.
|
순위 |
회사명 |
2017년 |
2018년 |
2019년 |
|
1 |
Johnson & Johnson |
7.1% |
9.0% |
7.0% |
|
2 |
Roche |
9.8% |
10.7% |
7.6% |
|
3 |
Pfizer |
7.3% |
9.5% |
7.1% |
|
4 |
Novartis |
8.9% |
10.2% |
7.6% |
|
5 |
Merck & Co. |
7.1% |
9.1% |
6.7% |
|
6 |
Bayer |
8.1% |
8.3% |
7.7% |
|
7 |
Sanofi |
7.5% |
8.2% |
6.4% |
|
8 |
GalxoSmithKline |
9.7% |
10.3% |
6.6% |
|
9 |
Abbvie |
7.9% |
10.7% |
7.0% |
|
10 |
Bristol-Myers Squibb |
8.9% |
9.0% |
5.9% |
|
10개사 평균 가중평균자본비용(WACC) |
8.2% |
9.5% |
7.0% |
|
|
최근 3개년 평균 WACC |
8.2% |
|||
출처: 블룸버그(Bloomberg)
위의 주요 가정을 적용하여 산출했던 각 파이프라인의 rNPV 사업가치와 총 거래가치는 아래와 같습니다.
| (단위: 백만원) |
| 구분 | 파이프라인 사업가치 | 거래가치 |
| Vax-DC | 122,605 | 24,521 |
| Vax-NK+DC | 137,945 | 27,589 |
| Vax-CAR-T | 68,120 | 13,624 |
| Vax-mCAR-T | 379,627 | 75,925 |
주1) 원/달러 환율은 2020년 7월말 기준 최근 3개년(2017.08.01~2020.07.31) 외국환거래소 매매기준율 평균이 1,145원임을 감안하여, 보수적으로 1,100원으로 가정하였습니다.
주2) 총 거래가치는 동사의 파이프라인 중 Vax-NK+DC 병용, Vax-CAR 시리즈가 각각 임상1/2a상과 전임상 단계에서 기술이전 하는 것을 가정하고 있는 점과 기술이전 파트너사와의 협상과정에서 거래가치가 조정될 수 있는 불확실성을 감안하여 기술료 비율을 보수적으로 20%를 적용하여 산출하였습니다.
주3) 총 거래가치를 추정매출로 반영하는 과정에서 임상단계별 Upfront fee와 Milestone은 아래와 같은 비중으로 각 파이프라인에 모두 동일하게 적용하였습니다.
|
구분 |
License-Out |
임상2상 성공 시 |
임상3상 성공 시 |
품목허가 시 |
합계 |
|
Upfront fee 및 |
10.00% |
20.00% |
30.00% |
40.00% |
100.00% |
2-2) 박스루킨-15
박스루킨-15로부터 유입될 당사의 매출 추정의 경우 기술이전 시 별도의 Upfront와 Milestone 없이 판매에 따른 로열티율을 적용하여 당사의 매출에 반영되도록 가정하였습니다. 박스루킨-15는 국내와 미국시장을 대상으로 판매할 계획으로 각 2021년과 2022년부터 판매에 따른 매출이 발생할 것으로 가정하였습니다.
| [박스루킨-15 매출액 추정] |
| (단위: 마리, 회, 백만원) |
| 구분 | 2020년(E) | 2021년(E) | 2022년(E) | 2023년(E) | 2024년(E) | 비고 | ||
| 국내 | 시장점유율 | 서울/경기 전체지역 | - | - | 0.13% | 0.25% | 0.50% | - |
| 서울/경기 주요 5개구 | - | 0.50% | 1.00% | 3.00% | 5.00% | - | ||
| 반려동물수(A) | 9,890,772 | 10,307,099 | 10,740,950 | 11,193,063 | 11,664,206 | CAGR 4.21% 적용 | ||
| 반려견수(B) | 7,254,191 | 7,559,537 | 7,877,737 | 8,209,330 | 8,554,881 | B=Ax73.34% | ||
| 암환견수(C) | 1,813,548 | 1,889,884 | 1,969,434 | 2,052,332 | 2,138,720 | C=Bx25% | ||
| 서울/경기 전체지역 암환견수(D) | 628,076 | 654,513 | 682,063 | 710,773 | 740,691 | D=Cx34.6% | ||
| 서울/경기 주요 5개구 암환견수(E) | 105,517 | 109,958 | 114,587 | 119,410 | 124,436 | E=Dx16.8% | ||
| 목표 암환견수(F) | - | 550 | 1,855 | 5,060 | 9,303 | 서울/경기 전체지역 및 서울/경기 주요5개구의 암환견수에 각각의 시장점유율 적용한 후 합산 |
||
| 총 치료횟수(G) | - | 743 | 3,125 | 9,320 | 18,247 | 목표암환견수에 6개월 단위로 총 3회의 공고요법 실시, 매회차당 이탈률 30% 적용 |
||
| 총 투여주사수(H) | - | 5,940 | 25,003 | 74,563 | 145,978 | H=Gx8회 | ||
| 매출액(I) | - | 492 | 2,070 | 6,174 | 12,087 | I=Hx10만원x임상 성공확률 | ||
| 동사 Royalty수익(J) | - | 49 | 207 | 617 | 1,209 | J=Ix10% | ||
| 미국 | 시장점유율 | - | - | 1.00% | 3.00% | 6.00% | ||
| 반려견수(A) | 94,193,069 | 95,740,226 | 97,312,796 | 98,911,196 | 100,535,850 | CAGR 1.64% 적용 | ||
| 반려동물보험 가입률(B) | 2.43% | 2.80% | 3.20% | 3.30% | 3.39% | - | ||
| 반려동물보험 가입 반려견수(C) | 2,292,094 | 2,679,204 | 3,114,009 | 3,260,113 | 3,413,071 | C=AxB | ||
| 암환견수(D) | 573,023 | 669,801 | 778,502 | 815,028 | 853,267 | D=Cx25% | ||
| 목표 암환견수(E) | - | - | 7,785 | 24,451 | 51,196 | 암환견수에 예상시장점유율 적용 | ||
| 총 치료횟수(F) | - | - | 10,510 | 41,589 | 99,611 | 목표암환견수에 6개월 단위로 총 3회의 공고요법 실시, 매회차당 이탈률 30% 적용 |
||
| 총 투여주사수(G) | - | - | 84,078 | 332,712 | 796,888 | G=Fx8회 | ||
| 매출액(H) | - | - | 7,658 | 30,303 | 72,581 | H=Gx100USDx임상 성공확률 | ||
| 동사 Royalty수익(I) | - | - | 766 | 3,030 | 7,258 | I=Hx10% | ||
주1) 미국시장 매출추정에 적용한 원/달러 환율은 2020년 7월말 기준 최근 3개년(2017.08.01~2020.07.31) 외국환거래소의 원/달러 환율 매매기준율 평균이 1,145원임을 감안하여, 보수적으로 1,100원으로 가정하였습니다.
| 출처: 당사 정정 증권신고서(2020.08.31) |
박스루킨-15의 매출액 추정을 위해 적용했던 주요 가정의 내용은 아래와 같습니다.
|
구분 |
가정내용 |
|
|
목표 암환견수 |
국내 |
- 연도별 국내 반려동물수를 추정(연평균증가율 4.21% 적용, '2017 반려동물 연관산업 발전방안연구'을 참고하여 추정)한 후, 반려동물 대비 반려견의 비율(73.34% 적용, '2018 반려동물 보유 현황 및 국민 인식 조사 보고서'와 '2017 반려동물 연관산업 발전방안 연구'를 참고하여 추정) 과 반려견의 발암율(25% 적용, American Veterinary Medical Association의 자료를 참고하여 추정)을 순차적으로 적용하여 암환견수를 추정함 - 서울/경기 주요 5개구(강남구, 송파구, 서초구, 분당구, 일산구)와 서울/경기 전체지역의 암환견을 각각 1순위, 2순위 Target으로 설정하여 전체 암환견수에서 각 Target시장의 비중(전국 대비 서울/경기의 비중 34.6% 적용, 서울/경기 대비 주요 5개구의 비중 16.8% 적용)을 추정함 |
|
미국 |
- 연도별 미국의 반려견수를 추정(연평균증가율 1.64% 적용, 'statista'의 미국 반려견수 현황 자료를 참고하여 추정)한 후, 반려동물보험에 가입한 반려견수의 비율(2017년 미국의 반려동물보험 가입율 1.6%, 2017년부터 2022년까지 5년간 2배로 성장하고 이후부터는 매년 3% 성장 가정)과 반려견의 발암율(25% 적용, American Veterinary Medical Association의 자료를 참고하여 추정)을 순차적으로 적용하여 목표 암환견수를 추정함 |
|
|
시장점유율 |
국내 |
- 서울/경기 주요 5개구와 서울/경기 전체지역의 목표 시장점유율을 차등 적용함. 서울/경기 주요 5개구는 점유율 목표치를 10%로 설정하고 2021년부터 점유율이 단계적으로 증가하여 2027년에 목표치를 달성하는 것으로 가정하였으며, 서울/경기 전체지역은 점유율 목표치를 5%로 설정하고 2022년부터 점유율이 단계적으로 증가하여 2028년에 목표치를 달성하는 것으로 가정함 |
|
미국 |
- 점유율 목표치를 20%로 설정하고 2022년부터 점유율이 단계적으로 증가하여 2028년에 목표치를 달성하는 것으로 가정함 |
|
|
총 치료횟수 |
- 임상시험 프로토콜에 따라 암환견 1마리당 최초 치료 후, 총 3회에 걸친 공고요법(6개월, 12개월, 18개월 후 치료)으로 치료를 진행하는 것으로 가정하되, 임상시험 기간 중 암환견의 증세가 호전되면 암환견의 보호자는 치료를 중단(이탈)하는 사례가 발생할 것으로 예상하여 매회차당 이탈비율 30%를 적용함 |
|
|
총 투여주사수 |
- 임상시험 프로토콜에 따라 1회 치료당 8회의 주사를 투여하는 것으로 가정함 |
|
|
주사 1회당 가격 |
- 국내는 주사 1회당 10만원을 가정하였으며, 미국은 100USD를 가정함 |
|
|
임상성공확률 |
- 반려견을 대상으로 한 임상성공확률 데이터가 별도로 없는 점을 감안하여 사람의 임상단계별 성공확률을 차용함 ('NDA/BLA 신청 → 승인' 성공률인 82.8%를 적용) |
|
|
Royalty율 |
- Elanco & Aratana 간의 동물용의약품 라이선스아웃의 Royalty Rate(중간 한자리수 ~ 낮은 두자리수, Elanco사의 SEC 보고서에서 발췌)를 참고하여 10%를 가정함 |
|
| 출처: 당사 정정 증권신고서(2020.08.31) |
상기의 실적추정 과정에 있어서 당사는 최대한 객관적인 근거를 바탕으로 신뢰성 있는 정보를 제공하고자 노력을 기울였으나, COVID-19의 특수한 상황으로 라이센스 아웃이 예상했던 일정보다 다소 연기된 점과 박스루킨-15의 품목허가 자진철회 등으로 상기에 제시된 추정 실적과 실제 실적 사이에 상당한 괴리가 발생하였습니다. 2021년부터 매출 시현을 예상했던 당사의 당초 추정과는 달리, 최근 사업년도인 2022년 기준 당사는 매출 미시현, 영업손실 8,213백만원, 당기순손실 6,825백만원을 기록하였습니다.
| [현재 기준 실제 및 추정 손익계산서] |
| (단위: 백만원) |
| 추정대상 | 계정과목 | 예측치 | 실적치 | 괴리율 |
|---|---|---|---|---|
| 2020년 | 매출액 | - | - | - |
| 영업이익 | -7,223 | -4,255 | 41 | |
| 당기순이익 | -7,136 | -3,984 | 44 | |
| 2021년 | 매출액 | 2,711 | - | - |
| 영업이익 | -10,740 | -5,904 | 45 | |
| 당기순이익 | -10,420 | -4,763 | 54 | |
| 2022년 | 매출액 | 12,687 | - | - |
| 영업이익 | -317 | -8,213 | -2,491 | |
| 당기순이익 | -109 | -6,825 | -6,162 |
| 출처: 당사 정기보고서 |
2021년~2022년 매출 예상치에는 Vax-DC, NK+DC, CAR-T, mCAR-T의 미국 기술이전 기술료와 박스루킨-15의 판매매출이 산정되어 있습니다.
이 중 2021년 매출이 발생할 것으로 예상했던 동물용의약품 박스루킨-15의 경우, 2020년 하반기에 품목허가를 접수하였고 2021년 초에 품목허가 승인과 동시에 국내 제품 출시 계획을 하고 있었습니다. 그러나 예상치 못하게 검역본부와의 협의 과정에서, 품목허가 신청을 자진철회하고 추가적인 임상연구를 수행하게 되어 박스루킨-15의 출시 시점이 미뤄지게 되었습니다.
박스루킨-15는 반려동물 전용 항암면역치료제로 검역본부에서도 전례가 없는 케이스였기 때문에, 임상시험 계획서를 승인받는 과정에서도 충분히 논의를 거쳐서 진행한 바 있습니다. 그러나 점차 반려동물에 대한 산업의 관심도가 높아지면서, 검역본부에서도 식약처의 기준에 따라 관련 규정이 더욱 까다로워 지는 등의 변화가 있었습니다. 최초 임상시험계획 승인 당시에는 15마리 이상의 환견 수로 승인받았고, 해당 마리 수에 대한 데이터로 품목허가를 신청하였으나, 당사가 품목허가를 신청한 시기에는 검역본부 판단에 모수가 부족하다는 의견을 전달받았고 통계적 유의성을 확보하기 위하여 추가 연구를 진행하라는 사항을 포함해 몇 가지 보완사항이 발생하였습니다. 결국 추가적인 임상시험을 진행해야 하는 까닭에, 예상 출시 시점이 미루어져 예상했던 매출 계획이 지연되었습니다.
현재는 유선종양 대조군 포함 60마리, 림프종 대조군 포함 60마리로 총 120마리에 대한 임상시험을 진행하고 있으며, 유선종양 대상 연구는 최종 투여가 마무리되고 모니터링 중에 있습니다. 연내 모니터링 및 분석을 마치고 품목허가를 재신청할 계획입니다.
Vax-DC와 NK+DC의 경우 당사의 파이프라인 전략 수정으로 Vax-DC 파이프라인은 중단하고 VAX-CARs 파이프라인 개발에 집중하고 있습니다. 본 증권신고서 사업위험 라. 에 기재한 바와 같이 VAX-CARs의 연구개발에 집중하는 것이 투자 대비 효율성 제고에 도움이 될 것이라고 판단하였기 때문입니다. 이에따라 DC 파이프라인 관련된 예상 매출은 시현하지 못하였습니다. 또한 VAX-CAR-T 및 VAX-mCAR-T의 경우 현재 비임상 진행으로 매출 계획이 지연되었습니다. 이에 따라 2,711백만원과 12,687백만원 규모의 매출이 발생할 것이라고 예상했던 2021년과 2022년에는 매출을 시현하지 못하였습니다.
이와 더불어 당사는 IPO신고서 제출 당시 Vax-NK에 대한 타임라인을 '22년~'24 년 2b상으로 제시하였습니다. 그러나 증권신고서 제출일 현재 Vax-NK는 2a상을 진행중이며, 과거에 예상했던 Vax-NK관련 매출 역시 지연될 가능성이 높습니다.
Vax-NK 관련 타임라인이 지연된 사유는 다음과 같으며, 임상연구 진행 현황은 다음과 같습니다.
첫 환자는 20년 초에 등록되었으나, 임상시험계획서에 기재된대로 환자를 선정하는데는 까다로운 기준이 정해져 있기에 모든 진행성간암 환자가 임상 시험 대상자가 될 수 없었고, 대상자 선정 과정에서 환자가 선정대상에서 탈락될 가능성 등이 있어 계획한 일정보다 더디게 진행되었습니다.
Vax-NK/HCC는 임상1상과 달리 임상2a상에서는 '공고요법'을 추가하면서 1주기 투여 4주 후 2주기로 한 번 더 주입하는 방식으로 디자인을 변경하였습니다. 이 과정에서 식약처와 논의한 결과, 처음 3명의 환자에 대한 안전성 심의 위원회를 거친 뒤 남은 임상시험을 진행하기로 결정하였습니다. 그리고 안전성 심의 위원회가 통과(21년 06월)된 후, 본격적으로 임상시험에 속도를 내기 위하여 기존 임상시험 실시기관 2곳에 3곳을 추가하여 총 5개 기관에서 임상시험을 진행하였으며 안전성을 한 번 더 입증하여 각 연구자분들께서 더욱 더 적극적으로 연구에 참여하게 되었습니다.
2022년 9월, 12명의 환자에 대한 데이터를 바탕으로 예비연구결과를 발표하였으며, 2023년 8월 기준 17번째 환자에 대한 임상시험용 의약품 투여를 완료하고 모니터링 중에 있습니다. 임상2a상은 17번째 환자를 마지막으로 임상시험 참여자 모집을 완료하고자 하며, 향후 예정된 종료를 위한 절차를 진행할 예정입니다.
상기와 같이 당사는 기업공개를 위한 공모 당시 당사의 적정주가를 도출하기 위해 제시한 당사의 추정손익과 현재 영업을 통해 달성한 실현 손익 간 괴리를 보이고 있습니다. 이는 당사와 같이 신약개발에 특화 된 바이오벤처 기업 특성상 개발하고 있는 신약 등 파이프라인에 대한 성공 가능성 및 라이선스 아웃 계약 가능성을 합리적으로 예상하는데는 제약이 존재함을 시사합니다. 투자자께서는 이 점 유의하시기 바랍니다.
|
차. 내부회계관리제도 및 내부통제 관련 위험 당사는 상장 이전 2018년에 내부회계관리제도를 조기 도입하여 내부통제시스템을 강화하였으며, 삼덕회계법인의 컨설팅 용역을 통해 내부회계관리시스템 구축과 함께 2019년 1월 1일 내부회계관리규정을 제정하였습니다. 증권신고서 제출일 현재 내부회계관리제도를 운영하기 위한 조직이 구축되어 있으며, 외부감사인이 운영 실태를 보고한 사항은 존재하지 않습니다. 당사는 내부회계관리제도를 철저히 운영하여 외부 감사인의 내부회계관리제도에 대한 검토의견을 받을 계획입니다. 종합적으로 당사는 내부통제를 위한 규정 및 조직을 구축하고 있으며, 우발상황 등이 발생하지 않도록 상시 모니터링을 통해 내부통제 강화를 위하여 상당한 노력을 기울이며 대비하고 있습니다. 그럼에도 불구하고, 내부회계관리조직이 적절하게 운영되지 않거나 혹은 외부감사인의 내부회계관리 운영실태를 감사한 결과 중요한 취약점이 발견될 시 각종 제재사항에 해당할 수 있습니다. 투자자 여러분께서는 공시된 당사의 내부회계관리 운영실태를 충분히 확인하시고 투자에 임해주시기 바랍니다. |
당사는 코스닥 상장법인으로「주식회사 등의 외부감사에 관한 법률」(이하 '외감법')에 따라 신뢰할 수 있는 회계정보의 작성과 공시를 위해 내부회계관리규정 및 내부회계관리제도를 갖추고 있어야 합니다. 또한, 외부감사인은 당사의 내부회계관리제도 운영실태를 검토 및 감사를 진행하여야 하며, 해당 결과는 감사보고서에 표명하도록 되어 있습니다. 최근 사업연도 기준 당사 외부감사인의 내부회계관리제도 검토 의견은 아래와 같습니다.
| 내부회계관리제도 검토의견 |
| 사업연도 | 감사인 | 내부회계관리제도 검토의견 | 지적사항 |
| 2022년 (제13기) |
신한회계법인 | 경영자의 내부회계관리제도 운영실태보고서에 대한 우리의 검토결과, 상기 경영자의운영실태보고 내용이 중요성의 관점에서 내부회계관리제도 모범규준 제5장 '중소기업에 대한 적용'의 규정에 따라 작성되지 않았다고 판단하게 하는 점이 발견되지 아니하였습니다. |
- |
| 2021년 (제12기) |
신한회계법인 | 경영자의 내부회계관리제도 운영실태보고서에 대한 우리의 검토결과, 상기 경영자의운영실태보고 내용이 중요성의 관점에서 내부회계관리제도 모범규준 제5장 '중소기업에 대한 적용'의 규정에 따라 작성되지 않았다고 판단하게 하는 점이 발견되지 아니하였습니다.. |
- |
당사는 상장 이전 2018년에 내부회계관리제도를 조기 도입하여 내부통제시스템을 강화하였으며, 삼덕회계법인의 컨설팅 용역을 통해 내부회계관리시스템 구축과 함께 2019년 1월 1일 내부회계관리규정을 제정하였습니다. 증권신고서 제출일 현재 내부회계관리제도를 운영하기 위한 조직이 구축되어 있으며, 외부감사인이 운영 실태를 보고한 사항은 존재하지 않습니다. 당사는 내부회계관리제도를 철저히 운영하여 외부 감사인의 내부회계관리제도에 대한 검토의견을 받을 계획입니다.
다만, 내부회계관리를 철저히 운영함에도 불구하고 회계처리 위반, 혹은 관련 임직원의 배임 및 횡령 등 발생으로 내부회계관리가 적절하게 운영되지 않을 경우 과태료 등의 법적 제재가 부과될 수 있습니다. 과태료 부과 시 법정최고금액에 과태료 예정금액 산정표에 따른 비율을 적용하여 예정금액을 산정하고, 가증, 감경하여 최종 과태료부과금액을 결정하고 있습니다.
| [과태료 부과기준(외감규정 별표9 참조)] |
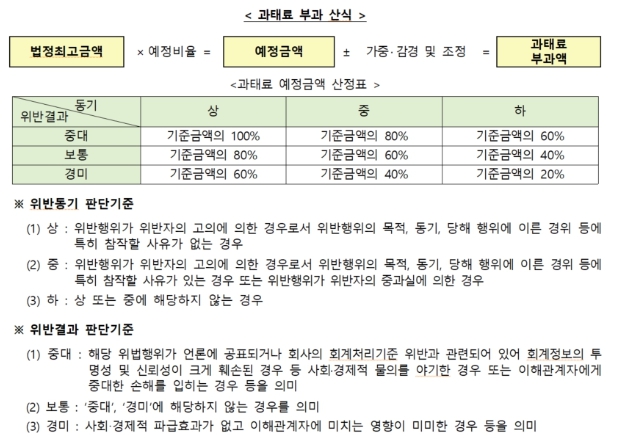 |
|
과태료 부과기준 |
| 출처: 금융감독원 보도자료 |
특히, 이사 등 내부회계관리제도 운영 관련자가 회계정보를 내부회계관리제도에 의하지 아니하고 위조, 변조, 훼손 또는 파기한 사실이 확인되는 경우, 5년 이하의 징역 또는 5천만원 이하의 벌금이 부과될 수 있습니다.
또한, 코스닥시장 상장규정에 따라 내부회계관리제도 비적정 시 투자주의환기종목에 지정될 수 있으며(「코스닥시장 상장규정」제52조), 2년 연속 내부회계관리제도 비적정 의견을 받는 경우 상장적격성 실질심사에 따른 상장폐지 요건에 해당할 수 있습니다(「코스닥시장 상장규정」제56조).
종합적으로 당사는 내부통제를 위한 규정 및 조직을 구축하고 있으며, 우발상황 등이 발생하지 않도록 상시 모니터링을 통해 내부통제 강화를 위하여 상당한 노력을 기울이며 대비하고 있습니다. 그럼에도 불구하고, 내부회계관리조직이 적절하게 운영되지 않거나 혹은 외부감사인의 내부회계관리 운영실태를 감사한 결과 중요한 취약점이 발견될 시 각종 제재사항에 해당할 수 있습니다. 투자자 여러분께서는 공시된 당사의 내부회계관리 운영실태를 충분히 확인하시고 투자에 임해주시기 바랍니다.
| 카. 원재료 매입관련 위험 당사의 항암제 제작과 관련된 원재료 대부분은 해외에서 구매 하고있습니다. 그러나 아직 당사의 파이프라인들은 제품화 단계인 상품이 없기 때문에 현재 대량의 원재료를 구해야하는 상황은 아니므로, 원재료 매입 관련하여 리스크가 발생할 가능성은 낮은 편입니다. 또한 당사가 매입하고 있는 원재료는 당사에 특수하게 맞추어 제작하고 있는 재료가 아닌 범용적인 재료로, 향후 당사의 파이프라인이 제품화 되는 단계에 도달 할 경우 식약처에서 주요 약품을 대체할 수 있는 타 사의 원재료에 대한 동등성 평가를 통해 원재료 조달에 따른 생산지연의 위험성을 회피할 수 있습니다. 그럼에도 불구하고 당사가 요구하는 원재료에 대한 가격변동이나 제조/판매처에서의 재고관리, 통관 등의 다양한 이유로 수급이 어려워질 경우 당사 파이프라인 제품화에 부정적인 영향을 끼칠 수 있으니 이점 양지하시기 바랍니다. |
당사의 항암제 제작과 관련된 원재료 대부분은 해외에서 구매 하고있습니다. 그러나 아직 당사의 파이프라인들은 제품화 단계인 상품이 없기 때문에 현재 대량의 원재료를 구해야하는 상황은 아니므로, 원재료 매입 관련하여 리스크가 발생할 가능성은 낮은 편입니다.
또한 당사가 매입하고 있는 원재료는 당사에 특수하게 맞추어 제작하고 있는 재료가 아닌 범용적인 재료로, 향후 당사의 파이프라인이 제품화 되는 단계에 도달 할 경우 식약처에서 주요 약품을 대체할 수 있는 타 사의 원재료에 대한 동등성 평가를 통해 원재료 조달에 따른 생산지연의 위험성을 회피할 수 있습니다.
그럼에도 불구하고 당사가 요구하는 원재료에 대한 가격변동이나 제조/판매처에서의 재고관리, 통관 등의 다양한 이유로 수급이 어려워질 경우 당사 파이프라인 제품화에 부정적인 영향을 끼칠 수 있으니 이점 양지하시기 바랍니다.
3. 기타위험
| 가. 환금성 제약 및 주가 변동에 따른 손실 위험 금번 유상증자 청약에 참여하여 신주를 배정받을 경우 신주의 추가상장일까지 환금성에 제약이 있으며, 청약 후 추가상장일 사이에 주가가 하락할 경우 원금에 대한 손해가 발생할 가능성이 있으니 투자자께서는 이 점 유의하시기 바랍니다. |
금번 유상증자 청약에 참여하여 신주를 배정받을 경우 신주의 추가상장일까지 환금성에 제약이 있으며, 청약 후 추가상장일 사이에 주가가 하락할 경우 원금에 대한 손해가 발생할 가능성이 존재하오니, 투자자께서는 이 점 유의하시기 바랍니다.
당사는 코스닥시장 상장법인으로서 이번 유상증자로 발행되는 신주는 코스닥시장에 상장되어 거래될 예정이므로 유동성과 관계된 심각한 환금성 위험은 존재하지 않습니다. 그러나 유상증자 청약에 참여하여 신주를 배정받을 경우, 신주가 상장되어 매매가 가능할 때까지 납입주금에 대한 유동성의 제약이 있습니다.
본 유상증자의 자세한 일정은 본 신고서의 "제1부 모집 또는 매출에 관한 사항 - I. 모집 또는 매출에 관한 일반사항" 중 '1. 공모개요'를 참고하시기 바랍니다.
또한 코스닥시장에 추가 상장될 때까지 유상증자로 발행되는 신주의 발행가액 수준의 주가가 유지되지 않을 수 있으며, 당사의 내적인 환경변화 또는 시장전체의 환경 변화 등에 의한 급격한 주가하락이 발생할 경우, 투자원금에 대한 손실이 발생할 수 있습니다.
| 나. 주가하락에 따른 발행금액 감소 위험 주식시장의 급격한 상황 악화로 인하여 회사의 금번 유상증자 발행가액이 크게 하락할 경우 당사가 계획했던 자금조달 계획 등에 차질이 발생할 수 있으며, 이러할 경우 당사의 재무적 안정성은 부정적인 영향을 받을 수 있으니 이 점 유의하시기 바랍니다. |
금번 유상증자의 확정발행가액은 1차 발행가액과 2차 발행가액 중 낮은 가액으로 결정됩니다. 다만 「자본시장과 금융투자업에 관한 법률」 제165조의6 및 「증권의 발행 및 공시 등에 관한 규정」 제5-15조의2에 의거하여 1차 발행가액과 2차 발행가액 중 낮은가액이 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격보다 낮은 경우 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격을 확정발행가액으로 합니다. (단, 발행가액이 액면가보다 낮을 경우 액면가를 발행가액으로 합니다.)
일반공모 후 미청약분에 대해서는 그 전부를 공동대표주관회사가 인수하므로 청약 미달에 따른 위험은 없으나, 주가 하락으로 발행가액이 낮아져 당사가 목표로 하는 규모의 자금을 조달하지 못할 수도 있습니다. 이 경우, 당사의 재무안정성이 부정적인 영향을 받을 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. 금번 유상증자를 통한 자금사용 목적은 V. 자금의 사용목적 부분을 참고하여 주시기 바랍니다.
| 다. 증권신고서 정정에 따른 일정 변경 위험 본 증권신고서는 공시심사 과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있습니다. |
「자본시장과 금융투자업에 관한 법률」 제120조 3항에 의거하여 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 투자자에게 귀속됩니다.
금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서(분기 및 반기보고서 포함) 및 감사보고서 등 기타 정기 공시사항과 수시 공시사항 등이 전자공시되어 있사오니 투자 의사를 결정하시는 데 참조하시기 바랍니다.
본 증권신고서는 공시 심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행과정에서 일정이 변경될 수도 있으므로 투자자들께서는 투자시 이러한 점을 감안하시기 바랍니다.
| 라. 분석정보의 한계 및 투자판단 관련 위험 금번 유상증자를 통해 취득한 당사의 주식가치가 하락할 수 있습니다. 본 증권신고서의 효력발생은 정부가 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나 이 유가증권의 가치를 보증 또는 승인한 것이 아니며, 기재사항은 청약일 이전에 변경될 수 있습니다. 또한 금번 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 투자자께서는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안 되며, 다양한 방면에서 신중한 검토를 병행하여 독자적으로 판단하시기 바랍니다. |
상기 서술한 바와 같이, 당사의 주식가치는 금번 유상증자 실시에 따른 전 과정에서 다양한 영향을 받아 하락할 수 있습니다.
본 증권신고서의 효력발생은 정부가 증권신고서의 기재사항이 진실 또는 정확하다는것을 인정하거나 이 유가증권의 가치를 보증 또는 승인한 것이 아니며, 기재사항은 청약일 이전에 변경될 수 있습니다. 본 주식을 청약하고자 하는 투자자께서는 투자결정을 하기 전에 본 증권신고서의 상기 투자위험요소 뿐만 아니라 다른 부분 또한 주의 깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 합니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 상기 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없습니다. 따라서 투자자께서는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안 되며, 다양한 방면에서 신중한 검토를 병행하여 독자적으로 판단할 필요가 있습니다.
당사는 상기에 기술된 투자위험요소 외에도 불안정한 경제상황 등에 의하여 직·간접적으로 영향을 받을 수 있습니다. 당사의 재무제표는 당사의 재무상태에 영향을 미칠 수 있는 경제상황에 대한 경영자의 현재까지의 평가를 반영하고 있으나, 실제 결과는 현재시점에서의 평가와는 상당히 다를 수 있는 점을 유의하시기 바랍니다.
만일 상기 투자위험요소가 실제로 발생할 경우, 당사의 사업환경과 재무상태, 기타 운영결과에 부정적인 영향을 미칠 수 있습니다. 이에 따른 주가 하락으로 투자자께서는 금번 공모 과정에서 취득하게 되는 주식의 투자금액의 일부 또는 전부를 잃을 수 있습니다.
또한 금번 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 대내외적으로 여러가지 요소들의 영향에 따라 최초에 예측했던 것과 다를 수 있는 점을 유의하시기 바랍니다.
| 마. 당사의 잘못된 정보 제공 등으로 손해 끼칠 가능성 당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있으니 이 점 유의하시기 바랍니다. |
「증권관련 집단소송법」 제12조(소송허가 요건)에 따라 50명 이상의 개인이 발행주식총수의 0.01% 이상 보유할 경우 한 명 이상의 대표 당사자가 상기 50인 이상의 당사자들을 대리하여 회사가 발행한 증권의 거래과정에서 발생한 피해에 대하여 소송을 제기할 수 있습니다.
| 「증권관련 집단소송법」제12조(소송허가 요건) |
| ① 증권관련집단소송 사건은 다음 각 호의 요건을 갖추어야 한다. 1. 구성원이 50인 이상이고, 청구의 원인이 된 행위 당시를 기준으로 그 구성원이 보유하고 있는 증권의 합계가 피고 회사의 발행 증권 총수의 1만분의 1 이상일 것 2. 제3조제1항 각 호의 손해배상청구로서 법률상 또는 사실상의 중요한 쟁점이 모든 구성원에게 공통될 것 3. 증권관련집단소송이 총원의 권리 실현이나 이익 보호에 적합하고 효율적인 수단일 것 4. 제9조에 따른 소송허가신청서의 기재사항 및 첨부서류에 흠이 없을 것 ② 증권관련집단소송의 소가 제기된 후 제1항제1호의 요건을 충족하지 못하게 된 경우에도 제소(提訴)의 효력에는 영향이 없다. |
증권신고서 및 투자설명서에서 기재된 잘못된 내용, 잘못된 사업보고서의 공시, 내부자거래에 의한 손해배상청구 및 회계부정으로 인한 손해배상 청구 등이 주요한 소송사유에 포함됩니다. 당사는 향후 이와 같은 집단소송의대상이 되지 않는다고 확신할 수 없으며, 만약 당사에 대하여 집단소송이 제기될 경우 상당한 소송비용이 발생할 수 있음을 유의하시기 바랍니다.
| 바. 유상증자 철회에 따른 위험 유상증자 진행 과정에서 모집 절차의 진행에 중대한 영향을 미칠만한 사유가 발생하여 당사 혹은 공동대표주관회사의 판단으로 유상증자가 철회될 수 있습니다. 유상증자 납입 전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회 시점에 따라 권리락에 따른 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있음을 투자자께서는 유의하시기 바랍니다. |
금번 주주배정 후 실권주 일반공모 유상증자 진행 과정에서 모집 절차의 진행에 중대한 영향을 미칠 만한 사유가 발생하여 당사 혹은 공동대표주관회사의 판단으로 유상증자가 철회될 수 있습니다.
유상증자 납입 전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회 시점에 따라 권리락에 따른 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있음을 투자자께서는 유의하시기 바랍니다.
| 사. 금융감독기관의 규제 강화에 따른 위험 최근 상장기업에 대한 관리감독기준이 강화되는 추세이며, 향후 당사가 상장기업 관리 감독기준을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지 실질심사, 상장폐지, 불성실법인 지정에 따른 벌금 및 벌점 부과 등의 조치가 취해질 수 있습니다. 향후 감독기관으로부터 당사가 현재 파악하지 못한 제재가 부과될 경우 주가하락 및 유동성(환금성)제약 등으로 인해 투자금에 막대한 손실이 발생할 수 있으니, 투자자께서는 이점 유의하시기 바랍니다. |
최근 금융감독기관 등의 상장기업에 대한 관리감독기준은 투자자보호 차원에서 엄격해지고 있는 상황이며, 회사가 관련 규정을 위반할 경우 회사 및 회사가 발행한 주식에 대해 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다.
당사는 현재 주권매매정지, 상장폐지, 관리종목 등의 사유에는 해당하지 않지만, 향후 감독기관으로부터 당사가 현재 파악하지 못한 제재가 부과될 경우 주가하락 및 유동성(환금성) 제약 등으로 인해 투자금에 막대한 손실이 발생할 수 있으니 투자자들께서는 관련 규정을 충분히 검토하신 후 투자에 임해주시기 바랍니다.
자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융법규서비스(http://fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
| 아. 차입공매도 유상증자 참여 제한 관련 위험 「자본시장과 금융투자업에 관한 법률 시행령」일부 개정령에 따라, 주권상장법인이 유상증자 계획을 공시한 이후 발행가격 산정을 위한 대상 거래기간의 마지막 날(발행가격 산정 기산일)까지, 해당 기업의 주식을 공매도 한 자는 증자 참여를 제한하되, 예외적인 경우에만 증자 참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 투자자께서는 이 점 유의하시기 바랍니다. |
금융위원회는 2021년 01월 13일 공매도 제도개선 관련 「자본시장과 금융투자업에 관한 법률 시행령」일부 개정령을 입법예고 하였습니다. 이에 따르면, 주권상장법인이 유상증자 계획을 공시한 이후 해당 기업의 주식을 공매도 한 자는 증자 참여를 제한하되, 예외적인 경우 증자 참여를 허용하고 있습니다. (「자본시장과 금융투자업에 관한 법률」제180조의4). 이와 관련 유상증자 참여가 제한되는 공매도 시점과, 증자참여가 허용되는 예외사유를 시행령에서 정하도록 위임하고 있습니다.
해당 시행령에 따르면, 유상증자 계획이 공시된 다음 날부터, 발행가격 산정을 위한 대상 거래기간의 마지막 날(발행가격 산정 기산일)까지 공매도한 경우 증자 참여가 제한됩니다. (「자본시장과 금융투자업에 관한 법률 시행령」208조의4제1항)
다만, 다음의 경우 공매도를 통해 발행가격에 부당한 영향을 미쳤다고 보지 않아 증자참여가 허용됩니다. (「자본시장과 금융투자업에 관한 법률 시행령」제208조의4제2항)
ⅰ) 마지막 공매도 이후 발행가격 산정 기산일까지 공매도 주문 수량 이상을 증권시장 정규거래시간에 매수(체결일 기준)
ⅱ) 금융위원회가 정하는 기준을 충족한 독립된 거래단위를 운영하는 법인 내에서 공매도를 하지 않은 거래단위가 증자 참여
ⅲ) 시장조성 또는 유동성공급을 위한 거래 과정에서 공매도
상기 공매도 제도 개선 관련 「자본시장과 금융투자업에 관한 법률 시행령」 개정안에 따라, 당사의 주식을 해당 기간 동안 공매도하는 투자자께서는 금번 유상증자 참여가 제한될 수 있음을 유의하시기 바랍니다. 해당 법령과 관련된 자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융법규서비스(http://fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
| 자. 개인종합자산관리계좌(ISA 납입한도에 따른 청약제한 위험 개인종합자산관리계좌(이하 ISA 계좌)는 연간 납입가능한도 제한(연간납입한도 2,000만원, 5년간 최대 1억원까지 납입가능하며 납입한도 이월가능)이 있는 계좌입니다. ISA계좌를 통한 신주인수권증서 보유자 청약시, 투자자별 유상증자 배정주수에 해당하는 청약증거금 납입금액이 ISA계좌 잔여납입한도를 초과할 경우 유상청약이 제한될 수 있으니, 투자자께서는 이 점 유의하시기바랍니다. |
| 차. 기타 투자자 유의사항 당사의 대내외적 경영환경 변화에 따라 당사 실적의 급변동이 있을 경우, 투자원금에 대한 손실이 발생할 수 있으므로, 상기 투자위험요소 및 본 증권신고서에 기재된 정보에만 의존하여 투자 판단을 해서는 안되며, 투자자 여러분의 독자적인 판단에 의해야 함을 유의하시어 투자에 임하시기 바랍니다. |
(1) 금번 유상증자 실시로 당사의 주식가치가 향후 하락할 수 있으므로 투자자 여러분들께서는 이 점을 유의하여 주시기 바랍니다.
(2)「자본시장과 금융투자업에 관한 법률」제120조 제3항에 의거하여 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 투자자에게 귀속됩니다.
(3) 이 증권신고서의 공시심사 과정에서 기재사항은 청약일 이전에 변경될 수 있고, 일부 내용은 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있습니다.
(4) 본 건 공모주식을 청약하고자 하는 투자자들은 투자결정을 하기 전에 본 증권신고서의 다른 기재 부분 뿐만 아니라 상기 투자위험요소를 주의 깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 합니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 상기 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 자신의 독자적인 판단에 의해야 합니다.
(5) 당사는 상기에 기술된 투자위험요소 외에도 전반적으로 불안정한 경제상황 등에 의하여 직접적으로 또는 간접적으로 영향을 받을 수 있습니다. 당사의 재무제표는 당사의 재무상태에 영향을 미칠 수 있는 경제상황에 대한 경영자의 현재까지의 평가를 반영하고 있으나, 그 실제결과는 현재시점에서의 평가와는 상당히 다를 수 있는 만큼, 투자자 여러분께서는 이 점을 유의하여 투자에 임하시기 바랍니다.
(6) 만일 상기 투자위험요소가 실제로 발생하는 경우 당사의 사업, 재무상태, 기타 운영결과에 중대한 부정적 영향을 미칠 수 있으며, 이에 따라 투자자가 금번 공모 과정에서 취득하게 되는 당사 주식의 시장가격이 하락하여 투자금액의 일부 또는 전부를 잃게 될 수도 있습니다.
(7) 본건 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 대내외적으로 여러가지 요소들의 영향에 따라 애초에 예측했던 것과 다를 수 있다는 점에 유의해야 합니다.
(8) 금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서(분기 및 반기보고서 포함) 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있으니 투자의사를 결정하시는 데 참조하시기 바랍니다.
이와 같이, 본 건 유상증자를 통해 취득한 당사의 주식 가치는 하락할 수 있으며, 본 증권신고서에서 제시된 투자위험요소 및 기타 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 투자자 여러분의 독자적인 판단에 의해야 함을 다시 한번 유의하여 주시기 바랍니다.
| 카. 신주 물량 출회에 따른 주가 하락 가능성 주식시장의 특성상 향후 주가에 대한 변동성이 있는 관계로 증자에 따른 모집가격 산정 시 결정된 1주당 모집가액보다 향후 추가 상장 후 거래 시점의 주가가 낮아져 투자자에게 금전적 손실을 끼칠 가능성이 있습니다. 또한 금번 유상증자로 인해 추가 발행되는 신주는 보호예수되지 않으므로 신주 상장 직후 주식의 물량 출회 및 주가희석화에 따른 주가하락의 가능성이 있는 점 유의하시기 바랍니다. |
당사는 금번 유상증자로 인해 총 15,223,000주의 약 25.9%에 해당하는 보통주 3,938,000주가 추가로 발행 및 상장될 예정입니다. 또한, 유상증자 직후 무상증자도 진행되므로 유상증자 이후 총 보통주 19,161,000주의 20%에 해당하는 3,832,200주(예정)의 보통주가 추가 발행 및 상장될 예정입니다.
| [당사의 금번 유무상증자 주식수 및 비율 요약] |
| 구분 | 내용 | 비고 | |
|---|---|---|---|
| 유상증자 전 기발행주식수 (보통주) |
자사주 | - | - |
| 자사주제외(A) | 15,223,000 | - | |
| 소계(B) | 15,223,000 | - | |
| 유상증자 신주 수 | 보통주(C) | 3,938,000 | 고정수량 |
| 유상증자비율 | 25.9% | C/B | |
| 유상증자 배정비율 | 0.25868751 | C/A | |
| 유상증자 후 기발행주식수 | 자사주 | - | - |
| 자사주제외 | 19,161,000 | - | |
| 소계 | 19,161,000 | - | |
| 무상증자 배정비율 | 보통주 | 20% | 고정비율 |
| 무상증자 신주 수 | 보통주 | 보통주 보유주식수 * 20% (1주 미만 절사) |
약 3,832,200주 |
| 주1) 실제 무상증자 신주는 기존 주주별 주식보유 수량에 대하여 일괄 배정비율을 적용하므로, 단수주로 인하여 예정보다 감소할 가능성이 있습니다. |
| 주2) 상기 무상증자 배정비율에 따라 각 주주에게 배정된 무상증자 신주 중 1주 미만의 단수주의 경우 신주의 상장 초일 종가를 기준으로 현금 지급합니다. |
주식시장의 특성상 향후 주가에 대한 변동성이 있는 관계로 증자에 따른 모집가격 산정 시 결정된 1주당 모집가액보다 향후 추가 상장 후 거래 시점의 주가가 낮아져 투자자에게 금전적 손실을 끼칠 가능성이 있습니다.
금번 유상증자에 따라 신규 상장되는 주식은 보호예수되지 않는 관계로, 신주의 추가 상장 시점에 대규모 물량이 일시에 출회될 가능성이 있으며 이로 인해 주가가 급락할 수 있습니다. 금번 유상증자에 따른 주권의 상장일은 2023년 11월 23일로 예정되어 있으며, 무상증자에(무상증자 여부는 회사의 유통주식 수에 영향을 미치나, 회사에 대한 주주의 권리 측면에서 변동은 없습니다) 따른 주권 상장일은 2023년 11월 30일로 예정되어 있으므로 유통주식수의 증가로 인하여 주가 희석화 위험이 발생할 수 있으며, 추가 상장일 이전이라도 유통주식수 희석화 우려가 당사의 주가가 상승하는데 제약 요인으로 작용할 가능성이 있습니다. 이 경우, 본 유상증자의 1주당 모집가액보다 추가상장 시점의 주가가 더 낮아 금전적 손실이 발생할 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
또한 당사는 임직원들에게 인센티브를 제공하고자 주식매수선택권을 부여하고 있습니다. 증권신고서 제출일 현재 행사 가능한 주식매수선택권은 총 4,500주입니다. 향후 2025년 02월까지 행사가능한 잠재적인 주식매수선택권은 총 29,500주입니다. 주식매수선택권의 행사가격은 증권신고서 제출일 기준 당사 주식의 시가를 상회하고 있어 행사될 가능성이 높지 않으나, 향후 시가가 상승하여 주식매수선택권이 행사 될 경우 기존 투자자들의 지분가치가 희석 될 가능성이 있으니 참고하시기바랍니다.
| [당사의 주식매수선택권 부여 현황] |
| (단위 : 원, 주) |
| 부여 받은자 |
관 계 | 부여일 | 부여방법 | 주식의 종류 |
최초 부여 수량 |
당기변동수량 | 총변동수량 | 기말 미행사수량 |
행사기간 | 행사 가격 |
의무 보유 여부 |
의무 보유 기간 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 행사 | 취소 | 행사 | 취소 | |||||||||||
| 김미화 | 미등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 4,500 | - | - | - | - | 4,500 | 23.03.25 ~ 28.03.24 | 118,712 | X | - |
| 하선아 | 미등기임원 | 2022년 02월 07일 | 신주교부 | 보통주 | 4,500 | - | - | - | - | 4,500 | 24.02.07 ~ 29.02.06 | 42,274 | X | - |
| OOO | 미등기임원 | 2022년 07월 15일 | 신주교부 | 보통주 | 4,500 | - | - | - | - | 4,500 | 24.07.15 ~ 29.07.14 | 41,940 | X | - |
| OOO | 미등기임원 | 2023년 02월 23일 | 신주교부 | 보통주 | 6,000 | - | - | - | - | 6,000 | 25.02.23 ~ 30.02.22 | 36,185 | X | - |
| OOO | 미등기임원 | 2023년 02월 23일 | 신주교부 | 보통주 | 5,000 | - | - | - | - | 5,000 | 25.02.23 ~ 30.02.22 | 36,185 | X | - |
| OOO | 미등기임원 | 2023년 02월 23일 | 신주교부 | 보통주 | 5,000 | - | - | - | - | 5,000 | 25.02.23 ~ 30.02.22 | 36,185 | X | - |
| 출처: 당사 정기보고서 |
또한 대량 실권이 발생하여 당사가 공동대표주관회사에게 실권수수료를 지급할 경우 당사 주가에 부정적인 영향을 미칠 수 있습니다. 공동대표주관회사가 당사 주식 인수 후 빠른 시일내에 인수한 주식를 장내에서 매각하게 된다면 단기적으로 당사 주가에 악영향을 미칠 것으로 예상할 수 있으며, 공동대표주관회사에서 인수한 주식을 일정기간 보유하더라도 동 인수물량이 잠재 매각물량으로 존재하여 주가 상승에 부담으로 작용할 가능성이 높다고 예상됩니다.
또한 공동대표주관회사는 실권수수료를 추가로 지급받게 되는 바, 이를 고려시 실권주 매입단가가 일반청약자들 보다 약 15.0% 낮은 것과 같은 결과가 초래되어 이 또한 당사 주가에 부정적 영향을 미칠 가능성이 있다고 판단됩니다. 투자자 여러분께서는 이 점에 유의하시어 투자에 임하시기 바랍니다.
|
타. 주가의 높은 변동성에 따른 시장조치 관련 위험 |
당사의 최근 1년 주가를 검토하였을 때, 2022년 07월부터 2023년 08월 중순까지 크게 세가지 이슈로 주가가 급등락하였습니다. '22년 7월 Vax-NK/HCC 데이터 발표와 함께 급등하였고, '22년 8월 Vax-DC 임상연구 조기종료로 급락한 바 있으며, '23년 4월 Vax-NK 진행성 간암 환자 대상 치료목적 사용 승인과 함께 급등하였습니다.
한국거래소는 시장감시규정 및 그 시행세칙에 의거하여 주가상승률, 거래 회전율 및 주가 변동성등이 과도할 경우 투자주의종목 및 투자경고종목을 지정하고 있습니다.
이에 따라 당사는 2022년 07월부터 2023년 08월 중순까지 코스닥시장 업무규정 제 조의 2와 같은 규정 시행세칙 제8조의 5에 따른 공매도 과열종목, 업무규정 제23조의 2와 같은 규정 시행세칙 28조의 3에 따른 단기과열종목 지정예고를 받은 바 있습니다 예고일부터 10거래일 이내 주가 상승률, 거래 회전율 및 주가 변동성과 관련하여 다음의 요건에 모두 해당하고, 해당일의 종가가 직전 거래일 종가 및 지정예고일 전일 종가 대비 상승한 경우에는 그 직후 매매거래일부터 단기과열종목에 지정됩니다.
당사는 신약 개발을 사업으로 영위하는 회사로 임상 결과에 따라 주가가 급등락할 수 있는 가능성이 상대적으로 높은 편입니다. 이에 따라 투자경고종목 지정 가능성이 타 산업군 대비 높을 수 있습니다. 실제로 당사는 상장 직후 임상진행상황 발표에 따라 주가가 급등락하여 2020년초부터 2021년까지 다수의 시장조치를 받은 이력이 있습니다. 투자경고종목 지정 후 실제 매매거래정지 조치가 취해져 해당 종목의 환금성이 제한될 가능성도 존재하므로 투자자께서는 이 점 유의하시기 바랍니다.
| [상장 이후 시장조치 이력 - 신주발행 관련 제외] |
| 일자 | 공시유형 |
|---|---|
| 2020-09-22 | [투자주의]단일계좌 거래량 상위종목 |
| 2020-10-30 | [투자주의]투자경고종목 지정예고 |
| 2020-11-02 | 투자경고종목지정 |
| 2020-11-03 | 매매거래정지 예고 |
| 2020-11-04 | 매매거래 정지 및 재개(투자경고종목 지정중) |
| 2020-11-06 | 투자위험종목 지정예고 |
| 2020-11-06 | 매매거래정지 예고 |
| 2020-11-17 | 투자위험종목 지정 |
| 2020-11-17 | 매매거래 정지 및 재개(투자위험종목 최초지정) |
| 2020-12-02 | 매매거래정지 예고 |
| 2020-12-03 | 투자위험종목 지정해제 |
| 2020-12-03 | 투자경고종목지정 |
| 2020-12-23 | [투자주의]투자경고종목 지정해제 및 재지정 예고 |
| 2020-12-29 | [투자주의]투자경고종목 지정예고 |
| 2020-12-30 | 투자경고종목지정(재지정) |
| 2021-01-04 | 투자위험종목 지정예고 |
| 2021-01-04 | 매매거래정지 예고 |
| 2021-01-05 | 매매거래 정지 및 재개(투자위험종목 최초지정) |
| 2021-01-05 | 투자위험종목 지정 |
| 2021-01-20 | 투자위험종목 지정해제 |
| 2021-01-20 | 투자경고종목지정 |
| 2021-02-03 | [투자주의]투자경고종목 지정해제 및 재지정 예고 |
| 2022-02-23 | 공매도 과열종목 지정(공매도 거래 금지 적용) |
| 2022-03-04 | 공매도 과열종목 지정(공매도 거래 금지 적용) |
| 2022-03-08 | 공매도 과열종목 지정(공매도 거래 금지 적용) |
| 2022-03-15 | 공매도 과열종목 지정(공매도 거래 금지 적용) |
| 2022-07-19 | 공매도 과열종목 지정(공매도 거래 금지 적용) |
| 2022-07-20 | (예고)단기과열종목(3거래일 단일가매매) 지정예고 |
| 2022-08-04 | 공매도 과열종목 지정(공매도 거래 금지 적용) |
| 2023-02-16 | 공매도 과열종목 지정(공매도 거래 금지 적용) |
| 2023-02-21 | 공매도 과열종목 지정(공매도 거래 금지 적용) |
| 2023-03-09 | 공매도 과열종목 지정(공매도 거래 금지 적용) |
| 2023-03-13 | 공매도 과열종목 지정(공매도 거래 금지 적용) |
| 2023-03-16 | 공매도 과열종목 지정(공매도 거래 금지 적용) |
| 2023-04-17 | [투자주의]스팸관여과다종목 |
| 출처 : KRX |
| [박셀바이오 주가 추이 차트(2022.07 ~ 2023.08)] |
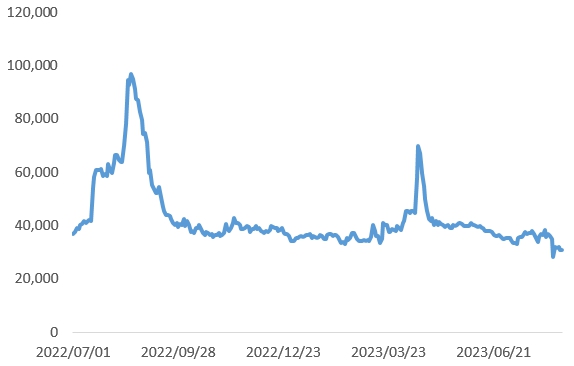 |
|
박셀바이오 주가 추이 차트(2022.07 ~ 2023.08) |
| 출처 : KRX |
| [단기과열종목 지정예고 조건] |
| 구 분 | 내 용 |
|---|---|
| ① 주가상승률 | 당일 종가가 직전 40거래일 종가 평균의 130% 이상 |
| ② 거래회전율 | 당일을 포함한 최근 2거래일 일별 거래회전율 평균이 직전 40거래일 일별 거래회전율 평균의 600% 이상 |
| ③ 주가변동성 | 당일을 포함한 최근 2거래일 일별 주가변동성 평균이 직전 40거래일 일별 주가변동성 평균의 150% 이상 |
| 출처: | 한국거래소 전자공시시스템 |
|
파. 공모자금 사용 관련 위험 |
당사는 금번 공모 유상증자 이전 2020년 9월 IPO를 통해 공모자금을 모집한 바 있습니다. 해당 자금은 약 293억원으로, 파이프라인 연구개발 및 임상 시험에 약 185억원, 운영자금 98억원 그리고 시설자금 97억원이 쓰일 계획이었습니다.
| [공모자금 사용 계획] |
| (단위: 백만원) |
| 구 분 | 내 역 | 2020년 | 2021년 | 2022년 | 합계 | 비고 |
|---|---|---|---|---|---|---|
| 시설자금 | 스마트 제조공정 개발실 설치 | - | 570 | - | 570 | - |
| 인력충원에 따른 사무집기 등 | - | 395 | - | 395 | - | |
| 연구개발비 | 차세대 Vax-CAR 연구개발 인건비, 소모품비 등 | 888 | 2,539 | 2,976 | 6,403 | - |
| 임상시험비 | Vax-NK/HCC, Vax-DC/MM 임상시험비 등 | 1,917 | 6,282 | 3,941 | 12,140 | 주1) |
| 운영자금 | 인건비 및 기타 부대비용 | 1,424 | 3,667 | 4,705 | 9,796 | - |
| 합 계 | 4,229 | 13,453 | 11,622 | 29,304 | - | |
| 주) | '임상시험비'의 세부내역은 다음과 같습니다. |
| (단위: 백만원) |
| 구분 | 내 역 | 금 액 | 시 기 |
|---|---|---|---|
| 임상시험비 | Vax-NK/HCC 임상 2a 및 2b상 임상시험 비용 | 3,958 | 2020년 4분기 ~ 2022년 4분기 |
| Vax-DC/MM 임상 2a 및 2b상 임상시험 비용 | 4,717 | 2021년 3분기 ~ 2022년 4분기 | |
| Vax/NK+DC GBM 비임상 및 1/2a상 임상시험 비용 | 1,665 | 2021년 1분기 ~ 2022년 4분기 | |
| Vax-CAR-T 비임상 시험비용 | 900 | 2021년 1분기 ~ 2021년 4분기 | |
| Vax-mCAR-T 비임상 시험비용 | 900 | 2021년 1분기 ~ 2021년 4분기 |
| 출처 : 당사 증권신고서 |
그러나 당사는 2023년 반기보고서 기준 2022년까지 사용 예정이었던 공모자금 293억원 중 135억원을 사용하였습니다. 일부 임상연구 진행이 지연되고, 파이프라인 변경 등의 사유로 공모자금이 IPO당시의 예상한 것보다 미진하게 사용되었습니다. 파이프라인 별 공모 자금 사용 내역은 다음과 같습니다.
| (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 증권신고서 등의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
| 코스닥 상장 공모(모집) |
1회 | 2020년 09월 15일 | 연구개발비, 임상시험비 등 연구자금 |
18,543 | 기타자금 (연구개발, 임상시험 등) |
7,629 |
자금의 사용이 완료되지 않았으며, 미사용자금은 안정성 있는 예적금 위주의 금융상품에 보관예정입니다. 미사용 자금은 자금의 사용계획에 맞추어 기타자금(연구개발비,임상시험비)으로 사용 예정입니다. |
| 코스닥 상장 공모(모집) |
1회 | 2020년 09월 15일 | 운영자금 | 9,796 | 운영자금 |
5,882 |
자금의 사용이 완료되지 않았으며, 미사용자금은 안정성 있는 예적금 위주의 금융상품에 보관예정입니다. 미사용 자금은 자금의 사용계획에 맞추어 운영자금으로 사용 예정입니다. |
| 코스닥 상장 공모(모집) |
1회 | 2020년 09월 15일 | 시설자금 | 965 | - | - | - |
| (단위 : 백만원) |
| 구 분 | 내 역 | 파이프라인 | 2020년 | 2021년 | 2022년 | 2023년 반기 |
합계 |
|---|---|---|---|---|---|---|---|
| 시설자금 | 스마트 제조공정 개발실 설치 | - | - | - | - | - | |
| 인력충원에 따른 사무집기 등 | - | - | - | - | - | ||
| 연구개발비 | 차세대 Vax-CAR 연구개발 인건비, 소모품비 등 | Vax-CAR T | 57 | 145 | 261 | 574 | 7,629 |
| Vax-DC | 16 | - | - | - | |||
| Vax-NK | 268 | - | 841 | - | |||
| 기초연구 | 30 | 279 | 323 | 48 | |||
| 박스루킨15 | 36 | 440 | 152 | 383 | |||
| 임상시험비 | Vax-NK/HCC, Vax-DC/MM 임상시험비 등 | Vax-CAR T | - | - | - | - | |
| Vax-DC | - | 130 | 55 | - | |||
| Vax-NK | 77 | 1,122 | 916 | 332 | |||
| 기초연구 | - | - | - | - | |||
| 박스루킨15 | - | 302 | 164 | 680 | |||
| 운영자금 | 인건비 및 기타 부대비용 | 586 | - | 2,714 | 2,583 | 5,882 | |
| 합 계 | 1,070 | 2,418 | 5,425 | 4,599 | 13,512 | ||
당사는 금번 유상증자를 통해 잔존한 공모자금과 새로 유입될 공모자금을 바탕으로 'V. 자금의 사용목적'에 기재한 바와 같이 사업계획을 구상하고 있습니다. 그러나 IPO 공모대금이 계획과 다르게 사용된 바와 같이 임상중단 및 지연, 임상위수탁 및 제조관련 비용 증가, 연구 및 운영 인력 모집 관련 어려움 등 당사의 사업계획과 다른 이벤트가 발생할 경우 증권신고서에 기재한 바와 상이하게 자금이 사용될 가능성이 존재합니다. 또한 당사 경영진은 금번 공모를 통해 조달한 공모자금을 투자자가 동의하지 않을 수 있는 또는 당사 주주에게 유리한 수익이 발생하지 않는 방식으로 사용할 수 있습니다. 이에 투자자께서는 주의하시기 바랍니다.
| ※ 상기 제반사항을 고려하시어 투자자 제위의 현명한 판단을 바랍니다. 투자자는 본건 공모주식에의 투자 여부를 결정함에 있어서 필요한 경우 스스로 별도의 독립된 자문을 받아야 하며, 이에 따른 투자의 결과에 대하여는 투자자가 책임을 부담합니다. |
IV. 인수인의 의견(분석기관의 평가의견)
| 본 장은 「자본시장과 금융투자업에 관한 법률」 제119조 및 제125조, 금융감독원의 '금융투자회사의 기업실사 모범규준'에 따라 본건 공모 지분증권 인수인이 당해 공모 지분증권에 대한 의견을 기재하고 있는 부분입니다. 따라서 본 장의 작성 주체는 공동대표주관회사인 한국투자증권(주) 및 신한투자증권(주)이며, 발행회사인 (주)박셀바이오는 "동사"로 기재였습니다. 본 장에 기재된 분석의견 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 여러가지 요소들의 영향에 따라 예측했던 것과 다를 수 있다는 점을 유의하시기 바랍니다. |
1. 분석기관
| 구 분 | 증 권 회 사 | |
|---|---|---|
| 회 사 명 | 고 유 번 호 | |
| 공동대표주관회사 | 한국투자증권(주) | 00160144 |
| 공동대표주관회사 | 신한투자증권(주) | 00162416 |
2. 분석의 개요
공동대표주관회사인 한국투자증권(주)와 신한투자증권(주)(이하 "공동대표주관회사"라 합니다.)는『자본시장과금융투자업에관한법률』제71조 및 동법시행령 제68조에 의거 공정한 거래질서 확립과 투자자 보호를 위해 다수인을 상대로 한 모집ㆍ매출 등에 관여하는 인수회사로서, 발행인이 제출하는 증권신고서 등에 허위의 기재나 중요한 사항의 누락을 방지하는데 필요한 적절한 주의를 기울였습니다.
공동대표주관회사는 인수 또는 모집ㆍ매출의 주선업무를 수행함에 있어 적절한 주의의무를 다하기 위해 금융감독원이 제정한「금융투자회사의 기업실사(Due Diligence) 모범규준」(이하 "모범규준"이라 한다)의 내용을 내부 규정에 반영하여 2012년 02월 01일부터 제출되는 지분증권, 채무증권 증권신고서를 대상(자산유동화증권 등 제외)으로 기업실사를 의무적으로 수행하도록 규정하고 있습니다.
다만, '모범규준' 제3조 제②항에 따라 발행회사의 재무 및 영업현황, 사업 환경, 투자위험, 인수 형태, 신용평가등급 등을 감안하여 강화하거나, 완화할 수 있으며, 동조 제⑤항에 따르면 금융투자회사의 이사회나 리스크관리위원회의 의사결정을 거쳐 '모범규준'의 내용(실사수준)을 생략하거나 강화 또는 완화 적용할 수 있도록 허용하였는 바, 주관회사는 지분증권의 인수 또는 모집·매출의 주선업무를 수행함에 있어서 지분증권의 특성 및 발행회사의 일정요건 충족여부 등에 따라 기업실사 수준을 완화하여 적용할 수 있도록 규정하고 있습니다.
본 지분증권은 공동대표주관회사인 한국투자증권(주)과 신한투자증권(주)의 내부 규정상 기업실사 기준을 적용하여 기업실사 업무를 수행하였습니다.
| 「금융투자회사의 기업실사 모범규준」 제3조(적용범위 등) ①이 규준은 법 제119조제3항의 규정에 의한 증권신고서 및 법 제122조의 규정에 의한 정정신고서를 제출하는 경우에 적용하며, 영업의 실체가 있는 발행회사가 제출하는 지분증권, 채무증권 증권신고서를 대상으로 하고 자산유동화증권 등은 적용대상에서 제외된다. ②이 규준은 주간회사가 업무수행 중 참고해야 할 기본적인 지침으로 발행회사의 재무 및 영업 현황, 사업 환경, 투자위험, 인수 형태 등을 감안하여 강화하거나 완화하는 등 탄력적으로 운용할 수 있다. ③기업공개의 경우 기업공개 실사절차의 특성을 감안하여 이 규준의 내용중 한국거래소의 상장심사지침 등에서 의무사항으로 규정하고 있는 내용과 중복되는 부분에 대해서는 이를 생략하거나 완화할 수 있다. ④채무증권의 경우 i)보증유무, 상환조건(만기, 옵션유무), 특약 등 해당 사채의 특성, ii)법 제119조제2항에서 규정하고 있는 일괄신고서에 의한 발행인지 여부, iii)발행회사가 시행령 제121조제6항의 요건을 충족하고 있는지 여부, iv)해당 사채권에 대한 신용평가등급(외부 및 내부) 등을 감안하여 합리적인 기준에 따라 이 규준을 완화할 수 있다. ⑤제2항 내지 제4항에 따라 이 규준을 생략하거나 강화 또는 완화하는 경우에는 이사회나 리스크관리위원회(이하 ‘리스크관리위원회 등’)의 의사결정을 거쳐야 한다. |
3. 기업실사 일정 및 주요 내용
| 일자 | 실사 내용 |
|---|---|
| 2023-07-03 | * 발행회사 초도 방문 - 발행회사의 유상증자 의사 확인 - 자금조달 희망금액 등 발행회사 의견 청취 |
| 2023-07-03 ~ 2023-07-10 |
* 발행회사의 유상증자 방식결정 협의 * 유상증자 일정 협의 및 확정 * 유상증자를 위한 사전 준비사항 및 진행절차 설명 - 발행가 산정 및 세부일정 설명 * 세부 증자관련 논의 - 유상증자 방식 결정 및 대주주 증자 참여 논의 * 유상증자 진행에 대한 질의/응답 * 실사 사전요청자료 송부 |
| 2023-07-10 ~ 2023-07-26 |
* 증자리스크 검토 - 발행시장 상황, 자금조달규모 적정성, 공모가액 희망 할인율 * 발행사와의 협의 - 발행가액 산정방식, 발행일정, 발행규모, 인수수수료 협의 * 기업실사 진행 및 추가자료 요청 - 기업실사 관련 자료요청 및 절차에 대한 설명 - 기업실사 관련 Q&A * 이사회 등 상법 절차 및 정관 등 검토 * 투자위험요소 실사 1) 사업위험관련 실사 - 기존사업 및 신규사업에 대한 세부사항 등 체크 2) 회사위험관련 실사 - 재무관련 위험 및 우발채무 등의 위험요소 등 체크 3) 기타위험관련 실사 - 주가 희석화관련 위험 등 체크 * 담당자 인터뷰 - 회사개요, 사업의 내용, 주요 재무적 이슈 확인 - 자금사용 계획 파악 - 향후 사업추진계획 및 발행회사의 비전 검토 |
| 2023-07-26 ~ 2023-08-07 |
* 증권신고서 작성 및 조언 * 이사회의사록 등 검토 * 인수계약서 체결 * 증권신고서 인수인의 의견 완료 * 첨부서류 등 검토 * 증권신고서 업데이트 |
4. 기업실사 참여자
[발행회사]
| 소속기관 | 부서 | 성명 | 직위 | 실사업무분장 | 주요경력 |
|---|---|---|---|---|---|
| (주)박셀바이오 | 경영관리본부 | 곽내신 | 본부장 | 발행업무 총괄 | 재무관리 26년 (CFO) |
| 경영관리본부 | 양승호 | 부장 | 발행업무 기획 및 실무 | 재무,IB 18년 | |
| 경영관리본부 | 강경인 | 사원 | 발행업무 실무 | 자금 3년 | |
| 전략기획본부 | 신의철 | 본부장 | 사업기획 실무 | 사업기획 19년 | |
| 전략기획본부 | 이진선 | 과장 | 경영기획 실무 | 경영기획 7년 |
[대표주관회사]
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 | 참여기간 | 주요경력 |
|---|---|---|---|---|---|---|
| 한국투자증권 | IB3본부 | 김영우 | 본부장 | 기업실사 총괄 | 2023년 07월 07일 ~ 2023년 08월 07일 | 기업금융업무 22년 |
| 한국투자증권 | 커버리지2담당 | 김동완 | 담당 | 기업실사 책임 | 2023년 07월 07일 ~ 2023년 08월 07일 | 기업금융업무 23년 |
| 한국투자증권 | ECM2부 | 장동욱 | 이사 | 기업실사 책임 | 2023년 07월 07일 ~ 2023년 08월 07일 | 기업금융업무 27년 |
| 한국투자증권 | ECM2부 | 박종욱 | 팀장 | 기업실사 책임 | 2023년 07월 07일 ~ 2023년 08월 07일 | 기업금융업무 11년 |
| 한국투자증권 | ECM2부 | 송규진 | 대리 | 기업실사 실무 | 2023년 07월 07일 ~ 2023년 08월 07일 | 기업금융업무 6년 |
| 한국투자증권 | ECM2부 | 박주혁 | 주임 | 기업실사 실무 | 2023년 07월 07일 ~ 2023년 08월 07일 | 기업금융업무 3년 |
| 신한투자증권 | 기업금융2본부 | 권혁준 | 본부장 | 기업실사 총괄 | 2023년 07월 07일 ~ 2023년 08월 07일 | 기업금융업무 25년 |
| 신한투자증권 | 기업금융1부 | 정재훈 | 이사 | 기업실사 책임 | 2023년 07월 07일 ~ 2023년 08월 07일 | 기업금융업무 24년 |
| 신한투자증권 | 기업금융1부 | 김영환 | 부장 | 기업실사 점검 | 2023년 07월 07일 ~ 2023년 08월 07일 | 기업금융업무 10년 |
| 신한투자증권 | 기업금융1부 | 조한주 | 차장 | 기업실사 실무 | 2023년 07월 07일 ~ 2023년 08월 07일 | 기업금융업무 8년 |
| 신한투자증권 | 기업금융1부 | 김지우 | 대리 | 기업실사 실무 | 2023년 07월 07일 ~ 2023년 08월 07일 | 기업금융업무 4년 |
| 신한투자증권 | 기업금융1부 | 강동수 | 대리 | 기업실사 실무 | 2023년 07월 07일 ~ 2023년 08월 07일 | 기업금융업무 3년 |
5. 기업실사 세부항목 및 점검 결과
- 동 증권신고서에 첨부되어 있는 기업실사 보고서를 참조해 주시기 바랍니다.
6. 종합의견
가. 공동대표주관회사인 한국투자증권(주)과 신한투자증권(주)는 (주)박셀바이오가 2022년 08월 07일 이사회에서 결의한 보통주식 3,938,000주에 대한 주주배정 후 실권주 일반공모 증자를 잔액인수함에 있어 (주)박셀바이오에 대하여 다음과 같이 평가합니다.
| 긍정적요인 | ▶ 동사의 주요 파이프라인인 Vax-NK/HCC는 임상계획을 예정대로 종료할 수 있는 15명 이상의 환자를 등록하였고('23년 7월 기준 17명), 메타 분석을 통해 동사 치료 프로토콜 결과의 통계적 유의성을 보완하고 있어 2a상이 순조롭게 진행되고 있습니다. '24년 내로 2a 승인과 매출 발생이 가능할 조건부 허가를 기대하고 있어 재무적인 성과를 낼 가능성이 높아졌습니다 ▶ 동사의 주요 파이프라인인 동물용 항암제 박스루킨의 경우, 세계 최초의 반려견 대상 항암제로 품목 허가 시 시장성이 높을 것으로 예상됩니다. 신고서 제출일 기준 품목허가 신청을 위한 환견 모집이 완료되었으며, '23년 하반기에 농림축산검역본부에 품목허가를 재신청 할 예정이며, 품목허가 승인을 받으면 상품화를 거쳐 매출 실현을 기대하고 있습니다. ▶ 연구개발비가 지속적으로 발생하고 있고 매출이 발생하지 않아 자본이 지속적으로 감소하고 있으나, 연구개발에 따른 비용을 자산처리하지 않아 향후 재무적으로 예상치 못한 손상이 발생할 가능성이 낮습니다. |
| 부정적요인 | ▶ 상장 이후 매출이 발생한 사실이 없습니다. 파이프라인 별 일정이 밀려 IPO당시 매출이 발생할 것으로 예상했던 '22년에도 매출이 발생하지 않았습니다. '23년 기준 순조롭게 진행되고 있는 파이프라인 또한 예상치 못하게 지연이 된다면 '24년에도 매출 발생이 어려울 수 있습니다. ▶ 최대주주와 주요 특수관계인이 배정물량의 30% 청약할 것으로 예정되어있어, 구주주청약률 제고에 어려움이 있을 수 있습니다. 또한 청약을 위해 구주를 매각하여 재원을 마련할 계획으로, 매각에 따른 주가 하락 위험이 있습니다. |
| 자금조달의 필요성 |
▶ 동사는 금번 유상증자를 통해 조달하는 자금을 운영자금 및 시설자금으로 활용할 계획입니다. ▶ 금번 유상증자를 통해 조달한 자금의 세부사용 내역은 "Ⅴ. 자금의 사용목적"을 참고하시기 바랍니다. |
나. 공동대표주관회사는 (주)박셀바이오가 제출한 자료와 객관적으로 정확하고 신뢰할 수 있다고 믿어지는 자료를 중심으로 실사를 수행하였으며, 객관적인 입장에서 공정을 기하기 위하여 최선의 노력을 다하였습니다.
다. 공동대표주관회사는 상기 실사를 통해 제공받는 자료들로부터 도출된 결과나 오류, 누락 등에 대하여 책임지지 않으며, 인간적 또는 기계적, 기타 그 외의 다른 요인에 의한 오류발생 가능성으로 인해 본 평가 내용에 대해 명시적으로 혹은 묵시적으로도 증명이나 서명 또는 보증 및 단언을 할 수 없습니다.
라. 동사의 금번 유상증자는 국내외 거시경제 변수 변화로 투자수익에 대한 확실성이 저하될 수 있습니다. 투자자 여러분께서는 상기 검토결과는 물론 동 증권신고서 및 투자설명서에 기재된 동사의 회사 전반에 걸친 현황 및 재무상의 위험과 산업 및 영업상의 위험요인 등을 감안하시어 투자에 유의하시기 바랍니다.
또한, 공동대표주관회사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 동 증권신고서 및 투자설명서에 기재하지 않은 사항이라 하더라도 동사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자께서는 동 증권신고서 및 투자설명서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 독자적이고도 세밀한 판단에 의해 투자결정을 하시기 바랍니다.
| 2023년 08월 07일 |
| 공동대표주관회사 : 한국투자증권 주식회사 |
| 대표이사 정 일 문 |
| 공동대표주관회사: 신한투자증권 주식회사 |
| 대표이사 김 상 태 |
V. 자금의 사용목적
1. 모집 또는 매출에 의한 자금조달 내역
가. 자금조달금액
|
(단위: 원) |
|
구 분 |
금 액 |
|---|---|
|
모집 또는 매출총액(1) |
71,789,740,000 |
|
발행제비용(2) |
1,179,389,570 |
|
순 수 입 금 [ (1)-(2) ] |
70,610,350,430 |
| 주1) | 상기 금액은 확정발행가액을 기준으로 산정한 금액입니다 |
| 주2) | 상기 모집총액은 우선적으로 하단에 기재된 자금의 사용 목적에 따라 사용할 예정입니다. |
| 주3) | 발행제비용은 공모금액 및 실권규모에 따라 변경될 수 있으며, 상기 기재 금액은 청약 초과로 인하여 실권이 발생하지 않은 상황을 가정하여 산정되었습니다. 또한 상장수수료는 상장신청일 직전일 주가에 따라 변동될 수 있습니다. |
나. 발행제비용의 내역
|
(단위: 원) |
|
구 분 |
금 액 |
지급일자 |
계산근거 |
|---|---|---|---|
|
발행분담금 |
12,922,150 |
신고서제출일 |
모집총액의 0.018%(10원 미만 절사) |
|
인수수수료 |
933,266,620 |
납입일익일 |
인수수수료 1.3% |
| 표준코드발급수수료 | 10,000 | 표준코드발급 신청일 | 신주인수권증서 건당 10,000원 |
|
상장수수료 |
8,860,000 |
신주상장일 |
730만원 + 700억원 초과금액의 10억원당 6만원 (코스닥시장상장규정 시행세칙 별표 14) |
| 주식발행등록수수료 | 1,000,000 | - | 1,000주당 300원(주식 및 신주인수권증서 각각 별도 징수, 수수료 건당 상한 50만원 및 하한 4천원) (주식·사채 등의 전자등록업무규정 시행세칙 별표 |
|
등록세 |
7,876,000 |
등기일 |
증자 자본금의 0.4% |
|
교육세 |
1,575,200 |
등기일 |
등록세의 20% |
|
기타비용 |
213,879,600 |
- |
투자설명서 인쇄 및 발송비, 표준코드발급비용 등 |
|
합 계 |
1,179,389,570 |
- |
- |
| 주1) | 상기 금액은 확정 발행가액을 기준으로 산정한 금액입니다. |
| 주2) | 발행제비용은 공모금액 및 상장신청일 직전일 한국거래소에서 거래되는 당사의 보통주식 종가, 유관기관 정책 등에 따라 변동될 수 있습니다. |
| 주3) | 기타비용은 예상금액으로 변동될 수 있습니다. |
2. 자금의 사용목적
가. 자금의 사용목적
당사가 금번 보통주 유상증자를 통해 조달 예정인 자금은 운영자금 및 시설자금으로 사용할 계획입니다.
| (기준일 : | 2023년 10월 30일 | ) | (단위 : 백만원) |
| 시설자금 | 영업양수 자금 |
운영자금 | 채무상환 자금 |
타법인증권 취득자금 |
기타 | 계 |
|---|---|---|---|---|---|---|
| 45,192 | - | 26,598 | - | - | - | 71,790 |
나. 자금의 세부 사용내역
하기 당사 자금 사용 계획의 우선순위에 따라 자금을 차례대로 집행할 계획입니다. 부족분은 당사의 자체자금으로 충당할 계획입니다.
| [자금 사용 계획] |
| [단위 : 백만원] |
| 구분 | 2024년 | 2025년 | 2026년 | 합계 | 자금사용 우선순위 |
||
| 연구개발비 (약 556억) |
연구개발비 및 임상시험비 |
Vax-NK >NK/HCC >NK/PDAC >NK/SCLC |
5,003 | 7,952 | 6,970 | 19,925 | HCC : 1 PDAC : 1 SCLC: 3 |
| Vax-CAR >CAR-T >CAR-NK >CAR-MIL |
7,610 | 7,659 | 5,109 | 20,378 | 3~5 | ||
| 동물용의약품 >박스루킨-15 |
1,241 | 833 | 0 | 2,074 | 1 | ||
| 인건비 | 연구개발 인건비 | 3,374 | 4,408 | 5,458 | 13,239 | - | |
| 시설자금 (약451억) |
신사옥 건립 | 신사옥 및 연구소 건축 (GMP 제조소 포함) | 21,424 | 18,313 | 1,560 | 41,296 | 2 |
| 생산시설 임차 | 세포치료제, CAR 치료제 생산시설 | 2,981 | 457 | 457 | 3,896 | 2 | |
| 운영자금 (약232억) |
인건비 | 연구개발비 미포함 인건비 | 2,198 | 3,075 | 4,226 | 9,499 | - |
| 기타 운영자금 | 판관비 등 | 1,940 | 2,540 | 3,240 | 7,720 | - | |
| 광고선전비 | Vax-NK/HCC 판촉비용 | 145 | 125 | 125 | 395 | 4 | |
| 박스루킨 및 기능성 액상사료 마케팅 | 430 | 330 | 330 | 1,090 | 1 | ||
| 동물사업부 | 박스루킨 및 기능성 액상사료 생산, 유통비용 | 749 | 1,384 | 2,304 | 4,437 | 1 | |
| 총 액 | 47,095 | 47,075 | 29,780 | 123,950 | - | ||
| 주) 상기 자금사용 계획은 금번 유상증자를 통해 조달할 예정인 증자대금 및 당사가 기존 보유한 현금성 자산 및 금융상품을 포함하여 구상한 계획안 입니다. |
상기 각 분류별 자금사용 세부사항은 다음과 같습니다.
(1)Vax-NK
당사의 Vax-NK 플랫폼 중 주력은 자연살해세포치료제인 Vax-NK/HCC(간암)으로 현재 2024년 상반기 내 2a상을 종료하는 것을 목표로 진행하고 있습니다. 자연살해세포 기반 치료제는 글로벌 수준에서 아직 처방되고 있지 않은 제품으로 현재 임상단계에 있는 몇몇 파이프라인들 만이 잠재적인 경쟁관계에 있습니다.
현재 당사와 같은 간세포종을 대상으로 국내에서 승인된 경쟁사 제품이 있습니다. 그러나 당사의 VAX-NK/HCC는 NK의 순도가 85%이상의 고순도 NK치료로, 경쟁사 제품 대비 높은 효과가 나타날 것으로 예상되어 당사의 VAX-NK/HCC가 3상을 마치고 시장에 나갔을 때 간암적응증에서의 우위를 점할 것 예상하고 있습니다. 이를 위해 본 유상증자로 조달한 자금 중 139억원을 투자하여 3상을 진행 할 것이고 추가 필요자금은 L/O 또는 2a상 종료 후 조건부 승인으로 인한 당사 매출로 유입된 현금을 사용할 예정입니다. 일반적으로 임상단계가 진행될 수록 임상인원이 많아지기 때문에, 전 단계보다 많은 비용이 소요됩니다. 당사 역시 3상의 경우 2026년도까지 3개년간 보수적으로 약 90명을 대상으로 임상을 진행할 계획이기 때문에(2상 17명으로 진행하였음) 기존보다 많은 금액이 소요 될 것으로 계획하고 있습니다.
췌장암은 교모세포종과 함께 암종 중 최악의 암으로 불리며 세계적으로 예후가 매우 나쁜 암이며 수술이 가능한 환자도 전체의 12.5%에 불과합니다. 본 암종을 대상으로 하는 면역항암제는 국제적으로도 없으며, 국내에서도 GC셀의 이뮨셀엘씨주, 젬백스의 리아백스주, 크리스탈지노믹스의 아이발티노스타트가 임상을 진행하고 있으며 당사 또한 췌장암을 타겟하는 Vax-NK/PDAC를 VAX-NK/HCC 기반으로 연구개발 하고 있었으며 최근 임상2a상을 신청하였습니다.
당사는 앞서 이야기 한 자가면역세포 치료제를 2a상 까지 끌어올린 노하우와 경험을 축척 하고 있는 상황으로 본 치료제는 병용처방을 통해 타사와의 치료제와도 상호 보완적인 시너지 효과를 발휘 할 수 있어 기대를 하고 있습니다.
현재 시점부터 2a상 종료 전까지 필요한 임상진행 자금은 금번에 진행할 유상증자 공모자금 중 일부인 약 39억원을 투자할 예정으로 HCC 임상연구를 진행한 경험으로 빠른 상업화를 추진하고 있습니다.
최근 임상연구(연구자임상:IIT) 승인이 된 Vax-NK/SCLC(소세포폐암)은 전체 폐암의 15~20%의 발병률에 지나지 않지만 암세포의 성장이 빠르고 초기단계에서의 전이도 쉽게 일어나 예후가 좋지 않은 암종으로 알려져 있고 5년 생존율도 10% 이하로 알려져 있으나 수요가 부족하여 그 시장은 매년 꾸준하게 성장해 KISTI에 따르면 2026년까지 세계시장은 약 3조 6천억원 규모로 2020년 기준, 연평균 성장률은 약19%로써 매년 증가 추세에 있습니다. 당사는 IIT, SIT를 연속으로 진행하며 2026년도 중 3상에 진입할 수 있게 최소 약 21억원 을 투여하여 개발을 진행하고자 합니다.
| [Vax-NK 관련 사용 계획] |
| 단위: 백만원 | 2024 | 2025 | 2026 | 합계 |
|---|---|---|---|---|
| Vax-NK/HCC 3상 | 1,545 | 6,182 | 6,182 | 13,909 |
| Vax-NK/PDAC 2a상 | 2,944 | 981 | 0 | 3,925 |
| Vax-NK/SCLC 2a상 - 연구자 주도 임상 | 514 | 0 | 0 | 514 |
| Vax-NK/SCLC 2a상 - 상업화 비교 임상 | 0 | 788 | 788 | 1,577 |
| 합계 | 5,003 | 7,951 | 6,970 | 19,925 |
| 출처: 당사 제시 주) 사용계획은 제조원가와 임상시험비로 구성되어있으며, 임상시험비는 영상분석비, 임상시험비(병원/CRO), 시험검사비 등으로 구성 되어있습니다 |
(2)Vax-CAR
Vax-CAR 플랫폼 중 차후 주력 파이프라인이 될 난치성 혈액암인 다발골수종에 대한 BCMA-CAR-T, BCMA-CAR-MIL 치료제와 난치성 고형암에 대한 PD-L1, MSLN, EphA2-CAR-T/NK 치료제 개발을 위해 비임상연구 및 공정개발을 진행 중입니다. 특히 CAR 치료제는 높은 치료효과를 나타내어 고가의 가격대가 형성되어있는 고부가가치 치료제 입니다.
이 시장은 2021년 현재 타유형의 치료제 시장보다 규모는 매우 낮지만. 연평장 성장률이 합성의약품 5.7%, 항체의약품 5.2%, 백신 -4.1% 보다 월등히 높은 49.4% 를 전망하며 2026년에는 550억 달러(한화 66조)의 시장으로 성장 할 것으로 보입니다.당사는 기존의 CAR-T 치료제가 가지고 있는 높은 부작용 발생률과 낮은 면역기억 유도의 문제점을 극복하기 위해 당사의 NK세포에 대한 노하우를 바탕으로 개발 중이며 특히 scFv CAR 세포치료제 뿐만 아니라 모노바디 수용체를 사용하는 새로운 기술 플랫폼을 통해 다양한 고형암을 모두 타겟할 수 있다는 점에서 경쟁사에 비해 큰 기술 우위를 가질 수 있을 것으로 보입니다.
또한 BCMA CAR-T와 골수침윤림프구에서 유래한 세포와 CAR 기술을 접합한 BCMA CAR-MILs 파이프라인을 개발하여 다발골수종을 목표질환으로 비임상연구를 진행하고 있습니다. 당사는 Vax-CAR 관련 플랫폼 연구관련 예산을 26년까지 약 204억으로 추산하며, 본 투자로 당사의 향후 성장동력 및 시장선점을 목표하고 있습니다.
CAR플랫폼의 경우 NK플랫폼 대비 제조원가가 높습니다. 시약의 원가가 더 높고 유전자조작 공정 등이 추가 되어 추가 시설이 요구되기 때문입니다. 또한 현재 CAR플랫폼은 비임상 단계로 임상비용이 크지 않은 상태입니다. 향후 1상 또는 2a상 진입 시 환자 수가 임상 프로토콜에 따라 모집이 될 계획이며 임상인원이 증가함에 따라 예상 소요 비용 역시 증가할 계획입니다.
| [Vax-CAR 관련 사용계획] |
| 단위 : 백만원 | 2024 | 2025 | 2026 | 합계 |
|---|---|---|---|---|
| Vax-CAR-T/BCMA 임상 1상 | 5,300 | 900 | - | 6,200 |
| Vax-CAR-T/BCMA 임상 2상 | - | 2,100 | 900 | 2,999 |
| Vax-CAR-T,-NK/PD-L1_EphA2 비임상 및 임상 1상 | 1,110 | 3,760 | 2,110 | 6,980 |
| Vax-CAR-MIL 비임상 및 임상 1상 | 1,200 | 900 | 2,100 | 4,199 |
| 합계 | 7,610 | 7,660 | 5,110 | 20,378 |
| 출처: 당사 제시 주) 사용계획은 주로 제조원가와 임상시험비로 구성되어있으며, 임상시험비는 영상분석비, 임상시험비(병원/CRO), 시험검사비 등으로 구성 되어있습니다. (파이프라인별로 IND, 비임상, 효능평가 및 타겟 발굴 비용이 포함된 파이프라인도 존재합니다) |
(4) 박스루킨-15
당사의 Vaxleukin-15는 세계최초 반려견 항암면역치료제로 연구개발을 진행하고 있습니다. 면역체계를 활성화 하는 물질인 인터루킨-15를 기반으로 개발하여 임상연구시 66.6%의 높은 질환조절률을 확인함으로 우수한 가치를 확인 하였습니다.
당사는 현재 유선종양, 림프종 등의 적응증을 대상으로 임상연구를 수행하고 있으며, 대조군과 비교해서 통계적 유의성이 확보되면 올해 하반기에 농림축산검역본부에 품목허가를 재신청 할 예정이며, 품목허가 승인을 받으면 상품화를 거쳐 매출 실현을 기대하고 있습니다.
또한 동시 진행하는 차세대 박스루킨 연구개발을 위해 향후 3개년간 약 21억원을 투자하여 더 효능높은 면역치료제를 개발하고자 합니다.
| [박스루킨 관련 사용계획] |
| 단위 : 백만원 | 2024 | 2025 | 2026 | 합계 |
|---|---|---|---|---|
| 박스루킨 보고 및 모니터링 | 245 | 245 | - | 490 |
| 박스루킨 SC제형 임상시험 | 560 | 172 | - | 732 |
| 2세대 박스루킨 연구개발 및 임상시험 (60마리) | 436 | 416 | - | 852 |
| 합계 | 1,241 | 833 | - | 2,074 |
| 출처: 당사 제시 |
(5)시설자금
당사는 현재 임상시험에 필요한 GMP설비 등을 임차하여 사용하고 있으나 본격적인 3상 임상시험 및 조건부 허가를 통한 매출시현을 위해 자가 시설을 확보하고자
본 유상증자를 통해 확보된 자금 중 약 451억을 투자할 예정입니다.
이 중 410억원은 화순군청에서 2021년 매입한 화순생물의약산업단지 내 (화순읍 감도리에 위치) 약 4천평의 토지를 기반으로 건물을 신축하고자 하며 사무동, 생산동(GMP시설 포함) 등을 건설해 안정적인 연구부터 생산에 이르는 일괄적인 시스템을 갖추고, 본 설비와 시설을 효율적으로 운영하기 위해 스마트공장의 형태로 구축할 계획이며 현재 설계중인 ERP포함, MES, WMS 등과 같은 전산체계를 적용하여 향후 진행되는 연구개발과 임상시험을 대응하고 안정적인 매출을 위해 생산 Capa를 확보하고자 합니다.
또한 생산시설 내재화를 위한 연구소 건립 전까지는 JBRC의 GMP시설을 추가로 임차하여 신사옥 건설 전까지 사용하고 하고 생산장비를 세팅하여 자체생산으로 임상연구를 진행할 계획입니다.
| [시설자금 관련 사용계획] |
| 단위 : 백만원 | 2024 | 2025 | 2026 | 합계 |
|---|---|---|---|---|
| 중앙연구소 및 본사 건축비 | 11,016 | 11,073 | - | 22,089 |
| 중앙연구소 및 본사 기자재 | 6,604 | 4,615 | - | 11,219 |
| 공정개발실 장비 구매 | 3,994 | 2,624 | 1,560 | 8,178 |
| 면역세포치료제 제조시설 - 임차비용(임차) | 237 | 237 | 237 | 710 |
| 면역세포치료제 제조시설 - 장비 세팅(임차) | 758 | - | - | 758 |
| CAR치료제 제조시설 - 임차비용(임차) | 220 | 220 | 220 | 661 |
| CAR치료제 제조시설 - 장비세팅(임차) | 1,982 | - | - | 1,982 |
| 합계 | 24,811 | 18,769 | 2,017 | 45,597 |
| 출처: 당사 제시 |
이와 더불어 각 분야의 우수 인재 영입, 안정적인 연구와 임상, 생산을 위한 신사옥 및 자가 설비 확보, 매출 시현을 위한 조직개편 및 영업활동을 개시하고자 하며 기존 인력의 전문성 보강, 매출 시현 등에 따른 마케팅 및 생산, 유통비용에 사용할 예정으로, 운영자금의 경우 2026년까지 약 231억원을 사용할 계획입니다.
특히 제품화가 임박할 것으로 예상되는 당사 파이프라인의 제조/품질 및 영업 관련 인력 충원을 비롯한 인력 관련 예상 소요 비용을 약 172억원 사용할 계획입니다.
| [인력 관련 예상 소요 비용] |
| 단위 : 백만원 | 2024년 | 2025년 | 2026년 | 합계 |
|---|---|---|---|---|
| 인건비 | 2,198 | 3,075 | 4,226 | 9,499 |
| 부대비용 | 1,940 | 2,540 | 3,240 | 7,720 |
| 합 계 | 4,138 | 5,615 | 7,466 | 17,219 |
| 출처: 당사 제시 |
| [제조/품질/관리/영업 인원충원계획] |
| (단위 : 명) | 2024 | 2025 | 2026 | 합 |
|---|---|---|---|---|
| 박사급/부장 | 1 | 2 | 1 | 4 |
| 석사급/과차장 | 2 | 3 | 4 | 9 |
| 원급/사원대리 | 10 | 10 | 15 | 35 |
| 13 | 15 | 20 | 48 |
| 출처: 당사 제시 |
| [제조/품질/관리/영업 인원누적계획] |
| (단위 : 명) | 2024 | 2025 | 2026 | 합 |
|---|---|---|---|---|
| 박사급/부장 | 7 | 9 | 10 | 10 |
| 석사급/과차장 | 8 | 11 | 15 | 15 |
| 원급/사원대리 | 26 | 36 | 51 | 51 |
| 41 | 56 | 76 | 76 |
| 출처: 당사 제시 |
상기 당사의 파이프라인 진행상황은 유관기관의 승인, 허가, 보완요청 등 다양한 사유로 계획한 일정과 괴리가 발생할 수 있습니다. 이에 자금사용 계획 또한 V.자금의 사용목적에 기재한 일정과 일부 다르게 진행될 수 있으니 투자자께서는 참고하시기 바랍니다.
VI. 그 밖에 투자자보호를 위해 필요한 사항
본 건의 경우 시장조성 또는 안정조작에 관한 사항은 해당사항 없습니다.
제2부 발행인에 관한 사항
I. 회사의 개요
1. 회사의 개요
가. 회사의 법적ㆍ상업적 명칭
- 국문명칭 : 주식회사 박셀바이오
- 영문명칭 : VaxCell Biotherapeutics Co., Ltd.
- 약식명칭 : VaxCell-Bio
나. 설립일자 및 상장여부
- 설립일자 : 2010년 2월 18일
- 상장일자 : 2020년 9월 22일 (코스닥)
다. 본사의 주소, 전화번호, 홈페이지 주소
| 구분 | 내용 |
|---|---|
| 본사의 주소 | 전라남도 화순군 화순읍 산단길 12-55 |
| 전화번호 | 061-373-0046 |
| 홈페이지 | http://www.vaxcell-bio.co.kr |
라. 주요사업의 내용
당사의 주요사업은 항암면역치료제 연구개발사업입니다.
당사의 파이프라인은 (1) Vax-NK 자연살해세포 항암면역치료제 플랫폼, (2) Vax-CAR 시리즈 차세대 첨단 항암면역치료제 플랫폼으로 구성되어 있으며, (3) 반려견 전용 항암면역치료제로 사이토카인 기반의 박스루킨-15 플랫폼을 보유하고 있습니다. 각 파이프라인은 개발단계에 있어 현재는 매출기록이 없습니다. 자세한 내용은 본 사업보고서의 『Ⅱ. 사업의 내용』부분을 참고하시기 바랍니다.
마. 연결대상 종속회사 현황(요약)
| (단위 : 사) |
| 구분 | 연결대상회사수 | 주요 종속회사수 |
|||
|---|---|---|---|---|---|
| 기초 | 증가 | 감소 | 기말 | ||
| 상장 | - | - | - | - | - |
| 비상장 | - | - | - | - | - |
| 합계 | - | - | - | - | - |
- 당사는 작성기준일 현재 해당사항이 없습니다.
바. 중소기업 등 해당 여부
| 중소기업 해당 여부 | 해당 | |
| 벤처기업 해당 여부 | 해당 | |
| 중견기업 해당 여부 | 미해당 | |
- 당사는 본 보고서 작성기준일 현재 중소기업기본법 제2조에 해당됩니다.
| 확인유형 | 유효기간 | 발급번호 | 확인기관 |
| 중소기업 (소기업) |
2023년 04월 1일 ~ 2024년 03월 31일 |
0010-2023-156288 | 중소벤처기업부 |
- 당사는 사업보고서 작성기준일 현재 벤처기업법 제2조의2 제1항제2호 가목의 요건을 충족하는 벤처기업에 해당됩니다.
| 확인유형 | 유효기간 | 발행번호 | 확인기관 |
| 혁신성장유형 | 2022년 05월 11일 ~ 2025년 05월 10일 |
제20220629030091호 | 한국벤처기업협회 |
아. 회사의 주권상장(또는 등록ㆍ지정)여부 및 특례상장에 관한 사항
| 주권상장 (또는 등록ㆍ지정)여부 |
주권상장 (또는 등록ㆍ지정)일자 |
특례상장 등 여부 |
특례상장 등 적용법규 |
|---|---|---|---|
| 코스닥시장 | 2020년 09월 22일 | 기술성장기업 |
코스닥시장상장규정 제7조 (신규상장심사요건의 특례) ② 기술성장기업의 신규상장의 경우에는 제6조의 심사요건 중 제6조제1항제6호의 요건은 적용하지 아니하고, 다음 각 호의 어느 하나의 요건을 충족하여야 한다. 1. 자기자본 : 상장예비심사청구일 현재 자기자본이 10억원 이상일 것 |
2. 회사의 연혁
가. 본점 소재지 및 그 변경
| 날 짜 | 주 소 | 비 고 |
| 2010.02.18 | 전라남도 화순군 화순읍 일심리 160-1 의생명과학 산학협력관 1층 |
최초 소재지 |
| 2012.03.21 | 전라남도 화순군 화순읍 산단길 12-55 | 소재지 변경 |
나. 경영진 및 감사의 중요한 변동
| 변동일자 | 주총종류 | 선임 | 임기만료 또는 해임 |
|
|---|---|---|---|---|
| 신규 | 재선임 | |||
| 2018년 03월 21일 | 정기주총 | - | 사외이사 이강오 | - |
| 2019년 03월 27일 | 정기주총 | 사외이사 정성창 | 대표이사,사내이사 이제중 사내이사 이준행 |
사외이사 이강오 사임 |
| 2019년 06월 24일 | - | 대표이사 이준행 | - | 대표이사 이제중 사임 |
| 2019년 07월 30일 | - | - | - | 사내이사 서인천 사임 |
| 2019년 09월 19일 | 임시주총 | 사내이사 정광준 감사 오택근 |
- | - |
| 2019년 11월 04일 | - | 공동대표이사 이준행, 정광준 | - | - |
| 2020년 03월 20일 | 정기주총 | 기타비상무이사 임신혁 | - | 감사 이현수 사임 |
| 2021년 02월 09일 | - | 대표이사 이준행, 대표이사 이제중 | - | 공동대표이사 정광준 사임 |
| 2021년 03월 31일 | - | - | - | 사내이사 정광준 사임 |
| 2022년 01월 10일 | - | - | - | 대표이사 이준행 사임 |
| 2022년 03월 27일 | 정기주총 | - | 대표이사,사내이사 이제중 사내이사 이준행 사외이사 정성창 감사 오택근 |
- |
| 2022년 05월 13일 | - | - | - | 기타비상무이사 임신혁 사임 |
- 당사 정관 제42조에 의거, 대표이사는 이사회에서 선임합니다.
다. 최대주주의 변동
- 해당사항 없습니다.
라. 상호의 변경
- 해당사항 없습니다.
마. 회사가 화의, 회사정리절차 그 밖에 이에 준하는 절차를 밟은 적이 있거나 현재 진행 중인 경우 그 내용과 결과
- 해당사항 없습니다.
바. 회사가 합병등을 한 경우 그 내용
- 해당사항 없습니다.
사. 회사의 업종 또는 주된 사업의 변화
- 해당사항 없습니다.
아. 그 밖에 경영활동과 관련된 중요한 사항의 발생내용
|
시 기 |
내 역 |
|
2015. 07. |
Vax-DC/MM 임상시험(1/2a) 완료 |
|
2016. 01. |
Vax-NK/HCC 임상시험계획승인(1상) |
|
2017. 08. |
Vax-DC/MM 임상시험계획승인(2b) |
|
2017. 12. |
Vax-NK/HCC 임상시험 1상 완료 |
|
2018. 05. |
Vax-NK/HCC 임상시험계획 승인(2a) |
|
2018. 09. |
박스루킨-15(동물약품) 임상시험 완료 |
|
2019. 02. |
박스루킨-15(동물약품) 위탁판매 MOU 체결 |
|
2019. 04. |
서울사무소 개소 |
|
2019. 06. |
우리사주조합 설립 |
|
2019. 12. |
기술성평가 등급 획득 (A, BBB) |
| 2020. 09 | 코스닥시장 상장 및 주권거래개시 |
| 2020. 10 | 박스루킨-15(동물약품) 품목허가 접수 |
|
2021. 04 |
전남 화순군 백신산업특구 내 사옥 신축 부지 매입 |
|
2021. 05 |
모노바디 기반 Vax-CAR 플랫폼 기술 특허 출원 |
|
2021. 06 |
NK세포 대량증식 관련 기술 특허 출원 |
|
2021. 06 |
Vax-NK/HCC 임상2a상 안전성심의위원회(SRM) 통과 |
| 2021. 12 | 박스루킨-15 품목허가 자진철회 |
| 2022. 08 | Vax-DC/MM 임상시험 연구개발 조기종료 |
| 2022. 10 | 전라남도 바이오기업 대표성공기업 선정 |
| 2023. 01 | 농림축산검역본부 동물용의약품 임상시험계획서(박스루킨-15주) 변경 승인 |
| 2023. 02 | 광주지방식품의약품안전청 "세포처리시설" 허가 |
| 2023. 07 | 첨단재생의료 임상연구 승인: Vax-NK/SCLC 임상연구 |
3. 자본금 변동사항
가. 자본금 변동추이
| (단위 : 원, 주) |
| 종류 | 구분 | 증권신고서 제출 전일 |
13기 (2022년 말) |
12기 (2021년말) |
|---|---|---|---|---|
| 보통주 | 발행주식총수 | 15,223,000 | 15,223,000 | (주1) 15,223,000 |
| 액면금액 | 500 | 500 | 500 | |
| 자본금 | 7,611,500,000 | 7,611,500,000 | 7,611,500,000 | |
| 우선주 | 발행주식총수 | - | - | - |
| 액면금액 | - | - | - | |
| 자본금 | - | - | - | |
| 기타 | 발행주식총수 | - | - | - |
| 액면금액 | - | - | - | |
| 자본금 | - | - | - | |
| 합계 | 자본금 | 7,611,500,000 | 7,611,500,000 | 7,611,500,000 |
(주1)
- 2021년 말 발행주식 총수 15,223,000주는 2021년 1월 4일 현재 주주명부에 등재된 주주에 대하여 1:1 비율로 신주를 배정하여 (11기) 2020년 말 발행주식 총수 7,523,000주에서 15,046,000주로 증가 하였으며 2021년 4월 14일 주식매수선택권 행사로 인해 177,000주가 신규 상장하였습니다.
- 해당 사항은 금융감독원 전자공시 [주요사항 보고서(무상증자결정)] 및 [2021년 3월 29일 주식매수선택권 행사]를 참고해주시기 바랍니다.
4. 주식의 총수 등
가. 주식의 총수 현황
| (기준일 : | 2023년 08월 04일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 비고 | |||
|---|---|---|---|---|---|
| 의결권 있는 주식 |
의결권 없는주식 |
합계 | |||
| Ⅰ. 발행할 주식의 총수 | 50,000,000 | - | 50,000,000 | - | |
| Ⅱ. 현재까지 발행한 주식의 총수 | 15,223,000 | - | 15,223,000 | - | |
| Ⅲ. 현재까지 감소한 주식의 총수 | - | - | - | - | |
| 1. 감자 | - | - | - | - | |
| 2. 이익소각 | - | - | - | - | |
| 3. 상환주식의 상환 | - | - | - | - | |
| 4. 기타 | - | - | - | - | |
| Ⅳ. 발행주식의 총수 (Ⅱ-Ⅲ) | 15,223,000 | - | 15,223,000 | - | |
| Ⅴ. 자기주식수 | - | - | - | - | |
| Ⅵ. 유통주식수 (Ⅳ-Ⅴ) | 15,223,000 | - | 15,223,000 | - | |
나. 자기주식의 취득 및 처분 현황
당사는 작성기준일 현재까지 취득한 자기주식이 없습니다.
다. 보통주 외의 주식
당사는 작성기준일 현재 보통주외에 발행한 주식이 없습니다.
라. 발행 이후 전환권 행사가 있을 경우
당사는 전환권이 가능한 주식은 작성기준일 현재 없습니다.
5. 정관에 관한 사항
가. 최근 개정일
당사 정관의 최근개정일은 2021년 3월 25일 입니다.
나. 정관 변경 이력
| 정관변경일 | 해당주총명 | 주요변경사항 | 변경이유 |
|---|---|---|---|
| 2018년 03월 21일 | 제8기 정기주주총회 | - | - |
| 2019년 03월 27일 | 제9기 정기주주총회 | 발행할 주식의 총수 | 발행할 주식의 총수 증가 |
| 2019년 03월 27일 | 제9기 정기주주총회 | 1주의 금액 | 1주의 금액 조정 |
| 2019년 03월 27일 | 제9기 정기주주총회 | 주식의 소각 명확화 | 주식의 소각 범위를 정하고방법을 구체화 함 |
| 2019년 03월 27일 | 제9기 정기주주총회 | 주주명부 폐쇄 및 기준일 | 기준일을 명확히 개정 |
| 2019년 03월 27일 | 제9기 정기주주총회 | 이익배당 | 이익배당을 주주총회 결의로만 가능한 것으로 개정 |
| 2019년 08월 01일 | 제9기 임시주주총회 | - 신주인수권 - 대표이사의 선임 |
- 3자 배정시 발행할 주식 종류 및 발행가격, 단주처리방법의 규정 - 공동 또는 각자 대표이사의 근거 명확화 |
| 2020년 03월 20일 | 제10기 정기주주총회 | 사업목적 추가 | 추후 사업확장 전략적 협력 추진,약품의 수출등에 대비한 사업목적 추가 (연구기술개발용역업, 수출입업 등) |
| 2020년 03월 20일 | 제10기 정기주주총회 | 주식의 종류 등 조항 개정 | 전자증권 도입시 업무처리 실무상 기존 통일주권의 내용을 유지하고 전자증권 도입 시 배제하는 형태로 조항 개정 |
| 2020년 03월 20일 | 제10기 정기주주총회 | 종류주식의 종류 명확화 | 종류주식의 일반적 내용을 규정하고 혼합하거나 선택하여 발행할 수 있도록 함. |
| 2020년 03월 20일 | 제10기 정기주주총회 | 기타 인용조문 오기 등 수정 | 정관의 내용 중 인용된 조문번호오기 등을 수정, 상법에 규정의 표현에 맞추어 관련된 정관의 표현 일부 수정 |
| 2020년 03월 20일 | 제10기 정기주주총회 | 이사의 임기 | 사내이사 및 사외이사의 임기에 관한 조건 통일을 위한 조문 개정 |
| 2020년 03월 20일 | 제10기 정기주주총회 | 이사회 소집기간단축 | 긴급한 의사결정이 필요할 때를 대비하여 이사회 소집기간 단축 |
| 2021년 03월 25일 | 제11기 정기주주총회 | 주식 등 전자등록 조항 개정 | 비상장 사채 등 의무등록 대상이 아닌 주식등에 대해서는 전자등록을 하지 않을 수 있도록 함 |
| 2021년 03월 25일 | 제11기 정기주주총회 | 우선주식 등 배당 조항 개정 | 동등배당에 따른 이사회 결의문구 삭제 |
| 2021년 03월 25일 | 제11기 정기주주총회 | 신주에 대한 배당원칙 개정 |
상법 개정에 따라 이익배당 기준일을 삭제하고 동등배당 원칙을 명시함. |
| 2021년 03월 25일 | 제11기 정기주주총회 | 전환사채 발행한도 | 전환사채의 발행 한도를 증액함 |
| 2021년 03월 25일 | 제11기 정기주주총회 | 신주인수권부사채 발행한도 | 신주인수권부사채의 발행한도 증액함 |
| 2021년 03월 25일 | 제11기 정기주주총회 | 주주총회 소집시기 | 정기주주총회 개최시기의 유연성을 확보하기 위하여 조문을 정비함 |
| 2021년 03월 25일 | 제11기 정기주주총회 | 감사의 선임 | 감사선임에 관한 조문을 정비함 |
| 2021년 03월 25일 | 제11기 정기주주총회 | 감사의 선임 | 전자투표 도입 시 감사선임의 주주총회 결의요건 완화에 관한 내용을 반영함 |
| 2021년 03월 25일 | 제11기 정기주주총회 | 감사 선임, 해임시 의결권제한 |
감사 선임 또는 해임 시 의결권 제한에 관한 내용을신설함 |
| 2021년 03월 25일 | 제11기 정기주주총회 | 이익배당 기준일 | 배당기준일을 이사회 결의로 정하는 날로 설정할 수 있도록 함 |
II. 사업의 내용
1. 사업의 개요
가. 회사의 현황
당사는 항암면역치료제 개발 전문 회사로 2010년 2월 18일자로 설립되어 인체의 면역체계를 활성화하거나 강화시켜 면역세포들로 하여금 암세포를 공격하게 유도하는 치료법을 개발하고 있습니다. 당사의 두 공동설립자인 이제중 대표이사, 이준행 사내 이사의 오랜 항암면역치료에 관한 연구개발에 기반하여 면역시스템에서 최상의 효과를 발휘할 수 있는 대표적인 구성요소로 파이프라인을 구성하였습니다.
면역체계를 구성하는 주요 요소 중 i) 선천 면역 체계에서 가장 강력한 항암면역능을 갖고 있는 자연살해세포를 기반으로 하는 Vax-NK 항암면역치료 플랫폼과 ii) 항암 적응 면역에 강력한 역할과 암에 대한 선택성과 특이도를 모두 갖춘 Vax-CAR 항암 면역 치료제 플랫폼 등 다양한 면역세포를 활용한 항암면역치료 플랫폼을 보유하고 있으며, iii) 이들 면역세포에 대해 모두 활성을 증가시키는 역할을 하는 동시에 사이토카인으로 알려진 인터 루킨-15를 기반으로 하는 동물용 항암면역치료제인 박스루킨-15까지, 항암 면역 전반을 아우르는 제품군을 연구개발하고 있습니다.
그 중에서도 현재 면역세포를 이용한 치료제를 주요 파이프라인으로 개발하고 있으며, 현재 환자의 혈액에서 확장 배양한 자연살해세포를 이용하여 Vax-NK 항암 면역 세포치료제를 개발하여 진행성 간암에 대한 임상연구를 수행 중입니다. 또한 Vax-NK 항암면역치료제 플랫폼의 적응증 확대를 위하여 진행성 췌장암 및 소세포성 폐암 등 추가 암종에 대한 임상연구를 계획 중이며 차세대 항암면역치료제인 Vax-CARs 플랫폼을 구축하여 CAR-T 세포치료제, CAR-NK 세포치료제, 그리고 골수에서 채취한 MIL을 이용하여 개발한 CAR-MIL 치료제를 개발하고 있습니다. 반려견 전용 면역 증강제 및 항암면역치료제인 Vaxleukin-15의 경우 품목허가를 위한 임상연구를 활발히 진행하고 있고, 다른 항암요법과 병합한 치료법 확장 및 적응 증 확대를 위한 추가 연구를 수행 중입니다. 아래는 당사의 파이프라인의 주요 진행상황입니다.
아래는 당사의 파이프라인의 주요 진행상황입니다.
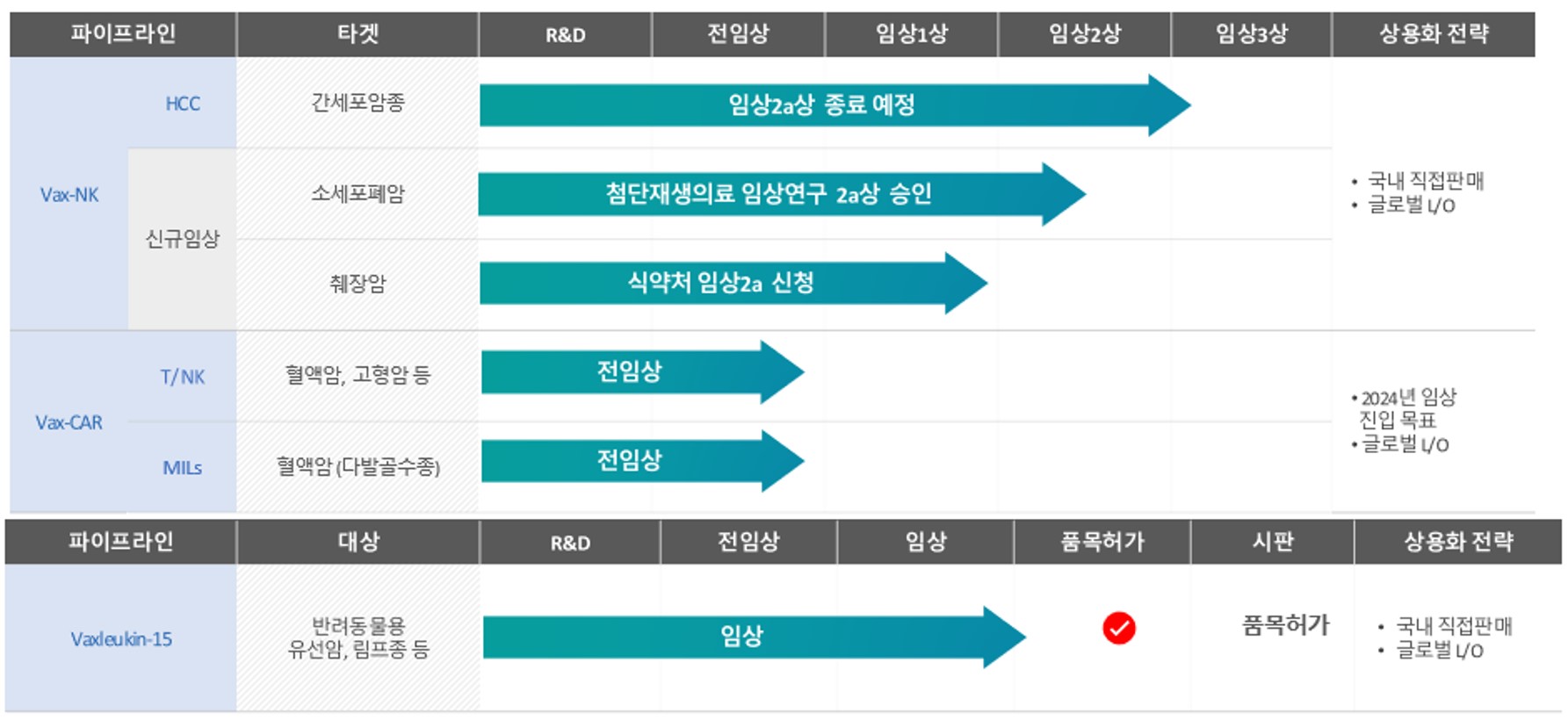 |
|
파이프라인_박셀바이오 |
2. 주요 제품 및 서비스
가. 주요 제품 및 서비스의 현황
|
품목 |
적응증 |
단계 |
임상 프로토콜 핵심 요약 |
임상인원 |
병합약물 |
|
Vax-NK |
간세포암 |
임상1상 완료 (2017) |
HAIC 후 Vax-NK 5회 주사, |
11 |
HAIC |
|
임상2a상 수행 중 |
HAIC 후 Vax-NK 10회 주사 |
20 |
|||
|
췌장암 |
임상 2a상 시험계획 변경승인 신청 | 총 3주기 (2,4,6 주기) 병합약물과 투여 1주기 당 매일 1회, 총 3일 투여, 1주기는 4주로 구성 |
20 |
mFOLFIRINOX |
|
|
소세포폐암 |
첨단재생의료 임상연구 승인 |
항암요법 완료 후, 주사 1주기는 매일 5회, 2주기는 1주기 투여 후 4주 후 매일 5회 | 12 |
Atezolizumab (아테졸리주맙) |
|
|
Vax-CAR |
다발골수종 및 고형암 |
CAR-T 비임상 수행 중 |
- |
|
|
|
CAR-NK 비임상 수행 중 |
- |
|
|||
|
다발골수종 |
CAR-MILs 비임상 수행 중 |
- |
|
||
|
박스루킨-15 |
반려견의 암 (유선종양, 림프종 등) |
단회임상 완료 (2018) |
8일간 매일 1회 투여 (정맥 내 투여) |
18마리 (대조군 3마리 포함) |
사이클로포스파마이드 |
|
임상시험계획서 변경 |
8일간 매일1회 정맥 내 투여 (주사 1주기는 매일 4회, 2주기는 1주기 투여 10일 후 매일 4회) |
132마리 (대조군60마리 포함) |
"수술요법"과 병용 (유선종양), "항암화학요법"과 병용 (림프종) |
||
(1) 세포·유전자치료제 사업
- Vax-NK 항암면역치료제 플랫폼
환자의 자연살해세포를 이용한 자가유래(Autologous) Vax-NK 치료제를 개발하여, 기존 치료에도 반응을 보이지 않거나 재발한 진행성 간세포암종을 대상으로 간동맥 내 항암주입요법(HAIC)와 병합치료 임상2a상을 수행 중입니다. 지난 2017년 12월 종료된 임상1상에서 안전성과 탐색적 유효성을 검증하였고, 이 결과를 바탕으로 SCI급 논문을 게재한 바 있습니다. 현재 화순전남대학교병원, 서울성모병원, 동아대학교병원, 부산대학교병원, 영남대학교병원 총 5곳에서 수행 중인 임상2a상의 경우 2023년 7월 기준으로 17명 환자 등록 완료하였으며 임상연구 기준에 맞게 예정된 임상연구 종료를 준비 중입니다.
Vax-NK 플랫폼의 적응증 확대를 위하여 지난 7월 진행성 췌장암에 대한 임상연구계획 변경승인을 신청하였고, 확장병기 소세포성 폐암을 목표 질환으로 하여 첨단재생의료 임상연구계획을 승인(23년 07월) 받아 신규 임상연구를 준비하고 있습니다.
- Vax-CARs 항암면역치료제 플랫폼
차세대 항암면역치료제로 각광받고 있는 키메릭항원수용체(Chimeric antigen receptor, CAR) 치료제인 Vax-CARs 플랫폼으로, CAR-T 세포치료제와 당사의 NK세포에 대한 노하우를 바탕으로 CAR-NK 세포치료제 또한 개발하고 있으며, 최근 골수침윤림프구(MIL)를 이용한 CAR-MILs 치료제의 예비연구를 마쳐 신규 파이프라인을 확대하였습니다
(2) 동물용의약품 사업
박스루킨-15는 반려견 전용 면역 증강제 및 항암 면역치료제입니다. 의료기술이 발달되고 반려견에 대한 인식이 높아지면서 반려견의 평균수명이 연장되고, 의약품 시장에 대한 수요도 꾸준히 성장하고 있는 추세입니다. 당사는 개의 유전체 정보를 바탕으로 항암면역능의 유도에 탁월한 효능을 갖추고 있으며, 부작용이 발생하지 않는 것으로 알려진 인터루킨-15를 기반으로 한 재조합 단백질 항암면역치료제인 박스루킨-15를 개발하여 반려견을 대상으로 임상연구를 수행 중입니다.
나. 주요 제품등의 가격변동추이
당사는 항암면역치료제를 개발하여 현재 임상시험 단계로, 수익성에 영향을 미치는 제품 또는 서비스의 판매가격의 변동추이를 산정할 수 없어 기재하지 않습니다.
3. 원재료 및 생산설비
가. 원재료 매입현황
당사의 주요 영업활동은 항암면역치료제 연구개발로 사업보고서 공시대상기간 중 생산 및 판매 중인 제품이 없어 원재료의 매입에 관한 해당사항이 없습니다.
나. 생산능력 및 생산실적
당사는 보고서 작성기준일 현재 임상시험용 의약품을 생산할 수 있는 GMP 시설을 운영하고 있습니다. 사업보고서 작성기준일 현재 진행성 간세포암 임상2a상 연구 및 치료목적 긴급사용승인에 대한 의약품 생산과 공정개발을 위한 연구용 주사제를 생산하고 있습니다.
(단위: batch)
|
제품 품목명 |
구 분 |
2023년도 상반기 (제14기) |
2022년도 (제13기) |
2021년도 (제12기) |
|||
|
수량 |
금액 |
수량 |
금액 |
수량 |
금액 |
||
|
Vax-NK (제1제조소) |
생산능력 |
81 |
- |
81 |
- |
- |
- |
|
생산실적 |
9 |
- |
19 |
- |
- |
- |
|
|
가 동 율 |
11.11% |
23.46% |
- |
||||
|
기말재고 |
- |
- |
- |
- |
- |
- |
|
|
Vax-NK (제2제조소) |
생산능력 |
81 |
- |
81 |
- |
81 |
- |
|
생산실적 |
6 |
- |
14 |
- |
18 |
- |
|
|
가 동 율 |
7.4% |
17.28% |
22.22% |
||||
|
기말재고 |
- |
- |
- |
- |
- |
- |
|
(1) 생산능력의 산출 기준은 아래와 같습니다.
|
구분 |
설비 |
생산 소요일수/ 인큐베이터 |
연간 생산가능 |
|
제1제조소 (Vax-NK) |
CO₂인큐베이터 4대 |
18 일 |
81 batch |
|
제2제조소 (Vax-NK) |
CO₂인큐베이터 4대 |
18 일 |
81 batch |
다. 생산설비에 관한 사항
(단위: 천원)
|
구분 |
자산 과목 |
자산명 |
기초 가액 |
2023년 상반기 |
비고 |
|||
|---|---|---|---|---|---|---|---|---|
|
증가 |
감소 |
당기 상각 |
기말 가액 |
|||||
|
유형 자산 |
토지 |
전라남도 화순군 생물의약산업단지 |
1,601,884 |
- |
- |
- |
1,601,884 |
- |
|
공구와기구 |
ATTUNE NXT AFC BRV6Y-LASER 외 |
651,923 |
2,600 |
- |
167,690 |
486,833 |
- |
|
|
건설중인자산 |
자가생산,설비, 건물 외 |
- |
22,511 |
- |
- |
22,511 |
- |
|
|
합 계 |
2,253,807 |
25,111 |
- |
167,690 |
2,111,228 |
- |
||
라. 설비의 신설/매입계획 (단위: 천원)
|
구 분 |
설비 능력 |
총소요자금 |
기지출액 |
지 출 예 정 |
비 고 |
|
|
2023년 |
2024년 이후 |
|||||
|
기 타 |
공구, 기구, 비품 |
4,144,400 |
556,776 |
432,624 |
3,155,000 |
- |
|
합 계 |
4,144,400 |
556,776 |
432,624 |
3,155,000 |
- |
|
마. 유형자산(토지)에 대한 내역 (단위: 천원)
|
구분 |
자산과목 |
자산명 |
기초가액 |
2023년 1분기 |
비고 |
|||
|
증가 |
감소 |
당기 상각 |
기말 가액 |
|||||
|
유형자산 |
토지 |
전라남도 화순군 |
1,601,884 |
- |
- |
- |
1,601,884 |
- |
|
합 계 |
1,601,884 |
- |
- |
- |
1,601,884 |
|
||
4. 매출 및 수주상황
가. 매출실적
당사는 연구개발 중심기업으로 보고서 제출일 현재 매출이 발생하고 있지 않습니다.
나. 매출경로 및 판매방법
(1)판매조직
당사에서 개발 중인 제품은 사람용 항암면역치료제와 동물용의약품인 Vaxleukin-15입니다. 모든 제품이 연구개발과 임상시험 단계에 있으며, 사업보고서 작성기준일 현재 별도의 제품 판매조직을 갖추고 있지는 않습니다. 다만 현재 활발히 임상연구를 수행 중인 세포치료제 사업의 경우, 임상연구실을 주축으로 하여 향후 Vax-NK 치료를 도입할 유명 종합병원 대학교수들과 인적 네트워크를 관리하고 있습니다.
이에 더해 기초연구단계에서부터 임상시험을 진행하는 단계까지 제품을 출시하기 전이라도 다른 바이오기업 또는 글로벌 제약사에 기술이전을 하거나 공동연구 계약을 체결하여 글로벌 임상을 추진하는 매출 모델도 계획하고 있습니다. 이러한 기술 영업을 하기 위해 다양한 분야와 글로벌 시장에서의 경험이 풍부한 보유한 임원을 영입하여 국내외 기술이전 및 사업화를 추진하고 있습니다. 이와 별개로 동물용 의약품인 Vaxleukin-15의 경우 전략기획본부와 동물의약품실에서 국내 제품 출시를 위하여 다양한 사업모델을 모색하고 있으며, 전국 수의사 네트워크를 활용하여 세미나를 개최하는 등 수의사를 중심으로 한 네트워크를 중점관리하고 있습니다.
(2)판매경로
항암 면역세포치료제인 Vax-NK의 경우 환자 자신의 혈액을 이용한 맞춤형 치료제이기 때문에, 종합병원과 당사가 직접 거래하는 방식으로 판매 경로를 구축할 계획입니다. 동물용의약품인 Vaxleukin-15의 경우 외주생산판매업체와 동물용의약품 유통업체와의 협력을 통하여 반려동물병원에 직접 납품할 수 있는 판매 경로를 구축할 예정이며, 매출채권의 회수는 외주생산판매업체가 부담하고 당사는 매년 연간 매출액에 대한 로열티를 수취하는 방식을 계획하고 있습니다. 기초연구단계 또는 임상시험 단계에서 공동연구 또는 기술이전 형태의 경우 국내외 제약사 및 바이기업과의 지속적인 네트워크 관리에 힘쓸 예정입니다. 또한 글로벌 시장 진출을 위해 해외 학회 및 컨퍼런스를 적극 활용하여 기술 영업을 추진할 계획입니다.
(3)판매전략
당사의 상업화 전략은 ① 자체 제조 및 판매와 ② 글로벌 제약사로의 기술이전으로 나뉩니다.
주요 파이프라인별 판매전략은 아래와 같습니다.
|
파이프라인 |
제조와 판매 전략 |
기술이전 전략 |
|
Vax-NK/HCC |
간세포암종을 목표질환으로 Vax-NK를 한국에서 직영 생산 및 판매 |
임상3상 혹은 조건부 허가 진행하며 해외 L/O 동시 진행 |
|
Vax-NK 동남아시아에서 위탁생산 및 판매 |
||
|
Vax-NK/PDAC |
진행성췌장암을 목표질환으로 Vax-NK를 한국에서 직영 생산 및 판매 |
임상3상 혹은 조건부 허가 진행하며 해외 L/O 동시 진행 |
| Vax-NK/SCLC | 소세포폐암을 목표질환으로 Vax-NK를 한국에서 직영 생산 및 판매 | 임상3상 혹은 조건부 허가 진행하며 해외 L/O 동시 진행 |
|
Vax-CAR |
혈액암 및 고형암을 목표질환으로 CAR-T, CAR-NK, CAR-MILs치료제를 한국에서 직영생산 및 판매 |
난치성 고형암을 목표질환으로 여러 개의 항원수용체(MSLN, EphA2, PD-L1 등) 적용 CAR-T/NK세포치료제, 그리고 난치성 혈액암인 다발골수종을 목표질환으로 CAR-T, CAR-MILs 치료제 각각에 대하여 글로벌 라이선스 아웃 |
|
박스루킨-15 |
동물(개)의 암을 목표질환으로 국내 동물약품제조사의 제조 및 판매에 대한 로열티 수취 |
동물(개)의 암을 목표질환으로 글로벌 라이선스 아웃 |
① 한국시장 자체제조 및 판매
당사는 Vax-NK 플랫폼의 항암면역치료제를 한국에서 직접 생산하고 판매할 전략입니다. 진행성 간세포암종을 대상으로 한 Vax-NK/HCC, 확장병기 소세포폐암을 대상으로 한 Vax-NK/SCLC, 진행성 췌장암을 대상으로 한 Vax-NK/PDAC의 경우 국내 임상시험 단계를 거친 뒤 한국에서 출시하여 국내 대학병원을 중심으로 주요 거점병원을 시작으로 전국 암 요양 병원을 대상으로 홍보 및 마케팅 활동을 추진할 예정입니다.
Vax-CAR 플랫폼 중에서 혈액암을 대상으로 한 CAR-T 세포치료제와 CAR-MILs 치료제의 경우 국내 임상시험을 수행하고, 고형암을 대상으로 한 CAR-T/-NK 세포치료제도 국내 임상시험을 시행한 후, 국내 주요대학병원을 대상으로 시장을 개척할 계획입니다.
Vaxleukin-15의 경우 동물용의약품을 생산하고 판매할 국내 동물용의약품 전문회사와 제조 위수탁 계약을 체결하였습니다. 이를 통해 국내 선두권 종합 동물용 의약품 회사인 케어사이드가 구축한 탄탄한 국내 유통망과 해외 거래선을 활용할 수 있게 되었으며, 국내 판매를 넘어 글로벌 시장 개척에도 함께 힘을 모으기로 하였습니다. 또한 동물백신 전문업체 씨티씨백과도 Vaxleukin-15의 제품 경쟁력 강화를 위한 협약을 체결하여 국내 시판과 글로벌 시장 진출을 차질 없이 진행할 수 있는 토대를 마련하였습니다.
2022년에는 동물의약품실에 품목허가 경험이 풍부한 전문임원을 영입하여 수의사 네트워크를 대상으로 세미나를 개최하는 등 Vaxleukin-15의 홍보에 힘쓰고 있으며, 향후에도 수의사 네트워크를 대상으로 한 적극적인 마케팅을 진행할 예정입니다.
② 기술이전(라이선스아웃)
Vax-NK 플랫폼은 진행성 간세포암, 확장병기 소세포폐암, 진행성 췌장암을 목표질환으로 삼고 있습니다. 국내에서 일차적으로 임상연구를 수행하면서, 동시에 동남아시아를 중심으로 Vax-NK 플랫폼의 기술 마케팅을 수행하여 글로벌 공동연구 또는 기술이전을 추진할 계획입니다.
Vax-CAR 플랫폼은 기존에 비임상시험을 진행하던 CAR-T, CAR-NK 세포치료제 뿐만 아니라 최근 다발골수종을 목표질환으로 하여 개발한 CAR-MILs 치료제의 예비연구를 마치고 본격적인 연구단계에 돌입하였습니다. Vax-CAR 플랫폼의 경우 일차적으로 비임상시험 데이터를 활용하여 적극적인 라이선스아웃을 추진할 계획입
니다. 본격적인 기술영업에 앞서 2022 KSMO, 2022 ICBMT 등의 글로벌 학회를 통해 당사의 Vax-NK 플랫폼 및 Vax-CAR 플랫폼 등의 파이프라인에 대한 홍보활동을 꾸준히 진행하고 있습니다.
다. 수주상황
당사는 보고서 작성기준일 현재 해당사항이 없습니다.
5. 위험관리 및 파생거래
가. 재무위험 관리
회사의 재무위험관리는 시장위험, 신용위험 및 유동성위험과 같은 다양한 재무위험하에서도 안정적이고 지속적인 경영성과를 창출할 수 있도록 재무구조 개선 및 자금운영의 효율성을 제고하는 데 있습니다.
재무위험관리활동은 주로 자금부서에서 주관하고 있으며 관련 부서와의 긴밀한 협조하에 재무위험 관리정책 수립 및 재무위험 식별, 평가, 헷지 등의 실행활동을 하고 있습니다. 또한, 정기적으로 재무위험 관리정책의 재정비, 재무위험 모니터링 등을 통해 재무위험으로부터 발생할 수 있는 영향을 최소화하는데 주력하고 있습니다.
(1) 신용위험
회사는 금융상품의 당사자 중 일방이 의무를 이행하지 않아 상대방에게 재무손실을 입힐 신용위험에 노출되어 있습니다.
신용위험은 주로 단기대여금 및 채무상품, 금융기관예치금으로부터 발생하고 있습니다.
회사는 신용위험을 관리하기 위하여 신용도가 일정 수준 이상인 거래처와 거래하고 있으며, 금융자산의 신용보강을 위한 정책과 절차를 마련하여 운영하고 있습니다.
회사는 신규 거래처와 계약시 공개된 재무정보와 신용평가기관에 의하여 제공된 정보 등을 이용하여 거래처의 신용도를 평가하고 이를 근거로 신용거래한도를 결정하고 있으며, 담보 또는 지급보증을 제공받고 있습니다.
또한, 회사는 주기적으로 거래처의 신용도를 재평가하여 신용거래한도를 재검토하고담보수준을 재조정하고 있으며, 회수가 지연되는 금융자산에 대하여는 정기적으로 회수지연 현황을 파악하고 회수대책을 마련하는 등 적절한 조치를 취하고 있습니다.
보고기간 종료일 현재 상각후원가로 분류된 금융상품의 신용위험에 노출된 최대금액은 장부금액과 유사합니다.
(2) 유동성위험
회사는 현금 등 금융자산을 인도하여 결제하는 금융부채에 관련된 의무를 충족하는 데 어려움을 겪게 될 유동성위험에 노출되어 있습니다.
회사는 정기적인 자금수지계획의 수립을 토대로 영업활동, 투자활동, 재무활동에서의 자금수지를 미리 예측해 금융부채와 금융자산의 만기구조를 대응시키고 있으며, 이를 통해 필요 유동성 규모를 사전에 확보하고 유지하여 향후에 발생할 수 있는 유동성리스크를 사전에 관리하고 있습니다.
보고기간 종료일 현재 파생금융상품이 아닌 주요 금융부채의 명목가액에 대한 연도별 상환계획은 다음과 같습니다.
1) 당반기말
| (단위: 원) |
| 구분 | 장부금액 | 계약상 원금 | 합계 | |
|---|---|---|---|---|
| 1년 이하 | 1년 초과 | |||
| 미지급금 | 356,749,758 | 125,726,818 | 231,022,940 | 356,749,758 |
| 미지급비용 | 157,060,024 | 157,060,024 | - | 157,060,024 |
| 리스부채 | 336,061,110 | 143,850,960 | 251,057,945 | 394,908,905 |
2) 전기말
| (단위: 원) |
| 구분 | 장부금액 | 계약상 원금 | 합계 | |
|---|---|---|---|---|
| 1년 이하 | 1년 초과 | |||
| 미지급금 | 277,710,071 | 58,601,545 | 219,108,526 | 277,710,071 |
| 미지급비용 | 118,230,936 | 118,230,936 | - | 118,230,936 |
| 리스부채 | 105,237,995 | 48,840,000 | 69,054,545 | 117,894,545 |
(3) 자본위험
회사의 자본위험관리 목적은 계속기업으로서 주주 및 이해당사자들에게 이익을 지속적으로 제공할 수 있는 능력을 보호하고 자본비용을 절감하기 위해 최적 자본구조를 유지하는 것입니다. 회사는 최적 자본구조를 달성하기 위하여 동종산업내의 타사와 마찬가지로 부채비율에 기초하여 자본을 관리하고 있습니다. 부채비율은 부채총계를자본총계로 나누어 산출하고 있습니다.
보고기간 종료일 현재 회사의 부채비율은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기말 | 전기말 |
|---|---|---|
| 부채총계(A) | 1,378,381,759 | 835,777,840 |
| 자본총계(B) | 18,696,472,616 | 23,327,267,446 |
| 부채비율(A/B) | 7.37% | 3.58% |
6. 주요계약 및 연구개발활동
가. 주요계약
1) 공동연구개발 관련 주요계약
|
계약 상대방 |
계약일(기간) |
계약의 목적 및 내용 |
계약금액 또는 대금수주방법 (기준) 등 |
비고 |
|
와이바이오로직스 |
2021.11.02 |
차세대 Chimeric Antigen Receptor 기술을 활용한 항암 세포치료제를 공동 연구개발 |
주1) |
- |
|
㈜디알큐어 |
2023.07.01~ 2024.02.29 |
사이토카인 IL-15 서방형 제제 개발 및 특허 출원 |
||
|
Senlang biotechnology co., LTD |
2023.04.12 |
Co-Development agreement on cellular immunotherapeutic drug (BCMA CAR-T) |
|
주1) 계약 세부 내용의 경우 영업기밀에 해당하므로 기재하지 않았습니다.
(2) License In 관련 계약 체결 내역
|
품목 |
계약 상대방 |
대상지역 |
계약 체결일 |
계약 종료일 |
계약의 목적 및 내용 |
총 계약 금액 |
지급금액 |
진행 단계 |
비고 |
|
종양 조직에 특이적 결합된 단백질 및 그 용도 |
전남대학교 산학협력단 |
국내 및 해외 전역 |
2019.10.01 |
특허 존속기간 만료일 |
‘인간 피브로넥틴 도메인III 기본 골격의 신규 인간 EphA2 특이적 결합 단백질 및 그의 용도 기술이전계약 (전용실시권) |
주1) |
주1) |
연구 단계 |
경상기술료 별도 |
|
수지상 세포 기능 강화 |
전남대학교 산학협력단 |
국내 |
2020.05.06 |
특허 존속기간 만료일 |
‘수지상세포의 성숙화 유도용 조성물’외 2건 기술이전계약 (전용실시권) |
주1) |
주1) |
연구 단계 |
경상기술료 별도 |
|
NK세포의 활성화 및 증폭을 위해 유전적으로 조작된 세포주 및 그 용도 |
서울대학교 산학협력단/삼성서울병원 |
국내 |
2022.04.29 |
특허 존속기간 만료일 |
‘NK세포의 활성화 및 증폭을 위해 유전적으로 조작된 세포주 및 그의 용도에 관한 특허 및 특허 관련 기술이전계약 (전용실시권) |
주 1) |
주 1) |
연구 단계 |
경상기술료 별도 |
주1) 계약 세부 내용의 경우 영업기밀에 해당하므로 기재하지 않았습니다.
(3) 특허 양수도 계약
|
계약 상대방 |
계약일 |
계약의 목적 및 내용 |
계약금액 또는 대금수주방법(기준)등 |
비고 |
|
삼성서울병원 |
2019.09.17 |
OX40L을 발현하는 배양보조세포 및 이를 이용한 자연살해세포 배양방법' 특허양수도 계약 |
주1) |
- |
|
공주대학교 |
2019.11.11 |
'개 인터루킨-15 체외 증폭용 프라이머 세트, 이의 용도 및 이를 이용한 재조합 개 인터루킨-15 제조방법' 특허양수도 계약 |
주1) |
- |
|
한국생명공학 |
2020.09.14 |
OX40L을 발현하는 배양보조세포 및 이를 이용한 자연살해세포 배양방법' 특허양수도 계약 |
주1) |
- |
|
한국생명공학 |
2020.11.11 |
'OX40L을 발현하는 배양보조세포 및 이를 이용한 자연살해세포 배양방법' 특허양수도 계약(PCT) |
주1) |
- |
주1) 계약 세부 내용의 경우 영업기밀에 해당하므로 기재하지 않았습니다.
(4) 임상 관련 계약
|
계약 상대방 |
계약일 (기간) |
계약의 목적 및 내용 |
계약금액 또는 대금수주방법(기준)등 |
비고 |
|
화순전남대학교병원 |
2018.10.08~2023. 12. 31 |
진행성 간세포암 환자에서 자연살해세포와 간동맥주입화학요법 병합치료에 관한 임상 2a상 연구 |
주1) |
- |
|
㈜씨엔알리서치 |
2019.01.07 |
진행성 간세포암 환자에서 자연살해세포와 간동맥주입화학요법 병합치료에 관한 임상 2a상 연구 |
- |
|
|
2019.09.03 |
진행성 간세포암 환자에서 자연살해세포와 간동맥주입화학요법 병합치료에 관한 임상 2a상 연구(독립적 영상평가) |
|||
|
가톨릭대학교 서울성모병원 |
2019.09.09~2023. 12. 31 |
진행성 간세포암 환자에서 자연살해세포와 간동맥주입화학요법 병합치료에 관한 임상 2a상 연구 |
- |
|
|
삼성서울병원 |
2019.10.10~2023.12.31 |
진행성 간세포암 환자에서 자연살해세포와 간동맥주입화학요법 병합치료에 관한 임상 2a상 연구의 항-종양 면역반응 분석 |
- |
|
|
동아대학교병원 |
2021.05.12~2023. 12. 31 |
진행성 간세포암 환자에서 자연살해세포와 간동맥주입화학요법 병합치료에 관한 임상 2a상 연구 |
- |
|
|
부산대학교병원 |
2021.06.10~2023. 04. 17 |
진행성 간세포암 환자에서 자연살해세포와 간동맥주입화학요법 병합치료에 관한 임상 2a상 연구 |
- |
|
|
영남대학교병원 |
2021.05.21~2023. 12. 31 |
진행성 간세포암 환자에서 자연살해세포와 간동맥주입화학요법 병합치료에 관한 임상 2a상 연구 |
- |
|
|
트라이얼인포매틱스 |
2021.12.01~2024.12.01 |
진행성 간세포암 환자에서 자연살해세포와 간동맥주입화학요법 병합치료에 관한 임상 2a상 연구를 위한 Onco Trial Board 사용 |
|
주1) 계약 세부 내용의 경우 영업기밀에 해당하므로 기재하지 않았습니다.
(5) 기타 계약
|
계약 상대방 |
계약일 (기간) |
계약의 목적 및 내용 |
계약금액 또는 대금수주방법(기준)등 |
비고 |
|
(재)전남생물산업진흥원 생물의약연구센터 |
2022.11.01~2023.10.31 |
창업보육센터 클린룸 보육시설 사용계약서 |
주 1) |
GMP 시설 계약 |
|
(재)전남생물산업진흥원 생물의약연구센터 |
2020.01.01~2023.12.31 |
세포치료제 시험 위수탁 계약 (무균시험, 마이코플라즈마부정시험,외래성바이러스부정시험,엔도톡신) |
주1) |
- |
주1) 계약 세부 내용의 경우 영업기밀에 해당하므로 기재하지 않았습니다.
나. 연구개발활동의 개요
(1) 연구개발 조직 개요
당사는 2010년 7월 기업부설연구소를 설립하여 한국산업기술진흥협회로부터 인증 받았으며, 이준행 CSO와 김미화 연구소장을 필두로 Vax-CAR 플랫폼 연구, 차세대 박스루킨-15 연구, Monobody 플랫폼 연구를 진행하고 있습니다.
2022년에는 공정개발실을 신설하여 10년 넘게 면역치료 분야의 연구에 몰두한 김상기 교수와 Vo Manh Cuong 박사를 영입하여 차세대 Vax-NK 공정개발, 박스루킨-15 공정개발, 차세대 박스루킨-15 연구와 더불어 Vax-CAR-T의 공정개발 및 Vax-CAR-MIL의 연구를 진행하고 있습니다.
당사 연구개발 담당조직은 본 보고서 작성기준일 현재 아래와 같습니다.
 |
|
2. 박셀바이오 연구개발 담당조직 |
(2) 연구개발 인력 현황
공시서류 기준일 현재 당사는 박사급 12명 등 총 28명의 연구개발 인력을 보유하고 있으며, 총 연구개발 인력은 대표이사를 포함하여 전체 인력(57명)중 50%를 차지합니다
|
구분 |
인원 (명) |
|||
|
박사 |
석사 |
기타 |
합계 |
|
| 기술연구소 | 2 | 2 | 3 | 7 |
| 임상연구실 | 1 | 1 | 2 | 4 |
| 공정개발실 | 1 | 2 | 2 | 5 |
| 동물의약품실 | 2 | 0 | 2 | 4 |
| 기타 핵심 연구 인력 | 6 | 2 | 0 | 8 |
| 합계 | 12 | 7 | 9 | 28 |
(3) 연구개발 핵심인력
당사의 주요 핵심 연구 인력 현황은 아래와 같습니다.
|
직책명 |
성 명 (출생년) |
담당업무 |
약 력 |
|
대표이사(CEO/CMO) |
이제중 |
총괄 |
99.02 전남대학교 의과대학 혈액종양학 박사 99.05~03.07 화순전남대학교병원 임상교수 00.07~01.01 일본 동경 국립암센터 방문연구원 06.03~07.12 미국 피츠버그대학교 암연구소 방문교수 10.02~19.06 ㈜박셀바이오 대표이사 (설립) 15.01~17.12 한국다발골수종연구회 위원장 03.07~전남의대/현재 화순전남대학교병원 혈액종양내과 교수 08.12~현재 화순전남대학교병원 암면역치료연구센터장 21.02~현재 ㈜박셀바이오 대표이사 |
|
사내이사 (CSO) |
이준행 |
기술연구소 총괄 (연구) |
92.02 전남대학교 의과대학 미생물학 박사 17.05~19.04 대한기초의학협의회 부회장 19.06~19.11 ㈜박셀바이오 대표이사 93.08~현재 전남대학교 의과대학 교수 17.01~현재 (재)백신글로벌산업화기반 구축사업단 선임이사 21.01~현재 ㈜박셀바이오 연구총괄 및 사내이사 |
|
이사 |
배우균 |
연구개발 |
11.03 전남대학교 의학박사 |
| 이사 (비등기/상근) |
김상기 (1960년) |
연구개발 (공정개발) |
93.08 전남대학교 수의학과 05.09~ 현재 화순전남대학교 병원 암면역세포치료연구센터 06.02~ 현재 공주대학교 산업과학대학 특수동물학과 교수 23.03~ 현재 (주)박셀바이오 공정개발실장 |
|
이사 (비등기/상근) |
하선아 (1971년) |
연구개발 (임상) |
02.02 미주리주립대학교 박사 (세포생물학) 02.08~04.04 가톨릭의과대학교 연구교수 04.06~06.04 Riken Institute (Yokohama) 박사후 연구원 (면역학) 06.05~18.01 가톨릭의과대 연구교수/기진싸이언스 겸직 17.04~18.01 서울대의과대학 (임상기획) 18.02~18.09 ㈜헤링스 (임상기획) 18.10~21.05 ㈜퓨쳐메디신 (임상/전임상 총괄) |
|
이사 (비등기/상근) |
김미화 |
기술연구소 총괄 |
03.02 전남대학교 의학 박사(병리학) 03.03~07.03 조선대학교 의과대학 약리학교실 계약교수 07.04~09.04 조선대학교 단백질소재연구센터 (ERC) 전임강사 09.05~12.02 조선대학교 한국인유전자손상연구센터 (KDRRC) 연구교수 12.05~14.02 전남대학교 치의학과 미네랄장애연구센터 (MRC) 연구교수 14.10~15.08 미국 텍사스 주립대 의과대학 약리학과 박사후 연구원 15.09~17.03 미국 텍사스 주립대 의과대학 생명과학과 연구원 17.04~20.08 미국 텍사스 주립대 의과대학 생물의학부 조교수 |
|
이사 (비등기/상근) |
이재일 |
연구개발 |
94.03 전남대학교 수의학 박사 |
|
이사 (비등기/상근) |
장윤영 |
연구개발 |
13.08 전남대학교 분자의과학협동과정 박사 02.02~03.07 조선대학교 유전공학 분자세포생물학 실험실 연구보조 03.08~04.02 전남대학교 치과대학 구강병리학교실 연구원 06.02~08.09 JB줄기세포연구소 동물실험팀장 08.11~10.08 암면역치료연구센터 연구원 13.01~현재 ㈜박셀바이오 제조소장 |
|
부 장 |
심재웅 |
연구개발 |
13.08 전남대학교 분자의과학 이학박사 13.09~15.07 전남대학교 알레르기내과 연구원 15.08~17.10 화순전남대병원 의생명연구원 연구교수 17.12~현재 ㈜박셀바이오 품질관리실장 |
|
부 장 |
Vo Manh Cuong (1983년) |
연구개발 (공정개발) |
11.03~16.02 전남대학교 분자의학과 석사, 박사 16.03~19.02 화순전남대병원 혈액종양내과 박사후 연구원 19.03~22.12 화순전남대병원 혈액종양내과 연구교수 22.12~현재 ㈜박셀바이오 공정개발실 |
|
수석연구원 |
백민우 (1978년) |
연구개발 (연구) |
06.03~10.08 전남대학교 생명과학기술학과 박사 10.09~12.01 한국기초과학지원연구원(KBSI) 박사후 연구원 12.02~13.03 전남대학교 치과대학 생체광물화질환 연구센터 연구교수 13.04~16.03 전남대학교 생명과학기술학과 박사후 연구원 16.04~17.08 텍사스대학교 UTRGV 의과대학 박사후 연구원 17.09~21.03 미네소타대학교 약학과 박사후 연구원 18.09~21.03 미네소타대학교 연구기기연구실 관리자 21.05~22.11 충북대학교 노화연구소 초빙 부교수 22.12~현재 ㈜박셀바이오 기술연구소 수석연구원 |
(4) 연구개발비용 (단위 : 천원)
|
구분 |
2023년도 (제14기 2분기) |
2022년도 (제13기) |
2021년도 (제12기) |
2020년도 (제11기) |
|
|
자산 처리 |
원재료비 |
- |
- |
- |
- |
|
인건비 |
- |
- |
- |
- |
|
|
감가상각비 |
- |
- |
- |
- |
|
|
위탁용역비 |
- |
- |
- |
- |
|
|
기타경비 |
- |
- |
- |
- |
|
|
소계 |
- |
- |
- |
- |
|
|
비용 |
제조원가 |
- |
- |
- |
- |
|
판관비(*) |
2,016,266 |
2,062,362 |
1,799,582 |
1,340,041 |
|
|
소계 |
2,016,266 |
2,062,362 |
1,799,582 |
1,340,041 |
|
|
(정부보조금) |
- |
- |
- |
- |
|
|
보조금차감후금액 |
2,016,266 |
2,062,362 |
1,799,582 |
1,340,041 |
|
|
합계 |
2,016,266 |
2,062,362 |
1,799,582 |
1,340,041 |
|
(*)연구개발비용은 전액판관비로 계상되어있으며, 정부보조금은 별도의 수익으로 처리하고 있습니다.
다. 연구개발 실적
(1) 연구개발 진행 현황
당사가 연구개발 진행 중인 프로젝트 현황은 다음과 같습니다.
|
구분 |
품목 |
적응증 |
현재 진행단계 |
비고 | |
|
단계(국가) |
승인년도 | ||||
|
항암제 |
Vax-NK |
진행성 간세포암 |
임상2a상(한국) |
2018년 |
Vax-NK + HAIC(5-FU/시스플라틴) 병용요법 |
|
진행성 췌장암 |
임상2a상 신청 |
- |
식품의약품안전처 임상시험계획 변경신청 (적응증 추가) |
||
|
소세포폐암 |
임상연구 승인 |
- |
첨단재생의료 임상연구계획 승인 (연구자임상) |
||
|
항암제 |
Vax-CAR (CAR-T, CAR-NK, CAR-MIL) |
MSLN, EphA2발현 난치성 고형암 |
비임상 |
- |
소동물 종양모델에서 효능시험 진행중 |
|
PD-L1 발현 난치성 고형암 |
비임상 |
- |
소동물 종양모델에서 효능시험 진행중 |
||
|
BCMA 발현난치성 다발골수종 |
비임상 |
- |
임상시험을 위한 생산공정 확립 중 | ||
|
동물용 |
박스루킨-15 |
개의 악성종양 |
임상시험(한국) |
- |
농림축산검역본부 임상시험 진행 후 품목허가 재신청 예정 |
(가) Vax-NK
|
구분 |
항암제(바이오 신약) |
|
적응증 |
진행성 간세포암(HAIC와의 병용 치료) 진행성 췌장암(mFOLFIRINOX 요법과 병용 치료) 소세포폐암(아테졸리주맙과 병용 투여) |
|
M제품설명 |
- Vax-NK는 백혈구분반술을 통해 대상환자의 말초혈액단핵구를 추출하여 자연살해(NK)세포를 분리 후, 방사선조사영양세포주 및 싸이토카인 칵테일에 의한 자극을 통하여 2주 동안 배양하여 제조하는 자가유래 NK세포 기반의 면역세포치료제임. |
|
제품의 특성 |
- 영양세포주와 낮은 농도 사이토카인를 이용한 NK세포의 증폭률(평균 300배 증폭) 및 순도(평균 85% 이상) 극대화 - 진행성 췌장암은 예후가 좋지 않고 워낙 발견이 늦은 경우가 많기 때문에 수술 가능한 환자는 전체 환자의 12.5%에 불과하며 췌장암에 특어적으로 작용하여 허가받은 면역항암제가 없는 실정이며, 표준치료인mOLFIRINOX 요법과 Vax-NK 병용 투여 시 우수한 효과를 보일 것이라 기대함 - 소세포 폐암은 암세포의 성장이 아주 빠르며 초기 단계에서도 전이가 쉽게 일어나는 암으로 예후가 좋지 않은 암종으로 알려져 있으며 5년 생존율도 5~10%로 매우 낮기 때문에 미충족 의료수요가 높은 암종임. 아테졸리주맙과 Vax-NK 병용 투여한 비임상 시험에서 높은 종양억제 효과를 확인했으며, 높은 항암효과를 가진 치료제가 될 것으로 기대함 |
|
진행경과 |
- 11명의 진행성 간세포암 환자 대상 임상 1상 완료 - 진행성 췌장암은 식약처에 적응증 추가를 위한 Vax-NK 임상시험계획변경 승인(임상2a상) 신청 완료 (2023.07.31) - 소세포폐암 대상 첨단재생의료 임상연구계획 승인(연구자임상) |
|
향후계획 |
- 진행성 간세포암 임상 2a상 완료 후 임상 2b상 또는 임상3상 진입 예정 - 진행성 췌장암 임상2a상 승인 후 실시 예정 (신청완료) - 소세포폐암 첨단재생의료 임상연구 실시 예정(승인완료) |
|
유사경쟁제품 |
- 간세포암에 대한 항암면역세포치료제로는 녹십자셀의 이뮨셀엘씨주(2007년 국내 조건부품목허가, 2012년 임상3상완료)가 있음. 그러나 이뮨셀엘씨주는 간세포암 제거술(수술, 고주파절제술, 경피적 에탄올 주입술) 후 종양제거가 확인된 환자에서 보조요법으로 사용되고 있으며, 주세포군은 활성화 T-림프구와 싸이토카인 유도 살해세포(Cytokine induced killer cell, CIK cell)로, NK세포를 기반으로 하는 Vax-NK와는 차이점이 있어 상호 배타적인 경쟁제품으로 특정하기 어려움. |
|
시장규모 |
시장형성 초기 단계이므로, 목표 시장을 특정하기 어려움. |
나) Vax-CAR-T/-NK (MSLN, EphA2)
|
구분 |
항암제(바이오 신약) |
|
적응증 |
MSLN, EphA2 발현 난치성 고형암 |
|
제품 설명 |
- CAR-T/-NK의 작용기전은 환자유래 T세포 또는 NK세포에 인위적으로 도입된 항원 특이적 키메라 항원 수용체(chimeric antigen receptor, CAR)에 의해 선택적으로 표적암을 사멸시킴. |
|
제품의 특성 |
- CAR-T/-NK 세포는 특정항원에 결합하는 CAR를 T/NK 세포에 도입하므로, MHC 분자의 도움 없이도 특정 암을 직접 인지하여 T세포 또는 NK세포의 선택적 살상능을 높임. |
|
진행경과 |
- 다양한 고형암 세포주(CAPAN2, OVCAR3, AsPC1)를 대상으로 한 in vitro 효능 시험에서 암세포 살상능을 확인함 |
|
향후계획 |
GLP수준의 비임상 독성 시험 및 기전 연구를 진행 후, 임상시험에 진입할 계획 |
|
유사경쟁 |
- CAR-T세포 치료제로는 노바티스사의 킴리아와 길리어드사의 예스카르타, 테카터스, BMS사의 브레얀지, 아벡마 그리고 J&J의 카빅티가 혈액암을 대상으로 시판되었음. |
|
시장규모 |
시장형성 초기 단계이므로, 목표 시장을 특정하기 어려움. |
다) Vax-CAR-T/-NK (PD-L1)
|
구분 |
항암제(바이오 신약) |
|
적응증 |
PD-L1 발현 난치성 고형암 |
|
제품 설명 |
- CAR-T/-NK의 작용기전은 환자유래 T세포 또는 NK세포에 인위적으로 도입된 항원 특이적 키메라 항원 수용체(chimeric antigen receptor, CAR)에 의해 선택적으로 표적암을 사멸시킴. |
|
제품의 특성 |
- CAR-T/-NK 세포는 특정 항원에 결합하는 CAR(anti-PD-L1)를 T/NK세포에 도입하므로, MHC 분자의 도움 없이도 특정 암을 직접 인지하여 T세포 또는 NK세포의 선택적 살상능을 높임. |
|
진행경과 |
- 다양한 고형암 세포주를 대상으로 한 in vitro 효능 시험에서 암세포 살상능을 확인함 |
|
향후계획 |
GLP수준의 비임상 독성 시험 및 기전 연구를 진행 후, 임상시험에 진입할 계획 |
|
유사경쟁 |
- CAR-T세포 치료제로는 노바티스사의 킴리아와 길리어드사의 예스카르타, 테카터스, BMS사의 브레얀지, 아벡마 그리고 J&J의 카빅티가 혈액암을 대상으로 시판되었음. |
|
시장규모 |
시장형성 초기 단계이므로, 목표 시장을 특정하기 어려움. |
라) Vax-CAR-T (BCMA)
|
구분 |
항암제 (바이오 신약) |
|
적응증 |
재발성/불응성 다발골수종 |
|
제품 설명 |
- B-cell maturation antigen (BCMA)를 표적으로 인식하는 항체를 T 세포에 도입하여 제조되며, 이 항체는 BCMA를 발현하는 다발골수종 세포를 선택적으로 인식하고 결합하는 선택적 암세포 파괴 능력을 가짐 - BCMA를 인식하는 항체를 도입한 T 세포를 대량 제조하며, 이렇게 제조된 CAR-T 세포는 BCMA를 발현하는 다발골수종 세포를 인식하고 결합함으로써 다양한 면역 반응 메커니즘을 발동함 - 활성화된 Vax-CAR-T 세포는 세포독성 작용, 사멸 프로그램을 유도하는 신호 분자의 분비, 면역 세포의 파괴를 돕는 다른 면역 세포와의 상호작용 등을 통해 암세포에 대한 파괴 작용을 수행함 |
|
제품의 특성 |
- BCMA CAR-T는 B-cell maturation antigen (BCMA)를 표적으로 하는 항체를 T 세포에 도입하여 제작되며, 이로 인해 BCMA를 발현하는 다발골수종 세포만을 선택적으로 인식하고 표적으로 함 - BCMA CAR-T는 제조된 T 세포가 항원 표적을 인식한 후 암세포를 파괴하는 능력을 가지며, 제조된 CAR-T 세포는 혈액 순환 속에서 암세포를 탐색하고 파괴하는 지속적인 활동을 수행함 - BCMA CAR-T는 환자 자체의 T 세포를 추출하여 제조되며, 이를 통해 개인의 면역 시스템과 유전자 프로필에 기반한 최적화된 맞춤형 치료를 제공함 |
|
진행경과 |
- Vax-CAR-T의 생산공정을 확립하는 중 |
|
향후계획 |
- GLP수준의 비임상 독성 시험 및 기전 연구를 진행 후, 임상시험에 진입할 계획 |
|
유사경쟁 |
- Janssen의 Carvykti는 한국에서 허가를 받았지만 아직 상용화 단계에 도달하지 않았음. - BMS(Bristol-Myers Squibb)의 Abecma는 한국에서는 아직 허가를 받지 않은 상황임. |
|
시장규모 |
- 시장형성 초기 단계이므로, 목표 시장을 특정하기 어려움. |
마) Vax-CAR-MIL (BCMA)
|
구분 |
항암제(바이오 신약) |
|
적응증 |
재발성 불응성 다발골수종 |
|
제품 설명 |
- MIL은 "말초혈액"에서 분리하여 개발되는 CAR-T, TCR-T, 종양침윤림프구(TIL) 등의 면역세포치료제와는 달리 ‘골수’에서 분리했다는 점에서 차이점을 보이며 골수 미세환경의 독특한 생물학적 특성 때문에 기억T세포가 풍부해 항암효과 및 지속성을 향상시킬 수 있음 - 다수의 암 항원에 대한 특이성을 가져 항원 손실에 의한 재발을 막을 수 있고 다양한 암 유형에 적용 가능함 - CAR 단일사슬 변수 단편 항체(scFV)와 결합하여 암세포 살상능이 더 증폭시킴 |
|
제품의 특성 |
- CAR-MIL은 환자의 골수에서 유래한 골수침윤림프구(MIL)과 당사의 CAR와 결합시켜 다발골수종에 매우 특이적이고 암세포 살상능이 매우 높을 것으로 기대됨 |
|
진행경과 |
- 다발골수종 세포를 대상으로 한 in vitro 효능 시험에서 높은 암세포 살상능을 확인함 |
|
향후계획 |
- GLP 수준 비임상 독성 시험과 공정개발을 확립한 후 임상시험에 진입할 계획 |
|
유사경쟁 |
- CAR-T세포 치료제로는 아베크마(Abecma, BMS, 2021년 FDA승인)와 카비티(CARVYKTI, J&J, 2022년 FDA승인)의 두 가지 제품이 재발성 불응성 다발골수종에 승인되었으며 처방되고 있음. 그러나 아직 한국시장에는 진입하지 못함 |
|
시장규모 |
- 시장형성 초기 단계이므로, 목표 시장을 특정하기 어려움. |
바). 박스루킨-15
|
구분 |
반려견 항암병용(보조)치료제 |
|
적응증 |
개의 악성종양(유선종양, 림프종 등) |
|
제품 설명 |
- 개 인터루킨-15 유전자를 기반으로 한 재조합 단백질로 동물용 항암면역증강제임. |
|
제품의 특성 |
- 반려견 전용 면역증강제(개의 유전체 정보를 바탕으로 한 설계 및 개발) - 항암화학효법과 병용 시 다양한 암종에 대한 높은 치료 효과를 보임 |
|
진행경과 |
- 랫드 및 비글견 대상 비임상 독성시험 완료(한국화학융합시험연구원 헬스케어연구소) - 21년 09월 품목허가 보완서류 제출 - 21년 11월 2차 보완요청 [시험군의 충분한 확보를 통한 통계적 유의성 확보 필요] - 21년 12월 품목허가 철회 [시험기관 추가 및 제품 생산 등 준비 중] - 국내 동물의약품 제약사와 생산 및 유통 협약 체결 - 전국 50여개의 동물병원을 대상으로 임상시험 진행 중 |
|
향후계획 |
- KVGMP 시설 위탁생산업체를 통한 대량생산 및 판매 |
|
유사경쟁제품 |
아직까지 동물 전용 항암면역치료제로 승인된 사례는 없음. |
|
시장규모 |
시장형성 초기 단계이므로, 목표 시장을 특정하기 어려움. |
(사) Vax-NK의 응급임상시험 실적
당사는 악성 종양 관련 신약을 연구개발하고 있는 상황으로, 협력 관계를 유지하고 있는 화순전남대병원과 다수의 응급임상(치료목적 사용승인)을 수행하였습니다. 방광암, 위암 등 9개 암종에 대한 Vax-NK의 응급임상시험에 대한 간략한 정리는 다음의 표와 같습니다.
|
나이 |
성별 |
질환 |
시험년월 |
결과 |
|
76 |
남 |
방광암 |
2016.09 |
질환진행 |
|
42 |
여 |
위암 |
2016.12 |
질환진행 |
|
31 |
여 |
급성림프구성백혈병 |
2016.12 |
질환진행 |
|
44 |
여 |
유방암 |
2017.05 |
질환진행 |
|
53 |
여 |
유방암 |
2017.05 |
질환진행 |
|
46 |
여 |
다발골수종 |
2017.07 |
완전반응 |
|
56 |
여 |
지방육종 |
2017.07 |
완전반응 |
|
45 |
여 |
교모세포종 |
2018.01 |
부분반응 |
|
61 |
여 |
췌장암 (*) |
2018.07 |
완전반응 |
|
51 |
남 |
간세포암종 |
2019.09 |
완전반응 |
|
74 |
남 |
췌장암 |
2021.12 |
질환진행 |
|
56 |
여 |
간암 |
2023.05 |
모니터링 중 |
(*) 해당환자는 췌장암의 간 전이로 인해 간동맥내 투여경로로 응급임상을 승인받았습니다.
(2) 연구개발 완료 실적
보고서 작성기준일 현재 모든 파이프라인이 연구개발 단계로 기초연구 또는 임상연구를 진행 중입니다. 박스루킨-15 품목의 경우 유선종양 및 림프종 환견 및 대조군에 대한 추가 임상연구를 진행하고 있으며, 2023년 내에 품목허가를 재신청할 계획입니다.
(3) 연구개발활동 및 판매 중단현황
|
제품명 |
적응증 |
내용 |
비고 |
|
Vax-DC/MM |
다발골수종 |
2013.10. 1/2a 임상시험 승인 2015.07. 1/2a 임상시험 완료 2017.08. 2b 임상시험 계획 승인 2019.04. 2a 임상시험 계획 승인 2022.07 임상시험 연구개발 조기종료 |
다발골수종 타겟 Vax-CARs 플랫폼으로 변경 |
(4) 연구개발계획
현재까지 수행한 Vax-NK/HCC의 임상1상 결과 및 임상2a상 데이터, 그리고 Vax-NK의 다수의 응급임상 데이터를 바탕으로 Vax-NK 자연살해세포치료제 플랫폼의 적응증 확대 가능성과, 더불어 환자의 삶의 질 향상에 대한 근거를 확보하였습니다. 이를 바탕으로 현재 당사가 계획하고 있는 연구개발계획은 다음과 같습니다.
|
No |
플랫폼 구분 |
프로젝트 |
임상 기관 (병원명) |
구분 |
비고 |
|
1 |
Vax-NK |
췌장암 |
미정 |
SIT |
Vax-NK 기반 mFOLFIRINOX 병합치료 |
|
2 |
Vax-NK |
소세포폐암 |
화순전남대학교병원 |
IIT |
Vax-NK 기반 CPI 복합치료; 국가 면역치료 혁신 플랫폼 과제 |
|
3 |
Vax-CAR (T, NK, MIL) |
고형암,혈액암 |
- |
- |
- |
당사는 Vax-NK에 대한 응급임상 결과를 바탕으로 본격적인 적응증 확대를 위하여 다수의 첨단재생의료 임상연구 및 상업화 임상시험(SIT)을 계획하고 있습니다.
췌장암, 소세포폐암 등의 적응증을 대상으로 당사와 협력관계에 있는 화순전남대학교병원 및 서울성모병원, 분당서울대병원 등과 협업을 통해 보다 안전하고 높은 치료효과를 보일 수 있는 임상시험 프로토콜을 개발하고 있습니다.
또한 치료목적 사용승인(구"응급임상")에서는 적극적으로 평가하지 못하였던 말기 암 환자의 '삶의 질'에 대한 평가를 수행하여 Vax-NK 항암면역치료 플랫폼의 장점을 검증할 계획입니다.
고형암 및 혈액암을 적응증으로 한 CAR-T/-NK/-MIL세포치료제의 경우 연구 개발 및 제조 공정개발 중에 있으며, 특히MILs의 경우IL-2, IL-7 및IL-15 등 사이토카인 프로파일을 사용하여 특허를 작성하고 있습니다. 또한, 이러한 플렛폼을 이용하여 in vivo/in vitro 연구에 매진하고 있습니다.
7. 기타 참고사항
당사는 증권신고서 작성기준일 현재 2건의 국책과제를 수행중이며, 국내외 총 10건의 특허를 보유하고 있으며, 세부사항은 아래와 같습니다.
가. 국책과제 선정 현황
|
번호 |
프로그램명 (시행부처/기관) |
과 제 명 |
총개발기간 (시작,종료일) |
총사업비 (백만원) |
비 고 |
|
1 |
기술혁신개발사업 (중소기업청) |
재조합 단백질 IL-15를 이용한 동물용 항암면역증강제 개발 |
2016.09.01 |
800 |
주관 |
|
2 |
사업화연계기술개발사업(R&BD) (산업통상자원부) |
간암치료제로써 자연살해세포인 Vax-NK/HCC의 안전성 평가 및 체내 항암효과 예측 평가법 확립 |
2016.07.01 |
1,995 |
주관 |
|
3 |
지역수요맞춤형연구개발사업 (전남테크노파크) |
다발골수종 특이 재조합 종양항원을 이용한 자가 수지상세포 항암백신의 안정성 평가 |
2018.06.01 |
202 |
주관 |
|
4 |
바이오의료기술개발사업 |
면역치료 혁신센터 (총괄) 면역치료 실용화 연구단 (3세부) |
2020.06.01 |
5,254 |
3세부 책임 |
|
5 |
반려동물전주기산업화기술개발사업 (농림축산식품부) |
항암 면역치료를 위한 개 키메라항원수용체-자연살해세포(CAR-NK cells) 치료제 및 개 면역관문저해제 (immune-checkpoint inhibitor) 개발 (총괄) |
2022.04.01 |
3,238 |
공동 |
나. 지적재산권 현황
| No. |
명칭 |
출원국 |
특허권자 |
등록번호 |
등록일 |
| 1 |
암-고환 항원을 포함하는 한국 난치성 다발골수종 예방 또는 치료용 세포 면역치료제 조성물 및 그 제조방법 |
대한민국 |
전남대학교 산학협력단/ (주)박셀바이오 |
10-1756073 PCT/KR2016/011178 |
2017.07.04 |
| 2 |
개 인터루킨-15 체외 증폭용 프라미어 세트, 이의 용도 및 이를 이용한 재조합 개 인터루킨-15 제조방법 |
대한민국 |
(주)박셀바이오 |
10-1440915 |
2014.09.05 |
| 3 |
수지상세포의 이동성 증진 및 수지상세포에 의해 제조된 세포독성 T세포의 세포살상능 증진방법 |
대한민국 |
전남대학교 산학협력단 |
10-1117186 |
2012.02.09 |
| 4 |
수지상세포의 이동성 증진 및 수지상세포에 의해 제조된 세포독성 T세포의 세포살상능 증진방법 |
대한민국 |
전남대학교 산학협력단 |
10-1083404 |
2011.11.08 |
| 5 |
수지상세포의 성숙화 유도용 조성물 |
대한민국 |
전남대학교 산학협력단 |
10-0997753 |
2010.11.25 |
| 6 |
OX40L을 발현하는 배양보조세포 및 이를 이용한 자연살해세포 배양 방법 |
대한민국 |
(주)박셀바이오 |
10-2227155 PCT/KR2019/006463 |
2021.03.08 |
| 7 |
인간 피브로넥틴 도메인 III 기본 골격의 신규 인간 EphA2 특이적 결합 단백질 및 그의 용도 |
대한민국 |
전남대학교 산학협력단 |
10-1636882 |
2016.06.30 |
| 8 |
모노바디 기반 키메라 항원 수용체 및 이를 포함하는 면역 세포 |
대한민국 |
㈜박셀바이오 |
10-2021-0067276 PCT/KR2022/007379 |
2021.05.25. PCT 출원2022.05.24. |
| 9 |
배양보조세포를 포함하는 자연살해세포 증식용 조성물 |
대한민국 |
㈜박셀바이오/ |
10-2021-0070778 PCT/KR2022/007782 |
2021.06.01. PCT 출원 2022.05.31 |
| 10 |
PD-L1 특이적 키메라 항원 수용체 및 이를 포함하는 면역세포 |
대한민국 |
㈜박셀바이오/ |
10-2022-0029633 |
2022.03.08 |
다. 산업의 특성
(1) 세포·유전자치료제 산업
세포치료제는 기존 암 치료법 (화학치료, 방사선치료 등)에 비해 표적 정확성이 높고 부작용이 적어 암 발병률 증가와 함께 항암제 R&D도 활발하게 진행되고 있으며 가장 ‘개인 맞춤형’에 근접한 치료제라는 점에서 매우 혁신적인 제품입니다. 바이오 협회에서 발간한 ‘2023년 글로벌 세포유전자 치료제 시장 동향’ 보고서에 따르면 전세계 세포유전자치료제 개발기업은 1,457개사로 전년 대비 11% 증가한 것으로 나타났습니다. 현재의 세포치료 관련 기술 장벽들로 인해 의약품 개발에 상대적으로 오랜 시간이 걸리고 있지만, 스핀라자, 졸겐스마, 킴리아 등 치료제들이 매년 수억 달러 이상의 매출액을 달성하며 성공적으로 시장에 정착한 사례들을 보면 세포치료제 분야는 아주 유망한 수익 창출 분야임에 틀림 없습니다. 특히, 현재 글로벌 차원에서 절대적 경쟁 우위에 있는 기업들이 극히 소수라는 점을 볼 때, 후발 기업들도 충분히 진입할 수 있는 분야입니다.
 |
|
3. 전세계 세포유전자치료제 개발사-한국바이오협회 2023 |
2022년에만 미국과 유럽에서 세포·유전자치료제가 처음으로 허가되었고, CAR-T 치료제인 Breyanzi(BMS사), Kymriah(Novartis사), Yescarta(Kite Pharma사) 등 3개와 유전자치료제인 Zynteglo, Zynteglo 및 Skysona(Bluebird bio사) 등 2개 품목이 새로운 지역 또는 새로운 적응증으로 허가되었습니다.
특히, ‘꿈의 항암제’라고 불리며 기대를 모았던 키메릭 항원수용체 T세포 (CAR-T) 치료제가 표적 및 항암 능력으로 주목받고 있습니다. 대표적으로 길리어드의 예스카타와 테카투스, 노바티스의 킴리아, BMS의 아베크마와 브레얀지 등을 필두로 현재 세계 여러 나라의 바이오 제약 회사들이 CAR-T치료제의 개발에 뛰어들고 있으며, 국내에서도 지난해와 올해 국가신약개발사업단 협약과제 227개 중에서 42.7%인 14개가 유전자치료제 과제였으며, 그 중 절반은 CAR-T 관련 연구로 나타났습니다.
 |
|
4. 글로벌 car-t 시장 규모 (research and market(2021)) |
글로벌 시장조사기관 Research and market에 따르면 2021년 글로벌CAR-T 치료제 시장 규모는 10억8500만 달러(약1조5700억원)으로 나타났으며, 연평균 성장률은 24.5%로 2028년에는 50억3100만 달러(약7조2600억원) 규모가 될 것으로 기대하고 있습니다.
(2) 동물용의약품 산업
반려동물을 키우는 1인 가구 증가, 반려동물의 수명 증가, 반려동물은 가족이라는 사회적 인식이 확대되면서 반려동물 관련 의약품 시장도 동반확장 중 입니다. 코로나19 팬데믹을 계기로 반려동물 관련 의약품 내수시장과 수출 규모도 늘어나, 자연스럽게 동물의약품 관련 유관된 기관과 제약사들이 산업 발전을 다양한 움직임을 보이고 있습니다.
![이미지: 데일리개원 2022년 8월 18일 [2022 동물약사업무 워크숍] 반려동물의약품 산업과 시장현황 ①](%EB%8D%B0%EC%9D%BC%EB%A6%AC%EA%B0%9C%EC%9B%90%202022%EB%85%84%208%EC%9B%94%2018%EC%9D%BC%20%5B2022%20%EB%8F%99%EB%AC%BC%EC%95%BD%EC%82%AC%EC%97%85%EB%AC%B4%20%EC%9B%8C%ED%81%AC%EC%88%8D%5D%20%EB%B0%98%EB%A0%A4%EB%8F%99%EB%AC%BC%EC%9D%98%EC%95%BD%ED%92%88%20%EC%82%B0%EC%97%85%EA%B3%BC%20%EC%8B%9C%EC%9E%A5%ED%98%84%ED%99%A9%20%E2%91%A0.jpg) |
|
데일리개원 2022년 8월 18일 [2022 동물약사업무 워크숍] 반려동물의약품 산업과 시장현황 ① |
하지만, 전체 반려견 중 25%이상이 8살 이후 50%확률로 암이 발생하는 높은 암 발병률을 보유하고 있음에도 불구하고 동물 전용 항암제가 없어 인체용 항암제를 사용하여 낮은 약효와 부작용으로 반려견 전용 면역항암제의 수요가 발생한 상황입니다.
이러한 수요에 대응 하여 당사는 반려견 전용 항암 면역치료제 플랫폼인 ‘Vaxleukin-15’의 개발에 박차를 가하고 있습니다.
라. 산업의 성장성
(1) 간암치료제 시장
[간세포암종의 비수술적 치료요법]
|
치료요법 구분 |
내용 |
권고 대상 |
||
|
1차 치료법 |
경동맥화학색전술 |
- 화학항암제인 독소루비신, 시스플라틴 또는 마이토마이신 C를 리피오돌에 혼합하여 에멀젼의 형태로 종양의 영양동맥에 선택적으로 주입하고색전물질(젤라틴스폰지, PVA, 미세구 등) 입자로동맥색전술을 시행하여 종양의 허혈을 유발하여 괴사시키는 치료법 |
- 간절제, 간이식, 국소치료를 적용하기 어려운 간세포암종 환자 - 간문맥 침범을 수반한 간세포암종에 대한 TACE 단독 및 체외방사선치료와 병행 치료 |
|
|
전신 |
소라페닙 (sorafenib) |
- VEGFR-2, PDGFR, Raf-1, c-kit 등을 표적하는 경구용 항암제 |
- 국소 림프절, 폐 등의 간외 전이 또는 간혈관 침범, 또는 다른 치료법들에 반응하지 않는 경우 |
|
|
렌바티닙 (lenvatinib) |
- VEGFR-1/2/3, FGFR-1/2/3/4, PDGFRα, RET, c-kit을 표적하는 경구용 항암제 |
- 종양면적이 전체 간의 50% 미만인 간세포암종 환자에서, 국소 림프절, 폐 등의 간외전이, 또는 Vp3 이하 간문맥침범이 있는 경우, 또는 다른 치료법들에 반응하지 않는 경우 |
||
|
아테졸리주맙(atezolizumab)& |
-아테졸리주맙:세포사멸 리간드-1에 결합하여 작용하는 정맥주사용 단클론항체 -베바시주맙:VEGF에 결합하여 작용하는 정맥주사용 단클론항체 |
-Child-Pugh 등급 A의 양호한 간기능과 ECOG 수행능력 1 이하의 양호한 전신상태이면서 이전에 전신치료를 받은 경험이 없는 진행성 간세포암종 환자 |
||
|
더발루맙(durvalumab)과 |
-더발루맙:PD-L1에 결합하는 정맥주사용 단클론항체 -트레멜리무맙:T세포 위에 발현하는(CTLA-4)에 결합하여 작용하는 정맥주사용 단클론항체 |
|||
|
-니볼루맙(nivolumab) -도나페닙(donafenib) |
-니볼루맙:PD-1 수용체에 결합하여 암세포 살상 기능을 회복시키는 정맥주사용 단클론항체 PD-1 억제제 -도나페닙:소라페닙의 분자적 구조를 개선한 multikinase inhibitor |
|||
|
보조요법 (adjuvant therapy) |
이뮨셀-LC |
-사이토카인유도살해세포(CIK) 면역세포치료제 |
- I, II 병기 간세포암종 환자에서 간절제, 고주파열치료술 또는 에탄올주입술로써 근치적 치료 재발을 막기 위해 추가적으로 시행 |
|
|
2차 치료법 |
전신 |
레고라페닙 (regorafenib) |
- 혈관신생, 종양발생, 전이, 종양면역 등에 관련된 신호를 차단하는 multikinase inhibitor인 경구용분자표적치료제 |
- 소라페닙 치료에도 간세포암종이 진행한 환자 |
|
니볼루맙(nivolumab) & |
- PD-1 타겟 면역관문억제제 - 정맥주사용 재조합 hIgG4 단클론항체 이필리무맙:T세포에서 발견되는 CTLA-4라는 물질에 결합하고 이를 차단하여 면역체계가 암세포를 죽일 수 있도록 도와주는 약제 |
-소라페닙에 실패한 Child-Pugh A 간기능, ECOG 0-1 수행능력을 지닌 환자 |
||
|
카보잔티닙 |
- MET, VEGFR2, RET 등을 동시에 차단하는 경구용 분자표적치료제 |
- 소라페닙 포함 2가지 이하의 전신치료에도 불구하고 간세포암종이 진행한 환자 |
||
|
라무시루맙 (ramucirumab) |
- VEGFR-2를 표적으로 하는 정맥주사용 단클론항체 |
소라페닙 치료 불응 및 부작용 있거나, 혈청 알파태아단백 400 ng/ml 이상인 환자 |
||
|
세포독성 화학요법 (cytotoxic chemotherapy) |
- oxaliplatin을 포함하는 FOLFOX(oxaliplatin/fluorouracil/leucovorin) 복합화학요법 - GEMOX(oxaliplatin/ gemcitabine) 복합화학요법 |
1차 및 2차 전신치료제에 실패하거나 사용할 수 없는 진행성 간세포암종 환자 |
||
|
펨브롤리주맙(pembrolizumab) |
-PD-1 수용체에 결합하여 PD-L1이나 PD-L2와 결합을 억제하는 사람 IgG4 단클론항체 |
-과거 소라페닙 치료를 받았던 환자 -소라페닙이나 옥살리플라틴 기반 세포독성항암치료를 받았으나 실패한 환자 |
||
|
아파티닙(apatinib)과 캄렐리주맙(camrelizumab) |
-아파티닙:VEGFR-2을 억제하는 tyrosine kinase inhibitor -캄렐리주맙:PD-1에 대한 사람 단클론항체 억제제 |
이전 전신치료에 실패한 환자 |
||
|
간동맥주입화학요법 |
- 세포독성화학요법의 다른 형태 - 5-fluorouracil 단독 혹은 시스플라틴 등과 병합한 세포독성 항암제를 간동맥에 직접 주입하여 간세포암종에 고농도의 항암제를 전달 |
1차 및 2차 전신치료제에 실패하거나 사용할 수 없는 진행성 간세포암종 환자가 간문맥침범을 동반한 경우 잔존 간기능이 좋고 종양이 간 내 국한된 경우 |
||
상기 간세포암종 치료 가이드라인에 적용되는 주요 치료제는 화학항암제, 표적항암제, 일부 면역관문억제제로당사의 간세포암종 치료제인 Vax-NK/HCC와 경쟁 관계라기 보다는 항암치료 효과를 상승시키는 협력 관계라 볼 수 있습니다. 당사의 치료제와 같은 면역세포치료제의 작용기전은 기존의 화학항암제나 표적항암제와 같이 일부의 부작용을 감수하더라도 암을 공격하고 위축시키는 전략이 아니며, 인체의 면역체계를 가급적 정상수준까지 회복시켜 인체 스스로 암을 제거하는 전략으로 기존 치료제들의 독성 문제와 내성 문제를 해결할 수 있는 치료제입니다.
특히 암 자체 혹은 항암 치료과정으로 인해 저하된 환자의 면역체계를 개선할 수 있기 때문에, 기존의 간세포암종치료를 받은 환자 중 면역력이 저하된 환자가 추가적으로 선택할 수 있는 치료 옵션이라 할 수 있습니다.
한편, 간세포암종을 대상으로 국내에서 승인된 면역세포치료제 제품으로는 GC녹십자셀의 이뮨셀-LC가 유일하며, 그 외 GC녹십자랩셀의MG4101, JW크레아젠의Creavax-HCC 등의 파이프라인이 임상단계에 있습니다.
2021년 국민건강보험공단이 공개한 진료데이터에 따르면, 간암 진료인원 80,853명 중 간세포암 진료 인원이 64,525명으로 79.8%를 차지하고 있으며, 5년전 59,040명보다 9.3% 증가한 수치를 보이고 있습니다
 |
|
6. 2021년 간암 유형별 진료인원 수 (국민건강보험공단 진료데이터(2021)) |
또한, 세계 185개국의 데이터가 포함된 IARC의 ‘GLOBOCAN 2020 데이터베이스’에서 원발성 간암 발병 및 사망에 대한 데이터에 따르면, 2020년 전 세계적으로 약 90만 5,700명이 간암을 진단받았으며, 83만 200명이 간암으로 사망했습니다. 연구진에 따르면 간암은 전 세계의 주요 사망원인 중 하나로 46개국에서 암 사망의 3대 원인, 그 외 90개국에서는 5대 원인인 것으로 나타났습니다. 현재 추세가 계속될 경우 2020~2040년 사이 간암 발병 및 사망자 수가 55.0% 이상 증가할 것으로 전망한 만큼 간암치료제에 대한 옵션이 시급한 실정입니다.
간암치료제는 바이엘의 ‘넥사바’는 2008년 국내에서 간세포암 치료제 적응증을 획득한 이후 10년간 간암시장을 독점했고, 2018년이 돼서야 두 번째 치료제인 에자이의 ‘렌비마’가 등장했을 정도로 그 동안의 간암치료제의 선택옵션이 제한되어 있었습니다. 하지만 2022년, 15년만에 ‘넥사바’를 뛰어넘는 효과를 보이는 로슈의 면역항암제 ‘티쎈트릭’이 1차 치료제로 보험 급여가 적용되면서 수술이 불가능했던 3기 이상 말기 간암 환자도 부담없이 사용할 수 있는 면역항암제가 등장하며 간암치료제 시장은 급변하고 있습니다.
그러나 늘어나는 환자의 수에 비해 현재까지 간암의 근치적 치료에 대한 해결책을 제시하지 못한 상황이라서, 간암치료제 시장은 앞으로도 꾸준히 성장할 것으로 보입니다.
(2) 췌장암치료제 시장
2021년 췌장암 진료 가이드라인에 따르면, 췌장암은 교모세포종과 함께 암 중에서도 최악의 암이라고 불리며 세계적으로 예후가 매우 나빠 유명한 암 중 하나입니다.
수술이 가능한 경우와 불가능한 경우로 나뉘는데 워낙 발견이 늦은 경우가 많기 때문에 수술 가능한 환자는 전체 환자의 12.5%에 불과합니다.
한국간담췌외과학회에서 발행한 2021 한국 췌장암 진료 가이드라인에 따르면 수술을 받더라도 일정 기간동안 항암제를 통해 보조치료를 받아야 하며, 항암제를 사용하는 요법은 다음과 같습니다.
|
수술 후 보조치료 |
보조 항암치료 |
환자의 임상적 상황에 따라서 mFOLFIRINOX치료나 gemcitabine기반 항암치료(gemcitabine 단독 또는 gemcitabine과 capecitabine 병합치료)또는5-FU기반 항암치료(5-FU와 leucovorin 또는 S-1 경구치료 등)이 권고될 수 있다. |
|
수행능력이 낮은 경우에는 gemcitabine 단독 또는 S-1 경구치료 등을 고려할 수 있다 |
||
|
고식적 항암치료 |
1차 항암치료 |
ECOG 수행능력 2 또는 기저질환으로 적극적인 항암치료가 어려울 것으로 여겨지는 환자 에 대해서는 gemcitabine 단독치료, gemcitabine과 erlotinib 병합치료가 가능하다. 또한 5-FU근간의 경구 항암치료로 S-1치료가 가능하다 |
|
ECOG 수행능력이 2 (Karnofsky 수행능력 70내외)로 평가되는 경우 극히 제한적으로 gemcitabine과 nab-paclitaxel의 병합치료를 시도할 수 있으나 근거는 부족하며 주의를 요한다. |
||
|
2차 항암치료 |
1차치료에서 FOLFIRINOX로 치료받은 후 진행이 된 환자에서 ECOG 수행능력 0 또는 1이면서 기저질환의 상태가 중증이 아니어서 전신상태가 좋은 경우라면, 또 다른 1차치료로 추천되고 있는 gemcitabine과 nab-paclitaxel 2제치료, gemcitabine 단독 또는 gemcitabine 과 erlotinib병합치료 또는 gemcitabine과 cisplatin 병합치료를 고려해볼 수 있다. |
|
|
1차치료에서 gemcitabine과 nab-paclitaxel 치료를 받은 환자이면서 역시 ECOG 수행능력이 0 또는 1이며 기저질환이 심하지 않고 전신상태가 좋은 경우라면, 5-FU기반의 병합치료(nanoliposomal irinotecan, 5-FU, leucovorin이나 FOLFIRINOX 또는 fluoropyrimidine, oxaliplatin 또는 irinotecan의 병합치료)를 고려할 수 있다. |
||
|
ECOG 수행능력 2인 경우 gemcitabine 단독 또는 S1, capecitabine치료, 5-FU의 지속치료를 고려해볼 수 있다. |
위 자료에서 알 수 있듯이 췌장암에 특이적으로 작용하여 허가받은 면역항암제는 없는 실정이며, 국내에서는 GC셀의 이뮨셀엘씨주, 젬백스, 삼성제약의 리아백스주, 크리스탈지노믹스의 아이발티노스타트가 임상을 진행하고 있습니다
근래에는 효과적인 항암제가 개발되면서 환자의 전신상태가 허락하는 경우라면 보다적극적인 보조 항암치료를 하는 것이 일반적으로 권고되고 있습니다.
췌장암 환자는 진행정도에 따라 절제가능, 경계성 절제가능, 국소진행성, 전이성으로 구분하는데 모두 항암치료를 요합니다. 하지만, 췌장암의 수술 후 보조적 치료에서 어떤 약제를 사용하여야 하는지에 대해서는 아직 정립되어 있지 않은 실정입니다.
이러한 의료수요를 충족시키기 위하여 유수의 제약바이오 기업들이 항암제 연구 및 개발에 몰두하고 있으며 The Business Research Company에서발간한‘Pancreatic Cancer Drugs Global Market Report 2023)에 따르면 세계췌장암치료제 시장은 2023년 39억달러(한화 약5조2천억원)에서 연평균 4.1%의 성장률로 꾸준하게 성장하여2027년에는49억달러(한화약6조1천억원)에 이를것으로 전망하고있습니다.
 |
|
그림7. 세계 췌장암 치료시장 규모 및 전망 (the business research company 2023) |
(3) 소세포성폐암치료제 시장
폐암은 진단 결과에 따라 크게 비소세포폐암과 소세포폐암으로 나눌 수 있는데 이중 환경적 요인 이외에도 유전자 변이와 같은 유전적 요인 등으로 인해 발생하는 비소세포폐암(Non-Small Cell Lung Cancer; NSCLC)이 전체 폐암의 80~85% 정도를 차지하며 나머지 15~20%는 소세포폐암(Small Cell Lung Cancer; SCLC)이 차지합니다.
소세포폐암은 비소세포성폐암에 비해 암세포의 크기가 작으며 신경내분비 암세포로 이루어져 있으며, 특히 암세포의 성장이 아주 빠르고 초기 단계에서도 전이가 쉽게 일어나는 암으로써 예후가 좋지 않은 암종으로 알려져 있습니다. 5년 생존율도 5%~10% 사이로 매우 낮기 때문에 소세포폐암 치료제에 대한 수요가 다급한 실정임에 따라 소세포폐암 치료제 시장 규모 역시 해년마다 꾸준히 성장하고 있습니다.
KISIT(한국과학기술정보연구원)이 발간한 AIST MARKET INSIGHT 2022-083 ‘폐암치료제 편’에 따르면 소세포 폐암(SCLC) 치료제 세계 시장은 2020년 기준 1,106백만 달러(약 1조 3천억 원) 규모에서 연평균성 장률 19.3%로 성장하여 2026년 3,188백만 달러(약 3조 6천억 원) 규모로 증가할 것으로 전망하고 있습니다.
[소세포폐암(SCLC) 세계 시장 규모 및 전망] (단위 : 백만달러)
|
구분 |
2020 |
2021 |
2022 |
2023 |
2024 |
2025 |
2026 |
CAGR(%) |
|
세계시장 |
1,106 |
1,361 |
1,595 |
1,760 |
1,903 |
2,414 |
3,188 |
19.3 |
출처 : ASTI MARKET INSIGHT 083(0712).pdf (kisti.re.kr)
(4) 다발골수종치료제 시장
미국종합암네트워크(NCCN)의 다발골수종 치료 가이드라인(2022)에 따르면, 다발골수종 치료는 2제 및 3제 병용요법이 권장되고 있습니다. 프로테아좀 억제제(골수종 세포가 생존할 수 있도록 하는 특정 단백질(프로테아즘)의 활동을 차단), 면역요법 약물(암에 대항하는 특정 면역계를 강화), 코르티코스테로이드(뇌의 흥분능력과 신경전달의물질의 대사에 영향)가 표준치료에 주로 이용되고 있으며 다발골수종에 대한 치료 약물 및 가이드는 다음과 같습니다.
[다발골수종 치료 유형에 따른 약물]
|
치료 유형 |
약물명 |
|
|
프로테아좀 억제제 |
골수종이 생존할 수 있도록 하는 특정 단백질(프로테아좀)을 차단 |
보르테조밉 (Velcade) |
|
카르필조밉 (Kyprolis) |
||
|
익사조밉 (Ninlaro) |
||
|
면역조절제 |
신체가 암세포를 찾아 공격하는 능력을 향상 |
레날리도마이드 (Revlimid) |
|
포말리도마이드 (Pomalyst) |
||
|
탈리도마이드 (Thalomid) |
||
|
단클론항체 |
암 세포에 있는 단백질에 부착되는 인공 항체 |
다라투무맙 (Darzalex) |
|
엘로투주맙 (Empliciti) |
||
|
이사툭시맙 (Sarclisa) |
||
|
CAR-T 세포 요법 |
암 항원을 표적하는 CAR를 T세포에 형질이입한 강력한 세포치료제 |
이데캅타겐 비클레우셀(Avecma) |
|
소분자 억제제 |
암세포 성장 및 분열 방해 |
셀리넥소르 (Xpovio) |
|
스테로이드 |
골수종치료에 단독으로 사용하거나 화학요법, 표적요법, 또는 둘 다와 병용하여 사용 |
덱사메타손 |
|
프레드니손 |
||
|
화학요법 |
암 세포를 사멸시키기 위한 약물 사용. (보통 14일, 21일 또는 28일 기간 주기로 사용) |
벤다무스틴 (Bendeka, Treanda) |
|
시스플라틴 |
||
|
시클로포스파미드 |
||
|
독소루비신 염산염 |
||
|
독소루비신 염산염 리포솜(Doxil) |
||
|
에포토시드 (Etopophos) |
||
|
멜팔란 (Alkeran) |
||
[다발골수종 치료 가이드]
|
다발골수종 치료 가이드 |
|||
|
무증상 |
-혈액 내 M단백질 존재 또는 소변 내 경쇄 (Bence Jones 단백질) 수치 상승 또는 골수 내 10%~59%의 이상 형질세포 또는/및 신장 손상, 골 손상, 빈형, 또는 혈중 칼슘 수치 상승 등 |
1)관찰:일부 환자를 위한 옵션. 정기적 추적관찰검사 2)임상시험:선호되는 무증상 골수종 환자의 일차치료옵션 3)추적관찰검사:3~6개월마다 추적관찰을 받아 치료의 필요성 확인 4)진행:증상 유발이 시작되면 활성 다발성 골수종으로 치료 |
|
|
활성 다발성 |
-골수 내 최소 10%의 이상 형질세포 또는 생검으로 확인된 형질세포종 및 -다음 중 하나 이상에 해당 1.골수 내 최소 60% 이상의 형질세포 2.혈중 칼슘 수치 상승 3.신장 손상 4.낮은 적혈구 수 5.골수의 용해성 병변 또는 병변 6.100이상의 혈정 유리경쇄 비율 |
고립성 형질 세포종 |
1)일차치료:국소요법 (방사선 및 수술) 2)임상시험 3)추적관찰검사:3~6개월마다 추적관찰 검사, 연 1회 영상검사 4)질병 진행:다발 골수종 진단에 요구되는 모든 검사 추가 실시 |
|
활성 다발성 골수종 |
1)일차치료 *3제요법 : -보르테조밉,레날리도마이드,덱사메타손 -보르테조밉,레날리도마이드,덱사메타손 -다라투무맙,레날리도마이드,덱사메타손 -보르테조밉,탈리도마이드,덱사메타손 -보르테조밉,시클로포스파미드,덱사메타손 -익사조밉,레날리도마이드,덱사메타손 *골 형성 요법: -비스포스포네이드 or 데노수맙 *보조 치료 및 지지치료 -부작용에 대한 치료 2)줄기세포이식 (이식 가능한 경우) 3)유지요법 -레날리도마이드 -익사조밉 -보르테조밉 |
||
Global Data(2019)에 따르면, 선진 8개국(미국, 프랑스, 독일, 이탈리아, 스페인, 영국,일본, 중국)의 다발골수종 치료제의 시장규모는 2017년 145억달러에서 2027년 278억달러로 연평균 6.7%로 성장할 것으로 전망하고 있습니다.
현재, 다발골수종의 대표적인 치료제는 매출액 기준 BMS의 Revlimid, Takeda / J&J의 Velcade, BMS의 Pomalyst 가 주력 3개 제품이나, 이들 제품의 특허 만료에 따라 제네릭/바이오시밀러의 등장으로 시장 판도에 변화가 올 것으로 예상됩니다.
단일 신규 제품으로 J&J(Janssen Biotech)의 Darzalex, Takeda의 Ninlaro, Amgen /Ono(Japan)의 Kyprolis가 새로운 주력 제품으로 교체될 것으로 전망됩니다.
특히 최근에 승인완료, 후기 임상을 진행 중인 제품들도 시장에 출시되어 다양한 치료 옵션이 제안될 것으로 전망되는 바, 미충족 수요와 함께 지속적인 시장 성장이 예상되고 있습니다.
(5) 동물용의약품 시장
한국제약바이오협회에 따르면 세계 동물의약품 시장 규모는 지난 2020년 기준 367억 달러 (한화 약 46조)로 2010년 약 200억 달러에 비해 10년만에150%이상이 올랐고, 오는 2025년에는 400억 달러를 넘길 것으로 전망되고 있습니다
국내시장 역시 국내 동물의약품 시장 규모는 2015년 한화 약 8,903억원에서 2021년에는 1조 3,481억원까지 증가했습니다. 2015년부터 2021년까지 연평균 성장률을 7%로 계산했을 때 오는 2025년에는 약 1조 7668억원까지 성장할 것으로 보입니다
 |
|
8. 동물용의약품 시장규모 (한국제약바이오협회(2021)) |
또한, 한국언론재단 빅데이터 분석시스템인 ‘빅카인즈’를 활용한 2023년 2월 기준 지난 3개월 간 보도된 전국 일간지 및 방송 기사 키워드 중 ‘신약 개발’과 ‘연구 개발’이 많이 언급되었습니다.
그 동안 이를 통해 복제약에 치중했던 동물용의약품 산업이 점차 신약개발로 가는 긍정적인 현상으로 해석할 수 있으며, 동물의약품의 R&D 시장은 더욱 확대될 것으로 기대하고 있습니다.
마. 경쟁형태 및 비교우위 사항
세포치료제는 세포를 체외에서 증식하거나 특성을 변화시키는 방법을 통해 제조하는 의약품이고, 유전자치료제는 유전자 조작을 이용, 치료 유전자를 환자의 세포 안으로 주입하여 유전자 결함을 치료하는 의약품을 말합니다.
특히 CAR-T 치료제는 단회 투약만으로도 효과를 나타내어 높은 가격대가 형성되어 있어 ‘블록버스터급’ 항암제로 불립니다.
이를 필두로 세계 제약/바이오 기업들이 세포 유전자 치료제 연구개발에 뛰어들어 관련 시장의 성장률은 타 유형의 치료제 시장의 약 10배 이상의 수치를 보이고 있습니다.
2022년 Evaluate Pharma의 자료에 따르면, 2021년 세포 유전자 치료제 시장은 타 유형의 치료제 시장보다 절대적인 규모는 매우 낮지만, 연평균 성장률은 합성의약품(5.7%), 항체의약품(5.2%), 백신(-4.1%)보다 월등히 높은 49.4%를 전망하며 2026년에는 약 550억달러 규모의 시장을 형성할 것으로 기대하고 있습니다.
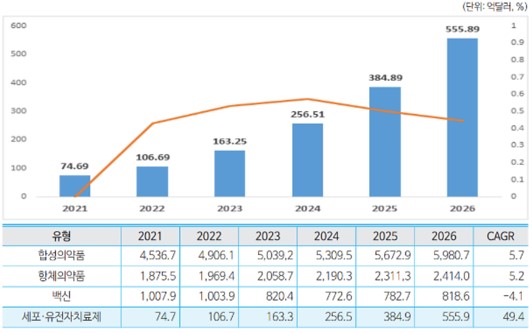 |
|
9. 세포-유전자치료제 시장 규모 (evaluate pharma(2022)) |
또한, 한국바이오협회에서 발표한 ‘세포·유전자치료제투자 및 임상 동향(2022)’ 에서도 22년 4월 기준 1,200개 이상의 세포 기반 면역항암제 임상이 진행되고 있으며 세포 기반 면역항암제가 항암제 임상시험 전체의 60%를 차지하고 있는 것을 알 수 있습니다.
따라서 혁신적인 치료제를 출시하기 위한 글로벌 바이오 기업들의 경쟁은 더욱 심화될 것이며, 당사 역시 세계 시장에 도전하는 것이 쉽지 만은 않을 것으로 예상하고 있습니다.
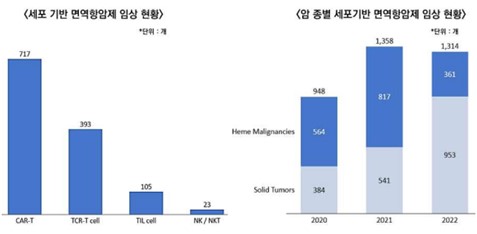 |
|
10. 세포-유전자치료제 투자 및 임상 동향 (한국바이오협회(2022)) |
하지만, 자가면역세포치료는 고도의 'personalized medicine'이고 상당한 노하우를 축적해야만 치료용 GMP 수준 치료제를 생산하고 실제 치료에 적용할 수 있게 되는 특성을 가지고 있습니다.
당사는 자가면역세포치료 노하우와 경험을 축적하고 있는 상황으로, 아래와 같이 선천면역과 관련된 자연살해세포를 기반으로 하는 치료제(Vax-NK와 Vax-CAR-NK), 다발골수종의 수많은 종양항원을 인식할 수 있는MIL(골수침윤림프구)에CAR을 접합한 치료제(Vax-CAR-MILs), 적응면역과 관련된T세포의 효능을 강화시킨CAR-T세포를 기반으로 하는 치료제(Vax-CAR-T) 및 면역세포 간 신호전달 역할을 수행하는 사이토카인을 기반으로 하는 동물용의약품(박스루킨-15)에 이르기까지 항암면역반응에 있어 가장 중요한 세포들과 항암효과 작동기전의 여러 단계를 포괄하고 상호 보완할 수 있는 접근전략을 추구하고 있습니다.
 |
|
파이프라인_박셀바이오 |
당사의 파이프라인 역시 단독 요법 보다는 기존 화학항암제, 표적항암제와의 병용요법, 다른 타겟의 면역항암제와의 상호 보완적인 병용요법을 통해 독성 문제 해결, 재발률 감소, 전체 생존률의 증대 등의 효과를 거둘 것으로 기대됩니다.
따라서 기존의 시장 내 주력제품들은 당사의 제품과 경쟁관계가 아닌 협력관계에 있으며, 병용 처방을 통해 상호 보완적인 시너지 효과를 발휘할 것으로 기대하고 있습니다.
특히 자연살해세포 기반 치료제는 일부 국가에서 조건부 허가를 받은 제품은 있지만, 글로벌 수준에서 아직 본격적으로 처방되고 있는 제품이 없는 상황으로, 현재 임상 단계에 있는 몇몇 파이프라인들 만이 잠재적인 경쟁 관계에 있습니다.
여기에 당사의 자연살해세포 파이프라인은 간암 대상 HAIC라는 약물투여방식을 활용하는 차별성을 가지고 있으며, 제조방법 변경 승인을 통해 기존 치료제의 단점을 극복하고 생산의 효율을 높이는 등의 경쟁력을 확보하였습니다. 한편, CAR-T 세포 기반 치료제는 2022년 기준 여섯 개(킴리아, 예스카타. 테카투스, 브레얀지, 아베크마, 카빅티)의 혈액암 치료 경쟁제품이 글로벌 시장에 출시되어 있습니다. 얀센, 화이자, 애브비, BMS, 아스트라제네카 등 유수의 글로벌 빅마파들은 후속 CAR-T 세포치료제 개발에 몰두하고 있으며, 국내 역시 SCM생명과학, 큐로셀, 앱클론 등 많은 바이오회사들의 CAR-T세포치료제 개발에 도전하고 있습니다. 이를 통해, CAR-T 세포치료제 시장은 여전히 성장성과 미충족 욕구 (Umnet Needs)가 높은 발전 단계의 시장임을 알 수 있습니다.
당사는 기존 CAR-T 치료제가 갖고 있는 높은 부작용 발생률과 낮은 면역기억 유도의 문제점을 극복하여 CAR-T 세포치료제 시장의 게임 체인저가 되기 위하여 차세대 모노바디 기반 CAR를 개발하고 있으며, 당사의 NK세포에 대한 노하우를 바탕으로 CAR-NK 세포치료제 또한 개발하고 있습니다.
특히 scFv CAR 세포치료제 뿐만 아니라모노바디를 수용체로 사용하는 새로운 기술플랫폼을 통해 2개 이상의 수용체를 동시에 발현시켜 고형암과 혈액암을 모두 타깃할 수 있다는 점에서 경쟁사에 비해 큰 기술우위를 갖고 있습니다 최근에는 골수침윤림프구(MILs)에서 유래한 세포와 CAR 기술을 접합한 CAR-MILs 파이프라인을 개발하여 다발골수종을 목표질환으로 하여 임상연구를 수행하기 위한 연구개발에 박차를 가하고 있습니다.
마지막으로 당사는 중·단기적인 수익사업으로 반려견용 면역항암제를 개발하고 있습니다. 이는 면역체계를 활성화하는 물질인 인터루킨-15를 이용한 치료제로, 이미 임상학적으로 유효한 것으로 알려진 사이토카인 면역항암 후보물질로서 박스루킨-15는 생체 내 주사 후 항암 면역세포인 NK세포와 CD8 세포독성 T세포의 증식과 활성을 유발하는 등 강력한 항암 면역기능을 자극하고 부작용이 거의 없어 암 치료제로서 우수한 효능을 가지고 있음을 증명하였습니다.
특히 임상시험 연구에서 악성 암환견에 박스루킨-15를 정맥주사한 후 치료반응을 확인한 결과 66.6%의 높은 질환 조절률을 관찰함으로써 우수한 항암면역치료제로서의 실제 가치를 확인하였습니다.
아직까지 동물용 면역항암제로 출시된 제품이 없으며, 당사는 이를 최초의 동물용 면역항암제로 출시하여 반려동물 시장을 선도하고자 하며, 최근 국내 메이저 동물용 의약품 생산 및 유통업체들과 협업을 추진하여 세 건의 MOU를 체결하였습니다 (고려비앤피, 케어사이드, 씨티씨바이오).
그리고 임상시험 실시기관 확대를 통해 임상시험의 빠른 진행과 함께 박스루킨-15의 우수성을 알리고자 하며, 품목 허가 진행과 함께 박스루킨-15 용법 확대 추진을 계획하고 있습니다.
특히 당사가 추구하는 자연살해세포, CAR 기반 세포치료제 연구개발사업은 기존의 의약품과는 차별화된 새로운 방식의 치료제인 신개념 치료제에 해당합니다.
세포치료제 연구개발을 위해서는 장시간이 소요된 세포분리 및 배양 기술, 유전자 편집 및 발현기술, 프로테오믹스 등 다양한 생명공학 기술과 노하우의 축적을 필요로 하므로, 타 제약 및 바이오 업체의 진입장벽이 높은 편이며, 비교적 성장 초기 단계이므로 독자 기술 확보를 통해 고부가가치 창출이 가능할 것으로 기대하고 있습니다
III. 재무에 관한 사항
1. 요약재무정보
(단위 : 원)
| 계 정 과 목 | 제 14 기 반기말 (2023.06.30.) |
제 13 기말 (2022.12.31.) |
제12기 (2021.12.31.) |
| 자산 | |||
| Ⅰ.유동자산 | 16,747,153,012 | 20,898,449,206 | 28,197,462,800 |
| 현금및현금성자산 | 793,250,717 | 389,660,587 | 2,308,792,152 |
| 기타 유형자산 | 15,953,902,295 | 20,508,788,619 | 25,888,670,648 |
| Ⅱ.비유동자산 | 3,327,701,363 | 3,264,596,080 | 3,078,895,758 |
| 유형자산 | 2,620,887,796 | 2,541,112,104 | 2,804,402,798 |
| 무형자산 | 205,454,315 | 229,458,479 | 147,623,970 |
| 기타비유동자산 | 501,359,252 | 494,025,497 | 126,868,990 |
| 자 산 총 계 | 20,074,854,375 | 24,163,045,286 | 31,276,358,558 |
| 부채 | |||
| Ⅰ.유동부채 | 488,358,495 | 307,041,990 | 392,301,472 |
| Ⅱ.비유동부채 | 890,023,264 | 528,735,850 | 803,673,869 |
| 부 채 총 계 | 1,378,381,759 | 835,777,840 | 1,195,975,341 |
| 자본 | |||
| I.자본금 | 7,611,500,000 | 7,611,500,000 | 7,611,500,000 |
| II.자본잉여금 | 48,888,442,989 | 48,888,442,989 | 48,888,442,989 |
| III.기타자본항목 | 344,453,006 | 210,354,661 | 85,394,010 |
| IV.결손금 | -38,147,923,379 | -33,383,030,204 | -26,504,953,782 |
| 자 본 총 계 | 18,696,472,616 | 23,327,267,446 | 30,080,383,217 |
| 부채 및 자본총계 | 20,074,854,375 | 24,163,045,286 | 31,276,358,558 |
| 계 정 과 목 | 제 14 기 반기말 (2023.06.30) |
제 13 기말 (2022.12.31.) |
제12기 (2021.12.31.) |
| I. 매출액 | 0 | 0 | 0 |
| II. 영업손실 | -5,269,091,874 | -8,212,602,189 | -5,904,060,364 |
| III. 법인세비용차감전순손실 | -4,737,147,819 | -6,825,051,481 | -4,762,778,542 |
| IV. 총포괄손익 | -4,764,893,175 | -6,878,076,422 | -5,217,377,980 |
| 기본및희석주당손실 | -311 | -448 | -315 |
2. 연결재무제표
- 해당사항 없습니다.
3. 연결재무제표 주석
- 해당사항 없습니다.
4. 재무제표
|
재무상태표 |
|
제 14 기 반기말 2023.06.30 현재 |
|
제 13 기말 2022.12.31 현재 |
|
(단위 : 원) |
|
제 14 기 반기말 |
제 13 기말 |
|
|---|---|---|
|
자산 |
||
|
Ⅰ.유동자산 |
16,747,153,012 |
20,898,449,206 |
|
현금및현금성자산 |
793,250,717 |
389,660,587 |
|
단기금융상품 |
15,000,000,000 |
20,002,461,519 |
|
기타금융자산 |
493,883,728 |
210,311,372 |
|
기타유동자산 |
435,288,007 |
215,780,908 |
|
당기법인세자산 |
24,730,560 |
80,234,820 |
|
Ⅱ.비유동자산 |
3,327,701,363 |
3,264,596,080 |
|
유형자산 |
2,259,507,634 |
2,391,724,532 |
|
사용권자산 |
361,380,162 |
149,387,572 |
|
무형자산 |
205,454,315 |
229,458,479 |
|
기타금융자산 |
448,168,543 |
431,153,904 |
|
기타비유동자산 |
53,190,709 |
62,871,593 |
|
자산총계 |
20,074,854,375 |
24,163,045,286 |
|
부채 |
||
|
Ⅰ.유동부채 |
488,358,495 |
307,041,990 |
|
기타금융부채 |
282,786,842 |
176,832,481 |
|
리스부채 |
135,789,973 |
46,514,819 |
|
기타유동부채 |
69,781,680 |
83,694,690 |
|
Ⅱ.비유동부채 |
890,023,264 |
528,735,850 |
|
기타금융부채 |
231,022,940 |
219,108,526 |
|
리스부채 |
200,271,137 |
58,723,176 |
|
순확정급여부채 |
458,729,187 |
250,904,148 |
|
부채총계 |
1,378,381,759 |
835,777,840 |
|
자본 |
||
|
Ⅰ.자본금 |
7,611,500,000 |
7,611,500,000 |
|
Ⅱ.자본잉여금 |
48,888,442,989 |
48,888,442,989 |
|
Ⅲ.기타자본항목 |
344,453,006 |
210,354,661 |
|
Ⅳ.이익잉여금(결손금) |
(38,147,923,379) |
(33,383,030,204) |
|
자본총계 |
18,696,472,616 |
23,327,267,446 |
|
부채및자본총계 |
20,074,854,375 |
24,163,045,286 |
|
포괄손익계산서 |
|
제 14 기 반기 2023.01.01 부터 2023.06.30 까지 |
|
제 13 기 반기 2022.01.01 부터 2022.06.30 까지 |
|
(단위 : 원) |
|
제 14 기 반기 |
제 13 기 반기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
Ⅰ.매출액 |
||||
|
Ⅱ.매출원가 |
||||
|
Ⅲ.매출총이익 |
||||
|
Ⅳ.판매관리비 |
2,773,916,497 |
5,269,091,874 |
1,549,707,121 |
3,316,551,536 |
|
Ⅴ.영업이익(손실) |
(2,773,916,497) |
(5,269,091,874) |
(1,549,707,121) |
(3,316,551,536) |
|
Ⅵ.금융수익 |
211,553,435 |
456,589,622 |
74,396,437 |
164,650,916 |
|
Ⅶ.금융원가 |
19,980,896 |
30,210,826 |
4,862,456 |
9,046,680 |
|
Ⅷ.기타수익 |
87,890,746 |
125,571,281 |
157,513,415 |
180,280,996 |
|
Ⅸ.기타비용 |
2 |
20,006,022 |
4 |
27,210,251 |
|
Ⅹ.법인세비용차감전순이익(손실) |
(2,494,453,214) |
(4,737,147,819) |
(1,322,659,729) |
(3,007,876,555) |
|
XI.법인세비용 |
||||
|
XⅡ.당기순이익(손실) |
(2,494,453,214) |
(4,737,147,819) |
(1,322,659,729) |
(3,007,876,555) |
|
XⅢ.기타포괄손익 |
(14,489,120) |
(27,745,356) |
(189,371,637) |
(189,371,637) |
|
당기손익으로 재분류되지 않는항목(세후기타포괄손익) |
||||
|
확정급여제도의 재측정요소 |
(14,489,120) |
(27,745,356) |
(189,371,637) |
(189,371,637) |
|
XIV.총포괄손익 |
(2,508,942,334) |
(4,764,893,175) |
(1,512,031,366) |
(3,197,248,192) |
|
XV.주당이익(손실) |
||||
|
기본및희석주당손익(손실) (단위 : 원) |
(164) |
(311) |
(87) |
(198) |
|
자본변동표 |
|
제 14 기 반기 2023.01.01 부터 2023.06.30 까지 |
|
제 13 기 반기 2022.01.01 부터 2022.06.30 까지 |
|
(단위 : 원) |
|
자본 |
||||||
|---|---|---|---|---|---|---|
|
자본금 |
자본잉여금 |
기타자본구성요소 |
이익잉여금 |
자본 합계 |
||
|
2022.01.01 (기초자본) |
7,611,500,000 |
48,888,442,989 |
85,394,010 |
(26,504,953,782) |
30,080,383,217 |
|
|
총포괄손익 |
당기순이익(손실) |
(3,007,876,555) |
(3,007,876,555) |
|||
|
확정급여제도의 재측정요소 |
(189,371,637) |
(189,371,637) |
||||
|
자본에 직접 인식된 소유주와의 거래 |
주식매수선택권의 인식 |
59,437,332 |
59,437,332 |
|||
|
주식매수선택권의 상실 |
(18,376,903) |
(18,376,903) |
||||
|
2022.06.30 (기말자본) |
7,611,500,000 |
48,888,442,989 |
126,454,439 |
(29,702,201,974) |
26,924,195,454 |
|
|
2023.01.01 (기초자본) |
7,611,500,000 |
48,888,442,989 |
210,354,661 |
(33,383,030,204) |
23,327,267,446 |
|
|
총포괄손익 |
당기순이익(손실) |
(4,737,147,819) |
(4,737,147,819) |
|||
|
확정급여제도의 재측정요소 |
(27,745,356) |
(27,745,356) |
||||
|
자본에 직접 인식된 소유주와의 거래 |
주식매수선택권의 인식 |
134,098,345 |
134,098,345 |
|||
|
주식매수선택권의 상실 |
||||||
|
2023.06.30 (기말자본) |
7,611,500,000 |
48,888,442,989 |
344,453,006 |
(38,147,923,379) |
18,696,472,616 |
|
|
현금흐름표 |
|
제 14 기 반기 2023.01.01 부터 2023.06.30 까지 |
|
제 13 기 반기 2022.01.01 부터 2022.06.30 까지 |
|
(단위 : 원) |
|
제 14 기 반기 |
제 13 기 반기 |
|
|---|---|---|
|
영업활동현금흐름 |
(4,455,033,546) |
(3,466,670,693) |
|
영업활동에서 창출된 현금 |
(4,671,132,166) |
(3,520,224,053) |
|
이자수취(영업) |
160,594,360 |
39,216,670 |
|
법인세납부(환급) |
55,504,260 |
14,336,690 |
|
투자활동현금흐름 |
4,930,549,156 |
4,877,630,739 |
|
단기금융상품의 감소 |
15,002,461,519 |
7,000,000,000 |
|
임차보증금의 감소 |
5,000,000 |
18,245,000 |
|
기타보증금의 감소 |
2,766,267 |
|
|
단기금융상품의 취득 |
(10,000,000,000) |
(2,000,000,000) |
|
유형자산의 취득 |
(63,412,363) |
(112,704,528) |
|
무형자산의 취득 |
(3,500,000) |
(20,676,000) |
|
임차보증금의 증가 |
(10,000,000) |
(10,000,000) |
|
재무활동현금흐름 |
(71,925,480) |
(103,629,070) |
|
리스부채의 상환 |
(71,925,480) |
(103,629,070) |
|
현금및현금성자산의순증가(감소) |
403,590,130 |
1,307,330,976 |
|
기초현금및현금성자산 |
389,660,587 |
2,308,792,152 |
|
기말현금및현금성자산 |
793,250,717 |
3,616,123,128 |
| "별첨 주석은 본 요약반기재무제표의 일부입니다." |
5. 재무제표 주석
| 제14(당)반기말 2023년 06월 30일 현재 |
| 제13(전)기말 2022년 12월 31일 현재 |
| 주식회사 박셀바이오 |
1. 회사의 개요
주식회사 박셀바이오(이하 "회사"라 함)는 2010년 2월에 설립되어 암 면역세포치료제 등의 개발 및 판매를 주요 사업으로 영위하고 있으며, 전라남도 화순군 화순읍 산단길 12-55에 본사를 두고 있습니다. 회사는 2020년 9월 22일 코스닥 시장에 상장하였습니다.
회사는 설립이후 수차례의 유ㆍ무상증자를 거쳐 당반기말 현재 납입자본금은 7,611,500천원이며, 주요 주주 내역은 다음과 같습니다.
| 주주명 | 주식수(주) | 지분율(%) |
|---|---|---|
| 이제중 외 28인 | 4,519,307 | 29.7 |
| 기타 주주 | 10,703,693 | 70.3 |
| 합 계 | 15,223,000 | 100.0 |
2. 중요한 회계정책
반기재무제표는 기업회계기준서 제1034호 '중간재무보고'에 따라 작성되었으며 연차재무제표에서 요구되는 정보에 비하여 적은 정보를 포함하고 있습니다. 반기재무제표는 보고기간말 현재 유효한 한국채택국제회계기준에 따라 작성되었으며, 반기재무제표를 작성하기 위하여 채택한 중요한 회계정책은 별도의 언급이 없는 한 전기 연차재무제표 작성시 채택한 회계정책과 동일하게 적용되었습니다.
반기재무제표 작성을 위하여 채택한 중요한 회계정책은 다음과 같습니다.
2.1 회계정책의 변경과 공시
2.1.1 회사가 채택한 제ㆍ개정 기준서
회사가 2023년 1월 1일 이후 개시하는 회계기간부터 적용한 제ㆍ개정 기준서 및 해석서는 다음과 같습니다.
1) 기업회계기준서 제 1001호 '재무제표 표시' (개정)
개정 기준서는 공시 대상 회계정책 정보를 '유의적인' 회계정책에서 '중요한' 회계정책으로 바꾸고 중요한 회계정책 정보의 의미를 설명하였습니다. 회사는 상기 개정 기준서의 적용이 재무제표에 미치는 영향이 유의적이지 아니할 것으로 예상하고 있습니다.
2) 기업회계기준서 제1008호 '회계정책, 회계추정의 변경 및 오류' (개정)
개정 기준서는 '회계추정치'를 측정불확실성의 영향을 받는 재무제표상 화폐금액으로 정의하고, 회계추정치의 예를 보다 명확히 하였습니다. 또한 새로운 정보의 획득, 새로운 상황의 전개나 추가 경험의 축적으로 투입변수나 측정기법을 변경한 경우 이러한 변경이 전기오류수정이 아니라면 회계추정치의 변경임을 명확히 하였습니다. 회사는 상기 개정 기준서의 적용이 재무제표에 미치는 영향이 유의적이지 아니할 것으로 예상하고 있습니다.
3) 기업회계기준서 제 1012호 '법인세' (개정)
개정 기준서는 이연법인세 최초 인식 예외규정을 추가하여 단일 거래에서 자산과 부채를 최초 인식할 때 동일한 금액으로 가산할 일시적차이와 차감할 일시적차이가 생기는 경우 각각 이연법인세 부채와 자산을 인식하도록 하였습니다.
단일 거래에서 생기는 자산과 부채에 관련되는 이연법인세는 비교 표시되는 가장 이른 기간의 시작일 이후에 이루어진 거래에 적용하며, 비교 표시되는 가장 이른 기간의 시작일에 이미 존재하는 (1) 사용권자산과 리스부채, (2) 사후처리 및 복구 관련 부채 및 이에 상응하여 자산 원가의 일부로 인식한 금액에 관련되는 모든 차감할 일시적 차이와 가산할 일시적 차이에 대해 이연법인세 자산과 부채를 인식하며, 최초 적용 누적 효과를 이익잉여금(또는 자본의 다른 구성요소) 기초 잔액을 조정하여 인식합니다. 회사는 상기 개정 기준서의 적용이 재무제표에 미치는 영향이 유의적이지 아니할 것으로 예상하고 있습니다.
4) 기업회계기준서 제1001호 ' 재무제표 표시 ' - 행사가격 조정 조건이 있는 금융부채 평가손익 공시
발행자의 주가 변동에 따라 행사가격이 조정되는 조건이 있는 금융상품의 전부나 일부가 금융부채로 분류되는 경우 그 금융부채의 장부금액과 관련 손익을 공시하도록 하였습니다. 회사는 상기 개정 기준서의 적용이 재무제표에 미치는 영향이 유의적이지 아니할 것으로 예상하고 있습니다.
2.1.2 공표되었으나 아직 시행되지 않은 제ㆍ개정 기준서 및 해석서
당반기말 현재 제정ㆍ공표되었으나 시행일이 도래하지 않아 회사가 채택하지 않은 한국채택국제회계기준의 기준서 및 해석서는 다음과 같습니다.
1) 기업회계기준서 제1001호 '재무제표 표시' (개정) - 부채의 유동·비유동 분류
보고기간말 현재 존재하는 실질적인 권리에 따라 유동 또는 비유동으로 분류되며, 부채의 결제를 연기할 수 있는 권리의 행사가능성이나 경영진의 기대는 고려하지 않습니다. 또한, 부채의 결제에 자기지분상품의 이전도 포함되나, 복합금융상품에서 자기지분상품으로 결제하는 옵션이 지분상품의 정의를 충족하여 부채와 분리하여 인식된경우는 제외됩니다. 동 개정사항은 2024년 1월 1일 이후 시작하는 회계연도부터 적용하며, 조기적용이 허용됩니다. 회사는 동 개정으로 인해 재무제표에 중요한 영향은없을 것으로 예상하고 있습니다.
2.2 중요한 회계정책
2.2.1 재무제표 작성기준
회사의 재무제표는 금융상품 등 아래 회계정책에서 별도로 언급하고 있는 사항을 제외하고는 역사적 원가를 기준으로 작성되었습니다.
2.2.2 기능통화와 표시통화
회사의 재무제표는 회사의 영업활동이 이루어지는 주된 경제환경의 통화(이하 "기능통화")로 표시하고 있습니다. 재무제표 작성을 위해 회사의 경영성과와 재무상태는 회사의 기능통화이면서 재무제표 작성을 위한 표시통화인 '원(KRW)'으로 표시하고 있습니다.
2.2.3 추정과 판단
한국채택국제회계기준에서는 재무제표를 작성함에 있어서는 경영진으로 하여금 회계정책의 적용이나, 보고기간말 현재 자산, 부채 및 수익, 비용의 보고금액에 영향을 미치는 판단, 추정치, 가정의 사용을 요구하고 있습니다. 보고기간말 현재 경영진의 최선의 판단을 기준으로 한 추정치와 가정이 실제 환경과 다를 경우 실제 결과는 이러한 추정치와 다를 수 있습니다.
2.2.4 법인세비용
회사의 영업활동으로 창출된 과세소득에 대한 최종 세효과를 산정하는 데에는 불확실성이 존재합니다. 회사는 보고기간말 현재까지의 영업활동의 결과로 미래에 부담할 것으로 예상되는 법인세효과를 최선의 추정과정을 거쳐 당기법인세 및 이연법인세로 인식하였습니다. 하지만 실제 미래 최종 법인세부담은 인식한 관련 자산ㆍ부채와 일치하지 않을 수 있으며, 이러한 차이는 최종 세효과가 확정된 시점의 당기법인세 및 이연법인세 자산ㆍ부채에 영향을 줄 수 있습니다.
2.2.5 금융자산의 손상
금융자산의 손실충당금은 부도위험 및 기대손실률 등에 대한 가정에 기초하여 측정됩니다. 회사는 이러한 가정의 설정 및 손상모델에 사용되는 투입변수의 선정에 있어서 회사의 과거 경험, 현재 시장 상황, 재무보고일 기준의 미래전망정보 등을 고려하여 판단합니다(주석 2.3.2 참조).
2.2.6 비금융자산의 손상
회사는 매 보고기간 종료일에 모든 비금융자산에 대하여 손상징후의 존재여부를 평가합니다. 비한정내용연수의 무형자산에 대해서는 매년 또는 손상징후가 있는 경우에 손상검사를 수행합니다. 기타 비금융자산에 대해서는 장부금액이 회수가능하지 않을 것이라는 징후가 있을 때 손상검사를 수행합니다. 사용가치를 계산하기 위하여 경영자는 해당 자산이나 현금창출단위로부터 발생하는 미래기대현금흐름을 추정하고 동 미래기대현금흐름의 현재가치를 계산하기 위한 적절한 할인율을 선택하여야 합니다.
2.3 유의적인 회계정책
2.3.1 현금및현금성자산
회사는 보유현금과 요구불예금, 유동성이 매우 높고 확정된 금액의 현금으로 전환이 용이하고 가치변동의 위험이 경미한 단기 투자자산을 현금및현금성자산으로 분류하고 있습니다. 지분상품은 현금성자산에서 제외하고 있으며 다만, 상환일이 정해져 있고 취득일로부터 상환일까지의 기간이 단기인 우선주와 같이 실질적인 현금성자산인경우에는 현금성자산에 포함하고 있습니다.
2.3.2 금융상품
금융상품은 거래당사자 어느 한쪽에게는 금융자산이 생기게 하고 거래상대방에게 금융부채나 지분상품이 생기게 하는 모든 계약입니다.
1) 금융자산
(가) 최초 인식과 측정
금융자산은 최초 인식 시점에 후속적으로 상각후원가로 측정되는 금융자산, 기타포괄손익-공정가치 측정 금융자산, 그리고 당기손익-공정가치 측정 금융자산으로 분류됩니다.
최초 인식 시점에 금융자산의 분류는 금융자산의 계약상 현금흐름 특성과 금융자산을 관리하기 위한 회사의 사업모형에 따라 달라집니다. 유의적인 금융요소가 포함되지 않거나 실무적 간편법을 적용하는 매출채권을 제외하고는, 회사는 금융자산을 최초에 공정가치로 측정하며, 당기손익-공정가치로 측정하는 금융자산의 경우가 아니라면 거래원가를 가감합니다. 유의적인 금융요소가 포함되지 않거나 실무적 간편법을 적용하지 않은 매출채권은 기업회계기준서 제1115호에 따라 결정된 거래원가로 측정합니다.
금융자산을 상각후원가 또는 기타포괄손익-공정가치로 측정하기 위해서는 현금흐름이 원리금만으로 구성(SPPI)되어야 합니다. 이 평가는 SPPI 테스트라고 하며, 개별 상품 수준에서 수행됩니다.
금융자산의 관리를 위한 회사의 사업모형은 현금흐름을 발생시키기 위해 금융자산을관리하는 방법과 관련됩니다. 사업모형은 현금흐름의 원천이 금융자산의 계약상 현금흐름의 수취인지, 매도인지 또는 둘 다 인지를 결정합니다.
(나) 후속측정
① 상각후원가 측정 금융자산 (채무상품)
다음의 조건을 충족하는 채무상품은 후속적으로 상각후원가로 측정합니다.
- 계약상 현금흐름을 수취하기 위하여 보유하는 것이 목적인 사업모형 하에서 금융자산을 보유
- 금융자산의 계약조건에 따라 특정일에 원금과 원금잔액에 대한 이자 지급만으로 구성되어 있는 현금흐름이 발생
상각후원가 측정 금융자산은 후속적으로 유효이자율법을 상용하여 측정되며, 손상을인식합니다. 자산의 제거, 변경 또는 손상에서 발생하는 이익과 손실은 당기손익으로인식됩니다.
② 기타포괄손익-공정가치측정항목으로 분류되는 채무상품
다음의 조건을 충족하는 채무상품은 후속적으로 기타포괄손익-공정가치로 측정합니다.
- 계약상 현금흐름의 수취와 금융자산의 매도 둘 다를 통해 목적을 이루는 사업모형 하에서 금융자산을 보유
- 금융자산의 계약조건에 따라 특정일에 원금과 원금잔액에 대한 이자 지급만으로 구성되어 있는 현금흐름이 발생
기타포괄손익-공정가치 측정 채무상품에서, 이자수익, 외화환산손익, 그리고 손상 또는 환입은 상각후원가 측정 금융자산과 동일한 방법으로 계산되어 당기손익으로 인식됩니다. 나머지 공정가치 변동부분은 기타포괄손익으로 인식됩니다. 금융자산의제거 시, 기타포괄손익으로 인식한 공정가치 누적 변동분은 당기손익으로 재순환됩니다.
③ 기타포괄손익-공정가치측정항목으로 지정된 지분상품
회사는 최초 인식시점에 지분상품에 대한 투자를 기타포괄손익-공정가치 항목으로 지정하는 취소 불가능한 선택을 할 수 있습니다. 만일 지분상품이 단기매매항목이거나 사업결합에서 취득자가 인식하는 조건부 대가인 경우에는 기타포괄손익-공정가치측정항목으로의 지정은 허용되지 아니합니다. 이러한 선택은 금융상품별로 이루어집니다.
이러한 기타포괄손익-공정가치 측정 지분상품에서 발생하는 손익은 당기손익으로 재순환되지 않습니다. 배당은 회사가 금융자산의 원가 중 일부를 회수하여 이익을 얻는 경우를 제외하고는, 받을 권리가 확정되었을 때 손익계산서에 기타수익으로 인식됩니다. 기타포괄손익-공정가치 측정 지분상품은 손상을 인식하지 않습니다.
④ 당기손익-공정가치 측정 금융자산
상기에서 설명한 상각후원가, 기타포괄손익-공정가치로 측정하지 않는 모든 금융상품은 모든 파생 금융자산을 포함하여 당기손익-공정가치로 측정합니다. 당기손익-공정가치측정금융자산은 매 보고기간말 공정가치로 측정하며, 위험회피관계로 지정된 부분을 제외한 공정가치 변동에 따른 손익을 당기손익으로 인식합니다.
회사는 상각후원가 또는 기타포괄손익-공정가치로 측정하는 요구사항을 충족하는 채무상품을 당기손익-공정가치 측정 항목으로 지정한다면 회계불일치를 제거하거나유의적으로 줄이는 경우에는 해당 채무상품을 당기손익-공정가치 측정 항목으로 지정할 수 있습니다. 다만, 이러한 지정은 취소할 수 없습니다
(다) 금융자산의 제거
금융자산의 현금흐름에 대한 계약상 권리가 소멸하거나, 금융자산을 양도하고 금융자산의 소유에 따른 위험과 보상의 대부분을 다른 기업에게 이전할 때에만 금융자산을 제거하고 있습니다. 만약 금융자산의 소유에 따른 위험과 보상의 대부분을 이전하지도 않고 보유하지도 않으며, 양도한 금융자산을 계속하여 통제하고 있다면, 회사는당해 금융자산에 대하여 지속적으로 관여하는 정도까지 계속하여 인식하고 있습니다. 만약 양도한 금융자산의 소유에 따른 위험과 보상의 대부분을 보유하고 있다면, 회사는 당해 금융자산을 계속 인식하고 수취한 대가는 담보 차입으로 인식하고 있습니다.
상각후원가로 측정하는 금융자산을 제거하는 경우, 당해 자산의 장부금액과 수취하거나 수취할 대가의 합계의 차이를 당기손익으로 인식합니다. 기타포괄손익-공정가치로 측정하는 채무상품에 대한 투자를 제거하는 경우 이전에 인식한 손익누계액을 당기손익으로 재분류합니다. 반면에 최초 인식시점에 기타포괄손익-공정가치항목으로 지정한 지분상품에 대한 투자는 이전에 인식한 손익누계액을 당기손익으로 재분류하지 않으나 이익잉여금으로 대체합니다.
(라) 금융자산의 손상
회사는 상각후원가나 기타포괄손익-공정가치로 측정하는 채무상품에 대한 투자, 리스채권, 매출채권 및 계약자산과 금융보증계약에 대한 기대신용손실을 손실충당금으로 인식합니다. 기대신용손실은 계약상 수취하기로 한 현금흐름과 회사가 수취할 것으로 예상하는 모든 현금흐름의 차이를 최초의 유효이자율로 할인하여 추정합니다. 예상되는 현금흐름은 보유한 담보를 처분하거나 계약의 필수조건인 그 밖의 신용보강으로부터 발생하는 현금흐름을 포함합니다.
2) 금융부채
금융부채는 최초 인식 시점에 당기손익-공정가치 측정 금융부채, 대출과 차입, 미지급금 또는 효과적인 위험회피 수단으로 지정된 파생상품으로 적절하게 분류됩니다. 모든 금융부채는 최초에 공정가치로 인식되고, 대여금, 차입금 및 미지급금의 경우에는 직접 관련된 거래원가를 차감합니다.
모든 금융부채는 후속적으로 유효이자율법을 사용하여 상각후원가로 측정하거나 당기손익-공정가치로 측정합니다. 그러나 금융자산의 양도가 제거요건을 충족하지 못하거나 지속적 관여 접근법이 적용되는 경우에 발생하는 금융부채와 발행한 금융보증계약은 아래에 기술하고 있는 특정한 회계정책에 따라 측정됩니다.
(가) 당기손익-공정가치 측정 금융부채
금융부채는 사업결합에서 취득자의 조건부대가이거나 단기매매항목이거나 최초 인식시 당기손익인식항목으로 지정할 경우 당기손익-공정가치측정금융부채로 분류하고 있습니다.
금융부채가 단기간 내에 재매입되는 경우에는 단기매매항목으로 분류됩니다. 이 범주는 또한 기업회계기준서 제1109호에서 정의된 위험회피관계에 있는 위험회피수단으로 지정되지 않은 파생상품을 포함합니다. 또한 분리된 내재파생상품은 위험회피에 효과적인 수단으로 지정되지 않았다면 단기매매항목으로 분류됩니다.
당기손익-공정가치측정금융부채는 공정가치로 측정하며 위험회피관계로 지정된 부분을 제외한 공정가치의 변동으로 인해 발생하는 평가손익은 당기손익으로 인식합니다. 그러나 금융부채를 당기손익-공정가치측정 항목으로 지정하는 경우에 부채의 신용위험 변동으로 인한 금융부채의 공정가치 변동금액은 부채의 신용위험 변동효과를기타포괄손익으로 인식하는 것이 당기손익에 회계불일치를 일으키거나 확대하는 것이 아니라면 기타포괄손익으로 인식합니다.
부채의 나머지 공정가치 변동은 당기손익으로 인식합니다. 기타포괄손익으로 인식된금융부채의 신용위험으로 인한 공정가치 변동은 후속적으로 당기손익으로 재분류되지 않으며, 금융부채가 제거될 때 이익잉여금으로 대체됩니다. 당기손익-공정가치측정항목으로 지정된 금융보증계약에서 발생한 손익은 당기손익으로 인식합니다.
(나) 상각후원가측정금융부채
금융부채는 사업결합에서 취득자의 조건부대가이거나 단기매매항목이거나 최초 인식시 당기손익인식항목으로 지정할 경우에 해당하지 않는 경우 후속적으로 유효이자율법을 사용하여 상각후원가로 측정됩니다.
유효이자율법은 금융부채의 상각후원가를 계산하고 관련 기간에 걸쳐 이자비용을 배분하는 방법입니다. 유효이자율은 금융부채의 기대존속기간이나 (적절하다면) 더 짧은 기간에 지급하거나 수취하는 수수료와 포인트(유효이자율의 주요 구성요소임), 거래원가 및 기타 할증액 또는 할인액을 포함하여 예상되는 미래현금지급액의 현재가치를 금융부채의 상각후원가와 정확히 일치시키는 이자율입니다.
(다) 금융보증부채
금융보증계약은 채무상품의 최초 계약조건이나 변경된 계약조건에 따라 지급기일에 특정 채무자가 지급하지 못하여 보유자가 입은 손실을 보상하기 위해 발행자가 특정금액을 지급하여야 하는 계약입니다.
금융보증부채는 공정가치로 최초 측정하며, 당기손익인식항목으로 지정되거나 자산의 양도로 인해 발생한 것이 아니라면 다음 중 큰 금액으로 후속측정하여야 합니다.
- 기업회계기준서 제1109호에 따라 산정한 손실충당금
- 최초 인식금액에서 기업회계기준서 제1115호에 따라 인식한 이익누계액을 차감한 금액
(라) 금융부채의 제거
금융부채는 지급 의무의 이행, 취소, 또는 만료된 경우에 제거됩니다. 기존 금융부채가 대여자는 동일하지만 조건이 실질적으로 다른 금융부채에 의해 교환되거나, 기존 부채의 조건이 실질적으로 변경된 경우에, 이러한 교환이나 변경은 최초의 부채를 제거하고 새로운 부채를 인식하게 합니다. 각 장부금액의 차이는 당기손익으로 인식합니다.
3) 금융상품의 상계
금융자산과 금융부채는 인식한 자산과 부채에 대해 법적으로 집행 가능한 상계 권리를 현재 가지고 있거나, 차액으로 결제하거나 자산을 실현하는 동시에 부채를 결제할의도가 있는 경우에 재무상태표에서 상계하여 순액으로 표시됩니다.
2.3.3 유형자산의 평가 및 감가상각
1) 인식과 측정
유형자산은 원가로 측정하여 인식하고 있으며, 최초 인식 후에는 원가에서 감가상각누계액과 손상차손누계액을 차감한 금액을 장부금액으로 하고 있습니다. 유형자산의원가에는 경영진이 의도하는 방식으로 자산을 가동하는데 필요한 장소와 상태에 이르게 하는데 직접 관련되는 원가 및 자산을 해체, 제거하거나 부지를 복구하는데 소요될 것으로 추정되는 원가가 포함됩니다.
유형자산을 구성하는 일부 요소의 원가의 내용연수가 자산 전체의 내용연수와 다른 경우에는, 별개의 자산으로 회계처리하고 있습니다.
유형자산의 제거로 인하여 발생하는 손익은 순매각금액과 장부금액의 차이로 결정되고 제거할 때 당기 손익으로 인식합니다.
2) 후속원가
유형자산의 일부를 대체할 때 발생하는 원가는 해당 자산으로부터 발생하는 미래 경제적 효익이 회사에 유입될 가능성이 높으며 그 원가를 신뢰성 있게 측정할 수 있는 경우에 자산의 장부금액에 포함하거나 적절한 경우 별도의 자산으로 인식하고 있습니다. 이 때 대체된 부분의 장부금액은 제거하고 있습니다. 그 외의 일상적인 수선ㆍ유지와 관련하여 발생하는 원가는 발생시점에 당기손익으로 인식하고 있습니다.
3) 감가상각
유형자산 중 토지 및 건설중인자산에 대해서는 감가상각을 하지 않으며, 그 외 유형자산은 자산의 취득원가에서 잔존가치를 차감한 금액에 대하여 아래에 제시된 경제적 내용연수에 걸쳐 해당자산에 내재되어 있는 미래경제적효익의 예상소비형태를 가장 잘 반영한 정액법으로 상각하고 있습니다.
유형자산을 구성하는 일부의 원가가 당해 유형자산의 전체원가와 비교하여 유의적이라면, 해당 유형자산을 감가상각할 때 그 부분은 별도로 구분하여 감가상각하고 있습니다.
한편, 유형자산의 감가상각은 다음의 추정내용연수에 걸쳐 정액법으로 상각하고 있습니다.
| 구분 | 내용연수 |
|---|---|
| 공구와기구 | 5년 |
| 비품 | 5년 |
| 시설장치 | 5년 |
2.3.4 무형자산의 평가 및 상각방법
회사는 무형자산을 원가로 측정하며, 최초 인식 후에 원가에서 상각누계액과 손상차손누계액을 차감한 금액을 장부금액으로 표시하고 있습니다. 무형자산은 당해 자산이 사용가능한시점부터 잔존가치를 영("0")으로 하여 아래에 제시된 개별 자산별로 추정된 경제적 내용연수 동안 정액법으로 상각하고 있습니다.
| 구분 | 내용연수 |
|---|---|
| 소프트웨어 | 5 년 |
| 특허권 | 7 년 |
내용연수가 유한한 무형자산의 상각방법과 내용연수에 대해서 매 회계연도말에 재검토하고, 내용연수가 비한정인 무형자산에 대해서는 그 자산의 내용연수가 비한정이라는 평가가 계속하여 정당한 지를 매 회계기간에 재검토하며, 이를 변경하는 것이 적절하다고 판단되는 경우 회계추정의 변경으로 회계처리하고 있습니다.
2.3.5 정부보조금
정부보조금은 부수되는 조건의 이행에 대한 합리적인 확신이 있는 경우에 인식하고
있습니다. 수익 관련 정부보조금은 정부보조금으로 보전하려 하는 관련원가와 대응시키기 위해 필요한 기간에 걸쳐 체계적인 기준에 따라 정부보조금을 수익으로 인식하며, 자산 관련 정부보조금은 자산의 장부금액을 결정할 때 차감하여 표시하고 감가상각자산의 내용연수에 걸쳐 감가상각비를 감소시키는 방식으로 당기손익으로 인식하고 있습니다.
회사는 비화폐성자산을 보조금으로 수취한 경우 자산과 보조금을 명목금액으로 기록
하고 관련자산의 추정내용연수에 걸쳐 정액으로 손익계산서에 수익으로 인식하고 있
습니다. 시장이자율보다 낮은 이자율의 대여금 혹은 유사한 지원을 제공받은 경우 낮
은 이자율로 인한 효익은 추가적인 정부보조금으로 인식하고 있습니다.
2.3.6 리스
리스는 리스제공자가 대가와 교환하여 식별되는 자산의 사용 통제권을 일정기간 동안 리스이용자에게 이전하는 계약입니다. 회사는 계약의 약정시점에, 계약 자체가 리스인지, 계약이 리스를 포함하는지를 판단합니다.
리스이용자 및 리스제공자는 리스계약이나 리스를 포함하는 계약에서 계약의 각 리스요소를 리스가 아닌 요소(이하'비리스요소'라고 함)와 분리하여 리스로 회계처리합니다. 다만, 회사는 리스이용자로서의 회계처리에서 실무적 간편법을 적용하여 비리스요소를 리스요소와 분리하지 않고 각 리스요소와 관련 비리스요소를 하나의 리스요소로 회계처리합니다.
회사는 리스개시일에 기초자산을 사용할 권리를 나타내는 사용권자산과 리스료를 지급할 의무를 나타내는 리스부채를 인식합니다. 다만 회사는 단기리스와 소액기초자산리스에 대하여 리스이용자의 인식, 측정 및 표시 규정을 적용하지 않는 예외규정을선택하였습니다.
사용권자산은 리스개시일에 원가로 측정하고, 후속적으로 원가에서 감가상각누계액과 손상차손누계액을 차감하고, 리스부채의 재측정에 따른 조정을 반영하여 측정합니다. 또한 사용권자산은 리스개시일부터 사용권자산의 내용연수 종료일과 리스기간종료일 중 이른 날까지 감가상각합니다.
리스부채는 리스개시일 현재 지급되지 않은 리스료의 현재가치로 측정됩니다. 리스의 내재이자율을 쉽게 산정할 수 있는 경우에는 그 이자율로 리스료를 할인하며 그 이자율을 쉽게 산정할 수 없는 경우에는 리스이용자의 증분차입이자율을 사용합니다. 리스부채는 후속적으로 리스부채에 대한 이자비용만큼 증가하고, 지급한 리스료를 반영하여 감소합니다.
잔존가치보증에 따라 지급할 것으로 예상되는 금액의 변동,지수나 요율(이율)의 변동, 리스기간의 변경, 매수선택권이나 연장선택권의 행사여부평가의 변동에 따라 미래 리스료가 변경되는 경우에 리스부채를 재측정합니다.
단기리스(리스개시일에 리스기간이 12개월 이하인 리스)와 소액자산리스의 경우 예외 규정을 선택하여 리스료를 리스기간에 걸쳐 정액기준으로 비용을 인식합니다.
2.3.7 종업원급여
1) 퇴직급여
회사는 퇴직연금제도를 운영하고 있으며, 일반적으로 주기적인 보험수리적 계산에 의해 산정된 금액을 보험회사나 수탁자가 관리하는 기금에 대한 지급을 통해 조달하고 있습니다. 회사는 노사협의회의 동의를 얻어 종업원에 대하여 확정급여제도인 확정급여형퇴직연금제도를 도입하였습니다.
확정급여제도는 보고기간 말 현재 확정급여제도와 관련된 순확정급여부채는 확정급여채무의 현재가치에서 사외적립자산의 공정가치를 차감하여 인식하고 있습니다.
순확정급여부채는 매년 독립적인 계리사에 의해 예측단위적립방식으로 계산되고 있습니다. 확정급여채무의 현재가치에서 사외적립자산의 공정가치를 차감하여 산출된순액이 자산일 경우, 제도로부터 환급받거나 제도에 대한 미래 기여금이 절감되는 방식으로 이용가능한 경제적 효익의 현재가치를 한도로 자산을 인식하고 있습니다.
확정급여원가는 근무원가, 순확정급여부채의 순이자 및 순확정급여부채의 재측정요소로 구성됩니다. 근무원가와 순확정급여부채의 순이자는 당기손익으로 인식되며 순확정급여부채의 재측정요소는 기타포괄손익으로 인식됩니다.
순확정급여부채의 순이자는 사외적립자산에 대한 이자수익, 확정급여채무에 대한 이자원가 및 자산인식상한효과에 대한 이자로 구성됩니다. 순확정급여부채의 순이자는연차보고기간 초에 결정된 순확정급여부채와 할인율을 곱하여 결정되며, 보고기간 동안의 기여금 납부와 급여지급으로 인한 순확정급여부채의 변동을 반영합니다. 순확정급여부채의 재측정요소는 보험수리적손익, 순확정급여부채의 순이자에 포함된 금액을 제외한 자산의 수익 및 순확정급여부채의 순이자에 포함된 금액을 제외한 자산인식상한효과의 변동으로 구성됩니다. 보험수리적손익은 보험수리적 가정의 변동과 경험조정으로 인하여 확정급여채무 현재가치의 증감이 있을 때 발생하고 있습니다.
2) 단기종업원급여
종업원이 관련 근무용역을 제공한 회계기간의 말부터 12개월 이내에 결제될 단기종업원급여는 근무용역과 교환하여 지급이 예상되는 금액을, 근무용역이 제공된 때에 당기손익으로 인식하고 있습니다. 단기종업원급여는 할인하지 않은 금액으로 측정하고 있습니다.
종업원이 과거 근무용역의 결과 회사가 지급해야 할 법적의무 또는 의제의무가 있고,그 채무금액을 신뢰성있게 추정할 수 있다면 이익분배금 및 상여금으로 지급이 예상되는 금액을 부채로 인식하고 있습니다.
2.3.8 법인세
법인세비용은 당기법인세와 이연법인세로 구성되어 있으며, 기타포괄손익이나 자본에 직접 인식되는 거래나 사건 또는 사업결합에서 발생하는 세액을 제외하고는 당기손익으로 인식하고 있습니다.
1) 당기법인세
당기 법인세는 당기의 과세소득을 기초로 산정하고 있습니다. 과세소득은 포괄손익계산서상의 이익에서 다른 과세기간에 가산되거나 차감될 손익 및 비과세항목이나 손금불인정항목을 제외하므로 과세소득과 손익계산서상 손익은 차이가 발생합니다. 회사의 당기법인세와 관련된 미지급법인세는 확정되었거나 실질적으로 확정된 세율을 사용하여 계산하고 있습니다.
2) 이연법인세
이연법인세는 재무제표상 자산과 부채의 장부금액과 과세소득 산출시 사용되는 세무기준액과의 차이를 바탕으로 인식되며, 자산부채법에 의하여 인식하고 있습니다. 이연법인세부채는 모든 가산할 일시적차이에 대하여 인식하며, 이연법인세자산은 차감할 일시적차이가 사용될 수 있는 과세소득의 발생가능성이 높은 경우에, 모든 차감할일시적차이에 대하여 인식합니다.
이연법인세자산의 장부금액은 매 보고기간 말에 검토하고, 이연법인세자산으로 인한혜택이 사용되기에 충분한 과세소득이 발생할 가능성이 더 이상 높지 않은 경우 이연법인세자산의 장부금액을 감소시키고 있습니다.
이연법인세자산과 부채는 보고기간 말 제정되었거나 실질적으로 제정된 세율(세법)에 근거하여 당해 자산이 실현되거나 부채가 지급될 회계기간에 적용될 것으로 기대되는 세율을 사용하여 측정하고 있습니다. 이연법인세자산과 이연법인세부채를 측정할 때에는 보고기간말 현재 회사가 관련 자산과 부채의 장부금액을 회수하거나 결제할 것으로 예상되는 방식에 따라 법인세효과를 반영하였습니다.
이연법인세자산과 부채는 동일 과세당국이 부과하는 법인세이고, 회사가 인식된 금액을 상계할 수 있는 법적 권한을 가지고 있으며 당기 법인세부채와 자산을 순액으로결제할 의도가 있는 경우에만 상계하고 있습니다.
2.3.9 비금융자산손상
회사는 매 보고기간 종료일에 모든 비금융자산에 대하여 손상징후의 존재여부를 평가합니다. 비한정내용연수의 무형자산에 대해서는 매년 또는 손상징후가 있는 경우에 손상검사를 수행합니다. 기타 비금융자산에 대해서는 장부금액이 회수가능하지 않을 것이라는 징후가 있을 때 손상검사를 수행합니다. 사용가치를 계산하기 위하여 경영자는 해당 자산이나 현금창출단위로부터 발생하는 미래기대현금흐름을 추정하고 동 미래기대현금흐름의 현재가치를 계산하기 위한 적절한 할인율을 선택하여야 합니다.
2.3.10 충당부채
회사는 지출의 시기 또는 금액이 불확실한 부채 중 과거사건이나 거래의 결과로 현재의무가 존재하며, 당해 의무를 이행하기 위하여 자원이 유출될 가능성이 매우 높고, 그 의무의 이행에 소요되는 금액을 신뢰성 있게 추정할 수 있는 경우는 부채로 계상하여 이를 의도한 목적과 용도에만 사용하고 있습니다. 또한 충당부채의 명목가액과 현재가치의 차이가 중요한 경우에는 의무를 이행하기 위하여 예상되는 지출액의 현재가치로 평가하고 있습니다.
2.3.11 주식기준보상
종업원과 유사용역제공자에게 부여한 주식결제형주식기준보상은 부여일에 지분상품의 공정가치로 측정하고 있습니다. 부여일에 결정되는 주식결제형주식기준보상거래의 공정가치는, 가득될 지분상품에 대한 회사의 추정치에 근거하여 가득기간에 걸쳐 정액기준으로 비용화됩니다. 각 보고기간 말에 회사는 가득될 것으로 기대되는 지분상품의 수량에 대한 추정치를 수정하고 있습니다. 최초 추정에 대한 수정치의 효과는 누적비용이 수정치를 반영하도록 잔여 가득기간 동안에 걸쳐 당기손익으로 인식하고 기타불입자본에 반영하고 있습니다. 종업원이 아닌 거래상대방에게 부여한 주식결제형기준보상은 제공받는 재화나 용역의 공정가치로 측정하고 있습니다. 다만 제공받는 재화나 용역의 공정가치를 신뢰성있게 추정할 수 없다면, 제공받는 재화나 용역은 재화나 용역을 제공받는 날을 기준으로 부여된 지분상품의 공정가치에 기초하여 측정하고 있습니다.
2.3.12 납입자본
보통주는 자본으로 분류하며 자본거래에 직접 관련되어 발생하는 증분원가에 대해서는 관련된 법인세혜택을 차감한 순액을 자본에서 차감하고 있습니다. 자기지분상품을 재취득하는 경우 (이하 "자기주식") 거래원가 중 당해 자본거래에 직접 관련되어 발생하는 증분원가에 대해서는 관련된 법인세혜택을 차감한 순액을 자본에서 차감하여 회계처리하고 있으며, 자기주식의 계정과목으로 하여 재무상태표상 총자본의 차감항목으로 표시하고 있습니다. 한편, 자기주식을 매입 또는 매도하거나 발행 또는 소각하는 경우의 손익은 당기손익으로 인식하지 아니하고 자본에서 직접 인식하고 있습니다.
2.3.13 금융수익과 금융비용
금융수익은 금융자산을 포함한 투자로부터의 이자수익, 배당수익, 금융자산처분손익을 포함하고 있습니다. 이자수익은 기간의 경과에 따라 유효이자율법을 적용하여 당기손익으로 인식하며, 배당수익은 주주로서 배당을 받을 권리가 확정되는 시점에 수익을 인식하고 있습니다.
금융비용은 차입금에 대한 이자비용을 포함하고 있습니다. 차입금에 대한 이자비용은 유효이자율법을 적용하여 기간의 경과에 따라 당기손익으로 인식하고 있습니다.
외환손익은 차익과 차손을 순액으로 표시하고 있습니다.
2.3.14 주당이익
주당순이익은 보통주 1주에 대한 당기순이익을 계산한 것으로서 보통주당기순이익을 가중평균유통보통주식수로 나누어 산정하고 있습니다. 희석주당순이익은 보통주 및 희석증권 1주에 대한 당기순이익을 계산한 것으로서 희석당기순이익을 가중평균유통보통주식수와 희석성 잠재적보통주의 주식수를 합한 수로 나누어 산정하고 있습니다.
2.3.15 외화자산 및 부채의 환산
회사의 재무제표 작성에 있어서 기능통화 외의 통화(외화)로 이루어진 거래는 거래일의 환율을 적용하여 기록하고 있습니다. 매 보고기간 말에 화폐성 외화항목은 보고기간 말의 마감환율로 환산하고 있습니다. 공정가치로 측정하는 비화폐성 외화항목은 공정가치가 결정된 날의 환율로 환산하고, 역사적원가로 측정하는 비화폐성항목은 거래일의 환율로 환산하고 있습니다.
화폐성항목의 결제시점에 생기는 외환차이와 해외사업장순투자 환산차이 또는 현금흐름위험회피로 지정된 금융부채에서 발생한 환산차이를 제외한 화폐성항목의 환산으로 인해 발생한 외환차이는 모두 당기손익으로 인식하고 있습니다. 비화폐성항목에서 발생한 손익을 기타포괄손익으로 인식하는 경우에는 그 손익에 포함된 환율변동효과도 기타포괄손익으로 인식하고, 당기손익으로 인식하는 경우에는 환율변동효과도 당기손익으로 인식하고 있습니다.
2.3.16 전환상환우선주
전환상환우선주는 계약의 조건에 기초하여 차입부채요소와 파생상품부채요소로 분리하여 인식하고 있습니다.
전환상환우선주의 발행에 있어 전환권 및 조기상환권의 파생상품부채요소는 공정가치로 측정되고 발행금액에서 파생상품부채요소의 공정가치를 제외한 잔여금액은 거래비용을 차감한 후 차입부채요소에 배분되어 유효이자율법을 적용한 상각후원가로측정합니다.
2.3.17 공정가치
공정가치는 가격이 직접 관측가능한지 아니면 가치평가기법을 사용하여 추정하는지의 여부에 관계없이 측정일에 시장참여자 사이의 정상거래에서 자산을 매도하면서 수취하거나 부채를 이전하면서 지급하게 될 가격입니다. 자산이나 부채의 공정가치를 추정함에 있어 회사는 시장참여자가 측정일에 자산이나 부채의 가격을 결정할 때 고려하는 자산이나 부채의 특성을 고려합니다. 기업회계기준서 제1102호 '주식기준보상'의 적용범위에 포함되는 주식기준보상거래, 기업회계기준서 제1017호 '리스'의적용범위에 포함되는 리스거래, 기업회계기준서 제1002호 '재고자산'의 순실현가능가치 및 기업회계기준서 제1036호 '자산손상'의 사용가치와 같이 공정가치와 일부 유사하나 공정가치가 아닌 측정치를 제외하고는 측정 또는 공시목적상 공정가치는 상기에서 설명한 원칙에 따라 결정됩니다.
또한 재무보고목적상 공정가치측정에 사용된 투입변수의 관측가능한 정도와 공정가치측정치 전체에 대한 투입변수의 유의성에 기초하여 다음에서 설명하는 바와 같이 공정가치측정치를 수준 1, 2 또는 3으로 분류합니다.
(수준 1) 측정일에 동일한 자산이나 부채에 대한 접근 가능한 활성시장의 (조정되지 않은) 공시가격
(수준 2) 수준 1의 공시가격 이외에 자산이나 부채에 대해 직접적으로 또는 간접적으 로 관측가능한 투입변수
(수준 3) 자산이나 부채에 대한 관측가능하지 않은 투입변수
3. 중요한 회계추정 및 가정
중요한 추정 및 가정은 계속적으로 평가되며 역사적인 경험과 주어진 환경 등에 따라합리적으로 발생가능하다고 판단되는 미래의 사건에 대한 기대를 포함하는 기타의 요인들에 의하여 근거하고 있습니다. 이러한 정의를 근거로 산출된 회계추정치는 실제 발생결과와 일치하지 않을 수 있습니다. 다음 회계연도에 자산과 부채의 장부가액을 중요하게 변동시킬 수 있는 중요한 위험을 포함하고 있는 주요한 회계추정과 가정은 다음과 같습니다.
(1) 순확정급여부채
순확정급여부채의 현재가치는 보험수리적방식에 의해 결정되는 다양한 요소들 특히,할인율의 변동에 영향을 받습니다.
(2) 법인세
회사는 보고기간말 현재까지의 영업활동의 결과로 미래에 부담할 것으로 예상되는 법인세효과를 최선의 추정과정을 거쳐 당기법인세 및 이연법인세로 인식하였습니다.하지만 실제 미래 최종 법인세부담은 인식된 관련 자산ㆍ부채와 일치하지 않을 수 있으며, 이러한 차이는 최종 세효과가 확정된 시점의 당기법인세 및 이연법인세자산ㆍ부채에 영향을 줄 수 있습니다.
(3) 금융상품의 공정가치
활성시장에서 거래되지 않는 금융상품의 공정가치는 원칙적으로 평가기법을 사용하여 결정됩니다. 회사는 보고기간말 현재 중요한 시장상황에 기초하여 다양한 평가기법의 선택 및 가정에 대한 판단을 하고 있습니다.
(4) 사용권자산 및 리스부채
회사는 리스기간을 리스의 해지불능기간과 리스 연장선택권을 행사할 것이 상당히 확실한 경우에 그 선택권의 대상기간 또는 리스 종료선택권을 행사하지 않을 것이 상당히 확실한 경우에 그 선택권의 대상기간을 포함하여 산정합니다
회사는 연장 및 종료 선택권을 포함하는 리스 계약들을 가지고 있습니다. 회사는 리스를 연장 또는 종료하기 위한 선택권을 행사할지 여부가 상당히 확실한지를 평가할 때 판단을 적용합니다. 즉, 연장선택권을 행사하거나 종료선택권을 행사하지 않을 경제적 유인이 생기게 하는 관련되는 사실 및 상황을 모두 고려합니다. 개시일 이후, 회사는 회사의 통제 하에 있는 상황에서 유의적인 사건이나 변화가 있고, 연장선택권을행사할지 종료선택권을 행사하지 않을지에 대한 능력에 영향을 미치는 경우 리스기간을 재평가합니다(예를 들어, 유의적인 리스개량 또는 리스자산에 대한 유의적인 고객맞춤화).
4. 재무위험관리
회사의 재무위험관리는 시장위험, 신용위험 및 유동성위험과 같은 다양한 재무위험하에서도 안정적이고 지속적인 경영성과를 창출할 수 있도록 재무구조 개선 및 자금운영의 효율성을 제고하는 데 있습니다.
재무위험관리활동은 주로 자금부서에서 주관하고 있으며 관련 부서와의 긴밀한 협조하에 재무위험 관리정책 수립 및 재무위험 식별, 평가, 헷지 등의 실행활동을 하고 있습니다. 또한, 정기적으로 재무위험 관리정책의 재정비, 재무위험 모니터링 등을 통해 재무위험으로부터 발생할 수 있는 영향을 최소화하는데 주력하고 있습니다.
(1) 신용위험
회사는 금융상품의 당사자 중 일방이 의무를 이행하지 않아 상대방에게 재무손실을 입힐 신용위험에 노출되어 있습니다.
신용위험은 주로 단기대여금 및 채무상품, 금융기관예치금으로부터 발생하고 있습니다.
회사는 신용위험을 관리하기 위하여 신용도가 일정 수준 이상인 거래처와 거래하고 있으며, 금융자산의 신용보강을 위한 정책과 절차를 마련하여 운영하고 있습니다.
회사는 신규 거래처와 계약시 공개된 재무정보와 신용평가기관에 의하여 제공된 정보 등을 이용하여 거래처의 신용도를 평가하고 이를 근거로 신용거래한도를 결정하고 있으며, 담보 또는 지급보증을 제공받고 있습니다.
또한, 회사는 주기적으로 거래처의 신용도를 재평가하여 신용거래한도를 재검토하고담보수준을 재조정하고 있으며, 회수가 지연되는 금융자산에 대하여는 정기적으로 회수지연 현황을 파악하고 회수대책을 마련하는 등 적절한 조치를 취하고 있습니다.
보고기간 종료일 현재 상각후원가로 분류된 금융상품의 신용위험에 노출된 최대금액은 장부금액과 유사합니다.
(2) 유동성위험
회사는 현금 등 금융자산을 인도하여 결제하는 금융부채에 관련된 의무를 충족하는 데 어려움을 겪게 될 유동성위험에 노출되어 있습니다.
회사는 정기적인 자금수지계획의 수립을 토대로 영업활동, 투자활동, 재무활동에서의 자금수지를 미리 예측해 금융부채와 금융자산의 만기구조를 대응시키고 있으며, 이를 통해 필요 유동성 규모를 사전에 확보하고 유지하여 향후에 발생할 수 있는 유동성리스크를 사전에 관리하고 있습니다.
보고기간 종료일 현재 파생금융상품이 아닌 주요 금융부채의 명목가액에 대한 연도별 상환계획은 다음과 같습니다.
1) 당반기말
| (단위: 원) |
| 구분 | 장부금액 | 계약상 원금 | 합계 | |
|---|---|---|---|---|
| 1년 이하 | 1년 초과 | |||
| 미지급금 | 356,749,758 | 125,726,818 | 231,022,940 | 356,749,758 |
| 미지급비용 | 157,060,024 | 157,060,024 | - | 157,060,024 |
| 리스부채 | 336,061,110 | 143,850,960 | 251,057,945 | 394,908,905 |
2) 전기말
| (단위: 원) |
| 구분 | 장부금액 | 계약상 원금 | 합계 | |
|---|---|---|---|---|
| 1년 이하 | 1년 초과 | |||
| 미지급금 | 277,710,071 | 58,601,545 | 219,108,526 | 277,710,071 |
| 미지급비용 | 118,230,936 | 118,230,936 | - | 118,230,936 |
| 리스부채 | 105,237,995 | 48,840,000 | 69,054,545 | 117,894,545 |
(3) 자본위험
회사의 자본위험관리 목적은 계속기업으로서 주주 및 이해당사자들에게 이익을 지속적으로 제공할 수 있는 능력을 보호하고 자본비용을 절감하기 위해 최적 자본구조를 유지하는 것입니다. 회사는 최적 자본구조를 달성하기 위하여 동종산업내의 타사와 마찬가지로 부채비율에 기초하여 자본을 관리하고 있습니다. 부채비율은 부채총계를자본총계로 나누어 산출하고 있습니다.
보고기간 종료일 현재 회사의 부채비율은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기말 | 전기말 |
|---|---|---|
| 부채총계(A) | 1,378,381,759 | 835,777,840 |
| 자본총계(B) | 18,696,472,616 | 23,327,267,446 |
| 부채비율(A/B) | 7.37% | 3.58% |
5. 범주별 금융상품
(1) 보고기간 종료일 현재 회사의 금융상품은 모두 상각후원가로 측정하는 금융자산 및 금융부채로 분류하고 있습니다.
(2) 공정가치의 서열체계
보고기간 종료일 현재 회사는 금융상품의 공정가치를 측정하고 공시하기 위해 다음과 같은 서열체계를 이용하고 있습니다.
| 구분 | 투입변수의 유의성 |
|---|---|
| 수준 1 | 동일한 자산이나 부채에 대한 활성시장의(조정되지 않은) 공시가격 |
| 수준 2 | 직접적 또는 간접적으로 관측가능한, 자산이나 부채에 대한 투입변수 (단, 수준 1에 포함된 공시가격은 제외) |
| 수준 3 | 관측 가능한 시장자료에 기초하지 않은, 자산이나 부채에 대한 투입변수 |
활성시장에서 거래되는 금융상품의 공정가치는 보고기간말 현재 고시되는 시장가격에 기초하여 산정됩니다. 이러한 상품들은 수준 1에 포함되며, 대부분 상장주식으로 구성됩니다.
활성시장에서 거래되지 않는 금융상품의 공정가치는 평가기법을 사용하여 결정하고 있습니다. 이러한 평가기법은 가능한 한 관측가능한 시장정보를 최대한 사용하고 기업 고유 정보는 최소한으로 사용합니다.
이때, 해당 상품의 공정가치 측정에 요구되는 모든 유의적인 투입변수가 관측가능하다면 해당 상품은 수준 2에 포함됩니다.
만약, 하나 이상의 유의적인 투입변수가 관측가능한 시장정보에 기초한 것이 아니라면 해당 상품은 수준 3에 포함됩니다.
금융상품의 공정가치를 측정하는 데에 사용되는 평가기법에는 다음이 포함됩니다.
- 유사한 상품의 공시시장가격 또는 딜러가격
- 파생상품의 공정가치는 보고기간말 현재의 선도환율을 사용하여 해당 금액을 현재 가치로 할인하여 측정
- 나머지 금융상품에 대해서는 현금흐름의 할인기법 등
기타금융상품과 같은 범주의 금융상품 장부가액은 공정가치의 합리적인 근사치로 추정하고 있습니다.
보고기간 종료일 현재 회사의 금융상품은 모두 상각후원가로 측정하는 금융자산 및 금융부채로 분류하고 있어 공정가치로 측정되는 금융상품은 없습니다.
(3) 금융상품의 범주별 손익
당반기 및 전반기 중 회사의 금융상품 범주별 순손익의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 |
|---|---|---|
| 상각후원가 측정 금융자산 | ||
| 이자수익 | 456,199,905 | 164,650,916 |
| 외환차익 | 389,717 | - |
| 상각후원가 측정 금융부채 | ||
| 이자비용 | (19,863,076) | (9,046,680) |
| 외환차손 | (10,347,750) | - |
| 합 계 |
426,378,796 | 155,604,236 |
6. 현금및현금성자산
보고기간 종료일 현재 현금및현금성자산의 구성내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기말 | 전기말 |
|---|---|---|
| 보통예금 | 81,345,128 | 97,255,812 |
| MMF | 711,905,589 | 292,404,775 |
| 합 계 | 793,250,717 | 389,660,587 |
7. 단기금융상품
보고기간 종료일 현재 단기금융상품의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기말 | 전기말 |
|---|---|---|
| 정기예금 | 15,000,000,000 | 20,002,461,519 |
8. 기타금융자산
보고기간 종료일 현재 기타금융자산의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기말 | 전기말 | ||
|---|---|---|---|---|
| 유동 | 비유동 | 유동 | 비유동 | |
| 미수금 | 84,599,070 | - | 84,617,620 | - |
| 미수수익 | 409,284,658 | - | 125,693,752 | - |
| 보증금 | - | 483,472,620 | - | 478,472,620 |
| 현재가치할인차금 | - | (35,304,077) | - | (47,318,716) |
| 합 계 | 493,883,728 | 448,168,543 | 210,311,372 | 431,153,904 |
9. 기타자산
보고기간 종료일 현재 기타유동자산의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기말 | 전기말 | ||
|---|---|---|---|---|
| 유동 | 비유동 | 유동 | 비유동 | |
| 선급금 | 110,284,458 | - | 25,468,624 | - |
| 선급비용 | 325,003,549 | 53,190,709 | 190,312,284 | 62,871,593 |
| 합 계 | 435,288,007 | 53,190,709 | 215,780,908 | 62,871,593 |
10. 유형자산
당반기 및 전반기 중 유형자산 장부금액의 변동내역은 다음과 같습니다.
(1) 당반기
| (단위: 원) |
| 구분 | 토지 | 공구와기구 | 비품 | 시설장치 | 건설중인자산 | 합계 |
|---|---|---|---|---|---|---|
| 기초 | 1,601,883,561 | 651,923,097 | 113,450,664 | 24,467,210 | - | 2,391,724,532 |
| 취득 | - | 2,600,000 | 35,228,636 | 3,072,727 | 22,511,000 | 63,412,363 |
| 상각 | - | (167,689,878) | (24,391,743) | (5,195,754) | - | (197,277,375) |
| 정부보조금에 의한 상계 | - | - | 1,648,114 | - | - | 1,648,114 |
| 기말 | 1,601,883,561 | 486,833,219 | 125,935,671 | 22,344,183 | 22,511,000 | 2,259,507,634 |
| 취득원가 | 1,601,883,561 | 2,057,380,200 | 333,979,513 | 61,527,981 | 22,511,000 | 4,077,282,255 |
| 감가상각누계액 | - | (1,570,546,981) | (201,726,093) | (39,183,798) | - | (1,811,456,872) |
| 정부보조금 | - | - | (6,317,749) | - | - | (6,317,749) |
(2) 전반기
| (단위: 원) |
| 구분 | 토지 | 공구와기구 | 비품 | 시설장치 | 합계 |
|---|---|---|---|---|---|
| 기초 | 1,601,883,561 | 890,139,826 | 121,330,009 | 22,531,220 | 2,635,884,616 |
| 취득 | - | 82,550,000 | 16,709,728 | 13,444,800 | 112,704,528 |
| 상각 | - | (177,157,163) | (23,179,843) | (5,663,304) | (206,000,310) |
| 정부보조금에 의한 상계 | - | - | 1,648,114 | - | 1,648,114 |
| 기말 | 1,601,883,561 | 795,532,663 | 116,508,008 | 30,312,716 | 2,544,236,948 |
| 취득원가 | 1,601,883,561 | 2,019,324,200 | 303,881,714 | 58,455,254 | 3,983,544,729 |
| 감가상각누계액 | - | (1,223,791,537) | (177,759,739) | (28,142,538) | (1,429,693,814) |
| 정부보조금 | - | - | (9,613,967) | - | (9,613,967) |
감가상각비 중 132,114,914원(전반기: 144,909,736원)은 경상연구개발비에 포함되어 있습니다.
11. 리스
(1) 당반기 및 전반기 중 기초자산 유형별 사용권자산 장부금액의 변동내역은 다음과 같습니다.
1) 당반기
| (단위: 원) |
| 구분 | 부동산 | 시설장치 | 차량운반구 | 합계 |
|---|---|---|---|---|
| 기초 | 122,756,871 | - | 26,630,701 | 149,387,572 |
| 취득 | 232,594,336 | 62,693,270 | - | 295,287,606 |
| 해지 | (11,965,097) | - | - | (11,965,097) |
| 상각 | (55,601,218) | (10,305,743) | (5,422,958) | (71,329,919) |
| 기말 | 287,784,892 | 52,387,527 | 21,207,743 | 361,380,162 |
| 취득원가 | 364,957,934 | 62,693,270 | 43,773,162 | 471,424,366 |
| 감가상각누계액 | (77,173,042) | (10,305,743) | (22,565,419) | (110,044,204) |
2) 전반기
| (단위: 원) |
| 구분 | 부동산 | 시설장치 | 차량운반구 | 합계 |
|---|---|---|---|---|
| 기초 | 70,623,194 | 43,962,738 | 53,932,250 | 168,518,182 |
| 취득 | 81,178,270 | - | - | 81,178,270 |
| 해지 | (4,520,633) | - | (15,277,158) | (19,797,791) |
| 상각 | (42,511,897) | (26,175,183) | (6,511,549) | (75,198,629) |
| 기말 | 104,768,934 | 17,787,555 | 32,143,543 | 154,700,032 |
| 취득원가 | 313,336,841 | 202,315,365 | 43,773,162 | 559,425,368 |
| 감가상각누계액 | (208,567,907) | (184,527,810) | (11,629,619) | (404,725,336) |
(2) 당반기 및 전반기 중 리스와 관련해 손익으로 인식된 금액은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 |
|---|---|---|
| 사용권자산의 감가상각비 | ||
| 부동산 | 55,601,218 | 42,511,897 |
| 시설장치 | 10,305,743 | 26,175,183 |
| 차량운반구 | 5,422,958 | 6,511,549 |
| 합 계 | 71,329,919 | 75,198,629 |
| 리스부채에 대한 이자비용 | 19,863,076 | 9,046,680 |
| 단기리스료 | 36,000,000 | 15,560,000 |
| 단기리스가 아닌 소액자산 리스료 | 6,321,684 | 5,249,445 |
사용권자산의 당반기 중 리스의 총 현금유출은 71,925,480원(전반기: 103,629,070원)입니다.
(3) 보고기간 종료일 현재 리스부채 및 금융리스부채의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기말 | 전기말 | ||
|---|---|---|---|---|
| 최소리스료 | 최소리스료의 현재가치 |
최소리스료 | 최소리스료의 현재가치 |
|
| 1년 이내 | 143,850,960 | 135,789,973 | 48,840,000 | 46,514,819 |
| 1년 초과 5년 이내 | 251,057,945 | 200,271,137 | 69,054,545 | 58,723,176 |
| 합 계 | 394,908,905 | 336,061,110 | 117,894,545 | 105,237,995 |
(4) 보고기간 종료일 현재 리스부채 및 금융리스부채의 유동성분류 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기말 | 전기말 |
|---|---|---|
| 유동 | 135,789,973 | 46,514,819 |
| 비유동 | 200,271,137 | 58,723,176 |
| 합 계 | 336,061,110 | 105,237,995 |
(5) 회사는 당반기말 현재 연장 및 종료선택권을 포함하는 몇 개의 리스계약을 체결하고 있습니다. 이러한 선택권은 리스자산 포트폴리오의 관리에 유연성을 제공하고 회사의 사업요구에 맞추기 위하여 경영진에 의해 협상됩니다. 경영진은 이러한 연장 및 종료선택권이 행사될 것이 상당히 확실한지 여부를 결정할 때 중요한 판단을 적용합니다(주석3 참조).
12. 무형자산
당반기 및 전반기 중 무형자산 장부금액의 변동내역은 다음과 같습니다.
(1) 당반기
| (단위 : 원) |
| 구분 | 소프트웨어 | 특허권 | 합계 |
|---|---|---|---|
| 기초 | 130,502,885 | 98,955,594 | 229,458,479 |
| 취득 | 3,500,000 | - | 3,500,000 |
| 상각 | (20,730,224) | (10,682,340) | (31,412,564) |
| 정부보조금에 의한 상계 | 3,908,400 | - | 3,908,400 |
| 기말 | 117,181,061 | 88,273,254 | 205,454,315 |
| 취득원가 | 207,969,000 | 149,552,750 | 357,521,750 |
| 상각누계액 | (58,869,339) | (61,279,496) | (120,148,835) |
| 정부보조금 | (31,918,600) | - | (31,918,600) |
무형자산상각비 중 433,328원은 경상연구개발비에 포함되어 있습니다.
(2) 전반기
| (단위 : 원) |
| 구분 | 소프트웨어 | 특허권 | 합계 |
|---|---|---|---|
| 기초 | 27,303,696 | 120,320,274 | 147,623,970 |
| 취득 | 20,676,000 | - | 20,676,000 |
| 상각 | (4,906,464) | (10,682,340) | (15,588,804) |
| 기말 | 43,073,232 | 109,637,934 | 152,711,166 |
| 취득원가 | 63,236,000 | 149,552,750 | 212,788,750 |
| 상각누계액 | (20,162,768) | (39,914,816) | (60,077,584) |
13. 기타금융부채
보고기간 종료일 현재 기타금융부채의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기말 | 전기말 | ||
|---|---|---|---|---|
| 유동 | 비유동 | 유동 | 비유동 | |
| 미지급금 | 125,726,818 | 231,022,940 | 58,601,545 | 219,108,526 |
| 미지급비용 | 157,060,024 | - | 118,230,936 | - |
| 합 계 | 282,786,842 | 231,022,940 | 176,832,481 | 219,108,526 |
14. 기타유동부채
보고기간 종료일 현재 기타유동부채의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기말 | 전기말 |
|---|---|---|
| 예수금 | 69,781,680 | 76,094,690 |
| 선수금 | - | 7,600,000 |
| 합 계 | 69,781,680 | 83,694,690 |
15. 순확정급여부채
회사는 종업원을 위하여 부분적으로 확정급여형 퇴직급여제도를 운영하고 있습니다.이와 관련하여 확정급여채무의 보험수리적 평가는 예측단위적립방식을 사용하고 있습니다.
(1) 보고기간 종료일 현재 순확정급여부채의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기말 | 전기말 |
|---|---|---|
| 확정급여채무의 현재가치 | 1,488,431,033 | 1,266,767,114 |
| 사외적립자산의 공정가치 | (1,029,701,846) | (1,015,862,966) |
| 순확정급여부채 | 458,729,187 | 250,904,148 |
(2) 당반기 및 전반기 중 확정급여제도 관련 비용의 세부 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 | ||
|---|---|---|---|---|
| 3개월 (검토받지 않은 재무제표) |
누적 | 3개월 (검토받지 않은 재무제표) |
누적 | |
| 당기근무원가 | 127,938,306 | 170,378,010 | 42,439,704 | 84,879,408 |
| 과거근무원가 | 29,054,794 | - | (116,219,178) | (116,219,178) |
| 순이자손익 | (49,088,713) | 12,641,093 | 5,102,442 | 10,204,884 |
| 합 계 | 107,904,387 | 183,019,103 | (68,677,032) | (21,134,886) |
(3) 당반기 및 전반기 중 확정급여제도 관련 비용의 계정과목별 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 | ||
|---|---|---|---|---|
| 3개월 (검토받지 않은 재무제표) |
누적 | 3개월 (검토받지 않은 재무제표) |
누적 | |
| 판매비와관리비 | 57,247,996 | 125,908,637 | (77,362,680) | (38,506,182) |
| 경상연구개발비 | 50,656,391 | 57,110,466 | 8,685,648 | 17,371,296 |
| 합 계 | 107,904,387 | 183,019,103 | (68,677,032) | (21,134,886) |
16. 자본금 및 자본잉여금
(1) 보고기간 종료일 현재 회사의 자본금 및 자본잉여금의 내역은 다음과 같습니다.
| (단위: 주, 원) |
| 구분 | 당반기말 | 전기말 |
|---|---|---|
| 수권주식수 | 50,000,000 | 50,000,000 |
| 1주당 금액 | 500 | 500 |
| 발행보통주식수 | 15,223,000 | 15,223,000 |
| 보통주자본금 | 7,611,500,000 | 7,611,500,000 |
| 자본잉여금 | 48,888,442,989 | 48,888,442,989 |
(2) 당반기 및 전반기 중 자본금 및 자본잉여금의 변동내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 | ||
|---|---|---|---|---|
| 자본금 | 자본잉여금 | 자본금 | 자본잉여금 | |
| 기초 | 7,611,500,000 | 48,888,442,989 | 7,611,500,000 | 48,888,442,989 |
| 기말 | 7,611,500,000 | 48,888,442,989 | 7,611,500,000 | 48,888,442,989 |
17. 기타자본항목
(1) 보고기간 종료일 현재 기타자본의 내용은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기말 | 전기말 |
|---|---|---|
| 주식매수선택권 | 344,453,006 | 210,354,661 |
(2) 당반기 및 전반기 중 기타자본의 변동내용은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 |
|---|---|---|
| 기초 | 210,354,661 | 85,394,010 |
| 주식매수선택권의 인식 | 134,098,345 | 59,437,332 |
| 주식매수선택권의 상실 | - | (18,376,903) |
| 기말 | 344,453,006 | 126,454,439 |
(3) 주식기준보상제도
1) 주식기준보상 약정의 내용은 다음과 같습니다.
| (단위: 주) |
| 구분 | 대상자 | 부여일 | 부여수량 | 최장만기 | 결제방식 | 가득조건 |
|---|---|---|---|---|---|---|
| 2차 | 임직원 | 2021-03-25 | 4,500 | 2028-03-24 | 신주발행 | 2년간 의무 근무 |
| 4차 | 임직원 | 2022-02-07 | 4,500 | 2029-02-06 | 신주발행 | 2년간 의무 근무 |
| 5차 | 임직원 | 2022-07-15 | 4,500 | 2029-07-14 | 신주발행 | 2년간 의무 근무 |
| 6차 | 임직원 | 2023-02-23 | 16,000 | 2030-02-22 | 신주발행 | 2년간 의무 근무 |
2) 당반기 및 전반기 중 주식매수선택권 부여주식수의 변동내용은 다음과 같습니다.
(가) 당반기
| (단위: 주) |
| 구분 | 2차 | 4차 | 5차 | 6차 | 합계 |
|---|---|---|---|---|---|
| 기초 | 4,500 | 4,500 | 4,500 | - | 13,500 |
| 부여 | - | - | - | 16,000 | 16,000 |
| 기말 | 4,500 | 4,500 | 4,500 | 16,000 | 29,500 |
(나) 전반기
| (단위: 주) |
| 구분 | 2차 | 3차 | 4차 | 합계 |
|---|---|---|---|---|
| 기초 | 4,500 | 1,500 | - | 6,000 |
| 부여 | - | - | 4,500 | 4,500 |
| 상실 (주) | - | 1,500 | - | 1,500 |
| 기말 | 4,500 | - | 4,500 | 9,000 |
(주) 전반기 중 3차 부여분 1,500주가 가득기간 미충족으로 상실되었습니다.
3) 주식매수선택권의 공정가치 산정에 사용된 방법과 가정은 다음과 같습니다.
| (단위: 원) |
| 구분 | 2차 | 4차 | 5차 | 6차 |
|---|---|---|---|---|
| 가중평균주가 | 113,100 | 35,900 | 42,000 | 37,050 |
| 행사가격 | 118,712 | 42,274 | 41,940 | 36,185 |
| 기대주가변동성 | 30.60% | 43.64% | 50.75% | 68.61% |
| 옵션만기 | 7년 | 7년 | 7년 | 7년 |
| 기대배당금 | - | - | - | - |
| 무위험이자율 (주) | 1.74% | 2.60% | 3.25% | 3.69% |
| 공정가치 | 38,552 | 15,907 | 23,347 | 25,402 |
(주) 무위험이자율은 7년 만기 국고채 이자율을 이용하였습니다.
4) 당반기 및 전반기 중 보상원가의 내용은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 |
|---|---|---|
| 총비용 : | ||
| 주식결제형보상원가 | 134,098,345 | 41,060,429 |
보상원가 중 37,473,182원(전반기:43,014,526원)은 경상연구개발비에 포함되어 있습니다.
18. 영업부문
회사는 기업회계기준서 제1108호(영업부문)에 따른 보고부문이 단일 부문이므로 부문별 정보를 공시하지 않습니다.
19. 판매비와 관리비
당반기 및 전반기 중 판매비와 관리비의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 | ||
|---|---|---|---|---|
| 3개월 (검토받지 않은 재무제표) |
누적 | 3개월 (검토받지 않은 재무제표) |
누적 | |
| 급여 | 522,712,134 | 1,071,249,297 | 556,279,457 | 1,116,575,496 |
| 퇴직급여 | 57,247,996 | 125,908,637 | (77,362,680) | (38,506,182) |
| 인력개발비 | 2,550,000 | 5,100,000 | 3,100,000 | 6,100,000 |
| 복리후생비 | 69,293,428 | 138,271,422 | 110,273,715 | 171,538,049 |
| 여비교통비 | 17,340,545 | 31,284,010 | 11,638,294 | 16,669,880 |
| 접대비 | 15,681,583 | 40,128,533 | 3,690,470 | 6,381,426 |
| 통신비 | 1,436,824 | 3,013,228 | 1,133,025 | 2,405,914 |
| 수도광열비 | 286,176 | 775,272 | 180,000 | 345,000 |
| 전력비 | 11,311,324 | 23,920,072 | 11,760,877 | 24,880,387 |
| 세금과공과금 | 3,867,980 | 8,382,170 | 3,508,780 | 7,001,770 |
| 감가상각비 | 67,650,817 | 134,844,266 | 67,046,681 | 134,641,089 |
| 무형자산상각비 | 13,535,418 | 27,070,836 | 8,019,635 | 15,588,804 |
| 지급임차료 | 10,852,731 | 25,826,838 | 4,438,727 | 15,112,080 |
| 보험료 | 306,354 | 619,554 | 586,611 | 1,161,171 |
| 차량유지비 | 821,000 | 2,262,000 | 5,044,340 | 9,295,306 |
| 경상연구개발비 | 1,151,038,592 | 2,016,265,745 | 409,615,000 | 834,194,316 |
| 운반비 | 7,740 | 16,120 | 22,181 | 22,181 |
| 교육훈련비 | 58,610 | 528,610 | 1,897,500 | 2,057,500 |
| 도서인쇄비 | 966,996 | 6,204,857 | 475,046 | 1,727,735 |
| 회의비 | 744,094 | 754,096 | - | - |
| 사무용품비 | 1,499,092 | 1,499,092 | - | 394,000 |
| 소모품비 | 94,192,636 | 263,356,597 | 42,548,511 | 116,197,169 |
| 지급수수료 | 651,718,758 | 1,220,171,192 | 369,027,004 | 856,799,819 |
| 광고선전비 | 6,227,273 | 7,127,273 | 1,300,000 | 3,300,000 |
| 건물관리비 | 7,554,652 | 14,529,542 | 4,982,490 | 9,994,980 |
| 주식보상비용 | 63,674,292 | 96,625,163 | 10,378,301 | (1,954,097) |
| 협회비 | 1,339,452 | 3,357,452 | 123,156 | 4,627,743 |
| 합 계 | 2,773,916,497 | 5,269,091,874 | 1,549,707,121 | 3,316,551,536 |
20. 비용의 성격별 분류
당반기 및 전반기 중 비용(판매비와관리비)의 성격별 분류 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 | ||
|---|---|---|---|---|
| 3개월 (검토받지 않은 재무제표) |
누적 |
3개월 (검토받지 않은 재무제표) |
누적 |
|
| 종업원급여 | 963,123,780 | 1,910,067,520 | 609,034,653 | 1,348,753,591 |
| 감가상각비 | 131,274,118 | 266,959,180 | 139,909,274 | 279,550,825 |
| 경상연구개발비 | 695,328,468 | 1,133,768,063 | 185,008,443 | 375,585,777 |
| 기타 | 984,190,131 | 1,958,297,111 | 615,754,751 | 1,312,661,343 |
| 합 계 | 2,773,916,497 | 5,269,091,874 | 1,549,707,121 | 3,316,551,536 |
21. 금융수익 및 금융원가
(1) 당반기 및 전반기 중 금융수익의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 | ||
|---|---|---|---|---|
| 3개월 (검토받지 않은 재무제표) |
누적 | 3개월 (검토받지 않은 재무제표) |
누적 | |
| 이자수익 | 211,163,718 | 456,199,905 | 74,396,437 | 164,650,916 |
| 외환차익 | 389,717 | 389,717 | - | - |
| 합 계 | 211,553,435 | 456,589,622 | 74,396,437 | 164,650,916 |
(2) 당반기 및 전반기 중 금융원가의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 | ||
|---|---|---|---|---|
| 3개월 (검토받지 않은 재무제표) |
누적 | 3개월 (검토받지 않은 재무제표) |
누적 | |
| 이자비용 | 9,633,146 | 19,863,076 | 4,862,456 | 9,046,680 |
| 외환차익 | 10,347,750 | 10,347,750 | - | - |
| 합 계 | 19,980,896 | 30,210,826 | 4,862,456 | 9,046,680 |
22. 기타수익 및 기타비용
(1) 당반기 및 전반기 중 기타수익의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 | ||
|---|---|---|---|---|
| 3개월 (검토받지 않은 재무제표) |
누적 | 3개월 (검토받지 않은 재무제표) |
누적 | |
| 리스해지이익 | 436,990 | 436,990 | - | - |
| 보조금수익 | 87,351,372 | 125,029,722 | 157,391,256 | 179,529,516 |
| 잡이익 | 102,384 | 104,569 | 122,159 | 751,480 |
| 합 계 | 87,890,746 | 125,571,281 | 157,513,415 | 180,280,996 |
(2) 당반기 및 전반기 중 기타비용의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 | ||
|---|---|---|---|---|
| 3개월 (검토받지 않은 재무제표) |
누적 | 3개월 (검토받지 않은 재무제표) |
누적 | |
| 리스해지손실 | - | - | - | 4,210,240 |
| 기부금 | - | 20,000,000 | - | 23,000,000 |
| 잡손실 | 2 | 6,022 | 4 | 11 |
| 합 계 | 2 | 20,006,022 | 4 | 27,210,251 |
23. 법인세비용
당반기 및 전반기의 법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균 연간법인세율의 추정에 기초하여 인식하였습니다. 당반기 및 전반기에는 세무상결손금으로 인하여 부담세액이 발생하지 아니하였으며, 보고기간 종료일 현재 실현 가능성이 낮아 이연법인세자산을 인식하지 아니하였습니다.
24. 주당손실
(1) 기본주당손실
당반기 및 전반기 중 회사의 기본주당손실의 내역은 다음과 같습니다.
| (단위: 주,원) |
| 구분 | 당반기 | 전반기 | ||
|---|---|---|---|---|
| 3개월 (검토받지 않은 재무제표) |
누적 | 3개월 (검토받지 않은 재무제표) |
누적 | |
| 보통주반기순손실 | (2,494,453,214) | (4,737,147,819) | (1,322,659,729) | (3,007,876,555) |
| 가중평균유통보통주식수 (주) | 15,223,000 | 15,223,000 | 15,223,000 | 15,223,000 |
| 기본주당손실 | (164) | (311) | (87) | (198) |
(주) 당반기 및 전반기의 가중평균 유통보통주식수는 보고기간 종료일 현재 유통보통주식수와 동일합니다.
(2) 희석주당손실
회사는 희석성 잠재적 보통주로 보고기간 종료일 현재 주식매수선택권(미행사 주식수: 29,500주(전반기말: 9,000주))이 있으나, 반희석효과로 인하여 희석주당손익은 기본주당손익과 동일합니다.
25. 현금흐름표
(1) 당반기 및 전반기 중 영업활동에서 창출된 현금흐름의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 |
|---|---|---|
| 반기순손실 | (4,737,147,819) | (3,007,876,555) |
| 손익조정항목: | 174,806,973 | 163,671,176 |
| 이자수익 | (456,199,905) | (164,650,916) |
| 이자비용 | 19,863,076 | 9,046,680 |
| 감가상각비 | 134,844,266 | 134,641,089 |
| 무형자산상각비 | 27,070,836 | 15,588,804 |
| 퇴직급여 | 125,908,637 | (38,506,182) |
| 경상연구개발비 | 227,131,890 | 205,295,558 |
| 리스해지이익 | (436,990) | - |
| 리스해지손실 | - | 4,210,240 |
| 주식보상비용 | 96,625,163 | (1,954,097) |
| 자산부채 증감: | (108,791,320) | (676,018,674) |
| 기타금융자산의 감소 | 18,550 | 8,013,507 |
| 기타유동자산의 증가 | (209,826,215) | (40,984,988) |
| 기타비유동자산의 증가 | - | (90,560,000) |
| 기타금융부채의 증가 | 117,868,775 | 47,941,769 |
| 기타유동부채의 증가(감소) | (13,913,010) | 99,369,710 |
| 순확정급여부채의 감소 | (2,939,420) | (699,798,672) |
| 영업활동 창출 현금흐름 | (4,671,132,166) | (3,520,224,053) |
(2) 당반기 및 전반기 중 재무활동으로부터 발생하는 부채의 변동 내역은 다음과 같습니다.
1) 당반기
| (단위: 원) |
| 구분 | 기초 | 재무활동 현금흐름에서 발생한 변동 | 비현금흐름 변동 | 기말 | |
|---|---|---|---|---|---|
| 이자비용 | 기타 | ||||
| 리스부채 | 105,237,995 | (71,925,480) | 19,863,076 | 282,885,519 | 336,061,110 |
2) 전반기
| (단위: 원) |
| 구분 | 기초 | 재무활동 현금흐름에서 발생한 변동 | 비현금흐름 변동 | 기말 | |
|---|---|---|---|---|---|
| 이자비용 | 기타 | ||||
| 리스부채 | 220,435,405 | (103,629,070) | 9,046,680 | 60,191,986 | 186,045,001 |
(3) 당반기 및 전반기 중 현금유출입이 없는 주요 거래의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 |
|---|---|---|
| 리스부채의 유동성 대체 | 19,705,124 | 6,721,845 |
| 사용권자산의 증가 | 295,287,606 | 81,178,270 |
| 리스종료 및 해지 | 16,217,515 | - |
| 사용권자산의 감소 | - | 111,968,383 |
| 선급비용의 유동성 대체 | 9,680,884 | 50,860,172 |
26. 특수관계자 거래
(1) 당반기 및 전반기 중 회사의 주요 경영진에 대한 보상내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 당반기 | 전반기 |
|---|---|---|
| 단기급여 | 150,000,000 | 137,500,000 |
| 퇴직급여 | 33,249,396 | (79,070,316) |
| 합 계 | 183,249,396 | 58,429,684 |
주요 경영진은 회사의 회사활동의 계획, 운영 및 통제에 중요한 권한과 책임을 가진 임원들입니다.
(2) 당반기말 현재 회사는 법인카드 사용과 관련하여 486,000,000원을 한도로 대표이사로부터 지급보증을 제공받고 있습니다.
27. 우발상황 및 약정사항
(1) 당반기말 현재 회사가 피고로서 계류중인 중요한 소송사건은 없습니다.
(2) 당반기말 현재 회사가 가입한 보험가입내용은 다음과 같습니다.
| (단위: 원) |
| 구분 | 가입처 | 부보자산 | 부보금액 |
|---|---|---|---|
| 화재보험 | 한화손해보험 | 본사 및 연구소 공구와기구 외 | 2,886,443,658 |
| 임상시험 배상책임보험 |
KB손해보험 | 행성 간세포암 환자에서 자연살해세포와 간동맥주입화학요법 병합치료의 임상 2a 상 연구 20명 | 500,000,000 |
28. 재무구조 개선 계획
회사는 신약 연구 및 개발 과정에 있어 제품이나 상품의 매출이 발생하지 않았고, 당반기말 현재 누적 결손금이 381억원이며, 부의 영업현금흐름이 지속되고 있어 재무 구조의 개선이 요구됩니다. 다만, 회사가 확보한 자금으로 단기간 회사의 존속에는 큰 영향을 미치지 못할 것으로 예상하고 있으며, 재무구조상 위험요소는 크지 않다고판단하고 있습니다.
회사는 재무구조의 개선을 위해 신약 파이프라인의 연구개발과 임상시험에 모든 역량을 집중하고 있고, 자체제조 및 판매와 기술이전(license-out : L/O)을 통한 상업화를 계획하고 있습니다. 또한, 회사의 모든 프로젝트가 연구개발 단계로서 진척에 속도를 높혀 상업화 시기를 앞당기고자 우수인력의 채용, 연구개발 기자재 확충, 신속한 임상연구 진행을 위해 거점병원 추가에 힘쓰고 있습니다.
현재 진행중인 각 파이프라인 별 판매전략은 다음과 같습니다.
| 파이프라인 | 진행 단계 |
제조와 판매 전략 |
라이선스 아웃 전략 |
|---|---|---|---|
| Vax-NK/HCC |
임상2a상 |
1. 간세포암종을 목표질환으로 Vax-NK를 한국에서 직영생산 및 판매 2. Vax-NK를 아시아국가에서 현지 위탁 생산 및 판매 |
임상 3상 혹은 조건부허가 진행하며 해외 L/O 동시 진행 |
| Vax-NK/PDAC |
비임상 |
진행성췌장암을 목표질환으로 Vax-NK를 한국에서 직영생산 및 판매 | 임상 3상 혹은 조건부 허가 진행하며 해외 L/O 동시 진행 |
|
Vax-CAR |
비임상 |
- |
난치성 고형암 및 혈액암을 목표질환으로 여러 개의 항원수용체(MSLN, EphA2, PD-L1) 적용 CAR-T/NK세포치료제, 그리고 다발골수종을 대상으로 한 CAR-T, CAR-MILs 치료제 각각에 대하여 글로벌 라이선스 아웃 |
|
박스루킨-15 |
임상연구 진행 중 |
동물(개)의 암을 목표질환으로 제조 및 판매에 대한 로열티 수취 |
동물(개)의 암을 목표질환으로 |
한편, 회사는 2020년 9월 22일 코스닥시장에 상장하였으며, 기술성장특례 적용 기업입니다. 관리종목 지정 요건과 관련하여, 매출액 요건의 경우 신규상장일이 속하는 사업연도(상장 후 사업연도말까지 3월 미만인 경우 다음 사업연도)를 포함한 연속하는 5개 사업연도, 세전이익 요건의 경우 신규상장일이 속하는 사업연도(상장 후 사업연도말까지 3월 미만인 경우 다음 사업연도)를 포함한 연속하는 3개 사업연도에 대해서는 해당 요건을 적용 받지 않습니다(영업이익 요건은 유예기간 없이 적용 면제).
회사의 재무제표는 자산과 부채가 정상적인 영업활동 및 재무구조 개선계획 실행 과정을 통하여 회수되거나 상환될 수 있다는 가정 하에 회계처리 되었으나, 부채상환 및 기타 자금수요를 위해 필요한 자금조달 계획과 안정적인 경상이익 달성을 위한 재무 및 경영개선계획의 성패에 따라 재무상태와 경영성과가 큰 폭으로 변동될 가능성이 있습니다. 만일 이러한 계획에 차질이 발생하는 경우, 회사의 자산과 부채를 정상적인 영업활동 과정을 통하여 장부금액으로 회수하거나 상환하지 못 할 수 있으며, 회사의 재무제표에는 이러한 불확실성으로 발생할 수도 있는 자산과 부채의 금액 및 분류표시와 관련 손익항목에 대한 조정사항이 반영되어 있지 않습니다.
6. 배당에 관한 사항
가. 배당에 관한 사항
당사는 별도의 배당에 관한 정책이 정해져있지 않으며, 정관에 따라 각 결산기 주주총회 결의를 통해 배당을 결정합니다.
당사의 정관상 배당에 관한 사항은 다음과 같습니다.
| 제53조(이익금의 처분) 회사는 매사업년도의 처분전 이익잉여금을 다음과 같이 처분한다. 1. 이익준비금 2. 기타의 법정준비금 3. 배당금 4. 임의적립금 5. 기타의 이익잉여금처분액 제54조(이익배당) ① 이익의 배당은 금전 또는 금전 외의 재산으로 할 수 있다. ② 이익의 배당을 주식으로 하는 경우 회사가 종류 주식을 발행한 때에는 주주총회의 결의로 그와 다른 종류의 주식으로도 할 수 있다. ③ 제1항의 배당은 매결산기말 현재의 주주명부에 기재된 주주 또는 등록된 질권자에게 지급한다. ④ 이익배당은 주주총회의 결의로 정한다 |
나. 주요배당지표
| 구 분 | 주식의 종류 | 당기 | 전기 | 전전기 |
|---|---|---|---|---|
| 제14기 상반기 | 제13기 | 제12기 | ||
| 주당액면가액(원) | 500 | 500 | 500 | |
| (연결)당기순이익(백만원) | - | - | - | |
| (별도)당기순이익(백만원) | -4,765 | -6,825 | -4,763 | |
| (연결)주당순이익(원) | -311 | -448 | -315 | |
| 현금배당금총액(백만원) | - | - | - | |
| 주식배당금총액(백만원) | - | - | - | |
| (연결)현금배당성향(%) | - | - | - | |
| 현금배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주식배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주당 현금배당금(원) | - | - | - | - |
| - | - | - | - | |
| 주당 주식배당(주) | - | - | - | - |
| - | - | - | - | |
다. 과거 배당 이력
| (단위: 회, %) |
| 연속 배당횟수 | 평균 배당수익률 | ||
|---|---|---|---|
| 분기(중간)배당 | 결산배당 | 최근 3년간 | 최근 5년간 |
| - | - | - | - |
7. 증권의 발행을 통한 자금조달에 관한 사항
7-1. 증권의 발행을 통한 자금조달 실적
가. 증자(감자)현황
| (기준일 : | 2023년 6월 30일 | ) | (단위 : 원, 주) |
| 주식발행 (감소)일자 |
발행(감소) 형태 |
발행(감소)한 주식의 내용 | ||||
|---|---|---|---|---|---|---|
| 종류 | 수량 | 주당 액면가액 |
주당발행 (감소)가액 |
비고 | ||
| 2018년 03월 14일 | 유상증자(제3자배정) | 종류주식(*) | 20,000 | 5,000 | 75,000 | 3자배정 |
| 2018년 03월 29일 | 유상증자(제3자배정) | 종류주식(*) | 13,400 | 5,000 | 75,000 | 3자배정 |
| 2018년 05월 29일 | 유상증자(제3자배정) | 종류주식(*) | 20,000 | 5,000 | 75,000 | 3자배정 |
| 2018년 05월 31일 | 유상증자(제3자배정) | 종류주식(*) | 40,000 | 5,000 | 75,000 | 3자배정 |
| 2018년 06월 01일 | 유상증자(제3자배정) | 종류주식(*) | 40,000 | 5,000 | 75,000 | 3자배정 |
| 2018년 06월 02일 | 유상증자(제3자배정) | 종류주식(*) | 26,666 | 5,000 | 75,000 | 3자배정 |
| 2019년 05월 11일 | 주식분할 | 보통주식 | 3,190,500 | 500 | - | 주식의 액면분할(1:10) |
| 2019년 05월 11일 | 주식분할 | 종류주식(*) | 2,520,594 | 500 | - | 주식의 액면분할(1:10) |
| 2019년 09월 16일 | 전환권행사 | 보통주식 | 2,800,660 | 500 | - | 전환권 행사로 인한 보통주 증가 |
| 2019년 09월 16일 | 전환권행사 | 종류주식(*) | 2,800,660 | 500 | - | 전환권 행사로 인한 종류주식 감소 |
| 2019년 11월 20일 | 유상증자(제3자배정) | 보통주식 | 162,625 | 500 | 8,000 | - |
| 2020년 09월 16일 | 유상증자(일반공모) | 보통주식 | 985,160 | 500 | 30,000 | 코스닥 상장 일반공모(모집) |
| 2020년 09월 16일 | 유상증자(제3자배정) | 보통주식 | 29,555 | 500 | 30,000 | 코스닥상장 상장주관사 의무인수 |
| 2021년 01월 04일 | 무상증자 | 보통주식 | 7,523,000 | 500 | 500 | 1주당 1주의 비율로 신주 배정 |
| 2021년 03월 29일 | 주식매수선택권행사 | 보통주식 | 177,000 | 500 | - | - |
(*) 발행된 종류주식은 종류주식 1주당 보통주식 1주로 전환할 수 있는 전환권과, 회사의 이익잉여금 내에서 상환을 청구할수 있는 상환권이 부여되고, 참가적 누적적으로 1%의 배당 우선권을 가지는 우선주입니다(전환상환우선주).
(*) 2018년 발행한 종류주식은 2019년 9월 16일 모두 전환권이 행사되어 현 보고서 작성 기준일 상 발행된 종류주식은 없습니다.
| [채무증권의 발행 등과 관련된 사항] |
채무증권 발행실적
| (기준일 : | 2023년 6월 30일 | ) | (단위 : 원, %) |
| 발행회사 | 증권종류 | 발행방법 | 발행일자 | 권면(전자등록)총액 | 이자율 | 평가등급 (평가기관) |
만기일 | 상환 여부 |
주관회사 |
|---|---|---|---|---|---|---|---|---|---|
| - | - | - | - | - | - | - | - | - | - |
| - | - | - | - | - | - | - | - | - | - |
| 합 계 | - | - | - | - | - | - | - | - | - |
기업어음증권 미상환 잔액
| (기준일 : | 2023년 6월 30일 | ) | (단위 : 원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
1년초과 2년이하 |
2년초과 3년이하 |
3년 초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | |
단기사채 미상환 잔액
| (기준일 : | 2023년 6월 30일 | ) | (단위 : 원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
합 계 | 발행 한도 | 잔여 한도 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
회사채 미상환 잔액
| (기준일 : | 2023년 6월 30일 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
신종자본증권 미상환 잔액
| (기준일 : | 2023년 6월 30일 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 5년이하 |
5년초과 10년이하 |
10년초과 15년이하 |
15년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
조건부자본증권 미상환 잔액
| (기준일 : | 2023년 6월 30일 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | - | |
7-2. 증권의 발행을 통해 조달된 자금의 사용실적
가. 공모자금의 사용내역
| (기준일 : | 2023년 06월 30일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 증권신고서 등의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
| 코스닥 상장 공모(모집) |
1회 | 2020년 09월 15일 | 연구개발비, 임상시험비 등 연구자금 |
18,543 | 기타자금 (연구개발, 임상시험 등) |
7,629 |
자금의 사용이 완료되지 않았으며, 미사용자금은 안정성 있는 예적금 위주의 금융상품에 보관예정입니다. 미사용 자금은 자금의 사용계획에 맞추어 기타자금(연구개발비,임상시험비)으로 사용 예정입니다. |
| 코스닥 상장 공모(모집) |
1회 | 2020년 09월 15일 | 운영자금 | 9,796 | 운영자금 |
5,882 |
자금의 사용이 완료되지 않았으며, 미사용자금은 안정성 있는 예적금 위주의 금융상품에 보관예정입니다. 미사용 자금은 자금의 사용계획에 맞추어 운영자금으로 사용 예정입니다. |
| 코스닥 상장 공모(모집) |
1회 | 2020년 09월 15일 | 시설자금 | 965 | - | - | - |
(*) 당사는 본 보고서 작성기준일 이후 2023년 8월 7일 이사회에서 주주배정 후 실권주 일반공모 유상증자에 대한 결정을 하였습니다. 자세한 사항은 2023년 8월 7일 금융감독원 전자공시시스템에 공시한 [주요사항보고서(유무상증자결정)]을 참고해주시기 바랍니다.
나. 사모자금의 사용내역
| (기준일 : | 2023년 6월 30일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 주요사항보고서의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
| 제3자배정 유상증자 |
10회 | 2020.09.15 | 연구개발비, 운영자금, 시설자금 |
886 | 연구개발비, 운영 자금, 시설자금 |
886 | 코스닥 상장 상장 주선인 의무인수분 |
주) 2022년도 반기 사업보고서 작성기준일까지 기존 자금사용 계획대로 연구개발자금과 설비투자 및 운영자금으로 모두 사용하였습니다.
다. 미사용자금의 운용내역
| (기준일 : | 2023년 6월 30일 | ) | (단위 : 백만원) |
| 종류 | 금융상품명 | 운용금액 | 계약기간 | 실투자기간 |
|---|---|---|---|---|
| 예ㆍ적금 |
보통예금 |
81 |
- |
- |
| 예ㆍ적금 |
MMF |
712 |
- |
- |
| 예ㆍ적금 |
정기예금 |
5,000 |
2022년 11월 ~ 2023년 11월 |
8개월 |
| 예ㆍ적금 |
정기예금 |
2,000 |
2022년 11월 ~ 2023년 08월 |
8개월 |
| 예ㆍ적금 |
정기예금 |
5,000 |
2022년 11월 ~ 2023년 11월 |
8개월 |
| 예ㆍ적금 |
정기예금 |
1,000 |
2023년 05월 ~ 2023년 07월 |
2개월 |
| 예ㆍ적금 |
정기예금 |
1,500 |
2023년 05월 ~ 2023년 08월 |
2개월 |
| 예ㆍ적금 |
정기예금 |
500 |
2023년 06월 ~ 2023년 09월 |
1개월 |
| 계 | 15,793 | - | ||
8. 기타 재무에 관한 사항
가. 재무제표 재작성 등의 유의사항
(1) 재무제표 재작성
- 당사는 보고서 작성기준일 현재 해당사항 없습니다.
(2) 합병, 분할, 자산양수도, 영업양수도
- 당사는 보고서 작성기준일 현재 해당사항 없습니다.
(3) 자산유동화와 관련한 자산매각의 회계처리 및 우발채무 등에 관한 사항
- 당사는 자산유동화와 관련한 자산매각이 발생하지 않았으며 우발채무 등에 관한 사항은「III. 재무에 관한 사항 → 5. 재무제표 주석 → 27. 우발상황 및 약정사항」을 참조하시기 바랍니다.
나. 대손충당금 현황
- 보고기간 기준일 현재 당사는 대손충당금 대상 자산이 존재하지 않아 대손충당금 설정 현황 및 변동내역이 없습니다.
다. 재고자산 현황
- 보고기간 기준일 현재 당사는 재고자산이 존재하지 않아 해당사항이 없습니다.
라. 공정가치 평가 내역
- 보고기간 종료일 현재 회사의 금융상품은 모두 상각후원가로 측정하는 금융자산 및 금융부채로 분류하고 있어 공정가치로 측정되는 금융상품은 없습니다.
IV. 회계감사인의 감사의견 등
1. 외부감사에 관한 사항
가. 회계감사인의 명칭 및 감사의견
| 사업연도 | 감사인 | 감사의견 | 강조사항 등 | 핵심감사사항 |
|---|---|---|---|---|
| 2023년 (제14기 반기 검토) | 신한회계법인 | 적정 | 해당사항 없음 | (주) |
| 2022년 (제13기) | 신한회계법인 | 적정 | 해당사항 없음 | 현금및현금성자산과 금융상품의 실재성 |
| 2021년 (제12기) | 신한회계법인 | 적정 | 해당사항 없음 | 현금및현금성자산과 금융상품의 실재성 |
(주) 보고서 작성기준일 현재 제14기(2023년) 상반기 검토가 진행 되었고 감사는 진행되지 아니하여 핵심감사사항은 기재하지 아니하였습니다.
2. 감사용역 체결현황
| 사업연도 | 감사인 | 내 용 | 감사계약내역 | 실제수행내역 | ||
|---|---|---|---|---|---|---|
| 보수 | 시간 | 보수 | 시간 | |||
| 2023년 (제14기) | 신한회계법인 | 재무제표 검토 및 감사 | 60,000 | 622 | (주) |
(주) |
| 2022년 (제13기) | 신한회계법인 | 재무제표 검토 및 감사 | 60,000 | 622 | 60,000 | 622 |
| 2021년 (제12기) | 신한회계법인 | 재무제표 검토 및 감사 | 60,000 | 613 | 60,000 | 613 |
(주) 보고서 작성기준일 현재 제14기(2023년) 사업연도에 대한 감사는 진행되지 아니하여 기재하지 아니하였습니다.
3. 회계감사인과의 비감사용역 계약체결 현황
| 사업연도 | 계약체결일 | 용역내용 | 용역수행기간 | 용역보수 | 비고 |
|---|---|---|---|---|---|
| 2023년 (제14기) | - | - | - | - | - |
| 2022년 (제13기) | - | - | - | - | - |
| 2021년 (제12기) | - | - | - | - | - |
4. 내부감사기구가 회계감사인과 논의한 결과
| 구분 | 일자 | 참석자 | 방식 | 주요 논의 내용 |
|---|---|---|---|---|
| 1 | 2022년 11월 11일 | 회사 : 감사 및 경영관리본부장 감사인 : 담당이사외 1명 |
서면회의 | 감사범위와 시기 등 감사계획 |
| 2 | 2023년 02월 15일 | 회사 : 감사 및 경영관리본부장 감사인 : 담당이사외 1명 |
서면회의 | 핵심감사사항, 기말감사 수행결과 논의 |
2. 내부통제에 관한 사항
가. 내부통제
- 내부통제에 대한 특이사항 없음.
나. 내부회계관리제도
- 회계감사인의 내부회계관리제도 검토의견
| 사업연도 | 감사인 | 내부회계관리제도 검토의견 | 지적사항 |
|---|---|---|---|
| 제14기 | 신한회계법인 | (주) | (주) |
| 제13기 | 신한회계법인 | 경영자의 내부회계관리제도 운영실태보고서에 대한 우리의 검토결과, 상기 경영자의운영실태보고 내용이 중요성의 관점에서 내부회계관리제도 모범규준 제5장 '중소기업에 대한 적용'의 규정에 따라 작성되지 않았다고 판단하게 하는 점이 발견되지 아니하였습니다. |
- |
| 제12기 | 신한회계법인 | 경영자의 내부회계관리제도 운영실태보고서에 대한 우리의 검토결과, 상기 경영자의운영실태보고 내용이 중요성의 관점에서 내부회계관리제도 모범규준 제5장 '중소기업에 대한 적용'의 규정에 따라 작성되지 않았다고 판단하게 하는 점이 발견되지 아니하였습니다. | - |
(주)보고서 작성기준일 현재 제14기(2023년) 사업연도에 대한 감사는 진행되지 아니하여 기재하지 아니하였습니다.
다. 내부통제구조의 평가
- 공시대상기간에 내부회계관리제도 이외의 내부통제구조를 평가받은 사실이 없습니다.
V. 이사회 등 회사의 기관에 관한 사항
1. 이사회에 관한 사항
가. 이사회 구성 개요
(1) 이사의 수 및 이사회의 구성 현황
당사의 이사회는 등기이사 전원으로 구성하고, 법령 또는 정관에 정하여진 사항, 주주총회로부터 위임받은 사항, 회사경영의 기본방침 및 업무집행에 관한 중요사항을 의결하며 이사 및 경영진의 직무의 집행을 감독하고 있습니다.
작성기준일 기준 당사의 이사회는 총 3명(사내이사 2명, 사외이사 1명)으로 구성되어 있으며, 이제중 대표이사가 이사회 의장을 겸직 하고 있으며 이사회 내 별도의 위원회는 구성되어 있지 않습니다.
당사 각 이사의 주요 이력 및 업무분장은 'VIII. 임원 및 직원 등에 관한 사항의 '1. 임원 및 직원 등의 현황'을 참조하시기 바랍니다.
(2) 이사회의 권한 내용
|
구 분 |
조 항 |
|---|---|
|
권한 |
제3조 (이사회의 권한) ① 이사회는 법령 또는 정관에 정하여진 사항, 주주총회로부터 위임받은 사항, 회사경영의 기본방침 및 업무집행에 관한 중요사항을 의결한다. ② 이사회는 이사의 직무집행을 감독한다. 제12조 (이사의 직무집행에 대한 감독권) ① 이사회는 각 이사가 직무를 집행함에 있어 법령 또는 정관에 위반하거나 현저히 부당한 방법으로 처리하거나, 처리할 염려가 있다고 인정한 때에는 해당이사에 대하여 관련자료의 제출, 조사 및 설명을 요청할 수 있다. ② 전항에 의하여 감독권을 행사한 이사회는 해당직무에 대하여 그 집행을중지 또는 변경하도록 요구할 수 있다. |
|
결의사항 |
제9조 (이사회의 결의사항) ① 이사회에서 결의할 사항은 다음 각 호와 같다. 단, 긴급한 사안에 대하여 이사회를 즉시 개최할 수 없는 경우에 는 대표이사가 집행 후 지체없이 이사회의 승인을 얻어야 한다. 1. 주주총회 소집 및 안건에 관한 사항 2. 영업보고서 및 재무제표 승인(온기 및 반기 재무제표를 포함) 3. 중간배당에 관한 사항(중간배당의 유무, 배당금액, 지급일, 기타 필요한 모든 사항) 4. 이사 등에 관한 사항 가. 대표이사의 선임 및 해임 나. 사장, 부사장, 전무이사, 상무이사 및 이사의 직함에 관한 자의 선임 및 해임 다. 이사들 사이에서의 대표이사 직무대행 순서 결정(정관에 규정이 있다면 이를 따른다) 라. 이사의 개인별 보수액, 상여금의 분배 마. 이사의 경업거래 승인 바. 회사와 이사 간의 거래 승인 사. 경쟁 타사의 임원 취임 승인 5. 주식 등에 관한 사항 가. 신주 발행 나. 사채, 전환사채 및 신주인수권부사채 발행 다. 기준일의 설정 라. 자기주식 취득 6. 업무집행에 관한 중요사항 가. 업무의 일부양도, 양수 중 중요한 것 나. 자회사, 지점, 영업소 등의 신설, 이전, 확장, 축소 및 폐지 중 10억원 이상의 지출을 수반한 것 다. 계약의 체결, 개폐 중 거래금액이 10억원 이상의 것 또는 경영상 특히 중요한 것 라. 소송 처리 중 소송액이 10억원 이상의 것 마. 인사 결정 중 중요한 것 바. 규정의 제정, 개폐 중 중요한 것 7. 자산 또는 재무에 관한 중요 사항(10억원 이상의 자금 등을 필요로 하는 것 또는 경영상 특히 중요한 것 가. 고정자산(토지 및 건물 포함)의 취득 처분, 임대차 나. 유가증권의 취득 처분 다. 특허권 기타 공업소유권 등 지적재산권의 취득 처분 라. 회사 자산에 대한 저당권, 질권 등 담보 설정 마. 차입금 바. 대출금 또는 신용공여(미수금, 선급금, 선급비용 등) 사. 부실채권처리 아. 재고자산처분 (불량품의 상각 및 평가손) 자. 기채·자금 운용 8. 연결자회사에 관한 중요 사항 가. 회사의 합병, 해산 나. 신회사(자회사)의 설립, 해산 중 10억원 이상의 지출 등을 필요로 하는 것 다. 증자, 감자, 사채 발행 라. 중요 자산의 취득, 처분 마. 계약의 체결, 개폐 중 거래금액이 10억원 이상인 것 바. 1건당 액수가 10억원 이상의 자금 대출, 차입, 채무보증, 담보제공 사. 경영참여를 목적으로 하거나 1건당 액수가 10억원 이상인 유가증권의취득, 처분 아. 중요 소송 자. 중요 지적재산권의 취득, 처분 9. 신규사업계획에 관한 사항 10. 장단기 경영계획 및 연도별 사업계획에 관한 사항 11. 계열회사 및 관계회사와의 거래 (회사의 입장에서 제3자와의 거래와 비교해 유리하지 않은 조건의 경우) 12. 합작법인의 설립, 전략적 제휴 및 파트너쉽 취득에 관한 사항(1건의 투자금액이 5억원을 초과하는 경우와 13. 사업부문 이상의 조직개편에 관한 사항 14. 회사의 타인을 위한 보증 15. 기타 의장이 특별히 부의하는 사항 ② 전항 이외의 사항은 대표이사에게 위임하여 집행하도록 한다. |
|
보고사항 |
제10조 (이사회 보고사항) 이사회에 보고하여야 할 사항은 다음과 같다. ① 이사가 법령 또는 정관에 위반한 행위를 하거나 그 행위를 할 염려가 있다고 감사가 인정한 사항 ② 기타 경영상 중요한 업무집행에 관한 사항 |
(3) 이사회 운영규정의 주요내용
|
구 분 |
조 항 |
|---|---|
|
이사회의 구성 |
제4조 (이사회의 구성) ① 이사회는 이사로서 구성된다(사외이사 포함). ② 감사는 이사회에 출석하여 의견을 진술할 수 있으나 결의에는 참가하지 못한다. 제6조 (의장) ① 이사회의 의장은 본 규정 제5조에 의한 이사회의 소집권자로 한다. ② 대표이사 유고시에는 정관 제35조를 준용한다. 제11조 (관계인의 출석) 의장은 필요하다고 인정할 경우에는 관계 임직원 또는 외부인사를 출석시켜 의견을 청취할 수 있다. |
|
이사회의 소집 |
제5조 (소집권자) ① 이사회의 소집권자는 대표이사 또는 이사회에서 따로 정한 이사가 있을 때에는 그 이사로 한다. ② 전항의 소집권자 이외의 이사는 소집권자인 이사에게 이사회 소집을 요구할 수 있으며, 소집권자인 이사가 정당한 사유없이 이를 거부할 경우 다른 이사가 이사회를 소집할 수 있다. ③ 감사는 필요한 경우 회의의 목적사항과 소집이유를 적은 서면을 본조 제1항의 소집권자에게 제출하여 이사회 소집을 청구할 수 있다. ④ 전항의 청구에도 불구하고 이사가 지체 없이 이사회를 소집하지 아니하면 그 청구한 감사가 이사회를 소집할 수 있다. 제7조(소집절차) ① 이사회를 소집함에는 회일을 정하고 그 1일전에 각 이사 및 감사에대하여 통지를 발송하여야 한다. ② 이사회는 이사 및 감사 전원의 동의가 있는 때에는 전항의 절차 없이 언제든지 회의를 열수 있다. |
|
결의방법 |
제8조 (결의방법) ① 이사회의 결의는 이사 과반수의 출석과 출석이사 과반수로 한다. ② 이사회는 이사가 직접 이사회에 참석하여야 한다. 다만 이사의 전부 또는 일부가 직접 회의에 출석하지 아니하고 모든 이사가 동영상 및 음성을 동시에 송, 수신하는 통신수단에 의하여 결의에 참가할 수 있으며, 이 경우 당해 이사는 이사회에 직접 출석한 것으로 본다. ③ 이사회의 결의에 관하여 특별한 이해관계가 있는 이사는 의결권을 행사하지 못한다. ④ 전항에 의하여 의결권을 행사할 수 없는 이사의 수는 출석한 이사의 수에 산입하지 아니한다. |
|
이사회의 의사록 |
제13조 (의사록) ① 이사회의 의사에 관하여는 의사록을 작성한다. ② 의사록에는 의사의 안건, 경과요령, 그 결과, 반대하는 자와 그 반대 이유를 기재하여 출석한 이사 및 감사가 기명날인 또는 서명한다. ③ 주주는 영업시간 내에 이사회 의사록의 열람 또는 등사를 청구할 수 있다. ④ 회사는 전항의 청구에 대하여 이유를 붙여 이를 거절할 수 있다. 이경우 주주는 법원의 허가를 얻어 이사회 의사록을 열람 또는 등사할 수 있다. |
나. 중요 의결사항 등
|
개최일자 |
의 안 내 용 |
가결 |
찬성/ |
이사의 성명 |
감사 |
|||
|---|---|---|---|---|---|---|---|---|
| 이제중 (출석률:100%) |
이준행 (출석률:100%) |
정성창 (출석률:100%) |
(*)임신혁 (출석률:100%) |
|||||
| 찬반여부 | ||||||||
| 2022.02.07. | 1. 제12기 재무제표 승인의 건 | 가결 | 4/4 | 찬성 | 찬성 | 찬성 | 찬성 | 참석 |
| 2022.02.07. | 2. 주식매수선택권 부여의 건 | 가결 | 4/4 | 찬성 | 찬성 | 찬성 | 찬성 | 참석 |
| 2022.03.08. | 1. 제12기 정기주주총회 소집의 건 | 가결 | 4/4 | 찬성 |
찬성 | 찬성 | 찬성 | 불참 |
| 2022.03.08. | 2. 전자투표 도입 승인의 건 | 가결 | 4/4 | 찬성 | 찬성 | 찬성 | 찬성 | 불참 |
| 2022.03.28. | 1. 대표이사 선임의 건 | 가결 | 4/4 | 찬성 | 찬성 | 찬성 | 찬성 | 참석 |
| 2022.07.15. | 1. 주식매수선택권 부여 취소의 건 | 가결 | 3/3 | 찬성 | 찬성 | 찬성 | - | 참석 |
| 2022.07.15. | 2. 주식매수선택권 부여의 건 | 가결 | 3/3 | 찬성 | 찬성 | 찬성 | - | 참석 |
| 2022.12.15. | 1. 명부폐쇄 기준일 설정의 건 | 가결 | 3/3 | 찬성 | 찬성 | 찬성 | - | 참석 |
| 2023.02.23 | 1. 제13기 재무제표 승인의 건 | 가결 | 3/3 | 찬성 | 찬성 | 찬성 | - | 참석 |
| 2023.02.23 | 2. 2022년도 (제13기)영업보고서 승인의 건 | 가결 | 3/3 | 찬성 | 찬성 | 찬성 | - | 참석 |
| 2023.02.23 | 3. 제13기 정기주주총회 개최 및 총회 목적사항 결정에 대한 건 | 가결 | 3/3 | 찬성 | 찬성 | 찬성 | - | 참석 |
| 2023.02.23 | 4. 전자투표제도 도입 승인의건 | 가결 | 3/3 | 찬성 | 찬성 | 찬성 | - | 참석 |
| 2023.02.23 | 5. 주식매수선택권 부여에 대한 건 | 가결 | 3/3 | 찬성 | 찬성 | 찬성 | - | 참석 |
| 2023.03.08 | 1. 제13기 정기주주총회 소집의 건 | 가결 | 3/3 | 찬성 | 찬성 | 찬성 | - | 참석 |
| 2023.08.07 | 1. 유상증자 시행의 건 | 가결 | 3/3 | 찬성 | 찬성 | 찬성 | - | 참석 |
| 2023.08.07 | 2. 무상증자 시행의 건 | 가결 | 3/3 | 찬성 | 찬성 | 찬성 | - | 참석 |
| (*) 기타비상무이사 임신혁의 경우 2022년 5월 13일 사임하였습니다. |
다. 이사의 독립성
(1) 이사의 선임
이사의 후보자는 이사회 결정으로 추천하고 주주총회의 결의로 선임하고 있습니다. 이사회 의장은 정관에 의하여 결정되며 작성기준일 현재 당사의 이사회 의장은 이제중 대표이사가 맡고 있습니다.
당사는 회사 경영의 중요한 의사결정과 업무집행을 이사회의 심의 및 의결을 통하여 수행하고 있으며, 대주주 등의 독단적인 경영과 이로인한 소액주주의 이익침해가 발생하지 않도록 이사회규정을 제정하여 성실히 준수하고 있습니다.
(2) 이사의 현황
작성기준일 현재 당사의 이사 현황은 다음과 같습니다.
| 구분 | 성명 | 추천인 | 선임배경 | 임기 (연임여부) |
담당업무 | 회사와의 거래 |
최대주주 등과의 관계 |
|---|---|---|---|---|---|---|---|
| 대표이사 | 이제중 | 이사회 | 당사의 공동창업자이자 현 대표이사로서 사업에 대한충분한 이해도와 전문성으로 면역세포치료제 제조 및 임상시험업무를 총괄하기 위함 | 22.03~25.03 (중임) |
대표이사 (경영총괄) |
해당없음 | 본인 |
| 사내이사 | 이준행 | 이사회 | 공동창업자로서 다년간 쌓아온 경험과 지식을 바탕으로 회사의 성장을 이끌었으며, 사업에 대한 이해도와 전문성으로 경영을 총괄하기 위함 | 22.03~25.03 (중임) |
연구총괄 | 해당 없음 | 타인 |
| 사외이사 | 정성창 | 이사회 | 내부통제 및 재무관련 업무에 다양한 경험을 가지고 있으며, 당사의 업무에 독립적인 자격으로 경영지원과 감독활동을 하기 위함 | 22.03~25.03 (중임) |
경영 자문 |
해당없음 | 타인 |
| (*) 기타비상무이사 임신혁은 2022년 5월 13일 사임하였습니다. |
라. 사외이사 현황
(1) 작성기준일 현재 당사의 사외이사는 다음과 같습니다.
|
성명 |
주요경력 |
최대주주등과의 |
결격요건 |
비고 |
|---|---|---|---|---|
|
정성창 |
83.02 전남대학교 경영대학 경영학 학사 85.02 서울대학교 경영학 석사 90.07 Georgia State University 경영학 박사 00.09~02.08 전남대학교 기업경영연구소장 09.03~12.02 전남대학교 경영전문대학원장 14.09~15.08 전남대학교 융합인재교육원장 90.09~23.03 전남대학교 경영대학 경영학부 교수 19.03~현재 ㈜박셀바이오 사외이사 20.03~현재 화천기공㈜ 사외이사 |
해당사항 없음 |
해당사항 |
- |
(2) 사외이사 및 그 변동현황
| (단위 : 명) |
| 이사의 수 | 사외이사 수 | 사외이사 변동현황 | ||
|---|---|---|---|---|
| 선임 | 해임 | 중도퇴임 | ||
| 3 | 1 | - | - | - |
- 이사 총수는 3인으로 사외이사 1인을 포함하고 있으며 회사내 지원조직은 사외이사가 이사회 및 이사회내 위원회에서 전문적인 직무 수행이 가능하도록 보조하고 있습니다. 이사회 개최 전에 해당 안건 내용을 충분히 검토할 수 있도록 사전에 자료를 제공하고 필요시 별도의 설명회를 개최하고 있습니다.
(3) 사외이사 지원조직 현황
| 부서명 | 직원수 | 직위 (근속년수/지원업무경력기간) |
주요 활동내역 |
|---|---|---|---|
| 경영관리본부 | 3 | - 상무 1명 (1년 / 26년) - 부장 1명 (1년 / 18년) - 대리 1명 (1년 / 9년) |
- 주주총회, 이사회, 위원회 운영 - 각 이사에게 의결을 위한 정보 제공 - 회의 진행을 위한 실무 지원 - 이사회 및 위원회의 회의내용 기록 |
(4) 사외이사 교육 미실시 내역
| 사외이사 교육 실시여부 | 사외이사 교육 미실시 사유 |
|---|---|
| 미실시 | 당사는 사외이사의 전문성 및 일정등을 고려하여, 중요한 경영상의 내용이 있을 경우, 경영진과의원활한 커뮤니케이션을 하고 있으며, 관련 사업내용 등에 대해 충분히 이해를 하고 있어, 별도의 교육은 실시하지 않았습니다. 향후 사외이사의 교육이 필요한 경우진행 예정입니다. |
2. 감사제도에 관한 사항
가. 감사의 인적사항
당사는 작성기준일 현재 감사위원회를 별도로 설치하고 있지 아니하며, 주주총회 결의로 선임된 비상근 감사 1명이 감사 업무를 수행하고 있습니다.
| 성명 | 사외이사 여부 |
경력 | 회계ㆍ재무전문가 관련 | ||
|---|---|---|---|---|---|
| 해당 여부 | 전문가 유형 | 관련 경력 | |||
| 오택근 | - |
·삼일회계법인, 한영회계법인 ·기획예산처 공공혁신본부 자산운용팀 사무관 ·기획재정부 재정정책국 성과관리과 사무관 ·현재 진회계법인 이사 |
예 | 제1호 유형 (공인회계사) |
삼일회계법인 한영회계법인 회계법인 새시대 진 회계법인 (근무기간 합산 18년 이상) |
(*) 전문가 유형은 관련법령 「상법 시행령」제37조 제2항에 따른 회계ㆍ재무전문가 유형입니다.
나. 감사의 독립성
감사는 이사회에 참석하여 독립적으로 이사의 업무를 감독할 수 있으며, 제반업무와 관련하여 관련장부 및 관계서류를 해당부서에 제출을 요구할 수 있습니다. 또한 필요시 회사로부터 영업에 관한 사항을 보고 받을수 있으며, 적절한 방법으로 경영정보에접근할 수 있습니다.
당사는 작성기준일 현재 정관 제47조(감사의 직무 등)에 감사업무에 필요한 경영정보접근을 위한 내부장치를 마련하고 있습니다.
| 규정 | 내 용 |
|---|---|
|
감사의 권한 |
제47조(감사의 직무와 의무) ① 감사는 회사의 회계와 업무를 감사한다. ② 감사는 회의의 목적사항과 소집의 이유를 기재한 서면을 이사회에 제출하여 임시주주총회의 소집을 청구할 수 있다. ③ 감사는 그 직무를 수행하기 위하여 필요한 때에는 자회사에 대하여 영업의보고를 요구할 수 있다. 이 경우 자회사가 지체없이 보고를 하지 아니할 때 또는 그 보고의 내용을 확인할필요가 있는 때에는 자회사의 업무와 재산상태를 조사할 수 있다. ④ 감사에 대해서는 정관 제36조 제3항의 규정을 준용한다. ⑤ 감사는 회사의 비용으로 전문가의 도움을 구할 수 있다. ⑥ 감사는 필요하면 회의의 목적사항과 소집이유를 적은 서면을 이사(소집권자가 있는 경우에는 소집권자)에게 제출하여 이사회 소집을 청구할 수 있다. ⑦ 제6항의 청구를 하였는데도 이사가 지체 없이 이사회를 소집하지 아니하면 그 청구한 감사가 이사회를 소집할 수 있다. |
|
감사의 구성 |
제44조(감사의 수) |
다. 감사의 주요활동내역
|
일자 |
종류 |
의 안 내 용 |
가결 |
|---|---|---|---|
| 2022.02.07. | 이사회 | 1. 제12기 재무제표 승인의 건 | 가결 |
| 2022.02.07. | 이사회 | 2. 주식매수선택권 부여의 건 | 가결 |
| 2022.03.28. | 이사회 | 1. 대표이사 선임의 건 | 가결 |
| 2022.07.15. | 이사회 | 1. 주식매수선택권 부여 취소의 건 | 가결 |
| 2022.07.15. | 이사회 | 2. 주식매수선택권 부여의 건 | 가결 |
| 2022.12.15. | 이사회 | 1. 명부폐쇄 기준일 설정의 건 | 가결 |
| 2023.02.23 | 이사회 | 1. 제13기 재무제표 승인의 건 | 가결 |
| 2023.02.23 | 이사회 | 2. 2022년도 (제13기)영업보고서 승인의 건 | 가결 |
| 2023.02.23 | 이사회 | 3. 제13기 정기주주총회 개최 및 총회 목적사항 결정에 대한 건 | 가결 |
| 2023.02.23 | 이사회 | 4. 전자투표제도 도입 승인의건 | 가결 |
| 2023.02.23 | 이사회 | 5. 주식매수선택권 부여에 대한 건 | 가결 |
| 2023.03.08 | 이사회 | 1. 제13기 정기주주총회 소집의 건 | 가결 |
| 2023.08.07 | 이사회 | 1. 유상증자 시행의 건 | 가결 |
| 2023.08.07 | 이사회 | 2. 무상증자 시행의 건 | 가결 |
라. 감사 교육 미실시 내역
| 감사 교육 실시여부 | 감사 교육 미실시 사유 |
|---|---|
| 미실시 | 감사의 전문성 및 일정등을 고려하여, 사업보고서 작성 기준일 현재 교육을 실시하지 않았으나, 업무수행 관련 교육이 필요할 경우 일정을 조율하여 진행 예정입니다. |
마. 감사 지원조직 현황
| 부서(팀)명 | 직원수(명) | 직위(근속연수) | 주요 활동내역 |
|---|---|---|---|
| 경영관리본부 | 8 | - 부장 2 (평균 4년) - 차장 1 (2년) - 과장 1 (2년) - 대리 2 (평균 2년) - 사원 2 (평균 2년) |
- 주주총회, 이사회 등 경영전반에 관한 감사업무 지원 - 재무제표 등 감사업무에 관한 감사업무 지원 |
바. 준법지원인 등 지원조직 현황
당사는 보고서 작성기준일 현재 별도의 준법지원인 및 준법지원인 지원조직이 없습니다.
3. 주주총회 등에 관한 사항
가. 투표제도 현황
| (기준일 : | 증권신고서 제출일 | ) |
| 투표제도 종류 | 집중투표제 | 서면투표제 | 전자투표제 |
|---|---|---|---|
| 도입여부 | 배제 | 도입 | 도입 |
| 실시여부 | - | 13기 정기주주총회 | 13기 정기주주총회 |
당사는 전자투표제를 제 11기 정기주주총회부터 도입하여 사용하고 있습니다.
나. 의결권 현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 주식수 | 비고 |
|---|---|---|---|
| 발행주식총수(A) | 보통주 | 15,223,000 | - |
| - | - | - | |
| 의결권없는 주식수(B) | - | - | - |
| - | - | - | |
| 정관에 의하여 의결권 행사가 배제된 주식수(C) | - | - | - |
| - | - | - | |
| 기타 법률에 의하여 의결권 행사가 제한된 주식수(D) |
- | - | - |
| - | - | - | |
| 의결권이 부활된 주식수(E) | - | - | - |
| - | - | - | |
| 의결권을 행사할 수 있는 주식수 (F = A - B - C - D + E) |
보통주 | 15,223,000 | - |
| - | - | - |
VI. 주주에 관한 사항
1. 최대주주 및 특수관계인의 주식소유 현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 주, %) |
| 성 명 | 관 계 | 주식의 종류 |
소유주식수 및 지분율 | 비고 | |
|---|---|---|---|---|---|
| 주식수 | 지분율 | ||||
| 이제중 | 본인 | 보통주 | 1,959,820 | 12.87% | - |
| 이준행 | 등기이사 | 보통주 | 1,478,060 | 9.71% | - |
| 박기원 | 특수관계인 | 보통주 | 241,680 | 1.59% | - |
| 이미란 | 특수관계인 | 보통주 | 56,400 | 0.37% | - |
| 박성현 | 특수관계인 | 보통주 | 12,905 | 0.08% | - |
| 박성찬 | 특수관계인 | 보통주 | 13,000 | 0.09% | - |
| 안옥선 | 특수관계인 | 보통주 | 93,514 | 0.61% | - |
| 이시은 | 특수관계인 | 보통주 | 8,879 | 0.06% | - |
| 안소연 | 특수관계인 | 보통주 | 4,730 | 0.03% | - |
| 이제완 | 특수관계인 | 보통주 | 316,000 | 2.08% | - |
| KO BYOUNG WE | 특수관계인 | 보통주 | 16,564 | 0.11% | - |
| LEE SOOK JA | 특수관계인 | 보통주 | 13,622 | 0.09% | - |
| KO HEE CHOUN | 특수관계인 | 보통주 | 13,421 | 0.09% | - |
| 이미란 | 특수관계인 | 보통주 | 9,597 | 0.06% | - |
| 이정효 | 특수관계인 | 보통주 | 12,350 | 0.08% | - |
| 선우준 | 특수관계인 | 보통주 | 6,000 | 0.04% | - |
| 이석현 | 특수관계인 | 보통주 | 8,600 | 0.06% | - |
| 이경연 | 특수관계인 | 보통주 | 10,598 | 0.07% | - |
| 이윤수 | 특수관계인 | 보통주 | 9,597 | 0.06% | - |
| 이미영 | 특수관계인 | 보통주 | 157,470 | 1.03% | - |
| 이창주 | 특수관계인 | 보통주 | 4,500 | 0.03% | - |
| 이세현 | 특수관계인 | 보통주 | 1,900 | 0.01% | - |
| 이창후 | 특수관계인 | 보통주 | 7,500 | 0.05% | - |
| 박진희 | 특수관계인 | 보통주 | 4,900 | 0.03% | - |
| 홍리라 | 특수관계인 | 보통주 | 6,000 | 0.04% | |
| 이승준 | 특수관계인 | 보통주 | 2,830 | 0.02% | |
| 이영채 | 특수관계인 | 보통주 | 4,800 | 0.03% | - |
| 최송자 | 특수관계인 | 보통주 | 1,000 | 0.01% | |
| 이정민 | 특수관계인 | 보통주 | 2,500 | 0.02% | |
| 이지원 | 특수관계인 | 보통주 | 2,500 | 0.02% | |
| 오택근 | 등기임원 | 보통주 | 630 | 0.00% | |
| 계 | 보통주 | 4,481,867 | 29.44% | - | |
| 우선주 | - | - | - | ||
* 보유주식수와 지분율은 2023년 2월 7일 공시 이후 본 증권신고서 제출일 기준으로 작성 되어 있습니다.
나. 최대주주의 주요경력 및 개요
|
성명 |
직책 |
주요경력 |
비고 |
|---|---|---|---|
| 이제중 | 대표이사/ CMO |
99.02 전남대학교 의과대학 혈액종양학 박사 99.05~03.07 화순전남대학교병원 임상교수 00.07~01.01 일본 동경 국립암센터 방문연구원 06.03~07.12 미국 피츠버그대학교 암연구소 방문교수 10.02~19.06 ㈜박셀바이오 대표이사 (설립) 15.01~17.12 한국다발골수종연구회 위원장 03.07~현재 전남의대/화순전남대학교병원 혈액종양내과 교수 08.12~현재 화순전남대학교병원 암면역치료연구센터장 19.06~현재 대한조혈모세포이식학회 세포치료연구회 위원장 21.02~현재 ㈜박셀바이오 대표이사 |
- |
다. 최대주주의 변동을 초래할수 있는 특정거래
- 해당사항 없습니다.
라. 최대주주의 최대주주(법인 또는 단체)의 개요
- 해당사항 없습니다.
2. 최대주주 변동내역
| (기준일 : | 증권신고서 제출일 | ) |
| 변동일 | 최대주주명 | 소유주식수 | 지분율(%) | 변동원인 | 비고 |
|---|---|---|---|---|---|
| - | - | - | - | - | - |
- 해당사항 없습니다.
3. 주식 소유현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 주) |
| 구분 | 주주명 | 소유주식수 | 지분율(%) | 비고 |
|---|---|---|---|---|
| 5% 이상 주주 | 이제중 | 1,959,820 | 12.87% | - |
| 이준행 | 1,478,060 | 9.71% | - | |
| 우리사주조합 | - | - | - | |
4. 소액주주현황
발행주식총수의 100분의 1에 미달하는 주식을 소유하고 있는 소액주주현황은 다음과 같습니다.
| (기준일 : | 2022년 12월 31일 | ) | (단위 : 주) |
| 구 분 | 주주 | 소유주식 | 비 고 | ||||
|---|---|---|---|---|---|---|---|
| 소액 주주수 |
전체 주주수 |
비율 (%) |
소액 주식수 |
총발행 주식수 |
비율 (%) |
||
| 소액주주 | 88,380 | 88,386 | 99.99 | 10,704,349 | 15,223,000 | 70.32 | - |
- 상기 소액주주 현황은 가장 최근의 주주명부폐쇄일(2022년 12월 31일)을 기준으로 작성하였습니다.
- 주주수는 주주명부상 계좌수 기준으로 산정합니다.
5. 주가 및 주식거래실적
국내 증권시장에서 최근 6개월간 당사의 주가 및 거래량에 관한 사항은 다음과 같습니다.
| 단위 : 원, 주 |
| 종 류 | 2023년 1월 | 2023년 2월 | 2023년 3월 | 2023년 4월 | 2023년 5월 | 2023년 6월 | |
|---|---|---|---|---|---|---|---|
| 보 통 주 | 최 고 | 36,700 | 37,100 | 40,800 | 69,900 | 41,800 | 40,800 |
| 최 저 | 34,050 | 32,900 | 33,600 | 38,200 | 38,950 | 34,850 | |
| 평 균 | 35,608 | 35,408 | 37,055 | 48,300 | 40,175 | 37,511 | |
| 월 거래량 (최고) | 184,138 | 1,978,247 | 6,571,336 | 9,070,618 | 798,222 | 347,444 | |
| 월 거래량 (최저) | 74,508 | 71,862 | 126,135 | 630,776 | 118,080 | 71,859 | |
| 월간 총 거래수량 | 2,205,822 | 6,130,382 | 30,839,886 | 50,397,817 | 5,936,206 | 3,339,266 | |
주1) 주가는 종가 기준이며, 평균주가는 단순 산술평균값이고, 월간 총 거래수량은 해당월의 주식거래 총 합계입니다.
주2) 거래정지일은 주가 및 거래량을 산정하는 기초데이터에서 제외하였습니다
VII. 임원 및 직원 등에 관한 사항
1. 임원 및 직원 등의 현황
가. 임원 현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 주) |
| 성명 | 성별 | 출생년월 | 직위 | 등기임원 여부 |
상근 여부 |
담당 업무 |
주요경력 | 소유주식수 | 최대주주와의 관계 |
재직 기간 |
임기 만료일 |
|
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 의결권 있는 주식 |
의결권 없는 주식 |
|||||||||||
| 이제중 | 남 | 1964.12 | 대표 이사 |
사내이사 | 상근 | 경영 총괄 |
99.02 전남대학교 의과대학 혈액종양학 박사 99.05~03.07 화순전남대학교병원 임상교수 00.07~01.01 일본 동경 국립암센터 방문연구원 06.03~07.12 미국 피츠버그대학교 암연구소 방문교수 10.02~19.06 ㈜박셀바이오 대표이사 (설립) 15.01~17.12 한국다발골수종연구회 위원장 03.07~현재 화순전남대학교병원 혈액종양내과 교수 08.12~현재 화순전남대학교병원 암면역치료연구센터장 21.02~현재 ㈜박셀바이오 대표이사 |
1,959,820 | - | 본인 | 14년 10개월 |
2025. 03.26 |
| 이준행 | 남 | 1960.03 | 이사 | 사내이사 | 상근 | 연구 총괄 |
92.02 전남대학교 의과대학 미생물학 박사 17.05~19.04 대한기초의학협의회 부회장 19.06~19.11 ㈜박셀바이오 대표이사 93.08~현재 전남대학교 의과대학 교수 17.01~현재 (재)백신글로벌산업화기반 구축사업단 선임이사 21.01~현재 ㈜박셀바이오 연구총괄 및 사내이사 |
1,478,060 | - | - | 14년 10개월 |
2025.03.26 |
| 정성창 | 남 | 1957.11 | 이사 | 사외이사 | 비상근 | 경영 자문 |
85.02 서울대학교 경영학 석사 90.07 Georgia State University 경영학 박사 14.09~15.08 전남대학교 융합인재교육원장 90.09~23.03 전남대학교 경영대학 경영학부 교수 19.03~현재 ㈜박셀바이오 사외이사 20.03~현재 화천기공㈜ 사외이사 |
- | - | - | 4년 4개월 |
2025.03.26 |
| 오택근 | 남 | 1976.12 | 감사 | 감사 | 비상근 | 감사 |
03.07 고려대학교 경영학 학사 15.07~18.09 회계법인 새시대 이사 18.10~현재 진회계법인 이사 19.09~현재 ㈜박셀바이오 감사 |
630 | - | - | 3년 10개월 |
2025.03.22 |
- 임신혁 기타비상무이사는 2022년 5월 13일 일신상의 이유로 사임하였습니다.
나. 타회사 임원 겸직 현황
| (기준일 : 증권신고서 제출일) |
|
성명 |
회사명 |
직책명 |
담당업무 |
재직기간 |
비고 |
|---|---|---|---|---|---|
|
이제중 |
전남대학교 의과대학 |
교수 |
연구 |
99.05~현재 |
비상근 겸직허가 |
|
이준행 |
전남대학교 의과대학 |
교수 |
연구 |
93.08~현재 |
비상근 겸직허가 |
|
정성창 |
화천기공(주) |
사외이사 |
경영자문 |
20.03~현재 |
- |
|
오택근 |
진회계법인 |
이사 |
회계감사등 |
18.10~현재 |
- |
다. 직원 등 현황
| (기준일 : | 2023년 6월 30일 | ) | (단위 : 백만원) |
| 직원 | 소속 외 근로자 |
비고 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 사업부문 | 성별 | 직 원 수 | 평 균 근속연수 |
연간급여 총 액 |
1인평균 급여액 |
남 | 여 | 계 | |||||
| 기간의 정함이 없는 근로자 |
기간제 근로자 |
합 계 | |||||||||||
| 전체 | (단시간 근로자) |
전체 | (단시간 근로자) |
||||||||||
| 관리 | 남 | 8 | - | - | - | 8 | 1.3 | 358 | 47 | - | - | - | - |
| 관리 | 여 | 6 | - | 1 | 1 | 7 | 3.3 | 174 | 25 | - | |||
| 연구 | 남 | 2 | - | - | - | 2 | 2.0 | 73 | 37 | - | |||
| 연구 | 여 | 5 | - | - | - | 5 | 2.4 | 139 | 29 | - | |||
| 제조 | 남 | 10 | - | - | - | 10 | 2.4 | 340 | 35 | - | |||
| 제조 | 여 | 21 | - | - | - | 21 | 3.7 | 482 | 25 | - | |||
| 합 계 | 52 | - | 1 | 1 | 53 | 2.8 | 1,566 | 31 | - | ||||
- 직원등 현황은 공시서식 작성기준에 따라 미등기임원의 내용이 포함되어 있습니다.
- 근로자 수는 본 보고서 작성 기준일 현재 재직자 수를 의미합니다.
- 평균근속연수 합계는 사업부문 전체의 평균근속연수를 기재하였습니다.
- 연간급여총액은 공시대상기간 퇴사한 직원을 포함한 금액입니다.
- 평균근속연수 및 1인 평균 급여액의 합계는 회사 전체의 평균입니다.
라. 미등기임원 보수 현황
| (기준일 : | 2023년 06월 30일 | ) | (단위 : 백만원) |
| 구 분 | 인원수 | 연간급여 총액 | 1인평균 급여액 | 비고 |
|---|---|---|---|---|
| 미등기임원 | 9 | 491 | 57 | - |
2. 임원의 보수 등
| <이사ㆍ감사 전체의 보수현황> |
가. 주주총회 승인금액
| (단위 : 백만원) |
| 구 분 | 인원수 | 주주총회 승인금액 | 비고 |
|---|---|---|---|
| 이 사 | 3 | 1,000 | 사외이사 포함 |
| 감 사 | 1 | 100 | - |
나. 보수지급금액
나-1. 이사ㆍ감사 전체
| (단위 : 백만원) |
| 인원수 | 보수총액 | 1인당 평균보수액 | 비고 |
|---|---|---|---|
| 4 | 150 | 38 | - |
나-2. 유형별
| (단위 : 백만원) |
| 구 분 | 인원수 | 보수총액 | 1인당 평균보수액 |
비고 |
|---|---|---|---|---|
| 등기이사 (사외이사, 감사위원회 위원 제외) |
2 | 138 | 69 | - |
| 사외이사 (감사위원회 위원 제외) |
1 | 6 | 6 | - |
| 감사위원회 위원 | - | - | - | - |
| 감사 | 1 | 6 | 6 | - |
3. 주식매수선택권의 부여 및 행사현황
<표1>
| (단위 : 원) |
| 구 분 | 부여받은 인원수 |
주식매수선택권의 공정가치 총액 | 비고 |
|---|---|---|---|
| 등기이사 (사외이사, 감사위원회 위원 제외) |
- | - | - |
| 사외이사 (감사위원회 위원 제외) |
- | - | - |
| 감사위원회 위원 또는 감사 | - | - | - |
| 업무집행지시자 등 | - | - | - |
| 계 | - | - | - |
- 작성기준일 현재 등기임원 등 <표1>의 구분에 적용되는 임직원은 없습니다.
<표2>
| (기준일 : | 2023년 06월 30일 | ) | (단위 : 원, 주) |
| 부여 받은자 |
관 계 | 부여일 | 부여방법 | 주식의 종류 |
최초 부여 수량 |
당기변동수량 | 총변동수량 | 기말 미행사수량 |
행사기간 | 행사 가격 |
의무 보유 여부 |
의무 보유 기간 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 행사 | 취소 | 행사 | 취소 | |||||||||||
| 김미화 | 미등기임원 | 2021년 03월 25일 | 신주교부 | 보통주 | 4,500 | - | - | - | - | 4,500 | 23.03.25 ~ 28.03.24 | 118,712 | X | - |
| 하선아 | 미등기임원 | 2022년 02월 07일 | 신주교부 | 보통주 | 4,500 | - | - | - | - | 4,500 | 24.02.07 ~ 29.02.06 | 42,274 | X | - |
| OOO | 미등기임원 | 2022년 07월 15일 | 신주교부 | 보통주 | 4,500 | - | - | - | - | 4,500 | 24.07.15 ~ 29.07.14 | 41,940 | X | - |
| OOO | 미등기임원 | 2023년 02월 23일 | 신주교부 | 보통주 | 6,000 | - | - | - | - | 6,000 | 25.02.23 ~ 30.02.22 | 36,185 | X | - |
| OOO | 미등기임원 | 2023년 02월 23일 | 신주교부 | 보통주 | 5,000 | - | - | - | - | 5,000 | 25.02.23 ~ 30.02.22 | 36,185 | X | - |
| OOO | 미등기임원 | 2023년 02월 23일 | 신주교부 | 보통주 | 5,000 | - | - | - | - | 5,000 | 25.02.23 ~ 30.02.22 | 36,185 | X | - |
※ 공시서류작성기준일(2023년 6월 30일) 현재 종가 : 35,250원
- 본 사업보고서 작성 기간 내 2023년 2월 23일, 당사 미등기임원 3인에게 총 16,000주를 상기 표2와 같이 구분하여 부여 하였으며 2022년 7월 15일 부여한 4,500주 까지 합하여 제13기 정기주주총회에서 이를 승인하였고 현재 주식매수선택권 총 부여수량은 29,500주입니다.
- 최근 부여된 주식매수선택권에 대한 자세한 사항은 금융감독원 전자공시시스템 2023년 2월 23일 당사가 공시한 [주식매수선택권부여에 관한 신고] 를 참고해주시기 바랍니다.
VIII. 계열회사 등에 관한 사항
가. 계열회사 현황(요약)
| (기준일 : | 2023년 06월 30일 | ) | (단위 : 사) |
| 기업집단의 명칭 | 계열회사의 수 | ||
|---|---|---|---|
| 상장 | 비상장 | 계 | |
| - | - | - | - |
나. 타법인출자 현황(요약)
| (기준일 : | 2023년 06월 30일 | ) | (단위 : 원) |
| 출자 목적 |
출자회사수 | 총 출자금액 | |||||
|---|---|---|---|---|---|---|---|
| 상장 | 비상장 | 계 | 기초 장부 가액 |
증가(감소) | 기말 장부 가액 |
||
| 취득 (처분) |
평가 손익 |
||||||
| 경영참여 | - | - | - | - | - | - | - |
| 일반투자 | - | - | - | - | - | - | - |
| 단순투자 | - | - | - | - | - | - | - |
| 계 | - | - | - | - | - | - | - |
IX. 대주주 등과의 거래내용
- 해당사항 없습니다.
X. 그 밖에 투자자 보호를 위하여 필요한 사항
1. 공시내용 진행 및 변경사항
- 해당사항 없습니다.
2. 우발부채 등에 관한 사항
가. 중요한 소송사건 등
- 해당 사항이 없습니다.
나. 견질 또는 담보용 어음ㆍ수표 현황
| (기준일 : 2023년 6월 30일) | (단위 : 매, 백만원) |
| 제 출 처 | 매 수 | 금 액 | 비 고 |
|---|---|---|---|
| 은 행 | - | - | - |
| 금융기관(은행제외) | - | - | - |
| 법 인 | - | - | - |
| 기타(개인) | - | - | - |
다. 당 분기말 현재 회사가 가입한 보험가입내용은 다음과 같습니다.
| (단위 : 원) |
라. 채무보증현황 및 채무인수약정 현황
- 해당사항 없습니다.
마. 그 밖의 우발채무 등
당 분기말 현재 회사는 이행보증과 관련하여 서울보증보험으로부터 112,800,000원의 지급보증을 받고 있고 그 외 견질 또는 담보용 어음 및 수표를 발행하지 않았습니다.
3. 제재 등과 관련된 사항
- 해당사항 없습니다.
4. 작성기준일 이후 발생한 주요사항 등 기타사항
가. 작성기준일 이후 발생한 주요사항
- 2023년 8월 7일, 이사회의 결정으로 3,938,000주를 발행하는 1,006억원 규모의 주주배정 후 실권주 일반공모 유상증자와 3,832,200주를 주식발행초과금을 재원으로 무상증자를 진행하게 되었습니다.
나. 외국지주회사의 자회사 현황
- 해당사항 없습니다.
다. 중소기업기준 검토표
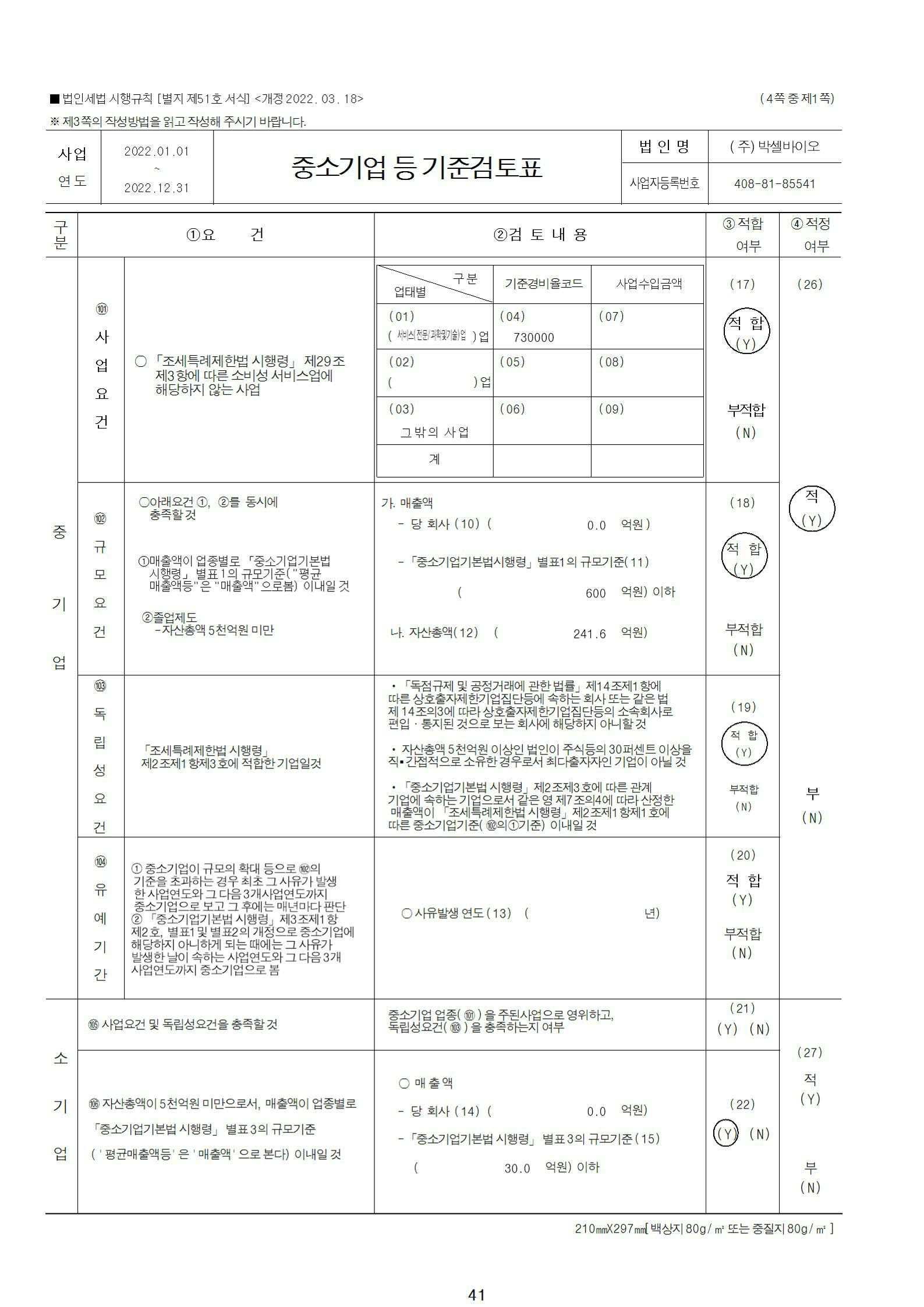 |
|
중소기업기준검토표_2022_박셀바이오_1 |
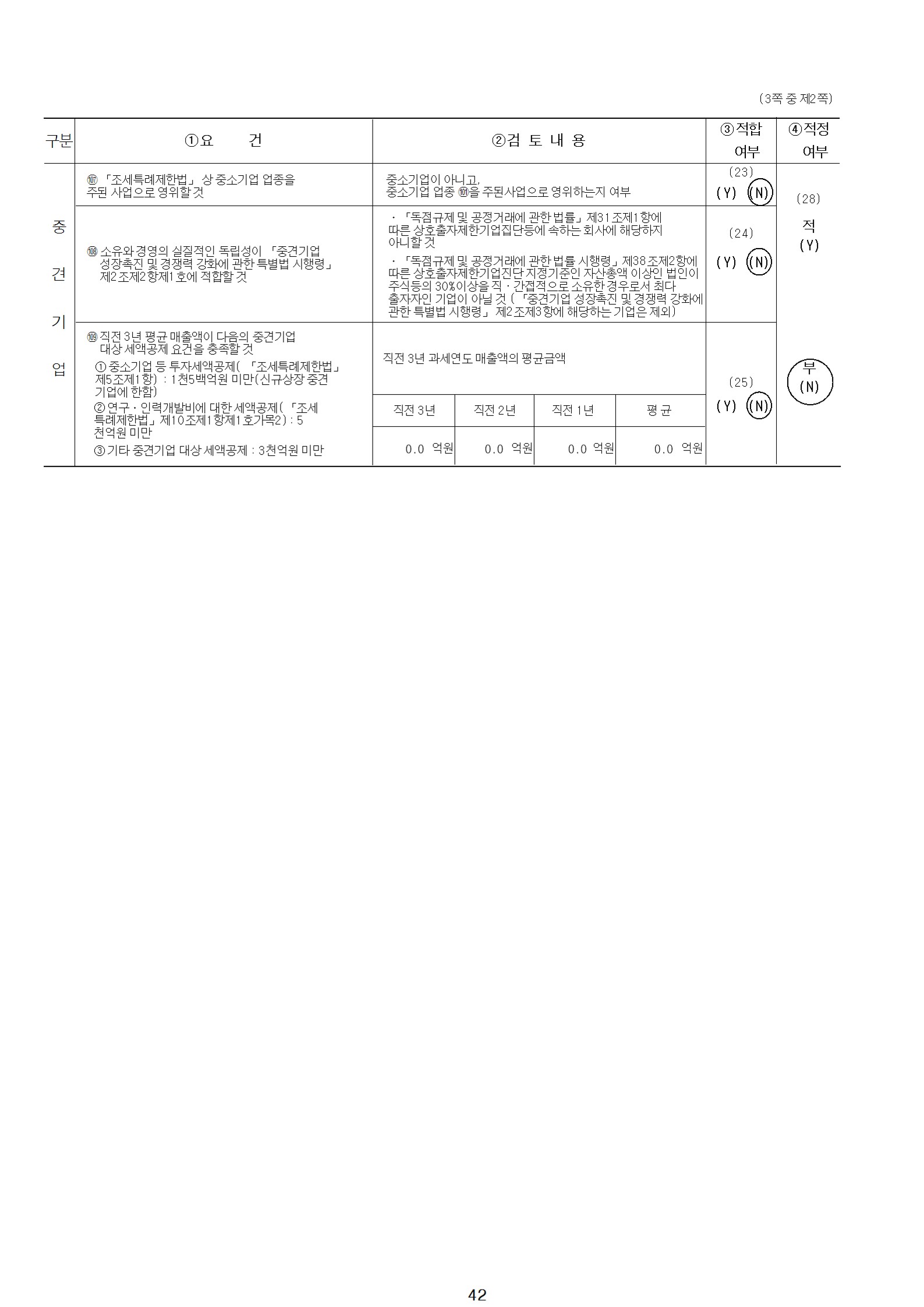 |
|
중소기업기준검토표_2022_박셀바이오_2 |
라. 보호예수 현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 주) |
| 주식의 종류 | 예수주식수 | 예수일 | 반환예정일 | 보호예수기간 | 보호예수사유 | 총발행주식수 |
|---|---|---|---|---|---|---|
| 보통주식 | 3,437,880 | 2020년 09월 22일 | 2023년 09월 22일 | 상장일로부터 3년 | 코스닥상장 의무보호예수 | 15,223,000 |
마. 특례상장기업의 재무사항 비교표
| (상장일 : | 2020년 09월 22일 | , 인수인 : | 하나금융투자(주 | ) | (단위 : 백만원) |
| 추정대상 | 계정과목 | 예측치 | 실적치 | 괴리율 |
|---|---|---|---|---|
| 2020년 | 매출액 | - | - | - |
| 영업이익 | -7,223 | -4,255 | 41 | |
| 당기순이익 | -7,136 | -3,984 | 44 | |
| 2021년 | 매출액 | 2,711 | - | - |
| 영업이익 | -10,740 | -5,904 | 45 | |
| 당기순이익 | -10,420 | -4,763 | 54 | |
| 2022년 | 매출액 | 12,687 | - | - |
| 영업이익 | -317 | -8,213 | -2,491 | |
| 당기순이익 | -109 | -6,825 | -6,162 |
주) 당사는 2020년 상장한 회사로서 특례상장기업의 재무사항 비교표에서 박스루킨-15의 품목허가 자진철회로 인해 2021~2022년 예상했던 매출액이 발생하지 않았습니다. 또한 COVID-19의 특수한 상황으로 라이선싱 아웃은 예상했던 일정보다 다소 연기되었으나 다국적 기업들과 접촉하여 계속 진행중이며, 현재 미국, 캐나다 업체 등과 공동연구 협약을 완료하여 공동투자를 통한 매출 및 시장 점유 극대화 전략으로 추진 중입니다.
바. 특례상장기업 관리종목 지정유예 현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 원, %) |
| 관리종목 지정요건 | 요건별 회사 현황 | 관리종목 지정요건 해당여부 |
관리종목지정유예 | |||
|---|---|---|---|---|---|---|
| 항목 | 사업연도 | 금액/비율 | 해당 여부 |
종료 시점 |
||
| 최근 사업연도말 매출액 30억원 미만 |
최근 사업연도말 매출액(별도) | 2022 | - | 미해당 | 해당 | 2024년 12월 31일 |
| 최근 4사업연도 연속 영업손실 발생 | 최근 4사업연도 각 영업손익 (별도) |
2022 | -8,212,602,189 | 미해당 | 해당 | - |
| 2021 | -5,904,060,364 | |||||
| 2020 | -4,254,895,557 | |||||
| 2019 | -4,010,646,639 | |||||
| 자기자본 50%이상(10억원 이상에 한함)의 법인세차감전계속사업손실이 최근 3년간 2회 이상 및 최근 사업연도 법인세차감전계속사업손실 발생 | 최근 3사업연도 각 자기자본 대비 법인세차감전 계속사업손익 비율(연결) |
2022 | -6,825,051,481 | 미해당 | 해당 | 2022년 12월 31일 |
| 2021 | -4,762,778,542 | |||||
| 2020 | -3,984,015,078 | |||||
- 당사는 2020년 9월 22일 코스닥시장에 '기술성장기업'으로서 상장하였습니다.
- 당사는 기술성장특례 적용 기업으로서 매출액 요건의 경우 신규 상장일이 속하는 사업연도 (상장 후 사업연도말까지 3월 미만인 경우 다음 사업연도)를 포함한 연속하는 5개 사업연도, 세전 이익 요건의 경우 신규 상장일이 속하는 사업연도(상장 후 사업연도말까지 3월 미만인 경우 다음 사업연도)를 포함한 연속하는 3개 사업연도에 대해서는 해당 요건을 적용 받지 않습니다. (영업이익 요건은 유예기간 없이 적용 면제)
XI. 상세표
1. 연결대상 종속회사 현황(상세)
| (단위 : 원) |
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| - | - | - | - | - | - | - |
- 해당사항 없습니다.
2. 계열회사 현황(상세)
| (기준일 : | 2023년 06월 30일 | ) | (단위 : 사) |
| 상장여부 | 회사수 | 기업명 | 법인등록번호 |
|---|---|---|---|
| 상장 | - | - | - |
| - | - | ||
| 비상장 | - | - | - |
| - | - |
- 해당사항 없습니다.
3. 타법인출자 현황(상세)
| (기준일 : | 2023년 06월 30일 | ) | (단위 : 원, 주, %) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
| - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - |
| - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - |
| 합 계 | - | - | - | - | - | - | - | - | - | - | - | ||||
- 해당사항 없습니다.
【 전문가의 확인 】
1. 전문가의 확인
해당사항 없습니다.
2. 전문가와의 이해관계
해당사항 없습니다.