 |
|
확인서(증권신고서)_22.10.11 |
정 정 신 고 (보고)
| 2022년 10월 11일 |
1. 정정대상 공시서류 : 증권신고서
2. 정정대상 공시서류의 최초제출일 : 2022년 08월 16일
| [증권신고서 제출 및 정정 연혁] |
| 제출일자 | 문서명 | 비고 |
|---|---|---|
| 2022년 08월 16일 | 증권신고서(지분증권) | 최초 제출 |
| 2022년 08월 17일 | [기재정정]증권신고서(지분증권) | 자진 정정(파란색) |
| 2022년 09월 07일 | [기재정정]증권신고서(지분증권) | 정정제출 요구 및 일정변경에 따른 정정(녹색) |
| 2022년 09월 23일 | [기재정정]증권신고서(지분증권) | 기재사항 정정 및 일정변경에 따른 자진정정 (빨간색) |
| 2022년 10월 11일 | [기재정정]증권신고서(지분증권) | 자진 정정(하늘색) |
3. 정정사항
*정정사항 확인의 편의를 위하여 1차 정정사항은 파란색 글씨로, 2차 정정사항은 녹색 글씨로, 3차 정정사항은 빨간색 글씨, 4차 정정사항은 하늘색 글씨로 정정하였습니다.
| 항 목 | 정정사유 | 정 정 전 | 정 정 후 |
|---|---|---|---|
| - 단순 오타 및 표현 수정 등은 별도의 색깔표시 없이 정정하였습니다. - 요약정보에는 본문의 정정사항을 반영하였으며, 정오표를 별도로 기재하지 않았습니다. |
|||
| 제 1부 III. 투자위험요소 | |||
| 1. 사업위험 | |||
| 바. 임상시험 실패 및 지연에 따른 위험 | 기재 정정 | (주1) 정정 전 | (주1) 정정 후 |
| 차. 리보세라닙 성분 신약 허가 관련 불확실성 | 기재 정정 | (주2) 정정 전 | (주2) 정정 후 |
| 2. 회사위험 | |||
| 나. 자체 사업의 영업실적과 주가 간의 괴리 관련 위험 | 기재 정정 | (주3) 정정 전 | (주3) 정정 후 |
| 차. Rivoceranib 신약 개발 사업에 관한 전반적인 사항 | 기재 정정 | (주4) 정정 전 | (주4) 정정 후 |
| IV. 인수인의의견(분석기관의 평가의견) | 기재 정정 | (주5) 정정 전 | (주5) 정정 후 |
| 제 2부 Ⅱ.사업의 내용 | |||
| 4. (제조서비스업)매출 및 수주상황 | 기재 정정 | (주6) 정정 전 | (주6) 정정 후 |
| 6. (제조서비스업)주요계약 및 연구개발활동 | 기재 정정 | (주7) 정정 전 | (주7) 정정 후 |
| 7. (제조서비스업)기타 참고사항 | 기재 정정 | (주8) 정정 전 | (주8) 정정 후 |
| Ⅸ. 대주주 등과의 거래내용 | 기재 정정 | (주9) 정정 전 | (주9) 정정 후 |
| XI. 상세표 | 기재 정정 | (주10) 정정 전 | (주10) 정정 후 |
(주1) 정정 전
4. 당사의 신약개발 현황
당사는 100% 지분을 보유한 연결대상 종속회사인 Elevar, 41.07% 지분을 보유한 연결대상 종속회사인 Immunomic을 포함해 제약ㆍ바이오 사업을 영위하고 있습니다. Elevar는 2개의 항암 신약물질((1) Rivoceranib("리보세라닙", 舊, Apatinib Mesylate) 및 (2) Apealea("아필리아")에 대해 라이센스를 취득하는 계약을 체결하였습니다. Elevar는 리보세라닙에 대하여 중국, 한국을 제외한 글로벌 전용실시권을 보유하고 있으며(한국판권은 에이치엘비생명과학㈜가 보유함), 아필리아에 대하여 러시아연방, 스칸디나비아반도국을 제외한 글로벌 전용실시권을 보유하고 있습니다.
| [연구개발 진행 총괄표] |
| 구 분 | 품 목 | 적응증 | 임상시작일 | 현재 진행단계 | 비 고 | 임상주도기업 | ||
|---|---|---|---|---|---|---|---|---|
| 단계(국가) | 승인일 | |||||||
| 화학합성 의약품 |
신약 | 리보세라닙 (HLB생명과학 주도 임상 포함) |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안전성평가 완료 | Elevar |
| 위암 (3차 단일요법) |
2017년 | 임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
Elevar | |||
| 위암 (1차 병용요법) [Combo with Camrelizumab] |
2021년 | 임상2상 (한국) |
2021년 09월 (임상2상 개시일) |
임상 진행 중 | Elevar | |||
| 간암 (1차 병용요법) [Combo with Camrelizumab] |
2019년 | 임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
임상 진행 중 9월 초록 발표 (1차 평가 지표 만족) |
Elevar | |||
| 선양낭성암종 (1/2차 단일요법) |
2020년 | 임상2상 (한국, 미국) |
2020년 4월 (임상2상 개시일) |
임상 2상 진행중 6월 초록 발표 |
Elevar | |||
| 위암 (2차 병용요법) [Combo with Paclitaxel] |
2018년 | 임상1/2a상 (한국, 미국) |
2018년 10월 (임상1상 개시일) |
임상1상 종료 후, 2a상 준비 중 |
Elevar | |||
| 대장암 (3차 병용요법) [Combo with Lonsurf] |
2019년 | 임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 진행 중 | Elevar | |||
| 황반변성치료제 (점안액) |
2018년 | 비임상 단계 | - | 타당성분석 중 | HLB 생명과학 |
|||
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상진입 준비 중 (농림축산검역본부) |
HLB 생명과학 |
|||
| 위암 (1차 병용요법) [Combo with Camrelizumab] |
2021년 | 임상2상 (한국) |
2021년 09월 (임상2상 개시일) |
임상 진행 중 | HLB 생명과학 |
|||
| 아필리아 | 난소암 2차 (백금계 약물 감수성) |
2018년 (유럽EMA 허가) |
유럽 허가 | 유럽 판매 준비 중 | Elevar | |||
| 바이오 의약품 |
IMMUNOMIC THERAPEUTICS ITI-1000 |
GBM | 2016년 | 임상 2상 (미국) |
2016년 8월 (임상 2상 개시일) |
임상 진행 중 | ITI | |
| IMMUNOMIC THERAPEUTICS ITI-1001 |
GBM | - | 비임상 단계 | - | 임상 1상 IND 준비 중 | ITI | ||
| IMMUNOMIC THERAPEUTICS ITI-3000 |
Merkel Cell Carcinoma | 2022년 | 임상 1상 (미국) |
2022년 02월 (임상 1상 개시일) |
임상 진행 중 | ITI | ||
| IMMUNOMIC THERAPEUTICS ITI-8000 |
NSCLC | - | 비임상 단계 | - | - | ITI | ||
| IMMUNOMIC THERAPEUTICS ITI-9001 |
JRC Pollinosis | - | 비임상 단계 | - | - | ITI | ||
(가) : 리보세라닙
| 구 분 | 화학합성의약품 |
| 적응증 | 위암 3/4차 치료제, 위암 2차 치료제, 선양낭성암 1,2차 치료제, 간암 1차 치료제, 대장암 3차 치료제 |
| 작용기전 | 신생혈관억제, VEGFR2-TKI |
| 제품의특성 | 혈관내피세포성장인자수용체2(VEGFR-2)를 타켓으로 암 조직의 신생혈관 성장을 억제하고, 암세포의 증식억제와면역세포의 정상화를 유도하는 경구용 표적 항암제입니다. |
| 진행경과 | 위암 3/4차 치료제: 단독 요법으로 글로벌 임상 3상 후 미국 NDA 신청 준비 중 위암 2차 치료제: 파클리탁셀과 병용으로 한국, 미국에서 임상1/2a 진행 (현재 임상 1상 환자 모집 종료) 선양낭성암 1,2차 치료제: 단독요법으로 미국, 한국에서 임상 2상 환자모집 완료 간암 1차 치료제: 항서제약의 캄렐리주맙과 병용으로 글로벌 13개국 임상 3상 진행하고 있고, 2022년 9월 ESMO에서 임상 결과 공개(1차 평가지표 만족) 대장암 3차 치료제: 타이호제약의 론서프와 병용으로 미국, 한국에서 임상 1b/2상 진행 |
| 향후계획 | 위암 3/4차 치료제: 미국 FDA pre-NDA 진행, FDA에서 요청한 보완 자료 준비 중, 자료 보완 후 NDA 제출 예정 위암 2차 치료제: 임상 1상 결과 분석 선양낭성암 1,2차 치료제: 임상 2상 결과 수집 및 분석 간암 1차 치료제: 임상 3상 결과 수집, 분석 및 Pre-NDA 준비 대장암 3차 치료제: 임상 1상 결과 수집 및 분석 |
| 경쟁제품 | 위암 3차 치료제: 론서프, 옵디보(한국, 일본, 대만 한정) 위암 2차 치료제: 시람자(cyramza), 파클리탁셀 선양낭성암 1,2차 치료제: 표준치료제 없음 (Off-label)로 치료 진행 간암 1차 치료제: 넥사바, 렌비마, 아바스틴, 티센트릭 대장암 3차 치료제: 론서프, 스티바가, 옵디보 |
| 관련논문등 | 위암 글로벌 임상 3상 결과 2019년 유럽암학회(ESMO) 발표: Best of ESMO 선정 중국 위암 3차 치료제 임상 3상 논문: 2016년, J Clin Oncol 34 중국 위암 2차 치료제 임상 2상 논문: 2013년, J Clin Oncol 31 중국 고형암 치료제 임상 1상 논문: 2010년, BMC cancer 10 선양낭성암 중국 선낭암 임상 2상: 2021년 Therapeutic Advances in Medical Oncology 13 미국, 한국 선낭암 임상 2상 결과: 2022년 미국암학회 발표 간암 중국 간암 임상 2상: 2021년 Clin Cancer Res 15:27(4) 글로벌 간암 임상 3상 결과: 2022년 9월 ESMO(유럽암학회)에서 공개 (1차 평가지표 만족) |
| 시장규모 | 위암 치료제 글로벌시장: 2017년 40억달러(4조7,236억원)에서 2026년에는 66억달러(7조7,939억원)로 성장 예상 선낭암 치료제 글로벌시장: 표준치료제가 없고 발병률이 낮아 글로벌 시장 규모 추산이 어려움 간암 치료제 글로벌시장: 2019년 17억3090만 달러 (약 2조 2,100억원) 대장암 치료제 글로벌시장: 2018년 64억4400만달러(7조2000억)에서 2028년 81억4700만달러(9조1000억)로 성장 예상 |
| 기타사항 | 특허 및 권리 보유 현황 - 리보세라닙의 물질특허: HLB - 글로벌 전용실시권은: Elevar - 한국 전용실시권: HLB생명과학 - 중국 전용실시권: 중국 항서제약이 보유 항서제약에서 2014년 위암 3차 치료제로 중국 내 시판허가를 득한 후 현재까지 꾸준한 매출 성장 유지 중입니다. 2015년 매출 약 450억에서 2018년 2,800억까지 매출 성장을 보여줘, 약효와 안전성을 입증하였습니다. 2021년 부터 간암 2차 치료제로 적응증을 확대하여, 중국 내 매출 확대가 기대 됩니다. |
(나) : 아필리아
| 구 분 | 화학합성의약품 |
| 적응증 | 백금계 약물 감수성이 있는 난소암 2차 치료제 |
| 작용기전 | 세포 분열에 필요한 RNA나 DNA 등을 손상시켜 세포 분열을 저지하는 세포 주기 선택적 항암제 |
| 제품의특성 | 파클리탁셀은 세포분열 과정 중 분열과 자가 복제의 기구인 미세소관이 분리되는 과정을 방해하는 "식물성 알칼로이드"로 분류되는 항암제입니다. 중증 과민반응 발현을 최소화하기 위해 투여 전에 전치료를 받아야 합니다. Apealea는 특허 출원된 Micelle 코팅을 적용하여 사전처치 필요없이 편의성을 증대시키며 부작용을 줄일 수 있도록 개발한 첨가제 형태 기반의 최적의 파크리탁셀 혼합제입니다. |
| 진행경과 | 유럽, 남미, 중동 지역 판매 준비 중 백금계 약물 저항성이 있는 난소암 환자 대상 임상 1상, 3상 동시 준비 중 |
| 향후계획 | -기 승인 받은 지역 대상 판매 준비 유럽, 중동, 북아프리카, 남미 지역 대상으로 판매 절차 진행 중 중국 진출을 위해 중국 현지업체와 JV를 통한 논의 중 -추가 적응증 개발 백금계 약물 저항성이 있는 난소암 환자를 대상으로 Rivoceranib과 병용 임상 계획 검토 중 |
| 경쟁제품 | 카보플라틴, 시스플라틴, 파클리탁셀, 아바스틴 |
| 관련논문등 | A randomized phase III trial in patients with recurrent platinum sensitive ovarian cancer comparing efficacy and safety of paclitaxel micellar and Cremophor EL-paclitaxel |
| 시장규모 | 글로벌 난소암 시장은 2021년 1억 7,500만달러 규모였으며, 2028년까지 매년 9.5% 성장하여 약 3억 3,973만 달러에 이를 것으로 예상 |
| 기타사항 | -특허 및 권리 보유 현황 Apealea 글로벌 전용실시권: Elevar (북유럽, 동유럽 일부국가 제외) -판매 승인 현황 2020년 유럽 EMA로 부터 난소암 2차 치료제로 판매 승인 (carboplatin 병용) 2022년 내 유럽 내 판매 개시 목표 |
(다) : ITI
| 구 분 | 바이오의약품 |
| 적응증 | GBM (교모세포종) |
| 작용기전 | UNITE 플랫폼은 리소좀관련막단백질(LAMP)에 특정 암에 발현되는 항원을 탑재해 면역세포를 빠르고 효율적으로 활성화시키는 기전 |
| 제품의특성 | 기존 기술 대비 CD4+ Helper T 세포 활성화에 가장 효과적 동일 APC 세포 내 MHC I & II Mediated Pathway 를 동시에 활성화 가능 (MHC II Pathway 직접적으로 관여) 다양한 질환 분야에 적용 가능 (암, 감염 질환, 자가면역 질환 등) 세포 기반 치료제, 핵산 (Nucleic Acid, DNA/RNA) 기반 치료제 개발 등 다양한 기술에 적용 가능 |
| 진행경과 | ITI-1000 교모세포종 (Dendritic Cell vaccine): 임상 2상 진행 중 ITI-1001교모세포종(DNA vaccine): 1상 IND 승인 후 임상 진행 중 ITI-3000 메르켈세포암(DNA vaccine): 1상 IND 승인 후 임상 진행 중 |
| 향후계획 | ITI-1000 연내 임상 2상 종료 후, FDA와 협의를 통해 조건부 허가 추진 |
| 경쟁제품 | 교모세포종: 테모졸로마이드 (2003년 승인) |
| 관련논문등 | 2009 Gene Therapy 16 2015 Nature 2017 Clinical Cancer Reserch 23(8) |
| 시장규모 | 글로벌 교모세포종 시장은 2025년까지 매년 7.4% 성장할 전망이며, 약 16억 4,340만달러 |
| 기타사항 | 현재 교모세포종 원발성 악성 뇌종양 중 가장 흔한 종양으로 진단 후 치료를 하지 않으면 3-6개월 내에 사망합니다. 현재 치료법이 제한적이고 5년 생존율이 5%미만으로 악성도가 높은 질환입니다. ITI-1000 교모세포종 임상 1상 시험에서 mOS을 38.3 개월로 크게 개선하였으며, 표준치료제로 알려진 TMZ/RT 요법 대비 23 개월 이상 생존 기간을 향상시키고 60개월 생존율 또한 36.4%로 증가해 임상 2상 결과 또한 기대하고 있음. |
Elevar는 리보세라닙 위암 말기 단독치료제를 목적으로 하는 3상 임상시험 완료 후 데이터를 확정하여 2019년 10월 미국 FDA와 Pre-NDA 미팅을 하였으며, 그 결과를바탕으로 최종 Data분석 및 적절한 허가 전략을 수립한 후, 신약허가를 신청할 계획입니다. 선양낭성암은 2022년 6월 미국종양학회(ASCO)에서 임상 데이터를 공개했고, 표준치료제가 없는 희귀암종의 이점을 살려 FDA의 가속승인(조건부판매)를 목표로 전략을 수립하고 있습니다. 그리고, 2022년 5월 통계적 유의성을 확보했다고 이미 밝힌 바 있는 간암 1차 치료제 글로벌 3상 임상은 2022년 8월 미국 FDA에 Pre-NDA를 신청했고, 최근 2022년 9월 ESMO(유럽종양학회)에서 데이터를 공개해 1차 평가지표를 만족했음을 밝혔습니다. 회사는 본 임상결과를 바탕으로 FDA와의 Pre-NDA미팅 준비 등 후속 개발에 박차를 가하고 있습니다. 앞서 언급한 위암 3차 치료제, 간암 1차 치료제, 선양낭성암 1차 치료제 모두 희귀의약품에 지정되어 있어 임상종료 후 개별 국 진입 시 시판허가에 대한 신속화, 수수료 감면 등의 혜택과 더불어 신약 허가를 득할 경우 그 이후 최소 8년에서 최대 13년동안 독점 판매할 수 있습니다.이와 관련해 리보세라닙이 희귀의약품으로 지정 받은 내역은 아래와 같습니다. 위암(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국), 간암 (2021년 11월 미국식품의약국), 선양낭성암 (2021년 2월 미국식품의약국) 특히, 리보세라닙은 현재 위암 3차 치료제와 간암 2차 치료제에 대해서는 중국에서 항서제약이 임상 3상을 종료 후 시판허가를 득하여 현재 중국에서 판매되고 있습니다.
(주1) 정정 후
4. 당사의 신약개발 현황
당사는 100% 지분을 보유한 연결대상 종속회사인 Elevar, 41.07% 지분을 보유한 연결대상 종속회사인 Immunomic을 포함해 제약ㆍ바이오 사업을 영위하고 있습니다. Elevar는 2개의 항암 신약물질((1) Rivoceranib("리보세라닙", 舊, Apatinib Mesylate)및 (2) Apealea("아필리아")에 대해 라이센스를 취득하는 계약을 체결하였습니다. Elevar는 리보세라닙에 대하여 중국, 한국을 제외한 글로벌 전용실시권을 보유하고 있으며(한국판권은 에이치엘비생명과학㈜가 보유함), 아필리아에 대하여 러시아연방, 스칸디나비아반도국을 제외한 글로벌 전용실시권을 보유하고 있습니다.
| [연구개발 진행 총괄표] |
| 구 분 | 품 목 | 적응증 | 임상시작일 | 현재 진행단계 | 기 타 | 임상주도기업 | 비고 | ||
|---|---|---|---|---|---|---|---|---|---|
| 단계(국가) | 승인일 | ||||||||
| 화학합성 의약품 |
신약 | 리보세라닙 (HLB생명과학 주도 임상 포함) |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안전성평가 완료 | Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
| 위암 (3차 단일요법) |
2017년 | 임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 | |||
| 간암 (1차 병용요법) [Combo with Camrelizumab] |
2019년 | 임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
임상 진행 중 9월 초록 발표 (1차 평가 지표 만족) |
Elevar | 항서제약과 공동개발 | |||
| 선양낭성암종 (1/2차 단일요법) |
2020년 | 임상2상 (한국, 미국) |
2020년 4월 (임상2상 개시일) |
임상 2상 진행중 6월 초록 발표 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 | |||
| 위암 (2차 병용요법) [Combo with Paclitaxel] |
2018년 | 임상1/2a상 (한국, 미국) |
2018년 10월 (임상1상 개시일) |
임상1상 종료 후, 2a상 준비 중 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 | |||
| 대장암 (3차 병용요법) [Combo with Lonsurf] |
2019년 | 임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 진행 중 | Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 | |||
| 황반변성치료제 (점안액) |
2018년 | 비임상 단계 | - | 타당성분석 중 | HLB 생명과학 |
HLB생명과학이 Rivoceranib 한국 내 전용실시권 L/I 후 자체 개발 | |||
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상진입 준비 중 (농림축산검역본부) |
HLB 생명과학 |
HLB생명과학이 Rivoceranib 한국 내 전용실시권 L/I 후 자체 개발 | |||
| 위암 (1차 병용요법) [Combo with Camrelizumab] |
2021년 | 임상2상 (한국) |
2021년 09월 (임상2상 개시일) |
임상 진행 중 | HLB 생명과학 |
HLB생명과학이 Rivoceranib 한국 내 전용실시권 L/I 후 개발 | |||
| 아필리아 | 난소암 2차 (백금계 약물 감수성) |
2018년 (유럽EMA 허가) |
유럽 허가 | 유럽 판매 준비 중 | Elevar | Elevar가 Apealea의 글로벌 (일부국가 제외) 전용실시권을 L/I 후 판매 준비 중 |
|||
| 바이오 의약품 |
IMMUNOMIC THERAPEUTICS ITI-1000 |
GBM | 2016년 | 임상 2상 (미국) |
2016년 8월 (임상 2상 개시일) |
임상 진행 중 | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
|
| IMMUNOMIC THERAPEUTICS ITI-1001 |
GBM | - | 비임상 단계 | - | 임상 1상 IND 준비 중 | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| IMMUNOMIC THERAPEUTICS ITI-3000 |
Merkel Cell Carcinoma | 2022년 | 임상 1상 (미국) |
2022년 02월 (임상 1상 개시일) |
임상 진행 중 | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| IMMUNOMIC THERAPEUTICS ITI-8000 |
NSCLC | - | 비임상 단계 | - | - | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| IMMUNOMIC THERAPEUTICS ITI-9001 |
JRC Pollinosis | - | 비임상 단계 | - | - | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| 주) 통상적으로 통계적으로 유효성을 만족하는 수준의 임상데이터 수집이 완료되면 임상 결과를 발표하나, 이는 임상의 완전한 종료를 뜻하는 바는 아닙니다. 모든 임상 참여 환자의 데이터가 축적된 후 임상결과보고서(CSR) 작성이 완료되면 공식적으로 임상시험이 종료됩니다. |
(가) : 리보세라닙
| 구 분 | 화학합성의약품 | ||||||||||||||||||||||||||||||
| 적응증 | 위암 3/4차 치료제(Rivoceranib 단독)위암 2차 치료제(파클리탁셀 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독), 간암 1차 치료제(항서제약 캄렐리주맙 병용), 대장암(타이호제약 론서프 병용)3차 치료제 | ||||||||||||||||||||||||||||||
| 작용기전 | 신생혈관억제, VEGFR2-TKI | ||||||||||||||||||||||||||||||
| 제품의특성 | 혈관내피세포성장인자수용체2(VEGFR-2)를 타켓으로 암 조직의 신생혈관 성장을 억제하고, 암세포의 증식억제와 면역세포의 정상화를 유도하는 경구용 표적 항암제입니다. | ||||||||||||||||||||||||||||||
| 진행경과 |
위암 3/4차 치료제: 단독 요법으로 글로벌 임상 3상 후 미국 NDA 신청 준비 중
|
||||||||||||||||||||||||||||||
| 향후계획 | 위암 3/4차 치료제(Rivoceranib 단독) 미국 FDA pre-NDA 진행, FDA에서 요청한 보완 자료 준비 중, 자료 보완 후 NDA 제출 예정 위암 2차 치료제(파클리탁셀 병용) 임상 1상 결과 분석 선양낭성암 1,2차 치료제(Rivoceranib 단독)1,2차 치료제: 임상 2상 결과 수집 및 분석 간암 1차 치료제(항서제약 캄렐리주맙 병용): 임상 3상 결과 수집, 분석 및 Pre-NDA 준비 대장암 3차 치료제(타이호제약 론서프 병용) : 임상 1상 결과 수집 및 분석 |
||||||||||||||||||||||||||||||
| 경쟁제품 | 위암 3차 치료제: 론서프, 옵디보(한국, 일본, 대만 한정) 위암 2차 치료제: 시람자(cyramza), 파클리탁셀 선양낭성암 1,2차 치료제: 표준치료제 없음 (Off-label)로 치료 진행 간암 1차 치료제: 넥사바, 렌비마, 아바스틴, 티센트릭 대장암 3차 치료제: 론서프, 스티바가, 옵디보 |
||||||||||||||||||||||||||||||
| 관련논문등 |
위암
|
||||||||||||||||||||||||||||||
| 시장규모 |
위암 치료제 글로벌 시장: 2021년 28억8000만 달러에서 2025년에는 31억1000만 달러로 성장 예상 선낭암 치료제 글로벌 시장: 표준치료제가 없고 발병률이 낮아 글로벌 시장 규모 추산이 어려움 간암 치료제 글로벌 시장: 2020년 20억3750만 달러에서 2027년 27억7571만 달러로 성장 예상 대장암 치료제 글로벌 시장: 2018년 92억6000만 달러에서 2026년 165억8000만 달러로 성장 예상 ※시장규모 관련 출처 |
||||||||||||||||||||||||||||||
| 기타사항 | 특허 및 권리 보유 현황 - 리보세라닙의 물질특허: HLB - 글로벌 전용실시권은: Elevar - 한국 전용실시권: HLB생명과학 - 중국 전용실시권: 중국 항서제약이 보유 항서제약에서 2014년 위암 3차 치료제(Rivoceranib 단독)로 중국 내 시판허가를 득한 후 현재까지 꾸준한 매출 성장 유지 중입니다. 2015년 매출 약 450억에서 2018년 2,800억까지 매출 성장을 보여줘, 약효와 안전성을 입증하였습니다. 2021년 부터 간암 2차 치료제로 적응증을 확대하여, 중국 내 매출 확대가 기대 됩니다. |
(나) : 아필리아
| 구 분 | 화학합성의약품 |
| 적응증 | 백금계 약물 감수성이 있는 난소암 2차 치료제 |
| 작용기전 | 세포 분열에 필요한 RNA나 DNA 등을 손상시켜 세포 분열을 저지하는 세포 주기 선택적 항암제 |
| 제품의특성 | 파클리탁셀은 세포분열 과정 중 분열과 자가 복제의 기구인 미세소관이 분리되는 과정을 방해하는 "식물성 알칼로이드"로 분류되는 항암제입니다. 중증 과민반응 발현을 최소화하기 위해 투여 전에 전치료를 받아야 합니다. Apealea는 특허 출원된 Micelle 코팅을 적용하여 사전처치 필요없이 편의성을 증대시키며 부작용을 줄일 수 있도록 개발한 첨가제 형태 기반의 최적의 파크리탁셀 혼합제입니다. |
| 진행경과 | 유럽, 남미, 중동 지역 판매 준비 중 백금계 약물 저항성이 있는 난소암 환자 대상 임상 1상, 3상 동시 준비 중 |
| 향후계획 | -기 승인 받은 지역 대상 판매 준비 유럽, 중동, 북아프리카, 남미 지역 대상으로 판매 절차 진행 중 중국 진출을 위해 중국 현지업체와 JV를 통한 논의 중 -추가 적응증 개발 백금계 약물 저항성이 있는 난소암 환자를 대상으로 Rivoceranib과 병용 임상 계획 검토 중 |
| 경쟁제품 | 카보플라틴, 시스플라틴, 파클리탁셀, 아바스틴 |
| 관련논문등 | A randomized phase III trial in patients with recurrent platinum sensitive ovarian cancer comparing efficacy and safety of paclitaxel micellar and Cremophor EL-paclitaxel |
| 시장규모 | 글로벌 난소암 시장은 2021년 1억 7,500만달러 규모였으며, 2028년까지 매년 9.5% 성장하여 약 3억 3,973만달러에 이를 것으로 예상 ※시장규모 관련 출처 - Market Research Guru "Global Ovarian Cancer Market Research Report 2022" (2022.07) |
| 기타사항 | -특허 및 권리 보유 현황 Apealea 글로벌 전용실시권: Elevar (북유럽, 동유럽 일부국가 제외) -판매 승인 현황 2020년 유럽 EMA로 부터 난소암 2차 치료제로 판매 승인 (carboplatin 병용) 2022년 내 유럽 내 판매 개시 목표 |
(다) : ITI
| 구 분 | 바이오의약품 |
| 적응증 | GBM (교모세포종) |
| 작용기전 | UNITE 플랫폼은 리소좀관련막단백질(LAMP)에 특정 암에 발현되는 항원을 탑재해 면역세포를 빠르고 효율적으로 활성화시키는 기전 |
| 제품의특성 | 기존 기술 대비 CD4+ Helper T 세포 활성화에 가장 효과적 동일 APC 세포 내 MHC I & II Mediated Pathway 를 동시에 활성화 가능 (MHC II Pathway 직접적으로 관여) 다양한 질환 분야에 적용 가능 (암, 감염 질환, 자가면역 질환 등) 세포 기반 치료제, 핵산 (Nucleic Acid, DNA/RNA) 기반 치료제 개발 등 다양한 기술에 적용 가능 |
| 진행경과 | ITI-1000 교모세포종 (Dendritic Cell vaccine): 임상 2상 진행 중 ITI-1001교모세포종(DNA vaccine): 1상 IND 승인 후 임상 진행 중 ITI-3000 메르켈세포암(DNA vaccine): 1상 IND 승인 후 임상 진행 중 |
| 향후계획 | ITI-1000 연내 임상 2상 종료 후, FDA와 협의를 통해 조건부 허가 추진 |
| 경쟁제품 | 교모세포종: 테모졸로마이드 (2003년 승인) |
| 관련논문등 | 2009 Gene Therapy 16 2015 Nature 2017 Clinical Cancer Reserch 23(8) |
| 시장규모 | 글로벌 교모세포종 시장은 2021년 약 22억 9천만 달러에서 2028년 약 42억 달러에 이를 것으로 예상됩니다. ※시장규모 관련 출처 - Grand View Reserach "Glioblastoma Multiforme Treatment Market Size, Share & Trends Analysis Report By Treatment (Radiation Therapy, Immunotherapy), By Drug Class, By End Use, By Region, And Segment Forecasts, 2021 - 2028" (2021.09) |
| 기타사항 | 현재 교모세포종 원발성 악성 뇌종양 중 가장 흔한 종양으로 진단 후 치료를 하지 않으면 3-6개월 내에 사망합니다. 현재 치료법이 제한적이고 5년 생존율이 5%미만으로 악성도가 높은 질환입니다. ITI-1000 교모세포종 임상 1상 시험에서 mOS을 38.3 개월로 크게 개선하였으며, 표준치료제로 알려진 TMZ/RT 요법 대비 23 개월 이상 생존 기간을 향상시키고 60개월 생존율 또한 36.4%로 증가해 임상 2상 결과 또한 기대하고 있음. |
Elevar는 리보세라닙 위암 말기 단독치료제를 목적으로 하는 3상 임상시험 완료 후 데이터를 확정하여 2019년 10월 미국 FDA와 Pre-NDA 미팅을 하였으며, 그 결과를바탕으로 최종 Data분석 및 적절한 허가 전략을 수립한 후, 신약허가를 신청할 계획입니다. 선양낭성암 1,2차 치료제(Rivoceranib 단독)은 2022년 6월 미국종양학회(ASCO)에서 임상 데이터를 공개했고, 표준치료제가 없는 희귀암종의 이점을 살려FDA의 가속승인(조건부판매)를 목표로 전략을 수립하고 있습니다. 그리고, 2022년 5월 통계적 유의성을 확보했다고 이미 밝힌 바 있는 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 3상 임상은 2022년 8월 미국 FDA에 Pre-NDA를 신청했고,최근 2022년 9월 ESMO(유럽종양학회)에서 데이터를 공개해 1차 평가지표를 만족했음을 밝혔습니다. 통상적으로 임상 결과의 유효성을 입증하는 1차 평가지표는 적응증, 치료방식, 대조군 등에 따라 다르게 이루어집니다. 당사가 진행한 간암 1차 치료제 글로벌 3상 임상(항서제약 캄렐리주맙 병용)의 경우 기존 1차 치료제인 소라페닙을 대조군으로 하여 OS와 PFS를 1차 평가지표로 하여 진행되었습니다. mOS의 경우 대조군인 소라페닙 대비 6.9개월 긴 22.1개월을기록했고, mPFS는 대조군 대비 1.9개월 증가한 5.6개월을 기록해(통계적 유의성 확보) 1차 평가지표의 유효성을 만족했습니다.
| [간암 1차 치료제 글로벌 임상 3상 주요 결과] |
| 주요 평가지표 | Rivoceranib + Camrelizumab |
Sorafenib (대조군) |
p-value | HR |
|---|---|---|---|---|
| mOS | 22.1개월 | 15.2개월 | < 0.0001 | 0.62 |
| mPFS | 5.6개월 | 3.7개월 | < 0.0001 | 0.52 |
| ORR | 25.40% | 5.90% | < 0.0001 | - |
| DCR | 78.30% | 53.90% | - | - |
| CR | 3명 | 1명 | - | - |
회사는 본 임상결과를 바탕으로 FDA와의 Pre-NDA미팅 준비 등 후속 개발에 박차를 가하고 있습니다. 앞서 언급한 위암 3차 치료제(Rivoceranib 단독), 간암 1차 치료제(항서제약 캄렐리주맙 병용), 선양낭성암 1차 치료제 모두 희귀의약품에 지정되어 있어 임상종료 후 개별 국 진입 시 시판허가에 대한 신속화, 수수료 감면 등의 혜택과 더불어 신약 허가를 득할 경우 그 이후 최소 8년에서 최대 13년동안 독점 판매할 수 있습니다.이와 관련해 리보세라닙이 희귀의약품으로 지정 받은 내역은 아래와 같습니다. 위암(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국), 간암 (2021년 11월 미국식품의약국), 선양낭성암 (2021년 2월 미국식품의약국) 특히, 리보세라닙은 현재 위암 3차 치료제와 간암 2차 치료제에 대해서는 중국에서 항서제약이 임상 3상을 종료 후 시판허가를 득하여 현재 중국에서 판매되고 있습니다.
(주2) 정정 전
Elevar는 미국, 일본, 한국, 대만, 유럽 등 12개 국가에서 리보세라닙 글로벌 위암 임상 3상을 완료하였으며, 2019년 10월 미국 FDA와 Pre-NDA 미팅을 완료하였습니다. Elevar는 임상 3상 결과 및 Pre-NDA meeting 결과를 바탕으로 신약허가 전문컨설팅회사의 도움을 받아 최선의 신약 허가전략을 수립한 후 FDA에 신약 허가(NDA)를 신청할 예정입니다. 그 외에도 선양낭성암 2상 결과를 토대로 가속승인(조건부승인)을 추진하고 있고, 2022년 5월 통계적 유의성이 확보 되었다고 밝힌 바 있는 간암 1차 치료제 글로벌 임상 3상의 경우 2022년 5월 통계적 유의성이 확보됐다고 밝혔고, 그 결과를 토대로 8월에 미국 FDA에 Pre-NDA 미팅 신청을 했습니다. 2022년 9월 ESMO(유럽종양학회)에서 공개한 3상 임상의 결과를 토대로(1차 평가지표 만족)Pre-NDA미팅 준비 등 후속 개발에 힘쓰고 있습니다. 하지만 신약에 대한규제가 강화되거나 예상하지 못한 자료가 요구되는 경우 리보세라닙(위암 말기 치료제)의 품목 허가 시점이 지연되거나 거절될 가능성이 존재하며, 품목허가가 되더라도상업화 성공이 보장되는 것은 아닙니다.
(중략)
리보세라닙 물질의 적용 분야 중 위암 3차 치료제와 간암 2차 치료제의 경우 이미 중국에서의 임상 3상 종료 후 시판허가를 득하여 현재 중국 내에서 판매되고 있음에 따라 그 효과와 안정성이 입증되고 있습니다. 리보세라닙은 위암 3차 치료제, 간암 1차 치료제, 선양낭성암 1차 치료제로서 희귀의약약품으로 지정 받아 유효성과 안전성을 인정받았습니다. 하지만 희귀의약품지정 사실이 개발신약의 성공을 보장하지는 않습니다. 투자자 여러분께서는 이점을 유의하시어 투자에 임하시기 바라며 희귀약품지정에 관한 상세한 내용은 "III. 투자위험요소 - 1. 사업위험 - 사."를 참고하시기 바랍니다.
리보세라닙은 2011년 11월 미국 FDA로부터 표준치료에 실패한 고형암 환자에 대해다국가(미국, 한국) 임상 1상/임상 2상a 시험을 위한 임상시험계획(IND, Investigational New Drug)을 승인(US FDA, 한국 식약처)받아 표적항암제 리보세라닙(아파티닙)다국가(미국-헌쯔만 암센터/한국-아산병원) 임상 1상/2a상을 완료하여 안전성에 대한 검증을 받았습니다. 2017년 위암 2차 이상 표준 치료에 실패한 환자 460명을 대상으로 다국가 임상 3상 진행을 개시한 후 그해 3월 첫 환자 투여를 시작으로 12개국, 88개 병원에서 진행하였으며, 2019년에 9월에 유럽종양학회(ESMO)에서 임상3상에 대한 결과발표를 하였습니다. 이러한 3상 결과를 간략히 요약하면, 리보세라닙의 무진행생존기간(PFS)는 2.83개월, 전체생존기간(OS)은 5.78개월로 나왔습니다. 당시 위암 3차 치료제는 표준요법이 없었기 때문에, 최적지지요법(Best Supportive Care)을 대조군으로 사용하였으며, 대조군 전체생존기간은 5.13개월로 무진행생존기간은 1.77개월로 나왔습니다. 상기 결과치 중 1차 유효성 평가 지표인 전체생존기간은 대조군 대비 높게 나오기는 했으나 통계적 유효성이 부족한 것으로 판단되었습니다. 이에 당사는 3상 종료 직후 OS가 최종 임상 목표치에 도달하지 못하였으며 FDA 승인 진행이 불투명하다는 내용으로 3상 결과 발표를 한 바 있습니다. 이후 당사는 임상 3상의 모든 데이터에 대한 종합적 분석을 진행하였고, 무진행생존기간에 대한 결과는 통계적 유의성을 확보하였고, 다른 평가지표인 객관적반응률 등의 결과도 대조군과 대비하여 월등한 결과를 나왔기 때문에 그 결과가 신약으로서의 가치가 충분하다는 판단하에 FDA와의 Pre NDA Meeting을 진행하였습니다. 이후 신약허가 전문컨설팅회사의 도움을 받아 최선의 신약허가 전략을 수립한 후, NDA 및 신약허가를 추진중에 있습니다.
2019년 4월부터 절제불가능한 간세포암 환자 543명을 대상으로 다국가 임상 3상을 13개국 136개 병원에서 진행하였습니다. 간세포암 1차 치료제로 리보세라닙과 항서제약의 면역항암제인 PD-1 항체인 캄렐리주맙(Camrelizumab)과 병용투여한 이번 임상은 전체생존기간(OS)과 무진행생존기간(PFS)을 1차 유효성 지표로 설정해 간암1차 표준치료제인 ‘소라페닙’(상품명 넥사바)과 대조하는 방식으로 진행되었습니다. 2022년 5월 1차 평가지표인 전체생존기간과 무진행생존기간 모두가 통계적 유의성을 확보하였다고 발표하였고, 본 임상의 결과는 2022년 9월 유럽종양학회(ESMO)에서 공개해 1차 평가지표를 만족했음을 밝혔습니다.
(주2) 정정 후
Elevar는 미국, 일본, 한국, 대만, 유럽 등 12개 국가에서 리보세라닙 글로벌 위암 임상 3상을 완료하였으며, 2019년 10월 미국 FDA와 Pre-NDA 미팅을 완료하였습니다. Elevar는 임상 3상 결과 및 Pre-NDA meeting 결과를 바탕으로 신약허가 전문컨설팅회사의 도움을 받아 최선의 신약 허가전략을 수립한 후 FDA에 신약 허가(NDA)를 신청할 예정입니다. 그 외에도 선양낭성암 1,2차 치료제(Rivoceranib 단독) 2상 결과를 토대로 가속승인(조건부승인)을 추진하고 있고, 2022년 5월 통계적 유의성이 확보 되었다고 밝힌 바 있는 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상 3상의 경우 2022년 5월 통계적 유의성이 확보됐다고 밝혔고, 그 결과를 토대로 8월에 미국 FDA에 Pre-NDA 미팅 신청을 했습니다. 2022년 9월 ESMO(유럽종양학회)에서 공개한 3상 임상의 결과를 토대로(1차 평가지표 만족)Pre-NDA미팅 준비 등 후속 개발에 힘쓰고 있습니다. 하지만 신약에 대한 규제가 강화되거나 예상하지 못한 자료가 요구되는 경우 리보세라닙(위암 말기 치료제)의 품목 허가 시점이 지연되거나 거절될 가능성이 존재하며, 품목허가가 되더라도 상업화 성공이 보장되는 것은 아닙니다.
(중략)
리보세라닙 물질의 적용 분야 중 위암 3차 치료제와 간암 2차 치료제의 경우 이미 중국에서의 임상 3상 종료 후 시판허가를 득하여 현재 중국 내에서 판매되고 있음에 따라 그 효과와 안정성이 입증되고 있습니다. 리보세라닙은 위암 3차 치료제, 간암 1차치료제(항서제약 캄렐리주맙 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독)로서 희귀의약약품으로 지정 받아 유효성과 안전성을 인정받았습니다. 하지만 희귀의약품지정 사실이 개발신약의 성공을 보장하지는 않습니다. 투자자 여러분께서는 이점을 유의하시어 투자에 임하시기 바라며 희귀약품지정에 관한 상세한 내용은 "III. 투자위험요소 - 1. 사업위험 - 사."를 참고하시기 바랍니다.
리보세라닙은 2011년 11월 미국 FDA로부터 표준치료에 실패한 고형암 환자에 대해다국가(미국, 한국) 임상 1상/임상 2상a 시험을 위한 임상시험계획(IND, Investigational New Drug)을 승인(US FDA, 한국 식약처)받아 표적항암제 리보세라닙(아파티닙)다국가(미국-헌쯔만 암센터/한국-아산병원) 임상 1상/2a상을 완료하여 안전성에 대한 검증을 받았습니다. 2017년 위암 2차 이상 표준 치료에 실패한 환자 460명을 대상으로 다국가 임상 3상 진행을 개시한 후 그해 3월 첫 환자 투여를 시작으로 12개국, 88개 병원에서 진행하였으며, 2019년에 9월에 유럽종양학회(ESMO)에서 임상3상에 대한 결과발표를 하였습니다. 이러한 3상 결과를 간략히 요약하면, 리보세라닙의 무진행생존기간(PFS)는 2.83개월, 전체생존기간(OS)은 5.78개월로 나왔습니다. 당시 위암 3차 치료제는 표준요법이 없었기 때문에, 최적지지요법(Best Supportive Care)을 대조군으로 사용하였으며, 대조군 전체생존기간은 5.13개월로 무진행생존기간은 1.77개월로 나왔습니다. 상기 결과치 중 1차 유효성 평가 지표인 전체생존기간은 대조군 대비 높게 나오기는 했으나 통계적 유효성이 부족한 것으로 판단되었습니다. 이에 당사는 3상 종료 직후 OS가 최종 임상 목표치에 도달하지 못하였으며 FDA 승인 진행이 불투명하다는 내용으로 3상 결과 발표를 한 바 있습니다. 이후 당사는 임상 3상의 모든 데이터에 대한 종합적 분석을 진행하였고, 무진행생존기간에 대한 결과는 통계적 유의성을 확보하였고, 다른 평가지표인 객관적반응률 등의 결과도 대조군과 대비하여 월등한 결과를 나왔기 때문에 그 결과가 신약으로서의 가치가 충분하다는 판단하에 FDA와의 Pre NDA Meeting을 진행하였습니다. 이후 신약허가 전문컨설팅회사의 도움을 받아 최선의 신약허가 전략을 수립한 후, NDA 및 신약허가를 추진중에 있습니다.
2019년 4월부터 절제불가능한 간세포암 환자 543명을 대상으로 다국가 임상 3상을 13개국 136개 병원에서 진행하였습니다. 간세포암 1차 치료제로 리보세라닙과 항서제약의 면역항암제인 PD-1 항체인 캄렐리주맙(Camrelizumab)과 병용투여한 이번 임상은 전체생존기간(OS)과 무진행생존기간(PFS)을 1차 유효성 지표로 설정해 간암1차 표준치료제인 ‘소라페닙’(상품명 넥사바)과 대조하는 방식으로 진행되었습니다. 2022년 5월 1차 평가지표인 전체생존기간과 무진행생존기간 모두가 통계적 유의성을 확보하였다고 발표하였고, 본 임상의 결과는 2022년 9월 유럽종양학회(ESMO)에서 공개해 1차 평가지표를 만족했음을 밝혔습니다. 통상적으로 임상 결과의 유효성을 입증하는 1차 평가지표는 적응증, 치료방식, 대조군 등에 따라 다르게 이루어집니다. 당사가 진행한 간암 1차 치료제 글로벌 3상 임상(항서제약 캄렐리주맙 병용)의 경우 기존 1차 치료제인 소라페닙을 대조군으로 하여 OS와 PFS를 1차 평가지표로 하여 진행되었습니다. mOS의 경우 대조군인 소라페닙 대비 6.9개월 긴 22.1개월을 기록했고, mPFS는 대조군 대비 1.9개월 증가한 5.6개월을 기록해(통계적 유의성 확보) 1차 평가지표의 유효성을 만족했습니다.
| [간암 1차 치료제 글로벌 임상 3상 주요 결과] |
| 주요 평가지표 | Rivoceranib + Camrelizumab |
Sorafenib (대조군) |
p-value | HR |
|---|---|---|---|---|
| mOS | 22.1개월 | 15.2개월 | < 0.0001 | 0.62 |
| mPFS | 5.6개월 | 3.7개월 | < 0.0001 | 0.52 |
| ORR | 25.40% | 5.90% | < 0.0001 | - |
| DCR | 78.30% | 53.90% | - | - |
| CR | 3명 | 1명 | - | - |
2020년 선양낭성암 환자에 대해 선양낭성암 1,2차 치료제(Rivoceranib 단독) 다국가 임상 2상 진행을 개시한 후, 그 해 3월 첫환자 투여를 시작으로 미국과 한국에서11개기관에서 진행하였으며, 2022년 6월 미국종양학회(ASCO)에서 결과발표를 하였습니다. 선양낭성암은 아직까지 표준치료제가 없어서, 이번 임상은 대조군 설정 없이 경구용 항암제인 리보세라닙 700mg을 일일 투여 후 객관적반응률과 함께 반응지속기간, 무진행생존기간 등을 확인하는 방식으로 진행됐었습니다. 그 결과를 간단히 요약하면, 80명의 환자를 모집하였으며 1차 지표인 객관적반응률(ORR)이 암의 크기변화를 기준으로 하는 반응평가기준(RECIST v1.1) 15.1%, 크기변화와 함께 밀도를 측정하는 CHOI 평가기준 50.8%에 도달해 선낭암 치료제로 높은 가능성을 확인하였습니다. 당사는 현재 이러한 2상 결과를 바탕으로 FDA에 가속승인(조건부판매)를 목표로 전략을 수립 중에 있습니다. 다만, 이러한 임상 결과에 대한 해석과 판단은 당사의 의견이며, 상기 임상 결과를 토대로 리보세라닙이 신약 허가를 받을 수 있다고 보장할 수는 없다는 점에 유의하시기 바랍니다.
(주3) 정정 전
Elevar는 리보세라닙을 중심으로 다양한 암종에 대하여 항암제 신약 개발 및 허가 취득을 추진하고 있으며, 특히 위암 말기 치료제 허가 과정은 임상 3상까지 완료되어 미 FDA의 최종 신약 허가 단계인 NDA 직전까지 진행된 바 있습니다. 그리고 최근 선양낭성암 2상 결과를 토대로 FDA에 가속승인(조건부판매)을 목표로 전략 수립 중이고, 2022년 8월엔 간암 1차 치료제 승인을 목표로 미국 FDA에 Pre-NDA 미팅 신청을 하였습니다. 그러나 증권신고서 제출일 현재까지 Elevar로부터 발생한 매출은 사실상 없으며, 오히려 실적 기준으로는 당사의 연결기준 연구개발비 지출로 인해 영업손실 기록의 직접적인 원인이 되고 있습니다.
| [실적 및 경상연구개발비/판관비 추이] | |
| (연결기준) | (단위: 원) |
| 2022년 반기 | 2021년 반기 | 2021년 | 2020년 | 2019년 | |
|---|---|---|---|---|---|
| 수익(매출액) | 123,305 | 15,957 | 69,826 | 56,177 | 38,421 |
| 매출원가 | 73,343 | 15,439 | 48,759 | 45,869 | 34,484 |
| 매출총이익 | 49,961 | 518 | 21,067 | 10,308 | 3,937 |
| 판매비와관리비 | 70,057 | 40,275 | 122,086 | 71,620 | 52,668 |
| 경상연구개발비 | 22,603 | 10,566 | 48,419 | 22,594 | 33,835 |
| 전체 판관비 중 경상연구개발비 비중 | 32.3% | 26.2% | 39.7% | 31.5% | 64.2% |
| 매출액 대비 경상연구개발비 비율 | 18.3% | 66.2% | 69.3% | 40.2% | 88.1% |
| 영업이익(손실) | (20,096) | (39,757) | (101,018) | (61,312) | (48,731) |
| 당기순이익(손실) | (19,100) | (57,078) | (111,607) | (88,716) | (59,660) |
당사의 연결기준 경상연구개발비는 매년 증가하여, 2019년 33,835백만원에서 2020년 22,594백만원 수준으로 일부 감소하였으나, 2021년에는 연간 경상연구개발비가 약 48,419백만원으로 2019년 연간 연구개발비 대비 43.1% 증가하였습니다. 2020년경상연구개발비는 22,594백만원으로 전년 동기 대비 33.2% 감소(11,241백만원 감소)한 모습을 나타내는데, 이는 위암말기치료제의 글로벌 임상3상이 종료에 기인했으며, 2022년 반기 경상연구개발비는 22,603백만원으로 전년 동기 대비 113.9% 증가(12,037백만원 증가)한 모습을 나타내는데, 이는 선양낭성암 2상 임상 및 간암 글로벌 임상3상 비용에 기인합니다.
2022년 하반기 또는 그 이후 당사가 계획하고 있는 간암1차, 선양낭성암 1차, 위암2차 및 대장암3차 치료제의 콤보임상 등이 차질 없이 진행될 경우 경상연구개발비는 추가적으로 증가할 수 있습니다. 경상연구개발비가 판매비와 관리비 중 차지하는 비중은 2021년 연간 기준 39.7%이며, 이는 연결기준 전체 매출액의 69.3%에 해당합니다. 당사의 연결기준 경상연구개발비 지출은 대부분 Elevar가 진행하는 임상 비용 등으로 사용되는 액수이며, 이는 당사가 자체적으로 영위하는 사업에서 지속적으로 매출총이익이 발생하고 있으나 판관비의 비용 처리 이후 영업손실으로 이어지는 직접적인 원인이라고 볼 수 있습니다.
(주3) 정정 후
Elevar는 리보세라닙을 중심으로 다양한 암종에 대하여 항암제 신약 개발 및 허가 취득을 추진하고 있으며, 특히 위암 말기 치료제 허가 과정은 임상 3상까지 완료되어 미 FDA의 최종 신약 허가 단계인 NDA 직전까지 진행된 바 있습니다. 그리고 최근 선양낭성암 1,2차 치료제(Rivoceranib 단독) 2상 결과를 토대로 FDA에 가속승인(조건부판매)을 목표로 전략 수립 중이고, 2022년 8월엔 간암 1차 치료제(항서제약 캄렐리주맙 병용) 승인을 목표로 미국 FDA에 Pre-NDA 미팅 신청을 하였습니다. 그러나 증권신고서 제출일 현재까지 Elevar로부터 발생한 매출은 사실상 없으며,오히려 실적 기준으로는 당사의 연결기준 연구개발비 지출로 인해 영업손실 기록의 직접적인 원인이 되고 있습니다.
| [실적 및 경상연구개발비/판관비 추이] | |
| (연결기준) | (단위: 원) |
| 2022년 반기 | 2021년 반기 | 2021년 | 2020년 | 2019년 | |
|---|---|---|---|---|---|
| 수익(매출액) | 123,305 | 15,957 | 69,826 | 56,177 | 38,421 |
| 매출원가 | 73,343 | 15,439 | 48,759 | 45,869 | 34,484 |
| 매출총이익 | 49,961 | 518 | 21,067 | 10,308 | 3,937 |
| 판매비와관리비 | 70,057 | 40,275 | 122,086 | 71,620 | 52,668 |
| 경상연구개발비 | 22,603 | 10,566 | 48,419 | 22,594 | 33,835 |
| 전체 판관비 중 경상연구개발비 비중 | 32.3% | 26.2% | 39.7% | 31.5% | 64.2% |
| 매출액 대비 경상연구개발비 비율 | 18.3% | 66.2% | 69.3% | 40.2% | 88.1% |
| 영업이익(손실) | (20,096) | (39,757) | (101,018) | (61,312) | (48,731) |
| 당기순이익(손실) | (19,100) | (57,078) | (111,607) | (88,716) | (59,660) |
당사의 연결기준 경상연구개발비는 매년 증가하여, 2019년 33,835백만원에서 2020년 22,594백만원 수준으로 일부 감소하였으나, 2021년에는 연간 경상연구개발비가 약 48,419백만원으로 2019년 연간 연구개발비 대비 43.1% 증가하였습니다. 2020년경상연구개발비는 22,594백만원으로 전년 동기 대비 33.2% 감소(11,241백만원 감소)한 모습을 나타내는데, 이는 위암말기치료제의 글로벌 임상3상이 종료에 기인했으며, 2022년 반기 경상연구개발비는 22,603백만원으로 전년 동기 대비 113.9% 증가(12,037백만원 증가)한 모습을 나타내는데, 이는 선양낭성암 1,2차 치료제(Rivoceranib 단독) 2상 임상 및 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상3상 비용에 기인합니다.
2022년 하반기 또는 그 이후 당사가 계획하고 있는 간암 1차 치료제(항서제약 캄렐리주맙 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독), 위암2차 및 대장암 3차 치료제(타이호제약 론서프 병용)의 콤보임상 등이 차질 없이 진행될 경우 경상연구개발비는 추가적으로 증가할 수 있습니다. 경상연구개발비가 판매비와 관리비 중 차지하는 비중은 2021년 연간 기준 39.7%이며, 이는 연결기준 전체 매출액의 69.3%에 해당합니다. 당사의 연결기준 경상연구개발비 지출은 대부분 Elevar가 진행하는 임상 비용 등으로 사용되는 액수이며, 이는 당사가 자체적으로 영위하는 사업에서 지속적으로 매출총이익이 발생하고 있으나 판관비의 비용 처리 이후 영업손실으로 이어지는 직접적인 원인이라고 볼 수 있습니다.
(주4) 정정 전
(1) License-in / 리보세라닙
| 계약상대방 | Advenchen Laboratories |
| 계약내용 | YN968D1-Small Molecule Angiogenesis Inhibitor의 계약상 명시된 지역에서의전용실시권 취득 |
| 대상지역 | 중국을 제외한 모든 국가 |
| 계약기간 | 계약체결일:2007. 12. 21(계약서 내용 조정일 2008, 11, 11) (계약서 내용 조정일 2015, 06, 15) (계약서 내용 조정일 2017, 02, 27) (계약서 내용 조정일 2019, 12, 20) 계약종료일: 유효특허의 만료일까지 (물질특허: 2024년 예상, 염조성물특허: 2029년 예상) |
| 총계약금액 | Upfront: 150,000 USD |
| 지급금액 | <환수 불가능 금액> 계약금(Upfront Payment): 150,000USD 2007년 기 지급 완료 마일스톤(Milestione): 임상 진행 단계에 진행에 따라 개발 Milestione $800,000USD 지급 로열티(Royalty): 매출없음 <환수 가능 금액> 해당사항 없음 |
| 계약조건 | 계약 조정 내역을 포함한 최종 계약 조건 계약금(Upfront Payment): 150,000USD - 지급조건: 계약 체결 45일 이내 마일스톤(Milestione): 적응증, 진입국가, 매출에 따라 단계별 마일스톤 실행 예정 로열티: 3.5%~10%,지역별 매출액 비율에 따른 로열티 실행 예정 Advenchen이 보유한 Appatinib(Rivoceranib)의 염조성물 특허를 LSKB에 허여한다. 국가별 특허(물질특허 및 염조성물특허) 유지 상태에 따라 상호 협의한 비율에 의거해 로열티를 조정한다. LSKB가 보유한 모든 권리는 Elevar가 승계한다. |
| 회계처리방법 | 최초 지급한 Upfront 150,000USD는 무형자산으로 인식해 감가상각 완료 이후 지급한 Milestone 비용은 당기비용으로 인식 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 Rivoceranib과 염특허 전용 특허 실시권 |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1/2차 치료제 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 ESMO에서 간암 1차 치료제 글로벌 임상 3상 결과 발표 (1차 평가지표 만족) |
| 기타사항 | 판매 승인 현황 중국 판권을 보유한 헝루이제약에서 2014년 위암 3차 치료제, 2020년 간암 2차 치료제로 시판 허가 득한 후 판매 중 |
(2) License-out / 리보세라닙
| 계약상대방 | 부광약품㈜ |
| 계약내용 | Rivoceranib에 대한 특정 지역의 개발, 판매에 대한 권리 Sublicense(한국, 유럽, 일본) 및 공동개발 |
| 대상지역 | 대한민국, 일본, 유럽 |
| 계약기간 | 계약체결일:2009. 1. 8 (계약서 내용 조정일 2012, 2, 1) (계약서 내용 조정일 2015, 7, 28) (계약서 내용 조정일 2015, 10, 30) (계약서 내용 조정일 2017, 1, 2) 계약종료일: 유효특허의 만료일까지 (물질특허: 2024년 예상, 염조성물특허: 2029년 예상) |
| 총계약금액 | Potential Sales Royalty: 매출액에 따라 6~10% 특허가 국가별로 개별 종료 될 시 최대 10년까지 상기 로열티의 10%를 지급 |
| 지급금액 | 해당사항 없음 |
| 계약조건 | 주요 계약 내용 1) 한국내 독점개발, 판매권 및 유럽, 일본에 대한 수익 지분 2) 국내 시판시 판매액의 6~10% 로열티 지불 (Sublicensing,진행시 수익의 30% 지불) |
| 회계처리방법 | 해당사항 없음 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 Rivoceranib 특허 전용실시권 |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1/2차 치료제 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 ESMO에서 간암 1차 치료제 글로벌 임상 3상 결과 발표 (1차 평가지표 만족) |
| 기타사항 | Elevar Therapeutics, Inc. 는 2009년 12월 부광약품㈜에게 리보세라닙의 한국 판권을 양도하는 조건으로 리보세라닙 공동개발을 하였으며, 이후 부광약품㈜은 2018년 08월 한국 판권에 대한 모든 권리 및 의무를 에이치엘비생명과학㈜으로 400억원에 양도하였습니다. (2018.8.14 공시 참조) |
Elevar가 현재 리보세라닙 신약 연구개발을 진행하고 있는 주요 항목 중 임상을 개시할 계획이 있거나 임상이 진행중인 항목은 리보세라닙의 단독 및 병용임상을 포함하여 5개 항목입니다. 상세 내용은 하기와 같습니다.
| [Elevar의 리보세라닙 신약 임상 진행 및 허가 추진 현황] |
|
치료군 |
임상종류 |
진행상태 |
시점별 진행 예상 |
|---|---|---|---|
| 선낭암 1차 치료제 | 단독 | 글로벌 임상 2상 완료 | 2022년 4분기 NDA 신청을 목표로 준비 중 |
| 간암 1차 치료제 | 캄렐리주맙 병용 | 글로벌 임상 3상 진행중 | 2023년 NDA 신청을 목표로 준비 중 |
| 위암 말기 치료제 | 단독 | 글로벌 3상 완료 | 2023년 NDA 신청을 목표로 준비 중 |
| 대장암 3차 치료제 | 론서프 병용 | 임상 1b/2상 진행중 | 2022년 임상 1상 종료 후 다음 단계 진입 목표로 준비 중 |
| 위암 2차 치료제 | 파클리탁셀 병용 | 임상 1/2a상 진행중 | 2022년 임상 1상 종료 후 다음 단계 진입 목표로 준비 중 |
| 난소암 2차 치료제 (백금계 항암제 저항성) |
아필리아 병용 | 1b/3상 IND 준비 중 | 2022년 임상(1b/3상) 진행 목표로 준비 중 |
| 주) 상기 진행 예상 시점은 당사의 예측이며, 향후 지연, 취소 등의 변동이 있을 가능성이 상존합니다. |
일반적으로 신약의 개발은 후보물질 발견에서부터 전임상 및 임상시험, 품목허가 이후 실질적인 수익창출로 연결되기까지 많은 단계를 거쳐야 합니다. 따라서, 개발과정에서의 불확실성이 존재하며 단계가 진행될 수록 추가 연구개발비가 소요됩니다.
Elevar가 개발을 추진하고 있는 리보세라닙 신약 중 위암 말기 치료제의 경우 이미 대중에 알려진 대로 임상 3상까지 완료하였으며, 미국에서의 신약 시판 개시를 위한 마지막 단계인 FDA와의 NDA(New Drug Application, 신약 허가 신청)를 앞두고 준비 중에 있습니다. Elevar는 NDA에 앞서 2019년 10월 FDA와 Pre-NDA meeting을 완료하였습니다. 2022년 6월 결과를 발표한 선양낭성암 1차 치료제 임상 2상은 표준치료제가 없는 희귀암의 특성을 살려 미국 FDA의 가속승인(조건부판매)을 목표로 전략을 수립 중입니다. 그리고 항서제약의 캄렐리주맙과 병용으로 진행된 간암 1차 치료제 글로벌 임상 3상은 2022년 8월 미국 FDA에 Pre-NDA 미팅 신청을 한 상태 입니다. 2022년 9월 유럽암학회(ESMO)에서는 임상 결과를 공개함과 동시에 1차 평가지표를 만족했다고 발표 했습니다.
(주4) 정정 후
당사의 연결대상 종속회사인 Elevar Therapeutics, Inc. 에서 체결한 상태인 리보세라닙 관련 라이센스 계약에 대한 상세내용은 아래와 같습니다.
(1) License-in / 리보세라닙
| 계약상대방 | Advenchen Laboratories |
| 계약내용 | YN968D1-Small Molecule Angiogenesis Inhibitor의 계약상 명시된 지역에서의전용실시권 취득 |
| 대상지역 | 중국을 제외한 모든 국가 |
| 계약기간 | 계약체결일:2007. 12. 21(계약서 내용 조정일 2008, 11, 11) (계약서 내용 조정일 2015, 06, 15) (계약서 내용 조정일 2017, 02, 27) (계약서 내용 조정일 2019, 12, 20) 계약종료일: 유효특허의 만료일까지 (물질특허: 2024년 예상, 염조성물특허: 2029년 예상) |
| 총계약금액 | Upfront: 150,000 USD |
| 지급금액 | <환수 불가능 금액> 계약금(Upfront Payment): 150,000USD 2007년 기 지급 완료 마일스톤(Milestione): 임상 진행 단계에 진행에 따라 개발 Milestione $800,000USD 지급 로열티(Royalty): 매출없음 <환수 가능 금액> 해당사항 없음 |
| 계약조건 | 계약 조정 내역을 포함한 최종 계약 조건 계약금(Upfront Payment): 150,000USD - 지급조건: 계약 체결 45일 이내 마일스톤(Milestione): 적응증, 진입국가, 매출에 따라 단계별 마일스톤 실행 예정 로열티: 3.5%~10%,지역별 매출액 비율에 따른 로열티 실행 예정 Advenchen이 보유한 Appatinib(Rivoceranib)의 염조성물 특허를 LSKB에 허여한다. 국가별 특허(물질특허 및 염조성물특허) 유지 상태에 따라 상호 협의한 비율에 의거해 로열티를 조정한다. LSKB가 보유한 모든 권리는 Elevar가 승계한다. |
| 회계처리방법 | 최초 지급한 Upfront 150,000USD는 무형자산으로 인식해 감가상각 완료 이후 지급한 Milestone 비용은 당기비용으로 인식 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 Rivoceranib과 염특허 전용 특허 실시권 |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1,2차 치료제(Rivoceranib 단독) 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 ESMO에서 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상 3상 결과 발표 (1차 평가지표 만족) |
| 기타사항 | 판매 승인 현황 중국 판권을 보유한 항서제약에서 2014년 위암 3차 치료제, 2020년 간암 2차 치료제로 시판 허가 득한 후 판매 중 |
(2) License-out / 리보세라닙
| 계약상대방 | 부광약품㈜ |
| 계약내용 | Rivoceranib에 대한 특정 지역의 개발, 판매에 대한 권리 Sublicense(한국, 유럽, 일본) 및 공동개발 |
| 대상지역 | 대한민국, 일본, 유럽 |
| 계약기간 | 계약체결일:2009. 1. 8 (계약서 내용 조정일 2012, 2, 1) (계약서 내용 조정일 2015, 7, 28) (계약서 내용 조정일 2015, 10, 30) (계약서 내용 조정일 2017, 1, 2) 계약종료일: 유효특허의 만료일까지 (물질특허: 2024년 예상, 염조성물특허: 2029년 예상) |
| 총계약금액 | Potential Sales Royalty: 매출액에 따라 6~10% 특허가 국가별로 개별 종료 될 시 최대 10년까지 상기 로열티의 10%를 지급 |
| 지급금액 | 해당사항 없음 |
| 계약조건 | 주요 계약 내용 1) 한국내 독점개발, 판매권 및 유럽, 일본에 대한 수익 지분 2) 국내 시판시 판매액의 6~10% 로열티 지불 (Sublicensing,진행시 수익의 30% 지불) |
| 회계처리방법 | 해당사항 없음 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 Rivoceranib 특허 전용실시권 |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제(Rivoceranib 단독)위암 3차 치료제 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1,2차 치료제(Rivoceranib 단독) 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 ESMO에서 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상 3상 결과 발표 (1차 평가지표 만족) |
| 기타사항 | Elevar Therapeutics, Inc. 는 2009년 12월 부광약품㈜에게 리보세라닙의 한국 판권을 양도하는 조건으로 리보세라닙 공동개발을 하였으며, 이후 부광약품㈜은 2018년 08월 한국 판권에 대한 모든 권리 및 의무를 에이치엘비생명과학㈜으로 400억원에 양도하였습니다. (2018.8.14 공시 참조) |
Elevar가 현재 리보세라닙 신약 연구개발을 진행하고 있는 주요 항목 중 임상을 개시할 계획이 있거나 임상이 진행중인 항목은 리보세라닙의 단독 및 병용임상을 포함하여 5개 항목입니다. 상세 내용은 하기와 같습니다.
| [Elevar의 리보세라닙 신약 임상 진행 및 허가 추진 현황] |
|
치료군 |
임상종류 |
진행상태 |
시점별 진행 예상 |
|---|---|---|---|
| 선낭암 1차 치료제 | 단독 | 글로벌 임상 2상 완료 | 2022년 4분기 NDA 신청을 목표로 준비 중 |
| 간암 1차 치료제 | 캄렐리주맙 병용 | 글로벌 임상 3상 진행중 | 2023년 NDA 신청을 목표로 준비 중 |
| 위암 말기 치료제 | 단독 | 글로벌 3상 완료 | 2023년 NDA 신청을 목표로 준비 중 |
| 대장암 3차 치료제 | 론서프 병용 | 임상 1b/2상 진행중 | 2022년 임상 1상 종료 후 다음 단계 진입 목표로 준비 중 |
| 위암 2차 치료제 | 파클리탁셀 병용 | 임상 1/2a상 진행중 | 2022년 임상 1상 종료 후 다음 단계 진입 목표로 준비 중 |
| 난소암 2차 치료제 (백금계 항암제 저항성) |
아필리아 병용 | 1b/3상 IND 준비 중 | 2022년 임상(1b/3상) 진행 목표로 준비 중 |
| 주) 상기 진행 예상 시점은 당사의 예측이며, 향후 지연, 취소 등의 변동이 있을 가능성이 상존합니다. |
일반적으로 신약의 개발은 후보물질 발견에서부터 전임상 및 임상시험, 품목허가 이후 실질적인 수익창출로 연결되기까지 많은 단계를 거쳐야 합니다. 따라서, 개발과정에서의 불확실성이 존재하며 단계가 진행될 수록 추가 연구개발비가 소요됩니다.
Elevar가 개발을 추진하고 있는 리보세라닙 신약 중 위암 말기 치료제의 경우 이미 대중에 알려진 대로 임상 3상까지 완료하였으며, 미국에서의 신약 시판 개시를 위한 마지막 단계인 FDA와의 NDA(New Drug Application, 신약 허가 신청)를 앞두고 준비 중에 있습니다. Elevar는 NDA에 앞서 2019년 10월 FDA와 Pre-NDA meeting을 완료하였습니다. 2022년 6월 결과를 발표한 선양낭성암 1,2차 치료제(Rivoceranib 단독) 임상 2상은 표준치료제가 없는 희귀암의 특성을 살려 미국 FDA의 가속승인(조건부판매)을 목표로 전략을 수립 중입니다. 그리고 항서제약의 캄렐리주맙과 병용으로 진행된 간암 1차 치료제 글로벌 임상 3상은 2022년 8월 미국 FDA에 Pre-NDA 미팅 신청을 한 상태 입니다. 2022년 9월 유럽암학회(ESMO)에서는 임상 결과를 공개함과 동시에 1차 평가지표를 만족했다고 발표 했습니다. 통상적으로 임상 결과의 유효성을 입증하는 1차 평가지표는 적응증, 치료방식, 대조군 등에 따라 다르게 이루어집니다. 당사가 진행한 간암 1차 치료제 글로벌 3상 임상(항서제약 캄렐리주맙 병용)의 경우 기존 1차 치료제인 소라페닙을 대조군으로 하여 OS와 PFS를 1차 평가지표로 하여 진행되었습니다. mOS의 경우 대조군인 소라페닙 대비 6.9개월 긴 22.1개월을 기록했고, mPFS는 대조군대비 1.9개월 증가한 5.6개월을 기록해(통계적 유의성 확보) 1차 평가지표의 유효성을 만족했습니다.
| [간암 1차 치료제 글로벌 임상 3상 주요 결과] |
| 주요 평가지표 | Rivoceranib + Camrelizumab |
Sorafenib (대조군) |
p-value | HR |
|---|---|---|---|---|
| mOS | 22.1개월 | 15.2개월 | < 0.0001 | 0.62 |
| mPFS | 5.6개월 | 3.7개월 | < 0.0001 | 0.52 |
| ORR | 25.40% | 5.90% | < 0.0001 | - |
| DCR | 78.30% | 53.90% | - | - |
| CR | 3명 | 1명 | - | - |
(주5) 정정 전
3. 기업실사 일정 및 주요내용
| 일자 | 기업 실사 내용 |
|---|---|
| 2022년 07월 27일 | 가) 발행회사방문 - 유상증자 의사 및 자금조달 관련 논의 - 유상증자 필요성 검토 및 주요일정 협의 나) 회사 기본사항 점검 - 경영진 면담(경영철학, 회사연혁 등) - 사업내용 청취 및 주요제품 열람 |
| 2022년 7월 29일~ 8월 02일 |
가) 발행회사방문 - 실사 요청자료 송부 - 본사 방문 나) 회사 일반사항 관련 검토 - 정관검토 및 이사회 등 상법 절차 확인 - 경영진 평판 리스크 검토 - 회사의 사업 및 영업구조 관련 면담 |
| 2022년 08월 03일 ~ 08월 08일 |
가) 회사 기본사항 검토 - 정관 등 기본자료 수령 - 대략적인 자금 사용 목적 등에 관한 청취 - 발행 방식 및 조건 등에 관한 협의 - 금융당국으로부터 제재조치 여부 확인 - 근로기준법 위반행위, 소송진행 여부 확인 나) 산업에 관한 사항 검토 - 산업에 대한 이해 - 산업 경쟁상황, 시장규모, 성장주기 등 확인 - 법률 및 정부규제에 관한 사항 검토 - 시장 내 중대한 환경, 제도 변화요인 검토 다) 회사 지배구조에 관한 사항 검토 - 경영진의 변동내역 및 근무경력 검토 - 종속회사에 관한 사항 검토 - 최대주주의 지분율 및 경영권 안정성 검토 - 사내규정 및 내부통제시스템 확인 - 공시시스템 검토 및 담당자 면담 |
| 2022년 08월 09일 ~ 08월 11일 |
가) 영업에 관한 사항 검토 - 제품별 매출 현황, 부문별 수익성추이 확인 - 주요 공급처, 매입처에 관한 사항 - 향후 투자계획에 관한 사항 - 향후 수익성 개선 계획에 관한 사항 나) 재무에 관한 사항 검토 - 매출채권, 재고자산 현황 및 연령분석 - 기타채권 현황 및 회수 내역 분석 - 수익성/성장성/안정성 지표 분석 - 차입금 만기구조 분석 - 현금흐름 구조, 유동성 분석 - 향후 유동성 개선 계획에 관한 사항 - 주식연계채권 내역 확인 - 환위험 관리 현황 분석 다) 기타 사항 검토 - 발행시장 상황 검토 - 자금 조달금액, 공모가액의 적정성 검토 - 이사회의사록, 인수계약서 등 주요 서류 확인 - 최대주주 및 특수관계인 등 청약 여부 체크 |
| 2022년 08월 12일 ~ 08월 16일 | - 실사보고서 작성 - 증권신고서 작성 가이드 및 추가자료 작성 |
| 2022년 08월 31일 ~ 09월 07일 |
- (정정) 금융감독원의 정정요구제출에 따른 증권신고서 작성 가이드 및 추가자료 작성 |
| 2022년 09월 21일 ~ 09월 23일 |
- (정정) 자진정정 증권신고서 제출에 따른 증권신고서 작성 가이드 및 추가자료 작성 |
4. 실사참여자
[공동대표주관회사]
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 | 참여기간 | 주요경력 |
|---|---|---|---|---|---|---|
| 케이비증권㈜ | SME금융부 | 이경재 | 이사 | 기업실사 총괄 | 2022년 07월 27일 ~ 2022년 09월 23일 |
기업금융업무 22년 |
| 케이비증권㈜ | SME금융부 | 김자환 | 이사 | 기업실사 책임 | 2022년 07월 27일 ~ 2022년 09월 23일 |
기업금융업무 21년 |
| 케이비증권㈜ | SME금융부 | 이형준 | 과장 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 09월 23일 |
기업금융업무 7년 |
| 케이비증권㈜ | SME금융부 | 백성종 | 대리 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 09월 23일 |
기업금융업무 6년 |
| 케이비증권㈜ | SME금융부 | 박진혁 | 주임 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 09월 23일 |
기업금융업무 4년 |
| 한국투자증권㈜ | ECM부 | 채승용 | 이사 | 기업실사 총괄 | 2022년 07월 27일 ~ 2022년 09월 23일 |
기업금융업무 20년 |
| 한국투자증권㈜ | ECM부 | 이용현 | 팀장 | 기업실사 책임 | 2022년 07월 27일 ~ 2022년 09월 23일 |
기업금융업무 17년 |
| 한국투자증권㈜ | ECM부 | 정인묵 | 대리 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 09월 23일 |
기업금융업무 5년 |
| 한국투자증권㈜ | ECM부 | 김하늘 | 주임 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 09월 23일 |
기업금융업무 3년 |
(주5) 정정 후
3. 기업실사 일정 및 주요내용
| 일자 | 기업 실사 내용 |
|---|---|
| 2022년 07월 27일 | 가) 발행회사방문 - 유상증자 의사 및 자금조달 관련 논의 - 유상증자 필요성 검토 및 주요일정 협의 나) 회사 기본사항 점검 - 경영진 면담(경영철학, 회사연혁 등) - 사업내용 청취 및 주요제품 열람 |
| 2022년 7월 29일~ 8월 02일 |
가) 발행회사방문 - 실사 요청자료 송부 - 본사 방문 나) 회사 일반사항 관련 검토 - 정관검토 및 이사회 등 상법 절차 확인 - 경영진 평판 리스크 검토 - 회사의 사업 및 영업구조 관련 면담 |
| 2022년 08월 03일 ~ 08월 08일 |
가) 회사 기본사항 검토 - 정관 등 기본자료 수령 - 대략적인 자금 사용 목적 등에 관한 청취 - 발행 방식 및 조건 등에 관한 협의 - 금융당국으로부터 제재조치 여부 확인 - 근로기준법 위반행위, 소송진행 여부 확인 나) 산업에 관한 사항 검토 - 산업에 대한 이해 - 산업 경쟁상황, 시장규모, 성장주기 등 확인 - 법률 및 정부규제에 관한 사항 검토 - 시장 내 중대한 환경, 제도 변화요인 검토 다) 회사 지배구조에 관한 사항 검토 - 경영진의 변동내역 및 근무경력 검토 - 종속회사에 관한 사항 검토 - 최대주주의 지분율 및 경영권 안정성 검토 - 사내규정 및 내부통제시스템 확인 - 공시시스템 검토 및 담당자 면담 |
| 2022년 08월 09일 ~ 08월 11일 |
가) 영업에 관한 사항 검토 - 제품별 매출 현황, 부문별 수익성추이 확인 - 주요 공급처, 매입처에 관한 사항 - 향후 투자계획에 관한 사항 - 향후 수익성 개선 계획에 관한 사항 나) 재무에 관한 사항 검토 - 매출채권, 재고자산 현황 및 연령분석 - 기타채권 현황 및 회수 내역 분석 - 수익성/성장성/안정성 지표 분석 - 차입금 만기구조 분석 - 현금흐름 구조, 유동성 분석 - 향후 유동성 개선 계획에 관한 사항 - 주식연계채권 내역 확인 - 환위험 관리 현황 분석 다) 기타 사항 검토 - 발행시장 상황 검토 - 자금 조달금액, 공모가액의 적정성 검토 - 이사회의사록, 인수계약서 등 주요 서류 확인 - 최대주주 및 특수관계인 등 청약 여부 체크 |
| 2022년 08월 12일 ~ 08월 16일 | - 실사보고서 작성 - 증권신고서 작성 가이드 및 추가자료 작성 |
| 2022년 08월 31일 ~ 09월 07일 |
- (정정) 금융감독원의 정정요구제출에 따른 증권신고서 작성 가이드 및 추가자료 작성 |
| 2022년 09월 21일 ~ 09월 23일 |
- (정정) 자진정정 증권신고서 제출에 따른 증권신고서 작성 가이드 및 추가자료 작성 |
| 2022년 10월 06일 ~ 10월 11일 |
- (정정) 자진정정 증권신고서 제출에 따른 증권신고서 작성 가이드 및 추가자료 작성 |
4. 실사참여자
[공동대표주관회사]
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 | 참여기간 | 주요경력 |
|---|---|---|---|---|---|---|
| 케이비증권㈜ | SME금융부 | 이경재 | 이사 | 기업실사 총괄 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 22년 |
| 케이비증권㈜ | SME금융부 | 김자환 | 이사 | 기업실사 책임 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 21년 |
| 케이비증권㈜ | SME금융부 | 이형준 | 과장 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 7년 |
| 케이비증권㈜ | SME금융부 | 백성종 | 대리 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 6년 |
| 케이비증권㈜ | SME금융부 | 박진혁 | 주임 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 4년 |
| 한국투자증권㈜ | ECM부 | 채승용 | 이사 | 기업실사 총괄 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 20년 |
| 한국투자증권㈜ | ECM부 | 이용현 | 팀장 | 기업실사 책임 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 17년 |
| 한국투자증권㈜ | ECM부 | 정인묵 | 대리 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 5년 |
| 한국투자증권㈜ | ECM부 | 김하늘 | 주임 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 3년 |
(주6) 정정 전
(3) 판매방법 및 조건
① 구명정 & DAVIT, GRP/GRE Pipe, 특수선
- 판매방법 : 개별 주문 생산, 제품공급계약에 의거 현금, 외상, 위탁판매
- 조 건 : 연불, 기성불, 납품불
② 제약, 바이오
동사가 보유한 리보세라닙의 글로벌 권리에 의거해 매년 중국 헝루이제약의 리보세라닙(중국명: 아파티닙)의 매출의 일정 비율을 로열티로 수령해 매출로 인식합니다. 2021년부터 중국 내 적응증 확대(간세포암 2차 치료제)로 로열티 수령액이 증가할 것으로 예상됩니다. 그리고, 엘레바에서 진행 중인 위암 3,4차 치료제(글로벌 임상 3상 종료), 간암 1차 치료제로 글로벌 3상(환자 모집 완료), 선양낭성암 임상 2상 (환자모집 완료) 등 다양한 임상시험이 진행 중입니다. 신약승인이 이루어질 경우를 대비해 대륙별 판매 전략 수립을 전개 중입니다. 리보세라닙의 판매로 인한 매출 발생 시,당사는 로열티 수익을 기대할 수 있습니다.
③ 의료기기(주사기)
- 판매방법: 각 병원 및 도,소매업체 주문량을 대리점을 통해 판매
- 판매조건: 판매 후 2개월 외상거래(현금 및 어음)
④ 체외진단 의료기기 및 의약외품
- 판매방법 : 제품공급계약 및 고객발주서에 의거한 현금, 외상, 위탁 판매
- 판매조건 : 제품공급계약서 및 고객발주서에 의거한 납품 및 대금 결제방식
(주6) 정정 후
(3) 판매방법 및 조건
① 구명정 & DAVIT, GRP/GRE Pipe, 특수선
- 판매방법 : 개별 주문 생산, 제품공급계약에 의거 현금, 외상, 위탁판매
- 조 건 : 연불, 기성불, 납품불
② 제약, 바이오
동사가 보유한 리보세라닙의 글로벌 권리에 의거해 매년 중국 항서제약의 리보세라닙(중국명: 아파티닙)의 매출의 일정 비율을 로열티로 수령해 매출로 인식합니다. 2021년부터 중국 내 적응증 확대(간세포암 2차 치료제)로 로열티 수령액이 증가할 것으로 예상됩니다. 그리고, 엘레바에서 진행 중인 위암 3/4차 치료제(Rivoceranib 단독, 글로벌 임상 3상 종료),간암 1차 치료제(항서제약 캄렐리주맙 병용)로 글로벌 3상(환자 모집 완료), 선양낭성암 1,2차 치료제(Rivoceranib 단독) 임상 2상 (환자모집 완료) 등 다양한 임상시험이 진행 중입니다. 신약승인이 이루어질 경우를 대비해 대륙별 판매 전략 수립을 전개 중입니다. 리보세라닙의 판매로 인한 매출 발생 시,당사는 로열티 수익을 기대할 수 있습니다.
③ 의료기기(주사기)
- 판매방법: 각 병원 및 도,소매업체 주문량을 대리점을 통해 판매
- 판매조건: 판매 후 2개월 외상거래(현금 및 어음)
④ 체외진단 의료기기 및 의약외품
- 판매방법 : 제품공급계약 및 고객발주서에 의거한 현금, 외상, 위탁 판매
- 판매조건 : 제품공급계약서 및 고객발주서에 의거한 납품 및 대금 결제방식
(주7) 정정 전
(1) 특허권 양수도 계약
|
품목 |
계약상대방 |
대상지역 |
계약 체결시기 |
계약상의 주요내용 |
계약 금액 |
비고 |
|
리보세라닙 구Apatinib Mesylate) |
Advenchen Laboratories Nanjing, Ltd. |
중국을 제외한 모든 국가 |
2020.09. |
YN968D1(글로벌은 리보세라닙 |
2,200 만불 |
- |
|
SFFT Developing Co., Ltd. |
중국 |
2,000 만불 |
- |
| * 본 특허권양수도 계약의 목적은 리보세라닙의 글로벌 로열티 수령을 통한 장기적이고 안정적인 캐시플로우 및 영업이익을 확보하고, 항서제약과의 긴밀한 협력관계를 통하여 현재 진행중인 NDA와 리보세라닙의 추가 적응증 임상시험에 속도를 내기 위함입니다. |
(1)
| 계약상대방 | Advenchen Nanjing |
| 계약내용 | Advenchen Nanjing이 보유한 Rivoceraninb 물질특허 권리 양수도 |
| 대상지역 | 미국, 캐나다, 유럽, 일본, 한국, PCT |
| 계약기간 | 해당 특허 만료일까지 (2024년 예상) |
| 총계약금액 | Upfront: 22,000,000USD |
| 지급금액 | Upfront: 22,000,000USD 기 지급 완료 Milestone: 미 발생 |
| 계약조건 | 개발 마일스톤(Development Milestione): 적응증, 진입국가, 매출에 따라 단계별 마일스톤 실행 예정 초과수익배분: 상호 협의된 연간 수익예측을 초과하는 매출의 50% 지급 |
| 회계처리방법 | 최초 지급한 Upfront 22,000,000USD는 무형자산으로 인식 비용 발생하지 않음. 차후 당기비용으로 인식 예정 |
| 대상기술 | Rivoceranib 물질특허 (미국, 캐나다, 유럽, 일본, 한국, PCT) |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1/2차 치료제 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 ESMO에서 간암 1차 치료제 글로벌 임상 3상 결과 발표 (1차 평가지표 만족) |
| 기타사항 | 판매 승인 현황 - 중국 판권을 보유한 헝루이제약에서 2014년 위암 3차 치료제, 2020년 간암 2차 치료제로 시판 허가 득한 후 판매 중 |
(2)
| 계약상대방 | SFFT |
| 계약내용 | SFFT가 보유한 Rivoceraninb의 중국 특허권리 양수도 |
| 대상지역 | 중국 |
| 계약기간 | 해당 특허 만료일까지 (2022년 11월 예상) |
| 총계약금액 | Upfront: 20,000,000USD |
| 지급금액 | Upfront: 20,000,000USD 기 지급 완료 Milestone: 미 발생 |
| 계약조건 | 초과수익배분 : 상호 협의된 연간 수익예측을 초과하는 매출의 70% 지급 |
| 회계처리방법 | 최초 지급한 Upfront 20,000,000USD는 무형자산으로 인식해 감가상각 완료 이후 지급한 Milestone 비용은 당기비용으로 인식 |
| 대상기술 | Rivoceranib 물질특허 (중국) |
| 개발진행경과 | <회사> 중국 내 전용실시권은 항서제약이 보유하고 있어 항서제약에서 개발 진행 중 |
| 기타사항 | 판매 승인 현황 - 중국 판권을 보유한 헝루이제약에서 2014년 위암 3차 치료제, 2020년 간암 2차 치료제로 시판 허가 득한 후 판매 중 |
(2) 연결대상 종속회사 경영상의 주요계약
(가) Elevar Therapeutics, Inc.
1) 라이센스 인(License-in)계약
|
품목 |
계약상대방 |
대상지역 |
계약 |
계약상의주요내용 |
계약금액 |
진행단계 | 비 고 |
|
리보세라닙 (Rivoceranib, 구Apatinib Mesylate) |
에이치엘비㈜(*1) |
중국을 제외한 모든 국가 |
2020. 12. | Rivoceranib의 중국을 제외한 글로벌 전용실시권 취득 |
(*2) |
- 위암말기 치료제 : 임상3상 종료 Pre-NDA 실시, 미국 FDA 신약허가 신청 (NDA) 준비 중,희귀의약품 지정(미국, 유럽, 한국) - 고형암 옵디보(Nivolumab) 병용 : 임상1상 종료 - 선양낭성암 단독 : 임상2상 진행 중, 희귀의약품 지정(미국) - 위암 2차 치료제(파클리탁셀 병용) : 임상1/2상 진행 중 - 간암 1차 치료제(캄렐리주맙 병용) : 임상3상 진행 중, 희귀의약품 지정(미국) - 대장암 3차 치료제(론서프 병용) : 임상1상 진행 중 - 난소암(Apealea 병용) : 임상 1상 준비 중 |
표적항암제 (VEGFR-2를 선택적으로 차단) |
|
아필리아 (Apealea) |
비베스토 (Vivesto, 舊 Oasmia) |
러시아연방, 스칸디나비아반도국을 제외한 모든 국가 |
2020. 03. | Apealea의 계약상 명시된 지역에서의 전용실시권 취득 |
(*2) | - 2020년 유럽 EMA로 부터 난소암 2차 치료제로 판매 승인 (carboplatin 병용) 2022년 내 유럽 내 판매 개시 목표 - 난소암(Rivoceranib 병용) : 임상 1상 준비 중 |
세포독성항암제 Paclitaxel 성분의 3세대 개량신약 항암제 |
|
(*1) Elevar Therapeutics,Inc.는 2007년 7월 Advenchen Laboratories,Inc., CA, USA와 리보세라닙 License-in 계약을 체결하였으나, 2020년 12월 당사와 Advenchen Laboratories와 ※ JAK3 License-in 계약은 자체 추진으로 사업방향을 전환하여 계약을 취소하였습니다. |
(1)
| 계약상대방 | Advenchen Laboratories |
| 계약내용 | YN968D1-Small Molecule Angiogenesis Inhibitor의 계약상 명시된 지역에서의전용실시권 취득 |
| 대상지역 | 중국을 제외한 모든 국가 |
| 계약기간 | 계약체결일:2007. 12. 21(계약서 내용 조정일 2021, 06, 17) 계약종료일: 유효특허의 만료일까지 (물질특허: 2024년 예상, 염조성물특허: 2029년 예상) |
| 총계약금액 | Upfront: 150,000 USD |
| 지급금액 | <환수 불가능 금액> 계약금(Upfront Payment): 150,000USD 2007년 기 지급 완료 마일스톤(Milestione): 임상 진행 단계에 진행에 따라 개발 Milestione $800,000USD 지급 로열티(Royalty): 매출없음 <환수 가능 금액> 해당사항 없음 |
| 계약조건 | 계약 조정 내역을 포함한 최종 계약 조건 계약금(Upfront Payment): 150,000USD - 지급조건: 계약 체결 45일 이내 마일스톤(Milestione): 적응증, 진입국가, 매출에 따라 단계별 마일스톤 실행 예정 로열티: 3.5%~10% 지역별 매출액 비율에 따른 로열티 실행 예정 Advenchen이 보유한 Appatinib(Rivoceranib)의 염조성물 특허를 LSKB에 허여한다. 국가별 특허(물질특허 및 염조성물특허) 유지 상태에 따라 상호 협의한 비율에 의거해 로열티를 조정한다. LSKB가 보유한 모든 권리는 Elevar가 승계한다. |
| 회계처리방법 | 최초 지급한 Upfront 150,000USD는 무형자산으로 인식해 감가상각 완료 이후 지급한 Milestone 비용은 당기비용으로 인식 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 Rivoceranib과 염특허 전용 특허 실시권 |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1/2차 치료제 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 ESMO에서 간암 1차 치료제 글로벌 임상 3상 결과 발표 (1차 평가지표 만족) |
| 기타사항 | 판매 승인 현황 중국 판권을 보유한 헝루이제약에서 2014년 위암 3차 치료제, 2020년 간암 2차 치료제로 시판 허가 득한 후 판매 중 |
(2)
| 계약상대방 | 비베스토(Vivesto, 舊 Oasmia) |
| 계약내용 | Apealea의 계약상 명시된 지역에서의 전용실시권 취득 |
| 대상지역 | 러시아연방, 스칸디나비아반도국을 제외한 모든 국가 |
| 계약기간 | 계약체결일:2020. 03. 25(계약서 내용 조정일 2021, 06, 17) 계약종료일: 유효특허의 만료일까지 (2036년 12월 예상) |
| 총계약금액 | Upfront: 20,000,000 USD |
| 지급금액 | <환수 불가능 금액> 계약금(Upfront Payment): 20,000,000USD 2019년 기 지급 완료 마일스톤(Milestione): Milestone 지급 조건 미달성으로 미지급 로열티(Royalty): Royalty 지급 조건 미달성으로 미지급 <환수 가능 금액> 해당사항 없음 |
| 계약조건 | 계약금(Upfront Payment): 20,000,000USD - 지급조건: 계약 체결 시 개발 마일스톤(Development Milestione): 적응증, 진입국가에 따라 단계별 마일스톤 실행 예정 판매 마일스톤(Sales Milestone): 매출액 비율에 따라 상호 협의한 비율의 판매 마일스톤 실행 예정 로열티(Royalty): 매출의 10%~25%, 지역별 매출액 비율에 따른 로열티 실행 예정 |
| 회계처리방법 | Upfront 20,000,000USD는 반환의무 및 기타 조건이 없어 수행할 추가적 의무가 존재하지 않아, 무형자산으로 인식 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 의약품 아필리아("Apealea")에 대한 전용특허 실시권 및 다음의 염조성물 특허 실시권 - 화학명 N-(all-trans-retinoyl)-L-cysteic acid methyl ester sodium salt - 화학명 N-(13-cis-reinoyl)-L-cysteic acid methyl ester sodium salt |
| 개발진행경과 | <거래상대방> 북유럽과 러시아에서 판매 중이며, 2018년 유럽 EMA 판매 승인 완료 |
| <회사> 미국 내 부인과종양학그룹 소속 임상의들과 백금계 약물 저항성이 있는 난소암 환자를 대상으로 Rivoceranib, Apealea 병용 임상에 대한 계획 검토 중이나, 구체적인 임상 개시 일정은 미정 |
|
| 기타사항 | 판매 승인 현황 2020년 유럽 EMA로 부터 난소암 2차 치료제로 판매 승인 (carboplatin 병용) 2022년 내 유럽 내 판매 개시 목표 |
2) 라이센스 아웃(License-out)계약
|
품목 |
계약 |
대상지역 |
계약 |
계약상의 주요내용 |
계약금액 |
진행단계 | 비 고 |
| 리보세라닙 (Rivoceranib, 구Apatinib Mesylate) |
에이치엘비 |
대한민국, 일본, 유럽 |
2018. 08. |
기존 부광약품㈜에게 인정되는 |
47억원(*) | - 위암말기 치료제 : 임상3상 종료 Pre-NDA 실시, 미국 FDA 신약허가 신청 (NDA) 준비 중, 희귀의약품 지정(미국, 유럽, 한국) - 선양낭성암 단독 : 임상2상 진행 중, 희귀의약품 지정(미국) - 위암 2차 치료제(파클리탁셀 병용) : 임상1/2상 진행 중 - 간암 1차 치료제(캄렐리주맙 병용) : 임상3상 진행 중, 희귀의약품 지정(미국) - 대장암 3차 치료제(론서프 병용) : 임상1상 진행 중 - 동물용항암제 : 임상 진행 중 |
에이치엘비 바이오 그룹의 사업 다각화 및 매출 증대 |
| (*)LSK Biopartners, Inc.에서 향후 계약상대방으로부터 지급받을 Development Milestones 내역은 다음과 같습니다. |
| 계약상대방 | 부광약품㈜ |
| 계약내용 | Rivoceranib에 대한 특정 지역의 개발, 판매에 대한 권리 Sublicense(한국, 유럽, 일본) 및 공동개발 |
| 대상지역 | 대한민국, 일본, 유럽 |
| 계약기간 | 계약체결일:2009. 1. 8 (계약서 내용 조정일 2012, 2, 1) (계약서 내용 조정일 2015, 7, 28) (계약서 내용 조정일 2015, 10, 30) (계약서 내용 조정일 2017, 1, 2) 계약종료일: 유효특허의 만료일까지 (물질특허: 2024년 예상, 염조성물특허: 2029년 예상) |
| 총계약금액 | Potential Sales Royalty: 매출액에 따라 6~10% 특허가 국가별로 개별 종료 될 시 최대 10년까지 상기 로열티의 10%를 지급 |
| 지급금액 | 해당사항 없음 |
| 계약조건 | 주요 계약 내용 1) 한국내 독점개발, 판매권 및 유럽, 일본에 대한 수익 지분 2) 국내 시판시 판매액의 6~10% 로열티 지불 (Sublicensing,진행시 수익의 30% 지불) |
| 회계처리방법 | 해당사항 없음 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 Rivoceranib 특허 전용실시권 |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1/2차 치료제 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 간암 1차 치료제 글로벌 임상 3상 종료 후 결과 발표 예정(2022년 9월 ESMO) |
| 기타사항 | Elevar Therapeutics, Inc. 는 2009년 12월 부광약품㈜에게 리보세라닙의 한국 판권을 양도하는 조건으로 리보세라닙 공동개발을 하였으며, 이후 부광약품㈜은 2018년 08월 한국 판권에 대한 모든 권리 및 의무를 에이치엘비생명과학㈜으로 400억원에 양도하였습니다. (2018.8.14 공시 참조) |
(중략)
다. 연구개발 실적
(1) 연구개발 진행 현황 및 향후계획
| [연구개발 진행 총괄표] |
| 구 분 | 품 목 | 적응증 | 임상시작일 | 현재 진행단계 | 비 고 | 임상주도기업 | ||
|---|---|---|---|---|---|---|---|---|
| 단계(국가) | 승인일 | |||||||
| 화학합성 의약품 |
신약 | 리보세라닙 (HLB생명과학 주도 임상 포함) |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안전성평가 완료 | Elevar |
| 위암 (3차 단일요법) |
2017년 | 임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
Elevar | |||
| 위암 (1차 병용요법) [Combo with Camrelizumab] |
2021년 | 임상2상 (한국) |
2021년 09월 (임상2상 개시일) |
임상 진행 중 | Elevar | |||
| 간암 (1차 병용요법) [Combo with Camrelizumab] |
2019년 | 임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
임상 진행 중 9월 초록 발표 (1차 평가 지표 만족) |
Elevar | |||
| 선양낭성암종 (1/2차 단일요법) |
2020년 | 임상2상 (한국, 미국) |
2020년 4월 (임상2상 개시일) |
임상 2상 진행중 6월 초록 발표 |
Elevar | |||
| 위암 (2차 병용요법) [Combo with Paclitaxel] |
2018년 | 임상1/2a상 (한국, 미국) |
2018년 10월 (임상1상 개시일) |
임상1상 종료 후, 2a상 준비 중 |
Elevar | |||
| 대장암 (3차 병용요법) [Combo with Lonsurf] |
2019년 | 임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 진행 중 | Elevar | |||
| 황반변성치료제 (점안액) |
2018년 | 비임상 단계 | - | 타당성분석 중 | HLB 생명과학 |
|||
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상진입 준비 중 (농림축산검역본부) |
HLB 생명과학 |
|||
| 위암 (1차 병용요법) [Combo with Camrelizumab] |
2021년 | 임상2상 (한국) |
2021년 09월 (임상2상 개시일) |
임상 진행 중 | HLB 생명과학 |
|||
| 아필리아 | 난소암 2차 (백금계 약물 감수성) |
2018년 (유럽EMA 허가) |
유럽 허가 | 유럽 판매 준비 중 | Elevar | |||
| 바이오 의약품 |
IMMUNOMIC THERAPEUTICS ITI-1000 |
GBM | 2016년 | 임상 2상 (미국) |
2016년 8월 (임상 2상 개시일) |
임상 진행 중 | ITI | |
| IMMUNOMIC THERAPEUTICS ITI-1001 |
GBM | - | 비임상 단계 | - | 임상 1상 IND 준비 중 | ITI | ||
| IMMUNOMIC THERAPEUTICS ITI-3000 |
Merkel Cell Carcinoma | 2022년 | 임상 1상 (미국) |
2022년 02월 (임상 1상 개시일) |
임상 진행 중 | ITI | ||
| IMMUNOMIC THERAPEUTICS ITI-8000 |
NSCLC | - | 비임상 단계 | - | - | ITI | ||
| IMMUNOMIC THERAPEUTICS ITI-9001 |
JRC Pollinosis | - | 비임상 단계 | - | - | ITI | ||
(가) : 리보세라닙
| 구 분 | 화학합성의약품 |
| 적응증 | 위암 3/4차 치료제, 위암 2차 치료제, 선양낭성암 1,2차 치료제, 간암 1차 치료제, 대장암 3차 치료제 |
| 작용기전 | 신생혈관억제, VEGFR2-TKI |
| 제품의특성 | 혈관내피세포성장인자수용체2(VEGFR-2)를 타켓으로 암 조직의 신생혈관 성장을 억제하고, 암세포의 증식억제와 면역세포의 정상화를 유도하는 경구용 표적 항암제입니다. |
| 진행경과 | 위암 3/4차 치료제: 단독 요법으로 글로벌 임상 3상 후 미국 NDA 신청 준비 중 위암 2차 치료제: 파클리탁셀과 병용으로 한국, 미국에서 임상1/2a 진행 (현재 임상 1상 환자 모집 종료) 선양낭성암 1,2차 치료제: 단독요법으로 미국, 한국에서 임상 2상 환자모집 완료 간암 1차 치료제: 항서제약의 캄렐리주맙과 병용으로 글로벌 13개국 임상 3상 진행하고 있고, 2022년 9월 ESMO에서 임상 결과 공개(1차 평가지표 만족) 대장암 3차 치료제: 타이호제약의 론서프와 병용으로 미국, 한국에서 임상 1b/2상 진행 |
| 향후계획 | 위암 3/4차 치료제: 미국 FDA pre-NDA 진행, FDA에서 요청한 보완 자료 준비 중, 자료 보완 후 NDA 제출 예정 위암 2차 치료제: 임상 1상 결과 분석 선양낭성암 1,2차 치료제: 임상 2상 결과 수집 및 분석 간암 1차 치료제: 임상 3상 결과 수집, 분석 및 Pre-NDA 준비 대장암 3차 치료제: 임상 1상 결과 수집 및 분석 |
| 경쟁제품 | 위암 3차 치료제: 론서프, 옵디보(한국, 일본, 대만 한정) 위암 2차 치료제: 시람자(cyramza), 파클리탁셀 선양낭성암 1,2차 치료제: 표준치료제 없음 (Off-label)로 치료 진행 간암 1차 치료제: 넥사바, 렌비마, 아바스틴, 티센트릭 대장암 3차 치료제: 론서프, 스티바가, 옵디보 |
| 관련논문등 | 위암 글로벌 임상 3상 결과 2019년 유럽암학회(ESMO) 발표: Best of ESMO 선정 중국 위암 3차 치료제 임상 3상 논문: 2016년, J Clin Oncol 34 중국 위암 2차 치료제 임상 2상 논문: 2013년, J Clin Oncol 31 중국 고형암 치료제 임상 1상 논문: 2010년, BMC cancer 10 선양낭성암 중국 선낭암 임상 2상: 2021년 Therapeutic Advances in Medical Oncology 13 미국, 한국 선낭암 임상 2상 결과: 2022년 미국암학회 발표 간암 중국 간암 임상 2상: 2021년 Clin Cancer Res 15:27(4) 글로벌 간암 임상 3상 결과: 2022년 9월 ESMO(유럽암학회)에서 공개 (1차 평가지표 만족) |
| 시장규모 | 위암 치료제 글로벌시장: 2017년 40억달러(4조7,236억원)에서 2026년에는 66억달러(7조7,939억원)로 성장 예상 선낭암 치료제 글로벌시장: 표준치료제가 없고 발병률이 낮아 글로벌 시장 규모 추산이 어려움 간암 치료제 글로벌시장: 2019년 17억3090만 달러 (약 2조 2,100억원) 대장암 치료제 글로벌시장: 2018년 64억4400만달러(7조2000억)에서 2028년 81억4700만달러(9조1000억)로 성장 예상 |
| 기타사항 | 특허 및 권리 보유 현황 - 리보세라닙의 물질특허: HLB - 글로벌 전용실시권은: Elevar - 한국 전용실시권: HLB생명과학 - 중국 전용실시권: 중국 항서제약이 보유 항서제약에서 2014년 위암 3차 치료제로 중국 내 시판허가를 득한 후 현재까지 꾸준한 매출 성장 유지 중입니다. 2015년 매출 약 450억에서 2018년 2,800억까지 매출 성장을 보여줘, 약효와 안전성을 입증하였습니다. 2021년 부터 간암 2차 치료제로 적응증을 확대하여, 중국 내 매출 확대가 기대 됩니다. |
(나) : 아필리아
| 구 분 | 화학합성의약품 |
| 적응증 | 백금계 약물 감수성이 있는 난소암 2차 치료제 |
| 작용기전 | 세포 분열에 필요한 RNA나 DNA 등을 손상시켜 세포 분열을 저지하는 세포 주기 선택적 항암제 |
| 제품의특성 | 파클리탁셀은 세포분열 과정 중 분열과 자가 복제의 기구인 미세소관이 분리되는 과정을 방해하는 "식물성 알칼로이드"로 분류되는 항암제입니다. 중증 과민반응 발현을 최소화하기 위해 투여 전에 전치료를 받아야 합니다. Apealea는 특허 출원된 Micelle 코팅을 적용하여 사전처치 필요없이 편의성을 증대시키며 부작용을 줄일 수 있도록 개발한 첨가제 형태 기반의 최적의 파크리탁셀 혼합제입니다. |
| 진행경과 | 유럽, 남미, 중동 지역 판매 준비 중 백금계 약물 저항성이 있는 난소암 환자 대상 임상 1상, 3상 동시 준비 중 |
| 향후계획 | -기 승인 받은 지역 대상 판매 준비 유럽, 중동, 북아프리카, 남미 지역 대상으로 판매 절차 진행 중 중국 진출을 위해 중국 현지업체와 JV를 통한 논의 중 -추가 적응증 개발 백금계 약물 저항성이 있는 난소암 환자를 대상으로 Rivoceranib과 병용 임상 계획 검토 중 |
| 경쟁제품 | 카보플라틴, 시스플라틴, 파클리탁셀, 아바스틴 |
| 관련논문등 | A randomized phase III trial in patients with recurrent platinum sensitive ovarian cancer comparing efficacy and safety of paclitaxel micellar and Cremophor EL-paclitaxel |
| 시장규모 | 글로벌 난소암 시장은 2021년 1억 7,500만달러 규모였으며, 2028년까지 매년 9.5% 성장하여 약 3억 3,973만달러에 이를 것으로 예상 |
| 기타사항 | -특허 및 권리 보유 현황 Apealea 글로벌 전용실시권: Elevar (북유럽, 동유럽 일부국가 제외) -판매 승인 현황 2020년 유럽 EMA로 부터 난소암 2차 치료제로 판매 승인 (carboplatin 병용) 2022년 내 유럽 내 판매 개시 목표 |
(다) : ITI
| 구 분 | 바이오의약품 |
| 적응증 | GBM (교모세포종) |
| 작용기전 | UNITE 플랫폼은 리소좀관련막단백질(LAMP)에 특정 암에 발현되는 항원을 탑재해 면역세포를 빠르고 효율적으로 활성화시키는 기전 |
| 제품의특성 | 기존 기술 대비 CD4+ Helper T 세포 활성화에 가장 효과적 동일 APC 세포 내 MHC I & II Mediated Pathway 를 동시에 활성화 가능 (MHC II Pathway 직접적으로 관여) 다양한 질환 분야에 적용 가능 (암, 감염 질환, 자가면역 질환 등) 세포 기반 치료제, 핵산 (Nucleic Acid, DNA/RNA) 기반 치료제 개발 등 다양한 기술에 적용 가능 |
| 진행경과 | ITI-1000 교모세포종 (Dendritic Cell vaccine): 임상 2상 진행 중 ITI-1001교모세포종(DNA vaccine): 1상 IND 승인 후 임상 진행 중 ITI-3000 메르켈세포암(DNA vaccine): 1상 IND 승인 후 임상 진행 중 |
| 향후계획 | ITI-1000 연내 임상 2상 종료 후, FDA와 협의를 통해 조건부 허가 추진 |
| 경쟁제품 | 교모세포종: 테모졸로마이드 (2003년 승인) |
| 관련논문등 | 2009 Gene Therapy 16 2015 Nature 2017 Clinical Cancer Reserch 23(8) |
| 시장규모 | 글로벌 교모세포종 시장은 2025년까지 매년 7.4% 성장할 전망이며, 약 16억 4,340만달러 |
| 기타사항 | 현재 교모세포종 원발성 악성 뇌종양 중 가장 흔한 종양으로 진단 후 치료를 하지 않으면 3-6개월 내에 사망합니다. 현재 치료법이 제한적이고 5년 생존율이 5%미만으로 악성도가 높은 질환입니다. ITI-1000 교모세포종 임상 1상 시험에서 mOS을 38.3 개월로 크게 개선하였으며, 표준치료제로 알려진 TMZ/RT 요법 대비 23 개월 이상 생존 기간을 향상시키고 60개월 생존율 또한 36.4%로 증가해 임상 2상 결과 또한 기대하고 있음. |
(주7) 정정 후
(1) 특허권 양수도 계약
|
품목 |
계약상대방 |
대상지역 |
계약 체결시기 |
계약상의 주요내용 |
계약 금액 |
비고 |
|
리보세라닙 구Apatinib Mesylate) |
Advenchen Laboratories Nanjing, Ltd. |
중국을 제외한 모든 국가 |
2020.09. |
YN968D1(글로벌은 리보세라닙 |
2,200 만불 |
- |
|
SFFT Developing Co., Ltd. |
중국 |
2,000 만불 |
- |
| * 본 특허권양수도 계약의 목적은 리보세라닙의 글로벌 로열티 수령을 통한 장기적이고 안정적인 캐시플로우 및 영업이익을 확보하고, 항서제약과의 긴밀한 협력관계를 통하여 현재 진행중인 NDA와 리보세라닙의 추가 적응증 임상시험에 속도를 내기 위함입니다. |
(1)
| 계약상대방 | Advenchen Nanjing |
| 계약내용 | Advenchen Nanjing이 보유한 Rivoceraninb 물질특허 권리 양수도 |
| 대상지역 | 미국, 캐나다, 유럽, 일본, 한국, PCT |
| 계약기간 | 해당 특허 만료일까지 (2024년 예상) |
| 총계약금액 | Upfront: 22,000,000USD |
| 지급금액 | Upfront: 22,000,000USD 기 지급 완료 Milestone: 미 발생 |
| 계약조건 | 개발 마일스톤(Development Milestione): 적응증, 진입국가, 매출에 따라 단계별 마일스톤 실행 예정 초과수익배분: 상호 협의된 연간 수익예측을 초과하는 매출의 50% 지급 |
| 회계처리방법 | 최초 지급한 Upfront 22,000,000USD는 무형자산으로 인식 비용 발생하지 않음. 차후 당기비용으로 인식 예정 |
| 대상기술 | Rivoceranib 물질특허 (미국, 캐나다, 유럽, 일본, 한국, PCT) |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1,2차 치료제(Rivoceranib 단독) 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 ESMO에서 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상 3상 결과 발표 (1차 평가지표 만족) |
| 기타사항 | 판매 승인 현황 - 중국 판권을 보유한 항서제약에서 2014년 위암 3차 치료제, 2020년 간암 2차 치료제로 시판 허가 득한 후 판매 중 |
(2)
| 계약상대방 | SFFT |
| 계약내용 | SFFT가 보유한 Rivoceraninb의 중국 특허권리 양수도 |
| 대상지역 | 중국 |
| 계약기간 | 해당 특허 만료일까지 (2022년 11월 예상) |
| 총계약금액 | Upfront: 20,000,000USD |
| 지급금액 | Upfront: 20,000,000USD 기 지급 완료 Milestone: 미 발생 |
| 계약조건 | 초과수익배분 : 상호 협의된 연간 수익예측을 초과하는 매출의 70% 지급 |
| 회계처리방법 | 최초 지급한 Upfront 20,000,000USD는 무형자산으로 인식해 감가상각 완료 이후 지급한 Milestone 비용은 당기비용으로 인식 |
| 대상기술 | Rivoceranib 물질특허 (중국) |
| 개발진행경과 | <회사> 중국 내 전용실시권은 항서제약이 보유하고 있어 항서제약에서 개발 진행 중 |
| 기타사항 | 판매 승인 현황 - 중국 판권을 보유한 항서제약에서 2014년 위암 3차 치료제, 2020년 간암 2차 치료제로 시판 허가 득한 후 판매 중 |
(2) 연결대상 종속회사 경영상의 주요계약
(가) Elevar Therapeutics, Inc.
1) 라이센스 인(License-in)계약
|
품목 |
계약상대방 |
대상지역 |
계약 |
계약상의주요내용 |
계약금액 |
진행단계 | 비 고 |
|
리보세라닙 (Rivoceranib, 구Apatinib Mesylate) |
에이치엘비㈜(*1) |
중국을 제외한 모든 국가 |
2020. 12. | Rivoceranib의 중국을 제외한 글로벌 전용실시권 취득 |
(*2) |
- 위암말기 치료제 : 임상3상 종료 Pre-NDA 실시, 미국 FDA 신약허가 신청 (NDA) 준비 중,희귀의약품 지정(미국, 유럽, 한국) - 고형암 옵디보(Nivolumab) 병용 : 임상1상 종료 - 선양낭성암 단독 : 임상2상 진행 중, 희귀의약품 지정(미국) - 위암 2차 치료제(파클리탁셀 병용) : 임상1/2상 진행 중 - 간암 1차 치료제(캄렐리주맙 병용) : 임상3상 진행 중, 희귀의약품 지정(미국) - 대장암 3차 치료제(론서프 병용) : 임상1상 진행 중 - 난소암(Apealea 병용) : 임상 1상 준비 중 |
표적항암제 (VEGFR-2를 선택적으로 차단) |
|
아필리아 (Apealea) |
비베스토 (Vivesto, 舊 Oasmia) |
러시아연방, 스칸디나비아반도국을 제외한 모든 국가 |
2020. 03. | Apealea의 계약상 명시된 지역에서의 전용실시권 취득 |
(*2) | - 2020년 유럽 EMA로 부터 난소암 2차 치료제로 판매 승인 (carboplatin 병용) 2022년 내 유럽 내 판매 개시 목표 - 난소암(Rivoceranib 병용) : 임상 1상 준비 중 |
세포독성항암제 Paclitaxel 성분의 3세대 개량신약 항암제 |
|
(*1) Elevar Therapeutics,Inc.는 2007년 7월 Advenchen Laboratories,Inc., CA, USA와 리보세라닙 License-in 계약을 체결하였으나, 2020년 12월 당사와 Advenchen Laboratories와 ※ JAK3 License-in 계약은 자체 추진으로 사업방향을 전환하여 계약을 취소하였습니다. |
(1)
| 계약상대방 | Advenchen Laboratories |
| 계약내용 | YN968D1-Small Molecule Angiogenesis Inhibitor의 계약상 명시된 지역에서의전용실시권 취득 |
| 대상지역 | 중국을 제외한 모든 국가 |
| 계약기간 | 계약체결일:2007. 12. 21(계약서 내용 조정일 2021, 06, 17) 계약종료일: 유효특허의 만료일까지 (물질특허: 2024년 예상, 염조성물특허: 2029년 예상) |
| 총계약금액 | Upfront: 150,000 USD |
| 지급금액 | <환수 불가능 금액> 계약금(Upfront Payment): 150,000USD 2007년 기 지급 완료 마일스톤(Milestione): 임상 진행 단계에 진행에 따라 개발 Milestione $800,000USD 지급 로열티(Royalty): 매출없음 <환수 가능 금액> 해당사항 없음 |
| 계약조건 | 계약 조정 내역을 포함한 최종 계약 조건 계약금(Upfront Payment): 150,000USD - 지급조건: 계약 체결 45일 이내 마일스톤(Milestione): 적응증, 진입국가, 매출에 따라 단계별 마일스톤 실행 예정 로열티: 3.5%~10% 지역별 매출액 비율에 따른 로열티 실행 예정 Advenchen이 보유한 Appatinib(Rivoceranib)의 염조성물 특허를 LSKB에 허여한다. 국가별 특허(물질특허 및 염조성물특허) 유지 상태에 따라 상호 협의한 비율에 의거해 로열티를 조정한다. LSKB가 보유한 모든 권리는 Elevar가 승계한다. |
| 회계처리방법 | 최초 지급한 Upfront 150,000USD는 무형자산으로 인식해 감가상각 완료 이후 지급한 Milestone 비용은 당기비용으로 인식 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 Rivoceranib과 염특허 전용 특허 실시권 |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제(Rivoceranib 단독) 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1,2차 치료제(Rivoceranib 단독) 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 ESMO에서 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상 3상 결과 발표 (1차 평가지표 만족) |
| 기타사항 | 판매 승인 현황 중국 판권을 보유한 항서제약에서 2014년 위암 3차 치료제, 2020년 간암 2차 치료제로 시판 허가 득한 후 판매 중 |
(2)
| 계약상대방 | 비베스토(Vivesto, 舊 Oasmia) |
| 계약내용 | Apealea의 계약상 명시된 지역에서의 전용실시권 취득 |
| 대상지역 | 러시아연방, 스칸디나비아반도국을 제외한 모든 국가 |
| 계약기간 | 계약체결일:2020. 03. 25(계약서 내용 조정일 2021, 06, 17) 계약종료일: 유효특허의 만료일까지 (2036년 12월 예상) |
| 총계약금액 | Upfront: 20,000,000 USD |
| 지급금액 | <환수 불가능 금액> 계약금(Upfront Payment): 20,000,000USD 2019년 기 지급 완료 마일스톤(Milestione): Milestone 지급 조건 미달성으로 미지급 로열티(Royalty): Royalty 지급 조건 미달성으로 미지급 <환수 가능 금액> 해당사항 없음 |
| 계약조건 | 계약금(Upfront Payment): 20,000,000USD - 지급조건: 계약 체결 시 개발 마일스톤(Development Milestione): 적응증, 진입국가에 따라 단계별 마일스톤 실행 예정 판매 마일스톤(Sales Milestone): 매출액 비율에 따라 상호 협의한 비율의 판매 마일스톤 실행 예정 로열티(Royalty): 매출의 10%~25%, 지역별 매출액 비율에 따른 로열티 실행 예정 |
| 회계처리방법 | Upfront 20,000,000USD는 반환의무 및 기타 조건이 없어 수행할 추가적 의무가 존재하지 않아, 무형자산으로 인식 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 의약품 아필리아("Apealea")에 대한 전용특허 실시권 및 다음의 염조성물 특허 실시권 - 화학명 N-(all-trans-retinoyl)-L-cysteic acid methyl ester sodium salt - 화학명 N-(13-cis-reinoyl)-L-cysteic acid methyl ester sodium salt |
| 개발진행경과 | <거래상대방> 북유럽과 러시아에서 판매 중이며, 2018년 유럽 EMA 판매 승인 완료 |
| <회사> 미국 내 부인과종양학그룹 소속 임상의들과 백금계 약물 저항성이 있는 난소암 환자를 대상으로 Rivoceranib, Apealea 병용 임상에 대한 계획 검토 중이나, 구체적인 임상 개시 일정은 미정 |
|
| 기타사항 | 판매 승인 현황 2020년 유럽 EMA로 부터 난소암 2차 치료제로 판매 승인 (carboplatin 병용) 2022년 내 유럽 내 판매 개시 목표 |
2) 라이센스 아웃(License-out)계약
|
품목 |
계약 |
대상지역 |
계약 |
계약상의 주요내용 |
계약금액 |
진행단계 | 비 고 |
| 리보세라닙 (Rivoceranib, 구Apatinib Mesylate) |
에이치엘비 |
대한민국, 일본, 유럽 |
2018. 08. |
기존 부광약품㈜에게 인정되는 |
47억원(*) | - 위암말기 치료제 : 임상3상 종료 Pre-NDA 실시, 미국 FDA 신약허가 신청 (NDA) 준비 중, 희귀의약품 지정(미국, 유럽, 한국) - 선양낭성암 단독 : 임상2상 진행 중, 희귀의약품 지정(미국) - 위암 2차 치료제(파클리탁셀 병용) : 임상1/2상 진행 중 - 간암 1차 치료제(캄렐리주맙 병용) : 임상3상 진행 중, 희귀의약품 지정(미국) - 대장암 3차 치료제(론서프 병용) : 임상1상 진행 중 - 동물용항암제 : 임상 진행 중 |
에이치엘비 바이오 그룹의 사업 다각화 및 매출 증대 |
| (*)LSK Biopartners, Inc.에서 향후 계약상대방으로부터 지급받을 Development Milestones 내역은 다음과 같습니다. |
| 계약상대방 | 부광약품㈜ |
| 계약내용 | Rivoceranib에 대한 특정 지역의 개발, 판매에 대한 권리 Sublicense(한국, 유럽, 일본) 및 공동개발 |
| 대상지역 | 대한민국, 일본, 유럽 |
| 계약기간 | 계약체결일:2009. 1. 8 (계약서 내용 조정일 2012, 2, 1) (계약서 내용 조정일 2015, 7, 28) (계약서 내용 조정일 2015, 10, 30) (계약서 내용 조정일 2017, 1, 2) 계약종료일: 유효특허의 만료일까지 (물질특허: 2024년 예상, 염조성물특허: 2029년 예상) |
| 총계약금액 | Potential Sales Royalty: 매출액에 따라 6~10% 특허가 국가별로 개별 종료 될 시 최대 10년까지 상기 로열티의 10%를 지급 |
| 지급금액 | 해당사항 없음 |
| 계약조건 | 주요 계약 내용 1) 한국내 독점개발, 판매권 및 유럽, 일본에 대한 수익 지분 2) 국내 시판시 판매액의 6~10% 로열티 지불 (Sublicensing,진행시 수익의 30% 지불) |
| 회계처리방법 | 해당사항 없음 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 Rivoceranib 특허 전용실시권 |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제(Rivoceranib 단독) 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1,2차 치료제(Rivoceranib 단독) 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상 3상 결과 ESMO 학회에서 발표(1차 평가지표 만족) |
| 기타사항 | Elevar Therapeutics, Inc. 는 2009년 12월 부광약품㈜에게 리보세라닙의 한국 판권을 양도하는 조건으로 리보세라닙 공동개발을 하였으며, 이후 부광약품㈜은 2018년 08월 한국 판권에 대한 모든 권리 및 의무를 에이치엘비생명과학㈜으로 400억원에 양도하였습니다. (2018.8.14 공시 참조) |
(중략)
다. 연구개발 실적
(1) 연구개발 진행 현황 및 향후계획
| [연구개발 진행 총괄표] |
| 구 분 | 품 목 | 적응증 | 임상시작일 | 현재 진행단계 | 기 타 | 임상주도기업 | 비고 | ||
|---|---|---|---|---|---|---|---|---|---|
| 단계(국가) | 승인일 | ||||||||
| 화학합성 의약품 |
신약 | 리보세라닙 (HLB생명과학 주도 임상 포함) |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안전성평가 완료 | Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
| 위암 (3차 단일요법) |
2017년 | 임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
| 간암 (1차 병용요법) [Combo with Camrelizumab] |
2019년 | 임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
임상 진행 중 9월 초록 발표 (1차 평가 지표 만족) |
Elevar | 항서제약과 공동개발 | |||
| 선양낭성암종 (1/2차 단일요법) |
2020년 | 임상2상 (한국, 미국) |
2020년 4월 (임상2상 개시일) |
임상 2상 진행중 6월 초록 발표 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
| 위암 (2차 병용요법) [Combo with Paclitaxel] |
2018년 | 임상1/2a상 (한국, 미국) |
2018년 10월 (임상1상 개시일) |
임상1상 종료 후, 2a상 준비 중 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
| 대장암 (3차 병용요법) [Combo with Lonsurf] |
2019년 | 임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 진행 중 | Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
| 황반변성치료제 (점안액) |
2018년 | 비임상 단계 | - | 타당성분석 중 | HLB 생명과학 |
HLB생명과학이 Rivoceranib 한국 내 전용실시권 L/I 후 자체 개발 | |||
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상진입 준비 중 (농림축산검역본부) |
HLB 생명과학 |
HLB생명과학이 Rivoceranib 한국 내 전용실시권 L/I 후 자체 개발 | |||
| 위암 (1차 병용요법) [Combo with Camrelizumab] |
2021년 | 임상2상 (한국) |
2021년 09월 (임상2상 개시일) |
임상 진행 중 | HLB 생명과학 |
HLB생명과학이 Rivoceranib 한국 내 전용실시권 L/I 후 개발 | |||
| 아필리아 | 난소암 2차 (백금계 약물 감수성) |
2018년 (유럽EMA 허가) |
유럽 허가 | 유럽 판매 준비 중 | Elevar | Elevar가 Apealea의 글로벌 (일부국가 제외) 전용실시권을 L/I 후 판매 준비 중 | |||
| 바이오 의약품 |
IMMUNOMIC THERAPEUTICS ITI-1000 |
GBM | 2016년 | 임상 2상 (미국) |
2016년 8월 (임상 2상 개시일) |
임상 진행 중 | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
|
| IMMUNOMIC THERAPEUTICS ITI-1001 |
GBM | - | 비임상 단계 | - | 임상 1상 IND 준비 중 | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| IMMUNOMIC THERAPEUTICS ITI-3000 |
Merkel Cell Carcinoma | 2022년 | 임상 1상 (미국) |
2022년 02월 (임상 1상 개시일) |
임상 진행 중 | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| IMMUNOMIC THERAPEUTICS ITI-8000 |
NSCLC | - | 비임상 단계 | - | - | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| IMMUNOMIC THERAPEUTICS ITI-9001 |
JRC Pollinosis | - | 비임상 단계 | - | - | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| 주) 통상적으로 통계적으로 유효성을 만족하는 수준의 임상데이터 수집이 완료되면 임상 결과를 발표하나, 이는 임상의 완전한 종료를 뜻하는 바는 아닙니다. 모든 임상 참여 환자의 데이터가 축적된 후 임상결과보고서(CSR) 작성이 완료되면 공식적으로 임상시험이 종료됩니다. |
(가) : 리보세라닙
| 구 분 | 화학합성의약품 |
| 적응증 | 위암 3/4차 치료제(Rivoceranib 단독), 위암 2차 치료제(파클리탁셀 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독), 간암 1차 치료제(항서제약 캄렐리주맙 병용), 대장암 3차 치료제(타이호제약 론서프 병용) |
| 작용기전 | 신생혈관억제, VEGFR2-TKI |
| 제품의특성 | 혈관내피세포성장인자수용체2(VEGFR-2)를 타켓으로 암 조직의 신생혈관 성장을 억제하고, 암세포의 증식억제와 면역세포의 정상화를 유도하는 경구용 표적 항암제입니다. |
| 진행경과 | 위암 3/4차 치료제: 단독 요법으로 글로벌 임상 3상 후 미국 NDA 신청 준비 중 위암 2차 치료제: 파클리탁셀과 병용으로 한국, 미국에서 임상1/2a 진행 (현재 임상 1상 환자 모집 종료) 선양낭성암 1,2차 치료제: 단독요법으로 미국, 한국에서 임상 2상 환자모집 완료 간암 1차 치료제: 항서제약의 캄렐리주맙과 병용으로 글로벌 13개국 임상 3상 진행하고 있고, 2022년 9월 ESMO에서 임상 결과 공개(1차 평가지표 만족) 대장암 3차 치료제: 타이호제약의 론서프와 병용으로 미국, 한국에서 임상 1b/2상 진행 |
| 향후계획 | 위암 3/4차 치료제(Rivoceranib 단독): 미국 FDA pre-NDA 진행, FDA에서 요청한 보완 자료 준비 중, 자료 보완 후 NDA 제출 예정 위암 2차 치료제(파클리탁셀 병용) 임상 1상 결과 분석 선양낭성암 1,2차 치료제(Rivoceranib 단독): 임상 2상 결과 수집 및 분석 간암 1차 치료제(항서제약 캄렐리주맙 병용): 임상 3상 결과 수집, 분석 및 Pre-NDA 준비 대장암 3차 치료제(타이호제약 론서프 병용): 임상 1상 결과 수집 및 분석 |
| 경쟁제품 | 위암 3차 치료제: 론서프, 옵디보(한국, 일본, 대만 한정) 위암 2차 치료제: 시람자(cyramza), 파클리탁셀 선양낭성암 1,2차 치료제: 표준치료제 없음 (Off-label)로 치료 진행 간암 1차 치료제: 넥사바, 렌비마, 아바스틴, 티센트릭 대장암 3차 치료제: 론서프, 스티바가, 옵디보 |
| 관련논문등 | 위암 글로벌 임상 3상 결과 2019년 유럽암학회(ESMO) 발표: Best of ESMO 선정 중국 위암 3차 치료제 임상 3상 논문: 2016년, J Clin Oncol 34 중국 위암 2차 치료제 임상 2상 논문: 2013년, J Clin Oncol 31 중국 고형암 치료제 임상 1상 논문: 2010년, BMC cancer 10 선양낭성암 중국 선낭암 임상 2상: 2021년 Therapeutic Advances in Medical Oncology 13 미국, 한국 선낭암 임상 2상 결과: 2022년 미국암학회 발표 간암 중국 간암 임상 2상: 2021년 Clin Cancer Res 15:27(4) 글로벌 간암 1차 치료제(항서제약 캄렐리주맙 병용) 임상 3상 결과: 2022년 9월 ESMO(유럽암학회)에서 공개 (1차 평가지표 만족) |
| 시장규모 | 위암 치료제 글로벌시장: 2017년 40억달러(4조7,236억원)에서 2026년에는 66억달러(7조7,939억원)로 성장 예상 선낭암 치료제 글로벌시장: 표준치료제가 없고 발병률이 낮아 글로벌 시장 규모 추산이 어려움 간암 치료제 글로벌시장: 2019년 17억3090만 달러 (약 2조 2,100억원) 대장암 치료제 글로벌시장: 2018년 64억4400만달러(7조2000억)에서 2028년 81억4700만달러(9조1000억)로 성장 예상 ※시장규모 관련 출처 간암 데이터 - Market Data Foercast "Global Liver Cancer Therapeutics Market Size, Share, Trends, COVID-19 Impact & Growth Analysis Report - Segmented By Type, Therapeutics, End-User & Region - Industry Forecast (2022 to 2027)" (2022.01) 위암 데이터 - Reserch And Markets "Gastric Cancer Drugs Global Market Report 2021: COVID-19 Impact and Recovery to 2030" (2021.06) 대장암 데이터 - Fortune Business Insights "Colorectal Cancer Therapeutics Market Size, Share & Industry Analysis, By Therapy (Targeted Therapy, Immunotherapy, Chemotherapy, Others), By Cancer Type (Colorectal Adenocarcinoma, Gastrointestinal Carcinoid Tumors, Others), By Distribution Channel (Hospitals Pharmacies, Retail Pharmacies, Online Pharmacies, Others) and Regional Forecast, 2019-2026" (2021.08) |
| 기타사항 | 특허 및 권리 보유 현황 - 리보세라닙의 물질특허: HLB - 글로벌 전용실시권은: Elevar - 한국 전용실시권: HLB생명과학 - 중국 전용실시권: 중국 항서제약이 보유 항서제약에서 2014년 위암 3차 치료제로 중국 내 시판허가를 득한 후 현재까지 꾸준한 매출 성장 유지 중입니다. 2015년 매출 약 450억에서 2018년 2,800억까지 매출 성장을 보여줘, 약효와 안전성을 입증하였습니다. 2021년 부터 간암 2차 치료제로 적응증을 확대하여, 중국 내 매출 확대가 기대 됩니다. |
(나) : 아필리아
| 구 분 | 화학합성의약품 |
| 적응증 | 백금계 약물 감수성이 있는 난소암 2차 치료제 |
| 작용기전 | 세포 분열에 필요한 RNA나 DNA 등을 손상시켜 세포 분열을 저지하는 세포 주기 선택적 항암제 |
| 제품의특성 | 파클리탁셀은 세포분열 과정 중 분열과 자가 복제의 기구인 미세소관이 분리되는 과정을 방해하는 "식물성 알칼로이드"로 분류되는 항암제입니다. 중증 과민반응 발현을 최소화하기 위해 투여 전에 전치료를 받아야 합니다. Apealea는 특허 출원된 Micelle 코팅을 적용하여 사전처치 필요없이 편의성을 증대시키며 부작용을 줄일 수 있도록 개발한 첨가제 형태 기반의 최적의 파크리탁셀 혼합제입니다. |
| 진행경과 | 유럽, 남미, 중동 지역 판매 준비 중 백금계 약물 저항성이 있는 난소암 환자 대상 임상 1상, 3상 동시 준비 중 |
| 향후계획 | -기 승인 받은 지역 대상 판매 준비 유럽, 중동, 북아프리카, 남미 지역 대상으로 판매 절차 진행 중 중국 진출을 위해 중국 현지업체와 JV를 통한 논의 중 -추가 적응증 개발 백금계 약물 저항성이 있는 난소암 환자를 대상으로 Rivoceranib과 병용 임상 계획 검토 중 |
| 경쟁제품 | 카보플라틴, 시스플라틴, 파클리탁셀, 아바스틴 |
| 관련논문등 | A randomized phase III trial in patients with recurrent platinum sensitive ovarian cancer comparing efficacy and safety of paclitaxel micellar and Cremophor EL-paclitaxel |
| 시장규모 | 글로벌 난소암 시장은 2021년 1억 7,500만달러 규모였으며, 2028년까지 매년 9.5% 성장하여 약 3억 3,973만달러에 이를 것으로 예상 ※시장규모 관련 출처 - Market Research Guru "Global Ovarian Cancer Market Research Report 2022" (2022.07) |
| 기타사항 | -특허 및 권리 보유 현황 Apealea 글로벌 전용실시권: Elevar (북유럽, 동유럽 일부국가 제외) -판매 승인 현황 2020년 유럽 EMA로 부터 난소암 2차 치료제로 판매 승인 (carboplatin 병용) 2022년 내 유럽 내 판매 개시 목표 |
(다) : ITI
| 구 분 | 바이오의약품 |
| 적응증 | GBM (교모세포종) |
| 작용기전 | UNITE 플랫폼은 리소좀관련막단백질(LAMP)에 특정 암에 발현되는 항원을 탑재해 면역세포를 빠르고 효율적으로 활성화시키는 기전 |
| 제품의특성 | 기존 기술 대비 CD4+ Helper T 세포 활성화에 가장 효과적 동일 APC 세포 내 MHC I & II Mediated Pathway 를 동시에 활성화 가능 (MHC II Pathway 직접적으로 관여) 다양한 질환 분야에 적용 가능 (암, 감염 질환, 자가면역 질환 등) 세포 기반 치료제, 핵산 (Nucleic Acid, DNA/RNA) 기반 치료제 개발 등 다양한 기술에 적용 가능 |
| 진행경과 | ITI-1000 교모세포종 (Dendritic Cell vaccine): 임상 2상 진행 중 ITI-1001교모세포종(DNA vaccine): 1상 IND 승인 후 임상 진행 중 ITI-3000 메르켈세포암(DNA vaccine): 1상 IND 승인 후 임상 진행 중 |
| 향후계획 | ITI-1000 연내 임상 2상 종료 후, FDA와 협의를 통해 조건부 허가 추진 |
| 경쟁제품 | 교모세포종: 테모졸로마이드 (2003년 승인) |
| 관련논문등 | 2009 Gene Therapy 16 2015 Nature 2017 Clinical Cancer Reserch 23(8) |
| 시장규모 | 글로벌 교모세포종 시장은 2021년 약 22억 9천만 달러에서 2028년 약 42억 달러에 이를 것으로 예상됩니다. ※시장규모 관련 출처 - Grand View Reserach "Glioblastoma Multiforme Treatment Market Size, Share & Trends Analysis Report By Treatment (Radiation Therapy, Immunotherapy), By Drug Class, By End Use, By Region, And Segment Forecasts, 2021 - 2028" (2021.09) |
| 기타사항 | 현재 교모세포종 원발성 악성 뇌종양 중 가장 흔한 종양으로 진단 후 치료를 하지 않으면 3-6개월 내에 사망합니다. 현재 치료법이 제한적이고 5년 생존율이 5%미만으로 악성도가 높은 질환입니다. ITI-1000 교모세포종 임상 1상 시험에서 mOS을 38.3 개월로 크게 개선하였으며, 표준치료제로 알려진 TMZ/RT 요법 대비 23 개월 이상 생존 기간을 향상시키고 60개월 생존율 또한 36.4%로 증가해 임상 2상 결과 또한 기대하고 있음. |
(주8) 정정 전
(나) 제약, 바이오 부문
2007년 넥사바의 간암 1차 치료제 시장 진입 이후 10년 동안 신규 승인 약물이 없어 시장 독식 체제를 형성하고 있었습니다. 그러던 2018년과 2020년에 렌비마(단독)와 티센트릭+아바스틴 병용요법이 FDA의 허가를 득했습니다. 그 중에서도 티센트릭+아바스틴 병용요법은 넥사바 대체할 새로운 표준치료제로 자리잡고 있습니다. 티센트릭(면역관문억제제)+아바스틴(신생혈관억제제)의 출현으로 처방 패러다임 변화하고 있으며, 면역관문억제제와 기존의 VEGFR-TKI 병용요법도 주목 받고 있습니다. 엘레바는 중국 헝루이제약과 공동으로 리보세라닙과 캄렐리주맙(면역관문억제제)의 임상 3상 환자를 모집을 종료하고 일차평가지표에 대해서 통계적 유의미성이 있는 top-line 결과를 확보하였습니다.
선양낭성암의 경우 현재까지 승인된 표준치료제가 없는 희귀암종으로 치료 방법이 제한적입니다. 현재 선양낭성암 환자들은 방사선 치료 및 의사 판단하에 Off-Label로 타 항암제가 사용되고 있는 실정입니다. 리보세라닙은 글로벌 최초로 대규모 상업화 임상 2상 (글로벌 80명)을 진행해 2022년 6월 ASCO에서 그 효능과 안전성을 입증했고, 현재 빠른 상업화를 위해 FDA의 가속승인제도(Accelerated Approval) 등 다양한 방안을 추진하고 있습니다. FDA 승인을 받게 될 경우, 선양낭성암 적응증에 대한 글로벌 첫 표준치료제로 등재될 가능성이 높습니다.
상기 두 적응증(간암(미국), 선양낭성암(미국))은 미국 FDA로부터 희귀의약품(Orphan Drug)으로 지정 받아 시장 가치를 더 높이고 있습니다. 시장조사기관 이벨류에이트(Evaluate)에 따르면 2026년까지 희귀의약품이 전체 처방약 매출의 1/5를 차지하고, 전세계 파이프라인 가치의 1/3을 차지할 것이라고 전망했습니다. 희귀의약품으로 지정될 경우 연구개발 비용의 25%(임상비용의 50%) 세액공제, 시판 후 7년간 시장독점권 부여 등 다양한 혜택을 기대할 수 있습니다.
그 외에도 2014년 중국 헝루이제약에서 위암 3차 치료제로 출시된 이후 현재까지 꾸준한 양적 성장을 이뤄왔습니다. 중국 현지 증권사 레포트 및 헝루이제약 공시에 따르면 리보세라닙 (중국명: 아파티닙)의 매출은 2015년 3억 위안 (한화 약 500억원)에서 2018년17억위안(한화 약 2,900억원)으로 증가하였습니다. 2020년 12월 간세포암2차 치료제로 중국내 판매 승인을 득해 중국 내 매출은 지속적으로 증가할 것으로 예상됩니다.
(다) 체외진단 의료기기 및 의약외품
식품의약품안전처 의료기기정보 포털에 의하면 국내 “검체채취용도구(1등급)”의 등록건수는 총 922건이며 이중 2020년에서 2021년 사이에 등록된 신규건수만 600건 이상이 등록되었으며 더불어 국내 “검체수송배지” 등록건수는 총 644건이며 이중 2020년에서 2021년 사이에 등록된 신규 건수의 경우 500여건의 신규 등록이 이루어진 상황입니다. 점차적으로 치료가 아닌 예방 및 검사에 대한 의료 시장의 변화가 이루어질 것으로 전망되는바 이러한 검체 채취용 제품에 대한 수요는 증가할 것으로 예상하고 있습니다. 하지만 COVID-19 상황에서 급조된 형태의 제품을 위주로 판매되었던 제품의 경우 금번 펜데믹 사태가 수그러질 경우 품질력과 생산 Capa를 보유하고 있지 않는 업체의 경우 시장에서 경쟁력을 확보하기 어려울 것으로 예상되고 있습니다.
알콜 스왑의 개인적인 사용 빈도가 높은 당뇨 환자의 증가 추이를 확인하였을 때 2020년 기준 501만명(츨처_강북삼성병원) 규모이며 이러한 당뇨 환자의 경우 매년 증가하고 있는 추세입니다. 2004년 대비 4배에 가까운 상승세를 나타내고 있으며 2020년기준 전세계 4억 6,300만명(출처_국제당뇨병연맹IDF)으로 추정되고 있습니다. 이러한 당뇨병의 경우 현대인에게 가장 많이 발병하는 만성질환으로 점차적으로 환자 추이는 증가할 것으로 전망되고 있으며, 2040년 6억 4,200만명으로 증가될 것으로 예상되고 있습니다(출처_이코노미조선). 국내 당뇨 환자의 체혈 후 사용되는 알콜 스왑제품을 기준으로 당뇨 환자 1일 2회 당뇨 측정을 가정으로 추산하였을 때 국내 시장의 경우 3억장/월 규모의 시장을 나타내고 있습니다.
(4) 회사 경쟁상의 강점과 단점
(가) 구명정 & DAVIT
국내 유일의 구명정 제조업체로써 해외 경정업체 대비 운송비 절감 및 빠른 A/S, 고객과 원활한 의사소통, 정확한 납기준수, 세계 일류상품으로 선정된 우수한 품질이 강점이며, 단점은 중국 구명정 대비 가격경쟁력, OFF-SHORE 시장에서의 선주 선호도가 낮은 것이나 자체개발한 엔진과 HOOK SYSTEM 등을 통해 가격 경쟁력을 확대하고 있습니다.
(나) GRP/GRE PIPE
경쟁업체 대비 우수한 가격 경쟁력과 빠른 A/S 및 생산공정 개선을 통한 생산능력, 국내조선사와의 원활한 의사소통이 강점이며, 경쟁사 대비 선주 선호도는 아직 낮은 것이 단점이나 점진적으로 홍보활동 및 영업을 통해 선호도가 올라가고 있습니다.
(다) 특수선박(관공선, 도선선, 유도선 등)
국내 최대 생산시설과 기술인력을 보유하고 있으며, 업무시스템이 경쟁사 대비 강점입니다. 경쟁사 대비 늦은 시장 진출로 인한 선주 선호도가 낮은 편이나 이 또한 점차개선될 것으로 기대하고 있습니다.
(라) 제약, 바이오
2세대 항암제인 표적치료제(Molecularly targeted therapy)는 정상세포와 암세포를 모두 공격할 수 있는 세포독성항암제와는 달리 암세포에 있는 특정 단백질 (표적)을 차단하여 암세포의 활동을 억제하는 약제로써 1세대인 세포독성 항암제에 비하여 부작용이 적은 장점을 가지고 있습니다.
동사가 권리를 보유한 리보세라닙은 2세대 표적항암제이면서 경구용이라는 복용 편의성을 확보했고, 부작용 또한 적어 병용치료제로 좋은 조건을 갖추고 있습니다. 실제로도, 기존 치료제들과의 다양한 병용요법으로 임상 연구결과들이 발표되고 있는 점 또한 앞으로의 성장성이 기대가 되는 부분입니다.
리보세라닙(중국명 아파티닙)은 2014년 위암 3차 치료제로 중국 내 판매 승인을 받은후 2020년 12월 간암 2차 치료제로 중국 내 시판 승인을 받았을 뿐만 아니라 비소세포폐암, 유방암, 난소암, 등 다양한 적응증을 대상으로 임상시험이 진행 되고 있어,향후 적응증 확대에 따른 매출증가가 및 가치의 상승으로 이어질 것으로 전망하고 있습니다. 그리고, 중국 지역 외 나머지 글로벌 판매 권리는 에이치엘비의 자회사인 엘레바가 보유하고 있습니다. 엘레바에서는 간암 1차, 위암 2차, 선양낭성암, 대장암 3차 등 적응증 확대를 위해 다방면으로 힘쓰고 있습니다.
(주8) 정정 후
(나) 제약, 바이오 부문
2007년 넥사바의 간암 1차 치료제 시장 진입 이후 10년 동안 신규 승인 약물이 없어 시장 독식 체제를 형성하고 있었습니다. 그러던 2018년과 2020년에 렌비마(단독)와 티센트릭+아바스틴 병용요법이 FDA의 허가를 득했습니다. 그 중에서도 티센트릭+아바스틴 병용요법은 넥사바 대체할 새로운 표준치료제로 자리잡고 있습니다. 티센트릭(면역관문억제제)+아바스틴(신생혈관억제제)의 출현으로 처방 패러다임 변화하고 있으며, 면역관문억제제와 기존의 VEGFR-TKI 병용요법도 주목 받고 있습니다. 엘레바는 중국항서제약과 공동으로 리보세라닙과 캄렐리주맙(면역관문억제제)의 임상 3상 환자를 모집을 종료하고 일차평가지표에 대해서 통계적 유의미성이 있는 top-line 결과를 확보하였습니다.
선양낭성암의 경우 현재까지 승인된 표준치료제가 없는 희귀암종으로 치료 방법이 제한적입니다. 현재 선양낭성암 환자들은 방사선 치료 및 의사 판단하에 Off-Label로 타 항암제가 사용되고 있는 실정입니다. 리보세라닙은 글로벌 최초로 대규모 상업화 임상 2상 (글로벌 80명)을 진행해 2022년 6월 ASCO에서 그 효능과 안전성을 입증했고, 현재 빠른 상업화를 위해 FDA의 가속승인제도(Accelerated Approval) 등 다양한 방안을 추진하고 있습니다. FDA 승인을 받게 될 경우, 선양낭성암 적응증에 대한 글로벌 첫 표준치료제로 등재될 가능성이 높습니다.
상기 두 적응증(간암(미국), 선양낭성암(미국))은 미국 FDA로부터 희귀의약품(Orphan Drug)으로 지정 받아 시장 가치를 더 높이고 있습니다. 시장조사기관 이벨류에이트(Evaluate)에 따르면 2026년까지 희귀의약품이 전체 처방약 매출의 1/5를 차지하고, 전세계 파이프라인 가치의 1/3을 차지할 것이라고 전망했습니다. 희귀의약품으로 지정될 경우 연구개발 비용의 25%(임상비용의 50%) 세액공제, 시판 후 7년간 시장독점권 부여 등 다양한 혜택을 기대할 수 있습니다.
그 외에도 2014년 중국 항서제약에서 위암 3차 치료제로 출시된 이후 현재까지 꾸준한 양적 성장을 이뤄왔습니다. 중국 현지 증권사 레포트 및 항서제약 공시에 따르면 리보세라닙 (중국명: 아파티닙)의 매출은 2015년 3억 위안 (한화 약 500억원)에서 2018년17억위안(한화 약 2,900억원)으로 증가하였습니다. 2020년 12월 간세포암2차 치료제로 중국내 판매 승인을 득해 중국 내 매출은 지속적으로 증가할 것으로 예상됩니다.
(다) 체외진단 의료기기 및 의약외품
식품의약품안전처 의료기기정보 포털에 의하면 국내 “검체채취용도구(1등급)”의 등록건수는 총 922건이며 이중 2020년에서 2021년 사이에 등록된 신규건수만 600건 이상이 등록되었으며 더불어 국내 “검체수송배지” 등록건수는 총 644건이며 이중 2020년에서 2021년 사이에 등록된 신규 건수의 경우 500여건의 신규 등록이 이루어진 상황입니다. 점차적으로 치료가 아닌 예방 및 검사에 대한 의료 시장의 변화가 이루어질 것으로 전망되는바 이러한 검체 채취용 제품에 대한 수요는 증가할 것으로 예상하고 있습니다. 하지만 COVID-19 상황에서 급조된 형태의 제품을 위주로 판매되었던 제품의 경우 금번 펜데믹 사태가 수그러질 경우 품질력과 생산 Capa를 보유하고 있지 않는 업체의 경우 시장에서 경쟁력을 확보하기 어려울 것으로 예상되고 있습니다.
알콜 스왑의 개인적인 사용 빈도가 높은 당뇨 환자의 증가 추이를 확인하였을 때 2020년 기준 501만명(츨처_강북삼성병원) 규모이며 이러한 당뇨 환자의 경우 매년 증가하고 있는 추세입니다. 2004년 대비 4배에 가까운 상승세를 나타내고 있으며 2020년기준 전세계 4억 6,300만명(출처_국제당뇨병연맹IDF)으로 추정되고 있습니다. 이러한 당뇨병의 경우 현대인에게 가장 많이 발병하는 만성질환으로 점차적으로 환자 추이는 증가할 것으로 전망되고 있으며, 2040년 6억 4,200만명으로 증가될 것으로 예상되고 있습니다(출처_이코노미조선). 국내 당뇨 환자의 체혈 후 사용되는 알콜 스왑제품을 기준으로 당뇨 환자 1일 2회 당뇨 측정을 가정으로 추산하였을 때 국내 시장의 경우 3억장/월 규모의 시장을 나타내고 있습니다.
(4) 회사 경쟁상의 강점과 단점
(가) 구명정 & DAVIT
국내 유일의 구명정 제조업체로써 해외 경정업체 대비 운송비 절감 및 빠른 A/S, 고객과 원활한 의사소통, 정확한 납기준수, 세계 일류상품으로 선정된 우수한 품질이 강점이며, 단점은 중국 구명정 대비 가격경쟁력, OFF-SHORE 시장에서의 선주 선호도가 낮은 것이나 자체개발한 엔진과 HOOK SYSTEM 등을 통해 가격 경쟁력을 확대하고 있습니다.
(나) GRP/GRE PIPE
경쟁업체 대비 우수한 가격 경쟁력과 빠른 A/S 및 생산공정 개선을 통한 생산능력, 국내조선사와의 원활한 의사소통이 강점이며, 경쟁사 대비 선주 선호도는 아직 낮은 것이 단점이나 점진적으로 홍보활동 및 영업을 통해 선호도가 올라가고 있습니다.
(다) 특수선박(관공선, 도선선, 유도선 등)
국내 최대 생산시설과 기술인력을 보유하고 있으며, 업무시스템이 경쟁사 대비 강점입니다. 경쟁사 대비 늦은 시장 진출로 인한 선주 선호도가 낮은 편이나 이 또한 점차개선될 것으로 기대하고 있습니다.
(라) 제약, 바이오
2세대 항암제인 표적치료제(Molecularly targeted therapy)는 정상세포와 암세포를 모두 공격할 수 있는 세포독성항암제와는 달리 암세포에 있는 특정 단백질 (표적)을 차단하여 암세포의 활동을 억제하는 약제로써 1세대인 세포독성 항암제에 비하여 부작용이 적은 장점을 가지고 있습니다.
동사가 권리를 보유한 리보세라닙은 2세대 표적항암제이면서 경구용이라는 복용 편의성을 확보했고, 부작용 또한 적어 병용치료제로 좋은 조건을 갖추고 있습니다. 실제로도, 기존 치료제들과의 다양한 병용요법으로 임상 연구결과들이 발표되고 있는 점 또한 앞으로의 성장성이 기대가 되는 부분입니다.
리보세라닙(중국명 아파티닙)은 2014년 위암 3차 치료제로 중국 내 판매 승인을 받은후 2020년 12월 간암 2차 치료제로 중국 내 시판 승인을 받았을 뿐만 아니라 비소세포폐암, 유방암, 난소암, 등 다양한 적응증을 대상으로 임상시험이 진행 되고 있어,향후 적응증 확대에 따른 매출증가가 및 가치의 상승으로 이어질 것으로 전망하고 있습니다. 그리고, 중국 지역 외 나머지 글로벌 판매 권리는 에이치엘비의 자회사인 엘레바가 보유하고 있습니다. 엘레바에서는 간암 1차 치료제(항서제약 캄렐리주맙 병용), 위암 2차 치료제(파클리탁셀 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독), 대장암 3차 치료제(타이호제약 론서프 병용)등 적응증 확대를 위해 다방면으로 힘쓰고 있습니다.
(주9) 정정 전
1-1) 대여거래
①당반기(2022년 반기)
| (기준일 : 2022년 06월 30일) | (단위 : 천원) |
| 성명(법인명) | 관계 | 계정과목 | 목적 | 변동내역 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
비고 | |||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 기초 (2022.01.01) |
증가 | 감소 | 기말 | ||||||||
| 화진메디칼 | 종속기업 | 장기대여금 | 운전자금, 개발자금 등 대여 | 1,700,000 | - | 1,700,000 | - | - | - | - | 2021-08-31 |
| 바다중공업 | 관계기업 | 장기대여금 | 공장인수로 인한 대여 | - | 2,000,000 | - | 2,000,000 | - | 10,334 | - | 2022-04-29 |
② 전기(2021년)
| (기준일 : 2021년 12월 31일) | (단위 : 천원) |
| 성명(법인명) | 관계 | 계정과목 | 목적 | 변동내역 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
비고 | |||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 기초 (2019.01.01) |
증가 | 감소 | 기말 (2021.12.31) |
||||||||
| 화진메디칼 | 종속기업 | 단기대여금 | 운영 자금 등 대여 | 500,000 | - | 500,000 | - | - | - | - | 2019-06-27 |
| 에이치엘비글로벌 | 관계기업 | 단기대여금 | 운영 자금 등 대여 | 9,000,000 | - | 9,000,000 | - | - | - | - | 2019-09-16 |
| 바다중공업 | 관계기업 | 단기대여금 | 운영 자금 등 대여 | 900,000 | - | 900,000 | - | - | - | - | 2020-01-15 |
| 에이치엘비인베스트먼트 | 종속기업 | 단기대여금 | 설립등기 취등록세 대여 | - | 45,490 | 45,490 | - | - | - | - | 2021-05-28 |
| 화진메디칼 | 종속기업 | 장기대여금 | 운전자금, 개발자금 등 대여 | - | 1,700,000 | - | 1,700,000 | - | 26,138 | - | 2021-08-31 |
| 합계 | 10,400,000 | 1,745,490 | 10,445,490 | 1,700,000 | - | 26,138 | - | - | |||
1-2) 대여거래 상세
1. 화진메디칼
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2019-06-27 | 2020-06-26 | 2019-06-27 | 이사회 결정 | 4.60% | 500,000 | - | - | 500,000 | - | - | - | - |
② 장기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2021-08-31 | 2023-08-31 | 2021-08-31 | 이사회 결정 | 4.60% | - | 1,700,000 | - | 1,700,000 | - | - | - | - |
2. 에이치엘비글로벌
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2019-09-16 | 2019-09-24 | 2019-09-16 | 이사회 결정 | 4.60% | 9,000,000 | - | - | 9,000,000 | - | - | - | - |
3. 에이치엘비인베스트먼트
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2021-05-28 | 2021-06-30 | - | 대표이사 의사결정 | 4.60% | - | 45,490 | - | 45,490 | - | - | - | - |
4. 바다중공업
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2020-01-15 | 2021-01-15 | 2020-10-15 | 이사회 결정 | 4.60% | 900,000 | - | - | 900,000 | - | - | - | - |
② 장기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2022-04-29 | 2027-04-28 | 2022-04-27 | 이사회 결정 | 4.60% | - | - | 2,000,000 | - | 2,000,000 | - | 10,334 | - |
1-2) 채무보증내역
①당반기(2022년 반기)
| (기준일 : 2022년 06월 30일) | (단위 : 천원) |
| 구분 | 회사명 | 보증처 | 내용 | 지급보증금액 | 보증기간 | |
|---|---|---|---|---|---|---|
| 기초 (2022.01.01) |
기말 (2022.06.30) |
|||||
| 관계기업 | 현대요트㈜ | 서울보증보험 | 하자이행보증 | 44,275 | 44,275 | 2018-06-23 ~ 2023-06-22 |
| 하자이행보증 | 347,080 | - | 2021-01-05 ~ 2022-01-04 | |||
| 하자이행보증 | 353,126 | - | 2021-01-05 ~ 2022-01-04 | |||
| 선급이행보증 | 294,439 | 297,756 | 2020-07-29 ~ 2022-09-29 | |||
| 선급이행보증 | 512,227 | - | 2020-12-07 ~ 2022-02-22 | |||
| 선급이행보증 | 379,696 | - | 2021-06-01 ~ 2022-02-22 | |||
| 계약이행보증 | 191,111 | 191,111 | 2021-12-17 ~ 2022-12-17 | |||
| 선급이행보증 | 1,166,593 | 1,166,593 | 2022-04-20 ~ 2023-02-15 | |||
| 합 계 | 3,288,547 | 1,699,735 | ||||
② 전기(2021년)
| (기준일 : 2021년 12월 31일) | (단위 : 천원) |
| 구분 | 회사명 | 보증처 | 내용 | 지급보증금액 | 보증기간 | |
|---|---|---|---|---|---|---|
| 기초 (2021.01.01) |
기말 (2021.12.31) |
|||||
| 관계기업 | 현대요트㈜ | 서울보증보험 | 하자이행보증 | 44,275 | 44,275 | 2018-06-23 ~ 2023-06-22 |
| 하자이행보증 | 82,479 | - | 2018-06-23 ~ 2021-06-22 | |||
| 하자이행보증 | - | 347,080 | 2021-01-05 ~ 2022-01-04 | |||
| 하자이행보증 | - | 353,126 | 2021-01-05 ~ 2022-01-04 | |||
| 계약이행보증 | 93,522 | - | 2020-07-17 ~ 2021-05-14 | |||
| 계약이행보증 | - | 191,111 | 2021-12-17 ~ 2022-12-17 | |||
| 선급이행보증 | 1,790,900 | - | 2020-07-17 ~ 2021-02-09 | |||
| 선급이행보증 | 1,790,447 | - | 2020-07-17 ~ 2021-02-09 | |||
| 선급이행보증 | 288,153 | 294,439 | 2020-07-29 ~ 2022-04-29 | |||
| 선급이행보증 | 509,008 | 512,227 | 2020-12-07 ~ 2022-02-22 | |||
| 선급이행보증 | - | 379,696 | 2021-06-01 ~ 2022-02-22 | |||
| 합 계 | 4,460,987 | 1,079,902 | ||||
2. 대주주와의 자산양수도 등
- 해당사항 없음
3. 대주주와의 영업거래
- 해당사항 없음
4. 대주주 이외의 이해관계자와의 거래
(1) 연결실체의 특수관계자는 관계기업 및 종속기업과 지배기업의 주요 경영진, 그리고 경영진이 출자 또는 임원으로 재직 중인 기업입니다.
| 구 분 | 회사명 |
|---|---|
| 관계기업 | 에이치엘비생명과학㈜ |
| 에이치엘비테라퓨틱스㈜ | |
| ㈜노터스 | |
| Verismo Therapeutics, Inc. | |
| 바다중공업㈜ | |
| 현대요트㈜ | |
| 기타특수관계자 | 에이치엘비글로벌㈜ (구. ㈜넥스트사이언스) |
| 에이치엘비제약㈜(구. ㈜메디포럼제약) | |
| 에이치엘비사이언스㈜ (구. 단디바이오사이언스㈜) |
|
| ㈜엘에스케이인베스트먼트 | |
| ㈜고션 | |
| 에이치엘비일렉㈜ | |
| 에이치엘비네트웍스㈜ | |
| Hyundai Lifeboats Singapore Pte. Ltd | |
| 오티에스중공업㈜ | |
| 현대코스모스요팅㈜ | |
| ㈜신화어드밴스 | |
| 에이치엘비엘이디㈜ | |
| 에이치엘비에너지㈜(구. 거림) | |
| ㈜펭귄오션레저 | |
| 의령태양광1호㈜ | |
| 에이치엘비생활건강㈜(구.엘리샤코이) | |
| 에이치엘비셀㈜(구.라이프리버㈜) | |
| ㈜프레시코 | |
| ㈜코아바이오 | |
| 에포케㈜(구.코르키㈜) | |
| 지트리파마슈티컬 | |
| REGENTREE | |
| OBLATO | |
| 바다엔지니어링㈜ | |
| ㈜새론바이오 | |
| 브이에스팜㈜ | |
| ㈜온힐 | |
| ㈜베리스모테라퓨틱스 아시아 | |
| 에이치엘비생명과학알앤디㈜(*) | |
| ㈜개밥왕(*) |
(*) 당반기 중 신규 편입되었습니다.
(2) 당반기 및 전반기 중 특수관계자와의 매출 및 매입 내역은 다음과 같습니다.
① 당반기
| (단위: 천원) | |||||
| 특수관계구분 | 특수관계자명 | 매출 | 매입 | ||
| 매출거래 | 기타 | 원재료 등 매입 | 기타 | ||
| 관계기업 | ㈜화진메디칼 | - | - | 7,258 | 38,101 |
| 에이치엘비생명과학㈜ | 120,000 | - | - | 186,023 | |
| 에이치엘비테라퓨틱스㈜ | - | 646,000 | 1,059,587 | 9,410,279 | |
| 바다중공업㈜ | 61,700 | - | 1,847,544 | - | |
| 현대요트㈜ | 291,890 | - | - | 31,818 | |
| 기타 | 에이치엘비글로벌㈜ (구.넥스트사이언스) |
- | - | - | 4,158 |
| 에이치엘비네트웍스㈜(*1) | 690,870 | - | - | 500 | |
| ㈜펭귄오션레저 | 41,200 | - | - | 2,430 | |
| 합 계 | 1,205,660 | 646,000 | 2,914,388 | 9,673,309 | |
(*) 연결실체는 기타특수관계자인 에이치엘비네트웍스㈜에 구명정 서비스 독점권을 부여하여 러닝개런티를 통한 로열티수익을 창출하고 있습니다.
② 전반기
| (단위: 천원) | |||||
| 특수관계구분 | 특수관계자명 | 매출 | 매입 | ||
| 매출거래 | 기타 | 매입거래 | 기타 | ||
| 관계기업 | 에이치엘비생명과학㈜ | 120,000 | - | - | 185,038 |
| 바다중공업㈜ | - | - | 1,573,305 | 3,000 | |
| 기타 | 에이치엘비글로벌㈜ | - | - | - | 4,158 |
| 에이치엘비일렉㈜ | - | 295,724 | - | - | |
| 에이치엘비네트웍스㈜ | 732,946 | - | - | 4,000 | |
| ㈜펭귄오션레저 | 36,400 | - | - | 29,400 | |
| 에이치엘비생활건강㈜ | - | - | - | 6,608 | |
| ㈜프레시코 | - | - | - | 6,839 | |
| 합 계 | 889,346 | 295,724 | 1,573,305 | 239,043 | |
(3) 당반기 및 전반기 중 특수관계자와의 자금거래 내역은 다음과 같습니다.
① 당반기
| (단위 : 천원) | |||||
| 특수관계구분 | 특수관계자명 | 자금 유출 거래 | 자금 유입 거래 | ||
| 자금대여 | 출자 | 대여금회수 | 이자수취 | ||
| 관계기업 | ㈜노터스 | - | 31,025,920 | - | - |
| 에이치엘비생명과학㈜(*) | 19,603,370 | - | - | - | |
| 바다중공업㈜ | 2,000,000 | - | - | - | |
| 기타특수관계자 | 에이치엘비제약㈜ (구. ㈜메디포럼제약) |
- | - | - | 50,000 |
| ㈜화진메디칼 | - | - | 1,700,000 | 51,633 | |
| 합 계 | 21,603,370 | 31,025,920 | 1,700,000 | 101,633 | |
(*) 에이치엘비생명과학㈜ 제9회 공모 신주인수권부사채에 청약하여 신주인수권부사채를 취득하였습니다.
② 전반기
| (단위: 천원) | |||||
| 특수관계구분 | 특수관계자명 | 자금 유출 거래 | 자금 유입 거래 | ||
| 자금대여 | 출자 | 대여금회수 | 이자수취 | ||
| 관계기업 | Verismo Therapeutics, Inc. | - | 5,586,000 | - | - |
| 기타특수관계자 | 에이치엘비제약㈜ (구. ㈜메디포럼제약) |
- | - | - | 50,000 |
| 합 계 | - | 5,586,000 | - | 50,000 | |
(4) 당반기말과 전기말 현재 특수관계자에 대한 채권ㆍ채무내역은 다음과 같습니다.
① 당반기말
| (단위: 천원) | |||||||||
| 구분 | 채권 | 채무 | |||||||
| 특수관계구분 | 특수관계자명 | 매출채권(*1) | 단기대여금(*1) | 미수금(*1) | 미수수익(*1) | 보증금(*1) | 매입채무 | 계약부채 | 기타 |
| 관계기업 | 에이치엘비테라퓨틱스㈜ | 73,172 | - | - | - | - | 996,241 | - | - |
| 에이치엘비생명과학㈜ | - | - | - | - | 22,469,317 | - | - | - | |
| 바다중공업㈜ | - | 2,000,000 | - | 10,334 | - | 228,292 | - | - | |
| 현대요트㈜ | 57,900 | - | - | - | - | - | 656,610 | 5,833 | |
| 기타특수관계자 | 에이치엘비글로벌㈜ (구.넥스트사이언스) |
- | - | - | - | - | - | - | 762 |
| 에이치엘비네트웍스㈜ | 319,039 | - | 70 | - | - | - | - | - | |
| ㈜펭귄오션레저(*1) | 660 | 23,600 | 53,306 | 1,628 | 93,293 | - | - | - | |
| 현대코스모스요팅㈜ | - | - | - | - | - | - | - | 54,000 | |
| 에이치엘비제약㈜ (구. ㈜메디포럼제약)(*2) | - | - | - | - | 23,272,820 | - | - | - | |
| 합 계 | 450,771 | 2,023,600 | 53,376 | 11,963 | 45,835,430 | 1,224,533 | 656,610 | 60,596 | |
(*1) 당반기말 현재 상기의 특수관계자 채권에 대해 대손충당금 171,021천원이 설정되어 있습니다.
(*2) 기타의 채권은 연결실체가 보유한 전환사채권이며, 공정가치평가 후 금액입니다.
② 전기말
| (단위: 천원) | |||||||||||
| 구분 | 채권 | 채무 | |||||||||
| 특수관계 구분 |
특수관계자명 | 매출채권 (*1) |
단기대여금 (*1) |
미수금 (*1) |
미수수익 (*1) |
보증금 (*1) |
기타 | 매입채무 | 계약부채 | 보증금 | 기타 |
| 관계기업 | 에이치엘비생명과학㈜(*2) | - | - | - | - | - | - | - | - | - | - |
| 바다중공업㈜ | 23,100 | - | - | - | - | - | 155,371 | - | - | - | |
| 현대요트㈜ | 57,900 | - | 18 | - | 53,897 | - | - | - | - | - | |
| 기타 | 에이치엘비셀㈜ (구.라이프리버㈜) |
- | - | 12 | - | - | - | - | - | - | - |
| 에이치엘비네트웍스㈜ | 235,296 | - | 70 | - | - | - | - | - | - | - | |
| 에이치엘비일렉㈜ | - | - | 265 | - | - | - | - | - | - | - | |
| ㈜펭귄오션레저(*2) | 660 | 23,600 | 53,306 | 1,628 | - | 93,293 | - | 12,000 | - | - | |
| 에이치엘비글로벌㈜ (구.넥스트사이언스) |
- | - | - | - | - | - | - | - | - | 762 | |
| 에이치엘비제약㈜ (구. ㈜메디포럼제약)(*2) |
- | - | - | - | - | 21,726,530 | - | - | - | - | |
| 합 계 | 316,956 | 23,600 | 53,670 | 1,628 | 53,897 | 21,819,823 | 155,371 | 12,000 | - | 762 | |
(*1) 전기말 현재 상기의 특수관계자 채권에 대해 대손충당금 224,918천원이 설정되어 있습니다.
(*2) 기타의 채권은 연결실체가 보유한 전환사채권이며, 공정가치평가 후 금액입니다.
(주9) 정정 후
1. 대주주 등에 대한 신용공여 등
가. 대여금 내역
1-1) 대여거래
①당반기(2022년 반기)
| (기준일 : 2022년 06월 30일) | (단위 : 천원) |
| 성명(법인명) | 관계 | 계정과목 | 목적 | 변동내역 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
비고 | |||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 기초 (2022.01.01) |
증가 | 감소 | 기말 | ||||||||
| 화진메디칼(*1) |
종속기업 | 장기대여금 | 운전자금, 개발자금 등 대여 | 1,700,000 | - | 1,700,000 | - | - | - | - | 2021-08-31 |
| 바다중공업 | 관계기업 | 장기대여금 | 공장인수로 인한 대여 | - | 2,000,000 | - | 2,000,000 | - | 10,334 | - | 2022-04-29 |
| (*1) 2022년 4월 29일, 이사회의 결정으로 그룹내 의료기기 사업 전문성 강화를 목적으로 종속회사인 ㈜화진메디스와 ㈜화진메디칼의 각각의 지분 100%를 에이치엘비테라퓨틱스㈜ 에 33억에 양도했으며, 상기 대여금은 2022년 04월 29일 전액 상환받았습니다. |
② 전기(2021년)
| (기준일 : 2021년 12월 31일) | (단위 : 천원) |
| 성명(법인명) | 관계 | 계정과목 | 목적 | 변동내역 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
비고 | |||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 기초 (2019.01.01) |
증가 | 감소 | 기말 (2021.12.31) |
||||||||
| 화진메디칼 | 종속기업 | 단기대여금 | 운영 자금 등 대여 | 500,000 | - | 500,000 | - | - | - | - | 2019-06-27 |
| 에이치엘비글로벌 | 관계기업 | 단기대여금 | 운영 자금 등 대여 | 9,000,000 | - | 9,000,000 | - | - | - | - | 2019-09-16 |
| 바다중공업 | 관계기업 | 단기대여금 | 운영 자금 등 대여 | 900,000 | - | 900,000 | - | - | - | - | 2020-01-15 |
| 에이치엘비인베스트먼트 | 종속기업 | 단기대여금 | 설립등기 취등록세 대여 | - | 45,490 | 45,490 | - | - | - | - | 2021-05-28 |
| 화진메디칼 | 종속기업 | 장기대여금 | 운전자금, 개발자금 등 대여 | - | 1,700,000 | - | 1,700,000 | - | 26,138 | - | 2021-08-31 |
| 합계 | 10,400,000 | 1,745,490 | 10,445,490 | 1,700,000 | - | 26,138 | - | - | |||
1-2) 대여거래 상세
1. 화진메디칼
1)신용공여의 대상자 이름 및 회사와의 관계
화진메디칼, 종속기업(대여 실행 및 상환 당시 종속기업)
2) 신용공여등의 종류
대여금
3) 신용공여등을 행한 일자, 금액, 조건, 최근 잔액 및 의사결정 방법
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2019-06-27 | 2020-06-26 | 2019-06-27 | 이사회 결정 | 4.60% | 500,000 | - | - | 500,000 | - | - | - | - |
② 장기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2021-08-31 | 2023-08-31 | 2021-08-31 | 이사회 결정 | 4.60% | - | 1,700,000 | - | 1,700,000 | - | - | - | - |
| (*1) 2022년 4월 29일, 이사회의 결정으로 그룹내 의료기기 사업 전문성 강화를 목적으로 종속회사인 ㈜화진메디스와 ㈜화진메디칼의 각각의 지분 100%를 에이치엘비테라퓨틱스㈜ 에 33억에 양도했으며, 상기 대여금은 2022년 04월 29일 전액 상환받았습니다. |
4) 신용공여의 목적
(1) 2019년 06월 27일 단기대여금 : 100% 종속회사인 화진메디칼의 운영자금 지원목적으로 신용공여를 실행함.
(2) 2021년 8월 31일 장기대여금 : 화진메디칼의 신제품 개발, 신규 유통사업 및 대출상환 등으로 일시적 자금 유동성 부족이 발생하여 신용공여를 실행함
5) 신용공여 등에 대하여 제공한 담보의 내용
해당사항 없음
6) 신용공여 등이 채무로 확정되어 회사에서 그 채무를 부담한 경우에는 이에관한 내용
해당사항 없음
2. 에이치엘비글로벌
1)신용공여의 대상자 이름 및 회사와의 관계
에이치엘비글로벌, 기타특수관계자(대여 실행 및 상환 당시 기타특수관계자)
2) 신용공여등의 종류
대여금
3) 신용공여등을 행한 일자, 금액, 조건, 최근 잔액 및 의사결정 방법
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2019-09-16 | 2019-09-24 | 2019-09-16 | 이사회 결정 | 4.60% | 9,000,000 | - | - | 9,000,000 | - | - | - | - |
4) 신용공여의 목적
풋옵션 행사로 인하여 일시적 자금부족이 발생하여 단기 금전대여 실행함.
5) 신용공여 등에 대하여 제공한 담보의 내용
해당사항 없음
6) 신용공여 등이 채무로 확정되어 회사에서 그 채무를 부담한 경우에는 이에관한 내용
해당사항 없음
3. 에이치엘비인베스트먼트
1)신용공여의 대상자 이름 및 회사와의 관계
에이치엘비인베스트먼트, 종속기업(대여 실행 및 상환 당시 종속기업)
2) 신용공여등의 종류
대여금
3) 신용공여등을 행한 일자, 금액, 조건, 최근 잔액 및 의사결정 방법
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2021-05-28 | 2021-06-30 | - | 대표이사 의사결정 | 4.60% | - | 45,490 | - | 45,490 | - | - | - | - |
4) 신용공여의 목적
설립 등기에 필요한 공과금 및 법무사 수임료 납부 비용을 위한 대여
5) 신용공여 등에 대하여 제공한 담보의 내용
해당사항 없음
6) 신용공여 등이 채무로 확정되어 회사에서 그 채무를 부담한 경우에는 이에관한 내용
해당사항 없음
4. 바다중공업
1)신용공여의 대상자 이름 및 회사와의 관계
바다중공업, 관계기업(대여 실행 및 상환 당시 관계기업)
2) 신용공여등의 종류
대여금
3) 신용공여등을 행한 일자, 금액, 조건, 최근 잔액 및 의사결정 방법
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2020-01-15 | 2021-01-15 | 2020-10-15 | 이사회 결정 | 4.60% | 900,000 | - | - | 900,000 | - | - | - | - |
② 장기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2022-04-29 | 2027-04-28 | 2022-04-27 | 이사회 결정 | 4.60% | - | - | 2,000,000 | - | 2,000,000 | - | 10,334 | - |
4) 신용공여의 목적
수주증가에 따른 이익 창출의 방안으로 효율적인 생산 및 원가 절감 및 대형선박 생산의 필요에 따른 대여
5) 신용공여 등에 대하여 제공한 담보의 내용
해당사항 없음
6) 신용공여 등이 채무로 확정되어 회사에서 그 채무를 부담한 경우에는 이에관한 내용
해당사항 없음
5. 펭귄오션레저
1)신용공여의 대상자 이름 및 회사와의 관계
펭귄오션레저, 기타특수관계자(대여 실행 당시 기타특수관계자)
2) 신용공여등의 종류
대여금
3) 신용공여등을 행한 일자, 금액, 조건, 최근 잔액 및 의사결정 방법
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2014-12-31 | 2015-12-31 | 2014-12-31 | 이사회 결정 | 6.9% | 23,600 | - | - | - | 23,600 | 23,600 | 1,628 | 1,628 |
4) 신용공여의 목적
말레이시아에서 영위하던 사업에 파견된 HLB 소속 직원에 대한 해외 영업비, 체류비 등의 명목으로 지급
5) 신용공여 등에 대하여 제공한 담보의 내용
해당사항 없음
6) 신용공여 등이 채무로 확정되어 회사에서 그 채무를 부담한 경우에는 이에관한 내용
2015년 12월 31일 회수가능성 부족으로 인해 대손처리
나. 채무보증내역
1)신용공여의 대상자 이름 및 회사와의 관계
현대요트, 관계기업(대여 실행 당시 관계기업)
2) 신용공여등의 종류
지급보증
3) 신용공여등을 행한 일자, 금액, 조건, 최근 잔액 및 의사결정 방법
①당반기(2022년 반기)
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 구분 | 회사명 | 보증처 | 이사회 결의일 | 판단근거 | 내용 | 지급보증금액 | 보증기간 | |
|---|---|---|---|---|---|---|---|---|
| 기초 (2022.01.01) |
기준일 (2022.10.07) |
|||||||
| 관계기업 | 현대요트㈜ | 서울보증보험 | 2018-06-28 | 이사회 결의 | 하자이행보증 | 44,275 | 44,275 | 2018-06-23 ~ 2023-06-22 |
| 2021-01-06 | 하자이행보증 | 347,080 | - | 2021-01-05 ~ 2022-01-04 | ||||
| 2021-01-06 | 하자이행보증 | 353,126 | - | 2021-01-05 ~ 2022-01-04 | ||||
| 2020-07-17 | 선급이행보증 | 294,439 | 297,756 | 2020-07-29 ~ 2022-09-29 | ||||
| 2020-12-07 | 선급이행보증 | 512,227 | - | 2020-12-07 ~ 2022-02-22 | ||||
| 2021-06-01 |
선급이행보증 | 379,696 | - | 2021-06-01 ~ 2022-02-22 | ||||
| 2021-12-16 | 계약이행보증 | 191,111 | 191,111 | 2021-12-17 ~ 2022-12-17 | ||||
| 2022-04-27 | 선급이행보증 | 1,166,593 | 1,166,593 | 2022-04-20 ~ 2023-02-15 | ||||
| 합 계 | 3,288,547 | 1,699,735 | - | |||||
② 전기(2021년)
| (기준일 : 2021년 12월 31일) | (단위 : 천원) |
| 구분 | 회사명 | 보증처 | 이사회 결의일 | 판단근거 | 내용 | 지급보증금액 | 보증기간 | |
|---|---|---|---|---|---|---|---|---|
| 기초 (2021.01.01) |
기말 (2021.12.31) |
|||||||
| 관계기업 | 현대요트㈜ | 서울보증보험 | 2018-06-28 |
이사회 결의 | 하자이행보증 | 44,275 | 44,275 | 2018-06-23 ~ 2023-06-22 |
| 2018-06-28 |
하자이행보증 | 82,479 | - | 2018-06-23 ~ 2021-06-22 | ||||
| 2021-01-06 |
하자이행보증 | - | 347,080 | 2021-01-05 ~ 2022-01-04 | ||||
| 2021-01-06 |
하자이행보증 | - | 353,126 | 2021-01-05 ~ 2022-01-04 | ||||
| 2020-07-17 |
계약이행보증 | 93,522 | - | 2020-07-17 ~ 2021-05-14 | ||||
| 2021-12-16 |
계약이행보증 | - | 191,111 | 2021-12-17 ~ 2022-12-17 | ||||
| 2020-07-17 | 선급이행보증 | 1,790,900 | - | 2020-07-17 ~ 2021-02-09 | ||||
| 2020-07-17 | 선급이행보증 | 1,790,447 | - | 2020-07-17 ~ 2021-02-09 | ||||
| 2020-07-17 |
선급이행보증 | 288,153 | 294,439 | 2020-07-29 ~ 2022-04-29 | ||||
| 2020-12-07 |
선급이행보증 | 509,008 | 512,227 | 2020-12-07 ~ 2022-02-22 | ||||
| 2021-06-01 |
선급이행보증 | - | 379,696 | 2021-06-01 ~ 2022-02-22 | ||||
| 합 계 | 4,460,987 | 1,079,902 | - | |||||
4) 신용공여의 목적
현대요트㈜가 선박 수주 계약을 진행할 시 보증서 제출의무에 따라 서울보증보험의 보증을 신청함. 보증 신청 과정에서 현대요트㈜의 신용이 부족하여 서울보증보험에서 최대주주(당사)의 연대보증을 요청함.
5) 신용공여 등에 대하여 제공한 담보의 내용
해당사항 없음
6) 신용공여 등이 채무로 확정되어 회사에서 그 채무를 부담한 경우에는 이에관한 내용
해당사항 없음
2. 대주주와의 자산양수도 등
가.[ ㈜화진메디칼, ㈜화진메디스 지분 양수도]
① 거래상대방: 에이치엘비테라퓨틱스㈜
② 거래종류: 종속회사 주식100% 양도
③ 거래일자 : 2022.04.29
④ 거래대상물 : ㈜화진메디칼,보통주 320,000주,
㈜화진메디스 보통주 50,000주
⑤ 거래목적 : 그룹내 의료기기 사업 전문성 강화 및 당사 수익구조 개선
⑥ 거래금액 : 3,300,000,000원
⑦ 금액산정기준 : 외부평가기관인 회계법인(삼도회계법인)의 주식가치평가를 통하여 양수도금액을 산정하였습니다.
⑧ 거래로 인한 손익발생 여부 : 에이치엘비㈜ 별도 손익에 800,000,000원 처분이익 발생됨.
⑨ 주주총회의 승인, 이사회 결의 등 해당 거래의 공정성 또는 합리성 등을 판단하기 위하여 내부통제절차를 거친 경우 그 내용 및 이러한 절차를 거치지 아니한 경우 그 사유 및 의사결정방법 : 이사회 결의(2022.04.29)
나.[ 에이치엘비제약㈜ 12CB 매각]
① 거래상대방: 에이치엘비생명과학㈜
② 거래종류: 보유채권매각
③ 거래일자 : 2022.10.07
④ 거래대상물 : 에이치엘비제약㈜ 12회차 CB
⑤ 거래목적 : 임상비용 및 운영자금 조달
⑥ 거래금액 : 23,700,000,000원
⑦ 금액산정기준 : 외부평가기관인 회계법인(삼도회계법인)의 주식가치평가를 통하여 양수도금액을 산정하였습니다.
⑧ 거래로 인한 손익발생 여부 : 에이치엘비㈜ 별도 손익에 1,200,000,000원 처분손실 발생됨.
⑨ 주주총회의 승인, 이사회 결의 등 해당 거래의 공정성 또는 합리성 등을 판단하기 위하여 내부통제절차를 거친 경우 그 내용 및 이러한 절차를 거치지 아니한 경우 그 사유 및 의사결정방법 : 이사회 결의(2022.08.12)
3. 대주주와의 영업거래
- 해당사항 없음
4. 대주주 이외의 이해관계자와의 거래
- 해당사항 없음
5. 기업인수목적회사의 추가기재사항
-해당사항 없음
(주10) 정정 전
1.연결대상 종속회사 현황 (상세)
| (단위 : 백만원) |
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| Elevar Therapeutics, Inc. (구 HLB USA, Inc.) |
2019.06.11 | Utah, USA | 항암제 연구개발 | 50,455 | 의결권의 과반수이상 보유(100.00%) | 미해당 |
| Immunomic Therapeutics,Inc. (*1) |
2005.09.28 | Rockville CityMaryland, USA | 항암제 연구개발 | 56,964 | 실질지배력 확보(41.07 %) | 미해당 |
| ㈜화진메디칼(*4) | 2000.04.25 | 동남구 성심원길 | 바이오 의료기기제조 및 판매 | 7,576 | 의결권의 과반수이상 보유(100.00%) | 미해당 |
| ㈜화진메디스(*4) | 2007.12.06 | 동남구 세성로 | 바이오 의료기기제조 및 판매 | 1,947 | 의결권의 과반수이상 보유(100.00%) | 미해당 |
| 에이치엘비인베스트먼트㈜(*2) | 2021.05.28 | 서울 강남구 선릉로 | 기타 금융업 | 10,227 | 의결권의 과반수이상 보유(100.00%) | 미해당 |
| Hyundai Lifeboats Shanghai Co.,Ltd(*3) | 2014.02.07 | Hi-Tech park, Pudong New District, Shanghai 201210, China | 서비스 | 913 | 의결권의 과반수이상 보유(100.00%) | 미해당 |
| (*1) 과반 미만의 의결권을 보유하고 있으나, 다른 의결권 보유자들의 주식 분산 정도 및 다른 주주의 집합적 의사결정 등을 고려한 결과 당사가 지배한다고 판단하였습니다. (*2) 2021년 5월 바이오와 헬스케어 등의 분야의 신기술사업자에 대한 투자 및 융자 등신기술사업 금융업을 통한 기업가치 극대화를 위해 에이치엘비인베스트먼트㈜의 보통주 600,000주를 30억원에 취득하였으며, 2021년 11월, 보통주1,400,000주를 70억원에 추가 취득하였습니다. (*3) 2022년 2월 리보세라닙 중국 로열티 수령 및 향후 중국사업진출을 위해 Hyundai Lifeboats Shanghai Co.,Ltd의 지분 100%를 약 1.1백만불에 취득하였습니다. (*4) 2022년 4월 29일, 이사회의 결정으로 그룹내 의료기기 사업 전문성 강화를 목적으로 종속회사인 ㈜화진메디스와 ㈜화진메디칼의 각각의 지분 100%를 에이치엘비테라퓨틱스㈜ 에 33억에 양도하여 종속회사에서 제외되었습니다. |
2. 계열회사 현황(상세)
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 사) |
| 상장여부 | 회사수 | 기업명 | 법인등록번호 |
|---|---|---|---|
| 상장 | 7 | 에이치엘비㈜(*1) | 170111-0021600 |
| 에이치엘비생명과학㈜ | 110111-1568885 | ||
| 에이치엘비글로벌㈜(구.㈜넥스트사이언스)(*2) | 144911-0000072 | ||
| 에이치엘비제약㈜(구.㈜메디포럼제약)(*3) | 110111-1538391 | ||
| 에이치엘비사이언스㈜ (구. 단디바이오사이언스㈜(*4) |
110111-6042363 | ||
| 에이치엘비테라퓨틱스㈜(*5) | 160111-0099451 | ||
| ㈜노터스(*6) | 284211-0063231 | ||
| 비상장 | 35 | Elevar Therpeutics,Inc.(*7) | - |
| Immunomic Therapeutics,Inc.(*8) | - | ||
| ㈜화진메디칼 | 111511-0039515 | ||
| ㈜화진메디스 | 161511-0094866 | ||
| 바다중공업㈜ | 180111-0288654 | ||
| 현대요트㈜ | 230111-0143435 | ||
| 에이치엘비셀㈜(구.라이프리버㈜)(*9) | 131311-0092331 | ||
| ㈜엘에스케이인베스트먼트 | 110111-6028595 | ||
| ㈜고션 | 205411-0015431 | ||
| 에이치엘비일렉㈜ | 284911-0134898 | ||
| 에이치엘비네트웍스㈜ | 230111-0155076 | ||
| Hyundai Lifeboats Singapore Pte. Ltd | - | ||
| 오티에스중공업㈜ | 201311-0051811 | ||
| 현대앤코스모스요팅㈜ | 110111-5137868 | ||
| ㈜신화어드밴스 | 110111-3790113 | ||
| 에이치엘비엘이디㈜ | 120111-0879348 | ||
| 에이치엘비에너지㈜(구, 거림) | 180111-0235332 | ||
| ㈜펭귄오션레저 | 230111-0222320 | ||
| 에이치엘비생활건강㈜(구.㈜엘리샤코이)(*10) | 110111-3920108 | ||
| ㈜프레시코 | 161311-0037563 | ||
| ㈜코아바이오 | 110111-5989128 | ||
| 에포케㈜(구.코르키㈜)(*11) | 110111-5998111 | ||
| VerismoTherapeutics,Inc.(*12) | - | ||
| 에이치엘비인베스트먼트㈜(*13) | 110111-7902657 | ||
| 지트리파마슈티컬(*14) | 131111-0379709 | ||
| REGENTREE(*15) | - | ||
| OBLATO(*16) | - | ||
| Hyundai Lifeboats Shanghai Co.,Ltd(*17) | - | ||
| 바다엔지니어링㈜ | 195511-0230907 | ||
| ㈜새론바이오(*18) | 135211-0033010 | ||
| 브이에스팜㈜(*19) | 110111-4752542 | ||
| ㈜온힐(*20) | 120111-******* | ||
| ㈜베리스모테라퓨틱스 아시아(*21) | 110111-8164199 | ||
| 에이치엘비생명과학알앤디㈜(*22) | 134811-0680620 | ||
| ㈜개밥왕(*23) | 284111-0185623 |
| (*1) 해당 기업집단의 지배회사입니다. (*2) 2022년 3월 넥스트사이언스㈜에서 에이치엘비글로벌㈜로 사명을 변경하였습니다. (*3) 2020년 10월 ㈜메디포럼제약에서 에이치엘비제약㈜로 사명을 변경하였습니다. (*4) 2020년 4월 단디바이오사이언스㈜는 코넥스시장에 상장되었습니다. 2022년 3월 단디바이오사이언스㈜에서 에이치엘비사이언스㈜로 사명을 변경하였습니다. (*5) 2021년 11월 지분취득을 통한 바이오 사업과의 시너지 극대화와 기업가치극대화를 위해 에이치엘비테라퓨틱스㈜ 보통주 530,899주를 약 50억에 취득하였습니다. (*6) 2022년 3월 지분취득을 통한 신규사업진출 및 기존사업과의 시너지 극대화를 위해 ㈜노터스 보통주 1,405,648주를 약 562억에 취득하였습니다. (*7) LSK BioPartners, Inc. 는 2019년 11월 27일을 합병기일로 당사의 100% 자회사인 HLB USA, Inc.에 흡수합병되어 소멸하였으며, 이후 HLB USA,Inc는 Elevar Therapeutics,Inc 로 법인명 변경하였습니다. (*8) 과반 미만의 의결권을 보유하고 있으나, 다른 의결권 보유자들의 주식 분산 정도 및 다른 주주의 집합적 의사결정 등을 고려한 결과 당사가 지배한다고 판단하였습니다. (*9) 2020년 4월 라이프리버㈜에서 에이치엘비셀㈜로 사명을 변경하였습니다. (*10) 2022년 3월 ㈜엘리샤코이에서 에이치엘비생활건강㈜로 사명을 변경하였습니다. (*11) 2021년 7월 코르키㈜는 에이치엘비파워㈜로부터 에이치엘비네트웍스㈜의 지분 75.19%를 취득하였습니다. (*12) 2021년 4월 신규 Pipeline 확보를 통한 지속적인 미래 기업가치의 극대화를 위해 2020년 6월에 설립된 미국 벤처기업 Verismo Therapeutics,Inc. 에 5백만불을 투자하였습니다. Verismo Therapeutics,Inc.은 KIR-CAR 기술의 기본특허와 KIR-CAR Mesothlin과 연관된 특허 및 생산공정과 관련된 특허를 보유하고 있으며, 차세대 CAR-T 플랫폼 기술을 기반으로 상용화 가능한 고형암 타깃 CAR-T 개발을 목표로 하고 있습니다. (*13) 2021년 5월, 바이오와 헬스케어 등의 분야의 신기술사업자에 대한 투자 및 융자 등신기술사업 금융업을 통한 기업가치 극대화를 위해 에이치엘비인베스트먼트㈜의 보통주 600,000주를 30억원에 취득하였으며, 2021년 11월, 보통주 1,400,000주를 70억원에 추가 취득하였습니다. (*14) 2021년 11월 지트리파마슈티컬은 에이치엘비테라퓨틱스의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*15) 2021년 11월 REGENTREE는 에이치엘비테라퓨틱스의 지분 61.5% 자회사로서 계열회사로 편입되었습니다. (*16) 2021년 11월 OBLATO는 에이치엘비테라퓨틱스의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*17) 2022년 2월 리보세라닙 중국 로열티 수령 및 향후 중국사업진출을 위해 Hyundai Lifeboats Shanghai Co.,Ltd의 지분 100%를 약 1.1백만불에 취득하였습니다. (*18) 2022년 3월 ㈜새론바이오는 ㈜노터스의 지분 60.0% 자회사로서 계열회사로 편입되었습니다. (*19) 2022년 3월 ㈜브이에스팜은 ㈜노터스의 지분 66.2% 자회사로서 계열회사로 편입되었습니다. (*20) 2022년 3월 ㈜온힐은 ㈜노터스의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*21) 2022년 1월 ㈜베리스모테라퓨틱스 아시아는 Verismo Therapeutics,Inc의 지분 62.0% 자회사로서 계열회사로 편입되었습니다. (*22) 2022년 4월 에이치엘비생명과학알앤디㈜는 에이치엘비생명과학㈜의 100% 자회사로서 계열회사로 편입되었습니다. (*23) 2022년 6월 ㈜개밥왕은 ㈜온힐의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*) 의령태양광1호㈜의 경우 2022년 6월부로 청산하여 계열회사에서 제외되었습니다. |
3. 타법인출자 현황(상세)
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 백만원, 천주, %) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
| 에이치엘비생명과학㈜ | 상장 | 2015.10.23 | 경영참여 | 7,000 | 18,721 | 19.60 | 131,066 | - | - | - | 18,721 | 19.60 | 131,066 | 270,800 | -49,292 |
| 현대요트㈜ | 비상장 | 2009.07.02 | 경영참여 | 300 | 328 | 39.43 | - | - | - | - | 328 | 39.43 | - | 12,036 | 9 |
| 바다중공업㈜ | 비상장 | 2009.05.28 | 경영참여 | 300 | 780 | 28.89 | 768 | - | - | - | 780 | 28.89 | 768 | 20,421 | 556 |
| 고션 | 비상장 | 2014.02.12 | 경영참여 | 105 | 21 | 18.76 | - | - | - | - | 21 | 18.76 | - | 40 | - |
| 에이치엘비파워㈜ | 상장 | 2016.09.06 | 단순투자 | 2,800 | 623 | 0.68 | 999 | - | - | -280 | 623 | 0.68 | 719 | 99,108 | -6,532 |
| ㈜화진메디칼 | 비상장 | 2018.02.21 | 경영참여 | 5,022 | 70 | 100.00 | 2,500 | -70 | -2,500 | - | - | - | - | 7,576 | 63 |
| ㈜화진메디스 | 비상장 | 2018.02.21 | 경영참여 | 500 | 50 | 100.00 | - | -50 | - | - | - | - | - | 1,947 | -172 |
| Elevar Therapeutics, Inc. | 비상장 | 2019.06.11 | 경영참여 | 188,792 | 56,579 | 100.00 | 337,384 | 5,000 | 31,513 | - | 61,579 | 100.00 | 368,896 | 50,455 | -63,462 |
| ㈜씨엘팜 | 비상장 | 2019.12.02 | 경영참여 | 5,000 | 64 | 7.72 | 5,074 | - | - | - | 64 | 7.72 | 5,074 | 31,605 | 1,211 |
| Immunomic Therapeutics, Inc. | 비상장 | 2020.01.31 | 경영참여 | 11,970 | 11,286 | 41.11 | 67,098 | - | - | - | 11,286 | 41.07 | 67,098 | 56,964 | -26,056 |
| Verismo Therapeutics, Inc. | 비상장 | 2021.04.12 | 경영참여 | 5,602 | 1,913 | 11.44 | 5,602 | - | - | - | 1,913 | 9.61 | 5,602 | 15,573 | -6,563 |
| 에이치엘비 인베스트먼트㈜ | 비상장 | 2021.05.28 | 경영참여 | 10,000 | 2,000 | 100.00 | 10,000 | - | - | - | 2,000 | 100.00 | 10,000 | 10,227 | -438 |
| 에이치엘비테라퓨틱스㈜ | 상장 | 2021.11.15 | 경영참여 | 500 | 531 | 1.69 | 5,000 | - | - | - | 531 | 1.69 | 5,000 | 189,711 | -17,764 |
| 에프에이㈜(*) | 비상장 | 2021.10.20 | 경영참여 | 102,126 | 28 | 100.00 | 102,126 | -28 | -102,126 | - | - | - | - | - | - |
| Hyundai Lifeboats Shanghai Co.,Ltd | 비상장 | 2022.02.10 | 경영참여 | 1,385 | - | - | - | 0 | 1,385 | - | 0 | 100.00 | 1,385 | 913 | 138 |
| ㈜노터스 | 상장 | 2022.03.30 | 경영참여 | 56,226 | - | - | - | 1,406 | 56,226 | - | 1,406 | 18.01 | 56,226 | 93,402 | 10,308 |
| 합 계 | - | - | 667,616 | 6,258 | -15,502 | -280 | - | - | 651,834 | 860,777 | -157,994 | ||||
(주10) 정정 후
1.연결대상 종속회사 현황 (상세)
| (단위 : 백만원) |
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| Elevar Therapeutics, Inc. (구 HLB USA, Inc.) |
2019.06.11 | Utah, USA | 항암제 연구개발 | 50,455 | 의결권의 과반수이상 보유(100.00%) | 미해당 |
| Immunomic Therapeutics,Inc. (*1) |
2005.09.28 | Rockville CityMaryland, USA | 항암제 연구개발 | 56,964 | 실질지배력 확보(41.07 %) | 미해당 |
| 에이치엘비인베스트먼트㈜(*2) | 2021.05.28 | 서울 강남구 선릉로 | 기타 금융업 | 10,227 | 의결권의 과반수이상 보유(100.00%) | 미해당 |
| Hyundai Lifeboats Shanghai Co.,Ltd(*3) | 2014.02.07 | Hi-Tech park, Pudong New District, Shanghai 201210, China | 서비스 | 913 | 의결권의 과반수이상 보유(100.00%) | 미해당 |
| (*) 2022년 4월 29일, 이사회의 결정으로 그룹내 의료기기 사업 전문성 강화를 목적으로 종속회사였던 ㈜화진메디스와 ㈜화진메디의 각각의 지분 100%를 에이치엘비테라퓨틱스㈜에 33억에 양도하여 종속회사에서 제외되었습니다. (*1) 과반 미만의 의결권을 보유하고 있으나, 다른 의결권 보유자들의 주식 분산 정도 및 다른 주주의 집합적 의사결정 등을 고려한 결과 당사가 지배한다고 판단하였습니다. (*2) 2021년 5월 바이오와 헬스케어 등의 분야의 신기술사업자에 대한 투자 및 융자 등신기술사업 금융업을 통한 기업가치 극대화를 위해 에이치엘비인베스트먼트㈜의 보통주 600,000주를 30억원에 취득하였으며, 2021년 11월, 보통주1,400,000주를 70억원에 추가 취득하였습니다. (*3) 2022년 2월 리보세라닙 중국 로열티 수령 및 향후 중국사업진출을 위해 Hyundai Lifeboats Shanghai Co.,Ltd의 지분 100%를 약 1.1백만불에 취득하였습니다. |
2. 계열회사 현황(상세)
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 사) |
| 상장여부 | 회사수 | 기업명 | 법인등록번호 |
|---|---|---|---|
| 상장 | 7 | 에이치엘비㈜(*1) | 170111-0021600 |
| 에이치엘비생명과학㈜ | 110111-1568885 | ||
| 에이치엘비글로벌㈜(구.㈜넥스트사이언스)(*2) | 144911-0000072 | ||
| 에이치엘비제약㈜(구.㈜메디포럼제약)(*3) | 110111-1538391 | ||
| 에이치엘비사이언스㈜ (구. 단디바이오사이언스㈜(*4) |
110111-6042363 | ||
| 에이치엘비테라퓨틱스㈜(*5) | 160111-0099451 | ||
| ㈜노터스(*6) | 284211-0063231 | ||
| 비상장 | 35 | Elevar Therpeutics,Inc.(*7) | - |
| Immunomic Therapeutics,Inc.(*8) | - | ||
| ㈜화진메디칼 | 111511-0039515 | ||
| ㈜화진메디스 | 161511-0094866 | ||
| 바다중공업㈜ | 180111-0288654 | ||
| 현대요트㈜ | 230111-0143435 | ||
| 에이치엘비셀㈜(구.라이프리버㈜)(*9) | 131311-0092331 | ||
| ㈜엘에스케이인베스트먼트 | 110111-6028595 | ||
| ㈜고션 | 205411-0015431 | ||
| 에이치엘비일렉㈜ | 284911-0134898 | ||
| 에이치엘비네트웍스㈜ | 230111-0155076 | ||
| Hyundai Lifeboats Singapore Pte. Ltd | - | ||
| 오티에스중공업㈜ | 201311-0051811 | ||
| 현대앤코스모스요팅㈜ | 110111-5137868 | ||
| ㈜신화어드밴스 | 110111-3790113 | ||
| 에이치엘비엘이디㈜ | 120111-0879348 | ||
| 에이치엘비에너지㈜(구, 거림) | 180111-0235332 | ||
| ㈜펭귄오션레저 | 230111-0222320 | ||
| 에이치엘비생활건강㈜(구.㈜엘리샤코이)(*10) | 110111-3920108 | ||
| ㈜프레시코 | 161311-0037563 | ||
| ㈜코아바이오 | 110111-5989128 | ||
| 에포케㈜(구.코르키㈜)(*11) | 110111-5998111 | ||
| VerismoTherapeutics,Inc.(*12) | - | ||
| 에이치엘비인베스트먼트㈜(*13) | 110111-7902657 | ||
| 지트리파마슈티컬(*14) | 131111-0379709 | ||
| REGENTREE(*15) | - | ||
| OBLATO(*16) | - | ||
| Hyundai Lifeboats Shanghai Co.,Ltd(*17) | - | ||
| 바다엔지니어링㈜ | 195511-0230907 | ||
| ㈜새론바이오(*18) | 135211-0033010 | ||
| 브이에스팜㈜(*19) | 110111-4752542 | ||
| ㈜온힐(*20) | 120111-******* | ||
| ㈜베리스모테라퓨틱스 아시아(*21) | 110111-8164199 | ||
| 에이치엘비생명과학알앤디㈜(*22) | 134811-0680620 | ||
| ㈜개밥왕(*23) | 284111-0185623 |
| (*1) 해당 기업집단의 지배회사입니다. (*2) 2022년 3월 넥스트사이언스㈜에서 에이치엘비글로벌㈜로 사명을 변경하였습니다. (*3) 2020년 10월 ㈜메디포럼제약에서 에이치엘비제약㈜로 사명을 변경하였습니다. (*4) 2020년 4월 단디바이오사이언스㈜는 코넥스시장에 상장되었습니다. 2022년 3월 단디바이오사이언스㈜에서 에이치엘비사이언스㈜로 사명을 변경하였습니다. (*5) 2021년 11월 지분취득을 통한 바이오 사업과의 시너지 극대화와 기업가치극대화를 위해 에이치엘비테라퓨틱스㈜ 보통주 530,899주를 약 50억에 취득하였습니다. (*6) 2022년 3월 지분취득을 통한 신규사업진출 및 기존사업과의 시너지 극대화를 위해 ㈜노터스 보통주 1,405,648주를 약 562억에 취득하였습니다. (*7) LSK BioPartners, Inc. 는 2019년 11월 27일을 합병기일로 당사의 100% 자회사인 HLB USA, Inc.에 흡수합병되어 소멸하였으며, 이후 HLB USA,Inc는 Elevar Therapeutics,Inc 로 법인명 변경하였습니다. (*8) 과반 미만의 의결권을 보유하고 있으나, 다른 의결권 보유자들의 주식 분산 정도 및 다른 주주의 집합적 의사결정 등을 고려한 결과 당사가 지배한다고 판단하였습니다. (*9) 2020년 4월 라이프리버㈜에서 에이치엘비셀㈜로 사명을 변경하였습니다. (*10) 2022년 3월 ㈜엘리샤코이에서 에이치엘비생활건강㈜로 사명을 변경하였습니다. (*11) 2021년 7월 코르키㈜는 에이치엘비파워㈜로부터 에이치엘비네트웍스㈜의 지분 75.19%를 취득하였습니다. (*12) 2021년 4월 신규 Pipeline 확보를 통한 지속적인 미래 기업가치의 극대화를 위해 2020년 6월에 설립된 미국 벤처기업 Verismo Therapeutics,Inc. 에 5백만불을 투자하였습니다. Verismo Therapeutics,Inc.은 KIR-CAR 기술의 기본특허와 KIR-CAR Mesothlin과 연관된 특허 및 생산공정과 관련된 특허를 보유하고 있으며, 차세대 CAR-T 플랫폼 기술을 기반으로 상용화 가능한 고형암 타깃 CAR-T 개발을 목표로 하고 있습니다. (*13) 2021년 5월, 바이오와 헬스케어 등의 분야의 신기술사업자에 대한 투자 및 융자 등신기술사업 금융업을 통한 기업가치 극대화를 위해 에이치엘비인베스트먼트㈜의 보통주 600,000주를 30억원에 취득하였으며, 2021년 11월, 보통주 1,400,000주를 70억원에 추가 취득하였습니다. (*14) 2021년 11월 지트리파마슈티컬은 에이치엘비테라퓨틱스의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*15) 2021년 11월 REGENTREE는 에이치엘비테라퓨틱스의 지분 61.5% 자회사로서 계열회사로 편입되었습니다. (*16) 2021년 11월 OBLATO는 에이치엘비테라퓨틱스의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*17) 2022년 2월 리보세라닙 중국 로열티 수령 및 향후 중국사업진출을 위해 Hyundai Lifeboats Shanghai Co.,Ltd의 지분 100%를 약 1.1백만불에 취득하였습니다. (*18) 2022년 3월 ㈜새론바이오는 ㈜노터스의 지분 60.0% 자회사로서 계열회사로 편입되었습니다. (*19) 2022년 3월 ㈜브이에스팜은 ㈜노터스의 지분 66.2% 자회사로서 계열회사로 편입되었습니다. (*20) 2022년 3월 ㈜온힐은 ㈜노터스의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*21) 2022년 1월 ㈜베리스모테라퓨틱스 아시아는 Verismo Therapeutics,Inc의 지분 62.0% 자회사로서 계열회사로 편입되었습니다. (*22) 2022년 4월 에이치엘비생명과학알앤디㈜는 에이치엘비생명과학㈜의 100% 자회사로서 계열회사로 편입되었습니다. (*23) 2022년 6월 ㈜개밥왕은 ㈜온힐의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*) 의령태양광1호㈜의 경우 2022년 6월부로 청산하여 계열회사에서 제외되었습니다. |
3. 타법인출자 현황(상세)
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 백만원, 천주, %) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
| 에이치엘비생명과학㈜ | 상장 | 2015.10.23 | 경영참여 | 7,000 | 18,721 | 19.60 | 131,066 | - | - | - | 18,721 | 19.60 | 131,066 | 270,800 | -49,292 |
| 현대요트㈜(*) |
비상장 | 2009.07.02 | 경영참여 | 300 | 328 | 39.43 | - | - | - | - | 328 | 39.43 | - | 12,036 | 9 |
| 바다중공업㈜ | 비상장 | 2009.05.28 | 경영참여 | 300 | 780 | 28.89 | 768 | - | - | - | 780 | 28.89 | 768 | 20,421 | 556 |
| 고션(*) |
비상장 | 2014.02.12 | 경영참여 | 105 | 21 | 18.76 | - | - | - | - | 21 | 18.76 | - | 40 | - |
| 에이치엘비파워㈜ | 상장 | 2016.09.06 | 단순투자 | 2,800 | 623 | 0.68 | 999 | - | - | -280 | 623 | 0.68 | 719 | 99,108 | -6,532 |
| ㈜화진메디칼 | 비상장 | 2018.02.21 | 경영참여 | 5,022 | 70 | 100.00 | 2,500 | -70 | -2,500 | - | - | - | - | 7,576 | 63 |
| ㈜화진메디스(*) |
비상장 | 2018.02.21 | 경영참여 | 500 | 50 | 100.00 | - | -50 | - | - | - | - | - | 1,947 | -172 |
| Elevar Therapeutics, Inc. | 비상장 | 2019.06.11 | 경영참여 | 188,792 | 56,579 | 100.00 | 337,384 | 5,000 | 31,513 | - | 61,579 | 100.00 | 368,896 | 50,455 | -63,462 |
| ㈜씨엘팜 | 비상장 | 2019.12.02 | 경영참여 | 5,000 | 64 | 7.72 | 5,074 | - | - | - | 64 | 7.72 | 5,074 | 31,605 | 1,211 |
| Immunomic Therapeutics, Inc. | 비상장 | 2020.01.31 | 경영참여 | 11,970 | 11,286 | 41.11 | 67,098 | - | - | - | 11,286 | 41.07 | 67,098 | 56,964 | -26,056 |
| Verismo Therapeutics, Inc. | 비상장 | 2021.04.12 | 경영참여 | 5,602 | 1,913 | 11.44 | 5,602 | - | - | - | 1,913 | 9.61 | 5,602 | 15,573 | -6,563 |
| 에이치엘비 인베스트먼트㈜ | 비상장 | 2021.05.28 | 경영참여 | 10,000 | 2,000 | 100.00 | 10,000 | - | - | - | 2,000 | 100.00 | 10,000 | 10,227 | -438 |
| 에이치엘비테라퓨틱스㈜ | 상장 | 2021.11.15 | 경영참여 | 500 | 531 | 1.69 | 5,000 | - | - | - | 531 | 1.69 | 5,000 | 189,711 | -17,764 |
| 에프에이㈜ | 비상장 | 2021.10.20 | 경영참여 | 102,126 | 28 | 100.00 | 102,126 | -28 | -102,126 | - | - | - | - | - | - |
| Hyundai Lifeboats Shanghai Co.,Ltd | 비상장 | 2022.02.10 | 경영참여 | 1,385 | - | - | - | 0 | 1,385 | - | 0 | 100.00 | 1,385 | 913 | 138 |
| ㈜노터스 | 상장 | 2022.03.30 | 경영참여 | 56,226 | - | - | - | 1,406 | 56,226 | - | 1,406 | 18.01 | 56,226 | 93,402 | 10,308 |
| 합 계 | - | - | 667,616 | 6,258 | -15,502 | -280 | - | - | 651,834 | 860,777 | -157,994 | ||||
| (*) 당사는 별도재무제표 상 종속기업 및 관계기업투자주식에 대해 원가법을 적용하고 있으며, 해당 투자주식의 회수가능액을 평가한 결과 장부금액에 미달하여 전액 손상차손을 인식하였습니다. |
【 대표이사 등의 확인 】
 |
|
확인서(증권신고서)_22.10.11 |
증 권 신 고 서
| ( 지 분 증 권 ) |
| [증권신고서 제출 및 정정 연혁] |
| 제출일자 | 문서명 | 비고 |
|---|---|---|
| 2022년 08월 16일 | 증권신고서(지분증권) | 최초제출 |
| 2022년 08월 17일 | [기재정정] 증권신고서(지분증권) | 자진정정(파란색) |
| 2022년 09월 07일 | [기재정정] 증권신고서(지분증권) | 정정제출 요구 및 일정변경에 따른 정정(녹색) |
| 2022년 09월 23일 | [기재정정] 증권신고서(지분증권) | 기재사항 정정 및 일정변경에 따른 자진정정 (빨간색) |
| 2022년 10월 11일 | [기재정정] 증권신고서(지분증권) | 자진정정(파란색) |
| 금융위원회 귀중 | 2022년 08월 16일 |
| 회 사 명 : |
에이치엘비(주) |
| 대 표 이 사 : |
진 양 곤, 김 동 건 |
| 본 점 소 재 지 : | 울산광역시 울주군 온산읍 당월로 216-53 |
| (전 화) 02-3453-4414 | |
| (홈페이지) http://www.hlbkorea.com | |
| 작 성 책 임 자 : | (직 책) 경영전략팀장 (성 명) 한 영 인 |
| (전 화) 02-3453-4414 | |
| 모집 또는 매출 증권의 종류 및 수 : | 기명식 보통주 9,562,408주 | |
| 모집 또는 매출총액 : | 325,599,992,400 | 원 |
| 증권신고서 및 투자설명서 열람장소 |
| 가. 증권신고서 |
| 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 나. 투자설명서 |
| 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 서면문서 : 에이치엘비㈜ → 울산광역시 울주군 온산읍 당월로 216-53 케이비증권㈜ → 서울특별시 영등포구 여의나루로 50 한국투자증권㈜ → 서울특별시 영등포구 의사당대로 88 유진투자증권㈜ → 서울특별시 영등포구 국제금융로 24 |
【 대표이사 등의 확인 】
 |
|
확인서(증권신고서)_22.08.16 |
요약정보
1. 핵심투자위험
| 하단의 핵심투자위험은 증권신고서 본문에 기재된 투자위험요소 중 중요한 항목만을 투자자의 이해도 제고를 위하여 간단ㆍ명료하게 요약한 것입니다. 자세한 투자위험요소는 "본문-제1부 모집 또는 매출에 관한 사항-Ⅲ. 투자위험요소"에 기재되어 있으니 참고하시기 바랍니다. |
| 구 분 | 내 용 |
| 사업위험 |
가. 조선경기 침체에 따른 위험 마. 바이오산업 성장성 관련 위험
카. 핵심인력 및 보유기술 유출에 따른 위험 당사는 지속적인 국내외 특허출원 및 등록을 통해 핵심기술에 대한 권리보호 전략을 실행하고 있으나, 이러한 인력들에 대하여 경쟁업체 및 잠재적 시장진입자 등으로부터의 스카우트 위험이 존재합니다. 핵심 연구인력의 유출은 당사가 축적해 온 기술 관련 노하우, 글로벌 임상시험의 개시 및 운영 노하우 등의 기술유출을 수반할 위험을 내포하고 있습니다. 따라서 당사 핵심 연구인력의 유출 및 보유 기술의 유출은 당사의 사업계획 및 파이프라인에 대한 연구개발계획의 진행에 차질을 발생시킬 수 있으며, 이로 인하여 당사의 성장성, 수익성의 부정적인 영향을 미칠 위험이 존재합니다. 타. 정부정책 및 규제에 관한 위험 제약산업은 인간의 생명 및 건강과 직결되는 의약품을 개발ㆍ제조ㆍ판매하는 산업으로, 제품의 개발ㆍ제조, 임상시험, 인ㆍ허가, 유통ㆍ판매에 이르기까지 전 과정에 걸쳐 각 국가의 규제 당국이 제시하는 엄격한 규정과 절차를 따라야 합니다. 당사는 내부에 담당 인력과 외부 전문가들을 통하여 국내 및 해외 제약 산업 정책 및 규제 환경을 지속적으로 모니터링하고 있으며, 각국의 규제 당국과의 소통을 통해 정책 및 규제 환경의 변화에 효과적으로 대비하기 위해 최선의 노력을 다하고 있습니다. 그러나 실제 효율적인 정책 지원이 이루어지지 않거나, 세부과제 추진에 어려움이 생길 수 있으며, 관련 법규의 제정 및 개정 단계, 예산 확보 등에 난항이 발생할 수 있습니다. 또한 해당 정책의 기대효과가 감소되는 경우 정책 기조의 변화로 정부 지원이 축소될 수 있으며, 조건부 허가와 같은 규제 완화에 대한 실효성이 크지 않을 경우, 규제 완화의 범위가 축소될 수 있습니다. 이러한 정부의 우호적인 정책 및 규제 완화의 변동 가능성은 당사의 사업에 부정적인 영향을 끼칠 수 있습니다.
|
| 회사위험 |
가. 관리종목 편입 가능성에 따른 위험 다. 성장성 및 수익성 관련 위험
아. 잦은 타법인 주식 양수도 관련 위험 당사의 금융수익 및 원가는 주로 당사가 보유하고 있는 관계회사들의 채권 평가 및 처분에 의한 금융자산손익에 의한 것으로 매분기 평가 및 처분 결과에 따라 손익이 결정되며, 당사의 금융수익 및 금융원가는 보유 금융자산의 평가손익에 따라 변동성이 있습니다. 따라서 당사가 안정적인 매출액을 바탕으로 영업이익을지속적으로 시현 하지 못하는 한, 당사의 수익성이 악화 될 위험이 있습니다. 또한, 당사는 사업다각화와 재무구조안정 등의 목적을 위해 과거부터 지속적을 타법인 출자를 진행하고 있으며, 추가적인 타법인 출자 및 자산양수도를 위한 전환사채 및 신주인수권부사채 발행 등의 차입이 발생할 경우, 당사의 재무안정성에 부정적인 영향을 미칠 수 있습니다. 투자자 여러분들께서는 이 점을 반드시 유의하시기 바랍니다. 또한, 신규사업 추진 및 금융수익 창출을 위한 막대한 자금의 소요에도 불구하고, 신규사업 진행에 차질이 생기거나 투자한 금융자산에 평가 및 처분 손실이 발생할 수 있습니다. 이 경우, 당사의 수익성이나 재무안정성이 악화될 수 있으며, 투자자께서는 이 점 유의하시기 바랍니다. 자. 신규 Pipeline 확보를 위한 타법인 지분 인수 관련 위험 당사의 이사회는 2021년 3월 29일 이사회 결의를 통해 미국 소재 법인인Verismo Therapeutics, Inc.(이하 Verismo)의 지분 취득을 결정하였으며, 2021년 04월 12일 미화 5백만 달러(한화 5,659백만원)을 지불하고 제3자배정 유상증자에 참여하여 Immunomic의 지분율 10.00%를 취득했습니다. Verismo Therapeutics, Inc.는 KIR-CAR 플랫폼 기술을 활용하여 중피종, 난소암 등을 대상으로 비임상을 진행하고 있는 바이오의약품 연구개발기업입니다. Verismo는 중피종, 난소암, 췌장암을 대상으로 SynKIR-110의 미국 임상 1상 시험을 위한 비임상시험을 마치고 2022년 9월 임상시험계획승인신청(Investigational New Drug Application, IND)을 승인을 득한 후 환자 모집을 위한 작업을 진행하고 있습니다. 그 외 후속 파이프라인으로는 SynKIR-210(유방암, 비소세포폐암, 대장암), SynKIR-310(DLBCL) 그리고 SynKIR-410(교모세포종)이 있습니다. 신약 개발 사업은 개발에 오랜 시간이 소요되며 수많은 변수가 상존하여 임상 진행 허가 및 신약 허가를 취득하여 개발에 최종 성공할 확률이 극히 낮으며, 개발에 성공한다고 해도 그 상업적 성공 여부는 보장되지 않습니다. 투자자께서는 본 증권신고서 제1부 "III. 투자위험요소 - 1. 사업위험 - 다."의 내용을 참고하시어 신약 개발 사업의 특성을 정확히 인지하시고 투자 판단에 임하시기 바랍니다. 차. Rivoceranib 신약 개발 사업에 관한 전반적인 사항 |
| 기타 투자위험 | 가. 최대주주 및 특수관계인의 청약 참여 관련 사항 금번 유상증자에 에이치엘비생명과학㈜와 에이치엘비셀㈜는 배정물량에 전량 참여할 예정이며, 최대주주인 진양곤 회장과 이현아, 이현수, 진유림, 진인혜는 배정받은 증서를 매각한 분만큼 청약에 참여할 예정이며, 기타특수관계인의 참여여부는 미확정인 상태입니다. 다만, 상기 최대주주의 유상증자 청약 참여 여부 및 규모는 최종 발행가액 및 소요자금, 개인의 자금 사정 등으로 인하여 변경될 가능성이 있습니다. 최대주주의 실제 청약 참여 규모에 따라 유상증자 이후 최대주주의 지분율은 하락할 수 있고, 최대주주 및 특수관계인이 전량 청약에 참여하지 않을 경우를 가정하면 최대주주 및 특수관계인의 지분율 합계는 9.60%까지 하락할 수 있습니다. 당사가 발행한 미상환 상태로 남아있는 전환사채가 주식으로 전환 될 경우 최대주주 및 특수관계인의 지분율이 추가로 하락할 가능성이 있습니다. 상기 전환사채의 전환권 행사로 발행될 수 있는 신주의 총수는 3,134,457주로 2022년 09월 23일 현재 당사의 보통주 발행주식 총수의 2.9%에 해당합니다. 최대주주 및 특수관계인의 전량 미청약을 가정할 시, 본 유상증자 이후 상기 전환사채가 전량 주식으로 전환될 경우 최대주주 진양곤의 지분율은 기존 8.05%에서 7.20%까지, 최대주주 및 특수관계인의 지분율 합계는 기존 10.46%에서 9.35%까지 변동될 수 있습니다. 향후 주식시장 및 시장상황에 따라 전환사채의 주식 전환으로 인한 최대주주 및 특수관계인의 지분변화 가능성을 배제하기는 어렵습니다. 투자자께서는 이 점에 유의하여 투자판단을 하시기 바랍니다. 나. 환금 제한 및 원금 손실 가능성 금번 유상증자 청약에 참여하여 신주를 배정받을 경우 신주의 추가상장일까지 환금성에 제약이 있으며, 청약 후 추가상장일 사이에 주가가 하락할 경우 원금에 대한 손해가 발생할 가능성이 있습니다. 투자자분들은 투자시 이점 유의하시기 바랍니다. 다. 주가 희석화 위험 당사의 금번 유상증자로 인하여 기발행주식 총수 106,910,669주의 8.94%에 해당하는 9,562,408주가 추가로 상장됩니다. 금번 증자로 인해 추가 발행되는 신주는 보호예수되지 않으므로 일시적인 물량출회에 따른 주가하락의 가능성이 있습니다. 금번 유상증자에 따른 모집예정주식 9,562,408주가 향후 코스닥 시장에 추가 상장될 경우 유통주식수의 증가로 인하여 주가 희석화 위험이 발생할 수 있습니다. 신주인수권증서를 매수하는 투자자는 할인율에 의해 발생하는 차익을 단기적으로 실현하기 위해 신주의 매매가 가능한 시점에서 즉시 장내에서 매각할 가능성이 높습니다. 이에 따라 주가가 하락할 수 있으니 투자자분들은 유의하시기 바랍니다. 라. 주가하락에 따른 발행금액 감소 위험 주식시장의 급격한 상황 악화로 인하여 회사의 금번 유상증자 발행가액이 하락할 경우 당사가 계획했던 자금운용계획 등에 차질이 빚어질 수 있으며, 이러할 경우 당사의 재무적 안정성은 부정적인 영향을 받을 수 있습니다. 마. 금융감독기관의 규제 강화에 따른 위험 최근 금융감독기관 등의 관리감독기준이 엄격해지고 있는 상황으로 관련 규정을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다. 향후 감독기관으로부터 당사가 현재 파악하지 못한 제재가 부과될 경우 주가하락 및유동성(환금성) 제약 등으로 인해 투자금에 막대한 손실이 발생할 수 있으니 투자자들께서는 관련 규정을 충분히 검토하신 후 투자에 임해주시기 바랍니다. 바. 경영환경변화 등에 따른 위험 대내외적 경영환경 변화에 따라 당사 실적의 급변동이 있을 경우 투자원금에 대한 손실이 발생할 수 있으므로, 상기 투자위험요소 및 본 증권신고서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 투자자 여러분이 독자적으로 결정해야 함을 유의하시기 바랍니다. 사. 증권신고서 정정에 따른 일정 변경 가능성 본 증권신고서는 공시심사 과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있습니다. 아. 집단 소송이 제기될 위험 당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있음을 유의하시기 바랍니다. 자. 유상증자에 따른 주식가치 하락 및 기재정보 의존에 따른 투자위험 금번 유상증자를 통해 취득한 당사의 주식가치가 하락할 수 있으며, 상기 투자위험요소 및 기타 기재된 정보에만 의존하여, 투자판단을 해서는 안되며 투자자 여러분의 독자적인 판단에 의해야 함을 유의하여 주시기 바랍니다. 차. 유상증자 철회에 따른 위험 유상증자 진행 중에 모집 절차의 진행에 중대한 영향을 미칠만한 사유가 발생하여 당사 혹은 공동대표주관회사 및 인수회사의 판단으로 유상증자가 철회될 수 있습니다. 유상증자 납입전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회시점에 따라 권리락에 따른 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있음을 투자자께서는 유의하시기 바랍니다. 또한, 당사가 계획한 자금사용목적의 자금이 조달되지 않기 때문에 당사는 단기간 유동성 위험에 직면하여 매우 위험한 상황이 발생할 수 있으니 이점 유의하시기 바랍니다. 카. 차입공매도 유상증자 참여 제한 관련 위험 「자본시장과 금융투자업에 관한 법률 시행령」일부 개정령에 따라, 주권상장법인이 유상증자 계획을 공시한 이후 발행가격 산정을 위한 대상 거래기간의 마지막 날(발행가격 산정 기산일)까지, 해당 기업의 주식을 공매도 한 자는 증자 참여를 제한하되, 예외적인 경우에만 증자 참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 투자자께서는 이 점 유의하시기 바랍니다. 타. 최대주주 보유주식의 담보권 설정 관련 위험 2022년 09월 22일 현재 당사의 최대주주인 진양곤 대표이사는 당사의 보통주 발행주식총수 106,910,669주의 약 8.05%에 해당하는 8,610,902주의 보통주를 보유하고 있으며,최대주주가 보유한 8,610,902주 중 약 3.83%에 해당하는 329,840주는 최대주주가 차입한 대출금에대하여 담보로 제공되어 있습니다. 동 물량은 당사 발행 보통주식총수의 약 0.31%에 해당합니다. 향후 최대주주가 체결한 주식담보대출약정에 의한 대출금을 기한 내 상환하지 못하거나, 통제할 수 없는 시장의 변수로 인하여 당사의 주가가 급락하게 될 경우, 담보로 제공된물량에 대하여 그 담보권이 실행되거나 반대매매 물량이 출회되어 주가의 추가적 하락을 야기할 가능성을 배제할 수 없습니다. 투자자께서는 당사의 주식 중 대출금에 대한 담보로 제공되어 있는 물량이 존재함에 유의하시고, 해당 위험성을 충분히 인지하신 후 투자판단에 임하시기 바랍니다. |
2. 모집 또는 매출에 관한 일반사항
| (단위 : 원, 주) |
| 증권의 종류 |
증권수량 | 액면가액 | 모집(매출) 가액 |
모집(매출) 총액 |
모집(매출) 방법 |
|---|---|---|---|---|---|
| 보통주 | 9,562,408 | 500 | 34,050 | 325,599,992,400 | 주주배정후 실권주 일반공모 |
| 인수(주선) 여부 | 지분증권 등 상장을 위한 공모여부 | ||
|---|---|---|---|
| 인수 | 아니오 | 해당없음 | 해당없음 |
| 인수(주선)인 | 증권의 종류 |
인수수량 | 인수금액 | 인수대가 | 인수방법 | |
|---|---|---|---|---|---|---|
| 대표 | 한국투자증권 | 보통주 | 4,781,204 | 162,799,996,200 | 인수수수료 : 모집총액의 1.1% 中 50% 실권수수료 : 잔액인수금액의 12.0% |
잔액인수 |
| 대표 | 케이비증권 | 보통주 | 3,824,964 | 130,240,024,200 | 인수수수료 : 모집총액의 1.1% 中 40% 실권수수료 : 잔액인수금액의 12.0% |
잔액인수 |
| 인수 | 유진증권 | 보통주 | 956,240 | 32,559,972,000 | 인수수수료 : 모집총액의 1.1% 中 10% 실권수수료 : 잔액인수금액의 12.0% |
잔액인수 |
| 청약기일 | 납입기일 | 청약공고일 | 배정공고일 | 배정기준일 |
|---|---|---|---|---|
| 2022년 12월 01일 ~ 2022년 12월 02일 | 2022년 12월 09일 | 2022년 12월 05일 | 2022년 12월 09일 | 2022년 10월 14일 |
| 청약이 금지되는 공매도 거래 기간 | |
|---|---|
| 시작일 | 종료일 |
| 2022년 08월 16일 | 2022년 11월 28일 |
| 자금의 사용목적 | |
|---|---|
| 구 분 | 금 액 |
| 타법인증권취득자금 | 282,700,000,000 |
| 시설투자자금 | 30,010,150,000 |
| 운영자금 | 8,210,000,000 |
| 채무상환자금 | 4,680,000,000 |
| 발행제비용 | 4,713,977,663 |
| 신주인수권에 관한 사항 | ||
|---|---|---|
| 행사대상증권 | 행사가격 | 행사기간 |
| - | - | - |
| 매출인에 관한 사항 | ||||
|---|---|---|---|---|
| 보유자 | 회사와의 관계 |
매출전 보유증권수 |
매출증권수 | 매출후 보유증권수 |
| - | - | - | - | - |
| 일반청약자 환매청구권 | ||||
|---|---|---|---|---|
| 부여사유 | 행사가능 투자자 | 부여수량 | 행사기간 | 행사가격 |
| - | - | - | - | - |
| 【주요사항보고서】 | [정정] 주요사항보고서(유상증자결정)-2022.09.23 |
| 【기 타】 | 1) 금번 에이치엘비㈜의 주주배정후 실권주 일반공모 유상증자의 공동대표주관회사는 케이비증권㈜ 및 한국투자증권㈜이며, 인수회사는 유진투자증권㈜입니다. 2) 금번 유상증자는 잔액인수방식에 의한 것입니다. 공동대표주관회사 및 인수회사는 주주배정후 실권주 일반공모 후 최종실권주를 잔액인수하게 되며, 인수방법 및 인수대가에 대한 자세한 내용은 '제1부 Ⅰ. 5. 인수 등에 관한 사항'을 참고하여 주시기 바랍니다. 3) 상기 모집가액 및 발행제비용은 예정 발행가액으로 산정된 것으로 향후 변경될 수 있습니다. 확정가액은 구구주 청약 초일 전 제3거래일(2022년 11월28일)에 확정되어 2022년 11월 29일에 회사 인터넷 홈페이지(http://www.hlbkorea.com)에 공고될 예정입니다. 4) 상기 청약기일은 구주주 청약 일정이며, 일반공모 청약은 2022년12월 06일과 2022년 12월 07일 2일간입니다. 일반공모 청약공고는 2022년 12월 05일에 회사 및 대표주관사의 인터넷 홈페이지에 공고할 예정입니다. 일반공모 청약은 공동대표주관사인 케이비증권㈜ 및 한국투자증권㈜ 본 ㆍ 지점 홈페이지 및 HTS에서 확인 가능합니다. 5) 「증권 인수업무 등에 관한 규정」 제9조 제2항에 의거 고위험고수익투자신탁, 벤처기업투자신탁 및 일반청약자에 대하여 배정하여야 할 주식이 50,000주(액면가 500원 기준) 이하 이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 청약자에게 배정하지 아니할 수 있습니다. 6) 금융감독원에서 본 증권신고서를 심사하는 과정에서 주요사항의변동으로 인한 기재 내용의 정정 등으로 동 신고서에 기재된 일정이변경될 수 있습니다. 7) 증권신고서의 효력의 발생은 본 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. 8) 상기 발행제비용은 당사 보유자금으로 지급할 예정입니다. |
제1부 모집 또는 매출에 관한 사항
I. 모집 또는 매출에 관한 일반사항
1. 공모개요
당사는 이사회 결의를 통하여 「자본시장과 금융투자업에 관한 법률」제165조의6 제2항 제1호에 의거 케이비증권㈜, 한국투자증권㈜, 유진투자증권㈜와 주주배정후 실권주를 인수하는 계약을 체결하고 사전에 그 실권주를 일반에 공모하기로 하여 기명식 보통주 9,562,408주를 주주배정후 실권주 일반공모 방식으로 발행하기로 결정하였으며, 동 증권의 개요는 다음과 같습니다.
| (단위 : 원, 주) |
| 증권의 종류 | 증권수량 | 액면가액 | 모집(매출)가액 | 모집(매출)총액 | 모집(매출) 방법 |
|---|---|---|---|---|---|
| 기명식보통주 | 9,562,408 | 500 | 34,050 | 325,599,992,400 | 주주배정후실권주일반공모 |
| 주1) 최초 이사회 결의일 : 2022년 08월 12일 주2) 1주의 모집가액 및 모집총액은 예정 발행가액 기준으로 한 예정금액이며, 확정되지 않은 금액입니다. |
발행가액은 「증권의 발행 및 공시 등에 관한 규정」 제5-18조 (유상증자의 발행가액 결정)에 의거, 주주배정증자시 할인율 등이 자율화 되어 자유롭게 산정할 수 있으나, 시장혼란 우려 및 기존 관행 등으로 「(구) 유가증권의 발행 및 공시 등에 관한 규정」 제57조를 일부 준용하여 산정할 예정입니다.
■ 모집예정가액의 산출근거
최초 이사회결의일 직전 거래일(2022년 08월 11일)을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와 1주일가중산술평균주가 및 기산일 가중산술평균주가를 산술평균하여 산정한 가액과 기산일 가중산술평균주가 중 낮은 금액을 기준주가로 하여, 아래의 산식에 따라 결정하며할인율은 25%를 적용합니다.(단, 호가단위 미만은 호가단위로 절상하며, 그 가액이 액면가액 미만인 경우 액면가액으로 합니다.)
| 기준주가 X 【 1 - 할인율(25%) 】 | ||
| ▶ 모집예정가액 | = | ---------------------------------------- |
| 1 + 【유상증자비율 X 할인율(25%)】 |
상기 방법에 따라 산정된 예정발행가액은 참고용이며, 구주주 청약일전 3거래일에 확정발행가액을 결정될 예정입니다.
| [모집예정가액 산정표] 기산일 : 2022년 08월 11일 |
(단위 : 원, 주) |
| 일자 | 종 가 | 거래량 | 거래대금 |
|---|---|---|---|
| 2022-08-11(목) | 46,750 | 1,293,092 | 60,616,208,200 |
| 2022-08-10(수) | 46,700 | 1,590,343 | 76,840,463,450 |
| 2022-08-09(화) | 49,800 | 1,905,457 | 94,262,324,750 |
| 2022-08-08(월) | 47,450 | 900,823 | 42,411,864,250 |
| 2022-08-07(일) | - | - | - |
| 2022-08-06(토) | - | - | - |
| 2022-08-05(금) | 47,600 | 1,223,057 | 58,012,464,550 |
| 2022-08-04(목) | 46,600 | 2,915,981 | 136,320,841,050 |
| 2022-08-03(수) | 44,150 | 1,185,083 | 51,571,565,800 |
| 2022-08-02(화) | 42,800 | 610,014 | 25,550,766,100 |
| 2022-08-01(월) | 41,450 | 434,615 | 18,132,953,950 |
| 2022-07-31(일) | - | - | - |
| 2022-07-30(토) | - | - | - |
| 2022-07-29(금) | 41,950 | 789,614 | 33,162,477,600 |
| 2022-07-28(목) | 40,650 | 442,735 | 18,167,033,400 |
| 2022-07-27(수) | 40,950 | 332,267 | 13,515,827,550 |
| 2022-07-26(화) | 40,500 | 313,658 | 12,765,337,900 |
| 2022-07-25(월) | 40,450 | 390,541 | 15,730,378,650 |
| 2022-07-24(일) | - | - | - |
| 2022-07-23(토) | - | - | - |
| 2022-07-22(금) | 40,700 | 442,691 | 18,258,058,100 |
| 2022-07-21(목) | 41,100 | 766,670 | 31,482,281,050 |
| 2022-07-20(수) | 42,150 | 1,499,868 | 63,127,016,050 |
| 2022-07-19(화) | 40,550 | 521,853 | 21,059,174,550 |
| 2022-07-18(월) | 40,600 | 1,935,231 | 78,064,478,350 |
| 2022-07-17(일) | - | - | - |
| 2022-07-16(토) | - | - | - |
| 2022-07-15(금) | 42,800 | 924,871 | 39,126,105,000 |
| 2022-07-14(목) | 42,550 | 1,762,471 | 76,130,747,250 |
| 2022-07-13(수) | 44,200 | 1,857,412 | 80,772,197,850 |
| 2022-07-12(화) | 41,850 | 1,309,259 | 53,763,719,700 |
| 1개월 가중산술평균주가 (A) | 44,140.04원 | - | |
| 1주일 가중산술평균주가 (B) | 48,047.78원 | - | |
| 기산일 가중산술평균주가 (C) | 46,876.95원 | - | |
| A,B,C의 산술평균 (D) | 46,354.92원 | (A+B+C)/3 | |
| 기준주가 (E) | 46,354.92원 | (C와 D중 낮은가액) | |
| 할인율 (F) | 25% | - | |
| 증자비율 (G) | 8.94% | - | |
| 예정발행가액 | 34,050원 | 기준주가 × (1-할인율) / 1 + (유상증자비율 × 할인율 ) |
|
■ 공모일정 등에 관한 사항
당사는 2022년 08월 12일 최초 이사회. 2022년 09월 07일 이사회 및 2022년 09월 23일 이사회를 통해 유상증자를 결의하였으며, 세부 일정은 다음과 같습니다.
| [주요일정] |
| 날짜 | 업 무 내 용 | 비고 |
|---|---|---|
| 2022년 08월 12일 | 이사회결의 | - |
| 2022년 08월 12일 |
신주발행 및 기준일 공고 | 당사 인터넷 홈페이지 (http://www.hlbkorea.com) |
| 2022년 08월 16일 |
증권신고서 제출 | - |
| 2022년 08월 17일 | [기재정정]증권신고서 제출 | |
| 2022년 09월 07일 | [기재정정]증권신고서 제출 | |
| 2022년 09월 23일 | [기재정정]증권신고서 제출 | |
| 2022년 10월 11일 |
1차 발행가액 확정 | 신주배정기준일 3거래일 전 |
| 2022년 10월 13일 |
권리락 | - |
| 2022년 10월 14일 |
신주배정 기준일(주주확정) | - |
| 2022년 10월 25일 |
신주배정 통지 | - |
| 2022년 11월 16일 ~ 2022년 11월 22일 |
신주인수권증서 상장 거래기간 | 5거래일 이상 거래 |
| 2022년 11월 23일 |
신주인수권증서 상장 폐지 | 구주주 청약초일 5거래일 전 폐지 |
| 2022년 11월 28일 |
확정 발행가액 산정 | 구주주 청약초일 3거래일 전 |
| 2022년 11월 29일 |
확정 발행가액 공고 | 당사 인터넷 홈페이지 (http://www.hlbkorea.com) 및 Dart전자공시시스템(http://dart.fss.or.kr) |
| 2022년 12월 01일 ~ 2022년 12월 02일 |
구주주 청약 및 초과청약 | - |
| 2022년 12월 05일 |
일반공모 청약 공고 | 당사 인터넷 홈페이지 (http://www.hlbkorea.com) 케이비증권㈜ 홈페이지 (www.kbsec.com) 한국투자증권㈜ 홈페이지 (www.truefriend.com) 유진투자증권㈜ 홈페이지 (www.eugenefn.com) |
| 2022년 12월 06일 ~ 2022년 12월 07일 |
일반공모 청약 | - |
| 2022년 12월 09일 |
환불 및 배정 공고 | 케이비증권㈜ 홈페이지 (www.kbsec.com) 한국투자증권㈜ 홈페이지 (www.truefriend.com) 유진투자증권㈜ 홈페이지 (www.eugenefn.com) |
| 2022년 12월 09일 |
주금 납입 | - |
| 2022년 12월 23일 |
신주유통 개시일 | - |
| 2022년 12월 23일 |
신주상장 예정일 | - |
| 주1) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. 주2) 2019년 9월 16일부터 전자증권제도가 시행됨에 따라 금번 유상증자 시 발행되는 신주인수권증서 및 신주가 전자증권으로 발행될 예정이며, 신주상장과 동시에 신주가 유통될 예정입니다. 주3) 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
2. 공모방법
[공모방법 : 주주배정후 실권주 일반공모]
| 모집대상 | 주식수 | 비 고 |
|---|---|---|
| 구주주 (신주인수권증서 보유자) 청약 |
9,562,408주 (100.0%) | - 구주 1주당 신주 배정비율 : 1주당 0.0895552192주 - 신주배정 기준일 : 2022년 10월 14일 - 보유한 신주인수권증서의 수량 한도로 청약가능(구주주에게는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율을 곱한 수량만큼의 신주인수권 증서가 배정됨) |
| 초과 청약 | - | - 「자본시장과 금융투자업에 관한 법률」 제165조의6의 제2항 제2호에 의거 초과청약 - 초과청약비율 : 배정신주(신주인수권증서) 1주당 0.2주 - 신주인수권증서 거래를 통해서 신주인수권증서를 매매시 보유자 기준으로 초과청약 가능 |
| 일반모집 청약 (고위험고수익투자신탁, 벤처기업투자신탁 청약 포함) |
- | - 구주주 및 초과청약 후 발생하는 단수주 및 실권주에 대해 배정됨 |
| 합 계 | 9,562,408주 (100.00%) | - |
| 주1) | 본 건 유상증자는 주주배정후 실권주 일반공모 방식으로 진행되며, 구주주 청약결과 발생하는 실권주 및 단수주는 우선적으로 초과청약자에게 배정되며, 이후 실권이 발생할 경우에 대해서는 일반에게 공모합니다. |
| 주2) | 구주주의 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율인 0.0895552192주를 곱하여 산정된 배정주식수로 하되, 1주 미만은 절사합니다. 단, 신주배정기준일 전 주식관련사채의 권리행사, 자기주식수의 변동으로 인하여 1주당 배정주식수가 변동될 수 있습니다. |
| 주3) |
신주인수권증서 보유자는 보유한 신주인수권증서 수량의 한도로 증서청약을 할 수 있고, 동 주식수에 초과청약비율(20%)를 곱한 수량을 한도로 초과청약 할 수 있습니다. 단, 1주 미만은 절사합니다. (ii) 신주인수권증서청약 한도주식수 = 보유한 신주인수권 증서의 수량 (iii) 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 X 초과청약 비율(20%) |
| 주4) | "고위험고수익투자신탁" 이란 「조세특례제한법」제91조의15제1항에 따른 투자신탁 등을 말합니다. 다만, 해당 투자신탁 등의 최초 설정일·설립일로부터 수요예측 참여일까지의 기간이 6개월 미만인 경우에는 같은 법 시행령 제93조제3항제1호 및 같은 조 제7항에도 불구하고 수요예측 참여일 직전 영업일의 비우량채권과 코넥스 상장주식을 합한 보유비율이 100분의 45 이상이고 이를 포함한 국내 채권의 보유비율이 100분의 60 이상이어야 합니다. |
| 주5) | "벤처기업투자신탁"이란 「조세특례제한법」 제16조제1항제2호의 벤처기업투자신탁(대통령령 제28636호 「조세특례제한법 시행령 일부개정령」 시행 이후 설정된 벤처기업투자신탁에 한한다. 이하 같다)을 말합니다. 다만 해당 벤처기업투자신탁의 최초 설정일로부터 수요예측 참여일까지의 기간이 1년 미만인 경우에는 같은 법 시행령 제14조제1항제3호에도 불구하고 수요예측 참여일 직전영업일의 벤처기업투자신탁 재산총액에서 같은 호 각 목에 따른 비율의 합계가 100분의 35이상이어야 합니다. |
| 주6) | 본 건 유상증자는 주권상장법인의 유상증자에 해당되므로, 「증권 인수업무 등에 관한 규정」 제9조제2항제3호에 의거하여, 고위험고수익투자신탁 총 배정분은 전체 일반공모주식수의 5% 이상을 배정하고, 「증권 인수업무 등에 관한 규정」 제9조제2항제4호에 의거하여, 벤처기업투자신탁 총 배정분은 전체 일반공모주식수의 30% 이상을 배정하기로 합니다. 이외 일반청약자 총 배정분은 전체 일반공모주식수의 65%를 배정합니다. ① 1단계: 총 청약물량이 일반공모 배정분 주식수를 초과하는 경우, 각 청약자에 5사6입을 원칙으로 안분 배정하여 잔여주식이 최소화되도록 합니다. 다만, 고위험고수익투자신탁에 대한 공모주식 5%와 벤처기업투자신탁에 대한 공모주식 30%, 개인투자자 및 기관투자자(집합투자업자포함)에 대한 공모주식 65%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정합니다. 다만, 어느 한 그룹에서 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다. ② 2단계: 1단계 배정 후 최종 잔여주식은 최대청약자부터 순차적으로 1주씩 우선배정하되, 동순위 최대청약자가 최종 잔여주식보다 많은 경우에는 대표주관회사가 합리적으로 판단하여 배정합니다. |
| 주7) | 일반공모를 거쳐 배정 후에도 미 청약된 잔여주식에 대하여는 대표주관회사가 자기계산으로 잔액인수하기로 합니다. |
| 주8) | 단, 공동대표주관회사는 「증권 인수업무 등에 관한 규정」 제9조제2항에 의거 고위험고수익투자신탁, 벤처기업투자신탁 및 일반청약자에 대하여 배정하여야 할 주식이 50,000주 이하(액면가 500원 기준)이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 일반 고위험고수익투자신탁, 벤처기업투자신탁 및 일반청약자에게 배정하지 아니하고 공동대표주관회사가 자기계산으로 인수할 수 있습니다. |
| 주9) |
자본시장법 제180조의4 및 같은 법 시행령 제208조의4제1항에 따라 2022년 08월 16일부터 2022년 11월 28일까지 공매도를 하거나 공매도 주문을 위탁한 자는 금번 모집(매출)에 청약할 수 없으며, 이를 위반하여 주식을 취득할 경우 같은 법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만 모집(매출)가액의 공정한 가격형성을 저해하지 않는 경우로서 같은 법 시행령 제208조의4제2항 및 금융투자업규정 제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다. ※ 예외적으로 모집(매출)에 따른 주식 취득이 허용되는 경우 ① 모집(매출)에 따른 주식 취득이 금지되는 공매도 거래 기간 중에 전체 공매도 주문수량보다 많은 수량의 주식을 가격경쟁에 의한 거래 방식으로 매수한 경우 (매매계약 체결일 기준으로 정규시장의 매매거래시간에 매수한 경우로 한정) ② 한국거래소의 증권시장업무규정 또는 파생상품시장업무규정에서 정한 유동성 공급 및 시장조성 목적을 위해 해당 주식을 공매도하거나 공매도 주문을 위탁한 경우 ③ 동일한 법인 내에서 모집(매출)에 따른 주식 취득 참여가 금지되는 공매도 거래 기간 중 공매도를 하지 않거나 공매도 주문을 위탁하지 않은 독립거래단위*가 모집(매출)에 따른 주식을 취득하는 경우 * 금융투자업규정 제6-30조 제5항에 따라 의사결정이 독립적이고 상이한 증권계좌를 사용하는 등의 요건을 갖춘 거래단위 |
※ 참고 : 구주주 1주당 배정비율 산출 근거
| A. 보통주식 | 106,903,481 |
| B. 우선주식 | 7,188 |
| C. 발행주식총수(A+B) | 106,910,669 |
| D. 자기주식 + 자기주식신탁 | 134,000 |
| E. 자기주식을 제외한 발행주식총수 (C-D) | 106,776,669 |
| F. 유상증자 주식수 | 9,562,408 |
| G. 증자비율 (F/C) | 8.94% |
| H. 우리사주조합 배정 | - |
| H. 구주주배정 (F-H) | 9,562,408 |
| I. 구주주 1주당 배정비율 (F/E) | 0.0895552192 |
3. 공모가격 결정방법
「증권의 발행 및 공시 등에 관한 규정」 제5-18조에 의거 주주배정 증자시 가격산정 절차 폐지 및 가격산정의 자율화에 따라 발행가격을 자유롭게 산정할 수 있으나, 시장 혼란 우려 및 기존 관행 등으로 (구)「유가증권의 발행 및 공시 등에 관한 규정」 제57조를 일부 준용하여 아래와 같이 발행가액을 산정합니다.
가. 1차 발행가액: 신주배정기준일 전 제3거래일을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와 1주일 가중산술평균주가 및 기산일 가중산술평균주가를 산술평균하여 산정한 가액과 기산일 가중산술평균주가 중 낮은 금액을 기준주가로 하여, 아래의 산식에 따라 결정하며 할인율은 25%를 적용합니다. 단, 호가단위 미만은 호가단위로 절상하며, 그 가액이 액면가액 미만인 경우 액면가액으로 합니다.
▶ 1차 발행가액 = 기준주가 × (1-할인율) / [1 + (증자비율 × 할인율)]
나. 2차 발행가액: 구주주 청약 초일 전 제3거래일을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1주일 가중산술평균주가 및 기산일 가중산술평균주가를 산술평균하여 산정한 가액과 기산일 가중산술평균주가 중 낮은 금액을 기준주가로 하여, 아래의 산식에 따라 결정하며 할인율은 25%를 적용합니다. 단, 호가단위 미만은 호가단위로 절상하며, 그 가액이 액면가액 미만인 경우 액면가액으로 합니다.
▶ 2차 발행가액 = 기준주가 × (1-할인율)
다. 확정 발행가액: 1차 발행가액과 2차 발행가액 중 낮은 가액을 확정 발행가액으로 합니다. 다만, 「자본시장과 금융투자업에 관한 법률」 제165조의6 주식의 발행 및 배정 등에 관한 특례 및 「증권의 발행 및 공시 등에 관한 규정」 제5-15조의2규정「실권주 철회의 예외 등」 에 의거하여 1차 발행가액과 2차 발행가액 중 낮은 가액이 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 할인율 40%를 적용하여 산정한 가격보다 낮은 경우 청약일전 과거 제3거래일로부터 제5거래일까지의 가중산술평균주가에서 할인율 40%를 적용하여 산정한 가격을 확정발행가액으로 합니다. 단, 호가단위 미만은 호가단위로 절상하며, 그 가액이 액면가액 미만인 경우 액면가액으로 합니다.
▶ 확정 발행가액 = MAX【MIN(1차 발행가액, 2차 발행가액), 기준주가의 60%】
*일반공모 발행가액은 구주주 청약시에 적용된 확정발행 가액을 동일하게 적용합니다.
라. 최종 발행가액은 구주주 청약일 초일 전 제3거래일에 결정되어 금융감독원 전자공시시스템에 2022년 11월 29일(화)에 공시될 예정이며, 회사의 인터넷 홈페이지(http://www.hlbkorea.com)에 공고하여 개별통지에 갈음할 예정입니다.
4. 모집 또는 매출절차 등에 관한 사항
가. 모집 또는 매출조건
| (단위 : 주, 원) |
| 항 목 | 내 용 | ||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 모집 또는 매출주식의 수 | 9,562,408 | ||||||||||||||||||||||||||||||||||||||
| 주당 모집가액 | 예정가액 | 34,050 | |||||||||||||||||||||||||||||||||||||
| 확정가액 | - | ||||||||||||||||||||||||||||||||||||||
| 모집총액 | 예정가액 | 325,599,992,400 | |||||||||||||||||||||||||||||||||||||
| 확정가액 | - | ||||||||||||||||||||||||||||||||||||||
| 청 약 단 위 |
(1) "구주주"(신주인수권 증서 보유자)의 청약단위는 1주로 하며, 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식수에 신주배정비율("주주 배정분"에 해당하는 주식수를 자기주식을 제외한 발행주식 총수로 나눈 비율을 말하며, 자기주식과 발행주식총수는 신주배정기준일 현재의 주식수를 말한다)을 곱하여 산정된 배정주식수로 합니다. 다만, 신주배정기준일 현재 신주배정율은 주식관련사채의 행사, 자기주식수의 변동 등으로 인하여 변경될 수 있습니다(단, 1주 미만은 절사한다).
|
||||||||||||||||||||||||||||||||||||||
| 청약기일 | 구주주 (신주인수권 증서 보유자) |
개시일 | 2022년 12월 01일 |
||||||||||||||||||||||||||||||||||||
| 종료일 | 2022년 12월 02일 |
||||||||||||||||||||||||||||||||||||||
| 실권주 일반공모 | 개시일 | 2022년 12월 06일 |
|||||||||||||||||||||||||||||||||||||
| 종료일 | 2022년 12월 07일 |
||||||||||||||||||||||||||||||||||||||
| 청약 증거금 |
구주주 (신주인수권 증서 보유자) |
청약금액의 100% | |||||||||||||||||||||||||||||||||||||
| 초 과 청 약 | 청약금액의 100% | ||||||||||||||||||||||||||||||||||||||
| 일반모집 또는 매출 | 청약금액의 100% | ||||||||||||||||||||||||||||||||||||||
| 납 입 기 일 | 2022년 12월 09일 |
||||||||||||||||||||||||||||||||||||||
| 배당기산일(결산일) | 2022년 01월 01일 | ||||||||||||||||||||||||||||||||||||||
| 주1) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. 주2) 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
나. 모집 또는 매출의 절차
1) 공고의 일자 및 방법
| 구 분 | 공고일자 | 공고방법 |
|---|---|---|
| 신주 발행 및 배정기준일(주주확정일) 공고 |
2022년 08월 16일 | 당사 인터넷 홈페이지 (http://www.hlbkorea.com) |
| 모집가액 확정의 공고 | 2022년 11월 29일 |
전자공시시스템(http://dart.fss.or.kr) 당사 인터넷 홈페이지 (http://www.hlbkorea.com) |
| 실권주 일반공모 청약공고 | 2022년 12월 05일 |
당사 인터넷 홈페이지 (http://www.hlbkorea.com) 케이비증권㈜ 홈페이지 (www.kbsec.com) 한국투자증권㈜ 홈페이지 (www.truefriend.com) 유진투자증권㈜ 홈페이지 (www.eugenefn.com) |
| 실권주 일반공모 배정공고 | 2022년 12월 09일 |
케이비증권㈜ 홈페이지 (www.kbsec.com) 한국투자증권㈜ 홈페이지 (www.truefriend.com) 유진투자증권㈜ 홈페이지 (www.eugenefn.com) |
주) 청약결과 초과청약금 환불에 대한 통지는 공동대표주관회사 홈페이지에 게시함으로써 개별통지에 갈음합니다.
2) 청약방법
가) 구주주 청약(신주인수권 보유자 청약): 구주주 중 주권을 증권회사에 예탁한 주주(기존 "실질주주")는 주권을 예탁한 증권회사의 본/지점, 공동대표주관회사의 본/지점에서 청약할 수 있습니다. 다만, "구주주" 중 명의개서대리인의 특별계좌에 주식을 가지고 있는 주주(기존 "명부주주")는 신주배정통지서를 첨부하여 실명확인증표를 제시한 후 "공동대표주관회사"의 본·지점에서 청약할 수 있습니다. 청약시에는 소정의청약서 2통에 필요한 사항을 기입하여 청약증거금과 함께 제출하여야 합니다..
| 2019년 9월 16일 전자증권제도가 시행되며, 주권 상장법인의 상장주식은 전자증권 의무전환대상으로 전자증권제도 시행일에 전자증권으로 일괄전환됩니다. 전자증권제도 시행전까지 증권회사에 예탁하고 있는 실질주주 주식은 해당 증권회사 계좌에 전자증권으로 일괄 전환되며, 기존 명부주주가 보유한 주식은 명의개서대행기관이 개설하는 특별계좌에 발행되어 소유자별로 관리됩니다. 금번 유상증자시 신주인수권증서는 전자증권제도 시행일 이후에 발행되고 상장될 예정으로 전자증권으로 발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다. '특별계좌 보유자(기존 '명부주주')'는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후 금번 유상증자 청약 참여또는 신주인수권증서의 매매가 가능합니다. '특별계좌 보유자(기존 '명부주주')'는 신주인수권증서의 '일반 전자등록계좌(증권회사 계좌)'로 이전 없이 공동대표주관회사인 케이비증권㈜ 및 한국투자증권㈜의 본ㆍ지점에서 직접 청약하는 방법으로도 금번 유상증자에 청약이 가능합니다. 다만 신주인수권증서의 매매는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후에만 가능하므로 이 점 유의하시기 바랍니다. |
|
「주식ㆍ사채 등의 전자등록에 관한 법률」 |
나) 신주인수권증서 청약을 한 자에 한하여 신주인수권증서 청약 한도 주식수의 20%를 추가로 청약할 수 있습니다. 이때, 신주인수권증서 청약 한도주식수의 20%에 해당하는 주식 중 소수점 이하인 주식은 청약할 수 없습니다.
다) 고위험고수익투자신탁, 벤처기업투자신탁 및 일반청약자는 “금융실명거래 및 비밀보장에 관한 법률”의 규정에 의한 실명자이어야 하며, 청약사무 취급처에 실명확인증표, 소정의 청약서, 청약증거금을 제시하고 청약한다. 각 청약처별 다중청약 가능하나, 한개의 청약처에서 이중청약은 불가능하며, 집합투자기구 중 운용주체가 다른 집합투자기구를 제외한 청약자의 한 개의 청약처에 대한 복수청약은 불가능하다. 고위험고수익투자신탁은 청약 시, 청약사무 취급처에 “증권 인수업무 등에 관 규정” 제2조 제18호에 따른 요건을 충족함을 확약하는 서류 및 자산총액이 기재되어 있는 서류를 함께 제출한다. 벤처기업투자신탁은 청약 시, 청약 사무 취급처에 ‘증권인수업무 등에 관한 규정’ 제 2조 제20호에 따른 요건을 충족하고, 제9조 제10항에 따른 확약서 및 자산총액이 기재되어 있는 서류를 함께 제출하여야 합니다.
라) 일반청약자의 청약은 청약주식의 단위에 따라 될 수 있으며 1인당 청약한도를 초과하는 청약부분에 대하여는 청약이 없는 것으로 하고 청약사무 취급처는 그 차액을 납입일까지 당해 청약자에게 반환하며, 이때 받은 날부터의 이자는 지급하지 않습니다.
마) 본 유상증자에 청약하고자 하는 투자자(「자본시장과 금융투자업에 관한 법률」 제9조제5항에 규정된 전문투자자 및 「자본시장과 금융투자업에 관한 법률 시행령」 제 132조에 따라 투자설명서의 교부가 면제되는자 제외)는 청약 전 반드시 투자설명서를 교부 받아야 하고, 이를 확인하는 서류에 서명 또는 기명날인하여야 합니다.
바) 「자본시장과 금융투자업에 관한 법률」 제180조의4 및 동법 시행령 제208조의4제1항에 의거, 2022년 08월 16일부터 2022년 11월 28일까지 당사의 주식을 공매도 하거나 공매도 주문을 위탁한 자는 금번 모집(매출)에 청약할 수 없으며, 이를 위반하여 주식을 취득할 경우 동법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만, 모집(매출)가액의 공정한 가격형성을 저해하지 않는 경우로서 동법 시행령 제208조의4제2항 및 금융투자업규정 제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다.
사) 일반공모 배정을 함에 있어서 이중청약이 있는 경우에는 그 청약자의 청약 전부를 청약하지 아니한 것으로 봅니다. 단, 구주주가 신주배정비율에 따라 배정받은주식을 청약한 후 일반공모에 참여하는 경우에는 금지되는 이중청약이 있는 경우로 보지 않습니다.
|
※ 예외적으로 모집(매출)에 따른 주식 취득이 허용되는 경우 ① 모집(매출)에 따른 주식 취득이 금지되는 공매도 거래 기간 중에 전체 공매도 주문수량보다 많은 수량의 주식을 가격경쟁에 의한 거래 방식으로 매수한 경우(매매계약 체결일 기준으로 정규시장의 매매거래시간에 매수한 경우로 한정) ② 한국거래소의 증권시장업무규정 또는 파생상품시장업무규정에서 정한 유동성 공급 및 시장조성 목적을 위해 해당 주식을 공매도하거나 공매도 주문을 위탁한 경우 ③ 동일한 법인 내에서 모집(매출)에 따른 주식 취득 참여가 금지되는 공매도 거래 기간 중 공매도를 하지 않거나 공매도 주문을 위탁하지 않은 독립거래단위*가 모집(매출)에 따른 주식을 취득하는 경우 * 금융투자업규정 제6-30조 제5항에 따라 의사결정이 독립적이고 상이한 증권계좌를 사용하는 등의 요건을 갖춘 거래단위 |
3) 청약취급처
| 청약대상자 | 청약취급처 | 청약일 | |
|---|---|---|---|
| 구주주 (신주인수권증서 보유자) |
특별계좌 보유자 (기존 '명부주주') |
케이비증권㈜ 본ㆍ지점 및 한국투자증권㈜ 본ㆍ지점 | 2022년 12월 01일~ 2022년 12월 02일 |
| 일반주주 (기존 '실질주주') |
1) 주주확정일 현재 에이치엘비㈜의 주식을 예탁하고 있는 당해 증권회사 본ㆍ지점 2) 케이비증권㈜ 본ㆍ지점 및 한국투자증권㈜ 본ㆍ지점 |
||
| 일반공모청약 (고위험고수익투자신탁, 벤처기업투자신탁 청약 포함) |
케이비증권㈜ 본ㆍ지점, 한국투자증권㈜ 본ㆍ지점, 유진투자증권㈜ 본ㆍ지점 | 2022년 12월 06일~ 2022년 12월 07일 |
|
4) 청약결과 배정방법
가) 구주주 청약 (신주인수권증서 청약): 보유하고 있는 신주인수권증서 수량 범위 내에서 청약한 주식수에 따라 배정됩니다.(「자본시장과 금융투자업에 관한 법률」 제165의6조3항 및 「증권의 발행 및 공시 등에 관한 규정」 제5-19조에 의거하여 구주주에게 신주인수권증서를 발행합니다.)
나) 구주주 청약 : 신주배정기준일(2022년 10월 14일 예정) 18:00 현재 주주명부에 등재된 주주(이하 "구주주"라 한다)에게 본 주식을 1주당 0.0895552192주를 곱하여 산정된 배정주식수(단, 1주 미만은 절사함)로 하고, 배정범위 내에서 청약한 수량만큼 배정합니다. 단, 신주배정기준일 전 주식관련사채의 행사, 자기주식수의 변동 등으로 인하여 1주당 배정주식수가 변동될 수 있습니다.
다) 초과청약 : "구주주"(신주인수권증서 보유자) 청약 이후 발생한 실권주가 있는 경우, 실권주를 "구주주"(신주인수권증서 보유자)가 초과청약(초과청약비율: 배정 신주1주당0.2주)한 주식수에 비례하여 배정하며, 1주 미만의 주식은 절사하여 배정하지 않습니다. (단, 초과청약 주식수가 실권주에 미달한 경우100% 배정)
(ⅰ) 청약한도 주식수 = 신주인수권증서 청약한도 주식수 + 초과청약한도 주식수
(ⅱ) 신주인수권증서 청약한도 주식수 = 보유한 신주인수권증서의 수량
(ⅲ) 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 × 초과청약 비율(20%)
라) 일반공모 청약: "구주주" 청약(초과청약 포함) 결과 발생한 미청약주식 및 단수주는 "공동대표주관회사"와 "인수회사"가 일반에게 공모하되, 「증권 인수업무 등에 관한 규정」 제9조 제2항 제6호에 따라 "고위험고수익투자신탁"에 일반공모 배정분의 5%를 배정하고, "벤처기업투자신탁"에 일반공모 배정분의 30%를 배정합니다. 나머지 주식은 개인청약자 및 기관투자자에 구분없이 배정합니다. "고위험고수익투자신탁"에 대한 일반공모 배정분5%, "벤처기업투자신탁”에 대한 일반공모 배정분 30% 및 개인투자자 및 기관투자자에 대한 일반공모 배정분 65%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정합니다. 다만, 한 그룹만 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다.
(i) 일반공모에 관한 배정수량 계산시 "공동대표주관회사"와 "인수회사"의 "청약물량"("공동대표주관회사"와 "인수회사"의 각 청약처에서 일반공모 방식으로 접수를 받은 청약주식수를 의미하며, "공동대표주관회사"와 "인수회사"에 대하여 개별적으로 산정한 청약주식수를 말한다)에 대해서는 "공동대표주관회사"와 "인수회사"의 "총청약물량"("공동대표주관회사"와 "인수회사"가 일반공모 방식으로 접수를 받은 "청약물량"의합을 말한다)을 "일반공모 배정분" 주식수로 나눈 통합청약경쟁률에 따라 "공동대표주관회사"와 "인수회사"의 각 청약자에 배정하는 방식(이하 "통합배정"이라 한다)으로한다.
(ii) 일반공모 청약결과 일반공모 총 청약자의 청약주식수가 일반공모 배정분을 초과하는 경우에는 청약경쟁률에 따라5사6입을 원칙으로 안분 배정하여 잔여주식이 최소화되도록 합니다. 이후 최종 잔여주식은 최대청약자부터 순차적으로 우선 배정하되, 동순위 최고청약자가 최종 잔여 주식보다 많은 경우에는 "공동대표주관회사"와 "인수회사"가 합리적으로 판단하여 배정합니다.
(iii) 일반공모 청약결과 일반공모 총 청약자의 청약주식수가 일반공모 배정분에 미달하는 경우에는 청약주식수대로 배정합니다. 배정결과 발생하는 잔여주식은 "공동대표주관회사"와 "인수회사"가 제2조 제3항에 따라 인수합니다. 단, "공동대표주관회사"와 "인수회사" 중 "청약초과회사"("청약물량"이 "인수한도 의무주식수"를 초과하는 회사를 말한다)가 있는 경우, "초과청약물량" ("청약초과회사"의 "청약물량"에서 "인수한도 의무주식수"를 차감한 주식수를 의미하되, 0이상으로 한다)을 "청약미달회사"("청약물량"이 "인수한도 의무주식수"보다 적은 회사를 말한다)에게 "청약미달회사"별 인수비율로 나누어 산정합니다.
마) 단, "공동대표주관회사"는 「증권 인수업무 등에 관한 규정」 제9조제2항에 의거 고위험고수익투자신탁, 벤처기업투자신탁 및 일반청약자에 대하여 배정하여야 할 주식이 50,000주(액면가 500원 기준) 이하 이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 일반청약자에게 배정하지 아니할 수 있습니다. 이 경우 "공동대표주관회사"가 자기의 계산으로 인수할 수 있습니다.
5) 투자설명서 교부에 관한 사항
- 「자본시장과 금융투자업에 관한 법률」 제124조에 의거, 본 주식의 청약에 대한 투자설명서 교부 의무는 당사, 공동대표주관회사 및 인수회사가 부담하며, 금번 유상증자의 청약에 참여하시는 투자자께서는 투자설명서를 의무적으로 교부받으셔야 합니다.
- 금번 유상증자에 청약하고자 하는 투자자께서는 (동법 제9조제5항에 규정된 전문투자자 및 동법 시행령 제132조에 따라 투자설명서의 교부가 면제되는 자 제외) 청약하시기 전 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
- 투자설명서 수령거부의사표시는 서면, 전화, 전신, Fax, 전자우편 및 이와 비슷한 전자통신, 그 밖에 금융위원회가 정하여 고시하는 방법으로 가능합니다.
-전자문서의 방법으로 투자설명서를 교부받고자 하는 투자자는 「자본시장과 금융투자업에 관한 법률」 제124조제1항 각호의 요건을 모두 충족하여야 합니다.
가) 투자설명서 교부 방법 및 일시
| 구분 | 교부방법 | 교부일시 |
|---|---|---|
| 구주주 청약자 |
1),2),3)을 병행 1) 우편 송부 2) "공동대표주관회사"의 본ㆍ지점에서 교부 3) "공동대표주관회사"의 홈페이지나 HTS에서 교부 |
1) 우편송부 시: 구주주 청약초일인 2022년 12월 01일 전 수취 가능 2) "공동대표주관회사"의 본, 지점 : 청약종료일(2022년 12월 02일)까지 3) "공동대표주관회사"의 홈페이지 또는 HTS 교부 |
| 일반 청약자 |
1), 2)를 병행 1) "공동대표주관회사"와 "인수회사"의 본ㆍ지점에서 교부 2) "공동대표주관회사"와 "인수회사"의 홈페이지나 HTS에서 교부 |
1) "공동대표주관회사"와 "인수회사"의 본ㆍ지점 2) "공동대표주관회사"와 "인수회사"의 홈페이지 또는 HTS 교부 |
※ 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
나) 확인절차
(1) 우편을 통한 투자설명서 수령 시
(가) 청약하시기 위해 지점을 방문하셨을 경우, 직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
(나) HTS를 통한 청약을 원하시는 경우, 청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
(다) 주주배정 유상증자 경우 유선청약이 가능합니다. 유선 상으로 신분확인을 하신 후, 투자설명서 교부 확인을 해주시고 청약을 진행하여 주시기 바랍니다.
(2) 지점 방문을 통한 투자설명서 수령 시
직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
(3) 홈페이지 또는 HTS를 통한 교부
청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
다) 기타
(1) 금번 유상증자에서 당사는 본 증권신고서의 효력발생 이후 주주명부상 주주분들에게 투자설명서를 우편으로 발송할 예정입니다. 우편의 반송 등에 의한 사유로 교부를 받지 못하신 투자자께서는 지점 방문을 통해 인쇄물을 받으실 수 있으며, 또한 동일한 내용의 투자설명서를 전자문서의 형태로 공동대표주관회사 및 인수회사의 홈페이지에서 다운로드 받으실 수 있습니다. 다만, 전자문서의 형태로 교부 받으실 경우, 「자본시장과 금융투자업에 관한 법률」 제124조제1항 각 호의 요건을 모두 충족해야만 청약이 가능합니다.
(2) 구주주 청약 시 "공동대표주관회사" 이외의 증권회사를 이용한 청약 방법 해당 증권회사의 청약 방법 및 규정에 의해 청약을 진행하시기 바랍니다. 이 경우에도, 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
※ 투자설명서 교부를 받지 않거나, 수령거부의사를 서면 등의 방법으로 표시하지 않을 경우, 본 유상증자의 청약에 참여할 수 없습니다.
|
※ 관련법규 제132조(투자설명서의 교부가 면제되는 자) 1. 제11조제1항제1호다목부터 바목까지 및 같은 항 제2호 각 목의 어느 하나에 해당하는 자 1의2. 제11조제2항제2호 및 제3호에 해당하는 자 2. 투자설명서를 받기를 거부한다는 의사를 서면, 전화ㆍ전신ㆍ팩스, 전자우편 및 이와 비슷한 전자통신, 그 밖에 금융위원회가 정하여 고시하는 방법으로 표시한 자 3. 이미 취득한 것과 같은 집합투자증권을 계속하여 추가로 취득하려는 자. 다만, 해당 집합투자증권의 투자설명서의 내용이 직전에 교부한 투자설명서의 내용과 같은 경우만 해당한다. |
6) 주권교부에 관한 사항
가) 주권유통개시 예정일: 2022년 12월 23일 (2019년 9월 16일 전자증권제도가 시행됨에 따라 실물 주권의 교부 없이 각 주주의 보유 증권계좌로 상장일에 주식이 등록발행되어 입고되며, 상장일부터 유통이 가능합니다. 단, 유관기관과의 업무 협의 과정에서 상기 일정은 변경될 수 있음을 유의하시기 바랍니다.)
7) 청약증거금의 대체 및 반환 등에 관한 사항
청약증거금은 청약금액의 100%로 하고, 주금납입기일에 주금납입금으로 대체하며, 청약증거금에 대해서는 무이자로 합니다.
8) 주금납입장소 : 국민은행 무역센터종합금융센터
다. 신주인수권증서에 관한 사항
| 신주배정기준일 | 신주인수권증서의 매매 금융투자업자 | |
|---|---|---|
| 회사명 | 회사고유번호 | |
| 2022년 10월 14일 |
케이비증권㈜ | 00164876 |
| 한국투자증권㈜ | 00160144 | |
1) 금번과 같이 주주배정방식의 유상증자를 실시할 때, 주주가 소유하고 있는 주식수 비율대로 신주를 인수할 권리인 신주인수권에 대하여 당사는 「자본시장과 금융투자업에 관한 법률」 제165의6조제3항 및 「증권의 발행 및 공시 등에 관한 규정」 제5-19조에 의거하여 주주에게 신주인수권증서를 발행합니다.
2) 금번 유상증자시 신주인수권증서는 전자증권제도 시행일(2019년 9월 16일) 이후에 발행되고 상장될 예정으로 전자증권으로 발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여 배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다.
3) 신주인수권증서 매매의 중개를 할 증권회사는 케이비증권㈜ 및 한국투자증권㈜로 합니다.
4) 신주인수권증서 매매 등
가) 신주인수권증서를 매매하고자 하는 주주는 신주인수권증서를 예탁하고 있는 증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
나) 신주인수권증서를 양수한 투자자의 청약방법
신주인수권증서를 증권회사에 예탁하고 있는 양수인은 당해 증권회사 점포 및 케이비증권㈜의 본ㆍ지점 및 한국투자증권㈜의 본ㆍ지점을 통해 해당 신주인수권증서에 기재되어 있는 수량만큼 청약할 수 있으며 청약 기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
5) 당사는 금번 주주배정후 실권주 일반공모 유상증자 관련 신주인수권증서의 상장을 한국거래소에 신청할 예정입니다. 동 신주인수권증서가 상장될 경우 상장기간은 2022년 11월 16일부터 2022년 11월 22일까지 5거래일간으로 예정하고 있으며, 동 기간 중 상장된 신주인수권증서를 한국거래소에서 매매할 수 있습니다. 동 신주인수권증서는 2022년 11월 23일에 상장폐지될 예정입니다. 「코스닥시장 상장규정」제16조 3(신주인수권증서의 신규상장)에 따라 5거래일 이상 상장되어야 하며, 동 규정 제44조의3 "신주인수권증서의 상장폐지기준"에 따라 신주청약 개시일 5거래일전에 상장폐지되어야 함)
7) 신주인수권증서의 거래 관련 추가사항
당사는 금번 유상증자의 신주인수권증서를 상장신청할 예정인 바, 현재까지 관계기관과의 협의를 통해 확인된 신주인수권증서 상장시의 제반 거래관련 사항은 다음과 같습니다.
가) 상장방식 : 전자등록발행된 신주인수권증서 전부를 상장합니다.
나) 주주의 신주인수권증서 거래
| 구분 | 상장거래방식 | 계좌대체 거래방식 |
|---|---|---|
| 방법 | 주주의 신주인수권증서를 전자등록발행하여 상장합니다. 상장된 신주인수권증서를 장내거래를 통하여 매수하여 증권사 계좌에 보유한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. 주주의 신주인수권증서는 전자등록발행되므로 실물 증서는 발행되지 않습니다. | 신주인수권증서를 매매하고자 하는 실질주주는 위탁증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. |
| 기간 | 2022년 11월 16일부터 2022년 11월 22일까지(5거래일간) 거래 | 2022년 10월 25일부터 2022년 11월 24일까지거래 |
(1) 상장거래 : 2022년 11월 16일부터 2022년 11월 22일까지(5영업일간) 거래 가능합니다.
(2) 계좌대체거래 : 신주배정통지일인 2022년 10월 25일(예정)부터 2022년 11월 24일까지 거래 가능 합니다.
* 신주인수권증서의 계좌대체(장외거래)는 신주인수권증서 상장거래의 결제일인 2022년 11월 24일까지 가능하며, 2022년 11월 24일 이후부터는 신주인수권증서의 청약권리 명세를 확정하므로 신주인수권증서의 계좌대체(장외거래)가 제한됩니다.
(3) 신주인수권증서는 전자등록발행되므로 실물은 발행되지 않습니다.
다) 특별계좌 소유주(기존 '명부주주')의 신주인수권증서 거래
(1) '특별계좌 보유자(기존 '명부주주')'는 명의개서대행기관에 '특별계좌'에서 '일반전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후 금번 유상증자 청약 참여또는 신주인수권증서의 매매가 가능합니다.
(2) '특별계좌 보유자(기존 '명부주주')'는 신주인수권증서의 '일반 전자등록계좌(증권회사 계좌)'로 이전 없이 공동대표주관회사인 케이비증권㈜ 및 한국투자증권㈜의 본ㆍ지점에서 직접 청약하는 방법으로도 금번 유상증자에 청약이 가능합니다. 다만 신주인수권증서의 매매는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후에만 가능하므로 이 점 유의하시기 바랍니다.
라. 기타 모집 또는 매출에 관한 사항
1) 본 증권신고서는 공시심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요 내용의 변경시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있으므로 투자자 여러분께서는 투자시 이러한 점을 감안하시기 바랍니다.
2) 「자본시장과 금융투자업에 관한 법률」 제120조3항에 의거 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다.
3) 본 증권신고서에 기재된 내용은 신고서 제출일 현재까지 발생된 것으로 본 신고서에 기재된 사항 이외에 자산, 부채, 현금흐름 또는 손익상황에 중대한 변동을 가져오거나 중요한 영향을 미치는 사항은 없습니다. 따라서, 주주 및 투자자가 투자의사를 결정함에 있어 유의하여야 할 사항이 본 증권신고서상에 누락되어 있지 않습니다.
4) 금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서, 반기보고서, 분기보고서 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있사오니 투자의사를 결정하시는 데 참조하시기 바랍니다.
5. 인수 등에 관한 사항
| [인수방법: 잔액인수] |
| 인수인 | 인수주식 종류 및 수 | 인수대가 | |
|---|---|---|---|
| 공동대표주관회사 | 한국투자증권㈜ | 인수주식의 종류: 기명식 보통주식 인수주식의 수: 최종 실권주 X 인수비율(50%) |
대표주관수수료: 모집총액의 0.3% 中 50% 인수수수료 : 모집총액의 1.1% 中 50% 실권수수료 : 잔액인수금액의 12% |
| 공동대표주관회사 | 케이비증권㈜ | 인수주식의 종류: 기명식 보통주식 인수주식의 수: 최종 실권주 X 인수비율(40%) |
대표주관수수료: 모집총액의 0.3% 中 50% 인수수수료 : 모집총액의 1.1% 中 40% 실권수수료 : 잔액인수금액의 12% |
| 인수회사 | 유진투자증권㈜ | 인수주식의 종류: 기명식 보통주식 인수주식의 수: 최종 실권주 X 인수비율(10%) |
인수수수료 : 모집총액의 1.1% 中 10% 실권수수료 : 잔액인수금액의 12% |
| 주1) 최종 실권주 : 구주주청약 및 일반공모 후 발생한 배정잔여주 또는 청약미달주식 주2) 모집총액 : 최종 발행가액 X 총 발행주식수 |
II. 증권의 주요 권리내용
당사가 금번 주주배정후 실권주 일반공모 유상증자를 통하여 발행할 증권은 기명식 보통주이며, 동 증권의 주요 권리내용은 다음과 같습니다.
1. 액면금액
제7조(1주의 금액)
주식 1주의 금액은 오백원으로 한다.
2. 주식의 발행 및 배정에 관한 사항
제5조(발행예정주식총수)
회사가 발행할 주식의 총수는 오억주로 한다.
제8조 (주식의 발행과 종류)
①이 회사가 발행할 주식의 종류는 기명식 보통주식과 기명식 종류주식으로 한다.
②회사가 발행하는 종류주식은 이익배당에 관한 우선주식, 의결권 배제에 관한주식, 상환주식, 전환주식 및 이들의 전부 또는 일부를 혼합한 주식으로 한다.
제8조의2 (주식등의 전자등록)
회사는 「주식.사채 등의 전자등록에 관한 법률」 제2조 제1호에 따른 주식등을 발행하는 경우에는 전자등록기관의 전자등록계좌부에 주식등을 전자등록하여야 한다..
제10조 (신주인수권)
① 주주는 그가 소유한 주식의 수에 비례하여 신주의 배정을 받을 권리를 갖는다.
② 회사는 제1항의 규정에도 불구하고 다음 각 호의 경우에는 주주이외의 자에게 신주를 배정할 수 있다.
1. 자본시장과 금융투자업에 관한 법률 제 165조의 6에 따라 이사회의 결의로 일반공모증자 방식으로 신주를 발행하는 경우
2. 상법 제542조의3에 따른 주식매수선택권의 행사로 인하여 신주를 발행하는 경우
3. 발행주식총수의 100분의 20을 초과하지 않는 범위 내에서 긴급한 자금조달을 위하여 국내외 금융기관 또는 기관투자자, 개인에게 신주를 발행하는 경우
4. 자본시장과 금융투자업에 관한 법률 제165조의 7 규정에 의하여 발행하는 주식총수의 100분의 20 범위 내에서 우리사주조합원에게 주식을 우선 배정하는 경우
5. 근로복지기본법 제39조 규정에 의한 우리사주매수선택권의 행사로 인하여 신주를 발행하는 경우
6. 발행주식총수의 100분의 20을 초과하지 않는 범위 내에서 사업상 중요한 기술도입, 연구개발, 생산ㆍ판매ㆍ자본제휴, 재무구조 개선 등 회사의 경영상 목적을 달성하기 위하여 그 상대방에게 신주를 발행하는 경우
7. 발행주식총수의 100분의 40을 초과하지 않는 범위 내에서 주권을 코스닥시장에 상장하기 위하여 신주를 모집하거나 인수인에게 인수하게 하는 경우
③ 제2항 각호의 어느 하나의 방식에 의해 신주를 발행할 경우에는 발행할 주식의 종류와 수 및 발행가격 등은 이사회의 결의로 정하고, 다만 발행가격은 증권의 발행 및 공시등에 관한 규정 제5-18조의 범위 내에서 정하여야 한다.
3. 배당에 관한 사항
제13조(신주의 배당기산일)
회사가 유상증자, 무상증자 및 주식배당에 의하여 발행한 신주에 대한 이익의 배당에관하여는 신주를 발행한 때가 속하는 영업연도의 직전영업연도말에 발행된 것으로 본다.
제55조 (이익금의 처분)
회사는 매사업년도의 처분전 이익잉여금을 다음과 같이 처분한다.
1. 이익준비금
2. 기타의 법정준비금
3. 배당금
4. 임의적립금
5. 기타의 이익잉여금처분액
제56조 (이익배당)
① 이익의 배당은 금전과 주식으로 할 수 있다.
② 이익의 배당을 주식으로 하는 경우 회사가 수종의 주식을 발행한 때에는 주주총회의 결의로 그와 다른 종류의 주식으로도 할 수 있다.
③ 제1항의 배당은 매결산기말 현재의 주주명부에 기재된 주주 또는 등록된 질권자에게 지급한다.
4. 의결권에 관한 사항
제27조(주주의 의결권)
주주의 의결권은 1주마다 1개로 한다.
제28조(상호주에 대한 의결권 제한)
회사, 회사와 회사의 자회사 또는 회사의 자회사가 다른 회사의 발행주식총수의 10분의 1을 초과하는 주식을 가지고 있는 경우, 그 다른 회사가 가지고 있는 이 회사의 주식은 의결권이 없다.
제29조 (의결권의 불통일행사)
① 2이상의 의결권을 가지고 있는 주주가 의결권의 불통일행사를 하고자 할 때에는 회일의 3일전에 회사에 대하여 서면으로 그 뜻과 이유를 통지하여야 한다.
② 회사는 주주의 의결권의 불통일행사를 거부할 수 있다. 그러나, 주주가 주식의 신탁을 인수하였거나 기타 타인을 위하여 주식을 가지고 있는 경우에는 그러하지 아니하다.
제30조 (의결권의 대리행사)
① 주주는 대리인으로 하여금 그 의결권을 행사하게 할 수 있다.
② 제1항의 대리인은 주주총회 개시전에 그 대리권을 증명하는 서면(위임장)을 제출하여야 한다.
제31조(주주총회의 결의방법)
주주총회의 결의는 법령과 정관에 다른 정함이 있는 경우를 제외하고는 출석한 주주의 의결권의 과반수와 발행주식 총수의 4분의 1 이상의 수로써 한다.
III. 투자위험요소
| 【투자자 유의사항】 |
|---|
| ■ 본 건 공모주식을 청약하고자 하는 투자자들은 투자결정을 하기 전에 본 공시서류의 다른 기재 부분 뿐만 아니라, 특히 아래에 기재된 「투자위험요소」를 주의깊게 검토한후 이를 고려하여 최종적인 투자판단을 해야 합니다. ■ 당사는 본 공시서류를 통하여 청약 전에 투자자께서 숙지하셔야 하는 부분에 대하여 성실히 기재하고자 노력하고 있습니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 아래 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수 없으므로, 투자자는 아래 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안 되며, 투자자 자신의 독자적이고도 세밀한 판단에 의해야 합니다. 따라서 본 공시서류에 기재된 사항은 투자 판단 시 참고 자료로 활용하실 것을 권고 드리며, 투자자의 투자 판단에 대한 결과는 투자자 본인에게 귀속됩니다. ■ 만일, 아래 기재한 투자위험요소가 실제로 발생하는 경우, 당사의 사업, 재무상태, 기타 영업활동에 중대한 부정적 영향을 미칠 수 있으며, 이에 따라 투자자가 금번 공모과정에서 취득하게 되는 당사 주식의 시장가격이 하락하여 투자금액의 일부 또는 전부를 잃게 될 수도 있음을 유의하시기 바랍니다. ■ 2009년 2월 4일 부로 시행된 「자본시장과 금융투자업에 관한 법률」 제124조에 의거 누구든지 증권신고의 효력이 발생한 증권을 취득하고자 하는 자 (전문투자자, 그밖에 대통령령으로 정하는 자를 제외함) 에게 적합한 투자설명서를 미리 교부하지 아니하면 그 증권을 취득하게 하거나 매도하여서는 안됩니다. 다만, 「자본시장과 금융투자업에 관한 법률 시행령」 제132조에 의거하여 투자설명서를 받기를 거부한다는 의사를 서면으로 표시한 자는 투자설명서의 교부없이 청약이 가능합니다. ■ 본 공시서류의 기재사항은 투자 결정을 위한 참고사항일 뿐이며, 투자에 대한 모든 손익 및 투자책임은 투자자 본인에게 귀속됨을 다시 한 번 말씀드립니다. |
당사는 주된 사업부문을 영위하는데 있어 중대한 영향을 미친다고 판단되는 사항들을 위주로 투자위험요소를 작성하였습니다. 그럼에도 불구하고, 당사가 관련성이 적다고 판단하거나 미처 파악하지 못한 원인으로 인해 경영환경이 악화될 가능성을 배제할 수 없습니다. 투자자께서는 아래 기재한 투자위험요소 뿐만 아니라 다양한 정보를 면밀히 검토하시어 금번 유상증자 참여에 대한 의사결정에 참고하시기 바랍니다.
1. 사업위험
① 복합소재사업부문(선박사업부, 파이프사업부)
|
가. 조선경기 침체에 따른 위험 |
당사의 복합소재사업부문의 선박사업부는 구명정을 생산하여 판매하고 있습니다. 구명정은 국제해사기구(IMO) 규정에 따라 500톤 이상 및 본선 길이 85M 이상의 모든 선박에 의무적으로 승선인원의 200% 이상 장착되어야 하는 필수품입니다. 당사는 46년간 구명정을 생산하여 왔으며 2000년 6월 현대정공으로부터 분리된 국내 유일의 구명정 제조업체로서 자체개발한 소형엔진과 다수의 구명정 모델을 개발하여 연간 700대의 구명정 생산 능력을 갖추었습니다.
당사의 복합소재사업부문은 구명정 이외에도 GRP 파이프를 생산하고 있으며, GRP 파이프는 해수담수화 설비 및 발전소 등 플랜트 사업과 조선소 시스템 등에 공급되고있습니다. 최근 친환경 선박 수요가 증가함에 따라 새롭게 규정된 스크러버 장착으로인해 선박의 신규 건조와 기존 운항선에 장착되는 수요 등으로 시장 규모가 확대됨에따라 국내 조선소의 수주가 증가하고 있습니다.
당사는 국내의 모든 조선소에 당사의 제품을 공급하고 있으며, 당사가 생산하는 구명정 및 파이프의 종류는 다음과 같습니다.
| [당사 주요 제품의 종류 및 사용 용도] |
| 종류 | 특징 | 사용용도 | |
|---|---|---|---|
| 구명정 | 일반형 | 가장 대표적인 구명정으로 데빗에 의해 진수할 수 있으며, SOLAS규정을 모두 만족하게 만들어졌으며, 위기발생시 신속한 탈출이 가능한 구조로 25인승부터 100인승까지 19개 모델을 보유하고 있어 선박의 규모에 따라 선택적용 가능 | 인명구조 |
| 자유낙하식 | 선박의 선미에 탑재되어 자유낙하 방식으로 진수되는 구명정으로 2007년 5월 이후부터 건조되는 모든 Bulk Carrier선박에 설치가 의무화 되어있으며, 일반형 구명정의 진수 시 Davit Winch를 이용하는 방식 때문에비상탈출 시간이 많이 소요되는 점과 본선의 양쪽에 각 한대 씩 설치되는 방식으로 인해 Deck House의 공간을 적절히 활용할수 없어 최근 자유낙하식 구명정을 선호하는 추세 | ||
| 구조정 | 선박의 선미에 장착하여 모선의 응급상황시 구조임무에 사용되는 보트로 보트 자유낙하식 구명정과 레스큐보트가 각 하나씩 한세트로 선박에 설치 | ||
| 특수선 | 관공선 | 대형선박, 어업지도선, 해경경비정 등 선미데크에 설치되어 작업 및 신속한 인명구조활동 및 불법어업단속 등에 사용 | 인명구조 및 불법어업 단속 |
| 도선선 | 선박이 입출항하는 항만에서 도선사들이 선박을 탑승 및 하선을 위해 사용됨으로 이동시 실내 편의성, 속도, 선박 탑승시 안전성이 많이 요구됨 | 도선사 선박 승,하선용 | |
| 유도선 | 유선은 일반적으로 유람선을 의미하며 도선은 강과 바다가 접하는 하구 또는 만의 형태를 갖춘 곳으로 양 해안을 오가는 선박이며 선령 교체시기에 따라 비정기적으로 발주되는 선박임 | 여객선, 유람선, 도선 | |
| GRP/GRE PIPE | 유리섬유로 강화된 플라스틱이라는 의미의 것으로 통상 강화플라스틱이라 하며, 철근과 콘크리트가 복합되어 좋은 강도를 얻는 것과 같이 내수, 내약, 내열성이 좋은 수지를 혼합하여 사용되어 내구성, 강도, 내부식성의 이점을 모두 가짐 | 밸러스트 라인, 해수관,소화배관,냉각수관, 상하수도관 등 | |
| DAVIT | 선외 물체를 올리고 내릴 때 그 물체가 선체에 부딪치는 일없이 작업하기 편리하게 회전할 수 있게 되어 있음 | 선외 물체를 올리고 내리기 위한 기둥 |
|
| 자료: 당사 반기보고서(2022.06) |
당사의 복합소재사업부문에서 생산하는 구명정 및 파이프는 조선소의 선박 건조량에크게 영향을 받고 있으며, 전방산업인 조선/해운사업의 사이클에 따라 호황과 불황을 반복하는 추세를 보입니다.
2022년 7월 26일 국제통화기금(IMF)이 발표한 '세계경제전망(World Economic Outlook)'에 따르면, 2021년 세계 경제성장률은 6.1%를 기록하였으며, 2022년에는 3.2%, 2023년에는 2.9%의 성장률을 기록하며 성장세가 둔화될 것으로 전망됩니다. 국제통화기금(IMF)은 미국, 유럽에서의 예상보다 높은 인플레이션, 러시아-우크라이나 전쟁, 코로나19 재확산, 중국 성장 둔화 등의 영향으로 인해 2022년 04월 전망치 대비 성장률을 대폭 감소하여 전망하였습니다.
2022년 선진국의 경제성장률은 2.5%로 전망하며 직전 전망치(2022년 04월) 대비 0.8%p 감소하였으며, 신흥국의 경제성장률은 3.6%로 직전 전망치 대비 0.2%p 감소하였습니다. 미국은 강력한 통화 긴축 및 구매력 하락으로 인해 성장률이 대폭 하향전망되었으며, 유럽 역시 2022년 04월 전망에서 대폭 하향조정 되었던 이탈리아를 제외하고는 러시아-우크라이나 전쟁 및 통화 긴축 등의 영향으로 직전 전망치 대비 성장률이 낮아졌습니다. 신흥국 중에서도 중국은 제로코로나 정책, 부동산 경기 침체 등으로 인해 직전 전망치 대비 -1.1%p 하향 조정되며 2022년 경제성장률 3.3%로 전망되며, 이는 코로나19 직후인 2020년 1분기 이후 최저수준입니다.
| [세계 경제 성장률 전망치] |
| (단위: %, %p) |
| 구분 | 2021년 | 2022년(E) | 2023년(E) | ||||
|---|---|---|---|---|---|---|---|
| 22년 4월 | 22년 7월 | 조정폭 | 22년 4월 | 22년 7월 | 조정폭 | ||
| (A) | (B) | (B-A) | (A) | (B) | (B-A) | ||
| 세계 | 6.1 | 3.6 | 3.2 | -0.4 | 3.6 | 2.9 | -0.7 |
| 선진국 | 5.2 | 3.3 | 2.5 | -0.8 | 2.4 | 1.4 | -1.0 |
| 미국 | 5.7 | 3.7 | 2.3 | -1.4 | 2.3 | 1.0 | -1.3 |
| 유로존 | 5.3 | 2.8 | 2.6 | -0.2 | 2.3 | 1.2 | -1.1 |
| 일본 | 1.6 | 2.4 | 1.7 | -0.7 | 2.3 | 1.7 | -1.9 |
| 신흥국 | 6.8 | 3.8 | 3.6 | -0.2 | 4.4 | 3.9 | -0.5 |
| 중국 | 8.1 | 4.4 | 3.3 | -1.1 | 5.1 | 4.6 | -0.5 |
| 한국 | 4.0 | 2.5 | 2.3 | -0.2 | 2.9 | 2.1 | -0.8 |
| 자료: | IMF, World Economic Outlook(2022.07) |
이처럼 IMF는 2022년 및 2023년의 세계 경제성장률 전망치를 각각 0.4%p, 0.7%p 하향 조정하였습니다. 이는 인플레이션 및 통화 긴축의 영향이 본격화될 경우 세계 경제 성장 동력이 급격히 약화될 수 있다는 인식이 반영된 것으로 판단됩니다.
조선업의 경우를 살펴보면, 2016년 수주량은 1980년대 이후 최저 수준을 기록하였으며, 전세계적으로 조선업황의 수주절벽을 보였으며, 2016년 이후 국내 조선 빅3업체는 잇따라 수주 목표를 하향 조정한 바 있습니다. 2020년에는 COVID-19로 인한 경기 침체 및 국가간 이동 제한으로 프로젝트 및 투자가 지연 또는 취소되어 2020년 글로벌 신조 발주량은 2019년 발주량 대비 큰폭으로 감소하였습니다. 다만, 2021년에는 2020년 하반기부터 반등하기 시작한 컨테이너 운반선 시장을 필두로 하여 대부분의 해운 섹터가 활황세를 보임에 따라 선주사들의 신조 발주 심리도 큰 폭으로 회복되며 직전년 대비 신조 발주량이 급증했습니다.
2019년 이후 국내 조선3사의 신규수주 추이는 아래와 같습니다.
| [조선 3사 등 신규수주 추이] |
| (단위: 천GT) |
| 구 분 | 2022년 1분기 | 2021년 | 2020년 | 2019년 | ||||
|---|---|---|---|---|---|---|---|---|
| 수주량 | 점유율 | 수주량 | 점유율 | 수주량 | 점유율 | 수주량 | 점유율 | |
| 현대중공업 | 1,519 | 17.1% | 8,444 | 25.8% | 3,877 | 22.7% | 4,473 | 25.5% |
| 현대삼호중공업 | 2,690 | 30.2% | 4,249 | 13.0% | 3,475 | 20.3% | 3,067 | 17.5% |
| 현대미포조선 | 730 | 8.2% | 2,030 | 6.2% | 1,245 | 7.3% | 1,562 | 8.9% |
| 대우조선해양 | 1,904 | 21.4% | 7,326 | 22.4% | 4,779 | 28.0% | 3,530 | 20.1% |
| 삼성중공업 | 1,968 | 22.1% | 9,451 | 28.8% | 3,628 | 21.2% | 4,841 | 27.6% |
| 기 타 | 89 | 1% | 1,268 | 3.8% | 80 | 0.5% | 59 | 0.4% |
| 계 | 8,900 | 100.0% | 32,768 | 100.0% | 17,084 | 100.0% | 17,532 | 100.0% |
| 자료 : 한국조선해양㈜ 분기보고서(2022.03) |
2022년 반기 국내 조선 수주량은 전년 대비 9.7% 감소한 979만CGT를 기록하며 전년대비 부진하였으나, 2020년 반기(133만CGT) 대비 636% 증가, 2019년 반기(388만CGT) 대비 152% 증가한 수치입니다. 특히, 카타르 LNG 운반선 건조계약, 러시아의 우크라이나 침공에 따른 LNG 수요 등에 따라 대형 LNG 운반선 발주가 크게 증가한 가운데, 전세계 발주량의 71%에 해당하는 63척(544만CGT)를 수주하였습니다. 2022년에도 양호한 해운시황이 이어지고 있고 선주사들 역시 신조 발주 의지를 강하게 보이고 있어, 연간 양호한 수준의 신조 발주량을 기록할 것으로 보여지나, 2021년대규모 신조 발주에 따라 조선소들의 판매 가능한 납기가 제한적인 상황으로, 2022년 신조 발주량은 2021년 수준에는 미치지 못할 것으로 예상됩니다.
향후 변동성이 높은 해운 시황 전망, COVID-19 지속 및 지정학적 리스크 증가 등의 상황을 감안할 경우 과거와 같은 조선업의 호황기가 본격적으로 오기까지는 다소 시간이 소요될 수 있으며, 추후에 신규수주가 부진할 경우 당사의 복합소재사업부문 또한 일감 축소로 인한 임금과 시설운영 등 고정비 부담이 확대되면서 수익성이 악화될가능성이 존재합니다.
|
나. 해운업황에 따른 사업위험 |
당사의 복합소재사업부문은 조선업 뿐만 아니라, 조선업의 전방산업인 해운업과의 상호 연관관계가 존재합니다. 해운업은 물동량, 선복량, 해체선가 등 시장상황에 민감하게 반응하며, 해운 물동량을 나타내는 BDI지수와 밀접한 관계를 보입니다. BDI는 선형별로 대표항로를 선정하고, 각 항로별 톤마일(Ton-Mile) 비중에 따라 가중치를 적용하는 업계 대표적인 시황 지수입니다. 최근 5년간 BDI 지수 추이는 아래와 같습니다.
| [BDI지수 추이] |
| (단위: pt) |
|
| 기간 : 2019년 08월 12일 ~ 2022년 08월 09일 자료: Bloomberg |
2019년 중국 춘절 기간동안 철광석, 석탄 등의 광물자원에 대한 재고 비축 수요가 중단되고, 곡물 수확기가 마무리되면서 계절적 비수기에 진입함에 따라 2019년 3월 BDI는 677.88pt로 낮은 수준을 기록하였습니다. 2020년 COVID-19로 인해 세계 경제가 일시적으로 침체되고, 원자재 물동량이 줄어들면서 BDI가 400pt 아래로 떨어지는 모습을 보였습니다.
2021년에 들어서는 중국의 경기 부양책을 시작으로 원자재 수요가 급등하고, 백신 보급 및 경제 회복에 대한 기대가 높아지면서 5,647pt까지 급격히 상승하였습니다. 그러나 2022년 변이 바이러스 출현, 스태그플레이션에 대한 우려와 인도네시아 석탄수출 중단 및 브라질 폭우, 철광석 생산 및 운송 차질 등의 이슈로 인해 연초 1,296pt까지 다시금 하락하는 모습을 보였습니다. 2022년 2분기에는 장기간의 발주 공백과 글로벌 항만 적체로 수요가 공급을 상회함에 따라 BDI가 2000~3300pt 선에서 움직이며 평년대비 높은 수준을 형성하고 있습니다. 그러나, 국제 경기와 교역량 변동, 국제 원자재 가격 및 수요 변동에 민감도가 높은 해운업 특성상 업황이 예기치 않은 요인이 발생하여 해운업의 후방에 위치하고 있는 당사의 수주 실적에도 부정적인 영향을 미칠 수 있습니다.
팬데믹 이후의 펜트업 효과, 러시아-우크라이나 전쟁 등으로 유가가 급등하면서 해운업계의 원가 부담이 증대되고 있습니다. 유류비는 해운사의 주요 변동비로 전체 매출원가에서 20% 내외의 비중을 차지하며, 선박의 주 연료인 고유황유(HSFO)와 저유황유(VLSFO)의 2022년 2분기 싱가포르항 기준 가격은 각각 679달러, 949달러로 2021년 연평균 가격인 416달러와 535달러 대비 77.4% 증가하였습니다. 최근 수요 둔화 우려로 유가 상승세가 소폭 하락하였으나, 여전히 평년 대비 높은 수준에 형성되어 있습니다. 고유가 기조가 계속된다면 장기적 관점에서 해운업계의 수익성이 악화될 위험이 있고, 러시아-우크라이나 간 전쟁이 장기화됨에 따라 지정학적 리스크 또한 잔존하고 있어 고유가 기조는 지속될 전망이며 해운업의 개선세 제한 요인으로 작용할 수 있습니다.
COVID-19 지속 및 지정학적 리스크 증가, 인플레이션, 원자재변동 등 여러 거시경제 변수들과 선박의 공급과잉 상태 역시 쉽게 해소되지 않을 것으로 예상됩니다. 향후 해운업황의 근본적인 개선이 이루어지지 않는다면 BDI 지수의 지속적인 상승세가 나타나기는 어려울 것으로 예상되며 이러한 해운업의 불황은 선박 발주 감소 등으로 이어져 조선업 및 당사의 복합소재사업부문에도 부정적 영향을 미칠 수 있습니다.
② 헬스케어 사업
| 다. 체외진단 의료기기 시장 위험 체외진단(IVD, In Vitro Diagnostics)은 혈액, 분뇨, 체액, 침 등 인체에서 유래한 물질을 이용해 몸 밖에서 신속하게 병을 진단하는 기술로, 임상의사 결정에 중요한 역할합니다. 흔히 주변에서 볼 수 있는 혈당측정기나 임신테스트기가 대표적인 체외진단기기이며, COVID-19 가 발병한 후 선별진료소 등에서 검사 시 사용되는 검체 채취용 면봉(swab)과 검사 후 검사실로 이동하기 위하여 면봉(swab)을 담아 옮기는 수송배지(VTM)가 이에 해당됩니다. 이러한 체외진단의 중요성으로 인해 글로벌 체외진단 시장은 지속적으로 성장하고 있습니다. 또한, 최근 감염질병의 유행과 인구고령화로 조기진단의 중요성이 커지고 의료 패러다임이 치료에서 진단과 예방으로 전환됨에 따라 체외진단 산업이 성장하고 있습니다. 그럼에도 불구하고, 당사가 예상하지 못한 체외진단 시장의 트렌드 변화, 체외진단 수요 감소 등으로 글로벌 체외진단 시장은 위축될 가능성이 존재하며, 이 경우 당사의매출에 부정적인 영향을 미칠 수 있습니다. |
당사는 현재 체외진단 의료기기 및 알콜스왑을 주축으로 한 헬스케어 사업부를 운영중에 있으며, 체외진단의료기기 및 의약외품 등을 생산하여 판매하고 있습니다.
당사가 생산하는 헬스케어사업부문의 주요 제품은 다음과 같습니다.
| [당사 주요 제품의 종류 및 사용 용도] |
| 종류 | 특징 | 사용용도 | |
|---|---|---|---|
|
체외진단 의료기기 |
검체 채취용 도구 |
비강/비인두, 구강/구인두 면봉(swab) - Virus, Chlamydia, Mycoplasma, & Ureaplasma 등을 포함한 임상 시료를채취하여 - 짧은 시간 내에 채취 부위에서 많은 양의 샘플 채취가 가능함 - USA FDA 등록 및 유럽 CE멸균 인증취득 완료 |
질병 및 감염병 검사를 |
|
검체 수송용 배지 |
- Virus, Chlamydia, Mycoplasma, & Ureaplasma 등을 포함한 임상 시료를 채취하여 - 바이러스 및 미생물 등이 최고 30℃의 조건에서 5일 이상 생존할 수 있도록 |
질병 및 감염병 검사를 위한 검체 이송용 |
|
| 의약외품 | 알콜스왑 |
- 알콜(에탄올/이소프로필) 액이 침지되어 있는 1회용 부직포 제품 - 피부 및 창상 부위의 소독 및 의료 용구의 소독을 위한 제품 |
창상 및 소독이 필요한 부위의 피부 소독용 |
| 손소독용 제품 |
에탄올(70% 함유) 베이스 투명 겔(gel), 액상(liquid), 티슈(wipes) 제품으로 손, 피부 |
질병 및 감염병 예방을 위한 손 등의 피부 소독용 |
|
| 자료: 당사 반기보고서(2022.06) |
체외진단 의료기기는 혈액, 객담, 타액, 분뇨, 체액, 등 인체로부터 채취한 대상물을 이용하여 몸 밖에서 신속하게 질병 등을 진단하는 기술로써, 임상 의사 결정에 중요한 역할을 하는 시장입니다. 흔히 주변에서 볼 수 있는 혈당측정기나 임신테스트기가대표적인 체외진단기기이며, COVID-19 가 발병한 후 선별진료소 등에서 검사 시 사용되는 검체 채취용 면봉(swab)과 검사 후 검사실로 이동하기 위하여 면봉(swab)을 담아 옮기는 수송배지(VTM)가 이에 해당됩니다.
이러한 체외진단 의료기기는 검사를 위한 검체를 채취하는 도구(Tool), 검사를 위하여 이송하는 배지(Transport Medium), 검사를 위한 시약(Reagent)으로 구분될 수 있으며 시약의 경우 혈액 검사용, 수혈 검사용, 요 또는 분변 검사용, 면역화학 검사용, 임상 미생물 검사용, 분자유전 검사용, 체외진단검사지, 병리검사용, 기타 검사용 시약으로 나눌 수 있습니다. 이러한 체외진단의료기기에 사용되는 제품은 개인 및 공중위해성 판단 기준에 따라 4단계의 등급으로 나누어질 수 있으며 각각의 등급에 따라 국내 식품의약품안전처(KFDA)에 신고 및 허가를 득한 후 제조 및 판매가 가능한 제품입니다.
특히, 혈액, 소변, 타액 등을 이용하여 질병의 진단, 예후, 확진을 하는 체외진단(IVD, In Vitro Diagnostics) 시장은 최근 크게 증가하는 추세입니다. Markets and Markets에서 2020년 발간한 In-Vitro Diagnostics Market, Forecast to 2025에 따르면 2020년 글로벌 체외진단 키트, 시약, 장비 등 전체 제품 시장 규모는 780억 달러이며, 2025년까지 연평균 4.4%씩 성장하여 2023년에는 전체 시장규모가 967억 달러에 달할 것으로 예상되고 있습니다.
| [글로벌 체외진단 시장 규모] |
| (단위: USD million, %) |
|
구분 |
2018 |
2019 |
2020 |
2025(E) |
CAGR |
|---|---|---|---|---|---|
|
시약 & |
52,658 |
56,100 |
60,139 |
76,493 |
4.9% |
|
진단장비 |
12,340 |
12,955 |
13,588 |
15,081 |
2.1% |
|
진단서비스 |
2,393 |
2,522 |
2,670 |
3,178 |
3.5% |
|
데이터 관리 |
1,546 |
1,615 |
1,694 |
1,921 |
2.5% |
|
합계 |
68,936 |
73,192 |
78,091 |
96,672 |
4.4% |
| (자료: In-Vitro Diagnostics Market Global Forecasts 2025, 2020, MarketsandMarkets) |
이처럼 글로벌 체외진단 시장은 다양한 질환 발생 및 이에 따른 진단 수요 증가, 기술의 발전 등으로 인하여 지속적인 성장이 예상되고 있습니다. 그럼에도 불구하고, 당사가 예상하지 못한 체외진단 시장의 트렌드 변화, 체외진단 수요 감소, 판매단가 하락 등으로 인하여 체외진단 시장 성장이 둔화될 경우 당사의 매출에 부정적인 영향을미칠 수 있습니다. 이 점 투자자께서는 유의하시기 바랍니다.
|
라. COVID-19 종식에 따른 제품 매출 감소 위험 |
당사의 헬스케어사업부(舊 ㈜에프에이)는 검체 채취용 도구, 수송용 배지 및 의약외품 등의 생산 및 판매 사업을 영위하고 있습니다. 당사의 2020년, 2021년 및 2022년반기 매출액은 COVID-19 확산에 따라 COVD-19 검체채취키트 수요가 급증하며 증가하였습니다. 추후 백신 및 치료제 추가 보급으로 인해 COVID-19 확산세가 진정된다면, 당사의 주력매출상품인 검체 채취용 도구 및 검체 채취용 배지에 대한 수요가 감소할 가능성이 있습니다. 현재 당사의 2022년 반기 매출구성을 살펴보면 전체매출액의 약 83.07%가 헬스케어 사업부 제품에 집중되어 있으므로, 검체채취도구에 대한 수요가 감소하게 된다면 당사의 수익성에 부정적인 영향을 미칠 수 있습니다.
| [당사의 매출 구성] |
| (단위: 백만원, %) |
| 구 분 | 주요 재화 및 용역 | 2022년 반기 | 2021년 반기 | 2021년 | 2020년 | 2019년 | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 매출액 | 비율(%) | 매출액 | 비율(%) | 매출액 | 비율(%) | 매출액 | 비율(%) | 매출액 | 비율(%) | ||
| 제품매출 | 구명정 외 | 3,559 | 2.89 | 3,706 | 23.23 | 11,747 | 16.82 | 16,496 | 29.36 | 13,135 | 34.19 |
| GRP/GRE PIPE | 2,816 | 2.28 | 5,918 | 37.09 | 9,254 | 13.25 | 19,904 | 35.43 | 14,877 | 38.72 | |
| 체외진단 의료기기 외 | 102,435 | 83.07 | - | 0.00 | 22,105 | 31.66 | - | 0.00 | 13 | 0.03 | |
| 주사기 외 | 2,198 | 1.78 | 3,644 | 22.84 | 7,571 | 10.84 | 7,567 | 13.47 | 8,515 | 22.16 | |
| 수수료매출 | 리보세라닙 중국 로열티 | 3,908 | 3.17 | - | 0.00 | 10,362 | 14.84 | 5,856 | 10.42 | - | 0.00 |
| 상품매출 | DAVIT | 2,124 | 1.72 | - | 0.00 | 3,843 | 5.50 | - | 0.00 | - | 0.00 |
| 수액세트 외 | 5,276 | 4.28 | 305 | 1.91 | 1,455 | 2.08 | 277 | 0.49 | 146 | 0.38 | |
| 기타매출 | 기타 서비스 | 988 | 0.80 | 2,383 | 14.93 | 3,490 | 5.00 | 6,077 | 10.82 | 1,735 | 4.52 |
| 합 계 | 123,305 | 100.00 | 15,957 | 100.00 | 69,826 | 100.00 | 56,177 | 100.00 | 38,421 | 100.00 | |
신종 코로나바이러스감염증(COVID-19)은 2019년 12월 1일 발견된 후 감염 확산세가 전세계로 확대되었으며, 현재까지도 일일 신규 확진자가 지속적으로 발병되고 있습니다. WHO는 2021년 08월 10일 기준 전세계 누적 확진자는 약 5억 9천만명, 사망자는 644만명으로 집계하였습니다.
2020년 12월 백신 접종 시작 후 1년 8개월이 2022년 8월 기준 전세계 일별 확진자수는 평균 90만명 내외를 기록하며 여전히 많은 확진자가 발생하고 있습니다. 다만, Global Market Insight에 따르면, 글로벌 코로나 진단키트시장의 경우 COVID -19 백신 접종률이 높아지고 집단면역이 형성되면서 진단키트 시장의 성장률이 점차 둔화되어 2021년 323억 달러에서 2028년 62억 달러까지 감소할 것으로 전망되었습니다.하지만 COVID-19 팬데믹이 끝나도 COVID-19와 증상이 비슷한 계절성 독감과 구분하기 위한 수요 및 백신 접종 후 중화 항체 생성여부에 대한 진단 등을 위한 진단키트 수요는 있을 것으로 전망되었습니다. 아울러 COVID-19가 계절성 독감과 같이 계절마다 유행할 것으로 업계는 예상함에 따라 COVID-19/Flu 동시진단 제품과 COVID-19의 일상적 진단 프로토콜에 따른 관련 진단 제품의 지속적인 수요 발생이 전망되고 있습니다.
현재 백신이 개발 및 보급중인 상황임에도 불구하고, 증권신고서 제출일 현재 인도, 일본 등 COVID-19 재확산이 계속되고 있고, 국내에서도 n차유행의 위험을 무시할 수 없는 상황입니다. 따라서 당분간 각국의 상황에 따라 전염병에 대응하기 위해 필요한 시간의 차이가 존재할 수 있으며, 국가차원의 수요는 상당기간 지속될 것으로 예상되고 있습니다. 다만, COVID-19 백신의 전세계적인 보급 이후 당사의 검체 채취용 도구 및 검체 채취용 배지에 대한 수요는 크게 감소할 가능성이 있으며, 이 경우당사의 매출실적에 부정적인 영향을 미칠 수 있습니다. 투자자께서는 이에 유의하시어 투자하시기 바랍니다.
③ 제약ㆍ바이오사업 부문
[주요 용어 설명]
|
용 어 |
설 명 |
|---|---|
|
의약품 |
사람, 동물의 질병 진단, 치료, 예방목적으로 사용되는 물품으로 기구,기계 장치가 아닌 것 |
|
바이오의약품 |
사람이나 다른 생물체에서 유래된 세포, 조직, 호르몬 등을 이용해 유전자 재조합 또는 세포 배양기술을 통해 개발한 의약품 |
|
신약 |
화학구조나 본질 조성이 전혀 새로운 신물질의약품 또는 신물질을 유효성분으로함유한 복합제제 의약품 |
|
의료기기 |
사람 또는 동물에게 단독 또는 조합하여 사용되는 기구, 기계, 장치, 재료 또는 이와 유사한 제품으로서 질병의 진단, 치료 또는 예방의 목적으로 사용되거나, 구조 또는 기능의 검사, 대체 또는 변형의 목적으로 사용되는 제품 등을 말함. |
|
FDA |
미국에서 식품과 의약품의 인허가를 주관하는 정부 기관. 1931년 설립되었으며, 의약품의 인허가 및 규제, 화장품, 식품 그리고 의료 기기 등에 대한 허가와 규제를 담당하고 있음. 국내에는 이와 유사한 기관으로 식품의약품안전처가 있음. |
|
파이프라인(Pipeline) |
신약 개발 계획을 뜻하는 말로 주로 연구 개발 단계에 있는 품목을 말함 |
|
마일스톤 |
신약 라이선스 계약은 대부분 마일스톤 방식으로 이루어지며, 계약 체결 후 받는<계약금>, 개발 단계별 성취도에 따라 받는 <단계별 기술료>로 구성됨. 제품 상용화 이후에는 마일스톤과 별개로 판매액 일정비율의 <로열티>를 받음. 마일스톤의 단계별 기술료 세부내역은 치열한 시장 경쟁 상황 등을 고려해 계약 당사자들간 협의에 따라 통상적으로 비공개로 함. ① 확정된 계약금 - 계약 체결 직후 또는 일정기간 내에 받게되는 금액. ② 단계별 기술료 - 전임상 → 임상 → 허가신청 → 허가완료 등 개발 단계별로 성공시에 받게 되는금액. 개발 종료 시점까지 수년에 걸쳐 나누어 받게 되며, 도중에 여건이 나빠지거나 임상에 실패하여 더 이상 개발하지 않을 경우 일정 금액을 받지 못할 수 있음. ③ 로열티 - 기술 이전으로 생산된 제품의 매출에 따라 받게 되는 금액. 대개 로열티는 매출액 대비 비율로 책정되는데, 로열티를 어느 정도로 할 것인가는 당사자의 협의에의하는 문제로서 일률적인 기준은 없음. |
|
IND |
Investigational New Drug Application, 임상시험계획신청, 동물실험에서 의약품의 효과와 독성을 확인한 후에 사람에게 임상시험을 하기위해 진행하는 절차. 의사의 엄중한 감시 아래 투약하고, 여러 단계의 임상을 통해서 유효성과 안전성이 최종 확인되면 NDA 신청하게됨 |
|
NDA |
New Drug Application, 신약허가신청, 연구개발부터 동물시험까지 비임상시험결과와 인체를 대상으로 하는 임상시험결과 및 제조까지를 종합하여 식품의약품안전처에 의약품허가를 신청하는 절차 |
|
세포독성 |
물질이 세포의 효소, 구조를 이루는 성분에 영향을 미쳐 세포를 죽일 수 있는 경우 또는 세포의 염색체나 유전자(즉, DNA)의 변형을 유발하는 것 |
|
안전성 |
신약후보물질이 사람이 복용하였을 때 독성이나 심각한 부작용이 없음을 입증하기 위해 실험동물을 통한 안전성 시험이 필수임. |
|
생물학적 안전성 평가 |
원재료 특성분석, 생물학적 안전성 시험 성적서, 관련 문헌 및 임상 보고 등을 통한 종합적인 생물학적 안전성 평가로, 인체에 접촉되는 모든 의료기기에 적용될 정도로 의료기기의 안전성 확보에 절대적인 영향을 미침 |
|
안정성 |
의약품 또는 의료기기가 실제로 취급되는 상황을 생각하여 빛, 열, 온도, pH 등의영향에 얼마나 안정한가를 알아보는 시험. 약물 또는 화합물이 화학변화를 쉽게 일으키지 않거나 반응속도가 느려 일정 기간동안 일정한 상태를 유지하는 성질 |
|
비임상시험 |
사람을 대상으로 하지 않는 생의학 시험으로 동물에서의 독성과 유효성 시험임 |
|
임상 1상 |
비임상시험(동물을 상대로 한 실험)을 거친 신약을 사람에서 처음으로 평가하는 과정. 비교적 제한된 수의 대상자(약 20-80명)에게 투여되며 약의 종류에 따라 다르지만 대개 건강한 성인을 대상으로 진행함. 안전성을 검토하여 안전용량의 범위를 확인하게 됨. 또한 약물의 체내에서의 흡수, 분포, 대사, 배설에 대한 자료를 수집함 |
|
임상 2상a |
임상시험에 사용되는 의약품의 안전성과 유효성을 증명하기 위하여 해당약물의 약동, 약력, 약리, 임상적 효과를 확인하고 이상반응 등을 평가하기 위하여 사람을 대상으로 실시하는 시험 또는 연구로 사람을 피시험자로 하는 것이기 때문에 윤리적인 배려와 함께 과학적인 방법으로 진행됨 |
|
임상 2상b |
임상 2a의 결과에 따라 설계된 용량을 가지고 다시 환자에 투여, 어느 만큼의 용량이 가장 효과가 있을지 적정 투여 용량의 범위를 정하는 과정 |
|
임상 3상 |
제 2상 임상시험에서 확인된 사항들을 종합적으로 판단하여 유용성이 인정될 때 대상질환 중 조건에 부합되는 다수 환자를 대상으로 효능효과, 용법용량, 사용상의 주의사항 등 전반적인 안전성, 유효성을 확인하여 의약품으로서의 유용성을 결정하는 시험 |
|
마. 바이오산업 성장성 관련 위험 당사는 100%의 지분을 보유한 Elevar 및 41.07%의 지분을 보유한 Immunomic를 통해 제약ㆍ바이오사업을 영위하고 있습니다. 글로벌 제약산업 분석서비스업체인 이벨류에이트파마(EvaluatePharma)사의 최근자료에 따르면, 첨단기술과 헬스케어의 융합이 현실화되고 새로운 치료제가 등장함에 따라 처방의약품(Prescription drug)의 매출은 지속적으로 확대될 것으로 예상하고 있습니다. 전세계 처방의약품의 매출액 연평균 성장률은 2010∼2018년 약 2.3%였으나, 2019∼2024년 약 3배 정도 증가한 6.9%의 성장률이 전망되고 있습니다. 특히 항암제분야의 경우 면역항암(Immuno-oncology) 계열의 확장은 제약산업 성장에 크게기여하며 기존의 세포독성항암제와 표적항암제와의 병용을 바탕으로 치료법의 발전과 더불어 시장을 확대하는데 큰 역할을 하고 있습니다. 특히 주목받는 치료영역으로는 시장 점유율 및 성장률이 높은 Oncology 분야의 지속강세 속에서 새로운 치료제 개발을 위한 연구개발도 활발하게 이루어지고 있습니다. 글로벌 제약시장 중에서 Oncology 분야의 매출 점유율이 가장 높으며(2018년 14.3%), 2024년까지의 성장률도 11.4%로 높은 수준을 예상하고 있으며 이에 따라 암 치료제(처방의약품+일반의약품) 매출은 2018년 1,238억 달러에서 2024년 2,366억 달러로 지속적으로 성장할 전망입니다.그럼에도 전체 제약산업의 환경이 악화되거나 새로운 방식의 의약품 산업이 발전하게 될경우 당사가 속해있는 바이오 의약품 산업의 전망이 악화될 수 있으며, 이는 당사의 사업에 부정적인 영향을 미칠 수 있습니다. |
당사는 100%의 지분을 보유한 연결대상종속회사인 Elevar Therapeutics("Elevar") 및 41.07%의 지분을 보유한 연결대상종속회사인 Immunomic Therapeutics("Immunomic")를 통해 제약ㆍ바이오사업을 영위하고 있습니다. Elevar는 표적항암제 리보세라닙(Rivoceranib, 舊 Apatinib Mesylate) 및 아필리아(Apealea) 관련 라이센스 인(License-in) 계약을 체결하였으며, Immunomic의 경우 암, 알레르기 등 질환에 대한 핵산 면역치료 플랫폼(nucleic acid immunotherapy platforms)을 연구개발하고 있습니다.
의약품은 크게, 반드시 전문의의 진단 및 처방이 요구되는 전문의약품과 진료 없이 일반인이 접근할 수 있는 일반의약품으로 나눌 수 있습니다. 일반의약품의 경우에는 날씨 및 기후 등 외부요인에 의한 계절적인 영향을 다소 받는 편이지만, 전문의약품은 환자의 선택권한이 제한되며 경기변동에 따라 치료를 중단하는 등의 일들이 일어나지 않으므로 변동이 크지않아 제약산업 전반적으로 안정적인 성장을 유지해 오고 있습니다. 당사의 100% 지분을 보유한 연결대상종속회사인 Elevar Therapeutics("Elevar") 및 41.07%의 지분을 보유한 연결대상종속회사인 Immunomic Therapeutics("Immunomic")에서 개발하고 있는 항암제, 알레르기와 같은 전문의약품의 가격 탄력성은 장기와 단기 모두 비탄력적인 특성을 보여줘, 신약이 출시 될 경우 안정적인 성장이 가능합니다.
글로벌 제약산업 분석서비스업체인 이벨류에이트파마(EvaluatePharma)사의 최근자료에 따르면, 첨단기술과 헬스케어의 융합이 현실화되고 새로운 치료제가 등장함에 따라 처방의약품(Prescription drug)의 매출은 지속적으로 확대될 것으로 예상하고 있습니다. 글로벌 처방의약품 매출액은 2012년부터 2019년까지 매출액 연평균 성장률 2.7%였으나, 희귀의약품 시장의 급성장과 혁신적 의약품 승인에 힘입어 2020년 9,040억 달러에서 연평균 7.4% 성장하여 2026년 1조 3,903억 달러가 될 것으로 전망하고 있습니다.특히, 코로나19 유행으로 헬스케어 전반에 단기적인 이슈가 있었으나, 혁신적이고 효과적인 치료법에 대한 산업 전반의 수요가 있어 산업의 성장을 견인할 것으로 전망하고 있습니다.
| [글로벌 처방의약품 매출액 추이] |
|
| 자료: EvaluatePharma, World Preview 2020. Outlook 2026 |
그 중에서도, 주목받는 치료영역으로는 시장 점유율 및 성장률이 높은 Oncology 분야의 지속강세 속에서 새로운 치료제 개발을 위한 연구개발도 활발하게 이루어지고 있습니다. 특히 항암제분야의 경우 면역항암(Immuno-oncology) 계열의 확장은 제약산업 성장에 크게기여하며 기존의 세포독성항암제와 표적항암제와의 병용을 바탕으로 치료법의 발전과 더불어 시장을 확대하는데 큰 역할을 하고 있습니다. 글로벌 제약시장 중에서 Oncology 분야의 매출 점유율이 가장 높으며(2018년 14.3%), 2024년까지의 성장률도 11.4%로 높은 수준을 예상하고 있으며 이에 따라 암 치료제(처방의약품+일반의약품) 매출은 2018년 1,238억 달러에서 2024년 2,366억 달러로 지속적으로 성장할 전망입니다.
| [글로벌 항암제 신약 개발 현황] |
|
| 자료: IQVIA Institue. Apr 2022. |
그럼에도 전체 제약산업의 환경이 악화되거나 새로운 방식의 의약품 산업이 발전하게 될 경우 당사가 속해있는 바이오 의약품 산업의 전망이 악화될 수 있으며, 이는 당사의 사업에 부정적인 영향을 미칠 수 있습니다.
|
바. 임상시험 실패 및 지연에 따른 위험 |
신약(New Drug)은 기존 약물에 모방이나 개량 합성에 의한 것이 아닌, 기존약물의 부작용과 현저한 기능 개선이 포함되어야 하며, 화학합성, 미생물·배양조직세포로부터 유전자재조합을 이용한 생산, 천연물 추출 등의 신물질 탐색 작업, 비임상시험, 임상시험 등을 거쳐 제조 승인을 받은 의약품 입니다. 신약개발 시 한국(식품의약품안전처) 및 미국(FDA)의 주요 과정 및 위험요인은 아래와 같습니다.
1. 한국(식품의약품안전처)
| [신약개발 R&D과정] |
|
| 자료: 식품의약품안전처 의약품통합정보시스템 |
신약개발의 과정은 발견단계(Discovery)와 개발단계(Development)로 구분하고 있습니다. 일반적으로 발견단계는 질병타겟을 정하고, 동물시험 등을 거쳐 신약후보물질을 도출하는 단계이며, 개발단계에서 사람에서의 안전성과 유효성을 확인하는 임상시험을 실시하는 단계입니다.
발견단계는 치료가능성이 있는 질병원인과 타겟을 규명 선택한 후, 이에 작용하여 기대하는 치료효과를 발휘할 수 있는 새로운 물질(molecule)을 만들거나 기존에 만들거나 수집된 분자 중에 선택하고 구조변경 등 최적화(optimization)하여 신약후보물질(newdrug candidate)을 선정하는 단계입니다. 이 후보물질은 광범위한 동물이나 실험적으로 안전성과 유효성을 시험하여 사람에게 임상시험을 실시해도 안전하며 유효한지를 결정합니다.
개발단계에서 실시되는 임상시험은 사람에게 사용되는 만큼 안전성과 윤리성이 보장되어야 하기 때문에 임상시험을 실시하기전에 식약처로부터 임상시험계획에 대한 승인을 받아야합니다. 임상시험에 대한 구분은 약사법 시행규칙에서 정의하고 있으며, "임상시험"이라 함은 의약품의 안정성과 유효성을 증명하기 위하여 사람을 대상으로 해당 약물의 약동ㆍ약력ㆍ약리ㆍ임상적 효과를 확인하고 이상반응을 조사하는 시험을 말합니다. 임상시험은 시판 허가 전의 3단계(1상, 2상, 3상)와 시판 후 임상시험(PMS)을 포함하여 총 4단계로 구분합니다. 각 임상 단계별 주요 내용은 아래와 같습니다.
| [임상시험 구분] |
| 구분 | 목적 | 내용 |
|---|---|---|
| Phase 1 (1상) |
ㆍ안전성 검토 ㆍ내약성 평가 ㆍPK/PD 정의/서술 ㆍ치료효과 추정 |
ㆍ용량-내약성 임상시험 ㆍ안전용량 범위와 부작용 확인 ㆍ체내 약물 동태 검토 ㆍ1a: SAD, 1b: MAD |
| Phase 2 (2상) |
ㆍ단기 유효성/안전성 검토 ㆍ목표 적응증에 대한 탐구 ㆍ후속 시험을 위한 용량 추정 ㆍ치료확증 시험을 위한 시험설계, 평가항목, 평가방법에 대한 근거 제공 |
ㆍ용량-반응 탐색 임상시험 ㆍ소수의 환자에서의 비교적 단기간에 걸친 초기 임상시험 ㆍ2a: 약효확인, 유효용량 검토 ㆍ2b: 약효입증, 유효용량 확인, 유효성 및 안전성의 균형 검토 |
| Phase 3 (3상) |
ㆍ안전성, 유효성 재확인 ㆍ임상적용을 위한 Risk/Benefit의 상대평가 근거제공 ㆍ용량과 반응에 대한 관계 확립 ㆍ효과에 대한 검증 |
ㆍ무작위 배정에 의한 용량-반응 임상시험 ㆍ유효성 확립을 위한 적절하고 잘 통제된 임상시험 ㆍ이환율/사망률을 위한 임상시험 ㆍ충분한 환자에서 유효성 및 안전성 확립 ㆍ대조군을 이용한 비교 임상시험 ㆍ대규모 임상시험 |
| Phase 4 (4상, PMS) |
ㆍ시판 후 안전성 조사 및 추가 임상시험 ㆍ일반 또는 특정 대상군/환경에서 Risk/Benefit에 대한 이해 ㆍ흔하지 않은 이상반응 확인 ㆍ추천되는 용량을 확인 ㆍ모든 시험 디자인이 가능 |
ㆍ장기투여시 부작용 검토 ㆍ안전성 재확립 ㆍ새로운 적응증 등 탐색 연구 ㆍ대조군을 이용한 유효성 임상시험 ㆍ이환율/사망률에 대한 임상시험 ㆍ부가적인 평가 항목에 대한 임상시험 ㆍ약물경제학적 측면의 임상시험 |
| 주1) 약물의 농도-반응 관계를 PK/PD라고 합니다. PK(Pharmacokinetics 약동학)는 약물의 흡수, 분포, 생체 내 변화 및 배설을 연구합니다. PD(Pharmacodynamics 약력학)는 생체에 대한 약물의 생리학적 및 생화학적 작용과 그 작용 기전, 즉 약물이 일으키는 생체의 반응을 주로 연구함 주2) SAD(단회용량상승, single ascending dose) : 단회용량을 투여한 후 안전성과 내약성을 확인함 주3) MAD(다중용량 상승, multiple ascending dose) : 반복 투여를 통해 더 높은 용량으로 증량해가면서 최대 내약 용량을 확인함 |
(가) 제1상
임상시험은 소규모(약 20명에서 100명)에게 투여되며 약의 종류에 따라 다르지만 대게 건강한 성인을 대상으로 시험하는 단계로서 의약품이 사람에게서 안전한지 여부를 확인하는 것을 목적으로 실시합니다.
(나) 제2상
임상시험은 임상시험용 의약품이 기대된 작용기전(mechanism)에 따라 작용되는지 검토하고, 의약품을 사용에 있어서 최적 용량(dose strength)과 투약방법(schedules)을 분석합니다.
(다) 제3상
제3상 임상시험은 대규모 환자를 대상으로 하는 시험으로 연구자는 후보의약품의 안전성과 유효성 및 전체적인 benefit-risk 관계에 대한 통계학적으로 유의한 데이터(significant data)를 만들기 위해서 약 1,000명에서 5,000명의 환자를 대상으로 연구가 실시됩니다. 이 단계는 의약품으로서 안전성과 유효성 여부결정의 핵심단계로서 적정한 의약품 사용을 보증하기 위한 다른 의약품과 상호작용 정보 등 표시사항의 기초가 되며, 임상시험동안 실생산 규모의 생산계획, 식약청에 품목허가를 받기 위해 필요하고 복잡한 서류준비 등을 위한 품질등에 관한 중요한 연구가 많이 수행됩니다. 유효물질 수준에서 5,000개에서 10,000개의 화합물이 연구개발(R&D)의 파이프라인으로 들어가지만 전임상단계에서 약 250개의 연구를 거쳐 결국 1개의 승인을 받게 됩니다. 이러한 신약개발 과정을 거쳐 환자가 이용할 수 있을 때까지 소요되는 기간과 비용은 약 10년~15년의 연구개발기간과 비용은 800백만달러에서 13억달러($1.3 billion)이상으로 추정하고 있습니다(식품의약품안전처 의약품통합정보시스템).
개발사들은 앞 단계의 연구에서 위험(독성) 대비 이익(유효성)이 충분하다고 판단될 때 다음 단계 임상시험의 진입을 결정하게 되며, 약사법에 따라 적합한 임상시험계획승인(IND) 신청 자료를 마련하여 규제기관의 심사를 받게 됩니다. 규제기관은 위험 대비 이익이 허용 가능하다고 판단되면 임상시험계획(IND) 승인을 해주며, 개발사는승인된 계획서와 의약품임상시험관리규정을 준수하여 임상시험을 실시하게 됩니다.
임상시험계획서에서 설정한 목표를 임상시험을 통해 입증했을 때 임상시험이 성공한것이며, 다음 단계 연구로 나아갈 수 있고, 목표를 입증하지 못하면 임상시험에 실패하게 됩니다. 임상시험의 목표는 단계별 목적과 질환별 치료목적에 따라 설정하며, 통계적 유의성 입증을 위한 대상자 수와 평가방법을 계획서에 명시해야 하며, 시험 진행 도중에 이러한 사항을 변경하기는 어렵습니다. 회사는 임상시험을 위해 자금과 시간을 투자해야 하기 때문에 다음 단계 임상시험로 진입여부를 결정할 때 성공 가능성에 대한 면밀한 검토를 하지만, 임상의 단계가 올라갈수록 대상자 조건이 다양해지고 관찰기간이 길어지기 때문에 앞단계에서 확인하지 못했던 결과가 나타날 수 있습니다.
1~3상 임상시험은 시험기관윤리위원회 심의 시 임상시험배상책임보험에 의무적으로 가입하도록 되어 있으며, 해당 보험을 통하여 시험 중 개발중인 약으로 인한 부작용 발생 시 대상자에게 적절한 배상을 하게 됩니다.
| [의약품 분류별 단계별 임상통과 확률 및 소요기간] |
|
구분 |
임상1상에서 |
임상2상에서 |
임상3상에서 |
승인신청서 |
임상1부터 |
|---|---|---|---|---|---|
|
합성의약품 |
61% |
26% |
49% |
78% |
6.2% |
|
바이오의약품 |
66% |
34% |
57% |
88% |
11.5% |
|
개량신약 |
70% |
48% |
74% |
90% |
22.6% |
|
소요기간 |
1.5년 |
2년 |
3년 |
0.5년 |
7년 |
| 자료: 생명공학정책연구센터 "의약품 유형별(합성, 바이오) 개발 특성", 한국바이오경제연구센터 "글로벌 제약시장 임상 파이프라인 분석" |
2018년 3월 발표된 생명공학정책연구센터의 보고서에 따르면 임상 1상에서부터 신약승인까지의 성공률은 바이오의약품의 경우 11.5%로 확인되었습니다. 단계별로 비임상 약 8년, 임상 6.5년, 허가 검토에 약 0.5년 정도의 시간이 필요합니다. 한국바이오경제연구센터에서는 임상1부터 승인까지 대략 7년의 시간이 소요된다는 결과를 나타냈습니다. 임상 1상 단계에 있는 신약 파이프라인 10개 중 1개 정도만이 최종적으로 품목허가를 받아 시장에 출시되는 것입니다. 또한 전임상 단계에서 안전성 및 효능이 검증되었음에도 불구하고 각 임상 단계에서 부작용 등 예상치 못한 결과로 인하여 의약품 개발에 실패할 위험이 상존합니다.
2. 미국(FDA)
FDA(Food and Drug Administration)는 미국의 식품의약국으로 미국에서 생산 및 유통, 판매되는 모든 종류의 의약품에서부터 의료기기, 화장품, 식품 등의 품목에 대 해 통제, 관리, 승인을 하는 기관입니다. FDA는 의약품 등에 대해 전세계에서 가장 엄격하고 신중하게 관리 및 승인하는 기관으로 FDA 에서 승인된 신약은 매우 안전 하고 뛰어난 약효를 가진 신약으로 인정을 받기 때문에 사실상 전세계 어디에서나 특별한 절차 없이 출시가 가능하게 됩니다.
FDA에서의 임상 단계별 성공 가능성을 추정하기 위해서, 2006년부터 2015년까지 과거 10년간 FDA에서 임상을 수행했거나 진행중인 자료를 조사해보면 여러 특징적인 사실들이 보여집니다. 모든 임상들에 대해 임상 1상에서 신약승인까지의 신약 승인 성공률은 평균 9.6%입니다. 임상 1상 통과 가능성은 63.2%이고, 임상 2상은 각 임상 단계별로 가장 낮은 30.7%입니다. 임상 3상은 58.1%이고, 신약 승인 단계 인 NDA/BLA는 가장 높은 85.3%로 나타나고 있습니다.
| [FDA 임상 시 각 단계별 성공 가능성] |
|
| 자료: FDA, Amplion, Biomedtracker, Biotechnology Innovation Organization, SK증권 주1) NDA - New Drug Application , 합성 의약품의 신약승인 단계 주2) BLA- Biologic License Application, 바이오 의약품의 신약승인 단계 |
3. 임상시험 지연 현황
상기의 신약개발은 코로나 19에 따른 전 세계적 팬데믹으로 악영향을 받는 것으로 파악되고 있으며, 특히 임상시험 건수의 감소 등에 따라 신약개발이 지연되는 상황이발생하고 있습니다. 메디데이터에 따르면, 2019년 10월을 COVID-19 이전 베이스라인으로 볼 때, 전 세계적으로 2020년 6월 말 기준 신규 임상시험 참여 시험대상자 수가 약 30% 감소하였으며, 2020년 4월 기준으로는 전 세계적으로 약 70%의 감소가 나타나고 있습니다.
| [시험기관 신규 참여 시험대상자 현황: 전 세계 vs 미국 vs 중국] |
|
| 자료: medidata, '메디데이터가 바라보는 COVID-19와 임상시험(2020.07.13)' |
상기 영향에 따라, 일부 대형 제약회사(Pfizer, Bristol Myers Squibb 및 Eli Lilly) 와 소규모 생명공학 회사(Moderna Therapeutics , Iveric Bio , Aslan , Provention Bio 및 Addex )들은 자사의 R&D 계획을 수정하고 있다고 공개 발표했습니다. R&D 계획수정에는 시험기관 활성화 및/또는 시험대상자 등록을 일시적으로 연기하는 것 등이포함됩니다. 실제로, Aveo Pharmaceuticals Inc.가 급성 골수성 백혈병 대상자 대상 ficlatuzumab 시험 실패의 이유를 COVID-19로 언급했듯이, COVID-19가 임상시험의 성공에 미치는 영향은 이미 중요한 이슈가 되었습니다. COVID-19 팬데믹으로 인한 영향 및 비용 부담을 줄이기 위해 바이오 제약사들이 임상시험을 연기 또는 중단하는 사례는 점차 증가하고 있습니다.
시험기관에 대한 팬데믹의 영향은 2020년 4월 말 메디데이터가 1,000곳이 넘는 시험기관의 담당자를 대상으로 실시한 설문조사에서도 확인되고 있습니다. 대부분의 시험기관이 현재 및 향후 임상시험, 특히 시험대상자의 등록 및 모집 지연과 관련해 팬데믹의 부정적인 영향을 느끼고 있는 것이 분명하게 나타났으며, 시험기관들은 또한 임상시험 지연 및 취소에 의한 재정적인 문제도 우려하고 있습니다. 응답자의 2/3 이상이 현재 진행 중인 임상시험의 대상자 모집을 중단했거나 곧 중단할 것이라고 했으며, 1/3은 무작위배정을 중단하고 있다고 했습니다. 응답자의 약 절반 가량은 현재 시험이 지연되고 있거나 지연될 것이라고 답했습니다.
2021년 2월 기준, 데이터 및 분석업체인 글로벌데이터에 따르면 전세계적으로 1,200건이 넘는 임상시험이 코로나19로 인해 지장을 받고 있으며, 특히 항암제 등 종양 관련 임상시험에 큰 영향을 받고 있어 COVID-19가 임상시험의 지연 등 끼치는 악영향이 지속되고 있는 상황입니다.
국내의 경우, 대한의학회지에 실린 논문(전주연, 김혜경, 유경상, 2020. The Impact of COVID-19 on the Conduct of Clinical Trials for Medical Products in Korea, 대한의학회지)에 따르면 국내 상위25개 제약사 중 절반 이상인 13개 제약사가 코로나19로 인해 임상시험 수행에 어려움을 겪는다고 답한 바 있으며, 특히 코로나19로 인해임상 site를 확보하기 어려운 점, 임상 환자가 내원하여 임상을 진행하기 어려운 점 등을 주요 요인으로 꼽았습니다.
종합적으로, COVID-19의 확산세가 지속될 경우 임상시험의 연기 혹은 중단 등 임상시험 지연에 따라 부정적인 영향이 발생하고 있으며, 이는 상기 한국 및 미국의 신약개발 단계에 악영향을 끼칠 수 있습니다. 또한 COVID-19 외, 여타 예상하지 못한 변수가 발생할 시 임상시험을 지연시키는 추가적인 요인으로 작용할 수 있습니다.
4. 당사의 신약개발 현황
당사는 100% 지분을 보유한 연결대상 종속회사인 Elevar, 41.07% 지분을 보유한 연결대상 종속회사인 Immunomic을 포함해 제약ㆍ바이오 사업을 영위하고 있습니다. Elevar는 2개의 항암 신약물질((1) Rivoceranib("리보세라닙", 舊, Apatinib Mesylate)및 (2) Apealea("아필리아")에 대해 라이센스를 취득하는 계약을 체결하였습니다. Elevar는 리보세라닙에 대하여 중국, 한국을 제외한 글로벌 전용실시권을 보유하고 있으며(한국판권은 에이치엘비생명과학㈜가 보유함), 아필리아에 대하여 러시아연방, 스칸디나비아반도국을 제외한 글로벌 전용실시권을 보유하고 있습니다.
| [연구개발 진행 총괄표] |
| 구 분 | 품 목 | 적응증 | 임상시작일 | 현재 진행단계 | 기 타 | 임상주도기업 | 비고 | ||
|---|---|---|---|---|---|---|---|---|---|
| 단계(국가) | 승인일 | ||||||||
| 화학합성 의약품 |
신약 | 리보세라닙 (HLB생명과학 주도 임상 포함) |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안전성평가 완료 | Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
| 위암 (3차 단일요법) |
2017년 | 임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 | |||
| 간암 (1차 병용요법) [Combo with Camrelizumab] |
2019년 | 임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
임상 진행 중 9월 초록 발표 (1차 평가 지표 만족) |
Elevar | 항서제약과 공동개발 | |||
| 선양낭성암종 (1/2차 단일요법) |
2020년 | 임상2상 (한국, 미국) |
2020년 4월 (임상2상 개시일) |
임상 2상 진행중 6월 초록 발표 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 | |||
| 위암 (2차 병용요법) [Combo with Paclitaxel] |
2018년 | 임상1/2a상 (한국, 미국) |
2018년 10월 (임상1상 개시일) |
임상1상 종료 후, 2a상 준비 중 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 | |||
| 대장암 (3차 병용요법) [Combo with Lonsurf] |
2019년 | 임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 진행 중 | Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 | |||
| 황반변성치료제 (점안액) |
2018년 | 비임상 단계 | - | 타당성분석 중 | HLB 생명과학 |
HLB생명과학이 Rivoceranib 한국 내 전용실시권 L/I 후 자체 개발 | |||
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상진입 준비 중 (농림축산검역본부) |
HLB 생명과학 |
HLB생명과학이 Rivoceranib 한국 내 전용실시권 L/I 후 자체 개발 | |||
| 위암 (1차 병용요법) [Combo with Camrelizumab] |
2021년 | 임상2상 (한국) |
2021년 09월 (임상2상 개시일) |
임상 진행 중 | HLB 생명과학 |
HLB생명과학이 Rivoceranib 한국 내 전용실시권 L/I 후 개발 | |||
| 아필리아 | 난소암 2차 (백금계 약물 감수성) |
2018년 (유럽EMA 허가) |
유럽 허가 | 유럽 판매 준비 중 | Elevar | Elevar가 Apealea의 글로벌 (일부국가 제외) 전용실시권을 L/I 후 판매 준비 중 | |||
| 바이오 의약품 |
IMMUNOMIC THERAPEUTICS ITI-1000 |
GBM | 2016년 | 임상 2상 (미국) |
2016년 8월 (임상 2상 개시일) |
임상 진행 중 | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
|
| IMMUNOMIC THERAPEUTICS ITI-1001 |
GBM | - | 비임상 단계 | - | 임상 1상 IND 준비 중 | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| IMMUNOMIC THERAPEUTICS ITI-3000 |
Merkel Cell Carcinoma | 2022년 | 임상 1상 (미국) |
2022년 02월 (임상 1상 개시일) |
임상 진행 중 | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| IMMUNOMIC THERAPEUTICS ITI-8000 |
NSCLC | - | 비임상 단계 | - | - | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| IMMUNOMIC THERAPEUTICS ITI-9001 |
JRC Pollinosis | - | 비임상 단계 | - | - | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| 주) 통상적으로 통계적으로 유효성을 만족하는 수준의 임상데이터 수집이 완료되면 임상 결과를 발표하나, 이는 임상의 완전한 종료를 뜻하는 바는 아닙니다. 모든 임상 참여 환자의 데이터가 축적된 후 임상결과보고서(CSR) 작성이 완료되면 공식적으로 임상시험이 종료됩니다. |
(가) : 리보세라닙
| 구 분 | 화학합성의약품 | ||||||||||||||||||||||||||||||
| 적응증 | 위암 3/4차 치료제(Rivoceranib 단독)위암 2차 치료제(파클리탁셀 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독), 간암 1차 치료제(항서제약 캄렐리주맙 병용), 대장암(타이호제약 론서프 병용)3차 치료제 | ||||||||||||||||||||||||||||||
| 작용기전 | 신생혈관억제, VEGFR2-TKI | ||||||||||||||||||||||||||||||
| 제품의특성 | 혈관내피세포성장인자수용체2(VEGFR-2)를 타켓으로 암 조직의 신생혈관 성장을 억제하고, 암세포의 증식억제와 면역세포의 정상화를 유도하는 경구용 표적 항암제입니다. | ||||||||||||||||||||||||||||||
| 진행경과 |
위암 3/4차 치료제: 단독 요법으로 글로벌 임상 3상 후 미국 NDA 신청 준비 중
|
||||||||||||||||||||||||||||||
| 향후계획 | 위암 3/4차 치료제(Rivoceranib 단독) 미국 FDA pre-NDA 진행, FDA에서 요청한 보완 자료 준비 중, 자료 보완 후 NDA 제출 예정 위암 2차 치료제(파클리탁셀 병용) 임상 1상 결과 분석 선양낭성암 1,2차 치료제(Rivoceranib 단독)1,2차 치료제: 임상 2상 결과 수집 및 분석 간암 1차 치료제(항서제약 캄렐리주맙 병용): 임상 3상 결과 수집, 분석 및 Pre-NDA 준비 대장암 3차 치료제(타이호제약 론서프 병용) : 임상 1상 결과 수집 및 분석 |
||||||||||||||||||||||||||||||
| 경쟁제품 | 위암 3차 치료제: 론서프, 옵디보(한국, 일본, 대만 한정) 위암 2차 치료제: 시람자(cyramza), 파클리탁셀 선양낭성암 1,2차 치료제: 표준치료제 없음 (Off-label)로 치료 진행 간암 1차 치료제: 넥사바, 렌비마, 아바스틴, 티센트릭 대장암 3차 치료제: 론서프, 스티바가, 옵디보 |
||||||||||||||||||||||||||||||
| 관련논문등 |
위암
|
||||||||||||||||||||||||||||||
| 시장규모 |
위암 치료제 글로벌 시장: 2021년 28억8000만 달러에서 2025년에는 31억1000만 달러로 성장 예상 선낭암 치료제 글로벌 시장: 표준치료제가 없고 발병률이 낮아 글로벌 시장 규모 추산이 어려움 간암 치료제 글로벌 시장: 2020년 20억3750만 달러에서 2027년 27억7571만 달러로 성장 예상 대장암 치료제 글로벌 시장: 2018년 92억6000만 달러에서 2026년 165억8000만 달러로 성장 예상 ※시장규모 관련 출처 |
||||||||||||||||||||||||||||||
| 기타사항 | 특허 및 권리 보유 현황 - 리보세라닙의 물질특허: HLB - 글로벌 전용실시권은: Elevar - 한국 전용실시권: HLB생명과학 - 중국 전용실시권: 중국 항서제약이 보유 항서제약에서 2014년 위암 3차 치료제(Rivoceranib 단독)로 중국 내 시판허가를 득한 후 현재까지 꾸준한 매출 성장 유지 중입니다. 2015년 매출 약 450억에서 2018년 2,800억까지 매출 성장을 보여줘, 약효와 안전성을 입증하였습니다. 2021년 부터 간암 2차 치료제로 적응증을 확대하여, 중국 내 매출 확대가 기대 됩니다. |
(나) : 아필리아
| 구 분 | 화학합성의약품 |
| 적응증 | 백금계 약물 감수성이 있는 난소암 2차 치료제 |
| 작용기전 | 세포 분열에 필요한 RNA나 DNA 등을 손상시켜 세포 분열을 저지하는 세포 주기 선택적 항암제 |
| 제품의특성 | 파클리탁셀은 세포분열 과정 중 분열과 자가 복제의 기구인 미세소관이 분리되는 과정을 방해하는 "식물성 알칼로이드"로 분류되는 항암제입니다. 중증 과민반응 발현을 최소화하기 위해 투여 전에 전치료를 받아야 합니다. Apealea는 특허 출원된 Micelle 코팅을 적용하여 사전처치 필요없이 편의성을 증대시키며 부작용을 줄일 수 있도록 개발한 첨가제 형태 기반의 최적의 파크리탁셀 혼합제입니다. |
| 진행경과 | 유럽, 남미, 중동 지역 판매 준비 중 백금계 약물 저항성이 있는 난소암 환자 대상 임상 1상, 3상 동시 준비 중 |
| 향후계획 | -기 승인 받은 지역 대상 판매 준비 유럽, 중동, 북아프리카, 남미 지역 대상으로 판매 절차 진행 중 중국 진출을 위해 중국 현지업체와 JV를 통한 논의 중 -추가 적응증 개발 백금계 약물 저항성이 있는 난소암 환자를 대상으로 Rivoceranib과 병용 임상 계획 검토 중 |
| 경쟁제품 | 카보플라틴, 시스플라틴, 파클리탁셀, 아바스틴 |
| 관련논문등 | A randomized phase III trial in patients with recurrent platinum sensitive ovarian cancer comparing efficacy and safety of paclitaxel micellar and Cremophor EL-paclitaxel |
| 시장규모 | 글로벌 난소암 시장은 2021년 1억 7,500만달러 규모였으며, 2028년까지 매년 9.5% 성장하여 약 3억 3,973만달러에 이를 것으로 예상 ※시장규모 관련 출처 - Market Research Guru "Global Ovarian Cancer Market Research Report 2022" (2022.07) |
| 기타사항 | -특허 및 권리 보유 현황 Apealea 글로벌 전용실시권: Elevar (북유럽, 동유럽 일부국가 제외) -판매 승인 현황 2020년 유럽 EMA로 부터 난소암 2차 치료제로 판매 승인 (carboplatin 병용) 2022년 내 유럽 내 판매 개시 목표 |
(다) : ITI
| 구 분 | 바이오의약품 |
| 적응증 | GBM (교모세포종) |
| 작용기전 | UNITE 플랫폼은 리소좀관련막단백질(LAMP)에 특정 암에 발현되는 항원을 탑재해 면역세포를 빠르고 효율적으로 활성화시키는 기전 |
| 제품의특성 | 기존 기술 대비 CD4+ Helper T 세포 활성화에 가장 효과적 동일 APC 세포 내 MHC I & II Mediated Pathway 를 동시에 활성화 가능 (MHC II Pathway 직접적으로 관여) 다양한 질환 분야에 적용 가능 (암, 감염 질환, 자가면역 질환 등) 세포 기반 치료제, 핵산 (Nucleic Acid, DNA/RNA) 기반 치료제 개발 등 다양한 기술에 적용 가능 |
| 진행경과 | ITI-1000 교모세포종 (Dendritic Cell vaccine): 임상 2상 진행 중 ITI-1001교모세포종(DNA vaccine): 1상 IND 승인 후 임상 진행 중 ITI-3000 메르켈세포암(DNA vaccine): 1상 IND 승인 후 임상 진행 중 |
| 향후계획 | ITI-1000 연내 임상 2상 종료 후, FDA와 협의를 통해 조건부 허가 추진 |
| 경쟁제품 | 교모세포종: 테모졸로마이드 (2003년 승인) |
| 관련논문등 | 2009 Gene Therapy 16 2015 Nature 2017 Clinical Cancer Reserch 23(8) |
| 시장규모 | 글로벌 교모세포종 시장은 2021년 약 22억 9천만 달러에서 2028년 약 42억 달러에 이를 것으로 예상됩니다. ※시장규모 관련 출처 - Grand View Reserach "Glioblastoma Multiforme Treatment Market Size, Share & Trends Analysis Report By Treatment (Radiation Therapy, Immunotherapy), By Drug Class, By End Use, By Region, And Segment Forecasts, 2021 - 2028" (2021.09) |
| 기타사항 | 현재 교모세포종 원발성 악성 뇌종양 중 가장 흔한 종양으로 진단 후 치료를 하지 않으면 3-6개월 내에 사망합니다. 현재 치료법이 제한적이고 5년 생존율이 5%미만으로 악성도가 높은 질환입니다. ITI-1000 교모세포종 임상 1상 시험에서 mOS을 38.3 개월로 크게 개선하였으며, 표준치료제로 알려진 TMZ/RT 요법 대비 23 개월 이상 생존 기간을 향상시키고 60개월 생존율 또한 36.4%로 증가해 임상 2상 결과 또한 기대하고 있음. |
Elevar는 리보세라닙 위암 말기 단독치료제를 목적으로 하는 3상 임상시험 완료 후 데이터를 확정하여 2019년 10월 미국 FDA와 Pre-NDA 미팅을 하였으며, 그 결과를바탕으로 최종 Data분석 및 적절한 허가 전략을 수립한 후, 신약허가를 신청할 계획입니다. 선양낭성암 1,2차 치료제(Rivoceranib 단독)은 2022년 6월 미국종양학회(ASCO)에서 임상 데이터를 공개했고, 표준치료제가 없는 희귀암종의 이점을 살려FDA의 가속승인(조건부판매)를 목표로 전략을 수립하고 있습니다. 그리고, 2022년 5월 통계적 유의성을 확보했다고 이미 밝힌 바 있는 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 3상 임상은 2022년 8월 미국 FDA에 Pre-NDA를 신청했고, 최근 2022년 9월 ESMO(유럽종양학회)에서 데이터를 공개해 1차 평가지표를 만족했음을 밝혔습니다. 통상적으로 임상 결과의 유효성을 입증하는 1차 평가지표는 적응증, 치료방식, 대조군 등에 따라 다르게 이루어집니다. 당사가 진행한 간암 1차 치료제 글로벌 3상 임상(항서제약 캄렐리주맙 병용)의 경우 기존 1차 치료제인 소라페닙을 대조군으로 하여 OS와 PFS를 1차 평가지표로 하여 진행되었습니다. mOS의 경우 대조군인 소라페닙 대비 6.9개월 긴 22.1개월을 기록했고, mPFS는 대조군 대비 1.9개월 증가한 5.6개월을 기록해(통계적 유의성 확보) 1차 평가지표의 유효성을 만족했습니다.
| [간암 1차 치료제 글로벌 임상 3상 주요 결과] |
| 주요 평가지표 | Rivoceranib + Camrelizumab |
Sorafenib (대조군) |
p-value | HR |
|---|---|---|---|---|
| mOS | 22.1개월 | 15.2개월 | < 0.0001 | 0.62 |
| mPFS | 5.6개월 | 3.7개월 | < 0.0001 | 0.52 |
| ORR | 25.40% | 5.90% | < 0.0001 | - |
| DCR | 78.30% | 53.90% | - | - |
| CR | 3명 | 1명 | - | - |
회사는 본 임상결과를 바탕으로 FDA와의 Pre-NDA미팅 준비 등 후속 개발에 박차를 가하고 있습니다. 앞서 언급한 위암 3차 치료제(Rivoceranib 단독), 간암 1차 치료제(항서제약 캄렐리주맙 병용), 선양낭성암 1차 치료제 모두 희귀의약품에 지정되어 있어 임상종료 후 개별 국 진입 시 시판허가에 대한 신속화, 수수료 감면 등의 혜택과 더불어 신약 허가를 득할 경우 그 이후 최소 8년에서 최대 13년동안 독점 판매할 수 있습니다.이와 관련해 리보세라닙이 희귀의약품으로 지정 받은 내역은 아래와 같습니다. 위암(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국), 간암 (2021년 11월 미국식품의약국), 선양낭성암 (2021년 2월 미국식품의약국) 특히, 리보세라닙은 현재 위암 3차 치료제와 간암 2차 치료제에 대해서는 중국에서 항서제약이 임상 3상을 종료 후 시판허가를 득하여 현재 중국에서 판매되고 있습니다.
아필리아의 경우 2020년 3월 아필리아(Apealea) 라이센스를 스웨덴 비베스토(Vivesto, 舊 Oasmia)로부터 러시아, 북유럽과 동유럽 일부 국가를 제외한 세계 판권을 취득하였습니다. 아필리아는 파클리탁셀(paclitaxel)의 3세대 개량 신약으로 비베스토의 독점 기술 플랫폼인 'XR17'을 사용하여 개발된 항암제로, 주입전에 사전 처치가 필요가 없고, 주사제 주입 시간이 짧아 환자의 편의성을 증대시키면서 부작용을 최소화했습니다. 유럽에서 난소암 2차 치료제로 카보플라틴(carboplatin)과 병용으로 허가 받았습니다. 현재 유럽, 중동, 남미 등에서 상업화를 추진중에 있습니다. 아필리아 판권 취득 및 향후 상업화 계획에 관한 내용은 본 증권신고서 "III. 투자위험요소 - 2. 회사위험 - 카." 를 참고하여 주시기 바랍니다.
| [Elevar의 신약 후보물질 개발 추진 현황] |
| 구 분 |
개발제품 |
적응증 |
개발현황 및 향후 계획 |
|---|---|---|---|
| 신약개발 | 리보세라닙 (Rivoceranib, 구Apatinib Mesylate) |
표적항암제 |
1) 위암 3차 치료제(단독요법) : 임상3상 종료 (2019.06), 2) 간암 1차 치료제(캄렐리주맙과 병용요법) : 임상3상 진행 중 3) 대장암 3차 치료제(론서프와 병용요법) : 임상1b/2상 진행 중 4) 위암 2차 치료제(파클리탁셀과 병용요법) : 임상 1/2a상 진행 중 5) 선양낭성암 1/2차 치료제(단독요법) : 임상2상 진행 중 |
| 아필리아 (Apealea) |
세포독성항암제 | 1) 난소암 2차 치료제(카보플라틴과 병용요법) : 유럽 판매 허가 2) 난소암 2차 치료제(리보세라닙 병용요법) : 1상 준비 중 |
종합적으로, 신약개발은 시간과 노력에 비해 성공확률이 낮기 때문에 높은 위험 부담이 있음에도 불구하고, 성공 시 창출되는 높은 경제적 가치를 고려했을 때 매력적인 산업일 수 있습니다. 하지만 새로운 의약품이 개발되어 소비자에게 전달되기까지는 많은 비용과 노력이 필요하며, 시판으로 이어질 확률은 10,000분의 1 정도로 낮은 편입니다. 따라서 당사에서 진행 중인 신약개발 역시 큰 실패위험 속에 진행되고 있으며, 신약개발에 성공하지 못할 경우 이는 당사의 미래 수익성과 주가에 부정적인 영향을 미칠 수 있음을 알려드립니다.
| 사. 희귀의약품 지정 신약 개발관련 위험 희귀의약품이란 환자 수가 매우 적은 질환의 진단, 예방, 치료를 위한 의약품으로 정의되며, 환자 수에 대한 규정은 국가마다 다릅니다. 한국의 경우 환자 수 2만명 이하, 미국은 20만명 미만, 일본은 5만명 이하, EU는 인구 1만명 당 5명 이하로 희귀질환의 환자 수를 규정합니다. 희귀의약품의 치료 대상인 희귀질환은 유전질환이 80%를 차지하며, 생명을위협하거나 만성적인 쇠약을 동반하는 중증질환인 경우가 많습니다. 국내의 경우 희귀질환은 환자수가 20,000명 이하인 질병을 말합니다. 이 때문에 치료제 개발을 위한 임상시험에 참여할 환자를 모집하기가 쉽지 않은 부분이 있습니다. 이는 세계 각국 정부가 임상3상까지 수행해야 하는 대부분의 의약품과 달리 희귀질환 의약품에는 2상만 완료해도 판매허가를 내주는 이유이기도 합니다. 당사의 종속회사인 Elevar의 리보세라닙은 위암(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국), 간암 (2021년 11월 미국식품의약국), 선양낭성암 (2021년 2월 미국식품의약국) 적응증으로 희귀의약품 지정을 받았습니다. 환자 수가 적은 희귀의약품 특성 상, 임상 환자 모집의 어려움으로 인한 연구 지연 또는 중단의 위험성 등으로 인해 희귀질환 신약개발의 차질이 있을 수 있습니다. 투자자 여러분께서는 이러한 희귀질환 신약개발의 실패 가능성 및 미래 시장성을 고려하여 투자에 임해 주시기 바랍니다. |
희귀의약품이란 환자 수가 매우 적은 질환의 진단, 예방, 치료를 위한 의약품으로 정의되며, 환자 수에 대한 규정은 국가마다 다릅니다. 한국의 경우 환자 수 2만 명 이하, 미국은 20만 명 미만, 일본은 5만 명 이하, EU는 인구 1만 명 당 5명 이하로 희귀질환의 환자 수를 규정합니다.
한국보건사회연구원에 따르면, 희귀의약품 지정요건은 희귀의약품의 특성을 반영하는 몇 가지 요소로 구성되는데, 가장 대표적인 요소가 질환의 희귀성이고 그 외 투자비용 회수 불가능, 질환의 심각성, 국민편익 등이 있습니다. 이러한 요소들을 중심으로 국가별로 상이한 지정요건을 운영하고 있는데 구체적인 주요 내용은 다음과 같습니다.
| [국가별 희귀의약품 지정요건] |
| 국가 | 희귀의약품 지정 요건 |
|---|---|
| 미국 | ① 미국에서 환자수가 20만 명 미만이거나 ② 미국에서 환자수가 20만 명 이상이고 미국에서 희귀질환에 대한 해당 의약품의 개발 및 미국내 시판비용이 미국내 판매액으로 회수될 수있을 것이라는 타당한 예측이 없어야 한다. |
| EU | ① 생명을 위협하거나 만성적인 쇠약을 동반하는 상태의 진단, 예방 또는 치료를 위해 사용되는 의약품으로 커뮤니티에 있는 인구 만 명 당 5명 이하의 비율로 영향을 미치는 의약품, 또는 생명을 위협하거나만성적으로 쇠약상태 또는 심각한 만성상태 를 진단, 예방, 치료하는 것으로 커뮤니티(Community)에서 시판했을 때 필요한 투자를 정당화할 만큼의 충분한 회수가 불가능한 경우 그리고 ② 커뮤니티(community)에서 시판허가된 진단, 예방, 치료를 위한 만족스러운 방법이 존재하지 않을 때 또는 그런 방법이 있다 하더라도 신청하는 제품이 해당 환자들에게 의미있는 편익(significant benefit)을줄 것으로 예상되는 경우 |
| 일본 | ① 일본에서 5만 명 이하의 환자에게 영향을 미치는 질병을 대상으로 하는 것 ② 의료 상 특히 그 필요성이 높은 것 (대체할 수 있는 적절한 의약품이나 치료법이 없고, 기존의 의약품과 비교해 현저하게 유효성 혹은 안전성이 높은 것) ③ 개발 가능성이 높은 것 (해당 의약품을 사용하는 것에 대해 강한 이론적 근거가 있고 개발 계획의 타당성이 높은 것) |
| (2006년부터 추가) ① 일본 내에서 드물게 발생하거나 또는 국외에서만 발생하여 일본 내제한된 집단(예를 들어 유행지역 방문자)에게만 영향을 미칠 수 있는 감염성 질환을 예방하기 위한 백신 ② 지정 및 신청 시점에서는 발견되지 않았지만 유전자 돌연변이로 인해 새롭게 발생하거나 재발할 가능성이 있는 감염성 질환(예를 들어 일단 발생하면 일본 국민의 생명과 건강에 상당히 영향을 미칠 수 있는 감염성인 경우)을 예방하기 위한 백신 |
|
| 한국 | ① 희귀의약품 지정기준은 다음 각 호에 적합하여야 한다. 1. 국내 환자수(유병인구)가 2만 명 이하인 질환에 사용되는 의약품 2. 적절한 치료방법과 의약품이 개발되지 않은 질환에 사용하거나 기존 대체의약품보다 현저히 안전성 또는 유효성이 개선된 의약품 3. 원칙적으로 동일제제의 연간 총 수입실적이 연간 150만 불(미화)이거나 연간 국내 총 생산실적이 15억 원 이하인 의약품 [국내 환자수(유병인구)가 500명 이하인 질환에 사용되는 의약품의 경우 동일제제의 연간 총 수입실적이 500만불(미화) 이하이거나 연간 국내 총 생산실적이 50억원 이하] ② 제1항에도 불구하고 국내에서 임상시험 단계(비임상시험 단계인 경우, 임상시험 진입이 가능하다는 근거가 확보된 경우를 포함한다)에있는 의약품(이하 “개발단계 희귀의약품”이라 한다)의 지정기준은 다음 각 호에 적합하여야 한다. 1. 국내 환자수(유병인구)가 2만명 이하인 질환에 사용되는 의약품 2. 다음 각 목의 어느 하나에 해당 할 것 가. 적절한 치료방법과 의약품(희귀의약품으로 지정/허가된 의약품은제외한다)이 개발되지 않은 질환에 사용하기 위해 개발하는 경우 나. 약리기전이나 비임상 시험등으로 볼 때 기존 대체의약품(희귀의약품으로 지정ㆍ허가된 의약품은 제외한다)보다 현저히 안전성 또는 유효성 개선이 예상되는 경우 3. 국내에서 희귀의약품으로서 개발 계획(임상시험 실시 계획을 포함한다)의 타당성이 인정될 것 ③ 제1항의 규정에도 불구하고 현 의약품 수급체계에 비추어 제한적으로 공급되는 경우 환자의 치료에 큰 지장을 초래할 우려가 있다고 식품의약품안전처장이 인정하는 의약품 |
| 자료 : 보건사회연구 |
희귀의약품은 유병률이 적은 질환을 타겟으로 하는 의약품으로 유병률이 적은 만큼 환자수가 적습니다. 희귀의약품은 각 국가에서 정부 차원 지원 정책으로 연구개발이 장려되고 있고, 적은 환자수 대비 높은 약가가 책정되고 있습니다. 각 국 정부는 희귀의약품을 개발하는 기업에 대해 연구개발 비용 세금공제, 특허수수료 면제, 최초 의약품에 대한 7년간 독점권 부여, 신속심사 대상지정 등 다양하게 지원을 하고 있습니다. 글로벌 희귀의약품 시장은 국가 지원, 상업화된 의약품의 적응증 확대, 기존 치료제와 병용투여 요법 개발 등을 통해 시장 규모가 확대될 것으로 예상됩니다. 경제적인 측면에서 희귀의약품의 임상 소요비용은 비희귀의약품의 50% 가량 소요되며, 미국의 경우 세금 혜택으로 약 27% 수준의 비용이 소요되는 것으로 나타나고 있습니다. 임상기간도 FDA 우선심사 등의 혜택을 통해 비희귀의약품 대비 평균 3개월 이상 단축시킬 수 있습니다.
특히 미국, 유럽, 일본을 비롯한 제약 선진국의 경우 정부가 직접적으로 개입하여 여러 지원정책을 실시하며 희귀질환 치료제의 개발을 독려하고 있습니다. 미국 등에서는 연구개발 단계에서부터 개발비 지원을 비롯하여 허가심사 신속화, 허가 심사수수료 감면, 시장독점권 부여 등을 통해 개발에서 의약품 판매 이후 단계까지 다양한 지원정책을 실시하고 있습니다.
| [주요 국가별 희귀의약품 지원제도] |
|
구분 |
미국 |
일본 |
유럽 | |
|---|---|---|---|---|
|
연구개발 |
연구비 |
임상시험 비용 지원 |
임상시험 비용 지원 |
- |
|
세액 공제 |
임상시험 비용 50% 세금 감면 |
임상시험 비용 |
- | |
|
사전 상담 |
자문 제공 |
자문 제공 |
- | |
|
시판 허가 |
심사 |
신속심사제도 통한 |
9월 이내 심사 종료 (일반 의약품 1년) |
긴급허가제도 운영 |
|
수수료 |
부과대상에서 제외 |
- |
기업규모별 감면 | |
|
시판 이후 (시장독점) |
독점 기간 |
7년 |
10년 |
5년 또는 10년 (5년 경과 후 재평가) |
|
독점 내용 |
동일/유사 의약품 |
후발 의약품 |
동일/유사 의약품 허가 금지 |
|
| 자료: 희귀의약품 제도의 국가별 비교 연구, 한국보건사회연구원, 2013.06 |
희귀의약품의 치료 대상인 희귀질환은 유전질환이 80%를 차지하며, 생명을 위협하거나 만성적인 쇠약을 동반하는 중증질환인 경우가 많습니다. 2014년 UCL(University College London) School of Pharmacy의 <Patients' Needs, Medicines Innovation and the Global Public's Interests>에 따르면 각각의 희귀질환은 환자 수가 적으나 희귀질환의 종류는 6천여 개에 이르며, OECD 국가전체에 약 1억 명에 이르는 환자가 존재하는 것으로 추산되고 있습니다. 또한 희귀의약품은 대체 치료제가 없고 소수의 위중한 환자를 대상으로 하기 때문에 매우 고가로 판매되는 경향이 있습니다.
하지만 희귀의약품지정은 개발신약의 성공을 보장하지는 않습니다. 특히 희귀질환은인구 대비 적은수의 환자들이 포진하고 있어 임상 환자 모집이 큰 변수로 작용할 수 있습니다. 국내의 경우 희귀질환은 환자수가 20,000명 이하인 질병을 말합니다. 이 때문에 치료제 개발을 위한 임상시험에 참여할 환자를 모집하기가 쉽지 않은 부분이 있습니다. 이는 세계 각국 정부가 임상 3상까지 수행해야 하는 대부분의 의약품과 달리 희귀질환 의약품에는 2상만 완료해도 판매허가를 내주는 이유이기도 합니다.
| 희귀의약품지정에 관한 규정 (식품의약품안전처 고시 제2018-41호) |
|
제2조(지정기준) 2. 적절한 치료방법과 의약품이 개발되지 않은 질환에 사용하거나 기존 대체의약품보다 현저히 안전성 또는 유효성이 개선된 의약품 ② 제1항에도 불구하고 국내에서 임상시험 단계(비임상시험 단계인 경우, 임상시험 진입이 가능하다는 근거가 확보된 경우를 포함한다)에 있는 의약품(이하 "개발단계 희귀의약품"이라 한다)의 지정기준은 다음 각 호에 적합하여야 한다. 1. 국내 환자수(유병인구)가 20,000명 이하인 질환에 사용되는 의약품 2. 다음 각 목의 어느 하나에 해당 할 것 가. 적절한 치료방법과 의약품(희귀의약품으로 지정·허가된 의약품은 제외한다)이 개발되지 않은 질환에 사용하기 위해 개발하는 경우 나. 약리기전이나 비임상 시험등으로 볼 때 기존 대체의약품(희귀의약품으로 지정·허가된 의약품은 제외한다)보다 현저히 안전성 또는 유효성 개선이 예상되는 경우 3. 국내에서 희귀의약품으로서 개발 계획(임상시험 실시 계획을 포함한다)의 타당성이 인정될 것 ③ 제1항의 규정에도 불구하고 현 의약품 수급체계에 비추어 제한적으로 공급되는 경우 환자의 치료에 큰 지장을 초래할 우려가 있다고 식품의약품안전처장(이하 "처장"이라고 한다)이 인정하는 의약품 |
| 자료: 국가법령정보센터 |
당사의 종속회사인 Elevar는 보유 파이프라인인 리보세라닙이 개발 중인 적응증에 대해 희귀의약품 지정을 받아 연구개발을 진행하고 있습니다. 리보세라닙이 희귀의약품으로 지정 받은 내역은 아래와 같습니다. 위암(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국), 간암 (2021년 11월 미국식품의약국), 선양낭성암 (2021년 2월 미국식품의약국) 이와 같이 희귀의약품으로 지정됨에 따라 임상종료후 시판허가에 대한 심사의 신속화, 수수료 감면 등의 혜택과 최소 8년에서 최대 13년동안 독점 판매할 수 있습니다.
| 당사 및 당사 자회사 보유 희귀의약품 파이프라인] |
| 회사명 | 파이프라인 | 내용 | 지정국가명 |
|---|---|---|---|
| 에이치엘비㈜ | - | - | 해당사항 없음 |
| Elevar Therapeutics | 리보세라닙(아파티닙) | 항종양 신생혈관 억제제 | 미국, 유럽, 한국 |
| 주1) 희귀의약품 해당 파이프라인만 표시함 |
Elevar가 License in 계약을 통해 보유하고 있는 리보세라닙 관련 특허 권리의 요약정보는 아래와 같으며, 특허에 대한 상세한 권리관계는 본 증권신고서 "III. 투자위험요소 - 2. 회사위험 - 차." 를 참고하여 주시기 바랍니다.
| [Elevar 보유 리보세라닙 관련 L/I 특허 권리 요약] |
| [전용실시권] (1) 혈관신생 억제제로서의 6환 아미노-아미드 유도체(물질 특허) : 2024년 만료 |
| [재실시권] (2) N-[4-(1-사이아노사이클로펜틸) 페닐]-2-(4-피리딜메틸) 아미노-3-피리딘카복스아마이드의 염 (염조성물특허) : 2029년 만료 (국가별 특허전략에 따라 최대 2034년까지 연장 가능) |
희귀질환은 환자수가 적어 치료제의 시장이 작고 질환에 대한 연구가 어려워 희귀의약품의 개발 가능성이 낮은 영역입니다. 이러한 희귀질환에 대한 치료제의 개발 성공시 높은 시장성이 기대됩니다. 다만, 당사 및 계열사인 Elevar에서 보유한 파이프라인의 신약개발 역시 임상 환자 모집의 어려움으로 인한 연구 지연 또는 중단의 위험성 등으로 인해 희귀질환 신약개발의 차질이 있을 수 있습니다. 투자자 여러분께서는이러한 희귀질환 신약개발의 실패 가능성 및 미래 시장성을 고려하여 투자에 임해 주시기 바랍니다.
| 아. 지적재산권 분쟁 관련 위험 제약/바이오의약품 산업은 특허의 확보가 사업의 핵심 성공 요인으로, 특허를 확보하지 못할 경우 원천적으로 사업이 불가능하거나 특허 소유자로부터 기술이전을 받아야 합니다. 당사는 보유 특허에 대한 보호 강화를 위해 특허보호와 관련된 국내외 정책 동향 및 법률적 사항 등을 확인 하는 등 당사의 지식재산권 보호를 위한 노력을 최대한 기울이고있습니다. 당사는 2020년 중 리보세라닙의 특허관련 권리 일체를 인수했고, 당사의 연결대상 종속회사인 Elevar는 가장 중점적으로 신약 개발을 추진 중인 신약후보물질 리보세라닙 성분 치료제에 대하여 중국과 한국을 제외한 글로벌 전용실시권을 특허권자와의 라이센스 계약을 통하여 확보한 상태이며, 그 중 한국 내 전용실시권은 당사의 계열회사인 에이치엘비생명과학㈜가 재실시권의 형태로 보유하고 있습니다. 다만, 향후 당사가 보유한 지적재산권을 적절히 보호하지 못하거나, 라이센스 계약 등에 있어서 당사의 지적재산권 관련 분쟁이 발생하는 경우 당사의 경쟁력은 약화될 수 있으며 이는 당사의 영업 및손익에 부정적인 영향을 미칠 수 있습니다. |
제약/바이오의약품 산업은 특허의 확보가 사업의 핵심 성공 요인으로, 특허를 확보하지 못할 경우 원천적으로 사업이 불가능하거나 특허 소유자로부터 기술이전을 받아야 합니다. 특허가 가장 중요한 경쟁요소이기 때문에 많은 바이오의약품 개발 회사와 제약사들은 특허기간을 최대한 보호하기 위한 다양한 전략 및 정책을 도입하고 있으며, 제품화 이후 특허 보호기간을 연장하기 위한 전략으로 공정 특허, 제법 특허 등의 방법을 활용하고 있습니다.
(1) 리보세라닙 관련 지적재산권
증권신고서 제출일 현재 당사의 100% 자회사인 Elevar가 가장 중점적으로 개발을 추진 중인 신약후보물질은 리보세라닙이며, 리보세라닙에 대한 특허는 물질특허와 염조성물특허로 나뉩니다. 리보세라닙 물질특허 및 염조성물특허 출원 및 원천 특허권자 현황은 아래와 같습니다.
| [리보세라닙 관련 글로벌 원천 특허권 등록 현황] |
| 구분 | 물질(리보세라닙)특허 | 염조성물특허(Salt Patent) | ||
|---|---|---|---|---|
| 혈관신생억제제로서의 6환 아미노-아미드 유도체 |
N-[4-(1-사이아노사이클로펜틸)페닐]-2- (4-피리딜메틸)아미노-3- 피리딘카복스아마이드의 염 |
|||
| 지역 | 등록번호 | 등록권자 | 등록번호 | 등록권자 |
| 미국 | US7129252 | 에이치엘비㈜ | US8362256 | 항서제약(중국) |
| 유럽 | EP1633712 | EP2327697 | ||
| 일본 | JP5046643 | JP5649132 | ||
| 한국 | 101159034 | 101674227 | ||
| 캐나다 | CA2568608 | CA2736664 | ||
| 호주 | - | - | AU2009295168 | |
| 홍콩 | - | - | HK1141514 | |
| 인도 | - | - | 출원번호: IN2011DN01596 공개번호: IN01596DN2011A |
항서제약(중국) |
| 멕시코 | - | - | 출원번호: MX20110002816 공개번호: MX2011002816 |
|
| 러시아 | - | - | 출원번호: RU20110113229 공개번호: RU2011113229/2499796 |
|
리보세라닙 성분 치료제를 특정 지역에서 독점 개발 및 판매하기 위하여는 해당 지역에서 최소한 그 물질특허 또는 염조성물특허 중 1에 대한 독점적 실시권(License)을 확보해야 합니다. 다시 말해, 특정 지역에 리보세라닙 물질특허가 등록되어 있지 않더라도 염조성물특허가 등록되어 있다면 해당 지역의 염조성물특허 실시권자는 리보세라닙 성분 치료제를 독점적으로 개발 및 판매할 수 있습니다.
증권신고서 제출일 현재 Elevar는 2020년 09월 체결한 특허권 양수도계약을 통해 리보세라닙에 대하여 원천권리 전부를 보유하고 있으며, 중국에서의 특허전용실시권은항서제약이, 한국에서의 특허전용실시권은 에이치엘비생명과학㈜가 보유하고 있고, 나머지 국가의 특허전용실시권은 Elevar가 보유하고 있습니다. 특허의 전용실시권은원천 특허권자가 제3자에게 허여하는 것으로, 실시권자(Licensee)는 해당 성분을 사용한 치료제를 제조ㆍ판매할 수 있으며, 이로부터 발생한 매출액에 대하여 전용실시권을 허여한 자(Licensor)에게 계약에 따라 일정 수준의 로열티를 지급합니다.
상기 물질특허 및 염조성물특허의 원천 특허권자들간의 계약, 그리고 당사의 100% 자회사인 Elevar와 원천 특허권자 및 전용실시권자들간의 라이센스 계약에 의하여 증권신고서 제출일 현재 리보세라닙 성분 치료제의 글로벌 판권은 아래와 같이 정리되어 있습니다.
| [리보세라닙 치료제 판권 현황] |
| 국가판권 | 판권 보유사 |
|---|---|
| 중국 판권 | 항서제약 |
| 국내(한국) 판권 | 에이치엘비생명과학㈜ |
| 나머지 국가 판권 | Elevar Therapeutics, Inc. |
| 주1) 일본ㆍ유럽 판권은 Elevar에서 보유하고 있으며, 에이치엘비생명과학㈜가 일본ㆍ유럽 발생 Revenue의 14.5%를 배분받기로 되어있습니다. |
2020년 9월 당사가 리보세라닙의 특허관련 권리 일체를 인수하기 전까지, 리보세라닙 물질에 대하여 미국 내에서는 Advenchen이, 미국 외에서는 Advenchen의 최대주주이자 물질 개발자인 Paul Chen 개인이 특허권자로 등록되어 있었습니다. 물질 특허와는 별도로 중국 항서제약은 리보세라닙의 염조성물 글로벌 특허(Salt Patent)를 출원(2009년 6월), 보유하고 있었으며, Advenchen은 항서제약으로부터 중국 이외 모든 지역에 대하여 염조성물 특허에 관한 전용실시권을 허여받았고, 또한 Advenchen이 전용실시권을 보유하는 지역 내에서 제3자에게 실시권을 허여할 수 있는 권리를 부여받았는바, 이에 기하여 2015년 당시 LSK Bio(現Elevar)에게 중국 외 모든 지역에 대한 염조성물 특허 재실시권을 허여하였습니다. 한편, 증권신고서 제출일 전일기준 당사가 지분 19.6%를 보유하고 있는 에이치엘비생명과학㈜는 리보세라닙의 글로벌 권리 중 Elevar로부터 허여받은 한국 시장에서의 독점적 재실시권을 보유하고 있으며, Elevar가 일본 및 유럽 시장에서 실시권을 행사하여 직접 얻는 수익 또는 특허권 재실시를 제3자에게 허여하여 수령하는 로열티 수익의 일부(14.5%)에 대한 권리를 보유하고 있습니다.
이후 당사는 2020년 02월 27일 언론을 통해 Advenchen이 Rivoceranib에 대하여 보유하는 특허 관련 권리 일체를 Advenchen으로부터 양수하기로 하였음을 발표했으며, 당사가 양도받은 권리는 YN968D1(이하 "리보세라닙")과 관련된 모든 특허 및 지적재산권입니다. 평가대상자산을 인수함에 따라 리보세라닙과 관련된 모든 권리를 획득하게 되어 글로벌 리보세라닙 관련 매출액에 대한 로열티를 수령하게 되었고, 2020년부터 중국의 항서제약을 통해 중국 내 리보세라닙 매출액에 대한 로열티를 수령하고 있습니다.
| [리보세라닙 성분 치료제 판권 라이센스 및 로열티 지급 관계 현황] |
|
리보세라닙 관련 권리관계에 관한 추가적인 내용은 본 증권신고서 ""III. 투자위험요소 - 2. 회사위험 - 차."를 참고하여 주시기 바랍니다.
(2) Elevar 및 Immunomic 보유 기타 지적재산권
Elevar 및 Immunomic은 리보세라닙뿐만 아니라 기타 보유 파이프라인에 대한 특허권을 주요국에 출원하여 권리 확보를 하였으며 증권신고서 제출일 현재 주요 특허권 현황은 다음과 같습니다.
| [아필리아 관련 특허권 현황(Elevar)] |
| 특허유형 | 출원일 | 등록일 | 만료일 | 국가명 | 상태 | 등록번호 | 비고 |
|---|---|---|---|---|---|---|---|
| 수용성의 양이온성 양친매성 제약학적 활성물질의 투여를 위한 약물전달시스템 |
2008-12-18 | 2012-12-04 | 2028-12-18 | Australia, Brazil Canada, China Eurasia, Europe India, Japan S Korea, Mexico Malaysia, New Zealand Ukraine, USA, South Africa |
Issued | Aus 2008339101/Brazil PI0821739-4/Canada 2709268/ China 200880127094.1/ Eurasia 18559/ Europe 2231193/ India 276371/ Japan 5466174/ S Korea 1016161340000/ Mexico 321507/ Malaysia 150820/ New Zealand 586858/ Ukraine 80243/ USA 8324274/ South Africa 2010/04992 | 수용성의 양이온성 양친매성 물질의 인체내 전달시스템에 대한 특허 |
| 물에 난용성인 제약학적 활성 물질의 투여를 위한 약물 전달시스템 |
2008-12-18 | 2015-04-07 | 2028-12-18 | Armenia, Azerbaijan | Issued | 15247 | 난용성 물질의 인체내 전달시스템에 대한 특허(파클리탁셀등) |
| 2012-09-18 | 2013-05-13 | 2032-09-18 | Ukraine | Issued | 79902 | ||
| Taxol containing compositions | 2003-10-28 | 2008-08-29 | 2023-10-28 | Malaysia | Issued | 136047-A | - |
| Therapeutic compounds | 2002-11-15 | 2006-04-18 | USA 2023-04-11 나머지 국가 2022-11-15 |
USA, EP | Issued | USA 7030158/ EP 02783947.1 |
약물 전달체 조성에 대한 특허 |
| Method for producing N-retinoylcysteic acid alkyl ester |
2018-10-11/ 2018-10-31 | 2018-11-27/ 2019-06-18 | 2036-12-09 | USA | Issued | 10138204/10322996 | 약물 전달체 제조방법 특허 |
| [Immunomic 보유 특허권 현황] |
| 특허유형 | 출원일 | 등록일 | 만료일 | 국가명 | 상태 | 등록번호 |
|---|---|---|---|---|---|---|
| (가) 알레르기 치료용 핵산(Nucleic Acids) | ||||||
| ITI-03-AU | 2014-11-28 | 2018-03-22 | 2032-06-15 | Australia | Issued | 2012382406 |
| ITI-03-AU-D1 | 2018-01-25 | 2020-01-02 | 2032-06-15 | Australia | Issued | 2018200625 |
| ITI-03-AU-D2 | 2019-10-18 | 2022-02-03 | 2032-06-15 | Australia | Issued | 2019250227 |
| ITI-03-BR | 2014-12-15 | 2022-02-01 | 2032-06-15 | Brazil | Issued | 1120140313270 |
| ITI-03-BR-D1 | 2020-04-06 | - | - | Brazil | Published | - |
| ITI-03-CA | 2014-12-15 | 2020-07-21 | 2032-06-15 | Canada | Issued | 2876824 |
| ITI-03-CN | 2015-02-06 | 2017-11-10 | 2032-06-15 | China | Issued | ZL201280075163.5 |
| ITI-03-EP | 2015-01-15 | 2020-09-09 | 2032-06-15 | EPO | Issued | EP2861240B |
| ITI-03-EP-D1 | 2020-09-07 | - | - | EPO | Pending | - |
| ITI-03-IL | 2014-11-12 | 2020-02-29 | 2032-06-15 | Israel | Issued | 236174 |
| ITI-03-IL-D1 | 2019-10-29 | 2020-12-01 | 2032-06-15 | Israel | Issued | IL 270260 |
| ITI-03-IL-D2 | 2019-10-29 | - | - | Israel | Pending | - |
| ITI-03-IL-D3 | 2019-10-29 | - | - | Israel | Pending | - |
| ITI-03-JP | 2014-12-11 | 2015-09-18 | 2032-06-15 | Japan | Issued | 5807994 |
| ITI-03-JP-D1 | 2015-02-02 | 2017-02-10 | 2032-06-15 | Japan | Issued | 6088584 |
| ITI-03-JP-D2 | 2016-10-20 | 2018-06-15 | 2032-06-15 | Japan | Issued | 6353510 |
| ITI-03-KR | 2015-01-12 | 2020-04-28 | 2032-06-15 | Republic of Korea | Issued | 10-2107646 |
| ITI-03-KR-D1 | 2020-04-28 | - | - | Republic of Korea | Pending | - |
| ITI-03-US-C1 | 2016-03-02 | 2017-08-29 | 2032-06-15 | United States | Issued | 9744230 |
| ITI-03-US-C1-D1 | 2017-07-31 | 2018-09-11 | 2032-06-15 | United States | Issued | 10072053 |
| ITI-03-US-C3 | 2020-09-22 | - | - | United States | Pending | - |
| (나) 땅콩 알레르기 치료용 핵산(Nucleic Acids for the Treatment of Peanut Allergy) | ||||||
| ITI-04-AU | 2016-12-07 | - | - | Australia | Pending | - |
| ITI-04-AU-D1 | 2020-06-26 | - | - | Australia | Pending | - |
| ITI-04-BR | 2016-12-23 | - | - | Brazil | Pending | - |
| ITI-04-EP | 2017-01-20 | - | - | EPO | Published | - |
| ITI-04-KR | 2017-01-18 | - | - | Republic of Korea | Pending | - |
| ITI-04-MY | 2016-12-07 | - | - | Malaysia | Pending | - |
| ITI-04-PCT | 2015-06-23 | - | - | WIPO | Published | - |
| ITI-04-UA | 2017-01-20 | - | - | Ukraine | Pending | - |
| (다) 알레르기 항원 생성(Allergen Constructs) | ||||||
| ITI-06-PCT | 2017-11-15 | - | - | WIPO | Published | - |
| ITI-06-CA | 2019-05-15 | - | - | Canada | Pending | - |
| ITI-06-CN | 2019-06-13 | - | - | China | Published | - |
| ITI-06-EP | 2019-05-23 | - | - | EPO | Published | - |
| ITI-06-EP-HK | 2019-12-10 | - | - | EPO | Published | - |
| ITI-06-JP | 2019-05-15 | - | - | Japan | Published | - |
| ITI-06-US | 2019-05-15 | - | - | United States | Published | - |
| (라) ITI 보유 기타 출원 (Other Patents owned by ITI) | ||||||
| ITI-07-AU | 2019-10-14 | - | - | Australia | Pending | - |
| ITI-07-BR | 2019-10-22 | - | - | Brazil | Pending | - |
| ITI-07-CA | 2019-10-21 | - | - | Canada | Pending | - |
| ITI-07-CN | 2019-10-22 | - | - | China | Published | - |
| ITI-07-EP | 2019-11-18 | - | - | EPO | Published | - |
| ITI-07-HK | 2020-03-02 | - | - | Hong Kong | Published | - |
| ITI-07-IL | 2019-11-17 | - | - | Israel | Pending | - |
| ITI-07-JP | 2019-10-21 | - | - | Japan | Published | - |
| ITI-07-KR | 2019-11-19 | - | - | Republic of Korea | Pending | - |
| ITI-07-US | 2019-10-21 | 2021-12-21 | 2039-10-21 | United States | Issued | 11203629 |
| ITI-07-US-D1 | 2021-10-29 | - | - | United States | Pending | - |
| ITI-13-CA | 2020-11-11 | - | - | Canada | Pending | - |
| ITI-13-EP | 2020-11-06 | - | - | EPO | Pending | - |
| ITI-13-JP | 2020-11-12 | - | - | Japan | Pending | - |
| ITI-13-US | 2020-11-08 | - | - | United States | Pending | - |
| ITI-08-AU | 2019-10-14 | - | - | Australia | Pending | - |
| ITI-08-BR | 2019-11-01 | - | - | Brazil | Pending | - |
| ITI-08-CA | 2019-10-29 | - | - | Canada | Pending | - |
| ITI-08-CN | 2019-11-04 | - | - | China | Published | - |
| ITI-08-EP | 2019-11-25 | - | - | EPO | Published | - |
| ITI-08-HK | 2020-03-18 | - | - | Hong Kong | Published | - |
| ITI-08-IL | 2019-10-29 | - | - | Israel | Pending | - |
| ITI-08-JP | 2019-11-01 | - | - | Japan | Published | - |
| ITI-08-KR | 2019-11-27 | - | - | Republic of Korea | Pending | - |
| ITI-08-US | 2019-11-01 | - | - | United States | Pending | - |
| ITI-15-PCT | 2020-10-17 | - | - | WIPO | Pending | - |
| ITI-19-PROV | 2020-12-30 | - | - | United States | Pending | - |
| ITI-19-PCT | 2021-12-29 | - | - | United States | Pending | - |
당사(연결대상 종속회사 포함)는 보유 특허에 대한 보호 강화를 위해 특허보호와 관련된 국내외 정책 동향 및 법률적 사항 등을 확인 하는 등 당사의 지식재산권 보호를위한 노력을 최대한 기울이고 있습니다. 다만, 향후 당사가 보유한 지적재산권을 적절히 보호하지 못하거나 당사가 사용하는 기술과 관련한 지적재산권 관련 분쟁이 발생하는 경우 당사의 경쟁력은 약화될 수 있으며 이는 당사의 영업 및 손익에 부정적인 영향을 미칠 수 있습니다.
| 자. 신약 연구개발의 전략 수립 실패에 따른 위험 연구개발을 통한 신약 개발은 일반적으로 막대한 연구개발비와 장기간에 걸친 투자 및 연구기간이 소요되며, 신약 개발에 성공한다 하더라도 기투자된 금액과 시간을 상쇄할 수 있을 정도의 수익 창출이 가능할지 여부는 불확실합니다. 또한 내외부적인 요인으로 인하여 개발이 지연되거나 추가적인 비용 지출이 요구될 경우도 존재합니다. 따라서 연결대상 종속회사의 연구개발 계획이 실패하거나, 장기적인 연구개발 전략과 사업계획, 그리고 그에 맞는 자금운용계획을 적정하게 수립하지 못할 경우 당사의 수익성 및 재무안정성에 부정적인 영향이 있을 수 있습니다. |
글로벌 신약 개발 시 평균 1조~2조 원 상당의 개발 비용과 평균 10~15년 정도의 장기간의 개발기간 소요됩니다. 신약개발은 크게 후보물질 탐색, 前임상, 임상시험 단계로 구분되는데, 임상 단계는 6~7년이 걸리고, 전문역량과 고비용이 요구되는 단계로 전체 신약개발 비용의 약 70% 소요됩니다.
최근 R&D 투자 효율성 하락으로 글로벌 제약기업들의 R&D 지출액 증가율이 둔화될 것으로 전망되고 있습니다. 의약품 산업은 연구개발에서부터 신약개발 성공과 제품 상용화 생산에 이르기까지 높은 R&D 비용과 10년 이상의 기간이 소요되는 기술, 자본집약적 산업이지만, 2000년 이후 글로벌 제약기업들의 투자 효율성(ROIC, 투자자본 수익률) 감소세를 보이고 있습니다. 글로벌 대형 제약기업들이 신약 1개 당 시판을 위해 드는 비용이 2010년 11.9억 달러에서 2018년 21.7억 달러로 급증하였습니다. 이는 각국 정부의 약가인하 유도 정책에 따른 수익성 감소 및 신약개발 비용,기간 증가와 경쟁 심화 등에 따른 투자의 증가 등에 기인합니다.
| [글로벌 5대 제약기업들의 ROIC 추이] |
|
| 자료 : 한국수출입은행, 세계 바이오의약품 산업 동향 및 전망(2019.7.22) Bloomberg, 이베스트투자증권 리서치센터 재인용 |
실제로 Evaluate pharma에서 발간한 자료에 따르면, 2020년 기준 글로벌 의약품 R&D 투자는 1,980억 달러로 추정됩니다. 그리고 2020~2026년 R&D 투자금액은 연평균 4.2% 증가하여 2026년에는 2,540억 달러에 이를 것으로 전망하고 있습니다. 이렇듯 제약사 간의 경쟁 및 감독기관의 보다 엄격해지는 규제로 인해 R&D 비용의 절대규모는 증가하고 있지만, 그 성장률은 점차 둔화되는 양상을 보이고 있습니다.
| [글로벌 제약기업들의 R&D 비용 추이] |
|
| 자료 : WorldPreview2021 Outlook to 2026, 바이오의약품 산업동향 보고서(2021.12) |
실제로 글로벌 제약 R&D 투자 상위 10대 기업의 개별 투자액과 그 비중을 살펴보면,2019년 대비 2026년 R&D 투자액은 10대 기업 모두 증가할 것으로 전망됩니다. 하지만 매출 총액 대비 R&D 투자액 비중은 10대 기업 중 Pfizer 및 GlaxoSmithKlinet 두 곳만 증가할 것으로 전망되며, 나머지 여덟개 업체의 경우 감소할 것으로 전망됩니다.
또한 Deloitte 연구 결과에 따르면, 주요 대형 바이오제약 기업의 R&D 수익률은 2010년 10.1%에서 2018년 1.9%로 큰 폭의 하락을 나타냈습니다. 다만 전문화된 제약·바이오 기업들은 높은 개발 비용에도 불구하고 높은 파이프라인 가치를 보유하고 있는 경우가 많아 실제 개발에 성공하는 경우 높은 수익률을 기대할 수 있습니다.
| [글로벌 의약품 R&D 투자 상위 10위 기업 전망] |
|
| 자료 : WorldPreview2021 Outlook to 2026, 바이오의약품 산업동향 보고서(2021.12) |
이처럼 글로벌 제약기업들은 글로벌 혁신 신약 확보를 위해 R&D활동과 더불어 M&A, 파이프라인 도입(라이센스인)과 같은 전략을 적극적으로 활용하고 있습니다. 2013년 이후 글로벌 제약기업의 M&A는 거래건수와 규모 모두 크게 증가하였고, 라이센스 거래의 경우 최근 건수는 감소하고 있으나, 거래규모는 과거 대비 증가한 모습을 보이고 있습니다.
연구개발을 통한 신약 개발은 일반적으로 막대한 연구개발비와 장기에 걸친 투자 및연구기간이 소요되며, 신약 개발에 성공한다 하더라도 기투자된 금액과 시간을 상쇄할 수 있을 정도의 수익 창출이 가능할지 여부는 불확실합니다. 또한 내외부적인 요인으로 인하여 개발이 지연되거나 추가적인 비용 지출이 요구될 경우도 존재합니다. 따라서 당사 및 당사계열회사의 연구개발 계획이 실패하거나, 장기적인 연구개발 전략과 사업계획, 그리고 그에 맞는 자금운용계획을 적정하게 수립하지 못할 경우 당사의 수익성 및 재무안정성에 부정적인 영향이 있을 수 있습니다.
|
차. 리보세라닙 성분 신약 허가 관련 불확실성 |
회사가 각종 연구 및 임상시험 결과를 통해 얻은 많은 데이터를 직접 평가하여 의약품의 유효성과 안전성을 확인한 경우라도 의약품은 사람의 생명 및 건강에 직접 영향을 주기 때문에 시판 전에 반드시 의약품의 제조 및 판매에 대한 품목허가를 받아야 합니다.
당사의 연결대상 종속회사인 Elevar Therapeutics는 2005년 7월 신약개발 컨설팅 회사로 설립되어, 2007년 12월 리보세라닙 표적항암제에 대하여 캘리포니아 소재 바이오테크 회사 어드벤첸(Advenchen Laboratories, Inc., Ca, USA)으로부터 라이센스를 취득하는 계약을 체결하였습니다. 리보세라닙(舊 아파티닙)은 2018년 1월 세계보건기구(WHO)의 국제일반명(INN)과 미국 의약품성분명(USAN)에 모두 'Rivoceranib(리보세라닙)'이라는 성분명으로 등록되었습니다.
Elevar는 미국, 일본, 한국, 대만, 유럽 등 12개 국가에서 리보세라닙 글로벌 위암 임상 3상을 완료하였으며, 2019년 10월 미국 FDA와 Pre-NDA 미팅을 완료하였습니다. Elevar는 임상 3상 결과 및 Pre-NDA meeting 결과를 바탕으로 신약허가 전문컨설팅회사의 도움을 받아 최선의 신약 허가전략을 수립한 후 FDA에 신약 허가(NDA)를 신청할 예정입니다. 그 외에도 선양낭성암 1,2차 치료제(Rivoceranib 단독) 2상 결과를 토대로 가속승인(조건부승인)을 추진하고 있고, 2022년 5월 통계적 유의성이 확보 되었다고 밝힌 바 있는 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상 3상의 경우 2022년 5월 통계적 유의성이 확보됐다고 밝혔고, 그 결과를 토대로 8월에 미국 FDA에 Pre-NDA 미팅 신청을 했습니다. 2022년 9월 ESMO(유럽종양학회)에서 공개한 3상 임상의 결과를 토대로(1차 평가지표 만족)Pre-NDA미팅 준비 등 후속 개발에 힘쓰고 있습니다. 하지만 신약에 대한 규제가 강화되거나 예상하지 못한 자료가 요구되는 경우 리보세라닙(위암 말기 치료제)의 품목 허가 시점이 지연되거나 거절될 가능성이 존재하며, 품목허가가 되더라도 상업화 성공이 보장되는 것은 아닙니다.
Elevar의 주요 개발 제품은 VEGFR-2(Vascular Edothelial Growth Factor Receptor2 : 혈관내피 세포증식인자수용체2)를 표적으로 하는 항종양 신생혈관 억제제인 리보세라닙입니다. 종양세포는 성장을 위해 신혈관 생성을 유도하게 되는데 VFGF(Vascular Edothelial Growh Factor: 혈관내피 생성인자)는 혈관신행을 유도하는 혈관생성인자로, 'VFGF'와 'VFGFR-2'와의 결합은 신혈관 생성에 있어 가장 핵심적인 역할을 하게 됩니다.
| VEGF | 혈관내피성장인자 (Vascular endothelial growth factor) |
| VEGFR-2 | 제2형 혈관내피성장인자 수용체 (Vascular endothelial growth factor receptor-2) |
| 혈관신생과 암 정복의 활용 |
| 혈관신생은 기존 혈관으로부터 새로운 혈관이 생성되는 기작이며 정상적인 생리작용으로 발생과정과 상처치유, 여성의 생식 주기에 중요한 역할을 합니다. 세포는 생존을 위해혈관으로부터 산소와 영양분의 공급을 요구하는데 이를 위해 세포는 혈관으로부터 산소의 확산범위에 해당하는 약 100 마이크로미터(μm) 이내에 존재합니다. 이 범위에서 벗어난 세포들은 생존을 위해 새로운 혈관의 생성이 필요한데 이 과정을 혈관신생이라고 합니다. 암세포는 정상 세포가 오작동으로 인해 죽지 않고 무한 증식하는 세포를 말합니다. 무한 증식하는 암세포 역시 생존하기 위해서는 새로운 혈관이 필요합니다. 암세포는 혈관신생을 통해 영양분을 공급받는데 문제는 이로 인해 주위 정상세포가 정상적으로 공급받아야할 영양분까지 암세포가 독식한다는 점입니다. 결과적으로 주위 정상세포는 아사하게 됩니다. 과학자들이 암 치료 전략으로 주목한 점은 혈관신생의 시작 포인트입니다. 인체 내에서 혈관신생을 유도하는 물질, 즉 혈관생성인자를 적절히 통제할 수 있다면 혈관신생을 억제할 수 있고 결과적으로 암세포의 성장을 차단할 수 있기 때문입니다. 암세포는 무한증식을 통해 세포를 지속적으로 만드는 데 암세포가 자신의 생존에 필요한혈관이 부족할 경우, 혈관생성인자를 분비함으로써 인체 내 혈관신생을 촉발합니다. 이렇게 분비된 혈관생성인자가 혈관신생을 진행하기 위해서는 혈관세포와의 결합이 이뤄져야 합니다. 세포 내에서 보통 혈관생성인자와 같은 단백질과 세포의 결합은 세포 표면에 위치한 수용체(리셉터, Receptor)를 통해 이루어집니다. 해당 단백질과 목표 세포 수용체는 상호간 특이적 결합을 합니다. 혈관생성인자가 혈관세포 수용체와 결합하면 혈관세포는 혈관신생을 진행함으로써 새로운 혈관이 생성되는 것입니다. |
| 자료: The Science Times |
VEGF는 ▲VEGF-A ▲VEGF-B ▲VEGF-C ▲VEGF-D 등의 VEGF 패밀리로 구성돼 있으며, 혈관세포는 VEGFR-1과 VEGFR-2 등의 수용체를 가지고 있습니다. VEGF는 주로 VEGFR2 수용체와 결합해 혈관신생을 유도하는 것으로 알려져 있습니다. 따라서 'VEGFR-2'의 활성을 차단하는 것은 암세포 성장에 반드시 필요한 신혈관 생성(Angiogenesis)을 효과적으로 억제하는 방법으로 볼 수 있습니다. 리보세라닙(아파티닙)은 암세포에서 분비하는 혈관신행인자인 'VEGF'가 결합하는 수용체중에서 'VEGFR-2'를 선택적으로 차단하여 암세포의 성장과 전이를 효과적으로 억제하는 동시에 부작용은 최소화시키는 작용기전을 가지고 있습니다.
|
| 자료: 당사 내부자료 |
중국에서는 2015년 Apatinib Mesylate(Rivoceranib의 舊 명칭)의 신약 허가가 완료되어 중국 내 독점 특허 실시권을 보유하고 있는 항서제약이 제품명 'Aitan'으로 판매를 개시하였습니다. 위암 후기 치료제 'Aitan'은 2016년부터 본격적인 매출을 시현하기 시작했으며, 항서제약은 Aitan의 매출에 따라 미국 Advenchen에 로열티를 지급해 왔습니다. 이후 2020년 당사가 특허 관련 권리 일체를 Advenchen으로부터 양수함에 따라, 리보세라닙과 관련된 모든 권리를 획득해 글로벌 리보세라닙 관련 매출액에 대한 로열티를 수령하게 되었고, 권리 양수 이후 당사의 리보세라닙 관련 로얄티 매출액 내역은 아래와 같습니다. 권리 양수에 대한 상세한 내용은 "III. 투자위험요소 - 2. 회사위험 - 차."를 참고해주시기 바랍니다.
| 리보세라닙 로열티 매출 현황 |
| (금액 : 백만원) |
| 연도 | 금액 |
|---|---|
| 2022년 반기 | 3,908 |
| 2021년 | 10,362 |
| 2020년 | 5,856 |
한편, 중국 이외의 지역에서는 리보세라닙의 신약 허가가 완료된 바 없으나 당사의 연결대상 종속회사인 Elevar가 미국 NDA 신청을 진행, 신약 허가가 이루어지고 중국 외 지역에서도 리보세라닙 성분의 치료제 매출이 발생하기 시작할 경우 Elevar는 원천 특허 권리 양수도계약에 따라 당사로 로열티를 지급할 예정입니다. 향후, 리보세라닙의 성분 치료제의 신약 허가 여부는 당사의 100% 자회사인 Elevar의 수익 실현 여부에 직접적인 영향을 미치게 되며, 결과적으로 당사의 연결기준 실적에 유의미한 영향을 미칠 것으로 판단됩니다.
리보세라닙 물질의 적용 분야 중 위암 3차 치료제와 간암 2차 치료제의 경우 이미 중국에서의 임상 3상 종료 후 시판허가를 득하여 현재 중국 내에서 판매되고 있음에 따라 그 효과와 안정성이 입증되고 있습니다. 리보세라닙은 위암 3차 치료제, 간암 1차치료제(항서제약 캄렐리주맙 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독)로서 희귀의약약품으로 지정 받아 유효성과 안전성을 인정받았습니다. 하지만 희귀의약품지정 사실이 개발신약의 성공을 보장하지는 않습니다. 투자자 여러분께서는 이점을 유의하시어 투자에 임하시기 바라며 희귀약품지정에 관한 상세한 내용은 "III. 투자위험요소 - 1. 사업위험 - 사."를 참고하시기 바랍니다.
리보세라닙은 2011년 11월 미국 FDA로부터 표준치료에 실패한 고형암 환자에 대해다국가(미국, 한국) 임상 1상/임상 2상a 시험을 위한 임상시험계획(IND, Investigational New Drug)을 승인(US FDA, 한국 식약처)받아 표적항암제 리보세라닙(아파티닙)다국가(미국-헌쯔만 암센터/한국-아산병원) 임상 1상/2a상을 완료하여 안전성에 대한 검증을 받았습니다. 2017년 위암 2차 이상 표준 치료에 실패한 환자 460명을 대상으로 다국가 임상 3상 진행을 개시한 후 그해 3월 첫 환자 투여를 시작으로 12개국, 88개 병원에서 진행하였으며, 2019년에 9월에 유럽종양학회(ESMO)에서 임상3상에 대한 결과발표를 하였습니다. 이러한 3상 결과를 간략히 요약하면, 리보세라닙의 무진행생존기간(PFS)는 2.83개월, 전체생존기간(OS)은 5.78개월로 나왔습니다. 당시 위암 3차 치료제는 표준요법이 없었기 때문에, 최적지지요법(Best Supportive Care)을 대조군으로 사용하였으며, 대조군 전체생존기간은 5.13개월로 무진행생존기간은 1.77개월로 나왔습니다. 상기 결과치 중 1차 유효성 평가 지표인 전체생존기간은 대조군 대비 높게 나오기는 했으나 통계적 유효성이 부족한 것으로 판단되었습니다. 이에 당사는 3상 종료 직후 OS가 최종 임상 목표치에 도달하지 못하였으며 FDA 승인 진행이 불투명하다는 내용으로 3상 결과 발표를 한 바 있습니다. 이후 당사는 임상 3상의 모든 데이터에 대한 종합적 분석을 진행하였고, 무진행생존기간에 대한 결과는 통계적 유의성을 확보하였고, 다른 평가지표인 객관적반응률 등의 결과도 대조군과 대비하여 월등한 결과를 나왔기 때문에 그 결과가 신약으로서의 가치가 충분하다는 판단하에 FDA와의 Pre NDA Meeting을 진행하였습니다. 이후 신약허가 전문컨설팅회사의 도움을 받아 최선의 신약허가 전략을 수립한 후, NDA 및 신약허가를 추진중에 있습니다.
2019년 4월부터 절제불가능한 간세포암 환자 543명을 대상으로 다국가 임상 3상을 13개국 136개 병원에서 진행하였습니다. 간세포암 1차 치료제로 리보세라닙과 항서제약의 면역항암제인 PD-1 항체인 캄렐리주맙(Camrelizumab)과 병용투여한 이번 임상은 전체생존기간(OS)과 무진행생존기간(PFS)을 1차 유효성 지표로 설정해 간암1차 표준치료제인 ‘소라페닙’(상품명 넥사바)과 대조하는 방식으로 진행되었습니다. 2022년 5월 1차 평가지표인 전체생존기간과 무진행생존기간 모두가 통계적 유의성을 확보하였다고 발표하였고, 본 임상의 결과는 2022년 9월 유럽종양학회(ESMO)에서 공개해 1차 평가지표를 만족했음을 밝혔습니다. 통상적으로 임상 결과의 유효성을 입증하는 1차 평가지표는 적응증, 치료방식, 대조군 등에 따라 다르게 이루어집니다. 당사가 진행한 간암 1차 치료제 글로벌 3상 임상(항서제약 캄렐리주맙 병용)의 경우 기존 1차 치료제인 소라페닙을 대조군으로 하여 OS와 PFS를 1차 평가지표로 하여 진행되었습니다. mOS의 경우 대조군인 소라페닙 대비 6.9개월 긴 22.1개월을 기록했고, mPFS는 대조군 대비 1.9개월 증가한 5.6개월을 기록해(통계적 유의성 확보) 1차 평가지표의 유효성을 만족했습니다.
| [간암 1차 치료제 글로벌 임상 3상 주요 결과] |
| 주요 평가지표 | Rivoceranib + Camrelizumab |
Sorafenib (대조군) |
p-value | HR |
|---|---|---|---|---|
| mOS | 22.1개월 | 15.2개월 | < 0.0001 | 0.62 |
| mPFS | 5.6개월 | 3.7개월 | < 0.0001 | 0.52 |
| ORR | 25.40% | 5.90% | < 0.0001 | - |
| DCR | 78.30% | 53.90% | - | - |
| CR | 3명 | 1명 | - | - |
2020년 선양낭성암 환자에 대해 선양낭성암 1,2차 치료제(Rivoceranib 단독) 다국가 임상 2상 진행을 개시한 후, 그 해 3월 첫환자 투여를 시작으로 미국과 한국에서11개기관에서 진행하였으며, 2022년 6월 미국종양학회(ASCO)에서 결과발표를 하였습니다. 선양낭성암은 아직까지 표준치료제가 없어서, 이번 임상은 대조군 설정 없이 경구용 항암제인 리보세라닙 700mg을 일일 투여 후 객관적반응률과 함께 반응지속기간, 무진행생존기간 등을 확인하는 방식으로 진행됐었습니다. 그 결과를 간단히 요약하면, 80명의 환자를 모집하였으며 1차 지표인 객관적반응률(ORR)이 암의 크기변화를 기준으로 하는 반응평가기준(RECIST v1.1) 15.1%, 크기변화와 함께 밀도를 측정하는 CHOI 평가기준 50.8%에 도달해 선낭암 치료제로 높은 가능성을 확인하였습니다. 당사는 현재 이러한 2상 결과를 바탕으로 FDA에 가속승인(조건부판매)를 목표로 전략을 수립 중에 있습니다. 다만, 이러한 임상 결과에 대한 해석과 판단은 당사의 의견이며, 상기 임상 결과를 토대로 리보세라닙이 신약 허가를 받을 수 있다고 보장할 수는 없다는 점에 유의하시기 바랍니다.
Elevar는 상기 임상 시험 3건을 바탕으로 신약허가 신청(NDA)을 진행할 예정입니다.다만, 의약품의 특성상 연구개발에는 오랜 시간과 많은 자금이 소요되는 반면 완제의약품이 시장에 출시되기 전까지는 본격적인 수익이 발생하지 않기 때문에 임상시험이 실패할 경우 개발회사에 미치는 타격은 막대할 수 있습니다. 따라서 신약허가가 당사가 예상하는대로 진행되지 않을 경우, 임상시험을 진행하고 NDA 신청을 위하여자금을 소요한 연결대상 종속회사인 Elevar의 수익성을 저해하므로, 당사의 연결재무제표에 부정적 영향을 미칠 수 있습니다. 이에, 투자자께서는 의약품 개발사업 특성상 신약허가 여부 및 신약의 상업적 타당성 등에 따라 당사의 재무상태와 실적에 미치는 영향에 유의하여 주시기 바랍니다.
|
카. 핵심인력 및 보유기술 유출에 따른 위험 당사는 지속적인 국내외 특허출원 및 등록을 통해 핵심기술에 대한 권리보호 전략을 실행하고 있으나, 이러한 인력들에 대하여 경쟁업체 및 잠재적 시장진입자 등으로부터의 스카우트 위험이 존재합니다. 핵심 연구인력의 유출은 당사가 축적해 온 기술 관련 노하우, 글로벌 임상시험의 개시 및 운영 노하우 등의 기술유출을 수반할 위험을 내포하고 있습니다. 따라서 당사 핵심 연구인력의 유출 및 보유 기술의 유출은 당사의 사업계획 및 파이프라인에 대한 연구개발계획의 진행에 차질을 발생시킬 수 있으며, 이로 인하여 당사의 성장성, 수익성의 부정적인 영향을 미칠 위험이 존재합니다. |
연구개발 능력은 당사가 속한 산업의 특성상 매우 중요한 요소이며, 지속적인 연구개발을 위해 우수한 인재를 보유 및 유치하는 것이 회사의 성과를 결정하는 가장 중요한 요소입니다. 이는 제약 산업을 영위하고 있는 업체들에 공통적으로 적용되는 사항으로, 업계 내에서 우수한 인력 유치에 관한 경쟁은 점차 심화되고 있습니다. 또한, 주요 연구 인력의 유출이 있을 경우 해당 연구 개발과제가 지연되거나 개발전략을 수정해야 할 가능성이 존재하며, 개발비 부담 등으로 당사의 경쟁력 및 성장 가능성이 악화될 수 있습니다.
당사의 100% 자회사인 Elevar Therapeutics Inc.("Elevar")은 의약품개발을 전문적으로 연구개발하는 NRDO(No Research Development Only) 업체로, 자체적인 신약 후보 물질의 초기 발굴 및 연구 단계 없이 외부에서 신약 기술에 대한 권리를 이전 받아 임상을 통한 신약 개발을 진행합니다. 임상 및 신약 허가 과정을 진행하는 회사의 특성상 연구인력이 Elevar Therapeutics Inc.의 핵심 자산이자 경쟁력이라고 볼 수 있습니다. 신약 연구개발 과정에서는 연구진의 연구개발능력 및 신약 개발 역량이 필수적인 요소이므로 지속적으로 우수한 인재들을 확보하는 것이 사업의 성공률을 높이고 신약을 개발하는데 매우 중요한 요소이기 때문입니다.
① Elevar Therapeutics Inc.
(1) 연구개발 조직 개요
당사의 연결대상 종속회사인 Elevar의 연구개발 조직도 및 조직구성은 다음과 같습니다.
| [Elevar Therapeutics, Inc. 연구개발 조직도] |
|
| (자료: Elevar Therapeutics, Inc. 제공) |
당사의 100% 자회사인 Elevar Therapeutics, Inc.는 임상개발 연구소(미국 솔트레이크 시티 및 샌프란시스코 소재) 산하 5개 팀, 규제과학 연구소 (미국 솔트레이크 시티및 샌프란시스코 소재)산하 2개 팀, 임상후보물질개발 및 생산관리 연구소 (미국 솔트레이크 시티 및 샌프란시스코 소재) 산하 1개 팀 그리고 지적재산권 연구소(미국 솔트레이크 시티) 등 총 4개 연구소 8개 팀으로 구성되어 있으며, 그 현황은 다음과 같습니다.
| [Elevar Therapeutics, Inc. 연구개발 조직구성] |
| 연구소 | 팀 | 주요 업무 |
|---|---|---|
| 임상개발 연구소 (Clinical Development) |
임상운영팀 | 임상 CRO 선정 및 관리, 임상 참여 기관 관리 |
| Medical Affairs | 표준치료제 승인 현황 모니터링 및 경쟁약물 승인관련 데이터 관리, 임상 프로토콜 기획 및 작성 |
|
| Clinical Development & Scientific Affairs |
Drug Metabolism and Pharmacokinetics, 임상 전략 수립, 전임상 데이터확보를 위한 프로젝트 관리 |
|
| Drug Safety and Pharmacovigilence |
시판 후 약물안전성 관리 및 소비자 대응 | |
| Biometrics | 임상 데이터 관리 및 분석 | |
| 규제과학 연구소 (Regulatory Development) |
Regulatory Affairs | FDA 가이드라인 및 정책동향 연구, FDA 미팅 및 제출문서 관리 총괄 |
| Quality Assurance | FDA 승인 및 시판 후 GMP관리를 위한 문서품질관리 및 감사 총괄 | |
| 임상 후보물질 개발 및 생산관리 연구소 (R&D Development) |
CMC | 임상 진행 물질 생산 및 재고관리, FDA 승인을 위한 GMP 생산관리 |
| 지적재산권 연구소 (IP Development) | 회사 보유 지적재산 통합관리 및 특허 연장전략 수립 및 실행 | |
| (자료: Elevar Therapeutics, Inc. 제공) |
임상개발 연구소는 임상 기획, 임상 프로토콜 작성, 임상 CRO(Contract Research Organization) 선정 및 관리, 임상참여 기관 관리, 임상 데이터 관리 등 임상 기획 및 운영 전반의 업무를 담당하는 조직입니다. 규제과학 연구소는 미국 FDA 등 전세계 주요 의약품 규제기관의 가이드라인과 요청사항 충족을 위한 법규 및 정책 동향을 연구하고 실행하며, FDA승인을 위한 GMP 문서의 품질관리 및 감사 등을 담당하는 조직입니다. 임상 후보물질 개발 및 생산관리 연구소는 회사의 신규 파이프라인 도입을 위한 임상후보물질을 검토하고 발굴하며,임상 진행 중인 약물에 대한 생산 및 재고관리를 담당합니다. 지적재산권 연구소는 회사 보유 물질에 대한 전세계 라이센스 및 특허 관리, 외부전문가와의 협업을 통해 특허 연장전략을 도출하는 조직입니다.
(2) 연구개발 인력 현황
2022년 8월 12일 기준 현재, 당사는 박사급 16명, 석사급 15명 등 총 48명의 연구인력을 보유하고 있으며, 그 상세 현황은 다음과 같습니다.
| [Elevar Therapeutics, Inc. 연구개발 핵심연구인력 현황] |
| 구분 | 인원 | ||||
|---|---|---|---|---|---|
| 박사 | 석사 | 기타 | 합계 | ||
| 임상개발 연구소 (Clinical Development) |
임상운영팀 | 7 | 8 | 0 | 15 |
| Medical Affairs | 1 | 1 | 0 | 2 | |
| Clinical Development & Scientific Affairs |
1 | 1 | 0 | 2 | |
| Drug Safety and Pharmacovigilence |
2 | 2 | 0 | 4 | |
| Biometrics | 0 | 0 | 4 | 4 | |
| 규제과학 연구소 (Regulatory Development) |
Regulatory Affairs | 2 | 2 | 1 | 5 |
| Quality Assurance | 1 | 1 | 9 | 12 | |
| 임상 후보물질 개발 및 생산관리 연구소 (R&D Development) |
CMC | 2 | 0 | 2 | 4 |
| 지적재산권 연구소 (IP Development) | 0 | 0 | 1 | 1 | |
| 합계 | 16 | 15 | 17 | 48 | |
| (자료: Elevar Therapeutics, Inc. 제공) |
(3) 핵심 연구인력
| 직책 | 성명 | 주요경력 | 주요연구실적 |
| CEO | Saeho Chong | - VP of nonclinical development, Alnylam Pharmaceuticals - Clinical Pharmacology Reviewer at US FDA - Professor at Seoul National University, College of Pharmacy - Head of Metabolism and Pharmacokinetics, Hopewell Site, Bristol-Myers Squibb R&D |
[Associated careers] 1. 4 NDA submission and approval in US and EU in the past five years 2. Discovered and developed new drug candidates in cardiovascular-, metabolic-, immunologic-diseases, and oncology 3. Over 90 publications in peer-reviewed scientific journals |
| Chief Medical Officer | Jan Van Tornout | - SVP, Head of Oncology, Radius Health, Inc. - Head of Clinical Research, ARIDA Phamaceutical, Inc. - Global Clinical Lead, Oncology, Pfizer |
[Publications] 1. Joaquin Mateo, David Olmos, Herlinde Dumez, Srinivasu Poondru, Nancy L. Samberg, Sharon Barr, Jan M. Van Tornout, Fei Jie, Shahneen Sandhu, D. S. Tan, Victor Moreno, P.(2016) "A first in man, dose-finding study of the mTORC1/mTORC2 inhibitor OSI-027 in patients with advanced solid malignancies" British Journal of Cancer. Apr;114(8):889-896. |
| Chief Operating Officer | Seong Hoon Jang | - Lead Pharmacologist at USFDA - PhD. In Pharmacetics at Ohio State Univ. - Ms. In Pharmacokinetics at Seoul National Univ. |
[Associated careers] 1. Reviews of >50 NDAs and >500 INDs 2. 28 publications in peer-reviewed scientific journals 3. Contributed to development of numerous FDA Guidances for Industry and NDA/IND Review Policies |
| Vice President, Clinical Pharmacology |
Honghui Zhou | - Head of Pharmacometrics (US), Janssen/Johnson & Johnson - Clinical Pharmacology Head of Immunology, Janssen/ Johnson & Johnson - Head of Pharmacological and Translational Modeling, Janssen/Johnson & Johnson - Head of Biotherapeutics PK/PD and Modeling & Simulation, Centocor/Johnson & Johnson - Director of Clinical Pharmacology, Pfizer |
[Associated careers] 1. Contributed to approvals of 8 first-time BLAs and a number of sBLAs/sNDAs 2. Co-edited three books in therapeutic protein drug development, translational ADME and drug-drug interactions 3. Authored and co-authored >150 publications in peer-reviewed scientific journals and book chapters 4. Advanced numerous clinical product candidates of early and late-stage assets for immune-mediated inflammatory diseases, oncology/hematology, cardiovascular/metabolic disease therapeutic areas |
| Vice President, Drug Safety and Pharmacovigilance | David Lilienfield | - Senior Director, Safety, Pharmacovigilance and Epidemiology, Recursion - MD, medicine, Univ. of Maryland School of Medicine |
[Associated careers] 1. Lilienfeld's Foundations of Epidemiology, 2015 2. Comparison of 2 Interventions for Liquid Aspiration on Pneumonia Incidence A Randomized Trial and over 70 articles and data |
| Vice President, Clinical Operations and Data Management | Jennifer Lee | - Executive Director, Head of Oncology Clinical Development, Radius Health - Head of Clinical Operations for startup biotech companies, Medeor and Iovance - Leadership role at Pfizer, Astellas, and Gilead |
[Associated careers] 1. Contributed to approvals of 7 novel treatments in global markets and subsequent filings 2. Contributed to successful global inspection outcomes with FDA/EMA/MHRA/PDMA/NMPA 3. 10 publications in peer-reviewed scientific journals and abstracts 4. Advanced numerous clinical product candidates of early and late stage assets for (Immuno)-oncology, neurological disorder, cardiovascular, and infectious disease therapeutic areas, resulted in global market applications, licensing agreements, and labeling changes |
| (자료: Elevar Therapeutics, Inc. 제공) |
이러한 핵심인력들이 경쟁회사 등 외부로 유출되거나 퇴직하는 경우, 추진 중인 개발사업이 지연되거나 개발 전략을 수정해야 할 수도 있습니다. 또한 회사의 외적 규모가 크거나 인지도가 높지 않아 대기업 또는 연구소, 대형병원 등에 비해 우수 인력 유치가 상대적으로 불리한 측면이 있고, 향후 핵심 인력의 유출로 인한 핵심 보유 기술의 유출이 발생할 가능성을 배제할 수 없습니다.
따라서 당사 및 당사의 100% 자회사인 Elevar Therapeutics Inc. 는 핵심인력의 유지 및 연구개발역량 강화를 위한 수단으로서 외부전문가를 활용하거나 주식매수선택권과 같은 성과 보상제도를 제공하여 핵심인력의 유출 방지에 최선을 다하고 있습니다.
| [Elevar Therapeutics, Inc.의 주식매수선택권 부여 및 행사현황] |
| 부여일 | 부여대상 | 부여주식매수선택권 수량 | 행사가격 | 행사수량 | 권리소멸수량 | 권리소멸사유 | 주식매수선택권의행사기간 |
|---|---|---|---|---|---|---|---|
| 2015-02-16 | Alex Kim | 359,227 | $ 3.38 | - | 51,319 | 퇴사 | - |
| 2015-03-01 | Arlo McGinn | 119,742 | $ 3.38 | 68,397 | - | - | 2025-03-01 |
| 2015-02-16 | Angie Price | 59,871 | $ 3.38 | 23,948 | - | - | 2025-02-16 |
| 2015-02-16 | Sung Chul Kim | 478,967 | $ 3.38 | 273,587 | 205,380 | 퇴사 | - |
| 2015-03-01 | Cheol Hee Park | 83,819 | $ 3.38 | 47,873 | - | - | 2025-03-01 |
| 2018-09-01 | Jiyeun Kim | 20,836 | $ 7.48 | 8,751 | 12,085 | 퇴사 | - |
| 2018-09-01 | Hyungsun Park | 13,890 | $ 7.48 | 5,834 | 8,056 | 퇴사 | - |
| 2018-09-01 | Yufei Chen | 20,836 | $ 7.48 | 8,751 | 12,085 | 퇴사 | - |
| 2018-09-01 | Yash Jain | 20,836 | $ 7.48 | 8,751 | 12,085 | 퇴사 | - |
| 2018-12-31 | Sung Chul Kim | 898,068 | $ 7.48 | - | 898,068 | 퇴사 | - |
| 2019-01-01 | Phaedra Kilbourn | 59,872 | $ 7.48 | - | - | - | 2028-12-31 |
| 2020-07-01 | Angie Price | 50,000 | $ 10.00 | 43,750 | 퇴사 | - | |
| 2020-07-01 | Abdalla Saad | 50,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Jessica Hearn | 20,000 | $ 10.00 | 17,500 | 퇴사 | - | |
| 2020-07-01 | Anthony Medina | 20,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Cheol Hee Park | 50,000 | $ 10.00 | - | - | - | 2030-07-01 |
| 2020-07-01 | Christian George | 20,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Jamison Pitcher | 7,500 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Phaedra Kilbourn | 10,000 | $ 10.00 | - | - | - | 2030-07-01 |
| 2020-07-01 | Sylvia Acacio | 20,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Dong-Gun Kim | 120,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Angie Price | 10,000 | $ 10.00 | 8,750 | 퇴사 | - | |
| 2020-08-20 | Phil Stevens | 50,000 | $ 10.00 | - | - | - | 2030-08-19 |
| 2020-08-31 | Bill Strickland | 50,000 | $ 10.00 | - | - | - | 2030-08-30 |
| 2020-09-14 | Ryan West | 7,500 | $ 10.00 | - | - | - | 2030-09-13 |
| 2020-09-24 | Gayathri Nagaraj | 7,500 | $ 10.00 | - | - | - | 2030-09-23 |
| 2020-10-07 | YoSeph Kuh | 35,000 | $ 10.00 | - | - | - | 2030-10-06 |
| 2020-10-19 | Sunam Tiwari | 5,000 | $ 10.00 | - | - | - | 2030-10-18 |
| 2020-11-02 | Jojo Maloles | 50,000 | $ 10.00 | - | - | - | 2030-11-01 |
| 2020-11-30 | Diane Dahill | 50,000 | $ 10.00 | - | - | - | 2030-11-29 |
| 2020-11-30 | Lativla Lee | 25,000 | $ 10.00 | - | 21,875 | 퇴사 | - |
| 2020-12-21 | Siva Gudi | 50,000 | $ 10.00 | - | - | - | 2030-12-20 |
| 2021-02-01 | Dong-Gun Kim | 100,000 | $ 10.00 | - | - | - | 2031-01-31 |
| 2021-02-16 | Ramya Surapaneni | 7,500 | $ 10.00 | - | - | - | 2031-02-15 |
| 2021-03-15 | Thomas Sanford | 7,500 | $ 10.00 | - | - | - | 2031-03-14 |
| 2021-05-01 | Ashley Contreras | 7,500 | $ 10.00 | - | - | - | 2031-04-30 |
| 2021-05-01 | Tara Blahnik | 6,000 | $ 10.00 | - | - | - | 2031-04-30 |
| 2021-05-10 | Brandi Cunningham | 6,000 | $ 10.00 | - | - | - | 2031-05-09 |
| 2021-06-08 | Dominick DiPaolo | 75,000 | $ 10.00 | - | - | - | 2031-06-07 |
| 2021-08-09 | Neena Chevalier | 6,000 | $ 10.00 | - | - | - | 2031-08-08 |
| 2021-08-10 | MaryEllen Lander | 35,000 | $ 10.00 | - | - | - | 2031-08-09 |
| 2021-08-16 | Temitope O Amosu | 20,000 | $ 10.00 | - | - | - | 2031-08-15 |
| 2021-08-16 | Jennifer H Lee | 75,000 | $ 10.00 | - | - | - | 2031-08-15 |
| 2021-08-23 | Simul Dharia | 20,000 | $ 10.00 | - | - | - | 2031-08-22 |
| 2021-08-23 | John Van Ngo | 6,000 | $ 10.00 | - | - | - | 2031-08-22 |
| 2021-08-30 | Gerald M Walis | 35,000 | $ 10.00 | - | - | - | 2031-08-29 |
| 2021-09-20 | Danette L Astolfi | 35,000 | $ 10.00 | - | - | - | 2031-09-19 |
| 2021-09-20 | Joseph Blackwell Reitano | 35,000 | $ 10.00 | - | - | - | 2031-09-19 |
| 2021-09-28 | Donna R Donigi-Gale | 35,000 | $ 10.00 | - | - | - | 2031-09-27 |
| 2021-10-11 | Jared M Brooslin | 20,000 | $ 10.00 | - | - | - | 2031-10-10 |
| 2021-10-18 | Jisui Zhang | 35,000 | $ 10.00 | - | - | - | 2031-10-17 |
| 2021-11-01 | David Marshall Tromblay | 6,000 | $ 10.00 | - | - | - | 2031-10-31 |
| 2021-12-06 | Karen Custodio | 20,000 | $ 10.00 | - | - | - | 2031-12-05 |
| 2021-12-06 | Heidi Quisito | 20,000 | $ 10.00 | - | - | - | 2031-12-05 |
| 2021-12-06 | Kathleen Wallace | 6,000 | $ 10.00 | - | - | - | 2031-12-05 |
| 2021-12-13 | Amy Brown | 6,000 | $ 10.00 | - | - | - | 2031-12-12 |
| 2022-01-01 | Yesenia Torres-Loya | 35,000 | $ 10.00 | - | - | - | 2031-12-31 |
| 2022-01-01 | Jonathan Azucena | 6,000 | $ 10.00 | - | - | - | 2031-12-31 |
| 2022-01-01 | Lynda Finis | 35,000 | $ 10.00 | - | - | - | 2031-12-31 |
| 2022-01-01 | Rupesh Patki | 35,000 | $ 10.00 | - | - | - | 2031-12-31 |
| 2022-01-18 | Alex Garner | 6,000 | $ 10.00 | - | - | - | 2032-01-17 |
| 2022-01-31 | Lisa Rivera | 20,000 | $ 10.00 | - | - | - | 2032-01-30 |
| 2022-02-07 | Lisa Palmisano | 6,000 | $ 10.00 | - | - | - | 2032-02-06 |
| 2022-02-07 | Karanjit Dhaliwal | 35,000 | $ 10.00 | - | - | - | 2032-02-06 |
| 2022-02-07 | Jacqueline Blazek | 35,000 | $ 10.00 | - | - | - | 2032-02-06 |
| 2022-02-07 | Amy Salveggio | 20,000 | $ 10.00 | - | - | - | 2032-02-06 |
| 2022-02-07 | Carolina Silva | 4,000 | $ 10.00 | - | - | - | 2032-02-06 |
| 2022-02-07 | Deanna Giglio | 6,000 | $ 10.00 | - | - | - | 2032-02-06 |
| 2022-02-07 | Vinoo Urity | 35,000 | $ 10.00 | - | - | - | 2032-02-06 |
| 2022-02-07 | Lissa Nazal | 35,000 | $ 10.00 | - | - | - | 2032-02-06 |
| 2022-02-07 | Allison Hoover | 20,000 | $ 10.00 | - | - | - | 2032-02-06 |
| 2022-02-07 | Michael Palucki | 75,000 | $ 10.00 | - | - | - | 2032-02-06 |
| 2022-05-09 | Daniel Benitez | 6,000 | $ 10.00 | - | - | - | 2032-05-08 |
| 2022-05-23 | Petchel Michael | 35,000 | $ 10.00 | - | - | - | 2032-05-22 |
| 2022-05-23 | Wiseman Tyler | 35,000 | $ 10.00 | - | - | - | 2032-05-22 |
| 2022-05-23 | Wilkins Shanita | 20,000 | $ 10.00 | - | - | - | 2032-05-22 |
| 2022-05-23 | Zhou Honghui | 75,000 | $ 10.00 | - | - | - | 2032-05-22 |
| 2022-05-23 | Schaffer Callissa | 6,000 | $ 10.00 | - | - | - | 2032-05-22 |
| 2022-06-06 | Lilienfeld David | 75,000 | $ 10.00 | - | - | - | 2032-06-05 |
| 2022-06-06 | Schooley Gordon | 75,000 | $ 10.00 | - | - | - | 2032-06-05 |
| 2022-06-20 | Huda Afra | 20,000 | $ 10.00 | - | - | - | 2032-06-19 |
| 2015-02-16 | Soo Whan Choi | 263,432 | $ 3.38 | 75,234 | - | - | 2025-02-16 |
| 2016-08-16 | Sunil Sharma | 941,175 | $ 3.38 | 564,705 | - | - | 2026-08-15 |
| 2018-09-01 | Mikyoung Hahn | 119,743 | $ 7.48 | 23,949 | 95,794 | 퇴사 | - |
| 2018-08-21 | Anton Gueth | 119,743 | $ 7.48 | - | - | - | 2028-08-20 |
| 2019-01-01 | Jae Hong Kim | 35,923 | $ 7.48 | - | - | - | 2028-12-31 |
| 2020-07-01 | Jaehong Kim | 50,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-10-01 | Yoon-Ku Kang | 60,000 | $ 10.00 | - | - | - | 2030-09-30 |
| 2020-07-01 | Anthony Severini | 340,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Arlo McGinn | 220,000 | $ 10.00 | - | 137,500 | 퇴사 | - |
| 2019-01-01 | Ki Hong Ahn | 59,872 | $ 7.48 | - | - | - | 2028-12-31 |
| 2020-07-01 | Bokhwan Chun | 70,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Yong-Hae Han | 70,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Sang Woo Nam | 60,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | soon Ki Do | 60,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Ki-Hwan Kim | 30,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Matthew Chang | 30,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | In Keun Jang | 30,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Ki Hong Ahn | 30,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Hyuk Joo Jee | 20,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Jeong Hwan Moon | 20,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 2020-07-01 | Dae Ho Lee | 20,000 | $ 10.00 | - | - | - | 2030-06-30 |
| 합 계 | 1,077,693 | 1,507,441 | - | - | |||
| (자료: Elevar Therapeutics, Inc. 제공) * 기 부여된 주식매수선택권 중 주식매수선택권 행사기간이 만료한 주식매수선택권 및 퇴사로 전량 소멸한 주식매수선택권은 기재하지 아니함 |
② Immunomic Therapeutics Inc.
| [Immunomic Therapeutics Inc. 연구개발 조직도] |
|
| (자료: Immunomic Therapeutics Inc. 제공) |
당사가 41.07% 보유한 자회사인 Immunomic Therapeutics, Inc.는 임상개발 연구소산하 3개 팀, 규제과학 연구소 산하 2개 팀 등 총 2개 연구소 5개 팀으로 구성되어 있으며, 그 현황은 다음과 같습니다.
| [Immunomic Therapeutics, Inc. 연구개발 조직구성] |
| 연구소 | 팀 | 주요 업무 |
|---|---|---|
| 임상개발 연구소 (Clinical Development) |
임상운영팀 | 임상 CRO 선정 및 관리, 임상 참여 기관 관리 |
| Cell Therapy Operation | Cell Therapy, CMC, Manufacturing & Supply, Process Development | |
| Research & Development | Research & Development | |
| 규제과학 연구소 (Regulatory Development) |
Regulatory Affairs | FDA 가이드라인 및 정책동향 연구, FDA 미팅 및 제출문서 관리 총괄 |
| Quality Assurance | FDA 승인 및 시판 후 GMP관리를 위한 문서품질관리 및 감사 총괄 |
임상개발 연구소는 임상 기획, 임상 프로토콜 작성, 임상 CRO(Contract Research Organization) 선정 및 관리, 임상참여 기관 관리, 임상 데이터 관리 등 임상 기획 및 운영 전반의 업무를 담당하는 조직입니다. 규제과학 연구소는 미국 FDA 등 전세계 주요 의약품 규제기관의 가이드라인과 요청사항 충족을 위한 법규 및 정책 동향을 연구하고 실행하며, FDA승인을 위한 GMP 문서의 품질관리 및 감사 등을 담당하는 조직입니다.
(2) 연구개발 인력 현황
2022년 8월 12일 기준 현재, 당사는 박사급 9명, 석사급 6명 등 총 26명의 연구인력을 보유하고 있으며, 그 상세 현황은 다음과 같습니다.
| [Immunomic Therapeutics, Inc. 연구개발 인력 현황] |
| 구분 | 인원 | ||||
|---|---|---|---|---|---|
| 박사 | 석사 | 기타 | 합계 | ||
| 임상개발 연구소 (Clinical Development) |
임상운영팀 | 0 | 1 | 3 | 4 |
| Cell Therapy Operation | 2 | 3 | 1 | 6 | |
| Research & Development | 7 | 1 | 3 | 11 | |
| 규제과학 연구소 (Regulatory Development) |
Regulatory Affairs | 0 | 1 | 1 | 2 |
| Quality Assurance | 0 | 0 | 3 | 3 | |
| 합계 | 9 | 6 | 11 | 26 | |
| (자료: Immunomic Therapeutics, Inc. 제공) |
(3) 핵심 연구인력
| 직책 | 성명 | 주요경력 | 주요연구실적 |
| CEO | William Hearl | CSO, Capital Genomix EVP, Kirkegaard & Perry Laboratories |
[Patents] 1. Nucleic Acids for the Treatment of Allergy (PCT/US2012/042552, issued Japan) 2. Nucleic Acids for the Treatment of Peanut Allergies (PCT/US2015/321,366) 3. Chimeric Vaccines (US Pat No. 8,445,660 & 8,318,173) [Publication] 1. W. G. Hearl, M. E. Boling, M. H. Jones and E. Volkin. (1982) "Compartmentation of the Nucleotide Pool." Fed. Proc. 41, 1295. 2. William G. Hearl and K. Bruce Jacobson. (1984) "Eye Pigment Granules of Drosophila melanogaster: Isolation and Characterization for Synthesis of Sepiapterin and Precursors of Drosopterin." Insect Biochem. 14, 329-335. 3. William G. Hearl and Jorge E. Churchich. (1984) "Interaction between 4-Aminobutyrate Aminotransferase and Succinic Semialdehyde Dehydrogenase, Two Mitochondrial Enzymes." J. Biol. Chem. 259, 11459-11463. |
| CSO | Teri Heiland, PhD | SVP, R&D VP, R&D Section Leader, Capital Genomix |
[Patents] 1. Genetic Immunization of transgenic animals with non-eukaryotic expression system (20060026697) 2. Combinatorial Oligonucleotide PCR: A Method for rapid global expression analysis (US Pat No. 6,221,600) 3. Combinatorial Oligonucleotide PCR (7,115,370) [Publication] 1. Hartman Z, Chen A, Xu R, Wang T, Wei J, Liu C, Lei G, Lyerly HK, Heiland T. (2020) HER2-LAMP vaccines effectively traffic to endolysosomal compartments and generate enhanced polyfunctional T cell responses that induce complete tumor regression. J Immunother Cancer 2020 Jun;8(1):e000258. doi: 10.1136/jitc-2019-000258 2. Su Y, Romeu-Bonilla E, Anagnostou A, Fitz-Patrick D, Hearl W, Heiland T (2017). Safety and long-term Immunological effects of CryJ2-LAMP plasmid vaccine in Japanese red cedar atopic subjects: A phase I study. Hum Vaccin Immunother. Dec 2; 13(12):2804-2813. 3. Su Y, Romeu-Bonilla E, and Heiland, T. (2017). Next generation immunotherapy for tree pollen allergies. Hum Vaccine Immunother. Oct 3; 13(10):2402-2415. |
| Director, Research & Development |
Mohan Karkada, PhD | Director, Research & Development Sr Staff Scientist, Wyss Institute at Harvard Medical School Director, Cancer Immunotherapy, Immunovaccine Inc. Sr Scientist, Dalhousie University Post-Doctoral Fellow, McGill University PhD, Immunology |
[Patents] 1. Use of Liposomes in a carrier comprising a continuous hydrophobic phase for deliver of polynucleotides in vivo (Pat No. US010232052B2) 2. Compositions Comprising Liposomes, An Antigen, A Polynucleotide and A Carrier Comprising a Continuous Phase of a Hydrophobic Substance(Pat No. US 20190290743A1) [Publication] 1. Super, M., Doherty, E.J., Cartwright, M.J., Mohan Karkada et al.(2022) "Biomaterial vaccines protect against bacterial infections and septic shock" Nature Biomed Eng. Jan;6(1):8-18 2. Heil L Berinstein, Mohan Karkada et al. (2015) "Survivin-targeted immunotherapy drives robust polyfunctional T cell generation and differentiation in advanced ovarian cancer patients" Oncoimmunology. May 7;4(8):e1026529 3. Sergio Rutella, Michael A Cannarile, Mohan Karkada, et al.(2020) "Society for Immunotherapy of Cancer clinical and biomarkers data sharing resource document - conceptual and practical challenges" J Immunother Cancer. Oct;8(2):e001472 [Associated careers] 1. Member, Society for Immunotherapy of Cancer Task Force, Clinical biomarker data sharing; 2018-2020 |
| Vice President, Clinical Operations |
Scott Rodgers | Sr. Director, Clinical Operations Sr. Director, Clinical Operations, Leadiant Biosciences Director, Clinical Affairs, Leadiant Biosciences Sr. Mgr., Clinical Research, Sigma Tau Pharmaceuticals Project Manager, SGS Life Sciences Services MS, Veterinary Science |
[Associated careers] 1. Contribution to leading and developing clinical operation divisions over 20 years 2. Focusing on clinical development strategy, clinical operations, sponsor oversight and project management over 35 Phase I-IV studies in biotechnology 3. Experience in government studies over 12 studies. 12 studies of Clinical Research Organization, and 11 studies of Sponsor in vaccines, drugs/biologic, and devices area |
| Vice President, Quality Assurance |
Cara Sholter | Director, Quality Assurance Head of QA, Lonza Deputy Director of QA, Sanofi Pasteur Biologics Quality Assurance Senior Manager, MedImmune BS in Chemistry |
[Associated careers] 1. Over 20 years of Pharmaceutical experience and 3 years of Medical Device experience 2. Primary areas of expertise are quality / compliance, quality operations, facilities, and manufacturing / process equipment, process control systems in pharmaceutical and medical device environments 3. Established a consistent and reliable release process to satisfy customer demands |
| Vice President, Operations |
Brian Stamper | Sr Director, Manufacturing, Kite Pharma Director, Manufacturing, Lonza Associate Director, Maufacturing, AstraZeneca MS in Biotechnology Enterprise & Entrepreneurship; Johns Hopkins Univ |
[Associated careers] 1. Cell Culture Engineering XIV 2014: “Technology Transfer: Process Fit and Scale-Up for Manufacturing of Biologicals” Joint presentation with colleague from Merck Research Labs 2. IBC Process2Product 2012: “Data Management Approach to Enable Successful Technology Transfer within a Trusted Partner Network” 3. Pharmaceutical Manufacturing, April 2009: “Bioreactor Operational Excellence: Best practices from Scale-Up to Control” [Publication] 1. Statistically Designed Calibration for Near Infrared Spectrometric Monitoring of Mammalian Cell Culture. Purdue University. 2017 |
| (자료: Immunomic Therapeutics, Inc. 제공) |
이러한 핵심인력들이 경쟁회사 등 외부로 유출되거나 퇴직하는 경우, 추진 중인 개발사업이 지연되거나 개발 전략을 수정해야 할 수도 있습니다. 또한 회사의 외적 규모가 크거나 인지도가 높지 않아 대기업 또는 연구소, 대형병원 등에 비해 우수 인력 유치가 상대적으로 불리한 측면이 있고, 향후 핵심 인력의 유출로 인한 핵심 보유 기술의 유출이 발생할 가능성을 배제할 수 없습니다.
따라서 당사의 자회사인 Immunomic Therapeutics Inc. 는 핵심인력의 유지 및 연구개발역량 강화를 위한 수단으로서 외부전문가를 활용하거나 주식매수선택권과 같은 성과 보상제도를 제공하여 핵심인력의 유출 방지에 최선을 다하고 있습니다.
| [Immunomic Therapeutics, Inc.의 주식매수선택권 부여 및 행사현황] |
| 부여일 | 부여대상 | 부여 주식매수선택권 수량 | 행사가격 | 행사수량 | 권리소멸수량 | 권리소멸사유 | 주식매수선택권의 행사기간 |
|---|---|---|---|---|---|---|---|
| 2012-12-31 | Andrew D Luber | 3,000 | $ 1.66 | 3,000 | - | - | 2022-12-30 |
| 2013-01-01 | W. Barry McDonald | 50,000 | $ 1.66 | - | - | - | 2022-12-31 |
| 2013-01-01 | Bruce Mackler | 25,000 | $ 1.66 | - | - | - | 2022-12-31 |
| 2013-01-01 | James W. Wishart | 25,000 | $ 1.66 | - | - | - | 2022-12-31 |
| 2013-01-01 | Ron Thiboutot / LSGPA | 25,000 | $ 1.66 | - | - | - | 2022-12-31 |
| 2013-01-02 | Teri Jones-Heiland | 15,000 | $ 1.66 | - | - | - | 2023-01-01 |
| 2013-01-02 | Athanasia Anagnostou | 12,500 | $ 1.66 | - | - | - | 2023-01-01 |
| 2013-01-02 | Bernard Rudnick | 10,000 | $ 1.66 | - | - | - | 2023-01-01 |
| 2013-01-02 | Michael Connolly | 5,000 | $ 1.66 | - | - | - | 2023-01-01 |
| 2013-01-02 | Anthony Marketon | 2,500 | $ 1.66 | 2,500 | - | - | 2023-01-01 |
| 2013-01-02 | Ira Wallace | 5,000 | $ 1.66 | - | - | - | 2023-01-01 |
| 2013-02-19 | William G. Hearl | 89,760 | $ 1.66 | 89,760 | - | - | 2023-02-18 |
| 2013-02-19 | William G. Hearl | 60,240 | $ 1.66 | 60,240 | - | - | 2023-02-18 |
| 2013-09-01 | Yan Su | 5,000 | $ 1.83 | 5,000 | - | - | 2023-08-31 |
| 2015-01-01 | Pivot Oncology | 10,000 | $ 1.83 | - | - | - | 2024-12-31 |
| 2015-01-01 | Shan Lu | 10,000 | $ 1.83 | 7,500 | - | - | 2024-12-31 |
| 2014-01-24 | Bruce Mackler | 15,000 | $ 2.20 | - | - | - | 2024-01-23 |
| 2014-01-24 | Bernard Rudnick | 15,000 | $ 2.20 | - | - | - | 2024-01-23 |
| 2014-01-24 | James W. Wishart | 15,000 | $ 2.20 | - | - | - | 2024-01-23 |
| 2014-01-24 | Ron Thiboutot / LSGPA | 15,000 | $ 2.20 | - | - | - | 2024-01-23 |
| 2014-01-24 | Michael Lack | 15,000 | $ 2.20 | - | - | - | 2024-01-23 |
| 2014-01-24 | W. Barry McDonald | 15,000 | $ 2.20 | - | - | - | 2024-01-23 |
| 2014-01-24 | William G. Hearl | 50,000 | $ 2.20 | 26,389 | - | - | 2024-01-23 |
| 2014-03-01 | Yan Su | 5,000 | $ 2.20 | 5,000 | - | - | 2024-02-28 |
| 2014-04-24 | Teri Jones-Heiland | 25,000 | $ 2.20 | - | - | - | 2024-04-23 |
| 2014-04-24 | Athanasia Anagnostou | 12,500 | $ 2.20 | - | - | - | 2024-04-23 |
| 2014-04-24 | Michael Connolly | 5,000 | $ 2.20 | - | - | - | 2024-04-23 |
| 2014-04-24 | Anthony Marketon | 2,500 | $ 2.20 | 2,500 | - | - | 2024-04-23 |
| 2014-04-24 | Melissa Kemp | 1,500 | $ 2.20 | - | - | - | 2024-04-23 |
| 2014-05-30 | Bruce Mackler | 40,000 | $ 2.20 | - | - | - | 2024-05-29 |
| 2014-05-30 | Bernard Rudnick | 25,000 | $ 2.20 | - | - | - | 2024-05-29 |
| 2014-05-30 | James W. Wishart | 55,000 | $ 2.20 | - | - | - | 2024-05-29 |
| 2014-05-30 | Ron Thiboutot / LSGPA | 25,000 | $ 2.20 | - | - | - | 2024-05-29 |
| 2014-05-30 | Michael Lack | 25,000 | $ 2.20 | - | - | - | 2024-05-29 |
| 2014-05-30 | W. Barry McDonald | 50,000 | $ 2.20 | - | - | - | 2024-05-29 |
| 2015-02-24 | William G. Hearl | 13,510 | $ 2.20 | 13,510 | - | - | 2025-02-23 |
| 2015-02-24 | William G. Hearl | 161,490 | $ 2.20 | 161,490 | - | - | 2025-02-23 |
| 2015-02-24 | James W. Wishart | 125,000 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | Bernard Rudnick | 125,000 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | W. Barry McDonald | 125,000 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | Bruce Mackler | 125,000 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | Colin Magowan | 50,000 | $ 2.20 | 50,000 | - | - | 2025-02-23 |
| 2015-02-24 | Teri Jones-Heiland | 31,569 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | Teri Jones-Heiland | 93,431 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | Michael Connolly | 5,000 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | Yan Su | 5,000 | $ 2.20 | 5,000 | - | - | 2025-02-23 |
| 2015-01-25 | Larry Weiner | 100,000 | $ 2.20 | - | - | - | 2025-01-24 |
| 2015-02-24 | Larry Weiner | 10,000 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | Melissa Kemp | 1,500 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | Athanasia Anagnostou | 25,000 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | Anthony Marketon | 5,000 | $ 2.20 | 5,000 | - | - | 2025-02-23 |
| 2015-02-24 | Eliezer Romeu-Bonilla | 5,000 | $ 2.20 | 5,000 | - | - | 2025-02-23 |
| 2015-02-24 | Timothy Coleman | 84,341 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | Timothy Coleman | 15,659 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | William G. Hearl | 67,675 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-02-24 | William G. Hearl | 32,325 | $ 2.20 | - | - | - | 2025-02-23 |
| 2015-05-05 | Eric Winzer | 90,908 | $ 2.20 | 15,000 | - | - | 2025-05-04 |
| 2015-05-05 | Eric Winzer | 34,092 | $ 2.20 | - | - | - | 2025-05-04 |
| 2015-05-05 | Louise Peltier | 50,000 | $ 2.20 | - | - | - | 2025-05-04 |
| 2015-05-28 | W. Barry McDonald | 65,000 | $ 3.20 | - | - | - | 2025-05-27 |
| 2015-05-28 | James W. Wishart | 40,000 | $ 3.20 | - | - | - | 2025-05-27 |
| 2015-05-28 | Ron Thiboutot / LSGPA | 40,000 | $ 3.20 | - | - | - | 2025-05-27 |
| 2015-05-28 | Michael Lack | 25,000 | $ 3.20 | - | - | - | 2025-05-27 |
| 2015-08-05 | Rhett K. Madison | 25,000 | $ 3.20 | 25,000 | - | - | 2025-08-04 |
| 2015-08-05 | Kal Vepuri | 25,000 | $ 3.20 | 25,000 | - | - | 2025-08-04 |
| 2015-08-05 | GBR Investments | 25,000 | $ 3.20 | 25,000 | - | - | 2025-08-04 |
| 2015-12-21 | William G. Hearl | 20,742 | $ 5.37 | - | - | - | 2025-12-20 |
| 2015-12-21 | William G. Hearl | 129,258 | $ 5.37 | - | - | - | 2025-12-20 |
| 2015-03-30 | Franco Pissani | 5,000 | $ 2.20 | 5,000 | - | - | 2025-03-29 |
| 2015-04-01 | Wei Shen | 5,000 | $ 2.20 | 5,000 | - | - | 2025-03-31 |
| 2015-05-01 | Thierry Olivry | 5,000 | $ 2.20 | 3,750 | - | - | 2025-04-30 |
| 2015-01-01 | Joseph G. Sanginiti | 10,000 | $ 1.33 | 10,000 | - | - | 2024-12-31 |
| 2015-01-01 | McDonald Ventures | 2,500 | $ 2.20 | 2,500 | - | - | 2024-12-31 |
| 2015-01-01 | Sherry Calvert | 2,500 | $ 2.20 | 2,500 | - | - | 2024-12-31 |
| 2016-02-01 | Eric Winzer | 25,000 | $ 5.37 | - | - | - | 2026-01-31 |
| 2016-02-01 | Teri Jones-Heiland | 25,000 | $ 5.37 | - | - | - | 2026-01-31 |
| 2016-02-01 | Louise Peltier | 25,000 | $ 5.37 | - | - | - | 2026-01-31 |
| 2016-02-01 | Athanasia Anagnostou | 25,000 | $ 5.37 | - | - | - | 2026-01-31 |
| 2016-02-01 | Yan Su | 5,000 | $ 5.37 | 4,168 | 832 | 퇴사 | |
| 2016-02-01 | Michael Connolly | 4,000 | $ 5.37 | - | - | - | 2026-01-31 |
| 2016-02-01 | Colin Magowan | 4,000 | $ 5.37 | - | - | - | 2026-01-31 |
| 2016-02-01 | Wei Shen | 3,000 | $ 5.37 | - | - | - | 2026-01-31 |
| 2016-02-01 | Juliete Macauley | 2,500 | $ 5.37 | - | - | - | 2026-01-31 |
| 2016-02-01 | Melissa Kemp | 1,500 | $ 5.37 | - | - | - | 2026-01-31 |
| 2016-02-01 | Lisa Salley | 5,000 | $ 5.37 | - | - | - | 2026-01-31 |
| 2016-02-01 | Gennaro D-Urso | 2,500 | $ 5.37 | - | - | - | 2026-01-31 |
| 2016-02-01 | Rick Schuman | 2,000 | $ 5.37 | - | - | - | 2026-01-31 |
| 2016-03-03 | Arthur Feldman | 10,000 | $ 5.37 | - | - | - | 2026-03-02 |
| 2016-12-01 | Yan Su | 5,000 | $ 5.47 | 2,779 | 2,221 | 퇴사 | |
| 2016-12-01 | Pratima Sinha | 5,000 | $ 5.47 | - | - | - | 2026-11-30 |
| 2016-12-01 | Wei Shen | 3,000 | $ 5.47 | - | - | - | 2026-11-30 |
| 2016-12-01 | Juliete Macauley | 1,000 | $ 5.47 | - | - | - | 2026-11-30 |
| 2016-12-01 | Thomas Murphy | 2,000 | $ 5.47 | - | - | - | 2026-11-30 |
| 2016-12-01 | Melissa Kemp | 1,500 | $ 5.47 | - | - | - | 2026-11-30 |
| 2016-12-01 | Michael Connolly | 3,000 | $ 5.47 | - | - | - | 2026-11-30 |
| 2016-12-01 | Brent Bingham | 2,000 | $ 5.47 | - | - | - | 2026-11-30 |
| 2016-12-01 | Yan Hui | 1,000 | $ 5.47 | - | - | - | 2026-11-30 |
| 2017-06-13 | W. Barry McDonald | 28,000 | $ 5.55 | - | - | - | 2027-06-12 |
| 2017-06-13 | James W. Wishart | 19,000 | $ 5.55 | - | - | - | 2027-06-12 |
| 2017-06-13 | Michael Lack | 19,000 | $ 5.55 | - | - | - | 2027-06-12 |
| 2018-02-01 | Eric Winzer | 24,435 | $ 6.29 | - | - | - | 2028-01-31 |
| 2018-02-01 | Eric Winzer | 565 | $ 6.29 | - | - | - | 2028-01-31 |
| 2018-02-01 | Teri Jones-Heiland | 24,435 | $ 6.29 | - | - | - | 2028-01-31 |
| 2018-02-01 | Teri Jones-Heiland | 565 | $ 6.29 | - | - | - | 2028-01-31 |
| 2018-02-01 | Louise Peltier | 15,000 | $ 6.29 | - | - | - | 2028-01-31 |
| 2018-02-01 | Timothy Coleman | 15,000 | $ 6.29 | - | - | - | 2028-01-31 |
| 2018-02-01 | Athanasia Anagnostou | 7,500 | $ 6.29 | - | - | - | 2028-01-31 |
| 2018-04-19 | Pratima Sinha | 5,000 | $ 6.29 | - | - | - | 2028-04-18 |
| 2018-04-19 | Wei Shen | 3,000 | $ 6.29 | - | - | - | 2028-04-18 |
| 2018-04-19 | Renhuan Xu | 3,000 | $ 6.29 | 3,000 | - | - | 2028-04-18 |
| 2018-04-19 | Michael Connolly | 3,000 | $ 6.29 | - | - | - | 2028-04-18 |
| 2018-04-19 | Greg Wilson | 2,000 | $ 6.29 | - | - | - | 2028-04-18 |
| 2018-04-19 | Thomas Murphy | 2,000 | $ 6.29 | - | - | - | 2028-04-18 |
| 2018-04-19 | Brent Bingham | 2,000 | $ 6.29 | - | - | - | 2028-04-18 |
| 2018-04-19 | Melissa Kemp | 1,500 | $ 6.29 | - | - | - | 2028-04-18 |
| 2018-04-19 | Juliete Macauley | 1,000 | $ 6.29 | - | - | - | 2028-04-18 |
| 2018-04-19 | Jeneice Hamilton | 1,000 | $ 6.29 | - | - | - | 2028-04-18 |
| 2018-04-19 | Yan Hui | 1,000 | $ 6.29 | - | - | - | 2028-04-18 |
| 2018-04-19 | JoAnn Roach | 500 | $ 6.29 | - | - | - | 2028-04-18 |
| 2018-05-03 | John Sampson | 25,000 | $ 6.29 | - | - | - | 2023-05-02 |
| 2018-06-12 | W. Barry McDonald | 25,000 | $ 6.29 | - | - | - | 2028-06-11 |
| 2018-06-12 | James W. Wishart | 19,000 | $ 6.29 | - | - | - | 2028-06-11 |
| 2018-06-12 | Michael Lack | 19,000 | $ 6.29 | - | - | - | 2028-06-11 |
| 2019-02-14 | William G. Hearl | 46,496 | $ 5.24 | - | - | - | 2029-02-13 |
| 2019-02-14 | William G. Hearl | 103,504 | $ 5.24 | - | - | - | 2029-02-13 |
| 2019-02-14 | Eric Winzer | 20,746 | $ 5.24 | - | - | - | 2029-02-13 |
| 2019-02-14 | Eric Winzer | 9,254 | $ 5.24 | - | - | - | 2029-02-13 |
| 2019-02-14 | Teri Jones-Heiland | 20,746 | $ 5.24 | - | - | - | 2029-02-13 |
| 2019-02-14 | Teri Jones-Heiland | 9,254 | $ 5.24 | - | - | - | 2029-02-13 |
| 2019-02-14 | Louise Peltier | 20,000 | $ 5.24 | - | - | - | 2029-02-13 |
| 2019-02-14 | Timothy Coleman | 20,000 | $ 5.24 | - | - | - | 2029-02-13 |
| 2019-02-14 | Athanasia Anagnostou | 15,000 | $ 5.24 | - | - | - | 2029-02-13 |
| 2019-04-01 | Pratima Sinha | 5,000 | $ 5.24 | - | - | - | 2029-03-31 |
| 2019-04-01 | Wei Shen | 5,000 | $ 5.24 | - | - | - | 2029-03-31 |
| 2019-04-01 | Renhuan Xu | 5,000 | $ 5.24 | 4,166 | 834 | 퇴사 | |
| 2019-04-01 | Wenhai Liu | 3,000 | $ 5.24 | 2,250 | 750 | 퇴사 | |
| 2019-04-01 | Michael Connolly | 3,000 | $ 5.24 | - | - | - | 2029-03-31 |
| 2019-04-01 | Greg Wilson | 2,000 | $ 5.24 | - | - | - | 2029-03-31 |
| 2019-04-01 | Juliete Macauley | 2,000 | $ 5.24 | - | - | - | 2029-03-31 |
| 2019-04-01 | Thomas Murphy | 2,000 | $ 5.24 | - | - | - | 2029-03-31 |
| 2019-04-01 | Brent Bingham | 2,000 | $ 5.24 | - | - | - | 2029-03-31 |
| 2019-04-01 | Melissa Kemp | 1,000 | $ 5.24 | - | - | - | 2029-03-31 |
| 2019-04-01 | Jeneice Hamilton | 1,000 | $ 5.24 | - | - | - | 2029-03-31 |
| 2019-04-01 | Yan Hui | 1,000 | $ 5.24 | - | - | - | 2029-03-31 |
| 2019-04-01 | JoAnn Roach | 500 | $ 5.24 | - | - | - | 2029-03-31 |
| 2019-05-03 | John Sampson | 25,000 | $ 5.24 | - | - | - | 2029-05-02 |
| 2019-05-01 | Robert Pierce | 5,000 | $ 5.24 | - | - | - | 2029-04-30 |
| 2019-05-15 | Peter M. Howley | 5,000 | $ 5.24 | - | - | - | 2029-05-14 |
| 2019-05-15 | Ana Tergas | 5,000 | $ 5.24 | - | - | - | 2029-05-14 |
| 2019-05-15 | Anna Giuliano | 5,000 | $ 5.24 | - | - | - | 2029-05-14 |
| 2019-05-15 | Neda Hashemi | 5,000 | $ 5.24 | - | - | - | 2029-05-14 |
| 2019-05-15 | Jeanne Jordan | 5,000 | $ 5.24 | - | - | - | 2029-05-14 |
| 2019-06-11 | James W. Wishart | 19,000 | $ 5.24 | - | - | - | 2029-06-10 |
| 2019-06-11 | Michael Lack | 19,000 | $ 5.24 | - | - | - | 2029-06-10 |
| 2020-04-01 | William G. Hearl | 20,012 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | William G. Hearl | 29,988 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Eric Winzer | 21,078 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Eric Winzer | 3,922 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Teri Jones-Heiland | 21,078 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Teri Jones-Heiland | 3,922 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Louise Peltier | 25,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Timothy Coleman | 25,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Athanasia Anagnostou | 20,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Pratima Sinha | 5,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Wei Shen | 5,000 | $ 3.90 | 1,000 | - | - | 2030-03-31 |
| 2020-04-01 | Renhuan Xu | 5,000 | $ 3.90 | 2,500 | 2,500 | 퇴사 | - |
| 2020-04-01 | Wenhai Liu | 3,000 | $ 3.90 | 1,250 | 1,750 | 퇴사 | - |
| 2020-04-01 | Michael Connolly | 3,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Claire Rosean | 2,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Greg Wilson | 2,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Juliete Macauley | 2,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Thomas Murphy | 2,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Brent Bingham | 2,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Melissa Kemp | 1,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Jeneice Hamilton | 1,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | Yan Hui | 1,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-01 | JoAnn Roach | 500 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-04-13 | William G. Hearl | 20,077 | $ 3.90 | - | - | - | 2030-04-12 |
| 2020-04-13 | William G. Hearl | 479,923 | $ 3.90 | - | - | - | 2030-04-12 |
| 2020-04-13 | Eric Winzer | 15,068 | $ 3.90 | - | - | - | 2030-04-12 |
| 2020-04-13 | Eric Winzer | 184,932 | $ 3.90 | - | - | - | 2030-04-12 |
| 2020-04-13 | Teri Jones-Heiland | 15,068 | $ 3.90 | - | - | - | 2030-04-12 |
| 2020-04-13 | Teri Jones-Heiland | 184,932 | $ 3.90 | - | - | - | 2030-04-12 |
| 2020-04-13 | Louise Peltier | 15,815 | $ 3.90 | - | - | - | 2030-04-12 |
| 2020-04-13 | Louise Peltier | 84,185 | $ 3.90 | - | - | - | 2030-04-12 |
| 2020-04-13 | Timothy Coleman | 15,815 | $ 3.90 | - | - | - | 2030-04-12 |
| 2020-04-13 | Timothy Coleman | 84,185 | $ 3.90 | - | - | - | 2030-04-12 |
| 2020-04-01 | Larry Wellman | 5,000 | $ 3.90 | - | - | - | 2030-03-31 |
| 2020-06-11 | James W. Wishart | 19,000 | $ 5.00 | - | - | - | 2030-05-31 |
| 2020-06-11 | Jee Hyuk Joo | 16,000 | $ 5.00 | - | - | - | 2030-05-31 |
| 2020-06-11 | Bokhwan Chun | 16,000 | $ 5.00 | - | 8,000 | 취소(forfeitures) | - |
| 2020-06-11 | Alex S. Kim | 16,000 | $ 5.00 | - | - | - | 2030-05-31 |
| 2020-06-11 | Arlo McGinn | 16,000 | $ 5.00 | - | - | - | 2030-05-31 |
| 2020-11-01 | Scott Rodgers | 10,000 | $ 5.00 | - | - | - | 2030-10-31 |
| 2020-11-01 | Erin Duffy | 10,000 | $ 5.00 | - | - | - | 2030-10-31 |
| 2020-11-01 | Brian Lee | 2,000 | $ 5.00 | - | - | - | 2030-10-31 |
| 2021-04-01 | Brent Bingham | 2,500 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Michael Connolly | 3,500 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Erin Duffy | 6,000 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Jeneice Hamilton | 2,000 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Yan Hui | 2,000 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Melissa Kemp | 2,000 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Brian Lee | 1,000 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Juliete Macauley | 2,000 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Thomas Murphy | 3,500 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | JoAnn Roach | 500 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Scott Rodgers | 10,000 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Claire Rosean | 2,000 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Wei Shen | 6,000 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Pratima Sinha | 6,000 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-04-01 | Greg Wilson | 2,000 | $ 4.53 | - | - | - | 2031-03-31 |
| 2021-06-22 | Yun-Ting Kao | 3,000 | $ 4.53 | - | - | - | 2031-06-21 |
| 2021-06-22 | Cara Sholter | 10,000 | $ 4.53 | - | - | - | 2031-06-21 |
| 2021-06-22 | Yong Ki Kim | 4,000 | $ 4.53 | - | - | - | 2031-06-21 |
| 2021-06-22 | Mohan Karkada | 10,000 | $ 4.53 | - | - | - | 2031-06-21 |
| 2021-06-22 | Ashley From | 2,000 | $ 4.53 | - | - | - | 2031-06-21 |
| 2021-06-22 | Richard Grimes | 10,000 | $ 4.53 | - | - | - | 2031-06-21 |
| 2021-06-22 | Hyuk Joo, Jee | 16,000 | $ 4.53 | - | - | - | 2031-06-21 |
| 2021-06-22 | Dong-Gun Kim | 19,000 | $ 4.53 | - | - | - | 2031-06-21 |
| 2021-06-22 | Steve S. Park | 16,000 | $ 4.53 | - | - | - | 2031-06-21 |
| 2021-06-22 | James W. Wishart | 19,000 | $ 4.53 | - | - | - | 2031-06-21 |
| 2021-07-19 | Robert Newman | 66,225 | $ 4.53 | - | - | - | 2031-07-18 |
| 2021-07-19 | Robert Newman | 233,775 | $ 4.53 | - | - | - | 2031-07-18 |
| 2021-09-21 | Veronica Gonzalez | 4,000 | $ 4.53 | - | - | - | 2031-09-20 |
| 2021-09-21 | Elizabeth Walsh | 8,000 | $ 4.53 | - | - | - | 2031-09-20 |
| 2021-09-21 | Hyerin Son | 6,000 | $ 4.53 | - | - | - | 2031-09-20 |
| 2022-03-14 | Timothy Coleman | 34,091 | $ 4.57 | - | - | - | 2032-03-13 |
| 2022-03-14 | Timothy Coleman | 909 | $ 4.57 | - | - | - | 2032-03-13 |
| 2022-03-14 | William G. Hearl | 20,834 | $ 4.57 | - | - | - | 2032-03-13 |
| 2022-03-14 | William G. Hearl | 29,166 | $ 4.57 | - | - | - | 2032-03-13 |
| 2022-03-14 | Teri Jones-Heiland | 40,341 | $ 4.57 | - | - | - | 2032-03-13 |
| 2022-03-14 | Teri Jones-Heiland | 9,659 | $ 4.57 | - | - | - | 2032-03-13 |
| 2022-03-14 | Robert Newman | 4,167 | $ 4.57 | - | - | - | 2032-03-13 |
| 2022-03-14 | Robert Newman | 45,833 | $ 4.57 | - | - | - | 2032-03-13 |
| 2022-03-14 | Louise Peltier | 34,091 | $ 4.57 | - | - | - | 2032-03-13 |
| 2022-03-14 | Louise Peltier | 909 | $ 4.57 | - | - | - | 2032-03-13 |
| 2022-03-14 | Eric Winzer | 40,341 | $ 4.57 | - | - | - | 2032-03-13 |
| 2022-03-14 | Eric Winzer | 9,659 | $ 4.57 | - | - | - | 2032-03-13 |
| 2022-04-05 | Brent Bingham | 3,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Michael Connolly | 5,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Erin Duffy | 9,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Ashley From | 2,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Priscilla Fussell | 5,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Marcus Gallon | 3,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Charles (Andy) Giglio | 9,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Veronica Gonzalez | 4,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Richard Grimes | 10,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Jeneice Hamilton | 2,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Yan Hui | 2,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Mohan Karkada | 6,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Yun-Ting Kao | 3,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Melissa Kemp | 2,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Yong Ki Kim | 6,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Kirk Kocan | 8,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Brian Lee | 2,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Erica Leyder | 2,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Juliete Macauley | 2,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Heather Metz | 5,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Thomas Murphy | 5,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | JoAnn Roach | 500 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Scott Rodgers | 10,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Claire Rosean | 6,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Wei Shen | 8,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Cara Sholter | 10,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Pratima Sinha | 8,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Hyerin Son | 8,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Ryan Stadel | 5,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Elizabeth Walsh | 9,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Greg Wilson | 2,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-04-05 | Larry Wellman | 9,000 | $ 4.57 | - | - | - | 2032-04-04 |
| 2022-06-21 | Hyuk Joo, Jee | 16,000 | $ 4.57 | - | - | - | 2032-06-20 |
| 2022-06-21 | Dong-Gun Kim | 19,000 | $ 4.57 | - | - | - | 2032-06-20 |
| 2022-06-21 | Steve S. Park | 16,000 | $ 4.57 | - | - | - | 2032-06-20 |
| 2022-06-21 | James W. Wishart | 19,000 | $ 4.57 | - | - | - | 2032-06-20 |
| 2022-06-21 | Brian Stamper | 65,643 | $ 4.57 | - | - | - | 2032-06-20 |
| 2022-06-21 | Brian Stamper | 134,357 | $ 4.57 | - | - | - | 2032-06-20 |
| 합계 | 494,252 | 16,887 | - | - |
|||
| (자료: Elevar Therapeutics, Inc. 제공) * 기 부여된 주식매수선택권 중 주식매수선택권 행사기간이 만료한 주식매수선택권 및 퇴사로 전량 소멸한 주식매수선택권은 기재하지 아니함 |
그러나 이러한 당사, Elevar 및 Immunomic의 노력 및 정책의 지속 여부와 관련없이 산업 경쟁심화에 따른 우수인력 스카우트 등에 따라 핵심인력이 경쟁회사 또는 다른 산업분야로 이탈할 가능성은 상존합니다. 이러한 경우 Elevar 및 Immunomic의 핵심기술 노하우의 유출 등은 당사의 의약품개발산업 내 경쟁력을 약화시킬 수 있으며, 이는 향후의 영업활동 및 수익성에 부정적인 영향을 미칠 수 있으니 투자판단 시 이 점에 유의하시기 바랍니다.
|
타. 정부정책 및 규제에 관한 위험 제약산업은 인간의 생명 및 건강과 직결되는 의약품을 개발ㆍ제조ㆍ판매하는 산업으로, 제품의 개발ㆍ제조, 임상시험, 인ㆍ허가, 유통ㆍ판매에 이르기까지 전 과정에 걸쳐 각 국가의 규제 당국이 제시하는 엄격한 규정과 절차를 따라야 합니다. 당사는 내부에 담당 인력과 외부 전문가들을 통하여 국내 및 해외 제약 산업 정책 및 규제 환경을 지속적으로 모니터링하고 있으며, 각국의 규제 당국과의 소통을 통해 정책 및 규제 환경의 변화에 효과적으로 대비하기 위해 최선의 노력을 다하고 있습니다. 그러나 실제 효율적인 정책 지원이 이루어지지 않거나, 세부과제 추진에 어려움이 생길 수 있으며, 관련 법규의 제정 및 개정 단계, 예산 확보 등에 난항이 발생할 수 있습니다. 또한 해당 정책의 기대효과가 감소되는 경우 정책 기조의 변화로 정부 지원이 축소될 수 있으며, 조건부 허가와 같은 규제 완화에 대한 실효성이 크지 않을 경우, 규제 완화의 범위가 축소될 수 있습니다. 이러한 정부의 우호적인 정책 및 규제 완화의 변동 가능성은 당사의 사업에 부정적인 영향을 끼칠 수 있습니다. |
제약산업은 인간의 생명 및 건강과 직결되는 의약품을 개발ㆍ제조ㆍ판매하는 산업으로, 제품의 개발 및 제조, 임상시험, 인허가, 유통 및 판매에 이르기까지 전 과정에 걸쳐 각 국가의 규제 당국이 제시하는 엄격한 규정과 절차를 따라야 합니다. 제약 및 신약개발 사업과 관련된 국내 법률 중 당사의 사업과 밀접하게 연관된 법률로는 식품의약품안전처 및 보건복지부 소관의「약사법」이 대표적이며, 그 외 보건복지부 소관의 「국민건강보험법」, 「생명윤리 및 안전에 관한 법률」, 「제약산업 육성 및 지원에 관한 특별법', 「희귀질환관리법」, 「첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률」과 식품의약품안전처 소관의 「실험동물에 관한 법률」 등이 있습니다.
특히, 「약사법」 하위 시행령/시행규칙 중 의약품 등의 안전에 관한 규칙, 의약품 등의 제조업 및 수입자의 시설기준령 시행규칙, 생물학적 제제 등의 제조ㆍ판매관리 규칙, 동물용 의약품등 취급규칙 등과 이의 하위 규정을 준수해야 합니다. 이에 따라, 신약 후보물질의 발굴에서부터 동물을 대상으로 하는 비임상시험, 인체를 대상으로 하는 임상시험, 품목허가에 이르기 까지 임상 승인에 관한 규정, 의약품의 약리 및 독성, 안정성 시험 기준, 임상시험 실시기관 지정에 관한 규정, 품목허가ㆍ심사 등의 규정 등을 반드시 준수하여 진행해야 합니다. 또한 제조 및 판매 단계에서도 제조소 시설 기준, 제조 및 품질관리 규정, 포장 및 공급에 관한 규정, 표시 등에 관한 규정을 준수해야 하며, 사후에도 정기적으로 규제기관으로부터 제품 생산 공정 및 품질관리 전반에 대한 실사 및 관리, 감독을 받게 됩니다. 이러한 규제 및 검증을 통해 제약산업의 선진화 정책을 시현할 수 있지만, 각종 규제 및 절차, 검증 강화로 인한 부담이 높아지는 경우, 당사의 사업에 부정적인 영향을 미칠 수 있습니다.
국내는 단일보험자(국민건강보험공단)에 의한 전국민 건강보험제도를 운영하고 있는상황으로, 건강보험의 지속가능성 제고와 적정수준의 국민의료비 유지, 불법 리베이트 차단 등의 목표 하에 약가에 대해 정책적 개입이 이루어지고 있습니다. 국내의 약가 사후관리제도는 대내외 보건의료 환경변화에 의하여 수 차례 변화되어, 현재는 실거래가 조사에 의한 약가 인하, 사용량-약가 연동 협상, 급여범위 확대 시 약가인하, 제네릭의약품 등재 시 오리지널의약품의 약가인하 등의 제도가 운영되고 있습니다. 약가는 산업 정책과 보건의료 정책이 상충하여 변동성이 상재해 있는 상황으로, 현재제네릭 약가 차등제가 시행 예정되어 있는 상황입니다. 이러한 점진적인 약가 인하 정책은 제약산업에서 간과할 수 없는 중요 요인이며, 당사의 사업에도 부정적인 영향을 미칠 수 있습니다.
| [약가 인하 정책 추이] |
|
시기 |
인하제도 |
내용 |
|---|---|---|
|
2000년 ~ 2009년 |
실거래가약가인하 (표본조사) |
표본조사(전국 80개 요양기관)를 통해 의약품 청구 실태 조사 후 약가인하 |
| 2002년 ~ 2012년 |
약가 재평가 |
최초 상한금액 산정이후 3년마다 7개국 조정 평균가를 |
| 2007년 ~ 2014년 |
기등재 목록정비 |
2007년 선별등재제도로 전환하면서 기존약재의 경우 20% |
| 2012년 |
일괄 약가인하 |
상한금액대비 53.55%수준까지 일괄 약가인하 |
| 2016년 ~ |
실거래가약가인하 (전수조사) |
유통정보센터 유통정보를 근거로 가중평가가격 까지 약가 인하 |
|
현행 |
특허만료 약가인하 |
개별약제 특허만료시 1년간 70%, 1년 후 53.55%로 약가인하 |
|
현행 |
사전 약가인하 |
개별약제 급여기준 확대 이전에 협의를 통하여 약가인하 |
|
현행 |
사용량 약가연동 |
개별약제 약가와 사용량을 연계하여 등재 후 사용량이 일정 % 증가할 때 약가 인하 |
국내의 식품의약품안전처는 희귀의약품이나 항암제, 일부 세포치료제(자가연골세포치료제, 자가피부세포치료제)에 대해 신속한 출시를 허용하는 목적으로 1997년부터 조건부허가제도를 도입하여 식약처 예규로 운영해 왔으며, 2016년부터는 생명을 위협하는 질환 또는 중증의 비가역질환을 대상으로 치료적 탐색(2상) 임상 시험의 허가요건과 그 결과를 충족하는 세포치료제의 경우에도 조건부 허가를 신청할 수 있도록 세포치료제 조건부 허가 범위를 확대하여 운영하고 있는 상황입니다. 이에 따라 해당운영 가이드라인 및 요건에 부합하는 세포치료제는 추후 임상 3상(치료적 확증) 시험자료를 제출하는 조건으로, 임상 2상(치료적 탐색) 시험 자료만으로 우선 허가받아 시판할 수 있게 되었습니다.
「생명윤리법」등에 산재한 바이오의약품 관련 규제를 일원화하며, 신속허가제도 도입 및 안전관리체계를 구축하는 것이 핵심입니다. 본 법이 시행되면 재생의료 임상연구가 가능해져 의료기술의 기술경쟁력을 제고하여 희귀ㆍ난치 질환자에게 새로운 치료 기회를 제공할 수 있을 뿐만 아니라, 품목허가 검증 체계를 첨단바이오의약품 특성에 맞게 재편하여 맞춤형 심사, 우선 심사, 조건부 허가 등의 혜택이 가능할 것으로기대됩니다.
[미국 관련 규제 당국 규제 관련]
미국 FDA는 인체 및 동물용 의약품, 생약 제제, 의료기기, 국가 식량 공급, 화장품, 방사선 제품의 안전성, 유효성 및 안전을 보장함으로써 공중보건을 보호하는 기관입니다. FDA는 식품 및 의약품의 유효성을 확보하고 자국민에게 보다 안전하고 비용부담이 적은 제품의 공급을 추진하며, 국민 건강 유지 및 개선을 위해 의약품과 식품 사용에 필요한 정확하고 과학적 기반을 가진 정보를 얻을 수 있도록 도움으로써 공중보건을 증진시키고 있습니다.
임상시험을 위해서는 임상시험계획승인 신청(Investigational New Drug application,IND)를 통과하여야 하며, 판매용 및 연구용(비판매용) 두가지 범주가 있고, 다음과 같은 세가지 신청 유형이 있습니다.
| [미국 임상시험계획 승인 신청] |
| 구 분 | 내 용 |
|---|---|
| 연구자 임상시험계획 승인신청 | 해당 신청은 임상시험을 개시하고 수행하는 의사가 제출하며, 의사의 직접적인 지시 하에 시험용 의약품이 투여 또는 조제됩니다. 의사는 미허가 의약품 또는 새로운 적응증이나 새로운 환자군에 대한 허가 의약품에 대한 시험을 제안하기 위해 연구용 임상시험계획 승인신청을 제출할 수 있습니다. |
| 응급상황 사용 임상시험계획 승인신청 | 해당 신청은 미국 식품의약품청이 『연방규정집』312.23조 또는 312.34조에 따른 임상시험계획 승인을 위한 시간이 허용되지 않는 상황에서의 시험약의 사용을 허가할 수 있도록 합니다. 또한 기존의 시험 계획 조건을 충족시키기 못하는 환자를 대상으로 또는 허가된 시험 계획서가 존재하지 않을 경우에 사용될 수 있습니다. |
| 치료목적 임상시험계획 승인신청 | 해당 신청은 임상 시험이 수행되고 미국 식품의약품청의 검토가 진행 중일 때, 임상 시험에서 중증 또는 즉각적으로 생명을 위협할 수 있는 증상에 대한 전망을 보이는 시험약을 위해 제출됩니다. 중증질환의 경우 임상 3상 중이거나 또는 모든 임상시험들이 완료된 의약품을 본 항에 따른 치료용 사용이 가능합니다. 즉각적으로 생명을 위협할 수 있는 질환의 경우, 임상 3상 이전이라 하더라도, 통상 임상 2상 이전이 아니라면 해당 의약품을 본 항에 따른 치료용으로 사용 가능할 수 있습니다. |
| 자료 : 식품의약품 안전처(미국 의약품 허가 제도, 2016.06.30) |
이후, 신약 허가신청(New Drug Application, NDA)은 미국 FDA이 미국에서 신약 판매 허가를 승인 받기 위해 의약품 의뢰자가 취하는 공식 단계로, 신약 허가신청은 의약품이 어떻게 체내에서 작용하고 어떻게 제조되는지에 대한 정보를 포함하여 모든 동물 및 인체 데이터와 그 분석을 포함합니다. 신약 허가신청 절차는 아래와 같은 단계를 따릅니다.
| [미국 신약 허가 신청 결과] |
| 구 분 | 내 용 |
|---|---|
| 신약 허가신청 사전회의(Pre-NDA Meeting) | - |
| 신약 허가신청서 제출 및 심사 | - 신약 허가가 신청되면 식품의약품청은 해당 신청이 정식으로 제출되어 심사 받을 수 있도록 할지 결정하는 60일의 기간이 주어집니다. 미국 식품의약품청은 완전하지 않은 신청에 대한 정식 제출을 거절할 수 있습니다. - 신약 허가신청이 정식 제출되면, 식품의약품청 심사팀(의사, 화학자, 통계학자, 미생물학자, 약리학자, 다른 전문가들)은 의뢰자가 제출한 시험이, 제안된 용법에서 해당 의약품이 안전하고 유효성이 있음을 나타내는지 평가합니다. 어떤 의약품도 절대적으로 안전하지 않으며 모든 의약품은 부작용이 있으나, “안전하다”라는 의미는 의약품의 유익성이 알려진 위해성을 상회한다는 뜻입니다. - 심사팀은 시험결과를 검토하고, 시험방법 또는 분석의 취약점과 같은 가능한 문제들에 대해 검토합니다. 심사자들은 의뢰자의 결과 및 결론에 동의할지 여부를 결정하거나, 결정을 내리기 위해 필요한 추가 정보가 필요한지 여부를 결정합니다. - 각 심사자는 신청에 대한 결론과 권고사항을 포함한 서면 평가서를 준비합니다. 이러한 평가는 이후 신청 종류에 따라 팀장, 부서장, 실장의 검토를 거칩니다. |
| 의약품 표시기재사항에 대한 심사 | 식품의약품청은 의약품 표시기재사항에 아래 정보가 포함되었는지 여부를 심사합니다. (1) 적응증, 용량, 투여 경로 및 방법, 투여 횟수 및 기간, 관련 경고문, 위험, 금기사항, 부작용, 주의사항 등 사용법에 대한 적절한 정보로서 의약품을 투여하는 법률상 허가된 의료인이 해당 의약품을 안전하게 사용할 수 있고, 광고되거나 표현된 모든 증상을 포함하여 본래 목적에 따라 사용될 수 있도록 하는 자료 (2) 라벨 및 표시기재사항 또는 의약품이 조제된 포장 내 표시된 의약품의 성분과 관련한 정보 |
| 실태조사 | 시설 등에 대한 실태조사는 식품의약품청이 수행하며, 미국의 의약품 제조 및 품질관리기준(GMP)을 따릅니다. |
| 의약품 허가 | - |
| 자료 : 식품의약품 안전처(미국 의약품 허가 제도, 2016.06.30) |
당사는 내부에 담당 인력과 외부 전문가들을 통하여 국내 및 해외 제약 산업 정책 및 규제 환경을 지속적으로 모니터링하고 있으며, 각국의 규제 당국과의 소통을 통해 정책 및 규제 환경의 변화에 효과적으로 대비하기 위해 최선의 노력을 다하고 있습니다. 그러나 상기 언급된 제약 및 신약개발 산업에 대한 우호적인 정책 기조 및 지원 계획, 규제 완화 노력에도 불구하고, 실제 효율적인 정책 지원이 이루어지지 않거나, 세부과제 추진에 어려움이 생길 수 있으며, 관련 법규의 제정 및 개정 단계, 예산 확보 등에 난항이 발생할 수 있습니다. 또한 해당 정책의 기대효과가 감소되는 경우 정책 기조의 변화로 정부 지원이 축소될 수 있으며, 조건부 허가와 같은 규제 완화에 대한 실효성이 크지 않을 경우, 규제 완화의 범위가 축소될 수 있습니다. 이러한 정부의 우호적인 정책 및 규제 완화의 변동 가능성은 당사의 사업에 부정적인 영향을 끼칠 수 있습니다.
| 파. 국제 환율 변동으로 인한 위험 당사는 연구개발비 지원을 목적으로 누적기준 미국소재 종속회사인 Elevar에 최근 8년간2억 9719만 달러, Immunomic에 최근 3년간 5,643만 달러를 출자하였으며, 원/달러 환율이 상승할 경우 당사가 연구개발비 목적으로 출자하는 금액의 부담이 가중될 가능성이 있습니다. 2022년 1월 6일 원달러환율은 1,203원을 기록하며 올해 처음으로 1,200원선을 돌파하였으며, 2022년 8월 중순기준 1,300원 내외를 기록중입니다. 연준 통화정책 정상화에 기반한 달러 강세 압력이 이어질 것으로 전망됩니다. 다만, 향후 연준의 추가 금리인상 시점에 따른 위험자산 선호 심리 개선, 신규 변이 바이러스로 인한 COVID-19 재확산 등 다양한 가능성이 상존해 있으며 러시아-우크라이나 전쟁 지속, 미 연준의 통화정책, 코로나19 사태 등에 따라 환율의 변동성은 커질 수 있습니다. 당사는 별도의 환헷지를 위한 통화선도계약을 체결하고 있지 않아 달러 가치 변동성이 지속될 경우 당사의 수익성 및 재무구조에 부정적인 영향을 미칠 수 있습니다. 투자자들께서는 투자하기에 앞서 환율변동에 대한 모니터링을 철저히 하신 후 투자해주시기 바랍니다. |
당사는 연구개발비 지원을 목적으로 누적기준 미국소재 종속회사인 Elevar에 최근 8년간 2억 9719만 달러, Immunomic에 최근 3년간 5,643만 달러를 출자하였으며, 원/달러 환율이 상승할 경우 당사가 연구개발비 목적으로 출자하는 금액의 부담이 가중될 가능성이 있습니다.
결론적으로, 당사는 종속회사 출자 등의 사유로 현금흐름상 순외화지출 포지션에 노출되어 있습니다. 환율 변동 위험의 경우는 미래 달러 부족량을 정확히 예측할 수 없다는 점에서 기본적으로 완전헤지가 불가능 합니다. 최근 COVID-19사태, 미 연준의 금리인상, 러시아-우크라이나 전쟁 등 국제정세 변동으로 인하여 환율의 변동성이 확대되었으며 당사가 종속회사에 출자하는 외화금액이 상승할경우 당사의 수익성에 부정적인 영향을 미칠수 있습니다.
| [최근 3년간 원/달러 환율 변화] |
| (단위 : 원/달러) |
|
| 기간 : | 2019년 08월 10일 ~ 2022년 08월 10일 |
| 자료 : | 서울외국환중개 |
최근 3년간 원/달러 환율 추이를 살펴보면, 2020년은 연초부터 국내 경제성장률 전망치 하향 조정 등 경기에 대한 불확실성이 제기된 가운데, 2월부터 불거진 COVID-19 감염증 확산에 대한 우려로 글로벌 안전자산 선호가 심화되기 시작했습니다. 그 결과, 국내외 시장금리는 하락세가 지속되고 원/달러 환율은 큰 상승을 보이면서 변동성이 확대되었습니다. 미국 연방공개시장위원회(FOMC)는 2020년 들어 3회에 걸친 긴급회의를 통해 기준금리를 0.00~0.25%로 전년대비 1.50% 전격 인하하고, 양적완화 실시 규모를 무제한 확대하기로 결의하는 등 COVID-19로 인한 경기하방 위험과 금융시장 불안을 안정시키기 위한 강력한 통화정책 수단을 연이어 발표하였습니다. 이렇게 미국이 달러를 대량 공급하고 있는 상황에서도 COVID-19로 인한 안전자산 선호심리 강화로 2020년 3월 19일에는 원/달러 환율이 1,280원을 기록하기도 하였으나, 같은 날 한-미 간 600억 달러 규모의 통화 스와프 계약 체결 및 백신에 대한 기대감을 바탕으로 달러 인덱스 하락이 발생하면서 원/달러 환율은 1,200원대 내외에서 거래되었습니다. 이후 미국 정부의 잇따른 추가 부양책 발표와 중앙은행의 제로금리 유지 선언 등으로 인하여 2020년 연말까지 환율은 지속해서 하락했습니다.
2021년초에는 장기 금리가 기대 인플레이션 상승 및 미국 경제의 회복 기대감을 반영해 상승하기 시작했고, 외국인의 국내 주식 순매도, 개인 투자자들의 해외투자 확대가 달러 수요를 이끌어 원달러 환율은 2021년 5월 15일 1,133원/달러 까지 상승하였습니다. 5월 말 들어 위안화 강세 랠리에 연동한 원화 강세 압력까지 더해지며 원달러 환율은 잠시 하락하였으나, 6월 FOMC 이후 미국에서의 테이퍼링 이슈, 변이 바이러스 출현 및 헝다그룹의 디폴트 가능성 등이 제기되며 안전자산 선호 심리에 따른 달러화 강세 모습이 다시 보였습니다. 또한 2021년 하반기 국제 유가 상승, 미국 국채 금리 상승 등 금융시장 변동성이 확대되고 오미크론 변이 바이러스로 인한 주요국의 확진자수 급증 등으로 불확실성이 증대됨에 따라 1,170원 ~ 1,190원의 박스권을 형성하였습니다. 2022년 1월 6일 기준 원달러환율은 1,203원을 기록하며 올해 처음으로 1,200원선을 돌파하였으며, 2022년 8월 중순 기준 1,300원 내외를 기록중입니다. 연준 통화정책 정상화 및 빅스텝 금리 인상전망, 안전자산 선호심리 상승에 기반한 달러 강세 압력이 이어질 것으로 전망됩니다. 다만, 향후 연준의 추가 금리인상 시점에 따른 위험자산 선호 심리 개선, 신규 변이 바이러스로 인한 COVID-19 재확산 등 다양한 가능성이 상존해 있으며 러시아-우크라이나 전쟁 지속, 미 연준의 통화정책, 코로나19 사태 등에 따라 환율의 변동성은 커질 수 있습니다.
최근 3년 및 2022년 반기 연결기준 당사가 보유하고 있는 외화표시 화폐성자산 및 부채의 장부금액은 다음과 같습니다.
| [외화표시 화폐성자산 및 부채 장부금액] |
| (단위: USD, CNY, JPY) |
| 구 분 | 2022년 반기 | 2021년 | 2020년 | 2019년 | 2018년 | ||||
|---|---|---|---|---|---|---|---|---|---|
| USD | CNY | USD | CNY | USD | CNY | USD | JPY | USD | |
| 자산: | |||||||||
| 외화예금 | 9,141,118 | - | 803,721 | - | 73,602 | - | 2,364 | - | 1,103,892 |
| 매출채권 | 5,046,357 | 60,825,380 | 416,440 | 90,706,765 | 629,299 | 35,073,816 | 2,867,582 | 1,382,700 | 438,917 |
| 기타금융자산 | - | - | 29,423 | - | - | - | - | - | - |
| 소계 | 14,187,475 | 60,825,380 | 1,249,583 | 90,706,765 | 702,901 | 35,073,816 | 2,869,946 | 1,382,700 | 1,542,809 |
| 부채: | |||||||||
| 매입채무 | 88,436 | - | - | - | - | - | - | - | - |
| 합계 | 14,099,039 | 60,825,380 | 1,249,583 | 90,706,765 | 702,901 | 35,073,816 | 2,869,946 | 1,382,700 | 1,542,809 |
당사는 외화 매출채권 및 매입채무, 외화예금, 종속회사 출자 등과 관련하여 환율변동위험에 노출되어 있습니다. 당사의 경영진은 내부회계관리규정에 의거 환위험에 대한 내부통제절차를 수립하여 매년 평가 및 운영하고 있습니다. 매년 말 다른 모든 변수가 일정하다고 가정할 때 각 외화에 대한 원화의 환율 5% 변동시 법인세차감전순손실에 미치는 영향은 다음과 같습니다.
| [환율 관련 순이익에 미치는 영향] |
| (단위: 천원) |
| 구분 | 2022년 반기 | 2021년 | 2020년 | 2019년 | 2018년 | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| 5% 상승시 | 5% 하락시 | 5% 상승시 | 5% 하락시 | 5% 상승시 | 5% 하락시 | 5% 상승시 | 5% 하락시 | 5% 상승시 | 5% 하락시 | |
| USD | 917,149 | (917,149) | 74,069 | (74,069) | 38,238 | (328,354 | (36,474) | 36,474 | (109,417) | 109,417 |
| CNY | 586,205 | (586,205) | 844,752 | (844,752) | 292,796 | (292,796) | - | - | - | - |
| JPY | - | - | - | - | - | - | 735 | (735) | - | - |
당사는 내부회계관리규정에 의거 환위험을 주기적으로 모니터링, 평가 및 관리하고 있으며 내부적으로 원화환율변동에 대한 환위험을 정기적으로 측정하는 등 노력을 기울이고 있습니다. 다만, 환율 변동 위험의 경우는 미래 달러 수요량을 정확히 예측할 수 없다는 점에서 기본적으로 완전헤지가 불가능하며, 완전헤지가 이루어진다고 하더라도 환율 상승이 물가 상승을 야기하여 당사의 수익성에 부정적 영향을 미칠 수있습니다. 더불어, 당사는 별도의 환헷지를 위한 통화선도계약을 체결하고 있지 않아COVID-19의 장기화, 미중 무역전쟁, 우크라이나 지정학적 리스크 등 외부적인 요인으로 달러 가치 변동성이 지속될 경우 당사의 수익성 및 재무구조에 부정적인 영향을 미칠 수 있습니다. 투자자들께서는 투자하기에 앞서 환율변동에 대한 모니터링을 철저히 하신 후 투자해주시기 바랍니다.
2. 회사위험
| 【투자자 유의사항】 |
|---|
|
○ 본 증권신고서는 당사의 영업활동 및 재무에 대해 보다 정확하고 실체적인 정보전달을 위해 연결기준으로 작성되었으며, 증권신고서 투자위험요소 중 회사위험은 별도의 언급이 있는 경우를 제외하고 기본적으로 연결재무제표 기준으로 작성되었습니다. 연결기준 재무제표는 [2부 발행인에 관한 사항] 및 감사보고서 등을 참조하시기 바랍니다. ○ 본 회사위험에는 당사의 재무적 위험요소들이 주로 기재되어 있습니다. 투자자 여러분들의 이해 편의를 위하여, 당사의 최근 3개년간 주요 재무사항 총괄표를 아래와 같이 요약 기재하였으니, 투자판단에 참고하시기 바랍니다. |
최근 3년간 주요 재무사항은 다음과 같습니다.
| [주요 재무사항 총괄표] | |
| (단위: 백만원) | |
| 구 분 | 2022년 반기 | 2021년 | 2020년 | 2019년 | 비 고 |
|---|---|---|---|---|---|
| 외부감사 회계법인 | 삼덕 | 삼덕 | 삼덕 | 삼정 | - |
| 외부감사인의 감사의견 | 적정 | 적정 | 적정 | 적정 | - |
| 감사인 핵심감사사항 | 해당 | 해당 | 해당 | 해당 | - |
| 계속기업 존속불확실성 해당여부 | 미해당 | 미해당 | 미해당 | 미해당 | - |
| 1. 자산총계 | 813,143 | 743,692 | 706,477 | 362,612 | - |
| - 유동자산 | 163,136 | 188,142 | 251,573 | 69,679 | - |
| - 비유동자산 | 650,008 | 555,550 | 454,905 | 292,933 | - |
| 2. 부채총계 | 277,827 | 231,507 | 149,048 | 173,370 | - |
| - 유동부채 | 123,300 | 121,819 | 98,027 | 67,699 | - |
| - 비유동부채 | 154,527 | 109,688 | 51,021 | 105,671 | - |
| 3. 자본총계 | 535,317 | 512,185 | 557,429 | 189,242 | - |
| - 자본금 | 53,445 | 53,309 | 26,492 | 21,371 | - |
| 4. 부채비율(%) | 51.9% | 45.2% | 26.7% | 91.6% | 부채총계/자본총계 |
| 5. 유동비율(%) | 132.3% | 154.4% | 256.6% | 102.9% | 유동자산/유동부채 |
| 6. 영업활동 현금흐름 | (33,915) | (54,765) | (56,514) | (48,657) | - |
| 7. 투자활동 현금흐름 | (20,876) | (68,496) | (98,022) | (26,825) | - |
| 8. 재무활동 현금흐름 | 32,566 | 1,335 | 341,017 | 86,663 | - |
| 9. 기말 현금및현금성자산 | 80,483 | 99,797 | 220,678 | 40,855 | - |
| 10. 매출액 | 123,305 | 69,826 | 56,177 | 38,421 | - |
| 11. 영업이익 | (20,096) | (101,018) | (61,312) | (48,731) | - |
| - 영업이익률(%) | -16.3% | -144.7% | -109.1% | -126.8% | 영업이익/매출액 |
| 12. 금융수익 | 9,738 | 7,155 | 20,565 | 18,970 | - |
| 13. 금융원가 | 4,800 | 11,320 | 12,566 | 24,950 | - |
| 14. 당기순이익 | (19,100) | (111,607) | (88,716) | (59,660) | - |
| - 당기순이익률(%) | -15.5% | -159.8% | -157.9% | -155.3% | 당기순이익/매출액 |
|
가. 관리종목 편입 가능성에 따른 위험 |
최근 금융감독기관 등의 상장기업에 대한 관리감독기준은 투자자보호 차원에서 엄격해지고 있는 상황이며, 회사가 관련 규정을 위반할 경우 회사 및 회사가 발행한 주식에 대해 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다.
코스닥시장 관리종목 지정 및 상장폐지 요건에 대한 검토결과는 다음과 같습니다.
| [코스닥시장 관리종목 지정 및 상장폐지 요건 검토] |
|
구분 |
분류 |
요건 |
||
|---|---|---|---|---|
|
매출액 미달 |
관리종목 |
최근년 30억원 미만 (지주회사는 연결기준) * 기술성장기업, 이익미실현기업은 각각 상장후 5년간 미적용 |
||
|
상장폐지 |
2년 연속 [실질심사] 이익미실현기업 관련, 관리종목지정 유예기간 중 최근 3사업연도 연속으로 매출액이 5억원 미만이면서 전년 대비 100분의 50 이상의 매출액 감소가 공시 등을 통해 확인되는 경우 |
|||
|
검토결과 |
(별도기준) 2022년 반기 1,204억원, 2021년 364억원, 2020년 487억원, 2019년 298억원, 2018년 273억원 | |||
|
법인세비용차감전계속사업손실 |
관리종목 |
자기자본50%이상 (&10억원이상)의 법인세비용차감전계속사업손실이 최근3년간 2회 이상 (&최근연도계속사업손실) * 기술성장기업 상장후 3년간 미적용, 이익미실현 기업 상장후 5년 미적용 |
||
|
상장폐지 |
관리종목 지정후 자기자본50%이상(&10억원이상)의 법인세비용차감전계속사업손실 발생 [실질심사] 이익미실현기업 관련, 관리종목지정 유예기간 중 최근 3사업연도 연속으로 매출액이 5억원 미만이면서 전년 대비 100분의 50 이상의 매출액 감소가 공시 등을 통해 확인되는 경우 |
|||
|
검토결과 |
21년 법인세비용차감전계속사업손실:110,449백만원 자기자본: 512,185백만원 비율: 21.56% |
20년 법인세비용차감전계속사업손실:93,202백만원 자기자본: 557,429백만원 비율: 16.72% |
19년 법인세비용차감전계속사업손실:59,763백만원 자기자본: 189,242백만원 비율: 31.58% |
|
|
장기영업손실 |
관리종목 |
최근 4사업연도 영업손실(지주회사는 연결기준) 기술성장기업(기술성장기업부)은 미적용 |
||
|
상장폐지 |
[실질심사] 관리종목 지정 후 최근 사업연도 영업손실 |
|||
|
검토결과 |
(별도기준) 2022년 반기 36,308백만원, 2021년 -14,452백만원, 2020년 -9,906백만원, 2019년 -4,939백만원, 2018년 1,654백만원 | |||
|
자본잠식/자기자본 |
관리종목 |
반기말 또는 사업연도 말을 기준으로 다음의 어느 하나에 해당하는 경우 (B)사업연도(반기)말 자기자본 10억원미만 (C)반기보고서 제출기한 경과후 10일내 반기검토(감사)보고서 미제출 or 검토(감사)의견 부적정·의견거절·범위제한한정 |
||
|
상장폐지 |
최근년말 완전자본잠식 A or C 후 사업연도(반기)말 자본잠식률 50%이상 B or C 후 사업연도(반기)말 자기자본 10억원미만 A or B or C 후 반기말 반기보고서 기한 경과후 10일내 미제출 or 감사의견 부적정·의견거절·범위제한한정 [실질심사] 사업보고서 또는 반기보고서의 법정제출 기한까지 당해 상장폐지 기준 해당사실을 해소하였음을 입증하는 재무제표 및 이에 대한 감사인(정기재무제표에 대한 감사인과 동일한 감사인에 한함)의 감사보고서를 제출하는 경우 |
|||
|
검토결과 |
(A)사업연도(반기)말 자본잠식률 50%이상 - 해당사항 없음 2022년 반기 자본금 : 53,445백만원 2021년 자본금 : 53,309백만원 2020년 자본금 : 26,492백만원 2022년 반기 자본총계 : 약 535,317백만원 2021년 자본총계 : 512,185백만원 2020년 자본총계 : 557,429백만원 (B)사업연도(반기)말 자기자본 10억원미만 - 해당사항 없음 2022년 반기 자기자본 : 약 535,317백만원 2021년 자기자본 : 512,185억원 2020년 자기자본 : 557,429백만원 (C)반기보고서 제출기한 경과후 10일내 반기검토(감사)보고서 미제출 or 검토(감사)의견 부적정ㆍ의견거절ㆍ범위제한한정 - 해당사항 없음 |
|||
|
감사의견 |
관리종목 |
- |
||
|
상장폐지 |
감사보고서 부적정·의견거절·범위제한한정 |
|||
|
검토결과 |
2022년 반기 감사보고서 적정의견 | |||
|
시가총액 |
관리종목 |
보통주시가총액 40억원미만 30일간 지속 |
||
|
상장폐지 |
관리종목 지정후 90일간 "연속10일 & 누적30일간 40억원이상"의 조건을 미충족 |
|||
|
검토결과 |
해당 없음 | |||
|
거래량 |
관리종목 |
분기 월평균거래량이 유동주식수의 1%에 미달 * 월간거래량 1만주(액면가액 5,000원 기준), 소액주주 300인이상이 20%이상 지분 보유, 신규상장법인(신규상장일이 속하는 분기에 한정) 등은 적용배제 |
||
|
상장폐지 |
2분기 연속 |
|||
|
검토결과 |
분기 월평균거래량이 유동주식수의 1% 이상 | |||
|
지분분산 |
관리종목 |
소액주주200인미만or소액주주지분20%미만 * 300인이상의 소액주주가 유동주식수의 10%이상으로서 100만주이상을 소유하는 경우는 적용배제 |
||
|
상장폐지 |
2년 연속 |
|||
|
검토결과 |
해당 없음 | |||
|
불성실공시 |
관리종목 |
- |
||
|
상장폐지 |
[실질심사] 1년간 불성실공시 벌점 15점 이상 |
|||
|
검토결과 |
해당 없음 | |||
|
공시서류 |
관리종목 |
(A)분기,반기, 사업보고서 미제출 (B)정기주총에서 재무제표 미승인 or 정기주총 미개최 |
||
|
상장폐지 |
2년간 3회 분기,반기,사업보고서 미제출 사업보고서 제출기한후 10일내 미제출 A(미제출상태유지) or B 후 다음회차에 A or B |
|||
|
검토결과 |
분기,반기, 사업보고서 제출기한까지 제출 완료 | |||
|
사외이사 등 |
관리종목 |
최근 사업연도 사업보고서상 A)사외이사의 수가 법에서 정하는 수에 미달 B)법에서 정하는 감사위원회를 구성하지 않거나 구성요건을 충족하지 아니하는 경우 *자산총액 1,000억원 미만의 코스닥 상장 벤처기업은 사외이사 선임 의무 면제 **자산총액 2조원 미만의 상장회사는 감사위원회 설치 의무 면제 |
||
|
상장폐지 |
2년 연속 |
|||
|
검토결과 |
사외이사 선임, 2021년(별도) 자산총액 802,223백만원이기에 자산총액 2조원 미만으로 감사위원회 설치 의무 면제 | |||
|
회생절차/파산신청 |
관리종목 |
「채무자 회생 및 파산에 관한 법률」 제34조에 의한 회생 절차개시 신청이 있는 경우 코스닥시장 상장법인에 대하여 「채무자 회생 및 파산에 관한 법률」 제294조에 의한 파산신청이 있는 경우 |
||
|
상장폐지 |
[실질심사] 개시신청기각,결정취소,회생계획 불인가등 |
|||
|
검토결과 |
- | |||
|
기타 |
상장폐지 |
최종부도 또는 은행거래정지 해산사유(피흡수합병, 파산선고) 정관 등에 주식양도제한 두는 경우 유가증권시장 상장의 경우 우회상장시 우회상장관련 규정 위반시 (심사종료전 기업결합완료 및 보호예수 위반 등) |
||
| 자료: 코스닥시장 상장규정 |
① 매출액(별도기준) 인한 관리종목 지정 사유 여부 검토
당사의 별도기준 매출액은 다음과 같습니다.
| [매출액(별도기준)] |
| (단위 : 백만원) |
| 구 분 | 2022년 반기 | 2021년 | 2020년 | 2019년 | 2018년 |
|---|---|---|---|---|---|
| 매출액 | 120,386 |
36,375 |
48,730 |
29,776 |
27,271 |
당사는 2018년 27,271백만원의 매출액을 기록한 이후 2019년 29,776백만원, 2020년 48,730백만원, 2021년 36,375백만원, 2022년 반기 120,386백만원의 매출액을 기록했습니다. 코스닥시장 상장규정에 따르면 최근 사업연도의 매출액이 30억원 미만인 경우 관리종목에 지정되므로 현재 당사가 매출액 감소로 인해 관리종목에 지정될 가능성은 낮습니다.
② 장기영업손실(별도기준) 인한 관리종목 지정 사유 여부 검토
코스닥시장 상장규정에 따르면 최근 4개 사업연도(별도기준)에서 영업손실을 기록할경우 관리종목에 지정되며 당사는 2016년 4,641백만원의 영업손실, 2017년 6,776백만원의 영업손실, 2018년 1,654백만원의 영업이익, 2019년 4,939백만원의 영업손실, 2020년 9,906백만원의 영업손실, 2021년 14,452백만원의 영업손실, 2022년 반기 36,308백만원의 영업이익을 기록하였습니다. 이에 따라, 당사가 2022년 영업손실을 기록하게 된다면 관리종목에 지정됩니다.
③ 법인세비용차감전계속사업손실(연결기준) 인한 관리종목 지정 사유 여부 검토
당사의 금번 반기 및 최근 3개년(2021년, 2020년, 2019년) 자본총계 및 법인세비용차감전순손실은 다음과 같습니다.
| (단위 : %, 백만원) |
| 구분 | 2022년 반기 | 2021 | 2020 | 2019 |
|---|---|---|---|---|
| (법인세비용차감전계속사업손실/자기자본)×100(%) | 2.27% | 21.56% | 16.72% | 31.58% |
| 법인세비용차감전계속사업손실 | 12,162 | 110,449 | 93,202 | 59,763 |
| 자기자본 | 535,317 | 512,185 | 557,429 | 189,242 |
당사는 2019년, 2020년 및 2021년 자기자본의 50%를 초과하는 법인세차감전순손실이 발생하지 않았습니다.
④ 자본잠식 지정 사유 여부 검토
| [자본금 관련 계정 내역] |
| (단위 : 백만원, %) |
| 구분 | 2022년 반기 | 2021년 | 2020년 | 2019년 | 2018년 |
|---|---|---|---|---|---|
| 자본금 | 53,445 | 53,309 | 26,492 | 21,371 | 19,587 |
| 자본총계 | 535,317 | 512,185 | 557,429 | 189,242 | 209,524 |
| 자본잠식여부 |
X | X | X | X | X |
| 자본금의 50% | 26,722 | 26,654 | 13,246 | 10,686 | 9,794 |
| 당기순이익 | (19,100) | (111,607) | (88,716) | (59,660) | 13,520 |
| 이익잉여(결손)금 | (62,494) | (183,022) | (85,449) | (5,216) | 39,618 |
당사는 2019년, 2020년, 2021년 및 2022년 반기 모두 자본잠식에 해당하지 않습니다.
관리종목 지정사유 확인 당일에는 코스닥시장에서의 거래는 정지되며, 이를 기한 내에 해결하지 못한다면 코스닥시장 상장폐지 사유에 해당하여, 당사 주식은 향후 장내에서 거래가 이루어지지 못할 수 있습니다. 투자자 여러분들께서는 당사의 주식이 상장폐지될 경우, 투자금액을 회수하지 못하게 될 수도 있는 점을 반드시 유의하여 주시기 바랍니다. 이에 투자자 여러분들께서는 코스닥시장에서의 관리종목, 상장폐지와 관련된 규정을 반드시 유의하시고, 당사의 영업 수익성 추이에 대하여 지속적으로모니터링하시기 바랍니다.
자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융감독법규정보시스템(http://law.fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
| 나. 자체 사업의 영업실적과 주가 간의 괴리 관련 위험 당사의 매출은 대부분 당사 자체 사업부인 구명정 및 파이프로부터 발생하나, 당사의 자회사인 Elevar가 영위하는 리보세라닙 신약 개발 사업이 부각되면서, 실질적으로 당사의 상장된 보통주식은 자체 사업인 구명정 및 파이프 제조업이나 그와 밀접하게 연관된 조선 및해운업보다 제약ㆍ바이오 산업의 업황 및 시장 상황의 영향을 직접적으로 받고 있습니다. 당사는 2019년 11월 미국에 설립한 100% 자회사인 HLB USA Inc.를 통하여 Elevar를 합병하면서 Elevar를 당사의 완전자회사로 개편하였는 바, 이로 인해 당사의 주가는 더욱 자체 영위 사업보다 자회사가 영위하는 사업에 대한 시장의 기대에 의해 변동하는 성향이 강해진 것으로 판단됩니다. Elevar는 아직 실질적으로 매출을 시현한 바 없으며 연구개발비 지출의 대부분을 소요하고 있는 바, 당사의 상장된 보통주 주가는 정기보고서 등에 기재되는재무수치 및 자체 영위 사업의 영업실적보다는 자회사 Elevar의 신약 연구개발 진행 관련 소식이나 신약 연구개발업 전반의 호재 및 악재성 소식에 보다 더 큰 영향을 받을 가능성이 높습니다. 금번 유상증자의 청약에 참여하여 당사의 상장된 보통주에 투자할 의향이 있는 투자자께서는 이 점에 특히 유의하시어 투자판단을 하시기 바랍니다. |
당사가 영위하는 주요 사업 중 하나인 합성수지선 건조업의 경우 연결기준 매출액 중2019년 기준 77.5%, 2020년 기준 75.3%를 차지했으나, 2021년 기준 약 36.9%, 2022년 반기 기준 약 7.3%를 차지합니다. 제품별 매출의 경우 구명정 및 파이프 매출액이 연결기준 매출 총액 중 2021년 연간 기준 약 30.1%, 2022년 반기 기준 약 5.2%를 구성합니다.
바이오의료기기 사업부문에서 발생하는 매출은 당사와 2022년 01월 01일 합병한 헬스케어사업부(舊 에프에이㈜)에서 발생하는 체외진단의료기기 매출, 당사가 중국 항서제약으로부터 수령하는 리보세라닙 로열티 수익, 금년 매각이 완료된 화진메디스㈜ 및 화진메디칼㈜에서 발생하는 의료기기 매출로 이루어져 있습니다.
| [당사 사업부문별 매출액 및 비중 추이] | |
| (단위: 백만원) | |
| 구 분 | 2022년 반기 | 2021년 반기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|---|
| 복합소재사업부문 매출액 | 8,966 | 11,858 | 25,773 | 42,316 | 29,776 |
| 연결기준 매출액 중 비중 | 7.3% | 74.3% | 36.9% | 75.3% | 77.5% |
| 바이오의료기기사업부문 매출액 | 114,338 | 4,099 | 44,053 | 13,861 | 8,645 |
| 연결기준 매출액 중 비중 | 92.7% | 25.7% | 63.1% | 24.7% | 22.5% |
| 연결기준 매출액 계 | 123,304 | 15,957 | 69,826 | 56,177 | 38,421 |
| [당사 매출유형별 매출액 및 비중 추이] | |
| (단위: 백만원) | |
| 구 분 | 주요 재화 및 용역 | 2022년 반기 | 2021년 반기 | 2021년 | 2020년 | 2019년 | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 매출액 | 비율(%) | 매출액 | 비율(%) | 매출액 | 비율(%) | 매출액 | 비율(%) | 매출액 | 비율(%) | ||
| 제품매출 | 구명정 외 | 3,559 | 2.89 | 3,706 | 23.23 | 11,747 | 16.82 | 16,496 | 29.36 | 13,135 | 34.19 |
| GRP/GRE PIPE | 2,816 | 2.28 | 5,918 | 37.09 | 9,254 | 13.25 | 19,904 | 35.43 | 14,877 | 38.72 | |
| 체외진단 의료기기 외 | 102,435 | 83.07 | - | 0.00 | 22,105 | 31.66 | - | 0.00 | 13 | 0.03 | |
| 주사기 외 | 2,198 | 1.78 | 3,644 | 22.84 | 7,571 | 10.84 | 7,567 | 13.47 | 8,515 | 22.16 | |
| 수수료매출 | 리보세라닙 중국 로열티 | 3,908 | 3.17 | - | 0.00 | 10,362 | 14.84 | 5,856 | 10.42 | - | 0.00 |
| 상품매출 | DAVIT | 2,124 | 1.72 | - | 0.00 | 3,843 | 5.50 | - | 0.00 | - | 0.00 |
| 수액세트 외 | 5,276 | 4.28 | 305 | 1.91 | 1,455 | 2.08 | 277 | 0.49 | 146 | 0.38 | |
| 기타매출 | 기타 서비스 | 988 | 0.80 | 2,383 | 14.93 | 3,490 | 5.00 | 6,077 | 10.82 | 1,735 | 4.52 |
| 합 계 | 123,305 | 100.00 | 15,957 | 100.00 | 69,826 | 100.00 | 56,177 | 100.00 | 38,421 | 100.00 | |
당사의 주가는 자체 사업인 구명정 및 파이프 제조업과 연관된 조선 및 해운업보다 당사의 100% 자회사인 Elevar Therapeutics Inc.(舊 LSK BioPartners Inc.)가 영위하는 리보세라닙 신약 개발 사업이 부각되면서, 제약ㆍ바이오 산업의 업황 및 시장 상황의 영향을 직접적으로 받고 있습니다.
당사는 2015년 2월 3일 이사회 결의 및 자산양수도계약을 통하여 미국 법인인 LSK BioPartners Inc.("LSK Bio")의 지분 31.21%를 약 360억원에 인수하면서 본격적으로 제약ㆍ바이오사업에 관여하기 시작했습니다. LSK Bio는 2005년 미국에서 Lifecord International USA Inc.라는 이름으로 설립되어 2007년 LSK BioPartners Inc.로 명칭을 변경한 신약개발 NRDO(No Research Development Only) 업체로, 신약후보물질 Rivoceranib("리보세라닙")의 원천 물질 특허권자인 미국 Advenchen Laboratories, LLC("Advenchen", 최대주주이자 리보세라닙 최초 개발자인 개인 Paul Chen 을 포함하여 지칭)으로부터 중국을 제외한 글로벌 특허 전용실시권을 허여받아 리보세라닙 성분의 신약을 개발하고 허가를 취득하는 과정에 집중적으로 역량을 투입해 온 회사입니다.
Elevar는 리보세라닙을 중심으로 다양한 암종에 대하여 항암제 신약 개발 및 허가 취득을 추진하고 있으며, 특히 위암 말기 치료제 허가 과정은 임상 3상까지 완료되어 미 FDA의 최종 신약 허가 단계인 NDA 직전까지 진행된 바 있습니다. 그리고 최근 선양낭성암 1,2차 치료제(Rivoceranib 단독) 2상 결과를 토대로 FDA에 가속승인(조건부판매)을 목표로 전략 수립 중이고, 2022년 8월엔 간암 1차 치료제(항서제약 캄렐리주맙 병용) 승인을 목표로 미국 FDA에 Pre-NDA 미팅 신청을 하였습니다. 그러나 증권신고서 제출일 현재까지 Elevar로부터 발생한 매출은 사실상 없으며, 오히려 실적 기준으로는 당사의 연결기준 연구개발비 지출로 인해 영업손실 기록의 직접적인 원인이 되고 있습니다.
| [실적 및 경상연구개발비/판관비 추이] | |
| (연결기준) | (단위: 원) |
| 2022년 반기 | 2021년 반기 | 2021년 | 2020년 | 2019년 | |
|---|---|---|---|---|---|
| 수익(매출액) | 123,305 | 15,957 | 69,826 | 56,177 | 38,421 |
| 매출원가 | 73,343 | 15,439 | 48,759 | 45,869 | 34,484 |
| 매출총이익 | 49,961 | 518 | 21,067 | 10,308 | 3,937 |
| 판매비와관리비 | 70,057 | 40,275 | 122,086 | 71,620 | 52,668 |
| 경상연구개발비 | 22,603 | 10,566 | 48,419 | 22,594 | 33,835 |
| 전체 판관비 중 경상연구개발비 비중 | 32.3% | 26.2% | 39.7% | 31.5% | 64.2% |
| 매출액 대비 경상연구개발비 비율 | 18.3% | 66.2% | 69.3% | 40.2% | 88.1% |
| 영업이익(손실) | (20,096) | (39,757) | (101,018) | (61,312) | (48,731) |
| 당기순이익(손실) | (19,100) | (57,078) | (111,607) | (88,716) | (59,660) |
당사의 연결기준 경상연구개발비는 매년 증가하여, 2019년 33,835백만원에서 2020년 22,594백만원 수준으로 일부 감소하였으나, 2021년에는 연간 경상연구개발비가 약 48,419백만원으로 2019년 연간 연구개발비 대비 43.1% 증가하였습니다. 2020년경상연구개발비는 22,594백만원으로 전년 동기 대비 33.2% 감소(11,241백만원 감소)한 모습을 나타내는데, 이는 위암말기치료제의 글로벌 임상3상이 종료에 기인했으며, 2022년 반기 경상연구개발비는 22,603백만원으로 전년 동기 대비 113.9% 증가(12,037백만원 증가)한 모습을 나타내는데, 이는 선양낭성암 1,2차 치료제(Rivoceranib 단독) 2상 임상 및 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상3상 비용에 기인합니다.
2022년 하반기 또는 그 이후 당사가 계획하고 있는 간암 1차 치료제(항서제약 캄렐리주맙 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독), 위암2차 및 대장암 3차 치료제(타이호제약 론서프 병용)의 콤보임상 등이 차질 없이 진행될 경우 경상연구개발비는 추가적으로 증가할 수 있습니다. 경상연구개발비가 판매비와 관리비 중 차지하는 비중은 2021년 연간 기준 39.7%이며, 이는 연결기준 전체 매출액의 69.3%에 해당합니다. 당사의 연결기준 경상연구개발비 지출은 대부분 Elevar가 진행하는 임상 비용 등으로 사용되는 액수이며, 이는 당사가 자체적으로 영위하는 사업에서 지속적으로 매출총이익이 발생하고 있으나 판관비의 비용 처리 이후 영업손실으로 이어지는 직접적인 원인이라고 볼 수 있습니다.
당사는 Elevar의 전신 LSK BioPartners, Inc.의 이전 명칭인 Lifecord International USA, Inc.에 2005년 최초로 출자하였고, 이후 지속적 증자 출자를 통해 지분을 확보하여 왔으며, 삼각합병을 거쳐 100% 자회사화 하였습니다. 또한, 당사는 2020년 Immunomic Therapeutics,Inc.의 3자배정 유상증자에 약 356억원 출자해 31.08%의 지분을 확보하였고, 이후 지속적 증자 출자를 통해 현재 41.07%의 지분을 보유하고 있습니다. 당사는 현재까지 미화 약 4억 2,577만 달러를 Elevar에, 미화 약 5,643만달러를 Immunomic에 출자했습니다. 당사의 종속기업인 Elevar 및 Immunomic에 대한 출자내역은 아래와 같습니다.
| [Elevar 向 출자 내역] |
| 납입일자 | 취득대상 지분증권의 발행회사 | 거래형태 | 취득한 주식의 종류 |
납입금액 | 취득 주식수 | 재원 | 납입 이후 보유주식수 |
||
|---|---|---|---|---|---|---|---|---|---|
| 외화(달러) | 원화 | 보유주식수 | 지분율 | ||||||
| 2005-09-29 | Lifecord International USA,Inc (최초 취득) | 신규출자 | 보통주 | 250,000 | 264,410,000 | 1,000 | - | 1,000 | 100.00% |
| 2007-02-01 | LSK BioPartners, Inc. (사명의 변경) | - | - | - | - | - | - | - | - |
| 2007-11-23 | LSK BioPartners, Inc | 대여금 출자전환 | 보통주 | 1,050,000 | 1,089,142,000 | 8,000 | - | 9,000 | 29.03% |
| 2008-06-25 | 무상증자 | 보통주 | - | - | 81,000 | - | 90,000 | 6.98% | |
| 2012-01-04 | 구주인수 | 보통주 | 1,877,400 | 2,100,000,000 | 220,000 | - | 310,000 | 20.16% | |
| 2012-03-14 | 제3자배정 유상증자 | 보통주 | 300,000 | 340,500,000 | 151,515 | - | 461,515 | 23.91% | |
| 2014-04-14 | 제3자배정 유상증자 | 보통주 | 2,000,000 | 2,080,000,000 | 123,500 | - | 585,015 | 19.65% | |
| 2015-01-05 | 제3자배정 유상증자 | 보통주 | 6,000,000 | 6,729,000,000 | 148,302 | - | 733,317 | 23.67% | |
| 2015-02-16 | 구주인수 | 보통주 | 32,449,988 | 35,979,646,088 | 817,586 | 제3자배정 유상증자(2015.02) | 1,550,903 | 59.19% | |
| 2017-08-09 | 제3자배정 유상증자 | 보통주 | 19,999,999 | 22,507,998,311 | 261,987 | 제26회 CB | 1,812,890 | 62.77% | |
| 2018-07-25 | 제3자배정 유상증자 | 보통주 | 19,999,939 | 22,703,998,297 | 223,463 | 제26회 및 제29회 CB 제30회 BW |
2,036,353 | 62.19% | |
| 2019-04-30 | 제3자배정 유상증자 | 보통주 | 9,999,999 | 11,581,988,418 | 81,900 | 제3자배정 유상증자(2018.10) 제31회 CB |
2,118,253 | 61.61% | |
| 2019-05-31 | 구주인수 | 보통주 | 4,478,628 | 5,329,567,320 | 36,680 | 제31회 CB | 2,154,933 | 59.83% | |
| 2019-06-11 | HLB USA | 신규출자 | 보통주 | 1 | 1,184 | 1 | - | 1 | 100.00% |
| 2019-11-05 | 삼각합병 주식대가 취득 재원 지원목적 출자 |
보통주 | 162,500,000 | 188,792,102,918 | 162,500,000 | 단기차입 | 162,500,001 | 100.00% | |
| 2019-11-27 | HLB USA (삼각합병) | - | - | - | - | - | - | - | - |
| 2019-11-27 | Elevar Therapeutics, Inc. (사명의 변경) | - | - | - | - | - | - | - | - |
| 2019-12-03 | Elevar Therapeutics, Inc. | 삼각합병 현금대가 지급 재원 지원목적 출자 |
보통주 | 10,000,000 | 11,804,000,000 | 10,000,000 | 제31회 CB 제33회 CB |
172,500,001 | 100.00% |
| 2019-12-27 | 보통주 | 13,000,000 | 15,095,600,000 | 13,000,000 | 제33회 CB | 185,500,001 | 100.00% | ||
| 2020-04-14 | 주주배정유증 | 보통주 | 10,000,000 | 12,160,000,000 | 10,000,000 | 단기차입, 유상증자 | 195,500,001 | 100.00% | |
| 2020-04-20 | 주주배정유증 | 보통주 | 10,000,000 | 12,200,000,000 | 10,000,000 | 단기차입, 유상증자 | 205,500,001 | 100.00% | |
| 2020-06-17 | 액면병합 | - | - | - | -159,520,558 | - | 45,979,443 | 100.00% | |
| 2020-08-13 | 주주배정유증 | 보통주 | 15,000,000 | 17,767,500,000 | 1,500,000 | 유상증자 | 47,479,443 | 100.00% | |
| 2020-09-17 | 주주배정유증 | 보통주 | 15,000,000 | 17,595,000,000 | 1,500,000 | 유상증자 | 48,979,443 | 100.00% | |
| 2021-07-01 | 주주배정유증 | 보통주 | 14,905,110 | 16,835,321,745 | 3,100,000 | 유상증자 | 52,079,443 | 100.00% | |
| 2021-12-22 | 주주배정유증 | 보통주 | 21,636,450 | 25,779,830,175 | 4,500,000 | 유상증자 | 56,579,443 | 100.00% | |
| 2022-04-27 | 주주배정유증 | 보통주 | 25,150,000 | 31,394,745,000 | 5,000,000 | 유상증자 | 61,579,443 | 100.00% | |
| 2022-08-26 | 주주배정유증 | 보통주 | 30,180,000 | 40,495,524,000 | 6,000,000 | 유상증자 | 67,579,443 | 100.00% | |
Elevar의 기업개황, 연혁 및 요약재무상태표는 아래와 같습니다.
| [Elevar 기업개황] |
| 구분 | 내용 |
|---|---|
| Office Location | 2755 E. Cottonwood Pkwy. Suite 540 Salt Lake City, UT 84121 U.S.A. |
| 회사명 | Elevar Therapeutics, Inc. |
| 설립년월 | 2019년 6월 |
| 자본금(주식수) | USD 297,189,620 (보통주식수 61,579,443주) |
| 홈페이지 | https://elevartherapeutics.com/ |
| 대표이사 | Saeho Chong |
| 상장여부 | 비상장 |
| 주요 주주 현황 | HLB Co., Ltd.(100%) |
| 주요 임원 (연구진) 현황 |
- Saeho Chong : CEO - Seong Hoon Jang : Chief Operating Officer - Jan Van Tornout : Chief Medical Officer - Gordon Schooley : Chief Regulatory Officer |
| 주요 치료제 | A. 리보세라닙 - ACC(선낭암) B. 리보세라닙 - HCC(간암) C. 리보세라닙 - GC(위암) D. 아필리아 - OC(난소암) |
| [Elevar 연혁] |
| 일 자 | 내 용 |
|---|---|
| 2019년 | HLB USA, Inc. 설립 (삼각합병 목적 설립법인) |
| 2019년 | LSK BioPartners, Inc.와 삼각합병 완료 |
| 2019년 | 사명변경 (HLB USA, Inc. → Elevar Therapeutics, Inc.) |
| 2020년 | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 선양낭성암종 글로벌 임상 2상 첫환자 등록 |
| 2020년 | Oasmia Pharmaceutical AB로부터 세포독성항암제 "Apealea"에 대한 일부 국가를 제외한 글로벌 권리 양수 |
| 2020년 | Tanner社와 "Apealea"에 대한 NPP(Named Patient Program) 파트너십 체결 |
| 2020년 | Taiba社와 "Apealea"에 대한 MENA지역 파트너십 체결 |
| 2020년 | Inceptua社와 "Apealea"에 대한 EU 및 UK 지역 파트너십 체결 |
| 2021년 | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 미국 FDA 희귀의약품 지정 (선양낭성암종) |
| 2021년 | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 미국 FDA 희귀의약품 지정(간암) |
| 2022년 | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 선양낭성암종 글로벌 임상 2상 결과 발표 (ASCO) |
| [Elevar 요약재무상태표] | |
| (US GAAP) | (단위: 천USD, %) |
| 결산연월 또는 결산기간 | 2021년 | 2020년 |
|---|---|---|
| 1. 자산총계 | 42,559 | 41,216 |
| - 유동자산 | 21,767 | 20,383 |
| 2. 부채총계 | 55,254 | 39,265 |
| - 유동부채 | 36,860 | 20,968 |
| 3. 자본총계 | (12,695) | 1,951 |
| 4. 부채비율 (%) | -435.2% | 2,012.6% |
| 5. 유동비율 (%) | 59.1% | 97.2% |
| 6. 영업손익 | (56,011) | (31,317) |
| 기타 손익 | 825 | 536 |
| 7. 당기순이익 | (55,186) | (30,781) |
| 8. 자본금 | 272,039 | 235,498 |
| 9. 영업활동 현금흐름 | (32,926) | (35,882) |
| 10. 투자활동 현금흐름 | 652 | (20,202) |
| 11. 재무활동 현금흐름 | 4,267 | (6,084) |
| 12. 현금 및 현금성자산 기말 잔고 | 19,644 | 15,377 |
| 자료 : | Elevar Therapeutics, Inc 감사보고서(KPMG LA) |
| 주1) Elevar는 외부감사 의무대상이 아니며, 회사 자체적으로 회계법인에 의뢰해 2020년 및 2021년 외부감사를 받았습니다. | |
당사는 Elevar 向 출자와 관련한 주식가치 평가를 위해 2014년 4월 14일출자부터 삼각합병 이전인 2018년 05월 31일 출자까지 외부회계법인의 평가보고서를 수령해 출자를 진행하였으며, 당사가 Elevar의 주식 100%를 취득한 이후인 2019년 11월부터 2021년 12월 22일 출자까지는 액면증자를 실시하였기에 별도의 평가보고서를 수령하지 않았습니다.
이후 2022년 출자 진행한 2건은 영업권손상검토목적으로 수령한 사용가치 평가보고서에 기반하여 출자를 진행했습니다. 당사에서 수령한 각 출자별 기업가치(주식가치)평가보고서 및 사용가치평가 보고서는 아래와 같습니다.
(1) 지암회계법인-2014년 03월 31일
당사는 Elevar 向 출자와 관련하여 주식 양수도가액의 적정성을 확인하기 위하여 지암회계법인으로부터 Elevar Therapeutics Inc.의 주식가치에 대한 기업가치평가보고서(평가기준일: 2013년 12월 31일)를 수령하였습니다. 그럼에도 불구하고 투자자들께서는 지암회계법인이 주식가치평가보고서에서 제시하는 평가대상회사의 주식가치의 평가 결과는 미래예측에 따른 근본적인 한계가 존재하며, 평가대상회사의 절대적인 가치를 의미하는 것은 아니라는 점에 유의하시기 바랍니다. 지암회계법인은 평가대상회사의 주식가치를 평가하기 위해 현금흐름할인법을 적용하였으며, 평가시 적용한 주요 가정은 다음과 같습니다.
| [평가시 적용된 주요 가정-외부평가기관의평가의견서(2014.03.31)] |
|
| 출처: 지암회계법인 주식가치 평가보고서 |
| [주식가치평가 주요 내용 요약-외부평가기관의평가의견서(2014.03.31)] |
| 구분 | 내용 |
|---|---|
| 매출 추정 | 1) 회사가 예상하는 임상실험 종료 스케줄에 의하면, 2014년 상반기경 중국 FDA 승인과 동시에 상업적 매출이 가능할 것으로 예상하고 있습니다. 이는 기 서술된 임상실험 진행 정도를 통해 예상한 것으로 그 타당성이 인정되고 있습니다. 2) 회사가 추정하는 매출규모의 경우 대장암과 폐암에서 적용되는 것만을 가정할 때 전 세계적으로약 25억불에 이르고 있으나 Pfizer 사의 경우를 예를 들면 성공적인 신약개발 이후에도 마케팅활동이 부진할 경우 10개의 제품 중 7개의 제품이 시장에서 잊혀질 수 있다는 점을 고려해Worldwide한 aggressive Marketing을 수행하는 점을 감안할 때 회사의 예상매출액이 100% 실현되기 위해서는 막대한 자금의 홍보비용 및 마케팅 방안 마련이 필수적인 것으로 예상되어 이를 전적으로 투자를 받는데 제약점이 존재할 것으로 보아 다소 보수적인 입장에서 이를 평가하였습니다. 3) 회사 제품의 매출품목은 Apatinib Mesylate 단일품목으로 한정하여 이를 추정하였습니다. |
| 매출원가 추정 | (1) 현금흐름의 추정에서 고려하고 있는 생산 위탁의 방식을 적용할 경우 생산단위당 일정금액의 외주가공비 발생형태가 될 것인 바, 매출액 대비 일정비율의 매출원가율을 적용하여 이를 획일적으로 평가하였습니다. (2) 판매단가의 경우에서 가정한 바와 마찬가지로 대규모생산에 돌입할 경우 이에 따른 규모의 경제 효과가 발생되어 단가인하의 요인으로 작용할 수는 있으나 대량생산의 기준이 막연하고 실제 다국적기업 등의 공장을 이용하여 생산한다는 가정을 감안할 때 추가적인 투자요인은 없을 것으로 보아 변동 없이 유지되는 것으로 가정하였습니다. |
| 판매비와관리비 추정 | (1) 인건비 인건비를 추정하기 위하여 현재 회사의 임직원 수를 고려하여 향후 매출의 발생에 따른 관리 직원의증가, 그리고 마케팅 활동 강화를 위한 임원의 추가영입 등을 고려하여 이를 산정하였습니다. (2) 일반관리비 접대비 및 광고선전비 그리고 연구개발비 등의 금액은 그 성격상 매출액의 증가에 비례적으로 연동하는 것으로 보아 추정매출액의 일정비율이 발생되는 것을 가정하였으며, 그 외 고정적 성격의 비용은 이를 개별적으로 산정하기가 곤란한 바, 회사의 현재 예상 Budget 등을 감안, 일정하게 발생되는것으로 가정하였습니다. (3) 영업외손익 영업외손익의 경우 회사의 경상적인 영업활동과는 무관한 항목들로 구성되어 있으며 실질적으로 이를 추정하는 것이 현실적으로 불가능한 것으로 판단하여 발생되지 않는 것으로 하였습니다. 특히 이자비용의 경우, DCF의 특성상 향후 일시적 자금차입에 의한 부채가 발생하더라도 회사의 가중평균비용에 의해 일괄적으로 반영되는 바, 이를 별도로 추정치 아니하였습니다. |
| 가중평균자본비용(WACC) 추정 | (1) 상기 가중평균자본비용 산출 시 자본구조(B/S)는 현재의 자본구조가 아니라 목표자본구조를 의미합니다. 그러나 현재 회사의 경우 사업구조 개편단계에 있으며, 현재 무부채 기업을 지향하고 있는 것으로 판단, 자본구조의 경우 타인자본이 없는 것으로 가정하여 이를 평가하였습니다. (2) 적용베타(β)의 경우 평가일이 속하는 2013년 회사와 유사한 업종을 영위하고 있는 미국 내 상장회사중 2개를 선택, 각 사의 시가총액을 기준으로 가중평균한 후 HAMADA Model에 따라 산정된 무부채기업 베타계수(1.28)을 회사의 베타계수로 보아 평가하였습니다. (3) 상기 가정을 근거로 한 자기자본비용은 11.75%로써 이의 산출내역은 다음과 같습니다. Ke = 3.04% + 9.83% * 1.28 |
| 출처: 지암회계법인 주식가치 평가보고서 |
본 평가인인 지암회계법인은 현금흐름할인법을 적용하여 Elevar Therapeutics Inc.을 평가한 결과, 평가기준일 당시 전체 주식 가치의 범위는 USD 34.2 million ~ USD 38.1 million의 범위에 있을 것으로 추정되었습니다.
| (단위: 천USD) |
| 구분 | 금액 |
|---|---|
| A. 추정기간 FCF의 현재가치 | 36,128 |
| B. 영구현금흐름의 현재가치 | - |
| C. 현금성자산 | - |
| D. 총기업가치(A+B+C) | 36,128 |
| E. 타인자본가치 | - |
| F. 자기자본가치(D-E) | 36,128 |
| G. 발행주식수 | 2,348,208주 |
| H. 평가대상회사의 주당 주식가치(F/G) | USD 15.38 |
| 출처: | 지암회계법인 주식 가치 평가 보고서 |
가중평균자본비용(WACC)를 변수로 하여 평가대상회사의 주식가치의 민감도분석을 수행한 결과는 다음과 같습니다.
| (단위: USD) |
| 구분 | WACC | ||
|---|---|---|---|
| 12.75% | 13.75% | 14.75% | |
| 총기업가치 | 38,122,579 | 36,128,048 | 34,258,709 |
| 주당 주식가치* | 16.23 | 15.39 | 14.59 |
| 출처: | 지암회계법인 주식가치 평가 보고서 |
| * 주당주식가치 = 발행주식총수 2,348,208주 기준 |
|
상기 주식가치평가보고서에 근거했을때, 당사가 2014년 04월 14일 출자한 Elevar의 1주당 가격인 주당 16USD는 중요성의 관점에서 부적정하다고 판단할 만한 근거가 발견되지 아니하였다고 판단되지만, 이는 미래 추정치에 근거한 가격임에 유의하시고, 해당 추정치는 전문가의 주관적 판단의 개입의 여지가 있음에 유의하시기 바랍니다.
(2) 회계법인성지-2014년 12월 15일
당사는 Elevar 向 출자와 관련하여 주식 양수도가액의 적정성을 확인하기 위하여 회계법인성지로부터 Elevar Therapeutics Inc.의 주식가치에 대한 기업가치평가보고서(평가기준일: 2014년 09월 30일)를 수령하였습니다. 그럼에도 불구하고 투자자들께서는 회계법인성지가 주식가치평가보고서에서 제시하는 평가대상회사의 주식가치의 평가 결과는 미래예측에 따른 근본적인 한계가 존재하며, 평가대상회사의 절대적인 가치를 의미하는 것은 아니라는 점에 유의하시기 바랍니다. 회계법인성지는 평가대상회사의 주식가치를 평가하기 위해 현금흐름할인법을 적용하였으며, 평가시 적용한 주요 가정은 다음과 같습니다.
| [평가시 적용된 주요 가정-외부평가기관의평가의견서(2014.12.15)] |
|
| 출처: 회계법인성지 주식가치 평가보고서 |
| [주식가치평가 주요 내용 요약-외부평가기관의평가의견서(2014.12.15)] |
| 구분 | 내용 |
|---|---|
| 매출 추정 | 1) 수익의 발생 시기는 현재 진행 중인 Apatinib의 2상 완료 단계를 2016년 하반기로 추정하고 있으므로 2016년도 말에 현재, 추진 중에 있는 제약사와의 License계약을 체결하여 Upfront Fee를 받고2017년말부터 3년간 Milestones Fee를 수령하는 것으로 추정하였습니다. 2) 회사는 2020년도 중에 3상이 완료될 것으로 예상하고있으며 이 시기부터 10년간 Royalty 수익이 발생할 것으로 예상하고 있습니다. |
| 영업비용 추정 | (1) Sub-license fee 회사는 2020년도 중에 3상이 완료될 것으로 예상하고 있으며 이 시기부터 10년간 Royalty 수익이 발생할 것으로 예상하고 있습니다. (2) Sub-license Royalty 회사가 수령하는 Royalty 수익의 20%를 지급하며 부광약품이 50%부담하므로 순 부담율은 10%임 (3) 급여 총 USD300,000을 지급하며 매년 임금인상율을 5%를 적용함 (4) 기타 영업비용 매출액 대비 3%의 기타 영업비용이 발생하는 것으로 추정함 |
| 영업활동 현금흐름 및 투자활동 현금흐름 추정 |
(1) 회사는 추가적인 License 투자를 통한 수익 창출을 도모할 계획을 가지고 있으나 본주식가치평가 편에서는 추가 License투자를 통한 영업수익과 비용, 예상되는 투자비를 구체적으로추정하는 것이 현실적으로 어려운 점을 감안하여 별도로 고려하지 아니하였습니다. (2) 다만, 추가적인 License투자를 통하여 회사의 기업가치와 주식가치는 증가할 것으로 추측해 볼 수 있는데 계약당사자 입장에서 보수적인 관점과 현실적인 추정의 어려운 점 등을 감안할 때 이러한 투자로 인한 주식가치 증감을 고려하지 않는 것이 타당할 것으로 사료됩니다. |
| 가중평균자본비용(WACC) 추정 | (1) 미국 뉴욕 증권시장에 상장된 회사 중 평가대상 사업과 유사한 업종을 영위하는 기업으로 분류할 수 있는 Johnson & Johnson과 Novartis의 베타를 이용하여 평가대상회사의 베타를 추정하는 방법을 이용하였습니다. 동사들의 무부채 베타계수(Unlevered β)를 산정하고 이를 단순 평균한 결과 무부채 베타계수의 평균은 0.49로 측정되었으며 평가대상회사의 목표자본구조는 비교대상회사들의 평균자본구조인 0%(부채/자본)를 목표자본구조로 가정하여 회사의 베타계수를 0.49로 동일하게 추정되었습니다. (2) 주식가치를 평가함에 있어서 잉여영업현금흐름(Free Cash Flow)에 대한 할인율은 14.09%를 기준으로 할인하여 산정하였습니다. |
| 출처: 회계법인성지 주식가치 평가보고서 |
본 평가인인 회계법인성지는 현금흐름할인법을 적용하여 Elevar Therapeutics Inc.을 평가한 결과, 평가기준일 당시 전체 주식 가치의 범위는 USD 78.48 million ~ USD 144.72 million의 범위에 있을 것으로 추정되었습니다.
| (단위: 백만 USD) |
| 구분 | 금액 |
|---|---|
| A. 영업수익 | 728.21 |
| B. 영업비용(현금지출) | 109.15 |
| C. 세전잉여현금흐름(A+B) | 619.06 |
| D. 잉여현금흐름에 대한 법인세 | 247.62 |
| E. 세후잉여현금흐름(C-D) | 371.44 |
| F. 가중평균자본비용(WACC) | 14.09% |
| G. 기업가치(Enterprise Value) | 103.19 |
| H. 부채 | - |
| I. 비영업용 자산 | 1.87 |
| J. 주식가치(Equity Value)(H+I) | 105.06 |
| 출처: | 회계법인성지 주식 가치 평가 보고서 |
매출액 증가율은 1%로 가정하고, 가중평균자본비용(WACC)를 변수로 하여 평가대상회사의 주식가치의 민감도분석을 수행한 결과는 다음과 같습니다.
| (매출액증가율 1%가정) | (단위: 백만USD, USD) |
| 구분 | WACC | ||||
|---|---|---|---|---|---|
| 10.09% | 12.09% | 14.09% | 16.09% | 18.09% | |
| 총기업가치 | 144.72 | 122.85 | 105.06 | 90.49 | 78.48 |
| 주당 주식가치* | 58.55 | 49.70 | 42.51 | 36.61 | 31.75 |
| 출처: | 회계법인성지 주식가치 평가 보고서 |
| * 주당주식가치 = 발행주식총수 2,471,705주 기준 |
|
당사가 2015년 01월 05일 및 2015년 02월 16일 출자한 Elevar의 1주당 가격인 주당 40USD는 중요성의 관점에서 부적정하다고 판단할 만한 근거가 발견되지 아니하였다고 판단되지만, 이는 미래 추정치에 근거한 가격임에 유의하시고, 해당 추정치는 전문가의 주관적 판단의 개입의 여지가 있음에 유의하시기 바랍니다.
(3) 대성회계법인-2017년 08월 08일
당사는 Elevar 向 출자와 관련하여 주식 양수도가액의 적정성을 확인하기 위하여 대성회계법인으로부터 Elevar Therapeutics Inc.의 주식가치에 대한 기업가치평가보고서(평가기준일: 2017년 03월 31일)를 수령하였습니다. 그럼에도 불구하고 투자자들께서는 대성회계법인이 주식가치평가보고서에서 제시하는 평가대상회사의 주식가치의 평가 결과는 미래예측에 따른 근본적인 한계가 존재하며, 평가대상회사의 절대적인 가치를 의미하는 것은 아니라는 점에 유의하시기 바랍니다. 대성회계법인은 평가대상회사의 주식가치를 평가하기 위해 현금흐름할인법을 적용하였으며, 평가시 적용한 주요 가정은 다음과 같습니다.
| [평가시 적용된 주요 가정-외부평가기관의평가의견서(2017.08.08)] |
|
| 출처: 대성회계법인 주식가치 평가보고서 |
| [주식가치평가 주요 내용 요약-외부평가기관의평가의견서(2017.08.08)] |
| 구분 | 내용 |
|---|---|
| 영업수익의 추정 | (1) 라이선스 수익 라이선스 수익의 경우 대만, 부광약품과의 판권계약에 의거한 유럽, 일본(한국은 부광약품 독점권리보유) 그리고 현재 임상진행중인 미국을 대상으로 하였습니다. 또한 라이선스 Fee 를 수령하는 스케줄과 국가별 라이선스 계약금액은 회사의 사업계획 자료를 사용하였습니다. (2) 로열티 수익 로열티 수익은 평가대상회사가 현재 임상진행중인 위암(3 기), 대장암(3,4 기), 간암(2 기)에 대한 partner 사의 매출을 추정하고, 6%의 로열티율(부광약품 계약근거)을 일괄적으로 적용하여 추정하였습니다. |
| 영업비용의 추정 | (1) 라이선스 비용 Advenchen, ㈜부광약품간의 계약에 의거, 원개발사인 Advenchen 의 경우 전세계(중국 제외) 수익 인식액의 25.25%(전체 32.5%이나 이중 ㈜부광약품 7.25%부담), ㈜부광약품의 경우 유럽 및 일본 매출액 관련 수익 인식액의 14.5%를 라이선스비용으로 부담합니다. (2) 로열티 비용 Advenchen, ㈜부광약품과의 계약에 의거, 원개발사인 Advenchen 의 경우 전세계(중국 제외) 수익인식액의 20%, ㈜부광약품의 경우 유럽 및 일본 매출액 관련 수익 인식액의 14.5%를 로열티비용으로 부담합니다. |
| 기타영업비용의 추정 | (1) 인건비 급여의 경우 평가대상회사가 제시한 인력계획과 기준일 현 grade 별 인당 급여 수준을 고려하였으며, 향후 임금상승계획 및 물가상승률을 반영하여 추정하였습니다. 또한 복리비의 경우 급여대비 일정비율을 적용하여 추정하였습니다. (2) 감가상각비 감가상각비는 보유하고있는 유무형자산에 대한 상각비로서, 향후 내용연수에 따라 추정하였습니다. 단, 본 사업을 위한 특허취득은 완료되었으며 향후 추가투자는 없음을 고려하였습니다. 이외 유형자산에 대한 재투자가정은 금액적 중요성이 낮아 별도로 고려하지 아니하였습니다. |
| 가중평균자본비용(WACC) 추정 | 가중평균자본비용은 자기자본비용(Ke)과 세후 타인자본비용(Kd)을 가중평균하여 산출하며, 가중평균을 위한 목표자본구조는 평가대상회사와 유사한 영업을 영위하는 회사의 자본구조(B/S) 산술평균값인 11.65%를 적용하였습니다. 이에 따라 산출된 가중평균자본비용은 16.09%입니다. |
| 출처: 대성회계법인 주식가치 평가보고서 |
본 평가인인 대성회계법인은 현금흐름할인법을 적용하여 Elevar Therapeutics Inc.을 평가한 결과, 평가기준일 당시 전체 주식 가치의 범위는 USD 196.2 million ~ USD 226.8 million의 범위에 있을 것으로 추정되었습니다.
| (단위: 천USD) |
| 구분 | 금액 |
|---|---|
| A. 추정기간 FCF의 현재가치 | 160,886 |
| B. 영구현금흐름의 현재가치 | 46,813 |
| C. 영업관련 현금흐름의 현재가치(A+B) | 207,699 |
| D. 비영업용자산 | 2,854 |
| E. 평가대상회사의 주식가치(C+D) | 210,553 |
| 출처: | 대성회계법인 주식 가치 평가 보고서 |
가중평균자본비용(WACC)를 변수로 하여 평가대상회사의 주식가치의 민감도분석을 수행한 결과는 다음과 같습니다.
| (단위: 천USD,USD) |
| 구분 | WACC | ||
|---|---|---|---|
| 15.09% | 16.09% | 17.09% | |
| 총기업가치 | 226,898 | 210,553 | 196,219 |
| 주당 주식가치 | 82.24 | 76.32 | 71.12 |
| 출처: | 대성회계법인 주식가치 평가 보고서 |
| * 주당주식가치 = 발행주식총수 2,758,870주 기준 |
|
상기 주식가치평가보고서에 근거했을때, 당사가 2017년 08월 09일 출자한 Elevar의 1주당 가격인 주당 76USD는 중요성의 관점에서 부적정하다고 판단할 만한 근거가 발견되지 아니하였다고 판단되지만, 이는 미래 추정치에 근거한 가격임에 유의하시고, 해당 추정치는 전문가의 주관적 판단의 개입의 여지가 있음에 유의하시기 바랍니다.
(4) 회계법인새시대-2018년 07월 25일
당사는 Elevar 向 출자와 관련하여 주식 양수도가액의 적정성을 확인하기 위하여 회계법인새시대로부터 Elevar Therapeutics Inc.의 주식가치에 대한 기업가치평가보고서(평가기준일: 2018년 03월 31일)를 수령하였습니다. 그럼에도 불구하고 투자자들께서는 회계법인새시대가 주식가치평가보고서에서 제시하는 평가대상회사의 주식가치의 평가 결과는 미래예측에 따른 근본적인 한계가 존재하며, 평가대상회사의 절대적인 가치를 의미하는 것은 아니라는 점에 유의하시기 바랍니다. 회계법인새시대는 평가대상회사의 주식가치를 평가하기 위해 현금흐름할인법을 적용하였으며, 평가시 적용한 주요 가정은 다음과 같습니다.
| [평가시 적용된 주요 가정-외부평가기관의평가의견서(2018.07.25)] |
|
| 출처: 회계법인새시대 주식가치 평가보고서 |
| [주식가치평가 주요 내용 요약-외부평가기관의평가의견서(2018.07.25)] |
| 구분 | 내용 |
|---|---|
| 영업수익의 추정 | (1) 판매단가 회사제시 사업계획 판매단가를 기준으로 물가상승률만큼 증가한다고 가정 미국 : 10,000 USD 유럽 : 5,100 USD 일본 : 6,300 USD (2) 판매수량 . 회사제시 사업계획 판매수량을 적용함 . . 판매수량 = 각국 인구수 * 발병률 * 전이율 * 임상성공률 * 시장점유율 * Cycle 등의 변수를 적용하여 추정 . Cycle:위암 3차(3회) / 위암 2차(5회) / 대장암 3차(2회) |
| 영업비용의 추정 | (1) 라이선스 비용 To Advenchen : 라이선스 수익에 대하여 Advenchen에 수익의 32.5%를 지급함 . 보전 By BK : 라이선스 수익의 7.25%를 보전하여줌 . LSKB.의 실제 지급은 25.25%가 됨. (2) 로열티 비용 To Advenchen : 전체 로열티 수익의 20% 를 지급함 . to BK : 유럽 & 일본 로열티 수익의 14.5%를 지급함 . |
| 기타영업비용의 추정 | (1) 인건비 직원 대부분이 관리인력이므로, 매출 증가에 둔감하게 증가 추정함. 로열티 수익이 발생하는 2021 년부터 매년 1명씩 증가함을 가정함 . (2) 변동비성 경비 / 고정비성 경비 영업수익 대비 1% 발생을 가정함. 회사제시 사업계획 및 외부전망기관의 물가상승률을 반영하여 추정함 . |
| 가중평균자본비용(WACC) 추정 | 베타( β) : 1.4911(회사제시 8개 동종업계 2개년 중위값) 목표자본구조(B/S) : 0.0% WACC : 16.79% 영구성장률 : 1.00% |
| 출처: 회계법인새시대 주식가치 평가보고서 |
본 평가인인 회계법인새시대는 현금흐름할인법을 적용하여 Elevar Therapeutics Inc.을 평가한 결과, 평가기준일 당시 전체 주식 가치의 범위는 USD 268.2 million ~ USD 274.1 million의 범위에 있을 것으로 추정되었습니다.
| (단위: 천USD) |
| 구분 | 금액 |
|---|---|
| A. PV of FCFF | 179,811 |
| B. Counting Value | 81,023 |
| C. 영업가치(A+B) | 260,834 |
| D. 비영업용자산 | 16,312 |
| E. 기업가치(C+D) | 277,146 |
| F. Net Debt | 6,112 |
| G.자기자본가치(E-F) | 271,034 |
| 출처: | 회계법인새시대 주식 가치 평가 보고서 |
영구성장률 1%로 가정하고, 가중평균자본비용(WACC)를 변수로 하여 평가대상회사의 주식가치의 민감도분석을 수행한 결과는 다음과 같습니다.
| (영구성장률 1%가정) | (단위: 천USD, USD) |
| 구분 | WACC | ||
|---|---|---|---|
| 16.29% | 16.79% | 17.29% | |
| 총 자기자본가치 | 288,290 | 271,034 | 255,180 |
| 주당 주식가치* | 95.43 | 89.72 | 84.47 |
| 출처: | 회계법인새시대 주식가치 평가 보고서 |
| * 주당주식가치 = 발행주식총수 3,020,857주 기준 |
|
상기 주식가치평가보고서에 근거했을때, 당사가 2018년 07월 25일 출자한 Elevar의 1주당 가격인 주당 90USD는 중요성의 관점에서 부적정하다고 판단할 만한 근거가 발견되지 아니하였다고 판단되지만, 이는 미래 추정치에 근거한 가격임에 유의하시고, 해당 추정치는 전문가의 주관적 판단의 개입의 여지가 있음에 유의하시기 바랍니다.
(5) 대주회계법인-2019년 04월 26일
당사는 Elevar 向 출자와 관련하여 주식 양수도가액의 적정성을 확인하기 위하여 대주회계법인으로부터 Elevar Therapeutics Inc.의 주식가치에 대한 기업가치평가보고서(평가기준일: 2018년 12월 31일)를 수령하였습니다. 그럼에도 불구하고 투자자들께서는 대주회계법인이 주식가치평가보고서에서 제시하는 평가대상회사의 주식가치의 평가 결과는 미래예측에 따른 근본적인 한계가 존재하며, 평가대상회사의 절대적인 가치를 의미하는 것은 아니라는 점에 유의하시기 바랍니다. 대주회계법인은 평가대상회사의 주식가치를 평가하기 위해 현금흐름할인법을 적용하였으며, 평가시 적용한 주요 가정은 다음과 같습니다.
| [평가시 적용된 주요 가정-외부평가기관의평가의견서(2019.04.26)] |
|
| 출처: 대주회계법인 주식가치 평가보고서 |
| [주식가치평가 주요 내용 요약-외부평가기관의평가의견서(2019.04.26)] |
| 구분 | 내용 |
|---|---|
| 영업수익의 추정 | (1) 판매단가 회사제시 사업계획 판매단가를 기준으로 물가상승률만큼 증가한다고 가정 미국 : 10,000USD / 유럽 : 5,100USD / 일본 : 6,300USD / 한국 : 2,500USD (2) 판매수량 . 회사제시 사업계획 판매수량을 적용함 . . 판매수량 = 각국 인구수 * 발병률 * 전이율 * 임상성공률 * 시장점유율 * Cycle 등의 변수를 적용하여 추정 . Cycle:위암 3차(5회) / 위암 2차(5회) / 대장암 3차(4회) / 선모낭포암1차(10회) / 간암1차(10회) |
| 영업비용의 추정 | (1) 라이선스 비용 To Advenchen : 전체 라이선스 수익의 32.46%를 Advenchen사에 지급(전체 지급액 35%의 7.25%를 HLB-LS에서 지급) To HLB-LS : 유럽 & 일본 라이선스 수익의 14.5%를 HLB-LS(에이치엘비생명과학)에 지급 (2) 로열티 비용 To Advenchen : 전체 로열티 수익의 20% 를 지급함 . to HLB-LS : 유럽 & 일본 로열티 수익의 14.5%를 지급함 . |
| 기타영업비용의 추정 | (1) 인건비 급여 인원수: 회사의 중장기 인력 계획을 고려하여 추정 인당 급여: 향후 명목임금상승률(EIU, 2018)에 따라 증가한다고 가정 (2) 고정비 임상비용: 회사 사업계획을 고려하여 추정(라이선스아웃 이후에는 전액파트너사가 부담) 향후 소비자물가상승률(EIU, 2018)에 따라 증가한다고 가정 |
| 가중평균자본비용(WACC) 추정 | 베타( β) : 1.246(동일업종을 영위하는 미국 상장사 6개의 과거 2년 Weekly adjusted beta의 중간값) 목표자본구조(B/S) : 0.0% WACC : 15.30% |
| 출처: 대주회계법인 주식가치 평가보고서 |
본 평가인인 대주회계법인은 현금흐름할인법을 적용하여 Elevar Therapeutics Inc.을 평가한 결과, 평가기준일 당시 전체 주식 가치의 범위는 USD 366.8 million ~ USD 456.0 million의 범위에 있을 것으로 추정되었습니다.
| (단위: 천USD) |
| 구분 | 금액 |
|---|---|
| A. 영업현금흐름의 현재가치 | 310,793 |
| B. Counting Value | 97,412 |
| C. 영업현금흐름 합계(A+B) | 408,205 |
| D. 비영업자산 | 14,017 |
| E. 기업가치(C+D) | 422,222 |
| F. Debt Like Item | - |
| G.주식가치(E-F) | 422,222 |
| 출처: | 대주회계법인 주식 가치 평가 보고서 |
영구성장률 -5%로 가정하고, 가중평균자본비용(WACC)를 변수로 하여 평가대상회사의 주식가치의 민감도분석을 수행한 결과는 다음과 같습니다.
| (영구성장률 -5% 가정) | (단위: 천USD, USD) |
| 구분 | WACC | ||
|---|---|---|---|
| 14.30% | 15.30% | 16.30% | |
| 총 영업현금흐름 가치 | 456,036 | 408,205 | 366,809 |
| 총 주식가치 | 470,053 | 422,222 | 380,826 |
| 주당 주식가치* | 143.56 | 128.95 | 116.31 |
| 출처: | 대주회계법인 주식가치 평가 보고서 |
| * 주당주식가치 = 발행주식총수 3,274,320주 기준 |
|
상기 주식가치평가보고서에 근거했을때, 당사가 2019년 04월 30일 및 2019년05월 31일 출자한 Elevar의 1주당 가격인 주당 122USD는 중요성의 관점에서부적정하다고 판단할 만한 근거가 발견되지 아니하였다고 판단되지만, 이는 미래 추정치에 근거한 가격임에 유의하시고, 해당 추정치는 전문가의 주관적 판단의 개입의 여지가 있음에 유의하시기 바랍니다.
(6) 삼도회계법인-2022년 03월 10일
당사는 Elevar의 영업권 손상평가와 관련하여 손상검사 목적으로 삼도회계법인으로부터 Elevar Therapeutics Inc.의 사용가치평가보고서(평가기준일: 2021년 09월 30일)를 수령하였습니다. 그럼에도 불구하고 투자자들께서는 삼도회계법인이 사용가치평가보고서에서 제시하는 평가대상회사의 주식가치의 평가 결과는 미래예측에 따른 근본적인 한계가 존재하며, 평가대상회사의 절대적인 가치를 의미하는 것은 아니라는 점에 유의하시기 바랍니다. 삼도회계법인은평가대상회사의 주식가치를 평가하기 위해 현금흐름할인법을 적용하였으며, 평가시 적용한 주요 가정은 다음과 같습니다.
| [평가시 적용된 주요 가정-외부평가기관의평가의견서(2022.03.10)] |
|
| [사용가치평가 주요 내용 요약-외부평가기관의평가의견서(2022.03.10)] |
| 구분 | 내용 |
|---|---|
| 영업수익의 추정 | (1) 영업 수익 국가별로 구분하여 대상회사의 사업계획(단계별 Upfront 및 Milestone Fee)에 근거한 예상매출액에 임상성공확률을 곱하여 추정 EU와 Japan 지역은 누적 Sales 규모에 따른 milestone 수입을 매출 추정에 따라 반영하였습니다. (2) 로열티 수익 국가별 추정 매출액(임상성공확률 반영 후) = 추정환자수 x 추정시장점유율 x 예상 판매가격 x 사이클 당 투약횟수 x 임상성공확률 국가별 로열티수익 = 국가별로 추정 매출액(임상성공확률 반영 후) x 예상 로열티율 (3) 판매 수익 국가별 추정 매출액(임상성공확률 반영 후)= 추정환자수 x 추정시장점유율 x 예상 판매가격 x 사이클 당 투약횟수 x 임상성공확률 국가별 판매수익 = 국가별로 추정 매출액(임상성공확률 반영 후) x 예상 판매수익률(50%) x Performance rate |
| 영업비용의 추정 | (1) 라이선스 비용 국가(파이프라인)별로 구분하여 각 세부항목별로 대응되는 영업수익에 비용률을 곱하여 추정. (2) 임상비용 파이프라인별로 구분하여 각 임상 단계별로 대응되는 평균 임상비용을 반영하여 추정 |
| 기타영업비용의 추정 | (1) 인건비 급여는 대상회사의 사업계획에 따른 인원수 및 EIU 추정 미국 임금상승률을 고려하여 추정하고, 퇴직급여 및 복리후생비는 과거 급여 대비 비율을 적용하여 추정함 (2) 고정비성 비용 EIU 추정 미국 소비자물가상승률을 적용하여 추정함 (주식기준보상은 회사제시 스케쥴 반영) (3) 변동비성 비용 변동비성 비용은 임상비용이며, 대상회사 제시 사업계획을 고려하여 추정함 |
| 가중평균자본비용(WACC) 추정 | 베타( β) : 0.91 목표자본구조(B/S) : 0.0% WACC : 14.00% |
| 출처: 삼도회계법인 사용가치 평가보고서 |
본 평가인인 삼도회계법인은 현금흐름할인법을 적용하여 Elevar Therapeutics Inc.을 평가한 결과, 평가기준일 당시 전체 주식 가치의 범위는 USD 278.5 million ~ USD 291.1 million의 범위에 있을 것으로 추정되었습니다.
| (단위: 천USD) |
| 구분 | 금액 |
|---|---|
| A. 영업가치 | 284,736 |
| B. 비영업자산 | - |
| C. 기업가치(A+B) | 284,736 |
| D. 이자발생부채 | - |
| E. 사용가치(C-D) | 284,736 |
| 출처: | 삼도회계법인 사용가치 평가 보고서 |
가중평균자본비용(WACC)를 변수로 하여 평가대상회사의 주식가치의 민감도분석을 수행한 결과는 다음과 같습니다.
| (단위: 천USD, USD) |
| 구분 | WACC | ||
|---|---|---|---|
| 13.75% | 14.00% | 14.25% | |
| 사용가치 | 315,002 | 307,020 | 299,230 |
| 주당 주식가치* | 5.57 | 5.43 | 5.29 |
| 출처: | 대주회계법인 주식가치 평가 보고서 |
| * 주당주식가치 = 발행주식총수 56,579,443주 기준 | |
상기 주식가치평가보고서에 근거했을때, 당사가 2022년 04월 27일 및 2022년08월 26일 출자한 Elevar의 1주당 가격인 주당 5.03USD는 중요성의 관점에서 부적정하다고 판단할 만한 근거가 발견되지 아니하였다고 판단되지만, 이는미래 추정치에 근거한 가격임에 유의하시고, 해당 추정치는 전문가의 주관적 판단의 개입의 여지가 있음에 유의하시기 바랍니다.
당사의 동 지분 취득과 관련하여 금융감독원 전자공시시스템에 공시한 내용은 다음과 같습니다.
| [타법인주식및출자증권취득결정](2022.04.27) |
| 1. 발행회사 | 회사명(국적) | Elevar Therapeutics,Inc | 대표이사 | Saeho Chong |
| 자본금(원) | 318,027,242,902 | 회사와 관계 | 종속회사 | |
| 발행주식총수(주) | 56,579,443 | 주요사업 | 바이오의약품 개발 | |
| -최근 6월 이내 제3자 배정에 의한 신주취득 여부 | 아니오 | |||
| 2. 취득내역 | 취득주식수(주) | 5,000,000 | ||
| 취득금액(원) | 31,394,745,000 | |||
| 자기자본(원) | 512,184,802,697 | |||
| 자기자본대비(%) | 6.13 | |||
| 대기업 여부 | 해당 | |||
| 3. 취득후 소유주식수 및 지분비율 | 소유주식수(주) | 61,579,443 | ||
| 지분비율(%) | 100 | |||
| 4. 취득방법 | 현금 취득(주주배정 유상증자 참여) | |||
| 5. 취득목적 | 종속회사 임상 자금 확보 등 | |||
| 6. 취득예정일자 | 2022-04-27 | |||
| 7. 자산양수의 주요사항보고서 제출대상 여부 | 아니오 | |||
| -최근 사업연도말 자산총액(원) | 743,692,264,095 | 취득가액/자산총액(%) | 4.22 | |
| 8. 우회상장 해당 여부 | 아니오 | |||
| -향후 6월이내 제3자배정 증자 등 계획 | 아니오 | |||
| 9. 발행회사(타법인)의 우회상장 요건 충족여부 | 아니오 | |||
| 10. 이사회결의일(결정일) | 2022-04-27 | |||
| -사외이사 참석여부 | 참석(명) | 3 | ||
| 불참(명) | 0 | |||
| -감사(감사위원) 참석여부 | 참석 | |||
| 11. 공정거래위원회 신고대상 여부 | 미해당 | |||
| 12. 풋옵션계약 등의 체결여부 | 아니오 | |||
| -계약내용 | - | |||
| 13. 기타 투자판단에 참고할 사항 | - 상기 자기자본은 2021년도말 연결재무제표를 기준으로 현재까지 증가된 자본금등을 반영한 금액입니다. - 상기 자산총액은 2021년도말 연결재무제표상 기준입니다. - 상기 취득금액은 USD25,150,000로 이사회결의일 당일 서울외국환중개(주)의 최초고시 매매기준환율(1,248.30 KRW/USD)를 적용하여 산정하였습니다. - 하기 발행회사의 요약재무상황은 2019년말, 2020년말, 2021년말 기준입니다. |
|||
[발행회사의 요약 재무상황] (단위 : 백만원)
| 구분 | 자산총계 | 부채총계 | 자본총계 | 자본금 | 매출액 | 당기순이익 |
|---|---|---|---|---|---|---|
| 당해년도 | 50,455 | 65,505 | -15,050 | 318,027 | 0 | -63,462 |
| 전년도 | 270,549 | 42,719 | 227,830 | 275,414 | 0 | -37,097 |
| 전전년도 | 267,340 | 51,597 | 215,744 | 215,692 | 0 | -42,590 |
[상대방에 관한 사항]
| 1. 인적사항 | |||
| - 기본사항 | |||
| 성명(명칭) | 국적 | 주소(본점소재지)[읍ㆍ면ㆍ동까지만 기재] | 생년월일(사업자등록번호 등) |
| Elevar Therapeutics,Inc | 미국 | 유타주 솔트레이크시티 | - |
| 직업(사업내용) | 바이오의약품 개발 | ||
| - 최대주주ㆍ대표이사ㆍ대표집행임원 현황 및 재무상황 등(상대방이 법인인 경우) | |||
| 구분 | 성명 | 주식수 | 지분율(%) |
| 최대주주 | 에이치엘비(주) | 56,579,443 | 100 |
| 대표이사 | Saeho Chong | - | - |
| (단위 : 백만원) | |||
| 해당 사업연도 | 2021 | 결산기 | 12월 |
| 자산총계 | 50,455 | 자본금 | 318,027 |
| 부채총계 | 65,505 | 매출액 | 0 |
| 자본총계 | -15,050 | 당기순손익 | -63,462 |
| 외부감사인 | - | 휴업 여부 | 아니오 |
| 감사의견 | - | 폐업 여부 | 아니오 |
| 2. 상대방과의 관계 | |||
| 1. 회사와 상대방과의 관계 | 종속회사 | ||
| 2. 회사의 최대주주ㆍ임원과 상대방과의 관계 | 성명 | 상대방과의 관계 | |
| 이사 | 진양곤 | 회사임원 | |
| 이사 | 김동건 | 회사임원 | |
| 사외이사 | 장인근 | 회사임원 | |
| 3. 최근 3년간 거래내역(일상적 거래 제외) | |||
| 구분 | 거래 내역 | ||
| 당해년도 | - | ||
| 전년도 | - | ||
| 전전년도 | - | ||
| 출처 : 금융감독원 전자공시시스템 |
| [타법인주식및출자증권취득결정](2022.08.24) |
| . 발행회사 | 회사명(국적) | Elevar Therapeutics,Inc | 대표이사 | Saeho Chong |
| 자본금(원) | 318,027,242,902 | 회사와 관계 | 종속회사 | |
| 발행주식총수(주) | 61,579,443 | 주요사업 | 바이오의약품 개발 | |
| -최근 6월 이내 제3자 배정에 의한 신주취득 여부 | 아니오 | |||
| 2. 취득내역 | 취득주식수(주) | 6,000,000 | ||
| 취득금액(원) | 40,495,524,000 | |||
| 자기자본(원) | 595,273,496,969 | |||
| 자기자본대비(%) | 6.80 | |||
| 대기업 여부 | 해당 | |||
| 3. 취득후 소유주식수 및 지분비율 | 소유주식수(주) | 67,579,443 | ||
| 지분비율(%) | 100 | |||
| 4. 취득방법 | 현금 취득(주주배정 유상증자 참여) | |||
| 5. 취득목적 | 종속회사 임상자금 확보 등 | |||
| 6. 취득예정일자 | 2022-08-26 | |||
| 7. 자산양수의 주요사항보고서 제출대상 여부 | 아니오 | |||
| -최근 사업연도말 자산총액(원) | 743,692,264,095 | 취득가액/자산총액(%) | 5.45 | |
| 8. 우회상장 해당 여부 | 아니오 | |||
| -향후 6월이내 제3자배정 증자 등 계획 | 아니오 | |||
| 9. 발행회사(타법인)의 우회상장 요건 충족여부 | 아니오 | |||
| 10. 이사회결의일(결정일) | 2022-08-24 | |||
| -사외이사 참석여부 | 참석(명) | 3 | ||
| 불참(명) | 0 | |||
| -감사(감사위원) 참석여부 | 참석 | |||
| 11. 공정거래위원회 신고대상 여부 | 미해당 | |||
| 12. 풋옵션계약 등의 체결여부 | 아니오 | |||
| -계약내용 | - | |||
| 13. 기타 투자판단에 참고할 사항 | - 상기 자기자본은 2021년도말 연결재무제표를 기준으로 현재까지 증가된 자본금등을 반영한 금액입니다. - 상기 자산총액은 2021년도말 연결재무제표상 기준입니다. - 상기 취득금액은 USD 30,180,000로 이사회결의일 당일 서울외국환중개(주)의 최초고시 매매기준환율(1,341.80 KRW/USD)를 적용하여 산정하였습니다. - 하기 발행회사의 요약재무상황은 2019년말, 2020년말, 2021년말 기준입니다. |
|||
[발행회사의 요약 재무상황] (단위 : 백만원)
| 구분 | 자산총계 | 부채총계 | 자본총계 | 자본금 | 매출액 | 당기순이익 |
|---|---|---|---|---|---|---|
| 당해년도 | 50,455 | 65,505 | -15,050 | 318,027 | 0 | -63,462 |
| 전년도 | 270,549 | 42,719 | 227,830 | 275,414 | 0 | -37,097 |
| 전전년도 | 267,340 | 51,597 | 215,744 | 215,692 | 0 | -42,590 |
[상대방에 관한 사항]
| 1. 인적사항 | |||
| - 기본사항 | |||
| 성명(명칭) | 국적 | 주소(본점소재지)[읍ㆍ면ㆍ동까지만 기재] | 생년월일(사업자등록번호 등) |
| Elevar Therapeutics,Inc | 미국 | 유타주 솔트레이크시티 | - |
| 직업(사업내용) | 바이오의약품 개발 | ||
| - 최대주주ㆍ대표이사ㆍ대표집행임원 현황 및 재무상황 등(상대방이 법인인 경우) | |||
| 구분 | 성명 | 주식수 | 지분율(%) |
| 최대주주 | 에이치엘비(주) | 61,579,443 | 100 |
| 대표이사 | Saeho Chong | - | - |
| (단위 : 백만원) | |||
| 해당 사업연도 | 2021 | 결산기 | 12월 |
| 자산총계 | 50,455 | 자본금 | 318,027 |
| 부채총계 | 65,505 | 매출액 | 0 |
| 자본총계 | -15,050 | 당기순손익 | -63,462 |
| 외부감사인 | - | 휴업 여부 | 아니오 |
| 감사의견 | - | 폐업 여부 | 아니오 |
| 2. 상대방과의 관계 | |||
| 1. 회사와 상대방과의 관계 | 종속회사 | ||
| 2. 회사의 최대주주ㆍ임원과 상대방과의 관계 | 성명 | 상대방과의 관계 | |
| 이사 | 진양곤 | 회사임원 | |
| 이사 | 김동건 | 회사임원 | |
| 사외이사 | 장인근 | 회사임원 | |
| 3. 최근 3년간 거래내역(일상적 거래 제외) | |||
| 구분 | 거래 내역 | ||
| 당해년도 | - | ||
| 전년도 | - | ||
| 전전년도 | - | ||
| 출처 : 금융감독원 전자공시시스템 |
Immunomic의 기업개황, 연혁 및 요약재무상태표는 아래와 같습니다.
| [Immunomic 기업개황] |
| 구분 | 내용 |
|---|---|
| Office Location | 15010 Broschart Road Suite 250 Rockville, MD 20850 USA |
| 회사명 | Immunomic Therapeutics, Inc. |
| 설립년월 | 2005년 9월 |
| 자본금(주식수) | USD 2,995.55(보통주식수 26,555,609주/우선주식수 463,330주) |
| 홈페이지 | https://www.immunomix.com/ |
| 대표이사 | William G. Hearl |
| 상장여부 | 비상장 |
| 주요 주주현황 | HLB Co., Ltd.(41.07%, 최대주주), Hummel Affiliates(5.42%), Life Sciences Greenhouse of Central PA (4.00%), HLB Global Co., Ltd. (3.64%) William G. Hearl(2.95%), 기타주주(42.92%) |
| 주요 임원 (연구진) 현황 |
- William G. Hearl : 설립자, CEO - Teri Jones-Heiland : CSO - Eric Winzer : CFO - Robert Newman : CBO |
| 주요 치료제 | A. ITI-1000 (교모세포종) B. ITI-1001 (교모세포종) C. ITI-3000 (메르켈 피부암) |
| [Immunomic 연혁] |
| 일 자 | 내 용 |
|---|---|
| 2006년 | Johns Hopkins Univ.와 LAMP 기술에 대한 전세계 독점 라이선스 권리 취득 |
| 2006년 | Geron Corp.에 Sub-Licensed 부여 |
| 2006년 | Nature Tech.와 cross-license vaccine technologies 기술 공유 합의 |
| 2009년 | AML 연구의 GRNVAC1 결과가 Phase I / II endpoint 충족결과 발표 |
| 2010년 | 2010 Frost & Sullivan Award - 백신분야에서 올해의 생명공학혁신상 수상 |
| 2011년 | 동물 제약 분야 및 다수의 백신 라이선스 적용을 위해 대규모 제약회사와 공동 연구 및 라이센스 계약 체결 |
| 2012년 | FDA로부터 Jananese Red cedar immunotherapeutic vaccine 1상 임상 연구 승인 |
| 2012년 | LAMP-vax IP “키메라 백신” 특허에 대한 EU 특허 승인. JRC-LAMP-vax의 임상 연구 1상 착수 |
| 2012년 | LAMP-vax IP “키메라 백신” 특허 미국내 승인 |
| 2013년 | JRC-LAMP-vax에 대한 IA 단계 실험 성공적 완료 |
| 2014년 | 다양한 땅콩 알레르기에 대한 SBIR Grant 수상 |
| 2015년 | Astellas Pharma.와 알레르기 예방 및 치료를 위한 LAMP-VAX Platform관련 글로벌 라이센스 계약 체결 |
| 2017년 | Phase II Cancer Immunotherapy Technology의 독점 라이센스 발표 |
| 2018년 | LAMP-vax 플랫폼을 UNITE(UNiversal Intracellular Targeted Expression 범용세포내 표적발현)로 변경 |
| 2019년 | JRC2-LAMP-vax에 대해 Astellas 사로부터 5백만불의 Milestone 수령 |
| 2020년 | 에이치엘비(주)의 종속회사로 편입 |
| 2020년 | ITI-1000(교모세포종 치료를 위한 면역항암제) 생산을 위한 CoImmune과 파트너쉽 체결 |
| 2021년 | Lineage Cell Therapeutics 사와 면역항암제 라이선스 계약 체결 |
| 2021년 | 일본 적삼나무(Japanese Red Cedar) 알레르기 백신의 개발 및 상용화를 위해 IDRI (Infectious Disease Research Institute)와 RNA 백신 플랫폼의 지적재산권에 대한 전세계 독점 라이선스 계약 체결 |
| 2022년 | Drew Pardoll 연구소(JHU)와 activin antibody 특허 자산(및 개선사항) 관련 라이선스 계약 체결 |
| [Immunomic 요약재무상태표] | |
| (K-IFRS) | (단위: USD, %) |
| 결산연월 또는 결산기간 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|
| 1. 자산총계 | 47,519 | 67,220 | 21,005 |
| - 유동자산 | 31,331 | 47,546 | 12,825 |
| 2. 부채총계 | 13,080 | 11,933 | 15,515 |
| - 유동부채 | 5,065 | 3,773 | 3,556 |
| 3. 자본총계 | 34,439 | 55,287 | 5,490 |
| 4. 부채비율 (%) | 38.0% | 21.6% | 282.6% |
| 5. 유동비율 (%) | 618.5% | 1,260.2% | 360.6% |
| 6. 영업손익 | 2,028 | 27 | 12,006 |
| 기타 손익 | (300) | (78) | 223 |
| 금융 손익 | (499) | (395) | (620) |
| 7. 당기순이익 | (23,210) | (10,699) | (5,107) |
| 8. 자본금 | 3 | 3 | 1 |
| 9. 영업활동 현금흐름 | (18,644) | (15,754) | (6,308) |
| 10. 투자활동 현금흐름 | (4,459) | (2,854) | (413) |
| 11. 재무활동 현금흐름 | (10) | 53,002 | (363) |
| 12. 현금 및 현금성자산 기말 잔고 | 23,484 | 46,597 | 12,204 |
| 자료 : | Immunomic Therapeutics, Inc 감사보고서(삼일회계법인) |
| 주1) Immunomic은 외부감사 의무대상이 아니며, 회사 자체적으로 회계법인에 의뢰해 2021년 기준 최근 3개년 외부감사를 받았습니다. | |
당사는 2020년 1월 Immunomic 주식을 최초로 취득하기 이전 Immunomic向 출자와 관련하여 주식 양수도가액의 적정성을 확인하기 위하여 지암회계법인으로부터 Immunomic Therapeutics Inc.의 주식가치에 대한 기업가치평가보고서(평가기준일: 2019년 12월 31일)를 수령하였습니다. 그럼에도 불구하고 투자자들께서는 지암회계법인이 주식가치평가보고서에서 제시하는 평가대상회사의 주식가치의 평가 결과는 미래예측에 따른 근본적인 한계가 존재하며, 평가대상회사의 절대적인 가치를 의미하는 것은 아니라는 점에 유의하시기 바랍니다. 지암회계법인은 평가대상회사의 주식가치를 평가하기 위해 현금흐름할인법을 적용하였으며, 평가시 적용한 주요 가정은 다음과 같습니다.
| [평가시 적용된 주요 가정-외부평가기관의평가의견서(2020.01.20)] |
|
| 출처: 지암회계법인 주식가치 평가보고서 |
| [주식가치평가 주요 내용 요약-외부평가기관의평가의견서(2020.01.20)] |
| 구분 | 내용 |
|---|---|
| 영업수익 추정 | (1) 매출의 경우 3개의 카테고리(1) Allergy Licenses and Other, 2) Allergy Royalties 및 3) Oncology)로 이를 구분, 각 세부항목별 매출 예상금액을 추정하여 이를 반영하였습니다. 한편, 이와 같은 연도별 추정내역은 회사에서 제시한 Data를 기준으로 현재까지의 진행상황 및 실현가능성 여부 등을 감안해 이를 반영하였습니다. (2) Astellas사와 기존에 계약하고 있는 License-out과 관련해 선수수익의 계정과목으로 장부상 부채로 계상하고 있으며, 매년 일정액을 수익으로 인식 중에 있으나 해당 매출액의 경우 이미 회사측에 대규모 현금으로 유입된 바 있으며, 실현시기만을 조정하는 것에 불과한 바, 이를 매출액 추정 시 별도로 반영치는 아니하였습니다. (3) 추정 대상기간은 회사가 제시한 연도별 예상 손익자료 상 제시되어 있는 2020년 ~ 2037년까지의 18년을 대상기간으로 하여 이를 평가하였습니다. |
| 영업비용 추정 | (1) Nature Royalty 비용의 경우 회사가 인식하는 Allergy 로열티 금액의 2%를 지급하는 계약을 의미하고 있으며, Annias Royalty 비용의 경우 Oncology 매출액 중 GBM1000 프로젝트와 관련해 매년 수입액의 8.5%를 지급하는 내용을 의미합니다. 이와 더불어 매년 종양학 관련 수입액 중 25%의 금액(2024년의 경우 40%)이 추가적으로 지출될 예정에 있는 것으로 예상되는 바, 이를 영업비용으로 반영하여 평가하였습니다. (2) Clinical Trials 비용의 경우 매년 유입되는 종양학 관련 연구의 진행에 필수적으로 수반되는 임상비용으로 수입액의 25%가 매년 비용으로 투입되는 것을 가정해 이를 평가하였습니다. |
| 판매비와관리비 추정 | (1) General & Administrative 관련 비용의 경우 향후 종양학 관련 매출액이 가장 큰 포션을 차지할 것인바, 해당 매출액의 5%가 매년 발생되는 것으로 가정해 이를 반영하였습니다. (2) R&D 관련 비용의 경우 회사가 매년 인식하는 총 매출액의 9%를 관련 비용의 발생으로 반영해 이를추정하였습니다. (3) 마케팅 관련 비용의 경우 매년 인식되는 종양학 관련 연구수입의 30%가 발생되는 것으로 이를 반영하였으며, 이는 관련 학회추진 관련 비용 및 신규 프로젝트 추진을 위한 Promotion 비용 등을 모두포함하는 것으로 이해할 수 있습니다. |
| 가중평균자본비용(WACC) 추정 | (1) 상기 가중평균자본비용 산출 시 자본구조(B/S)는 현재의 자본구조가 아니라 목표자본구조를 의미합니다. 그러나 현재 회사의 경우 사업구조 개편단계에 있으며, 현재 무부채 기업을 지향하고 있는 것으로 판단, 자본구조의 경우 타인자본이 없는 것으로 가정하여 이를 평가하였습니다. (2)적용 베타(β)의 경우 평가기준일 현재 회사와 유사한 업종을 영위하고 있는 미국 내 제약관련 상장회사 중 2개를 선택, 각 사의 시가총액을 기준으로 가중 평균한 후 HAMADA Model에 따라 산정된 무부채기업 베타계수(1.308)을 회사의 Proxy Beta로 평가하였습니다. (3) 상기가정을 근거로 한 자기자본비용은 14.80%로써 이의 산출내역은 다음과 같습니다. Ke = 1.92% + 7.19% * 1.308 + 3.48% |
| 출처: 지암회계법인 주식가치 평가보고서 |
본 평가인인 지암회계법인은 현금흐름할인법을 적용하여 Immunomic Therapeutics Inc.을 평가한 결과, 평가기준일 당시 1주당 주식 가치의 범위는 USD 4.18 ~ USD 6.75의 범위에 있을 것으로 추정되었습니다.
| (단위: 천USD) |
| 구분 | 금액 |
|---|---|
| A. 추정기간 FCF의 현재가치 | 53,869 |
| B. 영구현금흐름의 현재가치 | 38,031 |
| C. 현금성자산 | 11,742 |
| D. 총기업가치(A+B+C) | 103,642 |
| E. 타인자본가치 | 7,014 |
| F. 자기자본가치(D-E) | 96,628 |
| G. 발행주식수 | 18,061,356주 |
| H. 평가대상회사의 주당 주식가치(F/G) | USD 5.34 |
| 출처: | 지암회계법인 주식 가치 평가 보고서 |
가중평균자본비용(WACC)를 변수로 하여 평가대상회사의 주식가치의 민감도분석을 수행한 결과는 다음과 같습니다.
| (단위: USD) |
| 구분 | WACC | ||
|---|---|---|---|
| 13.80% | 14.80% | 15.80% | |
| 총기업가치 | 128,871 | 103,642 | 82,518 |
| 타인자본가치 | 7,014 | 7,014 | 7,014 |
| 자기자본가치 | 121,857 | 96,628 | 75,504 |
| 주당 주식가치* | 6.75 | 5.34 | 4.18 |
| 출처: | 지암회계법인 주식가치 평가 보고서 |
| * 주당주식가치 = 발행주식총수 18,061,356주 기준 |
|
투자자들께서는 당사의 2020년 01월 31일, 2020년 04월 23일, 2020년 12월 24일 Immunomic 지분 취득가격인 주당 5 USD가 미래 추정치에 근거한 가격임에 유의하시고, 해당 추정치는 전문가의 주관적 판단의 개입의 여지가 있음에 유의하시기 바랍니다.
금번 유상증자의 자금사용목적상에도 명시되어 있듯이, 당사는 금번 유상증자로 조달하는 자금 중 미화 약 1억 7천만 달러에 상당하는 금액을 Elevar에, 미화 약 4천만달러에 상당하는 금액을 Immunomic에 추가로 출자하여 다양한 적응증에 대한 신약의 임상실험비용 등 연구개발비용 및 신규 pipleline 확보 자금을 지속적으로 지원할 계획입니다.
다만, 당사의 지속적인 출자에도 불구하고 Elevar와 Immunomic는 바이오연구개발기업의 특성상 유의미한 매출이 발생하고 있지 않으며, 연구개발비 및 판관비로 인한 자금유출은 지속적으로 이루어지고 있습니다. 특히, Elevar는 2021년 말 재무제표를 기준으로 전액자본잠식 상태이며 업종의 특수성을 고려하였을 때, 유의미한 연구개발결과를 통한 신약개발 매출이 발생하지 않는다면추가적인 재무구조 악화 및 자본잠식은 지속될 가능성이 높다고 판단됩니다.
당사가 금번 유상증자를 통해 조달하는 자금 중 Elevar 증권취득 목적으로 약 2,297억원(미화 약 1억 7,635만 달러), Immunomic 증권취득 목적으로 약 530억원(미화 약 4,609만달러)를 출자할 계획이며, 해당 출자에 따라 종속회사의 재무현황 개선이 기대됩니다. 다만, 해당 출자는 종속회사의 임상시험 일정에 따라 증자 납입 직후부터 2025년까지 상대적으로 길게 분포되어 있으며, 해당 출자에도 불구하고 연구개발비 증가 및 수익 발생 지연이 지속되는 경우 추가적인 재무구조 악화의 우려가 있습니다. 투자자분들께서는 당사의 종속기업인 Elevar와 Immunomic의 악화된 재무구조에 대해 인식하시고, 양 사의 연구개발 활동 지속을 위해서는 당사의 지속적인 출자가 필요하다는 점에 유의하시기 바랍니다.
| [Elevar Therapeutics, Inc. 向 출자 계획] |
| 예정 시기 | 출자예정 대상회사 | 출자방법 | 출자예정금액 | 취득예정 주식수 |
출자 이후 | ||
|---|---|---|---|---|---|---|---|
| 외화(달러) | 원화 | 보유주식수(예정) | 지분율 | ||||
| 2022년 4분기 | Elevar Therapeutics, Inc. | 보통주 취득 | 24,145,676 | 31,449,742,990 | 4,800,333 | 72,379,776 | 100.00% |
| 2023년 2분기 | Elevar Therapeutics, Inc. | 보통주 취득 | 25,501,077 | 33,215,152,793 | 5,069,796 | 77,449,572 | 100.00% |
| 2023년 4분기 | Elevar Therapeutics, Inc. | 보통주 취득 | 30,256,200 | 39,408,700,500 | 6,015,149 | 83,464,721 | 100.00% |
| 2024년 2분기 | Elevar Therapeutics, Inc. | 보통주 취득 | 30,139,232 | 39,256,349,680 | 5,991,895 | 89,456,616 | 100.00% |
| 2024년 4분기 | Elevar Therapeutics, Inc. | 보통주 취득 | 25,277,198 | 32,923,550,395 | 5,025,287 | 94,481,903 | 100.00% |
| 2025년 2분기 | Elevar Therapeutics, Inc. | 보통주 취득 | 22,935,894 | 29,874,001,935 | 4,559,819 | 99,041,722 | 100.00% |
| 2025년 4분기 | Elevar Therapeutics, Inc. | 보통주 취득 | 18,097,890 | 23,572,501,725 | 3,597,990 | 102,639,712 | 100.00% |
| 주1) 상기 일정은 당사에서 계획중인 일정으로 규제기관의 정책변화, 시장 환경 변화, 내부 임상 개발 전략변경에 따라 변경될 수 있습니다. |
| [Immunomic Therapeutics, Inc. 向 출자 계획] |
| 예정 시기 | 출자예정 대상회사 | 출자방법 | 출자예정금액 | 취득예정 주식수 |
출자 이후 | ||
|---|---|---|---|---|---|---|---|
| 외화(달러) | 원화 | 보유주식수(예정) | 지분율 | ||||
| 2023년 1분기 | Immunomic Therapeutics, Inc. | 보통주 취득 | 22,939,538 | 29,878,748,245 | 4,587,907 | 15,873,553 | 57.76% |
| 2024년 1분기 | Immunomic Therapeutics, Inc. | 보통주 취득 | 11,342,612 | 14,773,752,130 | 2,268,522 | 18,142,075 | 66.01% |
| 2025년 1분기 | Immunomic Therapeutics, Inc. | 보통주 취득 | 6,408,829 | 8,347,499,773 | 1,281,765 | 19,423,840 | 70.68% |
| 주1) 상기 일정은 당사에서 계획중인 일정으로 규제기관의 정책변화, 시장 환경 변화, 내부 임상 개발 전략변경에 따라 변경될 수 있습니다. |
또한, 당사는 2015년부터 2021년까지 연결기준 영업손실 기록을 지속하고 있으며, 그 규모도 2019년 48,731백만원, 2020년 61,312백만원, 2021년 101,018백만원으로확대되어 왔습니다. 다만 2022년 반기의 경우, 매출액이 120억원 수준으로 전년 동기 대비 66.6% 증가한 등의 영향으로 2020년 1분기 영업손실 폭은 전년 동기 98.5억원 대비 감소한 62.3억원 수준을 나타냈습니다.
이러한 당사의 영업실적 추세로 보아, 자체적으로 영위하는 사업에서 시현하는 이익이나 현금흐름에 비하여 Elevar에 대한 출자 목적으로 지출되는 금액이 압도적으로 큰 편입니다. 이에 당사는 이러한 출자 자금을 대부분 사모 및 공모자금 조달을 통하여 충당해 왔습니다. 당사는 금번 유상증자를 통하여 Elevar의 리보세라닙 연구개발 및 신규 pipeline 도입에 대한 장기적 자금 지원책을 마련하고자 하며, 이를 통해 지속적 채무증권을 발행으로 인한 각종 금융비용의 절감, 자금의 적시 지원을 통한 Elevar의 연구개발활동 안정화를 도모할 계획입니다.
상기와 같은 자체 영업실적 대비 과도한 지출에도 불구하고, 당사의 상장된 보통주식시가총액은 2016년 말 4,719억원에서 2018년 말 3조 1,298억원, 2020년 말 4조 8,997억원, 2021년 말 3조 7,100억원 수준으로 급속하게 상승하였습니다. 2020년 08월12일 종가 기준 당사의 상장된 보통주 시가총액은 약 4조 8,471억원을 기록하였습니다.
한편, 당사의 주가가 급등락하는 경우는 영업실적 발표나 구명정ㆍ파이프 제조업의 업황과 관련된 이유라기보다는 Elevar의 임상 결과나 신약 허가 신청 진행 관련 소식, 또는 제약ㆍ바이오 업종 전반의 소식에 의한 것으로 파악됩니다.
당사의 주가 변동을 살펴보면, Elevar의 개별 이슈를 제외하고는 제약ㆍ바이오 업종의 다른 종목들과 일관된 움직임을 보이는 경향이 명확히 관찰됩니다. 특히, 최근 약 3년간 당사의 주가가 3거래일간 20% 수준 혹은 그 이상 급락했던 경우 주요 사유는 다음과 같습니다.
| [당사 주가 급락 CASE 및 그 사유] |
| 일자 | 종가 | 3거래일 낙폭 | 사유 |
|---|---|---|---|
| 2018-05-09 | 100,700 | -19.95% | 삼성바이오로직스 분식회계 이슈가 한창이던 시기로, 5월 8일 코스닥 제약 지수가 전일대비 3.97% 하락하며 셀트리온헬스케어(-6.67%), 신라젠(-12.75%), 에이치엘비(-16.98%), 메디톡스(-2.69%), 바이로메드(-2.85%), 셀트리온제약(-3.86%), 코오롱티슈진(-8.62%) 등 시가총액 상위 바이오 종목들 일제히 전일대비큰 폭 하락 -> 이후 10거래일만에 하락분 회복 (5/24 종가 \122,500) |
| 2018-11-12 | 79,100 | -18.87% | 여전히 불식되지 않고 있던 삼성바이오로직스 분식회계 의혹에 셀트리온의 어닝쇼크가 겹치며 삼성바이오로직스가 전일대비 22.42%하락하며 시가총액 5조원이 증발하였고, 그 외 셀트리온헬스케어(-10.30%), 에이치엘비(-10.32%) 신라젠(-9.14%) 코오롱티슈진(-8.25%) 바이로메드(-6.51%) 등 대형 바이오주 대부분이 전일대비 큰 폭 하락 |
| 2019-06-28 | 35,300 | -52.43% | 리보세라닙의 글로벌3상 결과 OS가 목표치에 미달했다는 소식이 시장에서 임상 3상 실패로 받아들여지며 급락 |
| 2019-07-30 | 23,900 | -23.03% | 6월 말 임상 결과가 시장에서 부정적으로 인식된 여파가 아직 가라앉지 않은 상황에서, 7월 30일 장중 유럽암학회(ESMO) 참가 논문 제출이 마감되었고, LSK Bio가 제출 기한 내에 논문을 제출하지 않았다는 소식에 급락 -> '최신임상연구(Late Breaking Abstract)' 해당으로 논문제출 추가 마감기한 허용에 대한 회사의 해명 및 이후 신약 가치 가능성 발표로 12거래일만에 하락분 회복(8/16 종가 32,650)하고 ESMO(유럽암학회)에서의 성공적 결과와 Pre NDA 진행 소식으로 10월까지 상승세 지속 (2019/10/24 종가 \185,000) |
| 2019-10-28 | 131,000 | -27.54% | Pre NDA 진행 소식 이후 FDA와의 Pre NDA 진행 결과에 대한 회사의 feedback이시장의 기대보다 지연되자 결과에 대한 우려로 급락 |
| 2020-09-24 | 99,700 | -17.12% | 코스닥 4.33% 하락(09/24) 및 미 FDA의 코로나백신 승인기준 강화 뉴스로 인해 전체 바이오 업체 큰폭으로 하락. |
| 2021-02-18 | 60,600 | -33.70% | 언론을 통해 증선위 허위공시 혐의 수사(리보세라닙 3상 시험결과 관련)에 대하여 신문기사가 나옴에 따라 급락 |
| (자료: 당사 작성) |
상기와 같이, 당사의 상장된 보통주 주가는 타 제약ㆍ바이오 업종의 주식과 유사한 움직임을 보이며 일반 제조업 대비 큰 변동성을 나타냅니다. 또한, 주가의 움직임은 정기보고서 등에 기재되는 재무수치 및 자체 영위 사업의 영업실적보다는 자회사 Elevar의 신약 연구개발 진행 관련 소식이나 신약 연구개발업 전반의 호재 및 악재성 소식에 보다 더 큰 영향을 받을 가능성이 높습니다. 금번 유상증자의 청약에 참여하여 당사의 상장된 보통주에 투자할 의향이 있는 투자자께서는 이 점에 특히 유의하시어 투자판단을 하시기 바랍니다.
|
다. 성장성 및 수익성 관련 위험 |
| [손익계산서 주요계정 및 수익성 추이] |
| (단위 : 백만원) |
|
구 분 |
2022년 반기 | 2021년 반기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|---|
|
매출액 |
123,305 | 15,957 | 69,826 | 56,177 | 38,421 |
| 매출액증가율 | 672.7% | -27.5% | 24.3% | 46.2% | 6.2% |
|
매출원가 |
73,343 | 15,439 | 48,759 | 45,869 | 34,484 |
| 매출원가율 | 59.5% | 96.8% | 69.8% | 81.7% | 89.8% |
| 매출총이익 | 49,961 | 518 | 21,067 | 10,308 | 3,937 |
| 매출총이익률 | 40.5% | 3.2% | 30.2% | 18.3% | 10.2% |
| 판매관리비 | 70,057 | 40,275 | 122,086 | 71,620 | 52,668 |
| 판매비와관리비 비율 | 56.8% | 252.4% | 174.8% | 127.5% | 137.1% |
|
영업이익(손실) |
(20,096) | (39,757) | (101,018) | (61,312) | (48,731) |
| 영업이익률 | -16.3% | -249.2% | -144.7% | -109.1% | -126.8% |
| 기타수익 | 521 | 3,086 | 5,948 | 882 | 571 |
| 기타비용 | 216 | 2,293 | 2,858 | 30,547 | 7,506 |
| 금융수익 | 9,738 | 1,026 | 7,155 | 20,565 | 18,970 |
| 금융비용 | 4,800 | 13,179 | 11,320 | 12,566 | 24,950 |
| 당기순손익 | (19,100) | (57,078) | (111,607) | (88,716) | (59,660) |
| 당기순이익률 | -15.5% | -357.7% | -159.8% | -157.9% | -155.3% |
| [당사 사업부문별 영업실적 추이] | |
| (연결기준) | (단위: 천원) |
| 구 분 | 복합소재사업 부문 | ||||
|---|---|---|---|---|---|
| 2022년 반기 | 2021년 반기 | 2021년 | 2020년 | 2019년 | |
| 매출액 | 8,966 | 11,858 | 25,773 | 42,316 | 28,983 |
| 전제 매출 대비 | 7.27% | 74.31% | 36.91% | 75.33% | 75.44% |
| 영업이익(손실) | (1,825) | (3,105) | (6,651) | (1,869) | (5,374) |
| 당기순이익(손실) | (1,299) | (3,568) | (7,313) | (2,162) | (31,663) |
| 유동자산 | 8,563 | 12,037 | 7,976 | 15,535 | 14,142 |
| 비유동자산 | 9,381 | 9,827 | 9,585 | 9,152 | 9,274 |
| 자산 계 | 17,943 | 21,864 | 17,560 | 24,687 | 23,416 |
| 유동부채 | 4,159 | 5,992 | 2,968 | 5,264 | 2,523 |
| 비유동부채 | 459 | 522 | 459 | 532 | 909 |
| 부채 계 | 4,618 | 6,514 | 3,427 | 5,796 | 3,432 |
| 구 분 | 바이오ㆍ의료기기 사업 부문 | ||||
|---|---|---|---|---|---|
| 2022년 반기 | 2021년 반기 | 2021년 | 2020년 | 2019년 | |
| 매출액 | 114,338 | 4,099 | 44,053 | 13,861 | 9,438 |
| 전제 매출 대비 | 92.73% | 25.69% | 63.09% | 24.67% | 24.56% |
| 영업이익(손실) | 21,921 | (36,652) | (94,367) | (59,443) | (43,357) |
| 당기순이익(손실) | (17,801) | (53,510) | (104,294) | (86,554) | (27,998) |
| 유동자산 | 154,573 | 203,919 | 180,166 | 236,038 | 55,537 |
| 비유동자산 | 640,627 | 442,939 | 545,966 | 445,753 | 283,659 |
| 자산 계 | 795,200 | 646,858 | 726,132 | 681,790 | 339,196 |
| 유동부채 | 119,141 | 86,272 | 118,851 | 92,763 | 65,176 |
| 비유동부채 | 154,067 | 53,046 | 109,229 | 50,489 | 104,762 |
| 부채 계 | 273,209 | 139,317 | 228,080 | 143,252 | 169,938 |
2020년 이전까지 당사 연결기준 매출액의 대부분을 차지하는 것은 구명정 및 파이프를 제조ㆍ판매하는 복합소재사업 부문으로, 당사가 직접 영위하는 자체 사업에 해당하며, 복합소재사업부문의 2019년 연간 매출 실적은 약 28,983백만원으로 동 기간 연결기준 전체 매출액의 75.4%를 차지하며, 2020년 매출 실적은 약 42,316백만원으로 총 매출액의 75.3%를 차지하였습니다.
이후 2021년 중 당사가 ㈜에프에이를 인수하면서 바이오ㆍ헬스케어 사업 부문의 매출비중이 높아지게되었고, 2021년 바이오ㆍ헬스케어 사업 부문의 매출 실적은 44,053백만원으로 총 매출액의 63.1%, 2022년 반기 매출 실적은 114,338백만원으로 총 매출액의 92.7%를 차지합니다.
당사의 헬스케어사업부문(舊 ㈜에프에이)는 검체 채취용키트, 배지 및 의약외품 등을제조ㆍ판매하며, 당 반기 중 매각한 ㈜화진메디칼 및 ㈜화진메디스는 주사기 등의 의료기기를 제조ㆍ판매하고, Elevar 및 Immunomic은 당사의 미국 자회사로, 항암제 신약 등의 연구개발 사업을 영위하고 있습니다. 바이오ㆍ헬스케어 사업부문에서 실제로 연결기준 매출 실적이 발생한 곳은 헬스케어사업부문, 화진메디칼㈜ 및 화진메디스㈜가 해당하며, Elevar 및 Immunomic은 증권신고서 제출일 현재까지 유의미한 매출이나 이익을 시현하지 못한 상황입니다. 또한, 당사는 2022년 4월 29일 지분 100%를 보유했던 종속기업인 ㈜화진메디칼, ㈜화진메디스의 지분 전부를 관계기업인 에이치엘비테라퓨틱스㈜에 매각하였습니다.
당사 복합소재사업부문에서 생산 및 판매하고 있는 주요 제품은 선박에 탑재되는 구명정과 구명정을 진수하는 장치, 기타 특수목적선박 및 선박과 해양플랜트 등에 사용되는 파이프 제품입니다. 이러한 주요 제품을 고려하였을 때 한국 시장 내에서 당사의 직접적인 peer가 되는 주권상장기업은 찾아보기 어렵습니다. 구명정 제조에 있어서는 당사가 국내 유일 제조업체이며, 당사가 생산하는 GRE/GRP 파이프 역시 국내에는 경쟁업체가 없습니다. 다만 전방산업인 조선업, 해양플랜트산업 및 해운업 업황의 영향을 받아 실적 변동성이 존재합니다.
복합소재사업부문 2019년 매출은 28,983백만원으로 전년 대비 증가했으나 원가율 상승으로 인하여 5,374백만원의 영업손실과 보유하고있던 에이치엘비생명과학 CB 평가손실 등으로 인한 31,663백만원의 순손실을 기록하며 실적이 전체적으로 전년 대비 악화된 모습을 보였습니다. 2020년 매출액은 공급망 정체로 인한 조선사업의 수주 증가로 42,316만원을 기록했으며 이는 전년 대비 46.0% 증가한 수치입니다. 다만, 중국 업체와의 가격 경쟁 심화, 구명정 탑재용 hook 등 고마진 제품 매출 모멘텀 하락 등의 영향으로 1,86백만원의 영업손실을 기록했습니다.
2021년 매출액은 선박 및 파이프부분 매출 부진으로 인해 25,773백만원을 기록했으며, 영업손실은 채권대손설정 723백만원 및 일시적인 퇴직급여 상승으로 인해 6,651백만원을 기록했습니다. 2022년 반기 매출액 또한 8,966백만원으로 전년 동기 11,858백만원 대비 24.4% 감소하였으며 영업손실은 1,825백만원으로 전년 동기 대비 1,279백만원 영업손실폭이 축소되었습니다. 분기순손실 역시 전년 동기 대비 2,268백만원 줄어든 모습을 보였습니다.
바이오ㆍ의료기기 사업부문의 경우 2019년 연간 동 사업부문의 매출액은 9,438백만원으로 43,357백만원의 영업손실과 27,998백만원의 순손실을 기록하였습니다. 2020년 매출 실적은 13,861백만원으로 성장하였으나, 영업손실 및 순손실 규모는 각각 59,443백만원과 86,554백만원으로 확대되었습니다. 2021년 매출 실적은 44,053백만원으로 전년대비 217.8% 증가하였고, 이는 ㈜프에이 인수에 따른 매출규모 상승에 기인합니다. 다만, 영업손실 규모는 94,367백만원, 순손실 규모는 104,294백만원수준으로 영업손실 규모 및 순손실의 규모는 2020년 대비 증가하였습니다.
2022년 반기 연결기준 당사 바이오ㆍ의료기기 사업부문 매출실적은 114,338백만원,으로 전년 동기 4,099백만원 대비 2,689.7% 증가하였으며, 영업이익은 21,921백만원을 기록했습니다. 이는 당반기 중 코로나 대유행에 따라 헬스케어사업부의 매출이 대폭 증가한점에 기인합니다. 다만, 당기순손실은 17,801백만원을 기록하였는데 이는 Elevar 및 Immunomic에 투입되는 글로벌 임상 진행 경상연구개발비(임상비용 등)에 상당부분 기인하는 것으로 판단됩니다.
| [영업비용 세부 내역] |
| (단위: 백만원) |
| 구분 | 2022년 반기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
| 급 여 | 24,299 | 26,818 | 15,295 | 7,658 |
| 퇴직급여 | 263 | 1,676 | 667 | 629 |
| 복리후생비 | 2,117 | 1,550 | 1,102 | 576 |
| 여비교통비 | 719 | 498 | 329 | 887 |
| 접대비 | 210 | 340 | 287 | 187 |
| 통신비 | 190 | 243 | 96 | 57 |
| 전력비 | 23 | 64 | 139 | 122 |
| 세금과공과금 | 1,468 | 1,555 | 875 | 183 |
| 감가상각비 | 1,432 | 2,550 | 1,947 | 851 |
| 지급임차료 | 302 | 473 | 138 | 236 |
| 보험료 | 263 | 1,472 | 891 | 549 |
| 차량유지비 | 59 | 120 | 80 | 49 |
| 경상연구개발비 | 22,603 | 48,419 | 22,594 | 33,835 |
| 소모품비 | 574 | 464 | 206 | 101 |
| 지급수수료 | 7,177 | 18,167 | 11,727 | 4,890 |
| 광고선전비 | 141 | 281 | 307 | 0 |
| 건물관리비 | 268 | 505 | 267 | 27 |
| 대손상각비 | 23 | 683 | (0) | 3 |
| 무형자산상각비 | 5,975 | 8,257 | 7,382 | 135 |
| 주식보상비 | 1,514 | 7,179 | 6,600 | 741 |
| 판매보증비(환입) | (21) | 78 | (66) | 37 |
| 기타 | 458 | 695 | 758 | 914 |
| 합 계 | 70,057 | 122,086 | 71,620 | 52,668 |
당사는 주식관련사채 발행 및 유상증자를 통하여 연구개발에 필요한 자금을 확보하여 주요 파이프라인의 임상진행 등 연구개발 활동을 가속화했습니다. 그 결과, 연구개발비용은 2019년 22,241백만원에서 2020년 33,835백만원, 2021년 22,594백만원, 2022년 반기 22,603백만원으로 급격히 상승했습니다. 또한, 당사 종업원 급여는 2019년 7,658백만원에서 2020년 15,295백만원, 2021년 26,818백만원으로 증가했습니다. 이는 최근 3년간 Immunomic, ㈜에프에이(現 헬스케어사업부) 등 연결대상 기업들이 증가하면서 연결기준 임직원수가 증가한점에 기인합니다.
2022년 반기에는 리보세라닙 중국 관련 권리 로열티 상각, ITI 측 자산 일부 상각으로 인해 무형자산 상각비가 5,975백만원으로 크게 상승했습니다. 당사의 무형자산상각과 관련된 위험은 ""III. 투자위험요소 - 2. 회사위험 - 마."를 참고 해주시기 바랍니다.
한편, 당사는 보유하고있는 공정가치측정 금융자산의 평가 및 처분에 따른 손익에 따라 금융손익이 발생하고, 관계기업들의 실적에 따라 지분법 손익을 인식하기 때문에 최근 3년간 당기순손실이 영업손실보다 손실폭이 더욱 증가하여 수익성 지표(영업이익률, 당기순이익률 등)가 악화되었습니다. 당사의 당기순이익 추이를 살펴보면, 2019년 -59,660백만원을 기록한 이후 2020년 -88,716백만원, 2021년 -111,607백만원의 당기순손실이 지속적으로 발생하였고, 이후 2022년 반기에는 -19,100백만원의당기순손실을 기록했습니다.
당사는 2020년에 61,312백만원의 영업손실을 기록한데 이어, 옵티머스 자산운용에 서 운영하는 펀드에 투자한 300억원 전액을 대손상각 처리하면서 기타비용이 30,547백만원 발생하여 공정가치측정금융자산 평가이익에 따른 8,000백만원의 금융수익에도 불구하고 당기순손실 88,716백만원을 기록했습니다. 대손상각비의 상세한 발생경위, 현황 및 향후계획에 "III. 투자위험요소 - 2. 사업위험 - 바."를 참고해주시기 바랍니다.
2021년에는 연결기준 당기순손실이 111,607백만원으로 당해 영업손실 101,018백만원이 발생했고, 에이치엘비제약㈜ 평가손실 6,280백만원 및 이자비용에 따른 금융비용 11,320백만원 및 지분법손익 8,356백만원 등으로 인해 당기순손실이 전년대비 큰폭으로 확대되었습니다. 2022년 반기에는 연결기준 영업손실 20,096백만원이 발생했고, 이자비용 등에 따른 금융비용 4,800백만원에도 불구하고 에이치엘비제약㈜ 평가이익 1,546백만원 및 이자 외화환산이익 1,020백만원에 따른 금융수익 9,738백만원 및 지분법손익 2,691백만원 등으로 인해 당기순손실은 19,100백만원으로 전년동기 대비 큰폭으로 감소하였습니다.
당기순이익의 상세 분석은 아래 표와 같습니다.
| [당기순이익 현황] |
| (단위: 백만원, %) |
|
구분 |
2022년 반기 | 2021년 반기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|---|
|
영업이익(손실) |
(20,096) | (39,757) | (101,018) | (61,312) | (48,731) |
|
영업이익률 |
-16.3% | -249.2% | -144.7% | -109.1% | -126.8% |
| 기타손익 | 305 | 794 | 3,090 | (29,665) | (6,935) |
|
기타수익 |
521 | 3,086 | 5,948 | 882 | 571 |
|
기타비용 |
216 | 2,293 | 2,858 | 30,547 | 7,506 |
| 금융손익 | 4,938 | (12,153) | (4,165) | 8,000 | (5,979) |
|
금융수익 |
9,738 | 1,026 | 7,155 | 20,565 | 18,970 |
|
금융비용 |
4,800 | 13,179 | 11,320 | 12,566 | 24,950 |
| 관계기업투자주식관련 손익 | 2,691 | (5,961) | (8,356) | (10,225) | 1,882 |
|
당기순이익(손실) |
(19,100) | (57,078) | (111,607) | (88,716) | (59,660) |
|
당기순이익률 |
-15.5% | -357.7% | -159.8% | -157.9% | -155.3% |
| 주1) 기타손익 = 기타손익 - 기타비용 주2) 금융손익 = 금융수익 - 금융비용 |
당사는 영업실적 부진 및 바이오사업 확장에 따른 비용 증가로 인해 지속적인 영업손실을 기록하고 있으며, 당사의 매출회복 및 적자구조 탈피를 위해 전사적으로 노력하고 있습니다. 특히, 헬스케어사업부 인수를 통한 수익성 향상 및 리보세라닙 원천기술 인수를 통한 로열티 매출 발생 등 재무구조를 개선하고 수익성을 확보하고자 노력하고 있으며, 당사가 권리를 보유한 리보세라닙, 아필리아 등 신약물질의 임상 통과 및 매출 실현을 목표로 하고 있습니다. 그러나 이와 같은 노력에도 불구하고 경쟁 심화로 인한 헬스케어 사업부의 매출 감소, 바이오 사업 임상시험 지연 및 비용 증가 등으로 인해 당사의 수익은 더욱 악화될 수 있습니다. 투자자 여러분께서는 이 점 각별히 유의하시기 바랍니다.
| 라. 부채성 조달 확대 및 재무안정성 관련 위험 당사는 지속적인 영업적자와 이에 따른 당기순손실이 지속적으로 발생했으나, 주식관련사채의 전환(행사) 및 유상증자 진행으로 자본총계가 크게 증가하여 최근 3년간 부채비율은 2019년 91.6%, 2021년 26.7%, 2022년 반기 27.9%를 기록중입니다. 당사 연구개발 등에 지속적으로 자금을 투입할 예정으로 당사의 사업계획에 차질이 발생하여 흑자전환 시기가 지연될 경우 재무안정성이 악화될 가능성이 있습니다. 최근 타법인 인수와 운영자금 목적으로 주식관련사채를 발행하였고, 이에 당사의 미상환 사채 잔액은 증권신고서 제출일 전일 현재 2021년 말 대비 증가한 모습을 나타내고 있습니다. 그러나, 상대적으로 높은 변동성을 보이는 당사의 주가 흐름을 고려했을 때, 향후 당사의 주가 흐름이 부진할 경우 현재 미상환 상태로 존재하는 채무증권에 대하여 투자자가 전환권 및 신주인수권을 행사하지 않고 조기상환청구권(Put Option)을 행사하거나 만기 상환을 요구할 가능성을 배제할 수 없습니다. 이 경우 원활한 차환이 이루어지지 않는다면 당사의 현금흐름 및 재무상태에 부정적인 영향을 끼칠 수 있는 바, 투자자께서는 당사의 차입금 현황 및 재무상태에 유의하여 투자 결정에 임하시기 바랍니다. |
당사의 최근 4년간의 재무안정성 지표 추이는 다음과 같습니다.
| [재무안정성 지표 추이] |
| (단위 : 백만원) |
| 구분 | 2022년 반기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
| 자산총계 | 668,722 | 743,692 | 706,477 | 362,612 |
| 유동자산 | 215,956 | 188,142 | 251,573 | 69,679 |
| 비유동자산 | 452,766 | 555,550 | 454,905 | 292,933 |
| 부채총계 | 145,832 | 231,507 | 149,048 | 173,370 |
| 유동부채 | 92,264 | 121,819 | 98,027 | 67,699 |
| 비유동부채 | 53,568 | 109,688 | 51,021 | 105,671 |
| 자본총계 | 522,890 | 512,185 | 557,429 | 189,242 |
| 유동비율 | 234.1% | 154.4% | 256.6% | 102.9% |
| 부채비율 | 27.9% | 45.2% | 26.7% | 91.6% |
당사는 지속적인 영업적자와 이에 따른 당기순손실이 지속적으로 발생했으나, 주식관련사채의 전환(행사) 및 유상증자 진행으로 자본총계가 크게 증가하여 최근 3년간 부채비율은 2019년 91.6%, 2020년 26.7%, 2021년 45.2% 2022년 반기 27.9%를 기록중입니다. 다만, "III. 투자위험요소 - 2. 회사위험 - 나."에서 제시된 바와 같이 당사는 연구개발 등에 지속적으로 자금을 투입할 예정으로 당사의 사업계획에 차질이 발생하여 흑자전환 시기가 지연될 경우 재무안정성이 악화될 가능성이 있습니다. 당사는 금번 유상증자를 통해 자금을 조달하여 임상시험, 연구개발비 및 헬스케어사업부분 공장 설립 등 대규모 자금을 투자할 계획을 가지고 있습니다. 이에 따라 현금흐름 및 유동성에 대하여 지속적으로 모니터링하면서 유동성 이슈가 발생하지 않도록 대응할 예정입니다.
2020년 기준 전기말 대비 당사의 연결기준 부채 규모 감소는 총차입금 규모가 약 42,014백만원 감소한 것에 가장 크게 기인합니다. 2019년 말 기준 당사의 연결기준 총 차입금 규모는 단기차입금 약 12,096백만원과 장기차입금 약 74,524백만원으로 구성되어 86,620백만원 수준이었으나, 2020년 중 주가 상승으로 인해 전환사채의 대규모 전환청구가 이뤄지면서 2020년 말 총차입금 규모는 총차입금은 약 44,606백만원으로 단기차입금 43,992백만원과 장기차입금 614백만원을 기록했습니다.
2022년 반기말 연결기준 당사의 총 차입금은 약 110,054백만원으로 전기말 대비 약 41,459백만원 증가하였으며, 단기차입금의 증가는 타법인 인수 및 운영자금 목적을 위한 주식관련사채의 발행에 기인합니다. 차입금은 단기 차입금 25,884백만원과 장기차입금 84,169백만원으로 구성되어 있으며, 당사의 2022년 반기말 차입금 상세 현황은 아래와 같습니다.
| [차입금 현황] | |
| (연결기준) | (단위: 백만원) |
| 차입처 | 이자율(%)(*1) | 2022년 반기말 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|---|
| 단기차입금: | |||||
| 우리은행 | - | - | 3,722 | 4,493 | 4,726 |
| 하나은행 | - | - | 6,000 | - | - |
| 산업은행 | - | - | - | 1,000 | 1,000 |
| 중소기업은행 | - | - | - | - | 4,000 |
| Bank of America | - | - | - | 668 | - |
| 전환사채 | - | 2,135 | 11,495 | 37,832 | 2,370 |
| 신주인수권부사채 | - | 23,749 | - | - | - |
| 소 계 | 25,884 | 21,217 | 43,992 | 12,096 | |
| 장기차입금: | |||||
| 중소기업은행(*2) | 1.5 | 320 | 320 | 320 | 3,320 |
| 우리은행 | - | - | 146 | 294 | 459 |
| 전환사채 | - | 19,579 | - | - | 70,746 |
| 신주인수권부사채 | - | 64,271 | 46,912 | - | - |
| 소 계 | 84,169 | 47,378 | 614 | 74,524 | |
| 합 계 | 110,054 | 68,595 | 44,606 | 86,620 | |
| (*1) 상기이자율은 2022년 반기말 기준 이자율입니다. (*2) 상기의 차입금과 관련하여 토지, 일부 건물 및 기계장치를 담보로 제공하고 있습니다. |
2021년 중 당사 연결기준 차입금 증가는 당사가 발행한 전환사채의 미상환 잔액의 영향으로 판단됩니다. 당사는 2021년중 ㈜에프에이의 인수를 위해 전자등록총액 57,000백만원의 제34회 사모 신주인수권부사채를 발행했으며, 단기 자금 차입을 목적으로 하나은행에서 6,000백만원을 차입했습니다. 2022년 반기중에는 ㈜노터스 인수 및 운영자금 목적으로 제36회 사모 전환사채 및 제35회, 제37회 사모 신주인수권부사채를 발행하면서 미상환주식관련사채가 증가했습니다. 당사가 발행한 사채 및 미상환 잔액의 내역은 아래와 같습니다.
| [미상환 주식관련 사채 발행현황] |
| (단위 : 백만원, 주) |
| 종 류 | 발행일 | 만기일 | 전자등록 총액 |
표면 이자율 |
만기 이자율 |
전환(행사)청구 가능기간 |
조기상환 청구권(Put option) |
전환(행사)가액 | 잔액 | 전환(행사)가능 주식수 |
|---|---|---|---|---|---|---|---|---|---|---|
| 33회차 사모 전환사채 |
19.12.18 |
22.12.18 |
40,000 |
0.0% | 1.0% | 20.12.18~22.11.18 |
21.08.18~22.11.18 (매 3개월) |
33,757 |
1,400 | 41,472 |
| 34회차 사모 비분리형 신주인수권부사채 |
21.10.20 |
26.10.20 |
57,000 |
0.0% | 1.0% | 22.10.20~26.09.20 |
23.10.20~26.07.20 (매 3개월) |
35,884 |
57,000 | 1,588,451 |
| 35회차 사모 비분리형 신주인수권부사채 |
22.03.30 |
25.03.30 |
25,200 |
0.0% | 2.0% | 23.03.30~25.02.30 |
23.03.30~24.12.30 (매 3개월) |
30,811 |
21,000 | 681,574 |
| 36회차 사모 전환사채 |
22.06.02 |
25.06.02 |
23,000 |
1.0% | 3.0% | 23.06.02~25.05.02 |
23.12.02~25.03.02 (매 3개월) |
48,605 |
23,000 | 473,202 |
| 37회차 사모 비분리형 신주인수권부사채 |
22.06.02 |
25.06.02 |
17,000 |
1.0% | 3.0% | 23.06.02~25.05.02 |
23.12.02~25.03.02 (매 3개월) |
48,605 |
17,000 | 349,758 |
| 계 | 162,200 | - | - | - | - | - | 119,400 | 3,134,457 | ||
당사는 경영에 필요한 자금 조달을 위하여 상기와 같이 다수 회차에 걸쳐 주식연계채권을 투자자들에게 사모 형태로 발행하였습니다. 각 사모방식 자금조달별 자금사용내역은 "III. 투자위험요소 - 2. 사업위험 - 바."를 참고해주시기 바랍니다.
최근 타법인 인수와 운영자금 목적으로 주식관련사채를 발행하였고, 이에 당사의 미상환 사채 잔액은 증권신고서 제출일 전일 현재 2021년 말 대비 증가한 모습을 나타내고 있습니다. 그러나, 상대적으로 높은 변동성을 보이는 당사의 주가 흐름을 고려했을 때, 향후 당사의 주가 흐름이 부진할 경우 현재 미상환 상태로 존재하는 채무증권에 대하여 투자자가 전환권 및 신주인수권을 행사하지 않고 조기상환청구권(Put Option)을 행사하거나 만기 상환을 요구할 가능성을 배제할 수 없습니다. 이 경우 원활한 차환이 이루어지지 않는다면 당사의 현금흐름 및 재무상태에 부정적인 영향을 끼칠 수 있는 바, 투자자께서는 당사의 차입금 현황 및 재무상태에 유의하여 투자 결정에 임하시기 바랍니다.
금번 유상증자가 완료 된 이후 자본확충 효과로 재무제표가 다소 개선될 수는 있으나, 당사 업종 특성상 지속적으로 많은 연구개발비가 발생하여 손실이 지속될 가능성이높으며 재차 재무안정성 지표가 악화될 가능성이 있습니다. 이는 추후 또 다른 유상증자나 주식관련사채의 발행을 통하여 개선할 수 밖에 없는 상황이 도래할 수 있습니다. 현재의 수익상황 및 당기순손실이 지속된다면 재무안정성 지표가 악화될 위험이 있으므로, 투자자께서는 이점 유의하시기 바랍니다.
| 마. 무형자산 손상 관련 위험 당사는 자산에서 발생하는 미래경제적효익이 기업에 유입될 가능성이 높고 자산의 원가를 신뢰성 있게 측정할 수 있는 경우에 무형자산으로 인식하고 있으며, 최초 인식 후에 무형자산은 원가에서 상각누계액과 손상차손누계액을 차감한 금액을 장부금액으로 하고있습니다. 특허권의 구성내역은 리보세라닙 글로벌 특허권 238억원, 리보세라닙 중국 특허권 217억으로 장부에 인식되어 있습니다. 상각은 해당 특허권으로 인하여 매출액 발생시 인식하고 있습니다. 고객관계는 당사가 당기초 ㈜에프에이와의 사업결합 시 취득 한 영업권 중 구분한 내용이며, 면봉 및 수송배지 관련 고객관계는 237억, 알콜스왑 및 기타관련 고객관계는 76억으로 장부에 인식되어 있습니다. 해당 자산의 상각은 각각 내용연수를 7년과 8년으로 하여 상각 진행 중입니다. 2022년 반기 연결 기준 당사의 무형자산 장부금액은 356,790백만원이며, 바이오 사업부문에서의 영업실적 악화로 인해 장부가액이 회수가액을 초과할 경우 전액 또는 일부에 대한 손상에 따른 감액이 발생할 수 있습니다. 또한, 한정된 내용연수를 지니는 무형자산에 대한 내용연수 기준 변경 등으로 인해 대규모 무형자산상각비가 발생하여, 당사의 손익에 부정적인 영향을 끼칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
당사는 자산에서 발생하는 미래경제적효익이 기업에 유입될 가능성이 높고 자산의 원가를 신뢰성 있게 측정할 수 있는 경우에 무형자산으로 인식하고 있으며, 최초 인식 후에 무형자산은 원가에서 상각누계액과 손상차손누계액을 차감한 금액을 장부금액으로 하고 있습니다.
개별취득한 무형자산의 경우 원가는 구입가격(매입할인과 리베이트를 차감하고 수입관세와 환급받을 수 없는 제세금을 포함)과 자산을 의도한 목적에 사용할 수 있도록 준비하는 데 직접 관련되는 원가로 구성되고 있습니다.
영업권의 경우 사업결합과 관련하여 이전대가, 피취득자에 대한 비지배지분의 금액 및 단계적으로 이루어지는 사업결합의 경우 연결실체가 이전에 보유하고 있던 피취득자에 대한 지분의 취득일의 공정가치의 합계금액이 취득일의 식별가능한 취득 자산과 인수 부채의 순액을 초과하는 경우 그 초과금액을 영업권으로 인식하고 있습니다.
사업결합으로 인한 취득의 경우 사업결합으로 취득하는 영업권과 분리하여 인식하는무형자산의 취득원가는 취득일의 공정가치로 측정하고 있습니다.
동일지배하 사업결합의 경우 연결실체의 연결재무제표를 구성하는 피합병법인의 자산 및 부채를 승계하여 장부금액으로 인식하고 있습니다.
당사는 내용연수가 유한한 무형자산의 경우 상각대상금액은 자산이 사용가능한 때부터 내용연수동안 정액법으로 배분하고 있습니다. 상각대상금액은 잔존가치를 차감하여 결정하고 있으며, 잔존가치는 내용연수 종료 시점에 제 3자가 자산을 구입하기로한 약정이 있거나, 무형자산의 활성시장이 있어 잔존가치를 그 활성시장에 기초하여 결정할 수 있고 그러한 활성시장이 내용연수 종료 시점에 존재할 가능성이 높은 경우를 제외하고는 영(0)으로 하고 있습니다. 내용연수가 유한한 무형자산의 상각기간과 상각방법은 매 보고기간말에 재검토하고 있으며 이를 변경하는 것이 적절하다고 판단되는 경우 회계추정의 변경으로 회계처리하고 있습니다. 내용연수가 비한정인 무형자산은 상각하지 아니하며, 매 보고기간말 혹은 손상을 시사하는 징후가 있을 때 회수가능액과 장부금액을 비교하여 손상검사를 수행하고 있습니다. 무형자산의 내용연수가 비한정이라는 평가를 계속하여 정당화하는지를 매 보고기간말에 재검토하여 적절하지 않은 경우 회계추정의 변경으로 처리하고 있습니다.
무형자산 항목별 내용연수 및 상각방법은 다음과 같습니다.
| [무형자산 항목별 추정 내용연수] |
| 구 분 | 내 용 연 수 | 상각방법 |
|---|---|---|
| 특허권 | 3년, 10년 | 정액법 |
| 소프트웨어 | 5년 | 정액법 |
| 고객관계 | 7, 8년 | 정액법 |
| 상표권 | 10년 | 정액법 |
| 의장권 | 10년 | 정액법 |
| 회원권 | 비한정 내용연수 | - |
| 영업권 | 비한정 내용연수 | - |
2022년 반기 연결 기준, 당사의 무형자산 내역은 다음과 같습니다.
| [무형자산 현황] |
| (단위: 백만원) |
| 구 분 | 2022.01.01 | 취 득 | 감가상각비 | 환율변동효과 | 기타 | 2022.06.30 |
|---|---|---|---|---|---|---|
| 산업재산권 | 38,726 | 480 | (3,779) | 612 | 2 | 36,040 |
| 영업권 | 62,346 | 551 | - | 3,057 | - | 65,954 |
| 기타의 무형자산 | 205,081 | - | - | 18,578 | - | 223,659 |
| 고객관계 | 30,673 | - | (2,175) | - | - | 28,498 |
| 회원권 | 2,384 | 153 | - | - | - | 2,537 |
| 소프트웨어 | 137 | 1 | (21) | - | (15) | 102 |
| 개발비 | 190 | 21 | - | - | (211) | - |
| 합 계 | 339,536 | 1,206 | (5,975) | 22,247 | (224) | 356,790 |
당사는 2022년 반기 연결 기준, 장부가액으로 기타의 무형자산 223,659백만원, 영업권 65,954백만원, 고객관계 28,498백만원 등을 보유하고 있습니다.
당사가 보유중인 특허권의 구성내역은 리보세라닙 글로벌 특허권 238억원, 리보세라닙 중국 특허권 217억으로 장부에 인식되어 있습니다. 상각은 해당 특허권으로 인하여 매출액 발생시 인식하고 있습니다. 현재, 보유 중인 특허권 중 리보세라닙 중국 특허권에 대해서만 상각을 진행하고 있으며 내용연수는 3년입니다. 추후, 글로벌 특허권은 매출액 발생시 상각 진행 예정입니다.
고객관계는 당사가 당기초 ㈜에프에이와의 사업결합 시 취득 한 영업권 중 구분한 내용이며, 면봉 및 수송배지 관련 고객관계는 237억, 알콜스왑 및 기타 관련 고객관계는 76억으로 장부에 인식되어 있습니다. 해당 자산의 상각은 각각 내용연수를 7년과 8년으로 하여 상각 진행 중입니다.
기타의 무형자산은 Immunomic Therapeutics, Inc.와의 사업결합 시 인식한 진행중인 연구개발(이하 기술력) 769억과 Elevar Therapeutics, Inc.와의 사업결합 시 인식한 기술력 1,209억, 그리고 항암제 "Apealea"에 대한 전용 특허 실시권 258억으로 구성되어 있습니다.
상기한 바와 같이, 당사는 영업권, 산업재산권 등의 무형자산을 계상하고 있으며, 당사 기준에 따라 매년 상각 및 손상검사를 수행하고 있습니다. 2022년 반기 연결 기준당사의 무형자산 장부금액은 356,790백만원이며, 바이오 사업부문에서의 영업실적 악화로 인해 장부가액이 회수가액을 초과할 경우 전액 또는 일부에 대한 손상에 따른감액이 발생할 수 있습니다. 또한, 한정된 내용연수를 지니는 무형자산에 대한 내용연수 기준 변경 등으로 인해 대규모 무형자산상각비가 발생하여, 당사의 손익에 부정적인 영향을 끼칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| 바. 잦은 자금조달 및 사용내역 변경에 따른 위험 당사는 2020년 6월 유상증자를 통해 공모 자금을 조달했습니다. 발행금액은 339,132백만원이며 당사는 해당 상장자금을 통해 영업양수, 운영자금, 채무상환, 타법인증권취득 등에 사용할 계획이였습니다. 당사는 증권신고서 제출일 현재까지 총 308,204백만원을 증권신고서상 자금사용목적과 동일하게 사용하였고, 잔여금액 30,928백만원을 예금 및 금융투자상품에 투자하여 보유하고자 했습니다. 다만, 당사는 유상증자 자금의 단기운용을 위하여 2020년 6월 금 30,000백만원을 옵티머스자산운용이 운용하고, 하이투자증권이 판매한 '옵티머스SMART전문투자형 사모혼합자산투자신탁제3호'에 투자하고자 예치했으나, 현재 판매사를 통한 환매가 중단되어 인출이 제한되고 있는 바, 회수가능성이 낮아 전액 충당금을 설정하였습니다. 사모방식으로 조달된 자금은 일부 사용 시점에서의 환율 차이에 비롯한 근소한 차이를 제외하면 주요사항보고서상에 명시된 대로 사용되었으며, 36회차의 경우 잔여금액을 운영자금으로 사용할 계획입니다. 당사는 공모 유상증자 납입대금 중 300억원을 증권신고서상 자금사용목적과 동일하게 추후에 사용하고자 금융상품에 투자했으나, 펀드의 상환중단으로 인해 투자손실을 기록했고 300억원의 대손충당금을 적립했습니다. 이는 결론적으로 당사에 대한 신뢰도를 악화시켰고, 당사는 자금 조달 및 운용계획을 제대로 세우지 못한바, 향후 철저한 자금 조달 및 운용계획을 수립하여 용도에 맞게 자금을 집행할 계획입니다 |
당사의 최근 3년간 공모 및 사모를 통해 조달한 자금 현황 및 사용내역 요약은 다음과 같습니다.
| [최근 3년간 공모 방식 자금조달 이력 및 자금사용내역] |
| (단위: 백만원) |
| 구 분 | 납입일 | 증권신고서상의 자금사용 계획 | 실제 자금사용내역 | 미사용자금운용내역 | 차이발생 사유 | ||||
|---|---|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 자금집행기간 | 금액 | 내용 | 금액 | |||
| 유상증자 | 20.06.05 | 영업양수자금 : 61,395 운영자금 : 4,000 채무상환자금 : 67,000 타법인증권취득자금 : 206,737 |
339,132 | 영업양수자금(*1) : 48,185 타법인증권취득자금(*1) : 13,210 |
2020.04 | 308,204 | 보통예금 : 928 기타(하이투자증권) : 30,000 |
30,928 | 하기 기재 |
| 운영자금 : 4,000 | 2020.06~2020.12 | ||||||||
| 채무상환자금 : 67,000 | 2020.06 | ||||||||
| 타법인증권 취득자금(*2) : 110,230 | 2020.08~2022.04 | ||||||||
| 타법인증권 취득자금(*3) : 15,659 | 2021.04~2021.11 | ||||||||
| 타법인증권 취득자금(*4) : 44,920 | 2021.10 | ||||||||
| 타법인증권 취득자금(*5) : 5,000 | 2022.04 | ||||||||
| (*1) 영업양수자금의 경우, 2020년 4월 유상증자 투자설명서에서의 예상계약금액(5,000만불)과 실제 계약체결시 계약금액(4,200만불)의 변경 및 환율 차이로 차액 132억원이 발생하였으며, 해당금액은 기업가치 극대화를 위하여 연결종속기업 (Immunomic Therapeutics,Inc.) 지분을 추가 취득하였습니다. (*2) 2020년 8월~2022년 4월, Camrelizumab-Rivoceranib 병용 간암 1차 치료제 글로벌 임상 3상비용(약320억원), 선낭암 1차 치료제 글로벌 단독임상 1상비용(약315억원), 론서프(타이호제약) - Rivoceranib 병용 대장암 3차 치료제 글로벌 임상 1상비용(약131억원) 등 기존 Pipeline 임상비용 지원을 위하여 Elevar Therapeutics,Inc. 유상증자에 참여를 통해 약91.7백만불을 납입하였습니다. 최근 Covid-19사태로 인한 임상지연 및 일정 미도래로 차이가 발생하여 해당금액은 안정성과 환금성을 확보할 수 있는 금융상품 등에 운용중입니다. (*3) 2021년 4월, 신규 Pipeline 확보를 통한 지속적인 미래 기업가치의 극대화를 위해 2020년 6월에 설립된 미국 벤처기업 Verismo Therapeutics,Inc.에 5백만불을 투자하였습니다. Verismo Therapeutics,Inc.은 KIR-CAR 기술의 기본특허와 KIR-CAR Mesothlin과 연관된 특허 및 생산공정과 관련된 특허를 보유하고 있으며, 차세대 CAR-T 플랫폼 기술을 기반으로 상용화 가능한 고형암 타깃 CAR-T 개발을 목표로 하고 있습니다. 그리고, 2021년 5월 바이오와 헬스케어 등의 분야의 신기술사업자에 대한 투자 및 융자 등 신기술사업 금융업을 통한 기업가치 극대화를 위해 에이치엘비인베스트먼트㈜의 보통주 600,000주를 30억원에 취득하였으며, 2021년 11월, 보통주 1,400,000주를 70억원에 추가 취득하였습니다. (*4) 2021년 10월, 안정적인 재무수익 창출 및 향후 예정된 바이오 사업과의 시너지 극대화를 위해 101,920백만원(현금 44,920백만원 지급 및 제34회차 신주인수권부사채 57,000백만원 대용납입(상계))을 투자하여 ㈜에프에이의 최대주주 등으로부터 지분 100%를 취득하였습니다. (*5) 2021년 11월, 지분취득을 통한 바이오 사업과의 시너지 극대화와 기업가치극대화를 위해 에이치엘비테라퓨틱스㈜ 보통주 530,899주를 약 50억원에 취득하였습니다. |
당사는 2020년 6월 유상증자를 통해 공모 자금을 조달했습니다. 발행금액은 339,132백만원이며 당사는 해당 상장자금을 통해 영업양수, 운영자금, 채무상환, 타법인증권취득 등에 사용할 계획이였습니다. 당사는 증권신고서 제출일 현재까지 총 308,204백만원을 증권신고서상 자금사용목적과 동일하게 사용하였고, 잔여금액 30,928백만원을 예금 및 금융투자상품에 투자하여 보유하고자 했습니다. 다만, 당사는 유상증자 자금의 단기운용을 위하여 2020년 6월 금 30,000백만원을 옵티머스자산운용이 운용하고, 하이투자증권이 판매한 '옵티머스SMART전문투자형 사모혼합자산투자신탁제3호'에 투자하고자 예치했으나, 현재 판매사를 통한 환매가 중단되어 인출이 제한되고 있는 바, 회수가능성이 낮아 전액 충당금을 설정하였습니다. 해당 투자의 목적 및 배경, 현황, 계획 등은 하기와 같습니다.
| [당사 투자 사모펀드 상세 현황 ] |
| (단위: 백만원) |
| 펀드명 | 판매사 | 운용사 | 취득금액 | 최초 기대수익률 |
펀드기한 | 펀드 내역 | 담보 등 | ||
|---|---|---|---|---|---|---|---|---|---|
| 최초 취득일 | 최초 만기일 | 변동 만기일 | |||||||
| 옵티머스SMART전문투자형 사모혼합자산투자신탁제3호 |
하이투자증권 | 옵티머스자산운용 | 30,000 | 5.00% | 2020-06-11 | 2020-12-11 | 만기상환 연기요청 | 부동산 관련 증권 및 수익권 부동산 개발과 관련된 법인에 대한 단기대출 부동산 개발(운영 포함)사업 관련법인이 발행하는 사모사채 |
- |
(1) 투자목적 및 배경
유상증자 자금의 단기운용을 위하여 국공채상품과 같은 채권형 안전자산에 투자를 옵티머스자산운용으로부터 권유를 받고 판매사인 하이투자증권에 문의한 후, 300억원을 예치하였으나(당시 하이투자증권은 해당 상품설명서를 보유하고 있었으나 당사가 자료 제공 요청함에도 불구하고 제공하지 아니함) , 해당 금융상품의 상품설명서를 추후에 수령하여 확인한 결과 당초 권유받은 내용 및 판매사로부터 구두설명받은 바와 달라 펀드 수익증권 매매계약의 가입절차를 거부하는 등 일체의 투자절차를 거절하였습니다. 이처럼 펀드 가입절차가 진행되지 않은 가운데 하이투자증권(판매사)은 옵티머스자산운용(운용사)에 예치금 300억원을 송금하였습니다. 해당 펀드는 2인투자자로부터 투자를 받아야 하며, 펀드 설정금액인 500억원에도 미치지 않아 펀드를 해산해야 함에도 불구하고 가입되지 않은 예치금을 운용사에 송금한 판매사에 수익증권 매매계약 불성립에 따른 부당이득 반환 청구와 예비적 청구로서 착오에 의한 의사표시, 제3자 사기에 의한 의사표시로 수익증권 매매계약 취소에 따른 부당이득 반환 청구, 투자자 보호의무 위반에 따른 손해배상 청구를 2020년 6월 29일 서울남부지방법원에 접수하여 현재 1심이 진행되고 있습니다.
(2) 손상인식시점 및 회계처리 현황
| 1) 2020년 6월 11일, 하이투자증권에 예치금 300억원 입금(회계처리. 선급금 처리) 2) 2020년 6월 29일, 하이투자증권 부당이득금 반환소송 접수에 따라 선급금(예치금 300억원)을 미수금으로 대체 3) 2020년 6월 30일, 판매사를 통해 환매가 중단되어 인출이 제한되고 있어 해당 미수금에 대한 대손충당금 100% 설정 |
(3) 당사 사모펀드 상환 중단 및 지급 지연 일지
| [당사 사모펀드 상환 중단 및 지급 지연 일지] | |
| (기준일 : 증권신고서 제출전일) | |
| 펀드명 | 일자 | 내 용 |
|---|---|---|
| 옵티머스SMART 전문투자형 사모혼합투자신탁제3호 |
2020-06-11 | 하이투자증권(옵티머스SMART전문투자형사모혼합자산투자신탁제3호) 판매사에 300억원 예치 |
| 2020-06-23 | 하이투자증권(판매사)으부터 이메일로 공문('집합투자증권 환매신청 중단의 건') 수령 | |
| 2020-06-29 | 하이투자증권(판매사)를 상대로 부당이득금 반환청구소송 제기 | |
| 2020-12-10 | 하이투자증권(판매사)으로부터 이메일로 공문('집합투자증권 만기상환 연기의 건') 수령 |
(4) 사모펀드 상환 중단 및 지급 지연요청 공문 주요 내용
| [당사 사모펀드 상환 중단 및 지급 지연 일지] | |
| (기준일 : 증권신고서 제출전일) | |
| 펀드명 | 요청 공문 주요 내용 |
|---|---|
| 옵티머스SMART전문투자형 사모혼합자산투자신탁제3호 |
[2020.06.23 공문 주요 내용] (중략) 2. 귀 사에서 투자중인 '옵티머스SMART전문투자형사모혼합자산투자신탁제3호' 펀드의 환매신청이 아래와 같이 중단되었음을 알려드립니다. - 아 래 - 1. 펀드명 : 옵티머스SMART전문투자형사모혼합자산투자신탁제3호 2. 환매중단 요청일 : 2020년 6월 19일 3. 사유 : 펀드 미상환 발생으로 투자자 보호 및 형평성을 위함 4. 환매 재개일 : 추후 공지 [2020.12.10 공문 주요 내용] (중략) 2. 귀 사에서 투자중인 '옵티머스SMART전문투자형사모혼합자산투자신탁제3호' 펀드의 만기상환이 연기되었음을 알려드립니다. - 아 래 - 1. 펀드명 : 옵티머스SMART전문투자형사모혼합자산투자신탁제3호 2. 사유 : 투자신탁재산의 정상적인 회수가 불가능하여 펀드의 정상 상환이 어려움 3. 상환예정일 : 추후 공지 |
(5) 향후 회수 및 소송 계획
| 2020년 6월 29일에 '옵티머스SMART전문투자형사모혼합자산투자신탁제3호'의 판매사(하이투자증권)에 수익증권 매매계약 불성립에 따른 부당이득 반환 청구와 예비적 청구로서 착오에 의한 의사표시, 제3자 사기에 의한 의사표시로 수익증권 매매계약 취소에 따른 부당이득 반환 청구, 투자자 보호의무 위반에 따른 손해배상 청구를 제기하였으며,현재까지 1심을 진행중에 있습니다. 현재까지 1심을 진행중에 있습니다. |
금융자산에 대한 충당금 적립 및 손상차손 인식은 당사의 재무상태에 직접적으로 악영향을 미칠 뿐 아니라, 현금흐름의 악화를 수반해 당사의 유동성에도 악영향을 미칠수 있습니다. 또한, 감독기관이 해당 미사용 자금 사용과 관련하여, 미사용 자금 운용방법에 대해 부실기재가 있다고 판단하게 될 경우 증권신고서 및 정기보고서(사업보고서, 반기 및 분기보고서) 허위기재 등 「자본시장과 금융투자업에 관한 법률」 제132조에 위반으로 과징금, 임원의 해임, 일정기간 증권의 발행제한 등의 조치를 받을 수 있으며, 해당 위반에 따른 부정적 이미지로 인해 주가 하락은 물론 금번 유상증자의 청약을 저하에 따른 실권 수수료 지급 등 재무적 손실 가능성이 있습니다.
| [최근 3년간 사모방식 자금조달 이력 및 자금사용내역] |
| (단위: 백만원) |
| 발행내역 | 납입일 | 조달(발행) 금액 |
주요사항보고서상의 자금사용목적 |
주요사항보고서상의 사용목적 금액 |
실제 자금사용 상세내용 |
실제 사용금액 |
|---|---|---|---|---|---|---|
| 제31회차 무보증 사모CB | 2019.01.30 | 20,000 | 타법인증권취득자금 | 10,000 | LSK BioPartner,Inc. 발행 보통주 81,900주 취득 |
2,268 |
| LSK BioPartner,Inc. 발행 보통주 36,680주 취득(구주인수) |
5,330 | |||||
| Elevar Therapeutice,Inc 발행 보통주, 10,000,000주 |
2,402 | |||||
| 운영자금 | 10,000 | 원재료 구매 등 | 7,143 | |||
| 인건비 등 | 1,768 | |||||
| 차입금 상환 | 266 | |||||
| 세금 등 | 242 | |||||
| 제비용 | 231 | |||||
| 외부감사비 등 | 189 | |||||
| 이자비용 | 161 | |||||
| 제32회차 무보증 사모CB | 2019.06.14 | 20,000 | 타법인증권취득자금 | 10,000 | 에이치엘비생명과학㈜ 발행 보통주, 217,901주 |
1,330 |
| 에이치엘비생명과학㈜ 발행 보통주, 574,366주 |
4,145 | |||||
| 에이치엘비생명과학㈜ 발행 보통주, 300,000주 |
2,137 | |||||
| 에이치엘비생명과학㈜ 발행 보통주, 344,668주 |
2,388 | |||||
| 운영자금 | 10,000 | 원재료 구매 등 | 5,190 | |||
| 삼각합병 관련비용 | 2,294 | |||||
| 인건비 등 | 1,824 | |||||
| 제비용 | 295 | |||||
| 세금 등 | 210 | |||||
| 보증금 | 187 | |||||
| 제33회차 무보증 사모CB | 2019.12.18 | 40,000 | 타법인증권취득자금 | 30,000 | Elevar Therapeutice,Inc 발행 보통주, 10,000,000주 |
9,455 |
| Elevar Therapeutice,Inc 발행 보통주, 13,000,000주 |
15,112 | |||||
| Immuomic Therapeutice,Inc 발행 보통주, 2,000,000주 |
5,433 | |||||
| 운영자금 | 10,000 | 원재료 구매 등 | 7,419 | |||
| 인건비 등 | 1,006 | |||||
| 차입금 상환 | 977 | |||||
| 제비용 | 195 | |||||
| 주총관련비용 | 116 | |||||
| 외부감사비 등 | 116 | |||||
| 세금 등 | 79 | |||||
| 삼각합병 관련비용 | 63 | |||||
| 이자비용 | 29 | |||||
| 제34회차 무보증 사모 비분리형 BW | 2021.10.20 | 57,000 | 타법인증권취득자금 | 57,000 | ㈜에프에이 취득자금 | 57,000 |
| 제35회차 무보증 사모 비분리형 BW | 2022.03.30 | 25,200 | 타법인증권취득자금 | 25,200 | ㈜노터스 취득자금 | 25,200 |
| 제36회차 무보증 사모 비분리형 BW | 2022.06.02 | 23,000 | 운영자금 | 23,000 | 일반경비 등 | 1,759 |
| 외주가공비 등 | 6,075 | |||||
| 유형자산 취득 등 | 947 | |||||
| 대여금 | 1,000 | |||||
| 제37회차 무보증 사모 비분리형 BW | 2022.06.02 | 17,000 | 운영자금 | 17,000 | 원재료 구매 등 | 13,617 |
| 일반경비 등 | 3,383 |
사모방식으로 조달된 자금은 일부 사용 시점에서의 환율 차이에 비롯한 근소한 차이를 제외하면 주요사항보고서상에 명시된 대로 사용되었으며, 36회차의 경우 잔여금액을 운영자금으로 사용할 계획입니다.
당사는 공모 유상증자 납입대금 중 300억원을 증권신고서상 자금사용목적과 동일하게 추후에 사용하고자 금융상품에 투자했으나, 펀드의 상환중단으로 인해 투자손실을 기록했고 300억원의 대손충당금을 적립했습니다. 이는 결론적으로 당사에 대한 신뢰도를 악화시켰고, 당사는 자금 조달 및 운용계획을 제대로 세우지 못한바, 향후 철저한 자금 조달 및 운용계획을 수립하여 용도에 맞게 자금을 집행할 계획입니다.
| 사. 영업현금흐름 및 유동성 관련 위험 당사는 지속적인 연구개발 활동으로 인해 음(-)의 영업활동현금흐름을 보이고 있으며,이를 재무활동현금흐름을 통하여 충당하고 있는 상황입니다. 당사는 향후 임상 파이프라인 및 임상 단계 진전에 따라 더 많은 연구개발비가 투입될 예정이며 이에 따라 영업비용 또한 확대될 것으로 보입니다. 비록 금번 주주배정 후 실권주 일반공모 유상증자를 통하여 재무활동현금이 유입될 예정이나 보유 파이프라인의 라이센스 아웃 및 영업활동 전반에 대한 모니터링이 필요하다고 판단되며, 지속적으로 영업 성과에 부정적인 영향으로 음(-)의 영업활동현금흐름이 발생할 경우 장기적으로 회사의 현금흐름에 문제가 발생할 소지가 있습니다. |
당사는 수익성 악화 및 지속적인 연구개발 활동으로 인해 음(-)의 영업활동현금흐름을 보이고 있으며, 투자활동현금흐름의 경우에도 지속적인 관계기업투자주식의 취득으로 인해 음(-)의 현금흐름을 보였습니다. 당사는 음(-)의 영업활동현금흐름을 대체적으로 재무활동현금흐름을 통하여 충당하고 있는 상황이며, 2022년 반기말 기준 당사는 80,483백만원의 현금 및 현금성자산을 보유하고 있습니다. 당사의 최근 4년간 요약 현금흐름 추이는 다음과 같습니다.
| [요약 현금흐름표] |
| (단위: 백만원, 주) |
| 구분 | 2022년 반기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
| 영업활동으로 인한 현금흐름 | (33,915) | (54,765) | (56,514) | (48,657) |
| 당기순이익 | (19,100) | (111,607) | (88,716) | (59,660) |
| 수익비용의 조정 | 10,391 | 35,303 | 42,331 | 14,501 |
| 영업활동으로 인한 자산부채의 변동 | (15,949) | 12,338 | (11,226) | (1,672) |
| 이자수취 | 405 | 1,622 | 1,543 | 718 |
| 이자지급 | (3) | (217) | (326) | (2,475) |
| 투자활동으로 인한 현금흐름 | (20,876) | (68,496) | (98,022) | (26,825) |
| 기타유동금융자산의 처분 | - | 975 | 31,768 | 274 |
| 공정가치측정금융자산의 처분 | 359 | 22,177 | 180,000 | 5,552 |
| 종속기업과 기타 사업의 지배력 획득에 따른 현금흐름 | (292) | 3,864 | 78,334 | - |
| 관계기업투자주식의 취득 | (25,026) | (11,602) | (70,318) | (10,000) |
| 무형자산의 취득 | (655) | (3,954) | (74,009) | (163) |
| 공정가치측정금융자산의 취득 | (19,672) | (1,247) | (193,242) | (10,500) |
| 재무활동으로 인한 현금흐름 | 32,566 | 1,335 | 341,017 | 86,663 |
| 지배기업의 유상증자 | - | - | 368,136 | - |
| 전환사채의 발행 | 23,000 | - | - | 79,799 |
| 단기차입금의 차입 | - | 6,002 | 62,817 | 184,180 |
| 단기차입금의 상환 | (6,168) | (2,623) | (63,695) | (183,476) |
| 비지배지분의 취득 | - | - | (25,202) | (24,805) |
| 기초 현금및현금성자산 | 99,797 | 220,678 | 40,855 | 30,226 |
| 기말 현금및현금성자산 | 80,483 | 99,797 | 220,678 | 40,855 |
2019년 당사는 연결기준으로 59,660백만원의 당기순손실이 발생하였으며, 감가상각비, 이자 관련 수취 및 지급 등 48,657백만원의 음(-)의 영업활동현금흐름이 발생하였습니다. 투자활동현금흐름의 경우 10,000백만원의 관계기업투자주식의 취득 등26,825백만원의 현금유출이 있었으며, 재무활동현금흐름의 경우 79,799백만원의 전환사채 발행 등 86,663백만원의 양(+)의 현금흐름이 발생하였습니다. 이에 2019년말연결기준 40,855백만원의 현금 및 현금성 자산을 보유하게 되었습니다.
2020년 당사는 연결기준으로 88,716백만원의 당기순손실이 발생하였으며, 56,514백만원 음(-)의 영업활동현금흐름을 기록하였습니다. 이는 전환사채의 전환권 행사에 따른 파생상품손실이 현금의 유출이 없는 비용등의 가감 항목으로 42,331백만원 상당이 가산조정 되었으나, 당기순손실 및 매출채권 증가에 따른 자산부채의 변동에 기인합니다. 투자활동현금흐름의 경우 관계기업투자주식의 취득 및 무형자산의 취득으로 인해 98,022백만원의 (-)음의 현금흐름이 발생하였으며, 재무활동현금흐름의 경우 당사가 진행한 유상증자에 등 341,017백만원 상당의 양(+)의 현금흐름이 발생하였습니다. 이에 2020년말 연결기준 220,678백만원의 현금 및 현금성 자산을 보유하게 되었습니다.
2021년에는 전년대비 증가한 111,607백만원의 당기순손실을 기록하였으며, 54,765백만원의 음(-)의 영업활동현금흐름이 발생하였습니다. 투자활동현금흐름의 경우 공정가치측정금융자산의 순처분에도 불구하고, 사업결합으로 인한 현금유출로 인해 68,496백만원의 음(-)의 현금흐름이 발생하게 되었습니다. 이에 2021년 연결기준 99,797백만원의 현금 및 현금성 자산을 보유하게 되었습니다.
2022년 반기에는 19,100백만원의 당기순손실이 발생하였으며, 현금 유출이 없는 비용 조정이 10,391백만원이 있었으나, 자산ㆍ부채의 변동으로 인한 현금유출이 발생하면서 33,915백만원의 음(-)의 영업활동현금흐름이 발생하였습니다. 투자활동현금흐름의 경우 20,876백만원의 음(-)의 현금흐름이 있었으며 이는 관계기업투자주식 취득 25,026백만원과 에이치엘비생명과학㈜ BW 취득 19,672백만원에 기인합니다.재무활동현금흐름은 운영자금 목적의 전환사채 및 신주인수권부사채 발행에 따라 32,566백만원의 양(+)의 현금흐름을 기록하였습니다. 이에 2022년 반기 연결기준 80,483백만원의 현금 및 현금성 자산을 보유하게 되었습니다.
당사는 현금흐름 및 유동성에 대하여 지속적으로 모니터링하면서 유동성 이슈가 발생하지 않도록 대응하고 있으나, 향후에도 유의미한 수준의 수익성이 발생하지 않아 음(-)의 영업활동현금흐름이 계속 발생할 경우 유동성 리스크가 부각될 위험이 있습니다. 때문에 보유 파이프라인의 개발현황 및 영업활동 전반에 대한 모니터링이 필요하다고 판단되며, 지속적으로 영업 성과에 부정적인 영향으로 음(-)의 영업활동현금흐름이 발생할 경우 장기적으로 회사의 현금흐름에 문제가 발생할 소지가 있습니다. 투자자께서는 회사의 현금흐름 및 유동성 관련 위험요인을 면밀히 검토하시고 투자에 임해주시기 바랍니다.
|
아. 잦은 타법인 주식 양수도 관련 위험 당사의 금융수익 및 원가는 주로 당사가 보유하고 있는 관계회사들의 채권 평가 및 처분에 의한 금융자산손익에 의한 것으로 매분기 평가 및 처분 결과에 따라 손익이 결정되며,당사의 금융수익 및 금융원가는 보유 금융자산의 평가손익에 따라 변동성이 있습니다. 따라서 당사가 안정적인 매출액을 바탕으로 영업이익을지속적으로 시현 하지 못하는 한,당사의 수익성이 악화 될 위험이 있습니다. 또한, 당사는 사업다각화와 재무구조안정 등의 목적을 위해 과거부터 지속적을 타법인 출자를 진행하고 있으며, 추가적인 타법인 출자 및 자산양수도를 위한 전환사채 및 신주인수권부사채 발행 등의 차입이 발생할 경우, 당사의 재무안정성에 부정적인 영향을 미칠 수 있습니다. 투자자 여러분들께서는 이 점을 반드시 유의하시기 바랍니다. 또한, 신규사업 추진 및 금융수익 창출을 위한 막대한 자금의 소요에도 불구하고, 신규사업 진행에 차질이 생기거나 투자한 금융자산에 평가 및 처분 손실이 발생할 수 있습니다. 이 경우, 당사의 수익성이나 재무안정성이 악화될 수 있으며, 투자자께서는 이 점 유의하시기 바랍니다. |
당사의 금융수익 및 원가는 주로 당사가 보유하고 있는 에이치엘비제약㈜의 전환사채 및 에이치엘비생명과학㈜ 채권의 평가 및 처분에 의한 금융자산손익에 의한 것으로 매분기 평가 및 처분 결과에 따라 손익이 결정됩니다. 당사의 2022년 반기 기준 주요 당기손익-공정가치측정금융자산의 내역, 장부금액 및 평가손익은 다음과 같습니다.
| [공정가치측정금융자산(당기손익) 주요 내역] | |
| (단위: 백만원) | |
| 구분 | 취득원가 | 장부금액 | 평가손익 | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 증권신고서 제출일 기준 | 2022년 반기 | 2021년 | 2020년 | 2019년 | 2022년 반기 | 2021년 | 2020년 | 2019년 | ||
| 에이치엘비생명과학㈜ 제7회차 CB | 10,000 | - | - | - | 18,663 | 21,627 | - | 4,190 | (2,964) | 11,042 |
| 에이치엘비제약㈜ 제12회차 CB(*1) | 10,000 | - | 24,937 | 21,727 | 28,007 | - | 1,546 | (6,280) | 18,007 | - |
| 에이치엘비생명과학㈜ 제9회차 BW(*2) | 19,603 | 19,603 | 19,603 | - | - | - | - | - | - | - |
| (*1) 당사는 2022년 08월 12일 에이치엘비제약 12CB 전량을 관계회사인 에이치엘비생명과학㈜에 매각함(평가금액 24.937백만원, 매각금액 23,700백만원) (*2) 에이치엘비생명과학㈜ 제9회차 BW 2022년 6월 중 취득으로 반기까지 큰 변동은 없는것으로 평가 진행하지 않음 |
| [당기손익-공정가치 측정 금융자산 연도별 손익] | |
| (기준 : 2022년 반기) | (단위 : 백만원) |
| 구 분 | 2022년 반기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
| [당기손익-공정가치측정금융자산] | ||||
| 평가이익 | 7,436 | 4,362 | 18,012 | 17,593 |
| 평가손실 | 175 | (7,506) | 2,964 | 4,713 |
| 처분이익 | - | 67 | - | - |
| 처분손실 | - | 22 | - | - |
2022년 반기 기준, 공정가치 측정 금융자산평가이익은 7,436백만원, 공정가치 측정 금융자산평가손실은 175백만원으로 합계 손익은 7,261백만원의 이익을 기록하였습니다. 상기와 같이, 당사의 금융수익 및 금융원가는 보유 금융자산의 평가손익에 따라 변동성이 있습니다. 따라서 당사가 안정적인 매출액을 바탕으로 영업이익을지속적으로 시현 하지 못하는 한, 당사의 수익성이 악화 될 위험이 있습니다.
또한, 당사는 기업 전반의 손익 개선 및 신성장동력확보를 위해 2015년부터 사업 다각화를 진행하여 왔고, 이 과정에서 주식양수도 등을 통하여 계열회사 지분을 지속적으로 취득하였습니다. 당사 타법인출자 현황은 다음과 같습니다.
| [타법인출자 현황] |
| (단위: 백만원, 천주, %) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 2022년 반기말 잔액 | 최근사업연도(2021년) 재무현황 |
||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
자산총계 | 부채총계 | 자본총계 | 매출액 | 당기순손익 | |||||
| 에이치엘비생명과학㈜ | 상장 | 2015.10.23 | 경영참여 | 7,000 | 18,721 | 19.60 | 131,066 | 270,800 | 24,188 | 246,612 | 53,494 | (49,292) |
| 현대요트㈜ | 비상장 | 2009.07.02 | 경영참여 | 300 | 328 | 39.43 | - | 12,036 | 10,761 | 1,275 | 14,246 | 9 |
| 바다중공업㈜ | 비상장 | 2009.05.28 | 경영참여 | 300 | 780 | 28.89 | 768 | 20,421 | 16,374 | 4,047 | 16,482 | 556 |
| 고션 | 비상장 | 2014.02.12 | 경영참여 | 105 | 21 | 18.76 | - | 38 | 1,283 | (1,245) | 0 | 0 |
| ㈜티에스넥스젠 | 상장 | 2016.09.06 | 단순투자 | 2,800 | 623 | 0.68 | 719 | 99,108 | 53,795 | 45,312 | 18,538 | (6,532) |
| ㈜화진메디칼(*1) | 비상장 | 2018.02.21 | 경영참여 | 5,022 | - | - | - | 7,576 | 5,532 | 1,929 | 6,165 | 63 |
| ㈜화진메디스(*1) | 비상장 | 2018.02.21 | 경영참여 | 500 | - | - | - | 1,947 | 1,852 | 119 | 1,480 | (172) |
| Elevar Therapeutics, Inc. | 비상장 | 2019.06.11 | 경영참여 | 188,792 | 61,579 | 100.00 | 368,896 | 50,455 | 51,345 | (8,210) | 0 | (63,462) |
| ㈜씨엘팜 | 비상장 | 2019.12.02 | 경영참여 | 5,000 | 64 | 7.72 | 5,074 | 31,605 | 16,703 | 14,902 | 10,829 | 1,211 |
| Immunomic Therapeutics, Inc. | 비상장 | 2020.01.31 | 경영참여 | 11,970 | 11,286 | 41.07 | 67,098 | 56,964 | 15,598 | 48,127 | 2,294 | (26,056) |
| Verismo Therapeutics, Inc. | 비상장 | 2021.04.12 | 경영참여 | 5,602 | 1,913 | 9.61 | 5,602 | 15,573 | 19 | 15,554 | 0 | (6,563) |
| 에이치엘비 인베스트먼트㈜ | 비상장 | 2021.05.28 | 경영참여 | 10,000 | 2,000 | 100.00 | 10,000 | 10,227 | 179 | 2,826 | 0 | (438) |
| 에이치엘비 테라퓨틱스㈜ | 상장 | 2021.11.15 | 경영참여 | 500 | 531 | 1.69 | 5,000 | 189,711 | 59,672 | 130,039 | 43,586 | (17,764) |
| 에프에이㈜(*2) | 비상장 | 2021.10.20 | 경영참여 | 102,126 | - | - | - | - | - | - | - | - |
| Hyundai Lifeboats Shanghai Co.,Ltd | 비상장 | 2022.02.10 | 경영참여 | 1,385 | 0 | 100.00 | 1,385 | 913 | 79 | 834 | 1,059 | 138 |
| ㈜노터스 | 상장 | 2022.03.30 | 경영참여 | 56,226 | 1,406 | 18.01 | 56,226 | 93,402 | 28,265 | 65,137 | 64,403 | 10,308 |
| 합 계 | - | - | 651,834 | - | ||||||||
| (*1) 2022년 4월 29일 관계기업인 에이치엘비테라퓨틱스㈜에 매각하였습니다. (*2) 2022년 1월 1일 당사와 합병하였습니다. |
당사의 연결대상종속회사를 제외한 타법인 출자에 대한 배경, 목적, 개요 등은 아래와 같습니다.
1) 에이치엘비생명과학㈜
| 구분 | 내용 |
|---|---|
| 출자배경 | 기업가치 극대화 |
| 출자목적 | 경영참여 |
| 주요사업 | 에너지사업, 의약품 도매사업, 제약·바이오사업 |
| '21년 이익 및 손실 발생 사유 | 의약품 도매사업 매출 부진, 공정가치평가손실 발생 |
| 추가 출자 계획 | - |
2) 현대요트㈜
| 구분 | 내용 |
|---|---|
| 출자배경 | 조선업 파이프라인의 다양화 |
| 출자목적 | 경영참여 |
| 주요사업 | 레저보트 판매, 보트 수리, 검사 등 |
| '21년 이익 및 손실 발생 사유 | 조선경기 악화로 인한 손실 발생 |
| 추가 출자 계획 | - |
3) 바다중공업㈜
| 구분 | 내용 |
|---|---|
| 출자배경 | 조선업 파이프라인의 다양화 |
| 출자목적 | 경영참여 |
| 주요사업 | 선박용 크레인, 특수선장비, 조선기자재 판매 |
| '21년 이익 및 손실 발생 사유 | 고부가가치 조선기자재 판매로 이익 발생 |
| 추가 출자 계획 | - |
4) ㈜고션
| 구분 | 내용 |
|---|---|
| 출자배경 | 조선업 파이프라인의 다양화 |
| 출자목적 | 경영참여 |
| 주요사업 | 레저 보트 개발, 생산, 판매 |
| '21년 이익 및 손실 발생 사유 | 휴업 중 |
| 추가 출자 계획 | - |
5) ㈜티에스넥스젠
| 구분 | 내용 |
|---|---|
| 출자배경 | 신규 사업진출 및 기업가치 극대화 |
| 출자목적 | 단순투자 |
| 주요사업 | 발전설비 등 |
| '21년 이익 및 손실 발생 사유 | 최대주주의 지분 매각(7월)으로 알수 없음 |
| 추가 출자 계획 | - |
6) ㈜씨엘팜
| 구분 | 내용 |
|---|---|
| 출자배경 | 신규 사업진출 및 기업가치 극대화 |
| 출자목적 | 경영참여 |
| 주요사업 | 건강식품 외 |
| '21년 이익 및 손실 발생 사유 | 코로나로 인한 건강기능 식품에 대한 수요 높아짐에 따라 이익 발생 |
| 추가 출자 계획 | - |
7) Verismo Therapeutics, Inc.
| 구분 | 내용 |
|---|---|
| 출자배경 | 기업가치 극대화, 파이프라인 확보 |
| 출자목적 | 경영참여 |
| 주요사업 | 바이오의약품 개발 |
| '21년 이익 및 손실 발생 사유 | 바이오 의약품 개발 단계라 손실 발생 |
| 추가 출자 계획 | - |
8) 에이치엘비테라퓨틱스㈜
| 구분 | 내용 |
|---|---|
| 출자배경 | 지분취득을 통한 기업가치 극대화 |
| 출자목적 | 경영참여 |
| 주요사업 | 백신 판매, 안구건조증, 신경영양성각막염 등 임상 |
| '21년 이익 및 손실 발생 사유 | 코로나로 인한 시장환경 악화로 인한 손실 발행 |
| 추가 출자 계획 | - |
9) Hyundai Lifeboats Shanghai Co.,Ltd
| 구분 | 내용 |
|---|---|
| 출자배경 | 리보세라닙 중국 로열티 수령 및 향후 중국사업 진출 |
| 출자목적 | 경영참여 |
| 주요사업 | 선박 수리, 검사 등 |
| '21년 이익 및 손실 발생 사유 | 조선경기는 악화되어 있으나 부품 공급, 수리, 검사 수요는 꾸준하여 이익 발생 |
| 추가 출자 계획 | - |
10) ㈜노터스
| 구분 | 내용 |
|---|---|
| 출자배경 | 신규사업진출 및 기존사업과의 시너지 극대화 |
| 출자목적 | 경영참여 |
| 주요사업 | 신약 등 신규 개발 물질에 대한 비임상 실험을 진행하는 비임상CRO |
| '21년 이익 및 손실 발생 사유 | 비임상 CRO 수요가 꾸준하여 이익 발생 |
| 추가 출자 계획 | - |
당사 종속기업의 손익은 당사 연결재무제표의 손익에 직접 영향을 미치며, 보고서 제출일 기준, 연결대상 종속회사인 Elevar, Immunomic, 에이치엘비인베스트먼트㈜, Hyundai Lifeboats Shanghai PTE.LTD는 관련 손익이 직접 연결제무제표에 계상되었습니다. 그 외 바다중공업㈜, 현대요트㈜, 에이치엘비생명과학㈜, Verismo, 에이치엘비테라퓨틱스㈜, ㈜노터스 같은 관계기업의 손익도 그 지분율만큼 지분법손익에 따라 영업외손익으로 인식하여 당사의 연결재무제표에 영향을 미칩니다.
| [지분법 평가내역 연도별 손익] | |
| (연결기준) | (단위 : 백만원) |
| 구 분 | 2022년 반기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
| 기초장부가액 | 133,624 | 106,500 | 115,039 | 36,029 |
| 취득액 | 56,226 | 34,455 | - | 72,799 |
| 지분법 평가손익 | (1,017) | (8,356) | (10,225) | (629) |
| 처분이익 | - | - | - | 2,511 |
| 지분법 자본변동 | 2,804 | 1,025 | 1,686 | 4,329 |
| 기말 장부가액 | 191,637 | 133,624 | 106,500 | 115,039 |
향후 당사의 종속 및 관계회사를 통한 시너지 효과 및 수익성 회복이 이루어지지 않고 당사가 투자한 종속기업 및 관계기업의 경영 악화로 인하여 해당회사들의 손실이 발생된다면, 당사의 손익에 부정적인 영향을 줄 수 있으며 당사의 재무건전성 역시 악화될 수 있습니다. 투자자 여러분께서는 이 점을 유의하시기 바랍니다.
㈜노터스 및 ㈜에프에이(합병이전 사명)에 대한 구체적인 투자결정 경위 및 투자 과정은 다음과 같습니다.
① ㈜노터스
[지분취득 경위]
2021년 12월 27일, 당사는 동물바이오 사업 진출 및 비임상CRO 사업과의 시너지를 위해 ㈜노터스의 기존 최대주주 정인성, 김도형으로부터 구주 1,405,648주(18.37%)를 취득하는 계약을 체결하였습니다. 이에 따라 당사는 계약금(21/12/27) 현금 60억원, 중도금(22/01/27) 60억원, 잔금(22/03/30) 현금 약 190.3억원 및 신주인수권부사채 252억원 등 총 인수금액 약 562억원을 지급하였으며, 이는 2020년 당사의 별도기준 자산총액 대비 7.96%에 해당하는 타법인 주식 양수입니다. 이와 관련한 2022년 01월 27일의 최종 공시는 다음과 같습니다.
| [[정정]타법인주식및출자증권취득결정](2022.01.27) |
| 1. 발행회사 | 회사명(국적) | 주식회사 노터스 | 대표이사 | 정인성, 김도형 |
| 자본금(원) | 765,186,800 | 회사와 관계 | - | |
| 발행주식총수(주) | 7,651,868 | 주요사업 | 비임상CRO 등 | |
| -최근 6월 이내 제3자 배정에 의한 신주취득 여부 | 아니오 | |||
| 2. 취득내역 | 취득주식수(주) | 1,405,648 | ||
| 취득금액(원) | 56,225,920,000 | |||
| 자기자본(원) | 585,368,619,300 | |||
| 자기자본대비(%) | 9.61 | |||
| 대기업 여부 | 해당 | |||
| 3. 취득후 소유주식수 및 지분비율 | 소유주식수(주) | 1,405,648 | ||
| 지분비율(%) | 18.37 | |||
| 4. 취득방법 | 현금 및 신주인수권부사채 발행 취득(구주취득) | |||
| 5. 취득목적 | 신규사업진출 및 기존사업과의 시너지 극대화 | |||
| 6. 취득예정일자 | 2022-03-30 | |||
| 7. 자산양수의 주요사항보고서 제출대상 여부 | 아니오 | |||
| -최근 사업연도말 자산총액(원) | 706,477,276,989 | 취득가액/자산총액(%) | 7.96 | |
| 8. 우회상장 해당 여부 | 아니오 | |||
| -향후 6월이내 제3자배정 증자 등 계획 | 아니오 | |||
| 9. 발행회사(타법인)의 우회상장 요건 충족여부 | 아니오 | |||
| 10. 이사회결의일(결정일) | 2021-12-27 | |||
| -사외이사 참석여부 | 참석(명) | 3 | ||
| 불참(명) | 0 | |||
| -감사(감사위원) 참석여부 | 참석 | |||
| 11. 공정거래위원회 신고대상 여부 | 미해당 | |||
| 12. 풋옵션계약 등의 체결여부 | 아니오 | |||
| -계약내용 | - | |||
| 13. 기타 투자판단에 참고할 사항 | - 상기 자기자본은 2020년도말 연결재무제표를 기준으로 현재까지 증가된 자본금등을 반영한 금액입니다. - 상기 자산총액은 2020년도말 연결재무제표상 기준입니다. - 하기 발행회사의 재무상황은 2018년말, 2019년 말, 2020년말 연결재무제표 기준입니다. - 상기 취득금액의 지급조건은 계약일당일(2021/12/27) 현금 60억원, 중도금(2022/01/27) 현금 60억원, 잔금(2022/03/30) 현금 약190.3억원 및 신주인수권부사채 발행(252억원)입니다. |
|||
[발행회사의 요약 재무상황] (단위 : 백만원)
| 구분 | 자산총계 | 부채총계 | 자본총계 | 자본금 | 매출액 | 당기순이익 |
|---|---|---|---|---|---|---|
| 당해년도 | 74,215 | 19,191 | 55,024 | 762 | 58,520 | 8,589 |
| 전년도 | 61,531 | 18,508 | 43,023 | 732 | 46,040 | 4,554 |
| 전전년도 | 43,741 | 22,239 | 21,502 | 617 | 37,237 | 3,856 |
[상대방에 관한 사항]
| 1. 인적사항 | |||
| - 기본사항 | |||
| 성명(명칭) | 국적 | 주소(본점소재지)[읍ㆍ면ㆍ동까지만 기재] | 생년월일(사업자등록번호 등) |
| 주식회사 노터스 | 대한민국 | 인천 연수구 아카데미로 | 132-86-05757 |
| 직업(사업내용) | 비임상CRO 등 | ||
| - 최대주주ㆍ대표이사ㆍ대표집행임원 현황 및 재무상황 등(상대방이 법인인 경우) | |||
| 구분 | 성명 | 주식수 | 지분율(%) |
| 최대주주 | 정인성 | 1,723,200 | 22.52 |
| 대표이사 | 김도형 | 1,637,448 | 21.40 |
| (단위 : 백만원) | |||
| 해당 사업연도 | 2020 | 결산기 | 12월 |
| 자산총계 | 74,215 | 자본금 | 762 |
| 부채총계 | 19,191 | 매출액 | 58,520 |
| 자본총계 | 55,024 | 당기순손익 | 8,589 |
| 외부감사인 | 동현회계법인 | 휴업 여부 | 아니오 |
| 감사의견 | 적정 | 폐업 여부 | 아니오 |
| 2. 상대방과의 관계 | |||
| 1. 회사와 상대방과의 관계 | - | ||
| 2. 회사의 최대주주ㆍ임원과 상대방과의 관계 | 성명 | 상대방과의 관계 | |
| - | - | - | |
| 3. 최근 3년간 거래내역(일상적 거래 제외) | |||
| 구분 | 거래 내역 | ||
| 당해년도 | - | ||
| 전년도 | - | ||
| 전전년도 | - | ||
| (자료: 금융감독원 전자공시시스템) |
당사는 "리보세라닙"이라는 표적항암제와 해외 자회사들의 항암제 파이프라인 등 당사와 자회사의 신약물질에 대하여 FDA 임상을 진행하고, 신약 물질을 개발하기 위한 연구를 지속하고 있으며, 오픈이노베이션을 표방하는 당사의 HBS(HLB Bio System) 구축의 일환으로 ㈜노터스의 인수를 결정하게 되었습니다. 특히 ㈜노터스는 비임상 CRO를 사업으로 영위하는 국내 1위 업체로, 당사에서는 ㈜노터스의 인수를 통하여 임상프로세스에 필요한 비임상 CRO 분야를 확보를 통한 HBS 구축 및 그룹 내 바이오회사와의 시너지효과를 기대하였습니다. 또한, 부채비율 35% 및 안정적인 영업이익을 확보하고 있는 측면도 인수 사유 중 하나입니다. 향후 당사의 글로벌 네트워크를 통하여 해외 CRO사업으로 진출할 것이며, 당사 해외 자회사의 비임상 CRO를 수행함으로써 그룹 내 시너지를 기대하고 있습니다. 또한 비임상 CRO 사업을 통하여 우수한 바이오 스타트업 회사를 초기부터 발굴할 수 있으며, 우수한 바이오 스타트업 회사를 대상으로 당사의 펀딩을 진행해 HBS로의 편입을 위한 투자도 진행할 계획입니다. 또한 ㈜노터스의 또다른 사업분야인 동물바이오 분야와 반려동물 사업분야에 추가 투자를 통하여 성장하고 있는 Pet Healthcare 시장의 진입도 검토중에 있습니다.
㈜노터스는 당사의 임원 및 최대주주와 직접적인 거래관계 및 인적관계 등 특별한 관계가 존재하지 않으나, 당사의 지분 1.31%를 보유한 관계기업인 에이치엘비생명과학㈜와 비임상CRO와 관련된 거래내역이 있습니다. 에이치엘비생명과학㈜와 ㈜노터스의 최근 3년간 거래내역은 아래와 같습니다.
| 에이치엘비생명과학㈜와 ㈜노터스의 최근 3년간 거래내역] | |
| (단위 : 원) | |
| 날짜 | 내용 | 금액 |
|---|---|---|
| 2020/09/04 | 리보세라닙 안구건조증 효력시험 1차 | 2,400,000 |
| 2020/09/15 | 리보세라닙 안구건조증 효력시험 2차 | 10,000,000 |
| 2020/09/18 | 리보세라닙 약물농도 측정시험 1차 | 18,000,000 |
| 2020/10/20 | 리보세라닙 약물농도 측정시험 2차 | 18,000,000 |
| 2020/10/27 | 리보세라닙 혈장 중 농도 분석시험 (1회/2회) | 10,000,000 |
| 2020/11/10 | 리보세라닙 황반변성 점안효과시험 (1차/4차) | 6,000,000 |
| 2020/11/10 | 리보세라닙 황반변성 점안효과시험 (2차/4차) | 8,000,000 |
| 2020/11/24 | 리보세라닙 안구건조증 효력시험 3차 | 7,300,000 |
| 2020/12/11 | 리보세라닙 약물농도 측정시험 3차 | 24,000,000 |
| 2020/12/23 | 리보세라닙 황반변성 점안효과시험 (3차/4차) | 8,000,000 |
| 2020/12/29 | 리보세라닙 안구건조증 효력시험 4차 | 7,300,000 |
| 2021/02/01 | 리보세라닙 황반변성 점안효과시험 (4차/4차) | 9,900,000 |
| 2021/02/01 | 리보세라닙 혈장 중 농도 분석시험 (2회/2회) | 23,000,000 |
| 2021/06/03 | 리보세라닙 황반변성 안구농도분석시험 (1차/2차) | 6,600,000 |
| 2021/07/01 | 리보세라닙 황반변성 안구농도분석시험 (2차/2차) | 6,600,000 |
| 2021/09/15 | 리보세라닙 경구용 동물용 항암제 위탁연구비 (1차/4차) | 35,000,000 |
㈜노터스 지분 18.37%에 대한 당사의 취득대금은 562.26억원으로, 당사는 이촌회계법인에 주식양수가액 적정성에 대한 평가를 의뢰하였습니다. 그럼에도 불구하고 투자자들께서는 이촌회계법인이 양수가격 평가의견서에서 제시하는 평가대상회사의 주식가치의 평가 결과는 미래예측에 따른 근본적인 한계가 존재하며, 평가대상회사의 절대적인 가치를 의미하는 것은 아니라는 점에 유의하시기 바랍니다.
이촌회계법인은 ㈜노터스의 가치 평가를 위하여 현금흐름할인법(DCF; Discounted Cash Flow Approach)을 적용하였습니다. 현금흐름할인법(DCF)은 해당 기업의 미래순현금흐름 (FCF) 및 잔존가치 (TV)를 추정 후 할인율 (WACC)을 사용하여 현재 시점의 기업가치를 추정 하는 방법으로, 이론적으로는 가장 우수한 방법 중 하나로 꼽히고 있습니다. 다만, 기업가치를 결정하는 요소인 미래순현금흐름(FCF), 할인율(WACC), 잔존가치(Terminal Value) 등의 결정시 평가자의 전문가적 판단이 요구되는 방법입니다. 전문가적 판단은 지극히 주관적일 수 있으며, 미래 가치나 할인율, 잔존가치는 언제까지나 현재시점에서 예상하는 합리적인 추정치를 사용한 것으로 향후 실제의 가치와는 차이가 발생할 수 있습니다.
투자자들께서는 당사의 ㈜노터스의 지분 18.37% 양수가격 562.26억원이 미래 추정치에 근거한 가격임에 유의하시고, 해당 추정치는 전문가의 주관적 판단의 개입의 여지가 있음에 유의하시기 바랍니다.
이촌회계법인이 추정한 ㈜노터스의 주요 손익 등은 다음과 같습니다.
| [㈜노터스 추정 주요 손익 등] |
| (단위: 백만원) |
| 구 분 | 추정 | |||||
|---|---|---|---|---|---|---|
| 2021년 | 2022년 | 2023년 | 2024년 | 2025년 | 영구현금흐름구간(*3) | |
| 영업수익 | 59,929 | 69,114 | 79,735 | 92,022 | 106,244 | 106,244 |
| 영업비용 | 44,112 | 48,668 | 53,246 | 59,238 | 66,158 | 66,158 |
| 영업이익 | 15,817 | 20,446 | 26,489 | 32,784 | 40,086 | 40,086 |
| 법인세 | 3,458 | 4,486 | 5,948 | 7,472 | 9,239 | 9,239 |
| 세후영업이익( | 12,359 | 15,960 | 20,541 | 25,312 | 30,847 | 30,847 |
| (+)상각비 | 2,025 | 2,025 | 2,025 | 2,025 | 2,025 | - |
| (±)순운전자본 | (8,678) | (1,228) | (1,276) | (1,614) | (1,862) | - |
| (-)CAPEX | 2,025 | 2,025 | 2,025 | 2,025 | 2,025 | - |
| 잉여현금흐름 | 3,681 | 14,732 | 19,265 | 23,698 | 28,985 | 30,847 |
| 현가계수 | 0.9535 | 0.8670 | 0.7883 | 0.7168 | 0.6518 | 0.6518 |
| 현재가치 | 3,509 | 12,773 | 15,186 | 16,987 | 18,893 | 223,893 |
| 산출결과 요약 | ||||||
| 추정기간 현재가치(A) | 67,348 | |||||
| 영구기간 현재가치(B) | 223,893 | |||||
| 영업가치(C=A+B) | 291,241 | |||||
| 비영업자산(D) | 29,783 | |||||
| 기업가치(E=C+D) | 321,024 | |||||
| 이자부부채의 가치(F) | 14,690 | |||||
| 자기자본 가치(G=E-F) | 306,334 | |||||
| 평가기준일 현재 보통주 발행주식 총수 | 7,651,868 | |||||
| 평가대상자산의 주당 가치(원) | 40,034 | |||||
| 자료: | 이촌회계법인 |
이촌회계법인은 추정한 손익을 바탕으로 평가기준일인 2021년 12월 31일 기준 평가대상회사의 주당 가치를 33,509원에서 50,241원의 범위로 산출했고, 실제 양수도 가액 주당 40,034원은 상기 평가액의 범위를 고려할 때 중요성의 관점에서 부적정하다고 판단할 만한 근거가 발견되지 아니하였다고 판단됩니다. 그러나, 투자자들께서는 평가법인 이촌회계법인의 해당 양수가격 적정성 평가는 해당 기업의 절대적인 가치를 제시하거나 보증하는 것이 아니라, 합리적으로 추정된 양수도가액의 범위 내에서 해당 양수도가액의 적정성을 검증하는 것임에 유의하시기 바랍니다.
또한, 평가의견서에 기술된 절차는 일반적인 회계감사기준에 따른 감사절차가 아니므로 평가인은 본 의견서에 포함된 내용에 대하여 감사의견을 표명하지 아니하며, 평가대상회사의 재무상태와 경영성과에 대한 어떠한 형태의 보증도 제공하지 아니합니다. 만약, 회계감사기준에 따른 추가적인 감사절차를 수행하였다면, 본 의견서에 언급되지 아니한 추가적인 발견사항, 변경사항 또는 기타 예외사항이 발견되었을 수도 있습니다.
[업체의 개요 및 사업현황]
㈜노터스는 신약 등 신규 개발 물질에 대한 비임상 실험을 진행하는 비임상CRO를 주된 사업으로 영위하고 있습니다. ㈜노터스는 질병치료를 목적으로 하는 의약품 개발과정에 있어서 실험동물을 대상으로 물질을 테스트하는 비임상 CRO를 통해 수익을 확보하고 있으며, 비임상 CRO 사업과 연계해 LAB 컨설팅 사업, 반려동물 용품 공급 및 수의사 교육센터 건립을 통해 사업다각화를 진행할 예정입니다. ㈜노터스의 기업개요 및 2019년부터 2022년 1분기까지 주요 재무현황은 다음과 같습니다.
| [㈜노터스 기업개황] |
| 구 분 | 내 용 | |
|---|---|---|
| 회사명 | ㈜노터스 | |
| 대표이사 | 문정환, 김도형(각자 대표) | |
| 최대주주 | 에이치엘비㈜(18.04%) 및 에이치엘비테라퓨틱스㈜(2.29%) | |
| 주소 | 본사 | 인천광역시 연수구 아카데미로79번길 38 |
| 연락처 | 032-833-8899 | |
| 주요사업 | 의학 및 약학 연구개발업 | |
| 설립연월 | 2012년 04월 | |
| 결산일 | 12월 | |
| 법인구분 | 코스닥시장 상장법인 | |
| 상장연월 | 2019년 11월 | |
| [주요 재무사항 총괄표] | |
| (K-IFRS, 연결 및 별도) | (단위: 백만원, %) |
| 결산연월 또는 결산기간 | 2022년 1분기 | 2021년 | 2020년 | 2019년 | ||||
|---|---|---|---|---|---|---|---|---|
| 구 분 | 연결 | 별도 | 연결 | 별도 | 연결 | 별도 | 연결 | 별도 |
| 외부감사인의 감사의견 | - | - | 적정 | 적정 | 적정 | 적정 | 적정 | 적정 |
| (계속기업으로서의 불확실성 관련 의견표명 및 주석사항 여부) |
(-) | (-) | (-) | (-) | (-) | (-) | (-) | (-) |
| 1. 자산총계 | 178,247 | 171,252 | 93,402 | 87,372 | 74,215 | 69,885 | 61,531 | 57,879 |
| - 유동자산 | 112,807 | 106,443 | 29,609 | 23,605 | 28,579 | 24,983 | 29,228 | 25,936 |
| 2. 부채총계 | 106,566 | 103,755 | 28,265 | 26,211 | 19,191 | 17,726 | 18,508 | 17,057 |
| - 유동부채 | 43,277 | 41,145 | 16,582 | 15,052 | 15,379 | 14,408 | 12,090 | 11,075 |
| 3. 자본총계 | 71,681 | 67,497 | 65,137 | 61,161 | 55,024 | 52,159 | 43,023 | 40,822 |
| 4. 부채비율 (%) | 148.67 | 153.72 | 43.39 | 42.86 | 34.88 | 33.98 | 43.02 | 41.78 |
| 5. 유동비율 (%) | 260.66 | 258.71 | 178.56 | 156.83 | 185.83 | 173.40 | 241.76 | 234.18 |
| 6. 매출액 | 17,917 | 12,467 | 64,403 | 47,004 | 58,520 | 43,576 | 46,040 | 32,453 |
| 7. 영업이익 | 2,163 | 1,721 | 9,823 | 8,544 | 8,841 | 8,018 | 6,733 | 5,672 |
| 기타 손익 | 62 | 58 | 2,164 | 1,923 | (1,759) | (1,764) | (1,239) | (1,180) |
| 금융 손익 | (649) | (632) | (206) | (213) | 2,446 | 2,440 | (118) | (104) |
| 8. 당기순이익 | 1,057 | 707 | 10,308 | 9,077 | 8,589 | 7,860 | 4,554 | 3,745 |
| 9. 자본금 | 779 | 779 | 765 | 765 | 762 | 762 | 732 | 732 |
| 10. 영업활동 현금흐름 | 1,902 | 1,857 | 8,463 | 7,693 | 11,464 | 10,758 | 5,182 | 4,351 |
| 11. 투자활동 현금흐름 | (83,184) | (82,613) | (19,568) | (19,713) | (7,744) | (7,595) | (15,848) | (15,767) |
| 12. 재무활동 현금흐름 | 81,570 | 81,589 | 9,212 | 9,412 | (877) | (724) | 12,945 | 12,681 |
| 13. 현금 및 현금성자산 기말 잔고 | 6,451 | 4,943 | 6,158 | 4,106 | 8,040 | 6,704 | 5,618 | 4,271 |
| 자료 : | ㈜노터스 정기보고서 |
상기 기재한 바와 같이 당사는 2022년 01월 27일 ㈜노터스의 최대주주로부터 구주 1,405,648주에 대한 인수계약을 체결한 바 있으며, 2022년 03월 30일 ㈜노터스는 당사의 관계기업으로 편입되었습니다. 이에 따라 당사는 바이오사업의 리보세라닙 편중 현상을 해결하고 ㈜노터스를 통해 비임상CRO시너지 및 동물 바이오사업의 진출을 기대하고 있으나, ㈜노터스의 사업 성과에 따라 영업 변동성은 확대될 가능성이 있습니다. ㈜노터스의 경우 최근 4개년 사업연도 동안 지속적으로 영업이익과 당기순이익이 발생하고 있으나, 유효성 비임상 CRO를 주력으로하는 회사의 특성상 해외기업과의 경쟁 심화와 관련한 불확실성이 있기 때문에 당사의 실적에 부정적인 영향을 미칠 가능성 또한 있습니다.
② ㈜에프에이
[지분취득 경위]
2021년 10월 20일, 당사는 안정적인 재무수익 창출 및 재무리스크 해소를 위해 2021년 10월 21 ㈜에프에이의 기존 주주 남윤제, 길영희, 박명숙으로부터 구주 28,000주(100.00%)를 취득하는 계약을 체결하였습니다. 이에 따라 당사는 현금 44,920백만원 및 신주인수권부사채 대용납입(상계) 57,000백만원 등 총 인수금액 101,920백만원을 지급하였으며, 이는 2020년 당사의 연결기준 자산총액 대비 14.43%에 해당하는 타법인 주식 양수입니다. 이와 관련한 2021년 10월 21일의 공시는 다음과 같습니다.
| [타법인주식및출자증권양수결정](2021.10.21) |
| 1. 발행회사 | 회사명 | 주식회사 에프에이 | |||
| 국적 | 대한민국 | 대표자 | 남윤제 | ||
| 자본금(원) | 400,000,000 | 회사와 관계 | - | ||
| 발행주식 총수(주) |
28,000 | 주요사업 | 의료용품 및 기타 의약관련제품 제조업 | ||
| - 최근 6월 이내 제3자 배정에 의한 신주취득 여부 |
아니오 | ||||
| 2. 양수내역 | 양수주식수(주) | 28,000 | |||
| 양수금액(원)(A) | 101,920,000,000 | ||||
| 총자산(원)(B) | 706,477,276,989 | ||||
| 총자산대비(%)(A/B) | 14.43 | ||||
| 자기자본(원)(C) | 557,429,418,586 | ||||
| 자기자본대비(%)(A/C) | 18.28 | ||||
| 3. 양수후 소유주식수 및 지분비율 | 소유주식수(주) | 28,000 | |||
| 지분비율(%) | 100.00 | ||||
| 4. 양수목적 | 안정적인 재무수익 창출 및 향후 예정된 바이오 사업과의 시너지 극대화 | ||||
| 5. 양수예정일자 | 2021년 10월 20일 | ||||
| 6. 거래상대방 | 회사명(성명) | 남윤제 외 2인 (매도자별 세부내역은 14. 기타 투자판단과 관련된 중요사항 참조) |
|||
| 자본금(원) | - | ||||
| 주요사업 | - | ||||
| 본점소재지(주소) | 세종특별자치시 다정남로 (매도자별 소재지는 하단의 거래상대방에 관한 사항 참조) |
||||
| 회사와의 관계 | 주요주주 | ||||
| 7. 거래대금지급 | 1) 지급형태 : - 현금 지급 및 신주인수권부사채 발행 지급 2) 지급시기 - 현금 : 2021년 10월 20일(계약체결일)에 44,920백만원 지급 - 신주인수권부사채 발행 : 당사가 발행하는 제 34회차 신주인수권부 사채의 권면총액 57,000백만원 대용납입(상계) 3) 자금조달 방법 : - 자체 보유 현금 및 제 34회차 신주인수권부사채 발행 지급 |
||||
| 8. 외부평가에 관한 사항 | 외부평가 여부 | 예 | |||
| - 근거 및 사유 | "자본시장과금융투자업에관한법률 제161조 및 동법 시행령 제171조"에 따라 주식의 양수가액의 적정성 평가 | ||||
| 외부평가기관의 명칭 | 삼도회계법인 | ||||
| 외부평가 기간 | 2021년 09월 27일 ~ 2021년 10월 19일 | ||||
| 외부평가 의견 | 평가기준일 현재 평가대상자산의 주식가치 평가액은 99,364백만원 ~ 109,167백만원의 범위로 산출되었으며, 양수 예정가액은 101,920백만원으로 중요성의관점에서 부적정하다고 판단할 만한 근거가 발견되지 아니하였습니다. | ||||
| 9. 이사회결의일(결정일) | 2021년 10월 20일 | ||||
| - 사외이사참석여부 | 참석(명) | 3 | |||
| 불참(명) | 0 | ||||
| - 감사(사외이사가 아닌 감사위원) 참석여부 | 불참 | ||||
| 10. 우회상장 해당 여부 | 아니오 | ||||
| - 향후 6월이내 제3자배정 증자 등 계획 | 아니오 | ||||
| 11. 발행회사(타법인)의 우회상장 요건 충족여부 | 아니오 | ||||
| 12. 공정거래위원회 신고대상 여부 | 미해당 | ||||
| 13. 풋옵션 등 계약 체결여부 | 아니오 | ||||
| - 계약내용 | - | ||||
|
* 본건의 주식양수는 안정적인 재무수익 창출 및 향후 예정된 바이오 사업과의 시너지 극대화를 위하여 주식회사 에프에이보통주식 28,000주를 취득하는 건이며, 본 건 발행회사의 구주 취득완료시 주식회사 에프에이의 100% 지분을 확보할 예정입니다. 1) 상기 '1. 발행회사의 자본금 및 발행주식의 총수'는 본 보고서의 제출일 2021년 10월 20일 현재기준입니다.
(주1) 본 보고서 제출일(2021.10.20) 현재 상기 기재된 거래상대방(매도자 3명)과 당사와의 특별한 이해관계가 없습니다.
※ 당해연도는 2020년, 전년도는 2019년, 전전년도는 2018년으로, 2020년 기준 외부감사대상 법인이나, 2019년, 2018년은 외부감사를 받지 않은 재무정보입니다. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| (자료: 금융감독원 전자공시시스템) |
당사는 "리보세라닙" 표적항암제와 해외 자회사들의 항암제 파이프라인 등 당사와 자회사의 신약물질에 대하여 FDA 임상을 진행하고, 신약물질을 개발하기 위한 연구를지속하고 있는 바이오 기업으로서 당사와의 사업적인 시너지 효과의 창출과, 당사의 취약점인 재무구조를 보완할 수 있는 대안으로써 ㈜에프에이의 인수를 결정하게 되었습니다.
㈜에프에이는 2008년 5월에 설립되어 알코올 스왑 등 손소독제, 소독티슈 등을 생산하던 회사이며, COVID-19의 등장과 확산으로 인하여 진단키트 수요가 폭발적으로 증가함에 따라 매출이 증가한 회사입니다. 당사는 ㈜에프에이가 유럽의 CE1639(체외진단의료기기, SGS) 인증을 보유하고 있으며, 검체체취용 도구(검체수송배지, 면봉)의 수요가 급격히 늘어남에 따라 매출이 2018년 87억에서 2020년 619억원으로 크게 성장한 점에 주목했습니다. 당사는 ㈜에프에이의 인수를 통해 헬스케어 분야로 사업을 확장하고 지속적인 Cash-Cow를 확보할 수 있을 것으로 판단하여 인수 및 합병을 결정하였으며, 당사의 자회사 및 계열사와 마케팅 측면에서도 바이오 밸류체인을 공유함으로써 시너지효과를 기대하였습니다. 당사는 인수 및 합병 이후 동사(現 헬스케어사업부)를 체외진단분야의 전문 기업으로 육성하여 해외의 신규시장으로의 진입을 시도할 것이며, 코로나 외 다른 분야로 사업을 확장시켜나갈 계획입니다.
㈜에프에이는 당사의 현 최대주주 및 임원진이 사업다각화 진행 과정에서 파악한 회사로, 당사의 최대주주 및 임원과는 과거 거래관계 및 인적관계 등 특별한 관계가 존재하지 않습니다.
㈜에프에이 지분 100%에 대한 당사의 취득대금은 1,019.2억원으로, 당사는 삼도회계법인에 주식양수가액 적정성에 대한 평가를 의뢰하였습니다. 그럼에도 불구하고 투자자들께서는 삼도회계법인이 양수가격 평가의견서에서 제시하는 평가대상회사의 주식가치의 평가 결과는 미래예측에 따른 근본적인 한계가 존재하며, 평가대상회사의 절대적인 가치를 의미하는 것은 아니라는 점에 유의하시기 바랍니다.
삼도회계법인은 ㈜에프에이의 가치 평가를 위하여 현금흐름할인법(DCF; Discounted Cash Flow Approach)을 적용하였습니다. 현금흐름할인법(DCF)은 해당 기업의 미래순현금흐름 (FCF) 및 잔존가치 (TV)를 추정 후 할인율 (WACC)을 사용하여 현재 시점의 기업가치를 추정 하는 방법으로, 이론적으로는 가장 우수한 방법 중 하나로 꼽히고 있습니다. 다만, 기업가치를 결정하는 요소인 미래순현금흐름(FCF), 할인율(WACC), 잔존가치(Terminal Value) 등의 결정시 평가자의 전문가적 판단이 요구되는 방법입니다. 전문가적 판단은 지극히 주관적일 수 있으며, 미래 가치나 할인율, 잔존가치는 언제까지나 현재시점에서 예상하는 합리적인 추정치를 사용한 것으로 향후실제의 가치와는 차이가 발생할 수 있습니다.
투자자들께서는 당사의 ㈜에프에이의 지분 100% 양수가격 1,019.2억원이 미래 추정치에 근거한 가격임에 유의하시고, 해당 추정치는 전문가의 주관적 판단의 개입의 여지가 있음에 유의하시기 바랍니다.
삼도회계법인이 추정한 ㈜에프에이의 주요 손익 등은 다음과 같습니다.
| [㈜에프에이 추정 주요 손익 등] |
| (단위: 백만원) |
| 구 분 | 실적 | 추정 | |||||
|---|---|---|---|---|---|---|---|
| 2021년 8월 | 2021년 4분기 | 2022년 | 2023년 | 2024년 | 2025년 | Terminal | |
| 매출 | 92,728 | 45,032 | 82,535 | 50,764 | 35,729 | 38,184 | 38,566 |
| 매출원가 | 46,813 | 23,524 | 51,785 | 31,929 | 22,739 | 23,969 | 24,209 |
| 매출총이익 | 45,915 | 21,508 | 30,750 | 18,836 | 12,990 | 14,215 | 14,357 |
| 판매관리비 | 6,852 | 8,580 | 5,776 | 4,052 | 3,480 | 3,390 | 3,424 |
| 영업이익 | 39,064 | 12,929 | 24,975 | 14,784 | 9,510 | 10,825 | 10,933 |
| Tax | 2,225 | 5,582 | 3,230 | 2,070 | 2,359 | 2,383 | |
| 세후 영업이익 | 10,704 | 19,393 | 11,553 | 7,440 | 8,465 | 8,550 | |
| Adjustment | 4,207 | 8,105 | 5,015 | 2,479 | -807 | -61 | |
| 잉여현금흐름 | 14,911 | 27,498 | 16,568 | 9,919 | 7,658 | 8,489 | |
| 가. 영업가치 | 87,117 | ||||||
| 나. 비영업용 자산 | 16,618 | ||||||
| 다. 기업가치(다 = 가 + 나) | 103,734 | ||||||
| 라. 이자발생부채 | - | ||||||
| 마. 주식가치(마 = 다 - 라) | 103,734 | ||||||
| 자료 : | 삼도회계법인 |
삼도회계법인은 추정한 손익을 바탕으로 평가기준일인 2021년 08월 31일 기준 평가대상회사의 총 주식가치 평가액을 99,364백만원에서 109,167백만원(주당 3,548,714원에서 3,898,821원)의 범위로 산출하였습니다. 삼도회계법인은 양수대상주식의 가치(지분 100.0%)는 99,364백만원에서 109,167백만원의 범위로 산출한 바, 실제 양수도 예정가액은 101,920백만원(주당 3,640,000원)으로 상기 평가액의 범위를 고려할 때 중요성의 관점에서 부적정하다고 판단할 만한 근거가 발견되지 아니하였다고 판단하였습니다. 그러나, 투자자들께서는 평가법인 삼도회계법인의 해당 양수가격 적정성 평가는 해당 기업의 절대적인 가치를 제시하거나 보증하는 것이 아니라, 합리적으로 추정된 양수도가액의 범위 내에서 해당 양수도가액의 적정성을 검증하는 것임에 유의하시기 바랍니다.
[업체의 개요 및 사업현황]
㈜에프에이는 의료용품 및 체외진단 의료키트 등 의약관련제품의 제조 및 판매사업을 영위했습니다. 당사는 ㈜에프에이의 지분 100%를 양수한 이후 2021년 10월 26일 이사회를 통해 당사의 ㈜에프에이 흡수합병을 결정했으며, 2022년 01월 01일을 기준으로 합병이 완료되어, ㈜에프에이는 당사의 헬스케어사업부로 편입되었습니다.해당 합병과 관련한 공시는 아래와 같습니다.
| [회사합병결정](2021.10.26) |
| 1. 합병방법 | 에이치엘비㈜가 ㈜에프에이를 흡수합병 -존속회사: 에이치엘비(주) -소멸회사 : ㈜에프에이 |
|||||
| - 합병형태 | 소규모합병 | |||||
| 2. 합병목적 | 안정적인 수익창출을 통한 재무안정성 구축 및 향후 예정된 바이오 사업과의 시너지극대화 | |||||
| 3. 합병의 중요영향 및 효과 | 1) 회사의 경영에 미치는 영향 본 보고서 제출일 현재 합병법인인 에이치엘비㈜는 피합병법인인 ㈜에프에이의 발행주식을 100% 소유하고 있으며, 합병신주를 발행하지 않는 무증자 합병으로 진행합니다. 본 합병 완료 시 에이치엘비㈜는 존속회사로 계속 남아있고 소멸회사인 ㈜에프에이는 합병 후 해산하게 되며, 본 합병 완료 후 에이치엘비㈜의 최대주주 변경은 없습니다. 2) 회사의 재무 및 영업에 미치는 영향 본 합병을 통해 합병법인인 에이치엘비㈜는 피합병법인 ㈜에프에이를 종속회사로 유지함에 따른 안정적인 수익창출을 통한 재무안정성 구축 및 향후 예정된 바이오 사업과의 시너지극대화가 예상됩니다. |
|||||
| 4. 합병비율 | 에이치엘비㈜ : ㈜에프에이 = 1.0000000 : 0.0000000 | |||||
| 5. 합병비율 산출근거 | 존속회사인 에이치엘비㈜는 소멸회사인 ㈜에프에이의 지분 100%를 소유하고 있으며, 합병시 존속회사는 소멸회사의 주식에 대해 신주를 발행하지 않으므로 합병비율을 1:0.0000000으로 산출하였습니다. | |||||
| 6. 외부평가에 관한 사항 | 외부평가 여부 | 미해당 | ||||
| - 근거 및 사유 | 「 자본시장과 금융투자업에 관한 법률」제165조의4 및 동법 시행령 제176조의5 제7항 제2호 나목 단서에 의하여 다른 회사의 발행주식 총수를 소유하고 있는 회사가 그 다른 회사를 합병하면서 신주를 발행하지 않는 경우에는 합병가액의 적정성에 대한 외부평가기관의 평가를 요구하지 않는 것으로 규정하고 있는 바, 본 합병은 이에 해당하므로 위 규정에 따라 외부평가기관의 평가를 거치지 아니하였습니다. | |||||
| 외부평가기관의 명칭 | - | |||||
| 외부평가 기간 | - | |||||
| 외부평가 의견 | - | |||||
| 7. 합병신주의 종류와 수(주) | 보통주식 | - | ||||
| 종류주식 | - | |||||
| 8. 합병상대회사 | 회사명 | ㈜에프에이 | ||||
| 주요사업 | 의료용품 및 기타 의약관련제품 제조업 | |||||
| 회사와의 관계 | 자회사 | |||||
| 최근 사업연도 재무내용(원) | 자산총계 | 53,494,129,389 | 자본금 | 400,000,000 | ||
| 부채총계 | 40,086,376,365 | 매출액 | 61,936,984,355 | |||
| 자본총계 | 13,407,753,024 | 당기순이익 | 12,034,508,675 | |||
| - 외부감사 여부 | 기관명 | 안세회계법인 | 감사의견 | 적정 | ||
| 9. 신설합병회사 | 회사명 | - | ||||
| 설립시 재무내용(원) | 자산총계 | - | 부채총계 | - | ||
| 자본총계 | - | 자본금 | - | |||
| - | 현재기준 | |||||
| 신설사업부문 최근 사업연도 매출액(원) | - | |||||
| 주요사업 | - | |||||
| 재상장신청 여부 | 해당사항없음 | |||||
| 10. 합병일정 | 합병계약일 | 2021년 10월 28일 | ||||
| 주주확정기준일 | 2021년 11월 11일 | |||||
| 주주명부 폐쇄기간 |
시작일 | 2021년 11월 12일 | ||||
| 종료일 | 2021년 11월 18일 | |||||
| 합병반대의사통지 접수기간 | 시작일 | 2021년 11월 11일 | ||||
| 종료일 | 2021년 11월 25일 | |||||
| 주주총회예정일자 | - | |||||
| 주식매수청구권 행사기간 |
시작일 | - | ||||
| 종료일 | - | |||||
| 구주권 제출기간 |
시작일 | - | ||||
| 종료일 | - | |||||
| 매매거래 정지예정기간 | 시작일 | - | ||||
| 종료일 | - | |||||
| 채권자이의 제출기간 | 시작일 | 2021년 11월 30일 | ||||
| 종료일 | 2021년 12월 31일 | |||||
| 합병기일 | 2022년 01월 01일 | |||||
| 종료보고 총회일 | 2022년 01월 03일 | |||||
| 합병등기예정일자 | 2022년 01월 04일 | |||||
| 신주권교부예정일 | - | |||||
| 신주의 상장예정일 | - | |||||
| 11. 우회상장 해당 여부 | 해당사항없음 | |||||
| 12. 타법인의 우회상장 요건 충족여부 | 해당사항없음 | |||||
| 13. 주식매수청구권에 관한 사항 | 행사요건 | 「상법」제527조의 3 규정에 의거한 소규모합병절차에 따라 진행되는 바, 에이치엘비㈜의 주주에게 주식매수청구권을 부여하지 않습니다 | ||||
| 매수예정가격 | - | |||||
| 행사절차, 방법, 기간, 장소 | - | |||||
| 지급예정시기, 지급방법 | - | |||||
| 주식매수청구권 제한 관련 내용 | - | |||||
| 계약에 미치는 효력 | - | |||||
| 14. 이사회결의일(결정일) | 2021년 10월 26일 | |||||
| - 사외이사참석여부 | 참석(명) | - | ||||
| 불참(명) | - | |||||
| - 감사(사외이사가 아닌 감사위원) 참석여부 | - | |||||
| 15. 풋옵션 등 계약 체결여부 | 아니오 | |||||
| - 계약내용 | - | |||||
| 16. 증권신고서 제출대상 여부 | 아니오 | |||||
| - 제출을 면제받은 경우 그 사유 | 합병은 합병신주를 발행하지 않는 무증자합병 방식으로 진행하므로, 본 합병의 과정에서는 증권신고서 제출이 필요한 증권의 모집이나 매출이 이루어지지 않습니다. | |||||
|
17. 기타 투자판단에 참고할 사항 1) 본 합병은 「상법」제527조의3 규정에 의한 소규모합병방식이므로 주식매수청구권이 인정되지 않으며 합병승인은 이사회 승인으로 갈음합니다. (7) 상기 10.'합병일정'은 현재시점에서의 예상 일정이며, 관련법령상의 인허가, 승인 및 관계기관과의 협의과정 등에 의해 변경될 수 있습니다. |
||||||
인수 및 합병 전 ㈜에프에이의 2019년부터 2021년까지 주요 재무현황은 다음과 같습니다.
| [주요 재무사항 총괄표] | |
| (K-IFRS, 별도) | (단위: 백만원, %, 배) |
| 결산연월 또는 결산기간 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|
| 외부감사인의 감사의견 | 적정 | 적정 | 적정 |
| (계속기업으로서의 불확실성 관련 의견표명 및 주석사항 여부) |
(-) | (-) | (-) |
| 1. 자산총계 | 70,499 | 53,494 | 13,316 |
| - 유동자산 | 49,901 | 41,333 | 2,603 |
| 2. 부채총계 | 21,336 | 40,086 | 11,102 |
| - 유동부채 | 21,336 | 35,598 | 5,471 |
| 3. 자본총계 | 49,163 | 13,408 | 2,213 |
| 4. 부채비율 (%) | 43.40 | 298.98 | 501.64 |
| 5. 유동비율 (%) | 233.88 | 116.11 | 47.57 |
| 6. 매출액 | 129,759 | 61,937 | 8,741 |
| 7. 영업이익 | 46,911 | 15,083 | 503 |
| 영업외수익 | 265 | 123 | 11 |
| 영업외비용 | 571 | 427 | 337 |
| 8. 당기순이익 | 35,755 | 12,035 | 170 |
| 9. 자본금 | 400 | 400 | 400 |
| 10. 영업활동 현금흐름 | 37,376 | 12,616 | 297 |
| 11. 투자활동 현금흐름 | (25,352) | (3,628) | (2,398) |
| 12. 재무활동 현금흐름 | (11,687) | 1,394 | 2,395 |
| 13. 현금 및 현금성자산 기말 잔고 | 11,013 | 10,676 | 295 |
| 자료 : | ㈜에프에이 감사보고서 |
상기 기재한 바와 같이 당사는 2021년 10월 21일 ㈜에프에이의 최대주주로부터 구주 28,000주에 대한 인수계약을 체결한 바 있으며, 2022년 01월 01일 ㈜에프에이는 당사에 합병되었습니다. 이에 따라 당사는 당사의 지속적인 영업손실에 따른 재무구조 악화 현상을 해결하고 헬스케어사업부의 제2공장 건립 및 사업 확장 통해 체외진단기기의 매출 다각화를 기대하고 있으나, COVID-19의 확산, 지속여부 및 신규 체외진단기기의 사업 성과에 따라 영업 변동성이 확대될 예정입니다. ㈜에프에이의 경우 합병전까지 최근 3개년 사업연도 동안 지속적으로 영업이익과 당기순이익이 발생했습니다. 다만, 코로나 채취용 도구 및 배지가 매출의 대부분을 차지하는 회사의 특성상 COVID-19의 확산여부와 경쟁 심화와 관련한 불확실성이 크기 때문에 향후 당사의 실적에 부정적인 영향을 미칠 가능성 또한 있습니다.
상기 기재한 바와 같이 당사는 사업다각화와 재무구조안정 등의 목적을 위해 과거부터 지속적을 타법인 출자를 진행하고 있으며, 추가적인 타법인 출자 및 자산양수도를위한 전환사채 및 신주인수권부사채 발행 등의 차입이 발생할 경우, 당사의 재무안정성에 부정적인 영향을 미칠 수 있습니다. 투자자 여러분들께서는 이 점을 반드시 유의하시기 바랍니다. 또한, 신규사업 추진 및 금융수익 창출을 위한 막대한 자금의 소요에도 불구하고, 신규사업 진행에 차질이 생기거나 투자한 금융자산에 평가 및 처분손실이 발생할 수 있습니다. 이 경우, 당사의 수익성이나 재무안정성이 악화될 수 있으며, 투자자께서는 이 점 유의하시기 바랍니다.
|
자. 신규 Pipeline 확보를 위한 타법인 지분 인수 관련 위험
|
자-1. Immunomic Therapeutics, Inc. 경영권지분 인수 관련
당사의 이사회는 2020년 2월 19일 이사회 결의를 통해 미국 메릴랜드주 소재 법인인Immunomic Therapeutics, Inc.(이하 Immunomic)의 지분 취득을 결정하였으며, 2020년 04월 30일 미화 3천만 달러(한화 35,643백만원)을 지불하고 제3자배정 유상증자에 참여하여 Immunomic의 지분율 31.08%를 보유한 대주주가 되었습니다. Immunomic Therapeutics, Inc.는 면역치료플랫폼기술을 활용하여 뇌종양치료제 임상 2상을 진행하고 있는 바이오의약품 연구개발기업입니다.
| [Immunomic 기업개황] |
| 구분 | 내용 |
|---|---|
| Office Location | 15010 Broschart Road Suite 250 Rockville, MD 20850 USA |
| 회사명 | Immunomic Therapeutics, Inc. |
| 설립년월 | 2005년 9월 |
| 자본금(주식수) | USD 2,995.55(보통주식수 26,555,609주/우선주식수 463,330주) |
| 홈페이지 | https://www.immunomix.com/ |
| 대표이사 | William G. Hearl |
| 상장여부 | 비상장 |
| 주요 주주현황 | HLB Co., Ltd.(41.07%, 최대주주), Hummel Affiliates(5.42%), Life Sciences Greenhouse of Central PA (4.00%), HLB Global Co., Ltd. (3.64%) William G. Hearl(2.95%), 기타주주(42.92%) |
| 주요 임원 (연구진) 현황 |
- William G. Hearl : 설립자, CEO - Teri Jones-Heiland : CSO - Eric Winzer : CFO - Robert Newman : CBO |
| 주요 치료제 | A. ITI-1000 (교모세포종) B. ITI-1001 (교모세포종) C. ITI-3000 (메르켈 피부암) |
| [Immunomic 연혁] |
| 일 자 | 내 용 |
|---|---|
| 2006년 | Johns Hopkins Univ.와 LAMP 기술에 대한 전세계 독점 라이선스 권리 취득 |
| 2006년 | Geron Corp.에 Sub-Licensed 부여 |
| 2006년 | Nature Tech.와 cross-license vaccine technologies 기술 공유 합의 |
| 2009년 | AML 연구의 GRNVAC1 결과가 Phase I / II endpoint 충족결과 발표 |
| 2010년 | 2010 Frost & Sullivan Award - 백신분야에서 올해의 생명공학혁신상 수상 |
| 2011년 | 동물 제약 분야 및 다수의 백신 라이선스 적용을 위해 대규모 제약회사와 공동 연구 및 라이센스 계약 체결 |
| 2012년 | FDA로부터 Jananese Red cedar immunotherapeutic vaccine 1상 임상 연구 승인 |
| 2012년 | LAMP-vax IP “키메라 백신” 특허에 대한 EU 특허 승인. JRC-LAMP-vax의 임상 연구 1상 착수 |
| 2012년 | LAMP-vax IP “키메라 백신” 특허 미국내 승인 |
| 2013년 | JRC-LAMP-vax에 대한 IA 단계 실험 성공적 완료 |
| 2014년 | 다양한 땅콩 알레르기에 대한 SBIR Grant 수상 |
| 2015년 | Astellas Pharma.와 알레르기 예방 및 치료를 위한 LAMP-VAX Platform관련 글로벌 라이센스 계약 체결 |
| 2017년 | Phase II Cancer Immunotherapy Technology의 독점 라이센스 발표 |
| 2018년 | LAMP-vax 플랫폼을 UNITE(UNiversal Intracellular Targeted Expression 범용세포내 표적발현)로 변경 |
| 2019년 | JRC2-LAMP-vax에 대해 Astellas 사로부터 5백만불의 Milestone 수령 |
| 2020년 | 에이치엘비(주)의 종속회사로 편입 |
| 2020년 | ITI-1000(교모세포종 치료를 위한 면역항암제) 생산을 위한 CoImmune과 파트너쉽 체결 |
| 2021년 | Lineage Cell Therapeutics 사와 면역항암제 라이선스 계약 체결 |
| 2021년 | 일본 적삼나무(Japanese Red Cedar) 알레르기 백신의 개발 및 상용화를 위해 IDRI (Infectious Disease Research Institute)와 RNA 백신 플랫폼의 지적재산권에 대한 전세계 독점 라이선스 계약 체결 |
| 2022년 | Drew Pardoll 연구소(JHU)와 activin antibody 특허 자산(및 개선사항) 관련 라이선스 계약 체결 |
| [Immunomic 요약재무상태표] | |
| (K-IFRS) | (단위: USD, %) |
| 결산연월 또는 결산기간 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|
| 1. 자산총계 | 47,519 | 67,220 | 21,005 |
| - 유동자산 | 31,331 | 47,546 | 12,825 |
| 2. 부채총계 | 13,080 | 11,933 | 15,515 |
| - 유동부채 | 5,065 | 3,773 | 3,556 |
| 3. 자본총계 | 34,439 | 55,287 | 5,490 |
| 4. 부채비율 (%) | 38.0% | 21.6% | 282.6% |
| 5. 유동비율 (%) | 618.5% | 1,260.2% | 360.6% |
| 6. 영업손익 | 2,028 | 27 | 12,006 |
| 기타 손익 | (300) | (78) | 223 |
| 금융 손익 | (499) | (395) | (620) |
| 7. 당기순이익 | (23,210) | (10,699) | (5,107) |
| 8. 자본금 | 3 | 3 | 1 |
| 9. 영업활동 현금흐름 | (18,644) | (15,754) | (6,308) |
| 10. 투자활동 현금흐름 | (4,459) | (2,854) | (413) |
| 11. 재무활동 현금흐름 | (10) | 53,002 | (363) |
| 12. 현금 및 현금성자산 기말 잔고 | 23,484 | 46,597 | 12,204 |
| 자료 : | Immunomic Therapeutics, Inc 감사보고서(삼일회계법인) |
| 주1) Immunomic은 외부감사 의무대상이 아니며, 회사 자체적으로 회계법인에 의뢰해 2021년 기준 최근 3개년 외부감사를 받았습니다. | |
당사는 Immunomic向 출자와 관련하여 주식 양수도가액의 적정성을 확인하기위하여 지암회계법인으로부터 Immunomic Therapeutics Inc.의 주식가치에 대한 기업가치평가보고서(평가기준일: 2019년 12월 31일)를 수령하였습니다. 그럼에도 불구하고 투자자들께서는 지암회계법인이 주식가치평가보고서에서 제시하는 평가대상회사의 주식가치의 평가 결과는 미래예측에 따른 근본적인 한계가 존재하며, 평가대상회사의 절대적인 가치를 의미하는 것은 아니라는 점에 유의하시기 바랍니다. 지암회계법인은 평가대상회사의 주식가치를 평가하기 위해 현금흐름할인법을 적용하였으며, 평가시 적용한 주요 가정은 다음과 같습니다.
| [평가시 적용된 주요 가정-외부평가기관의평가의견서(2020.01.20)] |
|
| [주식가치평가 주요 내용 요약-외부평가기관의평가의견서(2020.01.20)] |
| 구분 | 내용 |
|---|---|
| 영업수익 추정 | (1) 매출의 경우 3개의 카테고리(1) Allergy Licenses and Other, 2) Allergy Royalties 및 3) Oncology)로 이를 구분, 각 세부항목별 매출 예상금액을 추정하여 이를 반영하였습니다. 한편, 이와 같은 연도별 추정내역은 회사에서 제시한 Data를 기준으로 현재까지의 진행상황 및 실현가능성 여부 등을 감안해 이를 반영하였습니다. (2) Astellas사와 기존에 계약하고 있는 License-out과 관련해 선수수익의 계정과목으로 장부상 부채로 계상하고 있으며, 매년 일정액을 수익으로 인식 중에 있으나 해당 매출액의 경우 이미 회사측에 대규모 현금으로 유입된 바 있으며, 실현시기만을 조정하는 것에 불과한 바, 이를 매출액 추정 시 별도로 반영치는 아니하였습니다. (3) 추정 대상기간은 회사가 제시한 연도별 예상 손익자료 상 제시되어 있는 2020년 ~ 2037년까지의 18년을 대상기간으로 하여 이를 평가하였습니다. |
| 영업비용 추정 | (1) Nature Royalty 비용의 경우 회사가 인식하는 Allergy 로열티 금액의 2%를 지급하는 계약을 의미하고 있으며, Annias Royalty 비용의 경우 Oncology 매출액 중 GBM1000 프로젝트와 관련해 매년 수입액의 8.5%를 지급하는 내용을 의미합니다. 이와 더불어 매년 종양학 관련 수입액 중 25%의 금액(2024년의 경우 40%)이 추가적으로 지출될 예정에 있는 것으로 예상되는 바, 이를 영업비용으로 반영하여 평가하였습니다. (2) Clinical Trials 비용의 경우 매년 유입되는 종양학 관련 연구의 진행에 필수적으로 수반되는 임상비용으로 수입액의 25%가 매년 비용으로 투입되는 것을 가정해 이를 평가하였습니다. |
| 판매비와관리비 추정 | (1) General & Administrative 관련 비용의 경우 향후 종양학 관련 매출액이 가장 큰포션을 차지할 것인바, 해당 매출액의 5%가 매년 발생되는 것으로 가정해 이를 반영하였습니다. (2) R&D 관련 비용의 경우 회사가 매년 인식하는 총 매출액의 9%를 관련 비용의 발생으로 반영해 이를추정하였습니다. (3) 마케팅 관련 비용의 경우 매년 인식되는 종양학 관련 연구수입의 30%가 발생되는 것으로 이를 반영하였으며, 이는 관련 학회추진 관련 비용 및 신규 프로젝트 추진을 위한 Promotion 비용 등을 모두포함하는 것으로 이해할 수 있습니다. |
| 가중평균자본비용(WACC) 추정 | (1) 상기 가중평균자본비용 산출 시 자본구조(B/S)는 현재의 자본구조가 아니라 목표자본구조를 의미합니다. 그러나 현재 회사의 경우 사업구조 개편단계에 있으며, 현재 무부채 기업을 지향하고 있는 것으로 판단, 자본구조의 경우 타인자본이 없는 것으로 가정하여 이를 평가하였습니다. (2)적용 베타(β)의 경우 평가기준일 현재 회사와 유사한 업종을 영위하고 있는 미국 내 제약관련 상장회사 중 2개를 선택, 각 사의 시가총액을 기준으로 가중 평균한후 HAMADA Model에 따라 산정된 무부채기업 베타계수(1.308)을 회사의 Proxy Beta로 평가하였습니다. (3) 상기가정을 근거로 한 자기자본비용은 14.80%로써 이의 산출내역은 다음과 같습니다. Ke = 1.92% + 7.19% * 1.308 + 3.48% |
| 출처: 지암회계법인 주식가치 평가보고서 |
본 평가인인 지암회계법인은 현금흐름할인법을 적용하여 Immunomic Therapeutics Inc.을 평가한 결과, 평가기준일 당시 1주당 주식 가치의 범위는 USD 4.18 ~ USD 6.75의 범위에 있을 것으로 추정되었습니다.
| (단위: 천USD) |
| 구분 | 금액 |
|---|---|
| A. 추정기간 FCF의 현재가치 | 53,869 |
| B. 영구현금흐름의 현재가치 | 38,031 |
| C. 현금성자산 | 11,742 |
| D. 총기업가치(A+B+C) | 103,642 |
| E. 타인자본가치 | 7,014 |
| F. 자기자본가치(D-E) | 96,628 |
| G. 발행주식수 | 18,061,356주 |
| H. 평가대상회사의 주당 주식가치(F/G) | USD 5.34 |
| 출처: | 지암회계법인 주식 가치 평가 보고서 |
가중평균자본비용(WACC)를 변수로 하여 평가대상회사의 주식가치의 민감도분석을 수행한 결과는 다음과 같습니다.
| (단위: USD) |
| 구분 | WACC | ||
|---|---|---|---|
| 13.80% | 14.80% | 15.80% | |
| 총기업가치 | 128,871 | 103,642 | 82,518 |
| 타인자본가치 | 7,014 | 7,014 | 7,014 |
| 자기자본가치 | 121,857 | 96,628 | 75,504 |
| 주당 주식가치* | 6.75 | 5.34 | 4.18 |
| 출처: | 지암회계법인 주식가치 평가 보고서 |
| * 주당주식가치 = 발행주식총수 18,061,356주 기준 |
|
투자자들께서는 당사의 2020년 01월 31일, 2020년 04월 23일 및 2020년 12월 24일 Immunomic 지분 취득가격인 주당 5 USD가 미래 추정치에 근거한 가격임에 유의하시고, 해당 추정치는 전문가의 주관적 판단의 개입의 여지가 있음에 유의하시기 바랍니다.
당사가 동 지분 취득과 관련하여 금융감독원 전자공시시스템에 공시한 내용은 다음과 같습니다.
| [[정정]타법인주식및출자증권취득결정](2020.04.27) |
| 1. 발행회사 | 회사명(국적) | Immunomic Therapeutics,Inc. | 대표이사 | William G. Hearl |
| 자본금(원) | 1,444,585 | 회사와 관계 | 기타 | |
| 발행주식총수(주) | 12,923,463 | 주요사업 | 바이오의약품 개발 | |
| -최근 6월 이내 제3자 배정에 의한 신주취득 여부 | 아니오 | |||
| 2. 취득내역 | 취득주식수(주) | 6,000,000 | ||
| 취득금액(원) | 35,643,000,000 | |||
| 자기자본(원) | 485,628,745,774 | |||
| 자기자본대비(%) | 7.34 | |||
| 대기업 여부 | 해당 | |||
| 3. 취득후 소유주식수 및 지분비율 | 소유주식수(주) | 8,000,000 | ||
| 지분비율(%) | 31.08% | |||
| 4. 취득방법 | 현금취득(3자배정 유상증자 참여) | |||
| 5. 취득목적 | 지분 취득을 통한 기업가치극대화 | |||
| 6. 취득예정일자 | 2020-04-30 | |||
| 7. 자산양수의 주요사항보고서 제출대상 여부 | 아니오 | |||
| -최근 사업연도말 자산총액(원) | 304,040,778,357 | 취득가액/자산총액 (%) |
11.72 | |
| 8. 우회상장 해당 여부 | 아니오 | |||
| -향후 6월이내 제3자배정 증자 등 계획 | 아니오 | |||
| 9. 발행회사(타법인)의 우회상장 요건 충족여부 | 아니오 | |||
| 10. 이사회결의일(결정일) | 2020-02-19 | |||
| -사외이사 참석여부 | 참석(명) | 2 | ||
| 불참(명) | 1 | |||
| -감사(감사위원) 참석여부 | 불참 | |||
| 11. 공정거래위원회 신고대상 여부 | 미해당 | |||
| 12. 풋옵션계약 등의 체결여부 | 아니오 | |||
| -계약내용 | - | |||
| 13. 기타 투자판단에 참고할 사항 | - 상기 자산총액은 2018년도말 연결재무제표상 기준입니다. - 상기 자기자본은 2018년도말 연결재무제표를 기준에서 현재까지 증가된 자본금 및 자본잉여금 증감액을 반영한 금액입니다. - 상기 취득금액은 USD 30,000,000로 이사회결의일 당일 서울외국환중개㈜의 최초 고시 매매기준환율(1,188.10 KRW/USD)을 적용하여 산정하였습니다. - 하기 발행회사의 요약재무상황은 2018년말, 2017년 말, 2016년말 기준입니다. |
|||
[발행회사의 요약 재무상황](단위 : 백만원)
| 구분 | 자산총계 | 부채총계 | 자본총계 | 자본금 | 매출액 | 당기순이익 |
|---|---|---|---|---|---|---|
| 당해년도 | 22,962 | 26,153 | -3,190 | 1 | 1,827 | -13,800 |
| 전년도 | 30,683 | 21,793 | 8,890 | 1 | 206,673 | 110,073 |
| 전전년도 | 224,530 | 334,396 | -109,866 | 2 | 152,991 | 73,853 |
[상대방에 관한 사항]
| 1. 인적사항 | |||
| - 기본사항 | |||
| 성명(명칭) | 국적 | 주소(본점소재지) [읍ㆍ면ㆍ동까지만 기재] |
생년월일(사업자등록번호 등) |
| Immunomic Therapeutics,Inc. | 미국 | 메릴랜드주 락빌시 | - |
| 직업(사업내용) | 바이오의약품 개발 | ||
| - 최대주주ㆍ대표이사ㆍ대표집행임원 현황 및 재무상황 등(상대방이 법인인 경우) | |||
| 구분 | 성명 | 주식수 | 지분율(%) |
| 최대주주 | Hummel Family LP | 1,354,301 | 9.05 |
| 대표이사 | William G.Hearl | 857,590 | 5.73 |
| (단위 : 백만원) | |||
| 해당 사업연도 | 2018 | 결산기 | 12월 |
| 자산총계 | 22,962 | 자본금 | 1 |
| 부채총계 | 26,153 | 매출액 | 1,827 |
| 자본총계 | -3,190 | 당기순손익 | -13,800 |
| 외부감사인 | - | 휴업 여부 | 아니오 |
| 감사의견 | - | 폐업 여부 | 아니오 |
| 2. 상대방과의 관계 | |||
| 1. 회사와 상대방과의 관계 | - | ||
| 2. 회사의 최대주주ㆍ임원과 상대방과의 관계 | 성명 | 상대방과의 관계 | |
| - | - | - | |
| 3. 최근 3년간 거래내역(일상적 거래 제외) | |||
| 구분 | 거래 내역 | ||
| 당해년도 | 2020년 1월 31일 지분취득(제3자배정 유상증자) - USD10,000,000 | ||
| 전년도 | - | ||
| 전전년도 | - | ||
| (자료: 금융감독원 전자공시시스템) |
Immunomic Therapeutics, Inc.("ITI")는 2006년 미국 메릴랜드주에서 설립된 바이오기업으로 존스홉킨스 대학(Johns Hopkins University)과 듀크 대학(Duke University)의 원천기술을 기반으로 UNITE (Universal Intracellular Targeted Expression)라는면역 플랫폼 기술을 활용하여 면역세포치료제, 치료백신 등의 면역치료제를 개발하는 생명공학 기술 개발 전문회사입니다. 회사의 독보적 기술력을 대표하는 UNITE 플랫폼은 생물학적 항원 기술으로서 바이러스 항원, 암 항원, 신생 항원 및 항원 유래항체를 포함하여 종양학에서 광범위한 치료를 위해 다양하게 사용될 수 있으며, 회사는 8개의 종약학 프로그램과 4개의 알러지 프로그램으로 UNITE 플랫폼을 이용하여 대규모 파이프라인을 구축하고 있습니다.
UNITE (Universal Intracellular Targeted Expression) 플랫폼은 인간의 내인성 단백질(lysosomal associated membrane protein)을 활용하여 목표로 하는 특정 항원에 대한 신체의 면역반응을 활성화ㆍ증폭시킬 수 있는 기술입니다.
면역세포 중 수지상세포(Dendritic cells)와 대식세포(Macrophage)와 같은 항원전달제시세포(Antigen presenting cells)는 바이러스, 박테리아, 암 등의 항원에 대해 세포내 주조직적합성 복합체(MHC, major histocompatibility complex) class 2를 통해 Helper T 세포(CD4+ T cells)에 전달하게 되고, Helper T 세포는 세포독성림프구(cytotoxic T lymphocyte, CD8+ T cells)와 B 세포를 활성화하여 항원에 대한 면역 반응을 일으키게 됩니다.
| [UNITE 플랫폼의 면역 반응 활성화 기전] |
|
| (자료: ITI 제공) |
생체 내에서의 이러한 기전을 이용하는 기존 치료법의 한계는 항원의 다양성으로 인하여 특정 항원에 대한 면역 활성화가 제한적이라는 점입니다. UNITE 플랫폼 기술의 핵심은 특정 항원에 대한 강력하고 광범위한 면역 반응을 유도할 수 있다는 점입니다.
UNITE platform은 환자의 혈액을 사용하여 체외에서 항원전달제시세포(Antigen presenting cells)에 특정 항원을 감작시킨 후 환자에게 주입하는 면역세포치료제, 직접환자에게 주입하여 항원에 대한 면역반응을 유도하는 치료백신, 또는 항체(antibody)치료제 개발용 항원 전달 수단 등으로 활용될 수 있습니다. 면역세포치료제, 치료백신, 항체치료제 등의 다양한 치료제군 개발이 가능한 UNITE 플랫폼 기술은 항원의 선택에 따라 크게 항암제 및 알레르기 치료제의 2개 종류로 개발이 가능합니다.
| [UNITE 플랫폼의 활용] |
|
| (자료: ITI 제공) |
현재 ITI가 가장 집중하고 있는 pipeline은 뇌종양 중 악성에 속하는 교모세포종(Globlastoma)의 면역세포치료제로, 임상 2상이 진행 중에 있습니다. 임상 1상 종료 후 분석 결과, 기존 약물보다 5년 생존율이 약 7배 높게 나타났으며, 전체생존율(OS)의 중간값이 40개월을 상회하는 결과를 보여 교모세포종 치료에 있어서 획기적인 결과라는 평가를 받고 있습니다. 이러한 ITI의 플랫폼기술과 Pipeline의 우수성은 2019년 HTF Market Intelligence "Human DNA Market Astonishing Growth by 2025"에서 이분야의 leading 기업으로 선정되었고, 2020년 1월 30일 Data Bridge Market Research는 "2020년~2026년 글로벌 DNA 백신 마켓 분석보고서"에서 ITI를 global leading player로 선정하였습니다.
상기 교모세포종 면역세포치료제 외에도 회사는 현재 다수 항암제 및 알레르기 치료제를 연구ㆍ개발하고 있으며, UNITE platform 기술을 활용하여 다양한 파이프라인을 진행중에 있습니다. 회사의 주요 Pipeline을 요약하면 다음과 같습니다.
| [Immunomic Therapeutics Inc.의 주요 pipeline 요약] |
|
| (자료: ITI 제공) |
당사는 ITI의 pipeline을 통하여 기존 pipeline인 Rivoceranib 성분 항암 신약 외에 각종 종양 및 알레르기 에 대한 면역치료제 사업에 진출할 계획입니다. ITI가 영위하는 사업 역시 신약 개발의 영역으로, 개발에 오랜 시간이 소요되며 수많은 변수가 상존하여 임상 진행 허가 및 신약 허가를 취득하여 개발에 최종 성공할 확률이 극히 낮으며, 개발에 성공한다고 해도 그 상업적 성공 여부는 보장되지 않습니다. 투자자께서는 본 증권신고서 제1부 "III. 투자위험요소 - 1. 사업위험 - 다."의 내용을 참고하시어신약 개발 사업의 특성을 정확히 인지하시고 투자 판단에 임하시기 바랍니다.
자-2. Verismo Therapeutics, Inc. 지분 투자 관련
당사의 이사회는 2021년 3월 29일 이사회 결의를 통해 미국 소재 법인인Verismo Therapeutics, Inc.(이하 Verismo)의 지분 취득을 결정하였으며, 2021년 04월 12일 미화 5백만 달러(한화 5,659백만원)을 지불하고 제3자배정 유상증자에 참여하여 Immunomic의 지분율 10.00%를 취득했습니다. Verismo Therapeutics, Inc.는 KIR-CAR플랫폼 기술을 활용하여 중피종, 난소암 등을 대상으로 비임상을 진행하고 있는 바이오의약품 연구개발기업입니다.
당사가 동 지분 취득과 관련하여 금융감독원 전자공시시스템에 공시한 내용은 다음과 같습니다.
| [타법인주식및출자증권취득결정(자율공시)](2021.03.29) |
| 1. 발행회사 | 회사명(국적) | VERISMO THERAPEUTICS,INC. | 대표이사 | Bryan Byong Jin Kim |
| 자본금(원) | 1,199,041 | 회사와의관계 | - | |
| 발행주식총수(주) | 10,594,109 | 주요사업 | 바이오의약품 개발 | |
| 2. 취득내역 | 취득주식수(주) | 1,912,777 | ||
| 취득금액(원) | 5,659,000,000 | |||
| 자기자본(원) | 610,197,014,014 | |||
| 자기자본대비(%) | 0.93 | |||
| 대기업해당여부 | 해당 | |||
| 3. 취득후 소유주식수 및 지분비율 | 소유주식수(주) | 1,912,777 | ||
| 지분비율(%) | 10.00 | |||
| 4. 취득방법 | 현금취득(3자배정 유상증자 참여) | |||
| 5. 취득목적 | 지분 취득을 통한 기업가치극대화 | |||
| 6. 취득예정일자 | 2021-04-12 | |||
| 7. 자산양수의 주요사항보고서 제출대상 여부 | 아니오 | |||
| - 최근 사업연도말 자산총액(원) | 362,612,148,006 | 취득가액/자산총액(%) | 1.56 | |
| 8. 우회상장 해당 여부 | 아니오 | |||
| - 향후 6월이내 제3자배정 증자 등 계획 | 아니오 | |||
| 9. 발행회사(타법인)의 우회상장 요건 충족여부 | 아니오 | |||
| 10. 이사회결의일(결정일) | 2021-03-29 | |||
| - 사외이사 참석여부 | 참석(명) | 3 | ||
| 불참(명) | 0 | |||
| - 감사(감사위원) 참석여부 | 참석 | |||
| 11. 공정거래위원회 신고대상 여부 | 미해당 | |||
| 12. 풋옵션계약 등의 체결여부 | 아니오 | |||
| - 계약내용 | - | |||
| 13. 기타 투자판단에 참고할 사항 | - 상기 자산총액은 2019년도말 연결재무제표상 기준입니다. - 상기 자기자본은 2019년도말 연결재무제표를 기준에서 현재까지 증가된 자본금 및 자본잉여금 증감액을 반영한 금액입니다. - 상기 취득금액은 USD5,000,000.00로 이사회결의일 당일 서울외국환중개의 최초 고시 매매기준환율(1,131.80 KRW/USD)을 적용하여 산정하였습니다. - 하기 발행회사의 요약재무상황은 2020년 6월에 설립하여 최근사업연도 자본금만 기재하였습니다. |
|||
| ※ 관련공시 | - | |||
| (자료: 금융감독원 전자공시시스템) |
CAR-T 세포 치료제(키메라 항원 수용체-T 세포, chimeric antigen receptor-T cell)는 환자의 암세포에 특이적인 면역 능력만을 선택적으로 증강시키는 방법입니다. 환자의 면역 T 세포를 유전자 조작하여 암세포 표면 항원에 특이적으로 반응하도록 강화시키는 방법으로, 유전자 조작하여 강화시킨 면역 T 세포, 즉 CAR-T 세포는 환자의 기존 면역 세포보다 암세포를 더 잘 인지하고 더 잘 공격합니다.
CAR-T는 CAR를 발현하고 있는 T세포이므로, 핵심구조는 크게 표적 항원인지부위와 세포 내부로의 신호전달 부위입니다. 항원인지부위는 주로 항체에서 가져오며 암세포를 인지하는 역할을 하고, 신호전달부위는 T세포가 암세포를 인지하고 반응하는데 사용하는 신호전달부위의 일부를 조합하여 만들 수 있는데 T세포를 활성화시키는역할을 합니다. CAR-T는 현재 CAR의 구조에 따라 일반적으로 1~4세대로 분류합니다. 1세대는 Single Stimulatory, 2세대는1개의 Costimulatory, 3세대는 2개의 Costimulatory Signal을 가지고 있는 구조이고, 최근 들어 다양한 부작용을 극복하거나 효능을 높이기 위해 다양한 방식의 "4세대” CAR-T가 개발되고 있습니다.
| [CAR-T 치료제 작용 기전] |
|
| (자료: Verismo 제공) |
현재까지 6 개의 CAR-T 치료제가 FDA 승인을 받았습니다. 킴리아 (노바티스, 2017년 승인), 예스카타 (질리어드, 2017 년), 테카투스 (질리어드, 2020 년), 브레얀지 (브리스톨 마이어스 스퀴브, 2021 년), 아베크마 (브리스톨 마이어스 스퀴브, 2021 년), 그리고 카비크티 (존슨 앤 존슨, 2022 년) 가 승인되었고, 모두 혈액암에 대한 치료제입니다.
아직 고형암을 표적으로 하는 CAR-T 치료제는 시장에 출시되지 않는데, 이는 CAR-T 작용기전이 혈액암에서 뛰어난 항암효과를 보여줬음에도 불구하고 고형암에서 면역억제 종양미세환경(tumor micro-environment, TME), 종양세포 이질성(heterogeneity), CAR-T 세포의 전달 및 효과 지속 등 고려해야 할 점이 많기 때문입니다.
Verismo Therapeutics의 SynKIR™ 플렛폼은 세계 최초로 허가를 받은 CAR-T 치료제(킴리아)의 UPenn 개발팀이 개발한 기술로, 기존 CAR-T 치료제의 부족한 고형암 치료효과를 극복하기 위해 개발됐습니다. 기존 CAR와 달리 NK세포의 KIR (Killer immunoglobulin-like receptor)를 기반으로 하는데, KIR2DS2에 항원인지부위가 결합돼 있고 DAP12를 통해 T세포 활성신호가 전달되는 차별화된 구조를 채택하였습니다. 이는 세계 최초 항원인지부위와 신호전달부위를 분리시킨 구조로 면역세포 내 면역수용체들과 매우 유사한 구조와 기능을 수행할 수 있도록 설계하였습니다.
| [SynKIR 플랫폼 특징] |
|
| (자료: Verismo 제공) |
현재까지 6 개의 CAR-T 치료제가 FDA 승인을 받았습니다. 킴리아 (노바티스, 2017년 승인), 예스카타 (길리어드, 2017 년), 테카투스 (질리어드, 2020 년), 브레얀지 (브리스톨 마이어스 스퀴브, 2021 년), 아베크마 (브리스톨 마이어스 스퀴브, 2021 년), 그리고 카비크티 (존슨 앤 존슨, 2022 년) 가 승인되었고, 모두 혈액암에 대한 치료제입니다. 이중 가장 두각을 나타내는 치료제는 노바티스의 킴리아(성분명: 티사젠렉류셀·tisagenlecleucel)와 길리어드의 예스카타(성분명: 브렉수캅타진 오토류셀·brexucabtagene autoleucel) 입니다. 두 제품 모두 CD19 항원을 표적하는 CAR-T 치료제로, 지난해 기준 예스카타는 6억 9500만 달러(약 8,600억 원)의 매출을 기록하며 CAR-T 치료제 제품 매출 1위를 기록했고, 킴리아의 경우 2021년 5억 8700만 달러(약 7,200억 원)의 수익을 거두어 예스카타 뒤를 이었습니다. 특히, 예스카타가 22년 4월 미만성거대B세포림프종의 2차치료제로 미국내 시판허가를 받음으로써 기존 3차 이상 및 치료옵션이 없는 말기 환자를 대상으로 사용됐던 CAR-T 치료제가 조금 더 초기의 환자에게 사용 가능하게 되면서 CAR-T 치료제의 사용 범위가 더 넓어지게 됐습니다. 길리어드는 이번 시판허가로 기존 8,000명 미국 환자에서 14,000명 환자까지 치료가 가능해졌다고 발표했습니다.
아직 고형암을 표적으로 하는 CAR-T 치료제는 시장에 출시되지 않았습니다. 현재 연구개발이 활발하게 진행 중이며, 21년 기준 전 세계적으로 고형암 표적 CAR-T 치료제 임상시험은 198개가 실시되고 있습니다. 중국이 99개, 미국이 85개로 중국과 미국이 이 분야에서 주도하고 있습니다. Coherent Market insight에 따르면, 글로벌 CAR-T 치료제 시장은 2017년 7,200만 달러 규모를 형성하였고, 향후 11년간 연평균 성장률 53.9%로 급격히 성장하여 2028년에는 83억 달러 규모로 확대될 것으로 전망하고 있습니다.
Verismo는 중피종, 난소암, 췌장암을 대상으로 SynKIR-110의 미국 임상 1상 시험을 위한 비임상시험을 마치고 2022년 9월 임상시험계획승인신청(Investigational New Drug Application, IND)을 승인을 득한 후 환자 모집을 위한 작업을 진행하고 있습니다. 후속 파이프라인으로는 SynKIR-210(유방암, 비소세포폐암, 대장암), SynKIR-310(DLBCL) 그리고 SynKIR-410(교모세포종)이 있습니다.
| [Verismo Therapeutics Inc.의 주요 pipeline 요약] |
|
| (자료: Verismo 제공) |
신약 개발 사업은 개발에 오랜 시간이 소요되며 수많은 변수가 상존하여 임상 진행 허가 및 신약 허가를 취득하여 개발에 최종 성공할 확률이 극히 낮으며, 개발에 성공한다고 해도 그 상업적 성공 여부는 보장되지 않습니다. 투자자께서는 본 증권신고서제1부 "III. 투자위험요소 - 1. 사업위험 - 다."의 내용을 참고하시어 신약 개발 사업의특성을 정확히 인지하시고 투자 판단에 임하시기 바랍니다.
|
차. Rivoceranib 신약 개발 사업에 관한 전반적인 사항 |
차-1. 자회사를 통한 의약품개발사업 진출과 삼각합병
당사는 2015년 2월 미국 법인인 LSK BioPartners Inc.("LSK Bio")의 지분 31.21%를취득한다는 내용의 주요사항보고서를 공시하며 본격적으로 의약품개발사업에 관여하기 시작하였습니다. 결정 당시의 공시 내용은 아래와 같습니다.
| <주요사항보고서(중요한자산양수도결정)>(2015.02.03) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Ⅱ. 보고 내용 [자산양수도가액]
④ 대표이사: Sung Chul Kim
(주1) 보고서 제출일 현재 현황입니다.
(주1) 양도가액은 주당 43,966원을 적용하여 산출하였습니다.
4. 외부평가기관의 현황
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
LSK Bio는 2005년 7월 Lifecord International USA Inc. 라는 법인명으로 설립되었으며, 2007년 LSK Bio로 사명을 변경하였습니다.
LSK Bio는 NRDO(No Research Development Only) 업체로, 자체적인 신약 후보 물질의 초기 발굴 및 연구 단계 없이 외부에서 신약 기술에 대한 권리를 이전 받아 임상개발을 진행합니다. 당사가 LSK Bio의 지분을 취득하기 이전인 2007년 12월, LSK Bio는 신약후보물질 리보세라닙의 원천 특허권 보유자인 Advenchen Laboratories, LLC.("Advenchen") 및 그 최대주주이자 리보세라닙 물질 개발자인 Paul Chen으로부터 리보세라닙을 활용한 신약 기술을 개발하여 중국을 제외한 세계 모든 지역에서 독점적으로 판매할 권리를 이전받아 개발에 착수하였습니다. 중국 내에 한하여 LSK Bio와 동일한 권리를 취득한 업체는 중국의 항서제약으로, 중국 내에서는 리보세라닙 신약 판매가 2015년 최종 허가되어 판매 개시된 바 있습니다.
당사는 LSK Bio가 리보세라닙 신약 개발을 진행 중이던 2015년 상기 주요사항보고서의 내용과 같이 LSK Bio의 지분 31.21%를 취득하였으며, 이후 LSK Bio의 제3자배정 유상증자 참여 등을 통하여 2019년 3분기말 기준 지분율 59.83%의 최대주주가되었습니다.
| [삼각합병 전 당사 및 계열회사의 지분 구조] | |
| (기준일: 2019년 09월 30일) | |
|
2019년 6월, 당사는 회사합병결정 자율공시를 통해 LSK Bio와의 삼각합병 계획을 공개하였습니다. 당시 공시 내용은 아래와 같습니다.
| <회사합병 결정(자율공시)(종속회사의 주요경영사항)>(2019.06.13) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
[종속회사에 관한 사항]
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| (자료: 금융감독원 전자공시시스템) |
당사는 연결대상 종속회사인 LSK Bio를 직접 합병할 의사도 있었으나, 미국 법에 의하여 설립된 LSK Bio를 국내 법인인 당사가 직접 합병할 수 있는 법적 근거의 부재로 인하여, 당사의 100% 자회사 미국 법인인 HLB USA를 설립하여 HLB USA로 하여금 LSK Bio를 흡수합병하도록 하였습니다.
흡수합병 직전인 2019년 8월 LSK Bio는 사명을 Elevar Therapeutics Inc.("Elevar")로 변경하였습니다. HLB USA가 Elevar를 흡수합병하여 기존 Elevar는 소멸법인이 되었으며, HLB USA가 사명을 Elevar Therapeutics, Inc.로 변경하는 과정을 거쳐 증권신고서 제출일 현재와 같이 당사가 Elevar를 100% 자회사로 두는 구조가 완성되었습니다.
이 과정에서 당사를 제외한 LSK Bio의 기존 주주들에게는 당사가 정해진 합병비율에 따라 산출된 만큼 각 주주에게 합병대가로 당사의 보통주를 발행하여 교부하기로 하였는데, 합병대가로 교부된 당사의 보통주 수량은 총 2,609,387주입니다. 이는 지급 당시 당사의 100% 자회사인 HLB USA의 제3자배정 유상증자에 당사가 단독 참여하는 형태로 자금을 지원한 뒤, 해당 자금을 재원으로 HLB USA가 다시 당사의 제3자배정 유상증자에 참여하는 형태로 지급되었으며, 이 때 발행된 당사의 신주는 합병기일인 2019년 11월 27일자로 코스닥시장에 추가상장 완료되었고, 1년간 Elevar가 보유하고 있는 형태로 LSK Bio의 구주주들에게 배분하기 이전 보호예수 기간을 가졌습니다.
| [삼각합병 후 당사 및 계열회사의 지분 구조] | |
| (기준일: 2019년 11월 27일) | |
|
| 주) 상기 당사에 대한 에이치엘비생명과학㈜와 에이치엘비셀㈜(舊 라이프리버㈜)의 지분율 1.31% 및 0.88%는 에이치엘비생명과학㈜와 에이치엘비셀㈜가 보유하고 있던 LSK BioPartners, Inc.의 지분에 대하여 합병대가로 각각 지급받은 당사의 보통주 559,203주 및 376,461주에 해당하는 내용으로, 현재는 보호예수가 종료되어 구주주들에게 배분 완료 되었습니다. 동 지분율은 삼각합병당시 대가로 지급된 2,609,387주까지 반영된 당시 보통주식총수 42,657,495주 기준입니다. |
이후 보호예수기간 중인 2020년 03월 03일, 당사는 이사회를 통해 유무상증자를 진행했으며, 무상증자 결과 보호예수된 주식에도 1주당 0.1의 신주가 배정되었습니다. 유무상증자 진행 후 2020년 11월 27일, 해당 보호예수가 종료되면서 Elevar가 보유하고 있던 당사의 보통주는 Elevar의 구주주들에게 배분되었습니다. 관련된 구주주 중 당사의 특수관계인들의 보호예수 해제에 따른 세부변동내역은 아래와 같습니다.
| [보호예수 해제에 따른 주식보유변동내역](2020.11.27) |
| 성명 (명칭) |
생년월일 또는 사업자등록번호 등 |
변동일* | 취득/처분 방법 |
주식등의 종류 |
변동 내역 | 취득/처분 단가** |
비 고 | ||
|---|---|---|---|---|---|---|---|---|---|
| 변동전 | 증감 | 변동후 | |||||||
| 이현아 | 660417 | 2020.11.27 | 기타(-) | 기타 | 2,479 | -2,479 | 0 | - | (주1) |
| 이현아 | 660417 | 2020.11.27 | 기타(+) | 의결권있는 주식 | 677,881 | 2,479 | 680,360 | - | (주1) |
| Alex S. Kim | 680516 | 2020.11.27 | 기타(-) | 기타 | 247,516 | -247,516 | 0 | - | (주1) |
| Alex S. Kim | 680516 | 2020.11.27 | 기타(+) | 의결권있는 주식 | 967,584 | 247,516 | 1,215,100 | - | (주1) |
| 에이치엘비생명과학㈜ | 116-81-67278 | 2020.11.27 | 기타(-) | 기타 | 615,123 | -615,123 | 0 | - | (주1) |
| 에이치엘비생명과학㈜ | 116-81-67278 | 2020.11.27 | 기타(+) | 의결권있는 주식 | 84,492 | 615,123 | 699,615 | - | (주1) |
| 에이치엘비셀㈜ | 125-81-83269 | 2020.11.27 | 기타(-) | 기타 | 414,107 | -414,107 | 0 | - | (주1) |
| 에이치엘비셀㈜ | 125-81-83269 | 2020.11.27 | 기타(+) | 의결권있는 주식 | 0 | 414,107 | 414,107 | - | (주1) |
| 진유림 | 941017 | 2020.11.27 | 기타(-) | 기타 | 3,719 | -3,719 | 0 | - | (주1) |
| 진유림 | 941017 | 2020.11.27 | 기타(+) | 의결권있는 주식 | 396 | 3,719 | 4,115 | - | (주1) |
| 진인혜 | 961028 | 2020.11.27 | 기타(-) | 기타 | 3,719 | -3,719 | 0 | - | (주1) |
| 진인혜 | 961028 | 2020.11.27 | 기타(+) | 의결권있는 주식 | 371 | 3,719 | 4,090 | - | (주1) |
|
* 증권시장에서 주식등을 매매한 경우에는 그 계약체결일 ** 주식 외의 증권의 경우 해당 증권의 행사(전환ㆍ교환)가액 또는 해당 증권의 권리행사로 취득ㆍ처분하는 주식의 매매단가를 의미하며, ( )의 금액은 해당 증권의 매매단가를 의미 |
| 자료 : 금융감독원 전자공시시스템 |
차-2. 신약후보물질 Rivoceranib("리보세라닙") 개요 및 권리 관계
항암제는 일반적으로 1세대 세포독성항암제, 2세대 표적항암제, 3세대 면역항암제 등으로 분류됩니다. Elevar가 중국을 제외한 전 세계 시장에서 특허 실시권을 보유하고 있는 리보세라닙은 선택적 VEGFR2 저해제로 2세대 표적항암제인 신생혈관생성억제제에 해당하며, 새로운 혈관을 통해 영양분을 공급받아 커지는 암의 진행을 저지합니다. 암세포는 특유의 무한 증식 능력을 실현하기 위해 막대한 양의 산소와 영양분 공급을 필요로 하고, 이에 암 주변 혈관에 계속적으로 신생혈관형성 인자인 VEGF(Vascular Endothelial Growth Factor, 혈관내피 성장인자)를 분비하며, VEGF는 혈관 내피 세포 표면에 존재하는 VEGFR2(혈관내피 성장인자 수용체 2)에 붙어 혈관의 성장을 촉진합니다. 결론적으로, 리보세라닙은 VEGFR2 를 억제해 VEGF 가 수용체에 결합하지 못하게 함으로써 신생혈관형성을 억제해 암세포 증식과 전이를 막는 원리의 항암제 성분입니다. 리보세라닙의 작용기전 및 효과와 관련하여 더 상세한 내용은 본 증권신고서 "III. 투자위험요소 - 1. 사업위험 - 차."를 참고하여 주시기 바랍니다.
리보세라닙의 최초 개발자는, 미국 내 의약품연구개발법인인 Advenchen Laboratories, Inc.("Advenchen")의 최대주주인 연구개발자 Paul Chen 입니다. Paul Chen과 Advenchen은 리보세라닙의 글로벌 물질 특허권을 보유하며, 이를 토대로 리보세라닙을 사용하는 의약품을 개발 및 판매할 수 있는 권리(특허의 전용실시권)를 제3자에게허여하고 로열티를 수취합니다. Paul Chen과 Advenchen은 리보세라닙 물질 특허에대하여 2005년 중국 내 전용실시권을 중국 항서제약에, 이어 2007년 당시 LSK Bio(現 Elevar)에게 중국을 제외한 나머지 모든 지역에 대한 전용실시권을 허여하였습니다.
2009년 LSK Bio(現 Elevar)는 국내법인인 부광약품에 Advenchen 으로부터 허여받은 리보세라닙 실시권의 일부를 양도하였습니다. 부광약품이 양도받은 권리는 i) 한국내 시장에서의 리보세라닙 신약 독점 실시권 및 ii) LSK Bio가 일본ㆍ유럽 시장에서 제3자에게 실시권을 허여하여 로열티를 수취하거나 직접 판매하여 수익을 얻을 경우 그 일부(14.5%)를 수취할 권리입니다. 부광약품은 2018년 당사의 계열회사인 에이치엘비생명과학㈜에 동 권리 일체를 한화 400억원에 양도하는 양수도계약을 체결하였습니다. 당시 에이치엘비생명과학㈜가 공시한 내용은 아래와 같습니다.
| <주요사항보고서(중요한자산양수도결정(기타))>(2018.08.16) | |||||||||||||||||||||||||||
|
Ⅰ. 보고 사유
Ⅱ. 보고 내용 [자산양수도가액]
1-①. 자산 양수도에 관한 기본사항
(1) 자산양수도 가액
6. 양수도되는 자산의 내용
|
상기 권리의 양수도로 인해, 리보세라닙 신약의 글로벌 특허 실시권은 항서제약과 당사, 그리고 에이치엘비생명과학㈜가 보유하게 되었습니다. 동 권리 관계를 도식화하면 다음과 같습니다.
| [기존 리보세라닙 신약개발/판매 실시권 분포 및 로열티 지급 구조] |
|
| 주) 상기 구조도는 리보세라닙의 물질특허와 염조성물특허를 구분하지 않고, 물질특허와 염조성물특허를 포괄하여 성립되는 독점 판권의 수준에서 작성되었습니다. |
한편, 리보세라닙 물질 특허와는 별도로 리보세라닙 염조성물특허(Salt Patent)가 존재합니다. 염조성물특허는 통상 물질특허에 대한 실시권을 허여받은 제약사가 출원, 등록합니다. 리보세라닙 염조성물 특허는 중국 항서제약이 2009년 6월 출원하여 글로벌 원천 특허권자로 등록되어 있으나, 항서제약과 Advenchen 사이에 체결한 계약(2014년)에 의하여 물질특허와 염조성물특허 모두에 대해 항서제약은 중국 내에서의 전용실시권만을, 그 외 지역에 대해서는 Advenchen이 전용실시권을 보유하게 되었습니다. 이를 토대로 당사의 100% 자회사인 Elevar는 Advenchen과의 계약으로 중국 외에서의 재실시권을 허여받았습니다.
중국 항서제약은 중국 내 Apatinib Mesylate(Rivoceranib의 舊 명칭) 성분 신약 판매 허가 취득을 2015년 완료하여, 제품명 'Aitan'으로 판매를 시작하였으며, Advenchen은 항서제약으로부터 매출의 일부를 로열티로 수령한 내역이 있습니다. 마찬가지로 Elevar가 중국 외 다른 지역에서 리보세라닙 신약 판매 허가를 최종 취득하여 제품 판매를 개시할 경우, Elevar 또한 Advenchen에 매출의 일부를 로열티로 지급했어야 하지만, 증권신고서 제출일 현재까지 중국 외 지역에서 리보세라닙 신약 시판이 최종 허가된 바는 없습니다.
이후 당사는 2020년 02월 27일 언론을 통해 Advenchen이 Rivoceranib에 대하여 보유하는 특허 관련 권리 일체를 Advenchen으로부터 양수하기로 하였음을 발표했으며, 당사가 양도받은 권리는 YN968D1(이하 "리보세라닙")과 관련된 모든 특허 및 지적재산권입니다. 평가대상자산을 인수함에 따라 리보세라닙과 관련된 모든 권리를 획득하게 되어 글로벌 리보세라닙 관련 매출액에 대한 로열티를 수령하게 되었고, 2020년부터 중국의 항서제약을 통해 중국 내 리보세라닙 매출액에 대한 로열티를 수령하고 있습니다. 중국 이외의 글로벌 지역에서는 Elevar Therapeutics, Inc.를 통해 로열티 매출액을 수령하게 됩니다. 해당 양수도계약과 관련하여 당시 당사가 공시한 내용은 아래와 같습니다.
| <주요사항보고서(중요한자산양수도결정(기타))>(2018.08.16) | ||||||||||||||||||||||||||||||||||||||||
|
Ⅰ. 보고 사유
Ⅱ. 보고 내용 [자산양수도가액]
1-①. 자산 양수도에 관한 기본사항
(1) 자산양수도 가액
6. 양수도되는 자산의 내용 회사는 Advenchen Laboratories Nanjing, Ltd.와 SFFT Developing Co., Ltd.(이하 "양도인")로부터 YN968D1에 대한 특허권(이하 "평가대상자산" 또는 "양수도대상 자산")을 양수할 계획이며, 이전될 권리의 상세내역은 아래와 같습니다.
|
||||||||||||||||||||||||||||||||||||||||
상기 권리의 양수도로 인해, 리보세라닙 신약과 관련된 모든 권리를 획득하게 되어 글로벌 리보세라닙 관련 매출액에 대한 로열티를 수령하게 됩니다. 동 권리 관계를 도식화하면 다음과 같습니다.
| [양수도계약 이후 리보세라닙 신약개발/판매 실시권 분포 및 로열티 지급 구조] |
|
| 주) 상기 구조도는 리보세라닙의 물질특허와 염조성물특허를 구분하지 않고, 물질특허와 염조성물특허를 포괄하여 성립되는 독점 판권의 수준에서 작성되었습니다. |
차-3. 리보세라닙 관련 임상 및 신약 허가 절차 진행현황
본 보고서 작성기준일 현재 당사의 연결대상 종속회사인 Elevar Therapeutics, Inc. 에서 체결한 상태인 리보세라닙 관련 라이센스 계약은 다음과 같습니다.
|
계약종류 |
품목 |
계약상대방 |
대상지역 |
계약 |
계약상의주요내용 |
계약금액 |
진행단계 | 비 고 |
|---|---|---|---|---|---|---|---|---|
| License-in |
리보세라닙 (Rivoceranib, 구Apatinib Mesylate) |
에이치엘비㈜(*1) |
중국을 제외한 |
2020. 12. |
Rivoceranib의 중국을 제외한 글로벌 전용실시권 취득 |
(*2) |
- 위암말기 치료제 : 임상3상 종료 Pre-NDA 실시, 미국 FDA 신약허가 신청 (NDA) 준비 중 희귀의약품 지정(미국, 유럽, 한국) - 고형암 옵디보(Nivolumab) 병용 : 임상1상 종료 - 선양낭성암 단독 : 임상2상 진행 중, 희귀의약품 지정(미국) - 위암 2차 치료제(파클리탁셀 병용) : 임상1/2상 진행 중 - 간암 1차 치료제(캄렐리주맙 병용) : 임상3상 진행 중, 희귀의약품 지정(미국) - 대장암 3차 치료제(론서프 병용) : 임상1상 진행 중 - 난소암(Apealea 병용) : 임상 1상 준비 중 |
표적항암제 (VEGFR-2를 선택적으로 차단) |
| License-out | 리보세라닙 (Rivoceranib, 구Apatinib Mesylate) |
에이치엘비생명과학㈜ |
대한민국 |
2018. 08. |
기존 부광약품㈜에게 인정되는 |
47억(*3) | - 위암말기 치료제 : 임상3상 종료 Pre-NDA 실시, 미국 FDA 신약허가 신청 (NDA) 준비 중, 희귀의약품 지정(미국, 유럽, 한국) - 선양낭성암 단독 : 임상2상 진행 중, 희귀의약품 지정(미국) - 위암 2차 치료제(파클리탁셀 병용) : 임상1/2상 진행 중 - 간암 1차 치료제(캄렐리주맙 병용) : 임상3상 진행 중, 희귀의약품 지정(미국) - 대장암 3차 치료제(론서프 병용) : 임상1상 진행 중 - 동물용항암제 : 임상 진행 중 |
에이치엘비 바이오 그룹의 사업 다각화 및 매출 증대 |
| (*1) Elevar Therapeutics,Inc.는 2007년 7월 Advenchen Laboratories,Inc., CA, USA와 리보세라닙 License-in 계약을 체결하였으나, 2020년 12월 당사와 Advenchen Laboratories와 Rivoceranib의 물질특허권리 양수도에 따라 특허권자가 당사로 변경되었습니다. 이에 기존 Elevar와 Advenchen Laboratories간의 Rivoceranib특허전용실시권의 계약당사자는 Elevar와 당사로 변경되었습니다. |
| (*2) 계약금액의 경우 중요 영업기밀에 해당되므로 기재를 생략합니다. |
|
(*3) Elevar Therapeutics, Inc.는 2009년 12월 부광약품㈜에게 리보세라닙의 한국 판권 및 수익에 대한 일부 권리를 양도하는 조건으로 리보세라닙 공동개발을 하였으며, 이후 부광약품㈜은 2018년 08월 한국 판권을 포함한 모든 권리 및 의무를 에이치엘비생명과학㈜으로 400억원에 양도하였습니다. Elevar Therapeutics, Inc.에서 계약상대방인 에이치엘비생명과학㈜로부터 향후 지급받을 Development Milestones 내역은 다음과 같습니다. |
당사의 연결대상 종속회사인 Elevar Therapeutics, Inc. 에서 체결한 상태인 리보세라닙 관련 라이센스 계약에 대한 상세내용은 아래와 같습니다.
(1) License-in / 리보세라닙
| 계약상대방 | Advenchen Laboratories |
| 계약내용 | YN968D1-Small Molecule Angiogenesis Inhibitor의 계약상 명시된 지역에서의전용실시권 취득 |
| 대상지역 | 중국을 제외한 모든 국가 |
| 계약기간 | 계약체결일:2007. 12. 21(계약서 내용 조정일 2008, 11, 11) (계약서 내용 조정일 2015, 06, 15) (계약서 내용 조정일 2017, 02, 27) (계약서 내용 조정일 2019, 12, 20) 계약종료일: 유효특허의 만료일까지 (물질특허: 2024년 예상, 염조성물특허: 2029년 예상) |
| 총계약금액 | Upfront: 150,000 USD |
| 지급금액 | <환수 불가능 금액> 계약금(Upfront Payment): 150,000USD 2007년 기 지급 완료 마일스톤(Milestione): 임상 진행 단계에 진행에 따라 개발 Milestione $800,000USD 지급 로열티(Royalty): 매출없음 <환수 가능 금액> 해당사항 없음 |
| 계약조건 | 계약 조정 내역을 포함한 최종 계약 조건 계약금(Upfront Payment): 150,000USD - 지급조건: 계약 체결 45일 이내 마일스톤(Milestione): 적응증, 진입국가, 매출에 따라 단계별 마일스톤 실행 예정 로열티: 3.5%~10%,지역별 매출액 비율에 따른 로열티 실행 예정 Advenchen이 보유한 Appatinib(Rivoceranib)의 염조성물 특허를 LSKB에 허여한다. 국가별 특허(물질특허 및 염조성물특허) 유지 상태에 따라 상호 협의한 비율에 의거해 로열티를 조정한다. LSKB가 보유한 모든 권리는 Elevar가 승계한다. |
| 회계처리방법 | 최초 지급한 Upfront 150,000USD는 무형자산으로 인식해 감가상각 완료 이후 지급한 Milestone 비용은 당기비용으로 인식 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 Rivoceranib과 염특허 전용 특허 실시권 |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1,2차 치료제(Rivoceranib 단독) 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 ESMO에서 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상 3상 결과 발표 (1차 평가지표 만족) |
| 기타사항 | 판매 승인 현황 중국 판권을 보유한 항서제약에서 2014년 위암 3차 치료제, 2020년 간암 2차 치료제로 시판 허가 득한 후 판매 중 |
(2) License-out / 리보세라닙
| 계약상대방 | 부광약품㈜ |
| 계약내용 | Rivoceranib에 대한 특정 지역의 개발, 판매에 대한 권리 Sublicense(한국, 유럽, 일본) 및 공동개발 |
| 대상지역 | 대한민국, 일본, 유럽 |
| 계약기간 | 계약체결일:2009. 1. 8 (계약서 내용 조정일 2012, 2, 1) (계약서 내용 조정일 2015, 7, 28) (계약서 내용 조정일 2015, 10, 30) (계약서 내용 조정일 2017, 1, 2) 계약종료일: 유효특허의 만료일까지 (물질특허: 2024년 예상, 염조성물특허: 2029년 예상) |
| 총계약금액 | Potential Sales Royalty: 매출액에 따라 6~10% 특허가 국가별로 개별 종료 될 시 최대 10년까지 상기 로열티의 10%를 지급 |
| 지급금액 | 해당사항 없음 |
| 계약조건 | 주요 계약 내용 1) 한국내 독점개발, 판매권 및 유럽, 일본에 대한 수익 지분 2) 국내 시판시 판매액의 6~10% 로열티 지불 (Sublicensing,진행시 수익의 30% 지불) |
| 회계처리방법 | 해당사항 없음 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 Rivoceranib 특허 전용실시권 |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제(Rivoceranib 단독)위암 3차 치료제 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1,2차 치료제(Rivoceranib 단독) 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 ESMO에서 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상 3상 결과 발표 (1차 평가지표 만족) |
| 기타사항 | Elevar Therapeutics, Inc. 는 2009년 12월 부광약품㈜에게 리보세라닙의 한국 판권을 양도하는 조건으로 리보세라닙 공동개발을 하였으며, 이후 부광약품㈜은 2018년 08월 한국 판권에 대한 모든 권리 및 의무를 에이치엘비생명과학㈜으로 400억원에 양도하였습니다. (2018.8.14 공시 참조) |
Elevar가 현재 리보세라닙 신약 연구개발을 진행하고 있는 주요 항목 중 임상을 개시할 계획이 있거나 임상이 진행중인 항목은 리보세라닙의 단독 및 병용임상을 포함하여 5개 항목입니다. 상세 내용은 하기와 같습니다.
| [Elevar의 리보세라닙 신약 임상 진행 및 허가 추진 현황] |
|
치료군 |
임상종류 |
진행상태 |
시점별 진행 예상 |
|---|---|---|---|
| 선낭암 1차 치료제 | 단독 | 글로벌 임상 2상 완료 | 2022년 4분기 NDA 신청을 목표로 준비 중 |
| 간암 1차 치료제 | 캄렐리주맙 병용 | 글로벌 임상 3상 진행중 | 2023년 NDA 신청을 목표로 준비 중 |
| 위암 말기 치료제 | 단독 | 글로벌 3상 완료 | 2023년 NDA 신청을 목표로 준비 중 |
| 대장암 3차 치료제 | 론서프 병용 | 임상 1b/2상 진행중 | 2022년 임상 1상 종료 후 다음 단계 진입 목표로 준비 중 |
| 위암 2차 치료제 | 파클리탁셀 병용 | 임상 1/2a상 진행중 | 2022년 임상 1상 종료 후 다음 단계 진입 목표로 준비 중 |
| 난소암 2차 치료제 (백금계 항암제 저항성) |
아필리아 병용 | 1b/3상 IND 준비 중 | 2022년 임상(1b/3상) 진행 목표로 준비 중 |
| 주) 상기 진행 예상 시점은 당사의 예측이며, 향후 지연, 취소 등의 변동이 있을 가능성이 상존합니다. |
일반적으로 신약의 개발은 후보물질 발견에서부터 전임상 및 임상시험, 품목허가 이후 실질적인 수익창출로 연결되기까지 많은 단계를 거쳐야 합니다. 따라서, 개발과정에서의 불확실성이 존재하며 단계가 진행될 수록 추가 연구개발비가 소요됩니다.
Elevar가 개발을 추진하고 있는 리보세라닙 신약 중 위암 말기 치료제의 경우 이미 대중에 알려진 대로 임상 3상까지 완료하였으며, 미국에서의 신약 시판 개시를 위한 마지막 단계인 FDA와의 NDA(New Drug Application, 신약 허가 신청)를 앞두고 준비 중에 있습니다. Elevar는 NDA에 앞서 2019년 10월 FDA와 Pre-NDA meeting을 완료하였습니다. 2022년 6월 결과를 발표한 선양낭성암 1,2차 치료제(Rivoceranib 단독) 임상 2상은 표준치료제가 없는 희귀암의 특성을 살려 미국 FDA의 가속승인(조건부판매)을 목표로 전략을 수립 중입니다. 그리고 항서제약의 캄렐리주맙과 병용으로 진행된 간암 1차 치료제 글로벌 임상 3상은 2022년 8월 미국 FDA에 Pre-NDA 미팅 신청을 한 상태 입니다. 2022년 9월 유럽암학회(ESMO)에서는 임상 결과를 공개함과 동시에 1차 평가지표를 만족했다고 발표 했습니다. 통상적으로 임상 결과의 유효성을 입증하는 1차 평가지표는 적응증, 치료방식, 대조군 등에 따라 다르게 이루어집니다. 당사가 진행한 간암 1차 치료제 글로벌 3상 임상(항서제약 캄렐리주맙 병용)의 경우 기존 1차 치료제인 소라페닙을 대조군으로 하여 OS와 PFS를 1차 평가지표로 하여 진행되었습니다. mOS의 경우 대조군인 소라페닙 대비 6.9개월 긴 22.1개월을 기록했고, mPFS는 대조군대비 1.9개월 증가한 5.6개월을 기록해(통계적 유의성 확보) 1차 평가지표의 유효성을 만족했습니다.
| [간암 1차 치료제 글로벌 임상 3상 주요 결과] |
| 주요 평가지표 | Rivoceranib + Camrelizumab |
Sorafenib (대조군) |
p-value | HR |
|---|---|---|---|---|
| mOS | 22.1개월 | 15.2개월 | < 0.0001 | 0.62 |
| mPFS | 5.6개월 | 3.7개월 | < 0.0001 | 0.52 |
| ORR | 25.40% | 5.90% | < 0.0001 | - |
| DCR | 78.30% | 53.90% | - | - |
| CR | 3명 | 1명 | - | - |
또한 리보세라닙 위암 말기 치료제와 간암 2차 치료제로 중국에서 이미 항서제약을 통해 'Aitan'이라는 제품명으로 판매되고 있는 의약품이고, 매출이 증가하는 추세를 보이고 있기 때문에, 타 성분의 신약 개발 pipeline에 비하여 상대적으로 시장 및 보건당국의 신뢰를 얻기가 용이하다고 볼 여지가 있습니다. 당사는 2020년 리보세라닙 신약과 관련된 모든 권리를 획득하게 되어 현재 항서제약으로부터 'Aitan' 매출액에 대한 로열티를 수령하고있으며, 발생한 매출의 현황은 아래와 같습니다.
| 리보세라닙 로열티 매출 현황 |
| (금액 : 백만원) |
| 연도 | 금액 |
|---|---|
| 2022년 반기 | 3,908 |
| 2021년 | 10,362 |
| 2020년 | 5,856 |
이러한 상황에도 불구하고, 중국에서 신약 판매 허가를 얻는 과정과 다른 국가에서 허가를 얻는 과정이 상이하여 Elevar의 리보세라닙 위암 말기 치료제가 FDA로부터 NDA 승인을 얻을 수 있을지 여부는 증권신고서 제출일 현재 예측할 수 없습니다. 또한, 당사는 Elevar가 현재 진행중인 다수 임상의 결과가 성공적일 것을 보장할 수 없으며, 진행 중인 임상이 중도에 중단되지 않으리라 단언할 수 없습니다. 또한, 임상이성공적으로 완료된다고 하더라도 실제 제품 판매까지 이어지지 못할 가능성이 높으며, 신약 제품 판매 허가를 득하더라도 해당 제품이 시장성 및 수익성을 확보할 수 있을지 여부는 현재 시점에서 당사가 합리적으로 예측할 수 없습니다. 당사가 제시하는임상 및 신약 허가 절차의 진행 계획과 단계별 예상 시기 등은 시장 상황, 연구개발 환경 및 관계 당국 등에 의하여 변경ㆍ지연ㆍ취소될 가능성이 상존하는 바, 투자자께서는 이러한 바이오 신약 연구개발업의 특성을 확실하게 인지하신 후 신중히 판단하여 투자에 임하시기 바랍니다.
|
카. 리보세라닙 외 타 의약품 관련 사업 추진에 관한 위험 |
당사의 100% 자회사인 Elevar는 스웨덴 바이오 기업인 비베스토(Vivesto, 舊 Oasmia)로부터 세포독성항암제인 파클리탁셀(paclitaxel) 성분의 3세대 개량신약 항암제 "아필리아(Apealea)"에 대한 러시아, 북유럽과 동유럽 일부 국가를 제외한 글로벌 권리를 양수하는 라이센스 인(License-in) 계약을 2020년 03월 25일자로 체결하였습니다. 아필리아(Apealea)는 2020년 1월 유럽에서 난소암 치료제로 공식 시판허가를 받은 약물로, 당사는 최초 계약체결 당시 2020년 2분기부터 유럽 매출이 발생할 것으로 예상했으나, 판권계약 재조정으로 인해 매출발생이 지연되었으며 2021년 6월 17일 계약서 내용을 조정하여 다시 계약을 체결하였습니다.
| [Vivesto와 Elevar 간의 아필리아 권리 양수도 계약 주요 내용] |
| 구분 | 내용 | 비고 |
|---|---|---|
| 계약 체결 당사자 | - 비베스토(Vivesto, 舊 Oasmia) Pharmaceutical AB. ("Licensor") - Elevar Therapeutics, Inc. ("Licensee") |
- |
| 계약 법률자문 | LATHAM & WATKINS | - |
| 계약 체결일 | 2020-03-25 (계약의 효력 발생일) | 계약서내용 조정일 2021-06-17 |
| 양수도 대상 권리 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 의약품 아필리아("Apealea")에 대한 전용 특허 실시권 및 다음의 염조성물 특허 실시권 - 화학명 N-(all-trans-retinoyl)-L-cysteic acid methyl ester sodium salt - 화학명 N-(13-cis-reinoyl)-L-cysteic acid methyl ester sodium salt |
계약상 권리를 가지는 지역은 미국, 중국, 일본, 한국, 호주 등의 국가와 독일,영국, 스위스 등 유럽의 다수 국가를 포함 |
| 계약금(Upfront Payment) | "Licensee"는 환불 불가한 조건의 계약금 미화 2천만 달러(USD 20,000,000)를 계약의 효력 발생일로부터 30일이 되는 날 또는 그 이전에 지급 | - |
| 조건부 지불 | [상업화 승인에 따른 Milestones] - 미국내 상용화 FDA 첫 승인 시 ("최초 적응증"), 2천만 달러 - "최초 적응증" 이외의 적응증으로 미국내 상용화 FDA 첫 승인 시 ("두번째 적응증"), 1천 5백만달러 - "최초 적응증" 및 "두번째 적응증" 이외의 적응증으로 미국내 상용화 FDA 첫 승인 시("세번쨰 적응증),1천 5백만달러 - 중국내 상용화 NMPA(중국내 국가약품감독관리국) 첫 승인 시 : 난소암 1백만 달러, 비소세포 폐암 6백만 달러, 방광암 6백만 달러, 위암 2백만 달러 - 일본내 상용화 PMDA(일본내 의약품의료기기종합기구) 첫 승인 시 : 난소암 1백 5십만 달러, 비소세포 폐암 6백만 달러, 방광암 5백만 달러, 위암 2백 5십만 달러 - 미국, 중국, 일본, 캐나다 및 스위스 외 10개 국가의 관할 기관으로부터 첫 상용화 승인시 국가당 10만 달러(국가당 1회), 최대 1백만 달러이내 |
- |
| [판매 금액 기록에 따른 Milestones] 판권을 보유하는 지역에서의 판매금액 - 5천만 달러 이상 최초 달성 시, 5백만 달러 - 7천 5백만 달러 이상 최초 달성 시, 7백 5십만 달러 - 1억 달러 이상 최초 달성 시, 1천만 달러 - 5억 달러 이상 최초 달성 시, 5천만 달러 - 10억 달러 이상 최초 달성 시, 1억 달러 - 20억 달러 이상 최초 달성 시, 1억 5천 달러 - 40억 달러 이상 최초 달성 시, 2억 7천 5백만 달러 |
- | |
| [로열티율] 1) 판권을 보유하는 중국 내 지역에서 발생하는 연 순매출의 10% 로열티 2) 판권을 보유하는 중국 외 지역에서 발생하는 연 순매출의 경우, - 미국내 상용화 FDA 첫 승인 전, 10% 로열티 - 미국내 상용화 FDA 첫 승인 후, : 1억 달러 미만 15% 로열티, 1억 달러 이상 10억 달러 미만 20% 로열티, 10억 달러 이상 25% 로열티 |
연간 판매금액에 해당하는 지급률을 곱하여 산출된 금액을 분기별로 나누어 지급 |
| 주) 계약상 정해진 구체적인 milestone 금액이나 로열티 지급률은 당사의 경영상 및 계약상 기밀 유지 사항으로 본 증권신고서상에 상세히 기재할 수 없습니다. |
3세대 개량신약인 아필리아는 Vivesto의 독점 기술 플랫폼인 'XR17'을 사용하여 개발된 항암제로, 항암제 주입 전 사전처치가 필요 없고 짧은 주사제 주입 시간으로 환자의 편의성은 증대시키면서 부작용은 최소화한 의약품으로 평가받고 있습니다.
아필리아의 성분명 파클리탁셀(paclitaxel)은 1992년 BMS 사에서 탁솔(Taxol®)이라는 제품명의 1세대 항암제로 출시된 이후 유방암, 난소암, 폐암 등으로 적응증을 확대하며 28년째 판매 중인 세포독성항암제입니다. 파클리탁셀 성분의 2세대 개량 약물인 아브락산(Abraxane)의 2021년 연간 글로벌 매출이 약 11.8억 달러(약 1.5조원)임을 고려하면, 2세대 대비 개량된 3세대 개량신약 아필리아의 시장성 전망은 당사가 판단하기에 긍정적입니다.
Elevar는 계약에 의하여 Vivesto에게 2020년 04월 25일까지 계약금(Upfront) 2,000만 달러(약 240억원)를 지불할 예정이였으며, 당초 2020년에 진행한 주주배정후 실권주 일반공모 유상증자 납입 이후 납입금으로 당사가 Elevar에 지원하는 금원을 사용하여 지불할 예정이였습니다. 다만, 아필리아 권리 양수가 예상보다 조기에 진행되어, 계약금 조달을 위한 단기차입을 추진했으며 유상증자 납입 이후 해당 단기차입금을 즉시 상환했습니다. 당사가 동 지분 취득을 위한 단기차입금 증가 및 상환과 관련하여 금융감독원 전자공시시스템에 공시한 내용은 다음과 같습니다.
| [단기차입금 증가결정](2020.04.08) |
| 1. 단기차입내역 | 차입금액(원) | 60,000,000,000 | |
| 자기자본(원) | 211,541,924,711 | ||
| 자기자본대비(%) | 28.4 | ||
| 2. 단기차입금총액 변경내역(원) | 차입전 | 차입후 | |
| -기업어음(원) | - | - | |
| -금융기관 차입(원) | - | 60,000,000,000 | |
| -당좌차월한도(원) | - | - | |
| -금융기관외의 자로부터 차입(원) | - | - | |
| -사모사채(만기 1년이하)(원) | - | - | |
| -기타차입(원) | - | - | |
| -단기차입금 합계(원) | - | 60,000,000,000 | |
| 3. 차입목적 | 타법인주식취득을 위한 자금확보 | ||
| 4. 차입형태 | 금융기관 차입 | ||
| 5. 이사회결의일(결정일) | 2020-04-08 | ||
| -사외이사 참석여부 | 참석(명) | 3 | |
| 불참(명) | 0 | ||
| -감사(감사위원) 참석여부 | 불참 | ||
| 6. 공정거래위원회 신고대상 여부 | 미해당 | ||
| 7. 기타 투자판단에 참고할 사항 | - 상기 자기자본은 코스닥시장공시규정 제2조 제6항에 따라 최근 사업연도말(2019년 12월 31일) 연결재무제표 자기자본에서 공시사유 발생일까지의 자본금 및 자본잉여금의 증감액을 반영한 금액임 - 상기1. 단기차입내역상 차입금액의 담보는 당사가 보유한 에이치엘비생명과학㈜ 주식 8,700,000주임 - 차입기간은 2020년04월10일~2020년07월27일이며, 만기 약 3개월인 단기차입임 |
||
| ※관련공시 | - | ||
| [단기차입금 감소결정(자율공시)](2020.06.10) |
| 1. 단기차입금 감소금액(원) | 60,000,000,000 | ||
| -자기자본 (원) | 550,672,580,671 | ||
| -자기자본대비 (%) | 10.9 | ||
| 2. 단기차입금총액 변동내역(원) | 변동전 | 변동후 | |
| 60,000,000,000 | - | ||
| 3. 변경사유 | 단기차입금 상환 | ||
| 4. 이사회결의일(결정일) | 2020-06-10 | ||
| -사외이사 참석여부 | 참석(명) | 2 | |
| 불참(명) | 1 | ||
| -감사(사외이사가 아닌 감사위원) 참석여부 | 불참 | ||
| 5. 기타 투자판단에 참고할 사항 | - 상기 자기자본은 코스닥시장공시규정 제2조 제6항에 따라 최근 사업연도말(2019년 12월 31일) 연결재무제표 자기자본에서 공시사유 발생일까지의 자본금 및 자본잉여금의 증감 액을 반영한 금액임 - 상기 단기차입금 상환은 2020년 04월 08일 금융기관 차입건에 대한 만기일 이전 상환임 - 단기차입담보로 설정된 당사가 보유한 에이치엘비생명과학㈜ 주식 8,700,000주는 차입금상환에 따라 금일 담보권설정 해지됨 |
||
| ※관련공시 | 2020-04-08 단기차입금증가결정 | ||
| (자료: 금융감독원 전자공시시스템) |
아필리아는 현재 북유럽과 러시아에서 판매 중이며, Elevar에서는 이런 잠재력을 높이 평가해 2020년 3월 아필리아의 글로벌 판권(러시아, 북유럽 일부 국가 제외)을 인수하였습니다. 인수 후 2020년 4월 미국 FDA와 Pre-NDA 미팅을 진행하였고, 1차 평가지표에 대한 선정에 대한 이견으로 FDA 승인이 어렵다는 답변을 받게 되었습니다. 그 결과, 아필리아의 미국 FDA 승인을 위해선 추가 임상시험이 필요했고, 이는 시간과 임상 비용 추가 투입을 의미합니다. 이에, 당사는 회사와 주주의 피해를 줄이기 위해 원 개발사인 Vivesto와 Apealea 판권 계약 재조정을 요청했습니다. 재조정 위한 양사간 의견 차이를 좁히는데 시간이 소요되었고, 2021년 6월 판권 계약의 재조정이 완료되었습니다. 판권 계약 재조정 기간 동안 아필리아에 개발에 대한 부분은 부득이하게 지연 및 중단 상태였습니다.
다만 임상 개발과는 별개로, 당사와 Elevar는 계약 조정 이후 빠른 상업화를 위해 내부적으로 신규 적응증 개발 및 상업화 업무는 지속 전개해왔고, 그 내역은 아래와 같습니다.
(1) 기 승인받은 지역 대상 판매 준비
글로벌 제약 유통 기업인 Inceptua(유럽 지역 담당), Taiba(중동 북아프리카 지역 담당), Tanner(남미 지역 담당) 와 Apealea 유통 계약을 체결해 유럽과 중동 지역에 대한 판매 사전 준비를 하고 있습니다. 최근 독일, 영국 등 개별국 판매를 위한 절차가 진행되고 있으나, 2019년부터 발생된 코로나의 영향과 비베스토(Vivesto, 舊 Oasmia)와의 계약 재조정으로 인해 전체적인 일정이 지연되었습니다. 각 개별국 승인 이후 첫 판매 개시는 올 하반기로 예상됩니다.
(2) 중국 진출을 위한 JV 논의
아필리아의 상업화 지역 확대 전략으로 중국 진출을 적극 검토 중입니다. 중국 시장의 특수성을 감안해 독자 진출 보다는 현지 업체와의 JV를 통해 우회 진출이 유리하다고 판단하여, 현재 중국의 A社와 JV 설립을 위한 논의가 진행 중입니다.
(3) 추가 적응증 개발
아필리아는 2021년부터 미국 내 부인과종양학그룹인 GOG(Gynecologic Oncology Group) 소속 임상의들과 추가 적응증 개발을 위한 논의를 하고 있습니다. 현재 백금계 약물 저항성이 있는 난소암 환자를 대상으로 아필리아와 리보세라닙과의 병용 임상시험에 대해 계획하고 검토하고 있습니다.
당사는 아필리아의 시장성을 긍정적으로 전망하는 바이나, 이는 어디까지나 당사의 예상으로, 시판이 개시된 이후 판매량과 수익성에 대하여는 현재 시점에서 정확한 예측이 불가능하다는 점에 유의하시고 투자판단에 임하시기 바랍니다. 당사의 예상과 달리 아필리아의 판매 실적이 저조할 경우 권리 양수를 위해 지출한 비용에 비하여 향유하는 수익이 적거나 없을 가능성을 배제할 수 없습니다.
또한, 아필리아가 북유럽 일부 국가 및 러시아에서 이미 판매되고 있다는 사실에도 불구하고, 향후 다른 유럽 지역 국가들과 미주 및 아시아 지역에서 실제로 판매가 개시되는 시점은 당사가 현재 예상하고 있는 시점과 달라질 수 있는 가능성이 상존한다는 점에도 유의하시기 바랍니다.
|
타. 최대주주 및 특수관계인 지분희석 및 경영권 관련 위험 |
1) 대표이사 변경 이력 및 최대주주, 특수관계인의 현황
당사의 대표이사는 2017년 이후 증권신고서 제출일 전일까지 네 차례 변경되었습니다.
| [당사 대표이사 변동 내역] |
| 연도 | 변동 전 | 변동 후 |
|---|---|---|
| 2009. 01 | 대표이사 김영세 | 대표이사 남상우 |
| 2012. 01 | 대표이사 남상우 | 대표이사 박정민 |
| 2017. 06 | 대표이사 박정민 | 대표이사 진양곤 |
| 2019. 03 | 대표이사 진양곤 | 각자 대표이사 김하용, 김성철 |
| 2019. 06 | 각자 대표이사 김하용, 김성철 | 대표이사 진양곤 |
| 2021. 03 | 대표이사 진양곤 | 각자 대표이사 진양곤, 김동건 |
증권신고서 제출일 현재 당사의 대표이사는 진양곤 대표이사 회장으로, 2017년 6월 당사의 대표이사로 처음 선임되었다가 2019년 3월 김하용, 김성철 각자대표 체제로 변경된 후 3개월만인 2019년 6월 다시 단독 대표이사로 재선임되었습니다. 이후 2021년 03월 다시 경영효율성 제고 및 책임경영 강화를 위한 각자 대표이사 체제 구축을목적으로 진양곤 대표이사 및 김동건 대표이사 각자 대표이사 체제로 변경되었습니다. 짧은 시일 내에 잦은 경영진의 변동은 기업의 대외신뢰도 및 경영진의 전문성 및 조직의 운영 측면 등에 좋지 않은 영향을 미칠 가능성이 있으나, 현 각자대표이사 중 한명인 진양곤 대표이사는 10년 이상 당사의 임원을 역임하였으며, 객관적 지표 및 경력에서 경영능력에 결격사유가 없는 것으로 판단됩니다.
진양곤 대표이사 회장은 2009년 01월 에이치엘비㈜의 이사로 처음 취임하였으며, 2017년 06월 당사의 대표이사로 최초 선임된 후 현재 당사의 관계회사 다수의 이사직을 겸임하고 있습니다. 김동건 대표이사는 2021년 03월 에이치엘비㈜의 이사로 처음취임하였으며, 2021년 03월 당사의 각자 대표이사로 최초 선임된 후 현재 당사의 종속회사인 Elevar 및 Immunomic의 이사직을 겸임하고 있습니다.
| [대표이사의 관계회사 내 겸직현황] |
| 겸직임원 | 겸직회사 | |||
|---|---|---|---|---|
| (당사)직 책 | 성 명 | 회사명 | 직 책 | 상근여부 |
| 대표이사/ 회장 | 진양곤 | 에이치엘비생명과학㈜ | 이사 | O |
| Elevar Therapeutics,Inc | 이사 | X | ||
| Immunomic Therapeutics,Inc | 이사 | X | ||
| HLB글로벌㈜ | 이사 | X | ||
| 에이치엘비테라퓨틱스㈜ | 이사 | X | ||
| 에이치엘비네트웍스㈜ | 이사 | X | ||
| 에이치엘비제약㈜ | 이사 | X | ||
| 바다중공업㈜ | 이사 | X | ||
| 에이치엘비셀㈜ | 이사 | X | ||
| ㈜엘에스케이인베스트먼트 | 이사 | X | ||
| 에이치엘비일렉㈜ | 이사 | X | ||
| Hyundai Lifeboats Singapore Pte. Ltd | 이사 | X | ||
| HLB사이언스㈜ | 이사 | X | ||
| ㈜프레시코 | 이사 | X | ||
| ㈜코아바이오 | 이사 | X | ||
| 에포케㈜ | 이사 | X | ||
| 에이치엘비인베스트먼트㈜ | 이사 | X | ||
| ㈜노터스 | 이사 | X | ||
| Hyundai Lifeboats Shanghai Co.,Ltd | 감사 | X | ||
| 대표이사 | 김동건 | Elevar Therapeutics, Inc. | 이사 | O |
| Immunomic Therapeutics,Inc | 이사 | X | ||
증권신고서 제출일 현재 당사의 등기임원 현황은 다음과 같습니다.
| (기준일 : | 2022년 09월 23일 | ) | (단위 : 주) |
| 성명 | 성별 | 출생년월 | 직위 | 등기임원 여부 |
상근 여부 |
담당 업무 |
주요경력 | 소유주식수 | 최대주주와의 관계 |
재직기간 | 임기 만료일 |
|
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 의결권 있는 주식 |
의결권 없는 주식 |
|||||||||||
| 진양곤 | 남 | 1966.01 | 회장 / 대표이사 |
사내이사 | 상근 | 이사회의장 / 경영총괄 |
연세대학교 경제학 대학원 졸업(1993.02) 현. 에이치엘비㈜ 대표이사 현. 에이치엘비생명과학㈜ 이사 현. 에이치엘비제약㈜ 이사 |
8,610,902 | - | 최대주주 본인 | 12년 | 2023.03.30 |
| 김동건 | 남 | 1962.03 | 대표이사 | 사내이사 | 상근 | 경영총괄 | Harvard Law School 졸업(1986.06) 현. 에이치엘비㈜ 대표이사 전. 에이치엘비㈜ 경영총괄 사장 (2020.06~2021.02) 전. ㈜다날 부회장 (2019.02~2020.05) |
- | - | 계열회사 임원 | 1년 | 2024.03.30 |
| 도순기 | 남 | 1969.04 | 사장 | 사내이사 | 상근 | HLB ENG 사업부총괄 |
방송통신대학교 경영학과 졸업(2003.02) 현. 에이치엘비㈜ HLB ENG사업부 사장 전. 에이치엘비㈜ 노마드팀 사장 (2019.06~2021.10) 전. 에이치엘비㈜ 복합소재사업본부 사장 (2017.11~2019.06) |
4,864 | - | 계열회사 임원 | 4년 | 2023.03.30 |
| 황제이정환 | 남 | 1963.01 | 사장 | 사내이사 | 상근 | 마케팅총괄 | Univ. of Illinois at Urbana-Champaign 마케팅대학원 졸업(1992.05) 현. 에이치엘비㈜ 노마드팀 사장 전. JSAA Healthcare 대표이사 (2021.02~2021.10) 전. ㈜쎌바이오텍 해외사업본부장 (2019.02~2021.01) |
- | - | 해당사항 없음 | 1년 | 2025.03.30 |
| 문정환 | 남 | 1962.07 | 대표이사 | 사내이사 | 비상근 | 홍보총괄 | 고려대학교 경영대학원 졸업(1999.06) 현. ㈜노터스 대표이사 전. 에이치엘비㈜ 대외협력부문 부사장 (2019.07~2022.03) 전. 국가정보원(NIS) (1987.06~2015.06) |
- | - | 계열회사 임원 | 2년 | 2023.03.30 |
| Matthew Chang |
남 | 1974.01 | 상무 | 사내이사 | 상근 | 경영전략 / IR |
McGill University 경영대학원 졸업(2000.08) 현. 에이치엘비㈜ 상무 전. HLB USA, Inc. Secretary (2019.06~2019.11) 전. Mizuho Securities 이사 (2018.01~2018.12) |
- | - | 해당사항 없음 | 2년 | 2023.03.30 |
| William G. Hearl |
남 | 1957.04 | 이사 | 사내이사 | 비상근 | 바이오 | Univ. of Tennessee 생화학대학원 졸업 (1984.08) 현. Immunomic Therapeutics, Inc. 대표이사 전. Capital Genomix, Inc. 대표이사 (2000.08~2005.09) 전. Kirkegaard & Perry Laboratories 이사 (1994.05~2000.08) |
- | - | 계열회사 임원 | 2년 | 2023.03.31 |
| 박진국 | 남 | 1948.04 | 이사 | 사외이사 | 비상근 | 사외이사 | 뉴욕대학교 경영대학원 졸업(1986.06) 현. 에이치엘비㈜ 사외이사 현. 성도이현회계법인 고문 현. 제이씨현시스템㈜ 사외이사 |
- | - | 해당사항 없음 | 4년 | 2023.03.30 |
| 최규준 | 남 | 1964.10 | 이사 | 사외이사 | 비상근 | 사외이사 | 중앙대학교 무역학과 졸업(1988.02) 현. 에이치엘비㈜ 사외이사 현. ㈜엔솔바이오사이언스 사외이사 전. 한국IR협의회 부회장 (2017.01~2019.02) |
- | - | 해당사항 없음 | 3년 | 2025.03.30 |
| 심재철 | 남 | 1956.04 | 이사 | 사외이사 | 비상근 | 사외이사 | Univ. of Wisconsin 매스컴학대학원 졸업 (1992.05) 현. 에이치엘비㈜ 사외이사 현. 고려대학교 미디어학부 명예교수 전. 고려대학교 언론대학원장 (2015.04~2017.02) |
- | - | 해당사항 없음 | 2년 | 2023.03.30 |
| 김용웅 | 남 | 1958.06 | 감사 | 감사 | 상근 | 감사 | 서울대학교 경영학과 대학원 졸업(1985.08) 현. 에이치엘비㈜ 상근감사 전. 신용관리기금(現 금융감독원) (1986.09~1998.06) |
4,864 | - | 해당사항 없음 | 12년 | 2023.03.30 |
당사의 등기임원 11명 중 진양곤 대표이사와 김용웅 감사 등 2명은 재직기간이 10년이상으로, 안정적인 경영 체제를 유지하고 있습니다. 당사의 지분 1.31% 및 0.77%를 보유한 계열회사인 에이치엘비생명과학㈜ 및 에이치엘비셀㈜의 기업현황은 아래와 같습니다.
| [에이치엘비생명과학㈜ 기업 현황] |
| 구 분 | 내 용 |
|---|---|
| 기업명 | 에이치엘비생명과학㈜ |
| 기업의 형태 | 일반법인, 코스닥상장기업 |
| 소재지 | 경기도 화성시 동탄첨단산업1로 51-9 8층(영천동,엠타워지식산업센터) |
| 대표자 | 남상우, 한용해(각자대표) |
| 설립일 | 1998년 07월 24일 |
| 재무현황(21년, 연결) (주1) |
매출액 53,494백만원, 당기순이익 -49,292백만원 자산 270,799백만원, 부채 24,188백만원, 자본 246,612백만원 |
| 업종명 | 기타 엔지니어링 서비스업 |
| 최대주주 등 | 에이치엘비(19.60%) |
| 자료 : | 금융감독원 전자공시시스템 |
| [에이치엘비셀㈜ 기업 현황] |
| 구 분 | 내 용 |
|---|---|
| 기업명 | 에이치엘비셀㈜ |
| 기업의 형태 | 일반법인 |
| 소재지 | 경기도 화성시 동탄첨단산업1로 51-9, 8층 |
| 대표자 | 이두훈 |
| 설립일 | 2009년 09월 16일 |
| 재무현황(21년, 별도) | 매출액 12백만원, 당기순이익 -10,940백만원 자산 38,113백만원, 부채 1,055백만원, 자본 37,057백만원 |
| 사업의 내용 | 바이오의약품 개발 |
| 최대주주 등 | 에이치엘비생명과학㈜(99.27%) |
| 자료 : | 에이치엘비셀㈜ 제시 |
진양곤 대표이사는 당사의 지분 8.05%를 보유하고 있으나, 당사 최대주주가 당사에 행사 중인 지배력이 높지 않은 상황이기 때문에 당사의 지배구조는 적대적 M&A 또는 경영권 분쟁 등에 취약한 것으로 판단됩니다.
2) 지분율 변동 시뮬레이션
금번 유상증자에 있어서 최대주주인 진양곤 회장은 771,151주(유상증자 신주 수의 8.06%), 에이치엘비생명과학㈜는 125,308주(유상증자 신주 수의 1.31%), 에이치엘비셀㈜은 74,170주(유상증자 신주 수의 0.78%)를 배정 받았습니다.
금번 유상증자에 있어 에이치엘비생명과학㈜와 에이치엘비셀㈜는 배정물량에 전량 참여할 예정이며, 최대주주인 진양곤 회장과 이현아, 이현수, 진유림, 진인혜는 배정받은 증서를 매각한 분만큼 청약에 참여할 예정이며, 기타특수관계인의 참여여부는 미확정인 상태입니다. 다만, 상기 최대주주의 유상증자 청약 참여 여부 및 규모는 최종 발행가액 및 소요자금, 개인의 자금 사정 등으로 인하여 변경될 가능성이 있습니다. 최대주주의 실제 청약 참여 규모에 따라 유상증자 이후 최대주주의 지분율은 하락할 수 있고, 최대주주 및 특수관계인이 전량 청약에 참여하지 않을 경우를 가정하면 최대주주 및 특수관계인의 지분율 합계는 9.60%까지 하락할 수 있습니다.
| [최대주주 및 특수관계인 청약 가정 시 지분율 변동 시뮬레이션] |
| (단위 : 주, %) |
| 주주명 | 2022-08-12 기준 | 배정주식수 | 배정주식수 /신주발행주식수 |
청약(예정) 주식수 |
유상증자 후 | ||
|---|---|---|---|---|---|---|---|
| 보유주식수 | 지분율 | 보유주식수 | 지분율(%) | ||||
| 진양곤 | 8,610,902 | 8.05% | 771,151 | 8.06% | 100,250 | 8,711,152 | 7.48% |
| 에이치엘비생명과학㈜ | 1,399,230 | 1.31% | 125,308 | 1.31% | 125,308 | 1,524,538 | 1.31% |
| 에이치엘비셀㈜ | 828,214 | 0.77% | 74,170 | 0.78% | 74,170 | 902,384 | 0.77% |
| 이현아 | 230,772 | 0.22% | 20,666 | 0.22% | 2,687 | 233,459 | 0.20% |
| 이현수 | 89,756 | 0.08% | 8,038 | 0.08% | 1,045 | 90,801 | 0.08% |
| 진유림 | 8,230 | 0.01% | 737 | 0.01% | 57 | 8,287 | 0.01% |
| 진인혜 | 8,180 | 0.01% | 732 | 0.01% | 57 | 8,237 | 0.01% |
| 김용웅 | 4,864 | 0.00% | 435 | 0.00% | - | 4,864 | 0.00% |
| 도순기 | 4,864 | 0.00% | 435 | 0.00% | - | 4,864 | 0.00% |
| 합계 | 11,185,012 | 10.46% | 1,001,672 | - | 303,574 | 11,488,586 | 9.86% |
| (주1) 최대주주 및 특수관계인의 참여 주식을 제외한 잔여 신주인수권은 전액 기타주주에 매각됨을 가정하여 산정하였습니다. (주2) 진양곤 회장과 이현아, 이현수, 진유림, 진인혜는 배정수량의 13% 참여를 가정했으며, 참여 비율은 증서매각 가격에 따라 변동가능합니다. (주2) 지분율은 의결권이 있는 보통주식(총 106,903,481주)을 기준으로 산정되었습니다. (08-11 전환청구된 20,736주 반영) |
| [최대주주 및 특수관계인 청약 미참여 가정 시 지분율 변동 시뮬레이션] |
| (단위 : 주, %) |
| 주주명 | 2022-08-12 기준 | 배정주식수 | 배정주식수 /신주발행주식수 |
청약(예정) 주식수 |
유상증자 후 | ||
|---|---|---|---|---|---|---|---|
| 보유주식수 | 지분율 | 보유주식수 | 지분율(%) | ||||
| 진양곤 | 8,610,902 | 8.05% | 771,151 | 8.06% | - | 8,610,902 | 7.39% |
| 에이치엘비생명과학㈜ | 1,399,230 | 1.31% | 125,308 | 1.31% | - | 1,399,230 | 1.20% |
| 에이치엘비셀㈜ | 828,214 | 0.77% | 74,170 | 0.78% | - | 828,214 | 0.71% |
| 이현아 | 230,772 | 0.22% | 20,666 | 0.22% | - | 230,772 | 0.20% |
| 이현수 | 89,756 | 0.08% | 8,038 | 0.08% | - | 89,756 | 0.08% |
| 진유림 | 8,230 | 0.01% | 737 | 0.01% | - | 8,230 | 0.01% |
| 진인혜 | 8,180 | 0.01% | 732 | 0.01% | - | 8,180 | 0.01% |
| 김용웅 | 4,864 | 0.00% | 435 | 0.00% | - | 4,864 | 0.00% |
| 도순기 | 4,864 | 0.00% | 435 | 0.00% | - | 4,864 | 0.00% |
| 합계 | 11,185,012 | 10.46% | 1,001,672 | - | - | 11,185,012 | 9.60% |
| (주1) 상기 표는 최대주주 및 특수관계인의 전량 미참여를 가정하여 작성되었습니다. |
| (주2) 최대주주 및 특수관계인의 참여 주식을 제외한 잔여 신주인수권은 전액 기타주주에 매각됨을 가정하여 산정하였습니다. (주3) 지분율은 의결권이 있는 보통주식(총 106,903,481주)을 기준으로 산정되었습니다. |
상기 최대주주 등의 지분율 변화 시뮬레이션은 증권신고서 제출일 현재 예정발행가액 34,050원을 기준으로 산출하였으며, 예정발행가액을 기준으로 계산하였기 때문에, 향후 최종 발행가액이 확정됨에 따라서 최대주주 지분율 희석 정도가 변동될 수 있습니다. 최종발행가액이 하락할 경우, 최대주주의 지분율 희석은 제한적일 것으로 판단되나, 최종발행가액이 상승할 경우, 최대주주의 청약 및 납입 부담이 증가하여 참여 수량이 축소할 가능성이 있으며, 이 경우 지분율 희석 효과는 커질 것으로 판단됩니다. 이처럼, 향후 발행가액 최종 결정에 따라 최대주주의 지분율 희석 정도가 변동 가능한점 투자자께서는 유의하시기 바랍니다.
한편, 최대주주 등이 미참여하는 물량에 대한 신주인수권증서는 장외 및 상장시장을 통해 매도함으로써 다른 증서 인수인이 구주주 청약에 참여할 수 있도록 할 예정입니다. 신주인수권증서를 매수하는 투자자는 단기적으로 할인율에서 발생하는 차익을 실현하고자 신주가 상장되는 즉시 보유 주식을 장내매도할 수 있으며, 이에 따라 주가가 하락할 수 있으니 이에 유의하시기 바랍니다.
[유상증자 이후 전환사채(신주인수권부사채)의 보통주 전환(행사)]
한편, 당사가 발행한 전환사채 및 신주인수권부사채의 주식 전환(행사)시 최대주주 및 특수관계인의 지분율이 추가적으로 하락할 가능성이 있습니다. 2022년 09월 23일 증권신고서 제출일 기준 과거 발행된 미상환 주식관련사채의 발행 개요는 다음과 같습니다.
| [미상환 전환사채 및 신주인수권부사채 세부내역] |
| (기준일: 2022년 09월 23일) |
| 종 류 | 발행일 | 만기일 | 전자등록 총액 |
표면 이자율 |
만기 이자율 |
전환(행사)청구 가능기간 |
조기상환 청구권(Put option) |
전환(행사)가액 | 잔액 | 전환(행사)가능 주식수 |
|---|---|---|---|---|---|---|---|---|---|---|
| 33회차 사모 전환사채 |
19.12.18 |
22.12.18 |
40,000 |
0.0% | 1.0% | 20.12.18~22.11.18 |
21.08.18~22.11.18 (매 3개월) |
33,757 |
1,400 | 41,472 |
| 34회차 사모 비분리형 신주인수권부사채 |
21.10.20 |
26.10.20 |
57,000 |
0.0% | 1.0% | 22.10.20~26.09.20 |
23.10.20~26.07.20 (매 3개월) |
35,884 |
57,000 | 1,588,451 |
| 35회차 사모 비분리형 신주인수권부사채 |
22.03.30 |
25.03.30 |
25,200 |
0.0% | 2.0% | 23.03.30~25.02.30 |
23.03.30~24.12.30 (매 3개월) |
30,811 |
21,000 | 681,574 |
| 36회차 사모 전환사채 |
22.06.02 |
25.06.02 |
23,000 |
1.0% | 3.0% | 23.06.02~25.05.02 |
23.12.02~25.03.02 (매 3개월) |
48,605 |
23,000 | 473,202 |
| 37회차 사모 비분리형 신주인수권부사채 |
22.06.02 |
25.06.02 |
17,000 |
1.0% | 3.0% | 23.06.02~25.05.02 |
23.12.02~25.03.02 (매 3개월) |
48,605 |
17,000 | 349,758 |
| 합 계 | 119,400 | 3,134,457 | ||||||||
이렇듯 당사가 발행한 미상환 상태로 남아있는 전환사채가 주식으로 전환 될 경우 최대주주 및 특수관계인의 지분율이 추가로 하락할 가능성이 있습니다. 상기 전환사채의 전환권 행사로 발행될 수 있는 신주의 총수는 3,134,457주로 2022년 09월 23일 현재 당사의 보통주 발행주식 총수의 2.9%에 해당합니다.
최대주주 및 특수관계인의 전량 미청약을 가정할 시, 본 유상증자 이후 상기 전환사채가 전량 주식으로 전환될 경우 최대주주 진양곤의 지분율은 기존 8.05%에서 7.20%까지, 최대주주 및 특수관계인의 지분율 합계는 기존 10.46%에서 9.35%까지 변동될 수 있습니다. 향후 주식시장 및 시장상황에 따라 전환사채의 주식 전환으로 인한 최대주주 및 특수관계인의 지분변화 가능성을 배제하기는 어렵습니다. 투자자께서는 이 점에 유의하여 투자판단을 하시기 바랍니다.
상기 기술한 바와 같이 최대주주 및 특수관계인의 낮은 지분율은 적대적 M&A등의 위험성을 내포할 수 있으며, 이러한 점은 경영진 변동의 위험성으로 이어져 안정적인경영활동이 어려울 수 있습니다. 또한, 장기적으로 향후 추가적인 유상증자, 주식관련 사채의 발행, 우선주의 전환 등으로 최대주주 및 특수관계인 등의 지분율이 재차 희석될 가능성은 존재하며 이에 따른 지속적인 모니터링이 필요한점 투자자 여러분께서는 유의하여주시기 바랍니다.
|
파. 제재 관련 리스크 |
당사는 종속회사인 Elevar Therapeutics, Inc.(구,HLB USA, Inc.)를 통해 리보세라닙임상시험을 진행하고 있습니다. 현재 간암(Hepatocellular carcinoma) 1차 치료제, 대장암(Colorectal cancer) 3차 치료제, 위암(Gastric cancer) 2차 치료제, 선양낭성암(Adenoid cystic carcinoma)에 대해서 임상시험중에 있습니다. 간암 1차 치료제를 위해서 항서제약의 면역항암제 PD-1 inhibitor인 캄렐리주맙(Camrelizumab)과 병용요법으로 글로벌 임상 3상을 진행중에 있고, 대장암 3차 치료제로 타이호제약의 론서프(Lonsurf)와 임상 1/2상을 진행중에 있습니다. 위암 2차 치료제로서 파클리탁셀(Paclitaxel)과 병용요법으로 임상 1/2상을, 선양낭성암에 대해서 리보세라닙 단독요법으로 임상 2상을 진행하고 있습니다 그리고 미국 서던 캘리포니아 암센터에서육종(Sarcoma)에 대해서 BMS의 면역항암제 옵디보(Nivolumab)의 병용임상시험을 종료하였습니다.
리보세라닙 임상과 관련하여 금융감독원은 2019년 9월 당사의 미국 자회사 Elevar가 개발한 표적항암제 리보세라닙의 임상3상 시험 결과와 관련한 발표에 대해 자본시장법 위반 혐의가 있다고 보고 조사를 진행하였습니다. 당사는 글로벌 임상 3상 결과를 바탕으로 미국 FDA에 신약 허가를 신청할 계획이었으나, 금융감독원은 당사가임상 3상 결과를 자의적으로 해석한 것으로 판단하였습니다. 금융감독원은 당사에 대한 불공정거래 혐의 조사에 따라, 2020년 10월 16일 검찰 고발 의견으로 조치예정내용 사전통지서를 송부하였고, 이후 본 사건은 자본시장조사심의위원회 심의를 거쳐 증권선물위원회에 상정되었습니다.
증권선물위원회는 이 사건에 대해 수 차례에 걸친 논의 끝에 2021년 09월 15일 개최된 2021년도 제17차 정례회의에서 당사와 대표이사 1인에 대하여 한단계 수위를 낮춰 '검찰통보' 조치로 의결하였습니다. 이후 검찰 조사가 진행됐으며, 2022년 3월 14일 검찰은 당사와 대표이사1인의 불공정거래 혐의에 대해 '혐의없음(무혐의)' 처분을내리며 관련한 모든 조사가 종결됐습니다. 당사는 기업경영의 투명성을 더욱 높이고 내부통제를 강화해 향후금융당국의 불필요한 오해나 의심을 받지 않도록 최선을 다하겠습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| 구분 | 내용 |
|---|---|
| 일자 | 2022.03.14 |
| 처벌 또는 조치대상자 | 現대표이사 중 1인 |
| 처벌 또는 조치내용 | 금융감독원은 당사의 불공정거래 의혹에 대해 양벌규정을 적용, 당사의 現대표이사 중 1인에게도 동일한 혐의를 주장했으나, 2022년 3월 14일 검찰에서 ‘혐의없음(무혐의)’ 처분을 내림에 따라 어떤 처벌없이 모든 사건이 종결됐습니다. |
| 사유 및 근거법령 | 부정거래행위 금지 위반 등에 대한 조치 「자본시장조사 업무규정」 제36조 1항 |
| 처벌 또는 조치에 대한 회사의 이행현황 | 혐의없음(무혐의) |
| 재발방지를 위한 회사의 대책 | 관련 규정을 준수, 재발방지 만전 |
| 하. 특수관계자와의 거래에 따른 위험 당사는 2019년 특수관계자를 대상으로 약 17.7억원의 매출을 시현하였으며, 전년에는 특수관계자향 매출이 약 68.2억원 발생하였습니다. 2018년과 2019년 연간 특수관계자향 매출의 전체 연결기준 매출 대비 비중은 각각 18.86%와 4.61% 수준으로, 전년 대비 당사의 연결기준 특수관계자와의 매출거래 비중이 현저히 줄어들었습니다. 이는 2018년 특수관계자향 매출 중 가장 컸던 현대요트㈜와 에이치엘비네트웍스㈜로의 매출이 크게 감소한 것에 따릅니다. 당사의 매출 및 자산 규모에 비추어 보아 특수관계자와의 거래 비중은 유의미하게 크지 않은 것으로 판단되나, 향후 특수관계자향 매출이 증가하여 매출처의 편중이 나타날 가능성은 배제할 수 없으며, 이 경우 당사의 실질 영업경쟁력 약화로 해석될 우려가 있습니다. 또한, 특수관계자와의 거래 발생 시 거래 조건 등이 제3자와의 거래와 비교하여 적정성이 유지되지 않을 경우 당사의 주주가 향유하여야 할 이익이 특수관계자 측에 전가될 위험이 있습니다. 또한 특수관계자에 대한 채권 규모가 증가할수록 현금흐름 및 재무구조에는 부정적으로 작용할 가능성이 있습니다. 투자자분들께서는 이 점 유의하여 주시기 바랍니다. |
당사의 특수관계자는 관계기업 및 종속기업과 지배기업의 주요 경영진, 그리고 경영진이 출자 또는 임원으로 재직중인 기업입니다.
| [연결기준 특수관계자에 해당하는 기업] | |
| (기준일 : 2022년 06월 30일) | (연결기준) |
| 구 분 | 회사명 | 상장여부 |
|---|---|---|
| 관계기업 | 에이치엘비생명과학㈜ | 상장 |
| 에이치엘비테라퓨틱스㈜ | ||
| ㈜노터스 | ||
| Verismo Therapeutics, Inc. | 비상장 | |
| 바다중공업㈜ | ||
| 현대요트㈜ | ||
| 기타특수관계자 | HLB글로벌㈜ | 상장 |
| 에이치엘비제약㈜(구. ㈜메디포럼제약) | ||
| HLB사이언스㈜ (구. 단디바이오사이언스㈜) |
||
| ㈜엘에스케이인베스트먼트 | 비상장 | |
| ㈜고션 | ||
| 에이치엘비일렉㈜ | ||
| 에이치엘비네트웍스㈜ | ||
| Hyundai Lifeboats Singapore Pte. Ltd | ||
| 오티에스중공업㈜ | ||
| 현대코스모스요팅㈜ | ||
| ㈜신화어드밴스 | ||
| 에이치엘비엘이디㈜ | ||
| 에이치엘비에너지㈜(구. 거림) | ||
| ㈜펭귄오션레저 | ||
| 의령태양광1호㈜ | ||
| HLB생활건강㈜(구.엘리샤코이) | ||
| 에이치엘비셀㈜(구.라이프리버㈜) | ||
| ㈜프레시코 | ||
| ㈜코아바이오 | ||
| 에포케㈜(구.코르키㈜) | ||
| 지트리파마슈티컬 | ||
| REGENTREE | ||
| OBLATO | ||
| 바다엔지니어링㈜ | ||
| ㈜새론바이오 | ||
| 브이에스팜㈜ | ||
| ㈜온힐 | ||
| ㈜베리스모테라퓨틱스 아시아 | ||
| 에이치엘비생명과학알앤디㈜ | ||
| ㈜개밥왕 |
| [별도기준 특수관계자에 해당하는 기업] | |
| (기준일 : 2022년 06월 30일) | (별도기준) |
| 구 분 | 회사명 | 상장여부 |
|---|---|---|
| 종속기업 | Elevar Therapeutics, Inc. | 비상장 |
| Immunomic Therapeutics, Inc. | ||
| 에이치엘비인베스트먼트㈜ | ||
| Hyundai Lifeboats Shanghai PTE.LTD | ||
| 관계기업 | 에이치엘비생명과학㈜ | 상장 |
| 에이치엘비테라퓨틱스㈜ | ||
| ㈜노터스 | ||
| Verismo Therapeutics, Inc. | 비상장 | |
| 바다중공업㈜ | ||
| 현대요트㈜ | ||
| 기타특수관계자 | HLB글로벌㈜ | 상장 |
| 에이치엘비제약㈜ | ||
| HLB사이언스㈜ | ||
| ㈜화진메디칼 | 비상장 | |
| ㈜화진메디스 | ||
| ㈜엘에스케이인베스트먼트 | ||
| ㈜고션 | ||
| 에이치엘비일렉㈜ | ||
| 에이치엘비네트웍스㈜ | ||
| Hyundai Lifeboats Singapore Pte. Ltd | ||
| 오티에스중공업㈜ | ||
| 현대코스모스요팅㈜ | ||
| ㈜신화어드밴스 | ||
| 에이치엘비엘이디㈜ | ||
| 에이치엘비에너지㈜ | ||
| ㈜펭귄오션레저 | ||
| HLB생활건강㈜ | ||
| 에이치엘비셀㈜ | ||
| ㈜프레시코 | ||
| ㈜코아바이오 | ||
| 에포케㈜ | ||
| 지트리파마슈티컬 | ||
| REGENTREE | ||
| OBLATO | ||
| 바다엔지니어링㈜ | ||
| ㈜새론바이오 | ||
| 브이에스팜㈜ | ||
| ㈜온힐 | ||
| ㈜베리스모테라퓨틱스 아시아 | ||
| 에이치엘비생명과학알앤디㈜ | ||
| ㈜개밥왕 |
당사는 「상법」제382조(이사의 선임, 회사와의 관계 및 사외이사), 제542조의5(이사ㆍ감사의 선임방법) 및 제542조의8(사외이사의 선임)의 규정을 준수하고 있으며 증권신고서 제출전일 기준 당사 이사진의 계열회사 겸직 현황은 아래와 같습니다.
| [당사 이사진의 계열회사 겸직 현황] |
| 겸직임원 | 겸직회사 | |||
|---|---|---|---|---|
| (당사)직 책 | 성 명 | 회사명 | 직 책 | 상근여부 |
| 대표이사 / 회장 | 진양곤 | 에이치엘비생명과학㈜ | 이사 | O |
| Elevar Therapeutics,Inc | 이사 | X | ||
| Immunomic Therapeutics,Inc | 이사 | X | ||
| HLB글로벌㈜ | 이사 | X | ||
| 에이치엘비테라퓨틱스㈜ | 이사 | X | ||
| 에이치엘비네트웍스㈜ | 이사 | X | ||
| 에이치엘비제약㈜ | 이사 | X | ||
| 바다중공업㈜ | 이사 | X | ||
| 에이치엘비셀㈜ | 이사 | X | ||
| ㈜엘에스케이인베스트먼트 | 이사 | X | ||
| 에이치엘비일렉㈜ | 이사 | X | ||
| Hyundai Lifeboats Singapore Pte. Ltd | 이사 | X | ||
| HLB사이언스㈜ | 이사 | X | ||
| ㈜프레시코 | 이사 | X | ||
| ㈜코아바이오 | 이사 | X | ||
| 에포케㈜ | 이사 | X | ||
| 에이치엘비인베스트먼트㈜ | 이사 | X | ||
| ㈜노터스 | 이사 | X | ||
| Hyundai Lifeboats Shanghai Co.,Ltd | 감사 | X | ||
| 대표이사 | 김동건 | Elevar Therapeutics, Inc. | 이사 | O |
| Immunomic Therapeutics,Inc | 이사 | X | ||
| 상근감사 | 김용웅 | 현대요트㈜ | 감사 | X |
| 바다중공업㈜ | 감사 | X | ||
| 에이치엘비셀㈜ | 감사 | X | ||
| 에이치엘비네트웍스㈜ | 감사 | X | ||
| ㈜화진메디칼 | 감사 | X | ||
| ㈜신화어드밴스 | 감사 | X | ||
| ㈜프레시코 | 감사 | X | ||
| ㈜코아바이오 | 감사 | X | ||
| HLB생활건강㈜ | 감사 | X | ||
| 사내이사 | 문정환 | 노터스 | 대표이사 | O |
| 에이치엘비테라퓨틱스㈜ | 이사 | X | ||
| 사내이사 | 도순기 | 에이치엘비네트웍스㈜ | 이사 | X |
| 현대요트㈜ | 이사 | X | ||
| 현대코스모스요팅㈜ | 이사 | X | ||
| 에포케㈜ | 이사 | X | ||
| 사내이사 | William G. Hearl | Immunomic Therapeutics, Inc. | 대표이사 | O |
증권신고서 제출일 현재 당사 주요 임원은 종속법인 및 당사의 최대주주의 임원을 겸직하고 있었습니다. 이로 인하여 효율적인 경영 전략과 융합적 장기 성장 계획을 꿰할 수 있는 효과를 기대할 수 있습니다. 그러나 이러한 효과를 기대하는 것과는 다르게 겸직 회사간의 이해상충에 대한 문제점 또한 발생할 수 있습니다. 이로 인하여 당사에 불리한 경영 방침이나, 특수관계인의 지원 등이 적시에 이루어지지 않을 가능성이 내포되어 있으며 이러한 가능성이 현실화 될 경우 당사의 사업성 및 재무상태에 불리한 영향을 끼칠 수 있습니다.
| [특수관계자와의 거래내역] |
| (단위 : 백만원) |
| 특수관계구분 | 특수관계자명 | 2022년 반기 | 2021년 | 2020년 | 2019년 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 매출 | 매입 | 매출 | 매입 | 매출 | 매입 | 매출 | 매입 | ||||||||||
| 매출거래 | 기타 | 매입거래 | 기타 | 매출거래 | 기타 | 매입거래 | 기타 | 매출거래 | 기타 | 매입거래 | 기타 | 매출거래 | 기타 | 매입거래 | 기타 | ||
| 관계기업 | 에이치엘비생명과학㈜ | 120 | - | - | 186 | 240 | - | - | 371 | 132 | 1 | - | 129 | - | - | - | 18 |
| 에이치엘비테라퓨틱스㈜ | - | 646 | 1,059 | 9,410 | - | - | - | - | - | - | - | - | - | - | - | - | |
| 바다중공업㈜(*1) | 62 | - | 1,848 | - | 86 | - | 3,399 | 18 | 44 | 15 | 4,522 | - | 27 | 40 | 3,174 | 220 | |
| 현대요트㈜ | 292 | - | - | 32 | 117 | - | - | 9 | 7,235 | 1 | - | - | 1 | - | - | 0 | |
| ㈜화진메디칼 | - | - | 7 | 38 | - | - | - | - | - | - | - | - | - | - | - | - | |
| 기타 | 에이치엘비글로벌㈜ | - | - | - | 4 | - | - | - | 8 | - | 0 | - | 2 | - | 9 | - | 8 |
| 에이치엘비일렉㈜ | - | - | - | - | - | 296 | - | - | - | 31 | - | - | 30 | - | - | 31 | |
| 에이치엘비네트웍스㈜(*2) | 691 | - | - | 1 | 1,356 | - | 4 | 4 | 1,257 | 3 | 26 | 2 | 1,651 | - | - | 67 | |
| ㈜펭귄오션레저 | 41 | - | - | 2 | 87 | - | - | 51 | 2 | 0 | - | 37 | 55 | 16 | - | - | |
| ㈜엘리샤코이 | - | - | - | - | - | - | - | 7 | - | 1 | - | 11 | - | - | - | - | |
| ㈜프레시코 | - | - | - | - | - | - | - | 7 | - | - | - | 10 | - | - | - | - | |
| 에이치엘비파워㈜ | - | - | - | - | - | - | - | - | - | 1 | - | - | - | - | - | 480 | |
| 에이치엘비셀㈜ | - | - | - | - | - | - | - | - | - | 1 | - | - | - | - | - | 7 | |
| 에이치엘비제약㈜ | - | - | - | - | - | - | - | - | - | 1 | - | - | - | - | - | - | |
| ㈜데님오브벌츄코리아 | - | - | - | - | - | - | - | - | - | - | - | 3 | - | - | - | - | |
| 에이치엘비사이언스㈜ | - | - | - | - | - | - | - | - | - | 0 | - | - | - | - | - | - | |
| 현대코스모스요팅㈜ | - | - | - | - | - | - | - | - | - | - | - | - | 6 | - | - | 9 | |
| 에이치엘비에너지㈜ | - | - | - | - | - | - | - | - | - | - | - | - | - | - | - | 20 | |
| 합 계 | 1,206 | 646 | 2,914 | 9,673 | 1,886 | 296 | 3,403 | 475 | 8,674 | 55 | 4,548 | 194 | 1,769 | 66 | 3,174 | 861 | |
| (*1) 당사는 관계기업인 바다중공업㈜ DAVIT을 매입해서 상품으로 판매하고 있습니다. (*2) 당사는 기타특수관계자인 에이치엘비네트웍스㈜에 구명정 서비스 독점권을 부여하여 러닝개런티를 통한 로열티수익을 창출하고 있습니다. |
2020년과 2021년 연간 및 2022년 반기 연결기준 특수관계자향 매출의 전체 연결기준 매출 대비 비중은 각각 15.4%, 2.7% 및 1.5% 수준으로, 전체 매출 대비 특수관계자와의 매출거래 비중이 변동폭이 큽니다. 이는 2020년 중 현대요트㈜의 140억 및 70억 선박 입찰로 매출이 크게 증가한 것에 기인합니다. 2019년 매출은 기존 현대요트㈜로부터 발생하던 매출이 hook 부품 매출 모멘텀에 따라 감소하였고, IFRS 규정에 따라 에이치엘비네트웍스로부터 수령하는 수수료수익도 감소하였습니다. 2020년에는 현대요트㈜의 어업 지도선 신규 수주로 인해 현대요트㈜를 대상으로 한 매출이 증가하면서 특수관계자를 대상으로 한 총 매출이 8,674백만원 발생했습니다. 2022년 반기에는 관계기업인 에이치엘비테라퓨틱스를 대상으로 1,059백만원의 상품 매입 및 9,410백만원 외주가공비 지급이 발생하면서 특수관계자를 대상으로 한 총 매입이 12,587백만원 발생했습니다.
당사의 매출 및 자산 규모에 비추어 보아 특수관계자와의 매출 및 매입거래 비중은 유의미하게 크지 않은 것으로 판단되나, 향후 특수관계자향 매출이 증가하여 편중이 나타날 가능성은 배제할 수 없으며, 이 경우 당사의 실질 영업경쟁력 약화로 해석될 우려가 있습니다.
| [특수관계자와의 자금 거래 내역] |
| (단위 : 백만원) |
| 구분 | 특수관계자명 | 2022년 반기 | 2021년 | 2020년 | 2019년 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 자금 유출 | 자금 유입 | 자금 유출 | 자금 유입 | 기타 | 자금 유출 | 자금 유입 | 자금유출 | 자금유입 | |||||||||
| 대여 | 출자 | 대여금회수 | 이자수취 | 출자 | 대여금회수 | 이자수취 | 전환권행사 | 대여 | 대여금회수 | 유상증자 | 출자 | 대여 | 상환 | 대여금회수 | 차입 | ||
| 관계기업 | 에이치엘비생명과학㈜ | 19,603 | - | - | - | - | - | - | 10,000 | - | - | 4,396 | 62,799 | - | - | - | - |
| 관계기업 | Verismo Therapeutics, Inc | - | - | - | - | 5,586 | - | - | - | - | - | - | - | - | - | - | - |
| 관계기업 | 바다중공업 | 2,000 | - | - | - | - | - | - | - | 900 | 1,780 | - | - | - | - | - | - |
| 관계기업 | ㈜노터스 | - | 31,026 | - | - | - | - | - | - | - | - | - | - | - | - | - | - |
| 기타 | 현대요트㈜ | - | - | - | - | - | 781 | 541 | - | - | - | - | - | - | - | - | - |
| 기타 | 에이치엘비제약㈜ | - | - | - | 50 | - | - | 100 | - | - | - | - | - | - | - | - | - |
| 기타 | 에이치엘비글로벌㈜ | - | - | - | - | - | - | - | - | - | - | - | - | 9,000 | 3,000 | 9,000 | 3,000 |
| 기타 | ㈜화진메디칼 | - | - | 1,700 | 52 | - | - | - | - | - | - | - | - | - | - | - | - |
| 합계 | 21,603 | 31,026 | 1,700 | 102 | 5,586 | 781 | 641 | 10,000 | 900 | 1,780 | 4,396 | 62,799 | 9,000 | 3,000 | 9,000 | 3,000 | |
당사가 2019년 중 특수관계자와 맺은 자금거래로는 에이치엘비생명과학㈜가 발행한전환사채의 전환권을 행사하여 지분을 취득한 내용과, ㈜HLB글로벌(구, ㈜넥스트사이언스)에 90억원을 대여 후 회수, 30억원을 차입 후 상환한 내용이 있습니다. 2020년 중 연결실체는 관계기업인 바다중공업㈜에 약 9억원의 자금을 대여한 바 있으며, 17.8억원의 대여금을 회수했습니다. 2021년중에는 관계회사 Verismo의 유상증자에참여해 5,586백만원의 자금유출이 있었으며, 2014~2016년 중 현대요트에 대여해준781백만원 및 해당 대여금 관련 이자를 회수했습니다. 2022년 반기 중 당사는 에이치엘비생명과학㈜의 제9회 공모 신주인수권부사채 청약에 19,603백만원 참여하여 신주인수권부사채를 취득하였으며, 반기 중 매각한 ㈜화진메디칼로부터 1,700백만원의 대여금 및 관련이자를 회수했습니다.
당사는 주권상장법인으로서 이와 같은 관계기업과의 자금거래는 「상법」제542조의9의 적용을 받습니다. 이와 관련된 상세한 위험 내용은 본 증권신고서 "III. 투자위험요소 - 2. 회사위험 - 거."의 내용을 참고하여 주시기 바랍니다.
당사는 이사회 결의 등 적법절차를 준수하고 당사의 피해 또는 특수관계자에 대한 부당한 이익제공에 해당하지 않도록 특수관계자와의 거래를 진행하고 있습니다. 그러나 특수관계자와의 거래 발생 시 거래 조건 등이 제3자와의 거래와 비교하여 적정성이 유지되지 않을 경우 에이치엘비㈜의 주주가 향유하여야 할 이익이 특수관계자 측에 전가될 위험이 있습니다. 또한 특수관계자에 대한 채권 규모가 증가할수록 현금흐름 및 재무구조에는 부정적으로 작용할 가능성이 있습니다. 투자자분들께서는 이 점 유의하여 주시기 바랍니다.
| 거. 특수관계자에 대한 신용공여 관련 제재 위험 당사는 코스닥시장 주권상장법인으로, 법 제542조의9에 따라 주요주주 및 그 특수관계인에 대한 신용공여 제한의 적용을 받습니다. 당사는 증권신고서 제출일 현재까지 계열회사의 경영상 목적 달성을 위한 자금 지원 등을 목적으로 주요주주 및 그 특수관계자에 해당하는 주체를 대상으로 신용공여 거래를 진행한 바 있습니다. 특수관계자에 대한 자금 대여의 경우 그 규모가 크지 않고 대부분 단기간 내에 상환된 사례가 있으며 지급보증의 경우에도 그 금액이 당사의 자산 및 매출 규모를 고려할 때 크지 않은 바, 해당 사실이 당사에 미치는 실질적 영향은 크지 않을 것으로 판단됩니다. 그러나, 당사가 상기와 같이 진행한 거래 중에서 「상법」제542조의9에 대한 위반의 소지가 발견되었으며, 상법에 위배될 소지가 있는 사실이 존재함에 대하여는 향후 벌칙이 부과될 수 있습니다. 사법 당국이 상법 위반 소지가 있는 거래 내용에 대하여 위법임을 최종 판단하고 법에서 정하는 양형 규정에따라 제재 조치를 가할 경우 당사는 적용되는 법에 따라 벌금을 부담해야 할 가능성이 있으며, 이 경우 그 금액에 따라 당사에 재무적 부담으로 작용할 수 있습니다. 당사는 상기에기술된 거래와 같이 상법에 저촉될 가능성이 있는 거래에 대하여 사전에 인지하고, 거래가이루어지기 이전에 사전적으로 적법한 절차를 보장하기 위하여 현재 주요주주 등에 대한 신용공여 관련 내부 규정과 조직, 통제절차 등을 전반적으로 정비하여 상기와 같은 거래내용으로 인한 적법성 우려가 향후 발생하지 않도록 조치하였습니다. |
당사는 코스닥시장 주권상장법인으로, 「상법」제542조의9에 따라 주요주주 및 그 특수관계인에 대한 신용공여 제한의 적용을 받습니다. 원칙적으로 당사는 주요주주 및 그의 특수관계인을 상대방으로 하거나 그를 위하여 신용공여(금전 등 경제적 가치가 있는 재산의 대여, 채무이행의 보증, 자금 지원적 성격의 증권 매입, 그 밖에 거래상의 신용위험이 따르는 직접적ㆍ간접적 거래로서 「상법 시행령」 제35조 제1항으로 정하는 거래를 말함)를 하는 것이 금지됩니다.
| [HLB그룹 지배구조도] |
|
증권신고서 제출일 현재 대표이사 회장인 진양곤 및 그 특수관계인의 신용공여 상대회사에 대한 지분율이 신용공여 실행 당시에 현재와 동일함을 전제로, 당사가 「상법」 제542조의9의 제①항의 제한에도 불구하고 최대주주의 특수관계인에게 신용공여를 제공한 것으로 판단되는 신용공여 거래 내역은 다음과 같이 파악됩니다.
| [최대주주의 특수관계인 대상 신용공여 내역] | |
| (기준일: 2022년 09월 23일) | (단위: 원) |
| 신용공여 대상 | 신용공여 유형 | 결의된 신용공여 기간 | 금액 | 집행 결의 이사회 | 상태 |
|---|---|---|---|---|---|
| 고션 | 금전대여 | - | 70,000,000 | 2013년 현대라이프보트 합병 당시 승계 | 대손처리 |
| 오티에스중공업 | 금전대여 | 2013.11.15 ~ 2013.12.31 | 400,000,000 | 2013년 11월 15일 이사회의사록 | 대손처리 |
| 펭귄오션레저 | 금전대여 | 2014.12.31 ~ 2015.12.31 | 23,600,000 | 2014년 12월 31일 이사회의사록 | 대손처리 |
| 현대앤코스모스요팅 | 금전대여 | 2017.04.05 ~ 2017.07.31 | 500,000,000 | 2017.04.05. 이사회의사록 | 회수완료 |
| 금전대여 | 2017.07.03 ~ 2017.07.31 | 500,000,000 | 2017.07.03. 이사회의사록 | 회수완료 | |
| 에이치엘비글로벌㈜ | 금전대여 | 2019.09.16 ~ 2019.10.15 | 9,000,000,000 | 2019.09.16 이사회의사록 | 회수완료 |
| 바다중공업 | 연대보증 | 2012.05.29. ~ 2019.09.30. | 113,220,000 | - | 종결 |
| 연대보증 | 2012.06.01. ~ 2019.01.31. | 188,700,000 | - | 종결 | |
| 금전대여 | 2018.01.10 ~ 2018.03.30 | 500,000,000 | 2018.01.10. 이사회의사록 | 회수완료 | |
| 금전대여 | 2018.02.07 ~ 2018.06.30 | 880,000,000 | 2018.02.07. 이사회의사록 | 회수완료 | |
| 금전대여 | 2020.01.15 ~ 2021.01.15 | 900,000,000 | 2020.01.15. 이사회의사록 | 회수완료 | |
| 금전대여 | 2022,04,29 ~ 2027.04.28 | 2,000,000,000 | 2022.04.27 이사회의사록 | 잔존 | |
| 현대요트 | 금전대여 | 2014.04.10 ~ 2014.05.31(0.3억) 2014.05.29 ~ 2015.05.28(2억) 2015.01.08 ~ 2016.01.07(0.2억) 2015.01.16 ~ 2016.01.16(1.8억) 2015.01.30 ~ 2016.01.29(2억) 2015.03.03 ~ 2016.03.02(1억) 2015.06.18 ~ 2016.06.17(0.5억) |
781,000,000 | 2014.04.10자 이사회의사록 2014.05.29자 이사회의사록 2015.01.08자 이사회의사록 2015.01.16자 이사회의사록 2015.01.30자 이사회의사록 2015.03.03자 이사회의사록 2015.06.18자 이사회의사록 |
회수완료 |
| 금전대여 | 2017.08.01 ~ 2017.08.25 | 200,000,000 | 2017.07.31 이사회의사록 | 회수완료 | |
| 금전대여 | 2018.01.25 ~ 2018.03.26 | 708,000,000 | 2018.01.25 이사회의사록 | 회수완료 | |
| 선급금이행보증 | 2017.06.28 ~ 2018.05.09 | 212,511,250 | 2017.06.28. 이사회의사록 2017.12.04. 이사회의사록(조건변경) 2018.02.21. 이사회의사록(조건변경) |
종결 | |
| 계약이행보증 | 2017.07.21 ~ 2018.07.08 | 660,943,260 | 2017.07.21. 이사회의사록 2018.01.17. 이사회의사록(조건변경) 2018.03.13. 이사회의사록(조건변경) |
종결 | |
| 선금급이행보증 | 2017.08.01 ~ 2018.07.16. | 1,160,357,920 |
2017.07.21. 이사회의사록 2017.08.01. 이사회의사록(조건변경) |
종결 | |
| 하자이행보증 | 2018.06.23 ~ 2019.06.22 | 203,717,255 | 2018.06.28. 이사회의사록 | 종결 | |
| 하자이행보증 | 2018.06.23 ~ 2021.06.22 | 82,479,375 | 2018.06.28. 이사회의사록 | 종결 | |
| 하자이행보증 | 2018.06.23 ~ 2023.06.22 | 44,275,000 | 2018.06.28. 이사회의사록 | 잔존 | |
| 계약이행보증 | 2019.12.12 ~ 2020.12.11 | 694,159,100 | 2019.12.12 이사회의사록 2020.07.09 이사회의사록(조건변경) |
종결 | |
| 계약이행보증 | 2019.12.12 ~ 2020.12.11 | 706,251,040 | 2019.12.12 이사회의사록 2020.07.09 이사회의사록(조건변경) |
종결 | |
| 선금급이행보증 | 2020.01.20 ~ 2020.07.09 | 1,393,339,580 | 2020.01.16 이사회의사록 | 종결 | |
| 선금급이행보증 | 2020.01.20 ~ 2020.07.09 | 1,382,050,280 | 2020.01.16 이사회의사록 | 종결 | |
| 선금급이행보증 | 2020.07.17 ~ 2021.02.09 | 1,790,446,530 | 2020.06.26 이사회의사록 | 종결 | |
| 선금급이행보증 | 2020.07.17 ~ 2021.02.09 | 1,790,900,370 | 2020.06.26 이사회의사록 | 종결 | |
| 계약이행보증 | 2020.07.17 ~ 2021.05.14 | 93,522,000 | 2020.07.17 이사회의사록 | 종결 | |
| 선금급이행보증 | 2020.07.29 ~ 2022.09.29 | 297,755,550 | 2020.07.17 이사회의사록 2021.07.15 이사회의사록(조건변경) 2021.11.24 이사회의사록(조건변경) 2022.04.27 이사회의사록(조건변경) |
잔존 | |
| 선금급이행보증 | 2020.12.07 ~ 2022.02.22 | 512,226,600 | 2020.12.07 이사회의사록 2021.10.01 이사회의사록(조건변경) 2021.12.22 이사회의사록(조건변경) |
종결 | |
| 하자이행보증 | 2021.01.05 ~ 2022.01.04 | 700,205,064 | 2021.01.06 이사회의사록 | 종결 | |
| 선금급이행보증 | 2021.06.01 ~ 2022.02.22 | 379,696,040 | 2021.06.01 이사회의사록 2021.10.01 이사회의사록(조건변경) 2021.12.22 이사회의사록(조건변경) |
종결 | |
| 계약이행보증 | 2021.12.17 ~ 2022.12.17 | 191,110,700 | 2021.12.16 이사회의사록 2021.12.22 이사회의사록(조건변경) |
잔존 | |
| 선금급이행보증 | 2022.04.20 ~ 2023.02.15 | 1,166,592,800 | 2022.04.27 이사회의사록 | 잔존 |
| (자료: 당사 자료 재구성) |
| 주1) 상기 내역은 당사의 이사회의사록 및 정기보고서에 근거한 내용으로서, 위 기간 중 특수관계자에 대한 채권, 채무 내역 전체를 포괄하는 것은 아님 |
| 주2) 2013년 기준 당사의 최대주주인 진양곤 회장이 25.21%를 보유하고 있으며. 그 특수관계인인 진양우가 16.88%를 보유하고 있음 |
| 주3) 2014년 12월 31일 기준 당사의 최대주주인 진양곤 회장은 펭귄오션레저의 지분 72.48%를 보유하고 있으며, 그 특수관계인인 진양우가 7.75%를 보유하고 있음 |
| 주4) 2013년 11월 15일 기준 당사의 최대주주인 진양곤 회장은 오티에스중공업의 지분 48.89%를 보유하고 있으며, 당사 및 당사의 최대주주인 진양곤 회장이 합쳐 68.23%(당사 48.94%, 진양곤 회장 19.29%)의 지분을 보유한 바다중공업이 오티에스중공업의 지분 48.89%를 보유하고 있음 |
| 주5) 2017년 04월 05일 및 2017년 07월 03일기준 당사의 최대주주인 진양곤 회장이 현대앤코스모스요팅의 지분 24.14%를 보유하고 있으며, 그 특수관계인인 진양우가 17.24%를 보유하고 있음 |
| 주6) 2012년 05월 29일 및 2012년 06월 01일 기준 당사는 바다중공업의 지분 48.94%를 보유하고 있으며, 당사의 최대주주인 진양곤 회장이 19.29%를 보유하고 있음 2018년 01월 10일, 2018년 02월 07일, 2020년 01월 15일, 2022년 04월 09일 기준 당사는 바다중공업의 지분 28.89%를 보유하고 있으며, 당사의 최대주주인 진양곤 회장이 31.98%를 보유하고 있음 |
| 주7) 2014년04월 10일 기준 당사는 현대요트의 지분 46.21%를 보유하고 있으며, 당사의 최대주주인 진양곤 회장이 3.52%, 그 특수관계인인 진양우가 22.39%를 보유하고 있음. 2017년 08월 01일 이후부터 현재까지 당사는 현대요트의 지분 39.43%를 보유하고 있으며, 당사의 최대주주인 진양곤 회장이 4.35%, 그 특수관계인인 진양우가 37.05%를 보유하고 있음 |
| 주8) 2019년 09월 16일 기준 당사의 최대주주인 진양곤 회장이 HLB글로벌의 지분 0.84%를 보유하고 있음 |
당사는 최대주주의 특수관계인을 대상으로 금전대여 및 연대보증, 하자이행보증 등의 지급보증을 제공 한 바 있습니다.「상법」 제542조의9(주요주주 등 이해관계자와의 거래)에 따르면 상장회사는 주요주주 및 그의 특수관계인, 이사 및 집행임원, 감사에 대해서는 신용공여를 하여서는 안된다고 규정하고 있습니다. 상법 제542조의9는 다음과 같습니다.
| 「상법」 제542조의9(주요주주 등 이해관계자와의 거래) |
|
제542조의9(주요주주 등 이해관계자와의 거래) ① 상장회사는 다음 각 호의 어느 하나에 해당하는 자를 상대방으로 하거나 그를 위하여 신용공여(금전 등 경제적 가치가 있는 재산의 대여, 채무이행의 보증, 자금 지원적 성격의 증권 매입, 그 밖에 거래상의 신용위험이 따르는 직접적ㆍ간접적 거래로서 대통령령으로 정하는 거래를 말한다. 이하 이 조에서 같다)를 하여서는 아니 된다. 1. 주요주주 및 그의 특수관계인 2. 이사(제401조의2제1항 각 호의 어느 하나에 해당하는 자를 포함한다. 이하 이 조에서 같다) 및 집행임원 3. 감사 ② 제1항에도 불구하고 다음 각 호의 어느 하나에 해당하는 경우에는 신용공여를 할 수 있다. 1. 복리후생을 위한 이사ㆍ집행임원 또는 감사에 대한 금전대여 등으로서 대통령령으로 정하는 신용공여 2. 다른 법령에서 허용하는 신용공여 3. 그 밖에 상장회사의 경영건전성을 해칠 우려가 없는 금전대여 등으로서 대통령령으로 정하는 신용공여 ③ 자산 규모 등을 고려하여 대통령령으로 정하는 상장회사는 최대주주, 그의 특수관계인 및 그 상장회사의 특수관계인으로서 대통령령으로 정하는 자를 상대방으로 하거나 그를 위하여 다음 각 호의 어느 하나에 해당하는 거래(제1항에 따라 금지되는 거래는 제외한다)를 하려는 경우에는 이사회의 승인을 받아야 한다. 1. 단일 거래규모가 대통령령으로 정하는 규모 이상인 거래 2. 해당 사업연도 중에 특정인과의 해당 거래를 포함한 거래총액이 대통령령으로 정하는 규모 이상이 되는 경우의 해당 거래 ④ 제3항의 경우 상장회사는 이사회의 승인 결의 후 처음으로 소집되는 정기주주총회에 해당 거래의 목적, 상대방, 그 밖에 대통령령으로 정하는 사항을 보고하여야 한다. ⑤ 제3항에도 불구하고 상장회사가 경영하는 업종에 따른 일상적인 거래로서 다음 각 호의 어느 하나에 해당하는 거래는 이사회의 승인을 받지 아니하고 할 수 있으며, 제2호에 해당하는 거래에 대하여는 그 거래내용을 주주총회에 보고하지 아니할 수 있다. 1. 약관에 따라 정형화된 거래로서 대통령령으로 정하는 거래 2. 이사회에서 승인한 거래총액의 범위 안에서 이행하는 거래 |
다만, 동법 제2항에 따라 복리후생을 위한 이사·집행임원 또는 감사에 대한 금전대여 등으로서 대통령령으로 정하는 신용공여나 그 밖에 상장회사의 경영건전성을 해칠 우려가 없는 금전대여 등으로서 대통령령으로 정하는 신용공여는 가능합니다. 「상법 시행령」 제35조제3항에 따르면 '대통령령으로 정하는 신용공여'란 회사의 경영상 목적을 달성하기 위하여 필요한 경우라고 규정하고있고 그 대상을 회사의 지분율에 따라 제한하고 있습니다. 또한 경영상 목적을 달성하기 위한 경우 법인인 주요주주, 법인인 주요주주의 특수관계인 중 회사(자회사를 포함한다)의 출자지분과 해당 법인인 주요주주의 출자지분을 합한 것이 개인인 주요주주의 출자지분과 그의 특수관계인(해당 회사 및 자회사는 제외한다)의 출자지분을 합한 것보다 큰 법인의 경우에는 신용공여가 가능합니다.
| 상법 시행령 제35조(주요주주 등 이해관계자와의 거래) |
|
제35조(주요주주 등 이해관계자와의 거래) ② 법 제542조의9제2항제1호에서 “대통령령으로 정하는 신용공여”란 학자금, 주택자금 또는 의료비 등 복리후생을 위하여 회사가 정하는 바에 따라 3억원의 범위에서 금전을 대여하는 행위를 말한다. ③ 법 제542조의9제2항제3호에서 “대통령령으로 정하는 신용공여”란 회사의 경영상 목적을 달성하기 위하여 필요한 경우로서 다음 각 호의 자를 상대로 하거나 그를 위하여 적법한 절차에 따라 이행하는 신용공여를 말한다. 1. 법인인 주요주주 2. 법인인 주요주주의 특수관계인 중 회사(자회사를 포함한다)의 출자지분과 해당 법인인 주요주주의 출자지분을 합한 것이 개인인 주요주주의 출자지분과 그의 특수관계인(해당 회사 및 자회사는 제외한다)의 출자지분을 합한 것보다 큰 법인 3. 개인인 주요주주의 특수관계인 중 회사(자회사를 포함한다)의 출자지분과 제1호 및 제2호에 따른 법인의 출자지분을 합한 것이 개인인 주요주주의 출자지분과 그의 특수관계인(해당 회사 및 자회사는 제외한다)의 출자지분을 합한 것보다 큰 법인
|
당사는 최대주주의 특수관계인을 대상으로 한 상기 신용공여가 ① 상법에서 정한 요건에 흠결되는 거래가 존재하는지 ②만약 상법에 위반되는 거래가 있다면향후 당사의 경영건전성을 해할 우려가 있어 형사처벌의 대상이 되는지를 법무법인에 검토 의뢰했으며, 법무법인에서 검토한 법률의견서의 주요 내용은 아래와 같습니다.
| A법무법인 주요 검토의견(HLB(주) 신용공여 관한 법률 이슈) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
I. 검토배경 - 에이치엘비 주식회사(이하 'HLB')는 2014.경부터 고션, 펭귄오션레저, 오티에스중공업, 현대앤코스모스요팅, 바다중공업, 현대요트, 에이치엘비글로벌에 대하여 약 38회 가량의 신용공여(연대보증, 금전대여, 하자이행보증, 선금급이행보증, 이하 '본건 신용공여')를 한 사실이 있음. - 그 중 대다수의 거래는 이미 종결 또는 회수가 완료되었고 일부의 거래에 대하여는 대손처리를 하였으며 현재에도 종결되지 않은 신용공여 5 건이 존재함 - 위와 같은 사실관계를 전제로 ① 본건 신용공여 거래 중 상법에 서 정한 요건에 흠결되는 거래가 존재하는지 ② 만약 상법에 위반되는 거래가 있다면 향후 HLB의 경영건전성을 해할 우려가 있어 형사처벌의 대상이 되는지에 관하여 질의하여 주셨습니다. II. 검토 HLB의 고션에 대한 신용공여 당시 진양곤은 진양우와 합하여 고션의 주식 42.09%를 보유하고 있으므로 고션은 진양곤의 특수관계인에 해당하였고, 신용공여 당시 HLB 및 HLB 자회사가 보유한 고션의 주식은 없었던 것으로 보입니다. 따라서, HLB의 고션에 대한 신용공여는 상법에서 정한 형식적인 요건을 흠결한 것으로 판단됩니다.
다. 소결 (1) 고션에 대한 신용공여 HLB의 고션에 대한 신용공여 거래의 경우, 과거 HLB가 현대라이프보트를 합병할 당시에 발생한 것인데, 합병 당시 피인수회사인 현대라이프보트가 과거 고션에 대하여 한 신용공여 거래가 인수회사인 HLB에 승계된 경우에 해당합니다. 따라서 고션에 대한 신용공여의 경우 HLB의 의사에 기하여 진행된 것이라기 보다는 HLB와 현대라이프보트에 대한 합병 거래의 종결을 위하여 필요한 거래에 해당하였는바 이는 종국적으로 HLB가 인수한 현대라이프보트의 정상적인 사업 수행을 위하여 승계된 거래에 해당하므로 HLB의 경영상 목적 달성을 위하여 필요한 거래로 보입니다. 한편, 법률상 요건을 흠결한 신용공여의 경우 상법위반죄로 처벌될 수 있으나 그 공소시효가 7년에 해당합니다. HLB가 현대라이프보트를 인수한 시점이 2013.경이라는 점에서 고션에 대한 신용공여는 적어도 인수시점 이전에 이루어진 것으로 예상이 되는데, 설사 해당 거래에 상법 위반의 점이 인정된다고 하더라도 신용공여 거래 당시로부터 이미 7년이 도과하였는바 상법위반의 공소시효가 완성되어 처벌될 여지가 없다고 사료됩니다.
HLB의 펭귄오션레저에 대한 신용공여 거래의 배경은, 과거 펭귄오션레저가 말레이시아에서 영위하던 사업에 파견된 HLB 소속 직원에 대한 해외 영업비, 체류비 등의 명목으로 지급된 금원에 해당하였습니다. 당시 펭귄오션레저는 말레이시아에서 수상 레저 관련 사업을 영위하였는데, 이를 국내에 도입하고자 하였던 HLB가 그 소속 직원을 펭귄오션레저의 해외 영업지로 파견하게 된 것인바 이 역시 HLB의 경영상 목적에 의하여 이루어진 거래에 해당한다고 보입니다. 또한, 해당 신용공여 거래는 2014. 12. 31.이루어져 설사 상법위반의 점이 인정된다고 하더라도 이미 공소시효 7년이 완성되었는바 처벌의 가능성은 없는 것으로 사료됩니다. (3) 오티에스중공업에 대한 신용공여 HLB의 오티에스중공업에 대한 신용공여는 당시 HLB가 대우조선해양으로부터 수주 받은 대형크레인 제조용역을 오티에스중공업에 하청을 주면서 생긴 거래인데, 그 당시 HLB와 진양곤의 각 오티에스중공업 대한 지분관계에 비추어 판단하건대 일부 상법 위반의 점이 인정될 수도 있다고 보입니다. 다만, 오티에스중공업에 대한 신용공여는 2013. 11. 15.에 이루어졌으므로, 설사 상법위반의 점이인정된다고 하더라도 공소시효 7년이 완성되었는바 처벌의 가능성은 없다고 보입니다. (4) 현대앤코스모스요팅에 대한 신용공여 HLB의 현대앤코스모스요팅에 대한 신용공여가 이루어진 배경은 현대앤코스모스요팅이 본건 신용공여를 통하여 외국 소재 바바리아社의 레저용 요트의 수입을 위하여 긴급히 자금의 조달이 필요한 상황이었기 때문입니다. 현대앤코스모스요팅이 수입한 레저용 요트를 현대요트에 공급하고자 하였고 그 이후 현대요트가 공급받은 레저용 요트를 이용하여 요트 차터(대여) 서비스를 제공할 계획이었다고 합니다. 그렇다면 HLB가 39.43%의 주식을 보유한 현대요트의 매출 및 영업이익이 제고될 것으로 기대되었고 종국적으로는HLB의 경영성과 또한 개선되는 시너지 효과를 낼 수 있다 판단하여 HLB가 본건 신용공여 거래를 하게 되었다고 합니다. 그렇다면 본건 신용공여 거래 HLB의 경영상 목적 달성을 위하여 이루어졌다고 볼 수 있으며 그렇다면 상법 위반의 점이 있다고 단정하기는 어렵습니다. (5) 바다중공업에 대한 신용공여 HLB의 바다중공업에 대한 신용공여 중 순번 1, 2의 거래의 경우 국가기관과 계약 수주 당시 바다중공업 보다 그 신용도가 나은 HLB의 연대보증이 포함된 보증서가 필요하였기에 이루어졌습니다. 그 당시 HLB는 바다중공업 주식의 48.94%를 보유하였는바 바다중공업의 매출 증가가 HLB의 총 매출 및 영업이익 증대에 기여할 수 있을 것이라고 판단되었기에 해당 신용공여 거래는 경영상의 목적 달성을 위하여 이루어진 것으로 보이는바 상법에 위배되지 아니한 것으로 보입니다. 설사, 순번 1, 2의 거래가 상법을 위반하였다고 하더라도 순번 1, 2의 신용공여 거래 시점으로부터 이미 7년이 도과하여 공소시효가 완성되었는바 처벌의 가능성이 없다고 판단됩니다. 순번 3, 4, 5의 거래가 이루어졌던 배경은 바다중공업의 수주계약이 증가하고 있는 상황에서 효율적인 생산 체계를 확립할 필요가있었으며, 보다 고부가가치 창출을 위하여 대형선박 제조의 필요성이 존재하였기에 이를 위한 재원의 필요로 이루어진 자금의 대여에 해당합니다. 앞서 말씀드렸듯 바다중공업은 HLB의 계열회사 중 하나인바, 바다중공업의 경영 성과 증진은 곧 HLB의 경영성과, 특히나 매출 및 영업이익 증대에 도움이 될 것이라는 경영상의 판단 하에 이루어진 거래로 보여 상법 위반의 점이 인정된다고 단정하기어렵습니다. 순번 5의 거래 당시, 바다중공업은 (ⅰ) 효율적인 생산 및 원가 절감, 그리고 대형선박의 생산을 위하여 그 제작공간이 필요하였습니다. 바다중공업은 HLB로부터 대여한 금원을 이용하여해당 부지를 매수하였는데 이로 인하여 불필요하게 자재등 운반비용의 지출을 막을 수 있으며 생산시설 증축에 따른 외주비용을 감소시킬 수 있다는 기대이익이 있었습니다. (ⅱ) 또한 바다중공업은 HLB로부터 대여한 금원 중 일부를 인적관리 및 통합관리 비용에 지출함으로써 작업 중 이동으로 인한 인력 낭비를 막고 선박 생산프로세스를 개선하는 등 종국적으로 선박 제조 과정에서의 효율성을 증대하는 것을 그 기대이익으로 평가하였습니다.이 역시 계열회사인 바다중공업의 매출 및 영업이익 증대를 꾀하여 종국적으로 HLB의 경영성과 개선을 위하여 이루어진 거래에 해당하는바 경영상 목적 달성을 위하여 이루어진 것으로 볼 수 있고 이에 따라 상법 위반의 점이 있다고 보기 어렵습니다. (6) 현대요트에 대한 신용공여 HLB의 현대요트에 대한 순번 1, 2 신용공여 거래의 경우 현대요트가 사업 다각화의 일환으로서 요트 차터(대여)사업을 계획하였으나 이를 위한 유동자금이 부족하여 HLB로부터 금전대여를 받게 된 경우에 해당합니다. 거래 당시 향후 요트 차터서비스에 대한 수요가 증가할 것으로 예측되었고, 그때 HLB는 현대요트의 지분 46.21% 혹은 39.43%를 보유하였는바 현대요트의 경영성과 개선이 곧 HLB의 재무성과 개선에 도움이 될 것이라는 경영상 판단 하에 이루어진 거래에 해당한다고 볼 수 있어 상법 위반의 점이 인정된다고 보기 어렵습니다. 한편 순번 1거래의 경우 신용공여 거래 이후 7년이경과하여 공소시효 또한 완성되었는바, 상법 위반의 점이 인정된다고 하더라도 그 처벌 가능성은 없다고 보입니다. 순번 3 내지 22의 거래는 그 신용공여의 유형이 선급금이행보증, 계약이행보증, 하자이행보증임을 알 수 있습니다. 이러한 신용공여가 이루어졌던 배경을 보면 현대요트는 관공서로부터 선박의 건조를 수주하는 경우가 많았는데, 이 경우 관공서는 수주 계약 의무 이행을 보증하는 보증서의 제출을 요구하였습니다. 이에 따라 현대요트는 서울보증보험에 이행보증보험의 발급을 요청하였는데, 보증보험회사에서 현대요트 보다 월등히 신용등급이 좋은 최대주주 HLB의 연대보증을요청하여 현대요트에 대한 신용공여가 이루어졌습니다. 관공서와의 계약 수주는 다른 주체와의 계약과 비교하여 자금 지급 등의 안정성이 보장되어 보다 사업적 리스크가 적은 계약의 유형에 속하였는바, 현대요트의 매출 및 영업이익 제고에 큰 도움이 될 것으로 판단하였습니다. 현대요트의 매출 및 영업이익 증가는 현대요트의 주식 39.43%를 보유한 HLB의 연결재무제표상 매출 및 영업이익 증대의 결과를 가져올 것으로 판단하여 신용공여 거래가 이루어졌는바 이 역시 경영상 목적 달성의 일환으로 이루어진 거래에 해당한다고 할 수 있습니다. 따라서 기 역시도 상법 위반의 점이 인정될 것이라고 단정하기 어렵습니다. (7) 에이치엘비글로벌에 대한 신용공여 HLB의 에이치엘비글로벌에 대한 신용공여가 이루어진 배경은 에이치엘비글로벌이 발행한 사채의 투자가가 풋옵션(조기상환청구권)을 행사함에 따라 에이치엘비글로벌로서 그 당시 그 상환대금 상당의 자금이 필요로 하여 이루어진 거래에 해당합니다. 다만, 그 당시 진양곤은 에이치엘비글로벌의 특수관계인에 해당할 여지가 있었으므로 해당 신용공여 거래의 경우 상법에서 정한 신용공여의 요건을 흠결하였다고 볼 여지가 있습니다. 다만, 위 신용공여 거래 당시 (ⅰ) HLB가 에이치엘비글로벌이 보유한 ㈜동원리소스 보통주 10,518주에 대한 질권을 설정하여 안정적인 담보를 보유하였고, (ⅱ)위 신용공여 거래의 대여기간이 1개월에 불과하였으며, (ⅲ) 실제로 에이치엘비글로벌이 대여금을 전부 상환하였다는 점에서, 법원에서 위 신용공여 거래를 위법한 거래로써 형사처벌의 대상이 된다고 판단할 것인지는 의문입니다.
잔존 거래 중 현대요트에 대하여 제공한 연대보증 채무의 총 합계는 약 17억 원으로 HLB 총자산의 약 0.21%, 바다중공업에게 대여한 금액은 20억 원으로 HLB 총자산의 약 0.24% 정도로 확인됩니다. 이에 따라 설사 위 잔존 거래에서 주채무자가 모두 채무를 변제하지 못하는 경우를 상정한다고 하더라도 HLB의 총자산 중 약 0.45%에 영향을 미칠 뿐이어서 위 잔존 거래가 HLB의 경영건전성을 해할 우려가 적다고 할 것입니다. 아울러, HLB가 제공한 자료에 따르면 바다중공업에 대한 신용공여(금전대여)의 경우 HLB가 바다중공업 소유의 부동산[1]에 대하여 제2순위의 근저당권을 설정한 사실이 있어 해당 거래에서 채권을 회수하지 못할 위험은 다소 적다고 보이기도 한다는 점에서도 경영건전성을 해할 우려가 있다고 보기는 어렵습니다.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| [현대요트㈜ 기업개황] |
| 구 분 | 내 용 | |
|---|---|---|
| 회사명 | 현대요트 주식회사 | |
| 대표이사 | 이철웅 | |
| 최대주주 | 에이치엘비㈜ (39.43%) | |
| 주소 | 본사 | 울산광역시 울주군 온산읍 당월로 272-12 |
| 연락처 | 02-561-1975 | |
| 주요사업 | 선박 건조 | |
| 설립연월 | 2008.05.01 | |
| 결산일 | 12월 31일 | |
| 법인구분 | 비상장법인 | |
| [주요 재무사항 총괄표] | |
| (K-GAAP, 별도) | (단위: 백만원, %) |
| 결산연월 또는 결산기간 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|
| 외부감사인의 감사의견 | 적정 | - | - |
| (계속기업으로서의 불확실성 관련 의견표명 및 주석사항 여부) |
(-) | (-) | (-) |
| 1. 자산총계 | 12,036 | 14,975 | 1,254 |
| - 유동자산 | 11,494 | 14,095 | 382 |
| 2. 부채총계 | 10,761 | 17,549 | 4,072 |
| - 유동부채 | 10,578 | 15,365 | 1,386 |
| 3. 자본총계 | 12,036 | 14,975 | 1,254 |
| 4. 부채비율 (%) | 111% | 85% | 30% |
| 5. 유동비율 (%) | 92% | 109% | 362% |
| 6. 매출액 | 14,245 | 483 | 1,722 |
| 7. 영업이익 | 737 | 48 | 128 |
| 기타 손익 | 4,296 | 871 | 36 |
| 금융 손익 | 458 | 140 | 118 |
| 8. 당기순이익 | 3,849 | 244 | (547) |
| 9. 자본금 | 4,156 | 4,156 | 4,156 |
| 10. 현금 및 현금성자산 기말 잔고 | 10,393 | 953 | 312 |
나. 신용공여 개요, 조건 및 구조
| 신용공여 유형 | 결의된 신용공여 기간 | 금액(원) | 집행 결의 이사회 | 계약명 (대여목적) |
보증기관 (이자율) |
보증내용 (지연이자율) |
|---|---|---|---|---|---|---|
| 금전대여 | 2014.04.10 ~ 2014.05.31(0.3억) 2014.05.29 ~ 2015.05.28(2억) 2015.01.08 ~ 2016.01.07(0.2억) 2015.01.16 ~ 2016.01.16(1.8억) 2015.01.30 ~ 2016.01.29(2억) 2015.03.03 ~ 2016.03.02(1억) 2015.06.18 ~ 2016.06.17(0.5억) |
781,000,000 | 2014.04.10자 이사회의사록 2014.05.29자 이사회의사록 2015.01.08자 이사회의사록 2015.01.16자 이사회의사록 2015.01.30자 이사회의사록 2015.03.03자 이사회의사록 2015.06.18자 이사회의사록 |
운영자금 | 6.9% | - |
| 금전대여 | 2017.08.01 ~ 2017.08.25 | 200,000,000 | 2017.07.31 이사회의사록 | 운영자금 | 4.6% | - |
| 금전대여 | 2018.01.25 ~ 2018.03.26 | 708,000,000 | 2018.01.25 이사회의사록 | 운영자금 | 4.6% | - |
| 선금급이행보증 | 2017.06.28 ~ 2018.05.09 | 212,511,250 | 2017.06.28. 이사회의사록 2017.12.04. 이사회의사록(조건변경) 2018.02.21. 이사회의사록(조건변경) |
전라남도 어업지도선 대체 건조구매 (110톤, 130톤) 2건 |
서울보증보험 | 납품계약에 따른 선금급지급보증의연대보증 |
| 계약이행보증 | 2017.07.21 ~ 2018.07.08 | 660,943,260 | 2017.07.21. 이사회의사록 2018.01.17. 이사회의사록(조건변경) 2018.03.13. 이사회의사록(조건변경) |
어업지도선 충남 202호 대체 건조구매 | 서울보증보험 | 납품계약에 따른 계약이행보증의 연대보증 |
| 선금급이행보증 | 2017.08.01 ~ 2018.07.16. | 1,160,357,920 |
2017.07.21. 이사회의사록 2017.08.01. 이사회의사록(조건변경) |
어업지도선 충남 202호 대체 건조구매 | 서울보증보험 | 납품계약에 따른 선금급지급보증의 연대보증 |
| 하자이행보증 | 2018.06.23 ~ 2019.06.22 | 203,717,255 | 2018.06.28. 이사회의사록 | 어업지도선 충남 202호 대체 제조 구매 (선체 및 그외장비) |
서울보증보험 | 납품계약 종료에 따른 하자보증의 연대보증 |
| 하자이행보증 | 2018.06.23 ~ 2021.06.22 | 82,479,375 | 2018.06.28. 이사회의사록 | 어업지도선 충남 202호 대체 제조 구매 (주기관/감속기) |
서울보증보험 | 납품계약 종료에 따른 하자보증의 연대보증 |
| 하자이행보증 | 2018.06.23 ~ 2023.06.22 | 44,275,000 | 2018.06.28. 이사회의사록 | 어업지도선 충남 202호 대체 제조 구매 (워터제트) |
서울보증보험 | 납품계약 종료에 따른 하자보증의 연대보증 |
| 계약이행보증 | 2019.12.12 ~ 2020.12.11 | 694,159,100 | 2019.12.12 이사회의사록 2020.07.09 이사회의사록(조건변경) |
전라남도 어업지도선 대체 건조구매 (110톤) |
서울보증보험 | 납품계약에 따른 계약이행보증의 연대보증 |
| 계약이행보증 | 2019.12.12 ~ 2020.12.11 | 706,251,040 | 2019.12.12 이사회의사록 2020.07.09 이사회의사록(조건변경) |
전라남도 어업지도선 대체 건조구매 (130톤) |
서울보증보험 | 납품계약에 따른 계약이행보증의 연대보증 |
| 선금급이행보증 | 2020.01.20 ~ 2020.07.09 | 1,393,339,580 | 2020.01.16 이사회의사록 | 전라남도 어업지도선 대체 건조구매 (130톤) |
서울보증보험 | 납품계약 종료에 따른 하자보증의 연대보증 |
| 선금급이행보증 | 2020.01.20 ~ 2020.07.09 | 1,382,050,280 | 2020.01.16 이사회의사록 | 전라남도 어업지도선 대체 건조구매 (110톤) |
서울보증보험 | 납품계약에 따른 선금급지급보증의 연대보증 |
| 선금급이행보증 | 2020.07.17 ~ 2021.02.09 | 1,790,446,530 | 2020.06.26 이사회의사록 | 전라남도 어업지도선 대체 건조구매 (130톤) |
서울보증보험 | 납품계약에 따른 선금급지급보증의 연대보증 |
| 선금급이행보증 | 2020.07.17 ~ 2021.02.09 | 1,790,900,370 | 2020.06.26 이사회의사록 | 전라남도 어업지도선 대체 건조구매 (110톤) |
서울보증보험 | 납품계약에 따른 선금급지급보증의 연대보증 |
| 계약이행보증 | 2020.07.17 ~ 2021.05.14 | 93,522,000 | 2020.07.17 이사회의사록 | 안산시 시화호 뱃길 운항선박 건조 구매 | 서울보증보험 | 납품계약에 따른 계약이행보증의 연대보증 |
| 선금급이행보증 | 2020.07.29 ~ 2022.09.29 | 297,755,550 | 2020.07.17 이사회의사록 2021.07.15 이사회의사록(조건변경) 2021.11.24 이사회의사록(조건변경) 2022.04.27 이사회의사록(조건변경) |
안산시 시화호 뱃길 운항선박 건조 구매 | 서울보증보험 | 납품계약에 따른 선금급지급보증의 연대보증 |
| 선금급이행보증 | 2020.12.07 ~ 2022.02.22 | 512,226,600 | 2020.12.07 이사회의사록 2021.10.01 이사회의사록(조건변경) 2021.12.22 이사회의사록(조건변경) |
화천군 파로호 유람선 건조 구매(40%) | 서울보증보험 | 납품계약에 따른 선금급지급보증의 연대보증 |
| 하자이행보증 | 2021.01.05 ~ 2022.01.04 | 700,205,064 | 2021.01.06 이사회의사록 | 전라남도 어업지도선 대체 건조구매 (110톤, 130톤) 2건 |
서울보증보험 | 납품계약 종료에 따른 하자보증의 연대보증 |
| 선금급이행보증 | 2021.06.01 ~ 2022.02.22 | 379,696,040 | 2021.06.01 이사회의사록 2021.10.01 이사회의사록(조건변경) 2021.12.22 이사회의사록(조건변경) |
화천군 파로호 유람선 건조 구매(30%) | 서울보증보험 | 납품계약에 따른 선금급지급보증의 연대보증 |
| 계약이행보증 | 2021.12.17 ~ 2022.12.17 | 191,110,700 | 2021.12.16 이사회의사록 2021.12.22 이사회의사록(조건변경) |
항만순찰선(해청호) 대체선박 건조 (주기관, 추진기 제외) |
서울보증보험 | 납품계약에 따른 계약이행보증의 연대보증 |
| 선금급이행보증 | 2022.04.20 ~ 2023.02.15 | 1,166,592,800 | 2022.04.27 이사회의사록 | 항만순찰선(해청호) 대체선박 건조 (주기관, 추진기 제외) |
서울보증보험 | 납품계약에 따른 선금급지급보증의 연대보증 |
다. 신용공여 제공 배경
| 현대요트㈜가 선박 수주 계약을 진행할 시 보증서 제출의무에 따라 서울보증보험의 보증을 신청함. 보증 신청 과정에서 현대요트㈜의 신용이 부족하여 서울보증보험에서 최대주주(당사)의 연대보증을 요청함. |
라. 분기별 신용공여 증감 내역
| (단위 : 천원) |
| 보증처 | 내용 | 2019 1Q | 2019 2Q | 2019 3Q | 2019 4Q | 2020 1Q | 2020 2Q | 2020 3Q | 2020 4Q | 2021 1Q | 2021 2Q | 2021 3Q | 2021 4Q | 2022 1Q | 2022 2Q | 보증기간 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 서울보증보험 | 하자이행보증 | 203,717 | (203,717) | - | - | - | - | - | - | - | - | - | - | - | - | 2018-06-23 ~ 2019-06-22 |
| 82,479 | - | - | - | - | - | - | - | - | (82,479) | - | - | - | - | 2018-06-23 ~ 2021-06-22 | ||
| 44,275 | - | - | - | - | - | - | - | - | - | - | - | - | - | 2018-06-23 ~ 2023-06-22 | ||
| 계약이행보증 | - | - | - | 647,000 | - | - | 47,159 | (694,159) | - | - | - | - | - | - | 2019-12-12 ~ 2020-12-11 | |
| - | - | - | 659,100 | - | - | 47,151 | (706,251) | - | - | - | - | - | - | 2019-12-12 ~ 2020-12-11 | ||
| - | - | - | - | - | - | 93,522 | - | - | (93,522) | - | - | - | - | 2020-07-15 ~ 2021-05-14 | ||
| - | - | - | - | - | - | - | - | - | - | - | 191,111 | - | - | 2021-06-01 ~ 2022-12-17 | ||
| 선급이행보증 | - | - | - | - | 1,382,050 | - | (1,382,050) | - | - | - | - | - | - | - | 2020-01-20 ~ 2020-07-09 | |
| - | - | - | - | 1,393,339 | - | (1,393,339) | - | - | - | - | - | - | - | 2020-01-20 ~ 2020-07-09 | ||
| - | - | - | - | - | - | 1,790,900 | - | (1,790,900) | - | - | - | - | - | 2020-07-17 ~ 2021-02-09 | ||
| - | - | - | - | - | - | 1,790,447 | - | (1,790,447) | - | - | - | - | - | 2020-07-17 ~ 2021-02-09 | ||
| - | - | - | - | - | - | 288,153 | - | - | - | 3,013 | 3,273 | - | 3,316 | 2020-07-29 ~ 2022-09-29 | ||
| - | - | - | - | - | - | - | 509,008 | - | - | - | 3,219 | (512,227) | - | 2020-12-07 ~ 2021-11-25 | ||
| - | - | - | - | - | - | - | - | 347,080 | - | - | - | (347,080) | - | 2021-01-05 ~ 2022-01-04 | ||
| - | - | - | - | - | - | - | - | 353,126 | - | - | - | (353,126) | - | 2021-01-05 ~ 2022-01-04 | ||
| - | - | - | - | - | - | - | - | - | 377,182 | 377,182 | 2,514 | (379,696) | - | 2021-06-01 ~ 2021-11-25 | ||
| - | - | - | - | - | - | - | - | - | - | - | - | - | 1,166,593 | 2022-04-20 ~ 2023-02-15 | ||
| 합 계 | 330,471 | (203,717) | - | 1,306,100 | 2,775,389 | - | 1,281,943 | (891,402) | (2,881,141) | 201,181 | 380,195 | 200,117 | (1,592,129) | 1,169,909 | - | |
마. 신용공여의 내용
| 하자이행보증 : 납품 완료한 건에 대하여 이후 발생하는 하자에 대한 보증 선급이행보증 : 계약 완료 후 지급받은 기성금에 대한 보증 계약이행보증 : 국가(정부)기관 수주 시 계약시점부터 계약 종료일까지 계약 이행에 대한 보증 |
바. 내부통제를 거친 경우 그 내용
하기 [당사의 특수관계자 신용공여 등에 대한 운영 프로세스] 참조
사. 신용공여가 채무로 확정되어 회사에서 그 채무를 부담한 경우
해당사항 없음
아. 신용공여 해소방안 및 계획
| - 국가 기관 및 정부에서 보증서 제출에 따른 서울보증보험을 이용하고 있음 - 서울보증보험에서 현대요트 신용등급 (BB-~BB)으로는 보증증권 발급 불가. 현대요트의 기업가치가 낮은 수준이기에 최대주주인 HLB의 연대보증을 요청을 하여 보증증권을 발급 함.(신용공여 발생) - 차후 신용공여 발생 방지를 위해 현대요트 보유 현금담보 등의 방안을 모색중 |
(2) 바다중공업
가. 기업개황 및 재무사항 총괄표
| [바다중공업㈜ 기업개황] |
| 구 분 | 내 용 | |
|---|---|---|
| 회사명 | 바다중공업 주식회사 | |
| 대표이사 | 진양호 | |
| 최대주주 | 진양곤 (31.98%) | |
| 주소 | 본사 | 김해시 진영읍 진산대로 135-56 |
| 연락처 | 055-720-1000 | |
| 주요사업 | 선박부품, 산업기계제조 | |
| 설립연월 | 1999. 07. 01 | |
| 결산일 | 12월 | |
| 법인구분 | 비상장법인 | |
| [주요 재무사항 총괄표] | |
| (K-GAAP, 별도) | (단위: 백만원, %) |
| 결산연월 또는 결산기간 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|
| 외부감사인의 감사의견 | 적정 | 적정 | 적정 |
| (계속기업으로서의 불확실성 관련 의견표명 및 주석사항 여부) |
(-) | (-) | (-) |
| 1. 자산총계 | 20,421 | 20,740 | 10,982 |
| - 유동자산 | 14,340 | 13,890 | 6,545 |
| 2. 부채총계 | 16,373 | 17,249 | 8,620 |
| - 유동부채 | 14,599 | 15,590 | 8,068 |
| 3. 자본총계 | 4,047 | 3,491 | 2,362 |
| 4. 부채비율 (%) | 405% | 494% | 365% |
| 5. 유동비율 (%) | 98% | 89% | 81% |
| 6. 매출액 | 16,481 | 16,068 | 11,205 |
| 7. 영업이익 | 528 | 1,339 | 301 |
| 기타 손익 | 371 | 174 | 89 |
| 금융 손익 | 328 | 384 | 196 |
| 8. 당기순이익 | 556 | 1,129 | 194 |
| 9. 자본금 | 1,350 | 1,350 | 1,350 |
| 10. 현금 및 현금성자산 기말 잔고 | 848 | 1,434 | 1,535 |
나. 신용공여 개요, 조건 및 구조
| 신용공여 대상 | 신용공여 유형 | 신용공여 기간 | 금액 | 집행 결의 이사회 | 대여(보증)목적 | 이자율 및 조건 | 지연이자율 | 상태 |
|---|---|---|---|---|---|---|---|---|
| 바다중공업 | 연대보증 |
2012.05.29.~ 2019.09.30. |
113,220,000 |
- | 국가기관과 계약수주시 보증 필요로 인한 대여 | - | - | 종결 |
| 바다중공업 |
연대보증 |
2012.06.01.~ 2019.01.31. |
188,700,000 |
- | 국가기관과 계약수주시 보증 | - | - | 종결 |
| 바다중공업 |
금전대여 |
2018.01.10~ 2018.03.30 |
500,000,000 |
2018.1.10. 이사회의사록 |
운영자금 | 연 4.6% | 연 15.0% | 회수완료 |
| 바다중공업 |
금전대여 |
2018.02.07~ 2018.06.30. |
880,000,000 |
2018.2.7. 이사회의사록 |
운영자금 | 연 4.6% | 연 15.0% | 회수완료 |
| 바다중공업 |
금전대여 |
2020.01.15.~ 2021.01.15. |
900,000,000 |
2020.1.15. 이사회의사록 |
운영자금 | 연 4.6% |
연 5.0% | 회수완료 |
| 바다중공업 | 금전대여 | 2022.04.29 ~ 2027.04.28 | 2,000,000,000 | 2022.04.27 이사회의사록 | 관계사 공장인수에 따른 수익구조 개선 등 | 연 4.6% (3년거치, 2년 원금균등상환) |
연 15.0% | 잔존 |
다. 신용공여 제공 배경
| - 대여 목적: 관계사 공장인수에 필요한 자금 대여 - 공장 인수목적: 수주증가에 따른 이익 창출의 방안으로 효율적인 생산 및 원가 절감 및 대형선박 생산의 필요 - 공장인수에 따른 기대 효과: 1. 물류비 및 부대비용의 절감(연간 3억원의 절감효과) ① 제작공간 부족으로 인해 제품 및 지그 이동으로 인한 운반비용 절감 ② 생산시설(공간) 증축에 따른 외주비 감소 2. 효율적인 인적관리 및 통합운영 가능 ① 2공장, 3공장의 이동으로 인한 손실 감소 및 근로자의 기술적 소통 원활, 생산프로세스 개선, 대형제품 생산 가능 ② MHE, 특수선 장비 직접 제작으로 인한 기술 역량 상승(1공장 통합운영 및 기술이전, 외주제작 감소) ③ 대형화제품, 장기 납기에 필요한 적재장소 확충(대형화 제품 생산가능으로 인한 수주 증가 기대, 기존 조선소 및 발주사 홍보) ④ 단일공장이므로 안전, 품질, 환경 등 통합관리가 용이함 |
라. 분기별 신용공여 증감 내역
| (단위 : 천원) |
| 내용 | 2019 1Q | 2019 2Q | 2019 3Q | 2019 4Q | 2020 1Q | 2020 2Q | 2020 3Q | 2020 4Q | 2021 1Q | 2021 2Q | 2021 3Q | 2021 4Q | 2022 1Q | 2022 2Q |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 금전대여 | - | - | - | - | 900,000 | (900,000) | - | - | - | - | - | - | - | - |
| 금전대여 | - | - | - | - | - | - | - | - | - | - | - | - | - | 2,000,000 |
| 합 계 | - | - | - | - | 900,000 | - | - | - | - | - | - | - | - | 2,000,000 |
마. 관련 대여금의 회수가능성 여부
|
1. 취득자산(공장)의 감정가는 51.3억원이며, 기업은행에서 1순위 40.8억원 담보, 바다중공업에서 2순위 20억원 담보를 설정함.
- 2022년 04월 8일 기준 바다중공업의 수주잔고는 약 300억원으로, 2023년 수주목표의 50%이상 수주한 상태임. |
바. 내부통제를 거친 경우 그 내용
하기 [당사의 특수관계자 신용공여 등에 대한 운영 프로세스] 참조
사. 신용공여가 채무로 확정되어 회사에서 그 채무를 부담한 경우
해당사항 없음
(3) 펭귄오션레저
가. 기업개황 및 재무사항 총괄표
| [㈜펭귄오션레저 기업개황] |
| 구 분 | 내 용 | |
|---|---|---|
| 회사명 | ㈜펭귄오션레저 | |
| 대표이사 | 김자우 | |
| 최대주주 | 진양곤(81.61%) | |
| 주소 | 본사 | 울산광역시 울주군 온산읍 당월로 272-12 |
| 연락처 | 02-3443-1458 | |
| 주요사업 | 보트(잠수함) 제조 | |
| 설립연월 | 2017년 | |
| 결산일 | 12월 | |
| 법인구분 | 비상장법인 | |
| [주요 재무사항 총괄표] | |
| (K-GAAP, 별도) | (단위: 백만원, %) |
| 결산연월 또는 결산기간 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|
| 1. 자산총계 | 1,369 | 665 | 692 |
| - 유동자산 | 863 | 665 | 692 |
| 2. 부채총계 | 666 | 786 | 1,091 |
| - 유동부채 | 291 | 383 | 881 |
| 3. 자본총계 | 703 | 362 | 1 |
| 4. 부채비율 (%) | 49% | 118% | 158% |
| 5. 유동비율 (%) | 297% | 174% | 79% |
| 6. 매출액 | 522 | 178 | 544 |
| 7. 영업이익 | (907) | (197) | (145) |
| 기타 손익 | 1,269 | 135 | 61 |
| 금융 손익 | 1,057 | 29 | 22 |
| 8. 당기순이익 | 341 | (91) | (106) |
| 9. 자본금 | 721 | 721 | 271 |
| 10. 현금 및 현금성자산 기말 잔고 | - | - | - |
| 출처 : 자체자료, 감사받지 아니한 재무제표 |
나. 신용공여 개요, 조건 및 구조
| 신용공여 대상 | 신용공여 유형 | 신용공여 기간 | 금액 | 집행 결의 이사회 | 대여목적 | 이자율 및 조건 | 지연이자율 | 상태 |
|---|---|---|---|---|---|---|---|---|
| 펭귄오션레저 | 금전대여 | 2014-12-31 ~2015-12-31 | 23,600,000 | - | 운영자금 | 6.90% | 15% | 대손처리 |
다. 신용공여 제공 배경
| 말레이시아에서 영위하던 사업에 파견된 HLB 소속 직원에 대한 해외 영업비, 체류비 등의 명목으로 지급 |
라. 분기별 신용공여 증감 내역
| 구분 | 회사명 | 내용 | 2014 4Q | 2015 1Q | 2015 2Q | 2015 3Q | 2015 4Q | 대여기간 |
|---|---|---|---|---|---|---|---|---|
| 관계기업 | 펭귄오션레저 | 금전대여 | 23,600,000 | 23,600,000 | 23,600,000 | 23,600,000 | (23,600,000) | 2014-12-31 ~ 2015-12-31 |
| 합 계 | 23,600,000 | 23,600,000 | 23,600,000 | 23,600,000 | (23,600,000) | - | ||
마. 관련 대여금의 회수가능성 여부
2015년 12월 31일 회수가능성 부족으로 인해 대손처리 완료
바. 내부통제를 거친 경우 그 내용
하기 [당사의 특수관계자 신용공여 등에 대한 운영 프로세스] 참조
사. 신용공여가 채무로 확정되어 회사에서 그 채무를 부담한 경우
2015년 12월 31일 회수가능성 부족으로 인해 대손처리 완료
(4) 현대앤코스모스요팅㈜
가. 기업개황 및 재무사항 총괄표
| [현대앤코스모스요팅㈜ 기업개황] |
| 구 분 | 내 용 | |
|---|---|---|
| 회사명 | 현대앤코스모스요팅㈜ | |
| 대표이사 | 이철웅 | |
| 최대주주 | 진양곤(24.14%) | |
| 주소 | 본사 | 인천광역시 중구 왕산마리나길 143, 1층 A-1호 |
| 연락처 | 032-710-6975 | |
| 주요사업 | 차터 서비스 | |
| 설립연월 | 2013-05-21 | |
| 결산일 | 12월 | |
| 법인구분 | 비상장법인 | |
| [주요 재무사항 총괄표] | |
| (K-GAAP, 별도) | (단위: 백만원, %) |
| 결산연월 또는 결산기간 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|
| 1. 자산총계 | 3,279 | 2,181 | 2,673 |
| - 유동자산 | 1,242 | 36 | 492 |
| 2. 부채총계 | 392 | 2,157 | 2,502 |
| - 유동부채 | 380 | 785 | 511 |
| 3. 자본총계 | 2,887 | 24 | 171 |
| 4. 부채비율 (%) | 12% | 98% | 93% |
| 5. 유동비율 (%) | 326% | 4% | 96% |
| 6. 매출액 | 461 | 292 | 610 |
| 7. 영업이익 | (224) | (323) | (432) |
| 기타 손익 | 224 | 262 | 7 |
| 금융 손익 | 103 | 87 | 114 |
| 8. 당기순이익 | 2,862 | (147) | (539) |
| 9. 자본금 | 1,450 | 1,450 | 1,450 |
| 10. 현금 및 현금성자산 기말 잔고 | 1,242 | 36 | 110 |
| 출처 : 자체자료, 감사받지 아니한 재무제표 |
나. 신용공여 개요, 조건 및 구조
| 신용공여 대상 | 신용공여 유형 | 신용공여 기간 | 금액 | 집행 결의 이사회 | 대여목적 | 이자율 및 조건 | 지연이자율 | 상태 |
|---|---|---|---|---|---|---|---|---|
| 현대앤코스모스요팅 | 금전대여 | 2017.04.05 ~ 2017.07.31 | 500,000,000 | 2017-04-05 | 바바리아요트 수입관련 비용 | 4.60% | 15% | 종결 |
| 현대앤코스모스요팅 | 금전대여 | 2017.07.03 ~ 2017.07.31 | 500,000,000 | 2017-07-03 | 바바리아요트 수입관련 비용 | 4.60% | 15% | 종결 |
다. 신용공여 제공 배경
| 외국 소재 바바리아社의 레저용 요트의 수입을 위하여 긴급히 자금의 조달이 필요한 상황이었음. 현대앤코스모스요팅이 수입한 레저용 요트를 현대요트에 공급하고자 하였고 그 이후 현대요트가 공급받은 레저용 요트를 이용하여 요트 차터(대여) 서비스를 제공을 하기 위한 목적임 |
라. 분기별 신용공여 증감 내역
| 구분 | 회사명 | 내용 | 2017 1Q | 2017 2Q | 2017 3Q | 2017 4Q | 대여기간 |
|---|---|---|---|---|---|---|---|
| 관계기업 | 현대앤코스모스요팅 | 금전대여 | 500,000,000 | (500,000,000) | - | - | 2017-04-05 ~ 2017-06-30 |
| 금전대여 | - | - | 500,000,000 | (500,000,000) | 2017-07-03 ~ 2017-07-31 | ||
| 합 계 | 500,000,000 | (500,000,000) | 500,000,000 | (500,000,000) | |||
마. 관련 대여금의 회수가능성 여부
| 2017년 04월 05일 대여금 - 2017년 06월 30일 회수 완료 2017년 07월 03일 대여금 - 2017년 07월 31일 회수 완료 |
바. 내부통제를 거친 경우 그 내용
하기 [당사의 특수관계자 신용공여 등에 대한 운영 프로세스] 참조
사. 신용공여가 채무로 확정되어 회사에서 그 채무를 부담한 경우
해당사항 없음.
(6) 에이치엘비글로벌㈜
가. 기업개황 및 재무사항 총괄표
| [에이치엘비글로벌㈜ 기업개황] |
| 구 분 | 내 용 | |
|---|---|---|
| 회사명 | 에이치엘비글로벌㈜ | |
| 대표이사 | 김종원 | |
| 최대주주 | 진양곤(6.25%) | |
| 주소 | 본사 | 강원도 정선군 사북읍 동탄길 38-13 |
| 연락처 | 02-6925-4450 | |
| 주요사업 | 리소스사업, 리테일사업(화장품, 식품/음료) | |
| 설립연월 | 1962년 04월 | |
| 결산일 | 12월 | |
| 법인구분 | 상장법인 | |
| 상장연월 | 1990년 03월 | |
| [주요 재무사항 총괄표] | |
| (K-IFRS, 별도) | (단위: 백만원, %) |
| 결산연월 또는 결산기간 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|
| 외부감사인의 감사의견 | 적정 | 적정 | 적정 |
| (계속기업으로서의 불확실성 관련 의견표명 및 주석사항 여부) |
- | - | - |
| 1. 자산총계 | 131,215 | 99,046 | 115,162 |
| - 유동자산 | 43,262 | 28,444 | 47,103 |
| 2. 부채총계 | 24,363 | 37,666 | 43,750 |
| - 유동부채 | 24,218 | 18,710 | 29,272 |
| 3. 자본총계 | 106,852 | 61,381 | 71,412 |
| 4. 부채비율 (%) | 19% | 38% | 38% |
| 5. 유동비율 (%) | 179% | 152% | 161% |
| 6. 매출액 | 15,517 | 14,638 | 10,989 |
| 7. 영업이익 | (6,070) | (6,155) | (5,141) |
| 기타 손익 | 5,385 | 3,467 | 16,396 |
| 금융 손익 | 6,396 | 27,099 | 42,070 |
| 8. 당기순이익 | (6,556) | (28,924) | (29,301) |
| 9. 자본금 | 21,033 | 16,350 | 14,217 |
| 10. 현금 및 현금성자산 기말 잔고 | 5,824 | 11,684 | 18,157 |
| 출처 : 에이치엘비글로벌㈜ 정기보고서 |
나. 신용공여 개요, 조건 및 구조
| 신용공여 대상 | 신용공여 유형 | 신용공여 기간 | 금액 | 집행 결의 이사회 | 대여목적 | 이자율 및 조건 | 지연이자율 | 상태 |
|---|---|---|---|---|---|---|---|---|
| 에이치엘비글로벌 | 금전대여 | 2019-09-16 ~ 2019-10-15 | 9,000,000,000 | 2019.09.16 | 단기자금운영 | 4.60% | - | 종결 |
다. 신용공여 제공 배경
| 에이치엘비글로벌이 발행한 사채의 투자가가 풋옵션(조기상환청구권)을 행사함에 따라 에이치엘비글로벌로서 그 당시 그 상환대금 상당의 자금이 필요로 하여 제공 |
라. 분기별 신용공여 증감 내역
| 구분 | 회사명 | 내용 | 2019 3Q | 대여 기간 |
|---|---|---|---|---|
| 관계기업 | 에이치엘비글로벌 | 금전대여 | 9,000,000,000 | 2019-09-16 ~ 2019-09-24 |
| 금전대여 | (9,000,000,000) | |||
| 합 계 | - | - | ||
마. 관련 대여금의 회수가능성 여부
| 2019년 09월 24일 회수완료 |
바. 내부통제를 거친 경우 그 내용
하기 [당사의 특수관계자 신용공여 등에 대한 운영 프로세스] 참조
사. 신용공여가 채무로 확정되어 회사에서 그 채무를 부담한 경우
해당사항 없음
상기와 같이, 당사는 과거 최대주주의 특수관계인에 자금대여 및 지급보증을 제공한 사실이 있으며, 그 결과 상법 제542조의9 제1항을 위반하는 경우 상법 제624조의2에 의하여 5년 이하 징역 또는 2억원 이하의 벌금형 처벌을 받을 수도 있습니다. 위 「상법」 제624조의2에서는 구체적 행위(형사책임)주체를 규정하고 있지 않으나, 해당 신용공여행위를 한 이사 등이 책임을 부담할 것으로 예상됩니다.
「상법」 제624조의2는 위반시의 형벌을 아래와 같이 규정하고 있습니다.
| 상법 제624조의2(주요주주 등 이해관계자와의 거래 위반의 죄) |
| 제624조의2(주요주주 등 이해관계자와의 거래 위반의 죄) 제542조의9제1항을 위반하여 신용공여를 한 자는 5년 이하의 징역 또는 2억원 이하의 벌금에 처한다. |
또한 「상법」 제634조의3은 '회사의 대표자나 대리인, 사용인, 그 밖의 종업원이 그 회사의 업무에 관하여 제624조의2 위반행위를 하면 그 행위자를 벌하는 외에 그 회사에도 해당 조문의 벌금형을 과한다. 다만, 회사가 제542조의13에 따른 의무를 성실히 이행한 경우 등 회사가 그 위반행위를 방지하기 위하여 해당 업무에 관하여 상당한 주의와 감독을 게을리하지 아니한 경우에는 그러하지 아니하다'라고 규정하고 있습니다.
따라서 상법 제542조의9 제1항 위반으로 당사의 대표이사가 기소될 시 당사도 양벌규정에 따라 함께 기소될 수 있으며, 당사 역시 재판 결과에 따라 2억원이하의 벌금형에 처해질 수도 있습니다. 투자자들께서는 당사의 벌금 부과 가능성에 유의하시기 바랍니다.
또한, 이사가 고의/중대한 과실로 인하여 그 임무를 게을리한 때에는 그 이사는 제3자에 대하여 연대하여 손해를 배상할 책임(「상법」제401조)이 있으며, 법인은 이사 기타 대표자가 그 직무에 관하여 타인에게 가한 손해를 배상할 책임이 있습니다(「민법」 제35조 제1항).
신용공여금지를 위반한 이사들은 당사의 소속이었으므로 만약 이사들의 제3자에 대한 상법 제401조에 따른 책임이 인정될 경우 당사는 이사들과 연대하여 제3자에게 손해를 배상할 가능성이 존재합니다. 투자자들께서는 이 점 특히 유의하시기 바랍니다. 투자자들께서는 해당 신용공여로 인해 당사, 당사의 대표이사 및 이사 등에 대한 사법조치 가능성이 있으며 당사에 벌금 및 제재, 손해배상책임, 법률적 비용 등의 사법적 리스크 발생 가능성이 있음에 특히 유의하시기 바랍니다.
당사는 상기에 기술된 거래와 같이 상법에 저촉될 가능성이 있는 거래에 대하여 인지하고, 거래가 이루어지기 이전에 적법한 절차를 보장하기 위해 증권신고서 제출일 현재 자기거래 및 주요주주 등에 대한 신용공여 관련 내부 규정과 조직, 통제절차 등을 전반적으로 정비하여 「상법」, 「자본시장과 금융투자업에 관한 법률」, 「금융투자업규정」 및 「법인세법」 등을 사전적으로 면밀히 검토할 수 있도록 하였고, 상기와 같은 거래내용으로 인한 적법성 우려가 향후 발생하지 않도록 조치하였습니다.
| [당사의 특수관계자 신용공여 등에 대한 운영 프로세스] |
| (기준일: 2022년 08월 12일) |
|
사법 당국이 상법 위반 소지가 있는 거래 내용에 대하여 위법임을 최종 판단하고 법에서 정하는 양형 규정에 따라 제재 조치를 가할 경우 당사는 적용되는 법에 따라 벌금을 부담해야 할 가능성이 있으며, 이 경우 그 금액에 따라 당사에 재무적 부담으로 작용할 수 있습니다. 투자자께서는 이 점에 유의하시기 바랍니다.
| 너. 소송, 우발채무 및 제재 등 관련 위험 연결실체는 담보 및 보증제공으로 인한 우발부채를 보유하고 있으며, 당사가 제공한 담보 및 보증과 관련하여 우발부채가 현실화 되거나 추가적인 대손충당 등이 발생할 경우 당사 재무에 부정적인 영향을 줄 수 있습니다. 또한, 당사는 산업안전보건법 위반으로 제재를 받은 사실이 있으며, 위반사항 중 일부 입건 사항에 대하여는 법원에 약식명령 청구되어 벌금을 부과받은 사실이 있습니다. 동 건과 관련하여 당사에 기 부과된 과태료 및 벌금의 규모는 미미하여 당사의 재무적 상황에 유의미한 영향을 미치지 않으나, 향후 조사 결과 일부 위반 사실에 대하여 부정적인 명령을 선고하거나 정식재판 절차에 회부하는 경우 당사의 평판 등에 악영향을 미칠 가능성을 배제할 수 없습니다.투자자께서는 투자 판단 시 당사의 담보 및 보증 제공 등과 관련한 우발부채 현황, 소송 및 제재현황을 면밀히 확인하시고, 이로 인한 우발부채의 현실화 또는 사법기관 등의 제재로 인한 당사의 평판에 하락 가능성 등에 주의하시기 바랍니다. 또한 특수관계자를 대상으로 하는 지급보증 등 신용공여에 해당하는 항목에 대한 구체적 위험 내용은 본 증권신고서 " III. 투자위험요소 - 2. 회사위험 - 거."를 참고하여 주시기 바랍니다. |
증권신고서 제출일 현재 당사가 원고로 계류 중인 소송은 1건으로, 소송금액은 300억원 입니다. 당사는 2020년 06월 하이투자증권㈜를 통해 판매되었던 옵티머스자산운용 펀드에 300억원을 위탁하였습니다. 당사가 투자한 펀드가 운용사 및 판매사의 고지내용과 무관한 자산에 투자되었음에 따라 이에 대해 부당이득금반환청구 소송을 제기하였으며, 현재 1심 진행 중입니다. 소송 발생 경위 및 현황, 향후 계획 등은 "III. 투자위험요소 - 2. 회사위험 - 바."를 참고해주시기 바랍니다.
| [당사가 원고인 사건] |
| 소 제기일 | 사건내용 | 원고 | 피고 | 소송가액 | 진행상태 |
|---|---|---|---|---|---|
| 2020.6.29 | 부당이득금 반환 청구 소송 |
에이치엘비 주식회사 |
하이투자증권 주식회사 |
금 300억원 | 1심 진행중 |
증권신고서 제출일 현재 계류 중인 소송 사건에 대해서는 소송의 결과를 합리적으로 예측할 수 없으며, 연결실체는 동 시점 관계기업인 현대요트㈜에 약 1,683백만원 규모의 지급보증을 제공하고 있으며, 상세 내용은 다음과 같습니다.
[연결기준]
| (기준일: 2022년 06월 30일) | |
| (단위: 백만원) |
| 구분 | 회사명 | 보증처 | 내용 | 지급보증금액 | 보증기간 |
| 관계기업 | 현대요트㈜ | 서울보증보험 | 하자이행보증 | 44 | 2018-06-23 ~ 2023-06-22 |
| 선급이행보증 | 281 | 2020-07-29 ~ 2022-09-29 | |||
| 계약이행보증 | 191 | 2021-06-01 ~ 2022-12-17 | |||
| 선급이행보증 | 1,167 | 2022-04-20 ~ 2023-02-15 | |||
| 합 계 | 1,683 | ||||
당사는 주권상장법인으로서 상기와 같은 특수관계인을 대상으로 하는 신용공여 제공에 대하여 「상법」제542조의9의 적용을 받습니다. 이와 관련된 상세한 위험 내용은본 증권신고서 "III. 투자위험요소 - 2. 회사위험 - 거."의 내용을 참고하여 주시기 바랍니다.
한편, 당사는 서울보증보험으로부터 하자이행보증금 등에 대하여 지급보증 받고있으며, 내역은 다음과 같습니다.
| (기준일: 2022년 06월 30일) | |
| (단위: 백만원) |
| 제공자 | 제공처 | 보증금액 | 비고 |
|---|---|---|---|
| 서울보증보험 | 매출처 등 | 1,458 | 하자이행보증, 지급보증 등 |
증권신고서 제출일 전일 현재 연결실체가 금융기관 등과 맺은 대출약정의 내역은 다음과 같습니다.
| (기준일: 2022년 06월 30일) | |
| (단위: 천원) |
| 구 분 | 차입종별 | 약정금액 | 담보제공금액 |
|---|---|---|---|
| 중소기업은행(*) | 일반운전자금대출 등 | 320 | 384 |
| (*) 연결실체는 중소기업은행에 대하여 토지, 건물, 기계장치를 담보로 제공하고 있습니다. |
최근 3사업연도 이내에 연결실체가 금융, 조세 및 사법 당국 등으로부터 부과받은 제재의 내용은 다음과 같습니다.
| [연결실체가 부과받은 제재 현황] |
| 항목 | 제재 조치일 | 근거 법령 | 사유 | 제재 내용 | 회사의 이행현황 및 처리상태 |
|---|---|---|---|---|---|
| 산업안전보건법 위반 |
2019.12.3 | 산업안전보건법 제12조 제31조 제3항 제41조 제5항 |
A동 아세톤 보관용기 MSDS 경고표시 미게시(3개소) 엔진실의 변속기실 윤활유, 그리스 MSDS 경고표시 미게시 B동 성형경화제 MSDS경고표시 미게시(총6개소) A동 안전보건표시 미부착(방진마스크) 건조설비 담당자 특별교육 미실시 |
과태료: 304,000원 벌금: 1,500,000원 |
- 시정명령사항 9건에 대한 시정조치 완료 후 과태료 납부 완료 - 위반사항 중 입건 사항에 대하여는 법원에 약식명령 청구되어, 금 1,500,000원을 부과받음(사건번호 2020고약622) |
| 코스닥시장공시규정 위반 |
2022.01.13 | 코스닥시장공시규정 제27조, 제32조, 제34조 |
타법인 주식 및 출자증권 양수결정 지연공시 신주인수권부사채 발행결정 지연공시 |
공시위반제재금 : 24,000,000원 |
- 제재금 납부 완료 |
상기와 같이 연결실체는 담보 및 보증제공으로 인한 우발부채를 보유하고 있으며, 당사가 제공한 담보 및 보증과 관련하여 우발부채가 현실화 되거나 추가적인 대손충당 등이 발생할 경우 당사 재무에 부정적인 영향을 줄 수 있습니다. 또한 당사는 불성실산업안전보건법 위반으로 제재를 받은 사실이 있으며, 코스닥시장공시규정 위반으로제재금을 대체부과 받은 사실이 있습니다. 산업안전보건법 위반사항 중 일부는 입건 사항으로 법원의 약식명령에 따라 과태료 304,000원 및 벌금 1,500,000원을 부과 받았으며, 코스닥시장공시규정 위반사항은 '타법인 주식 및 출자증권 양수결정 지연공시' 및 '신주인수권부사채 발행결정 지연공시'로 인해 공시위반 제재금 2,400만원(합계 6점 * 400만원)을 부과받았습니다.
동 건으로 당사에 부과된 과태료, 벌금 및 공시위반제재금의 규모는 매우 작은 수준이며 사안의 중요성을 감안할 때 당사의 재무적 상황에 유의미한 영향을 미칠 수준은아닐 것으로 예상되나, 향후 사법 당국이 일부 위반 사실에 대하여 당사에 부정적인 명령을 선고하거나 정식재판 절차에 회부하는 경우 당사의 평판 등에 악영향을 미칠 가능성을 배제할 수 없습니다.
투자자께서는 투자 판단 시 상기와 같은 당사의 담보 및 보증 제공 등과 관련한 우발부채 현황, 소송 및 제재현황을 면밀히 확인하시고, 이로 인한 우발부채의 현실화 또는 당사의 평판에 하락 가능성 등에 주의하시기 바랍니다.
| 더. 매출채권 미회수 및 재고자산 진부화 관련 위험 당사의 매출채권 장부가액은 2019년 6,584백만원에서 2020년 11,747백만원으로 일부 증가하였으며 이는 2020년 중 리보세라닙 원천 특허를 인수함에 따라 항서제약으로부터 리보세라닙 로열티 5,856백만원이 발생한 점에 기인합니다. 2021년에는 ㈜에프에이 인수 및 합병으로 매출규모가 증가함에 따라 매출채권 규모도 동시에 증가했으며, 폐업으로 인해 회수가 불가능한 장기매출채권 31백만원을 제각처리했습니다. 2022년 반기의 경우 전년말 대비 5,967백만원 감소했습니다.매출채권회전율의 경우 2019년 5.9회, 2020년 6.1회를 기록했고, 2021년부터 매출액의 증가폭보다 매출채권 증가폭이 커지면서 3.1회까지 감소했으나, 2022년 반기 매출액이 증가하면서 8.0회로 증가했습니다. 그러나, 매출채권 부실 방지에 대한 적극적인 노력이 미진할 경우 당사의 자금수지 및 재무상태에 악영향을 줄 수 있으며, 충당금 설정율이 높아질 경우 손익에 부정적인 영향을 미칠 수 있습니다. 당사는 최근 3년 및 2022년 반기까지 평균 총자산 대비 재고자산 구성비율은 약 1.1%이며, 평가손실충당금 비율은 동기간 감소하는 추이를 보이고 있습니다. 총 재고자산은 2019년과 2020년 5,000백만원 내외를 기록했으나, 2021년에는 ㈜에프에이 인수에 따라 부재료 재고자산이 크게 증가하면서 13,811백만원까지 증가했습니다. 재고자산 회전율의 경우 2019년 7.9회에서 2021년 10.5회까지 증가하였으며, 2022년 반기(단순 매출원가 연환산한 금액)의 경우 매출액 증가에 따른 영향으로 9.4회까지 감소하였습니다. 당사 자산에 유의적인 영향을 미치고 있지 않으나, 향후 매출채권이 미회수되고 재고자산이 진부화될 경우 당사 손익 및 재무에 부정적인 영향을 미칠 수 있으므로 이 점 유의하여 투자해 주시기 바랍니다. |
[매출채권 미회수 관련 위험]
당사는 매출채권의 연령분석과 과거의 대손경험율을 토대로 대손충당금 설정비율을 다음과 같은 기준으로 설정하고 있습니다. 재무상태표일 현재 매출채권 잔액중 재무상태표일 이후에 회수된 금액 및 담보권이 설정되어 있는 채권은 설정대상에서 제외하고, 개별분석 및 과거의 대손경험율을 토대로 하여 대손충당금으로 설정하고 있습니다.
| [당사 연결기준 매출채권 추이] |
| (단위 : 백만원) |
|
구분 |
2022년 반기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
|
매출채권(유동) |
29,056 | 35,023 | 13,522 | 8,543 |
|
(대손충당금) |
(1,061) | (988) | (1,776) | (1,960) |
|
매출채권(유동) 장부가액 |
27,995 | 34,035 | 11,747 | 6,584 |
| 장기성 매출채권(비유동) | - | - | 31 | 31 |
| (대손충당금) | - | - | (31) | (31) |
| 장기성매출채권(비유동) 장부가액 | - | - | - | - |
| 매출채권 및 장기성매출채권 합계 | 27,995 | 34,035 | 11,747 | 6,584 |
| 대손충당금 설정률(%) | 3.7% | 2.8% | 13.1% | 22.9% |
|
자산총계 |
813,143 | 743,692 | 706,477 | 362,612 |
|
자산총계 대비 매출채권 비중(%) |
3.4% | 4.6% | 1.7% | 1.8% |
|
매출액 |
123,305 | 69,826 | 56,177 | 38,421 |
|
매출채권회전율(회) |
8.0 | 3.1 | 6.1 | 5.9 |
| 주1) 매출채권회전율 = 연환산 매출액÷{(전기매출채권+당기매출채권)÷2}] 주2) 2022년 반기 매출채권회전율(회)는 매출액을 단순 연환산하여 산정함. |
당사의 매출채권 장부가액은 2019년 6,584백만원에서 2020년 11,747백만원으로 일부 증가하였으며 이는 2020년 중 리보세라닙 원천 특허를 인수함에 따라 항서제약으로부터 리보세라닙 로열티 5,856백만원이 발생한 점에 기인합니다. 2021년에는 ㈜에프에이 인수 및 합병으로 매출규모가 증가함에 따라 매출채권 규모도 동시에 증가했으며, 폐업으로 인해 회수가 불가능한 장기매출채권 31백만원을 제각처리했습니다. 2022년 반기의 경우 전년말 대비 5,967백만원 감소했습니다.
매출채권회전율의 경우 2019년 5.9회, 2020년 6.1회를 기록했고, 2021년부터 매출액의 증가폭보다 매출채권 증가폭이 커지면서 3.1회까지 감소했으나, 2022년 반기 매출액이 증가하면서 8.0회로 증가했습니다.
대손충당금설정률은 2019년 22.9%, 2020년 13.1%를 기록했으나 2021년말 연결기준 2.8%, 2022년 반기 3.7%를 기록하고 있으며, 또한 2021년말 및 2022년 반기말 기준 자산총계 대비 매출채권 비중은 4.6% 및 3.4% 수준으로, 당사의 재무구조에 유의미한 영향을 미칠 가능성은 낮은 것으로 판단되고 있습니다. 그러나, 매출채권 부실 방지에 대한 적극적인 노력이 미진할 경우 당사의 자금수지 및 재무상태에 악영향을 줄 수 있으며, 충당금 설정율이 높아질 경우 손익에 부정적인 영향을 미칠 수 있습니다.
[재고자산 진부화 관련 위험]
재고자산의 취득원가는 매입원가, 전환원가 및 재고자산을 현재의 장소에 현재의 상태로 이르게 하는 데 발생한 기타 원가 모두를 포함하고 있으며, 재고자산의 단위원가는 선입선출법(미착품은 개별법)을 사용하여 결정하고 있습니다. 당사는 재고자산을 취득원가와 순실현가능가치 중 낮은 금액으로 측정하고 있으며, 재고자산의 판매시 관련된 수익을 인식하는 기간에 재고자산의 장부금액을 비용으로 인식하고, 재고자산을 순실현가능가치로 감액한 평가손실과 모든 감모손실은 감액이나 감모가 발생한 기간에 비용으로 인식하며, 순실현가능가치의 상승으로 인한 재고자산 평가손실의 환입은 환입이 발생한 기간의 비용으로 인식된 재고자산 금액의 차감액으로 인식하고 있습니다.
| [재고자산 현황] |
| (단위 : 백만원, 회) |
| 구분 | 2022년 반기 | 2021년말 | 2020년말 | 2019년말 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 취득원가 | 평가손실 충당금 |
장부금액 | 취득원가 | 평가손실 충당금 |
장부금액 | 취득원가 | 평가손실 충당금 |
장부금액 | 취득원가 | 평가손실 충당금 |
장부금액 | |
| 상품 | 3,745 | (204) | 3,541 | 3,594 | (2) | 3,592 | 2,075 | (367) | 1,708 | 2,151 | (251) | 1,900 |
| 제품 | 5,877 | (359) | 5,518 | 3,615 | (166) | 3,449 | 3,030 | (265) | 2,766 | 2,960 | (345) | 2,615 |
| 원재료 | 160 | - | 160 | 252 | - | 252 | 239 | (200) | 39 | 200 | (200) | - |
| 부재료 | 8,302 | (146) | 8,156 | 6,495 | - | 6,495 | 468 | (107) | 361 | 510 | (107) | 403 |
| 저장품 | - | - | - | 23 | - | 23 | - | - | - | - | - | - |
| 합 계 | 18,085 | (710) | 17,376 | 13,979 | (168) | 13,811 | 5,813 | (939) | 4,874 | 5,821 | (902) | 4,918 |
| 총자산 대비 재고자산 구성비율(%) | 2.1% | 1.9% | 0.7% | 1.4% | ||||||||
| 평가손실충당금 비율(%) | 3.9% | 1.2% | 16.1% | 15.5% | ||||||||
| 재고자산회전율(회) | 9.4 | 10.5 | 9.4 | 7.9 | ||||||||
|
주1) 총자산대비 재고자산 구성비율(%) = [재고자산÷기말자산총계×100] 주2) 재고자산회전율 = [연환산 매출원가÷{(기초재고+기말재고)÷2}] |
당사는 최근 3년 및 2022년 반기까지 평균 총자산 대비 재고자산 구성비율은 약 1.1%이며, 평가손실충당금 비율은 동기간 감소하는 추이를 보이고 있습니다. 총 재고자산은 2019년과 2020년 5,000백만원 내외를 기록했으나, 2021년에는 ㈜에프에이 인수에 따라 부재료 재고자산이 크게 증가하면서 13,811백만원까지 증가했습니다. 재고자산 회전율의 경우 2019년 7.9회에서 2021년 10.5회까지 증가하였으며, 2022년 반기(단순 매출원가 연환산한 금액)의 경우 매출액 증가에 따른 영향으로 9.4회까지 감소하였습니다.
매출이 발생하지 못해 재고자산이 증가할 경우 창고에 보관된 기간이 길어지는 것을 의미하므로 회사 입장에서는 재고 보관비용의 증가, 재고자산의 노후화 위험을 동시에 부담할 가능성을 시사합니다. 당사는 향후 보다 정확한 수요예측 및 생산량조절을통해 적정수준의 재고자산 보유를 위해 노력하고, 진부화된 재고자산에 대한 적시 평가를 통한 관리를 지속할 예정입니다. 다만, 향후 매출 증가 및 품목 다변화에 의한 재고자산 증가 및 산업환경 변화에 대한 적응 미숙으로 인한 재고자산의 진부화 가능성은 여전히 존재하며, 이에 따라 재고자산의 평가손실 및 폐기가 지속된다면 당사의 수익성에 악영향을 미칠 수 있습니다.
당사의 자산 중 매출채권 및 재고자산이 차지하는 비중은 2022년 반기 기준 5.6%로 높은 비중을 차지하고 있지 않으며, 당사 자산에 유의적인 영향을 미치고 있지 않으나, 향후 매출채권이 미회수되고 재고자산이 진부화될 경우 당사 손익 및 재무에 부정적인 영향을 미칠 수 있으므로 이 점 유의하여 투자해 주시기 바랍니다.
| 러. 외부감사 및 지정감사 위험 당사는 2019년 10월 14일 <직전 사업연도를 포함하여 과거 3년간 최대주주의 변경이 2회 이상 발생하거나 대표이사의 교체가 3회 이상 발생한 주권상장법인, 3개 사업연도 연속 영업이익이 0보다 작은 회사, 3개 사업연도 연속 영업현금흐름이 0보다 작은 회사, 3개 사업연도 연속 이자보상배율이 1 미만인 회사>에 해당하여 「주식회사 등의 외부감사에 관한 법률」제11조 제1항 및 제2항, 동법 시행령 제17조 및 「외부감사 및 회계 등에 관한 규정」 제10조 및 제15조 제1항에 따라 2020년부터 3년 동안 증권선물위원회로부터 지정받은 외부 감사인인 삼덕회계법인으로부터 회계 감사를 수감해야 합니다. 이처럼 지정감사로 인해 추후 당사에 대한 감사 강도가 강화될 수 있으며, 이 경우 당사의 감사의견에 영향을 끼칠 수 있습니다. 투자자께서는 당사가 지정감사 대상으로 선정되었음에 유의하시기 바랍니다. |
당사는 2019년 10월 14일 <직전 사업연도를 포함하여 과거 3년간 최대주주의 변경이 2회 이상 발생하거나 대표이사의 교체가 3회 이상 발생한 주권상장법인, 3개 사업연도 연속 영업이익이 0보다 작은 회사, 3개 사업연도 연속 영업현금흐름이 0보다 작은 회사, 3개 사업연도 연속 이자보상배율이 1 미만인 회사>에 해당하여 「주식회사 등의 외부감사에 관한 법률」제11조 제1항 및 제2항, 동법 시행령 제17조 및 「외부감사 및 회계 등에 관한 규정」 제10조 및 제15조 제1항에 따라 2020년부터 3년 동안 증권선물위원회로부터 지정받은 외부 감사인인 삼덕회계법인으로부터 회계 감사를 수감해야 합니다. 이처럼 지정감사로 인해 추후 당사에 대한 감사 강도가 강화될 수 있으며, 이 경우 당사의 감사의견에 영향을 끼칠 수 있습니다. 투자자께서는 당사가 지정감사 대상으로 선정되었음에 유의하시기 바랍니다.
(1) 직전 사업연도를 포함하여 과거 3년간 최대주주의 변경이 2회 이상 발생하거나 대표이사의 교체가 3회 이상 발생한 주권상장법인
| [당사 대표이사 변동 내역] |
| 연도 | 변동 전 | 변동 후 |
|---|---|---|
| 2009. 01 | 대표이사 김영세 | 대표이사 남상우 |
| 2012. 01 | 대표이사 남상우 | 대표이사 박정민 |
| 2017. 06 | 대표이사 박정민 | 대표이사 진양곤 |
| 2019. 03 | 대표이사 진양곤 | 각자 대표이사 김하용, 김성철 |
| 2019. 06 | 각자 대표이사 김하용, 김성철 | 대표이사 진양곤 |
| 2021.03 | 대표이사 진양곤 | 각자 대표이사 진양곤, 김동건 |
(2) 3개 사업연도 연속 영업이익이 0보다 작은 회사
| [최근 4년간 영업손익 내역(연결기준)] |
|
(단위: 백만원) |
|
구분 |
2021년 | 2020년 | 2019년 | 2018년 |
|---|---|---|---|---|
| 영업이익 | (101,018) | (61,312) | (48,731) | (29,315) |
(3) 3개 사업연도 연속 영업현금흐름이 0보다 작은 회사,
| [최근 4년간 영업활동현금흐름 내역(연결기준)] |
|
(단위: 백만원) |
|
구분 |
2021년 | 2020년 | 2019년 | 2018년 |
|---|---|---|---|---|
| 영업활동현금흐름 | (54,765) | (56,514) | (48,657) | (29,163) |
(4) 3개 사업연도 연속 이자보상배율이 1 미만인 회사
| [최근 4년간 이자보상배율 내역(연결기준)] |
|
(단위: 백만원) |
|
구분 |
2021년 | 2020년 | 2019년 | 2018년 |
|---|---|---|---|---|
| 이자비용 | 3,627 | 5,262 | 19,514 | 12,769 |
| 영업이익 | (101,018) | (61,312) | (48,731) | (29,315) |
| 이자보상배율 | (27.9) | (11.7) | (2.5) | (2.3) |
당사는 코스닥시장 주권상장법인으로 「주식회사 등의 외부감사에 관한 법률」(이하 "외감법")'에 의거하여 재무제표를 작성하여 회사로부터 독립된 외부의 감사인에 의해 회계감사를 받아야 합니다. 증권선물위원회는 외감법 제11조에 의거하여 증권선물위원회가 지정하는 회계법인을 감사인으로 선임하거나 변경선임할 것을 요구할 수 있습니다. 근거 법령의 내용은 아래와 같습니다.
| 『주식회사 등의 외부감사에 관한 법률』 |
| 제11조(증권선물위원회에 의한 감사인 지정 등) ① 증권선물위원회는 다음 각 호의 어느 하나에 해당하는 회사에 3개 사업연도의 범위에서 증권선물위원회가 지정하는 회계법인을 감사인으로 선임하거나 변경선임할 것을 요구할 수 있다. 1. 감사 또는 감사위원회(감사위원회가 설치되지 아니한 주권상장법인, 대형비상장주식회사 또는 금융회사의 경우는 감사인선임위원회를 말한다. 이하 이 조에서 같다)의 승인을 받아 제10조에 따른 감사인의 선임기간 내에 증권선물위원회에 감사인 지정을 요청한 회사 2. 제10조에 따른 감사인의 선임기간 내에 감사인을 선임하지 아니한 회사 3. 제10조제3항 또는 제4항을 위반하여 감사인을 선임하거나 증권선물위원회가 회사의 감사인 교체 사유가 부당하다고 인정한 회사 4. 증권선물위원회의 감리 결과 제5조에 따른 회계처리기준을 위반하여 재무제표를 작성한 사실이 확인된 회사. 다만, 증권선물위원회가 정하는 경미한 위반이 확인된 회사는 제외한다. 5. 제6조제6항을 위반하여 회사의 재무제표를 감사인이 대신하여 작성하거나, 재무제표 작성과 관련된 회계처리에 대한 자문을 요구하거나 받은 회사 6. 주권상장법인 중 다음 각 목의 어느 하나에 해당하는 회사 가. 3개 사업연도 연속 영업이익이 0보다 작은 회사 나. 3개 사업연도 연속 영업현금흐름이 0보다 작은 회사 다. 3개 사업연도 연속 이자보상배율이 1 미만인 회사 라. 그 밖에 대통령령으로 정하는 재무기준에 해당하는 회사 7. 주권상장법인 중 대통령령으로 정하는 바에 따라 증권선물위원회가 공정한 감사가 필요하다고 인정하여 지정하는 회사 8. 「기업구조조정 촉진법」 제2조제5호에 따른 주채권은행 또는 대통령령으로 정하는 주주가 대통령령으로 정하는 방법에 따라 증권선물위원회에 감사인 지정을 요청하는 경우의 해당 회사 9. 제13조제1항 또는 제2항을 위반하여 감사계약의 해지 또는 감사인의 해임을 하지 아니하거나 새로운 감사인을 선임하지 아니한 회사 10. 감사인의 감사시간이 제16조의2제1항에서 정하는 표준 감사시간보다 현저히 낮은 수준이라고 증권선물위원회가 인정한 회사 11. 직전 사업연도를 포함하여 과거 3년간 최대주주의 변경이 2회 이상 발생하거나 대표이사의 교체가 3회 이상 발생한 주권상장법인 12. 그 밖에 공정한 감사가 특히 필요하다고 인정되어 대통령령으로 정하는 회사 ② 증권선물위원회는 다음 각 호의 어느 하나에 해당하는 회사가 연속하는 6개 사업연도에 대하여 제10조제1항에 따라 감사인을 선임한 경우에는 증권선물위원회가 대통령령이 정하는 기준과 절차에 따라 지정하는 회계법인을 감사인으로 선임하거나 변경선임할 것을 요구할 수 있다. 1. 주권상장법인. 다만, 대통령령으로 정하는 주권상장법인은 제외한다. 2. 제1호에 해당하지 아니하는 회사 가운데 자산총액이 대통령령으로 정하는 금액 이상이고 대주주 및 그 대주주와 대통령령으로 정하는 특수관계에 있는 자가 합하여 발행주식총수(의결권이 없는 주식은 제외한다. 이하 같다)의 100분의 50 이상을 소유하고 있는 회사로서 대주주 또는 그 대주주와 특수관계에 있는 자가 해당 회사의 대표이사인 회사 (중 략) |
| 자료: 국가법령정보센터 |
외감법 제11조 제1항 제7호의 "주권상장법인 중 대통령령으로 정하는 바에 따라 증권선물위원회가 공정한 감사가 필요하다고 인정하여 지정하는 회사"는 아래의 외감법 시행령에 기재되어 있습니다.
| 『주식회사 등의 외부감사에 관한 법률 시행령』 |
| 제14조(증권선물위원회의 감사인 지정을 받는 회사) ① 삭제 ② 삭제 ③ 증권선물위원회는 법 제11조제1항제7호에 따라 다음 각 호의 어느 하나에 해당하는 회사 중에서 공정한 감사가 필요하다고 인정되는 회사를 지정한다. 1. 「자본시장과 금융투자업에 관한 법률」 제390조에 따른 상장규정(이하 "상장규정"이라 한다)에 따라 관리종목으로 지정된 회사. 다만, 다음 각 목의 어느 하나에 해당하여 관리종목으로 지정된 경우는 제외한다. 가. 주주 수 또는 상장주식 수 등 주식분산 기준을 충족하지 못한 경우 나. 주식거래량 기준을 충족하지 못한 경우 다. 시가총액 기준을 충족하지 못한 경우 2. 대통령령 제24697호 자본시장과 금융투자업에 관한 법률 시행령 일부개정령 부칙 제8조에 따른 코스닥시장(이하 "코스닥시장"이라 한다)에 대하여 별도로 정하는 상장규정에 따라 투자주의 환기종목으로 지정된 법인. 다만, 감사인이 회사가 법 제8조제6항에 따라 같은 조에서 정한 사항을 준수했는지 여부 및 같은 조 제4항에 따른 내부회계관리제도의 운영실태에 관한 보고 내용을 검토하거나 감사한 결과 다음 각 목의 어느 하나에 해당하여 투자주의 환기종목으로 지정된 경우는 제외한다. 가. 중요한 취약점이 발견된 경우 나. 감사인의 검토 또는 감사 범위에 제한이 있는 경우 다. 감사인의 검토 의견 또는 감사 의견이 표명되지 아니한 경우 ④ 법 제11조제1항제8호에서 "대통령령으로 정하는 주주"란 투자대상회사의 장기적인 가치 향상과 지속적인 성장을 추구함으로써 고객과 수익자의 중장기적인 이익을 도모할 책임(이하 "수탁자 책임"이라 한다)을 효과적으로 이행할 기관투자자인 주주로서 증권선물위원회가 인정하는 자를 말한다. 이 경우 증권선물위원회는 금융위원회가 정하는 바에 따라 다음 각 호의 사항을 고려하여야 한다. 1. 기관투자자가 수탁자 책임을 효과적으로 이행하는 데 필요한 핵심 원칙에 따라 주주활동을 수행하였는지 여부 2. 투자대상회사의 지분을 보유한 기간 3. 투자대상회사 지분율 4. 그 밖에 금융위원회가 정하는 사항 ⑤ 「기업구조조정 촉진법」 제2조제5호에 따른 주채권은행 및 제4항에 따른 기관투자자인 주주가 법 제11조제1항제8호에 따라 증권선물위원회에 감사인 지정을 요청하려면 금융위원회가 정하는 바에 따라 감사인 지정을 신청하는 서류를 작성하여 제출하여야 한다. 이 경우 제4항에 따른 기관투자자인 주주는 같은 항 각 호의 사항을 증명할 수 있는 자료를 첨부하여야 한다. ⑥ 법 제11조제1항제12호에서 "대통령령으로 정하는 회사"란 다음 각 호의 어느 하나에 해당하는 회사를 말한다. 1. 해당 사업연도 또는 다음 사업연도 중에 주권상장법인이 되려는 회사. 다만, 다음 각 목의 회사는 제외한다. 가. 코스닥시장에 상장된 주권을 발행한 법인(이하 "코스닥시장상장법인"이라 한다)이 되려는 「자본시장과 금융투자업에 관한 법률 시행령」 제176조의9제1항에 따른 유가증권시장에 상장된 주권을 발행한 법인(이하 "유가증권시장상장법인"이라 한다) 나. 유가증권시장상장법인이 되려는 코스닥시장상장법인 다. 코넥스시장에 주권을 상장하려는 법인 라. 주권상장법인이 되려는 기업인수목적회사 2. 제21조제1항제3호부터 제5호까지 및 같은 조 제3항제1호에 해당하여 감사인이 감사업무에 대한 계약을 해지한 회사 3. 다음 각 목의 어느 하나를 위반한 회사. 다만, 증권선물위원회가 정하는 경미한 위반 사항으로 확인된 경우는 제외한다. 가. 법 제6조제2항부터 제5항까지의 규정에 따른 재무제표 제출 및 공시 나. 법 제8조제1항부터 제5항까지 및 이 영 제9조에 따른 내부회계관리제도의 운영 다. 법 제9조제1항에 따른 감사인의 자격제한 라. 법 제10조제5항 및 제6항에 따른 감사인 선임 시 준수 사항 마. 법 제12조에 따른 감사인 선임 등의 보고ㆍ통지ㆍ공고 바. 법 제13조에 따른 감사인 해임 및 재선임 사. 법 제14조에 따른 의견진술권 아. 법 제21조에 따른 감사인의 권한 자. 법 제22조제3항부터 제6항까지의 규정에 따른 부정행위 등의 조사 및 시정요구 등 차. 법 제28조제2항 및 제3항에 따른 부정행위 신고자의 보호 4. 다른 법률에서 정하는 바에 따라 증권선물위원회에 감사인 지정이 의뢰된 회사 5. 금융위원회가 정하는 금액 이상의 횡령 또는 배임을 하였다는 이유로 주권상장법인이 소속 임직원(퇴임하거나 퇴직한 임직원을 포함한다. 이하 이 호에서 같다)을 고소하거나, 그 임직원에 대하여 공소가 제기된 회사 6. 회사가 제17조제1항을 위반한 경우(제17조제1항에 따라 증권선물위원회에 제출해야하는 자료에 거짓으로 기재되거나 표시된 내용이 있는 경우 또는 기재하거나 표시하여야 할 사항을 빠뜨린 경우를 포함한다) |
| 자료: 국가법령정보센터 |
이처럼 지정감사로 인해 추후 당사에 대한 감사 강도가 강화될 수 있으며, 이 경우 당사의 감사의견에 영향을 끼칠 수 있습니다. 투자자께서는 당사가 지정감사 대상으로 선정되었음에 유의하시기 바랍니다.
3. 기타위험
|
가. 최대주주 및 특수관계인의 청약 참여 관련 사항 |
금번 유상증자에 최대주주인 진양곤 회장은 771,151주(유상증자 신주 수의 8.06%), 에이치엘비생명과학㈜는 125,308주(유상증자 신주 수의 1.31%), 에이치엘비셀㈜은 74,170주(유상증자 신주 수의 0.78%)를 배정 받았습니다.
금번 유상증자에 있어 에이치엘비생명과학㈜와 에이치엘비셀㈜는 배정물량에 전량 참여할 예정이며, 최대주주인 진양곤 회장과 이현아, 이현수, 진유림, 진인혜는 배정받은 증서를 매각한 분만큼 청약에 참여할 예정이며, 기타특수관계인의 참여여부는 미확정인 상태입니다. 다만, 상기 최대주주의 유상증자 청약 참여 여부 및 규모는 최종 발행가액 및 소요자금, 개인의 자금 사정 등으로 인하여 변경될 가능성이 있습니다. 최대주주의 실제 청약 참여 규모에 따라 유상증자 이후 최대주주의 지분율은 하락할 수 있고, 최대주주 및 특수관계인이 전량 청약에 참여하지 않을 경우를 가정하면 최대주주 및 특수관계인의 지분율 합계는 9.60%까지 하락할 수 있습니다.
| [최대주주 및 특수관계인 청약 가정 시 지분율 변동 시뮬레이션] |
| (단위 : 주, %) |
| 주주명 | 2022-08-12 기준 | 배정주식수 | 배정주식수 /신주발행주식수 |
청약(예정) 주식수 |
유상증자 후 | ||
|---|---|---|---|---|---|---|---|
| 보유주식수 | 지분율 | 보유주식수 | 지분율(%) | ||||
| 진양곤 | 8,610,902 | 8.05% | 771,151 | 8.06% | 100,250 | 8,711,152 | 7.48% |
| 에이치엘비생명과학㈜ | 1,399,230 | 1.31% | 125,308 | 1.31% | 125,308 | 1,524,538 | 1.31% |
| 에이치엘비셀㈜ | 828,214 | 0.77% | 74,170 | 0.78% | 74,170 | 902,384 | 0.77% |
| 이현아 | 230,772 | 0.22% | 20,666 | 0.22% | 2,687 | 233,459 | 0.20% |
| 이현수 | 89,756 | 0.08% | 8,038 | 0.08% | 1,045 | 90,801 | 0.08% |
| 진유림 | 8,230 | 0.01% | 737 | 0.01% | 57 | 8,287 | 0.01% |
| 진인혜 | 8,180 | 0.01% | 732 | 0.01% | 57 | 8,237 | 0.01% |
| 김용웅 | 4,864 | 0.00% | 435 | 0.00% | - | 4,864 | 0.00% |
| 도순기 | 4,864 | 0.00% | 435 | 0.00% | - | 4,864 | 0.00% |
| 합계 | 11,185,012 | 10.46% | 1,001,672 | - | 303,574 | 11,488,586 | 9.86% |
| (주1) 최대주주 및 특수관계인의 참여 주식을 제외한 잔여 신주인수권은 전액 기타주주에 매각됨을 가정하여 산정하였습니다. (주2) 진양곤 회장과 이현아, 이현수, 진유림, 진인혜는 배정수량의 13% 참여를 가정했으며, 참여 비율은 증서매각 가격에 따라 변동가능합니다. (주2) 지분율은 의결권이 있는 보통주식(총 106,903,481주)을 기준으로 산정되었습니다. (08-11 전환청구된 20,736주 반영) |
| [최대주주 및 특수관계인 청약 미참여 가정 시 지분율 변동 시뮬레이션] |
| (단위 : 주, %) |
| 주주명 | 2022-08-12 기준 | 배정주식수 | 배정주식수 /신주발행주식수 |
청약(예정) 주식수 |
유상증자 후 | ||
|---|---|---|---|---|---|---|---|
| 보유주식수 | 지분율 | 보유주식수 | 지분율(%) | ||||
| 진양곤 | 8,610,902 | 8.05% | 771,151 | 8.06% | - | 8,610,902 | 7.39% |
| 에이치엘비생명과학㈜ | 1,399,230 | 1.31% | 125,308 | 1.31% | - | 1,399,230 | 1.20% |
| 에이치엘비셀㈜ | 828,214 | 0.77% | 74,170 | 0.78% | - | 828,214 | 0.71% |
| 이현아 | 230,772 | 0.22% | 20,666 | 0.22% | - | 230,772 | 0.20% |
| 이현수 | 89,756 | 0.08% | 8,038 | 0.08% | - | 89,756 | 0.08% |
| 진유림 | 8,230 | 0.01% | 737 | 0.01% | - | 8,230 | 0.01% |
| 진인혜 | 8,180 | 0.01% | 732 | 0.01% | - | 8,180 | 0.01% |
| 김용웅 | 4,864 | 0.00% | 435 | 0.00% | - | 4,864 | 0.00% |
| 도순기 | 4,864 | 0.00% | 435 | 0.00% | - | 4,864 | 0.00% |
| 합계 | 11,185,012 | 10.46% | 1,001,672 | - | - | 11,185,012 | 9.60% |
| (주1) 상기 표는 최대주주 및 특수관계인의 전량 미참여를 가정하여 작성되었습니다. |
| (주2) 최대주주 및 특수관계인의 참여 주식을 제외한 잔여 신주인수권은 전액 기타주주에 매각됨을 가정하여 산정하였습니다. (주3) 지분율은 의결권이 있는 보통주식(총 106,903,481주)을 기준으로 산정되었습니다. |
상기 최대주주 등의 지분율 변화 시뮬레이션은 증권신고서 제출일 현재 예정발행가액 34,050원을 기준으로 산출하였으며, 예정발행가액을 기준으로 계산하였기 때문에, 향후 최종 발행가액이 확정됨에 따라서 최대주주 지분율 희석 정도가 변동될 수 있습니다. 최종발행가액이 하락할 경우, 최대주주의 지분율 희석은 제한적일 것으로 판단되나, 최종발행가액이 상승할 경우, 최대주주의 청약 및 납입 부담이 증가하여 참여 수량이 축소할 가능성이 있으며, 이 경우 지분율 희석 효과는 커질 것으로 판단됩니다. 이처럼, 향후 발행가액 최종 결정에 따라 최대주주의 지분율 희석 정도가 변동 가능한점 투자자께서는 유의하시기 바랍니다.
한편, 최대주주 등이 미참여하는 물량에 대한 신주인수권증서는 장외 및 상장시장을 통해 매도함으로써 다른 증서 인수인이 구주주 청약에 참여할 수 있도록 할 예정입니다. 신주인수권증서를 매수하는 투자자는 단기적으로 할인율에서 발생하는 차익을 실현하고자 신주가 상장되는 즉시 보유 주식을 장내매도할 수 있으며, 이에 따라 주가가 하락할 수 있으니 이에 유의하시기 바랍니다.
[유상증자 이후 전환사채(신주인수권부사채)의 보통주 전환(행사)]
한편, 당사가 발행한 전환사채 및 신주인수권부사채의 주식 전환(행사)시 최대주주 및 특수관계인의 지분율이 추가적으로 하락할 가능성이 있습니다. 2022년 09월 23일 증권신고서 제출일 기준 과거 발행된 미상환 주식관련사채의 발행 개요는 다음과 같습니다.
| [미상환 전환사채 및 신주인수권부사채 세부내역] |
| (기준일: 2022년 09월 23일) |
| 종 류 | 발행일 | 만기일 | 전자등록 총액 |
표면 이자율 |
만기 이자율 |
전환(행사)청구 가능기간 |
조기상환 청구권(Put option) |
전환(행사)가액 | 잔액 | 전환(행사)가능 주식수 |
|---|---|---|---|---|---|---|---|---|---|---|
| 33회차 사모 전환사채 |
19.12.18 |
22.12.18 |
40,000 |
0.0% | 1.0% | 20.12.18~22.11.18 |
21.08.18~22.11.18 (매 3개월) |
33,757 |
1,400 | 41,472 |
| 34회차 사모 비분리형 신주인수권부사채 |
21.10.20 |
26.10.20 |
57,000 |
0.0% | 1.0% | 22.10.20~26.09.20 |
23.10.20~26.07.20 (매 3개월) |
35,884 |
57,000 | 1,588,451 |
| 35회차 사모 비분리형 신주인수권부사채 |
22.03.30 |
25.03.30 |
25,200 |
0.0% | 2.0% | 23.03.30~25.02.30 |
23.03.30~24.12.30 (매 3개월) |
30,811 |
21,000 | 681,574 |
| 36회차 사모 전환사채 |
22.06.02 |
25.06.02 |
23,000 |
1.0% | 3.0% | 23.06.02~25.05.02 |
23.12.02~25.03.02 (매 3개월) |
48,605 |
23,000 | 473,202 |
| 37회차 사모 비분리형 신주인수권부사채 |
22.06.02 |
25.06.02 |
17,000 |
1.0% | 3.0% | 23.06.02~25.05.02 |
23.12.02~25.03.02 (매 3개월) |
48,605 |
17,000 | 349,758 |
| 합 계 | 119,400 | 3,134,457 | ||||||||
이렇듯 당사가 발행한 미상환 상태로 남아있는 전환사채가 주식으로 전환 될 경우 최대주주 및 특수관계인의 지분율이 추가로 하락할 가능성이 있습니다. 상기 전환사채의 전환권 행사로 발행될 수 있는 신주의 총수는 3,134,457주로 2022년 09월 23일 현재 당사의 보통주 발행주식 총수의 2.9%에 해당합니다.
최대주주 및 특수관계인의 전량 미청약을 가정할 시, 본 유상증자 이후 상기 전환사채가 전량 주식으로 전환될 경우 최대주주 진양곤의 지분율은 기존 8.05%에서 7.20%까지, 최대주주 및 특수관계인의 지분율 합계는 기존 10.46%에서 9.35%까지 변동될 수 있습니다. 향후 주식시장 및 시장상황에 따라 전환사채의 주식 전환으로 인한 최대주주 및 특수관계인의 지분변화 가능성을 배제하기는 어렵습니다. 투자자께서는 이 점에 유의하여 투자판단을 하시기 바랍니다.
상기 기술한 바와 같이 최대주주 및 특수관계인의 낮은 지분율은 적대적 M&A등의 위험성을 내포할 수 있으며, 이러한 점은 경영진 변동의 위험성으로 이어져 안정적인 경영활동이 어려울 수 있습니다. 또한, 장기적으로 향후 추가적인 유상증자, 주식관련 사채의 발행, 우선주의 전환 등으로 최대주주 및 특수관계인 등의 지분율이 재차 희석될 가능성은 존재하며 이에 따른 지속적인 모니터링이 필요한점 투자자 여러분께서는 유의하여주시기 바랍니다.
| 나. 환금 제한 및 원금 손실 가능성 금번 유상증자 청약에 참여하여 신주를 배정받을 경우 신주의 추가상장일까지 환금성에 제약이 있으며, 청약 후 추가상장일 사이에 주가가 하락할 경우 원금에 대한 손해가 발생할 가능성이 있습니다. 투자자분들은 투자시 이점 유의하시기 바랍니다. |
당사는 코스닥 시장 상장법인으로서 이번 유상증자로 발행되는 신주는 코스닥 시장에 상장되어 거래될 예정이므로 유동성과 관계된 심각한 환금성 위험은 존재하지 않습니다. 그러나 유상증자 청약에 참여하여 신주를 배정받을 경우, 신주가 상장되어 매매가 가능할 때까지 납입주금에 대한 유동성의 제약이 있습니다.
본 유상증자의 자세한 일정은 본 신고서의 '제1부 모집 또는 매출에 관한 사항 - I. 모집 또는 매출에 관한 일반사항' 중 '1. 공모의 개요'를 참고하시기 바랍니다.
또한 신주가 코스닥 시장에 추가 상장될 때까지 당사의 주가가 유상증자로 발행되는 신주의 발행가액 수준으로 유지되지 않을 수 있으며, 당사의 내적인 요인 또는 시장전체의 환경 변화 등에 의해 주가가 급락할 경우, 투자원금에 대한 손실이 발생할 수 있습니다.
당사의 금번 발행되는 주식에 대해서는 전량 보호예수되지 않으므로 상장 후 즉시 물량 출회가 가능하여 주가 하락에 따른 환금성 위험 및 주가희석화에 노출될 수 있으니, 이점 투자에 유의하시기 바랍니다.
|
다. 주가 희석화 위험 |
당사의 금번 유상증자로 인하여 기발행주식 총수 106,910,669주의 8.94%에 해당하는 9,562,408주가 추가로 상장됩니다.
| [유상증자 모집예정 내역] |
| 구 분 | 내 용 |
|---|---|
| 모집예정 주식 종류 | 기명식보통주 |
| 모집예정주식수 | 9,562,408주 |
| 현재 발행주식총수 | 106,910,669주 |
| 증자비율 | 8.94% |
| 할인율 | 25% |
금번 유상증자에 따른 모집가액은 (舊)「유가증권의 발행 및 공시등에 대한 규정」 제57조에 의해 산출됩니다. 그러나 주식시장의 특성상 향후 주가에 대한 변동성이 있는 관계로 증자에 따른 모집가격 산정시 결정된 1주당 모집가액보다 향후 추가 상장 후 거래 시점의 주가가 낮아져 투자자에게 금전적 손실을 끼칠 가능성이 있습니다.
당사는 본 유상증자의 원활한 신주인수권증서 매매를 위하여 5거래일간 신주인수권증서를 상장하여 신주인수권증서를 통한 구주주 청약률을 제고할 계획입니다. 하지만 신주인수권증서의 원활한 매매 및 청약 참여를 위한 노력에도 불구하고 신주인수권증서를 통한 청약이 부진하여 대규모 실권이 발생할 경우, 투자심리에 악영향을 끼쳐 일반공모 청약에 부정적 영향을 끼칠 수도 있으며 향후 주가하락 가능성도 배제할수 없습니다.
금번 증자로 인해 추가 발행되는 신주는 보호예수되지 않으므로 일시적인 물량출회에 따른 주가하락의 가능성이 있습니다. 금번 유상증자에 따른 모집예정주식 9,562,408주가 향후 코스닥 시장에 추가 상장될 경우 유통주식수의 증가로 인하여 주가 희석화 위험이 발생할 수 있습니다. 또한 신주인수권증서를 매수하는 투자자는 할인율에 의해 발생하는 차익을 단기적으로 실현하기 위해 신주의 매매가 가능한 시점에서 즉시 장내에서 매각할 가능성이 높습니다. 이에 따라 주가가 하락할 수 있으니 투자자분들은 유의하시기 바랍니다.
| 라. 주가하락에 따른 발행금액 감소 위험 주식시장의 급격한 상황 악화로 인하여 회사의 금번 유상증자 발행가액이 하락할 경우 당사가 계획했던 자금운용계획 등에 차질이 빚어질 수 있으며, 이러할 경우 당사의 재무적 안정성은 부정적인 영향을 받을 수 있습니다. |
금번 유상증자의 확정발행가액은 1차 발행가액과 2차 발행가액 중 낮은 가액으로 결정됩니다. 다만 「자본시장과 금융투자업에 관한 법률」 제165조의6 및 「증권의 발행 및 공시 등에 관한 규정」 제5-15조의2에 의거하여 1차 발행가액과 2차 발행가액중 낮은가액이 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격보다 낮은 경우 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격을 확정발행가액으로 합니다. (단, 발행가액이 액면가보다 낮을 경우 액면가를 발행가액으로 합니다.)
일반공모 후 미청약분에 대해서는 그 전부를 공동대표주관회사인 케이비증권㈜, 한국투자증권㈜ 및 인수회사인 유진투자증권㈜가 자기 계산으로 인수하므로 청약 미달에 따른 위험은 없으나, 주가 하락으로 발행가액이 크게 하락할 경우 회사가 계획했던 자금운용계획에 차질이 빚어질 수 있습니다. 이러할 경우 당사의 재무적 안정성은부정적인 영향을 받을 수 있으니 투자자 여러분께서는 이 점 유의하시기 바랍니다.
| 마. 금융감독기관의 규제 강화에 따른 위험 최근 금융감독기관 등의 관리감독기준이 엄격해지고 있는 상황으로 관련 규정을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다. 향후 감독기관으로부터 당사가 현재 파악하지 못한 제재가 부과될 경우 주가하락 및유동성(환금성) 제약 등으로 인해 투자금에 막대한 손실이 발생할 수 있으니 투자자들께서는 관련 규정을 충분히 검토하신 후 투자에 임해주시기 바랍니다. |
최근 금융감독기관 등의 관리감독기준이 엄격해지고 있는 상황으로 관련 규정을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다.
향후 감독기관으로부터 당사가 현재 파악하지 못한 제재가 부과될 경우 주가하락 및유동성(환금성)제약 등으로 인해 투자금에 막대한 손실이 발생할 수 있으니 투자자들께서는 관련 규정을 충분히 검토하신 후 투자에 임해주시기 바랍니다.
특히, 「코스닥시장 상장규정」 제28조(관리종목), 「코스닥시장 상장규정」 제38조(상장의 폐지) 및 「코스닥시장 상장규정」 제38조의2(실질심사위원회의 심사 등)"에 유의하시기 바랍니다. 자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융법규서비스(http://fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
| 바. 경영환경변화 등에 따른 위험 대내외적 경영환경 변화에 따라 당사 실적의 급변동이 있을 경우 투자원금에 대한 손실이 발생할 수 있으므로, 상기 투자위험요소 및 본 증권신고서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 투자자 여러분이 독자적으로 결정해야 함을 유의하시기 바랍니다. |
당사의 주가는 국내외 주식시장 환경 변화와 같은 외부적 요인에 영향을 받아 변동할 가능성이 존재하며, 당사의 외부적인 경영환경 변화에 따라 당사 실적이 악화될 가능성이 높아질 경우 당사의 주가에 부정적인 영향을 미칠 수 있습니다.
본 건 공모 주식을 청약하고자 하는 투자자들은 투자결정을 하기 전에 본 증권신고서의 다른 기재 부분 뿐만 아니라 상기 투자위험요소를 주의 깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 하며, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 상기 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자는 상기 투자위험요소 및 본 신고서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 자신의 독자적인 판단에 의해서 투자하셔야 합니다.
만일 상기 투자위험요소에 기재한 내용 중 부정적인 요소가 현실화될 경우 당사 및 종속회사의 사업, 재무상태, 기타 운영결과에 중대한 부정적 영향을 미칠 수 있으며, 이에 따라 투자자가 금번 공모 과정에서 취득하게 되는 당사 주식의 시장가격이 하락하여 투자금액에 손실이 발생할 수도 있음을 유의하시기 바랍니다.
| 사. 증권신고서 정정에 따른 일정 변경 가능성 본 증권신고서는 공시심사 과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있습니다. |
「자본시장과 금융투자업에 관한 법률」제120조 3항에 의거하여 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 투자자에게 귀속됩니다.
금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서(분기 및 반기보고서 포함) 및 감사보고서 등 기타 정기 공시사항과 수시 공시사항 등이 전자공시되어 있사오니 투자 의사를 결정하시는 데 참조하시기 바랍니다.
본 증권신고서는 공시 심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행과정에서 일정이 변경될 수도 있으므로 투자자들께서는 투자시 이러한 점을 감안하시기 바랍니다.
| 아. 집단 소송이 제기될 위험 당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있음을 유의하시기 바랍니다. |
'증권관련 집단소송법' 제12조(소송허가 요건)에 따라 50명 이상의 개인이 발행주식총수의 0.01% 이상 보유할 경우 한 명 이상의 대표 당사자가 상기 50인 이상의 당사자들을 대리하여 회사가 발행한 증권의 거래과정에서 발생한 피해에 대하여 소송을 제기할 수 있습니다.
증권신고서 및 투자설명서에서 기재된 잘못된 내용, 잘못된 사업보고서의 공시, 내부자거래에 의한 손해배상청구 및 회계부정으로 인한 손해배상 청구 등이 주요한 소송사유에 포함됩니다. 당사는 향후 이와 같은 집단소송의대상이 되지 않는다고 확신할 수 없으며, 만약 당사에 대하여 집단소송이 제기될 경우 상당한 소송비용이 발생할 수 있음을 유의하시기 바랍니다.
| 자. 유상증자에 따른 주식가치 하락 및 기재정보 의존에 따른 투자위험 금번 유상증자를 통해 취득한 당사의 주식가치가 하락할 수 있으며, 상기 투자위험요소 및 기타 기재된 정보에만 의존하여, 투자판단을 해서는 안되며 투자자 여러분의 독자적인 판단에 의해야 함을 유의하여 주시기 바랍니다. |
금번 유상증자 실시로 당사의 주식가치가 향후 하락할 수 있으므로 투자자 여러분께서는 이 점 유의하시기 바랍니다.
이 증권신고서의 효력발생은 정부가 증권신고서의 기재사항이 진실 또는 정확하다는것을 인정하거나 이 유가증권의 가치를 보증 또는 승인한 것이 아니며, 기재사항은 청약일 이전에 변경될 수 있으며, 본 건 공모주식을 청약하고자 하는 투자자들은 투자결정을 하기 전에 본 증권신고서의 다른 기재 부분 뿐만 아니라 상기 투자위험요소를 주의 깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 합니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 상기 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 자신의 독자적인 판단에 의해야 합니다.
당사는 상기에 기술된 투자위험요소 외에도 전반적으로 불안정한 경제상황 등에 의하여 직접적으로 또는 간접적으로 영향을 받을 수 있습니다. 당사의 재무제표는 당사의 재무상태에 영향을 미칠 수 있는 경제상황에 대한 경영자의 현재까지의 평가를 반영하고 있으나 그 실제결과는 현재시점에서의 평가와는 상당히 다를 수 있는 만큼, 투자자 여러분께서는 이 점 유의하여 투자에 임하시기 바랍니다.
만일 상기 투자위험요소가 실제로 발생하는 경우 당사의 사업, 재무상태, 기타 운영결과에 부정적 영향을 미칠 수 있으며, 이에 따라 투자자가 금번 공모 과정에서 취득하게 되는 당사 주식의 시장가격이 하락하여 투자금액의 일부 또는 전부를 잃게 될 수도 있습니다. 또한 금번 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 대내외적으로 여러가지 요소들의 영향에 따라 애초에 예측했던 것과 다를 수 있다는 점에 유의해야 합니다.
| 차. 유상증자 철회에 따른 위험 유상증자 진행 중에 모집 절차의 진행에 중대한 영향을 미칠만한 사유가 발생하여 당사 혹은 공동대표주관회사 및 인수회사의 판단으로 유상증자가 철회될 수 있습니다. 유상증자 납입전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회시점에 따라 권리락에 따른 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있음을 투자자께서는 유의하시기 바랍니다. 또한, 당사가 계획한 자금사용목적의 자금이 조달되지 않기 때문에 당사는 단기간 유동성 위험에 직면하여 매우 위험한 상황이 발생할 수 있으니 이점 유의하시기 바랍니다. |
금번 주주배정후 실권주 일반공모 유상증자는 공동대표주관회사 및 인수회사의 잔액인수 방식으로 진행됩니다. 유상증자 진행 중에 모집 절차의 진행에 중대한 영향을 미칠만한 사유가 발생하여 당사 혹은 공동대표주관회사의 판단으로 유상증자가 철회될 수 있습니다.
유상증자 납입전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회시점에 따라 권리락에 따른 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있음을 투자자께서는 유의하시기 바랍니다.
또한, 당사가 계획한 자금사용목적의 자금이 조달되지 않기 때문에 당사는 단기간 유동성 위험에 직면하고, 장기적으로 당사의 성장을 위해 수립한 경영계획에 차질이 생길 수 있습니다. 유상증자가 철회될 경우 매우 위험한 상황이 발생할 수 있으니 이점 유의하시기 바랍니다.
| 카. 차입공매도 유상증자 참여 제한 관련 위험 「자본시장과 금융투자업에 관한 법률 시행령」일부 개정령에 따라, 주권상장법인이 유상증자 계획을 공시한 이후 발행가격 산정을 위한 대상 거래기간의 마지막 날(발행가격 산정 기산일)까지, 해당 기업의 주식을 공매도 한 자는 증자 참여를 제한하되, 예외적인 경우에만 증자 참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 투자자께서는 이 점 유의하시기 바랍니다. |
「자본시장과 금융투자업에 관한 법률 시행령」일부 개정령에 따르면, 주권상장법인이 유상증자 계획을 공시한 이후 해당 기업의 주식을 공매도 한 자는 증자 참여를 제한하되, 예외적인 경우 증자 참여를 허용하고 있습니다. (「자본시장과 금융투자업에관한 법률」제180조의4). 이와 관련 유상증자 참여가 제한되는 공매도 시점과, 증자참여가 허용되는 예외사유를 시행령에서 정하도록 위임하고 있습니다.
해당 시행령에 따르면, 유상증자 계획이 공시된 다음 날부터, 발행가격 산정을 위한 대상 거래기간의 마지막 날(발행가격 산정 기산일)까지 공매도한 경우 증자 참여가 제한됩니다. (「자본시장과 금융투자업에 관한 법률 시행령」208조의4제1항)
다만, 다음의 경우 공매도를 통해 발행가격에 부당한 영향을 미쳤다고 보지 않아 증자참여가 허용됩니다. (「자본시장과 금융투자업에 관한 법률 시행령」제208조의4제2항)
ⅰ) 마지막 공매도 이후 발행가격 산정 기산일까지 공매도 주문 수량 이상을 증권시장 정규거래시간에 매수(체결일 기준)
ⅱ) 금융위원회가 정하는 기준을 충족한 독립된 거래단위를 운영하는 법인 내에서 공매도를 하지 않은 거래단위가 증자 참여
ⅲ) 시장조성 또는 유동성공급을 위한 거래 과정에서 공매도
상기 공매도 제도 개선 관련 「자본시장과 금융투자업에 관한 법률 시행령」 개정안에 따라, 당사의 주식을 해당 기간 동안 공매도하는 투자자께서는 금번 유상증자 참여가 제한될 수 있음을 유의하시기 바랍니다. 해당 법령과 관련된 자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융법규서비스(http://fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
| 타. 최대주주 보유주식의 담보권 설정 관련 위험 2022년 09월 22일 현재 당사의 최대주주인 진양곤 대표이사는 당사의 보통주 발행주식총수 106,910,669주의 약 8.05%에 해당하는 8,610,902주의 보통주를 보유하고 있으며,최대주주가 보유한 8,610,902주 중 약 3.83%에 해당하는 329,840주는 최대주주가 차입한 대출금에 대하여 담보로 제공되어 있습니다. 동 물량은 당사 발행 보통주식총수의 약 0.31%에 해당합니다. 향후 최대주주가 체결한 주식담보대출약정에 의한 대출금을 기한 내 상환하지 못하거나, 통제할 수 없는 시장의 변수로 인하여 당사의 주가가 급락하게 될 경우, 담보로 제공된 물량에 대하여 그 담보권이 실행되거나 반대매매 물량이 출회되어 주가의 추가적 하락을 야기할 가능성을 배제할 수 없습니다. 투자자께서는 당사의 주식 중 대출금에 대한 담보로 제공되어 있는 물량이 존재함에 유의하시고, 해당 위험성을 충분히 인지하신 후 투자판단에 임하시기 바랍니다. |
2022년 09월 22일 기준 당사의 최대주주인 진양곤 대표이사는 당사의 보통주 발행주식총수 106,910,669주의 약 8.05%에 해당하는 8,610,902주의 보통주를 보유하고 있으며,최대주주가 보유한 8,610,902주 중 약 3.83%에 해당하는329,840주는 최대주주가 차입한 대출금에 대하여 담보로 제공되어 있습니다.
| [최대주주 보유주식의 담보제공 내역] |
| (기준일: 2022년 09월 22일) |
| 성명 (명칭) |
주식등의 종류 |
대상 주식등의 수량 |
계약 상대방 |
계약의 종류 |
계약체결 (변경)일 |
계약기간 | 비율 | 대출금액 | 이자율 | 담보유지비율(%) | 비고 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 진양곤 | 의결권있는 주식 | 300,000 | 광주은행 | 담보대출계약 | 2021.11.25 | 2021.11.25 ~2022.11.28 |
0.28 | 3,500,000,000 | 2.76 | 170 | 주식담보대출 |
| 진양곤 | 의결권있는 주식 | 29,840 | 한국투자증권 | 담보대출계약 | 2022.08.31 | 2022.08.31 ~2022.11.30 |
0.03 | 3,015,578,300 | 4.50 | 150 | 주식담보대출 (연장) |
| 합계(주식등의 수) | 329,840 | 합계(비율) | 0.31 | 6,515,578,300 | - | - | - | ||||
| (자료: 금융감독원 전자공시시스템 <주식등의 대량보유상황보고서>(2020.04.27) |
최대주주가 차입한 대출금에 대하여 담보로 제공되어 있는 329,840주는 당사 발행 보통주식총수의 약 0.31%에 해당합니다. 향후 최대주주가 체결한 주식담보대출약정에 의한 대출금을 기한 내 상환하지 못하거나, 통제할 수 없는 시장의 변수로 인하여 당사의 주가가 급락하게 될 경우, 담보로 제공된 물량에 대하여 그 담보권이 실행되거나 반대매매 물량이 출회되어 주가의 추가적 하락을 야기할 가능성을 배제할 수 없습니다. 투자자께서는 당사의 주식 중 대출금에 대한 담보로 제공되어 있는 물량이 존재함에 유의하시고, 해당 위험성을 충분히 인지하신 후 투자판단에 임하시기 바랍니다.
| ※ 상기 제반사항을 고려하시어 투자자 제위의 현명한 판단을 바랍니다. 투자자는 본건 공모주식에의 투자 여부를 결정함에 있어서 필요한 경우 스스로 별도의 독립된 자문을 받아야 하며, 이에 따른 투자의 결과에 대하여는 투자자가 책임을 부담합니다. |
IV. 인수인의 의견(분석기관의 평가의견)
| 본 장은 「자본시장과 금융투자업에 관한 법률」 제119조 및 제125조, 금융감독원의 '금융투자회사의 기업실사 모범규준'을 참조하여 작성된 공동대표주관회사인 케이비증권㈜ 및 한국투자증권㈜의 내부규정에 따라 본건 공모 지분증권 인수인이 당해 공모 지분증권에 대한 의견을 기재하고 있는 부분입니다. 따라서 본 장의 작성 주체는 공동대표주관회사인 케이비증권㈜ 및 한국투자증권㈜입니다. 발행회사인 에이치엘비㈜는 "동사"로 기재하였습니다. 본 장에 기재된 분석의견 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 여러가지 요소들의 영향에 따라 예측했던 것과 다를 수 있다는 점을 유의하시기 바랍니다. |
1. 분석기관
| 구 분 | 회 사 명 | 고 유 번 호 |
|---|---|---|
| 공동대표주관회사 | 케이비증권㈜ | 00164876 |
| 공동대표주관회사 | 한국투자증권㈜ | 00160144 |
2. 분석의 개요
공동대표주관회사인 케이비증권㈜ 및 한국투자증권㈜는「자본시장과 금융투자업에관한 법률」제71조 및 동법시행령 제68조에 의거 공정한 거래질서 확립과 투자자 보호를 위해 다수인을 상대로 한 모집ㆍ매출 등에 관여하는 인수회사로서, 발행인이 제출하는 증권신고서 등에 허위의 기재나 중요한 사항의 누락을 방지하는데 필요한 적절한 주의를 기울였습니다.
공동대표주관회사는 인수 또는 모집·매출의 주선업무를 수행함에 있어 적절한 주의의무를 다하기 위해 금융감독원이 제정한 '금융투자회사의 기업실사(Due Diligence) 모범규준'(이하 "모범규준"이라 한다)의 내용을 내부 규정에 반영하여 2012년 2월 1일부터 제출되는 지분증권, 채무증권 증권신고서를 대상(자산유동화증권 등 제외)으로 기업실사를 의무적으로 수행하도록 규정하고 있습니다.
본 장에 기재된 분석의견은 공동대표주관회사인 케이비증권㈜ 및 한국투자증권㈜가 기업실사과정을 통해 발행회사인 에이치엘비㈜로부터 제공받은 정보 및 자료에 기초한 합리적, 주관적 판단일 뿐이므로, 이로 인해 공동대표주관회사가 투자자에게 본 건 주주배정후 실권주 일반공모 유상증자의 투자여부에 관한 경영 및 재무상의 조언 또는 자문을 제공하는 것은 아닙니다.
또한 본 평가의견에 기재된 내용 중에는 예측정보가 포함되어 있으며, 예측정보에 대한 실제 결과는 여러 가지 요소들의 영향에 따라 최초 예측치와는 다른 결과를 가져올 수 있다는 점에 유의하시기 바랍니다.
| 「금융투자회사의 기업실사 모범규준」 제3조(적용범위 등) ① 이 규준은 법 제119조제3항의 규정에 의한 증권신고서 및 법 제122조의 규정에 의한 정정신고서를 제출하는 경우에 적용하며, 영업의 실체가 있는 발행회사가 제출하는 지분증권, 채무증권 증권신고서를 대상으로 하고 자산유동화증권 등은 적용대상에서 제외된다. ② 이 규준은 주관회사가 업무수행 중 참고해야 할 기본적인 지침으로 발행회사의 재무 및 영업 현황, 사업 환경, 투자위험, 인수 형태 등을 감안하여 강화하거나 완화하는 등 탄력적으로 운용할 수 있다. ③ 기업공개의 경우 기업공개 실사절차의 특성을 감안하여 이 규준의 내용중 한국거래소의 상장심사지침 등에서 의무사항으로 규정하고 있는 내용과 중복되는 부분에 대해서는 이를 생략하거나 완화할 수 있다. ④ 채무증권의 경우 i)보증유무, 상환조건(만기, 옵션유무), 특약 등 해당 사채의 특성, ii)법 제119조제2항에서 규정하고 있는 일괄신고서에 의한 발행인지 여부, iii)발행회사가 시행령 제121조제6항의 요건을 충족하고 있는지 여부, iv)해당 사채권에 대한 신용평가등급(외부 및 내부) 등을 감안하여 합리적인 기준에 따라 이 규준을 완화할 수 있다. ⑤ 제2항 내지 제4항에 따라 이 규준을 생략하거나 강화 또는 완화하는 경우에는 이사회나 리스크관리위원회(이하 ‘리스크관리위원회 등’)의 의사결정을 거쳐야 한다. |
분석의견의 상세한 내용은 동 증권신고서에 첨부되어 있는 기업실사 부분을 참고하시기 바랍니다.
3. 기업실사 일정 및 주요내용
| 일자 | 기업 실사 내용 |
|---|---|
| 2022년 07월 27일 | 가) 발행회사방문 - 유상증자 의사 및 자금조달 관련 논의 - 유상증자 필요성 검토 및 주요일정 협의 나) 회사 기본사항 점검 - 경영진 면담(경영철학, 회사연혁 등) - 사업내용 청취 및 주요제품 열람 |
| 2022년 7월 29일~ 8월 02일 |
가) 발행회사방문 - 실사 요청자료 송부 - 본사 방문 나) 회사 일반사항 관련 검토 - 정관검토 및 이사회 등 상법 절차 확인 - 경영진 평판 리스크 검토 - 회사의 사업 및 영업구조 관련 면담 |
| 2022년 08월 03일 ~ 08월 08일 |
가) 회사 기본사항 검토 - 정관 등 기본자료 수령 - 대략적인 자금 사용 목적 등에 관한 청취 - 발행 방식 및 조건 등에 관한 협의 - 금융당국으로부터 제재조치 여부 확인 - 근로기준법 위반행위, 소송진행 여부 확인 나) 산업에 관한 사항 검토 - 산업에 대한 이해 - 산업 경쟁상황, 시장규모, 성장주기 등 확인 - 법률 및 정부규제에 관한 사항 검토 - 시장 내 중대한 환경, 제도 변화요인 검토 다) 회사 지배구조에 관한 사항 검토 - 경영진의 변동내역 및 근무경력 검토 - 종속회사에 관한 사항 검토 - 최대주주의 지분율 및 경영권 안정성 검토 - 사내규정 및 내부통제시스템 확인 - 공시시스템 검토 및 담당자 면담 |
| 2022년 08월 09일 ~ 08월 11일 |
가) 영업에 관한 사항 검토 - 제품별 매출 현황, 부문별 수익성추이 확인 - 주요 공급처, 매입처에 관한 사항 - 향후 투자계획에 관한 사항 - 향후 수익성 개선 계획에 관한 사항 나) 재무에 관한 사항 검토 - 매출채권, 재고자산 현황 및 연령분석 - 기타채권 현황 및 회수 내역 분석 - 수익성/성장성/안정성 지표 분석 - 차입금 만기구조 분석 - 현금흐름 구조, 유동성 분석 - 향후 유동성 개선 계획에 관한 사항 - 주식연계채권 내역 확인 - 환위험 관리 현황 분석 다) 기타 사항 검토 - 발행시장 상황 검토 - 자금 조달금액, 공모가액의 적정성 검토 - 이사회의사록, 인수계약서 등 주요 서류 확인 - 최대주주 및 특수관계인 등 청약 여부 체크 |
| 2022년 08월 12일 ~ 08월 16일 | - 실사보고서 작성 - 증권신고서 작성 가이드 및 추가자료 작성 |
| 2022년 08월 31일 ~ 09월 07일 |
- (정정) 금융감독원의 정정요구제출에 따른 증권신고서 작성 가이드 및 추가자료 작성 |
| 2022년 09월 21일 ~ 09월 23일 |
- (정정) 자진정정 증권신고서 제출에 따른 증권신고서 작성 가이드 및 추가자료 작성 |
| 2022년 10월 06일 ~ 10월 11일 |
- (정정) 자진정정 증권신고서 제출에 따른 증권신고서 작성 가이드 및 추가자료 작성 |
4. 실사참여자
[공동대표주관회사]
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 | 참여기간 | 주요경력 |
|---|---|---|---|---|---|---|
| 케이비증권㈜ | SME금융부 | 이경재 | 이사 | 기업실사 총괄 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 22년 |
| 케이비증권㈜ | SME금융부 | 김자환 | 이사 | 기업실사 책임 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 21년 |
| 케이비증권㈜ | SME금융부 | 이형준 | 과장 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 7년 |
| 케이비증권㈜ | SME금융부 | 백성종 | 대리 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 6년 |
| 케이비증권㈜ | SME금융부 | 박진혁 | 주임 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 4년 |
| 한국투자증권㈜ | ECM부 | 채승용 | 이사 | 기업실사 총괄 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 20년 |
| 한국투자증권㈜ | ECM부 | 이용현 | 팀장 | 기업실사 책임 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 17년 |
| 한국투자증권㈜ | ECM부 | 정인묵 | 대리 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 5년 |
| 한국투자증권㈜ | ECM부 | 김하늘 | 주임 | 기업실사 실무 | 2022년 07월 27일 ~ 2022년 10월 11일 |
기업금융업무 3년 |
[발행회사]
| 소속기관 | 부서 | 성명 | 직급 | 실사업무분장 |
|---|---|---|---|---|
| 에이치엘비㈜ | 재무전략본부 | 백윤기 | 부사장 | 발행업무 총괄 |
| 바이오전략기획본부 | 장인근 | 부사장 | 발행업무 기획 및 실무 | |
| 경영전략본부 | 김도연 | 상무 | 발행업무 기획 및 실무 | |
| 해외법인관리팀 | 김경배 | 상무 | 발행업무기획 및 실무 | |
| 경영전략팀 | 한영인 | 이사 | 발행업무 기획 및 실무 | |
| 경영전략팀 | 박준영 | 부장 | 발행업무 기획 및 실무 |
5. 기업실사 세부 항목 및 점검 결과
- 동 증권신고서에 첨부되어 있는 기업실사 보고서를 참조해 주시기 바랍니다.
6. 종합 의견
가. 공동대표주관회사인 케이비증권㈜ 및 한국투자증권㈜는 에이치엘비㈜가 2022년08월 12일 최초 이사회에서 결의한 기명식 보통주 9,562,408주에 대한 주주배정후 실권주 일반공모 방식으로 발행을 결정하고 이에 잔액인수 함에 있어 다음과 같이 의견을 제시합니다.
| 긍정적 요인 | ▶ 당사는 지속적인 영업적자와 이에 따른 당기순손실이 지속적으로 발생했으나, 주식관련사채의 전환(행사) 및 유상증자 진행으로 자본총계가 크게 증가하여 최근 3년간 부채비율은 2019년 91.6%, 2020년 26.7%, 2021년 45.2%, 2022년 반기 27.9%를 기록중입니다. ▶ 2022년 반기 연결기준 당사 바이오ㆍ의료기기 사업부문 매출실적은 114,338백만원으로 전년 동기 4,099백만원 대비 2,689.7% 증가하였으며, 영업이익은 21,921백만원을 기록했습니다. 이는 당반기 중 코로나 대유행에 따라 헬스케어사업부의 매출이 대폭 증가한점에 기인합니다. |
| 부정적 요인 | ▶ 동사의 바이오 사업부문이 본격적인 궤도이 진입하지 못한 관계로 현재까지 매출규모는 제한적이며 과거 실적 성장률을 토대로 회사의 잠재성장성을 판단하는데 한계가 있습니다. ▶ 코스닥시장 상장규정에 따르면 최근 4개 사업연도(별도기준)에서 영업손실을 기록할 경우 관리종목에 지정되며 당사는 2016년 4,641백만원의 영업손실, 2017년 6,776백만원의 영업손실, 2018년 1,654백만원의 영업이익, 2019년 4,939백만원의 영업손실, 2020년 9,906백만원의 영업손실, 2021년 14,452백만원의 영업손실, 2022년 반기 36,308백만원의 영업이익을 기록하였습니다. 이에 따라, 당사가 2022년 영업손실을 기록하게 된다면 관리종목에 지정됩니다. ▶ 당사는 수익성 악화 및 지속적인 연구개발 활동으로 인해 음(-)의 영업활동현금흐름을 보이고 있으며, 투자활동현금흐름의 경우에도 지속적인 관계기업투자주식의 취득으로 인해 음(-)의 현금흐름을 보였습니다. 당사는 음(-)의 영업활동현금흐름을 대체적으로 재무활동현금흐름을 통하여 충당하고 있는 상황입니다. |
| 자금조달의 필요성 |
▶ 동사는 금번 유상증자를 통해 조달하는 자금을 타법인증권취득자금, 시설투자자금, 운영자금, 채무상환자금으로 활용할 계획입니다. |
나. 공동대표주관회사는 동사가 제출한 자료와 당사가 객관적으로 정확하고 신뢰할 수 있다고 믿어지는 자료를 중심으로 용역을 수행하였으며, 객관적인 입장에서 공정을 기하기 위하여 최선의 노력을 다 하였습니다.
다. 공동대표주관회사는 상기 실사를 통해 제공받는 자료들로부터 도출된 결과나 오류, 누락 등에 대하여 당사가 책임지지 않으며, 인간적 또는 기계적, 기타 그 외의 다른 요인에 의한 오류발생 가능성으로 인해 본 평가 내용에 대해 명시적으로 혹은 묵시적으로도 증명이나 서명 또는 보증 및 단언을 할 수 없습니다.
라. 동사의 금번 유상증자는 국내외 거시경제 변수변화로 투자수익에 대한 확실성이 저하될 수 있습니다. 투자자 여러분께서는 상기 검토결과는 물론 동 증권신고서 및 투자설명서에 기재된 동사의 회사 전반에 걸친 현황 및 재무상의 위험과 산업 및 영업상의 위험요인 등을 감안하시어 투자에 유의하시기 바랍니다.
또한, 공동대표주관회사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 동 증권신고서 및 투자설명서에 기재하지 않은 사항이라 하더라도 동사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자께서는 동 증권신고서 및 투자설명서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 독자적이고도 세밀한 판단에 의해 투자결정을 하시기 바랍니다.
| 2022년 10월 11일 |
| 공동대표주관회사 : 케이비증권 주식회사 |
| 대표이사 김 성 현 |
| 한국투자증권 주식회사 |
| 대표이사 정 일 문 |
V. 자금의 사용목적
1. 모집 또는 매출에 의한 자금조달 내역
가. 자금조달금액
|
(단위 : 원) |
|
구 분 |
금 액 |
|---|---|
|
모집 또는 매출총액(1) |
325,599,992,400 |
|
발행제비용(2) |
4,713,977,671 |
|
순 수 입 금 [ (1)-(2) ] |
320,886,014,729 |
|
주1) 상기 금액은 예정발행가액을 기준으로 산정한 금액으로 모집가액 확정시 변경될 수 있습니다. |
| 주2) 상기 모집총액은 우선적으로 하단에 기재된 자금의 사용 목적에 따라 사용할 예정입니다. |
| 주3) 발행제비용은 공모금액 및 실권규모에 따라 변경될 수 있으며, 상기 기재 금액은 청약 초과로 인하여 실권이 발생하지 않은 상황을 가정하여 산정되었습니다. 또한 상장수수료는 상장신청일 직전일 주가에 따라 변동될 수 있습니다. 발행제비용의 경우 자체 보유현금을 통하여 지급할 계획입니다. |
나. 발행제비용의 내역
|
(단위 : 원) |
|
구 분 |
금 액 |
지급일자 |
계산근거 |
|---|---|---|---|
|
발행분담금 |
58,607,990 |
신고서제출일 |
모집총액의 0.018% (10원 미만 절사) |
| 대표주관수수료 | 976,799,977 | 유상증자 납입일로부터 3영업일 이내 | 납입금액의 0.3% |
|
인수수수료 |
3,581,599,916 |
유상증자 납입일로부터 3영업일 이내 |
납입금액의 1.1% |
|
상장수수료 |
24,020,000 |
신주상장일 |
1,410만원+2,000억원 초과금액의 10억원당 4만원 (「코스닥시장 상장규정」 시행세칙) |
|
등록세 |
19,124,816 |
등기일 |
증자 자본금의 0.4% |
|
교육세 |
3,824,963 |
등기일 |
등록세의 20% |
|
기타비용 |
50,000,000 |
- |
구주주청약서, 투자설명서 인쇄 및 발송비 등 |
|
합 계 |
4,713,977,663 |
- |
- |
| 주1) 상기 금액은 예정 모집가액을 기준으로 산정한 금액입니다. |
| 주2) 발행제비용은 공모금액 및 상장신청일 직전일 한국거래소에서 거래되는 당사의 보통주식 종가, 유관기관 정책 등에 따라 변동될 수 있습니다. |
| 주3) 기타비용은 예상금액으로 변동될 수 있습니다. |
| 주4) 발행제비용은 자체 보유현금을 통하여 지급할 계획입니다. |
2. 자금의 사용목적
가. 자금의 사용목적
당사는 금번 유상증자를 통해 조달한 자금을 아래와 같이 사용할 예정입니다.
자금의 사용목적
| (기준일 : | 2022년 09월 07일 | ) | (단위 : 백만원) |
| 시설자금 | 영업양수 자금 |
운영자금 | 채무상환 자금 |
타법인증권 취득자금 |
기타 | 계 |
|---|---|---|---|---|---|---|
| 30,010 | - | 8,210 | 4,680 | 282,700 | - | 325,600 |
| 주1) 상기 자금조달 목적 금액 합계 대비 부족분은 당사 자체자금으로 충당할 계획입니다. |
나. 공모자금 세부 사용목적
당사가 금번 유상증자를 통하여 조달할 예정인 자금은 총 약 3,256억원 규모이며, 자금의 분류별 세부 사용내역은 아래와 같습니다.
| (외화단위: USD / 원화단위: 백만원) |
| 구분 | 지급처 | 금액(외화) | 금액(원화) | 사용 시기 | 내용 |
|---|---|---|---|---|---|
| 타법인증권취득자금 | Elevar Therapeutics, Inc. | 176,353,167 | 229,700 | 2022년~2025년 | 100% 자회사의 유상증자를 통한 기존 pipeline 임상비용 및 상업화 관련 비용 지원 |
| Immunomic Therapeutics, Inc. | 40,690,979 | 53,000 | 2023년 ~2025년 | 종속회사의 유상증자를 통한 기존 pipeline 임상비용 지원 |
|
| 시설자금 | - | 30,010 | 2023년 ~2024년 | 헬스케어사업부 둔곡 제2공장 건립 건축비 등 | |
| 운영자금 | - | 8,210 | 2023년 | 복합소재 사업부문 원재료 매입 대금 등 | |
| 채무상환자금 | 기업은행 | - | 4,360 | 2022년 이내 | 복합소재 사업부문 공장부지 매입을 위한 단기차입금 상환 |
| 기업은행 | - | 320 | 2022년 이내 | 기존 차입금 상환 | |
| 합계 | - | 325,600 | - | - | |
| 주1) 자금의 사용목적 중 외화로 필요한 금액에 대하여는 2022년 08월 12일 서울외국환중개 매매기준율(1,302.50원/달러)을 사용하여 산출하였으며, 상세 액수는 향후 당사의 주가 및 환율의 변동에 따라 변경될 수 있습니다. 주2) 상기 일정은 내부 임상개발전략, 규제기관의 정책변화, 시장 변동에 따라 변경될 수 있습니다. |
(1) 타법인증권취득자금
당사는 금번 유상증자로 조달하는 금액 약 3,256억원 중 약 2,827억원을 타법인증권취득자금으로 사용할 예정이며, 그 세부 내용은 아래와 같습니다.
| (외화단위: USD / 원화단위: 백만원) |
| 지급처 | 금액(외화) | 금액(원화) | 사용시기 | 세부목적 |
|---|---|---|---|---|
| Elevar Therapeutics Inc. | 176,353,167 | 229,700 | 2022년 4분기부터 지속적 지원 |
100% 자회사의 유상증자를 통한 기존 pipeline 임상비용 및 상업화 관련 비용 지원 |
| Immunomic Therapeutics Inc. | 40,690,979 | 53,000 | 2023년 1분기부터 지속적 지원 |
종속회사의 유상증자를 통한 기존 pipeline 임상비용 지원 |
| 주1) 자금의 사용목적 중 외화로 필요한 금액에 대하여는 2022년 08월 12일 서울외국환중개 매매기준율(1,302.50원/달러)을 사용하여 산출하였으며, 상세 액수는 향후 당사의 주가 및 환율의 변동에 따라 변경될 수 있습니다. |
당사는 당사의 100% 자회사인 Elevar Therapeutics Inc.를 통하여 의약품개발(항암제 등) 사업을 영위하고 있습니다. 증권신고서 제출일 전일 현재 Elevar Therapeutics Inc. 는 신약후보물질 'Rivoceranib' 성분에 대해 중국을 제외한 글로벌 시장에서의 독점 실시권을 보유하고 있는 바, 연구개발 및 임상실험을 진행하여 최종적으로 신약 판매 허가를 득하게 될 경우 그 제품에 대한 판권을 보유하게 됩니다.
증권신고서 제출일 전일 현재 Elevar Therapeutics Inc. 는 다양한 적응증에 대하여 Rivoceranib 성분 단독 신약 및 타 성분과의 병용요법을 연구ㆍ개발 중에 있으며, 임상 진행 등에 있어서 지속적으로 자금 소요가 발생합니다. 이에 당사는 금번 유상증자를 통해 조달한 자금 중 약 2,297억원을 Elevar Therapeutics Inc.의 유상증자 참여에 사용할 예정이며, 그 중 2,034억원은 임상개발지원비용에, 263억원은 상업화를 위한 마케팅 비용에 사용할 예정입니다. 유상증자 참여를 통해 당사가 Elevar Therapeutics Inc.에 지원하는 자금의 예상 사용처는 아래와 같습니다.
① Elevar 임상 비용
| (외화단위: USD / 원화단위: 백만원) |
|
내역 |
필요금액(외화) |
필요금액(원화) | 연도별 사용 예정금액(원화) | |||
|---|---|---|---|---|---|---|
| 2022 | 2023 | 2024 | 2025 | |||
|
선낭양성암 1차 치료제 글로벌 단독임상 3상 비용 |
17,965,451 | 23,400 | 7,020 | 9,360 | 7,020 | - |
| 간암 1차 치료제 글로벌 임상 4상(PMS) 비용 [Camrelizumab - Rivoceranib 병용] |
23,032,630 | 30,000 | - | 6,000 | 12,000 | 12,000 |
|
대장암 3차 치료제 글로벌 임상 2상 비용 |
10,364,683 | 13,500 | 5,400 | 8,100 | - | - |
| 대장암 3차 치료제 글로벌 임상 3상 비용 [론서프(타이호제약) - Rivoceranib 병용] |
57,581,574 | 75,000 | - | 15,000 | 30,000 | 30,000 |
| 난소암(PR) 2차 치료제 글로벌 임상 1상 비용 (아필리아 - Rivoceranib 병용) |
9,213,052 | 12,000 | 4,800 | 7,200 | - | - |
| 난소암(PR) 2차 치료제 글로벌 임상 3상 비용 (아필리아 - Rivoceranib 병용) |
38,003,839 | 49,500 | - | 9,900 | 19,800 | 19,800 |
|
합계 |
156,161,228 | 203,400 | 17,220 | 55,560 | 68,820 | 61,800 |
| 주1) 자금의 사용목적 중 외화로 필요한 금액에 대하여는 2022년 08월 12일 서울외국환중개 매매기준율(1,302.50원/달러)을 사용하여 산출하였으며, 상세 액수는 향후 당사의 주가 및 환율의 변동에 따라 변경될 수 있습니다. |
② Elevar 상업화 비용
| (외화단위: USD / 원화단위: 백만원) |
| 항목 | 내역 |
필요금액(외화) |
필요금액(원화) | 연도별 사용 예정금액(원화) | |||
|---|---|---|---|---|---|---|---|
| 2022 | 2023 | 2024 | 2025 | ||||
| NDA 준비 | NDA 위한 전문 컨설팅 | 3,071,017 | 4,000 | 2,000 | 2,000 | - | - |
| 생산 | 리보세라닙 시판용 제품 생산 | 7,677,543 | 10,000 | - | 4,000 | 3,000 | 3,000 |
| 온라인 마케팅 | 온라인 홍보 (병원, 제약사 등) | 3,301,344 | 4,300 | - | 2,350 | 1,050 | 900 |
| 오프라인 마케팅 | 오프라인 홍보 (학회, 제약사 등) | 4,606,526 | 6,000 | - | 2,800 | 1,600 | 1,600 |
| 조직 관리 | 협력업체 관리 및 운용 | 1,535,509 | 2,000 | - | 600 | 1,000 | 400 |
|
합계 |
20,191,939 | 26,300 | 2,000 | 11,750 | 6,650 | 5,900 | |
| 주1) 자금의 사용목적 중 외화로 필요한 금액에 대하여는 2022년 08월 12일 서울외국환중개 매매기준율(1,302.50원/달러)을 사용하여 산출하였으며, 상세 액수는 향후 당사의 주가 및 환율의 변동에 따라 변경될 수 있습니다. |
또한, 증권신고서 제출일 현재 Immunomic Therapeutics Inc. 는 다양한 적응증에 대하여 UNITE (Universal Intracellular Targeted Expression)라는 면역 플랫폼 기술을 활용하여 면역세포치료제, 치료백신 등의 면역치료제를 연구ㆍ개발 중에 있으며, 임상 진행 등에 있어서 지속적으로 자금 소요가 발생합니다. 이에 당사는 금번 유상증자를 통해 조달한 자금 중 약 530억원을 Immunomic Therapeutics Inc.의 유상증자 참여에 사용할 예정입니다.
③ Immunomic Therapeutics 임상개발
| (외화단위: USD / 원화단위: 백만원) |
|
내역 |
필요금액(외화) |
필요금액(원화) | 연도별 사용 예정금액(원화) | |||
|---|---|---|---|---|---|---|
| 2022 | 2023 | 2024 | 2025 | |||
|
교모세포종 1차 치료제 |
40,690,979 | 53,000 | - | 26,500 | 15,900 | 10,600 |
| 주1) 자금의 사용목적 중 외화로 필요한 금액에 대하여는 2022년 08월 12일 서울외국환중개 매매기준율(1,302.50원/달러)을 사용하여 산출하였으며, 상세 액수는 향후 당사의 주가 및 환율의 변동에 따라 변경될 수 있습니다. 주2) 전체 임상개발 필요비용 중 금번 유상증자 자금 530억원을 사용할 예정이며, 잔여 비용은 현지자금을 활용할 계획입니다. 주3) 상기 일정은 내부 임상개발전략, 규제기관의 정책변화, 시장 변동에 따라 변경될 수 있습니다. |
당사가 계획중인 파이프라인 일정, 각 임상계획별 임상시험비용 세부내역 및 임상시험 개요는 아래와 같습니다
|
| 주1) 상기 일정은 회사에서 추정한 일정으로 규제기관의 정책변화, 시장 환경 변화, 내부 임상 개발 전략변경에 따라 변경될 수 있습니다. |
1) 선양낭성암 1차 치료제
| (단위: 백만원) |
| 파이프라인 | 구분 | 구성 | 2022년 | 2023년 | 2024년 | 총금액 | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 4Q | 1Q | 2Q | 3Q | 4Q | 1Q | 2Q | 3Q | 4Q | ||||
| 선양낭성암(ACC) 1차 치료제 3상 임상 |
임상비용 | CRO Opration | 1,404 | 468 | 468 | 468 | 468 | 281 | 281 | 281 | 562 | 4,680 |
| 임상비용 | 임상 사이트 관리(환자 검사비 등) | 1,755 | 585 | 585 | 585 | 585 | 439 | 439 | 439 | 439 | 5,850 | |
| 데이터분석 | 통계 분석 비용 | 351 | 117 | 117 | 117 | 117 | 35 | 35 | 35 | 246 | 1,170 | |
| 임상약 생산/유통 | 제조/유통 | 1,404 | 468 | 468 | 468 | 468 | 351 | 351 | 351 | 351 | 4,680 | |
| 임상, NDA 컨설팅 등 | 컨설팅 | 1,053 | 983 | 281 | 70 | 70 | 53 | 53 | 316 | 632 | 3,510 | |
| 기타 판관비 | 내부 운영비(출장, KOL 섭외, 인력보강 등) | 1,053 | 421 | 421 | 421 | 140 | 105 | 105 | 421 | 421 | 3,510 | |
| 합계 | 7,020 | 3,042 | 2,340 | 2,129 | 1,849 | 1,264 | 1,264 | 1,843 | 2,650 | 23,400 | ||
| [선양낭성암 1차 치료제 글로벌 임상 3상 개요] |
| 구분 | 내용 |
|---|---|
| 임상시험 대상국가 | 미국, 유럽, 아시아 |
| 임상시험의 목적 | 임상시험의 주요 목표는 재발 또는 전이성 선양낭성암(Adnoid Cystic Carcinoma, ACC) 피험자를 대상으로 대조군과 비교하여 리보세라닙의 안전성과 유효성을 확인하기 위함 |
| 임상시험 시행 방법 | 시험 대상자 수: 재발 또는 전이성 선양낭성암 환자 약 156명 + 10% 환자 무작위(randomized), 이중눈가림(double-blind), 위약 대조로 진행되며, 리보세라닙 700mg과 위약을 투여하여 무진행생존기간(PFS)를 평가함 임상연구기간 : 전체 약 3년 (환자의 등록 상황 또는 투여기간 등에 따라 변동 가능) |
| 기대효과 | 선양낭성암의 진행은 혈관 형성과 밀접한 관계가 있는 것으로 알려져 있으며, 이러한 신생혈관은 VEGF와 VEGFR2에 의해 진행됨 리보세라닙은 신생혈관을 억제하는 표적항암제로 신생혈관의 주요한 표적인 VEGFR2를 타겟으로 하기 때문에 선양낭성암의 치료에 효과적일 것으로 기대됨. 선양낭성암은 희귀질환으로 현재 표준치료제가 없기 때문에 리보세라닙의 신약 승인되면 최초의 신약이 될 것으로 기대됨 |
| 임상비용 산정근거 | American Medical Association의 조사에 따르면, 항암제 임상3상에 소요 되는 비용은 최소 31백만USD~59백만USD로 알려져 있습니다. 실제 당사 과거 임상(GC3, ACC)에 투입된 비용을 분석한 결과, 환자 1인당 약 115천USD(한화 약150백만원)가 소요 되었습니다. 이를 근거로 향후 진행될 임상 비용을 산정하였으나 거시경제상황변화(물가상승, 환율), 임상프로토콜 수정 등에 의해 변동 가능성 또한 존재합니다. |
| 임상 시험 기관 | 미국: UCLA(University of California, Los Angeles), UCSF(San Francisco, Califonia), Dana-Farber Cancer Institute 등 유럽: 협의중 아시아: 서울대병원, 삼성서울병원 등 (임상시험기관들과 논의후 추가 및 변경 가능) |
2) 간암 (HCC) 1차 치료제 4상(PMS) 임상
| (단위: 백만원) |
| 파이프라인 | 구분 | 구성 | 2023년 | 2024년 | 2025년 | 총금액 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1Q | 2Q | 3Q | 4Q | 1Q | 2Q | 3Q | 4Q | 1Q | 2Q | 3Q | 4Q | ||||
| 간암 (HCC) 1차 치료제 4상 임상 |
임상비용 | CRO Opration | - | 720 | 360 | 120 | 600 | 600 | 600 | 600 | 360 | 360 | 360 | 1,320 | 6,000 |
| 임상비용 | 임상 사이트 관리(환자 검사비 등) | - | 450 | 450 | 600 | 750 | 750 | 750 | 750 | 750 | 750 | 750 | 750 | 7,500 | |
| 데이터분석 | 통계 분석 비용 | 210 | 30 | 30 | 30 | 150 | 150 | 150 | 150 | 60 | 60 | 240 | 240 | 1,500 | |
| 임상약 생산/유통 | 제조/유통 | 480 | 240 | 240 | 240 | 600 | 600 | 600 | 600 | 600 | 600 | 600 | 600 | 6,000 | |
| 임상, NDA 컨설팅 등 | 컨설팅 | 360 | 180 | 180 | 180 | 450 | 450 | 450 | 450 | 270 | 270 | 270 | 990 | 4,500 | |
| 기타 판관비 | 내부 운영비(출장, KOL 섭외, 인력보강 | 225 | 225 | 225 | 225 | 450 | 450 | 450 | 450 | 450 | 450 | 450 | 450 | 4,500 | |
| 합계 | 1,275 | 1,845 | 1,485 | 1,395 | 3,000 | 3,000 | 3,000 | 3,000 | 2,490 | 2,490 | 2,670 | 4,350 | 30,000 | ||
| [간암 1차 치료제 글로벌 임상 4상(PMS) 개요] |
| 구분 | 내용 |
|---|---|
| 임상시험 대상국가 | 미국, 유럽, 아시아 |
| 임상시험의 목적 | 임상시험의 주요 목표는 절재 불가능한 간세포암(hepatocellular carcinoma, HCC) 피험자를 대상으로 리보세라닙과 캄렐리주맙 투여시 안전성과 내약성을 확인하기 위함 |
| 임상시험 시행 방법 | 시험 대상자 수: 절재 불가능한 간세포암 환자 약 1,000명 리보세라닙과 캄렐리주맙을 투여받은 환자을 관찰하며 안전성과 내약성을 평가함 임상연구기간 : 전체 약 3년 (환자의 모집 상황 또는 투여기간 등에 따라 변동 가능) |
| 기대효과 | - 간암의 진행은 혈관 형성과 밀접한 관계가 있는 것으로 알려져 있으며, 이러한 신생혈관은 VEGF와 VEGFR2에 의해 진행됨. 또한 종양미세환경내에서 면역억제로 인해 간암의 진행을 촉진하고 있음. - 리보세라닙은 신생혈관을 억제하는 표적항암제로 신생혈관의 주요한 표적인 VEGFR2를 타겟으로 하기 때문에 간암의 치료에 효과적일 것으로 기대되고, 캄렐리주맙은 종양미세환경의 면역억제기전을 정상화시켜 면역활성화를 통해 간암 치료에 효과적일 것으로 기대되고 있기 때문에 두 제품의 병용은 간암 치료에 더욱 효과적일 것으로 기대됨 - 간암은 1차 치료제는 넥사바, 렌비마와 같은 저분자 신생혈관억제제 단독치료제와 아바스틴(항체치료제)과 티센트릭(항체치료제) 병용으로 허가되어 있으며, 캄렐리주맙과 리보세라닙이 신약 승인되면 최초의 면역항암제+저분자신생혈관억제 병용 신약이 될 것으로 기대됨 |
| 임상비용 산정근거 | 글로벌 조사 기관인 ERG (Eastern Research Group Inc.)에 따르면, 항암제 임상4상에 소요 되는 비용은 최소 38백만USD로 알려져 있습니다. |
| 임상 시험 기관 | 미국: MD Anderson, UCSC(University of California, San Diego), 등 유럽: 협의중 아시아: 서울아산병원, 삼성서울병원, 등 (임상시험기관들과 논의후 추가 및 변경 가능) |
3) 대장암 (CRC) 3차 치료제 2상 임상
| (단위: 백만원) |
| 파이프라인 | 구분 | 구성 | 2022년 | 2023년 | 총금액 | |||
|---|---|---|---|---|---|---|---|---|
| 4Q | 1Q | 2Q | 3Q | 4Q | ||||
| 대장암 (CRC) 3차 치료제 2상 임상 |
임상비용 | CRO Opration | 1,080 | 162 | 162 | 324 | 972 | 2,700 |
| 임상비용 | 임상 사이트 관리(환자 검사비 등) | 1,350 | 506 | 506 | 506 | 506 | 3,375 | |
| 데이터분석 | 통계 분석 비용 | 270 | 41 | 41 | 81 | 243 | 675 | |
| 임상약 생산/유통 | 제조/유통 | 1,080 | 405 | 405 | 405 | 405 | 2,700 | |
| 임상, NDA 컨설팅 등 | 컨설팅 | 810 | 851 | 243 | 61 | 61 | 2,025 | |
| 기타 판관비 | 내부 운영비(출장, KOL 섭외, 인력보강 등) | 810 | 365 | 365 | 365 | 122 | 2,025 | |
| 합계 | 5,400 | 2,329 | 1,721 | 1,742 | 2,309 | 13,500 | ||
| [대장암 3차 치료제 글로벌 임상 2상 개요] |
| 구분 | 내용 |
|---|---|
| 임상시험 대상국가 | 미국, 유럽, 아시아 |
| 임상시험의 목적 | 임상시험의 주요 목표는 전이성 대장암(Colorectal cancer, CRC) 피험자를 대상으로 리보세라닙과 트리플루리딘/티피라실(론서프) 투여시 안전성과 유효성을 확인하기 위함 |
| 임상시험 시행 방법 | 시험 대상자 수: 전이성 대장암 환자 약 100명 리보세라닙과 트리플루리딘/티피라실(론서프)을 투여받은 환자을 관찰하며 안전성과 유효성을 평가함 임상연구기간 : 전체 약 2년 (환자의 모집 상황 또는 투여기간 등에 따라 변동 가능) |
| 기대효과 | - 대장암의 진행은 혈관 형성과 밀접한 관계가 있는 것으로 알려져 있으며, 이러한 신생혈관은 VEGF와 VEGFR2에 의해 진행됨. - 리보세라닙은 신생혈관을 억제하는 표적항암제로 신생혈관의 주요한 표적인 VEGFR2를 타겟으로 하기 때문에 간암의 치료에 효과적일 것으로 기대되고, 트리플루리딘/티피라실(론서프)은 새로운 세포독성항암제로 대장암 3차 치료제 단독요법으로 허가받아 효과적임을 증명되었음. 이러한 두 제품이 병용요법은 대장암 치료에 더욱 효과적일 것으로 기대됨. |
| 임상비용 산정근거 | American Medical Association의 조사에 따르면, 항암제 임상3상에 소요 되는 비용은 최소 31백만USD~59백만USD로 알려져 있습니다. 실제 당사 과거 임상(GC3, ACC)에 투입된 비용을 분석한 결과, 환자 1인당 약 115천USD(한화 약150백만원)가 소요 되었습니다. 이를 근거로 향후 진행될 임상 비용을 산정하였으나 거시경제상황변화(물가상승, 환율), 임상프로토콜 수정 등에 의해 변동 가능성 또한 존재합니다. |
| 임상 시험 기관 | 미국: Vanderbilt University School of Medicine, Washington University School of Medicine 등 유럽: 협의중 아시아: 협의중 (임상시험기관들과 논의후 추가 및 변경 가능) |
4) 대장암 (CRC) 3차 치료제 3상 임상
| (단위: 백만원) |
| 파이프라인 | 구분 | 구성 | 2023년 | 2024년 | 2025년 | 총금액 | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 3Q | 4Q | 1Q | 2Q | 3Q | 4Q | 1Q | 2Q | 3Q | 4Q | ||||
| 대장암 (CRC) 3차 치료제 3상 임상 |
임상비용 | CRO Opration | 900 | 2,100 | 1,500 | 1,500 | 1,500 | 1,500 | 900 | 900 | 900 | 3,300 | 15,000 |
| 임상비용 | 임상 사이트 관리(환자 검사비 등) | 1,125 | 2,625 | 1,875 | 1,875 | 1,875 | 1,875 | 1,875 | 1,875 | 1,875 | 1,875 | 18,750 | |
| 데이터분석 | 통계 분석 비용 | 525 | 225 | 375 | 375 | 375 | 375 | 150 | 150 | 600 | 600 | 3,750 | |
| 임상약 생산/유통 | 제조/유통 | 1,500 | 1,500 | 1,500 | 1,500 | 1,500 | 1,500 | 1,500 | 1,500 | 1,500 | 1,500 | 15,000 | |
| 임상, NDA 컨설팅 등 | 컨설팅 | 1,800 | 450 | 1,125 | 1,125 | 1,125 | 1,125 | 675 | 675 | 675 | 2,475 | 11,250 | |
| 기타 판관비 | 내부 운영비(출장, KOL 섭외, 인력보강 등) | 1,125 | 1,125 | 1,125 | 1,125 | 1,125 | 1,125 | 1,125 | 1,125 | 1,125 | 1,125 | 11,250 | |
| 합계 | 6,975 | 8,025 | 7,500 | 7,500 | 7,500 | 7,500 | 6,225 | 6,225 | 6,675 | 10,875 | 75,000 | ||
| [대장암 3차 치료제 글로벌 임상 3상 개요] |
| 구분 | 내용 |
|---|---|
| 임상시험 대상국가 | 미국, 유럽, 아시아 |
| 임상시험의 목적 | 임상시험의 주요 목표는 전이성 대장암(Colorectal cancer, CRC) 피험자를 대상으로 리보세라닙과 트리플루리딘/티피라실(론서프) 투여시 안전성과 유효성을 확인하기 위함 |
| 임상시험 시행 방법 | 시험 대상자 수: 전이성 대장암 환자 약 500명 리보세라닙과 트리플루리딘/티피라실(론서프)을 투여받은 환자을 관찰하며 안전성과 유효성을 평가함 임상연구기간 : 전체 약 3년 (환자의 모집 상황 또는 투여기간 등에 따라 변동 가능) |
| 기대효과 | - 대장암의 진행은 혈관 형성과 밀접한 관계가 있는 것으로 알려져 있으며, 이러한 신생혈관은 VEGF와 VEGFR2에 의해 진행됨. - 리보세라닙은 신생혈관을 억제하는 표적항암제로 신생혈관의 주요한 표적인 VEGFR2를 타겟으로 하기 때문에 간암의 치료에 효과적일 것으로 기대되고, 트리플루리딘/티피라실(론서프)은 새로운 세포독성항암제로 대장암 3차 치료제 단독요법으로 허가받아 효과적임을 증명되었음. 이러한 두 제품의 병용요법은 대장암 치료에 더욱 효과적일 것으로 기대됨. |
| 임상비용 산정근거 | American Medical Association의 조사에 따르면, 항암제 임상3상에 소요 되는 비용은 최소 31백만USD~59백만USD로 알려져 있습니다. 실제 당사 과거 임상(GC3, ACC)에 투입된 비용을 분석한 결과, 환자 1인당 약 115천USD(한화 약150백만원)가 소요 되었습니다. 이를 근거로 향후 진행될 임상 비용을 산정하였으나 거시경제상황변화(물가상승, 환율), 임상프로토콜 수정 등에 의해 변동 가능성 또한 존재합니다. |
| 임상 시험 기관 | 미국: Vanderbilt University School of Medicine, Washington University School of Medicine 등 유럽: 협의중 아시아: 협의중 (임상시험기관들과 논의후 추가 및 변경 가능) |
5) 난소암 OC (PR) 2차 치료제 1상 임상
| (단위: 백만원) |
| 파이프라인 | 구분 | 구성 | 2022년 | 2023년 | 총금액 | ||
|---|---|---|---|---|---|---|---|
| 4Q | 1Q | 2Q | 3Q | ||||
| 난소암 OC (PR) 2차 치료제 1상 임상 |
임상비용 | CRO Opration | 960 | 576 | 720 | 144 | 2,400 |
| 임상비용 | 임상 사이트 관리(환자 검사비 등) | 1,200 | 720 | 900 | 180 | 3,000 | |
| 데이터분석 | 통계 분석 비용 | 240 | 72 | 72 | 216 | 600 | |
| 임상약 생산/유통 | 제조/유통 | 960 | 576 | 432 | 432 | 2,400 | |
| 임상, NDA 컨설팅 등 | 컨설팅 | 720 | 216 | 216 | 648 | 1,800 | |
| 기타 판관비 | 내부 운영비(출장, KOL 섭외, 인력보강 등) | 720 | 324 | 324 | 432 | 1,800 | |
| 합계 | 4,800 | 2,484 | 2,664 | 2,052 | 12,000 | ||
| [난소암(PR) 2차 치료제 글로벌 임상 1상 개요] |
| 구분 | 내용 |
|---|---|
| 임상시험 대상국가 | 미국 |
| 임상시험의 목적 | 임상시험의 주요 목표는 백금계항암제 저항성(Platinum-resistant)이 있는 난소암(Platinum-resistant epithelial Ovarian Cancer) 피험자를 대상으로 리보세라닙과 아필리아 투여시 안전성과 유효성을 확인하기 위함 |
| 임상시험 시행 방법 | 시험 대상자 수: 백금계항암제 저항성이 있는 난소암 환자 약 66 ~ 81명 아필리아와 리보세라닙의 투여시, 리보세라닙의 용량을 증가시키며 내약성과 안전성을 평가하여 용량을 결정 임상연구기간 : 전체 약 2년 (환자의 모집 상황 또는 투여기간 등에 따라 변동 가능) |
| 기대효과 | - 난소암의 진행은 혈관 형성과 밀접한 관계가 있는 것으로 알려져 있으며, 이러한 신생혈관은 VEGF와 VEGFR2에 의해 진행됨. - 리보세라닙은 신생혈관을 억제하는 표적항암제로 신생혈관의 주요한 표적인 VEGFR2를 타겟으로 하기 때문에 난소암의 치료에 효과적일 것으로 기대되고, 아필리아는 파클리탁셀(paclitaxel) 성분의 세포독성항암제로 난소암에 대해서 효과적임을 증명되었음. 이러한 두 제품의 병용요법은 난소암 치료에 더욱 효과적일 것으로 기대됨. |
| 임상비용 산정근거 | American Medical Association의 조사에 따르면, 항암제 임상3상에 소요 되는 비용은 최소 31백만USD~59백만USD로 알려져 있습니다. 실제 당사 과거 임상(GC3, ACC)에 투입된 비용을 분석한 결과, 환자 1인당 약 115천USD(한화 약150백만원)가 소요 되었습니다. 이를 근거로 향후 진행될 임상 비용을 산정하였으나 거시경제상황변화(물가상승, 환율), 임상프로토콜 수정 등에 의해 변동 가능성 또한 존재합니다. |
| 임상 시험 기관 | 미국: GOG(gynecologic oncology group)과 협력하여 선정 예정 (임상시험기관들과 논의후 추가 및 변경 가능) |
6) 난소암 OC (PR) 2차 치료제 3상 임상
| (단위: 백만원) |
| 파이프라인 | 구분 | 구성 | 2023년 | 2024년 | 2025년 | 총금액 | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 3Q | 4Q | 1Q | 2Q | 3Q | 4Q | 1Q | 2Q | 3Q | 4Q | ||||
| 난소암 OC (PR) 2차 치료제 3상 임상 |
임상비용 | CRO Opration | 1,188 | 792 | 990 | 990 | 990 | 990 | 594 | 594 | 594 | 2,178 | 9,900 |
| 임상비용 | 임상 사이트 관리(환자 검사비 등) | 1,485 | 990 | 1,238 | 1,238 | 1,238 | 1,238 | 1,238 | 1,238 | 1,238 | 1,238 | 12,375 | |
| 데이터분석 | 통계 분석 비용 | 297 | 198 | 248 | 248 | 248 | 248 | 99 | 99 | 396 | 396 | 2,475 | |
| 임상약 생산/유통 | 제조/유통 | 990 | 990 | 990 | 990 | 990 | 990 | 990 | 990 | 990 | 990 | 9,900 | |
| 임상, NDA 컨설팅 등 | 컨설팅 | 1,040 | 446 | 743 | 743 | 743 | 743 | 446 | 446 | 446 | 1,634 | 7,425 | |
| 기타 판관비 | 내부 운영비(출장, KOL 섭외, 인력보강 등) | 743 | 743 | 743 | 743 | 743 | 743 | 743 | 743 | 743 | 743 | 7,425 | |
| 합계 | 5,742 | 4,158 | 4,950 | 4,950 | 4,950 | 4,950 | 4,109 | 4,109 | 4,406 | 7,178 | 49,500 | ||
| [난소암(PR) 2차 치료제 글로벌 임상 3상 개요] |
| 구분 | 내용 |
|---|---|
| 임상시험 대상국가 | 미국 |
| 임상시험의 목적 | 임상시험의 주요 목표는 백금계항암제 저항성(Platinum-resistant)이 있는 난소암(Platinum-resistant epithelial Ovarian Cancer) 피험자를 대상으로 리보세라닙과 아필리아 투여시 안전성과 유효성을 확인하기 위함 |
| 임상시험 시행 방법 | 시험 대상자 수: 백금계항암제 저항성이 있는 난소암 환자 약 330명 아필리아와 리보세라닙를 투여받은 환자를 관찰하며 안전성과 유효성을 평가함 임상연구기간 : 전체 약 3년 (환자의 모집 상황 또는 투여기간 등에 따라 변동 가능) |
| 기대효과 | - 난소암의 진행은 혈관 형성과 밀접한 관계가 있는 것으로 알려져 있으며, 이러한 신생혈관은 VEGF와 VEGFR2에 의해 진행됨. - 리보세라닙은 신생혈관을 억제하는 표적항암제로 신생혈관의 주요한 표적인 VEGFR2를 타겟으로 하기 때문에 난소암의 치료에 효과적일 것으로 기대되고, 아필리아는 파클리탁셀(paclitaxel) 성분의 세포독성항암제로 난소암에 대해서 효과적임을 증명되었음. 이러한 두 제품의 병용요법은 난소암 치료에 더욱 효과적일 것으로 기대됨. |
| 임상비용 산정근거 | American Medical Association의 조사에 따르면, 항암제 임상3상에 소요 되는 비용은 최소 31백만USD~59백만USD로 알려져 있습니다. 실제 당사 과거 임상(GC3, ACC)에 투입된 비용을 분석한 결과, 환자 1인당 약 115천USD(한화 약150백만원)가 소요 되었습니다. 이를 근거로 향후 진행될 임상 비용을 산정하였으나 거시경제상황변화(물가상승, 환율), 임상프로토콜 수정 등에 의해 변동 가능성 또한 존재합니다. |
| 임상 시험 기관 | 미국: GOG(gynecologic oncology group)과 협력하여 선정 예정 (임상시험기관들과 논의후 추가 및 변경 가능) |
7) 교모세포종 1차 치료제 GBM(ITI-1000) 3상 임상
| (단위: 백만원) |
| 파이프라인 | 구분 | 구성 | 2023년 | 2024년 | 2025년 | 총금액 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1Q | 2Q | 3Q | 4Q | 1Q | 2Q | 3Q | 4Q | 1Q | 2Q | 3Q | 4Q | ||||
| 교모세포종 1차 치료제 GBM(ITI-1000) |
임상비용 | CRO Opration | 2,650 | 2,650 | - | - | 1,590 | - | 1,590 | - | 1,060 | - | 1,060 | - | 10,600 |
| 임상비용 | 임상 사이트 관리(환자 검사비 등) | - | 3,313 | - | 3,313 | - | 1,988 | - | 1,988 | - | 1,325 | - | 1,325 | 13,250 | |
| 데이터분석 | 통계 분석 비용 | 1,325 | - | - | - | - | - | 398 | 398 | - | - | 265 | 265 | 2,650 | |
| 임상약 생산/유통 | 제조/유통 | 2,385 | 2,385 | 1,590 | 1,590 | 1,193 | 1,193 | 1,193 | 1,193 | 795 | 795 | 795 | 795 | 15,900 | |
| 임상, NDA 컨설팅 등 | 컨설팅 | 663 | 663 | - | - | - | - | 636 | 159 | - | - | 424 | 106 | 2,650 | |
| 기타 판관비 | 내부 운영비(출장, KOL 섭외, 인력보강 등) | 994 | 994 | 994 | 994 | 596 | 596 | 596 | 596 | 398 | 398 | 398 | 398 | 7,950 | |
| 합계 | 8,016 | 10,004 | 2,584 | 5,896 | 3,379 | 3,776 | 4,412 | 4,333 | 2,253 | 2,518 | 2,942 | 2,889 | 53,000 | ||
| [교모세포종 1차 치료제 글로벌 임상 3상 개요] |
| 구분 | 내용 |
|---|---|
| 임상시험 대상국가 | 미국 |
| 임상시험의 목적 | 임상시험의 주요 목표는 교모세포종(Glioblastoma, GBM) 피험자를 대상으로 대조군과 비교하여 ITI-1000의 안전성과 유효성을 확인하기 위함 |
| 임상시험 시행 방법 | 시험 대상자 수: 교모세포종 환자 약 270명 ~ 600명 무작위(randomized), 위약 대조로 진행되며, ITI-1000과 위약을 투여하여 전체생존기간(OS)를 평가함 임상연구기간 : 전체 약 4.5년 (환자의 등록 상황 또는 투여기간 등에 따라 변동 가능) |
| 기대효과 | 교모세포종은 많은 환자에서 거대세포바이러스(Cytomegalovirus, CMV)가 발견되고 있기 때문에 좋은 타겟이 될 수 있음. ITI-1000은 CMV의 항원을 UNITE 플랫폼인 리소좀관련막단백질(LAMP)에 발현시켜 환자의 면역세포를 빠르고 효율적으로 활성화시키는 기전을 가지고 있기 때문에 교모세포종 치료에 효과적일 것으로 기대됨. 교모세포종은 현재 세포독성항암제인 테모달 외에는 치료제가 없기 때문에 ITI-1000이 신약 승인되면 최초의 바이오신약이 될 것으로 기대됨 |
| 임상비용 산정근거 | American Medical Association의 조사에 따르면, 항암제 임상3상에 소요 되는 비용은 최소 31백만USD~59백만USD로 알려져 있습니다. 환자 맞춤형 치료제의 특성상 환자별로 제조를 실시하여야 하기 때문에 일반적인 항암제에 비해 제조비용이 증가됩니다. 이를 근거로 향후 진행될 임상 비용을 산정하였으나 거시경제상황변화(물가상승, 환율), 임상프로토콜 수정 등에 의해 변동 가능성 또한 존재합니다. |
| 임상 시험 기관 | 미국: University of Florida, Duke University Medical Center 등 (임상시험기관들과 논의후 추가 및 변경 가능) |
상기 임상/NDA 진행 계획 및 자금 소요 예상 시기 등은 확정된 바가 아닌 당사의 목표이며, 당사의 의도와 관계 없이 예상치 못한 변수에 의해 변경되거나 취소될 가능성이 상존합니다. 상기 예정 사항이 불가피하게 변경 또는 취소되는 상황이 발생하는경우, 당사는 즉시 해당 내용에 대하여 공시를 통해 소명할 예정입니다.
당사는 현재까지 미화 약 4억 2,577만 달러를 Elevar에, 미화 약 5,643만 달러를 Immunomic에 출자했습니다. 당사는 종속기업 지분 취득과 관련한 영업권 손상검토를 위해 매년 3분기말 외부회계법인을 통해 영업권 손상검토를 진행하고 있습니다. 이에따라 출자시 주식가치산정은 납입 이전 가장 최근 영업권손상검토보고서에 기재된 수치를 사용하고 있습니다.
다만, 당사의 지속적인 출자에도 불구하고 Elevar와 Immunomic는 바이오연구개발기업의 특성상 유의미한 매출이 발생하고 있지 않으며, 연구개발비 및 판관비로 인한 자금지출이 지속적으로 이루어지고 있습니다. 특히, Elevar는 2021년 말 재무제표를 기준으로 전액자본잠식 상태이며 업종의 특수성을 고려하였을 때, 유의미한 연구개발결과가 나와 신약개발 매출로 이어지지 않는다면추가적인 재무구조 악화 및 자본잠식이 지속될 가능성이 높다고 판단됩니다.
당사가 금번 유상증자를 통해 조달하는 자금 중 Elevar 증권취득 목적으로 약 2,297억원(미화 약 1억 7,635만 달러), Immunomic 증권취득 목적으로 약 530억원(미화 약 4,609만달러)를 출자할 계획이며, 해당 출자에 따라 종속회사의 재무현황 개선이 기대됩니다. 다만, 해당 출자는 종속회사의 임상시험 일정에 따라 증자 납입 직후부터 2025년까지 상대적으로 길게 분포되어 있으며, 해당 출자에도 불구하고 연구개발비 증가 및 수익 발생 지연이 지속되는 경우 추가적인 재무구조 악화의 우려가 있습니다. 투자자분들께서는 당사의 종속기업인 Elevar와 Immunomic의 이익 미실현 및 악화된 재무구조에 대해 인식하시고, 양 사의 연구개발 활동 지속을 위해서는 당사의 지속적인 출자가 필요하다는 점에 유의하시기 바랍니다. Elevar 및 Immunomic의 요약재무상태표는 아래와 같습니다.
| [Elevar 요약재무상태표] | |
| (US GAAP) |
(단위: 천USD, %) |
| 결산연월 또는 결산기간 | 2021년 | 2020년 |
|---|---|---|
| 1. 자산총계 | 42,559 | 41,216 |
| - 유동자산 | 21,767 | 20,383 |
| 2. 부채총계 | 55,254 | 39,265 |
| - 유동부채 | 36,860 | 20,968 |
| 3. 자본총계 | (12,695) | 1,951 |
| 4. 부채비율 (%) | -435.2% | 2,012.6% |
| 5. 유동비율 (%) | 59.1% | 97.2% |
| 6. 영업손익 | (56,011) | (31,317) |
| 기타 손익 | 825 | 536 |
| 7. 당기순이익 | (55,186) | (30,781) |
| 8. 자본금 | 272,039 | 235,498 |
| 9. 영업활동 현금흐름 | (32,926) | (35,882) |
| 10. 투자활동 현금흐름 | 652 | (20,202) |
| 11. 재무활동 현금흐름 | 4,267 | (6,084) |
| 12. 현금 및 현금성자산 기말 잔고 | 19,644 | 15,377 |
| 자료 : | Elevar Therapeutics, Inc 감사보고서(KPMG LA) |
| 주1) Elevar는 외부감사 의무대상이 아니며, 회사 자체적으로 회계법인에 의뢰해 2020년 및 2021년 외부감사를 받았습니다. | |
| [Immunomic 요약재무상태표] | |
| (K-IFRS) | (단위: 천USD, %) |
| 결산연월 또는 결산기간 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|
| 1. 자산총계 | 47,519 | 67,220 | 21,005 |
| - 유동자산 | 31,331 | 47,546 | 12,825 |
| 2. 부채총계 | 13,080 | 11,933 | 15,515 |
| - 유동부채 | 5,065 | 3,773 | 3,556 |
| 3. 자본총계 | 34,439 | 55,287 | 5,490 |
| 4. 부채비율 (%) | 38.0% | 21.6% | 282.6% |
| 5. 유동비율 (%) | 618.5% | 1,260.2% | 360.6% |
| 6. 영업손익 | 2,028 | 27 | 12,006 |
| 기타 손익 | (300) | (78) | 223 |
| 금융 손익 | (499) | (395) | (620) |
| 7. 당기순이익 | (23,210) | (10,699) | (5,107) |
| 8. 자본금 | 3 | 3 | 1 |
| 9. 영업활동 현금흐름 | (18,644) | (15,754) | (6,308) |
| 10. 투자활동 현금흐름 | (4,459) | (2,854) | (413) |
| 11. 재무활동 현금흐름 | (10) | 53,002 | (363) |
| 12. 현금 및 현금성자산 기말 잔고 | 23,484 | 46,597 | 12,204 |
| 자료 : | Immunomic Therapeutics, Inc 감사보고서(삼일회계법인) |
| 주1) Immunomic은 외부감사 의무대상이 아니며, 회사 자체적으로 회계법인에 의뢰해 2021년 기준 최근 3개년 외부감사를 받았습니다. | |
당사가 금번 유상증자를 통해 조달하는 타법인(Elevar, Immunomic) 증권취득 목적 자금 약 2,827억원(미화 약 2억 1,704만 달러)의 사용 예정 시기는 증자 납입 직후부터 2025년까지 상대적으로 길게 분포되어 있습니다. (Elevar에 대한 당사의 세부 출자 계획은 본 증권신고서 "제1부 - III. 투자위험요소 - 2. 회사위험 - 가."를 참고하시기 바랍니다.) 이는 상기에 기재하였듯이 당사와 Elevar, Immunomic이 영위하는 사업의 특성상 자금 소요 시기를 확정적으로 예상하는 데 무리가 있기 때문입니다. 임상, NDA 및 상업화의 경우 연구 및 협상의 진행상황에 따라 당사가 본 증권신고서에기재한 일정보다 이르거나 늦게 진행될 가능성이 상존합니다.
(2) 시설자금 - 헬스케어 사업부 둔곡 제2공장 설립
㈜에프에이는 2008년 5월에 설립되어 알코올 스왑 등 손소독제, 소독티슈 등을 생산하던 회사였으나 코로나의 등장과 확산으로 인하여 진단키트 수요가 폭발적으로 증가함에 따라 매출이 증가한 회사입니다. 당사는 인수 및 합병 이후 동사(現 헬스케어사업부)를 체외진단분야의 전문 기업으로 육성하여 해외의 신규시장으로의 진입을 시도할 것이며, 코로나 외 다른 분야로 사업을 확장시킬 목적을 가지고 있습니다. 당사는 기존 ㈜에프에이가 2020년 10월 매매계약을 체결했던 유성구 구룡동 대덕R&D특구에 위치한 연구시설용지에 둔곡 제2공장을 설립하여 기존 생산설비 이전, 기업부설 연구소 이전 및 확장으로 품질관리와 함께 연구,개발(R&D)의 체계를 구축할 계획입니다.
| [둔곡 제2공장 부지] |
|
| [자금의 세부 사용 계획] |
| (단위 : 백만원) |
| 구분 | 내용 | 세부내역 | 금액 | |
|---|---|---|---|---|
| 신규시설투자 | 건설공사 | 건축, 토목, 기계설비, 전기설비, 통신설비, 소방설비 | 둔곡 제2공장 설립 | 20,700 |
| 생산시설 | 연구시설 설비투자 | 연구시설 | 8,680 | |
| 세금 및 제비용 | 신규 설립을 위한 세금 및 인허가 제비용 | 건축, 토목 등 전분야 | 720 | |
| 합계 | 30,010 | |||
헬스케어사업부(舊 ㈜에프에이)는 2020년 10월 13일 한국토지주택공사와 대전광역시 유성구 구룡동 대덕R&D특구에 위치한 연구시설용지 총 12,196㎡ 를 56.65억원에 분양계약을 체결하여, 2021년 10월 29일 중도금 및 잔금 납부를 완료하였습니다.이후 연구소 이전 및 제품 라인업 강화의 전략적 검토 등으로 신규공장 건립이 지연됐으나, 2공장(둔곡) 신축을 위해 '22. 7월부터 공장 신축을 위한 기초 정보 수집(설비 및 시설 정보) 및 설계, 컨설팅 등 단계별 진행중에 있으며, 2023년 1월 설계 계약을 시작 으로 2023년 6월 착공을 진행하여 최종 2024년 6월 공장 준공 및 설비 가동 셋팅 완료를 목표로 하고 있습니다.
(3) 운영자금
| [운영자금 상세 사용 목적] |
| (단위: 백만원) |
| 사업명 | 사용시기 | 합계 | |
|---|---|---|---|
| 2023년 상반기 | 2023년 하반기 | ||
| 판매비와관리비 | 4,105 | 4,405 | 8,210 |
금번 유상증자를 통한 공모 자금 중 약 8,210백만원은 당사 ENG 사업부의 운영자금으로 활용할 예정입니다. 당사의 별도기준 판매비와 관리비는 2019년 8,010백만원, 2020년 19,462백만원, 2021년 23,623백만원 등으로 매출액의 48.5%~79.3%를 차지하며, 2023년 판매비와관리비에 금번 유상증자 대금 중 일부를 활용할 계획입니다. 또한, 사용일까지는 특정금전신탁, MMDA 등 금융기관의 단기금융상품으로 운용할 예정입니다.
| [영업비용 세부 내역] | |
| (별도기준) | (단위: 백만원) |
| 구분 | 2022년 반기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
| 급 여 | 2,378 | 4,410 | 3,967 | 2,801 |
| 퇴직급여 | 189 | 534 | 325 | 137 |
| 복리후생비 | 424 | 585 | 620 | 452 |
| 여비교통비 | 114 | 167 | 173 | 368 |
| 접대비 | 166 | 291 | 270 | 169 |
| 통신비 | 16 | 30 | 34 | 32 |
| 전력비 | 23 | 64 | 139 | 122 |
| 세금과공과금 | 132 | 203 | 180 | 151 |
| 감가상각비 | 602 | 1,097 | 989 | 598 |
| 지급임차료 | 235 | 437 | 159 | 99 |
| 보험료 | 105 | 294 | 177 | 62 |
| 차량유지비 | 55 | 103 | 74 | 32 |
| 경상연구개발비 | 279 | 244 | 285 | 233 |
| 소모품비 | 10 | 32 | 50 | 50 |
| 지급수수료 | 154 | 123 | 186 | 85 |
| 광고선전비 | 2,136 | 6,639 | 3,969 | 1,831 |
| 건물관리비 | 51 | 150 | 265 | 273 |
| 대손상각비 | 3 | 0 | 36 | 9 |
| 무형자산상각비 | 23 | 723 | 0 | 3 |
| 주식보상비 | 5,816 | 7,273 | 7,263 | 17 |
| 판매보증비(환입) | (21) | 78 | (66) | 37 |
| 기타 | 293 | 146 | 368 | 448 |
| 합 계 | 13,185 | 23,623 | 19,462 | 8,010 |
(4) 채무상환자금
당사는 기업은행 시화중앙지점으로부터 320백만원을 차입하여 사용하고 있으며, 8월 말 중 기업은행으로부터 울산광역시 울주군에 위치한 ENG사업부 공장부지 입찰에 필요한 대금 4,360백만원을 기업은행으로부터 차입했습니다. 당사는 금번 유상증자로 조달하는 금액 중 4,680백만원을 동 대출금의 상환에 사용하여 재무건전성을 제고할 계획입니다.
| [상환예정 차입금 현황] |
| (단위: 백만원) |
| 은행 | 대출과목 | 차입금액 | 이자율 | 만기일 | 내용 |
|---|---|---|---|---|---|
| 기업 | 시설자금 | 360 | 4.24% |
2023.04.30 |
ENG사업부 공장부지 매입을 위한 단기 차입금 상환 |
| 4,000 | 4.04% | 2023.04.30 | |||
| 기업 | 시설자금 | 320 | 1.5% | 2031.06.15 | 기존 차입금 상환 |
| 계 | 4,680 | - | - | - | |
당사는 금번 유상증자를 통하여 조달하는 자금을 본 증권신고서에 기재한 사용목적대로 사용하기 위해 최선의 노력을 다하고 있으며, 매 분기별 공시하는 당사의 정기보고서에 공모자금의 실제 사용내역 및 변동상황에 관하여 성실하게 공시할 예정입니다. 또한 자금의 조달 이후 실제 사용 시기까지 동 자금은 신용등급이 우량한 국내 적격금융기관의 수시입출금 예금, 정기예금, MMF 및 MMDA 등 안정성과 환금성을확보할 수 있는 금융상품에 예치할 계획입니다.
당사는 과거 공모자금을 증권신고서에 기재된 내용과 상이하게 사용한 이력이 있습니다. 상이하게 사용한 이력에 대한 자세한 내역 및 사유는 동 증권신고서 <III. 투자위험요소 - 2. 회사위험 - 바.>를 참조 부탁드리며 투자자분들께서는 이점에 유의해주시기 바랍니다.
VI. 그 밖에 투자자보호를 위해 필요한 사항
해당사항 없습니다.
제2부 발행인에 관한 사항
I. 회사의 개요
1. 회사의 개요
HLB와 Elevar와 Immunomic은 다양한 신약개발(항암제, 면역치료제 등) 및 임상시험의 경험을 보유하고 있는 글로벌 바이오 의약품 전문회사입니다.
동사의 HLB 헬스케어사업부는 체외진단의료기기 등을 제조, 판매하는 체외진단 의료기기 및 의약외품을 제조하는 사업부이며, HLB ENG사업부는 LifeBoat & Davit, 특수선박 및 GRP/ GRE PIPE를 제조, 판매합니다.
앞으로도 HLB는 지속적인 혁신과 끊임없는 도전을 통하여 인류의 건강과 보다 안전한 미래를 책임지고 이끌어 나갈 계획입니다.
가. 연결대상 종속회사 현황(요약)
| (단위 : 사) |
| 구분 | 연결대상회사수 | 주요 종속회사수 |
|||
|---|---|---|---|---|---|
| 기초 | 증가 | 감소 | 기말 | ||
| 상장 | - | - | - | - | - |
| 비상장 | 6 | 1 | 3 | 4 | - |
| 합계 | 6 | 1 | 3 | 4 | - |
* 연결대상회사의 변동내용
| 구 분 | 자회사 | 사 유 |
|---|---|---|
| 신규 연결 |
Hyundai Lifeboats Shanghai Co.,Ltd | 당기 중 지분 취득 |
| - | - | |
| 연결 제외 |
㈜에프에이 | 당기 중 흡수합병 후 소멸 |
| ㈜화진메디칼 | 당기 중 양도 | |
| ㈜화진메디스 | 당기 중 양도 |
(*) 2022년 4월 29일, 이사회의 결정으로 그룹내 의료기기 사업 전문성 강화를 목적으로 종속회사인 ㈜화진메디스와 ㈜화진메디칼의 각각의 지분 100%를 에이치엘비테라퓨틱스㈜에 33억에 양도하여 종속회사에서 제외되었습니다.
나. 중소기업 등 해당 여부
| 중소기업 해당 여부 | 해당 | |
| 벤처기업 해당 여부 | 미해당 | |
| 중견기업 해당 여부 | 미해당 | |
다. 회사의 주권상장(또는 등록ㆍ지정)여부 및 특례상장에 관한 사항
| 주권상장 (또는 등록ㆍ지정)여부 |
주권상장 (또는 등록ㆍ지정)일자 |
특례상장 등 여부 |
특례상장 등 적용법규 |
|---|---|---|---|
| 코스닥시장 | 1996년 07월 27일 | 해당사항없음 | 해당사항없음 |
라. 회사의 법적ㆍ상업적 명칭
당사의 명칭은 "에이치엘비 주식회사"라고 표기합니다. 또한, 영문으로는 "HLB Co., LTD."라고 표기합니다.
마. 설립일자
당사는 1985년 10월 18일에 설립되었으며, 1996년 07월 27일자로 코스닥시장에 상장된 후 현재까지 상장을 유지하고 있습니다.
바. 본사의 주소, 전화번호, 홈페이지 주소
| 본사주소 | 울산광역시 울주군 온산읍 당월로 216-53 |
| 전화번호 | 02-3453-4414 |
| 홈페이지 | http://www.hlbkorea.com |
사. 주요사업의 내용
당사는 체외진단의료기기 등을 제조, 판매하는 체외진단 의료기기 및 의약외품을 제조와 합성수지선 건조업을 주요사업으로 영위하고 있으며, 체외진단 의료기기 및 의약외품, 구명정, GRP/GRE Pipe 등을 영업활동의 주요제품으로 하고 있습니다.
기타 주요사업에 대한 자세한 내용과 연결대상 종속회사가 영위하는 사업의 내용은
"Ⅱ.사업의 내용"을 참조하시기 바랍니다.
아. 신용평가에 관한 사항
| 평가일 | 결산일 | 평가회사 (신용평가등급범위) |
신용등급 | 등급내용 |
| 2022-04-08 | 2021-12-31 | 한국기업데이터 (AAA ~ D) | B+ | 보통 |
| 2021-04-09 | 2020-12-31 | 한국기업데이터 (AAA ~ D) | B+ | 보통 |
| 2020-04-10 | 2019-12-31 | 한국기업데이터 (AAA ~ D) | B+ | 보통 |
2. 회사의 연혁
가. 주요연혁
(지배회사의 주요 연혁)
| 회사명 | 연월 | 회사의 연혁 |
| 에이치엘비㈜ | 1985. 10. | 국제스텐레스밸브공업㈜ 설립 |
| 1990. 03. | 국제정공㈜로 상호변경 | |
| 1994. 12. | ISO 9001 인증서 취득(94-292, Intertek) | |
| 1996. 07. | 코스닥 상장법인 등록 | |
| 1996. 08. | 일본 NKK 품질 인증서 취득(일본) | |
| 2000. 02. | 회사정리계획안 인가결정(대구지방법원) | |
| 2001. 01. | ISO 9001 인증서 재 취득(한국표준협회, QMS-0431) | |
| 2002. 03. | 회사정리계획 변경계획안 인가(대구지방법원) | |
| 2002. 05. | 정리절차 종결 | |
| 2005. 04. | 사명변경(국제정공㈜ → 라이프코드인터내셔날㈜) | |
| 2007. 12. | 사명변경(라이프코드인터내셔날㈜ → ㈜이노GDN) | |
| 2009. 03. | 사명변경(㈜이노지디엔 → 에이치엘비㈜) | |
| 2009. 12. | 에이치엘비㈜와 ㈜동아산전 합병완료 | |
| 2010. 10. | 자본감소 결정 | |
| 2011. 11. | 파주사옥 이전 | |
| 2012. 01. | 대표이사 변경(남상우 → 박정민) | |
| 2013. 01. | 에이치엘비㈜와 현대라이프보트㈜ 합병완료 | |
| 2015. 01. | 전기계장사업부 에이치엘비일렉㈜ 분할완료 | |
| 2017. 06. | 대표이사 변경(박정민 → 진양곤) | |
| 2019. 03. | 대표이사 변경(진양곤 → 각자 대표이사 김하용, 김성철) | |
| 2019. 06. | 대표이사 변경(각자 대표이사 김하용, 김성철 → 진양곤) | |
| 2019. 11. | 100% 자회사인 HLB USA, Inc. 가 LSK BioPartners, Inc. 를 삼각합병 | |
| 2020. 06. | Immunomic Therapeutics,Inc. 종속회사 편입 | |
| 2020. 09. | 리보세라닙 글로벌 특허권 권리 양수 계약 체결 | |
| 2021. 03. | 대표이사 변경(진양곤 → 각자 대표이사 진양곤, 김동건) | |
| 2021. 06. | 에이치엘비인베스트먼트㈜ 종속회사 편입 | |
| 2021. 10. | ㈜에프에이 종속회사 편입 | |
| 2022. 01. | ㈜에프에이 합병완료 | |
| 2022. 02 | Hyundai Lifeboats Shanghai Co.,Ltd 종속회사 편입 |
(주요 종속회사등의 주요 연혁)
| 회사명 | 연월 | 회사의 연혁 |
| LSK BioPartners, Inc. | 2005. 07. | Lifecord International USA, Inc. 설립 |
| 2007. 02. | 사명변경(Lifecord International USA, Inc. → LSK BioPartners, Inc.) | |
| 2007. 12. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 라이센스 취득계약 체결(중국을 제외한 세계판권 취득) | |
| 2009. 01. | 부광약품과 표적항암제 Rivoceranib(구, Apatinib Mesylate) 서브라이센스 부여계약 체결 (유럽, 일본, 한국에 대한 판권이전 계약) | |
| 2011. 11. | 미국 FDA로부터 미국/한국 다국가 임상 1상/임상 2상a 시험을 위한 IND 승인 | |
| 2012. 04. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 다국가 임상 1상 시작 | |
| 2014. 08. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 다국가 임상 1상 종료 및 2상a 시작 | |
| 2015. 08. | BTK 저해제 기술도입 | |
| 2015. 10. | 표적항암제Rivoceranib(구, Apatinib Mesylate) 다국가 임상 2상a 종료 | |
| 2016. 02. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 국내 식약처 희귀의약품 지정(위암) | |
| 2016. 07. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 글로벌 임상 3상을 위한 미국 FDA와의 End-of-Phase 2(EOP2)미팅 마무리 | |
| 2016. 11. | 사옥이전(Salt Lake City, Utah 84111, USA → South San Francisco, CA 94110, USA) | |
| 2017. 01. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 한국/일본 글로벌 임상 3상 시험계획 승인 | |
| 2017. 02. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 대만 글로벌 임상 3상 승인 | |
| 2017. 03. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 유럽 EC 희귀의약품 지정(위암) | |
| 2017. 05. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 미국 글로벌 임상 3상 개시방문 실시 | |
| 2017. 06. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 미국 FDA 희귀의약품 지정(위암) | |
| 2017. 12. | 표적항암제 Rivoceranib(구, Apatinib Mesylate)와 면역항암제 Opdivo 병행임상시험 시작 | |
| 2018. 01. | 새로운 국제공식 명칭 "리보세라닙" 등록완료 (Apatinib Mesylate → Rivoceranib) | |
| 2018. 06. | 표적항암제 Rivoceranib(구, Apatinib Mesylate)과 면역항암제 Keytruda 병행임상시험 시작 | |
| 2018. 10. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 위암 말기 치료제 임상 3상 환자등록 모집완료(총460명) | |
| 2019. 02. | 표적항암제 Rivoceranib 전체생존기간(OS) 분석에 필요한 환자수 충족으로 임상 3상 결과 통계 분석 진행 | |
| 2019. 06. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 위암 말기 치료제 임상 3상 완료 | |
| 2019. 06. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 간암 글로벌 임상 3상 첫환자 등록 | |
| 2019. 08. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 위암 글로벌 임상 3상 데이터 확정과 분석에 따른 향후 방향성 및 일정 발표 | |
| 2019. 10. | 표적항암제 Rivoceranib 글로벌 임상 3상에 대한 미국 FDA와 Pre-NDA 미팅 | |
|
2019. 09. |
위암 글로벌 3상 임상(Angel Study) 유럽종양학회(ESMO)에서 Best of ESMO 선정 |
|
| 2019. 11. | HLB USA, Inc.와 삼각합병 완료 (피합병법인으로, 삼각합병 이후 소멸) | |
| Elevar Therapeutics, Inc. |
2019. 06. | HLB USA, Inc. 설립 (삼각합병 목적 설립법인) |
| 2019. 11. | LSK BioPartners, Inc.와 삼각합병 완료 | |
| 2019. 12. | 사명변경 (HLB USA, Inc. → Elevar Therapeutics, Inc.) | |
| 2020. 03. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 선양낭성암종 글로벌 임상 3상 첫환자 등록 | |
| 2020. 04. | 비베스토(Vivesto, 舊 Oasmia)로부터 세포독성항암제 "Apealea"에 대한 일부 국가를 제외한 글로벌 권리 양수 | |
| 2020. 07. | Tanner社와 "Apealea"에 대한 NPP(Named Patient Program) 파트너십 체결 | |
| 2020. 10. | Taiba社와 "Apealea"에 대한 MENA지역 파트너십 체결 | |
| 2020. 12. | Inceptua社와 "Apealea"에 대한 EU 및 UK 지역 파트너십 체결 | |
| 2021. 02. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 미국 FDA 희귀의약품 지정(선양낭성암종) | |
| 2021. 11. | 표적항암제 Rivoceranib(구, Apatinib Mesylate) 미국 FDA 희귀의약품 지정(간암) | |
|
2022. 06. |
표적항암제 Rivoceranib(구, Apatinib Mesylate) 선양낭성암종 글로벌 임상 2상 결과 발표 (ASCO) |
|
| Immunomic Therapeutics, Inc. |
2006. 09. | Johns Hopkins Univ.와 LAMP 기술에 대한 전세계 독점 라이선스 권리 취득 |
| 2006. 10. | Geron Corp.에 Sub-Licensed 부여 | |
| 2006. 12. | Nature Tech.와 cross-license vaccine technologies 기술 공유 합의 | |
| 2009. 12. | AML 연구의 GRNVAC1 결과가 Phase I / II endpoint 충족결과 발표 | |
| 2010. 03. | 2010 Frost & Sullivan Award - 백신분야에서 올해의 생명공학혁신상 수상 | |
| 2011. 12. | 동물 제약 분야 및 다수의 백신 라이선스 적용을 위해 대규모 제약회사와 공동 연구 및 라이센스 계약 체결 | |
| 2012. 04. | FDA로부터 Jananese Red cedar immunotherapeutic vaccine 1상 임상 연구 승인 | |
| 2012. 09. | LAMP-vax IP “키메라 백신” 특허에 대한 EU 특허 승인. JRC-LAMP-vax의 임상 연구 1상 착수 | |
| 2012. 12. | LAMP-vax IP “키메라 백신” 특허 미국내 승인 | |
| 2013. 03. | JRC-LAMP-vax에 대한 IA 단계 실험 성공적 완료 | |
| 2014. 09. | 다양한 땅콩 알레르기에 대한 SBIR Grant 수상 | |
| 2015. 10. | Astellas Pharma.와 알레르기 예방 및 치료를 위한 LAMP-VAX Platform관련 글로벌 라이센스 계약 체결 | |
| 2017. 05. | Phase II Cancer Immunotherapy Technology의 독점 라이센스 발표 | |
| 2018. 06. | LAMP-vax 플랫폼을 UNITE(UNiversal Intracellular Targeted Expression 범용세포내 표적발현)로 변경 | |
| 2019. 03. | JRC2-LAMP-vax에 대해 Astellas 사로부터 5백만불의 Milestone 수령 | |
| 2020. 06. | 에이치엘비㈜의 종속회사로 편입 | |
| 2020. 11. | ITI-1000(교모세포종 치료를 위한 면역항암제) 생산을 위한 CoImmune사와 파트너십 체결 | |
| 2021. 04. | Lineage Cell Therapeutics 사와 면역항암제 라이선스 계약 체결 | |
| 2021. 12. | 일본 적삼나무(Japanese Red Cedar) 알레르기 백신의 개발 및 상용화를 위해 IDRI (Infectious Disease Research Institute)와 RNA 백신 플랫폼의 지적재산권에 대한 전세계 독점 라이선스 계약 체결 |
|
| 2022. 06. | Drew Pardoll 연구소(JHU)와 activin antibody 특허 자산(및 개선사항) 관련 라이선스 계약 체결 | |
| ㈜에프에이 |
2008. 05. |
㈜에프에이 설립 |
|
2008. 10. |
의약외품 제조업 취득(식품의약품안전처) |
|
|
2008. 12. |
벤처기업등록(기술보증기금) |
|
|
2009. 07. |
ISO 13485 인증 취득(ITC 인증원) |
|
|
2010. 01. |
KFDA 의료기기제조업 및 GMP 취득(식품의약품안전처) |
|
|
2010. 04. |
기업부설 연구소 인정서 획득(한국산업기술진흥협회) |
|
|
2012. 01. |
FA SWAB CE 마크 인증(MT promedt) |
|
|
2014. 07. |
ISO 13485 인증 취득(SGS) |
|
|
2014. 11. |
우수기술대상(세종특별자치시장) |
|
|
2014. 12. |
인재 육성형 중소기업 지정(중소기업청) |
|
|
2014. 12. |
응급 의료발전 공로상(국민안전처장관) |
|
|
2015. 06. |
ISO 14001 인증취득(KSA) |
|
|
2016. 01. |
USA FDA 등록(FA Alcohol Swab, FA EOL Swab, NO-sting Swab) |
|
|
2016. 06. |
세종시 면학산업단지 본사 이전[명학 산단서로 10-5] |
|
|
2017. 03. |
FA Alcohol Swab 의료기재 허가취득(대만위생복리부) |
|
|
2017. 10. |
화장품 제조업/ 제조판매업 허가 취득(식품의약품안전처) |
|
|
2017. 12. |
교육부장관 표창장 수상 |
|
|
2018. 03. |
동물용 의약품 제조업 허가 취득(농림축산 검역본부) |
|
|
2018. 04. |
ISO 22716 인증 취득(BV) |
|
|
2018. 06. |
세종특별자치시 스타기업 선정 |
|
|
2018. 12. |
세종시 사회 공헌부분 표창 수상 |
|
|
2019. 10. |
본사확장 (R&D Center 증설) |
|
|
2020. 06. |
체외진단 의료기기 제조업 허가 취득(식품의약품안전처) |
|
|
2020. 06. |
체외진단 의료기기(검체채취스왑/수송배지) FDA 등록 |
|
|
2020. 06. |
체외진단 의료기기 CE 등록 |
|
|
2020. 11. |
법무부장관 표창장 수상 |
|
|
2020. 12. |
국무총리 표창장 수상 |
|
|
2021. 07. |
글로벌 공급 업체상 수상[Abbott / 2020 GLOBAL PROCUREMENT SUPPLIER AWARD] |
|
|
2021. 10. |
산업통상부장관 표창장 수상 |
|
| 2021. 10. | 에이치엘비㈜의 종속회사로 편입 | |
| 2022. 01. | 에이치엘비㈜에 합병완료(피합병법인으로, 합병 이후 소멸) |
나. 회사의 본점소재지 및 그 변경
| 연월 | 변경내역 |
| 2005. 05. | 대구 동구 신천동 → 대구 북구 산격동 |
| 2008. 01. | 대구 북구 산격동 → 서울 강남구 논현동 |
| 2008. 12. | 서울 강남구 논현동 → 서울 구로구 구로동 |
| 2009. 03. | 서울 구로구 구로동 → 울산 울주군 온산읍 |
다. 경영진 및 감사의 중요한 변동
| 변동일자 | 주총종류 | 선임 | 임기만료 또는 해임 |
|
|---|---|---|---|---|
| 신규 | 재선임 | |||
| 2019년 03월 27일 | - | 대표이사 김성철 대표이사 김하용(*1) |
- | - |
| 2019년 06월 10일 | - | 대표이사 진양곤(*2) | - | - |
| 2020년 03월 30일 | 정기주총 | 사내이사 전복환 사내이사 도순기 사내이사 안기홍 사내이사 문정환 사내이사 Matthew Chang 사내이사 William G.Hearl 사외이사 심재철 |
사내이사 진양곤 사외이사 박진국 상근감사 김용웅 |
사외이사 김성제 |
| 2020년 03월 30일 | - | - | 대표이사 진양곤 | - |
| 2021년 03월 30일 | 정기주총 | 사내이사 김동건 | - | - |
| 2021년 03월 30일 | - | 대표이사 김동건(*3) | - | - |
| 2022년 03월 30일 | 정기주총 | 사내이사 황제이정환 | 사외이사 최규준 | - |
※ 당사의 대표이사는 이사회를 통하여 선임 또는 해임합니다.
(*1) 2019년 3월 27일, 대표이사 진양곤은 일신상의 사유로 사임하였으며, 동일 개최한 이사회에서 사내이사 김성철, 김하용을 각자대표로 신규선임하였습니다.
(*2) 2019년 6월 10일, 각자 대표이사 김성철, 김하용은 일신상의 사유로 사임하였으며, 동일 개최한 이사회에서 사내이사 진양곤을 대표이사로 신규선임하였습니다.
(*3) 2021년 3월 30일, 이사회에서 사내이사 김동건을 각자대표로 신규선임하였습니다.
라. 회사가 합병등을 한 경우 그 내용
| 연월 | 내용 |
| 2013. 01. | 현대라이프보트㈜와 합병완료 |
| 2015. 01. | 전기계장사업부문 에이치엘비일렉㈜ 분할완료 |
| 2015. 02. | LSK BioPartners, Inc. 자산(주식)양수완료 |
| 2018. 03. | 라이프리버㈜ 자산(주식)양도완료 |
| 2019. 11. | LSK BioPartners, Inc.와 삼각합병 완료 |
| 2022. 01. | ㈜에프에이와 합병완료 |
마. 회사의 업종 또는 주된 사업의 변화
- 2018년 02월, 의료기기사업부를 신설하여 의료기기 유통업을 신규사업으로 추가하였습니다.
- 2020년 12월말, 의료기기사업부 폐지로 당사에서의 의료기기 유통업은 중단되었습니다
- 2022년 1월, HLB헬스케어 사업부를 신설하여 체외진단의료기기 등을 제조, 판매하는 체외진단 의료기기 및 의약외품 제조 사업을 추가하였습니다.
바. 그 밖에 경영활동과 관련된 중요한 사항의 발생내용
- 2020년 1월, 당사는 신규 Pipeline 확보를 위해 미국 면역치료플랫폼 바이오의약품연구개발기업인 Immunomic Therapeutics, Inc.("ITI")의 지분 2백만주를 미화 1천만불에 최초 취득하였고, 2020년 4월 지분 6백만주를 미화 3천만불, 2020년 12월 지분3,285,646주를 미화 약1.6천만불에 추가 취득하였습니다. 당사는 ITI의 Pipeline을통하여 기존 Pipeline인 Rivoceranib 성분 항암 신약 외에 각종 종양 및 알레르기에 대한 면역치료제 사업에 진출할 계획입니다.
- 2020년 3월, Elevar는 스웨덴 바이오기업 비베스토(Vivesto, 舊 Oasmia)로부터 세포독성항암제인 파클리탁셀(Paclitaxel) 성분의 3세대 개량신약 항암제 "아필리아(Apealea)"에 대한 러시아, 북유럽과 동유럽 일부 국가를 제외한 글로벌 권리를 양수하였습니다. 아필리아는 2020년 1월 유럽에서 난소암 치료제로 공식 시판허가를 받은 약물로, 최근 유럽 다수 국가에 보험 급여 산정 절차가 진행되고 있으나, 2019년부터 발생된 코로나의 영향으로 전체적인 일정이 지연되고 있는 상황입니다. 각 대륙의 개별국 승인 이후 첫 판매 개시는 2022년 하반기로 예상됩니다.
- 2020년 9월, Advenchen Laboratories Nanjing, Ltd.과 SFFT Developing Co, Ltd.와 자산양수도계약을 체결하고 양도인이 보유하고 있는 YN968D1(글로벌은 리보세라닙(Rivoceranib), 중국은 아파티닙(Apatinib)으로 명명)의 글로벌 특허권을 거래금액 4,200만불에 양수하기로 하였습니다. 해당 양수대금은 2020년 12월 4일에 지급하였습니다. 본 자산양수도로 리보세라닙의 글로벌 로열티 수령을 통한 장기적이고 안정적인 캐시플로우 및 영업이익을 확보하고, 항서제약과의 긴밀한 협력관계를 통하여 현재 진행중인 NDA와 리보세라닙의 추가 적응증 임상시험에 속도가 날 것으로 전망합니다.
- 2020년 12월, 리보세라닙 양도인인 Advenchen Laboratories Nanjing, Ltd.와 SFFT Developing Co., Ltd.는 당사의 제3자배정 유상증자에 참여, 당사 주식 295,950주를 취득하였습니다.
- 2021년 2월, 이사회 결의를 통하여 52,972,429주(보통주 52,968,898주, 우선주 3,531주)를 발행하는 무상증자를 결정하였으며, 2021년 4월 무상증자 신주를 상장하였습니다.
- 2021년 3월, 기업가치 극대화를 위해 미국 CAR-T(키메라 항원 수용체 T세포) 치료제 개발사인 "Verismo Therapeutics,Inc."의 보통주 1,912,777주를 5백만불에 취득하기로 결정하였으며, 2021년 4월 지분을 취득하였습니다.
- 2021년 5월, 바이오와 헬스케어 등의 분야의 신기술사업자에 대한 투자 및 융자 등신기술사업 금융업을 통한 기업가치 극대화를 위해 에이치엘비인베스트먼트㈜의 보통주 600,000주를 30억원에 취득하였으며, 2021년 11월, 보통주 1,400,000주를 70억원에 추가 취득하였습니다.
- 2021년 10월, 안정적인 재무수익 창출 및 향후 예정된 바이오 사업과의 시너지 극대화를 위해 ㈜에프에이의 최대주주 등으로부터 보통주 28,000주를 101,920백만원(현금 44,920백만원, 제34회차 신주인수권부사채 57,000백만원)에 취득하였습니다.
- 2021년 12월, 신규사업 진출 및 기존사업과의 시너지 극대화를 위해 ㈜노터스 최대주주 등으로부터 2022년 3월 30일에 보통주 1,405,648주를 약 562억원(현금 약310억원, 신주인수권부사채 252억원)에 취득하는 주식매매계약을 체결하였습니다.
- 2022년 1월, 2022년 1월 1일을 합병기일로 하여 100% 종속기업인 ㈜에프에이를 1:0의 합병비율로 흡수합병하였습니다.
- 2022년 2월, 이사회 결정으로 리보세라닙 중국 로열티 수령 및 향후 중국사업진출을 위해 약 1.1백만불을 지급하여 "Hyundai Lifeboats Shanghai Co.,Ltd" 의 지분 100%를 취득하였습니다.
- 2022년 4월, 이사회의 결정으로 그룹내 의료기기 사업 전문성 강화를 목적으로 종속회사인 ㈜화진메디스와 ㈜화진메디칼의 각각의 지분 100%를 에이치엘비테라퓨틱스㈜에 33억원에 양도하였습니다.
3. 자본금 변동사항
자본금 변동추이
| (단위 : 천원, 주) |
| 종류 | 구분 | 당반기말 | 37기 (2021년말) |
36기 (2020년말) |
35기 (2019년말) |
34기 (2018년말) |
|---|---|---|---|---|---|---|
| 보통주 | 발행주식총수 | 106,882,745 | 106,610,064 | 52,979,436 | 42,738,918 | 39,171,492 |
| 액면금액 | 500 | 500 | 500 | 500 | 500 | |
| 자본금 | 53,441,373 | 53,305,032 | 26,489,718 | 21,369,459 | 19,585,746 | |
| 우선주 | 발행주식총수 | 7,188 | 7,188 | 3,657 | 3,333 | 3,333 |
| 액면금액 | 500 | 500 | 500 | 500 | 500 | |
| 자본금 | 3,594 | 3,594 | 1,829 | 1,667 | 1,667 | |
| 기타 | 발행주식총수 | - | - | - | - | - |
| 액면금액 | - | - | - | - | - | |
| 자본금 | - | - | - | - | - | |
| 합계 | 자본금 | 53,444,967 | 53,308,626 | 26,491,547 | 21,371,126 | 19,587,413 |
4. 주식의 총수 등
가. 주식의 총수 현황
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 비고 | |||
|---|---|---|---|---|---|
| 보통주 | 우선주 | 합계 | |||
| Ⅰ. 발행할 주식의 총수 | 400,000,000 | 100,000,000 | 500,000,000 | - | |
| Ⅱ. 현재까지 발행한 주식의 총수 | 270,719,295 | 4,193,303 | 274,912,598 | - | |
| Ⅲ. 현재까지 감소한 주식의 총수 | 163,815,814 | 4,186,115 | 168,001,929 | - | |
| 1. 감자 | 163,815,814 | 3,996,667 | 167,812,481 | - | |
| 2. 이익소각 | - | - | - | - | |
| 3. 상환주식의 상환 | - | - | - | - | |
| 4. 기타 | - | 189,448 | 189,448 | 보통주 전환 | |
| Ⅳ. 발행주식의 총수 (Ⅱ-Ⅲ) | 106,903,481 | 7,188 | 106,910,669 | - | |
| Ⅴ. 자기주식수 | 133,874 | 126 | 134,000 | - | |
| Ⅵ. 유통주식수 (Ⅳ-Ⅴ) | 106,769,607 | 7,062 | 106,776,669 | - | |
나. 자기주식 취득 및 처분 현황
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 주) |
| 취득방법 | 주식의 종류 | 기초수량 | 변동 수량 | 기말수량 | 비고 | ||||
|---|---|---|---|---|---|---|---|---|---|
| 취득(+) | 처분(-) | 소각(-) | |||||||
| 배당 가능 이익 범위 이내 취득 |
직접 취득 |
장내 직접 취득 |
- | - | - | - | - | - | - |
| - | - | - | - | - | - | - | |||
| 장외 직접 취득 |
- | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 공개매수 | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 소계(a) | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 신탁 계약에 의한 취득 |
수탁자 보유물량 | - | - | - | - | - | - | - | |
| - | - | - | - | - | - | - | |||
| 현물보유물량 | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 소계(b) | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 기타 취득(c) | 보통주 | 133,874 | - | - | - | 133,874 | - | ||
| 우선주 | 126 | - | - | - | 126 | - | |||
| 총 계(a+b+c) | 보통주 | 133,874 | - | - | - | 133,874 | - | ||
| 우선주 | 126 | - | - | - | 126 | - | |||
다. 종류주식(명칭) 발행현황
- 우선주 발행현황
| (단위 : 원) |
| 발행일자 | 2020년 06월 08일 | |||
| 주당 발행가액(액면가액) | - | 500 | ||
| 발행총액(발행주식수) | - | 324 | ||
| 현재 잔액(현재 주식수) | 1,933,140 | 3,657 | ||
| 주식의 내용 |
이익배당에 관한 사항 | 종류주식에 대해서는 액면금액을 기준으로 년1%이상에서 발행시에 이사회에서 정한 우선비율에 따른 금액을 현금으로 우선배당한다. | ||
| 잔여재산분배에 관한 사항 | - | |||
| 상환에 관한 사항 |
상환조건 | - | ||
| 상환방법 | - | |||
| 상환기간 | - | |||
| 주당 상환가액 | - | |||
| 1년 이내 상환 예정인 경우 |
- | |||
| 전환에 관한 사항 |
전환조건 (전환비율 변동여부 포함) |
- | ||
| 전환청구기간 | - | |||
| 전환으로 발행할 주식의 종류 |
- | |||
| 전환으로 발행할 주식수 |
- | |||
| 의결권에 관한 사항 | 의결권 없음(무의결권) | |||
| 기타 투자 판단에 참고할 사항 (주주간 약정 및 재무약정 사항 등) |
- 현재잔액은 무상증자로 인해 변동이 없습니다. - 현재주식수는 무상증자로 인하여 증가된 수량이 반영된 주식수 입니다.. |
|||
| (단위 : 원) |
| 발행일자 | 2021년 03월 16일 | |||
| 주당 발행가액(액면가액) | - | 500 | ||
| 발행총액(발행주식수) | - | 3,531 | ||
| 현재 잔액(현재 주식수) | 1,933,140 | 7,188 | ||
| 주식의 내용 |
이익배당에 관한 사항 | 종류주식에 대해서는 액면금액을 기준으로 년1%이상에서 발행시에 이사회에서 정한 우선비율에 따른 금액을 현금으로 우선배당한다. | ||
| 잔여재산분배에 관한 사항 | - | |||
| 상환에 관한 사항 |
상환조건 | - | ||
| 상환방법 | - | |||
| 상환기간 | - | |||
| 주당 상환가액 | - | |||
| 1년 이내 상환 예정인 경우 |
- | |||
| 전환에 관한 사항 |
전환조건 (전환비율 변동여부 포함) |
- | ||
| 전환청구기간 | - | |||
| 전환으로 발행할 주식의 종류 |
- | |||
| 전환으로 발행할 주식수 |
- | |||
| 의결권에 관한 사항 | 의결권 없음(무의결권) | |||
| 기타 투자 판단에 참고할 사항 (주주간 약정 및 재무약정 사항 등) |
- 현재잔액은 무상증자로 인해 변동이 없습니다. - 현재주식수는 무상증자로 인하여 증가된 수량이 반영된 주식수 입니다. |
|||
5. 정관에 관한 사항
당사의 최근 정관 개정일은 2020년 3월 30일입니다.
정관 변경 이력
| 정관변경일 | 해당주총명 | 주요변경사항 | 변경이유 |
|---|---|---|---|
| 2020년 03월 30일 | 제35기 정기주주총회 | 제2조 (목적) 목적사업 추가 제33조 (이사의 수) 이사의 수 개정 제40조 (이사회 구성) 일부조항 삭제 제40조의 1 (이사회의 의장) 신설 제40조의 2 (이사회의 소집) 신설 |
사업영역확대, 이사회 의장 제도도입을 위한 근거마련 |
| 2019년 03월 27일 | 제34기 정기주주총회 | 제8조 (주식의 발행과 종류) 일부조항 삭제 제8조의 2 (주식등의 전자등록) 신설 제10조 (신주인수권) 일부조항 개정 제11조 (일반공모증자등) 일부조항 개정 제12조 (주식매수선택권) 일부조항 개정 제14조 (주식의 소각) 일부조항 삭제 제15조 (명의개서대리인) 일부조항 개정 제16조 (주주 등의 주소, 성명 및 인감 또는 서명 등 신고) 삭제 및 문구정비 제17조 (주주명부의 폐쇄 및 기준일) 개정 및 문구정비 제18조 (전환사채의 발행) 발행한도 증액 제19조 (신주인수권부사채의 발행) 발행한도 증액 제20조 (사채발행에 관한 준용규정) 조문정비 제22조 (소집권자) 조문정비 제25조 (의장) 조문정비 제48조 (감사의 임기와 보선) 조문정비 제49조 (감사의 직무와 의무) 조문정비 제51조 (감사의 보수와 퇴직금) 조문정비 제54조 (외부감사인의 선임) 조문정비 |
전자증권제도 도입(2019년 9월 16일 시행)과 외부감사 법 개정에 따른 내용변경 및 조문정비 |
II. 사업의 내용
1. (제조서비스업)사업의 개요
연결회사는 선박, 바이오, 헬스케어 사업부문의 총 3개 사업부 체제로 운영되고 있습니다.
각 사업부문별 주요 제품은 다음과 같습니다.
|
사업부문 |
주요제품 |
|
선박 |
구명정, DAVIT, PIPE, 특수선 등 |
|
바이오 |
리보세라닙 등 항암신약개발 |
|
헬스케어 |
체외진단 의료기기, 일회용 주사기 등 |
(1) 선박사업
선박사업은 조선기자재 및 특수선박, Ballast 라인 및 Sox Scrubber용 GRP파이프를전문으로 하고 있으며 구명정, 어업지도선, 순찰선, 고속단정 등 설계 및 건조기술을 보유하고 있으며 전세계 대형조선소를 주요고객으로 두고 있습니다. 조선경기 악화로 인하여 매출은 전년동기대비 약 24% 감소한 연간 매출 약 90억원입니다. 향후에는 전기 및 수소 등의 친환경에너지 추진선박과 보다 안전한 선박을 개발하여 성장기반을 마련하겠습니다.
(2) 헬스케어 사업
최근 Covid-19 변이바이러스인 오미크론의 확산 영향으로 체외진단도구 수요가 급 증하여 매출은 전년동기대비 약 154% 성장한 연간 매출 1,074억원을 달성하였습니다. 엔데믹 후에도 견조한 성장이 계속될 것으로 예상되는 가운데 성장 가속도를 높이기 위하여 나노 소자를 활용한 첨단 진단기술연구소를 설립하여 자체 면역 진단용 키트도 개발할 계획입니다.
2. (제조서비스업)주요 제품 및 서비스
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 천원) |
| 구 분 | 주요 재화 및 용역 | 매출액 | 비율(%) |
|---|---|---|---|
| 제품매출 | 구명정 외 | 3,559,403 | 2.89 |
| GRP/GRE PIPE | 2,815,743 | 2.28 | |
| 체외진단 의료기기 외 | 102,434,953 | 83.07 | |
| 주사기 외 | 2,198,183 | 1.78 | |
| 수수료매출 | 리보세라닙 중국 로열티 | 3,908,031 | 3.17 |
| 상품매출 | DAVIT | 2,124,031 | 1.72 |
| 기타 의약외품 | 5,276,483 | 4.28 | |
| 기타매출 | 기타 서비스 | 987,890 | 0.80 |
| 합 계 | 123,304,717 | 100.00 | |
※ 주요제품의 종류 및 사용 용도
| 종류 | 특징 | 사용용도 | |
|
체외진단 의료기기 |
검체 채취용 도구 |
비강/비인두, 구강/구인두 면봉(swab) - Virus, Chlamydia, Mycoplasma, & Ureaplasma 등을 포함한 임상 시료를채취하여 - 짧은 시간 내에 채취 부위에서 많은 양의 샘플 채취가 가능함 - USA FDA 등록 및 유럽 CE멸균 인증취득 완료 |
질병 및 감염병 검사를 |
|
검체 수송용 배지 |
- Virus, Chlamydia, Mycoplasma, & Ureaplasma 등을 포함한 임상 시료를 채취하여 채취 - 바이러스 및 미생물 등이 최고 30℃의 조건에서 5일 이상 생존할 수 있도록 설계된 제품 |
질병 및 감염병 검사를 위한 검체 이송용 |
|
| 의약외품 | 알콜스왑 |
- 알콜(에탄올/이소프로필) 액이 침지되어 있는 1회용 부직포 제품 - 피부 및 창상 부위의 소독 및 의료 용구의 소독을 위한 제품 |
창상 및 소독이 필요한 부위의 피부 소독용 |
| 손소독용 제품 |
에탄올(70% 함유) 베이스 투명 겔(gel), 액상(liquid), 티슈(wipes) 제품으로 손, 피부 등의 |
질병 및 감염병 예방을 위한 손 등의 피부 소독용 |
|
| 구명정 | 일반형 | 가장 대표적인 구명정으로 데빗에 의해 진수할 수 있으며, SOLAS규정을 모두 만족하게 만들어졌으며, 위기발생시 신속한 탈출이 가능한 구조로 25인승부터 100인승까지 19개 모델을 보유하고 있어 선박의 규모에 따라 선택적용 가능 |
인명구조 |
| 자유낙하식 | 선박의 선미에 탑재되어 자유낙하 방식으로 진수되는 구명정으로 2007년 5월 이후부터 건조되는 모든 Bulk Carrier선박에 설치가 의무화 되어 있으며, 일반형 구명정의 진수 시 Davit Winch를 이용하는 방식 때문에 비상탈출 시간이 많이 소요되는 점과 본선의 양쪽에 각 한대씩 설치되는 방식으로 인해 Deck House의 공간을 적절히 활용할 수 없는 점으로 인해 최근 자유낙하식 구명정을 선호하는 추세임 |
||
| 구조정 | 선박의 선미에 장착하여 모선의 응급상황시 구조임무에 사용되는 보트로 보트 자유낙하식 구명정과 레스큐보트가 각 하나씩 한세트로 선박에 설치 |
||
| 특수선 | 관공선 | 대형선박, 어업지도선, 해경경비정 등 선미데크에 설치되어 작업 및 신속한 인명구조활동 및 불법어업단속 등에 사용 |
인명구조 및 불법어업 단속 |
| 도선선 | 선박이 입출항하는 항만에서 도선사들이 선박을 탑승 및 하선을 위해 사용됨으로 이동시 실내 편의성, 속도, 선박 탑승시 안전성이 많이 요구되어짐 |
도선사 선박 승,하선용 | |
| 유도선 | 유선은 일반적으로 유람선을 의미하며 도선은 강과 바다가 접하는 하구 또는 만의 형태를 갖춘 곳으로 양 해안을 오가는 선박이며 선령 교체시기에 따라 비정기적으로 발주되는 선박임 |
여객선, 유람선, 도선 | |
| GRP/GRE PIPE | 유리섬유로 강화된 플라스틱이라는 의미의 것으로 통상 강화플라스틱이라 하며, 철근과 콘크리트가 복합되어 좋은 강도를 얻는 것과 같이 내수,내약, 내열성이 좋은 수지를 혼합하여 사용되어 내구성, 강도, 내부식성의이점을 모두 가짐 |
밸러스트 라인, 해수관,소화배관, 냉각수관, 상하수도관 등 |
|
| DAVIT | 선외 물체를 올리고 내릴 때 그 물체가 선체에 부딪치는 일없이 작업하기 편리하게 회전할 수 있게 되어 있음 |
선외 물체를 올리고 내리기 위한 기둥 |
|
| 선박 검사/수리 | 국제해사기구 IMO MSC 402(96) 규정에 의거 본선 인도가 완료된 모든 구명정과 그 진수장치의 정기검사 시행 및 수리 |
검사/ 수리 | |
| 선박 Spare parts | 운항 중인 선박의 구명정 및 진수장치에 대한 부품공급 및 교체서비스 | 부품 교체 | |
| 주사기 | 일회용주사기 |
주사기는 인체 주사액 주입 시 사용되는 의료기기이며 일회용 주사기와 멸균주사침을 |
안전용 |
| 멤브레인 필터주사기 |
멤브레인 필터주사기 제품은 의약품주입여과기와 주사기로 구성된 의료기기로써, 혼합 사용목적 : 혼합 액상의 약물 등을 주입할 때 오염 물질을 걸러내는 기능 |
약물주입, 앰플의 유리 조각 제거, 바이알의 고무파편 제거, 기타 불순물 제거 |
|
3. (제조서비스업)원재료 및 생산설비
가. 주요 원재료에 관한 사항
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 천원) |
| 주요매입처 | 매입액 | 비율(%) | 특수관계여부 | 독과점정도 | 비고 |
| 에프씨 | 12,877,575 | 31.94 | - | - | - |
| ㈜에프바이오 | 6,129,606 | 15.20 | - | - | - |
| 주식회사 일신화이바 | 5,542,350 | 13.75 | - | - | - |
| 주식회사 케이에스지 | 4,797,186 | 11.90 | - | - | - |
| Qingzhou Bright Package Printi | 1,036,208 | 2.57 | - | - | - |
| 기타 | 9,932,209 | 24.64 | - | - | - |
| 합 계 | 40,315,134 | 100.00 | - | - | - |
나. 생산 설비에 관한 사항
(1) 생산능력 및 산출 근거
[HLB 헬스케어사업부]
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 백만개) |
| 사업부문 | 품목 | 소재지 | 구분 | 제38기 당반기 | 제37기 | 제36기 |
| 의료용품 | 면봉 알콜스왑 |
세종 | 생산능력 |
1,453 |
1,602 | 797 |
| 생산실적 |
1,046 |
902 | 258 | |||
| 평균가동률 |
72% |
56% | 32% |
|
(*) 생산능력 산출근거 - 검체도구 : 조업시간 ÷ Cycle Time × 단위 생산수량(Cycle) X 생산 가능일 X 생산 설비(대) - 알콜스왑 : 생산 설비(대) X 시간당 Capa X 일 조업시간 X 생산 가능일 |
[HLB ENG사업부- 선박사업부]
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 대) |
| 사업부문 | 품목 | 소재지 | 구분 | 제38기 당반기 | 제37기 | 제36기 |
| 선박 | 구명정 | 울산 | 생산능력 | 110 | 231 | 231 |
| 생산실적 | 112 | 231 | 196 | |||
| 평균가동률 | 101% | 100% | 85% |
| (*) 생산능력 산출근거 : 구명정 조립 인당생산성(Capa) 이 1.63으로 이를 기준으로 월평균 인원 X 인당생산성 |
| (기준일 : | 2022년 06월 30일 | ) | (단위 : TON) |
| 사업부문 | 품목 | 소재지 | 구분 | 제38기 당반기 | 제37기 | 제36기 |
| 선박 | 특수선 | 울산 | 생산능력 | 113,580 | 227,160 | 227,160 |
| 생산실적 | 56,790 | 204,444 | 227,160 | |||
| 평균가동률 | 50% | 90% | 100% |
| (*) 생산능력 산출근거 : 1,500평 기준 - 특수선동 사용 면적(m2) 기준으로 제작총톤수/면적 지수 45.432를 기준으로 생산 제작 총 톤수를 곱하여 산출함. |
[HLB ENG사업부- 파이프사업부]
| (기준일 : | 2022년 06월 30일 | ) | (단위 : LOT) |
| 사업부문 | 품목 | 소재지 | 구분 | 제38기 당반기 | 제37기 | 제36기 |
| 파이프 | PIPE | 울산 | 생산능력 | 120 | 240 | 240 |
| 생산실적 | 110 | 140 | 199 | |||
| 평균가동률 | 92% | 58% | 83% |
| (*) 생산능력 산출근거 : 와인딩 장비 1대당 직관 월 1,600m 생산 가능 / 최대 생산 가능 Capa 는 와인딩 장비 2대 가동으로 3,200m 생산 가능 / 현재 1 Lot당 80m 소요 |
[화진메디칼/화진메디스]
| (기준일 : | 2022년 04월 30일 | ) | (단위 : 백만개) |
| 사업부문 | 품목 | 소재지 | 구분 | 제38기 당반기 | 제37기 | 제36기 |
| 의료기기 | 주사기 | 천안 | 생산능력 | 127 | 254 | 254 |
| 생산실적 | 80 | 148 | 145 | |||
| 평균가동률 | 63% | 58% | 57% |
| (*) 생산능력 산출근거 : 년 생산 실적 / 년 생산능력 254백만개 (*) 2022년 4월, ㈜화진메디스와 ㈜화진메디칼의 각각의 지분 100%를 에이치엘비테라퓨틱스㈜에 33억에 양도결정하여 4월 기준으로 작성하였습니다. |
(2) 생산설비 등의 현황
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 천원) |
| 구 분 | 기 초 | 취 득 | 처 분 | 감가상각비 | 환율변동효과 | 연결범위변동 | 기 말 |
|---|---|---|---|---|---|---|---|
| 토 지 | 6,477,381 | - | - | - | - | (697,293) | 5,780,088 |
| 건 물 | 10,570,043 | - | - | (164,554) | - | (884,543) | 9,520,946 |
| 구축물 | 230,061 | 10,000 | - | (14,649) | - | (95,676) | 129,736 |
| 기계장치 | 4,437,755 | 370,400 | (629,578) | (433,975) | - | (135,152) | 3,609,450 |
| 차량운반구 | 154,978 | 82,549 | - | (34,054) | - | (30,306) | 173,167 |
| 공기구비품 | 1,788,015 | 251,500 | (56,303) | (342,337) | 68,463 | (234,813) | 1,474,525 |
| 시설장치 | 42,661 | 64,000 | - | (50,123) | - | 64,411 | 120,949 |
| 사용권자산 | 9,470,200 | 3,406,680 | (22,737) | (1,121,959) | 890,240 | (55,580) | 12,566,844 |
| 임차자산개량권 | 167,885 | - | - | (27,099) | 5,444 | - | 146,230 |
| 건설중인자산 | 8,119,535 | 216,080 | - | - | 217 | - | 8,335,832 |
| 합 계 | 41,458,514 | 4,401,209 | (708,618) | (2,188,750) | 964,364 | (2,068,952) | 41,857,767 |
(3) 설비의 신설ㆍ매입 계획 등
- 해당사항 없습니다.
4. (제조서비스업)매출 및 수주상황
가. 매출현황
| (단위 : 천원) |
| 구 분 | 매출유형 | 제38기 당반기 | 제37기 | 제36기 |
| HLB ENG사업 부문 (구. 복합소재사업본부 부문) |
제품매출(내수) | 3,027,850 | 11,208,726 | 16,975,864 |
| 제품매출(수출) | 5,938,533 | 13,634,390 | 19,424,605 | |
| 기타매출 | - | 929,983 | 5,915,966 | |
| 소 계 | 8,966,383 | 25,773,100 | 42,316,435 | |
| 바이오 의료기기사업 부문 | 제품매출(내수) | 84,341,572 | 29,427,975 | 7,171,955 |
| 제품매출(수출) | 25,568,048 | 247,420 | 395,003 | |
| 수수료매출 | 3,908,031 | 10,362,193 | 5,855,924 | |
| 기타매출 | 520,684 | 4,015,304 | 438,084 | |
| 소 계 | 114,338,334 | 44,052,892 | 13,860,966 | |
| 합 계 | 제품매출(내수) | 87,369,422 | 40,636,701 | 24,147,818 |
| 제품매출(수출) | 31,506,581 | 13,881,810 | 19,819,608 | |
| 수수료매출 | 3,908,031 | 10,362,193 | 5,855,924 | |
| 기타매출 | 520,684 | 4,945,287 | 6,354,050 | |
| 합 계 | 123,304,717 | 69,825,991 | 56,177,401 |
나. 판매경로 및 판매방법 등
(1) 판매조직
① 영업본부 - 영업 담당
② 기술영업팀 - 영업 및 납품 담당
(2) 판매경로
① 구명정 & DAVIT
- 조선소 입찰을 통한 직접매매 계약형태
② GRP/GRE Pipe
- 조선소 직접매매 계약형태, 납품불
③ 특수선
- 조달청/조선소 입찰을 통한 직접매매 계약 형태
- 개인 수요자 발굴하여 개별 계약 형태
④ 의료기기(주사기)
- 판매대리점을 통한 간접매매 공급 계약형태
⑤ 체외진단 의료기기 및 의약외품
- 주요 고객사 직접판매 및 대리점 판매 방식 병행
- 기관등 입찰을 통한 직접 매매 계약형태
(3) 판매방법 및 조건
① 구명정 & DAVIT, GRP/GRE Pipe, 특수선
- 판매방법 : 개별 주문 생산, 제품공급계약에 의거 현금, 외상, 위탁판매
- 조 건 : 연불, 기성불, 납품불
② 제약, 바이오
동사가 보유한 리보세라닙의 글로벌 권리에 의거해 매년 중국 항서제약의 리보세라닙(중국명: 아파티닙)의 매출의 일정 비율을 로열티로 수령해 매출로 인식합니다. 2021년부터 중국 내 적응증 확대(간세포암 2차 치료제)로 로열티 수령액이 증가할 것으로 예상됩니다. 그리고, 엘레바에서 진행 중인 위암 3/4차 치료제(Rivoceranib 단독, 글로벌 임상 3상 종료),간암 1차 치료제(항서제약 캄렐리주맙 병용)로 글로벌 3상(환자 모집 완료), 선양낭성암 1,2차 치료제(Rivoceranib 단독) 임상 2상 (환자모집 완료) 등 다양한 임상시험이 진행 중입니다. 신약승인이 이루어질 경우를 대비해 대륙별 판매 전략 수립을 전개 중입니다. 리보세라닙의 판매로 인한 매출 발생 시,당사는 로열티 수익을 기대할 수 있습니다.
③ 의료기기(주사기)
- 판매방법: 각 병원 및 도,소매업체 주문량을 대리점을 통해 판매
- 판매조건: 판매 후 2개월 외상거래(현금 및 어음)
④ 체외진단 의료기기 및 의약외품
- 판매방법 : 제품공급계약 및 고객발주서에 의거한 현금, 외상, 위탁 판매
- 판매조건 : 제품공급계약서 및 고객발주서에 의거한 납품 및 대금 결제방식
(4) 판매전략
① 구명정 & DAVIT, GRP/GRE Pipe
- 조선소 요구에 따른 조선소별 차별대응
- 각종 홍보활동을 통한 대선주 판촉활동 강화
- 까다롭고 다양한 선주/조선소 요구에 대한 적극적인 대응
- 경쟁사와의 기술력, 서비스의 차별화
② 특수선
- 조달청 입찰 모니터링 및 입찰 참여
- 관공선 수요 사전 예측 후 요구선박의 기술 자문 및 영업활동
- 개인 수요자 발굴위한 프로그램 운영 준비
- 경쟁사와의 우수한 생산설비, 기술력 차별화 및 홍보
③ 의료기기(주사기)
- 가격 및 품질경쟁력
- 다수의 대형병원과의 안정적 거래
- 시장에 맞는 맞춤형 주사기 개발
- 다양한 국가의 유통채널 발굴
④ 체외진단 의료기기 및 의약외품
- 유수의 국내 및 글로벌 기업과의 지속적인 제품 및 서비스 품질에 대한 신뢰
유지를 통한 영업력 강화
- 서울대병원, 삼성서울병원 등 대표적인 대형 대학병원 및 종합병원 납품을 통한
안정적인 매출 확보
- 기관 등 입찰 모니터링 및 국내,외 입찰 참여를 통한 시장 확대
- 병원, 대학연구실, 표준검사실, 의사연구실, 연구기관, 거점병원, 검사기관 등의
신규 시장 발굴 및 확대
다. 주요 매출처에 관한 사항
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 천원) |
| 주요매출처 | 매출액 | 비율(%) | 비고 |
| 주식회사 한국애보트진단 | 29,524,922 | 48.09 | - |
| 에임 주식회사 | 25,679,211 | 20.83 | - |
| 에스디바이오센서㈜ | 11,235,684 | 9.11 | - |
| 주식회사오상헬스케어 | 4,916,460 | 3.99 | - |
| Jiangsu Hengrui Medicine Co.,Ltd. | 3,908,031 | 3.17 | - |
| 기타 | 48,040,409 | 14.82 | - |
| 합 계 | 123,304,717 | 100.00 | - |
라. 수주현황
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 백만원) |
| 품목 |
수주 기초 |
증가액 | 기납품액 | 수주잔고 |
|
구명정 |
14,149 | 1,442 | 4,915 | 10,676 |
|
데빗 |
103 | 4,201 | 2,839 | 1,465 |
|
특수선 |
572 | 2,246 | 371 | 2,447 |
|
파이프 |
5,260 | 11,948 | 4,239 | 12,969 |
|
합 계 |
20,084 | 19,837 | 12,364 | 27,557 |
마. 진행률적용 수주상황
- 해당사항 없습니다.
5. (제조서비스업)위험관리 및 파생거래
1. 위험관리
금융상품과 관련하여 연결실체는 신용위험, 유동성위험 및 시장위험에 노출되어 있습니다. 본 주석은 연결실체가 노출되어 있는 위의 위험에 대한 정보와 연결실체의 위험관리 목표, 정책, 위험 평가 및 관리 절차, 그리고 자본관리에 대해 공시하고 있습니다. 추가적인 계량적 정보에 대해서는 본 연결재무제표 전반에 걸쳐서 공시되어 있습니다.
(1) 금융위험관리
연결실체의 위험관리 체계를 구축하고 감독할 책임은 이사회에 있습니다. 이사회는 연결실체의 위험관리 정책을 개발하고 감독하고 있으며 중장기 경영계획 및 단기 경영전략에 대해 정기적으로 보고받고 승인하고 있습니다.
연결실체의 위험관리 정책은 연결실체가 직면한 위험을 식별 및 분석하고, 적절한 위험 한계치 및 통제를 설정하고, 위험이 한계치를 넘지 않도록 하기 위해 수립되었습니다. 위험관리 정책은 시장 상황과 연결실체의 활동의 변경을 반영하기 위해 정기적으로 검토되고 있습니다. 연결실체는 훈련 및 관리기준, 절차를 통해 모든 종업원들이 자신의 역할과 의무를 이해할 수 있는 엄격하고 구조적인 통제환경을 구축하는 것을 목표로 하고 있습니다.
1) 신용위험
① 신용위험에 대한 노출
금융자산의 장부금액은 신용위험에 대한 최대노출정도를 나타냅니다. 연결실체는 현금및현금성자산을 신용등급이 우수한 금융기관에 예치하고 있어, 금융기관으로부터의 신용위험은 제한적입니다. 또한, 연결실체가 보유하고 있는 채무증권은 채무불이행 위험이 낮고, 차입자가 계약상 현금흐름 지급의무를 이행할 수 있는 능력이 있기 때문에 신용위험이 낮은 것으로 보고 있습니다. 연결실체의 신용위험에 대한 최대 노출정도는 다음과 같습니다.
| (단위: 천원) | ||
| 구 분 | 당반기말 | 전기말 |
| 현금및현금성자산 | 80,483,163 | 99,796,601 |
| 매출채권 | 27,995,134 | 34,034,508 |
| 기타금융자산 | 20,633,974 | 37,952,824 |
| 당기손익-공정가치 측정 금융자산 | 54,433,682 | 22,049,993 |
| 합 계 | 183,545,953 | 193,833,926 |
당반기말 현재 연결실체는 관계기업인 현대요트㈜의 하자이행보증 및 계약이행보증에 대한 지급보증을 제공함에 따라 추가적인 신용위험에 노출되어 있습니다.
② 손상차손
연결실체는 매출채권과 기타채권에 대한기대신용손실을 측정하여 충당금을 설정하고 있습니다. 당반기말과 전기말 현재 기대신용손실과 각 연령별로 손상된 금액은 다음과 같습니다.
| (단위: 천원) | ||||||||
| 구 분 | 당반기말 | 전기말 | ||||||
| 기대손실율 | 채권잔액 | 손상된 금액 | 장부금액(*2) | 기대손실율 | 채권잔액 | 손상된 금액 | 장부금액 | |
| 3개월 이하(*1) | 0.02% | 64,539,271 | (14,537) | 64,524,734 | 0.14% | 58,533,082 | (83,868) | 58,449,214 |
| 3~6개월 | 11.33% | 715,287 | (81,063) | 634,224 | 11.57% | 24,130 | (2,791) | 21,339 |
| 6~9개월 | 7.04% | 95,522 | (6,722) | 88,800 | 18.32% | 15,887 | (2,911) | 12,976 |
| 9~12개월 | 69.93% | 12,429 | (8,692) | 3,737 | 0.00% | - | - | - |
| 12개월 초과(*2) | 41.23% | 16,450,332 | (6,781,859) | 9,668,473 | 41.98% | 16,163,291 | (6,785,739) | 9,377,552 |
| 합 계 | 81,812,841 | (6,892,873) | 74,919,968 | 74,736,390 | (6,875,309) | 67,861,081 | ||
(*1) 2021년 귀속분 리보세라닙 로열티 매출채권에 대한 추정치 11,724,092천원이 포함되어 있습니다.
(*2) 당반기말 현재, 2020년 귀속분 리보세라닙 로열티 9,663,745천원은 당사의 100% 자회사인 Hyundai Lifeboats Shanghai Co., Ltd.의 계좌에 예치되어 있습니다.
당반기와 전기 중 매출채권과 기타금융자산에 대한 대손충당금의 기중 변동내역은 다음과 같습니다.
| (단위: 천원) | ||
| 구 분 | 당반기 | 전기 |
| 기초금액 | 36,875,309 | 45,845,459 |
| 연결범위의 변동 | (3,880) | 93,923 |
| 대손상각비 | 22,941 | 683,167 |
| 기타의대손상각비(환입) | (1,497) | (1,197,316) |
| 제각(*) | - | (8,549,924) |
| 기말금액 | 36,892,873 | 36,875,309 |
(*) 폐업 등으로 회수가 불가능한 채권을 장부에서 제각하였습니다.
2) 유동성위험
당반기말 및 전기말 현재 금융부채의 계약상 만기는 다음과 같습니다. 금액은 이자지급액을 포함하고, 상계약정의 효과는 포함하지 않았습니다.
① 당반기말
| (단위: 천원) | ||||||
| 구 분 | 장부금액 | 계약상 현금흐름 | 3개월이내(*) | 3-12개월(*) | 1-2년(*) | 2년초과 |
| 매입채무 | 4,600,685 | 4,581,616 | 4,581,616 | - | - | - |
| 기타금융부채 | 97,889,804 | 103,092,039 | 81,329,818 | 2,000,977 | 2,070,216 | 17,691,028 |
| 차입금 | 110,053,697 | 127,564,030 | 2,136,478 | 25,707,600 | 99,366,752 | 353,200 |
| 합 계 | 212,544,186 | 235,237,685 | 88,047,912 | 27,708,577 | 101,436,968 | 18,044,228 |
(*) 전환사채 및 신주인수권부사채의 조기상환권이 청구 가능한 가장 빠른 시기에 행사됨을 가정하였습니다.
② 전기말
| (단위: 천원) | ||||||
| 구 분 | 장부금액 | 계약상 현금흐름 | 3개월이내(*) | 3-12개월 | 1-2년(*) | 2년초과 |
| 매입채무 | 5,084,230 | 5,084,230 | 5,084,230 | - | - | - |
| 기타금융부채 | 94,060,368 | 93,965,067 | 76,535,419 | 3,896,515 | 1,764,339 | 11,768,794 |
| 차입금 | 68,594,770 | 79,879,342 | 17,521,115 | 3,750,595 | 58,250,832 | 356,800 |
| 합 계 | 167,739,368 | 178,928,639 | 99,140,764 | 7,647,110 | 60,015,171 | 12,125,594 |
(*) 전환사채 및 신주인수권부사채의 조기상환권이 청구 가능한 가장 빠른 시기에 행사됨을 가정하였습니다.
3) 환위험
① 환위험에 대한 노출
연결실체는 기능통화인 원화 이외의 통화로 표시되는 거래로 인하여 환율변동위험에노출되어 있습니다. 당반기말 및 전기말 현재 외화로 표시된 화폐성자산 및 부채의 장부금액은 다음과 같습니다.
| (단위 : USD, CNY) | ||||
| 구 분 | 당반기말 | 전기말 | ||
| USD | CNY | USD | CNY | |
| 자산: | ||||
| 외화예금 | 9,141,118 | - | 803,721 | - |
| 매출채권 | 5,046,357 | 60,825,380 | 416,440 | 90,706,765 |
| 기타금융자산 | - | - | 29,423 | - |
| 소 계 | 14,187,475 | 60,825,380 | 1,249,584 | 90,706,765 |
| 부채: | ||||
| 매입채무 | 88,436 | - | - | - |
| 합 계 | 14,099,039 | 60,825,380 | 1,249,584 | 90,706,765 |
당반기말과 전기말 현재 적용된 환율은 다음과 같습니다.
| (단위: 원) | ||||
| 구 분 | 평균환율 | 기말환율 | ||
| 당반기 | 전반기 | 당반기말 | 전기말 | |
| USD | 1,232.94 | 1,117.73 | 1,292.90 | 1,185.50 |
| CNY | 190.04 | 172.75 | 192.75 | 186.26 |
② 민감도분석
연결실체는 내부적으로 원화 환율 변동에 대한 환위험을 정기적으로 측정하고 있습니다. 당반기 및 전기 중 각 외화에 대한 원화환율 5% 변동 시 환율변동이 세전손익에 미치는 영향은 다음과 같습니다.
| (단위 : 천원) | ||||
| 구 분 | 당반기 | 전기 | ||
| 5% 상승시 | 5 % 하락시 | 5% 상승시 | 5 % 하락시 | |
| USD | 917,149 | (917,149) | 74,069 | (74,069) |
| CNY | 586,205 | (586,205) | 844,752 | (844,752) |
4) 이자율위험
① 당반기말 및 전기말 현재 연결실체가 보유하고 있는 이자부 금융상품은 다음과 같습니다.
| (단위: 천원) | ||
| 구 분 | 당반기말 | 전기말 |
| 고정이자율 : | ||
| 금융자산 | 119,187,314 | 141,252,906 |
| 금융부채 | 110,053,697 | 64,726,776 |
| 합 계 | 9,133,617 | 76,526,130 |
| 변동이자율 : | ||
| 금융자산 | 375,789 | - |
| 금융부채 | - | 3,867,994 |
② 고정이자율 금융상품의 공정가치 민감도 분석
연결실체는 고정이자율 금융상품을 당기손익인식금융상품으로 처리하고 있지 않으며, 이자율스왑과 같은 파생상품을 공정가치위험회피회계의 위험회피수단으로 지정하지 않았습니다. 따라서, 이자율의 변동은 손익에 영향을 주지 않습니다.
③ 변동이자율 금융상품의 현금흐름 민감도 분석
당반기말 현재 이자율이 100베이시스포인트 변동한다면, 자본과 손익은 증가 또는 감소하였을 것입니다. 이 분석은 환율과 같은 다른 변수는 변동하지 않는다고 가정하였으며, 당반기 중 구체적인 세전자본 및 세전손익의 변동금액은 다음과 같습니다.
| (단위: 천원) | ||||
| 구 분 | 손익 | 자본 | ||
| 100bp상승 | 100bp하락 | 100bp상승 | 100bp하락 | |
| 당반기말: | ||||
| 변동이자율 금융상품 | ||||
| 장ㆍ단기금융자산 | 3,758 | (3,758) | 3,758 | (3,758) |
| 장ㆍ단기차입금 | - | - | - | - |
5) 공정가치
공정가치 서열체계를 포함한 금융자산과 금융부채의 장부금액과 공정가치는 다음과 같습니다. 장부금액이 공정가치의 합리적인 근사치에 해당하여 공정가치를 측정하지않은 금융자산과 금융부채에 대한 공정가치 정보는 포함하고 있지 않습니다.
① 당반기말
| (단위:천원) | ||||
| 구 분 | 장부금액 | 수준1 | 수준2 | 수준3 |
| 공정가치로 측정되는 금융자산: | ||||
| 당기손익-공정가치 측정 | 54,433,682 | 22,469,317 | 31,962,955 | 1,410 |
| 기타포괄손익-공정가치 측정 | 5,793,068 | 719,227 | - | 5,073,841 |
| 합 계 | 60,226,750 | 23,188,544 | 31,962,955 | 5,075,251 |
② 전기말
| (단위:천원) | ||||
| 구 분 | 장부금액 | 수준1 | 수준2 | 수준3 |
| 공정가치로 측정되는 금융자산: | ||||
| 당기손익-공정가치 측정 | 23,551,252 | - | 23,549,842 | 1,410 |
| 기타포괄손익-공정가치 측정 | 6,073,286 | 999,445 | - | 5,073,841 |
| 합 계 | 29,624,538 | 999,445 | 23,549,842 | 5,075,251 |
③ 가치평가기법
연결실체는 공정가치 서열체계에서 수준 2와 수준 3으로 분류되는 반복적인 공정가치측정치, 비반복적인 공정가치측정치, 공시되는 공정가치에 대해 다음의 가치평가기법을 사용하고 있습니다. 사용된 가치평가기업과 투입변수는 다음과 같습니다.
| (단위: 천원) | |||||
| 구 분 | 공정가치 | 가치평가기법 | 수준 | 투입변수 | 투입변수 범위 |
| 에이치엘비제약㈜ 전환사채(*) | 23,272,820 | 현재가치기법, 이항모형 |
2 | 가중평균자본비용 | 14.87% |
| 가격 변동성 | 76.70% | ||||
| 무위험 할인율 | 3.20% | ||||
| 에이치엘비㈜ 제36회 전환사채 매도청구권 | 2,355,384 | 현재가치기법, 이항모형 |
2 | 가중평균자본비용 | 17.54% |
| 가격 변동성 | 60.30% | ||||
| 무위험 할인율 | 3.16% | ||||
| 에이치엘비㈜ 제37회 신주인수권부사채 매도청구권 | 1,740,936 | 현재가치기법, 이항모형 |
2 | 가중평균자본비용 | 17.54% |
| 가격 변동성 | 60.30% | ||||
| 무위험 할인율 | 3.16% | ||||
| 노터스 제1회 전환사채 매도청구권 | 3,017,209 | 현재가치기법, 이항모형 |
2 | 가중평균자본비용 | 5.26% |
| 가격 변동성 | 68.42% | ||||
| 무위험 할인율 | 1.96% | ||||
| 저축성보험 | 1,576,605 | 순자산가치법 | 2 | 개별 자산 및 부채의 공정가치 | - |
| ㈜씨엘팜 지분 | 5,073,841 | 현금흐름할인법 | 3 | 가중평균자본비용 | 19.55% |
| 영구성장률 | 0.00% | ||||
| 무위험 할인율 | 2.26% | ||||
| 조합출자금 | 1,410 | 원가접근법 | 3 | 개별 자산 및 부채의 공정가치 | - |
(*) 투입변수 중 가격 변동성이 증가하거나 가중평균자본비용이 감소하면 공정가치가 증가하며, 무위험 할인율의 감소도 공정가치를 증가시킬 수 있습니다.
④ 수준 3 공정가치
당반기 중 수준 1과 수준 2간의 대체는 없었으며, 수준 3 공정가치 분류되는 금융자산의 당반기 중 변동내용은 없습니다.
⑤ 공정가치 서열체계
연결실체는 공정가치 측정에 사용된 투입변수의 유의성을 반영하는 공정가치 서열체계에따라 공정가치 측청치를 분류하고 있으며, 공정가치 서열체계의 수준은 다음과 같습니다.
| 구 분 | 투입변수의 유의성 |
| 수준 1 | 동일한 자산이나 부채에 대한 활성시장의 공시가격 |
| 수준 2 | 직접적으로 또는 간접적으로 관측가능한, 자산이나 부채에 대한 투입변수 |
| 수준 3 | 관측가능한 시장자료에 기초하지 않은, 자산이나 부채에 대한 투입변수 |
(2) 자본관리
연결실체의 자본관리는 건전한 자본구조를 유지하며, 주주이익의 극대화를 목적으로하고 있습니다. 연결실체는 최적 자본구조 달성을 위해 부채비율과 순차입금비율 등의 재무비율을 자본관리지표로 사용하고 있습니다. 부채비율은 부채총계를 자본총계로 나누어 산출하고 있으며, 순차입금비율은 순차입금을 자본총계로 나누어 산출하고 있습니다.
| (단위: 천원) | ||
| 구 분 | 당반기말 | 전기말 |
| 부채비율: | ||
| 부채총계(A) | 277,826,631 | 231,507,461 |
| 자본총계(B) | 535,316,641 | 512,184,803 |
| 부채비율(A/B) | 51.90% | 45.20% |
| 순차입금비율: | ||
| 현금및현금성자산(C) | 80,483,163 | 99,796,601 |
| 단기금융상품(D) | 5,025,000 | 9,320,000 |
| 차입금(E) | 110,053,697 | 68,594,770 |
| 순차입금(F=E-C-D) | 24,545,534 | - |
| 순차입금비율(F/B) | 4.59% | 0.00% |
2. 파생거래
(1) 파생상품의 거래내역은 다음과 같습니다.
| (단위:천원) | ||
| 구 분 | 당반기말 | 전기말 |
| 파생상품자산 | ||
| 에이치엘비 제36회차 전환사채 매도청구권(*1) | 2,355,384 | - |
| 에이치엘비 제37회차 신주인수권부사채 매도청구권(*1) | 1,740,936 | - |
| 노터스 제1회차 전환사채 매도청구권(*2) | 3,017,209 | - |
| 합 계 | 7,113,529 | - |
(*1) 총 발행금액의 30%에 대하여 당사 또는 당사가 지정하는 제3자에게 매도 요청 할 권리(콜옵션)를 보유하고 있으며, 당사는 동 콜옵션을 별도의 금융상품으로 인식하였습니다.
(*2) 총 발행금액의 30%에 대하여 당사가 매도청구권을 보유하고 있습니다.
(2) 당반기 중 파생상품관련 손익은 다음과 같습니다.
| (단위:천원) | |||||
| 상품분류 | 종류 | 거래이익 | 평가이익 | 거래손실 | 평가손실 |
| 주식연계옵션 | 매도청구권 | - | 3,017,209 | - | - |
6. (제조서비스업)주요계약 및 연구개발활동
가 . 경영상의 주요계약
본 보고서 작성기준일 현재 당사와 당사의 연결대상 종속회사가 체결한 라이센스 계약은 다음과 같습니다.
(1) 특허권 양수도 계약
|
품목 |
계약상대방 |
대상지역 |
계약 체결시기 |
계약상의 주요내용 |
계약 금액 |
비고 |
|
리보세라닙 구Apatinib Mesylate) |
Advenchen Laboratories Nanjing, Ltd. |
중국을 제외한 모든 국가 |
2020.09. |
YN968D1(글로벌은 리보세라닙 |
2,200 만불 |
- |
|
SFFT Developing Co., Ltd. |
중국 |
2,000 만불 |
- |
| * 본 특허권양수도 계약의 목적은 리보세라닙의 글로벌 로열티 수령을 통한 장기적이고 안정적인 캐시플로우 및 영업이익을 확보하고, 항서제약과의 긴밀한 협력관계를 통하여 현재 진행중인 NDA와 리보세라닙의 추가 적응증 임상시험에 속도를 내기 위함입니다. |
(1)
| 계약상대방 | Advenchen Nanjing |
| 계약내용 | Advenchen Nanjing이 보유한 Rivoceraninb 물질특허 권리 양수도 |
| 대상지역 | 미국, 캐나다, 유럽, 일본, 한국, PCT |
| 계약기간 | 해당 특허 만료일까지 (2024년 예상) |
| 총계약금액 | Upfront: 22,000,000USD |
| 지급금액 | Upfront: 22,000,000USD 기 지급 완료 Milestone: 미 발생 |
| 계약조건 | 개발 마일스톤(Development Milestione): 적응증, 진입국가, 매출에 따라 단계별 마일스톤 실행 예정 초과수익배분: 상호 협의된 연간 수익예측을 초과하는 매출의 50% 지급 |
| 회계처리방법 | 최초 지급한 Upfront 22,000,000USD는 무형자산으로 인식 비용 발생하지 않음. 차후 당기비용으로 인식 예정 |
| 대상기술 | Rivoceranib 물질특허 (미국, 캐나다, 유럽, 일본, 한국, PCT) |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1,2차 치료제(Rivoceranib 단독) 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 ESMO에서 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상 3상 결과 발표 (1차 평가지표 만족) |
| 기타사항 | 판매 승인 현황 - 중국 판권을 보유한 항서제약에서 2014년 위암 3차 치료제, 2020년 간암 2차 치료제로 시판 허가 득한 후 판매 중 |
(2)
| 계약상대방 | SFFT |
| 계약내용 | SFFT가 보유한 Rivoceraninb의 중국 특허권리 양수도 |
| 대상지역 | 중국 |
| 계약기간 | 해당 특허 만료일까지 (2022년 11월 예상) |
| 총계약금액 | Upfront: 20,000,000USD |
| 지급금액 | Upfront: 20,000,000USD 기 지급 완료 Milestone: 미 발생 |
| 계약조건 | 초과수익배분 : 상호 협의된 연간 수익예측을 초과하는 매출의 70% 지급 |
| 회계처리방법 | 최초 지급한 Upfront 20,000,000USD는 무형자산으로 인식해 감가상각 완료 이후 지급한 Milestone 비용은 당기비용으로 인식 |
| 대상기술 | Rivoceranib 물질특허 (중국) |
| 개발진행경과 | <회사> 중국 내 전용실시권은 항서제약이 보유하고 있어 항서제약에서 개발 진행 중 |
| 기타사항 | 판매 승인 현황 - 중국 판권을 보유한 항서제약에서 2014년 위암 3차 치료제, 2020년 간암 2차 치료제로 시판 허가 득한 후 판매 중 |
(2) 연결대상 종속회사 경영상의 주요계약
(가) Elevar Therapeutics, Inc.
1) 라이센스 인(License-in)계약
|
품목 |
계약상대방 |
대상지역 |
계약 |
계약상의주요내용 |
계약금액 |
진행단계 | 비 고 |
|
리보세라닙 (Rivoceranib, 구Apatinib Mesylate) |
에이치엘비㈜(*1) |
중국을 제외한 모든 국가 |
2020. 12. | Rivoceranib의 중국을 제외한 글로벌 전용실시권 취득 |
(*2) |
- 위암말기 치료제 : 임상3상 종료 Pre-NDA 실시, 미국 FDA 신약허가 신청 (NDA) 준비 중,희귀의약품 지정(미국, 유럽, 한국) - 고형암 옵디보(Nivolumab) 병용 : 임상1상 종료 - 선양낭성암 단독 : 임상2상 진행 중, 희귀의약품 지정(미국) - 위암 2차 치료제(파클리탁셀 병용) : 임상1/2상 진행 중 - 간암 1차 치료제(캄렐리주맙 병용) : 임상3상 진행 중, 희귀의약품 지정(미국) - 대장암 3차 치료제(론서프 병용) : 임상1상 진행 중 - 난소암(Apealea 병용) : 임상 1상 준비 중 |
표적항암제 (VEGFR-2를 선택적으로 차단) |
|
아필리아 (Apealea) |
비베스토 (Vivesto, 舊 Oasmia) |
러시아연방, 스칸디나비아반도국을 제외한 모든 국가 |
2020. 03. | Apealea의 계약상 명시된 지역에서의 전용실시권 취득 |
(*2) | - 2020년 유럽 EMA로 부터 난소암 2차 치료제로 판매 승인 (carboplatin 병용) 2022년 내 유럽 내 판매 개시 목표 - 난소암(Rivoceranib 병용) : 임상 1상 준비 중 |
세포독성항암제 Paclitaxel 성분의 3세대 개량신약 항암제 |
|
(*1) Elevar Therapeutics,Inc.는 2007년 7월 Advenchen Laboratories,Inc., CA, USA와 리보세라닙 License-in 계약을 체결하였으나, 2020년 12월 당사와 Advenchen Laboratories와 Rivoceranib의 물질특허권리 양수도에 따라 특허권자가 ※ JAK3 License-in 계약은 자체 추진으로 사업방향을 전환하여 계약을 취소하였습니다. |
(1)
| 계약상대방 | Advenchen Laboratories |
| 계약내용 | YN968D1-Small Molecule Angiogenesis Inhibitor의 계약상 명시된 지역에서의전용실시권 취득 |
| 대상지역 | 중국을 제외한 모든 국가 |
| 계약기간 | 계약체결일:2007. 12. 21(계약서 내용 조정일 2021, 06, 17) 계약종료일: 유효특허의 만료일까지 (물질특허: 2024년 예상, 염조성물특허: 2029년 예상) |
| 총계약금액 | Upfront: 150,000 USD |
| 지급금액 | <환수 불가능 금액> 계약금(Upfront Payment): 150,000USD 2007년 기 지급 완료 마일스톤(Milestione): 임상 진행 단계에 진행에 따라 개발 Milestione $800,000USD 지급 로열티(Royalty): 매출없음 <환수 가능 금액> 해당사항 없음 |
| 계약조건 | 계약 조정 내역을 포함한 최종 계약 조건 계약금(Upfront Payment): 150,000USD - 지급조건: 계약 체결 45일 이내 마일스톤(Milestione): 적응증, 진입국가, 매출에 따라 단계별 마일스톤 실행 예정 로열티: 3.5%~10% 지역별 매출액 비율에 따른 로열티 실행 예정 Advenchen이 보유한 Appatinib(Rivoceranib)의 염조성물 특허를 LSKB에 허여한다. 국가별 특허(물질특허 및 염조성물특허) 유지 상태에 따라 상호 협의한 비율에 의거해 로열티를 조정한다. LSKB가 보유한 모든 권리는 Elevar가 승계한다. |
| 회계처리방법 | 최초 지급한 Upfront 150,000USD는 무형자산으로 인식해 감가상각 완료 이후 지급한 Milestone 비용은 당기비용으로 인식 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 Rivoceranib과 염특허 전용 특허 실시권 |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제(Rivoceranib 단독) 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1,2차 치료제(Rivoceranib 단독) 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 ESMO에서 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상 3상 결과 발표 (1차 평가지표 만족) |
| 기타사항 | 판매 승인 현황 중국 판권을 보유한 항서제약에서 2014년 위암 3차 치료제, 2020년 간암 2차 치료제로 시판 허가 득한 후 판매 중 |
(2)
| 계약상대방 | 비베스토(Vivesto, 舊 Oasmia) |
| 계약내용 | Apealea의 계약상 명시된 지역에서의 전용실시권 취득 |
| 대상지역 | 러시아연방, 스칸디나비아반도국을 제외한 모든 국가 |
| 계약기간 | 계약체결일:2020. 03. 25(계약서 내용 조정일 2021, 06, 17) 계약종료일: 유효특허의 만료일까지 (2036년 12월 예상) |
| 총계약금액 | Upfront: 20,000,000 USD |
| 지급금액 | <환수 불가능 금액> 계약금(Upfront Payment): 20,000,000USD 2019년 기 지급 완료 마일스톤(Milestione): Milestone 지급 조건 미달성으로 미지급 로열티(Royalty): Royalty 지급 조건 미달성으로 미지급 <환수 가능 금액> 해당사항 없음 |
| 계약조건 | 계약금(Upfront Payment): 20,000,000USD - 지급조건: 계약 체결 시 개발 마일스톤(Development Milestione): 적응증, 진입국가에 따라 단계별 마일스톤 실행 예정 판매 마일스톤(Sales Milestone): 매출액 비율에 따라 상호 협의한 비율의 판매 마일스톤 실행 예정 로열티(Royalty): 매출의 10%~25%, 지역별 매출액 비율에 따른 로열티 실행 예정 |
| 회계처리방법 | Upfront 20,000,000USD는 반환의무 및 기타 조건이 없어 수행할 추가적 의무가 존재하지 않아, 무형자산으로 인식 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 의약품 아필리아("Apealea")에 대한 전용특허 실시권 및 다음의 염조성물 특허 실시권 - 화학명 N-(all-trans-retinoyl)-L-cysteic acid methyl ester sodium salt - 화학명 N-(13-cis-reinoyl)-L-cysteic acid methyl ester sodium salt |
| 개발진행경과 | <거래상대방> 북유럽과 러시아에서 판매 중이며, 2018년 유럽 EMA 판매 승인 완료 |
| <회사> 미국 내 부인과종양학그룹 소속 임상의들과 백금계 약물 저항성이 있는 난소암 환자를 대상으로 Rivoceranib, Apealea 병용 임상에 대한 계획 검토 중이나, 구체적인 임상 개시 일정은 미정 |
|
| 기타사항 | 판매 승인 현황 2020년 유럽 EMA로 부터 난소암 2차 치료제로 판매 승인 (carboplatin 병용) 2022년 내 유럽 내 판매 개시 목표 |
2) 라이센스 아웃(License-out)계약
|
품목 |
계약 |
대상지역 |
계약 |
계약상의 주요내용 |
계약금액 |
진행단계 | 비 고 |
| 리보세라닙 (Rivoceranib, 구Apatinib Mesylate) |
에이치엘비 |
대한민국, 일본, 유럽 |
2018. 08. |
기존 부광약품㈜에게 인정되는 |
47억원(*) | - 위암말기 치료제 : 임상3상 종료 Pre-NDA 실시, 미국 FDA 신약허가 신청 (NDA) 준비 중, 희귀의약품 지정(미국, 유럽, 한국) - 선양낭성암 단독 : 임상2상 진행 중, 희귀의약품 지정(미국) - 위암 2차 치료제(파클리탁셀 병용) : 임상1/2상 진행 중 - 간암 1차 치료제(캄렐리주맙 병용) : 임상3상 진행 중, 희귀의약품 지정(미국) - 대장암 3차 치료제(론서프 병용) : 임상1상 진행 중 - 동물용항암제 : 임상 진행 중 |
에이치엘비 바이오 그룹의 사업 다각화 및 매출 증대 |
| (*)LSK Biopartners, Inc.에서 향후 계약상대방으로부터 지급받을 Development Milestones 내역은 다음과 같습니다. |
| 계약상대방 | 부광약품㈜ |
| 계약내용 | Rivoceranib에 대한 특정 지역의 개발, 판매에 대한 권리 Sublicense(한국, 유럽, 일본) 및 공동개발 |
| 대상지역 | 대한민국, 일본, 유럽 |
| 계약기간 | 계약체결일:2009. 1. 8 (계약서 내용 조정일 2012, 2, 1) (계약서 내용 조정일 2015, 7, 28) (계약서 내용 조정일 2015, 10, 30) (계약서 내용 조정일 2017, 1, 2) 계약종료일: 유효특허의 만료일까지 (물질특허: 2024년 예상, 염조성물특허: 2029년 예상) |
| 총계약금액 | Potential Sales Royalty: 매출액에 따라 6~10% 특허가 국가별로 개별 종료 될 시 최대 10년까지 상기 로열티의 10%를 지급 |
| 지급금액 | 해당사항 없음 |
| 계약조건 | 주요 계약 내용 1) 한국내 독점개발, 판매권 및 유럽, 일본에 대한 수익 지분 2) 국내 시판시 판매액의 6~10% 로열티 지불 (Sublicensing,진행시 수익의 30% 지불) |
| 회계처리방법 | 해당사항 없음 |
| 대상기술 | 재실시권을 허여(Sub-License, 또는 License-out)할 수 있는 권리를 포함하여, 계약에서 명시된 지역에서의 Rivoceranib 특허 전용실시권 |
| 개발진행경과 | <회사> 2019년 위암 3차 치료제(Rivoceranib 단독) 글로벌 임상 3상 후 NDA 준비 중 2022년 선양낭성암 1,2차 치료제(Rivoceranib 단독) 미국/한국 임상 2상 종료 후 결과 발표(2022년 6월 ASCO) 2022년 9월 간암 1차 치료제(항서제약 캄렐리주맙 병용) 글로벌 임상 3상 결과 ESMO 학회에서 발표(1차 평가지표 만족) |
| 기타사항 | Elevar Therapeutics, Inc. 는 2009년 12월 부광약품㈜에게 리보세라닙의 한국 판권을 양도하는 조건으로 리보세라닙 공동개발을 하였으며, 이후 부광약품㈜은 2018년 08월 한국 판권에 대한 모든 권리 및 의무를 에이치엘비생명과학㈜으로 400억원에 양도하였습니다. (2018.8.14 공시 참조) |
(나) Immunomic Therapeutics, Inc.
1) 라이센스 인(License-in)계약
| 구분 | 계약 상대방 |
계약 체결시기 |
계약상의 주요내용 |
비 고 |
|---|---|---|---|---|
| (1) | Johns Hopkins University | 2006-09-26 | LAMP technology license contract | - |
| 2008-02-01 (1st amendment) |
||||
| 2009-09-29 (2nd amendment) |
||||
| 2009-12-04 (3rd amendment) |
||||
| (2) | Nature Technology Corp. | 2015-01-22 | Plasmid non-exclusive license contract | - |
| 2016-06-20 | ||||
| (3) | Annias Immunotherapeutics, Inc. | 2017-05-03 | CMV/pp65 license contract | - |
| 2019-10-14 (1st amendment) |
||||
| (4) | University of Florida Research Foundation, Inc. |
2018-06-28 | Cell Therapy Product development Standard exclusive license contract |
Know-how (No: 18021) |
| (5) | 2019-04-10 2020-02-19 (1st amendment) |
Cell Therapy Product development Exclusive Data license contract (1st amendment of the contract dated 19/04/10) |
(No: A19091) | |
| (6) | Replicate Bioscience, Inc. | 2020-03-10 | Self-amplifing RNA Research corporation contract |
Option to the technology generated |
| (7) | CoImmune, Inc. | 2020-11-10 | Non-exclusive rights to coImmune's proprietary DC manufacturing process |
- |
| (8) | Ichor Medical Systems, Inc. | 2020-05-31 | Non-Commercial Research & Phase I Clinical Trial License Agreement for the use of the Ichor TriGrid v2.0 Device |
- |
| (9) | Lineage Cell Therapeutics, Inc. | 2021-04-16 | License to allogenic vaccine technology | - |
(1)
| 계약상대방 | Johns Hopkins University (미국) |
| 계약내용 | LAMP 기술에 대한 전세계 독점 라이선스 계약 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일 : 2006.09.26 1차 개정 : 2008.02.01 2차 개정 : 2009.09.29 3차 개정 :2009.12.04 계약종료일:2025.11.24 |
| 총계약금액 | 1,341백만원(USD 995,000), ITI 보통주 15% (150,000 shares) |
| 지급금액 | 라이선스와 마일스톤 : - $10,000 계약금 (2006-09-26) - $65,000 ITI가 $1M 투자금 유치시 (2015-01-29) - $150,000 ITI가 $5M 투자금 유치시 (2015-01-29) - $100,000 JHU외부에서 Phase I 환자 첫 투약시 (2015-06.18) - $100,000 JHU외부에서 Phase II 환자 첫 투약시 (2017-08.11) 최소 연간 로열티 : - $5,000 5th year (2010-10-31) - $10,000 6th year (2011-10-31) - $25,000 7th year and beyond (2012-2021, 10 years) 로열티 : - 매출 발생에 의한 로열티 지급은 없었음 첫번째 계약변경 수수료 (2008-02-01) - 현금 $10,000 - Notes and warrants valued at $261,949 서브라이선스 : $750,000 on $15M Astellas JRC license (2015.02.20) $37,500,000 on $250M Astellas WW alergy license (2015.10.23) $750,000 on Zenoaq $5M license (2018.12.27) $750,000 on $5M Astellas Phase 2 milestone (2019.03.11) $300,000 on Zenoaq license fee (2019.09.26) $300,000 on Zenoaq option fee (2021.09.10) |
| 계약조건 | 계약금(Upfront Payment): 13백만원(USD 10,000) 마일스톤(Milestione): 1,328백만원(USD 985,000) - 지급조건:각 임상단계 성공, 판매 승인, 적응증 추가 등 로열티(Royalty): 매출액의 5% - 지급조건: 매출 발생시 - Sublicensing, 진행시 각 임상단계 성공, 판매 승인, 기타 계약 사항에 따라 15%~100%의 로열티율 적용 |
| 회계처리방법 | 계약금, 마일스톤 등 계약 대가 중에 자산화 요건을 충족하는 $1,028,199를 무형자산으로 계상하고 20년간 상각하고 있음 |
| 대상기술 | 다양한 적응증에 대한 LAMP 기술 |
| 개발진행경과 | LAMP 기술을 적용하여 현재 3개의 Pipeline (ITI-1000, ITI-1001, ITI-3000)에 대해 임상실험 진행 중 일본 Zenoaq사에 LAMP기술을 적용한 동물 알러지영역 신약개발에 대한 권리를 서브라이선스하여 임상실험 진행 중 일본 Astellas사에 일본삼나무알러지(JRC)와 전체 인간 알러지 영역 신약개발에 대한 권리를 서브라이선스하였음 그외에 LAMP기술을 적용할 수 있는 다양한 영역에 대한 기초연구 및 전임상 연구 진행 중 |
| 기타사항 | - |
(2)
| 계약상대방 | Nature Technology Corp. (미국) |
| 계약내용 | 백신 기술 공유 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일: 2015.01.22 (1차), 2016.06.20 (2차) 계약종료일 : 2035.08.18 |
| 총계약금액 | 135백만원(USD 100,000) |
| 지급금액 | 라이선스 : - $10,000 알러지 라이선스를 위한 계약금 (2015) - $100,000 암 포함 모든 다른 개발영역을 위한 계약금 (2016.07.15) 서브라이선스 : - $300,000 on $15M Astellas JRC license (2015.02.20) - $6,000,000 on $300M Astellas WW allergy license (2015.10.23) - $100,000 on $5M Astellas Phase 2 milestone (2019.12.02) - $140,000 on $7M in Zenoaq license fees (2020.05.01) - $40,000 on $2M Zenoaq option fee (2021.08.06) |
| 계약조건 | 계약금(Upfront Payment): 135백만원(USD 100,000) 로열티(Royalty): 매출액의 2%~5% - 지급조건: 제품 매출 발생, 라이선스 서비스 관련 매출 발생시 Sublicense 관련 수익의 2% |
| 회계처리방법 | 계약금, 마일스톤 등 계약 대가 중에 자산화 요건을 충족하는 $110,000를 무형자산으로 계상하였고 2019년까지 상각 완료 하였음 |
| 대상기술 | 플라스미드(Plasmid) 관련 비독점 라이선스 |
| 개발진행경과 | ITI는 NTC Plasmid를 사용하여 ITI-1001, ITI-3000 pDNA 암백신을 개발하고 있음. 또한 고효율pDNA 생산을 위한 HperGRO도 테스트 중에 있음 |
| 기타사항 | - |
(3)
| 계약상대방 | Annias Immunotherapeutics, Inc. (미국) |
| 계약내용 | CMV/pp65 관련 라이선스 계약 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일 : 2017.05.03 1차 갱신일 : 2019.10.14 계약종료일 : 2034.11.14 |
| 총계약금액 | 9,769백만원(USD 7,250,000), ITI 보통주 (250,000 shares) |
| 지급금액 | 계약금 : $250,000 현금 (2017.05.08) 250,000 warrants issued upfront valued at $295,000 연차 마일스톤 : $50,000 on 1st anniversary (2018.05.01) $100,000 on 2nd anniversary (2019.05.01) $350,000 on 3rd anniversary (2020.05.01) $1,000,000 on 4th anniversary (2021.05.01) |
| 계약조건 | 계약금(Upfront Payment): 337백만원(USD 250,000) 마일스톤(Milestione): 9,432백만원(USD 7,000,000) - 지급조건:각 임상단계 성공, 판매 승인, 적응증 추가 등 로열티(Royalty): 매출액의 5% - 지급조건: 매출 발생시 - Sublicensing: 매출액의 5%, 로열티를 제외한 Sublicense 관련 수익의 12.5% |
| 회계처리방법 | 계약금, 마일스톤 등 계약 대가 중에 자산화 요건을 충족하는 $2,045,000를 무형자산으로 계상하고 15년간 상각하고 있음 |
| 대상기술 | ITI-1000(교모세표종 치료를 위한 면역항암제) 및 기타 치료제에 대한 CMV/pp65 라이선스 |
| 개발진행경과 | ITI-1000 (1, 2상 임상)과 ITI-1001 (1상 임상)에 CMV Coding Sequences를 사용하고 있음 |
| 기타사항 | - |
(4)
| 계약상대방 | University of Florida Research Foundation, Inc. (미국) |
| 계약내용 | 세포치료제 개발 관련 계약 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일: 2018.06.28 계약종료일 : 미정; 2037.12.01으로 예상 |
| 총계약금액 | 67백만원(USD 50,000), ITI 보통주 (50,000 shares) |
| 지급금액 | $50,000 계약금 (2018.07.16) ITI보통주 50,000주 valued at $121,000 (2018.07) |
| 계약조건 | 계약금(Upfront Payment): 67백만원(USD 50,000) 로열티(Royalty): 매출액의 1% - 지급조건: 매출 발생시 |
| 회계처리방법 | 계약금, 마일스톤 등 계약 대가 중에 자산화 요건을 충족하는 $1,500를 무형자산으로 계상하고3년간 상각하고 있음 |
| 대상기술 | 세포치료제 개발관련 기술적 노하우(Know-how) |
| 개발진행경과 | 현재 UF (플로리다 대학)과의 협업은 ITI-1000의 임상 2상인 ATTAC-II study에 한정적으로 적용됨. |
| 기타사항 | - |
(5)
| 계약상대방 | University of Florida Research Foundation, Inc. (미국) |
| 계약내용 | 세포치료제 개발 관련 임상데이터 독점 라이선스 계약 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일: 2019.04.10 1차 갱신일 : 2020.02.19 계약종료일 : 미정; 2037.12.01으로 예상 |
| 총계약금액 | 674백만원(USD 500,000) |
| 지급금액 | 4번의 마일스톤 대금 지급 : $100,000 (2019.05.01) $50,000 (2019.10.16) $100,000 (2021.05.03) $50,000 (2021.05.03) |
| 계약조건 | 계약금(Upfront Payment): 135백만원(USD 100,000) 마일스톤(Milestione): 539백만원(USD 400,000) - 지급조건:각 임상단계 성공, 임상 데이터 수령 등 |
| 회계처리방법 | 자산화 요건 갖추지 못하여 발생 즉시 비용처리함 |
| 대상기술 | 세포치료제 개발 관련 임상데이터 독점 라이선스 |
| 개발진행경과 | 관련 연구에 플로리다 대학의 임상데이터 활용 중 |
| 기타사항 | - |
(6)
| 계약상대방 | Replicate Bioscience, Inc.(미국) |
| 계약내용 | Replicate 사의 지적재산권을 HPV, EBV, JRC, SARS-Cov-2에 사용하는 전세계 독점 라이선스 계약 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일 : 2021.07.13 계약종료일 : 무기한 |
| 총계약금액 | 25% of all sublicensing revenue (최소 Sublicensee 순매출의 2%) |
| 지급금액 | 연구개발 소요 비용을 지급, 라이선스 비용은 아직 발생 안함 |
| 계약조건 | 25% of all sublicensing revenue (최소 Sublicensee 순매출의 2%) |
| 회계처리방법 | 자산화 요건 갖추지 못하여 발생 즉시 비용처리함 |
| 대상기술 | Replicate사의 지적재산권 (Self-Amplifyng mRNA replicons와 formulated nanoparticles)을 HPV, EBV, JRC, SARS-Cov-2에 사용하는 전세계 독점 라이선스 |
| 개발진행경과 | 최초 데이터 확인결과 활용가능성이 높아, 광범위한 안전성과 POC(개념증명)을 위한 cGMP batch 결과를 기다리고 있음 |
| 기타사항 | - |
(7)
| 계약상대방 | CoImmune, Inc. (미국) |
| 계약내용 | ITI-1000(교모세포종 치료를 위한 면역항암제) 생산을 위한 CoImmune사와 파트너십 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일: 2020.11.10 계약종료일 : 미정; 2037.12.01으로 예상 |
| 총계약금액 | 10,780백만원(USD 8,000,000) |
| 지급금액 | $2,000,000 계약금 (2020.12.01) 기술이전에 따른 대금 지금: $82,500 (2021.02.16) $232,500 (2021.06.01) $253,929.60 (2022.03.01) |
| 계약조건 | 계약금(Upfront Payment): 2,695백만원(USD 2,000,000) 마일스톤(Milestione): 8,085백만원(USD 6,000,000) - 지급조건:각 임상단계 성공, 신규 파이프라인의 임상단계 성공 등 로열티(Royalty): 매출액의 0.5%~1% (계약 지역에 따라 상이) - 지급조건: 매출 발생시 |
| 회계처리방법 | 계약금, 마일스톤 등 계약 대가 중에 자산화 요건을 충족하는 $2,000,000를 무형자산으로 계상하였고 해당 기술과 관련된 신약승인 후 상각 시작 예정 |
| 대상기술 | ITI-1000(교모세포종 치료를 위한 면역항암제) 생산 노하우(Know-how) |
| 개발진행경과 | ITI는 "CoImmune Process"를 적용하여 ITI-1000 Commercial Product 생산을 테스트하고 있음 |
| 기타사항 | - |
(8)
| 계약상대방 | Ichor Medical Systems, Inc.(미국) |
| 계약내용 | Ichor사의 기술및 기기(=TridGrid v2.0 Device) 사용 관련 비상업적 연구 및 임상 1상 실험에 적용하는 것에 대한 라이선스 계약 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일 : 2020.05.31 계약종료일 : 2025.05.31 |
| 총계약금액 | 해당 기술/기기와 관련하여 ITI가 수령하는 모든 수익의 25%를 로열티 대금으로 지급 |
| 지급금액 | 기기를 테스트 기간동안 렌탈 비용 및 기타 부품 비용을 지급하였으나, 로열티 비용은 아직 발생하지 않음 |
| 계약조건 | 해당 기술/기기와 관련하여 ITI가 수령하는 모든 수익의 25%를 로열티 대금으로 지급 |
| 회계처리방법 | 자산화 요건 갖추지 못하여 발생 즉시 비용처리함 |
| 대상기술 | Ichor기업의 기술 및 기기(=TridGrid v2.0 Device) 사용 관련 비상업적 연구 및 임상 1상 실험에 적용하는 것에 대한 라이선스 |
| 개발진행경과 | Ichor사에서 관련 기기를 제공하였고, ITI-1001 임상 1상 연구에 활용될 예정임 |
| 기타사항 | - |
(9)
| 계약상대방 | Lineage Cell Therapeutics, Inc.(미국) |
| 계약내용 | 면역항암제 라이선스 계약 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일: 2021.04.16 계약종료일 : 2029.11.07 |
| 총계약금액 | 82,871백만원(USD 61,500,000) |
| 지급금액 | 라이선스 : $500,000 (2021.04.23) $500,000 (2021.08.11) 프로세스 개발 비용 : $179,213.00 (2021.08.16) $182,852.41 (2021.12.20) $182564.28 (2022.03.18) |
| 계약조건 | 계약금(Upfront Payment, R&D material 제공 등): 2,695백만원(USD 2,000,000) 마일스톤(Milestione): 80,176백만원(USD 59,500,000) - 지급조건:각 임상단계 성공, 판매 승인, 적응증 추가 등 |
| 회계처리방법 | 자산화 요건 갖추지 못하여 발생 즉시 비용처리함 |
| 대상기술 | Lineage Technology는 수지상세포(Dendritic Cell)에 Allogenic Delivery를 가능케 하는 기술로써 ITI-1000의 "Off the Shelf" 버전을 생산하기 위해 사용됨 |
| 개발진행경과 | Lineage 사에서 3개의 cGMP trial runs을 준비하였고, ITI는 이 프로그램을 임상시험에 어떻게 적용할지 연구하기 시작하였음. 2023년까지 이 기술을 적용한 임상시험 계획 (IND) 제출을 목표로 함 |
| 기타사항 | - |
2) 라이센스 아웃(License-out)계약
| 구분 | 계약 상대방 |
계약 체결시기 |
계약상의 주요내용 |
비 고 |
|---|---|---|---|---|
| (1) | Astellas Pharma Inc. | 2015-01-15 | Granted rights to the JRC-LAMP-vax vaccine to Astellas for the treatment of JRC Allergic Rhinitis via an ELA for Japan. |
Terminated Oct 2020 |
| (2) | Astellas Pharma Inc. | 2015-10-08 | An exclusive worldwide license to Astellas for the LAMP-vax products for the treatment or prevention of any and all allergic diseases in humans. |
- |
| (3) | Nippon Zenyaku Kogo Corp. | 2018-12-17 | A worldwide, exclusive, royalty-free, sublicensable license in the canine allergic diseases field. Additionally, there is an option for expanding the field to either infectious disease in animals, cancer in animals, or both. |
- |
| Licensed Technologies has been updated | As of 2020-03-11 | |||
| (4) | Genoa | 2007-09-14 | Non-exclusive license in South America to delelop LAMP-Vax products for treating HIV-1/HIV-2 and two additional cancer targets. |
Terminated May 2009 |
| (5) | Elanco | 2011-12-29 | Exclusive license worldwide to delelopup to five LAMP-Vax products in animal health |
- |
| (6) | Geron | 2006-10-30 | ITI granted Geron a worldwide, exclusive, royalty-bearing, sublicensable license for patent rights in the field of telomerase. |
- |
| (7) | On Therapeutics, Limited | 2021-05-11 | ITI granted On Therapeutics an exclusive royalty-bearing, sublicenseable license to develop, manufacture and commercialize the Licensed Assets and Products with respect to ITI-1000, 2000, 4000 and 6000 in China, Hong Kong, Macau, Taiwan, Indonesia, Malaysia, Philippines, singapore, Vietnam and Thailand |
- |
(1)
| 계약상대방 | Astellas Pharma Inc. (일본) |
| 계약내용 | 일본 적삼나무(Japanese Red Cedar, JRC) 알레르기에 의한 비염 치료용 JRC-LAMP-Vax 백신 라이선스 계약 |
| 대상지역 | Japan |
| 계약기간 | 계약체결일: 2015.01.15 계약종료일: 2020.10.22 |
| 총계약금액 | 80,850백만원 (USD 60,000,000) |
| 수익금액 | 라이선스와 마일스톤 : $15,000,000 upfront received 2015.02.13 $5,000,000 Phase 2 milestone received 2019.03.11 Various CMC production payments received 2015-2019 |
| 계약조건 | 계약금 (Upfront Fee) : 20,212 백만원 (USD 15,000,000) 마일스톤(Milestone) : 60,637 백만원 (USD 45,000,000) - 지급조건 : 임상단계 진행, 판매승인 등 로열티(Royalty): 매출액 구간에 따라 10% ~ 20% |
| 회계처리방법 | 계약금, 마일스톤은 수령시 라이선스 수익으로 인식, 로열티는 발생하지 않음 |
| 대상기술 | 일본 적삼나무(Japanese Red Cedar, JRC) 알레르기에 의한 비염 치료용 JRC-LAMP-Vax 백신 라이선스 |
| 개발진행경과 | Astellas 사가 임상 1상을 성공적으로 수행한 후 임상 2상을 진행하였으나, 임상 2상의 결과는 통계적 유의성을 만족하지 못함. Astellas 사가 추가 임상 진행을 포기함에 따라 라이선스는 ITI로 반환됨 (기수령 라이선스/마일스톤 반환 의무 없음). Astellas사가 임상 2상을 진행할 때, ITI의 프로토콜을 따르지 않음에 따라, ITI는 해당 라이선스 영역 (JRC Allergy)에 대한 개발 기회가 여전히 있다고 판단하고 자체 개발 계획을 진행하고 있음 (ITI-9001) |
| 기타사항 | 계약 종료 |
(2)
| 계약상대방 | Astellas Pharma Inc. (일본) |
| 계약내용 | 알레르기 예방 및 치료를 위한 LAMP-VAX Platform관련 글로벌 라이선스 계약 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일 : 2015.10.08 계약종료일 : 2022.07.06 |
| 총계약금액 | 404,250백만원(USD 300,000,000) |
| 수익금액 | $300,000,000 계약금 수령 2015.10.16 |
| 계약조건 | 계약금(Upfront Payment): 404,250백만원(USD 300,000,000) 로열티(Royalty): 매출액의 10% |
| 회계처리방법 | 계약금 3억불을 전체 계약 조건에 대한 선수금으로 판단하여 개발진행 상황을 고려하여 3개년에 걸쳐 수익인식함 (2015년~2017년) |
| 대상기술 | JRC를 제외한 전체 인간 알레르기 예방 및 치료를 위한 LAMP-VAX Platform관련 글로벌 라이선스 |
| 개발진행경과 | Astellas는 HDM(House Dust Mite, 집먼지 알러지)와 땅콩 알러지에 대해 임상 1상을 진행하여안정성 기준은 만족하였으나 효과성 목표를 달성하지 못하였음. Astellas가 추가 임상을 포기함에 따라 라이선스는 ITI로 반환됨. Astellas사가 임상 1상을 진행할 때, ITI의 프로토콜을 따르지않음에 따라, ITI는 해당 라이선스 영역 (Human Allergy)에 대한 개발 기회가 여전히 있다고 판단하고 자체 개발 계획을 염두에 두고 있음 |
| 기타사항 |
(3)
| 계약상대방 | Nippon Zenyaku Kogo Corp.(일본) |
| 계약내용 | 알레르기 질환 분야에 대한 전세계 독점 라이선스 계약 (동물의 전염병이나 암 분야로 확장 가능한 라이선스) |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일 : 2018.12.17 계약종료일 : 2039.05 |
| 총계약금액 | 16,170백만원(USD 12,000,000) |
| 수익금액 | 라이선스 : $350,000 received 2017.10.13 $4,650,000 received 2018.12.26 $2,000,000 received 2019.09.24 $2,000,000 option received 2021.08.30 Various other CMC production payments received |
| 계약조건 | 계약금(Upfront Payment): 6,738백만원(USD 5,000,000) 마일스톤(Milestione): 9,432백만원(USD 7,000,000) - 지급조건: 판매 승인, 적응증 추가 등 |
| 회계처리방법 | 수령시 라이선스 수익으로 인식 |
| 대상기술 | 알레르기 질환 분야에 대한 전세계 독점 라이선스 (동물의 전염병이나 암 분야로 확장 가능) |
| 개발진행경과 | Zenyaku (AKA Zenoaq)사에서 동물 알러지 분야의 여러 개 약품을 개발하고 있으며, 동물 암d영역 개발도 고려하고 있음. |
| 기타사항 |
(4)
| 계약상대방 | Genoa (Brazil) |
| 계약내용 | 남미에서 HIV-1/HIV-2 및 2개의 추가적인 암 표적 치료의 LAMP-Vax제품 개발을 위한 비독점 라이선스 계약 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일 : 2007.09.14 계약종료일 : 2009-05 |
| 총계약금액 | 2,021백만원(USD 1,500,000) |
| 수익금액 | 수령금액 없음 |
| 계약조건 | 계약금(Upfront Payment 등): 2,021백만원(USD 1,500,000) |
| 회계처리방법 | - |
| 대상기술 | 남미에서 HIV-1/HIV-2 및 2개의 추가적인 암 표적 치료의 LAMP-Vax제품 개발을 위한 비독점 라이선스 부여 |
| 개발진행경과 | Genoa의 계약 대금 지불 불이행에 따라 2009년 계약 해지함 |
| 기타사항 | 계약종료 |
(5)
| 계약상대방 | Elanco (미국) |
| 계약내용 | 수의(Animal health) 분야에서 5가지 LAMP-Vax 제품을 개발할 수 있는 전세계 독점 라이선스 계약 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일 : 2011.12.29 계약종료일 : 2015.05 |
| 총계약금액 | 9,769백만원(USD 7,250,000) |
| 수익금액 | $500,000 received 2012.03.07 |
| 계약조건 | 계약금(Upfront Payment 등): 2,021백만원(USD 1,500,000) 마일스톤(Milestione): 7,748백만원(USD 5,750,000) - 지급조건: 판매 승인, 파이프라인 개발 등 로열티(Royalty): 매출구간별, 지역별 계약사항에 따라 5%~7% |
| 회계처리방법 | 수령시 라이선스 수익으로 인식 |
| 대상기술 | 수의(Animal health) 분야에서 5가지 LAMP-Vax 제품을 개발할 수 있는 전세게 독점 라이선스 |
| 개발진행경과 | 동물에 대한 예비 연구(2012 ~ 2013) 이후 계약해지 함 (예비 연구결과는 긍정적) |
| 기타사항 | 계약종료, 계약상대방은 Eli Lilly사로 Elanco 동물연구부분과 계약함 |
(6)
| 계약상대방 | Geron (미국) |
| 계약내용 | 텔로머라아제(Telomerase) 관련 특허에 대한 전세계 독점 라이선스 계약 |
| 대상지역 | Worldwide |
| 계약기간 | 계약체결일 : 2006.10.30 계약종료일 : 2025.11.24 |
| 총계약금액 | 2,291백만원(USD 1,700,000) |
| 수익금액 | $150,000 received 2006.11.20 |
| 계약조건 | 계약금(Upfront Payment): 202백만원(USD 150,000) 마일스톤(Milestione): 2,089백만원(USD 1,550,000) - 지급조건:각 임상단계 성공, 판매 승인, 적응증 추가 등 로열티(Royalty): 매출액의 0.5% - 지급조건: 매출 발생시 - Sublicensing, 진행시 매출액의 0.5% |
| 회계처리방법 | 수령시 라이선스 수익으로 인식 |
| 대상기술 | 텔로머라아제(Telomerase) 관련 특허에 대한 전세계 독점 라이선스 계약 |
| 개발진행경과 | 라이선스 사용자 (Geron/Asterias/Lineage)는 LAMP를 인간 텔로머라아제(Human Telomerase)에 연결시키는 세포치료분야를 계속하여 개발하고 있으며 전립선암, AML, 폐암 등 분야에 대한 여러개의 임상시험을 진행하고 있음 |
| 기타사항 | Geron사는 세포치료 라인 부문을 분사하여 Asterias사를 설립하였고 해당 라이선스를 최근까지 유지하였음. 최근에 해당 라이선스를 Lineage 사에 이전함 |
(7)
| 계약상대방 | On Therapeutics, Limited (홍콩) |
| 계약내용 | 중국을 포함한 동남아시아 지역에 LAMP - base Vaccine 시장을 확대하기 위해 ONRx에 해당 라이선스를 부여함. 주로 HPV 치료에 중점을 둠 |
| 대상지역 | China, Hong Kong,Macau, Taiwan, Indonesia, Malaysia, Philippines, singapore, Vietnam and Thailand |
| 계약기간 | 계약체결일 : 2021.06.26 계약종료일 : 2022.07.31 |
| 총계약금액 | 109,282백만원(USD 81,100,000), On Therapeutics, Limited 보통주 15% |
| 수익금액 | 수령금액 없음 |
| 계약조건 | 계약금(Upfront Payment): 1,348백만원(USD 1,000,000) 마일스톤(Milestione): 107,934백만원(USD 80,100,000) - 지급조건:각 임상단계 성공, 판매 승인, 적응증 추가 등 로열티(Royalty): 매출액의 5%~8%(지역별, 매출구간별 상이) - 지급조건: 매출 발생시 - Sublicensing, 진행시 매출액의 20% |
| 회계처리방법 | - |
| 대상기술 | 중국을 포함한 동남아지역에 ITI-1000, 2000, 4000, 6000과 관련한 개발, 제조, 상업화를 위해On Therapeutics에 독점 Sub-Licensed 부여 |
| 개발진행경과 | OnRx사가 Funding Milestone 계약조건을 지키지 못하여 계약해지 통보하였음. 현재 90일 치유기간이 부여 중 |
| 기타사항 |
(다) 신규 pipeline 확보를 위한 타법인 지분 출자계약
1) Immunomic Therapeutics Inc.
| 당사는 2020년 02월 19일자로 신규 pipeline 확보를 위하여 미국 소재의 ImmunomicTherapeutics Inc. 의 최대주주 지분을 취득하기로 하는 출자 계약을 체결하였습니다. 당사는 해당 내용에 대하여 2020년 02월 19일자로 금융감독원 전자공시시스템에 공시하였으며, 공시된 내용은 아래와 같습니다. |
[타법인 주식 및 출자증권 취득결정(2020.02.19)]
| 회사 | 회사명(국적) | Immunomic Therapeutics,Inc. | 대표이사 | William G. Hearl |
| 자본금(원) | 1,444,585 | 회사와 관계 | 기타 | |
| 발행주식총수(주) | 12,923,463 | 주요사업 | 바이오의약품 개발 | |
| -최근 6월 이내 제3자 배정에 의한 신주취득 여부 |
아니오 | |||
| 2. 취득내역 | 취득주식수(주) | 6,000,000 | ||
| 취득금액(원) | 35,643,000,000 | |||
| 자기자본(원) | 485,628,745,774 | |||
| 자기자본대비(%) | 7.34 | |||
| 대기업 여부 | 해당 | |||
| 3. 취득후 소유주식수 및 지분비율 | 소유주식수(주) | 8,000,000 | ||
| 지분비율(%) | 38.16 | |||
| 4. 취득방법 | 현금취득(3자배정 유상증자 참여) | |||
| 5. 취득목적 | 지분 취득을 통한 기업가치극대화 | |||
| 6. 취득예정일자 | 2020-04-30 | |||
| 7. 자산양수의 주요사항보고서 제출대상 여부 | 아니오 | |||
| -최근 사업연도말 자산총액(원) | 304,040,778,357 | 취득가액/자산총액(%) | 11.72 | |
| 8. 우회상장 해당 여부 | 아니오 | |||
| -향후 6월이내 제3자배정 증자 등 계획 | 아니오 | |||
| 9. 발행회사(타법인)의 우회상장 요건 충족여부 | 아니오 | |||
| 10. 이사회결의일(결정일) | 2020-02-19 | |||
| -사외이사 참석여부 | 참석(명) | 2 | ||
| 불참(명) | 1 | |||
| -감사(감사위원) 참석여부 | 불참 | |||
| 11. 공정거래위원회 신고대상 여부 | 미해당 | |||
| 12. 풋옵션계약 등의 체결여부 | 아니오 | |||
| -계약내용 | - | |||
| 13. 기타 투자판단에 참고할 사항 | - 상기 자산총액은 2018년도말 연결재무제표상 기준입니다. - 상기 자기자본은 2018년도말 연결재무제표를 기준에서 현재까지 증가된 자본금 및 자본잉여금 증감액을 반영한 금액입니다. - 상기 취 득금액은 USD 30,000,000로 이사회결의일 당일 서울외국환중개㈜의 최초 고시 매매기준환율(1,188.10 KRW/USD)을 적용하여 산정하였습니다. - 하기 발행회사의 요약재무상황은 2018년말, 2017년 말, 2016년말 기준입니다. |
|||
[발행회사의 요약 재무상황]
| (단위 : 백만원) |
| 구분 | 자산총계 | 부채총계 | 자본총계 | 자본금 | 매출액 | 당기순이익 |
| 당해년도(2018년 말) | 22,962 | 26,153 | -3,190 | 1 | 1,827 | -13,800 |
| 전년도(2017년 말) | 30,683 | 21,793 | 8,890 | 1 | 206,673 | 110,073 |
| 전전년도(2016년 말) | 224,530 | 334,396 | -109,866 | 2 | 152,991 | 73,853 |
[상대방에 관한 사항]
| 1. 인적사항 | |||
| - 기본사항 | |||
| 성명(명칭) | 국적 | 주소(본점소재지)[읍ㆍ면ㆍ동까지만 기재] | 생년월일(사업자등록번호 등) |
| Immunomic Therapeutics,Inc. | 미국 | 메릴랜드주 락빌시 | - |
| 직업(사업내용) | 바이오의약품 개발 | ||
| - 최대주주ㆍ대표이사ㆍ대표집행임원 현황 및 재무상황 등(상대방이 법인인 경우) | |||
| 구분 | 성명 | 주식수 | 지분율(%) |
| 최대주주 | Hummel Family LP | 1,354,301 | 9.05 |
| 대표이사 | William G.Hearl | 857,590 | 5.73 |
| (단위 : 백만원) | |||
| 해당 사업연도 | 2018 | 결산기 | 12월 |
| 자산총계 | 22,962 | 자본금 | 1 |
| 부채총계 | 26,153 | 매출액 | 1,827 |
| 자본총계 | -3,190 | 당기순손익 | -13,800 |
| 외부감사인 | - | 휴업 여부 | 아니오 |
| 감사의견 | - | 폐업 여부 | 아니오 |
| 2. 상대방과의 관계 | |||
| 1. 회사와 상대방과의 관계 | - | ||
| 2. 회사의 최대주주ㆍ임원과 상대방과의 관계 | 성명 | 상대방과의 관계 | |
| - | - | - | |
| 3. 최근 3년간 거래내역(일상적 거래 제외) | |||
| 구분 | 거래 내역 | ||
| 당해년도 | 2020년1월31일 지분취득(제3자배정 유상증자)-USD10,000,000 | ||
| 전년도 | - | ||
| 전전년도 | - | ||
2) Verismo Therapeutics Inc.
| 당사는 2021년 03월 29일자로 신규 pipeline 확보를 위하여 미국 소재의 Verismo Therapeutics Inc. 의 지분을 취득하기로 하는 출자 계약을 체결하였습니다. 당사는 해당 내용에 대하여 2021년 03월 29일자로 금융감독원 전자공시시스템에 공시하였으며, 공시된 내용은 아래와 같습니다. |
[타법인 주식 및 출자증권 취득결정(자율공시)(2021.03.29)]
| 회사 | 회사명(국적) | VERISMO THERAPEUTICS,INC. | 대표이사 | Bryan Byong Jin Kim |
| 자본금(원) | 1,199,041 | 회사와의관계 | - | |
| 발행주식총수(주) | 10,594,109 | 주요사업 | 바이오의약품 개발 | |
| 2. 취득내역 | 취득주식수(주) | 1,912,777 | ||
| 취득금액(원) | 5,659,000,000 | |||
| 자기자본(원) | 610,197,014,014 | |||
| 자기자본대비(%) | 0.93 | |||
| 대기업해당여부 | 해당 | |||
| 3. 취득후 소유주식수 및 지분비율 | 소유주식수(주) | 1,912,777 | ||
| 지분비율(%) | 10.00 | |||
| 4. 취득방법 | 현금취득(3자배정 유상증자 참여) | |||
| 5. 취득목적 | 지분 취득을 통한 기업가치극대화 | |||
| 6. 취득예정일자 | 2021-04-12 | |||
| 7. 자산양수의 주요사항보고서 제출대상 여부 | 아니오 | |||
| - 최근 사업연도말 자산총액(원) | 362,612,148,006 | 취득가액/자산총액(%) | 1.56 | |
| 8. 우회상장 해당 여부 | 아니오 | |||
| - 향후 6월이내 제3자배정 증자 등 계획 | 아니오 | |||
| 9. 발행회사(타법인)의 우회상장 요건 충족여부 |
아니오 | |||
| 10. 이사회결의일(결정일) | 2021-03-29 | |||
| - 사외이사 참석여부 | 참석(명) | 3 | ||
| 불참(명) | 0 | |||
| - 감사(감사위원) 참석여부 | 참석 | |||
| 11. 공정거래위원회 신고대상 여부 | 미해당 | |||
| 12. 풋옵션계약 등의 체결여부 | 아니오 | |||
| - 계약내용 | - | |||
| 13. 기타 투자판단에 참고할 사항 | - 상기 자산총액은 2019년도말 연결재무제표상 기준입니다. - 상기 자기자본은 2019년도말 연결재무제표를 기준에서 현재까지 증가된 자본금 및 자본잉여금 증감액을 반영한 금액입니다. - 상기 취득금액은 USD5,000,000.00로 이사회결의일 당일 서울외국환중개㈜ 의 최초 고시 매매기준환율(1,131.80 KRW/USD)을 적용하여 산정하였습니다. - 하기 발행회사의 요약재무상황은 2020년 6월에 설립하여 최근사업연도 자본금만 기재하였습니다. |
|||
| ※ 관련공시 | - | |||
[발행회사의 요약 재무상황]
| (단위 : 백만원) |
| 구분 | 자산총계 | 부채총계 | 자본총계 | 자본금 | 매출액 | 당기순이익 |
| 당해연도(2020년 말) | - | - | - | 1 | - | - |
| 전연도(2019년도 말) | - | - | - | - | - | - |
| 전전연도(2018년 말) | - | - | - | - | - | - |
나. 연구개발 활동
[에이치엘비㈜]
(1) 연구개발활동의 개요
끊임없는 도전과 무한한 창조력으로 기술혁신의 새역사를 창조하는 기술연구소는 남보다 한 발 앞서가는 기술력과 최고의 제품을 향한 신념으로 미래를 개척하고 있습니다. 기술연구소의 주요업무로는 신제품 및 신기술 개발, 생산프로세스 개선, 신뢰성 있는 시험평가, 컴퓨터 시뮬레이션에 의한 사전 설계품질 검증 등을 추진하고 있습니다.
(2) 연구개발비용
(연결기준)
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 천원) |
| 구 분 | 제38기 당반기 | 제37기 | 제36기 | 비 고 | |
|---|---|---|---|---|---|
| 비용의 성격별 분류 |
원재료비 | - | - | - | - |
| 인건비 | - | - | - | - | |
| 감가상각비 | - | - | - | - | |
| 위탁용역비 | - | - | - | - | |
| 임상비용 | 22,308,040 | 47,912,224 | 22,272,570 | - | |
| 기타 | 470,053 | 896,847 | 1,187,498 | - | |
| 연구개발비용 합계 | 22,778,093 | 48,809,070 | 23,460,068 | - | |
| (정부보조금) | (174,884) | (389,994) | (866,183) | - | |
| 보조금 차감 후 금액 | 22,603,209 | 48,419,076 | 22,593,885 | - | |
| 회계처리 내역 |
판매비와 관리비 | 22,603,209 | 48,419,076 | 22,593,885 | - |
| 제조경비 | - | - | - | - | |
| 개발비(무형자산) | - | - | - | - | |
| 회계처리금액 계 | 22,603,209 | 48,419,076 | 22,593,885 | - | |
| 연구개발비 / 매출액 비율 [연구개발비용합계÷당기매출액×100] |
18.33 | 69.34 | 40.22 | - | |
(별도기준)
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 천원) |
| 구 분 | 제38기 당반기 | 제37기 | 제36기 | 비 고 | |
|---|---|---|---|---|---|
| 비용의 성격별 분류 |
원재료비 | - | - | - | - |
| 인건비 | - | - | - | - | |
| 감가상각비 | - | - | - | - | |
| 위탁용역비 | - | - | - | - | |
| 기타 | 454,321 | 634,437 | 1,151,257 | - | |
| 연구개발비용 합계 | 454,321 | 634,437 | 1,151,257 | - | |
| (정부보조금) | (174,884) | (389,994) | (866,183) | - | |
| 보조금 차감 후 금액 | 279,437 | 244,443 | 285,074 | - | |
| 회계처리 내역 |
판매비와 관리비 | 279,437 | 244,443 | 285,074 | - |
| 제조경비 | - | - | - | - | |
| 개발비(무형자산) | - | - | - | - | |
| 회계처리금액 계 | 279,437 | 244,443 | 285,074 | - | |
| 연구개발비 / 매출액 비율 [연구개발비용합계÷당기매출액×100] |
0.23 | 0.67 | 0.59 | - | |
[연결대상 종속회사(Elevar Therapeutics, Inc.)]
(1) 연구개발활동의 개요
종속회사인 Elevar Therapeutics, Inc.의 연구개발 조직은 신약개발에 대한 연구를 진행하고 있습니다. 그 동안 표적항암제를 연구개발해 오면서 축적된 기술력과 노하우를 바탕으로 새로운 가치창조를 이루어 가고 있습니다.
(2) 연구개발 담당조직
(가) 회사의 조직구성
종속회사인 Elevar Therapeutics, Inc.의 연구개발 조직구성은 다음과 같습니다.
 |
|
elevar 조직도 |
(나) Elevar Therapeutics, Inc. 연구개발 조직구성
1) Bio 연구, 개발, 허가, 임상을 담당하는 박사급 16명, 석사급 15명 등 총 48명의 연구인력을 보유하고 있습니다.
| (단위 : 명) |
| 구분 | 박사 | 석사 | 기타 | 계 |
| 인원수(Head Count) | 16 | 15 | 17 | 48 |
2) 핵심 연구인력
| 직책 | 성명 | 주요경력 | 주요연구실적 |
| CEO | Saeho Chong | - VP of nonclinical development, Alnylam Pharmaceuticals - Clinical Pharmacology Reviewer at US FDA - Professor at Seoul National University, College of Pharmacy - Head of Metabolism and Pharmacokinetics, Hopewell Site, Bristol-Myers Squibb R&D |
[Associated careers] 1. 4 NDA submission and approval in US and EU in the past five years 2. Discovered and developed new drug candidates in cardiovascular-, metabolic-, immunologic-diseases, and oncology 3. Over 90 publications in peer-reviewed scientific journals |
| Chief Medical Officer | Jan Van Tornout | - SVP, Head of Oncology, Radius Health, Inc. - Head of Clinical Research, ARIDA Phamaceutical, Inc. - Global Clinical Lead, Oncology, Pfizer |
[Publications] 1. Joaquin Mateo, David Olmos, Herlinde Dumez, Srinivasu Poondru, Nancy L. Samberg, Sharon Barr, Jan M. Van Tornout, Fei Jie, Shahneen Sandhu, D. S. Tan, Victor Moreno, P.(2016) "A first in man, dose-finding study of the mTORC1/mTORC2 inhibitor OSI-027 in patients with advanced solid malignancies" British Journal of Cancer. Apr;114(8):889-896. |
| Chief Operating Officer | Seong Hoon Jang | - Lead Pharmacologist at USFDA - PhD. In Pharmacetics at Ohio State Univ. - Ms. In Pharmacokinetics at Seoul National Univ. |
[Associated careers] 1. Reviews of >50 NDAs and >500 INDs 2. 28 publications in peer-reviewed scientific journals 3. Contributed to development of numerous FDA Guidances for Industry and NDA/IND Review Policies |
| Vice President, Clinical Pharmacology |
Honghui Zhou | - Head of Pharmacometrics (US), Janssen/Johnson & Johnson - Clinical Pharmacology Head of Immunology, Janssen/ Johnson & Johnson - Head of Pharmacological and Translational Modeling, Janssen/Johnson & Johnson - Head of Biotherapeutics PK/PD and Modeling & Simulation, Centocor/Johnson & Johnson - Director of Clinical Pharmacology, Pfizer |
[Associated careers] 1. Contributed to approvals of 8 first-time BLAs and a number of sBLAs/sNDAs 2. Co-edited three books in therapeutic protein drug development, translational ADME and drug-drug interactions 3. Authored and co-authored >150 publications in peer-reviewed scientific journals and book chapters 4. Advanced numerous clinical product candidates of early and late-stage assets for immune-mediated inflammatory diseases, oncology/hematology, cardiovascular/metabolic disease therapeutic areas |
| Vice President, Drug Safety and Pharmacovigilance | David Lilienfield | - Senior Director, Safety, Pharmacovigilance and Epidemiology, Recursion - MD, medicine, Univ. of Maryland School of Medicine |
[Associated careers] 1. Lilienfeld's Foundations of Epidemiology, 2015 2. Comparison of 2 Interventions for Liquid Aspiration on Pneumonia Incidence A Randomized Trial and over 70 articles and data |
| Vice President, Clinical Operations and Data Management | Jennifer Lee | - Executive Director, Head of Oncology Clinical Development, Radius Health - Head of Clinical Operations for startup biotech companies, Medeor and Iovance - Leadership role at Pfizer, Astellas, and Gilead |
[Associated careers] 1. Contributed to approvals of 7 novel treatments in global markets and subsequent filings 2. Contributed to successful global inspection outcomes with FDA/EMA/MHRA/PDMA/NMPA 3. 10 publications in peer-reviewed scientific journals and abstracts 4. Advanced numerous clinical product candidates of early and late stage assets for (Immuno)-oncology, neurological disorder, cardiovascular, and infectious disease therapeutic areas, resulted in global market applications, licensing agreements, and labeling changes |
(3) 임상 개발 실적
| 구 분 |
개발제품 |
적응증 |
개발현황 및 향후 계획 |
|
신약개발 |
리보세라닙 |
표적항암제 |
- 위암말기 치료제 : 임상3상 종료 Pre-NDA 실시, - 고형암 옵디보(Nivolumab) 병용 : 임상1상 종료 - 위암 2차 치료제(파클리탁셀 병용) : 임상1/2상 진행 중 - 대장암 3차 치료제(론서프 병용) : 임상1상 진행 중 |
(4) 특허권 보유 현황
(가) 리보세라닙(Rivoceranib, 구 Apatinib Mesylate)
|
특허유형 |
제출일 |
국가명 |
구분 |
상태 |
비 고 |
|
물질 특허 |
2004.06.02 |
United States Europe Japan Korea Canada |
특허권리 보유 |
Issued |
- 3가지 적응증에 대해 희귀의약품 지정 특허권 보장 받을 수 있음 |
|
염조성물 특허 |
2009.06.11 |
United States Europe Japan Korea Canada Russia Australia South Africa Hong Kong |
전용실시권 보유 |
Issued |
(나) 아필리아(Apealea)
|
특허유형 |
제출일 |
국가명 |
상태 |
비고 |
|
수용성의 양이온성 양친매성 |
2008-12-18 |
Australia Brazil Canada China Eurasia Europe India Japan S Korea Mexico Malaysia New Zealand Ukraine USA South Africa |
Issued |
만료일 2028-12-18 수용성의 양이온성 양친매성 물질의 인체내 전달시스템에 대한 특허 (도세탁셀, 독소루비신등) |
| 물에 난용성인 제약학적 활성 물질의 투여를 위한 약물 전달 시스템 |
2008-12-18 |
Armenia Azerbaijan Belarus Kyrgyzstan Kazakhstan R. Moldova Russian Tajikistan Turkmenistan Australia Canada Austria Bulgaria Swizerland Germany Denmark Estonia Spain Finland U.K. Ireland Iceland Liechtenstin Lithuania Luxenbourg Malta Norway Portugal Sweden Slovenia Slovakia Malaysia USA S. Africa China Belgium Cyprus Czechia France Greece Croatia Hungary Italy Latvia Monaco Netherlands Poland Romania Turkiye Japan R.Korea Mexico New Zealand |
Issued |
만료일 난용성 물질의 인체내 전달시스템에 |
|
2012-09-18 |
Ukraine |
Issued |
만료일 |
|
|
Taxol containing compositions |
2003-10-28 |
Malaysia |
Issued |
만료일 |
|
Therapeutic compounds |
2002-11-15 |
USA EP Germany U.K. China HongKong |
Issued |
만료일 USA 2023-04-11 나머지 국가 약물 전달체 조성에 대한 특허 |
|
Method for producing |
2016-12-09 |
USA HongKong |
Issued |
만료일 2036-12-09 약물 전달체 제조방법 특허 |
(5) 연구개발비용
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 천원) |
|
과 목 |
제38기 당반기 | 제37기 | 제36기 |
비 고 |
|
|
비용의 성격별 분류 |
재료비 | - | - | - | - |
| 인건비 | - | - | - | - | |
| 임상비용 | 18,258,505 | 38,967,133 | 18,117,113 | - | |
|
연구개발비용 합계 |
18,258,505 | 38,967,133 | 18,117,113 | - | |
|
(정부보조금) |
- | - | - | - | |
|
보조금 차감 후 금액 |
18,258,505 | 38,967,133 | 18,117,113 | - | |
|
회계처리 내역(*1) |
판매비와 관리비 |
18,258,505 | 38,967,133 | 18,117,113 | - |
|
제조경비 |
- | - | - | - | |
|
개발비(무형자산) |
- | - | - | - | |
|
회계처리금액 계 |
18,258,505 | 38,967,133 | 18,117,113 | - | |
|
연구개발비 / 매출액 비율(%)(*2) [연구개발비용계÷당기매출액×100] |
N/A | N/A | N/A | - | |
(*1) 연구개발비용을 자산으로 인식한 내용이 없습니다.
(*2) 종속회사인 Elevar Therapeutics, Inc.가 연구개발 중인 의약품개발사업 관련 매출액이 존재하지 않아, 매출액 대비 비율은 없습니다.
[연결대상 종속회사(Immunomic Therapeutics, Inc.)]
(1) 연구개발활동의 개요
종속회사인 이뮤노믹(Immunomic Therapeutics, Inc.)의 연구개발 조직은 암, 알레르기 등 질환에 대한 핵산 면역치료 플랫폼(nucleic acid immunotherapy platforms)을 연구개발하고 있습니다. 이뮤노믹은 백신 디자인, 개발, 생산 및 시험에 대한 전문성을 바탕으로 암, 알레르기와 동물치료제에 대한 면역치료(immunotherapy)가 가능한 백신으로 인간의 삶을 변화시키고자 노력하고 있습니다.
(2) 연구개발 담당조직
(가) 회사의 조직구성
종속회사인 Immunomic Therapeutics, Inc. 의 조직구성은 다음과 같습니다.
 |
|
Immunomic therapeutics, inc. 조직도 |
(나) Immunomic Therapeutics, Inc. 연구개발 조직구성
1) Bio 연구, 개발, 허가, 임상을 담당하는 박사급 9명, 석사급 6명 등 총 26명의 연구인력을 보유하고 있습니다.
| (단위 : 명) |
| 구분 | 박사 | 석사 | 기타 | 계 |
| 인원수 | 9 | 6 | 11 | 26 |
2) 핵심 연구인력
| 직책 | 성명 | 주요경력 | 주요연구실적 |
| CEO | William Hearl | CSO, Capital Genomix EVP, Kirkegaard & Perry Laboratories |
[Patents] 1. Nucleic Acids for the Treatment of Allergy (PCT/US2012/042552, issued Japan) 2. Nucleic Acids for the Treatment of Peanut Allergies (PCT/US2015/321,366) 3. Chimeric Vaccines (US Pat No. 8,445,660 & 8,318,173) 4. Genetic immunization of transgenic animals with non-eukaryotic expression systems (20060026697) 5. Genetic Immunization with Cationic Lipids (US Pat No. 6,890,554) 6. Genetic Immunization with Cationic Lipids (US Pat No. 7,166,298) 7. Combinatorial Oligonucleotide PCR: A Method for rapid global expression analysis (US Pat No. 6,221,600) 8. Combinatorial Oligonucleotide PCR (7,115,370) 9. Reversible Association of Nucleic Acid with Carboxylated Substrate (US Pat No. 7,052,840) 10. Method Of Reducing Background In Biotin-Based Assays (US Pat No. 6,096,508) 11. Formazan-based Immunoassay (US Pat No. 5,916,746) [Publication] 1. W. G. Hearl, M. E. Boling, M. H. Jones and E. Volkin. (1982) "Compartmentation of the Nucleotide Pool." Fed. Proc. 41, 1295. 2. William G. Hearl and K. Bruce Jacobson. (1984) "Eye Pigment Granules of Drosophila melanogaster: Isolation and Characterization for Synthesis of Sepiapterin and Precursors of Drosopterin." Insect Biochem. 14, 329-335. 3. William G. Hearl and Jorge E. Churchich. (1984) "Interaction between 4-Aminobutyrate Aminotransferase and Succinic Semialdehyde Dehydrogenase, Two Mitochondrial Enzymes." J. Biol. Chem. 259, 11459-11463. 4. William G. Hearl and Jorge E. Churchich. (1985) "A Mitochondrial NADP+-Dependent Reductase Related to the GABA Shunt: Purification, Characterization and Mechanism. J. Biol. Chem. 260, 16361-16366. 5. William G. Hearl and Margaret I. Johnston. (1986) "Misaligned Double-Stranded RNA Activates 2',5'- Oligoadenylate Synthetase In Vivo." Biochem. Biophys. Res. Comm. 138, 40-46. 6. Margaret I. Johnston and William G. Hearl. (1987) "Purification and Characterization of a 2'-Phosphodiesterase from Bovine Spleen." J. Biol. Chem. 262, 8377-8382. |
| CSO | Teri Heiland, PhD | SVP, R&D VP, R&D Section Leader, Capital Genomix |
[Patents] 1. Genetic Immunization of transgenic animals with non-eukaryotic expression system (20060026697) 2. Combinatorial Oligonucleotide PCR: A Method for rapid global expression analysis (US Pat No. 6,221,600) 3. Combinatorial Oligonucleotide PCR (7,115,370) 4. Reversible Association of Nucleic Acid with Carboxylated Substrate (US Pat No. 7,052,840) 5. Inventor on all ITI patents and patent applications [Publication] 1. Hartman Z, Chen A, Xu R, Wang T, Wei J, Liu C, Lei G, Lyerly HK, Heiland T. (2020) HER2-LAMP vaccines effectively traffic to endolysosomal compartments and generate enhanced polyfunctional T cell responses that induce complete tumor regression. J Immunother Cancer 2020 Jun;8(1):e000258. doi: 10.1136/jitc-2019-000258 2. Su Y, Romeu-Bonilla E, Anagnostou A, Fitz-Patrick D, Hearl W, Heiland T (2017). Safety and long-term Immunological effects of CryJ2-LAMP plasmid vaccine in Japanese red cedar atopic subjects: A phase I study. Hum Vaccin Immunother. Dec 2; 13(12):2804-2813. 3. Su Y, Romeu-Bonilla E, and Heiland, T. (2017). Next generation immunotherapy for tree pollen allergies. Hum Vaccine Immunother. Oct 3; 13(10):2402-2415. 4. Su Y, Connolly M, Marketon T, and Heiland, T (2016). CryJ-LAMP DNA Vaccines for Japanese Red Cedar Allergy Induce Robust Th1-Type Immune Responses in Murine Model. J Immunol Res. 5. Maeda R, Mood K, Jones TL, Aruga J, Buchberg AM, Daar IO. (2001). Xmeis1, a protooncogene involved in specifying neural crest cell fate in Xenopus embryos. Oncogene. Mar 15; 20(11):1329-42. 6. Jones TL, Chong LD, Kim J, Xu RH, Kung HF, Daar IO (1998). Loss of cell adhesion in Xenopus laevis embryos mediated by the cytoplasmic domain of XLerk, an erythropoietin-producing hepatocellular ligand. Proc Natl Acad Sci U S A. Jan 20; 95(2):576-81. 7. Jones TL, Karavanova I, Chong L, Zhou RP, Daar IO. (1997) Identification of XLerk, an Eph family ligand regulated during mesoderm induction and neurogenesis in Xenopus laevis. Oncogene. May 8; 14(18): 2159-66. 8. Jones TL, Karavanova I, Maeno M, Ong RC, Kung HF, Daar IO. (1995). Expression of an amphibian homolog of the Eph family of receptor tyrosine kinases is developmentally regulated. Oncogene. Mar 16; 10(6):1111-7. 9. Jones TL, Barnett L, Lafrenz D. (1994). Alteration of cell cycle kinetics and immunoglobulin genetranscription as the result of multiple agonist stimulation of murine B cells. Cell Immunol. Apr 15; 155(1):156-68. 10. Jones TL, Lafrenz D. (1992). Quantitative determination of the induction of apoptosis in a murine B cell line using flow cytometric bivariate cell cycle analysis. Cell Immunol. Jul; 142(2):348-60 |
| Director, Research & Development |
Mohan Karkada, PhD | Director, Research & Development Sr Staff Scientist, Wyss Institute at Harvard Medical School Director, Cancer Immunotherapy, Immunovaccine Inc. Sr Scientist, Dalhousie University Post-Doctoral Fellow, McGill University PhD, Immunology |
[Patents] 1. Use of Liposomes in a carrier comprising a continuous hydrophobic phase for deliver of polynucleotides in vivo (Pat No. US010232052B2) 2. Compositions Comprising Liposomes, An Antigen, A Polynucleotide and A Carrier Comprising a Continuous Phase of a Hydrophobic Substance(Pat No. US 20190290743A1) [Publication] 1. Super, M., Doherty, E.J., Cartwright, M.J., Mohan Karkada et al.(2022) "Biomaterial vaccines protect against bacterial infections and septic shock" Nature Biomed Eng. Jan;6(1):8-18 2. Heil L Berinstein, Mohan Karkada et al. (2015) "Survivin-targeted immunotherapy drives robust polyfunctional T cell generation and differentiation in advanced ovarian cancer patients" Oncoimmunology. May 7;4(8):e1026529 3. Sergio Rutella, Michael A Cannarile, Mohan Karkada, et al.(2020) "Society for Immunotherapy of Cancer clinical and biomarkers data sharing resource document - conceptual and practical challenges" J Immunother Cancer. Oct;8(2):e001472 [Associated careers] 1. Member, Society for Immunotherapy of Cancer Task Force, Clinical biomarker data sharing; 2018-2020 |
| Vice President, Clinical Operations |
Scott Rodgers | Sr. Director, Clinical Operations Sr. Director, Clinical Operations, Leadiant Biosciences Director, Clinical Affairs, Leadiant Biosciences Sr. Mgr., Clinical Research, Sigma Tau Pharmaceuticals Project Manager, SGS Life Sciences Services MS, Veterinary Science |
[Associated careers] 1. Contribution to leading and developing clinical operation divisions over 20 years 2. Focusing on clinical development strategy, clinical operations, sponsor oversight and project management over 35 Phase I-IV studies in biotechnology 3. Experience in government studies over 12 studies. 12 studies of Clinical Research Organization, and 11 studies of Sponsor in vaccines, drugs/biologic, and devices area 4. Success on track record throughout numerous Health Authority inspections from FDA, Health Canada, EMEA and sponsor audits without major findings 5. Success on achieving product approvals(FDA) and product launch on Revcovi. 05-Oct-2018 6. Experience in multiple IND transfers from Investigator Initiated Trials (IITs) to Sponsor INDs (ManNAC for GNE myopathy, Cystaran for cystinosis, pediatric ALL product from Enzon Pharmaceuticals to Sigma-Tau) 7. Proficient with building quality management systems, division infrastructure (SOPs, eTMF, training programs) and teams to enable ICH GCP and FDA regulation compliance from design and execution throughout clinical phases |
| Vice President, Quality Assurance |
Cara Sholter | Director, Quality Assurance Head of QA, Lonza Deputy Director of QA, Sanofi Pasteur Biologics Quality Assurance Senior Manager, MedImmune BS in Chemistry |
[Associated careers] 1. Over 20 years of Pharmaceutical experience and 3 years of Medical Device experience 2. Primary areas of expertise are quality / compliance, quality operations, facilities, and manufacturing / process equipment, process control systems in pharmaceutical and medical device environments 3. Established a consistent and reliable release process to satisfy customer demands 4. Increased compliance by establishing an on the floor Quality Assurance program 5. Successful FDA, AMVISA, PMDA audit history for focused business functional area |
| Vice President, Operations |
Brian Stamper | Sr Director, Manufacturing, Kite Pharma Director, Manufacturing, Lonza Associate Director, Maufacturing, AstraZeneca MS in Biotechnology Enterprise & Entrepreneurship; Johns Hopkins Univ |
[Associated careers] 1. Cell Culture Engineering XIV 2014: “Technology Transfer: Process Fit and Scale-Up for Manufacturing of Biologicals” Joint presentation with colleague from Merck Research Labs 2. IBC Process2Product 2012: “Data Management Approach to Enable Successful Technology Transfer within a Trusted Partner Network” 3. Pharmaceutical Manufacturing, April 2009: “Bioreactor Operational Excellence: Best practices from Scale-Up to Control” 4. Pharmaceutical Manufacturing Webinar 23 April 2009: “Mammalian Cell Culture Scale-up: Get it Right the First Time!” 5. AIChE Annual Meeting 2008: “Modeling the Platform: Leveraging Cross-Project Data to Understand Upstream BioProcess Scale-Up” 6. AIChE Annual Meeting(2004) “Effects of Process Parameters on Scaling Up and Scaling Down a GS-NS0 Process” [Publication] 1. Statistically Designed Calibration for Near Infrared Spectrometric Monitoring of Mammalian Cell Culture. Purdue University. 2017 |
(3) 임상 개발 실적
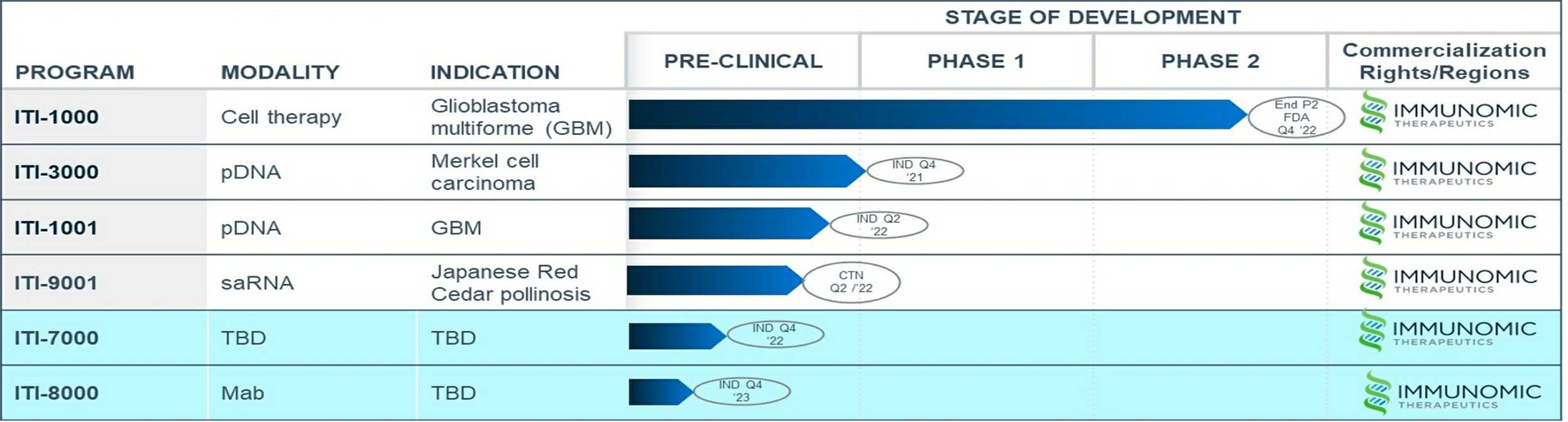 |
|
임상 개발 실적 |
(4) 특허권 보유 현황
(가) 알레르기 치료용 핵산(Nucleic Acids)
| Attorney Ref. No. | Country | Application No. | Filing Date | Patent Number | Issue Date | Status |
| ITI-03-AU | Australia | 2012382406.00 | 28-Nov-14 | 2012382406 | 22-Mar-18 | Issued |
| ITI-03-AU-D1 | Australia | 2018200625.00 | 25-Jan-18 | 2018200625 | 02-Jan-20 | Issued |
| ITI-03-AU-D2 | Australia | 2019250227.00 | 18-Oct-19 | - | - | Issued |
| ITI-03-BR | Brazil | 1120140313270.00 | 15-Dec-14 | - | - | Issued |
| ITI-03-BR-D1 | Brazil | 1220200069082.00 | 06-Apr-20 | - | - | Published |
| ITI-03-CA | Canada | 2876824.00 | 15-Dec-14 | 2876824 | 21-Jul-20 | Issued |
| ITI-03-CN | China | 201280075163.50 | 06-Feb-15 | ZL201280075163.5 | 10-Nov-17 | Issued |
| ITI-03-EP | EPO | 12878776.90 | 15-Jan-15 | EP2861240B | 09-Sep-20 | Issued |
| ITI-03-EP-D1 | EPO | 20194785.00 | 09-Jul-20 | - | - | Pending |
| ITI-03-IL | Israel | 236174.00 | 12-Nov-14 | 236174 | 29-Feb-20 | Issued |
| ITI-03-IL-D1 | Israel | IL 270260 | 29-Oct-19 | 270260 | 01-Dec-20 | Issued |
| ITI-03-IL-D2 | Israel | IL 270261 | 29-Oct-19 | - | - | Pending |
| ITI-03-IL-D3 | Israel | IL 270262 | 29-Oct-19 | - | - | Pending |
| ITI-03-JP | Japan | 2015-517226 | 11-Dec-14 | 5807994 | 18-Sep-15 | Issued |
| ITI-03-JP-D1 | Japan | 2015-119893 | 02-Feb-15 | 6088584 | 10-Feb-17 | Issued |
| ITI-03-JP-D2 | Japan | 2016-223108 | 20-Oct-16 | 6353510 | 15-Jun-18 | Issued |
| ITI-03-KR | Republic of Korea | 10-2015-7000696 | 12-Jan-15 | 10-2107646 | 28-Apr-20 | Issued |
| ITI-03-KR-D1 | Republic of Korea | 10-2020-7012427 | 28-Apr-20 | - | - | Pending |
| ITI-03-US-C1 | United States | 15/058,224 | 02-Mar-16 | 9744230 | 29-Aug-17 | Issued |
| ITI-03-US-C1-D1 | United States | 15/663,871 | 31-Jul-17 | 10072053 | 11-Sep-18 | Issued |
| ITI-03-US-C3 | United States | 17/028,762 | 22-Sep-20 | - | - | Pending |
| (나) 땅콩 알레르기 치료용 핵산(Nucleic Acids for the Treatment of Peanut Allergy) |
| Attorney Ref. No. | Country | Application No. | Filing Date | Status |
| ITI-04-AU | Australia | 2015280143.00 | 07-Dec-16 | Pending |
| ITI-04-AU-D1 | Australia | 2020204277.00 | 26-Jun-20 | Pending |
| ITI-04-BR | Brazil | 1120160304390.00 | 23-Dec-16 | Pending |
| ITI-04-EP | EPO | 15738190.50 | 20-Jan-17 | Published |
| ITI-04-KR | Republic of Korea | 10-2017-7001547 | 18-Jan-17 | Pending |
| ITI-04-MY | Malaysia | PI 2016704552 | 07-Dec-16 | Pending |
| ITI-04-PCT | WIPO | PCT/US2015/037240 | 23-Jun-15 | Published |
| ITI-04-UA | Ukraine | a 2017 00531 | 20-Jan-17 | Pending |
(다) 알레르기 항원 생성(Allergen Constructs)
| Attorney Ref. No. | Country | Application No. | Filing Date | Status |
| ITI-06-PCT | WIPO | PCT/US2017/061847 WO/2018/093932 | 15-Nov-17 | Published |
| ITI-06-CA | Canada | 3044074.00 | 15-May-19 | Pending |
| ITI-06-CN | China | 201780077275.70 | 13-Jun-19 | Published |
| ITI-06-EP | EPO | 17809419.90 | 23-May-19 | Published |
| ITI-06-EP-HK | EPO | 19133376.40 | 10-Dec-19 | Published |
| ITI-06-JP | Japan | 2019-524956 | 15-May-19 | Published |
| ITI-06-US | United States | 16/461,185 | 15-May-19 | Published |
(라) ITI 보유 기타 출원 (Other Patents owned by ITI)
| Attorney Ref. No. | Country | Application No. | Filing Date | Status |
| ITI-07-AU | Australia | 2018254776.00 | 14-Oct-19 | Pending |
| ITI-07-BR | Brazil | BR1120190221085 | 22-Oct-19 | Pending |
| ITI-07-CA | Canada | 3061206.00 | 12-Oct-19 | Pending |
| ITI-07-CN | China | 201880026665.60 | 22-Oct-19 | Published |
| ITI-07-EP | EPO | 18726576.40 | 18-Nov-19 | Published |
| ITI-07-HK | Hong Kong | 62020003600.70 | 02-Mar-20 | Published |
| ITI-07-IL | Israel | 270024.00 | 17-Nov-19 | Pending |
| ITI-07-JP | Japan | 2019-557386 | 12-Oct-19 | Published |
| ITI-07-KR | Republic of Korea | 10-2019-7034054 | 19-Nov-19 | Pending |
| ITI-07-US | United States | 16/607,082 | 21-Oct-19 | Issued |
| ITI-07-US-D1 | United States | 17/514,857 | 29-Oct-21 | Pending |
| ITI-13-CA | Canada | 3100004.00 | 11-Nov-20 | Pending |
| ITI-13-EP | EPO | 19 72 8214.8 | 06-Nov-20 | Pending |
| ITI-13-JP | Japan | 2020-563907 | 12-Nov-20 | Pending |
| ITI-13-US | United States | 17/053,784 | 08-Nov-20 | Pending |
| ITI-08-AU | Australia | 2018263923.00 | 14-Oct-19 | Pending |
| ITI-08-BR | Brazil | BR1120190230149 | 01-Nov-19 | Pending |
| ITI-08-CA | Canada | 3061950.00 | 29-Oct-19 | Pending |
| ITI-08-CN | China | 201880029699.00 | 04-Nov-19 | Published |
| ITI-08-EP | EPO | EP18729224.8 | 25-Nov-19 | Published |
| ITI-08-HK | Hong Kong | 62020004476.10 | 18-Mar-20 | Published |
| ITI-08-IL | Israel | 270271.00 | 29-Oct-19 | Pending |
| ITI-08-JP | Japan | 2019-560156 | 01-Nov-19 | Published |
| ITI-08-KR | Republic of Korea | 10-2019-7035028 | 27-Nov-19 | Pending |
| ITI-08-US | United States | 16/610,133 | 01-Nov-19 | Pending |
| ITI-15-PCT | WIPO | PCT/US20/56197 | 17-Oct-20 | Pending |
| ITI-19-PROV | United States | 63/131,829 | 30-Dec-20 | Pending |
| ITI-19-PCT | United States | PCT/US2021/065491 | 29-Dec-21 | Pending |
(마) ITI 라이선스 인(Licensed-in from Annias/Duke)
| Attorney Ref. No. | Country | Application No. | Filing Date | Patent No. | Issue Date | Status |
| ITI-L01-AU | Australia | 2009259923.00 | 19-Jun-09 | - | - | Published |
| ITI-L01-CA | Canada | 2728739.00 | 19-Jun-09 | 2728739 | 7/11/2017 | Issued |
| ITI-L01-EP1 | EPO | 9767844.50 | 19-Jun-09 | 2303319B1 | 10/5/2016 | Issued |
| ITI-L01-EP2 | EPO | 16184921.10 | 19-Jun-09 | 3 156 069 | 8/5/2020 | Issued |
| ITI-L01-EP3 | EPO | EP20181935.6 | 24-Jun-20 | - | - | Pending |
| ITI-L01-FR | France | 9767844.50 | 19-Jun-09 | 2728739 | 7/11/2017 | Issued |
| ITI-L01-JP3 | Japan | 2016-249706 | 22-Dec-16 | 6342982 | 6/13/2018 | Issued |
| ITI-L01-US1 | United States | 12/488,176 | 19-Jun-09 | 8425898 | 4/23/2013 | Issued |
| ITI-L01-US2 | United States | 13/748,096 | 23-Jan-13 | 9011835 | 4/21/2015 | Issued |
| ITI-L01-US3 | United States | 14/681,534 | 8-Apr-15 | 9764026 | 9/19/2017 | Issued |
| ITI-L01-US4 | United States | 15/676,330 | 14-Aug-17 | 10632190 | 4/28/2020 | Issued |
| ITI-L01-US5 | United States | 16/822,354 | 18-Mar-20 | - | - | Pending |
| ITI-L01-US5-C1 | United States | 16/935,813 | 22-Jul-20 | - | - | Pending |
| ITI-L01-US5-C2 | United States | 16/937,171 | 23-Jul-20 | - | - | Pending |
| ITI-L01-US5-C3 | United States | 16/937,801 | 24-Jul-20 | - | - | Pending |
| ITI-L02-EP-D1 | EPO | 20 207 148.6 | 12-Nov-20 | - | - | Pending |
| ITI-L02-HK | Hong Kong | 16114587.20 | 22-Dec-16 | - | - | Published |
| ITI-L02-US | United States | 15/024,200 | 23-Mar-16 | 9950056 | 4/24/2018 | Issued |
| ITI-L03-US1 | United States | 15/036,878 | 16-May-16 | 9974848 | 5/22/2018 | Issued |
| ITI-L03-US2 | United States | 15/956,909 | 19-Apr-18 | - | - | Issued |
| ITI-L03-US2-C1 | United States | 17/372,475 | 11-Jul-21 | - | - | Pending |
(바) ITI 라이선스 인(Licensed -in from JHU)
| Attorney Ref. No. | Country | Application No. | Filing Date | Patent No. | Issue Date | Status |
| ITI-L04-US1 | United States | 10/474,371 | 5-Apr-02 | 8318173 | 27-Nov-12 | Issued |
| ITI-L04-US2 | United States | 12/824,835 | 28-Jun-10 | 8445660 | 21-May-13 | Issued |
| ITI-L04-US3 | United States | 13/897,319 | 17-May-13 | 9499489 | 22-Nov-16 | Issued |
| ITI-L04-US4 | United States | 15/353,847 | 17-Nov-16 | 9993546 | 12-Jun-18 | Issued |
| ITI-L04-US5 | United States | 15/976,453 | 10-May-18 | 11110164 | 9-Sep-21 | Issued |
| ITI-L04-AU | Australia | 2002307145 | 5-Apr-02 | 2002307145 | 13-Mar-08 | Issued |
| ITI-L04-CA | Canada | 2446462 | 5-Apr-02 | 2446462 | 22-Dec-15 | Issued |
| ITI-L04-EP | Europe | 2002763958 | 5-Apr-02 | 1385538 | 17-Aug-12 | Issued |
| ITI-L04-JP | Japan | 2002578890 | 5-Apr-02 | 4588296 | 17-Sep-10 | Issued |
(사) 상표 출원 (Trademarks)
| Attorney Ref. No. | Country | Application No. | Filing Date | Patent Number | Issue Date | Status | ||
| UNITE - US | United States | 87942596.00 | 31-May-18 | - | - | Published | ||
| VAX-Unite - US | United States | 87942576.00 | 31-May-18 | - | - | Allowed | ||
| IMMUNOMIC THERAPEUTICS | United States | 97/295,519 | 4-Mar-22 | n/a | n/a | Pending | ||
|
United States | 97/295,474 | 4-Mar-22 | n/a | n/a | Pending |
(5) 연구개발비용
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 천원) |
|
과 목 |
제38기 당반기 | 제37기 | 제36기 |
비 고 |
|
|
비용의 성격별 분류 |
재료비 | - | - | - | - |
| 인건비 | - | - | - | - | |
| 임상비용 | 4,049,535 | 8,945,091 | 4,155,457 | - | |
|
연구개발비용 합계 |
4,049,535 | 8,945,091 | 4,155,457 | - | |
|
(정부보조금) |
- | - | - | - | |
|
보조금 차감 후 금액 |
4,049,535 | 8,945,091 | 4,155,457 | - | |
|
회계처리 내역 |
판매비와 관리비 |
4,049,535 | 8,945,091 | 4,155,457 | - |
|
제조경비 |
- | - | - | - | |
|
개발비(무형자산) |
- | - | - | - | |
|
회계처리금액 계 |
4,049,535 | 8,945,091 | 4,155,457 | - | |
|
연구개발비 / 매출액 비율(%)(*2) [연구개발비용계÷당기매출액×100] |
N/A | N/A | N/A | - | |
다. 연구개발 실적
(1) 연구개발 진행 현황 및 향후계획
| [연구개발 진행 총괄표] |
| 구 분 | 품 목 | 적응증 | 임상시작일 | 현재 진행단계 | 기 타 | 임상주도기업 | 비고 | ||
|---|---|---|---|---|---|---|---|---|---|
| 단계(국가) | 승인일 | ||||||||
| 화학합성 의약품 |
신약 | 리보세라닙 (HLB생명과학 주도 임상 포함) |
고형암 | 2011년 | 임상1/2a상 (한국, 미국) |
2011년 11월 (임상1/2a상 개시일) |
안전성평가 완료 | Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
| 위암 (3차 단일요법) |
2017년 | 임상3상 (글로벌 12개국) |
2017년 2월 (임상 3상 개시일) |
임상 3상 종료 NDA 준비 중 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
| 간암 (1차 병용요법) [Combo with Camrelizumab] |
2019년 | 임상3상 (글로벌 13개국) |
2019년 6월 (3상 개시일) |
임상 진행 중 9월 초록 발표 (1차 평가 지표 만족) |
Elevar | 항서제약과 공동개발 | |||
| 선양낭성암종 (1/2차 단일요법) |
2020년 | 임상2상 (한국, 미국) |
2020년 4월 (임상2상 개시일) |
임상 2상 진행중 6월 초록 발표 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
| 위암 (2차 병용요법) [Combo with Paclitaxel] |
2018년 | 임상1/2a상 (한국, 미국) |
2018년 10월 (임상1상 개시일) |
임상1상 종료 후, 2a상 준비 중 |
Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
| 대장암 (3차 병용요법) [Combo with Lonsurf] |
2019년 | 임상1b/2 (한국, 미국) |
2019년 11월 (1상 개시일) |
임상1b 진행 중 | Elevar | Rivoceranib 전용실시권 L/I 후 자체 개발 |
|||
| 황반변성치료제 (점안액) |
2018년 | 비임상 단계 | - | 타당성분석 중 | HLB 생명과학 |
HLB생명과학이 Rivoceranib 한국 내 전용실시권 L/I 후 자체 개발 | |||
| 동물용항암제 (동물임상) |
2020년 | 동물임상 (한국) |
2022년 03월 (단일임상 개시일) |
임상진입 준비 중 (농림축산검역본부) |
HLB 생명과학 |
HLB생명과학이 Rivoceranib 한국 내 전용실시권 L/I 후 자체 개발 | |||
| 위암 (1차 병용요법) [Combo with Camrelizumab] |
2021년 | 임상2상 (한국) |
2021년 09월 (임상2상 개시일) |
임상 진행 중 | HLB 생명과학 |
HLB생명과학이 Rivoceranib 한국 내 전용실시권 L/I 후 개발 | |||
| 아필리아 | 난소암 2차 (백금계 약물 감수성) |
2018년 (유럽EMA 허가) |
유럽 허가 | 유럽 판매 준비 중 | Elevar | Elevar가 Apealea의 글로벌 (일부국가 제외) 전용실시권을 L/I 후 판매 준비 중 | |||
| 바이오 의약품 |
IMMUNOMIC THERAPEUTICS ITI-1000 |
GBM | 2016년 | 임상 2상 (미국) |
2016년 8월 (임상 2상 개시일) |
임상 진행 중 | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
|
| IMMUNOMIC THERAPEUTICS ITI-1001 |
GBM | - | 비임상 단계 | - | 임상 1상 IND 준비 중 | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| IMMUNOMIC THERAPEUTICS ITI-3000 |
Merkel Cell Carcinoma | 2022년 | 임상 1상 (미국) |
2022년 02월 (임상 1상 개시일) |
임상 진행 중 | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| IMMUNOMIC THERAPEUTICS ITI-8000 |
NSCLC | - | 비임상 단계 | - | - | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| IMMUNOMIC THERAPEUTICS ITI-9001 |
JRC Pollinosis | - | 비임상 단계 | - | - | ITI | ITI에서 미국 듀크대학으로부터 핵심기술 L/I 후 자체 개발 |
||
| 주) 통상적으로 통계적으로 유효성을 만족하는 수준의 임상데이터 수집이 완료되면 임상 결과를 발표하나, 이는 임상의 완전한 종료를 뜻하는 바는 아닙니다. 모든 임상 참여 환자의 데이터가 축적된 후 임상결과보고서(CSR) 작성이 완료되면 공식적으로 임상시험이 종료됩니다. |
(가) : 리보세라닙
| 구 분 | 화학합성의약품 |
| 적응증 | 위암 3/4차 치료제(Rivoceranib 단독), 위암 2차 치료제(파클리탁셀 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독), 간암 1차 치료제(항서제약 캄렐리주맙 병용), 대장암 3차 치료제(타이호제약 론서프 병용) |
| 작용기전 | 신생혈관억제, VEGFR2-TKI |
| 제품의특성 | 혈관내피세포성장인자수용체2(VEGFR-2)를 타켓으로 암 조직의 신생혈관 성장을 억제하고, 암세포의 증식억제와 면역세포의 정상화를 유도하는 경구용 표적 항암제입니다. |
| 진행경과 | 위암 3/4차 치료제: 단독 요법으로 글로벌 임상 3상 후 미국 NDA 신청 준비 중 위암 2차 치료제: 파클리탁셀과 병용으로 한국, 미국에서 임상1/2a 진행 (현재 임상 1상 환자 모집 종료) 선양낭성암 1,2차 치료제: 단독요법으로 미국, 한국에서 임상 2상 환자모집 완료 간암 1차 치료제: 항서제약의 캄렐리주맙과 병용으로 글로벌 13개국 임상 3상 진행하고 있고, 2022년 9월 ESMO에서 임상 결과 공개(1차 평가지표 만족) 대장암 3차 치료제: 타이호제약의 론서프와 병용으로 미국, 한국에서 임상 1b/2상 진행 |
| 향후계획 | 위암 3/4차 치료제(Rivoceranib 단독): 미국 FDA pre-NDA 진행, FDA에서 요청한 보완 자료 준비 중, 자료 보완 후 NDA 제출 예정 위암 2차 치료제(파클리탁셀 병용) 임상 1상 결과 분석 선양낭성암 1,2차 치료제(Rivoceranib 단독): 임상 2상 결과 수집 및 분석 간암 1차 치료제(항서제약 캄렐리주맙 병용): 임상 3상 결과 수집, 분석 및 Pre-NDA 준비 대장암 3차 치료제(타이호제약 론서프 병용): 임상 1상 결과 수집 및 분석 |
| 경쟁제품 | 위암 3차 치료제: 론서프, 옵디보(한국, 일본, 대만 한정) 위암 2차 치료제: 시람자(cyramza), 파클리탁셀 선양낭성암 1,2차 치료제: 표준치료제 없음 (Off-label)로 치료 진행 간암 1차 치료제: 넥사바, 렌비마, 아바스틴, 티센트릭 대장암 3차 치료제: 론서프, 스티바가, 옵디보 |
| 관련논문등 | 위암 글로벌 임상 3상 결과 2019년 유럽암학회(ESMO) 발표: Best of ESMO 선정 중국 위암 3차 치료제 임상 3상 논문: 2016년, J Clin Oncol 34 중국 위암 2차 치료제 임상 2상 논문: 2013년, J Clin Oncol 31 중국 고형암 치료제 임상 1상 논문: 2010년, BMC cancer 10 선양낭성암 중국 선낭암 임상 2상: 2021년 Therapeutic Advances in Medical Oncology 13 미국, 한국 선낭암 임상 2상 결과: 2022년 미국암학회 발표 간암 중국 간암 임상 2상: 2021년 Clin Cancer Res 15:27(4) 글로벌 간암 1차 치료제(항서제약 캄렐리주맙 병용) 임상 3상 결과: 2022년 9월 ESMO(유럽암학회)에서 공개 (1차 평가지표 만족) |
| 시장규모 | 위암 치료제 글로벌시장: 2017년 40억달러(4조7,236억원)에서 2026년에는 66억달러(7조7,939억원)로 성장 예상 선낭암 치료제 글로벌시장: 표준치료제가 없고 발병률이 낮아 글로벌 시장 규모 추산이 어려움 간암 치료제 글로벌시장: 2019년 17억3090만 달러 (약 2조 2,100억원) 대장암 치료제 글로벌시장: 2018년 64억4400만달러(7조2000억)에서 2028년 81억4700만달러(9조1000억)로 성장 예상 ※시장규모 관련 출처 간암 데이터 - Market Data Foercast "Global Liver Cancer Therapeutics Market Size, Share, Trends, COVID-19 Impact & Growth Analysis Report - Segmented By Type, Therapeutics, End-User & Region - Industry Forecast (2022 to 2027)" (2022.01) 위암 데이터 - Reserch And Markets "Gastric Cancer Drugs Global Market Report 2021: COVID-19 Impact and Recovery to 2030" (2021.06) 대장암 데이터 - Fortune Business Insights "Colorectal Cancer Therapeutics Market Size, Share & Industry Analysis, By Therapy (Targeted Therapy, Immunotherapy, Chemotherapy, Others), By Cancer Type (Colorectal Adenocarcinoma, Gastrointestinal Carcinoid Tumors, Others), By Distribution Channel (Hospitals Pharmacies, Retail Pharmacies, Online Pharmacies, Others) and Regional Forecast, 2019-2026" (2021.08) |
| 기타사항 | 특허 및 권리 보유 현황 - 리보세라닙의 물질특허: HLB - 글로벌 전용실시권은: Elevar - 한국 전용실시권: HLB생명과학 - 중국 전용실시권: 중국 항서제약이 보유 항서제약에서 2014년 위암 3차 치료제로 중국 내 시판허가를 득한 후 현재까지 꾸준한 매출 성장 유지 중입니다. 2015년 매출 약 450억에서 2018년 2,800억까지 매출 성장을 보여줘, 약효와 안전성을 입증하였습니다. 2021년 부터 간암 2차 치료제로 적응증을 확대하여, 중국 내 매출 확대가 기대 됩니다. |
(나) : 아필리아
| 구 분 | 화학합성의약품 |
| 적응증 | 백금계 약물 감수성이 있는 난소암 2차 치료제 |
| 작용기전 | 세포 분열에 필요한 RNA나 DNA 등을 손상시켜 세포 분열을 저지하는 세포 주기 선택적 항암제 |
| 제품의특성 | 파클리탁셀은 세포분열 과정 중 분열과 자가 복제의 기구인 미세소관이 분리되는 과정을 방해하는 "식물성 알칼로이드"로 분류되는 항암제입니다. 중증 과민반응 발현을 최소화하기 위해 투여 전에 전치료를 받아야 합니다. Apealea는 특허 출원된 Micelle 코팅을 적용하여 사전처치 필요없이 편의성을 증대시키며 부작용을 줄일 수 있도록 개발한 첨가제 형태 기반의 최적의 파크리탁셀 혼합제입니다. |
| 진행경과 | 유럽, 남미, 중동 지역 판매 준비 중 백금계 약물 저항성이 있는 난소암 환자 대상 임상 1상, 3상 동시 준비 중 |
| 향후계획 | -기 승인 받은 지역 대상 판매 준비 유럽, 중동, 북아프리카, 남미 지역 대상으로 판매 절차 진행 중 중국 진출을 위해 중국 현지업체와 JV를 통한 논의 중 -추가 적응증 개발 백금계 약물 저항성이 있는 난소암 환자를 대상으로 Rivoceranib과 병용 임상 계획 검토 중 |
| 경쟁제품 | 카보플라틴, 시스플라틴, 파클리탁셀, 아바스틴 |
| 관련논문등 | A randomized phase III trial in patients with recurrent platinum sensitive ovarian cancer comparing efficacy and safety of paclitaxel micellar and Cremophor EL-paclitaxel |
| 시장규모 | 글로벌 난소암 시장은 2021년 1억 7,500만달러 규모였으며, 2028년까지 매년 9.5% 성장하여 약 3억 3,973만달러에 이를 것으로 예상 ※시장규모 관련 출처 - Market Research Guru "Global Ovarian Cancer Market Research Report 2022" (2022.07) |
| 기타사항 | -특허 및 권리 보유 현황 Apealea 글로벌 전용실시권: Elevar (북유럽, 동유럽 일부국가 제외) -판매 승인 현황 2020년 유럽 EMA로 부터 난소암 2차 치료제로 판매 승인 (carboplatin 병용) 2022년 내 유럽 내 판매 개시 목표 |
(다) : ITI
| 구 분 | 바이오의약품 |
| 적응증 | GBM (교모세포종) |
| 작용기전 | UNITE 플랫폼은 리소좀관련막단백질(LAMP)에 특정 암에 발현되는 항원을 탑재해 면역세포를 빠르고 효율적으로 활성화시키는 기전 |
| 제품의특성 | 기존 기술 대비 CD4+ Helper T 세포 활성화에 가장 효과적 동일 APC 세포 내 MHC I & II Mediated Pathway 를 동시에 활성화 가능 (MHC II Pathway 직접적으로 관여) 다양한 질환 분야에 적용 가능 (암, 감염 질환, 자가면역 질환 등) 세포 기반 치료제, 핵산 (Nucleic Acid, DNA/RNA) 기반 치료제 개발 등 다양한 기술에 적용 가능 |
| 진행경과 | ITI-1000 교모세포종 (Dendritic Cell vaccine): 임상 2상 진행 중 ITI-1001교모세포종(DNA vaccine): 1상 IND 승인 후 임상 진행 중 ITI-3000 메르켈세포암(DNA vaccine): 1상 IND 승인 후 임상 진행 중 |
| 향후계획 | ITI-1000 연내 임상 2상 종료 후, FDA와 협의를 통해 조건부 허가 추진 |
| 경쟁제품 | 교모세포종: 테모졸로마이드 (2003년 승인) |
| 관련논문등 | 2009 Gene Therapy 16 2015 Nature 2017 Clinical Cancer Reserch 23(8) |
| 시장규모 | 글로벌 교모세포종 시장은 2021년 약 22억 9천만 달러에서 2028년 약 42억 달러에 이를 것으로 예상됩니다. ※시장규모 관련 출처 - Grand View Reserach "Glioblastoma Multiforme Treatment Market Size, Share & Trends Analysis Report By Treatment (Radiation Therapy, Immunotherapy), By Drug Class, By End Use, By Region, And Segment Forecasts, 2021 - 2028" (2021.09) |
| 기타사항 | 현재 교모세포종 원발성 악성 뇌종양 중 가장 흔한 종양으로 진단 후 치료를 하지 않으면 3-6개월 내에 사망합니다. 현재 치료법이 제한적이고 5년 생존율이 5%미만으로 악성도가 높은 질환입니다. ITI-1000 교모세포종 임상 1상 시험에서 mOS을 38.3 개월로 크게 개선하였으며, 표준치료제로 알려진 TMZ/RT 요법 대비 23 개월 이상 생존 기간을 향상시키고 60개월 생존율 또한 36.4%로 증가해 임상 2상 결과 또한 기대하고 있음. |
(2) 연구개발 완료 실적
해당사항 없음.
(3) 연구개발활동 및 판매 중단 현황
해당사항 없음
7. (제조서비스업)기타 참고사항
가. 상표관리 정책 등
당사는 HLB 기업브랜드 및 브랜드의 가치제고 및 육성, 보호활동을 종합적으로 수행해나가고 있습니다. 각 사업부에서 주요 브랜드에 대한 의사결정을 시행하고 있으며,브랜드 개발부터 등록, 심의 등 제반 브랜드관리를 성실히 수행하고 있습니다.
나. 사업과 관련된 지적재산권
(1) HLB ENG사업부문
|
순 |
종류 |
특허명 |
특허 및 출원번호 |
특허출원일 |
특허등록일 |
특허만료일 |
비고 |
|
1 |
특허 |
선박엔진용 변속기 |
제10-0559484호 |
2004.08.11 |
2006.03.03 |
2024.08.11 |
HBG100 변속기 |
|
2 |
디자인 |
선박용 엔진 |
제30-0520757호 |
2008.07.14 |
2009.02.13 |
2028.07.14 |
23마력 엔진 |
|
3 |
디자인 |
구명보트 |
제30-0520758호 |
2008.09.10 |
2009.02.13 |
2028.09.10 |
44P 일반구명정 |
|
4 |
디자인 |
선박용 엔진 |
제30-0520759호 |
2008.09.10 |
2009.02.13 |
2028.09.10 |
29마력 엔진 |
|
5 |
특허 |
구명보트용 엔진제어 시스템 및 그 제어방법 |
제10-1137919호 |
2010.05.12 |
2012.04.12 |
2030.05.12 |
스마트키 |
|
6 |
특허 |
필라멘트 와인딩 장치 |
제10-1111964호 |
2010.01.14 |
2012.01.27 |
2030.02.27 |
PIPE |
|
7 |
특허 |
필라멘트 와인딩 장치 |
제10-1111965호 |
2010.03.09 |
2012.01.27 |
2030.02.27 |
PIPE |
|
8 |
디자인 |
구명보트 |
제30-0742562호 |
2012.12.13 |
2014.05.07 |
2032.12.13 |
구명정 |
|
9 |
디자인 |
구명보트 |
제30-0742562호 |
2012.12.13 |
2014.05.07 |
2032.12.13 |
구명정 |
|
10 |
특허 |
구명정용 압축공기 공급장치 |
제10-1826304호 |
2016.07.21 |
2018.01.31 |
2036.07.21 |
구명정 |
|
11 |
특허 |
선박용 엔진의 해수유입 방지장치 |
제10-1852592호 |
2016.07.21 |
2018.04.20 |
2036.07.21 |
엔진 |
|
12 |
디자인 |
립보트 특허 |
제30-0955142호 |
2017.06.14 |
2018.04.30 |
2037.06.14 |
고속구조정 |
|
13 |
디자인 |
구명정&텐더 특허 |
제30-0943079호 |
2017.06.14 |
2018.01.31 |
2037.06.14 |
구명정&텐더 |
|
14 |
일본특허 |
선박용 엔진의 해수유입 방지장치 |
제6452767호 |
2017.07.20 |
2018.12.21 |
2037.07.20 |
엔진 |
|
15 |
중국특허 |
선박용 엔진의 해수유입 방지장치 |
제201710599878.5호 |
2017.07.21 |
2019.12.27 |
2037.07.21 |
엔진 |
|
16 |
특허 |
구명정용 자가복원장치 |
제10-1929438호 |
2017.07.28 |
2018.12.10 |
2037.07.28 |
구명정 |
|
17 |
특허 |
고속단정용 자가복원장치 |
제10-1958958호 |
2017.07.28 |
2019.03.11 |
2037.07.28 |
고속구조정 |
|
18 |
특허 |
구명정 환기장치 |
제10-1929439호 |
2017.07.28 |
2018.12.10 |
2037.07.28 |
구명정 |
|
19 |
특허 |
고속보트용 주행 안전장치 |
제10-1958961호 |
2017.07.28 |
2019.03.11 |
2037.07.28 |
고속구조정 |
|
20 |
디자인 |
고속주행에 적합한 FRP 선체 |
제30-0954289호 |
2017.11.02 |
2018.04.20 |
2037.11.02 |
고속구조정 |
|
21 |
특허 |
고속 보트용 연료누유 방지 및 연료 회수 장치 |
제10-1879573호 |
2018.01.23 |
2018.07.19 |
2038.01.23 |
연료장치 |
|
22 |
디자인 |
보트 |
제30-1057213호 |
2019.10.23 |
2020.04.28 |
2039.10.23 |
구명정 |
|
23 |
특허 |
디젤엔진용 수동 시동장치 |
제10-2160727호 |
2019.12.19. |
2020.09.22. |
2039.12.19. |
엔진 |
(2) 제약, 바이오 부문
|
순 |
특허명 |
국가 |
특허 및 출원번호 |
특허등록일 |
특허만료일 |
비고 |
|
1 |
Six membered amino-amide derivatives an |
미국 |
7129252 |
2006.10 |
2024.06 |
- |
|
2 |
한국 |
10-1159034 |
2012.06 |
2024.06 |
- |
|
|
3 |
일본 |
5046643 |
2012.07 |
2024.06 |
- | |
|
4 |
캐나다 |
2568608 |
2012.01 |
2024.06 |
- | |
|
5 |
중국 |
02138671.4 |
2006.10 |
2022.11 |
- | |
|
6 |
유럽 |
1633712 |
2014.06 |
2024.06 |
- |
(3) HLB 헬스케어 사업부문
|
순 |
종류 |
특허명 |
등록번호 |
특허출원일 |
특허등록일 |
특허만료일 |
비고 |
|
1 |
디자인 |
포장용 상자 |
제 30-0841707호 |
2015.04.13 |
2016.02.22 |
2035.04.13 |
1매 스왑 |
|
2 |
디자인 |
포장용 포대 |
제 30-0841368호 |
2015.04.13 |
2016.02.19 |
2035.04.13 |
1매 스왑 |
|
3 |
디자인 |
한 벌의 응급키트 포장용 상자 세트 |
제 30-0891572호 |
2015.10.05 |
2017.01.18 |
2035.10.05 |
응급키트 |
|
4 |
디자인 |
응급처치키트 보관용 가방 |
제 30-0894768호 |
2016.06.08 |
2017.02.13 |
2036.06.08 |
응급키트 |
|
5 |
디자인 |
주사기용 주사액 이물질 여과장치 |
제 30-0894770호 |
2016.06.08 |
2017.02.13 |
2036.06.08 |
- |
|
6 |
디자인 |
포장용 상자 |
제 30-0944411호 |
2017.09.11 |
2018.02.08 |
2037.09.11 |
1매 스왑 |
|
7 |
디자인 |
포장용 상자 |
제 30-1067173호 |
2019.11.06 |
2020.07.14 |
2039.11.06 |
1매 스왑 |
|
8 |
디자인 |
포장용 상자 |
제 30-0808392호 |
2014.09.30 |
2015.07.27 |
2034.09.30 |
1매 스왑 |
|
9 |
상표 |
EOL SWAB |
제 40-0813065호 |
2008.12.15 |
2010.02.01 |
2030.02.01 |
1매 스왑 |
|
10 |
상표 |
이올스왑 |
제 40-0813063호 |
2008.12.15 |
2010.02.01 |
2030.02.01 |
1매 스왑 |
|
11 |
상표 |
(상표명 정보 없음) |
제 40-0861541호 |
2010.01.29 |
2011.04.18 |
2031.04.18 |
회사 CI |
|
12 |
상표 |
FAA+ ANYTIMP ANYWHERE |
제 40-0861456호 |
2010.01.29 |
2011.04.18 |
2031.04.18 |
- |
|
13 |
상표 |
FAA+ ANYTIMP ANYWHERE |
제 41-0215085호 |
2010.01.29 |
2011.08.12 |
2031.08.12 |
- |
|
14 |
상표 |
L+LIFE PLUS First Aid Kit |
제 40-0876368호 |
2010.01.29 |
2011.08.12 |
2031.08.12 |
응급키트 |
|
15 |
상표 |
SPLANT |
제 40-1046461호 |
2013.10.07 |
2014.07.04 |
2024.07.04 |
- |
|
16 |
상표 |
쿨네츄럴 모스키퍼액 |
제 40-1161777호 |
2015.06.10 |
2016.02.22 |
2026.02.22 |
모기기피제 |
|
17 |
상표 |
노스팅 |
제 40-1166982호 |
2015.08.11 |
2016.03.15 |
2026.03.15 |
1매 스왑 |
|
18 |
상표 |
FA |
제 40-1195244호 |
2015.10.02 |
2016.08.09 |
2026.08.09 |
회사 CI |
|
19 |
상표 |
FA |
제 41-0361351호 |
2015.10.02 |
2016.06.02 |
2026.06.02 |
회사 CI |
|
20 |
상표 |
베이비 브로 |
제 40-1250812호 |
2016.08.22 |
2017.05.08 |
2027.05.08 |
유아용 구강티슈 |
|
21 |
상표 |
아망 |
제 40-1250817호 |
2016.08.22 |
2017.05.08 |
2027.05.08 |
- |
|
22 |
상표 |
푸카치카 |
제 40-1250819호 |
2016.08.22 |
2017.05.08 |
2027.05.08 |
유아용제품 |
|
23 |
상표 |
VV VIVOSWAB |
제 40-1261420호 |
2016.10.20 |
2017.06.16 |
2027.06.16 |
유아용 1매 티슈 |
|
24 |
상표 |
Enodis |
제 40-1363544호 |
2017.07.25 |
2018.05.29 |
2028.05.29 |
1매 티슈 (화장품) |
|
25 |
상표 |
PETCARE |
제 40-1472998호 |
2018.02.06 |
2019.04.25 |
2029.04.25 |
동물용 1매 티슈 |
|
26 |
상표 |
PETCARE |
제 40-1434211호 |
2018.02.06 |
2019.01.07 |
2029.01.07 |
동물용 1매 티슈 |
|
27 |
상표 |
베베듀 |
제 40-1642545호 |
2019.08.21 |
2020.09.11 |
2030.09.11 |
유아용 1매 티슈 |
|
28 |
상표 |
PETCARE |
제 40-1519802호 |
2018.10.05 |
2019.09.10 |
2029.09.10 |
1매 티슈 |
|
29 |
상표 |
FA Eol Swab BLUE |
제 40-1644972호 |
2019.11.06 |
2020.09.21 |
2030.09.21 |
1매 스왑 |
|
30 |
상표 |
루첸티아 365 |
제 40-1645733호 |
2019.09.25 |
2020.09.23 |
2030.09.23 |
1매 티슈 |
|
31 |
상표 |
클리어뷰어 Clear Viewer |
제 40-1656295호 |
2019.11.05 |
2020.10.27 |
2030.10.27 |
1매 티슈 |
|
32 |
특허 |
소독지 포장케이스 |
제 10-1079926호 |
2008.12.15 |
2011.10.28 |
2028.12.15 |
1매 스왑 |
|
33 |
특허 |
인공호흡용 보호구 |
제 10-1161791호 |
2010.01.14 |
2012.09.26 |
2030.01.14 |
CPR 쉴드 |
|
34 |
특허 |
다용도 가방 |
제 10-1169366호 |
2010.01.28 |
2012.07.23 |
2030.01.28 |
응급키트 |
|
35 |
특허 |
인공호흡용 보호구 |
제 10-1245521호 |
2010.07.05 |
2013.03.14 |
2030.07.05 |
CPR 쉴드 |
|
36 |
특허 |
소독용 알코올 부직포가 내장된 포장지 |
제 10-1397061호 |
2012.08.07 |
2014.05.13 |
2032.08.07 |
1매 스왑 |
|
37 |
특허 |
역류 방지용 탄성 차단변 및 |
제 10-1495752호 |
2013.10.04 |
2015.02.16 |
2033.10.04 |
- |
|
38 |
특허 |
주사액 필터 장치 |
제 10-1663573호 |
2014.11.05 |
2016.09.30 |
2034.11.05 |
- |
|
39 |
특허 |
수영용 깁스 보호 커버 |
제 10-1765705호 |
2015.12.10 |
2017.08.01 |
2035.12.10 |
깁스커버 |
|
40 |
특허 |
주사기용 주사액 이물질 여과장치 |
제 10-1707884호 |
2016.05.10 |
2017.02.13 |
2036.05.10 |
- |
다. 관련 법률 및 규정 등
당사의 주력제품인 구명정 및 GRP/GRE Pipe, 체외진단 의료기기를 제조함에 따라 관련 법규(해양, 조선, 환경, 약사법 등)를 철저히 준수하고 있으며, 이를 성실히 준수하기 위해 최선의 노력을 아끼지 않고 있습니다.
라. 사업과 관련한 환경물질의 배출 또는 환경보호와 관련된 사항
당사는 구명정 및 GRP/GRE Pipe, 체외진단 의료기기 등 제작에 직,간접적으로 배출되는 환경물질의 관리를 정기적, 수시적 실사를 통하여 항시 환경보호에 앞장서고 있습니다.
마. 사업의 개요
(1) 산업의 특성
(가) 구명정 & DAVIT
구명정과 DAVIT은 국제해사기구(IMO) 규정에 따라 500톤 이상 및 본선 길이 85M 이상의 모든 선박에 의무적으로 승선인원의 200%이상 장착되어야 하는 선박에 없어서는 안되는 필수품이며, LAS CODE, SOLAS 등 각종 까다로운 규정을 모두 만족시켜 제작해야 하므로 신규시장 진입장벽이 매우 높은 산업입니다.
(나) GRP/GRE PIPE
GRP/GRE Pipe는 육상 분야로 해수담수화 설비 및 발전소 등 플랜트사업과 해상용으로 발라스트 시스템, 스크러버 시스템, 소화배관 시스템 등에 많이 요구되고 있으며, 주로 해수를 이용한 강관에 고질적 문제인 녹 발생이 전혀 발생하지 않는 대체 재료로서 널리 쓰이고 있습니다.
(다) 특수선박(관공선, 도선선, 유도선 등)
관공선은 조달청 입찰시스템인 나라장터를 통해 공정한 입찰로 발주처를 결정하고 있으며, 기본적으로 기관에서 요구하는 제품과 동일 또는 유사한 기술을 보유한 기업만이 그 우위를 차지할 수 있습니다. 일반적으로 선박의 발주는 국가 정책으로 인한 수요와 정기적인 교체 수요에 따라 선종에 따라 적게는 5개사에서 많게는 20개사 이상의 업체가 입찰에 참여하고 있습니다.
도선선은 국내 일정 도선 구역에서 입항 또는 출항하는 선박에 탑승하여 해당 선박을안전한 수로로 안내하는 일을 수행하는 선박으로써 국내 11개 지역에 위치하고 있으며 선박은 대략 100여척이 운항 중입니다. 도선선은 주로 FRP로 건조되어 도선사의요구와 교체 시기에 따라 발주되는 비정기적인 발주가 대부분입니다. 유도선은 일반적으로 유람선을 의미하며 도선은 강과 바다가 접하는 하구 또는 만의 형태를 갖춘 곳으로 양 해안을 오가는 선박을 의미합니다. 선주 요구사항과 선령에 따라 교체시기가 결정되는 비정기적인 발주로 볼 수 있습니다.
(라) 제약, 바이오
한국수출입은행 보고서상 글로벌 의약품 시장의 특징에 따르면, 신약개발은 많은 시간이 소요되고, 많은 자금이 투입되며 위험이 수반됩니다.
글로벌 신약 개발에는 수십억 달러 상당의 개발 비용과 약10년 이상의 예산과 기간이소요된다고 합니다.
신약개발의 단계는 후보물질 탐색, 비임상 실험, 임상시험 단계로 구분되며, 신약후보물질 검증을 위한 기초 R&D에 약 5년이 소요되며 이후 약 3년동안 비임상 단계에서 인간에게 약물을 투여하기 전에 동물대상으로 신약후보물질의 약물 효능 및 안전성 평가를 진행하게 되며 비임상 자료를 바탕으로 식약처에 IND((Investigational New Drug) 승인을 받고 임상단계에 진입하게 됩니다.
임상 단계는 최소6~7년가량이 소요되며, 임상시험 기관(병원)의 전문역량과 많은 비용이 소요되는 단계로 전체 신약개발 비용의 약 70%가량을 차지합니다.
임상시험은 신약의 안전성과 유효성 입증을 위해 인간을 대상으로 실시하는 시험으로써, 총4상(Phase)으로 구성되며, 제I상(임상 1단계)에서는 소수의 건강한 성인을 대상으로 약물의 체내 흡수, 분포, 대사, 배설 등에 대한 약동학적인 자료를 수집하면서 안전성을 평가하게 되며(약 1~2년), 제II상(임상 2단계)에서는 수백명 가량의 해당질환을 보유한 환자들을 대상으로 투약용량의 범위와 용법을 평가하게 됩니다(약 2년), 제III상(임상 3단계)에서는 수천명의 해당질환 환자를 대상으로 약물의 유효성과안전성을 최종적으로 검증하게 되며(약 3년), 임상 3상을 통과하면 보건당국에 NDA(New Drug Application)를 신청하여 약물 제조 및 판매허가를 받게 됩니다. 보건당국으로부터 판매허가를 득한 후에 대규모 상용화 단계로 진입합니다, 제IV상(임상 4단계)에서는 약물 허가 및 시판 후 부작용을 추적하여 안전성을 입증하고, 추가적 모니터링의 단계로 진행을 하게 됩니다.
타 산업 대비 연구개발 투자비율이 매우 높은 기술중심의 산업으로서, 연구개발비용 투입 상위기업 기준으로 매출액 대비 약20% 수준이며(일반제조업 약3%), 오랜 시간과 높은 비용이 소요되는 신약개발의 특성으로 인하여 중소업체 및 바이오벤처 등 소규모 기업이 신약개발 전 과정을 단독으로 진행하기 어렵습니다. 따라서, 높은 연구개발 투자 비용의 회수를 위해서는 큰 규모의 시장이 필요하여, 글로벌 진출 지향적인 산업구조를 가집니다.
글로벌 의약품산업 연구개발 투자비는 2015~2022년 지속적으로 성장할 것으로 2022년 약 1,800억 달러의 규모를 형성할 것으로 예측됩니다(Evaluate Pharma).
근래의 신약개발에 있어서 성공확률은 약1/5,000 수준으로 매우 낮은 상황입니다. 기초 탐색단계에서 5,000~10,000개 수준의 화합물(Compound) 중 비임상 단계로 약250여개, 임상단계까지 5개, 최종 신약승인 허가를 득하고 최종단계인 상용화 단계에 도달하는 것은 1개 정도에 불과합니다. 이와 같이 낮은 확률에도 불구하고 신약개발의 필요성이 대두되는 이유는 단 한 제품의 성공만으로도 글로벌 제약회사로 도약할 수 있으며, 특허 만료기간(약20년) 동안 물질특허를 인정받아 안정적으로 매출을 유지할 수 있다는 매력적인 장점을 가지고 있기 때문입니다. 이처럼 하나의 글로벌신약으로 연간 수십억 달러 이상의의 매출을, 십 수 년간 독점적인 시장을 가지고 사업을 영위할 수 있는 산업이 바로 제약산업인 것입니다.
(마) 체외진단 의료기기 및 의약외품
체외진단의료기기와 의약외품과 같은 헬스케어 & 바이오산업은 상대적으로 보다 높은 고부가가치를 창출할 수 있는 지식기반산업으로서 차세대 성장동력산업의 하나로주목받고 있습니다. 이는 생명공학기술이 정보통신기술(IT)이나 나노기술(NT) 등의 첨단기술과 함께 향후 산업 혁신에 있어서 매우 폭넓고 다양하게 기여할 것으로 예상하기 때문이며, 이러한 생명공학기술을 활용하여 인체 적합성이 강화된 의약품 및 의료기기를 개발할 수도 있으며 사용되는 원료의 재활용도를 높일 수 있을 뿐 아니라 친환경제품의 개발도 가능한 산업 분야입니다. 이러한 헬스케어 & 바이오산업은 다가오는 고령화 및 보건, 식량, 환경, 에너지 등 인류가 직면하고 있는 각종 문제점을 해결할 수 있는 미래 산업이라 할 수 있습니다.
의약외품 관련 제품의 경우, 사람이나 동물의 질병을 치료ㆍ경감ㆍ처치 또는 예방할 목적으로 사용되는 섬유ㆍ고무제품 또는 이와 유사한 것 이나 인체에 대한 작용이 약하거나 인체에 직접 작용하지 아니하며, 기구 또는 기계가 아닌 것과 이와 유사한 것 에 해당하는 물품으로 식품의약품안전처장이 지정하는 것을 말합니다. 각각의 의약외품 제품의 경우 허가와 신고 제품으로 나누어질 수 있으며, 허가 제품의 경우 각각의 필요 서류에 대한 부분과 증빙 등을 제출하여 식품의약품안전처(MFDS)의 승인을 득한 후 제조 및 판매가 가능한 품목입니다.
체외진단 의료기기는 혈액, 객담, 타액, 분뇨, 체액, 등 인체로부터 채취한 대상물을 이용하여 몸 밖에서 신속하게 질병 등을 진단하는 기술로써, 임상 의사 결정에 중요한 역할을 하며 환자 치료에 필수적이면서도 전문화된 요소가 되고 있는 시장입니다.흔히 주변에서 볼 수 있는 혈당측정기나 임신테스트기가 대표적인 체외진단기기이며, COVID-19 가 발병한 후 선별진료소 등에서 검사 시 사용되는 검체 채취용 면봉(swab)과 검사 후 검사실로 이동하기 위하여 면봉(swab)을 담아 옮기는 수송배지(VTM)가 이에 해당되며, 검사 방식에 따라 면역화학적 진단(Immunochemistry), 자가 혈당 측정(SMBG:Self-monitoring Blood Glucose), 현장진단(POCT:Point Of Care Testing), 분자진단(Molecular Diagnostics), 혈액진단(Hematology), 임상화학(Clinical Chemistry), 지혈진단(Hemostatis or Coagulation), 조직병리진단(TissueDiagnostics)으로 세분화 할 수 있습니다. 이러한 체외진단 의료기기는 검사를 위한 검체를 채취하는 도구(Tool), 검사를 위하여 이송하는 배지(Transport Medium), 검사를 위한 시약(Reagent)으로 구분될 수 있으며 시약의 경우 혈액 검사용, 수혈 검사용, 요 또는 분변 검사용, 면역화학 검사용, 임상 미생물 검사용, 분자유전 검사용, 체외진단검사지, 병리검사용, 기타 검사용 시약으로 나눌 수 있습니다. 이러한 체외진단의료기기에 사용되는 제품은 개인 및 공중위해성 판단 기준에 따라 4단계의 등급으로 나누어질 수 있으며 각각의 등급에 따라 국내 식품의약품안전처(MFDS)에 신고및 허가를 득한 후 제조 및 판매가 가능한 제품입니다.
의약외품 및 체외진단의료기기 제품은 기존 소비재 상품과는 상이하게 관련된 근거 자료 및 기술 자료 등에 대한 준비 및 확인이 필요한 산업 분야에 속하며 국내 식품의약품안전처(MFDS) 허가 외 ISO13485, CE, FDA 등의 국제 규격 인증에 관련한 자료가 필요한 제품이며 점차적으로 환경적인 오염 등의 사회 및 환경적인 변화에 따라신종 바이러스 및 신종 감염병 등이 발병하는 가운데 이러한 예방과 진단 기술의 제품들의 수요는 증가하는 추세이며 그에 따른 시장 확대가 이루어지고 있는 분야입니다. 기존의 진단 시장이 대형병원에서의 건강검진을 중심으로 영상진단 검사 분야인 내시경이나 초음파, 방사선 촬영 등 체내진단이 주로 위주였다면, 미래의 새로운 진단사업은 4P(예측, 예방, 개인, 참여) 중심의 차세대 체외진단 중심으로 변화되고 자리매김할 것으로 예상할 수 있습니다.
(2) 산업의 성장성
(가) 구명정 & DAVIT
조선산업은 2021년 1월 기준 클락슨 리서치에 따르면 작년 수주량 기준으로 세계시장점유율은 한국이 43%로 1위, 중국이 41%로 2위, 일본이 7%로 3위이며, CGT기준, 한국이 819만CGT, 중국이 793만CGT, 일본이 137만CGT를 달성하고 있습니다.전방산업인 조선산업의 성장에 따라 발주량도 영향을 받으며 최근엔 조선경기의 침체로 선박 발주량이 줄어 해양 및 조선기자재 업종의 성장이 정체되고 있으나 글로벌경제회복과 유가상승에 따른 해양 및 조선 업황이 호전되면 구명정의 수주와 생산이 다시 크게 늘어날 것으로 예상됩니다.
(나) GRP/GRE PIPE
GRP/GRE Pipe는 플랜트사업에서 주로 사용되고 있으나, 최근 친환경 선박 수요가 늘어남에 따라 새롭게 규정된 국제해양기구의 SOX, NOX 규제로 인한 스크러버 시장은 지속적으로 시장규모가 확대되고 있으며, LNG 선박의 수요와 국내조선소 수주증가로 인해 발라스트용 GRP/GRE Pipe시장도 크게 증가하는 추세입니다. 특히 유가의 고유황유와 저유황유의 OIL SPREAD가 커짐에 따라, 최근 SOX SCRUBBER를 설치하기 위한 시장 또한 크게 증가하고 있습니다.
(다) 특수선박(관공선, 도선선, 유도선 등)
최근 잦은 국내 해양 안전사고가 발생되고 있어 노후 선박에 대한 교체 필요성이 대두되어 국가정책에 따라 많은 관공선과 유도선 교체 수요가 발생될 것으로 예상되고 있으며, 강선 위주의 선박구조에서 고사양인 알루미늄 선박으로 교체되고 있는 추세입니다. 따라서, 현재 20년 이상 된 관공선, 도선선, 유도선의 교체 수요가 점차 증가할 것으로 예상됩니다.
(라) 제약, 바이오
글로벌 제약산업 분석서비스업체인 이벨류에이트파마(EvaluatePharma)사의 최근자료에 따르면, 첨단기술과 헬스케어의 융합이 현실화되고 새로운 치료제가 등장함에 따라 처방의약품(Prescription drug)의 매출은 지속적으로 확대될 것으로 예상하고 있습니다.
글로벌 시장조사기관인 Globaldata에 따르면, 2021년 글로벌 처방의약품 시장규모는 약 7,530억 달러로 예상되고, 향후 연 평균 약 7%의 성장을 이룰 것으로 전망하고있습니다. 또한, 다양한 새로운기술의 출현은 제약산업 진화의 터닝포인트가 되어 될것으로 예상됩니다. 그 중에서도 항암제분야의 경우 면역항암(Immuno-oncology) 계열의 확장은 제약산업 성장에 크게 기여하며 기존의 세포독성항암제와 표적항암제와의 병용을 바탕으로 치료법의 발전과 더불어 시장을 확대하는데 큰 역할을 하고 있습니다. 특히 주목받는 치료영역으로는 시장 점유율 및 성장률이 높은 Oncology 분야의 지속강세 속에서 새로운 치료제 개발을 위한 연구개발도 활발하게 이루어지고 있습니다. Oncology 분야의 시장규모는 2021년 1,673억 달러로 향후 연 평균 15%의 성장이 예상되는 거대 시장입니다.
(마) 체외진단 의료기기 및 의약외품
체외진단 의료기기 시장은 질환 치료 중심에서 고령화 시대에 질병 등의 조기 진단을통한 사전 예방 및 건강증진 중심의 트렌드 변화로 인해 빠르게 성장하고 있으며, 높은 정확도, 편리성, 빠른 진단 및 분석이 가능한 진단 방식이라는 측면에서 고성장세를 이어갈 것으로 전망되고 있습니다. 2019년 전세계적으로 발병한 COVID-19의 대응에서도 나타난 바와 같이 병원이 아닌 개인의 “자가진단” 키트를 이용하여 검사를 수행하는 사례처럼 진단이 필요한 환자의 수요보다 병원의 공급 부족 현상이 발생될 경우 이러한 체외진단 의료기기 시장의 제품군도 다양하게 개발될 것으로 예상되며 시장성 또한 증가할 것으로 전망하고 있습니다.
국내 진단용 의료기기 시장규모는 2019년 기준으로 약 1.5조원 규모였으나, 2019년 COVID-19 발병 이후 가파르게 성장하고 있는 추세입니다. 국내 진단용 의료기기 시장은 체외진단기기 시장의 비중이 약 52%를 차지하고 있으며 생체현상계측기기 시장의 비중은 10%로 상대적으로 낮은 경향을 보이고 있습니다. 글로벌 체외진단기기 시장의 경우에도 2019년 기준 약 298억 달러(약 34조원)으로 전체 진단용 의료기기 시장의 약 40%를 차지하고 있으며 2020~2027년 동안 5%대 이상의 연평균 성장률을 기록할 것으로 전망되며 2027년 910억 달러(약 105조원) 규모에 이를 것으로 예상되고 있습니다. 이러한 체외진단용 의료기기 시장은 지속적인 성장을 이룰 것으로 전망되고 있으며, 점차적으로 질병 예방 및 진단에 대한 수요가 늘어날 것으로 보임에 따라 이러한 시장 규모는 확대 성장할 것으로 전망할 수 있습니다.
(3) 경기변동의 특성
(가) 구명정 & DAVIT
원자재 가격, 환율, 유가 등 대외 경제변수 및 조선소의 선박 건조량에 크게 영향을 받고 있습니다. 이는 세계 해운경기와 직결되며, 경기 사이클에 따라 호황과 불황을 반복하는 추세를 보입니다. 최근 LNG선 폭등하는 등 LNG선 강세로 인한 업황 개선 기조에도 불구하고, 저유가로 인한 해양플랜트 발주 지연, 미중 무역분쟁에 따른 해상 물동량 증가세 둔화 등 부정적인 요소로 인해 많은 Risk도 공존하고 있습니다. 하지만, 중장기적으로 선진국, 신흥국을 필두로 한 글로벌 경제회복이 지속되면 선박생산량도 다시 크게 증가할 것으로 예측됩니다.
(나) GRP/GRE PIPE
플랜트/조선산업 경기에 따라 크게 영향을 받고 있으며, 국제해사기구의 환경규제에따른 대체수요가 증가할 것으로 예측됩니다. 신조시장 뿐만 아니라 RETROFIT 시장에도 최근 각광을 받고 있어, 몇 년 동안 경기변동이 심할 것으로 예상됩니다.
(다) 특수선박(관공선, 도선선, 유도선 등)
관공선과 유도선의 경우 정부 정책에 따라 크게 영향을 받고 있으며, 민간 기업인 도선선 외 기타 선박은 선주의 선호와 선령에 영향을 받습니다.
(라) 제약, 바이오
전반적인 제약산업은 인간의 건강과 삶의 질 향상에 직접적으로 영향을 주는 산업인 만큼 경기 변동에 따른 차이가 비교적 적은 보수적인 성향을 보입니다.
(마) 체외진단 의료기기 및 의약외품
제조업의 특성상 원부자재 가격, 환율, 유가 등 대외적인 환경 변화에 대한 경기 변동에 대한 영향을 받고 있습니다. 이러한 부분은 주요 원부자재 수입 업체 국가의 경기 변동에도 영향을 받고 있으며 국제 정세의 리스크도 공존하는 상황입니다. 하지만, 점차적으로 질병 예방 및 진단에 대한 부분은 팬데믹 현상이 도래되었을 때는 전세계적인 이슈로 대두되어 국제적인 경기 변동에 영향을 수반하게 되지만 의약외품 및 체외진단 의료기기 시장의 경우 직접적인 소비재 상품인 B2C 상품이기보다 기업 및 정부조직간의 거래 관계인 B2B 및 B2G 계약이 다수를 점유하기에 경기 변동에 따른 리스크는 상대적으로 미비한 영향을 받는다고 할 수 있겠습니다.
(4) 계절성
(가) 구명정 & DAVIT
계절적 영향은 크지 않다고 판단됩니다.
(나) GRP PIPE
계절적 영향은 크지 않다고 판단됩니다.
(다) 특수선박(관공선, 도선선, 유도선 등)
계절적 영향은 크지 않다고 판단됩니다.
(라) 제약, 바이오
의약품은 크게, 반드시 전문의의 진단 및 처방이 요구되는 전문의약품과 진료 없이 일반인이 접근할 수 있는 일반의약품으로 나눌 수 있습니다. 일반의약품의 경우에는 날씨 및 기후 등 외부요인에 의한 계절적인 영향을 다소 받는 편이지만, 전문의약품은 환자의 선택권한이 제한되며 경기변동에 따라 치료를 중단하는 등의 일들이 일어나지 않으므로 변동이 크지않아 제약산업 전반적으로 안정적인 성장을 유지해 오고 있습니다.
(마) 체외진단 의료기기 및 의약외품
계절적 영향은 크지 않다고 판단됩니다. 다만, 계절적인 요인으로 발생될 수 있는 감염병 및 수인성 질환 등이 발생되어 개인위생 및 소독 활동에 대한 부분이 증가될 경우 소폭의 매출 상승 요인으로 작용될 수는 있으나 전반적으로 계절성의 영향은 크지않습니다.
바. 사업의 현황
(1) 영업개황
(가) 구명정 & DAVIT
당사는 46년간 구명정을 생산하여 왔으며 2000년 6월 현대정공으로부터 분리된 국내 유일의 구명정 제조업체로서 자체 개발한 소형엔진과 다수의 구명정 모델을 개발하여 연간 700대의 구명정 생산능력을 갖추었습니다. 국내시장의 50% 이상을 점유하고있으며, 모든 조선소에 당사의 제품을 공급하고 있습니다. 최근 경쟁력 있는 36인승 제품을 신규 개발하여 해외시장 개척을 위한 교두보를 마련하였습니다.
(나) GRP/GRE PIPE
100% 해외 수입에 의존했던 제품을 국산화하는데 성공한 후 조선소에 경쟁력 있는 가격과 품질로 공급하고 있습니다. 개발 초창기에는 선주의 선호도로 인해 당사 제품이 선택되지 않는 등 어려움을 겪었으나, 활발한 홍보 활동과 영업을 통해 최근에는 당사 제품에 대한 인지도가 많이 상승되어 지속적으로 발주가 증가하는 추세를 보이고 있습니다. 특히 2022년에서는 국내 대부분 조선소에 공급되고 있고, 특정 조선소에는 점유율이 90%가 넘어가고 있으며, 일본 조선소에도 약 10곳에 독점으로 공급하고 있습니다.
(다) 특수선박(관공선, 도선선, 유도선 등)
고속정 개발을 통해 현대, 대선조선 등 국내외 조선소, 기관 등에 소요되는 관공선용 고속정을 수주 받아 생산하고 있으며, 110톤/130톤급 전남어업지도선의 ALUMINUM 선각 공사 및 보트를 납품하여 우수한 경금속선박을 생산하는 업체로 평가를 받고있습니다. 아울러, 낚시선, 도선선, 통선 등 다양한 선박을 개발하는데 성공하여 상용화를 완료, 공급하였으며, 또한 노후유도선 교체사업과 관련하여 발 빠른 준비로 다른 경쟁업체 보다 앞서 영업 진행 중입니다.
(라) 제약, 바이오
한국보건산업진흥원에서 발간한 정책보고서에 따르면, 국내 22대 질환별 사망률 추이를 조사한결과 신생물(암)으로 인한 사망이 압도적 1위를 차지하였으며 인구 10만명당 사망률은 2015년 153.6명에서 꾸준히 증가하여 2019년에는 161.4명을 기록하여 약 5%의 증가세를 보였습니다. 이에 따른 진료비는 2015년 5조7624억원에서 2019년 9조3003억원으로 약61.4%로 급증하였습니다. 그 중, 중국 시장의 경우 2019년 미국에 이어 2위 시장으로, 2014~2019년 연평균 성장률 6.7%를 보이며 급격히 성장하고있습니다. 동사의 매출에 직접적으로 영향을 줄 항암제 시장의 경우 최근 4년간(2014~2018년) 연평균 12.8% 성장했고, 2030년까지 연 12.7% 성장을 예상하고 있습니다.
(마) 체외진단 의료기기 및 의약외품
현재 사업분야는 체외진단 의료기기를 주축으로 한 바이오 사업과 알콜스왑을 주축으로 한 헬스케어 사업으로 세분화하여 운영중에 있으며, 2021년 한국보건산업진흥원에서 발간한 보건산업정책연구 보고서에 의하면 최근 의료기기산업은 지속적인 성장이 예상되는 고부가가치 유망산업으로 주목받고 있으며,의료기기의 사용은 의료기관에 국한되지 않고 자가진단 및 모바일기기 등을 통해 일상생활에 적용됨에 따라 활용 분야는 더욱 확대될 전망으로 나타나고 있습니다. 진단용 의료기기의 세부 분야는영상진단기기, 생체현상계측기기, 체외진단기기로 크게 3가지 형태로 분류되고 있으며, 세계 진단용 의료기기 시장 규모는 2019년 약 734억달러(약 85조원) 규모이며 이중 체외진단기기의 경우 298억 달러의 시장규모에서 지속 성장할 것으로 예상되며, 국내 진단용 의료기기 시장규모의 경우 글로벌 시장 대비 성장이 빠르다고 분석하고 있습니다. 이러한 시대적인 성장 구조에 맞추어 발 빠른 개발 대처와 상용화를 통해 시장 진입의 시간을 단축하고 성장할 수 있도록 하겠습니다.
(2) 경쟁현황
(가) 구명정 & DAVIT
국내 유일 제조업체로서 국내에는 경쟁업체가 없으며, 해외 중국 OEM업체인 VIKING, PALFINGER, NORSAFE와 중국 제조업체인 IAOYAN, BEIHAI 등이 있습니다.
(나) GRP/GRE PIPE
국내 유일 GRE PIPE 제조업체로서 국내에는 경쟁업체가 없으며, GRP PIPE의 경우국내 ISP와 GRE PIPE의 경우 해외AMERON 등이 있습니다.
(다) 특수선박(관공선, 도선선, 유도선 등)
주로 국내업체와 경쟁하고 있으며, FRP 소형선박의 경우 광동FRP, 한일뉴즈, 보고, 반도 마린 등이 있으며 ALUMINIUM 선박의 경우 신도, 휴먼중공업 등이 있습니다. 하지만 모두 당사 대비 소규모 시설과 인력을 갖추고 있습니다.
(라) 제약, 바이오
기존의 항암제는 분열이 활발히 진행되고 있는 세포의 각종 대사경로에 개입하여, 핵산의 합성을 억제하거나 세포 독성을 일으켜 항암활성을 나타내는 약제가 대부분이며, 암세포에만 선택적으로 작용하는 것이 아니라 정상세포, 특히 세포 분열이 활발한 조직 세포에도 손상을 입혀 구토, 위장장애, 탈모증, 골수기능저하로 인한 백혈구 감소증 등 심각한 부작용을 초래할 수 있습니다.
따라서 1세대 항암제인 세포독성(cytotoxic) 약물 대신 정상세포의 손상을 최소화할 수 있는 표적지향성을 가지는 표적 항암제의 이용이 확대되고 있으며, 대형 시장(미국, 일본, 영국, 독일 등)에서도 지속적으로 시장이 확대되고 있습니다. 표적 항암제들은 대부분 암세포가 특징적으로 가지고 있는 분자를 표적으로 하는데 암세포의 신호전달경로(signal transduction pathway), 혈관신생(angiogenesis), 세포간질(matrix), 세포주기조절인자(cell cycle regulator), 세포사멸(apoptosis) 등을 주요한표적으로하고 있으며, 이중 신호전달경로 억제제와 신생혈관생성 억제제가 가장 대표적인 표적 항암제로 사용되고 있습니다. 또한 최근 주목을 받고 있는 면역항암제의 경우 인체의 면역기능을 강화시켜 간접적으로 암을 치료한다는 점에서 기존의 치료제와는 다른 새로운 개념의 혁신적인 치료제로 각광을 받고 있으며 GBI 리서치에 따르면, 세계 면역항암제 시장규모는 매년 23.9% 성장을 통해 2017년 169억 달러에서 2022년 758억 달러까지 성장할 것으로 전망하고 있습니다.
다만, 암세포를 인식할 수 있는 항원 수용체의 선택성과 민감도에 따라 과도한 면역반응으로 인한 부작용이 발생할 수 있음이 한계점으로 남아있습니다. 이에 따라, 글로벌 제약사는 면역항암제의 한계점을 극복하고, 활용을 확대하기 위한 방법으로 2017년부터 병용요법 임상시험을 진행하고 있으며 최근에는 면역항암제와 세포독성, 표적항암제, 방사선요법 등과의 병용 요법에서 생존율 개선 등에 효과가 있다는 연구결과가 속속 발표되며 병용요법이 새로운 치료의 패러다임으로 자리를 잡고 있는 상황입니다.
(마) 체외진단 의료기기 및 의약외품
국내 바이오 중소ㆍ벤처기업 중 진단의료기기 관련한 기업의 경우 249개 업체가 사업을 운영 중에 있으며 2018년도 기준 1조 6천억원의 매출을 기록한 것으로 나타나고 있습니다. 또한 2020년도 의료기기 허가 및 인증 신고 현황을 기준으로 체외진단용 시약의 경우 2020년 총 1,500건이 품목허가를 득한 것으로 나타나고 있습니다. 이중 검체 수송배지의 경우 20년 기준으로 122건수가 신고 되었으며, 검체채취용 도구의 경우 69건이 신고된 상황입니다. COVID-19 영향으로 다수의 업체들이 시장 진입을 시행한 것으로 나타나고 있으며 관련한 의료기기인 핵산추출시약, 검체수송배지, 검체채취용도구의 경우 총 268건이 신고 되었으며, 수입신고 또한 검체채취용도구 61건 신고된 것으로 나타나고 있습니다.
국내 산발적인 업체들의 난립과 더불어 수입 물량으로 인해 검체 채취도구와 수송배지의 경우 경쟁력이 심화되고 있는 상황에서 원가 절감 및 품질, 납기 준수의 강점으로 경쟁사와의 차별화 정책을 시행중이며, 추가적인 제품들의 개발 기간을 단축하여 팬데믹 이후 후속 제품에 대한 시장 진출을 조속히 시행하여 점진적인 시장 점유율을확대할 계획입니다. 기존 글로벌 기업과의 연계 및 신시장 개척을 통해 시장 내에서 계속하여 점유율을 올려나가고 있는 상황입니다.
(3) 시장점유율 추이
(가) ENG사업부문(구명정 & DAVIT, GRP/GRE PIPE, 특수선박)
객관적인 자료출처를 통한 경쟁업체간 시장점유율 비교가 불가능하여 기재를 생략합니다.
(나) 제약, 바이오 부문
2007년 넥사바의 간암 1차 치료제 시장 진입 이후 10년 동안 신규 승인 약물이 없어 시장 독식 체제를 형성하고 있었습니다. 그러던 2018년과 2020년에 렌비마(단독)와 티센트릭+아바스틴 병용요법이 FDA의 허가를 득했습니다. 그 중에서도 티센트릭+아바스틴 병용요법은 넥사바 대체할 새로운 표준치료제로 자리잡고 있습니다. 티센트릭(면역관문억제제)+아바스틴(신생혈관억제제)의 출현으로 처방 패러다임 변화하고 있으며, 면역관문억제제와 기존의 VEGFR-TKI 병용요법도 주목 받고 있습니다. 엘레바는 중국 항서제약과 공동으로 리보세라닙과 캄렐리주맙(면역관문억제제)의 임상 3상 환자를 모집을 종료하고 일차평가지표에 대해서 통계적 유의미성이 있는 top-line 결과를 확보하였습니다.
선양낭성암의 경우 현재까지 승인된 표준치료제가 없는 희귀암종으로 치료 방법이 제한적입니다. 현재 선양낭성암 환자들은 방사선 치료 및 의사 판단하에 Off-Label로 타 항암제가 사용되고 있는 실정입니다. 리보세라닙은 글로벌 최초로 대규모 상업화 임상 2상 (글로벌 80명)을 진행해 2022년 6월 ASCO에서 그 효능과 안전성을 입증했고, 현재 빠른 상업화를 위해 FDA의 가속승인제도(Accelerated Approval) 등 다양한 방안을 추진하고 있습니다. FDA 승인을 받게 될 경우, 선양낭성암 적응증에 대한 글로벌 첫 표준치료제로 등재될 가능성이 높습니다.
상기 두 적응증(간암(미국), 선양낭성암(미국))은 미국 FDA로부터 희귀의약품(Orphan Drug)으로 지정 받아 시장 가치를 더 높이고 있습니다. 시장조사기관 이벨류에이트(Evaluate)에 따르면 2026년까지 희귀의약품이 전체 처방약 매출의 1/5를 차지하고, 전세계 파이프라인 가치의 1/3을 차지할 것이라고 전망했습니다. 희귀의약품으로 지정될 경우 연구개발 비용의 25%(임상비용의 50%) 세액공제, 시판 후 7년간 시장독점권 부여 등 다양한 혜택을 기대할 수 있습니다.
그 외에도 2014년 중국 항서제약에서 위암 3차 치료제로 출시된 이후 현재까지 꾸준한 양적 성장을 이뤄왔습니다. 중국 현지 증권사 레포트 및 항서제약 공시에 따르면리보세라닙 (중국명: 아파티닙)의 매출은 2015년 3억 위안 (한화 약 500억원)에서 2018년17억위안(한화 약 2,900억원)으로 증가하였습니다. 2020년 12월 간세포암2차 치료제로 중국내 판매 승인을 득해 중국 내 매출은 지속적으로 증가할 것으로 예상됩니다.
(다) 체외진단 의료기기 및 의약외품
식품의약품안전처 의료기기정보 포털에 의하면 국내 “검체채취용도구(1등급)”의 등록건수는 총 922건이며 이중 2020년에서 2021년 사이에 등록된 신규건수만 600건 이상이 등록되었으며 더불어 국내 “검체수송배지” 등록건수는 총 644건이며 이중 2020년에서 2021년 사이에 등록된 신규 건수의 경우 500여건의 신규 등록이 이루어진 상황입니다. 점차적으로 치료가 아닌 예방 및 검사에 대한 의료 시장의 변화가 이루어질 것으로 전망되는바 이러한 검체 채취용 제품에 대한 수요는 증가할 것으로 예상하고 있습니다. 하지만 COVID-19 상황에서 급조된 형태의 제품을 위주로 판매되었던 제품의 경우 금번 펜데믹 사태가 수그러질 경우 품질력과 생산 Capa를 보유하고 있지 않는 업체의 경우 시장에서 경쟁력을 확보하기 어려울 것으로 예상되고 있습니다.
알콜 스왑의 개인적인 사용 빈도가 높은 당뇨 환자의 증가 추이를 확인하였을 때 2020년 기준 501만명(츨처_강북삼성병원) 규모이며 이러한 당뇨 환자의 경우 매년 증가하고 있는 추세입니다. 2004년 대비 4배에 가까운 상승세를 나타내고 있으며 2020년기준 전세계 4억 6,300만명(출처_국제당뇨병연맹IDF)으로 추정되고 있습니다. 이러한 당뇨병의 경우 현대인에게 가장 많이 발병하는 만성질환으로 점차적으로 환자 추이는 증가할 것으로 전망되고 있으며, 2040년 6억 4,200만명으로 증가될 것으로 예상되고 있습니다(출처_이코노미조선). 국내 당뇨 환자의 체혈 후 사용되는 알콜 스왑제품을 기준으로 당뇨 환자 1일 2회 당뇨 측정을 가정으로 추산하였을 때 국내 시장의 경우 3억장/월 규모의 시장을 나타내고 있습니다.
(4) 회사 경쟁상의 강점과 단점
(가) 구명정 & DAVIT
국내 유일의 구명정 제조업체로써 해외 경정업체 대비 운송비 절감 및 빠른 A/S, 고객과 원활한 의사소통, 정확한 납기준수, 세계 일류상품으로 선정된 우수한 품질이 강점이며, 단점은 중국 구명정 대비 가격경쟁력, OFF-SHORE 시장에서의 선주 선호도가 낮은 것이나 자체개발한 엔진과 HOOK SYSTEM 등을 통해 가격 경쟁력을 확대하고 있습니다.
(나) GRP/GRE PIPE
경쟁업체 대비 우수한 가격 경쟁력과 빠른 A/S 및 생산공정 개선을 통한 생산능력, 국내조선사와의 원활한 의사소통이 강점이며, 경쟁사 대비 선주 선호도는 아직 낮은 것이 단점이나 점진적으로 홍보활동 및 영업을 통해 선호도가 올라가고 있습니다.
(다) 특수선박(관공선, 도선선, 유도선 등)
국내 최대 생산시설과 기술인력을 보유하고 있으며, 업무시스템이 경쟁사 대비 강점입니다. 경쟁사 대비 늦은 시장 진출로 인한 선주 선호도가 낮은 편이나 이 또한 점차개선될 것으로 기대하고 있습니다.
(라) 제약, 바이오
2세대 항암제인 표적치료제(Molecularly targeted therapy)는 정상세포와 암세포를 모두 공격할 수 있는 세포독성항암제와는 달리 암세포에 있는 특정 단백질 (표적)을 차단하여 암세포의 활동을 억제하는 약제로써 1세대인 세포독성 항암제에 비하여 부작용이 적은 장점을 가지고 있습니다.
동사가 권리를 보유한 리보세라닙은 2세대 표적항암제이면서 경구용이라는 복용 편의성을 확보했고, 부작용 또한 적어 병용치료제로 좋은 조건을 갖추고 있습니다. 실제로도, 기존 치료제들과의 다양한 병용요법으로 임상 연구결과들이 발표되고 있는 점 또한 앞으로의 성장성이 기대가 되는 부분입니다.
리보세라닙(중국명 아파티닙)은 2014년 위암 3차 치료제로 중국 내 판매 승인을 받은후 2020년 12월 간암 2차 치료제로 중국 내 시판 승인을 받았을 뿐만 아니라 비소세포폐암, 유방암, 난소암, 등 다양한 적응증을 대상으로 임상시험이 진행 되고 있어,향후 적응증 확대에 따른 매출증가가 및 가치의 상승으로 이어질 것으로 전망하고 있습니다. 그리고, 중국 지역 외 나머지 글로벌 판매 권리는 에이치엘비의 자회사인 엘레바가 보유하고 있습니다. 엘레바에서는 간암 1차 치료제(항서제약 캄렐리주맙 병용), 위암 2차 치료제(파클리탁셀 병용), 선양낭성암 1,2차 치료제(Rivoceranib 단독), 대장암 3차 치료제(타이호제약 론서프 병용)등 적응증 확대를 위해 다방면으로 힘쓰고 있습니다.
(마) 체외진단 의료기기 및 의약외품
당사는 GMP 시설과 ISO13485 관리 시스템을 기반으로 양산 체제를 갖추고 있으며,경쟁사 대비 압도적인 품질 경쟁력 및 대량생산 시스템을 보유하고 있습니다. 급변하는 고객의 요청사항에 빠르고 안정된 품질생산 시스템과 더불어 수주, 생산, 출고에 이르는 원스텝 시스템 경영을 통해 경쟁사 대비 신속한 대처를 시행하고 있으며 고품질 제품의 적정납기 준수에 대한 경쟁력을 보유하고 있습니다. 대표적 의약외품인 알콜스왑 제품의 경우 월 1억매의 양산 시스템을 보유하고 있으며 국내외 복합 협력사를 통해 안정적인 원부자재 수급을 수행하고 있습니다. 또한 체외진단의료기기 검체 채취용 도구 제품도 월 1억개 생산 Capa를 보유하고 있으며 이 또한 GMP 시설 및 ISO13485 관리 시스템을 이용하여 양산을 진행함으로써 경쟁사 대비 높은 품질 및 납기 경쟁력을 보유하고 있습니다. 품질관리의 경우 제품의 규격인증을 위해 FDA 등록, ISO13485, CE 인증을 획득하여 고객사에 품질에 대한 높은 신뢰도를 확보하고 있습니다.
아울러 자체 연구소를 보유함으로써 변화하는 시장 상황에 대응하기 위한 각 제품군별 다양한 파이프라인을 구축하여 지속적인 신제품 개발을 진행하고 있으며 빠르게 변화하는 다양한 시장 변화에 대응할 계획입니다. 또한, 가격경쟁력 제고 및 매출 증대를 위하여 공정 개선 및 자동화 설비 도입을 추진할 계획이며 향후 체외진단의료기기 및 헬스케어 관련 제품의 시장 확대를 위하여 힘쓰고 있습니다.
(5) 조직도
 |
|
에이치엘비(주) 조직도 |
사. 연결 대상 종속회사 사업 내용
당사는 사업다각화를 위해 종속회사의 제약ㆍ바이오사업 등에 주력하여 기업가치를 제고하고 있습니다. 관련된 사업은 Elevar Therapeutics, Inc., Immunomic Therapeutics, Inc., ㈜화진메디칼 및 ㈜화진메디스를 통해 진행되고 있으며, 해당 사업에 대한 자세한 내용은 다음과 같습니다.
(1) 제약ㆍ바이오사업 (Elevar Therapeutics, Inc., Immunomic Therapeutics, Inc.)
(가) 시장의 현황
한국보건산업진흥원에서 발간한 정책보고서에 따르면, 국내 22대 질환별 사망률 추이를 조사한결과 신생물(암)으로 인한 사망이 압도적 1위를 차지하였으며 인구 10만명당 사망률은 2015년 153.6명에서 꾸준히 증가하여 2019년에는 161.4명을 기록하여 약 5%의 증가세를 보였습니다. 이에 따른 진료비는 2015년 5조7624억원에서 2019년 9조3003억원으로 약 61.4%로 급증하였습니다.
또한 한국제약바이오협회에서 발간한 2020 제약바이오산업 데이터북에 따르면 세계의약품시장은 2014년 9830억 달러에서 2019년 1조2500억 달러 규모로 매년 3~8%가량 성장세를 보이고 있습니다.
Evaluate Pharma World Preview 2020에 따르면 2019년 1,454억달러 규모의 전세계 항암제 시장이 2026년까지 약11.5%의 연평균성장률을 보이며 3,112억 규모로 성장할것으로 예상하고 있습니다. 또한 전체 의약품 중 항암제가 차지하는 비율이 2019년 16%수준에서 2026년 21.7%로 확대될 것으로 예상하고 있습니다.
제약 연구개발비의 경우 2019년 기준 전세계 제약사의 R&D 지출액이 1,860억 달러이며 2026년 2,325억달러로 약 25%가량 증가할 것으로 예상하고 있으며 전세계 처방의약품 매출액은 2019년 8,720억달러에서 2026년 1조3900억 달러로 약 60%가량성장할것으로 예상해 R&D 지출액 대비 처방의약품의 매출액의 상승폭이 크기 때문에 이익구조가 개선될 것으로 전망됩니다.
중국과 인도 등 제네릭 합성기술을 앞세운 제약 신흥국들이 저가의 경쟁력을 앞세워 글로벌 시장에서 제네릭 공세를 펼치면서 수익률이 날로 저하되고 있는 상황이므로 주요 글로벌 제약회사들은 획기적인 파이프라인의 확보, M&A 및 유망기업에 투자를 활발하게 진행하고 있는 상황이며 갈수록 기업의 R&D능력과 신약의 글로벌 경쟁력이 더욱 중요해질 전망입니다.
(나) 회사의 현황
1) Elevar Therapeutics,Inc.
Elevar Therapeutics,Inc.는 2005년 7월 신약개발 컨설팅 회사로 설립되어 2007년 12월 Rivoceranib(구, Apatinib Mesylate) 표적항암제 라이센스 취득 계약 체결(Advenchen Laboratories, Inc., CA, USA)로 중국을 제외한 세계 판권을 취득하여 독자적인 바이오사업을 시작하였습니다. 본 Rivoceranib(구, Apatinib Mesylate)는 위암(2016.02 국내식약처 / 2017.03 유럽연합집행위원회 / 2017.06 미국식품의약국), 간암 (2021년 11월 미국식품의약국), 선양낭성암 (2021년 2월 미국식품의약국) 대상으로 희귀의약품 지정을 받아 임상종료 후 시판허가에 대한 심사의 신속화, 수수료감면 등의 혜택과 최소 8년(2029년)에서 최대 13년(2034년) 동안 독점 판매할 수 있습니다.
2011년11월 US FDA로부터 다국가(미국/한국) 1/2a 임상시험을 위한 IND 승인을 받아 표적항암제 리보세라닙(구, Apatinib Mesylate) 다국가(미국/한국) 1/2상 임상시험을 종료하였고, 2017년 표준치료법으로 2차 치료제 이상에서 치료에 실패한 진행성 또는 전이성 환자를 대상으로 글로벌(미국, 유럽, 한국, 일본, 대만 등 12개국) 3상 임상시험을 완료하였습니다. 그 이후 적응증 확대를 위해 간암 1차, 선양낭성암의글로벌 임상을 추진 하였고, 최근 두 임상 모두 환자 모집을 완료했습니다. 선양낭성암은 현재까지 표준치료제가 전무한 희귀암으로, 글로벌 최초 대규모 2상 임상을 진행하여 그 결과를 2022년 6월 미국 암학회(ASCO)에서 발표한 바 있습니다. 표준치료제가 없는 희귀암의 의료미충족수요가 높은 암종으로 First in Class를 기대하고 있습니다. 그리고, 간암 1차 치료제 글로벌 임상은 항서제약에서 개발한 PD-1 면역항암제 캄렐리주맙과 리보세라닙의 병용으로 실시 되었으며, 글로벌 543명의 임상 환자를 모집하였습니다. 회사는 임상 데이터를 면밀히 분석해 적절한 허가 전략을 수립한 후 신약허가를 신청할 계획입니다. 그 밖에도, 대장암(Colorectal cancer) 3차 치료제, 위암(Gastric cancer) 2차 치료제에 대해서 임상시험중에 있습니다. 대장암 3차 치료제는 타이호제약의 론서프(Lonsurf)와 병용으로 임상 1/2상을, 위암 2차 치료제는 파클리탁셀(Paclitaxel)과 병용요법으로 임상 1/2상을 진행 중입니다. 그리고 미국 서던 캘리포니아 암센터에서 육종(Sarcoma)에 대해서 BMS의 면역항암제 옵디보(Nivolumab)의 병용임상시험을 종료하였습니다.
2020년 3월 아필리아(Apealea) 라이센스를 스웨덴 비베스토(Vivesto, 舊 Oasmia)로부터 러시아, 북유럽과 동유럽 일부 국가를 제외한 세계 판권을 취득하였습니다. 아필리아는 파클리탁셀(paclitaxel)의 3세대 개량 신약으로 Vivesto의 독점 기술 플랫폼인 'XR17'을 사용하여 개발된 항암제로, 주입전에 사전 처치가 필요가 없고, 주사제 주입 시간이 짧아 환자의 편의성을 증대시키면서 부작용을 최소화했습니다. 유럽에서 난소암 2차 치료제로 카보플라틴(carboplatin)과 병용으로 허가 받았습니다. 2022년 5월 독일을 시작으로 본격적인 마케팅 활동을 시작하였으며, 점진적으로 시판국을 넓혀나갈 계획입니다.
※ Pipeline 현황
|
품목명 |
적응증 |
특징 및 임상현황 |
|
리보세라닙 |
위암 간암 대장암 선양낭성암 |
1. 특징 - Oral : 경구용 제품으로 낮은 생산단가 2. 임상시험 현황 - 위암 말기 : 단독요법 - 간암 1차 : 캄렐리주맙과 병용요법 - 대장암 3차 : 론서프와 병용요법 - 위암 2차 : 파클리탁셀과 병용요법 - 선양낭성암 : 단독요법 |
|
아필리아 (Apealea) |
난소암 |
1. 특징 - 파클리탁셀의 개량신약(주사제) - 기존 파클리탁셀과 달리 전처치가 필요없고, 가용화제인 크레모포어 2. 개발현황 - 유럽에서 난소암 2차 치료제로 카보플라틴과 병용요법으로 허가 |
2) Immunomic Therapeutics, Inc.
Immunomic Therapeutics, Inc. (이하 "이뮤노믹")는 핵산 면역치료 플랫폼(nucleic acid immunotherapy platforms) 연구에서 선구적인 임상 개발 단계에 있는 비상장 생명공학기업입니다. 회사의 연구기술은 암, 알레르기와 동물치료제에 대해 면역치료(immune therapy)로 활용될 수 있습니다. 이뮤노믹의 사명(mission)은 삶을 변혁시킬 백신을 개발하는 것입니다. 이뮤노믹은 백신 디자인, 개발, 생산 및 시험에 대한 전문성을 가지고 있습니다. 이뮤노믹의 주요 경쟁력은 회사가 직접 또는 협력사 혹은 기술이전한 회사를 통해 3개월 내에 선도물질(lead)에서 제품 후보물질(product candidate)로 빠르게 개발할 수 있도록 도움을 줄 수 있습니다.
이뮤노믹은 2006년 9월 26일 존스 홉킨스 대학으로부터 LAMP(Lysosomal Associated Membrane Protein) 기술과 관련된 지적 재산권, 정보에 대한 독점적 권리(proprietary information)를 확보하였습니다. 이뮤노믹은 LAMP 기술과 그 기술을 업그레이드한 UNITE(UNiversal Intracellular Targeted Expression) 플랫폼 기술을 활용하여 인간과 동물용 알레르기 치료용 백신 개발을 하였으며, 2015년 초부터는 면역항암분야(Immune-oncology)에 대해서 개발을 진행하고 있습니다.
2014년 이뮤노믹은 항암분야에서 면역치료의 가능성을 확인하였습니다. 2015년 이후 이뮤노믹은 항암분야에서 가능성을 강화하기로 결정하고, 알레르기 예방과 치료를 위한 LAMP-Vax™ 기술 사용권리는 아스텔라스(Astellas Pharmaceuticals, Inc.)에 기술을 이전하였습니다. 이 기술이전 계약에 따라 이뮤노믹은 3억 2천만달러 이상의 수입을 거두게 되었습니다.
이뮤노믹은 현재 항암분야에서UNITE™ 플랫폼 적용에 집중하고 있습니다. 기존 기술과 보완된 기술(항원의 선택과 최적화, 보조제 사용의 최적화, 전달 방법의 다양성,대규모 생산공정 확립)의 조합으로 완성된 이뮤노믹의 UNITE™ 플랫폼 기술은 항체생산, 사이토카인(cytokine) 분비, 중요 면역 기억을 포함한 광범위 면역반응을 유도할 수 있는 자연계에 존재하는 생화학적 기술(body’s natural biochemistry)을 활용하는 것입니다. 이러한 방법은 암, 알레르기, 감염질환을 포함한 다양한 면역치료에 UNITE기술을 활용할 수 있습니다.
* 이뮤노믹 기술설명
면역항암분야(Immuno-Oncology)
항암분야에서 UNITE 플랫폼 기술(The UNITE Platform in Oncology)
이뮤노믹은 UNITE 플랫폼 기술이 승인되고 연구되고 있는 접근방법을 보완함으로써 현재의 면역항암제 사용을 확장시킬 수 있을 것이라고 생각합니다. 비임상시험 결과는 UNITE 플랫폼이 2가지 방향으로 면역항암제(cancer immunotherapy) 개발의 가능성을 보여주고 있습니다.
- 면역체크포인트 억제제(checkpoint inhibitors)에 반응하는 면역반응(immune reaction)이 있는 종양(highly immunogenic tumor types)에 대해서는 면역 체계 활성화 유도
- 면역 체계의 중요한 구성 요소를 재구성(reconfiguring)하여 면역반응이 없는 종양에 대해서는 새롭고 강력한 면역반응을 생성
UNITE 플랫폼은 다양한 방법으로 면역체계를 재구성(reprogram)할 수 있습니다.
- 다양한 기능적(poly-functional) 면역반응 생성
- 암과 싸울 수 있는 면역체계에서 중요한 요소인 CD4+와 CD8+ T 세포 활성
- 종양에서 항원 특이적(antigen-specific) Th1 종양침투림프구(TIL)의 유도
UNITE는 현재 항암면역치료제(cancer immunotherapy)로 임상 2상에 진행중인 것에 적용되고 있습니다. 또한 이뮤노믹은 학계와 생명공학 회사들과 함께 협력하여 교모세포종(Glioblastoma)과 급성골수성백혈병(Acute myeloid leukemia)과 같이 치료제가 제한적인 질환을 포함하여 사망률이 높은 암에 대한 치료제 개발을 위해 UNITE 플랫폼 기술 활용하고 있습니다. 이뮤노믹은 이러한 초기단계 임상시험인 UNITE 기술을 증명해 줄 것이라고 믿고 있으며, 만약 성공한다면, 치료가 어려운 종양과 다른 질병에 대해 후속 연구를 확장해 나갈 것입니다.
파이프라인 확장을 위해서 기존의 항암제 개발방법과 다른 3가지의 방법으로 개발하고자 합니다. 다양한 암의 항원은 크게 3가지로 구분할 수 있습니다: 바이러스(viral),신항원(neoantigen), 다른 암 항원(other cancer antigens).
바이러스 항원은 특정 암의 연관되거나 직접적인 원인을 제공하는 것으로 이루어져 있습니다.
신항원(neoantigen)이라는 것은 유전자의 변이를 통해 생긴 항원을 말하는 것입니다.
다른 암 항원은 다시 하위 분류로 나눌 수 있는데, 대부분은 특정한 단백질이 적절하지 않은 시점이나 적절하지 않은 발현량으로 나타나게 됩니다.
이뮤노믹은 이러한 분류에 따라 새로운 개발전략을 가속화할 수 있도록 할 것입니다.
(2) 바이오 의료기기사업 (㈜화진메디칼/㈜화진메디스)
(가) 시장의 현황
Evaluate Med Tech, World Preview 및 Worldwide Medical Devices Market Factbook등에서 발표한 자료에 따르면 2019년 글로벌 의료기기 시장은 4,044억 달러(약 493.9조원) 규모이며, 미국이 1,729억 달러로 글로벌 의료기기 시장의 42.7%를 점유하고 있으며 그 뒤로 일본 289억 달러, 독일 285억 달러, 중국 273억 달러, 프랑스154억 달러, 영국 120억 달러, 이탈리아 102억 달러순이며 우리나라는 10위를 차지하나, 연평균 6%의 높은 성장률로 입지가 점차 확대될 것으로 기대되고 있습니다.
피치 솔루션(Fitch Solutions) 보고서에 의하면 글로벌 의료기기 시장은 2014년 3,336억 달러에서 연평균 3.9% 성장하여 2019년 4,044억 달러 규모로 확대되었습니다.
아시아 의료기기 시장은 일본 34%, 중국 32%로, 일본과 중국이 66% 차지하고 있으며 한국은 3위의 의료기기 시장을 보이며, 연평균 성장률로 볼 때 베트남, 필리핀, 인도네시아, 중국, 인도는 9% 이상의 높은 성장을 기록하고 있습니다.
※ 중국은 시장규모가 크며, 9.3%의 높은 성장률로 관련 시장은 더욱 확대될 전망입니다.
(나) 회사의 현황
㈜화진메디칼/㈜화진메디스는 주사기 등 바이오 의료기기 전문 제조업체로써 1회용 주사기 업계에서는 품질과 매출면에서 상위권에 위치하고 있으며, 2005년 5월 "Sofjec"이라는 상표를 출원하여 일회용주사기, 필터주사기 등을 제조, 판매하고 있습니다.국내 대형병원인 아산병원, 연세세브란스병원, 성모병원, 서울대병원을 비롯하여 중 ·소형 병원 및 동물병원에 납품하고 있으며 안정적인 영업이익률을 유지하고 있습니다.
또한, 지속적으로 베트남, 몽골, 사우디 등 동남아와 중동에 수출하고 있으며 최근 코로나 19로 인한 주사기 수요 증가로 미국, 유럽 등에 대한 판매도 추진하고 있습니다.그리고 주사기, 주사침, 멤브레인 필터주사기 등 기존 주력 제품 외에도 의료기기 신제품개발을 통해 새로운 미래 수익모델을 창출하고자 연구개발에 집중 투자하고 있습니다. 향후 미국 FDA 인증 추진과 유럽의 강화된 CE-MDR 인증(기존 CE-MDD 인증 대체)으로 최상의 품질보증시스템을 유지하고 경쟁력을 강화하여 국내 시장뿐 아니라 세계 시장으로 점유율을 확대하여 글로벌 의료기기 회사로 도약해 나갈 계획입니다.
1. (금융업)사업의 개요
에이치엘비인베스트먼트 주식회사는 2021년 5월 당사가 100% 출자하여 설립되었으며, 벤처투자 촉진에 관한 법률에 의거 중소벤처기업부에 등록된 중소기업창업투자회사로서 2022년 5월 등록허가가 완료 되었습니다.
주로 바이오, 헬스케어산업의 유망 신기술을 보유하고 있지만 자본과 경영기반이 취약한 중소기업창업자 및 벤처기업에게 자금과 경영서비스 등을 제공하고 추후 M&A, IPO, 지분매각을 통해 투자자금을 회수하는 벤처투자조합의 결성 및 업무의 집행 등을 주업무로 하고 있습니다.
2. (금융업)영업의 현황
일반적인 중소기업창업투자회사의 영업수익은 본계정 투자수익, 투자조합 및 PEF 관리&성과보수 수익, 투자조합 및 PEF 운용투자수익, 자문 등 기타 영업수익으로 구성되어 있습니다.
에이치엘비인베스트먼트㈜는 2021년 5월 설립되었으며, 2022년 5월 벤처투자 촉진에 관한 법률로 인가를 받은 이후 본격적으로 벤처투자조합 결성을 통해 영업을 확대하고자 하며 본 보고서 제출일 현재 벤처투자조합 1호(출자약정액 20억원)를 결성 하였습니다.
[벤처투자조합 결성 현황]
| (단위:억원) |
|
조합명 |
약정총액 |
결성일 |
존속기한 |
펀드단계 |
|
|---|---|---|---|---|---|
|
1 |
에이치엘비아이 알밤 제1호 투자조합 | 20 |
2022.06.30 |
7년 | 운용중 |
| 합 계 | 20 | - | - | - | |
3. (금융업)파생상품거래 현황
보고서 제출일 현재 해당사항 없습니다.
4. (금융업)영업설비
[지점 등 설치 현황]
| 지 역 | 본점 및 지점 | 출 장 소 | 사 무 소 | 합 계 |
|---|---|---|---|---|
| 서울 | 1 | - | - | 1 |
| 해외 | - | - | - | - |
| 계 | 1 | - | - | 1 |
- 당사는 창업투자회사로서 서울에 본점를 두고 별도의 지점 등을 설치하지 않고 있습니다.
5. (금융업)재무건전성 등 기타 참고사항
가. 사업의 개황
에이치엘비인베스트먼트㈜는 벤처투자 촉진에 관한 법률에 의거 중소벤처기업부에등록된 중소기업창업투자회사로서 벤처투자조합 등 조합 결성을 통한 창업자 및 중소벤처기업 투자를 주력 사업으로 영위하고 있는 벤처캐피탈(Venture Capital, VC)입니다.
지속적인 경제성장을 위해서는 새로운 가치와 신산업을 창출하기 위한 창의적인 아이디어나 융합에 바탕을 둔 새로운 사업기회로 자금이 원활히 유입될 필요가 있으며,이와 같이 장래성은 있으나 자본과 경영기반이 취약해 일반 금융기관에서 융자를 받기가 어려운 기업에 대해 창업 초기단계에 자본참여를 하는 것이 벤처캐피탈의 역할입니다. 벤처캐피탈은 투자한 기업의 성장 이후 인수합병(M&A), 상장(IPO)등을 통해서 투자자금을 회수하는 금융자본이며 동시에 금융회사라고 할 수 있습니다. 특히,벤처캐피탈은 은행과 같은 자금 대출이 아닌 지분투자방식의 대표적인 투자자로서 벤처기업의 혁신을 이끄는 중요한 기능을 수행합니다.
벤처캐피탈은 국내 관련법에 의거하여 "중소기업창업투자회사", "신기술사업금융회사"로 구분되고 있으며, 창업투자회사는 「벤처투자 촉진에 관한 법률」,신기술사업금융회사는 「여신전문금융업법」에 의해 설립 및 운영되고 있습니다. 이 중 당사가 영위하고 있는 중소기업창업투자회사는 「벤처투자 촉진에 관한 법률」에 의거 중소벤처기업부에 등록된 상법상 주식회사로서 주요 업무로는 창업자(창업한지 7년 이내의 중소기업) 및 벤처기업에 대한 투자, 벤처투자조합의 결성 및 업무의 집행, 해외기업의 주식 또는 지분인수 등 중소벤처기업부 장관이 정하는 방법에 따른 해외투자, 창업보육센터 설립 및 운영이 있습니다.
| [국내 벤처캐피탈 관련 법령에 따른 구분] |
|
구분 |
중소기업창업투자회사 |
신기술사업금융회사 |
|---|---|---|
|
설립근거 |
벤처투자 촉진에 관한 법률 |
여신전문금융업법 |
|
관할기관 |
중소벤처기업부 |
금융위원회 |
| 설립자본금 | 최소 20억원 | 최소 100억원 |
| 투자의무 | 등록 후 3년내 자본금의 40%를 창업자 등에 신규투자 |
없음 |
| 투자대상 | 중소, 벤처, 창업기업 | 신기술사업자 |
| 기대역할 | 초기단계 기업에 대한 투자 (중소기업 창업 지원) |
성장단계 기업에 대한 금융지원, 중간회수시장 활성화 |
중소기업창업투자회사는 일반적으로 주주가 자본금을 납입하여 설립하는 주식회사로서, 주주, 이사회 그리고 투자전문인력인 투자심사역으로 구성되어 있습니다. 중소기업창업투자회사의 투자방식으로는 크게 투자조합을 설립하여 외부자금(개인, 법인, 연기금, 금융기관, 정부기관 등)으로 조합 출자를 통한 투자와 회사의 고유계정을 이용한 직접투자로 나누어 볼 수 있습니다.
투자조합은 자금을 모집하는 Vehicle 성격을 가지고 있으며, 조합규정을 준용하여 사모(Private Equity Finance)방식의 투자자 간 계약형식을 취하고 있습니다. 중소기업창업투자회사는 업무집행조합원(General Partner: GP)으로서 투자조합을 운용할 수있는 법적주체로 조합의 설립, 투자, 분배, 기타 조합사무 등을 총괄하게 됩니다.
벤처캐피탈의 투자 활동의 시작은 투자재원의 조달입니다. 특히, 벤처기업에 대한 투자는 그 특성상 높은 리스크와 상대적으로 장기간의 투자를 요한다는 점에서 일반적인 기업에 대한 투자환경보다 자금 조달에 있어 어려움이 있습니다. 그러나 국내의 경우 정책부문의 자금지원을 통해 벤처기업 투자를 지원하고 있습니다. 정부는 공적 기관인 한국벤처투자㈜를 투자관리전문기관으로 하여 한국벤처투자조합을 전문적으로 관리하고 있습니다.
모태펀드(Fund of Funds)는 벤처기업이나 혁신기업에 직접 투자하는 것이 아니라 한국모태펀드의 자펀드인 벤처투자조합 등의 투자조합에 출자함으로써 벤처기업이나 혁신기업에 간접투자하는 방식을 취하고 있습니다. 이외에도 산업은행, 한국성장금융투자운용(성장사다리펀드), 우정사업본부 등 정책금융기관, 연기금 및 공제회(국민연금, 교직원공제회 등) 및 정부부처가 직접 출자하고 하위에 자펀드를 결성하여 투자조합 출자를 통한 자금지원도 이루어지고 있습니다. 이러한 정책자금의 지원을 통하여 많은 투자조합들이 설립되고 있으며 정부지원 또한 향후에도 지속될 것으로 예상되고 있습니다.
벤처캐피탈은 투자조합을 운영함으로써 운용에 따른 관리보수(Management fee)와 일정 기준수익률 이상의 투자 회수결과에 따른 성과보수(Carried interest) 및 투자조합에 GP로서 출자한 출자금에서 발생하는 조합에 대한 투자수익을 얻을 수 있습니다.
관리보수는 업무집행조합원(GP)에 대한 기본보수로서, 업무집행조합원은 관리보수를 기반으로 한 운영자금으로 운용인력을 확보하여 벤처기업을 발굴 및 심사하고 투자하게 되며 또한 투자조합의 공시 및 기타 사무 처리를 담당하게 됩니다. 관리보수의 경우 일반적으로 조합의 규약마다 다르지만 조합 설립 후 투자기간 동안은 결성 약정금액의 일정비율로 지급되며, 이후 회수기간에는 조합의 규약으로 별도 규정하여 업무집행조합원에게 지급이 됩니다.
성과보수는 조합운용 결과에 따라 지급되는 추가수익으로 조합마다 지급규정은 다르며, 일반적으로 규약상 기준수익률(IRR, 일반적으로 3~8%)을 초과하는 조합배분금액의 일정비율(일반적으로 20% 전후)을 업무집행조합원에게 지급하게 됩니다. 또한,운용 결과에 따라 최종 조합 출자자금 회수 시 출자자로서 지분 참여에 대한 추가적인 수익을 얻을 수 있습니다.
중소기업창업투자회사는 관련 규정에 의해 벤처투자조합을 설립 및 운영할 수 있습니다. 투자조합의 세부적인 조건인 모집금액, 출자비율, 투자기간, 투자대상 등은 각 조합의 설립시의 출자자(LP)와 합의한 규약을 기본으로 하며 각 조합의 성격에 따라 다양하게 결정이 됩니다.
또한, 중소기업창업투자회사는 벤처투자조합 이외에 「자본시장과 금융투자업에 관한 법률」(이하 자본시장법)에서 규정하는 경영참여형사모집합투자기구(이하 경영참여형 사모펀드 또는 PEF(Private Equity Fund)의 업무집행사원(GP)으로서 PEF를 설립 및 운용할 수 있습니다.
PEF는 전통적인 의미로는 개인적인 신뢰관계를 바탕으로 특정소수의 투자자로부터 자금을 모집하고, 공개시장이 아닌 곳에서 투자대상을 물색하여 협상 등의 과정을 거쳐 투자하고 장외 매각 을 통해 투자한 자금을 회수하는 펀드입니다.
나. 사업구조
벤처캐피탈은 (1) 투자재원 확보, (2) 투자발굴 및 집행, (3) 회수 및 수익실현으로 이어지는 순환적 주기의 사업구조를 가지고 있습니다. 즉, (1) 정부의 정책자금, 연기금등의 기관투자자, 민간/해외자금 등을 통해 재원을 조달하여 조합을 결성하여, (2) 유망하고 성장성이 높은 기업을 발굴, 평가하여 투자한 후 (3) 기업의 성장에 따라 해당기업의 상장, 또는 M&A, Secondary(구주매각) 등 회수시장을 통하여 매각함으로써 자본이득을 취하는 구조로 이루어집니다.
다. 산업 특성
1) 산업의 정의 및 특성
중소기업창업투자회사는 일반적으로 고도의 기술성과 장래성은 있으나 자본과 경영기반이 취약한 기업에 대하여 성공여부가 매우 불확실한 사업 초기단계에서 높은 위험을 벤처기업과 공동으로 부담하면서 자금, 경영관리, 기술지도 등 종합적인 지원을제공하고 높은 자본이득을 얻고자 하는 금융활동 즉 벤처캐피탈을 업으로 합니다.
벤처캐피탈은 성장잠재력이 있는 신생벤처기업을 투자대상으로 선정하여 벤처기업의 성장, 발전을 도모함으로써 기술개발을 촉진하고 산업구조의 고도화와 고용창출을 유발함으로써 국민경제의 활성화에 기여하는 역할을 담당하고 있습니다.
벤처캐피탈 산업의 특징은 (1) 창업 및 성장 단계의 벤처기업에 투자 (2) 창업에서 성장, 발전 단계까지의 자금, 기술, 영업지원 경영지도등 기업 활동 전반에 대한 서비스를 제공하여 (3) 벤처기업의 증권유통시장 상장을 통한 지분매각 방식으로 투자금을 회수하는 것을 주요 업무내용으로 하고 있습니다. 벤처, 창업기업의 경우 불확실성에따른 투자 위험도가 상대적으로 높습니다.
2) 창업투자회사 등록 현황
중소기업창업지원법 제정 후, 2001년 이후부터 중반까지 신규등록이 부진하다가 2005년과 2009년 설립자본금 요건이 완화되면서 많은 창업투자회사가 신규로 진입하게 되었습니다.
2021년 12월말 현재 창업투자회사는 38개사가 신규등록되는 한편 6개사가 말소 됨에 따라 전년도(2020년)말 165개사에서 32개사가 증가한 197개사가 현재 등록, 운영중입니다.
3) 창업투자회사 투자재원 현황
2021년 동안 신규 결성된 조합의 수는 404개로 총 약정금액은 9조 2,171억원이며, 12월 말 현재창업투자회사가 운영중인 조합의 수는 1,431개로 총 약정금액은 41조 2,356억원으로 전년 동기대비 24.12%의 투자재원이 증가하였습니다.
| [조합결성현황] |
| (단위: 개, 억원) |
|
구분 |
2017 |
2018 | 2019 | 2020 | 2021 | |
|---|---|---|---|---|---|---|
| 신규 | 조합 수 | 164 | 146 | 170 | 206 | 404 |
| 금액 | 45,856 | 48,427 | 42,411 | 68,808 | 92,171 | |
| 운영 | 조합 수 | 717 | 805 | 920 | 1,078 | 1,431 |
| 금액 | 203,614 | 240,786 | 273,351 | 332,224 | 412,356 | |
| 자료: | 한국벤처캐피탈협회 벤처투자정보센터 |
라. 경쟁 현황
1) 경쟁 상황
벤처캐피탈 산업의 주요 참가자는 법률적인 규정에 따라 중소기업창업투자회사, 신기술사업금융업자로 볼 수 있으며 이들은 관련 법령에 의하여 자본금, 인력 구성 등의 일정한 요건에 따라 등록 또는 신고하도록 되어 있으므로 법률적 진입 장벽이 존재합니다. 그러나, 정부의 벤처 활성화 정책에 따라 관련 진입 장벽이 지속 완화되고 있음에 따라 국내 벤처캐피탈의 경쟁 강도는 높아지고 있습니다.
2) 경쟁업체 현황
일반적으로 벤처기업 등에 자금을 투자하는 투자시장으로서 벤처캐피탈 시장의 경쟁강도는 높은 편입니다. 경쟁대상은 개인(엔젤투자자)부터 일반법인, 각종 금융기관(은행, 증권 등) 매우 다양하다고 할 수 있습니다. 그러나 투자조합을 설립 후 자금을 모집하여 벤처기업 등에 투자를 영위할 수 있는 회사는 관련법에 의거하여 규정되어 있으며, 관할 기관의 등록을 요하고 있습니다.
벤처캐피탈 산업에 있어서 경쟁의 특성은 협력적 경쟁의 성격을 띱니다. 협력과 경쟁이 결합된 형태로 서로 경쟁을 하면서도 상호협력을 하는 형태가 나타납니다. 이는 투자의 규모, 투자의 단계에 따른 특성에 기인합니다. 때문에 벤처캐피탈 상호간에는인적 교류를 통한 긴밀한 네트워크가 형성되어 있습니다. 이러한 네트워크를 통한 상호 협력은 제한된 정보하에서 교차 확인을 통한 정보의 비대칭성 극복, 투자기회의 확대, 위험의 분산, 추가투자 유치를 통한 투자기업의 성장 도모, 회수 용이성 확보 등의 이점을 제공합니다.
III. 재무에 관한 사항
1. 요약재무정보
가. 요약 연결재무정보
에이치엘비 주식회사와 그 종속회사
| (단위: 천원) |
| 구분 | 제38기(당)반기 | 제37기(전)기 | 제36(전전)기 |
|---|---|---|---|
| (검토받은 연결재무제표) | (감사받은 연결재무제표) | (감사받은 연결재무제표) | |
| (2022년 06월말) | (2021년 12월말) | (2020년 12월말) | |
| [유동자산] | 163,135,519 | 188,141,791 | 251,572,612 |
| ㆍ현금및현금성자산 | 80,483,163 | 99,796,601 | 220,677,816 |
| ㆍ매출채권 | 27,995,134 | 34,034,508 | 11,746,776 |
| ㆍ공정가치측정금융자산 | 7,113,529 | - | - |
| ㆍ기타유동금융자산 | 16,018,908 | 29,244,921 | 3,770,916 |
| ㆍ재고자산 | 17,375,524 | 13,810,969 | 4,874,065 |
| ㆍ미수법인세환급액 | 10,228,719 | 8,403,838 | 251,728 |
| ㆍ기타유동자산 | 3,920,542 | 2,850,955 | 7,034,591 |
| [비유동자산] | 650,007,753 | 555,550,473 | 454,904,665 |
| ㆍ공정가치측정금융자산 | 53,113,220 | 29,624,538 | 53,260,695 |
| ㆍ기타비유동금융자산 | 4,615,067 | 8,707,903 | 635,726 |
| ㆍ관계기업투자주식 | 191,637,423 | 133,623,849 | 106,499,613 |
| ㆍ기타비유동자산 | 1,975,095 | 1,218,276 | 756,706 |
| ㆍ투자부동산 | 19,173 | 19,173 | 2,586,076 |
| ㆍ유형자산 | 41,857,767 | 41,458,514 | 19,892,235 |
| ㆍ무형자산 | 356,790,008 | 339,536,102 | 263,845,216 |
| ㆍ이연법인세자산 | - | 1,362,117 | 7,428,397 |
| 자산총계 | 813,143,272 | 743,692,264 | 706,477,277 |
| [유동부채] | 123,299,896 | 121,819,304 | 98,026,815 |
| [비유동부채] | 154,526,736 | 109,688,157 | 51,021,044 |
| 부채총계 | 277,826,631 | 231,507,461 | 149,047,858 |
| [지배주주지분] | 461,775,797 | 435,957,351 | 479,751,330 |
| ㆍ자본금 | 53,444,967 | 53,308,626 | 26,491,547 |
| ㆍ주식발행초과금 | 660,162,652 | 779,883,721 | 775,814,984 |
| ㆍ연결기타자본항목 | (189,337,607) | (214,212,950) | (237,106,449) |
| ㆍ연결이익잉여금(결손금) | (62,494,215) | (183,022,047) | (85,448,752) |
| [비지배지분] | 73,540,844 | 76,227,452 | 77,678,089 |
| 자본총계 | 535,316,641 | 512,184,803 | 557,429,419 |
| 관계기업투자주식의 평가방법 | 지분법 | 지분법 | 지분법 |
| (2022.1.1 ~ 2022.06.30) | (2021.1.1 ~ 2021.12.31) | (2020.1.1 ~ 2020.12.31) | |
| 매출액 | 123,304,717 | 69,825,991 | 56,177,401 |
| 영업이익(손실) | (20,095,818) | (101,018,424) | (61,311,788) |
| 당기순이익(손실) | (19,100,090) | (111,606,826) | (88,716,232) |
| ㆍ지배기업의 소유주지분 | (9,472,168) | (98,125,466) | (80,093,074) |
| ㆍ비지배지분 | (9,627,922) | (13,481,360) | (8,623,158) |
| 총포괄이익(손실) | (15,696,327) | (86,340,340) | (103,887,537) |
| ㆍ지배기업의 소유주지분 | (10,821,053) | (75,370,359) | (95,264,379) |
| ㆍ비지배지분 | (4,875,274) | (10,969,981) | (8,623,158) |
| 기본주당순이익(손실) | (89)원 | (923)원 | (768)원 |
| 희석주당순이익(손실) | (89)원 | (923)원 | (768)원 |
| 연결에 포함된 회사의 수 | 5 개 | 7 개 | 4 개 |
나. 요약 재무정보
에이치엘비 주식회사
| (단위: 천원) |
| 구분 | 제38기(당)반기 | 제37기(전)기 | 제36(전전)기 |
|---|---|---|---|
| (검토받은 재무제표) | (감사받은 재무제표) | (감사받은 재무제표) | |
| (2022년 06월말) | (2021년 12월말) | (2020년 12월말) | |
| [유동자산] | 111,068,528 | 61,287,290 | 173,521,334 |
| ㆍ현금및현금성자산 | 48,724,359 | 36,642,797 | 153,999,757 |
| ㆍ매출채권 | 27,808,265 | 18,707,735 | 11,185,699 |
| ㆍ공정가치측정금융자산 | 7,113,529 | ||
| ㆍ기타유동금융자산 | 10,898,500 | 2,359,396 | 3,042,360 |
| ㆍ재고자산 | 14,452,027 | 3,006,977 | 4,086,441 |
| ㆍ미수법인세환급액 | - | 312,043 | 251,433 |
| ㆍ기타유동자산 | 2,071,847 | 258,341 | 955,644 |
| [비유동자산] | 819,868,939 | 740,936,084 | 617,965,138 |
| ㆍ공정가치측정금융자산 | 53,113,220 | 28,123,279 | 53,260,695 |
| ㆍ기타비유동금융자산 | 4,256,908 | 9,304,466 | 597,942 |
| ㆍ종속기업및관계기업투자주식 | 646,040,849 | 661,543,145 | 512,616,381 |
| ㆍ투자부동산 | 19,173 | 19,173 | 2,586,076 |
| ㆍ유형자산 | 28,903,757 | 8,820,831 | 8,779,800 |
| ㆍ무형자산 | 87,263,905 | 33,125,189 | 40,124,244 |
| ㆍ퇴직연금운용자산 | 271,127 | - | - |
| 자산총계 | 930,937,467 | 802,223,373 | 791,486,471 |
| [유동부채] | 49,124,856 | 24,296,879 | 45,234,621 |
| [비유동부채] | 91,350,882 | 47,501,801 | 1,023,326 |
| 부채총계 | 140,475,738 | 71,798,680 | 46,257,946 |
| ㆍ자본금 | 53,444,967 | 53,308,626 | 26,491,547 |
| ㆍ주식발행초과금 | 660,162,652 | 779,883,721 | 775,814,984 |
| ㆍ기타자본항목 | 13,599,169 | 12,386 | (8,839,258) |
| ㆍ이익잉여금(결손금) | 63,254,941 | (102,780,040) | (48,238,749) |
| 자본총계 | 790,461,729 | 730,424,693 | 745,228,525 |
| 종속 및 관계기업 투자주식의 평가방법 | 원가법 | 원가법 | 원가법 |
| (2022.1.1 ~ 2022.06.30) | (2021.1.1 ~ 2021.12.31) | (2020.1.1 ~ 2020.12.31) | |
| 매출액 | 120,386,478 | 36,375,293 | 48,730,105 |
| 영업이익(손실) | 36,308,380 | (14,452,296) | (9,905,938) |
| 당기순이익(손실) | 36,034,981 | (54,736,057) | (60,065,222) |
| 총포괄이익(손실) | 35,754,763 | (53,683,481) | (60,542,078) |
| 기본주당순이익(손실) | 338 원 | (515)원 | (576)원 |
| 희석주당순이익(손실) | 338 원 | (515)원 | (576)원 |
2. 연결재무제표
|
연결 재무상태표 |
|
제 38 기 반기말 2022.06.30 현재 |
|
제 37 기말 2021.12.31 현재 |
|
(단위 : 원) |
|
제 38 기 반기말 |
제 37 기말 |
|
|---|---|---|
|
자산 |
||
|
유동자산 |
163,135,518,859 |
188,141,790,615 |
|
현금및현금성자산 |
80,483,162,607 |
99,796,600,600 |
|
매출채권 |
27,995,134,136 |
34,034,507,841 |
|
공정가치측정금융자산 |
7,113,529,495 |
0 |
|
기타유동금융자산 |
16,018,907,567 |
29,244,921,050 |
|
재고자산 |
17,375,523,777 |
13,810,968,811 |
|
미수법인세환급액 |
10,228,719,164 |
8,403,837,507 |
|
기타유동자산 |
3,920,542,113 |
2,850,954,806 |
|
비유동자산 |
650,007,753,330 |
555,550,473,480 |
|
공정가치측정금융자산 |
53,113,220,246 |
29,624,538,434 |
|
기타비유동금융자산 |
4,615,066,877 |
8,707,902,857 |
|
관계기업투자주식 |
191,637,422,683 |
133,623,849,308 |
|
기타비유동자산 |
1,975,095,453 |
1,218,276,111 |
|
투자부동산 |
19,173,350 |
19,173,350 |
|
유형자산 |
41,857,767,028 |
41,458,513,994 |
|
무형자산 |
356,790,007,693 |
339,536,102,329 |
|
이연법인세자산 |
0 |
1,362,117,097 |
|
자산총계 |
813,143,272,189 |
743,692,264,095 |
|
부채 |
||
|
유동부채 |
123,299,895,646 |
121,819,304,371 |
|
매입채무 |
4,600,684,864 |
5,084,230,389 |
|
차입금 |
25,884,465,271 |
21,216,911,781 |
|
기타유동금융부채 |
83,318,090,382 |
84,011,524,934 |
|
금융보증부채 |
62,156,461 |
12,225,450 |
|
계약부채 |
1,734,286,755 |
563,168,429 |
|
기타유동부채 |
404,758,605 |
1,290,666,322 |
|
당기법인세부채 |
7,295,453,308 |
9,640,577,066 |
|
비유동부채 |
154,526,735,576 |
109,688,157,027 |
|
비유동차입금 |
84,169,231,853 |
47,377,858,171 |
|
기타비유동금융부채 |
14,571,713,890 |
10,048,843,005 |
|
기타비유동부채 |
25,000,000 |
25,000,000 |
|
비유동금융보증부채 |
0 |
44,275,000 |
|
이연법인세부채 |
55,760,789,833 |
52,253,751,145 |
|
확정급여채무의현재가치 |
0 |
(61,570,294) |
|
부채총계 |
277,826,631,222 |
231,507,461,398 |
|
자본 |
||
|
지배주주지분 |
461,775,797,334 |
435,957,350,662 |
|
자본금 |
53,444,966,500 |
53,308,626,000 |
|
주식발행초과금 |
660,162,652,436 |
779,883,721,324 |
|
기타자본항목 |
(189,337,606,644) |
(214,212,949,975) |
|
이익잉여금(결손금) |
(62,494,214,958) |
(183,022,046,687) |
|
비지배지분 |
73,540,843,633 |
76,227,452,035 |
|
자본총계 |
535,316,640,967 |
512,184,802,697 |
|
부채 및 자본총계 |
813,143,272,189 |
743,692,264,095 |
|
연결 포괄손익계산서 |
|
제 38 기 반기 2022.01.01 부터 2022.06.30 까지 |
|
제 37 기 반기 2021.01.01 부터 2021.06.30 까지 |
|
(단위 : 원) |
|
제 38 기 반기 |
제 37 기 반기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
매출액 |
57,791,933,158 |
123,304,716,976 |
8,393,039,545 |
15,956,824,335 |
|
매출원가 |
33,847,086,045 |
73,343,253,322 |
8,475,427,556 |
15,438,756,860 |
|
매출총이익 |
23,944,847,113 |
49,961,463,654 |
(82,388,011) |
518,067,475 |
|
판매비와관리비 |
37,542,843,689 |
70,057,281,274 |
20,910,889,140 |
40,274,984,959 |
|
영업이익(손실) |
(13,597,996,576) |
(20,095,817,620) |
(20,993,277,151) |
(39,756,917,484) |
|
기타수익 |
394,898,096 |
521,032,920 |
2,469,068,943 |
3,086,363,852 |
|
기타비용 |
117,687,527 |
216,284,644 |
1,499,637,391 |
2,292,827,448 |
|
금융수익 |
8,903,561,935 |
9,738,151,724 |
475,878,022 |
1,025,681,633 |
|
금융비용 |
(1,270,352,153) |
4,799,938,141 |
12,289,856,175 |
13,178,917,378 |
|
관계기업투자주식관련 손익 |
5,478,469,763 |
2,690,855,257 |
(3,143,105,944) |
(5,961,061,760) |
|
법인세비용차감전순이익(손실) |
2,331,597,844 |
(12,162,000,504) |
(34,980,929,696) |
(57,077,678,585) |
|
법인세비용(수익) |
1,146,695,361 |
6,938,089,424 |
0 |
0 |
|
당기순이익(손실) |
1,184,902,483 |
(19,100,089,928) |
(34,980,929,696) |
(57,077,678,585) |
|
당기순이익(손실)의 귀속 |
||||
|
지배기업의 소유주지분 |
6,282,902,369 |
(9,472,168,271) |
(31,912,974,620) |
(50,322,030,612) |
|
비지배지분 |
(5,097,999,886) |
(9,627,921,657) |
(3,067,955,076) |
(6,755,647,973) |
|
기타포괄손익 |
2,805,617,912 |
3,403,763,154 |
(2,419,526,762) |
4,032,902,197 |
|
당기손익으로 재분류되지 않는항목 |
||||
|
기타포괄손익-공정가치측정 지분상품 평가손익 |
(358,056,525) |
(280,218,150) |
1,467,248,400 |
1,155,458,115 |
|
당기손익으로 재분류될 수 있는 항목 |
||||
|
지분법자본변동 |
2,749,186,902 |
2,804,361,915 |
760,725,396 |
759,536,438 |
|
해외사업환산손익 |
414,487,535 |
879,619,389 |
(4,647,500,558) |
2,117,907,644 |
|
총포괄손익 |
3,990,520,395 |
(15,696,326,774) |
(37,400,456,458) |
(53,044,776,388) |
|
총 포괄손익의 귀속 |
||||
|
지배기업의 소유주지분 |
4,834,883,550 |
(10,821,053,087) |
(34,051,315,372) |
(47,418,171,362) |
|
비지배지분 |
(844,363,155) |
(4,875,273,687) |
(3,349,141,086) |
(5,626,605,026) |
|
주당이익 |
||||
|
기본주당이익(손실) (단위 : 원) |
59 |
(89) |
(301) |
(474) |
|
희석주당이익(손실) (단위 : 원) |
59 |
(89) |
(301) |
(474) |
|
연결 자본변동표 |
|
제 38 기 반기 2022.01.01 부터 2022.06.30 까지 |
|
제 37 기 반기 2021.01.01 부터 2021.06.30 까지 |
|
(단위 : 원) |
|
자본 |
|||||||
|---|---|---|---|---|---|---|---|
|
지배기업의 소유주에게 귀속되는 자본 |
비지배지분 |
자본 합계 |
|||||
|
자본금 |
자본잉여금 |
기타자본항목 |
이익잉여금(결손금) |
지배기업의 소유주에게 귀속되는 자본 합계 |
|||
|
2021.01.01 (기초자본) |
26,491,546,500 |
775,814,984,487 |
(237,106,449,191) |
(85,448,751,794) |
479,751,330,002 |
77,678,088,584 |
557,429,418,586 |
|
당기순이익(손실) |
0 |
0 |
0 |
(50,322,030,612) |
(50,322,030,612) |
(6,755,647,973) |
(57,077,678,585) |
|
지분법 자본변동 |
0 |
0 |
759,536,438 |
0 |
759,536,438 |
0 |
759,536,438 |
|
해외사업환산손익 |
0 |
0 |
988,864,697 |
0 |
988,864,697 |
1,129,042,947 |
2,117,907,644 |
|
기타포괄손익-공정가치측정 지분상품 투자손익 |
0 |
0 |
1,155,458,115 |
0 |
1,155,458,115 |
0 |
1,155,458,115 |
|
이익잉여금 대체 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
복합금융상품 전환 |
64,630,000 |
10,725,090,388 |
(1,154,570,358) |
0 |
9,635,150,030 |
0 |
9,635,150,030 |
|
복합금융상품 발행 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
주식기준보상거래 |
0 |
0 |
2,950,424,422 |
0 |
2,950,424,422 |
0 |
2,950,424,422 |
|
기타자본조정 |
0 |
0 |
3,984,128,796 |
0 |
3,984,128,796 |
2,178,593,564 |
6,162,722,360 |
|
무상증자 |
26,486,214,500 |
(26,728,737,240) |
0 |
0 |
(242,522,740) |
0 |
(242,522,740) |
|
자본 증가(감소) 합계 |
26,550,844,500 |
(16,003,646,852) |
8,683,842,110 |
(50,322,030,612) |
(31,090,990,854) |
(3,448,011,462) |
(34,539,002,316) |
|
2021.06.30 (기말자본) |
53,042,391,000 |
759,811,337,635 |
(228,422,607,081) |
(135,770,782,406) |
448,660,339,148 |
74,230,077,122 |
522,890,416,270 |
|
2022.01.01 (기초자본) |
53,308,626,000 |
779,883,721,324 |
(214,212,949,975) |
(183,022,046,687) |
435,957,350,662 |
76,227,452,035 |
512,184,802,697 |
|
당기순이익(손실) |
0 |
0 |
0 |
(9,472,168,271) |
(9,472,168,271) |
(9,627,921,657) |
(19,100,089,928) |
|
지분법 자본변동 |
0 |
0 |
2,804,361,915 |
0 |
2,804,361,915 |
0 |
2,804,361,915 |
|
해외사업환산손익 |
0 |
0 |
(3,873,028,581) |
0 |
(3,873,028,581) |
4,752,647,970 |
879,619,389 |
|
기타포괄손익-공정가치측정 지분상품 투자손익 |
0 |
0 |
(280,218,150) |
0 |
(280,218,150) |
0 |
(280,218,150) |
|
이익잉여금 대체 |
0 |
(130,000,000,000) |
0 |
130,000,000,000 |
0 |
0 |
0 |
|
복합금융상품 전환 |
136,340,500 |
10,278,931,112 |
(1,066,514,816) |
0 |
9,348,756,796 |
0 |
9,348,756,796 |
|
복합금융상품 발행 |
0 |
0 |
12,511,362,850 |
0 |
12,511,362,850 |
0 |
12,511,362,850 |
|
주식기준보상거래 |
0 |
0 |
117,796,356 |
0 |
117,796,356 |
1,374,793,409 |
1,492,589,765 |
|
기타자본조정 |
0 |
0 |
14,661,583,757 |
0 |
14,661,583,757 |
813,871,876 |
15,475,455,633 |
|
무상증자 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
자본 증가(감소) 합계 |
136,340,500 |
(119,721,068,888) |
24,875,343,331 |
120,527,831,729 |
25,818,446,672 |
(2,686,608,402) |
23,131,838,270 |
|
2022.06.30 (기말자본) |
53,444,966,500 |
660,162,652,436 |
(189,337,606,644) |
(62,494,214,958) |
461,775,797,334 |
73,540,843,633 |
535,316,640,967 |
|
연결 현금흐름표 |
|
제 38 기 반기 2022.01.01 부터 2022.06.30 까지 |
|
제 37 기 반기 2021.01.01 부터 2021.06.30 까지 |
|
(단위 : 원) |
|
제 38 기 반기 |
제 37 기 반기 |
|
|---|---|---|
|
영업활동현금흐름 |
(33,915,122,068) |
(28,656,912,636) |
|
당기순이익(손실) |
(19,100,089,928) |
(57,077,678,585) |
|
수익비용의 조정 |
10,390,826,050 |
28,918,788,872 |
|
영업활동으로 인한 자산부채의 변동 |
(15,949,312,918) |
(1,296,141,734) |
|
이자의 수취 |
405,193,276 |
548,939,185 |
|
이자의 지급 |
(2,991,781) |
(2,432,944) |
|
법인세의 납부(환급) |
(9,658,746,767) |
251,612,570 |
|
투자활동현금흐름 |
(20,876,134,730) |
(5,501,304,221) |
|
종속관계기업투자주식의 처분 |
3,300,000,000 |
0 |
|
기타유동금융자산의 처분 |
0 |
74,876 |
|
단기대여금의 회수 |
1,808,857,367 |
2,000,000 |
|
임차보증금의 감소 |
96,150,890 |
122,357,156 |
|
공정가치측정금융자산의 처분 |
358,699,450 |
3,491,578,856 |
|
투자부동산의 처분 |
0 |
2,848,000,000 |
|
무형자산의 처분 |
0 |
208,474,719 |
|
유형자산의 처분 |
705,719,986 |
0 |
|
단기금융상품의 처분 |
23,300,000,000 |
0 |
|
종속기업과 기타 사업의 지배력 상실에 따른 현금흐름 |
742,331,826 |
3,000,000,000 |
|
종속관계기업투자주식의 취득 |
(25,025,920,000) |
(8,602,000,000) |
|
기타유동금융자산의 취득 |
0 |
(17,808,000) |
|
단기대여금의 대여 |
0 |
(74,585,000) |
|
장기대여금의 취득 |
(2,000,000,000) |
0 |
|
선물거래예치금의 증가 |
(30,852,510) |
0 |
|
임차보증금의 증가 |
(47,858,505) |
(1,589,555,806) |
|
유형자산의 취득 |
(994,528,882) |
(1,391,744,026) |
|
무형자산의 취득 |
(655,212,789) |
(2,380,366,996) |
|
장기금융상품의 취득 |
0 |
(1,117,730,000) |
|
공정가치측정금융자산의 취득 |
(19,671,928,000) |
0 |
|
사업결합으로 인한 현금유출 |
(1,464,582,327) |
0 |
|
단기금융상품의 취득 |
(1,005,000,000) |
0 |
|
종속기업과 기타 사업의 지배력 획득에 따른 현금흐름 |
(292,011,236) |
0 |
|
재무활동현금흐름 |
32,566,052,348 |
(1,470,045,545) |
|
장기차입금의 증가 |
0 |
872,535,805 |
|
주식선택권행사로 인한 현금유입 |
18,370,806 |
278,917,204 |
|
전환사채의 증가 |
23,000,000,000 |
0 |
|
신주인수권부사채의 증가 |
17,000,000,000 |
0 |
|
단기차입금의 상환 |
(6,168,332,000) |
(1,030,855,885) |
|
주식발행비용 |
(18,715,233) |
(254,705,530) |
|
리스료의 지급 |
(1,264,891,145) |
(1,160,937,139) |
|
임대보증금의 감소 |
(380,080) |
(175,000,000) |
|
환율변동효과 반영전 현금및현금성자산의 순증가(감소) |
(22,225,204,450) |
(35,628,262,402) |
|
기초현금및현금성자산 |
99,796,600,600 |
220,677,816,166 |
|
현금및현금성자산에 대한 환율변동효과 |
2,911,766,457 |
2,166,944,324 |
|
기말현금및현금성자산 |
80,483,162,607 |
187,216,498,088 |
3. 연결재무제표 주석
| 2022년 6월 30일 현재 |
| 2021년 6월 30일 현재 |
| 에이치엘비 주식회사와 그 종속기업 |
1. 회사의 개요
(1) 지배기업의 개요
에이치엘비 주식회사(이하 "당사")는 1985년 10월에 설립되어 1996년 7월 20일에 주식을 코스닥시장에 상장한 공개법인으로서 2013년에 현대라이프보트㈜와 합병 및 2015년에 전기계장사업부문의 물적분할 후 구명정, 유리섬유파이프 제조 및 시공업 등을 주요 영업으로 하고 있으며, 2022년 1월 1일 ㈜에프에이와 합병하여 체외진단키트 등 의료기기사업에 진출하였습니다. 또한 기존사업과 더불어 Elevar Therapeutics Inc., Immunomic Therapeutics Inc. 등에 지분투자를 통해 항암 신약 개발 사업 등 바이오사업을 영위하고 있습니다.
당반기말 현재 납입자본금은 53,444,967천원 입니다.
지배기업의 주요 주주의 구성은 다음과 같습니다.
| 주주명 | 당반기말 | 전기말 | ||
|---|---|---|---|---|
| 주식수(주) | 지분율(%) | 주식수(주) | 지분율(%) | |
| 진양곤 | 8,610,902 | 8.06% | 8,610,902 | 8.08% |
| 이현아 | 230,772 | 0.22% | 230,772 | 0.22% |
| 에이치엘비생명과학㈜ | 1,399,230 | 1.31% | 1,399,230 | 1.31% |
| 에이치엘비셀㈜ (구. 라이프리버㈜) | 828,214 | 0.77% | 828,214 | 0.78% |
| 에이치엘비㈜ (자기주식) | 134,000 | 0.13% | 134,000 | 0.13% |
| 기타(*) | 95,686,815 | 89.52% | 95,414,134 | 89.49% |
| 합 계 | 106,889,933 | 100.00% | 106,617,252 | 100.00% |
(*) 전기 중 임원퇴임(Elevar Therapeutics, Inc.)으로 특수관계가 해소된 Alex S.Kim의 지분이 포함되어 있습니다.
상기 주식수에는 우선주(7,188주)가 포함되어 있습니다.
(2) 당반기말과 전기말 현재 종속기업의 내역은 다음과 같습니다.
| 종속기업명 | 소재지 | 주요 영업활동 | 당반기말 | 전기말 | ||
|---|---|---|---|---|---|---|
| 소유지분율 | 비지배 지분비율 |
소유지분율 | 비지배 지분비율 |
|||
| Elevar Therapeutics, Inc. | 미국 | 표적항암제 개발 | 100.00% | - | 100.00% | - |
| Immunomic Therapeutics,Inc.(*1) | 미국 | 바이오의약품 개발 | 41.07% | 58.93% | 41.11% | 58.89% |
| 에이치엘비인베스트먼트㈜ | 대한민국 | 투자 및 융자 | 100.00% | - | 100.00% | - |
| Hyundai Lifeboats Shanghai PTE.LTD | 중국 | 선박 구명정 수리 및 검사 | 100.00% | - | - | - |
| ㈜화진메디칼(*2) | 대한민국 | 바이오 의료기기 제조 및 판매 | - | - | 100.00% | - |
| ㈜화진메디스(*2) | 대한민국 | 바이오 의료기기 제조 및 판매 | - | - | 100.00% | - |
| 에프에이 주식회사(*3) | 대한민국 | 바이오 의료기기 제조 및 판매 | - | - | 100.00% | - |
(*1) 당사의 지분율은 50% 미만이나 해당법인의 이사회 구성 등을 고려한 결과 사실상 지배력을 보유하고 있다고 판단하여 종속기업투자주식으로 분류하였습니다.
(*2) 당반기 중 지분 100%를 관계기업인 에이치엘비테라퓨틱스에 매각하였습니다.
(*3) 당사의 안정적인 수익 창출 및 향후 예정된 바이오 사업과의 시너지 극대화를 위해 전기 중 지분을 취득하였으며 당반기 중 지배기업과 합병하였습니다.
(3) 당반기말과 전기말 현재 종속기업의 요약 재무정보는 아래와 같습니다.
① 당반기말
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 기업명 | 자산 | 부채 | 자본 | 매출 | 당기순이익(손실) |
| Elevar Therapeutics, Inc. | 44,933,790 | 70,513,940 | (25,580,150) | - | (39,972,207) |
| Immunomic Therapeutics,Inc. | 47,190,230 | 17,747,650 | 29,442,580 | - | (16,348,424) |
| ㈜화진메디칼 | - | - | - | 2,577,730 | 85,103 |
| ㈜화진메디스 | - | - | - | 684,257 | (122,319) |
| 에이치엘비인베스트먼트㈜ | 9,691,931 | 181,439 | 9,510,492 | - | (463,944) |
| Hyundai Lifeboats Shanghai PTE.LTD | 1,049,240 | 114,439 | 934,801 | 385,867 | 70,547 |
② 전기말
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 기업명 | 자산 | 부채 | 자본 | 매출 | 당기순이익(손실) |
| Elevar Therapeutics, Inc. | 50,454,601 | 65,504,557 | (15,049,956) | - | (63,462,256) |
| Immunomic Therapeutics,Inc. | 56,963,645 | 15,506,680 | 41,456,965 | 2,320,412 | (26,055,891) |
| ㈜화진메디칼 | 7,575,943 | 5,554,283 | 2,021,660 | 8,565,749 | 62,609 |
| ㈜화진메디스 | 1,946,628 | 1,856,004 | 90,624 | 2,011,911 | (171,504) |
| 에이치엘비인베스트먼트㈜ | 10,227,041 | 162,352 | 10,064,689 | - | (437,756) |
| 에프에이㈜ | 70,208,219 | 20,936,409 | 49,271,810 | 22,536,698 | 2,619,973 |
(4) 연결대상범위의 변동
1) 당반기 중 연결실체는 Hyundai Lifeboats Shanghai PTE.LTD의 100% 지분을 취득함에 따라 지배력을 획득하였습니다.
2) 전기 중 연결실체는 에이치엘비인베스트먼트㈜의 100% 지분을 취득함에 따라 지배력을획득하였습니다. 연결실체는 신기술사업자에 대한 투자 및 융자등의 업무를 영위할 목적으로 설립되었습니다.
3) 당반기 중 지배기업은 ㈜화진메디칼, ㈜화진메디스의 지분 100%를 관계기업인 에이치엘비테라퓨틱스㈜에 매각하였습니다.
2. 중요한 회계정책
(1) 회계정책의 변경과 공시
1) 연결실체가 채택한 제ㆍ개정 회계기준
연결실체는 2022년 1월 1일부터 개시하는 회계기간부터 다음의 제ㆍ개정 회계기준을 신규로 적용하였습니다.
(가) 기업회계기준서 제1103호 '사업결합' (개정) - 재무보고를 위한 개념체계 참조
식별할 수 있는 취득 자산과 인수 부채는 재무보고를 위한 개념체계의 정의를 충족하도록 개정되었으나, 기업회계기준서 제1037호 '충당부채, 우발부채 및 우발자산' 및 해석서 제2121호 '부담금' 의 적용범위에 포함되는 부채 및 우발부채에 대해서는 해당 기준서를 적용하도록 예외를 추가하고, 우발자산이 취득일에 인식되지 않는다는 점을 명확히 하였습니다. 동 개정사항은 2022년 1월 1일 이후 시작하는 회계연도부터 적용됩니다. 상기 개정 내용이 연결재무제표에 미치는 유의적인 영향은 없습니다.
(나) 기업회계기준서 제1016호 '유형자산' (개정) - 의도한 사용 전의 매각금액
개정 기준서는 경영진이 의도한 방식으로 유형자산을 가동할 수 있는 장소와 상태에 이르게 하는 동안에 생산된 재화를 판매하여 얻은 매각금액과 그 재화의 원가는 당기손익으로 인식하도록 요구하며, 이로 인해 당기손익에 포함한 매각금액과 원가를 공시하도록 요구하고 있습니다. 동 개정사항은 2022년 1월 1일 이후 시작하는 회계연도부터 적용됩니다. 상기 개정 내용이 연결재무제표에 미치는 유의적인 영향은 없습니다.
(다) 기업회계기준서 제1037호 '충당부채, 우발부채 및 우발자산' (개정) - 손실부담계약: 계약이행원가
개정 기준서는 손실부담계약을 식별할 때 계약이행원가는 계약을 이행하는 데 드는 증분원가와 계약을 이행하는 데 직접 관련되는 그 밖의 원가 배분액으로 구성됨을 명확히 하였습니다. 동 개정사항은 2022년 1월 1일 이후 시작하는 회계연도부터 적용됩니다. 상기 개정 내용이 연결재무제표에 미치는 유의적인 영향은 없습니다.
(라) 기업회계기준서 제 1116호 '리스' (개정) - 2021년 6월 30일 후에도 제공되는 코로나19 관련 임차료 할인 등
코로나19의 직접적인 결과로 발생한 임차료 할인 등(rent concession)이 리스변경에 해당하는지 평가하지 않을 수 있도록 하는 실무적 간편법의 적용대상이 2022년 6월 30일 이전에 지급하여야 할 리스료에 영향을 미치는 리스료 감면으로 확대되었습니다. 리스이용자는 비슷한 상황에서 특성이 비슷한 계약에 실무적 간편법을 일관되게 적용해야 합니다. 동 개정사항은 2021년 4월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 상기 개정 내용이 연결재무제표에 미치는 유의적인 영향은 없습니다.
(마) 한국채택국제회계기준 2018-2020 연차개선
기업회계기준서 제1109호 '금융상품': 금융부채 제거 목적의 10% 테스트관련 수수료에 차입자와 대여자 사이에서 지급하거나 수취한 수수료(상대방을 대신하여 지급하거나 수취한 수수료 포함)만 포함된다는 개정내용을 포함하여 기업회계기준서 제1101호 '한국채택국제회계기준의 최초 채택': 최초채택기업인 종속기업, 기업회계기준서 제1116호 '리스': 리스인센티브, 기업회계기준서 제1041호 '농림어업': 공정가치 측정에 대한 일부 개정내용이 있습니다. 동 연차개선은 2022년 1월 1일 이후 시작하는 회계연도부터 적용됩니다. 상기 개정 내용이 연결재무제표에 미치는 유의적인 영향은 없습니다.
2) 공표되었으나 아직 시행되지 않은 제ㆍ개정 기준서 및 해석서
당반기말 현재 제정ㆍ공표되었으나 시행일이 도래하지 않아 연결실체가 채택하지 않은 한국채택국제회계기준의 기준서 및 해석서는 다음과 같습니다.
(가) 기업회계기준서 제1001호 '재무제표 표시' (개정) - 부채의 유동·비유동 분류
부채의 분류는 기업이 보고기간 후 적어도 12개월 이상 부채의 결제를 연기할 권리의 행사 가능성에 영향을 받지 않으며, 부채가 비유동부채로 분류되는 기준을 충족한다면, 경영진이 보고기간 후 12개월 이내에 부채의 결제를 의도하거나 예상하더라도, 또는 보고기간말과 재무제표 발행승인일 사이에 부채를 결제하더라도 비유동부채로 분류합니다. 또한, 부채를 유동 또는 비유동으로 분류할 때 부채의 결제조건에 자기지분상품의 이전도 포함되나, 복합금융상품에서 자기지분상품으로 결제하는 옵션이 지분상품으로 분류되고 동 옵션을 부채와 분리하여 인식된 경우는 제외됩니다. 동개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 적용하며, 조기적용이 허용됩니다. 연결실체는 상기 개정 기준서의 적용이 연결재무제표에 미치는 영향이 유의적이지 아니할 것으로 예상하고 있습니다.
(나) 기업회계기준서 제 1001호 '재무제표 표시' (개정)
개정 기준서는 공시 대상 회계정책 정보를 '유의적인' 회계정책에서 '중요한' 회계정책으로 바꾸고 중요한 회계정책 정보의 의미를 설명하였습니다. 동 개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 연결실체는 상기 개정 기준서의 적용이 연결재무제표에 미치는 영향이 유의적이지 아니할 것으로 예상하고 있습니다.
(다) 기업회계기준서 제1008호 '회계정책, 회계추정의 변경 및 오류' (개정)
개정 기준서는 '회계추정치'를 측정불확실성의 영향을 받는 재무제표상 화폐금액으로 정의하고, 회계추정치의 예를 보다 명확히 하였습니다. 또한 새로운 정보의 획득, 새로운 상황의 전개나 추가 경험의 축적으로 투입변수나 측정기법을 변경한 경우 이러한 변경이 전기오류수정이 아니라면 회계추정치의 변경임을 명확히 하였습니다.
동 개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 전진 적용되며, 조기적용이 허용됩니다. 연결실체는 상기 개정 기준서의 적용이 연결재무제표에 미치는 영향이 유의적이지 아니할 것으로 예상하고 있습니다.
(라) 기업회계기준서 제 1012호 '법인세' (개정)
개정 기준서는 이연법인세 최초 인식 예외규정을 추가하여 단일 거래에서 자산과 부채를 최초 인식할 때 동일한 금액으로 가산할 일시적차이와 차감할 일시적차이가 생기는 경우 각각 이연법인세 부채와 자산을 인식하도록 하였습니다. 동 개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다.
'단일 거래에서 생기는 자산과 부채에 관련되는 이연법인세'는 비교 표시되는 가장 이른 기간의 시작일 이후에 이루어진 거래에 적용하며, 비교 표시되는 가장 이른 기간의 시작일에 이미 존재하는 (1) 사용권자산과 리스부채, (2) 사후처리 및 복구 관련 부채 및 이에 상응하여 자산 원가의 일부로 인식한 금액에 관련되는 모든 차감할 일시적 차이와 가산할 일시적 차이에 대해 이연법인세 자산과 부채를 인식하며, 최초 적용 누적 효과를 이익잉여금(또는 자본의 다른 구성요소) 기초 잔액을 조정하여 인식합니다.
연결실체는 상기 개정 기준서의 적용이 연결재무제표에 미치는 영향이 유의적이지 아니할 것으로 예상하고 있습니다.
(2) 재무제표 작성 기준
1) 회계기준
연결재무제표는 주식회사 등의 외부감사에 관한 법률에서 규정하고 있는 국제회계기준위원회의 국제회계기준을 채택하여 정한 회계처리기준인 한국채택국제회계기준에 따라 작성되었습니다.
2) 측정기준
연결재무제표는 금융상품 등 아래의 회계정책에서 별도로 언급하고 있는 사항을 제외하고는 역사적원가를 기준으로 작성되었습니다.
3) 기능통화와 표시통화
연결재무제표는 지배기업의 기능통화이면서 표시통화인 "원(KRW)"으로 표시되고 있으며 별도로 언급하고 있는 사항을 제외하고는 "원(KRW)" 단위로 표시되고 있습니다.
(3) 연결기준
종속기업은 연결실체의 지배를 받고 있는 기업이며, 연결실체는 피투자자에 대한 관여로 변동이익에 노출되거나 변동이익에 대한 권리가 있고 피투자자에 대하여 자신의 힘으로 그러한 이익에 영향을 미치는 능력이 있을 때 피투자자를 지배합니다. 연결실체가 다른 기업에 대한 지배력을 평가할 때는 다른 당사자가 보유한 잠재적 의결권뿐만 아니라 자신이 보유한 잠재적 의결권도 고려하고 있습니다.
연결재무제표는 지배기업과 종속기업의 자산, 부채, 자본, 수익, 비용 및 현금흐름을 같은 항목별로 합산하고, 지배기업의 각 종속기업에 대한 투자자산의 장부금액과 각 종속기업의 자본 중 지배기업지분을 상계(제거)하며, 연결실체 내 기업간의 거래와 관련된 연결실체 내의 자산과 부채, 자본, 수익, 비용 및 현금흐름을 모두 제거하여 작성되고 있으며, 종속기업의 수익과 비용은 연결실체가 종속기업에 대해 지배력을 획득하는 시점부터 지배력을 상실하기 전까지 연결재무제표에 포함되고 있습니다
연결재무제표를 작성할 때 사용되는 지배기업과 종속기업의 재무제표는 동일한 보고기간종료일을 가집니다. 지배기업의 보고기간종료일과 종속기업의 보고기간종료일이 다른 경우, 종속기업은 연결재무제표를 작성하기 위하여 지배기업이 종속기업의 재무정보를 연결할 수 있도록 지배기업의 재무제표와 동일한 보고기간종료일의 추가적인 재무정보를 작성하고 있습니다. 다만, 종속기업이 실무적으로 적용할 수 없는 경우, 지배기업은 종속기업의 재무제표일과 연결재무제표일 사이에 발생한 유의적인거래나 사건의 영향을 조정한 종속기업의 가장 최근의 재무제표를 사용하여 종속기업의 재무정보를 연결하며, 어떠한 경우라도 종속기업의 재무제표일과 연결재무제표일의 차이는 3개월을 초과하지 않고 있으며, 보고기간의 길이 그리고 재무제표일의 차이는 매 기간마다 동일하게 적용하고 있습니다.
연결실체는 연결재무제표 작성시 연결실체를 구성하는 기업이 유사한 상황에서 발생한 동일한 거래와 사건에 대하여 연결재무제표에서 채택한 회계정책과 다른 회계정책을 사용한 경우에는 연결실체의 회계정책과 일치하도록 그 재무제표를 적절히 수정하여 연결재무제표를 작성하고 있습니다.
비지배지분은 연결재무상태표에서 자본에 포함하되 지배기업의 소유주지분과는 구분하여 별도로 표시하고 있습니다. 당기순손익과 기타포괄손익의 각 구성요소는 지배기업의 소유주와 비지배지분에 귀속되며, 비지배지분이 부(-)의 잔액이 되더라도 총포괄손익은 지배기업의 소유주와 비지배지분에 귀속되고 있습니다.
종속기업에 대한 지배기업의 소유지분이 변동한 결과로 지배기업이 종속기업에 대한지배력을 상실하지 않는다면, 그것은 자본거래(즉, 소유주로서의 자격을 행사하는 소유주와의 거래)로 회계처리하고 있습니다.
지배기업이 종속기업에 대한 지배력을 상실한 경우 연결재무상태표에서 종전의 종속기업에 대한 자산과 부채를 제거하고, 종전의 종속기업에 대한 잔존 투자는 지배력을상실한 때의 공정가치로 인식하며, 그러한 투자 및 종전의 종속기업과 주고 받을 금액에 대해서는 관련 한국채택국제회계기준에 따라 후속적으로 회계처리하고 있으며,종전의 지배지분에 귀속되는 지배력 상실 관련 손익을 인식하고 있습니다.
(4) 사업결합
연결실체는 사업결합에 대하여 취득법을 적용하여 취득일 현재 영업권과 분리하여 식별가능한 취득 자산, 인수 부채 및 피취득자에 대한 비지배지분을 인식하고 있습니다.
연결실체는 식별가능한 취득 자산과 인수 부채를 취득일의 공정가치로 측정하며 취득관련원가는 원가가 발생하고 용역을 제공받은 기간에 비용으로 회계처리하고 있습니다. 취득일에 피취득자에 대한 비지배지분의 요소가 현재의 지분이며 청산시 보유자에게 기업 순자산의 비례적 몫에 대하여 권리를 부여하고 있는 경우 공정가치 혹은피취득자의 식별가능한 순자산에 대해 인식한 금액 중 현재의 지분상품의 비례적 몫중 하나의 방법으로 측정하고 있으며, 그 밖의 모든 비지배지분 요소는 한국채택국제회계기준에서 측정기준을 달리 요구하는 경우가 아니라면 취득일의 공정가치로 측정하고 있습니다.
일부 자산과 부채는 공정가치가 아닌 다른 한국채택국제회계기준에 따라 인식하고 측정하며 이에 영향을 받는 자산과 부채로는 사업결합으로 인한 취득 자산과 인수 부채에서 발생하는 이연법인세 자산이나 부채(기업회계기준서 제1012호 법인세), 피취득자의 종업원급여약정과 관련된 자산 및 부채(기업회계기준서 제1019호 종업원급여), 피취득자의 주식기준보상거래와 관련된 또는 피취득자의 주식기준보상을 취득자 자신의 주식기준보상으로 대체하는 경우와 관련된 부채 또는 지분상품(기업회계기준서 제1102호 주식기준보상) 및 매각예정자산으로 분류된 취득 비유동자산 또는 처분자산집단(기업회계기준서 제1105호 매각예정비유동자산과 중단영업) 등이 있습니다.
취득자가 피취득자에 대한 교환으로 이전한 대가에는 조건부 대가 약정으로 인한 자산이나 부채를 모두 포함하며 취득일의 공정가치로 인식하고 있습니다. 취득일 이후 측정기간 동안의 조정이 아닌 조건부 대가의 공정가치 변동과 관련하여 자본으로 분류된 조건부 대가는 재측정하지 않으며 그 후속 정산은 자본 내에서 회계처리하고, 그 밖의 조건부 대가의 경우 보고일에 공정가치로 재측정하고, 공정가치 변동은 당기손익으로 인식하고 있습니다.
연결실체는 이전대가, 피취득자에 대한 비지배지분의 금액 및 단계적으로 이루어지는 사업결합의 경우 연결실체가 이전에 보유하고 있던 피취득자에 대한 지분의 취득일의 공정가치의 합계금액이 취득일의 식별가능한 취득 자산과 인수 부채의 순액을 초과하는 경우 그 초과금액을 영업권으로 인식하며, 미달하는 경우 모든 취득 자산과인수 부채를 정확하게 식별하였는지에 대해 재검토하고 염가매수차익을 당기손익으로 인식하고 있습니다.
단계적으로 이루어지는 사업결합에서, 연결실체는 이전에 보유하고 있던 피취득자에대한 지분을 취득일의 공정가치로 재측정하고 그 결과 차손익이 있다면 당기손익 또는 기타포괄손익(적절한 경우)으로 인식하며, 이전의 보고기간에 연결실체가 피취득자에 대한 지분의 가치변동을 기타포괄손익으로 인식한 금액에 대해 연결실체가 이전에 보유하던 지분을 직접 처분한다면 적용하였을 동일한 근거로 인식하고 있습니다.
사업결합에 대한 최초 회계처리가 사업결합이 발생한 보고기간 말까지 완료되지 못한다면, 연결실체는 회계처리가 완료되지 못한 항목의 잠정 금액을 연결재무제표에 보고하고, 측정기간 동안에 취득일 현재 존재하던 사실과 상황에 대하여 새롭게 입수한 정보가 있는 경우 연결실체는 취득일에 이미 알았더라면 취득일에 인식한 금액의 측정에 영향을 주었을 그 정보를 반영하기 위하여 취득일에 인식한 잠정금액을 소급하여 조정하고 있으며, 식별가능한 자산(부채)으로 인식한 잠정 금액의 증가(감소)를 영업권의 감소(증가)로 인식하고 있습니다.
(5) 공동약정
연결실체는 둘 이상의 당사자들이 공동지배력을 보유하는 공동약정에 대하여 약정의구조와 법적 형식, 약정 당사자들에 의해 합의된 계약상 조건 등 권리와 의무를 고려하여, 약정의 공동지배력을 보유하는 당사자들이 약정의 자산에 대한 권리와 부채에 대한 의무를 갖는 공동약정은 공동영업으로, 약정의 공동지배력을 보유하는 당사자들이 약정의 순자산에 대한 권리를 갖는 공동약정은 공동기업으로 분류하고 있습니다.
공동영업에 대해서는 특정 자산, 부채, 수익 및 비용에 적용가능한 관련 IFRS에 따라약정에 대한 자신의 지분과 관련된 자산과 부채를 인식하고 측정(그리고 관련 수익과비용을 인식)하며, 공동기업에 대해서는 기업회계기준서 제1028호 '관계기업과 공동기업에 대한 투자'에 따라 지분법을 사용하여 그 투자자산을 인식하고 회계처리하고 있습니다.
(6) 관계기업과 공동기업에 대한 투자
연결실체는 관계기업이나 공동기업에 대한 투자에 대하여 매각예정으로 분류되는 경우 등을 제외하고는 지분법을 적용하여 회계처리하고 있습니다.
관계기업은 연결실체가 유의적인 영향력을 보유하는 기업으로, 연결실체가 유의적인영향력을 보유하는지를 평가할 때에는, 다른 기업이 보유한 잠재적 의결권을 포함하여 현재 행사할 수 있거나 전환할 수 있는 잠재적 의결권의 존재와 영향을 고려하고 있습니다.
지분법은 관계기업이나 공동기업에 대한 투자를 최초에 원가로 인식하고, 취득시점 이후 발생한 피투자자의 순자산 변동액 중 연결실체의 몫을 해당 투자자산에 가감하여 보고하고 있습니다. 연결실체의 당기순손익에는 피투자자의 당기순손익 중 투자자의 몫에 해당하는 금액을 포함하고 있으며, 연결실체의 기타포괄손익에는 피투자자의 기타포괄손익 중 투자자의 몫에 해당하는 금액을 포함하고 있습니다.
투자자산을 취득한 시점에 투자자산의 원가와 피투자자의 식별가능한 자산과 부채의순공정가치 중 연결실체의 몫에 해당하는 금액과의 차이 중 관계기업이나 공동기업에 관련된 영업권은 해당 투자자산의 장부금액에 포함하고 영업권의 상각은 수행하지 않고 있으며, 피투자자의 식별가능한 자산과 부채의 순공정가치 중 기업의 몫이 투자자산의 원가를 초과하는 부분은 투자자산을 취득한 회계기간의 관계기업이나 공동기업의 당기순손익 중 연결실체의 몫을 결정할 때 수익에 포함하고, 취득한 후 발생하는 관계기업이나 공동기업의 당기순손익 중 연결실체의 몫을 적절히 조정하는 회계처리를 수행하고 있습니다.
연결실체와 그 관계기업이나 공동기업 사이의 '상향'거래나 '하향'거래에서 발생한 손익에 대하여 연결실체는 그 관계기업이나 공동기업에 대한 지분과 무관한 손익까지만 인식하고 있습니다.
지분법을 적용하기 위하여 사용하는 관계기업이나 공동기업 재무제표의 보고기간종료일이 연결실체 재무제표의 보고기간종료일과 다른 경우에는 연결실체 재무제표의 보고기간종료일과 관계기업이나 공동기업 재무제표의 보고기간종료일 사이에 발생한 유의적인 거래나 사건의 영향을 반영하고 있으며, 이 경우 연결실체의 보고기간종료일과 관계기업이나 공동기업의 보고기간종료일 간의 차이는 3개월 이내이며, 보고기간의 길이 그리고 보고기간종료일의 차이는 매 기간마다 동일하게 적용하고 있습니다.
연결실체는 유사한 상황에서 발생한 동일한 거래와 사건에 대하여 동일한 회계정책을 적용하여 재무제표를 작성하고 있습니다. 관계기업이나 공동기업이 유사한 상황에서 발생한 동일한 거래와 사건에 대하여 연결실체의 회계정책과 다른 회계정책을 사용한 경우, 연결실체가 지분법을 적용하기 위하여 관계기업이나 공동기업의 재무제표를 사용할 때 관계기업이나 공동기업의 회계정책을 연결실체의 회계정책과 일관되도록 처리하고 있습니다.
관계기업이나 공동기업의 손실 중 연결실체의 지분이 관계기업이나 공동기업에 대한투자지분과 같거나 초과하는 경우, 연결실체는 해당 투자지분 이상의 손실에 대하여 인식을 중지하고 있습니다. 관계기업이나 공동기업에 대한 투자지분은 지분법을 사용하여 결정되는 관계기업이나 공동기업에 대한 투자자산의 장부금액과 실질적으로 기업의 관계기업이나 공동기업에 대한 순투자의 일부를 구성하는 장기투자지분 항목을 합한 금액이며, 연결실체의 지분이 '영(0)'으로 감소된 이후 추가 손실분에 대하여연결실체는 법적의무 또는 의제의무가 있거나 관계기업이나 공동기업을 대신하여 지급하여야 하는 경우, 그 금액까지만 손실과 부채로 인식하고 있으며, 만약 관계기업이나 공동기업이 추후에 이익을 보고할 경우 연결실체는 자신의 지분에 해당하는 이익의 인식을 재개하되, 인식하지 못한 손실을 초과한 금액만을 이익으로 인식하고 있습니다.
연결실체는 관계기업이나 공동기업에 대한 순투자자산에 대하여 추가적인 손상차손을 인식할 필요가 있는지 결정하기 위하여 기업회계기준서 제1028호 '관계기업과 공동기업에 대한 투자'을 적용하고 있습니다. 관계기업이나 공동기업에 대한 투자 장부금액의 일부를 구성하는 영업권은 분리하여 인식하지 않으므로 별도의 손상검사를 하지 않고 있으며, 그 대신에 투자자산이 손상될 수도 있는 징후가 나타날 때마다 투자자산의 전체 장부금액을 단일 자산으로서 회수가능액(순공정가치와 사용가치 중 큰 금액)과 비교하여 손상검사를 하고 있습니다. 이러한 상황에서 인식된 손상차손은 관계기업이나 공동기업에 대한 투자 장부금액의 일부를 구성하는 어떠한 자산(영업권 포함)에도 배분하지 않고 있으며, 이 손상차손의 모든 환입은 이러한 투자자산의 회수가능액이 후속적으로 증가하는 만큼 인식하고 있습니다.
연결실체는 투자가 관계기업이나 공동기업의 정의를 충족하지 못하게 된 시점부터 지분법의 사용을 중단하고 있습니다. 피투자기업이 종속기업이 되는 경우 그 투자를 기업회계기준서 제1103호 '사업결합'과 제1110호 '연결재무제표'에 따라 회계처리하고 있습니다. 종전 관계기업이나 공동기업에 대한 잔여 보유 지분이 금융자산인 경우, 잔여 보유 지분을 공정가치로 측정하며, 잔여 보유 지분의 공정가치와 관계기업이나 공동기업에 대한 지분의 일부 처분으로 발생한 대가의 공정가치와 지분법을 중단한 시점의 투자자산의 장부금액과의 차이를 당기손익으로 인식하고 있습니다. 지분법의 사용을 중단한 경우, 그 투자와 관련하여 기타포괄손익으로 인식한 모든 금액에 대하여 연결실체는 피투자자가 관련 자산이나 부채를 직접 처분한 경우의 회계처리와 동일한 기준으로 회계처리하고 있습니다.
(7) 외화환산
연결실체는 서로 다른 기능통화를 사용하는 개별기업으로 구성되어 있으며 연결재무제표를 작성하기 위하여 각 개별기업의 경영성과와 재무상태를 지배기업의 기능통화이면서 표시통화인 "원화(KRW)"로 표시하고 있습니다.
1) 외화거래
기능통화로 외화거래를 최초로 인식하는 경우에 거래일의 외화와 기능통화 사이의 현물환율을 외화금액에 적용하여 기록하며, 보고기간말 화폐성 외화항목은 마감환율로 환산하며, 역사적원가로 측정하는 비화폐성 외화항목은 거래일의 환율로 환산하고, 공정가치로 측정하는 비화폐성 외화항목은 공정가치가 결정된 날의 환율로 환산하고 있습니다.
화폐성항목의 결제시점에 생기는 외환차이와 화폐성항목의 환산에 사용한 환율이 회계기간 중 최초로 인식한 시점이나 전기의 재무제표 환산시점의 환율과 다르기 때문에 생기는 외환차이는 그 외환차이가 생기는 회계기간의 손익으로 인식하고 있으며,
일정요건을 충족하는 위험회피회계를 적용하는 외환차이(해외사업장에 대한 순투자의 위험회피 중 위험회피에 효과적인 부분 및 현금흐름위험회피수단의 요건을 갖춘 화폐성항목에 대한 외환차이 중 위험회피에 효과적인 부분 등)는 기타포괄손익으로 보고하고 있습니다.
연결실체가 해외사업장으로부터 수취하거나 해외사업장에 지급할 화폐성항목 중에서 예측할 수 있는 미래에 결제할 계획이 없고 결제될 가능성이 낮은 항목은 실질적으로 그 해외사업장에 대한 순투자의 일부인 화폐성항목에서 생기는 외환차이는 기타포괄손익으로 인식하고 관련 순투자의 처분시점에 자본에서 당기손익으로 재분류하고 있습니다.
비화폐성항목에서 생긴 손익을 기타포괄손익으로 인식하는 경우에 그 손익에 포함된환율변동효과도 기타포괄손익으로 인식하며, 비화폐성항목에서 생긴 손익을 당기손익으로 인식하는 경우에는 그 손익에 포함된 환율변동효과도 당기손익으로 인식하고있습니다.
2) 해외사업장의 환산
서로 다른 기능통화(초인플레이션 경제의 통화가 아님)를 사용하는 개별기업으로 구성되는 연결실체는 연결재무제표를 작성하기 위하여 각 개별기업의 경영성과와 재무상태를 연결실체의 표시통화로 환산하고 있습니다.
해외사업장의 재무상태표의 자산과 부채는 해당 보고기간말의 마감환율로 환산하며,포괄손익계산서의 수익과 비용은 해당기간의 평균환율로 환산하고, 환산에서 생기는 외환차이의 누계액은 해외사업장이 처분될 때까지기타포괄손익으로 인식하고 있습니다. 연결실체가 지분을 전부 소유하고 있지는 않지만 연결실체에 포함되는 해외사업장과 관련된 외환차이 중 비지배지분으로 인해 발생하는 외환차이의 누계액은 연결재무상태표의 비지배지분으로 배분하여 인식하고 있습니다.
해외사업장의 취득으로 생기는 영업권과 자산·부채의 장부금액에 대한 공정가치 조정액은 해외사업장의 기능통화로 표시하고 마감환율로 환산하고 있으며, 해외사업장을 처분하는 경우에는 기타포괄손익과 별도의 자본항목으로 인식한 해외사업장관련 외환차이의 누계액은 해외사업장의 처분손익을 인식하는 시점에 자본에서 당기손익으로 재분류하고 있습니다.
3) 해외사업장의 처분 또는 일부 처분
해외사업장을 처분하는 경우(해외사업장에 대한 연결실체의 전체지분의 처분뿐만 아니라 해외사업장을 포함한 종속기업에 대한 지배력을 상실하는 경우, 해외사업장을 포함한 관계기업에 대한 중대한 영향력을 상실하는 경우 및 해외사업장을 포함한 공동지배기업에 대한 공동지배력을 상실하는 경우를 포함)에는 기타포괄손익과 별도의자본항목으로 인식한 해외사업장관련 외환차이의 누계액은 해외사업장의 처분손익을 인식하는 시점에 자본에서 당기손익으로 재분류하고 있으며, 해외사업장을 포함한 종속기업의 처분시 비지배지분에 귀속되는 그 해외사업장과 관련된 외환차이의누계액은 제거하지만 당기손익으로 재분류하지는 않고 있습니다.
해외사업장을 포함한 종속기업을 일부 처분시 기타포괄손익에 인식된 외환차이의 누계액 중 비례적 지분을 그 해외사업장의 비지배지분으로 재귀속시키고 있으며, 이 외의 경우에는 해외사업장을 일부 처분한 때에 기타포괄손익에 인식된 외환차이의 누계액 중 비례적 지분만을 당기손익으로 재분류하고 있습니다.
(8) 현금및현금성자산
연결실체는 보유현금과 요구불예금, 유동성이 매우 높은 단기 투자자산으로서 확정된 금액의 현금으로 전환이 용이하고 가치변동의 위험이 경미한 자산을 현금 및 현금성자산으로 분류하고 있습니다. 지분상품은 현금성자산에서 제외하고 있으며 다만 상환일이 정해져 있고 취득일로부터 상환일까지의 기간이 단기인 우선주와 같이 실질적인 현금성자산인 경우에는 현금성자산에 포함하고 있으며, 금융회사의 요구에 따라 즉시 상환하여야 하는 당좌차월은 현금및현금성자산의 구성요소에 포함하고 있습니다.
(9) 금융상품
1) 금융자산
금융자산은 금융상품의 계약당사자가 되는 때에만 재무상태표에 인식하고 있으며, 금융자산의 정형화된 매입이나 매도는 매매일 또는 결제일에 인식하고 있습니다. 금융상품의 최초 인식시점에 사업모형과 금융자산의 계약상 현금흐름의 특성에 따라금융자산은 당기손익-공정가치측정금융자산, 기타포괄손익-공정가치측정금융자산,상각후원가측정금융자산으로 분류하고 있습니다.
금융자산은 최초인식시 공정가치로 측정하고 있으며, 당기손익-공정가치금융자산이아닌 경우 당해 금융자산의 취득과 직접 관련되는 거래원가는 최초인식하는 공정가치에 가산하여 측정하고 있습니다.
(가) 당기손익-공정가치측정금융자산
금융자산을 단기매매목적으로 보유하고 있거나, 당기손익-공정가치측정금융자산으로 지정하는 경우와 기타포괄손익-공정가치측정금융자산 또는 상각후원가측정금융자산으로 분류되지 않는 금융자산은 당기손익-공정가치측정금융자산으로 분류합니다.
또한 당기손익-공정가치측정금융자산의 지정이 서로 다른 기준에 따라 자산이나 부채를 측정하거나, 그에 따른 평가손익 등을 인식함으로써 발생할 수 있는 인식과 측정상의 불일치를 제거하거나 상당히 감소시킬 수 있는 경우에는 당기손익-공정가치 측정금융자산으로 지정할 수 있습니다.
당기손익-공정가치측정금융자산은 공정가치로 측정하며 공정가치 변동으로 인한 평가손익은 당기손익으로 인식하고 있습니다. 금융자산으로부터 획득한 배당금과 이자수익도 당기손익으로 인식합니다.
(나) 기타포괄손익-공정가치측정금융자산
채무증권 중 사업모형이 현금흐름 수취 및 매도 사업모형으로 분류되고 계약상 현금흐름이 원금과 이자만으로 구성되어 있는지에 대한 검토를 만족하는 금융자산이나 단기간 내 매도할 목적이 아닌 지분증권 중 기타포괄손익-공정가치측정금융자산으로 지정한 상품은 기타포괄손익-공정가치측정금융자산으로 분류하고 있습니다. 기타포괄손익-공정가치측정금융자산은 최초인식 후에 공정가치로 측정합니다. 공정가치의 변동으로 인하여 발생하는 손익은 유효이자율법에 따른 이자수익, 배당수익 및 손익으로 직접 인식되는 화폐성자산에 대한 외환차이를 제외하고는 자본의 기타포괄손익항목으로 인식하고 있습니다.
기타포괄손익-공정가치측정금융자산을 처분하는 경우 기타포괄손익으로 인식한 누적손익은 해당 기간의 당기손익으로 인식합니다. 다만, 기타포괄손익-공정가치측정 금융자산으로 지정한 지분증권에서 발생한 누적평가손익은 처분시 해당기간의 당기손익으로 인식되지 않습니다.
외화로 표시된 기타포괄손익-공정가치측정금융자산의 공정가치는 해당 외화로 측정되며 보고기간 말 현재 환율로 환산합니다. 공정가치 변동분 중 상각후원가의 변동으로 인한 환산차이에서 발생한 부분은 당기손익으로 인식하며 기타 변동은 자본으로 인식하고 있습니다.
(다) 상각후원가측정금융자산
사업모형이 현금흐름 수취로 분류되고 계약상현금흐름 특성 평가를 만족하는 금융자산은 상각후원가 측정 금융자산으로 분류합니다. 최초 인식 후에는 유효이자율법을 사용한 상각후원가로 측정하며, 이자수익은 유효이자율법을 사용하여 인식합니다.
(라) 금융자산의 제거
금융자산의 현금흐름에 대한 계약상 권리가 소멸하거나, 금융자산의 현금흐름에 대한 권리를 양도하고 금융자산의 소유에 따른 위험과 보상의 대부분을 이전할 때 금융자산을 제거하고 있습니다. 만약, 금융자산의 소유에 따른 위험과 보상의 대부분을 보유하지도 않고 이전하지도 아니한 경우, 연결실체가 금융자산을 통제하고 있지도 않다면 금융자산을 제거하고, 금융자산을 계속 통제하고 있다면 그 양도자산에 대하여 지속적으로 관여하는 정도까지 계속하여 인식하고, 관련 부채를 함께 인식하고 있습니다.
2) 금융자산(채무상품)의 기대신용손실
당기손익-공정가치측정금융자산을 제외한 상각후원가측정금융자산 및 기타포괄손익-공정가치측정채무상품은 매 보고기간 말에 기대신용손실을 평가하고 있습니다. 손실충당금의 측정방식은 신용위험의 유의적인 증가 여부에 따라 결정됩니다. 금융자산의 최초 인식 후 신용위험의 유의적인 증가 여부에 따라 아래 표와 같이 3단계로구분하여 12개월 기대신용손실이나 전체기간 기대신용손실에 해당하는 금액으로 손실충당금을 인식합니다.
|
구 분 |
손실충당금 |
|
|---|---|---|
|
Stage 1 |
최초 인식 후 신용위험이 유의적으로 증가하지 않은 경우(주1) |
12개월 기대신용손실: 보고기간 말 이후 12개월 내에 발생 가능한 금융상품의 채무불이행 사건으로 인한 기대신용손실 |
|
Stage 2 |
최초 인식 후 신용위험이 유의적으로 증가한 경우 |
전체기간 기대신용손실: 기대존속기간에 발생할 수 있는 모든 채무불이행 사건으로 인한 기대신용손실 |
|
Stage 3 |
신용이 손상된 경우 |
|
(주1) 보고기간 말 신용위험이 낮은 경우에는 신용위험이 유의적으로 증가하지 않은 것으로 간주할 수 있음
최초 인식 시점에 신용이 손상된 금융자산에 대하여 최초 인식 후 전체기간 기대신용손실의 누적변동분만을 손실충당금으로 계상합니다.
한편, 매출채권, 계약자산, 리스채권 등에 대해서는 전체기간 기대신용손실에 해당하는 금액으로 손실충당금을 측정하는 간편법을 적용하고 있습니다.
기대신용손실은 일정 범위의 발생 가능한 결과를 확률가중한 값으로, 화폐의 시간가치를 반영하고, 보고기간 말에 과거사건, 현재 상황과 미래 경제적 상황에 대한 예측에 대한 과도한 원가나 노력 없이 이용할 수 있는 정보를 반영해 측정합니다.
3) 금융부채
금융부채는 금융상품의 계약당사자가 되는 때에만 재무상태표에 인식하고 있으며, 금융부채의 최초 인식시 당기손익-공정가치측정금융부채 또는 기타금융부채로 분류하고 공정가치로 측정하고 있습니다. 당기손익-공정가치측정금융부채를 제외하고는해당 금융부채의 발생과 직접 관련되는 거래비용은 최초 측정시 공정가치에 차감하고 있습니다.
(가) 당기손익-공정가치측정부채
당기손익-공정가치측정금융부채는 최초 인식시점에 당기손익-공정가치측정금융부채로 지정한 금융부채를 포함하고 있습니다. 당기손익-공정가치측정금융부채는 최초 인식 후 공정가치로 측정하며, 공정가치의 변동은 당기손익으로 인식하고 있습니다. 한편,최초 인식시점에 발행과 관련하여 발생한 거래비용은 발생 즉시 당기손익으로 인식하고 있습니다.
(나) 당기손익-공정가치측정부채로 분류되지 않는 금융부채
당기손익-공정가치측정부채로 분류되지 않는 금융부채는 다음의 금융부채를 제외하고는 최초인식 후 유효이자율법을 사용하여 상각후원가로 측정하고 있습니다.
금융자산의 양도가 제거 조건을 충족하지 못하거나 지속적관여접근법이 적용되는 경우에 발생하는 금융부채의 경우, 양도자산을 상각후원가로 측정한다면 양도자산과 관련부채의 순장부금액이 양도자가 보유하는 권리와 부담하는 의무의 상각후원가가 되도록 관련부채를 측정하며, 양도자산을 공정가치로 측정한다면 양도자산과 관련부채의 순장부금액이 양도자가 보유하는 권리와 부담하는 의무의 독립적으로 측정된 공정가치가 되도록 관련부채를 측정하고 있습니다.
금융보증부채(금융자산의 양도가 제거 조건을 충족하지 못하거나 지속적관여접근법이 적용되는 경우에 발생하는 금융부채 제외)와 시장이자율보다 낮은 이자율로 대출하기로 한 약정은 기대신용손실모형에 따른 손실충당금과 최초인식금액에서 이익누계액을 차감한 금액 중 큰 금액으로 측정됩니다.
(다) 금융부채의 제거
금융부채(또는 금융부채의 일부)는 소멸한 경우(즉, 계약상 의무가 이행, 취소 또는 만료된 경우)에만 재무상태표에서 제거하고 있습니다. 기존 차입자와 대여자가 실질적으로 다른 조건으로 채무상품을 교환하거나 기존 금융부채(또는 금융부채의 일부)의 조건이 실질적으로 변경된 경우 최초의 금융부채를 제거하고 새로운 금융부채를 인식하고 있으며, 소멸하거나 제3자에게 양도한 금융부채(또는 금융부채의 일부)의 장부금액과 지급한 대가의 차액은 당기손익으로 인식하고 있습니다.
4) 금융자산과 금융부채의 상계
연결실체는 인식한 자산과 부채에 대해 법적으로 집행가능한 상계권리를 현재 보유하고 있으면서 순액으로 결제하거나 자산을 실현하는 동시에 부채를 결제할 의도를 가지고 있는 경우에 금융자산과 금융부채를 상계하고 재무상태표에 순액으로 표시하고 있습니다.
5) 부채와 자본의 분류
채무상품과 지분상품은 계약의 실질 및 금융부채와 지분상품의 정의에 따라 금융부채 또는 자본으로 분류하고 있습니다.
6) 파생상품
파생상품은 최초 인식시 계약일의 공정가치로 측정하고 이후 공정가치로 재측정하고있습니다.
(가) 내재파생상품
① 금융자산이 주계약인 복합계약
내재파생상품을 포함하는 금융자산은 복합계약 전체를 고려하여 분류를 결정하고 내재파생상품을 분리하여 인식하지 않습니다. 계약상 현금흐름이 원금과 이자로만 구성되어 있는지를 판단할 때에도 해당 복합계약 전체를 고려합니다.
② 그 밖의 복합계약(복합계약이 금융자산이 아닌 주계약을 포함하는 경우)
내재파생상품의 경제적 특성 및 위험이 주계약의 경제적 특성 및 위험과 밀접하게 관련되어 있지 않고, 내재파생상품과 동일한 조건을 가진 별도의 금융상품 등이 파생상품의 정의를 충족하며 복합계약의 공정가치 변동이 당기손익으로 인식되지 아니하는 경우 주계약과 분리하여 별도의 파생상품으로 회계처리하고 있습니다.
(나) 위험회피회계
연결실체는 특정위험으로 인해 인식된 자산이나 부채 또는 미인식된 확정계약의 전체 또는 일부의 공정가치 변동에 대한 위험회피의 경우 공정가치위험회피회계를 적용하며특정위험으로 인해 인식된 자산이나 부채 또는 발생가능성이 매우 높은 예상거래의 현금흐름 변동에 대한 위험회피의 경우 현금흐름위험회피회계를 적용하고 있습니다.
위험회피회계를 적용하기 위하여 연결실체는 위험회피관계, 위험관리목적, 위험회피전략,회피대상위험 및 위험회피효과 평가방법 등을 문서화하고 있습니다. 위험회피효과는 회피대상위험으로 인한 파생상품의 공정가치나 현금흐름의 변동이 위험회피대상항목의 공정가치나 현금흐름의 변동위험을 상쇄하는 효과를 의미합니다.
(다) 공정가치위험회피
위험회피수단으로 지정되고, 공정가치위험회피회계의 적용요건을 충족한 파생금융상품의 공정가치 변동은 당기손익으로 인식하고 있으며, 회피대상위험으로 인한 위험회피대상항목의 공정가치 변동도 당기손익으로 인식하고 있습니다. 단, 위험회피대상항목이 지분상품이며, 공정가치의 변동을 기타포괄손익으로 표시하기로 선택한 경우에는 위험회피수단의 손익 및 회피대상위험으로 인한 위험회피대상항목의 손익을 기타포괄손익으로 인식하고 있습니다. 공정가치위험회피회계는 위험회피수단이 소멸, 매각, 행사 또는 종료되거나 공정가치위험회피회계의 적용조건을 더 이상 충족하지 않을 경우 중단됩니다. 회피대상위험으로 인한 위험회피대상항목의 장부금액 조정액은 위험회피회계가 중단된 날부터 상각하여 당기손익으로 인식하고 있습니다.
(라) 현금흐름위험회피
위험회피수단으로 지정되고 현금흐름위험회피회계의 적용요건을 충족한 파생상품의 공정가치 변동분 중 위험회피에 효과적인 부분은 기타포괄손익으로 처리하며, 위험회피에 비효과적인 부분은 당기손익으로 인식하고 있습니다. 현금흐름위험회피회계는 위험회피수단이 소멸, 매각, 행사 또는 종료되거나, 현금흐름위험회피회계의 적용요건을 더 이상 충족하지 않을 경우 중단됩니다. 현금흐름위험회피회계를 중단하는 경우에 위험회피대상의 미래 현금흐름이 여전히 발생할 것으로 예상되는 경우에 현금흐름위험회피적립금 누계액은 미래 현금흐름이 생길 때까지 또는 현금흐름위험회피적립금이 차손이며 그 차손의 전부나 일부가 미래기간에 회복되지 않을 것으로 예상될 때까지 현금흐름위험회피적립금에 남겨두고 있습니다. 다만, 위험회피대상의 미래현금흐름이 더 이상 발생할 것으로 예상되지 않는 경우에는 현금흐름위험회피적립금 누계액은 즉시 당기손익으로 인식합니다.
(마) 해외사업장순투자의 위험회피
해외사업장에 대한 순투자 위험회피의 경우, 위험회피에 효과적인 부분은 기타포괄손익으로 인식하며, 위험회피에 비효과적인 부분은 당기손익으로 인식하고 있습니다. 위험회피에 효과적이어서 기타포괄손익으로 인식한 부분은 향후 그 해외사업장을 처분하거나 그 해외사업장의 일부를 처분하는 시점에 기업회계기준서 제1021호 '환율변동효과'에 따라 재분류조정으로 기타포괄손익에서 당기손익으로 재분류합니다.
(10) 재고자산
재고자산의 취득원가는 매입원가, 전환원가 및 재고자산을 현재의 장소에 현재의 상태로 이르게 하는 데 발생한 기타 원가 모두를 포함하고 있으며, 재고자산의 단위원가는 선입선출법(미착품은 개별법)을 사용하여 결정하고 있습니다.
재고자산은 취득원가와 순실현가능가치 중 낮은 금액으로 측정하고 있습니다. 순실현가능가치는 통상적인 영업과정의 예상 판매가격에서 예상되는 추가 완성원가와 판매비용을 차감한 금액으로서 매 후속기간에 순실현가능가치를 재평가하고 있습니다.
재고자산의 판매시 관련된 수익을 인식하는 기간에 재고자산의 장부금액을 비용으로인식하고 있으며 재고자산을 순실현가능가치로 감액한 평가손실과 모든 감모손실은 감액이나 감모가 발생한 기간에 비용으로 인식하며, 순실현가능가치의 상승으로 인한 재고자산 평가손실의 환입은 환입이 발생한 기간의 비용으로 인식된 재고자산 금액의 차감액으로 인식하고 있습니다.
(11) 투자부동산
투자부동산은 임대수익이나 시세차익 또는 두 가지 모두를 얻기 위하여 연결실체가 보유하고 있는 부동산으로서 최초 인식시점에 원가로 측정하고 거래원가는 최초 측정에 포함하고 있습니다. 최초 인식 이후 투자부동산은 취득원가에서 감가상각누계액과 손상차손누계액을 차감한 금액을 장부금액으로 표시하고 있습니다.
후속원가는 자산으로부터 발생하는 미래경제적효익이 유입될 가능성이 높으며, 자산의 원가를 신뢰성 있게 측정할 수 있는 경우 자산의 장부금액에 포함하거나 적절한 경우 별도의 자산으로 인식하고 있으며, 일상적인 수선ㆍ유지와 관련하여 발생하는 원가는 발생시점에 당기손익으로 인식하고 있습니다.
투자부동산 중 토지에 대해서는 감가상각을 하지 않으며, 토지를 제외한 투자부동산은 경제적 내용연수에 따라 40년을 적용하여 정액법으로 상각하고 있습니다. 투자부동산의 감가상각방법, 잔존가치 및 내용연수는 매 보고기간말에 재검토하고 있으며, 이를 변경하는 것이 적절하다고 판단되는 경우 회계추정의 변경으로 회계처리하고 있습니다.
부동산의 용도가 변경되는 경우에만 투자부동산의 대체가 발생하고 있으며 투자부동산, 자가사용부동산, 재고자산 사이에 대체가 발생할 때에 대체 전 자산의 장부금액을 승계하고 있습니다.
투자부동산을 처분하거나, 투자부동산의 사용을 영구히 중지하고 처분으로도 더 이상의 경제적효익을 기대할 수 없는 경우에는 연결재무상태표에서 제거하고 있으며, 투자부동산의 폐기나 처분으로 발생하는 손익은 순처분금액과 장부금액의 차액이며 폐기나 처분이 발생한 기간에 당기손익으로 인식(판매후리스계약은 기업회계기준서 제1116호를 적용하여 처분손익으로 인식)하고 있습니다.
(12) 유형자산
유형자산은 최초 인식시점에 원가로 측정하고 최초 인식 이후 취득원가에서 감가상각누계액과 손상차손누계액을 차감한 금액을 장부금액으로 표시하고 있습니다. 유형자산의 원가는 관세 및 환급불가능한 취득 관련 세금을 가산하고 매입할인과 리베이트 등을 차감한 구입가격, 경영진이 의도하는 방식으로 자산을 가동하는 데 필요한 장소와 상태에 이르게 하는 데 직접 관련되는 원가와 자산을 해체, 제거하거나 부지를 복구하는 데 소요될 것으로 최초에 추정되는 원가로 구성되고 있습니다.
후속원가는 자산으로부터 발생하는 미래경제적효익이 유입될 가능성이 높으며, 자산의 원가를 신뢰성 있게 측정할 수 있는 경우 자산의 장부금액에 포함하거나 적절한 경우 별도의 자산으로 인식하고 있으며, 일상적인 수선ㆍ유지와 관련하여 발생하는 원가는 발생시점에 당기손익으로 인식하고 있습니다.
유형자산 중 토지에 대해서는 감가상각을 하지 않으며, 토지를 제외한 유형자산은 아래의 내용연수와 감가상각방법을 적용하여 감가상각하고 있습니다.
| 과 목 | 추정 내용연수 | 감가상각방법 |
|---|---|---|
| 건 물 | 40년 | 정액법 |
| 구 축 물 | 20년 | 정액법 |
| 기 계 장 치 | 5~10년 | 정액법 |
| 차량운반구 | 5년 | 정액법 |
| 공구와기구 | 5년, 8년 | 정액법 |
| 집 기 비 품 | 3~ 5년 | 정액법 |
| 시 설 장 치 | 5년, 10년 | 정액법 |
| 사용권자산 | 임차기간 | 정액법 |
| 임차자산개량권 | 임차기간 | 정액법 |
유형자산을 구성하는 일부의 원가가 당해 유형자산의 전체원가에 비교하여 유의적이라면 해당 유형자산을 감가상각할 때 그 부분은 별도로 구분하여 감가상각하고 있습니다.
유형자산의 감가상각방법, 잔존가치 및 내용연수는 매 보고기간말에 재검토하고 있으며, 이를 변경하는 것이 적절하다고 판단되는 경우 회계추정의 변경으로 회계처리하고 있습니다.
유형자산의 장부금액은 처분하는 때, 사용이나 처분을 통하여 미래경제적효익이 기대되지 않을 때 제거하고 있으며 제거로 인하여 발생하는 손익은 자산을 제거할 때 당기손익으로 인식하고 있습니다.
(13) 무형자산
연결실체는 자산에서 발생하는 미래경제적효익이 기업에 유입될 가능성이 높고 자산의 원가를 신뢰성 있게 측정할 수 있는 경우에 무형자산으로 인식하고 있으며, 최초 인식 후에 무형자산은 원가에서 상각누계액과 손상차손누계액을 차감한 금액을 장부금액으로 하고 있습니다.
1) 개별취득
개별 취득하는 무형자산의 원가는 구입가격(매입할인과 리베이트를 차감하고 수입관세와 환급받을 수 없는 제세금을 포함)과 자산을 의도한 목적에 사용할 수 있도록 준비하는 데 직접 관련되는 원가로 구성되고 있습니다.
2) 영업권
사업결합과 관련하여 이전대가, 피취득자에 대한 비지배지분의 금액 및 단계적으로 이루어지는 사업결합의 경우 연결실체가 이전에 보유하고 있던 피취득자에 대한 지분의 취득일의 공정가치의 합계금액이 취득일의 식별가능한 취득 자산과 인수 부채의 순액을 초과하는 경우 그 초과금액을 영업권으로 인식하고 있습니다.
3) 사업결합으로 인한 취득
사업결합으로 취득하는 영업권과 분리하여 인식하는 무형자산의 취득원가는 취득일의 공정가치로 측정하고 있습니다.
동일지배하 사업결합의 경우 연결실체의 연결재무제표를 구성하는 피합병법인의 자산 및 부채를 승계하여 장부금액으로 인식하고 있습니다.
4) 내부적으로 창출한 무형자산
연구(또는 내부 프로젝트의 연구단계)에서 발생한 지출은 발생시점에 비용으로 인식하고 있으며, 무형자산을 사용하거나 판매하기 위해 그 자산을 완성할 수 있는 기술적 실현가능성,무형자산을 완성하여 사용하거나 판매하려는 기업의 의도, 무형자산을 사용하거나 판매할 수 있는 기업의 능력, 무형자산이 미래경제적효익을 창출하는 방법, 무형자산의 개발을 완료하고 그것을 판매하거나 사용하는 데 필요한 기술적, 재정적 자원 등의 입수가능성, 개발과정에서 발생한 무형자산 관련 지출을 신뢰성 있게 측정할 수 있는 기업의 능력을 모두 제시할 수 있는 경우에만 개발활동(또는 내부 프로젝트의 개발단계)에서 발생한 무형자산을 인식하고 있습니다. 내부적으로 창출한 무형자산의 원가는 무형자산의 인식기준을 최초로 충족시킨 이후에 발생한 지출금액의 합으로 하며 그 자산의 창출, 제조 및 경영자가 의도하는 방식으로 운영될 수 있게 준비하는 데 필요한 직접 관련된 모든 원가를 포함하고 있습니다. 내부적으로 창출한 영업권은 자산으로 인식하지 아니하고 있습니다.
5) 내용연수 및 상각
내용연수가 유한한 무형자산의 경우 상각대상금액은 자산이 사용가능한 때부터 내용연수동안 정액법으로 배분하고 있습니다. 상각대상금액은 잔존가치를 차감하여 결정하고 있으며, 잔존가치는 내용연수 종료 시점에 제 3자가 자산을 구입하기로 한 약정이 있거나, 무형자산의 활성시장이 있어 잔존가치를 그 활성시장에 기초하여 결정할 수 있고 그러한 활성시장이 내용연수 종료 시점에 존재할 가능성이 높은 경우를 제외하고는 영(0)으로 하고 있습니다. 내용연수가 유한한 무형자산의 상각기간과 상각방법은 매 보고기간말에 재검토하고 있으며 이를 변경하는 것이 적절하다고 판단되는 경우 회계추정의 변경으로 회계처리하고 있습니다.
내용연수가 비한정인 무형자산은 상각하지 아니하며, 매 보고기간말 혹은 손상을 시사하는 징후가 있을 때 회수가능액과 장부금액을 비교하여 손상검사를 수행하고 있습니다. 무형자산의 내용연수가 비한정이라는 평가를 계속하여 정당화하는지를 매 보고기간말에 재검토하여 적절하지 않은 경우 회계추정의 변경으로 처리하고 있습니다.
무형자산은 아래의 내용연수와 상각방법을 적용하고 있습니다.
| 구 분 | 내 용 연 수 | 상각방법 |
|---|---|---|
| 특허권 | 3년 | 정액법 |
| 소프트웨어 | 5년 | 정액법 |
| 고객관계 | 7, 8년 | 정액법 |
| 상표권 | 10년 | 정액법 |
| 의장권 | 10년 | 정액법 |
| 회원권 | 비한정 내용연수 | - |
| 영업권 | 비한정 내용연수 | - |
| 기타의무형자산 | 10년 | - |
6) 무형자산의 제거
무형자산은 처분하는 때, 사용이나 처분으로부터 미래경제적효익이 기대되지 않을 때 연결재무상태표에서 제거하며 무형자산의 제거로 인하여 발생하는 이익이나 손실은 순매각가액과 장부금액의 차이로 결정하고 자산을 제거할 때 당기손익으로 인식하고 있습니다.
(14) 차입원가
연결실체는 의도된 용도로 사용하거나 판매가능한 상태에 이르게 하는 데 상당한 기간을 필요로 하는 적격자산의 취득, 건설 또는 생산과 직접 관련된 차입원가는 당해 자산 원가의 일부로 자본화하고 있으며 기타 차입원가는 발생기간에 비용으로 인식하고 있습니다.
적격자산을 취득하기 위한 목적으로 특정하여 차입한 자금에 한하여 회계기간동안 그 차입금으로부터 실제 발생한 차입원가에서 당해 차입금의 일시적 운용에서 생긴 투자수익을 차감한 금액을 자본화가능차입원가로 결정하고 있습니다. 일반적인 목적으로 자금을 차입하고 이를 적격자산의 취득을 위해 사용하는 경우에 한하여 당해 자산관련 지출액에 자본화이자율을 적용하는 방식으로 자본화가능차입원가를 결정하고 있으며, 자본화이자율은 회계기간에 존재하는 기업의 차입금(적격자산을 취득하기 위해 특정 목적으로 차입한 자금 제외)에서 발생된 차입원가를 가중평균하여 산정하며 회계기간동안 자본화한 차입원가는 당해 기간동안 실제 발생한 차입원가를 초과할 수 없습니다.
(15) 정부보조금
연결실체는 정부보조금에 부수되는 조건의 준수와 보조금 수취에 대한 합리적인 확신이 있을 경우에만 정부보조금을 인식하고 있으며 시장이자율보다 낮은 이자율의 정부대여금의 효익은 정부보조금으로 처리하고 있습니다.
수익관련정부보조금은 정부보조금으로 보전하려 하는 관련원가와 대응시키기 위해 필요한 기간에 걸쳐 체계적인 기준에 따라 정부보조금을 수익으로 인식하며, 자산관련정부보조금은 자산의 장부금액을 결정할 때 차감하여 표시하고 감가상각자산의 내용연수에 걸쳐 감가상각비를 감소시키는 방식으로 당기손익으로 인식하고 있습니다.
이미 발생한 비용이나 손실에 대한 보전 또는 향후의 관련원가 없이 연결실체에 제공되는 즉각적인 금융지원으로 수취하는 정부보조금은 정부보조금을 수취할 권리가 발생하는 기간에 수익으로 인식하며, 비화폐성자산을 정부보조금으로 수취하는 경우 비화폐성자산의 공정가치를 평가하여 보조금과 자산 모두를 그 공정가치로 회계처리하고 있습니다.
상환의무가 발생하게 된 정부보조금은 회계추정의 변경으로 회계처리하고 있습니다.
(16) 리스
리스는 리스제공자가 대가와 교환하여 식별되는 자산의 사용 통제권을 일정기간 동안 리스이용자에게 이전하는 계약입니다. 연결실체는 계약의 약정시점에, 계약 자체가 리스인지, 계약이 리스를 포함하는지를 판단합니다.
리스이용자 및 리스제공자는 리스계약이나 리스를 포함하는 계약에서 계약의 각 리스요소를 리스가 아닌 요소(이하'비리스요소'라고 함)와 분리하여 리스로 회계처리합니다. 다만, 연결실체는 리스이용자로서의 회계처리에서 실무적 간편법을 적용하여 비리스요소를 리스요소와 분리하지 않고 각 리스요소와 관련 비리스요소를 하나의 리스요소로 회계처리합니다.
연결실체는 리스개시일에 기초자산을 사용할 권리를 나타내는 사용권자산과 리스료를 지급할 의무를 나타내는 리스부채를 인식합니다. 다만 연결실체는 단기리스와 소액기초자산리스에 대하여 리스이용자의 인식, 측정 및 표시 규정을 적용하지 않는 예외규정을 선택하였습니다.
사용권자산은 리스개시일에 원가로 측정하고, 후속적으로 원가에서 감가상각누계액과 손상차손누계액을 차감하고, 리스부채의 재측정에 따른 조정을 반영하여 측정합니다. 또한 사용권자산은 리스개시일부터 사용권자산의 내용연수 종료일과 리스기간종료일 중 이른 날까지 감가상각합니다. 사용권자산은 재무상태표에 '유형자산'으로 분류합니다.
리스부채는 리스개시일 현재 지급되지 않은 리스료의 현재가치로 측정됩니다. 리스의 내재이자율을 쉽게 산정할 수 있는 경우에는 그 이자율로 리스료를 할인하며 그 이자율을 쉽게 산정할 수 없는 경우에는 리스이용자의 증분차입이자율을 사용합니다. 리스부채는 후속적으로 리스부채에 대한 이자비용만큼 증가하고, 지급한 리스료를 반영하여 감소합니다.
잔존가치보증에 따라 지급할 것으로 예상되는 금액의 변동,지수나 요율(이율)의 변동, 리스기간의 변경, 매수선택권이나 연장선택권의 행사여부평가의 변동에 따라 미래 리스료가 변경되는 경우에 리스부채를 재측정합니다. 리스부채는 재무상태표에 '기타유동금융부채' 또는 '기타비유동금융부채'로 분류합니다.
단기리스(리스개시일에 리스기간이 12개월 이하인 리스)와 소액자산리스의 경우 예외 규정을 선택하여 리스료를 리스기간에 걸쳐 정액기준으로 비용을 인식합니다.
연결실체는 리스약정일에 리스자산의 소유에 따른 위험과 보상의 대부분을 이전하는리스는 금융리스로 분류하고, 금융리스 이외의 모든 리스는 운용리스로 분류합니다.
1) 금융리스
리스제공자는 금융리스의 리스순투자와 동일한 금액을 금융리스채권으로 인식하고 있으며, 금융리스에서 이자수익은 리스제공자의 금융리스 순투자 금액에 대하여 일정한 기간이자율이 산출되는 방식을 적용하여 인식하고 있습니다. 금융리스에서 제조자나 판매자인 리스제공자는 일반판매에 대하여 채택하고 있는 회계정책에 따라 매출손익을 인식하고 있으며, 만약 인위적으로 낮은 이자율이 적용되었다면 시장이자율을 적용하였을 경우의 금액을 한도로 매출이익을 인식하고 있습니다. 제조자나 판매자인 리스제공자로서 부담하는 금융리스 체결원가는 리스개시일에 비용으로 인식하고 있습니다.
2) 운용리스
운용리스에서 리스료수익은 리스자산의 사용으로 생기는 효익이 감소되는 형태를 더잘 나타내는 다른 체계적인 인식기준이 없다면 리스기간에 걸쳐 정액기준으로 인식하고 있습니다. 운용리스의 체결 과정에서 발생한 리스개설직접원가는 운용리스자산의 장부금액에 더하고 리스료 수익과 같은 기준으로 리스기간에 걸쳐 비용으로 인식하며 운용리스자산의 감가상각은 리스제공자가 소유한 비슷한 자산의 보통 감가상각정책과 일치하게 회계처리하고 있습니다.
자산 이전이 판매요건을 충족하는 경우 계속 보유하는 사용권에 관련되는 자산의 종전 장부금액에 비례하여 판매후리스에서 생기는 사용권자산을 측정합니다. 이에 따라 구매자-리스제공자에게 이전한 권리에 관련되는 차손익 금액만을 인식합니다.
자산 판매대가가 그 자산의 공정가치와 다른 경우에는 그 차이를 리스료의 선급이나 구매자가 제공한 추가 금융으로 회계처리합니다.
(17) 충당부채
충당부채는 과거사건의 결과로 현재의무가 존재하고, 당해 의무를 이행하기 위하여 경제적효익을 갖는 자원이 유출될 가능성이 높으며 당해 의무의 이행에 소요되는 금액을 신뢰성 있게 추정할 수 있는 경우에 인식하고 있습니다.
충당부채로 인식하는 금액은 현재의무를 보고기간말에 이행하기 위하여 소요되는 지출에 대한 최선의 추정치로서 최선의 추정치를 구할 때에는 관련된 사건과 상황에 대한 불가피한 위험과 불확실성을 고려하고 있습니다. 화폐의 시간가치 효과가 중요한 경우 충당부채는 의무를 이행하기 위하여 예상되는 지출액의 현재가치로 평가하고 있으며 할인율은 부채의 고유한 위험과 화폐의 시간가치에 대한 현행 시장의 평가를 반영한 세전 이율이며 이 할인율에 반영되는 위험에는 미래 현금흐름을 추정할 때 고려된 위험은 반영하지 아니하고 있습니다. 현재의무를 이행하기 위하여 소요되는 지출 금액에 영향을 미치는 미래사건이 발생할 것이라는 충분하고 객관적인 증거가 있는 경우에는 그러한 미래사건을 감안하여 충당부채 금액을 추정하고 있으며, 자산의 예상처분이익은 충당부채를 측정하는 데 고려하지 아니하고 있습니다.
충당부채를 결제하기 위하여 필요한 지출액의 일부 또는 전부를 제 3자가 변제할 것이 예상되는 경우 연결실체가 의무를 이행한다면 변제를 받을 것이 거의 확실하게 되는 때에 한하여 변제금액을 인식하고 별도의 자산으로 회계처리하고 있으며 자산으로 인식하는 금액은 관련 충당부채 금액을 초과할 수 없습니다.
매 보고기간말마다 충당부채의 잔액을 검토하고, 보고기간말 현재 최선의 추정치를 반영하여 조정하며 의무이행을 위하여 경제적효익을 갖는 자원이 유출될 가능성이 더 이상 높지 아니한 경우에는 관련 충당부채를 환입하고 있습니다. 충당부채는 최초인식과 관련있는 지출에만 사용하고 있습니다.
(18) 전환사채
연결실체가 발행한 전환사채는 계약의 실질에 따라 금융부채와 자본으로 각각 분류하고 있습니다. 최초인식시점에서 금융부채의 공정가치는 계약상 정해진 미래현금흐름을 당해 금융상품과 동일한 조건 및 유사한 신용상태를 가지며 실질적으로 동일한 현금흐름을 제공하지만 전환권이 없는 채무상품에 적용되는 그 시점의 시장이자율로할인한 현재가치로 추정하고 전환권의 행사로 인하여 소멸되거나 만기까지 유효이자율법을 적용한 상각후원가로 측정하며, 자본요소인 전환권의 장부금액은 전환사채 전체의 공정가치에서 금융부채의 공정가치를 차감하여 법인세효과를 반영한 금액으로 결정하고 이후 재측정하지 않고 있습니다. 전환사채의 발행과 관련된 거래원가는 배분된 발행금액에 비례하여 금융부채와 자본에 배분하고 있습니다.
(19) 자기주식
연결실체가 자기지분상품을 재취득하는 경우 이러한 지분상품은 자본에서 자기주식의 과목으로 하여 차감하고 있습니다. 자기지분상품을 매입 또는 매도하거나 발행 또는 소각하는 경우의 손익은 당기손익으로 인식하지 아니하며, 지배기업 혹은 연결실체 내의 다른 기업이 이러한 자기주식을 취득하여 보유하는 경우 지급하거나 수취한 대가는 자본에서 직접 인식하고 있습니다.
(20) 주식기준보상
주식기준보상거래에서 제공받는 재화나 용역은 그 재화나 용역을 제공받는 날에 인식하고 있습니다. 주식결제형 주식기준보상거래로 재화나 용역을 제공받는 경우에는그에 상응한 자본의 증가를 인식하고, 현금결제형 주식기준보상거래로 재화나 용역을 제공받는 경우에는 그에 상응한 부채의 증가를 인식하고 있으며, 주식기준보상거래에서 제공받는 재화나 용역이 자산의 인식요건을 충족하지 못하는 경우에는 비용으로 인식하고 있습니다.
1) 주식결제형 주식기준보상거래
연결실체가 재화나 용역을 제공받는 대가로 자신의 지분상품(주식 또는 주식선택권 등)을 부여하는 주식기준보상거래 혹은 재화나 용역을 제공받지만 이를 제공한 자에게 주식기준보상거래를 결제할 의무가 없는 주식기준보상거래에 대하여, 제공받는 재화나 용역과 그에 상응하는 자본의 증가를 제공받는 재화나 용역의 공정가치로 직접 측정하며, 제공받는 재화나 용역의 공정가치를 신뢰성 있게 추정할 수 없다면 제공받는 재화나 용역과 그에 상응하는 자본의 증가는 부여한 지분상품의 공정가치에 기초하여 간접 측정하고 있습니다. 특정기간의 용역을 제공하여야 부여된 지분상품이 가득되는 경우 지분상품의 대가에 해당하는 용역을 미래 가득기간에 제공받는 것으로 보아 당해 용역은 가득기간에 배분하여 인식하며 그에 상응하여 자본의 증가를 인식하고 있습니다.
시장조건이 아닌 가득조건은 거래금액 측정시 포함되는 지분상품의 수량을 조정할 때 고려하여 부여한 지분상품의 대가로 제공받는 재화나 용역에 대해 인식하는 금액이 궁극적으로 가득되는 지분상품의 수량에 기초하여 결정될 수 있도록 하고 있으며 후속적인 정보에 비추어 볼 때 미래에 가득될 것으로 예상되는 지분상품의 수량이 직전 추정치와 다르다면 당해 추정치를 변경하여 가득일에는 궁극적으로 가득된 지분상품의 수량과 일치하도록 당해 추정치를 변경하고 있습니다. 목표주가와 같은 시장조건은 부여한 지분상품의 공정가치를 추정할 때 고려하고 있습니다.
지정된 가득조건(시장조건 제외)이 충족되지 않아 지분상품이 가득되지 못하는 경우를 제외하고는 지분상품을 부여한 당시의 조건을 변경하는지, 부여한 지분상품을 취소하거나 중도청산하는지 여부와 관계없이 제공받는 근무용역은 최소한 지분상품의 부여일당시의 공정가치에 따라 인식하고 있으며 주식기준보상약정의 총공정가치를 증가시키거나 종업원에게 유리하게 조건을 변경하는 경우에는 추가로 조건변경의 효과를 인식하고 있습니다.
부여한 지분상품이 가득기간 중에 취소되거나 중도청산되는 경우에는 취소나 중도청산으로 인해 부여한 지분상품이 일찍 가득된 것으로 보아 취소나 중도청산이 없다면 잔여가득기간에 제공받을 용역에 대해 인식될 금액을 즉시 인식하며, 취소나 중도청산시 종업원 등에게 지급하는 금액은 자기지분상품의 재매입으로 보아 자본에서 차감하고 있습니다.
2) 현금결제형 주식기준보상거래
연결실체가 재화나 용역을 제공받는 대가로 지배기업 또는 연결실체 내 다른 기업의 지분상품(주식 또는 주식선택권 등)의 가격(또는 가치)에 기초한 금액만큼 현금이나 그 밖의 자산을 지급해야 하는 부채를 재화나 용역의 공급자에게 부담하는 주식기준보상거래에 대하여 제공받는 재화나 용역과 그 대가로 부담하는 부채를 부채의 공정가치로 측정하고 부채가 결제될 때까지 매 보고기간말과 결제일에 부채의 공정가치를 재측정하고 공정가치의 변동액은 당기손익으로 인식하고 있으며, 종업원에게서 제공받는 근무용역과 그 대가로 부담하는 부채는 근무용역을 제공받는 기간에 인식하고 있습니다.
(21) 수익
연결실체는 고객에게 약속한 재화나 용역, 즉 자산을 이전하여 수행의무를 이행할 때(또는, 기간에 걸쳐 이행하는대로) 수익을 인식하고 있습니다.
1) 재화의 판매
연결실체는 고객에게 구명정, 유리섬유파이프 및 의약외품(알콜스왑, 검체채취용 도구 등) 판매와 관련하여 고객에게 이전되어 고객이 인수할 때 수익을 인식합니다.
2) 로열티
연결실체는 판매량 또는 사용량에 따른 로열티는 라이선스 부여 후 후속적인 판매 또는 생산활동이 발생한 시점에 수익을 인식합니다.
연결실체는 구명정, 유리섬유파이프 및 의약외품 등을 제조 및 생산하여 고객에게 제공하는 사업을 영위하고 있으며, 연결실체의 대부분의 수익은 이와 관련되어 있습니다.
연결실체가 거래 당사자가 아니라 공급자의 대리인의 역할을 수행하는 경우 고객에게 청구한 금액에서 재화나 용역의 실질적인 공급자에게 지급해야 할 금액을 차감한 순액을 수수료 수익으로 인식하고 있습니다.
(22) 종업원급여
1) 단기종업원급여
단기종업원급여는 임금, 사회보장분담금, 종업원이 관련 근무용역을 제공하는 회계기간의 말부터 12개월 이내에 결제될 유급연차휴가 또는 유급병가 등과 같은 단기유급휴가, 종업원이 관련 근무용역을 제공하는 회계기간의 말부터 12개월 이내에 지급될 이익분배금과 상여금 및 현직종업원을 위한 비화폐성급여를 포함하고 있습니다. 종업원이 회계기간에 근무용역을 제공한 때 근무용역과 교환하여 지급이 예상되는 단기종업원급여의 할인되지 않은 금액을 이미 지급한 금액을 차감한 후 미지급비용으로 인식하며, 이미 지급한 금액이 해당 급여의 할인되지 않은 금액보다 많은 경우에는 그 초과액 때문에 미래 지급액이 감소하거나 현금이 환급되는 만큼을 선급비용으로 인식하며, 다른 한국채택국제회계기준서에 따라 해당 급여를 자산의 원가에 포함하는 경우를 제외하고는 비용으로 인식하고 있습니다.
2) 퇴직급여
(가) 확정기여제도
확정기여제도는 연결실체가 별개의 실체(기금)에 고정 기여금을 납부하고 연결실체의 법적의무나 의제의무는 기금에 출연하기로 약정한 금액으로 한정되며 종업원이 받을 퇴직급여액은 연결실체와 종업원이 퇴직급여제도나 보험회사에 출연하는 기여금과 그 기여금에서 발생하는 투자수익에 따라 결정되는 퇴직급여제도입니다. 일정기간 종업원이 근무용역을 제공하였을 때 그 근무용역과 교환하여 확정기여제도에 납부해야 할 기여금은 이미 납부한 기여금을 차감한 후 미지급비용으로 인식하고, 이미 납부한 기여금이 보고기간말 이전에 제공된 근무용역에 대해 납부하여야 하는 기여금을 초과하는 경우에는 초과 기여금 때문에 미래 지급액이 감소하거나 현금이 환급되는 만큼을 선급비용으로 인식하며, 다른 한국채택국제회계기준서에 따라 해당 기여금을 자산의 원가에 포함하는 경우를 제외하고는 비용으로 인식하고 있습니다.
(나) 확정급여제도
확정급여제도는 확정기여제도 이외의 모든 퇴직급여제도로서 순확정급여부채로 인식하는 금액은 보고기간말 현재 확정급여채무의 현재가치에서 관련 확정급여채무를 직접 결제하는 데 사용할 수 있는 사외적립자산의 보고기간말 현재 공정가치를 차감한 금액이며, 확정급여채무는 매년 독립적인 보험계리법인에 의해 예측단위적립방식에 따라 산정하고 있습니다.
확정급여채무의 현재가치는 급여가 지급될 통화로 표시되고 관련 확정급여부채의 지급시점과 만기가 유사한 우량회사채의 시장수익률로 기대미래현금유출액을 할인하여 산정하고 있습니다.
확정급여원가 중 근무원가와 순확정급여부채(자산)의 순이자는 당기손익으로 인식하며, 순확정급여부채(자산)의 재측정요소는 기타포괄손익으로 인식하고 있습니다. 한편, 기타포괄손익에 인식되는 순확정급여부채(자산)의 재측정요소는 후속기간에 당기손익으로 재분류하지 아니하고 있습니다.
부의 순확정급여부채인 순확정급여자산은 제도로부터 환급받거나 제도에 대한 미래기여금이 절감되는 방식으로 이용가능한 경제적효익의 현재가치의 합계를 한도로 인식하고 있습니다.
연결실체가 급여를 과거근무용역에 귀속시키는 확정급여제도를 새로 도입하거나 기존의 확정급여제도에서 과거근무용역에 대하여 지급해야 하는 급여를 변경하는 경우 발생하는 과거근무원가는 제도개정으로 인하여 발생하는 부채의 변동금액으로 측정하고 즉시 비용으로 인식하고 있습니다.
3) 기타장기종업원급여
기타장기종업원급여는 종업원이 관련 근무용역을 제공한 회계기간의 말부터 12개월이 지난 후에 결제될 것으로 예상되는 장기유급휴가, 그 밖의 장기근속급여, 장기장애급여, 이익분배금과 상여금, 이연보상을 포함하고 있습니다. 기타장기종업원급여와 관련하여 부채로 인식할 금액은 보고기간말 현재 확정급여채무의 현재가치에서 관련 확정급여채무를 직접 결제하는 데 사용할 수 있는 사외적립자산의 보고기간말 현재 공정가치를 차감하여 인식하고 있습니다.
4) 해고급여
해고급여에 대한 부채와 비용은 연결실체가 해고급여의 제안을 더 이상 철회할 수 없을 때와 기업회계기준서 제1037호 '충당부채, 우발부채, 우발자산'의 적용범위에 포함되고 해고급여의 지급을 수반하는 구조조정에 대한 원가를 인식할 때 중 이른 날에 인식합니다.
(23) 자산손상
재고자산, 기업회계기준서 제1115호 '고객과의 계약에서 생기는 수익'에 따라 인식하는 계약자산과 계약을 체결하거나 이행하기 위해 든 원가에서 생기는 자산, 이연법인세자산, 종업원급여에서 생기는 자산,금융자산, 공정가치로 측정되는 투자부동산, 매각예정비유동자산 등을 제외한 모든 자산의 손상은 아래의 방법으로 손상차손을 인식하고 있습니다.
내용연수가 비한정인 무형자산, 아직 사용할 수 없는 무형자산 및 사업결합으로 취득한 영업권에 대해서는 자산손상을 시사하는 징후가 있는지에 관계없이 매년 회수가능액을 추정하고 장부금액과 비교하여 손상검사를 하고 있으며, 그 외의 자산은 매 보고기간말마다 자산손상을 시사하는 징후가 있는지를 검토하고 그러한 징후가 있다면 개별 자산별로 회수가능액을 추정하며 개별 자산의 회수가능액을 추정할 수 없다면 그 자산이 속하는 현금창출단위의 회수가능액을 추정하고 있습니다.
자산의 회수가능액은 자산 또는 현금창출단위의 순공정가치와 사용가치 중 더 많은 금액으로 측정하고 있습니다. 자산의 회수가능액이 장부금액에 미달하는 경우 자산의 장부금액을 회수가능액으로 감소시키며, 손상차손은 즉시 당기손익으로 인식하고있습니다.
손상검사 목적상 사업결합으로 취득한 영업권은 사업결합으로 인한 시너지효과의 혜택을 받게 될 것으로 기대되는 각 현금창출단위에 취득일로부터 배분되고 있습니다. 영업권이 배분된 현금창출단위에 대해서는 매년 그리고 손상을 시사하는 징후가 있을 때마다 영업권을 포함한 현금창출단위의 장부금액과 회수가능액을 비교하여 손상검사를 하고 있으며 현금창출단위의 장부금액이 회수가능액을 초과하는 경우에는 손상차손을 인식하고 있습니다. 현금창출단위의 손상차손은 우선 현금창출단위에 배분된 영업권의 장부금액을 감소시키고 그 다음 현금창출단위에 속하는 다른 자산에 각각 장부금액에 비례하여 배분하고 있습니다.
매 보고기간말마다 영업권을 제외한 자산에 대해 과거에 인식한 손상차손이 더 이상 존재하지 않거나 감소된 것을 시사하는 징후가 있는지를 검토하여 징후가 있는 경우 당해 자산의 회수가능액을 추정하고 있으며 직전 손상차손의 인식시점 이후 회수가능액을 결정하는 데 사용된 추정치에 변화가 있는 경우에만 환입하고 있습니다. 손상차손환입으로 증가된 장부금액은 과거에 손상차손을 인식하기 전 장부금액의 감가상각 또는 상각 후 잔액을 초과할 수 없으며, 손상차손환입은 즉시 당기손익으로 인식하고 있습니다. 현금창출단위의 손상차손환입은 현금창출단위를 구성하는 자산들(영업권 제외)의 장부금액에 비례하여 배분하며, 영업권에 대해 인식한 손상차손은 후속기간에 환입하지 않고 있습니다.
(24) 법인세
법인세비용(수익)은 당기법인세비용(수익)과 이연법인세비용(수익)으로 구성되고 있습니다. 당기법인세와 이연법인세는 수익이나 비용으로 인식하여 당기손익에 포함하고 있으며, 동일 회계기간 또는 다른 회계기간에 자본에 직접 가감되는 항목과 관련된 당기법인세와 이연법인세는 자본에 직접 가감하고 있습니다.
1) 당기법인세
당기법인세는 회계기간의 과세소득(세무상결손금)에 대하여 납부할(환급받을) 법인세액이며, 과세소득(세무상결손금)은 과세당국이 제정한 법규에 따라 납부할(환급받을) 법인세를 산출하는 대상이 되는 회계기간의 이익(손실)으로서 포괄손익계산서의 손익과는 차이가 있습니다.
당기 및 과거기간의 당기법인세부채(자산)는 보고기간말까지 제정되었거나 실질적으로 제정된 세율(및 세법)을 사용하여, 과세당국에 납부할(과세당국으로부터 환급받을) 것으로 예상되는 금액으로 측정하고 있습니다.
당기 및 과거기간의 당기법인세 중 납부되지 않은 부분을 부채로 인식하며, 과거기간에 납부하여야 할 금액을 초과해서 납부하였다면 그 초과금액은 자산으로 인식하고 있으며, 과거 회계기간의 당기법인세에 대하여 소급공제가 가능한 세무상결손금과 관련된 혜택은 자산으로 인식하고 있습니다.
2) 이연법인세
연결실체는 모든 가산할 일시적차이에 대하여 이연법인세부채를 인식하고 있습니다.다만 영업권을 최초로 인식하는 경우와 자산·부채가 최초로 인식되는 거래가 사업결합거래가 아니고 거래 당시의 회계이익이나 과세소득(세무상결손금)에 영향을 미치지 아니하는 거래인 경우 및 종속기업·지점 및 관계기업에 대한 투자자산 그리고 공동약정투자지분과 관련된 가산할 일시적차이에 대하여 지배기업· 투자자 또는 참여자가 일시적차이의 소멸시점을 통제할 수 있고 예측가능한 미래에 일시적차이가소멸하지 않을 가능성이 높을 경우에 발생하는 이연법인세부채는 인식하지 아니하고있습니다.
연결실체는 차감할 일시적차이가 사용될 수 있는 과세소득의 발생가능성이 높은 경우에 모든 차감할 일시적차이에 대하여 이연법인세자산을 인식하고 있습니다. 다만, 자산이나 부채를 최초로 인식할 때 발생하는 거래로 사업결합거래가 아니고 거래 당시 회계이익이나 과세소득(세무상결손금)에 영향을 미치지 않는 거래인 경우 및 종속기업·지점 및 관계기업에 대한 투자자산 그리고 공동약정투자지분과 관련된 모든 차감할 일시적차이에 대하여 일시적차이가 예측가능한 미래에 소멸할 가능성이 높지않거나 일시적차이가 사용될 수 있는 과세소득이 발생할 가능성이 높지 않은 경우에는 이연법인세자산은 인식하지 아니하고 있습니다. 미사용 세무상결손금과 세액공제가 사용될 수 있는 미래 과세소득의 발생가능성이 높은 경우 그 범위 안에서 이월된 미사용 세무상결손금과 세액공제에 대하여 이연법인세자산을 인식하고 있습니다.
이연법인세자산의 장부금액은 매 보고기간말에 검토하며 이연법인세자산의 일부 또는 전부에 대한 혜택이 사용되기에 충분한 과세소득이 발생할 가능성이 더 이상 높지않다면 이연법인세자산의 장부금액을 감액시키고 감액된 금액은 사용되기에 충분한 과세소득이 발생할 가능성이 높아지면 그 범위 내에서 환입하고 있습니다.
이연법인세 자산과 부채는 보고기간말까지 제정되었거나 실질적으로 제정된 세율(및세법)에 근거하여 당해 자산이 실현되거나 부채가 결제될 회계기간에 적용될 것으로 기대되는 세율을 사용하여 측정하고 있으며 이연법인세 자산과 부채는 할인하지 아니하고 있습니다.
연결실체가 당기법인세자산과 당기법인세부채를 상계할 수 있는 법적으로 집행가능한 권리를 가지고 있으며, 동일한 과세당국에 의해서 부과되는 법인세와 관련하여 과세대상기업이 동일한 경우 혹은 과세대상기업은 다르지만 당기법인세 부채와 자산을순액으로 결제할 의도가 있거나 유의적인 금액의 이연법인세부채가 결제되거나 이연법인세자산이 회수될 미래의 각 회계기간마다 자산을 실현하는 동시에 부채를 결제할 의도가 있는 경우 이연법인세자산과 이연법인세부채를 상계하고 있습니다.
(25) 주당이익
연결실체는 기본주당이익과 희석주당이익을 지배기업의 보통주에 귀속되는 계속영업손익과 당기순손익에 대하여 계산하고 연결포괄손익계산서에 표시하고 있습니다.
기본주당이익은 지배기업의 보통주에 귀속되는 특정 회계기간의 당기순손익을 그 기간에 유통된 보통주식수를 가중평균한 주식수로 나누어 계산하고 있으며, 지배기업의 보통주에 귀속되는 금액은 지배기업에 귀속되는 계속영업손익과 당기순손익 각각의 금액에서 자본으로 분류된 우선주에 대한 세후 우선주 배당금,우선주 상환시 발생한 차액 및 유사한 효과를 조정한 금액입니다.
희석주당이익은 모든 희석효과가 있는 잠재적보통주의 영향을 고려하여 지배기업의 보통주에 귀속되는 당기순손익 및 가중평균유통보통주식수를 조정하여 계산하고 있습니다.
(26) 매각예정비유동자산
비유동자산(또는 처분자산집단)의 장부금액이 계속사용이 아닌 매각거래를 통하여 주로 회수될 것이라면 이를 매각예정으로 분류하며 순공정가치와 장부금액 중 작은 금액으로 측정하고, 그 자산은 감가상각(또는 상각)하지 아니하고 있습니다. 매각예정으로 분류된 비유동자산은 다른 자산과 별도로 연결재무상태표에 표시하며 매각예정으로 분류된 처분자산집단에 포함되는 자산이나 부채는 다른 자산이나 부채와 별도로 연결재무상태표에 표시하고 있습니다.
(27) 중단영업
연결실체는 별도의 주요 사업계열이나 영업지역을 처분하거나 매각예정으로 분류되는 경우 등을 중단영업으로 분류하고 있으며, 중단영업이 있는 경우 세후 중단영업손익 등을 포괄손익계산서에 단일금액으로 표시하고 중단영업의 수익, 비용 및 세전 중단영업손익 등을 공시하고 있습니다. 또한, 연결실체는 비교표시되는 과거재무제표에 중단영업관련 공시사항을 다시 표시하고 있습니다.
(28) 오류수정
특정기간에 미치는 오류의 영향이나 오류의 누적효과를 실무적으로 결정할 수 없는 경우를 제외하고는 중요한 전기오류가 발견된 이후 최초로 발행을 승인하는 재무제표에 오류가 발생한 과거기간의 재무제표가 비교표시되는 경우 그 재무정보를 재작성하고 있습니다.
(29) 중요한 회계추정 및 판단
연결재무제표의 작성시 경영진은 회계정책의 적용이나 자산, 부채, 수익, 비용의 장부금액 및 우발부채의 금액에 영향을 미칠 수 있는 판단과 추정 및 가정을 하여야 합니다. 보고기간말 현재 이러한 추정치는 경영진의 최선의 판단 및 추정에 따라 이루어지고 있으며 추정치와 추정에 대한 가정은 지속적으로 검토되고 있으나 향후 경영환경의 변화에 따라 실제 결과와는 중요하게 다를 수도 있습니다.
회계정책을 적용하는 과정에서 추정에 관련된 공시와는 별도로 연결재무제표에 인식되는 금액에 가장 유의적인 영향을 미칠 수 있는 경영진이 내린 판단 및 미래에 대한 가정과 보고기간말의 추정 불확실성과 관련하여 다음 회계연도에 자산과 부채의 장부금액에 대한 중요한 조정을 유발할 수 있는 유의적인 위험을 내포하고 있는 사항은다음과 같습니다.
ㆍ 주석 3: 공정가치평가
ㆍ 주석 6: 매출채권, 기타금융자산의 기대신용손실
ㆍ 주석 13: 영업권, 기타의무형자산
3. 위험관리
금융상품과 관련하여 연결실체는 신용위험, 유동성위험 및 시장위험에 노출되어 있습니다. 본 주석은 연결실체가 노출되어 있는 위의 위험에 대한 정보와 연결실체의 위험관리 목표, 정책, 위험 평가 및 관리 절차, 그리고 자본관리에 대해 공시하고 있습니다. 추가적인 계량적 정보에 대해서는 본 연결재무제표 전반에 걸쳐서 공시되어 있습니다.
(1) 금융위험관리
연결실체의 위험관리 체계를 구축하고 감독할 책임은 이사회에 있습니다. 이사회는 연결실체의 위험관리 정책을 개발하고 감독하고 있으며 중장기 경영계획 및 단기 경영전략에 대해 정기적으로 보고받고 승인하고 있습니다.
연결실체의 위험관리 정책은 연결실체가 직면한 위험을 식별 및 분석하고, 적절한 위험 한계치 및 통제를 설정하고, 위험이 한계치를 넘지 않도록 하기 위해 수립되었습니다. 위험관리 정책은 시장 상황과 연결실체의 활동의 변경을 반영하기 위해 정기적으로 검토되고 있습니다. 연결실체는 훈련 및 관리기준, 절차를 통해 모든 종업원들이 자신의 역할과 의무를 이해할 수 있는 엄격하고 구조적인 통제환경을 구축하는 것을 목표로 하고 있습니다.
1) 신용위험
① 신용위험에 대한 노출
금융자산의 장부금액은 신용위험에 대한 최대노출정도를 나타냅니다. 연결실체는 현금및현금성자산을 신용등급이 우수한 금융기관에 예치하고 있어, 금융기관으로부터의 신용위험은 제한적입니다. 또한, 연결실체가 보유하고 있는 채무증권은 채무불이행 위험이 낮고, 차입자가 계약상 현금흐름 지급의무를 이행할 수 있는 능력이 있기 때문에 신용위험이 낮은 것으로 보고 있습니다. 연결실체의 신용위험에 대한 최대 노출정도는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 현금및현금성자산 | 80,483,163 | 99,796,601 |
| 매출채권 | 27,995,134 | 34,034,508 |
| 기타금융자산 | 20,633,974 | 37,952,824 |
| 당기손익-공정가치 측정 금융자산(채무증권) | 54,433,682 | 22,049,993 |
| 합 계 | 183,545,953 | 193,833,926 |
당반기말 현재 연결실체는 관계기업인 현대요트㈜의 하자이행보증 및 계약이행보증에 대한 지급보증을 제공함에 따라 추가적인 신용위험에 노출되어 있습니다(주석 31참고).
② 손상차손
연결실체는 매출채권과 기타채권에 대한기대신용손실을 측정하여 충당금을 설정하고 있습니다. 당반기말과 전기말 현재 기대신용손실과 각 연령별로 손상된 금액은 다음과 같습니다.
| (단위: 천원) | ||||||||
|---|---|---|---|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | ||||||
| 기대손실율 | 채권잔액 | 손상된 금액 | 장부금액(*2) | 기대손실율 | 채권잔액 | 손상된 금액 | 장부금액 | |
| 3개월 이하(*1) | 0.02% | 64,539,271 | (14,537) | 64,524,734 | 0.14% | 58,533,082 | (83,868) | 58,449,214 |
| 3~6개월 | 11.33% | 715,287 | (81,063) | 634,224 | 11.57% | 24,130 | (2,791) | 21,339 |
| 6~9개월 | 7.04% | 95,522 | (6,722) | 88,800 | 18.32% | 15,887 | (2,911) | 12,976 |
| 9~12개월 | 69.93% | 12,429 | (8,692) | 3,737 | 0.00% | - | - | - |
| 12개월 초과(*2) | 41.23% | 16,450,332 | (6,781,859) | 9,668,473 | 41.98% | 16,163,291 | (6,785,739) | 9,377,552 |
| 합 계 | 81,812,841 | (6,892,873) | 74,919,968 | 74,736,390 | (6,875,309) | 67,861,081 | ||
(*1) 2021년 귀속분 리보세라닙 로열티 매출채권에 대한 추정치 11,724,092천원이 포함되어 있습니다.
당반기와 전기 중 매출채권과 기타금융자산에 대한 대손충당금의 기중 변동내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전기 |
| 기초금액 | 36,875,309 | 45,845,459 |
| 연결범위의 변동 | (3,880) | 93,923 |
| 대손상각비 | 22,941 | 683,167 |
| 기타의대손상각비(환입) | (1,497) | (1,197,316) |
| 제각(*) | - | (8,549,924) |
| 기말금액 | 36,892,873 | 36,875,309 |
(*) 폐업 등으로 회수가 불가능한 채권을 장부에서 제각하였습니다.
2) 유동성위험
당반기말 및 전기말 현재 금융부채의 계약상 만기는 다음과 같습니다. 금액은 이자지급액을 포함하고, 상계약정의 효과는 포함하지 않았습니다.
① 당반기말
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 장부금액 | 계약상 현금흐름 | 3개월이내(*) | 3-12개월(*) | 1-2년(*) | 2년초과 |
| 매입채무 | 4,600,685 | 4,581,616 | 4,581,616 | - | - | - |
| 기타금융부채 | 97,889,804 | 103,092,039 | 81,329,818 | 2,000,977 | 2,070,216 | 17,691,028 |
| 차입금 | 110,053,697 | 127,564,030 | 2,136,478 | 25,707,600 | 99,366,752 | 353,200 |
| 합 계 | 212,544,186 | 235,237,685 | 88,047,912 | 27,708,577 | 101,436,968 | 18,044,228 |
(*) 전환사채 및 신주인수권부사채의 조기상환권이 청구 가능한 가장 빠른 시기에 행사됨을 가정하였습니다.
② 전기말
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 장부금액 | 계약상 현금흐름 | 3개월이내(*) | 3-12개월 | 1-2년(*) | 2년초과 |
| 매입채무 | 5,084,230 | 5,084,230 | 5,084,230 | - | - | - |
| 기타금융부채 | 94,060,368 | 93,965,067 | 76,535,419 | 3,896,515 | 1,764,339 | 11,768,794 |
| 차입금 | 68,594,770 | 79,879,342 | 17,521,115 | 3,750,595 | 58,250,832 | 356,800 |
| 합 계 | 167,739,368 | 178,928,639 | 99,140,764 | 7,647,110 | 60,015,171 | 12,125,594 |
(*) 전환사채 및 신주인수권부사채의 조기상환권이 청구 가능한 가장 빠른 시기에 행사됨을 가정하였습니다.
3) 환위험
① 환위험에 대한 노출
연결실체는 기능통화인 원화 이외의 통화로 표시되는 거래로 인하여 환율변동위험에노출되어 있습니다. 당반기말 및 전기말 현재 외화로 표시된 화폐성자산 및 부채의 장부금액은 다음과 같습니다.
| (단위 : USD, CNY) | ||||
|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | ||
| USD | CNY | USD | CNY | |
| 자산: | ||||
| 외화예금 | 9,141,118 | - | 803,721 | - |
| 매출채권 | 5,046,357 | 60,825,380 | 416,440 | 90,706,765 |
| 기타금융자산 | - | - | 29,423 | - |
| 소 계 | 14,187,475 | 60,825,380 | 1,249,584 | 90,706,765 |
| 부채: | ||||
| 매입채무 | 88,436 | - | - | - |
| 합 계 | 14,099,039 | 60,825,380 | 1,249,584 | 90,706,765 |
당반기말과 전기말 현재 적용된 환율은 다음과 같습니다.
| (단위: 원) | ||||
|---|---|---|---|---|
| 구 분 | 평균환율 | 기말환율 | ||
| 당반기 | 전반기 | 당반기말 | 전기말 | |
| USD | 1,232.94 | 1,117.73 | 1,292.90 | 1,185.50 |
| CNY | 190.04 | 172.75 | 192.75 | 186.26 |
② 민감도분석
연결실체는 내부적으로 원화 환율 변동에 대한 환위험을 정기적으로 측정하고 있습니다. 당반기 및 전기 중 각 외화에 대한 원화환율 5% 변동 시 환율변동이 세전손익에 미치는 영향은 다음과 같습니다.
| (단위 : 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전기 | ||
| 5% 상승시 | 5 % 하락시 | 5% 상승시 | 5 % 하락시 | |
| USD | 917,149 | (917,149) | 74,069 | (74,069) |
| CNY | 586,205 | (586,205) | 844,752 | (844,752) |
4) 이자율위험
① 당반기말 및 전기말 현재 연결실체가 보유하고 있는 이자부 금융상품은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 고정이자율 : | ||
| 금융자산 | 119,187,314 | 141,252,906 |
| 금융부채 | 110,053,697 | 64,726,776 |
| 합 계 | 9,133,617 | 76,526,130 |
| 변동이자율 : | ||
| 금융자산 | 375,789 | - |
| 금융부채 | - | 3,867,994 |
② 고정이자율 금융상품의 공정가치 민감도 분석
연결실체는 고정이자율 금융상품을 당기손익인식금융상품으로 처리하고 있지 않으며, 이자율스왑과 같은 파생상품을 공정가치위험회피회계의 위험회피수단으로 지정하지 않았습니다. 따라서, 이자율의 변동은 손익에 영향을 주지 않습니다.
③ 변동이자율 금융상품의 현금흐름 민감도 분석
당반기말 현재 이자율이 100베이시스포인트 변동한다면, 자본과 손익은 증가 또는 감소하였을 것입니다. 이 분석은 환율과 같은 다른 변수는 변동하지 않는다고 가정하였으며, 당반기 중 구체적인 세전자본 및 세전손익의 변동금액은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 손익 | 자본 | ||
| 100bp상승 | 100bp하락 | 100bp상승 | 100bp하락 | |
| 당반기말: | ||||
| 변동이자율 금융상품 | ||||
| 장ㆍ단기금융자산 | 3,758 | (3,758) | 3,758 | (3,758) |
5) 공정가치
공정가치 서열체계를 포함한 금융자산과 금융부채의 장부금액과 공정가치는 다음과 같습니다. 장부금액이 공정가치의 합리적인 근사치에 해당하여 공정가치를 측정하지않은 금융자산과 금융부채에 대한 공정가치 정보는 포함하고 있지 않습니다.
① 당반기말
| (단위:천원) | ||||
|---|---|---|---|---|
| 구 분 | 장부금액 | 수준1 | 수준2 | 수준3 |
| 공정가치로 측정되는 금융자산: | ||||
| 당기손익-공정가치 측정 | 54,433,682 | 22,469,317 | 31,962,955 | 1,410 |
| 기타포괄손익-공정가치 측정 | 5,793,068 | 719,227 | - | 5,073,841 |
| 합 계 | 60,226,750 | 23,188,544 | 31,962,955 | 5,075,251 |
② 전기말
| (단위:천원) | ||||
|---|---|---|---|---|
| 구 분 | 장부금액 | 수준1 | 수준2 | 수준3 |
| 공정가치로 측정되는 금융자산: | ||||
| 당기손익-공정가치 측정 | 23,551,252 | - | 23,549,842 | 1,410 |
| 기타포괄손익-공정가치 측정 | 6,073,286 | 999,445 | - | 5,073,841 |
| 합 계 | 29,624,538 | 999,445 | 23,549,842 | 5,075,251 |
③ 가치평가기법
연결실체는 공정가치 서열체계에서 수준 2와 수준 3으로 분류되는 반복적인 공정가치측정치, 비반복적인 공정가치측정치, 공시되는 공정가치에 대해 다음의 가치평가기법을 사용하고 있습니다. 사용된 가치평가기업과 투입변수는 다음과 같습니다.
| (단위:천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 공정가치 | 가치평가기법 | 수준 | 투입변수 | 투입변수 범위 |
| 에이치엘비제약㈜ 전환사채(*) | 23,272,820 | 현재가치기법, 이항모형 | 2 | 가중평균자본비용 | 14.87% |
| 가격 변동성 | 76.70% | ||||
| 무위험 할인율 | 3.20% | ||||
| 에이치엘비㈜ 제36회 전환사채 매도청구권 | 2,355,384 | 현재가치기법, 이항모형 | 2 | 가중평균자본비용 | 17.54% |
| 가격 변동성 | 60.30% | ||||
| 무위험 할인율 | 3.16% | ||||
| 에이치엘비㈜ 제37회 신주인수권부사채 매도청구권 | 1,740,936 | 현재가치기법, 이항모형 | 2 | 가중평균자본비용 | 17.54% |
| 가격 변동성 | 60.30% | ||||
| 무위험 할인율 | 3.16% | ||||
| 노터스 제1회 전환사채 매도청구권 | 3,017,209 | 현재가치기법, 이항모형 | 2 | 가중평균자본비용 | 5.26% |
| 가격 변동성 | 68.42% | ||||
| 무위험 할인율 | 1.96% | ||||
| 저축성보험 | 1,576,605 | 순자산가치법 | 2 | 해지환급금 | - |
| ㈜씨엘팜 지분 | 5,073,841 | 현금흐름할인법 | 3 | 가중평균자본비용 | 19.55% |
| 영구성장률 | 0.00% | ||||
| 무위험 할인율 | 2.26% | ||||
| 조합출자금 | 1,410 | 원가접근법 | 3 | 개별 자산 및 부채의 공정가치 | - |
(*) 투입변수 중 가격 변동성이 증가하거나 가중평균자본비용이 감소하면 공정가치가 증가하며, 무위험 할인율의 감소도 공정가치를 증가시킬 수 있습니다.
④ 수준 3 공정가치
당반기 중 수준 1과 수준 2간의 대체는 없었으며, 수준 3 공정가치 분류되는 금융자산의 당반기 중 변동내용은 없습니다.
⑤ 공정가치 서열체계
연결실체는 공정가치 측정에 사용된 투입변수의 유의성을 반영하는 공정가치 서열체계에따라 공정가치 측청치를 분류하고 있으며, 공정가치 서열체계의 수준은 다음과 같습니다.
| 구 분 | 투입변수의 유의성 |
|---|---|
| 수준 1 | 동일한 자산이나 부채에 대한 활성시장의 공시가격 |
| 수준 2 | 직접적으로 또는 간접적으로 관측가능한, 자산이나 부채에 대한 투입변수 |
| 수준 3 | 관측가능한 시장자료에 기초하지 않은, 자산이나 부채에 대한 투입변수 |
(2) 자본관리
연결실체의 자본관리는 건전한 자본구조를 유지하며, 주주이익의 극대화를 목적으로하고 있습니다. 연결실체는 최적 자본구조 달성을 위해 부채비율과 순차입금비율 등의 재무비율을 자본관리지표로 사용하고 있습니다. 부채비율은 부채총계를 자본총계로 나누어 산출하고 있으며, 순차입금비율은 순차입금을 자본총계로 나누어 산출하고 있습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 부채비율: | ||
| 부채총계(A) | 277,826,631 | 231,507,461 |
| 자본총계(B) | 535,316,641 | 512,184,803 |
| 부채비율(A/B) | 51.90% | 45.20% |
| 순차입금비율: | ||
| 현금및현금성자산(C) | 80,483,163 | 99,796,601 |
| 단기금융상품(D) | 5,025,000 | 9,320,000 |
| 차입금(E) | 110,053,697 | 68,594,770 |
| 순차입금(F=E-C-D) | 24,545,534 | - |
| 순차입금비율(F/B) | 4.59% | 0.00% |
4. 영업부문
(1) 일반정보
연결실체의 보고부문에 대한 주요 내용은 다음과 같습니다.
| 구 분 | 주요 재화 및 용역 | 주요 고객정보 |
|---|---|---|
| 복합소재사업 부문 | 구명정 건조 및 수리, 파이프 제작 및 설치 | ㈜현대미포조선, 현대중공업㈜, 현대삼호중공업㈜, 대우조선해양㈜옥포조선소 등 |
| 바이오의료기기사업 부문 | 바이오의약품 개발 및 의료기기 제조, 판매 의약외품 등(알콜스왑, 검체채취용 도구 등) |
에임㈜, ㈜한국애보트진단, 에스디바이오센서㈜, 병원, 개인고객 등 |
(2) 당반기 및 전반기 연결실체의 부문별 재무정보는 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 복합소재사업 부문 | 바이오의료기기사업 부문 | ||
| 당반기 | 전반기 | 당반기 | 전반기 | |
| 매출액 | 8,966,383 | 11,858,185 | 114,338,334 | 4,098,640 |
| 영업이익(손실) | (1,825,427) | (3,104,753) | (18,270,390) | (36,652,164) |
| 당기순이익(손실) | (1,299,347) | (3,567,737) | (17,800,743) | (53,509,942) |
| 유동자산 | 8,562,842 | 12,037,252 | 154,572,677 | 203,919,124 |
| 비유동자산 | 9,380,565 | 9,826,564 | 640,627,188 | 442,939,356 |
| 자산 계 | 17,943,407 | 21,863,816 | 795,199,865 | 646,858,480 |
| 유동부채 | 4,158,694 | 5,992,383 | 119,141,201 | 86,271,728 |
| 비유동부채 | 459,383 | 522,016 | 154,067,352 | 53,045,753 |
| 부채 계 | 4,618,078 | 6,514,399 | 273,208,554 | 139,317,481 |
(3) 당반기 및 전반기 연결실체의 지역별 매출정보는 다음과 같습니다.
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||||
| 복합소재 사업 부문 |
바이오의료기기 사업 부문 |
합 계 | 복합소재 사업 부문 |
바이오의료기기 사업 부문 |
합 계 | |
| 주요 지역별: | ||||||
| 국내 | 3,027,850 | 84,518,633 | 87,546,483 |
6,437,987 |
3,800,429 |
10,238,416 |
| 해외 | 5,938,533 | 29,819,701 | 35,758,234 |
5,540,198 |
178,210 |
5,718,408 |
| 합 계 | 8,966,383 | 114,338,334 | 123,304,717 |
11,978,185 |
3,978,639 |
15,956,824 |
(4) 당반기말과 전기말 현재 연결실체의 지역별 비유동자산 정보는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 국내 | 296,487,971 | 241,543,312 |
| 미국 | 332,514,210 | 314,007,161 |
| 중국 | 21,005,573 | - |
| 합 계 | 650,007,754 | 555,550,473 |
5. 현금및현금성자산
당반기말과 전기말 현재 현금및현금성자산의 상세내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 구 분 | 연이자율(%) | 금 액 | |
| 당반기말 | 전기말 | ||
| 요구불예금 등 | 0.10 ~ 0.14 | 77,983,163 | 69,796,601 |
| 정기예금 | 0.90 ~ 1.37 | 2,500,000 | 30,000,000 |
| 합 계 | 80,483,163 | 99,796,601 | |
6. 매출채권 및 기타금융자산
(1) 당반기말과 전기말 현재 매출채권 및 기타금융자산의 내역은 다음과 같습니다.
| (단위: 천원) | |||||||
|---|---|---|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | |||||
| 채권잔액(*1) | 대손충당금 | 장부금액 | 채권잔액(*1) | 대손충당금 | 장부금액 | ||
| 유동항목: | |||||||
| 매출채권 | 29,056,136 | (1,061,002) | 27,995,134 | 35,022,553 | (988,045) | 34,034,508 | |
| 기타금융자산 | 정기예적금 | 5,055,853 | - | 5,055,853 | 27,320,000 | - | 27,320,000 |
| 단기대여금 | 5,328,600 | (5,328,600) | - | 5,434,611 | (5,328,600) | 106,011 | |
| 미수수익 | 19,114 | (1,628) | 17,486 | 93,022 | (1,628) | 91,394 | |
| 미수금 | 10,773,789 | (408,348) | 10,365,441 | 1,113,637 | (409,846) | 703,791 | |
| 펀드예치금(*2) | 30,000,000 | (30,000,000) | - | 30,000,000 | (30,000,000) | - | |
| 보증금 | 580,128 | - | 580,128 | 1,023,725 | - | 1,023,725 | |
| 금융리스채권 | 21,034 | (21,034) | - | 21,034 | (21,034) | - | |
| 소 계 | 51,778,518 | (35,759,610) | 16,018,908 | 65,006,029 | (35,761,108) | 29,244,921 | |
| 유동항목 합계 | 80,834,654 | (36,820,612) | 44,014,042 | 100,028,582 | (36,749,153) | 63,279,429 | |
| 비유동항목: | |||||||
| 기타금융자산 | 장기금융상품 | 271,127 | - | 271,127 | 213,500 | - | 213,500 |
| 장기대여금 | 2,000,000 | - | 2,000,000 | ||||
| 장기선급금 | - | - | - | 6,592,750 | - | 6,592,750 | |
| 보증금 | 2,343,940 | - | 2,343,940 | 1,955,550 | (53,897) | 1,901,653 | |
| 금융리스채권 | 72,259 | (72,259) | - | 72,259 | (72,259) | - | |
| 소 계 | 4,687,326 | (72,259) | 4,615,067 | 8,834,059 | (126,156) | 8,707,903 | |
| 비유동항목 합계 | 4,687,326 | (72,259) | 4,615,067 | 8,834,059 | (126,156) | 8,707,903 | |
(*1) 현재가치할인차금 차감 후 금액입니다.
(*2) 하이투자증권㈜의 사기적 부정거래 행위 및 불완전판매로 인하여 부당이득금 반환 청구 소송중인 예치금입니다. (주석 33 참조)
7. 파생상품
(1) 파생상품의 내역은 다음과 같습니다.
| (단위:천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 파생상품자산 | ||
| 에이치엘비 제36회차 전환사채 매도청구권(*1) | 2,355,384 | - |
| 에이치엘비 제37회차 신주인수권부사채 매도청구권(*1) | 1,740,936 | - |
| 노터스 제1회차 전환사채 매도청구권(*2) | 3,017,209 | - |
| 합 계 | 7,113,529 | - |
(*1) 총 발행금액의 30%에 대하여 당사 또는 당사가 지정하는 제3자에게 매도 요청 할 권리(콜옵션)를 보유하고 있으며, 당사는 동 콜옵션을 별도의 금융상품으로 인식하였습니다. (주석 15 참조)
(*2) 총 발행금액의 30%에 대하여 당사가 매도청구권을 보유하고 있습니다.
(2) 당반기 중 파생상품관련 손익은 다음과 같습니다.
| (단위:천원) | |||||
|---|---|---|---|---|---|
| 상품분류 | 종류 | 거래이익 | 평가이익 | 거래손실 | 평가손실 |
| 주식연계옵션 | 매도청구권 | - | 3,017,209 | - | - |
8. 기타자산
당반기말과 전기말 현재 기타자산의 세부내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
| 선급금 | 1,617,841 | - | 239,540 | - |
| 선급비용 | 2,302,701 | 1,975,095 | 2,611,415 | 1,218,276 |
| 합 계 | 3,920,542 | 1,975,095 | 2,850,955 | 1,218,276 |
9. 재고자산
(1) 당반기말과 전기말 현재 재고자산 내역은 다음과 같습니다.
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | ||||
| 취득원가 | 평가손실충당금 | 장부금액 | 취득원가 | 평가손실충당금 | 장부금액 | |
| 원재료 | 3,744,955 | (203,930) | 3,541,025 | 3,594,177 | (2,184) | 3,591,993 |
| 재공품 | 5,877,461 | (359,338) | 5,518,123 | 3,615,016 | (166,125) | 3,448,891 |
| 상품 | 160,455 | - | 160,455 | 251,757 | - | 251,757 |
| 제품 | 8,302,172 | (146,251) | 8,155,921 | 6,495,284 | - | 6,495,284 |
| 미착품 | - | - | - | 23,044 | - | 23,044 |
| 합 계 | 18,085,043 | (709,519) | 17,375,524 | 13,979,278 | (168,309) | 13,810,969 |
(2) 당반기 및 전기 중 재고자산과 관련하여 인식한 평가손실(환입)은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전기 |
| 매출원가: | ||
| -재고자산평가손실(환입) | 541,210 | (127,399) |
| -재해손실(*) | - | 511,314 |
| 기타영업비용: | ||
| 재고자산감모손실 | - | 20,801 |
(*) 전기 중 공장 화재로 인하여 재공품 등 재고자산이 소실되었습니다.
10. 공정가치측정금융자산
(1) 당반기말과 전기말 현재 공정가치측정금융자산의 내역은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 범주 | 당반기말 | 전기말 | ||
| 유동 | 비유동 | 유동 | 비유동 | ||
| 지분증권 | 기타포괄손익-공정가치 | - | 5,793,068 | - | 6,073,286 |
| 채무증권,출자금 | 당기손익-공정가치 | - | 45,743,547 | - | 23,551,252 |
| 장기금융상품 | 당기손익-공정가치 | - | 1,576,605 | - | - |
| 파생상품자산 | 당기손익-공정가치 | 7,113,529 | - | - | - |
| 합 계 | 7,113,529 | 53,113,220 | - | 29,624,538 | |
보유중인 당기손익-공정가치측정 채무증권은 전환사채권이며, 상환 및 전환조건 등은 아래와 같습니다.
| 발행회사 및 사채명 | 에이치엘비제약㈜ 제12회 무기명식 무보증 사모 전환사채 |
에이치엘비생명과학㈜ 제9회 무기명식 이권부 무보증 분리형 신주인수권부사채 |
|---|---|---|
| 취득금액 | 10,000,000,000원 | 19,603,370,000원 |
| 사채만기일 | 2023년 10월 19일 | 2025년 6월 15일 |
| 전환(행사)가액 (원/주) | 6,689원 | 11,925원 |
| 전환(행사)청구 시작일 | 2021년 10월 19일 | 2022년 7월 15일 |
| 전환(행사)청구 종료일 | 2023년 9월 19일 | 2025년 5월 15일 |
| 전환(행사)에 따라 발행할 주식 | 1,494,991주 | 1,643,888주 |
| 옵션에 관한 사항 | - | 조기상환(Put Option): 본 사채의 발행일로부터 24개월이 경과하는 날로부터 3개월에 해당하는 날에 본 사채 금액의 전부 또는 일부에 대하여 조기상환 청구 가능. |
| 기타 | - | "신주인수권증권"과 "신주인수권이 분리된 채권"이 각각 상장되어 유통되는 분리형 신주인수권부사채임. |
(2) 당반기와 전기 중 공정가치측정 금융자산의 변동내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전기 |
| 기초장부금액 | 29,624,538 | 56,477,415 |
| 취득 | 19,671,928 | 1,246,709 |
| 대체 | 4,307,820 | 280,682 |
| 보통주전환(*) | - | (22,852,986) |
| 연결범위의 변동 | - | 18,529,071 |
| 처분 | (358,439) | (22,131,713) |
| 평가이익-당기손익 | 7,435,741 | 4,362,344 |
| 평가손실-당기손익 | (174,621) | (7,506,366) |
| 평가이익-기타포괄손익 | (280,218) | 1,052,576 |
| 외화환산차이 | - | 166,806 |
| 기말장부금액 | 60,226,749 | 29,624,538 |
(*) 전기 중 에이치엘비생명과학㈜의 보통주 1,317,175주로 전환하였습니다.
11. 관계기업투자주식
(1) 당반기와 전기 중 관계기업투자주식의 변동내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전기 |
| 기초금액 | 133,623,850 | 106,499,613 |
| 취득 | 56,225,919 | 34,454,997 |
| 지분법손익 | (1,016,709) | (8,355,555) |
| 지분법자본변동 | 2,804,362 | 1,024,795 |
| 기말금액 | 191,637,422 | 133,623,850 |
(2) 당반기말과 전기말 현재 관계기업투자의 내역은 다음과 같습니다.
| (단위: 천원) | |||||||
|---|---|---|---|---|---|---|---|
| 구 분 | 소재국가 | 당반기말 | 전기말 | ||||
| 지분율(%) | 취득원가 | 순자산가액 | 장부금액 | 지분율(%) | 장부금액 | ||
| 바다중공업㈜ | 한국 | 28.89% | 905,735 | 1,991,183 | 586,517 | 28.89 | 1,107,167 |
| 현대요트㈜ | 한국 | 39.43% | 4,399,990 | 1,159,667 | 457,222 | 39.43 | 502,720 |
| 에이치엘비생명과학㈜(*1) | 한국 | 19.60% | 68,267,227 | 261,391,952 | 123,306,494 | 19.60 | 120,654,468 |
| Verismo Therapeutics, Inc(*1) | 미국 | 9.61% | 5,602,000 | 27,125,314 | 6,186,987 | 11.44 | 5,359,485 |
| 에이치엘비테라퓨틱스㈜(*1) | 한국 | 2.03% | 6,000,010 | 2,579,934 | 6,167,070 | 2.03 | 6,000,010 |
| ㈜노터스(*1)(*2) | 한국 | 18.01% | 56,225,920 | 64,049,011 | 54,933,133 | - | - |
| 합 계 | 141,400,882 | 358,297,061 | 191,637,423 | 133,623,850 | |||
(*1) 재무정책과 영업정책에 관한 의사결정에 유의적인 영향력의 행사가 가능함에 따라 지분율이 20% 미만임에도 불구하고 관계기업투자주식으로 분류하였습니다.
(*2) 연결실체가 신규 출자한 비임상 CRO 업체로서, 당사의 신규사업진출 및 기존사업과의 시너지 극대화를 위해 지분을 취득하였습니다.
(3) 당반기 및 전기 중 지분법평가내역은 다음과 같습니다.
① 당반기
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 기초 장부가액 |
취득액 | 지분법 평가손익 |
지분법 자본변동 |
기말 장부가액 |
| 바다중공업㈜ | 1,107,168 | - | (520,651) | - | 586,517 |
| 현대요트㈜ | 502,720 | - | (45,498) | - | 457,222 |
| 에이치엘비생명과학㈜ | 120,654,467 | - | (739,589) | 3,391,616 | 123,306,494 |
| Verismo Therapeutics, Inc | 5,359,485 | - | 726,283 | 101,219 | 6,186,987 |
| 에이치엘비테라퓨틱스㈜ | 6,000,010 | - | (79,702) | 246,762 | 6,167,070 |
| ㈜노터스 | - | 56,225,919 | (357,551) | (935,235) | 54,933,133 |
| 합 계 | 133,623,850 | 56,225,919 | (1,016,708) | 2,804,362 | 191,637,423 |
② 전기
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 기초 장부가액 |
취득액 | 지분법 평가손익 |
지분법 자본변동 |
기말 장부가액 |
| 바다중공업㈜ | 937,124 | - | 170,044 | - | 1,107,168 |
| 현대요트㈜ | - | - | - | 502,720 | 502,720 |
| 에이치엘비생명과학㈜ | 105,562,489 | 22,852,986 | (7,779,397) | 18,389 | 120,654,467 |
| Verismo Therapeutics, Inc | - | 5,602,000 | (746,202) | 503,687 | 5,359,485 |
| 에이치엘비테라퓨틱스㈜ | - | 6,000,010 | - | - | 6,000,010 |
| 합 계 | 106,499,613 | 34,454,996 | (8,355,555) | 1,024,796 | 133,623,850 |
(4) 당반기말과 전기말 현재 관계기업의 요약 재무정보는 다음과 같습니다.
① 당반기말
| (단위: 천원) | ||||||||
|---|---|---|---|---|---|---|---|---|
| 기업명 | 유동자산 | 비유동자산 | 유동부채 | 비유동부채 | 총수익 | 영업이익 (손실) |
당기순이익 (손실) |
총포괄손익 |
| 바다중공업㈜ | 14,960,255 | 6,115,872 | 15,162,344 | 3,922,600 | 7,943,000 | (1,975,294) | (2,056,687) | (2,056,687) |
| 현대요트㈜ | 7,287,627 | 830,887 | 6,747,578 | 211,270 | 5,888,388 | (143,948) | (115,396) | (115,396) |
| 에이치엘비생명과학㈜ | 245,792,974 | 121,641,524 | 15,225,325 | 90,401,067 | 32,659,828 | (4,984,520) | (2,948,259) | (2,870,409) |
| Verismo Therapeutics, Inc(*) | 27,156,172 | 1,180 | 32,039 | - | - | (2,907,504) | (2,255,682) | (2,255,682) |
| 에이치엘비테라퓨틱스㈜ | 95,433,330 | 110,322,573 | 63,547,219 | 3,292,121 | 22,644,513 | (1,369,899) | (4,271,998) | 8,917,124 |
| 노터스㈜ | 98,465,293 | 70,876,861 | 40,416,591 | 63,709,808 | 16,178,962 | 2,104,785 | (846,991) | 270,100 |
(*) 종속기업 및 관계기업 편입 전 발생한 손익은 포함되지 않았습니다.
② 전기말
| (단위: 천원) | ||||||||
|---|---|---|---|---|---|---|---|---|
| 기업명 | 유동자산 | 비유동자산 | 유동부채 | 비유동부채 | 총수익 | 영업이익 (손실) |
당기순이익 (손실) |
총포괄손익 |
| 바다중공업㈜ | 14,339,843 | 6,081,114 | 14,599,362 | 1,774,416 | 16,481,950 | 528,037 | 556,071 | 556,071 |
| 현대요트㈜ | 11,494,551 | 541,877 | 10,578,989 | 182,377 | 14,245,758 | 11,369 | 9,160 | 3,849,040 |
| 에이치엘비생명과학㈜ | 156,822,300 | 113,977,269 | 13,535,842 | 10,651,857 | 53,494,248 | (18,480,404) | (49,291,550) | (49,005,365) |
| Verismo Therapeutics, Inc(*) | 15,572,994 | - | 18,959 | - | - | (6,562,505) | (6,522,743) | (6,522,743) |
| 에이치엘비테라퓨틱스㈜(*) | 113,252,822 | 76,458,388 | 56,716,797 | 2,955,096 | - | - | - | - |
(*) 종속기업 및 관계기업 편입 전 발생한 손익은 포함되지 않았습니다.
(5) 시장성이 있는 관계기업
시장성이 있는 관계기업투자의 시장가격은 다음과 같습니다.
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 기업명 | 당반기말 | 전기말 | ||||
| 주당 공정가치 | 주식수 | 시장가격 | 주당 공정가치 | 주식수 | 시장가격 | |
| 에이치엘비생명과학㈜ | 12,150원 | 18,720,849 | 227,458,315 | 12,450원 | 18,720,849 | 233,074,570 |
| 에이치엘비테라퓨틱스㈜ | 13,300원 | 530,899 | 7,060,957 | 14,150원 | 530,899 | 7,512,221 |
| ㈜노터스 | 7,860원 | 12,650,832 | 99,435,540 | - | - | - |
12. 투자부동산
당반기말과 전기말 현재 투자부동산의 내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 과 목 | 소재지 | 당반기말 | 전기말 |
| 토 지 | 전남 여수시 화양면 화동리 산225-1 | 19,173 | 19,173 |
13. 유형자산
(1) 당반기와 전반기 중 유형자산 장부금액의 변동내역은 다음과 같습니다..
① 당반기
| (단위: 천원) | |||||||
|---|---|---|---|---|---|---|---|
| 구 분 | 기 초 | 취 득 | 처 분 | 감가상각비 | 환율변동효과 | 연결범위변동 | 기 말 |
| 토 지 | 6,477,381 | - | - | - | - | (697,293) | 5,780,088 |
| 건 물 | 10,570,043 | - | - | (164,554) | - | (884,543) | 9,520,946 |
| 구축물 | 230,061 | 10,000 | - | (14,649) | - | (95,676) | 129,736 |
| 기계장치 | 4,437,755 | 370,400 | (629,578) | (433,975) | - | (135,152) | 3,609,450 |
| 차량운반구 | 154,978 | 82,549 | - | (34,054) | - | (30,306) | 173,167 |
| 공기구비품 | 1,788,015 | 251,500 | (56,303) | (342,337) | 68,463 | (234,813) | 1,474,525 |
| 시설장치 | 42,661 | 64,000 | - | (50,123) | - | 64,411 | 120,949 |
| 사용권자산 | 9,470,200 | 3,406,680 | (22,737) | (1,121,959) | 890,240 | (55,580) | 12,566,844 |
| 임차자산개량권 | 167,885 | - | - | (27,099) | 5,444 | - | 146,230 |
| 건설중인자산 | 8,119,535 | 216,080 | - | - | 217 | - | 8,335,832 |
| 합 계 | 41,458,514 | 4,401,209 | (708,618) | (2,188,750) | 964,364 | (2,068,952) | 41,857,767 |
② 전반기
| (단위: 천원) | |||||||
|---|---|---|---|---|---|---|---|
| 구 분 | 기 초 | 취 득 | 처 분 | 감가상각비 | 기타증감(*) | 환율변동효과 | 기 말 |
| 토 지 | 2,769,657 | - | - | - | - | - | 2,769,657 |
| 건 물 | 4,614,599 | - | (5,738) | (103,885) | - | - | 4,504,976 |
| 구축물 | 301,785 | 10,700 | (63,584) | (17,771) | - | - | 231,130 |
| 기계장치 | 1,368,523 | 806,257 | (12,067) | (214,962) | - | - | 1,947,751 |
| 차량운반구 | 15,106 | - | (5) | - | - | - | 15,101 |
| 공기구비품 | 1,316,810 | 493,295 | (663) | (295,730) | - | 23,109 | 1,536,821 |
| 시설장치 | 57,581 | - | - | (57,297) | - | - | 284 |
| 사용권자산 | 9,269,018 | 631,605 | (36,963) | (992,882) | - | 316,248 | 9,187,026 |
| 임차자산개량권 | 155,157 | 42,991 | - | (98,134) | - | 2,909 | 102,923 |
| 건설중인자산 | 24,001 | 63,085 | - | - | (26,000) | - | 61,086 |
| 합 계 | 19,892,237 | 2,047,933 | (119,020) | (1,780,661) | (26,000) | 342,266 | 20,356,755 |
(*) 전반기 중 무형자산(소프트웨어)으로 대체하였습니다.
(2) 당반기와 전반기 중 매출원가와 판매비와관리비로 배분된 감가상각비는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 매출원가 | 730,041 | 534,815 |
| 판매비와관리비 | 1,431,945 | 1,245,846 |
| 기타 | 26,764 | - |
| 합 계 | 2,188,750 | 1,780,661 |
(3) 연결실체의 토지, 건물의 일부 및 기계장치는 연결실체의 차입금에 대한 담보로 제공되어 있으며, 당반기말 현재 담보제공금액은 384,000천원(장부금액 5,420,133천원)입니다(주석 15, 30 참조).
14. 무형자산
(1) 당반기와 전반기 중 무형자산 장부금액의 변동내역은 다음과 같습니다.
① 당반기
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 기 초 | 취 득 | 감가상각비 | 환율변동효과 | 기타 | 기 말 |
| 산업재산권 | 38,726,239 | 479,864 | (3,779,300) | 611,515 | 1,600 | 36,039,918 |
| 영업권(*1) | 62,345,749 | 550,818 | - | 3,057,282 | - | 65,953,849 |
| 기타의 무형자산(*2) | 205,080,979 | - | - | 18,578,338 | - | 223,659,317 |
| 고객관계(*3) | 30,672,570 | - | (2,174,710) | - | - | 28,497,860 |
| 회원권(*4) | 2,383,857 | 153,300 | - | - | - | 2,537,157 |
| 소프트웨어 | 137,011 | 1,140 | (21,312) | - | (14,932) | 101,907 |
| 개발비 | 189,697 | 20,909 | - | - | (210,606) | - |
| 합 계 | 339,536,102 | 1,206,031 | (5,975,322) | 22,247,135 | (223,938) | 356,790,008 |
(*1) 영업권의 경우 사업결합으로 인해 발생하였고, 매년 손상 여부를 검토하고 있습니다.
(*2) 기타의무형자산의 경우 사업결합으로 인해 발생한 진행 중인 연구개발이며, 개발이 완료한 때 상각을 시작합니다.
(*3) 고객관계의 경우 사업결합으로 인해 발생한 식별가능한 무형자산 금액입니다.
(*4) 연결실체는 회원권을 비한정내용연수를 가진 무형자산으로 분류하고 매년 손상여부를 검토하고 있습니다.
② 전반기
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 기 초 | 취 득 | 감가상각비 | 대체 | 환율변동효과 | 기 말 |
| 산업재산권 | 64,336,190 | 1,879,437 | (3,725,866) | (21,760,000) | 211,780 | 40,941,541 |
| 영업권(*1) | 30,971,352 | - | - | - | 1,195,585 | 32,166,937 |
| 기타의무형자산(*2) | 166,453,579 | 10,000 | - | 21,760,000 | 7,265,598 | 195,489,177 |
| 회원권(*3) | 1,668,457 | 204,400 | - | - | - | 1,872,857 |
| 소프트웨어(*4) | 103,721 | 49,000 | (16,983) | - | - | 135,738 |
| 개발비 | 64,391 | 55,055 | - | - | - | 119,446 |
| 합 계 | 263,597,690 | 2,197,892 | (3,742,849) | - | 8,672,963 | 270,725,696 |
(*1) 영업권의 경우 사업결합으로 인해 발생하였습니다.
(*2) 기타의무형자산의 경우 사업결합으로 인해 발생한 진행 중인 연구개발이며, 개발이 완료한 때 상각을 시작합니다.
(*3) 연결실체는 회원권을 비한정내용연수를 가진 무형자산으로 분류하고 매년 손상여부를 검토하고 있습니다.
(*4) 전반기 중 건설중인자산에서 대체된 금액입니다.
15. 차입금
(1) 당반기말과 전기말 현재 연결실체의 차입금 내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 차입처 | 이자율(%) | 당반기말 | 전기말 |
| 단기차입금: | |||
| 우리은행 | - | - | 3,721,996 |
| 하나은행 | - | - | 6,000,000 |
| 전환사채 | - | 2,135,278 | 11,494,916 |
| 신주인수권부사채 | 23,749,187 | - | |
| 소 계 | 25,884,465 | 21,216,912 | |
| 장기차입금: | |||
| 중소기업은행(*) | 1.5 | 320,000 | 320,000 |
| 우리은행 | - | - | 145,998 |
| 전환사채 | - | 19,578,662 | |
| 신주인수권부사채 | - | 64,270,570 | 46,911,860 |
| 소 계 | 84,169,232 | 47,377,858 | |
(*) 상기의 차입금과 관련하여 토지, 일부 건물 및 기계장치를 담보로 제공하고 있습니다(주석 13 참조).
(2) 당반기말과 전기말 현재 연결실체가 발행한 사채의 내역은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 발행일 | 최장 만기일 | 연이자율(%) | 당반기말 | 전기말 |
| 제33회 무기명식 전환사채 | 2019-12-18 | 2022-12-18 | - | 2,100,000 | 11,305,000 |
| 제34회 무기명식 신주인수권부사채 | 2021-10-20 | 2026-10-20 | - | 57,000,000 | 57,000,000 |
| 제35회 무기명식 신주인수권부사채 | 2022-03-30 | 2025-03-30 | - | 25,200,000 | - |
| 제36회 무기명식 전환사채 | 2022-06-02 | 2025-06-02 | - | 23,000,000 | - |
| 제37회 무기명식 신주인수권부사채 | 2022-06-02 | 2025-06-02 | - | 17,000,000 | - |
| 소 계 | 124,300,000 | 68,305,000 | |||
| 상환할증금(전환사채) | 732,132 | 189,916 | |||
| 전환권조정(전환사채) | (4,118,193) | - | |||
| 상환할증금(신주인수권) | 2,169,098 | 1,150,032 | |||
| 신주인수권조정(신주인수권) | (13,349,341) | (11,238,172) | |||
| 합 계 | 109,733,697 | 58,406,776 | |||
(3) 당반기말 현재 전환사채의 주요 발행조건은 다음과 같습니다.
| 구 분 | 내 용 | 내 용 | 내 용 | 내 용 | 내 용 |
|---|---|---|---|---|---|
| 사채의 명칭 | 제33회 무기명식 무보증 사모 전환사채 |
제34회 무기명식 무보증 사모 신주인수권 부사채 |
제35회 무기명식 무보증 사모 신주인수권 부사채 |
제36회 무기명식 무보증 사모 전환사채 |
제37회 무기명식 무보증 사모 신주인수권 부사채 |
| 권면총액 | 40,000,000천원 | 57,000,000천원 | 25,200,000천원 | 23,000,000천원 | 17,000,000천원 |
| 발행가액 | 권면금액의 100% | 권면금액의 100% | 권면금액의 100% | 권면금액의 100% | 권면금액의 100% |
| 보장수익률 | 연 1.00% | 연 1.00% | 연 2.00% | 연 3.00% | 연 3.00% |
| 유효이자율 | 연 8.71% | 연 12.717% | 연 11.303% | 연 15.355% | 연 15.355% |
| 원금상환방법 | 1. 만기일시상환 : 사채만기일에 미행사 사채권면총액에 대하여 사채원금의 103.0402% 의 금액을 일시상환함 2. 조기상환(Put Option): 발행일로부터 1년 8개월이 경과한날부터 사채권자의 조기상환청구 가능함 |
1. 만기일시상환 : 사채만기일에 미행사 사채권면총액에 대하여 사채원금의 105.1206% 의 금액을 일시상환함 2. 조기상환(Put Option): 발행일로부터 2년이 경과한날부터 사채권자의 조기상환청구 가능함 |
1. 만기일시상환 : 사채만기일에 미행사 사채권면총액에 대하여 사채원금의 106% 의 금액을 일시상환함 2. 조기상환(Put Option): 발행일로부터 1년이 경과한날부터 사채권자의 조기상환청구 가능함 3. 매도청구권(Call Option) 발행일로부터 1개월이 경과한날부터 1년이 경과한 날까지, 권면금액의 일부에 대하여 발행회사의 매도청구(조기상환 포함) 가능함 |
1. 만기일시상환 : 사채만기일까지 보유하고 있는 본사채의 원금에 대하여는 전자등록금액의 106.2426%의 금액을 일시상환함 2. 조기상환(Put Option): 발행일로부터 1년 6개월이 경과한날로부터 사채권자의 조기상환청구 가능함 3. 매도청구권(Call Option) 발행일로부터 1년이 경과한 날까지, 권면금액의 일부에 대하여 발행회사의 매도청구(조기상환 포함) 가능함 |
1. 만기일시상환 : 사채만기일까지 보유하고 있는 본사채의 원금에 대하여는 전자등록금액의 106.2426%의 금액을 일시상환함 2. 조기상환(Put Option): 발행일로부터 1년 6개월이 경과한날로부터 사채권자의 조기상환청구 가능함 3. 매도청구권(Call Option) 발행일로부터 1년이 경과한 날까지, 권면금액의 일부에 대하여 발행회사의 매도청구(조기상환 포함) 가능함 |
| 행사(전환)가액 | 33,757원(*1) | 35,884원(*2) | 30,811원 | 48,605원 | 48,605원 |
| 행사(전환)에 따라 발행할 주식의 종류 |
기명식 보통주 | 기명식 보통주 | 기명식 보통주 | 기명식 보통주 | 기명식 보통주 |
| 행사(전환청구)기간 | 2020년 12월 18일부터 2022년 11월 18일까지 |
2023년 10월 20일부터 2026년 10월 20일까지 |
2023년 03월 30일부터 2025년 02월 28일까지 |
2023년 06월 02일부터 2025년 05월 02일까지 |
2023년 06월 02일부터 2025년 05월 02일까지 |
| 신주의 배당분기산일 |
행사일이 속하는 사업연도의 개시일 |
행사일이 속하는 사업연도의 개시일 |
행사일이 속하는 사업연도의 개시일 |
행사일이 속하는 사업연도의 개시일 |
행사일이 속하는 사업연도의 개시일 |
(*1) 전기 중 무상증자 및 시가하락으로 인하여 전환가액이 조정되었으며, 조정 후 전환가액입니다.
(*2) 당반기 중 시가하락으로 인하여 전환가액이 조정되었으며, 조정 후 전환가액입니다.
(4) 당반기 중 전환사채의 전환으로 인한 주식수, 자본금 및 주식발행초과금의 증가 내역은 다음과 같습니다.
| (단위: 주, 천원) | |||
|---|---|---|---|
| 구 분 | 주식수 | 보통주자본금 | 주식발행초과금 |
| 제33회 무기명식 전환사채 | 272,681 | 136,341 | 10,278,931 |
(5) 사채 부채요소의 공정가치는 동일한 조건의 전환권이 없는 사채의 시장이자율을 적용하여 계산되었습니다. 발행가액에서 부채요소를 차감한 잔여가치는 전환권 가치에 해당하며 자본으로 계상하였습니다. 발행자 매도청구권의 공정가치는 파생상품자산으로 계상하였습니다.
(6) 행사기한이 종료되지 않은 전환권이 행사될 경우 발행될 주식수는 다음과 같습니다.
| (단위: 주, 원) | |||||
|---|---|---|---|---|---|
| 구 분 | 발행가능주식수 | 발행(소각)주식수 | 미발행주식수 | 행사가격 | 행사기간 |
| 제33회 전환사채 | 62,209 | - | 62,209 | 33,757 | 2020.12.18 ~ 2022.11.18 |
| 제34회 신주인수권부사채 | 1,588,451 | - | 1,588,451 | 35,884 | 2023.10.20 ~ 2026.10.20 |
| 제35회 신주인수권부사채 | 817,889 | - | 817,889 | 30,811 | 2023.03.30 ~ 2025.02.28 |
| 제36회 전환사채 | 473,202 | - | 473,202 | 48,605 | 2023.06.02 ~ 2025.05.02 |
| 제37회 신주인수권부사채 | 349,758 | - | 349,758 | 48,605 | 2023.06.02 ~ 2025.05.02 |
16. 기타금융부채
당반기말과 전기말 현재 기타금융부채의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
| 미지급금 | 54,275,732 | 80,202 | 57,097,839 | 45,428 |
| 미지급비용 | 29,474,247 | - | 25,693,342 | 270,031 |
| 금융리스부채 | (431,889) | 14,491,512 | 1,220,344 | 9,733,384 |
| 합 계 | 83,318,090 | 14,571,714 | 84,011,525 | 10,048,843 |
17. 리스
(1) 당반기말 및 전기말 현재 사용권자산 장부금액의 구성내역은 다음과 같습니다.
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | ||||
| 취득원가 | 상각누계액 | 장부금액 | 취득원가 | 상각누계액 | 장부금액 | |
| 토지 | 145,215 | (145,215) | - | 145,215 | (72,607) | 72,607 |
| 건물 | 16,898,159 | (4,692,610) | 12,205,549 | 12,478,905 | (3,548,294) | 8,930,611 |
| 차량운반구 | 808,618 | (447,323) | 361,295 | 903,672 | (436,886) | 466,787 |
| 공기구비품 | 7,894 | (7,894) | - | 7,238 | (7,043) | 195 |
| 합 계 | 17,859,886 | (5,293,042) | 12,566,844 | 13,535,030 | (4,064,830) | 9,470,200 |
(2) 사용권자산 장부금액의 변동내역은 다음과 같습니다.
| (단위: 천원) | |||||||
|---|---|---|---|---|---|---|---|
| 구 분 | 기초 | 취득 | 처분 | 상각 | 환율변동효과 | 연결범위변동 | 기말 |
| 토지 | 72,607 | - | - | (72,607) | - | - | - |
| 건물 | 8,930,611 | 3,305,533 | - | (899,256) | 890,231 | (21,570) | 12,205,549 |
| 차량운반구 | 466,787 | 101,147 | (22,737) | (149,892) | - | (34,010) | 361,295 |
| 공기구비품 | 195 | - | - | (204) | 9 | - | - |
| 합 계 | 9,470,200 | 3,406,680 | (22,737) | (1,121,959) | 890,240 | (55,580) | 12,566,844 |
(3) 리스부채의 변동 내역은 다음과 같습니다.
| (단위: 천원) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 구 분 | 기초 | 증가 | 감소 | 상환금액 | 이자비용 | 환율변동효과 | 기말 | 유동 | 비유동 |
| 리스부채 | 10,953,729 | 3,122,265 | (22,652) | (1,264,891) | 308,004 | 1,020,065 | 14,116,520 | (431,889) | 14,491,512 |
(4) 당반기와 전반기 중 리스와 관련하여 손익으로 인식한 금액은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 리스부채에 대한 이자비용 | (308,004) | (331,308) |
| 단기리스와 관련된 비용 | (239,106) | (209,014) |
| 소액자산 리스 중 단기리스를 제외한 리스에 관한 비용 | (16,735) | (17,014) |
| 합 계 | (563,845) | (557,336) |
(5) 당반기와 전반기 중 리스와 관련하여 현금흐름표에 인식한 금액은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 리스의 총 현금유출(이자비용 제외) | 1,264,891 | 1,160,937 |
18. 기타부채
(1) 당반기말과 전기말 현재 기타부채의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 유동 | ||
| 예수금 | 125,852 | 967,259 |
| 예수보증금 | 115,000 | 115,000 |
| 선수금 | - | 23,903 |
| 판매보증충당부채 | 138,007 | 158,604 |
| 복구충당부채(*) | 25,900 | 25,900 |
| 소 계 | 404,759 | 1,290,666 |
| 비유동 | ||
| 복구충당부채(*) | 25,000 | 25,000 |
| 소 계 | 25,000 | 25,000 |
| 합 계 | 429,759 | 1,315,666 |
(*) 임차계약상의 원상복구 의무에 따른 예상 복구비용을 충당부채로 인식하였습니 다.
(2) 당반기 및 전기 중 판매보증충당부채의 변동내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전기 |
| 기초 | 158,604 | 80,858 |
| 증가(감소) | (20,596) | 77,746 |
| 기말 | 138,007 | 158,604 |
연결실체는 판매된 제품에 대한 품질보증 등으로 인하여 향후 부담하게 될 비용을 관련 제품이 판매되는 시점에 비용으로 계상하고 있습니다.
19. 자본금과 주식발행초과금
지배기업의 정관에 의한 발행할 주식의 총수는 5억주(1주의 금액 : 500원)이며 당반기말 현재 당사가 발행한 보통주식 및 우선주식수는 각각 106,882,745주와 7,188주입니다.
| (단위: 주, 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 일 자 | 내 역 | 주식수 | 자본금 | 주식발행 초과금 | 합 계 |
| 보통주 | 전기초 | 52,979,436 | 26,489,718 | 775,815,152 | 802,304,870 | |
| 2021-01-04 | 전환사채 행사 | 4,420 | 2,210 | 376,449 | 378,659 | |
| 2021-01-05 | 전환사채 행사 | 13,262 | 6,631 | 1,129,517 | 1,136,148 | |
| 2021-01-06 | 전환사채 행사 | 9,725 | 4,863 | 828,273 | 833,135 | |
| 2021-01-07 | 전환사채 행사 | 3,094 | 1,547 | 263,514 | 265,061 | |
| 2021-01-08 | 전환사채 행사 | 3,094 | 1,547 | 263,514 | 265,061 | |
| 2021-01-15 | 전환사채 행사 | 61,891 | 30,946 | 5,271,222 | 5,302,167 | |
| 2021-01-21 | 전환사채 행사 | 442 | 221 | 37,645 | 37,866 | |
| 2021-01-25 | 전환사채 행사 | 27,408 | 13,704 | 2,334,324 | 2,348,028 | |
| 2021-03-16 | 무상증자 | 52,968,898 | 26,484,449 | (26,726,956) | (242,507) | |
| 2021-06-21 | 전환사채 행사 | 5,924 | 2,962 | 220,633 | 223,595 | |
| 2021-08-13 | 전환사채 행사 | 51,839 | 25,920 | 1,952,873 | 1,978,793 | |
| 2021-08-18 | 전환사채 행사 | 105,163 | 52,582 | 3,968,368 | 4,020,949 | |
| 2021-08-19 | 전환사채 행사 | 740 | 370 | 25,867 | 26,237 | |
| 2021-08-23 | 전환사채 행사 | 79,982 | 39,991 | 3,016,196 | 3,056,187 | |
| 2021-08-25 | 전환사채 행사 | 10,368 | 5,184 | 389,510 | 394,694 | |
| 2021-08-26 | 전환사채 행사 | 13,329 | 6,665 | 500,823 | 507,488 | |
| 2021-08-27 | 전환사채 행사 | 247,351 | 123,676 | 9,329,601 | 9,453,277 | |
| 2021-08-30 | 전환사채 행사 | 8,887 | 4,444 | 334,694 | 339,138 | |
| 2021-09-02 | 전환사채 행사 | 14,811 | 7,406 | 554,450 | 561,855 | |
| 전기말 | 106,610,064 | 53,305,032 | 779,885,671 | 833,190,703 | ||
| 2022-03-30 | 자본준비금의 이익잉여금 전입 | - | - | (130,000,000) | (130,000,000) | |
| 2022-05-16 | 전환사채 행사 | 41,472 | 20,736 | 1,563,321 | 1,584,057 | |
| 2022-05-17 | 전환사채 행사 | 20,736 | 10,368 | 781,660 | 792,028 | |
| 2022-05-19 | 전환사채 행사 | 10,368 | 5,184 | 390,830 | 396,014 | |
| 2022-05-25 | 전환사채 행사 | 155,523 | 77,762 | 5,862,565 | 5,940,327 | |
| 2022-05-26 | 전환사채 행사 | 41,472 | 20,736 | 1,563,321 | 1,584,057 | |
| 2022-06-15 | 전환사채 행사 | 3,110 | 1,555 | 117,234 | 118,789 | |
| 당반기말 | 106,882,745 | 53,441,373 | 660,164,601 | 713,605,974 | ||
| 우선주 | 전기초 | 3,657 | 1,829 | (167) | 1,661 | |
| 2021-03-16 | 무상증자 | 3,531 | 1,766 | (1,782) | (16) | |
| 전기말 | 7,188 | 3,594 | (1,949) | 1,645 | ||
| 당반기말 | 7,188 | 3,594 | (1,949) | 1,645 | ||
지배기업은 이사회에서 정한 우선비율(액면금액 기준 연 1% 이상)에 따른 금전배당을 받을 수 있는 누적적 참가적 무의결권 우선주식을 포함하는 종류주식을 발행주식총수의 2분의 1 범위 내에서 발행할 수 있도록 되어 있으며, 보통주식 또는 우선주식으로 전환할 수 있는 전환사채와 보통주식 또는 우선주식의 신주인수권을 부여하는 신주인수권부사채를 각각 2,000억원 범위 내에서 주주 이외의 자에게 발행할 수 있도록 하고 있습니다. 또한 당사는 주주총회의 특별결의로 발행주식총수의 100분의 15 범위 내에서 임직원에게 주식선택권을 부여할 수 있도록 되어 있습니다. 단, 발행주식총수의 100분의 3 범위 내에서는 이사회의 결의로 주식선택권을 부여할 수 있도록 되어 있습니다.
지배기업은 주주에게 배당할 이익으로 발행주식총수의 100분의 10 범위내에서 관계법령이 정하는 바에 따라 이사회 결의로 당사의 주식을 소각할 수 있도록 하고 있습니다.
지배기업은 2021년 3월 16일 보통주 및 우선주 1주당 1주를 지급하는 무상증자를 시행하였습니다.
20. 기타자본항목
(1) 당반기말과 전기말 현재 기타자본항목의 세부 구성내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 전환권대가 | 6,226,232 | 1,309,826 |
| 기타자본잉여금 | 22,651,147 | 16,909,929 |
| 자기주식 | (4,120,279) | (4,120,279) |
| 자기주식처분이익 | 5,086,818 | 5,086,818 |
| 기타자본조정 | (247,416,383) | (247,429,961) |
| 주식선택권 | 117,796 | - |
| 지분법자본변동 | 11,440,439 | 8,636,077 |
| 기타포괄손익-공정가치 측정 금융자산 평가손익 | (632,887) | (352,669) |
| 해외사업환산손익 | 17,309,510 | 5,747,309 |
| 합 계 | (189,337,607) | (214,212,950) |
(2) 자기주식
연결실체는 당반기말 현재 보통주 133,874주와 우선주 126주를 자기주식으로 계상하고 있으며, 향후 시장상황에 따라 처분할 예정입니다.
(3) 주식기준보상
종속기업인 Elevar Therapeutics, Inc.과 Immunomic Therapeutics, Inc.는 종속기업의 임직원에게 각각 Elevar Therapeutics, Inc.과 Immunomic Therapeutics, Inc.의 주식에 대하여 주식선택권을 부여하였으며, 당반기말 현재 연결실체가 보유하고 있는 주식기준 보상약정은 다음과 같습니다.
| 구 분 | 부여일 | 부여수량(주) | 행사수량(주) | 행사가격 | 만기일 | 가득조건 |
|---|---|---|---|---|---|---|
| Elevar Therapeutics, Inc. | 2015년 1분기 | 1,508,748 | 489,039 | USD 3.38 | 2025년 | 7년간 |
| 2016년 1분기 | 119,742 | - | USD 3.38 | 2026년 | 즉시 | |
| 2016년 3분기 | 941,175 | 564,705 | USD 7.47 | 2026년 | 1년간 | |
| 2018년 3분기 | 315,884 | 56,036 | USD 7.47 | 2028년 | 5년간 | |
| 2018년 4분기 | 898,068 | - | USD 7.47 | 2028년 | 5년간 | |
| 2019년 1분기 | 275,410 | - | USD 10.20, USD 10.00 | 2029년 | 5년간 | |
| 2019년 3분기 | 526,870 | - | USD 10.00 | 2029년 | 5년간 | |
| 2020년 3분기 | 3,302,500 | - | USD 10.00 | 2030년 | NDA제출, NDA제출및승인 | |
| 2020년 4분기 | 507,500 | - | USD 10.00 | 2030년 | NDA제출, NDA제출및승인 | |
| 2021년 1분기 | 242,500 | - | USD 10.00 | 2031년 | NDA제출, NDA제출및승인 | |
| 2021년 2분기 | 319,500 | - | USD 10.00 | 2031년 | NDA제출, NDA제출및승인 | |
| 2021년 3분기 | 522,000 | - | USD 10.00 | 2031년 | NDA제출, NDA제출및승인 | |
| 2021년 4분기 | 113,000 | - | USD 10.00 | 2031년 | NDA제출, NDA제출및승인 | |
| 2022년 1분기 | 408,000 | - | USD 10.00 | 2032년 | NDA제출, NDA제출및승인 | |
| 2022년 2분기 | 347,000 | - | USD 10.00 | 2032년 | NDA제출, NDA제출및승인 | |
| Immunomic Therapeutics, Inc. | 2014년 이전 | 1,333,000 | 1,085,500 | $0.10-$2.20 | 2016년 이후 | - |
| 2014년 1월 24일 | 90,000 | - | USD 2.20 | 2024년 1월 24일 | 즉시 | |
| 2014년 1월 24일 | 50,000 | 26,389 | USD 2.20 | 2024년 1월 24일 | 1년간 | |
| 2014년 3월 1일 | 5,000 | 5,000 | USD 2.20 | 2024년 3월 1일 | 1년간 | |
| 2014년 4월 24일 | 46,500 | 2,500 | USD 2.20 | 2024년 4월 24일 | 1년간 | |
| 2014년 5월 30일 | 220,000 | - | USD 2.20 | 2024년 5월 30일 | 즉시 | |
| 2015년 1월 1일 | 20,000 | 7,500 | USD 1.83 | 2025년 1월 1일 | 1년간 | |
| 2015년 1월 1일 | 10,000 | 10,000 | USD 1.33 | 2025년 1월 1일 | 즉시 | |
| 2015년 1월 1일 | 5,000 | 5,000 | USD 2.20 | 2025년 1월 1일 | 즉시 | |
| 2015년 1월 25일 | 100,000 | - | USD 2.20 | 2025년 1월 25일 | 즉시 | |
| 2015년 2월 24일 | 346,500 | 190,000 | USD 2.20 | 2025년 2월 24일 | 즉시 | |
| 2015년 2월 24일 | 560,000 | 50,000 | USD 2.20 | 2025년 2월 24일 | 즉시 | |
| 2015년 2월 24일 | 200,000 | - | USD 2.20 | 2025년 2월 24일 | 1년간 | |
| 2015년 3월 30일 | 5,000 | 5,000 | USD 2.20 | 2025년 1월 1일 | 즉시 | |
| 2015년 4월 1일 | 5,000 | - | USD 2.20 | 2025년 4월 1일 | 1년간 | |
| 2015년 5월 1일 | 5,000 | 3,750 | USD 2.20 | 2025년 5월 1일 | 1년간 | |
| 2015년 5월 5일 | 175,000 | 15,000 | USD 2.20 | 2025년 5월 5일 | 1년간 | |
| 2015년 5월 28일 | 170,000 | - | USD 3.20 | 2025년 5월 28일 | 기타 | |
| 2015년 8월 5일 | 75,000 | 75,000 | USD 3.20 | 2025년 8월 5일 | 즉시 | |
| 2015년 12월 21일 | 150,000 | - | USD 5.37 | 2025년 12월 21일 | 1년간 | |
| 2016년 2월 1일 | 125,168 | 4,168 | USD 5.37 | 2026년 2월 1일 | 1년간 | |
| 2016년 2월 1일 | 4,000 | - | USD 5.37 | 2026년 2월 1일 | 1년간 | |
| 2016년 2월 1일 | 9,500 | - | USD 5.37 | 2026년 2월 1일 | 즉시 | |
| 2016년 3월 3일 | 10,000 | - | USD 5.37 | 2026년 3월 3일 | 즉시 | |
| 2016년 12월 1일 | 26,279 | 2,779 | USD 5.47 | 2026년 12월 1일 | 1년간 | |
| 2016년 12월 1일 | - | - | USD 5.47 | 2026년 12월 1일 | 1년간 | |
| 2017년 5월 3일 | 25,000 | - | USD 5.47 | 2027년 5월 3일 | 1년간 | |
| 2017년 5월 17일 | 11,500 | - | USD 5.47 | 2027년 5월 17일 | 즉시 | |
| 2017년 6월 13일 | 66,000 | - | USD 5.55 | 2027년 6월 13일 | 기타 | |
| 2018년 2월 1일 | 87,500 | - | USD 6.29 | 2028년 2월 1일 | 1년간 | |
| 2018년 4월 19일 | 30,000 | 3,000 | USD 6.29 | 2028년 4월 19일 | 1년간 | |
| 2018년 5월 3일 | 25,000 | - | USD 6.29 | 2028년 5월 3일 | 1년간 | |
| 2018년 6월 12일 | 63,000 | - | USD 6.29 | 2028년 6월 12일 | 기타 | |
| 2019년 2월 14일 | 265,000 | - | USD 5.24 | 2029년 2월 14일 | 1년간 | |
| 2019년 4월 1일 | 37,916 | 6,416 | USD 5.24 | 2029년 4월 1일 | 1년간 | |
| 2019년 5월 1일 | 5,000 | - | USD 5.24 | 2029년 5월 1일 | 2년간 | |
| 2019년 5월 3일 | 25,000 | - | USD 5.24 | 2029년 5월 3일 | 2년간 | |
| 2019년 5월 15일 | 25,000 | - | USD 5.24 | 2029년 5월 15일 | 2년간 | |
| 2019년 6월 11일 | 38,000 | - | USD 5.24 | 2029년 6월 11일 | 기타 | |
| 2019년 7월 1일 | - | - | USD 5.24 | 2029년 7월 1일 | 1년간 | |
| 2020년 4월 1일 | 212,250 | 3,750 | USD 3.90 | 2030년 4월 1일 | 1년간 | |
| 2020년 4월 13일 | 800,000 | - | USD 3.90 | 2030년 4월 13일 | 3년간 | |
| 2020년 4월 13일 | 300,000 | - | USD 3.90 | 2030년 4월 13일 | 2년간 | |
| 2020년 9월 11일 | 75,000 | - | USD 5.00 | 2030년 9월 11일 | 기타 | |
| 2020년 11월 1일 | 22,000 | - | USD 5.00 | 2030년 11월 1일 | 1년간 | |
| 2021년 4월 1일 | 53,000 | - | USD 4.53 | 2031년 4월 1일 | 1년간 | |
| 2021년 6월 22일 | 42,000 | - | USD 4.53 | 2031년 6월 22일 | 1년간 | |
| 2021년 6월 22일 | 70,000 | - | USD 4.53 | 2031년 6월 22일 | 기타 | |
| 2021년 7월 19일 | 300,000 | - | USD 4.53 | 2031년 7월 19일 | 1년간 | |
| 2021년 9월 21일 | 18,000 | - | USD 4.53 | 2031년 9월 21일 | 1년간 | |
| 2022년 3월 14일 | 270,000 | USD 4.57 | 2023년 3월 13일 | 1년간 | ||
| 2022년 4월 5일 | 170,500 | USD 4.57 | 2032년 4월 4일 | 1년간 | ||
| 2022년 6월 21일 | 70,000 | USD 4.57 | 2032년 6월 20일 | 기타 | ||
| 2022년 6월 21일 | 200,000 | USD 4.57 | 2032년 6월 20일 | 1년간 |
한편, 가득조건이 없는 주식기준보상의 경우 부여일에 가득조건이 완료된 것으로 보아 보상원가 전부를 인식하였습니다.
향후 인식될 보상원가의 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 기인식 보상원가 | 당기인식 보상원가 |
향후 인식될 보상원가 |
합 계 |
| Elevar Therapeutics, Inc. | 10,369,046 | 222,139 | 1,614,574 | 12,205,759 |
| Immunomic Therapeutics, Inc. | 15,974,501 | 1,291,253 | 4,391,273 | 21,657,027 |
| 합 계 | 26,343,547 | 1,513,392 | 6,005,847 | 33,862,786 |
21. 주당손익
(1) 당반기 및 전반기의 기본주당손익의 계산내역은 다음과 같습니다.
① 기본주당손익(손실)
| (단위: 주, 원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 지배지분 순이익(손실) | 6,282,902,369 | (9,472,168,271) | (31,912,974,620) | (50,322,030,612) |
| 가중평균유통보통주식수 | 106,592,495 | 106,534,664 | 106,072,321 | 106,034,152 |
| 기본주당이익(손실) | 59 | (89) | (301) | (475) |
(*) 2021년 3월 16일 시행한 무상증자효과를 소급조정하여 비교표시 하였습니다.
② 가중평균유통보통주식수의 산정
| (단위: 주) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 기초 발행보통주식수 | 106,610,064 | 106,610,064 | 53,102,772 | 52,979,436 |
| 무상증자 조정(*1) | - | - | 53,102,772 | 52,979,436 |
| 수정 기초 발행보통주식수 | 106,610,064 | 106,610,064 | 106,205,544 | 105,958,872 |
| 전환권 행사(*2) | 116,306 | 58,474 | 651 | 228,345 |
| 자기주식 | (133,874) | (133,874) | (133,874) | (133,874) |
| 가중평균유통보통주식수 | 106,592,496 | 106,534,664 | 106,072,321 | 106,053,343 |
(*1) 2021년 3월 16일에 시행한 무상증자에 대한 조정으로, 100%의 무상증자 비율을 적용하였습니다.
(*2) 당반기 중 전환사채의 전환권 행사로 발행된 신주에 대한 가중평균 유통보통주식수의 계산내역은 다음과 같습니다.
① 당반기
| (단위: 주) | |||||
|---|---|---|---|---|---|
| 일자 | 조정 전 | 주식수 | 유통일수(일) | 적 수 | 가중평균 유통주식수 |
| 2022년 05월 16일 | 41,472 | 41,472 | 46 | 1,907,712 | 10,540 |
| 2022년 05월 17일 | 20,736 | 20,736 | 45 | 933,120 | 5,155 |
| 2022년 05월 19일 | 10,368 | 10,368 | 43 | 445,824 | 2,463 |
| 2022년 05월 25일 | 155,523 | 155,523 | 37 | 5,754,351 | 31,792 |
| 2022년 05월 26일 | 41,472 | 41,472 | 36 | 1,492,992 | 8,249 |
| 2022년 06월 15일 | 3,110 | 3,110 | 16 | 49,760 | 275 |
| 합 계 | 272,681 | 272,681 | 10,583,759 | 58,474 | |
② 전반기
| (단위: 주) | ||||||
|---|---|---|---|---|---|---|
| 일자 | 조정 전 | 무상증자 조정 (2021/3/16 100%) |
조정 후 | 유통일수(일) | 적 수 | 가중평균 유통주식수 |
| 2021년 01월 04일 | 4,420 | 4,420 | 8,840 | 178 | 1,573,520 | 8,693 |
| 2021년 01월 05일 | 13,262 | 13,262 | 26,524 | 177 | 4,694,748 | 25,938 |
| 2021년 01월 06일 | 9,725 | 9,725 | 19,450 | 176 | 3,423,200 | 18,913 |
| 2021년 01월 07일 | 3,094 | 3,094 | 6,188 | 175 | 1,082,900 | 5,983 |
| 2021년 01월 08일 | 3,094 | 3,094 | 6,188 | 174 | 1,076,712 | 5,949 |
| 2021년 01월 15일 | 61,891 | 61,891 | 123,782 | 167 | 20,671,594 | 114,208 |
| 2021년 01월 21일 | 442 | 442 | 884 | 161 | 142,324 | 786 |
| 2021년 01월 25일 | 27,408 | 27,408 | 54,816 | 157 | 8,606,112 | 47,548 |
| 2021년 06월 21일 | 5,924 | - | 5,924 | 10 | 59,240 | 327 |
| 합 계 | 129,260 | 123,336 | 252,596 | 41,330,350 | 228,345 | |
(2) 희석주당이익
당사의 당반기 및 전기 희석화증권의 희석화 효과가 존재하지 않아 희석주당손실은 기본주당손실과 동일합니다.
(3) 희석성 잠재적 보통주
희석효과가 없어 희석주당손익의 계산에 고려되지 않은 잠재적 보통주의 내역은 다음과 같습니다.
| 구 분 | 액면금액(천원) | 청구기간 | 발행될 주식수(주) | 전환조건 |
|---|---|---|---|---|
| 제33회 전환사채 | 2,100,000 | 2020-12-18 ~ 2022-11-18 | 62,209 | 행사가액 33,757원 |
| 제34회 신주인수권부사채 | 57,000,000 | 2023-10-20 ~ 2026-10-20 | 1,588,451 | 행사가액 35,884원 |
| 제35회 신주인수권부사채 | 25,200,000 | 2023-03-30 ~ 2025-02-28 | 817,889 | 행사가액 30,811원 |
| 제36회 전환사채 | 23,000,000 | 2023-06-02 ~ 2025-05-02 | 473,202 | 행사가액 48,605원 |
| 제37회 신주인수권부사채 | 17,000,000 | 2023-06-02 ~ 2025-05-02 | 349,758 | 행사가액 48,605원 |
22. 성격별 비용
당반기와 전반기 중 발생한 비용의 성격별 분류에 대한 정보는 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 재고자산의 변동 | (3,134,207) | (4,714,021) | (2,447,560) | (1,878,335) |
| 원재료 및 상품매입액 | 20,315,435 | 45,335,654 | 5,601,126 | 10,143,885 |
| 급여 | 14,731,659 | 26,988,405 | 8,319,806 | 12,101,600 |
| 퇴직급여 | 188,758 | 407,245 | 372,040 | 647,459 |
| 복리후생비 | 1,270,508 | 2,592,391 | 561,223 | 1,008,618 |
| 여비교통비 | 461,848 | 754,143 | 81,179 | 126,755 |
| 접대비 | 97,190 | 210,131 | 85,979 | 145,042 |
| 통신비 | 105,284 | 195,121 | 59,974 | 94,357 |
| 수도광열비 | 8,195 | 26,499 | 6,010 | 11,341 |
| 전력비 | 110,135 | 269,227 | 114,014 | 252,404 |
| 세금과공과금 | 678,412 | 1,543,504 | 360,962 | 739,733 |
| 감가상각비 | 1,075,138 | 2,188,750 | 899,032 | 1,780,661 |
| 지급임차료 | 229,201 | 442,098 | 132,828 | 259,219 |
| 보험료 | 182,964 | 409,270 | 381,993 | 725,410 |
| 차량유지비 | 42,816 | 78,615 | 38,216 | 68,588 |
| 운반비 | 431,871 | 843,523 | 181,374 | 307,246 |
| 도서인쇄비 | 12,742 | 26,854 | 18,211 | 32,066 |
| 소모품비 | 796,930 | 1,575,244 | 460,105 | 839,150 |
| 지급수수료 | 4,459,854 | 9,504,148 | 6,616,658 | 16,740,467 |
| 건물관리비 | 192,851 | 267,600 | 120,809 | 254,964 |
| 대손상각비(환입) | 69,604 | 22,941 | 708,964 | 705,714 |
| 무형자산상각비 | 2,989,000 | 5,975,322 | 3,906,767 | 3,967,447 |
| 외주용역비 | 12,138,095 | 23,369,740 | 1,455,974 | 2,622,485 |
| 판매보증비 | (12,248) | (20,596) | 593,401 | 626,469 |
| 기타비용 | 13,947,895 | 25,108,727 | 757,231 | 3,390,996 |
| 합 계 (*) | 71,389,930 | 143,400,535 | 29,386,316 | 55,713,741 |
(*) 연결포괄손익계산서의 매출원가와 판매비와관리비를 합산한 금액입니다.
23. 매출액
(1) 당반기와 전반기 중 매출액의 내역은 다음과 같습니다.
| (단위:천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 주요 지리적 시장: | ||||
| 국내 | 29,682,574 | 87,546,483 | 5,194,607 | 10,238,416 |
| 해외 | 28,109,359 | 35,758,234 | 3,198,433 | 5,718,408 |
| 합 계 | 57,791,933 | 123,304,717 | 8,393,040 | 15,956,824 |
| 수익 원천: | ||||
| 제품매출 | 51,647,938 | 111,008,282 | 7,003,995 | 13,468,212 |
| 수수료매출 | 4,150,989 | 4,374,217 | 213,163 | 446,836 |
| 상품매출 | 1,771,602 | 7,400,514 | 1,085,361 | 1,783,859 |
| 기타매출 | 221,404 | 521,704 | 90,521 | 257,917 |
| 합 계 | 57,791,933 | 123,304,717 | 8,393,040 | 15,956,824 |
| 수익인식 시기 | ||||
| 한 시점에 이행 | 53,625,882 | 118,854,838 | 8,302,519 | 15,804,804 |
| 기간에 걸쳐 이행 | 4,166,051 | 4,449,879 | 90,521 | 152,021 |
| 합 계 | 57,791,933 | 123,304,717 | 8,393,040 | 15,956,825 |
(2) 당반기 중 연결실체의 매출액의 10% 이상을 차지하는 2곳의 외부고객으로부터 발생한 매출액은 각각 59,295,775천원, 26,009,934천원 입니다.
(3) 당반기말과 전기말 현재 고객과의 계약에서 생기는 계약자산은 없으며, 계약부채내역은 다음과 같습니다.
| (단위:천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 계약부채 | 1,734,287 | 563,168 |
계약부채는 고객과의 계약과 관련하여 고객으로부터 선수취한 금액입니다.
24. 종업원급여
(1) 연결실체는 확정급여형퇴직금제도와 확정기여형퇴직연금제도를 운영하고 있습니다.
(2) 확정급여채무의 변동내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 기 초 | 1,275,146 | 521,826 |
| 당기근무원가 | 167,156 | 85,177 |
| 이자비용 | 14,734 | 5,829 |
| 퇴직금지급액 | (120,221) | (34,052) |
| 연결범위의 변동 | (595,267) | - |
| 기 말 | 741,548 | 578,780 |
(3) 당기손익으로 인식된 비용은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 당반기 | 3개월 | 전반기 | |
| 확정급여제도: | ||||
| 당기근무원가 | 70,096 | 167,156 | 42,589 | 85,177 |
| 순이자원가 | (10,209) | 4,186 | 3,837 | 5,829 |
| 소 계 | 59,887 | 171,342 | 46,426 | 91,006 |
| 확정기여제도: | ||||
| 당기비용인식 기여금 | 128,871 | 235,903 | 325,614 | 556,453 |
| 합 계 | 188,758 | 407,245 | 372,040 | 647,459 |
(4) 사외적립자산의 공정가치 변동내역은 다음과 같습니다.
| (단위: 천원) | ||
| 구 분 | 당반기 | 전반기 |
| 기 초 | 1,336,717 | 277,093 |
| 연결범위의 변동 | (236,157) | |
| 이자수익 | 10,548 | 2,735 |
| 당기기여금불입액 | 43,407 | 22,929 |
| 퇴직금지급액 | (141,840) | (25,817) |
| 기 말 | 1,012,675 | 276,940 |
25. 판매비와관리비
당반기와 전반기의 판매비와관리비의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 급 여 | 13,510,528 | 24,298,970 | 5,194,372 | 10,617,336 |
| 퇴직급여 | 106,119 | 263,166 | 344,113 | 577,110 |
| 복리후생비 | 1,001,468 | 2,116,864 | 445,426 | 795,083 |
| 여비교통비 | 438,843 | 719,173 | 64,397 | 101,287 |
| 접대비 | 96,860 | 209,688 | 76,284 | 145,203 |
| 통신비 | 102,948 | 190,158 | 56,126 | 89,070 |
| 전력비 | 9,853 | 22,675 | 13,370 | 34,871 |
| 세금과공과금 | 635,204 | 1,468,088 | 340,114 | 701,121 |
| 감가상각비 | 738,363 | 1,431,945 | 623,399 | 1,245,846 |
| 지급임차료 | 161,659 | 302,421 | 102,996 | 213,054 |
| 보험료 | 117,470 | 263,063 | 345,275 | 661,156 |
| 차량유지비 | 32,113 | 58,854 | 30,571 | 55,545 |
| 경상연구개발비 | 13,881,713 | 22,603,209 | 5,017,046 | 10,566,047 |
| 소모품비 | 258,954 | 573,777 | 30,916 | 70,131 |
| 지급수수료 | 3,265,324 | 7,176,767 | 2,829,343 | 5,977,669 |
| 광고선전비 | 99,418 | 141,468 | 94,459 | 183,668 |
| 건물관리비 | 192,851 | 267,600 | 120,809 | 254,964 |
| 대손상각비(환입) | 69,604 | 22,941 | 708,964 | 705,714 |
| 무형자산상각비 | 2,989,000 | 5,975,322 | 3,906,767 | 3,967,447 |
| 주식보상비용 | (334,085) | 1,513,762 | 392,304 | 2,950,424 |
| 판매보증비(환입) | (12,248) | (20,596) | 12,569 | 45,637 |
| 기타 | 180,884 | 457,966 | 161,270 | 316,601 |
| 합 계 | 37,542,843 | 70,057,281 | 20,910,890 | 40,274,984 |
26. 기타수익 및 기타비용
(1) 당반기 및 전반기 중 기타수익의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 수입임대료 | 28,772 | 55,745 | 24,853 | 55,515 |
| 외화환산이익 | - | - | 174,713 | 372,722 |
| 유형자산처분이익 | 60 | 21,419 | - | - |
| 대손충당금환입 | 1,497 | 1,497 | - | - |
| 투자자산처분이익 | 260 | 260 | - | 289,273 |
| 보험차익 | 382,866 | 382,866 | 1,633,036 | 1,633,036 |
| 국고보조금수익 | 2,352 | 2,352 | - | - |
| 잡이익 | (20,908) | 56,894 | 636,467 | 735,818 |
| 합 계 | 394,899 | 521,033 | 2,469,069 | 3,086,364 |
(2) 당반기 및 전반기 중 기타비용의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 기부금 | 126,351 | 145,642 | 67,780 | 98,416 |
| 기타의대손상각비 | (914) | - | - | - |
| 외환차손 | - | - | (995) | - |
| 외화환산손실 | - | - | 2,947 | 2,947 |
| 유형자산처분손실 | 1,583 | 1,583 | - | - |
| 유형자산폐기손실 | - | - | - | 59 |
| 투자부동산상각비 | - | - | - | 8,175 |
| 재해손실 | - | - | 1,571,200 | 2,164,512 |
| 재고자산감모손실 | (2,367) | (2,075) | 14,437 | 14,437 |
| 잡손실 | (6,966) | 71,135 | (155,732) | 4,281 |
| 합 계 | 117,687 | 216,285 | 1,499,637 | 2,292,827 |
(*)전반기 중 화재 피해로 인하여 재고자산 및 공장 일부가 소실되었습니다.
27. 금융수익 및 금융비용
(1) 당반기 및 전반기 중 금융수익의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 이자수익 | 184,004 | 398,538 | 360,849 | 698,125 |
| 외환차익 | 420,675 | 873,083 | 35,961 | 82,171 |
| 외화환산이익 | 855,838 | 1,020,290 | (3,948) | - |
| 매도가능금융자산처분이익 | (260) | - | - | - |
| 당기손익-공정가치측정 금융자산평가이익 | 7,432,804 | 7,435,741 | 536 | 162,905 |
| 통화선물거래이익 | 10,500 | 10,500 | - | - |
| 보증충당부채환입액 | - | - | 82,480 | 82,481 |
| 합 계 | 8,903,561 | 9,738,152 | 475,878 | 1,025,682 |
(2) 당반기 및 전반기 중 금융비용의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 이자비용 | 2,679,277 | 4,325,320 | 831,403 | 1,699,094 |
| 외환차손 | 172,932 | 282,375 | 83,137 | 101,806 |
| 외화환산손실 | (200,174) | 8,022 | - | - |
| 당기손익-공정가치측정 금융자산평가손실 | (3,931,987) | 174,621 | 11,374,517 | 11,377,192 |
| 통화선물거래손실 | 9,600 | 9,600 | - | - |
| 매출채권처분손실 | - | - | 799 | 825 |
| 합 계 | (1,270,352) | 4,799,938 | 12,289,856 | 13,178,917 |
28. 법인세비용
당반기 및 전반기 중 연결실체의 법인세비용 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 법인세부담액 | 7,416,853 | - |
| 이연법인세의 증감 | (478,764) | - |
| 법인세비용 | 6,938,089 | - |
29. 금융상품
(1) 금융상품의 범주별 분류
당반기말과 전기말 현재 범주별 금융상품의 장부금액은 다음과 같습니다.
① 당반기말
| (단위:천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 당기손익-공정가치측정 금융자산 | 기타포괄손익-공정가치측정 금융자산 | 상각후원가측정금융자산 | 상각후원가측정금융부채 | 합 계 |
| 현금및현금성자산 | - | - | 80,483,163 | - | 80,483,163 |
| 매출채권 및 기타금융자산 | - | - | 48,629,109 | - | 48,629,109 |
| 지분상품 | 1,410 | 5,793,068 | - | - | 5,794,478 |
| 복합금융상품 | 45,742,137 | - | - | - | 45,742,137 |
| 파생상품(*) | 7,113,529 | - | - | - | 7,113,529 |
| 채무상품 | 1,576,605 | - | - | - | 1,576,605 |
| 금융자산 합계 | 54,433,681 | 5,793,068 | 129,112,272 | - | 189,339,021 |
| 매입채무 | - | - | - | 4,600,685 | 4,600,685 |
| 기타금융부채 | - | - | - | 97,889,804 | 97,889,804 |
| 금융보증부채 | - | - | - | 62,156 | 62,156 |
| 차입금 | - | - | - | 110,053,697 | 110,053,697 |
| 금융부채 합계 | - | - | - | 212,606,342 | 212,606,342 |
(*) 복합금융상품의 내재파생상품(매도청구권)입니다. (주석7 참조)
② 전기말
| (단위:천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 당기손익-공정가치측정 금융자산 | 기타포괄손익-공정가치측정 금융자산 | 상각후원가측정 금융자산 |
상각후원가측정 금융부채 |
합 계 |
| 현금및현금성자산 | - | - | 99,796,601 | - | 99,796,601 |
| 매출채권 및 기타금융자산 | - | - | 71,987,332 | - | 71,987,332 |
| 지분상품 | 1,410 | 6,073,286 | - | - | 6,074,696 |
| 채무상품 | 23,549,842 | - | - | - | 23,549,842 |
| 금융자산 합계 | 23,551,252 | 6,073,286 | 171,783,933 | - | 201,408,471 |
| 매입채무 | - | - | - | 5,084,230 | 5,084,230 |
| 기타금융부채 | - | - | - | 94,060,368 | 94,060,368 |
| 금융보증부채 | - | - | - | 56,500 | 56,500 |
| 차입금 | - | - | - | 68,594,770 | 68,594,770 |
| 금융부채 합계 | - | - | - | 167,795,868 | 167,795,868 |
(2) 당반기와 전반기의 금융상품 범주별 금융수익과 금융비용의 상세내역은 다음과 같습니다.
① 당반기
| (단위: 천원) | ||||||||
| 구 분 | 이자수익/비용 | 기타금융수익/비용 | 순손익 | 기타포괄손익 | ||||
| 3개월 | 누적 | 3개월 | 누적 | 3개월 | 누적 | 3개월 | 누적 | |
| 기타포괄손익-공정가치 측정 금융상품 | - | - | - | - | - | - | (358,056) | (280,218) |
| 당기손익-공정가치 측정 채무상품 | - | - | 11,364,531 | 7,261,120 | 11,364,531 | 7,261,120 | - | - |
| 상각후원가측정금융자산(*) | 184,005 | 398,538 | 1,265,632 | 1,603,876 | 1,449,637 | 2,002,414 | - | - |
| 상각후원가측정금융부채 | (2,679,277) | (4,325,320) | - | - | (2,679,277) | (4,325,320) | - | - |
| 합 계 | (2,495,272) | (3,926,782) | 12,630,163 | 8,864,996 | 10,134,891 | 4,938,214 | (358,056) | (280,218) |
(*) 상각후원가측정금융자산에서 인식한 대손상각비 및 기타의 대손상각비는 판매비와 관리비 및 기타손익으로 분류되어 있으며 상기의 표에는 포함되어 있지 않습니다.(주석 25, 26 참조)
② 전반기
| (단위: 천원) | ||||||||
| 구 분 | 이자수익/비용 | 기타금융수익/비용 | 순손익 | 기타포괄손익 | ||||
| 3개월 | 누적 | 3개월 | 누적 | 3개월 | 누적 | 3개월 | 누적 | |
| 기타포괄손익-공정가치 측정 지분상품 | - | - | - | - | - | - | 1,467,248 | 1,155,458 |
| 당기손익-공정가치 측정 채무상품 | - | - | (11,373,981) | (11,214,287) | (11,373,981) | (11,214,287) | - | - |
| 상각후원가측정금융자산(*) | 360,849 | 698,125 | (51,923) | (20,460) | 308,926 | 677,665 | - | - |
| 상각후원가측정금융부채 | (831,403) | (1,699,094) | 82,479 | 82,479 | (748,924) | (1,616,615) | - | - |
| 합 계 | (470,554) | (1,000,969) | (11,343,425) | (11,152,268) | (11,813,979) | (12,153,237) | 1,467,248 | 1,155,458 |
(*) 상각후원가측정금융자산에서 인식한 대손상각비 및 기타의 대손상각비는 판매비와 관리비 및 기타손익으로 분류되어 있으며 상기의 표에는 포함되어 있지 않습니다.(주석 25, 26 참조)
30. 우발부채와 약정사항
(1) 당반기말 현재 연결실체와 금융기관 등과의 대출약정 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 차입종별 | 약정금액 | 차입금액 | 담보제공금액 |
| 중소기업은행(*1) | 일반운전자금대출 등 | 320,000 | 320,000 | 384,000 |
(*1) 연결실체는 중소기업은행에 대하여 토지, 건물, 기계장치를 담보로 제공하고 있습니다.
(2) 당반기말 현재 연결실체가 제3자로부터 제공받은 지급보증의 내역은 다음과 같습니다.
| (단위 : 천원) | |||
|---|---|---|---|
| 제공자 | 제공처 | 보증금액 | 비고 |
| 서울보증보험 | 매출처 등 | 1,457,711 | 하자이행보증, 지급보증 등 |
(3) 연결실체가 타인에게 제공한 지급보증의 내역은 다음과 같습니다.
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 특수관계구분 | 특수관계자명 | 보증처 | 내용 | 지급보증금액 | 연대보증인 | 보증기간 |
| 관계기업 | 현대요트㈜ | 서울보증보험 | 워터제트 | 44,275 | - | 2018-06-23 ~ 2023-06-22 |
| 선급이행 | 1,166,593 | - | 2022-04-20 ~ 2023-02-15 | |||
| 선급이행 | 191,111 | - | 2021-12-17 ~ 2022-12-17 | |||
| 선급이행 | 280,566 | - | 2020-07-29 ~ 2022-09-29 | |||
| 합 계 | 1,682,545 | |||||
31. 특수관계자
(1) 연결실체의 특수관계자는 관계기업 및 종속기업과 지배기업의 주요 경영진, 그리고 경영진이 출자 또는 임원으로 재직 중인 기업입니다.
| 구 분 | 회사명 | 상장여부 |
|---|---|---|
| 관계기업 | 에이치엘비생명과학㈜ | 상장 |
| 에이치엘비테라퓨틱스㈜ | ||
| ㈜노터스(*) | ||
| Verismo Therapeutics, Inc. | 비상장 | |
| 바다중공업㈜ | ||
| 현대요트㈜ | ||
| 기타특수관계자 | HLB글로벌㈜(구. ㈜넥스트사이언스) | 상장 |
| 에이치엘비제약㈜(구. ㈜메디포럼제약) | ||
| HLB사이언스㈜ (구. 단디바이오사이언스㈜) |
||
| ㈜엘에스케이인베스트먼트 | 비상장 | |
| ㈜고션 | ||
| 에이치엘비일렉㈜ | ||
| 에이치엘비네트웍스㈜ | ||
| Hyundai Lifeboats Singapore Pte. Ltd | ||
| 오티에스중공업㈜ | ||
| 현대코스모스요팅㈜ | ||
| ㈜신화어드밴스 | ||
| 에이치엘비엘이디㈜ | ||
| 에이치엘비에너지㈜(구. 거림) | ||
| ㈜펭귄오션레저 | ||
| 의령태양광1호㈜ | ||
| HLB생활건강㈜(구.엘리샤코이) | ||
| 에이치엘비셀㈜(구.라이프리버㈜) | ||
| ㈜프레시코 | ||
| ㈜코아바이오 | ||
| 에포케㈜(구.코르키㈜) | ||
| 지트리파마슈티컬 | ||
| REGENTREE | ||
| OBLATO | ||
| 바다엔지니어링㈜ | ||
| ㈜새론바이오 | ||
| 브이에스팜㈜ | ||
| ㈜온힐 | ||
| ㈜베리스모테라퓨틱스 아시아 | ||
| 에이치엘비생명과학알앤디㈜ | ||
| ㈜개밥왕 |
(*) 당반기 중 신규 편입되었습니다(주석 11참조).
(2) 당반기 및 전반기 중 특수관계자와의 매출 및 매입 내역은 다음과 같습니다.
① 당반기
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 특수관계구분 | 특수관계자명 | 매출 | 매입 | ||
| 매출거래 | 기타 | 매입거래 | 기타 | ||
| 관계기업 | ㈜화진메디칼 | - | - | 7,258 | 38,101 |
| 에이치엘비생명과학㈜ | 120,000 | - | - | 186,023 | |
| HLB테라퓨틱스㈜ | - | 646,000 | 1,059,587 | 9,410,279 | |
| 바다중공업㈜ | 61,700 | - | 1,847,544 | - | |
| 현대요트㈜ | 291,890 | - | - | 31,818 | |
| 기타 | HLB글로벌(구.넥스트사이언스) | - | - | - | 4,158 |
| HLB네트웍스㈜ (*) | 690,870 | - | - | 500 | |
| ㈜펭귄오션레저 | 41,200 | - | - | 2,430 | |
| 합 계 | 1,205,660 | 646,000 | 2,914,388 | 9,673,309 | |
(*) 연결실체는 기타특수관계자인 에이치엘비네트웍스㈜에 구명정 서비스 독점권을 부여하여 러닝개런티를 통한 로열티수익을 창출하고 있습니다.
② 전반기
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 특수관계구분 | 특수관계자명 | 매출 | 매입 | ||
| 매출거래 | 기타 | 매입거래 | 기타 | ||
| 관계기업 | 에이치엘비생명과학㈜ | 120,000 | - | - | 185,038 |
| 바다중공업㈜ | - | - | 1,573,305 | 3,000 | |
| 기타 | ㈜넥스트사이언스 | - | - | - | 4,158 |
| 에이치엘비일렉㈜ | - | 295,724 | - | - | |
| 에이치엘비네트웍스㈜ | 732,946 | - | - | 4,000 | |
| ㈜펭귄오션레저 | 36,400 | - | - | 29,400 | |
| ㈜엘리샤코이 | - | - | - | 6,608 | |
| ㈜프레시코 | - | - | - | 6,839 | |
| 합 계 | 889,346 | 295,724 | 1,573,305 | 239,043 | |
(3) 당반기 및 전반기 중 특수관계자와의 자금거래 내역은 다음과 같습니다.
① 당반기
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 특수관계구분 | 특수관계자명 | 자금 유출 거래 | 자금 유입 거래 | ||
| 자금대여 | 출자 | 대여금회수 | 이자수취 | ||
| 관계기업 | ㈜노터스 | - | 31,025,920 | - | - |
| 에이치엘비생명과학(*1) | 19,603,370 | - | - | - | |
| 바다중공업 | 2,000,000 | - | - | - | |
| 기타특수관계자 | HLB제약㈜(구. ㈜메디포럼제약) | - | - | - | 50,000 |
| 화진메디칼 | - | - | 1,700,000 | 51,633 | |
| 합 계 | 21,603,370 | 31,025,920 | 1,700,000 | 101,633 | |
(*1) 에이치엘비생명과학㈜ 제9회 공모 신주인수권부사채에 청약하여 신주인수권부사채를 취득하였습니다.
② 전반기
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 특수관계구분 | 특수관계자명 | 자금 유출 거래 | 자금 유입 거래 | ||
| 자금대여 | 출자 | 대여금회수 | 이자 수취 | ||
| 관계기업 | Verismo Therapeutics, Inc. | - | 5,586,000 | - | - |
| 기타특수관계자 | 에이치엘비제약㈜(구. ㈜메디포럼제약) | - | - | - | 50,000 |
| 합 계 | - | 5,586,000 | - | 50,000 | |
(4) 당반기말과 전기말 현재 특수관계자에 대한 채권ㆍ채무내역은 다음과 같습니다.
① 당반기말
| (단위: 천원) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 구분 | 채권 | 채무 | |||||||
| 특수관계 구분 |
특수관계자명 | 매출채권 | 단기대여금 | 미수금 | 미수수익 | 기타 | 매입채무 | 계약부채 | 기타 |
| 관계기업 | HLB테라퓨틱스㈜ | 73,172 | - | - | - | - | 996,241 | - | - |
| 에이치엘비생명과학(*2) | - | - | - | - | 22,469,317 | - | - | - | |
| 바다중공업㈜ | - | 2,000,000 | - | 10,334 | - | 228,292 | - | - | |
| 현대요트㈜ | 57,900 | - | - | - | - | - | 656,610 | 5,833 | |
| 기타 | HLB글로벌(구.넥스트사이언스) | - | - | - | - | - | - | - | 762 |
| HLB네트웍스㈜ | 319,039 | - | 70 | - | - | - | - | - | |
| ㈜펭귄오션레저(*1) | 660 | 23,600 | 53,306 | 1,628 | 93,293 | - | - | - | |
| 현대코스모스요팅 | - | - | - | - | - | - | - | 54,000 | |
| HLB제약㈜(구. ㈜메디포럼제약)(*2) | - | - | - | - | 23,272,820 | - | - | - | |
| 합 계 | 450,771 | 2,023,600 | 53,376 | 11,963 | 45,835,430 | 1,224,533 | 656,610 | 60,596 | |
(*1) 당반기말 현재 상기의 특수관계자 채권에 대해 대손충당금 171,021천원이 설정되어 있습니다.
(*2) 기타의 채권은 연결실체가 보유한 전환사채권 및 신주인수권부사채권 이며, 공정가치평가 후 금액입니다.(주석 3 참조)
② 전기말
| (단위: 천원) | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 구분 | 채권 | 채무 | |||||||||
| 특수관계 구분 |
특수관계자명 | 매출채권 (*1) |
단기대여금 (*1) |
미수금 (*1) |
미수수익 (*1) |
보증금 (*1) |
기타 | 매입채무 | 계약부채 | 보증금 | 기타 |
| 관계기업 | 에이치엘비생명과학㈜(*2) | - | - | - | - | - | - | - | - | - | - |
| 바다중공업㈜ | 23,100 | - | - | - | - | - | 155,371 | - | - | - | |
| 현대요트㈜ | 57,900 | - | 18 | - | 53,897 | - | - | - | - | - | |
| 기타 | 에이치엘비셀㈜ (구.라이프리버㈜) |
- | - | 12 | - | - | - | - | - | - | - |
| 에이치엘비네트웍스㈜ | 235,296 | - | 70 | - | - | - | - | - | - | - | |
| 에이치엘비일렉㈜ | - | - | 265 | - | - | - | - | - | - | - | |
| ㈜펭귄오션레저(*2) | 660 | 23,600 | 53,306 | 1,628 | - | 93,293 | - | 12,000 | - | - | |
| HLB글로벌㈜ (구.넥스트사이언스) |
- | - | - | - | - | - | - | - | - | 762 | |
| 에이치엘비제약㈜ (구. ㈜메디포럼제약)(*2) |
- | - | - | - | - | 21,726,530 | - | - | - | - | |
| 합계 | 316,956 | 23,600 | 53,670 | 1,628 | 53,897 | 21,819,823 | 155,371 | 12,000 | - | 762 | |
(*1) 전기말 현재 상기의 특수관계자 채권에 대해 대손충당금 224,918천원이 설정되어 있습니다.
(*2) 기타의 채권은 연결실체가 보유한 전환사채권이며, 공정가치평가 후 금액입니다.(주석 3 참조)
(5) 당반기말 현재 연결실체가 특수관계자에게 제공한 지급보증의 내역은 다음과 같습니다.
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 특수관계구분 | 특수관계자명 | 보증처 | 내용 | 지급보증금액 | 연대보증인 | 보증기간 |
| 관계기업 | 현대요트㈜ | 서울보증보험 | 하자이행 | 44,275 | - | 2018-06-23 ~ 2023-06-22 |
| 선급이행 | 1,166,593 | - | 2022-04-20 ~ 2023-02-15 | |||
| 선급이행 | 191,111 | - | 2021-12-17 ~ 2022-12-17 | |||
| 선급이행 | 280,566 | - | 2020-07-29 ~ 2022-09-29 | |||
(6) 지배기업의 주요 경영진에 대한 보상
주요경영진은 회사활동의 계획, 운영 및 통제에 대한 중요한 권한과 책임을 가진 등기임원들로 구성되어 있습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 급여 및 기타 단기종업원 급여 | 599,990 | 706,300 |
| 퇴직급여 | 43,092 | 68,191 |
| 합 계 | 643,082 | 774,491 |
32. 현금흐름표
(1) 당반기 및 전반기 중 영업활동 중 수익ㆍ비용의 조정 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 감가상각비 | 2,188,750 | 1,780,661 |
| 대손상각비(환입) | 22,941 | 705,714 |
| 기타의대손상각비(환입) | (1,497) | - |
| 무형자산상각비 | 5,975,322 | 3,967,447 |
| 투자부동산상각비 | - | 8,175 |
| 퇴직급여 | 407,245 | 627,784 |
| 유형자산처분손실 | 1,583 | - |
| 유형자산폐기손실 | - | 59 |
| 이자비용 | 4,220,642 | 1,699,094 |
| 외화환산손실 | 8,022 | 2,947 |
| 주식보상비용 | 1,631,187 | 2,950,424 |
| 판매보증비(환입) | (20,596) | 45,637 |
| 금융보증충당부채전입액(환입) | - | (82,479) |
| 당기손익-공정가치측정 금융자산 평가이익 | (4,418,532) | (162,905) |
| 지분법손실 | 1,742,992 | 5,961,062 |
| 이자수익 | (326,380) | (698,125) |
| 외화환산이익 | (1,020,290) | (372,722) |
| 유형자산처분이익 | (21,421) | - |
| 재해손실 | - | 1,360,712 |
| 투자자산처분이익 | - | (289,273) |
| 매출채권처분손실 | - | 825 |
| 재고자산평가손실 | 339,464 | 36,559 |
| 법인세비용(수익) | 6,938,089 | - |
| 무형자산폐기손실 | - | - |
| 당기손익-공정가치측정 금융자산 평가손실 | 174,621 | 11,377,192 |
| 지분법이익 | (726,283) | |
| 투자부동산처분이익 | (260) | - |
| 파생상품평가이익 | (3,017,209) | - |
| 종속및관계기업투자주식처분이익 | (3,707,564) | - |
| 합 계 | 10,390,826 | 28,918,788 |
(2) 당반기 및 전반기 중 영업활동으로 인한 자산ㆍ부채의 변동 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 매출채권의 감소(증가) | (4,727,072) | 4,173,990 |
| 기타유동자산의 증가(감소) | (826,117) | (2,243,567) |
| 재고자산의 증가(감소) | (5,100,165) | (2,426,209) |
| 기타유동금융자산의 증가(감소) | (10,962) | (182,017) |
| 사외적립자산의 감소(증가) | 78,525 | - |
| 기타비유동금융부채의 증가 | (246,064) | 102,346 |
| 매입채무의 증가 | (226,873) | 289,848 |
| 계약부채의 증가 | 1,158,795 | - |
| 기타유동부채의 증가(감소) | (793,266) | (91,809) |
| 기타비유동부채의 증가(감소) | - | (5,007) |
| 기타유동금융부채의 감소(증가) | (5,094,924) | (835,600) |
| 퇴직급여충당부채의 감소(증가) | - | (33,183) |
| 퇴직금의 지급 | (161,190) | (44,933) |
| 합 계 | (15,949,313) | (1,296,141) |
(3) 당반기 및 전반기 중 연결실체의 현금흐름 가운데 현금의 유입과 유출이 없는 중요한 거래내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 전환사채의 전환으로 인한 자본대체 | 16,409,073 | 9,647,333 |
| 신주인수권부사채의 발행으로 인한 대용납입 | 25,200,000 | - |
| 리스 계약 사용권자산 인식 | 3,406,680 | 383,860 |
| 리스 종료로 인한 사용권자산 감소 | 110,939 | 189,116 |
| 건설중인자산 본계정대체 | - | 26,000 |
| 주식발행초과금의 이익잉여금 전입 | 130,000,000 | - |
| 사업결합으로 인한 자산부채 승계 | 49,271,810 | - |
(4) 재무활동과 관련된 부채의 변동
당반기 중 재무활동에서 생기는 부채의 변동은 다음과 같습니다.
| (단위: 원) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 구 분 | 기초 | 현금흐름 | 비현금 변동 | 당기말 | |||||
| 취득 | 보통주전환 | 상각 | 환율변동효과 | 연결범위의 변동 | 유동성대체 | ||||
| 단기차입금 | 9,721,996 | (6,168,332) | - | - | - | - | (3,553,664) | - | - |
| 장기차입금 | 465,998 | - | - | - | - | - | (145,998) | - | 320,000 |
| 전환사채(유동) | 11,494,916 | - | - | (9,359,637) | - | - | - | - | 2,135,279 |
| 전환사채(비유동) | - | - | 23,696,854 | - | (4,118,193) | - | - | - | 19,578,661 |
| 신주인수권부사채(유동) | - | - | 25,704,000 | - | (1,954,813) | - | - | - | 23,749,187 |
| 신주인수권부사채(비유동) | 46,911,860 | - | 17,515,066 | - | (156,356) | - | - | - | 64,270,570 |
| 금융리스부채(유동) | 1,220,344 | - | - | - | (1,264,891) | - | - | (387,342) | (431,889) |
| 금융리스부채(비유동) | 9,733,384 | - | 3,099,613 | - | 308,004 | 1,020,067 | (56,898) | 387,342 | 14,491,512 |
| 합 계 | 79,548,498 | (6,168,332) | 70,015,533 | (9,359,637) | (7,186,249) | 1,020,067 | (3,756,560) | - | 124,113,320 |
33. 계류중인 소송사건
당반기말 현재 연결실체를 원고로 하는 계류중인 중요한 소송사건의 주요 내용은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 원 고 | 피 고 | 소 송 내 역 | 소 송 가 액(*) |
| 에이치엘비 주식회사 | 하이투자증권㈜ | 부당이득금 반환 청구 | 30,000,000 |
(*) 지배기업이 펀드투자를 위해 하이투자증권에 최초 예치한 금액이나, 사기적 부정거래행위 및 불완전판매 요소가 발견되어 부당이득금 반환 청구소송을 진행 중입니다. 지배기업의 대표이사는 본 사건과 관련하여 발생가능한 손실을 보전하기 위하여 대표이사가 보유한 지배기업의 주식을 법무법인에 위탁하는 계약을 체결하였습니다.
34. 종속회사인 Elevar Therapeutics, Inc.에 대한 가치평가 시, 리보세라닙 신약허가 관련 불확실성의 반영
연결실체의 종속회사인 Elevar Therapeutics, Inc. 는 표적항암제 리보세라닙의 주요Pipeline 중 하나인 위암말기 표준치료법의 글로벌 3상 임상시험을 완료하였습니다. 2019년 10월 Pre-NDA미팅(품목허가를 위한 사전상담)에서 FDA는 사전 제출한 1차 유효성 지표인 OS(전체생존기간) 결과가 통계학적 유의미성을 확보하지 못한 부분을 언급하였고, 이에 Elevar Therapeutics, Inc.는 임상3상 데이터 추가 수집 및 분석과 외부 임상 데이터의 수집 및 분석치를 제시하겠다는 제안을 하였습니다. 이에 추가적으로 FDA는 상기 제안과 별도로 약동학 실험, CMC(제조품질관리) 등의 자료보완을 권고하였습니다.
이에 대해 Elevar Therapeutics, Inc. 는 2020년 회계기간 동안 약동학 실험을 완료하였고, CMC(제조품질관리)에 대해서도 준비를 마쳤으며, 2021년 회계기간 동안 임상3상 데이터 추가수집 및 분석을 완료하였고, 외부 임상 데이터 역시 수집 완료 후 분석을 진행 중 입니다.
지배기업은 상기 외부 임상 데이터 분석결과의 불확실성과 COVID-19 펜데믹 상황에 따른 임상일정 지연 등을 고려하여 Elevar Therapeutics, Inc.의 가치평가 시 제반변수를 보수적관점으로 적용하였는 바, 당기 별도재무제표에 39,266,897천원의 종속기업투자주식 손상차손을 인식하였습니다. 한편, 리보세라닙 위암말기 표준치료법의 FDA 승인 성공확률을 0%로 가정할 경우 별도재무제표에 추가 반영되어야 하는 가치 감소 금액은 38,495,062천원입니다.
4. 재무제표
|
재무상태표 |
|
제 38 기 반기말 2022.06.30 현재 |
|
제 37 기말 2021.12.31 현재 |
|
(단위 : 원) |
|
제 38 기 반기말 |
제 37 기말 |
|
|---|---|---|
|
자산 |
||
|
유동자산 |
111,068,527,518 |
61,287,289,562 |
|
현금및현금성자산 |
48,724,359,117 |
36,642,797,341 |
|
매출채권 |
27,808,265,214 |
18,707,734,861 |
|
공정가치측정금융자산 |
7,113,529,495 |
0 |
|
기타유동금융자산 |
10,898,499,658 |
2,359,396,033 |
|
재고자산 |
14,452,027,295 |
3,006,976,997 |
|
미수법인세환급액 |
0 |
312,043,071 |
|
기타유동자산 |
2,071,846,739 |
258,341,259 |
|
비유동자산 |
819,868,939,288 |
740,936,083,588 |
|
공정가치측정금융자산 |
53,113,220,246 |
28,123,278,872 |
|
기타비유동금융자산 |
4,256,908,047 |
9,304,466,106 |
|
종속기업및관계기업투자주식 |
646,040,849,162 |
661,543,145,449 |
|
투자부동산 |
19,173,350 |
19,173,350 |
|
유형자산 |
28,903,757,122 |
8,820,831,217 |
|
무형자산 |
87,263,904,702 |
33,125,188,594 |
|
퇴직급여운용자산/퇴직연금운용자산 |
271,126,659 |
0 |
|
자산총계 |
930,937,466,806 |
802,223,373,150 |
|
부채 |
||
|
유동부채 |
49,124,855,837 |
24,296,879,231 |
|
매입채무 |
4,533,211,593 |
939,313,121 |
|
차입금 |
25,884,465,271 |
17,494,915,781 |
|
기타유동금융부채 |
9,251,533,956 |
5,299,290,148 |
|
금융보증부채 |
62,156,461 |
12,225,450 |
|
계약부채 |
1,455,268,992 |
306,600,000 |
|
기타유동부채 |
644,861,946 |
244,534,731 |
|
당기법인세부채 |
7,293,357,618 |
0 |
|
비유동부채 |
91,350,882,248 |
47,501,800,820 |
|
비유동차입금 |
84,169,231,853 |
47,231,860,171 |
|
기타비유동금융부채 |
214,284,628 |
225,665,649 |
|
기타비유동부채 |
0 |
0 |
|
비유동금융보증부채 |
0 |
44,275,000 |
|
이연법인세부채 |
6,967,365,767 |
0 |
|
부채총계 |
140,475,738,085 |
71,798,680,051 |
|
자본 |
||
|
자본금 |
53,444,966,500 |
53,308,626,000 |
|
주식발행초과금 |
660,162,652,436 |
779,883,721,324 |
|
기타자본항목 |
13,599,168,695 |
12,386,004 |
|
이익잉여금(결손금) |
63,254,941,090 |
(102,780,040,229) |
|
자본총계 |
790,461,728,721 |
730,424,693,099 |
|
부채 및 자본총계 |
930,937,466,806 |
802,223,373,150 |
|
포괄손익계산서 |
|
제 38 기 반기 2022.01.01 부터 2022.06.30 까지 |
|
제 37 기 반기 2021.01.01 부터 2021.06.30 까지 |
|
(단위 : 원) |
|
제 38 기 반기 |
제 37 기 반기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
매출액 |
56,948,468,857 |
120,386,477,545 |
6,471,965,081 |
11,978,184,568 |
|
매출원가 |
33,176,401,267 |
70,893,188,231 |
6,861,596,763 |
12,028,792,610 |
|
매출총이익 |
23,772,067,590 |
49,493,289,314 |
(389,631,682) |
(50,608,042) |
|
판매비와관리비 |
6,590,714,077 |
13,184,909,164 |
7,169,884,681 |
9,929,292,921 |
|
영업이익(손실) |
17,181,353,513 |
36,308,380,150 |
(7,559,516,363) |
(9,979,900,963) |
|
기타수익 |
365,051,559 |
462,260,041 |
1,581,321,870 |
1,976,215,879 |
|
기타비용 |
2,603,610 |
56,204,930 |
1,415,468,734 |
2,176,457,023 |
|
금융수익 |
9,097,366,507 |
9,739,012,935 |
618,154,812 |
1,180,613,515 |
|
금융비용 |
(1,296,645,396) |
4,292,876,085 |
12,077,384,208 |
12,746,958,484 |
|
종속및관계기업투자주식관련 손익 |
800,000,000 |
800,000,000 |
0 |
0 |
|
법인세비용차감전순이익(손실) |
28,737,813,365 |
42,960,572,111 |
(18,852,892,623) |
(21,746,487,076) |
|
법인세비용(수익) |
1,144,643,790 |
6,925,590,792 |
0 |
0 |
|
당기순이익(손실) |
27,593,169,575 |
36,034,981,319 |
(18,852,892,623) |
(21,746,487,076) |
|
기타포괄손익 |
(358,056,525) |
(280,218,150) |
1,467,248,400 |
1,155,458,115 |
|
당기손익으로 재분류되지 않는항목 |
||||
|
기타포괄손익-공정가치측정 지분상품 평가손익 |
(358,056,525) |
(280,218,150) |
1,467,248,400 |
1,155,458,115 |
|
총포괄손익 |
27,235,113,050 |
35,754,763,169 |
(17,385,644,223) |
(20,591,028,961) |
|
주당이익 |
||||
|
기본주당이익(손실) (단위 : 원) |
256 |
338 |
(178) |
(205) |
|
희석주당이익(손실) (단위 : 원) |
256 |
338 |
(178) |
(205) |
|
자본변동표 |
|
제 38 기 반기 2022.01.01 부터 2022.06.30 까지 |
|
제 37 기 반기 2021.01.01 부터 2021.06.30 까지 |
|
(단위 : 원) |
|
자본 |
|||||
|---|---|---|---|---|---|
|
자본금 |
자본잉여금 |
기타자본항목 |
이익잉여금(결손금) |
자본 합계 |
|
|
2021.01.01 (기초자본) |
26,491,546,500 |
775,814,984,487 |
(8,839,257,513) |
(48,238,748,664) |
745,228,524,810 |
|
당기순이익(손실) |
0 |
0 |
0 |
(21,746,487,076) |
(21,746,487,076) |
|
기타포괄손익-공정가치측정 지분상품 투자손익 |
0 |
0 |
1,155,458,115 |
0 |
1,155,458,115 |
|
이익잉여금 대체 |
0 |
0 |
0 |
0 |
0 |
|
무상증자 |
26,486,214,500 |
(26,728,737,240) |
0 |
0 |
(242,522,740) |
|
복합금융상품 전환 |
64,630,000 |
10,725,090,388 |
(1,154,570,358) |
0 |
9,635,150,030 |
|
복합금융상품 발행 |
0 |
0 |
0 |
0 |
0 |
|
사업결합 |
0 |
0 |
0 |
0 |
0 |
|
주식기준보상거래 |
0 |
0 |
0 |
0 |
0 |
|
자본 증가(감소) 합계 |
26,550,844,500 |
(16,003,646,852) |
887,757 |
(21,746,487,076) |
(11,198,401,671) |
|
2021.06.30 (기말자본) |
53,042,391,000 |
759,811,337,635 |
(8,838,369,756) |
(69,985,235,740) |
734,030,123,139 |
|
2022.01.01 (기초자본) |
53,308,626,000 |
779,883,721,324 |
12,386,004 |
(102,780,040,229) |
730,424,693,099 |
|
당기순이익(손실) |
0 |
0 |
0 |
36,034,981,319 |
36,034,981,319 |
|
기타포괄손익-공정가치측정 지분상품 투자손익 |
0 |
0 |
(280,218,150) |
0 |
(280,218,150) |
|
이익잉여금 대체 |
0 |
(130,000,000,000) |
0 |
130,000,000,000 |
0 |
|
무상증자 |
0 |
0 |
0 |
0 |
0 |
|
복합금융상품 전환 |
136,340,500 |
10,278,931,112 |
(1,066,514,816) |
0 |
9,348,756,796 |
|
복합금융상품 발행 |
0 |
0 |
12,511,362,850 |
0 |
12,511,362,850 |
|
사업결합 |
0 |
0 |
2,304,356,451 |
0 |
2,304,356,451 |
|
주식기준보상거래 |
0 |
0 |
117,796,356 |
0 |
117,796,356 |
|
자본 증가(감소) 합계 |
136,340,500 |
(119,721,068,888) |
13,586,782,691 |
166,034,981,319 |
60,037,035,622 |
|
2022.06.30 (기말자본) |
53,444,966,500 |
660,162,652,436 |
13,599,168,695 |
63,254,941,090 |
790,461,728,721 |
|
현금흐름표 |
|
제 38 기 반기 2022.01.01 부터 2022.06.30 까지 |
|
제 37 기 반기 2021.01.01 부터 2021.06.30 까지 |
|
(단위 : 원) |
|
제 38 기 반기 |
제 37 기 반기 |
|
|---|---|---|
|
영업활동현금흐름 |
22,433,229,292 |
(2,140,637,026) |
|
당기순이익(손실) |
36,034,981,319 |
(21,746,487,076) |
|
수익비용의 조정 |
9,007,058,315 |
18,201,751,046 |
|
영업활동으로 인한 자산부채의 변동 |
(13,356,641,801) |
609,449,855 |
|
이자의 수취 |
405,193,276 |
545,636,872 |
|
이자의 지급 |
(2,991,781) |
(2,392,813) |
|
법인세의 납부(환급) |
(9,654,370,036) |
251,405,090 |
|
투자활동현금흐름 |
(55,046,084,239) |
(8,513,175,724) |
|
단기금융상품의 처분 |
19,300,000,000 |
2,000,000 |
|
단기대여금의 회수 |
1,734,880,967 |
0 |
|
기타유동금융자산의 처분 |
0 |
74,876 |
|
공정가치측정금융자산의 처분 |
358,439,010 |
0 |
|
종속관계기업투자주식의 처분 |
3,300,000,000 |
0 |
|
유형자산의 처분 |
651,000,000 |
0 |
|
투자부동산의 처분 |
0 |
2,848,000,000 |
|
임차보증금의 감소 |
76,150,890 |
105,200,000 |
|
사업결합으로 인한 현금유출 |
0 |
0 |
|
종속관계기업투자주식의 취득 |
(57,885,247,327) |
(8,602,000,000) |
|
장기대여금의 취득 |
(2,000,000,000) |
0 |
|
공정가치측정금융자산의 취득 |
(19,671,928,000) |
0 |
|
유형자산의 취득 |
(707,079,779) |
(1,033,042,600) |
|
무형자산의 취득 |
(153,300,000) |
(227,400,000) |
|
기타비유동금융자산의 취득 |
0 |
(17,808,000) |
|
임차보증금의 증가 |
(19,000,000) |
(1,588,200,000) |
|
선물거래예치금의 증가 |
(30,000,000) |
0 |
|
재무활동현금흐름 |
33,477,231,292 |
(927,060,702) |
|
전환사채의 증가 |
23,000,000,000 |
0 |
|
신주인수권부사채의 증가 |
17,000,000,000 |
0 |
|
단기차입금의 상환 |
(6,000,000,000) |
0 |
|
리스료의 지급 |
(504,053,475) |
(497,355,172) |
|
임대보증금의 감소 |
0 |
(175,000,000) |
|
주식발행비용 |
(18,715,233) |
(254,705,530) |
|
환율변동효과 반영전 현금및현금성자산의 순증가(감소) |
864,376,345 |
(11,580,873,452) |
|
기초현금및현금성자산 |
36,642,797,341 |
153,999,756,616 |
|
사업결합으로 인한 현금 및 현금성 자산의 증가 |
11,013,305,431 |
0 |
|
현금및현금성자산에 대한 환율변동효과 |
203,880,000 |
83,885,102 |
|
기말현금및현금성자산 |
48,724,359,117 |
142,502,768,266 |
5. 재무제표 주석
| 2022년 6월 30일 현재 |
| 2021년 6월 30일 현재 |
| 에이치엘비 주식회사 |
1. 회사의 개요
에이치엘비 주식회사(이하 "당사")는 1985년 10월에 설립되어 1996년 7월 20일에 주식을 코스닥시장에 상장한 공개법인으로서 2013년에 현대라이프보트㈜와 합병 및 2015년에 전기계장사업부문의 물적분할 후 구명정, 유리섬유파이프 제조 및 시공업 등을 주요 영업으로 하고 있으며, 2022년 1월 1일 ㈜에프에이와 합병하여 체외진단키트 등 의료기기사업에 진출하였습니다. 또한 기존사업과 더불어 Elevar Therapeutics Inc., Immunomic Therapeutics Inc. 등에 지분투자를 통해 항암 신약 개발 사업 등 바이오사업을 영위하고 있습니다.
당반기말 현재 납입자본금은 53,444,967천원 입니다.
2022년 06월 30일 현재 주요 주주의 구성은 다음과 같습니다.
| 주주명 | 당반기말 | 전기말 | ||
|---|---|---|---|---|
| 주식수(주) | 지분율(%) | 주식수(주) | 지분율(%) | |
| 진양곤 | 8,610,902 | 8.06% | 8,610,902 | 8.08% |
| 이현아 | 230,772 | 0.22% | 230,772 | 0.22% |
| 에이치엘비생명과학㈜ | 1,399,230 | 1.31% | 1,399,230 | 1.31% |
| 에이치엘비셀㈜ (구. 라이프리버㈜) | 828,214 | 0.77% | 828,214 | 0.78% |
| 에이치엘비㈜ (자기주식) | 134,000 | 0.13% | 134,000 | 0.13% |
| 기타(*) | 95,686,815 | 89.52% | 95,414,134 | 89.49% |
| 합 계 | 106,889,933 | 100.00% | 106,617,252 | 100.00% |
(*) 전기 중 임원퇴임(Elevar Therapeutics, Inc.)으로 특수관계가 해소된 Alex S.Kim의 지분이 포함되어 있습니다.
상기 주식수에는 우선주(7,188주)가 포함되어 있습니다.
2. 재무제표 작성기준 및 중요한 회계정책
(1) 회계정책의 변경과 공시
1) 회사가 채택한 제ㆍ개정 기준서
회사가 2022년 1월 1일 이후 개시하는 회계기간부터 적용한 제ㆍ개정 기준서 및 해석서는 다음과 같습니다.
(가) 기업회계기준서 제1103호 '사업결합' (개정) - 재무보고를 위한 개념체계 참조
식별할 수 있는 취득 자산과 인수 부채는 재무보고를 위한 개념체계의 정의를 충족하도록 개정되었으나, 기업회계기준서 제1037호 '충당부채, 우발부채 및 우발자산' 및 해석서 제2121호 '부담금' 의 적용범위에 포함되는 부채 및 우발부채에 대해서는 해당 기준서를 적용하도록 예외를 추가하고, 우발자산이 취득일에 인식되지 않는다는 점을 명확히 하였습니다. 동 개정사항은 2022년 1월 1일 이후 시작하는 회계연도부터 적용됩니다. 상기 개정 내용이 재무제표에 미치는 유의적인 영향은 없습니다.
(나) 기업회계기준서 제1016호 '유형자산' (개정) - 의도한 사용 전의 매각금액
개정 기준서는 경영진이 의도한 방식으로 유형자산을 가동할 수 있는 장소와 상태에 이르게 하는 동안에 생산된 재화를 판매하여 얻은 매각금액과 그 재화의 원가는 당기손익으로 인식하도록 요구하며, 이로 인해 당기손익에 포함한 매각금액과 원가를 공시하도록 요구하고 있습니다. 동 개정사항은 2022년 1월 1일 이후 시작하는 회계연도부터 적용됩니다. 상기 개정 내용이 재무제표에 미치는 유의적인 영향은 없습니다.
(다) 기업회계기준서 제1037호 '충당부채, 우발부채 및 우발자산' (개정) - 손실부담계약: 계약이행원가
개정 기준서는 손실부담계약을 식별할 때 계약이행원가는 계약을 이행하는 데 드는 증분원가와 계약을 이행하는 데 직접 관련되는 그 밖의 원가 배분액으로 구성됨을 명확히 하였습니다. 동 개정사항은 2022년 1월 1일 이후 시작하는 회계연도부터 적용됩니다. 상기 개정 내용이 재무제표에 미치는 유의적인 영향은 없습니다.
(라) 기업회계기준서 제 1116호 '리스' (개정) - 2021년 6월 30일 후에도 제공되는 코로나19 관련 임차료 할인 등
코로나19의 직접적인 결과로 발생한 임차료 할인 등(rent concession)이 리스변경에 해당하는지 평가하지 않을 수 있도록 하는 실무적 간편법의 적용대상이 2022년 6월 30일 이전에 지급하여야 할 리스료에 영향을 미치는 리스료 감면으로 확대되었습니다. 리스이용자는 비슷한 상황에서 특성이 비슷한 계약에 실무적 간편법을 일관되게 적용해야 합니다. 동 개정사항은 2021년 4월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 상기 개정 내용이 재무제표에 미치는 유의적인 영향은 없습니다.
(마) 한국채택국제회계기준 2018-2020 연차개선
기업회계기준서 제1109호 '금융상품': 금융부채 제거 목적의 10% 테스트관련 수수료에 차입자와 대여자 사이에서 지급하거나 수취한 수수료(상대방을 대신하여 지급하거나 수취한 수수료 포함)만 포함된다는 개정내용을 포함하여 기업회계기준서 제1101호 '한국채택국제회계기준의 최초 채택': 최초채택기업인 종속기업, 기업회계기준서 제1116호 '리스': 리스인센티브, 기업회계기준서 제1041호 '농림어업': 공정가치 측정에 대한 일부 개정내용이 있습니다. 동 연차개선은 2022년 1월 1일 이후 시작하는 회계연도부터 적용됩니다. 상기 개정 내용이 재무제표에 미치는 유의적인 영향은 없습니다.
2) 공표되었으나 아직 시행되지 않은 제ㆍ개정 기준서 및 해석서
당반기말 현재 제정ㆍ공표되었으나 시행일이 도래하지 않아 회사가 채택하지 않은 한국채택국제회계기준의 기준서 및 해석서는 다음과 같습니다.
(가) 기업회계기준서 제1001호 '재무제표 표시' (개정) - 부채의 유동·비유동 분류
부채의 분류는 기업이 보고기간 후 적어도 12개월 이상 부채의 결제를 연기할 권리의 행사 가능성에 영향을 받지 않으며, 부채가 비유동부채로 분류되는 기준을 충족한다면, 경영진이 보고기간 후 12개월 이내에 부채의 결제를 의도하거나 예상하더라도, 또는 보고기간말과 재무제표 발행승인일 사이에 부채를 결제하더라도 비유동부채로 분류합니다. 또한, 부채를 유동 또는 비유동으로 분류할 때 부채의 결제조건에 자기지분상품의 이전도 포함되나, 복합금융상품에서 자기지분상품으로 결제하는 옵션이 지분상품으로 분류되고 동 옵션을 부채와 분리하여 인식된 경우는 제외됩니다. 동개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 적용하며, 조기적용이 허용됩니다. 회사는 상기 개정 기준서의 적용이 재무제표에 미치는 영향이 유의적이지 아니할 것으로 예상하고 있습니다.
(나) 기업회계기준서 제 1001호 '재무제표 표시' (개정)
개정 기준서는 공시 대상 회계정책 정보를 '유의적인' 회계정책에서 '중요한' 회계정책으로 바꾸고 중요한 회계정책 정보의 의미를 설명하였습니다. 동 개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 회사는 상기 개정 기준서의 적용이 재무제표에 미치는 영향이 유의적이지 아니할 것으로 예상하고 있습니다.
(다) 기업회계기준서 제1008호 '회계정책, 회계추정의 변경 및 오류' (개정)
개정 기준서는 '회계추정치'를 측정불확실성의 영향을 받는 재무제표상 화폐금액으로 정의하고, 회계추정치의 예를 보다 명확히 하였습니다. 또한 새로운 정보의 획득, 새로운 상황의 전개나 추가 경험의 축적으로 투입변수나 측정기법을 변경한 경우 이러한 변경이 전기오류수정이 아니라면 회계추정치의 변경임을 명확히 하였습니다.
동 개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 전진 적용되며, 조기적용이 허용됩니다. 회사는 상기 개정 기준서의 적용이 재무제표에 미치는 영향이 유의적이지 아니할 것으로 예상하고 있습니다.
(라) 기업회계기준서 제 1012호 '법인세' (개정)
개정 기준서는 이연법인세 최초 인식 예외규정을 추가하여 단일 거래에서 자산과 부채를 최초 인식할 때 동일한 금액으로 가산할 일시적차이와 차감할 일시적차이가 생기는 경우 각각 이연법인세 부채와 자산을 인식하도록 하였습니다. 동 개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다.
'단일 거래에서 생기는 자산과 부채에 관련되는 이연법인세'는 비교 표시되는 가장 이른 기간의 시작일 이후에 이루어진 거래에 적용하며, 비교 표시되는 가장 이른 기간의 시작일에 이미 존재하는 (1) 사용권자산과 리스부채, (2) 사후처리 및 복구 관련 부채 및 이에 상응하여 자산 원가의 일부로 인식한 금액에 관련되는 모든 차감할 일시적 차이와 가산할 일시적 차이에 대해 이연법인세 자산과 부채를 인식하며, 최초 적용 누적 효과를 이익잉여금(또는 자본의 다른 구성요소) 기초 잔액을 조정하여 인식합니다.
회사는 상기 개정 기준서의 적용이 재무제표에 미치는 영향이 유의적이지 아니할 것으로 예상하고 있습니다.
(2) 재무제표 작성기준
1) 회계기준
재무제표는 주식회사 등의 외부감사에 관한 법률에서 규정하고 있는 국제회계기준위원회의 국제회계기준을 채택하여 정한 회계처리기준인 한국채택국제회계기준에 따라 작성되었습니다.
2) 측정기준
재무제표는 금융상품 등 아래의 회계정책에서 별도로 언급하고 있는 사항을 제외하고는 역사적원가를 기준으로 작성되었습니다.
3) 기능통화와 표시통화
재무제표는 지배기업의 기능통화이면서 표시통화인"원(KRW)"으로 표시되고 있으며 별도로 언급하고 있는 사항을 제외하고는"원(KRW)" 단위로 표시되고 있습니다.
(3) 별도재무제표에서 종속기업, 관계기업 및 공동기업에 대한 투자
재무제표는 기업회계기준서 제1027호 '별도재무제표'에 따른 별도재무제표로서 지배기업, 관계기업의 투자자 또는 공동기업의 참여자가 투자자산을 피투자자의 보고된 성과와 순자산에 근거하지 않고 직접적인 지분투자에 근거하여 원가법으로 표시한 재무제표이며, 종속기업, 관계기업 또는 공동기업으로부터 배당을 받을 권리가 확정되는 시점에 그 배당금을 별도재무제표에 당기손익으로 인식하고 있습니다.
(4) 외화환산
기능통화로 외화거래를 최초로 인식하는 경우에 거래일의 외화와 기능통화 사이의 현물환율을 외화금액에 적용하여 기록하며, 보고기간말 화폐성 외화항목은 마감환율로 환산하며, 역사적원가로 측정하는 비화폐성 외화항목은 거래일의 환율로 환산하고, 공정가치로 측정하는 비화폐성 외화항목은 공정가치가 결정된 날의 환율로 환산하고 있습니다.
화폐성항목의 결제시점에 생기는 외환차이와 화폐성항목의 환산에 사용한 환율이 회계기간 중 최초로 인식한 시점이나 전기의 재무제표 환산시점의 환율과 다르기 때문에 생기는 외환차이는 그 외환차이가 생기는 회계기간의 손익으로 인식하고 있으며,
일정요건을 충족하는 위험회피회계를 적용하는 외환차이 등은 기타포괄손익으로 보고하고 있습니다.
비화폐성항목에서 생긴 손익을 기타포괄손익으로 인식하는 경우에 그 손익에 포함된환율변동효과도 기타포괄손익으로 인식하며, 비화폐성항목에서 생긴 손익을 당기손익으로 인식하는 경우에는 그 손익에 포함된 환율변동효과도 당기손익으로 인식하고있습니다.
(5) 현금및현금성자산
회사는 보유현금과 요구불예금, 유동성이 매우 높은 단기 투자자산으로서 확정된 금액의 현금으로 전환이 용이하고 가치변동의 위험이 경미한 자산을 현금 및 현금성자산으로 분류하고 있습니다. 지분상품은 현금성자산에서 제외하고 있으며 다만 상환일이 정해져 있고 취득일로부터 상환일까지의 기간이 단기인 우선주와 같이 실질적인 현금성자산인 경우에는 현금성자산에 포함하고 있으며, 금융회사의 요구에 따라 즉시 상환하여야 하는 당좌차월은 현금및현금성자산의 구성요소에 포함하고 있습니다.
(6) 금융상품
1) 금융자산
금융자산은 금융상품의 계약당사자가 되는 때에만 재무상태표에 인식하고 있으며, 금융자산의 정형화된 매입이나 매도는 매매일 또는 결제일에 인식하고 있습니다. 금융상품의 최초 인식시점에 사업모형과 금융자산의 계약상 현금흐름의 특성에 따라금융자산은 당기손익-공정가치측정금융자산, 기타포괄손익-공정가치측정금융자산,상각후원가측정금융자산으로 분류하고 있습니다.
금융자산은 최초인식시 공정가치로 측정하고 있으며, 당기손익-공정가치금융자산이 아닌 경우 당해 금융자산의 취득과 직접 관련되는 거래원가는 최초인식하는 공정가치에 가산하여 측정하고 있습니다.
(가) 당기손익-공정가치측정금융자산
금융자산을 단기매매목적으로 보유하고 있거나, 당기손익-공정가치측정금융자산으로 지정하는 경우와 기타포괄손익-공정가치측정금융자산 또는 상각후원가측정금융자산으로 분류되지 않는 금융자산은 당기손익-공정가치측정금융자산으로 분류합니다.
또한 당기손익-공정가치측정금융자산의 지정이 서로 다른 기준에 따라 자산이나 부채를 측정하거나, 그에 따른 평가손익 등을 인식함으로써 발생할 수 있는 인식과 측정상의 불일치를 제거하거나 상당히 감소시킬 수 있는 경우에는 당기손익-공정가치 측정금융자산으로 지정할 수 있습니다.
당기손익-공정가치측정금융자산은 공정가치로 측정하며 공정가치 변동으로 인한 평가손익은 당기손익으로 인식하고 있습니다. 금융자산으로부터 획득한 배당금과 이자수익도 당기손익으로 인식합니다.
(나) 기타포괄손익-공정가치측정금융자산
채무증권 중 사업모형이 현금흐름 수취 및 매도 사업모형으로 분류되고 계약상 현금흐름이 원금과 이자만으로 구성되어 있는지에 대한 검토를 만족하는 금융자산이나 단기간 내 매도할 목적이 아닌 지분증권 중 기타포괄손익-공정가치측정금융자산으로 지정한 상품은 기타포괄손익-공정가치측정금융자산으로 분류하고 있습니다. 기타포괄손익-공정가치측정금융자산은 최초인식 후에 공정가치로 측정합니다. 공정가치의 변동으로 인하여 발생하는 손익은 유효이자율법에 따른 이자수익, 배당수익 및 손익으로 직접 인식되는 화폐성자산에 대한 외환차이를 제외하고는 자본의 기타포괄손익항목으로 인식하고 있습니다.
기타포괄손익-공정가치측정금융자산을 처분하는 경우 기타포괄손익으로 인식한 누적손익은 해당 기간의 당기손익으로 인식합니다. 다만, 기타포괄손익-공정가치측정 금융자산으로 지정한 지분증권에서 발생한 누적평가손익은 처분시 해당기간의 당기손익으로 인식되지 않습니다.
외화로 표시된 기타포괄손익-공정가치측정금융자산의 공정가치는 해당 외화로 측정되며 보고기간 말 현재 환율로 환산합니다. 공정가치 변동분 중 상각후원가의 변동으로 인한 환산차이에서 발생한 부분은 당기손익으로 인식하며 기타 변동은 자본으로 인식하고 있습니다.
(다) 상각후원가측정금융자산
사업모형이 현금흐름 수취로 분류되고 계약상현금흐름 특성 평가를 만족하는 금융자산은 상각후원가 측정 금융자산으로 분류합니다. 최초 인식 후에는 유효이자율법을 사용한 상각후원가로 측정하며, 이자수익은 유효이자율법을 사용하여 인식합니다.
(라) 금융자산의 제거
금융자산의 현금흐름에 대한 계약상 권리가 소멸하거나, 금융자산의 현금흐름에 대한 권리를 양도하고 금융자산의 소유에 따른 위험과 보상의 대부분을 이전할 때 금융자산을 제거하고 있습니다. 만약, 금융자산의 소유에 따른 위험과 보상의 대부분을 보유하지도 않고 이전하지도 아니한 경우, 회사가 금융자산을 통제하고 있지도 않다면 금융자산을 제거하고, 금융자산을 계속 통제하고 있다면 그 양도자산에 대하여 지속적으로 관여하는 정도까지 계속하여 인식하고, 관련 부채를 함께 인식하고 있습니다.
2) 금융자산(채무상품)의 기대신용손실
당기손익-공정가치측정금융자산을 제외한 상각후원가측정금융자산 및 기타포괄손익-공정가치측정채무상품은 매 보고기간 말에 기대신용손실을 평가하고 있습니다. 손실충당금의 측정방식은 신용위험의 유의적인 증가 여부에 따라 결정됩니다. 금융자산의 최초 인식 후 신용위험의 유의적인 증가 여부에 따라 아래 표와 같이 3단계로 구분하여 12개월 기대신용손실이나 전체기간 기대신용손실에 해당하는 금액으로 손실충당금을 인식합니다.
|
구 분 |
손실충당금 |
|
|
Stage 1 |
최초 인식 후 신용위험이 유의적으로 증가하지 않은 경우(주1) |
12개월 기대신용손실: 보고기간 말 이후 12개월 내에 발생 가능한 금융상품의 채무불이행 사건으로 인한 기대신용손실 |
|
Stage 2 |
최초 인식 후 신용위험이 유의적으로 증가한 경우 |
전체기간 기대신용손실: 기대존속기간에 발생할 수 있는 모든 채무불이행 사건으로 인한 기대신용손실 |
|
Stage 3 |
신용이 손상된 경우 |
|
(주1) 보고기간 말 신용위험이 낮은 경우에는 신용위험이 유의적으로 증가하지 않은 것으로 간주할 수 있음
최초 인식 시점에 신용이 손상된 금융자산에 대하여 최초 인식 후 전체기간 기대신용손실의 누적변동분만을 손실충당금으로 계상합니다.
한편, 매출채권, 계약자산, 리스채권 등에 대해서는 전체기간 기대신용손실에 해당하는 금액으로 손실충당금을 측정하는 간편법을 적용하고 있습니다.
기대신용손실은 일정 범위의 발생 가능한 결과를 확률가중한 값으로, 화폐의 시간가치를 반영하고, 보고기간 말에 과거사건, 현재 상황과 미래 경제적 상황에 대한 예측에 대한 과도한 원가나 노력 없이 이용할 수 있는 정보를 반영해 측정합니다.
3) 금융부채
금융부채는 금융상품의 계약당사자가 되는 때에만 재무상태표에 인식하고 있으며, 금융부채의 최초 인식시 당기손익-공정가치측정금융부채 또는 기타금융부채로 분류하고 공정가치로 측정하고 있습니다. 당기손익-공정가치측정금융부채를 제외하고는 해당 금융부채의 발생과 직접 관련되는 거래비용은 최초 측정시 공정가치에 차감하고 있습니다.
(가) 당기손익-공정가치측정부채
당기손익-공정가치측정금융부채는 최초 인식시점에 당기손익-공정가치측정금융부채로 지정한 금융부채를 포함하고 있습니다. 당기손익-공정가치측정금융부채는 최초 인식 후 공정가치로 측정하며, 공정가치의 변동은 당기손익으로 인식하고 있습니다. 한편,최초 인식시점에 발행과 관련하여 발생한 거래비용은 발생 즉시 당기손익으로 인식하고 있습니다.
(나) 당기손익-공정가치측정부채로 분류되지 않는 금융부채
당기손익-공정가치측정부채로 분류되지 않는 금융부채는 다음의 금융부채를 제외하고는 최초인식 후 유효이자율법을 사용하여 상각후원가로 측정하고 있습니다.
금융자산의 양도가 제거 조건을 충족하지 못하거나 지속적관여접근법이 적용되는 경우에 발생하는 금융부채의 경우, 양도자산을 상각후원가로 측정한다면 양도자산과 관련부채의 순장부금액이 양도자가 보유하는 권리와 부담하는 의무의 상각후원가가 되도록 관련부채를 측정하며, 양도자산을 공정가치로 측정한다면 양도자산과 관련부채의 순장부금액이 양도자가 보유하는 권리와 부담하는 의무의 독립적으로 측정된 공정가치가 되도록 관련부채를 측정하고 있습니다.
금융보증부채(금융자산의 양도가 제거 조건을 충족하지 못하거나 지속적관여접근법이 적용되는 경우에 발생하는 금융부채 제외)와 시장이자율보다 낮은 이자율로 대출하기로 한 약정은 기대신용손실모형에 따른 손실충당금과 최초인식금액에서 이익누계액을 차감한 금액 중 큰 금액으로 측정됩니다.
(다) 금융부채의 제거
금융부채(또는 금융부채의 일부)는 소멸한 경우(즉, 계약상 의무가 이행, 취소 또는 만료된 경우)에만 재무상태표에서 제거하고 있습니다. 기존 차입자와 대여자가 실질적으로 다른 조건으로 채무상품을 교환하거나 기존 금융부채(또는 금융부채의 일부)의 조건이 실질적으로 변경된 경우 최초의 금융부채를 제거하고 새로운 금융부채를 인식하고 있으며, 소멸하거나 제3자에게 양도한 금융부채(또는 금융부채의 일부)의 장부금액과 지급한 대가의 차액은 당기손익으로 인식하고 있습니다.
4) 금융자산과 금융부채의 상계
회사는 인식한 자산과 부채에 대해 법적으로 집행가능한 상계권리를 현재 보유하고 있으면서 순액으로 결제하거나 자산을 실현하는 동시에 부채를 결제할 의도를 가지고 있는 경우에 금융자산과 금융부채를 상계하고 재무상태표에 순액으로 표시하고 있습니다.
5) 부채와 자본의 분류
채무상품과 지분상품은 계약의 실질 및 금융부채와 지분상품의 정의에 따라 금융부채 또는 자본으로 분류하고 있습니다.
6) 파생상품
파생상품은 최초 인식시 계약일의 공정가치로 측정하고 이후 공정가치로 재측정하고있습니다.
(가) 내재파생상품
① 금융자산이 주계약인 복합계약
내재파생상품을 포함하는 금융자산은 복합계약 전체를 고려하여 분류를 결정하고 내재파생상품을 분리하여 인식하지 않습니다. 계약상 현금흐름이 원금과 이자로만 구성되어 있는지를 판단할 때에도 해당 복합계약 전체를 고려합니다.
② 그 밖의 복합계약(복합계약이 금융자산이 아닌 주계약을 포함하는 경우)
내재파생상품의 경제적 특성 및 위험이 주계약의 경제적 특성 및 위험과 밀접하게 관련되어 있지 않고, 내재파생상품과 동일한 조건을 가진 별도의 금융상품 등이 파생상품의 정의를 충족하며 복합계약의 공정가치 변동이 당기손익으로 인식되지 아니하는 경우 주계약과 분리하여 별도의 파생상품으로 회계처리하고 있습니다.
(나) 위험회피회계
회사는 특정위험으로 인해 인식된 자산이나 부채 또는 미인식된 확정계약의 전체 또는 일부의 공정가치 변동에 대한 위험회피의 경우 공정가치위험회피회계를 적용하며특정위험으로 인해 인식된 자산이나 부채 또는 발생가능성이 매우 높은 예상거래의 현금흐름 변동에 대한 위험회피의 경우 현금흐름위험회피회계를 적용하고 있습니다.
위험회피회계를 적용하기 위하여 회사는 위험회피관계, 위험관리목적, 위험회피전략,회피대상위험 및 위험회피효과 평가방법 등을 문서화하고 있습니다. 위험회피효과는 회피대상위험으로 인한 파생상품의 공정가치나 현금흐름의 변동이 위험회피대상항목의 공정가치나 현금흐름의 변동위험을 상쇄하는 효과를 의미합니다.
(다) 공정가치위험회피
위험회피수단으로 지정되고, 공정가치위험회피회계의 적용요건을 충족한 파생금융상품의 공정가치 변동은 당기손익으로 인식하고 있으며, 회피대상위험으로 인한 위험회피대상항목의 공정가치 변동도 당기손익으로 인식하고 있습니다. 단, 위험회피대상항목이 지분상품이며, 공정가치의 변동을 기타포괄손익으로 표시하기로 선택한 경우에는 위험회피수단의 손익 및 회피대상위험으로 인한 위험회피대상항목의 손익을 기타포괄손익으로 인식하고 있습니다. 공정가치위험회피회계는 위험회피수단이 소멸, 매각, 행사 또는 종료되거나 공정가치위험회피회계의 적용조건을 더 이상 충족하지 않을 경우 중단됩니다. 회피대상위험으로 인한 위험회피대상항목의 장부금액 조정액은 위험회피회계가 중단된 날부터 상각하여 당기손익으로 인식하고 있습니다.
(라) 현금흐름위험회피
위험회피수단으로 지정되고 현금흐름위험회피회계의 적용요건을 충족한 파생상품의 공정가치 변동분 중 위험회피에 효과적인 부분은 기타포괄손익으로 처리하며, 위험회피에 비효과적인 부분은 당기손익으로 인식하고 있습니다. 현금흐름위험회피회계는 위험회피수단이 소멸, 매각, 행사 또는 종료되거나, 현금흐름위험회피회계의 적용요건을 더 이상 충족하지 않을 경우 중단됩니다. 현금흐름위험회피회계를 중단하는 경우에 위험회피대상의 미래 현금흐름이 여전히 발생할 것으로 예상되는 경우에 현금흐름위험회피적립금 누계액은 미래 현금흐름이 생길 때까지 또는 현금흐름위험회피적립금이 차손이며 그 차손의 전부나 일부가 미래기간에 회복되지 않을 것으로 예상될 때까지 현금흐름위험회피적립금에 남겨두고 있습니다. 다만, 위험회피대상의 미래현금흐름이 더 이상 발생할 것으로 예상되지 않는 경우에는 현금흐름위험회피적립금 누계액은 즉시 당기손익으로 인식합니다.
(마) 해외사업장순투자의 위험회피
해외사업장에 대한 순투자 위험회피의 경우, 위험회피에 효과적인 부분은 기타포괄손익으로 인식하며, 위험회피에 비효과적인 부분은 당기손익으로 인식하고 있습니다. 위험회피에 효과적이어서 기타포괄손익으로 인식한 부분은 향후 그 해외사업장을 처분하거나 그 해외사업장의 일부를 처분하는 시점에 기업회계기준서 제1021호 '환율변동효과'에 따라 재분류조정으로 기타포괄손익에서 당기손익으로 재분류합니다.
(7) 재고자산
재고자산의 취득원가는 매입원가, 전환원가 및 재고자산을 현재의 장소에 현재의 상태로 이르게 하는 데 발생한 기타 원가 모두를 포함하고 있으며, 재고자산의 단위원가는 선입선출법(미착품은 개별법)을 사용하여 결정하고 있습니다.
재고자산은 취득원가와 순실현가능가치 중 낮은 금액으로 측정하고 있습니다. 순실현가능가치는 통상적인 영업과정의 예상 판매가격에서 예상되는 추가 완성원가와 판매비용을 차감한 금액으로서 매 후속기간에 순실현가능가치를 재평가하고 있습니다.
재고자산의 판매시 관련된 수익을 인식하는 기간에 재고자산의 장부금액을 비용으로인식하고 있으며 재고자산을 순실현가능가치로 감액한 평가손실과 모든 감모손실은 감액이나 감모가 발생한 기간에 비용으로 인식하며, 순실현가능가치의 상승으로 인한 재고자산 평가손실의 환입은 환입이 발생한 기간의 비용으로 인식된 재고자산 금액의 차감액으로 인식하고 있습니다.
(8) 투자부동산
투자부동산은 임대수익이나 시세차익 또는 두 가지 모두를 얻기 위하여 회사가 보유하고 있는 부동산으로서 최초 인식시점에 원가로 측정하고 거래원가는 최초 측정에 포함하고 있습니다. 최초 인식 이후 투자부동산은 취득원가에서 감가상각누계액과 손상차손누계액을 차감한 금액을 장부금액으로 표시하고 있습니다.
후속원가는 자산으로부터 발생하는 미래경제적효익이 유입될 가능성이 높으며, 자산의 원가를 신뢰성 있게 측정할 수 있는 경우 자산의 장부금액에 포함하거나 적절한 경우 별도의 자산으로 인식하고 있으며, 일상적인 수선ㆍ유지와 관련하여 발생하는 원가는 발생시점에 당기손익으로 인식하고 있습니다.
투자부동산 중 토지에 대해서는 감가상각을 하지 않으며, 토지를 제외한 투자부동산은 경제적 내용연수에 따라 40년을 적용하여 정액법으로 상각하고 있습니다. 투자부동산의 감가상각방법, 잔존가치 및 내용연수는 매 보고기간말에 재검토하고 있으며, 이를 변경하는 것이 적절하다고 판단되는 경우 회계추정의 변경으로 회계처리하고 있습니다.
부동산의 용도가 변경되는 경우에만 투자부동산의 대체가 발생하고 있으며 투자부동산, 자가사용부동산, 재고자산 사이에 대체가 발생할 때에 대체 전 자산의 장부금액을 승계하고 있습니다.
투자부동산을 처분하거나, 투자부동산의 사용을 영구히 중지하고 처분으로도 더 이상의 경제적효익을 기대할 수 없는 경우에는 재무상태표에서 제거하고 있으며, 투자부동산의 폐기나 처분으로 발생하는 손익은 순처분금액과 장부금액의 차액이며 폐기나 처분이 발생한 기간에 당기손익으로 인식(판매후리스계약은 기업회계기준서 제1116호를 적용하여 처분손익으로 인식)하고 있습니다.
(9) 유형자산
유형자산은 최초 인식시점에 원가로 측정하고 최초 인식 이후 취득원가에서 감가상각누계액과 손상차손누계액을 차감한 금액을 장부금액으로 표시하고 있습니다. 유형자산의 원가는 관세 및 환급불가능한 취득 관련 세금을 가산하고 매입할인과 리베이트 등을 차감한 구입가격, 경영진이 의도하는 방식으로 자산을 가동하는 데 필요한 장소와 상태에 이르게 하는 데 직접 관련되는 원가와 자산을 해체, 제거하거나 부지를 복구하는 데 소요될 것으로 최초에 추정되는 원가로 구성되고 있습니다.
후속원가는 자산으로부터 발생하는 미래경제적효익이 유입될 가능성이 높으며, 자산의 원가를 신뢰성 있게 측정할 수 있는 경우 자산의 장부금액에 포함하거나 적절한 경우 별도의 자산으로 인식하고 있으며, 일상적인 수선ㆍ유지와 관련하여 발생하는 원가는 발생시점에 당기손익으로 인식하고 있습니다.
유형자산 중 토지에 대해서는 감가상각을 하지 않으며, 토지를 제외한 유형자산은 아래의 내용연수와 감가상각방법을 적용하여 감가상각하고 있습니다.
| 구 분 | 내 용 연 수 | 감가상각방법 |
| 건 물 | 40년 | 정액법 |
| 구 축 물 | 20년 | 정액법 |
| 기 계 장 치 | 8년 | 정액법 |
| 차량운반구 | 5년 | 정액법 |
| 공구와기구 | 5년 | 정액법 |
| 집 기 비 품 | 4년 | 정액법 |
| 시 설 장 치 | 5년 | 정액법 |
| 사용권자산 | 임차기간 | 정액법 |
| 임차자산개량권 | 임차기간 | 정액법 |
유형자산을 구성하는 일부의 원가가 당해 유형자산의 전체원가에 비교하여 유의적이라면 해당 유형자산을 감가상각할 때 그 부분은 별도로 구분하여 감가상각하고 있습니다.
유형자산의 감가상각방법, 잔존가치 및 내용연수는 매 보고기간말에 재검토하고 있으며, 이를 변경하는 것이 적절하다고 판단되는 경우 회계추정의 변경으로 회계처리하고 있습니다.
유형자산의 장부금액은 처분하는 때, 사용이나 처분을 통하여 미래경제적효익이 기대되지 않을 때 제거하고 있으며 제거로 인하여 발생하는 손익은 자산을 제거할 때 당기손익으로 인식하고 있습니다.
(10) 무형자산
회사는 자산에서 발생하는 미래경제적효익이 기업에 유입될 가능성이 높고 자산의 원가를 신뢰성 있게 측정할 수 있는 경우에 무형자산으로 인식하고 있으며, 최초 인식 후에 무형자산은 원가에서 상각누계액과 손상차손누계액을 차감한 금액을 장부금액으로 하고 있습니다.
1) 개별취득
개별 취득하는 무형자산의 원가는 구입가격(매입할인과 리베이트를 차감하고 수입관세와 환급받을 수 없는 제세금을 포함)과 자산을 의도한 목적에 사용할 수 있도록 준비하는 데 직접 관련되는 원가로 구성되고 있습니다.
2) 영업권
사업결합과 관련하여 이전대가, 피취득자에 대한 비지배지분의 금액 및 단계적으로 이루어지는 사업결합의 경우 회사가 이전에 보유하고 있던 피취득자에 대한 지분의 취득일의 공정가치의 합계금액이 취득일의 식별가능한 취득 자산과 인수 부채의 순액을 초과하는 경우 그 초과금액을 영업권으로 인식하고 있습니다.
3) 사업결합으로 인한 취득
사업결합으로 취득하는 영업권과 분리하여 인식하는 무형자산의 취득원가는 취득일의 공정가치로 측정하고 있습니다.
동일지배하 사업결합의 경우 당사의 연결재무제표를 구성하는 피합병법인의 자산 및 부채를 승계하여 장부금액으로 인식하고 있습니다.
4) 내부적으로 창출한 무형자산
연구(또는 내부 프로젝트의 연구단계)에서 발생한 지출은 발생시점에 비용으로 인식하고 있으며, 무형자산을 사용하거나 판매하기 위해 그 자산을 완성할 수 있는 기술적 실현가능성,무형자산을 완성하여 사용하거나 판매하려는 기업의 의도, 무형자산을 사용하거나 판매할 수 있는 기업의 능력, 무형자산이 미래경제적효익을 창출하는 방법, 무형자산의 개발을 완료하고 그것을 판매하거나 사용하는 데 필요한 기술적, 재정적 자원 등의 입수가능성, 개발과정에서 발생한 무형자산 관련 지출을 신뢰성 있게 측정할 수 있는 기업의 능력을 모두 제시할 수 있는 경우에만 개발활동(또는 내부 프로젝트의 개발단계)에서 발생한 무형자산을 인식하고 있습니다. 내부적으로 창출한 무형자산의 원가는 무형자산의 인식기준을 최초로 충족시킨 이후에 발생한 지출금액의 합으로 하며 그 자산의 창출, 제조 및 경영자가 의도하는 방식으로 운영될 수 있게 준비하는 데 필요한 직접 관련된 모든 원가를 포함하고 있습니다. 내부적으로 창출한 영업권은 자산으로 인식하지 아니하고 있습니다.
5) 내용연수 및 상각
내용연수가 유한한 무형자산의 경우 상각대상금액은 자산이 사용가능한 때부터 내용연수동안 정액법으로 배분하고 있습니다. 상각대상금액은 잔존가치를 차감하여 결정하고 있으며, 잔존가치는 내용연수 종료 시점에 제 3자가 자산을 구입하기로 한 약정이 있거나, 무형자산의 활성시장이 있어 잔존가치를 그 활성시장에 기초하여 결정할 수 있고 그러한 활성시장이 내용연수 종료 시점에 존재할 가능성이 높은 경우를 제외하고는 영(0)으로 하고 있습니다. 내용연수가 유한한 무형자산의 상각기간과 상각방법은 매 보고기간말에 재검토하고 있으며 이를 변경하는 것이 적절하다고 판단되는 경우 회계추정의 변경으로 회계처리하고 있습니다.
내용연수가 비한정인 무형자산은 상각하지 아니하며, 매 보고기간말 혹은 손상을 시사하는 징후가 있을 때 회수가능액과 장부금액을 비교하여 손상검사를 수행하고 있습니다. 무형자산의 내용연수가 비한정이라는 평가를 계속하여 정당화하는지를 매 보고기간말에 재검토하여 적절하지 않은 경우 회계추정의 변경으로 처리하고 있습니다.
무형자산은 아래의 내용연수와 상각방법을 적용하고 있습니다.
| 구 분 | 내 용 연 수 | 상각방법 |
| 특허권 | 3년, 10년 | 정액법 |
| 소프트웨어 | 5년 | 정액법 |
| 고객관계 | 7, 8년 | 정액법 |
| 상표권 | 10년 | 정액법 |
| 의장권 | 10년 | 정액법 |
| 회원권 | 비한정 내용연수 | - |
| 영업권 | 비한정 내용연수 | - |
6) 무형자산의 제거
무형자산은 처분하는 때, 사용이나 처분으로부터 미래경제적효익이 기대되지 않을 때 재무상태표에서 제거하며 무형자산의 제거로 인하여 발생하는 이익이나 손실은 순매각가액과 장부금액의 차이로 결정하고 자산을 제거할 때 당기손익으로 인식하고있습니다.
(11) 차입원가
회사는 의도된 용도로 사용하거나 판매가능한 상태에 이르게 하는 데 상당한 기간을 필요로 하는 적격자산의 취득, 건설 또는 생산과 직접 관련된 차입원가는 당해 자산 원가의 일부로 자본화하고 있으며 기타 차입원가는 발생기간에 비용으로 인식하고 있습니다.
적격자산을 취득하기 위한 목적으로 특정하여 차입한 자금에 한하여 회계기간동안 그 차입금으로부터 실제 발생한 차입원가에서 당해 차입금의 일시적 운용에서 생긴 투자수익을 차감한 금액을 자본화가능차입원가로 결정하고 있습니다. 일반적인 목적으로 자금을 차입하고 이를 적격자산의 취득을 위해 사용하는 경우에 한하여 당해 자산관련 지출액에 자본화이자율을 적용하는 방식으로 자본화가능차입원가를 결정하고 있으며, 자본화이자율은 회계기간에 존재하는 기업의 차입금(적격자산을 취득하기 위해 특정 목적으로 차입한 자금 제외)에서 발생된 차입원가를 가중평균하여 산정하며 회계기간동안 자본화한 차입원가는 당해 기간동안 실제 발생한 차입원가를 초과할 수 없습니다.
(12) 정부보조금
회사는 정부보조금에 부수되는 조건의 준수와 보조금 수취에 대한 합리적인 확신이 있을 경우에만 정부보조금을 인식하고 있으며 시장이자율보다 낮은 이자율의 정부대여금의 효익은 정부보조금으로 처리하고 있습니다.
수익관련정부보조금은 정부보조금으로 보전하려 하는 관련원가와 대응시키기 위해 필요한 기간에 걸쳐 체계적인 기준에 따라 정부보조금을 수익으로 인식하며, 자산관련정부보조금은 자산의 장부금액을 결정할 때 차감하여 표시하고 감가상각자산의 내용연수에 걸쳐 감가상각비를 감소시키는 방식으로 당기손익으로 인식하고 있습니다.
이미 발생한 비용이나 손실에 대한 보전 또는 향후의 관련원가 없이 회사에 제공되는즉각적인 금융지원으로 수취하는 정부보조금은 정부보조금을 수취할 권리가 발생하는 기간에 수익으로 인식하며, 비화폐성자산을 정부보조금으로 수취하는 경우 비화폐성자산의 공정가치를 평가하여 보조금과 자산 모두를 그 공정가치로 회계처리하고있습니다.
상환의무가 발생하게 된 정부보조금은 회계추정의 변경으로 회계처리하고 있습니다.
(13) 리스
리스는 리스제공자가 대가와 교환하여 식별되는 자산의 사용 통제권을 일정기간 동안 리스이용자에게 이전하는 계약입니다. 회사는 계약의 약정시점에, 계약 자체가 리스인지, 계약이 리스를 포함하는지를 판단합니다.
리스이용자 및 리스제공자는 리스계약이나 리스를 포함하는 계약에서 계약의 각 리스요소를 리스가 아닌 요소(이하'비리스요소'라고 함)와 분리하여 리스로 회계처리합니다. 다만, 회사는 리스이용자로서의 회계처리에서 실무적 간편법을 적용하여 비리스요소를 리스요소와 분리하지 않고 각 리스요소와 관련 비리스요소를 하나의 리스요소로 회계처리합니다.
회사는 리스개시일에 기초자산을 사용할 권리를 나타내는 사용권자산과 리스료를 지급할 의무를 나타내는 리스부채를 인식합니다. 다만 회사는 단기리스와 소액기초자산리스에 대하여 리스이용자의 인식, 측정 및 표시 규정을 적용하지 않는 예외규정을선택하였습니다.
사용권자산은 리스개시일에 원가로 측정하고, 후속적으로 원가에서 감가상각누계액과 손상차손누계액을 차감하고, 리스부채의 재측정에 따른 조정을 반영하여 측정합니다. 또한 사용권자산은 리스개시일부터 사용권자산의 내용연수 종료일과 리스기간종료일 중 이른 날까지 감가상각합니다. 사용권자산은 재무상태표에 '유형자산'으로 분류합니다.
리스부채는 리스개시일 현재 지급되지 않은 리스료의 현재가치로 측정됩니다. 리스의 내재이자율을 쉽게 산정할 수 있는 경우에는 그 이자율로 리스료를 할인하며 그 이자율을 쉽게 산정할 수 없는 경우에는 리스이용자의 증분차입이자율을 사용합니다. 리스부채는 후속적으로 리스부채에 대한 이자비용만큼 증가하고, 지급한 리스료를 반영하여 감소합니다.
잔존가치보증에 따라 지급할 것으로 예상되는 금액의 변동,지수나 요율(이율)의 변동, 리스기간의 변경, 매수선택권이나 연장선택권의 행사여부평가의 변동에 따라 미래 리스료가 변경되는 경우에 리스부채를 재측정합니다. 리스부채는 재무상태표에 '기타유동금융부채' 또는 '기타비유동금융부채'로 분류합니다.
단기리스(리스개시일에 리스기간이 12개월 이하인 리스)와 소액자산리스의 경우 예외 규정을 선택하여 리스료를 리스기간에 걸쳐 정액기준으로 비용을 인식합니다.
회사는 리스약정일에 리스자산의 소유에 따른 위험과 보상의 대부분을 이전하는 리스는 금융리스로 분류하고, 금융리스 이외의 모든 리스는 운용리스로 분류합니다.
1) 금융리스
리스제공자는 금융리스의 리스순투자와 동일한 금액을 금융리스채권으로 인식하고 있으며, 금융리스에서 이자수익은 리스제공자의 금융리스 순투자 금액에 대하여 일정한 기간이자율이 산출되는 방식을 적용하여 인식하고 있습니다. 금융리스에서 제조자나 판매자인 리스제공자는 일반판매에 대하여 채택하고 있는 회계정책에 따라 매출손익을 인식하고 있으며, 만약 인위적으로 낮은 이자율이 적용되었다면 시장이자율을 적용하였을 경우의 금액을 한도로 매출이익을 인식하고 있습니다. 제조자나 판매자인 리스제공자로서 부담하는 금융리스 체결원가는 리스개시일에 비용으로 인식하고 있습니다.
2) 운용리스
운용리스에서 리스료수익은 리스자산의 사용으로 생기는 효익이 감소되는 형태를 더잘 나타내는 다른 체계적인 인식기준이 없다면 리스기간에 걸쳐 정액기준으로 인식하고 있습니다. 운용리스의 체결 과정에서 발생한 리스개설직접원가는 운용리스자산의 장부금액에 더하고 리스료 수익과 같은 기준으로 리스기간에 걸쳐 비용으로 인식하며 운용리스자산의 감가상각은 리스제공자가 소유한 비슷한 자산의 보통 감가상각정책과 일치하게 회계처리하고 있습니다.
자산 이전이 판매요건을 충족하는 경우 계속 보유하는 사용권에 관련되는 자산의 종전 장부금액에 비례하여 판매후리스에서 생기는 사용권자산을 측정합니다. 이에 따라 구매자-리스제공자에게 이전한 권리에 관련되는 차손익 금액만을 인식합니다.
자산 판매대가가 그 자산의 공정가치와 다른 경우에는 그 차이를 리스료의 선급이나 구매자가 제공한 추가 금융으로 회계처리합니다.
(14) 충당부채
충당부채는 과거사건의 결과로 현재의무가 존재하고, 당해 의무를 이행하기 위하여 경제적효익을 갖는 자원이 유출될 가능성이 높으며 당해 의무의 이행에 소요되는 금액을 신뢰성 있게 추정할 수 있는 경우에 인식하고 있습니다.
충당부채로 인식하는 금액은 현재의무를 보고기간말에 이행하기 위하여 소요되는 지출에 대한 최선의 추정치로서 최선의 추정치를 구할 때에는 관련된 사건과 상황에 대한 불가피한 위험과 불확실성을 고려하고 있습니다. 화폐의 시간가치 효과가 중요한 경우 충당부채는 의무를 이행하기 위하여 예상되는 지출액의 현재가치로 평가하고 있으며 할인율은 부채의 고유한 위험과 화폐의 시간가치에 대한 현행 시장의 평가를 반영한 세전 이율이며 이 할인율에 반영되는 위험에는 미래 현금흐름을 추정할 때 고려된 위험은 반영하지 아니하고 있습니다. 현재의무를 이행하기 위하여 소요되는 지출 금액에 영향을 미치는 미래사건이 발생할 것이라는 충분하고 객관적인 증거가 있는 경우에는 그러한 미래사건을 감안하여 충당부채 금액을 추정하고 있으며, 자산의 예상처분이익은 충당부채를 측정하는 데 고려하지 아니하고 있습니다.
충당부채를 결제하기 위하여 필요한 지출액의 일부 또는 전부를 제 3자가 변제할 것이 예상되는 경우 회사가 의무를 이행한다면 변제를 받을 것이 거의 확실하게 되는 때에 한하여 변제금액을 인식하고 별도의 자산으로 회계처리하고 있으며 자산으로 인식하는 금액은 관련 충당부채 금액을 초과할 수 없습니다.
매 보고기간말마다 충당부채의 잔액을 검토하고, 보고기간말 현재 최선의 추정치를 반영하여 조정하며 의무이행을 위하여 경제적효익을 갖는 자원이 유출될 가능성이 더 이상 높지 아니한 경우에는 관련 충당부채를 환입하고 있습니다. 충당부채는 최초인식과 관련있는 지출에만 사용하고 있습니다.
(15) 전환사채
회사가 발행한 전환사채는 계약의 실질에 따라 금융부채와 자본으로 각각 분류하고 있습니다. 최초인식시점에서 금융부채의 공정가치는 계약상 정해진 미래현금흐름을 당해 금융상품과 동일한 조건 및 유사한 신용상태를 가지며 실질적으로 동일한 현금흐름을 제공하지만 전환권이 없는 채무상품에 적용되는 그 시점의 시장이자율로 할인한 현재가치로 추정하고 전환권의 행사로 인하여 소멸되거나 만기까지 유효이자율법을 적용한 상각후원가로 측정하며, 자본요소인 전환권의 장부금액은 전환사채 전체의 공정가치에서 금융부채의 공정가치를 차감하여 법인세효과를 반영한 금액으로 결정하고 이후 재측정하지 않고 있습니다. 전환사채의 발행과 관련된 거래원가는 배분된 발행금액에 비례하여 금융부채와 자본에 배분하고 있습니다.
(16) 자기주식
회사가 자기지분상품을 재취득하는 경우 이러한 지분상품은 자본에서 자기주식의 과목으로 하여 차감하고 있습니다. 자기지분상품을 매입 또는 매도하거나 발행 또는 소각하는 경우의 손익은 당기손익으로 인식하지 아니하고 있습니다.
(17) 주식기준보상
주식기준보상거래에서 제공받는 재화나 용역은 그 재화나 용역을 제공받는 날에 인식하고 있습니다. 주식결제형 주식기준보상거래로 재화나 용역을 제공받는 경우에는그에 상응한 자본의 증가를 인식하고, 현금결제형 주식기준보상거래로 재화나 용역을 제공받는 경우에는 그에 상응한 부채의 증가를 인식하고 있으며, 주식기준보상거래에서 제공받는 재화나 용역이 자산의 인식요건을 충족하지 못하는 경우에는 비용으로 인식하고 있습니다.
1) 주식결제형 주식기준보상거래
회사가 재화나 용역을 제공받는 대가로 자신의 지분상품(주식 또는 주식선택권 등)을부여하는 주식기준보상거래 혹은 재화나 용역을 제공받지만 이를 제공한 자에게 주식기준보상거래를 결제할 의무가 없는 주식기준보상거래에 대하여, 제공받는 재화나용역과 그에 상응하는 자본의 증가를 제공받는 재화나 용역의 공정가치로 직접 측정하며, 제공받는 재화나 용역의 공정가치를 신뢰성 있게 추정할 수 없다면 제공받는 재화나 용역과 그에 상응하는 자본의 증가는 부여한 지분상품의 공정가치에 기초하여 간접 측정하고 있습니다. 특정기간의 용역을 제공하여야 부여된 지분상품이 가득되는 경우 지분상품의 대가에 해당하는 용역을 미래 가득기간에 제공받는 것으로 보아 당해 용역은 가득기간에 배분하여 인식하며 그에 상응하여 자본의 증가를 인식하고 있습니다.
시장조건이 아닌 가득조건은 거래금액 측정시 포함되는 지분상품의 수량을 조정할 때 고려하여 부여한 지분상품의 대가로 제공받는 재화나 용역에 대해 인식하는 금액이 궁극적으로 가득되는 지분상품의 수량에 기초하여 결정될 수 있도록 하고 있으며 후속적인 정보에 비추어 볼 때 미래에 가득될 것으로 예상되는 지분상품의 수량이 직전 추정치와 다르다면 당해 추정치를 변경하여 가득일에는 궁극적으로 가득된 지분상품의 수량과 일치하도록 당해 추정치를 변경하고 있습니다. 목표주가와 같은 시장조건은 부여한 지분상품의 공정가치를 추정할 때 고려하고 있습니다.
지정된 가득조건(시장조건 제외)이 충족되지 않아 지분상품이 가득되지 못하는 경우를 제외하고는 지분상품을 부여한 당시의 조건을 변경하는지, 부여한 지분상품을 취소하거나 중도청산하는지 여부와 관계없이 제공받는 근무용역은 최소한 지분상품의 부여일당시의 공정가치에 따라 인식하고 있으며 주식기준보상약정의 총공정가치를 증가시키거나 종업원에게 유리하게 조건을 변경하는 경우에는 추가로 조건변경의 효과를 인식하고 있습니다.
부여한 지분상품이 가득기간 중에 취소되거나 중도청산되는 경우에는 취소나 중도청산으로 인해 부여한 지분상품이 일찍 가득된 것으로 보아 취소나 중도청산이 없다면 잔여가득기간에 제공받을 용역에 대해 인식될 금액을 즉시 인식하며, 취소나 중도청산시 종업원 등에게 지급하는 금액은 자기지분상품의 재매입으로 보아 자본에서 차감하고 있습니다.
2) 현금결제형 주식기준보상거래
회사가 재화나 용역을 제공받는 대가로 회사의 지분상품(주식 또는 주식선택권 등)의가격(또는 가치)에 기초한 금액만큼 현금이나 그 밖의 자산을 지급해야 하는 부채를 재화나 용역의 공급자에게 부담하는 주식기준보상거래에 대하여 제공받는 재화나 용역과 그 대가로 부담하는 부채를 부채의 공정가치로 측정하고 부채가 결제될 때까지 매 보고기간말과 결제일에 부채의 공정가치를 재측정하고 공정가치의 변동액은 당기손익으로 인식하고 있으며, 종업원에게서 제공받는 근무용역과 그 대가로 부담하는 부채는 근무용역을 제공받는 기간에 인식하고 있습니다.
(18) 수익
당사는 고객에게 약속한 재화나 용역, 즉 자산을 이전하여 수행의무를 이행할 때(또는, 기간에 걸쳐 이행하는대로) 수익을 인식하고 있습니다.
1) 재화의 판매
당사는 고객에게 구명정, 유리섬유파이프 및 의약외품(알콜스왑, 검체채취용 도구 등) 판매와 관련하여 고객에게 이전되어 고객이 인수할 때 수익을 인식합니다.
2) 로열티
당사는 판매량 또는 사용량에 따른 로열티는 라이선스 부여 후 후속적인 판매 또는 생산활동이 발생한 시점에 수익을 인식합니다.
당사는 구명정, 유리섬유파이프 및 의약외품 등을 제조 및 생산하여 고객에게 제공하는 사업을 영위하고 있으며, 당사의 대부분의 수익은 이와 관련되어 있습니다.
당사가 거래 당사자가 아니라 공급자의 대리인의 역할을 수행하는 경우 고객에게 청구한 금액에서 재화나 용역의 실질적인 공급자에게 지급해야 할 금액을 차감한 순액을 수수료 수익으로 인식하고 있습니다.
(19) 종업원급여
1) 단기종업원급여
단기종업원급여는 임금, 사회보장분담금, 종업원이 관련 근무용역을 제공하는 회계기간의 말부터 12개월 이내에 결제될 유급연차휴가 또는 유급병가 등과 같은 단기유급휴가, 종업원이 관련 근무용역을 제공하는 회계기간의 말부터 12개월 이내에 지급될 이익분배금과 상여금 및 현직종업원을 위한 비화폐성급여를 포함하고 있습니다. 종업원이 회계기간에 근무용역을 제공한 때 근무용역과 교환하여 지급이 예상되는 단기종업원급여의 할인되지 않은 금액을 이미 지급한 금액을 차감한 후 미지급비용으로 인식하며, 이미 지급한 금액이 해당 급여의 할인되지 않은 금액보다 많은 경우에는 그 초과액 때문에 미래 지급액이 감소하거나 현금이 환급되는 만큼을 선급비용으로 인식하며, 다른 한국채택국제회계기준서에 따라 해당 급여를 자산의 원가에 포함하는 경우를 제외하고는 비용으로 인식하고 있습니다.
2) 퇴직급여
(가) 확정기여제도
확정기여제도는 회사가 별개의 실체(기금)에 고정 기여금을 납부하고 회사의 법적의무나 의제의무는 기금에 출연하기로 약정한 금액으로 한정되며 종업원이 받을 퇴직급여액은 회사와 종업원이 퇴직급여제도나 보험회사에 출연하는 기여금과 그 기여금에서 발생하는 투자수익에 따라 결정되는 퇴직급여제도입니다. 일정기간 종업원이 근무용역을 제공하였을 때 그 근무용역과 교환하여 확정기여제도에 납부해야 할 기여금은 이미 납부한 기여금을 차감한 후 미지급비용으로 인식하고, 이미 납부한 기여금이 보고기간말 이전에 제공된 근무용역에 대해 납부하여야 하는 기여금을 초과하는 경우에는 초과 기여금 때문에 미래 지급액이 감소하거나 현금이 환급되는 만큼을 선급비용으로 인식하며, 다른 한국채택국제회계기준서에 따라 해당 기여금을 자산의 원가에 포함하는 경우를 제외하고는 비용으로 인식하고 있습니다.
(나) 확정급여제도
확정급여제도는 확정기여제도 이외의 모든 퇴직급여제도로서 순확정급여부채로 인식하는 금액은 보고기간말 현재 확정급여채무의 현재가치에서 관련 확정급여채무를 직접 결제하는 데 사용할 수 있는 사외적립자산의 보고기간말 현재 공정가치를 차감한 금액이며, 확정급여채무는 매년 독립적인 보험계리법인에 의해 예측단위적립방식에 따라 산정하고 있습니다.
확정급여채무의 현재가치는 급여가 지급될 통화로 표시되고 관련 확정급여부채의 지급시점과 만기가 유사한 우량회사채의 시장수익률로 기대미래현금유출액을 할인하여 산정하고 있습니다.
확정급여원가 중 근무원가와 순확정급여부채(자산)의 순이자는 당기손익으로 인식하며, 순확정급여부채(자산)의 재측정요소는 기타포괄손익으로 인식하고 있습니다. 한편, 기타포괄손익에 인식되는 순확정급여부채(자산)의 재측정요소는 후속기간에 당기손익으로 재분류하지 아니하고 있습니다.
부의 순확정급여부채인 순확정급여자산은 제도로부터 환급받거나 제도에 대한 미래기여금이 절감되는 방식으로 이용가능한 경제적효익의 현재가치의 합계를 한도로 인식하고 있습니다.
회사가 급여를 과거근무용역에 귀속시키는 확정급여제도를 새로 도입하거나 기존의 확정급여제도에서 과거근무용역에 대하여 지급해야 하는 급여를 변경하는 경우 발생하는 과거근무원가는 제도개정으로 인하여 발생하는 부채의 변동금액으로 측정하고 즉시 비용으로 인식하고 있습니다.
3) 기타장기종업원급여
기타장기종업원급여는 종업원이 관련 근무용역을 제공한 회계기간의 말부터 12개월이 지난 후에 결제될 것으로 예상되는 장기유급휴가, 그 밖의 장기근속급여, 장기장애급여, 이익분배금과 상여금, 이연보상을 포함하고 있습니다. 기타장기종업원급여와 관련하여 부채로 인식할 금액은 보고기간말 현재 확정급여채무의 현재가치에서 관련 확정급여채무를 직접 결제하는 데 사용할 수 있는 사외적립자산의 보고기간말 현재 공정가치를 차감하여 인식하고 있습니다.
4) 해고급여
해고급여에 대한 부채와 비용은 회사가 해고급여의 제안을 더 이상 철회할 수 없을 때와 기업회계기준서 제1037호 '충당부채, 우발부채, 우발자산'의 적용범위에 포함되고 해고급여의 지급을 수반하는 구조조정에 대한 원가를 인식할 때 중 이른 날에인식합니다.
(20) 자산손상
재고자산, 기업회계기준서 제1115호 '고객과의 계약에서 생기는 수익'에 따라 인식하는 계약자산과 계약을 체결하거나 이행하기 위해 든 원가에서 생기는 자산, 이연법인세자산, 종업원급여에서 생기는 자산,금융자산, 공정가치로 측정되는 투자부동산, 매각예정비유동자산 등을 제외한 모든 자산의 손상은 아래의 방법으로 손상차손을 인식하고 있습니다.
내용연수가 비한정인 무형자산, 아직 사용할 수 없는 무형자산 및 사업결합으로 취득한 영업권에 대해서는 자산손상을 시사하는 징후가 있는지에 관계없이 매년 회수가능액을 추정하고 장부금액과 비교하여 손상검사를 하고 있으며, 그 외의 자산은 매 보고기간말마다 자산손상을 시사하는 징후가 있는지를 검토하고 그러한 징후가 있다면 개별 자산별로 회수가능액을 추정하며 개별 자산의 회수가능액을 추정할 수 없다면 그 자산이 속하는 현금창출단위의 회수가능액을 추정하고 있습니다.
자산의 회수가능액은 자산 또는 현금창출단위의 순공정가치와 사용가치 중 더 많은 금액으로 측정하고 있습니다. 자산의 회수가능액이 장부금액에 미달하는 경우 자산의 장부금액을 회수가능액으로 감소시키며, 손상차손은 즉시 당기손익으로 인식하고 있습니다.
손상검사 목적상 사업결합으로 취득한 영업권은 사업결합으로 인한 시너지효과의 혜택을 받게 될 것으로 기대되는 각 현금창출단위에 취득일로부터 배분되고 있습니다. 영업권이 배분된 현금창출단위에 대해서는 매년 그리고 손상을 시사하는 징후가 있을 때마다 영업권을 포함한 현금창출단위의 장부금액과 회수가능액을 비교하여 손상검사를 하고 있으며 현금창출단위의 장부금액이 회수가능액을 초과하는 경우에는 손상차손을 인식하고 있습니다. 현금창출단위의 손상차손은 우선 현금창출단위에 배분된 영업권의 장부금액을 감소시키고 그 다음 현금창출단위에 속하는 다른 자산에 각각 장부금액에 비례하여 배분하고 있습니다.
매 보고기간말마다 영업권을 제외한 자산에 대해 과거에 인식한 손상차손이 더 이상 존재하지 않거나 감소된 것을 시사하는 징후가 있는지를 검토하여 징후가 있는 경우 당해 자산의 회수가능액을 추정하고 있으며 직전 손상차손의 인식시점 이후 회수가능액을 결정하는 데 사용된 추정치에 변화가 있는 경우에만 환입하고 있습니다. 손상차손환입으로 증가된 장부금액은 과거에 손상차손을 인식하기 전 장부금액의 감가상각 또는 상각 후 잔액을 초과할 수 없으며, 손상차손환입은 즉시 당기손익으로 인식하고 있습니다. 현금창출단위의 손상차손환입은 현금창출단위를 구성하는 자산들(영업권 제외)의 장부금액에 비례하여 배분하며, 영업권에 대해 인식한 손상차손은 후속기간에 환입하지 않고 있습니다.
(21) 법인세
법인세비용(수익)은 당기법인세비용(수익)과 이연법인세비용(수익)으로 구성되고 있습니다. 당기법인세와 이연법인세는 수익이나 비용으로 인식하여 당기손익에 포함하고 있으며, 동일 회계기간 또는 다른 회계기간에 자본에 직접 가감되는 항목과 관련된 당기법인세와 이연법인세는 자본에 직접 가감하고 있습니다.
1) 당기법인세
당기법인세는 회계기간의 과세소득(세무상결손금)에 대하여 납부할(환급받을) 법인세액이며, 과세소득(세무상결손금)은 과세당국이 제정한 법규에 따라 납부할(환급받을) 법인세를 산출하는 대상이 되는 회계기간의 이익(손실)으로서 포괄손익계산서의 손익과는 차이가 있습니다.
당기 및 과거기간의 당기법인세부채(자산)는 보고기간말까지 제정되었거나 실질적으로 제정된 세율(및 세법)을 사용하여, 과세당국에 납부할(과세당국으로부터 환급받을) 것으로 예상되는 금액으로 측정하고 있습니다.
당기 및 과거기간의 당기법인세 중 납부되지 않은 부분을 부채로 인식하며, 과거기간에 납부하여야 할 금액을 초과해서 납부하였다면 그 초과금액은 자산으로 인식하고 있으며, 과거 회계기간의 당기법인세에 대하여 소급공제가 가능한 세무상결손금과 관련된 혜택은 자산으로 인식하고 있습니다.
2) 이연법인세
회사는 모든 가산할 일시적차이에 대하여 이연법인세부채를 인식하고 있습니다. 다만 영업권을 최초로 인식하는 경우와 자산·부채가 최초로 인식되는 거래가 사업결합거래가 아니고 거래 당시의 회계이익이나 과세소득(세무상결손금)에 영향을 미치지 아니하는 거래인 경우 및 종속기업·지점 및 관계기업에 대한 투자자산 그리고 공동약정투자지분과 관련된 가산할 일시적차이에 대하여 지배기업· 투자자 또는 참여자가 일시적차이의 소멸시점을 통제할 수 있고 예측가능한 미래에 일시적차이가 소멸하지 않을 가능성이 높을 경우에 발생하는 이연법인세부채는 인식하지 아니하고 있습니다.
회사는 차감할 일시적차이가 사용될 수 있는 과세소득의 발생가능성이 높은 경우에 모든 차감할 일시적차이에 대하여 이연법인세자산을 인식하고 있습니다. 다만, 자산이나 부채를 최초로 인식할 때 발생하는 거래로 사업결합거래가 아니고 거래 당시 회계이익이나 과세소득(세무상결손금)에 영향을 미치지 않는 거래인 경우 및 종속기업·지점 및 관계기업에 대한 투자자산 그리고 공동약정투자지분과 관련된 모든 차감할 일시적차이에 대하여 일시적차이가 예측가능한 미래에 소멸할 가능성이 높지않거나 일시적차이가 사용될 수 있는 과세소득이 발생할 가능성이 높지 않은 경우에는 이연법인세자산은 인식하지 아니하고 있습니다. 미사용 세무상결손금과 세액공제가 사용될 수 있는 미래 과세소득의 발생가능성이 높은 경우 그 범위 안에서 이월된 미사용 세무상결손금과 세액공제에 대하여 이연법인세자산을 인식하고 있습니다.
이연법인세자산의 장부금액은 매 보고기간말에 검토하며 이연법인세자산의 일부 또는 전부에 대한 혜택이 사용되기에 충분한 과세소득이 발생할 가능성이 더 이상 높지않다면 이연법인세자산의 장부금액을 감액시키고 감액된 금액은 사용되기에 충분한 과세소득이 발생할 가능성이 높아지면 그 범위 내에서 환입하고 있습니다.
이연법인세 자산과 부채는 보고기간말까지 제정되었거나 실질적으로 제정된 세율(및세법)에 근거하여 당해 자산이 실현되거나 부채가 결제될 회계기간에 적용될 것으로 기대되는 세율을 사용하여 측정하고 있으며 이연법인세 자산과 부채는 할인하지 아니하고 있습니다.
회사가 당기법인세자산과 당기법인세부채를 상계할 수 있는 법적으로 집행가능한 권리를 가지고 있으며 동일한 과세당국에 의해서 부과되는 법인세와 관련하여 이연법인세자산과 이연법인세부채를 상계하고 있습니다.
(22) 주당이익
회사는 기본주당이익과 희석주당이익을 보통주에 귀속되는 계속영업손익과 당기순손익에 대하여 계산하고 포괄손익계산서에 표시하고 있습니다.
기본주당이익은 보통주에 귀속되는 특정 회계기간의 당기순손익을 그 기간에 유통된보통주식수를 가중평균한 주식수로 나누어 계산하고 있으며, 보통주에 귀속되는 금액은 계속영업손익과 당기순손익 각각의 금액에서 자본으로 분류된 우선주에 대한 세후우선주 배당금,우선주 상환시 발생한 차액 및 유사한 효과를 조정한 금액입니다.
희석주당이익은 모든 희석효과가 있는 잠재적보통주의 영향을 고려하여 보통주에 귀속되는 당기순손익 및 가중평균유통보통주식수를 조정하여 계산하고 있습니다.
(23) 매각예정비유동자산
비유동자산(또는 처분자산집단)의 장부금액이 계속사용이 아닌 매각거래를 통하여 주로 회수될 것이라면 이를 매각예정으로 분류하며 순공정가치와 장부금액 중 작은 금액으로 측정하고, 그 자산은 감가상각(또는 상각)하지 아니하고 있습니다. 매각예정으로 분류된 비유동자산은 다른 자산과 별도로 재무상태표에 표시하며 매각예정으로 분류된 처분자산집단에 포함되는 자산이나 부채는 다른 자산이나 부채와 별도로 재무상태표에 표시하고 있습니다.
(24) 중단영업
회사는 별도의 주요 사업계열이나 영업지역을 처분하거나 매각예정으로 분류되는 경우 등을 중단영업으로 분류하고 있으며, 중단영업이 있는 경우 세후 중단영업손익 등을 포괄손익계산서에 단일금액으로 표시하고 중단영업의 수익, 비용 및 세전 중단영업손익 등을 공시하고 있습니다. 또한, 회사는 비교표시되는 과거재무제표에 중단영업관련 공시사항을 다시 표시하고 있습니다.
(25) 오류수정
특정기간에 미치는 오류의 영향이나 오류의 누적효과를 실무적으로 결정할 수 없는 경우를 제외하고는 중요한 전기오류가 발견된 이후 최초로 발행을 승인하는 재무제표에 오류가 발생한 과거기간의 재무제표가 비교표시되는 경우 그 재무정보를 재작성하고 있습니다.
(26) 중요한 회계추정 및 판단
재무제표의 작성시 경영진은 회계정책의 적용이나 자산, 부채, 수익, 비용의 장부금액 및 우발부채의 금액에 영향을 미칠 수 있는 판단과 추정 및 가정을 하여야 합니다.보고기간말 현재 이러한 추정치는 경영진의 최선의 판단 및 추정에 따라 이루어지고 있으며 추정치와 추정에 대한 가정은 지속적으로 검토되고 있으나 향후 경영환경의 변화에 따라 실제 결과와는 중요하게 다를 수도 있습니다.
회계정책을 적용하는 과정에서 추정에 관련된 공시와는 별도로 재무제표에 인식되는금액에 가장 유의적인 영향을 미칠 수 있는 경영진이 내린 판단 및 미래에 대한 가정과 보고기간말의 추정 불확실성과 관련하여 다음 회계연도에 자산과 부채의 장부금액에 대한 중요한 조정을 유발할 수 있는 유의적인 위험을 내포하고 있는 사항은 다음과 같습니다.
ㆍ 주석 3: 공정가치평가
ㆍ 주석 5: 매출채권, 기타금융자산의 기대신용손실
ㆍ 주석 10: 종속기업 및 관계기업투자주식 손상차손
ㆍ 주석 13: 무형자산
3. 위험관리
금융상품과 관련하여 당사는 신용위험, 유동성위험 및 시장위험에 노출되어 있습니다. 본 주석은 당사가 노출되어 있는 위의 위험에 대한 정보와 당사의 위험관리 목표,정책, 위험 평가 및 관리 절차, 그리고 자본관리에 대해 공시하고 있습니다. 추가적인계량적 정보에 대해서는 본 재무제표 전반에 걸쳐서 공시되어 있습니다.
(1) 금융위험관리
당사의 위험관리 체계를 구축하고 감독할 책임은 이사회에 있습니다. 이사회는 당사의 위험관리 정책을 개발하고 감독하고 있으며 중장기 경영계획 및 단기 경영전략에 대해 정기적으로 보고받고 승인하고 있습니다.
당사의 위험관리 정책은 당사가 직면한 위험을 식별 및 분석하고, 적절한 위험 한계치 및 통제를 설정하고, 위험이 한계치를 넘지 않도록 하기 위해 수립되었습니다. 위험관리 정책은 시장 상황과 당사의 활동의 변경을 반영하기 위해 정기적으로 검토되고 있습니다. 당사는 훈련 및 관리기준, 절차를 통해 모든 종업원들이 자신의 역할과 의무를 이해할 수 있는 엄격하고 구조적인 통제환경을 구축하는 것을 목표로 하고 있습니다.
1) 신용위험
① 신용위험에 대한 노출
금융자산의 장부금액은 신용위험에 대한 최대노출정도를 나타냅니다. 당사는 현금및현금성자산을 신용등급이 우수한 금융기관에 예치하고 있어, 금융기관으로부터의 신용위험은 제한적입니다. 또한, 당사가 보유하고 있는 채무증권은 채무불이행 위험이 낮고, 차입자가 계약상 현금흐름 지급의무를 이행할 수 있는 능력이 있기 때문에 신용위험이 낮은 것으로 보고 있습니다.
당사의 신용위험에 대한 최대 노출정도는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 현금및현금성자산 | 48,724,359 | 36,642,797 |
| 매출채권 | 27,808,265 | 18,707,735 |
| 기타금융자산 | 15,155,408 | 11,663,862 |
| 당기손익-공정가치 측정 금융자산 | 47,318,742 | 22,048,583 |
| 합 계 | 139,006,775 | 89,062,977 |
당반기말 현재 당사는 종속기업인 Elevar Therapeutics, Inc.와 관계기업인 현대요트㈜의 거래대금, 차입금 및 계약이행보증 등에 대한 지급보증을 제공함에 따라 추가적인 신용위험에 노출되어 있습니다(주석 29 참조).
② 손상차손
당사는 매출채권과 기타채권에 대한 기대신용손실을 측정하여 충당금을 설정하고 있습니다. 기대신용손실과 각 연령별로 손상된 금액은 다음과 같습니다.
| (단위: 천원) | ||||||||
|---|---|---|---|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | ||||||
| 기대손실율 | 채권잔액 | 손상된 금액 | 장부금액 | 기대손실율 | 채권잔액 | 손상된 금액 | 장부금액 | |
| 3개월 이하(*1) | 0.02% | 64,162,005 | (14,537) | 64,147,468 | 0.16% | 43,783,095 | (69,193) | 43,713,902 |
| 3~6개월 | 11.33% | 715,287 | (81,063) | 634,224 | 4.99% | 2,702 | (135) | 2,567 |
| 6~9개월 | 7.04% | 95,522 | (6,722) | 88,800 | 18.32% | 15,887 | (2,911) | 12,977 |
| 9~12개월 | 69.93% | 12,429 | (8,692) | 3,737 | 0.00% | - | - | - |
| 12개월 초과(*2) | 41.23% | 16,450,332 | (6,781,859) | 9,668,474 | 42.06% | 16,124,010 | (6,781,859) | 9,342,152 |
| 합 계 | 81,435,576 | (6,892,872) | 74,542,704 | 59,925,694 | (6,854,097) | 53,071,597 | ||
(*1) 2021년 귀속분 리보세라닙 로열티 매출채권에 대한 추정치 11,724,092천원이 포함되어 있습니다.
(*2) 당반기말 현재, 2020년 귀속분 리보세라닙 로열티 9,663,745천원은 당사의 100% 자회사인 Hyundai Lifeboats Shanghai Co., Ltd.의 계좌에 예치되어 있습니다.
매출채권과 기타금융자산에 대한 대손충당금의 기중 변동내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전기 |
| 기초금액 | 36,854,097 | 45,840,878 |
| 합병승계 | 17,332 | - |
| 대손상각비(환입) | 22,941 | 723,133 |
| 기타의대손상각비(환입) | (1,497) | (1,163,013) |
| 제각(*) | - | (8,546,902) |
| 기말금액 | 36,892,872 | 36,854,097 |
(*) 폐업 등으로 회수가 불가능한 채권을 장부에서 제각하였습니다.
2) 유동성위험
금융부채의 계약상 만기는 다음과 같습니다. 금액은 이자지급액을 포함하고, 상계약정의 효과는 포함하지 않았습니다.
① 당반기말
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 장부금액 | 계약상 현금흐름 | 3개월이내(*) | 3~12개월(*) | 1~2년(*) | 2년초과 |
| 매입채무 | 4,533,212 | 4,533,212 | 4,533,212 | - | - | - |
| 기타금융부채 | 9,465,819 | 9,479,942 | 9,023,480 | 238,854 | 180,649 | 36,959 |
| 차입금 | 110,053,697 | 127,564,030 | 2,136,478 | 25,707,600 | 99,366,752 | 353,200 |
| 합 계 | 124,052,727 | 141,577,184 | 15,693,170 | 25,946,454 | 99,547,401 | 390,159 |
(*) 전환사채 및 신주인수권부사채의 조기상환권이 청구 가능한 가장 빠른 시기에 행사됨을 가정하였습니다.
② 전기말
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 장부금액 | 계약상 현금흐름 | 3개월이내(*) | 3-12개월 | 1-2년(*) | 2년초과 |
| 매입채무 | 939,313 | 939,313 | 939,313 | - | - | - |
| 기타금융부채 | 5,524,956 | 5,623,236 | 4,910,029 | 482,559 | 186,848 | 43,799 |
| 차입금 | 64,726,776 | 70,010,148 | 11,496,116 | 3,600 | 58,154,832 | 355,600 |
| 합 계 | 71,191,045 | 76,572,696 | 17,345,458 | 486,159 | 58,341,680 | 399,399 |
(*) 전환사채 및 신주인수권부사채의 조기상환권이 청구 가능한 가장 빠른 시기에 행사됨을 가정하였습니다.
3) 환위험
① 환위험에 대한 노출
당사는 기능통화인 원화 이외의 통화로 표시되는 거래로 인하여 환율변동위험에 노출되어 있습니다. 외화로 표시된 화폐성자산의 장부금액은 다음과 같습니다.
| (단위 : USD, CNY) | ||||
|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | ||
| USD | CNY | USD | CNY | |
| 자산: | ||||
| 외화예금 | 9,139,602 | - | 552,080 | - |
| 매출채권 | 5,046,357 | 60,825,380 | 416,440 | 90,706,765 |
| 미수금 | - | 50,156,511 | - | - |
| 소 계 | 14,185,958 | 110,981,891 | 968,519 | 90,706,765 |
| 부채: | ||||
| 매입채무 | - | - | - | - |
| 합 계 | 14,185,958 | 110,981,891 | 968,519 | 90,706,765 |
외화표시 화폐성자산에 적용된 환율은 다음과 같습니다.
| (단위: 원) | ||||
|---|---|---|---|---|
| 구 분 | 평균환율 | 기말환율 | ||
| 당반기 | 전반기 | 당반기말 | 전기말 | |
| USD | 1,232.94 | 1,117.73 | 1,292.90 | 1,185.50 |
| CNY | 190.04 | 172.75 | 192.75 | 186.26 |
② 민감도분석
당사는 내부적으로 원화 환율 변동에 대한 환위험을 정기적으로 측정하고 있습니다.
당반기 및 전기 중 각 외화에 대한 원화환율 5% 변동 시 환율변동이 세전손익에 미치는 영향은 다음과 같습니다.
| (단위 : 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전기 | ||
| 5% 상승시 | 5 % 하락시 | 5% 상승시 | 5 % 하락시 | |
| USD | 917,051 | (917,051) | 57,490 | (57,409) |
| CNY | 1,069,588 | (1,069,588) | 844,752 | (844,752) |
4) 이자율위험
① 당사가 보유하고 있는 이자부 금융상품은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당반기말 | 전기말 |
| 고정이자율: | ||
| 금융자산 | 98,043,102 | 61,496,653 |
| 금융부채 | 110,053,697 | 64,726,776 |
| 합 계 | (12,010,596) | (3,230,123) |
| 변동이자율: | ||
| 금융부채 | - | - |
② 고정이자율 금융상품의 공정가치 민감도 분석
당사는 고정이자율 금융상품을 당기손익인식금융상품으로 처리하고 있지 않으며, 이자율스왑과 같은 파생상품을 공정가치위험회피회계의 위험회피수단으로 지정하지 않았습니다. 따라서, 이자율의 변동은 손익에 영향을 주지 않습니다.
③ 변동이자율 금융상품의 현금흐름 민감도 분석
당반기말 현재 변동이자율 금융상품이 존재하지 않아, 이자율의 변동은 손익에 영향을 주지 않습니다.
5) 공정가치
공정가치 서열체계를 포함한 금융자산과 금융부채의 장부금액과 공정가치는 다음과 같습니다. 장부금액이 공정가치의 합리적인 근사치에 해당하여 공정가치를 측정하지않은 금융자산과 금융부채에 대한 공정가치 정보는 포함하고 있지 않습니다.
① 당반기말
| (단위:천원) | ||||
|---|---|---|---|---|
| 구 분 | 장부금액 | 수준1 | 수준2 | 수준3 |
| 공정가치로 측정되는 금융자산: | ||||
| 당기손익-공정가치 측정 | 54,433,682 | 22,469,317 | 31,962,955 | 1,410 |
| 기타포괄손익-공정가치 측정 | 5,793,068 | 719,227 | - | 5,073,841 |
| 합 계 | 60,226,750 | 23,188,544 | 31,962,955 | 5,075,251 |
② 전기말
| (단위:천원) | ||||
|---|---|---|---|---|
| 구 분 | 장부금액 | 수준1 | 수준2 | 수준3 |
| 공정가치로 측정되는 금융자산: | ||||
| 당기손익-공정가치 측정 | 22,049,993 | - | 22,048,583 | 1,410 |
| 기타포괄손익-공정가치 측정 | 6,073,286 | 999,445 | - | 5,073,841 |
| 합 계 | 28,123,279 | 999,445 | 22,048,583 | 5,075,251 |
③ 가치평가기법
당반기말 현재 당사는 공정가치 서열체계에서 수준 2와 수준 3으로 분류되는 반복적인 공정가치측정치, 비반복적인 공정가치측정치, 공시되는 공정가치에 대해 다음의 가치평가기법을 사용하고 있습니다.
사용된 가치평가기법과 투입변수는 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 공정가치 | 가치평가기법 | 수준 | 투입변수 | 투입변수 범위 |
| 에이치엘비제약㈜ 전환사채(*) | 23,272,820 | 현재가치기법, 이항모형 | 2 | 가중평균자본비용 | 14.87% |
| 가격 변동성 | 76.70% | ||||
| 무위험 할인율 | 3.20% | ||||
| 에이치엘비㈜ 제36회 전환사채 매도청구권 |
2,355,384 | 현재가치기법, 이항모형 | 2 | 가중평균자본비용 | 17.54% |
| 가격 변동성 | 60.30% | ||||
| 무위험 할인율 | 3.16% | ||||
| 에이치엘비㈜ 제37회 신주인수권부사채 매도청구권 |
1,740,936 | 현재가치기법, 이항모형 | 2 | 가중평균자본비용 | 17.54% |
| 가격 변동성 | 60.30% | ||||
| 무위험 할인율 | 3.16% | ||||
| 노터스 제1회 전환사채 매도청구권 | 3,017,209 | 현재가치기법, 이항모형 | 2 | 가중평균자본비용 | 5.26% |
| 가격 변동성 | 68.42% | ||||
| 무위험 할인율 | 1.96% | ||||
| 저축성보험 | 1,576,605 | 순자산가치법 | 2 | 해지환급금 | - |
| ㈜씨엘팜 지분 | 5,073,841 | 현금흐름할인법 | 3 | 가중평균자본비용 | 19.55% |
| 영구성장률 | 0.00% | ||||
| 무위험 할인율 | 2.26% | ||||
| 조합출자금 | 1,410 | 원가접근법 | 3 | 개별 자산 및 부채의 공정가치 | - |
(*)투입변수 중 가격 변동성이 증가하거나 가중평균자본비용이 감소하면 공정가치가 증가하며, 무위험 할인율의 감소도 공정가치를 증가시킬 수 있습니다.
④ 수준 3 공정가치
당반기 중 수준 1과 수준 2간의 대체는 없었으며, 수준 3 공정가치 분류되는 금융자산의 당반기 중 변동내용은 없습니다.
⑤ 공정가치 서열체계
당사는 공정가치 측정에 사용된 투입변수의 유의성을 반영하는 공정가치 서열체계에따라 공정가치 측청치를 분류하고 있으며, 공정가치 서열체계의 수준은 다음과 같습니다.
| 구 분 | 투입변수의 유의성 |
|---|---|
| 수준 1 | 동일한 자산이나 부채에 대한 활성시장의 공시가격 |
| 수준 2 | 직접적으로 또는 간접적으로 관측가능한, 자산이나 부채에 대한 투입변수 |
| 수준 3 | 관측가능한 시장자료에 기초하지 않은, 자산이나 부채에 대한 투입변수 |
6) 자본관리
당사의 자본관리는 건전한 자본구조를 유지하며, 주주이익의 극대화를 목적으로 하고 있습니다. 당사는 최적 자본구조 달성을 위해 부채비율과 순차입금비율 등의 재무비율을 자본관리지표로 사용하고 있습니다. 부채비율은 부채총계를 자본총계로 나누어 산출하고 있으며, 순차입금비율은 순차입금을 자본총계로 나누어 산출하고 있습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 부채비율: | ||
| 부채총계(A) | 140,475,738 | 71,798,680 |
| 자본총계(B) | 790,461,729 | 730,424,693 |
| 부채비율(A/B) | 17.77% | 9.83% |
| 순차입금비율: | ||
| 현금및현금성자산(C) | 48,724,359 | 36,642,797 |
| 차입금(D) | 110,053,697 | 64,726,776 |
| 순차입금(F=D-C) | 61,329,338 | 28,083,979 |
| 순차입금비율(F/B) | 7.76% | 3.84% |
4. 현금및현금성자산
현금및현금성자산의 상세내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 구 분 | 연이자율(%) | 금 액 | |
| 당반기말 | 전기말 | ||
| 현금시재 | - | 929 | - |
| 요구불예금 | 0.10 ~ 0.14 | 48,723,430 | 6,642,797 |
| 정기예금 | 0.90 ~ 1.37 | - | 30,000,000 |
| 합 계 | 48,724,359 | 36,642,797 | |
5. 매출채권 및 기타금융자산
(1) 매출채권 및 기타금융자산의 내역은 다음과 같습니다.
| (단위: 천원) | |||||||
|---|---|---|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | |||||
| 채권잔액(*1) | 대손충당금 | 장부금액 | 채권잔액(*1) | 대손충당금 | 장부금액 | ||
| 유동항목: | |||||||
| 매출채권 | 28,869,267 | (1,061,002) | 27,808,265 | 19,676,065 | (968,330) | 18,707,735 | |
| 기타금융자산 | 정기예적금 | - | - | - | 1,300,000 | - | 1,300,000 |
| 선물거래예치금 | 30,853 | - | 30,853 | - | - | - | |
| 단기대여금 | 5,328,600 | (5,328,600) | - | 5,328,600 | (5,328,600) | - | |
| 미수수익 | 11,963 | (1,628) | 10,334 | 97,391 | (1,628) | 95,763 | |
| 미수금 | 10,732,323 | (408,349) | 10,323,974 | 826,308 | (408,349) | 417,959 | |
| 펀드예치금(*2) | 30,000,000 | (30,000,000) | - | 30,000,000 | (30,000,000) | - | |
| 보증금 | 533,339 | - | 533,339 | 545,674 | - | 545,674 | |
| 금융리스채권 | 21,034 | (21,034) | - | 21,034 | (21,034) | - | |
| 소 계 | 46,658,111 | (35,759,611) | 10,898,500 | 38,119,007 | (35,759,611) | 2,359,396 | |
| 유동항목 합계 | 75,527,378 | (36,820,613) | 38,706,765 | 57,795,072 | (36,727,941) | 21,067,131 | |
| 비유동항목: | |||||||
| 매출채권 | - | - | - | - | - | - | |
| 기타금융자산 | 장기대여금 | 2,000,000 | - | 2,000,000 | 1,505,272 | - | 1,505,272 |
| 장기선급금 | - | - | - | 6,000,000 | - | 6,000,000 | |
| 보증금 | 2,256,908 | - | 2,256,908 | 1,853,091 | (53,897) | 1,799,194 | |
| 금융리스채권 | 72,259 | (72,259) | - | 72,259 | (72,259) | - | |
| 소 계 | 4,329,167 | (72,259) | 4,256,908 | 9,430,622 | (126,156) | 9,304,466 | |
| 비유동항목 합계 | 4,329,167 | (72,259) | 4,256,908 | 9,430,622 | (126,156) | 9,304,466 | |
(*1) 현재가치할인차금 차감 후 금액입니다.
(*2) 하이투자증권㈜의 사기적 부정거래 행위 및 불완전판매로 인하여 부당이득금 반환 청구 소송중인 예치금입니다. (주석 33~ 참조) 당사의 대표이사는 본 사건과 관련하여 발생가능한 손실을 보전하기 위하여 대표이사가 보유한 당사의 주식을 법무법인에 위탁하는 계약을 체결하였습니다.
6. 파생상품
(1) 파생상품의 내역은 다음과 같습니다.
| (단위:천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 파생상품자산 | ||
| 에이치엘비 제36회차 전환사채 매도청구권(*1) | 2,355,384 | - |
| 에이치엘비 제37회차 신주인수권부사채 매도청구권(*1) | 1,740,936 | - |
| 노터스 제1회차 전환사채 매도청구권(*2) | 3,017,209 | - |
| 합 계 | 7,113,529 | - |
(*1) 총 발행금액의 30%에 대하여 당사 또는 당사가 지정하는 제3자에게 매도 요청 할 권리(콜옵션)를 보유하고 있으며, 당사는 동 콜옵션을 별도의 금융상품으로 인식하였습니다. (주석 14 참조)
(*2) 총 발행금액의 30%에 대하여 당사가 매도청구권을 보유하고 있습니다.
(2) 당반기 중 파생상품관련 손익은 다음과 같습니다.
| (단위:천원) | |||||
|---|---|---|---|---|---|
| 상품분류 | 종류 | 거래이익 | 평가이익 | 거래손실 | 평가손실 |
| 주식연계옵션 | 매도청구권 | - | 3,017,209 | - | - |
7. 기타자산
기타자산의 세부내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
| 선급금 | 1,609,883 | - | 3,147 | 6,000,000 |
| 선급비용 | 461,963 | - | 255,194 | - |
| 합 계 | 2,071,847 | - | 258,341 | 6,000,000 |
8. 재고자산
(1) 재고자산 내역은 다음과 같습니다.
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | ||||
| 취득원가 | 평가손실충당금 | 장부금액 | 취득원가 | 평가손실충당금 | 장부금액 | |
| 원재료 | 2,892,856 | (203,930) | 2,688,926 | 1,368,806 | (2,184) | 1,366,622 |
| 재공품 | 4,026,741 | (359,338) | 3,667,402 | 1,783,436 | (166,125) | 1,617,311 |
| 상품 | 85,625 | - | 85,625 | - | - | - |
| 제품 | 8,156,326 | (146,251) | 8,010,075 | - | - | - |
| 미착품 | - | - | - | 23,044 | - | 23,044 |
| 합 계 | 15,161,547 | (709,519) | 14,452,027 | 3,175,286 | (168,309) | 3,006,977 |
(2) 재고자산과 관련하여 인식한 평가손실(환입)은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 매출원가: | ||
| 재고자산평가손실(환입) | 206,582 | (127,399) |
| 재해손실(*) | - | 511,314 |
(*) 전기 중 공장 화재로 인하여 재공품 등 재고자산이 소실되었습니다.
9. 공정가치측정금융자산
(1) 공정가치측정 금융자산의 내역은 다음과 같습니다.
| (단위: 천원) | |||||
| 구 분 | 범주 | 당반기말 | 전기말 | ||
| 유동 | 비유동 | 유동 | 비유동 | ||
| 지분상품 | 당기손익-공정가치 | - | 1,410 | - | 1,410 |
| 기타포괄손익-공정가치 | - | 5,793,068 | - | 6,073,286 | |
| 복합금융상품 | 당기손익-공정가치 | - | 45,742,137 | - | 21,726,530 |
| 파생상품 | 당기손익-공정가치 | 7,113,529 | - | - | - |
| 채무상품 | 당기손익-공정가치 | - | 1,576,605 | - | 322,053 |
| 합 계 | 7,113,529 | 53,113,220 | - | 28,123,279 | |
보유중인 복합금융상품은 전환사채 및 신주인수권부사채이며, 상환 및 전환조건 등은 아래와 같습니다.
| 발행회사 및 사채명 | 에이치엘비제약㈜ 제12회 무기명식 무보증 사모 전환사채 |
에이치엘비생명과학㈜ 제9회 무기명식 이권부 무보증 분리형 신주인수권부사채 |
|---|---|---|
| 취득금액 | 10,000,000,000원 | 19,603,370,000원 |
| 사채만기일 | 2023년 10월 19일 | 2025년 6월 15일 |
| 전환(행사)가액 (원/주) | 6,689원 | 11,925원 |
| 전환(행사)청구 시작일 | 2021년 10월 19일 | 2022년 7월 15일 |
| 전환(행사)청구 종료일 | 2023년 9월 19일 | 2025년 5월 15일 |
| 전환(행사)에 따라 발행할 주식 | 1,494,991주 | 1,643,888주 |
| 옵션에 관한 사항 | - | 조기상환(Put Option): 본 사채의 발행일로부터 24개월이 경과하는 날로부터 3개월에 해당하는 날에 본 사채 금액의 전부 또는 일부에 대하여 조기상환 청구 가능. |
| 기타 | - | "신주인수권증권"과 "신주인수권이 분리된 채권"이 각각 상장되어 유통되는 분리형 신주인수권부사채임. |
(2) 공정가치측정 금융자산의 변동내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전기 |
| 기초장부금액 | 28,123,279 | 53,260,695 |
| 합병승계(*1) | 1,712,760 | - |
| 취득 | 19,671,928 | 35,616 |
| 대체(*2) | 4,096,320 | 280,682 |
| 보통주전환(*3) | - | (22,852,986) |
| 처분 | (358,439) | (1,568,773) |
| 평가이익-당기손익 | 7,435,742 | 4,195,549 |
| 평가손실-당기손익 | (174,621) | (6,280,080) |
| 평가손익-기타포괄손익 | (280,218) | 1,052,576 |
| 기말장부금액 | 60,226,750 | 28,123,279 |
(*1) 2022년 1월 1일 당사는 지분 100%를 소유한 종속기업 에프에이㈜를 흡수합병하였으며, 동 사업결합에 대해 연결재무제표에 계상된 자산과 부채금액을 승계하는 장부가액법으로 회계처리하였습니다.
(*2) 당반기 중 당사가 발행한 전환사채 및 신주인수권부사채의 매도청구권 입니다. (주석 6 참조)
(*3) 전기 중 에이치엘비생명과학㈜의 보통주 1,317,175주로 전환하였습니다.
10. 종속기업 및 관계기업투자주식
(1) 종속기업 및 관계기업투자의 내역은 다음과 같습니다.
① 당반기말
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 회사명 | 소재국가 | 지분율(%) | 장부금액 |
| 종속기업 | Elevar Therapeutics, Inc. | 미국 | 100.00 | 368,896,315 |
| Immunomic Therapeutics, Inc.(*1) | 미국 | 41.07 | 67,097,768 | |
| HLB인베스트먼트㈜ | 대한민국 | 100.00 | 10,000,000 | |
| Hyundai Lifeboats Shanghai PTE.LTD | 중국 | 100.00 | 1,385,000 | |
| 소 계 | 447,379,083 | |||
| 관계기업 | HLB생명과학㈜(*2) | 대한민국 | 19.60 | 131,066,200 |
| Verismo Therapeutics, Inc.(*2) | 미국 | 9.61 | 5,602,000 | |
| 바다중공업㈜ | 대한민국 | 28.89 | 767,640 | |
| 현대요트㈜ | 대한민국 | 39.43 | - | |
| HLB테라퓨틱스㈜(*2) | 대한민국 | 1.69 | 5,000,007 | |
| ㈜노터스(*3) | 대한민국 | 18.01 | 56,225,920 | |
| 소 계 | 198,661,766 | |||
| 합 계 | 646,040,849 | |||
(*1) 당사의 지분율은 50% 미만이나 해당법인의 이사회 구성 등을 고려한 결과 사실상 지배력을 보유하고 있다고 판단하여 종속기업투자주식으로 분류하였습니다.
(*2) 재무정책과 영업정책에 관한 의사결정에 유의적인 영향력의 행사가 가능함에 따라 지분율이 20% 미만임에도 불구하고 관계기업투자주식으로 분류하였습니다.
(*3) 당사가 신규 출자한 비임상 CRO 업체로서, 당사의 신규사업진출 및 기존사업과의 시너지 극대화를 위해 지분을 취득하였습니다.
② 전기말
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 회사명 | 소재국가 | 지분율(%) | 장부금액 |
| 종속기업 | Elevar Therapeutics, Inc. | 미국 | 100.00 | 337,383,774 |
| Immunomic Therapeutics, Inc. | 미국 | 41.11 | 67,097,768 | |
| ㈜화진메디칼 | 대한민국 | 100.00 | 2,500,000 | |
| ㈜화진메디스 | 대한민국 | 100.00 | - | |
| HLB인베스트먼트㈜ | 대한민국 | 100.00 | 10,000,000 | |
| ㈜에프에이 | 대한민국 | 100.00 | 102,125,757 | |
| 소 계 | 519,107,299 | |||
| 관계기업 | HLB생명과학㈜ | 대한민국 | 19.60 | 131,066,200 |
| Verismo Therapeutics, Inc. | 미국 | 11.44 | 5,602,000 | |
| 바다중공업㈜ | 대한민국 | 28.89 | 767,640 | |
| 현대요트㈜ | 대한민국 | 39.43 | - | |
| HLB테라퓨틱스㈜ | 대한민국 | 1.69 | 5,000,007 | |
| 소 계 | 142,435,846 | |||
| 합 계 | 661,543,145 | |||
(2) 종속기업 및 관계기업 투자주식의 변동내역은 다음과 같습니다.
① 당반기
| (단위 : 천원) | ||||||
|---|---|---|---|---|---|---|
| 기업명 | 기초 | 취득 | 처분 | 대체(*1) | 손상차손 | 기말 |
| Elevar Therapeutics, Inc.(*1) | 337,383,774 | 31,394,745 | - | 117,796 | - | 368,896,315 |
| Immunomic Therapeutics, Inc. | 67,097,768 | - | - | - | - | 67,097,768 |
| ㈜화진메디칼(*4) | 2,500,000 | - | (2,500,000) | - | - | - |
| ㈜화진메디스(*4) | - | - | - | - | - | - |
| HLB인베스트먼트㈜ | 10,000,000 | - | - | - | - | 10,000,000 |
| ㈜에프에이(*2) | 102,125,757 | 79,583 | - | (102,205,340) | - | - |
| Hyundai Lifeboats Shanghai PTE.LTD | 1,385,000 | - | - | - | 1,385,000 | |
| HLB생명과학㈜ | 131,066,200 | - | - | - | - | 131,066,200 |
| Verismo Therapeutics, Inc. | 5,602,000 | - | - | - | - | 5,602,000 |
| 바다중공업㈜ | 767,640 | - | - | - | - | 767,640 |
| 현대요트㈜ | - | - | - | - | - | - |
| HLB테라퓨틱스㈜(*4) | 5,000,007 | - | - | - | - | 5,000,007 |
| ㈜노터스(*3) | - | 50,225,920 | - | 6,000,000 | - | 56,225,920 |
| 합 계 | 661,543,145 | 83,085,247 | (2,500,000) | (96,087,544) | - | 646,040,849 |
(*1) 당사는 당반기 중 Elevar Therapeutics, Inc.의 임원 2인에게 당사의 주식매수선택권을 부여하였으며, 주식보상비용으로 측정되는 금액에 대해 종속기업에 자본을 불입한 것으로 보아 투자지분의 증가로 회계처리하였습니다.
(*2) 2022년 1월 1일 당사가 흡수합병하였습니다. (주석 32 참조)
(*3) 지분 취득대금에 대한 신주인수권부사채 발행 대용납입 25,200,000천원이 포함되어 있습니다
(*4) 당반기 중 당사의 종속기업이던 ㈜화진메디칼, ㈜화진메디스의 지분 100%를 당사의 관계기업인 HLB테라퓨틱스㈜에 매각하였습니다. 거래대금은 총 3,300,000천원이며 800,000천원의 처분이익을 인식하였습니다.
② 전기
| (단위 : 천원) | ||||||
|---|---|---|---|---|---|---|
| 기업명 | 기초 | 취득 | 처분 | 대체 | 손상차손 | 기말 |
| Elevar Therapeutics, Inc. | 334,037,760 | 42,612,911 | - | - | (39,266,897) | 337,383,774 |
| Immunomic Therapeutics, Inc. | 67,097,768 | - | - | - | - | 67,097,768 |
| ㈜화진메디칼 | 2,500,000 | - | - | - | - | 2,500,000 |
| ㈜화진메디스 | - | - | - | - | - | - |
| HLB인베스트먼트㈜ | - | 10,000,000 | - | - | - | 10,000,000 |
| ㈜에프에이 | - | 102,125,757 | - | - | - | 102,125,757 |
| HLB생명과학㈜ | 108,213,213 | 22,852,986 | - | - | - | 131,066,200 |
| Verismo Therapeutics, Inc. | - | 5,602,000 | - | - | - | 5,602,000 |
| 바다중공업㈜ | 767,640 | - | - | - | - | 767,640 |
| 현대요트㈜ | - | - | - | - | - | - |
| HLB테라퓨틱스㈜ | - | 5,000,007 | - | - | - | 5,000,007 |
| 합 계 | 512,616,381 | 188,193,662 | - | - | (39,266,897) | 661,543,145 |
(3) 종속 및 관계기업의 요약 재무정보는 다음과 같습니다.
① 당반기
| (단위: 천원) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 기업명 | 당반기말 | 당반기 | |||||||
| 유동자산 | 비유동자산 | 유동부채 | 비유동부채 | 총수익 | 영업이익 (손실) |
당기순이익 (손실) |
총포괄손익 | ||
| 종속기업 | Elevar Therapeutics, Inc. | 18,533,891 | 26,399,899 | 70,250,213 | 263,727 | - | (39,873,277) | (39,972,207) | (42,147,077) |
| Immunomic Therapeutics, Inc. | 24,501,766 | 22,688,464 | 3,669,315 | 14,078,335 | - | (16,015,196) | (16,348,424) | (13,324,007) | |
| ㈜화진메디칼(*2) | - | - | - | - | 2,577,730 | 119,274 | 85,103 | 85,103 | |
| ㈜화진메디스(*2) | - | - | - | - | 684,257 | (102,444) | (122,319) | (122,319) | |
| HLB인베스트먼트㈜ | 8,003,100 | 1,688,831 | 141,072 | 40,368 | - | (479,749) | (463,944) | (554,197) | |
| Hyundai Lifeboats Shanghai PTE.LTD |
1,028,234 | 21,006 | 114,439 | - | 385,867 | 27,149 | 70,547 | 100,619 | |
| 관계기업 | 바다중공업㈜ | 14,960,255 | 6,115,872 | 15,162,344 | 3,922,600 | 7,943,000 | (1,975,294) | (2,056,687) | (2,056,687) |
| 현대요트㈜ | 7,287,627 | 830,887 | 6,747,578 | 211,270 | 5,888,388 | (143,948) | (115,396) | (115,396) | |
| HLB생명과학㈜ | 181,328,966 | 145,867,976 | 17,865,344 | 21,587,482 | 91,796,824 | (8,066,746) | (55,835,829) | (46,763,291) | |
| Verismo Therapeutics, Inc. | 27,156,172 | 1,180 | 32,039 | - | - | (2,907,504) | (2,255,682) | (2,255,682) | |
| HLB테라퓨틱스 | 95,433,330 | 110,322,573 | 63,547,219 | 3,292,121 | 22,644,513 | (1,369,899) | (4,271,998) | 8,917,124 | |
| ㈜노터스(*1) | 98,465,293 | 70,876,861 | 40,416,591 | 63,709,808 | - | - | - | - | |
(*1) 관계기업 편입 전 발생한 손익은 포함되지 않았습니다.
(*2) 종속기업 처분 후 발생한 손익은 포함되지 않았습니다.
② 전기
| (단위: 천원) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 기업명 | 전기말 | 전기 | |||||||
| 유동자산 | 비유동자산 | 유동부채 | 비유동부채 | 총수익 | 영업이익 (손실) |
전기순이익 (손실) |
총포괄손익 | ||
| 종속기업 | Elevar Therapeutics, Inc.(*2) | 25,925,129 | 24,529,473 | 65,234,805 | 269,752 | - | (64,377,991) | (63,462,256) | (44,441,190) |
| Immunomic Therapeutics, Inc. | 37,772,618 | 19,191,027 | 6,004,919 | 9,501,762 | 2,320,412 | (26,381,502) | (26,055,891) | (21,777,685) | |
| ㈜화진메디칼 | 4,297,596 | 3,278,347 | 3,423,845 | 2,130,438 | 8,565,749 | 215,976 | 62,609 | 67,201 | |
| ㈜화진메디스 | 385,472 | 1,561,156 | 1,799,978 | 56,027 | 2,011,911 | (108,734) | (171,504) | (148,081) | |
| 에이치엘비인베스트먼트㈜ | 8,425,492 | 1,801,548 | 101,738 | 60,614 | - | (448,355) | (437,756) | 64,688 | |
| 에프에이(*1) | 50,414,135 | 19,794,085 | 21,322,397 | (385,988) | 22,536,698 | 5,225,972 | 2,619,973 | 2,949,364 | |
| 관계기업 | 바다중공업㈜ | 14,339,843 | 6,081,114 | 14,599,362 | 1,774,416 | 16,481,950 | 528,037 | 556,071 | 556,071 |
| 현대요트㈜ | 11,494,551 | 541,877 | 10,578,989 | 182,377 | 14,245,758 | 11,369 | 9,160 | 3,849,040 | |
| 에이치엘비생명과학㈜ | 181,328,966 | 145,867,976 | 17,865,344 | 21,587,482 | 91,796,824 | (8,066,746) | (55,835,829) | (46,763,291) | |
| Verismo Therapeutics, Inc.(*1) | 15,572,994 | - | 18,959 | - | - | (6,562,505) | (6,522,743) | (6,522,743) | |
| 에이치엘비테라퓨틱스(*1) | 113,252,822 | 76,458,388 | 56,716,797 | 2,955,096 | - | - | - | - | |
(*1) 종속기업 및 관계기업 편입 전 발생한 손익은 포함되지 않았습니다.
(4) 시장성이 있는 관계기업
시장성이 있는 관계기업투자의 시장가격은 다음과 같습니다.
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 기업명 | 당반기말 | 전기말 | ||||
| 주당 공정가치 | 주식수 | 시장가격 | 주당 공정가치 | 주식수 | 시장가격 | |
| 에이치엘비생명과학㈜ | 12,150 | 18,720,849 | 227,458,315 | 12,450 | 18,720,849 | 233,074,570 |
| HLB테라퓨틱스 | 13,300 | 530,899 | 7,060,957 | 14,150 | 530,899 | 7,512,221 |
| ㈜노터스 | 7,860 | 12,650,832 | 99,435,540 | - | - | - |
11. 투자부동산
투자부동산의 내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 과 목 | 소재지 | 당반기말 | 전기말 |
| 토 지 | 전남 여수시 화양면 화동리 산225-1 | 19,173 | 19,173 |
12. 유형자산
(1) 유형자산 장부금액의 변동내역은 다음과 같습니다.
① 당반기
| (단위: 천원) | |||||||
|---|---|---|---|---|---|---|---|
| 구 분 | 기 초 | 합병승계(*) | 취 득 | 처 분 | 감가상각비 | 대 체 | 기 말 |
| 토 지 | 2,072,365 | 3,707,724 | - | - | - | - | 5,780,089 |
| 건 물 | 3,508,975 | 6,168,913 | - | - | (156,942) | - | 9,520,946 |
| 구축물 | 133,106 | 4,198 | - | - | (7,569) | - | 129,735 |
| 기계장치 | 1,687,258 | 2,584,765 | 356,000 | (629,578) | (388,995) | - | 3,609,450 |
| 차량운반구 | 9,201 | 131,590 | 50,292 | (1) | (17,915) | - | 173,167 |
| 공기구비품 | 645,114 | 141,915 | 25,177 | - | (156,494) | - | 655,712 |
| 시설장치 | 6 | 66,835 | 64,000 | - | (9,891) | - | 120,950 |
| 사용권자산 | 756,805 | - | 335,989 | (22,737) | (487,495) | - | 582,562 |
| 임차자산개량권 | 1 | - | - | - | - | - | 1 |
| 건설중인자산 | 8,000 | 8,111,535 | 211,611 | - | - | - | 8,331,146 |
| 합 계 | 8,820,831 | 20,917,474 | 1,043,069 | (652,316) | (1,225,301) | - | 28,903,757 |
(*) 2022년 1월 1일 당사는 지분 100%를 소유한 종속기업㈜에프에이를 흡수합병하였으며, 동 사업결합에 대해 연결재무제표에 계상된 자산과 부채금액을 승계하는 장부가액법으로 회계처리하였습니다.
② 전반기
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 기 초 | 취 득 | 처 분 | 감가상각비 | 대체(*) | 기 말 |
| 토 지 | 2,072,365 | - | - | - | - | 2,072,365 |
| 건 물 | 3,654,368 | - | (5,738) | (69,847) | - | 3,578,784 |
| 구축물 | 212,533 | - | (63,584) | (8,393) | - | 140,556 |
| 기계장치 | 1,106,390 | 759,900 | (12,067) | (130,789) | - | 1,723,434 |
| 차량운반구 | 23 | - | (5) | - | - | 18 |
| 공기구비품 | 738,003 | 213,643 | (663) | (147,546) | - | 803,437 |
| 시설장치 | 6 | - | - | - | - | 6 |
| 사용권자산 | 898,911 | 383,860 | (36,963) | (484,099) | - | 761,709 |
| 임차자산개량권 | 73,200 | 21,000 | - | (52,920) | - | 41,280 |
| 건설중인자산 | 24,001 | 38,500 | - | - | (26,000) | 36,501 |
| 합 계 | 8,779,800 | 1,416,903 | (119,019) | (893,594) | (26,000) | 9,158,089 |
(*) 전기 중 무형자산 등으로 대체하였습니다.
(2) 매출원가와 판매비와관리비로 배분된 감가상각비는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 매출원가 | 621,460 | 342,633 |
| 판매비와관리비 | 602,413 | 550,961 |
| 개발비 | 1,428 | - |
| 합 계 | 1,225,301 | 893,594 |
(3) 당사의 토지, 건물의 일부 및 기계장치는 당사의 차입금에 대한 담보로 제공되어 있으며, 당반기말 현재 담보제공금액은 384,000천원(장부금액 5,420,133 천원)입니다. (주석14, 29참조)
13. 무형자산
무형자산 장부금액의 변동내역은 다음과 같습니다.
① 당반기
| (단위: 천원) | ||||||||
| 구 분 | 기초 | 합병승계(*) | 취득 | 정부보조금 | 처분 | 상각 | 손상 | 기말 |
| 특허권 | 31,132,000 | 15,895 | - | (3,463) | - | (3,621,684) | - | 27,522,749 |
| 소프트웨어 | 120,332 | 27,753 | - | (26,458) | - | (19,720) | - | 101,907 |
| 회원권 | 1,872,857 | 511,000 | 153,300 | - | - | - | - | 2,537,157 |
| 영업권 | - | 28,598,931 | - | - | - | - | - | 28,598,931 |
| 고객관계 | - | 30,672,570 | - | - | - | (2,174,710) | - | 28,497,860 |
| 상표권 | - | 4,804 | - | - | - | (288) | - | 4,516 |
| 의장권 | - | 834 | - | - | - | (49) | - | 785 |
| 합 계 | 33,125,189 | 59,831,787 | 153,300 | (29,920) | - | (5,816,451) | - | 87,263,905 |
(*) 2022년 1월 1일 당사는 지분 100%를 소유한 종속기업 ㈜에프에이를 흡수합병하였으며, 동 사업결합에 대해 연결재무제표에 계상된 자산과 부채금액을 승계하는 장부가액법으로 회계처리하였습니다.
② 전반기
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 기초 | 취득 | 처분 | 상각 | 손상 | 기말 |
| 특허권 | 38,372,000 | - | - | (3,620,000) | - | 34,752,000 |
| 소프트웨어(*) | 83,787 | 49,000 | - | (14,709) | - | 118,078 |
| 회원권 | 1,668,457 | 204,400 | - | - | - | 1,872,857 |
| 합 계 | 40,124,244 | 253,400 | - | (3,634,709) | - | 36,742,935 |
(*) 전기 중 건설중인자산에서 대체된 금액이 포함되어 있습니다.
14. 차입금
(1) 당사의 차입금 내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 차입처 | 이자율(%) | 당반기말 | 전기말 |
| 단기차입금: | |||
| 하나은행 | 2.5 | - | 6,000,000 |
| 전환사채 | - | 2,135,278 | 11,494,916 |
| 신주인수권부사채 | - | 23,749,187 | - |
| 소 계 | 25,884,465 | 17,494,916 | |
| 장기차입금: | |||
| 중소기업은행(*) | 1.5 | 320,000 | 320,000 |
| 전환사채 | - | 19,578,661 | - |
| 신주인수권부사채 | - | 64,270,570 | 46,911,860 |
| 소 계 | 84,169,232 | 47,231,860 | |
| 합 계 | 110,053,697 | 64,726,776 | |
(*) 상기의 차입금과 관련하여 토지, 일부 건물 및 기계장치를 담보로 제공하고 있습니다. (주석 12 참조)
(2) 당사가 발행한 사채의 상세 내역은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 발행일 | 최장 만기일 | 연이자율(%) | 당반기말 | 전기말 |
| 제33회 무기명식 전환사채 | 2019-12-18 | 2022-12-18 | - | 2,100,000 | 11,305,000 |
| 제34회 무기명식 신주인수권부사채 | 2021-10-20 | 2026-10-20 | - | 57,000,000 | 57,000,000 |
| 제35회 무기명식 신주인수권부사채 | 2022-03-30 | 2025-03-30 | - | 25,200,000 | - |
| 제36회 무기명식 전환사채 | 2022-06-02 | 2025-06-02 | - | 23,000,000 | - |
| 제37회 무기명식 신주인수권부사채 | 2022-06-02 | 2025-06-02 | - | 17,000,000 | - |
| 소 계 | 124,300,000 | 68,305,000 | |||
| 상환할증금(전환사채) | 732,132 | 189,916 | |||
| 전환권조정(전환사채) | (4,118,193) | - | |||
| 상환할증금(신주인수권) | 2,169,098 | 1,150,032 | |||
| 신주인수권조정(신주인수권) | (13,349,341) | (11,238,172) | |||
| 합 계 | 109,733,697 | 58,406,776 | |||
(3) 전환사채 및 신주인수권부사채의 주요 발행조건은 다음과 같습니다.
| 구 분 | 내 용 | 내 용 | 내 용 | 내 용 | 내 용 |
|---|---|---|---|---|---|
| 사채의 명칭 | 제33회 무기명식 무보증 사모 전환사채 |
제34회 무기명식 무보증 사모 신주인수권 부사채 |
제35회 무기명식 무보증 사모 신주인수권 부사채 |
제36회 무기명식 무보증 사모 전환사채 |
제37회 무기명식 무보증 사모 신주인수권 부사채 |
| 권면총액 | 40,000,000천원 | 57,000,000천원 | 25,200,000천원 | 23,000,000천원 | 17,000,000천원 |
| 발행가액 | 권면금액의 100% | 권면금액의 100% | 권면금액의 100% | 권면금액의 100% | 권면금액의 100% |
| 보장수익률 | 연 1.00% | 연 1.00% | 연 2.00% | 연 3.00% | 연 3.00% |
| 유효이자율 | 연 8.71% | 연 12.717% | 연 11.303% | 연 15.355% | 연 15.355% |
| 원금상환방법 | 1. 만기일시상환 : 사채만기일에 미행사 사채권면총액에 대하여 사채원금의 103.0402% 의 금액을 일시상환함 2. 조기상환(Put Option): 발행일로부터 1년 8개월이 경과한날부터 사채권자의 조기상환청구 가능함 |
1. 만기일시상환 : 사채만기일에 미행사 사채권면총액에 대하여 사채원금의 105.1206% 의 금액을 일시상환함 2. 조기상환(Put Option): 발행일로부터 2년이 경과한날부터 사채권자의 조기상환청구 가능함 |
1. 만기일시상환 : 사채만기일에 미행사 사채권면총액에 대하여 사채원금의 106% 의 금액을 일시상환함 2. 조기상환(Put Option): 발행일로부터 1년이 경과한날부터 사채권자의 조기상환청구 가능함 3. 매도청구권(Call Option) 발행일로부터 1개월이 경과한날부터 1년이 경과한 날까지, 권면금액의 일부에 대하여 발행회사의 매도청구(조기상환 포함) 가능함 |
1. 만기일시상환 : 사채만기일까지 보유하고 있는 본사채의 원금에 대하여는 전자등록금액의 106.2426%의 금액을 일시상환함 2. 조기상환(Put Option): 발행일로부터 1년 6개월이 경과한날로부터 사채권자의 조기상환청구 가능함 3. 매도청구권(Call Option) 발행일로부터 1년이 경과한 날까지, 권면금액의 일부에 대하여 발행회사의 매도청구(조기상환 포함) 가능함 |
1. 만기일시상환 : 사채만기일까지 보유하고 있는 본사채의 원금에 대하여는 전자등록금액의 106.2426%의 금액을 일시상환함 2. 조기상환(Put Option): 발행일로부터 1년 6개월이 경과한날로부터 사채권자의 조기상환청구 가능함 3. 매도청구권(Call Option) 발행일로부터 1년이 경과한 날까지, 권면금액의 일부에 대하여 발행회사의 매도청구(조기상환 포함) 가능함 |
| 행사(전환)가액 | 33,757원(*1) | 35,884원(*2) | 30,811원 | 48,605원 | 48,605원 |
| 행사(전환)에 따라 발행할 주식의 종류 |
기명식 보통주 | 기명식 보통주 | 기명식 보통주 | 기명식 보통주 | 기명식 보통주 |
| 행사(전환청구)기간 | 2020년 12월 18일부터 2022년 11월 18일까지 |
2023년 10월 20일부터 2026년 10월 20일까지 |
2023년 03월 30일부터 2025년 02월 28일까지 |
2023년 06월 02일부터 2025년 05월 02일까지 |
2023년 06월 02일부터 2025년 05월 02일까지 |
| 신주의 배당분기산일 |
행사일이 속하는 사업연도의 개시일 |
행사일이 속하는 사업연도의 개시일 |
행사일이 속하는 사업연도의 개시일 |
행사일이 속하는 사업연도의 개시일 |
행사일이 속하는 사업연도의 개시일 |
(*1) 전기 중 무상증자 및 시가하락으로 인하여 전환가액이 조정되었으며, 조정 후 전환가액입니다.
(*2) 당반기 중 시가하락으로 인하여 전환가액이 조정되었으며, 조정 후 전환가액입니다.
(4) 당반기 중 전환사채의 전환으로 인한 주식수, 자본금 및 주식발행초과금의 증가 내역은 다음과 같습니다.
| (단위: 주, 천원) | |||
|---|---|---|---|
| 구 분 | 주식수 | 보통주자본금 | 주식발행초과금 |
| 제33회 무기명식 전환사채 | 272,681 | 136,341 | 10,278,931 |
(5) 사채 부채요소의 공정가치는 동일한 조건의 전환권이 없는 사채의 시장이자율을 적용하여 계산되었습니다. 발행가액에서 부채요소를 차감한 잔여가치는 전환권 가치에 해당하며 자본으로 계상하였습니다. 발행자 매도청구권의 공정가치는 파생상품자산으로 계상하였습니다. (주석 6 참조)
(6) 행사기한이 종료되지 않은 전환권이 행사될 경우 발행될 주식수는 다음과 같습니다.
| (단위: 주, 원) | |||||
|---|---|---|---|---|---|
| 구 분 | 발행가능주식수 | 발행(소각)주식수 | 미발행주식수 | 행사가격 | 행사기간 |
| 제33회 전환사채 | 62,209 | - | 62,209 | 33,757 | 2020.12.18 ~ 2022.11.18 |
| 제34회 신주인수권부사채 | 1,588,451 | - | 1,588,451 | 35,884 | 2023.10.20 ~ 2026.10.20 |
| 제35회 신주인수권부사채 | 817,889 | - | 817,889 | 30,811 | 2023.03.30 ~ 2025.02.28 |
| 제36회 전환사채 | 473,202 | - | 473,202 | 48,605 | 2023.06.02 ~ 2025.05.02 |
| 제37회 신주인수권부사채 | 349,758 | - | 349,758 | 48,605 | 2023.06.02 ~ 2025.05.02 |
15. 기타금융부채
기타금융부채의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
| 미지급금 | 4,113,453 | 80,202 | 1,240,995 | 45,429 |
| 미지급비용 | 4,690,597 | - | 3,474,371 | - |
| 리스부채 | 447,483 | 134,083 | 583,924 | 180,237 |
| 합 계 | 9,251,534 | 214,285 | 5,299,290 | 225,666 |
16. 리스
(1) 사용권자산 장부금액의 구성내역은 다음과 같습니다.
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 당반기말 | 전기말 | ||||
| 취득원가 | 상각누계액 | 장부금액 | 취득원가 | 상각누계액 | 장부금액 | |
| 토지 | 145,215 | (145,215) | - | 145,215 | (72,607) | 72,607 |
| 건물 | 1,237,392 | (973,753) | 263,639 | 971,423 | (682,428) | 288,995 |
| 차량운반구 | 741,347 | (422,424) | 318,923 | 782,265 | (387,063) | 395,202 |
| 합 계 | 2,123,953 | (1,541,391) | 582,562 | 1,898,903 | (1,142,098) | 756,805 |
(2) 당반기 중 사용권자산 장부금액의 변동내역은 다음과 같습니다
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 기초 | 취득 | 처분 | 상각 | 기말 |
| 토지 | 72,607 | - | - | (72,607) | - |
| 건물 | 288,995 | 265,969 | - | (291,325) | 263,639 |
| 차량운반구 | 395,202 | 70,020 | (22,737) | (123,562) | 318,923 |
| 합 계 | 756,805 | 335,989 | (22,737) | (487,495) | 582,562 |
(3) 당반기 중 리스부채의 변동 내역은 다음과 같습니다.
| (단위: 천원) | ||||||||
|---|---|---|---|---|---|---|---|---|
| 구 분 | 기초 | 증가 | 감소 | 상환금액 | 이자비용 | 기말 | 유동 | 비유동 |
| 리스부채 | 764,161 | 328,985 | (22,652) | (504,053) | 15,125 | 581,566 | 447,483 | 134,083 |
(4) 당반기 중 리스와 관련하여 손익으로 인식한 금액은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 리스부채에 대한 이자비용 | (15,125) | (18,112) |
| 단기리스와 관련된 비용 | (219,814) | (199,781) |
| 소액자산 리스 중 단기리스를 제외한 리스에 관한 비용 | (14,755) | (16,314) |
| 합 계 | (249,694) | (234,207) |
(5) 당반기 중 리스와 관련하여 현금흐름표에 인식한 금액은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 리스의 총 현금유출(이자비용 제외) | 504,053 | 497,355 |
17. 기타부채
(1) 기타부채의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 유동 | ||
| 예수금 | 86,937 | 60,031 |
| 판매보증충당부채 | 138,007 | 158,604 |
| 임대보증금 | 115,000 | - |
| 복구충당부채(*1) | 25,900 | 25,900 |
| 환불부채 | 279,018 | - |
| 소 계 | 644,862 | 244,535 |
| 비유동 | ||
| 합 계 | 644,862 | 244,535 |
(*1) 임차계약상의 원상복구 의무에 따른 예상 복구비용을 충당부채로 인식하였습니다.
(2) 당반기 및 전기 중 판매보증충당부채의 변동내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전기말 |
| 기초 | 158,604 | 80,858 |
| 증가(감소) | (20,596) | 77,746 |
| 기말 | 138,007 | 158,604 |
당사는 판매된 제품에 대한 품질보증, 하자보수 및 그에 따른 사후서비스 등으로 인하여 향후 부담하게 될 비용을 관련 제품이 판매되는 시점에 비용으로 계상하고 있습니다.
18. 자본금과 주식발행초과금
당사의 정관에 의한 발행할 주식의 총수는 5억주(1주의 금액 : 500원)이며, 당사가 발행한 보통주식 및 우선주식수는 각각 106,882,745주와 7,188주 입니다.
| (단위: 주, 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 일 자 | 내 역 | 주식수 | 자본금 | 주식발행 초과금 | 합 계 |
| 보통주 | 전기초 | 52,979,436 | 26,489,718 | 775,815,152 | 802,304,870 | |
| 2021-01-04 | 전환사채 행사 | 4,420 | 2,210 | 376,449 | 378,659 | |
| 2021-01-05 | 전환사채 행사 | 13,262 | 6,631 | 1,129,517 | 1,136,148 | |
| 2021-01-06 | 전환사채 행사 | 9,725 | 4,863 | 828,273 | 833,135 | |
| 2021-01-07 | 전환사채 행사 | 3,094 | 1,547 | 263,514 | 265,061 | |
| 2021-01-08 | 전환사채 행사 | 3,094 | 1,547 | 263,514 | 265,061 | |
| 2021-01-15 | 전환사채 행사 | 61,891 | 30,946 | 5,271,222 | 5,302,167 | |
| 2021-01-21 | 전환사채 행사 | 442 | 221 | 37,645 | 37,866 | |
| 2021-01-25 | 전환사채 행사 | 27,408 | 13,704 | 2,334,324 | 2,348,028 | |
| 2021-03-16 | 무상증자 | 52,968,898 | 26,484,449 | (26,726,956) | (242,507) | |
| 2021-06-21 | 전환사채 행사 | 5,924 | 2,962 | 220,633 | 223,595 | |
| 2021-08-13 | 전환사채 행사 | 51,839 | 25,920 | 1,952,873 | 1,978,793 | |
| 2021-08-18 | 전환사채 행사 | 105,163 | 52,582 | 3,968,368 | 4,020,949 | |
| 2021-08-19 | 전환사채 행사 | 740 | 370 | 25,867 | 26,237 | |
| 2021-08-23 | 전환사채 행사 | 79,982 | 39,991 | 3,016,196 | 3,056,187 | |
| 2021-08-25 | 전환사채 행사 | 10,368 | 5,184 | 389,510 | 394,694 | |
| 2021-08-26 | 전환사채 행사 | 13,329 | 6,665 | 500,823 | 507,488 | |
| 2021-08-27 | 전환사채 행사 | 247,351 | 123,676 | 9,329,601 | 9,453,277 | |
| 2021-08-30 | 전환사채 행사 | 8,887 | 4,444 | 334,694 | 339,138 | |
| 2021-09-02 | 전환사채 행사 | 14,811 | 7,406 | 554,450 | 561,855 | |
| 전기말 | 106,610,064 | 53,305,032 | 779,885,671 | 833,190,703 | ||
| 2022-03-30 | 자본준비금의 이익잉여금 전입 | - | - | (130,000,000) | (130,000,000) | |
| 2022-05-16 | 전환사채 행사 | 41,472 | 20,736 | 1,563,321 | 1,584,057 | |
| 2022-05-17 | 전환사채 행사 | 20,736 | 10,368 | 781,660 | 792,028 | |
| 2022-05-19 | 전환사채 행사 | 10,368 | 5,184 | 390,830 | 396,014 | |
| 2022-05-25 | 전환사채 행사 | 155,523 | 77,762 | 5,862,565 | 5,940,327 | |
| 2022-05-26 | 전환사채 행사 | 41,472 | 20,736 | 1,563,321 | 1,584,057 | |
| 2022-06-15 | 전환사채 행사 | 3,110 | 1,555 | 117,234 | 118,789 | |
| 당반기말 | 106,882,745 | 53,441,373 | 660,164,602 | 713,605,974 | ||
| 우선주 | 전기초 | 3,657 | 1,829 | (167) | 1,661 | |
| 2021-03-16 | 무상증자 | 3,531 | 1,766 | (1,782) | (16) | |
| 당반기말 | 7,188 | 3,594 | (1,949) | 1,645 | ||
당사는 이사회에서 정한 우선비율(액면금액 기준 연 1% 이상)에 따른 금전배당을 받을 수 있는 누적적 참가적 무의결권 우선주를 포함하는 종류주식을 발행주식총수의 2분의 1 범위내에서 발행할 수 있도록 되어 있으며, 보통주 또는 우선주로 전환할 수 있는 전환사채와 보통주 또는 우선주의 신주인수권을 부여하는 신주인수권부사채를 각각 2,000억원 범위 내에서 주주 이외의 자에게 발행할 수 있도록 하고 있습니다. 또한 당사는 주주총회의 특별결의로 발행주식총수의 100분의 15 범위 내에서 임직원에게 주식선택권을 부여할 수 있도록 되어 있습니다. 단, 발행주식총수의 100분의 3 범위 내에서는 이사회의 결의로 주식선택권을 부여할 수 있도록 되어 있습니다.
당사는 주주에게 배당할 이익으로 발행주식총수의 100분의 10 범위내에서 관계법령이 정하는 바에 따라 이사회 결의로 당사의 주식을 소각할 수 있도록 하고 있습니다.
당사는 2021년 3월 16일 보통주 및 우선주 1주당 1주를 지급하는 무상증자를 시행하였습니다.
19. 기타자본항목
(1) 기타자본항목의 세부구성내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 전환권대가 | 6,226,232 | 1,309,826 |
| 신주인수권대가 | 17,759,474 | 11,231,032 |
| 기타자본잉여금 | 4,206,088 | 1,901,731 |
| 자기주식 | (4,120,279) | (4,120,279) |
| 자기주식처분이익 | 5,086,818 | 5,086,818 |
| 주식매입선택권(*) | 117,796 | - |
| 기타자본조정 | (15,044,074) | (15,044,074) |
| 기타포괄손익-공정가치 측정 금융자산 평가손익 | (632,887) | (352,669) |
| 합 계 | 13,599,169 | 12,386 |
(*) 당사는 당반기 중 Elevar Therapeutics, Inc.의 임원 2인에게 당사의 주식매수선택권을 부여하였으며, 주식보상비용으로 측정되는 금액에 대해 종속기업에 자본을 불입한 것으로 보아 투자지분의 증가로 회계처리하였습니다.
(2) 자기주식
당반기말 현재 보통주 133,874주와 우선주 126주를 자기주식으로 계상하고 있으며, 향후 시장상황에 따라 처분할 예정입니다.
20. 주당손익
(1) 기본주당손익의 계산내역은 다음과 같습니다.
① 기본주당손익
| (단위: 주, 원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 보통주 순이익(손실) | 27,235,113,050 | 36,034,981,319 | (18,852,892,623) | (21,746,487,076) |
| 가중평균유통보통주식수(*) | 106,592,496 | 106,534,664 | 106,072,321 | 106,053,343 |
| 기본주당이익(손실)(*) | 256 | 338 | (178) | (205) |
(*) 2021년 3월 16일 시행한 무상증자효과를 소급 조정하여 비교 표시 하였습니다.
② 가중평균유통보통주식수의 산정
| (단위: 주) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 기초 발행보통주식수 | 106,610,064 | 106,610,064 | 53,102,772 | 52,979,436 |
| 무상증자 조정(*1) | - | - | 53,102,772 | 52,979,436 |
| 수정 기초 발행보통주식수 | 106,610,064 | 106,610,064 | 106,205,544 | 105,958,872 |
| 전환권 행사(*2) | 116,306 | 58,474 | 651 | 228,345 |
| 자기주식 | (133,874) | (133,874) | (133,874) | (133,874) |
| 가중평균유통보통주식수 | 106,592,496 | 106,534,664 | 106,072,321 | 106,053,343 |
(*1) 2021년 3월 16일에 시행한 무상증자에 대한 조정으로, 100%의 무상증자 비율을 적용하였습니다.
(*2) 당반기 중 전환사채의 전환권 행사로 발행된 신주에 대한 가중평균 유통보통주식수의 계산내역은 다음과 같습니다.
① 당반기
| (단위: 주) | |||||
|---|---|---|---|---|---|
| 일자 | 조정 전 | 주식수 | 유통일수(일) | 적 수 | 가중평균 유통주식수 |
| 2022년 05월 16일 | 41,472 | 41,472 | 46 | 1,907,712 | 10,540 |
| 2022년 05월 17일 | 20,736 | 20,736 | 45 | 933,120 | 5,155 |
| 2022년 05월 19일 | 10,368 | 10,368 | 43 | 445,824 | 2,463 |
| 2022년 05월 25일 | 155,523 | 155,523 | 37 | 5,754,351 | 31,792 |
| 2022년 05월 26일 | 41,472 | 41,472 | 36 | 1,492,992 | 8,249 |
| 2022년 06월 15일 | 3,110 | 3,110 | 16 | 49,760 | 275 |
| 합 계 | 272,681 | 272,681 | 10,583,759 | 58,474 | |
② 전반기
| (단위: 주) | ||||||
|---|---|---|---|---|---|---|
| 일자 | 조정 전 | 무상증자 조정 (2021/3/16 100%) |
조정 후 | 유통일수(일) | 적 수 | 가중평균 유통주식수 |
| 2021년 01월 04일 | 4,420 | 4,420 | 8,840 | 178 | 1,573,520 | 8,693 |
| 2021년 01월 05일 | 13,262 | 13,262 | 26,524 | 177 | 4,694,748 | 25,938 |
| 2021년 01월 06일 | 9,725 | 9,725 | 19,450 | 176 | 3,423,200 | 18,913 |
| 2021년 01월 07일 | 3,094 | 3,094 | 6,188 | 175 | 1,082,900 | 5,983 |
| 2021년 01월 08일 | 3,094 | 3,094 | 6,188 | 174 | 1,076,712 | 5,949 |
| 2021년 01월 15일 | 61,891 | 61,891 | 123,782 | 167 | 20,671,594 | 114,208 |
| 2021년 01월 21일 | 442 | 442 | 884 | 161 | 142,324 | 786 |
| 2021년 01월 25일 | 27,408 | 27,408 | 54,816 | 157 | 8,606,112 | 47,548 |
| 2021년 06월 21일 | 5,924 | - | 5,924 | 10 | 59,240 | 327 |
| 합 계 | 129,260 | 123,336 | 252,596 | 41,330,350 | 228,345 | |
(2) 희석주당이익
당사의 당기 및 전기 희석화증권의 희석화 효과가 존재하지 않아 희석주당손실은 기본주당손실과 동일합니다.
(3) 희석성 잠재적 보통주
희석효과가 없어 희석주당손익의 계산에 고려되지 않은 잠재적 보통주의 내역은 다음과 같습니다.
| 구 분 | 액면금액(천원) | 청구기간 | 발행될 주식수(주) | 전환조건 |
|---|---|---|---|---|
| 제33회 전환사채 | 2,100,000 | 2020-12-18 ~ 2022-11-18 | 62,209 | 행사가액 33,757원 |
| 제34회 신주인수권부사채 | 57,000,000 | 2023-10-20 ~ 2026-10-20 | 1,588,451 | 행사가액 35,884원 |
| 제35회 신주인수권부사채 | 25,200,000 | 2023-03-30 ~ 2025-02-28 | 817,889 | 행사가액 30,811원 |
| 제36회 전환사채 | 23,000,000 | 2023-06-02 ~ 2025-05-02 | 473,202 | 행사가액 48,605원 |
| 제37회 신주인수권부사채 | 17,000,000 | 2023-06-02 ~ 2025-05-02 | 349,758 | 행사가액 48,605원 |
21. 매출액
(1) 매출액의 내역은 다음과 같습니다.
| (단위:천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 주요 지리적 시장: | ||||
| 국내 | 28,972,505 | 85,056,209 | 3,345,847 | 6,437,987 |
| 해외 | 27,975,964 | 35,330,268 | 3,126,119 | 5,540,198 |
| 합 계 | 56,948,469 | 120,386,478 | 6,471,966 | 11,978,185 |
| 수익 원천: | ||||
| 제품매출 | 51,030,471 | 108,810,099 | 5,111,941 | 9,624,489 |
| 수수료매출 | 4,150,989 | 4,374,217 | 213,163 | 446,836 |
| 상품매출 | 1,706,409 | 7,080,962 | 1,085,361 | 1,783,859 |
| 기타매출 | 60,600 | 121,200 | 61,500 | 123,000 |
| 합 계 | 56,948,469 | 120,386,478 | 6,471,965 | 11,978,185 |
| 수익인식 시기 | ||||
| 한 시점에 이행 | 52,736,880 | 115,891,241 | 6,410,465 | 11,855,185 |
| 기간에 걸쳐 이행 | 4,211,589 | 4,495,237 | 61,500 | 123,000 |
| 합 계 | 56,948,469 | 120,386,478 | 6,471,965 | 11,978,185 |
(2) 당반기 중 당사의 매출액의 10% 이상을 차지하는 2곳의 외부고객으로부터 발생한 매출액은 각각 59,295,775천원, 26,009,934천원 입니다.
(3) 고객과의 계약에서 생기는 계약자산은 없으며, 계약부채내역은 다음과 같습니다.
| (단위:천원) | ||
|---|---|---|
| 구 분 | 당반기말 | 전기말 |
| 계약부채 | 1,455,269 | 306,600 |
계약부채는 고객과의 계약을 위해 고객으로부터 선수취한 것입니다.
22. 성격별 비용
비용의 성격별 분류에 대한 정보는 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 재고자산의 변동 | (2,780,118) | (3,423,823) | (1,152,799) | (1,539,262) |
| 원재료 및 상품매입액 | 19,939,462 | 43,523,608 | 5,234,398 | 8,381,369 |
| 급여 | 2,244,733 | 4,572,475 | 1,535,066 | 2,985,906 |
| 퇴직급여 | 174,621 | 350,697 | 129,964 | 254,591 |
| 복리후생비 | 456,281 | 836,375 | 203,169 | 423,352 |
| 여비교통비 | 98,020 | 147,750 | 51,047 | 77,385 |
| 접대비 | 85,636 | 166,860 | 71,695 | 130,759 |
| 통신비 | 9,894 | 20,194 | 9,824 | 20,531 |
| 수도광열비 | 10,114 | 27,031 | 3,853 | 9,041 |
| 전력비 | 94,601 | 196,548 | 68,311 | 149,275 |
| 세금과공과금 | 89,854 | 203,590 | 49,857 | 125,134 |
| 감가상각비 | 605,389 | 1,225,301 | 463,215 | 893,594 |
| 지급임차료 | 186,393 | 363,689 | 108,067 | 216,095 |
| 보험료 | 91,651 | 229,785 | 97,956 | 172,821 |
| 차량유지비 | 41,403 | 73,977 | 31,264 | 61,636 |
| 운반비 | 392,159 | 753,789 | 112,199 | 231,169 |
| 도서인쇄비 | 10,654 | 23,290 | 13,595 | 26,580 |
| 소모품비 | 566,661 | 1,063,946 | 374,340 | 674,163 |
| 지급수수료 | 2,250,432 | 4,342,658 | 737,416 | 1,534,321 |
| 건물관리비 | 1,413 | 2,826 | - | - |
| 대손상각비(환입) | 69,603 | 22,941 | 708,964 | 705,714 |
| 무형자산상각비 | 2,908,149 | 5,816,451 | 3,627,696 | 3,634,709 |
| 외주용역비 | 12,138,095 | 23,369,740 | 1,455,974 | 2,622,485 |
| 판매보증비(환입) | (12,248) | (20,596) | 12,569 | 45,637 |
| 기타비용 | 94,265 | 188,995 | 83,843 | 121,081 |
| 합 계 (*) | 39,767,115 | 84,078,097 | 14,031,481 | 21,958,086 |
(*) 포괄손익계산서의 매출원가와 판매비와관리비를 합산한 금액입니다.
23. 종업원급여
(1) 당사는 확정급여형퇴직금제도와 확정기여형퇴직연금제도를 운영하고 있습니다.
(2) 확정급여채무의 변동내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 기 초 | - | - |
| 합병승계 | 693,419 | - |
| 당기근무원가 | 113,227 | - |
| 이자비용 | 9,423 | - |
| 퇴직금지급액 | (74,520) | - |
| 기 말 | 741,548 | - |
(3) 당기손익으로 인식된 비용은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 당반기 | 3개월 | 전반기 | |
| 확정급여제도: | ||||
| 당기근무원가 | 56,614 | 113,227 | - | - |
| 순이자원가 | 4,712 | 9,423 | - | - |
| 소 계 | 61,324 | 122,649 | - | - |
| 확정기여제도: | ||||
| 당기비용인식 기여금 | 110,009 | 228,441 | 129,964 | 254,591 |
| 합 계 | 171,334 | 351,091 | 129,964 | 254,591 |
(4) 사외적립자산의 공정가치 변동내역은 다음과 같습니다.
| (단위: 천원) | ||
| 구 분 | 당반기 | 전반기 |
| 기 초 | - | - |
| 합병승계 | 1,079,408 | - |
| 이자수익 | 7,854 | - |
| 기여금 납부액 | 3,000 | - |
| 퇴직급여 지급액 | (77,587) | - |
| 기 말 | 1,012,675 | - |
24. 판매비와관리비
판매비와관리비의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 급여 | 1,142,721 | 2,378,015 | 1,131,960 | 2,211,366 |
| 퇴직급여 | 89,089 | 189,084 | 102,786 | 203,917 |
| 복리후생비 | 202,407 | 424,215 | 139,466 | 295,029 |
| 여비교통비 | 75,343 | 113,842 | 35,988 | 52,484 |
| 접대비 | 85,306 | 166,417 | 71,695 | 130,759 |
| 통신비 | 7,634 | 15,545 | 7,471 | 15,774 |
| 전력비 | 9,853 | 22,675 | 13,370 | 34,871 |
| 세금과공과금 | 47,340 | 132,333 | 32,647 | 92,201 |
| 감가상각비 | 300,285 | 602,413 | 282,960 | 550,961 |
| 지급임차료 | 121,233 | 234,569 | 108,067 | 216,095 |
| 보험료 | 31,508 | 105,137 | 79,382 | 138,699 |
| 차량유지비 | 30,856 | 54,787 | 27,609 | 49,577 |
| 경상연구개발비 | 197,819 | 279,437 | 73,034 | 165,586 |
| 도서인쇄비 | 2,849 | 10,451 | 6,070 | 17,404 |
| 소모품비 | 52,529 | 154,001 | 29,714 | 52,398 |
| 지급수수료 | 1,079,842 | 2,136,234 | 616,240 | 1,194,009 |
| 광고선전비 | 21,628 | 51,469 | 32,540 | 55,674 |
| 건물관리비 | 1,413 | 2,826 | - | - |
| 대손상각비 | 69,603 | 22,941 | 708,964 | 705,714 |
| 무형자산상각비 | 2,908,149 | 5,816,451 | 3,627,696 | 3,634,709 |
| 판매보증비(환입) | (12,248) | (20,596) | 12,569 | 45,637 |
| 기타 | 125,557 | 292,664 | 29,658 | 66,429 |
| 합 계 | 6,590,714 | 13,184,909 | 7,169,885 | 9,929,293 |
25. 기타수익 및 기타비용
(1) 기타수익의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 수입임대료 | - | - | - | 6,452 |
| 대손충당금환입 | 1,497 | 1,497 | - | - |
| 유형자산처분이익 | - | 21,421 | - | - |
| 투자자산처분이익 | 260 | 260 | - | 289,273 |
| 잡이익 | (21,925) | 53,863 | 40,313 | 47,456 |
| 보험차익 | 382,866 | 382,866 | 1,541,008 | 1,633,036 |
| 국고보조금 | 2,352 | 2,352 | - | - |
| 합 계 | 365,052 | 462,260 | 1,581,321 | 1,976,216 |
(2) 기타비용의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 기부금 | 15,000 | 15,000 | - | - |
| 기타의대손상각비 | (914) | - | - | - |
| 유형자산폐기손실 | - | - | - | 59 |
| 투자부동산상각비 | - | - | - | 8,175 |
| 재해손실(*) | - | - | 1,412,200 | 2,164,512 |
| 잡손실 | (11,483) | 41,205 | 3,269 | 3,711 |
| 합 계 | 2,604 | 56,205 | 1,415,469 | 2,176,457 |
(*) 전반기 중 화재 피해로 인하여 재고자산 및 공장 일부가 소실되었습니다.
26. 금융수익 및 금융비용
(1) 금융수익의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 이자수익 | 282,391 | 520,445 | 328,429 | 648,263 |
| 외환차익 | 746,601 | 796,374 | 35,874 | 80,604 |
| 외화환산이익 | 625,331 | 975,952 | 171,373 | 369,267 |
| 통화선물거래이익 | 10,500 | 10,500 | - | - |
| 당기손익-공정가치측정금융자산 처분이익 | (260) | - | - | - |
| 당기손익-공정가치측정금융자산 평가이익 | 4,415,595 | 4,418,532 | - | - |
| 파생상품평가이익 | 3,017,209 | 3,017,209 | - | - |
| 보증충당부채환입액 | - | - | 82,479 | 82,479 |
| 합 계 | 9,097,367 | 9,739,013 | 618,155 | 1,180,614 |
(2) 금융비용의 상세내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당반기 | 전반기 | ||
| 3개월 | 누적 | 3개월 | 누적 | |
| 이자비용 | 2,467,868 | 3,927,763 | 625,605 | 1,278,234 |
| 외환차손 | 167,552 | 180,109 | 79,610 | 95,676 |
| 외화환산손실 | (9,679) | 783 | - | 881 |
| 당기손익-공정가치측정금융자산 평가손실 | (3,931,987) | 174,621 | 11,372,168 | 11,372,168 |
| 통화선물거래손실 | 9,600 | 9,600 | - | - |
| 합 계 | (1,296,645) | 4,292,876 | 12,077,383 | 12,746,958 |
27. 법인세비용
법인세비용의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 법인세부담액 | 7,390,517 | - |
| 이연법인세의 증감 | (478,764) | - |
| 법인세추납액 | 13,837 | - |
| 법인세비용 | 6,925,591 | - |
28. 금융상품
(1) 금융상품의 범주별 분류
범주별 금융상품의 장부금액은 다음과 같습니다.
① 당반기말
| (단위:천원) | |||||
| 구 분 | 당기손익- 공정가치측정 금융자산 |
기타포괄손익- 공정가치측정 금융자산 |
상각후원가측정 금융자산 |
상각후원가측정 금융부채 |
합 계 |
| 현금및현금성자산 | - | - | 48,724,359 | - | 48,724,359 |
| 매출채권 및 기타금융자산 | - | - | 42,963,673 | - | 42,963,673 |
| 지분상품 | 1,410 | 5,793,068 | - | - | 5,794,478 |
| 복합금융상품 | 45,742,137 | - | - | - | 45,742,137 |
| 파생상품(*) | 7,113,529 | - | - | - | 7,113,529 |
| 채무상품 | 1,576,605 | - | - | - | 1,576,605 |
| 금융자산 합계 | 54,433,682 | 5,793,068 | 91,688,032 | - | 151,914,782 |
| 매입채무 | - | - | - | 4,533,212 | 4,533,212 |
| 기타금융부채 | - | - | - | 9,465,819 | 9,465,819 |
| 금융보증부채 | - | - | - | 62,156 | 62,156 |
| 차입금 | - | - | - | 110,053,697 | 110,053,697 |
| 금융부채 합계 | - | - | - | 124,114,884 | 124,114,884 |
(*) 복합금융상품의 내재파생상품(매도청구권) 입니다. (주석 6 참조)
② 전기말
| (단위:천원) | |||||
| 구 분 | 당기손익-공정가치측정 금융자산 |
기타포괄손익-공정가치측정 금융자산 |
상각후원가측정 금융자산 |
상각후원가측정 금융부채 |
합 계 |
| 현금및현금성자산 | - | - | 36,642,797 | - | 36,642,797 |
| 매출채권 및 기타금융자산 | - | - | 30,371,597 | - | 30,371,597 |
| 지분상품 | 1,410 | 6,073,286 | - | - | 6,074,696 |
| 복합금융상품 | 21,726,530 | - | - | - | 21,726,530 |
| 채무상품 | 322,053 | - | - | - | 322,053 |
| 금융자산 합계 | 22,049,993 | 6,073,286 | 67,014,394 | - | 95,137,673 |
| 매입채무 | - | - | - | 939,313 | 939,313 |
| 기타금융부채 | - | - | - | 5,524,956 | 5,524,956 |
| 금융보증부채 | - | - | - | 56,500 | 56,500 |
| 차입금 | - | - | - | 64,726,776 | 64,726,776 |
| 금융부채 합계 | - | - | - | 71,247,545 | 71,247,545 |
(2) 금융상품 범주별 금융수익과 금융비용의 상세내역은 다음과 같습니다.
① 당반기
| (단위: 천원) | ||||||||
| 구 분 | 이자수익/비용 | 기타금융수익/비용 | 순손익 | 기타포괄손익 | ||||
| 3개월 | 누적 | 3개월 | 누적 | 3개월 | 누적 | 3개월 | 누적 | |
| 기타포괄손익-공정가치측정 금융자산 | - | - | - | - | - | - | (358,057) | (280,218) |
| 당기손익-공정가치측정 금융자산 | - | 50,000 | 7,261,120 | 7,261,120 | 7,261,120 | 7,311,120 | - | - |
| 상각후원가측정금융자산(*) | 282,391 | 470,445 | 378,275 | 1,592,334 | 660,666 | 2,062,779 | - | - |
| 상각후원가측정금융부채 | (2,467,868) | (3,927,763) | - | - | (2,467,868) | (3,927,763) | - | - |
| 합 계 | (2,185,478) | (3,407,318) | 7,639,396 | 8,853,455 | 5,453,918 | 5,446,137 | (358,057) | (280,218) |
(*) 상각후원가측정금융자산에서 인식한 대손상각비 및 기타의 대손상각비는 판매비와 관리비 및 기타손익으로 분류되어 있으며 상기의 표에는 포함되어 있지 않습니다.
② 전반기
| (단위: 천원) | ||||||||
| 구 분 | 이자수익/비용 | 기타금융수익/비용 | 순손익 | 기타포괄손익 | ||||
| 3개월 | 누적 | 3개월 | 누적 | 3개월 | 누적 | 3개월 | 누적 | |
| 기타포괄손익-공정가치측정 금융자산 | - | - | - | - | - | - | - | 1,155,458 |
| 당기손익-공정가치측정 금융자산 | 25,000 | 50,000 | (11,372,168) | (11,372,168) | (11,347,168) | (11,322,168) | - | - |
| 상각후원가측정금융자산(*) | 303,429 | 598,263 | 28,665 | (15,072) | 332,093 | 583,191 | - | - |
| 상각후원가측정금융부채 | (625,605) | (1,278,234) | - | 82,479 | (625,605) | (1,195,754) | - | - |
| 합 계 | (297,177) | (629,970) | (11,343,504) | (11,304,761) | (11,640,680) | (11,934,732) | - | 1,155,458 |
(*) 상각후원가측정금융자산에서 인식한 대손상각비 및 기타의 대손상각비는 판매비와 관리비 및 기타손익으로 분류되어 있으며 상기의 표에는 포함되어 있지 않습니다.
29. 우발부채와 약정사항
(1) 당사와 금융기관 등과의 대출약정 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 차입종별 | 만기일 | 약정금액 | 담보제공금액 |
| 중소기업은행(*) | 일반운전자금대출 등 | 2031.06.15 | 320,000 | 384,000 |
(*) 당사는 중소기업은행에 대하여 토지, 건물, 기계장치를 담보로 제공하고 있습니다.
(2) 당반기말 현재 당사가 제3자로부터 제공받은 지급보증의 내역은 다음과 같습니다.
| (단위 : 천원) | |||
|---|---|---|---|
| 제공자 | 제공처 | 보증금액 | 비고 |
| 서울보증보험 | 매출처 등 | 1,457,711 | 하자이행보증, 지급보증 등 |
(3) 당반기말 현재 당사가 타인에게 제공한 지급보증의 내역은 다음과 같습니다.
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구분 | 회사명 | 보증처 | 내용 | 지급보증금액 | 연대 보증인 |
보증기간 |
| 종속기업 | Elevar Therapeutics, Inc.(*) | Baxter | 지급보증 | - | - | - |
| 소 계 | - | |||||
| 관계기업 | 현대요트㈜ | 서울보증보험 | 하자이행 | 44,275 | - | 2018-06-23 ~ 2023-06-22 |
| 선급이행 | 1,166,593 | - | 2022-04-20 ~ 2023-02-15 | |||
| 선급이행 | 191,111 | - | 2021-12-17 ~ 2022-12-17 | |||
| 선급이행 | 280,566 | - | 2020-07-29 ~ 2022-09-29 | |||
| 소 계 | 1,682,545 | |||||
| 합 계 | 1,682,545 | |||||
(*) 자회사 Elevar의 제품 위탁생산에 대한 대금 지급보증을 제공하였습니다.
30. 특수관계자
(1) 당사의 특수관계자는 관계기업 및 종속기업과 당사의 주요 경영진, 그리고 경영진이 출자 또는 임원으로 재직중인 기업입니다.
| 구 분 | 회사명 | 상장여부 |
|---|---|---|
| 종속기업 | Elevar Therapeutics, Inc. | 비상장 |
| Immunomic Therapeutics, Inc. | ||
| 에이치엘비인베스트먼트㈜ | ||
| Hyundai Lifeboats Shanghai PTE.LTD(*1) | ||
| 관계기업 | 에이치엘비생명과학㈜ | 상장 |
| 에이치엘비테라퓨틱스㈜(*2) | ||
| ㈜노터스(*1) | ||
| Verismo Therapeutics, Inc. | 비상장 | |
| 바다중공업㈜ | ||
| 현대요트㈜ | ||
| 기타특수관계자 | ㈜HLB글로벌 | 상장 |
| 에이치엘비제약㈜ | ||
| HLB사이언스㈜ | ||
| ㈜화진메디칼(*2) | 비상장 | |
| ㈜화진메디스(*2) | ||
| ㈜엘에스케이인베스트먼트 | ||
| ㈜고션 | ||
| 에이치엘비일렉㈜ | ||
| 에이치엘비네트웍스㈜ | ||
| Hyundai Lifeboats Singapore Pte. Ltd | ||
| 오티에스중공업㈜ | ||
| 현대코스모스요팅㈜ | ||
| ㈜신화어드밴스 | ||
| 에이치엘비엘이디㈜ | ||
| 에이치엘비에너지㈜ | ||
| ㈜펭귄오션레저 | ||
| HLB생활건강 | ||
| 에이치엘비셀㈜ | ||
| ㈜프레시코 | ||
| ㈜코아바이오 | ||
| 에포케㈜ | ||
| 지트리파마슈티컬 | ||
| REGENTREE | ||
| OBLATO | ||
| 바다엔지니어링㈜ | ||
| ㈜새론바이오 | ||
| 브이에스팜㈜ | ||
| ㈜온힐 | ||
| ㈜베리스모테라퓨틱스 아시아 | ||
| 에이치엘비생명과학알앤디㈜ | ||
| ㈜개밥왕 |
(*1) 당반기 중 신규 편입되었습니다. (주석 10 참조)
(*2) 당반기 중 지분 100%를 당사의 관계기업에 매각하였습니다. (주석 10 참조)
(2) 당사의 특수관계자와의 매출 및 매입 내역은 다음과 같습니다.
① 당반기말
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 특수관계구분 | 특수관계자명 | 매출 | 매입 | ||
| 매출거래 | 기타 | 원재료 등 매입 | 기타 | ||
| 관계기업 | ㈜화진메디칼 | - | - | 7,258 | 38,101 |
| 에이치엘비생명과학㈜ | 120,000 | - | - | 186,023 | |
| HLB테라퓨틱스㈜ | - | 646,000 | 1,059,587 | 9,410,279 | |
| 바다중공업㈜ | 61,700 | - | 1,847,544 | - | |
| 현대요트㈜ | 291,890 | - | - | 31,818 | |
| 기타특수관계자 | HLB글로벌 (구.넥스트사이언스) |
- | - | - | 4,158 |
| HLB네트웍스㈜(*1) | 690,870 | - | - | 500 | |
| ㈜펭귄오션레저 | 41,200 | - | - | 2,430 | |
| 합 계 | 1,205,660 | 646,000 | 2,914,388 | 9,673,309 | |
(*) 당사는 기타특수관계자인 에이치엘비네트웍스㈜에 구명정 서비스 독점권을 부여하여 러닝개런티를 통한 로열티수익을 창출하고 있습니다.
② 전반기말
| (단위: 천원) | |||||
| 특수관계구분 | 특수관계자명 | 매출 | 매입 | ||
| 매출거래 | 기타 | 원재료매입 | 기타 | ||
| 종속기업 | Elevar Therapeutics, Inc. | - | - | - | 58,805 |
| 관계기업 | 에이치엘비생명과학㈜ | 120,000 | - | - | 185,038 |
| 바다중공업㈜ | - | - | 1,573,305 | 3,000 | |
| 기타특수관계자 | ㈜넥스트사이언스 | - | - | - | 4,158 |
| 에이치엘비일렉㈜ | - | 295,724 | - | - | |
| 에이치엘비네트웍스㈜ | 732,946 | - | - | 4,000 | |
| ㈜펭귄오션레저 | 36,400 | - | - | 29,400 | |
| ㈜엘리샤코이 | - | - | - | 6,608 | |
| ㈜프레시코 | - | - | - | 6,839 | |
| 합 계 | 889,346 | 295,724 | 1,573,305 | 297,847 | |
당사는 기타특수관계자인 에이치엘비네트웍스㈜에 구명정 서비스 독점권을 부여하여 러닝개런티를 통한 로열티수익을 창출하고 있습니다.
(3) 특수관계자와의 자금거래 내역은 다음과 같습니다.
① 당반기
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 특수관계구분 | 특수관계자명 | 자금 유출 거래 | 자금 유입 거래 | 기타 | ||
| 자금대여 | 출자 | 대여금회수 | 이자수취 | 주식매수선택권 | ||
| 종속기업 | Elevar Therapeutics, Inc.(*1) | - | 31,394,745 | - | - | 117,796 |
| Hyundai Lifeboats Shanghai PTE.LTD | - | 1,385,000 | - | - | - | |
| 관계기업 | ㈜노터스 | - | 31,025,920 | - | - | - |
| 에이치엘비생명과학(*2) | 19,603,370 | |||||
| 바다중공업 | 2,000,000 | - | - | - | - | |
| 기타특수관계자 | HLB제약㈜(구. ㈜메디포럼제약) | - | - | - | 50,000 | - |
| 화진메디칼 | - | - | 1,700,000 | 51,633 | - | |
| 합 계 | 21,603,370 | 63,805,665 | 1,700,000 | 101,633 | 117,796 | |
(*1) 당사는 당반기 중 Elevar Therapeutics, Inc.의 임원 2인에게 당사의 주식매수선택권을 부여하였으며, 주식보상비용으로 측정되는 금액에 대해 종속기업에 자본을 불입한 것으로 보아 투자지분의 증가로 회계처리하였습니다.(주석 10 참조)
(*2) 에이치엘비생명과학㈜ 제9회 공모 신주인수권부사채에 청약하여 신주인수권부사채를 취득하였습니다.
② 전반기
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 특수관계구분 | 특수관계자명 | 자금 유출 거래 | 자금 유입 거래 | ||
| 자금대여 | 출자 | 대여금회수 | 이자 수취 | ||
| 종속기업 | 에이치엘비인베스트먼트주식회사 | 45,490 | 3,000,000 | 45,490 | 40 |
| 관계기업 | Verismo Therapeutics, Inc. | - | 5,586,000 | - | - |
| 기타특수관계자 | 에이치엘비제약㈜(구. ㈜메디포럼제약) | - | - | - | 50,000 |
| 합 계 | 45,490 | 8,586,000 | 45,490 | 50,040 | |
(4) 특수관계자에 대한 채권ㆍ채무내역은 다음과 같습니다.
① 당반기말
| (단위: 천원) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 구분 | 채권 | 채무 | |||||||
| 특수관계구분 | 특수관계자명 | 매출채권 | 대여금 | 미수금 | 미수수익 | 기타(*2) | 매입채무 | 계약부채 | 기타 |
| 종속기업 | Hyundai Lifeboats Shanghai PTE.LTD | - | - | 9,667,668 | - | - | - | - | - |
| 관계기업 | HLB테라퓨틱스㈜ | 73,172 | - | - | - | - | 996,241 | - | - |
| 에이치엘비생명과학 | - | - | - | - | 22,469,317 | - | - | - | |
| 바다중공업㈜ | - | 2,000,000 | - | 10,334 | - | 228,292 | - | - | |
| 현대요트㈜ | 57,900 | - | - | - | - | - | 656,610 | 5,833 | |
| 기타특수관계자 | HLB글로벌(구.넥스트사이언스) | - | - | - | - | - | - | - | 762 |
| HLB네트웍스㈜ | 319,039 | - | 70 | - | - | - | - | - | |
| ㈜펭귄오션레저(*1) | 660 | 23,600 | 53,306 | 1,628 | 93,293 | - | - | - | |
| 현대코스모스요팅 | - | - | - | - | - | - | - | 54,000 | |
| HLB제약㈜(구. ㈜메디포럼제약)(*2) | - | - | - | - | 23,272,820 | - | - | - | |
| 합 계 | 450,771 | 2,023,600 | 9,721,043 | 11,963 | 45,835,430 | 1,224,533 | 656,610 | 60,596 | |
(*1) 당반기말 현재 상기의 특수관계자 채권에 대해 대손충당금 171,021천원이 설정되어 있습니다.
(*2) 기타의 채권은 당사가 보유한 전환사채권 및 신주인수권사채권이며, 공정가치평가 후 금액입니다. (주석 3 참조)
② 전반기말
| (단위: 천원) | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 구분 | 채권 | 채무 | ||||||||
| 특수관계 구분 | 특수관계자명 | 매출채권 (*1) |
단기대여금 (*1) |
미수금 (*1) |
미수수익 (*1) |
보증금 (*1) |
기타 (*1) |
매입채무 | 계약부채 | 기타 |
| 종속기업 | Elevar Therapeutics, Inc. | - | - | - | - | - | - | - | - | 59,240 |
| ㈜화진메디칼 | - | - | - | - | - | - | - | - | 14,472 | |
| 관계기업 | 에이치엘비생명과학㈜(*2) | - | - | - | - | - | 13,171,760 | - | - | - |
| 바다중공업㈜ | - | - | - | - | - | 6,000 | 417,319 | - | - | |
| 현대요트㈜ | - | 781,000 | 13 | 378,763 | 53,897 | - | - | 58,000 | - | |
| 기타특수관계자 | 에이치엘비셀㈜(구.라이프리버㈜) | - | - | 6 | - | - | - | - | - | - |
| 에이치엘비네트웍스㈜ | 315,403 | - | 69 | - | - | - | - | - | - | |
| ㈜고션 | 198,000 | 70,000 | - | - | - | - | - | - | - | |
| 오티에스중공업㈜ | - | 400,000 | - | 3,478 | - | - | - | - | - | |
| ㈜펭귄오션레저(*2) | 660 | 23,600 | 53,176 | 1,628 | - | 93,293 | - | 4,900 | - | |
| ㈜넥스트사이언스 | - | - | - | - | - | - | - | - | 762 | |
| ㈜엘리샤코이 | - | - | - | - | - | - | - | - | 529 | |
| 에이치엘비제약㈜ (구. ㈜메디포럼제약)(*2) |
- | - | - | - | - | 22,125,882 | - | - | - | |
| 합 계 | 514,063 | 1,274,600 | 53,264 | 383,870 | 53,897 | 35,396,934 | 417,319 | 62,900 | 75,003 | |
(*1) 전반기말 현재 상기의 특수관계자 채권에 대해 대손충당금 2,056,160천원이 설정되어 있습니다.
(*2) 기타의 채권은 당사가 보유한 전환사채권이며, 공정가치평가 후 금액입니다. (주석 3 참조)
(5) 당반기말 현재 당사가 특수관계자에게 제공한 지급보증의 내역은 다음과 같습니다.
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구분 | 회사명 | 보증처 | 내용 | 지급보증금액 | 연대 보증인 |
보증기간 |
| 종속기업 | Elevar Therapeutics, Inc.(*) | Baxter | 지급보증 | - | - | - |
| 소 계 | - | |||||
| 관계기업 | 현대요트㈜ | 서울보증보험 | 하자이행 | 44,275 | - | 2018-06-23 ~ 2023-06-22 |
| 선급이행 | 1,166,593 | - | 2022-04-20 ~ 2023-02-15 | |||
| 선급이행 | 191,111 | - | 2021-12-17 ~ 2022-12-17 | |||
| 선급이행 | 280,566 | - | 2020-07-29 ~ 2022-09-29 | |||
| 소 계 | 1,682,545 | |||||
| 합 계 | 1,682,545 | |||||
(*) 자회사 Elevar의 제품 위탁생산에 대한 대금 지급보증을 제공하였습니다.
(6) 주요 경영진에 대한 보상
당사의 주요경영진은 회사활동의 계획, 운영 및 통제에 대한 중요한 권한과 책임을 가진 등기임원들로 구성되어 있습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당반기 | 전반기 |
| 급여 및 기타 단기종업원 급여 | 599,990 | 706,300 |
| 퇴직급여 | 43,092 | 68,191 |
| 합 계 | 643,082 | 774,491 |
31. 현금흐름표
(1) 영업활동 중 수익ㆍ비용의 조정 내역은 다음과 같습니다.
| (단위: 천원) | ||
| 구 분 | 당반기 | 전반기 |
| 이자비용 | 3,927,763 | 1,278,234 |
| 외화환산손실 | 783 | 881 |
| 법인세비용(수익) | 6,925,591 | - |
| 퇴직급여 | 350,697 | 254,591 |
| 감가상각비 | 1,225,301 | 893,594 |
| 무형자산상각비 | 5,816,451 | 3,634,709 |
| 투자부동산상각비 | - | 8,175 |
| 대손상각비(환입) | 22,941 | 705,714 |
| 기타의대손상각비(환입) | (1,497) | - |
| 재고자산평가손실(환입) | 339,464 | 36,559 |
| 유형자산폐기손실 | - | 59 |
| 재해손실 | - | 1,360,712 |
| 판매보증비(환입) | (20,596) | 45,637 |
| 당기손익-공정가치측정금융자산 평가손실 | 174,621 | 11,372,168 |
| 통화선물거래손실 | 9,600 | - |
| 이자수익 | (520,445) | (648,263) |
| 외화환산이익 | (975,952) | (369,267) |
| 유형자산처분이익 | (21,421) | - |
| 투자자산처분이익 | - | (289,273) |
| 보증충당부채환입액 | - | (82,479) |
| 통화선물거래이익 | (10,500) | - |
| 파생상품평가이익 | (3,017,209) | - |
| 당기손익-공정가치측정금융자산 평가이익 | (4,418,532) | - |
| 종속및관계기업투자주식처분이익 | (800,000) | - |
| 합 계 | 9,007,058 | 18,201,751 |
(2) 영업활동으로 인한 자산ㆍ부채의 변동 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 매출채권의 감소(증가) | (5,383,817) | 4,608,949 |
| 재고자산의 감소(증가) | (3,734,225) | (2,087,135) |
| 기타유동금융자산의 감소(증가) | (88,576) | (290,983) |
| 기타의 유동자산의 감소(증가) | (1,525,945) | (312,926) |
| 매입채무의 증가(감소) | (110,690) | 30,666 |
| 계약부채의 증가(감소) | 1,158,795 | - |
| 기타유동금융부채의 증가(감소) | (2,814,411) | (1,108,825) |
| 기타비유동금융부채의 증가(감소) | 34,773 | (33,629) |
| 기타의 유동부채의 증가(감소) | (831,734) | (130,326) |
| 사외적립자산의 감소(증가) | 77,874 | - |
| 퇴직금의 지급 | (138,685) | (66,341) |
| 합 계 | (13,356,642) | 609,450 |
(3) 당사의 현금흐름 가운데 현금의 유입과 유출이 없는 중요한 거래내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당반기 | 전반기 |
| 전환사채의 전환으로 인한 자본대체 | 16,409,073 | 9,647,333 |
| 관계기업 지분취득대금 신주인수권부사채발행 대용납입 | 25,200,000 | - |
| 리스 계약 사용권자산 인식 | 335,989 | 383,860 |
| 리스 종료로 인한 사용권자산 감소 | 110,939 | 189,116 |
| 건설중인자산 본계정대체 | - | 26,000 |
| 주식발행초과금의 이익잉여금 전입 | 130,000,000 | - |
| 사업결합으로 인한 자산 승계 | 134,039,064 | - |
| 사업결합으로 인한 부채 승계 | 28,579,380 | - |
| 사업결합으로 인한 종속기업투자주식 제거 | 102,205,340 | - |
| 주식매수선택권 부여로 인한 종속기업투자주식 증가 | 117,796 | - |
(4) 재무활동과 관련된 부채의 변동
당반기 중 재무활동에서 생기는 부채의 변동은 다음과 같습니다.
| (단위: 천원) | |||||||
|---|---|---|---|---|---|---|---|
| 구분 | 기초 | 현금흐름 | 비현금 변동 | 기말 | |||
| 취득 | 보통주전환 | 상각 | 유동성대체 | ||||
| 단기차입금 | 6,000,000 | (6,000,000) | - | - | - | - | - |
| 장기차입금 | 320,000 | - | - | - | - | - | 320,000 |
| 전환사채(유동) | 11,494,916 | - | - | (9,359,637) | - | - | 2,135,278 |
| 신주인수권부사채(유동)(*) | - | - | 23,090,422 | - | 658,765 | - | 23,749,187 |
| 전환사채(비유동) | - | 23,000,000 | (3,630,137) | - | 208,798 | - | 19,578,661 |
| 신주인수권부사채(비유동) | 46,911,860 | 17,000,000 | (2,683,163) | - | 3,041,873 | - | 64,270,570 |
| 금융리스부채(유동) | 583,924 | (504,053) | 306,334 | - | 15,125 | 46,154 | 447,483 |
| 금융리스부채(비유동) | 180,237 | - | - | - | - | (46,154) | 134,083 |
| 합계 | 65,490,937 | 33,495,947 | 17,083,456 | (9,359,637) | 3,924,561 | - | 110,635,263 |
(*) 관계기업의 지분 취득대금 대용납입 목적으로 발행하였습니다. (주석 10 참조)
32. 사업결합
(1) 합병의 개요
회사는 사업경쟁력 및 시너지효과를 극대화하기 위하여 2022년 1월 1일을 합병기일로 하여 종속기업 ㈜에프에이를 흡수합병하였습니다.
(2) 합병 참여회사 및 합병비율
| 구분 | 상호 | 대표이사 | 법인구분 | 주요영업 | 소재지 | 합병비율 |
|---|---|---|---|---|---|---|
| 합병후 존속회사 | 에이치엘비㈜ | 진양곤, 김동건 | 코스닥시장상장 | 제조업 | 울산광역시 울주군 | - |
| 합병후 소멸회사 | ㈜에프에이 | 남윤제 | 비상장 | 제조업 | 세종특별자치시 연동면 | 1:0 |
(3) 회계처리
상기 합병은 지배기업인 당사의 동일 지배하에 있는 종속회사와의 합병으로 당사의 연결재무제표를 구성하는 피합병법인의 자산 및 부채를 승계하여 장부금액으로 인식하였으며, 합병으로 승계한 자산과 부채의 내용은 다음과 같습니다.
| (단위 : 원) | |
|---|---|
| 구분 | 장부금액 |
| <자산> | |
| I. 유동자산 | 50,014,134,518 |
| 현금및현금성자산 | 11,013,305,431 |
| 매출채권 | 12,689,929,747 |
| 공정가치측정금융자산 | 18,000,000,000 |
| 기타유동금융자산 | 194,166,305 |
| 재고자산 | 8,050,289,352 |
| 기타유동자산 | 66,443,683 |
| II. 비유동자산 | 84,024,929,969 |
| 비유동공정가치측정금융자산 | 1,712,759,562 |
| 기타비유동금융자산 | 446,000,000 |
| 유형자산 | 20,917,474,344 |
| 무형자산 | 59,801,866,724 |
| 퇴직연금운용자산 | 1,079,407,604 |
| 이연법인세자산 | 67,421,735 |
| 자산총계 | 134,039,064,487 |
| <부채> | |
| I. 유동부채 | 21,065,828,927 |
| 매입채무 | 3,704,588,165 |
| 기타유동금융부채 | 6,735,322,357 |
| 계약부채 | 12,323,200 |
| 기타유동부채 | 973,640,210 |
| 당기법인세부채 | 9,639,954,995 |
| II. 비유동부채 | 7,513,551,370 |
| 이연법인세부채 | 7,513,551,370 |
| 부채총계 | 28,579,380,297 |
(4) 이전대가
당사는 2021년 10월 ㈜에프에이의 지분 100%를 총 이전대가 101,920,000천원에 취득하여 종속기업으로 편입하였는 바, 이전대가 중 44,920,000천원은 현금으로 납입하고 57,000,000천원은 신주인수권부사채를 발행하여 대용납입 하였습니다.
한편, 합병시에는 피합병회사의 주식 100%를 이미 소유하고 있으므로 합병신주를 발행하지 않는 무증자 방식으로 진행하였습니다.
33. 계류중인 소송 사건
당반기말 현재 당사를 원고로 하는 계류중인 중요한 소송사건의 주요 내용은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 원 고 | 피 고 | 소 송 내 용 | 소 송 가 액(*) |
| 에이치엘비 주식회사 | 하이투자증권㈜ | 부당이득금 반환 청구 | 30,000,000 |
(*) 당사가 펀드투자를 위해 하이투자증권에 최초 예치한 금액이나, 사기적 부정거래행위 및 불완전판매 요소가 발견되어 부당이득금 반환 청구소송을 진행 중입니다. 당사의 대표이사는 본 사건과 관련하여 발생가능한 손실을 보전하기 위하여 대표이사가 보유한 당사의 주식을 법무법인에 위탁하는 계약을 체결하였습니다.
34. 종속회사인 Elevar Therapeutics, Inc.에 대한 가치평가시, 리보세라닙 신약허가 관련 불확실성의 반영
당사의 종속회사인 Elevar Therapeutics, Inc. 는 표적항암제 리보세라닙의 주요 Pipeline 중 하나인 위암말기 표준치료법의 글로벌 3상 임상시험을 완료하였습니다. 2019년 10월 Pre-NDA미팅(품목허가를 위한 사전상담)에서 FDA는 사전 제출한 1차 유효성 지표인 OS(전체생존기간) 결과가 통계학적 유의미성을 확보하지 못한 부분을 언급하였고, 이에 Elevar Therapeutics, Inc.는 임상3상 데이터 추가 수집 및 분석과 외부 임상 데이터의 수집 및 분석치를 제시하겠다는 제안을 하였습니다. 이에 추가적으로 FDA는 상기 제안과 별도로 약동학 실험, CMC(제조품질관리) 등의 자료보완을 권고하였습니다.
이에 대해 Elevar Therapeutics, Inc. 는 2020년 회계기간 동안 약동학 실험을 완료하였고, CMC(제조품질관리)에 대해서도 준비를 마쳤으며, 2021년 회계기간 동안 임상3상 데이터 추가수집 및 분석을 완료하였고, 외부 임상 데이터 역시 수집 완료 후 분석을 진행 중 입니다.
당사는 상기 외부 임상 데이터 분석결과의 불확실성과 COVID-19 펜데믹 상황에 따른 임상일정 지연 등을 고려하여 Elevar Therapeutics, Inc.의 가치평가 시 제반변수를 보수적관점으로 적용하였는 바, 전기에 39,266,897천원의 종속기업투자주식 손상차손을 인식하였습니다. 한편, 리보세라닙 위암말기 표준치료법의 FDA 승인 성공확률을 0%로 가정할 경우 재무제표에 추가 반영되어야 하는 가치 감소 금액은 38,495,062천원입니다.
6. 배당에 관한 사항
당사는 정관에 의거 이사회 결의 및 주주총회 결의를 통하여 배당을 지급하고 있으며배당가능이익 범위 내에서 회사의 지속적 성장을 위한 투자 및 주주가치 제고, 경영환경 등을 고려하여 적정 수준의 배당율을 결정하고 있습니다.
배당에 관한 회사의 정관 규정은 다음과 같습니다.
|
제13조 (신주의 배당기산일) 제56조 (이익배당) ② 이익의 배당을 주식으로 하는 경우 회사가 수종의 주식을 발행한 때에는 주주총회의 ③ 제1항의 배당은 매결산기말 현재의 주주명부에 기재된 주주 또는 등록된 질권자에게 |
가. 주요배당지표
| 구 분 | 주식의 종류 | 당기 | 전기 | 전전기 |
|---|---|---|---|---|
| 제38기 당반기 | 제37기 | 제36기 | ||
| 주당액면가액(원) | 500 | 500 | 500 | |
| (연결)당기순이익(백만원) | -9,472 | -98,125 | -80,093 | |
| (별도)당기순이익(백만원) | 35,755 | -54,736 | -60,065 | |
| (연결)주당순이익(원) | -89 | -923 | -768 | |
| 현금배당금총액(백만원) | - | - | - | |
| 주식배당금총액(백만원) | - | - | - | |
| (연결)현금배당성향(%) | - | - | - | |
| 현금배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주식배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주당 현금배당금(원) | - | - | - | - |
| - | - | - | - | |
| 주당 주식배당(주) | - | - | - | - |
| - | - | - | - | |
나. 과거 배당 이력
| (단위: 회, %) |
| 연속 배당횟수 | 평균 배당수익률 | ||
|---|---|---|---|
| 분기(중간)배당 | 결산배당 | 최근 3년간 | 최근 5년간 |
| - | - | - | - |
7. 증권의 발행을 통한 자금조달에 관한 사항
7-1. 증권의 발행을 통한 자금조달 실적
| [지분증권의 발행 등과 관련된 사항] |
증자(감자)현황
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 원, 주) |
| 주식발행 (감소)일자 |
발행(감소) 형태 |
발행(감소)한 주식의 내용 | ||||
|---|---|---|---|---|---|---|
| 종류 | 수량 | 주당 액면가액 |
주당발행 (감소)가액 |
비고 | ||
| 2018.03.09 | 전환권행사 | 보통주 | 58,826 | 500 | 16,999 | - |
| 2018.04.17 | 전환권행사 | 보통주 | 88,239 | 500 | 16,999 | - |
| 2018.05.24 | 전환권행사 | 보통주 | 29,413 | 500 | 16,999 | - |
| 2018.06.25 | 전환권행사 | 보통주 | 29,413 | 500 | 16,999 | - |
| 2018.07.02 | 주식매수선택권행사 | 보통주 | 195,000 | 500 | 8,202 | - |
| 2018.07.31 | 전환권행사 | 보통주 | 1,308,670 | 500 | 14,442 | - |
| 2018.08.01 | 전환권행사 | 보통주 | 152,331 | 500 | 14,442 | - |
| 2018.08.14 | 전환권행사 | 보통주 | 29,413 | 500 | 16,999 | - |
| 2018.08.14 | 전환권행사 | 보통주 | 41,544 | 500 | 14,442 | - |
| 2018.08.29 | 전환권행사 | 보통주 | 29,413 | 500 | 16,999 | - |
| 2018.09.03 | 주식매수선택권행사 | 보통주 | 335,000 | 500 | 8,202 | - |
| 2018.09.03 | 전환권행사 | 보통주 | 110,786 | 500 | 14,442 | - |
| 2018.09.14 | 전환권행사 | 보통주 | 29,413 | 500 | 16,999 | - |
| 2018.09.14 | 전환권행사 | 보통주 | 69,242 | 500 | 14,442 | - |
| 2018.09.20 | 주식매수선택권행사 | 보통주 | 160,000 | 500 | 8,202 | - |
| 2018.10.02 | 유상증자(제3자배정) | 상환전환우선주 | 189,448 | 500 | 100,289 | - |
| 2018.10.11 | 전환권행사 | 보통주 | 48,469 | 500 | 14,442 | - |
| 2018.12.11 | 전환권행사 | 보통주 | 69,242 | 500 | 14,442 | - |
| 2019.02.26 | 전환권행사 | 보통주 | 63,690 | 500 | 40,817 | - |
| 2019.09.30 | 전환권행사 | 보통주 | 3,012 | 500 | 33,195 | - |
| 2019.10.15 | 전환권행사 | 보통주 | 32,035 | 500 | 74,914 | - |
| 2019.10.15 | 신주인수권행사 | 보통주 | 301,676 | 500 | 74,914 | - |
| 2019.10.18 | 전환권행사 | 상환전환우선주 | 119,654 | 500 | 100,289 | 감소 |
| 2019.10.18 | 전환권행사 | 보통주 | 170,937 | 500 | 70,203 | - |
| 2019.10.22 | 전환권행사 | 상환전환우선주 | 34,897 | 500 | 100,289 | 감소 |
| 2019.10.22 | 전환권행사 | 보통주 | 49,853 | 500 | 70,203 | - |
| 2019.10.24 | 전환권행사 | 상환전환우선주 | 13,960 | 500 | 100,289 | 감소 |
| 2019.10.24 | 전환권행사 | 보통주 | 19,943 | 500 | 70,203 | - |
| 2019.10.25 | 전환권행사 | 상환전환우선주 | 14,955 | 500 | 100,289 | 감소 |
| 2019.10.25 | 전환권행사 | 보통주 | 21,364 | 500 | 70,203 | - |
| 2019.10.28 | 전환권행사 | 상환전환우선주 | 5,982 | 500 | 100,289 | 감소 |
| 2019.10.28 | 전환권행사 | 보통주 | 8,545 | 500 | 70,203 | - |
| 2019.11.01 | 신주인수권행사 | 보통주 | 165,517 | 500 | 74,914 | - |
| 2019.11.01 | 전환권행사 | 보통주 | 40,044 | 500 | 74,914 | - |
| 2019.11.12 | 유상증자(제3자배정) | 보통주 | 2,609,387 | 500 | 72,012 | - |
| 2019.11.15 | 신주인수권행사 | 보통주 | 60,067 | 500 | 74,914 | - |
| 2019.11.15 | 전환권행사 | 보통주 | 21,356 | 500 | 74,914 | - |
| 2020.01.31 | 전환권행사 | 보통주 | 314,393 | 500 | 57,253 | - |
| 2020.02.03 | 전환권행사 | 보통주 | 33,533 | 500 | 57,253 | - |
| 2020.02.04 | 전환권행사 | 보통주 | 1,397 | 500 | 57,253 | - |
| 2020.03.13 | 전환권행사 | 보통주 | 138,484 | 500 | 14,072 | - |
| 2020.03.13 | 전환권행사 | 보통주 | 9,037 | 500 | 33,195 | - |
| 2020.06.05 | 유상증자(주주우선공모) | 보통주 | 4,309,157 | 500 | 78,700 | - |
| 2020.06.08 | 무상증자 | 보통주 | 4,744,806 | 500 | - | - |
| 2020.06.08 | 무상증자 | 우선주 | 324 | 500 | - | - |
| 2020.06.15 | 전환권행사 | 보통주 | 41,303 | 500 | 52,052 | - |
| 2020.06.16 | 전환권행사 | 보통주 | 100,859 | 500 | 52,052 | - |
| 2020.06.17 | 전환권행사 | 보통주 | 196,918 | 500 | 52,052 | - |
| 2020.06.26 | 전환권행사 | 보통주 | 17,290 | 500 | 52,052 | - |
| 2020.07.10 | 전환권행사 | 보통주 | 8,645 | 500 | 52,052 | - |
| 2020.12.08 | 유상증자(제3자배정) | 보통주 | 295,950 | 500 | 98,007 | - |
| 2020.12.09 | 전환권행사 | 보통주 | 19,211 | 500 | 52,052 | - |
| 2020.12.21 | 전환권행사 | 보통주 | 3,789 | 500 | 79,171 | - |
| 2020.12.23 | 전환권행사 | 보통주 | 442 | 500 | 79,171 | - |
| 2020.12.29 | 전환권행사 | 보통주 | 5,304 | 500 | 79,171 | - |
| 2021.01.04 | 전환권행사 | 보통주 | 4,420 | 500 | 79,171 | - |
| 2021.01.05 | 전환권행사 | 보통주 | 13,262 | 500 | 79,171 | - |
| 2021.01.06 | 전환권행사 | 보통주 | 9,725 | 500 | 79,171 | - |
| 2021.01.07 | 전환권행사 | 보통주 | 3,094 | 500 | 79,171 | - |
| 2021.01.08 | 전환권행사 | 보통주 | 3,094 | 500 | 79,171 | - |
| 2021.01.15 | 전환권행사 | 보통주 | 61,891 | 500 | 79,171 | - |
| 2021.01.21 | 전환권행사 | 보통주 | 442 | 500 | 79,171 | - |
| 2021.01.25 | 전환권행사 | 보통주 | 27,408 | 500 | 79,171 | - |
| 2021.03.16 | 무상증자 | 보통주 | 52,968,898 | 500 | - | - |
| 2021.03.16 | 무상증자 | 우선주 | 3,531 | 500 | - | - |
| 2021.06.21 | 전환권행사 | 보통주 | 5,924 | 500 | 33,757 | - |
| 2021.08.13 | 전환권행사 | 보통주 | 51,839 | 500 | 33,757 | - |
| 2021.08.18 | 전환권행사 | 보통주 | 105,163 | 500 | 33,757 | - |
| 2021.08.19 | 전환권행사 | 보통주 | 740 | 500 | 33,757 | - |
| 2021.08.23 | 전환권행사 | 보통주 | 79,982 | 500 | 33,757 | - |
| 2021.08.25 | 전환권행사 | 보통주 | 10,368 | 500 | 33,757 | - |
| 2021.08.26 | 전환권행사 | 보통주 | 13,329 | 500 | 33,757 | - |
| 2021.08.27 | 전환권행사 | 보통주 | 247,351 | 500 | 33,757 | - |
| 2021.08.30 | 전환권행사 | 보통주 | 8,887 | 500 | 33,757 | - |
| 2021.09.02 | 전환권행사 | 보통주 | 14,811 | 500 | 33,757 | - |
| 2022.05.16 | 전환권행사 | 보통주 | 41,472 | 500 | 33,757 | - |
| 2022.05.17 | 전환권행사 | 보통주 | 20,736 | 500 | 33,757 | - |
| 2022.05.19 | 전환권행사 | 보통주 | 10,368 | 500 | 33,757 | - |
| 2022.05.25 | 전환권행사 | 보통주 | 155,523 | 500 | 33,757 | - |
| 2022.05.26 | 전환권행사 | 보통주 | 41,472 | 500 | 33,757 | - |
| 2022.06.15 | 전환권행사 | 보통주 | 3,110 | 500 | 33,757 | - |
| 2022.08.11 | 전환권행사 | 보통주 | 20,736 | 500 | 33,757 | - |
미상환 전환사채 발행현황
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 원, 주) |
| 종류\구분 | 회차 | 발행일 | 만기일 | 권면(전자등록)총액 | 전환대상 주식의 종류 |
전환청구가능기간 | 전환조건 | 미상환사채 | 비고 | ||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 전환비율 (%) |
전환가액 | 권면(전자등록)총액 | 전환가능주식수 | ||||||||
| 제33회 무보증 사모 전환사채 |
33 | 2019년 12월 18일 | 2022년 12월 18일 | 40,000,000,000 | 기명식 보통주 |
2020.12.18~ 2022.11.18 |
100 | 33,757 | 1,400,000,000 | 41,472 | - |
| 제36회 무보증 사모 전환사채 |
36 | 2022년 06월 02일 | 2025년 06월 02일 | 23,000,000,000 | 기명식 보통주 |
2023.06.02~ 2025.05.02 |
100 | 48,605 | 23,000,000,000 | 473,202 | - |
| 합 계 | - | - | - | 63,000,000,000 | - | - | - | - | 24,400,000,000 | 514,674 | - |
미상환 신주인수권부사채 등 발행현황
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 원, 주) |
| 종류\구분 | 회차 | 발행일 | 만기일 | 권면(전자등록)총액 | 행사대상 주식의 종류 |
신주인수권 행사가능기간 | 행사조건 | 미상환 사채 |
미행사 신주 인수권 |
비고 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 행사비율 (%) |
행사가액 | 권면(전자등록)총액 | 행사가능주식수 | ||||||||
| 제34회 무보증 사모 비분리형 신주인수권부사채 |
34 | 2021년 10월 20일 | 2026년 10월 20일 | 57,000,000,000 | 기명식 보통주 |
2022. 10. 20~ 2026. 09.20 |
100 | 35,884 | 57,000,000,000 | 1,588,451 | - |
| 제35회 무보증 사모 비분리형 신주인수권부사채 |
35 | 2022년 03월 30일 | 2025년 03월 30일 | 25,200,000,000 | 기명식 보통주 |
2023. 03. 30~ 2025. 02.28 |
100 | 30,811 | 25,200,000,000 | 817,888 | - |
| 제37회 무보증 사모 비분리형 신주인수권부사채 |
37 | 2022년 06월 02일 | 2025년 06월 02일 | 17,000,000,000 | 기명식 보통주 |
2023.06.02~ 2025.05.02 |
100 | 48,605 | 17,000,000,000 | 349,758 | - |
| 합 계 | - | - | - | 99,200,000,000 | - | - | - | - | 99,200,000,000 | 2,756,097 | - |
| [채무증권의 발행 등과 관련된 사항] |
채무증권 발행실적
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 백만원, %) |
| 발행회사 | 증권종류 | 발행방법 | 발행일자 | 권면(전자등록)총액 | 이자율 | 평가등급 (평가기관) |
만기일 | 상환 여부 |
주관회사 |
|---|---|---|---|---|---|---|---|---|---|
| 에이치엘비㈜ | 회사채 | 사모 | 2018.02.05 | 5,000 | 표면: 0% 만기: 1% |
- | 2021.02.05 | 전액상환 | - |
| 에이치엘비㈜ | 회사채 | 사모 | 2018.02.20 | 3,000 | 표면: 0% 만기: 1% |
- | 2021.02.20 | 전액상환 | - |
| 에이치엘비㈜ | 회사채 | 사모 | 2018.06.29 | 7,000 | 표면: 0% 만기: 1% |
- | 2021.06.29 | 전액상환 | - |
| 에이치엘비㈜ | 회사채 | 사모 | 2018.06.29 | 39,500 | 표면: 0% 만기: 1% |
- | 2023.06.29 | 전액상환 | - |
| 에이치엘비㈜ | 회사채 | 사모 | 2019.01.30 | 20,000 | 표면: 0% 만기: 1% |
- | 2024.01.30 | 전액상환 | - |
| 에이치엘비㈜ | 회사채 | 사모 | 2019.06.14 | 20,000 | 표면: 0% 만기: 1% |
- | 2024.06.14 | 전액상환 | - |
| 에이치엘비㈜ | 회사채 | 사모 | 2019.12.18 | 40,000 | 표면: 0% 만기: 1% |
- | 2024.12.18 | 일부상환 | - |
| 에이치엘비㈜ | 회사채 | 사모 | 2021.10.20 | 57,000 | 표면: 0% 만기: 1% |
- | 2026.10.20 | 미상환 | - |
| 에이치엘비㈜ | 회사채 | 사모 | 2022.03.30 | 25,200 | 표면: 0% 만기: 2% |
- | 2025.03.30 | 미상환 | - |
| 에이치엘비㈜ | 회사채 | 사모 | 2022.06.02 | 23,000 | 표면: 1% 만기: 3% |
- | 2025.06.02 | 미상환 | - |
| 에이치엘비㈜ | 회사채 | 사모 | 2022.06.02 | 17,000 | 표면: 1% 만기: 3% |
- | 2025.06.02 | 미상환 | - |
| 합 계 | - | - | - | 256,700 | - | - | - | - | - |
기업어음증권 미상환 잔액
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
1년초과 2년이하 |
2년초과 3년이하 |
3년 초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | |
단기사채 미상환 잔액
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
합 계 | 발행 한도 | 잔여 한도 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
회사채 미상환 잔액
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
신종자본증권 미상환 잔액
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 5년이하 |
5년초과 10년이하 |
10년초과 15년이하 |
15년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
조건부자본증권 미상환 잔액
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | - | |
7-2. 증권의 발행을 통해 조달된 자금의 사용실적
가. 공모자금의 사용내역
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 증권신고서 등의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
| 유상증자 | - | 2020년 06월 05일 | 영업양수자금 | 61,395 | 영업양수자금 (물질특허 권리확보) |
48,185 | (*1) |
| - | - | - | - | - | 타법인증권취득자금 | 13,210 | (*1) |
| 유상증자 | - | 2020년 06월 05일 | 운영자금 | 4,000 | 운영자금 | 4,000 | - |
| 유상증자 | - | 2020년 06월 05일 | 채무상환자금 | 67,000 | 채무상환자금 | 67,000 | - |
| 유상증자 | - | 2020년 06월 05일 | 타법인증권취득자금 | 206,737 | 타법인증권취득자금 | 110,230 | (*2) |
| - | - | - | - | - | 타법인증권취득자금 | 15,659 | (*3) |
| - | - | - | - | - | 타법인증권취득자금 | 44,920 | (*4) |
| - | - | - | - | - | 타법인증권취득자금 | 5,000 | (*5) |
|
(*1) 영업양수자금의 경우, 2020년 4월 유상증자 투자설명서에서의 예상계약금액(5,000만불)과 실제 계약체결시 계약금액 |
나. 사모자금의 사용내역
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 주요사항보고서의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
| 제27회차 무보증 사모EB | 27 | 2018.02.05 | 운영자금 | 5,000 | 운영자금 | 5,000 | - |
| 제28회차 무보증 사모CB | 28 | 2018.02.20 | 지분취득 | 3,000 | 지분취득 | 3,000 | - |
| 제29회차 무보증 사모CB | 29 | 2018.06.29 | 지분취득 운영자금 |
7,000 | 지분취득 운영자금 |
7,000 | - |
| 제30회차 무보증 사모 비분리형 BW |
30 | 2018.06.29 | 지분취득 운영자금 |
39,500 | 지분취득 운영자금 |
39,500 | - |
|
제3자배정 유상증자 (상환전환우선주) |
1 | 2018.10.02 |
지분취득 운영자금 |
18,999 |
지분취득 운영자금 |
18,999 | - |
| 제31회차 무보증 사모CB | 31 | 2019.01.30 | 지분취득 운영자금 |
20,000 | 지분취득 운영자금 |
20,000 | - |
| 제32회차 무보증 사모CB | 32 | 2019.06.14 | 지분취득 운영자금 |
20,000 | 지분취득 운영자금 |
20,000 | - |
| 제33회차 무보증 사모CB | 33 | 2019.12.18 | 지분취득 운영자금 |
40,000 | 지분취득 운영자금 |
40,000 | - |
| 제34회차 무보증 사모 비분리형 BW |
34 | 2021.10.20 | 지분취득 | 57,000 | 지분취득 | 57,000 | - |
| 제35회차 무보증 사모 비분리형 BW |
35 | 2022.03.30 | 지분취득 | 25,200 | 지분취득 | 25,200 | - |
| 제36회차 무보증 사모CB | 36 | 2022.06.02 | 운영자금 | 23,000 | 운영자금 | 1,700 | 미집행 |
| 제37회차 무보증 사모 비분리형 BW |
37 | 2022.06.02 | 운영자금 | 17,000 | 운영자금 | 17,000 | - |
다. 미사용자금의 운용내역
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 백만원) |
| 종류 | 금융상품명 | 운용금액 | 계약기간 | 실투자기간 |
|---|---|---|---|---|
| 기타 | 하이투자증권 | 30,000 | - | - |
| 예ㆍ적금 | - | 928 | - | - |
| 계 | 30,928 | - | ||
8. 기타 재무에 관한 사항
가. 재무제표 재작성 등의 유의사항
(1) 합병에 관한 사항
본 보고서 항목 중 "XI. 그 밖에 투자자 보호를 위하여 필요한 사항 => 4. 작성기준일이후 발생한 주요사항 등 기타사항 => 다. 합병 등의 사후정보"를 참조하시기 바랍니다.
(2) 연결대상범위의 변동
- 당반기 중 연결대상범위의 변동 내역은 다음과 같습니다.
| 구 분 | 자회사 | 사 유 |
| 신규연결 | Hyundai Lifeboats Shanghai Co.,Ltd | 당반기 중 지분 취득 |
| 연결제외 | ㈜에프에이 | 당반기 중 흡수합병 후 소멸 |
| 연결제외 | ㈜화진메디칼 | 당반기 중 지분 100% 양도 |
| 연결제외 | ㈜화진메디스 | 당반기 중 지분 100% 양도 |
(3) 기타 재무제표 이용에 유의하여야 할 사항
핵심감사사항
영업권의 손상평가
연결재무제표에 대한 주석 14에서 설명하고 있는 바와 같이 당기말 현재 연결실체가보유한 영업권의 장부금액은 62,346백만원입니다. 경영진은 사업결합으로 취득한 영업권에 대해서 자산손상징후을 시사하는 징후와 관계없이 매년 회수가능액과 장부금액을 비교하여 손상평가를 수행하고 있습니다.
당반기말 현재 손상평가에 사용된 회수가능액은 사용가치이며, 회수가능액은 매출액, 영업비용, 성장률과 할인율의 예상치에 근거하여 산출됩니다. 연결실체가 사용가치를 산출하는데 있어서 경영진의 유의적인 판단이 포함되고, 연결재무제표에 미치는 잠재적 영향을 고려하여 외부감사인은 영업권의 손상평가를 핵심감사사항으로 식별하였습니다.
나. 대손충당금 설정현황
(1) 최근 3사업연도의 계정과목별 대손충당금 설정내용
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 백만원) |
| 구 분 | 계정과목 | 채권금액 | 대손충당금 | 대손충당금 설정률(%) |
| 제38기 당반기 | 매출채권 | 29,056 | (1,061) | 3.65 |
| 미수금 | 10,774 | (408) | 3.79 | |
| 단기대여금 | 5,329 | (5,329) | 100.00 | |
| 기타(*) | 36,377 | (30,095) | 82.73 | |
| 합계 | 81,535 | (36,893) | 45.25 | |
| 제37기 | 매출채권 | 35,023 | (988) | 2.82 |
| 미수금 | 3,080 | (410) | 13.31 | |
| 단기대여금 | 5,435 | (5,329) | 98.05 | |
| 기타(*) | 39,630 | (30,149) | 76.08 | |
| 합계 | 83,167 | (36,876) | 44.34 | |
| 제36기 | 매출채권 | 13,553 | (1,806) | 13.33 |
| 미수금 | 3,379 | (879) | 26.00 | |
| 단기대여금 | 11,642 | (11,640) | 99.98 | |
| 기타(*) | 39,657 | (32,234) | 81.28 | |
| 합계 | 68,232 | (46,560) | 68.24 |
(*) 하이투자증권㈜의 사기적 부정거래 행위 및 불완전판매로 인하여 부당이득금 반환 청구 소송중인 예치금 30,000백만원이 포함되어 있습니다. 당사의 대표이사는 본 사건과 관련하여 발생가능한 손실을 보전하기 위하여 대표이사가 보유한 당사의 주식을 법무법인에 위탁하는 계약을 체결하였습니다.
(2) 최근 3사업연도의 대손충당금 변동현황
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 백만원) |
| 구 분 | 제38기 당반기 | 제37기 | 제36기 |
| 기초금액 | 36,876 | 46,560 | 16,744 |
| 대손상각비(환입) | 23 | 683 | (0) |
| 기타의대손상각비(환입) | (1) | (1,197) | 30,000 |
| 제 각(*) | - | (9,264) | - |
| 종속기업의 변동으로 인한 증감 | (4) | 94 | (184) |
| 기말금액 | 36,893 | 36,876 | 46,560 |
(*) 폐업 등으로 회수가 불가능한 채권을 장부에서 제각하였습니다.
(3) 매출채권관련 대손충당금 설정방침
연결실체는 재무상태표일 현재 매출채권의 연령분석과 과거의 대손경험율을 토대로 대손충당금 설정비율을 다음과 같은 기준으로 설정하고 있습니다.
재무상태표일 현재 매출채권 잔액중 재무상태표일 이후에 회수된 금액 및 담보권이 설정되어 있는 채권은 설정대상에서 제외하고, 개별분석 및 과거의 대손경험율을 토대로 하여 대손충당금으로 설정하고 있습니다.
(4) 당반기말 현재 경과기간별 매출채권잔액 현황
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 백만원) |
| 구 분 | 3개월 이하 | 3-6개월 | 6-9개월 | 9~12개월 | 12개월이상 | 계 |
| 기대손실율(%) | 0.02% | 11.33% | 7.04% | 69.93% | 41.23% | |
| 채권잔액 | 64,539 | 715 | 96 | 12 | 16,450 | 81,813 |
| 손상된 금액 | (15) | (81) | (7) | (9) | (6,782) | (6,893) |
| 장부금액 | 64,525 | 634 | 89 | 4 | 9,668 | 74,920 |
| 구성비율(%) | 86.12% | 0.85% | 0.12% | 0.00% | 12.91% | 100% |
다. 재고자산 현황 등
(1) 최근 3사업연도의 재고자산의 사업부문별 보유현황
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 백만원) |
| 사업부문 | 계정과목 | 제38기 당반기 | 제37기 | 제36기 | 비고 |
| HLB ENG 사업부문 | 상품 | - | - | - | - |
| 제품 | - | - | - | - | |
| 원 재 료 | 1,277 | 1,367 | 1,321 | - | |
| 재 공 품 | 2,695 | 1,617 | 2,766 | - | |
| 소 계 | 3,972 | 2,984 | 4,086 | - | |
| 바이오 의료기기 사업부문 | 상 품 | 160 | 252 | 39 | - |
| 제 품 | 8,156 | 6,495 | 361 | - | |
| 원 재 료 | 2,264 | 2,225 | 387 | - | |
| 재 공 품 | 2,823 |
1,832 | - | - | |
| 소 계 | 13,404 |
10,804 | 788 | - | |
| 합 계 | 상 품 | 160 | 252 | 39 | - |
| 제 품 | 8,156 | 6,495 | 361 | - | |
| 원 재 료 | 3,541 | 3,592 | 1,708 | - | |
| 재 공 품 | 5,518 | 3,449 | 2,766 | - | |
| 소 계 | 17,376 | 13,788 | 4,874 | - | |
| 총자산대비 재고자산 구성비율(%) [재고자산합계÷기말자산총계×100] |
2.1 | 1.9 | 0.7 | - | |
| 재고자산회전율(회수) [연환산 매출원가÷{(기초재고+기말재고)÷2}] |
9.4 | 10.5 | 9.4 | - |
|
(2) 장기체화재고 등의 현황
- 해당사항 없습니다.
(3) 기타사항
- 연결실체의 금융기관 차입금에 대한 재고자산 담보제공 내역은 없습니다.
라. 공정가치평가 내역
- 공정가치 측정시 사용된 가정의 자세한 정보는 II. 사업의 내용 => "5.위험관리 및 파생거래"를 참조하시기 바랍니다.
마. 진행률적용 수주계약 현황
- 해당사항 없습니다
IV. 회계감사인의 감사의견 등
1. 외부감사에 관한 사항
가. 회계감사인의 명칭 및 연결감사의견(검토)의견
| 사업연도 | 감사인 | 감사의견 | 강조사항 등 | 핵심감사사항 |
|---|---|---|---|---|
| 제38기(당반기) | 삼덕회계법인 | 해당사항없음 | - | - |
| 제37기(전기) | 삼덕회계법인 | 적정 | 해당사항 없음 | 영업권의 손상평가 |
| 제36기(전전기) | 삼덕회계법인 | 적정 | 금융감독원의 불공정거래 조사 | 영업권의 손상평가 |
나. 회계감사인의 명칭 및 별도감사의견(검토)의견
| 사업연도 | 감사인 | 감사의견 | 강조사항 등 | 핵심감사사항 |
|---|---|---|---|---|
| 제38기(당반기) | 삼덕회계법인 | 해당사항없음 | - | - |
| 제37기(전기) | 삼덕회계법인 | 적정 | 해당사항 없음 | 영업권의 손상평가 |
| 제36기(전전기) | 삼덕회계법인 | 적정 | 금융감독원의 불공정거래 조사 | 영업권의 손상평가 |
다. 감사용역 체결현황
| 사업연도 | 감사인 | 내 용 | 감사계약내역 | 실제수행내역 | ||
|---|---|---|---|---|---|---|
| 보수 | 시간 | 보수 | 시간 | |||
| 38기(당반기) | 삼덕회계법인 | 1분기검토(2022.04.26~2022.05.10) 반기감사(2022.07.28 ~ 2022.08.04) |
460백만원 | 3,510 | 96백만원 | 960 |
| 제37기(전기) | 삼덕회계법인 | 1분기검토(2021.04.26~2021.05.07) 반기검토(2021.07.26~2021.08.06) 3분기검토(2021.10.25~2021.11.04) 내부회계감사(2021.11.15~2021.11.26) 별도감사(2022.01.24~2022.03.15) 연결감사(2022.01.24~2022.03.15) |
350백만원 | 2,600 | 369백만원 | 3,258 |
| 제36기(전전기) | 삼덕회계법인 | 반기검토(2020.07.29~2020.08.14) 중간감사(2020.11.30~2020.12.11) 별도감사(2021.02.01~2021.03.17) 연결감사(2021.02.01~2021.03.17) |
240백만원 | 1,800 | 300백만원 | 2,211 |
라. 회계감사인과의 비감사용역 계약체결 현황
| 사업연도 | 계약체결일 | 용역내용 | 용역수행기간 | 용역보수 | 비고 |
|---|---|---|---|---|---|
| 제38기(당반기) | 2022.07.25 | 2022년 법인세신고를 위한 세무조정업무 | 2022.03.05~2023.03.31 | 15백만원 | - |
| 제37기(전기) | - | - | - | - | - |
| 제36기(전전기) | - | - | - | - | - |
마. 내부감사기구가 회계감사인과 논의한 결과
| 구분 | 일자 | 참석자 | 방식 | 주요 논의 내용 |
|---|---|---|---|---|
| 1 | - | - | - | - |
바. 조정협의회 주요 협의내용
- 해당사항 없음
사. 전ㆍ당기 재무제표 불일치에 대한 세부정보
- 해당사항 없음
2. 내부통제에 관한 사항
가. 내부통제
회사의 감사는 회사의 내부통제의 유효성에 대하여 감사하며, 당사의 내부감시장치는 효과적으로 가동되고 있습니다.
나. 내부회계관리제도
당사는 신뢰할 수 있는 회계정보의 작성 및 공시를 위하여 내부회계관리제도를 운영하고 있습니다. 대표이사는 내부회계관리제도의 관리 및 운영을 책임지고 내부회계 관리제도의 효율적인 관리 및 운영을 위하여 내부회계관리자를 지정하도록 하고 있으며, 내부회계관리자는 내부회계관리제도의 운영을 총괄하고, 회계정보의 작성 및 공시, 회계정보의 전산처리 등에 관한 사항을 통제하며 이를 확인, 감독하고 있습니다. 또한, 내부회계관리자는 내부회계관리제도의 정비와 운영을 총괄하고, 연 1회의 이사회 및 감사위원회에 이 규정에 따른 운영실태에 관한 보고와 당사 조직관리 부서의 협조를 거친 후, 회계정보의 작성 및 공시를 담당하는 부서에 대한 적절하고 효율적인 업무분장을 수행하고 있습니다.
다. 내부회계관리제도의 문제점 또는 개선방안 등
- 해당사항 없습니다.
라. 회계감사인의 내부회계관리제도에 대한 감사 또는 검토의견
| 사업연도 | 회계감사인 | 감사 또는 검토의견 |
| 제37기(전기) | 삼덕회계법인 | 우리는 2021년 12월 31일 현재 내부회계관리제도 설계 및 운영 개념체계에 근거한 에이치엘비 주식회사(이하 "회사")의 내부회계관리제도를 감사하였습니다. 우리의 의견으로는 회사의 내부회계관리제도는 2021년 12월 31일현재 내부회계관리제도 설계 및 운영 개념체계에 따라 중요성의 관점에서 효과적으로 설계 및 운영되고 있습니다. |
| 제36기(전전기) | 삼덕회계법인 | 경영자의 내부회계관리제도 운영실태보고서에 대한 우리의 검토결과, 상기 경영자의운영실태보고 내용이 중요성의 관점에서 내부회계관리제도 모범규준 제5장 '중소기업에 대한 적용'의 규정에 따라 작성되지 않았다고 판단하게 하는 점이 발견되지 아니하였습니다. |
마. 회계감사인과 논의한 결과
- 해당사항 없습니다.
V. 이사회 등 회사의 기관에 관한 사항
1. 이사회에 관한 사항
가. 이사회 구성 개요
(1) 이사회 구성 개요
보고서 제출일 현재 당사의 이사회는 총 10명으로, 사내이사 7명과 사외이사 3명으로구성되어 있습니다. 각 이사의 주요 이력 및 담당업무는 "VIII. 임원 및 직원 등에 관한사항"을 참조하시기 바랍니다.
(2) 이사회 의장에 관한 사항
이사회 의장은 당사 정관 제40조 1에 의거, 진양곤 대표이사가 겸직하고 있습니다. 이사회 의장은 이사회의 소집과 안건의 주재를 담당한다는 점에서 이사회 안건, 운영등에 대하여 이해도가 높은 이사가 의장으로 적합하다고 볼 수 있습니다. 이에 따라, 당사의 대표이사로서 이사회에 부의되는 각종 현안을 가장 잘 파악하고 있는 진양곤 대표이사가 이사회 의장 직무를 수행하기에 가장 적합하다고 판단되어 이사들의 의결을 거쳐 이사회 의장으로 선임하였습니다.
나. 이사회의 중요의결사항 등
| 회차 | 개최일자 | 의안내용 | 가결 여부 |
이사 등의 성명 | |||||||||||
| 진양곤 (출석률: 100%) |
김동건 (출석률: 100%)(*1) |
전복환 (출석률: 100%)(*2) |
도순기 (출석률: 100%) |
황제이정환 (출석률: 100%)(*3) |
안기홍 (출석률: 100%)(*2) |
문정환 (출석률: 100%) |
Matthew Chang (출석률: 100%) |
William G. Hearl (출석률: 0%)(*4) |
박진국 (출석률: 100%) |
최규준 (출석률: 86%) |
심재철 (출석률: 80%) |
||||
| 찬 반 여 부 | |||||||||||||||
| 1 | 2022-01-03 | 의안1 합병종료 보고 및 공고의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 불참 | 불참 |
| 의안2 지점 설치의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 불참 | 불참 | ||
| 의안3 이사회 운영규정 개정의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 불참 | 불참 | ||
| 2 | 2022-01-12 | 의안1 ESG위원회 규정 제정의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 불참 |
| 의안2 지점 설치의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 불참 | ||
| 3 | 2022-01-27 | 타법인 주식 취득 내용에 관한 변경의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 4 | 2022-02-10 | 타법인 주식 취득의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 5 | 2022-02-23 | 의안1 재무제표(2021년) 확정의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 의안2 정기주주총회 소집에 관한 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 6 | 2022-03-14 | 의안1 주식매수선택권 부여의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 의안2 제37기 정기주주총회 안건 추가의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 의안3 내부회계관리제도 운영실태 보고의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 의안4 내부회계관리제도 운영평가 보고의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 의안5 자회사 차입에 대한 연대보증의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 의안6 부패방지 경영방침 보고의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 의안7 10대 인권정책 보고의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 의안8 기업지배구조 헌장 승인의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 7 | 2022-03-22 | 제37기 재무제표(2021년) 정정 확정의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 8 | 2022-03-29 | 제35회차 무기명식 무보증 사모 비분리형 신주인수권부사채 발행의 건 |
가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 9 | 2022-03-29 | 기업설명회(IR)개최 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 10 | 2022-03-29 | 제37기 정기주주총회 일부안건 철회의 건 | 가결 | 참석(찬성) | 참석(찬성) | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 11 | 2022-03-30 | 정기주주총회 의사록 | 가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | - | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 12 | 2022-04-13 | 자회사 자금보충약정 체결의 건 | 가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 13 | 2022-04-27 | 의안1 타법인 주식취득의 건 | 가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 의안2 관계사 금전대여의 건 | 가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 의안3 타법인 주식 양도의 건 | 가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 의안4 관계사 선금급 지급보증 연대보증의 건 | 가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 의안5 관계사 선금급 지급보증 연대보증 내용변경의 건 |
가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 14 | 2022-05-27 | 기업설명회(IR)개최의 건 | 가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 15 | 2022-05-31 | 의안1 제36회차 무기명식 무보증 사모 전환사채 발행의 건 |
가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 의안2 제37회차 무기명식 무보증 사모 비분리형 신주인수권부사채 발행의 건 |
가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 의안3 타법인 주권관련 사채권 취득의 건 | 가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) | ||
| 16 | 2022-06-10 | 기업설명회(IR)개최의 건 | 가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 참석(찬성) | 참석(찬성) |
| 17 | 2022-08-12 | 의안1 주주배정후 실권주 일반공모 유상증자 결의의 건 |
가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 불참 | 불참 |
| 의안2 타법인 주권관련 사채권 처분의 건 | 가결 | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | - | 참석(찬성) | 참석(찬성) | 불참 | 참석(찬성) | 불참 | 불참 | ||
| (*1) 2021년 3월 30일 제36기 정기주주총회에서 사내이사 김동건을 신규선임 하였습니다. (*2) 사내이사 전복환, 안기홍은 2022년 3월 29일 일신상의 사유로 사임하였습니다. (*3) 2022년 3월 30일 제37기 정기주주총회에서 사내이사 황제이정환을 신규선임 하였습니다. (*4) 사내이사 William G. Hearl은 해외(미국) 근무로 인한 시차문제로 인해 이사회 회의 참석이 불가능하여, 관련 의안내용은 e-mail로 통보하고 있습니다. |
다. 이사회의 운영에 관한 사항
(1) 이사회 운영규정의 주요내용
이사회에 관한 사항은 당사 정관 제2절(이사회) 규정에 따르고 있습니다.
| 제4조 [구 성] 1. 이사회는 주주총회에서 선임된 이사 전원으로 구성한다. 2. 감사는 이사회에 출석하여 의견을 진술할 수 있다. 3. 이사회의 업무처리를 위하여 1명의 간사를 둘 수 있다. 제5조 [의 장] 이사회의 의장은 이사회의 결의를 거쳐 이사 중에서 이사회가 선임하며, 대표이사의 유고시에는 회사의 정관에서 정한 순서로써 그 직무를 대행한다. 제7조 [소 집] 1. 이사회는 이사회의 의장이 소집하며 의장은 회일을 정하여 천재지변 등 불가피한 사유가 발생하는 경우를 제외하고는 늦어도 24시간 전에 각 이사 및 감사에게 문서, 전자문서 또는 구두로써 통지하여야 한다. 다만, 이사 및 감사 전원의 동의가 있을 때에는 소집절차를 생략할 수 있다. 2. 각 이사는 업무수행상 필요하다고 인정되는 경우 의장의 동의를 얻어 이사회를 소집할 수 있다. 소집권자인 이사가 정당한 이유없이 이사회 소집을 거절하는 경 우에는 각 이사가 이사회를 소집할 수 있다. 3. 이사회의 의장은 제1항 및 제2항의 규정에 의한 이사회의 소집권자로 한다. 제9조 [이사회의 결의방법] 1. 이사회의 결의는 관련법령 또는 이사회가 별도로 결의요건을 강화하는 경우를 제외 하고는 재적이사 과반수의 출석과 출석이사의 과반수로 한다. 2. 이사회는 이사의 전부 또는 일부가 직접 회의에 출석하지 아니하고, 모든 이사가 음성을 동시에 송, 수신하는 통신수단에 의하여 결의에 참가하는 것을 허용할 수 있다. 이 경우 당해 이사는 이사회에 직접 출석한 것으로 본다. 3. 이사회의 결의에 관하여 특별한 이해관계가 있는 자는 의결권을 행사하지 못한다. 이 경우 의결권을 행사할 수 없는 이사의 수는 출석한 이사의 수에 산입하지 아니한다. 제12조 [이사회의 의사록] 1. 이사회의 의사에 관하여는 의사록을 작성하여야 한다. 2. 의사록에는 의사의 안건, 경과요령, 그 결과 반대하는 자와 그 반대이유를 기재하고 출석한 이사 및 감사가 기명날인 또는 서명하여야 한다. |
라. 이사의 독립성
(1) 이사 선임은 상법 등 관련 법령상의 절차를 준수하여 선출되고 있으며, 이사 선출의 독립성에 관한 별도의 기준은 없습니다. 사외이사 선임은 관련법에서 정한 사외이사 자격기준을 충족한 후보자 중에서 이사회의 추천으로 주주총회에서 선임하고 있습니다.
(2) 각 이사에 대한 선임배경 등
| (기준일 : | 2022년 06월 30일 | ) |
| 직 위 (상근여부) |
성 명 | 추천인 | 선임배경 | 연임여부 (횟수) |
담당업무 | 회사와의 거래 | 최대주주와의 관계 |
| 회장/사내이사 (상근) |
진양곤 | 이사회 | 경영업무 총괄 및 대외적 업무의 안정적 수행 |
여(3) | 경영총괄 | 해당사항없음 | 최대주주 본인 |
| 사내이사 (상근) |
김동건 | 이사회 | 법무, 금융, 신사업 개발 등 오랜 경험을 보유 | 부 | 경영총괄 | 해당사항없음 | 계열회사 임원 |
| 사내이사 (상근) |
도순기 | 이사회 | 재직기간 성과 및 조직 전체에 대한 이해도가 높음 | 부 | HLB ENG 사업부총괄 |
해당사항없음 | 계열회사 임원 |
| 사내이사 (상근) |
황제이정환(*) | 이사회 | 해외 마케팅 전문가로서 다양한 경험 보유 | 부 | 마케팅총괄 | 해당사항없음 | 해당사항없음 |
| 사내이사 (비상근) |
문정환 | 이사회 | 홍보분야 전문가 및 인적네트워크 보유 | 부 | 홍보총괄 | 해당사항없음 | 계열회사 임원 |
| 사내이사 (상근) |
Matthew Chang |
이사회 | 글로벌 재무/금융 분야 전문지식 보유 및 경험 다수 | 부 | 경영전략/IR | 해당사항없음 | 해당사항없음 |
| 사내이사 (비상근) |
William G. Hearl |
이사회 | 면역치료 플랫폼 기술 보유 IT사 창업 및 대표이사, 생명공학 전문가 |
부 | 바이오 | 해당사항없음 | 계열회사 임원 |
| 사외이사 (비상근) |
박진국 | 이사회 | 회계, 금융분야 전문가 | 여(1) | 경영자문 | 해당사항없음 | 해당사항없음 |
| 사외이사 (비상근) |
최규준 | 이사회 | 자본시장, IR분야 전문가 | 여(1) | 경영자문 | 해당사항없음 | 해당사항없음 |
| 사외이사 (비상근) |
심재철 | 이사회 | 언론, 미디어 분야 전문가 | 부 | 경영자문 | 해당사항없음 | 해당사항없음 |
| (*) 2022년 3월 30일, 제37기 정기주주총회에서 사내이사 황제이정환을 신규선임 하였습니다. |
마. 사외이사의 전문성
(1) 사외이사 현황
| (기준일 : | 2022년 06월 30일 | ) |
| 성명 | 주 요 경 력 | 최대주주등과의 이해관계 |
회사와의 거래내역 |
비고 |
| 박진국 | 현. 에이치엘비㈜ 사외이사 현. 성도이현회계법인 고문 현. 제이씨현시스템㈜ 사외이사 |
해당사항 없음 |
- | 2020.03.30 재선임 |
| 최규준 | 현. 에이치엘비㈜ 사외이사 현. ㈜엔솔바이오사이언스 사외이사 전. 한국IR협의회 부회장 |
해당사항 없음 |
- | 2022.03.30 재선임 |
| 심재철 | 현. 에이치엘비㈜ 사외이사 현. 고려대학교 미디어학부 명예교수 전. 고려대학교 언론대학원장 |
해당사항 없음 |
- | 2020.03.30 신규선임 |
(2)사외이사 및 그 변동현황
| (단위 : 명) |
| 이사의 수 | 사외이사 수 | 사외이사 변동현황 | ||
|---|---|---|---|---|
| 선임 | 해임 | 중도퇴임 | ||
| 7 | 3 | - | - | - |
(3)사외이사 교육 미실시 내역
| 사외이사 교육 실시여부 | 사외이사 교육 미실시 사유 |
|---|---|
| 미실시 | 당사의 사외이사는 다양한 실무경험을 통해 전문지식과 역량을 갖추고 있음을 감안하여 별도의 교육은 미실시 하였습니다. |
(4) 사외이사 지원조직 현황
| 부서(팀)명 | 직원수(명) | 직위(근속연수) | 주요 활동내역 |
| 경영전략팀 | 6 | 상무 외 (평균 5년) | 이사회 간사 |
2. 감사제도에 관한 사항
가. 감사에 관한 사항
보고서 제출일 현재 별도의 감사위원회를 설치하고 있지 아니하며, 2020년 3월 30일정기주주총회에서 재선임된 김용웅 감사가 감사업무를 수행합니다.
감사는 이사의 직무집행에 관한 감사 및 영업에 관한 전반적 사항의 보고를 받고 있으며, 회사의 업무상태 및 재산상태를 조사할 수 있는 권한을 가지고 있습니다. 감사는 회사의 회계와 업무감사 및 이사회에 출석하여 의견을 진술할 수 있습니다.
나. 감사의 인적사항
| 성 명 | 재임기간 | 겸직현황(재임기간) | 계열회사 근무경력 | 주 요 경 력 | 비 고 |
| 김용웅 | 13년 | - 현대요트㈜ 비상근 감사 (5년) - 바다중공업㈜ 비상근 감사 (13년) - 에이치엘비셀㈜(*1) (구.라이프리버㈜) 비상근 감사 (5년) - 에이치엘비네트웍스㈜(5년) - ㈜화진메디칼 비상근 감사 (4년) - ㈜신화어드밴스 비상근 감사(*2) - ㈜프레시코 비상근 감사(*3) - ㈜코아바이오 비상근 감사(*4) - 에이치엘비생활건강㈜ 비상근 감사㈜(*5) |
해당사항 없음 | 신용관리기금 (現 금융감독원) |
- 2018.03.28 상근전환 - 2020.03.30 재선임 |
(*1) 2020년 4월 라이프리버㈜에서 에이치엘비셀㈜로 사명을 변경하였습니다.
(*2) 2022년 3월 ㈜신화어드밴스에 신규취임하였습니다.
(*3) 2022년 3월 ㈜프레시코에 신규취임하였습니다.
(*4) 2022년 3월 ㈜코아바이오에 신규취임하였습니다.
(*5) 2022년 3월 에이치엘비생활건강㈜에 신규취임하였습니다.
다. 감사의 독립성
당사의 감사는 1인이며, 감사의 독립성 강화를 위하여 감사 선임시, 감사에 대한 모든 정보(추천인, 최대주주와의 관계, 회사와의 거래 등을 포함)를 주주총회 전에 투명하게 공개하고 있습니다. 감사는 이사회에 참석하여 독립적으로 이사의 업무를 감독할 수 있으며, 제반업무와 관련하여 장부 및 관계서류를 해당부서에 제출하도록 요구할 수 있습니다. 또한 필요시 회사로부터 영업에 관한 사항을 보고받을 수 있으며, 적절한 방법으로 경영정보에 접근할 수 있습니다.
라. 감사의 주요 활동내역
| 회차 | 개최일자 | 의 안 내 용 | 가결여부 | 비 고 |
| 1 | 2022-01-03 | 의안1 합병종료 보고 및 공고의 건 | 가결 | - |
| 의안2 지점 설치의 건 | 가결 | - | ||
| 의안3 이사회 운영규정 개정의 건 | 가결 | - | ||
| 2 | 2022-01-12 | 의안1 ESG위원회 규정 제정의 건 | 가결 | - |
| 의안2 지점 설치의 건 | 가결 | - | ||
| 3 | 2022-01-27 | 타법인 주식 취득 내용에 관한 변경의 건 | 가결 | - |
| 4 | 2022-02-10 | 타법인 주식 취득의 건 | 가결 | - |
| 5 | 2022-02-23 | 의안1 재무제표(2021년) 확정의 건 | 가결 | - |
| 의안2 정기주주총회 소집에 관한 건 | 가결 | - | ||
| 6 | 2022-03-14 | 의안1 주식매수선택권 부여의 건 | 가결 | - |
| 의안2 제37기 정기주주총회 안건 추가의 건 | 가결 | - | ||
| 의안3 내부회계관리제도 운영실태 보고의 건 | 가결 | - | ||
| 의안4 내부회계관리제도 운영평가 보고의 건 | 가결 | - | ||
| 의안5 자회사 차입에 대한 연대보증의 건 | 가결 | - | ||
| 의안6 부패방지 경영방침 보고의 건 | 가결 | - | ||
| 의안7 10대 인권정책 보고의 건 | 가결 | - | ||
| 의안8 기업지배구조 헌장 승인의 건 | 가결 | - | ||
| 7 | 2022-03-22 | 제37기 재무제표(2021년) 정정 확정의 건 | 가결 | - |
| 8 | 2022-03-29 | 제35회차 무기명식 무보증 사모 비분리형 신주인수권부사채 발행의 건 | 가결 | - |
| 9 | 2022-03-29 | 기업설명회(IR)개최 건 | 가결 | - |
| 10 | 2022-03-29 | 제37기 정기주주총회 일부안건 철회의 건 | 가결 | - |
| 11 | 2022-03-30 | 정기주주총회 의사록 | 가결 | - |
| 12 | 2022-04-13 | 자회사 자금보충약정 체결의 건 | 가결 | - |
| 13 | 2022-04-27 | 의안1 타법인 주식취득의 건 | 가결 | - |
| 의안2 관계사 금전대여의 건 | 가결 | - | ||
| 의안3 타법인 주식 양도의 건 | 가결 | - | ||
| 의안4 관계사 선금급 지급보증 연대보증의 건 | 가결 | - | ||
| 의안5 관계사 선금급 지급보증 연대보증 내용변경의 건 | 가결 | - | ||
| 14 | 2022-05-27 | 기업설명회(IR)개최의 건 | 가결 | - |
| 15 | 2022-05-31 | 의안1 제36회차 무기명식 무보증 사모 전환사채 발행의 건 | 가결 | - |
| 의안2 제37회차 무기명식 무보증 사모 비분리형 신주인수권부사채 발행의 건 | 가결 | - | ||
| 의안3 타법인 주권관련 사채권 취득의 건 | 가결 | - | ||
| 16 | 2022-06-10 | 기업설명회(IR)개최의 건 | 가결 | - |
| 17 | 2022-08-12 | 의안1 주주배정후 실권주 일반공모 유상증자 결의의 건 |
가결 | - |
| 의안2 타법인 주권관련 사채권 처분의 건 | 가결 | - |
마. 감사 교육 미실시 내역
| 감사 교육 실시여부 | 감사 교육 미실시 사유 |
|---|---|
| 미실시 | 당사의 감사는 다년간 감사직을 수행하며 회사에 대한 높은 이해도를 보유하고, 금융분야에서 오랜기간 근무하며 충분한 자질을 확보하여 별도의 교육을 실시하지 않음 |
바. 감사 지원조직 현황
| 부서(팀)명 | 직원수(명) | 직위(근속연수) | 주요 활동내역 |
|---|---|---|---|
| 재무전략부문 | 6 | 부사장 외(평균 2년) | 내부회계관리제도 관련 제반 활동 |
사. 준법지원인 인적사항
- 당사는 상법 제542조의 13에 따라 자산총액 5천억원 이상 상장법인으로 준법지원인을 선임하여야 하지만 공시서류 작성기준일 현재 준법지원인 선임 내역이 없으나, 추후 선임 예정입니다.
아.준법지원인 등 지원조직 현황
| 부서(팀)명 | 직원수(명) | 직위(근속연수) | 주요 활동내역 |
|---|---|---|---|
| - | - | - | - |
* 공시서류 작성기준일 현재 준법지원인 선임 내역은 없으나, 추후 선임 예정이며 준법지원인 선임시 준법지원인 지원조직을 구성할 예정입니다.
3. 주주총회 등에 관한 사항
가. 투표제도 현황
| (기준일 : | 2022년 06월 30일 | ) |
| 투표제도 종류 | 집중투표제 | 서면투표제 | 전자투표제 |
|---|---|---|---|
| 도입여부 | 배제 | 미도입 | 도입 |
| 실시여부 | - | - | 제37기(21년도)정기주총 |
(1) 집중투표제의 채택여부
당사는 집중투표제를 채택하고 있지 않습니다.
(2) 서면투표제 또는 전자투표제의 채택여부
당사 이사회는 2020년 2월 26일 이사회결의를 통하여 제35기 정기주주총회부터 의결권 행사에 있어 주주의 편의를 제고하기 위하여 「상법」제368조의4에 따른 전자투표제도와「자본시장과 금융투자업에 관한 법률 시행령」제160조 제5호에 따른 전자위임장권유제도를 이번 주주총회에서 활용하기로 결의하였습니다.
당사는 주주총회 소집공고 시 전자적 방법으로 의결권을 행사할 수 있다는 내용을 공고하고 있으며, 매결산기 최종일에 의결권 있는 주식을 소유한 주주는 주주총회에 직접 참여하지 아니하고 삼성증권에서 제공하는 전자투표시스템을 통하여 주주총회 10일 전부터 주주총회일 전일까지 의결권을 행사할 수 있습니다.
나. 소수주주권의 행사 여부
- 해당사항 없습니다.
다. 경영권 경쟁
- 해당사항 없습니다.
라. 의결권 현황
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 주식수 | 비고 |
|---|---|---|---|
| 발행주식총수(A) | 보통주 | 106,882,745 | - |
| 우선주 | 7,188 | 우선주 | |
| 의결권없는 주식수(B) | 보통주 | 133,874 | 자기주식 |
| 우선주 | 7,188 | 우선주 | |
| 정관에 의하여 의결권 행사가 배제된 주식수(C) | - | - | - |
| - | - | - | |
| 기타 법률에 의하여 의결권 행사가 제한된 주식수(D) |
- | - | - |
| - | - | - | |
| 의결권이 부활된 주식수(E) | - | - | - |
| - | - | - | |
| 의결권을 행사할 수 있는 주식수 (F = A - B - C - D + E) |
보통주 | 106,748,871 | - |
| 우선주 | - | - |
마. 주식사무
| 신주인수권의 내용 |
① 주주는 그가 소유한 주식의 수에 비례하여 신주의 배정을 받을 권리를 갖는다. ② 회사는 제1항의 규정에도 불구하고 다음 각 호의 경우에는 주주이외의 자에게 신주를 배정할 수 있다. 1. 자본시장과 금융투자업에 관한 법률 제 165조의 6에 따라 이사회의 결의로 일반공모증자 방식으로 신주를 발행하는 경우 2. 상법 제542조의3에 따른 주식매수선택권의 행사로 인하여 신주를 발행하는 경우 3. 발행주식총수의 100분의 20을 초과하지 않는 범위 내에서 긴급한 자금조달을 위하여 국내외 금융기관 또는 기관투자자, 개인에게 신주를 발행하는 경우 4. 자본시장과 금융투자업에 관한 법률 제165조의 7 규정에 의하여 발행하는 주식총수의 100분의 20 범위 내에서 우리사주조합원에게 주식을 우선 배정하는 경우 5. 근로복지기본법 제39조 규정에 의한 우리사주매수선택권의 행사로 인하여 신주를 발행하는 경우 6. 발행주식총수의 100분의 20을 초과하지 않는 범위 내에서 사업상 중요한 기술도입, 연구개발, 생산,판매,자본제휴, 재무구조개선 등 회사의 경영상 목적을 달성하기 위하여 그 상대방에게 신주를 발행하는 경우 7. 발행주식총수의 100분의 40을 초과하지 않는 범위 내에서 주권을 코스닥시장에 상장하기 위하여 신주를 모집하거나 인수인에게 인수하게 하는 경우 ③ 제2항 각호의 어느 하나의 방식에 의해 신주를 발행할 경우에는 발행할 주식의 종류와 수 및 발행가격 등은 이사회의 결의로 정하고, 다만 발행가격은 증권의 발행 및 공시등에 관한 규정제5-18조의 범위 내에서 정하여야 한다. |
||
| 결 산 일 | 12월 31일 | 정기주주총회 | 매사업년도 종료 후 3월 이내 |
| 주주명부폐쇄시기 | 매년 01월 01일 부터 01월 07일까지 | ||
| 명의개서대리인 | 한국예탁결제원 | ||
| 공고방법 | 회사의 공고는 회사의 인터넷 홈페이지 (www.hlbkorea.com) 에한다. 다만, 전산장애 또는 그 밖의 부득이한 사유로 회사의인터넷 홈페이지 공고를 할 수 없는 때에는 서울특별시에서 발행되는 일간매일경제신문에 한다. | ||
바. 주주총회 의사록 요약
| 주총일자 | 안 건 | 결의내용 | 비 고 |
| 제37기 정기주주총회 (2022.03.30) |
제1호 의안 [제37기 재무제표 승인의 건] 제2호 의안 [정관 일부 변경의 건] 제3호 의안 [이사 선임의 건] 제3-1호 의안 사내이사 황제이정환 신규선임 제3-2호 의안 사외이사 최규준 재선임 제4호 의안 [이사 보수한도 승인의 건] 제5호 의안 [감사 보수한도 승인의 건] 제6호 의안 [자본준비금 감소의 건] 제7호 의안 [주식매수선택권의 부여 승인의 건] |
가결 철회 가결 가결 가결 가결 가결 가결 |
- |
| 제36기 정기주주총회 (2021.03.30) |
제1호 의안 [제36기 재무제표 승인의 건] 제2호 의안 [이사 선임의 건] 제2-1호 의안 사내이사 김동건 선임 제3호 의안 [이사 보수한도 승인의 건] 제4호 의안 [감사 보수한도 승인의 건] |
가결 가결 가결 가결 |
- |
| 제35기 정기주주총회 (2020.03.30) |
제1호 의안 [제35기 재무제표 승인의 건] 제2호 의안 [정관 일부 변경의 건] 제3호 의안 [이사 선임의 건] 제3-1호 의안 사내이사 진양곤 선임 제3-2호 의안 사내이사 전복환 선임 제3-3호 의안 사내이사 도순기 선임 제3-4호 의안 사내이사 안기홍 선임 제3-5호 의안 사내이사 문정환 선임 제3-6호 의안 사내이사 Matthew Chang 선임 제3-7호 의안 사내이사 William G.Hearl 선임 제3-8호 의안 사외이사 박진국 신규선임 제3-9호 의안 사외이사 심재철 신규선임 제4호 의안 [상근감사 김용웅 선임의 건] 제5호 의안 [이사 보수한도 승인의 건] 제6호 의안 [감사 보수한도 승인의 건] |
가결 가결 가결 가결 가결 가결 가결 가결 가결 가결 가결 가결 가결 가결 |
- |
VI. 주주에 관한 사항
1. 최대주주 및 특수관계인의 주식소유 현황
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 주, %) |
| 성 명 | 관 계 | 주식의 종류 |
소유주식수 및 지분율 | 비고 | |||||
|---|---|---|---|---|---|---|---|---|---|
| 2021/12/31 | 2022/06/30 | 2022/08/12 | |||||||
| 주식수 | 지분율 | 주식수 | 지분율 | 주식수 | 지분율 | ||||
| 진양곤 | 최대주주 | 보통주 | 8,610,902 | 8.08 | 8,610,902 | 8.06 | 8,610,902 | 8.05 | - |
| 이현아 | 친인척 | 보통주 | 230,772 | 0.22 | 230,772 | 0.22 | 230,772 | 0.22 | - |
| 이현수 | 친인척 | 보통주 | 89,756 | 0.08 | 89,756 | 0.08 | 89,756 | 0.08 | - |
| 김용웅 | 임원 | 보통주 | 4,864 | 0.00 | 4,864 | 0.00 | 4,864 | 0.00 | - |
| 도순기 | 임원 | 보통주 | 4,864 | 0.00 | 4,864 | 0.00 | 4,864 | 0.00 | - |
| 에이치엘비생명과학㈜ | 계열회사 | 보통주 | 1,399,230 | 1.31 | 1,399,230 | 1.31 | 1,399,230 | 1.31 | - |
| 에이치엘비셀㈜ | 계열회사 | 보통주 | 828,214 | 0.78 | 828,214 | 0.77 | 828,214 | 0.77 | - |
| 진유림 | 친인척 | 보통주 | 8,230 | 0.01 | 8,230 | 0.01 | 8,230 | 0.01 | - |
| 진인혜 | 친인척 | 보통주 | 8,180 | 0.01 | 8,180 | 0.01 | 8,180 | 0.01 | - |
| 계 | 보통주 | 11,185,012 | 10.49 | 11,185,012 | 10.46 | 11,185,012 | 10.46 | - | |
| 우선주 | - | 0.00 | - | 0.00 | - | ||||
※ 상기 지분율 산정 근거
- 보통주 발행주식 총수 : 106,610,064주(2021/12/31 기준)
- 보통주 발행주식 총수 : 106,882,745주(2022/06/30 기준)
- 보통주 발행주식 총수 : 106,903,481주(2022/08/12 기준)
가. 최대주주의 주요경력 및 개요
|
최대주주 성명 |
직위 | 담당업무 | 주요경력(최근 5년간) | ||
| 기간 | 경력사항 | 겸임현황 | |||
| 진양곤 | 회장/ 사내이사 |
이사회의장 |
2009.01.20 ~ 현재 |
현) 에이치엘비㈜ 대표이사 |
- 에이치엘비생명과학㈜ 이사 - 에이치엘비글로벌㈜(*1) 이사 - Elevar Therapeutics,Inc 이사 - 에이치엘비제약㈜(*2) 이사 - 에이치엘비테라퓨틱스㈜ 이사 - ㈜노터스 이사 |
| (*1) 2022년 3월, 넥스트사이언스㈜에서 에이치엘비글로벌㈜로 사명을 변경하였습니다 (*2) 2020년 10월 ㈜메디포럼제약에서 에이치엘비제약㈜로 사명을 변경하였습니다. |
나. 최대주주 보유주식에 관한 계약내용
| No. | 계약의 종류 | 성명 | 계약 상대방 | 계약체결(변경)일 | 담보내역 |
| 1 | 담보대출계약 | 진양곤 | 광주은행 | 2021.11.25 | 보유주식 300,000 주 |
| 2 | 담보대출계약 | 진양곤 | 한국투자증권 | 2022.05.27 | 보유주식 29,840 주 |
| 합계(주식등의 수) | 보유주식 329,840 주 | ||||
※ 상기 "최대주주 보유주식에 계약내용"은 보고서 제출일 기준입니다.
2. 최대주주 변동현황
최대주주 변동내역
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 주, %) |
| 변동일 | 최대주주명 | 소유주식수 | 지분율 | 변동원인 | 비 고 |
|---|---|---|---|---|---|
| - | - | - | - | - | - |
3. 주식 소유현황
| (기준일 : | 2022년 08월 12일 | ) | (단위 : 주) |
| 구분 | 주주명 | 소유주식수 | 지분율(%) | 비고 |
|---|---|---|---|---|
| 5% 이상 주주 | 진양곤 | 8,610,902 | 8.05 | - |
| - | - | - | - | |
| 우리사주조합 | - | - | - | |
소액주주현황
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 주) |
| 구 분 | 주주 | 소유주식 | 비 고 | ||||
|---|---|---|---|---|---|---|---|
| 소액 주주수 |
전체 주주수 |
비율 (%) |
소액 주식수 |
총발행 주식수 |
비율 (%) |
||
| 소액주주 | 149,399 | 149,402 | 99.99 | 94,829,732 | 106,610,064 | 88.95 | - |
| ※ 소액주주는 발행주식총수의 1%에 미달하는 주식수를 소유한 주주입니다. ※ 소유현황은 최근 주주명부폐쇄일인 2021년 12월 31일 기준입니다. |
4. 주가 및 주식거래실적
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 주) |
| 종 류 | 22년 1월 | 22년 2월 | 22년 3월 | 22년 4월 | 22년 5월 | 22년 6월 | ||
| 보통주 | 주가 | 최 고 | 36,300 | 33,000 | 34,050 | 31,250 | 52,300 | 44,950 |
| 최 저 | 29,750 | 28,850 | 28,900 | 29,050 | 28,900 | 31,800 | ||
| 평 균 | 33,988 | 30,825 | 31,019 | 30,181 | 40,807 | 36,115 | ||
| 거래량 | 최고(일) | 1,136,665 | 895,648 | 1,853,810 | 973,222 | 10,563,626 | 5,888,428 | |
| 최저(일) | 423,093 | 333,419 | 264,807 | 264,691 | 301,531 | 442,710 | ||
| 월 간 | 634,211 | 539,127 | 585,605 | 452,455 | 2,660,490 | 1,308,785 | ||
VII. 임원 및 직원 등에 관한 사항
1. 임원 및 직원 등의 현황
가. 임원 현황
| (기준일 : | 2022년 09월 23일 | ) | (단위 : 주) |
| 성명 | 성별 | 출생년월 | 직위 | 등기임원 여부 |
상근 여부 |
담당 업무 |
주요경력 | 소유주식수 | 최대주주와의 관계 |
재직기간 | 임기 만료일 |
|
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 의결권 있는 주식 |
의결권 없는 주식 |
|||||||||||
| 진양곤 | 남 | 1966.01 | 회장 / 대표이사 |
사내이사 | 상근 | 이사회의장 / 경영총괄 |
연세대학교 경제학 대학원 졸업(1993.02) 현. 에이치엘비㈜ 대표이사 현. 에이치엘비생명과학㈜ 이사 현. 에이치엘비제약㈜ 이사 |
8,610,902 | - | 최대주주 본인 | 12년 | 2023.03.30 |
| 김동건 | 남 | 1962.03 | 대표이사 | 사내이사 | 상근 | 경영총괄 | Harvard Law School 졸업(1986.06) 현. 에이치엘비㈜ 대표이사 전. 에이치엘비㈜ 경영총괄 사장 (2020.06~2021.02) 전. ㈜다날 부회장 (2019.02~2020.05) |
- | - | 계열회사 임원 | 1년 | 2024.03.30 |
| 도순기 | 남 | 1969.04 | 사장 | 사내이사 | 상근 | HLB ENG 사업부총괄 |
방송통신대학교 경영학과 졸업(2003.02) 현. 에이치엘비㈜ HLB ENG사업부 사장 전. 에이치엘비㈜ 노마드팀 사장 (2019.06~2021.10) 전. 에이치엘비㈜ 복합소재사업본부 사장 (2017.11~2019.06) |
4,864 | - | 계열회사 임원 | 4년 | 2023.03.30 |
| 황제이정환 | 남 | 1963.01 | 사장 | 사내이사 | 상근 | 마케팅총괄 | Univ. of Illinois at Urbana-Champaign 마케팅대학원 졸업(1992.05) 현. 에이치엘비㈜ 노마드팀 사장 전. JSAA Healthcare 대표이사 (2021.02~2021.10) 전. ㈜쎌바이오텍 해외사업본부장 (2019.02~2021.01) |
- | - | 해당사항 없음 | 1년 | 2025.03.30 |
| 문정환 | 남 | 1962.07 | 대표이사 | 사내이사 | 비상근 | 홍보총괄 | 고려대학교 경영대학원 졸업(1999.06) 현. ㈜노터스 대표이사 전. 에이치엘비㈜ 대외협력부문 부사장 (2019.07~2022.03) 전. 국가정보원(NIS) (1987.06~2015.06) |
- | - | 계열회사 임원 | 2년 | 2023.03.30 |
| Matthew Chang |
남 | 1974.01 | 상무 | 사내이사 | 상근 | 경영전략 / IR |
McGill University 경영대학원 졸업(2000.08) 현. 에이치엘비㈜ 상무 전. HLB USA, Inc. Secretary (2019.06~2019.11) 전. Mizuho Securities 이사 (2018.01~2018.12) |
- | - | 해당사항 없음 | 2년 | 2023.03.30 |
| William G. Hearl |
남 | 1957.04 | 이사 | 사내이사 | 비상근 | 바이오 | Univ. of Tennessee 생화학대학원 졸업 (1984.08) 현. Immunomic Therapeutics, Inc. 대표이사 전. Capital Genomix, Inc. 대표이사 (2000.08~2005.09) 전. Kirkegaard & Perry Laboratories 이사 (1994.05~2000.08) |
- | - | 계열회사 임원 | 2년 | 2023.03.31 |
| 박진국 | 남 | 1948.04 | 이사 | 사외이사 | 비상근 | 사외이사 | 뉴욕대학교 경영대학원 졸업(1986.06) 현. 에이치엘비㈜ 사외이사 현. 성도이현회계법인 고문 현. 제이씨현시스템㈜ 사외이사 |
- | - | 해당사항 없음 | 4년 | 2023.03.30 |
| 최규준 | 남 | 1964.10 | 이사 | 사외이사 | 비상근 | 사외이사 | 중앙대학교 무역학과 졸업(1988.02) 현. 에이치엘비㈜ 사외이사 현. ㈜엔솔바이오사이언스 사외이사 전. 한국IR협의회 부회장 (2017.01~2019.02) |
- | - | 해당사항 없음 | 3년 | 2025.03.30 |
| 심재철 | 남 | 1956.04 | 이사 | 사외이사 | 비상근 | 사외이사 | Univ. of Wisconsin 매스컴학대학원 졸업 (1992.05) 현. 에이치엘비㈜ 사외이사 현. 고려대학교 미디어학부 명예교수 전. 고려대학교 언론대학원장 (2015.04~2017.02) |
- | - | 해당사항 없음 | 2년 | 2023.03.30 |
| 김용웅 | 남 | 1958.06 | 감사 | 감사 | 상근 | 감사 | 서울대학교 경영학과 대학원 졸업(1985.08) 현. 에이치엘비㈜ 상근감사 전. 신용관리기금(現 금융감독원) (1986.09~1998.06) |
4,864 | - | 해당사항 없음 | 12년 | 2023.03.30 |
나. 직원 등 현황
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 천원) |
| 직원 | 소속 외 근로자 |
비고 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 사업부문 | 성별 | 직 원 수 | 평 균 근속연수 |
연간급여 총 액 |
1인평균 급여액 |
남 | 여 | 계 | |||||
| 기간의 정함이 없는 근로자 |
기간제 근로자 |
합 계 | |||||||||||
| 전체 | (단시간 근로자) |
전체 | (단시간 근로자) |
||||||||||
| 서울사무소 | 남 | 24 | - | - | - | 24 | 3.3 | 760,304 | 34,299 | - | - | - | - |
| 서울사무소 | 여 | 7 | - | - | - | 7 | 3.3 | 129,740 | 25,111 | - | |||
| ENG | 남 | 44 | - | - | - | 44 | 4.8 | 1,059,391 | 24,169 | - | |||
| ENG | 여 | 4 | - | - | - | 4 | 1.3 | 70,218 | 17,554 | - | |||
| 헬스케어 | 남 | 27 | - | - | - | 27 | 1.5 | 293,546 | 10,484 | - | |||
| 헬스케어 | 여 | 56 | - | - | - | 56 | 3.1 | 555,758 | 9,750 | - | |||
| 합 계 | 162 | - | - | - | 162 | 3.3 | 2,868,957 | 18,282 | - | ||||
|
- 직원수는 2022년 06월 30일 현재 근무중인 직원 기준으로 하여 작성하였습니다. - 1인 평균급여액은 연평균 재직자 기준으로 산출하였습니다. |
미등기임원 보수 현황
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 천원) |
| 구 분 | 인원수 | 연간급여 총액 | 1인평균 급여액 | 비고 |
|---|---|---|---|---|
| 미등기임원 | 11 | 505,660 | 45,969 | - |
2. 임원의 보수 등
| <이사ㆍ감사 전체의 보수현황> |
1. 주주총회 승인금액
| (단위 : 천원) |
| 구 분 | 인원수 | 주주총회 승인금액 | 비고 |
|---|---|---|---|
| 이사 | 10 | 2,000,000 | 사외이사포함 |
| 감사 | 1 | 100,000 | - |
2. 보수지급금액
2-1. 이사ㆍ감사 전체
| (단위 : 천원) |
| 인원수 | 보수총액 | 1인당 평균보수액 | 비고 |
|---|---|---|---|
| 13 | 599,990 | 46,153 | - |
| (*) 당기 중 퇴임한 이사 2명의 보수지급액이 포함되어 있습니다. |
2-2. 유형별
| (단위 : 천원) |
| 구 분 | 인원수 | 보수총액 | 1인당 평균보수액 |
비고 |
|---|---|---|---|---|
| 등기이사 (사외이사, 감사위원회 위원 제외) |
9 | 540,590 | 60,066 | - |
| 사외이사 (감사위원회 위원 제외) |
3 | 36,000 | 12,000 | - |
| 감사위원회 위원 | - | - | - | - |
| 감사 | 1 | 23,400 | 23,400 | - |
| <보수지급금액 5억원 이상인 이사ㆍ감사의 개인별 보수현황> |
1. 개인별 보수지급금액
| (단위 : 천원) |
| 이름 | 직위 | 보수총액 | 보수총액에 포함되지 않는 보수 |
|---|---|---|---|
| - | - | - | - |
2. 산정기준 및 방법
| (단위 : 천원) |
| 이름 | 보수의 종류 | 총액 | 산정기준 및 방법 | |
|---|---|---|---|---|
| - | 근로소득 | 급여 | - | - |
| 상여 | - | - | ||
| 주식매수선택권 행사이익 |
- | - | ||
| 기타 근로소득 | - | - | ||
| 퇴직소득 | - | - | ||
| 기타소득 | - | - | ||
| <보수지급금액 5억원 이상 중 상위 5명의 개인별 보수현황> |
1. 개인별 보수지급금액
| (단위 : 천원) |
| 이름 | 직위 | 보수총액 | 보수총액에 포함되지 않는 보수 |
|---|---|---|---|
| - | - | - | - |
2. 산정기준 및 방법
| (단위 : 천원) |
| 이름 | 보수의 종류 | 총액 | 산정기준 및 방법 | |
|---|---|---|---|---|
| - | 근로소득 | 급여 | - | - |
| 상여 | - | - | ||
| 주식매수선택권 행사이익 |
- | - | ||
| 기타 근로소득 | - | - | ||
| 퇴직소득 | - | - | ||
| 기타소득 | - | - | ||
<주식매수선택권의 부여 및 행사현황>
<표1>
| (단위 : 원) |
| 구 분 | 인원수 | 주식매수선택권의 공정가치 총액 | 비고 |
|---|---|---|---|
| 등기이사 | - | - | - |
| 사외이사 | - | - | - |
| 감사위원회 위원 또는 감사 | - | - | - |
| 업무집행지시자 | 2 | 3,429,470,000 | 계열회사 임원 |
| 계 | 2 | 3,429,470,000 | - |
| (*) 연결재무제표 주석 20. 기타자본항목 (3) 주식기준보상을 참고하시기 바랍니다. |
<표2>
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 원, 주) |
| 부여 받은자 |
관 계 | 부여일 | 부여방법 | 주식의 종류 |
최초 부여 수량 |
당기변동수량 | 총변동수량 | 기말 미행사수량 |
행사기간 | 행사 가격 |
의무 보유 여부 |
의무 보유 기간 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 행사 | 취소 | 행사 | 취소 | |||||||||||
| 정세호 | 계열회사 임원 | 2022년 03월 14일 | 신주교부 | 보통주 | 40,000 | - | - | - | - | 40,000 | 2024.03.14~2029.03.14 | 30,436 | X |
- |
| 정세호 | 계열회사 임원 | 2022년 03월 14일 | 신주교부 | 보통주 | 40,000 | - | - | - | - | 40,000 | 2025.03.14~2029.03.14 | 30,436 | X | - |
| 정세호 | 계열회사 임원 | 2022년 03월 14일 | 신주교부 | 보통주 | 40,000 | - | - | - | - | 40,000 | 2026.03.14~2029.03.14 | 30,436 | X | - |
| 정세호 | 계열회사 임원 | 2022년 03월 14일 | 신주교부 | 보통주 | 40,000 | - | - | - | - | 40,000 | 2027.03.14~2029.03.14 | 30,436 | X | - |
| 장성훈 | 계열회사 임원 | 2022년 03월 14일 | 신주교부 | 보통주 | 15,000 | - | - | - | - | 15,000 | 2024.03.14~2029.03.14 | 30,436 | X | - |
| 장성훈 | 계열회사 임원 | 2022년 03월 14일 | 신주교부 | 보통주 | 15,000 | - | - | - | - | 15,000 | 2025.03.14~2029.03.14 | 30,436 | X | - |
| 장성훈 | 계열회사 임원 | 2022년 03월 14일 | 신주교부 | 보통주 | 15,000 | - | - | - | - | 15,000 | 2026.03.14~2029.03.14 | 30,436 | X | - |
| 장성훈 | 계열회사 임원 | 2022년 03월 14일 | 신주교부 | 보통주 | 15,000 | - | - | - | - | 15,000 | 2027.03.14~2029.03.14 | 30,436 | X | - |
| 주) 2022년 3월 14일 이사회결의로 주식매수선택권을 부여하였으며, 2022년 3월 30일 정기주주총회에서 주식매수선택권의 부여를 승인받았습니다. |
VIII. 계열회사 등에 관한 사항
가. 계열회사 현황(요약)
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 사) |
| 기업집단의 명칭 | 계열회사의 수 | ||
|---|---|---|---|
| 상장 | 비상장 | 계 | |
| HLB그룹 | 7 | 35 | 42 |
나. 계열회사간의 계통도
| 피출자사 | 상장여부 | 출자사 | ||||||||||||||
| 에이치엘비㈜ | 에이치엘비 생명과학㈜ |
에이치엘비 셀㈜ |
에이치엘비 글로벌㈜ (구.㈜넥스트 사이언스) (*17) |
㈜엘에스케이 인베스트먼트 |
에이치엘비 네트웍스㈜ |
㈜프레시코 | 에포케㈜ (구.코르키㈜ (*18) |
에이치엘비 제약㈜ |
현대앤 코스모스 요팅㈜ |
에이치엘비 테라퓨틱스㈜ |
바다 중공업㈜ |
㈜노터스 | Verismo Therapeutics Inc |
㈜온힐 |
||
| Elevar Therapeutics, Inc. | 비상장 | 100.00% | - | - | - | - | - | - | - | - | - | - | - | - | - | |
| Immunomic Therapeutics,Inc. |
비상장 | 41.07% | - | - | 3.64% | - | - | - | - | - | - | - | - | - | - | |
| ㈜화진메디칼 | 비상장 | - | - | - | - | - | - | - | - | - | - | 100.00% | - | - | - | |
| ㈜화진메디스 | 비상장 | - | - | - | - | - | - | - | - | - | - | 100.00% | - | - | - | |
| 에이치엘비생명과학㈜ | 상장 | 19.60% | - | - | - | - | - | - | - | - | - | - | - | - | - | |
| 현대요트㈜ | 비상장 | 39.43% | - | - | - | - | - | - | - | - | 17.32% | - | - | - | - | |
| 바다중공업㈜ | 비상장 | 28.89% | - | - | - | - | - | - | - | - | - | - | - | - | - | |
| ㈜고션 | 비상장 | 18.76% | - | - | - | - | - | - | - | - | - | - | - | - | - | |
| 에이치엘비셀㈜(*1) | 비상장 | - | 99.27% | - | - | - | - | - | - | - | - | - | - | - | - | |
| ㈜엘에스케이인베스트먼트 | 비상장 | - | 9.00% | 29.00% | - | - | - | - | - | - | - | - | - | - | - | |
| 에이치엘비네트웍스㈜ | 비상장 | - | - | - | - | - | - | - | 75.19% | - | - | - | - | - | - | |
| ㈜신화어드밴스 | 비상장 | - | 100.00% | - | - | - | - | - | - | - | - | - | - | - | - | |
| 에이치엘비엘이디㈜ | 비상장 | - | 100.00% | - | - | - | - | - | - | - | - | - | - | - | - | |
| 에이치엘비에너지㈜(구, 거림) | 비상장 | - | 100.00% | - | - | - | - | - | - | - | - | - | - | - | - | |
| 에이치엘비생활건강㈜ (구. ㈜엘리샤코이)(*2) |
비상장 | - | - | - | 100.00% | - | - | - | - | - | - | - | - | - | - | |
| 에이치엘비사이언스㈜ (구.단디바이오사이언스㈜) (*3) |
상장 | - | - | - | 51.39% | - | - | - | - | - | - | - | - | - | - | |
| ㈜프레시코 | 비상장 | - | - | - | 55.74% | - | - | - | - | - | - | - | - | - | - | |
| ㈜코아바이오 | 비상장 | - | - | - | - | - | - | 69.75% | - | - | - | - | - | - | - | |
| Hyundai Lifeboats Singapore Pte. Ltd |
비상장 | - | - | - | - | - | 100.00% | - | - | - | - | - | - | - | - | |
| 에이치엘비제약㈜(*4) | 상장 | - | 11.35% | - | - | - | - | - | 1.62% | - | - | - | - | - | - | |
| Verismo Therapeutics Inc. (*5) |
비상장 | 9.61% | - | - | - | - | - | - | - | 35.24% | - | - | - | - | - | |
| 에이치엘비인베스트먼트㈜ (*6) |
비상장 | 100.00% | - | - | - | - | - | - | - | - | - | - | - | - | - | |
| 에이치엘비테라퓨틱스㈜(*7) | 상장 | 1.69% | - | 0.34% | 5.08% | 0.34% | - | - | 1.69% | 1.69% | 0.34% | - | - | - | - | |
| 지트리파마슈티컬(*8) | 비상장 | - | - | - | - | - | - | - | - | - | - | 100.00% | - | - | - | |
| REGENTREE(*9) | 비상장 | - | - | - | - | - | - | - | - | - | - | 61.50% | - | - | - | |
| OBLATO(*10) | 비상장 | - | - | - | - | - | - | - | - | - | - | 100.00% | - | - | - | |
| ㈜노터스(*11) | 상장 | 18.01% | - | - | - | - | - | - | - | 2.29% | - | - | - | |||
| ㈜브에이스팜(*12) | 비상장 | - | - | - | - | - | - | - | - | - | - | 66.20% | - | |||
| ㈜세론바이오(*13) | 비상장 | - | - | - | - | - | - | - | - | - | - | 60.00% | - | |||
| ㈜온힐(*14) | 비상장 | - | - | - | - | - | - | - | - | - | - | 60.77% | - | |||
| 바다엔지니어링㈜ | 비상장 | - | - | - | - | - | - | - | - | - | 100.00% | - | - | |||
| Hyundai Lifeboats Shanghai Co.,Ltd(*15) |
비상장 | 100.00% | - | - | - | - | - | - | - | - | - | - | - | - | - | |
| ㈜베리스모테라퓨틱스 아시아(*16) |
비상장 | - | - | - | - | - | - | - | - | - | - | - | - | - | 62.00% | |
| 에이치엘비일렉㈜ | 비상장 | - | - | - | - | - | 10.00% | - | - | - | - | - | - | - | - | - |
| 에이치엘비생명과학알앤디㈜ (*19) |
비상장 | - | 100.00% | - | - | - | - | - | - | - | - | - | - | - | - | - |
| ㈜개밥왕(*20) |
비상장 |
- | - | - | - | - | - | - | - | - | - | - | - | - | - | 100.00% |
| (*1) 2020년 4월 라이프리버㈜에서 에이치엘비셀㈜로 사명을 변경하였습니다. (*2) 2022년 3월 ㈜엘리샤코이에서 에이치엘비생활건강㈜로 사명을 변경하였습니다. (*3) 2020년 4월 에이치엘비사이언스㈜는 코넥스시장에 상장되었습니다. 2022년 3월 단디바이오사이언스㈜에서 에이치엘비사이언스㈜로 사명을 변경하였습니다. (*4) 2020년 10월 ㈜메디포럼제약에서 에이치엘비제약㈜로 사명을 변경하였습니다. (*5) 2021년 4월 신규 Pipeline 확보를 통한 지속적인 미래 기업가치의 극대화를 위해 2020년 6월에 설립된 미국 벤처기업 Verismo Therapeutics,Inc. 에 5백만불을 투자하였습니다. Verismo Therapeutics,Inc.은 KIR-CAR 기술의 기본특허와 KIR-CAR Mesothlin과 연관된 특허 및 생산공정과 관련된 특허를 보유하고 있으며, 차세대 CAR-T 플랫폼 기술을 기반으로 상용화 가능한 고형암 타깃 CAR-T 개발을 목표로 하고 있습니다. (*6) 2021년 5월 바이오와 헬스케어 등의 분야의 신기술사업자에 대한 투자 및 융자 등신기술사업 금융업을 통한 기업가치 극대화를 위해 에이치엘비인베스트먼트㈜의 보통주 600,000주를 30억원에 취득하였으며, 2021년 11월 보통주 1,400,000주를 70억원에 추가 취득하였습니다. (*7) 2021년 11월 지분취득을 통한 바이오 사업과의 시너지 극대화와 기업가치극대화를 위해 에이치엘비테라퓨틱스㈜ 보통주 530,899주를 약 50억에 취득하였습니다. (*8) 2021년 11월 지트리파마슈티컬은 에이치엘비테라퓨틱스의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*9) 2021년 11월 REGENTREE는 에이치엘비테라퓨틱스의 지분 61.5% 자회사로서 계열회사로 편입되었습니다. (*10) 2021년 11월 OBLATO는 에이치엘비테라퓨틱스의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*11) 2022년 3월 지분취득을 통한 신규사업진출 및 기존사업과의 시너지 극대화를 위해 ㈜노터스 보통주 1,405,648주를 약 562억에 취득하였습니다. (*12) 2022년 3월 ㈜브이에스팜은 ㈜노터스의 지분 66.2% 자회사로서 계열회사로 편입되었습니다. (*13) 2022년 3월 ㈜새론바이오는 ㈜노터스의 지분 60.0% 자회사로서 계열회사로 편입되었습니다. (*14) 2022년 3월 ㈜온힐은 ㈜노터스의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*15) 2022년 2월 리보세라닙 중국 로열티 수령 및 향후 중국사업진출을 위해 Hyundai Lifeboats Shanghai Co.,Ltd의 지분 100%를 약1.1백만불에 취득하였습니다 (*16) 2022년 1월 ㈜베리스모테라퓨틱스아시아는 Verismo Therapeutics,Inc의 지분 62.0% 자회사로서 계열회사로 편입되었습니다. (*17) 2022년 3월 넥스트사이언스㈜에서 에이치엘비글로벌㈜로 사명을 변경하였습니다. (*18) 2021년 7월 에포케㈜(구.코르키㈜)는 에이치엘비파워㈜로부터 에이치엘비네트웍스㈜의 지분 75.19%를 취득하였습니다. 2021년 10월 코르키㈜는 에포케㈜로 사명을 변경하였습니다. (*19) 2022년 4월 에이치엘비생명과학알앤디㈜는 에이치엘비생명과학의 100% 자회사로서 계열회사로 편입되었습니다. (*20) 2022년 6월 ㈜개밥왕은 온힐㈜의 100% 자회사로서 계열회사로 편입되었습니다. |
다. 계열회사간 임원 겸직 현황
| (기준일 : | 2022년 06월 30일 | ) |
| 구분 | 진양곤 | 김동건 | 김용웅 | 도순기 | William G.Hearl | 황제이정환 | 문정환 |
| 에이치엘비㈜ | 대표이사 (상근) |
대표이사 (상근) |
감사 (상근) |
이사 (상근) |
이사 (비상근) |
이사 (상근) |
이사 (비상근) |
| Elevar Therapeutics, Inc. | 이사 (비상근) |
이사 (상근) |
- | - | - | - | - |
| Immunomic Therapeutics,Inc. | 이사 (비상근) |
이사 (비상근) |
- | - | 대표이사 (상근) |
- | - |
| ㈜화진메디칼 | - | - | 감사 (비상근) |
- | - | - | - |
| 에이치엘비생명과학㈜ | 이사 (상근) |
- | - | - | - | - | - |
| 에이치엘비글로벌㈜ (구.넥스트사이언스㈜) |
이사 (비상근) |
- | - | - | - | - | - |
| 에이치엘비네트웍스㈜ |
이사 (비상근) |
- | 감사 (비상근) |
이사 (비상근) |
- | - | - |
| 현대요트㈜ | - | - | 감사 (비상근) |
이사 (비상근) |
- | - | - |
| 바다중공업㈜ | 이사 (비상근) |
- | 감사 (비상근) |
- | - | - | - |
| 에이치엘비셀㈜ (구.라이프리버㈜) |
이사 (비상근) |
- | 감사 (비상근) |
- | - | - | - |
| ㈜엘에스케이인베스트먼트 | 이사 (비상근) |
- | - | - | - | - | - |
| ㈜신화어드밴스 | - | - | 감사 (비상근) |
- | - | - | - |
| 에이치엘비일렉㈜ | 이사 (비상근) |
- | - | - | - | - | - |
| Hyundai Lifeboats Singapore Pte. Ltd |
이사 (비상근) |
- | - | - | - | - | - |
| 현대코스모스요팅㈜ | - | - | - | 이사 (비상근) |
- | - | - |
| 에이치엘비사이언스㈜ (구.단디바이오사이언스㈜) |
이사 (비상근) |
- | - | - | - | - | - |
| 에이치엘비생활건강㈜ (구. ㈜엘리샤코이) |
- | - | 감사 (비상근) |
- | - | - | - |
| ㈜프레시코 | 이사 (비상근) |
- | 감사 (비상근) |
- | - | - | - |
| ㈜코아바이오 | 이사 (비상근) |
- | 감사 (비상근) |
- | - | - | - |
| 에포케㈜ (구.코르키㈜) |
이사 (비상근) |
- | - | 이사 (비상근) |
- | - | - |
| 에이치엘비제약㈜ | 이사 (비상근) |
- | - | - | - | - | - |
| 에이치엘비인베스트먼트㈜ | 이사 (비상근) |
- | - | - | - | - | - |
| 에이치엘비테라퓨틱스㈜ | 이사 (비상근) |
- | - | - | - | - | 이사 (비상근) |
| ㈜노터스 | 이사 (비상근) |
- | - | - | - | - | 대표이사 (상근) |
| Hyundai Lifeboats Shanghai Co.,Ltd |
감사 (비상근) |
- | - | - | - | - | - |
| 에이치엘비생명과학알앤디㈜ | 이사 (비상근) |
라. 타법인출자 현황(요약)
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 백만원) |
| 출자 목적 |
출자회사수 | 총 출자금액 | |||||
|---|---|---|---|---|---|---|---|
| 상장 | 비상장 | 계 | 기초 장부 가액 |
증가(감소) | 기말 장부 가액 |
||
| 취득 (처분) |
평가 손익 |
||||||
| 경영참여 | 3 | 10 | 13 | 666,617 | -15,502 | - | 651,115 |
| 일반투자 | - | - | - | - | - | - | - |
| 단순투자 | 1 | - | 1 | 999 | - | -280 | 719 |
| 계 | 4 | 10 | 14 | 667,616 | -15,502 | -280 | 651,834 |
IX. 대주주 등과의 거래내용
1. 대주주 등에 대한 신용공여 등
가. 대여금 내역
1-1) 대여거래
①당반기(2022년 반기)
| (기준일 : 2022년 06월 30일) | (단위 : 천원) |
| 성명(법인명) | 관계 | 계정과목 | 목적 | 변동내역 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
비고 | |||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 기초 (2022.01.01) |
증가 | 감소 | 기말 | ||||||||
| 화진메디칼(*1) |
종속기업 | 장기대여금 | 운전자금, 개발자금 등 대여 | 1,700,000 | - | 1,700,000 | - | - | - | - | 2021-08-31 |
| 바다중공업 | 관계기업 | 장기대여금 | 공장인수로 인한 대여 | - | 2,000,000 | - | 2,000,000 | - | 10,334 | - | 2022-04-29 |
| (*1) 2022년 4월 29일, 이사회의 결정으로 그룹내 의료기기 사업 전문성 강화를 목적으로 종속회사인 ㈜화진메디스와 ㈜화진메디칼의 각각의 지분 100%를 에이치엘비테라퓨틱스㈜ 에 33억에 양도했으며, 상기 대여금은 2022년 04월 29일 전액 상환받았습니다. |
② 전기(2021년)
| (기준일 : 2021년 12월 31일) | (단위 : 천원) |
| 성명(법인명) | 관계 | 계정과목 | 목적 | 변동내역 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
비고 | |||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 기초 (2019.01.01) |
증가 | 감소 | 기말 (2021.12.31) |
||||||||
| 화진메디칼 | 종속기업 | 단기대여금 | 운영 자금 등 대여 | 500,000 | - | 500,000 | - | - | - | - | 2019-06-27 |
| 에이치엘비글로벌 | 관계기업 | 단기대여금 | 운영 자금 등 대여 | 9,000,000 | - | 9,000,000 | - | - | - | - | 2019-09-16 |
| 바다중공업 | 관계기업 | 단기대여금 | 운영 자금 등 대여 | 900,000 | - | 900,000 | - | - | - | - | 2020-01-15 |
| 에이치엘비인베스트먼트 | 종속기업 | 단기대여금 | 설립등기 취등록세 대여 | - | 45,490 | 45,490 | - | - | - | - | 2021-05-28 |
| 화진메디칼 | 종속기업 | 장기대여금 | 운전자금, 개발자금 등 대여 | - | 1,700,000 | - | 1,700,000 | - | 26,138 | - | 2021-08-31 |
| 합계 | 10,400,000 | 1,745,490 | 10,445,490 | 1,700,000 | - | 26,138 | - | - | |||
1-2) 대여거래 상세
1. 화진메디칼
1)신용공여의 대상자 이름 및 회사와의 관계
화진메디칼, 종속기업(대여 실행 및 상환 당시 종속기업)
2) 신용공여등의 종류
대여금
3) 신용공여등을 행한 일자, 금액, 조건, 최근 잔액 및 의사결정 방법
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2019-06-27 | 2020-06-26 | 2019-06-27 | 이사회 결정 | 4.60% | 500,000 | - | - | 500,000 | - | - | - | - |
② 장기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2021-08-31 | 2023-08-31 | 2021-08-31 | 이사회 결정 | 4.60% | - | 1,700,000 | - | 1,700,000 | - | - | - | - |
| (*1) 2022년 4월 29일, 이사회의 결정으로 그룹내 의료기기 사업 전문성 강화를 목적으로 종속회사인 ㈜화진메디스와 ㈜화진메디칼의 각각의 지분 100%를 에이치엘비테라퓨틱스㈜ 에 33억에 양도했으며, 상기 대여금은 2022년 04월 29일 전액 상환받았습니다. |
4) 신용공여의 목적
(1) 2019년 06월 27일 단기대여금 : 100% 종속회사인 화진메디칼의 운영자금 지원목적으로 신용공여를 실행함.
(2) 2021년 8월 31일 장기대여금 : 화진메디칼의 신제품 개발, 신규 유통사업 및 대출상환 등으로 일시적 자금 유동성 부족이 발생하여 신용공여를 실행함
5) 신용공여 등에 대하여 제공한 담보의 내용
해당사항 없음
6) 신용공여 등이 채무로 확정되어 회사에서 그 채무를 부담한 경우에는 이에관한 내용
해당사항 없음
2. 에이치엘비글로벌
1)신용공여의 대상자 이름 및 회사와의 관계
에이치엘비글로벌, 기타특수관계자(대여 실행 및 상환 당시 기타특수관계자)
2) 신용공여등의 종류
대여금
3) 신용공여등을 행한 일자, 금액, 조건, 최근 잔액 및 의사결정 방법
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2019-09-16 | 2019-09-24 | 2019-09-16 | 이사회 결정 | 4.60% | 9,000,000 | - | - | 9,000,000 | - | - | - | - |
4) 신용공여의 목적
풋옵션 행사로 인하여 일시적 자금부족이 발생하여 단기 금전대여 실행함.
5) 신용공여 등에 대하여 제공한 담보의 내용
해당사항 없음
6) 신용공여 등이 채무로 확정되어 회사에서 그 채무를 부담한 경우에는 이에관한 내용
해당사항 없음
3. 에이치엘비인베스트먼트
1)신용공여의 대상자 이름 및 회사와의 관계
에이치엘비인베스트먼트, 종속기업(대여 실행 및 상환 당시 종속기업)
2) 신용공여등의 종류
대여금
3) 신용공여등을 행한 일자, 금액, 조건, 최근 잔액 및 의사결정 방법
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2021-05-28 | 2021-06-30 | - | 대표이사 의사결정 | 4.60% | - | 45,490 | - | 45,490 | - | - | - | - |
4) 신용공여의 목적
설립 등기에 필요한 공과금 및 법무사 수임료 납부 비용을 위한 대여
5) 신용공여 등에 대하여 제공한 담보의 내용
해당사항 없음
6) 신용공여 등이 채무로 확정되어 회사에서 그 채무를 부담한 경우에는 이에관한 내용
해당사항 없음
4. 바다중공업
1)신용공여의 대상자 이름 및 회사와의 관계
바다중공업, 관계기업(대여 실행 및 상환 당시 관계기업)
2) 신용공여등의 종류
대여금
3) 신용공여등을 행한 일자, 금액, 조건, 최근 잔액 및 의사결정 방법
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2020-01-15 | 2021-01-15 | 2020-10-15 | 이사회 결정 | 4.60% | 900,000 | - | - | 900,000 | - | - | - | - |
② 장기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2022-04-29 | 2027-04-28 | 2022-04-27 | 이사회 결정 | 4.60% | - | - | 2,000,000 | - | 2,000,000 | - | 10,334 | - |
4) 신용공여의 목적
수주증가에 따른 이익 창출의 방안으로 효율적인 생산 및 원가 절감 및 대형선박 생산의 필요에 따른 대여
5) 신용공여 등에 대하여 제공한 담보의 내용
해당사항 없음
6) 신용공여 등이 채무로 확정되어 회사에서 그 채무를 부담한 경우에는 이에관한 내용
해당사항 없음
5. 펭귄오션레저
1)신용공여의 대상자 이름 및 회사와의 관계
펭귄오션레저, 기타특수관계자(대여 실행 당시 기타특수관계자)
2) 신용공여등의 종류
대여금
3) 신용공여등을 행한 일자, 금액, 조건, 최근 잔액 및 의사결정 방법
① 단기대여금
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 대여일 | 만기일 | 이사회결의일 | 판단근거 | 이자율 | 대여금액 | 상환금액 | 현재 잔액 | 대여금 대손충당금 |
미수이자 | 미수이자 대손충당금 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2021년 이전 | 2021년 | 당반기 | ||||||||||
| 2014-12-31 | 2015-12-31 | 2014-12-31 | 이사회 결정 | 6.9% | 23,600 | - | - | - | 23,600 | 23,600 | 1,628 | 1,628 |
4) 신용공여의 목적
말레이시아에서 영위하던 사업에 파견된 HLB 소속 직원에 대한 해외 영업비, 체류비 등의 명목으로 지급
5) 신용공여 등에 대하여 제공한 담보의 내용
해당사항 없음
6) 신용공여 등이 채무로 확정되어 회사에서 그 채무를 부담한 경우에는 이에관한 내용
2015년 12월 31일 회수가능성 부족으로 인해 대손처리
나. 채무보증내역
1)신용공여의 대상자 이름 및 회사와의 관계
현대요트, 관계기업(대여 실행 당시 관계기업)
2) 신용공여등의 종류
지급보증
3) 신용공여등을 행한 일자, 금액, 조건, 최근 잔액 및 의사결정 방법
①당반기(2022년 반기)
| (기준일 : 공시서류 제출 전일) | (단위 : 천원) |
| 구분 | 회사명 | 보증처 | 이사회 결의일 | 판단근거 | 내용 | 지급보증금액 | 보증기간 | |
|---|---|---|---|---|---|---|---|---|
| 기초 (2022.01.01) |
기준일 (2022.10.07) |
|||||||
| 관계기업 | 현대요트㈜ | 서울보증보험 | 2018-06-28 | 이사회 결의 | 하자이행보증 | 44,275 | 44,275 | 2018-06-23 ~ 2023-06-22 |
| 2021-01-06 | 하자이행보증 | 347,080 | - | 2021-01-05 ~ 2022-01-04 | ||||
| 2021-01-06 | 하자이행보증 | 353,126 | - | 2021-01-05 ~ 2022-01-04 | ||||
| 2020-07-17 | 선급이행보증 | 294,439 | 297,756 | 2020-07-29 ~ 2022-09-29 | ||||
| 2020-12-07 | 선급이행보증 | 512,227 | - | 2020-12-07 ~ 2022-02-22 | ||||
| 2021-06-01 |
선급이행보증 | 379,696 | - | 2021-06-01 ~ 2022-02-22 | ||||
| 2021-12-16 | 계약이행보증 | 191,111 | 191,111 | 2021-12-17 ~ 2022-12-17 | ||||
| 2022-04-27 | 선급이행보증 | 1,166,593 | 1,166,593 | 2022-04-20 ~ 2023-02-15 | ||||
| 합 계 | 3,288,547 | 1,699,735 | - | |||||
② 전기(2021년)
| (기준일 : 2021년 12월 31일) | (단위 : 천원) |
| 구분 | 회사명 | 보증처 | 이사회 결의일 | 판단근거 | 내용 | 지급보증금액 | 보증기간 | |
|---|---|---|---|---|---|---|---|---|
| 기초 (2021.01.01) |
기말 (2021.12.31) |
|||||||
| 관계기업 | 현대요트㈜ | 서울보증보험 | 2018-06-28 |
이사회 결의 | 하자이행보증 | 44,275 | 44,275 | 2018-06-23 ~ 2023-06-22 |
| 2018-06-28 |
하자이행보증 | 82,479 | - | 2018-06-23 ~ 2021-06-22 | ||||
| 2021-01-06 |
하자이행보증 | - | 347,080 | 2021-01-05 ~ 2022-01-04 | ||||
| 2021-01-06 |
하자이행보증 | - | 353,126 | 2021-01-05 ~ 2022-01-04 | ||||
| 2020-07-17 |
계약이행보증 | 93,522 | - | 2020-07-17 ~ 2021-05-14 | ||||
| 2021-12-16 |
계약이행보증 | - | 191,111 | 2021-12-17 ~ 2022-12-17 | ||||
| 2020-07-17 | 선급이행보증 | 1,790,900 | - | 2020-07-17 ~ 2021-02-09 | ||||
| 2020-07-17 | 선급이행보증 | 1,790,447 | - | 2020-07-17 ~ 2021-02-09 | ||||
| 2020-07-17 |
선급이행보증 | 288,153 | 294,439 | 2020-07-29 ~ 2022-04-29 | ||||
| 2020-12-07 |
선급이행보증 | 509,008 | 512,227 | 2020-12-07 ~ 2022-02-22 | ||||
| 2021-06-01 |
선급이행보증 | - | 379,696 | 2021-06-01 ~ 2022-02-22 | ||||
| 합 계 | 4,460,987 | 1,079,902 | - | |||||
4) 신용공여의 목적
현대요트㈜가 선박 수주 계약을 진행할 시 보증서 제출의무에 따라 서울보증보험의 보증을 신청함. 보증 신청 과정에서 현대요트㈜의 신용이 부족하여 서울보증보험에서 최대주주(당사)의 연대보증을 요청함.
5) 신용공여 등에 대하여 제공한 담보의 내용
해당사항 없음
6) 신용공여 등이 채무로 확정되어 회사에서 그 채무를 부담한 경우에는 이에관한 내용
해당사항 없음
2. 대주주와의 자산양수도 등
가.[ ㈜화진메디칼, ㈜화진메디스 지분 양수도]
① 거래상대방: 에이치엘비테라퓨틱스㈜
② 거래종류: 종속회사 주식100% 양도
③ 거래일자 : 2022.04.29
④ 거래대상물 : ㈜화진메디칼,보통주 320,000주,
㈜화진메디스 보통주 50,000주
⑤ 거래목적 : 그룹내 의료기기 사업 전문성 강화 및 당사 수익구조 개선
⑥ 거래금액 : 3,300,000,000원
⑦ 금액산정기준 : 외부평가기관인 회계법인(삼도회계법인)의 주식가치평가를 통하여 양수도금액을 산정하였습니다.
⑧ 거래로 인한 손익발생 여부 : 에이치엘비㈜ 별도 손익에 800,000,000원 처분이익 발생됨.
⑨ 주주총회의 승인, 이사회 결의 등 해당 거래의 공정성 또는 합리성 등을 판단하기 위하여 내부통제절차를 거친 경우 그 내용 및 이러한 절차를 거치지 아니한 경우 그 사유 및 의사결정방법 : 이사회 결의(2022.04.29)
나.[ 에이치엘비제약㈜ 12CB 매각]
① 거래상대방: 에이치엘비생명과학㈜
② 거래종류: 보유채권매각
③ 거래일자 : 2022.10.07
④ 거래대상물 : 에이치엘비제약㈜ 12회차 CB
⑤ 거래목적 : 임상비용 및 운영자금 조달
⑥ 거래금액 : 23,700,000,000원
⑦ 금액산정기준 : 외부평가기관인 회계법인(삼도회계법인)의 주식가치평가를 통하여 양수도금액을 산정하였습니다.
⑧ 거래로 인한 손익발생 여부 : 에이치엘비㈜ 별도 손익에 1,200,000,000원 처분손실 발생됨.
⑨ 주주총회의 승인, 이사회 결의 등 해당 거래의 공정성 또는 합리성 등을 판단하기 위하여 내부통제절차를 거친 경우 그 내용 및 이러한 절차를 거치지 아니한 경우 그 사유 및 의사결정방법 : 이사회 결의(2022.08.12)
3. 대주주와의 영업거래
- 해당사항 없음
4. 대주주 이외의 이해관계자와의 거래
- 해당사항 없음
5. 기업인수목적회사의 추가기재사항
- 해당사항 없음
X. 그 밖에 투자자 보호를 위하여 필요한 사항
1. 공시내용 진행 및 변경사항
- 해당사항 없습니다.
2. 우발부채 등에 관한 사항
가. 중요한 소송사건
보고서 제출일 현재 계류중인 소송사건은 다음과 같습니다.
| 소 제기일 | 사건번호 | 사건내용 | 원고 | 피고 | 소송가액 | 진행상태 |
| 2020.6.29 | 서울남부지방법원 2020가합109367 |
부당이득금 반환 청구 소송 |
에이치엘비 주식회사 |
하이투자증권 주식회사 |
금 300억원 | 1심 진행중 |
나. 견질 또는 담보용 어음ㆍ수표 현황
- 해당사항 없습니다.
다. 채무보증 현황
| (기준일 : 2022년 06월 30일) | (단위 : 천원) |
| 구분 | 회사명 | 보증처 | 내용 | 지급보증금액 | 보증기간 | |
|---|---|---|---|---|---|---|
| 기초 (2022.01.01) |
기말 (2022.06.30) |
|||||
| 관계기업 | 현대요트㈜ | 서울보증보험 | 하자이행보증 | 44,275 | 44,275 | 2018-06-23 ~ 2023-06-22 |
| 하자이행보증 | 347,080 | - | 2021-01-05 ~ 2022-01-04 | |||
| 하자이행보증 | 353,126 | - | 2021-01-05 ~ 2022-01-04 | |||
| 선급이행보증 | 294,439 | 297,756 | 2020-07-29 ~ 2022-09-29 | |||
| 선급이행보증 | 512,227 | - | 2020-12-07 ~ 2022-02-22 | |||
| 선급이행보증 | 379,696 | - | 2021-06-01 ~ 2022-02-22 | |||
| 계약이행보증 | 191,111 | 191,111 | 2021-12-17 ~ 2022-12-17 | |||
| 선급이행보증 | 1,166,593 | 1,166,593 | 2022-04-20 ~ 2023-02-15 | |||
| 합 계 | 3,288,547 | 1,699,735 | - | |||
라. 채무인수약정 현황
- 해당사항 없습니다.
마. 우발채무 및 약정사항
| (단위: 천원) | |||
| 구 분 | 차입종별 | 약정금액 | 담보제공금액 |
| 중소기업은행(*1) | 일반운전자금대출 등 | 320,000 | 384,000 |
(*) 연결실체는 중소기업은행에 대하여 토지, 건물, 기계장치를 담보로 제공하고 있습니다.
3. 제재 등과 관련된 사항
가. 제재 현황
| 제재 조치일 | 제재 기관 | 조치 대상자 | 조치내용 | 사유 | 근거법령 |
조치에 대한 이행 현황 |
재발 방지를 위한 대책 |
| 2019.12.3 | 부산지방 고용노동청 |
에이치엘비㈜ | 과태료 및 벌금부과 |
A동 아세톤 보관용기 MSDS 경고표시 미게시(3개소) 엔진실의 변속기실 윤활유, 그리스 MSDS 경고표시 미게시 B동 성형경화제 MSDS경고표시 미게시(총6개소) A동 안전보건표시 미부착(방진마스크) 건조설비 담당자 특별교육 미실시 |
산업안전보건법 제12조 제31조 제3항 제41조 제5항 |
과태료 납부 벌금 납부 (*1) |
담당자 메뉴얼 숙지 및 재발 방지 교육 실시 |
| 2022.01.13 | 한국거래소 | 에이치엘비㈜ | 공시위반 제재금 대체부과 |
타법인 주식 및 출자증권 양수결정 지연공시 신주인수권부사채 발행결정 지연공시 |
코스닥시장공시규정 제27조, 제32조, 제34조 |
제재금 납부 (*2) |
공시사유 발생시 거래소와 사전협의 진행 공시 담당자, 책임자 교육 강화 |
| (*1)당사는 부산지방고용노동청조사 결과 과태료 등을 1.8백만원을 납부하였습니다. (*2)당사는 코스닥시장공시위원회의 심의 결과에 따라 공시위반제재금 24백만원(합계 6.0점 * 400만원)을 납부하였습니다. |
4. 작성기준일 이후 발생한 주요사항 등 기타사항
작성기준일 이후 발생한 주요사항
- 2022년 8월 11일, 제33회 무보증 사모 전환사채 20,736주가 전환가액 33,757원에 전환 되었습니다.
- 2022년 8월 12일, 이사회의 결정으로 9,562,408주를 발행하는 3,256억원 규모의 주주배정 유상증자를 결정하였습니다.
- 2022년 8월 12일, 이사회의 결정으로 에이치엘비제약㈜의 전환사채 100억원을 에이치엘비생명과학㈜에 237억원에 양도하였습니다.
나. 중소기업기준 검토표
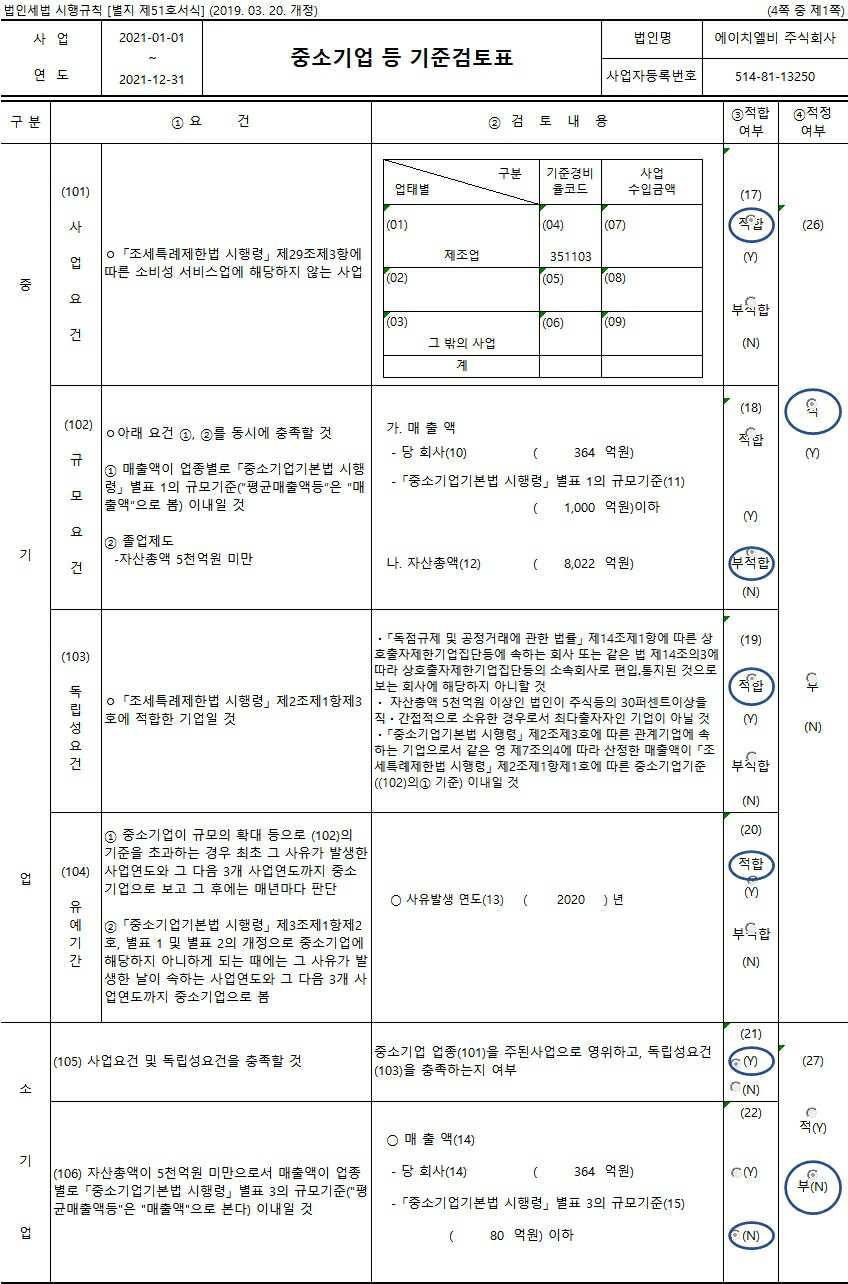 |
|
중소기업 등 기준검토표 |
다. 합병등의 사후 정보
(1) 중요한 자산양수도 - 리보세라닙(Rivoceranib) 글로벌 특허권
(가) 자산양수도 배경
당사는 Advenchen Laboratories Nanjing, Ltd.과 SFFT Developing Co., Ltd.(이하 "양도인")와 자산양수도계약을 체결하고 양도인이 보유하고 있는 YN968D1(글로벌은리보세라닙(Rivoceranib), 중국은 아파티닙(Apatinib)으로 명명의 글로벌 특허권을 거래금액 4,200만불에 양수하였습니다.
(나) 양수도가액
| 구 분 | 내 용 | 비 고 | |
| 법인명 | Advenchen Laboratories Nanjing, Ltd. |
杭州容立醫藥科技有限公司 (SFFT Developing Co., Ltd.) |
- |
| 특허권 지역 | 중국외 글로벌 | 중국 | - |
| 양수도금액 | 2,200만불 | 2,000만불 | - |
(다) 자산양수도 주요일정
| 구 분 | 일 자 | 비 고 |
| 외부평가계약 체결일 | 2020년 08월 07일 | - |
| 외부평가기관 평가 |
2020년 08일 07일 2020년 09월 02일 |
- |
| 이사회 결의일 | 2020년 09월 05일 | - |
| 계약 체결일 | 2020년 09월 05일 | 리보세라닙에 대한 Advenchen Laboratories Nanjing, Ltd.와 SFFT Developing Co., Ltd.가 보유하고 있는 YN968D1(글로벌은 리보세라닙(Rivoceranib), 중국은 아파티닙(Apatinib)으로 명명)의 글로벌 특허권 양수도 계약 체결 |
| 주요사항보고서 제출일 | 2020년 09월 07일 | - |
| 양수도대금 지급일 | 2020년 12월 04일 | 전액 현금 지급 |
(라) 회사에 미치는 중요영향 등
본 자산양수도 계약의 목적은 본 자산양수도로 리보세라닙의 글로벌 로열티 수령을 통한 장기적이고 안정적인 캐시플로우 및 영업이익을 확보하고, 항서제약과의 긴밀한 협력관계를 통하여 현재 진행중인 NDA와 리보세라닙의 추가 적응증 임상시험에 속도가 날 것이라 기대합니다.
※ 기타 자산양수도에 대한 자세한 사항은 주요사항보고서(2020.09.07) 공시를 참조하시기 바랍니다.
(3) 중요한 자산양수도 - ㈜에프에이
(가) 자산양수도 배경
당사는 2021년 10월 20일 ㈜에프에이와 자산양수도 계약을 체결하고, ㈜에프에이의주식 28,000주(지분율 : 100.00%)를 양수하였으며, 자산양수도 가격은
101,920백만원입니다.
(나) 양수도주식수 및 양수도가액
| (단위 : 주, 천원) |
| 양수인 | 양수주식수 | 양도가액 | 양도대금 수령방법 | 비 고 |
| ㈜에프에이 | 28,000 | 101,920,000 | 현금44,920,000천원 지급 및 신주인수권부사채의 권면총액 57,000,000천원 대용납입(상계) |
- |
(다) 자산양수도 주요일정
| 구 분 | 일 자 | 비 고 |
| 외부평가계약 체결일 | 2021년 09월 27일 | - |
| 외부평가기관 평가 |
2021년 09일 27일 2021년 10월 19일 |
- |
| 이사회 결의일 | 2021년 10월 20일 | - |
| 계약 체결일 | 2021년 10월 20일 | 안정적인 재무수익 창출 및 향후 예정된 바이오 사업과의 시너지 극대화를 위한 계약 체결 |
| 주요사항보고서 제출일 | 2021년 10월 20일 | - |
| 양수도대금 지급일 | 2021년 10월 20일 | - 현금 : 2021년 10월 20일(계약체결일)에 44,920백만원 지급 - 신주인수권부사채 발행 : 당사가 발행하는 제 34회차 신주인수권부사채의 권면총액 57,000백만원 대용납입(상계) |
(라) 회사에 미치는 중요영향 등
본 자산양수도 계약의 목적은 안정적인 재무수익 창출 및 향후 예정된 바이오 사업과의 시너지 극대화가 될 것을 기대합니다.
※ 기타 자산양수도에 대한 자세한 사항은 주요사항보고서(2021.10.20) 공시를 참조하시기 바랍니다.
(4) 회사 합병결정 - ㈜에프에이
(가) 합병 배경
당사는 안정적인 수익창출을 통한 재무안정성 구축 및 향후 예정된 바이오 사업과의 시너지극대화를 위해 2022년 1월 1일 ㈜에프에이와 합병하였습니다.
(나) 합병 당사회사의 개요
|
합병 후 존속회사 |
회사명 |
에이치엘비 주식회사 |
|
본점소재지 |
울산광역시 울주군 당월로 216-53 | |
|
대표이사 |
진양곤, 김동건 |
|
|
상장 여부 |
코스닥 상장법인 |
|
합병 후 소멸회사 |
회사명 |
주식회사 에프에이 |
|
본점소재지 |
세종 연동면 명학산단서로 10-5 | |
|
대표이사 |
남윤제 | |
|
상장 여부 |
비상장법인 |
(다) 합병 주요일정
|
구분 |
날짜 |
비고 |
|
|
합병 이사회 결의일 |
2021. 10. 26 |
- |
|
|
주요사항보고서 제출 |
2021. 10. 26 |
- |
|
|
주주확정기준일 공고 |
2021. 10. 26 |
- |
|
|
합병 계약 체결일 |
2021. 10. 28 |
- |
|
|
주주확정기준일 |
2021. 11. 11 |
- |
|
|
소규모합병 공고 |
2021. 11. 11 |
- |
|
|
주주명부 폐쇄기간 |
2021-11-12 ~ |
- |
|
|
합병반대의사 통지 접수기간 |
시작일 |
2021. 11. 11 |
- |
|
종료일 |
2021. 11. 25. |
||
|
합병승인 이사회 |
2021. 11. 29 |
주주총회 갈음 |
|
|
채권자 이의제출 공고 |
2021. 11. 30 |
- |
|
|
채권자 이의제출 기간 |
시작일 |
2021. 11. 30 |
- |
|
종료일 |
2021. 12. 31 | ||
|
합병기일 |
2022. 01. 01. |
- |
|
|
합병 종료보고 총회 |
2022. 01. 03 |
이사회 보고 |
|
|
합병 종료보고 공고 |
2022. 01. 03 |
- |
|
|
합병 등기 |
2022. 01. 04 |
- |
|
(라) 회사에 미치는 중요영향 등
당사는 주식회사 에프에이의 발행주식을 100% 소유하여 합병신주를 발행하지 않는 무증자 합병으로 진행되었으며, 합병 완료 후 당사의 주주변경은 없습니다.
본 합병은 상법 제527조의3에 근거하여 소규모 합병에 해당되며, 합병승인은 이사회승인으로서 갈음됩니다.
※ 기타 합병에 대한 자세한 사항은 주요사항보고서(2021.10.26) 및 합병등 종료보고서(2022.1.4)공시를 참조하시기 바랍니다.
(마)합병등 전후의 재무사항 비교표
* 합병등(합병, 중요한 영업ㆍ자산양수도, 주식의 포괄적교환ㆍ이전, 분할)
| (단위 : 백만원) |
| 대상회사 | 계정과목 | 예측 | 실적 | 비고 | ||||
|---|---|---|---|---|---|---|---|---|
| 1차연도 | 2차연도 | 1차연도 | 2차연도 | |||||
| 실적 | 괴리율 | 실적 | 괴리율 | |||||
| ㈜에프에이 | 매출액 | 82,535 | 50,764 | - | - | - | - | - |
| 영업이익 | 24,975 | 14,784 | - | - | - | - | - | |
| 당기순이익 | 19,393 | 11,553 | - | - | - | - | - | |
| ※ 상기 수치는 ㈜에프에이의 양수당시의 외부평가기관의 평가의견서에 의거하여 작성하였습니다. ※ 상기 합병법인인 ㈜에프에이는 2022년 1월 1일을 합병기일로 합병된 법인으로 제출일 현재 1차연도 실적은 없습니다. |
라. 보호예수 현황
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 주) |
| 주식의 종류 | 예수주식수 | 예수일 | 반환예정일 | 보호예수기간 | 보호예수사유 | 총발행주식수 |
|---|---|---|---|---|---|---|
| - | - | - | - | - | - | - |
XI. 상세표
1.연결대상 종속회사 현황 (상세)
| (단위 : 백만원) |
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| Elevar Therapeutics, Inc. (구 HLB USA, Inc.) |
2019.06.11 | Utah, USA | 항암제 연구개발 | 50,455 | 의결권의 과반수이상 보유(100.00%) | 미해당 |
| Immunomic Therapeutics,Inc. (*1) |
2005.09.28 | Rockville CityMaryland, USA | 항암제 연구개발 | 56,964 | 실질지배력 확보(41.07 %) | 미해당 |
| 에이치엘비인베스트먼트㈜(*2) | 2021.05.28 | 서울 강남구 선릉로 | 기타 금융업 | 10,227 | 의결권의 과반수이상 보유(100.00%) | 미해당 |
| Hyundai Lifeboats Shanghai Co.,Ltd(*3) | 2014.02.07 | Hi-Tech park, Pudong New District, Shanghai 201210, China | 서비스 | 913 | 의결권의 과반수이상 보유(100.00%) | 미해당 |
| (*) 2022년 4월 29일, 이사회의 결정으로 그룹내 의료기기 사업 전문성 강화를 목적으로 종속회사였던 ㈜화진메디스와 ㈜화진메디의 각각의 지분 100%를 에이치엘비테라퓨틱스㈜에 33억에 양도하여 종속회사에서 제외되었습니다. (*1) 과반 미만의 의결권을 보유하고 있으나, 다른 의결권 보유자들의 주식 분산 정도 및 다른 주주의 집합적 의사결정 등을 고려한 결과 당사가 지배한다고 판단하였습니다. (*2) 2021년 5월 바이오와 헬스케어 등의 분야의 신기술사업자에 대한 투자 및 융자 등신기술사업 금융업을 통한 기업가치 극대화를 위해 에이치엘비인베스트먼트㈜의 보통주 600,000주를 30억원에 취득하였으며, 2021년 11월, 보통주1,400,000주를 70억원에 추가 취득하였습니다. (*3) 2022년 2월 리보세라닙 중국 로열티 수령 및 향후 중국사업진출을 위해 Hyundai Lifeboats Shanghai Co.,Ltd의 지분 100%를 약 1.1백만불에 취득하였습니다. |
2. 계열회사 현황(상세)
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 사) |
| 상장여부 | 회사수 | 기업명 | 법인등록번호 |
|---|---|---|---|
| 상장 | 7 | 에이치엘비㈜(*1) | 170111-0021600 |
| 에이치엘비생명과학㈜ | 110111-1568885 | ||
| 에이치엘비글로벌㈜(구.㈜넥스트사이언스)(*2) | 144911-0000072 | ||
| 에이치엘비제약㈜(구.㈜메디포럼제약)(*3) | 110111-1538391 | ||
| 에이치엘비사이언스㈜ (구. 단디바이오사이언스㈜(*4) |
110111-6042363 | ||
| 에이치엘비테라퓨틱스㈜(*5) | 160111-0099451 | ||
| ㈜노터스(*6) | 284211-0063231 | ||
| 비상장 | 35 | Elevar Therpeutics,Inc.(*7) | - |
| Immunomic Therapeutics,Inc.(*8) | - | ||
| ㈜화진메디칼 | 111511-0039515 | ||
| ㈜화진메디스 | 161511-0094866 | ||
| 바다중공업㈜ | 180111-0288654 | ||
| 현대요트㈜ | 230111-0143435 | ||
| 에이치엘비셀㈜(구.라이프리버㈜)(*9) | 131311-0092331 | ||
| ㈜엘에스케이인베스트먼트 | 110111-6028595 | ||
| ㈜고션 | 205411-0015431 | ||
| 에이치엘비일렉㈜ | 284911-0134898 | ||
| 에이치엘비네트웍스㈜ | 230111-0155076 | ||
| Hyundai Lifeboats Singapore Pte. Ltd | - | ||
| 오티에스중공업㈜ | 201311-0051811 | ||
| 현대앤코스모스요팅㈜ | 110111-5137868 | ||
| ㈜신화어드밴스 | 110111-3790113 | ||
| 에이치엘비엘이디㈜ | 120111-0879348 | ||
| 에이치엘비에너지㈜(구, 거림) | 180111-0235332 | ||
| ㈜펭귄오션레저 | 230111-0222320 | ||
| 에이치엘비생활건강㈜(구.㈜엘리샤코이)(*10) | 110111-3920108 | ||
| ㈜프레시코 | 161311-0037563 | ||
| ㈜코아바이오 | 110111-5989128 | ||
| 에포케㈜(구.코르키㈜)(*11) | 110111-5998111 | ||
| VerismoTherapeutics,Inc.(*12) | - | ||
| 에이치엘비인베스트먼트㈜(*13) | 110111-7902657 | ||
| 지트리파마슈티컬(*14) | 131111-0379709 | ||
| REGENTREE(*15) | - | ||
| OBLATO(*16) | - | ||
| Hyundai Lifeboats Shanghai Co.,Ltd(*17) | - | ||
| 바다엔지니어링㈜ | 195511-0230907 | ||
| ㈜새론바이오(*18) | 135211-0033010 | ||
| 브이에스팜㈜(*19) | 110111-4752542 | ||
| ㈜온힐(*20) | 120111-******* | ||
| ㈜베리스모테라퓨틱스 아시아(*21) | 110111-8164199 | ||
| 에이치엘비생명과학알앤디㈜(*22) | 134811-0680620 | ||
| ㈜개밥왕(*23) | 284111-0185623 |
| (*1) 해당 기업집단의 지배회사입니다. (*2) 2022년 3월 넥스트사이언스㈜에서 에이치엘비글로벌㈜로 사명을 변경하였습니다. (*3) 2020년 10월 ㈜메디포럼제약에서 에이치엘비제약㈜로 사명을 변경하였습니다. (*4) 2020년 4월 단디바이오사이언스㈜는 코넥스시장에 상장되었습니다. 2022년 3월 단디바이오사이언스㈜에서 에이치엘비사이언스㈜로 사명을 변경하였습니다. (*5) 2021년 11월 지분취득을 통한 바이오 사업과의 시너지 극대화와 기업가치극대화를 위해 에이치엘비테라퓨틱스㈜ 보통주 530,899주를 약 50억에 취득하였습니다. (*6) 2022년 3월 지분취득을 통한 신규사업진출 및 기존사업과의 시너지 극대화를 위해 ㈜노터스 보통주 1,405,648주를 약 562억에 취득하였습니다. (*7) LSK BioPartners, Inc. 는 2019년 11월 27일을 합병기일로 당사의 100% 자회사인 HLB USA, Inc.에 흡수합병되어 소멸하였으며, 이후 HLB USA,Inc는 Elevar Therapeutics,Inc 로 법인명 변경하였습니다. (*8) 과반 미만의 의결권을 보유하고 있으나, 다른 의결권 보유자들의 주식 분산 정도 및 다른 주주의 집합적 의사결정 등을 고려한 결과 당사가 지배한다고 판단하였습니다. (*9) 2020년 4월 라이프리버㈜에서 에이치엘비셀㈜로 사명을 변경하였습니다. (*10) 2022년 3월 ㈜엘리샤코이에서 에이치엘비생활건강㈜로 사명을 변경하였습니다. (*11) 2021년 7월 코르키㈜는 에이치엘비파워㈜로부터 에이치엘비네트웍스㈜의 지분 75.19%를 취득하였습니다. (*12) 2021년 4월 신규 Pipeline 확보를 통한 지속적인 미래 기업가치의 극대화를 위해 2020년 6월에 설립된 미국 벤처기업 Verismo Therapeutics,Inc. 에 5백만불을 투자하였습니다. Verismo Therapeutics,Inc.은 KIR-CAR 기술의 기본특허와 KIR-CAR Mesothlin과 연관된 특허 및 생산공정과 관련된 특허를 보유하고 있으며, 차세대 CAR-T 플랫폼 기술을 기반으로 상용화 가능한 고형암 타깃 CAR-T 개발을 목표로 하고 있습니다. (*13) 2021년 5월, 바이오와 헬스케어 등의 분야의 신기술사업자에 대한 투자 및 융자 등신기술사업 금융업을 통한 기업가치 극대화를 위해 에이치엘비인베스트먼트㈜의 보통주 600,000주를 30억원에 취득하였으며, 2021년 11월, 보통주 1,400,000주를 70억원에 추가 취득하였습니다. (*14) 2021년 11월 지트리파마슈티컬은 에이치엘비테라퓨틱스의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*15) 2021년 11월 REGENTREE는 에이치엘비테라퓨틱스의 지분 61.5% 자회사로서 계열회사로 편입되었습니다. (*16) 2021년 11월 OBLATO는 에이치엘비테라퓨틱스의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*17) 2022년 2월 리보세라닙 중국 로열티 수령 및 향후 중국사업진출을 위해 Hyundai Lifeboats Shanghai Co.,Ltd의 지분 100%를 약 1.1백만불에 취득하였습니다. (*18) 2022년 3월 ㈜새론바이오는 ㈜노터스의 지분 60.0% 자회사로서 계열회사로 편입되었습니다. (*19) 2022년 3월 ㈜브이에스팜은 ㈜노터스의 지분 66.2% 자회사로서 계열회사로 편입되었습니다. (*20) 2022년 3월 ㈜온힐은 ㈜노터스의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*21) 2022년 1월 ㈜베리스모테라퓨틱스 아시아는 Verismo Therapeutics,Inc의 지분 62.0% 자회사로서 계열회사로 편입되었습니다. (*22) 2022년 4월 에이치엘비생명과학알앤디㈜는 에이치엘비생명과학㈜의 100% 자회사로서 계열회사로 편입되었습니다. (*23) 2022년 6월 ㈜개밥왕은 ㈜온힐의 지분 100% 자회사로서 계열회사로 편입되었습니다. (*) 의령태양광1호㈜의 경우 2022년 6월부로 청산하여 계열회사에서 제외되었습니다. |
3. 타법인출자 현황(상세)
| (기준일 : | 2022년 06월 30일 | ) | (단위 : 백만원, 천주, %) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
| 에이치엘비생명과학㈜ | 상장 | 2015.10.23 | 경영참여 | 7,000 | 18,721 | 19.60 | 131,066 | - | - | - | 18,721 | 19.60 | 131,066 | 270,800 | -49,292 |
| 현대요트㈜(*) |
비상장 | 2009.07.02 | 경영참여 | 300 | 328 | 39.43 | - | - | - | - | 328 | 39.43 | - | 12,036 | 9 |
| 바다중공업㈜ | 비상장 | 2009.05.28 | 경영참여 | 300 | 780 | 28.89 | 768 | - | - | - | 780 | 28.89 | 768 | 20,421 | 556 |
| 고션(*) |
비상장 | 2014.02.12 | 경영참여 | 105 | 21 | 18.76 | - | - | - | - | 21 | 18.76 | - | 40 | - |
| 에이치엘비파워㈜ | 상장 | 2016.09.06 | 단순투자 | 2,800 | 623 | 0.68 | 999 | - | - | -280 | 623 | 0.68 | 719 | 99,108 | -6,532 |
| ㈜화진메디칼 | 비상장 | 2018.02.21 | 경영참여 | 5,022 | 70 | 100.00 | 2,500 | -70 | -2,500 | - | - | - | - | 7,576 | 63 |
| ㈜화진메디스(*) |
비상장 | 2018.02.21 | 경영참여 | 500 | 50 | 100.00 | - | -50 | - | - | - | - | - | 1,947 | -172 |
| Elevar Therapeutics, Inc. | 비상장 | 2019.06.11 | 경영참여 | 188,792 | 56,579 | 100.00 | 337,384 | 5,000 | 31,513 | - | 61,579 | 100.00 | 368,896 | 50,455 | -63,462 |
| ㈜씨엘팜 | 비상장 | 2019.12.02 | 경영참여 | 5,000 | 64 | 7.72 | 5,074 | - | - | - | 64 | 7.72 | 5,074 | 31,605 | 1,211 |
| Immunomic Therapeutics, Inc. | 비상장 | 2020.01.31 | 경영참여 | 11,970 | 11,286 | 41.11 | 67,098 | - | - | - | 11,286 | 41.07 | 67,098 | 56,964 | -26,056 |
| Verismo Therapeutics, Inc. | 비상장 | 2021.04.12 | 경영참여 | 5,602 | 1,913 | 11.44 | 5,602 | - | - | - | 1,913 | 9.61 | 5,602 | 15,573 | -6,563 |
| 에이치엘비 인베스트먼트㈜ | 비상장 | 2021.05.28 | 경영참여 | 10,000 | 2,000 | 100.00 | 10,000 | - | - | - | 2,000 | 100.00 | 10,000 | 10,227 | -438 |
| 에이치엘비테라퓨틱스㈜ | 상장 | 2021.11.15 | 경영참여 | 500 | 531 | 1.69 | 5,000 | - | - | - | 531 | 1.69 | 5,000 | 189,711 | -17,764 |
| 에프에이㈜ | 비상장 | 2021.10.20 | 경영참여 | 102,126 | 28 | 100.00 | 102,126 | -28 | -102,126 | - | - | - | - | - | - |
| Hyundai Lifeboats Shanghai Co.,Ltd | 비상장 | 2022.02.10 | 경영참여 | 1,385 | - | - | - | 0 | 1,385 | - | 0 | 100.00 | 1,385 | 913 | 138 |
| ㈜노터스 | 상장 | 2022.03.30 | 경영참여 | 56,226 | - | - | - | 1,406 | 56,226 | - | 1,406 | 18.01 | 56,226 | 93,402 | 10,308 |
| 합 계 | - | - | 667,616 | 6,258 | -15,502 | -280 | - | - | 651,834 | 860,777 | -157,994 | ||||
| (*) 당사는 별도재무제표 상 종속기업 및 관계기업투자주식에 대해 원가법을 적용하고 있으며, 해당 투자주식의 회수가능액을 평가한 결과 장부금액에 미달하여 전액 손상차손을 인식하였습니다. |
【 전문가의 확인 】
1. 전문가의 확인
해당사항 없음.
2. 전문가와의 이해관계
해당사항 없음.