 |
|
s25c-0i22061012550 |
증 권 신 고 서
| ( 지 분 증 권 ) |
| 금융위원회 귀중 | 2022년 06월 10일 |
| 회 사 명 : |
주식회사 카이노스메드 |
| 대 표 이 사 : |
이기섭 |
| 본 점 소 재 지 : |
경기도 성남시 분당구 판교역로 184, JS타워 11층 |
| (전 화) 02-567-7419 | |
| (홈페이지) http://www.kainosmedicine.com | |
| 작 성 책 임 자 : | (직 책) 대표이사 (성 명) 이 기 섭 |
| (전 화) 02-567-7417 | |
| 모집 또는 매출 증권의 종류 및 수 : | 기명식 보통주 5,600,000주 | |
| 모집 또는 매출총액 : | 48,496,000,000 | 원 |
| 증권신고서 및 투자설명서 열람장소 |
| 가. 증권신고서 |
| 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 나. 투자설명서 |
| 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 서면문서 : (주)카이노스메드 → 경기도 성남시 분당구 판교역로 184 JS타워 1101호 한양증권(주) → 서울특별시 영등포구 국제금융로6길 7 |
【 대표이사 등의 확인 】
 |
|
s25c-0i22061012550 |
요약정보
1. 핵심투자위험
| 하단의 핵심투자위험은 증권신고서 본문에 기재된 투자위험요소 중 중요한 항목만을 투자자의 이해도 제고를 위하여 간단ㆍ명료하게 요약한 것입니다. 자세한 투자위험요소는 "본문-제1부 모집 또는 매출에 관한 사항-Ⅲ. 투자위험요소"에 기재되어 있으니 참고하시기 바랍니다. |
| 구 분 | 내 용 |
| 사업위험 | 가. COVID-19 유행, 러시아-우크라이나 전쟁 및 대내외 불확실성에 따른 신약개발에 미치는 위험 세계 각국은 백신 개발과 코로나-19 확산 방지에 총력을 다하고 있습니다. 2021년 백신 접종을 시작으로, 세계 각국은 일정 수준 이상의 백신 접종률 달성을 위해 총력을 기울이고 있습니다. 그러나 코로나-19는 여전히 종식되지 않았으며, 각종 변이 코로나-19가 확산되는 등 장기화될 가능성이 존재합니다. IMF는 러시아-우크라이나 전쟁, 긴축적 통화ㆍ재정정책, 중국의 성장 둔화, 코로나19 영향 등의 영향으로 세계 경제 회복세가 대폭 둔화될 것으로 전망하며, 2022년 경제성장률은 직전 전망치(2022년 01월) 4.4% 대비 0.8%p 하향한 3.6%를 전망하였고, 2023년 경제성장률은 직전 전망치(2022년 01월) 3.8% 대비 0.2%p 하향한 3.6%를 전망하였습니다. 국내 경기 또한 글로벌 COVID-19 팬데믹의 장기화 및 추후 재발 가능성과 더불어 소비 및 금융 시장 심리 악화, 러시아-우크라이나 전쟁의 장기화, 원자재 가격의 급격한 상승, 높은 인플레이션으로 인한 고강도 통화정책 실시 등 부정적인 요인들은 향후에도 경기 회복세가 둔화될 수 있는 가능성이 존재합니다. 나아가 COVID-19 이외에도 2022년 02월 24일 러시아가 우크라이나를 침공함으로써 러시아-우크라이나 전쟁이 발발하였습니다. 증권신고서 제출일 현재 러시아-우크라이나 전쟁이 당사에 직접적으로 영향을 미칠지 여부는 미지수입니다. 따라서 투자자께서는 러시아-우크라이나 전쟁이 당사 및 당사가 영위하는 사업에 미칠 미칠 영향에 대해 면밀히 검토하시기 바랍니다. 나. 연구개발 지연 및 실패 위험 당사가 주요사업으로 영위하는 바이오신약개발 산업의 특성상 현재 연구개발하고 있는 신약이 상업화되기까지는 막대한 비용과 시간이 필요합니다. 특히, 임상시험에 진입하여도 최소 8-9년이 소요되며 그에 필요한 비용이 요구됩니다. 또한, 임상시험을 진행한다고 하더라도 시험결과 효능이 부족하거나 안전성 평가에 적합하지 못한 결과가 나올 경우 해당 신약의 연구개발은 중단될 수 있으며, 이러할 경우 당사의 비용 및 시간 투자에도 불구하고 엄청난 손실을 야기할 수밖에 없습니다. 다양한 규모의 임상시험을 준비하고 진행하는 과정에서 코로나19 등 임상 계획 당시 예상치 못하였던 변수로 인하여 임상시험 개시 승인이 늦어지거나, 환자등록이 원활하지 않는 등의 문제가 발생할 수 있으며 이 경우 임상시험의 진행이 예정보다 지연될 위험이 존재합니다. 당사의 파이프라인별 물질들은 당사가 계획하고 있는 일정에 따라 임상시험 및 판매 허가를 득하고 있습니다. 그러나 당사가 예상치 못한 이유로 인해 신약 개발 일정이 지연된다면 제품화까지 당사 예상 대비 장기간이 소요될 수 있으며, 연구개발을 진행하는 동안에도 성과가 나오지 않을 경우 연구를 중단하게 되고 사용된 연구개발 비용은 따로 회수할 수 없어 당사의 수익성 및 성장성에 악영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. 이러한 임상 지연 및 실패는 당사의 수익성 및 재무안정성에 부정적인 영향을 미칠 수 있음을 투자자께서는 유의하시기 바랍니다. 다. 기술이전 지연 및 실패에 따른 위험 당사와 같은 바이오벤처는 신약 개발사업이 태생적으로 부담하고 있는 낮은 임상성공률, 대규모 개발비용, 오랜 개발기간에 따른 리스크를 국내외 대형 제약사와 분산하기 위하여 개발 초기단계에서 기술이전함으로써 조기에 수익을 시현하는 것을 기본적 수익모델로 삼고 있습니다. 당사는 전략적 기술이전을 통하여 파트너확보와 공동연구를 진행하고 있습니다. 당사의 기술이전 시점을 후보물질 및 초기 임상개발 완료 단계에서 이루어지며, 공동연구, 기술제휴를 통하여 미래의 전략적 파트너를 확보하고 있습니다. 하지만 당사의 이러한 노력에도 불구하고 글로벌 기술이전 거래 건수 및 규모의 감소, 제약/바이오 시장의 수요 감소, 글로벌 제약사들의 사업전략 변동 등의 이유로 인해 기술이전이 예상보다 지연되거나 실패하는 경우 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. 라. 기술 이전 파트너사의 약물 상업화 실패에 따른 수익 감소의 위험 당사의 매출발생은 기술이전을 통해서 이루어지며, 당사는 라이선스 아웃을 위한 국내외 제약회사를 대상으로 학회, 전시회 및 비즈니스 파트너링 행사 등 기술 교류의 장을 통한 지속적 개발 업데이트와 교류활동을 하고 있습니다. 일반적으로 기술이전이 이루어지게 되면, 추가개발은 라이선스 인을 한 기업에서 진행하며 계약에 따라 별도로 추가개발을 진행할 수도 있습니다. 라이선스 인한 기업에서는 추가개발 상황 및 임상시험결과에 따라 마일스톤 및 로열티를 지급하게 됩니다. 기술이전을 받은 기업이 추가개발에 실패하거나 상업화가 원활히 진행 되지 않는 경우, 반환의무가 있는 계약금이나 마일스톤 등은 기술이전을 완료했더라도 지급의무가 발생할 수 있습니다. 또한 총 금액은 임상시험 결과에 따라 중도에 해지되거나 금액이 감소 될 수 있습니다. 당사의 기술이전 파이프라인 및 향후 개발 진행 예정인 파이프라인의 임상 등에서의 예상치 못한 독성이 관찰되거나 효능이 기대에 미치지 못할 수 있습니다. 또한 기술이전한 파트너사의 임상수행 능력, 파트너사 내부적인 이유로 임상진행을 중단할 가능성도 존재합니다. 임상 개발에 실패할 경우 수취 예정인 마일스톤 및 로열티가 감소하여 수익성과 재무안정성에 부정적인 영향을 미칠 수 있습니다. 마. 연구개발파트너 계약 중단 관련 위험 당사는 개발물질의 사업화를 위해 전략적 파트너사, 다국적 제약회사 관계자, 각 분야의 전문가와 교류를 유지하고 있습니다. 특히, 해외 유수의 제약기업과의 파트너링을 지속적으로 진행함으로써 기술이전을 대비한 네트워킹 유지를 위해 노력하고 있습니다. 당사의 기술이전 전략인 제한적 실시권을 부여하는 동시에 공동연구개발을 추진함으로써 연구개발 결과를 추후에 활용하여 글로벌 제약사의 기술이전 기회를 확보하는 전략을 추진하고 있습니다. 당사의 공동연구파트너들은 공동연구 계약에 따라 해당 약물에 대한 공동연구개발을 수행하고 있으며, 당사의 경영진이나 주주로서 관계를 가지고 있지 않습니다. 따라서 공동연구개발 계약이 예기치 못한 사유로 인해 중단될 경우 약물의 상업화가 불투명해질 수 있습니다. 투자자 여러분들께서는 이 점 유의하시기 바랍니다. 바. 목표시장 내 수익성 감소에 따른 위험 현재 파킨슨병 치료제 연구개발 현황을 살펴보면, 질병의 진전을 제어할 수 있는 질병조절 치료제의 개발이 매우 시급한 상황이며 연구개발이 활발하게 진행되고 있으나 현재 적절한 치료제는 전무한 상황에 있습니다. 에이즈 치료제는 Sustiva을 포함하여 4개가 시판 중에 있으며, NNRTI 약물은 내성이 잘 생기고 장기복용시 독성 및 부작용의 문제로 인해 제한적으로 사용되고 있습니다. 당사는 파킨슨병 치료제 및 에이즈 치료제 등 현재 의학적 미충족 수요가 높은 질환 시장을 목표로 하여 각 파이프라인별로 경쟁구도 및 경쟁제품 개발 파이프라인 동향을 면밀하게 분석한 후 당사의 경쟁우위요소를 바탕으로 사업전략을 수립하고 있습니다. 하지만 당사의 이러한 노력에도 불구하고 의학적 미충족 수요의 변화, 경쟁제품의 연구개발 속도, 경쟁사의 가격정책 및 마케팅전략 변화, 새로운 치료제의 등장, 당사 파이프라인의 연구개발 속도 등의 이유로 인해 당사 파이프라인의 시장경쟁력이 약화되는 경우 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. 사. 업무 위탁 기관 관련 위험 당사가 영위하고 있는 신약 개발사업은 치료효과를 보이는 선도물질의 개발, 최적화 과정을 통한 후보물질의 개발, 비임상시험을 진행하기 위한 후보물질의 생산 및 제조, 동물을 대상으로 한 효능 및 독성 시험, 임상시험을 진행하기 위한 임상시료의 생산 및 제조, 정상인 및 환자를 대상으로 한 효능 및 독성 시험을 거쳐야 합니다. 하지만 당사가 생산 및 임상시험 업무를 위탁한 CMO 및 CRO 자체의 사정으로 인한 의도하지 않은 결과를 통제하기 어려울 수 있습니다. CMO의 경우 생산 시료의 품질 저하나 생산 일정의 지연 등으로 신약 개발에 부정적인 영향을 줄 수 있으며, CRO의 경우 시험 일정 지연으로 인하여 신약 개발 일정을 지연시키거나 시험 결과 분석 상의 오류로 신약 개발과 관련된 의사 결정을 어렵게 할 수 있습니다. 이와 같이 업무위탁 기관을 활용할 경우 당사가 통제할 수 없는 위험요소로 인하여 당사의 신약 개발 일정 지연 또는 부정적 결과 도출 등이 발생할 수 있으며 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. 아. 핵심연구인력유출 위험 연구개발 능력은 당사가 속한 산업의 특성상 매우 중요한 요소이며, 지속적인 연구개발을 위해 우수한 인재를 보유 및 유치하는 것이 회사의 성과를 결정하는 가장 중요한 요소입니다. 이는 제약 산업을 영위하고 있는 업체들에 공통적으로 적용되는 사항으로, 업계 내에서 우수한 인력 유치에 관한 경쟁은 점차 심화되고 있습니다. 또한, 주요 연구 인력의 유출이 있을 경우 해당 연구 개발과제가 지연되거나 개발전략을 수정해야 할 가능성이 존재하며, 개발비 부담 등으로 당사의 경쟁력 및 성장 가능성이 악화될 수 있습니다. 당사는 지식과 경험이 풍부한 인력이 신약 연구개발 사업의 핵심 경쟁력이라는 사실을 인지하고 우수한 인력을 지속적으로 확보하고자 노력하고 있으며, 현재 보유하고 있는 핵심 인력을 유지하기 위하여 능력에 따른 연봉제, 스톡옵션 제도, 회사 비전 공유, 각종 복리후생제도 강화 등 합리적인 보상구조 및 애사심 고취에 힘쓰고 있으며 향후에도 이와 같은 정책을 확대할 계획입니다. 하지만 당사의 이러한 노력에도 불구하고 우수한 전문인력의 부족, 국내외 경쟁사 또는 정부출연 연구기관으로의 유출 등의 사유로 인해 우수한 전문인력을 유지하거나 확보하는 데 어려움이 발생하여 당사의 사업경쟁력이 약화될 수 있으며 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. 자. 지적재산권 관련 위험 당사는 신약개발 기업으로서 지적재산권의 철저한 보호가 기업가치 유지의 핵심적인 요소입니다. 당사가 보유하고 있는 특허는 당사 주요 제품 개발의 핵심 요소이며 이러한 핵심 기술이 향후 성장을 결정하는 가장 중요한 사항인 만큼 지적재산권을 효과적으로 관리하지 못할 경우 경쟁 제품 출현 등으로 인해 경쟁력 확보에 어려움이 있을 수 있습니다. 당사는 보유하고 있는 기술에 대하여 향후 공동연구개발 추진, 라이선스 아웃, 경쟁회사의 유사 기술개발 방어 및 진입장벽 구축 등을 위해 지적재산권 확보 및 보호 전략을 수립하고 있습니다. 특히 파킨슨병 치료제 KM-819의 물질 특허가 19개국에 등록이 완료되어 있습니다. 당사는 물질특허 외에도 알파시누클라인(α-synuclein)에 대한 축적억제 작용기전을 규명(용도) 및 Salt form 제법에 대한 PCT 출원을 완료하였기 때문에, 특허 보호기간(또는 PMS기간) 동안 물질, 용도, 제재에 대한 모방은 원천적으로 막을 수 있습니다. 다만, 그럼에도 불구하고, 향후 제3자에 의하여 당사가 보유하고 있는 특허권에 대한 소송 또는 기타 분쟁이 발생할 가능성을 배제할 수 없으며, 임상시험 또는 제품 상용화에 실패하여 특허 연장을 하지 못할 경우, 특허가 만료되어 동일 기반 기술의 경쟁 제품이 개발될 수 있음에 따라 당사의 손익에 부정적인 영향을 미칠 수 있습니다. 차. 정부 정책 및 규제 변화에 따른 위험 제약산업은 인간의 생명 및 건강과 직결되는 의약품을 개발ㆍ제조ㆍ판매하는 산업으로, 제품의 개발ㆍ제조, 임상시험, 인ㆍ허가, 유통ㆍ판매에 이르기까지 전 과정에 걸쳐 각 국가의 규제 당국이 제시하는 엄격한 규정과 절차를 따라야 합니다. 국내의 약가 사후관리제도는 대내외 보건의료 환경변화에 의하여 수 차례 변화되어, 현재는 실거래가 조사에 의한 약가 인하, 사용량-약가 연동 협상, 급여범위 확대 시 약가인하, 제네릭의약품 등재 시 오리지널의약품의 약가인하 등의 제도가 운영되고 있습니다. 이러한 약가 인하 정책은 제약산업에서 간과할 수 없는 중요 요인이며, 당사의 사업에도 부정적인 영향을 미칠 수 있습니다. 당사는 내부에 담당 인력과 외부 전문가들을 통하여 국내 및 해외 제약 산업 정책 및 규제 환경을 지속적으로 모니터링하고 있으며, 각국의 규제 당국과의 소통을 통해 정책 및 규제 환경의 변화에 효과적으로 대비하기 위해 최선의 노력을 다하고 있습니다. 그럼에도 불구하고 국내를 포함한 주요 국가에서의 제약 산업 관련 정책이 비우호적 분위기로 전환되거나 규제가 강화되는 경우, 당사의 사업에 부정적인 영향을 미칠 수 있습니다. 제약 및 신약개발 산업에 대한 우호적인 정책 기조 및 지원 계획, 규제 완화 노력에도 불구하고, 실제 효율적인 정책 지원이 이루어지지 않거나, 세부과제 추진에 어려움이 생길 수 있으며, 관련 법규의 제정 및 개정 단계, 예산 확보 등에 난항이 발생할 수 있습니다. 또한 해당 정책의 기대효과가 감소되는 경우 정책 기조의 변화로 정부 지원이 축소될 수 있으며, 조건부 허가와 같은 규제 완화에 대한 실효성이 크지 않을 경우, 규제 완화의 범위가 축소될 수 있습니다. 이러한 정부의 우호적인 정책 및 규제 완화의 변동 가능성은 당사의 사업에 부정적인 영향을 끼칠 수 있습니다. |
| 회사위험 |
가. 현재 진행 중인 자본잠식이 심화될 위험 마. 재무안정성 관련 위험 당사 연결재무제표를 살펴보면 2022년 1분기말 연결기준 총자산 39,472백만원 및 유동자산 32,985백만원, 총 차입금 25,917백만원, 차입금 의존도 65.66%, 부채비율 237.88%, 유동비율 119.27%를 나타내고 있습니다. 부채총계의 대부분을 차지하고 있는 차입금의 규모를 살펴보면 2019년의 경우 차입금은 존재하지 않는데 이는 합병 이전 하나금융11호기업인수주식회사의 재무 현황을 기재하였습니다. 이외 2020년 06월 발행한 제2회 전환사채 및 은행 차입금으로 인해 2020년 23,264백만원, 2021년 25,080백만원, 2022년 1분기 기준 25,917백만원(각 사업연도말 기준 미상환 전환사채 전자등록총액 기재)이 존재합니다. 향후 유의미한 수준의 매출 발생으로 인한 수익 구조 개선 시기가 지연된다면 손실이 지속적으로 발생하거나, 현재 당사가 진행 중인 파이프라인의 임상 시험이 지연 또는 실패하여 소요된 연구개발비용 등을 회수하지 못할 경우 유동성 악화로 인해 당사의 재무안정성이 악화될 수 있습니다. 이러한 점을 투자자께서 유의하시어 투자에 임하시기를 바랍니다.
|
| 기타 투자위험 | 가. 유상증자 철회에 따른 위험 유상증자 진행 중에 모집 절차의 진행에 중대한 영향을 미칠만한 사유가 발생하여 당사 혹은 대표주관회사의 판단으로 유상증자가 철회될 수 있습니다. 당사가 진행하는 금번 유상증자가 예기치 못한 사유로 인해 철회될 경우 당사는 자본 확충을 위하여 무상감자 등 주주에게 손실을 끼치는 방안 등을 진행할 수 있습니다. 유상증자 납입전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회시점에 따라 권리락에 따른 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있음을 투자자께서는 유의하시기 바랍니다. 또한, 당사가 계획한 자금사용목적의 자금이 조달되지 않기 때문에 당사는 단기간 유동성 위험에 직면하여 매우 위험한 상황이 발생할 수 있으니 이 점 유의하시기 바랍니다. 나. 주가희석화 및 인수인의 실권주 인수분 물량 출회에 따른 주가하락 위험 당사는 증권신고서 제출 전일 현재 미발행 주식수가 총 9,754,725주가 존재하며, 그 내역은 미전환 제2회 전환사채 20,000백만원의 전환가능주식수 4,914,004주 및 미행사 주식매수선택권 4840,721주입니다. 전환사채 및 주식매수선택권 등 미발행 주식이 신규 발행될 경우 총발행주식수 110,565,888주(주식병합 후 22,113,177주)의 약 8.82%(금번 유상증자 5,600,000주 포함 7.04%)에 해당하며, 주가 희석화 및 물량출회로 인해 투자자의 손실을 초래할 위험이 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. 신주 상장예정일은 유관기관과의 협의에 따라 변경될 수 있으며, 금번 유상증자에 따른 5,600,000주의 유상신주가 코스닥시장에 추가 상장될 경우 전량 보호 예수되지 않습니다. 또한, 대표주관회사가 잔액인수한 물량은 수익을 확정하기 위해 신주상장일 2영업일 전부터 장내에서 대량 매도할 수 있습니다. 이 경우 일시적 물량 출회에 따른 주가 하락의 가능성이 존재하며, 인수한 실권주를 일정 기간 보유하더라도 동 인수물량이 잠재매각물량으로 존재하여 주가 상승에는 부담으로 작용할 가능성이 높습니다. 대표주관회사가 최종 실권주를 인수하게 되면 실권주 인수금액의 12%를 추가수수료로 지급하게 되며, 이를 고려 시 대표주관회사의 실권주 매입단가는 일반청약자들보다 12% 낮은 것과 같은 결과가 초래되어 대표주관회사의 실권주 매도단가가 신주의 발행가액보다 낮게 될 가능성이 존재합니다. 투자자께서는 이 점을 반드시 유의하여 주시기 바랍니다. 다. 경영환경변화 등에 따른 위험 대내외적 경영환경 변화에 따라 당사 실적의 급변동이 있을 경우 투자원금에 대한 손실이 발생할 수 있으므로, 상기 투자위험요소 및 본 증권신고서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 투자자 여러분이 독자적으로 결정해야 함을 유의하시기 바랍니다. 라. 청약 후 추가상장일까지 환금성 제약 및 주가의 급격한 변동에 따른 손실위험 당사의 금번 유상증자로 인한 발행신주는 주금 납입일 이후 코스닥시장에 추가 상장일까지 유동성이 제한될 수 있으며, 추가상장 시점에서 신주발행가액보다 시장의 수준이 낮은 경우 환금성 위험 및 원금 손실의 위험이 있습니다. 본 유상증자 기간동안 주가의 변동이 있을 수 있다는 점, 투자자께서는 유의하여 주시기 바랍니다. 마. 유상증자 일정 변경 가능성에 따른 위험 본 증권신고서는 공시심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 바. 당사의 잘못된 정보 제공 등으로 손해 끼칠 가능성 당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있음을 유의하시기 바랍니다. 사. 유상증자에 따른 주식가치 하락 및 기재정보 의존에 따른 투자위험 금번 유상증자를 통해 취득한 당사의 주식가치가 하락할 수 있으며, 상기 투자위험요소 및 기타 기재된 정보에만 의존하여, 투자판단을 해서는 안되며 투자자 여러분의 독자적인 판단에 의해야 함을 유의하여 주시기 바랍니다. 아. 관리감독기준 위반에 따른 위험 최근 상장 기업에 대한 관리감독기준이 강화되는 추세이며, 향후 당사가 상장기업 관리감독기준을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다. 자. 차입공매도 유상증자 참여 제한 관련 금융위원회의 공매도 제도개선 관련 「자본시장과 금융투자업에 관한 법률 시행령」일부개정에 따라, 주권상장법인이 유상증자 계획을 공시한 이후 발행가격 산정을 위한 대상 거래기간의 마지막날(발행가격 산정 기산일)까지, 해당 기업의 주식을 공매도 한 자는 증자참여를 제한하되, 예외적인 경우에만 증자참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 투자자께서는 이 점 유의하시기 바랍니다. 차. 재무제표 작성 기준일 이후 재무상황 변동에 따른 위험 본 공시서류 상 재무제표에 관한 사항은 2022년 1분기 재무제표 (K-IFRS 기준) 작성기준일 이후의 변동을 반영하지 않았습니다. 당사는 금번 유상증자를 진행하는 과정에서 투자 의사결정에 중대한 영향을 미칠 것으로 판단되는 변동사항을 향후에도 상세하게 반영하여 공시할 예정입니다. 그럼에도 불구하고, 당사가 중요하지 않다고 판단하여 기재 및 서술을 생략한 사항 중 당사의 기업가치에 영향을 미칠 만한 사건이 없다고 단정할 수는 없어 주기적이고 면밀한 검토가 필요합니다. |
2. 모집 또는 매출에 관한 일반사항
| (단위 : 원, 주) |
| 증권의 종류 |
증권수량 | 액면가액 | 모집(매출) 가액 |
모집(매출) 총액 |
모집(매출) 방법 |
|---|---|---|---|---|---|
| 기명식보통주 | 5,600,000 | 100 | 8,660 | 48,496,000,000 | 주주배정후 실권주 일반공모 |
| 인수인 | 증권의 종류 |
인수수량 | 인수금액 | 인수대가 | 인수방법 | |
|---|---|---|---|---|---|---|
| 대표 | 한양증권 | 기명식보통주 | - | - | 인수수수료 : 모집총액의 1.5% 실권수수료 : 잔액인수금액의 12.0% |
잔액인수 |
| 청약기일 | 납입기일 | 청약공고일 | 배정공고일 | 배정기준일 |
|---|---|---|---|---|
| 2022년 08월 02일 ~ 2022년 08월 03일 | 2022년 08월 11일 | 2022년 08월 04일 | 2022년 08월 11일 | 2022년 06월 29일 |
| 청약이 금지되는 공매도 거래 기간 | |
|---|---|
| 시작일 | 종료일 |
| 2022년 06월 11일 | 2022년 07월 28일 |
| 자금의 사용목적 | |
|---|---|
| 구 분 | 금 액 |
| 채무상환자금 | 20,000,000,000 |
| 운영자금 | 27,690,000,000 |
| 발행제비용 | 806,000,000 |
| 신주인수권에 관한 사항 | ||
|---|---|---|
| 행사대상증권 | 행사가격 | 행사기간 |
| - | - | - |
| 매출인에 관한 사항 | ||||
|---|---|---|---|---|
| 보유자 | 회사와의 관계 |
매출전 보유증권수 |
매출증권수 | 매출후 보유증권수 |
| - | - | - | - | - |
| 일반청약자 환매청구권 | ||||
|---|---|---|---|---|
| 부여사유 | 행사가능 투자자 | 부여수량 | 행사기간 | 행사가격 |
| - | - | - | - | - |
| 【주요사항보고서】 | 주요사항보고서(유상증자결정)-2022.06.10 |
| 【기 타】 | 1) (주)카이노스메드 주주배정후 실권주 일반공모 유상증자의 대표주관회사는 한양증권(주)입니다. 2) 금번 유상증자는 잔액인수방식에 의한 것으로 대표주관회사 는 주주배정후 실권주 일반공모 후 최종실권주를 잔액인수하게 되며, 인수방법 및 인수대가에 대한 자세한 내용은 '제1부 I. 5 인수등에 관한 사항'을 참고하여 주시기 바랍니다. 대표주관회사인 한양증권㈜는 투자중개업자로서 타인의 계산으로 증권의 발행ㆍ인수에대한 청약의 권유, 청약, 청약의 승낙 및 자본시장법상의 증권의 인수업무를 수행합니다. 3) 상기 모집가액, 모집총액 및 발행제비용은 예정모집가액 기준으로 산정된 것으로 향후 변경될 수 있습니다. 확정모집가액은 구주주 청약초일 전 제3거래일에 결정될 예정입니다. 또한, 현재 진행중인 주식병합(액면가 100원의 보통주 5주 -> 액면가 500원의 보통주 1주)완료를 감안한 모집예정주식수 및 모집예정가액이며, 2022년 05월 23일 임시주주총회에서 주식병합(액면가 100원의 보통주 5주 -> 액면가 500원의 보통주 1주) 안건이 승인되었으며, 주식병합 신주상장예정일은 2022년 07월 12일입니다. 4) 상기 청약기일은 구주주의 청약기일이며, 일반공모의 청약기일은 2022년 08월 08일 ~ 2022년 08월 09일(2영업일간)입니다. 5) 금융감독원에서 본 증권신고서를 심사하는 과정에서 정정요구 조치를 취할 수 있으며, 정정요구 등에 따라 본 신고서에 기재된 일정이 변경될 수 있습니다. 6) 증권신고서의 효력의 발생은 본 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. 7) 「자본시장과 금융투자업에 관한 법률」제180조의4 및 동법 시행령 제208조의4에 의거, 2022년 06월 11일부터 2022년 07월 28일까지 당사의 주식을 공매도 하거나 공매도 주문을 위탁한 자는 금번 모집에 청약할 수 없으며, 이를 위반하여 주식을 취득할 경우 동법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만, 모집가액의 공정한 가격형성을 저해하지 않는 경우로서 동법 시행령 제208조의4제2항 및 「금융투자업규정」 제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다. 8) 「증권 인수업무 등에 관한 규정」 제9조제2항에 의해 고위험고수익투자신탁 및 벤처기업투자신탁 및 일반청약자에 대하여 배정하여야 할 주식이 50,000주(주식병합 완료 후 액면가 500원 기준) 이하 이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 청약자에게 배정하지 아니하고 자기 계산으로 인수할 수 있습니다. 9) 당사는 2022년 06월 27일 기준일로 하는 액면가 100원의 보통주 5주를 액면가 500원의 보통주 1주로 주식병합을 진행 중이며, 주식병합 완료를 감안한 모집예정주식수 및 모집예정가액 입니다. |
제1부 모집 또는 매출에 관한 사항
I. 모집 또는 매출에 관한 일반사항
1. 공모개요
당사는 이사회 결의를 통하여 「자본시장과 금융투자업에 관한 법률」 제165조의6제2항제1호에 의거 당사와 대표주관회사인 한양증권㈜ 간에 주주배정 후 실권주를 인수하는 계약을 체결하고 사전에 그 실권주를 일반에 공모하기로 하여, 당사 기명식 보통주 5,600,000주를 주주배정 후 실권주 일반공모 방식으로 발행하기로 결정하였으며 동 증권의 개요는 다음과 같습니다.
| (단위 : 주, 원) |
| 증권의 종류 | 증권수량 | 액면가액 | 모집가액 | 모집총액 | 모집방법 |
| 기명식 보통주 | 5,600,000 | 100 | 8,660 | 48,496,000,000 | 주주배정후 실권주 일반공모 |
| 주1) | 이사회 결의일: 2022년 06월 10일 |
| 주2) | 1주의 모집가액 및 모집총액은 예정 발행가액 기준으로 산출한 예정금액입니다. |
| 주3) | 현재 진행중인 주식병합(액면가 100원의 보통주 5주 -> 액면가 500원의 보통주 1주)완료를 감안한 모집예정주식수 및 모집예정가액이며, 2022년 05월 23일 임시주주총회에서 주식병합(액면가 100원의 보통주 5주 -> 액면가 500원의 보통주 1주) 안건이 승인되었으며, 주식병합 신주상장예정일은 2022년 07월 12일입니다. |
| 주4) | 상기 액면가액은 현재 진행 중인 주식병합을 반영하지 않은 가액으로써 주식병합 완료 후 500원으로 변경 될 예정입니다. |
「증권의 발행 및 공시 등에 관한 규정」제5-18조에서 주주배정 증자시 가격산정 절차폐지 및 가격산정의 자율화에 따라 발행가격을 자유롭게 산정할 수 있으나, 시장 혼란 우려 및 기존 관행 등으로 (구)「유가증권의 발행 및 공시등에 관한 규정」 제57조를 일부 준용하여 아래와 같이 발행가액을 산정합니다.
■ 모집예정가액의 산출근거
이사회결의일 전일을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와, 1주일 가중산술평균주가 및 최근일 가중산술평균주가를 산술평균하여 산정한 가액과 최근일 가중산술평균주가 중 낮은 금액을 기준주가로 하여, 아래의 산식에 따라 결정하며 할인율은 25%를 적용합니다. (단, 호가단위 미만은 호가단위로 절상하기로하며, 그 가액이 액면가액 미만인 경우 액면가액으로 합니다.)
| ▶ 모집예정가액 | = | 기준주가 × [ 1 - 할인율(25%) ] |
| ------------------------------------------------ | ||
| 1 + [ 증자비율 × 할인율(25%) ] |
| [ 예정발행가액 산정표] | |
| 기산일 : 2022년 06월 09일 | (단위 : 원, 주) |
| 일자 | 가중산술평균주가 | 거래량 | 거래대금 |
| 2022-06-09 | 2,504 | 240,765 | 602,936,600 |
| 2022-06-08 | 2,478 | 300,368 | 744,370,880 |
| 2022-06-07 | 2,451 | 809,599 | 1,984,688,735 |
| 2022-06-03 | 2,361 | 100,447 | 237,181,415 |
| 2022-06-02 | 2,354 | 86,073 | 202,625,750 |
| 2022-05-31 | 2,385 | 190,771 | 454,954,820 |
| 2022-05-30 | 2,312 | 191,383 | 442,425,730 |
| 2022-05-27 | 2,221 | 107,632 | 239,048,800 |
| 2022-05-26 | 2,195 | 162,549 | 356,751,415 |
| 2022-05-25 | 2,187 | 170,439 | 372,746,905 |
| 2022-05-24 | 2,215 | 413,830 | 916,768,410 |
| 2022-05-23 | 2,349 | 309,092 | 725,965,190 |
| 2022-05-20 | 2,408 | 148,742 | 358,125,680 |
| 2022-05-19 | 2,420 | 150,353 | 363,921,665 |
| 2022-05-18 | 2,468 | 143,020 | 352,999,370 |
| 2022-05-17 | 2,549 | 97,682 | 248,987,025 |
| 2022-05-16 | 2,522 | 101,803 | 256,724,715 |
| 2022-05-13 | 2,485 | 91,523 | 227,477,330 |
| 2022-05-12 | 2,485 | 166,863 | 414,675,405 |
| 2022-05-11 | 2,551 | 144,644 | 369,007,510 |
| 2022-05-10 | 2,529 | 198,685 | 502,503,940 |
| 1개월 가중산술평균주가 (A) | 2,398 | 4,326,263 | 10,374,887,290 |
| 1주일 가중산술평균주가 (B) | 2,460 | 1,451,179 | 3,569,177,630 |
| 기산일 가중산술평균주가 (C) | 2,504 | 240,765 | 602,936,600 |
| A,B,C의 산술평균 (D) | 2,454 | (A+B+C)/3 | |
| 기산일 기준 기준주가 (E) | 2,454 | (C와 D중 낮은가액) | |
| 기준주가 (F) | 12,269.79 | (주1) | |
| 할인율 (G) | 25% | - | |
| 증자비율 (H) | 25.32% | - | |
| 예정발행가액 | 기준주가 × (1-할인율) / 1 + (유상증자비율 × 할인율 ) (단, 호가단위 미만은 호가단위로 절상하기로하며, 그 가액이 액면가액 미만인 경우 액면가액으로 합니다.) |
||
| 주1) 주식병합 (액면가 100원 → 500원) 완료를 감안한 기준주가입니다. |
■ 공모일정 등에 관한 사항
| [주요일정] |
| 날 짜 | 내 용 | 비 고 | |||||||||
|
2022년 06월 10일 |
이사회결의 | - | |||||||||
|
2022년 06월 10일 |
신주발행 및 기준일 공고 | 회사 인터넷 홈페이지 (www.kainosmedicine.com) |
|||||||||
|
2022년 06월 10일 |
증권신고서 제출 | - | |||||||||
| 2022년 06월 24일~ 2022년 07월 11일 |
주식 매매거래 정지 | 주식병합 기준일 전 영업일 ~ 변경상장 전일 | |||||||||
|
2022년 06월 24일 |
1차 발행가액 확정 | 신주배정기준일 3거래일 전 | |||||||||
|
2022년 06월 27일 |
주식병합 기준일 |
- 액면가 100원의 보통주 5주를 액면가 500원의 보통주 1주로 주식병합
|
|||||||||
|
2022년 06월 29일 |
신주배정기준일 | - | |||||||||
|
2022년 07월 11일 |
신주배정통지 | - | |||||||||
| 2022년 07월 12일 | 주식병합 후 신주상장 예정일 | - | |||||||||
|
2022년 07월 12일 |
권리락 | 주2) | |||||||||
|
2022년 07월 18일~ |
신주인수권증서 상장 및 거래기간 | 5영업일 간 거래 | |||||||||
|
2022년 07월 25일 |
신주인수권증서 상장폐지 | 구주주 청약초일 5거래일 이전에 폐지 | |||||||||
|
2022년 07월 28일 |
확정 발행가액 산정 | 구주주 청약초일 3거래일 전 산정 | |||||||||
|
2022년 07월 29일 |
확정 발행가액 공고 | 회사 인터넷 홈페이지 (www.kainosmedicine.com) |
|||||||||
|
2022년 08월 02일~ |
구주주 청약 및 초과청약 | - | |||||||||
|
2022년 08월 04일 |
일반공모 청약 공고 | 회사 인터넷 홈페이지 (www.kainosmedicine.com) 한양증권(주) 홈페이지 (www.hygood.co.kr) |
|||||||||
|
2022년 08월 08일~ |
일반공모 청약 | - | |||||||||
|
2022년 08월 11일 |
환불 및 배정 공고 | 한양증권(주) 홈페이지 (www.hygood.co.kr) |
|||||||||
|
2022년 08월 11일 |
주금 납입 / 환불 | - | |||||||||
|
2022년 08월 24일 |
신주상장 예정일 | - |
| 주1) | 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
| 주2) | 당사는 2022년 05월 23일 개최된 주주총회에서 액면가 100원의 보통주 5주를 액면가 500원의 보통주 1주로 주식병합을 결의 하였습니다. 이에 따라, 2022년 06월 24일부터 07월 11일까지 주식 매매거래 정지 기간으로 설정되었으며, 신주배정기준일이 매매거래 정지 기간 내에 존재하는 바, 본 유상증자에 따른 권리락은 「코스닥시장 업무규정 시행세칙」 제53조제1항2호에 의거하여 매매거래 정지 해제일인 2022년 07월 12일에 조치될 예정입니다. |
2. 공모방법
| [공모방법 : 주주배정후 실권주 일반공모] |
| 모집 대상 | 주 수(%) | 비 고 |
| 구주주 청약 (신주인수권증서 보유자 청약) |
5.600,000주(100%) | ▶ 구주주 청약일 : 2022년 08월 02일 ~ 08월 03일 ▶ 구주 1주당 신주 배정비율 : 1주당 0.05065381주 ▶ 신주배정기준일 : 2022년 06월 29일 ▶ 보유한 신주인수권증서의 수량 한도로 청약가능(구주주에게는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율을 곱한 수량만큼의 신주인수권증서가 배정됨) |
| 초과 청약 | - | ▶ 「자본시장과 금융투자업에 관한 법률」 제165조의6의제2항제2호에 의거 초과청약 ▶ 초과청약비율 : 배정신주(신주인수권증서) 1주당 0.2주 (단, 1주 미만은 절사함) ▶ 신주인수권증서 거래를 통해서 신주인수권증서를 매매시 보유자 기준으로 초과청약 가능 ▶ 구주주청약일에 초과청약 접수 |
| 일반모집 청약 (고위험고수익투자신탁, 벤처기업투자신탁 청약 포함) |
- | ▶ 구주주 청약 후 발생하는 단수주 및 실권주 배정 ▶ 일반모집 청약일 : 2022년 08월 08일 ~ 08월 09일 |
| 합계 | 5,600,000주(100%) |
| 주1) | 본 건 유상증자는 주주배정후 실권주 일반공모 방식으로 진행되며, 구주주 청약결과 발생하는 실권주 및 단수주는 우선적으로 초과청약자에게 배정되며, 이후 실권이 발생할 경우에 대해서는 일반에게 공모합니다. |
| 주2) | 구주주의 청약한도는 신주배정기준일 현재 주주명부에 등재된 주주(이하 "구주주"라 한다)에게 본 주식을 1주당 0.05065381주를 곱하여 산정된 배정주식수(단, 1주 미만은절사함)로 하고, 배정범위 내에서 청약한 수량만큼 배정합니다. 단, 상기 구주주 1주당 배정비율 0.05065381주는 주식병합 이전 발행주식총수(110,565,888주) 기준 비율이며, 주식병합 완료 이후 발행주식총수(22,113,177주) 기준 비율은 0.25326904주 입니다. 단, 신주배정기준일 전 신주 발행, 주식관련사채의 권리행사, 주식매수선택권의 행사, 자기주식 및 자기주식신탁 등의 자기주식 변동, 주식병합 과정에서 발생하는 단수주의 영향으로 인하여 1주당 배정주식수 및 증자비율이 변동될 수 있습니다. |
| 주3) |
신주인수권증서 보유자는 보유한 신주인수권증서 수량의 한도로 증서청약을 할 수 있고, 동 주식수에 초과청약비율(20%)을 곱한 수량을 한도로 초과청약 할 수 있습니다. 단, 1주 미만은 절사합니다. (ii) 신주인수권증서청약 한도주식수 = 보유한 신주인수권증서의 수량 (iii) 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 X 초과청약 비율(20%) (1주 미만 절사) |
| 주4) | 「증권 인수업무 등에 관한 규정」제2조(용어의 정의) 제18항, 제19항, 제20항에 의거 ① "고위험고수익투자신탁" 이란 「조세특례제한법」제91조의15제1항에 따른 투자신탁 등을 말합니다. 다만, 해당 투자신탁 등의 최초 설정일·설립일로부터 배정일까지의 기간이 6개월 미만인 경우에는 같은 법 시행령 제93조제3항제1호 및 같은 조 제7항에도 불구하고 배정일 직전 영업일의 비우량채권과 코넥스 상장주식을 합한 보유비율이 100분의 45 이상이고 이를 포함한 국내 채권의 보유비율이 100분의 60 이상이어야 합니다. ② "벤처기업투자신탁" 이란 「조세특례제한법」제16조제1항제2호의 벤처기업투자신탁(대통령령 제28636호 조세특례제한법 시행령 일부 개정령 시행 이후 설정된 벤처기업투자신탁에 한함)을 말합니다. 다만, 해당 벤처기업투자신탁의 최초 설정일로부터 배정일까지의 기간이 1년 미만인 경우에는 같은 법 시행령 제14조제1항제3호에도 불구하고 배정일 직전 영업일의 벤처기업투자신탁 재산총액에서 같은 호 각 목에 따른 비율의 합계가 100분의 35 이상이어야 합니다. |
| 주5) | 구주주 청약 및 초과청약 결과 발생한 실권주 및 단수주는 대표주관회사가 다음 각호와 같이 일반에게 공모하되, 「증권 인수업무 등에 관한 규정」제9조제2항제6호가목에 따라 고위험고수익투자신탁에 공모주식의 5%를 배정하고,「증권 인수업무 등에 관한 규정」 제9조제2항제6호나목에 따라 벤처기업투자신탁에 공모주식의 30%를 배정합니다. 나머지 일반공모 배정분의 65%에 해당하는 주식은 개인청약자 및 기관투자자에게 구분 없이 배정합니다. 고위험고수익투자신탁에 대한 공모주식의 5%와 벤처기업투자신탁에 대한 공모주식의 30%와 개인투자자 및 기관투자자에 대한 공모주식의 65%에 대한 청약경쟁률과 배정에 있어서는 별도로 산출합니다.다만, 다만, 어느 한 그룹에서 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다. |
| 주6) | 일반공모 청약결과 일반공모 총 청약자의 청약주식수가 공모주식수를 초과하는 경우에는 청약경쟁률에 따라 안분 배정하여 잔여주식이 최소화되도록 합니다. 이후 최종 잔여주식은 대표주관회사가 합리적으로 판단하여 배정합니다. |
| 주7) | 일반공모 청약결과 일반공모 총 청약자의 청약주식수가 공모주식수에 미달하는 경우에는 청약주식수대로 배정하되 잔여주식은 대표주관회사가 자기의 계산으로 인수합니다. 단, 「증권 인수업무 등에 관한 규정」 제9조제2항제7호에 의해 고위험고수익투자신탁, 벤처기업투자신탁, 일반청약자에 대하여 배정하여야 할 주식이 50,000주 이하(주식병합 완료 후 액면가 500원 기준)이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 청약자에게 배정하지 아니하고 자기 계산으로 인수할 수 있습니다. |
| ▶ 주의사항 |
|
「자본시장과 금융투자에 관한 법률」 제180조의4 및 같은 법 시행령 제208조의4제1항에 따라 2022년 06월 11일부터 2022년 07월 28일까지 공매도를 하거나 공매도 주문을 위탁한 자는 금번 모집에 청약할 수 없으며, 이를 위반하여 주식을 취득할 경우 같은 법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만 모집가액의 공정한 가격형성을 저해하지 않는 경우로서 같은 법 시행령 제208조의4제2항 및 「금융투자업규정」 제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다. ※ 예외적으로 모집(매출)에 따른 주식 취득이 허용되는 경우 ① 모집(매출)에 따른 주식 취득이 금지되는 공매도 거래 기간 중에 전체 공매도 주문수량보다 많은 수량의 주식을 가격경쟁에 의한 거래 방식으로 매수한 경우 (매매계약 체결일 기준으로 정규시장의 매매거래시간에 매수한 경우로 한정) ② 한국거래소의 증권시장업무규정 또는 파생상품시장업무규정에서 정한 유동성 공급 및 시장조성 목적을 위해 해당 주식을 공매도하거나 공매도 주문을 위탁한 경우 ③ 동일한 법인 내에서 모집(매출)에 따른 주식 취득 참여가 금지되는 공매도 거래 기간 중 공매도를 하지 않거나 공매도 주문을 위탁하지 않은 독립거래단위*가 모집(매출)에 따른 주식을 취득하는 경우 * 「금융투자업규정」 제6-30조 제5항에 따라 의사결정이 독립적이고 상이한 증권계좌를 사용하는 등의 요건을 갖춘 거래단위 |
| ▶ 구주주 1주당 배정비율 산출근거 |
| 구분 | 내용 |
|---|---|
| A. 보통주식 | 110,565,888주 |
| B. 우선주식 | - |
| C. 발행주식총수 (A + B) | 110,565,888주 |
| D. 자기주식 + 자기주식신탁 | 11,511주 |
| E. 자기주식을 제외한 발행주식총수 (C - D) | 110,554,377주 |
| F. 유상증자 주식수 | 5,600,000주 |
| G. 증자비율 (F / C) | 5.06% |
| H. 우리사주조합 배정 | - |
| I. 구주주 배정 (F - H) | 5,600,000주 |
| J. 구주주 1주당 배정비율 (I / E) | 0.05065381 |
| 주1) | J.구주주 1주당 배정비율 = I. 구주주 배정 (F - H) / E. 자기주식을 제외한 발행주식총수 (C - D) |
| 주2) | 상기 구주주 1주당 배정비율 0.05065381주는 주식병합 이전 발행주식총수 기준 비율이며, 주식병합 완료 이후 발행주식총수 기준 비율은 0.25326904주입니다. 단, 신주배정기준일 전 신주 발행, 주식관련사채의 권리행사, 주식매수선택권의 행사, 자기주식 및 자기주식신탁 등의 자기주식 변동, 주식병합 과정에서 발생하는 단수주의 영향으로 인하여 1주당 배정주식수 및 증자비율이 변동될 수 있습니다. |
3. 공모가격 결정방법
■ 발행가액 산정 방식
「증권의 발행 및 공시 등에 관한 규정」 제5-18조에서 주주배정 증자시 가격산정 절차 폐지 및 가격산정의 자율화에 따라 발행가격을 자유롭게 산정할 수 있으나, 시장 혼란 우려 및 기존 관행 등으로 (구)「유가증권의 발행 및 공시 등에 관한 규정」 제57조를 일부 준용하여 아래와 같이 발행가액을 산정합니다.
(1) 1차 발행가액 : 신주배정기준일 전 제3거래일을 기산일로 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가와, 1주일 가중산술평균주가 및 최근일 가중산술평균주가를 산술평균하여 산정한 가액과 최근일 가중산술평균주가 중 낮은 금액을 기준주가로 하여, 아래의 산식에 따라 결정하며 할인율은 25%를 적용합니다. (단, 호가단위 미만은 호가단위로 절상하기로하며, 그 가액이 액면가액 미만인 경우 액면가액으로 합니다.)
| 기준주가 ×【 1 - 할인율(25%)】 | ||
| ▶ 1차 발행가액 | = | ------------------------------------- |
| 1 + 【증자비율 × 할인율(25%)】 |
(2) 2차 발행가액 : 구주주 청약일 전 제3거래일을 기산일로 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1주일 가중산술평균주가 및 최근일 가중산술평균주가를 산술평균하여 산정한 가액과 최근일 가중산술평균주가 중 낮은 금액을기준주가로하여, 아래의 산식에 따라 결정하며 할인율은 25%를 적용합니다. (단, 호가단위 미만은 호가단위로 절상하기로하며, 그 가액이 액면가액 미만인 경우 액면가액으로 합니다.)
| ▶ 2차 발행가액 = 기준주가 ×【1 - 할인율(25%)】 |
(3) 확정 발행가액 : 확정발행가액은 1차 발행가액과 2차 발행가액 중 낮은 가액으로 합니다. 다만, 「자본시장과 금융투자업에 관한 법률」 제165조의6 및 「증권의 발행 및 공시 등에 관한 규정」 제5-15조의2에 의거하여 1차 발행가액과 2차 발행가액중 낮은 가액이 청약일 전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 할인율 40%를 적용하여 산정한 가액보다 낮은 경우에는 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 할인율 40%를 적용하여 산정한 가액을 확정발행가액으로 합니다. (단, 호가단위 미만은 호가단위로 절상하기로하며,그 가액이 액면가액 미만인 경우 액면가액으로 합니다.)
| ▶ 확정 발행가액 = MAX【MIN(1차 발행가액, 2차 발행가액), 청약일 전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가의 60%】 |
(4) 최종 발행가액은 구주주청약일 초일 전 제3거래일에 결정되어 금융감독원 전자공시시스템에 공시될 예정이며, 회사의 인터넷 홈페이지(www.kainosmedicine.com)에 공고하여 개별통지에 갈음할 예정입니다.
4. 모집 또는 매출절차 등에 관한 사항
가. 모집 또는 매출조건
| (단위 : 주, 원) |
| 항 목 | 내 용 | ||||||||||||||||||||||||||||||||
| 모집 또는 매출주식의 수 | 5,600,000 | ||||||||||||||||||||||||||||||||
| 주당 모집가액 | 예정가액 | 8,660 | |||||||||||||||||||||||||||||||
| 확정가액 | - | ||||||||||||||||||||||||||||||||
| 모집총액 | 예정가액 | 48,496,000,000 | |||||||||||||||||||||||||||||||
| 확정가액 | - | ||||||||||||||||||||||||||||||||
| 청 약 단 위 |
1) 구주주
|
||||||||||||||||||||||||||||||||
| 청약기일 | 구주주 및 초과청약 |
개시일 | 2022년 08월 02일 | ||||||||||||||||||||||||||||||
| 종료일 | 2022년 08월 03일 | ||||||||||||||||||||||||||||||||
| 실권주 일반공모 | 개시일 | 2022년 08월 08일 | |||||||||||||||||||||||||||||||
| 종료일 | 2022년 08월 09일 | ||||||||||||||||||||||||||||||||
| 청약 증거금 | 구주주 | 청약금액의 100% | |||||||||||||||||||||||||||||||
| 초과청약 | 청약금액의 100% | ||||||||||||||||||||||||||||||||
| 일반모집 또는 매출 | 청약금액의 100% | ||||||||||||||||||||||||||||||||
| 납입기일 | 2022년 08월 11일 | ||||||||||||||||||||||||||||||||
| 배당기산일(결산일) | 2022년 01월 01일 | ||||||||||||||||||||||||||||||||
| 주1) | 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. |
| 주2) | 현재 진행중인 주식병합(액면가 100원의 보통주 5주 -> 액면가 500원의 보통주 1주)완료를 감안한 모집예정주식수 및 모집예정가액이며, 2022년 05월 23일 임시주주총회에서 주식병합(액면가 100원의 보통주 5주 -> 액면가 500원의 보통주 1주) 안건이 승인되었으며, 주식병합 신주상장예정일은 2022년 07월 12일입니다. |
| 주3) | 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
나. 모집 또는 매출의 절차
(1) 공고의 일자 및 방법
| 구 분 | 공고일자 | 공고방법 |
| 신주발행(신주배정기준일)의 공고 | 2022년 06월 10일 | 회사 인터넷 홈페이지 (www.kainosmedicine.com) |
| 모집 또는 매출가액 확정의 공고 | 2022년 07월 29일 | 회사 인터넷 홈페이지 (www.kainosmedicine.com) |
| 실권주 일반공모 청약공고 | 2022년 08월 04일 | 회사 인터넷 홈페이지 (www.kainosmedicine.com) 한양증권(주) 홈페이지 (www.hygood.co.kr) |
| 실권주 일반공모 배정 및 환불 공고 | 2022년 08월 11일 | 한양증권(주) 홈페이지 (www.hygood.co.kr) |
(2) 청약방법
1) 구주주 중 주권을 증권회사에 예탁한 주주(기존 '실질주주')는 주권을 예탁한 증권회사의 본ㆍ지점 및 대표주관회사인 한양증권㈜의 본점ㆍ지점에서 보유 증서의 수량 한도내에서 청약할 수 있습니다. 다만, 구주주 중 명의개서대행기관 특별계좌에 주식을 가지고 있는 주주(기존 '명부주주')는 신주배정통지서를 첨부하여 실명확인증표를 제시한 후 "한양증권㈜"의 본점ㆍ지점에서 청약할 수 있습니다. 청약시에는 소정의 청약서 2통에 필요한 사항을 기입하여 청약증거금과 함께 제출하여야 합니다.
| 2019년 09월 16일 전자증권제도가 시행되며, 주권 상장법인의 상장주식은 전자증권 의무전환대상으로 전자증권제도 시행일에 전자증권으로 일괄전환됩니다. 전자증권제도 시행전까지 증권회사에 예탁하고 있는 기존 실질주주 주식은 해당 증권회사 계좌에 전자증권으로 일괄 전환되며, 기존 명부주주가 보유한 주식은 명의개서대행기관이 개설하는 특별계좌에 발행되어 소유자별로 관리됩니다. 금번 유상증자시 신주인수권증서는 전자증권제도 시행일 이후에 발행되고 상장될 예정으로 전자증권으로 발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다. '특별계좌 보유자(기존 '명부주주')'는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후 금번 유상증자 청약 참여또는 신주인수권증서의 매매가 가능합니다. '특별계좌 보유자(기존 '명부주주')'는 신주인수권증서의 '일반 전자등록계좌(증권회사 계좌)'로 이전 없이 대표주관회사인 한양증권㈜의 본점ㆍ지점에서 직접 청약하는 방법으로도 금번 유상증자에 청약이 가능합니다. 다만 신주인수권증서의 매매는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후에만 가능하므로 이 점 유의하시기 바랍니다. |
|
「주식ㆍ사채 등의 전자등록에 관한 법률」 |
| 제29조(특별계좌의 개설 및 관리) ① 발행인이 제25조부터 제27조까지의 규정에 따라 이미 주권등이 발행된 주식등을 전자등록하는 경우 제25조제1항에 따른 신규 전자등록의 신청을 하기 전에 제27조제1항제2호에 따른 통지를 하지 아니하거나 주권등을 제출하지 아니한 주식등의 소유자 또는 질권자를 위하여 명의개서대행회사, 그 밖에 대통령령으로 정하는 기관(이하 이 조에서 "명의개서대행회사등"이라 한다)에 기준일의 직전 영업일을 기준으로 주주명부등에 기재된 주식등의 소유자 또는 질권자를 명의자로 하는 전자등록계좌(이하 "특별계좌"라 한다)를 개설하여야 한다. ② 제1항에 따라 특별계좌가 개설되는 때에 제22조제2항 또는 제23조제2항에 따라 작성되는 전자등록계좌부(이하 이 조에서 "특별계좌부"라 한다)에 전자등록된 주식등에 대해서는 제30조부터 제32조까지의 규정에 따른 전자등록을 할 수 없다. 다만, 다음 각 호의 어느 하나에 해당하는 경우에는 그러하지 아니하다. 1. 해당 특별계좌의 명의자가 아닌 자가 주식등이 특별계좌부에 전자등록되기 전에 이미 주식등의 소유자 또는 질권자가 된 경우에 그 자가 발행인에게 그 주식등에 관한 권리가 표시된 주권등을 제출(주권등을 제출할 수 없는 경우에는 해당 주권등에 대한 제권판결의 정본·등본을 제출하는 것을 말한다. 이하 제2호 및 제3호에서 같다)하고 그 주식등을 제30조에따라 자기 명의의 전자등록계좌로 계좌간 대체의 전자등록을 하려는 경우(해당 주식등에 질권이 설정된 경우에는 다음 각 목의 어느 하나에 해당하는 경우로 한정한다) 가. 해당 주식등에 설정된 질권이 말소된 경우 나. 해당 주식등의 질권자가 그 주식등을 특별계좌 외의 소유자 명의의 다른 전자등록계좌로 이전하는 것에 동의한 경우 2. 해당 특별계좌의 명의자인 소유자가 발행인에게 전자등록된 주식등에 관한 권리가 표시된 주권등을 제출하고 그 주식등을 제30조에 따라 특별계좌 외의 자기 명의의 다른 전자등록계좌로 이전하려는 경우(해당 주식등에 질권이 설정된 경우에는 제1호 각 목의 어느 하나에 해당하는 경우로 한정한다) 3. 해당 특별계좌의 명의자인 질권자가 발행인에게 주권등을 제출하고 그 주식등을 제30조에 따라 특별계좌 외의 자기 명의의 전자등록계좌로 이전하려는 경우 4. 그 밖에 특별계좌에 전자등록된 주식등의 권리자의 이익을 해칠 우려가 없는 경우로서 대통령령으로 정하는 경우 ③ 누구든지 주식등을 특별계좌로 이전하기 위하여 제30조에 따른 계좌간 대체의 전자등록을 신청할 수 없다. 다만, 제1항에 따라 특별계좌를 개설한 발행인이 대통령령으로 정하는 사유에 따라 신청을 한 경우에는 그러하지 아니하다. ④ 명의개서대행회사등이 발행인을 대행하여 제1항에 따라 특별계좌를 개설하는 경우에는 「금융실명거래 및 비밀보장에 관한 법률」 제3조에도 불구하고 특별계좌부에 소유자 또는 질권자로 전자등록될 자의 실지명의를 확인하지 아니할 수 있다. |
2) 신주인수권증서 청약을 한 자에 한하여 신주인수권증서 청약 한도주식수의 20%를 추가로 청약할 수 있습니다. 이때 신주인수권증서 청약 한도주식수의 20%에 해당하는 주식 중 소수점 이하인 주식은 청약할 수 없습니다.
3) 고위험고수익투자신탁, 벤처기업투자신탁 및 일반청약자는 「금융실명거래 및 비밀보장에 관한 법률」의 규정에 의한 실명자이어야 하며, 청약사무 취급처에 실명확인증표를 제시하고 청약합니다. 고위험고수익투자신탁, 벤처기업투자신탁 및 일반청약자의 청약 시, 한 개의 청약처에서 이중청약은 불가능하며, 집합투자기구 중 운용주체가 다른 집합투자기구를 제외한 청약자의 한개 청약처에 대한 복수청약이 불가능합니다. 또한 고위험고수익투자신탁 및 벤처기업투자신탁은 청약 시, 청약사무 취급처에 「증권 인수업무 등에 관한 규정」 제2조제18호 내지 제20호 중 해당 요건을 충족하고, 제9조제4항에 해당하지 않음을(벤처기업투자신탁이 사모의 방법으로 설정된 경우, 설정일로부터 1년 6개월 이상의 기간동안 환매를 금지하고 있음을 포함하여) 확약하는 서류 및 자산총액이 기재되어 있는서류를 함께 제출하여야 합니다.
4) 1인당 청약한도를 초과하는 청약은 초과되는 부분에 대하여는 무효로 하며, 청약사무 취급처는 그 차액을 납입일까지 당해 청약자에게 반환하며, 받은 날부터의 이자는 지급하지 않습니다.
5) 기타
① 일반공모 배정을 함에 있어 이중청약이 있는 경우에는 그 청약자의 청약 전부를 청약하지 아니한 것으로 봅니다. 단, 신주인수권증서 보유자가 보유한 신주인수권증서 수량에 따라 청약을 한 후 일반공모에 참여하는 경우에는 금지되는 이중청약이 있는 경우로 보지 않습니다.
② 1인당 청약한도를 초과하는 청약부분에 대하여는 청약이 없는 것으로 합니다.
③ 청약자는 「금융실명거래 및 비밀보장에 관한 법률」에 의거 실지 명의에 의해 청약해야 합니다.
④ 「자본시장과 금융투자업에 관한 법률」 제180조의4 및 동법 시행령 제208조의4제1항에 따라 2022년 06월 11일부터 2022년 07월 28일까지 공매도를 하거나 공매도 주문을 위탁한 자는 금번 모집에 청약할 수 없으며, 이를 위반하여 주식을 취득할 경우 동법 제429조의3제2항에 따라 과징금이 부과될 수 있습니다. 다만 모집가액의 공정한 가격형성을 저해하지 않는 경우로서 동법 시행령 제208조의4제2항 및 「금융투자업규정」 제6-34조에 해당할 경우에는 예외적으로 주식 취득이 허용됩니다.
|
※ 예외적으로 모집(매출)에 따른 주식 취득이 허용되는 경우 ① 모집(매출)에 따른 주식 취득이 금지되는 공매도 거래 기간 중에 전체 공매도 주문수량보다 많은 수량의 주식을 가격경쟁에 의한 거래 방식으로 매수한 경우 (매매계약 체결일 기준으로 정규시장의 매매거래시간에 매수한 경우로 한정) ② 한국거래소의 증권시장업무규정 또는 파생상품시장업무규정에서 정한 유동성 공급 및 시장조성 목적을 위해 해당 주식을 공매도하거나 공매도 주문을 위탁한 경우 ③ 동일한 법인 내에서 모집(매출)에 따른 주식 취득 참여가 금지되는 공매도 거래 기간 중 공매도를 하지 않거나 공매도 주문을 위탁하지 않은 독립거래단위*가 모집(매출)에 따른 주식을 취득하는 경우 * 금융투자업규정 제6-30조 제5항에 따라 의사결정이 독립적이고 상이한 증권계좌를 사용하는 등의 요건을 갖춘 거래단위 |
(3) 청약취급처
| 청약대상자 | 청약취급처 | 청약일 | |
| 구주주 (신주인수권증서 보유자) |
특별계좌 보유자 (기존 '명부주주') |
한양증권㈜ 본ㆍ지점 | 2022년 08월 02일~ 2022년 08월 03일 |
| 일반주주 (기존 '실질주주') |
1) 주주확정일 현재 주식을 예탁하고 있는 해당 증권회사 본ㆍ지점 2) 한양증권㈜ 본ㆍ지점 |
||
| 일반공모청약 (고위험고수익투자신탁, 벤처기업투자신탁 청약 포함) |
한양증권㈜ 본ㆍ지점 | 2022년 08월 08일~ 2022년 08월 09일 |
|
(4) 청약결과 배정방법
1) 구주주 청약 : 신주배정기준일 현재 주주명부에 등재된 주주(이하 "구주주"라 한다)에게 본 주식을 1주당 0.05065381주를 곱하여 산정된 배정주식수(단, 1주 미만은절사함)로 하고, 배정범위 내에서 청약한 수량만큼 배정합니다. 단, 상기 구주주 1주당 배정비율 0.05065381주는 주식병합 이전 발행주식총수(110,565,888주) 기준 비율이며, 주식병합 완료 이후 발행주식총수(22,113,177주) 기준 비율은 0.25326904주입니다. 단, 신주배정기준일 전 신주 발행, 주식관련사채의 권리행사, 주식매수선택권의 행사, 자기주식 및 자기주식신탁 등의 자기주식 변동, 주식병합 과정에서 발생하는 단수주의 영향으로 인하여 1주당 배정주식수 및 증자비율이 변동될 수 있습니다.
2) 초과청약 : 구주주(신주인수권증서 보유자) 청약 이후 발생한 실권주가 있는 경우,실권주를 구주주(신주인수권증서 보유자)가 초과청약(초과청약비율 : 배정 신주 1주당 0.2주)한 주식수에 비례하여 배정하며, 1주 미만의 주식은 절사하여 배정하지 않습니다.(단, 초과청약 주식수가 실권주에 미달한 경우 100% 배정)
3) 일반공모 청약
① 상기 구주주 청약 및 초과청약 결과 발생한 실권주 및 단수주는 대표주관회사가 다음 각호와 같이 일반에게 공모하되, 「증권 인수업무 등에 관한 규정」제9조제2항제6호가목에 따라 고위험고수익투자신탁에 공모주식의 5%를 배정하고,「증권 인수업무 등에 관한 규정」제9조제2항제6호나목에 따라 벤처기업투자신탁에 공모주식의 30%를 배정합니다. 나머지 65%에 해당하는 주식은 개인청약자 및 기관투자자(집합투자업자)에게 구분 없이 배정합니다. 고위험고수익투자신탁에 대한 공모주식의 5%와 벤처기업투자신탁에 대한 공모주식의 30%와 개인투자자 및 기관투자자에 대한 공모주식의 65%에 대한 청약경쟁률과 배정에 있어서는 별도로 산출 및 배정합니다. 다만, 어느 한 그룹에서 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다.
② 일반공모 청약결과 일반공모 총 청약자의 청약주식수가 공모주식수를 초과하는 경우에는 청약경쟁률에 따라 안분 배정하여 잔여주식이 최소화되도록 합니다. 이후 최종 잔여주식은 대표주관회사가 합리적으로 판단하여 배정합니다.
③ 일반공모 청약결과 일반공모 총 청약자의 청약주식수가 공모주식수에 미달하는 경우에는 청약주식수대로 배정하되 잔여주식은 대표주관회사가 자기의 계산으로 인수합니다. 단, 대표주관회사는「증권 인수업무 등에 관한 규정」 제9조제2항제7호에 의해 배정하여야 할 주식이 50,000주 이하(주식병합 완료 후 액면가 500원 기준)이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 이를 청약자에게 배정하지 아니하고 자기 계산으로 인수할 수 있습니다.
(5) 투자설명서 교부에 관한 사항
- 「자본시장과 금융투자업에 관한 법률」 제124조에 의거, 본 주식의 청약에 대한 투자설명서 교부 의무는 ㈜카이노스메드, 대표주관회사가 부담하며, 금번 유상증자의 청약에 참여하시는 투자자께서는 투자설명서를 의무적으로 교부받으셔야 합니다.
- 금번 유상증자에 청약하고자 하는 투자자께서는 (「자본시장과 금융투자업에 관한법률」 제9조제5항에 규정된 전문투자자 및 「자본시장과 금융투자업에 관한 법률 시행령」 제132조에 따라 투자설명서의 교부가 면제되는 자 제외) 청약하시기 전 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
- 투자설명서 수령거부 의사 표시는 서면, 전화·전신·모사전송, 전자우편 및 이와비슷한 전자통신으로만 하여야 합니다.
1) 투자설명서 교부 방법 및 일시
|
구분 |
교부방법 |
교부일시 |
|
구주주 청약자 |
1),2),3)을 병행 |
- |
| 1) 우편 송부 | 구주주(신주인수권증서) 청약초일 전까지 | |
| 2) 한양증권㈜의 본ㆍ지점에서 교부 | 구주주(신주인수권증서) 청약종료일까지 | |
| 3) 한양증권㈜의 HTS에서 교부 | ||
|
일반 청약자 |
1),2)를 병행 |
- |
| 1) 한양증권㈜의 본ㆍ지점에서 교부 | 일반공모 청약종료일까지 | |
| 2) 한양증권㈜의 홈페이지나 HTS, MTS에서 교부 |
| 주) | 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다. |
2) 확인절차
① 우편을 통한 투자설명서 수령시(구주주 청약의 경우)
- 청약하시기 위해 지점을 방문하셨을 경우, 직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
- HTS를 통한 청약을 원하시는 경우, 청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
- 주주배정 유상증자 경우 유선청약이 가능합니다. 유선상으로 신분확인을 하신 후, 투자설명서 교부 확인을 해주시고 청약을 진행하여 주시기 바랍니다.
② 지점 방문을 통한 투자설명서 수령시
직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
③ 홈페이지 또는 HTS, MTS를 통한 교부
청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
3) 기타
① 금번 유상증자의 경우, 본 증권신고서의 효력발생 이후 주주명부상 주주분들에게 투자설명서를 우편으로 발송할 예정입니다. 우편의 반송 등에 의한 사유로 교부를 받지 못하신 투자자께서는, 지점방문을 통해 인쇄물을 받으실 수 있습니다. 다만, 전자문서의 형태로 교부받으실 경우, 「자본시장과 금융투자업에 관한 법률」 제124조제1항 각호의 요건을 모두 충족해야만 청약이 가능합니다.
② 구주주 청약시 한양증권㈜ 이외의 증권회사를 이용한 청약 방법
해당 증권회사의 청약방법 및 규정에 의해 청약을 진행하시기 바랍니다. 이 경우에도, 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
※ 투자설명서 교부를 받지 않거나, 수령거부의사를 서면 등의 방법으로 표시하지 않을 경우, 본 유상증자의 청약에 참여할 수 없습니다.
|
「자본시장과 금융투자업에 관한 법률」 1. 다음 각 목의 어느 하나에 해당하는 전문가 가. 전문투자자 나. 삭제 <2016. 6. 28.> 다. 「공인회계사법」에 따른 회계법인 라. 신용평가회사(법 제335조의3에 따라 신용평가업인가를 받은 자를 말한다. 이하 같다) 마. 발행인에게 회계, 자문 등의 용역을 제공하고 있는 공인회계사ㆍ감정인ㆍ변호사ㆍ변리사ㆍ세무사 등 공인된 자격증을 가지고 있는 자 바. 그 밖에 발행인의 재무상황이나 사업내용 등을 잘 알 수 있는 전문가로서 금융위원회가 정하여 고시하는 자 2. 다음 각 목의 어느 하나에 해당하는 연고자 가. 발행인의 최대주주[「금융회사의 지배구조에 관한 법률」 제2조제6호가목에 따른 최대주주를 말한다. 이 경우 "금융회사"는 "법인"으로 보고, "발행주식(출자지분을 포함한다.이하 같다)"은 "발행주식"으로 본다. 이하 같다]와 발행주식 총수의 100분의 5 이상을 소유한 주주 나. 발행인의 임원(「상법」 제401조의2제1항 각 호의 자를 포함한다. 이하 이 호에서 같다) 및 「근로복지기본법」에 따른 우리사주조합원 다. 발행인의 계열회사와 그 임원 라. 발행인이 주권비상장법인(주권을 모집하거나 매출한 실적이 있는 법인은 제외한다)인 경우에는 그 주주 마. 외국 법령에 따라 설립된 외국 기업인 발행인이 종업원의 복지증진을 위한 주식매수제도 등에 따라 국내 계열회사의 임직원에게 해당 외국 기업의 주식을 매각하는 경우에는그 국내 계열회사의 임직원 바. 발행인이 설립 중인 회사인 경우에는 그 발기인 사. 그 밖에 발행인의 재무상황이나 사업내용 등을 잘 알 수 있는 연고자로서 금융위원회가 정하여 고시하는 자
|
(6) 주권교부에 관한 사항
1) 주권유통개시일: 2022년 08월 24일 (2019년 09월 16일 전자증권제도가 시행됨에 따라 실물 주권의 교부 없이 각 주주의 보유 증권계좌로 상장일에 주식이 등록발행되어 입고되며, 상장일부터 유통이 가능합니다. 단, 유관기관과의 업무 협의 과정에서 상기 일정은 변경될 수 있음을 유의하시기 바랍니다.)
(7) 청약증거금의 대체 및 반환 등에 관한 사항
청약증거금은 청약금액의 100%로 하고, 주금납입기일에 주금납입금으로 대체하며, 청약증거금에 대해서는 무이자로 합니다.
(8) 주금납입장소 : 우리은행 여의도금융센터
다. 신주인수권증서에 관한 사항
| 신주배정기준일 | 신주인수권증서의 매매 금융투자업자 | |
| 회사명 | 회사고유번호 | |
| 2022년 06월 29일 | 한양증권㈜ | 00162416 |
(1) 금번과 같이 주주배정방식의 유상증자를 실시할 때, 주주가 소유하고 있는 주식수 비율대로 신주를 인수할 권리인 신주인수권에 대하여 당사는 「자본시장과 금융투자업에 관한 법률」 제165조의6제3항 및 「증권의 발행 및 공시 등에 관한 규정」제5-19조에 의거하여 주주에게 신주인수권증서를 발행합니다.
(2) 금번 유상증자시 신주인수권증서는 전자증권제도 시행일(2019년 09월 16일) 이후에 발행되고 상장될 예정으로 전자증권으로 발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여 배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다.
(3) 신주인수권증서 매매의 중개를 할 증권회사는 한양증권㈜로 합니다.
(4) 신주인수권증서 매매 등
1) 금번 유상증자시 신주인수권증서는 전자증권제도 시행 이후에 발행되고 상장될 예정으로 실물은 발행 되지 않고 전자증권으로 등록발행됩니다. 주주가 증권사 계좌에 보유하고 있는 주식(기존 '실질주주' 보유주식)에 대하여 배정되는 신주인수권증서는 해당 증권사 계좌에 발행되어 입고되며, 명의개서대행기관 특별계좌에 관리되는 주식(기존 '명부주주' 보유주식)에 대하여 배정되는 신주인수권증서는 명의개서대행기관 내 특별계좌에 소유자별로 발행 처리됩니다.
2) 신주인수권증서를 매매하고자 하는 주주는 신주인수권증서를 예탁하고 있는 증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자계좌를 통하여 신주인수권증서를 매수한 자는 그 수량(초과청약이 있는 경우 초과청약 가능수량이 합산된 수량)만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
(5) 신주인수권증서를 양수한 투자자의 청약방법
신주인수권증서를 증권회사에 예탁하고 있는 양수인은 당해 증권회사 점포 및 한양증권㈜의 본점 및 지점을 통해 해당 신주인수권증서에 기재되어 있는 수량(초과청약이 있는 경우 초과청약 가능수량이 합산된 수량)만큼 청약할 수 있으며 청약 기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
(6) 신주인수권증서의 상장
당사는 금번 주주배정후 실권주 일반공모 유상증자 관련 신주인수권증서의 상장을 한국거래소에 신청할 예정입니다. 동 신주인수권증서가 상장될 경우 상장기간은 2022년 07월 18일부터 2022년 07월 22일까지 5거래일간으로 예정하고 있으며, 동 기간중 상장된 신주인수권증서를 한국거래소에서 매매할 수 있습니다. 동 신주인수권증서는 2022년 07월 25일에 상장폐지될 예정입니다.(「코스닥시장 상장규정」 제16조의3에 근거하여 5거래일 이상 상장되어야 하며, 동 규정 제44조의3에 따라 신주청약개시일 5거래일 전에 상장폐지되어야 함)
(7) 신주인수권증서의 거래 관련 추가사항
당사는 금번 유상증자의 신주인수권증서를 상장신청할 예정인 바, 현재까지 관계기관과의 협의를 통해 확인된 신주인수권증서 상장시의 제반 거래관련 사항은 다음과 같습니다.
1) 상장방식 : 전자등록발행된 신주인수권증서 전부를 상장합니다.
2) 실질주주의 신주인수권증서 거래
| 구분 | 상장거래방식 | 계좌대체 거래방식 |
| 방법 | 주주의 신주인수권증서를 전자등록발행하여 상장합니다. 상장된 신주인수권증서를 장내거래를 통하여 매수하여 증권사 계좌에 보유한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. 주주의 신주인수권증서는 전자등록발행되므로 실물 증서는 발행되지 않습니다. | 신주인수권증서를 매매하고자 하는 기존 실질주주는 위탁증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의계좌대체를 청구합니다. 위탁자계좌를 통하여신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. |
| 기간 | 2022년 07월 18일부터 2022년 07월 22일까지(5거래일간) 거래 | 2022년 07월 11일(예정)부터 2022년 07월 26일까지 거래 |
| 주1) | 상장거래 : 2022년 07월 18일부터 2022년 07월 22일까지(5영업일간) 거래 가능합니다. |
| 주2) | 계좌대체거래 : 2022년 07월 11일(예정)부터 2022년 07월 26일까지 거래 가능 합니다. * 신주인수권증서 상장거래의 결제일인 2022년 07월 26일까지 계좌대체(장외거래) 가능하며, 동일 이후부터는 신주인수권증서의 청약권리 명세를 확정하므로 신주인수권증서의 계좌대체(장외거래)가 제한됩니다. |
| 주3) | 신주인수권증서는 전자등록발행되므로 실물은 발행되지 않습니다. |
3) 특별계좌 소유주(기존 '명부주주')의 신주인수권증서 거래
① '특별계좌 보유자(기존 '명부주주')'는 명의개서대행기관에 '특별계좌'에서 '일반전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후 금번 유상증자 청약 참여 또는 신주인수권증서의 매매가 가능합니다.
② '특별계좌 보유자(기존 '명부주주')'는 신주인수권증서의 '일반 전자등록계좌(증권회사 계좌)'로 이전 없이 대표주관회사인 한양증권㈜의 본ㆍ지점에서 직접 청약하는 방법으로도 금번 유상증자에 청약이 가능합니다. 다만 신주인수권증서의 매매는 명의개서대행기관에 '특별계좌'에서 '일반 전자등록계좌(증권회사 계좌)'로 신주인수권증서를 이전 신청한 후에만 가능하므로 이 점 유의하시기 바랍니다.
라. 주권교부일 이전의 주식양도의 효력에 관한 사항
주식교부일 이전의 주식의 양도는 발행회사에 대하여 효력이 없습니다. 다만, 「자본시장과 금융투자업에 관한 법률」 제311조제4항에 의거 주권발행전에 증권시장에서의 매매거래를 투자자계좌부 또는 예탁자계좌부상 계좌 간 대체의 방법으로 결제하는 경우에는 「상법」 제335조제3항에 불구하고 발행인에 대하여 그 효력이 있습니다.
|
※ 「자본시장과 금융투자업에관한 법률」 제311조 (계좌부기재의 효력) ① 투자자계좌부와 예탁자계좌부에 기재된 자는 각각 그 증권등을 점유하는 것으로 본다. ② 투자자계좌부 또는 예탁자계좌부에 증권등의 양도를 목적으로 계좌 간 대체의 기재를 하거나 질권설정을 목적으로 질물(質物)인 뜻과 질권자를 기재한 경우에는 증권등의 교부가 있었던 것으로 본다. ③ 예탁증권등의 신탁은 예탁자계좌부 또는 투자자계좌부에 신탁재산인 뜻을 기재함으로써 제삼자에게 대항할 수 있다. <개정 2011. 7. 25.> ④ 삭제 <2016. 3. 22.> |
마. 기타 모집 또는 매출에 관한 사항
(1) 청약자가 「금융실명거래 및 비밀보장에 관한 법률」에 의거 실명에 의하여 청약하지 아니한 경우에는 이를 무효처리합니다.
(2) 본 증권신고서는 공시 심사 과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용의 변경시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있으므로 투자자 여러분께서는 투자시 이러한 점을 감안하시기 바랍니다.
(3) 「자본시장과 금융투자업에 관한 법률」 제120조제3항에 의거 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부에서 그 증권의 가치를 보증 또는 승인하는 효력을 가지는 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다.
(4) 금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서, 반기보고서, 분기보고서 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있사오니 투자의사를 결정하시는 데 참조하시기 바랍니다.
5. 인수 등에 관한 사항
| [인수방법: 잔액인수] |
| 인수인 | 인수주식 종류 및 수 | 인수대가 | |
| 대표 | 한양증권㈜ | 인수주식의 종류: 기명식 보통주식 인수주식의 수: 최종 실권주 |
인수수수료 : 모집총액의 1.5% 실권수수료 : 잔액인수금액의 12.0% |
| 주1) | 최종 실권주 : 구주주청약 및 일반공모 후 발생한 배정잔여주 또는 청약미달주식 |
| 주2) | 모집총액 : 최종 발행가액 X 총 발행주식수 |
II. 증권의 주요 권리내용
당사가 금번 주주배정후 실권주 일반공모 유상증자를 통하여 발행할 증권은 기명식 보통주이며, 동 증권의 주요 권리내용은 다음과 같습니다.
1. 주식의 발행 및 배정에 관한 사항
제5조 (발행예정 주식의 총수)
당 회사가 발행할 주식의 총수는 300,000,000주로 한다.
제6조 (1주의 금액)
당 회사가 발행하는 주식 1주의 금액은 500원으로 한다.
제7조 (설립시에 발행하는 주식의 총수)
회사는 설립시에 901,000주(1주의 금액 100원 기준)의 주식을 발행하기로 한다.
제8조 (주식 등의 전자 등록)
1. 회사가 발행하는 주권은 기명식으로 한다.
2. 회사는 주식·사채 등의 전자등록에 관한 법률 제2조 제1호에 따른 주식 등을 발행하는 경우에는 전자등록기관의 전자등록계좌부에 주식 등을 전자등록하여야 한다.
제8조의 2 (주식의 종류)
1. 회사가 발행할 주식은 보통주식과 종류주식으로 한다.
2. 회사가 발행하는 종류주식은 이익배당 또는 잔여재산분배에 관한 우선주식, 의결권 배제 또는 제한에 관한 주식, 상환주식, 전환주식 및 이들의 전부 또는 일부를 혼합한 주식으로 한다.
3. 회사가 발행할 종류주식의 의결권은 1주당 1의결권을 갖는 것으로 하며, 그 발행 한도는 발행주식 총수의 4분의 1로 한다
4. 종류주식에 대한 최저배당률은 액면금액의 연 1%로 하며, 연 10% 이내에서 발행시에 이사회가 우선주식 배당률을 정한다.
5. 종류주식에 대하여 제4항에 따른 배당을 하고 보통주식에 대하여 종류주식의 배당률과 동률의 배당을 한 후, 잔여배당가능이익이 있으면 보통주식과 종류주식에 대하여 동등한 비율로 배당한다.
6. 종류주식에 대하여 제4항에 따른 배당을 하지 못한 사업연도가 있는 경우에는 미배당분을 누적하여 다음 사업연도의 배당시에 우선하여 배당한다.
7. 회사가 유상증자 또는 무상증자를 실시하는 경우 종류주식에 대한 신주의 배정은 유상증자의 경우에는 회사가 유상증자로 발행하는 주식으로, 무상증자의 경우에는 동일한 종류의 우선주식으로 한다.
8. 종류주식의 존속기간은 발행일로부터 10년 이하로 하고 이 기간 만료와 동시에 보통주식으로 전환된다. 다만, 위 기간 중에 소정의 배당을 하지 못한 경우에는 소정의 배당이 완료될 때까지 그 기간은 연장된다.
9. 제6항의 규정에 의해 발행되는 신주에 대한 이익의 배당에 관하여는 제11조의 규정을 준용한다.
10. 종류주식의 내용 중 본 정관에서 달리 정하지 아니한 사항은 발행 시에 이사회가 결정한다.
제9조 (신주인수권)
1. 당회사의 신주발행에 있어서 그가 소유한 주식의 수에 비례하여 신주의 배정을 받을 권리를 갖는다.
2. 1항의 규정에도 불구하고 다음 각 호의 경우에는 이사회의 결의로 주주 이외의 자에게 신주를 배정할 수 있다.
① 발행주식총수의 100분의 50을 초과하지 않는 범위 내에서 자본시장과 금융투자업에 관한 법률에 따라 일반공모증자 방식으로 신주를 발행하는 경우
② 발행하는 주식총수의 100분의 20 범위 내에서 우리사주조합원에게 주식을 우선 배정하는 경우
③ 상법에 따른 주식매수선택권의 행사로 인하여 신주를 발행하는 경우
④ 자본시장과 금융투자업에 관한 법률에 의하여 주식예탁증서(DR) 발행에 따라 신주를 발행하는 경우
⑤ 경영상 필요로 외국인투자촉진법에 의한 외국인 투자를 위하여 신주를 발행하는 경우
⑥ 발행주식총수의 100분의 20을 초과하지 않는 범위 내에서 회사가 첨단기술의 도입, 사업다각화, 해외진출, 원활한 자금조달 등 전략적 제휴를 위하여 상대회사에 신주를 발행하는 경우
⑦ 발행주식총수의 100분의 20을 초과하지 않는 범위내에서 긴급한 자금조달을 위하여 국내외 금융기관 또는 기관투자자에게 신주를 발행하는 겨우
⑧ 발행주식총수의 100분의 20을 초과하지 않는 범위내에서 사업상 중요한 기술도입, 연구개발, 생산?판매?자본제휴를 위하여 그 상대방에게 신주를 발행하는 경우
⑨ 주권을 유가증권 시장 또는 코스닥 시장에 상장하기 위하여 신주를 모집하거나 인수인에게 인수하게 하는 경우
⑩ 증권 인수업무 등에 관한 규정 제10조의2(신주인수권)에 의거하여 신주를 발행하는 경우
⑪ 중소기업창업지원법 및 벤처기업육성에 관한 특별법에 의하여 조성된 창업지원 기금의 관리기관이 출자하기 위하여 신주를 발행하는 경우
3. 제2항 각 호 중 어느 하나의 규정에 의해 신주를 발행할 경우 발행할 주식의 종류와 수 및 발행가격 등은 이사회의 결의로 정한다.
4. 주주가 신주인수권의 일부 또는 전부를 포기하거나 상실한 경우와 신주발행에 있어서 단주가 발생한 경우에는 그 처리방법은 이사회의 결의로 정한다.
5. 제2항에 따라 주주 외의 자에게 신주를 배정하는 경우 회사는 상법 제416조제1호, 제2호, 제2호의2, 제3호 및 제4호에서 정하는 사항을 그 납입기일의 2주 전까지 주주에게 통지하거나 공고하여야 한다.
2. 배당에 관한 사항
제11조 (신주의 배당기산일)
당 회사가 유무상증자 및 주식배당에 의하여 신주를 발행한 경우, 신주에 대한 이익의 배당에 관하여는 그 신주를 발행한 때가 속하는 회계년도의 직전 회계년도말에 발행된 것으로 본다.
제57조 (이익배당)
1. 이익배당은 금전 또는 금전 외의 재산으로 할 수 있다. 그러나 주식에 의한 배당은 이익배당총액의 2분의 1에 상당하는 금액을 초과하지 못한다.
2. 전항의 배당은 매결산기말 현재의 주주명부에 기재된 주주 또는 등록된 질권자에게 지급한다.
3. 이익의 배당을 주식으로 하는 경우 회사가 수종의 주식을 발행한 때에는 주주총회의 결의로 그와 다른 종류의 주식으로도 할 수 있다.
3. 의결권에 관한 사항
제27조 (주주의 의결권)
1. 주주의 의결권은 1주마다 1개로 한다.
2. 회사가 가진 자기주식은 의결권이 없다.
제28조 (상호주에 대한 의결권 제한)
당 회사, 모회사 및 자회사 또는 자회사가 다른 회사의 발행주식총수의 10분의 1을 초과하는 주식을 가지고 있는 경우 그 다른 회사가 가지고 있는 당 회사의 주식은 의결권이 없다.
제29조 (의결권의 불통일행사)
1. 2이상의 의결권을 가지고 있는 주주가 의결권의 불통일행사를 하고자 할 때에는 회의일의 3일전 회사에 대하여 서면 또는 전자문서로 그 뜻과 이유를 통지하여야 한다.
2. 회사는 주주의 의결권의 불통일행사를 거부할 수 있다. 그러나 주주가 주식의 신탁을 인수하였거나 기타 타인을 위하여 주식을 가지고 있는 경우에는 그러하지 아니하다.
제30조 (의결권의 대리행사)
1. 주주는 대리인으로 하여금 그 의결권을 행사하게 할 수 있다.
2. 제1항의 대리인은 주주총회 개시일전에 그 대리권을 증명하는 서면(위임장)을 회사에 제출하여야 한다.
제32조 (서면에 의한 의결권의 행사)
1. 주주는 총회에 출석하지 아니하고 서면에 의하여 의결권을 행사할 수 있다.
2. 회사는 제1항의 경우 총회의 소집통지서에 주주의 의결권 행사에 필요한 서면과 참고자 료를 첨부하여야 한다.
3. 서면에 의하여 의결권을 행사하고자 하는 주주는 제2항의 서면에 필요한 사항을 기재하 여, 회의일의 전일까지 회사에 제출하여야 한다.
III. 투자위험요소
| [투자자 유의사항] |
|---|
| ■ 금번 당사의 유상증자에 참여하고자 하는 투자자분들께서는 투자결정을 하기 전에 본 공시서류의 다른 기재 부분 뿐만 아니라, 특히 아래 기재된 투자위험요소를 주의 깊게 검토한 후 이를 고려하여, 최종적인 투자 판단을 해야 합니다. ■ 당사는 본 공시서류를 통하여 청약 전에 투자자께서 숙지하셔야 하는 부분에 대하여 성실히 기재하고자 노력하고 있습니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 아래 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수 없으므로, 투자자는 아래 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안 되며, 투자자 자신의 독자적이고도 세밀한 판단에 의해야 합니다. 따라서 본 공시서류에 기재된 사항은 투자 판단 시 참고 자료로 활용하실 것을 권고 드리며, 투자자의 투자 판단에 대한 결과는 투자자 본인에게 귀속됩니다. ■ 만일, 아래 기재한 투자위험요소가 실제로 발생하는 경우, 당사의 사업, 재무상태, 기타 영업활동에 중대한 부정적 영향을 미칠 수 있으며, 이에 따라 투자자가 금번 공모과정에서 취득하게 되는 당사 주식의 시장가격이 하락하여 투자금액의 일부 또는 전부를 잃게 될 수도 있음을 유의하시기 바랍니다. ■ 2009년 02월 04일 부로 시행된 「자본시장과 금융투자업에 관한 법률」제124조에 의거 누구든지 증권신고의 효력이 발생한 증권을 취득하고자 하는 자(전문투자자, 그 밖에 대통령령으로 정하는 자를 제외함)에게 적합한 투자설명서를 미리 교부하지 아니하면 그 증권을 취득하게 하거나 매도하여서는 안됩니다. 다만, 「자본시장과 금융투자업에 관한 법률 시행령」제132조에 의거하여 투자설명서를 받기를 거부한다는 의사를 서면으로 표시한 자는 투자설명서의 교부없이 청약이 가능합니다. ■ 본 공시서류의 기재사항이 진실 또는 정확하다는 것을 정부가 인정하거나, 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자의 책임은 전적으로 투자자에게 귀속됩니다. |
|
[주요 용어 정리] |
|
용어 |
설명 |
|---|---|
|
저분자유기화합물(small organic molecule) |
약학 분야에서 저분자 화합물(Small Molecule) 단백질이나 핵산과 같은 생체고분자에 결합하여 생체 고분자의 기능을 조절하는 분자량이 작은(<900 달톤) 유기 화합물을 말함 |
|
신약 개발 단계 |
일반적으로는 "연구→ 비임상→ 임상 1 상→ 임상 2 상→ 임상 3 상→ 품목 허가→ 출시"의 단계를 따름 |
|
선도물질 |
선도물질이란 후보물질의 전 단계를 의미하는데 약리작용이 우수하고 부작용이 적다고 판단될 경우 후보물질로 등록됨. |
|
후보물질 |
세포실험, 동물 실험등을 통해 효과가 기존약물에 비해 뛰어나 신약으로서 개발 가능한 물질을 말함. |
|
전임상 시험(pre-clinical study) |
임상 시험의 이전 과정에서 행하는 시험. 신약이 실험 대상의 체내에 투여되었을 때 어떤 반응을 일으키는지, 그 효능과 안전성을 동물모델에서 검증하는 시험 절차이다 |
|
임상 시험 |
한정된 수의 건강한 지원자를 대상으로 안전성에 중점을 두고 투여량, 약리 작용, 체내의 흡수/분포/대사/배설을 조사하는 시험 |
|
임상1상시험 |
실제 사람에게도 투여해 부작용이 없는지 처음으로 확인하는 단계임. 건강한 지원자 또는 약물군에 따른 적응환자를 대상으로 내약성 부작용 및 약물의 체내 작용상태 등 안전성 확인함. |
|
임상2상시험 |
1상을 통해 안전성이 확인된 후보물질의 효능을 본격적으로 알아보는 단계임. 대상질환 가운데 조건에 부합하는 환자를 대상으로 단기 투약에 따른 부작용 및 예상 적응증에 대한 효과를 탐색함. |
|
임상3상시험 |
신약허가를 받기 위한 최종 단계임. 위약 대조실험과 함께 임상2상보다 훨씬 광범위한 임상시험을 함으로써 임상2상에서 나타난 약효가 환자의 심리적 효과(플라시보 효과)로 인한 것인지, 아직 드러나지 않는 부작용은 없는지를 판단하는 단계임. 치료대상이 되는 질병에 대한 시험약의 유효성과 안전성에 대해 통계적인 검증을 통해 약물에 대한 최종평가를 내리고, 효능과 효과, 용법, 용량, 사용상의 주의사항 등을 결정함. |
|
도파민 (dopamine) |
카테콜아민 계열의 유기 화합물로, 다양한 동물들의 중추 신경계에서 발견되는 호르몬이나 신경전달물질 |
|
세포사멸(Apoptosis) |
세포사멸(Apoptosis)은 다세포 생물체에서 볼 수 있는 세포예정사(Programmed cell death) 혹은 세포자살이라고함. 형태와 내부의 생화학적 변화로 말미암아 세포가 정상적으로 조절되어 죽는 것으로 정리됨. 이 과정은 세포의 포막의 변화, 핵 단편화, 염색질 응축과 염색체 절단, 그리고 해당 세포가 다른 세포에 의해 처리됨. |
|
세포괴사 (necrosis) |
세포 괴사는 조절되지 않는 우연한 세포의 죽음이다. 주로 이온 항상성의 파괴나 세포막에 손상이 있는 경우에 일어난다. |
|
알파시누클라인(α-synuclein) |
인간의 뇌에 풍부한 단백질이다. 뇌에서, 알파시누클라인은 시냅스전말단이라 불리는 특수한 구조의 신경 세포 (뉴런)의 끝에서 주로 발견된다 |
|
약동력학 (Pharmacokinetics) |
약물의 흡수, 분포, 대사, 배설과정을 동역학적 관점에서 해석하고 예측하고자 하는 약물학의 세부 학문 |
|
약동학적(PK) |
Pharmacokunetics 약자. 약물의 흡수, 분포, 대사, 배설 과정 연구한 결과임. |
|
유효성(Proof-of-concept) |
환자를 통해서 약의 효능을 확인하는 것으로 약의 기전에 의한 제품의 적합성을 확인함. |
|
First-in-class |
혁신 신약, 혁신 의약품이라 부르며, 기존의 치료제가 없는 질병의 작용기전을 밝히고 질환을 고치는 신약임. 특정 질환에 대한 약의 효능이 기존에 나온 여타 약물과 구별됨. |
|
Best-in-class |
기존의 나온 의약품에 비해 효능이 뛰어나거나, 부작용이 낮은 등 의약품의 기능이 보완된 의약품 |
|
재실시권 |
기술제휴계약에 있어서 실시권을 허락받은 Licensee가 부여받은 권한의 범위 내에서 제3자에게 실시권을 허락하는 것을 말한다. |
|
전용실시권 |
특허 발명을 일정 범위 내에서 독점적으로 실시할 수 있는 권리. 특허권자와 실시권자 간에 전용 실시권 설정 계약을 체결하고 이를 특허청에 등록함으로써 발생하며, 전용 실시권자는 설정 계약의 범위 내에서 특허 발명을 독점적 · 배타적으로 실시할 수 있다. |
|
경상기술료 |
라이선스된 기술에 대한 이용료를 지불하는 방식 중의 하나로 일정한 비율과 산정 기준에 의한 금액을 주기적으로 지불하는 방법. |
|
마일스톤 |
프로젝트 진행과정에서 일정 기준을 마련하고 그 기준을 달성 하였을때 지금 되는 금액 |
|
로열티 |
특정한 권리를 이용하는 이용자가 권리를 가진 사람에게 지불하는 대가를 의미한다. 여기서 말하는 권리는 지적재산권에 속하는 특허권, 저작권, 상표권 등을 말한다. 즉, 의약품이 시장에 시판되면 판매되는 금액의 일정부분을 지급함. |
|
작용기전(MOA) |
MOA(Mechanism of Action) 약이 어떤 과정을 거쳐서 효과를 나타내는지를 설명 하는것. |
|
GLP |
Good Laboratories Practice. 임상 시험용 의약품의 안전성과 유효성을 증명할 목적으로, 해당 약물의 약동ㆍ약력ㆍ약리ㆍ임상적 효과를 확인하고 이상 반응을 조사하기 위하여 사람을 대상으로 실시하는 시험 또는 연구 |
|
GMP |
Good Manufacturing Practice. 식품· 의약품의 안정성과 유효성을 품질면에서 보증하는 기본 조건으로서의 우수 식품·의약품의 제조·관리의 기준, 품질이 고도화된 우수 식품· 의약품을 제조하기 위한 여러 요건을 구체화한 것으로 원료의 입고에서부터 출고에 이르기까지 품질관리의 전반에 있어 지켜야 할 규범임. 미국은 cGMP, 유럽은 EU-GMP, 한국은 kGMP 기준을 가지고 있음 |
|
CRO |
Contract Research Organization의 약자로 임상 시험 수탁기관을 뜻함. 비임상, 임상 시험과 관련된 의뢰자의 임무나 역할의 일부 또는 전부를 대행하기 위하여 의뢰자로부터 계약에 의해 위임받은 기관 |
|
IND |
Investigational New Drug Application(임상시험 계획 승인 신청) 인체를 대상으로 한 안전성ㆍ유효성 자료 수집을 목적으로 해당 의약품을 사용하여 임상시험을 실시하고자 하는 자가 식약처장의 승인을 신청하는 과정 |
|
FDA |
FDA는 미국 보건부의 산하기관으로 식품과 의약품에 대한 관리 규제를 담당하는 기관. Food and Drug Administration |
|
Fast-track review (신속심사) |
의약품의 심사기간과 절차를 간소화하여 빠른 결정이 가능하게 하는 방식으로 임상개발에 있어 기간을 단축할 수 있는 제도임. |
|
제네릭약물 |
최초로 개발된 의약품 (원개발 의약품)과 주성분 함량, 품질, 안전성, 약효 작용 원리, 효능, 복용방법 등이 동등한 의약품으로, 의약품동등성시험을 통해 원개발 의약품과 동등함을 식약처로부터 인정받은 의약품 |
|
바이오시밀러 |
특허가 만료된 생물의약품(바이오 의약품)에 대하여 원래의 의약품과 동일한 공정으로 제조하지 않으나 임상시험 등을 통해 동등성인증을 확보한 의약품 |
|
DNA |
Deoxyribonucleic Acid의 약자로서 핵산의 한 종류로 생물의 유전 정보 저장을 담당하는 물질. 유전정보는 핵 염기에 의해 구분되는 4종 뉴클레오타이드의 배열 (염기서열)로 저장되며, DNA를 주형으로 하여 mRNA가 생성되는 전사 과정을 통해 유전자의 발현이 개시됨 |
|
RNA |
Ribonucleic acid. 핵산의 한 종류로 유전 정보의 저장에 한정된 DNA와 달리 다양한 종류의 RNA가 각기 다른 생물학적 기능을 수행함. 특히, 유전자 발현 과정에서 mRNA, rRNA, tRNA 등이 전사 (transcription)와 번역 (translation) 단계의 핵심 분자로 기능하고 있으며, siRNA, miRNA 등 유전자 발현 조절 기능이 있는 RNA 분자도 존재함 |
|
Pre-mRNA |
Precursor mRNA를 통상적으로 줄인 pre-mRNA는 DNA에 저장된 유전정보를 바탕으로 전사과정 (transcription)에 의해 세포의 핵 안에서 합성되며 Exon과 Intron으로 구성되어 있으며 Splicing과정을 통해 Exon만을 보유하는 mRNA로 처리됨 |
|
miRNA |
상보적인 mRNA 분자에 결합하여 번역을 방해하거나 억제하여 RNA의 발현을 조절하는, 암호화가 되지 않은 작은 RNA 부류를 일컬음 |
|
PCT 출원 |
Patent Cooperation Treaty, 특허협력조약. PCT에 의해 하나의 방식 및 언어로 PCT 동맹국에 동시에 특허 출원하는 것. PCT 출원을 하면, 국제 단계를 거쳐 국내 단계로 진입하게 되며, 국제 단계는 국제조사, 국제공개 및 국제예비심사의 3개 절차로 세분화됨 |
|
Transcription |
먼저 핵 내에서 DNA(디옥시리보핵산)가 pre-mRNA를 만들어 낸다. DNA는 아데닌(adenine), 구아닌(guanine), 사이토신(cytosine), 타이민(thymine)의 서로 다른 4개의 핵산으로 구성되는데 이 가운데 타이민만이 RNA에서 유라실(uracil)로 바뀌고 나머지 3개의 핵산은 그대로 RNA로 전달됨. 이 과정을 전사(transcription)라 부름 |
|
Translation |
세포질 내에서 mRNA로 전사된 유전정보를 사용하여 아미노산서열을 만들어 단백질을 생성하는 과정을 Translation, 번역이라 함 |
|
In Vitro |
생체외, 시험관내를 뜻하며 생체에서 꺼낸 효소, 세포 등을 시험관 내에서 효능을 검증하는 단계를 In Vitro 효능 검증이라 함 |
|
In Vivo |
생체내. 일반적으로 In Vivo 효능 검증이란 동물에서의 효능 검증을 뜻함 |
|
API(원료의약품) |
Active Pharmaceutical Ingredient의 약자. 원료의약품(API)는 완제의약품 생산에 사용되는 약효를 나타내는 순수한 한 가지 물질을 뜻함. |
|
DP(임상완제의약품) |
Drug Product의 약자. 임상에 사용되는 약물을 뜻함. |
|
질병조절치료제(disease-modifying drug) |
병의 증상을 중단시키거나 오랜 시간 동안 늦출 수 있는 근본적인 치료제 |
|
루이소체(Lewy body) |
신경세포내에서 발달하는 비정상적인 단백질 집합체이다. 루이소체는 알파시누클라인이 유비퀴틴, 신경섬유 단백질등과 같은 단백질들과 결합하여 구성되어 있다. |
|
MRI(Magnetic Resonance Imaging) |
이 기술은 조직의 물분자의 극성화(polarity)를 분획이방성 (FA: Fractional Anisotropy) 값으로 측정하는 기술로서 동물과 사람(환자 포함)에서 사용 가능한 기술입니다. |
|
PET(Positron Emission Tomography) |
일반적으로 반감기가 아주 짧은 특수 동위원소로 표지 된 표지물질(probe)을 사용하여 체내에서의 probe의 분포를 이미지로 관찰함으로써 분포 및 PK 연구에 활용되는 기술입니다. 신경세포의 PET 표지물질(probe)은 [F-18]FE-PE2I를 사용하여 KM-819의 효능을 동물모델에서 하였습니다. 이 표지물질은 도파민 세포에서만 발현되고 세포막 단백질(membrane protein) 인 도파민 수송체(Dopamine transporter, DAT)에 결합함으로, DAT의 밀도(density) 와 도파민 세포의 밀도(density)를 측정하는 방법이며 그 결과는 PET 이미징(imaging) 즉 영상으로 얻게 되었습니다. |
|
레보도파(Levodopa) |
도파민의 아미노산 전구체임. 레보도파는 도파 디카르복실라아제에 의해 도파민으로 변환되고 혈액 순환 장벽을 통과할 수 있는 전구이다. 레보도파는 도파민을 분비하고 도파민 수용체를 자극하여 파킨슨병에서 보이는 내생적 도파민의 고갈을 막는다. |
|
비핵산역전사효소억제제(NNRTI) |
바이러스의 증식을 억제하는 저해제 |
|
항바이러스 |
바이러스를 억제하는 포괄적 의미 |
|
단일정 복합제(Single Tablet Regimen, STR) |
두가지 혹은 그 이상의 다른 HIV 저해 기작을 가진 성분이 한 개의 알약에 포함되어 있는 치료제 |
|
약물상호작용 |
한 약의 효과가 다른 물질(다른 약, 음식물, 건강보조식품)에 의해 변하는 것을 말함 |
|
역전사효소(reverse transcriptase) |
바이러스의 증식을 위해서 RNA를 DNA로 합성시에 필요한 효소 |
|
내성장벽 |
내성균에 의한 내성의 정도를 의미. 내성균에 의해 특정 약물이 효능이 떨어질때 내성장벽이 높다고 말함 |
|
병용용법(combination therapy) |
한가지 이상의 약물을 동시에 투여해서 치료하는 방법 |
|
GCP(Good Clinical Practice) |
사람을 대상으로 하는 임상시험을 설계, 수행, 기록 및 보고하는데 관한 국제적으로 통용되는 윤리적, 과학적 기준임 |
|
FAF1(Fas associated factor 1) |
세포자살(apoptosis)을 유도하는 단백질이며 동시에 세포괴사(necrosis)에 관여하는 단백질 |
|
파킨슨병 |
주로 진전, 근육의 강직, 그리고 몸동작이 느려지는 서동 등의 운동장애가 나타나는 질환 |
|
다계통위축증 |
임상적으로 파킨슨 증상을 보이지만 다른 신경계통의 이상증상이 동반되는 만성 진행성 퇴행성 뇌질환 |
|
파킨슨병 치매 |
파킨슨병의 대표증상인 보행장애, 떨림 등의 운동기능저하와 함께 또 다른 특징으로는 인지기능 저하 증상이 나타나는 증상. 이에 따라 주의를 인식하지 못하거나 얼이 빠져 보이는 등 주의력, 명료함에 심각한 장애를 보임. |
|
루이소체 치매 |
의학 대뇌 피질의 특정 핵 안에 루이 소체가 침착하여 생기는 뇌 질환. 운동 장애, 손발 떨림, 다리 끌며 걷기, 근육 경직, 환시, 망상, 치매, 우울증 등의 증상이 나타남 |
|
희귀질환 |
유병인구가 2만명 이하이거나 진단이 어려워 유병인구를 알 수 없는 질환 |
|
세포독성항암제 |
빠르게 성장하는 세포를 공격하는 항암제. 특히 암세포와 머리카락 위장관세포를 공격함. |
|
표적항암제 |
특정암세포의 특징적인 표면 (혹은 내부) 타겟을 찾아가도록 만들어진 항암제 |
|
에피제네틱항암제 |
DNA 염기서열 자체의 변화가 아닌 DNA에 일어나는 부분적인 변화 또는 DNA 주변 부위의 단백질 변화 등을 타겟으로 개발한 항암제 |
|
면역항암제 |
암 환자의 면역력을 키워 암과 싸우는 힘을 키워주는 치료제 |
|
NDA(New Drug Approval) |
규제기관으로부터 임상 결과 평가를 통해서 받는 신약판매 최종 허가 |
주식회사 카이노스메드는 2007년 06월 15일에 혁신신약 연구 및 개발 목적으로 설립되었으며, 2020년 06월 08일 하나금융11호기업인수목적 주식회사와 합병을 통해 코스닥시장에 상장되었습니다. 당사는 뇌질환, 암, 감염성 질환분야에서 혁신적인 치료제 신약을 연구 개발하는 글로벌 신약 개발 기업으로서, 신약후보물질 개발, 최적화 단계의 초기 연구개발 및 전임상, 초기 임상을 통해서 임상 개발을 하고 있습니다.
당사는 증권신고서 제출일 현재 전체 연구개발제품 현황은 다음과 같습니다.
| [신약 파이프라인 현황] |
|
프로젝트 |
타겟 단백질 /작용기전 |
타겟 질환 |
개발단계 |
|---|---|---|---|
|
파킨슨병 치료제 (KM-819) |
FAF1 저해, 세포사멸 저해 및 알파시누클라인 축적 저해 |
파킨슨병 |
임상2상(미국) |
|
다계통위축증 (KM-819) (주1) |
다계통위축증 |
임상 2상(한국) |
|
|
심부전 치료제 (KM-819) (주1) |
FAF1 저해 |
심부전 |
전임상 연구 |
|
에이즈 치료제 (KM023) |
HIV Reverse transcriptase 저해 |
에이즈 |
NDA 승인(중국) |
|
세포독성 항암제 (KM-630) |
DNA 합성 억제 |
혈액암/고형암 |
전임상 독성연구 |
|
에피제네틱스 항암제 (KM-635) |
BRD4 저해 |
혈액암/고형암 |
임상 1상 진행 |
|
PD-L1 (면역항암제) |
PD-L1 저해 |
Melanoma/ Lung cancer |
후보물질 최적화 |
|
CD73 (면역항암제) |
CD73 저해 |
Melanoma/ Lung cancer/ Ovarian cancer |
선도물질 최적화 |
|
혈액항암제 (KM-10544) |
IRAK4 저해 |
암 |
후보물질 최적화 |
| FAF1-Exosome (KM-1004) (주2) | FAF1 과발현 유도 항암제 | 암 | 후보물질 개발중 |
| 출처) 당사 정기보고서 및 당사 제시 |
| 주1) 다계통위축증, 심부전치료제는 KM-819(파킨슨병치료제)물질의 적응증 확대로 개발 중인 프로젝트 입니다. |
| 주2) IRAK4 저해 약물인 항암치료제 KM-10544는 2021년 10월 미국 엠마우스라이프사이언스(Emmaus life Science, Inc.)에 기술이전되어, 미국 내에서 임상 준비를 위한 전임상 연구 중에 있습니다. |
1. 사업위험
|
가. COVID-19 유행, 러시아-우크라이나 전쟁 및 대내외 불확실성에 따른 신약개발에 미치는 위험 |
신종 코로나 바이러스 감염증(이하 '코로나-19')은 중국 후베이성 우한시에서 2019년 12월 1일 처음 발생 후 확산 중인 급성 호흡기 질환입니다. 감염 확산세가 전세계로 이어지면서 2020년 03월 11일, 세계보건기구(WHO)는 감염병 경보를 기존 5단계에서 최고 단계인 6단계로 상향 조정하여 '세계적 대유행(Pandemic)'으로 선포하였습니다.
세계 각국은 백신 개발과 코로나-19 확산 방지에 총력을 다하고 있습니다. 2021년 백신 접종을 시작으로, 세계 각국은 일정 수준 이상의 백신 접종률 달성을 위해 총력을 기울이고 있습니다. 그러나 코로나-19는 여전히 종식되지 않았으며, 각종 변이 코로나-19가 확산되는 등 장기화될 가능성이 존재합니다. 2020년 10월 인도에서 처음 발견된 코로나-19 변이 바이러스인 델타 변이 바이러스는 기존 코로나-19 백신으로 방어가 가능한 것으로 알려져 있지만, 다른 변이 바이러스보다 전파 속도가 빠른 데다 더 심각한 증상을 유발하는 것으로 알려져 있습니다.
또한, 최근 유행한 오미크론 변이는 남아공 과학자들이 스파이크 단백질에 32가지 유전자 변이를 일으킨 새로운 변이, 'B.1.1.529'가 발견됐다고 보고하면서 알려졌습니다. 처음 발견된 것은 아프리카 보츠와나이고 남아공에서 확산되었으며, 세계보건기구(WHO)는 이날 전문가 회의를 열어 이 변이종에 오미크론이라는 이름을 붙이고 '우려 변이종'으로 분류했습니다. 그리고 이는 델타 변이와 같은 가장 높은 수준의 분류 단계입니다. 2021년 하반기 들어 백신 접종과 방역 체계가 강화되면서 위드 코로나 정책이 유지될 것으로 예상되었지만, 변이 바이러스인 오미크론의 등장과 확진자 수 급증으로 국내 방역조치는 재차 강화되었습니다.
2022년 4월 IMF(국제통화기금)가 발표한 세계경제전망에 따르면 2020년 세계 경제성장률은 -3.1%를 기록한 것으로 추정되며, 2021년에는 5.9%, 2022년에는 3.6%, 2023년에는 3.6%의 성장률을 기록할 것으로 전망되고 있습니다. IMF는 러시아-우크라이나 전쟁, 긴축적 통화ㆍ재정정책, 중국의 성장 둔화, 코로나19 영향 등의 영향으로 세계 경제 회복세가 대폭 둔화될 것으로 전망하며, 2022년 경제성장률은 직전 전망치(2022년 01월) 4.4% 대비 0.8%p 하향한 3.6%를 전망하였고, 2023년 경제성장률은 직전 전망치(2022년 01월) 3.8% 대비 0.2%p 하향한 3.6%를 전망하였습니다.
IMF(국제통화기금)은 선진국의 경우 공급망 정체, 에너지가격 상승 등을 근거로 2022년 선진국 경제성장률을 직전 전망치(2022년 01월) 3.9% 대비 0.6%p 하향한 3.3%로 전망하였으며 신흥국의 경우 중국 부동산 위축, 에너지가격 상승에 따른 국내수요 둔화, 발틱해 연안 공급망 병목, 러시아 농산물 수확 감소 등에 따라 2022년 신흥국 경제성장률을 직전 전망치(2022년 01월) 4.8% 대비 1.0%p 하향한 3.8%로 전망하였습니다.
이와 더불어, IMF는 백신 격차가 지속되는 가운데 변이 바이러스 확산과 변이 바이러스의 확산으로 글로벌 공급망 차질 장기화, 미 통화정책 정상화에 따라 신흥국 중심으로 글로벌 금융시장 충격과 위축된 노동시장에 따른 임금상승, 러시아-우크라이나 전쟁으로 인한 인플레이션 상방 압력 확대, 중국 주요도시 재봉쇄로 인한 중국 경제 추가 둔화 가능성 등을 하방위험 요소로 언급하였습니다.
| [IMF 주요국의 경제성장률 전망치] |
| (단위: %, %p) |
| 경제성장률 | 2020년 | 2021년 | 2022년 | 2023년 | ||||
|---|---|---|---|---|---|---|---|---|
| 전망 ('22.1월 기준) |
전망 ('22.4월 기준) |
조정폭 ('22.1월 대비) |
전망 ('22.1월 기준) |
전망 ('22.4월 기준) |
조정폭 ('22.1월 대비) |
|||
| 세계 | -3.1 | 5.9 | 4.4 | 3.6 | -0.8 | 3.8 | 3.6 | -0.2 |
| 선진국 | -4.5 | 5.0 | 3.9 | 3.3 | -0.6 | 2.6 | 2.4 | -0.2 |
| 미국 | -3.4 | 5.6 | 4.0 | 3.7 | -0.3 | 2.6 | 2.3 | -0.3 |
| 유로존 | -6.4 | 5.2 | 3.9 | 2.8 | -1.1 | 2.5 | 2.3 | -0.2 |
| 일본 | -4.5 | 1.6 | 3.3 | 2.4 | -0.9 | 1.8 | 2.3 | 0.5 |
| 신흥개도국 | -2.0 | 6.5 | 4.8 | 3.8 | -1.0 | 4.7 | 4.4 | -0.3 |
| 중국 | 2.3 | 8.1 | 4.8 | 4.4 | -0.4 | 5.2 | 5.1 | -0.1 |
| 인도 | -7.3 | 9.0 | 9.0 | 8.2 | -0.8 | 7.1 | 6.9 | -0.2 |
| 한국 | -0.9 | 4.0 | 3.0 | 2.5 | -0.5 | 2.9 | 2.9 | 0.0 |
| 출처) IMF World Economic Outlook (2022.04) |
한편, 국내 경기의 경우 2022년 02월 한국은행이 발표한 경제전망보고서에 따르면 최근 국내외 여건변화 등을 감안할때 경제성장률은 2022년 3.0%, 2023년 2.5% 수준을 나타낼 것이라고 전망하였습니다. 한국은행에 따르면 국내 경기는 대내외 불확실성 증대에도 글로벌 경제활동 재개 지속, 국내 방역조치 완화 기조 등에 힘입어 양호한 성장세를 지속할 것으로 예상하고 있습니다. 그러나, 향후 오미크론 변이에 의한 코로나19 재확산, 실업률 증가, 금융 여건 악화 등 팬데믹 관련 위험뿐만 아니라 우크라이나 사태, 주요국의 통화정책 조기 정상화 움직임 등이 세계 경제에 부정적인 영향을 끼칠 수 있으며 특히 코로나19 확산세가 2022년에도 지속될 경우 경기 회복세가 더뎌질 수 있습니다.
| [ 국내 주요 거시경제지표 전망 ] |
| (단위: 전년동기 대비 %) |
| 경제성장률 | 2020 | 2021 | 2022(E) | 2023(E) | ||||
|---|---|---|---|---|---|---|---|---|
| 연간 | 상반 | 하반 | 연간 | 상반 | 하반 | 연간 | 연간 | |
| GDP | -0.9 | 4.0 | 4.0 | 4.0 | 2.8 | 3.1 | 3.0 | 2.5 |
| 민간소비 | -5.0 | 2.4 | 4.8 | 3.6 | 3.9 | 3.2 | 3.5 | 2.6 |
| 설비투자 | 7.1 | 12.6 | 4.1 | 8.3 | -1.3 | 5.8 | 2.2 | 1.7 |
| 지식재산생산물 투자 | 4.0 | 4.0 | 3.7 | 3.9 | 4.2 | 3.7 | 3.9 | 3.8 |
| 건설투자 | -0.4 | -1.5 | -1.5 | -1.5 | 0.6 | 4.0 | 2.4 | 2.3 |
| 상품수출 | -0.5 | 14.4 | 6.0 | 9.8 | 4.5 | 2.5 | 3.4 | 2.2 |
| 상품수입 | -0.1 | 12.5 | 11.2 | 11.8 | 5.6 | 2.1 | 3.8 | 2.3 |
| 출처) 한국은행 경제전망보고(2022.02) |
정부는 악화된 실물 및 금융 경제를 부양하기 위하여 다양한 통화정책 및 재정정책을 실시하면서 경제 안정화를 위해 지속적으로 노력하고 있습니다. 하지만 글로벌 COVID-19 팬데믹의 장기화 및 추후 재발 가능성과 더불어 소비 및 금융 시장 심리 악화, 러시아-우크라이나 전쟁의 장기화, 원자재 가격의 급격한 상승, 높은 인플레이션으로 인한 고강도 통화정책 실시 등 부정적인 요인들은 향후에도 경기 회복세가 둔화될 수 있는 가능성이 존재합니다.
COVID-19 이외에도 2022년 02월 24일 러시아가 우크라이나를 침공함으로써 러시아-우크라이나 전쟁이 발발하였습니다. 러시아는 2022년 02월 21일 동부 우크라이나의 돈바스 지역에 군대를 진주시켰으며, 삼일 뒤인 2022년 02월 24일, 전면적인 침공을 개시했습니다. 러시아는 우크라이나의 수도 키예프를 비롯한 우크라이나 전역에 미사일을 발사했으며, 우크라이나 전역으로 지상군이 투입되었습니다. 바이든 대통령은 러시아의 기습 공격을 "정당한 이유 없는 공격", "계획된 전쟁"으로 규정하고 동맹과 함께 제재를 추가로 부과할 것이라고 예고했습니다. 러시아와 우크라이나는 세계 4대 곡물수출국인 데다 러시아가 유럽으로 향하는 천연가스 대부분을 공급한다는 점에서 양측의 군사충돌이 전 세계적으로 에너지, 곡물 등 원자재 가격의 가파른 상승을 일으킬 것이라는 전망이 높습니다. 증권신고서 제출 전일 현재 해당 이벤트가 당사에 직접적으로 영향을 미칠지 여부는 미지수입니다. 따라서 투자자께서는 상기 이벤트가 당사 및 당사가 영위하는 사업에 미칠 영향에 대해 면밀히 검토하시기 바랍니다.
| 나. 연구개발 지연 및 실패 위험 당사가 주요사업으로 영위하는 바이오신약개발 산업의 특성상 현재 연구개발하고 있는 신약이 상업화되기까지는 막대한 비용과 시간이 필요합니다. 특히, 임상시험에 진입하여도 최소 8-9년이 소요되며 그에 필요한 비용이 요구됩니다. 또한, 임상시험을 진행한다고 하더라도 시험결과 효능이 부족하거나 안전성 평가에 적합하지 못한 결과가 나올 경우 해당 신약의 연구개발은 중단될 수 있으며, 이러할 경우 당사의 비용 및 시간 투자에도 불구하고 엄청난 손실을 야기할 수밖에 없습니다. 다양한 규모의 임상시험을 준비하고 진행하는 과정에서 코로나19 등 임상 계획 당시 예상치 못하였던 변수로 인하여 임상시험 개시 승인이 늦어지거나, 환자등록이 원활하지 않는 등의 문제가 발생할 수 있으며 이 경우 임상시험의 진행이 예정보다 지연될 위험이 존재합니다. 당사의 파이프라인별 물질들은 당사가 계획하고 있는 일정에 따라 임상시험 및 판매 허가를 득하고 있습니다. 그러나 당사가 예상치 못한 이유로 인해 신약 개발 일정이 지연된다면 제품화까지 당사 예상 대비 장기간이 소요될 수 있으며, 연구개발을 진행하는 동안에도 성과가 나오지 않을 경우 연구를 중단하게 되고 사용된 연구개발 비용은 따로 회수할 수 없어 당사의 수익성 및 성장성에 악영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다. 이러한 임상 지연 및 실패는 당사의 수익성 및 재무안정성에 부정적인 영향을 미칠 수 있음을 투자자께서는 유의하시기 바랍니다. |
당사가 주요사업으로 영위하는 바이오신약개발 산업의 특성상 현재 연구개발하고 있는 신약이 상업화되기까지는 막대한 비용과 시간이 필요합니다. 특히, 임상시험에 진입하여도 최소 8-9년이 소요되며 그에 필요한 비용이 요구됩니다. 또한, 임상시험을 진행한다고 하더라도 시험결과 효능이 부족하거나 안전성 평가에 적합하지 못한 결과가 나올 경우 해당 신약의 연구개발은 중단될 수 있으며, 이러할 경우 당사의 비용 및 시간 투자에도 불구하고 엄청난 손실을 야기할 수밖에 없습니다.
한 개의 신약이 나오기 위해서는 여러 단계를 거치게 되는데, 먼저 신약 후보물질을 도출하기 위한 탐색 과정을 거칩니다. 이 과정에서는 신약의 효능이나 작용기전을 기반으로 신약개발 대상물질을 선정합니다. 유효물질(hit compound), 선도물질(lead compound)을 거쳐 신약 후보물질이 선정되면 후보물질의 안정성과 효과를 확인하기 위해 동물 모델을 대상으로 전임상시험(pre-clinical trial)을 진행합니다. 전임상시험을 통해 후보물질의 효과와 안전성을 검증하면 허가기관에 임상시험 허가신청(IND : Investigational New Drug Application)을 하고, 사람을 대상으로 약물의 효과의 부작용을 확인하는 임상시험(clinical trial)을 수행합니다. 임상시험을 마친 후에는 식약처에 임상시험 결과를 제출하게 되는데, 이를 신약 허가신청(NDA : New Drug Application) 이라고 합니다. 신약 허가신청이 정상적으로 이루어지면, 제4상 임상시험으로 분류되는 시판후안전성조사(PMS : Post-Market Surveillance)를 통해 임상시험에서 발견하기 어려웠던 부작용에 대해서 추적 조사를 수행합니다.
| [신약 개발 및 승인 프로세스] |
|
| 출처) 글로벌 제약시장 임상 파이프라인 분석(한국바이오경제연구센터) |
임상 1상은 주로 정상인을 대상으로 약물의 독성테스트를 합니다. 약물의 효과는 평가하지 않고 안전성에 주로 초점을 맞추기 때문에 대부분 성공률이 높습니다. 임상 2상은 인체(환자)를 대상으로 부작용 뿐 아니라 약효를 테스트하는 첫 번째 관문이기 때문에 성공률이 제일 낮을 수밖에 없습니다. 임상 3상은 임상 2상과 같이 환자를 대상으로 약효와 부작용을 보는 단계이지만, 환자 수가 훨씬 크고 약의 dose(복용량)를 결정하는 단계입니다. 임상 3상은 임상 2상에서 적은 수의 환자를 대상으로 이미 약효와 부작용을 테스트했기 때문에 성공 확률이 비교적 높은 69%입니다. 임상 3상은 규모가 가장 크고 비용이 제일 많이 드는 데다 임상 기간이 평균 3년으로 가장 깁니다. 임상에서 가장 성공률이 높은 단계는 신약의 제품허가 승인 단계인 NDA 입니다. NDA 단계는 임상 1상에서 3상까지 해당 적응증에 대한 모든 임상 테스트를 통과한 상태에서 다시 한번 최종 검토하는 과정이기 때문에 통상적으로 통과할 확률이 높습니다.
| [연구개발 진행 총괄표] |
|
구분 |
품목 |
적응증 |
연구시작일 |
현재 진행단계 |
비고 |
|
|---|---|---|---|---|---|---|
|
단계(국가) |
승인일 |
|||||
| 신약 |
파킨슨병 치료제 |
파킨슨병 |
2015 |
임상 2상 승인 (미국) |
2021년 |
IND 승인 기준 |
|
다계통위축증 치료제 |
다계통위축증 |
임상 2상 승인 (한국) |
2021년 |
IND 승인 기준 |
||
|
에이즈 치료제 |
에이즈 |
2010 |
NDA 승인(중국) 임상 3상(중국) |
2021년 |
NDA 승인 기준 |
|
|
에피제네틱 항암제 |
혈액암, 고형암 |
2012 |
임상 1상 진행(중국) |
2020년 |
IND 승인 기준 |
|
|
세포독성 항암제 |
혈액암, 고형암 |
전임상 |
- |
- |
||
|
면역항암제 (PD-L1) |
흑색종, 비소세포폐암 |
2016 |
후보물질 |
- |
- |
|
|
면역항암제 (CD73) |
혈액암, 고형암 |
선도물질 |
- |
- |
||
|
표적항암제 (IRAK4) |
혈액암, 건선 |
2017 |
후보물질 |
- |
- |
|
|
심혈관질환 심부전치료제 |
심부전 |
2020 |
선도물질 |
- |
- |
|
| FAF1-Exosome | 고형암, 혈액암 | 2021 | 선도물질 | - | - | |
| 출처) 당사 정기보고서 및 당사 제시 |
다양한 규모의 임상시험을 준비하고 진행하는 과정에서 코로나19 등 임상 계획 당시 예상치 못하였던 변수로 인하여 임상시험 개시 승인이 늦어지거나, 환자등록이 원활하지 않는 등의 문제가 발생할 수 있으며 이 경우 임상시험의 진행이 예정보다 지연될 위험이 존재합니다.
한편, 당사가 계획 중인 임상 일정이 지연되는 경우에는 임상시험 비용이 예산을 초과하여 발생하거나, 판매승인 지연으로 인하여 신약매출 발생이 늦어질 수 있으며, 임상 실패의 경우 기존에 발생한 비용에 대한 회수가 불가능합니다.
대한의학회지에 실린 논문(전주연, 김혜경, 유경상, 2020. The Impact of COVID-19 on the Conduct of Clinical Trials for Medical Products in Korea, 대한의학회지)에 따르면 국내 상위 25개 제약사 중 절반 이상인 13개 제약사가 코로나19로 인해 임상시험 수행에 어려움을 겪는다고 답한 바 있으며, 특히 코로나19로 인해 임상 site를 확보하기 어려운 점, 임상 환자가 내원하여 임상을 진행하기 어려운 점 등을 주요 요인으로 꼽았습니다. 또한, 데이터 및 분석업체인인 글로벌데이터에 따르면, 2021년 2월 기준 전세계적으로 1,200건이 넘는 임상시험이 코로나19로 인해 지장을 받고 있으며, 특히 항암제 등 종양 관련 임상시험에 큰 영향을 받고 있습니다. 이러한 지장은 임상 개시 지연, 환자 등록 중단, 환자 등록 지연 등 여러 요인으로 인해 발생하고 있습니다. 코로나19의 확산세가 지속될 경우 당사가 진행 중인 임상시험이 연기되고 중단될 수 있으며 이는 당사 기업가치 및 수익성에 부정적인 영향을 끼칠 수 있습니다. 투자자께서는 이점 유의하여 주시기 바랍니다.
임상 지연 및 실패는 당사의 수익성 및 재무안정성에 부정적인 영향을 미칠 수 있음을 투자자께서는 유의하시기 바랍니다.
또한 당사가 연구개발 중인 파이프라인 중 파킨슨병 치료제(KM-819)에 대하여 미국 FDA로부터 임상 2상 IND를 승인받았으며, 2022년 06월 이후 임상 2상을 진행할 예정입니다. 2019년 02월부터 KM-819의 적응증을 확대하여 개발 중인 다계통위축증 치료제(KM-819)은 2022년 03월부터 국내 임상 2상을 진행하고 있습니다. 또한 경구용 에이즈치료제(KM-023)의 경우 임상 1상 완료 이후 2014년 10월 중국 제약사 장수 아이디어(Jiangsu Aidea Pharmaceuticals)로 기술이전하여 ACC007라는 약물로 개발해왔으며, ACC007, 테노포비르(TDF), 라미부딘(3TC)를 함께 처방하는 방식으로 2021년 06월 NDA(New Drug Application, 의약품 품목 허가)를 승인받아 2022년부터 시판하고 있습니다. 또한 ACC007, 테노포비르(TDF), 라미부딘(3TC)를 단일 복합정으로 만든 ACC008을 개발하고 있으며, 현재 에이즈 치료 경험이 없는 환자를 대상으로는 NDA 신청 완료하였으며, 에이즈 치료 경험이 있는 환자를 대상으로 임상 3상 진행 중입니다.
상기 파이프라인별 물질들은 당사가 계획하고 있는 일정에 따라 임상시험 및 판매 허가를 득하고 있습니다. 그러나 당사가 예상치 못한 이유로 인해 신약 개발 일정이 지연된다면 제품화까지 당사 예상 대비 장기간이 소요될 수 있으며, 연구개발을 진행하는 동안에도 성과가 나오지 않을 경우 연구를 중단하게 되고 사용된 연구개발 비용은 따로 회수할 수 없어 당사의 수익성 및 성장성에 악영향을 미칠 수 있으니 투자자께서는 이 점 유의하시기 바랍니다.
| [신약 파이프라인 현황] |
|
프로젝트 |
타겟 단백질 /작용기전 |
타겟 질환 |
개발단계 |
|---|---|---|---|
|
파킨슨병 치료제 (KM-819) |
FAF1 저해, 세포사멸 저해 및 알파시누클라인 축적 저해 |
파킨슨병 |
임상 2상(미국) |
|
다계통위축증 (KM-819) (주1) |
다계통위축증 |
임상 2상(한국) |
|
|
심부전 치료제 (KM-819) (주1) |
FAF1 저해 |
심부전 |
전임상 연구 |
|
에이즈 치료제 (KM023) |
HIV Reverse transcriptase 저해 |
에이즈 |
NDA 승인(중국) |
|
세포독성 항암제 (KM-630) |
DNA 합성 억제 |
혈액암/고형암 |
전임상 독성연구 |
|
에피제네틱스 항암제 (KM-635) |
BRD4 저해 |
혈액암/고형암 |
임상 1상 진행 |
|
PD-L1 (면역항암제) |
PD-L1 저해 |
Melanoma/ Lung cancer |
후보물질 최적화 |
|
CD73 (면역항암제) |
CD73 저해 |
Melanoma/ Lung cancer/ Ovarian cancer |
선도물질 최적화 |
|
혈액항암제 (KM-10544) |
IRAK4 저해 |
암 |
후보물질 최적화 |
| FAF1-Exosome (KM-1004) (주2) | FAF1 과발현 유도 항암제 | 암 | 후보물질 개발중 |
| 출처) 당사 정기보고서 및 당사 제시 |
| 주1) 다계통위축증, 심부전치료제는 KM-819(파킨슨병치료제)물질의 적응증 확대로 개발 중인 프로젝트 입니다. |
| 주2) IRAK4 저해 약물인 항암치료제 KM-10544는 2021년 10월 미국 엠마우스라이프사이언스(Emmaus life Science, Inc.)에 기술이전되어, 미국 내에서 임상 준비를 위한 전임상 연구 중에 있습니다. |
① 파킨슨병 치료제
|
구분 |
합성 신약 |
|
적응증 |
뇌신경계 질환 (파킨슨병, 다계통 위축증 등) |
|
작용기전 |
FAF1 억제제로 도파민 신경세포를 보호하며, alpha-synuclein의 축적을 억제함. |
|
제품의 특성 |
Dopaminergic neuron의 소멸을 억제하여, PD 발생 후 운동능력 상실을 완화·지연함. 말기 단계를 제외한 대부분의 환자에서 현재의 운동능력을 유지시킬 것으로 예상됨. 운동능력 상실을 보완하는 현존 제품들의 효용성을 높이고 사용기간의 연장이 가능함. PD 환자들이 최소한의 일상생활이 가능한 정도의 운동능력을 보존함. Dopaminergic neuron의 사멸제어 작용기전: 파킨슨병 세포모델에서 KM-819의 신경세포 보호효과 확인 및 보호기전 규명 (disease-modifying drug) 파킨슨병 원인으로 알려진 alpha-synuclein의 축적을 억제함. 파킨슨병 동물모델(급성, 아급성, 만성모델)에서KM-819의 신경세포보호 및 행동개선효과 확인. |
|
진행경과 |
파킨슨병 치료제 미국 임상 2상 IND 승인(2021.11) |
|
향후계획 |
미국 임상 2상 성공 종료, 기술이전 추진 |
|
경쟁제품 |
Prothena/Roche(PRX-002), Neuropore/UCB(NPT200-11) : 당사와 같이 파킨슨병의 원인으로 주목받는 a-synuclein을 저해하는 저해제를 개발하고 있음. 당사의 임상 개발단계는 해외 경쟁 제약사들과 동일한 단계임. |
|
관련논문 |
Frontiers in Pharmacology, 2020.6 vol11 1-8 Drug Design, Development and Therapy 2019:13 1011-1022 Bioorganic & Medicinal Chemistry Letters 26(2016)1169-1172. |
|
시장 규모 |
전 세계적으로 인구고령화가 급속히 진행됨에 따라 향후 65세 이상의 파킨슨병 유병 환자 수는 점진적으로 증가할 전망임. GlobalData 보고에 따르면 2016년 주요 7개국(미국, 일본, 프랑스, 독일, 이탈리아, 스페인, 영국)의 파킨슨병 시장은 2016년 31억 달러였으며, 특히 미국 시장은 15억 달러로 주요 7개국 시장의 50.2%를 차지했음. 2016년을 기준으로 파킨슨병 시장은 연평균 11.1%의 증가율로 2026년 88억 달러로 증가할 것으로 예상하고 있음 (GlobalData, 2018). |
|
기타사항 |
- |
② 다계통위축증 치료제
|
구분 |
합성 신약 |
|
적응증 |
다계통위축증 |
|
작용기전 |
FAF1 억제제로 도파민 신경세포를 보호하며, alpha-synuclein의 축적을 억제함. |
|
제품의 특성 |
FAF-1의 과발현을 억제함으로써 Dopaminergic neuron의 사멸제어 하고, 다계통위축증의 원인인alpha-synuclein의 축적을 억제함. |
|
진행경과 |
다계통위축증 치료제 국내 임상 2상 IND 승인 (2021.10) |
|
향후계획 |
한국 임상 2상 성공 종료, 기술이전 추진 |
|
경쟁제품 |
Voyger Therapeutics Tau & alpha-synuclein program: 당사와 같이 파킨슨병과 다계통 위축증의 원인으로 주목받는a-synuclein을 저해하는 저해제를 개발하고 있음. 현재 임상 2상 진행 준비중. |
|
관련논문 |
- |
|
시장 규모 |
- |
|
기타사항 |
- |
③ 에이즈 치료제
|
구분 |
합성 신약 |
|
적응증 |
에이즈 치료제 |
|
작용기전 |
비핵산 역전사효소 억제제(Non-Nucleoside Reverse Transcriptase Inhibitor, NNRTI) |
|
제품의 특성 |
비핵산계열의 화합물로 하루 1회 투여의 편리성 확보하고 있으며 독성이나 CNS부작용이 없고 다른 약물과 병용투여(Combination)가 용이함. |
|
진행경과 |
2014.10 기술이전, Jiangsu Aidea Pharmaceutical (중국) 2016.12 중국 식품의약품관리감독총국 우선심사대상 지정 2017.03 중국 임상 승인 2018.10 임상 3상 개시 2021. 중국 NDA 승인 2021. 중국 단일정 NDA 제출 및 임상 3상 개시 (treated patients) |
|
향후계획 |
단일정의 중국내 NDA 허가 및 시판 |
|
경쟁제품 |
BMS(Efavirenz,EFV), 얀센(rilpivirine,RPV): 에이즈 시장에서의 주력제품은 이미 시장에서 판매되고 있는 EFV와 RPV가 있으며, EFV의 경우 특허가 만료되었음. 기존의 의약품의 중추신경계 및 다양한 부작용이 보고되고 있음. |
|
관련논문 |
Curr HIV Res. 2020 Jun 20 |
|
시장 규모 |
전 세계 HIV 약물 시장은 2019 년에 $ 30,891.48 million으로 평가되었으며, 2027 년까지 $ 36,495.47 million에 이를 것으로 예상됨 (2021 Allied Market Research). 2020 년부터 2027 년까지 3.8 %의 CAGR (연평균 성장률)을 기록할 것으로 예상. Datamonitor Healthcare의 2018년 보고서에 따르면 미국과 주요 EU 시장 (프랑스, 독일, 이탈리아, 스페인, 영국)의 HIV 시장은 2017년의 182억 달러에서 2026년 211억 달러로 연평균 1.7 % 성장할 것으로 예측. |
|
기타사항 |
- |
④ 브로모도메인 저해제 개발: 에피제네틱스 항암제
|
구분 |
합성 신약 |
|
적응증 |
혈액암(AML, AL, MM, DLBCL) 및 고형암(전립선, 유방암, NSCLC, neuroblastoma) |
|
작용기전 |
브로모도메인(BRD4) Inhibitor : 브로모도메인의 타킷인 c-MYC은 종양의 생존, 변이에 중요한 역할을 담당하는 중요한 전사 인자로서, c-MYC의 비정상적인 발현을 억제함. |
|
제품의 특성 |
KM-635는 임상 II상을 준비 중인 Merck사의 OTX-015와 비교하여 우수한 생체 대사성과 생체이용률, 대사 안정성, mouse xenograft model에서도 기존 임상 약물에 비해 월등한 비교 우위를 갖고 있는 화합물임. Human dose prediction실험을 통해, KM-635는 임상에서 OTX-015에 비해 1/2의 양을 사용하더라도 같은 효과를 나타낸다는 결론을 얻었음. 기존의 임상 약물보다 우수한 약효와 안정성을 기대할 수 있으며, 그 적응증을 확대하여 고형암의 치료제로써도 효과를 기대 할 수 있음. |
|
진행경과 |
2015.12.10 기술이전, Jiangsu Aidea Pharmaceutical (중국) |
|
향후계획 |
임상 1상 완료(중국) |
|
경쟁제품 |
Merck(OTX-015), GSK(I-BET762), 로셰(텐샤, TEN-010), 애브비(ABBV075): 현재 임상 진행중인 약물들은 약리 및 약동력학적 프로파일이 좋지 않음. OTX-015(MK-8628, Merck)의 경우 임상 1상 결과 체내 흡수와 대사안정성이 낮아 고용량에서만 약효가 나타나게 되어 안전성에 대한우려가 높음. |
|
관련논문 |
- |
|
시장 규모 |
항암제 분야의 2019년 점유율은 16%로 2026년까지 연평균 11.5%로 성장하여 2026년에는 21.75%로 점유율이 확대될 것으로 기대 2024년 글로벌 항암제 시장 규모는2,385억 달러로2018년 대비 약2배의 고성장 전망. |
|
기타사항 |
- |
⑤ 경구용/주사제 겸용의 핵산 (Nucleoside) 유사체 계열 세포독성 항암제
|
구분 |
합성 신약 |
|
적응증 |
혈액암(급성골수성백혈병)및 고형암 |
|
작용기전 |
시타라빈(Cytarabine, Ara-C) Inhibitor : 세포독성 항암제는 세포의 DNA를 알킬화시켜 세포독성을 나타내는 알킬화제와 DNA가 결성되는 것을 저해함으로써 세포의 미분화와 분열을 차단하고, RNA의 합성도 저해하여 광범위한 악성종양에 효과를 보이는 대사길항제임. |
|
제품의 특성 |
경쟁약물 Ara-C의 단점인 Cytidine deaminase (CDA) 작용에 대한 대사체 변이를 극복한 약물로 경구와 정맥주사가 모두 가능. KM-630은 경구용 혹은 정맥투여 시, 대사작용에서 우수한 안정성 및 생체이용률 (Bioavailability) 등 뛰어난 약리동력학적 안정성을 나타내어 고형암으로의 적응증 확대가 가능. |
|
진행경과 |
2015.12.10 기술이전, Jiangsu Aidea Pharmaceutical (중국) 동물모델에서의 효능 확인 |
|
향후계획 |
전임상 독성 연구 및 중국임상 1상 IND Filling |
|
경쟁제품 |
화이자(시타라빈), 일라이릴리(젬시타빈): 현재 시타라빈(Cytarabine, Ara-C) 과 같은 시판된 핵산계열 세포독성 항암제는 대부분 정맥주사제이며, 단독요법으로 사용되는 경우 하루 2,000mg의 고용량을 투여해야 함. 이로 인한 심각한 독성과 부작용의 문제점을 내포하고 있음. |
|
관련논문 |
- |
|
시장 규모 |
핵산계열 세포독성항암제의 주요 적응증은 백혈병을 비롯한 혈액암 계통이며, 자궁암, 유방암, 폐암 등 일부 고형암의 치료에도 사용되고 있음. 백혈병의 세계 시장 규모는2020년까지3.84% 성장. 환자수는 약80만명 이상으로 증가. |
|
기타사항 |
- |
⑥ 면역항암제(PD-L1)
|
구분 |
합성 신약 |
|
적응증 |
흑색종 및 비소세포폐암 |
|
작용기전 |
저분자화합물 PD-L1 저해제 : 암세포의 면역회피경로를 차단함으로써 체내 면역체계를 활성화시키고 면역세포가 선택적으로 암세포만을 공격하도록 유도하는 기전임. |
|
제품의 특성 |
당사는 기존의 표적항암제 개발 파이프라인을 통해 축적된 의약화학 전문기술을 바탕으로 기존 표적항암제의 부작용 및 내성문제와 항체의약품의 한계를 극복한 저분자 화합물을 기반으로 하는 효율적이고 안전하며 혁신적인 경구용 면역항암제 상용화를 위한 파이프라인을 구축하는 차별화 전략을 수립하였음. PD-L1 저분자 저해제는 기존 anti-PD-1/PD-L1 mAb인 주사제의 단점을 극복한 경구투여 약물로 개발함으로써 환자의 복용 편의성 증대, 항체보다 단시간 작용(short-acting)하여 immune-related adverse events (irAEs)에 대한 관리가 용이, 항체의 Fc region에 의한 항체의존세포매개세포독성(antibody-dependent cell-mediated cytotoxicity, ADCC)으로 인한 독성을 유발하지 않음 등과 같은 장점을 가지고 있음. |
|
진행경과 |
전임상 후보물질 도출 중 |
|
향후계획 |
전임상 후보물질 도출 및 전임상 연구 및 임상 진입 |
|
경쟁제품 |
Incyte(INCB086550, 저분자화합물), BMS(옵디보), MSD Japan/Merck(키트루다): 면역항암제 중에서, 면역체크포인트 치료제 시장의 선두주자는PD-1/PD-L1을target으로 하는BMS와Merck며, 현재 승인된 암 외의 다양한 암 종으로의 적응증을 확대하는 중임. |
|
관련논문 |
- |
|
시장 규모 |
항암제 시장의 높은 성장 요인은 면역항암제 시장의 높은 성장의 결과로, Research And Markets에 따르면 2017년 $ 10.5 billion에서 2022년 $ 100 billion을 넘어설 것으로 예상함. |
|
기타사항 |
- |
⑦ 면역항암제(CD73)
|
구분 |
합성 신약 |
|
적응증 |
혈액암(AML, AL, MM, DLBCL) 및 고형암(삼중음성 유방암, 흑색종, 비소세포폐암, 췌장암, 자궁암, 전립선암) |
|
작용기전 |
CD73 저분자 저해제 : 암세포의 면역회피경로를 차단함으로써 체내 면역체계를 활성화시키고 면역세포가 선택적으로 암세포만을 공격하도록 유도하는 기전임. |
|
제품의 특성 |
당사는 특허성이 있는 저분자 물질로써 다양한 ecto-효소 및 ADP-activated receptors에 대한 CD73효소의 선택성을 가지고, 경구 투여가 가능한 우수한 효능의 저분자 저해 물질의 발굴을 목표로 함 |
|
진행경과 |
후보물질 도출 (우수한 생리활성 및 약동학적 효능확보) |
|
향후계획 |
전임상 후보물질 확정 |
|
경쟁제품 |
저분자 화합물, Arcus(AB680), Eli Lilly(LY3475070); 항체치료제, 아스트라제네카(MEDI9447), BMS(BMS-986179) 등: 현재 임상진행 중인CD73타겟의 면역항암제는 항체의약품이 주 축을 이루고 있으며 이에 뒤따라 저분자화합물 기반의 약물은 2종(임상1상)으로써 저분자화합물이 가지는 특장점을 확보하는 미충족의학적수요를 충족시킬 만한 약물개발에 관심이 집중되는 상황임. 그 외에는 대부분 개발 초기 단계이거나 2-3개 회사 정도가 비임상 단계임 상태임. |
|
관련논문 |
- |
|
시장 규모 |
항암제 시장의 높은 성장 요인은 면역항암제 시장의 높은 성장의 결과로, Evaluate Pharma 조사 결과 2014년 14억 달러에 불과했던 면역항암제 시장은 2022년 300억 달러로 증가할 것으로 예상함. |
|
기타사항 |
- |
⑧ 표적 항암제
|
구분 |
합성 신약 |
|
적응증 |
관절염, 건선, 혈액암(lymphoma) ACB-DLBCL |
|
작용기전 |
IRAK4 (Interleukin 1 Receptor Associated Kinase 4)저해제 : Interleukin 1 Receptor Associated Kinase 4는 세포의 표면에 존재하는 Toll Like Receptor/IL-1beta(TLR/1L-1b)라고 불리 우는 수용체로부터 전달되는 세포 신호 전달의 매개체로서 중요한 역할을 하는 serine/threonine 인산화효소(Kinase)의 일종임..MyD88과 IRAK4, IRAK1과의 복합체를 형성하게 되고 형성된 복합체는 NF-kB 신호전달을 통해 세포핵에서의 전사인자를 활성화시켜 면역 및 염증 반응을 유발함. |
|
제품의 특성 |
자가면역질환 및 항암효능을 극대화시킬 수 있는 dual inhibitor 개발을 목표함. |
|
진행경과 |
2018.11 기술도입(충남대 학교 산학협력단) 리드최적화를 통해 확보된 약물의 in vitro & in vivo POC 검증 완료 |
|
향후계획 |
전임상 후보물질 도출 |
|
경쟁제품 |
항암제로서는 Aurigene/Curis(CA-4948)가 임상에 진입한 것 외에는 IRAK4 저해제는 전임상 단계 및 biological testing단계에 대부분 머무르고 있음. 관절염치료제로서는 PF-06650833이 임상 2상 완료됨 |
|
관련논문 |
- |
|
시장 규모 |
DLBCL 시장은 2016년 2.2 billion 달러에서 2025년 3.5 billion달러로 성장 예측되며 이 기간 사이에 DLBCL의 표준치료제인 Rituximab이 2019년 특허가 만료됩니다. 따라서 Rituximab의 biosimiliar가 시장의 판도에 영향을 미치게 되면서 전체 마켓은 점차적으로 성장되는 것으로 예측되고 있음. |
|
기타사항 |
- |
당사가 영위하는 바이오산업의 특성 상 전임상에 대한 성공 후 진행될 임상시험에서 임상실패로 인하여 예상 임상시험비용을 초과하여 비용이 지출되거나, 소요된 연구개발비용의 회수 가능성이 현저히 낮아지는 경우 당사의 수익성 및 재무안정성에 부정적인 영향을 미칠 수 있습니다. 투자자께서는 이와 같이 당사가 지니고 있는 바이오의약품 연구개발의 파이프라인별 임상성공 확률과 임상실패 위험 및 임상시험 비용 등을 면밀히 검토하여 투자에 임하시길 바랍니다.
|
다. 기술이전 지연 및 실패에 따른 위험 |
당사와 같은 바이오벤처는 신약 개발사업이 태생적으로 부담하고 있는 낮은 임상성공률, 대규모 개발비용, 오랜 개발기간에 따른 리스크를 국내외 대형 제약사와 분산하기 위하여 개발 초기단계에서 기술이전함으로써 조기에 수익을 시현하는 것을 기본적 수익모델로 삼고 있습니다. 국내외 대형 제약사 또한 대규모 개발비용을 감수하고 성공확률이 높은 약제로의 선택과 집중을 통해 최상의 결과를 얻고자 사내 연구개발에만 의존하지 않고 외부에서 신약 개발의 기회를 찾는 오픈 이노베이션(open innovation) 전략을 적극적으로 추진하는 추세에 있습니다.
Evaluate Pharma의 'Evaluate Pharma World Preview 2021 Outlook to 2026'에 따르면 글로벌 의약품 R&D 투자는 2012년 1,370억달러에서 2020년 1,980억달러로 연 평균 4.7% 성장한 것으로 추정하였습니다. 또한 향후 6년간 연평균 4.2% 증가하여 2026년에는 2,540억달러에 이를 것으로 전망하였습니다.
2026년 의약품 연구개발(R&D) 투자액 상위 1위 기업은 로슈(Roche)로, 연구 개발 투자액 140억달러에 달할 것으로 전망하였고, 다음으로는 존슨앤존슨(Johnson & Johnson) 122억달러, 머크(Merck & Co) 114억달러 화이자(Pfizer) 105억달러 등의 순으로 전망하였습니다.
| [글로벌 제약기업들의 R&D 비용 추이 및 전망] |
|
| 출처) 바이오의약품 산업동향 보고서, KoBIA, 2021.12 |
한편, 2022년 2월 Biotechnology Innovation Organization(BIO) 발간 'The State of Innovation in Antibacterial Therapeutics'에 따르면 2011년부터 2021년 3분기까지 10년 동안 전세계 제약ㆍ바이오 벤처회사의 라이선스 아웃 딜(계약금 규모 1천만 달러 이상)을 분석한 결과 거래건수는 2011년 109건에서 2020년 238건, 2021년 3분기 195건으로 증가하였고, 계약금(upfront) 규모는 2011년 34억달러에서 2020년 162억달러, 2021년 3분기 73억달러로 증가하였습니다.
해당 기간 라이선스 아웃 딜 중 매년 발생하는 건수 중 평균 55.3%가 전임상 단계에서 체결되었습니다. 전임상 단계에서 발생하는 라이선스 아웃 계약금(upfront) 총 규모는 평균 23억달러이며 이는 매해 발생하는 계약금의 평균 37.7% 비중입니다.
이에 더해 라이선스 아웃 딜 총 규모(계약금, 임상/허가/세일즈 마일스톤 등 모든 금전적 보상의 합산금액) 기준 전임상 단계에서 발생하는 금액은 평균 422억달러이며, 매해 발생하는 금액 대비 평균 58.5%입니다.
상기 사실로 미루어 볼 때 신약 후보물질의 안전성과 효능이 임상 단계에서 입증되기 전이라고 하더라도 그 잠재력만으로도 높은 가치를 인정받을 수 있음을 알 수 있습니다.
| [제약ㆍ바이오 벤처회사의 라이선스 아웃 딜 현황 (임상단계별)] |
| (단위 : 건, 십억달러) |
|
구분 |
2011년 |
2012년 |
2013년 |
2014년 |
2015년 |
2016년 |
2017년 |
2018년 |
2019년 | 2020년 | 2021년 3분기 | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | 건수 | 계약금 | 총 규모 | |
|
전임상 |
65 |
1.6 |
13.1 | 50 |
0.6 |
13.6 | 63 |
1.3 |
15.1 | 69 |
1.6 |
16.8 | 79 |
2.4 |
29.7 | 78 |
2.6 |
47 | 78 |
1.9 |
38 | 111 |
3.7 |
62.4 | 107 | 2.9 | 64.1 | 134 | 4.7 | 105.3 | 95 | 1.8 | 59 |
|
임상1상 |
10 |
0.2 |
4.1 | 13 |
0.2 |
2.7 | 14 |
0.5 |
8 | 16 |
0.5 |
3.3 | 16 |
1.8 |
8.6 | 9 |
0 |
1.5 | 22 |
0.7 |
10.9 | 18 |
0.4 |
6 | 14 | 0.5 | 7.7 | 24 | 2.3 | 12.4 | 18 | 0.4 | 5.1 |
|
임상2상 |
21 |
0.6 |
6.3 | 22 |
0.9 |
5.4 | 21 |
0.5 |
4.2 | 26 |
1.3 |
10 | 31 |
1.8 |
13 | 22 |
0.6 |
6.8 | 24 |
1.2 |
5.8 | 33 |
1.8 |
18.6 | 32 | 3.7 | 15.7 | 38 | 4.3 | 18 | 41 | 2.8 | 18.1 |
|
임상3상 |
13 |
1 |
5.2 | 13 |
0.5 |
3.4 | 10 |
0.2 |
1.7 | 18 |
2.2 |
9.6 | 19 |
1 |
4.9 | 20 |
0.6 |
3.7 | 33 |
0.7 |
5.6 | 29 |
3.5 |
11.7 | 33 | 6 | 18.4 | 42 | 4.9 | 18.3 | 41 | 2.3 | 13.5 |
|
합계 |
109 | 3.4 | 28.7 | 98 | 2.2 | 25.1 | 108 | 2.5 | 29 | 129 | 5.6 | 39.7 | 145 | 7 | 56.2 | 129 | 3.8 | 59 | 157 | 4.5 | 60.3 | 191 | 9.4 | 98.7 | 186 | 13.1 | 105.9 | 238 | 16.2 | 154 | 195 | 7.3 | 95.7 |
| 출처) Emerging Therapeutic Company Investment and Deal Trends(BIO, 2022) |
| 주) 라이선스 아웃 딜 계약금 규모 1천만 달러 이상 |
당사가 주력하고 있는 퇴행성 신경질환 및 항암제 시장은 새로운 치료제에 대한 의약적 요구가 높고, 시장의 관심이 주목되어 있는 분야로, 일반적인 경우와 비교하여 신약개발의 초기단계라고 할 수 있는 후보물질 도출 혹은 전임상 단계에서도 활발한 기술이전 및 기업합병이 일어나고 있습니다. 따라서 기술의 주요 수요자인 글로벌제약사들의 기술도입(in-licensing) 건수나 계약규모가 빠른 성장을 하고 있고 이러한 추세는 향후 더욱 가속화될 것으로 판단됩니다.
기술수요자인 글로벌 제약사들은 최근 보유제품의 특허 만료에 따른 급격한 매출감소 등 제약시장의 환경변화로 대부분의 글로벌제약사가 개발후보를 외부에서 아웃소싱 하는 전략을 점차 강화하고 있습니다. 따라서 수요측면에서 보면 단기, 중기, 장기적으로 기술이전의 건수나 규모가 성장할 것으로 추정됩니다.
반면 공급의 측면에서 보면 긴 개발기간과 막대한 개발자금 더불어 전문연구인력과 오랜 경험이 필요한 신약연구 개발의 특성을 고려할 때 기술 공급자의 수가 급격히 증가하기는 어려울 것으로 판단됩니다. 줄기세포치료제 등의 새로운 기술들이 지속적으로 개발되고 있으나 신약개발후보를 급격히 증가시킬 수 있는 급격한 기술 변동은 쉽지 않을 것으로 전망 됩니다.
당사는 전략적 기술이전을 통하여 파트너확보와 공동연구를 진행하고 있습니다. 당사의 기술이전 시점을 후보물질 및 초기 임상개발 완료 단계에서 이루어지며, 공동연구, 기술제휴를 통하여 미래의 전략적 파트너를 확보하고 있습니다. 연구개발을 통해 확보된 기술을 더욱 높은 가치로 효과적으로 판매하기위해 사업개발 부서의 조직의 전문성을 강화하여 사업성과로 인한 이익실현을 앞당기고 협상의 역량을 높여 매출실적을 확대해 나아갈 계획입니다.
더불어 당사의 기술자문위원회(SAB)의 전문적 기술 네트워킹을 확대해 기술이전의 가능성을 높이고 개발 물질의 유효성과 경쟁력을 각종 전문학술 학회와 비즈니스 컨퍼런스에 통해 높은 우수성을 입증하고 당사의 인지도 및 기술력을 높이는 기회의 창구로 활용할 예정입니다.
당사의 Risk 최소화를 하기위해서 각 분야의 전문가(변호사, 변리사)들의 자문 및 역량을 강화하여 기술이전을 위한 전략을 수립하여 성공적 기술 사업화 활동을 지속해 나아갈 예정입니다.
하지만 당사의 이러한 노력에도 불구하고 글로벌 기술이전 거래 건수 및 규모의 감소, 제약/바이오 시장의 수요 감소, 글로벌 제약사들의 사업전략 변동 등의 이유로 인해 기술이전이 예상보다 지연되거나 실패하는 경우 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
|
라. 기술 이전 파트너사의 약물 상업화 실패에 따른 수익 감소의 위험 |
높은 비용과 임상실패율, 오랜시간이 소요된다는 신약개발 사업의 특성상 많은 바이오벤처기업들이 일정한 파이프라인에 대해서는 기술이전을 사업모델로 하고 있습니다.
당사의 매출발생 또한 기술이전을 통해서 이루어지며, 당사는 라이선스 아웃을 위한 국내외 제약회사를 대상으로 학회, 전시회 및 비즈니스 파트너링 행사 등 기술 교류의 장을 통한 지속적 개발 업데이트와 교류활동을 하고 있습니다.
당사는 보유 약물에 대한 기술이전시 아래와 같은 과정을 거치게 됩니다. 당사 신약개발 물질에 대한 데이터 및 경쟁사 대비 경쟁력을 분석, 상업화 전략을 수립하며, Non-Confidential, Confidential 자료를 제작하여 잠재고객의 관심도에 따라 지속적으로 업데이트를 합니다. 잠재 고객군 확보 후 당사의 물질에 대한 관심이 높으면, Confidential 자료를 제공하게 되는데, 이에 앞서 양사간 비밀유지협약을 체결하게 됩니다. 이 단계에서는 Confidential 자료 제공과 함께 자료검증에 관한 실사도 진행됩니다. 기술에 대한 실사가 완료되어 기술이전이 더 진전될 경우, 양사는 기술이전에 대한 주요 계약사항을 협의하게 됩니다. 이후 세부 계약사항을 조율하고 확정하여 계약체결을 완료하게 됩니다.
| [기술이전 프로세스] |
|
| 출처) 당사 정기보고서 및 당사 제시 |
일반적으로 기술이전이 이루어지게 되면, 추가개발은 라이선스 인을 한 기업에서 진행하며 계약에 따라 별도로 추가개발을 진행할 수도 있습니다. 라이선스 인한 기업에서는 추가개발 상황 및 임상시험결과에 따라 마일스톤 및 로열티를 지급하게 되는데 이러한 수익구조는 다음과 같이 정리할 수 있습니다.
| [라이선스 계약 수익구조] |
| 구분 | 내용 | |
|---|---|---|
| 총계약금액 | 계약금 | 계약 체결 직후 또는 일정기간 내에 받게 되는 금액 |
| 마일스톤 | 전임상, 임상, 허가신청, 허가완료 등 개발 단계별로 성공시 받게 되는 금액 | |
| 로열티 | 기술 이전으로 생산된 제품의 매출에 따라 받게 되는 금액 (통상 매출액 대비 비율로 책정) |
|
계약금은 계약 직후 수령하게 되는데, 계약조건에 따라 반환의무가 있을 수 있습니다. 마일스톤의 경우 추가개발 진행상황에 따라 수취하게 되는 금액이며, 로열티는 최종 허가 이후 해당 제품이 매출을 발생시킬 경우 받게 되는 수수료입니다.
기술이전을 받은 기업이 추가개발에 실패하거나 상업화가 원활히 진행 되지 않는 경우, 반환의무가 있는 계약금이나 마일스톤 등은 기술이전을 완료했더라도 지급의무가 발생할 수 있습니다. 또한 총 금액은 임상시험 결과에 따라 중도에 해지되거나 금액이 감소 될 수 있습니다.
당사는 증권신고서 제출 전일 현재 6건의 라이선스아웃 계약을 체결하였으며, 그 현황과 상세 내역은 아래와 같습니다.
|
[라이선스 아웃 계약 총괄표] |
| 구분 |
품목 |
계약상대방 |
대상지역 |
계약체결일 |
계약종료일 |
총 계약금액 |
수취금액 |
진행단계 |
|---|---|---|---|---|---|---|---|---|
| 1 |
에이즈치료제 |
Jiangsu Aidea Pharmaceutical |
중국, 홍콩, 대만 |
2014.10.10 |
특허 만료일 |
USD 1,700,000 |
USD 1,700,000 |
NDA승인, |
| 2 |
항암제 |
Jiangsu Aidea Pharmaceutical |
중국, 홍콩, 대만 |
2015.12.10 |
특허 만료일 |
USD 1,500,000 |
USD 1,500,000 |
임상 1상 진행 |
| 3 |
항암제 |
Jiangsu Aidea Pharmaceutical |
중국, 홍콩, 대만 |
2015.12.10 |
특허 만료일 |
USD 2,500,000 |
USD 1,000,000 |
전임상 |
| 4 |
대사질환치료제 |
CROWN BIO |
전세계 |
2014.07.22 |
특허 만료일 |
USD 3,600,000 |
- |
전임상 |
| 5 | 뇌신경질환 치료제 (KM819) |
FAScinate Therapeutics | 전세계 (한국 제외) |
2021.09.27 | 특허 만료일 | USD 2,000,000 | USD 2,000,000 | 임상2상 진행 (미국) |
| 6 | 항암제 (KM-10544) |
Emmaus Life Science, Inc. | 미국, 유럽, 영국 | 2021.10.06 | 특허 만료일 | USD 1,500,000 | USD 1,500,000 | 전임상 진행 |
| 합계 | USD 12,800,000 | USD 7,700,000 | - | |||||
(1) 에이즈 치료제(KM-023)
|
계약상대방 |
Jiangsu Aidea Pharmaceutical (중국) |
|
계약 내용 |
Jiangsu Aidea Pharmaceutical은 에이즈치료제(KM-023)에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
중국, 홍콩, 대만 |
|
계약 기간 |
계약체결일: 2014.10.10 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 1,700,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 1,700,000 - 수취조건: 계약 체결시 마일스톤(Milestone) - 해당사항 없음 로열티(Royalty): 단일정을 포함한 복합제제 매출액의 2% - 수취조건: 매출 발생시 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
|
회계처리방법 |
계약금 수취액 USD 200,000은 2014년 10월 ~ 2015월 09월까지 12개월 동안 분할하여 수익인식 USD 1,500,000은 2017년 12월 일시 수익 인식 |
(2) 항암제(KM-635)
|
계약상대방 |
Jiangsu Aidea Pharmaceutical (중국) |
|
계약 내용 |
Jiangsu Aidea Pharmaceutical은 항암제(KM-635)에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
중국, 홍콩, 대만 |
|
계약 기간 |
계약체결일: 2015.12.10 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 1,500,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 1,500,000 - 수취조건: 계약 체결시 마일스톤(Milestone) - 해당사항 없음 로열티(Royalty): 순매출액의 10% - 수취조건: 매출 발생시 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
|
회계처리방법 |
계약금 수취액 USD 1,000,000은 2015년 12월 ~ 2016년 11월까지 12개월 동안 분할하여 수익인식 USD 500,000은 2017년 12월 일시 수익 인식 |
(3) 항암제(KM-630)
|
계약상대방 |
Jiangsu Aidea Pharmaceutical (중국) |
|
계약 내용 |
Jiangsu Aidea Pharmaceutical은 항암제(KM-630)에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
중국, 홍콩, 대만 |
|
계약 기간 |
계약체결일: 2015.12.10 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 2,500,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 1,000,000 - 수취조건: 계약 체결시 마일스톤(Milestone) - Upon Initiation of Phase 2 Clinical Trial USD 500,000, Initiation of Phase 3 Clinical Trial USD 500,000, Regulatory approval by SFDA USD 500,000 로열티(Royalty): 순매출액의 10% - 수취조건: 매출 발생시 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
|
회계처리방법 |
계약금 수취액 USD 1,000,000은 2015년 12월 ~ 2016년 11월까지 12개월 동안 분할하여 수익인식 |
(4) 대사질환 치료제
|
계약상대방 |
CROWN BIO (중국) |
|
계약 내용 |
CROWN BIO는 대사질환 치료제에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
전세계 |
|
계약 기간 |
계약체결일: 2014.07.22 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 3,600,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): - 해당사항 없음. 마일스톤(Milestone): USD 3,600,000 - 수취조건: 중국 임상 1상 개시 USD 100,000, 중국 임상 2상 개시 USD 500,000, 중국 임상 3상 개시 USD 1,000,000, 중국 의약품허가 USD 2,000,000 로열티(Royalty): 순매출액의 10% - 수취조건: 매출 발생시 재실시권 수익 분배비율: 각 단계별 지분율 IND (50%), 임상 1상 (40%), 임상 2상 (25%), 임상 3상 (10%)
|
|
회계처리방법 |
- |
(5) 뇌신경계 치료제(KM-819)
|
계약상대방 |
FAScinate Therapeutics Inc. |
|
계약 내용 |
FAScinate Therapeutics는 뇌신경계 치료제에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
전세계 (한국 제외) |
|
계약 기간 |
계약체결일: 2021.09.27 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 2,000,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 2,000,000 - 해당사항 없음 로열티(Royalty): 순매출액의 10%
|
|
회계처리방법 |
USD 2,000,000은 2021년 9월 일시 수익 인식 |
(6) 표적항암제 (IRAK4 저해제)
- IRAK4 저해제의 경우, 엠마우스라이프 사이언스와 공동연구개발 계약에 이어 기술이전으로까지 확장되여 계약이 체결되었습니다.
|
계약상대방 |
엠마우스라이프사이언스(Emmaus life Science, Inc.) (미국) |
|
공동연구/기술이전 계약 내용 |
공동연구: IRAK4 저해제에 대한 치료작용기전(MOA) 연구, 전임상연구 등에 관한 공동연구개발 계약 |
|
공동연구/기술이전 |
공동연구 계약체결일: 2021.03.02 ~ 기술이전과 동시에 계약 종료 |
|
총 계약금액 |
공동연구 계약시: USD 1,000,000 (50% 현금 수취, 50%는 계약상대방의 주식 수취) |
|
계약조건 |
계약금(Upfront payment): USD 1,000,000 (50% 현금 수취, 50%는 계약상대방의 주식 수취)
|
|
회계처리방법 |
기술이전과 동시에 공동연구개발 계약 및 기술이전에 따른 계약금을 2021.10.06에 일시에 수익 인식 |
이러한 당사의 향후 계획에도 불구하고 당사의 기술이전 파이프라인 및 향후 개발 진행 예정인 파이프라인의 임상 등에서의 예상치 못한 독성이 관찰되거나 효능이 기대에 미치지 못할 수 있습니다. 또한 기술이전한 파트너사의 임상수행 능력, 파트너사 내부적인 이유로 임상진행을 중단할 가능성도 존재합니다.
한편, 당사는 경구용 에이즈치료제(KM-023)를 임상 1상 완료 이후 2014년 10월 중국 제약사 장수 아이디어(Jiangsu Aidea Pharmaceuticals)로 기술이전하여 ACC007라는 약물로 개발해왔으며, ACC007, 테노포비르(TDF), 라미부딘(3TC)를 함께 처방하는 방식으로 2021년 06월 NDA(New Drug Application, 의약품 품목 허가)를 승인받아 2022년부터 시판하고 있습니다. 당사는 시판 예정인 단일 복합정 ACC008을 포함하여 라이선스 아웃 계약에 매출의 2%를 로열티로 수취 예정입니다. 그러나 해당 약물의 수요가 예상치를 하회하여 로열티 매출 규모가 부진할 경우 당사의 수익성 개선에 악영향을 미칠 수 있습니다.
이처럼 임상 개발 또는 약물의 상업화에 실패할 경우 수취 예정인 마일스톤 및 로열티가 감소하여 수익성과 재무안정성에 부정적인 영향을 미칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| 마. 연구개발파트너 계약 중단 관련 위험 당사는 개발물질의 사업화를 위해 전략적 파트너사, 다국적 제약회사 관계자, 각 분야의 전문가와 교류를 유지하고 있습니다. 특히, 해외 유수의 제약기업과의 파트너링을 지속적으로 진행함으로써 기술이전을 대비한 네트워킹 유지를 위해 노력하고 있습니다. 당사의 기술이전 전략인 제한적 실시권을 부여하는 동시에 공동연구개발을 추진함으로써 연구개발 결과를 추후에 활용하여 글로벌 제약사의 기술이전 기회를 확보하는 전략을 추진하고 있습니다. 당사의 공동연구파트너들은 공동연구 계약에 따라 해당 약물에 대한 공동연구개발을 수행하고 있으며, 당사의 경영진이나 주주로서 관계를 가지고 있지 않습니다. 따라서 공동연구개발 계약이 예기치 못한 사유로 인해 중단될 경우 약물의 상업화가 불투명해질 수 있습니다. 투자자 여러분들께서는 이 점 유의하시기 바랍니다. |
당사는 혁신적인 신약 개발을 위한 후보물질 창출 및 초기 임상까지의 연구개발을 자체적으로 수행하고 이를 기술이전 전략을 통한 글로벌 시장으로 진출하고자 하는 신약개발 전문 기업입니다.
당사는 개발물질의 사업화를 위해 전략적 파트너사, 다국적 제약회사 관계자, 각 분야의 전문가와 교류를 유지하고 있습니다. 특히, 해외 유수의 제약기업과의 파트너링을 지속적으로 진행함으로써 기술이전을 대비한 네트워킹 유지를 위해 노력하고 있습니다. 기술이전 잠재고객 확보를 위해서 각종 학회 및 바이오 전문 파트너링 컨퍼런스 참여를 하는 등 다양한 방법으로 기술이전 및 사업화를 적극적으로 추진하며, 전략적 기술이전과 공동연구(파트너)를 진행하고 있습니다.
당사의 기술이전 전략인 제한적 실시권을 부여하는 동시에 공동연구개발을 추진함으로써 연구개발 결과를 추후에 활용하여 글로벌 제약사의 기술이전 기회를 확보하는 전략을 추진하고 있습니다.
또한, 당사는 파이프라인의 가치를 극대화하기 위하여 지적재산권을 확보하고, 추가 연구를 통한 특허 취득으로 지적 재산권 확대를 지속적으로 수행하고 있습니다. 당사의 주요기술이전과 공동연구 실적은 다음과 같습니다.
|
[기술이전 및 주요공동연구 실적] |
|
구분 |
파트너사 |
파이프라인/년도 |
권리범위 |
|---|---|---|---|
|
기술이전 및 공동연구 |
장수 아이디어(Jiangsu Aidea Pharmaceuticals) |
에이즈 치료제 (KM023)/2014년 |
중국시장에 대한 전용 재실시권 이전 글로벌 시장 전용실시권 보유 |
|
에피제네틱 항암제 (KM-635)/2015년 |
중국시장에 대한 전용 실시권 이전 글로벌 시장 실시권 보유 |
||
|
세포독성 항암제 (KM-630)/2015년 |
중국시장에 대한 전용 실시권 이전 글로벌 시장 실시권 보유 |
||
|
기술이전 및 공동연구 |
Crown Bio |
비만/당뇨 치료제 (KM001)/2014년 |
전 실시권 이전 |
|
공동연구 |
PICC |
파킨슨병 치료제 (KM-819)/2018년 |
공동연구/공동임상 개발 |
|
공동연구 |
UCSD |
파킨슨병 치료제 (KM-819)/2018년 |
공동연구 |
|
공동연구 |
신테카바이오 |
파킨슨병 치료제 (KM-819)/2018년 |
공동연구 |
|
공동연구/기술이전 |
Emmaus |
급성백혈병치료제 (KM-10544)/2021년 |
미국, 유럽, 영국 지역에 대한 전용실시권 이전 |
| 공동연구/기술이전 | 엠디뮨 | 항암제 (FAF1-exosome)/2021년 |
전세계 통상실시권 확보 |
| 출처) 당사 정기보고서 및 당사 제시 |
당사의 공동연구파트너들은 공동연구 계약에 따라 해당 물질에 대한 공동연구개발을 수행하고 있으며, 당사의 경영진이나 주주로서 관계를 가지고 있지 않습니다. 따라서 공동연구개발 계약이 예기치 못한 사유로 인해 중단될 경우 물질의 상업화가 불투명해질 수 있습니다. 투자자 여러분들께서는 이 점 유의하시기 바랍니다.
| 바. 목표시장 내 수익성 감소에 따른 위험 현재 파킨슨병 치료제 연구개발 현황을 살펴보면, 질병의 진전을 제어할 수 있는 질병조절 치료제의 개발이 매우 시급한 상황이며 연구개발이 활발하게 진행되고 있으나 현재 적절한 치료제는 전무한 상황에 있습니다. 에이즈 치료제는 Sustiva을 포함하여 4개가 시판 중에 있으며, NNRTI 약물은 내성이 잘 생기고 장기복용시 독성 및 부작용의 문제로 인해 제한적으로 사용되고 있습니다. 당사는 파킨슨병 치료제 및 에이즈 치료제 등 현재 의학적 미충족 수요가 높은 질환 시장을 목표로 하여 각 파이프라인별로 경쟁구도 및 경쟁제품 개발 파이프라인 동향을 면밀하게 분석한 후 당사의 경쟁우위요소를 바탕으로 사업전략을 수립하고 있습니다. 하지만 당사의 이러한 노력에도 불구하고 의학적 미충족 수요의 변화, 경쟁제품의 연구개발 속도, 경쟁사의 가격정책 및 마케팅전략 변화, 새로운 치료제의 등장, 당사 파이프라인의 연구개발 속도 등의 이유로 인해 당사 파이프라인의 시장경쟁력이 약화되는 경우 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. |
당사가 보유하고 있는 파이프라인의 경쟁구도, 경쟁제품 개발현황 및 당사 사업전략은 다음과 같습니다.
1) 파킨슨병(Parkinson's Disease)
GlobalData 보고에 따르면 주요 7개국(미국, 일본, 프랑스, 독일, 이탈리아, 스페인, 영국)의 파킨슨병 치료제(현재 시판 중인 증상완화제) 시장은 2019년 35억 달러였으며, 특히 미국 시장은15억 달러로 주요 7개국 시장의 50.2%를 차지하였습니다. 2019년을 기준으로 파킨슨병 시장은 CAGR(복리법연평균성장률) 12.6%의 증가율로 2029년 115억 달러로 증가할 것으로 예상하고 있습니다(GlobalData, 2021).
| [주요 7개국 파킨슨병 치료제 시장동향] |
|
| 출처) GlobalData, 2021 |
주요 7개국(미국, 일본, 프랑스, 독일, 이탈리아, 스페인, 영국)을 기준으로 2019년 243.4만명이 파킨슨병으로 진단받았으며, 2029년에는 299.9만명이 파킨슨병으로 진단받아 AGR(단순연평균성장률) 2.32%를 기록할 것으로 예측하였습니다. 이중에서도 미국 시장에서의 환자수 78.2만명에서 105.6만명으로 가장 가파른 환자 증가율인 AGR(단순연평균성장률) 3.50%를 보일 것으로 예측하였습니다. (Globaldata, 2021)
현재 퇴행성 뇌 질환 치료제 개발은 전세계적 글로벌 제약사부터 바이오 벤처까지 활발히 연구되고 있습니다. 미국 임상 시험 등록 사이트 (ClinicalTrials.gov)에 등록된 파킨슨병 치료제 임상 시험은 총 3,194건으로 대부분 알츠하이머병 치료제의 적응증 확장, 레보도파(Levodopa) 계열의 신규 제형 약물과 같은 일시적 증상 완화제입니다.
현재 파킨슨병 치료제 연구개발 현황을 살펴보면, 질병의 진전을 제어할 수 있는 질병조절 치료제의 개발이 매우 시급한 상황이며 연구개발이 활발하게 진행되고 있으나 현재 적절한 치료제는 전무한 상황에 있습니다. 따라서 도파민을 보충해주는 증상완화제로 병의 증상을 줄여 생활에 도움이 되는 방법이 현재 표준 치료제로 사용되고 있습니다. 증상 완화제는 도파민 대체제, 도파민 효현제, MAO-B 저해제, COMT 저해제 등이 있습니다. 이러한 증상 완화제는 부족한 효능, 약물에 대한 빠른 내성과 약물소진 현상으로 인한 심각한 부작용 등의 문제가 있으며 질병의 진전은 계속적으로 이뤄져 중기 이후 더 이상 큰 효능이 없습니다.
최근 파킨슨병의 근본적 치료제 개발이 활발히 이루어지고 있으며 생물학적 제제인 항체치료제로는 Roche, Biogen, Denali Therapeutics 가 개발을 하고 있습니다. 그러나 대부분의 항체 의약품의 경우 혈액 뇌 관문(BBB) 통과율이 낮아 개발의 한계를 가지고 있습니다. 환자의 복용 편의성을 고려하여 경구용 제제로의 합성 의약품 개발이 필요하며 Abbvie, GSK, UCB 가 개발 중에 있으나, 아직 임상에서의 유효성을 확인한 약물은 없으며 타깃과 기전이 당사의 KM-819와는 다르기 때문에 경쟁보다는 시너지효과를 기대할 수 있습니다.
| [임상개발 중인 파킨슨병 치료제 파이프라인] |
|
| 출처) GlobalData, 2021 |
| [후기 개발 단계에 있는 파킨슨병 치료제] |
|
| 출처) GlobalData, 2021 |
2) 에이즈
NNRTI 계열의 에이즈 치료제는 Sustiva을 포함하여 4개가 시판 중에 있습니다. 에이즈치료제의 경우 여러 계열의 약물을 복합제제 형태로 복용하는 병행요법(combination therapy)을 표준용법으로 사용하고 있습니다. 가장 많이 사용되는 병용용법이 2개의 NRTI 약물과 1개의 NNRTI 약물의 병용용법으로 알려져 있습니다. 현재 시판중인 NNRTI 약물은 내성이 잘 생기고 장기복용시 독성 및 부작용의 문제로 인해 제한적으로 사용되고 있습니다. 에이즈는 만성질환으로 발전하고 있으며, 기존의 약제가 가진 부작용 및 복용의 제한과 같은 문제를 해결하기 위한 의약적 수요가 있으며 당사의 에이즈 치료제 KM-023(2014년 10월 중국 제약사 장수 아이디어(Jiangsu Aidea Pharmaceuticals)에 라이선스 아웃)은 기존 약제가 가진 항바이러스 활성을 유지하고 CNS 부작용에 안전하며 복용에 편의성을 높인 약제로 시장에서의 경쟁력을 갖추고 있습니다.
상기 내용과 같이 당사는 의학적 미충족 수요가 높은 질환 시장을 목표로 하여 각 파이프라인별로 경쟁구도 및 경쟁제품 개발 파이프라인 동향을 면밀하게 분석한 후 당사의 경쟁우위요소를 바탕으로 사업전략을 수립하고 있습니다. 하지만 당사의 이러한 노력에도 불구하고 의학적 미충족 수요의 변화, 경쟁제품의 연구개발 속도, 경쟁사의 가격정책 및 마케팅전략 변화, 새로운 치료제의 등장, 당사 파이프라인의 연구개발 속도 등의 이유로 인해 당사 파이프라인의 시장경쟁력이 약화되는 경우 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다.
| 사. 업무 위탁 기관 관련 위험 당사가 영위하고 있는 신약 개발사업은 치료효과를 보이는 선도물질의 개발, 최적화 과정을 통한 후보물질의 개발, 비임상시험을 진행하기 위한 후보물질의 생산 및 제조, 동물을 대상으로 한 효능 및 독성 시험, 임상시험을 진행하기 위한 임상시료의 생산 및 제조, 정상인 및 환자를 대상으로 한 효능 및 독성 시험을 거쳐야 합니다. 하지만 당사가 생산 및 임상시험 업무를 위탁한 CMO 및 CRO 자체의 사정으로 인한 의도하지 않은 결과를 통제하기 어려울 수 있습니다. CMO의 경우 생산 시료의 품질 저하나 생산 일정의 지연 등으로 신약 개발에 부정적인 영향을 줄 수 있으며, CRO의 경우 시험 일정 지연으로 인하여 신약 개발 일정을 지연시키거나 시험 결과 분석 상의 오류로 신약 개발과 관련된 의사 결정을 어렵게 할 수 있습니다. 이와 같이 업무위탁 기관을 활용할 경우 당사가 통제할 수 없는 위험요소로 인하여 당사의 신약 개발 일정 지연 또는 부정적 결과 도출 등이 발생할 수 있으며 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. |
당사가 영위하고 있는 신약 개발사업은 치료효과를 보이는 선도물질의 개발, 최적화 과정을 통한 후보물질의 개발, 비임상시험을 진행하기 위한 후보물질의 생산 및 제조, 동물을 대상으로 한 효능 및 독성 시험, 임상시험을 진행하기 위한 임상시료의 생산 및 제조, 정상인 및 환자를 대상으로 한 효능 및 독성 시험을 거쳐야 합니다.
비임상시험은 GLP(Good Laboratory Practice) 허가를 획득한 기관에서, 임상시험을 위한 시료의 생산은 GMP(Good Manufacturing Practice) 허가를 획득한 기관에서, 임상시험은 GCP(Good Clinical Practice) 허가를 획득한 기관에서 이루어져야 하며 GMP 시설 및 GCP 시설을 자체적으로 구축하는 데에는 막대한 시간과 비용이 투입되어야 합니다. 이에 따라 당사를 포함하여 신약 개발사업을 영위하고 있는 많은 벤처회사는 신약개발의 효율성을 높이고 리스크를 감소시키기 위하여 임상시험에 필요한 원료 및 완제 생산을 GMP 허가를 받은 의약품 생산 전문대행기관(Contract Manufacturing Organization, CMO)을 통해, 비임상 및 임상시험 실시는 GLP 및 GCP 허가를 받은 임상시험 전문수탁기관(Contract Research Organization, CRO)을 통해 위탁하고 있습니다.
당사의 파킨슨병 치료제의 의약품의 경우, 임상 1상 원료 의약품은 국내의 STpharm 에서 생산하였으며, 완제의약품은 cGMP 업체인 BioDuro에서 GMP 기준에 맞추어 생산을 완료한 경험이 있습니다. 이 업체를 통해 당사는 임상 2상을 위한 완제의약품의 생산할 계획입니다. 그 외에도 에이즈 치료제의 경우 파트너사인 장수아이디어가 GMP 인증을 받은 기관으로 완제의약품을 생산하여 임상을 진행하고 있습니다.
하지만 당사의 이러한 노력에도 불구하고 당사가 생산 및 임상시험 업무를 위탁한 CMO 및 CRO 자체의 사정으로 인한 의도하지 않은 결과를 통제하기 어려울 수 있습니다. CMO의 경우 생산 시료의 품질 저하나 생산 일정의 지연 등으로 신약 개발에 부정적인 영향을 줄 수 있으며, CRO의 경우 시험 일정 지연으로 인하여 신약 개발 일정을 지연시키거나 시험 결과 분석 상의 오류로 신약 개발과 관련된 의사 결정을 어렵게 할 수 있습니다. 이와 같이 업무위탁 기관을 활용할 경우 당사가 통제할 수 없는 위험요소로 인하여 당사의 신약 개발 일정 지연 또는 부정적 결과 도출 등이 발생할 수 있으며 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다.
|
아. 핵심연구인력유출 위험 하지만 당사의 이러한 노력에도 불구하고 우수한 전문인력의 부족, 국내외 경쟁사 또는 정부출연 연구기관으로의 유출 등의 사유로 인해 우수한 전문인력을 유지하거나 확보하는 데 어려움이 발생하여 당사의 사업경쟁력이 약화될 수 있으며 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다. |
연구개발 능력은 당사가 속한 산업의 특성상 매우 중요한 요소이며, 지속적인 연구개발을 위해 우수한 인재를 보유 및 유치하는 것이 회사의 성과를 결정하는 가장 중요한 요소입니다. 이는 제약 산업을 영위하고 있는 업체들에 공통적으로 적용되는 사항으로, 업계 내에서 우수한 인력 유치에 관한 경쟁은 점차 심화되고 있습니다. 또한, 주요 연구 인력의 유출이 있을 경우 해당 연구 개발과제가 지연되거나 개발전략을 수정해야 할 가능성이 존재하며, 개발비 부담 등으로 당사의 경쟁력 및 성장 가능성이 악화될 수 있습니다.
당사의 연구개발조직은 보고서 작성일 기준일, 대표이사 산하에 프로젝트 승인위원회를 중심으로 바이오의약연구본부, 임상개발본부, 헬스케어사업본부로 이루어져 있습니다. 바이오의약연구본부는 신약개발 프로젝트 기반으로 조직을 운영하고 있으며 각 프로젝트 책임자는 인력을 구성하여 프로젝트를 수행합니다. 이는 각 프로젝트의 특성을 고려하여 효율적이며 체계적인 관리 및 운영을 위해 도입된 시스템입니다.
| [연구개발 조직도] |
|
| 출처) 당사 정기보고서 및 당사 제시 |
당사는 박사급 5명, 석사급 4명 총 9명의 연구인력을 보유하고 있으며, 그 현황은 다음과 같습니다.
| [연구개발 인력 현황] |
| 구분 | 연구개발 | 사업개발/경영지원 | 합계 |
|---|---|---|---|
| 박사 | 5명 | - | 5명(19%) |
| 석사 | 6명 | 3명 | 9명(35%) |
| 학사 | - | 12명 | 12명(46%) |
| 합계 | 11명(36%) | 15명(64%) | 26명(100%) |
| 출처) 당사 정기 보고서 및 당사 제시 |
당사의 핵심 연구인력은 김인철 부회장, 이재문 사장, 김은희 바이오의약본부장이며, 그 현황은 다음과 같습니다.
| [핵심 연구개발 인력 현황] |
|
소속 |
근무지 |
직위 |
성 명 |
생년월일 |
담당업무 |
주요경력 |
주요 연구실적 |
|---|---|---|---|---|---|---|---|
|
경영 |
한국, 미국 |
부회장 |
김인철 |
1951.7.7 |
경영전략 및 사업개발 |
85.03 일리노이대학교 약리학박사 |
2009: 한국 CEO 연구포럼,머니투데이 서울대 경영연구소: 대한민국 CEO 그랑프리 의약품 부문 |
|
경영, 임상 |
한국, 미국 |
사장 |
이재문 |
1958.1.15 |
임상개발, 최고경영책임 |
89.05 미국 Duke University 생화학박사 01.01~10.12 EXELIXIS Pharmaceuticals 책임연구원 11.01~12.06 ARAGEN BIOSCIENCES 책임연구원 12.07~14.06 ㈜카이노스메드 이사 15.09~21.5 현재 ㈜카이노스메드 부사장 21.6~ 현재 ㈜카이노스메드 사장 |
생화학, 분자생물학, 유전학, 호르몬학, 세포생물학, 신경생물학 전공 |
|
바이오의약본부, 경영 |
한국 |
부사장 |
김은희 |
1958.5.12 |
바이오의약본부장 |
81. 서울대학교 미생물학과 학사 |
FAF1 단백질의 기능 연구 세계 1인자, 6편 이상의 논문 저자 |
김인철 부회장은 1951년생으로, 2019년 09월부터 당사에 합류하여 사내 약물 연구개발 프로젝트 총괄로 근무하고 있습니다. 당사가 임상연구를 진행하고 있는 모든 파이프라인의 연구 프로젝트를 총괄하고 있습니다.
이재문 사장은 1958년생으로, 2012년 07월부터 당사에 합류하여 회사 경영 및 KM-819 약물의 임상개발 책임자로 근무하고 있습니다. 당사가 연구개발하고 있는 KM-819(파킨슨병 치료제, 다계통위축증 치료제)의 임상연구를 총괄하고 있습니다.
김은희 본부장은 1958년생으로, 2021년 03월부터 당사에 합류하여 바이오의약본부장으로 근무하고 있습니다. 현재 당사와 엠디뮨이 공동연구개발하고 있는 FAF1-Exosome 항암제의 전임상연구를 총괄하고 있습니다.
당사는 지식과 경험이 풍부한 인력이 신약 연구개발 사업의 핵심 경쟁력이라는 사실을 인지하고 우수한 인력을 지속적으로 확보하고자 노력하고 있으며, 현재 보유하고 있는 핵심 인력을 유지하기 위하여 능력에 따른 연봉제, 스톡옵션 제도, 회사 비전 공유, 각종 복리후생제도 강화 등 합리적인 보상구조 및 애사심 고취에 힘쓰고 있으며 향후에도 이와 같은 정책을 확대할 계획입니다.
하지만 당사의 이러한 노력에도 불구하고 우수한 전문인력의 부족, 국내외 경쟁사 또는 정부출연 연구기관으로의 유출 등의 사유로 인해 우수한 전문인력을 유지하거나 확보하는 데 어려움이 발생하여 당사의 사업경쟁력이 약화될 수 있으며 이로 인하여 당사의 재무상태 및 영업실적에 부정적인 영향이 있을 수 있습니다.
| 자. 지적재산권 관련 위험 당사는 신약개발 기업으로서 지적재산권의 철저한 보호가 기업가치 유지의 핵심적인 요소입니다. 당사가 보유하고 있는 특허는 당사 주요 제품 개발의 핵심 요소이며 이러한 핵심 기술이 향후 성장을 결정하는 가장 중요한 사항인 만큼 지적재산권을 효과적으로 관리하지 못할 경우 경쟁 제품 출현 등으로 인해 경쟁력 확보에 어려움이 있을 수 있습니다. 당사는 보유하고 있는 기술에 대하여 향후 공동연구개발 추진, 라이선스 아웃, 경쟁회사의 유사 기술개발 방어 및 진입장벽 구축 등을 위해 지적재산권 확보 및 보호 전략을 수립하고 있습니다. 특히 파킨슨병 치료제 KM-819의 물질 특허가 19개국에 등록이 완료되어 있습니다. 당사는 물질특허 외에도 알파시누클라인(α-synuclein)에 대한 축적억제 작용기전을 규명(용도) 및 Salt form 제법에 대한 PCT 출원을 완료하였기 때문에, 특허 보호기간(또는 PMS기간) 동안 물질, 용도, 제재에 대한 모방은 원천적으로 막을 수 있습니다. 다만, 그럼에도 불구하고, 향후 제3자에 의하여 당사가 보유하고 있는 특허권에 대한 소송 또는 기타 분쟁이 발생할 가능성을 배제할 수 없으며, 임상시험 또는 제품 상용화에 실패하여 특허 연장을 하지 못할 경우, 특허가 만료되어 동일 기반 기술의 경쟁 제품이 개발될 수 있음에 따라 당사의 손익에 부정적인 영향을 미칠 수 있습니다. |
당사와 같은 신약 연구개발기업은 특허의 출원 및 등록 관련제도를 통한 지적재산권의 철저한 보호 등 핵심 원천기술 확보가 기업가치 유지의 핵심적인 요소입니다.
당사의 지적재산권을 파이프라인별로 살펴보면 파킨슨병 치료제 KM-819의 물질 특허가 19개국에 등록이 완료되어 있습니다. 당사는 물질특허 외에도 알파시누클라인(α-synuclein)에 대한 축적 억제 작용기전을 규명(용도) 및 Salt form 제법에 대한 PCT 출원을 완료하였기 때문에, 특허 보호기간 (또는 PMS기간) 동안 물질, 용도, 제재에 대한 모방은 원천적으로 막을 수 있습니다. 또한 당사의 KM-023의 경우에는 2028년까지 특허로 보호받고 있으며, 2022년 시판 및 빠른 성장률을 고려할 때 성숙기 유지에 충분한 기간입니다. 또한 신약의 경우 나라별 시판 후 조사(PMS)기간이 있어, 제품의 특허 존속 기간이 여의치 않더라도 적어도 4~6년의 보호기간이 주어집니다. KM-023의 물질 특허는 10개국에 등록이 완료되어 있습니다. 기 개발된 또는 개발 중인 의약품과 동일하게, 당사 약물에 대한 모방 가능성이 없다고는 볼 수 없으나 이는 모든 약물이 가지고 있는 특성입니다. 당사는 물질특허 및 제법 특허등록을 마쳤으며, 특허 보호기간 (또는 PMS기간) 동안 제네릭의 진입을 막을 수 있습니다.
증권신고서 제출일 기준 당사가 보유한 지적재산권 현황은 아래와 같습니다.
| [지적재산권 현황] |
| 구분 |
현황 |
출원명칭 (내용) |
권리자 |
출원일 |
등록일 |
출원국 |
적응증 |
|---|---|---|---|---|---|---|---|
| 1 |
등록 |
신규한 HIV 역전사효소 억제제 |
한국화학 연구원 |
09.12.28 |
15.02.26 |
독일 |
에이즈 |
| 2 |
15.02.27 |
스페인 |
|||||
| 3 |
15.02.28 |
프랑스 |
|||||
| 4 |
15.03.01 |
영국 |
|||||
| 5 |
15.03.02 |
이탈리아 |
|||||
| 6 |
09.12.25 |
14.10.22 |
중국 |
||||
| 7 |
09.12.21 |
17.08.14 |
인도 |
||||
| 8 |
09.12.16 |
13.06.06 |
멕시코 |
||||
| 9 |
08.06.26 |
12.12.18 |
미국 |
||||
| 10 |
10.01.28 |
15.06.26 |
대한민국 |
||||
| 11 |
등록 |
PROCESSES FOR PREPARING HIV REVERSE TRANSCRIPTASE INHIBITORS |
한국화학 연구원 |
11.07.25 |
13.12.10 |
미국 |
에이즈 |
| 12 |
등록 |
COMPOUNDS AS INHIBITORS OF DIACYLGLYCEROL |
㈜카이노스메드 |
13.02.06 |
16.03.01 |
미국 |
비만당뇨 |
| 13 |
출원 |
브로모도메인-억제 화합물 및 상기 화합물을 포함하는 암 예방 또는 치료용 약학 조성물 |
㈜카이노스메드 |
16.09.26 |
- |
중국 |
브로모도메인 |
| 14 |
등록 |
16.11.04 |
19.06.26 |
오스트리아 |
|||
| 15 |
16.11.04 |
19.06.26 |
벨기에 |
||||
| 16 |
16.11.04 |
19.06.26 |
스위스 |
||||
| 17 |
16.11.04 |
19.06.26 |
독일 |
||||
| 18 |
16.11.04 |
19.06.26 |
덴마크 |
||||
| 19 |
16.11.04 |
19.06.26 |
스페인 |
||||
| 20 |
16.11.04 |
19.06.26 |
핀란드 |
||||
| 21 |
16.11.04 |
19.06.26 |
프랑스 |
||||
| 22 |
16.11.04 |
19.06.26 |
영국 |
||||
| 23 |
16.11.04 |
19.06.26 |
이탈리아 |
||||
| 24 |
16.11.04 |
19.06.26 |
네덜란드 |
||||
| 25 |
16.11.04 |
19.06.26 |
폴란드 |
||||
| 26 |
16.11.04 |
19.06.26 |
스웨덴 |
||||
| 27 |
16.09.27 |
20.12.22 |
인도 |
||||
| 28 |
16.10.07 |
18.05.11 |
일본 |
||||
| 29 |
16.09.27 |
18.02.06 |
미국 |
||||
| 30 |
16.11.03 |
18.12.06 |
대한민국 |
||||
| 31 |
등록 |
MUTUAL PRODRUG COMPRISING SHORT CHAIN FATTY ACIDS AND ZEBULARINE OR 1’-CYANO-CYTARABINE FOR CANCER TREATMENT |
㈜카이노스메드 |
16.11.03 |
18.06.15 |
대한민국 |
세포독성 |
| 32 |
출원 |
16.05.05 |
- |
중국 |
|||
| 33 |
등록 |
16.04.15 |
19.12.10 |
미국 |
|||
| 34 |
출원 |
16.04.27 |
- |
인도 |
|||
| 35 |
등록 |
16.05.13 |
17.09.29 |
일본 |
|||
| 36 |
출원 |
16.04.20 |
- |
브라질 |
|||
| 37 |
등록 |
16.06.01 |
20.01.08 |
오스트리아 |
|||
| 38 |
16.06.01 |
20.01.08 |
벨기에 |
||||
| 39 |
16.06.01 |
20.01.08 |
스위스 |
||||
| 40 |
16.06.01 |
20.01.08 |
독일 |
||||
| 41 |
16.06.01 |
20.01.08 |
덴마크 |
||||
| 42 |
16.06.01 |
20.01.08 |
스페인 |
||||
| 43 |
16.06.01 |
20.01.08 |
프랑스 |
||||
| 44 |
16.06.01 |
20.01.08 |
영국 |
||||
| 45 |
16.06.01 |
20.01.08 |
헝가리 |
||||
| 46 |
16.06.01 |
20.01.08 |
아일랜드 |
||||
| 47 |
16.06.01 |
20.01.08 |
이탈리아 |
||||
| 48 |
16.06.01 |
20.01.08 |
네덜란드 |
||||
| 49 |
16.06.01 |
20.01.08 |
노르웨이 |
||||
| 50 |
16.06.01 |
20.01.08 |
폴란드 |
||||
| 51 |
16.06.01 |
20.01.08 |
스웨덴 |
||||
| 52 | 등록 |
아미노피라졸 유도체, 이의 제조 방법 및 이를 함유하는 허혈성 질환의 예방 또는 치료용 조성물 |
한국화학 연구원 |
09.03.12 |
15.08.26 |
오스트리아 |
파킨슨 |
| 53 |
09.03.12 |
15.08.26 |
벨기에 |
||||
| 54 |
09.03.12 |
15.08.26 |
스위스 |
||||
| 55 |
09.03.12 |
15.08.26 |
독일 |
||||
| 56 |
09.03.12 |
15.08.26 |
덴마크 |
||||
| 57 |
09.03.12 |
15.08.26 |
스페인 |
||||
| 58 |
09.03.12 |
15.08.26 |
프랑스 |
||||
| 59 |
09.03.12 |
15.08.26 |
영국 |
||||
| 60 |
09.03.12 |
15.08.26 |
이탈리아 |
||||
| 61 |
09.03.12 |
15.08.26 |
네덜란드 |
||||
| 62 |
09.03.12 |
15.08.26 |
폴란드 |
||||
| 63 |
09.03.12 |
15.08.26 |
스웨덴 |
||||
| 64 |
09.03.12 |
15.08.26 |
터키 |
||||
| 65 |
09.05.26 |
11.08.11 |
호주 |
||||
| 66 |
09.04.15 |
11.11.15 |
캐나다 |
||||
| 67 |
09.04.27 |
12.03.14 |
중국 |
||||
| 68 |
09.04.27 |
12.09.28 |
일본 |
||||
| 69 |
09.04.27 |
11.05.10 |
미국 |
||||
| 70 |
06.10.27 |
08.05.21 |
대한민국 |
||||
| 71 | 출원 |
알파-시누클레인 조절제 |
㈜카이노스메드 |
19.12.23 |
- |
대한민국 |
파킨슨 |
| 72 |
20.01.16 |
- |
뉴질랜드 |
||||
| 73 |
19.12.12 |
- |
미국 |
||||
| 74 |
19.12.16 |
- |
멕시코 |
||||
| 75 |
19.12.19 |
- |
중국 |
||||
| 76 |
20.01.08 |
- |
유럽 |
||||
| 77 |
20.01.16 |
- |
러시아 |
||||
| 78 |
19.12.19 |
- |
사우디아라비아 |
||||
| 79 |
19.12.05 |
- |
싱가포르 |
||||
| 80 |
19.12.18 |
- |
브라질 |
||||
| 81 |
20.01.16 |
- |
호주 |
||||
| 82 |
20.06.30 |
- |
홍콩 |
||||
| 83 |
19.12.10 |
- |
일본 |
||||
| 84 |
19.12.12 |
- |
캐나다 |
||||
| 85 |
19.12.11 |
- |
이스라엘 |
||||
| 86 |
출원 |
Salt forms of organic compound |
㈜카이노스메드 |
19.01.30 |
- |
PCT |
파킨슨 |
| 87 |
20.07.28 |
- |
브라질 |
||||
| 88 | 출원 |
18.01.31 |
- |
미국 |
|||
| 89 | 출원 |
20.07.31 |
- |
캐나다 |
|||
| 90 |
20.07.28 |
- |
유럽 |
||||
| 91 |
20.08.18 |
- |
중국 |
||||
| 92 |
20.07.21 |
- |
이스라엘 |
||||
| 93 |
20.08.05 |
- |
멕시코 |
||||
| 94 |
20.07.29 |
- |
호주 |
||||
| 95 |
20.08.13 |
- |
인도 |
||||
| 96 |
출원 |
Compounds and compositions for Ectonucleotidase inhibition |
㈜카이노스메드 |
20.08.24 |
- |
PCT |
항암제 |
| 97 |
출원 |
Novel N-(1H-imidazol-2-yl)Benzamide compounds and pharmaceutical composition containing the same as an active ingredient |
㈜카이노스메드 |
20.09.29 |
- |
PCT |
항암제 |
| 98 |
가출원 |
PYRIDINE DERIVATIVES AS IMMUNOMODULATORS |
㈜카이노스메드 |
20.06.03 |
- |
미국/ |
항암제 |
| 99 | 출원 | FAF1(Fas-associated factor 1)이 로딩된 엑소좀 및 이를 포함하는 자궁경부암 치료용 약학적 조성물 | ㈜카이노스메드 | 21.03.30 | - | 대한민국 | FAF1-Exosome |
| 100 | 출원 | FAF1-loaded exosomes and composition for cervical cancer treatment comprising the same | ㈜카이노스메드 | 22.03.30 | - | PCT | |
| 101 |
출원 |
N-(1H-IMIDAZOL-2-YL)BENZAMIDE COMPOUND AND PHARMACEUTICAL COMPOSITION COMPRISING THE SAME AS ACTIVE INGREDIENT | ㈜카이노스메드 |
20.09.29 |
- |
PCT |
항암제 |
| 102 | 22.04.12 | - | 호주 | ||||
| 103 |
22.03.21 |
- | 인도 | ||||
| 104 |
22.03.21 |
- | 싱가포르 | ||||
| 105 | 22.03.25 | - | 중국 | ||||
| 106 | 22.03.29 | - | 멕시코 | ||||
| 107 | 22.03.29 | - | 미국 | ||||
| 108 | 22.03.30 | - | 캐나다 | ||||
| 109 | 22.03.31 | - | 브라질 | ||||
| 110 | - | - | 일본 | ||||
| 111 | - | - | 러시아 |
| 출처) 당사 정기보고서 및 당사 제시 |
당사는 보유하고 있는 기술에 대하여 향후 공동연구개발 추진, 라이선스 아웃, 경쟁회사의 유사 기술개발 방어 및 진입장벽 구축 등을 위해 지적재산권 확보 및 보호 전략을 수립하고 있습니다. 그럼에도 불구하고, 향후 제3자에 의하여 당사가 보유하고 있는 특허권에 대한 소송 또는 기타 분쟁이 발생할 가능성을 배제할 수 없으며, 임상시험 또는 제품 상용화에 실패하여 특허 연장을 하지 못할 경우, 특허가 만료되어 동일 기반 기술의 경쟁 제품이 개발될 수 있음에 따라 당사의 손익에 부정적인 영향을 미칠 수 있습니다.
|
차. 정부 정책 및 규제 변화에 따른 위험 |
제약산업은 인간의 생명 및 건강과 직결되는 의약품을 개발ㆍ제조ㆍ판매하는 산업으로, 제품의 개발 및 제조, 임상시험, 인허가, 유통 및 판매에 이르기까지 전 과정에 걸쳐 각 국가의 규제 당국이 제시하는 엄격한 규정과 절차를 따라야 합니다. 제약 및 신약개발 사업과 관련된 국내 법률 중 당사의 사업과 밀접하게 연관된 법률로는 식품의약품안전처 및 보건복지부 소관의 '약사법'이 대표적이며, 그 외 보건복지부 소관의 「국민건강보험법」, 「생명윤리 및 안전에 관한 법률」, 「제약산업 육성 및 지원에 관한 특별법」, 「희귀질환관리법」, 「첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률」과 식품의약품안전처 소관의 「실험동물에 관한 법률」 등이 있습니다.
특히, 「약사법」 하위 시행령/시행규칙 중 의약품 등의 안전에 관한 규칙, 의약품 등의 제조업 및 수입자의 시설기준령 시행규칙, 생물학적 제제 등의 제조ㆍ판매관리 규칙, 동물용 의약품등 취급규칙 등과 이의 하위 규정을 준수해야 합니다. 이에 따라, 신약 후보물질의 발굴에서부터 동물을 대상으로 하는 비임상시험, 인체를 대상으로 하는 임상시험, 품목허가에 이르기 까지 임상 승인에 관한 규정, 의약품의 약리 및 독성, 안정성 시험 기준, 임상시험 실시기관 지정에 관한 규정, 품목허가ㆍ심사 등의 규정 등을 반드시 준수하여 진행해야 합니다. 또한 제조 및 판매 단계에서도 제조소 시설 기준, 제조 및 품질관리 규정, 포장 및 공급에 관한 규정, 표시 등에 관한 규정을 준수해야 하며, 사후에도 정기적으로 규제기관으로부터 제품 생산 공정 및 품질관리 전반에 대한 실사 및 관리, 감독을 받게 됩니다. 이러한 규제 및 검증을 통해 제약산업의 선진화 정책을 시현할 수 있지만, 각종 규제 및 절차, 검증 강화로 인한 부담이 높아지는 경우, 당사의 사업에 부정적인 영향을 미칠 수 있습니다.
또한, 국내는 단일보험자(국민건강보험공단)에 의한 전국민 건강보험제도를 운영하고 있는 상황으로, 건강보험의 지속가능성 제고와 적정수준의 국민의료비 유지, 불법 리베이트 차단 등의 목표 하에 약가에 대해 정책적 개입이 이루어지고 있습니다. 국내의 약가 사후관리제도는 대내외 보건의료 환경변화에 의하여 수 차례 변화되어, 현재는 실거래가 조사에 의한 약가 인하, 사용량-약가 연동 협상, 급여범위 확대 시 약가인하, 제네릭의약품 등재 시 오리지널의약품의 약가인하 등의 제도가 운영되고 있습니다. 약가는 산업 정책과 보건의료 정책이 상충하여 변동성이 상존해 있는 상황으로, 현재 제네릭 약가 차등제가 시행 예정되어 있는 상황입니다. 이러한 점진적인 약가 인하 정책은 제약산업에서 간과할 수 없는 중요 요인이며, 당사의 사업에도 부정적인 영향을 미칠 수 있습니다.
당사는 내부에 담당 인력과 외부 전문가들을 통하여 국내 및 해외 제약 산업 정책 및 규제 환경을 지속적으로 모니터링하고 있으며, 각국의 규제 당국과의 소통을 통해 정책 및 규제 환경의 변화에 효과적으로 대비하기 위해 최선의 노력을 다하고 있습니다. 그럼에도 불구하고 국내를 포함한 주요 국가에서의 제약 산업 관련 정책이 비우호적 분위기로 전환되거나 규제가 강화되는 경우, 당사의 사업에 부정적인 영향을 미칠 수 있습니다.
한편, 국내를 비롯한 미국, 유럽 등 글로벌 선진국에서는 제약·바이오 산업을 국민의 건강을 증진하고 일자리와 고부가가치를 창출하는 핵심 기간산업이자 미래 신성장 동력 산업으로 인지하고, 제약ㆍ바이오 산업에 대한 우호적 정책을 펼치고 있는 상황입니다. 국내 정부의 경우, 한-미 FTA 발효, 약가제도 개편 등 제약산업의 환경 악화로 2012년 제약산업 육성대책 마련 필요성이 제기되었으며, 제약산업 발전기반 조성 및 국제 경쟁력 강화를 촉진하기 위하여, 2012년 '제약산업 육성 및 지원에 관한 특별법'을 시행하였습니다. 이에 따라 2013년부터 5년 단위의 제약산업육성ㆍ지원 종합계획과 1년 단위의 제약산업육성ㆍ지원 시행계획을 수립ㆍ시행하여 세부 과제를 추진하고 있습니다.
또한 국내 정부는 2019년 5월, 바이오헬스 분야 기술개발, 인허가, 생산, 시장출시 등 전주기에 걸쳐 단계별 지원내용을 담고 있는 '바이오헬스 산업 혁신전략'을 발표하였습니다. 이러한 정부 방침에 지방자치단체들도 바이오 산업을 지역 역점산업으로 육성하기 위해 노력하고 있습니다.
국내 및 미국, 유럽 등 글로벌 선진국은 제약사들의 신약 R&D 및 인허가에 소요되는 막대한 비용 부담을 줄일 수 있도록 다양한 규제장벽을 완화하는 정책을 적극적으로 펼치고 있습니다. 대표적으로, 의학적 미충족 수요에 부응할 가능성이 있는 제약/바이오 기술들을 위중한 상태에 있는 환자들에게 신속하게 전달할 기회를 제공하기 위해 조건부 신속허가를 제도적으로 정착하려는 노력이 진행되고 있습니다. 미국은 가속 승인(Accelerated Approval) 제도를 통해 기존의 치료 요법으로는 해결되지 않는 중증질환을 대상으로 하는 치료제의 경우 대리 평가변수(surrogate endpoint)를 이용한 연구결과로 조기에 승인해주는 제도를 운영하고 있으며, 유럽은 미충족 의료수요를 충족하는 일부 의약품에 대해 시판 후 임상적 확증시험 이행을 조건으로 조기 허가하는 조건부허가(Conditional marketing authorization)와 임상적 확증시험이 어려운 희귀 질환을 대상으로 하는 예외적 허가(Marketing authorization under exceptional circumstances) 등의 제도가 시행되고 있습니다.
이에 더불어, 최근에는 재생의료 임상연구실시 및 첨단바이오의약품 패스트트랙을 골자로 하는 「첨단재생의료법(첨단재생의료 및 첨단바이오의약품의 안전ㆍ지원에 관한 법률)」이 국회 본회의를 통과하여 2020년 8월부터 시행되고 있습니다. 첨단바이오의약품은 세포치료제, 유전자체료제, 조직공학제 등 살아있는 세포ㆍ조직 또는 유전자를 원료로 제조한 의약품을 의미합니다. 첨단재생의료법은 첨단재생의료의 안전성 확보 체계 및 기술 혁신ㆍ실용화 방안을 마련하고, 약사법, 생명윤리법 등에 산재한 바이오의약품 관련 규제를 일원화하며, 신속허가제도 도입 및 안전관리체계를 구축하는 것이 핵심입니다. 본 법을 통해 재생의료 임상연구가 가능해져 의료기술의 기술경쟁력을 제고하여 희귀ㆍ난치 질환자에게 새로운 치료 기회를 제공할 수 있을 뿐만 아니라, 품목허가 검증 체계를 첨단바이오의약품 특성에 맞게 재편하여 맞춤형 심사, 우선 심사, 조건부 허가 등의 혜택이 가능할 것으로 기대됩니다.
상기 언급된 제약 및 신약개발 산업에 대한 우호적인 정책 기조 및 지원 계획, 규제 완화 노력에도 불구하고, 실제 효율적인 정책 지원이 이루어지지 않거나, 세부과제 추진에 어려움이 생길 수 있으며, 관련 법규의 제정 및 개정 단계, 예산 확보 등에 난항이 발생할 수 있습니다. 또한 해당 정책의 기대효과가 감소되는 경우 정책 기조의 변화로 정부 지원이 축소될 수 있으며, 조건부 허가와 같은 규제 완화에 대한 실효성이 크지 않을 경우, 규제 완화의 범위가 축소될 수 있습니다. 이러한 정부의 우호적인 정책 및 규제 완화의 변동 가능성은 당사의 사업에 부정적인 영향을 끼칠 수 있습니다.
2. 회사위험
| 【투자자 유의사항】 |
|---|
|
○ 회사위험에는 당사의 주요 재무적 위험요소들이 기재되어 있습니다. 투자자 여러분들의 이해 편의를 위하여, 당사의 최근 3개년간 주요 재무사항 총괄표를 아래와 같이 요약 기재하였으니, 투자 판단에 참고하시기 바랍니다. |
| [주요재무사항 총괄표] | |
| (K-IFRS, 연결) | (단위: 백만원) |
| 구 분 | 2022년 1분기 | 2021년 1분기 | 2021년 | 2020년 | 2019년 | 비 고 | ||
| 외부감사인 | 삼덕회계법인 | 삼덕회계법인 | 삼덕회계법인 | 삼일회계법인 | 삼정회계법인 | - | ||
| 감사의견 | - | - | 적정 | 적정 | 적정 | - | ||
| (계속기업 불확실성 관련 의견표명) | - | - | 해당사항 없음 | 해당사항 없음 | 해당사항 없음 | - | ||
| 1. 자산총계 | 39,472 | 34,664 | 41,957 | 34,779 | 5,571 | - | ||
| 유동자산 | 32,985 | 31,258 | 36,873 | 31,987 | 4,145 | - | ||
| 비유동자산 | 6,487 | 0 | 5,084 | 2,792 | 1,427 | - | ||
| 2. 부채총계 | 27,790 | 23,673 | 27,357 | 21,758 | 620 | - | ||
| 유동부채 | 27,655 | 5,351 | 25,655 | 4,167 | 570 | - | ||
| 비유동부채 | 135 | 18,321 | 1,701 | 17,591 | 50 | - | ||
| 3. 자본총계 | 11,682 | 10,992 | 14,600 | 13,020 | 4,952 | - | ||
| 지배지분 | 8,765 | 9,964 | 12,104 | 12,353 | 4,952 | - | ||
| 자본금 | 11,040 | 10,507 | 11,029 | 10,494 | 7,056 | - | ||
| 자본잉여금 | 86,826 | 72,034 | 86,373 | 70,945 | 55,535 | - | ||
| 결손금 | (89,100) | (72,577) | (85,298) | (69,087) | (57,639) | - | ||
| 비지배지분 | 2,917 | 1,028 | 2,497 | 668 | 0 | - | ||
| 4. 부채비율(%) | 237.88% | 215.36% | 187.37% | 167.11% | 12.52% | 부채총계 ÷ 자본총계 | ||
| 5. 유동비율(%) | 119.27% | 584.13% | 143.72% | 767.56% | 727.55% | 유동자산 ÷ 유동부채 | ||
| 6. 총차입금 | 23,632 | 24,162 | 25,080 | 23,264 | 0 | 유동성 차입금 + 비유동성 차입금 | ||
| 유동성 차입금 | 25,917 | 23,401 | 23,557 | 3,264 | 0 | - | ||
| 단기차입금 | 2,285 | 0 | 0 | 0 | 0 | - | ||
| 전환사채 | 20,000 | 20,000 | 20,000 | 0 | 0 | - | ||
| 전환우선주 | 3,632 | 3,401 | 3,557 | 3,264 | 0 | |||
| 비유동성 차입금 | 0 | 762 | 1,523 | 20,000 | 0 | - | ||
| 장기차입금 | 0 | 762 | 1,523 | 0 | 0 | - | ||
| 전환사채 | 0 | 0 | 0 | 20,000 | 0 | |||
| - 총차입금 의존도(%) | 65.66% | 69.70% | 59.78% | 66.89% | 0.00% | 총차입금 ÷ 자산총계 | ||
| - 유동성 차입금 비중(%) | 100.00% | 96.85% | 93.93% | 14.03% | 0.00% | 유동성 차입금 ÷ 총차입금 | ||
| 7. 영업활동 현금흐름 | (1,748) | (2,087) | (9,195) | (7,608) | (6,947) | - | ||
| - 영업활동현금흐름 총부채 비율(%) | -6.29% | -8.81% | -33.61% | -34.97% | -1,120.87% | 영업활동현금흐름 ÷ 부채총계 | ||
| 8. 투자활동 현금흐름 | (3,672) | (1,893) | (5,753) | 1,811 | 2,852 | - | ||
| 9. 재무활동 현금흐름 | 810 | 863 | 14,667 | 25,775 | 4,134 | - | ||
| 10. 현금 및 현금성자산 | 18,554 | 19,617 | 23,231 | 21,952 | 3,811 | - | ||
| 11. 순차입금 | 5,079 | 4,545 | 1,849 | 1,312 | (3,811) | 총차입금 - 현금 및 현금성자산 | ||
| - 순차입금 의존도(%) | 12.87% | 13.11% | 4.41% | 3.77% | -68.40% | 순차입금 ÷ 자산총계 | ||
| 12. 매출액 | 4 | 92 | 1,662 | 0 | 0 | - | ||
| 13. 매출원가 | 1 | 0 | 2 | 0 | 0 | - | ||
| - 매출원가율(%) | 29.95% | 0.00% | 0.13% | 0.00% | 0.00% | 매출원가 ÷ 매출액 | ||
| 14. 매출총이익 | 3 | 92 | 1,660 | 0 | 0 | - | ||
| 15. 판매비와관리비 | 3,880 | 3,620 | 12,880 | 9,386 | 8,087 | - | ||
| - 판매비와관리비율(%) | 105,813.75% | 3,929.09% | 774.74% | N/A | N/A | 판매비와관리비 ÷ 매출액 | ||
| 16. 영업이익(손실) | (3,878) | (3,528) | (11,219) | (9,386) | (8,087) | - | ||
| - 영업이익률(%) | -105,743.70% | -3,829.09% | -674.87% | N/A | N/A | 영업이익 ÷ 매출액 | ||
| 17. 기타이익 | 30 | 28 | 245 | 1,363 | 3 | - | ||
| 18. 기타손실 | 2 | 1 | 81 | 3,733 | 0 | - | ||
| 19. 금융수익 | 71 | 19 | 92 | 153 | 60 | - | ||
| 20. 금융원가 | 10 | 13 | 5,260 | 1,160 | 8 | - | ||
| 이자비용 | 10 | 13 | 1,676 | 763 | 8 | - | ||
| - 이자보상배수(배) | (400.38) | (277.81) | (6.69) | (12.29) | (995.11) | 영업이익 ÷ 이자비용 | ||
| 21. 법인세비용차감전계속사업이익(손실) | (3,789) | (3,495) | (16,224) | (12,763) | (8,032) | - | ||
| 22. 법인세비용 | (19) | 4 | 1 | (1,315) | 0 | - | ||
| 23. 당기순이익(손실) | (3,808) | (3,491) | (16,225) | (11,448) | (8,032) | - | ||
| - 당기순이익률(%) | -103,828.18% | -3,788.30% | -976.01% | N/A | N/A | 당기순이익 ÷ 매출액 | ||
| 출처) 당사 정기보고서 및 당사 제시 |
| 주) 차입금 내역 중 전환사채의 경우 전자등록금액으로 기재하였습니다. |
| 가. 현재 진행 중인 자본잠식이 심화될 위험 자본잠식이란 자본총계가 지속적으로 감소하여 자본금보다 적은 경우를 의미합니다. 2022년 1분기 당사의 자본금 및 비지배지분 제외 자본총계는 각각 11,040백만원 및 8,765백만원으로 2021년 대비 비지배지분 제외 자본총계는 3,338백만원이 감소하였으며, 2022년 1분기 기준 자본잠식률은 20.6%를 기록하고 있습니다. 자본잠식 규모가 지속적으로 증가하여 매 반기 또는 사업연도 말 기준 자본금의 100분의 50 이상이 잠식될 경우「코스닥시장 상장규정」제53조제1항제4호에 따라 관리종목으로 지정될 수 있으며, 이후 자본금 전액이 잠식되거나 자본잠식으로 인한 관리종목 지정 이후 사업연도 말에도 해당 사유가 지속될 경우 「코스닥시장 상장규정」제54조제1항제8호에 따라 상장폐지가 될 수 있습니다. 당사는 2022년 1분기 기준 20.6%의 자본잠식이 발생하고 있어 2022년 반기말까지 3,245백만원 이상의 순손실이 발생하고, 추가로 자본확충이 이루어지지 않는다면 자본잠식률 50% 이상 기록하여 관리종목에 지정될 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
회사의 적자폭이 커져 결손금 규모가 커져서 자본총계가 납입자본금 이하로 감소하는 것을 '(부분)자본잠식'이라고 합니다. 이후 회사의 적자가 계속되어 납입자본금 이상의 결손금이 발생하여 자기자본이 0 이하로 감소하게 되면 이를 '자본 전액잠식' 또는 '완전 자본잠식'이라 합니다. 자본잠식에 이르게 되면 회사가 영위하는 사업을 통해 벌어들이는 수익이 비용을 감당하지 못한다고 볼 수 있습니다.
자본잠식을 해소하기 위한 방안은 다음과 같습니다.
| [자본잠식 해소 방안] |
| 구분 | 내용 |
|---|---|
| 흑자시현 | 흑자 시현으로 당기순이익을 발생시켜 결손금을 감소시키는 방법을 말한다. |
| 무상감자 | 회사의 과도한 결손금을 보전하기 위하여 주주에게 아무런 보상 없이 자본금을 감소시키고 잉여금을 증가시키는 것을 말한다. 주주가 납입한 자본금을 감소시켜 결손금을 보전하기 때문에 기업이 경영 활동을 통해 누적된 결손금을 주주에게 전가하게 된다. 감자는 액면감소, 주식병합, 주식소각 등으로 진행된다. |
| 자산 재평가 | 부동산 등의 보유 자산에 대하여 원가로 평가한 공정가치를 시가로 재산정하여 발생한 평가이익을 통해 자본을 확충하는 방법을 말한다. |
| 유상증자 | 신주를 발행하여 자본을 확충하는 방법을 말한다. 신주의 가격을 지불하는 유상증자와 무상으로 교부받는 무상증자로 나뉜다. |
| 출처) 당사 제시 |
2022년 1분기 당사의 자본금 및 비지배지분 제외 자본총계는 각각 11,040백만원 및 8,765백만원으로 2021년 대비 비지배지분 제외 자본총계는 3,338백만원이 감소하였으며, 2022년 1분기 기준 자본잠식률은 20.6%를 기록하고 있습니다.
| [자본금 및 자본총계 추이] | |
| (K-IFRS, 연결) | (단위: 백만원) |
| 구분 | 2022년 1분기 | 2021년 |
|---|---|---|
| 자본금 | 11,040 | 11,029 |
| 자본총계 | 11,682 | 14,600 |
| 비지배지분 | 2,917 | 2,497 |
| 비지배지분 제외 자본총계 | 8,765 | 12,104 |
| 자본금의 50% | 5,520 | 5,515 |
| 50% 자본잠식까지 한도 여유분 |
3,245 | 6,589 |
| 당(분)기순이익 | (3,808) | (16,225) |
| 이익잉여금(결손금) | (89,100) | (85,298) |
| 자본잠식률 | 20.6% | N/A |
| 출처) 당사 정기보고서 및 당사 제시 |
| 주1) 자본잠식률 = 1 - {비지배지분 제외 자본총계 / 자본금} |
| 주2) 연결기준 자본잠식률은 자기자본에서 비지배지분을 제외한 지배기업 소유지분을 기준으로 산정합니다. |
자본잠식 규모가 지속적으로 증가하여 매 반기 또는 사업연도 말 기준 자본금의 100분의 50 이상이 잠식될 경우「코스닥시장 상장규정」제53조제1항제4호에 따라 관리종목으로 지정될 수 있으며, 이후 자본금 전액이 잠식되거나 자본잠식으로 인한 관리종목 지정 이후 사업연도 말에도 해당 사유가 지속될 경우 「코스닥시장 상장규정」제54조제1항제8호에 따라 상장폐지가 될 수 있습니다.
당사는 2021년 기준 자본잠식에 해당되지 않아 관리종목지정 사유에 해당되지 않습니다. 그러나 2022년 1분기 기준 20.6%의 자본잠식이 발생하고 있어 추가적으로 2022년 반기말 또는 연말까지 3,245백만원 이상의 순손실이 발생하고, 자본확충이 이루어지지 않는다면 자본잠식률 50% 이상 기록하여 관리종목에 지정될 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| [코스닥시장 관리종목 지정요건 및 상장폐지요건] |
| 구 분 | 관리종목 지정(코스닥 상장규정 제53조) | 상장폐지(코스닥 상장규정 제54조, 제56조) |
|---|---|---|
| 1) 매출액 미달(별도) |
최근 사업연도 30억원 미만 (지주회사는 연결기준) |
2년 연속 매출액 30억원 미만 [실질심사] 이익미실현기업 관련 관리종목지정 유예기간 중 최근 3사업연도 연속으로 매출액이 5억원 미만이면서 전년 대비 100분의 50 이상의 매출액 감소가 공시 등을 통해 확인되는 경우 |
| 1) 매출액 미달(별도) |
최근 사업연도 30억원 미만 (지주회사는 연결기준) |
2년 연속 매출액 30억원 미만 [실질심사] 이익미실현기업 관련 관리종목지정 유예기간 중 최근 3사업연도 연속으로 매출액이 5억원 미만이면서 전년 대비 100분의 50 이상의 매출액 감소가 공시 등을 통해 확인되는 경우 |
| 2) 법인세비용차감전 계속사업손실(연결) | 최근 3사업연도중 2사업연도에 각각 당해 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 있고 최근사업연도에 법인세비용차감전계속사업손실이 있는 경우 - 이익미실현 기업은 상장 후 5년간 미적용 - 기술성장기업은 상장후 3년간 미적용 |
관리종목 지정후 자기자본50%이상(&10억원이상)의 법인세비용차감전계속사업손실 발생 [실질심사] 이익미실현기업 관련, 관리종목지정 유예기간 중 최근 3사업연도 연속으로 매출액이 5억원 미만이면서 전년 대비 100분의 50 이상의 매출액 감소가 공시 등을 통해 확인되는 경우 |
| 3) 영업손실(별도) |
최근 4사업연도 영업손실(지주회사는 연결기준) |
[실질심사]관리종목 지정법인이 최근 사업연도에 영업손실이 있는 경우 |
| 4) 자본잠식 등 | 반기말 또는 사업연도 말을 기준으로 다음의 어느 하나에 해당하는 경우 A) 최근 반기말 또는 사업연도말을 기준으로 자본잠식률 50%이상 B) 최근 반기말 또는 사업연도말을 기준으로 자기자본 10억원 미만 C) 반기보고서 감사(검토)의견이 부적정 또는 의견 거절이거나 감사범위제한으로 인한 한정인 경우 D) 반기보고서 법정제출기한 다음날부터 10일 이내에 반기검토(감사)보고서를 제출하지 아니한 경우 |
가. 최근 사업연도말 현재 완전자본잠식의 경우 나. (A) or (C) 관리종목 지정후 도래하는 반기말이나 사업연도말 자본잠식률이 50%이상인 경우 다. (B) or (C) 관리종목 지정후 도래하는 반기말이나 사업연도말 자기자본이 10억원 미만인 경우 라. (A) or (B) or (C) 관리종목 지정법인이 최근 반기의 재무제표에 대한 감사인의 감사의견이 부적정,의견거절 또는 감사범위제한으로 인한 한정이거나 반기보고서 법정제출기한의 다음날부터 10일 이내에 반기검토(감사)보고서를 제출하지 아니한 경우 [실질심사] 사업보고서 또는 반기보고서의 법정제출 기한까지 당해 상장폐지 기준 해당사실을 해소하였음을 입증하는 재무제표 및 이에 대한 감사인(정기재무제표에 대한 감사인과 동일한 감사인에 한함)의 감사보고서를 제출하는 경우 가~다목까지의 규정을 적용하지 않음. |
| 5) 시가총액 미달 | 보통주 시가총액 40억원 미만 30일간 지속 -천재지변, 시장상황의 급격한 변동 등으로 거래소가 시장 관리를 위하여 필요하다고 인정될 경우 적용배제 가능 |
관리종목 지정후 90일 기간 경과하는 동안 i) 시가총액 40억 이상으로 10일 이상 계속 ii) 시가총액 40억 이상인 일수가 30일 이상 둘중 하나라도 충족하지 못하면 상장폐지 |
| 6) 정기보고서 미제출 | 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않거나, 정기주총에서 재무제표 미승인 or 정기주총 미개최할 경우 | 관리종목 지정법인이 다음 회차에 다음 어느 하나에 해당하는 경우 가)분기,반기,사업보고서를 법정제출기한내에 미제출 나)사업보고서의 법정제출기한까지 정기주주총회를 미개최하거나 정기주주총회에서 재무제표 미승인 다)최근 2년간 3회 이상 분기, 반기, 사업보고서 법정제출기한까지 제출하지 아니한 경우 라)법정제출기한까지 사업보고서를 제출하지 아니한 후 법정제출기한의 다음날부터 10일 이내 사업보고서 미제출 |
| 7) 불성실공시 | - | [실질심사]1년간 불성실공시 벌점 15점 이상 |
| 8) 지배구조 미달 | 최근 사업연도 사업보고서상 A)사외이사의 수가 법에서 정하는 수에 미달 B)법에서 정하는 감사위원회를 구성하지 않거나 구성요건을 충족하지 아니하는 경우 |
관리종목 지정법인이 다음 사업연도에 동일한 상태에 해당하는 경우 |
| 9) 거래량 미달 |
분기 월 평균거래량이 유동주식수의 1%에 미달 |
관리종목 지정법인이 다음 분기에도 연속하여 동 규정에 의한 거래량 미달상태가 계속되는 경우 |
| 10) 주식분산 미달 |
소액주주 200인 미만 or 소액주주지분 20% 미만 |
관리종목 지정법인이 1년 이내에 동 규정에 의한 주식분산기준미달을 해소하지 아니하는 경우 |
| 11) 회생절차 개시신청 | "채무자 회생 및 파산에 관한 법률" 제34조에 의한 회생 절차개시 신청이 있는 경우 | [실질심사] 관리종목 지정법인이 다음의 어느 하나에 해당하는 경우 코스닥시장 상장폐지실질심사위원회의 심사를 거쳐 상장폐지 가)법원의 회생절차개시신청 기각, 회생절차개시결정 취소, 회생계획 불인가 또는 회생절차폐지의 결정 등이 있은 때 나) 실질심사 제출서류 상 투자자 보호를 위하여 중요한 사항이 누락되거나 거짓 기재된 경우 |
| 12) 파산신청 | 코스닥시장 상장법인에 대하여 「채무자 회생 및 파산에 관한 법률」 제294조에 의한 파산신청이 있는 경우 | |
| 13) 기타 |
- 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 |
- 감사보고서 부적정·의견거절·범위제한한정 - 해산사유(피흡수합병, 파산선고) - 정관 등에 주식양도제한 두는 경우 - 유가증권시장 상장의 경우 - 우회상장시 우회상장관련 규정 위반시(심사종료전 기업결합완료 및 보호예수 위반 등) |
| 출처) 한국거래소 |
이로 인해 당사는 금번 유상증자를 통해 추가적인 자본확충 및 재무구조개선을 진행하여 자본잠식 문제를 해소할 계획입니다. 하기 표를 통해 금번 유상증자 이후 당사의 자본금은 2,800백만원 증가한 13,840백만원을 기록할 예정이며, 자본총계는 48,486백만원(예정 발행가액 기준)으로 증가할 예정이기 때문에 자본잠식은 해소될 것으로 판단됩니다.
| [유상증자에 따른 재무구조 개선] |
| (단위: 백만원) |
| 구분 | 2022년1분기 | 유상증자 납입금 | 유상증자 후 |
|---|---|---|---|
| 자산총계 | 39,472 | 48,496 | 87,968 |
| 부채총계 | 27,790 | - | 27,790 |
| 자본총계 | 11,682 | 48,496 | 60,178 |
| 자본금 | 11,040 | 2,800 | 13,840 |
| 자본잠식률 | 20.6% | - | N/A |
| 부채비율 | 237.88% | 46.18% |
| 출처) 당사 정기보고서 및 당사 제시 |
| 주1) 주식병합으로 인한 단수주 발생, 유상증자 진행 중 전환사채 전환 및 주식매수선택권 행사 등으로 인해 자본금 및 자본총계가 변동될 수 있습니다. |
그러나 「코스닥시장 상장규정」에 따른 자본잠식 여부 판단 시기는 최근 반기말 혹은 사업연도 말 기준이므로 당사의 경우 유상증자 납입 이후에도 현재와 같이 운영비용을 충당할 수 있는 수준의 매출이 발생하지 않을 경우, 금번 유상증자를 통해 자본확충이 이루어졌음에도 불구하고 자본잠식 가능성을 배제할 수 없습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| [유상증자 후 자본금 및 자본총계 추이] |
| (단위: 백만원, %) |
| 구분 | 유상증자 후 |
|---|---|
| 자본금 | 13,840 |
| 자본총계 | 60,178 |
| 비지배지분 | 2,917 |
| 비지배지분 제외 자본총계 | 57,261 |
| 자본금의 50% | 6,920 |
| 50% 자본잠식까지 한도 여유분 | 50,341 |
| 출처) 당사 제시 |
| 주1) 연결기준 자본잠식률은 자기자본에서 비지배지분을 제외한 지배기업소유지분을 기준으로 산정합니다. |
당사가 진행하는 금번 유상증자가 예기치 못한 사유로 인해 철회될 경우 당사는 자본 확충을 위하여 무상감자 등 주주에게 손실을 끼치는 방안 등을 진행할 수 있습니다. 무상감자는 회사는 주주가 납입한 자본금을 감소시켜 회사가 경영활동을 통해 누적된 결손금을 보전하는 방법으로, 무상감자가 추진될 경우 주주께서는 이로 인해 회사의 주가가 급격히 하락하여 손실이 발생할 수 있으니 이 점 유의하시기 바랍니다.
| 나. 관리종목 지정 및 상장폐지 위험 당사는 기술성장특례 적용 기업으로서 2020년 06월 08일 하나금융11호기업인수목적 주식회사와의 합병을 통해 코스닥시장에 상장하였습니다. 당사는 보유 파이프라인의 비임상 및 임상시험의 진행으로 인원확충에 따른 인건비 증가, 연구개발비용 증가로 설립 이후 현재까지 지속적으로 적자를 기록하고 있습니다. 지속적인 신약후보물질의 발굴과 보유 파이프라인의 적응증 증가를 위하여 많은 비임상 및 임상시험을 준비하고 있으며 이에 따라 관련비용도 증가하여 이러한 추세는 일정기간 지속될 것으로 예상하고 있습니다. 당사는 최근 상장 이후 2020년, 2021년 매출액이 30억원 이상을 달성하지 못하여 관리종목 지정 사유에 해당되나, 당사는 기술성장특례 적용 기업으로서 신규상장일이 속한 사업연도를 포함하여 연속하는 5개 사업연도(2024년 12월 31일)까지 관리종목지정 유예를 적용받습니다. 당사는 최근 3사업연도(2019년~2021년) 중 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 2회 발생하여 관리종목 지정요건에 해당됩니다. 다만, 당사는 기술성장특례 적용 기업으로서 「코스닥시장 상장규정」제53조제1항제2호나목에 따라 신규상장일이 속한 사업연도를 포함하여 연속하는 3개 사업연도(2022년 12월 31일)까지 관리종목지정 유예를 적용받습니다. 당사는 최근 4사업연도 지속적으로 영업손실이 발생하여 관리종목 지정요건에 해당합니다. 다만, 당사는 기술성장특례 적용 기업으로서 「코스닥시장 상장규정」제53조제1항제3호 후단에 따라 이 호를 적용받지 않고 관리종목지정 유예를 적용받습니다. 당사는 A) 최근 사업연도말(2021년말) 자본잠식상태가 아니고, B) 최근 사업연도말(2021년말) 자기자본이 12,104백만원으로 10억원 이상이며, C) 최근 반기보고서(2021년 반기) 검토의견이 적정, D) 최근 반기보고서(2021년 반기) 제출일이 2021년 08월 12일로 법정제출기한 내에 제출하였습니다. 이에 따라 당사는 자본잠식 요건에 의한 관리종목 지정요건에 해당하지 않습니다. 그러나 2022년 1분기 기준 20.6%의 자본잠식이 발생하고 있어 2022년 반기말 또는 연말까지 3,245백만원 이상의 순손실이 발생하고, 추가로 자본확충이 이루어지지 않는다면 자본잠식률 50% 이상 기록하여 관리종목에 지정될 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
당사는 기술성장특례 적용 기업으로서 2020년 06월 08일 하나금융11호기업인수목적 주식회사와의 합병을 통해 코스닥시장에 상장하였습니다. 당사는 보유 파이프라인의 비임상 및 임상시험의 진행으로 인원확충에 따른 인건비 증가, 연구개발비용 증가로 설립 이후 현재까지 지속적으로 적자를 기록하고 있습니다. 지속적인 신약후보물질의 발굴과 보유 파이프라인의 적응증 증가를 위하여 많은 비임상 및 임상시험을 준비하고 있으며 이에 따라 관련비용도 증가하여 이러한 추세는 일정기간 지속될 것으로 예상하고 있습니다.
| [코스닥시장 관리종목 지정요건 및 상장폐지요건 & 해당여부 검토] |
| 구 분 | 관리종목 지정(코스닥 상장규정 제53조) | 상장폐지(코스닥 상장규정 제54조, 제56조) | 회사현황 | 관리종목 지정요건 해당여부 |
관리종목지정유예 | ||
|---|---|---|---|---|---|---|---|
| 사업연도 | 금액(백만원) /비율(%) /내용 |
해당 여부 |
종료시점 | ||||
| 1) 매출액 미달(별도) |
최근 사업연도 30억원 미만 (지주회사는 연결기준) |
2년 연속 매출액 30억원 미만 [실질심사] 이익미실현기업 관련 관리종목지정 유예기간 중 최근 3사업연도 연속으로 매출액이 5억원 미만이면서 전년 대비 100분의 50 이상의 매출액 감소가 공시 등을 통해 확인되는 경우 |
2021년(별도) | 4,013 | 미해당 | 해당 | 2024년 12월 31일 |
| 2) 법인세비용차감전 계속사업손실(연결) | 최근 3사업연도중 2사업연도에 각각 당해 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 있고 최근사업연도에 법인세비용차감전계속사업손실이 있는 경우 - 이익미실현 기업은 상장 후 5년간 미적용 - 기술성장기업은 상장후 3년간 미적용 |
관리종목 지정후 자기자본50%이상(&10억원이상)의 법인세비용차감전계속사업손실 발생 [실질심사] 이익미실현기업 관련, 관리종목지정 유예기간 중 최근 3사업연도 연속으로 매출액이 5억원 미만이면서 전년 대비 100분의 50 이상의 매출액 감소가 공시 등을 통해 확인되는 경우 |
2021년(연결) 2020년(연결) 2019년(연결) |
-16,224 / 111.13% -12,763 / 98.02% - / - |
해당 | 해당 | 2022년 12월 31일 |
| 3) 영업손실(별도) |
최근 4사업연도 영업손실(지주회사는 연결기준) |
[실질심사]관리종목 지정법인이 최근 사업연도에 영업손실이 있는 경우 | 2021년(별도) 2020년(별도) 2019년(별도) 2018년(별도) |
-5,900 -8,417 -44 -26 |
해당 | 해당 | - |
| 4) 자본잠식 등 | 반기말 또는 사업연도 말을 기준으로 다음의 어느 하나에 해당하는 경우 A) 최근 반기말 또는 사업연도말을 기준으로 자본잠식률 50%이상 B) 최근 반기말 또는 사업연도말을 기준으로 자기자본 10억원 미만 C) 반기보고서 감사(검토)의견이 부적정 또는 의견 거절이거나 감사범위제한으로 인한 한정인 경우 D) 반기보고서 법정제출기한 다음날부터 10일 이내에 반기검토(감사)보고서를 제출하지 아니한 경우 |
가. 최근 사업연도말 현재 완전자본잠식의 경우 나. (A) or (C) 관리종목 지정후 도래하는 반기말이나 사업연도말 자본잠식률이 50%이상인 경우 다. (B) or (C) 관리종목 지정후 도래하는 반기말이나 사업연도말 자기자본이 10억원 미만인 경우 라. (A) or (B) or (C) 관리종목 지정법인이 최근 반기의 재무제표에 대한 감사인의 감사의견이 부적정,의견거절 또는 감사범위제한으로 인한 한정이거나 반기보고서 법정제출기한의 다음날부터 10일 이내에 반기검토(감사)보고서를 제출하지 아니한 경우 [실질심사] 사업보고서 또는 반기보고서의 법정제출 기한까지 당해 상장폐지 기준 해당사실을 해소하였음을 입증하는 재무제표 및 이에 대한 감사인(정기재무제표에 대한 감사인과 동일한 감사인에 한함)의 감사보고서를 제출하는 경우 가~다목까지의 규정을 적용하지 않음. |
2021년(연결) | 자본잠식상태가 아님 자기자본 12,104 (비지배지분 제외) |
미해당 | - | - |
| 5) 시가총액 미달 | 보통주 시가총액 40억원 미만 30일간 지속 -천재지변, 시장상황의 급격한 변동 등으로 거래소가 시장 관리를 위하여 필요하다고 인정될 경우 적용배제 가능 |
관리종목 지정후 90일 기간 경과하는 동안 i) 시가총액 40억 이상으로 10일 이상 계속 ii) 시가총액 40억 이상인 일수가 30일 이상 둘중 하나라도 충족하지 못하면 상장폐지 |
증권신고서 제출 전일 기준 | 해당사항 없음 | 미해당 | - | - |
| 6) 정기보고서 미제출 | 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않거나, 정기주총에서 재무제표 미승인 or 정기주총 미개최할 경우 | 관리종목 지정법인이 다음 회차에 다음 어느 하나에 해당하는 경우 가)분기,반기,사업보고서를 법정제출기한내에 미제출 나)사업보고서의 법정제출기한까지 정기주주총회를 미개최하거나 정기주주총회에서 재무제표 미승인 다)최근 2년간 3회 이상 분기, 반기, 사업보고서 법정제출기한까지 제출하지 아니한 경우 라)법정제출기한까지 사업보고서를 제출하지 아니한 후 법정제출기한의 다음날부터 10일 이내 사업보고서 미제출 |
2021년 | 사업보고서 제출일 2022년 03월 23일 |
미해당 | - | - |
| 7) 불성실공시 | - | [실질심사]1년간 불성실공시 벌점 15점 이상 | |||||
| 8) 지배구조 미달 | 최근 사업연도 사업보고서상 A)사외이사의 수가 법에서 정하는 수에 미달 B)법에서 정하는 감사위원회를 구성하지 않거나 구성요건을 충족하지 아니하는 경우 |
관리종목 지정법인이 다음 사업연도에 동일한 상태에 해당하는 경우 | 2021년 | 해당사항 없음 | 미해당 | - | - |
| 9) 거래량 미달 |
분기 월 평균거래량이 유동주식수의 1%에 미달 |
관리종목 지정법인이 다음 분기에도 연속하여 동 규정에 의한 거래량 미달상태가 계속되는 경우 | 2022년 1분기 | 11,291,441주 / 10.2% | 미해당 | - | - |
| 10) 주식분산 미달 |
소액주주 200인 미만 or 소액주주지분 20% 미만 |
관리종목 지정법인이 1년 이내에 동 규정에 의한 주식분산기준미달을 해소하지 아니하는 경우 | 2021년말 | 소액주주수 17,499인 소액주주지분 71.67% |
미해당 | - | - |
| 11) 회생절차 개시신청 | "채무자 회생 및 파산에 관한 법률" 제34조에 의한 회생 절차개시 신청이 있는 경우 | [실질심사] 관리종목 지정법인이 다음의 어느 하나에 해당하는 경우 코스닥시장 상장폐지실질심사위원회의 심사를 거쳐 상장폐지 가)법원의 회생절차개시신청 기각, 회생절차개시결정 취소, 회생계획 불인가 또는 회생절차폐지의 결정 등이 있은 때 나) 실질심사 제출서류 상 투자자 보호를 위하여 중요한 사항이 누락되거나 거짓 기재된 경우 |
신고서 제출일기준 |
해당사항 없음 | 미해당 | - | - |
| 12) 파산신청 | 코스닥시장 상장법인에 대하여 「채무자 회생 및 파산에 관한 법률」 제294조에 의한 파산신청이 있는 경우 | 신고서 제출일기준 |
해당사항 없음 | 미해당 | - | - | |
| 13) 기타 |
- 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 |
- 감사보고서 부적정·의견거절·범위제한한정 - 해산사유(피흡수합병, 파산선고) - 정관 등에 주식양도제한 두는 경우 - 유가증권시장 상장의 경우 - 우회상장시 우회상장관련 규정 위반시(심사종료전 기업결합완료 및 보호예수 위반 등) |
신고서 제출일기준 |
해당사항 없음 | 미해당 | - | - |
| 출처) 한국거래소 |
| 주) 2020년 이전 회사현황은 합병 전 하나금융11호기업인수목적 주식회사의 현황입니다. |
(1) 매출액 미달 여부 검토
| [관리종목 지정 관련 주요 재무사항 검토] | |
| (K-IFRS, 연결 및 별도) | (단위 : 백만원, %) |
| 구분 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|
| 매출액(별도) | 4,013 | 0 | 0 |
| 출처) 당사 정기보고서 및 당사 제시 |
「코스닥시장 상장규정」 제53조제1항제1호에 따라 최근 사업연도의 매출액이 30억 미만일 경우 관리종목으로 지정되게 됩니다.
당사는 2021년 매출액은 4,013백만원으로, 30억원 이상을 달성하여 현재 관리종목 지정 사유에 해당되지 않습니다. 또한, 당사는 기술성장특례 적용 기업으로서 2020년 06월 08일 하나금융11호기업인수목적 주식회사와 합병을 통해 코스닥시장에 상장하여 「코스닥시장 상장규정」제53조제1항제1호가목에 따라 신규상장일이 속한 사업연도를 포함하여 연속하는 5개 사업연도(2024년 12월 31일)까지 관리종목지정 유예를 적용받습니다. 2025년 이후부터는 매출액(별도 기준) 30억원을 유지하지 못할 경우 관리종목으로 지정될 수 있습니다.
(2) 법인세비용차감전계속사업손실 발생 여부 검토
| [관리종목 지정 관련 주요 재무사항 검토] | |
| (K-IFRS, 연결 및 별도) | (단위 : 백만원, %) |
| 구분 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|
| 세전계속사업손익(연결) | -16,224 | -12,763 | - |
| 자기자본(연결) | 14,600 | 13,020 | 9,907 |
| 세전계속사업손익/자기자본(연결) | 111.13 | 98.02 | - |
| 출처) 당사 정기보고서 및 당사 제시 |
| 주) 2019년 재무현황은 합병 전 하나금융11호기업인수목적 주식회사의 현황입니다. |
「코스닥시장 상장규정」 제53조제1항제2호에 따라 최근 3사업연도 중 2사업연도에 각각 당해 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 있고 최근 사업연도에 법인세비용차감전계속사업손실이 있는 경우 관리종목으로 지정되게 됩니다.
당사는 최근 3사업연도(2019년~2021년) 중 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 2회 발생하여 관리종목 지정요건에 해당됩니다. 다만, 당사는 기술성장특례 적용 기업으로서 「코스닥시장 상장규정」제53조제1항제2호나목에 따라 신규상장일이 속한 사업연도를 포함하여 연속하는 3개 사업연도(2022년 12월 31일)까지 관리종목지정 유예를 적용받습니다. 2023년 이후부터는 기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 발생할 경우 관리종목으로 지정될 수 있습니다.
(3) 영업손실 발생 여부 검토
| [관리종목 지정 관련 주요 재무사항 검토] | |
| (K-IFRS, 연결 및 별도) | (단위 : 백만원, %) |
| 구분 | 2021년 | 2020년 | 2019년 | 2018년 |
|---|---|---|---|---|
| 영업손익(별도) | -5,900 | -8,418 | -44 | -26 |
| 출처) 당사 정기보고서 및 당사 제시 |
| 주) 2020년 이전 회사현황은 합병 전 하나금융11호기업인수목적 주식회사의 현황입니다. |
「코스닥시장 상장규정」제53조제1항제3호에 따라 최근 4사업연도 영업손실이 발생하는 경우 관리종목으로 지정되게 됩니다.
당사는 최근 4사업연도 지속적으로 영업손실이 발생하여 관리종목 지정요건에 해당합니다. 다만, 당사는 기술성장특례 적용 기업으로서 「코스닥시장 상장규정」제53조제1항제3호 후단에 따라 이 호를 적용받지 않고 관리종목지정 유예를 적용받습니다.
(4) 자본잠식 여부 검토
| [관리종목 지정 관련 주요 재무사항 검토] | |
| (K-IFRS, 연결) | (단위 : 백만원, %) |
| 구분 | 2022년 1분기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
| 비지배지분 제외 자기자본(연결) | 8,765 | 12,104 | 12,353 | 4,951 |
| 자본금(연결) | 11,040 | 11,029 | 10,494 | 7,056 |
| 자본잠식여부(연결) | 자본잠식(20.6%) | - | - | - |
| 감사의견 | - | 적정 | 적정 | 적정 |
| 출처) 당사 정기보고서 및 당사 제시 |
| 주) 2020년 이전 회사현황은 합병 전 하나금융11호기업인수목적 주식회사의 현황입니다. |
「코스닥시장 상장규정」제53조제1항제4호에 따라 매 반기말 또는 사업연도 말을 기준으로 다음의 어느 하나에 해당하는 경우 A) 최근 반기말 또는 사업연도말을 기준으로 자본잠식률 50%이상 / B) 최근 반기말 또는 사업연도말을 기준으로 자기자본 10억원 미만 / C) 반기보고서 감사(검토)의견이 부적정 또는 의견 거절이거나 감사범위제한으로 인한 한정인 경우 / D) 반기보고서 법정제출기한 다음날부터 10일 이내에 반기검토(감사)보고서를 제출하지 아니한 경우 관리종목으로 지정됩니다.
당사는 A) 최근 사업연도말(2021년말) 자본잠식상태가 아니고, B) 최근 사업연도말(2021년말) 자기자본이 12,104백만원으로 10억원 이상이며, C) 최근 반기보고서(2021년 반기) 검토의견이 적정, D) 최근 반기보고서(2021년 반기) 제출일이 2021년 08월 12일로 법정제출기한 내에 제출하였습니다. 이에 따라 당사는 자본잠식 요건에 의한 관리종목 지정요건에 해당하지 않습니다.
그러나 2022년 1분기 기준 20.6%의 자본잠식이 발생하고 있어 2022년 반기말 또는 연말까지 3,245백만원 이상의 순손실이 발생하고, 추가로 자본확충이 이루어지지 않는다면 자본잠식률 50% 이상 기록하여 관리종목에 지정될 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
(5) 시가총액 미달여부 검토
| [관리종목 지정 관련 주요 재무사항 검토] | |
| (K-IFRS, 연결 및 별도) | (단위 : 백만원, %) |
| 구분 | 시가총액(최고) | 시가총액(최저) | 시가총액(평균) |
|---|---|---|---|
| 2022년 1분기 | 292,555 | 202,029 | 239,652 |
| 출처) 당사 정기보고서 및 당사 제시 |
「코스닥시장 상장규정」제53조제1항제5호에 따라 보통주 시가총액 40억원 미만 30일간 지속되는 경우 관리종목으로 지정됩니다.
당사의 2022년 1분기 시가총액은 최고 2,923억원, 최저 2,020억원, 평균 2,397억원으로 시가총액 40억원 미만을 기록한 바가 없어 관리종목 지정요건에 해당하지 않습니다.
(6) 정기보고서 미제출 여부 검토
「코스닥시장 상장규정」제53조제1항제6호에 따라 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않은 경우 관리종목으로 지정됩니다.
당사는 2022년 03월 23일 사업보고서를 제출하여 법정제출기한 내에 제출한 바 관리종목 지정요건에 해당하지 않습니다.
(7) 지배구조 미달 여부 검토
「코스닥시장 상장규정」제53조제1항제7호에 따라 최근 사업연도 사업보고서상 A)사외이사의 수가 법에서 정하는 수에 미달 B) 법에서 정하는 감사위원회를 구성하지 않거나 구성요건을 충족하지 아니하는 경우 관리종목으로 지정됩니다.
당사는 최근 사업연도말(2021년) 당사의 자산총액은 420억원으로 「상법」 제542조의8제1항 사외이사 정족수 규정 적용 대상인 자산총액 1,000억원 이상, 동법 제542조의11제1항 감사위원회 설치 규정 적용 대상인 자산총액 2조원 이상의 기업에 해당하지 않습니다.
(8) 거래량 미달 여부 검토
「코스닥시장 상장규정」코스닥시장 상장규정 제53조제1항제8호에 따라 분기월평균거래량이 유동주식수의 1%에 미달하는 경우 관리종목으로 지정됩니다.
당사는 2022년 1분기 평균거래량이 11,291,441주로 유동주식수의 10.2%에 해당하여 1% 이상이므로 거래량 미달에 의한 관리종목 지정요건에 해당하지 않습니다.
(9) 주식분산 미달 여부 검토
「코스닥시장 상장규정」제53조제1항제9호에 따라 최근 사업연도말 소액주주가 200인 미만이거나 소액주주지분이 20% 미만일 경우 관리종목으로 지정됩니다.
당사의 최근사업연도말(2021년) 소액주주수는 17,499인, 소액주주지분율은 71.67%로 주식분산 미달에 의한 관리종목 지정요건에 해당하지 않습니다.
(10) 기타사항
상기의 사유 등에 따라 당사의 주권은 관리종목으로 지정되거나 상장폐지 될수 있으니 투자자분들께서는 이 점 유의하시기 바랍니다.
| 다. 청약 이후 관리종목으로 지정에 따른 대규모 손실 발생 위험 2022년 반기보고서 제출 결과 당사 재무구조의 악화로 인하여 자본잠식률 50% 이상 발생하거나 감사인의 검토의견이 부적정, 의견거절 및 감사범위제한으로 인한 한정으로 나오는 등의 사유가 발생하면 관리종목으로 지정될 수 있습니다. 당사는 반기보고서 제출 결과 신주상장 예정일(2022년 08월 24일) 이전에 관리종목 으로 지정될 수 있으며, 이 경우 관리종목 지정 이슈로 인하여 당사의 주가가 하락하여 유상증자 최종발행가액을 하회할 수 있습니다. 그러나 배정받은 신주는 신주상장 예정일 3영업일 전(2022년 08월 19일)까지 매도가 불가능하기 때문에 투자자께서는 즉각적인 대응이 어려울 수 있으며, 이로 인해 대규모 손실이 발생할 수 있습니다. 투자자께서는 이 점 유의하시어 청약에 참여하시기 바랍니다. 당사의 주식이 향후 경영실적 부진 또는 유관 법률 및 규정 위반으로 인해 관리종목으로 지정되거나 상장폐지 사유가 발생할 경우, 당사에 대한 자본시장의 신뢰도와 평판이 악화되어 주가에 중대한 부정적인 영향을 미칠 수 있습니다. 특히 관리종목 등으로 지정된다면 현재 진행 중인 유상증자를 포함한 직접조달활동이 중단될 수 있습니다. 이 경우, 당사는 지속적인 영업손실이 발생하고 있는 상황상 금융기관의 차입금 만기연장 거부 또는 기한이익상실로 인한 조기상환 압박을 받아 유동성 부족위험이 급격하게 증가할 수 있습니다. 투자자께서는 당사의 이러한 경영 현황으로 인해 금번 유상증자에 참여한 이후에 대규모 손실이 발생할 수 있는 점에 특히 유의하시기 바랍니다. |
당사가 현재 진행하고 있는 공모 유상증자의 예상 일정에 따르면 2022년 08월 02일~08월 03일의 구주주청약 및 2022년 08월 08일~08월 09일 일반공모 청약 이후 2022년 08월 16일 반기보고서 제출이 예정되어 있습니다.
현재 당사가 진행하고 있는 금번 공모 유상증자의 일정은 다음과 같습니다.
| [공모 관련 주요일정] |
| 날 짜 | 내 용 | 비 고 | |||||||||
|
2022년 06월 10일 |
이사회결의 | - | |||||||||
|
2022년 06월 10일 |
신주발행 및 기준일 공고 | 회사 인터넷 홈페이지 (www.kainosmedicine.com) |
|||||||||
|
2022년 06월 10일 |
증권신고서 제출 | - | |||||||||
| 2022년 06월 24일~ 2022년 07월 11일 |
주식 매매거래 정지 | 주식병합 기준일 전 영업일 ~ 변경상장 전일 | |||||||||
|
2022년 06월 24일 |
1차 발행가액 확정 | 신주배정기준일 3거래일 전 | |||||||||
|
2022년 06월 27일 |
주식병합 기준일 |
- 액면가 100원의 보통주 5주를 액면가 500원의 보통주 1주로 주식병합
|
|||||||||
|
2022년 06월 29일 |
신주배정기준일 | - | |||||||||
|
2022년 07월 11일 |
신주배정통지 | - | |||||||||
| 2022년 07월 12일 | 주식병합 후 신주상장 예정일 | - | |||||||||
|
2022년 07월 12일 |
권리락 | 주2) | |||||||||
|
2022년 07월 18일~ |
신주인수권증서 상장 및 거래기간 | 5영업일 간 거래 | |||||||||
|
2022년 07월 25일 |
신주인수권증서 상장폐지 | 구주주 청약초일 5거래일 이전에 폐지 | |||||||||
|
2022년 07월 28일 |
확정 발행가액 산정 | 구주주 청약초일 3거래일 전 산정 | |||||||||
|
2022년 07월 29일 |
확정 발행가액 공고 | 회사 인터넷 홈페이지 (www.kainosmedicine.com) |
|||||||||
|
2022년 08월 02일~ |
구주주 청약 및 초과청약 | - | |||||||||
|
2022년 08월 04일 |
일반공모 청약 공고 | 회사 인터넷 홈페이지 (www.kainosmedicine.com) 한양증권(주) 홈페이지 (www.hygood.co.kr) |
|||||||||
|
2022년 08월 08일~ |
일반공모 청약 | - | |||||||||
|
2022년 08월 11일 |
환불 및 배정 공고 | 한양증권(주) 홈페이지 (www.hygood.co.kr) |
|||||||||
|
2022년 08월 11일 |
주금 납입 / 환불 | - | |||||||||
| 2022년 08월 16일 | 2022년 반기 보고서 제출(예정) | - | |||||||||
|
2022년 08월 24일 |
신주상장 예정일 | - |
| 주1) | 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
| 주2) | 당사는 2022년 05월 23일 개최된 주주총회에서 액면가 100원의 보통주 5주를 액면가 500원의 보통주 1주로 주식병합을 결의 하였습니다. 이에 따라, 2022년 06월 24일부터 07월 11일까지 주식 매매거래 정지 기간으로 설정되었으며, 신주배정기준일이 매매거래 정지 기간 내에 존재하는 바, 본 유상증자에 따른 권리락은 「코스닥시장 업무규정 시행세칙」 제53조제1항2호에 의거하여 매매거래 정지 해제일인 2022년 07월 12일에 조치될 예정입니다. |
2022년 반기보고서 제출 결과 당사 재무구조의 악화로 인하여 자본잠식률 50% 이상 발생하거나 감사인의 검토의견이 부적정, 의견거절 및 감사범위제한으로 인한 한정으로 나오는 등의 사유가 발생하면 관리종목으로 지정될 수 있습니다.
특히 당사는 2022년 1분기 기준 20.6%의 자본잠식이 발생하고 있어 2022년 반기말까지 3,245백만원 이상의 순손실이 발생하고, 추가로 자본확충이 이루어지지 않는다면 자본잠식률 50% 이상 기록하여 관리종목에 지정될 수 있습니다.
당사는 반기보고서 제출 결과 신주상장 예정일(2022년 08월 24일) 이전에 관리종목 으로 지정될 수 있으며, 이 경우 관리종목 지정 이슈로 인하여 당사의 주가가 하락하여 유상증자 최종발행가액을 하회할 수 있습니다.
그러나 배정받은 신주는 신주상장 예정일 3영업일 전(2022년 08월 19일)까지 매도가 불가능하기 때문에 투자자께서는 즉각적인 대응이 어려울 수 있으며, 이로 인해 대규모 손실이 발생할 수 있습니다. 투자자께서는 이 점 유의하시어 청약에 참여하시기 바랍니다.
한편, 관리종목으로 지정될 경우 중요 사유 발생시마다 한국거래소는 일정기간 매매거래정지 명령을 발동할 수 있습니다. 이외에도 주식의 미수나 신용거래가 금지되며, 미수나 신용거래의 증거금이 되는 대용유가증권으로도 사용할 수 없습니다. 투자자께서는 관리종목 지정에 따른 위험을 인지하시고 투자에 임하시기 바랍니다.
또한, 이러한 관리종목 지정사유 확인 당일 코스닥시장에서의 거래는 정지됩니다. 이를 기한 내에 해결하지 못한다면 코스닥시장 상장폐지 사유에 해당하여, 당사 주식은 향후 장내에서 거래가 이루어지지 못할 수 있습니다. 투자자 여러분들께서는 당사의 주식이 상장폐지될 경우, 투자금액을 회수하지 못하게 될 수도 있는 점을 반드시 유의하여 주시기 바랍니다.
당사의 주식이 향후 경영실적 부진 또는 유관 법률 및 규정 위반으로 인해 관리종목으로 지정되거나 상장폐지 사유가 발생할 경우, 당사에 대한 자본시장의 신뢰도와 평판이 악화되어 주가에 중대한 부정적인 영향을 미칠 수 있습니다. 특히 관리종목 등으로 지정된다면 현재 진행 중인 유상증자를 포함한 직접조달활동이 중단될 수 있습니다. 이 경우, 당사는 지속적인 영업손실이 발생하고 있는 상황상 금융기관의 차입금 만기연장 거부 또는 기한이익상실로 인한 조기상환 압박을 받아 유동성 부족위험이 급격하게 증가할 수 있습니다. 투자자께서는 당사의 이러한 경영 현황으로 인해 금번 유상증자에 참여한 이후에 대규모 손실이 발생할 수 있는 점에 특히 유의하시기 바랍니다.
| 라. 매출 저조로 인한 수익성 악화 위험 당사의 매출은 표적항암제(IRAK4 저해제) 라이선스 아웃 매출 및 에이즈 치료제(KM-023)의 로얄티 등 2가지 형태로 라이선스 수수료와 기타 매출이 발생하고 있습니다. 2021년 라이선스 아웃 매출 1,662백만원은 표적항암제(IRAK4 저해제)에 대하여 미국 엠마우스라이프사이언스(Emmaus life Science, Inc.)와 공동연구개발 및 기술이전 계약을 체결하여 발생하였습니다. 2021년 기타 매출 7백만원 및 2022년 1분기 기타 매출 4백만원은 에이즈 치료제(KM-023)에 대하여 중국 장수 아이디(Jiangsu Aidea Pharmaceutical)와 2014년 10월 체결한 기술이전 계약에 따라 제품 판매에 따른 로열티를 수취하여 발생하였습니다. 당사는 신약개발기업으로 연구개발에 지속적인 투자가 필요하며 후보물질 발굴 이후 기술이전 또는 신약출시까지 상당한 시간과 자금이 소요됩니다. 이러한 당사가 속한 산업 특성상 당사는 2007년 설립 이후부터 지속적으로 적자를 시현하고 있습니다. 연구개발속도를 높이기 위한 연구인력 확충으로 인건비가 증가하고, 다양한 물질을 라이선스 인 하여 임상 시험을 진행하는 당사 비즈니스 모델에 따른 경상연구개발비 증가, 핵심인력 이탈 방지를 위한 주식매수선택권 부여로 인한 주식기준보상비용 등이 증가하여 적자의 폭이 증가하고 있는 추세입니다. |
당사의 매출은 2가지 형태로 라이선스 수수료와 기타 매출이 발생하고 있습니다.
| [매출액 추이] | |
| (K-IFRS 연결) | (단위 : 백만원) |
| 구 분 | 2022년 1분기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
| 라이선스 아웃 | - | 1,662 | - | - |
| 기타 | 4 | 7 | - | - |
| 합 계 | 4 | 1,669 | - | - |
| 출처) 당사 정기보고서 및 당사 제시 |
1) 표적항암제(IRAK4 저해제)
2021년 라이선스 아웃 매출 1,662백만원은 표적항암제(IRAK4 저해제)에 대하여 미국 엠마우스라이프사이언스(Emmaus life Science, Inc.)와 공동연구개발 및 기술이전 계약을 체결하여 발생하였습니다. 이와 관련하여 계약 세부내용은 아래와 같습니다.
| [표적항암제(IRAK4 저해제) 라이선스 아웃 계약 상세 내역] |
|
계약상대방 |
엠마우스라이프사이언스(Emmaus life Science, Inc.) (미국) |
|
공동연구/기술이전 계약 내용 |
공동연구: IRAK4 저해제에 대한 치료작용기전(MOA) 연구, 전임상연구 등에 관한 공동연구개발 계약 |
|
공동연구/기술이전 |
공동연구 계약체결일: 2021.03.02 ~ 기술이전과 동시에 계약 종료 |
|
총 계약금액 |
공동연구 계약시: USD 1,000,000 (50% 현금 수취, 50%는 계약상대방의 주식 수취) |
|
계약조건 |
계약금(Upfront payment): USD 1,000,000 (50% 현금 수취, 50%는 계약상대방의 주식 수취) 카이노스메드는 치료작용기전(MOA) 연구 완료 후 기술이전에 대한 우선협상권을 엠마우스에 부여하였고, 기술이전 계약으로 확대성사되어 KM-10544의 특허에 대한 미국, 유럽, 영국 지역의 전용실시권을 엠마우스에게 이전함. |
|
회계처리방법 |
기술이전과 동시에 공동연구개발 계약 및 기술이전에 따른 계약금을 2021.10.06에 일시에 수익 인식 |
| 출처) 당사 정기보고서 및 당사 제시 |
2) 에이즈 치료제(KM-023)
2021년 기타 매출 7백만원 및 2022년 1분기 기타 매출 4백만원은 에이즈 치료제(KM-023)에 대하여 중국 장수 아이디어(Jiangsu Aidea Pharmaceutical)와 2014년 10월 체결한 기술이전 계약에 따라 제품 판매에 따른 로열티를 수취하여 발생하였습니다. 이와 관련하여 계약 세부내용은 아래와 같습니다.
| [에이즈치료제(KM-023) 라이선스 아웃 계약 상세 내역] |
|
계약상대방 |
Jiangsu Aidea Pharmaceutical (중국) |
|
계약 내용 |
Jiangsu Aidea Pharmaceutical은 에이즈치료제(KM-023)에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
중국, 홍콩, 대만 |
|
계약 기간 |
계약체결일: 2014.10.10 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 1,700,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 1,700,000 - 수취조건: 계약 체결시 마일스톤(Milestone) - 해당사항 없음 로열티(Royalty): 단일정을 포함한 복합제제 매출액의 2% - 수취조건: 매출 발생시 - 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
|
회계처리방법 |
계약금 수취액 USD 200,000은 2014년 10월 ~ 2015월 09월까지 12개월 동안 분할하여 수익인식 USD 1,500,000은 2017년 12월 일시 수익 인식 |
| 출처) 당사 정기보고서 및 당사 제시 |
당사는 신약개발기업으로 연구개발에 지속적인 투자가 필요하며 후보물질 발굴 이후 기술이전 또는 신약출시까지 상당한 시간과 자금이 소요됩니다. 이러한 당사가 속한 산업 특성상 당사는 2007년 설립 이후부터 지속적으로 적자를 시현하고 있습니다. 연구개발속도를 높이기 위한 연구인력 확충으로 인건비가 증가하고, 다양한 물질을 라이선스 인 하여 임상 시험을 진행하는 당사 비즈니스 모델에 따른 경상연구개발비 증가, 핵심인력 이탈 방지를 위한 주식매수선택권 부여로 인한 주식기준보상비용 등이 증가하여 적자의 폭이 증가하고 있는 추세입니다. 당사의 최근 3년 및 당해연도 재무성과는 다음과 같습니다.
| [주요 성장성 지표] | |
| (K-IFRS, 연결) | (단위 : 백만원) |
| 구 분 | 2022년 1분기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
| 자산총계 | 39,472 | 41,957 | 34,779 | 5,571 |
| 자산총계 성장률 | -5.92% | 20.64% | 524.24% | -31.97% |
| 자본총계 | 11,682 | 14,600 | 13,020 | 4,952 |
| 자본총계 성장률 | -19.99% | 12.13% | 162.96% | -38.26% |
| 매출액 | 4 | 1,662 | 0 | 0 |
| 매출액 성장률 | -96.02% | - | - | - |
| 영업이익(손실) | (3,878) | (11,219) | (9,386) | (8,087) |
| 영업이익 성장률 | 적자지속 | 적자지속 | 적자지속 | 적자지속 |
| 당기순이익(순손실) | (3,808) | (16,225) | (11,448) | (8,032) |
| 당기순이익 성장률 | 적자지속 | 적자지속 | 적자지속 | 적자지속 |
| 출처) 당사 정기보고서 및 당사 제시 |
| 주1) 2022년 1분기 자산총계 성장률, 자본총계 성장률은 2021년과 비교하였으며, 매출액 성장률, 영업이익성장률, 당기순이익 성장률은 2021년 1분기와 비교하였습니다. |
| 주2) 당사 2019년 자산총계 및 자본총계는 합병 이전 하나금융11호기업인수목적 주식회사의 2019년 재무상태표입니다. |
당사는 설립 이후 지속적으로 연구개발을 통해 다수의 파이프라인을 개발 및 확장 중에 있으나, 2021년부터 비로소 기술이전을 통한 매출인식이 시작되었습니다. 향후 당사는 보유하고 있는 파이프라인 및 신규개발 예정인 파이프라인의 기술이전 및 지속적인 연구개발을 통하여 매출액 규모를 확장해 나갈 계획입니다.
| [주요 수익성 지표] | |
| (K-IFRS, 연결) | (단위 : 백만원) |
| 구 분 | 2022년 1분기 | 2021년 1분기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|---|
| 매출액 | 4 | 92 | 1,662 | - | - |
| 매출총이익 | 3 | 92 | 1,660 | - | - |
| 매출총이익률 | 70.05% | 100.00% | 99.87% | - | - |
| 영업이익(손실) | (3,878) | (3,528) | (11,219) | (9,386) | (8,087) |
| 영업이익률 | -105,743.70% | -3,829.09% | -674.87% | - | - |
| 당기순이익(순손실) | (3,808) | (3,491) | (16,225) | (11,448) | (8,032) |
| 당기순이익률 | -103,828.18% | -3,788.30% | -976.01% | - | - |
| 출처) 당사 정기보고서 및 당사 제시 |
당사는 설립 이후 지속적으로 영업손실을 기록하고 있고 영업손실의 주요 원인은 무형자산 인식요건을 충족하지 못한 경상연구개발비, 임직원 인건비, 임직원에게 부여한 주식매수선택권과 관련한 주식보상비 등이 있습니다.
특히 연구개발비의 경우 2019년 5,046백만원, 2020년 5,239백만원, 2021년 5,559백만원으로 매년 일정 수준의 비용을 지출하고 있습니다. 경상연구개발비는 최근 3개년 평균 전체 판매비와관리비에서 53.83%를 차지하고 있습니다. 2022년 1분기 기준 경상연구개발비는 2,082백만원이고, 전체 판매비와관리비에서 53.66%를 차지하고 있습니다.
| [판매비와관리비 요약] | |
| (K-IFRS, 연결) | (단위: 백만원) |
| 구분 | 2022년 1분기 | 2021년 1분기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|---|
| 연구개발비 | 2,082 | 1,960 | 5,559 | 5,239 | 5,046 |
| 인건비성 항목 | 932 | 759 | 2,669 | 1,888 | 1,190 |
| 지급수수료 | 152 | 173 | 651 | 730 | 539 |
| 주식보상비 | 376 | 551 | 2,441 | 1,059 | 662 |
| 기타 | 338 | 178 | 1,560 | 470 | 650 |
| 합계 | 3,880 | 3,620 | 12,880 | 9,386 | 8,087 |
| 출처) 당사 정기보고서 및 당사 제시 |
| 주) 인건비성 항목 : 급여, 퇴직급여, 복리후생비 |
당사는 본격적인 매출이 발생하지 않아 판매비와관리비가 그대로 영업이익에 영향을 미치고 있습니다. 판매비와관리비 의 증가와 반비례하여 영업손실은 2019년 8,087백만원, 2020년 9,386백만원, 2021년 11,219백만원, 2022년 1분기 3,878백만원을 기록하며 직전 동기 대비 매년 증가 추이를 나타내고 있습니다.
| [손익계산서 요약] | |
| (K-IFRS, 연결) | (단위: 백만원) |
| 구분 | 2022년 1분기 | 2021년 1분기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|---|
| 영업이익(손실) | (3,878) | (3,528) | (11,219) | (9,386) | (8,087) |
| 기타수익 | 30 | 28 | 245 | 1,363 | 3 |
| 기타비용 | 2 | 1 | 81 | 3,733 | 0 |
| 금융수익 | 71 | 19 | 92 | 153 | 60 |
| 금융비용 | 10 | 13 | 5,260 | 1,160 | 8 |
| 법인세비용차감전순이익(손실) | (3,789) | (3,495) | (16,224) | (12,763) | (8,032) |
| 당기순이익(손실) | (3,808) | (3,491) | (16,225) | (11,448) | (8,032) |
| 출처) 당사 정기보고서 및 당사 제시 |
당사의 영업외손익은 영업손실에 규모에 비해 낮은 수준이나 2019년 이자수익 60백만원으로 인하여 적자폭을 일부 축소하여 영업손실 8,087백만원, 당기순손실 8,032백만원을 기록하였습니다.
2020년의 경우 이자비용 763백만원 및 2020년 06월 30월 발행한 제2회 전환사채 평가로 인한 파생상품부채평가손실 397백만원으로 인하여 영업손실 9,386백만원에서 당기순손실 11,448백만원으로 적자폭이 증가하였습니다.
2021년은 이자비용 1,676백만원 및 파생상품자산(Call Option) 및 파생상품부채(Put Option)에 대한 평가 결과 파생상품평가손실 3,584백만원으로 인하여 영업손실 11,219백만원에서 당기순손실 16,225백만원으로 적자폭이 증가하였습니다.
2022년 1분기에는 영업손실 3,878백만원을 기록하였으며, 기타수익 및 기타비용은 미미하게 발생하였으며, 이자수익 71백만원이 발생하여 당기순손실 3,808백만원을 기록하였습니다. 판관비 소폭 상승의 영향으로 2021년 1분기 대비 적자폭이 소폭 증가하였습니다.
당사는 2020년 06월 30일 제2회 사모 전환사채를 발행한 바 있으며, 이와 관련하여 전환사채에 존재하는 매도청구권(Call Option)을 파생상품자산으로, 조기상환청구권(Put Option)에 대하여 파생상품부채로 회계 처리하고 있습니다. 당사는 한국채택 국제회계기준에 따라 아래와 같은 변수에 따라 공정가치를 평가하여 유사기업의 주가변동성이 높아지고, 위험조정할인율 및 무위험 이자율이 낮아지면 파생상품자산(Call Option)의 공정가치가 증가하여 파생상품평가이익을, 유사기업의 주가변동성이 낮아지고, 위험조정할인율 및 무위험 이자율이 높아지면 파생상품자산(Call Option)의 공정가치가 하락하여 파생상품평가손실을 인식하고 있습니다.
또한 국고채이자율변동성이 높아지고, 위험조정할인율 및 무위험 이자율이 낮아지면파생상품부채(Put Option)의 공정가치가 증가하여 파생상품평가손실을, 국고채이자율변동성이 낮아지고, 위험조정할인율 및 무위험 이자율이 높아지면 파생상품부채(Put Option)의 공정가치가 하락하여 파생상품평가이익을 인식하고 있습니다.
| [전환사채 관련 파생상품자산 및 부채 평가] |
| (기준일: 2021년 12월 31일) |
| 구 분 |
평가기법 |
유의적이지만 관측가능하지 |
공정가치측정과 유의적이지만 |
|---|---|---|---|
| 파생상품자산(전환사채매도청구권) | 이항모형 | 유사기업주가변동성 : 67.59% 위험조정할인율 : 19.66% 무위험이자율 : 1.86% |
공정가치는 다음에 따라 증가(감소)됩니다. ㆍ변동성이 높아지는(낮아지는) 경우 ㆍ위험조정할인율 및 무위험이자율이 낮아지는(높아지는) 경우 |
| 파생상품부채(전환사채상환청구권) | BDT모형 | 국고채이자율변동성 : 28.95% 위험조정할인율 : 19.66% 무위험이자율 : 1.86% |
공정가치는 다음에 따라 증가(감소)됩니다. ㆍ변동성이 높아지는(낮아지는) 경우 ㆍ위험조정할인율 및 무위험이자율이 낮아지는(높아지는) 경우 |
| 출처) 당사 정기보고서 및 당사 제시 |
| 주1) 파생상품자산 및 부채에 대한 평가는 매 반기마다 진행하기 때문에 투입변수는 2021년말 기준으로 작성하였습니다. |
과거 2020년의 경우 파생상품평가손실이 397백만원 발생하였고, 2021년의 경우 파생상품평가손실이 3,584백만원 발생하였습니다. 향후 상기 기재한 전환사채 파생상품자산 및 파생상품부채에 대한 평가의 주요변수의 변동에 따라 파생상품평가손실이 추가로 발생할 수 있으며, 이는 당사의 당기순이익에 부정적인 영향을 미칠수 있음을 투자자께서는 유의 하시기 바랍니다.
당사가 보유한 파이프라인에서의 임상진행과 신약후보물질들에 대한 연구개발로 인하여 향후 일정기간 동안 낮은 매출수준이 지속될 수 있습니다. 당사는 보유 파이프라인의 조속한 기술이전과 제품출시를 통해 매출시현을 계획하고 있으나 기술이전 및 임상 지연으로 인한 매출 발생이 지연되어 본격적인 매출 발생 및 흑자전환 시점이 늦춰질 수 있습니다. 이로 인해 성장성 및 수익성을 포함한 각종 재무지표에 악영향을 미칠 수 있으니 투자자께서는 이점 유의하시기 바랍니다.
|
마. 재무안정성 관련 위험 당사 연결재무제표를 살펴보면 2022년 1분기말 연결기준 총자산 39,472백만원 및 유동자산 32,985백만원, 총 차입금 25,917백만원, 차입금 의존도 65.66%, 부채비율 237.88%, 유동비율 119.27%를 나타내고 있습니다. 부채총계의 대부분을 차지하고 있는 차입금의 규모를 살펴보면 2019년의 경우 차입금은 존재하지 않는데 이는 합병 이전 하나금융11호기업인수주식회사의 재무 현황을 기재하였습니다. 이외 2020년 06월 발행한 제2회 전환사채 및 은행 차입금으로 인해 2020년 23,264백만원, 2021년 25,080백만원, 2022년 1분기 기준 25,917백만원(각 사업연도말 기준 미상환 전환사채 전자등록총액 기재)이 존재합니다. 향후 유의미한 수준의 매출 발생으로 인한 수익 구조 개선 시기가 지연된다면 손실이 지속적으로 발생하거나, 현재 당사가 진행 중인 파이프라인의 임상 시험이 지연 또는 실패하여 소요된 연구개발비용 등을 회수하지 못할 경우 유동성 악화로 인해 당사의 재무안정성이 악화될 수 있습니다. 이러한 점을 투자자께서 유의하시어 투자에 임하시기를 바랍니다. |
당사 연결재무제표를 살펴보면 2022년 1분기말 연결기준 총자산 39,472백만원 및 유동자산 32,985백만원, 총 차입금 25,917백만원, 차입금 의존도 65.66%, 부채비율 237.88%, 유동비율 119.27%를 나타내고 있습니다. 당사가 속한 업종인 한국은행 2020년 기업경영분석 상 C21(의료용 물질 및 의약품 중 중소기업) 기준 업종평균 수치를 살펴보면, 부채비율 70.86%, 유동비율 178.71%, 차입금의존도 20.53%입니다. 해당 업종평균 수치를 당시 2022년 1분기 재무 수치와 비교시 유동비율을 제외하고 모두 상회하고 있습니다.
| [요약 재무 현황] | |
| (K-IFRS, 연결) | (단위: 백만원, %) |
| 구 분 | 2022년 1분기 | 2021년 | 2020년 | 2019년 | 업종평균(주2) |
|---|---|---|---|---|---|
| 자산총계 | 39,472 | 41,957 | 34,779 | 5,571 | - |
| 유동자산 | 32,985 | 36,873 | 31,987 | 4,145 | - |
| 비유동자산 | 6,487 | 5,084 | 2,792 | 1,427 | - |
| 부채총계 | 27,790 | 27,357 | 21,758 | 620 | - |
| 유동부채 | 27,655 | 25,655 | 4,167 | 570 | - |
| 비유동부채 | 135 | 1,701 | 17,591 | 50 | - |
| 자본총계 | 11,682 | 14,600 | 13,020 | 4,952 | - |
| 자본금 | 11,040 | 11,029 | 10,494 | 7,056 | - |
| 부채비율 | 237.88% | 187.37% | 167.11% | 12.52% | 70.86% |
| 유동비율 | 119.27% | 143.72% | 767.56% | 727.55% | 178.71% |
| 총차입금 | 25,917 | 25,080 | 23,264 | 0 | - |
| 단기 차입금 | 2,285 | 0 | 0 | 0 | - |
| 장기 차입금 | 0 | 1,523 | 0 | 0 | - |
| 전환사채 | 20,000 | 20,000 | 20,000 | 0 | - |
| 전환우선주 | 3,632 | 3,557 | 3,264 | 0 | |
| 현금및현금성자산 | 18,554 | 23,231 | 21,952 | 3,811 | - |
| 단기금융상품 | 13,000 | 11,000 | 6,000 | 0 | - |
| 차입금의존도 | 65.66% | 59.78% | 66.89% | 0.00% | 20.53% |
| 출처) 당사 정기보고서 및 당사 제시 |
| 주1) 2019년의 경우 하나금융11호기업인수목적 주식회사의 재무 현황을 작성하였습니다. |
| 주2) 업종평균은 한국은행 2020년 기업경영분석 C21(의료용 물질 및 의약품 중 중소기업) 기준 |
| 주3) 전환사채의 경우 투자자의 이해를 돕기 위해 전자등록총액으로 작성하였습니다. |
부채총계의 대부분을 차지하고 있는 차입금의 규모를 살펴보면 2019년의 경우 차입금은 존재하지 않는데 이는 합병 이전 하나금융11호기업인수주식회사의 재무 현황을 기재하였습니다. 이외 2020년 06월 발행한 제2회 전환사채 및 은행 차입금으로 인해 2020년 23,264백만원, 2021년 25,080백만원, 2022년 1분기 기준 25,917백만원(각 사업연도말 기준 미상환 전환사채 전자등록총액 기재)이 존재합니다.
해당 차입금의 주된 사용처는 1) 미국 자회사의 KM-819 임상시험에 대한 자금 조달 목적의 유상증자 참여, 2) 운영자금, 3) 당사가 분양 받은 과천 지식산업센터 사무실 및 연구실의 중도금 납부 등입니다.
당사가 현재까지 발행한 전환사채의 상세 내역은 다음과 같습니다.
| [전환사채 상세 내역] |
| (단위: 백만원) |
| 구 분 | 2022년 1분기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|
| 비유동부채 | ||||
| 전환사채 액면금액 | 20,000 | 20,000 | 20,000 | - |
| 전환권조정 | (8,556) | (8,556) | (10,285) | - |
| 상환할증금 | 1,024 | 1,024 | 1,024 | - |
| 합계 | 12,468 | 12,468 | 10,739 | - |
| 자본 | ||||
| 전환권대가 | 4,515 | 4,515 | 4,515 | |
| 출처) 당사 정기보고서 및 당사 제시 |
| [전환사채 발행 개요] |
| (단위 : 원) |
| 구분 | 전환사채 |
|---|---|
| 사채의 명칭 | 주식회사 카이노스메드 제2회 무기명식 이권부 무보증 사모 전환사채 |
| 발행일 | 2020년 06월 30일 |
| 만기일 | 2025년 06월 30일 |
| 액면가액 | 20,000,000,000원 |
| 상환방법 | 만기일에 원금의 105.1205%를 일시상환한다. |
| 사채의 이율 | 표면금리 0% (만기보장수익률은 3개월 단위 복리계산 1%) |
| 조기상환청구권(Put Option) | 사채권자는 사채의 발행일로부터 24개월 이후 45개월까지의 기간중 원금의 전부 및 일부에 대하여 조기상환수익률 연 1.0%(3개월 단위 복리계산)가 적용된 청구 금액을 조기상환 청구할 수 있음. |
| 매도청구권(Call Option) | 회사는 사채권자로부터 회사 또는 회사가 지정하는 제3자(매수인)에게사채의 발행일로부터 12개월 이후 24개월까지의 기간 중 매 3개월에 해당되는 날에 원금의 25/100에 대하여 매도 청구할 수 있음. 매수인이 매도청구 행사시 연1.0%(3개월 단위 복리계산)의 이율을 적용하여 계산한 금액을 지급하여야 함. |
| 전환가격(주) | 5,813원/주 (최초 발행당시 전환가격) |
| 전환기간 | 2021년 6월 30일부터 2025년 3월 30일 |
| 전환가격의 조정 | 발행회사가 시가를 하회하는 발행가액으로 유상증자, 무상증자, 주식배당 및 준비금의 자본전입 등으로 주식을 발행하는 경우, 시가를 하회하는 전환가액 또는 행사가액으로 전환사채 또는 신주인수권부사채를 발행하는 경우에는 전환가격이 조정될 수 있으며, 발행회사의 보통주식 주가가 하락할 경우 발행일로부터 매 3개월마다 약정에 따라 조정전 전환가격의 70%까지 전환가격 조정 |
| 전환가격 |
(1)최초 전환가액: 5,813원/주 (3)2차 조정전환가액: 4,386원/주 (2020년 12월 30일 조정) (4)3차 조정전환가액: 4,070원/주 (2021년 03월 30일 조정) |
| 출처) 당사 정기보고서 및 당사 제시 |
2022년 1분기말 현재 장단기차입금 내역은 다음과 같습니다.
| [차입금 상세 내역] | |
| (K-IFRS, 연결) | (단위 : 백만원) |
| 채권자 | 목적 | 만기일 | 이자율 | 상환조건 | 2022년 1분기 | 2021년 | 2020년 | 2019년 | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 단기차입금 | 장기차입금 | 단기차입금 | 장기차입금 | 단기차입금 | 장기차입금 | 단기차입금 | 장기차입금 | |||||
| 기업은행 | 시설자금 | 2023년 02월 28일 | 2.759% | 만기일시상환 | 2,285 | 0 | 0 | 1,523 | 0 | 0 | 0 | 0 |
| 출처) 당사 정기보고서 및 당사 제시 |
당사가 분양 받은 과천 지식산업센터 사무실 및 연구실의 중도금 납부를 위하여 기업은행과 시설자금 차입약정을 체결하였으며, 2022년 1분기말까지 2,285백만원 차입을 진행하였습니다.
한편, 이자보상배율의 경우 영업활동을 통해 벌어들인 이익으로 차입금에 대한 이자비용을 감내할 수 있는지를 확인할 수 있는 지표로서 활용됩니다.
| [이자보상배율 현황] | |
| (K-IFRS, 연결) | (단위: 백만원) |
| 구분 | 2022년 1분기 | 2021년 | 2020년 | 2019년 | 비고 |
|---|---|---|---|---|---|
| 매출액 | 4 | 1,662 | - | - | - |
| 영업이익(손실) | (3,878) | (11,219) | (9,386) | (8,087) | - |
| 영업이익률(손실률) | -105,743.70% | -674.87% | - | - | 영업이익(손실) ÷ 매출액 |
| 자산총계 | 39,472 | 41,957 | 34,779 | 5,571 | - |
| 총자산 회전율(회) | 0.0001 | 0.04 | - | - | 매출액 ÷ 평균총자산 |
| 이자비용 | 10 | 1,676 | 763 | 8 | - |
| 이자보상배율(배) | -400.38 | -6.69 | -12.29 | -995.11 | 영업이익(손실) ÷ 이자비용 |
| 이자비용 부담률 | 264.11% | 100.84% | - | - | 이자비용 ÷ 매출액 |
| 차입금 총계 | 25,917 | 25,080 | 23,264 | - | - |
| 차입금 평균이자율 | 0.04% | 6.68% | 3.28% | - | 이자비용 ÷ 차입금 총계 |
| 차입금 의존도 | 65.66% | 59.78% | 66.89% | - | 차입금 총계 ÷ 자산총계 |
| 출처) 당사 정기보고서 및 당사 제시 |
| 주) 차입금 총계는 제2회 전환사채의 전자등록총액, 전환우선주 및 은행 차입금을 기재하였습니다. |
2019년부터 2020년까지 연결기준 매출액이 발생하지 않았으며, 2021년 1,662백만원, 2022년 1분기 4백만원의 매출액이 발생하였습니다. 영업손실의 경우 2019년 8,087백만원, 2020년 9,386백만원, 2021년 11,219백만원, 2022년 1분기 3,878백만원이 발생하였으며, 이자비용의 경우 2019년 8백만원, 2020년 763백만원, 2021년 1,676백만원, 2022년 1분기 10백만원이 발생하였고, 당사의 이자보상배율은 지속적으로 1배 미만을 기록하여 영업을 통한 이익으로 이자비용을 충당하지 못하는 상황입니다. 이는 당사의 채무상환능력이 취약하다는 것을 나타내며, 미미한 매출 수준으로 인해 영업 적자가 심화되고 있음에 기인합니다.
당사의 파이프라인별 임상 진행 단계에 따라 라이선스 아웃 계약 및 로열티 수취 시기가 지연되거나, 매출 실적이 부진할 경우 영업실적 개선이 이루어지 지않아 향후에도 이자보상배율이 1배를 하회할 수 있습니다. 향후 매출 성장 및 수익성 개선이 이루어지지 않는다면, 이자비용으로 인한 재무적 부담으로 인해 당사의 재무 안정성이 훼손될 가능성이 있으니 투자자께서는 이 점 유의하시기 바랍니다.
향후 유의미한 수준의 매출 발생으로 인한 수익 구조 개선 시기가 지연된다면 손실이 지속적으로 발생하거나, 현재 당사가 진행 중인 파이프라인의 임상 시험이 지연 또는 실패하여 소요된 연구개발비용 등을 회수하지 못할 경우 유동성 악화로 인해 당사의 재무안정성이 악화될 수 있습니다. 이러한 점을 투자자께서 유의하시어 투자에 임하시기를 바랍니다.
한편, 당사는 개발 초기 단계의 약물을 라이선스 인하여 임상 시험을 진행하고 글로벌 제약사에 라이선스 아웃하여 매출이 발생하는 사업 모델을 영위하고 있습니다. 설립 이후 현재까지 총 6건의 라이선스 아웃 계약을 체결하였으며, 총 계약금은 12,800천달러, 수취 금액은 7,700천달러입니다. 라이선스 아웃 계약에 따른 로열티 지급 세부 조건은 다음과 같습니다.
.
|
라이선스아웃 계약 총괄표 |
| 구분 |
품목 |
계약상대방 |
대상지역 |
계약체결일 |
계약종료일 |
총 계약금액 |
수취금액 |
진행단계 |
|---|---|---|---|---|---|---|---|---|
| 1 |
에이즈치료제 |
Jiangsu Aidea Pharmaceutical |
중국, 홍콩, 대만 |
2014.10.10 |
특허 만료일 |
USD 1,700,000 |
USD 1,700,000 |
NDA승인, |
| 2 |
항암제 |
Jiangsu Aidea Pharmaceutical |
중국, 홍콩, 대만 |
2015.12.10 |
특허 만료일 |
USD 1,500,000 |
USD 1,500,000 |
임상 1상 진행 |
| 3 |
항암제 |
Jiangsu Aidea Pharmaceutical |
중국, 홍콩, 대만 |
2015.12.10 |
특허 만료일 |
USD 2,500,000 |
USD 1,000,000 |
전임상 |
| 4 |
대사질환치료제 |
CROWN BIO |
전세계 |
2014.07.22 |
특허 만료일 |
USD 3,600,000 |
- |
전임상 |
| 5 | 뇌신경질환 치료제 (KM819) |
FAScinate Therapeutics | 전세계 (한국 제외) |
2021.09.27 | 특허 만료일 | USD 2,000,000 | USD 2,000,000 | 임상2상 진행 (미국) |
| 6 | 항암제 (KM-10544) |
Emmaus Life Science, Inc. | 미국, 유럽, 영국 | 2021.10.06 | 특허 만료일 | USD 1,500,000 | USD 1,500,000 | 전임상 진행 |
| 합계 | USD 12,800,000 | USD 7,700,000 | - | |||||
| 출처) 당사 정기보고서 및 당사 제시 |
(1) 에이즈 치료제(KM-023)
|
계약상대방 |
Jiangsu Aidea Pharmaceutical (중국) |
|
계약 내용 |
Jiangsu Aidea Pharmaceutical은 에이즈치료제(KM-023)에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
중국, 홍콩, 대만 |
|
계약 기간 |
계약체결일: 2014.10.10 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 1,700,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 1,700,000 - 수취조건: 계약 체결시 마일스톤(Milestone) - 해당사항 없음 로열티(Royalty): 단일정을 포함한 복합제제 매출액의 2% - 수취조건: 매출 발생시 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
|
회계처리방법 |
계약금 수취액 USD 200,000은 2014년 10월 ~ 2015월 09월까지 12개월 동안 분할하여 수익인식 USD 1,500,000은 2017년 12월 일시 수익 인식 |
(2) 항암제(KM-635)
|
계약상대방 |
Jiangsu Aidea Pharmaceutical (중국) |
|
계약 내용 |
Jiangsu Aidea Pharmaceutical은 항암제(KM-635)에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
중국, 홍콩, 대만 |
|
계약 기간 |
계약체결일: 2015.12.10 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 1,500,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 1,500,000 - 수취조건: 계약 체결시 마일스톤(Milestone) - 해당사항 없음 로열티(Royalty): 순매출액의 10% - 수취조건: 매출 발생시 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
|
회계처리방법 |
계약금 수취액 USD 1,000,000은 2015년 12월 ~ 2016년 11월까지 12개월 동안 분할하여 수익인식 USD 500,000은 2017년 12월 일시 수익 인식 |
(3) 항암제(KM-630)
|
계약상대방 |
Jiangsu Aidea Pharmaceutical (중국) |
|
계약 내용 |
Jiangsu Aidea Pharmaceutical은 항암제(KM-630)에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
중국, 홍콩, 대만 |
|
계약 기간 |
계약체결일: 2015.12.10 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 2,500,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 1,000,000 - 수취조건: 계약 체결시 마일스톤(Milestone) - Upon Initiation of Phase 2 Clinical Trial USD 500,000, Initiation of Phase 3 Clinical Trial USD 500,000, Regulatory approval by SFDA USD 500,000 로열티(Royalty): 순매출액의 10% - 수취조건: 매출 발생시 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
|
회계처리방법 |
계약금 수취액 USD 1,000,000은 2015년 12월 ~ 2016년 11월까지 12개월 동안 분할하여 수익인식 |
(4) 대사질환 치료제
|
계약상대방 |
CROWN BIO (중국) |
|
계약 내용 |
CROWN BIO는 대사질환 치료제에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
전세계 |
|
계약 기간 |
계약체결일: 2014.07.22 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 3,600,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): - 해당사항 없음. 마일스톤(Milestone): USD 3,600,000 - 수취조건: 중국 임상 1상 개시 USD 100,000, 중국 임상 2상 개시 USD 500,000, 중국 임상 3상 개시 USD 1,000,000, 중국 의약품허가 USD 2,000,000 로열티(Royalty): 순매출액의 10% - 수취조건: 매출 발생시 재실시권 수익 분배비율: 각 단계별 지분율 IND (50%), 임상 1상 (40%), 임상 2상 (25%), 임상 3상 (10%)
|
|
회계처리방법 |
- |
(5) 뇌신경계 치료제(KM-819)
|
계약상대방 |
FAScinate Therapeutics Inc. |
|
계약 내용 |
FAScinate Therapeutics는 뇌신경계 치료제에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
전세계 (한국 제외) |
|
계약 기간 |
계약체결일: 2021.09.27 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 2,000,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 2,000,000 - 해당사항 없음 로열티(Royalty): 순매출액의 10%
|
|
회계처리방법 |
USD 2,000,000은 2021년 9월 일시 수익 인식 |
(6) 표적항암제 (IRAK4 저해제)
- IRAK4 저해제의 경우, 엠마우스라이프 사이언스와 공동연구개발 계약에 이어 기술이전으로까지 확장되여 계약이 체결되었습니다.
|
계약상대방 |
엠마우스라이프사이언스(Emmaus life Science, Inc.) (미국) |
|
공동연구/기술이전 계약 내용 |
공동연구: IRAK4 저해제에 대한 치료작용기전(MOA) 연구, 전임상연구 등에 관한 공동연구개발 계약 |
|
공동연구/기술이전 |
공동연구 계약체결일: 2021.03.02 ~ 기술이전과 동시에 계약 종료 |
|
총 계약금액 |
공동연구 계약시: USD 1,000,000 (50% 현금 수취, 50%는 계약상대방의 주식 수취) |
|
계약조건 |
계약금(Upfront payment): USD 1,000,000 (50% 현금 수취, 50%는 계약상대방의 주식 수취)
|
|
회계처리방법 |
기술이전과 동시에 공동연구개발 계약 및 기술이전에 따른 계약금을 2021.10.06에 일시에 수익 인식 |
상기 라이선스 아웃 계약을 체결한 약물이 임상, 등록, 상업화에 실패할 경우 당사가 수취하는 마일스톤 및 로열티의 규모가 예상치보다 감소할 수 있으며 이는 당사의 수익성 및 재무구조에 악영향을 미칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
|
바. 영업현금흐름 및 유동성 관련 위험 당사는 현금흐름 및 유동성에 대하여 지속적으로 모니터링하면서 유동성 이슈가 발생하지 않도록 대응하고 있으나, 최근 3년간 지속적으로 유동성 지표가 악화되어 왔으며, 향후에도 유의미한 수준의 매출이 발생하지 않아 음(-)의 영업활동현금흐름이 계속 발생할 경우 유동성 리스크가 부각될 위험이 있습니다. 때문에 보유 파이프라인의 라이선스 아웃 및 영업활동 전반에 대한 모니터링이 필요하다고 판단되며, 지속적으로 영업 성과에 부정적인 영향으로 음(-)의 영업활동현금흐름이 발생할 경우 장기적으로 회사의 현금흐름에 문제가 발생할 소지가 있습니다. 투자자께서는 회사의 현금흐름 및 유동성 관련 위험요인을 면밀히 검토하시고 투자에 임해주시기 바랍니다. |
당사는 미미한 수준의 매출 발생 및 지속적인 연구개발 활동으로 인해 음(-)의 영업활동현금흐름을 보이고 있으며, 투자활동현금흐름의 경우, 2021년 및 2022년 1분기에는 단기금융상품의 취득으로 인해 음(-)의 현금흐름을 보였습니다. 당사는 음(-)의 영업활동현금흐름을 대체적으로 재무활동현금흐름을 통하여 충당하고 있는 상황이며, 2022년 1분기말 기준 당사는 18,554백만원의 현금 및 현금성자산을 보유하고 있습니다. 당사의 최근 3년 및 당분기까지 요약 현금흐름 추이는 다음과 같습니다.
| [주요 현금흐름 추이] | |
| (K-IFRS, 연결) | (단위: 백만원) |
| 구분 | 2022년 1분기 | 2021년 1분기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|---|
| Ⅰ.영업활동현금흐름 | (1,748) | (2,087) | (9,195) | (7,608) | (6,947) |
| (1)영업에서 창출된 현금 | (1,815) | (2,104) | (9,272) | (7,759) | (7,017) |
| 1.당기순이익(손실) | (3,808) | (3,491) | (16,225) | (11,448) | (8,032) |
| 2.조정 | 652 | 767 | 8,730 | 3,816 | 1,025 |
| 3.영업활동으로 인한 자산부채의 변동 | 1,341 | 619 | (1,776) | (128) | (10) |
| (2)이자수취 | 67 | 21 | 77 | 163 | 70 |
| (3)이자지급(영업) | - | (1) | - | - | - |
| (4)법인세의 납부 | - | (2) | (1) | (12) | (0) |
| Ⅱ.투자활동현금흐름 | (3,672) | (1,893) | (5,753) | 1,811 | 2,852 |
| (1)투자활동으로 인한 현금유입 | 3,011 | 2,019 | 2,278 | 9,186 | 8,016 |
| 1.단기금융상품의 감소 | 3,000 | - | - | 9,136 | 8,016 |
| 2.보증금의 감소 | 10 | 159 | 204 | 50 | - |
| 3.유동당기손익-공정가치측정금융자산의 처분 | - | 1,860 | 1,860 | - | - |
| 4.유형자산처분 | 1 | - | 213 | - | - |
| (2)투자활동으로 인한 현금유출액 | (6,682) | (3,912) | (8,031) | (7,375) | (5,164) |
| 1.단기금융상품 취득 | 5,000 | 3,000 | 5,000 | 6,000 | 5,000 |
| 2.비유동당기손익-공정가치측정금융자산 취득 | 605 | - | 517 | - | - |
| 3.장기대여금의 증가 | - | - | - | - | 11 |
| 4.유형자산의 취득 | 716 | 887 | 1,939 | 1,021 | 149 |
| 5.무형자산의 취득 | 361 | 0 | 456 | 200 | 3 |
| 6.보증금의 증가 | 1 | 10 | 119 | 154 | - |
| 7.장기선급금의 증가 | - | 15 | - | - | - |
| Ⅲ.재무활동현금흐름 | 810 | 863 | 14,667 | 25,775 | 4,134 |
| (1)재무활동으로 인한 현금유입액 | 909 | 942 | 15,029 | 26,032 | 4,303 |
| 1.전환사채 발행 | - | - | - | 20,000 | - |
| 2.주식선택권의 행사 | 148 | 181 | 808 | 1,743 | 305 |
| 3.유상증자 | 12,500 | - | 3,997 | ||
| 4.장기차입금 증가 | 762 | 762 | 1,523 | - | - |
| 5.비지배지분의 증가 | - | - | 198 | - | - |
| 6.합병으로 인한 현금및현금성자산의 증가 | - | - | - | 1,024 | - |
| 7.우선주부채의 발행 | - | - | - | 3,264 | - |
| (2)재무활동으로 인한 현금유출액 | (100) | (79) | (363) | (257) | (169) |
| 1.리스부채의 지급 | 100 | 79 | 363 | 257 | 169 |
| Ⅳ.현금및현금성자산의 증가(감소) | (4,610) | (3,117) | (282) | 19,977 | 38 |
| Ⅴ.기초현금및현금성자산 | 23,231 | 21,952 | 21,952 | 3,811 | 3,774 |
| Ⅵ.현금및현금성자산에 대한 환율변동 | (67) | 782 | 1,561 | (1,836) | (1) |
| Ⅶ.기말현금및현금성자산 | 18,554 | 19,617 | 23,231 | 21,952 | 3,811 |
| 출처) 당사 정기보고서 및 당사 제시 |
당사는 파킨슨병, 다계통위축증, 항암제 등 다양한 질병을 적응증으로 하는 신약을 개발하고 있으며, 이에 따라 2019년 3,278백만원, 2020년 2,884백만원, 2021년 3,685백만원, 2022년 1분기 1,840백만원의 경상연구개발비용이 지출되었습니다. 향후 파이프라인별 임상 단계 진전에 따라 더 많은 연구개발비가 투입될 예정이며 이에 따라 영업비용 또한 확대될 것으로 보입니다.
당사는 2021년말 기준 현금성 자산 19,617백만원 및 단기금융상품 9,000백만원, 2022년 1분기말 기준 현금성자산 18,554백만원 및 단기금융상품 13,000백만원을 보유하고 있습니다. 당사는 매년 매출이 미미한 수준으로 발생하여 영업비용을 충당이 불가능하고, 연구개발비용 등 대규모 순 현금 소요가 발생하고 있어 이를 외부자금 조달 및 금융자산의 처분 등을 통해 충당하고 있습니다. 금번 유상증자를 통해 유입된 자금을 당사는 기발행 전환사채 상환 및 연구개발비에 사용할 예정입니다.
당사는 현금흐름 및 유동성에 대하여 지속적으로 모니터링하면서 유동성 이슈가 발생하지 않도록 대응하고 있으나, 최근 3년간 지속적으로 유동성 지표가 악화되어 왔으며, 향후에도 유의미한 수준의 매출이 발생하지 않아 음(-)의 영업활동현금흐름이 계속 발생할 경우 유동성 리스크가 부각될 위험이 있습니다. 때문에 보유 파이프라인의 라이선스 아웃 및 영업활동 전반에 대한 모니터링이 필요하다고 판단되며, 지속적으로 영업 성과에 부정적인 영향으로 음(-)의 영업활동현금흐름이 발생할 경우 장기적으로 회사의 현금흐름에 문제가 발생할 소지가 있습니다. 투자자께서는 회사의 현금흐름 및 유동성 관련 위험요인을 면밀히 검토하시고 투자에 임해주시기 바랍니다.
| 사. 종속회사 관련 위험 당사는 증권신고서 제출 전일 현재 2개의 종속회사가 있으며 이들의 경영실적은 당사의 연결재무제표에 반영하고 있습니다. 당사의 종속회사에 대한 지분투자 금액은 K-IFRS 회계처리 기준에 따라 해당 개별 종속회사의 영업실적에 의한 재무제표 작성 후, 연결 재무제표로 합산 작성되어 공시되고 있어 종속회사의 실적에 따라 당사의 연결재무제표 손익에 직접적인 영향을 미치고 있습니다. 종속회사인 FAScinate Therapeutics는 미국 California, San Diego에 소재하고 있는 회사로서 주 업무는 중추신경계 질환 치료제 개발입니다. KAIDEA는 당사의 파이프라인 중 2014년 10월 중국 파트너사 장수 아이디어와 KM-023(에이즈 치료제)의 라이선스 아웃 계약 체결 당시 대상 지역을 중국, 홍콩, 대만으로 한정하였으나, 그 외 시장을 개척하기 위하여 당사와 장수 아이디어가 함께 설립한 Joint Venture입니다. 종속회사의 손익은 모두 당사의 연결 재무손익로 반영되고 있음에 따라 KM-819(파킨슨병 치료제)의 미국 FDA 임상 2상 승인 여부 등 대내외적인 변수로 인해 매출 지연이 발생하여 종속회사의 영업활동이 사업계획과 다르게 진행될 경우, 당사가 납입한 자본금이 손상처리되어 수익성 및 재무 안정성에 부정적인 영향을 미칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. |
당사는 증권신고서 제출 전일 현재 2개의 종속회사가 있으며 이들의 경영실적은 당사의 연결재무제표에 반영하고 있습니다. 당사의 종속회사에 대한 지분투자 금액은 K-IFRS 회계처리 기준에 따라 해당 개별 종속회사의 영업실적에 의한 재무제표 작성 후, 연결 재무제표로 합산 작성되어 공시되고 있어 종속회사의 실적에 따라 당사의 연결재무제표 손익에 직접적인 영향을 미치고 있습니다.
증권신고서 제출 전일 현재 종속회사 현황은 다음과 같습니다.
| [종속회사 현황] |
| (기준일 : 증권신고서 제출 전일 현재) |
| 구분 | 회사명 | 설립일 | 지분율 | 설립목적 |
|---|---|---|---|---|
| 1 |
FAScinate Therapeutics Inc. |
2018.01.17 | 94% | 개발제품 해외 진출(전세계, 한국 제외) |
| 2 |
KAIDEA GLOBAL PTE.LTD |
2021.09.17 | 55% | 개발제품 해외 진출(중국, 홍콩, 대만) |
| 출처) 당사 정기보고서 및 당사 제시 |
[종속회사 내역 및 상세]
(1) FAScianate Therapeutics, Inc.
종속회사인 FAScinate Therapeutics는 미국 California, San Diego에 소재하고 있는 회사로서 주 업무는 중추신경계 질환 치료제 개발입니다. 2020년 최초 투자를 통해 지분 100% 취득하였으며, 2021년 KM-819(파킨슨병 치료제)의 한국을 제외한 글로벌 개발권을 기술이전하였습니다. 현재 FAScinate의 지분구조는 당사 94%, The Wells Investment 6%를 보유하고 있습니다.
| 회사명 | FAScinate Therapeutics, Inc. | |||
| 대표이사 | 이기섭 | |||
| 주소 | 4365 Executive Drive Suite 660, San Diego, CA 92121 | |||
| 설립일 | 2018년 1월 17일 | |||
| 사업내용 | 신약개발 | |||
| 종업원수 | 3명 (2022년 1분기말 기준) |
|||
| 연혁 | 2018년 | 2018.01 FAScinate Therapeutics Inc. 설립 | ||
| 2019년 | - | |||
| 2020년 | COI 수정 (이기섭 CEO and Chairman, 이재문 President and CFO), 9월 운영 사무실 San Diego 에 오픈 | |||
| 2021년 | KM-819 기술이전 완료 | |||
| 구분(단위 : 백만원) | 2022년 1분기 | 2021년 | 2020년 | 2019년 |
| 자산총계 | 19,094 | 19,813 | 19,726 | 7 |
| 부채총계 | 21,937 | 21,629 | 20,011 | 12 |
| 자본총계 | (2,843) | (1,816) | (285) | (5) |
| 매출액 | - | - | - | - |
| 영업이익(손실) | (1,405) | (3,090) | (968) | (4) |
| 당기순이익(손실) | (1,406) | (3,099) | (979) | (5) |
| 출처) 당사 정기보고서 및 당사 제시 |
(2) KAIDEA GLOBAL PTE.LTD
KAIDEA는 당사의 파이프라인 중 2014년 10월 중국 파트너사 장수 아이디어와 KM-023(에이즈 치료제)의 라이선스 아웃 계약 체결 당시 대상 지역을 중국, 홍콩, 대만으로 한정하였으나, 그 외 시장을 개척하기 위하여 당사와 장수 아이디어가 함께 설립한 Joint Venture입니다. 당사가 해당 법인의 지분 55%를 보유하고 있습니다.
| 회사명 | KAIDEA GLOBAL PTE.LTD | |||
| 대표이사 | 김문호(Julian Kim) | |||
| 주소 | 60 Paya Lebar Road#05-08 Paya Lebar Square Singaproe 409051 | |||
| 설립일 | 2021년 04월 23일 | |||
| 사업내용 | 카이노스메드가 보유한 의약품 및 헬스케어 기술/품목들의 아시아지역 시장진출 추진 |
|||
| 종업원수 | 5명 | |||
| 연혁 | 2021년 | 2021. 04. 설립 | ||
| 구분(단위 : 백만원) | 2022년 1분기 | 2021년 | 2020년 | 2019년 |
| 자산총계 | 407 | 408 | - | - |
| 부채총계 | 4 | 0 | - | - |
| 자본총계 | 403 | 408 | - | - |
| 매출액 | - | - | - | - |
| 영업이익(손실) | (16) | (31) | - | - |
| 당기순이익(손실) | (13) | (31) | - | - |
| 출처) 당사 정기보고서 및 당사 제시 |
당사는 매년 상기 종속회사들과 채권, 채무 및 거래내역이 있습니다. FAScinate Therapeutics, Inc.의 경우 당사가 진행하는 KM-819(파킨슨병 치료제)의 미국 임상 2상을 진행하고, 추후 해외 제약사와의 기술이전을 추진하기 위하여 2020년 전환우선주를 인수하여 자금을 조달하였습니다. 이후 2021년 09월 27일 KM-819(파킨슨병 치료제)의 라이선스 아웃 계약을 체결하고 이에 대한 계약금 2,351백만원을 수취하였습니다.
KAIDEA GLOBAL PTE.LTD의 경우 당사의 파이프라인 중 2014년 10월 중국 파트너사 장수 아이디어와 KM-023(에이즈 치료제)의 라이선스 아웃 계약 체결 당시 대상 지역을 중국, 홍콩, 대만으로 한정하였으나, 그 외 시장을 개척하기 위하여 당사와 장수 아이디어가 함께 설립한 Joint Venture이며, 2021년 242백만원을 출자하여 55% 지분을 보유하고 있습니다.
당사의 주요 종속회사와의 거래 내역과 채권 및 채무 내역은 다음과 같습니다.
| [주요 종속회사와의 채권 및 채무 내역] |
| (단위 : 백만원) |
|
회사명 |
특수관계자성격 |
거래종류 |
2022년 1분기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|---|---|
| FAScinate Therapeutics, Inc. |
종속회사 |
단기대여금 | - | - | 11 | - |
| 장기대여금 | - | - | 42 | 12 | ||
| 전환우선주투자 | 10,316 | 11,459 | 15,367 | - | ||
| 미수수익 | - | - | 2 | 1 | ||
| 미수금 | 9 | 73 | - | - | ||
| 미지급금 | - | - | 375 | - |
| 출처) 당사 정기보고서 및 당사 제시 |
| [주요 종속회사와의 거래 내역] |
| (단위 : 백만원) |
|
회사명 |
특수관계자성격 |
거래내역 |
2022년 1분기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|---|---|
| FAScinate Therapeutics, Inc. |
종속회사 |
이자수익 | - | 0 | 2 | 1 |
| 매출 | - | 2,351 | - | - | ||
| 연구개발비 | 9 | 375 | 375 | - |
| 출처) 당사 정기보고서 및 당사 제시 |
| [주요 종속회사와의 자금 거래 내역] |
| (단위 : 백만원) |
|
회사명 |
특수관계자성격 |
거래내역 |
2022년 1분기 | 2021년 | 2020년 | 2019년 |
|---|---|---|---|---|---|---|
| FAScinate Therapeutics, Inc. |
종속회사 |
대여 | - | - | 58 | 12 |
| 회수 | - | 53 | 17 | - | ||
| 출자 | - | - | 2 | - | ||
| 전환우선주취득 | - | - | 18,213 | - | ||
| KAIDEA GLOBAL PTE.LTD | 종속회사 | 출자 | - | 242 | - | - |
| 출처) 당사 정기보고서 및 당사 제시 |
종속회사의 손익은 모두 당사의 연결 재무손익로 반영되고 있음에 따라 KM-819(파킨슨병 치료제)의 미국 FDA 임상 2상 승인 여부 등 대내외적인 변수로 인해 종속회사의 영업활동이 사업계획과 다르게 진행될 경우, 당사가 납입한 자본금 및 전환우선주가 손상처리되어 수익성 및 재무 안정성에 부정적인 영향을 미칠 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| 아. 최대주주 및 특수관계인 지분희석 및 경영권 관련 위험 증권신고서 제출 전일 기준 당사 최대주주는 대표이사 이기섭으로 15,163,144주(지분율 13.71%) 보유하고 있으며, 특수관계인을 포함할 시 27,085,917주(지분율 24.50%)를 보유 중에 있습니다. 금번 유상증자에서 최대주주는 자금 여력에 따라 최대한 참여할 예정으로, 현재는 최대주주인 이기섭 대표이사는 배정분의 약 15% 정도 참여를 계획 중이며, 특수관계인들에 대한 청약 참여 여부는 미정입니다. 만약 최대주주 및 특수관계인이 전액 미참여할 경우 지분율은 현재 24.50%에서 19.55%까지 감소할 수 있으며, 최대주주가 배정분의 15% 참여하고, 특수관계인이 전액 미참여할 경우 최대주주 및 특수관계인의 지분율은 현재 24.50%에서 19.96%까지 감소할 수 있습니다. 유상증자 후 최대주주 지분율은 13.71%(최대주주 등 24.50%)에서 제2회 전환사채 및 행사가능가격대 주식매수선택권이 모두 전환 및 행사될 경우 10.79%(최대주주 등 18.97%)로 하락할 수 있습니다. 지분율이 감소할 경우 당사에 대한 적대적 M&A 등의 위험성이 존재하며, 이는 경영진 변동의 위험성으로 이어져 안정적인 경영활동이 어려울 수 있습니다. 투자자분들은 투자 시, 이 점 유의해주시기 바랍니다. |
증권신고서 제출 전일 기준 당사 최대주주는 대표이사 이기섭으로 15,163,144주(지분율 13.71%) 보유하고 있으며, 특수관계인을 포함할 시 27,085,917주(지분율 24.50%)를 보유 중에 있습니다.
| [최대주주 등 지분 현황] | |
| (기준일: 증권신고서 제출 전일 현재) | (단위: 주, %) |
| 주주 | 관계 | 주식의 종류 | 주식병합 전 | 주식병합 후 | ||
|---|---|---|---|---|---|---|
| 주식수 | 지분율 | 주식수 | 지분율 | |||
| 이기섭 | 최대주주 | 보통주 | 15,163,144 | 13.71 | 3,032,628 | 13.71 |
| 이애주 | 공동보유자 | 보통주 | 5,029,066 | 4.55 | 1,005,813 | 4.55 |
| 최인석 | 공동보유자 | 보통주 | 3,004,354 | 2.72 | 600,870 | 2.72 |
| 이건환 | 공동보유자 | 보통주 | 2,560,906 | 2.32 | 512,181 | 2.32 |
| 노미란 | 특수관계인 | 보통주 | 337,430 | 0.31 | 67,486 | 0.31 |
| 노미숙 | 특수관계인 | 보통주 | 331,200 | 0.30 | 66,240 | 0.30 |
| BRIANA BOHAE LEE | 특수관계인 | 보통주 | 146,907 | 0.13 | 29,381 | 0.13 |
| MIRIAM B LEE | 특수관계인 | 보통주 | 146,907 | 0.13 | 29,381 | 0.13 |
| 이광호 | 특수관계인 | 보통주 | 110,400 | 0.10 | 22,080 | 0.10 |
| 이원영 | 특수관계인 | 보통주 | 58,636 | 0.05 | 11,727 | 0.05 |
| 이태길 | 특수관계인 | 보통주 | 52,515 | 0.05 | 10,503 | 0.05 |
| 이재문 | 등기임원 | 보통주 | 63,800 | 0.06 | 12,760 | 0.06 |
| 이기세 | 특수관계인 | 보통주 | 17,868 | 0.02 | 3,573 | 0.02 |
| 이미경 | 특수관계인 | 보통주 | 10,350 | 0.01 | 2,070 | 0.01 |
| 최광재 | 미등기임원 | 보통주 | 52,434 | 0.05 | 10,486 | 0.05 |
| 합 계 | 27,085,917 | 24.50 | 5,417,179 | 24.50 | ||
| 출처) 당사 정기보고서 및 당사 제시 |
당사는 안정적인 경영권 확보를 위하여 최대주주의 우호지분 보유자와 의결권 공동보유 약정을 체결하였으며, 주요 내용은 다음과 같습니다.
| [의결권 공동보유 약정 주요 내용] |
|
구분 |
내용 |
|---|---|
|
약정주주 및 대상주식 |
이애주 5,029,066주(4.55%) 최인석 3,004,354주(2.72%) 이건환 2,560,906주(2.32%) |
|
약정기간 |
2020년 06월 08일 ~ 2023년 06월 07일 |
|
약정내용 |
약정기간 동안 청구회사 이기섭 대표이사와 의결권 공동 행사, 지분 매각시 이기섭 대표이사에게 우선매수권 부여 |
| 출처) 당사 제시 |
금번 당사의 주주배정 후 실권주 일반공모 유상증자로 인하여 구주주들은 1주당 주식병합 전 0.05065381주, 주식병합 후 0.25326904의 배정비율로 신주인수권증서를 교부받게 됩니다.(신주배정기준일 전 주식매수선택권의 행사, 자기주식 수의 변동, 주식병합으로 인한 단수주 발생 등에 의하여 변동 가능성이 있습니다.) 이에 따라 최대주주인 이기섭 대표이사는 주식병합 완료 후 768,070주, 특수관계인들은 총 603,927주를 배정받게 됩니다.
금번 유상증자에서 최대주주는 자금 여력에 따라 최대한 참여할 예정으로, 현재는 최대주주인 이기섭 대표이사는 배정분의 약 15% 정도 참여를 계획 중이며, 특수관계인들에 대한 청약 참여 여부는 미정입니다. 만약 최대주주 및 특수관계인이 전액 미참여할 경우 지분율은 현재 24.50%에서 19.55%까지 감소할 수 있으며, 최대주주가 배정분의 15% 참여하고, 특수관계인이 전액 미참여할 경우 최대주주 및 특수관계인의 지분율은 현재 24.50%에서 19.96%까지 감소할 수 있습니다.
| [최대주주 및 특수관계인 청약률에 따른 지분변동 가정] |
| 성명 | 현재 | 주식병합(액면가 100원 → 500원) | 증자 후 | 증자 후 | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| (최대주주 및 특수관계인 미참여) | (이기섭 대표 15% 참여, 특수관계인 미참여) | |||||||||
| 주식수(주) | 지분율(%) | 배정주식수(주) | 주식수(주) | 지분율(%) | 배정주식수(주) | 주식수(주) | 지분율(%) | 주식수(주) | 지분율(%) | |
| 이기섭 | 15,163,144 | 13.71 | 3,840,354 | 3,032,628 | 13.71 | 768,070 | 3,032,628 | 10.94 | 3,147,838 | 11.36 |
| 이애주 | 5,029,066 | 4.55 | 1,273,706 | 1,005,813 | 4.55 | 254,741 | 1,005,813 | 3.63 | 1,005,813 | 3.63 |
| 최인석 | 3,004,354 | 2.72 | 760,909 | 600,870 | 2.72 | 152,181 | 600,870 | 2.17 | 600,870 | 2.17 |
| 이건환 | 2,560,906 | 2.32 | 648,598 | 512,181 | 2.32 | 129,719 | 512,181 | 1.85 | 512,181 | 1.85 |
| 노미란 | 337,430 | 0.31 | 85,460 | 67,486 | 0.31 | 17,092 | 67,486 | 0.24 | 67,486 | 0.24 |
| 노미숙 | 331,200 | 0.30 | 83,882 | 66,240 | 0.30 | 16,776 | 66,240 | 0.24 | 66,240 | 0.24 |
| BRIANA BOHAE LEE | 146,907 | 0.13 | 37,206 | 29,381 | 0.13 | 7,441 | 29,381 | 0.11 | 29,381 | 0.11 |
| MIRIAM B LEE | 146,907 | 0.13 | 37,206 | 29,381 | 0.13 | 7,441 | 29,381 | 0.11 | 29,381 | 0.11 |
| 이광호 | 110,400 | 0.10 | 27,960 | 22,080 | 0.10 | 5,592 | 22,080 | 0.08 | 22,080 | 0.08 |
| 이원영 | 58,636 | 0.05 | 14,850 | 11,727 | 0.05 | 2,970 | 11,727 | 0.04 | 11,727 | 0.04 |
| 이태길 | 52,515 | 0.05 | 13,300 | 10,503 | 0.05 | 2,660 | 10,503 | 0.04 | 10,503 | 0.04 |
| 이재문 | 63,800 | 0.06 | 16,158 | 12,760 | 0.06 | 3,231 | 12,760 | 0.05 | 12,760 | 0.05 |
| 이기세 | 17,868 | 0.02 | 4,525 | 3,573 | 0.02 | 904 | 3,573 | 0.01 | 3,573 | 0.01 |
| 이미경 | 10,350 | 0.01 | 2,621 | 2,070 | 0.01 | 524 | 2,070 | 0.01 | 2,070 | 0.01 |
| 최광재 | 52,434 | 0.05 | 13,279 | 10,486 | 0.05 | 2,655 | 10,486 | 0.04 | 10,486 | 0.04 |
| 합계 | 27,085,917 | 24.50 | 6,860,014 | 5,417,179 | 24.50 | 1,371,997 | 5,417,179 | 19.55 | 5,532,389 | 19.96 |
| 출처) 당사 제시 |
| 주1) 상기 이기섭 대표이사의 15% 참여에 따른 청약 참여주식수는 115,210주입니다. |
| 주2) 현재 발행주식총수 110,565,888주 > 주식병합(액면가 100원 → 500원) 후 발행주식총수 22,113,177주 → 증자 후 발행주식 총수 27,713,177주 |
| 주3) 주식병합 후 발행주식총수는 1주 미만의 단수주 발생에 따라 변경 될 수 있습니다. |
증권신고서 제출일 현재 당사는 희석가능한 미발행 주식으로 제2회 전환사채, 주식매수선택권이 존재하고 있습니다.
당사는 2020년 06월 30일 제2회 전환사채 20,000백만원을 발행한 바 있으며, 증권신고서 제출일 현재 미상환사채는 20,000백만원, 수 차례의 전환가액 조정에 의하여 현재 전환가액은 4,070원, 전환가능주식수는 4,914,004주입니다. 주식병합 후 전환가액 20,350원, 전환가능주식수는 982,800주로 조정될 예정입니다. 이는 주식병합 후 총발행주식수 22,113,177주의 약 4.44%(금번 유상증자 5,600,000주 포함 3.55%)에 해당합니다. 이후 금번 유상증자로 인하여 전환가액 19,141원, 전환가능주식수 1,044,877주로 조정될 예정입니다.
| [미상환 전환사채 내역] | |
| (기준일 : 증권신고서 제출 전일 현재) | (단위 : 백만원) |
| 종류\구분 | 발행일 | 만기일 | 전자등록총액 | 전환대상 주식의 종류 |
전환청구가능기간 | 전환조건 | 미상환사채 | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 전환비율 (%) |
전환가액 | 주식병합 후 전환가액 |
전자등록총액 | 전환가능주식수 | 주식병합 후 전환가능주식수 |
||||||
| 제2회 무기명식 이권부 무보증 사모 전환사채 |
2020년 06월 30일 | 2025년 06월 30일 | 20,000 |
기명식 보통주 |
2021년 06월 30일 ~ 2025년 03월 30일 |
100 | 4,070 | 20,350 | 20,000 | 4,914,004 | 982,800 |
| 합계 | - | - | 20,000 | - | - | - | - | 20,000 | 4,914,004 | 982,800 | |
| 출처) 당사 정기보고서 및 당사 제시 |
한편, 당사의 최근 3개년 주식매수선택권 잔여 현황은 다음과 같습니다.
| [당사 최근 3개년 주식매수선택권 잔여 현황] |
| (단위: 주) |
| 구 분 | 2019년 | 2020년 | 2021년 | 2022년 1분기 | 증권신고서 제출 전일 현재 |
|---|---|---|---|---|---|
| 기초 부여수량 | 4,736,160 | 5,486,955 | 5,029,928 | 5,555,020 | 5,583,655 |
| 신규 부여 | 2,294,250 | 1,483,500 | 1,595,800 | 425,000 | - |
| 행사 | 404,955 | 1,369,071 | 665,536 | 108,459 | 167,626 |
| 기타 조정 | 1,138,500 | 571,457 | 404,872 | 287,906 | 329,750 |
| 기말 부여수량 | 5,486,955 | 5,029,928 | 5,555,020 | 5,583,655 | 5,086,279 |
| 기말 행사가능수량 | 2,526,856 | 2,217,907 | 1,877,911 | 2,233,847 | 2,066,221 |
| 행사가능가격대 수량 | 2,526,856 | 2,217,907 | 1,877,911 | 2,233,847 | 2,066,221 |
| 주식병합 후 행사가능가격대 수량 | 505,371 | 443,581 | 375,582 | 446,769 | 413,244 |
| 주1) 기타 조정에는 무상증자 및 퇴사 등으로 인한 행사수량 변동이 포함되어 있습니다. |
| 주2) 행사가능가격대 수량의 경우, 기말 행사가능 수량 중 각 연도별 말일 및 2022년 1분기의 경우 03월 31일의 종가 기준으로 비교하였습니다. |
| 주3) 증권신고서 제출전일 현재의 행사가능가격대 수량은 예정발행가액을 기준으로 비교하였습니다. 다만, 주가와 발행가액의 변동으로 인하여 행사가능가격대 수량은 추후 변동될 수 있으므로 투자자께서는 이 점 유의해주시기 바랍니다. |
또한 주식병합 완료를 가정하면, 예정발행가액 8,660원(주식병합 완료 가정)을 기준으로 행사가능가격대 주식매수선택권 수량은 413,244주입니다.
이에 따라 유상증자 후 최대주주 지분율은 13.71%(최대주주 등 24.50%)에서 제2회 전환사채 및 행사가능가격대 주식매수선택권이 모두 전환 및 행사될 경우 10.79%(최대주주 등 18.97%)로 하락할 수 있습니다. 동 가정에서 제2회 전환사채는 예정발행가액 8,660원을 기준으로 전환가액을 조정하였으며, 행사가능가격대 주식매수선택권도 예정발행가액과 비교하여 산정하였습니다.
이에 따라 향후 주가가 하락하여 확정발행가액이 예정발행가액보다 낮아질 경우 시뮬레이션보다 최대주주의 지분율 희석이 심화될 예정이며, 주가가 상승하여 확정발행가액이 예정발행가액보다 높아질 경우 시뮬레이션보다 최대주주 지분율 희석이 감소될 예정입니다. 본 가정의 경우 예정발행가액을 기준으로 계산하였기 때문에, 향후 최종 발행가액이 확정됨에 따라서 최대주주 지분율 희석 정도가 변동될 예정이오니 투자자께서는 이 점 유의하시기 바랍니다.
| [유상증자 조정후 전환가액] |
| (단위 : 원, 주) |
| 구 분 | 제2회 전환사채 |
|---|---|
| 증권신고서 제출 전일 현재 | |
| 전환가액 | 4,070 |
| 전환가능주식수 | 4,914,004 |
| 주식병합(액면가 100원 → 500원) | |
| 전환가액 | 20,350 |
| 전환가능주식수 | 982,800 |
| 유상증자 조정(주식병합 반영) | |
| 조정전 전환가액 | 20,350 |
| 기발행주식수(A) | 22,113,177 |
| 신발행주식수(B) | 5,600,000 |
| 예정발행가격(C) | 8,660 |
| 시가(D) | 12,269.79 |
| 조정 후 전환가액 = 조정 전 전환가액 × [{A+(B×C/D)} / (A+B)] |
19,141 |
| 유상증자 조정후 | |
| 전환가액 | 19,141 |
| 전환가능주식수 | 1,044,877 |
| 출처) 당사 제시 |
| [최대주주 등의 지분율 시뮬레이션(전환사채 및 주식매수선택권 전환 후)] |
| (단위: 주, %) |
| 구분 | 유상증자 후 | 전환사채 | 주식매수선택권 | 전환사채 및 주식매수선택권 전환 후 |
|||
|---|---|---|---|---|---|---|---|
| 보유주식 | 지분율 | 전환주식수 | 전환주식수 | 보유주식 | 지분율 | ||
| 이기섭 | 최대주주 | 3,147,825 | 11.36 | - | - | 3,147,838 | 10.79 |
| 이애주 | 공동보유자 | 1,005,813 | 3.63 | - | - | 1,005,813 | 3.45 |
| 최인석 | 공동보유자 | 600,870 | 2.17 | - | - | 600,870 | 2.06 |
| 이건환 | 공동보유자 | 512,181 | 1.85 | - | - | 512,181 | 1.76 |
| 노미란 | 특수관계인 | 67,486 | 0.24 | - | - | 67,486 | 0.23 |
| 노미숙 | 특수관계인 | 66,240 | 0.24 | - | - | 66,240 | 0.23 |
| BRIANA BOHAE LEE | 특수관계인 | 29,381 | 0.11 | - | - | 29,381 | 0.10 |
| MIRIAM B LEE | 특수관계인 | 29,381 | 0.11 | - | - | 29,381 | 0.10 |
| 이광호 | 특수관계인 | 22,080 | 0.08 | - | - | 22,080 | 0.08 |
| 이원영 | 특수관계인 | 11,727 | 0.04 | - | - | 11,727 | 0.04 |
| 이태길 | 특수관계인 | 10,503 | 0.04 | - | - | 10,503 | 0.04 |
| 이재문 | 등기임원 | 12,760 | 0.05 | - | - | 12,760 | 0.04 |
| 이기세 | 특수관계인 | 3,573 | 0.01 | - | - | 3,573 | 0.01 |
| 이미경 | 특수관계인 | 2,070 | 0.01 | - | - | 2,070 | 0.01 |
| 최광재 | 미등기임원 | 10,486 | 0.04 | - | - | 10,486 | 0.04 |
| 최대주주 및 특수관계인 소계 | 5,532,376 | 19.96 | - | - | 5,532,376 | 18.97 | |
| 기타주주 | 22,183,301 | 80.04 | 1,044,877 | 413,244 | 23,641,422 | 81.03 | |
| 합계 | 27,715,677 | 100 | 1,044,877 | 413,244 | 29,173,798 | 100 | |
| 출처) 당사 제시 |
| 주1) 이기섭 대표이사는 배정분의 15% 청약, 그 외 특수관계인은 미청약을 가정하였습니다. |
| 주2) 주식매수선택권의 경우 행사가능가격대의 수량의 행사를 가정하였습니다. |
상기와 같이 당사는 금번 유상증자 및 미발행 잠재주식으로 인해 희석이 발생하여 최대주주의 지분율이 하락할 수 있고 이로 인해 적대적 M&A 등의 경영권 분쟁이 발생할 수 있습니다. 투자자께서는 이점 유의하시기 바랍니다.
| 자. 우리사주조합 미배정에 관한 사항 「자본시장과 금융투자업에 관한 법률」제165조의7(우리사주조합원에 대한 주식의 배정 등에 관한 특례) 및 「자본시장과 금융투자업에 관한 법률 시행령」제176조의9에 따르면 유가증권시장에 상장된 법인이 주식의 모집하거나 매출하는 경우 우리사주조합에 발행예정주식수의 20%를 배정하여야 합니다. 그러나「자본시장과 금융투자업에 관한 법률 시행령」제176조의9제3항제1호에 의거 당사 우리사주조합에 대한 배정을 실시하지 않습니다. 당사 우리사주조합은 증권신고서 제출 전일 현재 존재하지 않는 관계로 당사 우리사주조합원에 대한 우선배정을 실시하지 않을 계획입니다. 우리사주조합은 회사의 내부 관계자로서 조합원의 유상증자 참여 여부가 투자자에게 중요한 투자판단 근거로써 활용될 수 있습니다. 다만, 금번 유상증자의 경우 우리사주조합에 우선배정을 진행하지 않을 예정으로, 투자자께서는 이 점 유의하시기 바랍니다. |
「자본시장과 금융투자업에 관한 법률」제165조의7(우리사주조합원에 대한 주식의 배정 등에 관한 특례) 및 「자본시장과 금융투자업에 관한 법률 시행령」제176조의9에 따르면 유가증권시장에 상장된 법인이 주식의 모집하거나 매출하는 경우 우리사주조합에 발행예정주식수의 20%를 배정하여야 합니다.
반면 코스닥시장 상장법인의 공모증자의 경우「근로복지기본법」제38조제2항 및「증권 인수업무 등에 관한 규정」제9조제2항제1호에 근거하여 우리사주조합의 우선배정에 대하여 자율로 정하도록 하고 있습니다.
당사 우리사주조합은 증권신고서 제출 전일 현재 존재하지 않는 관계로 당사 우리사주조합원에 대한 우선배정을 실시하지 않을 계획입니다.
이에 따라 당사는 관련 법률을 근거로 금번 진행하는 유상증자의 경우 우리사주조합에 우선배정하지 않고 기존 주주에게 공모 주식 100%를 배정할 예정입니다. 금번 유상증자의 배정 방법은 다음과 같습니다.
| [(주)카이노스메드 주주배정 후 실권주 일반공모 유상증자 배정 방법] |
| 모집 대상 | 주 수(%) | 비 고 |
| 구주주 청약 (신주인수권증서 보유자 청약) |
5.600,000주(100%) | ▶ 구주주 청약일 : 2022년 08월 02일 ~ 08월 03일 ▶ 구주 1주당 신주 배정비율 : 1주당 0.05065381주 ▶ 신주배정기준일 : 2022년 06월 29일 ▶ 보유한 신주인수권증서의 수량 한도로 청약가능(구주주에게는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율을 곱한 수량만큼의 신주인수권증서가 배정됨) |
| 초과 청약 | - | ▶ 「자본시장과 금융투자업에 관한 법률」 제165조의6의제2항제2호에 의거 초과청약 ▶ 초과청약비율 : 배정신주(신주인수권증서) 1주당 0.2주 (단, 1주 미만은 절사함) ▶ 신주인수권증서 거래를 통해서 신주인수권증서를 매매시 보유자 기준으로 초과청약 가능 ▶ 구주주청약일에 초과청약 접수 |
| 일반모집 청약 (고위험고수익투자신탁, 벤처기업투자신탁 청약 포함) |
- | ▶ 구주주 청약 후 발생하는 단수주 및 실권주 배정 ▶ 일반모집 청약일 : 2022년 08월 08일 ~ 08월 09일 |
| 합계 | 5,600,000주(100%) |
| 주1) | 본 건 유상증자는 주주배정후 실권주 일반공모 방식으로 진행되며, 구주주 청약결과 발생하는 실권주 및 단수주는 우선적으로 초과청약자에게 배정되며, 이후 실권이 발생할 경우에 대해서는 일반에게 공모합니다. |
| 주2) | 구주주의 청약한도는 신주배정기준일 현재 주주명부에 등재된 주주(이하 "구주주"라 한다)에게 본 주식을 1주당 0.05065381주를 곱하여 산정된 배정주식수(단, 1주 미만은절사함)로 하고, 배정범위 내에서 청약한 수량만큼 배정합니다. 단, 상기 구주주 1주당 배정비율 0.05065381주는 주식병합 이전 발행주식총수(110,565,888주) 기준 비율이며, 주식병합 완료 이후 발행주식총수(22,113,177주) 기준 비율은 0.25326904주 입니다. 단, 신주배정기준일 전 신주 발행, 주식관련사채의 권리행사, 주식매수선택권의 행사, 자기주식 및 자기주식신탁 등의 자기주식 변동, 주식병합 과정에서 발생하는 단수주의 영향으로 인하여 1주당 배정주식수 및 증자비율이 변동될 수 있습니다. |
| 주3) |
신주인수권증서 보유자는 보유한 신주인수권증서 수량의 한도로 증서청약을 할 수 있고, 동 주식수에 초과청약비율(20%)을 곱한 수량을 한도로 초과청약 할 수 있습니다. 단, 1주 미만은 절사합니다. (ii) 신주인수권증서청약 한도주식수 = 보유한 신주인수권증서의 수량 (iii) 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 X 초과청약 비율(20%) (1주미만 절사) |
| 주4) | 「증권 인수업무 등에 관한 규정」제2조(용어의 정의) 제18항, 제19항, 제20항에 의거 ① "고위험고수익투자신탁" 이란 「조세특례제한법」제91조의15제1항에 따른 투자신탁 등을 말합니다. 다만, 해당 투자신탁 등의 최초 설정일·설립일로부터 배정일까지의 기간이 6개월 미만인 경우에는 같은 법 시행령 제93조제3항제1호 및 같은 조 제7항에도 불구하고 배정일 직전 영업일의 비우량채권과 코넥스 상장주식을 합한 보유비율이 100분의 45 이상이고 이를 포함한 국내 채권의 보유비율이 100분의 60 이상이어야 합니다. ② "벤처기업투자신탁" 이란 「조세특례제한법」제16조제1항제2호의 벤처기업투자신탁(대통령령 제28636호 조세특례제한법 시행령 일부 개정령 시행 이후 설정된 벤처기업투자신탁에 한함)을 말합니다. 다만, 해당 벤처기업투자신탁의 최초 설정일로부터 배정일까지의 기간이 1년 미만인 경우에는 같은 법 시행령 제14조제1항제3호에도 불구하고 배정일 직전 영업일의 벤처기업투자신탁 재산총액에서 같은 호 각 목에 따른 비율의 합계가 100분의 35 이상이어야 합니다. |
| 주5) | 구주주 청약 및 초과청약 결과 발생한 실권주 및 단수주는 대표주관회사가 다음 각호와 같이 일반에게 공모하되, 「증권 인수업무 등에 관한 규정」제9조제2항제6호가목에 따라 고위험고수익투자신탁에 공모주식의 5%를 배정하고,「증권 인수업무 등에 관한 규정」 제9조제2항제6호나목에 따라 벤처기업투자신탁에 공모주식의 30%를 배정합니다. 나머지 일반공모 배정분의 65%에 해당하는 주식은 개인청약자 및 기관투자자에게 구분 없이 배정합니다. 고위험고수익투자신탁에 대한 공모주식의 5%와 벤처기업투자신탁에 대한 공모주식의 30%와 개인투자자 및 기관투자자에 대한 공모주식의 65%에 대한 청약경쟁률과 배정에 있어서는 별도로 산출합니다.다만, 다만, 어느 한 그룹에서 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다. |
| 주6) | 일반공모 청약결과 일반공모 총 청약자의 청약주식수가 공모주식수를 초과하는 경우에는 청약경쟁률에 따라 안분 배정하여 잔여주식이 최소화되도록 합니다. 이후 최종 잔여주식은 대표주관회사가 합리적으로 판단하여 배정합니다. |
| 주7) | 일반공모 청약결과 일반공모 총 청약자의 청약주식수가 공모주식수에 미달하는 경우에는 청약주식수대로 배정하되 잔여주식은 대표주관회사가 자기의 계산으로 인수합니다. 단, 「증권 인수업무 등에 관한 규정」 제9조제2항제7호에 의해 고위험고수익투자신탁, 벤처기업투자신탁, 일반청약자에 대하여 배정하여야 할 주식이 50,000주 이하(주식병합 완료 후 액면가 500원 기준)이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 청약자에게 배정하지 아니하고 자기 계산으로 인수할 수 있습니다. |
우리사주조합은 회사의 내부 관계자로서 조합원의 유상증자 참여 여부가 투자자에게 중요한 투자판단 근거로써 활용될 수 있습니다. 다만, 금번 유상증자의 경우 우리사주조합에 우선배정을 진행하지 않을 예정으로, 투자자께서는 이 점 유의하시기 바랍니다.
| 「자본시장과 금융투자업에 관한 법률」 |
|---|
|
제165조의7(우리사주조합원에 대한 주식의 배정 등에 관한 특례) 1. 「외국인투자 촉진법」에 따른 외국인투자기업 중 대통령령으로 정하는 법인이 주식을 발행하는 경우 2. 그 밖에 해당 법인이 우리사주조합원에 대하여 우선배정을 하기 어려운 경우로서 대통령령으로 정하는 경우 ② 우리사주조합원이 소유하는 주식수가 신규로 발행되는 주식과 이미 발행된 주식의 총수의 100분의 20을 초과하는 경우에는 제1항을 적용하지 아니한다. ③ 제165조의6제1항제1호의 방식으로 신주를 발행하는 경우 제1항에 따른 우리사주조합원에 대한 배정분에 대하여는 「상법」 제419조제1항부터 제3항까지의 규정을 적용하지 아니한다. ④ 금융위원회는 제1항에 따른 우리사주조합원에 대한 주식의 배정과 그 주식의 처분 등에 필요한 기준을 정하여 고시할 수 있다. |
| 「자본시장과 금융투자업에 관한 법률 시행령」 |
|---|
|
제176조의9(우리사주조합원에 대한 주식의 배정 등에 관한 특례의 예외 등) ② 법 제165조의7제1항 각 호 외의 부분 본문에서 "대통령령으로 정하는 증권시장"이란 유가증권시장을 말한다. ③ 법 제165조의7제1항제2호에서 "대통령령으로 정하는 경우"란 다음 각 호의 어느 하나에 해당하는 경우를 말한다. 1. 주권상장법인(유가증권시장에 주권이 상장된 법인을 말한다)이 주식을 모집 또는 매출하는 경우 우리사주조합원(「근로복지기본법」에 따른 우리사주조합의 조합원을 말한다. 이하 이 조에서 같다)의 청약액과 법 제165조의7제1항 각 호 외의 부분 본문에 따라 청약 직전 12개월간 취득한 해당 법인 주식의 취득가액(취득가액이 액면액에 미달하는 경우에는 액면액을 말한다. 이하 이 조에서 같다)을 합산한 금액이 그 법인으로부터 청약 직전 12개월간 지급받은 급여총액(소득세과세대상이 되는 급여액을 말한다)을 초과하는 경우 ④ 법 제165조의7제2항에 따른 우리사주조합원의 소유주식수는 법 제119조제1항에 따라 증권의 모집 또는 매출에 관한 신고서를 금융위원회에 제출한 날(법 제119조제2항 전단에 따른 일괄신고서를 제출하여 증권의 모집 또는 매출에 관한 신고서를 제출하지 아니하는 경우에는 주주총회 또는 이사회의 결의가 있은 날)의 직전일의 주주명부상 우리사주조합의 대표자 명의로 명의개서된 주식에 따라 산정한다. 다만, 「근로복지기본법」 제43조제1항에 따른 수탁기관(이하 이 항에서 "수탁기관"이라 한다)을 통해서 전자등록(「주식ㆍ사채 등의 전자등록에 관한 법률」 제2조제2호에 따른 전자등록을 말한다. 이하 같다)된 주식의 경우에는 같은 법 제22조제2항에 따른 고객계좌부에 따라 산정하고, 수탁기관이 예탁결제원에 예탁한 주식의 경우에는 법 제310조제1항에 따른 투자자계좌부에 따라 산정한다. |
| 「증권 인수업무 등에 관한 규정」 |
|---|
|
제9조(주식의 배정) |
| 「근로복지기본법」 |
|---|
|
제38조(우리사주조합원에 대한 우선배정의 범위) ② 제1항의 법인 외의 법인이 「자본시장과 금융투자업에 관한 법률」에 따라 모집 또는 매출하거나 유상증자를 하는 경우 그 모집 등을 하는 주식 총수의 100분의 20의 범위에서 「상법」 제418조에도 불구하고 우리사주조합원에게 해당 주식을 우선적으로 배정할 수 있다. |
| 「근로복지기본법 시행령」 |
|---|
|
제19조의2(우리사주조합원에 대한 우선배정의 범위) ② 법 제38조제1항에서 "대통령령으로 정하는 증권시장"이란 유가증권시장을 말한다. |
| 출처) 국가법령정보센터 |
| 차. 신 「주식회사 등의 외부감사에 관한 법률」 도입으로 인한 감사인의 감사의견 제시 관련 위험 2018년 「주식회사 등의 외부감사에 관한 법률」, 「자본시장과 금융투자업에 관한 법률」, 「공인회계사법」 및 회계감사기준의 일부 개정이 이루어져, 재무제표에 대한 회사와 감사인의 권한 및 책임이 확대되는 한편, 감사인의 독립적 지위가 강화되었고 감사인은 감사절차 수행 및 의견표명에 있어 더욱 보수적인 접근방식을 취할 것으로 예상됩니다. 당사는 2022년 1분기말 기준 자본잠식률 20.6%를 기록하고 있으며, 2022년 반기 자본잠식률 50% 이상 발생할 가능성이 존재합니다. 자본잠식 규모가 지속적으로 증가하여 매 반기 또는 사업연도 말 기준 자본금의 100분의 50 이상이 잠식될 경우「코스닥시장 상장규정」제53조제1항제4호에 따라 관리종목으로 지정될 수 있으며, 이에 따라 당사의 2022년 반기 연결검토보고서 및 검토보고서에 감사인의 비적정 의견이 기재될 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. 감사인의 비적정 감사의견 표명은 회사의 1) 재무제표의 신뢰성 저하 2) 대규모 손실 발생 또는 전기 재무제표 재작성에 따른 자본 감소 3) 자본시장 접근성 저하와 유동성 위험 증폭 4) 신규 자금조달 및 차입금 만기 연장 실패 등으로 작용할 수 있으니, 투자자께서는 유의하시기 바랍니다. |
2018년 「주식회사 등의 외부감사에 관한 법률」, 「자본시장과 금융투자업에 관한 법률」, 「공인회계사법」 및 회계감사기준의 일부 개정이 이루어졌습니다. 이에 따라 재무제표에 대한 회사와 감사인의 권한 및 책임이 확대되는 한편, 감사인의 독립적 지위가 강화되었고 감사인은 감사절차 수행 및 의견표명에 있어 더욱 보수적인 접근방식을 취할 것으로 예상됩니다.
| [감사인 책임 강화와 관련된 최근 주요 법률 개정 내용] |
| 적용 법률(기준) | 구 분 | 내 용 |
|---|---|---|
| 주식회사 등의 외부감사에 관한 법률 (2018년 11월 시행) |
외부감사 적용범위 확대 | 1) 유한회사 포함, 외감대상 판단시 매출액 기준 추가 |
| 회사의 재무제표 작성 책임 강화 | 1) 회사 재무제표 작성 및 제출 의무 부여, 미제출 시 사유에 대한 공시 필요 | |
| 회사의 내부통제 책임 강화 | 1) 내부회계관리제도에 대한 감사의견 요구(기존: 검토의견) | |
| 감사인 지정 요건 확대 | 1) 상장회사, 소유경영 미분리 회사는 6년 주기로 감사인 지정 2) 그 외 재무제표 작성 의무 위반, 영업손실, 부의 영업현금흐름 등 일정 요건에 해당하는 회사는 증선위가 감사인 지정 |
|
| 감사품질 강화를 위한 제도 개선 | 1) 금융위 등록 회계법인만 상장사 감사 기능 2) 표준 감사시간을 준수할 것을 의무화 |
|
| 회계부정 및 부실감사에 대한 제재 | 1) 회계처리 기준 위반 임직원 및 감사인에게 과징금, 직무정지 등 처벌 강화 | |
| 공인회계사법 (2018년 05월 시행) |
직무제한 대상 및 범위 확대 | 1)특정 회사의 재무제표를 감사하는 경우 비감사 용역 수행 금지 → 직무제한 대상과 범위를 확대 |
| 회계감사기준 (2018년 10월 시행) |
핵심감시제(KAM) 도입 | 1) 핵심감사사항을 선정하고 감사보고서에 선정 이유, 감사인이 수행한 절차 및 그 결과를 기술 |
| 감사보고서 실명제 | 1) 감사 업무를 담당한 업무담당이사(Engagement Team leader) 성명을 감사보고서에 기재 | |
| 계속기업 가정 공시내용 강화 | 1) 계속기업 가정에 의문을 제기할 수 있는 사건이나 상황에 대한 공시를 하고 감사인은 그 적정성을 평가해야 하며, 이에 관하여 KAM으로 기재할 수도 있음 |
|
| 감사보고서 체계 개편 | 1) '감사의견'을 감사보고서 가장 앞부분에 표시 2) 감사의견 근거 단락 신설 3) 계속기업 불확실성 별도 단락으로 표시 |
| 출처) 입법조사처, 삼일회계법인 |
상기 표와 같이 회계투명성 제고를 위해 시행되는 여러 조치들로 인해 감사인의 비적정 의견(한정, 부적정, 의견거절, 감사기준서 상의 변형의견을 의미합니다.)이 증가할 것으로 예상됩니다.
당사는 2022년 1분기말 기준 자본잠식률 20.6%를 기록하고 있으며, 2022년 반기 자본잠식률 50% 이상 발생할 가능성이 존재합니다. 자본잠식 규모가 지속적으로 증가하여 매 반기 또는 사업연도 말 기준 자본금의 100분의 50 이상이 잠식될 경우「코스닥시장 상장규정」제53조제1항제4호에 따라 관리종목으로 지정될 수 있으며, 이에 따라 당사의 2022년 반기 연결검토보고서 및 검토보고서에 감사인의 비적정 의견이 기재될 수 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
감사인의 비적정 감사의견 표명은 회사의 1) 재무제표의 신뢰성 저하 2) 대규모 손실 발생 또는 전기 재무제표 재작성에 따른 자본 감소 3) 자본시장 접근성 저하와 유동성 위험 증폭 4) 신규 자금조달 및 차입금 만기 연장 실패 등으로 작용할 수 있습니다.
투자자께서는 상기와 같은 감사인의 독립적 지위 강화로 인한 감사의견 거절 표명 가능성 확대 및 감사의견 거절 시 회사에 미칠 수 있는 부정적인 영향 등에 유의하시기 바랍니다.
3. 기타위험
| 가. 유상증자 철회에 따른 위험 유상증자 진행 중에 모집 절차의 진행에 중대한 영향을 미칠만한 사유가 발생하여 당사 혹은 대표주관회사의 판단으로 유상증자가 철회될 수 있습니다. 당사가 진행하는 금번 유상증자가 예기치 못한 사유로 인해 철회될 경우 당사는 자본 확충을 위하여 무상감자 등 주주에게 손실을 끼치는 방안 등을 진행할 수 있습니다. 유상증자 납입전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회시점에 따라 권리락에 따른 주가하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있음을 투자자께서는 유의하시기 바랍니다. 또한, 당사가 계획한 자금사용목적의 자금이 조달되지 않기 때문에 당사는 단기간 유동성 위험에 직면하여 매우 위험한 상황이 발생할 수 있으니 이 점 유의하시기 바랍니다. |
금번 주주배정후 실권주 일반공모 유상증자는 대표주관회사의 잔액인수 방식으로 진행됩니다. 유상증자 진행 중에 모집 절차의 진행에 중대한 영향을 미칠만한 사유가 발생하여 당사 혹은 대표주관회사의 판단으로 유상증자가 철회될 수 있습니다.
당사가 진행하는 금번 유상증자가 예기치 못한 사유로 인해 철회될 경우 당사는 자본 확충을 위하여 무상감자 등 주주에게 손실을 끼치는 방안 등을 진행할 수 있습니다. 무상감자는 회사는 주주가 납입한 자본금을 감소시켜 회사가 경영활동을 통해 누적된 결손금을 보전하는 방법으로, 무상감자가 추진될 경우 주주께서는 이로 인해 회사의 주가가 급격히 하락하여 손실이 발생할 수 있으니 이 점 유의하시기 바랍니다.
유상증자 진행 도중 납입일 전에 철회될 경우 청약으로 인한 손실은 발생하지 않으나, 철회시점에 따라 권리락에 따른 주가 하락, 신주인수권증서 매매로 인한 손실 등이 발생할 수 있으며, 당사가 계획한 자금사용목적의 자금이 조달되지 않기 때문에 당사는 단기간 유동성 위험에 직면하여 매우 위험한 상황이 발생할 수 있으니 이 점 유의하시기 바랍니다.
| 나. 주가희석화 및 인수인의 실권주 인수분 물량 출회에 따른 주가하락 위험 당사는 증권신고서 제출 전일 현재 미발행 주식수가 총 9,754,725주가 존재하며, 그 내역은 미전환 제2회 전환사채 20,000백만원의 전환가능주식수 4,914,004주 및 미행사 주식매수선택권 4,840,721주입니다. 전환사채 및 주식매수선택권 등 미발행 주식이 신규 발행될 경우 총발행주식수 110,565,888주(주식병합 후 22,113,177주)의 약 8.82%(금번 유상증자 5,600,000주 포함 7.04%)에 해당하며, 주가 희석화 및 물량출회로 인해 투자자의 손실을 초래할 위험이 있습니다. 투자자께서는 이 점 유의하시기 바랍니다. 신주 상장예정일은 유관기관과의 협의에 따라 변경될 수 있으며, 금번 유상증자에 따른 5,600,000주의 유상신주가 코스닥시장에 추가 상장될 경우 전량 보호 예수되지 않습니다. 또한, 대표주관회사가 잔액인수한 물량은 수익을 확정하기 위해 신주상장일 2영업일 전부터 장내에서 대량 매도할 수 있습니다. 이 경우 일시적 물량 출회에 따른 주가 하락의 가능성이 존재하며, 인수한 실권주를 일정 기간 보유하더라도 동 인수물량이 잠재매각물량으로 존재하여 주가 상승에는 부담으로 작용할 가능성이 높습니다. 대표주관회사가 최종 실권주를 인수하게 되면 실권주 인수금액의 12%를 추가수수료로 지급하게 되며, 이를 고려 시 대표주관회사의 실권주 매입단가는 일반청약자들보다 12% 낮은 것과 같은 결과가 초래되어 대표주관회사의 실권주 매도단가가 신주의 발행가액보다 낮게 될 가능성이 존재합니다. 투자자께서는 이 점을 반드시 유의하여 주시기 바랍니다. |
당사는 증권신고서 제출 전일 현재 미발행 주식수가 총 9,754,725주가 존재하며, 그 내역은 미전환 제2회 전환사채 20,000백만원의 전환가능주식수 4,914,004주 및 미행사 주식매수선택권 4,840,721주입니다. 주식병합 완료 후 미발행 주식수는 제2회 전환사채 전환가능주식수 982,800주, 미행사 주식매수선택권 968,144주 등 1,950,944주가 존재합니다.
| [미상환 전환사채 내역] | |
| (기준일 : 증권신고서 제출 전일 현재) | (단위 : 백만원) |
| 종류\구분 | 발행일 | 만기일 | 전자등록총액 | 전환대상 주식의 종류 |
전환청구가능기간 | 전환조건 | 미상환사채 | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 전환비율 (%) |
전환가액 | 주식병합 후 전환가액 |
전자등록총액 | 전환가능주식수 | 주식병합 후 전환가능주식수 |
||||||
| 제2회 무기명식 이권부 무보증 사모 전환사채 |
2020년 06월 30일 | 2025년 06월 30일 | 20,000 |
기명식 보통주 |
2021년 06월 30일 ~ 2025년 03월 30일 |
100 | 4,070 | 20,350 | 20,000 | 4,914,004 | 982,800 |
| 합계 | - | - | 20,000 | - | - | - | - | 20,000 | 4,914,004 | 982,800 | |
| 출처) 당사 정기보고서 및 당사 제시 |
제2회 전환사채의 전환가능기간은 2021년 06월 30일부터 2025년 03월 30일까지이며, 상기 기발행된 전환사채가 당사 보통주로 전환될 경우, 최대주주를 포함한 기존 주주의 지분율이 희석될 위험이 있습니다.
또한 당사는 증권신고서 제출 전일 현재 주식매수선택권 총 4,840,721주를 임직원에게 부여하고 있습니다.
| [행사가능한 주식매수선택권 현황] | |
| (기준일 : 증권신고서 제출 전일 현재) | (단위 : 원, 주) |
| 부여 받은자 |
관 계 | 부여일 | 부여방법 | 주식의 종류 |
행사기간 | 주식병합 전 | 주식병합 후 | ||
|---|---|---|---|---|---|---|---|---|---|
| 미행사수량 | 행사 가격 | 미행사수량 | 행사 가격 | ||||||
| 이재문 | 등기임원 | 2016.03.29 | 신주교부 | 보통주 | 2018.03.29~ 2028.03.28 | 331,200 | 1,266 | 66,240 | 6,330 |
| 변OO 외 8명 | 직원 | 2016.03.29 | 신주교부 | 보통주 | 2018.03.29~ 2028.03.28 | 1,150 | 1,266 | 230 | 6,330 |
| 이재문 | 등기임원 | 2017.03.24 | 신주교부 | 보통주 | 2019.03.24~ 2029.03.24 | 660,000 | 665 | 132,000 | 3,325 |
| 변OO 외19명 | 직원 | 2017.03.24 | 신주교부 | 보통주 | 2019.03.24~ 2029.03.24 | 81,335 | 665 | 16,267 | 3,325 |
| 이재문 | 등기임원 | 2018.03.26 | 신주교부 | 보통주 | 2020.03.26~2030.03.26 | 345,000 | 1,772 | 69,000 | 8,860 |
| 변OO 외 18명 | 직원 | 2018.03.26 | 신주교부 | 보통주 | 2020.03.26~2030.03.26 | 199,036 | 1,772 | 39,807 | 8,860 |
| 이재문 | 등기임원 | 2019.03.25 | 신주교부 | 보통주 | 2022.03.25~2032.03.25 | 69,000 | 2,405 | 13,800 | 12,025 |
| 변OO 외 21명 | 직원 | 2019.03.25 | 신주교부 | 보통주 | 2022.03.25~2032.03.25 | 828,000 | 2,405 | 165,600 | 12,025 |
| 김인철 | 미등기임원 | 2020.03.13 | 신주교부 | 보통주 | 2023.03.13~2033.03.12 | 690,000 | 2,688 | 138,000 | 13,440 |
| 최OO 외 4명 | 직원 | 2020.03.13 | 신주교부 | 보통주 | 2023.03.13~2033.03.12 | 103,500 | 2,688 | 20,700 | 13,440 |
| 신용일 | 미등기임원 | 2021.01.15 | 신주교부 | 보통주 | 2024.01.15~2034.01.14 | 250,000 | 4,406 | 50,000 | 22,030 |
| 배종덕 | 미등기임원 | 2021.01.15 | 신주교부 | 보통주 | 2024.01.15~2034.01.14 | 172,500 | 4,406 | 34,500 | 22,030 |
| 고수영 | 미등기임원 | 2021.01.15 | 신주교부 | 보통주 | 2024.01.15~2034.01.14 | 150,000 | 4,406 | 30,000 | 22,030 |
| 백OO 외 4인 | 직원 | 2021.01.15 | 신주교부 | 보통주 | 2024.01.15~2034.01.14 | 235,000 | 4,406 | 47,000 | 22,030 |
| 김은희 | 미등기임원 | 2021.03.15 | 신주교부 | 보통주 | 2024.03.15~2034.03.14 | 500,000 | 1,762 | 100,000 | 8,810 |
| 서태환 | 등기임원 | 2021.03.31 | 신주교부 | 보통주 | 2024.03.31~2034.03.30 | 50,000 | 1,531 | 10,000 | 7,655 |
| 노치용 | 등기임원 | 2022.03.14 | 신주교부 | 보통주 | 2025.03.14~2035.03.13 | 50,000 | 2,275 | 10,000 | 11,375 |
| 남OO 외 3인 | 직원 | 2022.03.14 | 신주교부 | 보통주 | 2025.03.14~2035.03.13 | 125,000 | 2,275 | 25,000 | 11,375 |
| 합계 | - | 4,840,721 | - | 968,144 | - | ||||
| 출처) 당사 정기보고서 및 당사 제시 |
전환사채 및 주식매수선택권 등 미발행 주식이 신규 발행될 경우 총발행주식수 110,565,888주(주식병합 후 22,113,177주)의 약 8.82%(금번 유상증자 5,600,000주 포함 7.04%)에 해당하며, 주가 희석화 및 물량출회로 인해 투자자의 손실을 초래할 위험이 있습니다. 투자자께서는 이 점 유의하시기 바랍니다.
| [주식병합 후 당사 잠재주식수 비율] |
| 구분 | 주식수 |
|---|---|
| 주식병합 후 총발행주식수 (A) | 22,113,177주 |
| 제2회 전환사채 전환 가능 주식수 (B) | 982,800주 |
| 주식매수선택권 (C) | 968,144주 |
| 총발행주식수 대비 잠재주식수 (B+C) / (A) | 8.82% |
| 금번 유상증자 발행예정 주식 수 (D) | 5,600,000주 |
| 총발행주식수 및 발행예정 주식 수 대비 잠재주식수 (B+C) / (A+D) | 7.04% |
| 출처) 당사 제시 |
금번 유상증자에 따른 모집가액은 「증권의 발행 및 공시 등에 관한 규정」 제5-18조에 의거 주주배정 증자 시 가격 산정절차 폐지 및 가격 산정의 자율화에 따라 발행가액을 자유롭게 산정할 수 있으나, (구)「유가증권의 발행 및 공시 등에 관한 규정」 제57조를 적용하여 산정합니다(Ⅰ. 모집 또는 매출에 관한 일반사항, 3. 공모가격 결정방법 참조). 그러나 주식시장의 특성상 향후 주가에 대한 변동성이 있는 관계로 증자에 따른 모집가격 산정시 결정된 1주당 모집가액보다 향후 추가 상장 후 거래 시점의 주가가 낮아져 투자자에게 금전적 손실을 끼칠 가능성이 있습니다.
신주 상장예정일은 유관기관과의 협의에 따라 변경될 수 있으며, 금번 유상증자에 따른 5,600,000주의 유상신주가 코스닥시장에 추가 상장될 경우 전량 보호 예수되지 않습니다.
한편, 구주주 청약주식 및 실권주 일반공모 청약시 기관 및 일반 투자자들의 청약으로 추가 발행되는 주식은 보호예수되지 않으므로 일시적인 물량출회에 따른 주가하락의 가능성이 있습니다.
또한, 대표주관회사가 잔액인수한 물량은 수익을 확정하기 위해 신주상장일 2영업일 전부터 장내에서 대량 매도할 수 있습니다. 이 경우 일시적 물량 출회에 따른 주가 하락의 가능성이 존재하며, 인수한 실권주를 일정 기간 보유하더라도 동 인수물량이 잠재매각물량으로 존재하여 주가 상승에는 부담으로 작용할 가능성이 높습니다. 대표주관회사가 최종 실권주를 인수하게 되면 실권주 인수금액의 12%를 추가수수료로 지급하게 되며, 이를 고려 시 대표주관회사의 실권주 매입단가는 일반청약자들보다 12% 낮은 것과 같은 결과가 초래되어 대표주관회사의 실권주 매도단가가 신주의 발행가액보다 낮게 될 가능성이 존재합니다. 투자자께서는 이 점을 반드시 유의하여 주시기 바랍니다.
| 다. 경영환경변화 등에 따른 위험 대내외적 경영환경 변화에 따라 당사 실적의 급변동이 있을 경우 투자원금에 대한 손실이 발생할 수 있으므로, 상기 투자위험요소 및 본 증권신고서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 투자자 여러분이 독자적으로 결정해야 함을 유의하시기 바랍니다. |
당사의 주가는 국내외 주식시장 환경 변화와 같은 외부적 요인에 영향을 받아 변동할 가능성이 존재하며, 당사의 외부적인 경영환경 변화에 따라 당사 실적이 악화될 가능성이 높아질 경우 당사의 주가에 부정적인 영향을 미칠 수 있습니다.
본 건 공모 주식을 청약하고자 하는 투자자들은 투자결정을 하기 전에 본 증권신고서의 다른 기재 부분 뿐만 아니라 상기 투자위험요소를 주의 깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 하며, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 상기 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자는 상기 투자위험요소 및 본 신고서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 자신의 독자적인 판단에 의해서 투자하셔야 합니다.
만일 상기 투자위험요소에 기재한 내용 중 부정적인 요소가 현실화될 경우 당사 및 종속회사의 사업, 재무상태, 기타 운영결과에 중대한 부정적 영향을 미칠 수 있으며, 이에 따라 투자자가 금번 공모 과정에서 취득하게 되는 당사 주식의 시장가격이 하락하여 투자금액에 손실이 발생할 수도 있음을 유의하시기 바랍니다.
| 라. 청약 후 추가상장일까지 환금성 제약 및 주가의 급격한 변동에 따른 손실위험 당사의 금번 유상증자로 인한 발행신주는 주금 납입일 이후 코스닥시장에 추가 상장일까지 유동성이 제한될 수 있으며, 추가상장 시점에서 신주발행가액보다 시장의 수준이 낮은 경우 환금성 위험 및 원금 손실의 위험이 있습니다. 본 유상증자 기간동안 주가의 변동이 있을 수 있다는 점, 투자자께서는 유의하여 주시기 바랍니다. |
당사는 코스닥시장 상장법인으로써, 이번 유상증자로 발행되는 신주는 코스닥시장에 상장되어 거래될 예정이므로 유동성과 관계된 심각한 환금성 위험은 존재하지 않습니다. 그러나 유상증자 청약에 참여하여 신주를 배정받을 경우, 신주가 상장되어 매매가 가능할 때까지 납입주금에 대한 유동성의 제약이 있습니다.
그리고 금번 유상증자로 인해 발행되는 신주가 코스닥시장에 추가 상장될 때까지 유상증자로 발행되는 신주의 발행가액 수준의 주가가 유지되지 않을 수 있으며, 당사의 내적인 환경변화 또는 시장전체의 환경 변화 등에 의한 급격한 주가 하락이 발생할 경우, 투자원금에 대한 손실이 발생할수 있습니다.
| 마. 유상증자 일정 변경 가능성에 따른 위험 본 증권신고서는 공시심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. |
「자본시장과 금융투자업에 관한 법률」제120조3항에 의거하여 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 투자자에게 귀속됩니다.
| ※「자본시장과 금융투자업에관한 법률」제120조(신고의 효력발생시기 등) |
|---|
| ① 제119조제1항 및 제2항에 따른 증권의 신고(이하 "증권신고"라 한다)는 그 증권신고서가 금융위원회에 제출되어 수리된 날부터 증권의 종류 또는 거래의 특성 등을 고려하여 총리령으로 정하는 기간이 경과한 날에 그 효력이 발생한다. ② 금융위원회는 증권신고서의 형식을 제대로 갖추지 아니한 경우 또는 그 증권신고서 중 중요사항에 관하여 거짓의 기재 또는 표시가 있거나 중요사항이 기재 또는 표시되지 아니한 경우를 제외하고는 그 수리를 거부하여서는 아니 된다. ③ 제1항의 효력의 발생은 그 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나 정부에서 그 증권의 가치를 보증 또는 승인하는 효력을 가지지 아니한다. ④ 증권의 발행인은 증권신고를 철회하고자 하는 경우에는 그 증권신고서에 기재된 증권의 취득 또는 매수의 청약일 전일까지 철회신고서를 금융위원회에 제출하여야 한다 |
금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서(분기 및 반기보고서 포함) 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있사오니 투자의사를 결정하시는 데 참조하시기 바랍니다.
본 증권신고서는 공시심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요내용이 변경될 경우에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행과정에서 일정이 변경될 수도 있으므로 투자자들께서는 투자시 이러한 점을 감안하시기 바랍니다.
| 바. 당사의 잘못된 정보 제공 등으로 손해 끼칠 가능성 당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있음을 유의하시기 바랍니다. |
「증권관련 집단소송법」 제12조(소송허가 요건)에 따라 50명 이상의 개인이 발행주식총수의 0.01% 이상 보유할 경우 한 명 이상의 대표 당사자가 상기 50인 이상의 당사자들을 대리하여 회사가 발행한 증권의 거래과정에서 발생한 피해에 대하여 소송을 제기할 수 있습니다.
| 「증권관련 집단소송법」제12조(소송허가 요건) |
|---|
| ① 증권관련집단소송 사건은 다음 각 호의 요건을 갖추어야 한다. 1. 구성원이 50인 이상이고, 청구의 원인이 된 행위 당시를 기준으로 그 구성원이 보유하고 있는 증권의 합계가 피고 회사의 발행 증권 총수의 1만분의 1 이상일 것 2. 제3조제1항 각 호의 손해배상청구로서 법률상 또는 사실상의 중요한 쟁점이 모든 구성원에게 공통될 것 3. 증권관련집단소송이 총원의 권리 실현이나 이익 보호에 적합하고 효율적인 수단일 것 4. 제9조에 따른 소송허가신청서의 기재사항 및 첨부서류에 흠이 없을 것 ② 증권관련집단소송의 소가 제기된 후 제1항제1호의 요건을 충족하지 못하게 된 경우에도 제소(提訴)의 효력에는 영향이 없다. |
당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있습니다. 본 증권신고서 및 투자설명서에 서 기재된 잘못된 내용, 잘못된 사업보고서의 공시, 내부자거래에 의한 손해배상청구 및 회계부정으로 인한 손해배상 청구 등이 주요한 소송사유에 포함됩니다. 당사는 향후 이와 같은 집단소송의 대상이 되지 않는다고 확신할 수 없으며, 만약 당사에 대하여 집단소송이 제기될 경우 상당한 소송비용이 발생할 수 있습니다.
| 사. 유상증자에 따른 주식가치 하락 및 기재정보 의존에 따른 투자위험 금번 유상증자를 통해 취득한 당사의 주식가치가 하락할 수 있으며, 상기 투자위험요소 및 기타 기재된 정보에만 의존하여, 투자판단을 해서는 안되며 투자자 여러분의 독자적인 판단에 의해야 함을 유의하여 주시기 바랍니다. |
금번 유상증자 실시로 당사의 주식가치가 향후 하락할 수 있으므로 투자자 여러분께서는 이 점 유의하시기 바랍니다.
이 증권신고서의 효력발생은 정부가 증권신고서의 기재사항이 진실 또는 정확하다는것을 인정하거나 이 유가증권의 가치를 보증 또는 승인한 것이 아니며, 기재사항은 청약일 이전에 변경될 수 있으며, 본 건 공모주식을 청약하고자 하는 투자자들은 투자결정을 하기 전에 본 증권신고서의 다른 기재 부분 뿐만 아니라 상기 투자위험요소를 주의 깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 합니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 상기 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 자신의 독자적인 판단에 의해야 합니다.
당사는 상기에 기술된 투자위험요소 외에도 전반적으로 불안정한 경제상황 등에 의하여 직접적으로 또는 간접적으로 영향을 받을 수 있습니다. 당사의 재무제표는 당사의 재무상태에 영향을 미칠 수 있는 경제상황에 대한 경영자의 현재까지의 평가를 반영하고 있으나 그 실제결과는 현재시점에서의 평가와는 상당히 다를 수 있는 만큼, 투자자 여러분께서는 이 점 유의하여 투자에 임하시기 바랍니다.
만일 상기 투자위험요소가 실제로 발생하는 경우 당사의 사업, 재무상태, 기타 운영결과에 부정적 영향을 미칠 수 있으며, 이에 따라 투자자가 금번 공모 과정에서 취득하게 되는 당사 주식의 시장가격이 하락하여 투자금액의 일부 또는 전부를 잃게 될 수도 있습니다. 또한 금번 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 대내외적으로 여러가지 요소들의 영향에 따라 애초에 예측했던 것과 다를 수 있다는 점에 유의해야 합니다.
| 아. 관리감독기준 위반에 따른 위험 최근 상장 기업에 대한 관리감독기준이 강화되는 추세이며, 향후 당사가 상장기업 관리감독기준을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다. |
최근 상장 기업에 대한 금융감독기관 등의 관리감독기준이 엄격해지고 있는 상황으로 관련 규정을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다.
특히, 「코스닥시장 상장규정」 제53조(관리종목), 「코스닥시장 상장규정」 제54조(형식적 상장폐지) 및 「코스닥시장 상장규정」 제56조(상장적격성 실질심사에 다른 상장폐지)"에 유의하시기 바랍니다.
자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융감독법규정보시스템(http://law.fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
| [코스닥시장 관리종목 지정 및 상장폐지 주요요건] |
| 구 분 | 관리종목 지정(「코스닥시장 상장규정」 제53조) | 상장폐지(「코스닥시장 상장규정」 제54조, 제56조) |
|---|---|---|
| 1) 매출액 미달(별도) |
최근 사업연도 30억원 미만 (지주회사는 연결기준) - 이익미실현기업 또는 기술성장기업은 상장후 5년간 미적용 |
2년 연속 매출액 30억원 미만 [실질심사] 이익미실현기업 관련 관리종목지정 유예기간 중 최근 3사업연도 연속으로 매출액이 5억원 미만이면서 전년 대비 100분의 50 이상의 매출액 감소가 공시 등을 통해 확인되는 경우 |
| 2) 법인세비용차감전 계속사업손실(연결) | 최근 3사업연도중 2사업연도에 각각 당해 사업연도말 자기자본의 50%를 초과하는 법인세비용차감전계속사업손실이 있고 최근사업연도에 법인세비용차감전계속사업손실이 있는 경우 - 이익미실현 기업은 상장 후 5년간 미적용 - 기술성장기업은 상장후 3년간 미적용 |
관리종목 지정후 자기자본50%이상(&10억원이상)의 법인세비용차감전계속사업손실 발생 [실질심사] 이익미실현기업 관련, 관리종목지정 유예기간 중 최근 3사업연도 연속으로 매출액이 5억원 미만이면서 전년 대비 100분의 50 이상의 매출액 감소가 공시 등을 통해 확인되는 경우 |
| 3) 시가총액 | 보통주 시가총액 40억원 미만인 상태가 연속 30일간 (매매거래일기준)지속 | 관리종목 지정후 90일 기간 경과하는 동안 i) 시가총액 40억 이상으로 10일 이상 계속 ii) 시가총액 40억 이상인 일수가 30일 이상 둘중 하나라도 충족하지 못하면 상장폐지 |
| 4) 자본잠식 등 | (A) 최근 반기말 또는 사업연도말을 기준으로 자본잠식률 50%이상 | 가. 최근 사업연도말 현재 완전자본잠식의 경우 나. (A) or (C) 관리종목 지정후 도래하는 반기말이나 사업연도말 자본잠식률이 50%이상인 경우 다. (B) or (C) 관리종목 지정후 도래하는 반기말이나 사업연도말 자기자본이 10억원 미만인 경우 라. (A) or (B) or (C) 관리종목 지정법인이 최근 반기의 재무제표에 대한 감사인의 감사의견이 부적정,의견거절 또는 감사범위제한으로 인한 한정이거나 반기보고서 법정제출기한의 다음날부터 10일 이내에 반기검토(감사)보고서를 제출하지 아니한 경우 [실질심사] 사업보고서 또는 반기보고서의 법정제출 기한까지 당해 상장폐지 기준 해당사실을 해소하였음을 입증하는 재무제표 및 이에 대한 감사인(정기재무제표에 대한 감사인과 동일한 감사인에 한함)의 감사보고서를 제출하는 경우 가~다목까지의 규정을 적용하지 않음. |
| (B) 최근 반기말 또는 사업연도말을 기준으로 자기자본 10억원 미만 | ||
| (C) 반기보고서 감사(검토)의견이 부적정 또는 의견 거절이거나 감사범위제한으로 인한 한정인 경우이거나, 반기보고서 법정제출기한 다음날부터 10일 이내에 반기검토(감사)보고서를 제출하지 아니한 경우 | ||
| 5) 시가총액 | 보통주 시가총액 40억원 미만 30일간 지속 -천재지변, 시장상황의 급격한 변동 등으로 거래소가 시장 관리를 위하여 필요하다고 인정될 경우 적용배제 가능 |
관리종목 지정후 90일간 "연속10일 & 누적30일간 40억원이상"의 조건을 미충족 |
| 6) 영업손실(별도) |
최근 4사업연도 영업손실(지주회사는 연결기준) - 기술성장기업은 미적용 |
[실질심사]관리종목 지정법인이 최근 사업연도에 영업손실이 있는 경우 |
| 7) 거래량 |
분기월평균거래량이 유동주식수의 1%에 미달 - 신규상장법인(신규상장일이 속하는 분기에 한정), 월평균거래량 1만주 이상, 법에 따른 유동성공급계약 체결, 소액주주 300인 이상이 20% 이상 지분 보유 등은 적용배제 |
관리종목 지정법인이 다음 분기에도 연속하여 동 규정에 의한 거래량 미달상태가 계속되는 경우 |
| 8) 주식분산 미달 |
소액주주 200인미만 or 소액주주지분 20%미만 - 300인 이상의 소액주주가 유동주식수의 10% 이상으로서 100만주 이상을 소유, 해외증권시장에 상장된 경우는 적용배제 |
관리종목 지정법인이 1년 이내에 동 규정에 의한 주식분산기준미달을 해소하지 아니하는 경우 |
| 9) 불성실공시 | - | [실질심사]1년간 불성실공시 벌점 15점 이상 |
| 10) 지배구조 미달 | 최근 사업연도 사업보고서상 ⅰ)사외이사의 수가 법에서 정하는 수에 미달 ⅱ)법에서 정하는 감사위원회를 구성하지 않거나 구성요건을 충족하지 아니하는 경우 |
관리종목 지정법인이 다음 사업연도에 동일한 상태에 해당하는 경우 |
| 11) 회생절차 개시신청 | 「채무자 회생 및 파산에 관한 법률」 제34조에 의한 회생 절차개시 신청이 있는 경우 | [실질심사] 관리종목 지정법인이 다음의 어느 하나에 해당하는 경우 코스닥시장 상장폐지실질심사위원회의 심사를 거쳐 상장폐지 가)법원의 회생절차개시신청 기각, 회생절차개시결정 취소, 회생계획 불인가 또는 회생절차폐지의 결정 등이 있은 때 나) 실질심사 제출서류 상 투자자 보호를 위하여 중요한 사항이 누락되거나 거짓 기재된 경우 |
| 12) 파산신청 | 코스닥시장 상장법인에 대하여 "채무자 회생 및 파산에 관한 법률" 제294조에 의한 파산신청이 있는 경우 | |
| 13) 정기보고서 미제출 | 사업보고서, 반기보고서 또는 분기보고서를 법정제출기한 내에 제출하지 않거나, 정기주총에서 재무제표 미승인 or 정기주총 미개최할 경우 |
관리종목 지정법인이 다음 회차에 다음 어느 하나에 해당하는 경우 가)분기,반기,사업보고서를 법정제출기한내에 미제출 나)사업보고서의 법정제출기한까지 정기주주총회를 미개최하거나 정기주주총회에서 재무제표 미승인 다)최근 2년간 3회 이상 분기, 반기, 사업보고서 법정제출기한까지 제출하지 아니한 경우 라)법정제출기한까지 사업보고서를 제출하지 아니한 후 법정제출기한의 다음날부터 10일 이내 사업보고서 미제출 |
| 14) 기타 |
- 형식적 상장폐지 사유 또는 상장적격성 실질심사에 따른 상장폐지 사유가 발생한 경우 |
- 감사보고서 부적정·의견거절·범위제한한정 - 해산사유(피흡수합병, 파산선고) - 정관 등에 주식양도제한 두는 경우 - 유가증권시장 상장의 경우 - 우회상장시 우회상장관련 규정 위반시(심사종료전 기업결합완료 및 보호예수 위반 등) |
| 출처) 한국거래소 |
| 자. 차입공매도 유상증자 참여 제한 관련 금융위원회의 공매도 제도개선 관련 「자본시장과 금융투자업에 관한 법률 시행령」일부개정에 따라, 주권상장법인이 유상증자 계획을 공시한 이후 발행가격 산정을 위한 대상 거래기간의 마지막날(발행가격 산정 기산일)까지, 해당 기업의 주식을 공매도 한 자는 증자참여를 제한하되, 예외적인 경우에만 증자참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 투자자께서는 이 점 유의하시기 바랍니다. |
주권상장법인이 유상증자 계획을 공시한 이후 해당 기업의 주식을 공매도 한 자는 증자참여를 제한하되, 예외적인 경우 증자참여를 허용하고 있습니다(「자본시장과 금융투자업에 관한 법률」제180조의4). 이와 관련 유상증자 참여가 제한되는 공매도 시점과 증자참여가 허용되는 예외사유를 시행령에서 정하도록 위임하고 있습니다.
시행령에 따르면, 유상증자 계획이 공시된 다음 날부터, 발행가격 산정을 위한 대상 거래기간의 마지막날(발행가격 산정 기산일)까지 공매도 한 경우 증자참여가 제한됩니다. (「자본시장과 금융투자업에 관한 법률 시행령」제208조의4제1항)
다만, 다음의 경우 공매도를 통해 발행가격에 부당한 영향을 미쳤다고 보지 않아 증자참여가 허용됩니다(「자본시장과 금융투자업에 관한 법률 시행령」제208조의4제2항).
ⅰ) 마지막 공매도 이후 발행가격 산정 기산일까지 공매도 주문 수량 이상을 증권시장 정규거래시간에 매수(체결일 기준)
ⅱ) 금융위원회가 정하는 기준을 충족한 독립된 거래단위를 운영하는 법인 내에서 공매도를 하지 않은 거래단위가 증자참여
ⅲ) 시장조성 또는 유동성공급을 위한 거래과정에서 공매도
상기 공매도제도 개선 관련 자본시장법 시행령 개정안에 따라, 당사의 주식을 해당 기간 동안 공매도하는 투자자께서는 금번 유상증자 참여가 제한될 수 있음을 유의하시기 바랍니다. 해당 법령과 관련된 자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융법규서비스(http://fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
| 차. 재무제표 작성 기준일 이후 재무상황 변동에 따른 위험 본 공시서류 상 재무제표에 관한 사항은 2022년 1분기 재무제표 (K-IFRS 기준) 작성기준일 이후의 변동을 반영하지 않았습니다. 당사는 금번 유상증자를 진행하는 과정에서 투자 의사결정에 중대한 영향을 미칠 것으로 판단되는 변동사항을 향후에도 상세하게 반영하여 공시할 예정입니다. 그럼에도 불구하고, 당사가 중요하지 않다고 판단하여 기재 및 서술을 생략한 사항 중 당사의 기업가치에 영향을 미칠 만한 사건이 없다고 단정할 수는 없어 주기적이고 면밀한 검토가 필요합니다. |
본 공시서류에 기재된 재무제표에 관한 사항과 감사인의 의견에 관한 사항은 2022년 1분기 재무제표 작성기준일 이후의 변동을 반영하지 않았으므로 투자에 유의하시기 바랍니다.
다만, 본 공시서류에 기재된 재무제표의 작성기준일 이후 본 공시서류 제출일 사이에 발생한 것으로 증권신고서에 기재된 사항 이외에 자산, 부채, 현금흐름 또는 손익사항에 중대한 변동을 가져오거나 중요한 영향을 미치는 사항은 없습니다.
당사는 금번 유상증자를 진행하는 과정에서 투자 의사결정에 중대한 영향을 미칠 것으로 판단되는 변동사항을 향후에도 상세하게 반영하여 공시할 예정입니다. 그럼에도 불구하고, 당사가 중요하지 않다고 판단하여 기재 및 서술을 생략한 사항 중 당사의 기업가치에 영향을 미칠 만한 사건이 없다고 단정할 수는 없어 주기적이고 면밀한 검토가 필요합니다. 투자자께서는 이 점 유의하시기 바랍니다.
IV. 인수인의 의견(분석기관의 평가의견)
| 본 장은 「자본시장과 금융투자업에 관한 법률」 제119조 및 제125조, 금융감독원의 「금융투자회사의 기업실사 모범규준」에 따라 본건 공모 지분증권 인수인이 당해 공모 지분증권에 대한 의견을 기재하고 있는 부분입니다. 따라서 본 장의 작성 주체는 대표주관회사인 한양증권(주)입니다. 발행회사인 (주)카이노스메드는 "동사"로 기재하였습니다. 본 장에 기재된 분석의견 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 여러가지 요소들의 영향에 따라 예측했던 것과 다를 수 있다는 점을 유의하시기 바랍니다. |
1. 분석기관
| 구 분 | 금융투자업자(분석기관) | |
| 회 사 명 | 고 유 번 호 | |
| 대표주관회사 | 한양증권(주) | 00162416 |
2. 분석의 개요
대표주관회사인 한양증권(주)는 「자본시장과 금융투자업에 관한 법률」 제71조 및 동법 시행령 제68조에 의거 공정한 거래질서 확립과 투자자 보호를 위해 다수인을 상대로 한 모집ㆍ매출 등에 관여하는 인수회사로서, 발행인이 제출하는 증권신고서 등에 허위의 기재나 중요한 사항의 누락을 방지하는데 필요한 적절한 주의를 기울였습니다.
대표주관회사는 인수 또는 모집ㆍ매출의 주선업무를 수행함에 있어 적절한 주의의무를 다하기 위해 금융감독원이 제정한 「금융투자회사의 기업실사(Due Diligence) 모범규준」(이하 "모범규준"이라 한다)의 내용을 내부 규정에 반영하여 지분증권, 채무증권 증권신고서를 대상으로 기업실사를 의무적으로 수행하도록 규정하고 있습니다.
본 장에 기재된 분석의견은 대표주관회사가 기업실사 과정을 통해 발행회사부터 제공받은 정보 및 자료에 기초한 합리적, 주관적 판단일 뿐이므로, 이로 인해 대표주관회사가 투자자에게 본 건 유상증자의 투자여부에 관한 경영 및 재무상의 조언 또는 자문을 제공하는 것은 아닙니다.
또한 본 평가의견에 기재된 내용 중에는 예측정보가 포함되어 있으며, 예측정보에 대한 실제 결과는 여러 가지 요소들의 영향에 따라 최초 예측치와는 다른 결과를 가져올 수 있다는 점에 유의하시기 바랍니다.
| 「금융투자회사의 기업실사 모범규준」 제3조(적용범위 등) ① 이 규준은 법 제119조제3항의 규정에 의한 증권신고서 및 법 제122조의 규정에 의한 정정신고서를 제출하는 경우에 적용하며, 영업의 실체가 있는 발행회사가 제출하는 지분증권, 채무증권 증권신고서를 대상으로 하고 자산유동화증권 등은 적용대상에서 제외된다. ② 이 규준은 주관회사가 업무수행 중 참고해야 할 기본적인 지침으로 발행회사의 재무 및 영업 현황, 사업 환경, 투자위험, 인수 형태 등을 감안하여 강화하거나 완화하는 등 탄력적으로 운용할 수 있다. ③ 기업공개의 경우 기업공개 실사절차의 특성을 감안하여 이 규준의 내용중 한국거래소의 상장심사지침 등에서 의무사항으로 규정하고 있는 내용과 중복되는 부분에 대해서는 이를 생략하거나 완화할 수 있다. ④ 채무증권의 경우 i)보증유무, 상환조건(만기, 옵션유무), 특약 등 해당 사채의 특성, ii)법 제119조제2항에서 규정하고 있는 일괄신고서에 의한 발행인지 여부, iii)발행회사가 시행령 제121조제6항의 요건을 충족하고 있는지 여부, iv)해당 사채권에 대한 신용평가등급(외부 및 내부) 등을 감안하여 합리적인 기준에 따라 이 규준을 완화할 수 있다. ⑤ 제2항 내지 제4항에 따라 이 규준을 생략하거나 강화 또는 완화하는 경우에는 이사회나 리스크관리위원회(이하 '리스크관리위원회 등')의 의사결정을 거쳐야 한다. |
분석의견의 상세한 내용은 동 증권신고서에 첨부되어 있는 기업실사 부분을 참고하시기 바랍니다.
3. 기업실사 일정 및 주요 내용
| 일자 | 실사내용 |
| 2022-05-09 | 초도방문 - 상견례 인사 - 유상증자 의사 및 자금조달 관련 논의 - 유상증자 필요성 검토 및 주요일정 협의 - 공시 및 뉴스 내용 등을 통한 발행회사 및 소속산업 사전 조사 - 사업내용 청취 및 주요제품 열람 - 실사 사전 요청자료 송부 |
| 2022-05-10~ 2022-05-16 |
실사자료 요청 - 실사 요청자료 송부 회사 일반사항 관련 검토 - 정관검토 및 이사회 등 상법 절차 확인 - 경영진 평판 리스크 검토 - 회사의 사업 및 영업구조 관련 면담 |
| 2022-05-17~ 2022-05-18 |
회사방문 - 실무진 상견례 회사 기본사항 검토 - 정관 등 기본자료 수령 - 자금 사용 목적 등에 관한 의견 청취 - 발행 방식 및 조건 등에 관한 협의 - 금융당국으로부터의 제재조치 여부 확인 - 근로기준법 위반행위, 소송진행 여부 확인 산업에 관한 사항 검토 - 산업 경쟁상황, 시장규모, 성장주기 등 확인 - 법률 및 정부규제에 관한 사항 검토 - 시장 내 중대한 환경, 제도 변화요인 검토 회사 지배구조에 관한 사항 검토 - 경영진의 변동내역 및 근무경력 검토 - 계열회사에 관한 사항 검토 - 최대주주의 지분율 및 경영권 안정성 검토 - 사내규정 및 내부통제시스템 확인 - 공시시스템 검토 및 담당자 면담 |
| 2022-05-19 ~ 2022-05-26 |
영업에 관한 사항 검토 - 제품별 매출 현황, 부문별 수익성추이 확인 - 외주업체 관한 사항 - 향후 투자계획에 관한 사항 - 향후 수익성 개선, 원가절감 계획에 관한 사항 재무에 관한 사항 검토 - 매출채권, 재고자산 현황 및 연령분석 - 기타채권 현황 및 회수 내역 분석 - 유형자산 취득/처분 현황 분석 - 수익성/성장성/안정성 지표 분석 - 차입금의 적정성 여부 분석 - 차입금 연장 가능성 및 협의, 상환일정 등 - 지급보증 등의 우발채무현실화에 따른 동사의 유동성 분석 - 현금흐름 구조 기타 사항 검토 - 발행시장 상황 검토 - 최대주주 및 특관자 참여여부 검토 - 자금 조달금액, 공모가액의 적정성 검토 |
| 2022-05-27 ~ 2022-06-10 |
- 실사 추가 자료 요청 - 증권신고서 작성에 대한 조언 - 이사회의사록 검토/인수계약서 작성 및 검토 - 실사이행보고서 작성 및 증권신고서 검토 |
4. 기업실사 참여자
[대표주관회사]
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 | 참여기간 | 주요경력 |
|---|---|---|---|---|---|---|
| 한양증권 | 기업금융부 | 유문성 | 이사 | 증자업무 총괄 | 2022년 05월 09일 ~ 2022년 06월 10일 |
기업금융업무 18년 |
| 한양증권 | 기업금융부 | 전대희 | 상무 | 기업실사 | 2022년 05월 09일 ~ 2022년 06월 10일 |
기업금융업무 25년 |
| 한양증권 | 기업금융부 | 안병종 | 상무 | 기업실사 | 2022년 05월 09일 ~ 2022년 06월 10일 |
기업금융업무 22년 |
| 한양증권 | 기업금융부 | 정경훈 | 차장 | 실사책임 및 검토 | 2022년 05월 09일 ~ 2022년 06월 10일 |
기업금융업무 10년 |
| 한양증권 | 기업금융부 | 장창환 | 대리 | 기업실사 및 서류작성 등 | 2022년 05월 09일 ~ 2022년 06월 10일 |
기업금융업무 4년 |
[ 발행회사 ]
| 소속 | 부서 | 성명 | 직급 | 담당업무 |
| (주)카이노스메드 | - | 이기섭 | 대표이사 | 경영총괄 |
| (주)카이노스메드 | - | 이재문 | 사장 | 연구, 경영 |
| (주)카이노스메드 | 사업개발본부 | 고수영 | 이사 | 사업개발 총괄 |
5. 기업실사 세부 항목 및 점검 결과
- 동 증권신고서에 첨부되어 있는 기업실사 보고서를 참조해 주시기 바랍니다.
6. 종합 의견
가. 대표주관회사인 한양증권(주)는 (주)카이노스메드가 2022년 06월 10일 이사회에서 결의한 기명식 보통주 5,600,000주에 대한 주주배정후 실권주 일반공모 방식으로 발행을 결정하고 이에 잔액인수 함에 있어 다음과 같이 의견을 제시합니다.
| 긍정적 요인 | ▶ 동사 파킨슨병 치료제(KM-819) 미국 FDA 임상 2상 IND 승인을 받았으며, 다계통위축증(KM-819)의 국내 임상 2상 IND 승인을 득하였습니다. ▶ 동사 에이즈 치료제(KM-023)은 2021년 06월 중국에서 ACC007라는 제품명으로 NDA(New Drug Application) 승인 받았으며 현재 시판 중이라 판매량에 따라 로열티 매출이 성장할 수 있습니다. |
| 부정적 요인 |
▶2022년 1분기 동사의 자본금 및 비지배지분 제외 자본총계는 각각 11,040백만원 및 8,765백만원으로 2021년 대비 비지배지분 제외 자본총계는 3,338백만원이 감소하였으며, 2022년 1분기 기준 자본잠식률은 20.6%를 기록하고 있습니다. ▶향후 유의미한 수준의 매출 발생으로 인한 수익 구조 개선 시기가 지연된다면 손실이 지속적으로 발생하거나, 현재 동사가 진행 중인 파이프라인의 임상 시험이 지연 또는 실패하여 소요된 연구개발비용 등을 회수하지 못할 경우 유동성 악화로 인해 당사의 재무안정성이 악화될 수 있습니다. |
| 자금조달의 필요성 |
▶ 동사는 금번 유상증자를 통해 조달하는 자금을 채무상환자금 및 운영자금(임상시험비용, 연구개발비용) 등으로 활용할 계획입니다. ▶ 동사는 KM-819의 미국 및 국내 임상 2상을 진행할 예정으로 추가 임상비용이 필요한 상황입니다. 제2회 전환사채 조기상환일이 도래하여 상환을 위한 채무상환자금이 필요하여 유상증자를 실시하게 되었습니다. ▶ 금번 유상증자를 통해 조달한 자금의 세부사용 내역은 "Ⅴ. 자금의 사용목적"을 참고하시기 바랍니다. |
나. 대표주관회사는 상기 실사를 통해 제공받는 자료들로부터 도출된 결과나 오류, 누락 등에 대하여 당사가 책임지지 않으며, 인간적 또는 기계적, 기타 그 외의 다른 요인에 의한 오류발생 가능성으로 인해 본 평가 내용에 대해 명시적으로 혹은 묵시적으로도 증명이나 서명 또는 보증 및 단언을 할 수 없습니다.
다. 동사의 금번 유상증자는 국내외 거시경제 변수변화로 투자수익에 대한 확실성이 저하될 수 있습니다. 투자자 여러분께서는 상기 검토결과는 물론 동 증권신고서 및 투자설명서에 기재된 동사의 회사 전반에 걸친 현황 및 재무상의 위험과 산업 및 영업상의 위험요인 등을 감안하시어 투자에 유의하시기 바랍니다. 또한, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 동 증권신고서 및 투자설명서에 기재하지 않은 사항이라 하더라도 동사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자께서는 동 증권신고서 및 투자설명서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 독자적이고도 세밀한 판단에 의해 투자결정을 하시기 바랍니다.
| 2022년 06월 10일 |
| 대표주관회사 : 한양증권 주식회사 |
| 대표이사 임 재 택 |
V. 자금의 사용목적
1. 모집 또는 매출에 의한 자금조달 내역
가. 자금조달금액
|
(단위 : 원) |
|
구 분 |
금 액 |
|---|---|
|
모집 또는 매출총액(1) |
48,496,000,000 |
|
발행제비용(2) |
806,000,000 |
|
순 수 입 금 [ (1)-(2) ] |
47,690,000,000 |
|
주1) 상기 금액은 예정발행가액을 기준으로 산정한 금액으로 모집가액 확정시 변경될 수 있습니다. |
| 주2) 상기 모집총액은 우선적으로 하단에 기재된 자금의 사용 목적에 따라 사용할 예정입니다. |
| 주3) 발행제비용은 공모금액 및 실권규모에 따라 변경될 수 있으며, 상기 기재 금액은 청약 초과로 인하여 실권이 발생하지 않은 상황을 가정하여 산정되었습니다. 또한 상장수수료는 상장신청일 직전일 주가에 따라 변동될 수 있습니다. |
나. 발행제비용의 내역
|
(단위 : 원) |
|
구 분 |
금 액 |
계산근거 |
|---|---|---|
|
발행분담금 |
8,729,280 |
모집총액의 0.018% (10원 미만 절사) |
|
인수수수료 |
727,440,000 |
납입금액의 1.5% |
|
상장수수료 |
7,300,000 | 590만원 + 500억원 초과금액의 10억원당 7만원 |
|
등록세 |
11,200,000 |
증자 자본금의 0.4% |
|
교육세 |
2,240,000 |
등록세의 20% |
|
기타비용 |
49,090,720 |
구주주 청약서, 투자설명서 인쇄 및 발송비 등 |
|
합 계 |
806,000,000 |
- |
| 주1) 상기 금액은 예정 모집가액을 기준으로 산정한 금액입니다. |
| 주2) 발행제비용은 공모금액 및 상장신청일 직전일 한국거래소에서 거래되는 당사의 보통주식 종가, 유관기관 정책 등에 따라 변동될 수 있습니다. |
| 주3) 기타비용은 예상금액으로 변동될 수 있습니다. |
| 주4) 발행제비용은 공모금액에서 지급될 예정입니다. |
2. 자금의 사용목적
가. 자금의 사용목적
당사는 금번 유상증자를 통해 조달한 자금을 다음과 같이 사용할 예정입니다.
| (기준일 : | 2022년 06월 09일 | ) | (단위 : 원) |
| 시설자금 | 영업양수 자금 |
운영자금 | 채무상환 자금 |
타법인증권 취득자금 |
기타 | 계 |
|---|---|---|---|---|---|---|
| - | - | 27,690,000,000 | 20,000,000,000 | - | 806,000,000 | 48,496,000,000 |
나. 공모자금 세부 사용목적
당사는 금번 유상증자로 조달된 자금을 현재 연구 중인 파이프라인 중 KM-819의 미국 임상 2상 및 국내 임상 2상의 임상시험비용, 추가적인 임상 진입을 위한 R&D비용 및 연구개발비용, 제2회 전환사채 채무상환자금 등으로 사용할 예정입니다. 만약 금번 유상증자의 공모금액이 당초 계획한 금액에 미달할 경우 당사는 아래에 표기한 자금사용계획 우선순위에 따라 집행 시기를 고려하여 세부적으로 조정할 예정이며, 부족분 및 전환사채의 이자, 발행제비용은 당사의 자체자금으로 충당할 계획입니다. 금번 유상증자를 통한 공모자금의 세부 사용 내역은 아래와 같습니다.
|
[유상증자 자금사용의 우선순위] |
|
(단위 : 백만원) |
|
구분 |
자금용도 |
세부 내용 |
금액 |
|---|---|---|---|
|
1 |
채무상환자금 | 제2회 전환사채 상환자금 | 20,000 |
|
2 |
운영자금 |
임상시험비용(KM-819(파킨슨병), KM-819(다계통위축증)) |
22,990 |
|
3 |
운영자금 |
연구개발비용(R&D비용, FAF1-Exosome 항암제 개발) |
4,700 |
| 4 | 기타자금 | 발행제비용 | 806 |
|
합계 |
48,328 | ||
1. 채무상환자금 : 제2회 전환사채 상환자금
당사는 2020년 06월 연구개발비 등 임상 시험을 진행 중인 자회사의 운영자금 및 당사 자체 운영자금을 조달하기 위해 20,000백만원 규모의 제2회 사모 전환사채를 발행하였으며, 신고서 제출 전일 기준 조기상환청구 및 전환청구 건수는 전무하여 현재 채권 잔액은 20,000백만원(전자등록총액 기준)입니다.
제2회 전환사채의 전환가액은 시가하락에 의한 전환가격 조정이 완료된 4,070원이며, 최근 주가대비 전환가액이 상회하는 외가격(OTM, Out of Money) 상태로 채권자들의 조기상환 청구 가능성이 높다고 판단됩니다.
| [전환사채 발행 개요] |
| (단위 : 원) |
| 구분 | 전환사채 |
|---|---|
| 사채의 명칭 | 주식회사 카이노스메드 제2회 무기명식 이권부 무보증 사모 전환사채 |
| 발행일 | 2020년 06월 30일 |
| 만기일 | 2025년 06월 30일 |
| 발행금액(전자등록총액 기준) | 20,000백만원 |
| 잔액(전자등록총액 기준) | 20,000백만원 |
| 상화방법 | 만기일에 원금의 105.1205%를 일시상환한다. |
| 사채의 이율 | 표면금리 0% (만기보장수익률은 3개월 단위 복리계산 1%) |
| 조기상환청구권(Put Option) | 사채권자는 사채의 발행일로부터 24개월 이후 45개월까지의 기간중 원금의 전부 및 일부에 대하여 조기상환수익률 연 1.0%(3개월 단위 복리계산)가 적용된 청구 금액을 조기상환 청구할 수 있음. |
| 매도청구권(Call Option) | 회사는 사채권자로부터 회사 또는 회사가 지정하는 제3자(매수인)에게사채의 발행일로부터 12개월 이후 24개월까지의 기간 중 매 3개월에 해당되는 날에 원금의 25/100에 대하여 매도 청구할 수 있음. 매수인이 매도청구 행사시 연1.0%(3개월 단위 복리계산)의 이율을 적용하여 계산한 금액을 지급하여야 함. |
| 전환가격(주) | 5,813원/주 (최초 발행당시 전환가격) |
| 전환기간 | 2021년 6월 30일부터 2025년 3월 30일 |
| 전환가격의 조정 | 발행회사가 시가를 하회하는 발행가액으로 유상증자, 무상증자, 주식배당 및 준비금의 자본전입 등으로 주식을 발행하는 경우, 시가를 하회하는 전환가액 또는 행사가액으로 전환사채 또는 신주인수권부사채를 발행하는 경우에는 전환가격이 조정될 수 있으며, 발행회사의 보통주식 주가가 하락할 경우 발행일로부터 매 3개월마다 약정에 따라 조정전 전환가격의 70%까지 전환가격 조정 |
| 전환가격 |
(1)최초 전환가액: 5,813원/주 (3)2차 조정전환가액: 4,386원/주 (2020년 12월 30일 조정) (4)3차 조정전환가액: 4,070원/주 (2021년 03월 30일 조정) |
| 최초 인수인 |
(1)NH투자증권(파인밸류PreIPO플러스 전문투자형 사모증권투자신탁의 신탁업자지위에서) 5,000백만원 |
| 출처) 당사 정기보고서 및 당사 제시 |
| [제2회 전환사채로 조달한 자금사용내역] |
| (단위 : 백만원) |
| 항목 | 금액 |
|---|---|
| 타법인증권취득(미국 자회사 FAScinate Therapeutics, Inc.) - KM-819(파킨슨병 치료제)의 미국 임상 2상 진행을 위한 자금 조달 |
18,052 |
| R&D 운영비 | 1,542 |
| 일반운영비 | 400 |
| 발행제비용 | 6 |
| 합계 | 20,000 |
| 출처) 당사 정기보고서 및 당사 제시 |
| [제3회 전환사채 조기상환일 및 청구기간] |
|
구분 |
조기상환 청구기간 |
조기상환지급일 |
조기상환수익률 |
|
|---|---|---|---|---|
|
FROM |
TO |
|||
|
1차 |
2022-05-01 |
2022-05-31 |
2022-06-30 |
102.0176% |
|
2차 |
2022-08-01 |
2022-08-31 |
2022-09-30 |
102.2726% |
|
3차 |
2022-10-31 |
2022-11-30 |
2022-12-30 |
102.5283% |
|
4차 |
2023-01-29 |
2023-02-28 |
2023-03-30 |
102.7846% |
|
5차 |
2023-05-01 |
2023-05-31 |
2023-06-30 |
103.0416% |
|
6차 |
2023-08-01 |
2023-08-31 |
2023-09-30 |
103.2992% |
|
7차 |
2023-10-31 |
2023-11-30 |
2023-12-30 |
103.5574% |
|
8차 |
2024-01-30 |
2024-02-29 |
2024-03-30 |
103.8163% |
|
9차 |
2024-05-01 |
2024-05-31 |
2024-06-30 |
104.0759% |
|
10차 |
2024-08-01 |
2024-09-02 |
2024-09-30 |
104.3361% |
|
11차 |
2024-10-31 |
2024-12-02 |
2024-12-30 |
104.5969% |
|
12차 |
2025-01-29 |
2025-02-28 |
2025-03-30 |
104.8584% |
| 출처) 2020.06.26 당사 주요사항보고서(전환사채발행결정) |
제2회 전환사채의 전환가격은 4,070원은 최근 당사의 주가수준(증권신고서 제출 전일 종가 2,495원)에 비해 외가격(OTM, Out of Money) 상태에 있기 때문에 채권자들의 조기상환 청구가 이루어질 것으로 예상하고 있습니다. 제2회 전환사채 20,000백만원에 대하여 당사는 금번 유상증자를 통해 조달된 자금을 조기상환에 사용할 예정이며, 상환시 발생하는 이자는 자체자금을 활용하여 상환할 예정입니다. 금번 진행하는 유상증자가 완료되기 전에 조기상환 청구가 이루어질 경우 선제적으로 당사의 자체자금으로 상환할 예정입니다.
2. 운영자금 : 임상시험비용
당사는 인간의 불치병, 난치병, 삶의 질 개선을 위한 혁신적인 신약을 연구하고 이를 적정 개발단계의 신약후보물질로 License-Out 함으로써 수익을 창출하는 것을 사업으로 영위하고 있습니다.
당사가 현재 개발중인 프로젝트들을 타겟 시장(질환)별로 분류해보면 뇌질환(파킨슨병 치료제, 다계통위축증), 항바이러스(에이즈 치료제), 항암제(IRAK4, FAF1-exosome 등) 등으로 분류할 수 있으며, 당사는 현재 적절한 치료약물이 없는 질환들을 대상으로 합성의약 및 바이오의약들을 개발하고 있습니다.
파킨슨병 치료제는 미국 자회사(FAScinate Therapeutics, Inc.)를 통해 미국 FDA 임상 2상 IND승인을 받고 임상 2상의 1단계 진입 준비 중에 있습니다. 다계통위축증 치료제(KM-819의 적응증 확대)는 2021년 10월 22일 국내 식약처에서 임상 2상 IND승인을 받았으며, 현재 임상 시험 시행을 준비하고 있습니다.
| [임상비용 세부지출 계획] |
| (단위: 백만원) |
| 구분 | 과제 | 세부과제명 | 기간 | 금액 |
|---|---|---|---|---|
| KM-819 | 파킨슨병 임상 2상(미국) | 용량결정 시험 | 2022.04 - 2022.12 | 3,000 |
| 환자모집, 스크리닝 288명 | 2023.01 - 2023.04 | 3,000 | ||
| 투여, 치료 (2년) | 2023.05 - 2025.05 | 8,690 | ||
| 데이터 통계분석, CSR | 2025.05 - 2025.10 | 500 | ||
| 약물추가생산 | 2023.01 -2023.12 | 800 | ||
| 소계 | 15,990 | |||
| 다계통위축증 임상 2상(한국) | 환자 모집, 스크리닝 78명 | 2022.07 - 2022.10 | 1,500 | |
| 1차 9개월 투여 | 2022.11 - 2023.07 | 2,500 | ||
| 2차 9개월 투여 | 2023.09 - 2024.05 | 2,500 | ||
| 데이터 통계분석, CSR | 2024.06 - 2024.10 | 500 | ||
| 소계 | 7,000 | |||
| 합계 | 22,990 | |||
| 출처) 당사 제시 |
| 주) 다계통위축증은 KM-819(파킨슨병 치료제)물질의 적응증 확대로 개발 중인 프로젝트 입니다. |
(1) 파킨슨병 미국 임상 2상
퇴행성 뇌질환 (degenerative brain disease)은 노화가 진행됨에 따라 발생하는 퇴행성 질환 중에서 뇌에서 발생하는 질환을 뜻합니다. 현재까지 알려지지 않은 원인으로 뇌와 척수의 특정 뇌세포군이 서서히 그 기능을 잃고 뇌신경계의 정보전달에 가장 중요한 뇌신경세포의 사멸, 뇌신경세포 사이의 정보를 전달하는 시냅스의 형성이나 기능상의 문제, 뇌신경의 전기적 활동성의 이상적 증가나 감소로 인하여 야기되는 것으로 알려져 있습니다. 뇌와 척수의 신경세포들은 위치에 따라 매우 다양한 기능을 하고 있어 어느 부위의 신경세포들이 먼저 손상되고 기능을 소실함에 따라, 또 이러한 기능장애가 어떤 형태로 진행되는가에 따라 매우 다양한 임상 양상을 보이게 됩니다. 퇴행성 뇌질환 은 나타나는 주요 증상과 침범되는 뇌 부위를 고려하여 구분할 수 있으며, 알츠하이머병, 파킨슨병, 헌팅턴병, 다발성경화증, 루게릭병으로 알려진 근위축성 측색 경화증 등이 포함됩니다.
당사가 질병조절 치료제로서 개발중인 퇴행성 뇌질환은 파킨슨병입니다. 중뇌에 위치한 흑색질(substantia nigra pars compacta, SNpc)에 존재하는 도파민 생성 신경세포의 사멸로 인해서 운동장애를 나타내는 질환입니다. 임상적으로는 운동 완서, 근육의 경직, 강직, 떨림, 자세이상 등의 증상이 대표적입니다. 이 외에도 인지 기능의 장애, 정신 이상 증상 그리고 감각 이상 등과 같은 다양한 임상적 특징을 보이며, 지속적인 세포의 사멸로 인한 신체이상으로 정상적인 생활이 불가능하며, 진단 후 약 10-15년의 수명을 보입니다. 인구 고령화에 따라 향후 퇴행성 뇌질환 유병률 및 관련 의료비용이 지속적으로 증가할 것으로 예상되며, 이에 따라 효과적 치료제 개발에 대한 수요가 확대될 전망입니다. 퇴행성 뇌질환은 환경적인 요인 및 유전적 요인 등에 의해 발병하는 것으로 추정되고 있으나 아직 정확한 원인 규명 및 근본적인 치료제 개발은 이루어지지 않은 특발성질환(idiopathic)입니다. 그 결과로 인해 단편적인 증상완화 및 간병을 위한 경제적·사회적 비용 부담이 장기화되고 있습니다.
질병을 근본적으로 억제하는 치료제가 현재까지는 없으며, 현재 시판되고 있는 치료제는 알츠하이머병과 파킨슨병의 인지기능 및 운동능력 유지 등의 증상 완화 및 진행 속도 지연을 위한 증상완화 의약품이 대부분입니다. 그 결과 퇴행성신경질환 환자의 지속적인 증가가 예상됨에 따라 병의 진행을 근원적으로 억제할 수 있는 질병조절치료제(Disease-modifying treatments) 의약품 개발이 더욱 중요해지고 있습니다.
노인인구 증가는 건강한 노년 준비 트렌드, 퇴행성신경질환에 대한 관심 증가, 적절한 환자 치료계획을 제공할 수 있는 전문 의료 인프라 및 효과적 질환 치료제의 수요 확대 등을 초래하여 관련 시장 성장을 견인할 것으로 전망됩니다. 또한, 증상 완화 위주의 기존 약물 요법에서 나아가 근본적인 발병 기전을 표적으로 하는 질환 조절 치료제의 개발은 퇴행성 뇌질환 치료 분야에 혁명을 일으킬 것으로 기대하고 있습니다.
| [파킨슨병 치료제 미국 임상 2상 개요] |
| 구분 | 내용 |
|---|---|
| 임상시험의 목적 |
- 임상시험의 주요 목표는 파킨슨병의 진행을 늦추는 안전하고 효과적인 치료법으로서 KM-819 연구의약물의 유효성을 확인하고 안전성과 약동학을 평가하기 위함 |
| 임상시험 시행 방법 |
- 시험 대상자 수: 파킨슨병 환자 288명 - 1차 용량결정시험, 단계 Part 1a, 건강한 노인층 상대, 200, 400, 800 mg 용량증가, 단계 Part 1b, 파킨슨병 환자 상대 200, 400, 600 mg 용량증가. 1주일간 투여 - 2차 치료시험: 288 면 파킨슨병 환자, 2년간 투여, KM-819 또는 위약을 받기 위해 1: 1 비율로 무작위 배정됨. 무작위배정, 이중 눈가림, 위약 대조, 평행군 비교. - 임상연구기간 : 용량결정시험과 치료시험 전체 약 3년. (환자의 등록 상황 또는 투여기간 등에 따라 변동 가능) |
| 기대효과 |
- KM-819 연구의약물은 파킨슨병의 병리적 진행악화를 늦추는 치료제로써 세포사멸을 유도하는 FAF1의 과발현을 억제하여 새로운 약리작용 방식으로 도파민 생성 뉴런을 사멸로부터 보호할 것으로 기대됨 - 본 임상시험에서는 시험군의 KM-819 복용시 임상적으로 유의미한 차이로 대조군에 비교하여 파킨슨병의 진행속도가 늦춰지고 신경학적 평가의 결과가 개선될 것으로 기대됨 - 난치성 질환이며 증상완화제만 있으며 근본적 치료제가 전혀 없는 파킨슨 질환에 질환의 진전을 막아주는 효과는 환자의 삶의 지질을 높이고 거의 정상적 사회생활을 가능하게 함. 알츠하이머 다음으로 많은 노인질환으로 65세 이상 인구의 약 2-3% 가 호나자이고 미국에만 1백만병 이상임. 성공하면 새로운 메커니즘과 타겟에 의한 혁신적 신약이 될것임. |
| 임상 시험 기관 |
Part 1a: 미국 켈리포니아주 Glendale 에 있는 Parexel 의 Early Clinical Unit. Part 1b: 미국 켈리포니아 San Diego 에 있는 University of California San Diego Hospital, 미국 Michigan 주 Farmington Hills 에 있는 Quest Research Institute Part 2: 위 두곳 외에 8곳 (미정) |
| 출처) 당사 제시 |
현재 KM-819(파킨슨병 치료제)는 미국 FDA에 임상 2상 시험 IND를 승인받았으며 미국 파킨슨병 환자를 대상으로 KM-819의 치료제로서 유효성 및 안전성 평가 목적의 임상 2상 시험을 진행하기 위하여 15,990백만원을 사용할 계획입니다.
상세 내역을 살펴보면, 파킨슨병 치료제의 투여 용량을 결정하기 위한 시험 비용으로 3,000백만원, 미국 파킨슨병 환자 288명 모집 3,000백만원, 약 2개월의 투여 및 치료에 필요한 비용 등 8,690백만원, 임상 데이터 분석에 500백만원, 약물 추가 생산을 위하여 800백만원을 사용할 예정입니다.
(2) 다계통위축증 국내 임상 2상
당사가 연구하고 있는 KM-819의 적응증인 다계통위축증은 비정형 파킨슨증 중 하나이며 임상적 특징으로 파킨슨증, 소뇌성운동실조증 및 자율신경기능 장애를 보이는 등 파킨슨병과 증세가 비슷하나 파킨슨병 치료제 즉 증상 완화제도 거의 효과가 없으며 병의 진행 속도가 빨라서 최고로 심각한 질환 중 하나로 분류되고 있습니다. PET 이미징 등 정밀검사를 하여 진단하며, 수명은 5년에서 6년 정도이고, 환자 수는 파킨슨병에 비해 5 ~ 10% 정도로서 대부분의 국가에서 희귀질환으로 규정되어 있습니다. 병의 원인은 alpha-synuclein이 뇌에서 신경세포를 지원하는 oligodendrocyte 라는 세포에서 축적됨에 기인하며, 그 결과로 뇌조직의 큰 손상이 오며 신경세포에도 손상이 오게 됩니다.
| [다계통위축증 치료제 국내 임상 2상 개요] |
| 구분 | 내용 |
|---|---|
| 임상시험의 목적 | - 임상시험의 주요 목표는 MSA의 진행을 늦추는 안전하고 효과적인 치료법으로서 KM-819 연구의약물의 유효성을 확인하거나 반박하고 KM-819의 약동학을 평가하기 위함 |
| 임상시험 시행 방법 | - 시험 대상자 수: 다계통위축증 환자 78명 - MSA 환자를 대상으로 한 무작위배정, 이중 눈가림, 위약 대조, 평행군 비교 - 스크리닝 기간 후, 대상자들은 KM-819 또는 위약을 받기 위해 1: 1 비율로 무작위 배정됨 - 임상연구기간 : 임상 승인일로부터 24개월 (환자의 등록 상황 또는 투여기간 등에 따라 변동 가능) |
| 기대효과 |
- KM-819 연구의약물은 다계통 위축증의 병리적 진행악화를 늦추는 치료제로써 세포사멸을 유도하는 FAF1의 과발현을 억제하여 새로운 약리작용 방식으로 도파민 생성 뉴런을 사멸로부터 보호할 것으로 기대됨 |
| 임상 시험 기관 | 차의과학대학교 분당차병원 |
| 출처) 당사 제시 |
현재 KM-819(다계통위축증 치료제)는 식품의약안전처에 임상 2상 시험 IND를 승인받았으며 국내 다계통위축증 환자를 대상으로 KM-819의 치료제로서 유효성 및 안전성 평가 목적의 임상 2상 시험을 진행하기 위하여 7,000백만원을 사용할 계획입니다.
상세 내역을 살펴보면, 국내 다계통위축증 환자 78명 모집 1,500백만원, 약 9개월의 1차 투여에 필요한 약물 생산 비용 등 2,500백만원, 약 9개월의 2차 투여에 필요한 약물 생산 비용 등 2,500백만원, 임상 데이터 분석에 500백만원을 사용할 예정입니다.
3. 운영자금: 연구개발비용(FAF1-Exosome 항암제 개발)
| 구분 | 과제 | 세부과제명 | 기간 | 금액 |
|---|---|---|---|---|
| FAF1-exosome 항암제(KM-1004) | 후보물질 개발 | 용량 최적화, 효능 | 2022.04 - 2023.12 | 500 |
| 생산 최적화 | 2022.09 - 2023.10 | 700 | ||
| 1차 독성시험 | 2023.10 - 2014.10 | 500 | ||
| GMP 생산 | 2023.10 - 2024.05 | 1,200 | ||
| GLP 독성 | 2024.06 - 2025.07 | 1,500 | ||
| 임상 1상 IND 제출 | 2025.08 - 2026.12 | 300 | ||
| 합계 | 4,700 | |||
당사는 2021년 10월 28일 다양한 인체 유래세포에서 압출 방식으로 CDV를 생산하는 핵심 기술을 보유하고 있는 엠디뮨과 공동연구개발 계약을 체결하였습니다. CDV(Cell-Derived Vesicle)는 세포외소포의 한 종류로 세포 간 정보 전달체 역할을 하는 엑소좀(Exosome)과 유사한 물리적ㆍ화학적 특성을 보이며, 저분자 화합물을 포함한 다양한 유전자 물질을 탑재할 수 있는 신개념 약물 전달 시스템입니다.
당사는 엠디뮨과 공동연구개발을 통해 FAF1을 엑소좀에 탑재해 암세포 및 생쥐의 암 조직에 전달했을 때 다양한 종류의 종양에서 종양 크기가 감소되는 효과를 확인하였고, FAF1을 항암제로 개발하려는 논거에 대한 동물 실험에서의 개념 입증(proof of concept)을 마쳤습니다. FAF1은 암세포의 세포 분열을 억제하고, 세포 죽음을 유발할 뿐 아니라, 암 전이를 억제하는 강력한 종양 억제 인자입니다. 여러 종류의 암환자 조직에서 FAF1의 발현이 저하된다는 데이터가 있어 높은 임상적 연관성을 가지고 있는 특징이 있습니다.
당사는 해당 약물을 더욱 개발하여 FAF1-Exosome 항암제의 효능조건과 생산의 최적화를 이루고, 더 나아가 전임상에서 GMP 생산과 GLP 독성을 완수하여 임상 진입으로 나아갈 계획입니다.
상세 내역을 살펴보면, FAF-Exosome 항암제에 대한 용량 최적화와 효능 검사를 위해 500백만원, 생산 최적화 과정에서 소요되는 비용 700백만원, 1차 독성시험 진행 비용 5백만원, 임상 1상을 위해 GMP 시설에서 약물 생산에 1,200백만원, GLP 독성 시험 1,500백만원, 임상 1상 IND 제출에 소요되는 비용 300백만원을 사용할 예정입니다.
3. 자금의 운용계획
당사가 금번 유상증자를 통해 조달한 자금 중 일부 자금은 조달시기와 사용시기가 다소 차이가 있을 수 있습니다. 이에 조달로부터 사용시까지 미사용 자금에 대해서는 자금 사용시점 및 금리에 따라 적격 금융기관의 수시입출금 예금, 정기예금 등 금융상품으로 운용할 예정입니다.
VI. 그 밖에 투자자보호를 위해 필요한 사항
제2부 발행인에 관한 사항
I. 회사의 개요
1. 회사의 개요
| 주식회사 카이노스메드는 하나금융11호기업인수목적 주식회사와 2020년 05월 20일 합병등기를 완료한 후, 상호 변경된 법인 입니다. 2020년 4월 16일 합병임시주주총회를 통해 하나금융11호기업인수목적 주식회사와 소멸법인인 주식회사 카이노스메드의 합병이 승인되었고, 합병비율에 의한 합병신주로 2020년 6월 8일에 한국거래소 코스닥시장에 상장하였습니다. 하나금융11호기업인수목적 주식회사는 기업인수가 목적인 명목회사이며, 합병 후 존속하는 사업은 소멸법인인 주식회사 카이노스메드가 영위하는 사업이므로, 실질적으로는 소멸법인인 주식회사 카이노스메드가 존속법인인 하나금융11호기업인수목적 주식회사를 흡수하는 역합병의 결과가 됩니다. 본 보고서는 경제적 실질에 따라 기존 주식회사 카이노스메드의 내용을 기준으로 작성하되, 법적 실체인 기존 하나금융11호기업인수목적 주식회사의 내용으로 표기된 부분은 별도 표기하였음을 알려드립니다. |
가. 연결대상 종속회사 개황
| (단위 : 사) |
| 구분 | 연결대상회사수 | 주요 종속회사수 |
|||
|---|---|---|---|---|---|
| 기초 | 증가 | 감소 | 기말 | ||
| 상장 | - | 0 | 0 | 0 | - |
| 비상장 | 2 | 0 | 0 | 0 | 2 |
| 합계 | 2 | 0 | 0 | 0 | 2 |
※상세 현황은 '상세표-1. 연결대상 종속회사 현황(상세)' 참조
나. 회사의 법적.상업적 명칭
당사의 명칭은 "주식회사 카이노스메드”라고 표기합니다. 또한 영문으로는 “Kainos Medicine, Inc.”라 표기합니다.
다. 설립일자 및 존속기간
당사는 혁신신약 연구 및 개발 목적으로 2007년 06월 15일에 설립되었습니다.
또한, 당사는 2017년 11월 3일 설립된 하나금융11호기업인수목적 주식회사와 2020년 5월 20일자로 합병을 완료하였습니다. 하나금융11호기업인수목적 주식회사가 당사를 흡수합병하는 방법으로 합병을 진행하였으며, 존속법인은 합병완료 후에 상호를 주식회사 카이노스메드로 변경하였습니다.
라. 본사의 주소, 전화번호, 홈페이지 주소
주소: 경기도 성남시 분당구 판교역로 184 (상대원동) JS타워 11층
전화번호: 02-567-7419
홈페이지: http://www.kainosmedicine.com
마. 중소기업 등 해당 여부
| 중소기업 해당 여부 | 해당 | |
| 벤처기업 해당 여부 | 해당 | |
| 중견기업 해당 여부 | 미해당 | |
바. 주요 사업의 내용
당사는 인간의 불치병, 난치병, 삶의 질 개선을 위한 혁신적인 신약을 연구하고 이를 적정 개발단계의 신약후보물질로 License-Out 함으로써 수익을 창출하는 것을 주요사업으로 영위하고 있습니다.
당사가 현재 개발중인 프로젝트들을 타겟 시장(질환)별로 분류해보면 뇌질환(파킨슨치료제), 항바이러스(에이즈치료제), 항암제(IRAK4, FAF1-exosome 등) 등으로 분류할 수 있으며, 다양한 혁신 신약개발 후보 창출에 전념을 하고 있습니다.
상세한 내용은 동 보고서의 『II. 사업의 내용』을 참조하시기 바랍니다.
사. 신용평가에 관한 사항
- 해당사항 없습니다.
아. 회사의 주권상장(또는 등록ㆍ지정)여부 및 특례상장에 관한 사항
| 주권상장 (또는 등록ㆍ지정)여부 |
주권상장 (또는 등록ㆍ지정)일자 |
특례상장 등 여부 |
특례상장 등 적용법규 |
|---|---|---|---|
| 코스닥시장 | 2020년 06월 08일 | 기술특례상장 | 코스닥상장규정 7조 |
자. 대리인이 있는 경우 대리인에 관한 사항
[코스닥시장공시규정에 따른 공시대리인]
- 공시대리인 명칭 : (주)씨에스컨설팅
- 대표자 : 길봉
- 주 소 : 서울특별시 영등포구 국제금융로6길 26
- 전 화 : 82-2-780-1655
- 팩 스 : 82-2-780-1639
2. 회사의 연혁
가. 회사의 연혁
|
년도 |
내 용 |
비고 |
|---|---|---|
|
2007. 06 |
회사 설립 |
|
|
2007. 09 |
기술 라이센싱관리 지원사업 선정 |
한국기술거래소 |
|
2007. 11 |
KM015(당뇨병치료제) 기술이전 계약 체결 |
한국화학연구원 |
|
2007. 12 |
벤처기업인증 |
기술보증기금 |
|
2008. 05 |
특허기술 가치평가 사업 선정 - KM015 |
특허청 |
|
2008. 07 |
KM552(구강건조증 치료제)라이선스계약 체결 |
패리언사이언스 |
|
2008. 07 |
바이오기술유효성평가 및 독성분석사업 선정 |
산업자원부 |
|
2008. 10 |
KM552 바이오 스타프로젝트 선정 |
지식경제부 |
|
2010. 03 |
KM552(구강건조증치료제) 미국임상2a상 |
미국 내 12개 병원 |
|
2010. 04 |
KM023(에이즈치료제)공동개발협약 체결 |
한국화학연구원 |
|
2010. 07 |
대한민국보건산업대상 수상 |
|
|
2011. 02 |
제2기업부설연구소설립 |
서울아산병원 내 |
|
2011. 03 |
KM023(에이즈치료제) 국내임상1상 IND승인 |
KFDA |
|
2011. 06 |
KM023(에이즈치료제) 국내 임상 1상 개시 |
서울대 임상센터 |
|
2012. 08 |
KM023(에이즈치료제) 국내 임상 1상 종료 |
서울대 임상센터 |
|
2012. 09 |
KM023(에이즈치료제) 라이선스 계약 체결 |
한국화학연구원 |
|
2014. 07 |
KM001(비만당뇨치료제) 중국으로 기술이전 |
CROWN BIO |
|
2014. 10 |
KM023(에이즈치료제) 중국제약사에 기술이전 |
Yangzhou Aidea Biotech |
|
2015. 09 |
한국거래소 코넥스시장 상장 |
|
|
2015. 09 |
KM-819(파킨슨씨병 치료제) 기술도입계약 체결 |
한국화학연구원/충남대학교 산학협력단 |
|
2015. 12 |
KM-630(세포독성항암제), KM-635(BRD4 저해제) 중국제약사에 기술이전 |
Yangzhou Aidea Biotech |
|
2016.01 |
본사 및 부설연구소, 성남시 한국파스퇴르연구소로 이전 |
|
|
2016.05 |
충남대, 서울대와 ‘파킨슨 치료제 공동연구 계약”체결 |
충남대,서울대학교 |
|
2016.09 |
한국파스퇴르와 ‘B형간염 치료제 공동연구 계약’ 체결 |
한국파스퇴르연구소 |
|
2016.09 |
신테카바이오와 파킨슨 치료제 공동개발 연구 협정 |
신테카바이오 |
|
2016.10 |
KM-819(파킨슨치료제) 임상1상 IND 승인 및 개시 |
|
| 2017.01 | 부설연구소(대전) 신설 | |
| 2017.10 | University of California San Diego 와 '파킨슨병 치료제 공동연구 계약" 체결 | University of California San Diego |
| 2017.10 | KM-819 임상 1상 완료 | |
| 2018.01 | 미국 현지법인(FAScinate Therapeutics,Inc) 설립 | |
| 2018.01 | 유성은 각자 대표이사 선임 | |
| 2018.05 | Parkinson's Institute and Clinical Center 와 '파킨슨병 치료제 공동연구 계약'체결 | |
| 2018.10 | 에이즈치료제 중국 임상 3상 돌입 | |
| 2019.05 | 기술성평가 통과 | |
| 2019.11 | 회사합병결정; 코스닥 예비심사청구 | 하나금융11호기업인수목적 주식회사 |
| 2020.02 | 한국거래소 코스닥시장 상장예비심사결과 승인 | |
| 2020.06 | 합병신주의 코스닥 상장 | |
| 2020.06 | 대표이사 변경(이기섭, 유성은 각자대표 -> 이기섭 대표) | 유성은 대표의 사내이사직 사임 |
| 2020.11 | KM-819(파킨슨병 치료제) 임상1상b IND 승인 및 개시 | 美FDA |
| 2021.04 | KM-819(다계통위축증 치료제) 임상2상 IND 제출 | 한국 식품의약품안전처 |
| 2021.06 | 에이즈치료제 중국 NDA 승인 | |
| 2021.10 | KM-819(파킨슨병 치료제) 미국임상2상 IND 제출 | 美FDA |
|
2021.10 |
KM-819(다계통위축증 치료제) 국내임상2상 IND승인 |
한국 식품의약품안전처 |
| 2021.11 | KM-819(파킨슨병 치료제) 미국임상2상 IND승인 | 美FDA |
나. 회사의 본점 소재지 및 그 변경
당사는 설립 후 현재까지의 본점소재지의 변경은 아래와 같습니다.
|
일시 |
본점소재지 |
|---|---|
|
2007.06.15 |
서울특별시 강남구 역삼동 824 12 메가시티오피스텔 1502호 |
|
2007.07.03 |
서울특별시 강남구 역삼동 708-22 닷컴빌딩 6층 |
|
2007.12.11 |
서울특별시 강남구 대치동 889-51 프레티늄빌딩 2층 |
|
2008.04.30 |
서울특별시 강남구 대치동 889-51 프레티늄빌딩 |
|
2010.12.31 |
서울특별시 송파구 풍납동 388-1 |
|
2014.08.13 |
경기도 성남시 중원구 둔촌대로 541번길 29, 3층(상대원동, 동방렌탈빌딩) |
|
2016.01.27 |
경기도 성남시 분당구 대왕판교로712번길 16, 4층(삼평동, 한국파스퇴르연구소) |
| 2020.12.16 | 경기도 성남시 중원구 둔촌대로541번길 29, 3층(상대원동) |
| 2022.01.01 | 경기도 성남시 분당구 판교역로 184 JS타워 1101호 |
다. 경영진 및 감사의 중요한 변동
| 변동일자 | 주총종류 | 선임 | 임기만료 또는 해임 |
|
|---|---|---|---|---|
| 신규 | 재선임 | |||
| 2020년 06월 30일 | - | - | - | 유성은 각자대표이사 사임 주1) |
| 2020년 02월 15일 | 임시주총 | 2 | - | 배종덕 감사 사임 |
| 2021년 02월 16일 | - | - | - | 유성근 사외이사 사임 주2) |
주1) SPAC 합병에 따라 법적 실체인 하나금융11호기업인수목적 주식회사의 기존 임원인 남강욱, 이윤형, 권승택, 오광준, 김경은 합병 등기일인 2020년 5월 20일부로전원 사임하였습니다.
주2) 유성근 사외이사도 2021년 02월 16일부로 사임하였습니다.
라. 최대주주의 변동
최대주주의 변동은 법률적 존속법인인 하나금융11호기업인수목적 주식회사를 기준으로 작성하였습니다. 하나금융11호기업인수목적 주식회사는 소멸법인인 주식회사 카이노스메드의 기명식 보통주식 및 우선주식 1주에 대하여 하나금융11호기업인수목적 주식회사의 기명식 보통주식 및 우선주식 6.9000주를 교부하였습니다. 소멸법인이지만 경제적 실체인 주식회사 카이노스메드의 최대주주 변동사항은 없습니다.
| 일자 | 변경 전 | 변경 후 | 비고 |
| 2020.5.20 | (주)에이씨피씨 | 이기섭 외 12인 | 합병에 따른 최대주주 변경 |
*이기섭 외 12인은 소멸법인의 최대주주였습니다.
마. 상호의 변경
흡수합병에 따른 존속법인의 상호는 아래와 같이 변경되었으나, 경제적 실체인 소멸법인 주식회사 카이노스메드는 변동이 없습니다.
| 일자 | 변경 전 | 변경 후 | 비고 |
| 2020.5.20 | 하나금융11호기업인수목적 주식회사 | 주식회사 카이노스메드 | 합병에 따른 상호 변경 |
바. 회사 합병 등을 한 경우 그 내용
당사는 하나금융11호기업인수목적 주식회사와 2020년 2월 18일부터 3월 27일에 걸쳐 합병계약을 체결하였으며, 2020년 5월 20일(합병등기일) 합병을 완료하였습니다.
1)합병 당시 회사의 개요
| 구분 | 합병회사 (실질 피취득회사) | 피합병회사 (실질 취득회사) |
|---|---|---|
| 회사명 | 하나금융11호기업인수목적 주식회사 | 주식회사 카이노스메드 |
| 대표이사 | 남강욱 | 이기섭, 유성은(각자대표) |
| 본점소재지 | 서울특별시 영등포구 의사당대로 82 | 경기도 성남시 분당구 대왕판교로712번길 16, 4층(삼평동, 한국파스퇴르연구소) |
| 법인구분 | 코스닥 상장법인 | 코넥스 상장법인 |
2) 합병 진행 경과
| 구분 | 일자 |
|---|---|
| 이사회 결의, 합병 계약일 | 2019년 11월 29일 |
| 합병승인을 위한 주주총회일 | 2020년 4월 16일 |
| 합병기일 | 2020년 5월 19일 |
| 합병등기일 | 2020년 5월 20일 |
3) 합병비율 및 교부
| 구분 | 합병회사 (실질 피취득회사) | 피합병회사 (실질 취득회사) |
|---|---|---|
| 회사명 | 하나금융11호기업인수목적 주식회사 | 주식회사 카이노스메드 |
| 합병비율 | 1 | 6.9000000 |
법률적 합병회사인 하나금융11호기업인수목적 주식회사는 주식회사 카이노스메드 기명식 보통주식 및 우선주식 1주에 대하여 하나금융11호기업인수목적 주식회사의 기명식 보통주식 및 우선주식(액면가 : 100원) 6.9000000주를 교부했 습니다. 이로 인하여 하나금융11호기업인수목적 주식회사는 주식회사 카이노스메드의 주주에 대하여 기명식 보통주식 97,057,042주, 기명식 우선주식 316,516주의 신주를 발행하였습니다.
사. 회사의 업종 또는 주된 사업의 변화
합병에 의한 실질 취득회사인 주식회사 카이노스메드는 보고서 제출일 현재 해당사항이 없습니다.
아. 그 밖에 경영활동과 관련된 중요한 사항의 발생내용
합병에 의한 실질 취득회사인 주식회사 카이노스메드는 동 분기보고서 제출일 현재 해당사항이 없습니다.
3. 자본금 변동사항
가.자본금 변동추이
| (단위 : 원, 주) |
| 종류 | 구분 | 6기 (당분기말) |
5기 (전기말) |
4기 (전전기말) |
3기 (2019년말) |
2기 (2018년말) |
1기 (2017년말) |
|---|---|---|---|---|---|---|---|
| 보통주 | 발행주식총수 | 110,398,262 | 110,289,803 | 104,942,629 | 5,401,000 | 5,401,000 | 901,000 |
| 액면금액 | 100 | 100 | 100 | 100 | 100 | 100 | |
| 자본금 | 11,039,826,200 | 11,028,980,300 | 10,494,262,900 | 540,100,000 | 540,100,000 | 90,100,000 | |
| 우선주 | 발행주식총수 | - | - | - | - | - | - |
| 액면금액 | - | - | - | - | - | - | |
| 자본금 | - | - | - | - | - | - | |
| 기타 | 발행주식총수 | - | - | - | - | - | - |
| 액면금액 | - | - | - | - | - | - | |
| 자본금 | - | - | - | - | - | - | |
| 합계 | 자본금 | 11,039,826,200 |
11,028,980,300 | 10,494,262,900 | 540,100,000 | 540,100,000 | 90,100,000 |
- 당사는 주식병합(액면가 100원의 보통주 5주 -> 액면가 500원의 보통주 1주)을 2022.04.11 이사회, 2022년 05.23 임시주주총회에서 승인한 바 있습니다. 자세한 내용은 2022.04.11 "주식병합결정" 공시를 참고해주시기 바랍니다.
4. 주식의 총수 등
가. 주식의 총수 현황
| (기준일 : | 증권신고서 제출 전일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 비고 | |||
|---|---|---|---|---|---|
| 보통주 | 우선주 | 합계 | |||
| Ⅰ. 발행할 주식의 총수 | 300,000,000 | - | 300,000,000 | - | |
| Ⅱ. 현재까지 발행한 주식의 총수 | 110,565,888 |
- | 110,565,888 |
- | |
| Ⅲ. 현재까지 감소한 주식의 총수 | - | - | - | - | |
| 1. 감자 | - | - | - | - | |
| 2. 이익소각 | - | - | - | - | |
| 3. 상환주식의 상환 | - | - | - | - | |
| 4. 기타 | - | - | - | - | |
| Ⅳ. 발행주식의 총수 (Ⅱ-Ⅲ) | 110,565,888 | - | 110,565,888 | - | |
| Ⅴ. 자기주식수 | 11,511 | - | 11,511 | - | |
| Ⅵ. 유통주식수 (Ⅳ-Ⅴ) | 110,554,377 | - | 110,554,377 | - | |
- 당사는 주식병합(액면가 100원의 보통주 5주 -> 액면가 500원의 보통주 1주)을 2022.04.11 이사회, 2022년 05.23 임시주주총회에서 승인한 바 있습니다. 자세한 내용은 2022.04.11 "주식병합결정" 공시를 참고해주시기 바랍니다.
나. 자기주식 취득 및 처분 현황
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 주) |
| 취득방법 | 주식의 종류 | 기초수량 | 변동 수량 | 기말수량 | 비고 | ||||
|---|---|---|---|---|---|---|---|---|---|
| 취득(+) | 처분(-) | 소각(-) | |||||||
| 배당 가능 이익 범위 이내 취득 |
직접 취득 |
장내 직접 취득 |
- | - | - | - | - | - | - |
| - | - | - | - | - | - | - | |||
| 장외 직접 취득 |
- | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 공개매수 | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 소계(a) | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 신탁 계약에 의한 취득 |
수탁자 보유물량 | - | - | - | - | - | - | - | |
| - | - | - | - | - | - | - | |||
| 현물보유물량 | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 소계(b) | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 기타 취득(c) | 보통주 | 0 | 11,511 | 0 | 0 | 11,511 | (주1) | ||
| - | - | - | - | - | - | - | |||
| 총 계(a+b+c) | 보통주 | 0 | 11,511 | 0 | 0 | 11,511 | (주1) | ||
| - | - | - | - | - | - | - | |||
(주1) 합병과정에서 주주의 주식매수청구구권 행사로 취득한 자기주식입니다.
5. 정관에 관한 사항
당사 정관의 최근 개정일은 2022년 05월 23일입니다. 또한, 보고서 제출일 현재 안건으로 상정하였거나 상정 예정인 정관의 변경 예정사항은 없습니다.
가. 정관 변경 이력
| 정관변경일 | 해당주총명 | 주요변경사항 | 변경이유 |
|---|---|---|---|
| 2022년 05월 23일 | 제6기 임시주주총회 | 액면가 변경(100원 → 500원) | 적정 유통 주식수 유지를 통한 주가 안정화 및 기업가치 제고 |
II. 사업의 내용
1. 사업의 개요
당사는 인간의 불치병, 난치병, 삶의 질 개선을 위한 혁신적인 신약을 연구하고 이를 적정 개발단계의 신약후보물질로 License-Out 함으로써 수익을 창출하는 것을 사업으로 영위하고 있습니다.
당사가 현재 개발중인 프로젝트들을 타겟 시장(질환)별로 분류해보면 뇌질환(파킨슨치료제), 항바이러스(에이즈치료제), 항암제(IRAK4, FAF1-exosome 등) 등으로 분류할 수 있으며, 당사는 현재 적적한 치료약물이 없는 질환들을 대상으로 합성의약 및 바이오의약들을 개발하고 있습니다.
파킨슨병 치료제는 미국 자회사(FASCINATE)를 통해 미국 FDA 임상 2상 IND승인을 받고 임상2상의 1단계를 준비중에 있습니다. 다계통위축증 치료제는 국내 식약처에서 임상2상 IND승인을 받고 실행을 준비하고 있습니다.
에이즈 치료제는 중국 파트너사인 장수아이디로 기술이전한 이래, 중국에서 신약승인을 받고 마케팅 및 판매를 하고 있습니다.
산업 및 시장 등에 관한 자세한 사항은 "7. 기타 참고사항"을 참조하시기 바랍니다.
2. 주요 제품 및 서비스
가. 주요 제품 등의 현황
|
(단위 : 천원,%) |
|
품 목 |
매출액(비율) |
주요상표 |
제 품 설 명 |
|||
|---|---|---|---|---|---|---|
|
2019년 |
2020년 |
2021년 |
2022년 1분기 |
|||
| 라이센스아웃 | - | - | 4,005,766 | - | - | KM819,IRAK4 기술이전 |
| 기타 | - | - | 7,260 | 3,667 | - | 기타 |
| 총합계 | - | - | 4,013,026 | 3,667 | - | - |
- 비율은 전년도, 전전년도 매출액이 발생하지 않아 비율을 정할 수 없어 작성하지 않았습니다.
당사는 퇴행성 뇌질환 치료제, 항바이러스제, 항암제 개발에 주력하고 있습니다. 이중 파킨슨병 치료제(KM819)는 미국에서 임상2상 단계 개발중이며, 동 물질로 다계통 위축증(MSA) 질환을 대상으로 한국에서 임상2상을 개발하고 있습니다. 당사는 KM819를 글로벌 시장에 경쟁력을 가진 약물로 개발하고, 글로벌 제약사로의 기술이전을 보다 높은 가치로 진행하기 위하여 현재 자회사인 FAScinate(미국)가 미국에서 임상을 실시하고 있습니다. 이 물질은 심부전 치료제 영역으로도 확장할 수 있는 권리도 확보하고 있기 때문에 다양한 질환으로의 확장성과 잠재력을 가진 약물이라고 할 수 있습니다.
에이즈 치료제(KM023)는 중국으로 기술이전을 완료하였고, 중국의 장수아이디社에서 2021년 NDA 승인 후 올해 판매가 이루어질 예정입니다.
또한, 초기단계에서 개발하고 있는 항암제(IRAK4)는 백혈병, 림프종 등과 같은 혈액암을 주로 타겟으로 하는 약물로, 미국 Emmaus와 2021년 공동연구개발 계약을 체결하고, 타겟 시장을 보다 명확히 하여 기술이전을 완료하였습니다. Emmaus는 미국, 유럽의 지역의 상업적 권리를 확보하고, 해당 지역내 상용화를 추진할 예정이며, 당사는 그 외 지역에서 연구개발 및 상용화를 추진할 예정입니다.
2021년 당사는 FAF1-exosome 형태의 약물을 활용하여 초기 후보물질 창출 연구 단계에서 연구중에 있습니다. 최근 초기 물질 확보 연구를 완료하고 특허를 준비중에 있습니다.
당사의 전체 연구개발제품 현황은 다음과 같습니다.
|
프로젝트 |
타겟 단백질 /작용기전 |
타겟 질환 |
개발단계 |
|
파킨슨병 치료제 (KM-819) |
FAF1 저해, 세포사멸 저해 및 알파시누클라인 축적 저해 |
파킨슨병 |
임상2상(미국) |
|
다계통위축증 (KM-819) (주1) |
다계통위축증 |
임상 2상(한국) |
|
|
심부전 치료제 (KM-819) (주1) |
FAF1 저해 |
심부전 |
전임상 연구 |
|
에이즈 치료제 (KM023) |
HIV Reverse transcriptase 저해 |
에이즈 |
NDA 승인(중국) |
|
세포독성 항암제 (KM-630) |
DNA 합성 억제 |
혈액암/고형암 |
전임상 독성연구 |
|
에피제네틱스 항암제 (KM-635) |
BRD4 저해 |
혈액암/고형암 |
임상 1상 진행 |
|
PD-L1 (면역항암제) |
PD-L1 저해 |
Melanoma/ Lung cancer |
후보물질 최적화 |
|
CD73 (면역항암제) |
CD73 저해 |
Melanoma/ Lung cancer/ Ovarian cancer |
선도물질 최적화 |
|
혈액항암제 (KM-10544) |
IRAK4 저해 |
암 |
후보물질 최적화 |
| FAF1-Exosome (KM-1004) (주2) | FAF1 과발현 유도 항암제 | 암 | 후보물질 개발중 |
| 주1) 다계통위축증, 심부전치료제는 KM-819(파킨슨병치료제)물질의 적응증 확대로 개발 중인 프로젝트 입니다. |
| 주2) IRAK4 저해 약물인 항암치료제 KM-10544는 2021년 10월 미국 엠마우스라이프사이언스(Emmaus life Science, Inc.)에 기술이전되어, 미국 내에서 임상 준비를 위한 전임상 연구 중에 있습니다. |
나. 주요 제품의 가격변동 추이
당사의 주요 매출은 당사가 개발한 후보물질에 대한 기술이전 및 마일스톤 등의 수취를 통해 발생되고 있으며, 현재 제품 출시가 완료되어 판매되고 있는 제품은 없습니다. 따라서 제품의 가격변동 추이를 명확히 기재할 수 없으며, 각 과제별 기술이전에 대한 기대가치는 당사 후보물질의 약효 및 안전성 등에 대한 차별적 장점 보유 여부, 글로벌제약사의 수요 정도, 경쟁상태, 시장규모, 예상 시장점유율 등의 다양한 요인에 의하여 결정되므로 쉽게 예측하기 어렵습니다.
그럼에도 불구하고 기존 기술이전 사례나 최근 시장동향 등을 고려하여 일반적으로 개발단계가 진행될수록 성공확률이 높아지며 계약규모가 기하급수적으로 커질 가능성이 높습니다.
3. 원재료 및 생산설비
당사의 주요 영업활동은 신약연구개발로서 제품 제조를 위한 별도의 원재료 매입 및 생산설비 등에 관한 해당사항이 없습니다.
4. 매출 및 수주상황
가. 매출실적
당사는 혁신의약품을 시장에 출시하기 전인 임상개발 및 연구개발 단계에 있기 때문에 현재까지 제품이나 상품의 판매를 통한 매출 및 관련 매출원가가 사실상 발생하지않으며, 기술이전 마일스톤에 따른 계약금 기술료 또는 로열티 매출이 발생합니다.
나. 판매경로 및 판매전략
(1) 판매조직
당사의 판매대상 제품은 신약연구개발 후보물질로서 후보물질 도출단계에서 임상2상 사이의 적정한 단계에서 국내제약사 및 글로벌제약사에 기술이전 하는 것입니다.
당사는 이기섭 대표이사와 이재문 사내이사를 중심으로 사업개발 부서를 통해 기술이전 또는 전략적 제휴를 지속적으로 진행해 오고 있습니다. 또한 미국, 유럽의 시장진출을 위한 미국 현지법인 설립 및 중국의 파트너사와의 네트워크 유지, 공동연구 개발 진행, 외부 기술이전 컨설팅사 관리 및 공동 업무, 국내외 기술이전 대상 업체 파트너링 계약을 포함한 모든 기술이전 프로세스 진행을 담당하는 부서를 운영하고 있습니다.
(2) 판매경로
당사의 매출발생은 기술이전을 통해서 이루어지며, 당사는 라이선스 아웃을 위한 국내외 제약회사를 대상으로 학회, 전시회 및 비즈니스 파트너링 행사 등 기술 교류의 장을 통한 지속적 개발 업데이트와 교류활동을 하고 있습니다.
당사의 기술이전시 아래와 같은 과정을 거치게 됩니다. 당사 신약개발 물질에 대한 데이터 및 경쟁사 대비 경쟁력을 분석, 상업화 전략을 수립하며, Non-Confidential, Confidential 자료를 제작하여 잠재고객의 관심도에 따라 지속적으로 업데이트를 합니다. 잠재 고객군 확보 후 당사의 물질에 대한 관심이 높으면, Confidential 자료를 제공하게 되는데, 이에 앞서 양사간 비밀유지협약을 체결하게 됩니다. 이 단계에서는 confidential 자료 제공과 함께 자료검증에 관한 실사도 진행됩니다.
|
기술에 대한 실사가 완료되어 기술이전이 더 진전될 경우, 양사는 기술이전에 대한 주요 계약사항을 협의하게 됩니다. 이후 세부 계약사항을 조율하고 확정하여 계약체결을 완료하게 됩니다.
(3) 판매전략
당사는 전략적 기술이전을 통하여 파트너 확보와 공동연구를 진행하고 있습니다. 당사의 기술이전 시점을 후보물질 및 초기 임상개발 완료 단계에서 이루어지며, 공동연구, 기술제휴를 통하여 미래의 전략적 파트너를 확보하고 있습니다. 연구개발을 통해 확보된 기술을 더욱 높은 가치로 효과적으로 판매하기 위해 사업개발 부서의 조직의 전문성을 강화하여 사업성과로 인한 이익실현을 앞당기고 협상의 역량을 높여 매출실적을 확대해 나아갈 것입니다.
더불어 당사의 과학기술자문위원회(SAB)의 전문적 기술 네트워킹을 확대해 기술이전의 가능성을 높이고 개발 물질의 유효성과 경쟁력을 각종 전문학술 학회와 비즈니스 컨퍼런스를 통해 높은 우수성을 입증하고 당사의 인지도 및 기술력을 높이는 기회의 창구로 활용하고 있으며, 리스크 최소화를 하기 위해서 각 분야의 전문가(변호사, 변리사 등)들의 자문 및 역량을 강화하여 기술이전을 위한 전략을 수립하여 성공적 기술 사업화 활동을 지속하고 있습니다.
다. 수주 상황
당사와 같은 기술이전을 주 수익모델로 하는 신약연구개발 회사의 경우 일반 제조업이나 용역업체와 같은 수주는 발생하지 않습니다.
5. 위험관리 및 파생거래
당사는 금리위험, 가격위험, 환위험 등 다양한 시장위험에 노출되어 있습니다. 당사는 이러한 위험요소들을 관리하기 위하여 각각의 위험요인에 대해 면밀하게 모니터링하고 대응하는 위험관리 정책을 운용하고 있습니다.
가. 위험관리
(1) 금융위험 관리
1) 위험관리 체계
당사의 위험관리 체계를 구축하고 감독할 책임은 이사회에 있습니다. 당사의 위험관리 정책은 당사가 직면한 위험을 식별하고, 적절한 위험 한계치 및 통제를 설정하며, 위험이 한계치를 넘지 않도록 하기 위해 수립되었습니다. 위험관리 정책과 시스템은 시장 상황과 당사의 당사 활동의 변경을 반영하기 위해 정기적으로 검토되고 있습니다. 당사는 훈련 및 관리기준, 절차를 통해 모든 종업원들이 자신의 역할과 의무를 이해할 수 있는 엄격하고 구조적인 통제환경을 구축하는 것을 목표로 하고 있습니다.
2) 시장위험
시장위험이란 시장가격의 변동으로 인하여 금융상품의 공정가치나 미래현금흐름이 변동할 위험을 의미합니다. 시장가격 관리의 목적은 수익은 최적화하는 반면 수용가능한 한계 이내로 시장위험 노출을 관리 및 통제하는 것입니다.
① 외환위험
연결회사의 외환위험은 주로 인식된 자산과 부채의 환율변동과 관련하여 미래 예상거래 및 인식된 자산ㆍ부채가 기능통화 외의 통화로 표시될 때 발생하고 있습니다.
당기말과 전기말 현재 기능통화 이외의 외화로 표시된 화폐성 자산 및 부채의 장부금액은 다음과 같습니다.
| (외화단위: USD, 원화단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 외 화 | 제 6(당분기) 기 1분기 | 제 5(전) 기 | ||
| 외화금액 | 원화금액 | 외화금액 | 원화금액 | ||
| 외화자산: | |||||
| 현금및현금성자산 | USD | 885,721 | 1,072,432 | 1,235,845 | 1,465,094 |
당기말과 전기말 현재 다른 모든 변수가 일정하고 각 외화에 대한 원화의 환율이 10% 변동시 연결회사의 세전이익 및 자본에 미치는 영향은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 외 화 | 제 6(당분기) 기 1분기 | 제 5(전) 기 | ||
| 10% 상승시 | 10% 하락시 | 10% 상승시 | 10% 하락시 | |
| USD | 107,243 | (107,243) |
146,509 |
(146,509) |
② 이자율위험
이자율위험은 시장이자율의 변동으로 인하여 금융상품의 공정가치나 미래현금흐름
이 변동할 위험입니다.
③ 신용위험
신용위험은 보유하고 있는 수취채권에 대한 신용위험 뿐 아니라, 현금및현금성자산,
금융기관 예치금으로부터 발생하고 있습니다. 이러한 위험을 줄이기 위하여 연결회
사는 신용도가 높은 거래처 및 금융기관들에 대해서 거래를 하고 있습니다.
당기말과 전기말 현재 신용위험에 대한 최대 노출정도는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당분) 기 1분기 |
제 5(전) 기 |
|
현금및현금성자산 |
18,553,535 |
23,230,922 |
|
단기금융상품 |
13,000,000 |
11,000,000 |
|
파생상품자산 |
309,735 |
309,735 |
|
매출채권및기타채권 |
163,203 |
300,888 |
|
유동당기손익-공정가치측정금융자산 |
- |
- |
|
장기매출채권및기타채권 |
185,244 |
179,668 |
|
비유동당기손익-공정가치측정금융자산 |
1,248,187 |
642,787 |
| 합 계 |
33,459,904 |
35,664,000 |
④ 유동성 위험
연결회사는 매 6개월 및 1년 단위로 자금수지계획을 수립함으로써 영업활동, 투자활동, 재무활동에서의 자금수지를 미리 예측하고 있으며, 이를 통해 필요한 유동성 규모를 사전에 확보하고 유지하여 향후에 발생할 수 있는 유동성 리스크를 사전에 관리하고 있습니다. 또한, 신중한 유동성 위험관리는 충분한 현금성자산 및 금융상품의 유지, 적절히 약정된 신용한도금액으로부터의 자금 여력 등을 포함하고 있습니다.
당기말과 전기말 현재 유동성 위험 분석내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 장부금액 | 계약상현금흐름 | 1년 미만 | 1년 ~ 5년 |
| 당기말: | ||||
|
미지급금및기타채무 |
625,720 |
625,720 |
625,720 |
- |
|
전환사채 |
12,467,965 |
20,403,520 |
20,403,520 |
- |
|
리스부채 |
292,825 |
314,245 |
235,914 |
78,331 |
|
단기차입금 |
2,285,014 |
2,285,014 |
2,285,014 |
- |
|
우선주부채 |
3,632,400 |
3,632,400 |
- |
3,632,400 |
|
합 계 |
19,303,924 |
27,260,899 |
23,550,168 |
3,710,731 |
| 전기말: | ||||
|
미지급금및기타채무 |
846,101 |
846,101 |
846,101 |
- |
|
전환사채 |
12,467,965 |
20,403,520 |
20,403,520 |
- |
|
리스부채 |
380,217 |
410,983 |
288,871 |
122,112 |
| 장기차입금 |
1,523,343 |
1,523,343 |
- |
1,523,343 |
|
우선주부채 |
3,556,500 |
3,556,500 |
- |
3,556,500 |
|
합 계 |
18,774,126 |
26,740,447 |
21,538,492 |
5,201,955 |
(2) 자본위험 관리
자본관리의 주 목적은 연결회사의 영업활동을 유지하고 주주가치를 극대화하기 위하여 높은 신용등급과 건전한 자본비율을 유지하기 위한 것입니다. 연결회사의 자본구조는 부채총계에서 현금및현금성자산 등을 차감한 순부채와 자본으로 구성되며, 전반적인자본위험 관리 정책은 전기와 동일합니다.
당기말과 전기말 현재 연결회사의 부채비율은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당분기) 기 1분기 | 제 5(전) 기 |
|
부채총계(A) |
27,789,772 |
27,356,580 |
|
자본총계(B) |
11,682,027 |
14,600,182 |
|
부채비율(A/B) |
237.88% |
187.37% |
나. 파생거래
(1) 파생상품 거래 현황
당사는 현재 별도로 보유하고 있는 파생상품은 없습니다.
6. 주요계약 및 연구개발활동
가. 라이선스아웃(License-out) 계약
|
라이선스아웃 계약 총괄표 |
|
(외화단위: USD) |
|
품목 |
계약상대방 |
대상지역 |
계약체결일 |
계약종료일 |
총 계약금액* |
수취금액* |
진행단계 |
|---|---|---|---|---|---|---|---|
|
에이즈치료제 |
Jiangsu Aidea Pharmaceutical |
중국, 홍콩, 대만 |
2014.10.10 |
특허 만료일 |
USD 1,700,000 |
USD 1,700,000 |
NDA승인, |
|
항암제 |
Jiangsu Aidea Pharmaceutical |
중국, 홍콩, 대만 |
2015.12.10 |
특허 만료일 |
USD 1,500,000 |
USD 1,500,000 |
임상 1상 진행 |
|
항암제 |
Jiangsu Aidea Pharmaceutical |
중국, 홍콩, 대만 |
2015.12.10 |
특허 만료일 |
USD 2,500,000 |
USD 1,000,000 |
전임상 |
|
대사질환치료제 |
CROWN BIO |
전세계 |
2014.07.22 |
특허 만료일 |
USD 3,600,000 |
- |
전임상 |
| 뇌신경질환 치료제 (KM819) |
FAScinate Therapeutics | 전세계 (한국 제외) |
2021.09.27 | 특허 만료일 | USD 2,000,000 | USD 2,000,000 | 임상2상 진행 (미국) |
| 항암제 (KM-10544) |
Emmaus Life Science, Inc. | 미국, 유럽, 영국 | 2021.10.06 | 특허 만료일 | USD 1,500,000 | USD 1,500,000 | 전임상 진행 |
(1) 에이즈 치료제(KM-023)
|
계약상대방 |
Jiangsu Aidea Pharmaceutical (중국) |
|
계약 내용 |
Jiangsu Aidea Pharmaceutical은 에이즈치료제(KM-023)에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
중국, 홍콩, 대만 |
|
계약 기간 |
계약체결일: 2014.10.10 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 1,700,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 1,700,000 - 수취조건: 계약 체결시 마일스톤(Milestone) - 해당사항 없음 로열티(Royalty): 단일정을 포함한 복합제제 매출액의 2% - 수취조건: 매출 발생시 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
|
회계처리방법 |
계약금 수취액 USD 200,000은 2014년 10월 ~ 2015월 09월까지 12개월 동안 분할하여 수익인식 USD 1,500,000은 2017년 12월 일시 수익 인식 |
(2) 항암제(KM-635)
|
계약상대방 |
Jiangsu Aidea Pharmaceutical (중국) |
|
계약 내용 |
Jiangsu Aidea Pharmaceutical은 항암제(KM-635)에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
중국, 홍콩, 대만 |
|
계약 기간 |
계약체결일: 2015.12.10 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 1,500,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 1,500,000 - 수취조건: 계약 체결시 마일스톤(Milestone) - 해당사항 없음 로열티(Royalty): 순매출액의 10% - 수취조건: 매출 발생시 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
|
회계처리방법 |
계약금 수취액 USD 1,000,000은 2015년 12월 ~ 2016년 11월까지 12개월 동안 분할하여 수익인식 USD 500,000은 2017년 12월 일시 수익 인식 |
(3) 항암제(KM-630)
|
계약상대방 |
Jiangsu Aidea Pharmaceutical (중국) |
|
계약 내용 |
Jiangsu Aidea Pharmaceutical은 항암제(KM-630)에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
중국, 홍콩, 대만 |
|
계약 기간 |
계약체결일: 2015.12.10 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 2,500,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 1,000,000 - 수취조건: 계약 체결시 마일스톤(Milestone) - Upon Initiation of Phase 2 Clinical Trial USD 500,000, Initiation of Phase 3 Clinical Trial USD 500,000, Regulatory approval by SFDA USD 500,000 로열티(Royalty): 순매출액의 10% - 수취조건: 매출 발생시 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
|
회계처리방법 |
계약금 수취액 USD 1,000,000은 2015년 12월 ~ 2016년 11월까지 12개월 동안 분할하여 수익인식 |
(4) 대사질환 치료제
|
계약상대방 |
CROWN BIO (중국) |
|
계약 내용 |
CROWN BIO는 대사질환 치료제에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
전세계 |
|
계약 기간 |
계약체결일: 2014.07.22 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 3,600,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): - 해당사항 없음. 마일스톤(Milestone): USD 3,600,000 - 수취조건: 중국 임상 1상 개시 USD 100,000, 중국 임상 2상 개시 USD 500,000, 중국 임상 3상 개시 USD 1,000,000, 중국 의약품허가 USD 2,000,000 로열티(Royalty): 순매출액의 10% - 수취조건: 매출 발생시 재실시권 수익 분배비율: 각 단계별 지분율 IND (50%), 임상 1상 (40%), 임상 2상 (25%), 임상 3상 (10%)
|
|
회계처리방법 |
- |
(5) 뇌신경계 치료제(KM-819)
|
계약상대방 |
FAScinate Therapeutics Inc. |
|
계약 내용 |
FAScinate Therapeutics는 뇌신경계 치료제에 대한 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
전세계 (한국 제외) |
|
계약 기간 |
계약체결일: 2021.09.27 계약종료일: 특허 만료일 기준 |
|
총 계약금액 |
USD 2,000,000, 로열티 별도 |
|
계약조건 |
계약금(Upfront payment): USD 2,000,000 - 해당사항 없음 로열티(Royalty): 순매출액의 10%
|
|
회계처리방법 |
USD 2,000,000은 2021년 9월 일시 수익 인식 |
(6) 표적항암제 (IRAK4 저해제)
- IRAK4 저해제의 경우, 엠마우스라이프 사이언스와 공동연구개발 계약에 이어 기술이전으로까지 확장되여 계약이 체결되었습니다.
|
계약상대방 |
엠마우스라이프사이언스(Emmaus life Science, Inc.) (미국) |
|
공동연구/기술이전 계약 내용 |
공동연구: IRAK4 저해제에 대한 치료작용기전(MOA) 연구, 전임상연구 등에 관한 공동연구개발 계약 |
|
공동연구/기술이전 |
공동연구 계약체결일: 2021.03.02 ~ 기술이전과 동시에 계약 종료 |
|
총 계약금액 |
공동연구 계약시: USD 1,000,000 (50% 현금 수취, 50%는 계약상대방의 주식 수취) |
|
계약조건 |
계약금(Upfront payment): USD 1,000,000 (50% 현금 수취, 50%는 계약상대방의 주식 수취)
|
|
회계처리방법 |
기술이전과 동시에 공동연구개발 계약 및 기술이전에 따른 계약금을 2021.10.06에 일시에 수익 인식 |
나. 라이선스인(License-in) 계약
현재 당사가 체결한 라이선스인(License-in) 계약의 현황은 다음과 같습니다.
|
[라이선스인 계약 총괄표] |
|
(원화단위: 백만원, 외화단위: 1USD) |
|
품목 |
계약상대방 |
대상지역 |
계약체결일 |
계약종료일 |
총 계약금액* |
지급금액 |
진행단계 |
|---|---|---|---|---|---|---|---|
|
파킨슨병 치료제(KM-819) |
한국화학연구원/충남대학교산학협력단 |
대한민국포함 전세계 |
2015.09.24 |
2028.02.29 |
1,800 |
200 |
임상1b상 진행 |
|
에이즈 치료제 (KM-023) |
한국화학연구원 |
대한민국포함 전세계 |
2012.11.07 |
2029.01.19 |
USD 7,520,000 |
USD 520,000 |
임상 3상 |
|
항암제(KM-10544) |
충남대학교 산학협력단 |
대한민국포함 전세계 |
2018.11.14 |
IND 승인취득 시기 |
150 |
50 |
후보물질 창출 |
| 항암제(FAF1-exosome) | 엠디뮨 | 대한민국포함 전세계 | 2021.10.28 | 특허만료일까지 | 900 | 100 | 후보물질 창출 |
(1) 파킨슨병 치료제(KM-819)
|
계약상대방 |
한국화학연구원/충남대학교 산학협력단 |
|
계약 내용 |
FAF1을 표적으로 하는 허혈성 질환치료제의 전용실시권을 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
대한민국 포함 전세계 |
|
계약 기간 |
계약체결일: 2015.09.24 계약종료일: 2028.02.29(특허 만료일 기준) |
|
총 계약금액 |
1,800백만원, 로열티는 별도 |
|
계약조건 |
계약금(Upfront payment): 200백만원 - 지급조건: 계약 체결시 마일스톤(Milestone): 1,600백만원 - 지급조건: In vivo imaging 연구완료 100백만원, 임상 2상 개시 300백만원, 임상 3상 개시 400백만원, NDA 제출 400백만원, KFDA 허가 400백만원 로열티(Royalty): 순매출액의 4% - 지급조건: 매출 발생시 재실시료: 계약일로부터 임상1상 완료까지 30%, 임상 2상 개시부터 임상 2a 상 완료까지 20%, 임상 2b상 개시부터 임상 2상 완료까지 15%, 임상 3상 개시부터 임상 3상 완료까지 10% (※배분대상이 되는 재실시에 의한 기술료에는 경상 기술료도 포함됨). 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
(2) 에이즈 치료제(KM-023)
|
계약상대방 |
한국화학연구원 |
|
계약 내용 |
에이즈 치료제로 NNRTI타겟의 KM-023의 재실시 가능한 전용실시권 갖고 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
대한민국 포함 전세계 |
|
계약 기간 |
계약체결일: 2012.11.07 계약종료일: 2029.01.19 (특허 만료일) |
|
총 계약금액 |
USD 7,520,000, 로열티는 별도 |
|
계약조건 |
계약금(Upfront payment): USD 520,000 - 지급조건: 계약 체결시 마일스톤(Milestone): USD 7,000,000 초과 못함 - 지급조건: 임상 2상 완료 USD 1,000,000, 임상 3상 완료 USD 2,000,000, 미국에서 첫 판매 USD 4,000,000 - 지급분배비율 : 중국지역 마일스톤(Milestone) 지급 조건, 계약금의 10%, 마일스톤의 20% 로열티(Royalty) 지급 조건 : - 매출발생시 순매출액의 3%를 지급 - 단, 중국지역 로열티(Royalty) 지급 조건은 당사가 수령하는 Royalty의 30%를 지급. 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
(3) 항암제(KM-10544)
|
계약상대방 |
충남대학교 산학협력단 |
|
계약 내용 |
암 및 염증 치료를 위한 IRAKs및 TAK 저해제 개발 기술로 임상 시험, 허가, 생산, 상업화 등을 진행 |
|
대상 지역 |
대한민국 포함 전세계 |
|
계약 기간 |
계약체결일: 2018.11.14 계약종료일: 임상시험 승인취득 시기(마일스톤 종료시점) |
|
총 계약금액 |
150백만원, 로열티는 별도 |
|
계약조건 |
계약금(Upfront payment): 50백만원 - 지급조건: 계약 체결시 마일스톤(Milestone): 100백만원 - 지급조건: 임상 시험 승인을 취득하는 시기 본 계약에 따라 행해진 모든 지불은 여하한 이유라도 (기술수요자)에게 반환하지 않는다. |
(4) 항암제 (FAF1-Exosome)
- 본 계약은 공동연구개발 계약과 기술도입 계약을 동시에 체결하였습니다.
|
계약상대방 |
주식회사 엠디뮨 |
|
계약 내용 |
공동연구: FAF1탑재 CDV 생산 및 효능 평가/ 효능 비교 |
|
계약 기간 |
계약체결일: 2021.10.28 계약종료일: 특허만료일까지 |
|
총 계약금액 |
9억원 |
|
계약조건 |
계약금(Upfront payment): 4억원
|
다. 판매계약 및 기타계약
- 해당사항이 없습니다.
라. 연구개발활동
(1) 연구개발활동 개요
당사는 인간의 불치병, 난치병, 삶의 질 개선을 위한 혁신적인 신약을 연구하는 바이오 벤처회사입니다. 주로 퇴행성 뇌신경계 질환, 항바이러스, 항암제 등을 개발하고 있습니다. 당사의 신약개발을 위한 부설연구소에서는 자체 기초연구를 수행하면서, 한편으로 대학이나 기타 외부 연구소에서 검증된 연구 성과를 도입하여 추가 연구 및임상개발을 통해 가치를 극대화시키는 연구개발 활동을 수행하고 있습니다.
(2) 연구개발 조직
1) 연구개발 조직 개요
당사의 연구개발조직은 보고서 작성일 기준일, 대표이사 산하에 프로젝트 승인위원회를 중심으로 바이오의약연구본부, 임상개발본부, 헬스케어사업본부로 이루어져 있습니다. 바이오의약연구본부는 신약개발 프로젝트 기반으로 조직을 운영하고 있으며 각 프로젝트 책임자는 인력을 구성하여 프로젝트를 수행합니다. 이는 각 프로젝트의 특성을 고려하여 효율적이며 체계적인 관리 및 운영을 위해 도입된 시스템입니다.
당사의 주요 연구인력은 각 분야의 전문가로 구성되어 있으며, 신약개발 성공경험을 보유하고 있어 당사의 연구개발의 중요업무를 총괄하고 있습니다. 각 프로젝트의 책임자는 10년 이상의 연구개발 경험과 지식을 축적한 고급 전문 인력으로 의약품의 개발 단계과정에 있어 시기 적절한 의사결정을 내리는데 많은 도움이 되고 있습니다.
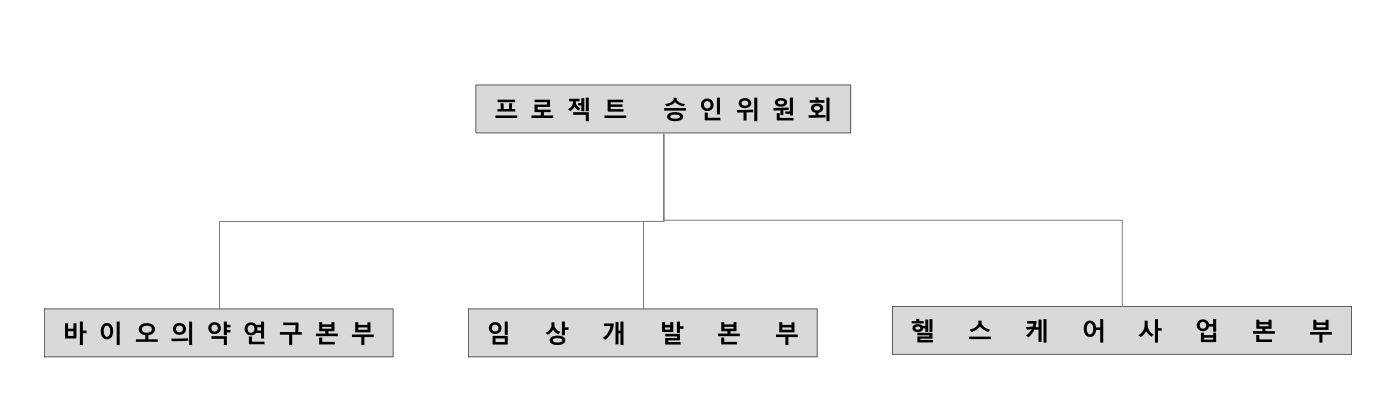 |
|
연구개발조직도 |
2) 연구개발 인력 현황
보고서 작성 기준일 현재, 당사의 임직원 수는 총 28명이며, 전체 임직원 중 10명이 연구개발 인력으로 구성되어 있습니다. 또한 연구개발을 통한 사업개발 등 연구지원 인력과 기타 경영관리 인력은 총 18명입니다.
임직원 중 박사 학위 소지자 7명, 석사 학위 소지자는 11명이며, 여성이 11명으로 전체 임직원 중 39%를 차지하고 있습니다.
|
[연구개발 인력 현황] |
|
구분 |
연구개발 |
사업개발/경영지원 |
합계 |
|---|---|---|---|
|
박사 |
5명 | - | 5명(19%) |
|
석사 |
6명 | 3명 | 9명(35%) |
|
학사 |
- | 12명 | 12명(46%) |
|
합계 |
11명(36%) | 15명(64%) | 26명(100%) |
3) 핵심 연구인력
|
소속 |
근무지 |
직위 |
성 명 |
생년월일 |
담당업무 |
주요경력 |
주요 연구실적 |
|---|---|---|---|---|---|---|---|
|
경영 |
한국, 미국 |
부회장 |
김인철 |
1951.7.7 |
경영전략 및 사업개발 |
85.03 일리노이대학교 약리학박사 |
2009: 한국 CEO 연구포럼,머니투데이 서울대 경영연구소: 대한민국 CEO 그랑프리 의약품 부문 |
|
경영, 임상 |
한국, 미국 |
사장 |
이재문 |
1958.1.15 |
임상개발, 최고경영책임 |
89.05 미국 Duke University 생화학박사 01.01~10.12 EXELIXIS Pharmaceuticals 책임연구원 11.01~12.06 ARAGEN BIOSCIENCES 책임연구원 12.07~14.06 ㈜카이노스메드 이사 15.09~21.5 현재 ㈜카이노스메드 부사장 21.6~ 현재 ㈜카이노스메드 사장 |
생화학, 분자생물학, 유전학, 호르몬학, 세포생물학, 신경생물학 전공 |
|
바이오의약본부, 경영 |
한국 |
부사장 |
김은희 |
1958.5.12 |
바이오의약본부장 |
81. 서울대학교 미생물학과 학사 |
FAF1 단백질의 기능 연구 세계 1인자, 6편 이상의 논문 저자 |
(3) 연구개발비용
당사는 일반적으로 신약 개발 프로젝트가 임상3상 단계를 완료한 이후 발생한 지출을 무형자산으로 인식하고, 이전 단계에서 발생한 지출은 당기비용으로 회계처리 하고 있습니다.
<연구개발비용 현황 (연결재무제표 기준)>
|
(단위: 백만원,%) |
|
구 분 |
2019년 |
2020년 |
2021년 |
2022년 1분기 |
|
|---|---|---|---|---|---|
|
자산처리 |
원재료비 |
- |
- |
- |
- |
|
인건비 |
- |
- |
- |
- | |
|
감가상각비 |
- |
- |
- |
- | |
|
위탁용역비 |
- |
- |
- |
- | |
|
기타 경비 |
- |
- |
- |
- | |
|
소 계 |
- |
- |
- |
- | |
|
비용처리 |
제조원가 |
- |
- |
- |
- |
|
판관비 |
5,046 | 5,239 | 5,559 |
2,082 |
|
|
합 계 (매출액 대비 비율) |
5,046 |
5,239 |
5,559 |
2,082 |
|
*당사는 후보물질 단계에서 License-In 하여 공동개발을 진행하는 연구과제의 경우, Licensing 단계에서 후보물질 사용을 위해 지급한 비용 및 개발 과정에서 지급한 비용은 무형자산(위탁용역비)로 계상하고 있음. 상기 무형자산(위탁용역비)은 기술이전 계약 통한 매출 발생 시점부터 License Fee 수취 마감 시점까지 제조원가 상 감가상각비 계정으로 비용 처리 진행함
*당사는 보고서 제출일 현재 연결 자회사의 연구개발비용이 미미하여, 연구개발비용에 대하여 연결/별도 재무제표를 구분하지 않고 연결기준으로 기재하였습니다.
(4) 연구개발실적
1) 연구개발 진행 현황 및 향후 계획
보고서 작성기준일 현재 당사가 연구개발 진행중인 주요 프로젝트 현황은 다음과 같습니다.
<연구개발 진행 총괄표>
|
구분 |
품목 |
적응증 |
연구시작일 |
현재 진행단계 |
비고 |
|
|---|---|---|---|---|---|---|
|
단계(국가) |
승인일 |
|||||
| 신약 |
파킨슨병 치료제 |
파킨슨병 |
2015 |
임상 2상 승인 (미국) |
2021년 |
IND 승인 기준 |
|
다계통위축증 치료제 |
다계통위축증 |
임상 2상 승인 (한국) |
2021년 |
IND 승인 기준 |
||
|
에이즈 치료제 |
에이즈 |
2010 |
NDA 승인(중국) 임상 3상(중국) |
2021년 |
NDA 승인 기준 |
|
|
에피제네틱 항암제 |
혈액암, 고형암 |
2012 |
임상 1상 진행(중국) |
2020년 |
IND 승인 기준 |
|
|
세포독성 항암제 |
혈액암, 고형암 |
전임상 |
- |
- |
||
|
면역항암제 (PD-L1) |
흑색종, 비소세포폐암 |
2016 |
후보물질 |
- |
- |
|
|
면역항암제 (CD73) |
혈액암, 고형암 |
선도물질 |
- |
- |
||
|
표적항암제 (IRAK4) |
혈액암, 건선 |
2017 |
후보물질 |
- |
- |
|
|
심혈관질환 심부전치료제 |
심부전 |
2020 |
선도물질 |
- |
- |
|
| FAF1-Exosome | 고형암, 혈액암 | 2021 | 선도물질 | - | - | |
① 파킨슨병 치료제
|
구분 |
합성 신약 |
|
적응증 |
뇌신경계 질환 (파킨슨병, 다계통 위축증 등) |
|
작용기전 |
FAF1 억제제로 도파민 신경세포를 보호하며, alpha-synuclein의 축적을 억제함. |
|
제품의 특성 |
Dopaminergic neuron의 소멸을 억제하여, PD 발생 후 운동능력 상실을 완화·지연함. 말기 단계를 제외한 대부분의 환자에서 현재의 운동능력을 유지시킬 것으로 예상됨. 운동능력 상실을 보완하는 현존 제품들의 효용성을 높이고 사용기간의 연장이 가능함. PD 환자들이 최소한의 일상생활이 가능한 정도의 운동능력을 보존함. Dopaminergic neuron의 사멸제어 작용기전: 파킨슨병 세포모델에서 KM-819의 신경세포 보호효과 확인 및 보호기전 규명 (disease-modifying drug) 파킨슨병 원인으로 알려진 alpha-synuclein의 축적을 억제함. 파킨슨병 동물모델(급성, 아급성, 만성모델)에서KM-819의 신경세포보호 및 행동개선효과 확인. |
|
진행경과 |
파킨슨병 치료제 미국 임상 2상 IND 승인(2021.11) |
|
향후계획 |
미국 임상 2상 성공 종료, 기술이전 추진 |
|
경쟁제품 |
Prothena/Roche(PRX-002), Neuropore/UCB(NPT200-11) : 당사와 같이 파킨슨병의 원인으로 주목받는 a-synuclein을 저해하는 저해제를 개발하고 있음. 당사의 임상 개발단계는 해외 경쟁 제약사들과 동일한 단계임. |
|
관련논문 |
Frontiers in Pharmacology, 2020.6 vol11 1-8 Drug Design, Development and Therapy 2019:13 1011-1022 Bioorganic & Medicinal Chemistry Letters 26(2016)1169-1172. |
|
시장 규모 |
전 세계적으로 인구고령화가 급속히 진행됨에 따라 향후 65세 이상의 파킨슨병 유병 환자 수는 점진적으로 증가할 전망임. GlobalData 보고에 따르면 2016년 주요 7개국(미국, 일본, 프랑스, 독일, 이탈리아, 스페인, 영국)의 파킨슨병 시장은 2016년 31억 달러였으며, 특히 미국 시장은 15억 달러로 주요 7개국 시장의 50.2%를 차지했음. 2016년을 기준으로 파킨슨병 시장은 연평균 11.1%의 증가율로 2026년 88억 달러로 증가할 것으로 예상하고 있음 (GlobalData, 2018). |
|
기타사항 |
- |
② 다계통위축증 치료제
|
구분 |
합성 신약 |
|
적응증 |
다계통위축증 |
|
작용기전 |
FAF1 억제제로 도파민 신경세포를 보호하며, alpha-synuclein의 축적을 억제함. |
|
제품의 특성 |
FAF-1의 과발현을 억제함으로써 Dopaminergic neuron의 사멸제어 하고, 다계통위축증의 원인인alpha-synuclein의 축적을 억제함. |
|
진행경과 |
다계통위축증 치료제 국내 임상 2상 IND 승인 (2021.10) |
|
향후계획 |
한국 임상 2상 성공 종료, 기술이전 추진 |
|
경쟁제품 |
Voyger Therapeutics Tau & alpha-synuclein program: 당사와 같이 파킨슨병과 다계통 위축증의 원인으로 주목받는a-synuclein을 저해하는 저해제를 개발하고 있음. 현재 임상 2상 진행 준비중. |
|
관련논문 |
- |
|
시장 규모 |
- |
|
기타사항 |
- |
③ 에이즈 치료제
|
구분 |
합성 신약 |
|
적응증 |
에이즈 치료제 |
|
작용기전 |
비핵산 역전사효소 억제제(Non-Nucleoside Reverse Transcriptase Inhibitor, NNRTI) |
|
제품의 특성 |
비핵산계열의 화합물로 하루 1회 투여의 편리성 확보하고 있으며 독성이나 CNS부작용이 없고 다른 약물과 병용투여(Combination)가 용이함. |
|
진행경과 |
2014.10 기술이전, Jiangsu Aidea Pharmaceutical (중국) 2016.12 중국 식품의약품관리감독총국 우선심사대상 지정 2017.03 중국 임상 승인 2018.10 임상 3상 개시 2021. 중국 NDA 승인 2021. 중국 단일정 NDA 제출 및 임상 3상 개시 (treated patients) |
|
향후계획 |
단일정의 중국내 NDA 허가 및 시판 |
|
경쟁제품 |
BMS(Efavirenz,EFV), 얀센(rilpivirine,RPV): 에이즈 시장에서의 주력제품은 이미 시장에서 판매되고 있는 EFV와 RPV가 있으며, EFV의 경우 특허가 만료되었음. 기존의 의약품의 중추신경계 및 다양한 부작용이 보고되고 있음. |
|
관련논문 |
Curr HIV Res. 2020 Jun 20 |
|
시장 규모 |
전 세계 HIV 약물 시장은 2019 년에 $ 30,891.48 million으로 평가되었으며, 2027 년까지 $ 36,495.47 million에 이를 것으로 예상됨 (2021 Allied Market Research). 2020 년부터 2027 년까지 3.8 %의 CAGR (연평균 성장률)을 기록할 것으로 예상. Datamonitor Healthcare의 2018년 보고서에 따르면 미국과 주요 EU 시장 (프랑스, 독일, 이탈리아, 스페인, 영국)의 HIV 시장은 2017년의 182억 달러에서 2026년 211억 달러로 연평균 1.7 % 성장할 것으로 예측. |
|
기타사항 |
- |
④ 브로모도메인 저해제 개발: 에피제네틱스 항암제
|
구분 |
합성 신약 |
|
적응증 |
혈액암(AML, AL, MM, DLBCL) 및 고형암(전립선, 유방암, NSCLC, neuroblastoma) |
|
작용기전 |
브로모도메인(BRD4) Inhibitor : 브로모도메인의 타킷인 c-MYC은 종양의 생존, 변이에 중요한 역할을 담당하는 중요한 전사 인자로서, c-MYC의 비정상적인 발현을 억제함. |
|
제품의 특성 |
KM-635는 임상 II상을 준비 중인 Merck사의 OTX-015와 비교하여 우수한 생체 대사성과 생체이용률, 대사 안정성, mouse xenograft model에서도 기존 임상 약물에 비해 월등한 비교 우위를 갖고 있는 화합물임. Human dose prediction실험을 통해, KM-635는 임상에서 OTX-015에 비해 1/2의 양을 사용하더라도 같은 효과를 나타낸다는 결론을 얻었음. 기존의 임상 약물보다 우수한 약효와 안정성을 기대할 수 있으며, 그 적응증을 확대하여 고형암의 치료제로써도 효과를 기대 할 수 있음. |
|
진행경과 |
2015.12.10 기술이전, Jiangsu Aidea Pharmaceutical (중국) |
|
향후계획 |
임상 1상 완료(중국) |
|
경쟁제품 |
Merck(OTX-015), GSK(I-BET762), 로셰(텐샤, TEN-010), 애브비(ABBV075): 현재 임상 진행중인 약물들은 약리 및 약동력학적 프로파일이 좋지 않음. OTX-015(MK-8628, Merck)의 경우 임상 1상 결과 체내 흡수와 대사안정성이 낮아 고용량에서만 약효가 나타나게 되어 안전성에 대한우려가 높음. |
|
관련논문 |
- |
|
시장 규모 |
항암제 분야의 2019년 점유율은 16%로 2026년까지 연평균 11.5%로 성장하여 2026년에는 21.75%로 점유율이 확대될 것으로 기대 2024년 글로벌 항암제 시장 규모는2,385억 달러로2018년 대비 약2배의 고성장 전망. |
|
기타사항 |
- |
⑤ 경구용/주사제 겸용의 핵산 (Nucleoside) 유사체 계열 세포독성 항암제
|
구분 |
합성 신약 |
|
적응증 |
혈액암(급성골수성백혈병)및 고형암 |
|
작용기전 |
시타라빈(Cytarabine, Ara-C) Inhibitor : 세포독성 항암제는 세포의 DNA를 알킬화시켜 세포독성을 나타내는 알킬화제와 DNA가 결성되는 것을 저해함으로써 세포의 미분화와 분열을 차단하고, RNA의 합성도 저해하여 광범위한 악성종양에 효과를 보이는 대사길항제임. |
|
제품의 특성 |
경쟁약물 Ara-C의 단점인 Cytidine deaminase (CDA) 작용에 대한 대사체 변이를 극복한 약물로 경구와 정맥주사가 모두 가능. KM-630은 경구용 혹은 정맥투여 시, 대사작용에서 우수한 안정성 및 생체이용률 (Bioavailability) 등 뛰어난 약리동력학적 안정성을 나타내어 고형암으로의 적응증 확대가 가능. |
|
진행경과 |
2015.12.10 기술이전, Jiangsu Aidea Pharmaceutical (중국) 동물모델에서의 효능 확인 |
|
향후계획 |
전임상 독성 연구 및 중국임상 1상 IND Filling |
|
경쟁제품 |
화이자(시타라빈), 일라이릴리(젬시타빈): 현재 시타라빈(Cytarabine, Ara-C) 과 같은 시판된 핵산계열 세포독성 항암제는 대부분 정맥주사제이며, 단독요법으로 사용되는 경우 하루 2,000mg의 고용량을 투여해야 함. 이로 인한 심각한 독성과 부작용의 문제점을 내포하고 있음. |
|
관련논문 |
- |
|
시장 규모 |
핵산계열 세포독성항암제의 주요 적응증은 백혈병을 비롯한 혈액암 계통이며, 자궁암, 유방암, 폐암 등 일부 고형암의 치료에도 사용되고 있음. 백혈병의 세계 시장 규모는2020년까지3.84% 성장. 환자수는 약80만명 이상으로 증가. |
|
기타사항 |
- |
⑥ 면역항암제(PD-L1)
|
구분 |
합성 신약 |
|
적응증 |
흑색종 및 비소세포폐암 |
|
작용기전 |
저분자화합물 PD-L1 저해제 : 암세포의 면역회피경로를 차단함으로써 체내 면역체계를 활성화시키고 면역세포가 선택적으로 암세포만을 공격하도록 유도하는 기전임. |
|
제품의 특성 |
당사는 기존의 표적항암제 개발 파이프라인을 통해 축적된 의약화학 전문기술을 바탕으로 기존 표적항암제의 부작용 및 내성문제와 항체의약품의 한계를 극복한 저분자 화합물을 기반으로 하는 효율적이고 안전하며 혁신적인 경구용 면역항암제 상용화를 위한 파이프라인을 구축하는 차별화 전략을 수립하였음. PD-L1 저분자 저해제는 기존 anti-PD-1/PD-L1 mAb인 주사제의 단점을 극복한 경구투여 약물로 개발함으로써 환자의 복용 편의성 증대, 항체보다 단시간 작용(short-acting)하여 immune-related adverse events (irAEs)에 대한 관리가 용이, 항체의 Fc region에 의한 항체의존세포매개세포독성(antibody-dependent cell-mediated cytotoxicity, ADCC)으로 인한 독성을 유발하지 않음 등과 같은 장점을 가지고 있음. |
|
진행경과 |
전임상 후보물질 도출 중 |
|
향후계획 |
전임상 후보물질 도출 및 전임상 연구 및 임상 진입 |
|
경쟁제품 |
Incyte(INCB086550, 저분자화합물), BMS(옵디보), MSD Japan/Merck(키트루다): 면역항암제 중에서, 면역체크포인트 치료제 시장의 선두주자는PD-1/PD-L1을target으로 하는BMS와Merck며, 현재 승인된 암 외의 다양한 암 종으로의 적응증을 확대하는 중임. |
|
관련논문 |
- |
|
시장 규모 |
항암제 시장의 높은 성장 요인은 면역항암제 시장의 높은 성장의 결과로, Research And Markets에 따르면 2017년 $ 10.5 billion에서 2022년 $ 100 billion을 넘어설 것으로 예상함. |
|
기타사항 |
- |
⑦ 면역항암제(CD73)
|
구분 |
합성 신약 |
|
적응증 |
혈액암(AML, AL, MM, DLBCL) 및 고형암(삼중음성 유방암, 흑색종, 비소세포폐암, 췌장암, 자궁암, 전립선암) |
|
작용기전 |
CD73 저분자 저해제 : 암세포의 면역회피경로를 차단함으로써 체내 면역체계를 활성화시키고 면역세포가 선택적으로 암세포만을 공격하도록 유도하는 기전임. |
|
제품의 특성 |
당사는 특허성이 있는 저분자 물질로써 다양한 ecto-효소 및 ADP-activated receptors에 대한 CD73효소의 선택성을 가지고, 경구 투여가 가능한 우수한 효능의 저분자 저해 물질의 발굴을 목표로 함 |
|
진행경과 |
후보물질 도출 (우수한 생리활성 및 약동학적 효능확보) |
|
향후계획 |
전임상 후보물질 확정 |
|
경쟁제품 |
저분자 화합물, Arcus(AB680), Eli Lilly(LY3475070); 항체치료제, 아스트라제네카(MEDI9447), BMS(BMS-986179) 등: 현재 임상진행 중인CD73타겟의 면역항암제는 항체의약품이 주 축을 이루고 있으며 이에 뒤따라 저분자화합물 기반의 약물은 2종(임상1상)으로써 저분자화합물이 가지는 특장점을 확보하는 미충족의학적수요를 충족시킬 만한 약물개발에 관심이 집중되는 상황임. 그 외에는 대부분 개발 초기 단계이거나 2-3개 회사 정도가 비임상 단계임 상태임. |
|
관련논문 |
- |
|
시장 규모 |
항암제 시장의 높은 성장 요인은 면역항암제 시장의 높은 성장의 결과로, Evaluate Pharma 조사 결과 2014년 14억 달러에 불과했던 면역항암제 시장은 2022년 300억 달러로 증가할 것으로 예상함. |
|
기타사항 |
- |
⑧ 표적 항암제
|
구분 |
합성 신약 |
|
적응증 |
관절염, 건선, 혈액암(lymphoma) ACB-DLBCL |
|
작용기전 |
IRAK4 (Interleukin 1 Receptor Associated Kinase 4)저해제 : Interleukin 1 Receptor Associated Kinase 4는 세포의 표면에 존재하는 Toll Like Receptor/IL-1beta(TLR/1L-1b)라고 불리 우는 수용체로부터 전달되는 세포 신호 전달의 매개체로서 중요한 역할을 하는 serine/threonine 인산화효소(Kinase)의 일종임..MyD88과 IRAK4, IRAK1과의 복합체를 형성하게 되고 형성된 복합체는 NF-kB 신호전달을 통해 세포핵에서의 전사인자를 활성화시켜 면역 및 염증 반응을 유발함. |
|
제품의 특성 |
자가면역질환 및 항암효능을 극대화시킬 수 있는 dual inhibitor 개발을 목표함. |
|
진행경과 |
2018.11 기술도입(충남대 학교 산학협력단) 리드최적화를 통해 확보된 약물의 in vitro & in vivo POC 검증 완료 |
|
향후계획 |
전임상 후보물질 도출 |
|
경쟁제품 |
항암제로서는 Aurigene/Curis(CA-4948)가 임상에 진입한 것 외에는 IRAK4 저해제는 전임상 단계 및 biological testing단계에 대부분 머무르고 있음. 관절염치료제로서는 PF-06650833이 임상 2상 완료됨 |
|
관련논문 |
- |
|
시장 규모 |
DLBCL 시장은 2016년 2.2 billion 달러에서 2025년 3.5 billion달러로 성장 예측되며 이 기간 사이에 DLBCL의 표준치료제인 Rituximab이 2019년 특허가 만료됩니다. 따라서 Rituximab의 biosimiliar가 시장의 판도에 영향을 미치게 되면서 전체 마켓은 점차적으로 성장되는 것으로 예측되고 있음. |
|
기타사항 |
본 프로젝트는 2021.10.06 미국의 Emmaus life Science, Inc.로 미국, 유럽(영국령 지역 포함) 지역을 대상으로 기술이전을 완료하였음. 추후 연구개발은 Emmaus에서 주도적으로 진행할 예정이며, Emmaus에서 수행한 연구결과들을 바탕으로 당사는 그 외 지역의 사업화를 추진할 계획임. |
2) 연구개발 완료 실적
- 해당 사항이 없습니다.
3) 연구개발활동 및 판매 중단 현황
- 해당 사항이 없습니다.
7. 기타 참고사항
가. 산업의 개요 및 특성
제약/바이오산업은 생명공학기술을 바탕으로 인류의 건강증진, 질병예방, 진단, 치료에 관련된 다양한 부가가치를 생산하는 산업입니다. 특히 신약개발분야는 연구개발비 비중이 전체 매출액의 15~20%에 이르는 연구중심 산업이며, 성공시에는 높은 순익을 얻을 수 있는 고부가가치 산업입니다.
제약/바이오산업은 의약품의 원료물질에 따라 합성의약품, 천연물 의약품, 그리고 바이오 의약품으로 나눠지며, 허가기준에 따라 신약, 개량신약, 제네릭 의약품, 바이오시밀러로 구분됩니다. 이중, 합성 신약의 경우는 이전에 허가되지 않은 새로운 활성 성분을 함유한 화합물로 이루어진 의약품으로 정의됩니다.
지적재산권 보호, 신약허가 및 보험 약가에 엄격한 규제가 따르는 특성을 가지고 있습니다.
(1) 연구집약적, 고위험/고부가가치/장기투자 산업
신약개발을 위해서는 기초연구부터 허가과정까지 의학, 약학, 화학, 생물학 등 제반 기능이 유기적으로 결합되어야 하며 평균적으로 약 10여 년 이상의 개발과정을 거쳐야 하므로 그 어떤 산업보다 연구개발 비중이 높습니다.
통계에 따르면 신약 1개를 개발하는데 소요되는 연구개발비는 평균 12~17억 달러이며, 제약 산업의 연구개발비는 매출액 대비 평균 20% 이상 수준으로 매년(2018-24) 3%씩 증가를 예상하고 있습니다(출처: Evaluate Pharma, May 2019). 글로벌 상위 10개 의약품 기업의 2018년 연구개발 비용은 연간 50~98억 달러이며, 이는 매출액의 16%~25% 수준에 이르고 있습니다.
바이오산업은 투자 금액이 높은 반면 회수기간이 길어 장기투자가 필수적이며, 성공시 높은 수익이 보장되나 성공에 대한 위험성도 존재하는 산업입니다. 특히 신약개발은 막대한 R&D 투자를 통한 비용 부담과 시간이 소요되지만 그 성공률은 높지 않습니다. 신약개발 전 과정을 거치면 신약 출시까지 평균 12~15년의 기간과 약 1조원의 비용이 소요되는 것으로 발표되고 있습니다.
그러나 일단 좋은 신약개발에 성공하면 그로부터 천문한적인 수익을 거두는 경우가 많으며 글로벌 Top Tier 다국적 제약사들은 평균 20% 내외의 순이익률을 매년 유지하고 있습니다. 신약개발은 평균적으로 10년이상의 기간과 수천 억원의 비용이 소요되고 까다로운 규제를 통과해야 하지만, 제품 출시에 성공하면 연간 10억~50억 달러의 매출과 약 20%~50%의 순이익 창출이 기대되는 대표적인 고위험-고수익 (High risk, High return) 산업입니다.
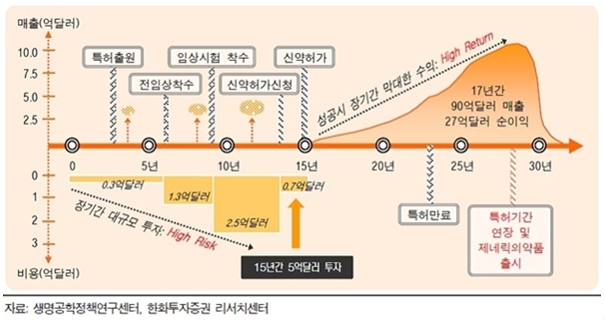 |
|
출처 : 생명공학정책센터 |
(2) 지적재산권 보호
바이오산업분야에서 "기술이전"이나 "전략적 제휴" 모두 특허를 중심으로 이루어지고 있고, 특정제품의 특허 만료가 전체 산업 구조에 영향을 끼칠 정도로 특허의 중요성이 높은 산업입니다. 특허 출원 후 20년 이상을 독점적으로 보호받기 때문에 개발기간을 감안하면 신약 출시 후 약 10년 정도의 독점 판매기간을 확보할 수 있습니다. 특히 신약개발과 같은 개발기간이 긴 물질의 경우 새로운 물질 특허 연장 법률(Hatch & Waxman Act)에 의하여 최대 5년까지 연장이 가능합니다. 따라서, 의약품의 적응증 확대 및 기술적 보완 등 다양한 고도화 작업을 통한 특허권 연장 및 보호를 하고 있으며 독점판매기간을 추가로 확보하여 회사는 이익증가 및 생산성 증대, 진입장벽을 높임으로써 특허로 보호받는 기간 내에 해당 회사는 그 동안 신약개발에 투여했던 거액의 연구개발비를 회수할 수 있습니다.
(3) 바이오산업의 조직적 특성
제약/바이오산업은 약의 종류가 매우 많고 각 질환마다 다른 전문성을 요하기 때문에 한 회사가 모든 질환에 대한 가장 좋은 약을 개발할 수 없습니다. 따라서 전체 세계시장의 10%의 점유율을 넘는 기업이 없을 정도로, 제약사들은 몇몇 질환과 약효군에 대해 전문성을 갖고 시장을 세분화하여 점유하고 있습니다.
따라서 제품 포트폴리오의 확대, 새로운 지역으로의 진출, 기술적 보완관계를 통한 시너지 창출, 비용구조 개선 및 연구개발 생산성 증대 등을 이유로 인수·합병이 매우 활발합니다. 특히, 글로벌 제약사가 진출하지 않은 첨단제제 영역에서는 기술개발에 성공한 벤처기업이 신흥강자로 나타날 수 있고 기존의 제약기업이 분야 확대를 위한 수단으로써 기술벤처를 인수합병 하거나 전략적 제휴를 활발히 진행하고 있습니다.
제약 산업은 인간의 생명에 직접적인 영향을 미침으로 신약의 안전성 확보를 위해 각국 정부가 엄격하게 규제하는 특징을 갖고 있습니다. 이에 따라 새로운 치료제를 개발한 후 판매하기 위해서는 정부가 정하는 여러 단계의 임상실험을 하여야 하며 식품의약품안전처에 모든 자료를 제출한 후에 판매승인을 받아야 합니다.
나. 회사 사업 개요
당사는 혁신적인 신약 개발을 위한 후보물질 창출 및 초기 임상까지의 연구개발을 자체적으로 수행하고 이를 기술이전 전략을 통한 글로벌 시장으로 진출하고자 하는 신약개발 전문 기업입니다.
(1) 글로벌 기술이전과 전략적 제휴
당사는 개발물질의 사업화를 위해 전략적 파트너사, 다국적 제약회사 관계자, 각 분야의 전문가와 교류를 유지하고 있습니다. 특히, 해외 유수의 제약기업과의 파트너링을 지속적으로 진행함으로써 기술이전을 대비한 네트워킹 유지를 위해 노력하고 있습니다. 기술이전 잠재고객 확보를 위해서 각종 학회 및 바이오 전문 파트너링 컨퍼런스 참여를 하는 등 다양한 방법으로 기술이전 및 사업화를 적극적으로 추진하며, 전략적 기술이전과 공동연구(파트너)를 진행하고 있습니다.
당사의 기술이전 전략인 제한적 실시권을 부여하는 동시에 공동연구개발을 추진함으로써 연구개발 결과를 추후에 활용하여 글로벌 제약사의 기술이전 기회를 확보하는 전략을 추진하고 있습니다.
당사는 파이프라인의 가치를 극대화하기 위하여 지적재산권을 확보하고, 추가 연구를 통한 특허 취득으로 지적 재산권 확대를 지속적으로 수행하고 있습니다. 당사의 주요기술이전과 공동연구 실적은 다음과 같습니다.
|
[기술이전 및 주요공동연구 실적] |
|
구분 |
파트너사 |
파이프라인/년도 |
권리범위 |
|---|---|---|---|
|
기술이전 및 공동연구 |
장수 아이디어(Jiangsu Aidea Pharmaceuticals) |
에이즈 치료제 (KM023)/2014년 |
중국시장에 대한 전용 재실시권 이전 글로벌 시장 전용실시권 보유 |
|
에피제네틱 항암제 (KM-635)/2015년 |
중국시장에 대한 전용 실시권 이전 글로벌 시장 실시권 보유 |
||
|
세포독성 항암제 (KM-630)/2015년 |
중국시장에 대한 전용 실시권 이전 글로벌 시장 실시권 보유 |
||
|
기술이전 및 공동연구 |
Crown Bio |
비만/당뇨 치료제 (KM001)/2014년 |
전 실시권 이전 |
|
공동연구 |
PICC |
파킨슨병 치료제 (KM-819)/2018년 |
공동연구/공동임상 개발 |
|
공동연구 |
UCSD |
파킨슨병 치료제 (KM-819)/2018년 |
공동연구 |
|
공동연구 |
신테카바이오 |
파킨슨병 치료제 (KM-819)/2018년 |
공동연구 |
|
공동연구/기술이전 |
Emmaus |
급성백혈병치료제 (KM-10544)/2021년 |
미국, 유럽, 영국 지역에 대한 전용실시권 이전 |
| 공동연구/기술이전 | 엠디뮨 | 항암제 (FAF1-exosome)/2021년 |
전세계 통상실시권 확보 |
당사가 현재 추진중인 글로벌 개발 프로젝트인 파킨슨병 치료제(KM-819)는 각 분야의 전문기관과 공동연구를 통해 기존의 증상완화제가 아닌 근본적 치료제로써 혁신적 글로벌 신약후보임을 확인하였습니다. 퇴행성 뇌질환 관련 추가 적응증 확대에도 개발 가능성이 존재하기 때문에 그 가치는 더욱 커짐에 따라 기술이전 확률도 높을 것으로 판단됩니다.
또한 전략적 기술이전을 추진한 사례로 에이즈 치료제가 있습니다. 중국에 대한 제한적 재실시권(sub-license)부여로, 파트너사의 중국내 매출에 따른 로열티 수익을 기대하고 있으며, 중국에서 진행한 임상결과 자료 활용으로 글로벌 시장 진출의 기회를 확보하였습니다.
전임상개발 파이프라인 혹은 임상개발 파이프라인이 글로벌 제약사 등으로 기술이전되어지면 또 다른 후속 파이프라인이 신속히 그 뒤를 이어야 합니다. 뿐만 아니라 신약의 속성 상 임상개발 성공률이 높지 않은 바, 그 실패 위험성에 대비하기 위해서라도 후속 파이프라인이 확보되어야 합니다. 따라서 개발 파이프라인들의 연속성을 유지하고 각각의 파이프라인을 성공적으로 개발하여 기술이전 등 차세대 신규사업으로 발전시키는 것이 회사의 성장전략에서 가장 중요한 핵심 요소라고 판단됩니다.
하지만 후보물질을 창출하는 연구단계부터, 안전성과 유효성을 확보하는 전임상개발 및 임상 1-2-3상 개발까지 신약 연구개발은 여러 단계를 거치고, 의약품으로서 최종 승인받기까지 많은 시간과 개발 비용이 소요되며 그 과정에는 또한 수많은 난관들이 있습니다. 당사는 신규 개발파이프라인을 확보하기 위해 내부 연구소에서 자체 신약연구를 수행하는 한편, 외부로부터의 전략적 기술도입을 동시에 추진하여 차세대 주력 파이프라인 확보하는데 있어서 그 성공률을 높이고자 합니다.
전략적 기술도입의 경우, "혁신신약" 후보물질의 전세계 독점실시권을 확보한 이후 글로벌 개발을 신속하게 진행하고 적절한 개발 단계에서 글로벌 제약사에 다시 독점실시권을 이전하는 전략을 추진하고자 합니다. 이를 위해 빅파마들의 스카우터들이 찾는 분야들을 중점적으로 검토하고자 하며, 이는 글로벌 제약사들이 결국 환자들의 미충족의료수요(unmet medical needs)를 집중적으로 살피기 때문에 관심도가 높아지고 있는 분야를 선택하기 때문입니다.
당사는 신약개발과 파이프라인 확대와 기술이전이라는 사업이외에 헬스케어 분야 사업을 준비하고 있습니다. 이를 위해 미국내 헬스케어 상품 판매를 위한 채널 확보, 전략적 파트너쉽 체결 등의 사업을 추진하고 있습니다.
(3) 진입장벽
글로벌 신약개발의 진입장벽은 그 어느 분야 보다 높다고 할 수 있습니다. 신약개발 과정은 후보물질 발굴을 위한 연구단계와 비임상, 임상 단계의 개발 단계 그리고 허가과정으로 구분되어 있습니다. 하나의 신약을 개발하는데 있어 평균 10년 이상의 기간이 소요되며, 개발 비용 역시 수조원이 필요합니다. 이러한 높은 진입장벽을 낮추기 위해서는 타겟 발굴부터 허가까지의 전주기적 신약개발 경험과 노하우가 필요합니다. 당사는 신약개발의 경험이 많은 전문가를 내부 인력으로 확보하고 있으며 의약관련 분야의 전문가를 SAB(Scientific Advisory Board)로 영입하여 신약개발의 효율성 및 성공률을 높이고자 합니다. 글로벌 제약회사와는 차별화할 수 있는 기술을 개발하여 세계적 경쟁력을 가진 글로벌 신약을 발굴해 낼 수 있는 가능성이 있다고 볼 수 있습니다.
다. 대상 질환별 특성 및 시장 현황
(1) 퇴행성 뇌질환 - 파킨슨병
퇴행성 뇌질환 (degenerative brain disease)은 노화가 진행됨에 따라 발생하는 퇴행성 질환 중에서 뇌에서 발생하는 질환을 뜻합니다. 현재까지 알려지지 않은 원인으로 뇌와 척수의 특정 뇌세포군이 서서히 그 기능을 잃고 뇌신경계의 정보전달에 가장 중요한 뇌신경세포의 사멸, 뇌신경세포 사이의 정보를 전달하는 시냅스의 형성이나 기능상의 문제, 뇌신경의 전기적 활동성의 이상적 증가나 감소로 인하여 야기되는 것으로 알려져 있습니다. 뇌와 척수의 신경세포들은 위치에 따라 매우 다양한 기능을 하고 있어 어느 부위의 신경세포들이 먼저 손상되고 기능을 소실함에 따라, 또 이러한 기능장애가 어떤 형태로 진행되는가에 따라 매우 다양한 임상 양상을 보이게 됩니다. 퇴행성 뇌질환 은 나타나는 주요 증상과 침범되는 뇌 부위를 고려하여 구분할 수 있으며, 알츠하이머병, 파킨슨병, 헌팅턴병, 다발성경화증, 루게릭병으로 알려진 근위축성 측색 경화증 등이 포함됩니다.
당사가 질병조절 치료제로서 개발중인 퇴행성 뇌질환은 파킨슨병입니다. 중뇌에 위치한 흑색질(substantia nigra pars compacta, SNpc)에 존재하는 도파민 생성 신경세포의 사멸로 인해서 운동장애를 나타내는 질환입니다. 임상적으로는 운동 완서, 근육의 경직, 강직, 떨림, 자세이상 등의 증상이 대표적입니다. 이 외에도 인지 기능의 장애, 정신 이상 증상 그리고 감각 이상 등과 같은 다양한 임상적 특징을 보이며, 지속적인 세포의 사멸로 인한 신체이상으로 정상적인 생활이 불가능하며, 진단 후 약 10-15년의 수명을 보입니다. 인구 고령화에 따라 향후 퇴행성 뇌질환 유병률 및 관련 의료비용이 지속적으로 증가할 것으로 예상되며, 이에 따라 효과적 치료제 개발에 대한 수요가 확대될 전망입니다. 퇴행성 뇌질환은 환경적인 요인 및 유전적 요인 등에 의해 발병하는 것으로 추정되고 있으나 아직 정확한 원인 규명 및 근본적인 치료제 개발은 이루어지지 않은 특발성질환(idiopathic)입니다. 그 결과로 인해 단편적인 증상완화 및 간병을 위한 경제적·사회적 비용 부담이 장기화되고 있습니다.
질병을 근본적으로 억제하는 치료제가 현재까지는 없으며, 현재 시판되고 있는 치료제는 알츠하이머병과 파킨슨병의 인지기능 및 운동능력 유지 등의 증상 완화 및 진행 속도 지연을 위한 증상완화 의약품이 대부분입니다. 그 결과 퇴행성신경질환 환자의 지속적인 증가가 예상됨에 따라 병의 진행을 근원적으로 억제할 수 있는 질병조절치료제(Disease-modifying treatments) 의약품 개발이 더욱 중요해지고 있습니다.
노인인구 증가는 건강한 노년 준비 트렌드, 퇴행성신경질환에 대한 관심 증가, 적절한 환자 치료계획을 제공할 수 있는 전문 의료 인프라 및 효과적 질환 치료제의 수요 확대 등을 초래하여 관련 시장 성장을 견인할 것으로 전망됩니다. 또한, 증상 완화 위주의 기존 약물 요법에서 나아가 근본적인 발병 기전을 표적으로 하는 질환 조절 치료제의 개발은 퇴행성 뇌질환 치료 분야에 혁명을 일으킬 것으로 기대하고 있습니다.
GlobalData 보고에 따르면 주요 7개국(미국, 일본, 프랑스, 독일, 이탈리아, 스페인, 영국)의 파킨슨병 치료제(현재 시판 중인 증상완화제) 시장은 2019년 35억 달러였으며, 특히 미국 시장은15억 달러로 주요 7개국 시장의 50.2%를 차지하였습니다. 2019년을 기준으로 파킨슨병 시장은 CAGR(복리법연평균성장률) 12.6%의 증가율로 2029년 115억 달러로 증가할 것으로 예상하고 있습니다(GlobalData, 2021).
| [주요 7개국 파킨슨병 치료제 시장동향] |
|
| 출처) GlobalData, 2021 |
주요 7개국(미국, 일본, 프랑스, 독일, 이탈리아, 스페인, 영국)을 기준으로 2019년 243.4만명이 파킨슨병으로 진단받았으며, 2029년에는 299.9만명이 파킨슨병으로 진단받아 AGR(단순연평균성장률) 2.32%를 기록할 것으로 예측하였습니다. 이중에서도 미국 시장에서의 환자수 78.2만명에서 105.6만명으로 가장 가파른 환자 증가율인 AGR(단순연평균성장률) 3.50%를 보일 것으로 예측하였습니다. (Globaldata, 2021)
파킨슨병의 유병률은 국가별 차이가 있지만, 연간 10만 명당 4.5명~ 19명의 환자가 새롭게 파킨슨병으로 진단받는 것으로 추정되고 있습니다(WHO, 2017).
건강보험심사평가원에 따르면 국내 파킨슨병으로 진료받은 환자는 2013년 8만명에서 2017년 10만 716명으로 4년 새 13% 증가하였습니다. 2017년 기준으로 국내 파킨슨병 치료제 시장규모는 약 780억원으로 산출되었으며, 노인성 뇌신경질환 치료제 시장에서 알츠하이머병 다음으로 큰 시장을 형성하고 있습니다.
특히 파킨슨병은 연령이 높아질수록 유병률 또한 증가 양상을 보이며, 50대 유병률은 10만 명당 35.8명에서 60대 이상의 경우 141.41명으로 급증하였습니다. 또한 전체 파킨슨병 환자 중 50대 이상의 환자가 약 93%, 60대 이상의 환자는 79%를 차지하고 있습니다.
(나) 에이즈(AIDS)
2018년 기준으로 전세계적으로 HIV 감염자 수는 3,790만명으로 추산되며 antiretroviral therapy를 받은 환자는 2,170만명으로 2016년에 비해 230만명이 증가하였습니다. (UNAIDS) 2018 년에 에이즈에 기인한 사망자는 약 77만명이며, 감염률이 가장 높은 사하라 아프리카에서 압도적으로(74 %) 발생하였습니다 (UNAIDS (June 2019) Core epidemiology slides).
선진국의 에이즈 감염자 수는 감소하고 있는 반면, 아프리카를 포함해 경제적 수준이 낮은 국가에서는 계속 증가하고 있습니다. 에이즈 치료를 받는 환자수가 증가함에 따라 에이즈로 인한 사망자수가 감소하여 전체 에이즈 환자의 수는 증가추세를 보이고 있습니다.
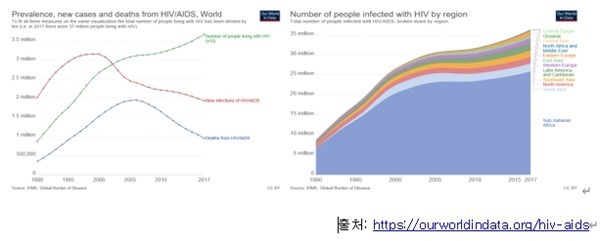 |
|
전세계 에이즈 환자 증가 추세 |
또한 중국을 비롯한 이머징(emerging) 국가의 에이즈 환자는 급격히 증가하고 있는 추세이며, 이에 따라 고가의 에이즈 치료제를 사용할 수 없는 국가에서는 합리적인 가격의 자국내 치료제개발을 위한 노력이 이루어지고 있습니다.
에이즈치료제는 단일약물 사용으로 인한 내성발성/효과부족을 보완함과 동시에 복용 순응도 향상을 위해 단일정복합제(STRs)가 등장하였고, 그 시장 점유율이 매년 증가하고 있습니다. 2018년 STRs이 HIV 시장의 top 10 상위권을 점유하고 있으며, 이 중 Atripla [EFV + 3TC + TDF]가 2017년 시장 점유율 13% 로 미국시장 1위를 차지하고 있습니다 (Datamonitor, 2017).
미국과 주요 유럽시장에서는 NNRTIs 약물 중 에파비렌즈(efavirenz, EFV)와 릴피비린(rilpivirine, RPV)이 계속해서 시장을 이끌 것으로 보이며 rilpivirine (RPV)이 efavirenz (EFV)에 비해 중추신경계 독성이 낮아 매출이 증가할 것으로 전망하고 있습니다.
의사들을 대상으로 한 Datamonitor Healthcare 2018 설문조사 결과 미국 및 유럽의 5개국에서 HIV 치료의 미 충족 의학적 수요 1순위는 치료비용의 감소로 집계되었습니다. 고가의 HIV 치료제 비용은 개인 보험자 및 사회 건강관리 기관 모두에게 경제적 부담이 되는 것으로 나타났습니다.
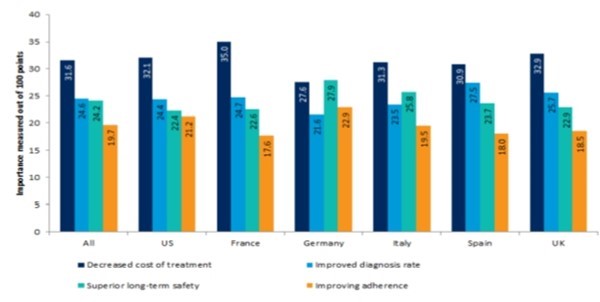 |
|
미국 및 유럽 5개국에서의 HIV 치료제 미충족 의학 수요 |
에이즈 치료제는 평생복용을 해야 하는 질환으로 장기복용에 따른 약제의 부작용은 매우 중요한 부분입니다. 기존의NNRTI 치료제의 경우 우수한 활성을 가졌지만, 기형아 출산, 퇴행성 뇌질환 관련 부작용 등의 이유로 사용의 제한이 있어 환자의 복용편의성이 낮습니다. 이러한 이유로 부작용이 낮고 복약 순응도를 높이고 매일 복용하는 불편함을 덜기 위해long-acting 제제의 개발이 시도되고 있습니다.
미국과 주요 EU 시장 (프랑스, 독일, 이탈리아, 스페인, 영국)의 HIV 시장은 2017년의 182억 달러에서 2026년 211억 달러로 연평균 1.7 % 성장할 것으로 예측하고 있습니다. 이는 HIV 유병률의 증가뿐만 아니라 단일 타블렛 요법 (STR) 및 tenofovir alafenamide (TAF) 기반 요법의 지속적인 증가에 기인합니다.
Prezista (darunavir), Reyataz (atazanavir), Isentress (raltegravir) 및Descovy (Emtricitabine + TAF)와 같은 주요 약물의 특허 만료로 인해, 2024년 227억 달러로 절정에 이른 후 점차적으로 시장이 위축될 것으로 보입니다. 그 이유는 제네릭 의약품 출시에 의해 시장을 대체하는 신규 약품의 시장 점유율이 증가하기 때문인 것으로 분석됩니다.
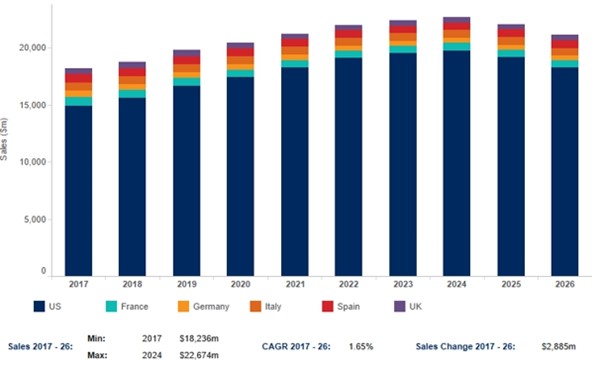 |
|
HIV total market value across the US and five major EU markets, 2017-2026 |
*출처: Datamonitor Healthcare, 2018
(다) 항암제
고령화 사회의 가속으로 인한 노인인구의 증가와 더불어 서구화된 식습관, 각종 환경적 영향 및 유전학적 요인으로 암환자의 발생률은 지속적으로 증가하는 추세입니다. 2016년 미국에서는 연간 168만 명의 신규 암환자가 발생하고, 60만명이 암으로 사망하였으며, 국내 또한 매년 20만명의 새로운 암환자가 발생하고 매년 4조원이 넘는 의료비가 암 치료에 사용되고 있습니다.
[항암제 종류 및 특징]
|
구분 |
특징 |
|
|---|---|---|
|
1세대 |
세포독성 |
◆ 무분별하게 증식하는 암세포를 공격하는 방식 ◆ 암세포뿐만 아니라 정상세포도 무작위로 공격하여 구토, 탈모 등 부작용 동반 |
|
2세대 |
표적항암제 |
◆ 암세포와 발현 조직을 표적으로 하여 세포독성항암제 대비 치료율 향상 및 부작용 개선 |
|
3세대 |
면역항암제 |
◆ 환자의 면역세포를 활성화하여 암세포의 특징인 면역회피경로를 차단하거나 직접 암세포를 공격 |
세포독성 항암제는 암세포의 각 대사 경로에 개입하여(주로DNA에 직접 작용하여 방사선 치료와 마찬가지로DNA의 이중 나선구조를 파괴) 암세포를 괴멸하는 약제들을 총칭하며 현재 약50여종의 약물이 사용되고 있습니다. 그러나 암 세포뿐 아니라, 정상 세포도 공격하여 다양한 전신적 부작용을 나타내고, 어린 세포에게 보다 더 효과적으로 작용하므로 종양 세포의 세대가 길어질수록 화학요법에 대한 감수성이 떨어지게 됩니다. 따라서 고형암과 같이 암 조직이 세포분열을 멈추게 되면 약물이 거의 작용하지 않는 단점이 있습니다.
표적항암제는 단순히 모든 종류의 빠르게 증식하는 세포들을 방해하기 보다는 발암과 종양의 성장에 필요한 특정한 표적 분자의 형성을 방해함으로써 암 세포의 증식을 막습니다. 암 세포 표적치료 방법은 정상 세포에 해롭지 않으면서 기존의 방법보다 효과적인 방법으로 예측되고 있습니다.
면역항암제는 인체의 면역체계를 활성화시켜 암 세포를 사멸하도록 유도하는 치료제로 3세대 항암제로 불리고 있으며, 인체의 면역체계를 강화하기 때문에 부작용이 적고, 효과가 광범위하며 면역체계의 기억능력을 통해 장기간 효과가 지속된다는 장점을 가지고 있습니다. 2011년 면역관문억제제(immune checkpoint inhibitor)인 BMS의 여보이(Yervoy®)를 시작으로 면역항암제 개발이 본격화되었으며, 2018년 9월까지 미국, 일본, 중국 등 글로벌 주요 국가에 18개의 면역항암제가 시판 승인되었습니다. 면역관문억제제가 기존 항암 치료제 대비 높은 효과성을 보여주고 있으나, 20~30% 내외의 환자에게만 반응하는 문제를 해결하기 위해 병용 연구가 활발하게 이루어지고 있으며, 이와 더불어 새로운 면역관문억제단백질을 타겟으로 하는 임상연구도 진행되고 있습니다.
IQVIA가 발표한 “2018년 전세계 항암제 트렌드” 신규보고서에 따르면 2022년에는 전세계 항암제 매출 규모는 2,000억 달러로 확대될 것으로 예상했습니다. 미국의 항암제 시장은 연간 12 ~ 15%의 성장율을 기록하면서 2020년에는 1,000억 달러 규모에 달할 것으로 전망하였고, 미국 이외의 항암제 시장도 10 ~ 13% 성장율로 1,000억달러 매출액을 돌파할 것으로 예측하였습니다.
당사가 연구개발중인 표적항암제의 타겟질환인 혈액암 치료제 시장은 GBI Research 보고에 따르면 2015년 307억에서 연 평균 성장률 12.5%로 증가하여 2022년 701억으로 예상하고 있습니다. 컨설팅 업체인 GlobalData에 따르면 급성골수성백혈병(acute myeloid leukemia, AML) 치료제 시장은 연 평균 10.5%로 빠르게 성장하여 2014년 342.7 백만 달러에서 2024년 932.6 백만 달러로 증가할 것으로 전망하고 있습니다. 급성골수성백혈병 환자의 약 10%를 브로모도메인 저해제로 치료가 가능할 것으로 예상되며(Blood 2016 127:42-52), 브로모도메인의 급성골수성백혈병에 대한 치료 시장규모는 2024년 약 93 백만 달러 규모로 추정됩니다.
당사가 연구중인 IRAK4 저해제의 주타겟 질환인 전체 DLBCL(ABC-DLBCL 포함)시장은 2016년 2.2 billion 달러에서 2025년 3.5 billion달러로 성장 예측되며 이 기간 사이에 DLBCL의 표준치료제인 Rituximab이 2019년 특허가 만료됨에 따라 Rituximab의 biosimiliar가 시장의 판도에 영향을 미치게 되면서 전체 마켓은 점차적으로 성장되는 것으로 예측되고 있습니다. 각각의 DLBCL subtype 별로 oncogenic mechanism 이 존재하는데 이중에서 기존 치료제에 대한 예후가 가장 좋지 않은 type이 ABC-DLBCL입니다(인용자료 : Datamonitor 2017).
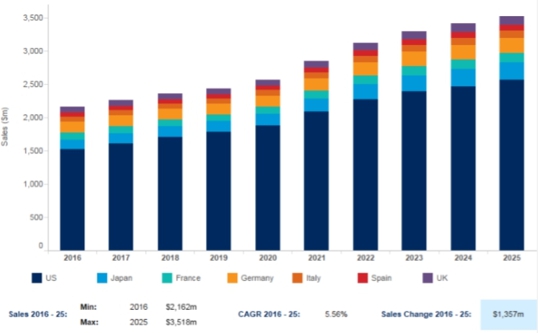 |
|
ABC-DLBCL Global 마켓 규모 예상 |
ABC-DLBCL subtype중에서 MyD88 mutation이 있는 경우는 대략 30%에 해당되며, 이러한 환자군은 기존 치료제에 대한 반응성 및 예후가 극히 좋지 않아 MyD88 mutation을 극복할 수 있는 치료제의 개발이 절실한 상황입니다.
(라) 심부전
심부전(Heart Failure)은 심장근육이 신체가 필요로 하는 충분한 혈액을 펌프질할 수 없을 때 일어나는 질환으로 관상동맥질환(동맥경화), 심근경색, 심근증, 고혈압, 심장내 판막 손상, 빈맥 등에 의해 발생합니다.
2017년 글로벌데이터는 주요7개국 심부전치료제 시장 규모가 연평균15.7%의 높은 성장율을 보이며2026년에는161억달러 규모로 확대될 것이라고 전망했습니다. 이러한 성장요인으로는 노바티스의 엔트레스토의 처방액 증가와 암젠과 사이토키네틱스의 오메캄티브 메카빌의 발매 및 만성심부전 유병율 증가, 급성심부전 발생율 증가 등이 꼽혔습니다. 다만, 기존의 만성심부전 치료제들은 수축기 심부전(HFrEF)에만 사망률과 이환율을 감소시켰지만 수축기 심부전에 대한 치료효과가 미비하다는 분석 결과가 있습니다.
2017년 7월에 세계적 시장조사기관인 글로벌데이터는 주요7개국 심부전치료제 시장 규모가 연평균15.7%의 높은 성장율을 보이며2016년 기준 37억달러에서 2026년에는 161억달러 규모로 확대될 것이라고 전망했습니다. 이러한 성장요인으로는 노바티스의 엔트레스토의 처방액 증가와 암젠과 사이토키네틱스의 오메캄티브 메카빌의 발매 및 만성심부전 유병율 증가, 급성심부전 발생율 증가 등이 꼽혔습니다.
4. 개발 및 경쟁 현황
(1) 파킨슨병 치료제
파킨슨병의 진전을 제어할 수 있는 질병조절 치료제의 개발이 매우 시급한 상황이며 연구개발이 활발하게 진행되고 있으나 적절한 치료제는 전무한 상황에 있습니다. 따라서 도파민을 보충해주는 증상완화제로 병의 증상을 줄여 생활에 도움이 되는 방법이 현재 표준 치료제로 사용되고 있습니다. 증상 완화제는 도파민 대체제, 도파민 효현제, MAO-B 저해제, COMT 저해제 등이 있습니다. 이러한 증상 완화제는 부족한 효능, 약물에 대한 빠른 내성과 약물소진 현상으로 인한 심각한 부작용 등의 문제가 있으며 질병의 진전은 계속적으로 이뤄져 중기 이후 더 이상 큰 효능이 없습니다.
최근 파킨슨병의 근본적 치료제 개발이 활발히 이루어지고 있으며 생물학적 제제인 항체치료제로는 Roche, Biogen, Denali Therapeutics 가 개발을 하고 있습니다. 그러나 대부분의 항체 의약품의 경우 혈액 뇌 관문(BBB) 통과율이 낮아 개발의 한계를 가지고 있습니다. 환자의 복용 편의성을 고려하여 경구용 제제로의 합성 의약품 개발이 필요하며 Abbvie, GSK, UCB 가 개발 중에 있으나, 아직 임상에서의 유효성을 확인한 약물은 없으며 타깃과 기전이 당사의 KM-819와는 다르기 때문에 경쟁보다는 시너지효과를 기대할 수 있습니다.
| [임상개발 중인 파킨슨병 치료제 파이프라인] |
|
| 출처) GlobalData, 2021 |
| [후기 개발 단계에 있는 파킨슨병 치료제] |
|
| 출처) GlobalData, 2021 |
당사가 개발중인 KM-819는 현재 파킨슨병 처방 약물의 대부분을 차지하는 증상완화제와는 명확히 구별되는, 병의 진전을 억제하고 정제하는 근본적 치료제이며, 타경쟁사와는 다른 전혀 새로운 작용기전을 가지고 있습니다. 파킨슨병 진전의 주된 두 원인으로는 도파민성 세포의 사멸(apoptosis)과 알파시누클라인(α-synuclein)의 응집에 기인한 세포 독성을 들 수 있습니다. KM-819는 이 두 타겟에 듀얼액션(Dual-action) 억제 기능을 작용하기 위해 FAF1이라는 단백질을 타겟으로 하는 유일한 약물입니다.
당사와 마찬가지로 저분자화합물 경구용 제재로 치료제를 개발중인 업체중에는 LRRK2 저해제로써 약물을 개발하거나, 엑서나타이드(Exernatide)처럼 당뇨병 치료제로 쓰이는 약을 파킨슨병에 적용하여 개발하는 곳이 있습니다. 하지만, LRRK 저해제는 해당 유전자의 변이를 가진 환자수가 다소 적으며, 당뇨병 치료제를 적용한 경우 역시 파킨슨병 임상에서는 어느 정도 효과가 있으나 근본치료제인지 증상 완화제 인지의 구별이 명확하지 않은 상황입니다.
주요 글로벌 경쟁 약물 현황 (질병조절 치료제)
|
개발명 |
제재/투여경로 |
경쟁업체/파트너제약사(국적) |
기술현황 |
|
|---|---|---|---|---|
|
개발 단계 |
타겟/적응증 |
|||
|
KM-819 |
저분자화합물/경구용 |
Kainos Medicine (한국) |
임상2상 승인 |
FAF1/파킨슨, 다계통위축증 |
|
Tau/a-synuclein program |
Vectorized 항체/주사제 |
Voyager(미국) |
임상 2상 진입 |
a-synuclein/파킨슨, 알파시누클라인병증(루이소체치매, 파킨슨병치매, 다계통위축증) |
|
PRX-002 |
항체/주사제 |
Prothena/Roche (스위스) |
임상 2b상 |
a-synuclein/파킨슨병 |
|
NPT200-11 |
저분자화합물/경구용 |
Neuropore/UCB (벨기에) |
임상 2a상 |
a-synuclein/파킨슨병 |
|
DNL151 |
저분자화합물/경구용 |
Denali Therapeutics (미국) |
임상 1b상 |
LRRK2/파킨슨병 |
|
BIIB054 |
항체/주사제 |
Biogen (미국) |
임상 2상 중단 |
a-synuclein/파킨슨병 |
|
GZ/SAR402671 |
항제/주사제 |
Sanofi Genzyme(프랑스) |
임상 2상 중단 |
Glucosylceramide synthase/파킨슨병 |
국내외적으로 파킨슨병에 대한 근본적 치료제에 대한 수요가 크지만, 아직까지 개발에 성공한 약물이 없는 상황입니다. 또한 인구 고령화로 인한 잠재 환자수의 급증, 치료제의 부재 등은 연구개발의 촉진요인으로 작용할 수 있습니다. 의약적 미충족 수요가 존재하는 근본적 치료제를 신약개발로 성공시키려면 임상에서 안정성과 효능(Proof of Concept)을 증명해야 하는 것이 가장 큰 진입 장벽이라고 할 수 있습니다. 현재 경쟁업체와 당사의 개발단계는 임상1b상~2상 초기 진행 등 크게 차이나지 않는 수준으로, KM-819 개발단계는 해외 경쟁사에 뒤쳐지지 않고, 효능증명에 의해 시장선점이 충분히 가능할 것으로 예상합니다.
또한 적응증 확대 대상인 다계통위축증은 발병 후 6~10년 사이에 사망에 이르게 되는 만큼 병의 진행속도가 빠른 퇴행성 신경질환 중 하나로 시장 의학적 수요가 매우 높은 질환입니다. 환자수는 파킨슨병의 5-10% 정도의 희귀질환으로 치료 효과가 거의 없어 치료제 개발이 시급한 상황에 있습니다. 몇 개의 임상이 진행 중에는 있으나, 아직 효능을 보인 약물이 없어 빠른 시장 진입은 가능할 것으로 예상합니다.
(2) 에이즈 치료제
NNRTI 계열의 에이즈 치료제는 Sustiva을 포함하여 4개가 시판 중에 있습니다. 에이즈치료제의 경우 다양한 계열의 약물을 복합제제 형태로 복용하는 병행요법(combination therapy)을 표준용법으로 사용하고 있습니다. 가장 많이 사용되는 병용용법이 2개의 NRTI 약물과 1개의 NNRTI약물의 병용용법으로 알려져 있습니다. 현재 시판중인 NNRTI 약물은 내성이 잘 생기고 장기복용시 독성 및 부작용의 문제로 인해 제한적으로 사용되고 있습니다. 에이즈는 만성질환으로 발전하고 있으며, 기존의 약제가 가진 부작용 및 복용의 제한과 같은 문제를 해결하기 위한 의약적 수요가 있으며 당사가 개발중인 KM023은 기존약제가 가진 항바이러스 활성을 유지하고 CNS 부작용에 안전하며 복용에 편의성을 높인 약제로 시장에서의 경쟁력을 갖추고 있습니다.
에이즈 시장에서의 주력제품은 시장에서 판매되고 있는 에파비렌즈(Efavirenz, EFV)와 릴피브린(Rilpivirine, RPV) 등을 비롯해 다양한 NNRTI계열의 약제가 판매되고 있으나, 중추신경게 부작용을 비롯한 다 양한 부작용이 보고되고 있습니다. 따라서 시장에서는 낮은 부작용과 복약편의성이 보완된 새로운 치료제의 의학적 수요가 있어 당사가 개발중인 제품은 충분한 경쟁력을 보유하고 있다고 판단됩니다.
|
[주요 경쟁업체 현황 ] |
|
분명 (약어) 상품명 |
경쟁업체 |
기술현황 |
||
|---|---|---|---|---|
|
용량/용법 |
Elimination/Metabolic Pathway |
부작용 |
||
|
Efavirenz (EFV) Sustiva |
BMS |
600 mg 1일 1회 부작용을 줄이기 위해 공복 |
EFV: CYPs 2B6 (primary), 3A4 및2A6에 의해 대사됨. CYP3A4 mixed inducer/inhibitor (억제보다 유도작용이 강함) CYP2C9 and 2C19 inhibitor; 2B6 inducer |
발진, 신경 정신병 증상, 간독성, 고지 질 혈증, 일부 카나비노이드 및 벤조디아제핀 선별 검사에서 가양성 결과 보고됨. |
|
Rilpivirine (RPV) Edurant |
J&J |
25 mg 1일 1회 식후 복용 |
RPV: CYP3A4 substrate |
발진, 우울증, 불면증, 두통, 간독성, QT interval prolongation |
|
Doravirine (DOR) |
머크 |
100mg 1일 1회 음식섭취와 무관 |
CYP3A4 substrate |
현기증, 구역질, 설사, 졸음 |
UNAIDS 2018에 따르면 에이즈 환자의 74.5%가 인도, 아프리카, 라틴아메리카에 거주하고 있으며, 글로벌 제약사가 개발한 기존의 에이즈 치료제는 대부분 고가의 약제로 소득수준이 낮은 개발도상국 및 이머징 시장으로의 진입에 제한적일 수 있습니다. 따라서 글로벌 제약사, WHO를 비롯한 다양한 기관의 지원으로 충당하고 있습니다. 당사가 개발중인 KM023은 낮은 생산 비용으로 인도, 아프리카, 남아메리카, 이머징 시장 등의 진입에 다소 우위에 있다고 볼 수 있습니다. 특히, 중국은 에이즈 환자가 급격히 증가하고 있기에 중국 정부에서 적극적으로 지원하는 제품으로 높은 시장 점유율을 기대하고 있습니다. 중국 정부는2018년 Beijing Summit of the Forum on China-Africa Cooperation에서 브라질, 아프리카 국가에 의약품을 지원하겠다는 발표와 함께 당사의 기술이전사인 중국Jiangsu Aidea와 해당 지원에 대한 논의 중으로, 중국 정부를 통한KM023의 해외 수출 가능성이 더욱 높아졌습니다.
(3) 항암제
○ 에피제네틱스 항암제 : 브로모도메인4 저해제(BRD4 inhibitor)
브로모도메인 저해제중 경구투여 약물로 머크의 OTX-015가 가장 앞서 있습니다. 경쟁약물 OTX-015(MK-8628, Merck)는 임상1상 결과 체내 흡수와 대사안정성이 낮고 고용량에서만 약효가 나타나게 되어 안전성에 대한 우려가 높습니다. 당사의 후보물질 KM-635는 혈액암과 고형암 치료에 효과적이며 약동력학적 성질이 경쟁약물대비 월등히 향상되어 경구투여가 가능한 “Best-in-Class”의 신약후보 물질입니다.
|
제품명/제약사 |
작용기전 |
개발단계 현황 |
비교 우위 |
|---|---|---|---|
|
OTX-015(MK-8628) / 머크 |
브로모도메인 저해제 |
임상 2상 |
◆경구투여 시 PK프로파일이 좋지 않아 고용량에서만 약효가 나타남. ◆경구용 저용량 투여약물의 필요성 대두됨. |
|
KM-635 /Kainos Medicine |
브로모도메인 저해제 |
임상 1상 |
◆월등히 향상된 약동력학적 성질: 경구투여 시 Dog에서 생체이용률: 92.3 % ◆다양한 혈액암과 고형암에 대한 우수한 약리효능이 동물실험에서 확인됨. ◆경구용 저용량 투여약물 후보물질. |
○ 세포독성 항암제 : 뉴클레오사이드 세포독성 항암제
대부분의 항암제를 차지하는 비경구 항암제에 비해 경구용 항암제는 매번 병원을 방문할 필요없이 복용의 편리성을 극대화시키며 주사 항암제에서 요구되는 혈관 확보가 불필요하며 비용을 감소시키고, 혈액 내 약물 농도의 유지를 가능케 합니다. 또한 경과 관찰 중 일시적인 투여 중지로 인한 심각한 독성을 예방할 수 있다는 장점이 보고되고 있습니다.
당사가 개발중인 KM-630은 급성골수성 백혈병의 표준 치료제로 사용되고 있는 Ara-C와 유사한 작용기전을 가지고 있습니다. 그러나 Ara-C와 같은 Cytidine계열의 화합물들은 체내에 존재하는 효소에 의해 탈아미노화가 일어나 약효가 없는 대사체로 바꿔주는 역할을 하는 효소인 Cytidine deaminase (CDA) 작용에 대한 저항성이 없습니다. 이러한 이유로 인하여 정맥에 의한 계속적인 주입식으로 환자에게 투여됩니다. 그러나 KM-630의 경우 이러한 문제를 완전히 극복하여 경구 혹은 정맥용 약물로 모두 활용이 가능하여 고형암으로의 적응증 확대가 가능 합니다.
◆ 우수한 대사안정성 및 생체이용률
◆ 고형암 세포를 대상으로 항암효과
◆ HDAC 저해제와의 중합 (hybrid)에 의한 시너지효과
◆ 복합항암화학요법(Combination Chemotherapy)의 수요에 부합
|
[경구용 항암 핵산 유사체 현황] |
|
약물명 |
개발현황 |
적응증 |
특이점 |
|---|---|---|---|
|
Sapacitabine |
임상3상 |
급성백혈병 비소세포 폐암 |
경구용, DNA 합성 억제 |
|
Capecitabine |
판매중(Xeloda) |
전이성 직장암, 유방암 |
경구용, DNA 합성 억제 |
|
LY2334737 |
임상 1상 |
비소세포 폐암, 유방암, 난소암 |
경구용 |
|
Cytarabineocfosfate |
임상1상 |
급성백혈병 |
경구용, DNA 합성 억제 |
|
Elacytarabine |
임상3상 중단 |
- |
Ara-C보다 우수한 결과 없음, DNA 합성 억제 |
○ 면역항암제 : CD 73 저분자 저해제(Small molecule inhibitor)
현재 CD73을 표적으로 하는 항체치료제는 AstraZeneca가 개발 중인 Oleclumab (MEDI9447)와 BMS의 BMS-986179, Norvatis의 SRF373/NZV930, Corvus사의 CPI-006이 있으며 각각 임상 1상 및 1/2a에 진행 중입니다. 국내에서는 한미약품이 미국 Phanes Therapeutics사를 통하여 CD47, CD73, LAG3/TIM-3 항체서열을 도입한 바 있습니다 (09, 17, 2019).
저분자화합물 기반의 CD73 저해제로는 가장 먼저Arcus사의 AB680이 주사용 약물로서 2018년 9월에 임상1상을 시작하여 현재 난치성전립선암(castration-resistant prostate cancer, CRPC) 환자를 대상으로 임상1b/2를 진행 중이며, 췌장선암(pancreatic-adenocarcinoma) 환자를 대상으로 임상 1상 진행중에 있으며 동일 약물의 경구용 약물개발을 위해 formulation단계에 있습니다. 미국의 Gilead Science가 Arcus의 면역항암제 임상 및 비임상 파이프라인에 대하여 향후 10년간 공동 개발 파트너로서 지원할 것을 발표하고 upfront로 $175Million의 현금지급과 $200Million의 지분출자를 한 바 있습니다(2020년 4월). Arcus사에 이어 Eli Lilly사에서 비핵산계열의 저분자물질인 LY3475070 이라는 경구용 약물로 유방암, 췌장암, 폐암, 신장암, 흑색종, 전립선암, 자궁암 등의 고형암환자(advanced solid cancer)를 환자를 대상으로 단독 혹은 펨브롤리주맙(Pembrolizumab)과의 복합투여로 임상1상을 시작하였으며(01, 16, 2020) Merk Sharp&Dohm Corp.(MSD)와의 공동연구로 임상을 진행하고 있습니다. 그 외에 경구용 약물로서 후보물질을 도출하고 비임상 준비 중인 제약사들은 Oric Pharmaceticals, Calithera, Peloton Therapeutics 등이 있으며 개발 초기 단계에 있는 회사들로는 Evotec, Selvita, X-chem, Aurigene, Bioardis LLC, Abbisko therapeutics등이 있습니다. 이 중 Peloton Therapeutics는 $1.05 billion (upfront) + $1.15 billion (milestone)으로 Merck에 인수합병 되었습니다(2019년 5월). 이렇듯 아직까지 경구용 저분자 약물로서 임상에 진입한 글로벌제약사는 없지만 지난 한 해 동안 CD73타겟의 면역체크포인트 저해제 파이프라인을 갖는 바이오텍 회사들을 글로벌 제약사들이 인수합병 하거나 공동연구 및 개발 형태의 비즈니스딜을 하는 등 눈에 띄는 관심과 성과들이 급속히 증가하였습니다.
이에 당사는 기존의 표적항암제 개발 파이프라인을 통해 축적된 의약화학 전문기술을 바탕으로 기존 표적항암제의 부작용 및 내성문제와 항체의약품의 한계를 극복한 저분자화합물을 기반으로 하는 효율적이고 안전하며 혁신적인 경구용 면역항암제 상용화를 위한 파이프라인을 구축하는 차별화 전략을 수립하였습니다.
○ 면역항암제 : PD-L1 저분자 저해제(Small molecule inhibitor)
PD-1 및 PD-L1을 타깃으로 하는 치료제는 현재 다수가 시판 중에 있으나, 모두가 mAb (monoclonal antibody)라는 점에서 매우 고가이고 경구투여가 불가능하다는 단점이 있으며, 그 외에도 저분자 저해제(small molecule inhibitor)와 비교하여 여러가지 단점이 존재합니다.
당사는 기존anti-PD-1/PD-L1 mAb (monoclonal antibody)의 단점을 극복한 PD-L1 저분자 저해제(small molecule inhibitor)를 개발하고 있으며, 항체에 비해 가격이 매우 저렴하고, 경구투여가 가능하여 환자의 복용 편의성이 높습니다. 또한 항체보다 단시간 작용하여 면역과 관련한 부작용(irAEs)에 대한 관리가 용이하고, 항체의Fc region에 의한 항체의존세포매개세포독성(ADCC)으로 인한 독성을 유발하지 않는다는 장점을 가지고 있습니다.
○ 표적항암제 : IRAK4 저해제 (IRAK4 inhibitor)
Integrity prous의 자료에 따르면 IRAK4 저해제는 주로 inflammation 관련 질환(염증성 장염 및 염증성 질환)의 보고사례가 많고, 국내외 각 회사별 개발 현황은 신약발굴 단계 및 전임상 단계에 대부분 분포하고 있습니다.
이중 Pfizer의 Pf-06650833이 류마티스성 관절염으로 임상 2상을 완료하여 Clinicaltrials.com에 결과를 공유하였습니다. 본 임상 study를 통해 Methotrexate불응 환자를 대상으로 Tofacitinib과의 병용투여를 통해 약효를 입증하는 연구를 수행하였고 유의성 있는 결과를 도출하여 향후 개발 진행에 대한 기대감을 높였습니다.
항암제로서의 IRAK4 저해제는 전임상 단계 및 biological testing단계에 대부분 머무르고 있었지만 최근에 변화된 동향으로는Curis가 Aurigene의 IRAK4 저해제를 2015년 1월에 License-in 하면서 개발에 뛰어들었고 전임상 단계를 수행 완료하여 2017년 12월 28일 ABC-DLBCL을 타겟 질환으로 임상에 진입하였습니다. 현재는 임상 1상을 미국에서 진행 중에 있습니다.
Curis의 CA-4948은 IRAK4저해 작용 항암제로서 가장 앞서 나가는 경쟁자가 되었으며, 특히 MyD88 mutation된 ABC-DLBCL 질환을 주타겟 질환으로 선정하여 개발을 진행하고 있는 점이 당사와 매우 일치합니다. 따라서 당사는 경쟁자인 Curis의 CA-4948의 추가연구 결과 및 임상 결과 등을 지속적으로 확인 및 분석하여 당사 제품의 경쟁력 및 성공가능성이 높은 개발전략을 확보하는 것에 활용할 예정입니다.
당사의 IRAK4 저해제 개발 프로젝트는 현재 리드최적화 단계를 통해 개발후보물질을 도출하였고 이 물질을 통한 in vitro, in vivo POC 검증을 수행 중입니다. Curis의 개발전략을 참조하되 당사만의 독창적인 연구결과를 통해 보다 나은 적응증을 찾으려는 연구도 병행하여 진행 중인 전략으로 연구과제가 관리되고 있습니다.
(4) 심부전 치료제
심부전은 심장의 좌심실박출률에 따라 좌심실박출률 저하 심부전(HFeRF) 및 좌심실박출률보전 심부전(HFpRF)로 나뉘며 좌심실 박출률 저하 심부전(HFrEF)의 약물 치료는 레닌-안지오텐신계 차단제(안지오텐신전환효소억제제, 안지오텐신수용체길항제), 베타차단제, 알도스테론 차단제, Ivabradine, EntrestoTM (valsartan/sacubitril)등이 사용됩니다. 이중에서 EntrestoTM는 안지오텐신수용체와 네프릴리신길항제 복합제로서 임상에서 뚜렷한 사망률 감소 및 안정성 증가 효과를 보여주어 현재로서 가장 주목받는 심부전 치료제입니다.
이와 반면에 좌심실 박출률 보존 심부전(HFpEF)의 치료는 뚜렷한 약제 치료가 확립되어 있지 않습니다. 전체적으로는 EntrestoTM으로 인해 심부전 치료의 많은 도움이 되고 있으나, 아직까지도 새로운 기전의 심부전 치료제의 개발이 의학적 수요로 남아있고 따라서 기존의 약물 치료의 작용기전과는 차별화되는 신규 작용기전의 약물 개발이 시급하다고 할 수 있습니다.
5. 지적재산권 현황
|
현황 |
출원명칭 (내용) |
권리자 |
출원일 |
등록일 |
출원국 |
적응증 |
|---|---|---|---|---|---|---|
|
등록 |
신규한 HIV 역전사효소 억제제 |
한국화학 연구원 |
09.12.28 |
15.02.26 |
독일 |
에이즈 |
|
15.02.27 |
스페인 |
|||||
|
15.02.28 |
프랑스 |
|||||
|
15.03.01 |
영국 |
|||||
|
15.03.02 |
이탈리아 |
|||||
|
09.12.25 |
14.10.22 |
중국 |
||||
|
09.12.21 |
17.08.14 |
인도 |
||||
|
09.12.16 |
13.06.06 |
멕시코 |
||||
|
08.06.26 |
12.12.18 |
미국 |
||||
|
10.01.28 |
15.06.26 |
대한민국 |
||||
|
등록 |
PROCESSES FOR PREPARING HIV REVERSE TRANSCRIPTASE INHIBITORS |
한국화학 연구원 |
11.07.25 |
13.12.10 |
미국 |
에이즈 |
|
등록 |
COMPOUNDS AS INHIBITORS OF DIACYLGLYCEROL |
㈜카이노스메드 |
13.02.06 |
16.03.01 |
미국 |
비만당뇨 |
|
출원 |
브로모도메인-억제 화합물 및 상기 화합물을 포함하는 암 예방 또는 치료용 약학 조성물 |
㈜카이노스메드 |
16.09.26 |
- |
중국 |
브로모도메인 |
|
등록 |
16.11.04 |
19.06.26 |
오스트리아 |
|||
|
16.11.04 |
19.06.26 |
벨기에 |
||||
|
16.11.04 |
19.06.26 |
스위스 |
||||
|
16.11.04 |
19.06.26 |
독일 |
||||
|
16.11.04 |
19.06.26 |
덴마크 |
||||
|
16.11.04 |
19.06.26 |
스페인 |
||||
|
16.11.04 |
19.06.26 |
핀란드 |
||||
|
16.11.04 |
19.06.26 |
프랑스 |
||||
|
16.11.04 |
19.06.26 |
영국 |
||||
|
16.11.04 |
19.06.26 |
이탈리아 |
||||
|
16.11.04 |
19.06.26 |
네덜란드 |
||||
|
16.11.04 |
19.06.26 |
폴란드 |
||||
|
16.11.04 |
19.06.26 |
스웨덴 |
||||
|
16.09.01 |
20.12.22 |
인도 |
||||
|
16.10.07 |
18.05.11 |
일본 |
||||
|
16.09.27 |
18.02.06 |
미국 |
||||
|
16.11.03 |
18.12.06 |
대한민국 |
||||
|
등록 |
MUTUAL PRODRUG COMPRISING SHORT CHAIN FATTY ACIDS AND ZEBULARINE OR 1’-CYANO-CYTARABINE FOR CANCER TREATMENT |
㈜카이노스메드 |
16.11.03 |
18.06.15 |
대한민국 |
세포독성 |
|
출원 |
16.05.05 |
- |
중국 |
|||
|
등록 |
16.04.15 |
19.12.10 |
미국 |
|||
|
출원 |
16.04.27 |
- |
인도 |
|||
|
등록 |
16.05.13 |
17.09.29 |
일본 |
|||
|
출원 |
16.04.20 |
- |
브라질 |
|||
|
등록 |
16.06.01 |
20.01.08 |
오스트리아 |
|||
|
16.06.01 |
20.01.08 |
벨기에 |
||||
|
16.06.01 |
20.01.08 |
스위스 |
||||
|
16.06.01 |
20.01.08 |
독일 |
||||
|
16.06.01 |
20.01.08 |
덴마크 |
||||
|
16.06.01 |
20.01.08 |
스페인 |
||||
|
16.06.01 |
20.01.08 |
프랑스 |
||||
|
16.06.01 |
20.01.08 |
영국 |
||||
|
16.06.01 |
20.01.08 |
헝가리 |
||||
|
16.06.01 |
20.01.08 |
아일랜드 |
||||
|
16.06.01 |
20.01.08 |
이탈리아 |
||||
|
16.06.01 |
20.01.08 |
네덜란드 |
||||
|
16.06.01 |
20.01.08 |
노르웨이 |
||||
|
16.06.01 |
20.01.08 |
폴란드 |
||||
|
16.06.01 |
20.01.08 |
스웨덴 |
||||
|
등록 |
아미노피라졸 유도체, 이의 제조 방법 및 이를 함유하는 허혈성 질환의 예방 또는 치료용 조성물 |
한국화학 연구원 |
09.03.12 |
15.08.26 |
오스트리아 |
파킨슨 |
|
09.03.12 |
15.08.26 |
벨기에 |
||||
|
09.03.12 |
15.08.26 |
스위스 |
||||
|
09.03.12 |
15.08.26 |
독일 |
||||
|
09.03.12 |
15.08.26 |
덴마크 |
||||
|
09.03.12 |
15.08.26 |
스페인 |
||||
|
09.03.12 |
15.08.26 |
프랑스 |
||||
|
09.03.12 |
15.08.26 |
영국 |
||||
|
09.03.12 |
15.08.26 |
이탈리아 |
||||
|
09.03.12 |
15.08.26 |
네덜란드 |
||||
|
09.03.12 |
15.08.26 |
폴란드 |
||||
|
09.03.12 |
15.08.26 |
스웨덴 |
||||
|
09.03.12 |
15.08.26 |
터키 |
||||
|
09.05.26 |
11.08.11 |
호주 |
||||
|
09.04.15 |
11.11.15 |
캐나다 |
||||
|
09.04.27 |
12.03.14 |
중국 |
||||
|
09.04.27 |
12.09.28 |
일본 |
||||
|
09.04.27 |
11.05.10 |
미국 |
||||
|
06.10.27 |
08.05.21 |
대한민국 |
||||
|
출원 |
알파-시누클레인 조절제 |
FAScinate |
18.06.19 |
- |
대한민국 |
파킨슨 |
| 18.06.19 | - | PCT | ||||
|
19.12.12 |
- |
미국 |
||||
|
19.12.16 |
- |
멕시코 |
||||
|
19.12.19 |
- |
중국 |
||||
|
20.01.08 |
- |
유럽 |
||||
|
20.01.16 |
- |
러시아 |
||||
|
19.12.19 |
- |
사우디아라비아 |
||||
|
19.12.18 |
- |
브라질 |
||||
|
20.01.16 |
- |
호주 |
||||
|
19.12.10 |
- |
일본 |
||||
|
19.12.12 |
- |
캐나다 |
||||
|
19.12.11 |
- |
이스라엘 |
||||
|
출원 |
Salt forms of organic compound |
㈜카이노스메드 |
19.01.31 |
- |
대한민국 |
파킨슨 |
| FAScinate |
19.01.31 |
- |
PCT |
|||
|
20.07.28 |
- |
브라질 |
||||
| 등록 |
18.01.31 |
22.02.28 |
미국 |
|||
| 출원 |
20.07.31 |
- |
캐나다 |
|||
|
20.07.28 |
- |
유럽 |
||||
|
20.08.18 |
- |
중국 |
||||
|
20.07.21 |
- |
이스라엘 |
||||
|
20.08.05 |
- |
멕시코 |
||||
|
20.07.29 |
- |
호주 |
||||
|
20.08.13 |
- |
인도 |
||||
| 20.07.29 | - | 일본 | ||||
|
출원 |
Compounds and compositions for Ectonucleotidase inhibition |
㈜카이노스메드 |
20.08.24 |
- |
PCT |
항암제 |
|
출원 |
Novel N-(1H-imidazol-2-yl)Benzamide compounds and pharmaceutical composition containing the same as an active ingredient |
㈜카이노스메드 |
20.09.29 |
- |
PCT |
항암제 |
|
출원 |
PYRIDINE DERIVATIVES AS IMMUNOMODULATORS |
㈜카이노스메드 |
20.06.03 |
- |
|
항암제 |
| 출원 | FAF1(Fas-associated factor 1)이 로딩된 엑소좀 및 이를 포함하는 자궁경부암 치료용 약학적 조성물 | ㈜카이노스메드 | 21.03.30 | - | 대한민국 | FAF1-Exosome |
| 출원 | FAF1-loaded exosomes and composition for cervical cancer treatment comprising the same | ㈜카이노스메드 | 22.03.30 | - | PCT | |
|
출원 |
N-(1H-IMIDAZOL-2-YL)BENZAMIDE COMPOUND AND PHARMACEUTICAL COMPOSITION COMPRISING THE SAME AS ACTIVE INGREDIENT | ㈜카이노스메드 |
20.09.29 |
- |
PCT |
항암제 |
| 22.04.12 | - | 호주 | ||||
|
22.03.21 |
- | 인도 | ||||
|
22.03.21 |
- | 싱가포르 | ||||
| 22.03.25 | - | 중국 | ||||
| 22.03.29 | - | 멕시코 | ||||
| 22.03.29 | - | 미국 | ||||
| 22.03.30 | - | 캐나다 | ||||
| 22.03.31 | - | 브라질 | ||||
| - | - | 일본 | ||||
| - | - | 러시아 |
| 구분 |
현황 |
출원명칭 (내용) |
권리자 |
출원일 |
등록일 |
출원국 |
적응증 |
|---|---|---|---|---|---|---|---|
| 1 |
등록 |
신규한 HIV 역전사효소 억제제 |
한국화학 연구원 |
09.12.28 |
15.02.26 |
독일 |
에이즈 |
| 2 |
15.02.27 |
스페인 |
|||||
| 3 |
15.02.28 |
프랑스 |
|||||
| 4 |
15.03.01 |
영국 |
|||||
| 5 |
15.03.02 |
이탈리아 |
|||||
| 6 |
09.12.25 |
14.10.22 |
중국 |
||||
| 7 |
09.12.21 |
17.08.14 |
인도 |
||||
| 8 |
09.12.16 |
13.06.06 |
멕시코 |
||||
| 9 |
08.06.26 |
12.12.18 |
미국 |
||||
| 10 |
10.01.28 |
15.06.26 |
대한민국 |
||||
| 11 |
등록 |
PROCESSES FOR PREPARING HIV REVERSE TRANSCRIPTASE INHIBITORS |
한국화학 연구원 |
11.07.25 |
13.12.10 |
미국 |
에이즈 |
| 12 |
등록 |
COMPOUNDS AS INHIBITORS OF DIACYLGLYCEROL |
㈜카이노스메드 |
13.02.06 |
16.03.01 |
미국 |
비만당뇨 |
| 13 |
출원 |
브로모도메인-억제 화합물 및 상기 화합물을 포함하는 암 예방 또는 치료용 약학 조성물 |
㈜카이노스메드 |
16.09.26 |
- |
중국 |
브로모도메인 |
| 14 |
등록 |
16.11.04 |
19.06.26 |
오스트리아 |
|||
| 15 |
16.11.04 |
19.06.26 |
벨기에 |
||||
| 16 |
16.11.04 |
19.06.26 |
스위스 |
||||
| 17 |
16.11.04 |
19.06.26 |
독일 |
||||
| 18 |
16.11.04 |
19.06.26 |
덴마크 |
||||
| 19 |
16.11.04 |
19.06.26 |
스페인 |
||||
| 20 |
16.11.04 |
19.06.26 |
핀란드 |
||||
| 21 |
16.11.04 |
19.06.26 |
프랑스 |
||||
| 22 |
16.11.04 |
19.06.26 |
영국 |
||||
| 23 |
16.11.04 |
19.06.26 |
이탈리아 |
||||
| 24 |
16.11.04 |
19.06.26 |
네덜란드 |
||||
| 25 |
16.11.04 |
19.06.26 |
폴란드 |
||||
| 26 |
16.11.04 |
19.06.26 |
스웨덴 |
||||
| 27 |
16.09.27 |
20.12.22 |
인도 |
||||
| 28 |
16.10.07 |
18.05.11 |
일본 |
||||
| 29 |
16.09.27 |
18.02.06 |
미국 |
||||
| 30 |
16.11.03 |
18.12.06 |
대한민국 |
||||
| 31 |
등록 |
MUTUAL PRODRUG COMPRISING SHORT CHAIN FATTY ACIDS AND ZEBULARINE OR 1’-CYANO-CYTARABINE FOR CANCER TREATMENT |
㈜카이노스메드 |
16.11.03 |
18.06.15 |
대한민국 |
세포독성 |
| 32 |
출원 |
16.05.05 |
- |
중국 |
|||
| 33 |
등록 |
16.04.15 |
19.12.10 |
미국 |
|||
| 34 |
출원 |
16.04.27 |
- |
인도 |
|||
| 35 |
등록 |
16.05.13 |
17.09.29 |
일본 |
|||
| 36 |
출원 |
16.04.20 |
- |
브라질 |
|||
| 37 |
등록 |
16.06.01 |
20.01.08 |
오스트리아 |
|||
| 38 |
16.06.01 |
20.01.08 |
벨기에 |
||||
| 39 |
16.06.01 |
20.01.08 |
스위스 |
||||
| 40 |
16.06.01 |
20.01.08 |
독일 |
||||
| 41 |
16.06.01 |
20.01.08 |
덴마크 |
||||
| 42 |
16.06.01 |
20.01.08 |
스페인 |
||||
| 43 |
16.06.01 |
20.01.08 |
프랑스 |
||||
| 44 |
16.06.01 |
20.01.08 |
영국 |
||||
| 45 |
16.06.01 |
20.01.08 |
헝가리 |
||||
| 46 |
16.06.01 |
20.01.08 |
아일랜드 |
||||
| 47 |
16.06.01 |
20.01.08 |
이탈리아 |
||||
| 48 |
16.06.01 |
20.01.08 |
네덜란드 |
||||
| 49 |
16.06.01 |
20.01.08 |
노르웨이 |
||||
| 50 |
16.06.01 |
20.01.08 |
폴란드 |
||||
| 51 |
16.06.01 |
20.01.08 |
스웨덴 |
||||
| 52 | 등록 |
아미노피라졸 유도체, 이의 제조 방법 및 이를 함유하는 허혈성 질환의 예방 또는 치료용 조성물 |
한국화학 연구원 |
09.03.12 |
15.08.26 |
오스트리아 |
파킨슨 |
| 53 |
09.03.12 |
15.08.26 |
벨기에 |
||||
| 54 |
09.03.12 |
15.08.26 |
스위스 |
||||
| 55 |
09.03.12 |
15.08.26 |
독일 |
||||
| 56 |
09.03.12 |
15.08.26 |
덴마크 |
||||
| 57 |
09.03.12 |
15.08.26 |
스페인 |
||||
| 58 |
09.03.12 |
15.08.26 |
프랑스 |
||||
| 59 |
09.03.12 |
15.08.26 |
영국 |
||||
| 60 |
09.03.12 |
15.08.26 |
이탈리아 |
||||
| 61 |
09.03.12 |
15.08.26 |
네덜란드 |
||||
| 62 |
09.03.12 |
15.08.26 |
폴란드 |
||||
| 63 |
09.03.12 |
15.08.26 |
스웨덴 |
||||
| 64 |
09.03.12 |
15.08.26 |
터키 |
||||
| 65 |
09.05.26 |
11.08.11 |
호주 |
||||
| 66 |
09.04.15 |
11.11.15 |
캐나다 |
||||
| 67 |
09.04.27 |
12.03.14 |
중국 |
||||
| 68 |
09.04.27 |
12.09.28 |
일본 |
||||
| 69 |
09.04.27 |
11.05.10 |
미국 |
||||
| 70 |
06.10.27 |
08.05.21 |
대한민국 |
||||
| 71 | 출원 |
알파-시누클레인 조절제 |
㈜카이노스메드 |
19.12.23 |
- |
대한민국 |
파킨슨 |
| 72 |
20.01.16 |
- |
뉴질랜드 |
||||
| 73 |
19.12.12 |
- |
미국 |
||||
| 74 |
19.12.16 |
- |
멕시코 |
||||
| 75 |
19.12.19 |
- |
중국 |
||||
| 76 |
20.01.08 |
- |
유럽 |
||||
| 77 |
20.01.16 |
- |
러시아 |
||||
| 78 |
19.12.19 |
- |
사우디아라비아 |
||||
| 79 |
19.12.05 |
- |
싱가포르 |
||||
| 80 |
19.12.18 |
- |
브라질 |
||||
| 81 |
20.01.16 |
- |
호주 |
||||
| 82 |
20.06.30 |
- |
홍콩 |
||||
| 83 |
19.12.10 |
- |
일본 |
||||
| 84 |
19.12.12 |
- |
캐나다 |
||||
| 85 |
19.12.11 |
- |
이스라엘 |
||||
| 86 |
출원 |
Salt forms of organic compound |
㈜카이노스메드 |
19.01.30 |
- |
PCT |
파킨슨 |
| 87 |
20.07.28 |
- |
브라질 |
||||
| 88 | 출원 |
18.01.31 |
- |
미국 |
|||
| 89 | 출원 |
20.07.31 |
- |
캐나다 |
|||
| 90 |
20.07.28 |
- |
유럽 |
||||
| 91 |
20.08.18 |
- |
중국 |
||||
| 92 |
20.07.21 |
- |
이스라엘 |
||||
| 93 |
20.08.05 |
- |
멕시코 |
||||
| 94 |
20.07.29 |
- |
호주 |
||||
| 95 |
20.08.13 |
- |
인도 |
||||
| 96 |
출원 |
Compounds and compositions for Ectonucleotidase inhibition |
㈜카이노스메드 |
20.08.24 |
- |
PCT |
항암제 |
| 97 |
출원 |
Novel N-(1H-imidazol-2-yl)Benzamide compounds and pharmaceutical composition containing the same as an active ingredient |
㈜카이노스메드 |
20.09.29 |
- |
PCT |
항암제 |
| 98 |
가출원 |
PYRIDINE DERIVATIVES AS IMMUNOMODULATORS |
㈜카이노스메드 |
20.06.03 |
- |
미국/ |
항암제 |
III. 재무에 관한 사항
1. 요약재무정보
가. 요약 연결재무제표
(단위 : 원)
| 구 분 | 제6기 1분기 | 제5기 | 제4기 |
|---|---|---|---|
| [유동자산] | 32,984,886,423 | 36,872,532,277 | 31,986,741,328 |
| [비유동자산] | 6,486,913,481 | 5,084,230,116 | 2,791,822,268 |
| 자산총계 | 39,471,799,904 | 41,956,762,393 | 34,778,563,596 |
| [유동부채] | 27,654,752,803 | 25,655,366,297 | 4,167,332,703 |
| [비유동부채] | 135,019,852 | 1,701,213,795 | 17,590,775,496 |
| 부채총계 | 27,789,772,655 | 27,356,580,092 | 21,758,108,199 |
| [지배기업 소유지분] | 8,765,467,404 | 12,103,530,375 | 12,352,647,873 |
| - 자본금 | 11,039,826,200 | 11,028,980,300 | 10,494,262,900 |
| - 주식발행초과금 | 77,089,276,005 | 76,912,501,241 | 63,950,642,778 |
| - 기타자본항목 | 9,736,435,418 | 9,460,459,263 | 6,994,589,247 |
| - 이익잉여금 | -89,100,070,219 | -85,298,410,429 | -69,086,847,052 |
| [비지배지분] | 2,916,559,845 | 2,496,651,926 | 667,807,524 |
| 자본총계 | 11,682,027,249 | 14,600,182,301 | 13,020,455,397 |
| 구분 | 2022년 1월~3월 | 2021년 1월~12월 | 2020년 1월~12월 |
| 매출액 | 3,667,259 | 1,662,425,507 | |
| 영업이익 | -3,877,895,251 | -11,219,274,373 | -9,385,681,209 |
| 당기순이익 | -3,807,648,313 | -16,225,404,831 | -11,447,653,059 |
| 주당이익(손실) | |||
| 기본주당순이익(원) | -34 | -153 | -113 |
| 희석주당순이익(원) | -34 | -153 | -113 |
나. 요약 재무제표
(단위 : 원)
| 구 분 | 제6기 1분기 | 제5기 | 제4기 |
|---|---|---|---|
| [유동자산] | 16,466,845,706 | 19,220,124,258 | 13,016,751,462 |
| [비유동자산] | 16,317,888,706 | 16,466,476,231 | 17,833,817,484 |
| 자산총계 | 32,784,734,412 | 35,686,600,489 | 30,850,568,946 |
| [유동부채] | 23,894,303,311 | 21,892,515,588 | 1,010,526,249 |
| [비유동부채] | 124,963,698 | 1,690,554,526 | 17,487,394,824 |
| 부채총계 | 24,019,267,009 | 23,583,070,114 | 18,497,921,073 |
| - 자본금 | 11,039,826,200 | 11,028,980,300 | 10,494,262,900 |
| - 주식발행초과금 | 77,089,276,005 | 76,912,501,241 | 63,950,642,778 |
| - 기타자본항목 | 9,783,317,696 | 9,886,841,510 | 8,887,589,085 |
| - 이익잉여금 | -89,146,952,498 | -85,724,792,676 | -70,979,846,890 |
| 자본총계 | 8,765,467,403 | 12,103,530,375 | 12,352,647,873 |
| 구분 | 2022년 1월~3월 | 2021년 1월~12월 | 2020년 1월~12월 |
| 매출액 | 3,667,259 | 4,013,025,507 | |
| 영업이익 | -2,577,650,590 | -5,900,250,010 | -8,417,500,666 |
| 당기순이익 | -3,422,159,822 | -14,744,945,786 | -13,340,652,897 |
| 주당이익(손실) | |||
| 기본주당순이익(원) | -31 | -139 | -131 |
| 희석주당순이익(원) | -31 | -139 | -131 |
2. 연결재무제표
|
연결 재무상태표 |
|
제 6 기 1분기말 2022.03.31 현재 |
|
제 5 기말 2021.12.31 현재 |
|
(단위 : 원) |
|
제 6 기 1분기말 |
제 5 기말 |
|
|---|---|---|
|
자산 |
||
|
Ⅰ.유동자산 |
32,984,886,423 |
36,872,532,277 |
|
(1)현금및현금성자산 |
18,553,535,500 |
23,230,921,994 |
|
(2)단기금융상품 |
13,000,000,000 |
11,000,000,000 |
|
(3)파생상품자산 |
309,735,458 |
309,735,458 |
|
(4)매출채권 및 기타채권 |
163,203,162 |
300,888,253 |
|
(5)선급금 |
1,840,000 |
1,975,000 |
|
(6)선급비용 |
845,291,298 |
1,951,303,891 |
|
(7)부가세대급금 |
98,624,255 |
68,297,331 |
|
(8)당기법인세자산 |
12,656,750 |
9,410,350 |
|
(9)유동 당기손익-공정가치 의무 측정 금융자산 |
||
|
Ⅱ.비유동자산 |
6,486,913,481 |
5,084,230,116 |
|
(1)당기손익-공정가치 측정 지정 금융자산 |
1,248,186,695 |
642,786,695 |
|
(2)유형자산 |
3,539,898,311 |
2,871,508,712 |
|
(3)사용권자산 |
366,481,469 |
462,108,251 |
|
(4)무형자산 |
905,587,905 |
689,035,141 |
|
(5)장기매출채권및기타채권 |
185,243,806 |
179,667,923 |
|
(6)장기선급금 |
241,515,295 |
239,123,394 |
|
자산총계 |
39,471,799,904 |
41,956,762,393 |
|
부채 |
||
|
Ⅰ.유동부채 |
27,654,752,803 |
25,655,366,297 |
|
(1)차입금 |
2,285,014,200 |
|
|
(2)미지급금 및 기타채무 |
625,720,358 |
846,100,706 |
|
(3)예수금 |
(16,853,163) |
79,954,451 |
|
(4)유동리스부채 |
231,928,069 |
276,267,801 |
|
(5)전환우선주 |
3,632,400,000 |
3,556,500,000 |
|
(6)전환사채 |
12,467,965,487 |
12,467,965,487 |
|
(7)파생상품부채 |
8,428,577,852 |
8,428,577,852 |
|
Ⅱ.비유동부채 |
135,019,852 |
1,701,213,795 |
|
(1)장기차입금 |
1,523,342,800 |
|
|
(2)장기미지급금 |
||
|
(3)비유동리스부채 |
60,897,708 |
103,949,551 |
|
(4)복구충당부채 |
74,122,144 |
73,921,444 |
|
(5)전환사채 |
||
|
(6)비유동파생상품부채 |
||
|
부채총계 |
27,789,772,655 |
27,356,580,092 |
|
자본 |
||
|
Ⅰ.지배기업의 소유주에게 귀속되는 자본 |
8,765,467,404 |
12,103,530,375 |
|
(1)자본금 |
11,039,826,200 |
11,028,980,300 |
|
(2)주식발행초과금 |
77,089,276,005 |
76,912,501,241 |
|
(3)기타자본구성요소 |
9,736,435,418 |
9,460,459,263 |
|
(4)결손금 |
(89,100,070,219) |
(85,298,410,429) |
|
Ⅱ.비지배지분 |
2,916,559,845 |
2,496,651,926 |
|
자본총계 |
11,682,027,249 |
14,600,182,301 |
|
자본과부채총계 |
39,471,799,904 |
41,956,762,393 |
|
연결 포괄손익계산서 |
|
제 6 기 1분기 2022.01.01 부터 2022.03.31 까지 |
|
제 5 기 1분기 2021.01.01 부터 2021.03.31 까지 |
|
(단위 : 원) |
|
제 6 기 1분기 |
제 5 기 1분기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
Ⅰ.매출액 |
3,667,259 |
3,667,259 |
92,141,667 |
92,141,667 |
|
Ⅱ.매출원가 |
1,098,361 |
1,098,361 |
||
|
Ⅲ.매출총이익 |
2,568,898 |
2,568,898 |
92,141,667 |
92,141,667 |
|
Ⅳ.판매비와관리비 |
3,880,464,149 |
3,880,464,149 |
3,620,325,955 |
3,620,325,955 |
|
Ⅴ.영업이익(손실) |
(3,877,895,251) |
(3,877,895,251) |
(3,528,184,288) |
(3,528,184,288) |
|
Ⅵ.기타수익 |
29,718,109 |
29,718,109 |
28,364,755 |
28,364,755 |
|
Ⅶ.기타비용 |
2,264,207 |
2,264,207 |
1,423,612 |
1,423,612 |
|
Ⅷ.금융수익 |
71,312,393 |
71,312,393 |
19,358,195 |
19,358,195 |
|
Ⅸ.금융비용 |
9,685,562 |
9,685,562 |
12,700,208 |
12,700,208 |
|
Ⅹ.법인세비용차감전순이익(손실) |
(3,788,814,518) |
(3,788,814,518) |
(3,494,585,158) |
(3,494,585,158) |
|
XI.법인세비용(수익) |
(18,833,795) |
(18,833,795) |
3,984,257 |
3,984,257 |
|
XⅡ.당기순이익(손실) |
(3,807,648,313) |
(3,807,648,313) |
(3,490,600,901) |
(3,490,600,901) |
|
XⅢ.연결당기순이익(손실)의 귀속 |
||||
|
(1)지배기업의 소유주에게 귀속되는 당기순이익(손실) |
(3,801,659,790) |
(3,801,659,790) |
(3,490,600,901) |
(3,490,600,901) |
|
(2)비지배지분에 귀속되는 당기순이익(손실) |
(5,988,523) |
(5,988,523) |
||
|
XIV.기타포괄손익 |
317,626,431 |
317,626,431 |
696,848,658 |
696,848,658 |
|
(1)후속적으로 당기손익으로 재분류되는 항목 |
||||
|
1.해외사업환산손익 |
(61,873,536) |
(61,873,536) |
14,348,716 |
14,348,716 |
|
2.해외사업장순투자환산손실 |
379,499,967 |
379,499,967 |
682,499,942 |
682,499,942 |
|
XV.총포괄손익 |
(3,490,021,882) |
(3,490,021,882) |
(2,793,752,243) |
(2,793,752,243) |
|
XVI.당기총포괄손익의 귀속 |
||||
|
(1)지배기업의 소유주에게 귀속되는 총포괄손익 |
(3,487,768,399) |
(3,487,768,399) |
(2,793,752,243) |
(2,793,752,243) |
|
(2)비지배지분에 귀속되는 총포괄손익 |
(2,253,483) |
(2,253,483) |
||
|
XVII.주당이익(손실) |
||||
|
(1)기본주당이익(손실) (단위 : 원) |
(34) |
(34) |
(33) |
(33) |
|
(2)희석주당이익(손실) (단위 : 원) |
(34) |
(34) |
(33) |
(33) |
|
연결 자본변동표 |
|
제 6 기 1분기 2022.01.01 부터 2022.03.31 까지 |
|
제 5 기 1분기 2021.01.01 부터 2021.03.31 까지 |
|
(단위 : 원) |
|
자본 |
|||||||
|---|---|---|---|---|---|---|---|
|
지배기업의 소유주에게 귀속되는 자본 |
비지배지분 |
자본 합계 |
|||||
|
자본금 |
주식발행초과금 |
기타자본구성요소 |
결손금 |
지배기업의 소유주에게 귀속되는 자본 합계 |
|||
|
2021.01.01 (Ⅰ.기초자본) |
10,494,262,900 |
63,950,642,778 |
6,994,589,247 |
(69,086,847,052) |
12,352,647,873 |
667,807,524 |
13,020,455,397 |
|
Ⅱ.당기순이익(손실) |
(3,490,600,901) |
(3,490,600,901) |
(3,490,600,901) |
||||
|
Ⅲ.해외사업환산손익 |
14,348,716 |
14,348,716 |
14,348,716 |
||||
|
Ⅳ.해외사업장순투자환산손익 |
682,499,942 |
682,499,942 |
682,499,942 |
||||
|
Ⅴ.주식보상비용 |
224,698,562 |
224,698,562 |
359,966,099 |
584,664,661 |
|||
|
Ⅵ.주식선택권 |
13,186,300 |
213,221,937 |
45,886,165 |
180,522,072 |
180,522,072 |
||
|
2021.03.31 (Ⅶ.기말자본) |
10,507,449,200 |
64,163,864,715 |
7,870,250,302 |
72,577,447,953 |
9,964,116,264 |
1,027,773,623 |
10,991,889,887 |
|
2022.01.01 (Ⅰ.기초자본) |
11,028,980,300 |
76,912,501,241 |
9,460,459,263 |
85,298,410,429 |
12,103,530,375 |
2,496,651,926 |
14,600,182,301 |
|
Ⅱ.당기순이익(손실) |
(3,801,659,790) |
(3,801,659,790) |
(5,988,523) |
(3,807,648,313) |
|||
|
Ⅲ.해외사업환산손익 |
(65,608,576) |
(65,608,576) |
3,735,040 |
(61,873,536) |
|||
|
Ⅳ.해외사업장순투자환산손익 |
379,499,967 |
379,499,967 |
379,499,967 |
||||
|
Ⅴ.주식보상비용 |
2,107,305 |
2,107,305 |
422,161,402 |
424,268,707 |
|||
|
Ⅵ.주식선택권 |
10,845,900 |
176,774,764 |
40,022,541 |
147,598,123 |
147,598,123 |
||
|
2022.03.31 (Ⅶ.기말자본) |
11,039,826,200 |
77,089,276,005 |
9,736,435,418 |
89,100,070,219 |
8,765,467,404 |
2,916,559,845 |
11,682,027,249 |
|
연결 현금흐름표 |
|
제 6 기 1분기 2022.01.01 부터 2022.03.31 까지 |
|
제 5 기 1분기 2021.01.01 부터 2021.03.31 까지 |
|
(단위 : 원) |
|
제 6 기 1분기 |
제 5 기 1분기 |
|
|---|---|---|
|
Ⅰ.영업활동현금흐름 |
(1,747,993,288) |
(2,086,664,017) |
|
(1)영업에서 창출된 현금 |
(1,814,984,796) |
(2,104,112,064) |
|
1.당기순이익(손실) |
(3,807,648,313) |
(3,490,600,901) |
|
2.조정 |
651,825,998 |
766,989,759 |
|
3.영업활동으로 인한 자산부채의 변동 |
1,340,837,519 |
619,499,078 |
|
(2)이자수취 |
66,991,508 |
20,560,866 |
|
(3)이자지급(영업) |
(744,419) |
|
|
(4)법인세의 납부 |
(2,368,400) |
|
|
Ⅱ.투자활동현금흐름 |
(3,671,756,103) |
(1,892,896,243) |
|
(1)투자활동으로 인한 현금유입 |
3,010,600,000 |
2,019,056,500 |
|
1.단기금융상품의 감소 |
3,000,000,000 |
|
|
2.보증금의 감소 |
10,000,000 |
158,656,500 |
|
3.유동당기손익-공정가치측정금융자산의 처분 |
1,860,400,000 |
|
|
4.유형자산처분 |
600,000 |
|
|
(2)투자활동으로 인한 현금유출액 |
(6,682,356,103) |
(3,911,952,743) |
|
1.단기금융상품 취득 |
5,000,000,000 |
3,000,000,000 |
|
2.비유동당기손익-공정가치측정금융자산 취득 |
605,400,000 |
|
|
3.유형자산의 취득 |
715,500,000 |
886,605,482 |
|
4.무형자산의 취득 |
360,956,103 |
171,818 |
|
5.보증금의 증가 |
500,000 |
10,000,000 |
|
6.장기선급금의 증가 |
15,175,443 |
|
|
Ⅲ.재무활동현금흐름 |
809,540,153 |
863,003,394 |
|
(1)재무활동으로 인한 현금유입액 |
909,269,523 |
942,193,472 |
|
1.주식선택권의 행사 |
147,598,123 |
180,522,072 |
|
2.장기차입금 증가 |
761,671,400 |
761,671,400 |
|
(2)재무활동으로 인한 현금유출액 |
(99,729,370) |
(79,190,078) |
|
1.리스부채의 지급 |
99,729,370 |
79,190,078 |
|
Ⅳ.현금및현금성자산의 증가(감소) |
(4,610,209,238) |
(3,116,556,866) |
|
Ⅴ.기초현금및현금성자산 |
23,230,921,994 |
21,951,844,586 |
|
Ⅵ.현금및현금성자산에 대한 환율변동 |
(67,177,256) |
782,091,951 |
|
Ⅶ.기말현금및현금성자산 |
18,553,535,500 |
19,617,379,671 |
3. 연결재무제표 주석
| 제 6(당) 분기 2022년 03월 31일 현재 |
| 제 5(전) 기 2021년 12월 31일 현재 |
| 주식회사 카이노스메드와 종속기업 |
1. 일반사항
(1) 지배기업의 개요
주식회사 카이노스메드("당사" 또는 "지배기업")는 의약품, 신기술 연구 및 개발업 등을 영위할 목적으로 2007년 6월 15일자로 설립되었고, 경기도 성남시 분당구 판교역로 184에 본사를 두고 있습니다.
회사는 2017년 11월 3일 설립된 하나금융11호기업인수목적 주식회사와 2019년 11월 29일 합병계약을 체결하였으며, 2020년 5월 20일을 합병기일로 하여 합병을 완료하였습니다. 하나금융11호기업인수목적 주식회사가 당사를 흡수합병하였으며, 합병 후 사명은 주식회사 카이노스메드입니다.
당사의 설립시 자본금은 50백만원이었으나, 수차례의 증자를 거쳐 당분기말 현재 회사의 자본금은 11,040백만원(보통주자본금 11,040백만원)이며, 최대주주인 대표이사 이기섭 및 특수관계자가 13.7%를 보유하고 있습니다.
(2) 종속기업
기업회계기준서 제1110호 '연결재무제표'에 의한 지배기업인 당사는 종속기업(이하 "연결회사")을 연결대상으로 하여 연결재무제표를 작성하였습니다.
1) 현황
연결재무제표에 포함된 종속기업의 현황은 다음과 같습니다.
| 회사명 | 소재지 | 보고기간 종료일 |
지분율 | 지분취득일 | |
|---|---|---|---|---|---|
| 제6(당)분기 | 제5(전)기 | ||||
| FAScinate Therapeutics, Inc. | 미국 | 12월31일 | 94% | 94% | 2020년 6월 26일 |
| KAIDEA GLOBAL PTE.LTD | 싱가포르 | 12월31일 | 55% | 55% | 2021년 9월 17일 |
2) 요약재무정보
제 6(당) 분기
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 회사명 | 자산 | 부채 | 자본 | 매출 | 분기순손익 | 총포괄손익 |
| FAScinate Therapeutics, Inc. | 19,093,958 | 21,937,215 | (2,843,257) | - | (1,405,890) | (1,405,890) |
| KAIDEA GLOBAL PTE.LTD | 406,752 | 4,144 | 402,608 | - | (13,308) | (13,308) |
2. 재무제표 작성기준
연결회사의 분기연결재무제표는 한국채택국제회계기준에 따라 작성되는 중간재무제표입니다. 동 재무제표는 기업회계기준서 제1034호 '중간재무보고'에 따라 작성되었으며, 연차재무제표에서 요구되는 정보에 비하여 적은 정보를 포함하고 있습니다. 선별적 주석은 직전 연차보고기간말 후 발생한 연결회사의 재무상태와 경영성과의 변동을 이해하는데 유의적인 거래나 사건에 대한 설명을 포함하고 있습니다.
3. 회계정책의 변경과 공시
1) 연결회사가 채택한 제ㆍ개정 기준서
연결회사는 2022년 1월 1일로 개시하는 회계기간부터 다음의 제ㆍ개정 기준서 및 해석서를 신규로 적용하였습니다.
(1) 기업회계기준서 제 1116호 '리스' 개정 - 2021년 6월 30일 후에도 제공되는 코로나19 관련 임차료 할인 등
코로나19의 직접적인 결과로 발생한 임차료 할인 등이 리스변경에 해당하는지 평가하지 않을 수 있도록 하는 실무적 간편법의 적용대상이 2022년 6월 30일 이전에 지급하여야 할 리스료에 영향을 미치는 리스료 감면으로 확대되었습니다. 리스이용자는 비슷한 상황에서 특성이 비슷한 계약에 실무적 간편법을 일관되게 적용해야 합니다.
(2) 기업회계기준서 제1103호 '사업결합' 개정 - 개념체계의 인용
사업결합 시 인식할 자산과 부채의 정의를 개정된 재무보고를 위한 개념체계를 참조하도록 개정되었으나, 기업회계기준서 제1037호 ‘충당부채, 우발부채 및 우발자산’ 및 해석서 제2121호 ‘부담금’의 적용범위에 포함되는 부채 및 우발부채에 대해서는 해당 기준서를 적용하도록 예외를 추가하고, 우발자산이 취득일에 인식되지 않는다는 점을 명확히 하였습니다.
(3) 기업회계기준서 제1016호 '유형자산' 개정 - 의도한 사용 전의 매각금액
기업이 자산을 의도한 방식으로 사용하기 전에 생산된 품목의 판매에서 발생하는 수익을 생산원가와 함께 당기손익으로 인식하도록 요구하며, 유형자산의 취득원가에서 차감하는 것을 금지하고 있습니다.
(4) 기업회계기준서 제1037호 '충당부채, 우발부채 및 우발자산' 개정 - 손실부담계약: 계약이행원가
손실부담계약을 식별할 때 계약이행원가의 범위를 계약 이행을 위한 증분원가와 계약 이행에 직접 관련되는 다른 원가의 배분이라는 점을 명확히 하였습니다.
(5) 한국채택국제회계기준 연차개선 2018-2020
한국채택국제회계기준 연차개선 2018-2020은 2022년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다.
·기업회계기준서 제1101호 '한국채택국제회계기준의 최초 채택’: 최초채택기업인 종속기업
·기업회계기준서 제1109호 '금융상품’: 금융부채 제거 목적의 10% 테스트 관련 수수료
·기업회계기준서 제1041호 '농림어업’: 공정가치 측정
2) 연결회사가 적용하지 않은 제ㆍ개정 기준서 및 해석서
제정 또는 공표되었으나 시행일이 도래하지 않아 적용하지 아니한 제ㆍ개정 기준서 및 해석서는 다음과 같습니다.
(1) 기업회계기준서 제1001호 '재무제표 표시' 개정 - 부채의 유동/비유동 분류
보고기간말 현재 존재하는 실질적인 권리에 따라 유동 또는 비유동으로 분류되며, 부채의 결제를 연기할 수 있는 권리의 행사가능성이나 경영진의 기대는 고려하지 않습니다. 또한, 부채의 결제에 자기지분상품의 이전도 포함되나, 복합금융상품에서 자기지분상품으로 결제하는 옵션이 지분상품의 정의를 충족하여 부채와 분리하여 인식된 경우는 제외됩니다. 동 개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 적용하며, 조기적용이 허용됩니다.
(2) 기업회계기준서 제1001호 '재무제표 표시' - '회계정책'의 공시
중요한 회계정책을 정의하고 공시하도록 하며, 중요성 개념을 적용하는 방법에 대한 지침을 제공하기 위하여 국제회계기준 실무서 2 '회계정책 공시'를 개정하였습니다.
동 개정 사항은 2023년 1월 1일 이후 최초로 시작하는 회계연도부터 적용되며 조기적용이 허용됩니다.
(3) 기업회계기준서 제1008호 '회계정책, 회계추정의 변경 및 오류' - '회계추정'의 정의
회계추정을 정의하고, 회계정책의 변경과 구별하는 방법을 명확히 하였습니다. 동 개정 사항은 2023년 1월 1일 이후 최초로 시작하는 회계연도부터 적용되며 조기적용이 허용됩니다.
(4) 기업회계기준서 제1012호 '법인세' - 단일거래에서 생기는 자산과 부채에 대한 이연법인세
자산 또는 부채가 최초로 인식되는 거래의 최초 인식 예외 요건에 거래시점 동일한 가산할 일시적차이와 차감할 일시적차이를 발생시키지 않는 거래라는 요건을 추가하였습니다. 동 개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 적용하며, 조기적용이 허용됩니다.
(5) 기업회계기준서 제1117호 '보험계약' 제정
기업회계기준서 제1117호 '보험계약'은 기업회계기준서 제1104호 '보험계약’을 대체합니다. 보험계약에 따른 모든 현금흐름을 추정하고 보고시점의 가정과 위험을 반영한 할인율을 사용하여 보험부채를 측정하고, 매 회계연도별로 계약자에게 제공한 서비스(보험보장)를 반영하여 수익을 발생주의로 인식하도록 합니다. 또한, 보험사건과 관계없이 보험계약자에게 지급하는 투자요소(해약/만기환급금)는 보험수익에서 제외하며, 보험손익과 투자손익을 구분 표시하여 정보이용자가 손익의 원천을 확인할 수 있도록 하였습니다. 동 기준서는 2023년 1월 1일 이후 최초로 시작하는 회계연도부터 적용되며, 기업회계기준서 제1109호 '금융상품'을 적용한 기업은 조기적용이 허용됩니다.
4. 회계정책 및 중요한 회계추정 및 가정
4.1 회계정책
분기연결재무제표의 작성에 적용된 유의적 회계정책과 계산방법은 주석 3에서 설명하는 제ㆍ개정 기준서의 적용으로 인한 변경 및 아래 문단에서 설명하는 사항을 제외하고는 전기 연결재무제표 작성에 적용된 회계정책이나 계산방법과 동일합니다.
(1) 법인세비용
중간기간의 법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균연간법인세율, 즉 추정평균연간유효법인세율을 중간기간의 세전이익에 적용하여 계산합니다.
4.2 중요한 회계추정 및 가정
연결회사는 미래에 대하여 추정 및 가정을 하고 있습니다. 추정 및 가정은 지속적으로 평가되며, 과거 경험과 현재의 상황에서 합리적으로 예측가능한 미래의 사건과 같은 다른 요소들을 고려하여 이루어집니다. 이러한 회계추정은 실제 결과와 다를 수도 있습니다.
분기연결재무제표 작성시 사용된 중요한 회계추정 및 가정은 법인세비용을 결정하는데 사용된 추정의 방법을 제외하고는 전기 재무제표 작성에 적용된 회계추정 및 가정과 동일합니다.
4.3 COVID-19 영향
COVID-19의 확산은 국내 및 세계 경제에 중대한 영향을 미치고 있습니다. 이로 인해 당사의 향후 수익과 기타 재무성과에도 잠재적으로 부정적인 영향이 발생할 수 있습니다. COVID-19가 재무상태 및 영업성과에 미칠 영향의 범위를 예측하는 것은 현재 시점에는 매우 불확실하며, 연결회사의 영업활동 및 글로벌 시장 전반에 다양한 요인에 의해 영향을 미칠 것이므로 COVID-19의 효과는 당분간 연결회사의 영업성과에 완전히 반영되지 않을 수 있습니다.
분기연결재무제표 작성시 사용된 중요한 미래에 대한 회계추정 및 가정은 COVID-19에 따른 불확실성의 변동에 따라 조정을 유발할 수 있으며, 따라서 COVID-19와 영업활동 변경이 연결회사의 사업, 재무상태 및 성과, 유동성에 미칠 궁극적인 영향은 현재로는 예측할 수 없습니다.
5. 현금성자산 및 단기금융상품
(1) 당분기말과 전기말 현재 현금및현금성자산의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 기 |
| 보통예금 | 18,553,535 | 23,230,922 |
(2) 당분기말과 전기말 현재 단기금융상품 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 기 |
| 정기예금 | 13,000,000 | 11,000,000 |
6. 매출채권및기타채권
당분기말과 전기말 현재 매출채권및기타채권의 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 기 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
| 기타채권: | ||||
| 미수금 | 85,369 | - | 257,412 | - |
| 미수수익 | 77,834 | - | 33,476 | - |
| 보증금 | - | 185,244 | 10,000 | 179,668 |
| 합 계 | 163,203 | 185,244 | 300,888 | 179,668 |
당분기말과 전기말 현재 연체된 매출채권및기타채권은 없습니다.
7. 공정가치
연결회사는 공정가치를 산정하는 데 사용한 투입변수의 신뢰성에 대한 정보를 제공하기 위하여 금융상품을 기준서에서 정한 세 수준으로 분류합니다. 공정가치로 측정되는 금융상품은 공정가치 서열체계에 따라 구분되며 정의된 수준들은 다음과 같습니다.
| - |
측정일에 동일한 자산이나 부채에 대해 접근할 수 있는 활성시장의 (조정하지 않은) 공시가격 (수준 1) |
| - |
수준 1의 공시가격 외에 자산이나 부채에 대해 직접적으로나 간접적으로 관측할 수 있는 투입변수 (수준 2) |
| - | 자산이나 부채에 대한 관측할 수 없는 투입변수 (수준 3) |
당분기말과 전기말 현재 반복적으로 공정가치로 측정되고 인식된 연결회사의 금융상품은 다음과 같습니다.
① 제 6(당) 분기
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 수준1 | 수준2 | 수준3 | 합계 |
| 공정가치로 측정되는 금융자산: | ||||
| 파생상품자산 | - | - | 309,735 | 309,735 |
| 비유동당기손익-공정가치측정금융자산(투자주식) | - | - | 1,248,187 | 1,248,187 |
| 공정가치로 측정되는 금융부채: | ||||
| 파생상품부채 | - | - | 8,428,578 | 8,428,578 |
② 제 5(전) 기
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 수준1 | 수준2 | 수준3 | 합계 |
| 공정가치로 측정되는 금융자산: | ||||
| 파생상품자산 | - | - | 309,735 | 309,735 |
| 비유동당기손익-공정가치측정금융자산(투자주식) | - | - | 642,787 | 642,787 |
| 공정가치로 측정되는 금융부채: | ||||
| 파생상품부채 | - | - | 8,428,578 | 8,428,578 |
8. 유형자산
(1) 당분기말과 전기말 현재 유형자산의 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 비 품 | 임차개량권 | 건설중인자산 | 합계 |
| 당분기말: | ||||
| 취득원가 | 724,408 | 228,410 | 3,002,322 | 3,955,140 |
| 감가상각누계액 | (262,191) | (153,052) | - | (415,243) |
| 장부가액 | 462,217 | 75,358 | 3,002,322 | 3,539,897 |
| 전기말: | ||||
| 취득원가 | 725,659 | 228,410 | 2,286,822 | 3,240,891 |
| 감가상각누계액 | (232,455) | (136,927) | - | (369,382) |
| 장부가액 | 493,204 | 91,483 | 2,286,822 | 2,871,509 |
(2) 당분기와 전분기 중 유형자산 취득원가의 변동내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 비 품 | 임차개량권 | 건설중인자산 | 합계 |
| 당기초 | 725,659 | 228,410 | 2,286,822 | 3,240,891 |
| 취득액 | - | - | 715,500 | 715,500 |
| 처분액 | (3,773) | - | - | (3,773) |
| 환율차이 | 2,523 | - | - | 2,523 |
| 당분기말 | 724,409 | 228,410 | 3,002,322 | 3,955,141 |
| 전기초 | 1,061,333 | 206,110 | 753,900 | 2,021,343 |
| 취득액 | 175,642 | - | 715,500 | 891,142 |
| 전분기말 | 1,236,975 | 206,110 | 1,469,400 | 2,912,485 |
(3) 당분기와 전분기 중 유형자산 감가상각누계액의 변동내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 구 분 | 비 품 | 임차개량권 | 합계 |
| 당기초 | 674,753 | 118,231 | 792,984 |
| 처분 | (2,704) | - | (2,704) |
| 감가상각비(*) | 31,852 | 16,125 | 47,977 |
| 환율차이 | (441,710) | 18,696 | (423,014) |
| 당분기말 | 262,191 | 153,052 | 415,243 |
| 전기초 | 674,753 | 118,231 | 792,984 |
| 감가상각비(*) | 40,607 | 11,938 | 52,545 |
| 전분기말 | 715,360 | 130,169 | 845,529 |
(*) 당분기와 전분기 중 유형자산 감가상각비를 연구개발비 및 기타 판매비와관리비로 구분한 내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 구분 | 연구비 | 판관비 | 합계 |
| 당분기 | 23,346 | 24,632 | 47,977 |
| 전분기 | 34,954 | 17,590 | 52,544 |
(4) 당분기말 현재 연결회사는 유형자산에 대하여 삼성화재해상보험(주) 및 현대해상화재보험(주)의 화재보험에 가입하고 있습니다.
(5) 유형자산의 취득약정
연결회사는 토지 및 설비투자와 관련한 취득약정을 체결하고 있습니다(주석16참고).
9. 리스
(1) 리스이용자(기업회계기준서 제1116호)
연결회사는 기타비품 등을 1년에서 3년간 리스하고 있습니다. 이러한 리스는 단기리스이거나 소액자산 리스에 해당합니다. 연결회사는 이러한 리스에 사용권자산과 리스부채를 인식하지 않는 실무적 간편법을 적용합니다.
. 리스기간이 12개월 이내인 리스에 대하여 사용권자산과 리스부채를 인식하지 않음
. 소액 기초자산 리스에 대하여 사용권자산과 리스부채를 인식하지 않음
. 최초 적용일의 사용권자산 측정치에서 리스개설직접원가를 제외함
. 리스기간을 산정할 때 사후판단을 사용함
(2) 당분기와 전분기 사용권자산 및 리스부채의 변동내역은 다음과 같습니다.
① 제 6(당) 분기
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 사용권자산(*) | 리스부채(*) |
| 당기초 | 462,108 | 380,217 |
| 증가/변경 | - | - |
| 감가상각 | (98,677) | - |
| 이자비용 | - | 9,485 |
| 지급 | - | (99,729) |
| 외화환산 | 3,050 | 2,852 |
| 당분기말 | 366,481 | 292,825 |
(*) 연결회사는 임차건물에 대한 리스 인식을 비롯하여 원상복구 의무가 있는 임차건물의 계약 종료 시 발생할 수 있는 복구비용과 관련하여 지출할 것으로 예상되는 금액의 현재가치를 추정하여 사용권자산과 리스부채에 계상하고 있습니다.
② 제 5(전) 분기
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 사용권자산(*) | 리스부채(*) |
| 전기초 | 622,965 | 554,720 |
| 증가/변경 | - | - |
| 감가상각 | (66,034) | - |
| 이자비용 | - | 12,700 |
| 지급 | - | (70,258) |
| 전분기말 | 556,931 | 497,162 |
(*) 연결회사는 임차건물에 대한 리스 인식을 비롯하여 원상복구 의무가 있는 임차건물의 계약 종료 시 발생할 수 있는 복구비용과 관련하여 지출할 것으로 예상되는 금액의 현재가치를 추정하여 사용권자산과 리스부채에 계상하고 있습니다.
(3) 당분기와 전분기 중 포괄손익계산서에 인식된 금액은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 사용권자산의 감가상각비 | 98,677 | 66,034 |
| 리스부채의 이자비용 | 9,485 | 12,700 |
| 리스료 - 단기 리스 | 7,500 | 2,522 |
| 리스료 - 소액 기초자산 리스 | - | 2,458 |
| 포괄손익계산서에 인식된 총 금액 | 115,662 | 83,714 |
(4) 당분기와 전분기 중 현금흐름표에 인식된 금액은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 현금유출 | (99,729) | (70,258) |
(*) 그 외 소액리스료 및 단기리스료를 포함하여 당분기에 107,229천원(전분기: 75,238천원)이 유출 되었습니다.
(5) 연장선택권
일부 건물 리스는 연결회사가 계약의 해지불능기간 종료 전에 리스기간을 1년 연장 할 수있는 선택권을 포함합니다. 연결회사는 운영의 효율성을 위하여 가능하면 새로운 리스계약에 연장선택권을 포함하려고 노력합니다. 연결회사는 리스개시일에 연장선택권을 행사할 것이 상당히 확실한지 평가합니다. 연결회사는 연결회사가 통제 가능한 범위에 있는 유의적인 사건이일어나거나 상황에 유의적인 변화가 있을 때 연장선택권을 행사할 것이 상당히 확실한지 다시 평가합니다.
10. 무형자산
(1) 당분기말과 전기말 현재 무형자산의 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 기술사용권 | 소프트웨어 | 기타의무형자산 | 합계 |
| 당분기말: | ||||
| 취득원가 | 300,000 | 1,305,515 | 93,534 | 162,168 |
| 감가상각누계액 | (15,517) | (783,058) | (61,895) | (95,158) |
| 장부가액 | 284,483 | 522,457 | 31,639 | 67,010 |
| 전기말: | ||||
| 취득원가 | - | 1,275,515 | 93,534 | 131,212 |
| 감가상각누계액 | - | (663,297) | (59,246) | (88,682) |
| 장부가액 | - | 612,218 | 34,288 | 42,530 |
(2) 당분기와 전분기 중 무형자산의 장부가액의 변동내역은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 특허권 | 기술사용권 | 소프트웨어 | 기타의무형자산 | 합계 |
| 당기초 | - | 612,218 | 34,288 | 42,529 | 689,035 |
| 취득 | 300,000 | 30,000 | - | 30,956 | 360,956 |
| 무형자산상각비 | (15,517) | (119,761) | (2,649) | (6,476) | (144,403) |
| 당분기말 | 284,483 | 522,457 | 31,639 | 67,009 | 905,588 |
| 전기초 | - | 390,263 | 27,025 | 64,305 | 481,593 |
| 취득 | - | - | 172 | - | 172 |
| 무형자산상각비 | - | (19,511) | (2,968) | (5,444) | (27,923) |
| 전분기말 | - | 370,752 | 24,229 | 58,861 | 453,842 |
(3) 당분기와 전분기 중 무형자산상각비의 배분내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 무형자산상각비(판매비와관리비) | 143,967 | 26,402 |
| 연구개발비(판매비와관리비) | 436 | 1,520 |
| 합 계 | 144,403 | 27,922 |
11. 미지급금 및 기타채무
당분기말과 전기말 현재 미지급금 및 기타채무의 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 제 6(당) 분기 | 제 5(전) 기 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
| 미지급금 | 169,834 | - | 270,588 | - |
| 미지급비용 | 455,886 | - | 575,512 | - |
| 합 계 | 625,720 | - | 846,100 | - |
12. 차입금
(1) 당분기말과 전기말 현재 차입부채의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 제 6(당) 분기 | 제 5(전) 기 |
| 전환사채 | 12,467,965 | 12,467,965 |
| 전환우선주 | 3,632,400 | 3,556,500 |
| 차입금 | 2,285,014 | 1,523,343 |
| 합계 | 18,385,379 | 17,547,808 |
(2) 당분기말 현재 전환사채의 발행내역은 다음과 같습니다.
| 구 분 | 내 용 |
|---|---|
| 사채의명칭 | 제2회 무기명식 이권부 무보증 사모전환사채 |
| 발행일 | 2020년 06월 30일 |
| 만기일 | 2025년 06월 30일 |
| 액면금액 | 20,000,000,000원 |
| 표면이자율(만기보장수익율) | 0.00%(1.00%) |
| 상환방법 | 만기일에 원금의 105.1205%를 일시상환한다 |
| 조기상환청구권(Put Option) | 사채권자는 사채의 발행일로부터 24개월 이후 45개월까지의 기간중 원금의 전부 및 일부에 대하여 조기상환수익률 연 1.0%(3개월 단위 복리계산)가 적용된 청구 금액을 조기상환 청구할 수 있음. |
| 매도청구권(Call Option) | 회사는 사채권자로부터 회사 또는 회사가 지정하는 제3자(매수인)에게 사채의 발행일로부터12개월 이후 24개월까지의 기간 중 매3개월에 해당되는 날에 원금의 25/100에 대하여 매도 청구할 수 있음. 매수인이 매도청구 행사시 연1.0%(3개월 단위 복리계산)의 이율을 적용하여 계산한 금액을 지급하여야 함. |
| 전환시 발행할 주식의 종류 | 기명식보통주 |
| 전환청구기간 | 2021년 6월 30일부터 2025년 3월 30일 |
| 전환가격 |
(1)최초 전환가액: 5,813원/주 (3)2차 조정전환가액: 4,386원/주 (2020년12월30일 조정) (4)3차 조정전환가액: 4,070원/주 (2021년03월30일 조정) |
(3) 당분기말과 전기말 현재 전환사채의 내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 구분 | 제 6(당) 분기 | 제 5(전) 기 | |
| 제2회 무보증 사모전환사채 | 액면금액 | 20,000,000 | 20,000,000 |
| 전환권조정 | (8,556,145) | (8,556,145) | |
| 상환할증금 | 1,024,110 | 1,024,110 | |
| 합계 | 12,467,965 | 12,467,965 | |
(4) 당분기말 현재 전환우선주의 발행내역은 다음과 같습니다.
| 구분 | 내용 |
|---|---|
| 발행일 | 2020년 12월 21일 |
| 최초발행주식수 | 1,916,688주 |
| 주당발행가액 | USD 1.57 |
| 전환비율 | 우선주 : 보통주 = 1 : 1 (Refixing 조항 있음) |
| 전환가격 | 1주당 발행가액과 동일 |
| 전환가격의 조정 | 행사일 또는 간주행사일 현재 전환가격보다 주가가 낮을 경우 아래와 같이 전환가격을 조정 - 조정후 전환가격 = 조정전 전환가격 * (기발행 주식수 + 조정전 전환가격에 따라 발행 됐을 주식수)/(기발행 주식수 + 신발행주식수) |
| 발행할 주식의 종류 | 보통주식 |
| 성격 | 이익배당 및 잔여재산 청구권에 대한 우선적 권리를 보유함. |
| 의결권에 관한 사항 | 보통주와 동일한 의결권 존재 |
| 이익배당에 관한 사항 | 이익배당율은 8%이며 매년 지급해야 할 의무는 없으나, 매년 배당액은 별도의 결의 없이 누적됨 |
| 상환청구권 | N/A |
(5) 차입금의 내용은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구분 | 차입처 | 연이자율 | 제 6(당) 분기 | 제 5(전) 기 | 상환방법 |
| 원화장기차입금 | 기업은행 | 2.759% | 2,285,014 | 1,523,343 | 만기상환 |
| 합 계 | 2,285,014 | 1,523,343 | |||
| 유동성대체액 | 2,285,014 | - | |||
| 비유동성잔액 | - | 1,523,343 | |||
(6) 차입금 상환일정은 다음과 같습니다.
| (단위: 천원) | |
|---|---|
| 구분 | 차입금 |
| 1년이내 | 2,285,014 |
| 1년초과 5년이내 | - |
| 5년초과 | - |
| 합 계 | 2,285,014 |
(*) 상기 현금흐름은 현재가치할인을 고려하지 아니한 금액입니다.
13. 자본금 및 주식발행초과금
(1) 당분기말과 전기말 현재 자본금의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 제 6(당) 분기 | 제 5(전) 기 |
| 발행할주식의 총수 | 300,000,000주 | 300,000,000주 |
| 1주당 액면금액 | 100원 | 100원 |
| 발행한 주식수 | 110,398,262 | 110,289,803주 |
| 보통주자본금 | 11,039,826 | 11,028,980 |
| 발행한 우선주 주식수 | 0주 | 0주 |
| 우선주자본금 | - | - |
(2) 당분기와 전기 중 자본금 및 주식발행초과금의 변동내역은 다음과 같습니다.
| (단위:주, 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 내 역 | 주식수 | 자본금 | 주식발행초과금 | ||
| 보통주 | 우선주 | 보통주 | 우선주 | |||
| 2021.01.01 | 전기초 | 104,942,629 | - | 10,494,263 | - | 63,950,643 |
| 2021.01.25 | 주식선택권 행사 | 131,863 | - | 13,186 | - | 213,222 |
| 2021.04.22 | 주식선택권 행사 | 168,316 | - | 16,832 | - | 166,344 |
| 2021.07.27 | 주식선택권 행사 | 114,926 | - | 11,492 | - | 177,624 |
| 2021.10.22 | 주식선택권 행사 | 43,970 | - | 4,397 | - | 34,726 |
| 2021.11.12 | 주식선택권 행사 | 130,812 | - | 13,081 | - | 141,037 |
| 2021.11.12 | 유상증자 | 4,681,638 | - | 468,164 | - | 12,031,809 |
| 2021.12.22 | 주식선택권 행사 | 75,649 | - | 7,565 | - | 197,097 |
| 2021.12.31 | 전기말 | 110,289,803 | - | 11,028,980 | - | 76,912,502 |
| 2022.01.01 | 당기초 | 110,289,803 | - | 11,028,980 | - | 76,912,502 |
| 2022.01.18 | 주식선택권 행사 | 108,459 | - | 10,846 | - | 176,775 |
| 2022.03.31 | 당분기말 | 110,398,262 | - | 11,039,826 | - | 77,089,277 |
14. 기타자본구성요소
당분기말과 전기말 현재 기타자본구성요소는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 기 |
| 전환권대가(*1) | 4,515,420 | 4,515,420 |
| 기타자본잉여금(*2) | 5,438,846 | 5,476,761 |
| 자기주식(*3) | (22,721) | (22,721) |
| 해외사업환산손익 | (144,110) | (78,502) |
| 해외사업장순투자환산손익 | (51,000) | (430,500) |
| 합 계 | 9,736,435 | 9,460,458 |
(*1) 전환사채 평가에 따라 제2회 전환사채에 대한 전환권가치를 4,515,420천원 인식하였습니다.
(*2) 기타자본잉여금에는 2020년 합병으로 인한 자기주식처분이익 2,627,141천원, 합병법인인 하나금융11호스팩의 합병계약일과 합병등기일 간 순자산 차액 259,593천원이 포함되어 있습니다.
(*3) 2020년 합병 과정에서 하나금융11호기업인수목적 주식회사의 기존 주주가 주식매수청구권을 행사하여 보통주 자기주식을 취득하였습니다.
15. 주식기준보상
(1) 당분기말 현재 주식선택권의 주요 내용은 다음과 같습니다.
| 구 분 | 내 용 | FAScinate Therapeutics Inc |
|---|---|---|
| 부여할 주식의 종류 | 보통주식 | 보통주식 |
| 부여방법 | 주식결제형 | 주식결제형 |
| 권리행사가능기간 | 1. (13차) 부여일부터 2년후 100% 행사 (14차, 15차) 부여일부터 2년후 50%, 이후 2년간 나머지를 매월말 분할 행사 (16차, 17차, 18차, 19차, 20차) 부여일부터 3년후 50%, 이후 2년간 나머지를 매월말 분할 행사 2. 행사가능일부터 10년 이내 (또는 퇴사시 퇴사일부터 1개월 이내 행사) |
1. (1차) 부여일부터 2년후 50%, 이후 2년간 나머지를 매월말 분할 행사 (2차) 부여일부터 1년후 50%, 이후 3년간 나머지를 매월말 분할 행사 2. 행사가능일부터 10년 이내 (또는 퇴사시 퇴사일부터 3개월 이내 행사) |
| 가득조건 | 근무용역제공 2년~5년 | 근무용역제공 1년~4년 |
(2) 당분기말 현재 주식선택권의 내역은 다음과 같습니다.
① (주)카이노스메드
| (단위: 주, 원) | |||
|---|---|---|---|
| 차 수 | 부여일 | 행사가격 | 주식수 |
| 13차 | 2016.03.29 | 1,266 | 332,350 |
| 14차 | 2017.03.24 | 1,266 | 814,648 |
| 15차 | 2018.03.26 | 665 | 687,657 |
| 16차 | 2019.03.25 | 2,405 | 897,000 |
| 17차 | 2020.03.13 | 2,405 | 1,069,500 |
| 18차 | 2021.01.15 | 4,406 | 807,500 |
| 19차 | 2021.03.15 | 4,406 | 500,000 |
| 20차 | 2021.03.31 | 4,406 | 50,000 |
| 21차 | 2022.03.14 | 2,275 | 425,000 |
| 합 계 | 5,583,655 | ||
② FAScinate Therapeutics, Inc.
| (단위: 주, 원) | |||
|---|---|---|---|
| 차 수 | 부여일 | 행사가격 | 주식수 |
| 1차 | 2020.07.03 | 0.28 | 2,400,000 |
| 2차 | 2020.10.07 | 0.28 | 150,000 |
| 3차 | 2021.05.24 | 0.45 | 50,000 |
| 합 계 | 2,600,000 | ||
(3) 연결회사는 부여된 주식선택권의 보상원가를 이항모형을 이용한 공정가치접근법을 적용하여 산정하였으며, 보상원가를 산정하기 위한 제반 가정 및 변수는 다음과 같습니다.
① (주)카이노스메드
| (단위: 원) | ||||
|---|---|---|---|---|
| 차 수 | 내부 산출주가 | 무위험수익률 | 주가변동성 | 부여일의 공정가치 |
| 13차 | 4,000 | 1.85% | 14.40% | 27 |
| 14차 | 4,000 | 2.21% | 6.60% | 317 |
| 15차 | 11,400 | 2.70% | 39.00% | 3,832 |
| 16차 | 16,400 | 1.90% | 32.08% | 6,531 |
| 17차 | 15,400 | 1.61% | 32.80% | 4,571 |
| 18차 | 4,290 | 1.61% | 42.32% | 2,086 |
| 19차 | 4,050 | 1.98% | 58.32% | 2,562 |
| 20차 | 3,895 | 1.92% | 50.84% | 2,214 |
| 21차 | 2,070 | 2.66% | 61.20% | 1,333 |
② FAScinate Therapeutics, Inc.
| (단위: USD) | |
|---|---|
| 차 수 | 부여일의 공정가치 |
| 1차 | 1.3 |
| 2차 | 1.29 |
| 3차 | 1.14 |
(4) 당분기 및 전분기 중 주식선택권의 변동내역은 다음과 같습니다.
① (주)카이노스메드
| (단위: 주) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 기초수량 | 5,555,020 | 5,029,928 |
| 부여 | 425,000 | 1,595,500 |
| 취소 또는 소멸 | (287,906) | (404,872) |
| 행사 | (108,459) | (665,536) |
| 분기말수량 | 5,583,655 | 5,555,020 |
② FAScinate Therapeutics, Inc.
| (단위: 주) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 기초수량 | 2,600,000 | 2,550,000 |
| 부여 | - | 50,000 |
| 취소 또는 소멸 | - | - |
| 행사 | - | - |
| 분기말수량 | 2,600,000 | 2,600,000 |
(5) 당분기말 현재 행사가능한 주식선택권은 2,233,847주이며, 당분기 중 행사된 주식선택권은 다음과 같습니다.
① (주)카이노스메드
| (단위: 원,주) | ||
|---|---|---|
| 구 분 | 행사가격 | 행사주식수 |
| 14차 | 665 | 39,675 |
| 15차 | 1,772 | 68,784 |
| 합 계 | 108,459 | |
② FAScinate Therapeutics, Inc.의 행사된 주식선택권은 없습니다.
(6) 당분기 및 전분기 중 인식한 주식보상비용은 각각 424,268천원 및 622,015천원입니다. 당분기에 인식한 주식보상비용 중 47,928천원은 연구개발비로 인식하였습니다.
16. 우발상황 및 약정사항
(1) 자본적 지출 약정
당분기말 및 전기말 현재 체결 된 자본적 지출 약정사항은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 기 |
| 유형자산 | 7,616,714 | 7,616,714 |
(*) 연결회사는 예정된 유형자산 취득 중도금 지급을 위해서 중소기업은행과 한도 3,047백만원의 여신거래약정을 체결하였으며, 당분기말 현재 1, 2, 3차중도금에 대하여 장기차입금 2,285백만원을 인식하였습니다.
(2) 기술이전 및 라이선스 약정
① 한국화학연구원
연결회사는 2010년 9월 1일부터 한국화학연구원과 공동으로 동 연구원의 소유인 KRV-2219(NNRTI) 화합물을 이용한 HIV치료제 개발을 위한 임상 1상 연구를 수행하여 2012년 중 완료하였으며, 동 화합물의 임상 2상 및 이후의 개발과 상업화를 포함한 권리를 이전 받는 계약을 2012년 11월 7일자로 체결하였습니다.
연결회사는 동 연구원이 제공한 개발성과에 대한 보상으로 USD 350,000의 License fee를 지급하였고, 향후 개발단계에 따라 Milestone fee를 지급하기로 하였으나, 2018년1월 중 계약의 조건 및 세부사항이 변경됨에 따라 royalty를 제외한 Milestone 총액에서 동 연구원의 분배비율만큼 지급하였으며, 향후 royalty만 개발성공시 지급하기로 하였습니다.
② Crown Bioscience, Inc.
연결회사는 후보물질 도출단계를 마친 대사질환 치료제인 DGAT1(Diacylglycerol acyltransferase1) 의 저해제를 중국의 CRO 업체인 Crown Bioscience, Inc.로 2014년 8월에 기술이전 및 중국에서의 상업화에 대한 권리를 이전하는 계약을 체결하였습니다.
향후 개발 성공시에 계약서에 명시되어 있는 조건에 따라 개발 단계별로 경상기술료 및 로열티를 수령하기로 하였습니다.
③ Jiangsu Aidea Pharmaceutical Co., Ltd. (구, Yangzhou AIDEA Biotech Co., LTD)
연결회사는 연결회사가 보유한 기술을 적용하여 Jiangsu Aidea Pharmaceutical사와 HIV치료제 관련 기술이전 및 중국에서의 상업화에 대한 권리를 이전하는 계약을 2014년 10월 10일자로 체결하였습니다. 연결회사는 제공한 플랫폼 기술에 대한 보상으로 USD 200,000의 License fee를 수령하였으며, 향후 개발단계에 따라 Milestone fee를 수령하기로 하였고, 기술개발 완료 후 시판으로 발생하는 판매금액의 계약서상 명시된 조건으로 royalty를 수령하기로 하였습니다.
또한, 연결회사가 개발 중인 2개 항암제의 중국 지역에 국한된 포괄적 권리를 이전하는 계약을 Jiangsu Aidea Pharmaceutical사와 2015년 12월 10일자로 체결하였으며, 초기 정액기술료 USD 2,000,000와 향후 개발단계에 따라 Milestone fee를 수령하기로하였고, 기술개발 완료 후 시판으로 발생하는 판매금액의 계약서상 명시된 조건으로 royalty를 수령하기로 하였습니다.
한편, 2017년 12월 18일 HIV치료제와 항암제 중 에피제네틱스 항암제 BRD4 저해제에 대하여 계약변경을 실시하였으며, royalty를 제외한 Milestone 총액에서 HIV치료제는 USD 1,500,000을, 그리고 BRD4 저해제는 USD 500,000을 계약일로부터 30일 이내에 수령하였습니다. 해당 계약변경으로 인해 기존 royalty 수령조건은 변경되지 않았습니다.
④ 충남대학교 산학협력단 및 한국화학연구원
연결회사는 충남대학교산학협력단과 한국화학연구원이 공동개발한 FAF1을 표적으로 하는 허혈성 질환 치료제 관련 전용실시에 대한 권리를 이전 받는 계약을 2015년 9월 24일자로 체결하였습니다.
동 협력단 및 연구원이 제공한 개발성과에 대한 보상으로 200,000천원의 License Fee를 지급하였으며, 향후 개발단계에 따라 Milestone fee를 지급하기로 하였고, 경상기술료는 계약제품 순매출액의 4%를 지급하기로 하였습니다. 그리고 재실시의 경우계약서상 명시된 분배비율로 지급하기로 하였습니다.
⑤ 한국화학연구원
연결회사는 2017년 8월 25일부터 한국화학연구원과 공동으로 '심순환계 질환 치료 선도물질' 도출 과제를 수행하였으며, 이를 통해 약학적으로 허용가능한 다수의 화합물을도출하는데 성공하였습니다. 이 과제에서 도출된 화합물을 활용한 이후의 연구개발 및 상업화를 포함한 상용화 권리를 확보하기 위하여 연결회사는 한국화학연구원으로부터본 기술도입을 결정하고, 2020년 10월 21일자로 기술도입 계약을 체결하였습니다. 연결회사는 동연구원이 제공한 성과에 대한 보상으로 총 300,000천원(이중 100,000천원은 전기에, 100,000천원은 당분기에 지급하였습니다.)의 선급실시료를 지급하고 무형자산으로 계상하였으며, 향후 매출 발생시 1%의 경상실시료를 지급할 예정입니다.
이와 관련하여 연결회사는 서울보증보험과 2020년 10월 21부터 2022년 9월 30일까지 피보험자를 한국화학연구원으로하여 220,000천원의 이행(지급)보증보험 계약을 체결하였습니다.
⑥ 충남대학교 산학협력단
연결회사는 충남대학교산학협력단으로부터 암 및 염증 치료를 위한 IRAKs 및 TAK 저해제 개발 관련 노하우에 대한 권리를 이전 받는 계약을 2018년 11월 14일자로 체결하였습니다.
동 협력단이 제공한 성과에 대한 보상으로 2018년 11월 50,000천원의 정액기술료를지급하였고, 향후 최초로 임상시험 승인시 실적기술료로 100,000천원을 지급하기로 하였습니다.
⑦ FAScinate Therapeutics Inc.
당사는 미국 현지법인 FAScinate Therapeutics Inc. 에 당사가 개발하고 있는 파킨슨병 치료제의 미국임상을 진행하고 추후 해외 제약사와의 기술이전을 추진하기 위하여, 2021년 9월 27일자로 기술이전계약을 체결하였습니다.
총 계약금 USD 2,000,000 및 향후 파킨슨병으로 발생하는 모든 수입의 10%를 로열티로 받는 것으로 약정하였습니다.
⑧ 기술이전계약과 관련된 불확실성 및 기타사항
연결회사의 향후 마일스톤 및 로열티 수익은 임상시험, 관계당국의 허가 등 개발의 성공여부에 따라 달라질 수 있으므로 발생가능성에 불확실성이 내포되어 있습니다.
(3) 보험가입내역
연결회사는 주석 8 이외에 DB손해보험 등에 임직원 단체보험 및 환경책임보험을 가입하고 있습니다.
17. 기타수익과 기타비용
(1) 당분기와 전분기 중 기타수익의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 외환차익 | 5,181 | 27,449 |
| 외화환산이익 | 21,700 | 236 |
| 잡이익 | 2,837 | 680 |
| 합 계 | 29,718 | 28,365 |
(2) 당분기와 전분기 중 기타비용의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 외환차손 | 1,270 | 1,424 |
| 외화환산손실 | 525 | - |
| 유형자산처분손실 | 469 | - |
| 합 계 | 2,264 | 1,424 |
18. 금융수익과 금융비용
(1) 당분기와 전분기 중 금융수익의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 이자수익 | 71,312 | 19,358 |
(2) 당분기와 전분기 중 금융비용의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 이자비용 | 9,686 | 12,700 |
19. 법인세비용과 이연법인세
(1) 당분기 중 법인세비용의 구성내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 법인세부담액 | - | - |
| 일시적차이 등의 발생과 소멸로 인한 이연법인세비용 | - | - |
| 당기손익 이외로 인식되는 항목과 관련된 법인세비용 | 18,834 | (3,984) |
| 법인세비용(수익) | 18,834 | (3,984) |
(2) 중간기간의 법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균연간법인세율, 즉 추정평균연간유효법인세율을 중간기간의 세전이익에 적용하여 계산하였습니다.
20. 비용의 성격별 분류
당분기와 전분기 중 비용의 성격별 분류 내역은 다음과 같습니다.
| (단위: 천원) | |||||||
|---|---|---|---|---|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 | |||||
| 매출원가 | 기타판매비와관리비 | 연구개발비 | 합계 | 기타판매비와관리비 | 연구개발비 | 합계 | |
| 급여 | - | 784,957 | 98,661 | 883,618 | 672,435 | 280,108 | 952,543 |
| 퇴직급여 | - | 55,488 | 18,130 | 73,618 | 39,082 | 21,006 | 60,088 |
| 보험료 | - | 5,478 | 980 | 6,458 | 3,661 | 1,986 | 5,647 |
| 복리후생비 | - | 91,523 | 24,772 | 116,295 | 47,470 | 27,755 | 75,225 |
| 여비교통비 | - | 15,115 | 257 | 15,372 | 5,912 | 375 | 6,287 |
| 접대비 | - | 11,778 | 785 | 12,563 | 9,447 | 253 | 9,700 |
| 임차료 | - | 7,500 | - | 7,500 | 10,787 | 1,133 | 11,920 |
| 감가상각비 | - | 110,450 | 36,202 | 146,652 | 79,693 | 48,001 | 127,694 |
| 무형자산상각비 | - | 143,967 | 436 | 144,403 | 26,402 | 1,520 | 27,922 |
| 세금과공과 | - | 8,690 | 490 | 9,180 | 8,512 | 2,246 | 10,758 |
| 연구개발비(외주) | - | - | 1,840,308 | 1,840,308 | - | 1,416,070 | 1,416,070 |
| 연구개발비(재료) | - | - | 120 | 120 | - | 48,786 | 48,786 |
| 지급수수료 | 1,098 | 151,767 | 9,057 | 161,922 | 172,790 | 29,599 | 202,389 |
| 소모품비 | - | 2,495 | 600 | 3,095 | 5,167 | 1,611 | 6,778 |
| 수선유지비 | - | - | - | - | 1,152 | - | 1,152 |
| 통신비 | - | 10,412 | - | 10,412 | 10,089 | 734 | 10,823 |
| 광고선전비 | - | 1,777 | - | 1,777 | - | - | - |
| 교육훈련비 | - | 66 | 111 | 177 | 1,025 | 150 | 1,175 |
| 관리비 | - | 13,161 | 3,358 | 16,519 | 10,918 | 6,795 | 17,713 |
| 도서인쇄비 | - | 6,820 | - | 6,820 | 919 | 255 | 1,174 |
| 잡비 | - | 482 | - | 482 | 4,405 | 64 | 4,469 |
| 주식보상비용 | - | 376,340 | 47,928 | 424,268 | 550,740 | 71,275 | 622,015 |
| 합 계 | 1,098 | 1,798,266 | 2,082,195 | 3,881,559 | 1,660,606 | 1,959,722 | 3,620,328 |
21. 종업원급여
당분기와 전분기 중 비용으로 인식된 종업원급여의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 급여 | 883,619 | 952,543 |
| 퇴직급여 | 73,619 | 60,088 |
| 주식보상비용 | 424,269 | 622,015 |
| 합 계 | 1,381,507 | 1,634,646 |
22. 주당손익
(1) 기본주당이익(손실)
당분기와 전분기의 주당이익(손실)의 산출내역은 다음과 같습니다.
① 기본주당이익(손실)
| (단위: 원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 당기순이익(손실) | (3,807,648,313) | (3,490,600,901) |
| 가중평균유통보통주식수 | 110,377,775 | 105,039,329 |
| 기본주당이익(손실) | (34) | (33) |
② 가중평균유통보통주식수
(당분기)
| (단위: 주,원) | ||||
|---|---|---|---|---|
| 구 분 | 기간 | 일수 | 유통주식수 | 적 수 |
| 기초 | 2022.01.01~2022.03.31 | 90 | 110,289,803 | 9,926,082,270 |
| 주식선택권 행사 | 2022.01.18~2022.03.31 | 73 | 108,459 | 7,917,507 |
| 합 계 | 9,933,999,777 | |||
| 가중평균유통보통주식수 | 110,377,775 | |||
(전분기)
| (단위: 주,원) | ||||
|---|---|---|---|---|
| 구 분 | 기간 | 일수 | 유통주식수 | 적 수 |
| 기초 | 2021.01.01~2021.03.31 | 90 | 104,942,629 | 9,444,836,610 |
| 주식선택권 행사 | 2021.01.25~2021.03.31 | 66 | 131,863 | 8,702,958 |
| 합 계 | 9,453,539,568 | |||
| 가중평균유통보통주식수 | 105,039,329 | |||
(2) 희석주당손익
연결회사가 발행한 잠재적인 보통주인 주식선택권, 전환우선주 및 전환사채에 의한 희석효과가 발생하지 아니하므로 당분기와 전분기 중 희석주당손익은 기본주당순손익과 동일합니다.
(3) 잠재적 보통주
반희석효과로 인하여 희석주당이익을 계산할 때 고려하지 않았지만 잠재적으로 미래에 기본주당이익을 희석화 할 수 있는 잠재적 보통주의 내용은 다음과 같습니다.
| (단위: 주) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 주식선택권 | 5,583,655 | 6,413,352 |
| 전환사채 | 4,559,963 | 4,559,963 |
| 합 계 | 10,143,618 | 10,973,315 |
23. 영업부문 정보
(1) 연결회사의 영업부문은 의약품, 신기술 연구 및 개발업 등을 주요 사업으로 하는 단일의 영업부문으로 이루어져 있습니다.
(2) 당분기말과 전기말 현재 연결회사의 국내와 해외의 비유동자산은 다음과 같습니다.
| (단위: 주) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 대한민국 | 5,009,394 | 4,159,158 |
| 미국 | 2,368,414 | 2,495,219 |
24. 특수관계자와의 거래
(1) 당분기말과 전기말 현재 연결회사의 주요경영진에 대한 보상 이외에는 특수관계자 거래는 없습니다.
(2) 주요 경영진에 대한 보상
주요 경영진은 이사(등기 및 비등기), 이사회의 구성원, 재무책임자 및 내부감사책임자를 포함하고 있습니다. 종업원 용역의 대가로서 주요 경영진에게 지급되었거나 지급될 보상금액은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 급여 | 683,904 | 498,416 |
| 퇴직급여 | 57,170 | 38,346 |
| 주식기준보상 | 668,217 | 530,515 |
| 합 계 | 1,409,291 | 1,067,277 |
25. 현금흐름표
(1) 당분기와 전분기 중 영업활동현금흐름의 조정내역 및 영업활동으로 인한 자산부채의 변동은 다음과 같습니다.
① 영업활동현금흐름의 조정내역
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 감가상각비 | 146,653 | 127,694 |
| 무형자산상각비 | 144,403 | 27,923 |
| 주식보상비용 | 424,269 | 622,015 |
| 이자비용 | 9,686 | 12,700 |
| 외화환산손실 | 525 | - |
| 유형자산처분손실 | 469 | - |
| 법인세비용(수익) | 18,834 | (3,984) |
| 외화환산이익 | (21,700) | - |
| 이자수익 | (71,312) | (19,358) |
| 합 계 | 651,827 | 766,990 |
② 영업활동으로 인한 자산부채의 변동
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 미수금의 감소(증가) | 576,286 | 32,692 |
| 미수수익의 감소(증가) | (44,358) | - |
| 선급금의 감소(증가) | 135 | (6) |
| 선급비용의 감소(증가) | 1,130,360 | 16,393 |
| 부가세대급금의 감소(증가) | (30,327) | 50,858 |
| 유동당기손익-공정가치측정금융자산 증가 | - | (564,700) |
| 장기선급금의 감소(증가) | (2,392) | - |
| 당기법인세자산의 감소(증가) | (3,246) | - |
| 장기미지급금의 증가(감소) | (92,747) | - |
| 선수금의 증가 | - | 1,013,558 |
| 미지급금의 증가(감소) | - | (2,371) |
| 예수금의 증가(감소) | (96,808) | (47,403) |
| 미지급비용의 증가(감소) | (96,065) | 120,478 |
| 합 계 | 1,340,838 | 619,499 |
(2) 당분기와 전분기 중 현금의 유입과 유출이 없는 중요한 거래는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 장기차입금의 유동성 대체 | 2,285,014 | 34,329 |
| 장기리스부채의 유동성 대체 | 42,449 | 15,866 |
| 선급금의 기타무형자산 대체 | - | 16,214 |
| 주식선택권의 주식발행초과금 대체 | 40,023 | - |
| 보증금의 유동성 대체 | 10,000 | - |
(3) 당분기 중 재무활동으로 인한 부채의 변동은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 기초금액 | 현금흐름 | 비현금 변동 | 기말금액 | |
| 유동성대체 | 이자비용 | ||||
| 단기차입금 | - | - | - | 2,285,014 | - |
| 장기차입금 | 1,523,343 | 761,671 | - | (2,285,014) | - |
| 리스부채 | 380,217 | (99,729) | 2,852 | - | 9,485 |
| 우선주부채 | 3,556,500 | - | 75,900 | - | - |
| 합 계 | 5,460,060 | 661,942 | 78,752 | - | 9,485 |
4. 재무제표
|
재무상태표 |
|
제 6 기 1분기말 2022.03.31 현재 |
|
제 5 기말 2021.12.31 현재 |
|
(단위 : 원) |
|
제 6 기 1분기말 |
제 5 기말 |
|
|---|---|---|
|
자산 |
||
|
Ⅰ.유동자산 |
16,466,845,706 |
19,220,124,258 |
|
(1)현금및현금성자산 |
2,763,844,695 |
6,216,697,895 |
|
(2)단기금융상품 |
13,000,000,000 |
11,000,000,000 |
|
(3)파생상품자산 |
309,735,458 |
309,735,458 |
|
(4)매출채권 및 기타채권 |
97,384,473 |
300,888,253 |
|
(5)선급금 |
1,840,000 |
1,975,000 |
|
(6)선급비용 |
182,760,075 |
1,313,119,971 |
|
(7)부가세대급금 |
98,624,255 |
68,297,331 |
|
(8)당기법인세자산 |
12,656,750 |
9,410,350 |
|
Ⅱ.비유동자산 |
16,317,888,706 |
16,466,476,231 |
|
(1)당기손익-공정가치 측정 금융자산 |
11,087,060,961 |
12,083,129,663 |
|
(2)종속기업투자주식 |
221,434,188 |
224,188,444 |
|
(3)유형자산 |
3,451,946,731 |
2,779,484,891 |
|
(4)사용권자산 |
261,232,303 |
307,224,253 |
|
(5)무형자산 |
905,587,899 |
689,035,141 |
|
(6)장기매출채권및기타채권 |
149,111,330 |
144,290,445 |
|
(7)장기선급금 |
241,515,294 |
239,123,394 |
|
자산총계 |
32,784,734,412 |
35,686,600,489 |
|
부채 |
||
|
Ⅰ.유동부채 |
23,894,303,311 |
21,892,515,588 |
|
(1)차입금 |
2,285,014,200 |
|
|
(2)미지급금 및 기타채무 |
581,941,372 |
775,161,944 |
|
(3)예수금 |
(16,853,163) |
79,954,451 |
|
(4)유동리스부채 |
147,657,563 |
140,855,854 |
|
(5)전환사채 |
12,467,965,487 |
12,467,965,487 |
|
(6)파생상품부채 |
8,428,577,852 |
8,428,577,852 |
|
Ⅱ.비유동부채 |
124,963,698 |
1,690,554,526 |
|
(1)장기차입금 |
1,523,342,800 |
|
|
(2)비유동리스부채 |
50,841,554 |
93,290,282 |
|
(3)복구충당부채 |
74,122,144 |
73,921,444 |
|
부채총계 |
24,019,267,009 |
23,583,070,114 |
|
자본 |
||
|
Ⅰ.자본금 |
11,039,826,200 |
11,028,980,300 |
|
Ⅱ.주식발행초과금 |
77,089,276,005 |
76,912,501,241 |
|
Ⅲ.기타자본구성요소 |
9,783,317,696 |
9,886,841,510 |
|
Ⅳ.결손금 |
(89,146,952,498) |
(85,724,792,676) |
|
자본총계 |
8,765,467,403 |
12,103,530,375 |
|
자본과부채총계 |
32,784,734,412 |
35,686,600,489 |
|
포괄손익계산서 |
|
제 6 기 1분기 2022.01.01 부터 2022.03.31 까지 |
|
제 5 기 1분기 2021.01.01 부터 2021.03.31 까지 |
|
(단위 : 원) |
|
제 6 기 1분기 |
제 5 기 1분기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
Ⅰ.매출액 |
3,667,259 |
3,667,259 |
92,141,667 |
92,141,667 |
|
Ⅱ.매출원가 |
1,098,361 |
1,098,361 |
||
|
Ⅲ.매출총이익 |
2,568,898 |
2,568,898 |
92,141,667 |
92,141,667 |
|
Ⅳ.판매비와관리비 |
2,580,219,488 |
2,580,219,488 |
2,805,646,022 |
2,805,646,022 |
|
Ⅴ.영업이익(손실) |
(2,577,650,590) |
(2,577,650,590) |
(2,713,504,355) |
(2,713,504,355) |
|
Ⅵ.기타수익 |
406,383,338 |
406,383,338 |
710,237,297 |
710,237,297 |
|
Ⅶ.기타비용 |
2,264,207 |
2,264,207 |
1,423,612 |
1,423,612 |
|
Ⅷ.금융수익 |
69,759,658 |
69,759,658 |
17,297,180 |
17,297,180 |
|
Ⅸ.금융비용 |
6,839,458 |
6,839,458 |
7,671,275 |
7,671,275 |
|
Ⅹ.지분법손실 |
1,292,714,768 |
1,292,714,768 |
817,020,451 |
817,020,451 |
|
XI.법인세비용차감전순이익(손실) |
(3,403,326,027) |
(3,403,326,027) |
(2,812,085,216) |
(2,812,085,216) |
|
XⅡ.법인세비용(수익) |
18,833,795 |
18,833,795 |
(3,984,257) |
(3,984,257) |
|
XⅢ.당기순이익(손실) |
(3,422,159,822) |
(3,422,159,822) |
(2,808,100,959) |
(2,808,100,959) |
|
XIV.기타포괄손익 |
(65,608,579) |
(65,608,579) |
14,348,716 |
14,348,716 |
|
(1)후속적으로 당기손익으로 재분류되는 항목 |
||||
|
1.해외사업환산손익 |
1,165,783 |
1,165,783 |
222,714 |
222,714 |
|
2.지분법자본변동 |
(66,774,362) |
(66,774,362) |
14,126,002 |
14,126,002 |
|
XV.총포괄손익 |
(3,487,768,401) |
(3,487,768,401) |
(2,793,752,243) |
(2,793,752,243) |
|
XVI.주당이익(손실) |
||||
|
(1)기본주당이익(손실) (단위 : 원) |
(31) |
(31) |
(27) |
(27) |
|
(2)희석주당이익(손실) (단위 : 원) |
(31) |
(31) |
(27) |
(27) |
|
자본변동표 |
|
제 6 기 1분기 2022.01.01 부터 2022.03.31 까지 |
|
제 5 기 1분기 2021.01.01 부터 2021.03.31 까지 |
|
(단위 : 원) |
|
자본 |
|||||
|---|---|---|---|---|---|
|
자본금 |
주식발행초과금 |
기타자본구성요소 |
결손금 |
자본 합계 |
|
|
2021.01.01 (Ⅰ.기초자본) |
10,494,262,900 |
63,950,642,778 |
8,887,589,085 |
(70,979,846,890) |
12,352,647,873 |
|
Ⅱ.당기순이익(손실) |
(2,808,100,959) |
(2,808,100,959) |
|||
|
Ⅲ.해외사업환산손익 |
222,714 |
222,714 |
|||
|
Ⅳ.지분법자본변동 |
14,126,002 |
14,126,002 |
|||
|
Ⅴ.주식보상비용 |
224,698,562 |
224,698,562 |
|||
|
Ⅵ.주식선택권 |
13,186,300 |
213,221,937 |
(45,886,165) |
180,522,072 |
|
|
2021.03.31 (Ⅶ.기말자본) |
10,507,449,200 |
64,163,864,715 |
9,080,750,198 |
(73,787,947,849) |
9,964,116,264 |
|
2022.01.01 (Ⅰ.기초자본) |
11,028,980,300 |
76,912,501,241 |
9,886,841,510 |
(85,724,792,676) |
12,103,530,375 |
|
Ⅱ.당기순이익(손실) |
(3,422,159,822) |
(3,422,159,822) |
|||
|
Ⅲ.해외사업환산손익 |
1,165,783 |
1,165,783 |
|||
|
Ⅳ.지분법자본변동 |
(66,774,362) |
(66,774,362) |
|||
|
Ⅴ.주식보상비용 |
2,107,306 |
2,107,306 |
|||
|
Ⅵ.주식선택권 |
10,845,900 |
176,774,764 |
(40,022,541) |
147,598,123 |
|
|
2022.03.31 (Ⅶ.기말자본) |
11,039,826,200 |
77,089,276,005 |
9,783,317,696 |
(89,146,952,498) |
8,765,467,403 |
|
현금흐름표 |
|
제 6 기 1분기 2022.01.01 부터 2022.03.31 까지 |
|
제 5 기 1분기 2021.01.01 부터 2021.03.31 까지 |
|
(단위 : 원) |
|
제 6 기 1분기 |
제 5 기 1분기 |
|
|---|---|---|
|
Ⅰ.영업활동현금흐름 |
(1,276,346,202) |
(1,579,151,109) |
|
(1)영업에서 창출된 현금 |
(1,341,784,975) |
(1,591,581,634) |
|
1.당기순이익(손실) |
(3,422,159,822) |
(2,808,100,959) |
|
2.조정 |
1,082,894,587 |
462,480,777 |
|
3.영업활동으로 인한 자산부채의 변동 |
997,480,260 |
754,038,548 |
|
(2)이자수취 |
65,438,773 |
14,798,925 |
|
(3)법인세의 납부 |
(2,368,400) |
|
|
Ⅱ.투자활동현금흐름 |
(3,066,356,103) |
(1,839,584,243) |
|
(1)투자활동으로 인한 현금유입액 |
3,010,600,000 |
2,072,368,500 |
|
1.단기금융상품의 처분 |
3,000,000,000 |
|
|
2.보증금의 감소 |
10,000,000 |
158,656,500 |
|
3.대여금의 감소 |
53,312,000 |
|
|
4.유동당기손익-공정가치측정금융자산 처분 |
1,860,400,000 |
|
|
5.유형자산의 처분 |
600,000 |
|
|
(2)투자활동으로 인한 현금유출액 |
(6,076,956,103) |
(3,911,952,743) |
|
1.단기금융상품의 취득 |
5,000,000,000 |
3,000,000,000 |
|
2.유형자산의 취득 |
715,500,000 |
886,605,482 |
|
3.무형자산의 취득 |
360,956,103 |
171,818 |
|
4.보증금의 증가 |
500,000 |
10,000,000 |
|
5.장기선급금의 증가 |
15,175,443 |
|
|
Ⅲ.재무활동현금흐름 |
866,983,746 |
898,487,669 |
|
(1)재무활동으로 인한 현금유입액 |
909,269,523 |
942,193,472 |
|
1.주식선택권의 행사 |
147,598,123 |
180,522,072 |
|
2.장기차입금의 증가 |
761,671,400 |
761,671,400 |
|
(2)재무활동으로 인한 현금유출액 |
(42,285,777) |
(43,705,803) |
|
1.리스부채의 상환 |
42,285,777 |
43,705,803 |
|
Ⅳ.현금및현금성자산의 증가(감소) |
(3,475,718,559) |
(2,520,247,683) |
|
Ⅴ.기초현금및현금성자산 |
6,216,697,895 |
2,975,718,422 |
|
Ⅵ.현금및현금성자산에 대한 환율변동 |
22,865,359 |
222,714 |
|
Ⅶ.기말현금및현금성자산 |
2,763,844,695 |
455,693,453 |
5. 재무제표 주석
| 제 6(당) 분기 2022년 03월 31일 현재 |
| 제 5(전) 기 2021년 12월 31일 현재 |
| 주식회사 카이노스메드 |
1. 일반사항
주식회사 카이노스메드("당사")는 의약품, 신기술 연구 및 개발업 등을 영위할 목적으로 2007년 6월 15일자로 설립되었고, 경기도 성남시 중원구 둔촌대로 541번길 29에 본사 및 미국에 사무소를 두고 있습니다.
회사는 2017년 11월 3일 설립된 하나금융11호기업인수목적 주식회사와 2019년 11월 29일 합병계약을 체결하였으며, 2020년 5월 20일을 합병기일로 하여 합병을 완료하였습니다. 하나금융11호기업인수목적 주식회사가 당사를 흡수합병하였으며, 합병 후 사명은 주식회사 카이노스메드입니다.
당사의 설립시 자본금은 50백만원이었으나, 수차례의 증자를 거쳐 당기말 현재의 자본금 11,040백만원(보통주자본금 11,040백만원)이며, 최대주주는 13.7%를 보유하고 있는 대표이사 이기섭입니다.
2. 재무제표 작성기준
분기재무제표는 기업회계기준서 제1034호 '중간재무보고'에 따라 작성되었으며 연차재무제표에서 요구되는 정보에 비하여 적은 정보를 포함하고 있습니다. 분기재무제표는 보고기간말 현재 유효한 한국채택국제회계기준에 따라 작성되었으며, 분기재무제표를 작성하기 위하여 채택한 중요한 회계정책은 별도의 언급이 없는 한 전기 연차재무제표 작성시 채택한 회계정책과 동일하게 적용되었습니다.
분기재무제표 작성을 위하여 채택한 중요한 회계정책은 다음과 같습니다.
3. 회계정책의 변경과 공시
1) 당사가 채택한 제ㆍ개정 기준서
회사는 2022년 1월 1일로 개시하는 회계기간부터 다음의 제ㆍ개정 기준서 및 해석서를 신규로 적용하였습니다.
(1) 기업회계기준서 제 1116호 '리스' 개정 - 2021년 6월 30일 후에도 제공되는 코로나19 관련 임차료 할인 등
코로나19의 직접적인 결과로 발생한 임차료 할인 등이 리스변경에 해당하는지 평가하지 않을 수 있도록 하는 실무적 간편법의 적용대상이 2022년 6월 30일 이전에 지급하여야 할 리스료에 영향을 미치는 리스료 감면으로 확대되었습니다. 리스이용자는 비슷한 상황에서 특성이 비슷한 계약에 실무적 간편법을 일관되게 적용해야 합니다.
(2) 기업회계기준서 제1016호 '유형자산' 개정 - 의도한 사용 전의 매각금액
기업이 자산을 의도한 방식으로 사용하기 전에 생산된 품목의 판매에서 발생하는 수익을 생산원가와 함께 당기손익으로 인식하도록 요구하며, 유형자산의 취득원가에서 차감하는 것을 금지하고 있습니다.
(3) 기업회계기준서 제1037호 '충당부채, 우발부채 및 우발자산' 개정 - 손실부담계약: 계약이행원가
손실부담계약을 식별할 때 계약이행원가의 범위를 계약 이행을 위한 증분원가와 계약 이행에 직접 관련되는 다른 원가의 배분이라는 점을 명확히 하였습니다.
(4) 한국채택국제회계기준 연차개선 2018-2020
한국채택국제회계기준 연차개선 2018-2020은 2022년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다.
·기업회계기준서 제1101호 '한국채택국제회계기준의 최초 채택’: 최초채택기업인 종속기업
·기업회계기준서 제1109호 '금융상품’: 금융부채 제거 목적의 10% 테스트 관련 수수료
·기업회계기준서 제1041호 '농림어업’: 공정가치 측정
2) 공표되었으나 아직 시행되지 않은 제ㆍ개정 기준서 및 해석서
당분기말 현재 제정ㆍ공표되었으나 시행일이 도래하지 않아 당사가 채택하지 않은 한국채택국제회계기준의 기준서 및 해석서는 다음과 같습니다.
(1) 기업회계기준서 제1001호 '재무제표 표시' 개정 - 부채의 유동/비유동 분류
보고기간말 현재 존재하는 실질적인 권리에 따라 유동 또는 비유동으로 분류되며, 부채의 결제를 연기할 수 있는 권리의 행사가능성이나 경영진의 기대는 고려하지 않습니다. 또한, 부채의 결제에 자기지분상품의 이전도 포함되나, 복합금융상품에서 자기지분상품으로 결제하는 옵션이 지분상품의 정의를 충족하여 부채와 분리하여 인식된 경우는 제외됩니다. 동 개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 적용하며, 조기적용이 허용됩니다.
(2) 기업회계기준서 제1001호 '재무제표 표시' - '회계정책'의 공시
중요한 회계정책을 정의하고 공시하도록 하며, 중요성 개념을 적용하는 방법에 대한 지침을 제공하기 위하여 국제회계기준 실무서 2 '회계정책 공시'를 개정하였습니다.
동 개정 사항은 2023년 1월 1일 이후 최초로 시작하는 회계연도부터 적용되며 조기적용이 허용됩니다.
(3) 기업회계기준서 제1008호 '회계정책, 회계추정의 변경 및 오류' - '회계추정'의 정의
회계추정을 정의하고, 회계정책의 변경과 구별하는 방법을 명확히 하였습니다. 동 개정 사항은 2023년 1월 1일 이후 최초로 시작하는 회계연도부터 적용되며 조기적용이 허용됩니다.
(4) 기업회계기준서 제1012호 '법인세' - 단일거래에서 생기는 자산과 부채에 대한 이연법인세
자산 또는 부채가 최초로 인식되는 거래의 최초 인식 예외 요건에 거래시점 동일한 가산할 일시적차이와 차감할 일시적차이를 발생시키지 않는 거래라는 요건을 추가하였습니다. 동 개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 적용하며, 조기적용이 허용됩니다.
(5) 기업회계기준서 제1117호 '보험계약' 제정
기업회계기준서 제1117호 '보험계약'은 기업회계기준서 제1104호 '보험계약’을 대체합니다. 보험계약에 따른 모든 현금흐름을 추정하고 보고시점의 가정과 위험을 반영한 할인율을 사용하여 보험부채를 측정하고, 매 회계연도별로 계약자에게 제공한 서비스(보험보장)를 반영하여 수익을 발생주의로 인식하도록 합니다. 또한, 보험사건과 관계없이 보험계약자에게 지급하는 투자요소(해약/만기환급금)는 보험수익에서 제외하며, 보험손익과 투자손익을 구분 표시하여 정보이용자가 손익의 원천을 확인할 수 있도록 하였습니다. 동 기준서는 2023년 1월 1일 이후 최초로 시작하는 회계연도부터 적용되며, 기업회계기준서 제1109호 '금융상품'을 적용한 기업은 조기적용이 허용됩니다.
4. 회계정책 및 중요한 회계추정 및 가정
4.1 회계정책
분기재무제표의 작성에 적용된 유의적 회계정책과 계산방법은 주석 3에서 설명하는 제ㆍ개정 기준서의 적용으로 인한 변경 및 아래 문단에서 설명하는 사항을 제외하고는 전기 재무제표 작성에 적용된 회계정책이나 계산방법과 동일합니다.
(1) 법인세비용
중간기간의 법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균연간법인세율, 즉 추정평균연간유효법인세율을 중간기간의 세전이익에 적용하여 계산합니다.
4.2 중요한 회계추정 및 가정
당사는 미래에 대하여 추정 및 가정을 하고 있습니다. 추정 및 가정은 지속적으로 평가되며, 과거 경험과 현재의 상황에서 합리적으로 예측가능한 미래의 사건과 같은 다른 요소들을 고려하여 이루어집니다. 이러한 회계추정은 실제 결과와 다를 수도 있습니다.
분기재무제표 작성시 사용된 중요한 회계추정 및 가정은 법인세비용을 결정하는데 사용된 추정의 방법을 제외하고는 전기 재무제표 작성에 적용된 회계추정 및 가정과 동일합니다.
4.3 COVID-19 영향
COVID-19의 확산은 국내 및 세계 경제에 중대한 영향을 미치고 있습니다. 이로 인해 당사의 향후 수익과 기타 재무성과에도 잠재적으로 부정적인 영향이 발생할 수 있습니다. COVID-19가 재무상태 및 영업성과에 미칠 영향의 범위를 예측하는 것은 현재 시점에는 매우 불확실하며, 당사의 영업활동 및 글로벌 시장 전반에 다양한 요인에 의해 영향을 미칠 것이므로 COVID-19의 효과는 당분간 당사의 영업성과에 완전히 반영되지 않을 수 있습니다.
분기재무제표 작성시 사용된 중요한 미래에 대한 회계추정 및 가정은 COVID-19에 따른 불확실성의 변동에 따라 조정을 유발할 수 있으며, 따라서 COVID-19와 영업활동 변경이 당사의 사업, 재무상태 및 성과, 유동성에 미칠 궁극적인 영향은 현재로는 예측할 수 없습니다.
5. 현금성자산 및 단기금융상품
(1) 당분기말과 전기말 현재 현금및현금성자산의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 기 |
| 보통예금 | 2,763,845 | 6,216,698 |
(2) 당분기말과 전기말 현재 단기금융상품의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 기 |
| 정기예금 | 13,000,000 | 11,000,000 |
6. 매출채권및기타채권
당분기말과 전기말 현재 매출채권및기타채권의 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 기 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
| 기타채권: | ||||
| 미수금 | 19,551 | - | 257,412 | - |
| 미수수익 | 77,834 | - | 33,476 | - |
| 보증금 | - | 149,111 | 10,000 | 144,290 |
| 합 계 | 97,385 | 149,111 | 300,888 | 144,290 |
당분기말과 전기말 현재 연체된 매출채권및기타채권은 없습니다.
7. 공정가치
당사는 공정가치를 산정하는 데 사용한 투입변수의 신뢰성에 대한 정보를 제공하기 위하여 금융상품을 기준서에서 정한 세 수준으로 분류합니다. 공정가치로 측정되는 금융상품은 공정가치 서열체계에 따라 구분되며 정의된 수준들은 다음과 같습니다.
| - |
측정일에 동일한 자산이나 부채에 대해 접근할 수 있는 활성시장의 (조정하지 않은) 공시가격 (수준 1) |
| - |
수준 1의 공시가격 외에 자산이나 부채에 대해 직접적으로나 간접적으로 관측할 수 있는 투입변수 (수준 2) |
| - | 자산이나 부채에 대한 관측할 수 없는 투입변수 (수준 3) |
당분기말과 전기말 현재 반복적으로 공정가치로 측정되고 인식된 당사의 금융상품은다음과 같습니다.
① 제 6(당) 분기
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 수준1 | 수준2 | 수준3 | 합계 |
| 공정가치로 측정되는 금융자산: | ||||
| 파생상품자산 | - | - | 309,735 | 309,735 |
| 비유동당기손익-공정가치측정금융자산(투자주식) | - | - | 642,787 | 642,787 |
| 비유동당기손익-공정가치측정금융자산(전환우선주) | - | - | 10,444,274 | 10,444,274 |
| 공정가치로 측정되는 금융부채: | ||||
| 유동파생상품부채 | - | - | 8,428,578 | 8,428,578 |
② 제 5(전) 기
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 수준1 | 수준2 | 수준3 | 합계 |
| 공정가치로 측정되는 금융자산: | ||||
| 파생상품자산 | - | - | 309,735 | 309,735 |
| 비유동당기손익-공정가치측정금융자산(투자주식) | - | - | 642,787 | 642,787 |
| 비유동당기손익-공정가치측정금융자산(전환우선주) | - | - | 11,440,343 | 11,440,343 |
| 공정가치로 측정되는 금융부채: | ||||
| 파생상품부채 | - | - | 8,428,578 | 8,428,578 |
8. 유형자산
(1) 당분기말과 전기말 현재 유형자산의 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 비 품 | 임차개량권 | 건설중인자산 | 합계 |
| 당분기말: | ||||
| 취득원가 | 603,695 | 228,410 | 3,002,322 | 3,834,427 |
| 감가상각누계액 | (229,429) | (153,052) | - | (382,481) |
| 장부가액 | 374,266 | 75,358 | 3,002,322 | 3,451,946 |
| 전기말: | ||||
| 취득원가 | 607,468 | 228,410 | 2,286,822 | 3,122,700 |
| 감가상각누계액 | (206,289) | (136,927) | - | (343,216) |
| 장부가액 | 401,179 | 91,483 | 2,286,822 | 2,779,484 |
(2) 당분기와 전분기 중 유형자산 취득원가의 변동내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 비 품 | 임차개량권 | 건설중인자산 | 합계 |
| 당기초 | 607,468 | 228,410 | 2,286,822 | 3,122,700 |
| 취득액 | - | - | 715,500 | 715,500 |
| 처분액 | (3,773) | - | - | (3,773) |
| 당분기말 | 603,695 | 228,410 | 3,002,322 | 3,834,427 |
| 전기초 | 952,863 | 206,110 | 753,900 | 1,912,873 |
| 취득액 | 171,105 | - | 715,500 | 886,605 |
| 전분기말 | 1,123,968 | 206,110 | 1,469,400 | 2,799,478 |
(3) 당분기와 전분기 중 유형자산 감가상각누계액의 변동내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 비 품 | 임차개량권 | 건설중인자산 | 합계 |
| 당기초 | 206,289 | 136,927 | - | 343,216 |
| 처분 | (2,704) | - | - | (2,704) |
| 감가상각비(*) | 25,844 | 16,125 | - | 41,969 |
| 당분기말 | 229,429 | 153,052 | - | 382,481 |
| 전기초 | 672,432 | 118,231 | - | 790,663 |
| 감가상각비(*) | 34,859 | 11,938 | - | 46,797 |
| 전분기말 | 707,291 | 130,169 | - | 837,460 |
(*) 당분기와 전분기 중 유형자산 감가상각비를 연구개발비 및 기타 판매비와관리비로 구분한 내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 구분 | 연구개발비 | 판매비와관리비 | 합계 |
| 당분기 | 23,344 | 18,625 | 41,969 |
| 전분기 | 34,954 | 11,842 | 46,796 |
(4) 당분기말 현재 당사는 유형자산에 대하여 삼성화재해상보험(주) 및 현대해상화재보험(주)의 화재보험에 가입하고 있습니다.
(5) 유형자산의 취득약정
당사는 토지 및 설비투자와 관련한 취득약정을 체결하고 있습니다(주석 17 참고).
9. 종속기업투자
당분기말과 전기말 현재 종속기업투자의 내역은 다음과 같습니다.
| (단위: 천원,%) | ||||||
|---|---|---|---|---|---|---|
| 구분 | 소재지 | 주요 영업활동 | 제 6(당) 분기 | 제 5(전) 기 | ||
| 지분율(%) | 장부금액 | 지분율(%) | 장부금액 | |||
| FAScinate Therapeutics, Inc.(*1) | 미국 | 연구개발업 | 100 | - | 100 | - |
| KAIDEA GLOBAL PTE.LTD | 싱가포르 | 연구개발업 | 55 | 221,434 | 55 | 224,188 |
(*1) 지분법손실로 인해 종속기업투자주식 장부금액을 전액 감액하였습니다.
(*2) 전기 중 신규 출자로 설립된 법인입니다.
10. 리스
(1) 리스이용자(기업회계기준서 제1116호)
당사는 기타비품 등을 1년에서 3년간 리스하고 있습니다. 이러한 리스는 단기리스이거나 소액자산 리스에 해당합니다. 당사는 이러한 리스에 사용권자산과 리스부채를 인식하지 않는 실무적 간편법을 적용합니다.
. 리스기간이 12개월 이내인 리스에 대하여 사용권자산과 리스부채를 인식하지 않음
. 소액 기초자산 리스에 대하여 사용권자산과 리스부채를 인식하지 않음
. 최초 적용일의 사용권자산 측정치에서 리스개설직접원가를 제외함
. 리스기간을 산정할 때 사후판단을 사용함
(2) 당분기와 전분기 사용권자산 및 리스부채의 변동내역은 다음과 같습니다.
① 제 6(당) 분기
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 사용권자산(*) | 리스부채(*) |
| 당기초 | 307,224 | 234,146 |
| 증가/변경 | - | - |
| 감가상각 | (45,992) | - |
| 이자비용 | - | 6,639 |
| 지급 | - | (42,286) |
| 당분기말 | 261,232 | 198,499 |
(*) 당사는 임차건물에 대한 리스 인식을 비롯하여 원상복구 의무가 있는 임차건물의계약 종료 시 발생할 수 있는 복구비용과 관련하여 지출할 것으로 예상되는 금액의 현재가치를 추정하여 사용권자산과 리스부채에 계상하고 있습니다. 사용권 자산은 모두 건물로 이루어져 있습니다.
② 제 5(전) 분기
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 사용권자산(*) | 리스부채(*) |
| 전기초 | 386,520 | 326,231 |
| 증가/변경 | - | - |
| 감가상각 | (42,151) | - |
| 이자비용 | - | 7,580 |
| 지급 | - | (43,706) |
| 전분기말 | 344,369 | 290,105 |
(*) 당사는 임차건물에 대한 리스 인식을 비롯하여 원상복구 의무가 있는 임차건물의계약 종료 시 발생할 수 있는 복구비용과 관련하여 지출할 것으로 예상되는 금액의 현재가치를 추정하여 사용권자산과 리스부채에 계상하고 있습니다. 사용권 자산은 모두 건물로 이루어져 있습니다.
(3) 당분기와 전분기 중 포괄손익계산서에 인식된 금액은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 사용권자산의 감가상각비 | 45,992 | 42,152 |
| 리스부채의 이자비용 | 6,639 | 7,580 |
| 리스료 - 단기 리스 | 7,500 | 2,522 |
| 리스료 - 소액 기초자산 리스 | - | 2,458 |
| 포괄손익계산서에 인식된 총 금액 | 60,131 | 54,712 |
(4) 당분기와 전분기 중 현금흐름표에 인식된 금액은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 현금유출 | (42,286) | (43,706) |
(*) 그 외 소액리스료 및 단기리스료를 포함하여 당분기에 49,786천원 (전분기: 48,686천원)이 유출 되었습니다.
(5) 연장선택권
일부 건물 리스는 당사가 계약의 해지불능기간 종료 전에 리스기간을 1년 연장 할 수있는 선택권을 포함합니다. 당사는 운영의 효율성을 위하여 가능하면 새로운 리스계약에 연장선택권을 포함하려고 노력합니다. 당사는 리스개시일에 연장선택권을 행사할 것이 상당히 확실한지 평가합니다. 당사는 당사가 통제 가능한 범위에 있는 유의적인 사건이 일어나거나 상황에 유의적인 변화가 있을 때 연장선택권을 행사할 것이 상당히 확실한지 다시 평가합니다.
11. 무형자산
(1) 당분기말과 전기말 현재 무형자산의 내역은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 특허권 | 기술사용권 | 소프트웨어 | 기타의무형자산 | 합계 |
| 당분기말: | |||||
| 취득원가 | 300,000 | 1,305,515 | 93,534 | 162,169 | 1,861,218 |
| 감가상각누계액 | (15,517) | (783,058) | (61,895) | (95,158) | (955,628) |
| 장부가액 | 284,483 | 522,457 | 31,639 | 67,011 | 905,590 |
| 전기말: | |||||
| 취득원가 | - | 1,275,515 | 93,534 | 131,212 | 1,500,261 |
| 감가상각누계액 | - | (663,297) | (59,246) | (88,682) | (811,225) |
| 장부가액 | - | 612,218 | 34,288 | 42,530 | 689,036 |
(2) 당분기와 전분기 중 무형자산의 장부가액의 변동내역은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 특허권 | 기술사용권 | 소프트웨어 | 기타의무형자산 | 합계 |
| 당기초 | - | 612,218 | 34,288 | 42,529 | 689,035 |
| 취득 | 300,000 | 30,000 | - | 30,956 | 360,956 |
| 무형자산상각비 | (15,517) | (119,761) | (2,649) | (6,476) | (144,403) |
| 당분기말 | 284,483 | 522,457 | 31,639 | 67,009 | 905,588 |
| 전기초 | - | 390,263 | 27,025 | 64,305 | 481,593 |
| 취득 | - | - | 172 | - | 172 |
| 무형자산상각비 | - | (19,511) | (2,968) | (5,444) | (27,923) |
| 전분기말 | - | 370,752 | 24,229 | 58,861 | 453,842 |
(3) 당분기와 전분기 중 무형자산상각비의 배분내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 무형자산상각비(판매비와관리비) | 143,967 | 26,402 |
| 연구개발비(판매비와관리비) | 436 | 1,520 |
| 합 계 | 144,403 | 27,922 |
12. 미지급금 및 기타채무
당분기말과 전기말 현재 미지급금 및 기타채무의 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 제 6(당) 분기 | 제 5(전) 기 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
| 미지급금 | 169,164 | - | 261,494 | - |
| 미지급비용 | 412,777 | - | 513,668 | - |
| 합 계 | 581,941 | - | 775,162 | - |
13. 차입금
(1) 당분기말과 전기말 현재 차입부채의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 제 6(당) 분기 | 제 5(전) 기 |
| 차입금 | 2,285,014 | - |
| 전환사채 | 12,467,965 | 12,467,965 |
| 장기차입금 | - | 1,523,343 |
| 합 계 | 14,752,979 | 13,991,308 |
(2) 당분기말 현재 전환사채의 발행내역은 다음과 같습니다.
| 구 분 | 내 용 |
|---|---|
| 사채의명칭 | 제2회 무기명식 이권부 무보증 사모전환사채 |
| 발행일 | 2020년06월30일 |
| 만기일 | 2025년06월30일 |
| 액면금액 | 20,000,000,000원 |
| 표면이자율(만기보장수익율) | 0.00%(1.00%) |
| 상환방법 | 만기일에 원금의 105.1205%를 일시상환한다 |
| 조기상환청구권(Put Option) | 사채권자는 사채의 발행일로부터 24개월 이후 45개월까지의 기간중 원금의 전부 및 일부에 대하여 조기상환수익률 연 1.0%(3개월 단위 복리계산)가 적용된 청구 금액을 조기상환 청구할 수 있음. |
| 매도청구권(Call Option) | 회사는 사채권자로부터 회사 또는 회사가 지정하는 제3자(매수인)에게 사채의 발행일로부터 12개월 이후 24개월까지의 기간 중 매3개월에 해당되는 날에 원금의 25/100에 대하여 매도 청구할 수 있음. 매수인이 매도청구 행사시 연1.0%(3개월 단위 복리계산)의 이율을 적용하여 계산한 금액을 지급하여야 함. |
| 전환시 발행할 주식의 종류 | 기명식보통주 |
| 전환청구기간 | 2021년 6월 30일부터 2025년 3월 30일 |
| 전환가격 | (1)최초 전환가액: 5,813원/주 (2)1차 조정전환가액: 4,852원/주 (2020년 9월 30일 조정) (3)2차 조정전환가액: 4,386원/주 (2020년12월30일 조정) (4)3차 조정전환가액: 4,070원/주 (2021년 03월30일 조정) |
(3) 당분기말과 전기말 현재 전환사채의 내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 구분 | 제 6(당) 분기 | 제 5(전) 기 | |
| 제2회 무보증 사모전환사채 |
액면금액 | 20,000,000 | 20,000,000 |
| 전환권조정 | (8,556,145) | (8,556,145) | |
| 상환할증금 | 1,024,110 | 1,024,110 | |
| 합 계 | 12,467,965 | 12,467,965 | |
(4) 차입금의 내용은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구분 | 차입처 | 연이자율 | 제 6(당) 분기 | 제 5(전) 기 | 상환방법 |
| 원화장기차입금 | 기업은행 | 2.759% | 2,285,014 | 1,523,343 | 만기상환 |
| 합 계 | 2,285,014 | 1,523,343 | |||
| 유동성대체액 | 2,285,014 | - | |||
| 비유동성잔액 | - | 1,523,343 | |||
(5) 차입금 상환일정은 다음과 같습니다.
| (단위: 천원) | |
|---|---|
| 구분 | 차입금 |
| 1년이내 | 2,285,014 |
| 1년초과 5년이내 | - |
| 5년초과 | - |
| 합 계 | 2,285,014 |
(*) 상기 현금흐름은 현재가치할인을 고려하지 아니한 금액입니다.
14. 자본금 및 주식발행초과금
(1) 당분기말과 전기말 현재 자본금의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 제 6(당) 분기 | 제 5(전) 기 |
| 발행할주식의 총수 | 300,000,000주 | 300,000,000주 |
| 1주당 액면금액 | 100원 | 100원 |
| 발행한 주식수 | 110,398,262주 | 110,289,803주 |
| 보통주자본금 | 11,039,826 | 11,028,980 |
| 발행한 우선주 주식수 | 0주 | 0주 |
| 우선주자본금 | - | - |
(2) 당분기와 전기 중 자본금 및 주식발행초과금의 변동내역은 다음과 같습니다.
| (단위:주, 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 내 역 | 주식수 | 자본금 | 주식발행초과금 | ||
| 보통주 | 우선주 | 보통주 | 우선주 | |||
| 2021.01.01 | 전기초 | 104,942,629 | - | 10,494,263 | - | 63,950,643 |
| 2021.01.25 | 주식선택권 행사 | 131,863 | - | 13,186 | - | 213,222 |
| 2021.04.22 | 주식선택권 행사 | 168,316 | - | 16,832 | - | 166,344 |
| 2021.07.27 | 주식선택권 행사 | 114,926 | - | 11,492 | - | 177,624 |
| 2021.10.22 | 주식선택권 행사 | 43,970 | - | 4,397 | - | 34,726 |
| 2021.11.12 | 주식선택권 행사 | 130,812 | - | 13,081 | - | 141,037 |
| 2021.11.12 | 유상증자 | 4,681,638 | - | 468,164 | - | 12,031,809 |
| 2021.12.22 | 주식선택권 행사 | 75,649 | - | 7,565 | - | 197,097 |
| 2021.12.31 | 전기말 | 110,289,803 | - | 11,028,980 | - | 76,912,502 |
| 2022.01.01 | 당기초 | 110,289,803 | - | 11,028,980 | - | 76,912,502 |
| 2022.01.18 | 주식선택권 행사 | 108,459 | - | 10,846 | - | 176,775 |
| 2022.03.31 | 당분기말 | 110,398,262 | - | 11,039,826 | - | 77,089,277 |
15. 기타자본구성요소
당분기말과 전기말 현재 기타자본구성요소는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 5(당) 분기 | 제 4(전) 기 |
| 전환권대가(*1) | 4,515,420 | 4,515,420 |
| 기타자본잉여금(*2) | 3,136,281 | 3,136,281 |
| 자기주식(*3) | (22,721) | (22,721) |
| 주식매입선택권 | 2,302,565 | 2,340,480 |
| 지분법자본변동 | (145,397) | (78,622) |
| 해외사업환산손익 | (2,831) | (3,997) |
| 합 계 | 9,783,317 | 9,886,841 |
(*1) 전환사채 평가에 따라 제2회 전환사채에 대한 전환권가치를 4,515,420천원 인식하였습니다.
(*2) 기타자본잉여금에는 전기 합병으로 인한 자기주식처분이익 2,627,141천원, 합병법인인 하나금융11호스팩의 합병계약일과 합병등기일 간 순자산 차액 259,593천원이 포함되어 있습니다.
(*3) 전기 합병 과정에서 하나금융11호기업인수목적 주식회사의 기존 주주가 주식매수청구권을 행사하여 보통주 자기주식을 취득하였습니다.
16. 주식기준보상
(1) 당분기말 현재 주식선택권의 주요 내용은 다음과 같습니다.
| 구 분 | 내 용 |
|---|---|
| 부여할 주식의 종류 | 보통주식 |
| 부여방법 | 주식결제형 |
| 권리행사가능기간 | 1. (13차) 부여일부터 2년후 100% 행사 (14, 15차) 부여일부터 2년후 50%, 이후 2년간 나머지를 매월말 분할 행사 (16차, 17차, 18차, 19차, 20차, 21차) 부여일부터 3년후 50%, 이후 2년간 나머지를 매월말 분할 행사 2. 행사가능일부터 10년 이내 (또는 퇴사시 퇴사일부터 1개월 이내 행사) |
| 가득조건 | 근무용역제공 2년~5년 |
(2) 당분기말 현재 주식선택권의 내역은 다음과 같습니다.
| (단위: 주, 원) | |||
|---|---|---|---|
| 차 수 | 부여일 | 행사가격 | 주식수 |
| 13차 | 2016.03.29 | 1,266 | 332,350 |
| 14차 | 2017.03.24 | 665 | 814,648 |
| 15차 | 2018.03.26 | 1,772 | 687,657 |
| 16차 | 2019.03.25 | 2,405 | 897,000 |
| 17차 | 2020.03.13 | 2,688 | 1,069,500 |
| 18차 | 2021.01.15 | 4,406 | 807,500 |
| 19차 | 2021.03.15 | 4,018 | 500,000 |
| 20차 | 2021.03.31 | 3,955 | 50,000 |
| 21차 | 2022.03.14 | 2,275 | 425,000 |
| 합 계 | 5,583,655 | ||
(3) 당사는 부여된 주식선택권의 보상원가를 이항모형을 이용한 공정가치접근법을 적용하여 산정하였으며, 보상원가를 산정하기 위한 제반 가정 및 변수는 다음과 같습니다.
| (단위: 원) | ||||
|---|---|---|---|---|
| 차 수 | 내부 산출주가 | 무위험수익률 | 주가변동성 | 부여일의 공정가치 |
| 13차 | 4,000 | 1.85% | 14.40% | 27 |
| 14차 | 4,000 | 2.21% | 6.60% | 317 |
| 15차 | 11,400 | 2.61% | 28.00% | 3,832 |
| 16차 | 16,400 | 1.88% | 31.65% | 6,531 |
| 17차 | 15,400 | 1.54% | 28.37% | 4,571 |
| 18차 | 4,290 | 1.61% | 42.32% | 2,086 |
| 19차 | 4,050 | 1.98% | 58.32% | 2,562 |
| 20차 | 3,895 | 1.92% | 50.84% | 2,214 |
| 21차 | 2,070 | 2.66% | 61.20% | 1,333 |
(4) 당분기 및 전분기 중 주식선택권의 변동내역은 다음과 같습니다.
| (단위: 주) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 기초수량 | 5,555,020 | 5,029,928 |
| 부여 | 425,000 | 1,595,500 |
| 취소 또는 소멸 | (287,906) | (80,213) |
| 행사 | (108,459) | (131,863) |
| 분기말수량 | 5,583,655 | 6,413,352 |
(5) 당분기말 현재 행사가능한 주식선택권은 2,233,847주이며, 당분기 중 행사된 주식선택권은 다음과 같습니다.
| (단위: 원,주) | ||
|---|---|---|
| 구 분 | 행사가격 | 행사주식수 |
| 14차 | 665 | 39,675 |
| 15차 | 1,772 | 68,784 |
| 합 계 | 108,459 | |
(6) 당분기 및 전분기 중 인식한 주식보상비용은 각각 2,107천원 및 224,699천원입니다. 당분기에 인식한 주식보상비용 중 47,928천원은 연구개발비로 인식하였습니다.
17. 우발상황 및 약정사항
(1) 자본적 지출 약정
당분기말 및 전기말 현재 체결 된 자본적 지출 약정사항은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 기 |
| 유형자산 | 7,616,714 | 7,616,714 |
(*) 당사는 예정된 유형자산 취득 중도금 지급을 위해서 중소기업은행과 한도 3,047백만원의 여신거래약정을 체결하였으며, 당분기말 현재 1,2,3차중도금에 대하여 차입금 2,285백만원을 인식하였습니다.
(2) 기술이전 및 라이선스 약정
① 한국화학연구원
당사는 2010년 9월 1일부터 한국화학연구원과 공동으로 동 연구원의 소유인 KRV-2219(NNRTI) 화합물을 이용한 HIV치료제 개발을 위한 임상 1상 연구를 수행하여 2012년 중 완료하였으며, 동 화합물의 임상 2상 및 이후의 개발과 상업화를 포함한 권리를 이전 받는 계약을 2012년 11월 7일자로 체결하였습니다.
당사는 동 연구원이 제공한 개발성과에 대한 보상으로 USD 350,000의 License fee를 지급하였고, 향후 개발단계에 따라 Milestone fee를 지급하기로 하였으나, 2018년1월 중 계약의 조건 및 세부사항이 변경됨에 따라 royalty를 제외한 Milestone 총액에서 동 연구원의 분배비율만큼 지급하였으며, 향후 royalty만 개발성공시 지급하기로 하였습니다.
② Crown Bioscience, Inc.
당사는 후보물질 도출단계를 마친 대사질환 치료제인 DGAT1(Diacylglycerol acyltransferase1) 의 저해제를 중국의 CRO 업체인 Crown Bioscience, Inc.로 2014년 8월에 기술이전 및 중국에서의 상업화에 대한 권리를 이전하는 계약을 체결하였습니다.
향후 개발 성공시에 계약서에 명시되어 있는 조건에 따라 개발 단계별로 경상기술료 및 로열티를 수령하기로 하였습니다.
③ Jiangsu Aidea Pharmaceutical Co., Ltd. (구, Yangzhou AIDEA Biotech Co., LTD)
당사는 당사가 보유한 기술을 적용하여 Jiangsu Aidea Pharmaceutical사와 HIV치료제 관련 기술이전 및 중국에서의 상업화에 대한 권리를 이전하는 계약을 2014년 10월 10일자로 체결하였습니다. 당사는 제공한 플랫폼 기술에 대한 보상으로 USD 200,000의 License fee를 수령하였으며, 향후 개발단계에 따라 Milestone fee를 수령하기로 하였고, 기술개발 완료 후 시판으로 발생하는 판매금액의 계약서상 명시된 조건으로 royalty를 수령하기로 하였습니다.
또한, 당사가 개발 중인 2개 항암제의 중국 지역에 국한된 포괄적 권리를 이전하는 계약을 Jiangsu Aidea Pharmaceutical사와 2015년 12월 10일자로 체결하였으며, 초기 정액기술료 USD 2,000,000와 향후 개발단계에 따라 Milestone fee를 수령하기로하였고, 기술개발 완료 후 시판으로 발생하는 판매금액의 계약서상 명시된 조건으로 royalty를 수령하기로 하였습니다.
한편, 2017년 12월 18일 HIV치료제와 항암제 중 에피제네틱스 항암제 BRD4 저해제에 대하여 계약변경을 실시하였으며, royalty를 제외한 Milestone 총액에서 HIV치료제는 USD 1,500,000을, 그리고 BRD4 저해제는 USD 500,000을 계약일로부터 30일 이내에 수령하였습니다. 해당 계약변경으로 인해 기존 royalty 수령조건은 변경되지 않았습니다.
④ 충남대학교 산학협력단 및 한국화학연구원
당사는 충남대학교산학협력단과 한국화학연구원이 공동개발한 FAF1을 표적으로 하는 허혈성 질환 치료제 관련 전용실시에 대한 권리를 이전 받는 계약을 2015년 9월 24일자로 체결하였습니다.
동 협력단 및 연구원이 제공한 개발성과에 대한 보상으로 200,000천원의 License Fee를 지급하였으며, 향후 개발단계에 따라 Milestone fee를 지급하기로 하였고, 경상기술료는 계약제품 순매출액의 4%를 지급하기로 하였습니다. 그리고 재실시의 경우계약서상 명시된 분배비율로 지급하기로 하였습니다.
⑤ 한국화학연구원
당사는 2017년 8월 25일부터 한국화학연구원과 공동으로 '심순환계 질환 치료 선도물질' 도출 과제를 수행하였으며, 이를 통해 약학적으로 허용가능한 다수의 화합물을도출하는데 성공하였습니다. 이 과제에서 도출된 화합물을 활용한 이후의 연구개발 및 상업화를 포함한 상용화 권리를 확보하기 위하여 당사는 한국화학연구원으로부터본 기술도입을 결정하고, 2020년 10월 21일자로 기술도입 계약을 체결하였습니다. 당사는 동연구원이 제공한 성과에 대한 보상으로 총 300,000천원(이중 100,000천원은 전기에, 100,000천원은 당분기에 지급하였습니다.)의 선급실시료를 지급하고 무형자산으로 계상하였으며, 향후 매출 발생시 1%의 경상실시료를 지급할 예정입니다.
이와 관련하여 당사는 서울보증보험과 2020년 10월 21부터 2022년 9월 30일까지 피보험자를 한국화학연구원으로하여 220,000천원의 이행(지급)보증보험 계약을 체결하였습니다.
⑥ 충남대학교 산학협력단
당사는 충남대학교산학협력단으로부터 암 및 염증 치료를 위한 IRAKs 및 TAK 저해제 개발 관련 노하우에 대한 권리를 이전 받는 계약을 2018년 11월 14일자로 체결하였습니다.
동 협력단이 제공한 성과에 대한 보상으로 2018년 11월 50,000천원의 정액기술료를지급하였고, 향후 최초로 임상시험 승인시 실적기술료로 100,000천원을 지급하기로 하였습니다.
⑦ FAScinate Therapeutics Inc.
당사는 미국 현지법인 FAScinate Therapeutics Inc. 에 당사가 개발하고 있는 파킨슨병 치료제의 미국임상을 진행하고 추후 해외 제약사와의 기술이전을 추진하기 위하여, 2021년 9월 27일자로 기술이전계약을 체결하였습니다.
총 계약금 USD 2,000,000 및 향후 파킨슨병으로 발생하는 모든 수입의 10%를 로열티로 받는 것으로 약정하였습니다.
⑧ 기술이전계약과 관련된 불확실성 및 기타사항
당사의 향후 마일스톤 및 로열티 수익은 임상시험, 관계당국의 허가 등 개발의 성공여부에 따라 달라질 수 있으므로 발생가능성에 불확실성이 내포되어 있습니다.
(3) 보험가입내역
당사는 주석 10 이외에 DB손해보험 등에 임직원 단체보험 및 환경책임보험을 가입하고 있습니다.
18. 기타수익과 기타비용
(1) 당분기와 전분기 중 기타수익의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 외환차익 | 5,181 | 27,449 |
| 외화환산이익 | 21,700 | 682,736 |
| 잡이익 | 3 | 52 |
| 당기손익공정가치측정금융자산평가이익 | 379,500 | - |
| 합 계 | 406,384 | 710,237 |
(2) 당분기와 전분기 중 기타비용의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 외환차손 | 1,270 | 1,424 |
| 외화환산손실 | 525 | - |
| 유형자산처분손실 | 469 | - |
| 합 계 | 2,264 | 1,424 |
19. 금융수익과 금융비용
(1) 당분기와 전분기 중 금융수익의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 금융수익-유효이자율법에 따른 이자수익 | ||
| 이자수익 | 69,760 | 17,297 |
(2) 당분기와 전분기 중 금융비용의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 이자비용 | 6,839 | 7,671 |
20. 법인세비용과 이연법인세
(1) 당분기와 전분기 중 법인세비용의 구성내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 법인세부담액 | - | - |
| 일시적차이 등의 발생과 소멸로 인한 이연법인세비용 | - | - |
| 당기손익 이외로 인식되는 항목과 관련된 법인세비용 | 18,834 | (3,984) |
| 법인세비용(수익) | 18,834 | (3,984) |
(2) 중간기간의 법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균연간법인세율, 즉 추정평균연간유효법인세율을 중간기간의 세전이익에 적용하여 계산하였습니다.
21. 비용의 성격별 분류
당분기와 전분기 중 비용의 성격별 분류 내역은 다음과 같습니다.
| (단위: 천원) | |||||||
|---|---|---|---|---|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 | |||||
| 매출원가 | 기타판매비와관리비 | 연구개발비 | 합계 | 기타판매비와관리비 | 연구개발비 | 합계 | |
| 급여 | - | 472,979 | 98,661 | 571,640 | 644,583 | 280,108 | 924,691 |
| 퇴직급여 | - | 55,488 | 18,130 | 73,618 | 39,082 | 21,006 | 60,088 |
| 보험료 | - | 2,123 | 980 | 3,103 | 2,521 | 1,986 | 4,507 |
| 복리후생비 | - | 69,621 | 24,772 | 94,393 | 42,924 | 27,755 | 70,679 |
| 여비교통비 | - | 4,059 | 257 | 4,316 | 3,883 | 375 | 4,258 |
| 접대비 | - | 10,848 | 785 | 11,633 | 7,110 | 253 | 7,363 |
| 임차료 | - | 7,500 | - | 7,500 | 1,390 | 1,133 | 2,523 |
| 감가상각비 | - | 51,759 | 36,202 | 87,961 | 40,948 | 48,001 | 88,949 |
| 무형자산상각비 | - | 143,967 | 436 | 144,403 | 26,402 | 1,520 | 27,922 |
| 세금과공과 | - | 8,690 | 490 | 9,180 | 8,459 | 2,246 | 10,705 |
| 연구개발비(외주) | - | - | 1,444,695 | 1,444,695 | - | 1,154,655 | 1,154,655 |
| 연구개발비(재료) | - | - | 120 | 120 | - | 48,786 | 48,786 |
| 지급수수료 | 1,098 | 88,472 | 9,057 | 98,627 | 117,497 | 29,599 | 147,096 |
| 소모품비 | - | 2,354 | 600 | 2,954 | 4,397 | 1,611 | 6,008 |
| 수선유지비 | - | - | - | - | 1,152 | - | 1,152 |
| 통신비 | - | 2,087 | - | 2,087 | 2,185 | 734 | 2,919 |
| 교육훈련비 | - | 66 | 111 | 177 | - | 150 | 150 |
| 관리비 | - | 12,521 | 3,358 | 15,879 | 10,216 | 6,795 | 17,011 |
| 도서인쇄비 | - | 6,820 | - | 6,820 | 919 | 255 | 1,174 |
| 잡비 | - | 102 | - | 102 | 248 | 64 | 312 |
| 주식보상비용 | - | (45,821) | 47,928 | 2,107 | 153,424 | 71,275 | 224,699 |
| 합 계 | 1,098 | 893,635 | 1,686,582 | 2,581,315 | 1,107,340 | 1,698,307 | 2,805,647 |
22. 종업원급여
당분기와 전분기 중 비용으로 인식된 종업원급여의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 급여 | 571,641 | 924,691 |
| 퇴직급여 | 73,619 | 60,088 |
| 주식보상비용 | 2,107 | 224,699 |
| 합 계 | 647,367 | 1,209,478 |
23. 주당손익
(1) 기본주당이익(손실)
당분기와 전분기 중 주당이익(손실)의 산출내역은 다음과 같습니다.
① 기본주당이익(손실)
| (단위: 원) | ||
|---|---|---|
| 구 분 | 제 5(당) 분기 | 제 4(전) 분기 |
| 당기순이익(손실) | (3,422,159,821) | (2,808,100,959) |
| 가중평균유통보통주식수 | 110,377,775 | 105,039,329 |
| 기본주당이익(손실) | (31) | (27) |
② 가중평균유통보통주식수
(당분기)
| (단위: 주,원) | ||||
|---|---|---|---|---|
| 구 분 | 기간 | 일수 | 유통주식수 | 적 수 |
| 기초 | 2022.01.01~2022.03.31 | 90 | 110,289,803 | 9,926,082,270 |
| 주식선택권 행사 | 2022.01.18~2022.03.31 | 73 | 108,459 | 7,917,507 |
| 합 계 | 9,933,999,777 | |||
| 가중평균유통보통주식수 | 110,377,775 | |||
(전분기)
| (단위: 주,원) | ||||
|---|---|---|---|---|
| 구 분 | 기간 | 일수 | 유통주식수(*) | 적 수 |
| 기초 | 2021.01.01~2021.03.31 | 90 | 104,942,629 | 9,444,836,610 |
| 주식선택권 행사 | 2021.01.25~2021.03.31 | 66 | 131,863 | 8,702,958 |
| 합 계 | 9,453,539,568 | |||
| 가중평균유통보통주식수 | 105,039,329 | |||
(2) 희석주당손익
당사가 발행한 잠재적인 보통주인 주식선택권 및 전환우선주에 의한 희석효과가 발생하지 아니하므로 당분기와 전분기 중 희석주당손익은 기본주당순손익과 동일합니다.
(3) 잠재적 보통주
반희석효과로 인하여 희석주당이익을 계산할 때 고려하지 않았지만 잠재적으로 미래에 기본주당이익을 희석화 할 수 있는 잠재적 보통주의 내용은 다음과 같습니다.
| (단위: 주) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 주식선택권 | 5,583,655 | 6,413,352 |
| 전환사채 | 4,559,963 | 4,559,963 |
| 합 계 | 10,143,618 | 10,973,315 |
24. 특수관계자와의 거래
(1) 당분기말 현재 특수관계자 현황은 다음과 같습니다.
| 구분 | 회사명 |
|---|---|
| 종속기업 | FAScinate Therapeutics, Inc. |
| 종속기업 | KAIDEA GLOBAL PTE.LTD |
(2) 당분기말 및 전기말 특수관계자에 대한 채권·채무의 주요 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 특수관계자명 | 계정과목 | 당분기말 | 전기말 |
| 종속기업 | FAScinate Therapeutics, Inc. | 전환우선주투자 | 10,315,608 | 11,459,383 |
| 미수금 | 8,855 | 73,113 | ||
(3) 당분기와 전분기특수관계자와의 주요 거래내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 특수관계자명 | 계정과목 | 제 6(당) 분기 | 제 5(전) 분기 |
| 종속기업 | FAScinate Therapeutics, Inc. | 연구개발비 | 8,961 | 375,042 |
(4) 당분기와 전분기 특수관계자와의 자금 거래는 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구분 | 특수관계자명 | 제 6(당) 분기 | 제 5(전) 분기 | ||
| 대여 | 회수 | 대여 | 회수 | ||
| 종속기업 | FAScinate Therapeutics, Inc. | - | - | - | 57,875 |
(5) 주요 경영진에 대한 보상
주요 경영진은 이사(등기 및 비등기), 이사회의 구성원, 재무책임자 및 내부감사책임자를 포함하고 있습니다. 종업원 용역의 대가로서 주요 경영진에게 지급되었거나 지급될 보상금액은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 급여 | 385,293 | 470,565 |
| 퇴직급여 | 57,170 | 38,346 |
| 주식기준보상 | 262,697 | 164,935 |
| 합 계 | 705,160 | 673,846 |
25. 현금흐름표
(1) 당분기와 전분기 중 영업활동현금흐름의 조정내역 및 영업활동으로 인한 자산부채의 변동은 다음과 같습니다.
① 영업활동현금흐름의 조정내역
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 감가상각비 | 87,961 | 88,949 |
| 무형자산 감가상각비 | 144,403 | 27,923 |
| 이자비용 | 6,839 | 7,671 |
| 주식보상비용 | 2,107 | 224,699 |
| 지분법손실 | 1,292,715 | 817,020 |
| 이자수익 | (69,760) | (17,297) |
| 법인세수익 | - | (3,984) |
| 외화환산이익 | (21,700) | (682,500) |
| 외화환산손실 | 525 | - |
| 유형자산처분손실 | 469 | - |
| 법인세비용 | 18,834 | - |
| 당기손익공정가치측정금융자산평가이익 | (379,500) | - |
| 합 계 | 1,082,893 | 462,481 |
② 영업활동으로 인한 자산부채의 변동
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 미수금의 증감 | 237,755 | 26,504 |
| 미수수익의 증감 | (44,358) | 3,412 |
| 선급금의 증감 | 135 | (6) |
| 선급비용의 증감 | 1,130,360 | 16,398 |
| 부가세대급금의 증감 | (30,327) | 50,858 |
| 유동당기손익-공정가치측정금융자산의 증감 | - | (564,700) |
| 당기법인세자산의 증감 | (3,246) | - |
| 장기선급금의 증감 | (2,392) | - |
| 미지급금의 증감 | (92,747) | 15,213 |
| 예수금의 증감 | (96,808) | (47,403) |
| 미지급비용의 증감 | (100,892) | 240,204 |
| 선수금의 증감 | - | 1,013,558 |
| 합 계 | 997,480 | 754,038 |
(2) 당분기와 전분기 중 현금의 유입과 유출이 없는 중요한 거래는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 제 6(당) 분기 | 제 5(전) 분기 |
| 장기차입금의 유동성 대체 | 2,285,014 | 34,329 |
| 장기리스부채의 유동성 대체 | 42,449 | 15,866 |
| 선급금의 기타무형자산 대체 | - | 16,214 |
| 주식선택권의 주식발행초과금 대체 | 40,023 | - |
| 보증금의 유동성 대체 | 10,000 | - |
(3) 당분기와 전분기 중 재무활동으로 인한 부채의 변동은 다음과 같습니다.
① 제 6(당) 분기
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 기초금액 | 현금흐름 | 비현금 변동 | 기말금액 | |
| 유동성대체 | 이자비용 | ||||
| 단기차입금 | - | - | 2,285,014 | - | 2,285,014 |
| 장기차입금 | 1,523,343 | 761,671 | (2,285,014) | - | - |
| 리스부채 | 234,146 | (42,286) | - | 6,639 | 198,499 |
| 합 계 | 1,757,489 | 719,385 | - | 6,639 | 2,483,513 |
② 제 5(전) 분기
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 기초금액 | 현금흐름 | 비현금 변동 | 기말금액 | |
| 유동성대체 | 이자비용 | ||||
| 장기차입금 | - | 761,671 | - | - | 761,671 |
| 리스부채 | 326,231 | (43,706) | - | 7,580 | 290,105 |
| 합 계 | 326,231 | 717,965 | - | 7,580 | 1,051,776 |
6. 배당에 관한 사항
가. 배당에 관한 사항
이익 배당과 관련해서 당사의 정관에 규정하고 있는 사항은 다음과 같습니다.
|
제57조 (이익배당) 1. 이익배당은 금전 또는 금전 외의 재산으로 할 수 있다. 그러나 주식에 의한 배당은 이익배당총액의 2분의 1에 상당하는 금액을 초과하지 못한다. 2. 전항의 배당은 매결산기말 현재의 주주명부에 기재된 주주 또는 등록된 질권자에게 지급한다. 3. 이익의 배당을 주식으로 하는 경우 회사가 수종의 주식을 발행한 때에는 주주총회의 결의로 그와 다른 종류의 주식으로도 할 수 있다. |
나. 주요배당지표
| 구 분 | 주식의 종류 | 당기 | 전기 | 전전기 |
|---|---|---|---|---|
| 제6기 1분기 |
제5기 | 제4기 | ||
| 주당액면가액(원) | 100 | 100 | 100 | |
| (연결)당기순이익(백만원) | -3,807 | -16,225 | -11,448 | |
| (별도)당기순이익(백만원) | -3,422 | -14,744 | -13,341 | |
| (연결)주당순이익(원) | -34 | -153 | -113 | |
| 현금배당금총액(백만원) | - | - | - | |
| 주식배당금총액(백만원) | - | - | - | |
| (연결)현금배당성향(%) | - | - | - | |
| 현금배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주식배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주당 현금배당금(원) | - | - | - | - |
| - | - | - | - | |
| 주당 주식배당(주) | - | - | - | - |
| - | - | - | - | |
다. 과거 배당 이력
| (단위: 회, %) |
| 연속 배당횟수 | 평균 배당수익률 | ||
|---|---|---|---|
| 분기(중간)배당 | 결산배당 | 최근 3년간 | 최근 5년간 |
| - | - | - | - |
- 해당사항이 없습니다.
7. 증권의 발행을 통한 자금조달에 관한 사항
7-1. 증권의 발행을 통한 자금조달 실적
가. 증자(감자)현황
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 원, 주) |
| 주식발행 (감소)일자 |
발행(감소) 형태 |
발행(감소)한 주식의 내용 | ||||
|---|---|---|---|---|---|---|
| 종류 | 수량 | 주당 액면가액 |
주당발행 (감소)가액 |
비고 | ||
| 2020년 05월 20일 | - | 보통주 | 97,057,042 | 100 | - | 합병신주 (주1) |
| 2020년 05월 20일 | - | 우선주 | 316,516 | 100 | - | 상동 |
| 2020년 06월 08일 | 전환권행사 | 보통주 | 316,516 | 100 | - | (주2) |
| 2020년 06월 22일 | 주식매수선택권행사 | 보통주 | 809,456 | 100 | 1,267 | |
| 2020년 07월 21일 | 주식매수선택권행사 | 보통주 | 433,669 | 100 | 1,293 | |
| 2020년 08월 13일 | 주식매수선택권행사 | 보통주 | 799,000 | 100 | 1,000 | (주3) |
| 2020년 10월 22일 | 주식매수선택권행사 | 보통주 | 125,946 | 100 | 1,303 | |
| 2021년 01월 21일 | 주식매수선택권행사 | 보통주 | 131,863 | 100 | 1,374 | |
| 2021년 04월 21일 | 주식매수선택권행사 | 보통주 | 168,316 | 100 | 941 | |
| 2021년 07월 23일 | 주식매수선택권행사 | 보통주 | 114,926 | 100 | 1,349 | |
| 2021년 10월 21일 | 주식매수선택권행사 | 보통주 | 43,970 | 100 | 903 | |
| 2021년 11월 12일 | 주식매수선택권행사 | 보통주 | 130,812 | 100 | 1,231 | |
| 2021년 11월 13일 | 유상증자(제3자배정) | 보통주 | 4,681,638 | 100 | 2,670 | |
| 2021년 12월 21일 | 주식매수선택권행사 | 보통주 | 75,649 | 100 | 1,629 | |
| 2022년 01월 18일 | 주식매수선택권행사 | 보통주 | 108,459 | 100 | 1,218 | |
*당사는 SPAC 합병된 법인으로 증자(감자)현황의 공시대상기간은 법적 실체를 따라 기재하였습니다.
*주식매수선택권행사 시 주당 발행가액은 부여 회차별로 행사가격이 상이하여 해당 증자에 대한 평균발행가액을 기재하였습니다
(주1) 피합병회사인 주식회사 카이노스메드와의 합병비율은 1:6.9 입니다.
(주2) 전환우선주의 전환권 행사로 잔여 우선주는 없습니다.
(주3) 제1회 전환사채의 전환권 행사(SPAC 법인 당시 발행했던 전환사채)입니다.
나. 미상환 전환사채 발행현황
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 백만원, 주) |
| 종류\구분 | 회차 | 발행일 | 만기일 | 권면(전자등록)총액 | 전환대상 주식의 종류 |
전환청구가능기간 | 전환조건 | 미상환사채 | 비고 | ||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 전환비율 (%) |
전환가액 | 권면(전자등록)총액 | 전환가능주식수 | ||||||||
| 제2회 무기명식 무보증 사모 전환사채 |
2 | 2020년 06월 30일 | 2025년 06월 30일 | 20,000 | 기명식 보통주 | 2021.06.30 ~2025.03.30 |
100 | 4,070 | 20,000 | 4,914,004 | (주1) |
| 합 계 | - | - | - | 20,000 | 기명식 보통주 | - | - | - | 20,000 | 4,914,004 | - |
(주1) 발행 당시 전환가액은 5,813원이며, 상기 전환가액 및 전환가능주식수는 정해진 기준에 따른 전환가액조정이 반영된 금액입니다.
| [채무증권의 발행 등과 관련된 사항] |
다. 채무증권 발행실적
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 백만원, %) |
| 발행회사 | 증권종류 | 발행방법 | 발행일자 | 권면(전자등록)총액 | 이자율 | 평가등급 (평가기관) |
만기일 | 상환 여부 |
주관회사 |
|---|---|---|---|---|---|---|---|---|---|
| 주식회사 카이노스메드 |
회사채 | 사모 | 2020년 06월 30일 | 20,000 | 1 | - | 2025년 06월 30일 | 미상환 | - |
| 합 계 | - | - | - | 20,000 | 1 | - | - | - | - |
<채무증권 현황>
|
발행일 |
2020년 6월 30일 |
|
|
발행금액 |
20,000백만원 |
|
|
발행목적 |
타법인 취득자금 및 운영자금 |
|
|
발행방법 |
사모 |
|
|
상장여부 |
비상장 |
|
|
미상환잔액 |
20,000백만원 |
|
|
자본인정에 |
회계처리 근거 |
전환권의 전환가격 조정조건이 "회제이-0009"4에 따른 확정대확정 조건에 해당함에 따라 전환권대가를 자본으로 인식함. |
|
신용평가기관의 |
해당 사항 없음 | |
|
미지급 누적이자 |
- | |
|
만기 및 조기상환 가능일 |
만기일 : 2025년 6월 30일 발행일로부터 2년이 경과된 2022년 6월 30일 및 이후 매 3개월에 해당되는 날 |
|
|
발행금리 |
발행일로부터 상환기일 전일까지 전자등록금액에 대하여 표면금리 0%, 만기보장수익률은 1%(3개월 단위 복리계산) | |
|
우선순위 |
후순위(일반채권, 후순위채권보다 후순위) |
|
|
부채분류 시 재무구조에 |
해당 사항 없음 (전환권 대가를 부채로 분류할 경우엔 별도 외부 평가기관의 공정가치 평가를 통해 영향을 측정해볼 수 있음) |
|
|
기타 중요한 발행조건 등 |
- |
|
라. 기업어음증권 미상환 잔액
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
1년초과 2년이하 |
2년초과 3년이하 |
3년 초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | |
마. 단기사채 미상환 잔액
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
합 계 | 발행 한도 | 잔여 한도 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
바. 회사채 미상환 잔액
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | 20,000 | - | - | - | 20,000 | |
| 합계 | - | - | - | 20,000 | - | - | - | 20,000 | |
사. 신종자본증권 미상환 잔액
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 1년 이하 | 1년초과 5년이하 |
5년초과 10년이하 |
10년초과 15년이하 |
15년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
아. 조건부자본증권 미상환 잔액
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | - | |
7-2. 증권의 발행을 통해 조달된 자금의 사용실적
가. 공모자금의 사용내역
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 증권신고서 등의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
| 코스닥 상장 (SPAC) |
- | 2020년 05월 20일 | 연구개발비용 | 8,800 | 연구개발비용 | 8,800 | - |
| 상동 | - | - | 시설비용 | 503 | 연구기자재 등 | 57 | 순차적으로 운영/집행 중 |
| 상동 | - | - | 운영자금 | 876 | 운영자금 | 876 | 상동 |
나. 사모자금의 사용내역
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 주요사항보고서의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
| 유상증자 (3자배정)* |
24 | 2019년 08월 10일 | 운영자금 | 4,000 | 운영자금 | 4,000 | - |
| 전환사채 | 2 | 2020년 06월 30일 | 타법인증권취득자금 등 | 20,000 | 타법인증권취득자금 등 | 20,000 | - |
| 유상증자 (3자배정) |
30 | 2021년 11월 12일 | 운영자금 | 12,500 | 운영자금 | - | 사용 예정 |
다. 미사용자금의 운용내역
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 백만원) |
| 종류 | 금융상품명 | 운용금액 | 계약기간 | 실투자기간 |
|---|---|---|---|---|
| 예ㆍ적금 | 정기예금 | 8,000 | - |
4개월 |
| 예ㆍ적금 | 정기예금 | 5,000 | - |
2개월 |
| 계 | 13,000 | - | ||
8. 기타 재무에 관한 사항
- 해당사항이 없습니다.
IV. 회계감사인의 감사의견 등
1. 외부감사에 관한 사항
가. 회계감사인의 명칭 및 감사의견
| 사업연도 | 감사인 | 감사의견 | 강조사항 등 | 핵심감사사항 |
|---|---|---|---|---|
| 제6기(당분기) 1분기 |
삼덕회계법인 | 해당사항없음 | - | 해당사항없음 |
| 제5기(전기) | 삼덕회계법인 | 적정 | - | (주4) |
| 제4기(전전기) | 삼일회계법인 | 적정 | (주3) | (주2) |
(주1)
① 합병계약의 체결
재무제표에 대한 주석 16에 기술하고 있는 바와 같이, 당사는 2019년 11월 29일자 하나금융11호기업인수목적(주)과 합병계약을 체결하였으며, 2020년 5월 6일을 합병기일로 결정하였습니다. 이와 관련하여 2020년 2월 13일 한국거래소의 합병상장 예비심사 승인을 득하였으며 이후 2020년 4월 1일 개최될 양 사의 주주총회에서 합병에 대한 승인 예정입니다.
② 재무제표 재작성
재무제표에 대한 주석 28에서 설명하고 있는 바와 같이 회사는 주식기준보상 및 연구개발비 회계처리 오류를 수정하여 2019년 12월 31일과 2018년 12월 31일 현재의 재무상태표와 2019년 12월31일과 2018년 12월 31일로 종료되는 양 보고기간의 포괄손익계산서, 자본변동표 및 현금흐름표의 내용을 재작성하였습니다. 이러한 재작성으로 인하여 2019년 12월 31일 현재 회사의 순자산은 39백만원 감소하였으며, 2019년 12월 31일과 2018년 12월 31일로 종료되는 양 보고기간의 당기순손실은 각각 96백만원 및 83백만원 증가하였습니다.
(주2)
핵심감사사항은 우리의 전문가적 판단에 따라 당기 재무제표감사에서 가장 유의적인 사항들입니다. 해당 사항들은 재무제표 전체에 대한 감사의 관점에서 우리의 의견 형성 시 다루어졌으며, 우리는 이런 사항에 대하여 별도의 의견을 제공하지는 않습니다.
하나금융11호기업인수목적주식회사와의 합병
핵심감사사항으로 결정된 이유 :
재무제표에 대한 주석 34에 기술되어 있는 바와 같이, 회사는 당기중 하나금융11호기업인수목적주식회사와 합병하였으며, 한국채택국제회계기준 제1102호 주식기준보상을 적용하여 회계처리 하였습니다.
당기손익으로 인식한 합병비용은 3,720백만원으로 유의적이며, 회계처리에는 회계처리 기준일의 결정 및 공정가치 추정 등 경영진의 판단이 포함됩니다. 회사는 합병비용 산정에 필요한 공정가치를 평가하기 위하여 독립적인 외부전문가를 활용하였습니다.
우리는 합병비용의 규모와 회계처리와 관련된 유의적인 경영진의 판단이 포함된다는 점을 고려하여 이 영역에 관심을 기울였습니다.
핵심감사사항이 감사에서 다루어진 방법 :
핵심감사사항에 대응하기 위하여 우리는 다음을 포함한 감사절차를 수행하였습니다.
ㆍ합병 계약서를 열람하여 합병조건과 주요약정을 확인
ㆍ합병과 관련하여 적용한 회계정책이 관련 회계기준에 부합하는지 검토
ㆍ합병에 따라 발행한 것으로 간주하게 되는 주식의 공정가치의 공정가치 결정에 사용된 방법과 공정가치 결정에 사용된 주요 기초 가정 및 변수의 적정성 평가
ㆍ합병을 통해 취득한 식별가능한 자산/부채의 공정가치 결정에 사용된 방법과 공정가치 결정에 사용된 주요 기초 가정 및 변수의 적정성 평가
ㆍ합병과 관련하여 공시사항의 적정성을 평가
(주3)
감사의견에는 영향을 미치지 않는 사항으로서 이 보고서의 이용자는 다음 사항들에 주의를 기울여야 할 필요가 있습니다.
별도재무제표에서 한국채택국제회계기준의 최초채택
재무제표에 대한 주석 2에서 설명하고 있는 바와 같이 회사는 2020년 1월 1일 이후 개시하는 보고기간부터 기업회계기준서 제1027호에 따른 별도재무제표를 작성하게 되었으며, 이 재무제표는 2020년 12월 31일의 한국채택국제회계기준에 따른 최초 별도재무제표의 일부분이므로 기업회계기준서 제1101호의 적용을 받습니다. 별도재무제표에서 한국채택국제회계기준으로의 전환일과 채택일은 각각 2019년 1월 1일과 2020년 1월 1일이며, 이 재무제표는 작성일(2020년 12월 31일) 현재 유효한 한국채택국제회계기준 및 관련 선택사항을 근거로 작성한 것입니다.
(주4)
핵심감사사항은 우리의 전문가적 판단에 따라 당기 재무제표감사에서 가장 유의적인사항들입니다. 해당 사항들은 재무제표 전체에 대한 감사의 관점에서 우리의 의견형성 시 다루어졌으며, 우리는 이런 사항에 대하여 별도의 의견을 제공하지는 않습니다.
- 기술이전 수익인식의 적정성 평가
1. 핵심감사사항으로 결정한 이유
회사는 유의적인 규모의 License Out 형태의 매출(이하 '기술이전수익’)거래를 수행하고 있습니다. 매출은 고객과의 계약 및 거래 조건에 따라 다양한 수행의무가 존재하고, 각 재화나 용역의 통제 이전시기가 다르기 때문에 수익인식 시점에 대한 경영진의 판단이 요구됩니다. 따라서, 우리는 해당 거래의 규모가 유의적이고, 거래 조건 별로 수익 인식의 귀속 시기에 오류가 발생할 위험이 높다고 판단하여 유의적인 위험으로 식별하였습니다.
2. 감사절차에서 다루어진 방법
핵심감사사항에 대응하기 위하여 우리는 다음을 포함한 감사절차를 수행하였습니다.
- 기술이전 수익인식 기준 및 회사의 회계정책의 검토
- 주요 거래처에 대한 기술이전 계약서를 입수하고 계약조건 등 내용 검토
- 기술이전 수익인식의 귀속시기와 관련하여, 회사가 수익인식기준에 따라 인식되고 기록되었는지 당기 중 발생한 매출거래 중 주요 거래에 대하여 적정성 검토
나. 감사용역 체결현황
| 사업연도 | 감사인 | 내 용 | 감사계약내역 | 실제수행내역 | ||
|---|---|---|---|---|---|---|
| 보수 | 시간 | 보수 | 시간 | |||
| 제6기(당분기) 1분기 |
삼덕회계법인 | 재무제표 등 검토 및 감사 | 92,000천원 | - | - | - |
| 제5기(전기) | 삼덕회계법인 | 재무제표 등 검토 및 감사 | 92,000천원 | - | 92,000천원 |
1,002 |
| 제4기(전전기) | 삼일회계법인 | 재무제표 등 검토 및 감사 | 100,000천원 | 898 | 100,000천원 | 1,072 |
다. 회계감사인과의 비감사용역 계약체결 현황
| 사업연도 | 계약체결일 | 용역내용 | 용역수행기간 | 용역보수 | 비고 |
|---|---|---|---|---|---|
| 제6기(당분기) 1분기 |
- | - | - | - | - |
| - | - | - | - | - | |
| 제5기(전기) | - | - | - | - | - |
| - | - | - | - | - | |
| 제4기(전전기) | - | - | - | - | - |
| - | - | - | - | - |
라. 재무제표 중 이해관계자의 판단에 상당한 영향을 미칠 수 있는 사항
| 구분 | 일자 | 참석자 | 방식 | 주요 논의 내용 |
|---|---|---|---|---|
| 1 | 2021년 02월 02일 | 회사: 이사회구성원 감사인: 업무수행이사 외 2명 |
서면회의 | -감사업무 요약 -중점감사항목의 감사결과 -독립성 |
마. 회계감사인의 변경
당사는 코스닥시장으로 이전상장을 하기 위한 목적으로 금융감독원에 감사인 지정을 요청하였고, 2018년 5월 14일 삼정회계법인으로 지정을 받아 2018년과 2019년 외부감사를 수감받았습니다. 다시 2019년 11월 12일에 금융감독원으로터 삼일회계법인을 감사인으로 지정 받아 2020년 감사를 수감받았습니다. 2021년(제5기)는 지정감사 종료로 인하여 외부감사인선임위원회를 통하여 삼덕회계법인을 선임하여 수감받았습니다.
2. 내부통제에 관한 사항
가. 내부통제
- 해당사항 없습니다.
나. 내부회계관리제도
[회계감사인의 내부회계관리제도 검토의견]
당사는 신뢰할 수 있는 회계 정보 작성 및 공시를 위하여 회계의 부정과 오류를 예방하고 적시에 발견할 수 있도록 2015년 내부회계관리제도를 도입하였습니다. 이에 감사인으로부터 2021년 12월 31일로 종료되는 회계연도의 내부회계관리제도를 대상으로 검토받았으며, 검토결과 중요성의 관점에서 내부회계관리제도 모범규준의 규정에 따라 작성되지 않았다고 판단하게 하는 점이 발견되지 아니하였습니다.
다. 내부통제구조의 평가
- 해당사항이 없습니다.
V. 이사회 등 회사의 기관에 관한 사항
1. 이사회에 관한 사항
가. 이사회 구성 개요
당사의 이사회는 법령 또는 회사 정관에서 정한 사항, 주주총회로부터 위임 받은 사항, 회사 경영의 기본방침 및 업무집행에 관한 중요사항을 의결하며, 이사회는 이사의 직무집행을 감독하고 있습니다. 사업보고서 작성 기준일 현재 당사의 이사회는 사외이사 1명을 포함한 총 3명으로, 2명의 상근이사와 1명의 비상근 이사로 구성되어 있습니다.
나. 사외이사 및 그 변동현황
| (단위 : 명) |
| 이사의 수 | 사외이사 수 | 사외이사 변동현황 | ||
|---|---|---|---|---|
| 선임 | 해임 | 중도퇴임 | ||
| 3 | 1 | 0 | 0 | 0 |
다. 주요의결사항 등
| 회차 | 일자 | 의안내용 | 가결여부 | 사내이사 | 사외이사 | |
| 이기섭 | 이재문 | 서태환 | ||||
| 1 | 2022.02.10 | 내부회계관리제도 운영실태 보고 내부회계관리제도 평가보고 |
승인 | 찬성 | 찬성 | 찬성 |
| 2 | 2022.02.16 | 제5기 결산 재무제표 승인의 건 제5기 영업보고서 승인의 건 제5기 정기주주총회 소집의 건 |
승인 | 찬성 | 찬성 | 찬성 |
| 3 | 2022.03.14 | 제5기 정기주주총회에서의 전자투표제 시행의 건 임직원에 대한 주식매수선택권 부여의 건 퇴사자에 대한 주식매수선택권 부여 취소의 건 제5기 정기주주총회 부의안건 추가/확정의 건 제5기 정기주주총회의 일시/장소 변경권한 위임의 건 |
승인 | 찬성 | 찬성 | 찬성 |
| 4 | 2022.04.11 | 제6기 임시주주총회 소집의 건 제6기 임시주주총회 소집에서의 전자투표제 시행의 건 |
승인 | 찬성 | 찬성 | 찬성 |
라. 이사회내의 위원회 구성현황
당사는 사업보고서 제출일 현재 이사회내에 위원회를 설치하지 않았습니다.
마. 이사의 독립성
보고서 작성 기준일 현재 당사는 사내이사 2인과 사외이사 1인으로 구성되어 있으며, 사외이사를 포함한 모든 이사를 주주총회에서 선임합니다. 주주총회 개최 전 이사 후보자에 대한 추천인, 최대주주와의 관계, 회사와의 거래 등에 대한 내역을 공개하고 있으며, 주주총회에서 선임된 이사는 아래와 같습니다.
| 구분 | 성명 | 추천인 | 담당업무 | 회사와의 거래 | 최대주 주등과의 관계 |
임기 | 비고 |
| 사내이사 | 이기섭 | 이사회 | 경영총괄 | - | 본인 | 3년 | - |
| 사내이사 | 이재문 | 이사회 | 임상개발 | - | - | 3년 | - |
| 사외이사 | 서태환 | 이사회 | - | - | - | 3년 | - |
회사 경영의 중요한 의사 결정과 업무 집행은 이사회의 심의 및 결정을 통하여 이루어지고 있습니다. 또한, 당사는 대주주 등의 독단적인 경영과 이로 인한 소액주주의 이익이 침해 받지 않도록 이사회 운영규정 및 이해관계자와의 거래에 대한 통제 규정을 제정하여 성실히 준수하고 있습니다.
바. 사외이사 교육 미실시 내역
| 사외이사 교육 실시여부 | 사외이사 교육 미실시 사유 |
|---|---|
| 미실시 | 당사의 사외이사는 전문성을 충분히 갖추고 있어 사외이사를 대상으로 교육을 실시하거나 위탁교육 등 외부기관이 제공하는 교육을 이수한 바 없습니다. |
2. 감사제도에 관한 사항
가. 감사기구에 관한 사항
(1) 감사위원회 설치여부, 구성방법 등
당사는 사업보고서 제출일 현재 감사위원회를 별도로 설치하고 있지 아니하며, 주주총회 결의로 선임된 상근 감사 1명이 감사 업무를 수행하고 있습니다. 당사 정관에 규정된 감사의 주요 권한과 책임은 아래와 같습니다.
|
구분 |
권한과 책임 |
|---|---|
|
감사의 |
- 이사 등에 대한 영업보고 청구권, 회사의 업무, 재산 및 손익상태조사권 - 회사 내 모든 정보에 대한 요구권 - 관계자의 출석 및 답변 요구권 - 회사 거래처로부터 자료징구 및 조회권 - 기타 감사업무수행에 필요한 사항의 요구권 |
|
감사의 |
- 감사계획의 수립, 집행, 결과평가, 보고 및 사후조치 - 감사결과 지적사항에 대한 조치내용 확인 - 관계 법령 또는 정관에 정한 사항의 처리 - 감사가 필요하다고 인정하는 사항에 대한 감사 |
(2) 감사위원회(감사)의 감사업무에 필요한 경영정보접근을 위한 내부장치마련 여부
당사는 감사 업무에 필요한 경영정보접근을 위하여 정관 및 이사회운영규정 상 다음과 같은 조항을 명시하고 있습니다.
|
구분 |
내용 |
|---|---|
|
감사계획 |
감사는 외부감사인과 긴밀히 협력하여 사안의 중요성, 시기의 적정 여부를 고려하여 조사범위를 정하고 감사계획서를 작성하여야 한다 |
|
감사의 |
① 감사는 감사직무를 수행함에 있어 피감사부서장에게 소속 직원의 근무지원을 요청할 수 있다. 이 경우 피감사부서장은 이에 협조하여야 한다. ④ 감사는 감사를 함에 있어 다음 각 호의 사항을 검토하고 확인하여야 한다. - 거래기록의 신뢰성 |
|
이사의 |
① 이사는 회사재산의 보전과 손해를 유발시킬 수 있는 등의 우려사항 또는 긴급을 요하는 중대 한 사항이 있을 경우에는 즉시 감사에게 구두나 서면으로 보고 또는 통보하여야 한다. ② 감사는 이사로부터 회사에 현저한 손해가 발생할 염려가 있다는 보고를 받은 경우에는 회사에 미치는 영향 등을 조사하고 감사로서 조언 또는 권고 등 필요한 조치를 강구하여야 한다. |
|
이사회의 |
① 감사는 이사회에 출석하여 의견을 진술한다. ④ 감사는 직무수행과 관련 필요한 경우 회의의 목적사항과 소집의 이유를 기재한 서면을 이사회에 제출하여 임시주주총회의 소집을 청구할 수 있다. |
|
문서 등의 열람 |
① 감사는 업무진행에 관한 중요한 문서를 적시에 열람하고 필요한 때에는 이사 또는 직원에게 그 설명을 요구한다. ② 감사는 열람할 문서에 관하여 이사와 협의하여 그 범위를 정해 두어야 한다. ③ 감사는 중요한 기록, 기타 중요 정보의 정비, 보존 등의 관리상황을 조사하고 필요에 따라 이 사 또는 직원에게 설명을 요구한다 |
|
재산의 |
감사는 중요한 회사재산의 관리, 취득 및 처분과 통상적이 아닌 중요한 거래 등에 관하여 조사하 고 만약 법령 또는 정관에 위반하거나 현저하게 부당한 사실을 발견한 경우에는 이사회에 보고하 여야 한다. |
|
거래의 |
감사는 회사의 중요한 재산상의 이익을 무상으로 공여하거나 자회사 또는 주주와 통상적이 아닌 거래를 하는 경우에는 사전에 이사와 협의하여 그 내용을 보고하도록 이사에게 요구하고 이사의 의무에 위반하는 사실을 발견한 경우에는 이사회에 보고하여야 한다 |
|
자회사의 조사 |
모회사의 감사는 그 직무를 수행하기 위하여 필요한 때에는 자회사에 대하여 영업의 보고를 요구 하고 자회사의 업무와 재산상태를 조사한다 |
|
현장 조사 |
감사는 본·지점, 사무소 등을 조사하고 회사의 업무전반에 관한 실정을 파악함과 동시에 업무가 적법하고 적정하게 행하여지고 있는지의 여부를 확인한다. |
(3) 감사위원회(감사)의 인적사항
|
성 명 |
주요 경력 |
결격요건여부 |
비 고 |
|---|---|---|---|
| 노치용 |
현대증권 부사장 산은캐피탈 대표이사 사장 |
해당사항 없음 |
- |
*감사 노치용은 2020년 12월 15일부로 선임 되었습니다.
나. 감사위원회(감사)의 독립성
감사는 이사회에 참석하여 독립적으로 이사의 업무를 감독할 수 있으며, 제반업무와 관련하여 관련장부 및 관계서류를 해당부서에 제출을 요구할 수 있습니다. 또한 필요시 회사로부터 영업에 관한 사항을 보고 받을 수 있으며, 적절한 방법으로 경영정보에 접근해 감사업무를 수행할 수 있는 등 감사인의 독립성을 충분히 확보하고 있다고 판단됩니다.
라. 감사위원회(감사)의 주요활동내역
|
회차 |
개최일자 |
의 안 내 용 |
가결 여부 |
비고 |
|---|---|---|---|---|
| 1 | 2022.02.10 | 내부회계관리제도 운영실태 보고 내부회계관리제도 평가보고 |
승인 | - |
| 2 | 2022.02.16 | 제5기 결산 재무제표 승인의 건 제5기 영업보고서 승인의 건 제5기 정기주주총회 소집의 건 |
승인 | - |
| 3 | 2022.03.14 | 제5기 정기주주총회에서의 전자투표제 시행의 건 임직원에 대한 주식매수선택권 부여의 건 퇴사자에 대한 주식매수선택권 부여 취소의 건 제5기 정기주주총회 부의안건 추가/확정의 건 제5기 정기주주총회의 일시/장소 변경권한 위임의 건 |
승인 | - |
| 4 | 2022.04.11 | 제6기 임시주주총회 소집의 건 제6기 임시주주총회 소집에서의 전자투표제 시행의 건 |
승인 | - |
마. 감사 교육 미실시 내역
| 감사 교육 실시여부 | 감사 교육 미실시 사유 |
|---|---|
| 미실시 | 당사의 감사는 전문성을 충분히 갖추고 있어 감사를 대상으로 교육을 실시하거나 위탁교육 등 외부기관이 제공하는 교육을 이수한 바 없습니다. |
바. 감사 지원조직 현황
| 부서(팀)명 | 직원수(명) | 직위(근속연수) | 주요 활동내역 |
|---|---|---|---|
| 재무팀 | 2 | 부장(9년) | 재무제표, 이사회 및 내부통제 활동 보고 등 경영전반에 관한 감사직무 수행지원 |
사. 준법지원인 등 지원조직 현황
- 당사는 해당사항이 없습니다.
3. 주주총회 등에 관한 사항
가. 집중투표제
당사는 보고서 제출일 현재 정관 제35조 제3항에 의거 집중투표제를 채택하고 있지 않습니다.
|
구분 |
내용 |
|---|---|
|
해당 조항 |
제35조(이사의 선임) 3. 2인 이상의 이사를 선임하는 경우 상법 제382조의 2에서 규정하는 집중투표제는 적용하지 아니 한다. |
나. 서면투표제 또는 전자투표제의 채택여부
당사는 보고서 제출일 현재 정관 제32조 서면투표제를 통한 의결권 행사를 적용하고 있습니다. 또한 전자투표제는 의사회 결의를 통해 일회성으로 시행하고 있습니다.
|
구분 |
내용 |
|---|---|
|
해당 조항 |
제32조(서면에 의한 의결권의 행사) |
다. 투표제도 현황
| (기준일 : | 2022년 03월 31일 | ) |
| 투표제도 종류 | 집중투표제 | 서면투표제 | 전자투표제 |
|---|---|---|---|
| 도입여부 | 배제 | 도입 | 도입 |
| 실시여부 | - | - | 제5기 정기주주총회 |
라. 의결권 현황
| (기준일 : | 증권신고서 제출 전일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 주식수 | 비고 |
|---|---|---|---|
| 발행주식총수(A) | 보통주 | 110,565,888 | - |
| - | - | - | |
| 의결권없는 주식수(B) | 보통주 | 11,511 | 자기주식 |
| - | - | - | |
| 정관에 의하여 의결권 행사가 배제된 주식수(C) | - | - | - |
| - | - | - | |
| 기타 법률에 의하여 의결권 행사가 제한된 주식수(D) |
- | - | - |
| - | - | - | |
| 의결권이 부활된 주식수(E) | - | - | - |
| - | - | - | |
| 의결권을 행사할 수 있는 주식수 (F = A - B - C - D + E) |
보통주 | 110,554,377 | - |
| - | - | - |
VI. 주주에 관한 사항
최대주주 및 특수관계인의 주식소유 현황
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 주, %) |
| 성 명 | 관 계 | 주식의 종류 |
소유주식수 및 지분율 | 비고 | |||
|---|---|---|---|---|---|---|---|
| 기 초 | 기 말 | ||||||
| 주식수 | 지분율 | 주식수 | 지분율 | ||||
|
이기섭 |
최대주주 |
보통주 |
15,123,144 |
13.71 |
15,163,144 | 13.71 | - |
|
이애주 |
공동보유자 |
보통주 |
5,029,066 |
4.56 |
5,029,066 | 4.55 | - |
|
최인석 |
공동보유자 |
보통주 |
2,790,000 |
2.53 |
3,004,354 | 2.72 | - |
|
이건환 |
공동보유자 |
보통주 |
2,560,906 |
2.32 |
2,560,906 | 2.32 | - |
|
노미란 |
특수관계인 |
보통주 |
337,430 |
0.31 |
337,430 | 0.31 | - |
|
노미숙 |
특수관계인 |
보통주 |
331,200 |
0.30 |
331,200 | 0.30 | - |
|
BRIANA BOHAE LEE |
특수관계인 |
보통주 |
146,907 |
0.13 |
146,907 | 0.13 | - |
|
MIRIAM B LEE |
특수관계인 |
보통주 |
146,907 |
0.13 |
146,907 | 0.13 | - |
|
이광호 |
특수관계인 |
보통주 |
110,400 |
0.10 |
110,400 | 0.10 | - |
|
이원영 |
특수관계인 |
보통주 |
58,636 |
0.05 |
58,636 | 0.05 | - |
|
이태길 |
특수관계인 |
보통주 |
52,515 |
0.05 |
52,515 | 0.05 | - |
|
이재문 |
등기임원 | 보통주 |
43,800 |
0.04 |
63,800 | 0.06 | - |
|
이기세 |
특수관계인 |
보통주 |
17,868 |
0.02 |
17,868 | 0.02 | - |
|
이미경 |
특수관계인 |
보통주 |
10,350 |
0.01 |
10,350 | 0.01 | - |
| 최광재 | 미등기임원 | 보통주 | 52,434 | 0.05 | 52,434 | 0.05 | - |
| 계 | 보통주 | 26,811,563 | 24.31 | 27,085,917 | 24.50 | - | |
| - | - | - | - | - | - | ||
| (주) | 기초는 2021년 12월 31일 기준으로 전체주식수 110,289,803주를 기준으로 지분율을 산정하였으며, 기말은 증권신고서 제출 전일 기준으로 전체주식수 110,565,888주를 기준으로 지분율을 산정하였습니다 |
나. 최대주주의 주요경력 및 개요
|
성명 |
학력 |
경력 |
|---|---|---|
|
이기섭 |
1975.02 한양대학교 |
- 75.01~78.12 현대건설 해외부 대리 - 94.01~99.12 미국 캘리포니아 Silicon Image Inc., USA 전략협력부 창립자/부사장 - 00.01~03.05 미국 캘리포니아 GCT Semiconductor Inc., USA 창립자/CEO |
다. 최대주주의 최대주주(법인 또는 단체)의 개요
- 해당사항이 없습니다.
바. 주식 소유현황
| (기준일 : | 증권신고서 제출 전일 | ) | (단위 : 주) |
| 구분 | 주주명 | 소유주식수 | 지분율(%) | 비고 |
|---|---|---|---|---|
| 5% 이상 주주 | 이기섭 | 15,163,144 | 13.71 | - |
| - | - | - | - | |
| 우리사주조합 | - | - | - | |
사. 소액주주현황
| (기준일 : | 2021년 12월 31일 | ) | (단위 : 주) |
| 구 분 | 주주 | 소유주식 | 비 고 | ||||
|---|---|---|---|---|---|---|---|
| 소액 주주수 |
전체 주주수 |
비율 (%) |
소액 주식수 |
총발행 주식수 |
비율 (%) |
||
| 소액주주 | 17,499 | 17,507 | 99.95 | 79,041,472 | 110,289,803 | 71.67 | - |
아. 주가 및 주식거래실적
■ 최근 6개월 간의 주가 및 주식 거래 실적
(1) 국내증권시장
(단위 : 원, 주)
| 분류 | '21년 10월 | '21년 11월 | '21년 12월 | '22년 1월 | '22년 2월 | '22년 3월 | ||
|---|---|---|---|---|---|---|---|---|
| 기명식 보통주 |
주가 | 최고 | 3,675 | 3,110 | 2,710 | 2,495 | 2,150 | 2,650 |
| 최저 | 3,055 | 2,565 | 2,320 | 1,895 | 1,830 | 2,000 | ||
| 거래량 | 17,399,700 | 6,914,540 | 5,790,689 | 5,521,927 | 2,616,210 | 25,736,185 | ||
※ 출처 : 한국거래소
(2) 해외증권시장
※ 해당사항 없음
VII. 임원 및 직원 등에 관한 사항
1. 임원 및 직원 등의 현황
| (기준일 : | 증권신고서 제출 전일 | ) | (단위 : 주) |
| 성명 | 성별 | 출생년월 | 직위 | 등기임원 여부 |
상근 여부 |
담당 업무 |
주요경력 | 소유주식수 | 최대주주와의 관계 |
재직기간 | 임기 만료일 |
|
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 의결권 있는 주식 |
의결권 없는 주식 |
|||||||||||
| 이기섭 | 남 | 1950년 11월 | 대표이사 | 사내이사 | 상근 | 경영총괄 |
75.02 한양대학교 전기공학과 졸업 75.01~78.12 현대건설 해외부 79.01~81.12 한화건설 해외부 82.01~93.12 미국 뉴저지 Kernel Enterprise Inc., USA President/CEO 94.01~99.12 미국 Silicon Image Inc., USA 전략협력부 창립자/부사장 00.01~03.05 미국 GCT Semiconductor Inc., USA 창립자/CEO 03.06~07.05 미국 Altos Venture, USA Special Partner 07.06~현재 ㈜카이노스메드 대표이사 |
15,163,144 | - | 본인 | 2007.06~현재 | 2023년 05월 19일 |
| 이재문 | 남 | 1958년 01월 | 사장 | 사내이사 | 상근 | 임상개발 |
89.05 듀크대학교 생화학박사 01.01~10.12 EXELIXIS Pharmaceuticals 책임 11.01~12.06 ARAGEN BIOSCIENCES 책임 12.07~14.06 ㈜카이노스메드 부사장 15.09~현재 ㈜카이노스메드 부사장 |
63,800 | - | 등기임원 | 2015.09~현재 | 2024년 02월 17일 |
| 서태환 | 남 | 1955년 03월 | 사외이사 | 사외이사 | 비상근 | 사외이사 |
87.05 미국 펜실베니아대학교 와튼스쿨 경영학 석사 89.02~97.07 현대증권㈜ 이사/국제영업본부장 97.08~08.08 현대중공업 CFO 겸 그룹기획실 재무팀장 08.09~16.03 하이투자증권㈜ CEO 17.03~현재 ㈜카이노스메드 사외이사 |
- | - | 등기임원 | 2017.03~현재 | 2023년 05월 19일 |
| 노치용 | 남 | 1952년 05월 | 감사 | 감사 | 상근 | 감사 | 1997~2007 현대증권 부사장 2008~2010 산은캐피탈 대표이사 2010~2013 KB투자증권 대표이사 |
- | - | - | 2020.12~현재 | 2023년 12월 23일 |
| 김인철 | 남 | 1951년 07월 | 부회장 | 미등기 | 상근 | 경영전략 | 85.03 일리노이대학교 약리학박사 85.04~86.06 미국Rockefeller 대학교 Post-Doc 86.07~87.09 미국 Duke Medical Center Research Fellow 88.10~93.02 미국 Glaxo Inc.R&D Center Research Investigator 93.03~11.03 LG 생명과학 대표이사/사장/이사회 의장 11.04~17.03 시스템통합적항암신약개발사업단 단장(국립암센터) 19.04~현재 ㈜씨엔알리서치 감사 19.09~현재 ㈜카이노스메드 경영전략사장 |
- | - | - | 2019.09~현재 | - |
| 신용일 | 남 | 1958년 12월 | 사장 | 미등기 | 상근 | 신사업 |
1985.~1993. LG International 1994.~1997 LG Group 1998.~1999. LG Capital 1999.~2001. LG Card 2001.~2003. Citi Bank 2003.~2013. Deutsch Bank Korea. 2013.~2018. Chicago Business Management 2019.~ 2020. S&T Logix CEO 2021.~현재 ㈜카이노스메드 경영전략본부장 |
- | - | - | 2021.01~현재 | - |
| 배종덕 | 남 | 1952년 10월 | 부사장 | 미등기 | 상근 | 경영지원본부장 |
74.02 서울대학교 경제학과 졸업 77.01~85.10 현대건설 재정부 과장 85.10~94.12 풀무원/부사장 95.01~98.06 링크웨어/대표이사 98.07~01.02 PricewaterhouseCoopers(PwC)Korea/부사장 01.02~02.12 보나비젼/대표이사 03.01~09.06 KFT/대표이사 09.03~11.06 한국렌탈주식회사/상임감사 19.06~20.01 ㈜이안앤 대표이사 17.05~20.12 ㈜카이노스메드 감사 |
- | - | - | 2020.12~현재 | - |
| 김은희 | 여 | 1958년 05월 | 부사장 | 미등기 | 상근 | 바이오의약본부장 |
1990. Tufs University 졸업 2005.~현재 충남대학교 교수 |
- | - | - | 2021.03~현재 | - |
| 최광재 | 남 | 1965년 06월 | 이사 | 미등기 | 상근 | 신사업팀 |
95. 뉴욕대학교 석사 07. Helsinki School of Economics MBA 96~18 한국다우코닝 18~현재 ㈜카이노스메드 이사 |
- | - | - |
2018.04~현재 |
- |
| 고수영 | 여 | 1978년 08월 | 이사 | 미등기 | 상근 | 사업개발본부장 |
02~18 바이로메드 19~20 엔케이맥스 20~현재 ㈜카이노스메드 이사 겸 사업개발본부장 |
- | - | - |
2020.09~현재 |
- |
나. 직원 등 현황
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 원) |
| 직원 | 소속 외 근로자 |
비고 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 사업부문 | 성별 | 직 원 수 | 평 균 근속연수 |
연간급여 총 액 |
1인평균 급여액 |
남 | 여 | 계 | |||||
| 기간의 정함이 없는 근로자 |
기간제 근로자 |
합 계 | |||||||||||
| 전체 | (단시간 근로자) |
전체 | (단시간 근로자) |
||||||||||
| 관리/연구 | 남 |
16 |
- | - | - |
16 |
3.8년 |
388,376,062 |
24,273,504 |
- | - | - | - |
| 관리/연구 | 여 |
10 |
- | - | - |
10 |
3.6년 |
154,690,032 |
15,469,003 |
- | |||
| 합 계 |
26 |
- | - | - |
26 |
3.77년 |
543,066,094 |
20,887,157 |
- | ||||
다. 미등기임원 보수 현황
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 백만원) |
| 구 분 | 인원수 | 연간급여 총액 | 1인평균 급여액 | 비고 |
|---|---|---|---|---|
| 미등기임원 | 7 | 189 | 27 | - |
2. 임원의 보수 등
| <이사ㆍ감사 전체의 보수현황> |
가. 주주총회 승인금액
| (단위 : 백만원) |
| 구 분 | 인원수 | 주주총회 승인금액 | 비고 |
|---|---|---|---|
|
이 사 |
3 |
1,000 |
- |
|
감 사 |
1 |
100 |
- |
나. 보수지급금액
나-1. 이사ㆍ감사 전체
| (단위 : 백만원) |
| 인원수 | 보수총액 | 1인당 평균보수액 | 비고 |
|---|---|---|---|
| 4 | 1,100 | 43 | - |
나-2. 유형별
| (단위 : 백만원) |
| 구 분 | 인원수 | 보수총액 | 1인당 평균보수액 |
비고 |
|---|---|---|---|---|
| 등기이사 (사외이사, 감사위원회 위원 제외) |
2 |
152 |
76 |
- |
| 사외이사 (감사위원회 위원 제외) |
1 |
6 |
6 |
- |
| 감사위원회 위원 |
- |
- |
- |
- |
| 감사 |
1 |
16 |
16 |
- |
<주식매수선택권의 부여 및 행사현황>
<표1>
| (단위 : 천원) |
| 구 분 | 인원수 | 주식매수선택권의 공정가치 총액 | 비고 |
|---|---|---|---|
| 등기이사 | 1 | 289,960 | - |
| 사외이사 | 1 | 76,550 | - |
| 감사위원회 위원 또는 감사 | 1 | 66,650 | - |
| 업무집행지시자 | 2 | 366,510 | - |
| 계 | 2 | 366,510 | - |
<표2>
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 원, 주) |
| 부여 받은자 |
관 계 | 부여일 | 부여방법 | 주식의 종류 |
최초 부여 수량 |
당기변동수량 | 총변동수량 | 기말 미행사수량 |
행사기간 | 행사 가격 |
의무 보유 여부 |
의무 보유 기간 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 행사 | 취소 | 행사 | 취소 | |||||||||||
| 이재문 | 미등기임원 | 2016년 03월 29일 | 신주교부 | 보통주 | 345,000 | 0 | 0 | 13,800 | 0 | 331,200 | 2018.03.29~ 2028.03.28 | 1,266 | X | - |
| 정연태 | 미등기임원 | 2016년 03월 29일 | 신주교부 | 보통주 | 20,700 | 0 | 0 | 20,700 | 0 | 0 | 2018.03.29~ 2028.03.28 | 1,266 | X | - |
| 변OO외 8명 | 직원 | 2016년 03월 29일 | 신주교부 | 보통주 | 1,194,810 | 5,260 | 0 | 827,960 | 365,700 | 1,150 | 2018.03.29~ 2028.03.28 | 1,266 | X | - |
| 이재문 | 미등기임원 | 2017년 03월 24일 | 신주교부 | 보통주 | 690,000 | 30,000 | 0 | 30,000 | 0 | 660,000 | 2019.03.24~ 2029.03.24 | 665 | X | - |
| 정연태 | 미등기임원 | 2017년 03월 24일 | 신주교부 | 보통주 | 34,500 | 7,188 | 0 | 34,500 | 0 | 0 | 2019.03.24~ 2029.03.24 | 665 | X | - |
| 정재욱 | 미등기임원 | 2017년 03월 24일 | 신주교부 | 보통주 | 103,500 | 51,750 | 0 | 103,500 | 0 | 0 | 2019.03.24~ 2029.03.24 | 665 | X | - |
| 변OO외19명 | 직원 | 2017년 03월 24일 | 신주교부 | 보통주 | 1,922,340 | 73,313 | 0 | 851,213 | 989,792 | 81,335 | 2019.03.24~ 2029.03.24 | 665 | X | - |
| 이재문 | 미등기임원 | 2018년 03월 26일 | 신주교부 | 보통주 | 345,000 | 0 | 0 | 0 | 0 | 345,000 | 2020.03.26~2030.03.26 | 1,772 | X | - |
| 정연태 | 미등기임원 | 2018년 03월 26일 | 신주교부 | 보통주 | 69,000 | 56,062 | 12,938 | 56,062 | 12,938 | 0 | 2020.03.26~2030.03.26 | 1,772 | X | - |
| 정재욱 | 미등기임원 | 2018년 03월 26일 | 신주교부 | 보통주 | 69,000 | 61,812 | 7,188 | 61,812 | 7,188 | 0 | 2020.03.26~2030.03.26 | 1,772 | X | - |
| 변OO외18명 | 직원 | 2018년 03월 26일 | 신주교부 | 보통주 | 1,217,850 | 94,313 | 1,941 | 440,003 | 235,535 | 199,036 | 2020.03.26~2030.03.26 | 1,772 | X | - |
| 이재문 | 미등기임원 | 2019년 03월 25일 | 신주교부 | 보통주 | 69,000 | 0 | 0 | 0 | 0 | 69,000 | 2022.03.25~2032.03.25 | 2,405 | X | - |
| 정연태 | 미등기임원 | 2019년 03월 25일 | 신주교부 | 보통주 | 34,500 | 0 | 34,500 | 0 | 34500 | 0 | 2022.03.25~2032.03.25 | 2,405 | X | - |
| 정재욱 | 미등기임원 | 2019년 03월 25일 | 신주교부 | 보통주 | 69,000 | 0 | 69,000 | 0 | 69000 | 0 | 2022.03.25~2032.03.25 | 2,405 | X | - |
| 변OO외21명 | 직원 | 2019년 03월 25일 | 신주교부 | 보통주 | 2,121,750 | 0 | 258,750 | 0 | 1,293,750 | 0 | 2022.03.25~2032.03.25 | 2,405 | X | - |
| 김인철 | 미등기임원 | 2020년 03월 13일 | 신주교부 | 보통주 | 690,000 | 0 | 0 | 0 | 0 | 690,000 | 2023.03.13~2033.03.12 | 2,688 | X | - |
| 이 구 | 미등기임원 | 2020년 03월 13일 | 신주교부 | 보통주 | 345,000 | 0 | 345,000 | 0 | 345,000 | 0 | 2023.03.13~2033.03.12 | 2,688 | X | - |
| 정재욱 | 미등기임원 | 2020년 03월 13일 | 신주교부 | 보통주 | 69,000 | 0 | 69,000 | 0 | 69,000 | 0 | 2023.03.13~2033.03.12 | 2,688 | X | - |
| 최OO 외 4명 | 직원 | 2020년 03월 13일 | 신주교부 | 보통주 | 379,500 | 0 | 207000 | 0 | 276000 | 103,500 | 2023.03.13~2033.03.12 | 2,688 | X | - |
| 신용일 | 미등기임원 | 2021년 01월 15일 | 신주교부 | 보통주 | 250,000 | 0 | 0 | 0 | 0 | 250,000 | 2024.01.15~2034.01.14 | 4,377 | X | - |
| 배종덕 | 미등기임원 | 2021년 01월 15일 | 신주교부 | 보통주 | 172,500 | 0 | 0 | 0 | 0 | 172,500 | 2024.01.15~2034.01.14 | 4,377 | X | - |
| 정형석 | 미등기임원 | 2021년 01월 15일 | 신주교부 | 보통주 | 138,000 | 0 | 138,000 | 0 | 138,000 | 0 | 2024.01.15~2034.01.14 | 4,377 | X | - |
| 고수영 | 미등기임원 | 2021년 01월 15일 | 신주교부 | 보통주 | 150,000 | 0 | 0 | 0 | 0 | 150,000 | 2024.01.15~2034.01.14 | 4,377 | X | - |
| 백OO 외 4인 | 직원 | 2021년 01월 15일 | 신주교부 | 보통주 | 335,000 | 0 | 100,000 | 0 | 100,000 | 235,000 | 2024.01.15~2034.01.14 | 4,377 | X | - |
| 김은희 | 미등기임원 | 2021년 03월 15일 | 신주교부 | 보통주 | 500,000 | 0 | 0 | 0 | 0 | 500,000 | 2024.03.15~2034.03.14 | 1,762 | X | - |
| 서태화 | 등기임원 | 2021년 03월 31일 | 신주교부 | 보통주 | 50,000 | 0 | 0 | 0 | 0 | 50,000 | 2024.03.31~2034.03.30 | 1,531 | X | - |
| 노치용 | 등기임원 | 2022년 03월 14일 | 신주교부 | 보통주 | 50,000 | 0 | 0 | 0 | 0 | 50,000 | 2025.03.14~2035.03.13 | 2,275 | X | - |
| 남OO 외 3인 | 직원 | 2022년 03월 14일 | 신주교부 | 보통주 | 125,000 | 0 | 0 | 0 | 0 | 125,000 | 2025.03.14~2035.03.13 | 2,275 | X | - |
VIII. 계열회사 등에 관한 사항
가. 계열회사 현황(요약)
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 사) |
| 기업집단의 명칭 | 계열회사의 수 | ||
|---|---|---|---|
| 상장 | 비상장 | 계 | |
| - | - | 2 | 1 |
※상세 현황은 '상세표-2. 계열회사 현황(상세)' 참조
나. 임원 겸직 현황
|
성명 |
겸직현황 |
비고 |
|---|---|---|
|
이기섭 |
FAScinate Therapeutics Inc. 대표이사(상근) | 해외 계열회사 |
| 이재문 | FAScinate Therapeutics Inc. 이사(상근) | 해외 계열회사 |
다. 타법인출자 현황(요약)
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 원) |
| 출자 목적 |
출자회사수 | 총 출자금액 | |||||
|---|---|---|---|---|---|---|---|
| 상장 | 비상장 | 계 | 기초 장부 가액 |
증가(감소) | 기말 장부 가액 |
||
| 취득 (처분) |
평가 손익 |
||||||
| 경영참여 | - | 2 | 2 |
242 |
0 |
0 |
244 |
| 일반투자 | - | - | - | - | - | - | - |
| 단순투자 | - | - | - | - | - | - | - |
| 계 | - | 2 | 2 | 242 | 0 | 0 | 244 |
※상세 현황은 '상세표-3. 타법인출자 현황(상세)' 참조
IX. 대주주 등과의 거래내용
가. 대주주등에 대한 신용공여등
- 당사는 보고서 제출 기준일 현재 해당사항이 없습니다.
나. 대주주와의 자산양수도 등
- 당사는 보고서 제출 기준일 현재 해당사항이 없습니다.
다. 대주주와의 영업거래
- 당사는 보고서 제출 기준일 현재 해당사항이 없습니다.
라. 대주주 이외의 이해관계자와의 거래
- 당사는 보고서 제출 기준일 현재 해당사항이 없습니다.
X. 그 밖에 투자자 보호를 위하여 필요한 사항
1. 공시내용 진행 및 변경사항
가. 공시사항의 진행ㆍ변경상황
| 공시일자 | 제목 | 내용 | 진행사항 | 예정사항 | 비고 |
|---|---|---|---|---|---|
| 2022.04.11 | 주식병합결정 | 1) 주식병합의 목적: 적정 유통주식수 유지를 통한 주가 안정화 및 기업가치 제고 2) 주식병합의 내용: 액면가 100원의 보통주 5주를 액면가 500원의 보통주 1주로 병합 |
1) 주주총회소집 | - 주식병합 공고: 2022 년 5 월 23 일 - 매매거래정지예정기간: 2022 년 6 월 24 일 ~ 7 월 11 일 - 신주배정기준일: 2022 년 6 월 27 일 - 신주 주식병합 효력발생일: 2022 년 6 월 28 일 - 신주권상장예정일: 2022 년 7 월 12 일 |
해당 일정은 주주총회결과와 관계기관과의 협의과정에 따라 변경될 수 있습니다. |
| 2022-04-14 | 주주총회소집공고 |
1. 일 시 : 2022년 5월 23일 (월) 오전 09시
|
1) 주주총회소집결의 공시 2) 주주명부폐쇄 3) 주주총회소집공고 |
1. 일 시 : 2022년 5월 23일 (월) 오전 09시
|
세부사항은 공시참조 |
나. 주주총회 의사록 요약
|
회차 |
개최일자 |
안건 |
결의 내용 |
비고 |
|---|---|---|---|---|
| 13기 정기 | 2019-03-25 | 1) 제12기 재무제표 승인의 건 | 원안대로 승인 | - |
| 2)이사 선임의 건 | ||||
| 3)이사 보수 한도액 승인의 건 | ||||
| 4)감사 보수한도액 승인의 건 | ||||
| 5)정관 변경의 건 | ||||
| 6)주식매수선택권 부여의 건 | ||||
| 14기 정기 | 2020-03-13 | 1) 제13기 재무제표 승인의 건 | 원안대로 승인 | - |
| 2) 이사 선임의 건 | ||||
| 3) 감사 선임의 건 | ||||
| 4) 이사 보수한도 승인의 건 | ||||
| 5) 감사 보수한도 승인의 건 | ||||
| 6) 주식매수선택권 부여의 건 | ||||
| 14기 임시 | 2020-04-16 | 1) 합병승인 결의 | 원안대로 승인 | - |
| 4기 임시 | 2020-12-15 | 1) 정관 일부 변경의 건 | 원안대로 승인 | - |
| 2) 이사 선임의 건 | ||||
| 3) 감사 선임의 건 | ||||
| 4) 임원 퇴직금 규정 개정의 건 | ||||
| 4기 정기 | 2021-03-31 | 1) 제4기(구.제14기) 재무제표 승인의 건 | 원안대로 승인 | - |
| 2) 주식매수수선택권 부여의 건 | ||||
| 3) 이사 보수한도액 승인의 건 | ||||
| 4) 감사 보수한도액 승인의 건 | ||||
| 5기 정기 | 2022-03-31 | 1) 제5기(구.제15기) 재무제표 승인의 건 | 원안대로 승인 | - |
| 2) 이사 보수한도액 승인의 건 | ||||
| 3) 감사 보수한도액 승인의 건 | ||||
| 4) 주식매수수선택권 부여의 건 | ||||
| 6기 임시 | 2022-05-23 | 1) 정관일부 변경의 건 | 원안대로 승인 | - |
| 주식(액면)병합 승인의 건 |
*회계기수는 합병이전까지 경제적 실체를, 이후 현재기준으로 작성하였습니다.
2. 우발부채 등에 관한 사항
본 보고서 제출일 기준 해당 사항이 없습니다.
3. 제재 등과 관련된 사항
본 보고서 제출일 기준 해당 사항이 없습니다.
4. 작성기준일 이후 발생한 주요사항 등 기타사항
가. 작성기준일 이후 발생한 주요사항
| 공시일자 | 제목 | 내용 | 진행사항 | 예정사항 |
|---|---|---|---|---|
| 2022.04.11 | 주식병합결정 | 1) 주식병합의 목적: 적정 유통주식수 유지를 통한 주가 안정화 및 기업가치 제고 2) 주식병합의 내용: 액면가 100원의 보통주 5주를 액면가 500원의 보통주 1주로 병합 |
1) 주주총회소집 | - 주식병합 공고: 2022 년 5 월 23 일 - 매매거래정지예정기간: 2022 년 6 월 24 일 ~ 7 월 11 일 - 신주배정기준일: 2022 년 6 월 27 일 - 신주 주식병합 효력발생일: 2022 년 6 월 28 일 - 신주권상장예정일: 2022 년 7 월 12 일 |
| 2022-04-14 | 주주총회소집공고 |
1. 일 시 : 2022년 5월 23일 (월) 오전 09시
|
1) 주주총회소집결의 공시 2) 주주명부폐쇄 3) 주주총회소집공고 |
1. 일 시 : 2022년 5월 23일 (월) 오전 09시
|
나. 중소기업확인서
다. 합병등 전후의 재무사항 비교표
* 합병등(합병, 중요한 영업ㆍ자산양수도, 주식의 포괄적교환ㆍ이전, 분할)
| (단위 : 백만원) |
| 대상회사 | 계정과목 | 예측 | 실적 | 비고 | ||||
|---|---|---|---|---|---|---|---|---|
| 1차연도 | 2차연도 | 1차연도 | 2차연도 | |||||
| 실적 | 괴리율 | 실적 | 괴리율 | |||||
| 주식회사 카이노스메드 | 매출액 | 0 | 0 | 0 | 0 | 1,662 | - | - |
| 영업이익 | -20,550 | -22,185 | -11,448 | 44 | -15,735 | 29 | - | |
| 당기순이익 | -20,550 | -22,185 | -11,448 | 44 | -15,735 | 29 | - | |
라. 보호예수 현황
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 주) |
| 주식의 종류 | 예수주식수 | 예수일 | 반환예정일 | 보호예수기간 | 보호예수사유 | 총발행주식수 |
|---|---|---|---|---|---|---|
| 보통주 | 16,445,235 | 2020년 06월 08일 | 2023년 06월 07일 | 36개월 | 최대주주 및 특수관계인 | 105,357,734 |
| 보통주 | 4,681,638 | 2021년 11월 26일 | 2022년 11월 25일 | 12개월 | 3자배정 사모 유상증자 | 110,289,803 |
마. 특례상장기업의 재무사항 비교표
| (상장일 : | 2020년 06월 08일 | , 인수인 : | - | ) | (단위 : 백만원) |
| 추정대상 | 계정과목 | 예측치 | 실적치 | 괴리율 |
|---|---|---|---|---|
| 2020년 | 매출액 | - | - | - |
| 영업이익 | -22,550 | -9,386 | 58 | |
| 당기순이익 | -22,550 | -11,448 | 49 | |
| 2021년 | 매출액 | - | 1,662 | - |
| 영업이익 | -22,185 | -11,219 | 49 | |
| 당기순이익 | -22,185 | -16,225 | 26 | |
| 2022년 | 매출액 |
5,269 |
- | - |
| 영업이익 |
-3,910 |
- | - | |
| 당기순이익 |
-3,000 |
- | - |
바. 특례상장기업 관리종목 지정유예 현황
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 원, %) |
| 관리종목 지정요건 | 요건별 회사 현황 | 관리종목 지정요건 해당여부 |
관리종목지정유예 | |||
|---|---|---|---|---|---|---|
| 항목 | 사업연도 | 금액/비율 | 해당 여부 |
종료 시점 |
||
| 최근 사업연도말 매출액 30억원 미만 |
최근 사업연도말 매출액(별도) | 2021 | 4,013,025,507 | 미해당 | 해당 | 2024년 12월 31일 |
| 최근 4사업연도 연속 영업손실 발생 | 최근 4사업연도 각 영업손익 (별도) |
2021 | -5,900,250,010 | 미해당 | 해당 | - |
| 2020 | -8,417,500,666 | |||||
| 2019 | -44,177,300 | |||||
| 2018 | -25,917,490 | |||||
| 자기자본 50%이상(10억원 이상에 한함)의 법인세차감전계속사업손실이 최근 3년간 2회 이상 및 최근 사업연도 법인세차감전계속사업손실 발생 | 최근 3사업연도 각 자기자본 대비 법인세차감전 계속사업손익 비율(연결) |
2021 | -16,224,489,295 | 미해당 | 해당 | 2022년 12월 31일 |
| 2020 | -12,762,888,232 | |||||
| 2019 | - | |||||
XI. 상세표
1. 연결대상 종속회사 현황(상세)
| (단위 : 원) |
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| FAScinate Therapeutics Inc. |
2018.1 |
South Dupont Highway, City of Dover, County of Kent, Delaware |
연구개발업 |
19,093,958 |
100% 지분 |
해당 |
| KAIDEA GLOBAL PTE.LTD |
2021.04 |
60 Paya Lebar Road#05-08 Paya Lebar Square Singapore 409051 |
연구개발업 |
406,752 |
55% 지분 |
해당 |
2. 계열회사 현황(상세)
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 사) |
| 상장여부 | 회사수 | 기업명 | 법인등록번호 |
|---|---|---|---|
| 상장 | 0 | - | - |
| - | - | ||
| 비상장 | 2 | FAScinate Therapeutics Inc. | - |
| KAIDEA GLOBAL PTE.LTD | - |
3. 타법인출자 현황(상세)
| (기준일 : | 2022년 03월 31일 | ) | (단위 : 백만원, 천주, %) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
|
FAScinate Therapeutics Inc. |
비상장 | 2020년 06월 26일 | 개발제품 해외 진출 |
- |
20,000 |
100 |
2 |
- | - | - |
20,000 |
100 |
2 |
19,094 |
-1,406 |
|
KAIDEA GLOBAL PTE.LTD |
비상장 | 2021년 09월 17일 | 개발제품 해외 진출 |
242 |
275,000 |
55 |
242 |
- | - | - |
275,000 |
55 |
242 |
407 |
-13 |
| 합 계 |
295,000 |
0 |
244 |
- | - | - |
295,000 |
0 |
244 |
19,501 |
-1,419 |
||||
【 전문가의 확인 】
1. 전문가의 확인
- 해당사항이 없습니다.
2. 전문가와의 이해관계
- 해당사항이 없습니다.