 |
|
(자료: nanokorea.net) |
주주총회소집공고
| 2022 년 03 월 10일 | ||
| 회 사 명 : | (주)바이오시네틱스 | |
| 대 표 이 사 : | 김 갑 식 | |
| 본 점 소 재 지 : | 서울특별시 금천구 가산디지털2로 184, 708호 (가산동, 벽산디지털밸리 2차) |
|
| (전 화) 02-2113-1285 | ||
| (홈페이지)http://www.bio-synectics.com | ||
| 작 성 책 임 자 : | (직 책) 부사장 | (성 명) 이 주 환 |
| (전 화) 02-2113-1280 | ||
주주총회 소집공고
| (제18기 정기) |
주주님의 건승과 댁내의 평안을 기원합니다.
상법 제 363조와 정관 제20조에 의거, 제 18기 정기 주주총회를 아래와 같이
개최하고자 하오니 참석하여 주시기 바랍니다.
| --- 아 래 --- |
1. 일시 : 2022년 3월 31일(목요일) 오전 10시
2. 장소 : 서울시 금천구 가산디지털2로 184, 지하 2층 회의실
(가산동, 벽산디지털밸리2차)
3. 회의 목적사항
가. 보고사항 : 감사보고, 영업보고, 내부회계관리제도 운영실태보고
나. 부의 안건
제 1호 의안 : 제 18기(2021.1.1 ~ 2021.12.31) 재무제표 승인의 건
제 2호 의안 : 사내이사 김갑식 선임의 건
제 3호 의안 : 이사 보수한도 승인의 건
제 4호 의안 : 감사 보수한도 승인의 건
4. 경영참고사항 비치
상법 제 542조의 4에 의거 경영참고사항을 우리 회사의 본점, 금융위원회, 한국거래소에 비치하오니 참고하시기 바랍니다,
5. 실질주주의 의결권 행사에 관한 사항
우리 회사의 주주총회에는 한국예탁결제원이 주주님들의 의결권을 행사할 수 없습니다. 따라서 주주님들께서는 한국예탁결제원에 의결권행사에 관한 의사표시를 하실 필요가 없으며, 종전과 같이 주주총회에 참석하여 의결권을 직접적으로 행사하시거나, 또는 위임장에 의거 의결권을 간접행사 할 수 있습니다.
6. 주주총회 참석시 준비물
-직접행사 : 주주총회 참석장, 본인신분증
-대리행사 : 주주총회 참석장, 위임장(주주와 대리인의 인적사항 기재,
본인 인감날인) 대리인의 신분증
2022년 3월 10일
주식회사 바이오시네틱스
대표이사 김 갑 식 (직인생략)
I. 사외이사 등의 활동내역과 보수에 관한 사항
1. 사외이사 등의 활동내역
가. 이사회 출석률 및 이사회 의안에 대한 찬반여부
| 회차 | 개최일자 | 의안내용 | 사외이사 등의 성명 |
|---|---|---|---|
| - | |||
| 찬 반 여 부 | |||
| 1 | - | - | - |
| 2 | - | - | - |
| 3 | - | - | - |
나. 이사회내 위원회에서의 사외이사 등의 활동내역
| 위원회명 | 구성원 | 활 동 내 역 | ||
|---|---|---|---|---|
| 개최일자 | 의안내용 | 가결여부 | ||
| - | - | - | - | - |
2. 사외이사 등의 보수현황
| (단위 : 원) |
| 구 분 | 인원수 | 주총승인금액 | 지급총액 | 1인당 평균 지급액 |
비 고 |
|---|---|---|---|---|---|
| - | - | - | - | - | - |
II. 최대주주등과의 거래내역에 관한 사항
1. 단일 거래규모가 일정규모이상인 거래
- 해당사항 없습니다.
2. 해당 사업연도중에 특정인과 해당 거래를 포함한 거래총액이 일정규모이상인 거래
- 해당사항 없습니다.
III. 경영참고사항
1. 사업의 개요
가. 업계의 현황
(1) 나노 의약기술 개요
나노기술(Nanotechnology)은 물질을 나노미터 크기의 범주에서 조작, 분석하고 이를 제어함으로써 새롭거나 개선된 물리적, 화학적, 생물학적 특성을 나타내는 소재, 소자 또는 시스템을 창출하는 과학기술을 말합니다. 물질을 제조 또는 합성하는데 있어서 기존의 방법은 구성 성분인 조성을 변화시키거나 결정구조 등 물질의 구조를 변형시키는 것이었고 그 외의 방법으로는 크기를 변화시켜 새로운 물성을 지닌 물질을 제조 또는 합성하는 방법이 있습니다. 나노기술의 경우는 크기를 변화시킴에 따라 새로운 특성의 새로운 물질을 탄생시킬 수 있다는 것이 주요 핵심이라고 할 수 있습니다.
나노(Nano)란 10억분의 1배의 뜻을 가진 접두어로서 인간은 미터 크기(m)의 세계에서 살고 있다고 할 수 있는데, 1미터의 백분의 1인 1센티미터(㎝)는 대략 개미의 크기이고, 바늘 직경이 1밀리미터(㎜) 정도입니다. 우리 몸에서는 머리카락 굵기는 100마이크로미터(㎛)보다 작고, 적혈구 직경은 약 7~8 마이크로미터 정도입니다. 나노미터(㎚)의 크기는 1 마이크로미터의 천분의 1로서, DNA의 폭 정도 크기이며 일반적으로 원자 3~4 개를 이어 놓은 크기라고 할 수 있습니다. 일반적으로 나노 기술에서 다루고 있는 크기는 대략 100나노(0.1㎛)이하를 의미하지만 의약품의 나노입자는 서브마이크론(submicron) 영역을 말하기도 합니다.
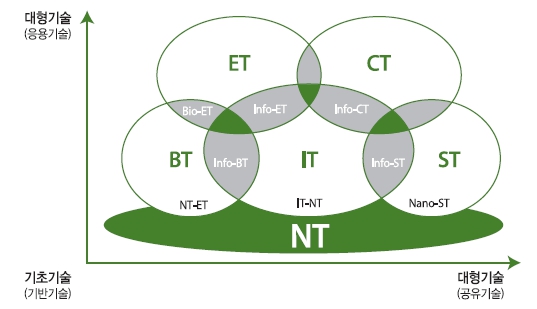
나노기술은 기존의 기술분야(물리, 화학, 재료, 전자 등)들을 횡적으로 연결하는 등 학문간 경계가 없는 학제간 연구 분야이며, 재료, 전자, 에너지, 우주공학, 의학 등 거의 모든 산업분야에 응용이 가능함에 따라 높은 경제적 파급성을 지니고 있습니다.
[나노기술과 타기술의 상호관계]
 |
|
(자료: nanokorea.net) |
당사가 속해 있는 나노 의약(Nanomedicine)기술은 일반적으로 1~500㎚ 크기의 기능성 나노 입자의 물적 특성을 기존의 의학기술에 접목하는 첨단 융합 기술로 정의할 수 있으며, 현대의학의 난제를 극복할 기술로서 전 세계적인 이슈를 모으고 있는 기술분야입니다.
[나노의약 기술 개념 및 적용사례]
 |
|
(자료: 화학세계 2014.05) |
의약품 약물의 입자크기를 나노미터 수준에서 제어하는 나노기술을 이용하여 개발된 나노 의약품은 기존 시판되는 의약품 및 신약물질의 난용성을 해결하여 제형을 소형화 할 수 있으며, 특정 질병부위에 대한 선택적 표적화 치료요법이 가능하기 때문에 질병치료의 새로운 수단으로서 각광 받고 있습니다.
시중에 판매되고 있는 의약품의 40%, 신약 후보물질의 90% 이상이 물에서 잘 녹지 않는 난용성 약물로 알려져 있으며, 이러한 약물을 그대로 복용하였을 경우 우리의 신체 내에서 흡수가 제대로 일어나지 않아 약효를 발휘하지 못하게 됩니다. 그렇기 때문에 이러한 난용성 문제를 해결하여 물에 잘 분산이 되는 약물을 제조하는 기술이 필요합니다. 이러한 난용성 문제를 해결하기 위해, 전통적으로는 약물에 염(salt)을 붙여 약물 자체의 구조를 변형시켜 물에서 잘 녹게 변화를 주거나, 약물 자체의 구조는 변화시키지 않되 배열을 바꿔 물에 조금 더 잘 녹게 하는 방법 등이 사용되었으며, 2000년대 초부터는 Elan사의 NanoCrystal® 기술을 선두로 하여 나노입자화(Nanoparticulation)라는 나노 기술을 적용하여 난용성 문제를 극복하고자 하는 움직임이 활발히 진행되고 있습니다.
(2) 나노 약물전달시스템 적용 분야
① 신약(New drug) 제조
현재 전세계적으로 개발 파이프라인에 있는 신약 후보 물질의 약 90%는 난용성 문제가 있는 것으로 알려져 있습니다. 기존에는 신약개발 과정에서 효능 및 독성 연구를 완료한 후 제형 연구를 수행하였으며, 이 경우 난용성의 문제를 극복하지 못하여 신약개발이 중단되는 경우가 종종 발생하였습니다. 그러나 최근에는 목표화합물(target compound)이 발굴되면 먼저 나노입자화 기술을 비롯한 다양한 가용화 기술을 이용한 제형화 연구를 동시에 수행하고 있는 추세입니다. 그리하여 신약 개발 초기부터 제제화 기술(나노입자 기술)을 적용하여 난용성 문제를 해결한 신약을 제조하고자 하는 움직임이 활발합니다.
나노 약물전달시스템 기술을 신약에 적용함으로써, 난용성 약물을 물에서 분산이 잘 되는 약물로 변화시켜 신약 개발 성공률을 높일 수 있으며, 타 회사들의 진입 장벽을 높게 만들어서 제조한 신약의 개량신약 또는 복제약이 쉽게 만들어지지 않도록 방어할 수 있습니다.
② 개량신약(IMD: Incrementally Modified Drug) 제조
최근 1개의 신약개발에는 5조원 이상의 비용과 10~15년의 시간이 소요되고 있지만, 새로운 신약으로 승인되는 약품의 수는 매년 줄어 드는 추세입니다. 이러한 상황을 타개하기 위해 많은 다국적 제약사들은 기존에 자신들이 보유하고 있는 블록버스터 제품(blockbuster drug)의 수명연장을 위해 많은 노력을 경주할 뿐만 아니라, 타 회사의 약물에 대해서도 개량을 통한 시장 선점을 위해 많은 노력을 하고 있습니다.
이렇듯 많은 다국적 제약사들이 비교적 짧은 개발기간(3~6년)과 적은 투자비용(약 100억원)으로 성공 가능한 개량 신약 연구에 몰두하면서 개량 신약 시장은 계속적으로 증가해 가고 있습니다. 다만, 단순 염변경을 한 개량신약의 경우, 시장에 1년 이상 먼저 진입한다고 해도 오리지널 제품 대비 강점 부재로 시장 확보를 실패하는 경우가 속출하기 때문에, 기존제제 대비 효능 증대, 부작용 감소, 투여 방법 개선 등의 유효성 및 편의성이 증대된 개량 신약의 개발이 절실히 요구되고 있습니다.
또한 전세계에서 시판되는 의약품의 40%는 난용성으로 인한 낮은 생체이용률, 식전 식후 생체이용률(BA) 편차, 개인간의 BA 편차 등의 문제를 갖고 있습니다. 이러한 약물의 경우, 효능을 발휘하게 하기 위해 활성물질의 투여 용량을 높이고 부형제(Excipient)를 과다 사용함으로써 약물 또는 부형제에 의한 많은 부작용이 나타나고 있습니다. 경구 제형의 경우, 의약품의 사이즈가 커져 환자들의 약물 복용에 많은 불편함이 있어 복약 순응도가 떨어지고, 이로 인해 치료 효능까지도 감소하는 경향이 있습니다 (2015년 미국 FDA 가이드 라인에 따르면 경구 제형의 사이즈가 8 mm가 넘으면 환자들의 약물 복용에 불편함이 있음으로, 의약품의 사이즈를 줄일 것을 권고하고 있습니다).
나노 약물전달시스템 기술을 적용하여 기존제제의 문제점을 극복한 개량신약을 제조하여 성공한 사례 (예: 나노의약품 Tricor®, Megace®ES 등)를 바탕으로 나노 약물전달시스템을 통해 생체이용률의 증가, 식전식후 BA 편차 및 개개인간의 BA 편차문제 등을 해결할 수 있다고 알려지면서 시판되고 있는 의약품 중 난용성의 문제가 있는 의약품들에 나노 기술을 적용하고자 노력하는 제약사들의 노력이 계속되고 있습니다.
③ 복제약(generic) 제조
당사의 나노기술의 경쟁사인 Alkermes사(Elan사)의 NanoCrystal® (wet-milling technology) 기술을 사용한 나노 의약품 중, 2000년 8월 처음으로 FDA의 승인을 받은 Rapamune®의 특허가 2018년에 만료된 것을 선두로, 나노입자화 기술을 적용한 초창기 의약품들의 특허 만료가 임박한 시점입니다. 이러한 나노 의약품의 경우, 나노 기술이 아닌 다른 전통적인 기술로는 시판되고 있는 의약품과 동등한 효능을 맞추기가 어려워서 제네릭 개발이 난항에 부딪히는 경우가 많습니다. 이러한 문제를 해결하기 위해서는 NanoCrystal®처럼 나노기술을 적용할 수밖에 없으며, 당사의 NUFS™ 기술은 NanoCrystal® 기술을 대체할 훌륭한 도구가 될 수 있습니다.
이 밖에도 나노기술은 의약분야 이외에도 기능성 식품 및 화장품 등 다양한 분야에까지 적용이 가능합니다. 식품의 경우 기존 기능성 식품원료 중 난용성으로 인하여 제형의 한계 및 낮은 효능을 가진 물질에 나노기술을 적용하여 관련 문제점을 극복할 수 있습니다. 화장품 산업에 있어서는 기존 화장품 원료 중에서 기능성은 뛰어나지만 난용성 등의 문제로 인하여 그 적용에 제한이 있는 원료들에 나노기술 적용을 적용하여 기능 개선 및 완제품의 품질 향상을 이룰 수 있습니다.
(3) 시장규모 및 전망
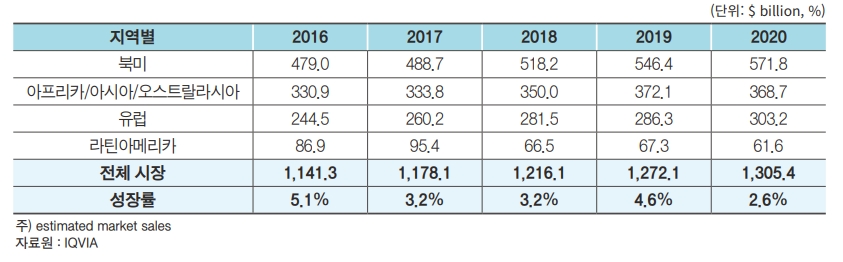
한국제약바이오협회의 2021 제약바이오산업 databook자료(2021년 12월)에 따르면 2020년도 세계 의약품 시장 규모는 1조 3,054억 달러였으며, 고령화뿐만 아니라 코로나 19로 인해 그 성장세는 더욱 가속화될 것으로 예상됩니다.
[세계 의약품 시장 규모]
 |
|
(한국제약바이오협회의 '2021 제약바이오산업 DATABOOK', 2021년 12월 자료) |
아이큐비아 인류 데이터과학 연구소가 2021년 4월에 공개한 '세계 의약품 지출 및 이용동향 전망 보고서'에 따르면 전세계 의약품 시장의 규모는 연평균 3-6% 성장하여, 2025년 연간 1조 6천억 달러에 달할 것으로 전망되었으며, 한국제약 바이오협회의 글로벌 제약산업관련 자료에 따르면, 질환별 시장 분석 시 항암제와 항당뇨제, 자가면역질환 치료제의 증가세가 두드러지고 있으며, 앞으로도 이같은 경향을 이어갈 것으로 예상된다고 합니다.
UnivDatos Market Insights에 따르면, 약물전달 시장(drug delivery market) 내에서 나노입자관련 매출은 약 19.4%의 연평균 성장률을 바탕으로 2027년까지 481 억 달러까지 성장할 것으로 예상되며, 특히 Asia-Pacific 지역(한국, 중국, 일본, 인도, 호주, 그 외 아시아 태평양 지역)은 약 22.5%의 연평균 성장률을 보이며, 약물전달 시장 내 나노기술관련 가장 큰 성장을 할 것으로 기대됩니다.
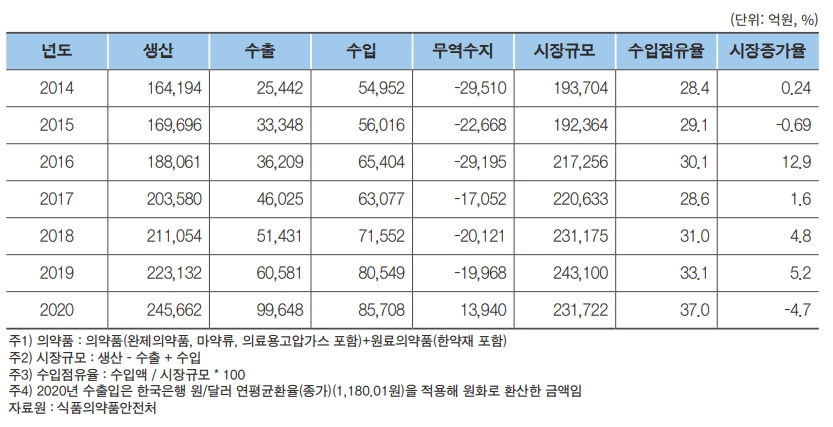
한국제약바이오협회의 2021제약바이오산업 databook자료(2021년12월)에 따르면 생산기준2020년도 국내 의약품 시장 규모는 24조 5,662억원으로 국내 의약품시장 역시 세계 의약품 시장 성장에 발맞추어 지속적으로 성장하고 있는 상황입니다.
[국내 의약품 시장 규모]
 |
|
(한국제약바이오협회의 '2021 제약바이오산업 DATABOOK', 2021년 12월 자료) |
더욱이 인구 노령화은 국내 및 세계 의약품 시장의 지속적인 성장에 크게 기여할 것입니다. 통계청 자료에 따르면 한국은 2000년 노인 비중이 7.3%에 이르며 고령화 사회에 진입한 뒤 17년 만인 2017년에 전체 인구에서 노인이 차지하는 비중이 14.2%로 증가되며 세계에서 가장 빠른 속도로 고령 사회에 진입하게 되었습니다. 그리고 이러한 속도로 계속 증가될 경우 2026년도에 초고령화 사회 (노인비중이 20%이상)에 진입할 것으로 예상된다고 합니다. 이러한 노인 인구 증가는 코로나19 팬데믹과 같은 전염병과 더불어 의약품 수요 증가에 크게 기여할 것으로 예상됩니다.
나. 회사의 현황
(1) 사업 개황
당사는 물에서 거의 녹지 않는 난용성 물질을 물에서 잘 풀리는(분산되는) 물질로 변형시키는 특허화된 원천 나노기술을 보유하고 있으며, 이를 활용하여 1) 자체 개발한 나노 분말을 제조·판매하거나 2) 나노기술 자체를 기술 이전하는 사업을 영위하고 있습니다.
 |
|
. |
현재 당사의 주 사업은 난용성 약물을 나노입자화하여 나노의약품 신약, 개량신약, 복제약을 제조하고 이를 국내외 대형 제약사에 기술 이전하는 것이며, 그 외에 화장품 및 식품 분야의 난용성 물질을 나노입자화한 나노 분말을 제조·판매하며 수익을 창출하고 있습니다.
[회사의 성장 과정]
|
구분 |
주요 성과 |
영업상 주요전략 |
|
설립시 (2004년 ~2006년) |
- 신기술보육(TBI)사업 신기술 사업자 선정 - 벤처기업으로 지정 (신기술 기업) - NUFS™ 기술 국내 특허 취득 |
- 신기술 특허 획득 |
|
1차 성장기 (2007년 ~2012년) |
- 중외제약과 공동기술개발계약 체결 (BS-OXL 개량신약) - Korea BizBiz Day (프랑크푸르트/뉴저지/오사카) 기술발표 및 Partnering 참가 - 파마킹과 연구개발계약 체결 (BS-108 개량신약) - NUFS™기술 미국/유럽 주요국/호주/중국/일본 특허 취득 - 국제 부인암 학회 IGCS 2010에서 NUFS™기술 적용성과 발표 (BS-102) - ㈜두산과 나노세라마이드 공동연구개발 및 사업화 계약 체결 - 보건복지부 선도형 암연구 사업단 과제로 선정 (서울아산병원 주관, BS-102) - Biopartnering North America에서 나노입자화 기술 발표 - Amway와 연구개발계약 체결 (Bioavailability 향상된 소재개발) |
- 원천 나노기술 홍보 - 국내외 주요 제약사에 나노화 서비스 제공 및 공동 연구 추진 |
|
2차 성장기 (2013년 ~2018년) |
- 대웅제약과 공동연구개발 및 기술이전계약 체결 - cGMP 공정 적합성 확인 - ㈜대웅제약의 전략적 투자 유치 - SENS™기술 미국 및 중국 특허 취득 - 한국투자파트너스, 프리미어파트너스 투자 유치 - 산기평 산업핵심기술개발사업 과제로 선정 (BS-103 & BS-104, 약 40억/4년) - 소재사업을 위한 공장 설립 - GMP 설비 구축 (의약사업) - 삼양바이오팜 기술이전 계약 체결 (BS-104) - 美.국립암연구소 산하 NCL (나노기술특성분석연구소)의 - 아리조나대학교와 나노소재관련 공동연구 진행 |
- 기술의 상업화 가능성 확증 - 자체 Pipeline 약물 구축 및 기술이전 |
|
3차 성장기 (2019년 ~2020년) |
- 나노코리아 2019 산업통상자원부 장관상 수상 - 건강기능식품 GMP 획득 - 가톨릭대학교와 개량신약 후보물질 관련 물질이전 계약(MTA) 체결 - 유럽 Z사와 개량신약 후보물질 관련 MTA체결 - 국내 S사와 신약후보물질관련 MTA 체결 - 국내 A사와 신약후보물질관련 MTA 체결 |
- 자체 Pipeline 약물 구축 및 기술이전 - 해외 사업화 추진 |
(2) 주요 사업분야
(가) 의약품 사업
당사의 주사업은 난용성 약물을 물에 잘 풀리는 나노약물로 변형시켜 나노의약품을 제조하는것으로, 나노 의약품 제조에 쓰이는 나노 원천기술을 약물별로 국내외 대형 제약사에 기술이전하여 계약금 (upfront), 단계별 기술료(milestone), 로열티 (royalty) 수익을 창출하는 것입니다.
2015년 이전까지는 원천 나노기술의 상업화 가능성을 확인하는데 주력하며, 국내외 제약사에서 나노화를 의뢰하는 난용성 약물을 나노화하는 용역 위주로 사업을 진행하였습니다. 하지만 2015년 투자 유치 이후, 타 제약회사의 난용성 약물을 나노분말로 제조하는 것에서 그치는 것이 아니라 자체 역량을 키우고자 시장성, 특허성 등을 바탕으로 후보 약물을 선정하고 이를 독자적으로 연구하며, 약물 파이프라인을 구축해 나가고 있습니다.
2017년 초부터는 (1)Bio, Interbiz, CPhI 등의 사업 파트너링 행사에 참여, (2) 특허 출원 및 논문 게재, (3) 전문 기술이전 컨설팅 업체 고용 등을 바탕으로 나노원천기술 및 파이프라인 약물들을 홍보하는 것에 주력하며, 독자적으로 연구를 진행한 나노의약품을 국내외 대형 제약사에 기술이전하기 위해 노력하고 있습니다. 뿐만아니라, 기존 파이프라인 약물의 성공사례를 바탕으로 국내외 대형 제약사에서 자체 진행 중인 약물에 당사의 나노 원천기술을 적용하여 나노의약품을 개발하고자 나노화 의뢰를 요청하는 건수가 지속적으로 증가하고 있습니다.
① NUFS™ 기술
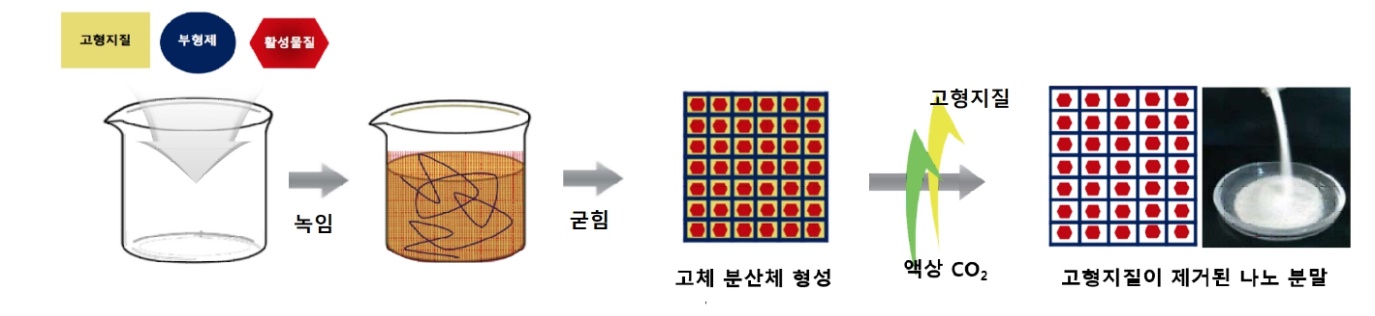
NUFS™ (Nanoparticulation Using Fat and Supercritical fluid) 나노기술은 ㈜바이오시네틱스의 특허화된 나노 원천기술로, 고형지질(상온에서 고체상태, 활성물질을 녹이는 용매로 사용 가능)과 액상 이산화탄소(고형지질을 제거하는 용매로 사용됨)를 사용하여 활성물질을 나노화 하는 기술입니다.
[NUFS™ 기술 소개]
 |
|
. |
나노입자를 제조하는 한 예는 다음과 같습니다. 1) 난용성 활성물질, 부형제(응집방지제 역할), 고형지질 (용매로 사용. 상온에서 고체상태이며 약 40 ℃이상의 온도에서는 액체상태)을 함께 녹이고 굳혀 고체분산체를 형성시킵니다. 이 때, 용매로 사용한 고형지질이 상온에서는 고체상태이기에, 혼합물의 온도를 40℃ 이상에서 약 30℃ 이하로 변화시켜주면, 혼합물 속에 녹아있던 고형지질이 굳으면서, 활성물질의 입자 성장이 나노 단위에서 멈춰지게 됩니다. 2) 고체분산체 내에 존재하는 고형지질을 액상 이산화탄소를 사용하여 녹여내서, 활성물질과 부형제만이 존재하는 분말을 수득하게 됩니다.
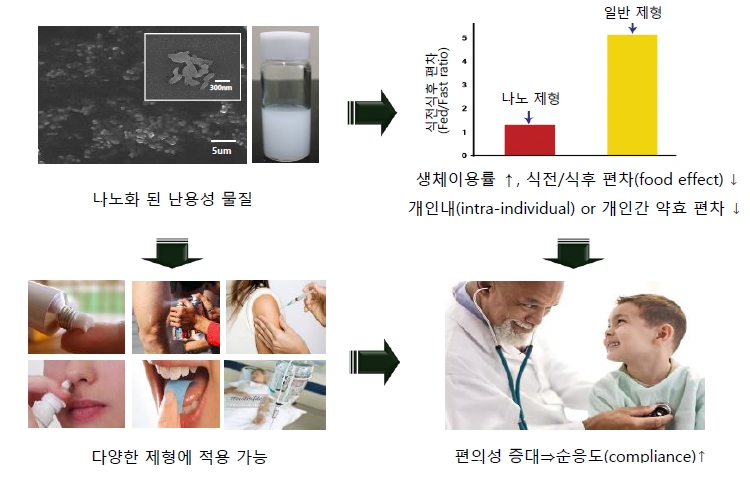
이러한 NUFS 나노기술을 적용함으로써 얻을 수 있는 효과는 다음과 같습니다.
 |
|
. |
1) 난용성 약물을 아주 작은 나노입자로 만들어서 물에서 잘 분산되게 만들어 체내에서 흡수율이 증가
2) 나노입자의 경우, 음식의 영향을 덜 받을 수 있기에 꼭 공복에 또는 꼭 음식과 함께 약물을 복용해야 하는 불편함 없이, 환자들이 편하게 약물을 복용할 수 있음
3) 나노입자의 경우, 균일한 속도로 녹아 나오기 때문에 녹는 속도를 예측하여 서방형 제제(주약물을 천천히 방출해서 일정한 혈중농도를 유지할 수 있도록 설계된 제품)로 사용하는 것이 용이할 뿐만 아니라 개체편차도 줄일 수 있기에 환자간 약효 편차가 덜 발생할 수 있음
4) 물에서도 쉽게 분산되기에, 현탁액, 주사제, 점안제 등 다양한 제형에 적용이 가능하여 개발사가 다양한 마케팅 전략을 세울 수 있음
② 경쟁 기술 비교
당사가 현재 영위하는 사업의 주요 경쟁기술은 Alkermes사의 NanoCrystal®과 Leon-nanodrugs사의 MJR® (Micro JetReactor)로, 이는 유기화합물을 나노입자로 제조하는 대표적 기술입니다. 당사의 기술은 Alkermes사의 나노크리스탈 (NanoCrystal®)기술과 같이 부형제를 사용하여 나노입자를 안정화시킨 결정형 나노입자를 제조하는 기술입니다.
나노입자를 제조하는 방법은 크게 하향식(Top-down)과 상향식(Bottom-up)으로 나뉘는데, 하향식은 본래의 큰 입자를 물리적인 힘을 가해 작은 나노입자로 작게 분쇄하는 방식이며, 상향식은 분자단위까지 물질을 녹인 후에 입자성장 속도를 제어하여 나노입자 크기의 물질을 제조하는 방식입니다. 보통 상향식 방식으로 입도를 제조하는 것이 더욱 균일하고 안정된 나노입자를 제조할 수 있으나, 대량 생산시 입자 성장을 균일하게 제어하는 것이 쉽지 않아 스케일업이나 상업화가 어렵다고 알려져 있습니다.
[주요 경쟁업체 현황]
|
구분 |
바이오시네틱스 |
Alkermes(Elan) |
Leon-nanodrugs |
|
기술명 |
NUFS™ & SENS™ |
NanoCrystal® |
MJR® |
|
입도(㎛) |
Below 1 |
Below 1 |
Below 1 |
|
제조방식 |
Bottom-up & Top-down & Combination |
Top-down |
Bottom-up |
|
제품형태 |
분말 (휘산성, 정전기 우려 없음) |
액상 ⇒ 분말 (추가 건조 공정 필요) |
액상 ⇒ 분말 (추가 건조 공정 필요) |
|
오염우려 |
없음 |
분쇄 매체로 인한 오염 |
잔존 유기 용매로 인한 |
|
부형제 |
1↓ |
1↓ |
5↑ |
주1. 약물대비 부형제량이 1배 이상으로 많아질 경우, 최종 의약품의 크기가 커지게 되어 환자의 복용편의성이 저하됨
Alkermes사의 NanoCrystal®은 2000년도에 최초 나노 결정(NanoCrystal) 의약품으로 미국 FDA 승인을 받은 라파뮨(Rapamune®)에 사용된 기술로, 하향식 방식으로 나노입자를 제조하는 기술입니다. 이는 수환경 속에 약물과 부형제를 넣어주고 분쇄 매체 (grinding media)로 약물을 분쇄하여 나노입자를 제조하는 기술입니다. 때문에 엘로티닙(Erlotinib) 염과 같이 물에서 안정하지 못한 약물이나 분쇄 열로 인해 구조가 깨지거나, 너무 무른 성질로 분쇄가 용이하지 않은 약물들의 경우에는 기술 적용이 어렵습니다. 더욱이 분쇄 매체로 인한 오염우려 또한 존재하기에 주사제나 안약과 같은 제형에는 적용이 용이하지 않을 수 있습니다. 더욱이 최종 제품이 액상형태이기에 정제나 캡슐로 제조하기 위해서는 추가 건조 공정이 필요하며 이때 입자 크기 증가가 일어날 수 있기에 추가 부형제 (응집 방지제)를 과량 첨가해야 할 수 있습니다.
Leon-nanodrugs사의 MJR® 기술은 상향식 방식으로 나노입자를 제조하는기술로, 약물을 유기용매에 녹이고, 입자 응집방지제와 같은 부형제를 물에 녹인 후, 미세한 노즐로 두 용매를 고속 충돌시켜 분자단위의 약물을 석출시켜 나노입자로 제조하는 기술입니다. 때문에 유기용매 잔존에 대한 우려가 있으며, Alkermes사의 기술과 같이 최종제품이 액상형태이기에 분말로 제조하기 위해 추가 건조 공정이 필요하여 시간 및 비용이 더 발생할 수 있습니다. 더욱이 Alkermes사나 당사의 기술과 달리 사용하는 부형제량이 보통 5배이상이기에 최종 의약품의 크기가 커질 수 밖에 없고, 이는 환자의 복용 편의성을 저해하는 요소가 됩니다.
이에 반해, 당사의 나노기술 NUFS™는 약물대비 1배 이하 (보통 0.5배)의 소량의 부형제만을 사용하여 의약품을 제조하기에 최종 제형의 크기나 개수를 줄여 환자의 복용 편의성을 높일 수 있으며, 최종 제품 형태가 분말이기에 추가 공정이 필요 없는 경제적인 기술입니다. 뿐만 아니라 MJR® 기술과 달리, 약물을 녹이는 용매가 FDA에서 부형제로 승인되어 섭취해도 무해한 물질이며, 사용한 용매도 또한 재사용이 가능한 친환경 기술입니다. 더욱이 NanoCrystal® 기술과 달리 분쇄 매체에 대한 우려가 없기에, 주사제 및 안약에도 적용 가능합니다.
현재 국내에는 상업화 가능한 약물전달시스템(Drug Delivery System) 기술로서 의약품과 같은 유기화합물을 나노 입자화 하는 원천 나노기술을 보유한 회사는 당사가 유일합니다. 국내 일부 제약 회사에서 특허가 끝난 NanoCrystal® 기술을 활용하여 의약품을 개발하고자 시도하였으나, 앞서 언급된 바와 같이, NanoCrystal® 기술을 적용할 경우 정제화 또는 캡슐화 하기 위해서는 추가 건조 공정이 필요하고, pre-milling이라는 전처리 단계도 필요하며, 특히 수 환경에서 안정하지 못한 약물들에는 NanoCrystal® 기술의 적용이 어렵기에, 당사의 기술을 대체 사용해보고자 하는 의뢰가 증가하고 있습니다.
③ 파이프라인
기술 이전이 완료된 제품은 BS-101, BS-OXL, BS-108로, BS-101의 경우 시판되고 있는 MSD사 나노 항구토제의 나노 제형 특허를 회피하고자, 당사의 NUFS™ 나노 기술을 이용하여 제조한 나노 의약품(복제약)이며, 현재 대웅제약에 기술이전이 완료되었습니다. BS- OXL은 Sanofi-Aventis사 대장암 주사제를 경구제로 변형시켜 환자의 복용 편의성을 향상시킨 제품으로 JW중외제약에 기술이전 하였습니다. BS-108은 MSD사 천식치료제의 개량신약으로, 전임상 시험을 통해 기존제품 대비 동등 이상의 흡수율 및 감소된 개체편차를 확인할 수 있었으며 파마킹에 기술이전을 완료하였습니다.
BS-104는 NUFS™ 나노 기술을 이용하여 생체이용률을 향상시킨 표적항암제입니다. 향상된 생체이용률을 보이는 동물 시험 및 임상 1상(Pilot) 결과를 바탕으로 허가용 임상1상을함께 수행할 파트너를 물색 중에 있습니다.
BS-102의 경우 시판제제대비 독성을 감소한 제품으로, 현재 미국 국립암연구소(NCI) 산하 NCL에서 독성시험을 진행하고 있습니다.
나노 항응고제 BS-112는 비임상시험을 통해 음식물에 의한 생체이용률 편차가 감소되었음을 확인하였으며, 해당 결과를 바탕으로2021년 하반기에 1차 임상 1상을 수행하여, 인체 내에서도 기존 시판제(자렐토정)대비 식전식후편차가 개선됨을 확인하였습니다. 현재 1차 임상 1상 시험 결과를 바탕으로, 2차 임상 1상을 수행하고자 준비 중에 있습니다.
나노 코로나19 치료제 BS-120은 기존에 구충제로 40년이상 사람에게 사용되고 있는 안전한 의약품을 코로나19 치료제로 신약재창출(Drug Repositioning)한 제품입니다. 해당 주원료는 니클로사마이드로, 기존에 암, 당뇨병, 자궁내막증, 동맥 협착, 류마티스관절염 등에 효능을 보였던 니클로사마이드가 코로나19 항바이러스 효능(에볼라치료제 렘데시비르보다 40배, 말라리아 치료제 클로로퀸보다 26배 높은 코로나19 항바이러스 활성도)까지 있다는 것이 최근 실험실관 내 실험(in vitro)으로 확인되었습니다. 하지만 니클로사마이드의 난용성 성질 때문에 알려진 효능들을 생체 내 (in vivo) 실험에서는 구현하기 어려운 것이 현실이었습니다. 때문에 당사는 니클로사마이드의 나노화를 통해 생체이용률을 향상시킴으로써 해당 난용성 문제를 해결하여 코로나19 치료 효과를 증대시키고자 합니다. 최근 비임상시험을 통해 기존 니클로사마이드 제제대비 생체이용률이 10배이상, 최고혈중농도가 60배 이상 향상된 것을 확인하였으며, BS-112의 임상시험들을 통해 바이오시네틱스의 나노기술이 생체이용률을 향상시킬 수 있다는 것을 인체 내에서 확인했기에, 니클로사마이드의 나노화를 통한 생체이용률 향상 또한 가능할 것으로 기대되고 있습니다. 더욱이 해당 제제는 경구용 고형제로 제품화할 예정이기에 주사제로 개발되고 있는 제제들 대비 높은 복용 편의성을 바탕으로 경증환자들의 치료 또는 정상인을 대상으로 한 예방약으로도 활용될 수 있을 것으로 기대됩니다.
[주요 파이프라인 현황]
|
구분 |
제품명 |
효능 |
단계 |
주요 내용 |
|
이전 완료 |
BS-101 |
항구토제 |
- |
MSD사 항구토제 나노의약품의 복제약으로, 당사의 나노기술을 적용하여, MSD사의 나노 제형 특허를 회피할 수 있었음. 현재 대웅제약에 기술이전을 마침 |
|
BS-OXL |
세포 독성 |
- |
Sanofi-Aventis사 대장암 주사제를 경구제로 변형시켜 환자의 복용 편의성을 향상시킨 제품으로 JW 중외제약에 기술이전 완료 |
|
|
BS-108 |
천식 치료제 |
- |
MSD사 천식치료제의 개량신약으로, 전임상 시험을 통해 기존제품 대비 동등 이상의 흡수율 및 감소된 개체편차를 확인할 수 있었음. 파마킹에 기술이전 후 현재 임상 1상을 완료 |
|
|
자체 연구 |
BS-104 |
표적 항암제 |
국내 임상 1상 |
Bayer사 간암치료제의 개량신약으로, 당사의 나노 기술을 적용하여, 흡수율을 향상시킨 제품. 임상 1상 (Pilot) 완료 후, 허가용 임상 1상을 위한 파트너 물색 중 |
|
BS-102 |
세포 독성 |
국내외 비임상 |
여러 암 종에 사용이 가능한 나노 항암제로, Sanofi-Aventis사의항암제 대비 동등이상의 항암효과에도 불구하고 독성작용이 크게 감소함. NCL과 공동연구 수행 중 |
|
| BS-112 |
항응고제 |
국내 임상 |
당사의 나노 기술을 통해 식전 생체이용률을 향상시킴으로써 식전식후 흡수율 편차가 감소될 것으로 기대됨. 2021년 하반기에 수행된 1차 임상1상을 통해 대조약 자렐토정 대비 식전식후 흡수율 편차감소를 확인하였으며, 2022년 상반기에 2차 임상 1상을 수행하고자 준비 중 |
|
|
BS-120 |
코로나19 치료제 |
제제 연구 |
Bayer사에서 구충제로 판매하고 있는 약물을 코로나19 치료제로 drug repositioning (신약 재창출)한 제품으로, 해당 물질의 코로나19치료제 효능은 in vitro 실험을 통해 확인 완료된 상태임. 하지만 매우 낮은 난용성 성질로 인해 in vivo상 해당 효능을 기대하기 어렵기에, 나노화를 통해 난용성 문제를 해결하여 생체내 코로나19 치료 효능을 증대하고자 함. 현재 비임상 시험을 통해 기존제제 대비10배 이상 향상된 생체이용률을 지님을 확인함 |
④ 기술이전
1) 파이프라인 약물
의약품 사업의 경우, 의약품 별로 (더욱 세부적으로는 지역별로) 각 나노의약품을 제조하는데 사용되는 당사 나노 원천기술을 기술이전하는 것을 주 사업으로 진행하고 있습니다. 그리하여 앞서 언급된 자체 연구를 진행하고 있는 제품을 포함하여, 현재 2026년 이후에 물질 특허가 만료되는 시장성이 뛰어난 2종의 의약품에 대해 자체적으로 나노화 연구를 진행하고 있으며 약물 파이프라인을 지속적으로 늘려가고자 노력하고 있습니다.
이렇게 구축된 파이프라인 약물들의 경우, 기술이전을 진행하기 전, 용출 및 간이 제형 연구를 진행하여 목표로 한 효과를 달성하였는지 1차적으로 확인을 진행합니다. 그 이후, BioKorea, BioUSA, Interbiz, CPhI, AAPS 등에 참석하여 파트너링 미팅과 포스터 발표 등을 통해 연구한 내용을 발표, 홍보하며 나노 의약품의 기술이전을 추진합니다.
2) 나노원천기술
앞서 언급된 자체 개발 중인 파이프라인 약물들의 기술이전과는 별개로, 파이프라인 모델 약물들의 성공사례를 바탕으로, 나노 원천 기술 자체의 특장점을 홍보하며 국내외 제약사에서 자체 개발하고 있는 약물에 당사의 기술을 적용할 수 있도록, 약물 별로 나노원천기술 자체를 기술이전하는 사업또한 추진하고 있습니다. 현재 2종 이상의 신약후보물질에 대해, 당사의 원천 나노기술을 약물전달시스템(Drug Delivery System)으로 사용하여 용해도 및 용해 속도를 향상시키는 연구를 진행하고 있습니다. 뿐만 아니라 기존제품의 제품 수명 주기관리(life cycle management)를 위한 도구로써 나노원천기술을 사용할 수 있기에, 파이프라인 약물들의 성공사례를 바탕으로, 당사의 나노기술을 적용하여 기존 제품의 문제점을 개선한 개량신약을 제조하여 제품의 수명주기를 늘리는 것이 가능함을 홍보하며, 기술이전을 추진하고 있습니다.
|
[참조] 신약 개발 및 제품 허가 과정 ① 비임상 (Non-clinical study) : 새로 개발한 약을 사람에게 사용하기 전에 여러 종류의 동물에게 사용하여 부작용/독성 및 유효성 등을 확인하고 임상 시험에 사용할 제제에 대한 제제화 연구를 병행하여 제형/처방 등을 결정하는 시험 ② 신약 임상시험 승인 신청 (IND, Investigational New Drug Application) : 신약 후보 물질을 사람에게 투여하는 시험을 허가할 것인지를 결정하기 위해 전임상 시험 자료를 심사하는 제도로 임상시험용 의약품 허가를 받기 위하여 동물시험까지의 전임상자료와 임상시험계획서를 취합하여 신청/승인하는 절차 ③ 임상 1상 (Phase 1 clinical trial) : 처음으로 인체에 약품을 투여하는 연구로 건강한 피험자(보통 건강한 성인 남자 20~80명 정도가 대상)에 투여해 대사, 배설 과정에서 전임상에서 발견하지 못한 독성이 있는지 여부를 관찰함. ④ 임상 2상 (Phase 2 clinical trial) - 임상 2a상 (Phase 2a clinical trial) : 사용할 의약품의 용량을 단계적으로 높여주며 시험대상인 약이 효과가 있는지 여부를 결정하는 과정임. - 임상 1/2a상 (Phase 1/2a clinical trial) : 치료제로 환자에게만 적용되는 신약 중 비임상 시험 결과 등을 통해 임상 1상 단계의 결과에 대한 충분한 근거가 확보된 경우 2a 단계까지 동시에 관리기관(식약처)의 승인을 받아 임상시험을 진행할 수 있으며, 임상 1/2a상 승인을 받아 임상을 진행할 경우 관리기관과의 협의 및 임상 절차 진행에 소요되는 시간, 비용 및 인력 투입 등의 전반적 절감이 가능함. - 임상 2b상 (Phase 2b clinical trial) : 임상2b에서는 2a의 결과에 따라 설계된 용량을 갖고 다시 환자에 투여, 어떤 용량이 가장 효과가 있을지 적정 투여용량의 범위를 정하는 연구 단계임. ⑤ 임상 3상 (Phase 3 clinical trial) : 2상 결과 가장 효과적이라고 생각되는 용량, 용법대로 다수의 환자들에 약품을 투여, 약품의 안전성 및 유효성에 대해 관찰하는 단계임. 3상은 1상과 2상에서 안전성에 대한 자료가 어느 정도 확보되었기 때문에 2상 보다 환자의 수를 늘려 안전성과 유효성을 함께 관찰함. ⑥ 신약승인신청 (NDA, New Drug Application) : 전임상시험결과와 인체를 대상으로 하는 임상시험결과를 종합하여 관리기관에 의약품 시판허가를 신청하는 절차임. |
(나) 소재(식품/화장품)사업
기능성 식품이나 화장품에 사용되는 다양한 기능성 소재들 중에도 난용성 소재가 많이 있습니다.
바이오시네틱스는 기능성이 과학적으로 입증되고 널리 사용되고 있는 소재 중에서 물에 대한 용해도가 극히 낮아서 그 효능을 충분히 발휘하지 못하거나 다양한 완제품 제형에 적용이 어려운 소재들을 엄선하여 나노수분산이 가능한 제형으로 개발하고 하이드로파티클(HydroParticle) 시리즈 브랜드로 제품화 하였습니다.
① 기능성식품 소재
건강기능식품 소재 하이드로파티클 제품들은 난용성 소재의 생체이용율을 크게 올려줄 수 있고 또한 음료 등 다양한 형태의 건강기능식품을 용이하게 제조할 수 있도록 해줍니다. 당사는 식품의약품 안전처로부터 인증받은 우수건강기능식품 제조기준 (GMP) 설비를 갖추고 하이드로파티클 제품을 제조·판매하고 있습니다. 국내는 건강기능식품회사에 직접 또는 소재전문 유통회사를 통하여 제품을 공급하고 있으며 Vitafoods, Hi 등 해외전시회에 지속적으로 참가하여 해외 고객들을 발굴하고 있습니다. 현재 대만과 베트남, 말레이시아에 대리점 망을 구축하였으며 아직 소량이지만 제품이 수출되고 있습니다.
1) 하이드로커큐민(HydroCurcumin)
하이드로커큐민(HydroCurcumin)은 항산화 작용 및 항암효과, 면역력 증진, 치매 예방 및 기억력 향상에 탁월한 강황의 주성분인 커큐민을 나노화한 분말 제품으로, 물에 잘 분산되는 분말로 제조하여 음료를 포함한 다양한 식품에 적용이 용이한 제품입니다.
 |
|
. |
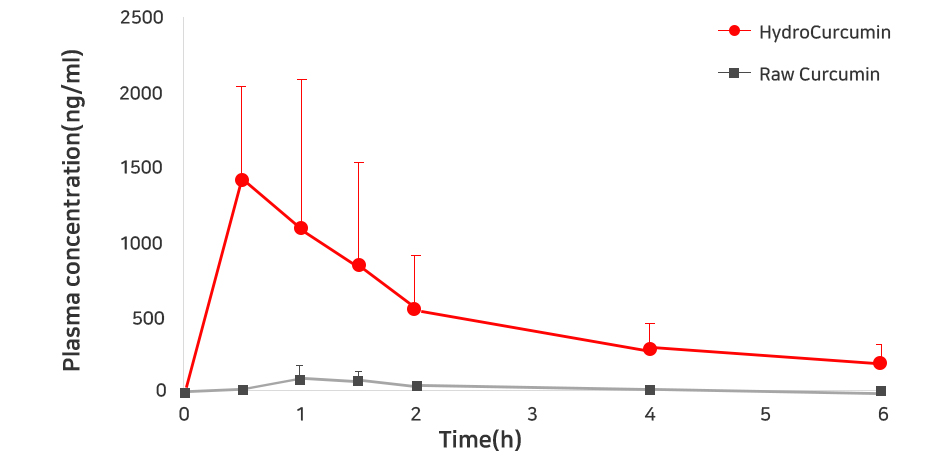 |
|
. |
[Figure1] Mean plasma concentration-time profiles of total curcumin in rats after administration of raw curcumin and HydroCurcumin™ (50mg/kg body weight of curcumin, mean ± SD, n=5)
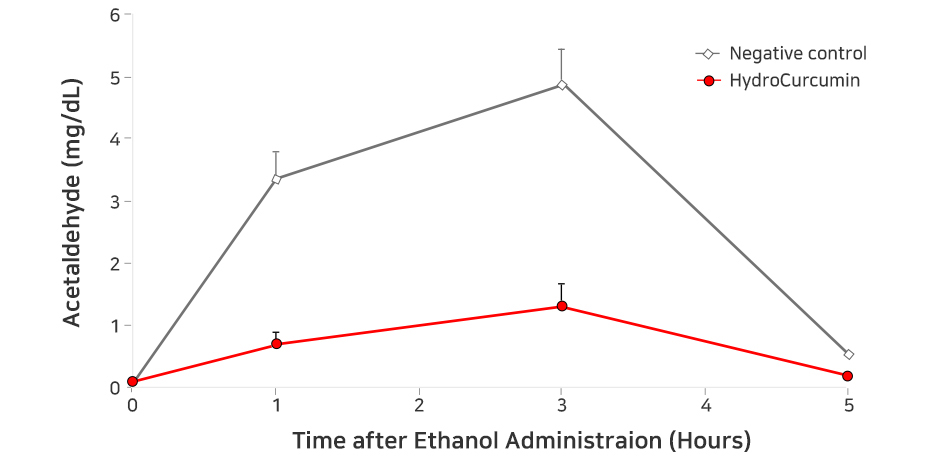 |
|
. |
[Figure2] Mean plasma concentration of acetaldehyde in SD rats(n=8) with or without intake of HydroCurcumin™ (50mg/kg by curcumin) and successive intake of 30% ethanol(10ml/kg)
2) 하이드로코큐텐(HydroCoQ10)
코큐텐(코엔자임Q10)은 인체의 모든 세포에 존재하여 에너지 생성에 관여하는 물질입니다. 코큐텐은 간에서 생성되지만 나이가 들수록 그 양이 줄어듭니다. 코큐텐은 식품의약품안전처가 지정한 건강기능식품 소재로서 항산화 및 고혈압 감소에 도움을 줍니다. 코큐텐은 매우 난용성이서 인체 흡수율이 낮은 것으로 알려져 있습니다.
HydroCoQ10™ 은 코큐텐의 난용성 문제를 극복할 수 있도록 바이오시네틱스가 나노입자화 기술로 탄생시킨 혁신 소재입니다.
동물시험 결과 단순히 물에 분산시킨 HydroCoQ10™이 식물성기름에 완전히 녹인 CoQ10에 비해 동등이상의 흡수율을 나타냈습니다. (Hyang-Mok OK et al. 2012. J Korean Soc Appl Biol Chem 55, 619-623).
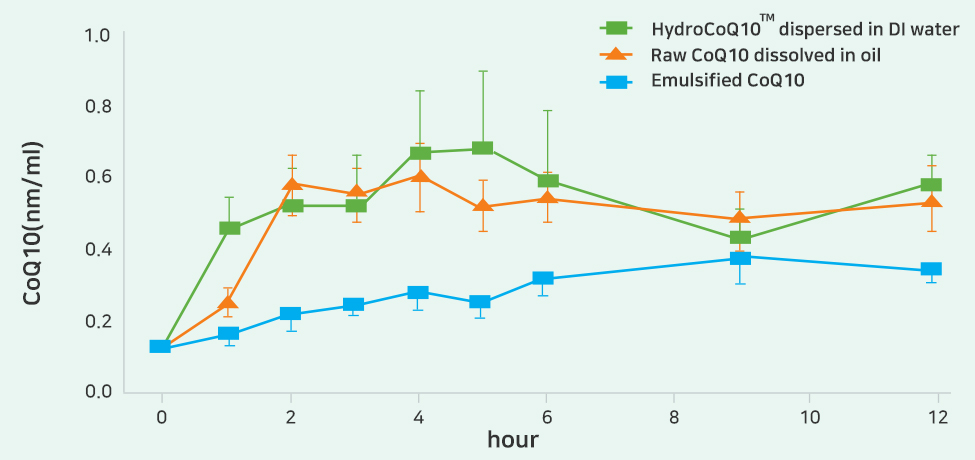 |
|
. |
[Figure] Time curves of total CoQ10 in plasma of rats after oral administration (60mg Coenzyme Q10/kg body weight of rat as a single dose, n=9)
바이오시네틱스는 코큐텐이 40% 함유된 하이드로코큐텐 HQ40을 식약처에 품목제조보고를 완료하고 건강기능식품(원료성)으로 출시하여 국내외 고객들에게 공급하고 있습니다.
3) 하이드로밀크씨슬(HydroMilkThistle)
하이드로밀크씨슬(HydroMilkThistle)은 간건강에 탁월한 성분인 밀크씨슬을 나노화한 제품이며, 밀크씨슬은 엉겅퀴라고도 불리는 국화과 식물로써 전통적으로 간질환의 치료제로 사용되어 왔습니다. 밀크씨슬 추출물의 주성분은 실리마린으로서, 우리나라의 건강기능식품 기준에 따르면 하루에 실리마린 130mg 이상을 섭취하면 간건강에 도움을 줄 수 있습니다.
HydroMilkthistle™은 밀크씨슬 추출물에 하이드로파티클 기술을 적용하여 나노수분산이 가능하도록 개발한 원료성 제품입니다. 캡슐이나 타블렛 등 전통적인 형태뿐 아니라 음료 등 다양한 형태로 생체이용율이 증가된 밀크씨슬 추출물 함유 건강기능식품을 제품화 할 수 있도록 해줍니다.
② 화장품 소재
항산화, 주름개선, 미백 등 다양한 기능성을 가진 화장품 소재 등에도 물에 대한 용해도가 매우 낮아서 완제품 적용이 까다롭고 따라서 기능성을 충분히 발휘하기 어려운 경우가 많습니다.
바이오시네틱스의 하이드로파티클 기술이 적용된 화장품 소재 제품들은 고농도로 수분산이 가능하므로 유기용매나 오일에 녹이지 않고도 고함량의 유용성분이 함유된 다양한 제형의 화장품 제조를 가능하게 합니다.
하이드로파티클 소재가 함유된 화장품을 피부에 적용하면, 수백 나노미터 크기의 지질 친화적인 기능성 소재 입자들로 피부 접촉면적을 크게 넓힐 수 있으며 따라서 수동 확산을 통한 피부 흡수율이 크게 증가합니다.
1) 하이드로세라마이드50(DS-HydroCeramide50)
DS-HydroCeramide50는 피부개선, 노화방지 등의 피부 미용뿐만 아니라 아토피성 피부염을 억제 하는 등 피부 질환에도 효과가 있는 세라마이드를 주 원료로 50% 함유한 분말입니다. 나노기술을 적용하여 기존에는 적용할 수 없었던 수(水) 함량이 높은 스킨/에센스 등과 같은 투명한 제형에도 적용이 가능하고, 재결정(Recrysatlization)문제로 기존에 크림이나 로션에 고함량 첨가할 수 없었던 제품의 문제점도 해결하였습니다. 뿐만 아니라 나노화를 통해 기존 제형 대비 보습 기능도 향상시킨 제품입니다.
당사에서 사용하고 있는 DS-HydroCeramide50의 세라마이드 원료는 독일의 Evonik사에 이어 세계 두 번째로 천연 세라마이드를 개발한 솔루스첨단소재㈜((구)두산 솔루스㈜)의 세라마이드로, 기존에 많이 유통되고 있었던 유사(pseudo) 세라마이드가 아닌 천연 세라마이드 원료를 사용하였다는 것에서 차별성을 지닙니다. 또한 DS-HydroCeramide50의 경우, 나노화를 통해 로션이나 크림과 같이 유지(oil)성분이 많은 제형에서 스킨이나 에센스와 같이 수(water) 성분이 많은 제형까지 모두 적용이 가능하기에 경쟁제품 대비 더 다양한 제형에 적용이 가능할 뿐만 아니라 고함량을 첨가하여도 제품 생산에 어려움이 없으며 완제품상의 안정성 향상으로 품질을 장시간 유지할 수 있다는 강점이 있습니다.
당사의 제품인 DS-HydroCeramide50의 국내외 마케팅은 협력사인 솔루스첨단소재㈜가 담당하고 있으며, 현재 중국과 유럽의 몇몇 화장품 회사들이 이 DS-HydroCeramide50를 첨가한 화장품을 판매하고 있습니다. 더불어 세계적 화장품 회사인 라프레리, 에스티로더, 존슨앤존슨 등에 마케팅 하여 매출 확대를 추진하고 있습니다.
2) 하이드로코큐텐(HydroCoQ10)
코엔자임Q10 (코큐텐)은 강력한 항산화제로서 피부노화 방지 및 개선효과가 있는 우수한 화장품 소재이지만 난용성이 매우 심하여 화장품으로 적용 시에 제형화에 어려움이 많이 있습니다.
당사가 개발한 HydroCoQ10은 이러한 CoQ10의 단점을 극복한 제품으로서 나노입자로 수분산이 가능한 분말 제형입니다.
특히 HydroCoQ10은 액상제형에서 탁월한 안정성을 보이기 때문에 크림, 로션 등 오일 성분이 많은 완제품 제형뿐 아니라 스킨, 토너 등 수분이 주성분인 완제품 제형에도 용이하게 적용할 수 있고 강력한 항산화제인 CoQ10을 고함량으로 함유한 화장품을 개발하는데 매우 유용하게 활용될 수 있습니다.
.
다. 경영상의 주요계약
|
계약명 |
계약기간 |
계약상대방 |
계약의 목적 및 내용 |
계약금액 |
|
연구계약서 |
2007.04 결정한 종료시점까지) |
중외제약 |
나노 입자 제조 기술을 기반으로 |
사업상 기밀사항 |
|
연구개발 및 기술실시권 |
2009.08 존속기간 만료 시까지) |
파마킹 |
BS-108 연구개발 및 사업화 |
사업상 기밀사항 |
|
공동 연구 개발 및 |
2011.11 나타내지 않으면 |
솔루스 첨단소재(주) |
나노세라마이드 공동연구개발 및 |
사업상 기밀사항 |
|
연구 개발 계약서 |
2012.07 |
Amway |
연구개발계약 체결 |
사업상 기밀사항 |
|
공동연구 및 |
2013.11 |
대웅제약 |
BS-101 공동연구 및 기술이전 계약 |
사업상 기밀사항 |
|
산업핵심 기술개발사업 |
2016.09 -2019.12 |
산업 통상자원부 |
산업핵심기술개발사업(나노 분말화 기술을 이용하여 용법과 용량이 개선된 표적항암제 개발) 협약 체결 |
사업상 기밀사항 |
|
기술이전 계약서 |
2017.12-2019.05 |
삼양바이오팜 |
BS-104 공동연구 및 기술이전 계약 |
사업상 기밀사항 |
|
물질이전계약서 |
2018.08 |
美국립암연구소 (나노기술특성 |
BS-102 관련 MTA 체결 |
사업상 기밀사항 |
|
물질이전계약서 |
2018.10 |
아리조나대학교 |
HydroCurcumin 관련 MTA 체결 |
사업상 기밀사항 |
|
BS-119 |
2020.03 |
가톨릭대학교 |
사업상 기밀사항 |
|
|
BS-112 |
2020.04 |
유럽 Z사 |
사업상 기밀사항 |
|
|
신약후보물질 |
2020.05 |
국내 S사 |
사업상 기밀사항 |
|
|
신약후보물질 |
2020.12 |
국내 A사 |
사업상 기밀사항 |
|
| Nano-A4368 | 2021.03 | 오토파지사이언스 | Nano-A4368의 나노기술연구 및 기술이전 계약 | 사업상 기밀사항 |
(5) 조직도
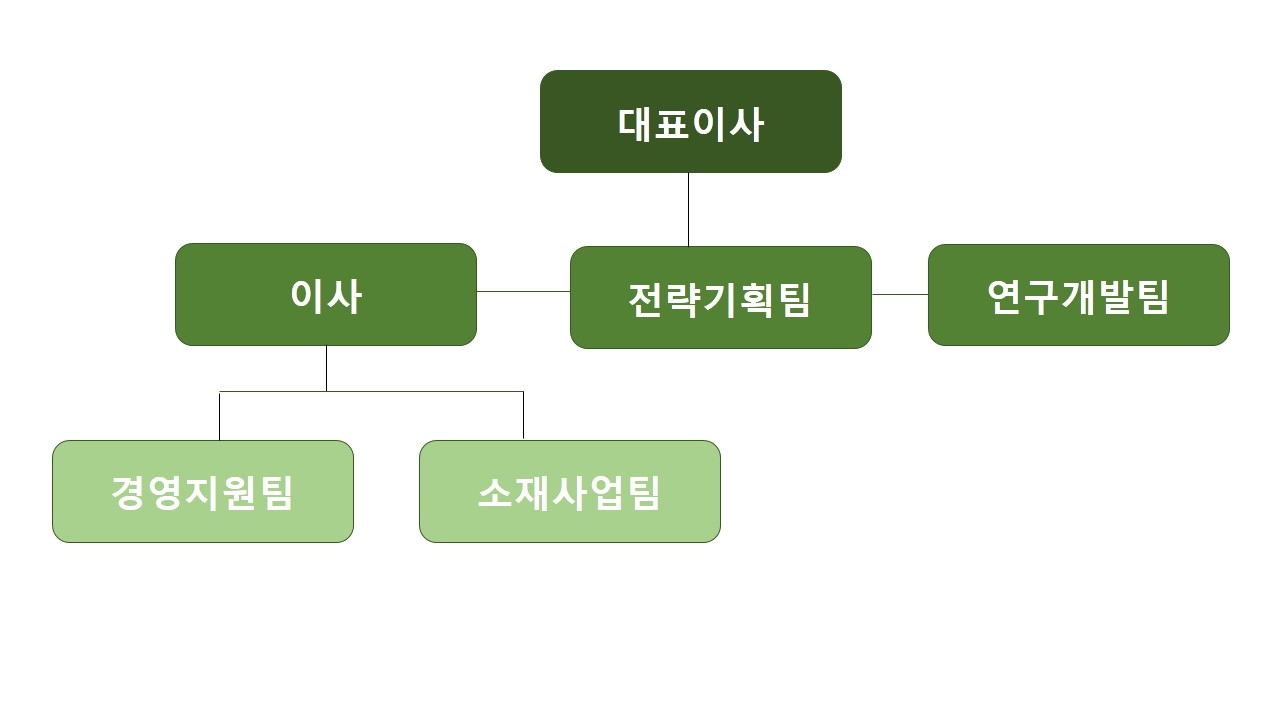 |
|
. |
2. 주주총회 목적사항별 기재사항
□ 재무제표의 승인
가. 해당 사업연도의 영업상황의 개요
「III. 경영참고사항. 1. 사업의 개요. 나. 회사의 현황」참고
나. 해당 사업연도의 대차대조표(재무상태표)ㆍ손익계산서(포괄손익계산서)ㆍ자본변동표ㆍ이익잉여금처분계산서(안) 또는 결손금처리계산서(안)ㆍ현금흐름표
※ 해당 재무제표 등은 외부감사인 감사가 완료되지 않은 상태에서 작성된 감사전
재무제표입니다. 외부감사인의 회계감사과정 및 주주총회 결의내용에 따라 변경될 수 있습니다.
※ 상세한 주석사항은 향후 전자공시시스템(http://dart.fss.or.kr)에
공시예정인 당사의 감사보고서를 참조하시기 바랍니다
- 재무상태표
| < 재 무 상 태 표 > |
|
| 제 18(당) 기 2021년 12월 31일 현재 | |
| 제 17(당) 기 2020년 12월 31일 현재 | |
| 주식회사 바이오시네틱스 | (단위 : 원) |
| 과 목 | 제 18(당) 기 | 제 17(당) 기 | ||
|---|---|---|---|---|
| 자 산 | ||||
| Ⅰ. 유동자산 | 539,160,417 | 1,306,173,448 | ||
| (1) 당좌자산 | 440,575,555 | 1,209,641,501 | ||
| 1. 현금및현금성자산 | 339,914,975 | 1,098,559,672 | ||
| 2. 단기금융상품 | - | - | ||
| 3. 매출채권. | 36,492,000 | 44,149,000 | ||
| 4. 미수금 | 500,000 | 21,255,939 | ||
| 5. 선급금 | 63,407,390 | 43,181,390 | ||
| 6. 당기법인세자산 | 261,190 | 2,495,500 | ||
| (2) 재고자산 | 98,584,862 | 96,531,947 | ||
| 1. 제품 | 66,615,534 | 86,236,287 | ||
| 2. 원재료 | 31,969,328 | 10,295,660 | ||
| Ⅱ. 비유동자산 | 272,799,069 | 400,176,289 | ||
| (1) 유형자산 | 198,403,169 | 325,697,889 | ||
| 1.기계장치 | 1,134,120,985 | 1,134,120,985 | ||
| 감가상각누계액 | (12,452,400) | (784,028,181) | ||
| 정부보조금 | (923,265,416) | (24,394,915) | ||
| 2. 비품 | 46,329,470 | 46,329,470 | ||
| 감가상각누계액 | (41,870,032) | (41,870,032) | ||
| 정부보조금 | - | - | ||
| 유형자산손상차손누계액 | (4,459,438) | (4,459,438) | ||
| 3. 구축물 | 167,000,000 | 199,000,000 | ||
| 감가상각누계액 | (105,665,500) | (121,131,683) | ||
| 유형자산손상차손누계액 |
(61,334,500) | (77,868,317) | ||
| 4. 임차개량자산 | 21,742,255 | 24,044,334 | ||
| 감가상각누계액 | (12,174,590) | (12,941,616) | ||
| 유형자산손상차손누계액 | (9,567,665) | (11,102,718) | ||
| (2) 무형자산 | - | - | ||
| 1. 산업재산권 | 125,131,126 | 125,131,126 | ||
| 무형자산손상차손누계액 | (125,131,126) | (125,131,126) | ||
| 2. 건설중인무형자산 | 261,881,899 | 241,263,502 | ||
| 무형자산손상차손누계액 | (261,881,899) | - | ||
| 정부보조금 | - | (241,263,502) | ||
| (3) 기타비유동자산 | 74,395,900 | 74,478,400 | ||
| 1. 임차보증금 | 73,065,000 | 73,065,000 | ||
| 2. 기타보증금 | 1,330,900 | 1,413,400 | ||
| 자 산 총 계 | 811,959,486 | 1,706,349,737 | ||
| 부 채 | ||||
| Ⅰ. 유동부채 | 265,510,952 | 185,374,351 | ||
| 1. 매입채무 | 27,500,000 | - | ||
| 2. 미지급금 | 168,666,734 | 121,210,986 | ||
| 3. 예수금 | 3,172,820 | 8,257,230 | ||
| 4. 선수금 | - | 44,179,826 | ||
| 5. 미지급비용 |
54,695,973 | 250,884 | ||
| 6. 복구충당부채 | 11,475,425 | 11,475,425 | ||
| Ⅱ. 비유동부채 | 444,678,360 | 395,126,921 | ||
| 1. 퇴직급여충당부채 | 432,794,093 | 381,796,800 | ||
| 2. 복구충당부채 | 11,884,267 | 13,330,121 | ||
| 부 채 총 계 | 710,189,312 | 580,501,272 | ||
| 자 본 | ||||
| Ⅰ. 자본금 | 1,795,337,500 | 1,787,337,500 | ||
| 1. 보통주자본금 | 1,325,445,000 | 1,317,445,000 | ||
| 2. 우선주자본금 | 469,892,500 | 469,892,500 | ||
| Ⅱ. 자본잉여금 | 7,362,327,979 | 7,306,327,979 | ||
| 1. 주식발행초과금 | 7,362,327,979 | 7,306,327,979 | ||
| Ⅲ. 자본조정 | 49,766,435 | 36,506,504 | ||
| 1. 주식매입선택권 | 49,766,435 | 36,506,504 | ||
| Ⅳ. 결손금 | 9,105,661,740 | 8,004,323,518 | ||
| 1. 미처리결손금 | (9,105,661,740) | (8,004,323,518) | ||
| 자 본 총 계 | 101,770,174 | 1,125,848,465 | ||
| 부 채 및 자 본 총 계 | 811,959,486 | 1,706,349,737 | ||
- 손익계산서
| < 손 익 계 산 서 > |
|
| 제 18(당) 기 2021년 1월 1일부터 2021년 12월 31일까지 | |
| 제 17(당) 기 2020년 1월 1일부터 2020년 12월 31일까지 | |
| 주식회사 바이오시네틱스 | (단위 : 원) |
| 과 목 | 제 18(당) 기 | 제 17(당) 기 | ||
|---|---|---|---|---|
| Ⅰ. 매출액 | 569,576,782 | 229,187,298 | ||
| 1. 제품매출 | 498,076,782 | 212,987,298 | ||
| 2. 용역매출 | 71,500,000 | 16,200,000 | ||
| 3. 로열티매출 | - | - | ||
| Ⅱ. 매출원가 | 332,480,367 | 174,579,305 | ||
| 1. 제품매출원가 | 312,925,075 | 157,643,550 | ||
| 기초제품재고액 | 86,236,287 | 76,768,057 | ||
| 당기제품제조원가 | 295,346,932 | 169,245,799 | ||
| 타계정으로 대체 | (11,533,320) | (2,134,019) | ||
| 제품재고평가손실 | 9,490,710 | - | ||
| 기말제품재고액 | (66,615,534) | (86,236,287) | ||
| 2. 기타매출원가 | 19,555,292 | 16,935,755 | ||
| Ⅲ. 매출총이익 | 237,096,415 | 54,607,993 | ||
| Ⅳ. 판매비와관리비 | 1,310,787,090 | 1,332,085,923 | ||
| 1. 급여 | 313,285,896 | 359,006,120 | ||
| 2. 퇴직급여 | 42,885,238 | 10,704,191 | ||
| 3. 복리후생비 | 9,062,562 | 11,499,696 | ||
| 4. 여비교통비 | 1,096,297 | 3,318,325 | ||
| 5. 접대비 | 534,500 | 1,144,700 | ||
| 6. 통신비 | 2,682,914 | 2,347,609 | ||
| 7. 수도광열비 | 2,208,073 | 1,832,304 | ||
| 8. 세금과공과 | 523,230 | 388,230 | ||
| 9. 감가상각비 | - | 2,773,041 | ||
| 10. 무형자산상각비 | - | 369,966 | ||
| 11. 지급임차료 | 28,678,885 | 31,628,553 | ||
| 12. 수선비 | 2,705,364 | 5,150,000 | ||
| 13. 보험료 | 3,866,000 | 1,200,000 | ||
| 14. 경상연구개발비 | 697,059,121 | 723,041,300 | ||
| 15. 운반비 | 4,060,330 | 3,876,441 | ||
| 16. 교육훈련비 | 348,000 | 28,000 | ||
| 17. 도서인쇄비 | 345,000 | 298,880 | ||
| 18. 소모품비 | 4,556,113 | 2,981,837 | ||
| 19. 지급수수료 | 170,626,870 | 138,356,812 | ||
| 20. 건물관리비 | 8,426,788 | 7,001,730 | ||
| 21. 판매촉진비 | 17,835,909 | 25,138,188 | ||
| Ⅴ. 영업손실 | 1,073,690,675 | 1,277,477,930 | ||
| Ⅵ. 영업외수익 | 5,394,011 | 16,364,481 | ||
| 1. 이자수익 | 1,768,860 | 16,277,041 | ||
| 2. 잡이익 | 3,625,151 | 87,440 | ||
| Ⅶ. 영업외비용 | 33,041,558 | 577,120,441 | ||
| 1. 이자비용 | 856,225 | 451,419 | ||
| 2. 외환차손 | - | 220,730 | ||
| 3. 조업도손실 | 10,610,019 | 131,141,924 | ||
| 4. 유형자산손상차손 | - | 93,006,449 | ||
| 5. 무형자산손상차손 | 20,618,397 | 352,299,482 | ||
| 6. 잡손실 | 956,917 | 437 | ||
| Ⅷ. 법인세비용차감전순손실 | 1,101,338,222 | 1,838,233,890 | ||
| Ⅸ. 법인세비용 | - | - | ||
| Ⅹ. 당기순손실 | 1,101,338,222 | 1,838,233,890 | ||
| Ⅵ. 주당손익 | ||||
| 기본주당손실 | 415 | 698 | ||
- 자본변동표
| < 자 본 변 동 표 > |
|
| 제 18(당) 기 2021년 1월 1일부터 2021년 12월 31일까지 | |
| 제 17(당) 기 2020년 1월 1일부터 2020년 12월 31일까지 | |
| 주식회사 바이오시네틱스 | (단위 : 원) |
| 과 목 | 자 본 금 | 자 본 잉여금 |
자 본 조 정 |
이 익 잉여금 |
총 계 |
|---|---|---|---|---|---|
| 2020.1.1 (보고금액) | 1,787,337,500 | 7,306,327,979 | 26,243,921 | (6,166,089,628) | 2,953,819,772 |
| 주식매입선택권 인식 | - | - | 10,262,583 | - | 10,262,583 |
| 당기순손실 | - | - | - | (1,838,233,890) | (1,838,233,890) |
| 2020.12.31 (당기말) | 1,787,337,500 | 7,306,327,979 | 36,506,504 | (8,004,323,518) | 1,125,848,465 |
| 2021.1.1 (보고금액) | 1,787,337,500 | 7,306,327,979 | 36,506,504 | (8,004,323,518) | 1,125,848,465 |
| 유상증자(주식매입선택권) | 8,000,000 | 56,000,000 | - | - | 64,000,000 |
| 주식매입선택권 인식 | - | - | 13,259,931 | - | 13,259,931 |
| 당기순손실 | - | - | - | (1,101,338,222) | (1,101,338,222) |
| 2021.12.31 (당기말) | 1,795,337,500 | 7,362,327,979 | 49,766,435 | (9,105,661,740) | 101,770,174 |
- 현금흐름표
| < 현 금 흐 름 표 > |
|
| 제 18(당) 기 2021년 1월 1일부터 2021년 12월 31일까지 | |
| 제 17(당) 기 2020년 1월 1일부터 2020년 12월 31일까지 | |
| 주식회사 바이오시네틱스 | (단위 : 원) |
| 과 목 | 제 18(당) 기 | 제 17(당) 기 | ||
|---|---|---|---|---|
| Ⅰ. 영업활동으로 인한 현금흐름 | (834,108,800) | (995,154,212) | ||
| 1. 당기순손실 | (1,101,338,222) | (1,838,233,890) | ||
| 2. 현금의 유출이 없는 비용 등의 가산 | 217,447,497 | 690,159,519 | ||
| 가. 감가상각비 | 111,061,511 | 175,367,619 | ||
| 나. 무형자산상각비 | - | 26,823,690 | ||
| 다. 퇴직급여 | 89,720,303 | 59,507,407 | ||
| 라. 주식보상비용 | - | 10,262,583 | ||
| 마. 복구충당부채 전입액 | 856,225 | 451,419 | ||
| 바. 무형자산손상차손 | 20,618,397 | 324,740,352 | ||
| 사. 유형자산손상차손 | (18,068,870) | 93,006,449 | ||
| 아. 주식매입선택권 | 13,259,931 | |||
| 3. 영업활동으로 인한 자산부채의 변동 | 49,781,925 | 152,920,159 | ||
| 가. 매출채권의 감소(증가) | 7,657,000 | (43,559,000) | ||
| 나. 미수금의 감소(증가) | 20,755,939 | 209,384,356 | ||
| 다. 선급금의 감소(증가) | (20,226,000) | 72,580,250 | ||
| 라. 당기법인세자산의 감소(증가) | 2,234,310 | 4,869,920 | ||
| 마. 재고자산의 증가 | (2,052,915) | (8,028,897) | ||
| 바. 미지급금의 감소 | 47,455,748 | (5,035,040) | ||
| 사. 예수금의 증가 | (5,084,410) | 352,090 | ||
| 아. 선수금의 증가(감소) | 27,249,116 | 250,884 | ||
| 자. 선수수익의 감소 | - | - | ||
| 차. 미지급비용의 증가(감소) | 10,516,147 | (24,890,324) | ||
| 카. 퇴직금 지급 | (38,723,010) | (25,504,080) | ||
| 타. 매입채무의 증가(감소) | - | (27,500,000) | ||
| Ⅱ. 투자활동으로 인한 현금흐름 | 11,464,103 | 989,675,597 | ||
| 1. 투자활동으로 인한 현금유입액 | - | 1,000,000,000 | ||
| 가. 단기금융상품의 감소 | - | 1,000,000,000 | ||
| 2. 투자활동으로 인한 현금유출액 | (11,464,103) | (10,324,403) | ||
| 가. 기계장치의 취득 | - | (9,000,000) | ||
| 나. 비품의 취득 | - | - | ||
| 다. 구축물의 취득 | (32,000,000) | - | ||
| 라. 건설중인무형자산의 취득 | 20,618,397 | (1,324,403) | ||
| 마. 임차보증금의 증가 | (82,500) | - | ||
| Ⅲ. 재무활동으로인한 현금흐름 | 64,000,000 | - | ||
| 1. 재무활동으로 인한 현금유입액 | 64,000,000 | - | ||
| 가. 정부보조금의 수령 | - | - | ||
| 나. 유상증자(주식매입선택권) | 64,000,000 | - | ||
| 2. 재무활동으로 인한 현금유출액 | - | - | ||
| Ⅳ. 현금의 증가(감소) (Ⅰ+ Ⅱ + Ⅲ) |
(758,644,697) | (5,478,615) | ||
| Ⅴ. 기초의 현금 |
1,098,559,672 | 1,104,038,287 | ||
| Ⅵ. 기말의 현금 |
339,914,975 | 1,098,559,672 | ||
- 최근 2사업연도의 배당에 관한 사항
해당사항 없습니다.
□ 이사의 선임
가. 후보자의 성명ㆍ생년월일ㆍ추천인ㆍ최대주주와의 관계ㆍ사외이사후보자 등 여부
| 후보자성명 | 생년월일 | 사외이사 후보자여부 |
감사위원회 위원인 이사 분리선출 여부 |
최대주주와의 관계 | 추천인 |
|---|---|---|---|---|---|
| 김갑식 | 1966.12.01 | 부 | - | 본인 | 이사회 |
| 총 ( 1 ) 명 | |||||
나. 후보자의 주된직업ㆍ세부경력ㆍ해당법인과의 최근3년간 거래내역
| 후보자성명 | 주된직업 | 세부경력 | 해당법인과의 최근3년간 거래내역 |
|
|---|---|---|---|---|
| 기간 | 내용 | |||
| 김갑식 | 대표이사 | 2004년 ~ 현재 | 현) (주)바이오시네틱스 대표이사 전) (주)바이오시네틱스 대표이사 |
- |
다. 후보자의 체납사실 여부ㆍ부실기업 경영진 여부ㆍ법령상 결격 사유 유무
| 후보자성명 | 체납사실 여부 | 부실기업 경영진 여부 | 법령상 결격 사유 유무 |
|---|---|---|---|
| 김갑식 | 해당없음 | 해당없음 | 해당없음 |
라. 후보자의 직무수행계획(사외이사 선임의 경우에 한함)
| 해당사항 없습니다. |
마. 후보자에 대한 이사회의 추천 사유
□ 사내이사 김갑식
| 김갑식 사내이사 후보자는 당사의 대표이사로 오랜기간 재직하면서 다양한 경험과 고도의 전문성을 축적해 왔으며, 이를 기반으로 회사의 경영을 감독하고 이사회의 의사결정에 기여할 것으로 판단되어 이사회에서 재선임을 추천함. |
확인서
 |
|
. |
※ 기타 참고사항
□ 이사의 보수한도 승인
가. 이사의 수ㆍ보수총액 내지 최고 한도액
(당 기)
| 이사의 수 (사외이사수) | 5명( 0명 ) |
| 보수총액 또는 최고한도액 | 5억원 |
(전 기)
| 이사의 수 (사외이사수) | 5명( 0명 ) |
| 실제 지급된 보수총액 | 16백만원 |
| 최고한도액 | 5억원 |
※ 기타 참고사항
실제 지급된 보수총액은 모두 포함한 금액입니다.
□ 감사의 보수한도 승인
가. 감사의 수ㆍ보수총액 내지 최고 한도액
(당 기)
| 감사의 수 | 1명 |
| 보수총액 또는 최고한도액 | 1억원 |
(전 기)
| 감사의 수 | 1명 |
| 실제 지급된 보수총액 | 5백만원 |
| 최고한도액 | 1억원 |
※ 기타 참고사항
해당사항 없습니다.
IV. 사업보고서 및 감사보고서 첨부
가. 제출 개요
| 제출(예정)일 | 사업보고서 등 통지 등 방식 |
|---|---|
| 2022년 03월 23일 | 1주전 회사 홈페이지 게재 |
나. 사업보고서 및 감사보고서 첨부
1) 사업보고서 및 감사보고서는 상기 제출(예정)일까지 금융감독원 공시홈페이지 (http://dart.fss.or.kr)와 당사 홈페이지(http://www.bio-synectics.com) 공지사항에 게재할 예정입니다.
2) 제출(예정)일 게재될 사업보고서는 주주총회 이전 보고서 입니다.
주주총회에서 부결/수정이 발생할 경우 정정보고서를 금융감독원 전자공시
시스템에 공시 예정입니다. 주주총회 이후 정정공시 여부를 확인 부탁 드립니다.
(금융감독원 전자공시시스템 - 정기공시)
※ 참고사항
|
1. 주주총회 개최일 : 2022년 3월 31일 |