 |
|
확인서 정정 |
정 정 신 고 (보고)
| 2021년 11월 15일 |
1. 정정대상 공시서류 : 3분기 사업보고서
2. 정정대상 공시서류의 최초제출일 : 2021년 11월 15일
3. 정정사항
| 항 목 | 정정사유 | 정 정 전 | 정 정 후 |
|---|---|---|---|
| 재무제표 | 오류 | - | 재무제표 수정 |
*) 사업보고서 본문의 요약재무제표 및 재무제표는 수정된 재무제표입니다.
【 대표이사 등의 확인 】
 |
|
확인서 정정 |
분 기 보 고 서
(제 14기 3분기)
| 사업연도 | 2021년 01월 01일 | 부터 |
| 2021년 09월 30일 | 까지 |
| 금융위원회 | |
| 한국거래소 귀중 | 2021년 11월 15일 |
| 제출대상법인 유형 : | 주권상장법인 |
| 면제사유발생 : | 해당사항 없음 |
| 회 사 명 : | 주식회사 알테오젠 |
| 대 표 이 사 : | 박순재 |
| 본 점 소 재 지 : | 대전시 유성구 유성대로1628번길 62(전민동) |
| (전 화) 042-384-8780 | |
| (홈페이지) http://www.alteogen.com | |
| 작 성 책 임 자 : | (직 책) 경영기획상무 (성 명) 이중석 |
| (전 화) 042-384-8780 | |
【 대표이사 등의 확인 】
 |
|
대표이사 확인서 |
I. 회사의 개요
1. 회사의 개요
가. 연결대상 종속회사 개황
| (단위 : 사) |
| 구분 | 연결대상회사수 | 주요 종속회사수 |
|||
|---|---|---|---|---|---|
| 기초 | 증가 | 감소 | 기말 | ||
| 상장 | - | - | - | - | - |
| 비상장 | 4 | - | 1 | 3 | 2 |
| 합계 | 4 | - | 1 | 3 | 2 |
| ※상세 현황은 '상세표-1. 연결대상 종속회사 현황(상세)' 참조 |
가-1. 연결대상회사의 변동내용
| 구 분 | 자회사 | 사 유 |
|---|---|---|
| 신규 연결 |
- | - |
| - | - | |
| 연결 제외 |
(주)알토스바이오 사이언스 |
피합병으로 소멸 (2021.08.12자로 종속회사인 주식회사 엘에스메디텍을 존속회사로 하는 피흡수합병으로 소멸) |
| - | - |
나. 회사의 법적ㆍ상업적 명칭
당 회사는 '주식회사 알테오젠' 이라 표기 합니다. 또한 영문으로는 'ALTEOGEN Inc.'이라 표기합니다.
다. 설립일자 및 존속기간
당 회사는 2008년 5월 13일에 설립되었으며, 계속사업기업으로 존속기간이 정해져 있지 않습니다.
라. 본사의 주소, 전화번호, 홈페이지 주소
○ 주소 : 대전시 유성구 유성대로 1628번길 62
○ 전화번호 : 032-384-8780
○ 홈페이지 : http://www.alteogen.com
마. 중소기업 등 해당 여부
| 중소기업 해당 여부 | 해당 | |
| 벤처기업 해당 여부 | 해당 | |
| 중견기업 해당 여부 | 미해당 | |
바. 주요 사업의 내용
당사는 바이오의약품 연구, 개발 및 판매를 주요 사업으로 영위하고 있으며,
자세한 사항은 "Ⅱ.사업의 내용"을 참조하시기 바랍니다.
사. 신용평가에 관한 사항
| 평가일 | 결산일 | 평가회사 (신용평가등급범위) |
신용등급 | 등급내용 |
| 2021-05-13 | 2020-12-31 | 한국기업데이터 (AAA ~ D) | BBB- | 양호 |
아. 회사의 주권상장(또는 등록ㆍ지정)여부 및 특례상장에 관한 사항
| 주권상장 (또는 등록ㆍ지정)여부 |
주권상장 (또는 등록ㆍ지정)일자 |
특례상장 등 여부 |
특례상장 등 적용법규 |
|---|---|---|---|
| 코스닥시장 | 2014년 12월 12일 | 기술성장기업의 코스닥시장 상장 | 코스닥시장상장규정 제7조2항 |
2. 회사의 연혁
가. 회사의 본점소재지 및 그 변경
당사는 2015년 8월 27일 본점을 대전시 유성구 유성대로 1662, 305호에서 대전시 유성구 유성대로 1628번길 62로 변경했습니다.
나. 경영진의 중요한 변동
| 변동일자 | 주총종류 | 선임 | 임기만료 또는 해임 |
|
|---|---|---|---|---|
| 신규 | 재선임 | |||
| 2019년 03월 27일 | 정기주총 | - | 대표이사 박순재 | - |
| 2020년 03월 26일 | 정기주총 | - | 사내이사 정혜신 사내이사 박문환 |
- |
| 2021년 03월 29일 | 정기주총 | 사내이사 이승주 사내이사 강상우 사외이사 최종인 사외이사 고인영 기타비상무이사 김양우 |
- | 사외이사 전형식 |
주) 제13기 정기주주총회(21.03.29)에서 총 6명의 이사중 5명이 신규선임됨
다. 최대주주의 변동
해당사항 없음
라. 상호의 변경
해당사항 없음
마. 회사가 화의, 회사정리절차 그 밖에 이에 준하는 절차를 밟은 적이 있거나 현재 진행중인 경우 그 내용과 결과
해당사항 없음
바. 회사가 합병등을 한 경우 그 내용
해당사항 없음
사. 회사의 업종 또는 주된 사업의 변화
해당사항 없음
아. 그 밖에 경영활동과 관련된 중요한 사항의 발생내용
|
일자 |
내용 |
|---|---|
|
2008.05.13 |
회사 설립 |
|
2008.12.26 |
연구개발전담부서 인정(한국산업기술진흥협회 제2008250266호) |
|
2009.07.17 |
기업부설연구소 인정(제20092108282호) |
|
2009.08.24 |
벤처기업 확인(1차, 기술평가보증기업, 제20090107651호) |
|
2010.06.01 |
박순재 대표이사 취임 |
|
2010.07.30 |
벤처캐피탈 투자 유치 |
|
2010.09.10 |
CJ제일제당㈜에 지속형 성장호르몬 라이센스아웃 계약 체결 |
|
2010.12.16 |
박순재 대표이사, 한국공학한림원 "대한민국 100대 기술 및 주역" 수상 |
|
2011.06.01 |
지식경제부 산업융합원천과제 선정(ADC, 항체-약물접합 치료제) |
|
2011.06.01 |
지역 Star 기업 선정(지식경제부) |
|
2011.06.11 |
항체 바이오시밀러(엔브렐, 허셉틴) 라이센스아웃 계약 체결(브라질 크리스탈리아) |
|
2011.07.15 |
본사 이전(대전 바이오벤처타운) |
|
2011.08.24 |
벤처기업 확인(2차, 벤처투자기업, 제20110300189호) |
|
2011.11.28 |
항체 바이오시밀러(휴미라) 라이센스아웃 계약 체결(브라질 크리스탈리아) |
|
2012.03.06 |
자회사 ㈜알토스바이오사이언스, 동물의약품 라이센스아웃 계약 체결(브라질 UQ) |
|
2012.04.12 |
병역지정업체(벤처기업부설연구소) 선정 (병무청) |
|
2012.09.10 |
NexP™ 융합기술 관련 특허 등록(대한민국) |
|
2012.11.27 |
지역발전 유공기업 표창(대전광역시) |
|
2013.01.26 |
벤처캐피탈 투자 유치 |
|
2013.05.24 |
중기청 글로벌 강소기업 육성사업 선정(항체 바이오시밀러) |
|
2013.08.09 |
코스닥시장 상장을 위한 대표주관계약 체결(한국투자증권) |
|
2013.08.24 |
벤처기업 확인(3차, 벤처투자기업, 제20130300194호) |
|
2013.10.24 |
NexP™ 융합기술 관련 특허 등록(호주) |
|
2014.01.10 |
NexP™ 융합기술 관련 특허 등록(러시아) |
|
2014.02.12 |
항체 바이오시밀러(아일리아) 라이센스아웃 계약 체결(일본 Kissei 제약) |
|
2014.02.22 |
일본 Kissei 제약 지분투자 유치 |
|
2014.02.18 |
"IP스타기업" 선정(특허청) |
|
2014.03.03 |
NexP™ 융합기술 관련 특허 등록(멕시코) |
|
2014.05.27 |
유전자 재조합 A1AT 관련 특허 등록(대한민국) |
|
2014.07.09 |
엔브렐 바이오시밀러 제형특허 등록(대한민국) |
|
2014.08.06 |
한국거래소 기술평가 승인 |
|
2014.09.01 |
코스닥시장 상장을 위한 상장예비심사청구서 제출 |
| 2014.12.12 | 코스닥시장 상장 |
| 2014.12.23 | "두뇌역량우수전문기업" 선정(산업통상자원부) |
|
2015.04.21 |
NexP™ 융합기술 관련 특허 등록(일본) |
|
2015.04.21 |
NexP™ 융합기술 관련 특허 등록(미국) |
| 2015.06.09 | 유전자 재조합 A1AT 관련 특허 등록(미국) |
| 2015.07.29 | 항체-약물 접합 기술(ADC) 관련 특허 등록(대한민국) |
| 2015.08.20 | 유전자 재조합 A1AT 관련 특허 등록(호주) |
| 2015.08.27 | 본점 소재지 변경(대전시 유성구 전민동 → 대전시 유성구 전민동) |
| 2015.09.18 | 지속형 인성장호르몬(hGH-NexP™) 임상1상 시험 종료 |
| 2015.10.09 |
ADC 유방암치료제(항체-약물접합 치료제) 라이센스아웃 계약 체결(중국 3SBio) |
| 2015.12.07 | 유전자 재조합 A1AT 관련 특허 등록(러시아) |
| 2015.12.08 | NexP™ 융합기술 관련 특허 등록(캐나다) |
| 2015.12.11 | 유전자 재조합 A1AT 관련 특허 등록(중국) |
| 2016.02.27 | 허셉틴 바이오시밀러 임상1상 승인(캐나다) |
| 2016.03.18 | NexMab™ ADC 관련 특허 등록(러시아) |
| 2016.05.31 | NexMab™ ADC 관련 특허 등록(호주) |
| 2016.06.01 | 두뇌역량우수전문기업기술개발 과제 선정 |
| 2016.06.03 | (주)엘에스메디텍 지분 100% 및 경영권 인수 |
| 2016.07.04 | 유전자재조합 A1AT 관련 특허 등록(캐나다) |
| 2016.09.08 | 3자배정 유상증자 9,999백만원(보통주, KB-솔리더스 글로벌헬스케어펀드 대상) |
| 2016.09.09 | 유전자 재조합 A1AT 관련 특허 등록(일본) |
|
2016.09.21 |
엔브렐 바이오시밀러 제형특허 등록(미국) |
| 2016.12.22 | 허셉틴 바이오시밀러 임상1상 완료(캐나다) |
| 2017.02.02 | 휴미라 바이오시밀러 관련 제형특허 등록(한국) |
| 2017.02.02 | NexMab™ ADC 관련 특허 등록(한국) |
| 2017.03.07 | NexP™ 융합기술 관련 특허 등록(중국) |
| 2017.03.14 | 고당화된 지속형 인간 성장호르몬 단백질 및 이의 제조방법(중국 특허) |
| 2017.03.29 | 허셉틴 바이오시밀러 라이센스아웃 계약 체결(중국 QiLu 사) |
| 2017.06.16 | ALT-P7(HER2 양성 유방암 ADC치료제) 1상 임상시험 계획 승인 |
| 2017.07.11 | ALT-P1(재조합 지속형 인성장호르몬) 1/2상 임상시험 계획 승인 |
| 2017.07.21 | 신규한 알파-1 안티트립신 변이체, 이의 제조방법 및 용도(유럽 특허) |
| 2017.07.26 | 신규한 알파-1 안티트립신 변이체, 이의 제조방법 및 용도(멕시코 특허) |
| 2017.08.23 |
유방암 항체-약물접합(ADC) 바이오베터 국내 최초 임상1상 개시 |
| 2017.09.12 | 중국의 차세대 항체 기업인 LEVENA Biopharma 와 ADC 공동개발을 위한 업무 협약 |
| 2017.09.28 | 디엠바이오 와 황반변성치료제 위탁생산 계약 체결 |
| 2017.10.10 |
유방암 항체-약물접합(ADC) 치료제 범부처신약개발사업단 국가신약개발사업 선정 |
| 2017.10.13 | 단백질 안정화용 조성물 및 이를 포함하는 약제학적 제제(미국 특허) |
| 2017.10.19 | 고당화된 지속형 인간 성장호르몬 단백질 및 이의 제조방법(일본 등록) |
| 2017.10.31 |
NexP™ 융합 원천 기술, 지속형 인간 성장호르몬 임상2상 개시 |
| 2017.12.06 | 아일리아(Eylea) 바이오시밀러 제제 제형 기술 국내 특허 등록 |
| 2017.12.06 | 2017 산업부 바이오분야 우수 기업 산업부 장관상 수상 |
| 2017.12.22 | 무상증자(추가 상장) |
| 2017.12.23 |
NexP™ 융합 원천 기술에 성장호르몬 수용체 길항제를 이용한 말단치료제 공동 개발(세브란스) |
| 2017.12.26 | 고당화된 지속형 인간 성장호르몬 단백질 및 이의 제조방법(유럽 특허) |
| 2018.01.19 | 시스테인 잔기를 포함하는 모티프가 결합된 변형항체, 상기 변형항체를 포함하는 변형항체-약물 접합체 및 그 제조방법(멕시코 특허) |
| 2018.04.10 | IgG Fc 도메인을 가지는 융합 단백질의 안정한 액상 제제 (미국 특허) |
| 2018.04.20 | 320억원 제3자배정 유상증자(제2회 기명식 전환우선주) 발행 |
| 2018.06.15 | 자회사 신규법인 설립(주식회사 세레스에프앤디) |
| 2018.07.14 | 시스테인 잔기를 포함하는 모티프가 결합된 변형항체, 상기 변형항체를 포함하는 변형항체-약물 접합체 및 그 제조방법(중국 특허) |
| 2018.07.25 | 유형자산 취득 오송첨단의료복합단지내 연구시설 용지 |
| 2018.07.25 | 피하주사용 항체치료제 원천기술 특허 출원 |
| 2018.08.02 | ADC 위암치료제(ALT-P7) 미국 FDA 희귀의약품 지정 |
| 2018.08.30 | 체내 지속성을 유지함으로 체내 반감기가 증가된 단백질 또는 펩티드 유합체, 및 이를 이용하여 체내 반감기를 증시키는 방법(인도 특허) |
| 2018.09.18 | 알테오젠 대한민국 바이오의약품 대상 수상 |
| 2018.11.14 | 항체-약물접합(ADC) 유방암치료제 성과 월드ADC 학회 발표 |
| 2018.12.18 | 항체-약물접합(ADC) 유방암치료제 생산을 위한 DGMIF와 공동협력 계약체결 |
| 2018.12.19 | 글로벌 라이센스아웃을 위한 글로벌 CBO 전문가 영입 |
| 2019.01.02 | 아일리아(Eylea) 바이오시밀러 개발을 위한 융합단백질의 생산방법 등록(국내 특허) |
| 2019.01.04 | 보건복지부 혁신형 제약기업 선정 |
| 2019.02.22 | 아일리아(Eylea) 바이오시밀러 국내 임상1상 IND 신청 |
| 2019.03.26 | 허셉틴SC 및 피하주사용 항암제 국내 특허 출원 |
| 2019.04.12 | 항체-약물접합(ADC) 유방암치료제 2019 PEGS 보스톤 학회 발표 |
| 2019.05.13 | 아일리아(Eylea) 바이오시밀러 융합 단백질의 생산방법 특허 등록(러시아) |
| 2019.05.21 | 피하주사용(ALT-B4) 항체치료제 원천기술 글로벌 제약사와 라이센스 옵션계약 체결 |
| 2019.05.22 | 아일리아(Eylea) 바이오시밀러 최초 국내 임상1상 IND 개시 승인 |
| 2019.06.10 | 아일리아(Eylea) 바이오시밀러 융합 단백질의 생산방법 특허 등록(일본) |
| 2019.06.25 | 피하주사용 허셉틴SC 국내 특허 출원 |
| 2019.07.03 | 허셉틴 바이오시밀러 중국 임상 IND 개시 승인 |
| 2019.07.12 | 아일리아(Eylea) 바이오시밀러 융합 단백질의 생산방법 특허 등록(호주) |
| 2019.07.15 | 변형항체를 포함하는 항체-약물 접합체 국내 특허 등록 |
| 2019.07.22 | 지속형 인성장호르몬 크리스탈리아(Cristalia) 사와 공동개발 및 기술이전계약 체결 |
| 2019.07.25 | 신규한 인간 히알루로니다제(ALT-B4) 개발 범부처신약개발사업단 R&D 지원과제 선정 |
| 2019.07.26 | 피하주사(SC) 원천 기술인 인간 히알루로니다제 해외 PCT출원 |
| 2019.07.31 | 피하주사(SC) 원천 기술 인간 히알루로니다제 GMP 생산 CMO 계약 |
| 2019.10.16 | 자회사 (주)세레스에프앤디 타크로리무스 공급을 위한 업무협약 |
| 2019.10.31 | 디엠바이오와 아일리아(Eylea) 바이오시밀러 글로벌 임상3상을 위한 생산 업무협약 |
| 2019.11.29 | 피하주사(SC) 원천기술 인간 히알루로니다제 10대 글로벌 제약회사와 기술이전 계약체결 |
| 2020.01.27 | 인간 히알루로니다제 집단에 대한 권리 추가 특허 |
| 2020.02.10 | 아일리아(Eylea) 바이오시밀러 국내 임상 첫 환자 투입 |
|
2020.02.21 |
지속형 인성장호르몬(ALT-P1), 인도 글로벌 임상1상 개시승인 |
| 2020.02.24 | 한국거래소 2019년도 코스닥 공시 우수법인 및 공시 업무 유공자 선정 |
| 2020.03.17 | ADC 유방암치료제(ALT-P7) 국내 최초 국내 임상1상 시험완료 |
| 2020.03.24 | 허셉틴SC, 리툭산SC, 키트루다SC 등 피하주사용 항체치료제 PCT 국제 특허 출원 |
| 2020.03.25 | 한림제약과 아일리아(Eylea) 바이오시밀러 국내판매를 위한 업무협약 |
| 2020.04.01 | ADC 유방암치료제 국내 임상1상 결과 초록 2020 ASCO 채택 |
| 2020.04.03 | 아일리아(Eylea) 바이오시밀러 제형특허 등록(캐나다) |
| 2020.04.06 | 아일리아(Eylea) 바이오시밀러 제형특허 등록(호주) |
| 2020.05.29 | Abstract Notification 2020 ASCO annual meeting ADC 유방암치료제 임상1상 내용 발표 |
| 2020.06.24 | 시스테인 잔기를 포함하는 모티프가 결합된 변형항체(유럽 특허) |
| 2020.06.24 | 피하주사(SC) 하이브로자임 기술 10대 글로벌제약사와 비독점적 기술이전계약 체결 |
| 2020.07.01 | 한국거래소 "2020년 코스닥 라이징스타" 로 선정 |
| 2020.07.10 | 혈액 응고 인자 VII/VIIa 융합단백질의 제조방법 국내 특허 |
| 2020.07.24 | 무상증자(신주배정기준일) |
| 2020.08.28 | 효소 활성과 열 안정성이 증가한 새로운 히알루론산 가수분해 효소 및 이의 제조방법 국내 특허 등록 |
| 2020.10.14 | 신규한 성장호르몬 수용체 길항제 및 이의 융합단백질 국내 특허 등록 |
| 2020.10.15 | 바이오시밀러 개발/임상 전문 자회사 (주)알토스바이오로직스 설립 |
| 2020.10.21 | 아일리아(Eylea) 바이오시밀러 IgG Fc 도메인을 가지는 융합 단백질의 생산방법 등록(일본 특허) |
| 2020.10.21 | 한국 IR 대상 우수기업 선정 |
| 2020.11.04 | 제3자배정 유상증자(제3회 기명식 전환우선주) 결정 |
| 2020.12.14 | 제3자배정 유상증자(제4회 기명식 전환우선주) 결정 |
| 2021.01.07 | 피하주사(SC) 하이브로자임 기술 Intas Pharmaceuticals 사와 라이센스아웃 계약 체결 |
| 2021.01.15 | (주)알토스바이오로직스 시리즈 A 605억원 투자유치 완료 |
| 2021.01.25 | 기존의 인간 히알루로니다제 추가 특허 PCT출원으로 독점 권리 유지 및 확대 |
| 2021.01,28 | 지속형 인간성장호르몬 글로벌 제품 출시를 위한 임상 진입 |
| 2021.02.25 | 피하주사(SC) 원천 기술 인간히알루로니다제 유럽 CMO 생산 |
|
2021.02.26 |
대한민국신약개발상 수상(기술이전 부문, 한국신약개발연구조합) |
| 2021.03.08 | (주)알토스바이오로직스 한림MS와 아일리아(Eylea) 바이오시밀러 국내 공급 판매 계약 체결 |
| 2021.03.10 | 무상증자 50% 결정 |
| 2021.04.16 | 아일리아(Eylea) 바이오시밀러 완제품 제형 프리필드 실린지(PFS) 특허 출원 |
|
2021.06.28 |
지속형 인성장호르몬(ALT-P1), 인도 글로벌 임상1상 시험종료(LPO) |
|
2021.06.28 |
"2021년 코스닥 라이징스타" 선정 (한국거래소) |
|
2021.08.03 |
ADC 유방암치료제(ALT-P7) 임상1상 시험결과보고서 (CSR) 완료 |
|
2021.08.04 |
아일리아 바이오시밀러(ALT-L9) 임상1상 시험결과보고서 (CSR) 완료 |
|
2021.09.16 |
재조합 인간히알루로니다아제 완제품 테르가제 품목허가를 위한 임상 IND 승인 |
3. 자본금 변동사항
가. 자본금 변동추이
| (단위 : 원, 주) |
| 종류 | 구분 | 당분기말 (2021.09.30) |
13기 (2020년말) |
12기 (2019년말) |
|---|---|---|---|---|
| 보통주 | 발행주식총수 | 42,264,250 | 28,082,900 | 13,896,750 |
| 액면금액 | 500 | 500 | 500 | |
| 자본금 | 21,132,125,000 | 14,041,450,000 | 6,948,375,000 | |
| 우선주 | 발행주식총수 | 1,029,015 | 203,385 | - |
| 액면금액 | 500 | 500 | - | |
| 자본금 | 514,507,500 | 101,692,500 | - | |
| 기타 | 발행주식총수 | - | - | - |
| 액면금액 | - | - | - | |
| 자본금 | - | - | - | |
| 합계 | 자본금 | 21,646,632,500 | 14,143,142,500 | 6,948,375,000 |
4. 주식의 총수 등
가. 주식의 총수 현황
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 비고 | |||
|---|---|---|---|---|---|
| 보통주 | 우선주 | 합계 | |||
| Ⅰ. 발행할 주식의 총수 | 80,000,000 | 20,000,000 | 100,000,000 | - | |
| Ⅱ. 현재까지 발행한 주식의 총수 | 42,264,250 | 2,119,295 | 44,383,545 | - | |
| Ⅲ. 현재까지 감소한 주식의 총수 | - | 1,090,280 | 1,090,280 | - | |
| 1. 감자 | - | - | - | - | |
| 2. 이익소각 | - | - | - | - | |
| 3. 상환주식의 상환 | - | - | - | - | |
| 4. 기타 | - | 1,090,280 | 1,090,280 | 전환우선주의 보통주 전환 |
|
| Ⅳ. 발행주식의 총수 (Ⅱ-Ⅲ) | 42,264,250 | 1,029,015 | 43,293,265 | - | |
| Ⅴ. 자기주식수 | 9,010 | 2 | 9,012 | 주) | |
| Ⅵ. 유통주식수 (Ⅳ-Ⅴ) | 42,255,240 | 1,029,013 | 43,284,253 | - | |
주) 당사는 2021년 4월 20일자로 상법 421조의 2에 따라 무상증자에 따른 단주(端株)의 처리를 위하여 필요한 자기주식을 취득함 (보통주식 9,010주 및 3회차 우선주식 2주)
나. 자기주식 취득 및 처분 현황
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 주) |
| 취득방법 | 주식의 종류 | 기초수량 | 변동 수량 | 기말수량 | 비고 | ||||
|---|---|---|---|---|---|---|---|---|---|
| 취득(+) | 처분(-) | 소각(-) | |||||||
| 배당 가능 이익 범위 이내 취득 |
직접 취득 |
장내 직접 취득 |
- | - | - | - | - | - | - |
| - | - | - | - | - | - | - | |||
| 장외 직접 취득 |
- | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 공개매수 | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 소계(a) | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 신탁 계약에 의한 취득 |
수탁자 보유물량 | - | - | - | - | - | - | - | |
| - | - | - | - | - | - | - | |||
| 현물보유물량 | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 소계(b) | - | - | - | - | - | - | - | ||
| - | - | - | - | - | - | - | |||
| 기타 취득(c) | 보통주 | - | 9,010 | - | - | 9,010 | 단주처리 | ||
| 우선주 | - | 2 | - | - | 2 | 단주처리 | |||
| 총 계(a+b+c) | 보통주 | - | 9,010 | - | - | 9,010 | - | ||
| 우선주 | - | 2 | - | - | 2 | - | |||
주) 당사는 2021년 4월 20일자로 상법 421조의 2에 따라 무상증자에 따른 단주(端株)의 처리를 위하여 필요한 자기주식을 취득함 (보통주식 9,010주 및 3회차 우선주식 2주)
다. 종류주식(명칭) 발행현황
종류주식(제3회 기명식 전환우선주식) 발행현황
| (단위 : 원) |
| 발행일자 | 2020년 11월 13일 | |||
| 주당 발행가액(액면가액) | 147,500 | 500 | ||
| 발행총액(발행주식수) | 29,999,287,500 | 203,385 | ||
| 현재 잔액(현재 주식수) | 29,999,287,500 | 305,078 | ||
| 주식의 내용 |
이익배당에 관한 사항 | 액면가액의 연 1.0% (누적적, 참가적) | ||
| 잔여재산분배에 관한 사항 | 보통주에 우선하는 분배청구권 | |||
| 상환에 관한 사항 |
상환조건 | - | ||
| 상환방법 | - | |||
| 상환기간 | - | |||
| 주당 상환가액 | - | |||
| 1년 이내 상환 예정인 경우 |
- | |||
| 전환에 관한 사항 |
전환조건 (전환비율 변동여부 포함) |
- 전환가격 : 74,608원 신주인수계약서에 따른 전환가액 조정(무상증자, 보통주 주가하락 등)을 반영한 보통주로의 주당 전환가격 - 전환비율* : 1 : 1.3179 (2021.09.30 기준) -새로운 전환가격은 발행 당시 전환가격(조정일 전에 신주의 할인발행 등의 사유로 전환가격을 이미 조정한 경우에는 이를 감안하여 산정한 가격)의 70%이상으로 한다. |
||
| 전환청구기간 | 발행일로부터 1년 경과후 존속기간 내 (존속기간은 발행일로부터 5년) 2021.11.13~2025.11.12 |
|||
| 전환으로 발행할 주식의 종류 |
기명식 보통주 | |||
| 전환으로 발행할 주식수 |
402,092 | |||
| 의결권에 관한 사항 | 우선주 1주당 1 의결권 | |||
| 기타 투자 판단에 참고할 사항 (주주간 약정 및 재무약정 사항 등) |
1. 상기 발행일은 납입일 익일입니다. 2. 상기 현재 잔액은 잔여 전환우선주식수에 조정된 발행가액(무상증자반영)을 곱한 금액 입니다. |
|||
종류주식(제4회차 기명식 전환우선주식) 발행현황
| (단위 : 원) |
| 발행일자 | 2021년 01월 08일 | |||
| 주당 발행가액(액면가액) | 155,400 | 500 | ||
| 발행총액(발행주식수) | 74,999,925,000 | 482,625 | ||
| 현재 잔액(현재 주식수) | 74,999,925,000 | 723,937 | ||
| 주식의 내용 |
이익배당에 관한 사항 | 액면가액의 연 1.0% (누적적, 참가적) | ||
| 잔여재산분배에 관한 사항 | 보통주에 우선하는 분배청구권 | |||
| 상환에 관한 사항 |
상환조건 | - | ||
| 상환방법 | - | |||
| 상환기간 | - | |||
| 주당 상환가액 | - | |||
| 1년 이내 상환 예정인 경우 |
- | |||
| 전환에 관한 사항 |
전환조건 (전환비율 변동여부 포함) |
- 전환가격 : 72,520원 신주인수계약서에 따른 전환가액 조정(무상증자, 보통주 주가하락 등)을 반영한 보통주로의 주당 전환가격 - 전환비율* : 1 : 1.4285(2021.09.30 기준) -새로운 전환가격은 발행 당시 전환가격(조정일 전에 신주의 할인발행 등의 사유로 전환가격을 이미 조정한 경우에는 이를 감안하여 산정한 가격)의 70%이상으로 한다. |
||
| 전환청구기간 | 발행일로부터 1년 경과후 존속기간 내 (존속기간은 발행일로부터 7년) 2022.01.08~2028.01.07 |
|||
| 전환으로 발행할 주식의 종류 |
기명식 보통주 | |||
| 전환으로 발행할 주식수 |
1,034,196 | |||
| 의결권에 관한 사항 | 우선주 1주당 1 의결권 | |||
| 기타 투자 판단에 참고할 사항 (주주간 약정 및 재무약정 사항 등) |
1. 상기 발행일은 납입일 익일입니다. 2. 상기 현재 잔액은 잔여 전환우선주식수에 조정된 발행가액(무상증자반영)을 곱한 금액 입니다. |
|||
5. 정관에 관한 사항
사업보고서에 첨부된 정관의 최근 개정일은 2019년 03월 27일(제11기 정기주총일)입니다. 이후 2021년 3월 29일 제13기 정기주주총회까지 정관 변경은 없습니다.
정관 변경 이력
| 정관변경일 | 해당주총명 | 주요변경사항 | 변경이유 |
|---|---|---|---|
| 2018년 03월 27일 | 제11기 정기주총 |
제8조 (주권의 발행과 종류) | 주권 전자등록 의무화에 따라 삭제 |
| - | 상동 | 제8조의2 (주식의 전자등록) | 주권 전자등록 의무화에 따라 신설 |
| - | 상동 | 제9조 (주식의 종류) | 조문 정비 |
| - | 상동 | 제9조의2 (이익배당, 주식의 상환 및 전환에 관한 종류주식) | 종류 주식의 발행 조건 변경 및 조문 정비 |
| - | 상동 | 제12조 (우리사주매수선택권) | 조문정비 |
| - | 상동 | 제15조 (명의개서대리인) | 주식 등의 전자등록에 따른 주식사무처리 변경내용 반영 |
| - | 상동 | 제16조 (주주 등의 주소, 성명 및 인감 또는 서명 등 신고) | 조항 삭제 |
| - | 상동 | 제16조의2 (주주명부) | 조문 신설 |
| - | 상동 | 제17조 (주주명부의 폐쇄 및 기준일) | 조문 정비 |
| - | 상동 | 제18조 (전환사채의 발행) | 조문 정비 |
| - | 상동 | 제21조 (사채발행에 관한 준용 규정) | 조문 정비 |
| - | 상동 | 제22조 (소집시기) | 조문 정비 |
| - | 상동 | 제55조 (외부감사인의 선임) | 조문 정비 |
| - | 상동 | 부칙 | 시행일자 |
II. 사업의 내용
1. 사업의 개요
당사는 고유의 원천 기술을 확보하여 이를 통해 히알루로니다제, 차세대 항암 항체의약품(ADC), 지속형 바이오의약품 및 바이오시밀러 등을 개발하고 있습니다.
| 당사 고유의Hybrozyme™ 은 단백질 공학 기술을 이용한 인간 히알루로니다제(Hyaluronidase) 원천 기술로써 기존의 항체치료제나 단백질 바이오의약품의 정맥주사(iv) 약물전달 투여 방식을 피하주사(sc) 투여 방식으로 전환할 수 있으며 기존의 많은 용량의 정맥주사 제제의 항체의약품이나 바이오의약품에 적용이 가능합니다. |
| 당사가 자체적으로 개발한NexMab™ 기술을 활용한 항체-약물접합(ADC, Antibody-Drug Conjugate) 물질은 기존의 항암 항체치료제보다 월등한 효능과 부작용을 감소시킨 치료제로 개발 중이며 현재 유방암치료제 적응증으로 국내 최초로 임상1상을 완료하고 결과보고서를 제출하였습니다. 또한 당사는 면역항암제 등 다른 약물과의 병용요법을 통해 차후 임상2상을 검토 준비 중에 있습니다. 특이사항 으로는ADC 위암치료제의 경우, 미국FDA에 희귀의약품으로 등록되어 있습니다. |
| 당사 고유의 기술로 개발한NexP™ 단백질은 바이오의약품과 융합(Fusion)하여 기존의 바이오의약품보다 체내 지속성이 증가된 차세대 지속형(Long-acting) 바이오베터입니다. 당사는 지속형 인성장호르몬의 국내 임상2상을 완료하였으며 2021년에 글로벌 소아용 임상을 완료하였으며 조만간 결과보고서를 제출할 예정입니다. 당사는 파트너 고객사와 인성장호르몬의 글로벌 임상을 지속적으로 수행할 목적으로 협의를 진행하고 있습니다. |
| 당사는 오리지널 신약 황반변성 치료제인 아일리아(Eylea)의 바이오시밀러를 당사 고유의 기술로 개발하였으며, 당사의 아일리아 바이오시밀러는 오리지널 제품과 비교하여 열안정성이 뛰어나며, 미국, 일본 등에 제형 특허를 등록하였고 융합단백질의 생산을 위한 제법(배양) 특허를 국내, 일본, 호주 및 러시아에 등록함으로써(유럽 및 미국은 출원 중) 아일리아 바이오시밀러 사업에 대한 차별화된 경쟁 우위를 확보하고 있습니다. 당사는 전세계 유일하게 임상1상을 성공적으로 완료하였고 결과보고서를 제출하였습니다. 당사는 글로벌 임상3상 추진을 위해 자회사인 알토스바이오로직스와 공동으로 준비 중에 있습니다. |
| 허셉틴(Herceptin, 성분명 Trastuzumab) 물질 특허 만료 이후 바이오시밀러의 경쟁적 출시에 대응하여 로슈(Roche) 사가 피하주사(sc) 제형을 출시함으로써 시장의 판도가 재편되였고 이에 따른 허셉틴 바이오시밀러 시장의 경쟁은 더욱 심화되고 있는 상황에서 당사는 자체 보유한 피하주사(sc) 원천기술인 히알루로니다제를 혼합한 허셉틴 sc 바이오시밀러 개발 등 차별화된 틈새 경쟁력을 보유하고 있습니다. |
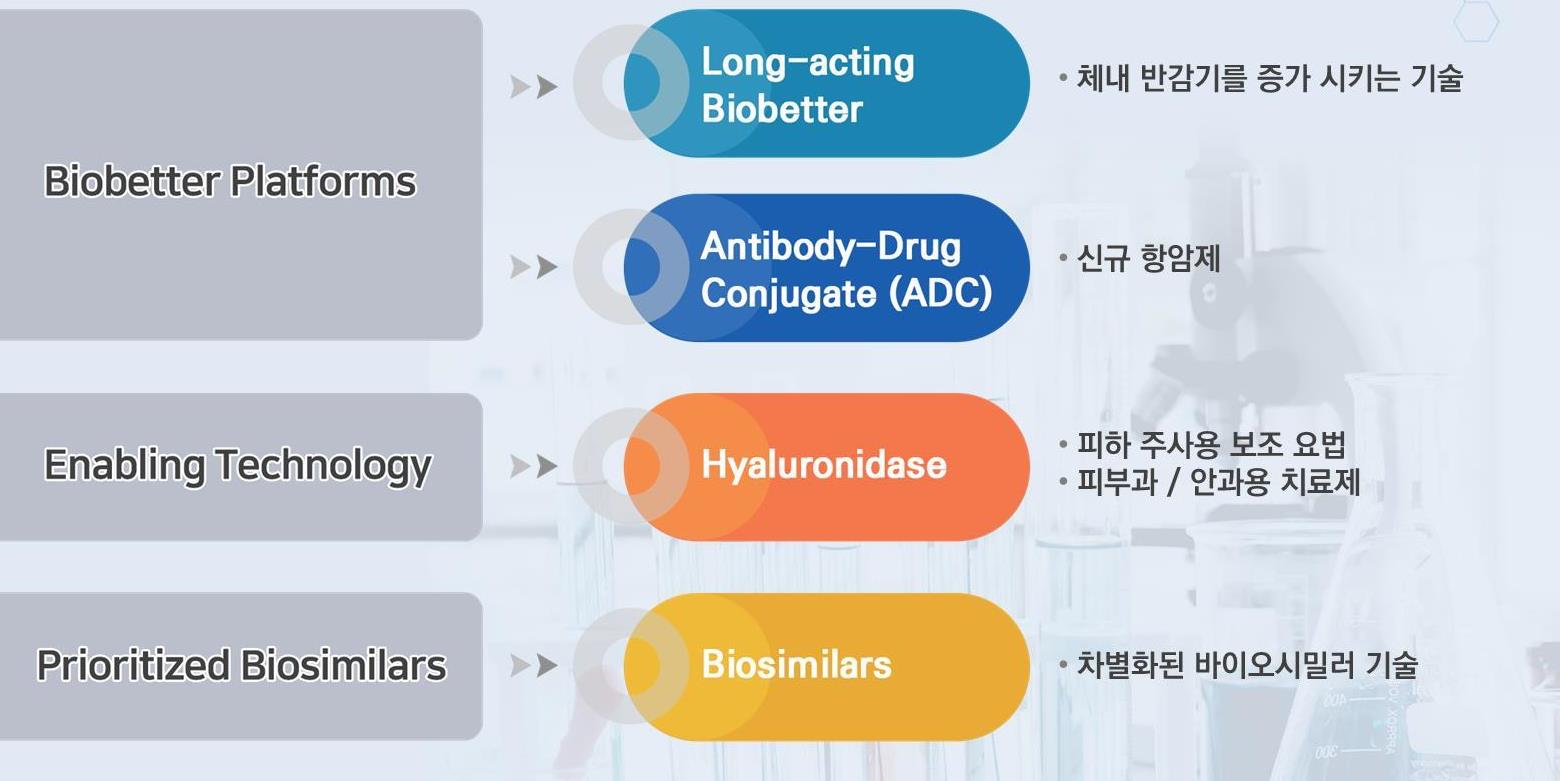 |
|
알테오젠 파이프라인 개요 |
가. 산업의 이해
(1) 바이오의약품이란?
의약품은 일반적으로 화학합성의약품(저분자 의약품이라고도 함)과 바이오의약품으로 구분할 수 있으며 바이오의약품은 유전자 재조합, 세포배양, 세포융합 등 생물공학 기술(biotechnology)를 이용하여 생산되는 의약품을 말합니다.
|
화학합성의약품 (Small Molecule Drug) |
- 분자구조 단순 - 분자량 (0.1~1kDa) - 비교적 간단한 유기 화학합성 공정을 통해 제조 - 알약, 가루약 등의 경구용(oral) 제형 - 약효 물질에 대한 기술 및 특허가 중요 - 신약, 복제약(제네릭), 개량신약 등으로 구분 |
|
바이오의약품 (Bio-pharmaceutical Drug) |
- 분자구조 복잡 - 분자량 큼(단백질의약품은 20~25kDA, 항체의약품은 150kDa) - 복잡하고 변화가 많은 생물(세포) 배양공정을 거쳐 생산 - 경구용 제형은 위에서 분해되므로 주사제(iv) 형태로 제품화 - 물질 뿐만 아니라 공정 및 제형에 대한 기술과 특허도 중요 - 바이오신약, 바이오시밀러, 바이오베터 등으로 구분 |
바이오의약품은 특히 생산공정이 복잡하고 그에 따라 판매 가격이 고가임에도 불구하고 질환 별로 표적치료제 개발이 가능해 화학합성의약품보다 부작용이 적으며, 임상 성공률이 높고 희귀성 및 난치성 질병 등 기존에 화학합성의약품으로 치료하지 못했던 질병에 대한 치료가 가능합니다.
바이오의약품은 신규 치료제인 오리지널 바이오신약과 오리지널의 특허가 만료됨에 따라 복제의약품이라고 할 수 있는 바이오시밀러(Biosimilar) 및 기존 1세대 바이오의약품의 지속성, 효능, 기능 등을 개선시킨 바이오베터(Bio-better) 등으로 구분할 수 있으며, 특히 바이오베터는 의약품 허가 과정에서 신약으로 분류가 되어 신약에 준하는 허가 절차를 거치게 됩니다.
전세계 의약품 시장을 주도하고 있는 바이오의약품 중 오리지널 항체의약품들은 대부분 2015~2020년 사이에 특허가 만료되고 있으며 그 때까지는 시장에서 독점적 지위를 누리고 있지만 높은 약가로 인해 의료보험 재정에 부담이 크고 약가 인하에 대한 시장의 요구가 증가하고 있어 많은 제약사들이 특허 오리지널 물질 특허 만료 이후 이를 복제한 바이오시밀러 제품을 출시하기 위해 개발 중에 있으며 바이오시밀러 르네상스가 도래하였습니다. 이미 인슐린, 성장호르몬, 항암보조제(G-CSF) 등 대부분의 단백질의약품들은 오리지널 제품의 특허가 만료되었고 바이오시밀러 제품들이 연이어 출시되었으며 오리지널 제품과 바이오시밀러 제품들의 구분이 어려울 정도로 다수의 제품들이 시장에서 공존, 경쟁하고 있습니다.
최근에는 신종 코로나 바이러스 감염증(COVID-19)으로 인하여 항 바이러스 제제에 관심이 집중되면서 백신과 치료제 개발에 더 많은 관심을 가지게 되었습니다. 백신의 경우에는 해당 바이러스를 정제하여 이를 불활화하는 과정을 거쳐 바이러스의 활성을 없앤 후에 인체에 주입함으로써 우리 몸에서 항체를 만들어 바이러스로 부터 예방을 하는 방식이고, 치료제의 경우는 기존에 사용하던 면역과 관련이 있는 항 바이러스 제제의 적응증을 바꾸어 치료제로 개발하거나, 바이러스 표면의 단백질을 중화(차단)할 수 있는 항체를 만들어 이를 치료제로 개발하고 있습니다. 현재까지 허가된 코로나19 바이러스 백신들은 변이 바이러스에 대한 빠른 대응 및 접종 후 항체 생성률은 높은 반면 장기적인 면역원성에 대한 임상적 보고는 아직 없는 상태여서 당사가 개발 예정인 서브유닛 백신(Subunit Vaccine)은B형 간염 백신 등에서 이미 장기면역 효과가 확인되었기에 코로나19 변이 바이러스에 적절하게 대응할 수 있을 것으로 예상하고 있습니다.
(2) 바이오시밀러(Biosimilar)
제약분야에서 20 년 정도의 특허기간이 지나면 다른 제약회사도 특허 의약품의 주성분을 합성하여 판매할 수 있습니다. 최초의 특허개발 의약품을 오리지널(original)이라 하며, 특허가 만료된 의약품을 구조적으로 동일하게 제조하여 만든 의약품을 복제약(generic drug)이라 합니다. 의약품 중에는 화학적 합성으로 생산할 수 없는 항체와 같은 바이오의약품이 있으며, 이들은 주로 동물세포를 이용하여 배양/정제 과정을 거쳐 생산합니다. 바이오시밀러(biosimilar)는 특허가 끝난 오리지널을 모델로 타 제약회사가 자체적으로 개발한 기술로 생산하는 바이오의약품으로 기존의 특허 받은 오리지널 대비 임상시험을 통하여 동등성이 입증된 바이오의약품입니다.
(3) 바이오베터(Bio-better)
바이오베터(Bio-better)는 기존 바이오의약품의 효능 및 환자 편의성을 개선한 일종의 개량형 바이오의약품으로서 화학합성의약품의 개량 신약과는 차이가 있습니다. 화학합성의약품의 개량 신약은 특허가 만료된 원천물질을 단순히 치환하거나 제형을 개선하여 추가 임상시험 없이 개발되는 반면 바이오베터는 바이오 신약에 준하는 연구개발과 승인 과정을 거치게 됩니다. 이는 또한 오리지널 바이오의약품 특허 만료에 따른 임상시험 등 개발 과정이 비교적 용이한 바이오시밀러와는 차이점이 있습니다. 전세계 제약회사들은 이미 시장에 출시된 바이오의약품의 효능을 개선하거나 주사 시기를 획기적으로 줄여서 환자 편의성을 극대화 시킨 지속형(Long-acting) 제제 등과 같이 기존 제품보다 개선된 바이오베터 제품들을 개발하고 있으며, 이와 같은 바이오베터가 출시될 경우 이미 기존 제품에 의해 형성된 시장에서 기존 제품보다 차별화된 경쟁력을 보유할 수 있습니다.
단백질의약품의 바이오베터로는 매일 투여형에서 주1회 투여가 가능하도록 체내 반감기를 늘린 지속형 빈혈치료제(EPO)인 아라네스프(Aranesp)와 지속형 항암보조제 (G-CSF)인 뉴라스타(NEULASTA)가 있으며(두 제품 모두 미국의 바이오 기업인AMGEN 사가 개발), 항체의약품의 바이오베터로는 항체-약물 접합(ADC) 기술을 이용하여 항체의약품의 장점(타겟 지향성)과 화학합성의약품의 장점(강한 암세포 독성)을 결합한 ROCHE사의 캐사일라(Kadcyla)가 있습니다.
[ 바이오의약품 비교]
|
특징 |
바이오신약 (Biologics) |
바이오시밀러 |
바이오베터 |
|
유사성 |
오리지널과 동일 |
유사하지만 오리지널과 동일하지 않음 |
오리지널 보다 우수 |
|
개발비용 |
20억~30억 달러 |
1억~3억 달러 |
2억~5억 달러 |
|
약물개발기간 |
약 10~12년 |
약 5~7년 |
약 5~7년 |
|
규제 |
지금까지 미국 시장에서 바이오시밀러의 상호교환 가능한 지정이 부족하여 보호됨 |
국가별 별도의 승인 절차 |
오리지널 의약품보다 |
|
의약품가격 |
일반적으로 특허 독점 |
오리지널 의약품의 |
안전성/효능이 우수하여 20~30% 높음 |
[출처] Frost&Sullivan, Access to New Therapy Areas to Drive Major Growth in the Global Biosimilars Market 2020-2026 (2020.12)
나. 시장 현황
(1) 바이오의약품 시장의 특성
바이오의약품은 일반적으로 합성의약품에 비해 크기가 크고 복잡한 구조를 가지고 있으며, 생물체를 이용하여 복잡한 제조공정(세포 배양공정)을 거쳐야 되므로 변화에 민감하고 특히 오염 및 불순물 관리에 유의해야 하는 반면, 생물유래 물질로 고유의 독성이 낮고 작용기전이 명확하여 난치성 및 만성질환에 뛰어난 치료 효과를 가지고 있습니다.
[ 바이오의약품 제조 과정 ]
|
바이오의약품을 생산하고자 할 때 특정 단백질(바이오의약품)의 유전자를 세포에 삽입하고 배양하는 과정을 유전공학적인 방법으로 제조 → 유전자를 박테리아나 동물세포(CHO)에 삽입하여 세포주(Cell Line) 제조 → 온도, pH, 용존산소 및 배지 등을 조절하여 세포주를 배양하고, 세포 수를 증식 → 증식된 세포에서 필요한 단백질만 분리, 정제하여 이를 의약품으로 사용 |
한국바이오의약품협회가 국내외 바이오의약산업 정보 및 동향을 수집 분석한 "2020 바이오의약품 산업동향 보고서"에 따르면 글로벌 바이오의약품 시장은 2019년 기준 2,660억 달러로 전체 의약품에서 차지하는 비중은 29%로 나타났습니다. 글로벌 바이오의약품 시장은 향후 6년(2020~2026년)간 연평균 10.1% 성장해 2026년에는 5,050억 달러에 달하며 이는 전체의약품 시장의35% 수준으로 증가할 것으로 전망된다고 밝혔습니다.
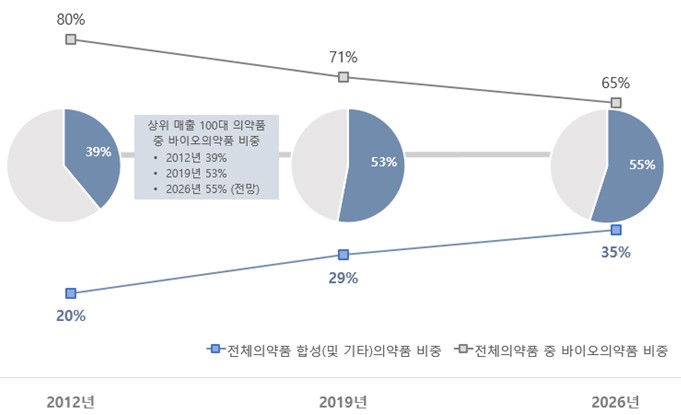 |
|
바이오의약품시장비중 |
[출처] EvaluatePharma, World Preview 2020, Outlook to 2026 (2020.07)
또한 동 보고서에 따르면 2019년 전세계 10대 의약품 중에서 바이오의약품이 7개를 차지하고 있으며 전세계에서 가장 많이 팔리는 의약품 역시 휴미라(Humira, 류마티스 관절염 자가면역질환 치료제)로 바이오의약품에 해당합니다. 2003년 전세계 10대 의약품 중 바이오의약품이 1개 밖에 없었던 것과 비교하면 지난 10년 사이에 바이오의약품의 성장은 급속히 진행되고 있습니다. 이러한 경향은 앞으로도 지속되어 향후 전세계 의약품 시장의 발전은 바이오의약품이 주도할 것으로 예상됩니다. 매출 상위 10대 의약품 중 바이오의약품은 휴미라(Humira, 류마티스 관절염 자가면역질환 치료제), 키트루다(Keytruda 면역항암제), 옵디보(Opdivo 면역항암제), 아일리아(Eylea) 등의 품목입니다. 특히 COVID-19 팬데믹 상황은 2020년 글로벌 제약사의 매출 품목에도 변화가 발생했습니다. 휴미라는 바이오시밀러 제품 출시로 매출액이 13.6% 하락한 반면 키트루다는 30% 증가하여 144억 달러 매출을 기록했으며 2023년에는 매출액 기준으로 1위를 탈환할 것으로 전망하고 있습니다. 옵디보 매출은 소폭 하락하였고 다잘렉스와 스텔라라 매출 성장이 눈에 띄었습니다.
[2019년 글로벌 Top 10 의약품] (단위: 십억 미화 달러)
|
제품명 |
제조사 |
적응증 |
2019년 |
2018년 |
| Humira (adalimumab) |
Abbvie | Immunology (Organ Transplant, Arthritis etc.) | 20.97 | 20.2 |
| Revlimid (Lenalidomide) |
Celgene | Treatment of Multiple Myloma | 10.94 | 9.2 |
| Keytruda (pembrolizumab) |
Merck(MSD) | Lung cancer called non-small cell lung cancer (NSCLC) | 9.17 | 6.1 |
| Opdivo (nivolumab) |
Bristol-Myers Squibb | Non-small cell lung cancer (NSCLC) | 7.80 | - |
| Eliquis (apixaban) |
Bristol-Myers Squibb (US) & Pfizer (US) |
Atrial fibrillation and Deep Vein Thrombosis (DVT) | 7.69 | - |
| Eylea (aflibercept) |
Regeneron and Bayer | Anti-VEGF therapy | 7.32 | 6.5 |
| Xarelto (rivaroxaban) |
Bayer (Germany) & Johnson & Johnson (US) |
Deep Vein Thrombosis (DVT) and Pulmonary Embolism (PE) | 6.98 | 6.1 |
| Enbrel (etanercept) |
Amgen/Pfizer Inc | Immunology (Organ Transplant, Arthritis etc.) | 6.65 | 7.3 |
| Avastin (bevacizumab) |
Genentech/Roche | Metastatic Colorectal cancer | 6.30 | 6.4 |
| Prevnar 13 | Pfizer | Pneumococcal 13-valent Conjugate Vaccine | 5.82 | - |
주) 바이오의약품: Humira, Keytruda, Opdivo, Eylea, Enbrel, Avastin, Prevnar 13
출처 : EvaluatePharma, EP Vantage 2021 Preview (2020.12)
바이오의약품 중 특히 항체의약품의 시장 규모는 점차 증가하고 있으며, 항체의약품은 면역세포 신호전달 체계에 관여하는 단백질 항원이나 암세포 표면에서 발현되는 표지 인자를 표적으로 하는 단일 단세포군 항체(mAb, Monoclonal Antibody)를 제작하고 인체 적용시 부작용을 최소화할 수 있도록 단백질을 개량해 질병의 개선 및 치료 효과를 발휘하는 바이오의약품입니다. 항체의약품은 종양(암), 자가면역질환, 신생혈관, 바이러스와 같은 광범위한 분야의 치료에 사용되며 이러한 의약품 시장의 성장을 이끌고 있는 요인으로는 화학합성의약품에 비해 임상 1상에서의 성공 확률이 2.5배 정도로 월등히 높고, 후보물질 발굴단계에서의 실패 확률이 극히 낮으며, 화학합성의약품 개발 실패의 주요 원인인 부작용 및 독성에 있어서도 비교적 자유롭다는 것입니다.
바이오의약품은 신규 치료제인 오리지널 바이오신약과 오리지널의 특허가 만료됨에 따라 복제의약품이라고 할 수 있는 바이오시밀러(Biosimilar) 및 기존 1세대 바이오의약품의 지속성, 효능, 기능 등을 개선시킨 바이오베터(Bio-better) 등으로 구분할 수 있으며, 특히 바이오시밀러 개발은 전세계적으로 활발히 진행되고 있으나, 오리지널 원료 물질에 대한 지적재산권 확보가 불가능하여 국내/외적으로 업체 간 경쟁이 치열할 것으로 예상되며 마케팅 능력이 월등한 거대 다국적 제약사와 정면으로 승부하기에는 절대적으로 불리한 분야이기에 국내 제약사 및 바이오 기업이 바이오시밀러 개발을 하더라도 글로벌 마케팅 파트너 사와 제휴 하지 못하면 성공시키기가 매우 어려울 것으로 판단됩니다.
바이오신약의 개발은 향후 시장에서의 성장 잠재력은 크지만, 신약 개발의 속성상 전임상 혹은 임상 과정 중에 실패할 가능성이 높기 때문에 리스크가 매우 큰 분야입니다. 특히 현재 대학 연구 기관 및 일부 기관에서 추진 중인 세포 치료제 혹은 유전자 치료제 등은 임상을 통하여 효과와 안전성이 입증된다면 전체 바이오의약품 시장을 크게 성장시킬 수 있는 미래 가치가 충분한 분야이기는 하나 여전히 기술적으로 해결해야될 과제들이 산적해 있습니다. 따라서 이들 분야는 상업적 성공을 기대하기에 앞으로도 많은 시간과 비용 그리고 노력이 투입되어야 할 분야입니다.
(2) 바이오베터(Bio-better) 시장의 특성
바이오베터(Bio-better)란 오리지널 바이오의약품을 개량한 것으로 오리지널 의약품의 효능과 부작용을 개선함으로써 소위 수퍼 바이오시밀러(Super Biosimilar)라고도 불리며, 오리지널 의약품처럼 20년간 특허가 인정됩니다. 오리지널 바이오 신약으로부터 유래한다는 점은 바이오시밀러와 같으나 오리지널에 비하여 우수한 품질을 요구하지 않는 바이오시밀러와 달리 새로운 기술을 적용하여 오리지널 바이오 의약품에 비하여 개량된 품질이나 약효를 나타낼 수 있는 의약품입니다.
또한 바이오베터는 독자적인 특허가 인정되기 때문에 오리지널 의약품의 특허 만료와 상관없이 시장에 출시될 수 있습니다. 바이오시밀러의 가격은 오리지널 의약품의 70% 수준에서 결정되는 반면 바이오베터는 오리지널 대비 2~3배의 높은 가격을 형성할 뿐만 아니라 오리지널 및 바이오시밀러와는 다른 독자적 효능을 가지고 있기 때문에 오리지널 및 바이오시밀러와의 경쟁에서도 자유로울 수 있다는 장점이 있습니다.
현재 바이오의약품 시장은 지난 20년 동안 다수의 바이오 신약들의 성공을 기반으로 매년 큰 폭의 성장을 거듭해 왔으며, 현재 바이오의약품 전체 시장의 성장을 견인하는 두 분야는 항체의약품과 바이오베터 의약품입니다.
바이오베터는 독자적인 물질 특허가 인정되기 때문에, 오리지널 의약품의 특허로부터 비교적 자유로우며 아래 그림에 나타난 바와 같이 차별화된 상품성 및 효능에 힘입어 오리지널 또는 바이오시밀러와의 경쟁에서도 벗어날 수 있습니다. 따라서 임상에서 성공을 거둔다면 전체 바이오의약품의 성장을 견인하는 추가된 가치 뿐만 아니라 시장성도 입증되며 바이오 신약에 비해 개발 관련 리스크가 크지 않기 때문에 사업적으로 가장 매력 있는 제품군에 해당됩니다.
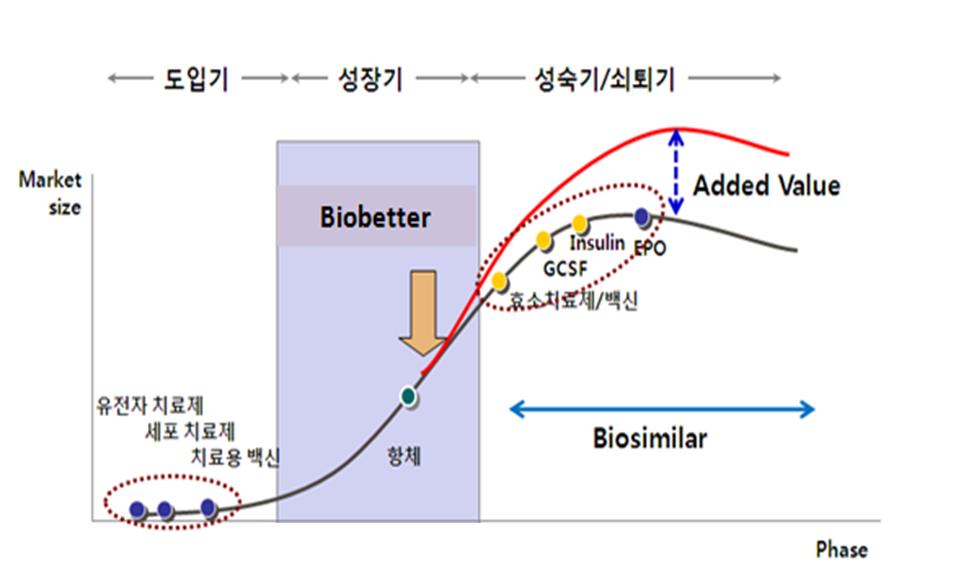 |
|
바이오의약품의 성장 곡선 |
성공적인 바이오베터 의약품 개발을 위해서는,
1) 기존의 치료제보다 우월한 치료 효과를 제공하고,
2) 환자의 삶의 질(QOL: Quality of Life)을 향상시키며,
3) 의료 재정의 건전성에 도움이 되는
방향으로 기술개발 전략이 필요합니다.
특히 모든 바이오의약품은 단백질이라는 물질의 특성상 경구용(Oral) 제제로 투여가 불가능하고 정맥주사제(iv)로 사용해야 하는 한계가 있습니다. 따라서, 투약 빈도를 최소화할 수 있는 지속형 제품으로의 전환이 필요하며 투여 빈도가 개선된 차세대 바이오의약품이 기존 시장에 도입되면 그 장점에 힘입어 시장규모가 크게 성장하게 됩니다.
![이미지: [지속형 바이오베터의 매출]](%EC%A7%80%EC%86%8D%ED%98%95%20%EB%B0%94%EC%9D%B4%EC%98%A4%EB%B2%A0%ED%84%B0%EC%9D%98%20%EB%A7%A4%EC%B6%9C.jpg) |
|
[지속형 바이오베터의 매출] |
또한 환자의 치료 편의성 증진을 위하여 평균 2.5시간 투여하는 정맥주사(iv) 제형을 5분 이내로 투여 완료할 수 있는 피하주사(sc) 제형의 바이오베타 개발이 활발히 진행되고 있습니다. 이는 의료진이 주사용 제제로 준비하는 시간을 절약할 수 있으며 체중에 따라 부하 용량이 필요한 정맥주사 제형 대비 고정 용량으로 투여량 계산이 불필요하고 전체 치료 비용 절감과 효율성 증진 효과가 있습니다.
세계 최초로 피하주사(sc) 제형 항체의약품을 유럽에서 출시한 Roche 사의 발표에 따르면 Rituxan Hycela (Rituxan sc 미국 FDA 허가 명칭)와 Rituxan iv 의 상호 비교 임상 3b 에서 투여 완료한 환자 620명 중 477명(77%)이 Rituxan Hycela를 선호했으며 Rituxan Hycela는 2017년 6월 미국에 출시되었고, Herceptin iv의 피하주사 제형인 Herceptin Hylecta(Herceptin sc 미국 FDA 허가 명칭)는 2018년 2월에 시판 허가를 받았습니다.
피하주사(sc) 제형으로 변경 임상 중인 주요 항체의약품은 Perjeta(Roche), Opdivo (BMS), Darzalex(J&J) 등으로 2018년 예상 합산 매출은 미화 112억 달러에 달하고 있습니다. 피하주사(sc) 제형 변경은 특허 연장 및 환자의 편의성 증대를 통해 바이오시밀러 침투에 대응하기 위한 글로벌 제약사의 에버그린(Evergreen) 전략에서 시작되어 신약 개발의 중요한 이정표로 변모 중에 있습니다.
EPO(빈혈치료제)와 G-CSF(항암보조제, 백혈구 촉진제)의 지속형 바이오의약품 출시 사례에서 볼 수 있듯이 2세대 지속형 바이오의약품(바이오베터)이 출시되면 시장 점유율을 늘리며 기존의 1세대 제품의 시장을 성공적으로 대체하면서 전체적인 시장 규모도 증가하였습니다.
결론적으로 중요한 시사점은 바이오베터의 출시 이후 성장률이 기존의 1세대 제품이 보여주었던 성장률보다 크게 높아졌다는 것입니다. 이는 피하주사(sc) 제형 바이오베터가 기존 1세대 제품의 효능은 그대로 유지하면서 환자 편의성을 획기적으로 개선시켜 바이오의약품이 가지는 주사제(iv) 로서의 단점을 극복할 경우 시장에 성공적으로 진입할 수 있음을 보여준 사례들입니다.
다. 회사 사업개요
(1) 기반 기술
당사는 지속형 바이오의약품 기반기술인 NexP™ 융합(Fusion) 기술과 차세대 항암 항체치료제 기반기술인 NexMab™ ADC 기술, 정맥주사(iv)를 피하주사(sc)로 바꾸어 주는 Hybrozyme™ 기술 등 3개의 플랫폼 기술을 보유하고 있습니다.
|
NexP™ |
- 당사 자체적으로 개발한 단백질 캐리어(Carrier)인 NexP™와 1세대 단백질치료제를 융합하여 체내 지속성이 증가하고 투여 편의성 및 치료 효과가 향상된 차세대 단백질치료제를 개발하는 원천기술임 |
|
NexMab™ |
- 항체-약물 접합체(ADC, Antibody-Drug Conjugate)는 항체와 약물(Payload)을 링커(Linker)로 접합 시켜 암세포 내에서만 약물이 분리 방출되면서 암세포를 사멸시키는 표적지향 항암제로 합성 약물의 장점인 강한 효능(Cytotoxicity)과 항체치료제의 장점인 선택성(Selectivity) 및 지속성을 결합하여 항체의약품보다 효능은 뛰어나고 합성 약물보다 독성에 의한 부작용이 적은 항체 바이오베터임 |
|
히알루로니다제 원천 기술 |
- 기존의 항체치료제나 단백질 의약품의 경우 인체에 많은 용량 투여를 통해 치료 효과가 나타남에 따라 정맥주사(iv) 투여 방식이 불가피하나 환자가 병원에 입원하여 집중 관리 하에 약 4~5시간 정도의 투여 시간이 소요되므로 환자에게는 장시간 병원에 머물러야 하는 불편함이 있었고 이에 따른 의료수가를 높이는 원인으로 지목됨 |
(2) 개발 중인 제품
|
개발 제품 |
제품 설명 |
개발 단계 |
|
지속형 인성장 |
NexP™와 결합하여 지속성이 증가된 인성장호르몬(hGH) |
국내 임상2a상 완료, |
|
비알코올성 |
신규 GLP-1 유사체와 A1AT 융합단백질로 비알코올성 지방간염치료제(NASH) |
원천기술 확보 |
|
ADC 유방암/위암치료제 |
NexMab™ ADC 기술을 이용하여 유방암 타겟 항체와 항암약물을 접합한 유방암치료제 |
국내 최초 임상1상 완료, |
|
피하주사용(sc) |
피하주사용 원천기술인 재조합 히알루로니다제(Hyaluronidase) |
2019년/2020년/2021년 연이어 글로벌 10대 제약사 및 다국적 제약사와 라이센스아웃 계약 체결, 글로벌 10대 제약사에 임상1상 진입을 위한 CTD 제공 |
|
독자제품형 (Stand-alone) |
외과 수술 후 통증 및 부종 완화 적응증으로 피부과/성형외과에서 시판 중인 동물유래 히알루로니다제 대체 목표인 재조합 히알루로니다제 (테르가제 Tergase) |
Pivotal 임상시험계획서(IND) |
|
아일리아(Eylea) |
습성황반변성(wAMD) 환자 대상 융합단백질인 아일리아(Eylea) 바이오시밀러 |
국내 임상1상 완료 |
|
허셉틴 sc |
유방암 및 위암 항체치료제인 허셉틴 바이오시밀러의 피하주사(sc) 제형 |
임상 1상 준비 단계 |
|
허셉틴 iv |
유방암 및 위암 항체치료제인 허셉틴 바이오시밀러 |
중국 임상 3상 협의 중 |
라. 시장 규모 및 전망
글로벌 의약품 시장조사기관인 '이벨류에이트파마(EvaluatePharma)' 는 2020년 6월'World Preview 2020, Outlook to 2026' 보고서를 통해 글로벌 제약산업의 현황과 전망을 발표했습니다. COVID-19 팬데믹 상황 속에서도 혁신적이고 효과적인 치료제에 대한 지속적인 요구로 인해 전세계 처방의약품(Prescription drug) 매출액은 2020년 9,040억 달러에서 연평균 7.4%씩 성장해 2026년에는 1조 3,903억 달러 규모가 될 전망되며 이는 지난 2012∼2019년 처방의약품 매출액 연평균 성장률이 2.7%에 그친 것과 비교할 때 매우 빠른 성장세로 볼 수 있습니다.
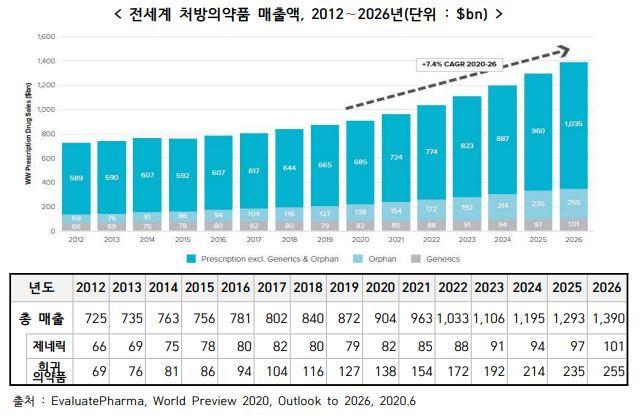 |
|
전세계 의약품 시장 규모 |
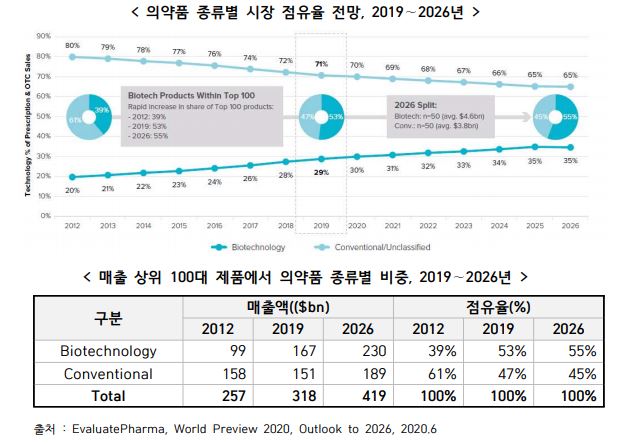
전체 의약품 시장에서 바이오의약품이 차지하는 매출 비중은 지속적으로 증가하는 추세로 2019년 29%에서 2026년에는 55%를 차지할 것으로 전망되며 글로벌 매출 상위 100대 제품 중에서 바이오의약품 비중은 2012년 39%에서 2019년에는 53%로 Small molecules 등 기존제품을 추월함으로써 의약품 산업은 바이오의약품으로 계속 이동 중이며 2026년에는 바이오의약품의 비중이 55%를 차지할 전망입니다. 이는 특허로 보호받는 바이오의약품 신약이 많고, 바이오의약품의 판매 단가가 고가이기 때문인 것으로 추정됩니다.
 |
|
바이오의약품 매출 비중 추이 |
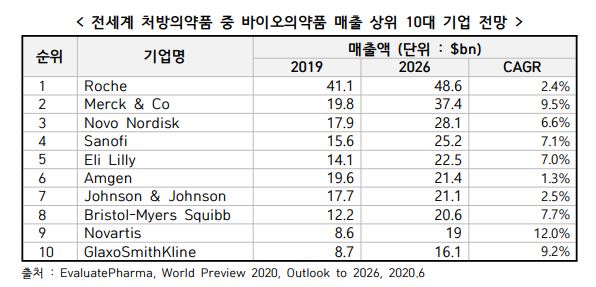
바이오의약품 시장의 대표 주자는 Roche로 판매액은 2019년 411억 달러에서 2026년 486억 달러로 예측되어 2026년에도 시장 선두 자리를 유지할 것으로 전망됩니다.Roche는 2018과 2019년 자사의 블록버스터 3개 제품 Avastin, Herceptin, Rituxan의 특허가 만료됨에 따라 시장 점유율이 5.8% 하락했음에도 불구하고 여전히 선두 바이오의약품 기업의 지위를 유지할 것으로 전망되며 Tecentriq, Perjeta 등 을 포함하여 2026년 매출 상위 100대 제품 중에서 9개를 보유할 것으로 예측됩니다.
 |
|
바이오의약품 매출 상위기업 |
치료영역은 항암(Oncology) 분야가 2019년 16%에서 2026년 21.7%로 확대될 것으로 예상되어(연평균 성장률 11.5%) 가장 높은 시장 점유율 및 성장률을 지속하고 있습니다. 이는 면역항암제인 Keytruda와 Opdivo가 견인하고 있으며 이들 제품의 2019년~2026년 연평균 성장률은 20.2%로 전망됩니다. 또한 2026년까지 면역억제제(Immunosuppressant)와 피부(Dermatologicals) 분야의 연평균 성장률은 각각 14.3%와 12.7%로 고속 성장이 예상됩니다.
한편 2020년부터 글로벌 블록버스터 오리지널 바이오의약품의 특허가 만료됨에 따라 고령화 사회 진입으로 인한 노년층 인구 및 만성질환자 수의 증가로 전반적인 의료 수요가 높아지는 추세에서 오리지널 의약품 대비 저렴한 비용으로 치료 기회의 확대 차원에서 소위 바이오의약품에 대한 복제약을 칭하는 바이오시밀러(Biosimilar) 시장에 대한 수요가 발생하게 되었습니다. 이에 각국의 의료비 재정부담 축소 및 의약품 환자 접근성 확대 차원에서 가격이 상대적으로 저렴한 바이오시밀러의 사용이 장려되고 있으며 최근 전세계를 강타한 COVID-19 팬데믹의 여파로 의료비 절감의 필요성이 더욱 대두됨에 따라 바이오시밀러 시장의 활성화가 더욱 가속화될 것으로 예상되며 시장 규모도 급격히 확대될 전망입니다.
바이오시밀러에 대한 주요 감독기관별 정의는 다음과 같습니다.
|
기관 |
정 의 |
|
FDA |
미국 허가 기준 생물학적 제품과 매우 유사하며, 제품의 안전성, 순도 및 효력 측면에서 오리지널 의약품과 임상적으로 의미 있는 차이가 없는 생물학적 제품 |
|
EMA |
이미 승인된 오리지널 의약품의 활성 물질을 포함하는 생물학적 의약품으로, 종합적인 품질 특성, 생물학적 활동, 안전성 및 효과 측면에서 기준 제품과 유사성이 입증된 제품 |
|
WHO |
오리지널 의약품과 품질, 안전 및 효과 면에서 유사한 바이오의약품 |
[출처] 생명공학정책연구센터, BioINdustry No.156 글로벌 바이오시밀러 시장현황 및 전망(2020-2026) (2021.02)
바이오신약 개발은 시장에서의 성장 잠재력이 크지만 신약 개발의 속성상 전임상 혹은 임상 과정에서 실패할 가능성이 높습니다. 신약 출시를 위해 평균 12~15년 소요되며 평균 26억달러의 천문학적 비용 투입 등 소위 "0.01%의 성공 확률에 도전" 한다고 알려져 있으며 최근 의약품의 R&D 생산성 저하 등 리스크가 큰 분야로 인식되는 반면 바이오시밀러는 오리지널 의약품과 성분면에서 유사하고 효과를 유지하면서도 동일하지는 않으며 개발비용도 오리지널 대비 10% 수준이고 판매 가격도 오리지널 대비 50~80% 수준으로 형성되고 있습니다. 개발 소요기간도 임상2상 면제 등으로 절반 정도로 줄어드는 반면 성공 확률은 10배 가량 높아 효율적인 사업모델로 평가되어 허셉틴의 경우, 미국 시장에 5개의 바이오시밀러 제품이 품목 허가를 받았으며 유럽 시장은 6번째에 이어 7번째 품목 허가가 예정되어 있습니다.
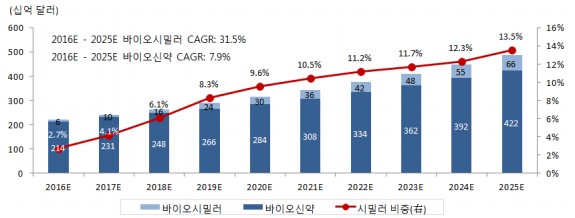
시장조사 업체인 Frost&Sullivan(프로스트앤설리번)에 따르면 전세계 바이오시밀러 시장 규모가 2015년 27억달러에서 2021년 360억달러, 2025년 663억달러 등 2016~2025년 연평균 성장률 31.5%에 이를 것으로 전망하였습니다.
세계 바이오시밀러의 시장은 시장조사 업체인 Frost & Sullivan에 의하면 2015년 27억달러에서 2025년에는 663억달러에 이를 것으로 추정하였습니다.
 |
|
전세계 바이오시밀러 시장규모 추이 및 전망 |
출처: 한국수출입은행
바이오 신약의 특허 만료에 따른 바이오시밀러 시장이 열리면서 (바이오시밀러 '르네상스' 시대 도래) 기존 오리지널 제품에 대한 가격 부담으로 치료 혜택을 받지 못한 개발도상국 환자들에게까지 치료 기회가 확대될 것으로 예상되며 특히, 후발주자들에게 전략적으로 선택되는 이유는 이미 오리지널 제품이 시장에 출시되어 안전성과 유효성이 검증되었기에 신약개발에 비해 현저하게 낮은 연구개발 비용과 단축된 개발 기간에 대한 장점으로 인해 시장 진입을 더욱 촉발시키고 있습니다.
마. 개발 제품의 품목별 시장 현황 및 전망
|
히알루로니다제 |
- 기존의 항체치료제나 단백질 의약품의 경우 인체에 많은 용량 투여를 위해 정맥주사(iv) 제형으로 투여하게 되는데 이를 위해 환자가 병원에 입원하여 집중 관리 하에 투여시간이 약 4~5시간 정도 소요되므로 환자에게 많은 불편함이 있었고 이에 따른 의료수가를 높이는 원인으로 제공 |
|
차세대 항암 |
- 항체-약물 접합체(Antibody-Drug Conjugate, ADC)는 항체에 세포독성 약물(Cytotoxic agent)을 링커(Linker)로 접합시킨 구조이며, ADC가 암세포 표면 수용체를 인식하고 결합하면 암세포 내로 유입되고 약물이 분리되면서 암세포 사멸을 유도하는 원리 |
|
아일리아(Eylea) |
- 습성황반변성(wAMD, Wet Age-related Macular Degeneration)은 혈관성장인자(VEGF, Vascular Endothelial Growth Factor)의 과발현으로 망막에 비정상적인 혈관이 자라면서 출혈이 발생하고 이로 인해 부종이 생기고 삼출물이 발생되면서 황반(망막 중심의 노란색을 띠는 부위로 중심 시야에 해당)이 압박을 받으며 시력을 잃게되는 대표적인 노인성 질환 - 습성황반변성 환자는 전 세계적으로 2013년 기준 2,400만명으로 추정되며 미국의 유병률만 해도 1,100만 명에 달하는 사람들이 연령 관련 황반변성 환자군으로 분류되고 있으며 2050년까지 2,200만 명으로 두 배 증가할 것으로 예상 - 한국에서도 보고된 환자 수만 2010년 9만명에 달하고 인구 고령화로 인해 2025년에는 3배까지 증가할 것으로 예상되지만 실제로 20% 에도 못 미치는 환자 만이 진료를 받을 정도로 질환에 대한 인지도가 낮고 치료제에 대한 비용 부담으로 처방을 받는 환자 수는 진료를 받은 환자 수의 20% 에도 못 미치는 상황 - 글로벌 습성황반변성 시장은 2012년 48억 달러에서 2019년 114억 달러로 연평균 성장률 13.0% 성장 추이를 보이고 있고 '루센티스(Lucentis)' 와 '아일리아(Eylea)'가 시장을 양분하고 있는 상황이며 2018년 기준 루센티스와 아일리아가 전세계 시장 점유율 88%를 장악 - 아일리아는 습성황반변성, 망막중심정맥폐쇄성(CRVO) 황반부종, 당뇨병성 황반부종(DME) 등 다양한 시력 손상 치료제로 매출이 2019년에는 74억달러, 2020년에는 79억달러를 기록했으며 2021년에는 89억달러로 전망 - 기회요인으로는 가격이 고가여서 오리지널 대비 저렴한 바이오시밀러가 출시될 경우 고가의 의료비 부담으로 그 동안 치료 혜택을 누리지 못하는 잠재 환자들로 인해 시장 규모가 확대될 것으로 예상 |
|
허셉틴 iv / |
- HER2 타겟 유방암 항체치료제인 허셉틴은 2028년까지 11.3조원 이상이 판매될 것으로 예상되며 연평균4.4%의 성장률을 기록할 전망 - 추가된 위암 적응증으로 위암 환자가 많은 아시아 지역을 중심으로 다른 항체치료제에 비해서 높은 성장률을 보일 것으로 전망 - 2019년 6월 미국 시장에 허셉틴 바이오시밀러 5개가 출시됨에 따라 경쟁이 치열한 가운데 허셉틴 sc 제제(Herceptin Hylecta)가 2019년 3월에 시판 허가되어 허셉틴 바이오시밀러와 뜨거운 경쟁 국면 |
|
지속형 |
- 전세계 성장호르몬결핍증(GHD) 시장 규모는 2020년에 32억달러 이상으로 예상되며 2021년에서 2027년 사이에 7.1%이상의 CAGR로 성장할 것으로 전망 - 매일 투여 받아야 하는 Daily제제 주사에서 1주일 단위 투여의 장기 지속형 제제 개발이 시장 성장을 견인할 것으로 예측 - 성장호르몬은 성장 촉진 등과 같은 외양 개선을 위해서 주로 선진국에서 사용되며, 전세계적으로 성장호르몬 수요환자는 연간 2백만 명 이상으로 추정 - 주 1회 투여하는 지속형 제품이 등장할 경우 빈번한 주사의 불편함과 주사 바늘에 대한 공포감 때문에 성장호르몬 투여를 주저하는 소아 및 성인에게 편의성을 제공함으로써 성장호르몬 시장을 확대시킬 수 있을 것으로 예상 |
|
비알코올성 |
- 비알코올성 지방간염(NASH, Non-Alcoholic Steatohepatitis)은 알코올 섭취와는 관계없이 간세포 사이 중성지방이 축적돼 간 무게의 5% 이상을 차지하는 지방간 증상과 동반해 간세포가 괴사하는 염증성 징후까지 나타나는 질환으로 심각해지면 간암으로까지 발전할 수 있는 질병 |
바. 경쟁 현황
|
히알루로니다제 |
- 정맥주사용(iv) 항체 및 단백질 의약품을 피하주사용(sc) 의약품으로 대체할 수 있는 인간 히알루로니다제(ALT-B4)의 재조합 단백질을 세계 2번째로 개발하여 제형 및 제조방법에 관한 국내 특허 및 PCT 출원함 |
|
차세대 항암 |
- 항암 항체의약품은 타겟(암세포)에만 작용한다는 장점이 있지만 치료 효능이 낮거나 장기 투여시 약물에 대한 저항성을 나타내는 경우가 종종 발견됨 - 이에 다국적제약사들을 비롯하여 많은 회사들이 항체의약품에 항암약물을 접합하여 효능을 강화한 차세대 항체의약품(ADC 항체-약물 접합치료제)를 개발 중임 - 최근 글로벌 제약사들이 ADC 치료제에 관심을 증대시키면서 전세계적으로 다양한 암을 타겟으로 하는 70 여 가지 차세대 항체의약품이 개발 중이며 시장 성장의 견인차 역할을 하고 있음 |
|
아일리아(Eylea) |
- 최근 특허 만료가 임박한 아일리아의 바이오시밀러 개발에 착수한 경쟁사는 국내 및 해외에서 수개 업체에 이르고 당사가 취득한 특허 부분의 진입 장벽으로 인해 당사의 제품이 최초의 아일리아 바이오시밀러가 될 가능성이 높아짐 |
|
허셉틴 iv / |
- 허셉틴 iv 오리지널의 물질 특허는 유럽과 미국에서 각각 2014년과 2019년에 만료되었으며 이에 맞춰 수많은 제약사들이 허셉틴 바이오시밀러를 개발 중임 |
|
지속형 |
- 유전자 재조합 방식의 성장호르몬을 최초로 개발한 회사는 미국의 Genentech (Roche 사에게 피인수됨)이며 1985년 소마토트로핀이 출시된 이후 Pfizer, Novo Nordisk, Eli Lilly와 같은 글로벌 제약사들이 유전자 재조합 성장호르몬을 개발하여 시장을 주도하고 있고 한국에서는 LG화학, 동아제약, 한국 화이자, 한국 머크 등의 제품도 판매 중임 - 유전자 재조합 성장호르몬 오리지널 제품의 원천 특허는 이미 종료되어 2006년부터 유럽을 시작으로 바이오시밀러 제품이 출시되었으며 현재 전세계 시장에서 판매 중인 오리지널 제품과 바이오시밀러 제품은 대부분 매일 투여하는 1세대 제품들로 성능상 큰 차이가 없음 - 바이오시밀러 제품의 우후죽순 출시로 경쟁이 심화되고 지속형 제품에 대한 시장의 수요가 높아짐에 따라 글로벌 제약회사들은 제품 차별화를 위해 다양한 기술을 이용하여 지속형 제품을 개발하고 있으나 현재까지 성공적으로 시장에 진입한 제품은 없음 |
|
비알코올성 |
- 미국의 링코젠 사와 비알코올성 지방간염(NASH) 치료제 개발을 위해 2018년 7월 독점 옵션 계약을 체결함 |
사. 신규 사업
당사는 바이오의약품을 전문적으로 연구개발하고 있으며, 보고서 제출일 현재 바이오의약품 연구개발 이외에 추진 중인 신규 사업은 없으나, 현재 개발 중인 파이프라인 이외에 당사의 기반기술인 NexP™ 융합 기술, NexMab™ ADC 기술 및 Hybrozyme™기술을 활용하여 추가 파이프라인을 개발하기 위한 연구개발 활동을 지속하고 있습니다.
2. 주요 제품 및 서비스
가. 주요 제품 등의 현황
| (단위: 천원) |
|
품 목 |
2021년 3분기 | 2020년 | 2019년 |
제 품 설 명 |
||||
|---|---|---|---|---|---|---|---|---|
| 매출액 | 비율 | 매출액 | 비율 | 매출액 | 비율 | |||
| 기술이전 수수료 |
지속형 성장호르몬 |
364,580 | 1% | 223,645 | 1% | 513,598 | 2% | 브라질 크리스탈리아사로의 기술이전에 따른 기술이전 수수료 |
| 히알루로니다제 | 6,570,000 | 27% | 25,457,721 | 60% | 11,688,058 | 40% | L/O계약에 따른 기술이전 계약금 및 수익 인식분 | |
|
허셉틴/엔브렐/휴미라 바이오시밀러 |
- | 0% | 530,452 | 1% | 1,113,847 | 4% | 중국 QiLu제약으로의 기술이전에 따른 기술이전 수수료 | |
|
아일리아 바이오시밀러 |
- | - | - | 0% | - | 0% | 국내외 판권 계약에 따른 수수료(주1) | |
|
기술개발 용역 |
- | 0% | - | 0% | 7,057 | 0% |
기타 연구개발 용역 |
|
| 상품 매출 | 16,751,037 | 69% | 14,294,554 | 33% | 14,343,483 | 49% | 상품 매출 | |
| 제품 매출 | 711,002 | 3% | 1,919,470 | 5% | 1,563,138 | 5% | 원재료 매출 | |
|
합 계 |
24,396,619 | 100% | 42,425,842 | 100% | 29,229,182 | 100% |
- |
|
당사는 국내외 제약사들과 바이오베터 및 바이오시밀러를 공동개발 및 사업화에 대한 라이센스아웃(License-out)계약을 체결하고 있으며, 공동개발 과정에서 임상 추진 등 단계적인 기술개발 지표를 달성할 때마다 이에 따른 마일스톤(Milestone) 기술료를 받고 있습니다. 또한 제품화 성공 이후에는 시장에 출시되어 매출이 발생되면 매출액의 일정 부분을 경상기술료(로열티)로 받게됩니다.
주1)연결회사인 (주)알토스바이오로직스는 한림MS 으로의 국내 판권 계약에 따른 수수료를 수취하고 있으나(보고서 작성 기준일 현재까지 누적금액으로 20억원), K-IFRS기준에 따라 판매개시 시점까지 수익인식을 하지 않고 장기선수금으로 처리하고 있습니다.
나. 주요 제품 설명
(1) 인간 히알루로니다제 : 약물 전달방식 피하주사(sc) 제형 변환물질
|
제품명 |
항체치료제의 기존 정맥주사(iv) 약물전달 방식은 환자의 불편함과 부작용 이외에 비용과 투약시간 면에서도 단점으로 작용하므로 환자의 편의성을 증대시키기 위해 약물전달 방식을 피하주사(sc) 제형으로 변환하게 하는 독보적인 플랫폼(기반) 기술인 Hybrozyme™ 을 통해 전세계 2번째로 개발한 재조합 히알루로니다제 |
||
|
주요 사용범위 |
- 항체치료제 개발/판매 신약 및 바이오시밀러 등에 첨가제(exipient, active ingredient) - 피부과 성형외과 및 정형외과 수술 후 통증 완화, 부종 경감 등 독자형 제품 (stand alone) |
||
| 히알루로니 다제 원리 |
- 피하 조직에는 다당류와 단백질이 얽히고 설켜 있어 일종의 보호막이면서 약물의 흐름을 저해하는 단백질 중 hyaluronan(이하 HA) 층을 분해하여 약물의 흡수 및 확산을 용이하게 하는 히알루로니다제는 히알루론산을 분해해 히알루론산의 연결을 일시적으로 끊어 피부 아래에 작은 통로를 만들어 줌으로써 정맥주사(iv) 로만 가능했던 항암제가 이 통로를 통해 흡수되어 혈관에 도달하는 원리임
|
||
| 히알루로니 다제 기술 개발 현황 |
- 현재 시중에 유통되고 있는 동물 유래 히알루로니다제는 1950년 대에 개발되어 정형외과, 성형외과, 안과, 산부인과 등 광범위하게 사용되어 왔으나 99% 이상이 이종단백질로 구성되어 있는 저순도 제품으로 아나필락시스 반응, 가려움, 알러지, 호흡곤란 등 부작용 보고 건수가 해마다 증가하고 있어 고순도의 안전성이 담보된 재조합 히알루로니다제의 개발이 필요한 상황에서 미국의 할로자임 사가 rHuPH20를 세계 최초로 개발하여 로슈 사가 항체치료제에 피하주사(sc) 변환기술로 적용하여 전세계적으로 그 기술을 주목받게 됨 - 당사가 개발한 재조합 히알루로니다제(ALT-B4)는 경쟁사 제품(rHuPH20) 대비 생산성, 효소 활성도가 높고 열 안정성과 면역원성 면에서도 우월한 것으로 평가받고 있으며 기존 인간 히알루로니다제 특허에 대해 기존 특허의 독점적인 권리를 확고히 하면서 차별성이 강조된 히알루로니다제의 집단에 대한 추가 특허를 국제특허출원(PCT) 함으로써 이후에 경쟁사들의 히알루로니다제 개발에 따른 시장 진입을 원천적으로 봉쇄 가능함 |
(2) 차세대 항암 항체치료제(항체-약물 접합 치료제, ADC)
|
제품명 |
항체-약물 접합 기술(ADC) 기술을 활용한 차세대 항암 항체치료제 |
||||
|
주요 사용범위 |
- 다양한 종류의 암의 치료 - 기존 항암 항체치료제에 저항성을 나타내는 암의 치료 |
||||
| 항체-약물 접합체(ADC, Antibody- Drug Conjugate) |
- ADC는 항체(mAb)와 세포독성약물(payload, cytotoxic agent)을 링커(linker)로 접합시킨 구조이며 ADC가 암세포 표면의 수용체를 인식하고 결합하면 암세포 내로 유입되고 약물이 분리되면서 암세포 사멸을 유도하는 원리임 - 일반적으로 항암 약물은 강력한 세포 독성(cytotoxicity)을 나타내어 암 세포가 아닌 정상 세포에도 작용을 하는 반면 항암 항체는 암 세포에 대한 선택성(selectivity)은 있으나 강력한 세포 독성은 없으므로 ADC는 항체의 선택성과 항암 약물의 세포 독성의 장점을 살려 항체의약품보다 효능은 우수하고 합성 약물보다 독성에 의한 부작용이 적은 신개념 기술의 바이오베터임
- 세포독성 약물이 부착된 항체가 암세포의 세포막에 있는 수용체에 선택적으로 결합하면 항체-약물 접합체는 암세포 내로 들어가서 여러 절편으로 절단되며, 이때 분리된 세포독성약물이 추가적으로 암세포의 성장억제 및 사멸 작용을 하며 또한 분리된 세포독성약물은 이웃에 있는 다른 암 세포에도 작용해 암 세포를 사멸하는(Bystander effect) 작용을 함
|
||||
| ADC 기술 개발 동향 |
- 항암 항체치료제의 개발 성공률이 점진적으로 저하되고 있기 때문에 이를 타파하기 위한 새로운 개념의 ADC(Antibody-drug conjugate, 항체-약물 접합체) 개발이 전세계 제약회사들의 커다란 관심사임 - 2013년 미국에서 승인을 받아 시판되고 있는 ADC 기반 유방암 치료제인 Genentech/Roche의 캐사일라(Kadcyla)는 항체인 허셉틴에 항암 약물을 무작위로 접합시킨 것으로 약물을 일단 항체 표면에 비선택적(Non-selective)으로 접합한 후 복잡한 정제 과정을 통해 비교적 균일한 제품으로 생산한 것임 - 캐사일라는 허셉틴 저항성 유방암 환자에게도 뛰어난 효능을 보여 주지만 고가의 항체치료제 중의 하나임 |
||||
| NexMab™ ADC 기술의 특징 |
- 당사의 ADC 기술인 NexMab™ ADC 기술은 항체의 특정부위(C-말단)에만 선택적으로 항암 약물을 접합하는 방식으로 항체의 구조를 가능한 한 원형 그대로 유지하면서 항체에 약물이 선택적으로 접합되도록 하며 생산 수율이 높고 항체 고유의 활성을 저해하지 않으면서 혈액 내에서도 접합이 쉽게 절단되지 않아 체내 지속성이 우수한 2세대 ADC 기술 중의 하나임
|
||||
| NexMab™ ADC 개발 현황 |
- 당사는 NexMab™ 기술을 활용하여 2019년 7월에 미국 FDA에 위암 치료용 희귀의약품으로 등록하면서 임상 절차를 간소화했으며 본 NexMab™ADC 기술을 전세계 8개국에 특허 등록하였고 이를 적용하여 기존 유방암 치료제인 허셉틴보다 약효가 향상된 ADC 유방암치료제(ALT-P7)를 개발하고 있음 - 당사의 ALT-P7 는 암 세포를 이용한 시험에서 항체치료제 대비 뛰어난 약효를 나타내어 투여량 감소, 기존 항암제 내성 환자 및 암 재발 환자에 대해서도 효과적일 것으로 기대되며 임상시험에서 화학약물 요법보다 부작용이 적고 약물병용 요법보다 우수한 약효를 나타낼 것으로 예상되어 상업화 되면 이 분야의 "Best-in-class" 약물이 될 수 있을 것으로 기대됨 |
(3) 아일리아 바이오시밀러
|
제품명 |
황반변성 항체치료제인 아일리아(Eylea)와 동등한 약효를 나타내는 바이오시밀러 |
||
|
주요 사용범위 |
습성 연령 관련 황반변성(wAMD, wet Age-related Macular Degeneration), 망막중심정맥폐쇄성 황반 부종(macular edema following Central Retinal Vein Occlusion), 당뇨성 황반부종(DME, Diabetic Macular Edema) 등 실명성 안과 질환 |
||
| 습성 연령관련 황반변성 (wAMD)이란? |
- 습성 연령관련 황반변성(WAMD, Wet Age-related Macular Degeneration)은 혈관 성장인자(VEGF, Vascular Endothelial Growth Factor)의 과발현으로 망막에 비정상적인 혈관이 자라면서 삼출물이 발생하고 이로 인해 부종이 생기면서 황반(망막 중심의 노란색을 띠는 부위로 중심시야에 해당함)이 압박을 받으며 시력을 잃게 되는 질환임 - WAMD는 산소 결핍과 감염에 의해 발병하는데, 고연령 층일수록 산소 결핍과 감염의 위험이 높아 50세 이상 연령층에서 WAMD의 발병률이 높음 - WAMD 환자는 전세계적으로 2013년 기준 2,400만명으로 추정되며 한국은 보고된 환자 수만 2010년에 9만명에 달하고 인구 고령화로 2025년에는 세 배까지 증가할 것으로 예상되나 미국의 사례로 보았을 때 추정 환자들 중에서 실제 20% 에도 못 미치는 환자만이 진료를 받을 정도로 인지도가 낮고 고가의 항체치료제 비용 부담으로 처방을 받는 환자 수는 진료를 받은 환자 수의 20% 에도 못 미치는 상황임 |
||
| 아일리아 (Eylea) 작용 기전 |
- 아일리아는 안구 내 VEGF에 선택적으로 결합하여 VEGF의 활동을 억제하여 새로운 혈관이 자라지 못하게하고 체액의 누출을 차단해 WAMD 환자의 시력을 유지하거나 회복시키도록 고안된 항체치료제임 - VEGF가 세포의 VEGF 수용체(VEGFR, VEGR Receptor)와 결합하여 혈관의 생성을 촉진하게 되는데, 아일리아는 VEGF에 결합하여 VEGF가 세포의 VEGFR과 결합하는 것을 방해함
|
||
| 당사의 아일리아 바이오시밀러 개발 현황 |
- 엔브렐, 허셉틴 등 다른 항체 바이오시밀러와 달리 아일리아는 아직 전세계적으로도 바이오시밀러 개발이 거의 없는 상황에서 조기 개발을 통해 세계 최초로 제품을 출시할 경우 세계 시장을 선점할 가능성이 큼 - 당사는 2014년 2월 일본의 Kissei 제약과 공동 연구, 개발, 생산 및 판매를 위한 계약을 체결 하였으므로 제품 개발에 성공할 경우 일본 내에서 판매가 가능한 마케팅 기반을 확보하였음 - 당사는 엔브렐 바이오시밀러 개발을 통해 축적한 Fc 기반 바이오시밀러 개발 경험과 노하우를 통해 신속한 기술 개발이 진행되었으며 아일리아 오리지널의 제형 특허를 회피한 독자적인 제형 기술을 확보하여 아일리아 오리지널의 물질 특허가 만료되는 2024년 이후에 출시가 가능함 |
(4) 허셉틴 iv 바이오시밀러와 허셉틴 피하주사(sc) 바이오시밀러
|
제품명 |
유방암 항체치료제인 허셉틴과 동등한 약효를 나타내는 바이오시밀러 |
||||||||||||||||||
|
주요 사용범위 |
- 유방암(HER2 양성 전이성 유방암) ※ HER2 양성 유방암 환자는 전체 유방암 환자의 30% 수준 - 위암(HER2 양성 전이성 위암) |
||||||||||||||||||
| 허셉틴 시장 현황 |
- 2019년 6월을 기점으로 매년 글로벌 시장에서 8조원 규모인 유방암 치료제 허셉틴의 물질 특허가 만료됨에 따라 글로벌 바이오시밀러 시장에 출사표를 내민 바이오기업은 7개사 5종에 이르며 시장 선점을 위한 경쟁이 본격화 됨
|
||||||||||||||||||
| 당사 개발 현황 |
- 허셉틴 바이오시밀러의 경우 당사는 고발현 세포주와 생산 공정 모두를 자체 개발하였기 때문에 원가 경쟁력을 확보하고 저렴한 가격에 허셉틴 바이오시밀러를 출시할 수 있어 바이오시밀러 간 경쟁에서 경쟁력이 있을 것으로 판단됨 - 허셉틴 바이오시밀러는 캐나다에서 임상1상을 완료하였고 중국의 QiLu제약에 기술 이전 계약을 체결한 상황이며 라이센스아웃 이후 중국에서 임상 1,3상 IND를 신청하여 IND 승인을 받은 상태임 - 추가로 당사는 하이브로자임(Hybrozyme™) 원천 기술을 통해 허셉틴 sc 바이오시밀러 개발을 추진 중이며 세계 유일 제품인 로슈사의 허셉틴 sc(하이렉타)와 동등성 시험을 완료하여 동등성 결과를 확보하였고 글로벌 제약사와 기술 이전 협약을 통해 세계 최초의 허셉틴 sc 바이오시밀러 출시를 목표로 하고 있음 |
(5) 지속형 인성장호르몬(hGH-NexP™)
|
제품명 |
NexP™와 결합하여 체내 지속성이 증가된 차세대 지속형 인성장호르몬(hGH) |
||
|
주요 사용범위 |
- 성장호르몬 결핍으로 인한 소아 저성장증(PGHD) 치료 - 성인 성장호르몬 결핍(AGHD) 치료 및 노화억제 효능 |
||
| 성장호르몬의 기능 |
- 성장호르몬(hGH, human Growth Hormone)은 191개의 아미노산으로 구성된 단일 분자 폴리펩타이드이며 뇌하수체 전엽에서 분비되는 단백질 호르몬임 - 뇌하수체에서 분비된 성장호르몬은 간(liver)에서 IGF-1(Insulin-like Growth Factor-1)을 분비시키고, 분비된 IGF-1과 성장호르몬은 체내 여러 조직의 세포증식에 작용하여 인체의 성장을 유도함
|
||
| 성장호르몬 시장 현황 |
- 과거에는 죽은 사람에게서 추출한 성장호르몬을 사용하기도 하였으나, 감염 위험성으로 인해 1985년 이후 사체에서 추출한 성장호르몬은 시장에서 점차 사라지게 됨 - 1985년 Genentech에 의해 최초로 유전자재조합 성장호르몬이 출시된 이후 Eli Lilly, Pfizer, Novo Nordisk 등이 유전자재조합 성장호르몬을 개발하여 판매하고 있으며 한국의 LG화학, 동아제약 등의 업체가 자체 개발하여 국내에서 판매 중임 - 성장호르몬은 2018년 기준 연간 약 4조원이 판매된 주요 블록버스터 바이오의약품 중의 하나이며 국내 시장도 연 500억원에 달함 - 현재 판매되는 성장호르몬 제품들은 모두 1세대 제품으로 뛰어난 약효와 안전성에도 불구하고 매일 주사를 맞아야하는 불편함이 있어 투여 횟수를 줄일 수 있는 1주형 2세대 지속형 성장호르몬의 개발이 요구되고 있음 |
||
|
hGH-NexP™ 특징 및 |
- 1세대 성장호르몬은 물론 다른 지속형 성장호르몬에 비해서도 월등히 우월한 지속성과 약효를 보임 - hGH-NexP™는 주 1회 주사 제품이므로 매일 주사하는 1세대 제품 대비 환자의 투약 순응도가 높기 때문에 치료 효과가 증대되고 잦은 주사의 불편함과 공포감 때문에 성장호르몬 투여를 주저했던 환자들에게 편의를 제공할 수 있으며 제조효율이 뛰어나 가격 경쟁력이 있음 - 2015년 9월 임상 1상 및 2a을 성공적으로 완료하고 인도에서 파트너 사인 브라질 크리스탈리아와 소아용으로 글로벌 임상 진입 및 임상 2/3상을 추진할 예정임 |
3. 원재료 및 생산설비
가. 주요 원재료 매입현황
| (단위: 천원, 미 달러) |
|
매입유형 품 목 |
구 분 |
2019년 (제12기) |
2020년도 |
2021년도 3분기 |
|
원재료 |
국 내 |
2,563,195 | 5,217,607 | 2,187,652 |
|
수 입 |
118,616 $102,449 |
1,255,021 $1,153,512 |
1,061,150 $939,07 |
|
| 국고보조금 | (1,110,130) | (497,179) | (246,949) | |
|
소 계 |
1,571,680 | 5,975,448 | 3,001,853 | |
|
외주가공비 |
국 내 |
3,013,992 | 6,489,705 | 12,689,090 |
|
수 입 |
944,992 $816,197 |
1,797,227 $1,651,863 |
1,637,736 $1,449,324 |
|
| 국고보조금 | (754,826) | (1,432,699) | (248,915) | |
|
소 계 |
3,204,158 | 6,854,233 | 14,077,912 | |
|
합 계 |
국 내 |
5,577,186 | 11,707,312 | 14,876,742 |
|
수 입 |
1,063,608 | 3,052,248 | 2,698,886 | |
| 국고보조금 | (1,864,956) | (1,929,878) | (495,863) | |
|
합 계 |
4,775,839 | 12,829,682 | 17,079,765 |
| 주) | 원재료 제조사가 해외업체이지만 국내의 대리점을 통해 구매하여 원화결재하는 경우에는 '국내'로 분류 |
원재료는 바이오의약품 연구개발 과정에서 필요한 시약 및 실험도구 등을 의미하며, 외주가공비는연구개발 과정에서 일부 실험에 대해 외부에 위탁하여 수행하거나 전임상 또는 임상시료를 외부에 위탁하여 생산하는 경우 지급하는 외주용역비용을 의미합니다.
나. 주요 원재료 가격변동추이
연구개발용 시료 및 도구 등은 대부분 장기간 동안 지속적인 반복 구매를 하게 되는데 국내 대리상을 통해 수입되는 품목이 많아 해외 제조사의 제조원가 상승에 따른 가격 인상 정책 또는 환율 변동에 따라 가격이 변동하게 되며, 구입시마다 거래처와의 협의를 통해 가격을 결정하게 됩니다.
다. 생산능력 및 생산실적
당사는 50리터 규모의 동물세포(CHO cell) 배양기와 정제 설비를 보유하고 있으나, 이는 연구 및 공정 개발(Scale-up) 목적의 소규모 생산 설비로서 양산용 생산시설은 아직 보유하고 있지 않으며, 현재 당사 개발 제품의 전임상 및 임상 시료는 국내외의 CMO(Contract Manufacturing Organization: 위탁 전문 생산기관)를 통해 생산하고 있습니다.
라. 생산설비에 관한 사항
(1) 현황
| (단위: 천원) |
|
공장별 |
자산별 |
소재지 |
2021년 기초 가액 |
2021년 3분기 증감 |
2021년 3분기 상각 |
2021년 |
|
|
증가 |
감소 |
||||||
| 본사 | 토지 | 대전 전민동 | 1,800,512 | - | - | - | 1,800,512 |
| 건물 | 대전 전민동 | 1,860,247 | 1,544,687 | - | 112,715 | 3,292,219 | |
| 연구용기자재 | 대전 전민동 | 6,881,116 | 83,868 | 33,984 | - | 6,931,000 | |
| (감가상각누계액) | (3,539,901) | - | - | 699,745 | (4,239,646) | ||
| (국고보조금) | (2,464) | - | - | (1,109) | (1,355) | ||
| 계 | 3,338,751 | 83,868 | 33,984 | 698,636 | 2,689,999 | ||
| 세레스 F&D | 토지 | 충북 제천 | 984,190 | - | - | - | 984,190 |
| 건물 | 충북 제천 | 3,387,404 | - | - | 66,427 | 3,320,977 | |
| 구축물 | 충북 제천 | 33,063 | - | - | 658 | 32,405 | |
| 기계장치 | 충북 제천 | 3,636,848 | 476,776 | - | 4,113,624 | ||
| (감가상각누계액) | (483,608) | - | 306,139 | (789,747) | |||
| (국고보조금) | - | - | - | ||||
| 계 | 3,153,240 | 476,776 | - | 306,139 | 3,323,877 | ||
| 시설장치 | 충북 제천 | 1,026,836 | 258,200 | - | 1,285,036 | ||
| (감가상각누계액) | (83,367) | - | 86,660 | (170,027) | |||
| (국고보조금) | - | - | - | ||||
| 계 | 943,469 | 258,200 | - | 86,660 | 1,115,009 | ||
| 연구용기자재 | 서울연구소 | 292,186 | 81,765 | - | 373,951 | ||
| (감가상각누계액) | (18,702) | - | 25,501 | (44,203) | |||
| (국고보조금) | (48,721) | 64,557 | (113,278) | ||||
| 계 | 224,763 | 81,765 | - | 90,058 | 216,470 | ||
| 주) 국고보조금으로 구입한 연구용기자재는 재무제표에 국고보조금을 유형자산의 차감계정으로 기재하였습니다. |
(2) 설비의 신설 및 매입 계획
당사는 당사가 개발 중인 바이오의약품의 임상시료 및 상업용 제품 생산시설을 위해 부지를 매입하였으며 향후 순차적으로 생산 시설을 구축해 나갈 계획입니다
4. 매출 및 수주상황
가. 품목별 매출 현황
| (단위 : 천원, 미 달러) |
|
매출유형 |
품 목 |
2019년도 (제12기) |
2020년도 (제13기) |
2021년도 3분기 (제14기 3분기) |
|
| 기술이전 수수료 |
지속형 성장호르몬 |
수 출 |
513,598 ($423,377) |
223,645 ($184,358) |
364,580 ($300,536) |
|
내 수 |
- | - | - | ||
|
소 계 |
513,598 | 223,645 | 364,580 | ||
| 히알루로니다제 |
수 출 |
11,688,058 ($9,894,737) |
25,457,721 ($21,052,632) |
6,570,000 ($6,00,000) |
|
|
내 수 |
- | - | - | ||
|
소 계 |
11,688,058 | 25,457,721 | 6,570,000 | ||
|
허셉틴/엔브렐/휴미라 바이오시밀러 |
수 출 |
1,113,847 ($936,321) |
530,453 ($468,019) |
- - |
|
|
내 수 |
- | - | - | ||
|
소 계 |
1,113,847 | 530,453 | - | ||
|
아일리아 바이오시밀러 |
수 출 |
- | - | - | |
|
내 수 |
- | - | - | ||
|
소 계 |
- | - | - | ||
|
기술개발 용역 |
수 출 |
- - |
- - |
- - |
|
|
내 수 |
7,057 | - | - | ||
|
소 계 |
7,057 | - | - | ||
| 상품매출 |
수 출 |
- - |
- - |
- - |
|
|
내 수 |
14,343,483 | 14,294,554 | 16,751,037 | ||
|
소 계 |
14,343,483 | 14,294,554 | 16,751,037 | ||
| 제품매출 | 수출 | - - |
994,597 ($872,750) |
599,704 ($547,986) |
|
| 내수 | 1,563,138 | 924,873 | 111,299 | ||
| 소계 | 1,563,138 | 1,919,470 | 711,002 | ||
|
합 계 |
수 출 |
13,315,503 ($11,254,434) |
27,206,416 ($22,577,759) |
7,534,284 ($6,848,522) |
|
|
내 수 |
15,913,679 | 15,219,427 | 16,862,336 | ||
|
합 계 |
29,229,182 | 42,425,842 | 24,396,619 | ||
당사는 바이오의약품 개발 초기부터 국/내외 제약사와 공동 개발 및 제품화에 대한 라이센스아웃(License-out) 계약을 체결하고, 제휴사와 공동 연구개발을 진행하면서계약시 라이선스의 대가로써 착수금(Upfront)을 수취하고 계약의 진행에 따라 개발 단계별로 제휴사로부터 마일스톤(Milestone)을 받고 있습니다.
착수금과 마일스톤 금액은 개발 단계별로 개별 계약에 의해 정해진 금액이 다르며, 수익의 인식은 K-IFRS(1115호)를 회계처리 기준으로 채택함에 따라 계약서에 따른 청구금액 기준이 아닌 연구개발 진행율 등을 산정하여 진행기준에 의해 매출액을 인식하는 경우가 발생할 수 있기 때문에 수익의 인식금액과 현금흐름과는 차이가 있습니다.
나. 판매경로 등
(1) 판매조직
당사는 영업을 위한 판매조직을 별도로 갖추고 있지 않습니다.
당사는 국/내외 제약사와의 라이센스아웃(License-out) 계약을 통해 바이오의약품을 공동개발하고 있으며, 개발에 성공할 경우 라이센스아웃(License-out) 계약을 맺은 지역에 대해서는 해당 제휴사가 판매를 담당하게 됩니다.
당사와 라이센스아웃(License-out) 계약을 맺은 주요 파트너들은 모두 해당 지역에서 의약품 마케팅을 위한 인력, 조직, 영업망 및 Know-how 등을 확보하고 있는 글로벌 제약사들이며, 라이센스아웃(License-out) 계약이 체결되지 않은 지역에 대해서는 추가적인 라이센스아웃(License-out) 계약 파트너를 물색하여 라이센스아웃(License-out) 계약 파트너를 통한 판매를 시도할 계획입니다.
(2) 판매경로
당사가 개발 중인 제품들은 개발에 성공하게 될 경우 라이센스아웃(License-out) 계약을 맺은 국/내외 제약사들이 라이센스아웃(License-out) 계약을 맺은 지역에 대해서 판매를 담당하게 되고, 지역별로 의약품의 유통구조 및 경로가 다양하여 판매 경로를 일괄적으로 기술하기는 어렵습니다.
제휴사와 공동 연구개발을 진행하면서 계약시 라이선스의 대가로써 착수금(Upfront)을 수취하고 계약의 진행에 따라 개발 단계별로 제휴사로부터 마일스톤(Milestone)을 받고 있습니다.
현재 당사의 매출은,
국/내외 제약사들과의 라이센스아웃(License-out) 계약에 따라
1. 계약시 라이선스의 대가로써 수취하는 착수금(Upfront)과
2. 개발 단계별로 수령하는 마일스톤(Milestone) 수익 및
3. 품목허가 이후 발생되는 매출에 대한 상호 협의된 비율로 수령하는 경상기술료(로열티) 수익이며,
당사가 라이센스아웃(License-out) 계약을 위해 국/내외 제약사들과 접촉하는 방법은 다음과 같습니다.
- 전시회 및 비즈니스 파트너링 행사 참여
- 국/내외 제약사들의 연락
- 국/내외 대리인(제약업계 출신의 개인 자문위원, 금융회사, 비즈니스 제휴 전문회사 등)를 통한 국/내외 제약사들에 연락
- 국/내외 제약사들에 대한 직접 연락
다. 주요 매출처
| (단위 : 천원, 미 달러) |
|
매출 유형 |
품 목 |
매 출 처 |
2019년도 (제12기) |
2020년도 (제13기) |
2021년도 3분기 (제14기 3분기) |
결제조건 |
|
| 기술이전 수수료 |
지속형 성장호르몬 바이오베터 |
수출 | Cristalia(브) | 513,598 ($423,377) |
223,645 ($184,358) |
364,580 ($300,536) |
청구 후 1개월 내 |
| 히알루로니다제 | 수출 | 글로벌 제약사 (3 개사) |
11,688,058 ($9,894,737) |
25,457,721 ($21,052,632) |
6,570,000 ($6,000,000) |
청구 후 1개월 내 |
|
|
허셉틴/엔브렐/휴미라 바이오시밀러 |
수출 |
Cristalia(브)/ |
1,113,847 ($936,321) |
530,453 ($468,019) |
- - |
청구 후 1개월 내 |
|
|
아일리아 바이오시밀러(주1) |
내수 | 국내 L/O | - | - | - |
청구 후 1개월 내 |
|
|
기술개발 용역 |
수출 |
- |
- | - | - |
청구 후 1개월 내 |
|
|
내수 |
- | 7,057 | - | - | - | ||
|
소계 |
- |
7,057 | - | - | - | ||
| 상품매출 |
수출 |
- | - - |
- - |
- - |
- | |
|
내수 |
- | 14,343,483 | 14,294,554 | 16,751,037 | - | ||
|
소계 |
- | 14,343,483 | 14,294,554 | 16,751,037 | - | ||
| 제품매출 | 수출 | - | - - |
994,597 ($872,750) |
599,704 ($547,986) |
- | |
| 내수 | - | 1,563,138 | 924,873 | 111,299 | - | ||
| 소계 | - | 1,563,138 | 1,919,470 | 711,002 | - | ||
|
합 계 |
수출 |
- |
13,315,503 ($11,254,434) |
27,206,416 ($22,577,759) |
7,534,284 ($6,848,522) |
- | |
|
내수 |
- |
15,913,679 | 15,219,427 | 16,862,336 | - | ||
|
합계 |
- |
29,229,182 | 42,425,842 | 24,396,619 | - | ||
주1)연결회사인 (주)알토스바이오로직스는 한림MS 으로의 국내 판권 계약에 따른 수수료를 수취하고 있으나(보고서 작성 기준일 현재까지 누적금액으로 20억원), K-IFRS기준에 따라 판매개시 시점까지 수익인식을 하지 않고 장기선수금으로 처리하고 있습니다.
라. 수주현황
당사의 바이오의약품 사업은 업종의 특성상 수주와는 관련이 없습니다. 당사는 국/내외 제약사와의 라이센스아웃(License-out) 계약에 따라 공동 연구개발을 수행하면서 단계별로 마일스톤 수익을 받고 있고, 제품 출시 이후에는 상호 협의된 비율에 따라 판매액의 일정부분을 로열티로 받는 사업구조를 가지고 있습니다.
|
제휴사 |
품 목 |
계약일 |
계약만기 |
라이센스아웃 |
계약조건 |
|---|---|---|---|---|---|
| QiLu (중국) |
허셉틴 바이오시밀러 |
17.03.29 | 제품출시후 10년 |
중국 |
- 임상 단계별 기술료 수익 - 중국 판매액에 대한 로열티 수익 |
|
Cristalia (브라질) |
지속형 성장 호르몬 | 19.07.22 | 종료기간 없음 |
남미 |
- 해외 임상을 위한 공동개발 및 기술이전 등 |
| GPC(글로벌 제약사) | 재조합 히알루로니다제 | 19.12.02 | 종료기간 없음 |
전세계 | - 개발(임상/품목허가) 단계별 마일스톤 수익 - 상업화단계의 로열티 수익 |
| TTPC (글로벌 10대 제약사) |
재조합 히알루로니다제 | 20.06.24 | 종료기간 없음 |
전세계 | - 개발(임상/품목허가) 단계별 마일스톤 수익 - 상업화단계의 로열티 수익 |
| Intas (인도) | 인간 히알루로니다아제 | 21.01.07 | 제품출시후 10년 |
전세계 (일부 아시아 국가 제외) |
- 2개 품목에 대하여 개발(임상/품목허가) 단계별 마일스톤 수익 - 품목허가 이후 판매로 인한 로열티 수익 |
| 알토스바이오로직스 (자회사) |
아일리아 바이오시밀러 | 20.12.10 | 2032.12.09 | 전세계 | - 개발(임상/품목허가) 단계별 마일스톤 수익 - 품목허가 이후 판매 발생시 이익배분 |
5. 위험관리 및 파생거래
당사는 글로벌 영업활동을 수행함에 따라 표시통화와 다른 외화 수입, 지출이 발생하고 있으며 이로 인해 환포지션이 발생합니다.
주요 외화로는 미국 달러, 유로화, 일본 엔화 등이 있으며, 당사는 투기적 외환거래는 금지하고 환위험이 최소화될 수 있도록 주기적으로 모니터링, 평가 및 보고하고 있습니다.
당사는 시장위험(금리, 상품가격, 환율 등)과 관련하여 투기적 거래를 금지하는 정책을 시행하고 있으며, 금리나 상품 또는 환율 관련 파생금융상품의 거래내역은 공시대상기간중 없습니다.
당사는 현금성자산에 대하여 정기예금 등 시장위험이 없는 예금상품을 활용하고, 미달러화 등 보유 외화는 외환수급을 고려하여 일정금액을 달러 또는 현지통화로 계속 보유하고 있습니다.
(외환위험)
보고기간종료일 현재 기능통화와 다른 주요 외화로 표시된 금융자산 및 금융부채에 대하여 환율이 5% 변동할 경우 당기손익(법인세효과 반영 전)에 미치는 영향은 다음과 같습니다.
(단위:백만원)
| 구 분 | 당분기말 | 전기말 | ||
| 환율 상승시 | 환율 하락시 | 환율 상승시 | 환율 하락시 | |
| USD | 6,517 | △6,517 | 5,548 | △5,548 |
| EUR | 61 | △61 | - | - |
[△는 부(-)의 값임]
6. 주요계약 및 연구개발활동
당사는 기술이전 계약, 정부과제 계약 등의 주요 경영상의 계약들이 있으며 최근 주요 계약 현황은 다음과 같습니다.
가. 라이센스아웃(License-out) 계약
공시서류 작성기준일 현재 당사가 체결 중인 라이센스아웃(License-out) 계약의 현황은 다음과 같습니다.
< 라이센스아웃(License-out) 계약 총괄표 >
| 품목 | 계약상대방 | 대상지역 |
계약체결일 | 계약종료일 | 총 계약금액 (US$M) |
수취금액 (US$M) |
진행단계 |
| 허셉틴 바이오시밀러 | QiLu 제약 (중국) | 중국 | 2017.03.29 | 제품출시후 10년 |
(공시 유보) | (공시 유보) | 중국 임상3상 준비중 |
| 지속형 인성장흐르몬 | Cristalia (브라질) | 남미 | 2019.07.23 | 종료기간 없음 |
2.0 | 2.0 | 글로벌(인도) 임상1상 완료 |
| 재조합 히알루로니다제 | GPC (글로벌 제약사) |
전세계 | 2019.11.29 | 종료기간 없음 |
1,373.0 | 16.0 | 임상1상 준비중 |
| 재조합 히알루로니다제 | TTPC (글로벌 10대 제약사) |
전세계 | 2020.06.24 | 종료기간 없음 |
3,865.0 | 16.0 | 임상1상 개시 |
| 재조합 히알루로니다제 | Intas Pharmaceuticals (인도) |
전세계 (일부 아시아 국가 제외) |
2021.01.07 | 제품출시후 10년 |
109.0 (+ 로열티) |
6.0 | 임상1상 준비중 |
| 아일리아 바이오시밀러 | 알토스바이오로직스 (자회사) |
전세계 | 2020.12.10 | 2032.12.09 | 7.4 (80억원) |
1.8 (20억원) |
글로벌 임상3상 준비중 |
| 합 계 | 5,363.9 | 38.8 | |||||
(주) L/O계약에 따른 쉬취금액(현금기준)은 K-IFRS기준에 따른 수익인식금액(수익기준)과 일치하지 않습니다.
(1) 품목 : ALT-L2 (허셉틴 바이오시밀러)
| ①계약상대방 | QiLu 제약 (중국) |
| ②계약내용 | 허셉틴 바이오시밀러 독점적 기술 이전 및 중국내 임상시험, 허가, 생산, 상업화 등을 진행 |
| ③대상지역 | 중국 |
| ④계약기간 | - 계약체결일 : 2017.03.29 - 계약종료일 : 제품 출시후 10년 |
| ⑤계약금 총액 | (계약조건에 따라 공시 유보) |
| ⑥수취금액 | <반환의무 없는 금액> - 계약금(Upfront payment) : (공시 유보) <반환의무 발생가능 금액> - 해당사항 없음 |
| ⑦계약조건 | 계약금(Upfront payment) : (공시 유보) - 수취조건 : 계약 체결시 마일스톤(Milestone) : - 개발 마일스톤 (공시 유보) (수취조건 : 각 임상 단계별 진입, 성공, 판매 승인 등) - 연간 매출 마일스톤 (공시 유보) (수취조건 : 매출 발생 시) 로열티(Royalty) : - 수취조건 : 매출 발생시 매출액의 일정부분(공시 유보), 10년간 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 이에 따른 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
| ⑧회계처리방법 | 계약금 수취액은 일시에 수익 인식 마일스톤 수취액은 수취시 일시에 수익 인식 |
| ⑨대상기술 | ALT-L2 (허셉틴 바이오시밀러), 유방암 및 위암 블록버스터 항체치료제인 허셉틴에 대한 바이오시밀러 |
| ⑩개발진행경과 | <거래상대방> - 중국 임상3상 준비중 |
| ⑪기타사항 | 해당사항 없음 |
(2) 품목 : ALT-P1 (지속형 인성장호르몬)
| ①계약상대방 | Cristalia (브라질) |
| ②계약내용 | 지속형 인성장호르몬 해외 임상 개발을 위한 공동개발 및 독점적 기술 이전 |
| ③대상지역 | 남미 지역 |
| ④계약기간 | - 계약체결일 : 2019.07.23 - 계약종료일 : 임상 완료 및 제품 출시 까지 |
| ⑤계약금 총액 | (계약조건에 따라 공시 유보) |
| ⑥수취금액 | <반환의무 없는 금액> - 계약금(Upfront payment) : US$1,000,000 (2019년 8월 수취) <반환의무 발생가능 금액> - 계약금(Upfront payment) : US$1,000,000 US$250,000 (2019년 10월 수취) US$250,000 (2020년 2월 수취) US$250,000 (2020년 2월 수취) US$250,000 (2020년 7월 수취) |
| ⑦계약조건 | 계약금(Upfront payment) : US$2,000,000 - 수취조건 : 1차분 US$1,000,000 계약 체결 후 30일 이내 2차분 US$1,000,000 4회 분할 수령 로열티(Royalty) : - 수취조건 : 매출 발생시 매출액의 일정비율(공시 유보) 임도 임상1상 실패시 계약은 종료될 수 있으며, 이에 따른 계약 종료시에도 계약금 일부인 US$1,000,000 에 대한 반환 의무 있음 |
| ⑧회계처리방법 | 계약금 수취액은 약20개월 동안 분할하여 수익 인식(코로나사태로 인한 정지기간 6.6개월 포함시 26.7개월) 마일스톤 수취액은 수취시 일시에 수익 인식 |
| ⑨대상기술 | ALT-P1 (지속형 인성장호르몬), NexP™ 당사 고유 융합기술에 인성장호르몬을 결합하여 몸속에서 성장호르몬을 오랜 기간 지속시켜 약효를 유지하게하는 차세대 기술 |
| ⑩개발진행경과 | <거래상대방> - 글로벌 임상1상이 2020년 2월에 승인되었으나 코로나-19 사태로 2020년 인도내 셧다운(Shutdown) 발생으로 순연된 임상을 재개하였으며, 2021년 6월 시험을 종료하고 결과보고를 준비중임 - 임상1상이 마무리되면 브라질에서 임상2상을 진행할 계획임 |
| ⑪기타사항 | 해당사항 없음 |
(3) 품목 : ALT-B4 (인간 히알루로니다아제) - ①
| ①계약상대방 | GPC (글로벌 제약사) |
| ②계약내용 | 바이오의약품 정맥주사(iv) 제형을 피하주사(sc) 제형으로 변환시켜 주는 재조합 히알루로니다제 원천 기술에 대한 비독점적 기술 이전 |
| ③대상지역 | 전세계 |
| ④계약기간 | - 계약체결일 : 2019.11.29 - 계약종료일 : 2039.12.01 |
| ⑤계약금 총액 | 최대 US$1.373B(1조 6천억원) |
| ⑥수취금액 | <반환의무 없는 금액> - 계약금(Upfront payment) : US$13,000,000 (2019년 12월 수취) - 마일스톤(Milestone) : 1차 US$3,000,000 (2020년 4월 수취) 2차 US$3,000,000 (2022년 3월 예정) <반환의무 발생가능 금액> - 해당사항 없음 |
| ⑦계약조건 | 계약금(Upfront payment) : US$13,000,000 - 수취조건 : 계약 체결 후 영업일 30일 이내 마일스톤(Milestone) : - 개발 마일스톤/매출 마일스톤/누적 매출 마일스톤 으로 구분 (수취조건 : 각 임상 단계별 진입, 성공, 판매 승인 및 판매금액 달성, 적응증 추가 등) 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 이에 따른 계약 종료시에도 회사의 위약금 지급 의무는 없음 (최대 수령가능 금액은 US$1.373B 이나, 일부 품목이 임상을 실패하거나 판매금액이 적을 경우 축소될 가능성이 있음) |
| ⑧회계처리방법 | 계약금 수취액은 라이선스 제공의 대가로 일시에 수익 인식 마일스톤 수취액은 수취시 일시에 수익 인식 |
| ⑨대상기술 | ALT-B4 (인간 히알루로니다아제), 바이오의약품 정맥주사(iv) 제형을 피하주사(sc) 제형으로 변환시켜 주는 인간 히알루로니다아제 원천 기술 |
| ⑩개발진행경과 | <거래상대방> - 계약 상대방이 지정하는 해외 CMO 기술이전 완료시 조건부 마일스톤 수취 예정 - 협의 중인 첫번째 품목 임상1상 진입 부터 개발 마일스톤 수취 예정 |
| ⑪기타사항 | - 해외 CMO 위탁생산 계약 체결 완료 |
(4) 품목 : ALT-B4 (인간 히알루로니다아제) - ②
| ①계약상대방 | TTPC(글로벌 10대 제약사) |
| ②계약내용 | 바이오의약품 정맥주사(iv) 제형을 피하주사(sc) 제형으로 변환시켜 주는 재조합 히알루로니다제 원천 기술에 대한 비독점적 기술 이전 |
| ③대상지역 | 전세계 |
| ④계약기간 | - 계약체결일 : 2020.06.24 - 계약종료일 : 2040.03.24 |
| ⑤계약금 총액 | 최대 US$3.865B(4조 7천억원) |
| ⑥수취금액 | <반환의무 없는 금액> - 계약금(Upfront payment) : 1차분 US$8,000,000 (2020년 7월 수취) 2차분 US$8,000,000 (2020년 8월 수취) <반환의무 발생가능 금액> - 해당사항 없음 |
| ⑦계약조건 | 계약금(Upfront payment) : US$16,000,000 - 수취조건 : 계약 체결 후 1차분 영업일 30일 이내, 2차분 비임상 독성 자료 전달 후 영업일 30일 이내 마일스톤(Milestone) : - 개발 마일스톤 (수취조건 : 각 임상 단계별 진입, 성공, 판매 승인, 적응증 추가 등) - 매출 마일스톤 (수취조건 : 판매금액 달성 시) - 누적 매출 마일스톤 (수취조건 : 누적 매출 달성 시) 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 이에 따른 계약 종료시에도 회사의 위약금 지급 의무는 없음 (최대 수령가능 금액은 US$3.865B 이나, 일부 품목이 임상을 실패하거나 판매금액이 적을 경우 축소될 가능성이 있음) |
| ⑧회계처리방법 | 계약금 수취액은 라이선스 제공의 대가로 일시에 수익 인식 마일스톤 수취액은 수취시 일시에 수익 인식 |
| ⑨대상기술 | ALT-B4 (인간 히알루로니다아제), 바이오의약품 정맥주사(iv) 제형을 피하주사(sc) 제형으로 변환시켜 주는 인간 히알루로니다아제 원천 기술 |
| ⑩개발진행경과 | <거래상대방> - 협의 중인 첫번째 품목 임상1상 진입 부터 개발 마일스톤 수취 예정 |
| ⑪기타사항 | - 해외 CMO 위탁생산 계약 체결 완료 |
(5) 품목 : ALT-B4 (인간 히알루로니다아제) - ③
| ①계약상대방 | Intas Pharmaceuticals (인도 소재 다국적 제약사) |
| ②계약내용 | 바이오의약품 정맥주사(iv) 제형을 피하주사(sc) 제형으로 변환시켜 주는 재조합 히알루로니다제 원천 기술에 대해 계약 상대방이 개발 중인 2개 품목에 대해 독점적 기술 이전 |
| ③대상지역 | 전세계(일부 아시아 국가 제외) |
| ④계약기간 | - 계약체결일 : 2021.01.07 - 계약종료일 : 2개 품목에 대한 제품 출시 후 10년 |
| ⑤계약금 총액 | 최대 US$109M(1,180억원) + 로열티(판매금액에 따른 최대 두 자릿수 비율 %) |
| ⑥수취금액 | <반환의무 없는 금액> - 계약금(Upfront payment) : US$6,000,000 (2021년 1월 수취) <반환의무 발생가능 금액> - 해당사항 없음 |
| ⑦계약조건 | 계약금(Upfront payment) : US$6,000,000 - 수취조건 : 계약 체결 후 10일 이내 마일스톤(Milestone) : - 개발 마일스톤 (수취조건 : 각 임상 단계별 진입, 성공, 판매 승인, 적응증 추가 등) - 매출 마일스톤 (수취조건 : 판매금액 달성 시) - 누적 매출 마일스톤 (수취조건 : 누적 매출 달성 시) 로열티(Royalty) : - 수취조건 : 매출 발생시 상호 협의된 비율 (최대 두자릿수 %) 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 이에 따른 계약 종료시에도 회사의 위약금 지급 의무는 없으며 일부 품목이 임상을 실패하거나 판매금액이 적을 경우 축소될 가능성이 있음 |
| ⑧회계처리방법 | 계약금 수취액은 라이선스 제공의 대가로 일시에 수익 인식 마일스톤 수취액은 수취시 일시에 수익 인식 |
| ⑨대상기술 | ALT-B4 (인간 히알루로니다아제), 바이오의약품 정맥주사(iv) 제형을 피하주사(sc) 제형으로 변환시켜 주는 인간 히알루로니다아제 원천 기술 |
| ⑩개발진행경과 | <거래상대방> - 협의 중인 첫번째 품목 임상1상 진입 부터 개발 마일스톤 수취 예정 |
| ⑪기타사항 | - 해당 사항 없음 |
(6) 품목 : ALT-L9 (아일리아 바이오시밀러)
| ①계약상대방 | 알토스 바이오로직스 (자회사) |
| ②계약내용 |
습성황반변성(WAMD, Wet Age-related Macular Degeneration) 노인성 안과질환 치료제인 오리지널 신약 아일리아(성분명 애플리버셉) 바이오시밀러의 글로벌 임상 및 품목허가, 판매 등 독점 실시권 부여 |
| ③대상지역 | 전세계 |
| ④계약기간 | - 계약체결일 : 2020.12.10 - 계약종료일 : 2032.12.09 |
| ⑤계약금 총액 | 80억원 + 이익분배 (비율 약정) |
| ⑥수취금액 | <반환의무 없는 금액> - 계약금(Upfront payment) : 20억원 (2021년 1월 수취) <반환의무 발생가능 금액> - 해당사항 없음 |
| ⑦계약조건 | 계약금(Upfront payment) : 20억원 - 수취조건 : 계약 체결 후 30일 이내 마일스톤(Milestone) : - 개발 마일스톤 (수취조건 : 임상3상 진입 및 만료, 품목허가 시) 이익분배(Profit Sharing) : - 수취조건 : 매출 발생시 약정 비율에 따라 이익을 배분하기로 함 임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 이에 따른 계약 종료시에도 회사의 위약금 지급 의무는 없음 |
| ⑧회계처리방법 | 계약금 및 품목허가시까지 마일스톤 수취액은 51개월 동안 분할하여 수익 인식 상업생산시 이익분배 수취액은 수취시 일시에 수익 인식을 예정임 |
| ⑨대상기술 | 습성황반변성(WAMD, Wet Age-related Macular Degeneration) 노인성 안과질환 치료제인 오리지널 신약 아일리아(성분명 애플리버셉) 바이오시밀러(ALT-L9) |
| ⑩개발진행경과 | <거래상대방> - 협의 중인 첫번째 품목 임상3상 진입 부터 마일스톤 수취 예정 |
| ⑪기타사항 | - 해당 사항 없음 |
나. 라이센스인(License-in) 계약
해당사항 없습니다
다. 기술제휴 계약
해당사항 없습니다
라. 진행중인 정부과제 계약
| 계약상대방 | 사업기간 | 총 사업비(백만원) | 계약명칭 |
|
산업통상자원부 |
2018.04.01~ 2022.06.30 |
8,776 |
차세대 지속형 인성장호르몬 의약품의 개발 |
| 중소기업기술정보진흥원 | 2020.07.01~2021.06.30 | 187 | 의료기기 해외인증을 위한 고순도 hyaluronidase 제조기술 개발 |
| 한국보건산업진흥원 | 2020.07.01~2021.12.31 | 960 | 면역억제제 제조공정 개발 및 사업화 |
| 국가신약개발사업단 | 2021.09.01~2023.08.31 | 1,200 | 차세대 지속형 성장호르몬 수용체 길항제의 개발 |
7. 기타 참고사항
가. 연구개발 활동 개요
당사는 대덕연구개발특구에 위치한 차세대 바이오 의약품 개발 전문 바이오벤처기업으로 환자의 편이성을 높이는 정맥주사(iv)의 피하주사(sc)형으로 전환하는 Hybrozyme™ 기술, 차세대 표적 항암 항체 치료제 NexMab™ ADC 기술 및 기존 바이오 의약품보다 효능이 개선된 바이오베터 의약품 NexP™ Fusion Protein 기술 등을 연구개발하고 있습니다.
1. Hybrozyme™ 기술: 당사 고유 기술인 Hybrozyme™ 는 단백질 공학 기술에 기반한 신규의 재조합 히알루로니다제 개발에 적용한 원천기술로 정맥주사(iv) 만이 가능했던 기존 항체치료제나 단백질 의약품의 투여 방법에 대해 환자의 편의성을 도모하고 투여가 매우 간편하도록 피하주사(sc) 방식으로 전환할 수 있도록 하는 기반기술로 활용 범위가 크고 다양한 장점을 가지고 있습니다.
2. NexMab™ ADC 기술: 항체-약물 접합기술(ADC)은 표적 물질이 발현된 세포에 선택적으로 약물을 전달하여 약물의 효과를 극대화하는 차세대 신약 기술이며 당사의 NexMab™ 기술을 활용하여 기존 항암 항체 치료제 대비 개선된 효능을 보이면서 부작용은 적은 항암치료제를 개발하여 현재 유방암치료제로 임상 1상 투여를 완료하였습니다. 위암치료제로는 미국 FDA에 희귀의약품으로도 등록되었으며 병용투여 등 추가 임상시험 준비 중입니다.
3. NexP™ Fusion Protein 기술: 당사 고유의 기술로 개발한 NexP™라는 Carrier protein과 바이오의약품을 융합(Fusion)하여 기존의 바이오의약품보다 체내 지속성이 증가된 차세대 지속형(Long-acting) 단백질의약품 개발이 가능하게 되었으며 이러한 기반기술을 활용하여 지속형 성장호르몬의 국내2상을 완료하고 저신장 소아를 대상으로 하는 글로벌 임상을 인도에서 진행 중이며, 아울러 지속형 혈우병치료제로 개발을 확대하고 있습니다.
4. 바이오시밀러 대량생산 Know-how: 당사의 고유한 제형 및 생산 기술을 적용하여 바이오시밀러 제품을 개발하고 있습니다.
당사는 2008년 설립되었고 2014년 12월 기술성장기업 특례로 코스닥시장에 상장되었으며, 현재까지 해외 제약사와 10건 이상의 공동 연구/개발 계약을 체결하고 기술 사업화에 매진하고 있습니다.
창업 초기부터 지속 경영이 가능한 자생력을 갖춘 바이오벤처 기업의 위상을 갖추고자 플랫폼(기반) 기술을 바탕으로 한 바이오신약 개발을 목표로 하면서도 바이오시밀러(Biosimilar) 개발 사업을 병행함으로써 연구개발 경험을 축적하고 수익을 창출하는 Cash-cow 전략을 마련하여 장기간의 연구개발 및 기업 운영에 필요한 현금흐름을 창출하고자 노력하였습니다. 이러한 안정적인 재무구조를 바탕으로 글로벌 경쟁력을 갖춘 바이오베터 원천기술 기반의 차세대 바이오베터 사업부문을 성장 동력으로 확보하였습니다.
벤처기업 확인(기술보증기금, 2009-2021), 병역지정업체(병무청, 2012) 및 시정발전유공기업(대전광역시, 2012), 글로벌IP스타기업(특허청, 2019-2021), 두뇌역량우수전문기업(산업부, 2014-2020), 지역산업진흥 유공기업( 산업부, 2016), 청년친화강소기업(고용부, 2016-2020), 혁신형 제약기업(복지부, 2018-2021), IP경영인증기업(특허청, 2019-2022)으로 선정되었으며, 2017년 바이오분야우수기업으로 산업부장관상 수상, 2018년 제1회 대한민국 바이오의약품대상에서 대상인 복지부장관상을 수상하였습니다.
나. 연구개발 담당 조직
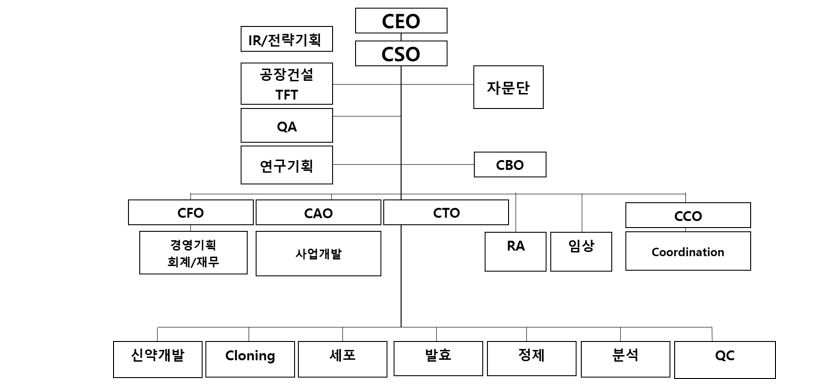
당사의 주요 연구개발조직은 기업부설연구소 산하 6개 연구개발 부서 및 2개 연구관리 부서로 구성되어 프로젝트 및 기능에 따라 조직을 구성하여 연구, 개발 업무의 효율성을 극대화 할 수 있는 조직 체계를 갖추고 있습니다.
당사의 연구조직은 기능(function)별 조직과 프로젝트별 조직이 matrix 형태로 구성된 조직으로서 적은 인원으로 많은 프로젝트를 효율적으로 수행할 수 있다는 장점이 있습니다. 또한 각 연구원들은 matrix 체제 하에서 어느 한 기능에 대한 전문가가 되는 것은 물론, 여러 프로젝트들에 대한 이해도를 높여 연구개발 전문가로서 폭 넓은 시야를 확보할 수 있다는 점에서 개개인의 발전 가능성이 큰 연구원 중심의 조직 체계라고 할 수 있습니다.
 |
|
연구소 조직도 |
다. 연구개발관련 전문인력 현황
당사의 주요 연구개발 조직은 기업부설연구소 산하 8개 부서로 구성되어 있습니다.
| 구 분 | 인 원 | ||||
| 박사 | 석사 | 기타 | 합계 | ||
| 기업부설연구소 총괄 | 1 | 2 | 1 | 4 | |
| 연구소 | Cloning 그룹 | 1 | 1 | 1 | 3 |
| 세포 그룹 | 2 | 2 | 0 | 4 | |
| 발효 그룹 | 0 | 9 | 0 | 9 | |
| 정제 그룹 | 0 | 11 | 2 | 13 | |
| 분석 그룹 | 1 | 11 | 4 | 16 | |
| 신약개발 | 7 | 6 | 0 | 13 | |
| 연구전담 Total | 12 | 42 | 8 | 62 | |
| 연구관리 | 연구지원 | 0 | 2 | 3 | 5 |
| 연구행정 | 1 | 3 | 2 | 6 | |
| 연구관리 Total | 1 | 5 | 5 | 11 | |
| 합 계 | 13 | 47 | 13 | 73 | |
라. 핵심 연구인력
당사의 핵심 연구인력은 최고경영자(CEO)인 박순재 대표이사, CSO인 정혜신 박사, CTO 겸 연구소장인 이승주 부사장, 정경훈 전무, 김규완 상무, 이상미 상무, 유선아 박사, 이선배 박사 등입니다.
| 직위 | 성명 | 담당업무 | 주요 경력 | 주요 연구실적(최근 5건) |
| 대표이사 (CEO) |
박순재 | 최고 경영책임자 |
- 미국 MIT, Post-Doc - ㈜LG생명과학, 바이오텍연구소 - ㈜LG생명과학, 상무이사, 사업개발 및 해외 라이센싱 - 한화케미칼, 상무 - 바이넥스, 대표이사 |
1. Chung H-S, Kim J-S, Lee SM, Park SJ (2017) Role of the P2 residue of human alpha 1-antitrypsin in determining target protease specificity. PLoS ONE 12(9): e0185074. 2. Chung H-S, Lee S, Park SJ (2016) Oxidation Protection in Metal-Binding Peptide Motif and Its Application to Antibody for Site-Selective Conjugation. PLoS ONE 11(7): e0159451. 3. Chung H-S, Kim J-S, Lee SM, Park SJ (2016) Additional N-glycosylation in the N-terminal region of recombinant human alpha-1 antitrypsin enhances the circulatory half-life in Sprague-Dawley rats. Glycoconj J (2016) 33:201-208 4. Chung H-S, Lee SM, Park SJ et al. (2013) N-glycan analysis of human α1-antitrypsin produced in Chinese hamster ovary cells. Glycoconj J (2013) 30:537-547 5. Yoon, W.H., Park, S.J., Kim, I.C., and Lee, M.G. (1997) Pharmacokinetics of Recombinant Human Erythropoietin in Rabbits and 3/4 Nephrectomized Rats. Research Communications in Molecular Pathology and Pharmacology. 96, 227-240 |
| CSO | 정혜신 | 최고사업 전략책임자 |
- Boston Biomedical Research Institute, Post-Doc - ㈜LG생명과학, 바이오텍연구소 책임연구원 - 한남대, 생명시스템과학과 교수 |
1. Chung H-S, Kim J-S, Lee SM, Park SJ (2017) Role of the P2 residue of human alpha 1-antitrypsin in determining target protease specificity. PLoS ONE 12(9): e0185074. 2. Chung H-S, Lee S, Park SJ (2016) Oxidation Protection in Metal-Binding Peptide Motif and Its Application to Antibody for Site-Selective Conjugation. PLoS ONE 11(7): e0159451. 3. Chung H-S, Kim J-S, Lee SM, Park SJ (2016) Additional N-glycosylation in the N-terminal region of recombinant human alpha-1 antitrypsin enhances the circulatory half-life in Sprague-Dawley rats. Glycoconj J (2016) 33:201-208 4. Chung H-S, Lee SM, Park SJ et al. (2013) N-glycan analysis of human α1-antitrypsin produced in Chinese hamster ovary cells. Glycoconj J (2013) 30:537-547 5. Y-M Kim, SM Lee & H-S Chung (2013) Novel AGLP-1 albumin fusion protein as a long-lasting agent for type 2 diabetes. BMB Rep. 2013; 46(12): 606-610 |
| 연구소장 (CTO) |
이승주 | 연구개발 총괄 |
- ㈜LG생명과학 - 제넥셀세인/ 에이프로젠 - ㈜LG화학, 생명과학연구소 연구위원 |
1. Cell culture engineering XIV Poster Presentations(2014. May), Jun Jung, Wonseok Song, Juneok Lee, Raeung Jeong, Yeon Chul Kim, Seung Joo Lee, Influence of osmolarity in culture medium on galactosylation of a biosimilar monoclonal antibody 2. Jae Seong Lee, Tae Kwang Ha, Seung Joo Lee, Gyun Min Lee, “Current state and perspectives on erythropoietin production”, Appl Microbiol Biotechnol. (2012) Sep;95(6):1405-16 3. Woo Suk Ahn, Jae-Jin Jeon, Yeong-Ran Jeong, Seung Joo Lee, Sung Kwan Yoon, "Effect of Culture Temperature on Erythropoietin Production and Glycosylation in a Perfusion Culture of Recombinant CHO Cells", Biotechnol Bioeng. (2008) Dec 15;101(6):1234-44. 4. Cell Culture Engineering XII Poster Presentations(2010. 4), Jong Kwang Hong, Gyun Min Lee, Seung Joo Lee, Sung Kwan Yoon, Enhancing Recombinant Protein Production and Extending Culture Longevity in CHO Cell Culture 5. Cell Culture Engineering XII Poster Presentations, 2010. 4. Su Jeong Hwang, Gyun Min Lee, Gou Young Koh, Seung Joo Lee, Sung Kwan Yoon, Chemical Chaperones Provide Improved Productivity and Reduce Aggregation of Recombinant FLAG-COMP-ANG1 in CHO Cells |
| 전무 (CCO) |
정경훈 | Chief Coordination Officer |
- ㈜LG화학, 바이오텍연구소 연구원 - Harvard Medical School, Instructor in Medicine - 머젠스(현 KT&G생명과학), CSO/연구이사 - 가천대학교 길병원 임상의학연구소 |
1. Oh H*, Jeong K-H*, Han HY, Son HJ, Kim SS, Lee HJ, Kim S, Sa JH, Jun H-S, Ryu JH, and Choi CS. A potent and selective 11b-hydroxysteroid dehydrogenase type 1 inhibitor, SKI2852, ameliorates metabolic syndrome in diabetic mice models. (*co-first authors), European Journal of Pharmacology(2015), 768:139-148. 2. Zhou L, Park S-Y, Xu L, Xia X, Ye J, Su L, Jeong K-H, Hur JH, Oh H, Tamori Y, Zingaretti CM, Cinti S, Argente J, Yu M, Wu L, Ju S, Guan F, Yang H, Choi CS, Savage DB, and Li P. Insulin resistance and white adipose tissue inflammation are uncoupled in energetically challenged Fsp27-deficient mice., Nature Communications(2015), 6:5949. 3. Shim KH, Jeong K-H, Bae SO, Kang MO, Maeng EH, Choi CS, Kim Y-R, Hulme J, Lee EK, Kim M-K, and An SSA. Assessment of ZnO and SiO2 nanoparticle permeability through and toxicity to the blood-brain barrier using Evans blue and TEM.,International Journal of Nanomedicine (2014) 9(suppl 2):225-233. 4. Lee H-Y, Jeong K-H, and Choi CS. In-depth metabolic phenotyping of genetically engineered mouse models in obesity and diabetes.Mammalian Genome (2014) 25(9-10):508-521. 5. Shin S, Park J, Li Y, Min KN, Kong G, Hur GM, Kim JM, Shong M, Jung M-S, Park JK, Jeong K-H, Park MG, Kwak TH, Brazil DP, and Park JS. b-Lapachone alleviates alcoholic fatty liver diseases in rats.,Cellular Signalling (2014) 26(2):295-305. |
| 상무 | 김규완 | 신약개발 총괄 |
㈜LG생명과학, 바이오텍연구소 책임연구원/부장 |
1. Properties of Acetyl-CoA Synthetase from Pseudomonas fluorescens, J. Biochem. Mol. Biol.(1996) |
| 상무 | 이상미 | 연구기획 담당 |
- ㈜LG생명과학, 바이오텍연구소 선임연구원 - 미국 메릴랜드주립대학, 연구원 - Cangenbio, 연구원 |
1. Chung H-S, Kim J-S, Lee SM, Park SJ (2017) Role of the P2 residue of human alpha 1-antitrypsin in determining target protease specificity. PLoS ONE 12(9): e0185074. 2. Chung H-S, Lee S, Park SJ (2016) Oxidation Protection in Metal-Binding Peptide Motif and Its Application to Antibody for Site-Selective Conjugation. PLoS ONE 11(7): e0159451. 3. Chung H-S, Kim J-S, Lee SM, Park SJ (2016) Additional N-glycosylation in the N-terminal region of recombinant human alpha-1 antitrypsin enhances the circulatory half-life in Sprague-Dawley rats. Glycoconj J (2016) 33:201-208 4. Chung H-S, Lee SM, Park SJ et al. (2013) N-glycan analysis of human α1-antitrypsin produced in Chinese hamster ovary cells. Glycoconj J (2013) 30:537-547 5. Y-M Kim, SM Lee & H-S Chung (2013) Novel AGLP-1 albumin fusion protein as a long-lasting agent for type 2 diabetes. BMB Rep. 2013; 46(12): 606-610 |
| 팀장 | 유선아 | 비임상 총괄 |
- 미국 Case Western Reserve University, Post-Doc - 미국 Cleveland Clinic Foundation, Post-Doc - 시드바이오칩스, 팀장 - 솔젠트㈜, 이사 |
1. Fan C, Quyang P, Timur AA, He P, You SA, Hu Y, Ke T, David DJ, Chen Q, Wang QK. (2009) Novel roles of GATAa1 in regulation of angiogenic factor AGGF1 and endothelial cell function. J Biol Chem. 284(35): 23331-23343.] 2. Du W, Bautista JF, Yang H, Diez-Sampedro A, You SA, Wang L, Kotagal P, L Ders HO, Shi J, Cui J, Richerson GB, Wang QK. (2005) Calcium-sensitive potassium channelopathy in human epilepsy and paroxysmal movement disorder. Nat. Genet. 37(7): 733-738. 3. *Tian XL, *Kadaba R, *You SA, *Liu M, Timur AA, Yang L, Chen Q, Szafranski P, Rao, S, Wu L, Housman DE, DiCorleto PE, Driscoll DJ, Borrow J, Wang Q. (2004) dentification of an angiogenic factor that when mutated causes susceptibility to Klippel-Trenaunay syndrome. Nature 427(6975): 640-645. (*These authors contributed equally to this work) 4. You SA, Archacki SR, Angeloui G, Moravec CS, Rao S, Kinter M, Topol EJ, and Wang Q. (2003) Proteomic approach to coronary atherosclerosis shows ferritin light chain as a significant marker: evidence consistent with iron hypothesis in atherosclerosis. Physiol. Genomics 13(1): 25-30. 5. Basu A, You SA and Haldar S. (2000) Regulation of Bcl2 phosphorylation by stress response kinase pathway. Int. J. Oncol. 16: 497-500. |
| 팀장 | 이선배 | RA 총괄 | - 미국 Univ. of Texas, Post-Doc - 이화여대 연구교수 |
1. Chung H-S, Lee S, Park SJ (2016) Oxidation Protection in Metal-Binding Peptide Motif and Its Application to Antibody for Site-Selective Conjugation. PLoS ONE 11(7): e0159451. 2. Sunbae Lee, Yoon Soo Bae, “Monomeric and Dimeric Model of ERK2 in Conjunction with Studies on Cellular Localization, Nuclear Translocation, and In Vitro Analysis”, Mol. Cells, (2012). 33(4), 325. 3. Sunbae Lee, Mangalika Warthaka, Chunli Yan, Tamer Kaoud, Pengyu Ren, Kevin N. Dalby, “Examining Docking Interactions on ERK2 with Modular Peptide Substates”, Biochemistry (2011), 50 (44), 9500. 4. Sunbae Lee, Mangalika Warthaka, Chunli Yan, Tamer Kaoud, Andrea Piserchio, Ranajeet Ghose, Pengyu Ren, Kevin N Dalby, “A Model of a MAPK-Substrate Complex in an Active Conformation: A Computational and Experimental Approach”, Plos One (2011), 6(4), e18594. 5. Yan, Chunli; Kaoud, Tamer; Lee, Sunbae; Dalby, Kevin; Ren, Pengyu, “Understanding the specificity of a docking interaction between JNK1 and the scaffolding protein JIP1 between JNK1 and the scaffolding protein JIP1”, J. Phys. Chem. B (2011), 115, 1491. |
마. 연구개발비용
당사의 최근 3년간 연구개발비용은 다음과 같습니다.
당사는 개발 중인 파이프라인별로 연구인력의 인건비, 실험 시약 및 재료비, 외주용역비 등을 당기 비용으로 회계처리하고 있으며, 개발비 조건을 충족 시 무형자산으로 인식 할 예정입니다.
< 연구개발비용 현황 (별도 재무제표 기준) >
| (단위 : 천원) |
| 과목 | 2021년 3분기 (14기) | 2020년 (13기) | 2019년 (12기) | |
| 원재료비 | 1,973,493 | 4,559,148 | 2,681,810 | |
| 인건비 | 3,075,458 | 3,257,389 | 3,566,404 | |
| 감가상각비 | 803,501 | 1,037,492 | 558,031 | |
| 외주용역비 | 13,428,354 | 7,919,929 | 3,958,984 | |
| 기타 | 1,500,602 | 1,734,355 | 1,008,248 | |
| 연구개발비용 합계 | 20,781,408 | 18,508,313 | 11,773,478 | |
| (정부보조금) | (582,254) | (2,268,032) | (2,278,631) | |
| 보조금 차감 후 금액 | 20,199,154 | 16,240,281 | 9,494,846 | |
| 회계처리 | 판매비와 관리비 | 11,617,559 | 7,583,530 | 6,457,060 |
| 매출원가 | 8,581,596 | 8,656,750 | 3,037,786 | |
| 개발비(무형자산) | - | - | - | |
| 연구개발비 / 매출액 비율 [연구개발비용계÷당기매출액×100] |
283.13% | 70.61 | 88.37% | |
* 정부보조금(국고보조금)을 차감하기 전의 연구개발비용 지출총액을 기준으로 산정
< 연구개발비용 현황 (연결 재무제표 기준) >
| (단위 : 천원) |
| 과목 | 2021년 3분기 (14기) | 2020년 (13기) | 2019년 (12기) | |
| 원재료비 | 2,251,852 | 4,559,148 | 2,681,810 | |
| 인건비 | 3,159,133 | 3,257,389 | 3,566,404 | |
| 감가상각비 | 803,501 | 1,037,492 | 558,031 | |
| 외주용역비 | 14,040,084 | 7,919,929 | 3,958,984 | |
| 기타 | 1,603,688 | 1,842,057 | 1,008,248 | |
| 연구개발비용 합계 | 21,858,257 | 18,616,014 | 11,773,478 | |
| (정부보조금) | (90,135) | (2,268,032) | (2,278,631) | |
| 보조금 차감 후 금액 | 20,783,885 | 16,347,982 | 9,494,846 | |
| 회계처리 | 판매비와 관리비 | 11,743,487 | 7,691,232 | 6,457,060 |
| 매출원가 | 8,986,864 | 8,656,750 | 3,037,786 | |
| 개발비(무형자산) | - | - | - | |
| 연구개발비 / 매출액 비율 [연구개발비용계÷당기매출액×100] |
89.60% | 43.88% | 40.28% | |
* 정부보조금(국고보조금)을 차감하기 전의 연구개발비용 지출총액을 기준으로 산정
바. 연구개발실적
(1) 연구개발 진행 현황 및 향후계획
공시서류 작성기준일 현재 당사가 연구개발 진행 중인 신약[복제약(시밀러)]의 현황은 다음과 같습니다.
< 연구개발 진행 총괄표 >
|
구 분 |
품 목 |
적응증 |
연구 시작일 |
현재 진행단계 |
비 고 |
||
|
단계(국가) |
승인일 |
||||||
|
바이오 |
신약 |
ALT-P1 |
성장호르몬 |
2008년 |
임상 1상(한국) 임상 1b/2a(한국) 임상 1상(인도) |
2014년 2017년 2020년 |
해외 L/O |
|
ALT-P7 |
유방암 |
2011년 |
임상 1상(한국) |
2017년 |
임상 2상 준비 | ||
|
ALT-B4 |
피하주사 |
2017년 |
전임상 완료 |
- |
해외 L/O (3건), |
||
| ALT-BB4 | 부종/통증 완화 |
2017년 | 임상 1상 IND (한국) |
2021년 | Pivotal 임상 (품목허가용) |
||
|
바이오 |
ALT-L9 |
습성 |
2014년 |
임상 1상(한국) |
2019년 |
자회사 L/O |
|
| ALT-L2 | 유방암/위암 | 2011년 | 임상 1상(캐나다) | - | 해외 L/O (2건) 임상 3상 준비중 |
||
품 목: ALT-P1
|
①구 분 |
바이오 신약 |
|
②적응증 |
[주 적응증] 성장호르몬 결핍증 |
|
③작용기전 |
성장호르몬 수용체에 결합하여 펩타이드 호르몬인 IGF-1을 분비시켜 골조직 세포 분열 및 미분화 연골세포의 분화를 자극하여 성장을 촉진 |
|
④제품의 특성 |
- 지속형 인성장호르몬인 ALT-P1은 알파-1 안티트립신을 모체로 하여 당사가 자체 개발한 지속형 플랫폼 기술인 NexP™ (지속형 단백질 기술)을 인성장호르몬과 융합(fusion)하여 기존의 인성장호르몬보다 체내 지속성이 증가(체내 반감기 |
|
⑤진행경과 |
1. 한국 임상1상: 건강한 성인(HV) 대상으로 단회투여 안전성 시험 - 2014년 4월 23일 임상승인 - 2017년 7월 11일 임상승인 - 2020년 2월 21일 임상승인 (COVID-19 pandemic 인도 셧다운으로 지연됨) |
|
⑥향후계획 |
- 브라질의 크리스탈리아 사와 기술이전 계약후 인도 임상1상 진입 (2021년 12월 임상시험결과보고서 완료 예정). |
|
⑦경쟁제품 |
시판 중인 인성장호르몬 현황 2. 지속형 인성장호르몬 - 트랜스콘T (어센디스 파마, 2020년 6월 FDA BLA 제출) |
|
⑧관련논문 등 |
해당사항없음 |
|
⑨시장규모 |
- 전세계 성장호르몬결핍증(GHD) 시장 규모는 2016년 14.2억 달러에서 2026년 |
|
⑩기타사항 |
한국산업기술평가관리원의 바이오산업핵심기술개발사업(유망바이오 IP 사업화 촉진)의 연구비 지원 받음. |
품 목: ALT-P7
|
①구 분 |
바이오 신약 |
|
②적응증 |
[주 적응증] HER2 양성 유방암 |
|
③작용기전 |
- 항체에 링커(Linker)로 접합된 세포독성 물질(Cytotoxic agent, Payload)이 암세포 표면의 수용체를 인식하고 결합하면 암세포 내로 유입되고 세포독성 물질이 분리 되면서 암세포 사멸을 유도하는 원리 - 일반적으로 세포독성 항암 약물은 강력한 세포 독성(cytotoxicity)을 나타내어 |
|
④제품의 특성 |
- 당사가 자체 개발한 NexMab™ 기술(항체-약물접합기술, ADC Antibody-Drug Conjugate 항체-약물접합체)을 활용하여 기존의 항암 항체치료제보다 월등한 효능을 가지며 부작용은 적은 항체-약물접합 항암치료제로 개발 - 2013년 미국에서 승인을 받아 시판되고 있는 ADC 기반 1세대 유방암 치료제인 Genentech/Roche의 캐사일라(Kadcyla)는 항체인 허셉틴에 항암 약물을 무작위로 접합시킨 것으로 약물을 일단 항체 표면에 비선택적(Non-selective)으로 접합한 후 복잡한 정제 과정을 통해 비교적 균일한 제품을 생산한 것에 비해 당사 제품은 항체 C 말단 부위에 위치 선택적으로 접합하여 생산성이 높고, 체내 안전성이 탁월한 차세대 원천 기술("위치 특이적 결합") - 당사는 NexMab™ 기술을 활용하여 2019년 7월에 미국 FDA에 위암 치료용 희귀 의약품(Orphan drug)으로 등록하면서 임상 절차를 간소화했으며 본 NexMab™ ADC 기술을 미국, 중국을 포함한 전세계 8개국에 특허 등록하였고 이를 적용하여 기존 유방암 치료제인 허셉틴보다 약효/접합안전성/생산성/부작용 등 면에서 상대적으로 우수한 ADC 유방암치료제(ALT-P7)를 개발 중 |
|
⑤진행경과 |
1. 세계적인 GLP 인증 전임상시험 기관인 미국 MPI Research 에서 원숭이 독성 시험 진행 - 경쟁사 ADC 항암제 대비 월등한 안전성 확인(동일한 payload를 사용하는 경쟁사 ADC 항암제보다 2배 고용량을 투여한 경우에도 원숭이에게서 독성 반응이 나타나지 않음) 2. 상기 전임상시험 결과를 바탕으로 삼성서울병원과 가천대 길병원에서 진행한 최초 인간 대상(FIH, First-in-Human) 임상1상 2017년 6월 승인, 2017년 11월 개시, 2021년 1월 마지막 대상자 방문 종료 - 최대 허용 용량(MTD, Maximum Tolerated Dose) 결정 - 약품 안전성(safety)과 약동학(pharmacokinetics) 및 유효성(efficacy) 평가 - 진행성 또는 재발성 HER2 양성 유방암 환자를 대상으로 단일군 용량 상승 연구투여 용량을 경쟁사 ADC 항암제 보다 2배 이상 증가시킴 - 임상 1상 중간 결과 2020년 미국임상종양학회(ASCO)와 2020년 대한종양내과 학회(KSMO)에서 발표 - 2021년 8월 3일 임상 1상 임상시험결과보고서 (CSR) 완료 (국내유일임상1상완료) |
|
⑥향후계획 |
- ADC 유방암치료제 및 위암치료제 뿐만 아니라 침샘암, 요로 상피암 등 타 HER2 양성 암에 대한 임상 개발 논의 중이며 타 약물과의 병용 요법을 통한 임상 2상 진행 방향 검토 |
|
⑦경쟁제품 |
- 2013년, 항체-약물 접합체 중에서 HER2 양성 유방암에 대해 최초 허가를 받은 - 2019년, HER2 양성 유방암에 대해 다이이치산쿄 사의 인허투(Enhertu) |
|
⑧관련논문 등 |
- 2020년, ASCO 학회 발표 "First-in-human phase I study of ALT-P7, a HER-tar - 2020년, KSMO 학회 발표 "First-in-human(FIH), phase I study of ALT-P7, a HER2 -targeting antibody-drug conjugate, in patients with HER2 positive advanced |
|
⑨시장규모 |
- HER2 표적치료제 시장은 2025년 50억 달러 규모 예상 (HER2 양성 유방암시장 - 미국 머크(MSD) 사는 시애틀제네틱스와 2가지 항암 신약 개발을 위해 5조원이 |
|
⑩기타사항 |
- 전임상 단계까지 산업부에서 연구비 지원 받음 - 임상 단계에서는 범부처항암사업단의 연구비 지원 받음 |
품 목: ALT-B4
|
①구 분 |
바이오 신약 |
|
②적응증 |
당사가 독자적으로 개발하여 기존 정맥주사(iv) 약물전달 방식을 피하주사(sc) 제형으로 변환하게 하는 플랫폼(기반) 기술인 Hybrozyme™ 을 통해 전세계 2번째로 개발한 재조합 히알루로니다제 - 피부과 성형외과 및 정형외과 수술 후 통증 완화, 부종 경감 등 독자적인 제품 |
|
③작용기전 |
- 피부를 구성하는 히알루론산을 일시적/국소적으로 분해하여 통로를 만들고 함께 투여된 분자량이 큰 항체 바이오의약품의 피부 투과 및 흡수를 촉진 - 피하 조직에는 다당류와 단백질이 복잡한 구조를 이루어 물질의 이동을 제한하는 차단막 혹은 보호막의 기능을 함. - ALT-B4를 포함하는 히알루로니다제는 피하조직을 구성하는 고분자 물질인 히알루론산을 저분자 물질로 분해함으로써, 일시적으로 약물의 흡수 및 확산을 용이하게 하는 역할. - 기존 정맥주사로만 사용될 수 있었던 고분자 바이오 약물을 히알루로니다제와 병용하여 피하로 투약함으로써, 약물의 혈관으로의 흡수율을 높임. |
|
④제품의 특성 |
- 히알루로니다제는 원래 돼지나 소, 양의 고환에서 추출한 동물 유래 히알루로니다제를 정제한 약물이 시장에 주로 나와있음. - 히알루로니다제는 정자의 첨두에 위치한 세포막 단백질 효소로써, 정자가 난자와 만나 착상하기 위해 난자를 둘러싼 보호막을 분해시키는 물질. - 재조합 인간 히알루로니다제는 미국의 할로자임 (Halozyme) 사가 rHuPH20 를 세계 최초로 개발. °정맥주사를 피하주사로 변환시켜주는 부형제(excipient) °피부 미용 °히알루론산 필러 사용 후 필러 용해용 °외과 수술 후 통증이나 부종을 완화시키는 용도 - 재조합 인간 히알루로니다아제는 동물 유래 제품과 비교하여 °알러지 반응이나 면역 원성이 낮은 장점이 있음 °성형 및 미용 시장에서의 적용 분야에서 확장 가능성 °바이오의약품 시장에서 정맥주사(iv)를 피하주사(sc)로 변환시키는 일종의 Game Changer 로 주목받게 됨 - 고순도의 안전성이 담보된 재조합 히알루로니다제의 개발이 필요한 상황에서 |
|
⑤진행경과 |
- 2020년 12월, 독자형 제품("테르가제" Tergase)으로 Pivotal 임상1상 신청 (한국) - 2019년, 2020년 및 2021년에 걸쳐 3차례의 라이센스아웃 계약을 통해 각각 |
|
⑥향후계획 |
- 독자제품은 2021년 한국 임상1상 완료 후 품목허가 신청 예정 (Pivotal study) |
|
⑦경쟁제품 |
- 동물유래 히알루로니다제 제품 및 할로자임 사가 출시한 재조합 인간 히알 - 할로자임 사가 로슈 사 등이 시판 중인 기존 항체치료제에 첨가제(Excipient, |
|
⑧관련논문 등 |
해당사항 없음 |
|
⑨시장규모 |
- 미국 할로자임 사는 2012년까지만 하더라도 계약금 및 마일스톤 이 매출의 |
|
⑩기타사항 |
- 전임상 단계까지 범부처 신약개발 지원단의 지원 받음 |
품 목: ALT-L9
|
①구 분 |
바이오시밀러 |
|
②적응증 |
[주 적응증] 신생혈관성(습성) 연령관련 황반변성(wAMD) [기타 적응증] 당뇨병성 황반부종(DME), 망막정맥폐쇄성 황반부종, 당뇨성 망막병증 |
|
③작용기전 |
- 체내의 VEGF(혈관내피성장인자)가 세포의 VEGF 수용체(VEGFR, VEGR Receptor)와 결합하여 혈관의 생성을 촉진하게 되는데, 수용체와 VEGF 결합을 방해 억제 |
|
④제품의 특성 |
- 애플리버셉트(Aflibercept)를 주성분으로 하는 오리지널 신약 아일리아(Eylea)는 |
|
⑤진행경과 |
- 국내 최초로 미국 전임상 시험 완료 |
|
⑥향후계획 |
- 2022년 상반기 다국적 임상3상 개시 예정 |
|
⑦경쟁제품 |
[시판] 아일리아(Regeneron/Bayer 사) [임상 3상 진행중인 바이오시밀러] ABP938(Amgen), SB15(삼성바이오에피스) 등 |
|
⑧관련논문 등 |
해당사항 없음 |
|
⑨시장규모 |
- 습성 연령관련 황반변성(wAMD, Wet Age-related Macular Degeneration)은 혈관 |
|
⑩기타사항 |
해당사항 없음 |
품 목: ALT-L2
|
①구 분 |
바이오시밀러 |
|
②적응증 |
[주 적응증] HER2 양성 유방암/위암 |
|
③작용기전 |
- HER2/NEU 수용체를 표적으로 하여 세포내 신호 전달 경로를 억제 |
|
④제품의 특성 |
- Trastuzumab을 주성분으로 하는 허셉틴에 대한 당사 개발 바이오시밀러 |
|
⑤진행경과 |
캐나다 임상 1상 - 2016년 2월 임상승인, 2016년 8월 마지막 대상자 방문 종료 |
|
⑥향후계획 |
- 최근 5종의 허셉틴 바이오시밀러 이외에 추가로 2종 이상의 바이오시밀러가 유럽 |
|
⑦경쟁제품 |
Herzuma(Celltrion), Ogivri(Mylan/Biocon), Ontruzant(Samsung Bioepis), Trazimera(Pfizer), Kanjinti(Amgen) 등 |
|
⑧관련논문 등 |
해당사항 없음 |
|
⑨시장규모 |
- 2019년 6월을 기점으로 매년 글로벌 시장에서 8조원 규모인 허셉틴의 미국 특허가 만료됨에 따라 글로벌 바이오시밀러 시장에 출사표를 내민 바이오기업은 7개사 |
|
⑩기타사항 |
해당사항 없음 |
(2) 연구개발 완료 실적
공시서류 작성기준일 현재 개발이 완료된 신약{복제약(시밀러) 등 포함}의 현황은 다음과 같습니다.
< 연구개발 완료 실적 >
|
구 분 |
품 목 |
적응증 |
개발완료일 |
현재 현황 |
비 고 |
|
|
바이오 |
신약 |
ALT-P1 | 성장호르몬 결핍증 |
- | 글로벌(인도) 임상1상 완료 |
브라질 크리스탈리아 |
| ALT-B4 | 피하주사 변환 |
- |
글로벌 임상1상 준비중 |
글로벌 10대 제약사 |
||
| ALT-BB4 | 부종/통증 완화 |
- | 한국 임상1상(허가임상) 개시승인 |
Pivotal (품목허가용) 임상1상 |
||
|
바이오시밀러 |
ALT-L2 | 유방암/위암 | - | 중국 임상3상 IND |
중국 QiLu 제약 |
|
| ALT-L9 | 습성 황반변성 |
- |
한국 임상1상 완료 (생산: 알테오젠, 임상: 알토스바이오로직스) |
알토스바이오로직스 라이센스 아웃 |
||
(3) 연구개발활동 및 판매 중단 현황
해당사항 없습니다
(4) 기타 연구개발 실적
해당사항 없습니다
사. 지적재산권 보유 및 출원 현황
| 구분 | 내용 | 권리자 | 출원국 | 출원일 | 등록일 |
| 상표 | ㈜알테오젠 국문/영문 명칭 | 알테오젠 | 대한민국 | 13.03.27 | 14.03.31 |
| 상표 | ㈜알테오젠 로고 | 알테오젠 | 대한민국 | 13.03.27 | 14.03.31 |
| 서비스표 | NexP™ | 알테오젠 | 대한민국 | 10.04.14 | 11.07.29 |
| 서비스표 | NexMab™ | 알테오젠 | 대한민국 | 14.04.09 | 15.01.19 |
| 상표 | Hybrozyme™ | 알테오젠 | 대한민국 | 18.10.31 | 19.08.07 |
| 상표 | Hybrizyme™ | 알테오젠 | 대한민국 | 18.11.05 | 19.07.24 |
| 상표 | DILUASE | 알테오젠 | 대한민국 | 20.04.28 | - |
| 미 국 | 20.09.02 | - | |||
| 일 본 | 20.09.02 | - | |||
| 중 국 | 20.09.02 | 21.02.03 | |||
| 유 럽 | 20.09.02 | 21.02.25 | |||
| 상표 | TERGASE | 알테오젠 | 대한민국 | 20.09.24 | - |
| 미 국 | 20.10.16 | - | |||
| 일 본 | 20.10.16 | - | |||
| 중 국 | 20.10.16 | 21.03.04 | |||
| 유 럽 | 20.10.16 | - | |||
| 상표 | Altos Biologics Inc. | 알테오젠 | 대한민국 | 20.10.05 | - |
| 특허 | 체내 지속성을 유지함으로 체내 반감기가 증가된 단백질 또는 펩티드 융합체, 및 이를 이용하여 체내 반감기를 증가시키는 방법 | 알테오젠 | 대한민국 | 10.04.22 | 12.09.10 |
| PCT | 10.04.22 | - | |||
| 호 주 | 11.09.30 | 13.10.24 | |||
| 러시아 | 11.11.21 | 14.01.10 | |||
| 미 국 | 11.10.21 | 15.04.21 | |||
| 일 본 | 11.10.18 | 15.04.10 | |||
| 중 국 | 11.10.21 | 14.08.13 | |||
| 유 럽 | 11.09.29 | 15.03.11 | |||
| 캐나다 | 11.10.12 | 16.02.16 | |||
| 인 도 | 11.10.19 | 18.08.30 | |||
| 브라질 | 11.10.19 | 21.05.25 | |||
| 멕시코 | 11.10.21 | 14.03.11 | |||
| 말레이시아 | 11.10.20 | - | |||
| 이집트 | 11.10.20 | - | |||
| 특허 | 신규한 알파-1 안티트립신 변이체, 이의 제조방법 및 용도 | 알테오젠 | 대한민국 | 12.06.01 | 14.05.27 |
| PCT | 12.08.13 | - | |||
| 호 주 | 14.04.08 | 15.08.20 | |||
| 러시아 | 14.04.14 | 15.10.27 | |||
| 미 국 | 14.03.12 | 15.06.09 | |||
| 일 본 | 14.03.14 | 16.09.09 | |||
| 중 국 | 14.03.14 | 15.12.11 | |||
| 유 럽 | 14.04.10 | 17.09.27 | |||
| 캐나다 | 14.03.14 | 16.09.13 | |||
| 인 도 | 14.04.11 | 20.07.06 | |||
| 브라질 | 14.03.13 | 21.01.12 | |||
| 멕시코 | 14.03.14 | 17.07.26 | |||
| 말레이시아 | 14.03.14 | - | |||
| 특허 | 신규한 지속형 인간 성장호르몬의 정제 방법 | CJ헬스케어 | 대한민국 | 12.06.05 | 14.11.04 |
| 알테오젠 | |||||
| 특허 | 신규한 지속형 인간 성장호르몬 단량체를 제조하는 방법 | CJ헬스케어 | 대한민국 | 12.11.21 | 15.04.22 |
| 알테오젠 | PCT | 13.11.21 | - | ||
| 특허 | 고당화된 지속형 인간 성장호르몬 단백질 및 이의 제조방법 | CJ헬스케어 | 대한민국 | 13.05.31 | 15.03.16 |
| 알테오젠 | PCT | 13.06.05 | - | ||
| 중 국 | 14.12.05 | 17.04.05 | |||
| 미 국 | 14.12.05 | 18.02.27 | |||
| 일 본 | 14.12.05 | 17.10.27 | |||
| 유 럽 | 14.12.31 | 18.02.24 | |||
| 특허 | GLP-1 유사체의 융합체, 및 이를 유효성분으로 함유하는 당뇨병의 예방 또는 치료용 조성물 | 알테오젠 | 대한민국 | 10.05.12 | 13.01.29 |
| 한남대 | |||||
| 특허 | 시스테인 잔기를 포함하는 모티프가 결합된 변형항체, 상기 변형항체를 포함하는 변형항체-약물 결합체 및 그 제조방법 | 알테오젠 | 대한민국 | 13.02.22 | 15.07.29 |
| PCT | 13.02.22 | - | |||
| 캐나다 | 14.08.18 | - | |||
| 호 주 | 14.09.24 | 16.06.23 | |||
| 중 국 | 14.09.28 | 18.07.14 | |||
| 유 럽 | 14.09.24 | 20.08.26 | |||
| 일 본 | 14.08.22 | 17.01.06 | |||
| 멕시코 | 14.08.21 | 18.01.19 | |||
| 미 국 | 14.08.20 | 17.11.14 | |||
| 러시아 | 14.09.24 | 16.03.18 | |||
| 브라질 | 14.08.22 | - | |||
| 특허 | 단백질과 Fc 도메인을 융합한 융합 단백질의 안정화용 조성물 | 알테오젠 | 대한민국 | 13.10.23 | 14.07.09 |
| PCT | 13.10.23 | - | |||
| 일 본 | 15.05.07 | 16.10.21 | |||
| 미 국 | 15.04.29 | 16.09.21 | |||
| 유 럽 | 15.05.07 | - | |||
| 중 국 | 15.06.16 | - | |||
| 특허 | 단백질 안정화용 조성물 및 이를 포함하는 약제학적 제제 | 알테오젠 | 대한민국 | 15.10.16 | 17.02.02 |
| PCT | 15.10.16 | - | |||
| 미 국 | 15.10.15 | 17.11.21 | |||
| 특허 | IgG Fc 도메인을 가지는 융합 단백질의 안정한 액상 제제 | 알테오젠 | 대한민국 | 16.06.22 | 17.12.06 |
| PCT | 16.06.23 | - | |||
| 미국 | 16.06.23 | 18.04.16. | |||
| 호주 | 17.11.27 | 20.07.23 | |||
| 일본 | 17.12.11 | 19.06.21 | |||
| 멕시코 | 17.12.19 | - | |||
| 중국 | 17.12.20 | - | |||
| 캐나다 | 17.12.21 | 20.06.09 | |||
| 인도 | 17.12.21 | - | |||
| 브라질 | 17.12.22 | - | |||
| 인도네시아 | 18.01.11 | - | |||
| 유럽 | 18.01.19 | - | |||
| 러시아 | 18.01.22 | 19.05.22 | |||
| 유럽 | 20.09.11 | - | |||
| 특허 | IgG Fc 도메인을 가지는 융합 단백질의 생산방법 | 알테오젠 | 대한민국 | 16.10.13 | 19.01.02 |
| PCT | 16.10.14 | - | |||
| 호주 | 18.03.15 | 19.11.07 | |||
| 미국 | 18.04.12 | - | |||
| 유럽 | 18.04.16 | - | |||
| 일본 | 18.04.16 | 20.10.23 | |||
| 중국 | 18.04.12 | - | |||
| 브라질 | 18.04.13 | - | |||
| 멕시코 | 18.04.13 | - | |||
| 캐나다 | 18.04.13 | - | |||
| 러시아 | 18.05.14 | 20.09.14 | |||
| 인도 | 18.05.04 | - | |||
| 특허 | 항체-약물 접합체 및 그 제조방법 | 알테오젠 | 대한민국 | 15.10.27 | 17.02.02 |
| PCT | 16.10.25 | - | |||
| 캐나다 | 18.09.21 | - | |||
| 미국 | 18.09.26 | - | |||
| 일본 | 18.10.04 | 20.05.25 | |||
| 중국 | 18.11.05 | - | |||
| 유럽 | 18.11.02 | - | |||
| 특허 | 항체-약물 접합체 및 그 제조방법 | 알테오젠 | 대한민국 | 17.03.30 | 19.07.15 |
| PCT | 17.03.30 | - | |||
| 특허 | FOLR1에 특이적으로 결합하는 항체 및 그의 용도 | 알테오젠 | 대한민국 | 18.03.14 | 21.07.06 |
| PCT | 18.03.13 | - | |||
| 미국 | 20.09.11 | - | |||
| 유럽 | 20.09.22 | - | |||
| 일본 | 20.09.10 | - | |||
| 캐나다 | 20.10.13 | - | |||
| 중국 | 20.10.23 | - | |||
| 특허 | 혈액응고인자 Ⅶ/Ⅶa 또는 이의 융합단백질의 제조 방법 | 알테오젠 | 대한민국 | 18.06.15 | 20.07.10 |
| 특허 | 효소 활성과 열 안정성이 증가한 새로운 히알루론산 가수분해 효소 및 이의 제조 방법 | 알테오젠 | PCT | 19.07.25 | - |
| 대한민국 | 20.01.30 | 20.08.28 | |||
| 신규 히알루론산 가수분해 효소 변이체 및 이를 포함하는 약제학적 조성물 | 미국 | 20.01.02 | - | ||
| 유럽 | 20.01.06 | - | |||
| 일본 | 20.01.06 | - | |||
| 대한민국 | 20.08.27 | - | |||
| 캐나다 | 20.09.11 | - | |||
| 인도 | 20.09.17 | - | |||
| 러시아 | 20.09.21 | - | |||
| 멕시코 | 20.09.21 | - | |||
| 브라질 | 20.09.23 | - | |||
| 중국 | 20.09.28 | - | |||
| 오스트레일리아 | 21.01.20 | - | |||
| 남아프리카공화국 | 21.02.03 | - | |||
| 특허 | 신규한 성장 호르몬 수용체 길항제 및 이의 융합 단백질 | 알테오젠 | 대한민국 | 18.11.26 | 20.10.14 |
| PCT | 18.12.20 | - | |||
| 미국 | 20.06.17 | - | |||
| 유럽 | 20.06.09 | - | |||
| 일본 | 20.06.19 | - | |||
| 중국 | 20.06.22 | - | |||
| 특허 | 안정성이 향상된 신규 히알루론산 가수분해 효소 변이체 및 이를 포함하는 약제학적 조성물 | 알테오젠 | 대한민국 | 20.01.23 | - |
| PCT | 21.01.25 | - | |||
| 대만 | 21.01.25 | - | |||
| 특허 | 재조합 히알루로니다제의 단백질의 제조 방법 | 알테오젠 | 대한민국 | 20.08.06 | - |
|
PCT |
21.08.06 |
- | |||
|
대만 |
21.08.20 |
- | |||
| 특허 | 인간 히알루로니다제 PH20의 변이체와 약물을 포함하는 피하투여용 약학 조성물 | 알테오젠 | PCT | 20.03.24 | - |
| 대한민국 | 20.10.21 | - | |||
| 유럽 | 20.10.30 | - | |||
| 미국 | 20.11.04 | - | |||
| 중국 | 20.11.27 | - | |||
| 일본 | 20.12.14 | - | |||
|
러시아 |
21.09.22 |
- |
|||
|
캐나다 |
21.09.20 |
- |
|||
|
호주 |
21.09.22 |
- |
|||
|
인도 |
21.09.23 |
- |
|||
|
브라질 |
21.09.24 |
- |
|||
|
멕시코 |
21.09.15 |
- |
|||
| 특허 | FGF19변이체를 포함하는 신규 융합 단백질 및 이의 용도 | 알테오젠 | 대한민국 | 20.11.20 | - |
| 특허 | 저용량 약액 충전 사전 충전형 주사기 | 알테오젠 | 대한민국 | 21.04.15 | - |
III. 재무에 관한 사항
1. 요약재무정보
가. 연결요약재무정보
| (단위 : 원) |
| 과 목 | 2021년도 (제14기 3분기) |
2020년도 (제13기) |
2019년도 (제12기) |
|---|---|---|---|
| [유동자산] | 220,989,235,522 | 137,906,946,065 | 65,209,451,868 |
| 당좌자산 | 220,042,121,775 | 137,447,283,146 | 64,327,877,844 |
| 재고자산 | 947,113,747 | 459,662,919 | 881,574,024 |
| [비유동자산] | 32,081,037,844 | 21,299,982,060 | 20,769,660,404 |
| 투자자산 | 266,191,071 | 224,992,048 | 95,717,152 |
| 유형자산 | 29,987,112,596 | 19,483,925,836 | 19,191,523,552 |
| 무형자산 | 1,106,159,504 | 1,020,435,105 | 743,496,550 |
| 기타비유동자산 | 721,574,673 | 570,629,071 | 738,923,150 |
| 자산총계 | 253,070,273,366 | 159,206,928,125 | 85,979,112,272 |
| [유동부채] | 75,153,063,933 | 52,352,716,473 | 11,372,929,137 |
| [비유동부채] | 3,655,172,756 | 1,582,874,025 | 4,402,030,126 |
| 부채총계 | 78,808,236,689 | 53,935,590,498 | 15,774,959,263 |
| [지배기업소유주지분] | 170,273,411,571 | 131,163,684,335 | 69,982,449,224 |
| - 자본금 | 21,646,632,500 | 14,143,142,500 | 6,948,375,000 |
| - 기타불입자본 | 177,042,118,006 | 106,007,922,458 | 76,272,355,475 |
| - 연결이익잉여금 | (28,162,148,818) | (14,213,912,090) | (13,238,281,251) |
| [비지배지분] | 3,735,434,989 | (665,815,241) | 221,703,785 |
| 자본총계 | 174,262,036,377 | 105,271,337,627 | 70,204,153,009 |
| 종속기업 투자주식의 평가방법 | 원가법 | 원가법 | 원가법 |
| 2021년 1월 1일~ 2021년 9월 30일 |
2020년 1월 1일~ 2020년 12월 31일 |
2019년 1월 1일~ 2019년 12월 31일 |
|
| 매출액 | 24,649,809,350 | 42,425,842,457 | 29,229,181,883 |
| 영업이익 | (22,135,894,863) | 103,718,349 | (2,252,031,255) |
| 법인세비용차감전순이익 | (13,073,298,489) | (2,839,347,168) | (1,680,700,203) |
| 연결당기순이익 | (13,948,236,728) | (3,428,438,058) | (1,738,267,459) |
| 총포괄이익 | (13,948,236,728) | (3,422,404,578) |
(1,738,267,459) |
| 지배기업소유주지분 | (13,224,217,545) | (969,597,359) | (704,513,309) |
| 비지배지분 | 724,019,183 | (2,452,807,219) | (1,033,754,150) |
|
주당이익 |
|||
|
기본주당이익(손실) |
(337) | (35) | (26) |
|
희석주당이익(손실) |
(337) | (35) | (26) |
| 연결에 포함된 회사 수 | 3 | 4 | 3 |
※ 상기 재무정보는 한국채택국제회계기준에 따라 작성되었습니다
나. 별도요약재무정보
| (단위 : 원) |
| 과 목 | 2021년도 (제14기 3분기) |
2020년도 (제13기) |
2019년도 (제12기) |
|---|---|---|---|
| [유동자산] | 151,529,900,713 | 96,701,169,737 | 61,037,198,278 |
| 당좌자산 | 151,529,900,713 | 96,701,169,737 | 61,037,198,278 |
| 재고자산 | - | - | - |
| [비유동자산] | 29,003,484,477 | 18,665,010,952 | 18,499,362,444 |
| 투자자산 | 7,273,820,751 | 3,741,630,352 | 3,124,353,652 |
| 유형자산 | 20,523,092,426 | 10,414,008,846 | 11,100,538,924 |
| 무형자산 | 861,925,411 | 769,734,021 | 495,500,204 |
| 장기대여금 | - | 3,000,000,000 | 3,000,000,000 |
| 기타비유동자산 | 344,645,889 | 739,637,733 | 778,969,664 |
| 자산총계 | 180,280,195,073 | 115,366,180,689 | 79,536,560,722 |
| [유동부채] | 5,417,191,415 | 6,076,850,186 | 5,031,829,732 |
| [비유동부채] | 2,513,517,469 | 828,770,008 | 3,376,010,258 |
| 부채총계 | 7,930,708,884 | 6,905,620,194 | 8,407,839,990 |
| [자본금] | 21,646,632,500 | 14,143,142,500 | 6,948,375,000 |
| [기타불입자본] | 169,633,529,507 | 100,817,995,987 | 74,742,743,305 |
| [이익잉여금] | (18,677,485,701) | (6,500,577,992) | (10,562,397,573) |
| 자본총계 | 172,349,486,189 | 108,460,560,495 | 71,128,720,732 |
| 매출액 | 7,593,038,202 | 26,211,818,564 | 13,322,560,593 |
| 영업이익 | (16,511,508,898) | 5,648,881,966 | 911,579,878 |
| 법인세비용차감전순이익 | (12,176,907,709) | 4,573,455,839 | 1,773,167,784 |
| 당기순이익 | (12,176,907,709) | 4,061,819,581 | 1,754,111,415 |
| 총포괄이익 | (12,176,907,709) | 4,061,819,581 | 1,754,111,415 |
|
주당이익 |
- | - | - |
|
기본주당이익(손실) |
(295) | 145 | 66 |
|
희석주당이익(손실) |
(295) | 145 | 62 |
※ 상기 재무정보는 한국채택국제회계기준에 따라 작성되었습니다
2. 연결재무제표
|
연결 재무상태표 |
|
제 14 기 3분기말 2021.09.30 현재 |
|
제 13 기말 2020.12.31 현재 |
|
(단위 : 원) |
|
제 14 기 3분기말 |
제 13 기말 |
|
|---|---|---|
|
자산 |
||
|
유동자산 |
220,989,235,522 |
137,906,946,065 |
|
현금및현금성자산 |
17,792,558,590 |
38,922,455,345 |
|
단기금융상품 |
195,950,559,892 |
94,822,000,000 |
|
매출채권 및 기타유동채권 |
5,080,443,185 |
2,692,677,487 |
|
당기법인세자산 |
833,848,459 |
135,297,680 |
|
기타유동자산 |
384,711,649 |
874,852,634 |
|
재고자산 |
947,113,747 |
459,662,919 |
|
비유동자산 |
32,081,037,844 |
21,299,982,060 |
|
기타비유동금융자산 |
980,847,095 |
775,142,320 |
|
유형자산 |
29,987,112,596 |
19,483,925,836 |
|
영업권 |
112,983,012 |
112,983,012 |
|
영업권 이외의 무형자산 |
993,176,492 |
907,452,093 |
|
기타비유동자산 |
6,918,649 |
9,117,672 |
|
이연법인세자산 |
0 |
11,361,127 |
|
자산총계 |
253,070,273,366 |
159,206,928,125 |
|
부채 |
||
|
유동부채 |
75,153,063,933 |
52,352,716,473 |
|
매입채무 및 기타유동채무 |
12,417,565,016 |
17,858,462,431 |
|
단기매입채무 |
2,330,857,676 |
440,241,691 |
|
유동계약부채 |
3,717,397,895 |
4,081,977,958 |
|
단기차입금 |
2,800,000,000 |
2,800,000,000 |
|
유동성장기차입금 |
250,000,000 |
250,000,000 |
|
유동성전환상환우선주부채 |
3,319,309,445 |
10,286,242,782 |
|
전환우선주부채 |
60,500,000,000 |
31,000,000,000 |
|
당기법인세부채 |
64,610,582 |
31,693,239 |
|
기타유동금융부채 |
1,205,183,182 |
2,323,728,355 |
|
유동파생상품부채 |
458,040,168 |
932,275,121 |
|
기타유동부채 |
507,664,985 |
206,557,327 |
|
비유동부채 |
3,655,172,756 |
1,582,874,025 |
|
장기매입채무 및 기타비유동채무 |
2,500,000,000 |
687,500,000 |
|
장기선수금 |
2,000,000,000 |
0 |
|
장기차입금 |
500,000,000 |
687,500,000 |
|
기타비유동금융부채 |
1,079,192,570 |
895,374,025 |
|
이연법인세부채 |
75,980,186 |
0 |
|
부채총계 |
78,808,236,689 |
53,935,590,498 |
|
자본 |
||
|
지배기업의 소유주에게 귀속되는 자본 |
170,526,601,688 |
105,937,152,868 |
|
자본금 |
21,646,632,500 |
14,143,142,500 |
|
보통주자본금 |
21,132,125,000 |
14,041,450,000 |
|
우선주자본금 |
514,507,500 |
101,692,500 |
|
자본잉여금 |
175,482,863,344 |
104,429,703,197 |
|
주식발행초과금 |
167,498,519,268 |
98,664,021,149 |
|
자기주식처분이익 |
575,755,577 |
575,755,577 |
|
기타자본잉여금 |
7,408,588,499 |
5,189,926,471 |
|
기타자본구성요소 |
1,559,254,662 |
1,578,219,261 |
|
자기주식 |
(793,980,301) |
0 |
|
주식선택권 |
2,353,234,963 |
1,578,219,261 |
|
이익잉여금(결손금) |
(28,162,148,818) |
(14,213,912,090) |
|
비지배지분 |
3,735,434,989 |
(665,815,241) |
|
자본총계 |
174,262,036,677 |
105,271,337,627 |
|
자본과부채총계 |
253,070,273,366 |
159,206,928,125 |
|
연결 포괄손익계산서 |
|
제 14 기 3분기 2021.01.01 부터 2021.09.30 까지 |
|
제 13 기 3분기 2020.01.01 부터 2020.09.30 까지 |
|
(단위 : 원) |
|
제 14 기 3분기 |
제 13 기 3분기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
수익(매출액) |
6,446,723,113 |
24,649,809,350 |
14,011,661,613 |
37,324,330,061 |
|
매출원가 |
11,988,043,134 |
25,118,374,556 |
5,246,885,996 |
16,034,193,767 |
|
매출총이익 |
(5,541,320,021) |
(468,565,206) |
8,764,775,617 |
21,290,136,294 |
|
판매비와관리비 |
4,609,434,683 |
21,667,329,657 |
4,492,289,474 |
13,201,587,967 |
|
영업이익(손실) |
(10,150,754,704) |
(22,135,894,863) |
4,272,486,143 |
8,088,548,327 |
|
기타이익 |
1,847,334,225 |
8,366,714,736 |
(27,800,959) |
838,005,982 |
|
기타손실 |
36,596,307 |
370,319,774 |
491,558,250 |
901,516,151 |
|
금융수익 |
514,364,905 |
1,590,184,847 |
168,260,425 |
643,065,547 |
|
금융원가 |
106,024,954 |
523,983,435 |
19,548,596 |
371,262,547 |
|
법인세비용차감전순이익(손실) |
(7,931,676,835) |
(13,073,298,489) |
3,901,838,763 |
8,296,841,158 |
|
법인세비용 |
113,205,307 |
150,919,056 |
57,973,305 |
428,311,598 |
|
당기순이익(손실) |
(8,044,882,142) |
(13,224,217,545) |
3,843,865,458 |
7,868,529,560 |
|
기타포괄손익 |
0 |
0 |
0 |
0 |
|
총포괄손익 |
(8,044,882,142) |
(13,224,217,545) |
3,843,865,458 |
7,868,529,560 |
|
총 포괄손익의 귀속 |
||||
|
총 포괄손익, 지배기업의 소유주에게 귀속되는 지분 |
(8,001,948,832) |
(13,948,236,728) |
4,142,247,372 |
9,189,090,133 |
|
총 포괄손익, 비지배지분 |
(42,933,310) |
724,019,183 |
(297,381,914) |
(1,320,560,573) |
|
주당이익 |
||||
|
기본주당이익(손실) (단위 : 원) |
(478) |
(337) |
98 |
219 |
|
희석주당이익(손실) (단위 : 원) |
(478) |
(337) |
98 |
219 |
|
연결 자본변동표 |
|
제 14 기 3분기 2021.01.01 부터 2021.09.30 까지 |
|
제 13 기 3분기 2020.01.01 부터 2020.09.30 까지 |
|
(단위 : 원) |
|
자본 |
|||||||
|---|---|---|---|---|---|---|---|
|
지배기업의 소유주에게 귀속되는 자본 |
비지배지분 |
자본 합계 |
|||||
|
자본금 |
자본잉여금 |
기타자본구성요소 |
이익잉여금 |
지배기업의 소유주에게 귀속되는 자본 합계 |
|||
|
2020.01.01 (기초자본) |
6,948,375,000 |
75,400,813,207 |
871,542,268 |
(13,238,281,251) |
69,982,449,224 |
221,703,785 |
70,204,153,009 |
|
연결대상범위의 변동 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
당기순이익(손실) |
0 |
0 |
0 |
9,189,090,133 |
9,189,090,133 |
(1,320,560,573) |
7,868,529,560 |
|
무상증자 |
6,997,975,000 |
(7,033,299,280) |
0 |
0 |
(35,324,280) |
0 |
(35,324,280) |
|
전환우선주의발행 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
자기주식 거래로 인한 증감 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
주식기준보상거래 |
0 |
0 |
803,706,669 |
0 |
803,706,669 |
0 |
803,706,669 |
|
기타거래 |
95,100,000 |
2,660,024,190 |
(362,547,670) |
0 |
2,392,576,520 |
0 |
2,392,576,520 |
|
2020.09.30 (기말자본) |
14,041,450,000 |
71,027,538,117 |
1,312,701,267 |
(4,049,191,118) |
82,332,498,266 |
(1,098,856,788) |
81,233,641,478 |
|
2021.01.01 (기초자본) |
14,143,142,500 |
104,429,703,197 |
1,578,219,261 |
(14,213,912,090) |
105,937,152,868 |
(665,815,241) |
105,271,337,627 |
|
연결대상범위의 변동 |
0 |
2,218,662,028 |
0 |
0 |
2,218,662,028 |
3,677,231,047 |
5,895,893,075 |
|
당기순이익(손실) |
0 |
0 |
(14,201,426,845) |
(14,201,426,845) |
724,019,183 |
(13,224,217,545) |
|
|
무상증자 |
7,192,227,500 |
(7,228,689,370) |
0 |
0 |
(36,461,870) |
0 |
(36,461,870) |
|
전환우선주의발행 |
241,312,500 |
74,599,720,350 |
0 |
0 |
74,841,032,850 |
0 |
74,841,032,850 |
|
자기주식 거래로 인한 증감 |
0 |
0 |
(793,980,301) |
0 |
(793,980,301) |
0 |
(793,980,301) |
|
주식기준보상거래 |
0 |
0 |
1,031,059,001 |
0 |
1,031,059,001 |
0 |
1,031,059,001 |
|
기타거래 |
69,950,000 |
1,463,467,139 |
(256,043,299) |
0 |
1,277,373,840 |
0 |
1,277,373,840 |
|
2021.09.30 (기말자본) |
21,646,632,500 |
175,482,863,344 |
1,559,254,662 |
(28,415,338,935) |
170,273,411,571 |
3,735,434,989 |
174,262,036,677 |
|
연결 현금흐름표 |
|
제 14 기 3분기 2021.01.01 부터 2021.09.30 까지 |
|
제 13 기 3분기 2020.01.01 부터 2020.09.30 까지 |
|
(단위 : 원) |
|
제 14 기 3분기 |
제 13 기 3분기 |
|
|---|---|---|
|
영업활동현금흐름 |
(17,829,184,690) |
8,337,773,438 |
|
당기순이익(손실) |
(13,477,407,662) |
7,868,529,560 |
|
당기순이익조정을 위한 가감 |
(5,725,172,387) |
2,692,043,566 |
|
기타 현금의 유입 없는 수익등 |
(9,322,126,688) |
(855,665,237) |
|
기타 현금의 유출 없는 비용등 |
3,596,954,301 |
3,547,708,803 |
|
영업활동으로인한자산ㆍ부채의변동 |
1,152,746,469 |
(2,746,094,684) |
|
이자지급(영업) |
308,297,332 |
0 |
|
이자수취(영업) |
717,542,923 |
489,062,146 |
|
법인세납부(환급) |
(805,191,365) |
34,232,850 |
|
투자활동현금흐름 |
(111,123,207,228) |
(16,139,530,218) |
|
임차보증금의 감소 |
0 |
80,855,000 |
|
임차보증금의 증가 |
(183,558,969) |
(415,559,401) |
|
유형자산의 처분 |
0 |
31,836,642 |
|
유형자산의 취득 |
(11,894,028,390) |
(3,406,130,969) |
|
무형자산의 취득 |
(154,868,336) |
(109,111,013) |
|
단기금융상품의 처분 |
117,150,000,000 |
359,984,340 |
|
단기금융상품의 취득 |
(215,999,552,510) |
(7,584,620,000) |
|
장기금융상품의 취득 |
(41,199,023) |
(96,784,817) |
|
당기손익인식금융자산의 취득 |
0 |
(5,000,000,000) |
|
재무활동현금흐름 |
107,518,590,524 |
10,237,042,686 |
|
주식의 발행 |
74,841,032,850 |
(35,324,280) |
|
무상증자 |
(36,461,870) |
0 |
|
장기차입금의 상환 |
(187,500,000) |
0 |
|
주식선택권행사로 인한 현금유입 |
1,277,373,840 |
2,392,576,520 |
|
자기주식의 취득 |
(793,980,301) |
0 |
|
종속기업유상증자 |
3,021,256,541 |
0 |
|
전환우선주의 발행 |
29,500,000,000 |
0 |
|
상환전환우선주부채의 증가 |
0 |
8,000,011,030 |
|
리스부채의 증가 |
0 |
2,464,896 |
|
리스부채의 상환 |
(103,130,536) |
(122,685,480) |
|
환율변동효과 반영전 현금및현금성자산의 순증가(감소) |
(21,433,801,394) |
2,435,285,906 |
|
기초현금및현금성자산 |
38,922,455,345 |
4,413,477,774 |
|
현금및현금성자산에 대한 환율변동효과 |
303,904,639 |
(288,501,027) |
|
기말현금및현금성자산 |
17,792,558,590 |
6,560,262,653 |
3. 연결재무제표 주석
주석
| 당분기 : 2021년 9월 30일 현재 |
| 전분기 : 2020년 9월 30일 현재 |
| 주식회사 알테오젠과 그 종속기업 |
1. 일반 사항
(1) 지배기업의 개요
주식회사 알테오젠과 그 종속기업(이하 "연결실체")의 지배기업인 주식회사 알테오젠(이하 "지배기업")은 2008년 5월 13일에 설립되어 유전자 개발과 형질전환 동식물 개발 등 생명공학 관련 연구개발을 주요 목적으로 사업을 영위하고 있습니다.
본사는 대전광역시 유성구 유성대로 1628번길 62에 위치하고 있으며, 지배기업은 2014년 12월 코스닥 시장에 상장하였습니다.
지배기업의 설립시 자본금은 100,000천원이었으며, 수차례의 유상증자 등을 통하여 당분기말 현재의 발행보통주식수는 42,264,250주, 보통주자본금은 21,132,125천원이며,발행우선주식수는 1,029,015주, 우선주자본금은 514,507천원입니다.
한편, 당분기말 현재 지배기업의 주요 주주현황은 다음과 같습니다.
| 주 주 명 | 보통주 주식수(주) | 우선주 주식수(주) | 소 계(주) | 지분율(%) | 비 고 |
|---|---|---|---|---|---|
| 박순재 | 8,505,000 | - | 8,505,000 | 19.65% | 대표이사 |
| 정혜신 | 1,680,000 | - | 1,680,000 | 3.88% | 특수관계인 |
| 박수민 | 232,500 | - | 232,500 | 0.54% | 특수관계인 |
| 형인우 | 2,500,000 | - | 2,500,000 | 5.77% | - |
| KisseiPharmaceutical,co.,Ltd | 1,297,992 | - | 1,297,992 | 3.00% | 외국법인 |
| 기타 | 28,048,758 | 1,029,015 | 29,077,773 | 67.16% | - |
| 합 계 | 42,264,250 | 1,029,015 | 43,293,265 | 100.00% |
(2) 종속기업의 개요
1) 당분기말 및 전기말 현재 종속기업 현황은 다음과 같습니다.
| (단위 : 주, 원) |
| 회사명 | 보통주자본금 | 보유주식수 | 지분율 | 업 종 | 소재지 | 보고기간종료일 | |
|---|---|---|---|---|---|---|---|
| 당분기말 | 전기말 | ||||||
| ㈜알토스바이오사이언스 | - | - | - | 100.0% | 의학 및 약학 연구개발업 | 대한민국 | 12월 31일 |
| ㈜엘에스메디텍 | 520,000,000 | 104,000 | 100.00% | 100.0% | 의약품 도매업 | 대한민국 | 12월 31일 |
| ㈜세레스에프엔디 | 1,318,819,500 | 2,637,639 | 50.08% | 63.9% | 식품첨가물 제조업 | 대한민국 | 12월 31일 |
| ㈜알토스바이오로직스 | 2,500,000,000 | 5,000,000 | 72.56% | 83.8% | 의학 및 약학 연구개발업 | 대한민국 | 12월 31일 |
2) 당분기말 및 전기말 현재 종속기업의 요약 재무상태는 다음과 같습니다.
| (당분기말) | (단위 : 원) |
| 회사명 | 자산 | 부채 | 자본 |
|---|---|---|---|
| ㈜엘에스메디텍 | 2,259,780,753 | 420,308,286 | 1,839,472,467 |
| ㈜세레스에프엔디 | 18,368,026,188 | 9,986,956,709 | 8,381,069,479 |
| ㈜알토스바이오로직스 | 61,538,989,221 | 62,664,994,788 | (1,126,005,567) |
| (전기말) | (단위 : 원) |
| 회사명 | 자산 | 부채 | 자본 |
|---|---|---|---|
| ㈜알토스바이오사이언스 | 512,390,392 | - | 512,390,392 |
| ㈜엘에스메디텍 | 1,313,069,216 | 113,368,126 | 1,199,701,090 |
| ㈜세레스에프엔디 | 17,386,289,227 | 19,236,466,993 | (1,850,177,766) |
| ㈜알토스바이오로직스 |
31,399,833,254 | 31,015,771,350 | 384,061,904 |
3) 당분기 및 전분기 중 종속기업의 요약 경영성과는 다음과 같습니다.
| (당분기) | (단위 : 원) |
| 회사명 | 매출 | 분기순손익 | 총포괄이익 |
|---|---|---|---|
| ㈜엘에스메디텍 | 10,964,608,697 | 639,771,377 | 639,771,377 |
| ㈜세레스에프엔디 | 6,497,430,473 | 898,775,510 | 898,775,510 |
| ㈜알토스바이오로직스 | - | (2,071,712,618) | (2,071,712,618) |
| (전분기) | (단위 : 원) |
| 회사명 | 매출 | 분기순손익 | 총포괄이익 |
|---|---|---|---|
| (주)알토스바이오사이언스 | - | 3,572,706 | 3,572,706 |
| (주)LS메디텍 | 9,350,343,880 | 196,911,722 | 196,911,722 |
| (주)세레스에프엔디 | 2,314,445,361 | (4,491,814,255) | (4,491,814,255) |
2. 중요한 회계정책
(1) 재무제표 작성기준
연결실체의 2021년 6월 30일로 종료하는 6개월 보고기간에 대한 요약분기연결재무제표는 기업회계기준서 제1034호 '중간재무보고'에 따라 작성되었습니다. 이 요약분기연결재무제표는 보고기간말인 2021년 6월 30일 현재 유효하거나 조기 도입한 한국채택국제회계기준에 따라 작성되었습니다.
1) 연결실체가 채택한 제ㆍ개정 기준서 및 해석서
연결실체는 2021년 1월 1일로 개시하는 회계기간부터 다음의 제ㆍ개정 기준서 및 해석서를 신규로 적용하였습니다.
- 기업회계기준서 제 1116호 '리스' 개정 - 코로나19 관련 임차료 할인 등에 대한 실무적 간편법
실무적 간편법으로, 리스이용자는 코로나19의 직접적인 결과로 발생한 임차료 할인 등이 리스변경에 해당하는지 평가하지 않을 수 있습니다. 이러한 선택을 한 리스이용자는 임차료 할인 등으로 인한 리스료 변동을 그러한 변동이 리스변경이 아닐 경우에이 기준서가 규정하는 방식과 일관되게 회계처리하여야 합니다. 해당 기준서의 개정이 연결재무제표에 미치는 중요한 영향은 없습니다.
- 기업회계기준서 제1109호 '금융상품', 제1039호 '금융상품: 인식과 측정', 제1107호 '금융상품: 공시', 제 1104호 '보험계약' 및 제 1116호 '리스' 개정 - 이자율지표 개혁(2단계 개정)
이자율지표개혁과 관련하여 상각후원가로 측정되는 금융상품의 이자율지표대체시 장부금액이 아닌 유효이자율을 조정하고, 위험회피관계에서 이자율지표대체가 발생한 경우에도 중단없이 위험회피회계를 계속할 수 있도록 하는 등의 예외규정을 포함하고 있습니다. 해당 기준서의 개정이 연결재무제표에 미치는 중요한 영향은 없습니다.
2) 연결실체가 적용하지 않은 제ㆍ개정 기준서 및 해석서
제정 또는 공표되었으나 시행일이 도래하지 않아 적용하지 아니한 제ㆍ개정 기준서 및 해석서는 다음과 같습니다.
- 기업회계기준서 제1103호 '사업결합' 개정 - 개념체계의 인용
인식할 자산과 부채의 정의를 개정된 재무보고를 위한 개념체계를 참조하도록 개정되었으나, 기업회계기준서 제1037호 '충당부채, 우발부채 및 우발자산' 및 해석서 제2121호 '부담금'의 적용범위에 포함되는 부채 및 우발부채에 대해서는 해당 기준서를 적용하도록 예외를 추가하고, 우발자산이 취득일에 인식되지 않는다는 점을 명확히 하였습니다. 동 개정사항은 2022년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 연결실체는 동 개정으로 인해 연결재무제표에 중요한 영향은 없을 것으로 예상하고 있습니다.
- 기업회계기준서 제1016호 '유형자산' 개정 - 의도한 사용 전의 매각금액
기업이 자산을 의도한 방식으로 사용하기 전에 생산된 품목의 판매에서 발생하는 수익을 생산원가와 함께 당기손익으로 인식하도록 요구하며, 유형자산의 취득원가에서차감하는 것을 금지하고 있습니다. 동 개정사항은 2022년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 연결실체는 동 개정으로 인한 연결재무제표의 영향을 검토 중에 있습니다.
- 기업회계기준서 제1037호 '충당부채, 우발부채 및 우발자산' 개정 - 손실부담계약:계약이행원가
손실부담계약을 식별할 때 계약이행원가의 범위를 계약 이행을 위한 증분원가와 계약 이행에 직접 관련되는 다른 원가의 배분이라는 점을 명확히 하였습니다. 동 개정사항은 2022년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 연결실체는 동 개정으로 인해 연결재무제표에 중요한 영향은 없을 것으로 예상하고 있습니다.
- 한국채택국제회계기준 연차개선 2018-2020
한국채택국제회계기준 연차개선 2018-2020은 2022년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 연결실체는 동 개정으로 인해 연결재무제표에 중요한 영향은 없을 것으로 예상하고 있습니다.
·기업회계기준서 제1101호 '한국채택국제회계기준의 최초 채택' : 최초채택기업인 종속기업
·기업회계기준서 제1109호 '금융상품' : 금융부채 제거 목적의 10% 테스트 관련 수수료
·기업회계기준서 제1116호 '리스' : 리스 인센티브
·기업회계기준서 제1041호 '농립어업' : 공정가치 측정
- 기업회계기준서 제1001호 '재무제표 표시' 개정 - 부채의 유동/비유동 분류
보고기간말 현재 존재하는 실질적인 권리에 따라 유동 또는 비유동으로 분류되며, 부채의 결제를 연기할 수 있는 권리의 행사가능성이나 경영진의 기대는 고려하지 않습니다. 또한, 부채의 결제에 자기지분상품의 이전도 포함되나, 복합금융상품에서 자기지분상품으로 결제하는 옵션이 지분상품의 정의를 충족하여 부채와 분리하여 인식된경우는 제외됩니다. 동 개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 적용하며, 조기적용이 허용됩니다. 연결실체는 동 개정으로 인한 연결재무제표의 영향을 검토 중에 있습니다.
- 기업회계기준서 제 1116호 '리스' 개정 - 2021년 6월 30일 후에도 제공되는 코로나19 관련 임차료 할인 등
코로나19의 직접적인 결과로 발생한 임차료 할인 등(rent concession)이 리스변경에 해당하는지 평가하지 않을 수 있도록 하는 실무적 간편법의 적용대상이 2022년 6월 30일 이전에 지급하여야 할 리스료에 영향을 미치는 리스료 감면으로 확대되었습니다. 리스이용자는 비슷한 상황에서 특성이 비슷한 계약에 실무적 간편법을 일관되게 적용해야 합니다. 동 개정사항은 2021년 4월 1일 이후 시작하는 회계연도부터 적용되며, 조기도입이 가능합니다. 연결실체는 동 개정으로 인해 연결재무제표에 중요한 영향은 없을 것으로 예상하고 있습니다.
(2) 회계정책
요약분기연결재무제표의 작성에 적용된 유의적 회계정책과 계산방법은 주석 2.(1).1)에서 설명하는 제ㆍ개정 기준서의 적용으로 인한 변경 및 아래 문단에서 설명하는 사항을 제외하고는 전기 연결재무제표 작성에 적용된 회계정책이나 계산방법과 동일합니다.
1) 법인세비용
중간기간의 법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균연간법인세율, 즉 추정평균연간유효법인세율을 중간기간의 세전이익에 적용하여 계산합니다.
3. 중요한 회계추정 및 가정
연결실체는 미래에 대하여 추정 및 가정을 하고 있습니다. 추정 및 가정은 지속적으로 평가되며, 과거 경험과 현재의 상황에서 합리적으로 예측가능한 미래의 사건과 같은 다른 요소들을 고려하여 이루어집니다. 이러한 회계추정은 실제 결과와 다를 수도있습니다.
요약분기연결재무제표 작성시 사용된 중요한 회계추정 및 가정은 법인세비용을 결정하는데 사용된 추정의 방법을 제외하고는 전기 연결재무제표 작성에 적용된 회계추정 및 가정과 동일합니다.
COVID-19의 확산은 국내외 경제에 중대한 영향을 미치고 있습니다. 이는 생산성 저하와 매출의 감소나 지연, 기존 채권의 회수 등에 부정적인 영향을 미칠 수 있습니다. 이로 인해 연결실체의 재무상태와 재무성과에도 부정적인 영향이 발생할 수 있으며, 이러한 영향은 2021년 연차재무제표에도 지속될 것으로 예상됩니다.
중간기간의 재무제표 작성시 사용된 중요한 회계추정 및 가정은 COVID-19에 따른 불확실성의 변동에 따라 조정될 수 있으며, COVID-19로 인하여 연결실체의 사업, 재무상태 및 경영성과 등에 미칠 궁극적인 영향은 현재 예측할 수 없습니다.
4. 영업부문
연결실체의 주요 수익은 유전자 개발과 형질전환 동식물 개발 등 생명공학 관련 연구개발로부터 창출되며, 성과에 대한 최고영업의사결정자에게 보고되는 정보 또한 상기 주요 수익 관련 정보가 단일부문으로 보고됩니다. 따라서 한국채택국제회계기준 제1108호(영업부문)에 따른 보고부문은 단일부문으로 기업전체 수준에서의 부문별 정보는 다음과 같습니다.
(1) 당분기 및 전분기 영업수익에 대한 정보는 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 연구용역매출 | 6,934,580,063 | 25,659,540,820 |
| 상품매출 | 16,751,037,141 | 10,564,123,581 |
| 제품매출 | 711,002,029 | 1,100,665,660 |
| 합 계 | 24,396,619,233 | 37,324,330,061 |
(2) 당분기 및 전분기 영업수익의 지역에 대한 정보는 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 국 내 | 해 외 | 계 |
|---|---|---|---|
| 연구용역매출 | - | 6,934,580,063 | 6,934,580,063 |
| 상품매출 | 16,751,037,141 | - | 16,751,037,141 |
| 제품매출 | 550,352,029 | 160,650,000 | 711,002,029 |
| 합 계 | 17,301,389,170 | 7,095,230,063 | 24,396,619,233 |
| (전분기) |
(단위: 원) |
| 구 분 | 국 내 | 해 외 | 계 |
|---|---|---|---|
| 연구용역매출 | - | 25,659,540,820 | 25,659,540,820 |
| 상품매출 | 9,933,255,340 | 630,868,241 | 10,564,123,581 |
| 제품매출 | 23,250,000 | 1,077,415,660 | 1,100,665,660 |
| 합 계 | 9,956,505,340 | 27,367,824,721 | 37,324,330,061 |
(3) 당분기 및 전분기 중 연결실체 수익의 10% 이상을 차지하는 주요 거래처는 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 주요거래처 A(*) | - | 6,246,521,053 |
| 주요거래처 B(*) | - | 19,211,200,000 |
| 주요거래처 C | 4,147,857,000 | - |
| 주요거래처 D | 6,570,000,000 | - |
| 주요거래처 E | 2,973,370,219 | 2,743,353,252 |
| 합 계 | 13,691,227,219 | 28,201,074,305 |
(*) 당분기 및 전분기 수익의 10% 이상을 차지하는 거래처에 포함되지 아니하였으나, 전분기 중 매출액 증가로 인하여 주요거래처에 포함되었습니다.
5. 범주별 금융상품
(1) 당분기말 및 전기말 현재 금융자산 범주별 장부금액은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | |
|---|---|---|---|
| 상각후원가로 측정하는 금융자산 |
현금및현금성자산 | 17,792,558,590 | 38,922,455,345 |
| 장.단기금융상품 | 196,216,750,963 | 95,046,992,048 | |
| 매출채권및기타채권 | 4,827,253,068 | 2,692,677,487 | |
| 기타비유동금융자산 | 714,656,024 | 550,150,272 | |
| 합 계(*) | 219,551,218,645 | 137,212,275,152 | |
(*) 당분기말 및 전기말 현재 금융자산의 장부금액은 공정가치의 합리적인 근사치인 금액입니다.
(2) 당분기말 및 전기말 현재 금융부채 범주별 장부금액은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | |
|---|---|---|---|
| 상각후원가로 측정하는 금융부채 |
매입채무 | 2,330,857,676 | 440,241,691 |
| 장.단기차입금 | 3,550,000,000 | 3,737,500,000 | |
| 기타유동금융부채 | 1,063,399,358 | 2,216,725,480 | |
| 기타비유동금융부채 |
1,006,135,217 | 810,719,563 | |
| 상환전환우선주부채 | 3,319,309,445 | 10,286,242,782 | |
| 기타 금융부채 | 유동리스부채 | 141,783,824 | 107,002,875 |
| 비유동리스부채 | 149,037,539 | 84,654,462 | |
| 당기손익-공정가치 측정 금융부채 | 전환우선주부채 | 60,500,000,000 | 31,000,000,000 |
| 파생상품부채 | 458,040,168 | 932,275,121 | |
| 합 계(*) | 72,518,563,227 | 49,615,361,974 | |
(*) 당분기말 및 전기말 현재 금융부채의 장부금액은 공정가치의 합리적인 근사치인 금액이며, 범주별 금융부채 기준을 적용 받지 않는 리스부채를 포함하였습니다.
(3) 당분기 및 전분기 금융상품 범주별 순손익은 다음과 같습니다.
| (당분기) |
(단위: 원) |
|
구 분 |
상각후원가로 |
상각후원가로 측정하는 금융부채 |
당기손익-공정가치 금융부채 | 합 계 |
|---|---|---|---|---|
| 이자수익 | 1,590,184,847 | - | - | 1,590,184,847 |
| 이자비용(*) | - | 523,983,435 | - | 523,983,435 |
| 외환차익 | 239,281,078 | 21,004,062 | - | 260,285,140 |
| 외환차손 | 10,331,981 | 55,737,907 | - | 66,069,888 |
| 외화환산이익 | 2,596,893,315 | 359,524 | - | 2,597,252,839 |
| 외화환산손실 | 10,789,372 | 900,860 | - | 11,690,232 |
| 파생상품평가손실 | - | - | 196,675,517 | 196,675,517 |
(*) 범주별 금융부채 기준을 적용 받지 않는 리스부채의 이자비용을 포함한 금액입니다.
| (전분기) |
(단위: 원) |
|
구 분 |
상각후원가로 |
당기손익-공정가치 금융자산 |
상각후원가로 측정하는 금융부채 |
당기손익-공정가치 금융부채 |
합 계 |
|---|---|---|---|---|---|
| 이자수익 | 643,065,547 | - | - | - | 643,065,547 |
| 이자비용 | - | - | 371,262,547 | - | 371,262,547 |
| 당기손익인식금융자산평가이익 | - | 41,643,835 | - | - | 41,643,835 |
| 외환차익 | 344,180,094 | - | 38,010,605 | - | 382,190,699 |
| 외환차손 | 300,495,997 | - | 7,220,571 | - | 307,716,568 |
| 외화환산이익 | 128,840,672 | - | 205,499 | - | 129,046,171 |
| 외화환산손실 | 417,547,198 | - | 412,103 | - | 417,959,301 |
| 파생상품평가손실 | - | - | - | 165,001,962 | 165,001,962 |
(*) 범주별 금융부채 기준을 적용 받지 않는 리스부채의 이자비용을 포함한 금액입니다.
6. 현금및현금성자산과 금융상품
(1) 당분기말 및 전기말 현재 현금및현금성자산과 금융상품의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 금융기관 | 이자율(%) | 당분기말 | 전기말 | |
|---|---|---|---|---|---|
| 현금및현금성자산 | 요구불예금 등 | KEB하나은행 등 | - | 17,792,558,590 | 38,922,455,345 |
| 단기금융상품 | 정기예금 | KEB하나은행 등 | 0.10~2.11 | 195,950,559,892 | 94,822,000,000 |
| 장기금융상품 | 저축성보험 | 하나생명 등 | - | 266,191,071 | 224,992,048 |
| 합 계 | 214,009,309,553 | 133,969,447,393 | |||
(2) 당분기말 및 전기말 현재 사용이 제한된 금융상품은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 내 역 | 당분기말 | 전기말 |
|---|---|---|---|
| 단기금융상품 | 우리사주대출에 대한 담보제공(*1) | - | 88,000,000 |
| 외상매출채권담보대출에 대한 담보제공(*2) | 1,000,000,000 | - |
(*1) 연결실체는 우리사주조합의 대출 지원을 위해 대출기관인 KEB하나은행에 예금담보를 제공하고 있습니다(주석31 참조).
(*2) 연결실체는 외상매출채권담보대출을 위해 대촐기관이 KEB하나은행에 예금담보를 제공하고 있습니다(주석31 참조).
7. 매출채권및기타채권
(1) 당분기말 및 전기말 현재 매출채권및기타채권의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 매출채권 | 2,863,061,819 | 1,564,046,574 |
| (-)대손충당금 | (3,769,200) | (7,827,250) |
| 미수금 | 742,068,569 | 770,440,243 |
| 미수수익 | 1,225,891,880 | 366,017,920 |
| 합 계 | 4,827,253,068 | 2,692,677,487 |
(2) 신용위험 및 대손충당금
상기 매출채권및기타채권은 대여금및수취채권으로 분류되며 상각후원가로 측정됩니다.
연결실체의 평균 신용공여기간은 60일입니다. 대금청구일로부터 최초 60일 동안은 매출채권에 대한 별도의 대손충당금을 설정하지 않고 있으며, 60일 초과 경과 매출채권에 대해서는 거래상대방의 과거 채무불이행 경험 및 현재의 재무상태 분석에 근거하여 결정된 미회수 추정금액을 대손충당금으로 설정하고 있습니다.
연결실체는 당분기말 현재 회수기일이 경과하였거나 신용등급에 중요한 변동이 있는채권에 대해 대손충당금을 인식하고 있습니다. 이에 따라 대여금및수취채권에 대하여 설정한 대손충당금은 3,769,200원(전기 7,827,250원)입니다.
대손충당금의 감소는 일반적으로 과거 대손설정의 사유가 해소되거나 회수가능성이 없는 채권을 제각할 경우 발생하고 있습니다. 이에 따라 대여금및수취채권의 대손충당금에 대하여 당분기에 인식한 대손충당금환입액은 없습니다 (전기 1,039,157원). 환입된 금액은 연결포괄손익계산서의 '판매비와관리비'에 포함됩니다.
8. 재고자산
(1) 당분기말 및 전기말 현재 재고자산의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 원재료 | 165,599,431 | 181,816,053 |
| 재공품 | 419,397,118 | 73,376,838 |
| 상품 | 362,117,198 | 204,470,028 |
| 합 계 | 947,113,747 | 459,662,919 |
(2) 비용으로 인식되어 '매출원가'에 포함된 재고자산의 원가는 16,536,778,868원(전분기: 10,672,131,414원) 입니다.
9. 유형자산
(1) 당분기말 및 전기말 현재 유형자산의 구성내역은 다음과 같습니다.
| (당분기말) | (단위: 원) |
| 구 분 | 취득원가 | 정부보조금 | 감가상각누계액 | 장부금액 |
|---|---|---|---|---|
| 토지 | 2,784,702,179 | - | - | 2,784,702,179 |
| 조경 | 12,000,000 | - | - | 12,000,000 |
| 건물 | 7,578,305,432 | - | (965,109,554) | 6,613,195,878 |
| 구축물 | 39,386,000 | - | (6,978,550) | 32,407,450 |
| 기계장치 | 4,113,625,491 | - | (789,748,248) | 3,323,877,243 |
| 차량운반구 | 115,970,660 | - | (64,493,917) | 51,476,743 |
| 비품 | 580,207,134 | - | (314,047,900) | 266,159,234 |
| 건설중인자산 | 12,530,444,600 | - | - | 12,530,444,600 |
| 연구용기자재 | 7,304,952,420 | (114,632,852) | (4,283,849,313) | 2,906,470,255 |
| 시설장치 | 1,335,691,891 | - | (178,617,376) | 1,157,074,515 |
| 합 계 | 36,395,285,807 | (114,632,852) | (6,602,844,858) | 29,677,808,097 |
| (전기말) | (단위: 원) |
| 구 분 | 취득원가 | 정부보조금 | 감가상각누계액 | 장부금액 |
|---|---|---|---|---|
| 토지 | 2,784,702,179 | - | - | 2,784,702,179 |
| 조경 | 12,000,000 | - | - | 12,000,000 |
| 건물 | 6,033,618,524 | - | (785,967,488) | 5,247,651,036 |
| 구축물 | 39,386,000 | - | (6,320,200) | 33,065,800 |
| 기계장치 | 3,636,848,691 | - | (483,608,285) | 3,153,240,406 |
| 차량운반구 | 115,970,660 | - | (47,098,320) | 68,872,340 |
| 비품 | 481,173,358 | - | (269,872,652) | 211,300,706 |
| 건설중인자산 | 3,235,600,260 | - | - | 3,235,600,260 |
| 연구용기자재 | 7,173,302,825 | (51,185,186) | (3,558,603,098) | 3,563,514,541 |
| 시설장치 | 1,058,871,891 | - | (94,696,334) | 964,175,557 |
| 합 계 | 24,571,474,388 | (51,185,186) | (5,246,166,377) | 19,274,122,825 |
(2) 당분기 및 전분기 중 유형자산 장부금액의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 기초금액 | 취 득 | 처 분 | 상 각 | 대 체 | 기 타 | 손상 | 기말금액 |
|---|---|---|---|---|---|---|---|---|
| 토지 | 2,784,702,179 | - | - | - | - | - | - | 2,784,702,179 |
| 조경 | 12,000,000 | - | - | - | - | - | - | 12,000,000 |
| 건물 | 5,247,651,036 | - | - | (179,142,066) | 1,544,686,908 | - | - | 6,613,195,878 |
| 구축물 | 33,065,800 | - | - | (658,350) | - | - | - | 32,407,450 |
| 기계장치 | 3,153,240,406 | 247,776,800 | - | (306,139,963) | 229,000,000 | - | - | 3,323,877,243 |
| 차량운반구 | 68,872,340 | - | - | (17,395,597) | - | - | - | 51,476,743 |
| 비품 | 211,300,706 | 106,076,775 | (7,000) | (51,211,247) | - | - | - | 266,159,234 |
| 건설중인자산 | 3,235,600,260 | 11,278,831,248 | - | - | (1,918,186,908) | - | (65,800,000) | 12,530,444,600 |
| 연구용기자재(*) | 3,563,514,541 | 165,634,154 | (745,529) | (750,806,124) | - | (71,126,787) | - | 2,906,470,255 |
| 시설장치 | 964,175,557 | 159,420,000 | (17,728,328) | (93,292,714) | 144,500,000 | - | - | 1,157,074,515 |
| 합 계 | 19,274,122,825 | 11,957,738,977 | (18,480,857) | (1,398,646,061) | - | (71,126,787) | (65,800,000) | 29,677,808,097 |
(*) 정부보조금의 변동내역을 포함하고 있습니다.
| (전분기) | (단위: 원) |
| 구 분 | 기초금액 | 취 득 | 상 각 | 대 체 | 기말금액 |
|---|---|---|---|---|---|
| 토지 | 5,441,751,169 | - | - | - | 5,441,751,169 |
| 조경 | - | 12,000,000 | - | - | 12,000,000 |
| 건물 | 4,009,801,318 | 95,480,330 | (157,705,125) | 1,362,332,000 | 5,309,908,523 |
| 구축물 | 34,582,700 | - | (1,137,679) | - | 33,445,021 |
| 기계장치 | 1,218,258,326 | 335,804,091 | (230,704,386) | 1,889,183,200 | 3,212,541,231 |
| 차량운반구 | 110,316,768 | - | (21,717,634) | - | 88,599,134 |
| 비품 | 143,402,906 | 103,304,962 | (43,570,554) | - | 203,137,314 |
| 건설중인자산 | 4,913,166,640 | 967,639,370 | - | (3,433,015,200) | 2,447,790,810 |
| 연구용기자재(*) | 3,022,875,752 | 1,341,033,064 | (691,641,750) | - | 3,672,267,066 |
| 시설장치 | 155,074,787 | 529,636,182 | (58,091,895) | 181,500,000 | 808,119,074 |
| 합계 | 19,049,230,366 | 3,384,897,999 | (1,204,569,023) | - | 21,229,559,342 |
(*) 정부보조금의 변동내역을 포함하고 있습니다.
(3) 당분기 및 전분기 감가상각비가 포함된 항목은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
|
매출원가 |
580,234,961 | 337,662,945 |
| 판매비와관리비(*) | 818,411,100 | 866,906,078 |
| 합 계 | 1,398,646,061 | 1,204,569,023 |
(*) 판매비와관리비의 감가상각비에는 경상연구개발비 및 시험생산비 665,656,728원(전분기 753,364,195원)이 포함되어 있습니다.
(4) 당분기말 및 전기말 현재 유형자산의 담보제공내역은 다음과 같습니다.
| (당분기말) | (단위: 원) |
| 담보제공자산 |
장부금액 |
담보설정금액 |
관련 계정과목 |
관련 금액 |
담보권자 |
|---|---|---|---|---|---|
|
토지 |
984,189,870 | 4,560,000,000 | 차입금(*) | 3,550,000,000 | 하나은행 |
|
건물 |
3,320,977,241 | ||||
| 기타(기계,시설장치) | 4,438,886,275 |
| (전기말) | (단위: 원) |
| 담보제공자산 |
장부금액 |
담보설정금액 |
관련 계정과목 |
관련 금액 |
담보권자 |
|---|---|---|---|---|---|
|
토지 |
984,189,870 | 4,560,000,000 | 차입금(*) | 3,737,500,000 | KEB하나은행 |
|
건물 |
3,387,404,478 | ||||
| 기타(기계,시설장치) | 4,096,709,650 |
(*) 연결실체는 KEB하나은행의 차입금과 관련하여 토지와 건물 및 기계,시설장치를 담보로 제공하고 있습니다(주석14 참조).
10. 리스
연결실체는 건물과 차량운반구를 리스하였으며 평균리스기간은 3년입니다. 연결실체는 일부 차량운반구에 대하여 리스계약 종료시점에 행사할 수 있는 매수선택권을 가지고 있습니다. 사용권자산에 대한 법적 소유권은 리스부채에 대한 담보로 리스제공자가 보유하고 있습니다.
(1) 당분기말 및 전기말 현재 기초자산 유형별 사용권자산 및 리스부채의 내역은 다음과 같습니다.
|
(단위: 원) |
|
구 분 |
당분기말 | 전기말 |
|---|---|---|
| 사용권자산 | ||
| 차량운반구 | 208,468,371 | 107,521,883 |
| 건물 | 100,836,128 | 101,254,088 |
| 장비 | - | 1,027,040 |
| 합 계 | 309,304,499 | 209,803,011 |
상기 리스자산 계산에서 사용된 증분차입이자율은 2.23%~4.02%입니다.
|
(단위: 원) |
|
구 분 |
당분기말 |
전기말 |
|---|---|---|
|
리스부채 |
||
|
유동 |
141,783,824 | 107,002,875 |
|
비유동 |
149,037,539 | 84,654,462 |
| 합 계 | 290,821,363 | 191,657,337 |
(2) 당분기 및 전분기 중 손익으로 인식된 금액은 다음과 같습니다.
|
(단위: 원) |
|
구 분 |
당분기 |
전분기 |
|---|---|---|
|
사용권자산의 감가상각비 |
||
| 차량운반구 | 55,123,440 | 38,228,797 |
| 건물 | 63,180,964 | 63,088,551 |
| 장비 | 1,027,040 | 821,632 |
| 합 계 | 119,331,444 | 102,138,980 |
| 리스부채 이자비용 | 6,380,618 | 4,825,474 |
| 단기리스 관련 비용 | 53,807,809 | 33,808,360 |
연결실체가 당분기말 현재 체결하고 있는 단기리스의 리스약정 금액은 10,388,400원(전기말: 38,852,200원)입니다.
당분기 중 리스로 인한 총 현금유출 금액은 163,318,963원(전분기: 132,124,866원)입니다.
11. 무형자산
(1) 당분기말 및 전기말 현재 무형자산의 구성내역은 다음과 같습니다.
| (당분기말) | (단위: 원) |
| 구 분 | 취득원가 | 정부보조금 | 상각누계액 | 장부금액 |
|---|---|---|---|---|
| 특허권 | 703,543,669 | (115,179,841) | (273,462,212) | 314,901,616 |
| 소프트웨어 | 336,449,667 | (17,459,276) | (120,518,301) | 198,472,090 |
| 상표권 | 2,553,404 | - | (2,552,404) | 1,000 |
| 건설중인자산 | 457,728,239 | (59,926,453) | - | 397,801,786 |
| 회원권 | 82,000,000 | - | - | 82,000,000 |
| 영업권 | 112,983,012 | - | - | 112,983,012 |
| 합 계 | 1,695,257,991 | (192,565,570) | (396,532,917) | 1,106,159,504 |
| (전기말) | (단위: 원) |
| 구 분 | 취득원가 | 정부보조금 | 상각누계액 | 장부금액 |
|---|---|---|---|---|
| 특허권 | 668,247,058 | (117,528,457) | (221,494,117) | 329,224,484 |
| 소프트웨어 | 266,049,667 | (18,841,936) | (83,891,325) | 163,316,406 |
| 상표권 | 2,553,404 | - | (2,552,404) | 1,000 |
| 건설중인자산 | 407,075,869 | (74,165,666) | - | 332,910,203 |
| 회원권 | 82,000,000 | - | - | 82,000,000 |
| 영업권 | 112,983,012 | - | - | 112,983,012 |
| 합 계 | 1,538,909,010 | (210,536,059) | (307,937,846) | 1,020,435,105 |
(2) 당분기 및 전분기 중 무형자산 장부금액의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 기초금액 | 취 득 | 대 체 | 상 각 | 정부보조금 수령 | 기말금액 |
|---|---|---|---|---|---|---|
| 특허권(*) | 329,224,484 | - | 21,057,398 | (35,380,266) | - | 314,901,616 |
| 소프트웨어(*) | 163,316,406 | 70,400,000 | - | (33,763,671) | (1,480,645) | 198,472,090 |
| 상표권 | 1,000 | - | - | - | - | 1,000 |
| 건설중인자산(*) | 332,910,203 | 85,948,981 | (21,057,398) | - | - | 397,801,786 |
| 회원권 | 82,000,000 | - | - | - | - | 82,000,000 |
| 영업권 | 112,983,012 | - | - | - | - | 112,983,012 |
| 합 계 | 1,020,435,105 | 156,348,981 | - | (69,143,937) | (1,480,645) | 1,106,159,504 |
(*) 특허권 취득과 관련한 정부보조금의 변동내역을 포함하여 작성하였습니다.
| (전분기) | (단위: 원) |
| 구 분 | 기초금액 | 취 득 | 대 체 | 상 각 | 손 상 | 기말금액 |
|---|---|---|---|---|---|---|
| 특허권(*) | 229,816,457 | - | 94,737,597 | (27,313,708) | (453,767) | 296,786,579 |
| 소프트웨어 | 76,021,019 | 35,815,000 | - | (16,787,021) | - | 95,048,998 |
| 상표권 | 1,000 | - | - | - | - | 1,000 |
| 건설중인자산(*) | 242,675,062 | 73,296,013 | (94,737,597) | - | (9,048,242) | 212,185,236 |
| 회원권 | 82,000,000 | - | - | - | 82,000,000 | |
| 영업권 | 112,983,012 | - | - | - | - | 112,983,012 |
| 합 계 | 743,496,550 | 109,111,013 | - | (44,100,729) | (9,502,009) | 799,004,825 |
(*) 특허권 취득과 관련한 정부보조금의 변동내역을 포함하여 작성하였습니다.
(3) 당분기 및 전분기 무형자산상각비는 전액 판매비와관리비에 포함되어 있습니다.
(4) 연결실체가 비용으로 인식한 연구와 개발 지출의 총액은 12,129,288,726원(전분기: 5,339,916,599원)입니다.
12. 정부보조금
(1) 당분기말 및 전기말 현재 정부기관 등과 체결한 국책연구과제와 관련하여 수령한 정부보조금의 미사용 및 반환예정액은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 보통예금 | 33,333,336 | 20,833,335 |
| 장기미지급금(*) | 930,155,031 | 810,719,563 |
| 합 계 | 963,488,367 | 831,552,898 |
(*) 상환의무가 있는 경우 장기미지급금으로 계상하고 있습니다.
(2) 당분기 및 전분기 중 정부보조금의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 기 초 | 수 령 | 사 용 | 기 타 | 기 말 |
|---|---|---|---|---|---|
| 정부보조금 | 831,552,898 | 1,263,281,037 | (1,131,143,430) | (202,138) | 963,488,367 |
| (전분기) | (단위: 원) |
| 구 분 | 기 초 | 수 령 | 사 용 | 기 타 | 기 말 |
|---|---|---|---|---|---|
| 정부보조금 | 2,487,589,277 | 815,590,799 | (2,107,707,108) | (178,267,528) | 1,017,205,440 |
(3) 당분기 및 전분기 중 정부보조금의 지출내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 유/무형자산의 취득 | 72,607,432 | 2,657,143 |
| 선급금(기업부담금)의 감소 | 125,005,100 | 74,384,531 |
| 비용상계 | 933,530,897 | 2,030,665,434 |
| 합 계 | 1,131,143,430 | 2,107,707,108 |
13. 기타자산
당분기말 및 전기말 현재 기타자산의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | |
|---|---|---|---|
| 유동자산 | 선급금 | 267,467,845 | 765,001,228 |
| 선급비용 | 117,243,804 | 109,851,406 | |
| 소 계 | 384,711,649 | 874,852,634 | |
| 비유동자산 | 장기선급비용 | 6,918,649 | 9,117,672 |
| 소 계 | 6,918,649 | 9,117,672 | |
| 합 계 | 391,630,298 | 883,970,306 | |
14. 차입금
당분기말 및 전기말 현재 차입금의 내역은 다음과 같습니다.
| (단위: 원) |
| 구분 | 금융기관 | 종류 | 이자율 | 당분기말 | 전기말 |
|---|---|---|---|---|---|
| 단기차입금 | KEB하나은행(*) | 기업시설일반자금대출 | 2.951%(변동금리) | 800,000,000 | 1,300,000,000 |
| KEB하나은행(*) | 기업시설일반자금대출 | 1.781%(변동금리) | 1,500,000,000 | 1,500,000,000 | |
| KEB하나은행(*) | 기업시설일반자금대출 | 0.254% | 500,000,000 | - | |
| 합 계 | 2,800,000,000 | 2,800,000,000 | |||
| 유동성장기차입금 | KEB하나은행(*) | 기업시설기타시설자금대출 | 2.320%(변동금리) | 250,000,000 | 250,000,000 |
| 장기차입금 | KEB하나은행(*) | 기업시설기타시설자금대출 | 2.320%(변동금리) | 500,000,000 | 687,500,000 |
(*) KEB하나은행 차입금에 대해서는 연결실체의 토지와 건물 및 기계, 시설장치가 담보로 설정되어 있습니다(주석9, 주석31 참조).
15. 매입채무 및 기타금융부채
당분기말 및 전기말 현재 매입채무 및 기타금융부채의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | ||
|---|---|---|---|---|
| 유 동 | 비유동 | 유 동 | 비유동 | |
| 매입채무 | 2,330,857,676 | - | 440,241,691 | - |
| 미지급금 | 831,856,452 | 930,155,031 | 1,939,152,232 | 810,719,563 |
| 미지급비용 | 231,542,906 | - | 277,573,248 | - |
| 이연법인세부채 | - | 75,980,186 | - | - |
| 합 계 | 3,394,257,034 | 1,006,135,217 | 2,656,967,171 | 810,719,563 |
16. 기타부채
당분기말 및 전기말 현재 기타부채의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | |
|---|---|---|---|
| 유동부채 | 예수금 | 335,664,699 | 165,699,024 |
| 선수금 | 153,378,070 | 12,938,667 | |
| 부가세예수금 | 18,622,216 | 27,919,636 | |
| 소 계 | 507,664,985 | 206,557,327 | |
| 비유동부채 | 장기선수금 | 2,000,000,000 | - |
| 합 계 | 2,507,664,985 | 206,557,327 | |
17. 상환전환우선주
(1) 당분기말과 전기말 현재 종속기업인㈜세레스에프엔디가 발행한 상환전환우선주부채의 세부내역은 다음과 같습니다.
| (당분기말) |
| 구 분 | 제2차 상환전환우선주 |
|---|---|
| 발행일 | 2020년 02월 18일 |
| 발행주식수(최초 발행시) | 264,783주 |
| 1주당 발행가액(최초발행시) | 11,330원 |
| 총발행가액(최초발행시) | 2,999,991,390 원 |
| 전환대상 및 전환비율 | 우선주와 1:1로 전환가능 |
| 전환가액 조정 | 전환가액을 하회하는 발행가액으로 유상증자를 하는 경우 등 |
| 전환권 행사기간 | 발행일 익일로부터 존속기간 내 (존속기간은 발행일 익일부터 10년) |
| (전기말) |
| 구 분 | 제1차 상환전환우선주(*) | 제2차 상환전환우선주(*) |
|---|---|---|
| 발행일 | 2019년 02월 01일 | 2020년 02월 18일 |
| 발행주식수(최초 발행시) | 307,694주 | 706,091주 |
| 1주당 발행가액(최초발행시) | 4,875원 | 11,330원 |
| 총발행가액(최초발행시) | 1,500,008,250원 | 8,000,011,030원 |
| 전환대상 및 전환비율 | 보통주와 1:1로 전환가능 | 보통주와 1:1로 전환가능 |
| 전환가액 조정 | 전환가액을 하회하는 발행가액으로 유상증자를 하는 경우 등 |
전환가액을 하회하는 발행가액으로 유상증자를 하는 경우 등 |
| 전환권 행사기간 | 발행일 익일로부터 존속기간 내 (존속기간은 발행일 익일부터 10년) |
발행일 익일로부터 존속기간 내 (존속기간은 발행일 익일부터 10년) |
| 투자자의 조기상환권 | 본건 우선주식의 주주는 본건 우선주식의 납입기일 다음날로부터 3 년이 경과한 날로부터 회사에 대하여 본조에 따라 본건 우선주식의 전부 또는 일부의 상환을 청구할 수 있음 | 본건 우선주식의 주주는 본건 우선주식의 납입기일 다음날로부터 3 년이 경과한 날로부터 회사에 대하여 본조에 따라 본건 우선주식의 전부 또는 일부의 상환을 청구할 수 있음 |
(*) 2021년 6월 30일 일부 상환전환우선주 보유 투자자와 합의로 제1차 전환상환우선주 전체 및 제2차 상환전환우선주 일부인 5,000,109,640원의 상환전환우선주가 전환우선주로 전환되었으며, 해당금액은 자본으로 인식하였습니다.
연결실체는 상기 전환상환우선주를 상각후원가로 측정하는 금융부채와 파생상품부채로 나누어 연결재무상태표상 금융부채로 분류하였으며, 발행 이후 상각 및 가치변동에 대하여 당기손익에 반영하고 있습니다.
(2) 당분기 및 전기 중 상환전환우선주 장부금액의 변동내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 기초금액 | 10,286,242,782 | 1,609,268,717 |
| 발행 | - | 7,927,361,327 |
| 전환 | (7,338,415,066) | - |
| 상각후원가 측정(이자비용) | 371,481,729 | 749,612,738 |
| 기말금액 | 3,319,309,445 | 10,286,242,782 |
(3) 당분기 및 전기 중 상환전환우선주와 관련된 파생상품부채의 변동내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 기초금액 | 932,275,121 | 1,680,009 |
| 발행 | - | 72,649,703 |
| 평가 | 196,675,517 | 857,945,409 |
| 전환 | (670,910,470) | - |
| 기말금액 | 458,040,168 | 932,275,121 |
18. 전환우선주
(1) 당분기말과 전기말 현재 종속기업인 ㈜알토스바이오로직스가 발행한 전환우선주의 세부내역은 다음과 같습니다.
| (당분기말) |
| 구 분 | 제1차 전환우선주(*1) | 제2차 전환우선주(*1) |
|---|---|---|
| 발행일 | 2020년 12월 11일 | 2021년 01월 21일 |
| 발행주식수(무상증자반영) | 968,750주 | 921,875주 |
| 1주당 발행가액(무상증자반영) | 32,000원 | 32,000원 |
| 총발행가액(최초발행시) | 31,000,000,000원 | 29,500,000,000원 |
| 전환대상 및 전환비율 | 보통주와 1:1로 전환가능 | 보통주와 1:1로 전환가능 |
| 전환가액 조정 | 전환가액을 하회하는 발행가액으로 유상증자를 하는 경우 등 | 전환가액을 하회하는 발행가액으로 유상증자를 하는 경우 등 |
| 전환권 행사기간 | 발행일 익일로부터 존속기간 내(존속기간은 발행일로부터 10년) | 발행일 익일로부터 존속기간 내(존속기간은 발행일로부터 10년) |
| 투자자의 주식매수청구권 | 투자금의 목적과 다른 사용, 계약사항 위배등의 사유 발생시 행사 가능 | 투자금의 목적과 다른 사용, 계약사항 위배등의 사유 발생시 행사 가능 |
(*1) 2021년 02월 17일자 무상증자로 인하여 1주당 발행가액과 발행주식수가 변동 하였습니다.
| (전기말) |
| 구 분 | 제1차 전환우선주 |
|---|---|
| 발행일 | 2020년 12월 11일 |
| 발행주식수(최초 발행시) | 193,750주 |
| 1주당 발행가액(최초 발행시) | 160,000원 |
| 총발행가액(최초발행시) | 31,000,000,000원 |
| 전환대상 및 전환비율 | 보통주와 1:1로 전환가능 |
| 전환가액 조정 | 전환가액을 하회하는 발행가액으로 유상증자를 하는 경우 등 |
| 전환권 행사기간 | 발행일 익일로부터 존속기간 내(존속기간은 발행일로부터 10년) |
| 투자자의 주식매수청구권 | 투자금의 목적과 다른 사용, 계약사항 위배등의 사유 발생시 행사 가능 |
상기 전환우선주는 투자자에게 부여된 주식매수청구권과 전환가액 조정 조항이 자본의 인식 요건을 충족하지 못하여 전기말 재무제표 상 자본에서 금융부채로 재분류하였습니다.
(2) 당분기말 현재 종속기업인㈜세레스에프엔디가 발행한 전환우선주의 세부내역은 다음과 같습니다.
| (당분기말) |
| 구 분 | 제1차 전환우선주(*) | 제2차 전환우선주(*) |
|---|---|---|
| 발행일 | 2019년 02월 01일 | 2020년 02월 18일 |
| 발행주식수(최초 발행시) | 334,450주 | 479,664주 |
| 1주당 발행가액(최초발행시) | 4,485원 | 10,424원 |
| 총발행가액(최초발행시) | 1,500,008,250원 | 5,000,019,640원 |
| 전환대상 및 전환비율 | 보통주와 1:1로 전환가능 | 보통주와 1:1로 전환가능 |
| 전환가액 조정 | 전환가액을 하회하는 발행가액으로 유상증자를 하는 경우 등 |
전환가액을 하회하는 발행가액으로 유상증자를 하는 경우 등 |
| 전환권 행사기간 | 발행일 익일로부터 존속기간 내(존속기간은 발행일로부터 10년) | 발행일 익일로부터 존속기간 내(존속기간은 발행일로부터 10년) |
| 투자자의 주식매수청구권 | 투자금의 목적과 다른 사용, 계약사항 위배등의 사유 발생시 지배기업이 고의 또는 중과실인 경우에만 지배기업에 행사가능 | 투자금의 목적과 다른 사용, 계약사항 위배등의 사유 발생시 지배기업이 고의 또는 중과실인 경우에만 지배기업에 행사가능 |
(*) 2021년 6월 30일 일부 상환전환우선주 보유 투자자와 합의로 제1차 전환상환우선주 전체 및 제2차 상환전환우선주 일부인 5,000,109,640원의 상환전환우선주가 전환우선주로 전환되었으며, 자본의 인식요건을 충족하여 자본으로 분류하였습니다(주석17 참조).
19. 고객과의 계약에서 발생하는 수익 및 관련 계약자산과 계약부채
(1) 고객과의 계약에서 생기는 수익의 구분
연결실체는 재화나 용역을 기간에 걸쳐 이전하거나 한 시점에 이전함으로써 수익을 창출합니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 수익인식 시점 | ||
|
한 시점에 인식 |
24,032,039,170 | 34,699,789,241 |
|
기간에 걸쳐 인식 |
364,580,063 | 2,624,540,820 |
| 합 계 | 24,396,619,233 | 37,324,330,061 |
(2) 당분기 및 전분기 중 계약부채 장부금액의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 선수수익 | |
|---|---|---|
| 유동 | 비유동 | |
| 기초 금액 | 4,081,977,958 | - |
| 증가 | - | - |
| 감소 | (364,580,063) | - |
| 유동성대체 | - | - |
| 기말 금액 | 3,717,397,895 | - |
| (전분기) | (단위: 원) |
| 구 분 | 선수수익 | |
|---|---|---|
| 유동 | 비유동 | |
| 기초 금액 | 3,420,997,871 | 2,422,721,052 |
| 증가 | 3,307,346,052 | - |
| 감소 | (2,624,540,820) | - |
| 유동성대체 | - | (2,422,721,052) |
| 기말 금액 | 4,103,803,103 | - |
(3) 계약부채와 관련하여 인식한 수익
당분기 및 전분기에 인식한 수익 중 전기에서 이월된 계약부채와 과거 보고기간에 이행한(또는 부분적으로 이행한) 수행의무와 관련된 금액은 다음과 같습니다.
|
(단위: 원) |
|
구 분 |
당분기 | 전분기 |
|---|---|---|
|
기초의 계약부채 잔액 중 당분기에 인식한 수익 |
||
| 라이선스계약 | 364,580,063 | 2,624,540,820 |
20. 퇴직급여제도
연결실체는 2012년 1월 1일부터 확정기여형(DC형) 퇴직급여제도로 전환하였으며, 보고기간종료일 현재 자격을 갖춘 모든 종업원들을 위해 확정기여형(DC형) 퇴직급여제도를 운영하고 있습니다.
사외적립자산은 수탁자인 KEB하나은행의 관리하에서 기금형태로 연결실체의 자산들로부터 독립적으로 운용되고 있으며, 종업원들이 확정기여형의 가득조건을 충족하기 전에 퇴사하는 경우 연결실체가 지불해야 할 기여금은 상실되는 기여금만큼 감소하게 됩니다.
당분기 및 전분기 중 연결포괄손익계산서에 인식된 총비용은 퇴직급여제도에서 규정하고있는 비율에 따라 연결실체가 퇴직급여제도에 납입한 기여금을 나타내고 있습니다.
당분기 중 확정기여제도와 관련해 비용으로 인식한 금액은 551,846,732원(전분기: 302,086,236원)입니다.
21. 자본금 및 기타불입자본
(1) 자본금
1) 당분기말 및 전기말 현재 자본금의 구성내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 수권주식수 | 발행주식수 | 1주의 금액 | 당분기말 | 전기말 |
|---|---|---|---|---|---|
| 보통주 | 80,000,000 | 42,264,250 | 500 | 21,132,125,000 | 14,041,450,000 |
| 우선주 | 20,000,000 | 1,029,015 | 500 | 514,507,500 | 101,692,500 |
| 합 계 | 100,000,000 | 43,293,265 | 21,646,632,500 | 14,143,142,500 |
2) 당분기 및 전분기 중 자본금의 변동내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 보통주 | 우선주 | 보통주 | 우선주 | |
| 기초 금액 | 14,041,450,000 | 101,692,500 | 6,948,375,000 | - |
| 유상증자 | - | 241,312,500 | - | - |
| 무상증자 | 7,020,725,000 | 171,502,500 | 6,997,975,000 | - |
| 주식선택권의 행사(*) | 69,950,000 | - | 95,100,000 | - |
| 기말 금액 | 21,132,125,000 | 514,507,500 | 14,041,450,000 | - |
(*) 주식선택권의 일부가 행사되었습니다(주석28 참조).
3) 우선주는 전환우선주로 구성되며, 상세내역은 다음과 같습니다.
| 구 분 | 제3차 전환우선주 | 제4차 전환우선주 |
|---|---|---|
| 발행일 | 2020년 11월 13일 | 2021년 01월 08일 |
| 발행주식수(무상증자반영) | 305,078주 | 723,937주 |
| 1주당 발행가액(무상증자반영) | 98,333원 | 103,600원 |
| 총발행가액(최초발행시) | 29,999,287,500원 | 74,999,925,000원 |
| 전환대상 및 전환비율 | 보통주와 1:1로 전환가능 | 보통주와 1:1로 전환가능 |
| 전환가액 조정 | 전환가액을 하회하는 발행가액으로 유상증자를 하는 경우 등 | 전환가액을 하회하는 발행가액으로 유상증자를 하는 경우 등 |
| 전환권 행사기간 | 발행일로부터 1년이 경과한 날부터 존속기간 내(존속기간은 발행일로부터 5년) | 발행일로부터 1년이 경과한 날부터 존속기간 내(존속기간은 발행일로부터 7년) |
(2) 기타불입자본
1) 당분기말 및 전기말 현재 기타불입자본의 구성내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | |
|---|---|---|---|
| 자본잉여금 | 주식발행초과금 | 167,498,519,268 | 98,664,021,149 |
| 연결자본잉여금 | 7,408,588,499 | 5,189,926,471 | |
| 자기주식처분이익 | 575,755,577 | 575,755,577 | |
| 기타자본항목 | 주식선택권 | 2,353,234,963 | 1,578,219,261 |
| 자기주식 | (793,980,301) | - | |
| 합 계 | 177,042,118,006 | 106,007,922,458 | |
2) 당분기 및 전분기 중 지배기업의 기타불입자본의 세부 변동 내역은 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 주식발행초과금 | 연결자본잉여금 | 자기주식 | 자기주식처분이익 | 주식선택권(*1) | 합 계 |
|---|---|---|---|---|---|---|
| 기초 금액 | 98,664,021,149 | 5,189,926,471 | - | 575,755,577 | 1,578,219,261 | 106,007,922,458 |
| 유상증자 | 74,599,720,350 | - | - | - | - | 74,599,720,350 |
| 무상증자 | (7,228,689,370) | - | - | - | - | (7,228,689,370) |
| 자기주식취득 | - | - | (793,980,301) | - | - | (793,980,301) |
| 주식선택권의 행사 | 1,463,467,139 | - | - | - | (256,043,299) | 1,207,423,840 |
| 주식기준보상거래의 인식 | - | - | - | - | 1,031,059,001 | 1,031,059,001 |
| 연결실체의 변동 | - | 2,218,662,028 | - | - | - | 2,218,662,028 |
| 기말 금액 | 167,498,519,268 | 7,408,588,499 | (793,980,301) | 575,755,577 | 2,353,234,963 | 177,042,118,006 |
| (전분기) | (단위: 원) |
| 구 분 | 주식발행초과금 | 연결자본잉여금 | 자기주식 처분이익 | 주식선택권(*1) | 합 계 |
|---|---|---|---|---|---|
| 기초 금액 | 73,295,554,796 | 1,529,502,834 | 575,755,577 | 871,542,268 | 76,272,355,475 |
| 무상증자 | (7,033,299,280) | - | - | - | (7,033,299,280) |
| 주식선택권의 행사 | 2,660,024,190 | - | - | (362,547,670) | 2,297,476,520 |
| 주식기준보상거래의 인식 | - | - | - | 803,706,669 | 803,706,669 |
| 기말 금액 | 68,922,279,706 | 1,529,502,834 | 575,755,577 | 1,312,701,267 | 72,340,239,384 |
(*1) 주식결제형 종업원급여적립금은 종업원주식옵션제도에 의해 종업원에게 부여된 주식옵션과 관련된 것입니다. 종업원에 대한 주식기준보상에 대한 상세정보는 주석 28에서 설명하고 있습니다.
22. 이익잉여금(결손금)
당분기 및 전분기 중 결손금의 변동내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 기초 금액 | (14,213,912,090) | (13,238,281,251) |
| 분기순이익(손실) | (14,201,426,845) | 9,189,090,133 |
| 기말 금액 | (28,415,338,935) | (4,049,191,118) |
23. 판매비와관리비
당분기 및 전분기의 판매비와관리비 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 급여 | 3,220,327,632 | 2,378,363,051 |
| 퇴직급여 | 268,548,130 | 121,733,724 |
| 주식기준보상 | 1,203,331,666 | 409,172,762 |
| 복리후생비 | 421,145,886 | 217,810,246 |
| 여비교통비 | 35,727,069 | 39,881,634 |
| 접대비 | 48,186,468 | 53,758,615 |
| 통신비 | 18,962,936 | 28,412,143 |
| 수도광열비 | 5,314,160 | 1,886,066 |
| 전력비 | 15,561,921 | 14,652,487 |
| 세금과공과금 | 153,202,860 | 107,916,976 |
| 감가상각비 | 272,085,816 | 215,680,863 |
| 지급임차료 | 52,014,809 | 34,237,396 |
| 수선비 | 17,171,270 | 27,986,583 |
| 보험료 | 207,981,134 | 112,549,229 |
| 차량유지비 | 38,533,179 | 33,466,871 |
| 경상연구개발비 | 12,129,288,726 | 5,339,916,599 |
| 운반비 | 19,920,654 | 10,330,980 |
| 교육훈련비 | 7,414,294 | 8,679,970 |
| 도서인쇄비 | 6,614,406 | 9,786,324 |
| 회의비 | 5,400,558 | 5,575,922 |
| 사무용품비 | 17,965,054 | 33,983,567 |
| 소모품비 | 63,136,651 | 92,245,835 |
| 지급수수료 | 998,505,646 | 1,085,511,863 |
| 광고선전비 | 12,280,107 | 10,989,455 |
| 판매촉진비 | 1,000,000 | 1,000,000 |
| 건물관리비 | 26,442,485 | 25,160,548 |
| 무형자산상각비 | 69,143,937 | 44,100,729 |
| 잡비 | 390,000 | 880,000 |
| 시험생산비 | 1,917,367,327 | 2,516,389,012 |
| 외주용역비 | 378,345,753 | 174,122,800 |
| 협회비 | 16,751,000 | 12,870,000 |
| 자문비 | 21,000,000 | 37,500,000 |
| 대손상각비 | (4,058,050) | (4,964,283) |
| 견본비 | 2,326,173 | - |
| 합 계 | 21,667,329,657 | 13,201,587,967 |
24. 영업외수익
당분기 및 전분기의 영업외수익은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 | |
|---|---|---|---|
| 금융수익 | 이자수익 | 1,590,184,847 | 643,065,547 |
| 소 계 | 1,590,184,847 | 643,065,547 | |
| 기타영업외수익 | 외환차익 | 260,285,140 | 382,190,699 |
| 외화환산이익 | 2,597,252,839 | 129,046,171 | |
| 부채상환이익 | 5,134,689,002 | - | |
| 당기손익-공정가치 측정 금융자산평가이익 | - | 41,643,835 | |
| 보조금 | - | 155,238,190 | |
| 채무면제이익 | - | 41,909,684 | |
| 기타 | 374,487,755 | 87,977,403 | |
| 소 계 | 8,366,714,736 | 838,005,982 | |
| 합 계 | 9,956,899,583 | 1,481,071,529 | |
25. 영업외비용
당분기 및 전분기의 영업외비용은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 | |
|---|---|---|---|
| 금융비용 | 이자비용 | 523,983,435 | 371,262,547 |
| 소 계 | 523,983,435 | 371,262,547 | |
| 기타영업외비용 | 외환차손 | 66,069,888 | 307,716,568 |
| 외화환산손실 | 11,690,232 | 417,959,301 | |
| 파생상품평가손실 | 196,675,517 | 165,001,962 | |
| 유형자산처분손실 | 18,480,857 | - | |
| 유형자산손상차손 | 65,800,000 | - | |
| 무형자산손상차손 | - | 9,502,009 | |
| 기부금 | 11,500,000 | - | |
| 기타 | 103,280 | 1,336,311 | |
| 소 계 | 370,319,774 | 901,516,151 | |
| 합 계 | 894,303,209 | 1,272,778,698 | |
26. 법인세비용
법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균 연간법인세율의 추정에 기초하여 인식하였습니다. 추정연간유효법인세율과 법정세율의 차이는 주로 이연법인세의 실현가능성 평가 등에 기인합니다.
27. 주당손익
(1) 당분기 및 전분기의 기본주당이익의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 기본주당이익 계산에 사용된 손익 | (14,201,426,845) | 9,189,090,133 |
| 기본주당이익을 위한 가중평균유통보통주식수 | 42,149,047 | 41,890,785 |
| 기본주당손익 | (337) | 219 |
(2) 당분기 및 전분기의 희석주당이익 계산 내역은 다음과 같습니다.
| (단위: 원, 주) |
| 구 분 | 당분기(*) | 전분기(*) |
|---|---|---|
| 1)희석주당이익에 계산에 사용된 이익 | (13,170,367,844) | 9,991,090,632 |
| 기본주당이익 계산에 사용된 이익 | (14,201,426,845) | 9,189,090,133 |
| 상환전환우선주 이자비용 | - | - |
| 주식보상비용 | 1,031,059,001 | 802,000,499 |
| 2)희석주당이익 산출에 사용된 가중평균유통보통주식수 | 44,670,991주 | 42,080,592주 |
| 기본주당이익 산출에 사용된 가중평균유통보통주식수 | 42,149,047주 | 41,890,785주 |
| 주식선택권 | 993,892주 | 189,807주 |
| 전환우선주 | 1,528,052주 | - |
| 3)희석주당이익 | (337) | 219 |
(*) 지배기업은 유통되는 보통주식수나 잠재적보통주식수가 당분기 중 무상증자로 증가하여 비교표시하는 전분기 기본주당이익과 희석주당이익을 수정하였습니다.
한편, 당분기말 현재 보유중인 잠재적보통주인 주식선택권의 행사와 전환우선주의 전환으로 인한 희석화 효과가 없으므로 당분기의 희석주당순손실은 기본주당순손실과 동일합니다.
28. 주식기준보상
연결실체는 경영진과 종업원에 대하여 주식기준보상제도를 시행하고 있습니다.
종업원주식선택권은 행사시점에 ㈜알테오젠 및 ㈜세레스에프엔디 및 ㈜알토스바이오로직스의 주식으로 전환됩니다. 종업원이 주식선택권을 부여 받을 때 지급하였거나 지급할 금액은 없습니다.주식선택권은 배당에 대한 권리나 의결권을 가지지 않습니다. 주식선택권은 가득일로부터 만기일까지의 기간 동안에 행사될 수 있습니다.
(1) 당분기말에 존재한 주식기준보상계약
| (단위: 주, 원) |
| 구 분 | 부여일 | 권리행사시작일 | 권리행사종료일 | 총 부여수량 | 소멸수량 | 잔존부여수량 | 미행사수량 | 행사가격(*) | |
|---|---|---|---|---|---|---|---|---|---|
| (주)알테오젠 | 제14차 | 2017-09-01 | 2020-09-01 | 2023-08-31 | 120,000 | - | 120,000 | 35,000 | 5,167 원 |
| 제15차 | 2018-03-09 | 2021-03-09 | 2024-03-08 | 138,000 | 27,000 | 111,000 | 58,100 | 6,900 원 | |
| 제16차 | 2018-04-23 | 2021-04-23 | 2024-04-22 | 36,000 | 9,000 | 27,000 | - | 12,167 원 | |
| 제17차 | 2018-08-02 | 2021-08-02 | 2024-08-01 | 210,000 | - | 210,000 | 160,000 | 10,667 원 | |
| 제18차 | 2019-03-08 | 2022-03-08 | 2025-03-07 | 141,600 | 4,500 | 137,100 | 137,100 | 12,000 원 | |
| 제19차 | 2019-04-30 | 2022-04-30 | 2025-04-29 | 39,000 | 18,000 | 21,000 | 21,000 | 14,334 원 | |
| 제20차 | 2019-08-05 | 2022-08-05 | 2025-08-04 | 195,000 | - | 195,000 | 195,000 | 10,700 원 | |
| 제21차 | 2020-03-26 | 2023-03-26 | 2026-03-25 | 105,000 | - | 105,000 | 105,000 | 25,333 원 | |
| 제22차 | 2020-04-14 | 2023-04-14 | 2026-04-13 | 181,500 | 150,000 | 31,500 | 31,500 | 28,600 원 | |
| 제23차 | 2020-06-11 | 2023-06-11 | 2026-06-10 | 90,000 | - | 90,000 | 90,000 | 76,667 원 | |
| 제24차 | 2021-05-03 | 2024-05-03 | 2027-05-02 | 14,500 | - | 14,500 | 14,500 | 87,450 원 | |
| 소 계 | 1,270,600 | 208,500 | 1,062,100 | 847,200 | |||||
| (주)세레스에프엔디 | 제1차 | 2019-05-14 | 2022-05-14 | 2029-05-13 | 51,000 | 26,000 | 25,000 | 25,000 | 4,880 원 |
| 제2차 | 2020-01-13 | 2023-01-13 | 2030-01-12 | 77,000 | 33,500 | 43,500 | 43,500 | 5,000 원 | |
| 제3차 | 2021-03-24 | 2024-03-24 | 2031-03-23 | 10,000 | - | 10,000 | 10,000 | 14,728 원 | |
| 제4차 | 2021-09-01 | 2024-09-01 | 2031-08-31 | 66,500 | - | 66,500 | 66,500 | 15,000 원 | |
| 소 계 | 204,500 | 59,500 | 145,000 | 145,000 | |||||
| (주) 알토스바이오로직스 | 제1차 | 2021-03-24 | 2024-03-24 | 2029-03-23 | 115,000 | - | 115,000 | 115,000 | 30,000 원 |
| 제2차 | 2021-06-21 | 2024-06-01 | 2029-06-20 | 21,500 | - | 21,500 | 21,500 | 30,000 원 | |
| 제3차 | 2021-08-05 | 2024-08-05 | 2029-08-04 | 30,000 | - | 30,000 | 30,000 | 30,000 원 | |
| 소 계 | 166,500 | - | 166,500 | 166,500 | |||||
| 합 계 | 1,641,600 | 268,000 | 1,373,600 | 1,158,700 | |||||
(*) (주)알테오젠의 주식선택권은 2017년 11월 23일, 2020년 7월 7일, 2021년 3월 10일 무상증자로 인하여 수량 및 행사가격이 조정되었습니다.
(2) 회계기간에 부여한 주식선택권의 공정가치
주식선택권의 가격은 이항옵션가격결정모형에 따라 산정되었습니다. 옵션평가를 위해 사용하는 변동성은 부여 당시 유사상장기업의 업종지수(코스닥/제약)를 기준으로변동성을 산출하였습니다.
1) (주)알테오젠
| 구 분 | 모형 적용 변수 | |
|---|---|---|
| 부여된 선택권의 가중평균 공정가치 | 4,389.97~72,818.2 | |
| 부여일 주식가격 | 제14차~24차 | 19,800원~230,400원 |
| 기대변동성 | 9.9~60.8 | |
| 옵션만기 | 3 년 | |
| 배당수익률 | - | |
| 무위험이자율 | 1.31% ~ 2.65% | |
(*) 무상증자 전 부여일 기준 자료입니다
2) (주)세레스에프엔디
| 구 분 | 모형 적용 변수 | |
|---|---|---|
| 부여된 선택권의 가중평균 공정가치 | 12.34~2,395.61 | |
| 부여일 주식가격 | 제1차~4차 | - |
| 기대변동성 | 23.33~65.6 | |
| 옵션만기 | 10 년 | |
| 배당수익률 | - | |
| 무위험이자율 | 1.70%~2.02% | |
3) (주)알토스바이오로직스
| 구 분 | 모형 적용 변수 | |
|---|---|---|
| 부여된 선택권의 가중평균 공정가치 | 24,043.44원~24,535.6원 | |
| 부여일 주식가격 | 제1차~3차 | - |
| 기대변동성 | 76.77~79.57 | |
| 옵션만기 | 8 년 | |
| 배당수익률 | - | |
| 무위험이자율 | 1.84%~1.93% | |
(3) 보고기간 중 주식선택권의 변동
당분기 및 전분기 중 주식선택권의 변동내용은 다음과 같습니다.
1) (주)알테오젠
| (단위: 주, 원) |
| 구 분 | 당분기(*) | 전분기 | ||
|---|---|---|---|---|
| 주식선택권 수량 | 가중평균행사가격 | 주식선택권 수량 | 가중평균행사가격 | |
| 기초 | 648,400 | 27,854 | 786,800 | 12,702 |
| 무상증자로 인한 변동 | 324,200 | 18,569 | - | - |
| 기중 부여수량 | 14,500 | 87,450 | 251,000 | 58,769 |
| 기중 권리상실분 | - | - | (100,000) | 42,900 |
| 기중 행사분 | (139,900) | 9,059 | (289,400) | (8,273) |
| 기말 | 847,200 | 21,306 | 648,400 | 27,854 |
(*) 2017년 11월 23일, 2020년 7월 7일, 2021년 3월 10일 무상증자로 인하여 수량 및 행사가격이 조정되었습니다.
2) (주)세레스에프엔디
| (단위: 주, 원) |
| 구 분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 주식선택권 수량 | 가중평균행사가격 | 주식선택권 수량 | 가중평균행사가격 | |
| 기초 | 70,000 | 4,955 | 42,000 | 4,880 |
| 기중 부여수량 | 76,500 | 14,964 | 77,000 | 5,000 |
| 기중 권리상실분 | (1,500) | 4,920 | (49,000) | 4,961 |
| 기말 | 145,000 | 10,236 | 70,000 | 4,955 |
3) (주)알토스바이오로직스
| (단위: 주, 원) |
| 구 분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 주식선택권 수량 | 가중평균행사가격 | 주식선택권 수량 | 가중평균행사가격 | |
| 기초 | - | - | - | - |
| 기중 부여수량 | 166,500 | 30,000 | - | - |
| 기말 | 166,500 | 30,000 | - | - |
(4) 당분기 중 행사된 주식선택권은 다음과 같습니다.
| (단위: 주, 원) |
| 구 분 | 부 여 일 | 행사수량 | 주당 행사가격 | 행사일 |
|---|---|---|---|---|
| 제14차 | 2017-09-01 | 10,000 | 5,167 원 | 2021-06-02 |
| 제15차 | 2018-03-09 | 23,000 | 6,900 원 | 2021-06-02 |
| 29,900 | 6,900 원 | 2021-09-01 | ||
| 제16차 | 2018-04-23 | 22,000 | 12,167 원 | 2021-06-02 |
| 5,000 | 12,167 원 | 2021-09-01 | ||
| 제17차 | 2018-08-03 | 50,000 | 10,667 원 | 2021-09-01 |
| 합 계 | 139,900 | |||
(5) 당분기 및 전분기 중 발생한 주식선택권 관련 보상원가 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 총 보상원가 | 12,418,447,355 | 7,773,338,594 |
| 당기보상원가 | 1,603,054,139 | 803,706,669 |
| 잔여보상원가 | 5,585,826,574 | 2,811,734,330 |
(6) 보고기간말 현재 존속하는 주식선택권
1) (주)알테오젠
당분기말 현재 존속하는 주식옵션의 가중평균행사가격이 21,306원(전기말: 27,854원)이며, 가중평균 잔여계약 만기는 3.63년(전기말: 4.20년)입니다.
2) (주)세레스에프엔디
당분기말 현재 존속하는 주식옵션의 가중평균행사가격이 10,236원(전기말: 4,955원)이며, 가중평균 잔여계약 만기는 9.01년(전기말: 8.79년)입니다.
3) (주)알토스바이오로직스
당분기말 현재 존속하는 주식옵션의 가중평균행사가격이 30,000원이며, 가중평균 잔여계약 만기는 7.58년입니다.
29. 비용의 성격별 분류
당분기 및 전분기 중 발생한 비용의 성격별로 분류한 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 상품원가 | 15,839,832,831 | 9,921,810,605 |
| 종업원급여 | 6,787,825,354 | 4,762,745,296 |
| 주식기준보상 | 1,603,054,139 | 807,377,412 |
| 퇴직급여 | 551,846,732 | 302,086,236 |
| 연구관련 시약 및 소모품 구입 | 3,375,238,811 | 3,100,420,009 |
| 위탁연구용역비 | 13,439,408,489 | 3,456,316,058 |
| 지급수수료 | 1,210,177,225 | 1,412,926,996 |
| 세금과공과 | 286,288,240 | 196,333,493 |
| 임차료 | 52,194,809 | 35,047,396 |
| 감가상각비 | 1,517,977,505 | 1,306,708,003 |
| 무형자산상각비 | 69,143,937 | 44,100,729 |
| 시험생산비 | 8,417,533 | 2,535,560,420 |
| 기타비용 | 2,044,298,608 | 1,354,349,081 |
| 합 계 | 46,785,704,213 | 29,235,781,734 |
30. 특수관계자와의 거래
(1) 당분기말 현재 연결실체의 특수관계자 현황은 다음과 같습니다.
| 구 분 | 특수관계자의 명칭 | 비 고 |
|---|---|---|
| 대표이사 | 박순재 | 최대주주 본인 |
| 미등기임원 | 정혜신 | CSO, 최대주주 등 |
| 기타 특수관계자 | 이재상 | 지배회사의 미등기 임원, 종속기업 (주)LS메디텍의 대표이사 |
| 기타 특수관계자 | 손재민 | 종속기업 ㈜세레스에프엔디의 대표이사 |
| 미등기임원 | 강상우 | CFO, 종속기업 (주)LS메디텍 및 (주)알토스바이오로직스 등기임원 |
(2) 당분기 및 전분기 중 특수관계자와의 거래는 없습니다.
(3) 당분기말 및 전기말 현재 특수관계자에 대한 채권ㆍ채무 잔액은 없습니다.
(4) 당분기 및 전분기 중 특수관계자에 대한 대여 및 차입 거래내역은 없습니다.
(5) 지급보증 및 담보제공
당분기말 및 전기말 현재 연결실체가 특수관계자로부터 제공받고 있는 담보 및 지급보증 내역은 다음과 같습니다(주석30 참조).
| (단위: 원) |
| 보증처 | 당분기말 | 전기말 | 보증내용 |
|---|---|---|---|
| 기타 특수관계자(이재상) |
900,000,000 | 900,000,000 | 종속기업 (주)엘에스메디텍의 외상매입거래에 대한 담보 제공 |
| 기타 특수관계자(이재상) |
660,000,000 | 660,000,000 | 종속기업 (주)엘에스메디텍의 신한은행이 제공하는 보증에 대한 담보제공 |
| 기타 특수관계자(이재상) |
360,000,000 | 360,000,000 | 종속기업 (주)엘에스메디텍의 신한은행 대출(한도)에 대한 보증제공 |
| 합 계 | 1,920,000,000 | 1,920,000,000 |
(6) 당분기 및 전분기 중 주요 경영진에 대한 보상내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 단기종업원급여 | 2,170,105,300 | 1,491,711,071 |
| 퇴직급여 | 198,715,390 | 115,332,159 |
| 주식기준보상 | 1,270,525,443 | 536,402,172 |
| 합 계 | 3,639,346,133 | 2,143,445,402 |
31. 우발채무 및 주요 약정사항
(1) 당분기말 현재 연결실체가 금융기관 등으로부터 제공받은 지급보증의 내역은 다음과 같습니다.
| (단위: 원) |
|
제공한 기업 |
보증금액 | 보증내용 |
|---|---|---|
| 서울보증보험 | 51,300,000 | 정부 및 지방자치단체 보조금 반환보증 |
| 73,200,000 | 종속회사 (주)세레스에프엔디의 도시가스 사용료 납부보증 | |
| 신한은행 | 550,000,000 | 종속회사 (주)LS메디텍의 외상매입거래에 대한 보증 제공 |
| 기타 특수관계자(이재상) | 900,000,000 | 종속회사 (주)LS메디텍의 외상매입거래에 대한 담보 제공 |
| 660,000,000 | 종속회사 (주)LS메디텍의 신한은행이 제공하는 보증에 대한 담보제공 | |
| 360,000,000 | 종속회사 (주)LS메디텍의 신한은행 대출(한도)에 대한 보증제공 | |
| 합 계 | 2,594,500,000 |
(2) 당분기말 현재 연결실체가 금융기관과 체결한 주요 약정사항은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 금융기관 | 약정한도액 | 대출잔액 | 비 고 |
|---|---|---|---|---|
| 시설자금대출 | KEB하나은행 | 1,500,000,000 | 1,500,000,000 | 부동산 담보제공 |
| 시설자금대출 | KEB하나은행 | 1,300,000,000 | 800,000,000 | 부동산 담보제공 |
| 시설자금대출 | KEB하나은행 | 1,000,000,000 | 750,000,000 | 부동산 담보제공 |
| 시설자금대출 | KEB하나은행 | 500,000,000 | 500,000,000 | 정기예금 담보제공 |
| 일반자금대출 | 신한은행 | 300,000,000 | - | 대표이사 연대보증 제공 |
(3) 지배기업은 종속기업인 (주)세레스에프앤디 및 (주)알토스바이오로직스의 상환전환우선주 및 전환우선주 투자자와의 약정에 의해서 투자자와의 동의없이는 해당 종속기업에 대한 보유 주식을 처분할 수 없습니다. 또한 지배기업이 해당 종속기업에 대한 보유 주식을 처분하는 경우 투자자는 공동매도권을 행사할 권리를 가지며, 투자자가 공동매도권을 행사하는 경우 지분 양수 예정자가 지배기업 및 투자자로부터 회사와 투자자의 지분(주식 및 주식연계사채) 비율에 따라 지분을 양수하지 않는 한, 지배기업은 해당 종속기업에 대한 보유 주식을 처분할 수 없습니다.
32. 위험관리
(1) 자본위험관리
연결실체는 부채와 자본 잔액의 최적화를 통하여 주주이익을 극대화시키는 동시에 계속기업으로서 지속될 수 있도록 자본을 관리하고 있습니다. 연결실체는 자본관리지표로 부채비율을 이용하고 있으며, 이는 총부채를 총자본으로 나누어 산출하고 있습니다.
당분기말 및 전기말 현재 부채비율은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 부채(A) | 78,808,236,689 | 22,935,590,498 |
| 자본(B) | 174,008,846,560 | 136,271,337,627 |
| 부채비율(A/B) | 45.29% | 16.83% |
(2) 금융자산, 금융부채 및 자본의 각 범주별로 채택한 주요 회계정책 및 방법(인식기준과 측정기준 그리고 수익과 비용)은 주석 2에 상세히 공시되어 있으며, 금융자산과금융부채의 범주별 장부금액은 주석 5에서 작성하였습니다.
(3) 당분기말 및 전기말 현재 공정가치로 후속측정하는 금융자산 및 금융부채는 다음과 같습니다.
| (단위: 원) |
| 구 분 |
당분기말 |
전기말 | ||
|---|---|---|---|---|
| 장부금액 | 공정가치 | 장부금액 | 공정가치 | |
| 당기손익-공정가치금융부채 | 63,819,309,445 | 63,819,309,445 | 10,286,242,782 | 10,286,242,782 |
당분기말 전기말 현재 공정가치 측정방법 별 분류는 다음과 같습니다.
| (당분기말) | (단위: 원) |
| 구 분 | 수 준 1 | 수 준 2 | 수 준 3 | 합 계 |
|---|---|---|---|---|
| 당기손익-공정가치금융부채 |
- | - | 63,819,309,445 | 63,819,309,445 |
| (전기말) | (단위: 원) |
| 구 분 | 수 준 1 | 수 준 2 | 수 준 3 | 합 계 |
|---|---|---|---|---|
| 당기손익-공정가치금융부채 |
- | - | 10,286,242,782 | 10,286,242,782 |
(4) 금융위험관리
연결실체는 금융상품과 관련하여 시장위험(이자율변동위험, 환율변동위험), 신용위험, 유동성위험, 가격위험과 같은 다양한 금융위험에 노출되어 있습니다. 연결실체의위험관리는 연결실체의 재무적 성과에 영향을 미치는 잠재적 위험을 식별하여 연결실체가 허용가능한 수준으로 감소, 제거 및 회피하는 것을 그 목적으로 하고 있습니다.
1) 이자율변동위험
연결실체의 이자율변동위험은 주로 변동이자부 차입금에 연관되어 있으며, 이와 관련된 이자비용은 이자율위험에 노출되어 있습니다. 당분기말과 전기말 현재 이자율 위험에 노출된 차입금 내용은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 유동성장기차입금 | 250,000,000 | 250,000,000 |
| 장기차입금 | 500,000,000 | 687,500,000 |
| 단기차입금 | 2,800,000,000 | 2,800,000,000 |
| 합 계 | 3,550,000,000 | 3,737,500,000 |
당분기말 및 전분기말 현재 관련 이자율 1% 변동시 세전이익에 미치는 영향은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | ||
|---|---|---|---|---|
| 1% 상승시 | 1% 하락시 | 1% 상승시 | 1% 하락시 | |
| 세전손익 | (35,500,000) | 35,500,000 | (37,375,000) | 37,375,000 |
2) 환율변동위험
연결실체는 용역매출 등과 관련하여 주로 USD의 환율변동위험에 노출되어 있으며, 내부적으로 환율변동에 따른 환율변동위험을 정기적으로 측정하고 있습니다.
당분기말 및 전기말 현재 연결실체의 외화금융자산 및 외화금융부채의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|
| 외화금액 | 원화장부금액 | 외화금액 | 원화장부금액 | |||
| 현금및현금성자산 | USD | 3,558,550.56 | 4,216,526,558 | USD | 2,065,057.06 | 2,246,782,081 |
| JPY | - | - | JPY | 190,950.00 | 2,013,109 | |
| 단기금융상품 | USD | 24,000,000.00 | 28,437,600,000 | USD | 23,000,000.00 | 25,024,000,000 |
| 매출채권및기타채권 | USD | - | - | USD | 526,152.88 | 572,454,333 |
| 외화금융자산 합계 | 32,654,126,558 | 27,845,249,523 |
||||
| 미지급비용 | USD | - | - | USD | 95,358.00 | 103,749,504 |
| 미지급금 | USD | 57,068.56 | 67,620,537 | USD | - | - |
| EUR | 222,800.00 | 306,196,268 | EUR | - | - | |
| CHF | 6,489.00 | 8,226,884 | CHF | - | - | |
| 외화금융부채 합계 | 382,043,689 | 103,749,504 |
||||
당분기말 및 전기말 현재 관련 통화에 대한 환율이 10% 변동 시 세전이익에 미치는 영향은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | ||
|---|---|---|---|---|
| 10% 상승시 | 10% 하락시 | 10% 상승시 | 10% 하락시 | |
| 세전손익 | 6,454,416,574 | (6,454,416,574) | 2,774,150,002 | (2,774,150,002) |
3) 신용위험
신용위험은 계약상대방이 계약서상의 의무를 불이행하여 회사에 재무적 손실을 미칠위험을 의미합니다. 신용위험은 보유하고 있는 수취채권 및 확정계약을 포함한 거래처에 대한 신용위험 뿐 아니라 현금및현금성자산, 은행 및 금융기관 예치금으로부터 발생하고 있습니다. 은행 및 금융기관의 경우 신용등급이 우수한 금융기관과 거래하고 있으므로 금융기관으로부터의 신용위험은 제한적입니다.
일반거래처의 경우 고객의 재무상태, 과거 경험 등 기타 요소들을 고려하여 신용을 평가하게 됩니다. 연결실체는 거래 상대방에 대한 개별적인 위험 한도 관리정책은 보유하고 있지 않습니다.
연결실체는 기대신용손실 모형이 적용되는 다음의 금융자산을 보유하고 있습니다.
· 재화 및 용역의 제공에 따른 매출채권
· 상각후원가로 측정하는 기타금융자산
연결실체는 금융자산에 대해 전체 기간 기대신용손실을 손실충당금으로 인식하는 간편법을 적용합니다. 기대신용손실을 측정하기 위해 매출채권은 신용위험 특성과 연체일을 기준으로 구분하였습니다.
4) 유동성위험
유동성위험관리에 대한 궁극적인 책임은 연결실체의 단기 및 중장기 자금조달과 유동성관리규정을 적절하게 관리하기 위한 기본정책을 수립하는 이사회에 있습니다. 연결실체는 충분한 적립금과 차입한도를 유지하고 예측현금흐름과 실제현금흐름을 계속하여 관찰하고 금융자산과 금융부채의 만기구조를 대응시키면서 유동성위험을 관리하고 있습니다.
다음 표는 연결실체의 비파생금융부채에 대한 계약상 잔존만기를 상세하게 나타내고있습니다. 해당 표는 금융부채의 할인되지 않은 현금흐름을 기초로 연결실체가 지급하여야 하는 가장 빠른 만기일에 근거하여 작성되었으며, 원금 및 이자의 현금흐름을모두 포함하고 있습니다. 이자의 현금흐름이 변동이자율에 근거하는 경우, 할인되지 않은 현금흐름은 보고기간 종료일 현재의 수익률곡선에 근거하여 도출되었습니다.
| (당분기말) | (단위: 원) |
| 구 분 | 가중평균 유효이자율 |
1년 미만 | 1년 ~ 5년 | 5년 초과 | 합 계 |
|---|---|---|---|---|---|
| 매입채무 | - | 2,330,857,676 | - | - | 2,330,857,676 |
| 차입금 | 1.781~2.951% | 3,050,000,000 | 500,000,000 | - | 3,550,000,000 |
| 기타금융부채 | - | 1,063,399,358 | 1,006,135,217 | - | 2,069,534,575 |
| 리스부채 | 2.22%~4.02% | 141,783,824 | 149,037,539 | - | 290,821,363 |
| 합 계 | 6,586,040,858 | 1,655,172,756 | - | 8,241,213,614 |
| (전기말) | (단위: 원) |
| 구 분 | 가중평균 유효이자율 |
1년 미만 | 1년 ~ 5년 | 5년 초과 | 합 계 |
|---|---|---|---|---|---|
| 매입채무 | - | 440,241,691 | - | - | 440,241,691 |
| 차입금 | 5.59% | 3,050,000,000 | 687,500,000 | - | 3,737,500,000 |
| 기타금융부채 | - | 2,216,725,480 | 810,719,563 | - | 3,027,445,043 |
| 리스부채 | 2.23%~4.02% | 107,002,875 | 84,654,462 | - | 191,657,337 |
| 합 계 | 5,813,970,046 | 1,582,874,025 | - | 7,396,844,071 |
5) 가격위험
연결실체는 상장주식을 보유하고 있지 않아 가격위험에 노출되어 있지 않습니다.
33. 현금흐름 관련사항
(1) 당분기 및 전분기 중 영업활동으로부터 창출된 현금흐름의 조정내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 1. 현금유출이 없는 비용 가산 | 3,596,954,301 | 3,547,708,803 | ||
| 감가상각비 | 1,517,977,505 | 1,306,708,002 | ||
| 무형자산상각비 | 69,143,937 | 44,100,729 | ||
| 주식기준보상 | 1,031,059,001 | 803,706,669 | ||
| 외화환산손실 | 11,690,232 | 417,959,301 | ||
| 유형자산처분손실 | 18,480,857 | - | ||
| 유형자산손상 | 65,800,000 | - | ||
| 무형자산손상차손 | - | 9,502,009 | ||
| 법인세비용 | 150,919,056 | 428,311,598 | ||
| 퇴직급여 | - | (9,231,248) | ||
| 대손상각비 | (4,058,050) | - | ||
| 현재가치할인차금 | 15,282,811 | 10,387,234 | ||
| 이자비용 | 523,983,435 | 371,262,547 | ||
| 파생상품평가손실 | 196,675,517 | 165,001,962 | ||
| 2. 현금유입이 없는 수익 차감 | (9,322,126,688) | (855,665,237) | ||
| 이자수익 | (1,590,184,847) | (643,065,547) | ||
| 외화환산이익 | (2,597,252,839) | (129,046,171) | ||
| 채무면제이익 | - | (41,909,684) | ||
| 당기손익-공정가치금융자산평가이익 | - | (41,643,835) | ||
| 부채상환이익 | (5,134,689,002) | - | ||
| 3. 영업활동으로 인한 자산ㆍ부채의 변동 | 1,152,746,469 | (2,746,094,684) | ||
| 매출채권의 감소(증가) | (1,295,823,323) | 108,030,124 | ||
| 기타채권의 감소(증가) | 28,371,674 | 224,335,874 | ||
| 재고자산의 증가 | (487,450,828) | 324,409,630 | ||
| 기타자산의 증가 | 492,340,008 | (76,546,248) | ||
| 파생상품부채의 증가(감소) | - | 299,129,989 | ||
| 매입채무의 증가(감소) | 1,890,615,985 | (691,436,739) | ||
| 계약부채의 증가 | (364,580,063) | (1,739,915,820) | ||
| 기타금융부채의 증가 | (1,487,814,828) | (1,395,087,737) | ||
| 기타부채의 증가(감소) | 2,377,087,844 | 201,421,240 | ||
| 퇴직급여의 지급 | - | (434,997) | ||
(2) 당분기 및 전분기 중 현금의 유입과 유출이 없는 거래 중 중요한 거래의 내용은 다음과 같습니다.
| (단위: 원) |
| 거 래 내 용 | 당분기 | 전분기 |
|---|---|---|
| 연구용기자재 국고보조금 상계 | 7,679,121 | 1,743,703 |
| 건설중인자산에서 유형자산 대체 | 1,773,686,908 | 3,433,015,200 |
| 건설중인자산의 무형자산 대체 | 21,057,398 | 112,959,948 |
| 주식매입선택권 행사 | 256,043,299 | 362,547,670 |
| 리스부채의 유동성대체 | 150,371,355 | 130,913,689 |
| 무상증자 | 7,192,227,500 | 6,997,975,000 |
| 리스부채 및 사용권자산의 인식 | 253,225,676 | 219,311,642 |
| 비유동계약부채의 유동성 대체 | - | 2,422,721,052 |
| 유형자산 취득 관련 미지급금 감소 | (7,416,200) | - |
34. 주요기술이전 계약 및 수익 인식 내역
(1) 연결실체는 다국적 기업 A사와 2019년 12월 2일, 다국적 기업 B사와 2020년 6월 24일자로 회사가 보유한 인간 히알루로니다제 원천 기술(ALT-B4)에 대한 기술이전 계약을 각각 체결하였습니다. 동 기술이전 계약은 비독점적 라이센스계약으로 인간히알루로니다제 원천기술로 바이오의약품의 정맥주사를 피하주사로 바꾸어 주는 원천 기술입니다.
2019년 12월 2일 A사와의 계약에 따라 반환조건 없는 계약금(Upfront payment) USD 13,000,000을 2019년에 일시에 수령하였으며, 2020년에 USD 3,000,000 추가 수령액을 포함하여 USD 5,052,631을 총 수익으로 인식하였습니다.
또한 2020년 6월 24일 B사의 계약에 따라 반환조건 없는 계약금(Upfront payment) USD 16,000,000을 2020년에 두번에 나눠서 수령하였으며, 2021년 1월 7일 C사의 계약에 따라 반환조건 없는 계약금(Upfront payment) USD 6,000,000을 일시에 수령하였습니다. 동 계약 모두 계약과 동시에 재화의 공급과 수행의무가 종료되어 수익으로 인식하였습니다.
연결실체는 두 건의 계약 관련하여 상대회사인 A사와 B사에서 임상진행 및 각 국가별 허가 및 판매 이정표를 달성하면 마일스톤 금액(Milestone payment)을 수령할 수 있습니다.
(2) 연결실체는 2021년 3월3일자로 ALT-L9의 국내 판매에 대한 라이선스를 ㈜한림MS에 부여하는 계약(공급 및 판매계약서)을 체결하였습니다.
연결실체는 계약의 체결과 동시에 ㈜한림MS로 부터 기술료(계약금)로 20억을 수령하였으며, ALT-L9의 품목허가시까지 기술이전 기간동안의 동 기술료의 수익을 기간배분하여 인식하고 있습니다.
4. 재무제표
|
재무상태표 |
|
제 14 기 3분기말 2021.09.30 현재 |
|
제 13 기말 2020.12.31 현재 |
|
(단위 : 원) |
|
제 14 기 3분기말 |
제 13 기말 |
|
|---|---|---|
|
자산 |
||
|
유동자산 |
151,529,900,713 |
96,701,169,737 |
|
현금및현금성자산 |
5,158,801,273 |
5,214,927,929 |
|
단기금융상품 |
143,437,600,000 |
89,324,000,000 |
|
매출채권 및 기타유동채권 |
1,918,052,489 |
1,468,853,729 |
|
당기법인세자산 |
790,234,999 |
130,320,390 |
|
기타유동자산 |
225,211,952 |
563,067,689 |
|
비유동자산 |
29,003,484,477 |
18,665,010,952 |
|
장기금융상품 |
225,647,875 |
193,448,852 |
|
장기매출채권 및 기타비유동채권 |
0 |
3,000,000,000 |
|
장기대여금 |
0 |
3,000,000,000 |
|
유형자산 |
20,523,092,426 |
10,414,008,846 |
|
영업권 이외의 무형자산 |
861,925,411 |
769,734,021 |
|
기타비유동금융자산 |
337,727,240 |
730,520,061 |
|
종속기업, 조인트벤처와 관계기업에 대한 투자자산 |
7,048,172,876 |
3,548,181,500 |
|
종속기업에 대한 투자자산 |
7,048,172,876 |
3,548,181,500 |
|
기타비유동자산 |
6,918,649 |
9,117,672 |
|
자산총계 |
180,533,385,190 |
115,366,180,689 |
|
부채 |
||
|
유동부채 |
5,417,191,415 |
6,076,850,186 |
|
매입채무 및 기타유동채무 |
4,289,595,875 |
4,081,977,958 |
|
유동계약부채 |
4,289,595,875 |
4,081,977,958 |
|
기타유동금융부채 |
854,551,250 |
1,881,758,274 |
|
기타유동부채 |
273,044,290 |
113,113,954 |
|
비유동부채 |
2,513,517,469 |
828,770,008 |
|
장기매입채무 및 기타비유동채무 |
1,622,533,998 |
0 |
|
비유동계약부채 |
1,622,533,998 |
0 |
|
기타비유동금융부채 |
890,983,471 |
828,770,008 |
|
부채총계 |
7,930,708,884 |
6,905,620,194 |
|
자본 |
||
|
자본금 |
21,646,632,500 |
14,143,142,500 |
|
보통주자본금 |
21,132,125,000 |
14,041,450,000 |
|
우선주자본금 |
514,507,500 |
101,692,500 |
|
자본잉여금 |
168,074,274,845 |
99,239,776,726 |
|
주식발행초과금 |
167,498,519,268 |
98,664,021,149 |
|
자기주식처분이익 |
575,755,577 |
575,755,577 |
|
기타자본구성요소 |
1,559,254,662 |
1,578,219,261 |
|
자기주식 |
(793,980,301) |
0 |
|
주식선택권 |
2,353,234,963 |
1,578,219,261 |
|
이익잉여금(결손금) |
(18,677,485,701) |
(6,500,577,992) |
|
자본총계 |
172,602,676,306 |
108,460,560,495 |
|
자본과부채총계 |
180,533,385,190 |
115,366,180,689 |
|
포괄손익계산서 |
|
제 14 기 3분기 2021.01.01 부터 2021.09.30 까지 |
|
제 13 기 3분기 2020.01.01 부터 2020.09.30 까지 |
|
(단위 : 원) |
|
제 14 기 3분기 |
제 13 기 3분기 |
|||
|---|---|---|---|---|
|
3개월 |
누적 |
3개월 |
누적 |
|
|
수익(매출액) |
355,394,688 |
7,593,038,202 |
9,216,354,313 |
25,659,540,820 |
|
매출원가 |
5,892,211,951 |
8,581,595,688 |
851,313,698 |
5,362,062,353 |
|
매출총이익 |
(5,536,817,263) |
(988,557,486) |
8,365,040,615 |
20,297,478,467 |
|
판매비와관리비 |
2,227,347,686 |
15,522,951,412 |
3,201,384,763 |
8,512,163,787 |
|
영업이익(손실) |
(7,764,164,949) |
(16,511,508,898) |
5,163,655,852 |
11,785,314,680 |
|
기타이익 |
1,866,888,025 |
3,200,574,279 |
(53,273,838) |
751,419,889 |
|
기타손실 |
21,518,873 |
87,163,589 |
478,886,138 |
2,887,315,556 |
|
금융수익 |
323,327,328 |
1,225,683,009 |
194,207,826 |
717,384,156 |
|
금융원가 |
2,304,473 |
4,492,510 |
1,173,637 |
3,436,572 |
|
법인세비용차감전순이익(손실) |
(5,597,772,942) |
(12,176,907,709) |
4,824,530,065 |
10,363,366,597 |
|
법인세비용 |
0 |
0 |
36,454,666 |
370,168,710 |
|
당기순이익(손실) |
(5,597,772,942) |
(12,176,907,709) |
4,788,075,399 |
9,993,197,887 |
|
기타포괄손익 |
0 |
0 |
0 |
0 |
|
총포괄손익 |
(5,597,772,942) |
(12,176,907,709) |
4,788,075,399 |
9,993,197,887 |
|
주당이익 |
||||
|
기본주당이익(손실) (단위 : 원) |
(451) |
(295) |
115 |
239 |
|
희석주당이익(손실) (단위 : 원) |
(451) |
(295) |
115 |
239 |
|
자본변동표 |
|
제 14 기 3분기 2021.01.01 부터 2021.09.30 까지 |
|
제 13 기 3분기 2020.01.01 부터 2020.09.30 까지 |
|
(단위 : 원) |
|
자본 |
|||||
|---|---|---|---|---|---|
|
자본금 |
자본잉여금 |
기타자본구성요소 |
이익잉여금 |
자본 합계 |
|
|
2020.01.01 (기초자본) |
6,948,375,000 |
73,871,310,373 |
871,432,932 |
(10,562,397,573) |
71,128,720,732 |
|
당기순이익(손실) |
0 |
0 |
0 |
9,993,197,887 |
9,993,197,887 |
|
무상증자 |
6,997,975,000 |
(7,033,299,280) |
0 |
0 |
(35,324,280) |
|
전환우선주의발행 |
0 |
0 |
0 |
0 |
0 |
|
자기주식 거래로 인한 증감 |
0 |
0 |
0 |
0 |
0 |
|
주식기준보상거래 |
0 |
0 |
802,000,499 |
0 |
802,000,499 |
|
기타거래 |
95,100,000 |
2,660,024,190 |
(362,574,670) |
0 |
2,392,576,520 |
|
2020.09.30 (기말자본) |
14,041,450,000 |
69,498,035,283 |
1,310,885,761 |
(569,199,686) |
84,281,171,358 |
|
2021.01.01 (기초자본) |
14,143,142,500 |
99,239,776,726 |
1,578,219,261 |
(6,500,577,992) |
108,460,560,495 |
|
당기순이익(손실) |
0 |
0 |
0 |
(12,430,097,826) |
(12,176,907,709) |
|
무상증자 |
7,192,227,500 |
(7,228,689,370) |
0 |
0 |
(36,461,870) |
|
전환우선주의발행 |
241,312,500 |
74,599,720,350 |
0 |
0 |
74,841,032,850 |
|
자기주식 거래로 인한 증감 |
0 |
0 |
(793,980,301) |
0 |
(793,980,301) |
|
주식기준보상거래 |
0 |
0 |
1,031,059,001 |
0 |
1,031,059,001 |
|
기타거래 |
69,950,000 |
1,463,467,139 |
(256,043,299) |
0 |
1,277,373,840 |
|
2021.09.30 (기말자본) |
21,646,632,500 |
168,074,274,845 |
1,559,254,662 |
(18,930,675,818) |
172,602,676,306 |
|
현금흐름표 |
|
제 14 기 3분기 2021.01.01 부터 2021.09.30 까지 |
|
제 13 기 3분기 2020.01.01 부터 2020.09.30 까지 |
|
(단위 : 원) |
|
제 14 기 3분기 |
제 13 기 3분기 |
|
|---|---|---|
|
영업활동현금흐름 |
(12,087,680,168) |
11,886,973,302 |
|
당기순이익(손실) |
(12,430,097,826) |
9,993,197,887 |
|
당기순이익조정을 위한 가감 |
(1,755,691,635) |
3,785,589,125 |
|
기타 현금의 유입 없는 수익등 |
(3,804,163,708) |
(911,043,174) |
|
기타 현금의 유출 없는 비용등 |
2,048,472,073 |
4,696,632,299 |
|
영업활동으로인한자산ㆍ부채의변동 |
1,844,760,872 |
(2,438,454,101) |
|
이자수취(영업) |
913,263,030 |
458,968,751 |
|
법인세납부(환급) |
(659,914,609) |
87,671,640 |
|
투자활동현금흐름 |
(63,513,666,658) |
(12,769,344,339) |
|
임차보증금의 감소 |
61,964,837 |
43,855,000 |
|
임차보증금의 증가 |
0 |
(353,679,401) |
|
유형자산의 처분 |
0 |
26,305,439 |
|
유형자산의 취득 |
(11,058,759,497) |
(2,067,993,887) |
|
무형자산의 취득 |
(150,088,981) |
(103,411,013) |
|
장기대여금및수취채권의 처분 |
3,000,000,000 |
0 |
|
단기금융상품의 처분 |
114,652,000,000 |
359,984,340 |
|
단기금융상품의 취득 |
(166,486,592,618) |
(5,586,620,000) |
|
장기금융상품의 취득 |
(32,199,023) |
(87,784,817) |
|
당기손익인식금융자산의 취득 |
0 |
(5,000,000,000) |
|
종속기업투자 순변동 |
(3,499,991,376) |
0 |
|
재무활동현금흐름 |
75,247,561,935 |
2,268,957,164 |
|
주식의 발행 |
74,841,032,850 |
(35,324,280) |
|
무상증자 |
(36,461,870) |
0 |
|
주식선택권행사로 인한 현금유입 |
1,277,373,840 |
2,392,576,520 |
|
자기주식의 취득 |
(793,980,301) |
0 |
|
리스부채의 상환 |
(40,402,584) |
(88,295,076) |
|
환율변동효과 반영전 현금및현금성자산의 순증가(감소) |
(353,784,891) |
1,386,586,127 |
|
현금및현금성자산에 대한 환율변동효과 |
297,658,235 |
(301,769,650) |
|
기초현금및현금성자산 |
5,214,927,929 |
2,898,863,772 |
|
기말현금및현금성자산 |
5,158,801,273 |
3,983,680,249 |
5. 재무제표 주석
주석
| 당분기 : 2021년 9월 30일 현재 |
| 전분기 : 2020년 9월 30일 현재 |
| 주식회사 알테오젠 |
1. 회사의 개요
주식회사 알테오젠(이하 '당사')은 2008년 5월 13일에 설립되어 유전자 개발과 형질전환 동식물 개발 등 생명공학 관련 연구개발을 주요 목적으로 사업을 영위하고 있습니다.
본사는 대전광역시 유성구 유성대로 1628번길 62에 위치하고 있으며, 당사는 2014년 12월 코스닥 시장에 상장하였습니다.
당사의 설립시 자본금은 100,000천원이었으며, 수차례의 유상증자 등을 통하여 당분기말 현재의 발행보통주식수는 42,264,250주, 보통주자본금은 21,132,125천원이며, 발행우선주식수는 1,029,015주, 우선주자본금은 514,507천원입니다.
한편, 당분기말 현재 당사의 주요 주주현황은 다음과 같습니다.
| 주 주 명 | 보통주 | 우선주 | 소계 | 지 분 율 | 비 고 |
|---|---|---|---|---|---|
| 박순재 | 8,505,000 | - | 8,505,000 | 19.65% | 대표이사 |
| 정혜신 | 1,680,000 | - | 1,680,000 | 3.88% | 특수관계인 |
| 박수민 | 232,500 | - | 232,500 | 0.54% | 특수관계인 |
| 형인우 | 2,500,000 | - | 2,500,000 | 5.77% | 5%이상 주주 |
| Kissei Pharmaceutical Co., Ltd. | 1,297,992 | - | 1,297,992 | 3.00% | 외국법인 |
| 기타 | 28,048,758 | 1,029,015 | 29,077,773 | 67.16% | - |
| 합 계 | 42,264,250 | 1,029,015 | 43,293,265 | 100.00% | - |
2. 중요한 회계정책
(1) 재무제표 작성기준
당사의 2021년 6월 30일로 종료하는 6개월 보고기간에 대한 요약분기재무제표는 기업회계기준서 제1034호 '중간재무보고'에 따라 작성되었습니다. 이 요약분기재무제표는 보고기간말인 2021년 6월 30일 현재 유효하거나 조기 도입한 한국채택국제회계기준에 따라 작성되었습니다.
1) 당사가 채택한 제ㆍ개정 기준서 및 해석서
당사는 2021년 1월 1일로 개시하는 회계기간부터 다음의 제ㆍ개정 기준서 및 해석서를 신규로 적용하였습니다.
- 기업회계기준서 제 1116호 '리스' 개정 - 코로나19 관련 임차료 할인 등에 대한 실무적 간편법
실무적 간편법으로, 리스이용자는 코로나19의 직접적인 결과로 발생한 임차료 할인 등이 리스변경에 해당하는지 평가하지 않을 수 있습니다. 이러한 선택을 한 리스이용자는 임차료 할인 등으로 인한 리스료 변동을 그러한 변동이 리스변경이 아닐 경우에이 기준서가 규정하는 방식과 일관되게 회계처리하여야 합니다. 해당 기준서의 개정이 재무제표에 미치는 중요한 영향은 없습니다.
- 기업회계기준서 제1109호 '금융상품', 제1039호 '금융상품: 인식과 측정', 제1107호 '금융상품: 공시', 제 1104호 '보험계약' 및 제 1116호 '리스' 개정 - 이자율지표 개혁(2단계 개정)
이자율지표개혁과 관련하여 상각후원가로 측정되는 금융상품의 이자율지표대체시 장부금액이 아닌 유효이자율을 조정하고, 위험회피관계에서 이자율지표대체가 발생한 경우에도 중단없이 위험회피회계를 계속할 수 있도록 하는 등의 예외규정을 포함하고 있습니다. 해당 기준서의 개정이 재무제표에 미치는 중요한 영향은 없습니다.
2) 당사가 적용하지 않은 제ㆍ개정 기준서 및 해석서
제정 또는 공표되었으나 시행일이 도래하지 않아 적용하지 아니한 제ㆍ개정 기준서 및 해석서는 다음과 같습니다.
- 기업회계기준서 제1103호 '사업결합' 개정 - 개념체계의 인용
인식할 자산과 부채의 정의를 개정된 재무보고를 위한 개념체계를 참조하도록 개정되었으나, 기업회계기준서 제1037호 '충당부채, 우발부채 및 우발자산' 및 해석서 제2121호 '부담금'의 적용범위에 포함되는 부채 및 우발부채에 대해서는 해당 기준서를 적용하도록 예외를 추가하고, 우발자산이 취득일에 인식되지 않는다는 점을 명확히 하였습니다. 동 개정사항은 2022년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 당사는 동 개정으로 인해 재무제표에 중요한 영향은 없을 것으로 예상하고 있습니다.
- 기업회계기준서 제1016호 '유형자산' 개정 - 의도한 사용 전의 매각금액
기업이 자산을 의도한 방식으로 사용하기 전에 생산된 품목의 판매에서 발생하는 수익을 생산원가와 함께 당기손익으로 인식하도록 요구하며, 유형자산의 취득원가에서차감하는 것을 금지하고 있습니다. 동 개정사항은 2022년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 당사는 동 개정으로 인한 재무제표의 영향을 검토 중에 있습니다.
- 기업회계기준서 제1037호 '충당부채, 우발부채 및 우발자산' 개정 - 손실부담계약:계약이행원가
손실부담계약을 식별할 때 계약이행원가의 범위를 계약 이행을 위한 증분원가와 계약 이행에 직접 관련되는 다른 원가의 배분이라는 점을 명확히 하였습니다. 동 개정사항은 2022년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 당사는 동 개정으로 인해 재무제표에 중요한 영향은 없을 것으로 예상하고 있습니다.
- 한국채택국제회계기준 연차개선 2018-2020
한국채택국제회계기준 연차개선 2018-2020은 2022년 1월 1일 이후 시작하는 회계연도부터 적용되며, 조기적용이 허용됩니다. 당사는 동 개정으로 인해 재무제표에 중요한 영향은 없을 것으로 예상하고 있습니다.
·기업회계기준서 제1101호 '한국채택국제회계기준의 최초 채택' : 최초채택기업인 종속기업
·기업회계기준서 제1109호 '금융상품' : 금융부채 제거 목적의 10% 테스트 관련 수수료
·기업회계기준서 제1116호 '리스' : 리스 인센티브
·기업회계기준서 제1041호 '농립어업' : 공정가치 측정
- 기업회계기준서 제1001호 '재무제표 표시' 개정 - 부채의 유동/비유동 분류
보고기간말 현재 존재하는 실질적인 권리에 따라 유동 또는 비유동으로 분류되며, 부채의 결제를 연기할 수 있는 권리의 행사가능성이나 경영진의 기대는 고려하지 않습니다. 또한, 부채의 결제에 자기지분상품의 이전도 포함되나, 복합금융상품에서 자기지분상품으로 결제하는 옵션이 지분상품의 정의를 충족하여 부채와 분리하여 인식된경우는 제외됩니다. 동 개정사항은 2023년 1월 1일 이후 시작하는 회계연도부터 적용하며, 조기적용이 허용됩니다. 당사는 동 개정으로 인한 재무제표의 영향을 검토 중에 있습니다.
- 기업회계기준서 제 1116호 '리스' 개정 - 2021년 6월 30일 후에도 제공되는 코로나19 관련 임차료 할인 등
코로나19의 직접적인 결과로 발생한 임차료 할인 등(rent concession)이 리스변경에 해당하는지 평가하지 않을 수 있도록 하는 실무적 간편법의 적용대상이 2022년 6월 30일 이전에 지급하여야 할 리스료에 영향을 미치는 리스료 감면으로 확대되었습니다. 리스이용자는 비슷한 상황에서 특성이 비슷한 계약에 실무적 간편법을 일관되게 적용해야 합니다. 동 개정사항은 2021년 4월 1일 이후 시작하는 회계연도부터 적용되며, 조기도입이 가능합니다. 당사는 동 개정으로 인해 재무제표에 중요한 영향은 없을 것으로 예상하고 있습니다.
(2) 회계정책
요약분기재무제표의 작성에 적용된 유의적 회계정책과 계산방법은 주석 2.(1).1)에서 설명하는 제ㆍ개정 기준서의 적용으로 인한 변경 및 아래 문단에서 설명하는 사항을 제외하고는 전기 재무제표 작성에 적용된 회계정책이나 계산방법과 동일합니다.
1) 법인세비용
중간기간의 법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균연간법인세율, 즉 추정평균연간유효법인세율을 중간기간의 세전이익에 적용하여 계산합니다.
3. 중요한 회계추정 및 가정
당사는 미래에 대하여 추정 및 가정을 하고 있습니다. 추정 및 가정은 지속적으로 평가되며, 과거 경험과 현재의 상황에서 합리적으로 예측가능한 미래의 사건과 같은 다른 요소들을 고려하여 이루어집니다. 이러한 회계추정은 실제 결과와 다를 수도있습니다.
요약분기재무제표 작성시 사용된 중요한 회계추정 및 가정은 법인세비용을 결정하는데 사용된 추정의 방법을 제외하고는 전기 재무제표 작성에 적용된 회계추정 및 가정과 동일합니다.
COVID-19의 확산은 국내외 경제에 중대한 영향을 미치고 있습니다. 이는 생산성 저하와 매출의 감소나 지연, 기존 채권의 회수 등에 부정적인 영향을 미칠 수 있습니다. 이로 인해 당사의 재무상태와 재무성과에도 부정적인 영향이 발생할 수 있으며, 이러한 영향은 2021년 연차재무제표에도 지속될 것으로 예상됩니다.
중간기간의 재무제표 작성시 사용된 중요한 회계추정 및 가정은 COVID-19에 따른 불확실성의 변동에 따라 조정될 수 있으며, COVID-19로 인하여 당사의 사업, 재무상태 및 경영성과 등에 미칠 궁극적인 영향은 현재 예측할 수 없습니다.
4. 영업부문
당사의 주요 수익은 유전자 개발과 형질전환 동식물 개발 등 생명공학 관련 연구개발로부터 창출되며, 성과에 대한 최고영업의사결정자에게 보고되는 정보 또한 상기 주요 수익 관련 정보가 단일부문으로 보고됩니다. 따라서 한국채택국제회계기준 제1108호(영업부문)에 따른 보고부문은 단일부문으로 기업전체 수준에서의 부문별 정보는다음과 같습니다.
(1) 당분기 및 전분기 영업수익에 대한 정보는 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 연구용역매출 | 7,339,848,085 | 25,659,540,820 |
(2) 당분기 및 전분기 영업수익의 지역에 대한 정보는 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 국 내 | 해 외 | 계 |
|---|---|---|---|
| 연구용역매출 | 405,268,022 | 6,934,580,063 | 7,339,848,085 |
| (전분기) | (단위: 원) |
| 구 분 | 국 내 | 해 외 | 계 |
|---|---|---|---|
| 연구용역매출 | - | 25,659,540,820 | 25,659,540,820 |
(3) 당분기 및 전분기 중 당사 수익의 10% 이상을 차지하는 주요 거래처는 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 주요거래처 A | 6,570,000,000 | - |
| 주요거래처 B | - | 19,211,200,000 |
| 주요거래처 C | - | 6,246,521,053 |
| 합 계 | 6,570,000,000 | 25,457,721,053 |
5. 범주별 금융상품
(1) 당분기말 및 전기말 현재 금융자산 범주별 장부금액은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | |
|---|---|---|---|
| 상각후 원가로 측정하는 금융자산 |
현금및현금성자산 | 5,158,801,273 | 5,214,927,929 |
| 장.단기금융상품 | 143,663,247,875 | 89,517,448,852 | |
| 매출채권및기타채권 | 1,664,862,372 | 1,468,853,729 | |
| 장.단기대여금 | - | 3,000,000,000 | |
| 기타비유동금융자산 | 337,727,240 | 730,520,061 | |
| 합 계(*) | 150,824,638,760 | 99,931,750,571 | |
(*) 당분기말 및 전기말 현재 금융자산의 장부금액은 공정가치의 합리적인 근사치인 금액입니다.
(2) 당분기말 및 전기말 현재 금융부채 범주별 장부금액은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | |
|---|---|---|---|
| 상각후원가로 측정하는 금융부채 |
기타유동금융부채 | 814,490,515 | 1,812,268,937 |
| 기타비유동금융부채 | 853,420,972 | 788,443,728 | |
| 기타 금융부채 | 유동리스부채 | 40,060,735 | 69,489,337 |
| 비유동리스부채 | 37,562,499 | 40,326,280 | |
| 합 계(*) | 1,745,534,721 | 2,710,528,282 | |
(*) 당분기말 및 전기말 현재 금융부채의 장부금액은 공정가치의 합리적인 근사치인 금액이며, 범주별 금융부채 기준을 적용 받지 않는 리스부채를 포함하였습니다.
(3) 당분기 및 전분기 금융상품 범주별 순손익은 다음과 같습니다.
| (당분기) |
(단위: 원) |
|
구 분 |
상각후원가로 |
상각후원가로 측정하는 금융부채 |
합 계 |
|---|---|---|---|
| 이자수익 | 1,225,683,009 | - | 1,225,683,009 |
| 이자비용(*) | - | 4,492,510 | 4,492,510 |
| 외환차익 | 227,341,729 | 21,004,062 | 248,345,791 |
| 외환차손 | 940,721 | 55,737,907 | 56,678,628 |
| 외화환산이익 | 2,578,121,175 | 359,524 | 2,578,480,699 |
| 외화환산손실 | - | 900,860 | 900,860 |
(*) 범주별 금융부채 기준을 적용 받지 않는 리스부채의 이자비용을 포함한 금액입니다.
| (전분기) |
(단위: 원) |
|
구 분 |
상각후원가로 |
당기손익- 공정가치금융자산 |
상각후원가로 측정하는 금융부채 |
합 계 |
|---|---|---|---|---|
| 이자수익 | 717,384,156 | - | - | 717,384,156 |
| 당기손익-공정가치 측정 금융자산평가이익 | - | 41,643,835 | - | 41,643,835 |
| 이자비용(*) | - | - | 3,436,572 | 3,436,572 |
| 외환차익 | 334,852,886 | - | 38,010,605 | 372,863,491 |
| 외환차손 | 290,399,732 | - | 7,220,571 | 297,620,303 |
| 외화환산이익 | 109,900,000 | - | 205,499 | 110,105,499 |
| 외화환산손실 | 412,599,048 | - | 412,103 | 413,011,151 |
(*) 범주별 금융부채 기준을 적용 받지 않는 리스부채의 이자비용을 포함한 금액입니다.
6. 현금및현금성자산과 금융상품
(1) 당분기말 및 전기말 현재 현금및현금성자산과 금융상품의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 금융기관 | 이자율(%) | 당분기말 | 전기말 | |
|---|---|---|---|---|---|
| 현금및현금성자산 | 요구불예금 등 | KEB하나은행 등 | - | 5,158,801,273 | 5,214,927,929 |
| 단기금융상품 | 정기예금 | KEB하나은행 등 | 0.39 ~2.11 | 143,437,600,000 | 89,324,000,000 |
| 장기금융상품 | 저축성보험 | 하나생명 | - | 225,647,875 | 193,448,852 |
| 합 계 | 148,822,049,148 | 94,732,376,781 | |||
(2) 당분기말 및 전기말 현재 사용이 제한된 금융상품은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 내 역 | 당분기말 | 전기말 |
|---|---|---|---|
| 단기금융상품 | 우리사주대출에 대한 담보제공(*1) | - | 88,000,000 |
(*1) 당사는 우리사주조합의 대출 지원을 위해 대출기관인 KEB하나은행에 예금담보를 제공하고 있습니다(주석28 참조).
7. 매출채권및기타채권
(1) 당분기말 및 전기말 현재 매출채권및기타채권의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 매출채권 | - | 509,204,542 |
| 미수금 | 663,133,011 | 597,515,596 |
| 미수수익 | 1,001,729,361 | 362,133,591 |
| 합 계 | 1,664,862,372 | 1,468,853,729 |
(2) 신용위험 및 대손충당금
상기 매출채권및기타채권은 대여금및수취채권으로 분류되며 상각후원가로 측정됩니다.
당사의 평균 신용공여기간은 60일입니다. 대금청구일로부터 최초 60일 동안은 매출채권에 대한 별도의 대손충당금을 설정하지 않고 있으며, 60일 초과 경과 매출채권에 대해서는 거래상대방의 과거 채무불이행 경험 및 현재의 재무상태 분석에 근거하여 결정된 미회수 추정금액을 대손충당금으로 설정하고 있습니다.
당사는 당분기말 현재 회수기일이 경과하였거나 신용등급에 중요한 변동이 있는 채권을 보유하고 있지 않고 있으며, 이에 따라 대여금및수취채권에 대하여 설정한 대손충당금은 없습니다.
8. 종속기업투자
(1) 당분기말 및 전기말 현재 종속기업의 세부내역은 다음과 같습니다.
| (단위: 원) |
| 종속기업명 | 주요 영업활동 | 소재지 | 지분율 | 당분기말 | 전기말 | 비 고 |
|---|---|---|---|---|---|---|
| ㈜알토스바이오사이언스(*1) | 의학 및 약학 연구개발업 | 대한민국 | 100% | - | 361,520,000 | 2013년 12월 19일 취득 |
| ㈜엘에스메디텍 | 의약품 도매업 | 대한민국 | 100% | 881,520,000 | 520,000,000 | 2016년 6월 3일 취득 |
| ㈜세레스에프앤디 | 식품첨가물 제조업 |
대한민국 | 50.80% | 5,666,652,876 | 2,166,661,500 | 2018년 6월 15일 취득 |
| ㈜알토스바이오로직스(*2) | 의학 및 약학 연구개발업 | 대한민국 | 72.56% | 500,000,000 | 500,000,000 | 2020년 12월 15일 취득 |
| 합 계 | 7,048,172,876 | 3,548,181,500 | ||||
(*1) 당기 중 (주)알토스바이오사이언스는 ㈜LS메디텍에 흡수 합병되었습니다.
(*2) 전기 중 당사는 (주)알토스바이오로직스의 지분을 신규 취득하였습니다.
(2) 당분기 및 전분기 중 종속기업의 변동내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 기초 장부금액 | 3,548,181,500 | 3,048,181,500 |
| 취득 | 3,499,991,376 | - |
| 손상 | - | - |
| 기말 장부금액 | 7,048,172,876 | 3,048,181,500 |
9. 유형자산
(1) 당분기말 및 전기말 현재 유형자산의 구성내역은 다음과 같습니다.
| (당분기말) | (단위: 원) |
| 구 분 | 취득원가 | 정부보조금 | 감가상각누계액 | 장부금액 |
|---|---|---|---|---|
| 토지 | 1,800,512,309 | - | - | 1,800,512,309 |
| 건물 | 4,035,519,832 | - | (743,301,195) | 3,292,218,637 |
| 구축물 | 4,274,000 | - | (4,272,000) | 2,000 |
| 비품 | 448,415,500 | - | (272,846,654) | 175,568,846 |
| 건설중인자산 | 12,452,944,600 | - | - | 12,452,944,600 |
| 연구용기자재 | 6,931,000,411 | (1,355,179) | (4,239,646,286) | 2,689,998,946 |
| 시설장치 | 4,200,000 | - | (870,003) | 3,329,997 |
| 차량운반구 | 36,388,348 | - | (14,555,338) | 21,833,010 |
| 합 계 | 25,713,255,000 | (1,355,179) | (5,275,491,476) | 20,436,408,345 |
| (전기말) | (단위: 원) |
| 구 분 | 취득원가 | 정부보조금 | 감가상각누계액 | 장부금액 |
|---|---|---|---|---|
| 토지 | 1,800,512,309 | - | - | 1,800,512,309 |
| 건물 | 2,490,832,924 | - | (630,586,366) | 1,860,246,558 |
| 구축물 | 4,274,000 | - | (4,272,000) | 2,000 |
| 비품 | 374,314,904 | - | (246,478,766) | 127,836,138 |
| 건설중인자산 | 3,113,300,260 | - | - | 3,113,300,260 |
| 연구용기자재 | 6,881,116,516 | (2,464,430) | (3,539,901,152) | 3,338,750,934 |
| 시설장치 | 29,300,000 | - | (8,981,666) | 20,318,334 |
| 차량운반구 | 36,388,348 | - | (9,097,085) | 27,291,263 |
| 합 계 | 14,730,039,261 | (2,464,430) | (4,439,317,035) | 10,288,257,796 |
(2) 당분기 및 전분기 중 유형자산 장부금액의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 기초금액 | 취 득 | 대 체 | 처 분 | 상 각 | 기말금액 |
|---|---|---|---|---|---|---|
| 토지 | 1,800,512,309 | - | - | - | - | 1,800,512,309 |
| 건물 | 1,860,246,558 | - | 1,544,686,908 | - | (112,714,829) | 3,292,218,637 |
| 구축물 | 2,000 | - | - | - | - | 2,000 |
| 비품 | 127,836,138 | 81,143,595 | - | (7,000) | (33,403,887) | 175,568,846 |
| 건설중인자산 | 3,113,300,260 | 10,884,331,248 | (1,544,686,908) | - | - | 12,452,944,600 |
| 연구용기자재(*) | 3,338,750,934 | 83,868,454 | - | (745,529) | (731,874,913) | 2,689,998,946 |
| 시설장치 | 20,318,334 | 2,000,000 | - | (17,728,328) | (1,260,009) | 3,329,997 |
| 차량운반구 | 27,291,263 | - | - | - | (5,458,253) | 21,833,010 |
| 합 계 | 10,288,257,796 | 11,051,343,297 | - | (18,480,857) | (884,711,891) | 20,436,408,345 |
(*) 정부보조금의 변동내역을 포함하고 있습니다.
| (전분기) |
(단위: 원) |
| 구 분 | 기초금액 | 취 득 | 상 각 | 기말금액 |
|---|---|---|---|---|
| 토지 | 4,457,561,299 | - | - | 4,457,561,299 |
| 건물 | 1,984,788,204 | - | (93,406,242) | 1,891,381,962 |
| 구축물 | 641,100 | - | (479,329) | 161,771 |
| 비품 | 88,576,436 | 71,936,236 | (32,433,840) | 128,078,832 |
| 건설중인자산 | 1,419,351,440 | 823,839,370 | - | 2,243,190,810 |
| 연구용기자재(*) | 3,022,875,752 | 1,134,650,207 | (679,781,918) | 3,477,744,041 |
| 시설장치 | 6,825,000 | 18,800,000 | (3,841,670) | 21,783,330 |
| 차량운반구 | 34,568,932 | - | (5,458,253) | 29,110,679 |
| 합 계 | 11,015,188,163 | 2,049,225,813 | (815,401,252) | 12,249,012,724 |
(*) 정부보조금의 변동내역을 포함하고 있습니다.
(3) 당분기 및 전분기 감가상각비가 포함된 항목은 다음과 같습니다.
| (단위: 원) |
| 구 분 |
당분기 |
전분기 |
|---|---|---|
|
매출원가 |
404,214,213 | 245,985,217 |
| 판매비와관리비(*) | 480,497,678 | 569,416,035 |
| 합 계 | 884,711,891 | 815,401,252 |
(*) 판매비와관리비의 감가상각비에는 경상연구개발비 398,177,663원(전분기 511,676,377원)이 포함되어 있습니다.
10. 리스
(1) 당분기말 및 전기말 현재 기초자산 유형별 사용권자산 및 리스부채의 내역은 다음과 같습니다.
|
(단위: 원) |
|
구 분 |
당분기말 | 전기말 |
|---|---|---|
| 사용권자산 | ||
| 차량운반구 | 79,646,052 | 48,939,476 |
| 건물 | 7,038,029 | 76,811,574 |
| 합 계 | 86,684,081 | 125,751,050 |
상기 리스자산 계산에서 사용된 증분차입이자율은 2.49%~4.02%입니다.
| (단위: 원) |
|
구 분 |
당분기말 |
전기말 |
|---|---|---|
| 리스부채 | ||
|
유동 |
40,060,735 | 69,489,337 |
|
비유동 |
37,562,499 | 40,326,280 |
| 합 계 | 77,623,234 | 109,815,617 |
(2) 당분기 및 전분기 중 손익으로 인식된 금액은 다음과 같습니다.
|
(단위: 원) |
|
구 분 |
당분기 | 전분기 |
|---|---|---|
|
사용권자산의 감가상각비 |
||
| 차량운반구 | 29,976,609 | 32,843,433 |
| 건물 | 19,585,125 | 34,452,334 |
| 합 계 | 49,561,734 | 67,295,767 |
| 리스부채 이자비용 | 2,628,129 | 3,436,572 |
| 단기리스 관련 비용 | 29,072,519 | 27,823,855 |
당사가 당분기말 현재 체결하고 있는 단기리스의 리스약정 금액은 2,563,200원(전기말 17,243,200원)입니다.
당분기 중 리스로 인한 총 현금유출 금액은 72,103,232원(전분기 93,661,519원)입니다.
11. 무형자산
(1) 당분기말 및 전기말 현재 무형자산의 구성내역은 다음과 같습니다.
| (당분기말) | (단위: 원) |
| 구 분 | 취득원가 | 정부보조금 | 상각누계액 | 장부금액 |
|---|---|---|---|---|
| 특허권 | 703,543,669 | (115,179,841) | (273,462,212) | 314,901,616 |
| 소프트웨어 | 239,289,667 | - | (90,068,658) | 149,221,009 |
| 상표권 | 2,553,404 | - | (2,552,404) | 1,000 |
| 건설중인자산 | 457,728,239 | (59,926,453) | - | 397,801,786 |
| 합 계 | 1,403,114,979 | (175,106,294) | (366,083,274) | 861,925,411 |
| (전기말) | (단위: 원) |
| 구 분 | 취득원가 | 정부보조금 | 상각누계액 | 장부금액 |
|---|---|---|---|---|
| 특허권 | 668,247,058 | (117,528,457) | (221,494,117) | 329,224,484 |
| 소프트웨어 | 175,149,667 | - | (67,551,333) | 107,598,334 |
| 상표권 | 2,553,404 | - | (2,552,404) | 1,000 |
| 건설중인자산 | 407,075,869 | (74,165,666) | - | 332,910,203 |
| 합 계 | 1,253,025,998 | (191,694,123) | (291,597,854) | 769,734,021 |
(2) 당분기 및 전분기 중 무형자산 장부금액의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 기초금액 | 취 득 | 대 체 | 상 각 | 기말금액 |
|---|---|---|---|---|---|
| 특허권(*) | 329,224,484 | - | 21,057,398 | (35,380,266) | 314,901,616 |
| 소프트웨어 | 107,598,334 | 64,140,000 | - | (22,517,325) | 149,221,009 |
| 상표권 | 1,000 | - | - | - | 1,000 |
| 건설중인자산(*) | 332,910,203 | 85,948,981 | (21,057,398) | - | 397,801,786 |
| 합 계 | 769,734,021 | 150,088,981 | - | (57,897,591) | 861,925,411 |
(*) 특허권 취득과 관련한 정부보조금의 변동내역을 포함하여 작성하였습니다.
| (전분기) | (단위: 원) |
| 구 분 | 기초금액 | 취 득 | 대 체 | 상 각 | 손 상 | 기말금액 |
|---|---|---|---|---|---|---|
| 특허권(*) | 229,816,457 | - | 94,737,597 | (27,313,708) | (453,767) | 296,786,579 |
| 소프트웨어 | 23,007,685 | 30,115,000 | - | (8,267,019) | - | 44,855,666 |
| 상표권 | 1,000 | - | - | - | - | 1,000 |
| 건설중인자산(*) | 242,675,062 | 73,296,013 | (94,737,597) | - | (9,048,242) | 212,185,236 |
| 합 계 | 495,500,204 | 103,411,013 | - | (35,580,727) | (9,502,009) | 553,828,481 |
(*) 특허권 취득과 관련한 정부보조금의 변동내역을 포함하여 작성하였습니다.
(3) 당분기 및 전반기 무형자산상각비는 전액 판매비와관리비에 포함되어 있습니다.
(4) 당사가 비용으로 인식한 연구와 개발 지출의 총액은 11,617,558,788원(전분기: 3,109,258,035원)입니다.
12. 정부보조금
(1) 당분기말 및 전기말 현재 정부기관 등과 체결한 국책연구과제와 관련하여 수령한 정부보조금의 미사용 및 반환예정액은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 보통예금 | 33,333,336 | 20,833,335 |
| 장기미지급금(*) | 853,420,972 | 788,443,728 |
| 합 계 | 886,754,308 | 809,277,063 |
(*) 상환의무가 있는 경우 장기미지급금으로 계상하고 있습니다.
(2) 당분기 및 전분기 중 정부보조금의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 기 초 | 수 령 | 사 용 | 기 타 | 기 말 |
|---|---|---|---|---|---|
| 정부보조금 | 809,277,063 | 698,161,906 | (620,684,661) | - | 886,754,308 |
| (전분기) | (단위: 원) |
| 구 분 | 기 초 | 수 령 | 사 용 | 기 타 | 기 말 |
|---|---|---|---|---|---|
| 정부보조금 | 2,487,589,277 | 811,753,790 | (2,104,207,859) | (178,267,528) | 1,016,867,680 |
(3) 당분기 및 전분기 중 정부보조금의 지출내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 선급금(기업부담금)의 감소 | 106,684,877 | 74,278,034 |
| 비용상계 | 513,999,783 | 2,029,929,825 |
| 합 계 | 620,684,661 | 2,104,207,859 |
13. 기타자산
당분기말 및 전기말 현재 기타자산의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | |
|---|---|---|---|
| 유동자산 | 선급금 | 160,709,662 | 515,796,100 |
| 선급비용 | 64,502,290 | 47,271,589 | |
| 소 계 | 225,211,952 | 563,067,689 | |
| 비유동자산 | 장기선급비용 | 6,918,649 | 9,117,672 |
| 소 계 | 6,918,649 | 9,117,672 | |
| 합 계 | 232,130,601 | 572,185,361 | |
14. 기타금융부채
당분기말 및 전기말 현재 기타금융부채의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | ||
|---|---|---|---|---|
| 유 동 | 비유동 | 유 동 | 비유동 | |
| 미지급금 | 621,714,545 | 853,420,972 | 1,650,359,719 | 788,443,728 |
| 미지급비용 | 192,775,970 | - | 161,909,218 | - |
| 합 계 | 814,490,515 | 853,420,972 | 1,812,268,937 | 788,443,728 |
15. 기타부채
당분기말 및 전기말 현재 기타부채의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | |
|---|---|---|---|
| 유동부채 | 예수금 | 273,044,290 | 113,113,954 |
16. 고객과의 계약에서 발생하는 수익 및 관련 계약부채
(1) 고객과의 계약에서 생기는 수익의 구분
당사는 재화나 용역을 기간에 걸쳐 이전하거나 한 시점에 이전함으로써 수익을 창출합니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 수익인식 시점 | ||
|
한 시점에 인식 |
6,570,000,000 | 23,035,000,000 |
|
기간에 걸쳐 인식 |
769,848,085 | 2,624,540,820 |
| 합 계 | 7,339,848,085 | 25,659,540,820 |
(2) 당분기 및 전분기 중 계약부채 장부금액의 변동내역은 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 선수수익 | |
|---|---|---|
| 유동 | 비유동 | |
| 기초 금액 | 4,081,977,958 | - |
| 증가 | - | 2,600,000,000 |
| 감소 | (769,848,085) | - |
| 유동성대체 | 977,466,002 | (977,466,002) |
| 기말 금액 | 4,289,595,875 | 1,622,533,998 |
| (전분기) | (단위: 원) |
| 구 분 | 선수수익 | |
|---|---|---|
| 유동 | 비유동 | |
| 기초 금액 | 3,420,997,871 | 2,422,721,052 |
| 증가 | 3,307,346,052 | - |
| 감소 | (2,624,540,820) | - |
| 유동성대체 | - | (2,422,721,052) |
| 기말 금액 | 4,103,803,103 | - |
(3) 계약부채와 관련하여 인식한 수익
당분기 및 전분기에 인식한 수익 중 전기에서 이월된 계약부채와 과거 보고기간에 이행한(또는 부분적으로 이행한) 수행의무와 관련된 금액은 다음과 같습니다.
|
(단위: 원) |
|
구 분 |
당분기 | 전분기 |
|---|---|---|
|
기초의 계약부채 잔액 중 당분기에 인식한 수익 |
||
| 라이선스계약 | 364,580,063 | 2,624,540,820 |
17. 퇴직급여제도
당사는 2012년 1월 1일부터 확정기여형(DC형) 퇴직급여제도로 전환하였으며, 보고기간종료일 현재 자격을 갖춘 모든 종업원들을 위해 확정기여형(DC형) 퇴직급여제도를 운영하고 있습니다.
사외적립자산은 수탁자인 KEB하나은행의 관리하에서 기금형태로 당사의 자산들로부터 독립적으로 운용되고 있으며, 종업원들이 확정기여형의 가득조건을 충족하기 전에 퇴사하는 경우 당사가 지불해야 할 기여금은 상실되는 기여금만큼 감소하게 됩니다.
당분기 및 전분기 중 포괄손익계산서에 인식된 총비용은 퇴직급여제도에서 규정하고 있는 비율에 따라 당사가 퇴직급여제도에 납입한 기여금을 나타내고 있습니다.
당분기 중 확정기여제도와 관련해 비용으로 인식한 금액은 360,234,330원(전분기: 259,944,546원)입니다.
18. 자본금 및 기타불입자본
(1) 자본금
1) 당분기말 및 전기말 현재 자본금의 구성내역은 다음과 같습니다.
| (단위: 주, 원) |
| 구 분 | 수권주식수 | 발행주식수 | 1주의 금액 | 당분기말 | 전기말 |
|---|---|---|---|---|---|
| 보통주 | 80,000,000 | 42,264,250 | 500 | 21,132,125,000 | 14,041,450,000 |
| 우선주 | 20,000,000 | 1,029,015 | 500 | 514,507,500 | 101,692,500 |
| 합 계 | 100,000,000 | 43,293,265 | 21,646,632,500 | 14,143,142,500 |
2) 당분기 및 전분기 중 자본금의 변동내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 보통주 | 우선주 | 보통주 | 우선주 | |
| 기초 금액 | 14,041,450,000 | 101,692,500 | 6,948,375,000 | - |
| 유상증자 | - | 241,312,500 | - | - |
| 무상증자 | 7,020,725,000 | 171,502,500 | 6,997,975,000 | - |
| 주식선택권의 행사(*) | 69,950,000 | - | 95,100,000 | - |
| 기말 금액 | 21,132,125,000 | 514,507,500 | 14,041,450,000 | - |
(*) 주식선택권의 일부가 행사되었습니다(주석26 참조).
3) 우선주는 전환우선주로 구성되며, 상세내역은 다음과 같습니다.
| 구 분 | 제3차 전환우선주 | 제4차 전환우선주 |
|---|---|---|
| 발행일 | 2020년 11월 13일 | 2021년 01월 08일 |
| 발행주식수(무상증자반영) | 305,078주 | 723,937주 |
| 1주당 발행가액(무상증자반영) | 98,333원 | 103,600원 |
| 총발행가액(최초발행시) | 29,999,287,500원 | 74,999,925,000원 |
| 전환대상 및 전환비율 | 보통주와 1:1로 전환가능 | 보통주와 1:1로 전환가능 |
| 전환가액 조정 | 전환가액을 하회하는 발행가액으로 유상증자를 하는 경우 등 | 전환가액을 하회하는 발행가액으로 유상증자를 하는 경우 등 |
| 전환권 행사기간 | 발행일로부터 1년이 경과한 날부터 존속기간 내(존속기간은 발행일로부터 5년) | 발행일로부터 1년이 경과한 날부터 존속기간 내(존속기간은 발행일로부터 7년) |
(2) 기타불입자본
1) 당분기말 및 전기말 현재 기타불입자본의 구성내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 과 목 | 당분기말 | 전기말 |
|---|---|---|---|
| 자본잉여금 | 주식발행초과금 | 167,498,519,268 | 98,664,021,149 |
| 자기주식처분이익 | 575,755,577 | 575,755,577 | |
| 기타자본항목 | 주식선택권 | 2,353,234,963 | 1,578,219,261 |
| 자기주식 | (793,980,301) | - | |
| 합 계 | 169,633,529,507 | 100,817,995,987 | |
2) 당분기 및 전분기 중 당사의 기타불입자본의 세부 변동 내역은 다음과 같습니다.
| (당분기) | (단위: 원) |
| 구 분 | 주식발행초과금 | 자기주식처분이익 | 주식선택권(*1) | 자기주식 | 합 계 |
|---|---|---|---|---|---|
| 기초 금액 | 98,664,021,149 | 575,755,577 | 1,578,219,261 | - | 100,817,995,987 |
| 유상증자 | 74,599,720,350 | - | - | - | 74,599,720,350 |
| 무상증자 | (7,228,689,370) | - | - | - | (7,228,689,370) |
| 자기주식의 취득 | - | - | - | (793,980,301) | (793,980,301) |
| 주식선택권의 행사 | 1,463,467,139 | - | (256,043,299) | - | 1,207,423,840 |
| 주식기준보상거래의 인식 | - | - | 1,031,059,001 | - | 1,031,059,001 |
| 기말 금액 | 167,498,519,268 | 575,755,577 | 2,353,234,963 | (793,980,301) | 169,633,529,507 |
| (전분기) | (단위: 원) |
| 구 분 | 주식발행초과금 | 자기주식처분이익 | 주식선택권(*1) | 합 계 |
|---|---|---|---|---|
| 기초 금액 | 73,295,554,796 | 575,755,577 | 871,432,932 | 74,742,743,305 |
| 무상증자 | (7,033,299,280) | - | - | (7,033,299,280) |
| 주식선택권의 행사 | 2,660,024,190 | - | (362,547,670) | 2,297,476,520 |
| 주식기준보상거래의 인식 | - | - | 802,000,499 | 802,000,499 |
| 기말 금액 | 68,922,279,706 | 575,755,577 | 1,310,885,761 | 70,808,921,044 |
(*1) 주식결제형 종업원급여적립금은 종업원주식옵션제도에 의해 종업원에게 부여된 주식옵션과 관련된 것입니다. 종업원에 대한 주식기준보상에 대한 상세정보는 주석 25에서 설명하고 있습니다.
19. 이익잉여금(결손금)
당분기 및 전분기 중 결손금의 변동내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 기초 금액 | (6,500,577,992) | (10,562,397,573) |
| 분기순이익(손실) | (12,430,097,826) | 9,993,197,887 |
| 기말 금액 | (18,930,675,818) | (569,199,686) |
20. 판매비와관리비
당분기 및 전분기의 판매비와관리비 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 급여 | 1,328,986,487 | 1,197,979,502 |
| 퇴직급여 | 123,394,260 | 79,592,034 |
| 주식기준보상 | 634,607,836 | 404,177,393 |
| 복리후생비 | 290,461,604 | 118,875,721 |
| 여비교통비 | 14,319,876 | 24,960,771 |
| 접대비 | 18,897,368 | 18,496,655 |
| 통신비 | 8,941,702 | 20,326,690 |
| 수도광열비 | 2,815,038 | 1,886,066 |
| 전력비 | 15,561,921 | 14,652,487 |
| 세금과공과 | 82,385,570 | 48,612,690 |
| 감가상각비 | 131,881,749 | 125,035,425 |
| 지급임차료 | 27,279,519 | 27,823,855 |
| 수선비 | 139,546 | 9,657,274 |
| 보험료 | 115,115,753 | 37,473,438 |
| 차량유지비 | 5,238,407 | 7,163,366 |
| 경상연구개발비 | 11,617,558,788 | 5,271,112,401 |
| 운반비 | 526,540 | 250,290 |
| 교육훈련비 | 3,548,121 | 6,452,970 |
| 도서인쇄비 | 4,873,555 | 1,764,932 |
| 회의비 | 5,400,558 | 5,575,922 |
| 사무용품비 | 4,141,394 | 2,401,101 |
| 소모품비 | 6,916,099 | 5,962,497 |
| 지급수수료 | 725,471,187 | 830,252,677 |
| 광고선전비 | 10,580,107 | 10,875,455 |
| 건물관리비 | 9,606,199 | 17,398,648 |
| 무형자산상각비 | 57,897,591 | 35,580,727 |
| 외주용역비 | 259,263,637 | 174,122,800 |
| 협회비 | 16,751,000 | 12,870,000 |
| 잡비 | 390,000 | 830,000 |
| 합 계 | 15,522,951,412 | 8,512,163,787 |
21. 영업외수익
당분기 및 전분기의 영업외수익은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 | |
|---|---|---|---|
| 금융수익 | 이자수익 | 1,225,683,009 | 717,384,156 |
| 소 계 |
1,225,683,009 | 717,384,156 | |
| 기타영업외수익 | 외환차익 | 248,345,791 | 372,863,491 |
| 외화환산이익 | 2,578,480,699 | 110,105,499 | |
| 채무면제이익 | - | 41,909,684 | |
| 정부보조금 | - | 103,333,200 | |
| 당기손익-공정가치 측정 금융자산평가이익 |
- | 41,643,835 | |
| 기타 | 373,747,789 | 81,564,180 | |
| 소 계 | 3,200,574,279 | 751,419,889 | |
| 합 계 | 4,426,257,288 | 1,468,804,045 | |
22. 영업외비용
당분기 및 전분기의 영업외비용은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 | |
|---|---|---|---|
| 금융비용 | 이자비용 | 4,492,510 | 3,436,572 |
| 소 계 | 4,492,510 | 3,436,572 | |
| 기타영업외비용 | 외환차손 | 56,678,628 | 297,620,303 |
| 외화환산손실 | 900,860 | 413,011,151 | |
| 기부금 | 11,000,000 | - | |
| 종속기업투자주식손상차손 | - | 2,166,661,500 | |
| 유형자산처분손실 | 18,480,857 | - | |
| 무형자산손상차손 | - | 9,502,009 | |
| 기타 | 103,244 | 520,593 | |
| 소 계 | 87,163,589 | 2,887,315,556 | |
| 합 계 | 91,656,099 | 2,890,752,128 | |
23. 법인세비용
법인세비용은 전체 회계연도에 대해서 예상되는 최선의 가중평균 연간법인세율의 추정에 기초하여 인식하였습니다. 추정연간유효법인세율과 법정세율의 차이는 주로 이연법인세의 실현가능성 평가 등에 기인합니다.
24. 주당손익
(1) 당분기 및 전분기의 기본주당이익의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 기본주당이익 계산에 사용된 손익 | (12,430,097,826) | 9,993,197,887 |
| 기본주당이익을 위한 가중평균유통보통주식수 | 42,149,047 | 41,890,785 |
| 기본주당손익 | (295) | 239 |
(2) 당분기 및 전분기의 희석주당이익 계산 내역은 다음과 같습니다.
| (단위: 원, 주) |
| 구 분 | 당분기(*) | 전분기(*) |
|---|---|---|
| 희석주당이익에 계산에 사용된 이익 | (11,399,038,825) | 10,795,198,386 |
| 기본주당이익 계산에 사용된 이익 | (12,430,097,826) | 9,993,197,887 |
| 주식선택권 보상비용 | 1,031,059,001 | 802,000,499 |
| 희석주당이익 산출에 사용된 가중평균유통보통주식수 | 44,670,991 | 42,080,592 |
| 기본주당이익 산출에 사용된 가중평균유통보통주식수 | 42,149,047 | 41,890,785 |
| 주식선택권 | 993,892 | 189,807 |
| 전환우선주 | 1,528,052 | - |
| 희석주당이익 | (295) | 239 |
(*) 당사는 유통되는 보통주식수나 잠재적보통주식수가 당분기 중 무상증자로 증가하여 비교표시하는 기본주당이익과 희석주당이익을 소급하여 수정하였습니다.
한편, 당분기말 현재 보유중인 잠재적보통주인 주식선택권의 행사와 전환우선주의 전환으로 인한 희석화 효과가 없으므로 당분기의 희석주당순손실은 기본주당순손실과 동일합니다.
25. 주식기준보상
당사는 경영진과 종업원에 대하여 주식기준보상제도를 시행하고 있습니다.
종업원주식선택권은 행사시점에 당사의 주식으로 전환됩니다. 종업원이 주식선택권을 부여 받을 때 지급하였거나 지급할 금액은 없습니다. 주식선택권은 배당에 대한 권리나 의결권을 가지지 않습니다. 주식선택권은 가득일로부터 만기일까지의 기간 동안에 행사될 수 있습니다.
(1) 당분기말 현재 존재하는 주식기준보상계약
| (단위: 주, 원) |
| 구 분 | 부여일 | 권리행사시작일 | 권리행사종료일 | 총 부여수량(*) | 소멸수량 | 잔존부여수량 | 미행사수량 | 행사가격(*) |
|---|---|---|---|---|---|---|---|---|
| 제14차 | 2017-09-01 | 2020-09-01 | 2023-08-31 | 120,000 | - | 120,000 | 35,000 | 5,167 원 |
| 제15차 | 2018-03-09 | 2021-03-09 | 2024-03-08 | 138,000 | 27,000 | 111,000 | 58,100 | 6,900 원 |
| 제16차 | 2018-04-23 | 2021-04-23 | 2024-04-22 | 36,000 | 9,000 | 27,000 | - | 12,167 원 |
| 제17차 | 2018-08-02 | 2021-08-02 | 2024-08-01 | 210,000 | - | 210,000 | 160,000 | 10,667 원 |
| 제18차 | 2019-03-08 | 2022-03-08 | 2025-03-07 | 141,600 | 4,500 | 137,100 | 137,100 | 12,000 원 |
| 제19차 | 2019-04-30 | 2022-04-30 | 2025-04-29 | 39,000 | 18,000 | 21,000 | 21,000 | 14,333 원 |
| 제20차 | 2019-08-05 | 2022-08-05 | 2025-08-04 | 195,000 | - | 195,000 | 195,000 | 10,700 원 |
| 제21차 | 2020-03-26 | 2023-03-26 | 2026-03-25 | 105,000 | - | 105,000 | 105,000 | 25,333 원 |
| 제22차 | 2020-04-14 | 2023-04-14 | 2026-04-13 | 181,500 | 150,000 | 31,500 | 31,500 | 28,600 원 |
| 제23차 | 2020-06-11 | 2023-06-11 | 2026-06-10 | 90,000 | - | 90,000 | 90,000 | 76,667 원 |
| 제24차 | 2021-05-03 | 2024-05-03 | 2027-05-02 | 14,500 | - | 14,500 | 14,500 | 87,450 원 |
| 합 계 | 1,270,600 | 208,500 | 1,062,100 | 847,200 | ||||
(*) 2017년 11월 23일, 2020년 7월 7일, 2021년 3월 10일 무상증자로 인하여 조정된 수량 및 행사가격입니다.
(2) 회계기간에 부여한 주식선택권의 공정가치
주식선택권의 가격은 이항옵션가격결정모형에 따라 산정되었습니다. 옵션평가를 위해 사용하는 변동성은 부여 당시 유사상장기업의 업종지수(코스닥/제약)를 기준으로변동성을 산출하였습니다.
| 구 분 | 모형 적용 변수 | |
|---|---|---|
| 부여된 선택권의 가중평균 공정가치 | 4,389.97~72,818.2 | |
| 부여일 주식가격 | 제14차~24차 | 19,800원~230,400원 |
| 기대변동성 | 9.9~60.8 | |
| 옵션만기 | 3 년 | |
| 배당수익률 | - | |
| 무위험이자율 | 1.22%~2.65% | |
(*) 무상증자 전 부여일 기준 자료입니다
(3) 보고기간 중 주식선택권의 변동
당분기 및 전분기 중 주식선택권의 변동내용은 다음과 같습니다.
| (단위: 주, 원) |
| 구 분 | 당분기(*) | 전분기 | ||
|---|---|---|---|---|
| 주식선택권 수량 | 가중평균행사가격 | 주식선택권 수량 | 가중평균행사가격 | |
| 기초 | 648,400 | 27,854 | 786,800 | 12,702 |
| 무상증자로 인한 변동 | 324,200 | 18,569 | - | - |
| 기중 부여수량 | 14,500 | 87,450 | 251,000 | 58,769 |
| 기중 권리상실분 | - | - | (100,000) | 42,900 |
| 기중 행사분 | (139,900) | 9,059 | (289,400) | 8,273 |
| 기말 | 847,200 | 21,306 | 648,400 | 27,854 |
(*) 2017년 11월 23일, 2020년 7월 7일, 2021년 3월 10일 무상증자로 인하여 조정된 수량 및 행사가격입니다.
(4) 당분기 중 행사된 주식선택권은 다음과 같습니다.
| (단위: 주, 원) |
| 구 분 | 부 여 일 | 행사수량 | 주당 행사가격 | 행사일 |
|---|---|---|---|---|
| 제14차 | 2017-09-01 | 10,000 | 5,167 원 | 2021-06-02 |
| 제15차 | 2018-03-09 | 23,000 | 6,900 원 | 2021-06-02 |
| 29,900 | 6,900 원 | 2021-09-01 | ||
| 제16차 | 2018-04-23 | 22,000 | 12,167 원 | 2021-06-02 |
| 5,000 | 12,167 원 | 2021-09-01 | ||
| 제17차 | 2018-08-03 | 50,000 | 10,667 원 | 2021-09-01 |
| 합 계 | 139,900 | |||
(5) 당분기 및 전분기 중 발생한 주식선택권 관련 보상원가의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 총 보상원가 | 8,291,255,026 | 7,765,853,572 |
| 당기보상원가 | 1,031,059,001 | 802,000,499 |
| 잔여보상원가 | 2,033,073,767 | 2,806,064,814 |
(6) 보고기간말 현재 존속하는 주식선택권
당분기말 현재 발행되어 있는 주식옵션의 가중평균행사가격이 21,306원(전기말: 27,854원)이며, 가중평균 잔여계약 만기는 3.63년(전기말: 4.20년)입니다.
26. 비용의 성격별 분류
당분기 및 전분기 중 발생한 비용의 성격별로 분류한 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 종업원급여 | 4,138,731,872 | 3,366,148,733 |
| 주식기준보상 | 1,031,059,001 | 802,000,499 |
| 퇴직급여 | 360,234,330 | 259,944,546 |
| 연구관련 시약 및 소모품 구입 | 1,965,877,580 | 3,069,329,378 |
| 위탁연구용역비 | 13,192,204,146 | 3,400,039,536 |
| 지급수수료 | 849,294,161 | 1,146,368,627 |
| 세금과공과 | 187,214,280 | 133,097,930 |
| 임차료 | 27,459,519 | 28,633,855 |
| 감가상각비 | 934,273,625 | 882,697,019 |
| 무형자산상각비 | 57,897,591 | 35,580,727 |
| 기타비용 | 1,360,300,995 | 750,385,290 |
| 합 계 | 24,104,547,100 | 13,874,226,140 |
27. 특수관계자와의 거래
(1) 당분기말 및 전기말 현재 당사의 특수관계자 현황은 다음과 같습니다.
| 구 분 | 당분기말(*) | 전기말 |
|---|---|---|
| 종속기업 | - | ㈜알토스바이오사이언스 |
| ㈜엘에스메디텍 |
㈜엘에스메디텍 |
|
| ㈜세레스에프앤디 | ㈜세레스에프앤디 | |
| ㈜알토스바이오로직스 |
㈜알토스바이오로직스 |
(*) 당기 중 (주)알토스바이오사이언스는 ㈜LS메디텍에 흡수 합병되었습니다.
(2) 당분기 및 전기 중 특수관계자와의 채권채무 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 거래구분 | 당분기 | 전 기 | |
|---|---|---|---|---|
| 종속기업 | ㈜세레스에프앤디 | 대여금 | - | 3,000,000,000 |
| 종속기업 | ㈜세레스에프앤디 | 미수수익 | - | 335,636,165 |
| 종속기업 | ㈜알토스바이오로직스 | 계약부채 | 2,194,731,978 | - |
(3) 당분기 및 전분기 중 특수관계자와의 거래내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 거래구분 | 당분기 | 전분기 | |
|---|---|---|---|---|
| 종속기업 | ㈜세레스에프앤디 | 이자수익 | - | 103,594,519 |
| 종속기업 | ㈜알토스바이오로직스 | 용역매출 | 405,268,022 | - |
(4) 당분기 및 전분기 중 주요 경영진에 대한 보상내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 |
|---|---|---|
| 단기종업원급여 | 1,464,367,590 | 1,290,877,731 |
| 퇴직급여 | 134,803,570 | 91,006,050 |
| 주식기준보상 | 738,462,074 | 536,400,101 |
| 합 계 | 2,337,633,234 | 1,918,283,882 |
28. 우발채무 및 주요 약정사항
(1) 당분기말 현재 당사가 금융기관 등으로부터 제공받은 지급보증의 내역은 다음과 같습니다.
| (단위: 원) |
| 금융기관 | 보증금액 | 보증내용 |
|---|---|---|
| 서울보증보험 | 51,300,000 | 정부 및 지방자치단체 보조금 반환보증 |
(2) 당사는 종속기업인 (주)세레스에프앤디 및 (주)알토스바이오로직스의 상환전환우선주 및 전환우선주 투자자와의 약정에 의해서 투자자와의 동의없이는 해당 종속기업에 대한 보유 주식을 처분할 수 없습니다. 또한 당사가 해당 종속기업에 대한 보유 주식을 처분하는 경우 투자자는 공동매도권을 행사할 권리를 가지며, 투자자가 공동매도권을 행사하는 경우 지분 양수 예정자가 당사 및 투자자로부터 당사와 투자자의 지분(주식 및 주식연계사채) 비율에 따라 지분을 양수하지 않는 한, 당사는 해당 종속기업에 대한 보유 주식을 처분할 수 없습니다.
29. 위험관리
(1) 자본위험관리
당사는 부채와 자본 잔액의 최적화를 통하여 주주이익을 극대화시키는 동시에 계속기업으로서 지속될 수 있도록 자본을 관리하고 있습니다. 당사는 자본관리지표로 부채비율을 이용하고 있으며, 이 비율은 부채를 자본으로 나누어 산출하고 있습니다.
당분기말 및 전기말 현재의 부채비율은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 |
|---|---|---|
| 부채(A) | 7,930,708,884 | 6,905,620,194 |
| 자본(B) | 172,349,486,189 | 108,460,560,495 |
| 부채비율(A/B) | 4.60% | 6.37% |
(2) 금융자산, 금융부채 및 자본의 각 범주별로 채택한 주요 회계정책 및 방법(인식기준과 측정기준 그리고 수익과 비용)은 주석 2에 상세히 공시되어 있으며, 금융자산과금융부채의 범주별 장부금액은 주석 5에서 작성하였습니다.
(3) 당분기말 현재 공정가치로 후속측정하는 금융자산과 공정가치로 후속측정하는 금융부채는 없습니다.
(4) 금융위험관리
당사는 금융상품과 관련하여 시장위험(이자율변동위험, 환율변동위험), 신용위험, 유동성위험, 가격위험과 같은 다양한 금융위험에 노출되어 있습니다. 당사의 위험관리는 당사의 재무적 성과에 영향을 미치는 잠재적 위험을 식별하여 당사가 허용가능한 수준으로 감소, 제거 및 회피하는 것을 그 목적으로 하고 있습니다.
1) 이자율변동위험
당사의 이자율변동위험은 주로 변동이자부 차입금에 연관되어 있으며, 이와 관련된 이자비용은 이자율위험에 노출되어 있습니다. 당분기말 및 전기말 현재 당사가 부담하고 있는 변동이자부 차입금은 없습니다.
2) 환율변동위험
당사는 용역매출 등과 관련하여 주로 USD의 환율변동위험에 노출되어 있으며, 내부적으로 환율변동에 따른 환율변동위험을 정기적으로 측정하고 있습니다.
당분기말 및 전기말 현재 당사의 외화금융자산 및 외화금융부채의 내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | ||||
|---|---|---|---|---|---|---|
| 외화금액 | 원화장부금액 | 외화금액 | 원화장부금액 | |||
| 현금및현금성자산 | USD | 3,356,083.57 | 3,976,623,422 | USD | 1,232,037.26 | 1,340,456,539 |
| 단기금융상품 | USD | 24,000,000.00 | 28,437,600,000 | USD |
23,000,000.00 | 25,024,000,000 |
| 매출채권및기타채권 | USD | - | - | USD | 526,152.88 | 572,454,333 |
| 외화금융자산 합계 | 32,414,223,422 | 26,936,910,872 | ||||
| 미지급비용 | USD | - | - | USD | 95,358.00 | 103,749,504 |
| 미지급금 | USD | 57,068.56 | 67,620,537 | USD | - | - |
| EUR | 222,800.00 | 306,196,268 | EUR | - | - | |
| CHF | 6,489.00 | 8,226,884 | CHF | - | - | |
| 외화금융부채 합계 | 382,043,689 | 103,749,504 | ||||
당분기말 및 전기말 현재 관련 통화에 대한 환율이 10% 변동 시 세전이익에 미치는 영향은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기말 | 전기말 | ||
|---|---|---|---|---|
| 10% 상승시 | 10% 하락시 | 10% 상승시 | 10% 하락시 | |
| 세전손익 | 3,203,217,973 | (3,203,217,973) | 2,683,316,137 | (2,683,316,137) |
3) 신용위험
신용위험은 계약상대방이 계약서상의 의무를 불이행하여 당사에 재무적 손실을 미칠위험을 의미합니다. 신용위험은 보유하고 있는 수취채권 및 확정계약을 포함한 거래처에 대한 신용위험 뿐 아니라 현금및현금성자산, 은행 및 금융기관 예치금으로부터 발생하고 있습니다. 은행 및 금융기관의 경우 신용등급이 우수한 금융기관과 거래하고 있으므로 금융기관으로부터의 신용위험은 제한적입니다.
일반거래처의 경우 고객의 재무상태, 과거 경험 등 기타 요소들을 고려하여 신용을 평가하게 됩니다. 당사는 거래 상대방에 대한 개별적인 위험 한도 관리정책은 보유하고 있지 않습니다.
당사는 기대신용손실 모형이 적용되는 다음의 금융자산을 보유하고 있습니다.
· 재화 및 용역의 제공에 따른 매출채권
· 상각후원가로 측정하는 기타금융자산
당사는 금융자산에 대해 전체 기간 기대신용손실을 손실충당금으로 인식하는 간편법을 적용합니다. 기대신용손실을 측정하기 위해 매출채권은 신용위험 특성과 연체일을 기준으로 구분하였습니다. 기초와 기말의 매출채권에 대한 손실충당금은 없습니다.
4) 유동성위험
유동성위험관리에 대한 궁극적인 책임은 당사의 단기 및 중장기 자금조달과 유동성관리규정을 적절하게 관리하기 위한 기본정책을 수립하는 이사회에 있습니다. 당사는 충분한 적립금과 차입한도를 유지하고 예측현금흐름과 실제현금흐름을 계속하여 관찰하고 금융자산과 금융부채의 만기구조를 대응시키면서 유동성위험을 관리하고 있습니다.
다음 표는 당사의 비파생금융부채에 대한 계약상 잔존만기를 상세하게 나타내고 있습니다. 해당 표는 금융부채의 할인되지 않은 현금흐름을 기초로 당사가 지급하여야 하는 가장 빠른 만기일에 근거하여 작성되었으며, 원금 및 이자의 현금흐름을 모두 포함하고 있습니다. 이자의 현금흐름이 변동이자율에 근거하는 경우, 할인되지 않은 현금흐름은 당분기말 및 전기말 현재의 수익률곡선에 근거하여 도출되었습니다.
| (당분기말) | (단위: 원) |
| 구 분 | 가중평균 유효이자율 |
1년 미만 | 1년 ~ 5년 | 5년 초과 | 합 계 |
|---|---|---|---|---|---|
| 리스부채 | 2.49%~4.02% | 40,060,735 | 37,562,499 | - | 77,623,234 |
| 기타금융부채 | - | 814,490,515 | 853,420,972 | - | 1,667,911,487 |
| 합계 | - | 854,551,250 | 890,983,471 | - | 1,745,534,721 |
| (전기말) | (단위: 원) |
| 구 분 | 가중평균 유효이자율 |
1년 미만 | 1년 ~ 5년 | 5년 초과 | 합 계 |
|---|---|---|---|---|---|
| 리스부채 | 3.35%~4.02% | 69,489,337 | 40,326,280 | - | 109,815,617 |
| 기타금융부채 | - | 1,812,268,937 | 788,443,728 | - | 2,600,712,665 |
| 합계 | - | 1,881,758,274 | 828,770,008 | - | 2,710,528,282 |
5) 가격위험
당사는 상장주식을 보유하고 있지 않음에 따라 가격위험에 노출되어 있지 않습니다.
30. 현금흐름 관련사항
(1) 당분기 및 전분기 중 영업활동으로부터 창출된 현금흐름의 조정내역은 다음과 같습니다.
| (단위: 원) |
| 구 분 | 당분기 | 전분기 | ||
|---|---|---|---|---|
| 1. 현금유출이 없는 비용 가산 | 2,048,472,073 | 4,696,632,299 | ||
| 이자비용 | 4,492,510 | 2,760,670 | ||
| 외화환산손실 | 900,860 | 413,011,151 | ||
| 감가상각비 | 934,273,625 | 882,697,019 | ||
| 무형자산상각비 | 57,897,591 | 35,580,727 | ||
| 주식기준보상 | 1,031,059,001 | 802,000,499 | ||
| 무형자산감액손실 | - | 9,502,009 | ||
| 종속기업투자주식손상차손 | - | 2,166,661,500 | ||
| 유형자산처분손실 | 18,480,857 | - | ||
| 현재가치할인차금 | 1,367,629 | 14,250,014 | ||
| 법인세비용(수익) | - | 370,168,710 | ||
| 2. 현금유입이 없는 수익 차감 | (3,804,163,708) | (911,043,174) | ||
| 이자수익 | (1,225,683,009) | (717,384,156) | ||
| 외화환산이익 | (2,578,480,699) | (110,105,499) | ||
| 채무면제이익 | - | (41,909,684) | ||
| 금융자산평가이익 | - | (41,643,835) | ||
| 3. 영업활동으로 인한 자산ㆍ부채의 변동 | 1,844,760,872 | (2,438,454,101) | ||
| 매출채권의 감소(증가) | 509,204,542 | - | ||
| 기타채권의 감소(증가) | (64,161,857) | (26,854,190) | ||
| 기타자산의 증가(감소) | 340,054,760 | 70,048,805 | ||
| 매입채무의 증가(감소) | - | (329,260,000) | ||
| 계약부채의 증가(감소) | 1,830,151,915 | (1,739,915,820) | ||
| 기타금융부채의 증가(감소) | (930,418,824) | (424,902,896) | ||
| 기타부채의 증가(감소) | 159,930,336 | 12,430,000 | ||
(2) 당분기 및 전분기 중 현금의 유입과 유출이 없는 거래 중 중요한 거래의 내용은 다음과 같습니다.
| (단위: 원) |
| 거 래 내 용 | 당분기 | 전분기 |
|---|---|---|
| 주식매입선택권 행사 | 256,043,299 | 362,547,670 |
| 무상증자 | 7,192,227,500 | 6,997,975,000 |
| 대여금의 유동성 대체 | 3,000,000,000 | - |
| 사용권자산 및 리스부채의 인식 | 57,802,977 | 138,603,171 |
| 유형자산 취득관련 미지급금 증가 | 7,416,200 | - |
31. 주요기술이전 계약
(1) 당사는 다국적 기업 A사와 2019년 12월 2일, 다국적 기업 B사와 2020년 6월 24일, 다국적 제약사 C사와 2021년 1월 7일자로 당사가 보유한 인간 히알루로니다제 원천 기술(ALT-B4)에 대한 기술이전 계약을 각각 체결하였습니다. A, B사와 기술이전 계약은 비독점적 라이센스계약, C사와의 기술이전 계약은 독점적 라이센스 계약으로 인간히알루로니다제 원천기술로 바이오의약품의 정맥주사를 피하주사로 바꾸어 주는 원천 기술입니다.
2019년 12월 2일 A사와의 계약에 따라 반환조건 없는 계약금(Upfront payment) USD 13,000,000을 2019년에 일시에 수령하였으며, 2020년에 USD 3,000,000 추가 수령액을 포함하여 USD 5,052,631을 총 수익으로 인식하였습니다.
또한 2020년 6월 24일 B사의 계약에 따라 반환조건 없는 계약금(Upfront payment) USD 16,000,000을 2020년에 두번에 나눠서 수령하였으며, 2021년 1월 7일 Intas Pharmaceuticals Ltd. 사의 계약에 따라 반환조건 없는 계약금(Upfront payment) USD 6,000,000을 일시에 수령하였습니다. 동 계약 모두 계약과 동시에 재화의 공급과 수행의무가 종료되어 수익으로 인식하였습니다.
당사는 세 건의 계약 관련하여 상대회사에서 임상진행 및 각 국가별 허가 및 판매 이정표를 달성하면 마일스톤 금액(Milestone payment)을 수령할 수 있습니다.
(2) 당사는 종속기업인 ㈜알토스바이오로직스와 2020년 12월10일자로 ALT-L9의 임상과 판매에 대한 라이선스를 부여하는 계약(라이선스계약)을 체결하였습니다.
당사는 동 계약의 체결직후인 2020년 1월 7일자로 종속기업인 ㈜알토스바이오로직스로 부터 기술료로 20억을 수령하였으며, 기술이전과 라이선스의 권리를 이전하는 기간동안 동 기술료의 수익을 기간배분하여 인식하고 있습니다.
(3) ㈜알토스바이오로직스는 2021년 3월3일자로 ALT-L9의 국내 판매에 대한 라이선스를 ㈜한림MS에 부여하는 계약(공급 및 판매계약서)을 체결하였습니다.
㈜알토스바이오로직스는 계약의 체결과 동시에 ㈜한림MS로 부터 기술료(계약금)로 20억을 수령하였으며, ALT-L9의 품목허가시까지 기술이전 기간동안의 동 기술료의 수익을 기간배분하여 인식하고 있습니다.
당사는 ㈜알토스바이오로직스와 체결한 계약(라이선스계약)의 제3자 라이선스 수익배분 조항(제9조4항)에 따라, ㈜알토스바이오로직스가 ㈜한림MS에 제3자 라이선스 부여로 수령하는 대금의 30%에 해당하는 금액인 6억원을 ㈜알토스바이오로직스로부터 수령하였으며, 제3자 라이선스로 발생하는 수익을 기술이전과 라이선스의 권리를 이전하는 기간동안의 수익으로 기간배분하여 인식하고 있습니다.
6. 배당에 관한 사항
가. 배당에 관한 사항
당사의 정관에 기재된 배당에 관한 사항은 다음과 같습니다.
|
제 13 조 (신주의 배당기산일) 회사가 유상증자, 무상증자 및 주식배당에 의하여 발행한 신주에 대한 이익의 배당에 관하여는 신주를 발행한 때가 속하는 영업 연도의 직전영업년도말에 발행된 것으로 본다.
① 이익배당은 금전 또는 금전 외의 재산으로 할 수 있다. ② 이익의 배당을 주식으로 하는 경우 회사가 수종의 주식을 발행한 때에는 주주총회의 결의로 그와 다른 종류의 주식으로도 할 수 있다. ③ 제1항의 배당은 매 결산기말 현재의 주주명부에 기재된 주주 또는 등록된 질권자에게 지급한다. ④ 이익배당은 주주총회의 결의로 정한다. 제 58 조 (배당금지급청구권의 소멸시효) ② 제1항의 시효의 완성으로 인한 배당금은 이 회사에 귀속한다. |
나. 주요배당지표
| 구 분 | 주식의 종류 | 당기 | 전기 | 전전기 |
|---|---|---|---|---|
| 제14기 3분기 | 제13기 | 제12기 | ||
| 주당액면가액(원) | 500 | 500 | 500 | |
| (연결)당기순이익(백만원) | -14,201 | -970 | -705 | |
| (별도)당기순이익(백만원) | -12,430 | 4,062 | 1,754 | |
| (연결)주당순이익(원) | -337 | -35 | -26 | |
| 현금배당금총액(백만원) | - | - | - | |
| 주식배당금총액(백만원) | - | - | - | |
| (연결)현금배당성향(%) | - | - | - | |
| 현금배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주식배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주당 현금배당금(원) | - | - | - | - |
| - | - | - | - | |
| 주당 주식배당(주) | - | - | - | - |
| - | - | - | - | |
주) 주당 순이익은 기본주당 순이익 입니다.
※ 기본주당이익 산출근거는 III. 재무에 관한 사항의 3.연결재무제표 주석 중 주당이익 항목을 참조하시기 바랍니다.
다. 과거 배당 이력
| (단위: 회, %) |
| 연속 배당횟수 | 평균 배당수익률 | ||
|---|---|---|---|
| 분기(중간)배당 | 결산배당 | 최근 3년간 | 최근 5년간 |
| - | - | - | - |
※ 당사는 최근 5년간 배당을 지급하지 않아 과거 배당이력 산출이 불가합니다.
7. 증권의 발행을 통한 자금조달에 관한 사항
7-1. 증권의 발행을 통한 자금조달 실적
| [지분증권의 발행 등과 관련된 사항] |
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 원, 주) |
| 주식발행 (감소)일자 |
발행(감소) 형태 |
발행(감소)한 주식의 내용 | ||||
|---|---|---|---|---|---|---|
| 종류 | 수량 | 주당 액면가액 |
주당발행 (감소)가액 |
비고 | ||
| 2008.05.13 | 유상증자(제3자배정) | 보통주 | 20,000 | 5,000 | 5,000 | 설립 |
| 2009.02.13 | 유상증자(제3자배정) | 보통주 | 15,000 | 5,000 | 100,000 | - |
| 2010.07.30 | 유상증자(제3자배정) | 상환전환우선주 | 5,001 | 5,000 | 200,000 | - |
| 2011.01.18 | 주식분할 | 보통주 | 315,000 | 500 | - | 액면분할(5,000원→500원) |
| 2011.01.18 | 주식분할 | 상환전환우선주 | 45,009 | 500 | - | 액면분할(5,000원→500원) |
| 2012.01.03 | 무상증자 | 보통주 | 525,000 | 500 | 500 | 150% 무상증자 |
| 2012.01.03 | 무상증자 | 상환전환우선주 | 75,015 | 500 | 500 | 150% 무상증자 |
| 2013.01.26 | 유상증자(제3자배정) | 상환전환우선주 | 13,000 | 500 | 23,000 | - |
| 2013.03.11 | 무상증자 | 보통주 | 1,750,000 | 500 | 500 | 200% 무상증자 |
| 2013.03.11 | 무상증자 | 상환전환우선주 | 276,050 | 500 | 500 | 200% 무상증자 |
| 2013.09.09 | 전환권행사 | 보통주 | 60,000 | 500 | 500 | 상환전환우선주의 보통주 전환 |
| 2014.02.21 | 주식매수선택권행사 | 보통주 | 18,000 | 500 | 2,005 | - |
| 2014.02.22 | 유상증자(제3자배정) | 보통주 | 225,888 | 500 | 19,703 | - |
| 2014.04.18 | 주식매수선택권행사 | 보통주 | 6,000 | 500 | 2,667 | - |
| 2014.04.23 | 무상증자 | 보통주 | 1,467,445 | 500 | 500 | 50% 무상증자 |
| 2014.04.23 | 무상증자 | 상환전환우선주 | 177,037 | 500 | 500 | 50% 무상증자 |
| 2014.07.18 | 전환권행사 | 보통주 | 50,000 | 500 | 500 | 상환전환우선주의 보통주 전환 |
| 2014.08.19 | 전환권행사 | 보통주 | 200,000 | 500 | 500 | 상환전환우선주의 보통주 전환 |
| 2014.12.06 | 유상증자(일반공모) | 보통주 | 927,000 | 500 | 26,000 | 코스닥 상장 공모증자 |
| 2015.02.02 | 전환권행사 | 보통주 | 281,112 | 500 | 500 | 상환전환우선주의 보통주 전환 |
| 2015.02.02 | 주식매수선택권행사 | 보통주 | 500 | 500 | 2,222 | - |
| 2015.03.30 | 주식매수선택권행사 | 보통주 | 34,000 | 500 | 3,267 | - |
| 2015.04.07 | 주식매수선택권행사 | 보통주 | 10,000 | 500 | 2,222 | - |
| 2016.04.01 | 주식매수선택권행사 | 보통주 | 26,500 | 500 | 4,000 | - |
| 2016.06.22 | 주식매수선택권행사 | 보통주 | 16,500 | 500 | 4,000 | - |
| 2016.09.08 | 유상증자(일반공모) | 보통주 | 279,720 | 500 | 35,750 | - |
| 2016.12.05 | 주식매수선택권행사 | 보통주 | 22,000 | 500 | 5,333 | - |
| 2017.01.05 | 주식매수선택권행사 | 보통주 | 43,500 | 500 | 5,333 | - |
| 2017.11.02 | 주식매수선택권행사 | 보통주 | 12,000 | 500 | 5,333 | - |
| 2017.12.08 | 무상증자 | 보통주 | 6,305,165 | 500 | 0 | 100% 무상증자 |
| 2018.04.20 | 유상증자(제3자배정) | 전환우선주 | 1,090,280 | 500 | 29,350 | - |
| 2018.05.16 | 주식매수선택권행사 | 보통주 | 32,900 | 500 | 20,645 | - |
| 2019.03.20 | 주식매수선택권행사 | 보통주 | 12,900 | 500 | 20,645 | - |
| 2019.03.20 | 주식매수선택권행사 | 보통주 | 25,000 | 500 | 18,560 | - |
| 2019.05.02 | 전환권행사 | 보통주 | 578,779 | 500 | 29,013 | 전환우선주의 보통주 전환 |
| 2019.05.21 | 전환권행사 | 보통주 | 317,342 | 500 | 29,013 | 전환우선주의 보통주 전환 |
| 2019.07.08 | 주식매수선택권행사 | 보통주 | 12,700 | 500 | 20,645 | - |
| 2019.07.08 | 주식매수선택권행사 | 보통주 | 100,000 | 500 | 18,950 | - |
| 2019.09.17 | 전환권행사 | 보통주 | 34,466 | 500 | 29,013 | 전환우선주의 보통주 전환 |
| 2019.10.24 | 전환권행사 | 보통주 | 113,401 | 500 | 29,013 | 전환우선주의 보통주 전환 |
| 2019.11.11 | 전환권행사 | 보통주 | 58,932 | 500 | 29,013 | 전환우선주의 보통주 전환 |
| 2020.04.08 | 주식매수선택권행사 | 보통주 | 21,500 | 500 | 20,645 | - |
| 2020.04.08 | 주식매수선택권행사 | 보통주 | 6,500 | 500 | 18,560 | - |
| 2020.04.08 | 주식매수선택권행사 | 보통주 | 71,200 | 500 | 14,500 | - |
| 2020.07.24 | 무상증자 | 보통주 | 13,995,950 | 500 | - | 100% 무상증자 |
| 2020.09.09 | 주식매수선택권행사 | 보통주 | 28,000 | 500 | 10,323 | - |
| 2020.09.09 | 주식매수선택권행사 | 보통주 | 13,000 | 500 | 9,280 | - |
| 2020.09.09 | 주식매수선택권행사 | 보통주 | 50,000 | 500 | 7,750 | - |
| 2020.11.13 | 유상증자(제3자배정) | 전환우선주 | 203,385 | 500 | 147,500 | - |
| 2021.01.08 | 유상증자(제3자배정) | 전환우선주 | 482,625 | 500 | 155,400 | - |
| 2021.03.25 | 무상증자 | 보통주 | 14,041,450 | 500 | - | 50% 무상증자 |
| 2021.03.25 | 무상증자 | 전환우선주 | 343,005 | 500 | - | 50% 무상증자 |
| 2021.06.02 | 주식매수선택권행사 | 보통주 | 10,000 | 500 | 5,167 | - |
| 2021.06.02 | 주식매수선택권행사 | 보통주 | 23,000 | 500 | 6,900 | - |
| 2021.06.02 | 주식매수선택권행사 | 보통주 | 22,000 | 500 | 12,167 | - |
| 2021.09.01 | 주식매수선택권행사 | 보통주 | 29,900 | 500 | 6,900 | - |
| 2021.09.01 | 주식매수선택권행사 | 보통주 | 5,000 | 500 | 12,167 | - |
| 2021.09.01 | 주식매수선택권행사 | 보통주 | 50,000 | 500 | 10,667 | - |
| [채무증권의 발행 등과 관련된 사항] |
채무증권 발행실적
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 원, %) |
| 발행회사 | 증권종류 | 발행방법 | 발행일자 | 권면(전자등록)총액 | 이자율 | 평가등급 (평가기관) |
만기일 | 상환 여부 |
주관회사 |
|---|---|---|---|---|---|---|---|---|---|
| - | - | - | - | - | - | - | - | - | - |
| - | - | - | - | - | - | - | - | - | - |
| 합 계 | - | - | - | - | - | - | - | - | - |
※ 당사는 공시기준일 현재 채무증권 발행내역이 없습니다.
기업어음증권 미상환 잔액
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
1년초과 2년이하 |
2년초과 3년이하 |
3년 초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | |
※ 당사는 공시기준일 현재 기업어음증권 발행 및 미상환내역이 없습니다.
단기사채 미상환 잔액
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
합 계 | 발행 한도 | 잔여 한도 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
※ 당사는 공시기준일 현재 단기사채 발행 및 미상환내역이 없습니다.
회사채 미상환 잔액
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
※ 당사는 공시기준일 현재 회사채 발행 및 미상환내역이 없습니다.
신종자본증권 미상환 잔액
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 5년이하 |
5년초과 10년이하 |
10년초과 15년이하 |
15년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
※ 당사는 공시기준일 현재 신종자본증권 발행 및 미상환내역이 없습니다.
조건부자본증권 미상환 잔액
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | - | |
※ 당사는 공시기준일 현재 조건부자본증권 발행 및 미상환내역이 없습니다.
7-2. 증권의 발행을 통해 조달된 자금의 사용실적
가. 공모자금의 사용내역
해당사항 없음
나. 사모자금의 사용내역
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 백만원) |
| 구 분 | 회차 | 납입일 | 주요사항보고서의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | ||||
| 전환우선주 제3자배정 유상증자 |
3 | 2020.11.12 | 개발 제품 자체 생산 공장 건설을 위한 시설 투자비 주요 Pipeline 임상 및 연구개발 등 운영자금 |
29,999 | 시설자금 및 운영자금 |
13,999 | 주석참조 |
| 전환우선주 제3자배정 유상증자 |
4 | 2021.01.07 | 개발 제품 자체 생산 공장 건설을 위한 시설 투자비 주요 Pipeline 임상 및 연구개발 등 운영자금 |
75,000 | 시설자금 및 운영자금 |
8,000 | 주석참조 |
| 합 계 | - | - | - | 104,999 | - | 21,999 | 미사용자금의 정기예금운용 (83,000백만원) |
(주) 전환우선주 유상증자 자금사용 내역 (단위 : 백만원)
| 구 분 | 제3회차 전환우선주 유상증자 |
제4회차 전환우선주 유상증자 |
합 계 |
| 정기예금운용(미사용자금) | 16,000 | 67,000 | 83,000 |
| 시설자금 | 8,377 | 926 | 9,304 |
| 운영자금 | 5,622 | 7,074 | 12,696 |
| 채무상환자금 | - | - |
- |
| 타법인증권취득자금 | - | - |
- |
| 기타 | - | - |
- |
| 합계 | 29,999 | 75,000 | 104,999 |
미사용자금의 운용내역
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 백만원) |
| 종류 | 금융상품명 | 운용금액 | 계약기간 | 실투자기간 |
|---|---|---|---|---|
| 예ㆍ적금 | 하나은행 정기예금 | 3,000 | 2021.02 ~ 2022.02 | 7.8개월 |
| 예ㆍ적금 | 하나은행 정기예금 | 5,000 | 2021.07 ~ 2022.04 | 2.1개월 |
| 예ㆍ적금 | 하나은행 정기예금 | 22,000 | 2021.04 ~ 2022.04 | 5.7개월 |
| 예ㆍ적금 | 우리은행 정기예금 | 3,000 | 2021.07 ~ 2022.04 | 2.1개월 |
| 예ㆍ적금 | 우리은행 정기예금 | 10,000 | 2021.04 ~ 2022.04 | 5.6개월 |
| 예ㆍ적금 | 한국투자 정기예금 | 5,000 | 2020.10 ~ 2021.10 | 11.9개월 |
| 예ㆍ적금 | 하나은행 정기예금 | 5,000 | 2020.10 ~ 2021.10 | 11.4개월 |
| 예ㆍ적금 | 우리은행 정기예금 | 10,000 | 2020.11 ~ 2021.11 | 10.5개월 |
| 예ㆍ적금 | 하나은행 정기예금 | 10,000 | 2020.11 ~ 2021.11 | 10.5개월 |
| 예ㆍ적금 | 한국투자 정기예금 | 5,000 | 2020.11 ~ 2021.11 | 10.5개월 |
| 예ㆍ적금 | 하나은행 정기예금 | 5,000 | 2020.12 ~ 2021.12 | 9.4개월 |
| 계 | 83,000 | - | ||
8. 기타 재무에 관한 사항
가. 재무제표 재작성 등 유의사항
(1) (연결)재무제표를 재작성한 경우 재작성사유, 내용 및 (연결)재무제표에 미치는 영향
종속회사인 (주)알토스바이오로직스가 2020년 12월 16일에 발행한 1차 전환우선주는 투자자에게 부여된 주식매수청구권과 전환가액 조정 조항이 자본의 인식 요건을 충족하지 못하여 전기말 재무제표 상 자본에서 금융부채로 재분류하였습니다.
전기말 전환우선주의 내역
|
구 분 |
제1차 전환우선주 |
|
발행일 |
2020년 12월 16일 |
|
발행주식수(최초 발행시) |
193,750주 |
|
1주당 발행가액(최초 발행시) |
160,000원 |
|
총발행가액(최초발행시) |
31,000,000,000원 |
|
전환대상 및 전환비율 |
보통주와 1:1로 전환가능 |
|
전환가액 조정 |
전환가액을 하회하는 발행가액으로 |
|
전환권 행사기간 |
발행일 익일로부터 존속기간 내 |
|
투자자의 주식매수청구권 |
투자금의 목적과 다른 사용, 계약사항 위배등의 |
제1차 전환우선주의 금융상품 재분류(자기자본에서 금융부채로)에 따른 직전 사업년도말 연결재무제표에 미치는 영향은 아래와 같습니다.
|
구 분 |
전기말(변경후) |
전기말(변경전) |
|
기초장부금액 |
- |
- |
|
1차CPS발행(우선주자본금) |
- |
96,875,000 |
|
1차CPS발행(주식발행초과금) |
- |
30,903,125,000 |
|
우선주자본금차감 |
(96,875,000) |
- |
|
주식발행초과금차감 |
(30,903,125,000) |
- |
|
전환우선주부채증가 |
31,000,000,000 |
- |
|
기말장부금액 |
31,000,000,000 |
31,000,000,000 |
|
금융상품의 분류 |
금융부채 |
자기지분상품 |
(2) 최근 3사업연도 중 합병, 분할, 자산양수도 또는 영업양수도 사항
- 해당 사항은 없습니다.
(3) 자산유동화와 관련한 자산매각의 회계처리 및 우발채무 등에 관한 사항
- 해당 사항은 없습니다.
(4) 재무제표 이용에 유의할 사항
당사의 재무제표는 한국채택국제회계기준에 따라 작성되었습니다. 한국채택국제회계기준은 국제회계기준위원회("IASB")가 발표한 기준서와 해석서 중 대한민국이 채택한 내용을 의미합니다.
한국채택국제회계기준은 재무제표 작성시 중요한 회계추정의 사용을 허용하고 있으며, 회계정책을 적용함에 있어 경영진의 판단을 요구하고 있습니다. 보다 복잡하고 높은 수준의 판단이 요구되는 부분이나 중요한 가정 및 추정이 요구되는 부분은 본 보고서의 III. 재무에 관한 사항 중 3. 연결재무제표 주석 및 5. 재무제표 주석을 참고해 주시기 바랍니다
나. 대손충당금 설정 현황
(1) 계정과목별 대손충당금 설정내역
(단위 : 천원)
| 구 분 | 계정과목 | 채권금액 | 대손충당금 | 장부금액 | 대손충당금 설정률 |
| 2021년 3분기 (제14기) |
외상매출금 | 1,527,557 | -3,769 | 1,523,788 | 0.25% |
| 받을어음 | 1,335,505 | 0 | 1,335,505 | 0.00% | |
| 미수금 | 742,069 | - | 742,069 | 0.00% | |
| 미수수익 | 1,225,892 | - | 1,225,892 | 0.00% | |
| 합계 | 4,831,022 | -3,769 | 4,827,253 | 0.08% | |
| 2020년 (제13기) |
외상매출금 | 1,564,047 | -7,827 | 1,556,219 | 0.50% |
| 받을어음 | - | - | - | 0.00% | |
| 미수금 | 770,440 | - | 770,440 | 0.00% | |
| 미수수익 | 366,018 | - | 366,018 | 0.00% | |
| 합계 | 2,700,505 | -7,827 | 2,692,677 | 0.29% | |
| 2019년 (제12기) |
외상매출금 | 521,629 | -2,871 | 518,759 | 0.55% |
| 받을어음 | 482,097 | -4,821 | 477,276 | 1.00% | |
| 미수금 | 532,392 | - | 532,392 | 0.00% | |
| 미수수익 | 308,565 | - | 308,565 | 0.00% | |
| 합계 | 1,844,683 | -7,692 | 1,836,992 | 0.42% |
(2) 대손충당금 변동현황
(단위 : 천원)
| 구 분 | 2021 3분기 (제14기) |
2020년 (제13기) |
2019년 (제12기) |
| 1. 기초 대손충당금 잔액합계 | -7,827 | -7,692 | -14,813 |
| 2. 순대손처리액(①-②±③) | - | - | - |
| ① 대손처리액(상각채권액) | - | - | - |
| ② 상각채권회수액 | - | - | - |
| ③ 기타증감액 | - | - | - |
| 3. 대손상각비 계상(환입)액 | 4,058 | -136 | 7,121 |
| 4. 기말 대손충당금 잔액합계 | -3,769 | -7,827 | -7,692 |
(3) 매출채권관련 대손충당금 설정방침
연결실체의 평균 신용공여기간은 60일입니다. 대금청구일로부터 최초 60일 동안은 매출채권에 대한 별도의 대손충당금을 설정하지 않고 있으며, 60일 초과 경과 매출채권에 대해서는 거래상대방의 과거 채무불이행 경험 및 현재의 재무상태 분석에 근거하여 결정된 미회수 추정금액을 대손충당금으로 설정하고 있습니다.
(4) 기준일 현재 경과기간별 매출채권잔액 현황
(단위 : 천원)
| 구분 | 6월 이하 | 6월 초과 1년이하 | 1년 초과 | 계 | |
| 금액 | 일반 | 2,859,293 | - | - | 2,859,293 |
| 특수관계자 | - | - | - | - | |
| 계 | 2,859,293 | - | - | 2,859,293 | |
| 구성비율 | 100.00% | - | - | 100.00% | |
다. 재고자산 현황
(1) 재고자산의 보유현황
(단위 : 천원,%)
| 계정과목 | 2021년 (제14기 3분기) |
2020년 (제13기) |
2019년 (제12기) |
비고 |
| 상품 | 362,117 | 204,470 | 366,236 | - |
| 제품 | - | - | - | - |
| 원재료 | 165,599 | 181,816 | 166,447 | - |
| 재공품 | 419,397 | 73,377 | 348,892 | |
| 합 계 | 947,114 | 459,663 | 881,574 | - |
| 총자산대비 재고자산 구성비율(%) [재고자산합계÷기말자산총계×100] |
0.4% | 0.3% | 1.0% | - |
| 재고자산회전율(회수) [연환산 매출원가÷{(기초재고+기말재고)÷2}] |
47.61 | 35.3 | 29.0 | - |
주) 연결기준으로 작성 되었습니다.
(2) 재고자산의 실사현황
① 실사일자
실사는 매년 12월말 ~ 익년 1월초 기준으로 외부감사인 입회 하에 년 1회 실시하며,내부기준에 따라 자체적으로 매 분기초 실사를 시행하고 있습니다.
실사일과 재무상태표일 사이의 입출고 발생분은 입/출고지시서 등으로 확인하였습니다.
재고자산이 담보로 제공된 경우는 없습니다.
② 장기체화재고 등의 내역
연결회사는 주기적으로 재고자산에 대한 감액의 징후를 검토하여 원가와 순실현가능가치 중 작은 금액을 재무상태표가액으로 표시하고 있습니다.
당기말 현재 재고자산에 대한 평가내역은 다음과 같습니다.
( 단위 : 천원 )
| 계정과목 | 취득원가 | 보유금액 | 당기평가손실 | 기말잔액 | 비고 |
| 상 품 | 362,117 | 362,117 | - | 362,117 | - |
| 원 재 료 | 165,599 | 165,599 | - | 165,599 | - |
| 재 공 품 | 419,397 | 419,397 | - | 419,397 | - |
| 합 계 | 947,114 | 947,114 | - | 947,114 | - |
* 취득원가와 보유금액의 차이는 없으며, 당기평가손실은 없습니다.
라. 공정가치평가 내역
(1) 보고기간종료일 현재 금융자산과 금융부채의 장부금액과 공정가치는 다음과 같습니다.
(단위 : 원)
| 구 분 | 당분기말 | 전기말 | ||
| 장부금액 | 공정가치 | 장부금액 | 공정가치 | |
| 금융자산 | ||||
| 상각후원가로 측정하는 금융자산 | ||||
| 현금및현금성자산 | 17,792,558,590 | 17,792,558,590 | 38,922,455,345 | 38,922,455,345 |
| 장단기금융상품 | 196,216,750,963 | 196,216,750,963 | 95,046,992,048 | 95,046,992,048 |
| 매출채권 및 기타채권 | 4,827,253,068 | 4,827,253,068 | 2,692,677,487 | 2,692,677,487 |
| 임차보증금 | 595,396,535 | 595,396,535 | 449,779,728 | 449,779,728 |
| 기타보증금 | 119,259,489 | 119,259,489 | 100,370,544 | 100,370,544 |
| 합 계 | 219,551,218,645 | 219,551,218,645 | 137,212,275,152 | 137,212,275,152 |
| 금융부채 | ||||
| 상각후원가 측정 금융부채 | ||||
| 매입채무및기타채무 | 2,330,857,676 | 2,330,857,676 | 440,241,691 | 440,241,691 |
| 장단기차입금 | 3,550,000,000 | 3,550,000,000 | 3,737,500,000 | 3,737,500,000 |
| 기타유동금융부채 | 1,063,399,358 | 1,063,399,358 | 2,216,725,480 | 2,216,725,480 |
| 기타비유동금융부채 | 1,006,135,217 | 1,006,135,217 | 810,719,563 | 810,719,563 |
| 상환전환우선주부채 | 3,319,309,445 | 3,319,309,445 | 10,286,242,782 | 10,286,242,782 |
| 합 계 | 11,269,701,696 | 11,269,701,696 | 17,491,429,516 | 17,491,429,516 |
(2) 공정가치 서열체계
공정가치로 측정되거나 공정가치가 공시되는 금융상품은 공정가치 서열체계에 따라 구분되며 정의된 수준들은 다음과 같습니다.
- 동일한 자산이나 부채에 대한 활성시장의(조정되지 않은) 공시가격(수준 1)
- 직접적으로(예: 가격) 또는 간접적으로(예: 가격에서 도출되어) 관측가능한, 자산 이나 부채에 대한 투입변수. 단, 수준 1에 포함된 공시가격은 제외함(수준 2)
- 관측가능한 시장자료에 기초하지 않은, 자산이나 부채에 대한 투입변수
(관측가능 하지 않은 투입변수)를 이용하여 산정한 공정가치(수준 3)
연결회사의 공정가치로 측정되거나 공정가치가 공시되는 금융상품, 금융부채는 다음과 같습니다.
<당분기> (단위:천원)
| 구 분 | 수준 1 | 수준 2 | 수준 3 | 합 계 |
| 공정가치측정 금융자산 | - | - | - | - |
| 공장가치측정 금융부채 | - | - | 60,958,040 | 60,958,040 |
<전기> (단위:천원)
| 구 분 | 수준 1 | 수준 2 | 수준 3 | 합 계 |
| 공정가치측정 금융자산 | - | - | - | - |
| 공장가치측정 금융부채 | - | - | 31,932,275 | 31,932,275 |
(2) 반복적인 공정가치 측정치의 수준3의 변동 내용
연결회사는 공정가치 서열체계의 수준 간 이동을 보고기간 말에 인식합니다. 당기 및 전기 중 반복적인 측정치의 수준 1과 수준 2간의 이동 내역은 없습니다.
IV. 이사의 경영진단 및 분석의견
금융위원회가 정한 '증권의 발행 및 공시 등에 관한 규정' 제4-3조(사업보고서등의 기재사항) 제②항에 따라 분·반기보고서에는 이사의 경영진단 및 분석의견을 기재하지 않을 수 있으므로, 본 보고서에는 '이사의 경영진단 및 분석의견'의 기재를 생략합니다.
V. 회계감사인의 감사의견 등
1. 외부감사에 관한 사항
1. 회계감사인의 명칭 및 감사의견(검토의견 포함한다. 이하 이 조에서 같다)을 다음의 표에 따라 기재한다.
| 사업연도 | 감사인 | 감사의견 | 강조사항 등 | 핵심감사사항 |
|---|---|---|---|---|
| 제14기(당기) | 이촌회계법인 | - | - | - |
| 제13기(전기) | 이촌회계법인 | 적정 | - | 기술이전계약에 따른 수익인식의 정확성 |
| 제12기(전전기) | 이촌회계법인 | 적정 | - | - |
2. 감사용역 체결현황은 다음의 표에 따라 기재한다.
| 사업연도 | 감사인 | 내 용 | 감사계약내역 | 실제수행내역 | ||
|---|---|---|---|---|---|---|
| 보수 | 시간 | 보수 | 시간 | |||
| 제14기(당기) | 이촌회계법인 | K-IFRS 감사 | 91,000,000원 | 1,300 시간 | - | - |
| 제13기(전기) | 이촌회계법인 | K-IFRS 감사 | 75,000,000원 | 1,103 시간 | 75,000,000원 | 1,103 시간 |
| 제12기(전전기) | 이촌회계법인 | K-IFRS 감사 | 65,000,000원 | 828 시간 | 65,000,000원 | 828 시간 |
3. 회계감사인과의 비감사용역 계약체결 현황은 다음의 표에 따라 기재한다.
| 사업연도 | 계약체결일 | 용역내용 | 용역수행기간 | 용역보수 | 비고 |
|---|---|---|---|---|---|
| 제14기(당기) | - | - | - | - | - |
| - | - | - | - | - | |
| 제13기(전기) | - | - | - | - | - |
| - | - | - | - | - | |
| 제12기(전전기) | - | - | - | - | - |
| - | - | - | - | - |
4. 재무제표 중 이해관계자의 판단에 상당한 영향을 미칠 수 있는 사항에 대해 내부감사기구가 회계감사인과 논의한 결과를 다음의 표에 따라 기재한다.
| 구분 | 일자 | 참석자 | 방식 | 주요 논의 내용 |
|---|---|---|---|---|
| - | - | - | - | - |
| - | - | - | - | - |
| - | - | - | - | - |
5. 회계감사인의 변경
보고서 작성 기준일 현재 해당사항 없습니다.
2. 내부통제에 관한 사항
감사인은 감사보고서에 첨부된 주식회사 알테오젠의 2020년 12월 31일 현재의 내부회계관리제도의 운영실태보고서에 대하여 검토를 실시하였습니다. 내부회계관리제도를 설계, 운영하고 그에 대한 운영실태보고서를 작성할 책임은 주식회사 알테오젠의 경영진에게 있으며, 우리의 책임은 동 보고내용에 대하여 검토를 실시하고 검토결과를 보고하는데 있습니다. 회사의 경영진은 첨부된 내부회계관리제도 운영실태보고서에서 "2020년 12월 31일 현재 내부회계관리제도 운영실태 평가결과, 2020년 12월 31일 현재 당사의 내부회계관리제도는 내부회계관리제도 모범규준에 근거하여볼 때, 중요성의 관점에서 효과적으로 설계되어 운영되고 있다고 판단된다"고 기술하고 있습니다.
감사인은 내부회계관리제도 검토기준에 따라 검토를 실시하였습니다. 이 기준은 감사인이 중요성의 관점에서 경영진이 제시한 내부회계관리제도의 운영실태보고서에 대하여 회계감사보다는 낮은 수준의 확신을 얻을 수 있도록 검토절차를 계획하고 실시할 것을 요구하고 있습니다. 검토는 회사의 내부회계관리제도를 이해하고 경영진의 내부회계관리제도의 운영실태보고내용에 대한 질문 및 필요하다고 판단되는 경우 제한적 범위 내에서 관련 문서의 확인 등의 절차를 포함하고 있습니다. 그러나 회사는 상장중소기업으로서 경영자의 내부회계관리제도 구축과 운영, 그리고 이에 대한 운영실태평가보고는 내부회계관리제도 모범규준 제5장 '중소기업에 대한 적용'의 규정에따라 상장대기업보다는 현저하게 완화된 방식으로 이루어 졌습니다. 따라서 우리는 내부회계관리제도 검토기준 중 '14. 중소기업 등에 대한 검토특례'에 따라 검토를 실시하였습니다.
회사의 내부회계관리제도는 신뢰할 수 있는 회계정보의 작성 및 공시를 위하여 기업회계기준에 따라 작성한 재무제표의 신뢰성에 대한 합리적인 확신을 줄 수 있도록 제정한 내부회계관리규정과 이를 관리ㆍ운영하는 조직을 의미합니다. 그러나 내부회계관리제도는 내부회계관리제도의 본질적인 한계로 인하여 재무제표에 대한 중요한 왜곡표시를 적발하거나 예방하지 못할 수 있습니다. 또한, 내부회계관리제도의 운영실태보고 내용을 기초로 미래기간의 내용을 추정시에는 상황의 변화 혹은 절차나 정책이 준수되지 않음으로써 내부회계관리제도가 부적절하게 되어 미래기간에 대한 평가 및 추정내용이 달라질 위험에 처할 수 있다는 점을 고려하여야 합니다.
경영진의 내부회계관리제도 운영실태보고서에 대한 우리의 검토결과, 상기 경영진의운영실태보고 내용이 중요성의 관점에서 내부회계관리제도 모범규준 제5장 '중소기업에 대한 적용'의 규정에 따라 작성되지 않았다고 판단하게 하는 점이 발견되지 아니하였습니다.
감사인 검토는 2020년 12월 31일 현재의 내부회계관리제도를 대상으로 하였으며 2020년 12월 31일 이후의 내부회계관리제도는 검토하지 않았습니다. 본 검토보고서는 주식회사등의외부감사에관한법률에 근거하여 작성된 것으로서 기타 다른 목적이나 다른 이용자를 위하여는 적절하지 않을 수 있습니다.
VI. 이사회 등 회사의 기관에 관한 사항
1. 이사회에 관한 사항
가. 이사회의 구성
당사의 이사회는 이사로 구성되고 법령 또는 정관에 정하여진 사항, 주주총회로부터 위임받은 사항, 회사의 기본방침 및 업무집행에 관한 주요사항을 의결하며 이사 및 경영진의 직무집행을 감독하고 있습니다. 본 보고서 제출일 현재 당사의 이사회는 4명의 사내이사와 2명의 사외이사로 구성되어 있으며, 이사회 내 별도의 위원회는 구성되어 있지 않습니다.
이사회 의장을 겸직하고 있는 대표이사(박순재)는 회사를 대표하고 업무를 총괄하고 있으며, 이사는 대표이사를 보좌하고 이사회에서 정하는 바에 따라 회사의 업무를 분장 집행하고 있습니다.
대표이사의 이사회 의장 선임 사유는 당사의 정관에 따른 것입니다.
|
제 43 조 (이사회의 구성과 소집) ① 이사회는 이사로 구성한다. ② 이사회는 대표이사(사장) 또는 이사회에서 따로 정한 이사가 있을 때에는 그 이사가 회일 3일 전에 각 이사 및 감사에게 통지하여 소집한다. ③ 제2항의 규정에 의하여 소집권자로 지정되지 않은 다른 이사는 소집권자인 이사에게 이사회 소집을 요구할 수 있다. 소집권자인 이사가 정당한 이유 없이 이사회 소집을 거절하는 경우에는 다른 이사가 이사회를 소집할 수 있다. ④ 이사 및 감사 전원의 동의가 있을 때에는 제2항의 소집절차를 생략할 수 있다. ⑤ 이사회의 의장은 제2항 및 제3항의 규정에 의한 이사회의 소집권자로 한다. ⑥ 이사는 3개월에 1회 이상 업무의 집행상황을 이사회에 보고하여야 한다. |
이사의 주요 이력 및 인적사항은 본 보고서 「Ⅷ. 임원 및 직원 등에 관한 사항」을 참조하시기 바랍니다.
나. 이사회 운영규정의 주요내용
|
구분 |
내용 |
|
권한사항 |
제3조 (이사회의 권한) ① 이사회는 법령 또는 정관에 정하여진 사항, 주주총회로부터 위임 받은 사항, 이 규정에서 정한 사항을 의결한다. ② 이 규정에서 이사회의 결의사항으로 정하여지지 않은 업무집행에 관한 사항은 대표이사에게 일임한다 ③ 이사회는 이사의 직무집행을 감독한다. |
|
소집 및 |
제8조 (이사회의 구분 및 소집) ① 이사회는 정기이사회와 임시이사회로 구분한다. ② 정기이사회는 매 3개월마다 개최하며, 필요에 따라 소집권자가 개최시기 및 장소를 정할 수 있다. ③ 임시이사회는 소집권자가 필요하다고 인정할 때와 이사의 요구가 있을 때 이를 개최한다. ④ 이사회의 소집권자는 의장으로 하며, 의장이 직무를 수행할 수 없는 경우에는 이사회에서 정한 순서로 소집권자가 된다. ⑤ 감사규정 제21조의 각호 사항이 발생한 경우에는 감사가 이사회를 소집할 수 있다. |
|
결의방법 |
제10조 (결의방법) ① 이사는 각 1개의 의결권을 갖는다. ② 이사회의 결의는 이사 과반수의 출석과 출석이사 과반수로 결정한다. 단, 가부 동수인 경우에는 의장이 결정한다. ③ 이사회는 이사의 전부 또는 일부가 직접 회의에 출석하지 아니하고 모든 이사가 음성을 동시에 송수신하는 원격통신수단에 의하여 결의에 참가하는 것을 허용할 수 있다. 이 경우 당해 이사는 이사회에 직접 출석한 것으로 본다. ④ 사외이사는 제11조제1호 라목, 바목, 사목 및 하목, 제4호 나목의 사항이 부의되는 이사회에는 반드시 출석하여야 한다. ⑤ 이사회의 결의에 관하여 특별한 이해관계가 있는 자는 의결권을 행사하지 못하며 의결권의 수에 산입하지 않는다. ⑥이사회의 의결권은 대리하지 못한다. |
|
의결사항 |
제11조 (의결사항) 이사회는 다음 사항을 심의·의결한다. 1. 상법 및 정관상 결의사항 가. 주주총회의 소집(상법 제362조, 정관 제23조) 나. 영업보고서 및 재무제표의 승인(상법 제447조) 다. 대표이사 등의 선임(상법 제389조, 정관 제37조) 라. 신주의 발행사항 결정(상법 제416조, 정관 제9조의2와 제10조) 마. 준비금의 자본전입(상법 제461조) 바. 전환사채의 발행(상법 제513조, 정관 제18조) 사. 신주인수권부사채의 발행(상법 제516조의2, 정관 제19조) 아. 사채의 발행(상법 제469조) 자. 지점의 설치, 이전 또는 폐지(상법 제393조, 정관 제3조) 차. 자본의 감소(상법 제438조) 카. 자기주식의 취득 및 소각(상법 제341조, 정관 제14조) 타. 주식매수선택권 부여(상법 제340조의3, 정관 제11조) 파. 우리사주매수선택권 부여(정관 제12조) 하. 영업의 양도, 양수, 임대 등(상법 제374조) 거. 정관의 변경(상법 제434조) 너. 회사의 합병 및 분할(상법 제522조와 제530조의3) 더. 주식의 분할(상법 제329조의2) 러. 명의개서대리인의 선정(정관 제15조) 2. 회사경영에 관한 사항 가. 회사경영의 기본방침 결정 및 변경 나. 신규사업의 추진 다. 중요한 규칙의 제정 및 개정 3. 자산에 관한 사항 가. 중요한 계약의 체결 나. 중요한 재산의 취득 또는 처분 다. 결손의 처분 라. 장기 자금의 차입 4. 기타 가. 주요한 소송의 제기와 화해에 관한 사항 나. 이해관계자거래에대한통제규정에 규정된 사항 다. 기타법령 또는 정관에 정한 사항 및 대표이사가 필요하다고 인정하는 사항 |
|
의사록 |
제15조 (의사록) ① 이사회의 의사에 관하여는 의사록을 작성한다. ② 의사록에는 의사의 경과요령과 그 결과를 기재하고, 출석한 이사 및 감사가 기명날인 또는 서명한다 ③ 의사록의 원본은 본점에 비치한다. |
다. 이사회의 권한 내용
|
구분 |
내용 |
|
주주총회 |
제11조 (의결사항) 제1항 상법 및 정관상 결의사항 가. 주주총회의 소집 |
|
경영일반 |
제11조 (의결사항) 제2항 회사경영에 관한 사항 가. 회사경영의 기본방침 결정 및 변경 나. 신규사업의 추진 다. 중요한 규칙의 제정 및 개정 |
|
자산 |
제11조 (의결사항) 제3항 자산에 관한 사항 가. 중요한 계약의 체결 나. 중요한 재산의 취득 또는 처분 다. 결손의 처분 |
|
장기자금조달 |
제11조 (의결사항) 제1항 상법 및 정관상 결의사항 라. 신주의 발행사항 결정 바. 전환사채의 발행 사. 신주인수권부사채의 발행 아. 사채의 발행 제11조 (의결사항) 제3항 자산에 관한 사항 라. 장기 자금의 차입 |
|
기타 |
제11조 (의결사항) 제4항 기타 가. 주요한 소송의 제기와 화해에 관한 사항 나. 이해관계자거래에대한통제규정에 규정된 사항 다. 기타법령 또는 정관에 정한 사항 및 대표이사가 필요하다고 인정하는 사항 |
라. 주요 의결사항
|
개최일자 |
의안내용 |
가결 여부 |
이사의 성명 |
||||||||
|
사내이사 |
사내이사 |
사내이사 |
사외이사 |
사외이사 |
기타비상무이사 |
사내이사 |
사내이사 |
사외이사 |
|||
|
박순재 |
이승주 |
강상우 |
최종인 |
고인영 |
김양우 |
정혜신 |
박문환 |
전형식 |
|||
|
출석율 |
100% |
100% |
100% |
100% |
100% |
100% |
100% |
100% |
|||
|
참석 및 찬반여부 |
|||||||||||
|
2021.01.07 |
ALT-B4 라이선스 계약체결 |
가결 |
찬성 |
- |
- |
- |
- |
- |
찬성 |
- |
찬성 |
|
2021.01.15 |
알토스바이오로직스 2차CPS투자계약_이해관계인 |
가결 |
찬성 |
- |
- |
- |
- |
- |
찬성 |
- |
찬성 |
|
2021.02.15 |
내부회계관리운영실태보고(제13기) |
가결 |
찬성 |
- |
- |
- |
- |
- |
찬성 |
- |
찬성 |
|
2021.03.04 |
전자투표제도 도입 |
가결 |
찬성 |
- |
- |
- |
- |
- |
찬성 |
- |
찬성 |
|
2021.03.10 |
제 13기 정기주주총회 소집의 건 |
가결 |
찬성 |
- |
- |
- |
- |
- |
찬성 |
- |
찬성 |
|
2021.03.10 |
재무제표 승인 및 영업보고의 건 |
가결 |
찬성 |
- |
- |
- |
- |
- |
찬성 |
- |
찬성 |
|
2021.03.10 |
주식발행초과금 자본전입(무상증자) 실시의 건 |
가결 |
찬성 |
- |
- |
- |
- |
- |
찬성 |
- |
찬성 |
|
2021.05.03 |
주식매수선택권 부여의 건 |
가결 |
찬성 |
찬성 |
찬성 |
찬성 |
찬성 |
찬성 |
- |
- |
- |
|
2021.06.18 |
둔곡지구(공장건설) 매입 및 은행차입 (예금담보대출) 건 |
가결 |
찬성 |
찬성 |
찬성 |
찬성 |
찬성 |
찬성 |
- |
- |
- |
| 2021.07.16 | 종속회사 세레스에프엔디의 3자배정 유상증자 참여의 건 |
가결 |
찬성 |
찬성 |
찬성 |
찬성 |
찬성 |
찬성 |
|||
마. 이사회 내의 위원회 구성현황과 그 활동내역
본 보고서 제출일 현재 당사의 이사회 내에는 위원회가 구성되어 있지 않습니다.
바. 이사의 독립성
당사의 이사회는 사내이사 3인(대표이사 포함)과 사외이사 1인으로 구성되어 있으며, 회사 경영의 중요한 의사결정과 업무집행은 이사회의 심의 및 결정을 통하여 이루어지고 있습니다. 또한 당사는 대주주 등의 독단적인 경영과 이로 인한 소액주주의 이익 침해가 발생하지 않도록 이사회 운영규정을 제정하여 성실히 준수하고 있습니다.
사. 사외이사의 전문성
회사 내 지원조직은 사외이사가 이사회에서 전문적인 직무수행이 가능하도록 보조하고 있습니다. 이사회 전에 해당 안건 내용을 충분히 검토할 수 있도록 사전에 자료를 제공하고 기타 사내 주요 현안에 대해서도 수시로 정보를 제공하고 있습니다.
사외이사 및 그 변동현황
| (단위 : 명) |
| 이사의 수 | 사외이사 수 | 사외이사 변동현황 | ||
|---|---|---|---|---|
| 선임 | 해임 | 중도퇴임 | ||
| 6 | 2 | 2 | - | 1 |
※ 2020년 3월 29일 주주총회를 통해 최종인, 고인영 사외이사 신규 선임
※ 2020년 3월 27일에 전형식 사외이사의 임기가 만료됨
사외이사 교육 미실시 내역
| 사외이사 교육 실시여부 | 사외이사 교육 미실시 사유 |
|---|---|
| 미실시 | - 당사는 이사가 업무 수행함에 있어 전문적인 직무수행이 가능하도록 보조하고 있습니다. - 관련 내용을 충분히 검토할 수 있도록 사전에 자료를 제공하고기타 주요 현안에 대해서도 수시로 정보를 제공하고 있습니다. - 향후 직무관련 교육의 기회가 있으면 적극적으로 참여할 계획입니다.. |
2. 감사제도에 관한 사항
가. 감사위원회 설치 여부
당사는 보고서 제출일 현재 감사위원회를 별도로 설치하고 있지 않으며, 주주총회 결의로 선임된 상근 감사 1명이 감사 업무를 수행하고 있습니다.
나. 감사의 인적사항
|
성명 |
주요경력 |
최대주주등과의 이해관계 |
결격요건 여부 |
비고 |
| 이정민 |
서울대학교 경영학 석사 KDB산은금융지주 리스트 관리실장 |
관계없음 |
해당없음 |
2021.03.29 |
| 이병규 | 고려대 경영학 석사 하나은행(기업금융지점장) |
관계없음 | 해당없음 | 2021.03.29 신규 선임 |
※ 상기 이정민 감사의 사임으로, 2021년 3월 29일 제 13기 정기 주주총회에서 이병규 감사가 신규 상임감사로 선임됨
다. 감사의 독립성
감사는 회계와 업무를 감사하며 이사회 및 타 부서로부터 독립된 위치에서 업무를 수행하고 있습니다. 또한 당사는 감사의 감사업무에 필요한 경영정보접근을 위하여 당사 정관에 다음과 같은 조항을 두고 있습니다.
|
제50조 (감사의 직무 등) ① 감사는 회사의 회계와 업무를 감사한다. ② 감사는 회의의 목적사항과 소집의 이유를 기재한 서면을 이사회에 제출하여 임시주주총회의 소집을 청구할 수 있다. ③ 감사는 그 직무를 수행하기 위하여 필요한 때에는 종속회사에 대하여 영업의 보고를 요구할 수 있다. 이 경우 종속회사가 지체 없이 보고를 하지 아니할 때 또는 그 보고의 내용을 확인할 필요가 있는 때에는 종속회사의 업무와 재산 상태를 조사할 수 있다. ④ 감사에 대하여는 제40조 제3항을 준용한다. ⑤ 감사는 회사의 비용으로 전문가의 도움을 구할 수 있다. ⑥ 감사는 필요하면 회의의 목적사항과 소집이유를 적은 서면을 이사회 소집권자에게 제출하여 이사회 소집을 청구할 수 있다. ⑦ 제6항의 청구를 하였는데도 이사가 지체 없이 이사회를 소집하지 아니하면 그 청구한 감사가 이사회를 소집할 수 있다. |
라. 감사의 활동내역
|
개최일자 |
의안내용 |
가결 여부 |
감사 참석여부 |
|
2012.02.15 |
2011년 재무제표 승인의 건, 2011년 영업보고의 건, 정기주주총회 소집의 건 |
가결 |
참석 |
|
2012.03.12 |
㈜알토스바이오사이언스와의 연구용역 계약 체결 |
가결 |
참석 |
|
2012.09.18 |
대표이사 박순재의 2012년도 사업연도 월급 책정 의결 건 |
가결 |
참석 |
|
2012.12.28 |
신주 발행의 건 |
가결 |
불참 |
|
2013.02.13 |
2012년 재무제표 승인의 건, 2012년 영업보고의 건, 정기주주총회 소집의 건 |
가결 |
참석 |
|
2013.02.22 |
준비금 자본전입에 관한 건 |
가결 |
불참 |
|
2013.03.29 |
대표이사 선임의 건 |
가결 |
참석 |
|
2013.06.14 |
주식매수선택권 부여의 건 |
가결 |
참석 |
|
2013.11.07 |
㈜알토스바이오사이언스 주식 양수의 건, 임시주주총회 소집의 건 |
가결 |
참석 |
|
2013.12.30 |
사규 제정의 건 |
가결 |
참석 |
|
2014.02.07 |
유상증자(제3자배정) 결의의 건 |
가결 |
참석 |
|
2014.03.06 |
2013년 재무제표 승인의 건, 2013년 영업보고의 건, 정관 변경의 건, 이사 및 감사 후보자 추천의 건, 정기주주총회 소집의 건 |
가결 |
참석 |
|
2014.04.08 |
준비금의 자본전입에 관한 건, 주식매수선택권 행사에 따른 신주 발행의 건 |
가결 |
참석 |
|
2014.07.28 |
명의개서대리인 선임의 건 |
가결 |
참석 |
|
2014.08.22 |
코스닥시장 상장을 위한 신주발행 |
가결 |
참석 |
| 2014.11.24 | 우리사주 취득자금 대출을 위한 예금담보 제공 | 가결 | 참석 |
| 2015.01.16 | 우선주 주주명부 폐쇄 기준일 설정 |
가결 |
참석 |
| 2015.02.16 | 재무제표 및 영업보고서 승인 |
가결 |
참석 |
| 2015.03.12 | 주총소집, 스톡옵션부여, 자산양수도 |
가결 |
참석 |
| 2015.03.20 | 감사 후 재무제표 승인 |
가결 |
참석 |
| 2015.08.27 | 본점 주소지 변경 | 가결 | 불참 |
| 2016.02.15 | 재무제표 및 영업보고서 승인 | 가결 | 참석 |
| 2016.03.04 | 주총소집, 스톡옵션부여 |
가결 |
참석 |
| 2016.03.29 | 대표이사 선임 |
가결 |
참석 |
| 2016.06.03 | (주)엘에스메디텍 인수의 건 |
가결 |
참석 |
| 2016.06.13 | 주식매수선택권 부여 |
가결 |
참석 |
| 2016.08.31 | 유상증자(제3자배정) 결의의 건 | 가결 | 참석 |
| 2016.12.12 | 자기주식 취득 신탁계약체결 | 가결 | 참석 |
| 2017.02.10 | 재무제표 및 영업보고서 승인 |
가결 |
참석 |
| 2017.03.10 | 주총소집, 이사선임, 감사선임, 스톡옵션부여 |
가결 |
참석 |
| 2017.09.01 | 주식매수선택권 부여 | 가결 | 참석 |
| 2017.11.23 | 무상증자 | 가결 | 참석 |
| 2018.03.09 | 주총소집, 이사선임, 스톡옵션부여 |
가결 |
참석 |
| 2018.04.12 | 신주발행의 건 (전환우선주 발행) |
가결 |
참석 |
| 2018.04.23 | 스톡옵션 부여의 건 (직원 대상) |
가결 |
참석 |
| 2018.05.24 | 자산(토지) 양수의 건 |
가결 |
참석 |
| 2018.06.14 | 종속회사 신규 법인 설립의 건 |
가결 |
참석 |
| 2018.07.01 | 종속회사(세레스에프엔디) 자금대여의 건 |
가결 |
참석 |
| 2018.07.30 | 종속회사(세레스에프엔디) 자금대여의 건 |
가결 |
참석 |
| 2018.08.01 | 임직원 대출 예금담보 제공 |
가결 |
참석 |
| 2018.08.03 | 임원 스톡옵션 부여의 건 |
가결 |
참석 |
| 2019.03.08 | 재무제표 승인, 영업보고, 내부회계관리제도 운영 평가 보고, 주식매수선택권 부여의 건 |
가결 |
참석 |
| 2019.03.11 | 주총소집, 정관변경의 건 |
가결 |
참석 |
| 2019.03.27 | 대표이사 선임의 건 |
가결 |
참석 |
| 2019.04.10 | 자산 양수의 건 |
가결 |
참석 |
| 2019.04.30 | 스톡옵션부여의 건 |
가결 |
참석 |
| 2019.05.16 | 라이센스 옵션계약 체결의 건 |
가결 |
참석 |
| 2019.07.01 | 세레스 주주배정 유상증자 참여의 건 |
가결 |
찬성 |
| 2019.07.02 | 세레스 대여금 만기 연장의 건 |
가결 |
찬성 |
| 2019.07.30 | 세레스 대여금 만기 연장의 건 |
가결 |
찬성 |
| 2019.08.05 | 스톡옵션부여의 건 |
가결 |
찬성 |
| 2019.08.06 | 임직원 예금담보 제공의 건 |
가결 |
찬성 |
| 2019.11.29 | 인간 히알루로니다제 원천기술 비독점적 라이센스 계약 체결건 |
가결 |
참석 |
| 2020.02.12 | 재무제표 승인, 영업보고 승인의 건 |
가결 |
참석 |
| 2020.02.19 | 내부회계 관리 실태 보고 및 운영실태 평가결과 보고의 건 |
가결 |
참석 |
| 2020.03.02 | 정기주주총회 소집의 건 |
가결 |
참석 |
| 2020.04.14 | 주식매수 선택권 부여의 건 |
가결 |
참석 |
| 2020.06.11 | 주식매수선택권 부여의 건 |
가결 |
참석 |
| 2020.06.24 | 인간 히알루로니다제 원천기술 비독점적 라이센스 계약 체결건 |
가결 |
참석 |
| 2020.07.02 | 세레스 대여금 만기 연장의 건 |
가결 |
참석 |
| 2020.07.07 | 무상증자 결정의 건 |
가결 |
참석 |
| 2020.07.30 | 세레스 대여금 만기 연장의 건 |
가결 |
참석 |
| 2020.08.05 | 임직원 예금담보 제공의 건 |
가결 |
참석 |
| 2020.10.15 | 자회사 알토스바이오로직스 설립 |
가결 |
참석 |
| 2020.11.04 | 기명식 사모 전환우선주 발행의 건 |
가결 |
참석 |
| 2021.01.07 | ALT-B4 라이선스 계약체결 |
가결 |
참석 |
| 2021.01.15 | 알토스바이오로직스_2차CPS투자계약_이해관계인 |
가결 |
참석 |
| 2021.02.15 | 내부회계관리운영실태보고(제13기, FY2020) |
가결 |
참석 |
| 2021.03.04 | 전자투표제도 도입 |
가결 |
참석 |
| 2021.03.10 | 제 13기 정기주주총회 소집의 건 |
가결 |
참석 |
| 2021.03.10 | 재무제표 승인 및 영업보고의 건 |
가결 |
참석 |
| 2021.03.10 | 주식발행초과금 자본전입(무상증자) 실시의 건 |
가결 |
참석 |
|
2021.05.03 |
주식매수선택권 부여의 건 |
가결 |
참석 |
|
2021.06.18 |
둔곡지구(공장건설) 매입 및 은행차입 (예금담보대출) 건 |
가결 |
참석 |
| 2021.07.16 | 종속회사 세레스에프엔디의 3자배정 유상증자 참여의 건 |
가결 |
참석 |
마. 감사 교육실시 현황
| 교육일자 | 교육실시주체 | 주요 교육내용 |
|---|---|---|
| 2021.10.28 | 코스닥협회 | 내부회계관리제도 전문연수 |
| 2021.11.01 | 코스닥협회 | 상장법인 사외이사 등을 위한 자본시장관련 주요이슈 설명회 |
바. 감사 지원조직 현황
| 부서(팀)명 | 직원수(명) | 직위(근속연수) | 주요 활동내역 |
|---|---|---|---|
| 재무회계팀 | 5 | 부장1명, 과장1, 대리2명, 사원1명(평균5.6년) | 재무제표, 이사회 등 경영전반에 관한 감사직무 수행지원 |
| 내부회계 관리팀 |
1 | 과장1명(근속년수 0.2년) | 내부회계관리 전반에 관한 감사직무 수행지원 |
사. 준법지원인 등 지원조직 현황
| 부서(팀)명 | 직원수(명) | 직위(근속연수) | 주요 활동내역 |
|---|---|---|---|
| - | - | - | - |
| - | - | - | - |
※해당사항없음
3. 주주총회 등에 관한 사항
가. 투표제도 현황
| (기준일 : | 2021년 09월 30일 | ) |
| 투표제도 종류 | 집중투표제 | 서면투표제 | 전자투표제 |
|---|---|---|---|
| 도입여부 | 배제 | 미도입 | 도입 |
| 실시여부 | - | - | 제13기(20년도) 정기주총 |
나. 소수주주권의 행사여부
해당사항 없음
다. 경영권 경쟁 여부
해당사항 없음
라. 의결권 현황
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 주식수 | 비고 |
|---|---|---|---|
| 발행주식총수(A) | 보통주 | 42,264,250 | - |
| 우선주 | 1,029,015 | - | |
| 의결권없는 주식수(B) | 보통주 | 9,010 | 자기주식 |
| 우선주 | 2 | 자기주식 | |
| 정관에 의하여 의결권 행사가 배제된 주식수(C) | 보통주 | - | - |
| 우선주 | - | - | |
| 기타 법률에 의하여 의결권 행사가 제한된 주식수(D) |
보통주 | - | - |
| 우선주 | - | - | |
| 의결권이 부활된 주식수(E) | 보통주 | - | - |
| 우선주 | - | - | |
| 의결권을 행사할 수 있는 주식수 (F = A - B - C - D + E) |
보통주 | 42,255,240 | - |
| 우선주 | 1,029,013 | - |
※당사는 2021년 4월 20일자로 상법 421조의 2에 따라 무상증자에 따른 단주(端株)의 처리를 위하여 필요한 자기주식을 취득함(보통주식 9,010주 및 3회차우선주식 2주)
마. 주식사무
|
정관상 |
제10조(신주인수권) ① 주주는 그가 소유한 주식의 수에 비례하여 신주의 배정을 받을 권리를 받는다. ② 회사는 제1항의 규정에도 불구하고 다음 각 호의 어느 하나에 해당하는 경우 이사회의 결의로 주주 외의 자에게 신주를 배정할 수 있다. 1. 발행주식총수의 100분의 30을 초과하지 않는 범위 내에서 자본시장과 금융투자업에 관한 법률 제165조의6에 따라 일반공모증자 방식으로 신주를 발행하는 경우 2. 상법 제542조의 3에 따른 주식매수선택권의 행사로 인하여 신주를 발행하는 경우 3. 발행하는 주식총수의 100분의 20 범위 내에서 우리사주조합원에게 주식을 우선 배정하는 경우 4. 근로복지기본법 제39조의 규정에 의한 우리사주매수선택권의 행사로 인하여 신주를 발행하는 경우 5. 발행주식총수의 100분의 20을 초과하지 않는 범위 내에서 긴급한 자금조달을 위하여 국내외 금융기관 또는 기관투자자에게 신주를 발행하는 경우 6. 발행주식총수의 100분의 20을 초과하지 않는 범위 내에서 사업상 중요한 기술도입, 연구개발, 생산/판매/자본제휴를 위하여 그 상대방에게 신주를 발행하는 경우 7. 외국인투자촉진법에 의해 외국인투자유치를 위해 신주를 발행하는 경우 8. 주권을 코스닥시장 혹은 코스피시장에 상장하기 위하여 신주를 모집하거나 인수인에게 인수하게 하는 경우 ③ 제2항 각 호 중 어느 하나의 규정에 의해 신주를 발행할 경우 발행할 주식의 종류와 수 및 발행가격 등은 이사회의 결의로 정한다. ④ 신주인수권의 포기 또는 상실에 따른 주식과 신주배정에서 발생한 단주의 처리방법은 이사회의 결의로 정한다. ⑤ 제2항에 따라 주주 외의 자에게 신주를 배정하는 경우 회사는 상법 제416조제1호, 제2호, 제2호의2, 제3호 및 제4호에서 정하는 사항을 그 납입기일의 2주 전까지 주주에게 통지하거나 공고하여야 한다. |
||
|
결산일 |
12월 31일 |
정기주주총회 |
매 사업연도 종료 후 3개월 이내 |
|
주주명부폐쇄시기 |
매년 1월 1일부터 1월 31일까지 |
||
|
주권의 종류 |
일주권, 오주권, 일십주권, 오십주권, 일백주권, 오백주권, 일천주권, 일만주권( 8종) |
||
|
명의개서대리인 |
하나은행 증권대행부 |
||
|
주주의 특전 |
해당사항 없음 |
공고게재 |
홈페이지(www.alteogen.com) 및 |
바. 주주총회 의사록 요약
| 주총일자 | 안 건 | 결 의 내 용 | 비 고 |
|---|---|---|---|
| 제13기 주주총회 (2021.03.29) |
1. 제13기 재무제표 승인의 건 2. 이사 및 상근감사 선임의 건 3. 제14기 이사보수한도 결정의 건 4. 제14기 감사보수한도 결정의 건 5. 주식매수선택권 부여 승인의 건 |
원안대로 승인 〃 〃 〃 〃 |
- |
| 제12기 주주총회 (2020.03.26) |
1. 제12기 재무제표 승인의 건 2. 이사 및 감사 선임의 건 3. 제13기 이사보수한도 결정의 건 4. 제13기 감사보수한도 결정의 건 5. 주식매수선택권 부여 승인의 건 |
원안대로 승인 〃 〃 〃 〃 |
- |
| 제11기 주주총회 (2019.03.27) |
1. 제11기 재무제표 승인의 건 2. 이사 선임의 건 3. 제12기 이사보수한도 결정의 건 4. 제12기 감사보수한도 결정의 건 5. 주식매수선택권 부여 승인의 건 6. 정관 개정(안)의 승인 |
원안대로 승인 〃 〃 〃 〃 〃 |
- |
| 제10기 주주총회 (2018.03.27) |
1. 제10기 재무제표 승인의 건 2. 사외 이사 선임의 건 3. 제11기 이사보수한도 결정의 건 4. 제11기 감사보수한도 결정의 건 5. 주식매수선택권 부여 승인의 건 6. 정관 개정(안)의 승인 |
원안대로 승인 〃 〃 〃 〃 〃 |
- |
VII. 주주에 관한 사항
1. 최대주주 및 특수관계인의 주식소유 현황
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 주, %) |
| 성 명 | 관 계 | 주식의 종류 |
소유주식수 및 지분율 | 비고 | |||
|---|---|---|---|---|---|---|---|
| 기 초 | 기 말 | ||||||
| 주식수 | 지분율 | 주식수 | 지분율 | ||||
| 박순재 | 본인 | 보통주 | 5,670,000 | 20.05 | 8,505,000 | 19.65 | 대표이사 |
| 정혜신 | 등기임원 | 보통주 | 1,120,000 | 3.96 | 1,680,000 | 3.88 | - |
| 박수민 | 자녀 | 보통주 | 155,000 | 0.55 | 232,500 | 0.54 | - |
| 이재상 | 미등기임원 | 보통주 | 46,000 | 0.16 | 69,000 | 0.16 | - |
| 이상미 | 미등기임원 | 보통주 | 135,324 | 0.48 | 202,986 | 0.47 | - |
| 이민석 | 미등기임원 | 보통주 | 57,040 | 0.20 | 85,560 | 0.20 | - |
| 고인영 | 등기임원 | 보통주 | 0 | 0.00 | 150 | 0.00 | 주) |
| 계 | 보통주 | 7,183,364 | 25.40 | 10,775,196 | 24.89 | - | |
| 우선주 | - | - | - | - | - | ||
주) 고인영 사외이사는 3월29일 주주총회에서 선임되었습니다.
※기초와 기말의 소유주식수 변동사유는 무상증자로 인한 소유주식수 증가입니다.
※위의 표 기말 지분율은 보고서 작성 기준일 발행주식 총수(의결권있는 우선주포함)를 기준으로 작성하였습니다
2. 최대주주의 주요경력 및 개요
| 성명 | 출생년월 | 주요경력 | 겸임현황 |
|
박순재 |
1954년 12월 | Purdue Univ. 생화학 박사 M.I.T Post Doc. ㈜LG생명과학 상무 ㈜한화석유화학/㈜드림파마 상무 ㈜바이넥스 대표이사 현) ㈜알테오젠 대표이사 |
㈜알토스바이오사이언스 이사 ㈜세레스에프엔디 이사 ㈜알토스바이오로직스 대표이사 |
3. 최대주주 변동내역
최대주주 변동내역
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 주, %) |
| 변동일 | 최대주주명 | 소유주식수 | 지분율 | 변동원인 | 비 고 |
|---|---|---|---|---|---|
| - | - | - | - | - | - |
※해당사항없음
4. 주식의 분포
가. 주식소유현황
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 주) |
| 구분 | 주주명 | 소유주식수 | 지분율(%) | 비고 |
|---|---|---|---|---|
| 5% 이상 주주 | 박순재 | 8,505,000 | 19.65 | 대표이사 |
| 형인우 | 2,500,000 | 5.77 | - | |
| 우리사주조합 | - | - | - | |
나. 소액주주현황
소액주주현황
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 주) |
| 구 분 | 주주 | 소유주식 | 비 고 | ||||
|---|---|---|---|---|---|---|---|
| 소액 주주수 |
전체 주주수 |
비율 (%) |
소액 주식수 |
총발행 주식수 |
비율 (%) |
||
| 소액주주 | 57,355 | 57,367 | 99.98 | 26,865,168 | 43,293,265 | 62.05 | - |
※위의 표 지분율은 보고서 작성 기준일 발행주식 총수(의결권있는 우선주포함) 기준으로 작성하였습니다.
5. 주가 및 주식거래실적
| 한국거래소 코스닥 시장 - 보통주(196170) | (단위 : 원, 주) |
| 구 분 | 2021년 4월 | 2021년 5월 | 2021년 6월 | 2021년 7월 | 2021년 8월 | 2021년 9월 | |
| 주 가 | 최 고 | 93,000 | 79,300 | 83,700 | 96,300 | 91,000 | 86,100 |
| 최 저 | 80,700 | 67,100 | 69,900 | 80,000 | 71,700 | 72,600 | |
| 월간 거래량 | 4,483,092 | 5,462,541 | 5,869,150 | 3,291,177 | 6,432,921 | 6,496,315 | |
| 출처: KRX Market Data |
| (주1) 최고가, 최저가는 종가 기준입니다. |
6. 기업인수목적회사의 추가기재사항
해당사항 없음
VIII. 임원 및 직원 등에 관한 사항
1. 임원 및 직원 등의 현황
가. 임원 현황
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 주) |
| 성명 | 성별 | 출생년월 | 직위 | 등기임원 여부 |
상근 여부 |
담당 업무 |
주요경력 | 소유주식수 | 최대주주와의 관계 |
재직기간 | 임기 만료일 |
|
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 의결권 있는 주식 |
의결권 없는 주식 |
|||||||||||
|
박순재 |
남 | 1954년 12월 | 대표이사 | 사내이사 | 상근 |
대표이사 |
Purdue Univ. 생화학 박사 M.I.T Post Doc. ㈜LG생명과학 상무 ㈜한화석유화학/㈜드림파마 상무 ㈜바이넥스 대표이사 |
8,505,000 |
- |
본인 | 2010.06.24~현재 | 2022.03.29 |
| 이승주(주1) | 남 | 1963년 08월 | 부사장 | 사내이사 | 상근 | CTO/연구소장 | 연세대 생화학 석사 (주)LG화학 바이오 연구위원 |
- | - | 미등기임원-> 등기임원 |
2018.08.01~현재 | 2024.03.28 |
| 강상우(주1) | 남 | 1966년 03월 | 상무 | 사내이사 | 상근 | CFO | 연세대 생화학 학사 미국 Univ. of Michigan MBA 씨티은행, 삼성전자, 삼성증권, 벤처캐피탈 바이오 벤처기업 사업개발 및 M&A 담당 |
- | - | 미등기임원-> 등기임원 |
2020.06.01~현재 | 2024.03.28 |
| 최종인(주1) | 남 | 1964.08 | 사외이사 | 사외이사 | 비상근 | - | 한밭대학교 산학협력단장, 산학협력교육원장 (前) 대덕벤처협회 연구소장 과학기술자문회의 전문위원 美 리하이(Lehigh) 대학교 Post-Doc 고려대학교 경영학 박사 |
- | - | 등기임원 | 2021.03.29~현재 | 2024.03.28 |
| 고인영(주1) | 남 | 1956.04 | 사외이사 | 사외이사 | 비상근 | - | 강원대 의생명공학과 교수 춘천바이오산업진흥원 원장 유한양행 중앙연구소 이사 캐나다, 캘거리대학교 분자면역학 박사 서울대 자연대 미생물학과 학사 |
150 | - | 등기임원 | 2021.03.29~현재 | 2024.03.28 |
| 김양우(주1) | 남 | 1969.11 | 기타비상무이사 | 기타비상무이사 | 비상근 | - | SGPE 본부장 마이다스 PE 부대표 CJ제일제당 전략기획실 보스톤컨설팅, 삼성물산 美 Univ. of Virginia MBA 서울대학교 경영학과 학사 |
- | - | 등기임원 | 2021.03.29~현재 | 2024.03.28 |
| 이병규(주1) | 남 | 1966.11 | 감사 | 감사 | 상근 | 감사 | 하나은행 (기업금융지점장) 고려대 경영학 석사 |
- | - | 등기임원 | 2021.03.29~현재 | 2024.03.28 |
|
정혜신(주3) |
여 | 1957년 08월 | 사장 | 미등기 | 상근 |
CSO |
Purdue Univ. 생화학 박사 Boston Biomedical Research Institute Post Doc. ㈜LG화학 바이오텍연구소 책임연구원 한남대 생명시스템과학과 교수 |
1,680,000 |
- |
특수관계인 | 2008.05.13~ 현재 |
- |
| 정경훈 | 남 | 1961년 07월 | 전무 | 미등기 | 상근 | QA총괄 | Boston Univ. 신경내분비학 박사 ㈜LG화학 바이오텍연구소 연구원 Harvard Medical School Instructor 가천대학교 길병원 임상의학연구소 |
7,500 | - | 미등기임원 | 2017.04.01~현재 | - |
| 이민석 | 남 | 1963년 04월 | 전무 | 미등기 | 상근 | 전략기획 IR 총괄 |
연세대 생화학 석사 CJ제일제당 제약사업부 연구원 인텍창업투자 투자팀장 한국바이오협회 전략기획실장 |
85,560 | - | 미등기임원 | 2017.07.01~현재 | - |
| 김규완 | 남 | 1966년 01월 | 상무 | 미등기 | 상근 | 신약개발 총괄 |
연세대 생화학 석사 ㈜LG화학 바이오텍연구소 선임연구원 |
30,000 | - | 미등기임원 | 2016.06.01~현재 | - |
|
이상미 |
여 | 1967년 05월 | 상무 | 미등기 | 상근 | 연구기획 총괄 |
연세대 생화학 ㈜LG화학 바이오텍연구소 선임연구원 메릴랜드주립대학(미국) 연구원 Cangenbio(미국) 연구원 메릴랜드주립대학(미국) 연구원 |
202,986 |
- |
미등기임원 | 2008.05.13~현재 | - |
| 이재상 | 남 | 1956년 01월 | 이사 | 미등기 | 비상근 | - | 조선대 화학공학과 (주)LG생명과학 G/W 사업 담당 현)엘에스메디텍 대표이사 |
69,000 |
- |
미등기임원 | 2016.06.01~현재 | - |
| 전형식(주2) | 남 | 1955년 03월 | 사외이사 | 사외이사 | 비상근 | - | 고려대 식품생명공학 박사 ㈜종근당 종합연구소 수석연구원 ㈜종근당 개발전략팀장/이사 ㈜종근당, 해외등록 및 수출담당/이사 현) 한국폴리텍 바이오대학 교수 |
- | - | 등기임원 (임기만료) |
2015.05.01~2021.03.29 | 2021.03.27 |
| 이정민(주3) | 남 | 1960년 06월 | 감사 | 감사 | 비상근 | - | 서울대 경영학 석사 대우증권 재무담당 KDB 산은금융지주 리스크관리실장 대우증권 경영지원본부장 한화투자증권 리스크관리실장 |
- | - | 비상근감사 (사임) |
2020.03.26~2021.03.29 | - |
(주1) 제13기 정기주주총회(2021년 3월 29일)에서 등기임원(이사/감사)으로 신규선임 되었습니다.
(주2) 2021년 3월 27일 임기만료 되었습니다.
(주3) 2021년 3월 29일 주주총회에서 등기임원 사임하였습니다.
나. 직원 현황
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 원) |
| 직원 | 소속 외 근로자 |
비고 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 사업부문 | 성별 | 직 원 수 | 평 균 근속연수 |
연간급여 총 액 |
1인평균 급여액 |
남 | 여 | 계 | |||||
| 기간의 정함이 없는 근로자 |
기간제 근로자 |
합 계 | |||||||||||
| 전체 | (단시간 근로자) |
전체 | (단시간 근로자) |
||||||||||
| 본사/연구소 | 남 | 52 | - | - | - | 52 | 3.8 | 2,144,911,620 | 41,248,300 | - | - | - | - |
| 본사/연구소 | 여 | 46 | - | - | - | 46 | 4.3 | 1,726,904,600 | 37,541,404 | - | |||
| 합 계 | 98 | - | - | - | 98 | - | 3,871,816,220 | 39,508,329 | - | ||||
주1) 연간급여총액란에 기재된 수치는 퇴직자의 급여를 포함한 제14기(2021.1.1~2021.9.30) 9개월 급여총액입니다.
주2) 평균 근속년수는 2021년 9월 30일 현재 근무중인 직원을 기준으로 산출 하였습니다.
다. 미등기임원 보수 현황
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 원) |
| 구 분 | 인원수 | 연간급여 총액 | 1인평균 급여액 | 비고 |
|---|---|---|---|---|
| 미등기임원 | 10 | 941,499,080 | 94,149,908 | - |
2. 임원의 보수 등
| <이사ㆍ감사 전체의 보수현황> |
1. 주주총회 승인금액
| (단위 : 원) |
| 구 분 | 인원수 | 주주총회 승인금액 | 비고 |
|---|---|---|---|
| 등기이사 및 사외이사 | 8 | 1,500,000,000 | - |
| 감사 | 2 | 100,000,000 | - |
2. 보수지급금액
2-1. 이사ㆍ감사 전체
| (단위 : 원) |
| 인원수 | 보수총액 | 1인당 평균보수액 | 비고 |
|---|---|---|---|
| 10 | 941,499,080 | 94,149,908 | - |
2-2. 유형별
| (단위 : 원) |
| 구 분 | 인원수 | 보수총액 | 1인당 평균보수액 |
비고 |
|---|---|---|---|---|
| 등기이사 (사외이사, 감사위원회 위원 제외) |
4 | 4,209,620,120 | 1,052,405,030 | - |
| 사외이사 (감사위원회 위원 제외) |
4 | 25,000,050 | 8,333,350 | - |
| 감사위원회 위원 | - | - | - | - |
| 감사 | 2 | 33,648,330 | 16,824,165 | - |
주1) 기타비상무이사는 보고서 제출일 현재 보수지급금액이 없으므로 1인당 평균보수액 산출시 제외하였습니다.
주2) 상기 인원수는 보고서 작성기준일 현재 재직 및 퇴사한 인원을 포함하였습니다.
주3) 상기 보수총액에는 등기임원 신규 선임 후 급여와 사임한 등기 임원의 급여 및 퇴직급여가 포함되어 있습니다.
주4) 1인당 평균보수액은 보수총액을 공시대상 기간중 현재 재직 및 퇴사한 임원의 인원수로 나눈 금액입니다.
<이사ㆍ감사 및 상위 5명의 개인별 보수현황>
개인별 보수현황은 2016년 3월「자본시장과 금융투자업에 관한 법률」개정으로
연 2회 공시(반기보고서 및 사업보고서)하고 있습니다.
<주식매수선택권의 부여 및 행사현황>
<표1>
| (단위 : 원) |
| 구 분 | 인원수 | 주식매수선택권의 공정가치 총액 | 비고 |
|---|---|---|---|
| 등기이사 | 2 | 2,881,121,500 | - |
| 사외이사 | - | - | - |
| 감사위원회 위원 또는 감사 | - | - | - |
| 계 | 2 | 2,881,121,500 | - |
<표2>
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 원, 주) |
| 부여 받은자 |
관 계 | 부여일 | 부여방법 | 주식의 종류 |
최초 부여 수량 |
당기변동수량 | 총변동수량 | 기말 미행사수량 |
행사기간 | 행사 가격 |
||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 행사 | 취소 | 행사 | 취소 | |||||||||
| 정경훈 | 미등기임원 | 2017.09.01 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 60,000 | 10,000 | 0 | 25,000 | 0 | 35,000 | 2020.09.01~2023.08.31 | 5,167 |
| OOO 외 18인 | 직원 | 2018.03.09 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 138,000 | 52,900 | 0 | 52,900 | 27,000 | 58,100 | 2021.03.09~2024.03.08 | 6,900 |
| OOO 외 3인 | 직원 | 2018.04.23 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 36,000 | 27,000 | 0 | 27,000 | 9,000 | 0 | 2021.04.23~2024.04.22 | 12,167 |
| 이승주(주2) | 등기임원 | 2018.08.03 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 150,000 | 50,000 | 0 | 50,000 | 0 | 100,000 | 2021.08.03~2024.08.02 | 10,667 |
| 이민석 | 미등기임원 | 2018.08.03 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 30,000 | 0 | 0 | 0 | 0 | 30,000 | 2021.08.03~2024.08.02 | 10,667 |
| 정경훈 | 미등기임원 | 2018.08.03 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 30,000 | 0 | 0 | 0 | 0 | 30,000 | 2021.08.03~2024.08.02 | 10,667 |
| OOO 외 20인 | 직원 | 2019.03.08 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 141,600 | 0 | 0 | 0 | 4,500 | 137,100 | 2022.03.08~2025.03.07 | 12,000 |
| OOO 외 4인 | 직원 | 2019.04.30 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 39,000 | 0 | 0 | 0 | 18,000 | 21,000 | 2022.04.30~2025.04.29 | 14,333 |
| 이재상 | 미등기임원 | 2019.08.05 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 45,000 | 0 | 0 | 0 | 0 | 45,000 | 2022.08.05~2025.08.04 | 10,700 |
| 이승주(주2) | 등기임원 | 2019.08.05 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 150,000 | 0 | 0 | 0 | 0 | 150,000 | 2022.08.05~2025.08.04 | 10,700 |
| OOO 외 16인 | 직원 | 2020.03.26 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 105,000 | 0 | 0 | 0 | 0 | 105,000 | 2023.03.26~2026.03.25 | 25,333 |
| OOO 외 5인 | 직원 | 2020.04.14 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 181,500 | 0 | 150,000 | 0 | 150,000 | 31,500 | 2023.04.14~2026.04.13 | 28,600 |
| 강상우(주2) | 등기임원 | 2020.06.11 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 90,000 | 0 | 0 | 0 | 0 | 90,000 | 2023.06.11~2026.06.10 | 76,667 |
| OOO 외 5인 | 직원 | 2021.05.03 | 신주교부, 자기주식 교부, 현금 차액보상 또는 자기주식 차액보상 |
보통주 | 14,500 | 0 | 0 | 0 | 0 | 14,500 | 2024.05.03~2027.05.02 | 87,450 |
(주1) 2017년 11월 23일, 2020년 7월 7일, 2021년 3월 10일 무상증자로 인하여 조정된 수량 및 행사가격입니다.
(주2) 2021년 3월 29일 주주총회에서 등기임원으로 선임되었습니다.
IX. 계열회사 등에 관한 사항
가. 계열회사 현황(요약)
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 사) |
| 기업집단의 명칭 | 계열회사의 수 | ||
|---|---|---|---|
| 상장 | 비상장 | 계 | |
| (주)알테오젠 기업집단 | 1 | 3 | 4 |
| ※상세 현황은 '상세표-2. 계열회사 현황(상세)' 참조 |
타법인출자 현황(요약)
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 백만원) |
| 출자 목적 |
출자회사수 | 총 출자금액 | |||||
|---|---|---|---|---|---|---|---|
| 상장 | 비상장 | 계 | 기초 장부 가액 |
증가(감소) | 기말 장부 가액 |
||
| 취득 (처분) |
평가 손익 |
||||||
| 경영참여 | - | 3 | 3 | 3,548 | 3,500 | - | 7,048 |
| 일반투자 | - | - | - | - | - | - | - |
| 단순투자 | - | - | - | - | - | - | - |
| 계 | - | 3 | 3 | 3,548 | 3,500 | - | 7,048 |
| ※상세 현황은 '상세표-3. 타법인출자 현황(상세)' 참조 |
X. 대주주 등과의 거래내용
1. 대주주등에 대한 신용공여등
해당사항 없음
2. 대주주와의 자산양수도 등
해당사항 없음
3. 대주주와의 영업거래
해당사항 없음
4. 대주주 이외의 이해관계자와의 거래
| (단위: 천원) |
| 이해관계자명 | 회사와의 관계 | 제 14기 | 소유지분(%) | |||||
| 매출채권 | 매입채무 | 대여금 | 매출 | 매입 | 피출자 | 출자 | ||
| (주)세레스에프엔디(주1) | 계열회사 | - | - | - | - | - | - | 50.80 |
| (주)알토스바이오로직스(주2) | 계열회사 | - | - | - | 2,600,000 | - | - | 72.56 |
주1) 종속회사인 (주)세레스에프엔디는 21.07.22자에 대여금 30억원을 당사에 상환하였으며. 보고서 작성 기준일 현재 ㈜세레스에프엔디관련 대여금은 없습니다.
주2) 당사는 종속회사인 (주)알토스바이오로직스와 라이선스계약에 따라,
2021년 1월에 (주)알토스바이오로직스로 부터 20억원의 기술료를 수령하였으며,
2021년 4월에 (주)알토스바이오로직스로 부터 6억원의 제3자 라이선스에 따른 기술료를 수령하였습니다(실제 수익인식금액은 현금으로 수령한 26억원과 달리 K-IFRS 수익인식기준에 따라 개별재무제표에 별도로 인식하였으며, 지배종속회사간 내부거래로서 연결재무제표상 수익인식금액은 없습니다).
※종속회사 소유지분율은 보고서 작성 기준일 현재 의결권기준으로 작성하였습니다.
XI. 그 밖에 투자자 보호를 위하여 필요한 사항
1. 공시내용 진행 및 변경사항
해당사항 없음
2. 우발부채 등에 관한 사항
가. 중요한 소송사건
해당사항 없음
나. 견질 또는 담보용 어음ㆍ수표 현황
| (기준일 : 2021.09.30) | (단위 : 매, 백만원) |
| 제 출 처 | 매 수 | 금 액 | 비 고 |
|---|---|---|---|
| 은 행 | - | - | - |
| 금융기관(은행제외) | - | - | - |
| 법 인 | - | - | - |
| 기타(개인) | - | - | - |
다. 채무보증 현황
해당사항 없음
라. 채무인수약정 현황
해당사항 없음
마. 그 밖의 우발채무 등
우발채무 및 약정사항은 「Ⅲ. 재무에 관한사항, 3. 연결재무제표 주석, 주석31.우발채무와 약정사항」과 「Ⅲ. 재무에 관한사항, 5. 재무제표 주석, 주석28. 우발채무와 약정사항」을 참고하시기 바랍니다.
3. 제재 등과 관련된 사항
가. 제재현황
해당사항 없음
나. 한국거래소 등으로부터 받은 제재
해당사항 없음
다. 단기매매차익의 발생 및 반환에 관한 사항
해당사항 없음
4. 작성기준일 이후 발생한 주요사항 등 기타사항
가. 작성기준일 이후 발생한 주요사항
- 종류주식(제3회차 기명식 전환우선주식)의 전환가격 조정
신주인수계약서에 따른 제3회차 기명식 전환우선주식의 전환가격 시가조정으로 인하여(전환가격조정일 : 2021년 11월 13일), 동 우선주의 보통주 전환비율은 1: 1.3838 이며, 전환가격은 71,057원으로 조정되어 공시제출일 현재 우선주의 보통주 전환청구시 발행가능 보통주 주식수는 422,186주입니다.
나. 중소기업기준 검토표
 |
|
중소기업기준검토표-1 |
 |
|
중소기업기준검토표-2 |
다. 외국지주회사의 자회사 현황
해당사항 없음
| (기준일 : ) | (단위 : 백만원) |
| 구 분 | A지주회사 | B법인 | C법인 | D법인 | ... | 연결조정 | 연결 후 금액 |
|---|---|---|---|---|---|---|---|
| 매출액 | - | - | - | - | - | (-) | - |
| 내부 매출액 | ( -) | ( -) | ( -) | (-) | (-) | - | - |
| 순 매출액 | - | - | - | - | - | - | |
| 영업손익 | - | - | - | - | - | ( ) | |
| 계속사업손익 | - | - | - | - | - | ( ) | |
| 당기순손익 | - | - | - | - | - | ( ) | |
| 자산총액 | - | - | - | - | - | ( ) | |
| 현금및현금성자산 | - | - | - | - | - | ||
| 유동자산 | - | - | - | - | - | ||
| 단기금융상품 | - | - | - | - | - | ||
| 부채총액 | - | - | - | - | - | ( ) | |
| 자기자본 | - | - | - | - | - | ( ) | |
| 자본금 | - | - | - | - | - | ( ) | |
| 감사인 | - | - | - | - | - | - | |
| 감사ㆍ검토 의견 | - | - | - | - | - | - | |
| 비 고 | - | - | - | - | - |
라. 법적위험 변동사항
해당사항 없음
마. 금융회사의 예금자 보호 등에 관한 사항
해당사항 없음
바. 기업인수목적회사의 요건 충족 여부
해당사항 없음
사. 기업인수목적회사의 금융투자업자의 역할 및 의무
해당사항 없음
아. 합병등의 사후정보
해당사항 없음
자. 녹색경영
해당사항 없음
차. 정부의 인증 및 그 취소에 관한 사항
해당사항 없음
카. 조건부자본증권의 전환·채무재조정 사유등의 변동현황
해당사항 없음
타. 보호예수 현황
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 주) |
| 주식의 종류 | 예수주식수 | 예수일 | 반환예정일 | 보호예수기간 | 보호예수사유 | 총발행주식수 |
|---|---|---|---|---|---|---|
| 우선주(주1) | 305,078 | 2020.11.25 | 2021.11.25 | 1년 | 사모 3자배정 유상증자에 따른 의무보유 예탁 | 305,078 |
| 우선주(주2) | 723,937 | 2021.01.22 | 2022.01.22 | 1년 | 사모 3자배정 유상증자에 따른 의무보유 예탁 | 723,937 |
주1) 2021년 3월 10일 무상증자 이사회결의로 101,693주가 추가 발행되어 보고서 작성 기준일 현재 보호예수 수량은 305,078주 입니다.
주2) 2021년 1월 7일 납입완료되었으며, 2021년 3월 10일 무상증자 이사회결의로 241,312주가 추가 발행되어 보고서 작성 기준일 현재 보호예수 수량은 723,937주 입니다.
파. 특례상장기업 관리종목 지정유예 현황
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 원) |
| 관리종목 지정요건 | 요건별 회사 현황 | 관리종목 지정유예 여부 |
항목별 지정유예 종료시점 |
|||
|---|---|---|---|---|---|---|
| 항목 | 사업연도 | 금액 | 해당 | 미해당 | ||
| 최근 사업연도말 매출액 30억미만 |
최근 사업연도말 매출액(별도) | 2020 | 26,211,818,564 | - | O | 2019.12.31 |
| 최근 4사업연도 연속 영업손실 발생 | 최근 4사업연도 각 영업손익 (별도) |
2020 | 5,648,881,966 | - | O (주1) |
- |
| 2019 | 911,579,878 | |||||
| 2018 | -7,042,994,527 | |||||
| 2017 | -6,315,112,703 | |||||
| 자기자본 50%이상(10억원 이상에 한함)의 법인세차감전계속사업손실이 최근 3년간 2회 이상 및 최근 사업연도 법인세차감전계속사업손실 발생 | 최근 3사업연도 각 법인세차감전 계속사업손익 (연결) |
2020 | -2,839,347,168 | - | O | 2017.12.31 |
| 2019 | -1,680,700,203 | |||||
| 2018 | -6,033,294,114 | |||||
XII. 상세표
1. 연결대상 종속회사 현황(상세)
| ☞ 본문 위치로 이동 |
| (단위 : 백만원) |
| 상호 | 설립일 | 주소 | 주요사업 | 최근사업연도말 자산총액 |
지배관계 근거 | 주요종속 회사 여부 |
|---|---|---|---|---|---|---|
| (주)엘에스메디텍 | 2006.12.19 | 서울시 마포구 잔다리로 89, 5층(서교동, 성제빌딩) |
의약품 도소매업 |
1,313 | 기업 의결권의 과반수 소유 (지분율 100.0%) (회계기준서 1110호) |
미해당 |
| (주)알토스 바이오사이언스 (주1) |
2011.04.20 | 대전시 유성구 유성대로1628번길 62(전민동) |
의약품 연구 개발업 |
512 | 기업 의결권의 과반수 소유 (지분율 100.0%) (회계기준서 1110호) |
미해당, 피흡수합병으로 소멸(21.08.12) |
| (주)세레스에프엔디 | 2018.06.15 | 충청북도 제천시 바이오밸리2로 100(왕암동) | 의약품 제조 및 판매업 |
17,386 | 기업 의결권의 과반수 소유 (지분율 63.1%) (회계기준서 1110호) |
해당 (직전연도 자산총액이 지배회사 자산총액의 10% 이상인 종속회사) |
| (주)알토스 바이오로직스 |
2020.10.15 | 대전시 유성구 유성대로1628번길 62, 3층(전민동) |
바이오의약품 개발 |
31,400 | 기업 의결권의 과반수 소유 (지분율 100.0%) (회계기준서 1110호) |
해당 (직전연도 자산총액이 지배회사 자산총액의 10% 이상인 종속회사) |
주1) 당사의 종속회사인 주식회사 알토스바이오사이언스와 주식회사 엘에스메디텍은 2021.08.12자로 합병하였으며, 동합병에서 존속회사는 주식회사 엘에스메디텍이며 피흡수합병 소멸회사는 알토스바이오사이언스입니다.
※종속회사 지분율은 보통주 소유지분율입니다.
2. 계열회사 현황(상세)
| ☞ 본문 위치로 이동 |
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 사) |
| 상장여부 | 회사수 | 기업명 | 법인등록번호 |
|---|---|---|---|
| 상장 | 1 | (주)알테오젠 | 160111-0242050 |
| - | - | ||
| 비상장 | 3 | (주)엘에스메디텍 (주1) | 110111-3582271 |
| (주)세레스에프엔디 | 160111-0487226 | ||
| (주)알토스바이오로직스 | 160111-0569206 |
주1) 당사의 종속회사인 주식회사 알토스바이오사이언스와 주식회사 엘에스메디텍은 2021.08.12자로 합병하였으며, 동합병에서 존속회사는 주식회사 엘에스메디텍이며 피흡수합병 소멸회사는 알토스바이오사이언스입니다.
3. 타법인출자 현황(상세)
| ☞ 본문 위치로 이동 |
| (기준일 : | 2021년 09월 30일 | ) | (단위 : 백만원, 주, %) |
| 법인명 | 상장 여부 |
최초취득일자 | 출자 목적 |
최초취득금액 | 기초잔액 | 증가(감소) | 기말잔액 | 최근사업연도 재무현황 |
|||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 수량 | 지분율 | 장부 가액 |
취득(처분) | 평가 손익 |
수량 | 지분율 | 장부 가액 |
총자산 | 당기 순손익 |
||||||
| 수량 | 금액 | ||||||||||||||
| (주)알토스사이언스(주1) | 비상장 | 2013.12.16 | 경영상의 목적 | 361 | 40,000 | 100.00 | 361 | - | - | - | - | - | - | 512 | 5 |
| (주)엘에스메디텍 | 비상장 | 2016.06.03 | 경영상의 목적 | 520 | 104,000 | 100.00 | 520 | - | - | - | 104,000 | 100.00 | 881 | 1,313 | 273 |
| (주)세레스에프엔디 | 비상장 | 2018.06.15 | 경영상의 목적 | 167 | 2,399,997 | 50.34 | 2,167 | 237,642 | 3,500 | - | 2,637,639 | 50.08 | 5,667 | 17,386 | -7,631 |
| (주)알토스바이오로직스(주2) | 비상장 | 2020.10.15 | 경영상의 목적 | 500 | 1,000,000 | 83.77 | 500 | 4,000,000 | - | - | 5,000,000 | 72.56 | 500 | 31,400 | -116 |
| 합 계 | 3,543,997 | - | 3,548 | 4,237,642 | 3,500 | - | 7,741,639 | - | 7,048 | 50,611 | -7,460 | ||||
주1) 당사의 종속회사인 주식회사 알토스바이오사이언스와 주식회사 엘에스메디텍은 2021.08.12자로 합병하였으며, 동합병에서 존속회사는 주식회사 엘에스메디텍이며 피흡수합병 소멸회사는 알토스바이오사이언스입니다.
주2) (주)알토스바이오로직스는 2021년 2월 1일자로 무상증자 400%를 결의하고 무상신주를 발행하였습니다.
【 전문가의 확인 】
1. 전문가의 확인
해당사항 없음
2. 전문가와의 이해관계
해당사항 없음