 |
|
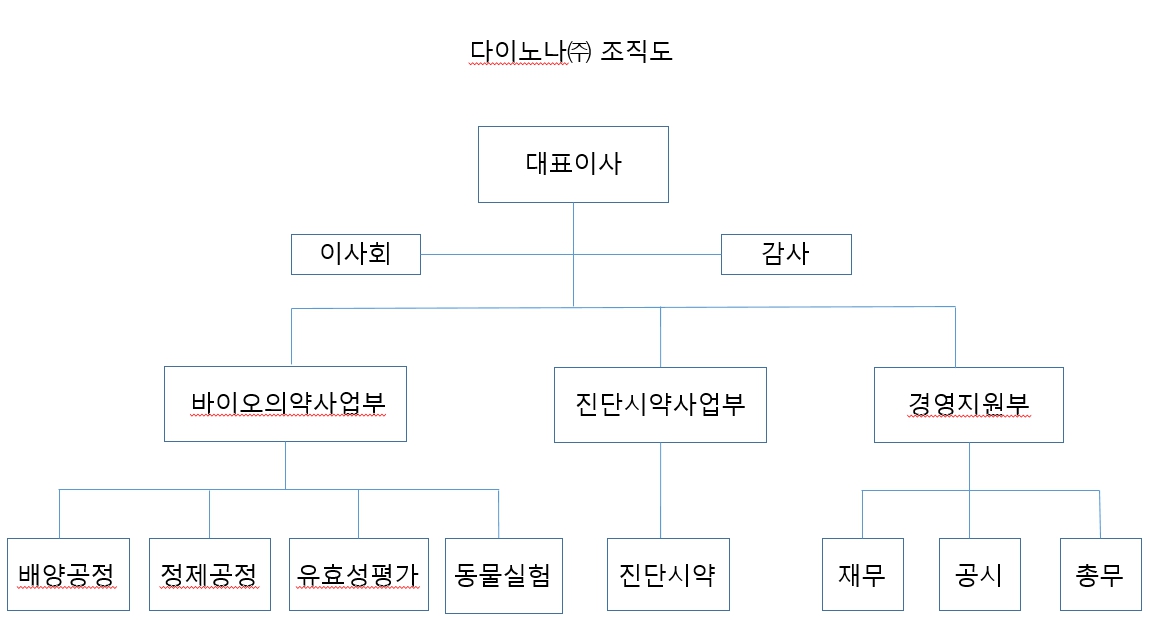
다이노나(주) 조직도 |
주주총회소집공고
| 2021 년 09월 14 일 | ||
| 회 사 명 : | 다이노나 주식회사 | |
| 대 표 이 사 : | 조 경 숙 | |
| 본 점 소 재 지 : | 경기도 성남시 분당구 판교로 228번길 15, 3동 902호 (삼평동, 판교세븐처밸리1) | |
| (전 화) 02-578-0810 | ||
| (홈페이지)http://www.dinonainc.com | ||
| 작 성 책 임 자 : | (직 책) 이사 | (성 명) 김 유 정 |
| (전 화) 02-578-0810 | ||
주주총회 소집공고
| (제23기 임시) |
주주님의 깊은 관심과 성원에 감사드립니다. 본 회사의 정관 제21조에 의하여 다음과 같이 임시주주총회를 개최하오니 참석하여 주시기 바랍니다.
--- 다 음 ---
1. 일시 : 2021년 09월 29일 (수) 오전 09시
2. 장소 : 경기도 성남시 분당구 판교로 228번길 15, 3동 1층 대강당
3. 회의 목적사항 :
<< 부의안건 >>
제 1호 의안 : 회사합병 계약서 승인의 건
4. 경영참고사항
상법 제542조의4에 의한 경영참고사항은 당사 인터넷 홈페이지에 게재하고 본점과 한국예탁원 증권대행부에 비치하였으며, 금융위원회 및 한국거래소에 전자공시하오니 참조하시기 바랍니다.
5. 실질주주의 의결권 행사에 관한 사항
금번 당사의 임시주주총회에는 한국예탁결제원이 주주님들의 의결권을 행사할 수 없습니다. 따라서 주주님께서는 한국예탁결제원에 의결권행사에 관한 의사표시를 하실 필요가 없으며, 종전과 같이 주주총회 참석장에 의거 의결권을 직접행사 하시거나 또는 위임장에 의거 의결권을 간접행사 하실 수 있습니다.
6. 주주총회 참석시 준비물
가. 직접행사 : 주주총회 참석장, 신분증
나. 간접행사 : 주주총회 참석장, 위임장
- 주주의 위임장 원본
(주주와 대리인의 인적사항 기재 후 서명 또는 날인, 법인은 인감날인 필수)
- 주주의 신분증 사본
(법인은 인감증명서 필수)
- 대리인의 신분증
I. 사외이사 등의 활동내역과 보수에 관한 사항
1. 사외이사 등의 활동내역
가. 이사회 출석률 및 이사회 의안에 대한 찬반여부
| 회차 | 개최일자 | 의안내용 | 사외이사 등의 성명 | |||
|---|---|---|---|---|---|---|
| A (출석률: %) |
B (출석률: %) |
C (출석률: %) |
D (출석률: %) |
|||
| 찬 반 여 부 | ||||||
| - | - | - | - | - | - | - |
나. 이사회내 위원회에서의 사외이사 등의 활동내역
| 위원회명 | 구성원 | 활 동 내 역 | ||
|---|---|---|---|---|
| 개최일자 | 의안내용 | 가결여부 | ||
| - | - | - | - | - |
2. 사외이사 등의 보수현황
| (단위 : 원) |
| 구 분 | 인원수 | 주총승인금액 | 지급총액 | 1인당 평균 지급액 |
비 고 |
|---|---|---|---|---|---|
| - | - | - | - | - | - |
II. 최대주주등과의 거래내역에 관한 사항
1. 단일 거래규모가 일정규모이상인 거래
| (단위 : 억원) |
| 거래종류 | 거래상대방 (회사와의 관계) |
거래기간 | 거래금액 | 비율(%) |
|---|---|---|---|---|
| - | - | - | - | - |
2. 해당 사업연도중에 특정인과 해당 거래를 포함한 거래총액이 일정규모이상인 거래
| (단위 : 억원) |
| 거래상대방 (회사와의 관계) |
거래종류 | 거래기간 | 거래금액 | 비율(%) |
|---|---|---|---|---|
| - | - | - | - | - |
III. 경영참고사항
1. 사업의 개요
가. 업계의 현황
(1) 바이오산업의 정의 및 개념
바이오산업(Bioindustry)은 DNA·단백질·세포 등의 생명체관련 기술(Biotechnology)을 직접 활용해 의약품(의약바이오), 농업(그린바이오)뿐만 아니라 화학. 에너지(산업바이오) 및 IT. NT 등 첨단 기술과의 융합(융합바이오)으로 응용 범위가 확대되고 있습니다.
의약 바이오 (Red Biotechnology)는 질병의 치료 등에 활용되는 의약품을 개발하는 분야로서 바이오산업의 최대 구성비를 차지하고 있습니다. 의약 바이오 산업은 재조합 바이오의약품, 저분자 의약품, 재생 의약품 및 의약바이오 기반기술 등으로 구성됩니다.
|
의약바이오 |
재조합 바이오 의약품 |
항체치료제, 단백질의약품, 백신, 유전자의약품 |
|
저분자 의약품 |
저분자 의약품, 천연물 의약품 |
|
|
재생 의약품 |
세포치료제, 조직치료제, 바이오인공장기 등 |
|
|
바이오의약기반 구축기술 |
기반 구축 기술 |
(2) 바이오산업의 특성
(가) 새로운 형태의 첨단기술산업
바이오산업은 바이오기술기반 산업으로서 제품 중심으로 구분하는 타 산업과는 달리 기술 적용 여부에 기초한 새로운 형태의 Biotechnology-based 산업입니다.
(3) 기술 및 지식기반 고부가가치산업
바이오산업은 건강, 식량, 환경부문 등의 인류 난제의 해결과 직결된 기술 및 두뇌집약적인 고부가치 지식기반 산업이며, 최근 5년간 생산액 기준의 국내 바이오산업 연평균 성장률은 28% 이르고 있습니다. 글로벌 신약 1개의 연간 부가가치는 자동차 300만대 수출과 동일합니다.
|
구분 |
신약 1개 품목 |
자동차 300 만 대 |
|
수익률 |
30% |
0.96% |
|
순이익 |
3,000 억원 |
2,900 억원 |
(4) High Risk / High Return, Long Term Investment 산업
투자 금액이 높고 회수기간이 길어 장기투자가 필수적이며, 성공시 높은 수익이 보장되나 성공에 대한 위험성이 존재하는 산업으로서 신약 개발을 위해서는 최소 10년간약 수 억 달러 이상의 자금이 소요됩니다.
(5). 바이오의약품바이오 의약품 산업으로의 변화
기존 저분자 의약품 산업이 심각한 위기에 직면한 가운데, 바이오의약품바이오 의약품 분야가 전체 의약바이오 산업의 성장을 견인하는 동력으로 작용하고 있습니다. 다국적 제약사들의 바이오 신약은 이미 전 세계 의약품 매출의 성장을 견인하고 있고, 국내에서도 최근에는 기존 제약사들은 물론 대기업까지 바이오의약품바이오 의약품 산업에 진출하고 있습니다.
이벨류에이트에 의하면 2018년 세계 Top 100 제약품목 중에서 바이오의약품바이오 의약품은 53%에 달하고 있으며, 2024년에도 50%를 유지할 것으로 전망되며, 매출 측면에서도 2018년에 이미 화학화합물보다 바이오의약품바이오 의약품이 앞서는 것으로 알려졌습니다.
(6). 바이오신약개발 시장자료
(6)-1. 바이오의약품바이오 의약품 시장
2018년 기준 전체 의약품 시장은 8,640억 달러이며 바이오의약품바이오 의약품 시장은 2,430억 달러로 전체 의약품 시장의 28%을 차지하는 것으로 추정됩니다. 바이오의약품바이오 의약품 시장은 2024년까지 5년 연평균 8.5% 성장을 지속하여 2024년 3,880억 달러 규모 시장으로 성장할 것입니다.
출처: Evaluate Pharma(2019)
2017년 전세계 매출 상위 의약품중에서 오리지널 바이오의약품바이오 의약품이 매출 상위 10위 중에서 8종을 차지하고 있어 오리지널 바이오의약품바이오 의약품의 저력을 확인할 수 있습니다.
2017년 10대 의약품 매출액
|
순위 |
제품명 |
판매 기업명 |
2017년 매출액(십억 달러) |
구분 |
|
1 |
Humira |
AbbVie |
18.4 |
단클론항체단클론 항체 |
|
2 |
Revlimid |
Celgene |
8.2 |
합성의약품 |
|
3 |
Rituxan |
Roche |
7.5 |
단클론항체단클론 항체 |
|
4 |
Herceptin |
Roche |
7.1 |
단클론항체단클론 항체 |
|
5 |
Avastin |
Roche |
6.8 |
단클론항체단클론 항체 |
|
6 |
Remicade |
Johnson & Johnson |
5.8 |
단클론항체단클론 항체 |
|
7 |
Prevnar 13 |
Pfizer |
5.6 |
백신 |
|
8 |
Enbrel |
Amgen/Pfizer |
5.4 |
융합단백질 |
|
9 |
Lantus |
Sanofi |
5.2 |
재조합단백질 |
|
10 |
Lyrica |
Pfizer |
5.1 |
합성의약품 |
출처: Nature Reviews Drug Discovery vol.17, 232 (2018)
의료비 재정부담 축소, 의약품 환자 접근성 개선 차원에서 저렴함 바이오 복제의약품 사용이 장려되고, 블록버스터급 신약의 특허가 2020년에 대거 만료되어 바이오시밀러의 시장점유율이 증가하는 추세입니다만, 바이오의약품바이오 의약품 신약 시장은 2025년까지 4,220억 달러의 시장규모로 확대되고 여전히 매우 높은 86.5% 점유율을 차지할 것으로 예상됩니다.
출처: Frost&Sullivan (2016)
(6)-2. 유망한 바이오 의약품
세계 의약품 시장은 항암제, 면역억제제 및 피부질환치료제가 향후 성장을 견인할 것으로 예측됩니다. 또한 예상치 못했던 COVID-19 발발에 의하여 COVID-19 비상상황을 해결할 수 있는 치료제 및 백신의 수요가 폭발적으로 증가하였습니다.
항암제 부문은 단클론 항체를을 포함한 신약의 출시 및 승인, 항암제 영역 전문기업의 활동역량강화, 암 진환의 초기 진단 증가등의 원인으로 2024년까지 최대 의약품 시장 지위를 강화할 것으로 예상됩니다. 2019년 세계 항암제 시장은 1413억 달러로 평가되고 있으며 연평균 11.6%로 성장하여 2027년에는 3942 달러까지 성장할 것으로 예측됩니다.
출처: Fortune Business Insights
항암제 뒤를 이어 면역 억제제와 피부질환치료제는 연평균 성장률 15.7%, 12.6%로 각각성장 할 것으로 전망됩니다.
(6)-3. 항체치료제 시장
항체치료제는 가장 유망하고 빠르게 성장하고 있는 치료제 영역의 한 분야입니다. 항체치료제는 1980년대에 첫 선을 보였으나, 임상적으로나 상업적으로 성공을 거두지 못하다가 1990년대에 이르러 분자생물학, 유전학, 세포생물학, 면역학과 같은 기초과학의 발전과 더불어 파지 디스플레이 및 형질전환 생쥐와 같은 항체공학기술이 제약 산업에 응용됨으로써 새로운 관심을 가지게 되었습니다. 전 세계적으로 65여 종의 이상의 항체치료제가 승인되어 항암, 항 염증, 자가면역 질환, 안구질환, 항 감염 등의 치료에 이용되고 있으며, 약 350개 정도의 항체치료제 후보물질이 임상개발 단계에 진입해 있습니다.
전세계 항체치료제 분야를 보면, 2016년 866억불에서 2024년 1,386억불까지 가파른 성장세를 보일 것으로 전망되며, 질환 별로는 항암용 항체치료제 (2024년 688억불)와 자가면역질환 항체치료제 (2024년 316억불)가 1위, 2위를 점할 것으로 보고되고 있습니다.
최근의 의약품 분야 Top 10에 대한 전망 보고서를 보더라도 항암분야가 단일 분야로서 약 20%의 점유율과 12%의 성장률을 2024년까지 꾸준히 유지할 것으로 전망됩니다. 자가면역질환 분야는 류마티스성 질환, 당뇨성 질환, 면역억제 분야 등으로 세분화되어 각각 시장점유율은 유사한 반면, 성장률 전망은 각 시장 상황에 따라 다르게 전망되고 있습니다.
치료제 분야에서 가장 시장 규모가 큰 분야인 항암제 시장에서, 단연 주목을 받고 있으며 더욱 폭발적 성장세를 끌고 갈 분야는 면역항암제 분야입니다. 면역체크포인트에 대한 항체치료제로서 항암제 분야의 시장을 선두에서 이끌고 있습니다.
위 2018년 및 2024년 Top10 제약 매출액 및 전망을 보면, 항 PD-1 항체 Keytruda는 2018년 매출액 7,198백만불에서 2024년에는 매출 1위인 휴미라를 뛰어넘어 20,485백만불이 될 것으로 전망되고 있습니다.
나. 회사의 현황
(1) 연구개발개황
1. 다이노나 연구개발 현황
아사는 항체기술을 기반으로 항체 관련 치료 및 진단제를 연구, 개발하고 있으며 기술이전 등을 통한 사업화를 기본 비즈니스 모델로 하는 바이오신약 개발 전문기업입니다. 동사의 주력 연구분야는 항암제와 면역억제제로서 주요 적응증은 위암, 대장암, 비소세포폐암, 췌장암, 자가면역질환 및 장기이식입니다.
[다이노나㈜ 신약개발 진행현황 요약]
|
질환군 |
과제 코드명 |
적응증 |
연구개발 단계 |
|
면역항암제 |
DNP002 |
위암, 대장암, 비소세포폐암, 췌장암 |
임상1상 |
|
DNP005 |
고형암 |
Humanization In vivo 효능 최적화 |
|
|
면역조절제 |
DNP007 |
자가면역질환(류마티스 관절염, 다발성경화증) |
임상1상 시험을 위한 IND 제출완료 |
|
장기 이식 면역 억제 |
|||
|
감염병치료제 |
DNP019 |
COVID-19 |
비임상 진입 |
한편, 동사는 상기와 같은 파이프라인을 바탕으로 기술이전을 통한 중·장기 성장전략을 추구하고 있습니다. 암세포 특이적이며 에피토프 특이적인 항체 후보를 발굴하여 비임상 및 임상 개발 진도에 따라 기술이전 등을 통해 수익을 확보해 나가고 있습니다. 또한 이렇게 확보한 수익을 통해 추가적인 파이프라인 개발, 시장 및 적응증 확대를 위해 노력하고 있습니다.
이러한 노력의 결과, 2018년 2월에는 유가증권시장 상장법인인 에이프로젠케이아이씨를 대상으로 DNP004, DNP001, 항-CD47 및 항-PD-1 단클론항체단클론 항체 파이프라인에 대해 기술이전 계약을 체결하였습니다.
이러한 글로벌 제약사 및 국내 기업과의 기술이전은 향후 더욱 확대될 것으로 예상되고 있으며, 또한 해당 물질의 임상시험의 긍정적인 진행, 추가 파이프라인 임상 및 개발 등으로 인해 향후 추가 기술이전에 대한 긍정적 결과가 예상됩니다.
DNP002 프로젝트는 현재 1상 임상시험을 위한 IND 승인을 득하고 안전성/내약성 및 임상효과를 확인하기 위한 초기 임상시험에 진입하였습니다. DNP007 과제 또한 1상 임상시험을 위한 IND 제출을 완료한 상태이입니다. 2021년 IND 승인을 득하고 임상시험준비 과정을 거쳐 며 20212022년 1분기에 임상시험에 진입할 것으로 예상하고 있습니다. 이외에 COVID-19 감염병 치료를 위한 DNP019 프로젝트와 고형암 전반에 응용가능한 DNP005 프로젝트는 초기 연구를 완료하고 비임상 개발에 진입할 예정입니다.
2. 주요 파이프라인 개발현황
(1)-1. DNP002 항체치료제 개발현황
DNP002는 CEACAM-6 (CD66c)을 인지하는 단클론항체단클론 항체로 CEACAM6를 과 발현하는 암세포와 면역을 억제하여 종양 세포 성장을 조력하는 MDSC (Myeloid-derived suppressor cells)을 동시에 제거할 수 있는 신규항암항체 치료제입니다.
[Target Product Profile]
|
Code Name |
DNP002 (Humanized IgG1/kappa, afucosylated antibody) |
|
Target |
CEACAM6 (CD66c) |
|
MOA |
Enhanced ADCC, dual targeting (CEACAM6 expressing tumor and MDSC) |
|
Parma/Tox |
Efficacy: cancer cell lines (in vitro) and mouse model (in vivo) 4 week repeated dose toxicity study in monkey |
|
Development Stage |
Phase 1 study in South Korea |
|
CMC (DS, DP) |
DS production: CHO-K1 based MCB established, 6 g/L, purification yield: 60%, DP: Colorless to pale yellow clear solution (10.0 mg/mL, 10.0 mL/vial) |
|
Route/Dosing |
IV/Every 2 or 3 weeks |
|
Indication |
Gastric, Colorectal, Lung, Pancreatic Cancer etc |
|
Competitor |
Bayer, PrecisionBiologics, Merck |
|
Originator |
DiNonA INC. |
(1)-2. DNP002 작용기전
DNP002는 NK 세포 매개 ADCC (Antibody dependent cellular cytotoxicity) 활성으로 표적 종양세포 및 MDSC 세포를 동시에 제거할 수 있습니다. 더욱이 DNP002는 당쇄 푸코스 함량을 낮추어 현저히 강화된 ADCC 효능을 구현한 afucosylated 단클론 항체입니다.
DNP002는 MDSC를 제거하여 미세종양환경의 면역 억제 상황을 면역 활성으로 유도하고 직접 종양세포 사멸까지 유도할 수 있어 전반적인 항암 작용을 상승시킬 것으로 기대됩니다.
(1)-3. 핵심 경쟁 우의
DNP002는 강화된 ADCC 기전으로 종양세포 성장을 저해할 수 있을 뿐만 아니라 MDSC를 함께 공략하여 미세종양환경을 면역활성 상태로 되돌릴 수 있어 항암효능 시너지 효과를 나타낼 수 있습니다.
현재 사용되고 있는 대장암을 포함한 종양치료제들과는 전혀 다른 표적을 타깃하고 있고 기전도 달라 기존 항암제와 병용화과를 기대할 수 있습니다.
(1)-4. 개발진척 현황
2018년 10월 15일 국가 항암 신약개발사업단 후보로 선정 (프로젝트명: NOV1803, 후보명: H2319)되어 2020년까지 비임상 개발 완료하였습니다. 2020년 6월 22일 한국 식약처에 고형암 대상 임상1상 시험에 대한 IND를 제출하여 2020년 8월 26일 임상시험계획을 승인받았습니다. 2020년 12월 현재 임상시험 피험자 권리와 안전을 담보하기 위한 생명윤리위원회 승인절차를 두 개 임상기관 (서울아산병원, 국립 암센터)에서 진행하고 있습니다. 실질적인 1상 임상시험은 2021년 1~2월에 진입할 수 있을 것으로 예상하고 있습니다.
[DNP002 개발 예상일정]
|
|
2020년 |
2021년 |
2022년 |
2023년 |
2024년 |
2025년 |
|
DNP002 개발 일정 |
IND 및 IRB 승인 |
1상 임상시험 (한국) |
Global 2상 임상시험 |
Global 3상 임상시험 |
||
(1)-5. 시장현황
비소세포폐암, 대장암, 위암, 췌장암등에서 DNPP002 표적항원 CEACAM6가 과 발현하고 NK 세포를 이용한 ADCC 기전으로 종양세포를 제거할 수 있으므로 DNP002 1차 적응증은 상기 4개 암종으로 압축할 수 있습니다. 그러나 DNP002는 MDSC를 제거하여 항암 효과를 유도할 수 있으므로 종양세포에 CEACAM6 표적항원이 없더라도 항암효능을 기대할 수 있어 모든 종양으로 시장이 확장될 가능성이 있습니다.
DNP002 1차 적응증에 해당하는 4개 종양치료제 시장은 2026년 732억 달러까지 성장할 것으로 예상됩니다.
[DNP002 적응증 및 시장규모]
|
|
연평균 성장률 |
2026년 시장규모 |
|
비소세포폐암 |
13.4% |
437억 달러 |
|
대장암 |
7.6% |
166억 달러 |
|
위암 |
15.3% |
82억 달러 |
|
췌장암 |
10.2% |
47억 달러 |
|
소계 |
|
732억 달러 |
비소세포폐암은 2018년 기준 160억 달러 시장 가치였으며 연평균 13.4%로 성장하여 2026년에는 437억 달러 시장으로 성장 예상됩니다. 치료제 기전을 중심으로 시장을 나눠보면 표적치료제 (bevasizumab, dabrafenib/trametinib, erlotinib, hydrochloride, osimetrinib 등), 면역치료제 (durvalumab, nivolumab, atezolizumab, pembrolizumab) 그리고 화학항암제로 삼분할 수 있으며 2018년 기준 표적치료제가 약 50% 점유유를 차지하고 있습니다.
DNP002는 암세포를 직접 제거하는 표적치료제의 특성과 면역억제 MDSC 세포를 제거하여 면역증진을 유발하는 면역 함암제 기전을 함께 보유하고 있습니다. 그러나 DNP002는 기존 혈관생성억제, B-Raf 또는 EGRF 신호전이 억제제제와 같은 표적치료제와 전혀 다른 타깃(CEACAM6)을 표적하기 때문에 경쟁관계 약물이 될 수 도 있으나 병용치료로 응용하여 시너지효과를 유발 수도 있습니다. 반면 비소세포폐암 치료용도의 면역 항암제는 모두 PD-1/PDL-1 상호작용을 억제하는 치료제로 구성 되어있습니다.
전세계 대장암 치료제 시장은 2018년 기준 92억 달러로 집계되었고 연평균 7.6%씩 성장하여 2026년에는 166억 달러에 달하는 시장으로 성장 전망됩니다.
전세계 위암(stomach/gastric cancer) 치료제 시장은 2018년 기준 26억 달러에 달하고 연평균 15.3%씩 성장하여 2026년에는 82억 달러에 달하는 시장으로 전망됩니다.
전세계 췌장암 치료제 시장은 연평균 10.2%씩 성장하여 2027년에는 47억 달러에 달하는 시장으로 성장 전망됩니다(Oct 06, 2020, Market Insight Reports).
(2)-1. DNP007 항체치료제 개발현황
DNP007은 ICAM-1에 결합하는 인간화항체로 수지상세포 성숙을 조절하여 T-세포 면역을 억제할 수 있는 항체 치료제입니다. DNP007은 자가면역질환 또는 장기이식에 필요한 면역관용을 유도할 수 있는 신규한 기전을 가지고 있어 전반적인 면역 억제를 유도하여 부작용이 심각한 면역억제제와 차별성을 가지고 있습니다.
[Target Product Profile]
|
Code Name |
DNP007 (Humanized IgG4/kappa) |
|
Target |
ICAM-1 (CD54) |
|
MOA |
Immune tolerance through induction of tolerogenic dendritic cell |
|
Parma/Tox |
Efficacy: Immune cells (in vitro) and nonhuman primate model (in vivo) 4 week repeated dose toxicity study in monkey |
|
Development Stage |
IND Submission |
|
CMC (DS, DP) |
DS production: CHO-K1 based MCB established, 1 g/L, purification yield: 70%, DP: Slightly brown and opalescent solution (20.0 mg/mL, 10.0 mL/vial) |
|
Route/Dosing |
Intravenous |
|
Indication |
Autoimmune disease, Organ transplantation |
|
Competitor |
Abbvie, Pfizer, Janssen |
|
Originator |
DiNonA INC. |
(2)-2. DNP007 작용기전
DNP007는 ICAM-1 domain-2을 인지하는 인간화 항체로 수용체-리간드 결합에는 영향을 주지 않고 수지상세포를 통해 면역반응을 조절합니다. DNP007은 면역관용 수지상세포를 이용한 T-세포 활성과 증식억제 기전을 가지고 있습니다.
항원 특이적으로 면역관용을 유도하는 DNP007 특성을 이용하여 이종이식 (당뇨병 원숭이에 돼지 췌도 이식) 및 동종 장기 이식(영장류)등의 시험으로 면역관용 효과 및 임상적가치를 증명하였습니다. DNP007은 장기이식 뿐만 아니라 대표적인 자가면역질환으로 알려진 류마티스 관절염모델에서도 자가면역으로 관절을 보호하는 효능을 나타냈습니다.
[DNP007 면역관용 유도 효력 시험]
|
응용분야 |
모델/이식장기 |
치료방법 |
면역관용 유도기간 |
|
장기이식 |
돼지-인간화항체/췌도 |
장기 이식 이전 3회 단독투여 |
70일 이상 |
|
돼지-원숭이/췌도 |
장기 이식 이전 3회 병용투여 |
150-362일 |
|
|
원숭이-원숭이/간 |
장기 이식 이전 3회 병용투여이후 3달 투여, 모든 약제 투여 종료 |
<750일 |
|
|
류마티스 관절염 |
원숭이 |
콜라겐 면역 1주전 후 4회 단독투여(초기 발병환자 대상) |
56일 |
|
원숭이 |
콜라겐 면역 2주전 후 2회 단독투여(경증, 중증도 환자 대상) |
76일 |
(2)-3. 핵심 경쟁 우의
현재까지 개발된 면역억제제들은 골수를 포함한 장기이식 성공율을 크게 개선하였고 자가면역질환 치료에도 효과적으로 쓰이고 있으나, 전신면역기능 억제에 따른 세균 및 바이러스 감염, 신장독성, 당뇨, 고지질혈증, 동맥성 고혈압, 심혈관질환, 골다공증, 신경독성, 조혈계 독성, 그리고 암 발생 등의 부작용이 있습니다.
새로이 개발되는 면역억제 약물로는 면역기능에 관여하는 세포표면 분자를 표적하는 약제, 세포내 신호전달 억제 약물, T 세포 증식 억제제 그리고 면역세포이동에 영향을 주는 약물 들이 있으며, 특히 장기이식에서는 부작용이 많은 calcineurin 억제제와 스테로이드가 필요 없는 면역억제 프로토콜을 확립에 주력하는 상황입니다.
DNP007 치료제는 장기이식, 골수이식, 및 자가면역질환에서 면역관용 유도방식의 치료법은 장기간 면역 억제제를 투여할 필요가 없으므로 현재 면역억제요법의 수많은 문제점을 해결할 수 있는 최선의 대안입니다.
(8)-2-3. 개발진척 현황
본 과제는 산업기술혁신사업 제1세부 바이오 의약품용[김1] 세포배양 시스템개발 과제로 선정되어 2020년까지 비임상 개발 완료하였습니다. 2020년 11월 16일 한국 식약처에 일반 임상시험에 대한 IND를 제출하였으며 2021년 01월경 임상시험계획 승인을 예상하고 있습니다.
2020년 12월 현재 임상시험 기관 선정, 생명윤리위원회 승인을 위한 준비 작업을 진행하고 있습니다.
[DNP007개발 예상일정]
|
|
2020년 |
2021년 |
2022년 |
2023년 |
2024년 |
2025년 |
|
DNP007 개발 일정 |
IND 제출 |
IND, IRB 승인 |
임상1상(자가면역질환, 장기이식) |
Global 임상2상 |
||
(2)-4. 시장분석
면역관용을 유도할 수 있는 DNP007은 장기이식용 면역억제제와 자가면역질환 치료제로 응용 가능합니다.
장기이식용 면역억제제는 calcineurin inhibitor, mTOR inhibitor, 증식억제제, 스테로이드와 항-CD3, CD20, CD25 단클론항체단클론 항체 치료제들이 사용되며, 대부분 T-세포 활성과 증식을 억제하거나 T-세포를 제거하는 기전입니다. 2018년 기준 전세계 장기이식 면역억제제 시장은 46억 달러로 조사되었고 3.3% 연평균성장률을 나타내고 있습니다.
자가면역질환을 대표하는 류마티스 관절염 치료제 시장은 2017년 기준 238억 달러로 조사되었고 연평균성장류 4.6%로 성장하여 2025년에는 340억 시장으로 성장 전망됩니다.
류마티스 관절염 치료제는 생물학제제와 비생물학제제로 나눌 수 있으나 생물학제제가 대부분의 시장을 차지하고 있고, 생물학제제 중 대부분은 TNF (Tumor necrosis factor) inhibitor입니다.
전세계 TNF inhibitor 시장은 2018년 기준 400억 달러로 평가되었고 연평균 0.5% 성장률이 기대됩니다. TNF inhibitor 치료제로 Humira (Adalimumab)와 Remicade (Infliximab) 항체치료제, 항체 Fc를 TNF 수용체에 접합한 Enbrel (Etanercept)이 시장 대부분을 차지하고 있습니다. TNF inhibitor는 TNF cytokine에 의해여 유발되는 염증성 질환 치료에 사용되며 대상 질환으로 류마티스 관절염, 건선, Crohn’s disease 등이 있습니다. DNP007은 수지상세포를 경유하여 면역관용을 유도하므로 TNF inhibitor 보다 더 효과적으로 자가면역질환을 치료할 수 있을 것으로 예상되면 TNF inhibitor 시장을 대체할 수 있을 것으로 기대됩니다.
DNP007은 상술한 바와 같이 장기이식용 억제제와 TNF inhibitor을 대체할 수 있으므로 글로벌 3상 임상시험이 개시될 것으로 기대하고 있는 2026년 기준으로 476억 달러 시장으로 예측됩니다.
[DNP007 시장규모]
|
구분 |
연평균 성장률 |
2026년 시장규모 |
|
장기이식 면역억제제 |
3.3% |
60억 달러 |
|
TNF 저해제 |
0.5% |
416억 달러 |
|
소계 |
|
476억 달러 |
(3)-1. DNP005 항체치료제 개발현황
DNP005는 수지상세포, B-림프구, 단핵구등에 발현하여 선천성면역과 후천성면역을 연결하고 면역을 조절하는 CD40 타깃 인간화항체로 수지상세포 활성화를 유발하여 전반적인 면역활성을 유도할 수 있습니다. DNP005는 면역활성 유발 특성을 이용하여 항암제와 면역증강보조제 등으로 응용가능 합니다.
[Target Product Profile]
|
Code Name |
DNP005 (Humanized IgG2/kappa) |
|
Target |
CD40 |
|
MOA |
Immune activation through acceleration of dendritic cell differentiation |
|
Pharmacology |
Efficacy: Immune cells (in vitro) and mouse model (in vivo) |
|
Development Stage |
Non-clinical development |
|
CMC |
Humanization |
|
Route/Dosing |
Intravenous |
|
Indication |
Hematological cancer, Neoplasm |
|
Competitor |
Roche, Apexigen, Seattle genetics |
|
Originator |
DiNonA INC. |
(3)-2. DNP005 작용기전
수지상세포, B-세포 및 단핵구등은 CD40을 발현하고 CD40L와 상호작용하여 면역반응을 활성화할수 있습니다. CD40 길항제는 CD40L 기능을 대체하여 수지상세포 분화를 촉진함으로써 후천면역 중심세포인 T-세포 활성화와 증식까지 유도할 수 있습니다.
DNP005는 강력한 CD40 길항제 기전으로 면역증진 및 항암 효능을 유도할 수 있습니다.
참조: Clinical Development of Immunostimulatory Monoclonal Antibodies and Opportunities for Combination, Clinical Cancer Research, 19(5): 997, 2013, 그림 1.
(3)-3. 핵심 경쟁 우의
DNP005는 면역을 활성화하여 항암효과를 유도하는 주요 기전을 가지므로 모든 종양 치료에 응용 가능하여 시장잠재력이 막대합니다.
임상개발중인 경쟁물질 대비하여 DNP005는 동등이상의 길항제 효과를 나타낼 뿐만 아니라 B-세포 유래 림프종 자가살상을 유도하는 특성을 가지고 있어 림프종 치료제로 뛰어난 잠재력이 있습니다.
(3)-4 개발진전척 현황
마우스 유래 항체에서 CDR(Complementarity-determining region) 부위를 인간항체로 옮겨 인간화항체 제작을 완료하였으며 생물학적, 물리화학적 특성평가를 완료하였습니다. 가장 안전하고 효과적인 항체 포맷을 설정하기 위하여 3가지 아형(IgG1, IgG2, IgG4)을 개발하고 평가완료 하였습니다.
(3)-5. 시장분석
면역항암제는 Yervoy (항 CTLA-4 항체), Opdivo (항 PD-1 항체), Keytruda (항 PD-1 항체)가 시장에 출시되면서 기존 표적치료제 중심의 항암시장의 패러다임을 면역시스템을 적극 활용하는 방향으로 전환시킨 새로운 범주의 치료제입니다. 면역항암제는 악성흑색종(melanoma)으로 승인되어 시장에 출시되었지만, 특정 암에 고정된 것이 아니라 다양한 종류의 암에 적용할 수 있기 때문에, 시장 규모 또한 기존 단일 적응증 시장에 비해 매우 큰 규모입니다. 면역체크포인트 억제제 뿐만 아니라, 면역활성을 촉진하는 항체치료제 및 다양한 새로운 면역항암제와 병용 치료 시장을 동력으로 하여 성장률 또한 21.8%로서 매우 높게 평가되고 있습니다.
면역항암제는 2019년 기준으로 120억 달러 규모로 평가되었으며 연평균 21.8% 비율로 20205년까지 급속하게 성장할 것으로 예상됩니다.
DNP002는 MDSC 제거 기전의 면역항암제로, DNP005는 면역활성 촉진제로 서로 다른 작용기전이나 결과적으로는 면역시스템 활성화를 통한 항암 효능을 유발할 수 있는 유사 기능의 항체치료제 입니다.
(4)-1. DNP019 항체치료제 개발현황
SARS-CoV-2는 ACE-2(Angiotensin-Converting Enzyme 2, 이하 ACE-2)을 수용체로 사용하여 인체 세포로 침입하는데, ACE-2에 결합하는 바이러스 단백질을 spike protein라 합니다. Spike protein은 두 개의 S1과 S2로 명명한 subunit으로 구성됩니다. S1 subunit은 ACE-2을 인지하여 결합겹합하는[김2] 역할을 하고 S2 subunit은 바이러스와 숙주세포막의 융합을 유발하는 기능을 담당하고 있습니다.
DNP019는 S1 protein 중에서도 ACE-2와 직접 접촉하는 RBD (Receptor Binding Domain, 이하 RBD)을 인지/결합하는 인간 항체이다. SARS-CoV-2 바이러스 감염은 ACE2와 Spike protein 간의 상호작용이 1차적으로 필요하나 DNP019는 S1과 ACE2 상호작용을 방해하여 SARS-Cov-2 감염경로를 차단하고 인간 숙주세포를 보호할 수 있습니다.
(4)-2. 핵심 경쟁 우의
DNP019는 사람 B-림프구에서 분리한 항체로서 아사에서 개발하고 있는 인간화항체와 달리 완전한 인간 항체입니다. DNP019 항체는 10 ug/mL 이상의 농도에서 S1 spike protein과 ACE-2 단백질간의 상호작용을 완전하게 억제하는 효능을 나타내었습니다.나타냈습니다.
(4)-3. 개발진척현황
SARS-CoV-2 감염억제 유효활성을 가지는 후보 인간화항체를 발굴하고 물리화학적 안정성을 확인하였습니다. 2020년 12월 현재 비임상 개발을 준비중입니다.
(4)-4. 시장분석
전세계 항-바이러스 의약품은 2019년 약 522억 달러에서 2020년 599억 달러로 증가하였고, 2023년까지 약 4.6% 연평균성장률을 나타낼 것으로 전망됩니다. 항-바이어스 치료제는 human immunodeficiency virus (HIV), hepatitis, influenza 그리고 SARS-Cov-2 등과 같은 바이러스 감염병 치료제로 구성됩니다. 그러나 SARS-Cov-2는 2019년 말경 갑자기 발병하였고 현재까지 선행치료제도 없어 구체적인 시장분석은 어려운 상황입니다.
3. 연구개발 실적
가. 개발실적
다이노나㈜는 암세포 특이적이며 에피토프 특이적인 항체 발굴 기술, 면역기능을 조절하는 항체 발굴 기술을 기반으로 현재까지 5 종류의 항체치료제 후보와 추가적인 후보항체를 개발하였습니다.
|
질환군 |
과제 코드 명 |
적응증 |
연구개발 단계 |
|
면역조절제 |
DNP007 |
류마티스성 관절염 |
1상 임상시험 IND 제출(자가면역질환) 장기이식 비임상 유효성 실험 (서울대학교 병원) 산자부 창의산업미래성장동력사업 진행중 서울대병원 연구중심병원 과제 진행중 |
|
다발성 경화증 치료제 (Multiple sclerosis) |
|||
|
장기 이식 면역 억제 |
|||
|
면역항암제 |
DNP002 |
비소세포폐암 |
임상 1상 시험 진행중 |
|
DNP005 |
고형암 |
- Humanization 완료 - In vivo 효능 최적화 완료 |
|
|
PD-1 |
고형암 |
후보발굴 완료, 2018년2월 에이프로젠KIC 기술이전, 에이프로젠KIC 에서 후속 개발 |
|
|
TIM-3, LAG-3 |
고형암 |
후보발굴 완료 |
|
|
표적치료제 |
DNP004 |
유방암 |
- GMP 공정 개발 중. - in vivo 효능 최적화 * 2018년2월 에이프로젠KIC 기술이전, 에이프로젠KIC 에서 후속 개발 |
|
DNP001 |
급성백혈병 /골수이형성증후군(MDS)/위암 |
- CAR-T 또는 이중항체로 최적화 * 2018년2월 에이프로젠KIC 기술이전, 에이프로젠KIC 에서 후속 개발 |
당사는 위 제품들의 개발과 관련하여 정부 및 유관 기관에서 지원하는 연구개발 과제들을 수행 중이거나 성공적으로 완료하였습니다.
|
|
DNP001 프로젝트 |
|
|
연구과제 |
급성백혈병에 대한 신규 항체치료제 DNP001의 임상 1상 개발 |
DNP001 CAR-T 개발 |
|
연구기관 |
다이노나㈜ 범부처전주기신약개발사업단과제 (14.09.01~16.09.30), 정부출연금: 2,020백만원 |
다이노나㈜ 내부과제 (DN-16-01) |
|
연구결과 및 기대효과 |
* 급성백혈병 환자 18명 1상 완료 * 임상용의약품에 의한 부작용없음 * NK비율 높은 환자에서 효능확인 |
* 종양특이적 반응에 기반한 DNP001 항체의 특성을 살린 CAR-T 제작, In vitro 효능 확인 * 급성백혈병 및 위암 세포주 이용한 in vitro 활성 확인 |
|
연구결과가 상품화된 경우 그 내용 |
해당없음. |
해당없음. |
|
연구결과가 상품화되지 않은 경우 그 이유 |
* 에이프로젠KIC 에 기술이전 계약 체결 (2018.02.27)되어, 에이프로젠KIC 에서 후속 개발 중. |
|
|
|
DNP004 프로젝트 |
|
|
연구과제 |
스마트 바이오 생산시스템 개발 |
DNP004 비임상 개발 |
|
연구기관 |
다이노나㈜ 미래선도산업 기술개발사업 (산업통상자원부) 과제 (15.06.01~17.05.31), 정부출연금: 499백만원 |
다이노나㈜ 내부과제 (DN-11-02) |
|
연구결과 및 기대효과 |
* 인간화 항체 개발 * 제조 공정 개발, 국산화 리액터 배양 공정 개발 * 삼중음성 유방암 동물모델에서 뛰어난 효능 확인 |
* 4 g/L 수준의 고생산 세포주 및 공정 개발 * 유방암, 신장암, 대장암 등 다양한 고형암 동물모멜에서 추가 효능 확인 |
|
연구결과가 상품화된 경우 그 내용 |
해당없음. |
해당없음. |
|
연구결과가 상품화되지 않은 경우 그 이유 |
* 에이프로젠KIC 에 기술이전 계약 체결 (2018.02.27)되어, 에이프로젠KIC 에서 후속 개발 중. |
|
|
|
DNP007 프로젝트 |
|
|
연구과제 |
동종 췌도 이식 면역유도요법을 위한 MD3 치료용항체의 개발 (마일스톤 1) |
영장류 류마티스성 관절염 및 다발성 경화증 모델에서의 효능 개발 |
|
연구기관 |
다이노나㈜ 범부처전주기신약개발사업단과제 (13.02.14~15.02.13), 정부출연금: 499백만원 |
창의상업미래성장동력 사업, 바이오의약품바이오 의약품용 세포생산 시스템개발(과제번호: 10053256) 참여기관(2015.06.01~2020.11.30) |
|
연구결과 및 기대효과 |
* 영장류 동종췌도 이식 면역거부반응 억제 효능 확인 * 세계 최장기의 당뇨성 치료 모델 확인 및 논문 발표 * 세포주 개발 및 CMC 개발완료 |
* 영장류 류마티스성 모델에서 DNP007 에 의한 치료 효능 확인 (LSIM 용역 결과) * 1상 임상시험 IND 제출 * 다수의 다국적 기업과 기술이전 협의 중 |
|
연구결과가 상품화된 경우 그 내용 |
해당없음. |
해당없음. |
|
연구결과가 상품화되지 않은 경우 그 이유 |
* 치료제 후보로서 현재 임상 개발 준비중 |
|
|
|
DNP002 프로젝트 |
|
연구과제 |
NOV1803 개발 |
|
연구기관 |
국가항암신약개발사업단 과제 선정 (2018년 10월) : 국가항암신약개발사업단과 다이노나㈜가 공동개발 진행 중. |
|
연구결과 및 기대효과 |
* 새로운 개념의 MOA 로서, 표적 및 면역항암제의 특성 동시 보유 * 인간화 항체 완료, 5.28 g/L 수준의 고생산 세포주 및 공정 개발 * 위암, 대장암, 폐암 등 다양한 CEACAM6 양성 암세포 동물모델에서 뛰어난 항암 효능 확인 |
|
연구결과가 상품화된 경우 그 내용 |
해당없음 |
|
연구결과가 상품화되지 않은 경우 그 이유 |
* 국가항암신약개발사엄단과 공동으로 2020년 임상 1상을 위한 공동 개발 중. |
|
|
DNP005 프로젝트 |
|
연구과제 |
면역항암제 Agonistic CD40 항체 개발 |
|
연구기관 |
다이노나㈜ 내부과제 (DN-18-01) |
|
연구결과 및 기대효과 |
* CD40을 경유해 면역세포를 활성화 시키는 agonistic 항체 * 백혈병 동물모델에서 완전관해를 유도하는 뛰어난 동물 모델 효능 데이터 확보 * 인간화 항체 개발 완료, 세포주 개발 진행 중 |
|
연구결과가 상품화된 경우 그 내용 |
해당없음 |
|
연구결과가 상품화되지 않은 경우 그 이유 |
* 치료제 후보로서 현재 비임상 개발 중. |
|
|
신규 항체 개발 (PD-1) |
|
연구과제 |
면역항암용 PD-1 항체 개발 |
|
연구기관 |
다이노나㈜ 내부과제 (DN-18-03) |
|
연구결과 및 기대효과 |
* 기존 PD-1 항체인 Nivolumab 과 Pembrolizumab 과 유사한 epitope 이면서, T 세포 활성 유도가 더 뛰어난 bio-better 버전의 PD-1 항체 * 인간화 항체 개발 진행 중 |
|
연구결과가 상품화된 경우 그 내용 |
해당없음. |
|
연구결과가 상품화되지 않은 경우 그 이유 |
* 치료제 후보로서 현재 비임상 개발 중. * 에이프로젠KIC 에 기술이전 계약 체결 (2018.02.27) |
4. 매출예상
아사는 항체기술을 기반으로 항체 관련 치료 및 진단제를 연구, 개발하고 있으며 기술이전 등을 통한 사업화를 추진하고 있으며 부수적으로 진단용 항체사업을 병행하고 있습니다.
항체치료제 기술이전을 위하여 대형 제약사와 논의를 진행하고 있으며 진단용 항체 기술이전도 함께 추진중에 있습니다.
DNP002 과제는 글로벌 중견 제약사를 중심으로 기술이전 논의를 진행하고 있으며, 계약이 성사된다면 약 600 억원 규모의 기술이전 수익이 2025년까지 발생할 것으로 예측하고 있습니다. 기술이전 시기는 비임상 및 임상시험 일정과 연동하여 예상하였고, 규모는 기술이전계약 전문회사 Myriad사의 경험적 예측을 차용하여 기술하였습니다.
DNP002의 1차 적응증은 비소세포폐암, 대장암, 위암 그리고 췌장암으로 설정하였고, 해당 질환의 2026년 시장규모는 732억달러에 달하므로 예측한 600억원 기술이전 예상실적은 전체시장의 약 0.07%를 차지하는 규모입니다. DNP002는 종양뿐만 아니라 MDSC에 작용하므로 CECAM6 종양세포 과발현과 상관없이 모든 암에 적용할 가능성도 있어 시장규모 확장 가능성이 있습니다.
DNP007은 류마티스 관절염을 포함한 다양한 자가면역질환과 장기 이식 면역억제제로 사용할 수 있어 자가면역질환 치료제 또는 장기이식 시장에 관심을 가지는 글로벌 대형 제약사와 기술이전 논의를 진행하고 있습니다. DNP007은 안전하며 효능이 뛰어나고 지속적인 투여가 필요 없는 새로운 개념의 치료제로서 자가면역질환과 장기이식시장 기존치료제를 대체할 수 있을 것으로 기대하고 있습니다. DNP007 프로젝트는 2025년까지 약 2250억원의 기술료 수익을 달성할 것으로 예상하고 있습니다. 기술이전 규모는 기술이전계약 전문업체 BL&H USA사 경험적 예측을 차용하여 기술하였습니다. 자가면역질환 치료로 사용되고 있는 TNF-alpha blocker와 장기이식 면역억제제 시장은 2026년 476억 달러에 달할 것으로 추정되므로 2025년가지 예측한 2250억원의 기술이전 예상실적은 전체시장의 약 0.4%를 차지하는 규모입니다.
대내에서 제조/판매했던 진단용 항체들을 기술 이전하고자 해외 바이오업체와 기술이전계약을 논의하고 있습니다. 항-당화혈색소 7F10 단클론항체단클론 항체를 포함하여 2종 진단항체는 중국 소재 H사와 최종합의를 앞두고 있으며 계약금액은 약 2억으로 예상됩니다. 이외 7종의 진단용항체는 춘천 소재 M사와 계약금액 없이 순매출에 대한 로열티 정산 방법으로 계약을 추진 중에 있습니다.
(5) 조직도
 |
|
다이노나(주) 조직도 |
2. 주주총회 목적사항별 기재사항
□ 회사의 합병
가. 합병의 목적 및 경위
(1) (주)금호에이치티의 안정적인 현금창출력과 다이노나(주)가 보유한 항체치료제 파이프라인의 결합을 통해 바이오 혁신 신약개발에 박차를 가하여 차세대 성장동력 확보하고자 합니다.
(2) 관계회사인 다이노나(주)의 신약개발 임상 진입이 본격화함에 따라 (주)금호에이치티 자동차 램프사업 뿐만 아니라 글로벌 바이오 전문기업으로서의 회사의 핵심사업을 명확히 하고 이를통하여 대외적인 신임도를 높이고자 합니다
(3) 합병을 통해 당사회사간의 사업분야를 정비하여 경영의 효율성을 제고하고 기업지배구조 개선을 통해 합병법인의 지속적인 기업가치 향상을 통한 주주가치 극대화를 달성하고자 합니다.
(4) 주요일정
| 합병계약일 | 2021년 01월 26일 | |
| 주주확정기준일 | 2021년 08월 23일 | |
| 주주명부 폐쇄기간 |
시작일 | 2021년 08월 24일 |
| 종료일 | 2021년 08월 30일 | |
| 합병반대의사통지 접수기간 | 시작일 | 2021년 09월 14일 |
| 종료일 | 2021년 09월 28일 | |
| 주주총회예정일자 | 2021년 09월 29일 | |
| 주식매수청구권 행사기간 |
시작일 | 2021년 09월 29일 |
| 종료일 | 2021년 10월 19일 | |
| 구주권 제출기간 |
시작일 | - |
| 종료일 | - | |
| 매매거래 정지예정기간 | 시작일 | 2021년 10월 28일 |
| 종료일 | 2021년 11월19일 | |
| 채권자이의 제출기간 | 시작일 | 2021년 09월 29일 |
| 종료일 | 2021년 10월 29일 | |
| 합병기일 | 2021년 11월 01일 | |
| 종료보고 총회일 | - | |
| 합병등기예정일자 | 2021년 11월 08일 | |
| 신주권교부예정일 | - | |
| 신주의 상장예정일 | - | |
나. 합병계약서의 주요내용의 요지
(1) 합병의 상대방
| 합병후 존속회사 (합병회사) |
상 호 | 주식회사 금호에이치티 |
| 소재지 | 광주광역시 광산구 용아로 717 | |
| 대표이사 | 김진곤, 김두인 | |
| 법인구분 | 유가증권시장 상장법인 |
| 합병후 소멸회사 (피합병회사) |
상 호 | 다이노나 주식회사 |
| 소재지 | 경기도 성남시 분당구 판교로 228번길 15, 3동 902호 (삼평동, 판교세븐벤처밸리1) | |
| 대표이사 | 조경숙 | |
| 법인구분 | 코넥스 상장법인 |
(2) 계약의 선행 조건
본 계약에 따라 합병을 하여야 하는 "갑'"과 "을"의 의무는 다음과 같은 조건이 합병기일 또는 그 이전에 성취될 것을 선행조건으로 한다. 다만 "갑'"과 "을"은 각자 서면으로 아래에서 규정하고 있는 선행조건의 일부 또는 전부를 포기, 면제할 수 있다.
1. 본 계약을 체결하고 본 계약에 예정된 거래들을 이행하기 위하여 요구되는 "갑'"과 "을"의 각 이사회, 주주총회의 승인, 독점규제 및 공정거래에 관한 법률상 기업결합 신고에 따라 공정거래위원회의 승인을 포함하여 관련 정부, 규제당국의 인허가 등을 취득하여 대한민국 관련 법령 및 정관에 따른 모든 요건들이 충족되어야 한다.
2. 본 계약 제14조에 따른 "갑'"과 "을"의 모든 진술 및 보증들이 본 계약 체결일은 물론 합병기일에도 중요한 점에서 사실과 부합하여야 한다.
3. "갑'"과 "을"이 본 계약 제15조에 정하는 바에 따라 이행할 것이 요구되는 모든 확약사항 기타 의무들을 중요한 점에서 이행하여야 한다.
4. 본 계약 체결일 이후 합병기일까지 "갑'"과 "을"의 재산 및 영업상태에 중대한 부정적 변경이 발행하지 아니하여야 한다.
(3) 계약의 해제 조건
본 합병 계약서에 기재된 계약의 해제 및 효력 소멸 조건은 아래와 같으며, "갑"은 (주)금호에이치티, "을"은 다이노나(주)를 지칭합니다.
| 제17조~제18조 (계약의 해제 및 효력 소멸) |
|
① 본 계약은 합병기일 이전에는 아래와 같은 사유로 해제될 수 있다. 단 각 해제 사유의 발생에 책임이 있는 회사는 본 계약을 해제할 수 없다. 1) “갑”과 “을”이 본 계약을 해제하기로 서면으로 상호 합의하는 경우 2) “갑”또는 “을”에 관하여 부도, 해산, 청산, 파산, 회생절차의 개시 또는 그러한 절차의 개시를 위한 신청이 있는 경우 3) (i) 본건 합병의 승인을 목적으로 하여 소집되는 “갑”과 “을”의 주주총회에서 의결권을 행사할 주주를 확정하기 위한 주주명부폐쇄일로부터 [3]개월 이내에 본건 합병에 대한 “갑”과 “을”의 주주총회 승인을 득하지 못하거나, (ii) 법령 또는 정부의 규제가 변경되어 본 계약에 따른 합병의 실행이 불가능해지거나 불법화되는 것이 확실해지고 당해 사정의 발생일로부터 [30]일 이내에 “갑”과 “을”이 달리 합의하지 아니하는 경우 4) “갑”또는 “을”이 본 계약상의 진술보증 또는 확약, 약정 사항을 위반하여 중대한 부정적인 영향이 발생하고 상대방 회사로부터 이를 시정할 것을 서면으로 요청 받고도 [30]일 내에 시정하지 못하는 경우 5) 본 계약 체결일 이후 합병기일까지 “갑” 또는 “을”의 재무상태, 경영실적, 영업상태 또는 전망에 중대한 부정적 변경이 발생한 경우 ① “갑”과 “을”이 제6조의 주주총회에서 각각 본 계약을 승인한 후, “갑”과 “을”의 주주들이 각 회사에 대하여 본건 합병에 반대하여 주식매수청구권을 행사하는 주식의 합계가 발행주식총수의 20.00%를 초과하는 경우 또는 각 회사에 대하여 주식매수청구권을 행사함으로 인하여 “갑”과 “을”이 반대주주에게 지급하여야 할 주식매수대금의 합계가 금 [10,000,000,000]원을 초과하는 경우에는 양 당사자는 본 계약을 해제할 수 있다. ② 본 계약이 해제되는 경우의 효과는 다음과 같다. 1) 본 계약이 해제되는 경우 일방 당사자는 본 계약의 해제일로부터 14일 이내에 상대방 당사자로부터 제공받은 자료 또는 정보를 상대방 당사자가 요청하는 바에 따라 반환하거나 폐기하여야 한다. 2) 본 계약이 해제되더라도 본 계약의 불이행 또는 위반으로 인하여 일방 당사자가 상대방 당사자에 대하여 갖는 손해배상청구권 기타 다른 권리나 구제방법에는 영향을 미치지 아니한다. |
다. 합병당사회사(합병회사 및 피합병회사)의 최근 사업연도의 대차대조표(재무상태표) 및 손익계산서(포괄손익계산서)
(합병회사) 【주식회사 금호에이치티】
<연 결 재 무 상 태 표>
| 제 33(당) 기 2020년 12월 31일 현재 |
| 제 32(전) 기 2019년 12월 31일 현재 |
| (단위 : 원) |
| 과 목 |
제 33(당) 기말 | 제 32(전) 기말 | ||
| 자산 | ||||
| I. 유동자산 | 181,051,169,818 | 204,929,137,680 | ||
| 현금및현금성자산 | 63,068,392,876 | 64,327,394,965 | ||
| 매출채권및기타채권 | 54,789,231,773 | 65,216,649,318 | ||
| 기타금융자산 | 20,817,626,308 | 20,629,492,094 | ||
| 재고자산 | 36,939,732,585 | 48,755,714,700 | ||
| 기타유동자산 | 5,436,186,276 | 5,999,886,603 | ||
| II. 매각예정비유동자산 | 23,800,500,000 | |||
| III. 비유동자산 | 139,446,918,767 | 117,149,055,411 | ||
| 관계기업투자주식 | 67,488,457,982 | 6,742,667,738 | ||
| 기타금융자산 | 8,838,855,885 | 27,657,899,103 | ||
| 투자부동산 | 724,887,066 | 24,113,315,095 | ||
| 유형자산 | 57,264,213,800 | 55,766,044,047 | ||
| 사용권자산 | 950,932,138 | 902,038,729 | ||
| 무형자산 | 2,062,054,968 | 86,501,256 | ||
| 확정급여자산 | 931,790,521 | 1,568,621,558 | ||
| 이연법인세자산 | 1,185,726,407 | 311,967,885 | ||
| 자산총계 | 344,298,588,585 | 322,078,193,091 | ||
| 부채 | ||||
| I. 유동부채 | 120,052,684,220 | 132,504,380,717 | ||
| 매입채무 | 26,407,493,664 | 28,762,189,137 | ||
| 차입부채 | 47,178,400,000 | 37,129,600,000 | ||
| 사채 | 29,960,926,927 | 52,511,871,125 | ||
| 기타금융부채 | 11,861,547,400 | 11,757,480,299 | ||
| 당기법인세부채 | 36,348,333 | 206,763,105 | ||
| 기타유동부채 | 4,607,967,896 | 2,136,477,051 | ||
| II. 비유동부채 | 1,106,039,141 | 16,943,123,345 | ||
| 차입부채 | 16,000,000,000 | |||
| 기타금융부채 | 817,915,171 | 483,390,529 | ||
| 기타비유동부채 | 284,715,148 | 459,732,816 | ||
| 이연법인세부채 | 3,408,822 | |||
| 부채총계 | 121,158,723,361 | 149,447,504,062 | ||
| 자본 | ||||
| I. 지배기업 소유주지분 | 221,232,295,293 | 172,630,689,029 | ||
| 자본금 | 58,952,363,500 | 11,804,291,000 | ||
| 자본잉여금 | 79,592,597,105 | 53,439,239,991 | ||
| 기타자본항목 | 3,480,066,595 | 18,893,357,038 | ||
| 이익잉여금 | 79,207,268,093 | 88,493,801,000 | ||
| II. 비지배지분 | 1,907,569,931 | - | ||
| 자본총계 | 223,139,865,224 | 172,630,689,029 | ||
| 부채와 자본총계 | 344,298,588,585 | 322,078,193,091 | ||
<연 결 손 익 계 산 서>
| 제 33(당) 기 2020년 01월 01일부터 2020년 12월 31일까지 |
| 제 32(전) 기 2019년 01월 01일부터 2019년 12월 31일까지 |
| (단위 : 원) |
| 과 목 |
제 33(당) 기 | 제 32(전) 기 | ||
| Ⅰ. 매출액 | 219,632,557,451 | 251,095,061,695 | ||
| Ⅱ. 매출원가 | 212,816,091,705 | 236,522,955,993 | ||
| Ⅲ. 매출총이익 | 6,816,465,746 | 14,572,105,702 | ||
| Ⅳ. 판매비와관리비 | 11,527,389,671 | 10,512,958,134 | ||
| Ⅴ. 영업이익(손실) | (4,710,923,925) | 4,059,147,568 | ||
| 금융수익 | 8,836,813,654 | 6,398,350,519 | ||
| 금융비용 | 11,092,080,272 | 12,141,005,775 | ||
| 기타영업외수익 | 5,767,568,959 | 3,923,397,944 | ||
| 기타영업외비용 | 4,629,349,801 | 1,869,571,469 | ||
| 지분법손실 | 2,545,131,406 | 46,305,638 | ||
| Ⅵ. 법인세비용차감전순이익(손실) | (8,373,102,791) | 324,013,149 | ||
| Ⅶ. 법인세비용 | 1,440,108,001 | 399,235,831 | ||
| Ⅷ. 당기순이익(손실) | (9,813,210,792) | (75,222,682) | ||
| 지배기업의 소유주지분 | (9,548,657,136) | (75,222,682) | ||
| 비지배지분 | (264,553,656) | |||
| Ⅸ. 기타포괄손익 | 1,509,374,583 | 1,122,028,470 | ||
| 후속적으로 당기손익으로 재분류되지 않는 포괄손익 | 262,124,229 | 1,178,123,659 | ||
| 확정급여제도의 재측정요소 | 336,056,703 | 1,510,414,947 | ||
| 당기손익으로 재분류되지 않는 항목의 법인세 | (73,932,474) | (332,291,288) | ||
| 후속적으로 당기손익으로 재분류되는 포괄손익 | 1,247,250,354 | (56,095,189) | ||
| 해외사업환산손익 | (1,015,004,104) | 143,733,979 | ||
| 지분법자본변동 | 2,262,254,458 | (199,829,168) | ||
| Ⅹ. 총포괄이익 | (8,303,836,209) | 1,046,805,788 | ||
| 지배기업의 소유주지분 | (7,796,468,427) | 1,046,805,788 | ||
| 비지배지분 | (507,367,782) | |||
| ⅩI. 주당이익 | ||||
| 기본주당이익 | (105) | (1) | ||
| 희석주당이익 | (105) | (1) | ||
<별 도 재 무 상 태 표>
| 제 33(당) 기 2020년 12월 31일 현재 |
| 제 32(전) 기 2019년 12월 31일 현재 |
| (단위 : 원) |
| 과 목 |
제 33(당) 기말 | 제 32(전) 기말 | ||
| 자산 | ||||
| I. 유동자산 | 160,757,427,598 | 183,830,342,319 | ||
| 현금및현금성자산 | 59,780,293,033 | 61,308,445,949 | ||
| 매출채권및기타채권 | 51,865,021,317 | 68,204,434,695 | ||
| 기타금융자산 | 20,809,926,662 | 20,617,527,013 | ||
| 재고자산 | 24,739,863,029 | 31,972,894,407 | ||
| 기타유동자산 | 3,562,323,557 | 1,727,040,255 | ||
| II. 매각예정비유동자산 | 23,800,500,000 | - | ||
| III. 비유동자산 | 148,794,801,906 | 130,835,726,753 | ||
| 관계기업투자주식 | 67,342,069,636 | 6,988,802,544 | ||
| 종속기업투자주식 | 30,096,002,597 | 23,630,093,012 | ||
| 기타금융자산 | 8,803,529,436 | 27,625,814,110 | ||
| 투자부동산 | 24,113,315,095 | |||
| 유형자산 | 40,194,999,925 | 46,469,308,171 | ||
| 사용권자산 | 311,694,878 | 128,060,259 | ||
| 확정급여자산 | 931,790,521 | 1,568,621,558 | ||
| 이연법인세자산 | 1,114,714,913 | 311,712,004 | ||
| 자산총계 | 333,352,729,504 | 314,666,069,072 | ||
| 부채 | ||||
| I. 유동부채 | 106,106,676,623 | 117,617,127,320 | ||
| 매입채무 | 20,230,924,272 | 21,828,406,229 | ||
| 차입부채 | 40,500,000,000 | 30,500,000,000 | ||
| 사채 | 29,960,926,927 | 52,511,871,125 | ||
| 기타금융부채 | 10,804,218,218 | 10,763,149,974 | ||
| 당기법인세부채 | 36,348,333 | 206,763,105 | ||
| 기타유동부채 | 4,574,258,873 | 1,806,936,887 | ||
| II. 비유동부채 | 435,718,475 | 16,278,975,554 | ||
| 차입부채 | 16,000,000,000 | |||
| 기타금융부채 | 268,636,665 | 114,497,278 | ||
| 기타비유동부채 | 167,081,810 | 164,478,276 | ||
| 부채총계 | 106,542,395,098 | 133,896,102,874 | ||
| 자본 | ||||
| I. 자본금 | 58,952,363,500 | 11,804,291,000 | ||
| II. 자본잉여금 | 79,389,461,802 | 53,236,104,688 | ||
| III. 기타자본항목 | 3,407,137,170 | 20,310,492,093 | ||
| IV. 이익잉여금 | 85,061,371,934 | 95,419,078,417 | ||
| 자본총계 | 226,810,334,406 | 180,769,966,198 | ||
| 부채와 자본총계 | 333,352,729,504 | 314,666,069,072 | ||
<별 도 손 익 계 산 서>
| 제 33(당) 기 2020년 01월 01일부터 2020년 12월 31일까지 |
| 제 32(전) 기 2019년 01월 01일부터 2019년 12월 31일까지 |
| (단위 : 원) |
| 과 목 |
제 33(당) 기 | 제 32(전) 기 | ||
| Ⅰ. 매출액 | 181,173,914,349 | 221,734,443,473 | ||
| Ⅱ. 매출원가 | 177,410,040,620 | 209,805,965,723 | ||
| Ⅲ. 매출총이익 | 3,763,873,729 | 11,928,477,750 | ||
| Ⅳ. 판매비와관리비 | 8,236,134,282 | 7,398,106,445 | ||
| Ⅴ. 영업이익(손실) | (4,472,260,553) | 4,530,371,305 | ||
| 금융수익 | 8,911,198,319 | 6,499,515,732 | ||
| 금융비용 | 10,655,975,488 | 11,712,255,983 | ||
| 기타영업외수익 | 2,952,871,938 | 3,470,820,053 | ||
| 기타영업외비용 | 5,890,363,886 | 992,792,606 | ||
| Ⅵ. 법인세비용차감전순이익(손실) | (9,154,529,670) | 1,795,658,501 | ||
| Ⅶ. 법인세비용 | 1,465,301,042 | 896,272 | ||
| Ⅷ. 당기순이익(손실) | (10,619,830,712) | 1,794,762,229 | ||
| Ⅸ. 기타포괄손익 | 262,124,229 | 1,178,123,659 | ||
| 후속적으로 당기손익으로 재분류되지 않는 포괄손익 | 262,124,229 | 1,178,123,659 | ||
| 확정급여제도의 재측정요소 | 336,056,703 | 1,510,414,948 | ||
| 당기손익으로 재분류되지 않는 항목의 법인세 | (73,932,474) | (332,291,289) | ||
| Ⅹ. 총포괄이익(손실) | (10,357,706,483) | 2,972,885,888 | ||
| ⅩI. 주당이익(손실) | ||||
| 기본주당이익(손실) | (117) | 27 | ||
| 희석주당이익(손실) | (117) | 26 | ||
(피합병회사) 【다이노나 주식회사】
<연 결 재 무 상 태 표>
| 제 22(당)기 2020년 12월 31일 현재 |
| 제 21(전)기 2019년 12월 31일 현재(감사받지 않은 재무제표) |
| (단위 : 원) |
| 과 목 |
제 22(당) 기말 | 제 21(전) 기말 | ||
| 자산 | ||||
| I.유동자산 | 47,865,737,928 | 24,054,286,451 | ||
| 현금및현금성자산 | 46,399,006,431 | 8,632,244,935 | ||
| 단기금융상품 | 14,200,000,000 | |||
| 매출채권및기타채권 | 1,061,443,327 | 548,482,343 | ||
| 재고자산 | 65,151,519 | 124,913,293 | ||
| 기타유동자산 | 287,367,681 | 466,176,730 | ||
| 당기법인세자산 | 52,768,970 | 82,469,150 | ||
| Ⅱ. 비유동자산 | 47,095,266,244 | 1,817,746,245 | ||
| 매출채권및기타채권 | 86,777,417 | 281,030,121 | ||
| 유형자산 | 1,673,043,463 | 1,434,803,217 | ||
| 영업권 이외의 무형자산 | 81,168,747 | 101,912,907 | ||
| 관계기업투자주식 | 45,254,276,617 | |||
| 자 산 총 계 | 94,961,004,172 | 25,872,032,696 | ||
| 부채 | ||||
| I.유동부채 | 5,720,008,061 | 7,075,915,079 | ||
| 매입채무및기타채무 | 282,796,472 | 277,035,496 | ||
| 유동금융부채 | 767,935,251 | 5,208,622,101 | ||
| 당기손익-공정가치측정금융부채 | 1,086,471,146 | 1,191,257,486 | ||
| 기타유동부채 | 8,471,200 | 28,994,318 | ||
| 파생금융상품부채 | 3,446,663,938 | 282,992,088 | ||
| 리스부채 | 127,670,054 | 42,712,187 | ||
| 복구충당부채 | 44,301,403 | |||
| Ⅱ. 비유동부채 | 19,774,137,411 | 151,498,975 | ||
| 매입채무및기타채무 | 172,243,781 | 132,182,185 | ||
| 전환사채 | 19,506,493,622 | |||
| 리스부채 | 60,000,847 | 19,316,790 | ||
| 복구충당부채 | 35,399,161 | |||
| 부 채 총 계 | 25,494,145,472 | 7,227,414,054 | ||
| 자본 | ||||
| 자본금 | 16,465,543,000 | 7,771,573,500 | ||
| 기타불입자본 | 111,908,273,541 | 58,260,879,552 | ||
| 기타자본구성요소 | 815,041,456 | |||
| 결손금 | (59,721,999,297) | (47,387,834,410) | ||
| 자 본 총 계 | 69,466,858,700 | 18,644,618,642 | ||
| 부 채 및 자 본 총 계 | 94,961,004,172 | 25,872,032,696 | ||
<연 결 손 익 계 산 서>
| 제 22(당)기 2020년 1월 1일부터 2020년 12월 31일까지 |
| 제 21(전)기 2019년 1월 1일부터 2019년 12월 31일까지(감사받지 않은 재무제표) |
| (단위 : 원) |
| 과 목 | 제 22(당) 기 | 제 21(전) 기 |
| I.매출액 | 1,690,254,042 | 708,917,279 |
| II.매출원가 | 889,273,909 | 453,360,473 |
| III.매출총이익 | 800,980,133 | 255,556,806 |
| IV.판매비와관리비 | 9,257,067,641 | 6,828,112,495 |
| Ⅴ.영업손실 | (8,456,087,508) | (6,572,555,689) |
| VI. 금융수익 | 4,135,416,503 | 997,768,534 |
| VII. 금융원가 | 1,584,824,777 | 314,437,296 |
| Ⅷ. 기타영업외수익 | 14,335,322 | 43,477,507 |
| X. 기타영업외비용 | 28,537,338 | 15,282,011 |
| XI. 관계기업투자손익 | (6,414,467,089) | |
| XII. 법인세비용차감전순손실 | (12,334,164,887) | (5,861,028,955) |
| XIII. 계속사업법인세비용 | ||
| XIV. 계속사업손실 | (12,334,164,887) | (5,861,028,955) |
| XV. 중단사업손실 | (1,288,330,664) | |
| XVI. 당기순손실 | (12,334,164,887) | (7,149,359,619) |
| XVII. 기타포괄손익 | ||
| XⅧI. 당기총포괄손익 | (12,334,164,887) | (7,149,359,619) |
| XⅧII. 주당손익 | ||
| 기본주당계속사업손실 | (546) | (382) |
| 기본주당중단사업손실 | (83) | |
| 기본주당손실 | (546) | (465) |
| 희석주당계속사업손실 | (548) | (397) |
| 희석주당중단사업손실 | (82) | |
| 희석주당손실 | (548) | (479) |
<별 도 재 무 상 태 표>
| 제 22(당)기 2020년 12월 31일 현재 |
| 제 21(전)기 2019년 12월 31일 현재(감사받지 않은 재무제표) |
| (단위 : 원) |
| 과 목 |
제 22(당) 기말 | 제 21(전) 기말 | ||
| 자산 | ||||
| I.유동자산 | 47,468,479,758 | 24,054,286,451 | ||
| 현금및현금성자산 | 46,001,881,921 | 8,632,244,935 | ||
| 단기금융상품 | 14,200,000,000 | |||
| 매출채권및기타채권 | 1,061,312,527 | 548,482,343 | ||
| 재고자산 | 65,151,519 | 124,913,293 | ||
| 기타유동자산 | 287,367,681 | 466,176,730 | ||
| 당기법인세자산 | 52,766,110 | 82,469,150 | ||
| Ⅱ. 비유동자산 | 47,495,266,244 | 1,817,746,245 | ||
| 장기매출채권및기타채권 | 86,777,417 | 281,030,121 | ||
| 유형자산 | 1,673,043,463 | 1,434,803,217 | ||
| 영업권 이외의 무형자산 | 81,168,747 | 101,912,907 | ||
| 관계기업투자주식 | 45,254,276,617 | |||
| 종속기업투자주식 | 400,000,000 | |||
| 자 산 총 계 | 94,963,746,002 | 25,872,032,696 | ||
| 부채 | ||||
| I.유동부채 | 5,720,008,061 | 7,075,915,079 | ||
| 매입채무및기타채무 | 282,796,472 | 277,035,496 | ||
| 유동금융부채 | 767,935,251 | 5,208,622,101 | ||
| 당기손익-공정가치측정금융부채 | 1,086,471,146 | 1,191,257,486 | ||
| 기타유동부채 | 8,471,200 | 28,994,318 | ||
| 파생금융상품부채 | 3,446,663,938 | 282,992,088 | ||
| 리스부채 | 127,670,054 | 42,712,187 | ||
| 복구충당부채 | 44,301,403 | |||
| Ⅱ. 비유동부채 | 19,774,137,411 | 151,498,975 | ||
| 매입채무및기타채무 | 172,243,781 | 132,182,185 | ||
| 전환사채 | 19,506,493,622 | |||
| 리스부채 | 60,000,847 | 19,316,790 | ||
| 복구충당부채 | 35,399,161 | |||
| 부 채 총 계 | 25,494,145,472 | 7,227,414,054 | ||
| 자본 | ||||
| 자본금 | 16,465,543,000 | 7,771,573,500 | ||
| 기타불입자본 | 111,908,273,541 | 58,260,879,552 | ||
| 결손금 | (59,719,257,467) | (47,387,834,410) | ||
| 기타포괄손익누계액 | 815,041,456 | |||
| 자 본 총 계 | 69,469,600,530 | 18,644,618,642 | ||
| 부 채 및 자 본 총 계 | 94,963,746,002 | 25,872,032,696 | ||
<별 도 손 익 계 산 서>
| 제 22(당)기 2020년 1월 1일부터 2020년 12월 31일까지 |
| 제 21(전)기 2019년 1월 1일부터 2019년 12월 31일까지(감사받지 않은 재무제표) |
| (단위 : 원) |
| 과 목 | 제 22(당) 기 | 제 21(전) 기 |
| I.매출액 | 1,690,254,042 | 708,917,279 |
| II.매출원가 | 889,273,909 | 453,360,473 |
| III.매출총이익 | 800,980,133 | 255,556,806 |
| IV.판매비와관리비 | 9,254,307,181 | 6,828,112,495 |
| Ⅴ.영업손실 | (8,453,327,048) | (6,572,555,689) |
| VI. 금융수익 | 4,135,397,873 | 997,768,534 |
| VII. 금융원가 | 1,584,824,777 | 314,437,296 |
| Ⅷ. 기타영업외수익 | 14,335,322 | 43,477,507 |
| X. 기타영업외비용 | 28,537,338 | 15,282,011 |
| XI. 관계기업투자손익 | (6,414,467,089) | |
| XII. 법인세비용차감전순손실 | (12,331,423,057) | (5,861,028,955) |
| XIII. 계속사업법인세비용 | ||
| XIV. 계속사업손실 | (12,331,423,057) | (5,861,028,955) |
| XV. 중단사업손실 | (1,288,330,664) | |
| XVI. 당기순손실 | (12,331,423,057) | (7,149,359,619) |
| XVII. 기타포괄손익 | ||
| XVIII. 당기총포괄손익 | (12,331,423,057) | (7,149,359,619) |
| XⅧII. 주당손익 | ||
| 기본주당계속사업손실 | (546) | (382) |
| 기본주당중단사업손실 | (83) | |
| 기본주당손실 | (546) | (465) |
| 희석주당계속사업손실 | (547) | (397) |
| 희석주당중단사업손실 | (82) | |
| 희석주당손실 | (547) | (479) |
※ 기타 참고사항
IV. 사업보고서 및 감사보고서 첨부
가. 제출 개요
| 제출(예정)일 | 사업보고서 등 통지 등 방식 |
|---|---|
| - | - |
나. 사업보고서 및 감사보고서 첨부
- 해당사항 없음
※ 참고사항
|
코로나바이러스 감염증-19(COVID-19)의 감염 및 전파를 예방하기 위하여 임시주주총회 개최 시 총회장 입구에서 총회 참석 주주님들의 체온을 측정할 수 있으며, 발열이 감지되는 경우 부득이하게 주주총회 장소에의 출입을 제한할 수 있음을 안내드립니다. 또한 질병예방을 위해 주주총회 참석 시 반드시 마스크 착용을 요청 드립니다. |