 |
|
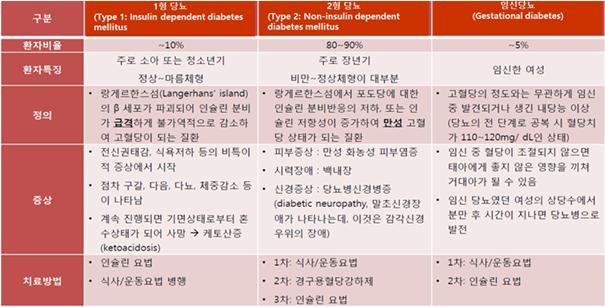
당뇨질환의 형태별 구분 |
주주총회소집공고
| 2021년 03월 05일 | ||
| 회 사 명 : | 주식회사 이도바이오 | |
| 대 표 이 사 : | 리송알렉스인근 | |
| 본 점 소 재 지 : | 경기도 안양시 동안구 벌말로123, 에이동2009호,2010호 | |
| (전 화) 031-433-6620 | ||
| (홈페이지)http://www.yidobio.com | ||
| 작 성 책 임 자 : | (직 책) 이사 | (성 명) 엄보열 |
| (전 화) 031-352-5035 | ||
주주총회 소집공고
| (제 7기 정기) |
제7기 정기주주총회 소집통지서
주주님의 건승과 댁내의 평안을 기원합니다.
당사는 상법 제363조와 정관 제 22 조에 의거 제 7 기 정기주주총회를 아래와 같이 개최 하오니 참석하여 주시기 바랍니다.
- 아 래 -
1. 일 시 : 2021년 3월 23일(화요일) 오전 10시 00분
2. 장 소 : 경기도 안양시 동안구 벌말로123, 1501호(평촌스마트베이 15층 회의실)
3. 회의 목적 사항
가. 보고사항 : 영업보고 및 감사보고, 내부회계관리실태보고, 외부감사인 선임보고
나. 부의안건
제 1호 의안: 제7기 재무제표 승인의 건
제 2호 의안: 이사보수한도액 승인의 건(3억)
제 3호 의안: 감사보수한도액 승인의 건(1억)
4. 경영참고사항 비치
상법 제542조의4에 의한 경영참고사항은 당사 인터넷 홈페이지에 게재하고 본점과 명의개서대행회사(국민은행 증권대행부)에 비치하였으며, 금융위원회 및 한국거래소에 전자공시하여 조회가 가능하오니 참고하시기 바랍니다.
5. 실질주주의 의결권 행사에 관한 사항
우리 회사의 이번 주주총회에서는 한국예탁결제원이 주주님들의 의결권을 행사할 수 없습니다. 따라서 주주님들께서는 한국예탁결제원에 의결권행사에 관한 의사표시를 하실 필요가 없으며, 종전과 같이 주주총회에 참석하여 의결권을 직접행사하시거나 또는 위임장에 의거 의결권을 간접행사할 수 있습니다.
6. 주주총회 참석시 준비물
- 직접행사 : 신분증
- 대리행사 : 주주 인감증명서, 대리인의 신분증, 위임장(주주와 대리인의 인적사 항 기재, 인감날인)
| 당사 주주총회에서는 참석 주주님들에 대해 별도의 기념품을 지급하지 아니하오니 이점 양지하여 주시기 바랍니다.(문의 : 031-433-6620) |
2021년 03월 05일
주식회사 이도바이오
대표이사 리송알렉스인근 (직인생략)
I. 사외이사 등의 활동내역과 보수에 관한 사항
1. 사외이사 등의 활동내역
가. 이사회 출석률 및 이사회 의안에 대한 찬반여부
| 회차 | 개최일자 | 의안내용 | 사외이사 등의 성명 | |||
|---|---|---|---|---|---|---|
| A (출석률: %) |
B (출석률: %) |
C (출석률: %) |
D (출석률: %) |
|||
| 찬 반 여 부 | ||||||
| - | - | - | - | - | - | - |
나. 이사회내 위원회에서의 사외이사 등의 활동내역
| 위원회명 | 구성원 | 활 동 내 역 | ||
|---|---|---|---|---|
| 개최일자 | 의안내용 | 가결여부 | ||
| - | - | - | - | - |
2. 사외이사 등의 보수현황
| (단위 : 원) |
| 구 분 | 인원수 | 주총승인금액 | 지급총액 | 1인당 평균 지급액 |
비 고 |
|---|---|---|---|---|---|
| - | - | - | - | - | - |
II. 최대주주등과의 거래내역에 관한 사항
1. 단일 거래규모가 일정규모이상인 거래
| (단위 : 억원) |
| 거래종류 | 거래상대방 (회사와의 관계) |
거래기간 | 거래금액 | 비율(%) |
|---|---|---|---|---|
| - | - | - | - | - |
2. 해당 사업연도중에 특정인과 해당 거래를 포함한 거래총액이 일정규모이상인 거래
| (단위 : 억원) |
| 거래상대방 (회사와의 관계) |
거래종류 | 거래기간 | 거래금액 | 비율(%) |
|---|---|---|---|---|
| - | - | - | - | - |
III. 경영참고사항
1. 사업의 개요
가. 업계의 현황
당사가 영위하는 사업내용의 이해를 돕기 위해 아래와 같이 주요 용어에 대하여 간략히 설명드립니다.
[용어 정리]
|
용 어 |
설 명 |
|
당뇨병 |
대사성 질환으로 췌장의 베타세포가 파괴되어 인슐린을 분비하지 못하는 1형 당뇨병과 인슐린은 분비되지만 간, 근육, 지방에서 인슐린 신호전달이 제대로 되지 않는 2형 당뇨병으로 크게 분류할 수 있음 |
|
췌도 |
췌장에 있는 인슐린 분비 세포 덩어리로 약 천개의 세포로 구성되어 있으며 인슐린을 분비하는 베타세포, 글루카곤을 분비하는 알파세포 등으로 구성되어 있음 |
|
성체줄기세포 |
골수, 지방, 탯줄 등 체내 여러 기관에 존재하는 소수의 세포로 인체의 여러 계열의 세포로 분화할 수 있는 다분화능을 가지고 있음 |
|
역분화줄기세포 |
성체에서 얻어진 세포에 야마나카 인자(Sox2, Oct4, Klf4, c-Myc)를 도입하여 얻어진 배아줄기세포 유사 세포로 인체의 모든 세포로 분화할 수 있는 전분화능을 가지고 있음 |
|
배아줄기세포 |
수정난이 분열하여 얻어진 배반포 내부에 있는 inner cell mass에서 유래한 세포로 인체의 모든 세포로 분화할 수 있는 전분화능을 가지고 있음 |
|
줄기세포 구상체 |
줄기세포를 단층배양하지 않고 3차원 배양하여 얻어진 구형의 세포덩어리로 다양한 직경을 가지고 있으며, 줄기세포능력과 면역조절능력이 우수함 |
|
CMC |
Chemistry, Manufacturing and Control 의 약자로서 화학 합성 (Chemistry), 공장 생산 (Manufacturing), 품질 관리 (Control 또는 quality control)의 약어로 의약품 개발 과정에서 의약품 (원료, 완제)의 품질과 연관된 연구 개발 및 제조 공정이 일관성 있게 조절 및 관리되고 있음을 문서화하여 입증하는 것을 의미함. |
|
CRO |
Contract Research Organization의 약자로 시험 수탁기관을 뜻함. 비임상, 임상 시험과 관련된 의뢰자의 임무나 역할의 일부 또는 전부를 대행하기 위하여 의뢰자로부터 계약에 의해 위임받은 기관 |
|
FDA |
Food and Drug Administration의 약자로 미국 보건부의 산하기관. 식품과 의약품에 대한 관리 규제를 담당하는 기관 |
|
PCT |
Patent Cooperation Treaty, 특허협력조약. PCT에 의해 하나의 방식 및 언어로 PCT 동맹국에 동시에 특허출원하는 것. PCT 출원을 하면, 국제 단계를 거쳐 국내 단계로 진입하게 되며, 국제 단계는 국제조사, 국제공개 및 국제예비심사의 3개 절차로 세분됨 |
|
신약 개발 단계 |
일반적으로는 "연구→ 비임상→ 임상 1 상→ 임상 2 상→ 임상 3 상→ 품목 허가→ 출시"의 단계를 따름 |
|
생체모사형 세포 |
COP필름 위에 실리카겔 입자를 정렬하여 만든 배양 필름으로 세포 배양용기 아래에 부착하여 다양한 종류의 세포 구상체를 만들 수 있음 |
|
면역억제 |
조직 및 장기를 공여자에서 수여자로 이식했을 경우 수여자의 체내 면역세포에 의해 면역 거부 반응이 나타나기 때문에 이를 방지하기 위한 약물 |
|
임상시험 |
임상 시험용 의약품의 안전성과 유효성을 증명할 목적으로, 해당 약물의 약동ㆍ약력ㆍ약리ㆍ임상적 효과를 확인하고 이상 반응을 조사하기 위하여 사람을 대상으로 실시하는 시험 또는 연구 |
|
전임상 시험 |
세포치료제 또는 신약 개발 과정에서 생쥐, 개, 원숭이 등을 이용하여 효능 및 안전성을 시험하는 연구 |
|
임상 1상 시험 |
한정된 수의 건강한 지원자를 대상으로 안전성에 중점을 두고 투여량, 약리 작용, 체내의 흡수/분포/대사/ 배설을 조사하는 시험 |
|
임상 2상 시험 |
전기 2상(early phase II 또는 phase IIa)과 후기 2 상(late phase II 또는 Phase IIb)으로 나뉨. 전자는 소수의 환자에게 투여하여 유효성과 안전성을 조사하는 시험이며, 후자는 대상 환자층을 늘려서 전기 2상에서 추정한 용법·용량이 적절한지 조사하는 시험. 후기 2상을 사용량 검토 시험(dose finding study, DFS)이라고도 함 |
|
임상 3상 시험 |
다수의 환자를 대상으로 하여 유효성·안전성 및 투여량을 확증하는 시험이며, 적응증을 확정하고 사용상의 주의 사항 등을 설정하는 단계. 기존약 또는 위약을 사용하여 이중 맹검법(double-blinded)으로 시험 |
|
기술이전 |
단일 회사가 신약개발의 전 과정을 수행하는 것이 아니라, 임상 단계별로 역할을 분담해 신약개발의 위험도를 줄이면서도 빠르게 상업화할 수 있도록 신약 후보물질의 권리 (기술ㆍ물질ㆍ제품ㆍ특허) 등을 도입 또는 이전하는 것을 말함 |
|
IND |
Investigation new drug의 약자로 전임상 연구에서의 효능과 안전성 데이터를 기반으로 세포치료제 또는 신약을 환자에게 적용해보는 임상 1상 시험에 필요한 임상시험계획 승인과정 |
|
In Vitro |
생체외, 시험관내를 뜻하며 생체에서 꺼낸 효소, 세포 등을 시험관 내에서 효능을 검증하는 단계를 In Vitro 효능 검증이라 함 |
|
In Vivo |
생체내. 일반적으로 In Vivo 효능 검증이란 동물에서의 효능 검증을 뜻함 |
당사의 사업부문별 주요 사업내용을 요약하면 아래와 같습니다.
|
구 분 |
주요 사업내용 |
|
연구개발 부문 |
당뇨질환 줄기세포치료제 연구개발 |
|
의료기기 판매 부문 |
혈당측정기, 펜니들, 혈압측정기 등 상품 판매 |
(1) 당뇨질환의 구분과 산업의 구성
(가) 당뇨질환의 구분
당뇨질환은 발병 요인에 따라 1형 당뇨(insulin dependent diabetes mellitus), 2 형 당뇨(Non- insulin dependent diabetes millitus), 그리고 임신당뇨(Gestationa l diabetes)로 구성되며 각 형태별 특성과 증상, 관리와 치료 방법이 상이합니다.
 |
|
당뇨질환의 형태별 구분 |
(출처: 내부 제공 자료)
당뇨병은 말기까지 진행되지 않는 한 그 자체로 생명을 위협하는 질환은 아니지만 장기간에 걸친 고혈당으로 인해 망막증(diabetic retinopathy), 신경병증(diabeteic neuropathy), 신증(diabetic renal disease), 심근경색(cardiac infarction) 등의 합병증을 유발하며 이러한 당뇨 합병증으로 인해 사람의 수명이 평균 10년 이상 감소합니다.
[ 당뇨병으로 인한 합병증 발생 위험도]
| Complication | Renal Failure | Myocardial Infarct |
Stroke | Accompanying hyperipidemia |
| Relative Risk | 25배 | 5배 | 3배 | 2~4배 |
(출처 : N. Eng. J. Med. 1993)
(나) 당뇨질환 산업의 구성
1) 당뇨질환 의료기기 산업
비교적 어린 시절에 발병하는 1형 당뇨병과 주로 40대 이상에서 발병하는 2형 당뇨병은 모든 만성적인 질환으로 수십년동안 혈당 관리가 필요하며 엄격한 혈당관리는 합병증을 예방하거나 지연시킬 수 있습니다. 자가 혈당 측정기, 혈당을 인지하고 정상혈당치를 유지하기 위해 인슐린 주사를 동시에 할 수 있는 인슐린 펌프, 3개월간의 혈당치를 예측할 수 있는 당화혈색소 측정기, 그 외 인슐린 주사기를 포함한 부대기기 등이 주요한 의료기기입니다.
2) 당뇨질환 치료제 산업
1921년 발견된 인슐린의 상용화로 인해 많은 당뇨병 환자들이 생명을 연장할 수 있었으며, 1980년대 유전공학의 등장으로 재조합 단백질 인슐린이 생산되었습니다. 인슐린은 현재까지 당뇨병 치료제의 주축으로 여겨지고 있으며, 이 외에도 여러 가지 메카니즘(간에서의 포도당 생성 저해, 소장에서 포도당 흡수 저해, 근육 및 지방에서 인슐린 작용 촉진, 인슐린 분비 촉진)으로 혈당을 낮추는 약물들이 개발되었습니다. 2000년 캐나다 알버타 대학의 제임스 샤피로 박사팀에 의해 뇌사자의 췌장에서 인슐린 분비세포인 췌도를 분리하여 1형 당뇨병 환자에 이식하는 췌도이식술이 임상적으로 큰 효과를 거두었습니다. 이러한 췌도이식술의 성공으로 부족한 췌도를 얻기 위해 성체, 배아, 역분화 줄기세포를 인슐린 분비세포로 분화하는 세포치료제들이 개발되고 있으며, 줄기세포이 면역조절 효과를 이용하여 당뇨병 증상을 개선하려는 노력들이 병행되고 있습니다.
(2) 당뇨질환 시장 현황 및 전망
(가) 당뇨질환 의료기기 시장 현황 및 전망
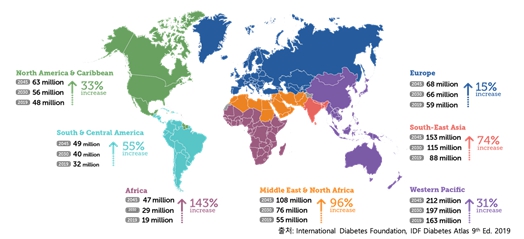
당뇨병 환자는 세계적으로 2018년 기준 4.6억 명에 이르며, 2045년에는 약 7억 명에 이를 것으로 전망되고 있고, 특히 중국을 포함한 동아시아지역의 당뇨병 환자가 가장 많은 비중을 차지하고 있습니다.
 |
|
세게 당뇨병환자의 분포 및 증가추이 |
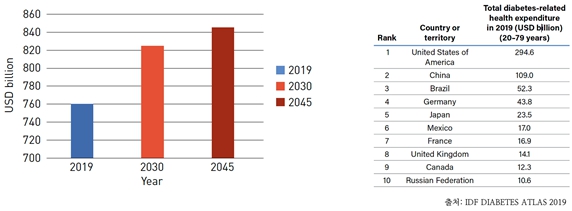
세계 당뇨병 의료비 지출 규모는 2019년 기준 7,600억 달러에서 2045년 8,450억 달러로 증가할 것으로 전망되며, 국가별로 환자 수는 중국과 인도가 가장 많으나, 의료비 지출 규모는 미국이 가장 큰 2,946억 달러를 형성하고 있습니다.
 |
|
세계당뇨병의료비지출규모(좌)및상위10개국(우) |
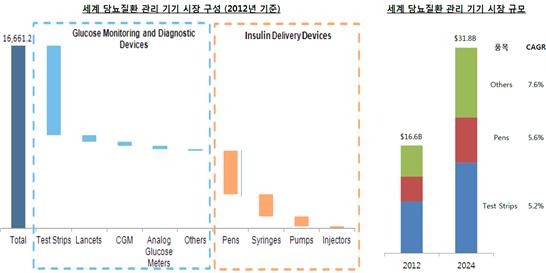
일반적으로 당뇨병은 완치되기가 어려워 의료기기 등을 통해 관리 치료하고 있으며, 당뇨병 관리용 의료기기는 크게 혈당측정기와 인슐린 주사기 및 소모품으로 구성됩니다. 당뇨병 관리용 의료기기 시장의 규모는 2012년 166억 달러에서 2024년 318억 달러로 증가할 것으로 전망되고 있습니다.
 |
|
세계 당뇨관리 의료기기 시장 구성 |
(출처: TMR Diabetes Devices and Drugs 2014, GVR Diabetes Devices Market 2016)
당뇨병 관리용 의료기기 시장의 성장 요인은 국가별로 경제가 발전하면서 물질적 풍요가 확산되고 인구가 고령화되며 의료적 관심이 높아질수록 혈당측정 등의 건강관리 수요가 증가하는 것에 기인하고 있습니다. IDF가 발표한 Diabetes Atlas 2017에 따르면 고소득 국가와 중간소득 국가, 저소득구가를 구분하여 해당 국가들의 1인당 평균 의료비용 지출금액과 총 지출금액을 구분하였는데, 저소득국가 대비 고소득국가의 1인당 평균 의료비용 지출금액이 약 96.7배에 달했습니다. 2017년 기준 당뇨환자가 가장 높은 국가는 중국(약 114백만 명)과 인도(약 73백만 명)이며, 향후 해당 국가들의 경제성장과 함께 당뇨병에 대한 시장규모가 커질 것으로 추정됩니다.
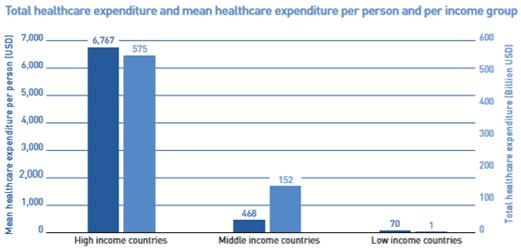 |
|
고소득국가와 중간소득국가,저소득국가별 의료비용 지출액 |
출처: IDF Diabetes Atlas 2017
또한 20세에서 79세까지의 인구들을 조사한 결과, 당뇨병 환자임에도 불구하고 아직 당뇨병에 대한 확진을 받지 않는 등의 사유로 그 사실을 모르고 있는 인구는 세계적으로 약 50%에 달합니다.
 |
|
지역별 당뇨병으로 진단되지 않은 비율 및 진단되지 않은 당뇨별 사례 |
(나) 당뇨병 치료제 시장의 현황
당뇨병을 치료하기 위해서는 인슐린을 생성 및 분비하는 췌장의 기능을 재생시키고 신체의 인슐린 반응성을 회복시키는 등의 근원적 방법이 필요하며, 현재까지 1세대 약물부터 4세대 약물까지 다양한 신약이 출시되었으나 각종 부작용 등이 발견되어 지속적인 연구개발이 필요한 영역으로 알려져 있습니다.
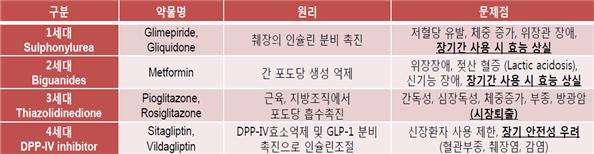 |
|
당뇨질환 치료물질 개요 |
(출처: 내부 제공 자료)
최근 단독요법 외에 대부분 2제 심지어 3제 병합요법까지 처방하고 있으며, 2016년에는 병합요법이 약 70% 이상을 차지할 정도로 증가하였습니다. 최근에는 DPP-4 억제제와 메트포르민의 2제 병합요법이 급증하였으나 결국 인위적인 인슐린 생성, 분비 촉진과 인슐린 반응성 향상에 따르는 부작용이 수반되는 신약 형태의 당뇨병 치료제는 구조적인 한계를 지니고 있으며, 이에 당뇨의 치료를 위해서는 정상 기능을 수행하는 건강한 췌도를 환자에게 이식하는 것이 가장 효율적인 방법으로 인정되고 있으나, 뇌사자의 장기기증에 의존되는 췌도 수급 측면에서의 난관은 극복이 필요합니다. 이에 궁극적으로는 인간의 줄기세포를 활용한 췌도 배양 후 이식요법이 대안으로 제시되고 있으며, 이에 당사는 성체 줄기세포, 역분화 배아줄기세포, 배아줄기 세포 등 다양한 줄기세포를 인슐린 분비세포로 분화하는 기술에 기반한 국내 최초의 당뇨병 세포치료제를 연구개발하고 있습니다.
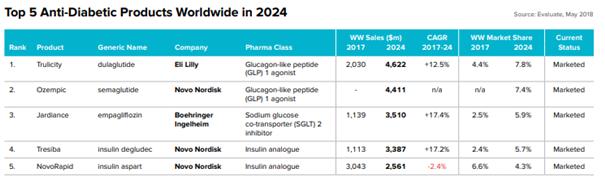 |
|
당뇨질환 치료제 판매순위 |
출처: Evaluate Pharma 2018
(3) 세포치료산업의 특성 및 시장 동향
세포치료제는 현재 치료제가 없는 난치성 질환을 해결할 새로운 치료대안으로 개발되는 경우가 대부분으로 시장에서 다른 치료제와의 경쟁이 없거나 매우 적습니다. 특히 세포치료제의 임상기간은 일반 신약에 비해 단축이 가능하며, 일반적으로 신약개발을 위해서는 임상 1상부터 임상 3상까지 최소 7년의 기간이 필요합니다. 하지만 세포치료제 임상시험은 임상 1, 2상을 동시에 진행할 수 있으며 총 임상기간 또한 최소 4년으로 완료가 가능합니다. 특히 희귀질환의 경우 임상 1, 2상 동시진행을 완료한 후에 품목허가 신청이 가능합니다. 세포치료제는 향후 경제적, 기술적 파급효과가 큰 유망기술로 주목 받고 있기 때문에 세계 각국 정부에서는 적극적으로 연구개발 지원하고 있습니다.
[일반 신약과 세포치료제의 임상 기간 및 조건 비교]
|
임상시험 |
일반신약개발 |
세포치료제 개발 |
||
|
일반질환 |
희귀질환 |
|||
|
기간 |
1상 |
2년 |
1년 |
1년 |
|
2상 |
2년 |
|||
|
3상 |
3년 |
3년 |
조건부 품목허가 |
|
|
합계 |
최소 7년 |
최소 4년 |
최소 1년 |
|
|
환자수 |
1상 |
20~100명 |
10~50명 |
|
|
2상 |
100~500명 |
|||
|
3상 |
1,000~5,000명 |
50~100명 |
- |
|
|
총 임상비용 |
약 3,000억원 |
약 20~50억원 |
약 10~15억원 |
|
(자료: 내부 제공 자료)
세포치료제는 대부분 바이오 벤처기업들에 의해 개발 및 상용화가 진행되고 있고, 글로벌 제약사들은 직접 시장에 참여하지 않고 있는 상황입니다. 이는 살아있는 세포를 제품화하는 노하우, 세포치료제 개발에 중요한 제조공정(배양, 분화, 이식) 기술에 대한 노하우가 부족하기 때문이며, 글로벌 제약사들은 세포치료제 연구개발하는 바이오벤처기업을 인수합병하거나 기술이전계약을 체결하는 등의 활발한 Business Deal이 이루어지고 있습니다. 특히 최근 세포치료제 시장 성장에 따라 비임상, 기초연구 단계에서의 기술이전/M&A 사례나 역분화 플랫폼기술의 공동연구계약 체결 등 기술력 있는 바이오벤처기업들이 높은 Upfront대금(대부분 100억 원 이상, 마일스톤 / 로열티는 별도)을 수취하는 사례가 증가하고 있습니다.
[최근 글로벌 세포치료제 Business Deal 주요 사례]
|
연도 |
업체명 |
상대방 |
질환분야 |
Upfront |
개발단계 |
비고 |
|
2014 |
Capricor |
Janssen |
심장계질환 |
$12.5M |
임상1상 |
비독점 기술이전 (독점전환시 $337.5M) |
|
2015 |
Mesoblast |
Celgene |
이식편대숙주질환 |
$45.0M |
임상1상 |
지분투자 (Deal우선권 확보) |
|
2015 |
Evotec |
Sanofi |
당뇨질환 |
€3.0M |
기초연구 |
기술이전 |
|
2016 |
RetroSense |
Allergan |
망막색소변성증 |
$60.0M |
임상1상 |
M&A |
|
2016 |
Evotec |
Celgene |
신경계질환 (역분화플랫폼기술) |
$45.0M |
기초연구 |
5년간 독점공동개발 (후보물질 스크리닝) |
|
2016 |
Ceylad |
Ono |
백혈병/골수종 |
$12.0M |
비임상 |
기술이전 (한국, 일본, 대만) |
|
2017 |
Ceylad |
Novartis |
이식편대숙주질환 |
$12.0M |
기초연구 |
미국특허 이전 (비독점) |
|
2017 |
Editas |
Allergan |
선천성흑내장 |
$90.0M |
비임상 |
기술이전 |
|
2017 |
Calimmune |
CSL Behring |
조혈모세포분화기술 |
$91.0M |
기초연구 |
M&A |
|
2017 |
Kite Pharma |
Gilead |
비호지킨림프종 외 |
$11.9B |
판매승인 등 |
M&A |
(출처: Cell Therapy News 2014~2017)
생명공학정책연구센터의 Global Stem Cell Industry Outlook에 따르면 세포치료제 시장은 2017년 13.5억달러에서 연평균 16.5% 성장하여 2023년 33.8억 달러에 이를 것이라 전망되고 있습니다.
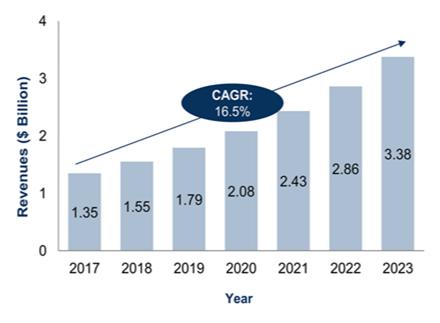 |
|
글로벌 줄기세포치료제 시장현황 및 전망(2017~2023년) |
| (단위 : 십억달러) |
(출처: 생명공학정책연구센터, Global Stem Cell Industry Outlook(Frost & Sullivan 분석), 2018.11)
또한 전 세계에서 시판된 7개의 세포치료제 중 국내에서 개발된 치료제가 4개로서 국내 세포치료제 산업의 경쟁력은 높은 편이며, 2016년 식약처에서 집계한 글로벌 통계에 따르면 현재 진행중인 세포치료제 임상 중 미국(155건) 다음으로 한국(46건)이 많은 비중을 차지하고 있습니다. 현재 세포치료제 시장은 초기단계에서 개화하고 있고 향후 성장 잠재력이 높으며, 국내 기업들이 세계 최초의 세포치료제 다수를 출시하였습니다. 현재도 활발한 연구개발을 진행하고 있어 향후 글로벌 제약사들의 국내 세포치료제 산업에 대한 접근 매력도는 높을 것으로 보이며, 이는 현재 다수의 세포치료제 개발 플랫폼 기술과 다양한 당뇨 질환 세포치료제 후보물질을 연구개발하고 있는 당사에 기회 요인이 될 것으로 예상됩니다.
(4) 당뇨병 치료용 세포치료제 연구개발 동향
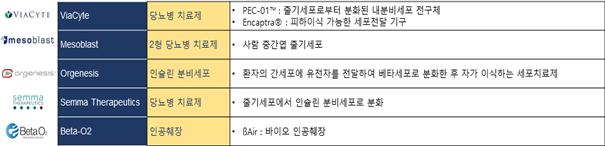
당뇨병 세포치료제를 개발하고 있는 국내 회사는 없는 것으로 파악되고 있으며, 국외에는 아래의 표와 같이 대표적으로 5개의 회사가 있습니다. 크게 성체줄기세포의 면역조절능력을 이용한 회사, 역분화 또는 배아줄기세포를 인슐린 분비세포로 분화하는 회사, 이들 세포를 면역반응 없이 이식하는 이식재 회사로 분류할 수 있으며, 이 중 대표적인 회사는 미국의 SEMMA Therapeutics사로 역분화 및 배아줄기세포를 인슐린 분비 베타세포로 분화하는 기술을 가지고 있습니다. 최근 이 회사는 Vertex Therapeutics사에 약 1조 원($950M)에 흡수 합병되었습니다(출처: Vertex 社 공식 홈페이지 news&event). 현재의 기술 수준은 성체줄기세포의 경우 그 치료 효과가 미미하고, 역분화줄기세포 기반의 경우 마우스 등 소동물에서만 효능이 검증되었을 뿐 환자를 대상으로 한 작은 규모의 임상실험에서 효능이 미미하였습니다.
 |
|
당뇨질환 세포치료제의 글로벌 연구동향 |
(출처: 내부 제공 자료)
(5) 줄기세포치료제 산업의 과제
배아줄기세포의 경우 분화효율이 월등히 좋은 장점이 있는 반면 사람 수정란을 인위적으로 파괴해야 하는 윤리적인 문제가 있습니다. 성체줄기세포와 역분화줄기세포의 경우 상대적으로 이런 문제가 없기 때문에 당사는 성체줄기세포와 역분화줄기세포를 이용하여 인슐린 분비세포로 분화하는 기술을 개발하고 있으며, 배아줄기세포도 확보하여 역분화세포의 비교 실험군으로 이용하고 있습니다.
전세계적으로 줄기세포 연구가 활발히 진행되고 있고, 미국과 중국의 경우 이미 임상에 사용할 배아줄기세포와 역분화줄기세포의 세포주를 지정하여 세포의 안정성 및 안전성을 국가가 담보하는 형태로 진행하고 있습니다. 우리나라도 이러한 추세에 동참할 것으로 예상되며 본사는 선제적으로 모든 종류의 줄기세포를 확보하여 연구를 진행하고 있습니다.
줄기세포로부터 인슐린분비세포로 분화하여 세포치료제로 임상에 적용할 때 췌도이식과 같이 간문맥에 직접 이식할 경우, 낮지만 완전히 배제할 수 없는 종양 발생 가능성이 있습니다. 따라서 당사는 처음 시도할 때는 Encapsulation 방법을 사용할 계획입니다. 현재 alginate 및 hyaluronic acid 기반의 micro-capsule과 생체 적합성이 좋은 PEG를 이용한 macro-device 개발을 위해 국내외 연구진과 협력하고 있습니다. 또한 미분화된 줄기세포 제거 기술 확보를 통해 안전한 세포치료제 개발을 진행하고 있습니다.
나. 회사의 현황
(1) 영업개황 및 사업부문의 구분
(가) 영업개황
당사는 혈당측정기 제조업체 아이센스(코스닥), 바이오의약품 생산 세포주 개발업체 팬젠(코스닥)의 핵심인력으로 근무한 대표이사 리송알렉스인근이 2014년 3월 창업한 회사로서 당뇨병 종합솔루션 제공을 목표로 1) 당뇨관리 의료기기 판매업과 2) 당뇨 세포치료제 연구개발 사업을 영위하고 있습니다.
당사 사업의 기본전략은 아이센스와의 협업관계를 기반으로 고사양의 프리미엄 제품군 혈당측정기 판권을 취득하여 유의미한 규모의 매출과 이익실현 구조를 정착시키고, 안정적인 환경속에서 국내 최초의 당뇨병 세포치료제 연구개발을 진행하고 있습니다. 이를 통해 당사는 지속적으로 회사의 기업가치를 높여가는 것을 목표로 하고 있습니다.
1) 당뇨질환 관리용 의료기기(혈당측정기 및 기타 소모품 등)
당사 경영진은 아이센스에 근무하면서 혈당측정기 제품 영업, 국내 유통망 및 해외 판로 개척, 인허가 대응 등의 당뇨의료기기 사업화(Business Development)를 담당했던 주요 인물들로 구성되어 있습니다.
아이센스는 다양한 사양과 규격의 혈당측정기를 대리점, 총판, 판매업체들을 통해 위탁 판매하고 있으며, 당사에는 최상위 혈당측정기 브랜드 2개(Acura Plus, Maxima)의 국내 독점판권을 부여하였고, 또한 아이센스가 ODM 방식으로 생산하는 고가의 해외브랜드(일본 아크레이사 등) 혈당측정기도 국내 독점판권 계약 체결하여 판매 중에 있습니다.
 |
|
당사 당뇨 의료기기 사업 개요 |
2) 당뇨질환 세포치료제 연구개발
① 세포치료제(줄기세포)의 개요
줄기세포는 신체의 모든 세포와 조직의 근간이 되는 세포로서, 세포분화 단 계에 따라 배아줄기세포, 성체줄기세포, 역분화 줄기세포로 구분되며, 줄기 세포의 기원에 따라 자가유래(Autologous), 동종유래(Allogenic), 이종유래(X enograft)로 구분됩니다.
[줄기세포의 종류와 기원별 특성]
|
종류별 |
특성 |
|
배아줄기세포 (체세포복제) |
모든 세포로 분화가능하며 대량생산 가능 윤리적 문제 내제(난자 사용) |
|
성체줄기세포 (제대혈/골수/지방 유래) |
윤리적 문제 없음 분화 능력 제한적 (특정세포 분화경향 내제) |
|
역분화줄기세포(*) (유도만능) |
모든 세포로 분화가능하며 윤리적 문제 없음 분화 효율이 낮음 (생산 비용이 높음) |
|
기원별 |
특성 |
|
자가유래 (Autologous) |
환자 본인의 세포나 조직을 이용하여 제조 면역거부반응 없음 |
|
동종유래 (Allogenic) |
타인에게서 분리된 세포나 조직을 이용하여 제조 면역거부반응 있음 |
|
이종유래 (Xenograft) |
동물로부터 분리된 세포나 조직을 이용하여 제조 면역거부반응 및 바이러스감염위험 있음 |
*) 역분화줄기세포(Induced Pluripotent Stem Cell)는 2006년 일본 교토대의 야마나카 신야가 4개의 유전자물질을 분화종료된 체세포에 삽입하여 역분화시키는데 성공하고 노벨상을 수상하였음. 이후 국내외에서 역분화 기술의 지속적인 개량이 이루어졌으며, 분화 효율 개선과 줄기세포 생산 공정의 효율성 향상, 제한적 역분화(당사의 경우)를 통해 목표기능세포로 단기간내 분화 등 다양한 개선기술이 현재 활용되고 있음.
② 당사 세포치료제 사업화 추진 개요
당사는 2015년부터 당뇨 세포치료제 연구개발사업을 개시하여 성균관대 김경규 교수로부터 동종유래 체세포 역분화 기술을 이전받고, 성균관대 황혜연 박사를 CSO(Chief Scientific Officer)로 영입하였습니다. 또한 2019년 서울대 의과대학에서 이종장기이식(당뇨병 치료용 돼지 췌도 이종이식) 연구로 세계 최우수 연구를 이끌었던 신준섭 박사를 연구소장으로 영입하였습니다. 외부와의 균형과 협력관계 유지를 위하여, 2016년부터 서울대병원 박경수 교수와 자가줄기세포를 활용한 당뇨병 세포치료제 공동연구개발을 시작하였습니다. 그 동안 연구개발한 다양한 줄기세포 중에서 동종지방줄기세포 유래 당뇨병 세포치료제 후보물질을 개발하여 아산병원 김송철 교수 팀과 공동으로 in vivo 효능 평가를 진행하고 있으며, 자가골수줄기세포 유래 당뇨병 세포치료제(서울대병원 박경수 교수와 공동개발)는 in vivo 전임상시험을 진행하고 있습니다. 역분화줄기세포 유래 당뇨병 세포치료제의 경우, 당사의 세포치료제 생산 플랫폼 확보를 위한 원천기술 개발 및 in vitro / in vivo 전임상 시험을 진행하고 있습니다.
③ 당사 세포치료제 R&D 네트워크
세포치료제 연구개발이 성공하기 위해서는 결국 세포치료제 이식 및 진료를 수행하는 의사/병원과의 협업관계 구축이 필수적이며, 당사는 서울대학교병원, 섬성서울병원, 아산병원 교수진과의 협력관계를 구축하였습니다.
[당사 R&D 참여 교수진 프로필]
|
성명 |
전공/학력 |
현 소속/전문분야 |
주요 경력/당사 관계 |
|
이문규 |
서울대 의학과 (의학박사) |
삼성서울병원 내분비대사과 |
前 성균관대 의대 부교수 現 삼성서울병원 당뇨병센터 센터장 現 대한당뇨병학회 이사장 당사 동종지방줄기세포유래 당뇨세포치료제 In Vivo 효능평가 진행 |
|
박경수 |
서울대 의학과 (의학박사) |
서울대학교병원 내분비내과 |
前 서울대 의대 부교수 前 당뇨 및 내분비질환 유전체연구센터 센터장 (11년 근무) 당사와 자가골수줄기세포유래 당뇨 세포치료제 공동 개발 중 |
|
김송철 |
서울대 의학과 (의학박사) |
아산병원 외과 |
現 울산의대 교수 로봇수술센터 소장 당사와 역분화줄기세포유래 당뇨 세포치료제 공동 개발 중 |
|
김경규 |
서울대 화학과 (이학박사) |
성균관대 의대 정교수 성균관대 융합의과학원 교수 |
동종유래 체세포 역분화 기술을 이도바이오에 이전 (2015.7월) 체세포 역분화 관련 기술에 대해 Royal Society of Chemistry Invited Review 논문 기고 (2017.5월) |
④ 당사 세포치료제 파이프라인과 주요 기술
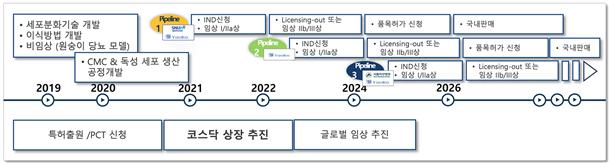
당사 보유 핵심기술은 1) 자가유래 골수줄기세포 분화(Autologous bone marrow derived mesenchymal stem cell, BMMNC differentiation) 기술, 2) 동종유래 지방줄기세포 분화 (Allogenic adipose tissue derived mesenchymal stem cell, AdMSC differentiation) 기술, 3) 동종유래 체세포 역분화 (Allogenic Somatic Cell Re-Programming) 기술, 4) 역분화줄기세포 분화(induced pluripotent stem cell, iPSC differentiation) 기술로 구분되며, 각각의 기술은 당뇨병을 포함한 다양한 질환의 세포치료제 개발을 위한 플랫폼 기술의 역할을 하고 있습니다.
 |
|
당사 당뇨치료 세포치료제 개발현황 및 계획 |
출처 : 당사내부제공
[당사 보유 플랫폼 기술 및 연구 현황]
|
기술구분 |
기술원천 |
후보물질 |
개발단계/비고 |
|
자가유래 골수줄기세포 직접분화 |
서울대의대 박경수 교수 공동개발 |
당뇨질환 |
- In Vivo(체내) 효능평가 완료(서울대병원) - 2023년 임상 신청/개시 추진 |
|
동종유래 간엽줄기세포 직접분화 |
자체 개발 |
당뇨질환 세포치료제 |
- In Vitro(체외) 완료 - In Vivo(체내) 효능평가 진행 중(아산병원) - 2023년 임상 신청/개시 추진 |
|
동종유래 체세포 역분화/분화 |
성균관대 김경규 교수 기술이전 |
당뇨질환 세포치료제 신경질환 세포치료제 심장질환 세포치료제 |
- 당뇨질환 세포치료제는 In Vitro(체외) 단계 최적화 진행중 - 신경계, 심장 등 다양한 질환의 세포치료제 개발을 위한 분화기술 연구중 |
|
역분화줄기세포 |
자체 개발 |
당뇨질환 세포치료제 |
- 역분화줄기세포 유도 방법 확립 |
자가유래 골수줄기세포를 이용한 당뇨병세포치료제는 CMC 및 독성 검사를 진행하고 있으며, 2021년 식약처에 당뇨병 환자 대상 안전성 및 유효성 확인을 위한 임상 1/2a IND 신청을 진행할 계획입니다. 안전성과 유효성이 확인되면 더 많은 환자를 대상으로 임상 2b를 진행하고자 합니다. 련재 추진하고 있는 연구개발 현황을 고려하여, 아래 표와 같이 동종유래 지방줄기세포, 동종유래 체세포, 역분화줄기세포로부터 분화된 당뇨병 세포치료제에 대한 연구 개발 및 임상시험을 순차적으로 진행할 계획이며 임상 1상/2상 이후에는 기술이전(L/O) 또는 대규모 임상 3상을 진행할 예정입니다.
[당뇨병 세포치료제 개발 현황 및 계획]
|
세포치료제 유래 |
개발단계 |
||||
|
in vitro 최적화 |
in vivo /전임상시험 |
*CMC /GLP-Tox |
IND filing |
임상1상/2상 |
|
|
자가 유래 골수줄기세포 |
완료 |
완료 |
2021년 |
2022년 |
2024년 |
|
동종 유래 간엽줄기세포 |
완료 |
진행중 |
2022년 |
2023년 |
2024년 |
|
동종 및 자가 유래 역분화줄기세포 |
진행중 |
진행중 |
2023년 |
2024년 |
2025년 |
*CMC : Chemistry Manufacturing and Controls, 출처: 당사 내부 제공
⑤ 당사 대표이사/경영진의 연구개발 총괄 역량
당사의 이인근 대표이사는 서울대 미생물학과를 졸업하고 미국 퍼듀대학에서 박사학위를 할 때 지도교수가 세운 회사가 나스닥에 상장되는 것을 지켜보면서 벤처회사에 대한 큰 관심을 가지게 되었습니다. 사업을 잘 하려면 회사 경영 등 다양한 경험이 필요할 것 같아서 박사학위 후에 퍼듀대학에서 경영학과를 1년 다녔고 시드니대학 로스쿨에서 법학 박사학위도 취득하여 변호사 경험도 쌓았습니다.
한국에 귀국하여 3년간 ㈜팬젠(코스닥 상장사, 바이오의약품 생산 세포주 및 신약연구개발) 대표이사를 역임하면서 바이오 벤처기업을 경영하고 연구개발을 총괄한 경험이 있습니다. 2007년부터는 KT&G 자회사였던 ㈜한국췌도이식연구소에서 대표이사를 하면서 인간 췌도를 증식하여 1형당뇨병을 치료하는 세포치료제를 개발하기 위해 3년간 연구개발을 총괄하였습니다. 대표이사의 부친과 장인어른이 2형당뇨 합병증으로 사망하는 것을 지켜보고, 또 매일 인슐린 주사를 맞아야 하는 많은 당뇨환자의 불편함을 알게 되면서 꼭 세포치료제 개발을 성공시키겠다는 각오를 다졌습니다. 하지만 당시에는 한국뿐 아니라 세계적으로도 줄기세포 기술이 많이 부족한 상태였기 때문에 만족할만한 결과를 얻지 못했습니다.
세포치료제 개발에 실패한 큰 아쉬움을 뒤로 하고 당뇨병 환자의 혈당을 측정하는 제품을 제조하는 ㈜아이센스에 입사하여 법률고문으로서 주로 회사의 해외업무를 관장하며 현재 당사의 부사장으로 일하고 있는 송민선 박사와 함께 10여년간 일하였습니다. 아이센스에서 당뇨병 진단 사업 관련 국제적인 경험을 쌓으며 아이센스가 급속히 성장하는 것을 지켜 보았습니다. 당뇨병 관련 시장은 고령화로 인해 환자가 계속 늘어나고 있으면서도 근본적인 치료방법은 아직 없기 때문에 이 분야에 지속적으로 관심을 가지고, 기술 발전 동향에 대해 연구하고 있었습니다.
근래에 들어 세계적으로 줄기세포 기술이 빠르게 발달되고 있는 것을 확인하고는 성공할 가능성이 많이 커졌다고 판단하여 2014년 3월에 ㈜이도바이오를 창업하였습니다. 팬젠에서 같이 일했던 황혜연 박사가 초기에 합류하였으며, 한국췌도이식연구소에서 같이 일했던 신준섭 박사 민병훈 박사가 추가로 합류하면서 세포치료제 연구에 가속이 붙게 되었습니다.
당뇨병 환자는 대부분 수십 년 동안 관리를 해야 하는 질병이라서 대부분의 선진국 정부 입장에서는 단일질병으로 가장 많은 비용이 들고 있습니다. 인슐린을 생산하는 췌장이 망가진 1형 당뇨병을 위해 줄기세포를 이용한 세포치료제를 만들게 되면 가장 근본적인 치료법이 되는 것이기 때문에 본 기술개발에 성공하기만 하면 그 가치는 엄청날 것으로 예상됩니다.
2019년 하반기 들어 같은 분야에서 앞서나가던 미국의 Semma 라는 회사가 Vertex 회사에 1조원이 넘는 가치로 M&A 되면서 이 분야에 대해 세계적인 관심도가 높아졌습니다. Semma 가 아직 임상에 들어간다는 소식이 없는 상태에서도 이렇게 높은 가치를 인정받았다는 것을 보면 세포치료제 개발에 대한 기대감이 매우 크다는 것을 짐작할 수 있습니다.
인간의 췌장을 완전히 대체할 만한 수준의 세포치료제를 만들어 당뇨병을 완전히 치료한다면 가장 좋겠지만, 단기적으로는 당뇨병 환자의 생명을 위협하는 심한 저혈당 증세를 완화하고, 투여 받는 인슐린의 양을 어느 정도 줄일 수 있는 수준의 세포치료제만 개발해도 그 가치는 매우 클 것으로 예상됩니다. 장기적으로는 당뇨병을 완전히 치유할 수 있는 세포치료제를 목표로 하고 있습니다.
공동창업자인 송민선 부사장은 서울대 미생물학과 학사, 퍼듀대학 생물리학박사, 시드니로스쿨 법학박사를 받고 아이센스와 당사에서 당뇨병 관련 많은 경험을 가지고 있습니다. 아이센스에서 미국지사장을 하며 해외 거래처 개발을 전문으로 했으며 당사에서도 해외 라인센싱 아웃, 임상 등을 담당하고 있습니다.
연구소장(Chief Technical Officer)인 신준섭 박사는 고려대 학사, 석사, 박사 이후 한국췌도이식연구소에서 이인근 대표이사와 3년간 일한 후 서울대 바이오이종장기개발사업단에서 연구리더로서 10년간 일하며 당뇨병 세포치료제 개발을 전문으로 일해왔습니다. 특히, 돼지 췌도를 당뇨병 원숭이에 이식하여 최장 1000일 동안 인슐린 주사없이 정상혈당을 유지시킨 결과를 발표하면서 전세계적으로 이종이식 분야의 선도연구자가 되었습니다. 그 외에도 60여편이 넘는 논문을 발표하며 이 분야의 전문인력으로 자리 잡았습니다. 민병훈박사 역시 한림대 학사 석사 박사 이후 한국췌도이식연구소 서울대 바이오이종장기개발사업단에서 신준섭박사와 함께 일하며 호흡을 맞춰왔습니다.
당사는 서울대 의과대학의 박경수 교수 연구팀과 골수유래 줄기세포를 이용한 인슐린 분비세포 분화 기술을 임상에 적용하기 위한 공동연구를 준비하고 있고, 아산병원 김송철 교수 연구팀과는 다양한 환자로부터 얻어진 역분화 줄기세포 중 인슐린 분비세포로 분화가 잘 되는 세포주를 확보하여 대량배양 시스템을 개발하고 있습니다. 대량 배양 시스템을 위해 아주대 김재호 교수 연구팀과 공동으로 개발한 Pamcell 배양기판을 이용하고 있으며, 최적화를 위해 지속적인 공동연구를 수행하고 있습니다. 국내 당뇨병 최고의 전문가이신 가톨릭 성모병원 윤건호 교수, 가천대 김광원, 김병준 교수 연구팀의 지원을 받고 있고, ㈜셀투인, ㈜Myxengo, ㈜ANK 등의 벤처기업들과도 활발한 공동연구를 진행하고 있습니다. 당뇨병 세포치료제 개발 전반에 대해 마이애미 대학의 Midhat 박사, 루이스빌 대학의 Bala 박사, Uppsala대학의 Bergren 박사로부터 자문도 받고 있습니다.
최근에 미국의 Semma Therapeutics사가 높은 가치를 인정받게 된 계기는 배아줄기세포를 인슐린 분비세포로 분화하여 당뇨병 마우스를 치료한 결과를 바탕으로 하고 있습니다. 신준섭 연구소장은 서울대학교 바이오이종장기개발사업단에 근무할 당시 당뇨병 원숭이에 돼지 췌도를 이식하여 세계 최장 정상혈당 유지 결과를 도출하였습니다. 신준섭 연구소장의 풍부한 대동물 전임상 연구경험과 서울대 의과대학, 아산병원 등 국내 최고의 임상의사들과의 긴밀한 협조체계를 바탕으로 향후 당뇨병 환자들에게 안전하면서도 효과적인 당뇨병 세포치료제를 개발할 자신감을 가지고 있습니다. 당사는 당뇨병 세포치료제 개발에 있어서 국내 최고의 실력을 갖춘 벤처회사로 자리매김 했으며, 국제적으로 가장 경쟁력 있는 세포치료제 개발회사 중 하나로 성장해 나갈 것입니다.
(2) 시장점유율
1) 당뇨질환 관리용 의료기기 부문
혈당측정기 및 혈당스트립 시장은 객관적이고 합리적인 자료 제시가 불가능하여 시장시장점유율을 산정하는 것이 매우어려워 당사가 취득한 내용으로 추정해보 면 2017년 기준으로 세계시장점유율은 로슈(Roche) 약27%,라이프스캔(LifeSca n) 약 23%, 아센시아(Ascensia) 약 14%, 애보트(Abbot) 약 14%를 차지하고 있 습니다.
2) 당뇨질환 세포치료제 연구부문
- 세포치료제의 경우, 전 세계적으로 상용화된 기업은 없으며, 임상시험이 진행되 고 있는 실정임.
- 당뇨병을 포함하는 대사질환 치료제 시장 현황은 아래와 같음.
[세계 시장 ]
- 대사질환 치료제 중 항암제와 당뇨병 질환 치료제 비율은 2014년부터 2020 년까지 각각 5%, 8% 증가, 심혈관 질환 치료제 비율은 10% 감소할 것으로 전망
- 질환별 치료제 비율은 2014년 심혈관 질환(45%), 암(22%), 당뇨병(21%) 순 이었고, 2020년 심혈관 질환(35%), 당뇨병(29%), 암(27%) 순이 될 것으로 전 망
[ 국내 시장 ]
- 항암제와 당뇨병 질환 치료제 비율은 2014년부터 2020년까지 각각 8%, 1% 증 가, 심혈관 질환 치료제 비율은 3% 감소할 것으로 전망
- 질환별 치료제 비율은 2014년 심혈관 질환(49%), 암(18%), 당뇨병(15%) 순이 었고, 2020년 심혈관질환(46%), 암(26%), 당뇨병(16%) 순이 될 것으로 전망
- 기존의 대사질환치료제 시장 중 당뇨병 시장은 거의 포화 수준에 다다른 것으로 파악되며 최근에는 골대사 질환, 지방간, 비만 질환 시장의 규모가 증가하는 추 세임.
,
(3) 시장의 특성
1) 당뇨질환 관리용 의료기기 부문
자가혈당측정기 관련 산업은 당뇨병환자수의 증가 및 진단율 확대 추세 등을 통해 지속적으로 성장하고 있습니다. 또한, 평균 수명의 연장, 높아진 건강에 대한 관심 , 향상된 건강보험 제도 및 기술의 진보 등은 혈당측정기 시장을 성장시키는 요인 이 되어 왔으며, 앞으로도 시장을 성장시키는 요인이 될 것입니다.
혈당측정기 시장의 특징은 프린터 시장과 유사한 특성을 가지고 있습니다. 혈당측 정기 시장도 한번 구입하면 긴 시간 사용 할 수 있는 혈당측정기(Meter)와 1회용 소모품인 혈당스트립(Strip), 채혈침, 알콜솜등으로 구성되어 있습니다. 장기간 사 용하게되는 혈당측정기보다는 1회 측정시 소모되는 측정 소모품인 혈당스트립의 시장규모가 크고 빠른 속도로 증가하고 있습니다.
2) 당뇨질환 세포치료제 연구부문
- 세계적으로 당뇨병 환자는 2019년 4.6억 명(한국 500만명)에 이르며 (IDF Atals 2019), 췌도이식은 제1형 당뇨병 치료의 최선책으로 알려져 있으며, 미국 등지에 서 의료보험 적용 예정으로 세계적으로 확대 적용될 전망임 (Diabetes Care, 201 6).
- 하지만 인슐린을 분비하는 췌도가 존재하는 장기인 췌장의 경우, 신장과 간 등과 같이 생체장기제공자로부터 장기 기증을 받아 이식을 하는 것이 아니라 뇌사자로 부터 공여 받아야하는 제한요소가 있음.
- 이러한 특성은 장기이식을 위한 대기시간이 2536일(약 7년; 2018 장기 등 이식 및 인체조직 기증 통계 연보, 통계청)으로 이식을 위한 장기 부족이 극심한 상황임.
- 이를 해결하기 위해 줄기세포 기반 인슐린분비세포 분화 연구가 국내·외에서 활 발히 진행되고 있음.
- 세계 인공 장기 시장 규모는 연평균 7.33% 증가하여 2024 년에는 448억달러(약 5 3 조원)에 이를 것으로 전망됨 (mordor Intelligence, 2018).
- 국내 장기이식 시장은 약 5.6조원으로 예상하고 있으며, 세포치료제의 경우 예상되 는 환자는 10-20% 선으로 추정됨.
(4) 신규사업 등의 내용 및 전망
신규로 추진하는 사업이 없으므로 작성을 생략합니다.
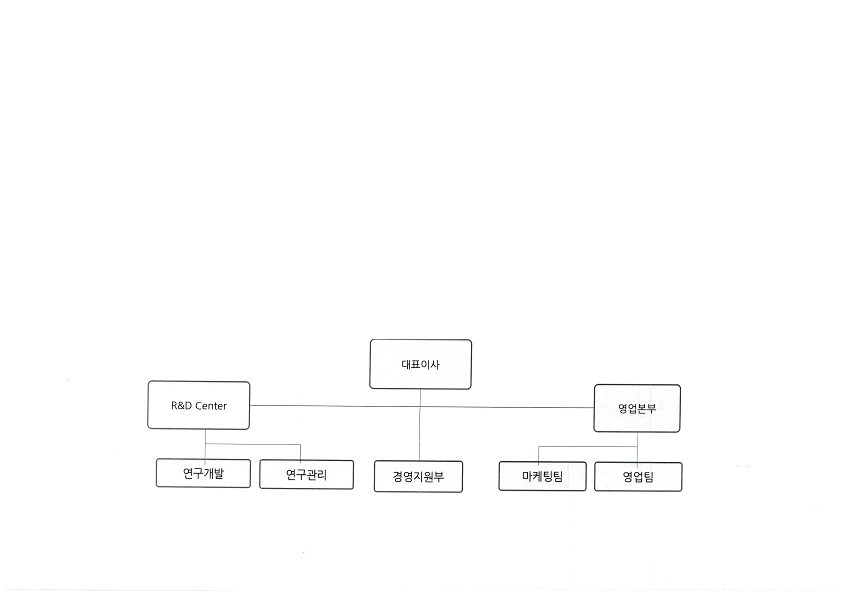
(5) 조직도
 |
|
조직도 |
2. 주주총회 목적사항별 기재사항
□ 재무제표의 승인
가. 해당 사업연도의 영업상황의 개요
(Ⅲ-1. '사업의 개요' 참조)
나. 해당 사업연도의 대차대조표(재무상태표)ㆍ손익계산서(포괄손익계산서)ㆍ이익잉여금처분계산서(안) 또는 결손금처리계산서(안)
※ 아래의 재무제표는 감사전 재무제표입니다. 외부감사인의 감사의견을 포함한 최종 재무제표는 향후 전자공시시스템(http://dart.fss.or.kr)에 공시예정인 당사의 감사보고서를 참조하시기 바랍니다.
- 대차대조표(재무상태표)
<대 차 대 조 표(재 무 상 태 표)>
| 제 7 기 2020년 12월 31일 현재 |
| 제 6 기 2019년 12월 31일 현재 |
| (단위 : 원) |
| 과 목 | 제 7 기 | 제 6 기 | ||
|---|---|---|---|---|
| 자 산 | ||||
| I. 유동자산 | 5,766,449,557 | 8,060,079,001 | ||
| (1) 당좌자산 | 4,393,570,633 | 6,718,454,540 | ||
| 1. 현금및현금성자산 | 1,765,987,329 | 3,828,378,805 | ||
| 국고보조금 | - | (31,039,293) | ||
| 2. 매출채권 | 2,652,941,587 | 3,028,303,912 | ||
| 대손충당금 | (220,145,273) | (190,250,594) | ||
| 3. 미수금 | 145,590,940 | 23,188,170 | ||
| 4. 선급금 | 42,927,250 | 54,372,400 | ||
| 5. 선급비용 | 5,884,360 | 5,259,080 | ||
| 6. 부가세대급금 | - | |||
| 7. 당기법인세자산 | 384,440 | 242,060 | ||
| (2) 재고자산 | 1,372,878,924 | 1,341,624,461 | ||
| 1. 상품 | 1,616,954,031 | 1,357,205,815 | ||
| 상품평가충당금 | (244,075,107) | (15,581,354) | ||
| 2. 제품 | - | - | ||
| 3. 원재료 | - | - | ||
| II. 비유동자산 | 565,746,343 | 1,480,710,135 | ||
| (1) 투자자산 | 300,000 | 300,000 | ||
| 1. 매도가능증권(주석4) | 300,000 | 300,000 | ||
| (2) 유형자산(주석5) | 322,827,375 | 548,571,111 | ||
| 1. 구축물 | - | - | ||
| 감가상각누계액 | - | - | ||
| 2. 기계장치 | 177,407,000 | 716,810,000 | ||
| 감가상각누계액 | (72,160,588) | (515,005,103) | ||
| 3. 차량운반구 | 155,536,384 | 153,180,623 | ||
| 감가상각누계액 | (56,643,735) | (51,373,528) | ||
| 4. 비품 | 496,613,231 | 547,329,836 | ||
| 감가상각누계액 | (381,794,663) | (346,003,883) | ||
| 5. 시설장치 | 14,654,000 | 84,117,790 | ||
| 감가상각누계액 | (10,784,254) | (63,954,781) | ||
| 6. 금형 | - | 119,920,000 | ||
| 감가상각누계액 | - | (96,449,843) | ||
| (3) 무형자산(주석6) | 4,318,968 | 633,539,024 | ||
| 1. 소프트웨어 | 4,318,968 | 6,521,701 | ||
| 2. 영업권 | - | 627,017,323 | ||
| (4) 기타비유동자산 | 238,300,000 | 298,300,000 | ||
| 1. 임차보증금 | 237,000,000 | 298,300,000 | ||
| 2. 기타보증금 | 1,300,000 | 300,000 | ||
| 자산총계 | 6,332,195,900 | 9,540,789,136 | ||
| 부 채 | ||||
| I. 유동부채 | 3,290,219,419 | 3,399,726,790 | ||
| 1. 매입채무 | 2,619,574,100 | 2,936,650,707 | ||
| 2. 단기차입금(주석8) | 240,000,000 | 300,000,000 | ||
| 3. 미지급금 | 72,477,138 | 98,005,654 | ||
| 4. 미지급비용 | 33,861,907 | 25,800,732 | ||
| 5. 예수금 | 4,573,460 | 4,653,830 | ||
| 6. 선수금 | 7,339,750 | 34,615,867 | ||
| 7. 유동성전환사채 | 299,997,500 | - | ||
| 8. 유동성사채상환할증 | 47,781,824 | - | ||
| 9. 유동성잔환권조정 | (35,386,260) | - | ||
| II. 비유동부채 | 1,124,195,111 | 1,263,942,858 | ||
| 1. 퇴직급여충당부채 | 176,529,872 | 109,270,960 | ||
| 2. 전환사채(주석10) | 1,000,000,000 | 1,299,997,500 | ||
| 사채상환할증금 | 276,281,563 | 324,063,387 | ||
| 전환권조정 | (328,616,324) | (469,388,989) | ||
| 부채총계 | 4,414,414,530 | 4,663,669,648 | ||
| 자 본 | ||||
| I. 자본금(주석11) | 1,539,737,500 | 1,536,700,000 | ||
| 1. 보통주자본금 | 1,170,987,500 | 1,142,950,000 | ||
| 2. 우선주자본금 | 368,750,000 | 393,750,000 | ||
| II. 자본잉여금 | 10,935,665,870 | 10,911,703,370 | ||
| 1. 주식발행초과금 | 10,690,765,460 | 10,666,802,960 | ||
| 2. 전환권대가 | 244,900,410 | 244,900,410 | ||
| III. 이익잉여금(결손금) | (10,557,622,000) | (7,571,283,882) | ||
| 1. 미처분이익잉여금(미처리결손금) | (10,557,622,000) | (7,571,283,882) | ||
| 자본총계 | 1,917,781,370 | 4,877,119,488 | ||
| 부채와자본총계 | 6,332,195,900 | 9,540,789,136 | ||
- 손익계산서(포괄손익계산서)
<손 익 계 산 서(포 괄 손 익 계 산 서)>
| 제 7 기 2020년 1월 1일부터 2020년 12월 31일까지 |
| 제 6 기 2019년 1월 1일부터 2019년 12월 31일까지 |
| (단위 : 원) |
| 과 목 | 제 7 기 | 제 6 기 | ||
|---|---|---|---|---|
| I. 매출액 | 9,097,634,672 | 8,644,433,540 | ||
| 1. 상품매출 | 9,095,807,384 | 8,530,970,591 | ||
| 2. 제품매출 | - | 158,400 | ||
| 3. 임대료수입 | - | 28,000,000 | ||
| 4. 제품수출액 | - | 15,287,703 | ||
| 5. 수수료수입 | 1,827,288 | 70,016,846 | ||
| II. 매출원가 | 8,549,292,549 | 8,111,698,458 | ||
| 1. 상품매출원가 | 8,549,292,549 | 7,643,916,007 | ||
| 2. 제품매출원가 | - | 467,782,451 | ||
| III. 매출총이익 | 548,342,123 | 532,735,082 | ||
| IV. 판매비와관리비 | 3,088,143,885 | 2,746,202,563 | ||
| 1. 급여 | 747,343,795 | 732,449,161 | ||
| 2. 퇴직급여 | 75,448,758 | 90,344,274 | ||
| 3. 복리후생비 | 56,273,464 | 69,334,921 | ||
| 4. 여비교통비 | 34,453,465 | 30,148,537 | ||
| 5. 접대비 | 34,678,220 | 29,667,471 | ||
| 6. 통신비 | 7,128,821 | 8,658,175 | ||
| 7. 수도광열비 | 34,310 | 148,230 | ||
| 7. 전력비 | 5,804,976 | 6,624,297 | ||
| 9. 세금과공과 | 41,589,630 | 56,793,120 | ||
| 10. 감가상각비 | 26,403,678 | 26,648,560 | ||
| 11. 지급임차료 | 88,800,000 | 134,201,900 | ||
| 12. 수선비 | 13,543,020 | 820,500 | ||
| 13. 보험료 | 27,921,181 | 25,690,485 | ||
| 14. 차량유지비 | 30,845,428 | 38,679,977 | ||
| 15. 경상연구개발비 | 1,237,632,180 | 506,262,180 | ||
| 16. 운반비 | 41,771,639 | 28,581,563 | ||
| 17. 교육훈련비 | 50,000 | 720,000 | ||
| 18. 도서인쇄비 | 2,429,150 | 2,438,092 | ||
| 19. 회의비 | - | 270,500 | ||
| 20. 사무용품비 | 1,848,651 | 1,240,767 | ||
| 21. 소모품비 | 18,415,724 | 4,742,740 | ||
| 22. 지급수수료 | 155,427,000 | 154,696,890 | ||
| 23. 광고선전비 | 150,000 | 3,555,000 | ||
| 24. 판매촉진비 | 171,584,502 | 389,927,649 | ||
| 25. 대손상각비 | 29,894,679 | 152,431,002 | ||
| 26. 건물관리비 | 6,894,627 | 18,013,320 | ||
| 27. 수출제비용 | - | 1,465,932 | ||
| 28. 무형자산상각비 | 231,776,987 | 231,647,320 | ||
| V. 영업이익(손실) | (2,539,801,762) | (2,213,467,481) | ||
| VI. 영업외수익 | 75,466,451 | 194,876,006 | ||
| 1. 수입임대료 | - | 4,300,000 | ||
| 2. 이자수익 | 2,568,566 | 1,633,387 | ||
| 3. 외환차익 | 27,122 | 1,658,722 | ||
| 4. 외화환산이익 | 1,565,866 | 3,929,132 | ||
| 5. 유형자산처분이익 | 49,269,550 | 175,428,053 | ||
| 6. 국고보조금 | - | - | ||
| 7. 잡이익 | 22,035,347 | 7,926,712 | ||
| VII. 영업외비용 | 522,002,807 | 292,496,430 | ||
| 1. 이자비용 | 116,096,189 | 68,908,866 | ||
| 2. 외환차손 | 7,029 | 428,800 | ||
| 3. 외화환산손실 | 3,896,057 | 4,842,120 | ||
| 4. 재고자산평가손실 | - | 126,542,426 | ||
| 5. 유형자산처분손실 | 94,214 | 21,609,947 | ||
| 6. 전기오류수정손실 | - | - | ||
| 7. 기타의 감가상각비 | - | 69,871,600 | ||
| 8. 잡손실 | 4,466,249 | 292,671 | ||
| 9. 무형자산손상차손 | 397,443,069 | - | ||
| VIII. 법인세비용차감전순이익(손실) | (2,986,338,118) | (2,311,087,905) | ||
| IX. 법인세등 | - | - | ||
| X. 당기순이익(손실) | (2,986,338,118) | (2,311,087,905) | ||
- 결손금처리계산서(안)
<결손금처리계산서>
| 제 7 기 2020년 1월 1일부터 2020년 12월 31일까지 |
| 제 6 기 2019년 1월 1일부터 2019년 12월 31일까지 |
| (단위 : 원) |
| 과 목 | 제 7 기 | 제 6 기 | ||
|---|---|---|---|---|
| I.미처리결손금 | 10,557,622,000 | 7,571,283,882 | ||
| 1.전기이월미처리결손금 | 7,571,283,882 | 5,260,195,977 | ||
| 2.회계변경의기준효과 | ||||
| 3.전기오류수정이익 | ||||
| 4.전기오류수정손실 | ||||
| 5.당기순손실 | 2,986,338,118 | 2,311,087,905 | ||
| II.결손금처리액 | ||||
| 임의적립금이입액 | ||||
| III.이익잉여금처분액 | ||||
| 1.이익준비금 | ||||
| 2.기업합리화적립금 | ||||
| 3.배당금 | ||||
| 가.현금배당 | ||||
| 나.주식배당 | ||||
| 4.사업확장적립금 | ||||
| 5.감채적립금 | ||||
| 6.배당평균적립금 | ||||
| IV.차기이월결손금 | 10,557,622,000 | 7,571,283,882 |
||
- 최근 2사업연도의 배당에 관한 사항
| 구분 | 제6기 | 제5기 | ||||
| 보통주 | 우선주 | 계 | 보통주 | 우선주 | 계 | |
| 주당배당금(원) | - | - | - | - | - | - |
| 배당금총액(백만원) | - | - | - | - | - | - |
| 시가배당율(%) | - | - | - | - | - | - |
□ 이사의 보수한도 승인
가. 이사의 수ㆍ보수총액 내지 최고 한도액
(당 기)
| 이사의 수 (사외이사수) | 3( 1 ) |
| 보수총액 또는 최고한도액 | 300백만원 |
(전 기)
| 이사의 수 (사외이사수) | 3( 1 ) |
| 실제 지급된 보수총액 | 235백만원 |
| 최고한도액 | 300백만원 |
※ 기타 참고사항
□ 감사의 보수한도 승인
가. 감사의 수ㆍ보수총액 내지 최고 한도액
(당 기)
| 감사의 수 | 1 |
| 보수총액 또는 최고한도액 | 100백만원 |
(전 기)
| 감사의 수 | 1 |
| 실제 지급된 보수총액 | 0 |
| 최고한도액 | 100백만원 |
※ 기타 참고사항
IV. 사업보고서 및 감사보고서 첨부
가. 제출 개요
| 제출(예정)일 | 사업보고서 등 통지 등 방식 |
|---|---|
| 2021년 03월 15일 | 1주전 회사 홈페이지 게재 |
※ 사업보고서 및 감사보고서는 2021년 3월 15일 회사 홈페이지 및 전자공시시스템(DART)을 통해 공시할 예정입니다.
나. 사업보고서 및 감사보고서 첨부
상법시행령 제31조(주주총회의 소집공고)에 의거하여 사업보고서 및 감사보고서는 주주총회 1주전까지 홈페이지에 게재하고, 전자공시시스템(DART)를 통하여 공시 예정입니다.
※ 홈페이지 주소 : http://www.yidobio.com
향후 사업보고서는 주주총회 이후 변경된 사항 및 오기 등이 있는 경우 수정사항을 반영하여 전자공시시스템(DART)에 업데이트 될 예정입니다.
※ 참고사항
| □ 코로나바이러스 감염증-19(COVID-19)의 감염 및 전파를 예방하기 위하여, 총회 입장전 '체온계'의 측정 결과에 따라 발열이 의심되는 경우 출입이 제한될 수 있음을 알려드립니다. 또한, 질병 예방을 위해 주주총회에 참석시 반드시 마스크 착용을 부탁드립니다. □ 주총 집중일 주총 개최 사유 : 해당사실이 없음 |