[ 의약품 분류 ]
[ 바이오의약품 분류 ]
 |
|
의약품 분류 |
 |
|
바이오의약품 분류 |
주주총회소집공고
| 2020년 03월 13일 | ||
| 회 사 명 : | 주식회사 셀리버리 | |
| 대 표 이 사 : | 조대웅 | |
| 본 점 소 재 지 : | 서울시 마포구 상암동 189 중소기업DMC타워 9층 | |
| (전 화) 02-3151-8900 | ||
| (홈페이지) http://www.cellivery.com | ||
| 작 성 책 임 자 : | (직 책) 부사장 | (성 명) 기정욱 |
| (전 화) 02-3151-8900 | ||
주주총회 소집공고
| (제06기 정기) |
주주님의 건승과 댁내의 평안을 기원합니다.
당사는 상법 제 363조와 정관 제 18조에 의거 제6기 정기주주총회를 아래와 같이 개최 하오니 참석하여 주시기 바랍니다.
- 아 래 -
1. 일시 : 2020년 3월 30일(월요일) 오전 09시 00분
2. 장소 : 서울특별시 마포구 성암로189 (상암동1622) 중소기업DMC타워 2층 DMC홀
3. 회의 목적 사항
가. 보고사항
1) 감사보고
2) 영업보고
3) 내부회계관리제도 운영보고
나. 결의사항
제1호 의안 : 제6기 재무제표 승인의 건
제2호 의안 : 이사 선임의 건
제2-1호 의안 : 사내이사 조대웅 선임의 건 (재선임)
제2-2호 의안 : 사내이사 기정욱 선임의 건 (재선임)
제2-3호 의안 : 사내이사 최영실 선임의 건 (신규선임)
제2-4호 의안 : 사외이사 김형준 선임의 건 (신규선임)
제3호 의안 : 주식매수선택권 부여의 건
제4호 의안 : 이사 보수한도 승인의 건
제5호 의안 : 감사 보수한도 승인의 건
4. 실질주주의 의결권 행사에 관한 사항
금번 당사의 주주총회에는 자본시장과 금융투자업에 관한 법률 제314조에 의거 한국예탁결제원이 주주님들의 의결권을 대리 행사할 수 없습니다. 따라서 주주님이 주주총회에 참석하여 의결권을 직접적으로 행사하시거나, 대리인에 위임하여 의결권을 간접적으로 행사하실 수 있습니다.
5. 경영참고사항 등의 비치
상법 제542조의4에 의거 경영참고사항은 당사의 본사와 KB국민은행 증권대행부에 비치하였고, 금융감독원 또는 한국거래소에 전자공시하여 조회가 가능하오니 참고하시기 바랍니다.
6. 주주총회 참석 시 준비물
- 직접행사 : 신분증(주민등록증, 운전면허증, 여권만 인정됨)
- 대리행사 : 위임장(주주와 대리인의 인적사항 기재, 인감날인), 인감증명서, 대리인 신분증
※ 금번 제6기 정기주주총회에서는 주주님들에게 선물을 지급하지 않을 예정이오니 양해 바랍니다.
2020년 03월 13일
주식회사 셀리버리
대표이사 조대웅(직인생략)
주주총회 소집공고
본인(위임하는 자)은 2020년 3월 30일에 개최하는 (주) 셀리버리의 제06기 정기 주주총회와 관련하여 그 위임받는 자를 정하고 다음의 내용과 같이 찬반표시에 따라 의결권을 행사할 것을 위임합니다.
- 다 음 -
1. 주주명 :
2. 소유 주식수 : 주
3. 의결권 있는 주식수 : 주
4. 위임할 주식수 : 주
5. 주주총회 목적사항 및 목적사항별 찬반여부
|
구 분 |
주주총회 목적사항 |
찬 성 |
반 대 |
|
|
제1호 의안 |
제06기 재무제표 승인의 건 |
|||
|
제2호 의안 |
2-1호 의안 사내이사 선임의 건 |
사내이사 후보 조대웅 | ||
| 2-2호 의안 사내이사 선임의 건 |
사내이사 후보 기정욱 | |||
| 2-3호 의안 사내이사 선임의 건 |
사내이사 후보 최영실 | |||
| 2-4호 의안 사외이사 선임의 건 |
사외이사 후보 김형준 | |||
|
제3호 의안 |
주식매수선택권 부여 승인의 건 | |||
|
제4호 의안 |
이사보수한도 승인의 건 | |||
|
제5호 의안 |
감사보수한도 승인의 건 | |||
6. 새로 상정된 안건이나 변경ㆍ수정 안건 등에 대한 의결권의 행사위임
- 주주총회시 새로이 상정된 안건이나 각호 의안에 대한 수정안이 상정될 경우에는 대리인이 주주의 의사표시가 찬반의 취지에 합치된다고 합리적으로 판단되는 바에 따라 의결권을 행사할 것을 위임합니다.
- 다만 아래에 명시적으로 지시한 사항에 대해서는 주주가 주주총회 전까지 별도의 의사표시가 없는 한 아래의 지시한 대로 의결권을 행사하겠습니다.
|
항 목 |
지 시 내 용 |
|
|
|
7. 위임받는자
성명:
주민등록번호:
주소:
주주명 (위임하는 자): (인)
주민등록번호(사업자등록번호):
주소:
I. 사외이사 등의 활동내역과 보수에 관한 사항
1. 사외이사 등의 활동내역
가. 이사회 출석률 및 이사회 의안에 대한 찬반여부
| 회차 | 개최일자 | 의안내용 | 사외이사 | 기타비상무이사 |
|---|---|---|---|---|
| 김형곤 (출석률: 100%) |
이장휘 (출석률: 100%) |
|||
| 찬 반 여 부 | ||||
| 1 | 2019.02.08 | 1. 주식매수선택권 부여 취소의 건 2. 외부감사인 선임의 건 3. 임원복리후생의 건 |
찬성 | 찬성 |
| 2 | 2019.02.27 | 1. 주주총회소집의 건 2. 재무제표 승인의 건 |
찬성 | 찬성 |
| 3 | 2019.03.25 | 1. 신주 발행의 건 | 찬성 | 찬성 |
| 4 | 2019.04.02 | 1. 대표이사로부터의 자산 취득의 건 | 찬성 | 찬성 |
| 5 | 2019.12.12 | 1. 내부회계관리규정 개정의 건 | 찬성 | 찬성 |
나. 이사회내 위원회에서의 사외이사 등의 활동내역
| 위원회명 | 구성원 | 활 동 내 역 | ||
|---|---|---|---|---|
| 개최일자 | 의안내용 | 가결여부 | ||
| - | - | - | - | - |
해당사항없습니다.
2. 사외이사 등의 보수현황
| (단위 : 백만원) |
| 구 분 | 인원수 | 주총승인금액 | 지급총액 | 1인당 평균 지급액 |
비 고 |
|---|---|---|---|---|---|
| 사외이사 (비상근) |
1 | 1,000 | - | - | - |
| 기타비상무이사 | 1 | 1,000 | - | - | - |
※ 상기의 주총승인금액은 등기이사 4명에 대한 보수총액 한도액 입니다.
II. 최대주주등과의 거래내역에 관한 사항
1. 단일 거래규모가 일정규모이상인 거래
| (단위 : 원) |
| 거래종류 | 거래상대방 (회사와의 관계) |
거래기간 | 거래금액 | 비율(%) |
|---|---|---|---|---|
| - | - | - | - | - |
해당사항이 없습니다.
2. 해당 사업연도중에 특정인과 해당 거래를 포함한 거래총액이 일정규모이상인 거래
| (단위 : 억원) |
| 거래상대방 (회사와의 관계) |
거래종류 | 거래기간 | 거래금액 | 비율(%) |
|---|---|---|---|---|
| - | - | - | - | - |
해당사항이 없습니다.
III. 경영참고사항
1. 사업의 개요
가. 업계의 현황
(1) 사업 환경
1) 바이오의약품 정의
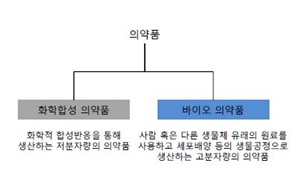
바이오의약품은 사람이나 다른 생물체에서 유래하는 세포, 단백질, 유전자 등을 원료로 하여 제조한 의약품으로 성분에 따라 다양하게 구분된다. 대표적인 바이오의약품으로는 항체의약품, 백신, 세포치료제, 유전자치료제 등이 있으며 ETC 의약품 중 널리 상용화된 합성의약품 대비 분자량이 크고 구조가 복잡한 특징을 가지고 있습니다. 바이오의약품은 생물공정을 거치기 때문에 상대적으로 가격이 높게 형성되어 있으며 화학의약품 대비 개발/생산이 복잡하여 높은 진입장벽을 형성하고 있습니다. 게다가 화학합성의약품보다 부작용이 적고 특정 질환에 대한 효과가 뛰어나기 때문에 의약품시장에서 영향력이 점차 커지고 있습니다.
사이언스타임즈에 따르면 바이오의약품의 기원은 1909년에 독일의 면역학자인 에를리히(PaulEhrlich)의 연구에서 시작되었으며, 매독균만 선택적으로 배양할 수 있는 화학물질의 배양에 성공하였고, 이를 이용한 매독 치료제는 맞춤치료제의 출발로 큰 인기를 누렸습니다. 이후 1980년대 전후로 바이오의약품의 큰 발전이 있었는데, 1973년에 유전자재조합기술을 이용하여 코헨(StanleyCohen)과 보이어(Herbert Boyer)가 최초의 재조합 DNA인 박테리아 플라스미드(plasmid)의 합성에 성공하면서 유전자재조합의약품 생산의 길이 열리게 되었습니다. 1982년에 Eli Lilly & Company사에서 인간 인슐린(insulin)인 휴뮬린(Humulin)을 출시하였고, 이어서 인간성장호르몬인 프로트로핀(Protropin, 1985), 인터페론(interferon)인 인트로에이(Intron-A, 1986), 빈혈치료제인 에포젠(Epogen, 1989) 등 획기적 제품들이 출시되면서 바이오의약품은 의약산업의 한 부분으로 자리잡게 되었습니다.
|
[ 의약품 분류 ] |
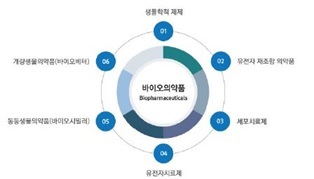
[ 바이오의약품 분류 ] |
||||
|
|
2) 바이오산업의 특성
의약품 산업은 국민의 건강관리 및 질병의 예방, 치료, 처치, 진단을 위한 약품을 개발ㆍ제조ㆍ판매하는 산업으로서 전 세계적으로 빠르게 진행되고 있는 인구 고령화, 경제성장으로 인한 평균 수명 증가 등에 따라 향후 급속한 성장이 예상되는 분야입니다.
의약품 산업은 크게 화학적 합성 의약품이 중심이 되는 저분자 의약품과 바이오 기술의 접목을 통해 단백질 및 백신 등이 중심이 되는 고분자 의약품으로 구분됩니다. 최근에는 생명공학을 바탕으로 생물체의 기능 및 정보를 활용하여 만들어진 고분자(바이오) 의약품이 전통적인 합성물 의약품 시장보다 빠르게 성장하고 있는데, 이런 바이오의약품은 항체치료제, 세포치료제, 유전자치료제, 줄기세포치료제, 백신 등을 포함하고 있습니다.
바이오의약품의 특성은 일반적으로 합성의약품에 비해 크기가 크고, 복잡한 구조를 가지고 있으며, 생물체를 이용하여 복잡한 제조공정을 거쳐야 되므로 변화에 민감하고, 특히 오염 및 불순물 관리에 유의해야 하는 반면 생물유래 물질로 고유의 독성이 낮고 작용기전이 명확하여 난치성 및 만성 질환에 뛰어난 효과를 가지고 있습니다.
바이오의약품은 백신과 혈액제제 등으로 일컬어지는 1세대 바이오의약품을 시작으로 유전자조작 및 세포배양기술을 도입한 재조합의약품과 세포배양의약품 그리고 최근에는 세포융합기술 및 정보기술 등을 접목한 항체의약품, 유전자치료제, 세포치료제, DNA 백신 등과 같은 첨단 바이오의약품으로 발전되고 있습니다.
① 철저한 규제 의존성
새로운 의약품이 환자에게 판매되기 위해서는 신약후보물질의 발굴에서부터 동물을 대상으로 하는 전임상 시험, 인체를 대상으로 하는 임상시험, 시판승인이라는 각 단계를 모두 거쳐야 하며, 모든 단계에서 각 국가의 규제당국이 제시하는 규정을 모두 준수해야 합니다.
특히 인체를 그 시험대상으로 하는 임상시험을 진행하고자 할 때에는 효능과 안전성에 대한 각 국가의 정부규제가 엄격하여, 인체에 대한 임상시험 이전 단계부터 엄격한 규제에 의해 축적된 다양한 데이터를 각 국가의 규제당국에 제출하여야 합니다. 또한, 임상개시를 허용받고 임상시험을 진행 중인 경우에도 심각한 부작용 등이 보고되는 경우에는 진행 중인 임상이 규제당국에 의해 중단되거나 철회될 수 있습니다. 또한, 임상시험을 성공적으로 마치고 시판승인을 받은 신약을 생산 및 판매하는 과정에서도 규제당국이 제시하는 엄격한 규정을 따라야 합니다.
 |
|
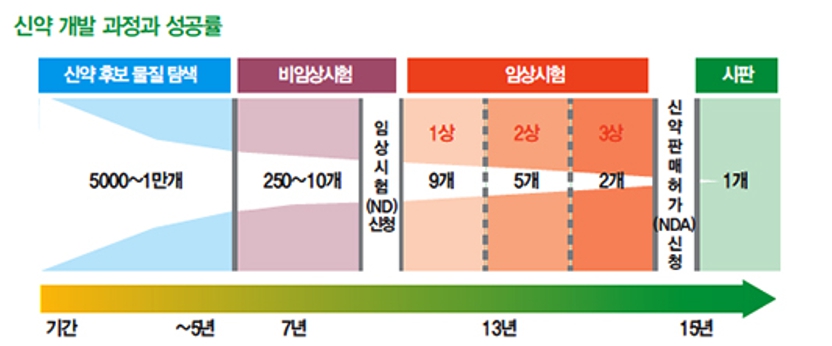
신약 개발 과정과 성공률 |
자료: 식품의약품안전처
다만, 개발중인 신약의 안정성이 일정 수준 이상 확인되고 그 의학적 효능이 기존 치료제 대비 월등하거나, 희귀질환을 치료할 수 있는 경우에는 전체 규정된 임상단계가 완료되지 않은 단계에서도 조건부 혹은 전면 조기시판승인이 허용되기도 합니다.
② 높은 진입장벽
신약후보물질이 초기 연구 및 임상시험을 거쳐 시판승인을 이루기까지는 짧게는 수년에서 길게는 15년 이상의 기간이 소요되며, 그 과정에서 많은 개발비용이 발생하게됩니다. 즉, 제약 및 신약 개발산업은 높은 개발비용에 따른 진입 장벽이 존재합니다.
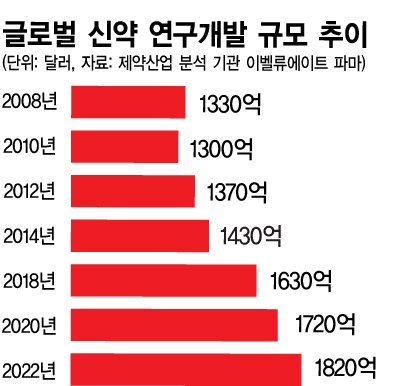
조사결과에 따르면 신약개발 과정에서 발생하는 개발비용은 지속적으로 증가하는 추세를 보이고 있습니다. 2010년 1,300억불에서 2020년에는 1,720억불로 증가가 예상되며 2022년에는 1,820억불에 달할 것으로 예상되고 있습니다. 이는 신약의 성공확률이 과거대비 하락하고 있어 시판에 성공하는 신약 당 연구개발비용의 증가세가 두드러지는 것으로 이해되며, 결과적으로 신약개발에 따른 진입장벽이 갈수록 높아지고 있는 추세를 보이고 있는 것으로 파악됩니다.
 |
|
글로벌신약연구개발비 |
한편, 오랜 기간에 걸쳐 개발된 신약은 통상적으로 특허권에 의해 일정기간 동안 그 권리를 보호받게 되며, 희귀질환 치료제의 경우 신약개발의 인센티브를 부여하기 위하여 규제당국으로부터 시판승인 후 일정기간 동안 독점판매기간을 허용 받을 수도 있습니다. 또한, 한번 시판된 신약에 대해서는 그 사업성을 보장해주기 위해, 타 신약 후보군의 비열등성이 입증되고, 이미 시판된 신약과 비슷한 기전과 효능 및 부작용을 가질 경우에는 시판승인을 불허하고 있는 추세입니다.
대부분의 국가에서 특허 존속기간은 출원 후 20년이고, 해당 신약이 희귀의약품(orphan drug)으로 지정되는 경우에는 특허 존속기간과 관계없이 미국은 시판 승인후 7년, 유럽은 10년간 독점판매권을 보장받기 때문에 해당 기간 동안 유사한 효능을 가지는 신약이나 복제약이 시장진입을 하기 힘든 구조입니다.
주요국의 특허 존속기간 및 의약품 독점 판매 기간
|
구분 |
특허 존속기간 |
희귀의약품 지정시 독점 판매기간 |
|---|---|---|
|
미국 |
출원 후 20년 |
신약 시판승인 후 7년 |
|
유럽 |
출원 후 20년 |
신약 시판승인 후 10년 |
|
한국 |
출원 후 20년 |
- 주) |
자료: 각 국 특허청 및 식약청
주) 한국은 희귀의약품에 대한 독점 판매기간 부여제도를 운영하고 있지 아니합니다.
각 국가의 규제당국은 신약에 대한 시판 승인 이전이라 하더라도 기존에 진행 중인 임상시험과 동일하거나 유사한 개념의 신규 임상시험 신청에 대해서는 승인을 불허하여 선행 임상진행 신약후보군에 대한 보호조치를 시행합니다.
오랜 신약개발 과정동안 발생하는 높은 개발비, 특허권 또는 독점판매기간으로 보장되는 권리 등으로 인하여 제약 및 신약개발 산업은 여타 산업 대비 강력한 진입장벽을 가집니다.
③ 고위험, 고부가가치 (high risk, high return)
전술한 바와 같이 제약 및 신약개발 산업은 철저한 규제의존성 및 높은 진입장벽이라는 위험이 존재하는 만큼 일단 시판승인을 획득하게 되면 특허권을 통한 자체적 권리보호조치 및 허용된 독점판매기간 등을 통해 판매할 신약에 대한 가격결정력의 행사가 가능하게 되어 높은 부가가치를 창출합니다. 또한, 신약을 개발하기 위해 많은 비용이 투입되지만, 시판 이후에는 생산 및 마케팅 비용 대비 약가가 높은 수준에 형성이 되어 높은 수준의 수익성 시현이 가능합니다.
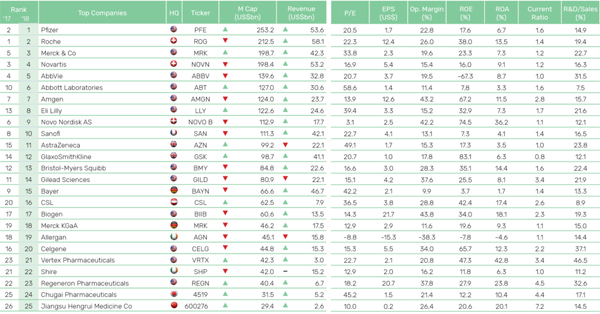
2018년 톱 25대 제약사는 평균 영업이익이 21.6%인 반면 톱10은 평균 22.8%로 보고 되었으며, 이는 일반 제조업 등에 비해 매우 높은 수익성입니다.
[ 글로벌 제약사의 2018년 영업이익률 ]
 |
|
글로벌제약사의 2018년 영업이익률 |
자료: 글로벌데이터
④ 연구 집약적
신약개발을 위해서는 기초연구부터 허가과정까지 의학, 약학, 화학, 생물학 등 제반 기능이 유기적으로 결합되어야 하며 10여 년의 개발과정을 거쳐야 하므로 그 어떤 산업보다 연구개발 비중이 높습니다. 2015년 기준 제약산업의 1인 평균 R&D 비용은 산업 중 가장 많은 13만$ 이며 이는 반도체 산업의 약 3배에 달하는 수치입니다. (2015 Profile Biopharmaceutical Research Industry_PhRMA)
⑤ 지적 재산권 확보가 경쟁력의 핵심
제약 산업은 물질특허의 확보가 사업의 핵심 성공 요인으로, 이 물질 특허를 얻지 못하면 원천적으로 사업이 불가능하거나 물질특허 소유자로부터 기술이전을 받아야 합니다. 임상2상a 이상을 수행하기 어려운 중소규모 제약사나 벤처는 임상2상a 단계 이전에 글로벌제약사에 기술이전을 함으로써 수익을 창출할 수 있습니다. 특허가 가장 중요한 경쟁요소이기 때문에 대부분의 국가에서는 특허기간을 최대한 보호하기 위한 다양한 전략 및 정책을 도입하고 있습니다.
3) 바이오산업의 성장성(가) 글로벌 의약품 시장
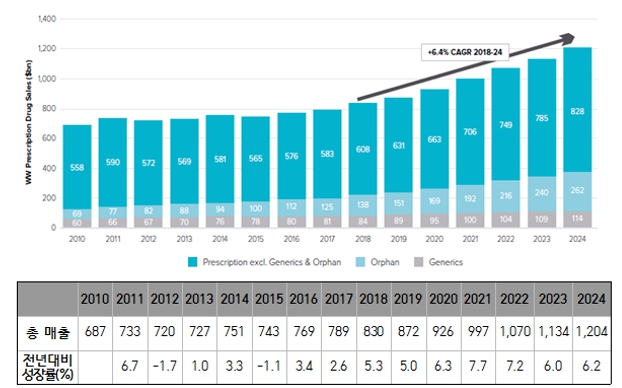
세계 전문의약품 시장은 매년 지속적으로 성장하고 있습니다. 글로벌 제약시장 조사기관인 EvaluatePharma에 따르면, 세계 전문의약품 시장규모는 2018년 8300억 달러에서 2024년까지 6.4% 성장하여 매출액 1조 2004억달러가 예상됩니다. 이러한 급격한 성장 배경은 최근 산업 환경변화에 따른 영향으로 세계적인 인구 고령화 추세에 따라 노인성, 만성질환에 대한 치료수요가 빠르게 증가하고 있고, 삶의 질 향상으로 건강증진 및 유지를 위한 의료분야의 지출이 확대되고 있기 때문입니다.
 |
|
글로벌의약품 시장 |
자료: 글로벌 의약품 시장 (EvaluatePharma, World Preview 2018, Outlook to 2024)
글로벌 의약품 시장에서 바이오 의약품이 차지하는 비중은 매년 증가 추세이며, 글로벌 의약품 전체시장에서 바이오의약품 비중은 2017년 25%에서 2024년 31%로 증가할 전망입니다.
또한, 글로벌 매출 상위 100대 제품에서 바이오의약품 비중은 2017년 49%에서 2024년 52%로 증가할 전망입니다.
CPP 기반으로한 바이오의약품 개발은 임상3상까지 진행되고 있는 성장기에 있는 기술입니다. 당사에서 개발 완료한 가장 진보된 hydrophobic CPP인 aMTD-융합 재조합단백질 기반 바이오신약/바이오베터 및 연구용시약 분야는 당사의 독보적인 기술입니다. 기전특이적인 효능 (mechanism-specific activity)를 가지고 있는 약리물질은 특정 질병 또는 특정 기전에만 작용할 수 있기 때문에 세포 내로 전송 가능 하다면, 부작용이 낮아 매우 안전합니다. 또한, 강력한 생체 내 세포 간 연속전송능 (cell-to-cell systemic delivery)을 통한 우수한 약효를 가진 바이오 의약품 개발이 가능할 것입니다. 독보적인 기술 확보 및 limitation이 없는 제품 개발, 그리고 바이오 의약품 시장의 큰 폭의 성장성으로 당사의 "약리물질 생체 내 전송기술" 을 이용한 바이오의약품 연구 및 개발도 지속적으로 성장해 나갈 것이며, 또한, 당사의 기술수명주기는 매우 길 것으로 판단됩니다.
4) 목표시장의 구성- 바이오 의약품 (Biotherapeutics)
(가) 바이오 의약품 현황
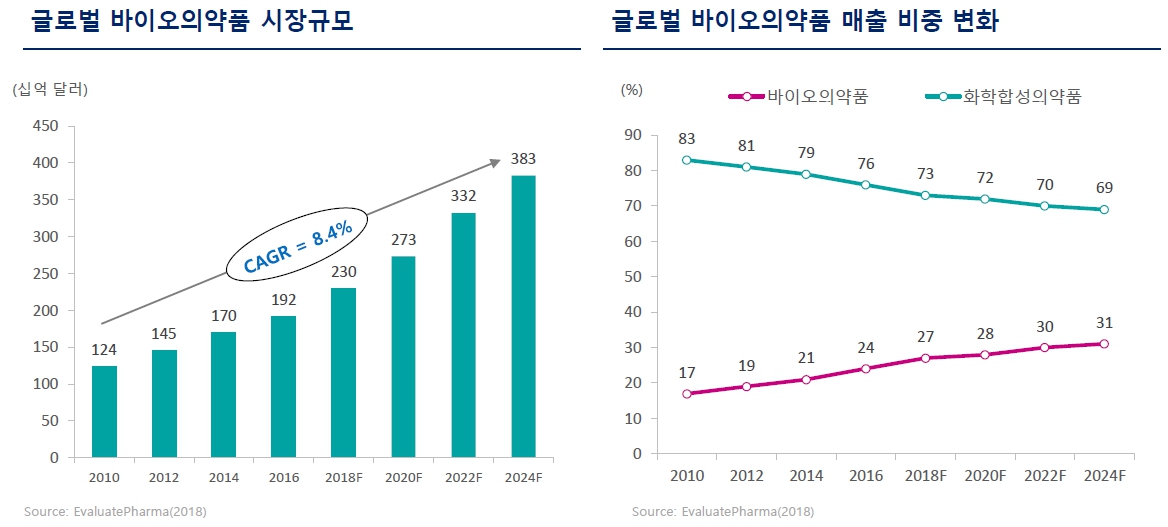
글로벌 의약품 시장의 추세는 점진적으로 합성의약품에서 바이오의약품으로 이동하고 있습니다. 글로벌 의약품 시장에서 바이오의약품이 차지하는 비중은 매년 증가 추세이며 매출 비중은 2010년 17%에서 2020년 28%로 증가하였습니다.
그 성장세는 지속되어 2024년에는 바이오의약품의 시장내 비중이 31% 로 증가할 전망입니다.
 |
|
글로벌 바이오의약품 시장 규모와 매출비중 변화 |
자료: 글로벌 바이오의약품 시장규모와 매출비중 변화 (EvaluatePharma, 삼정KPMG 경제연구원)
(나) 바이오 의약품의 분류
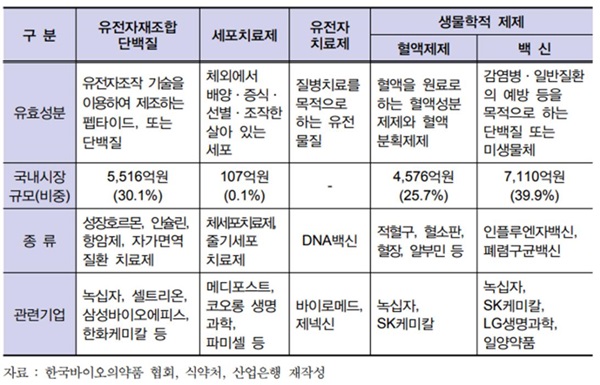
바이오의약품은 유효성분에 따라 유전자재조합단백질 (recombinant protein), 세포치료제 (cell therapy products), 유전자치료제 (gene therapy products), 혈액제제 (blood medicine), 백신 (vaccine)등으로 구분할 수 있습니다. 생산조건 및 환경에 민감한 생물체를 이용하여 생산하고 있고, 그 제조공정이 복잡하여, 생산시설 구축과 생산기술 확보 등의 진입장벽이 매우 높습니다. 한편, 당사의 주력 기술 제품은 유전자재조합단백질 바이오 의약품에 해당합니다.
| [ 바이오의약품의 종류] |
 |
|
바이오 의약품의 종류 |
자료 : 바이오의약품의 종류 (한국바이오의약품 협회, 식약처, 산업은행)
(다) 유전자재조합단백질 (Recombinant protein)
(다)-1 유전자재조합단백질의 분류
유전자재조합단백질은 유전자재조합 (gene recombinant), 세포배양 (cell culture), 단백질공학 (protein engineering) 기술 등을 기반으로 합니다. 유전자재조합단백질은 미생물, 동물세포를 이용하여 대량생산이 가능하며 인체 천연 단백질과 유사한 구조로 체내 부족한 단백질을 보충해주는 치료용단백질 (therapeutic protein), 항체의약품 (therapeutic antibody), 바이오시밀러 (bio-simillar), 바이오베터 (bio-better) 등으로 나눌 수 있습니다. 당사의 기술개발제품은 치료용 세포투과성 재조합단백질 (cell-permeable therapeutic recombinant protein), 세포투과성 바이오베터가 있습니다
|
구분 |
치료용단백질 |
항체의약품 |
바이오시밀러 |
바이오베터 |
|---|---|---|---|---|
|
개요 |
- 인체 천연 단백질과 유사한 구조와 기능을 보유 - 체내 부족한 유용 단백질 보충 |
- 안정한 구조를 가진 항체 - 발병기전에 작용하는 인자가 표적 |
- 특허가 만료된 의약품과의 비교 동등선이 입증된 복제약 |
- 기존 의약용 단백질의 효능, 안전성, 환자편의성 등을 개선한 신약 |
자료: 유전자재조합단백질의 분류 (산업은행, 바이오의약품 기술 및 산업 동향)
(다)-2 유전자재조합단백질 시장 및 임상추진 현황
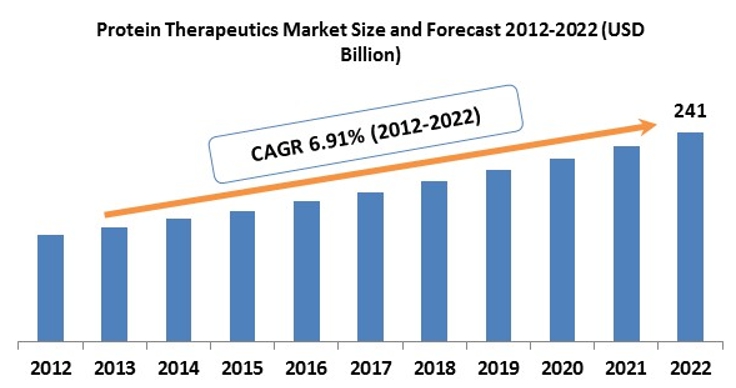
세계 단백질제제 시장의 10년간 (2012년-2022년) 평균성장율은 6.91%로 2022년에는 약 290조원에 달할것으로 예상됩니다
 |
|
단백질치료제 시장 및 예측 |
자료: Crystal Market Research
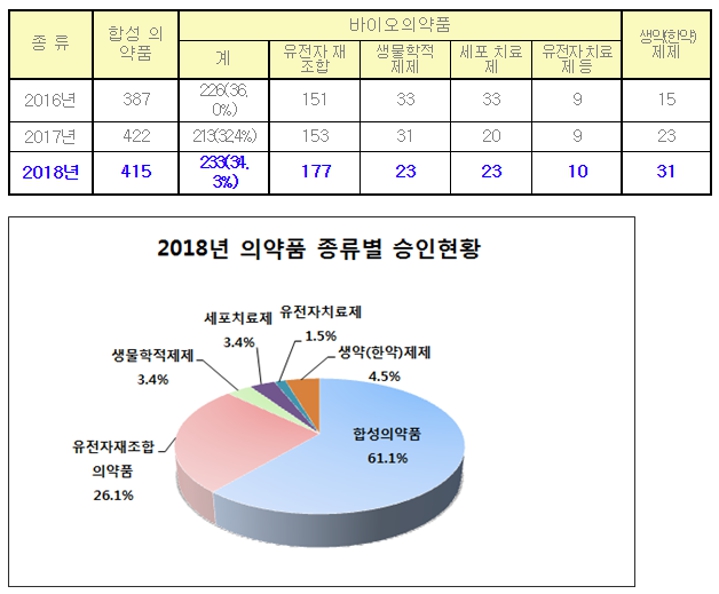
국내 바이오의약품 시장의 파이프라인도 글로벌트렌드와 유사한 증가세를 보이고 있습니다. 국내 바이오의약품 중 유전자재조합단백질의약품 임상개발이 가장 활발하며, 2018년 국내 전체 의약품 종류별 임상 승인 비중은 유전자 재조합이 26.1%, 생물학적 제재 3.4%, 유전자치료제가 1.5%를 차지합니다.
 |
|
의약품 종류별 승인현황 |
자료 : 식약처, 2018년 임상시험 승인 현황 결과 발표
시장 내 보고서에 따르면, 유전자재조합단백질의 임상 실패율은 매우 낮으며 이에 당사의 안전하고 기전특이적인 단백질소재 바이오신약 개발제품의 성공율도 매우 높을 것입니다.
(라) 비임상 단계에서의 라이센싱 사례
2016년도 비임상 단계에서 대규모의 기술이전 사례는 11건이 있었으며, 그 중 특히 파킨슨병 치료제와 같은 퇴행성뇌질환 분야는 1건으로 Allergan과 Heptares간의 기술이전으로서 (계약금)upfront fee만 125백만 달러 (1,500억 원) 규모로 성사되었습니다. Heptares 에서 개발된 의약품은 알츠하이머 및 다른 뇌질환에 적용 가능한 치료제로서 가능성을 보여 총 3.3십억 달러 (한화 4조 원)의 계약규모로 기술이전 되어 파킨슨병 및 알츠하이머병 치료제로서 사용 가능한 당사 iCP-Parkin(파킨슨병 치료제)기술이전 거래의 좋은 사례일 것으로 판단됩니다.
|
No. |
Licensor/Licensee |
Disease Area |
Phase |
Upfront |
BioBucks |
|---|---|---|---|---|---|
|
1 |
Allergan/Heptares |
Neurology(신경학) |
Preclinical(비임상) |
$125M |
$3.3B |
|
2 |
Celgene/Jounce |
Immuno-oncology(면역항암제) |
Preclinical(비임상) |
$261M |
$2.5B |
|
3 |
Novartis/Xencor |
Immuno-oncology(면역항암제) | Preclinical(비임상) |
$150M |
$2.5B |
|
4 |
Sanofi/DiCE Molecules |
Multiple(질병분야 미정) |
Preclinical(비임상) |
$50M |
$2.3B |
|
5 |
Baxalta/Symphogen |
Immuno-oncology(면역항암제) |
Preclinical(비임상) |
$175M |
$1.8B |
|
6 |
Regeneron/Intellia |
CRISPR/Cas9(유전자가위) |
Preclinical(비임상) |
$125M |
$1.7B |
|
7 |
Baxalta/Precision |
Immuno-oncology(면역항암제) |
Preclinical(비임상) |
$105M |
$1.7B |
|
8 |
Celgene/Agios |
mmuno-oncology(면역항암제) | Preclinical(비임상) |
$200M |
$1.2B |
|
9 |
Novartis/Cerulean |
Nanotech Drugs(질병분야 미정) |
Preclinical(비임상) |
$5M |
$1.2B |
|
10 |
Bluebird/Medigene |
mmuno-oncology(면역항암제) | Preclinical(비임상) |
$15M |
$1.0B |
|
11 |
Roche/Blueprint |
mmuno-oncology(면역항암제) | Preclinical(비임상) |
$45M |
$1.0B |
자료: 비임상 (Preclinical trial) 단계의 후보물질 라이센싱 deal size (2016) (Source: Bio Industry Analysis, November 2016)
당사는 기술기반 기업으로 최종 의약품 생산 및 판매를 목적으로 하고 있지 않으며, 전임상 단계에서의 기술이전을 목표로 하고 있습니다.
(2) 정부정책 및 법규 등 규제환경
1) 사회/문화적 환경
세계 전문의약품 시장은 매년 지속적으로 성장하고 있습니다. 이러한 급격한 성장 배경은 최근 산업 환경변화에 따른 영향으로 세계적인 인구 고령화 추세에 따라 노인성, 만성질환에 대한 치료수요가 빠르게 증가하고 있고, 삶의 질 향상으로 건강증진 및 유지를 위한 의료분야의 지출이 확대되고 있기 때문입니다. 이에 따라 국가의 의료복지에 비용이 증가하고 있습니다. 그리고 약물의 안전성과 유효성, 효율적인 치료법에 관심이 집중되면서, 보다 안전성이 확보된 바이오 의약품에 대한 요구가 증가되고 있습니다.
2) 정치/제도적 환경
주요선진국들을 중심으로 바이오 의약품을 미래 성장 동력으로 확보하고 기술 선점을 위한 정부 차원의 육성 전략 수립을 추진하고 있습니다. 미국, EU, 일본 등 주요국가들이 바이오산업을 전략적으로 육성하여 중점 투자하는 것은 차세대 핵심산업으로 성장 가능성이 뚜렷하기 때문입니다. 신 정부는 출범 시 제약 바이오산업의 육성을 위해 아래와 같이 3가지 공약을 제시하였습니다.
- 국제적 규제기준에 부합하는 합리적 기준마련, 정책의 예측가능성을 높이도록 중장기 종합계획 설정
- 국내 개발 신약 글로벌 진출 활성화를 위한 보험 약가 결정구조 개선
- 산학연 연계 신약개발 협력시스템 구축으로 신약개발 생태계 조성
정부는 대통령 직속의 4차 산업혁명위원회에 제약, 의료기기, 바이오 분과 설치를 추진하였고, 치매국가책임제에 따라 향후에 정부의 지속적인 육성 지원을 약속하였습니다.
또한 보건복지부는 제2차 제약산업 육성 지원 종합계획을 공개하였고, 특히 첨단 바이오 의약품 R&D 지원 확대를 약속하였습니다. 세제 혜택 확대 방안으로는 신약 후보물질 발굴, 임상시험 수행 등 R&D에 대한 세액공제를 추가적으로 확대하며, 바이오 의약품이 경제성평가를 통해 비용효과성을 입증하기 어려운 점을 감안해 보다 합리적인 약가 결정제도를 마련하기로 하였습니다.
정부는 바이오산업이 기술혁신 및 융합에 의한 사업화 선점이 가능한 분야로 판단하여 차세대 핵심산업으로 국가에서 전략적으로 육성하고 있으며 이를 통해서 중장기적 연구개발에 따른 국가경쟁력을 강화할 수 있을 것으로 기대하고 있습니다.
3) 법적 환경
식품의약품안전처는 최근 바이오 의약품 예비심사제도 도입 등 현제도의 운영상 나타난 일부 미비점을 보완 개정하기 위해 “생물학적제제 등의 품목허가 심사규정”을 일부 개정 고시하였습니다. 예비심사 (Pre-review)란 품목허가 신청에 대해 정식 심사 개시 전 미리 해당 제출자료 요건에 따른 자료 구비 여부를 신속히 확인해 필요할 경우 자료를 요청하고 심사하여 바이오 의약품의 신속한 허가·심사와 이를 통한 제품화 등을 지원하기 위함 입니다. 이처럼 정부는 합리적인 절차 진행을 통해 제품화와 글로벌 제약시장 진출에 도움을 줄 목적으로 법적 제도적 환경을 개정하고 있습니다.
(주)셀리버리 기술 제품의 개발 및 사업화 전략은 최종 의약품 생산 및 판매를 목적으로 하고 있지 않으며, 전임상 또는 임상 단계에서 기술이전을 목표로 하고 있기 때문에 이에 대한 법적 제약 요인은 없습니다.
나. 회사의 현황
(1) 영업개황 및 사업부문의 구분
(가) 영업개황
당사는 약리물질 생체 내 전송기술 TSDT 플랫폼을 이용하여 4종의 단백질 소재 세포/조직투과성 바이오신약 후보물질인 iCP-Parkin(파킨슨병 치료제), iCP-SOCS3(췌장암 치료제), CP-BMP2(골형성 촉진제), CP-ΔSOCS3(고도비만/당뇨 치료제 ) 와 1종의 펩타이드 소재 세포/조직투과성 바이오신약 후보물질인 iCP-NI(감염성 급성간염 패혈증 치료제) 및 3종의 단백질 소재 세포투과성 연구용 시약인 iCP-Cre(유전체 조절효소), iCP-RFs(역분화 유도인자군 6종), CP-Cas9(유전자 가위)을 개발하고 있습니다.
|
핵심기술 |
주변기술 |
|---|---|
|
- 약리물질 생체 내 전송기술 (TSDT) : 높은 세포/조직투과성 (cell-/tissue-permeability), 용해도 (solubility)와 생산수율 (manufacturing yield)을 갖는 융합 재조합단백질을 만들기 위한 플랫폼 기술 |
-유전자 조작 기술 - 재조합단백질 정제 기술 - 재조합단백질에 활성 검증 기술 - 재조합단백질의 세포/조직투과성 검증 기술 |
[당사 제품 개요]
|
구분 |
후보물질 |
적응증 |
개요 |
|---|---|---|---|
|
신약 후보물질 |
iCP-Parkin |
파킨슨병 (Neurodegenerative Disease-Parkinson’s Disease) |
혈뇌장벽 (blood brain barrier: BBB)을 투과하여 파킨슨병의 근본 원인인 ‘도파민생성 뇌신경 세포 (dopaminergic neurons)의 손상’을 막고 정상화 시켜 증상을 치료하는 First-In-Class 기전특이적 바이오 신약 후보물질 (mechanism-specific biotherapeutic agent) 임. |
|
iCP-SOCS3 |
췌장암 및 고형암 (Pancreatic Cancer & Other Solid Tumors) |
암 특이적 신호전달체계 JAK/STAT signaling을 억제하는 기전특이적 표적치료제 (mechanism-specific targeted biotherapeutic agent) 임. |
|
|
CP-BMP2 |
골절(fracture) 및 골다공증(osteoporosis) 등의 골 질환 |
외과적 수술과 전달체 (carrier)가 동반해야 하는 기존 BMP2를 세포 조직투과성 주사제로 개발하여, 적용방법과 골 재생 및 골 관련 치료 효능을 개선시킨 바이오베터 (bio-better) 임. |
|
|
CP-△SOCS3 |
고도비만 및 2형 당뇨병 (Obesity & Type II Diabetes Mellitus) |
고도비만 환자들의 렙틴 저항성 (leptin-resistance)을 극복한 식욕억제 기전의 비만 치료제이며, 인슐린 저항성 (insulin-resistance)을 갖는 2형 당뇨병에도 효능이 있음. |
|
| iCP-NI | 감염성 급성간염 패혈증 (Sepsis Due to Infectious Acute Hepatitis) |
과도한 급성 염증 상황에서 발생하는 ‘사이토카인’ 폭풍으로 인한 패혈증의 활성을 억제하는 기전 특이적 항염증 치료 효능 | |
|
연구용 시약 |
iCP-Cre |
유전체 조절효소 (DNA Recombinase) |
개체 전체 (whole-body recombination) 및 특정 장기특이적 (organ-specific recombination) 형질전환 동물모델 제작을 동물 개체 간 교배가 아닌 간단하고 단기간 투여만으로도 가능하게 개발된 조직투과성 유전체 조절효소 (cell-/tissue-permeable genome engineering enzyme) 임. |
|
iCP-RFs 6종 (NANOG, CMYC, LIN28, SOX2, OCT4 & KLF4 ) |
역분화 유도인자 (Reprogramming Factors: RFs) |
유도만능줄기세포 (induced-pluripotent stem cell: iPSC)를 유도하는데 있어서, 역분화 유도인자 (RFs)의 세포 내 발현 시 안전성 (safety) 문제를 해결하여 임상적용 (clinical application)이 가능한 iPSC를 제조할 수 있게 하는 세포투과성 역분화 유도인자군 임. |
|
|
CP-Cas9 |
유전체 조절효소 (DNA Nuclease) |
CRISPR/Cas9 시스템의 단점인 세포의 물리적 자극 (physical stress) 없이 유전자 교정 (gene editing)을 가능케 하는 세포투과성 유전체 조절효소 (genome engineering enzyme) 임. |
(1) 주력제품 1 : iCP-Parkin (Improved Cell-Permeable Parkin)
(퇴행성뇌질환 파킨슨병 치료제)
가) 제품의 주요 사용범위
1) 주요 사용범위/적용증
iCP-Parkin은 약리물질 생체 내 전송기술 (TSDT)을 적용한 세포/조직투과성 aMTD-융합 Parkin 재조합단백질로, 운동성을 조절하는 뇌의 흑질 부위 도파민성 신경세포가 퇴행적으로 소실되어 유발되는 운동성 장애를 동반한 퇴행성뇌질환인 파킨슨병 치료를 위한 바이오의약품 후보물질 입니다.
2) 적용증: 파킨슨병
파킨슨병은 다양한 요인에 의해 α-Synuclein 이라는 독소물질이 분비되고 이것이 도파민성 신경세포를 소실시키면서 발생되는 퇴행성 뇌질환 입니다. α-Synuclein은 체내의 파킨 (Parkin) 단백질이 제거할 수 있는데 이 Parkin 단백질의 부족으로 α-Synuclein이 과발현 되면서 병을 유발합니다. 당사의 후보물질인 iCP-Parkin은 이러한 Parkin 단백질을 세포투과성으로 제작하여 세포 내부에서 작용할 수 있게 한 물질로서 파킨승병의 원인물질인 α-Synuclein을 제거하는 작용기전을 가지고 있습니다.
나) 파킨슨병 치료제 시장 및 현황
1) 글로벌 주요 8개국 파킨슨병 유병환자는 2019년 1,000만명이었으며, 10년 간 2.9%의 성장률로 증가하여 2030년 까지 1,290만명으로 증가할 것으로 전망하고 있습니다. 또한, 파킨슨병 치료제 시장 규모는 2018년 45억 달러에서 연평균 8.1%로 성장하여 2026년 84억 달러 규모에 이를 것으로 전망하고 있습니다 (Parkinson's Foundation, 2020 / Fortune Business Insights, 2019).
2) 전통적인 파킨슨병 치료법은 상실된 도파민을 보충하는 것으로, 혈뇌장벽 (blood-brain barrier: BBB)을 통과할 수 있는 도파민의 전구물질인 L-dopa를 투여하면 뇌의 신경세포가 이를 도파민으로 전환시켜 상실된 운동기능을 회복하게 만듭니다. 그러나, L-dopa는 증세를 완화시키기는 하지만, 병의 근본원인을 치료하지 못하기 때문에 파킨슨병 진행을 늦추지는 못하고 시간이 지남에 따라 병이 악화되며 다양한 부작용이 나타납니다.
다) 기존 치료제의 한계점
1) 기존 파킨슨병 치료는 근본적인 병증개선은 불가능하고 오히려 심각한 부작용을 야기한다는 점에서 환자의 안전성 및 약효를 만족시키지 못하고 있습니다. 이러한 시장 요구에 따라 파킨슨병의 진행을 근원적으로 억제할 수 있는 질병조절치료제 (disease-modifying therapy) 개발이 더욱 중요한 추세입니다.
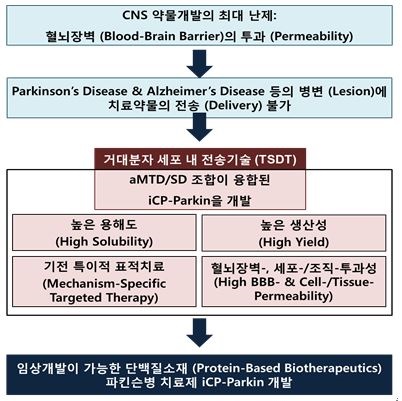
2) 파킨슨병에 대한 치료방식에 있어서 가장 중요하면서 어려운 점은 약물이 혈뇌장벽 (BBB)을 통과해야 한다는 것이며, 당사의 플랫폼 기술인 「약리물질 생체 내 전송기술 TSDT」는 혈뇌장벽 투과능을 가지고 있기 때문에 뇌질환 관련 바이오 신약 연구개발에 매우 적합한 기술입니다.
 |
|
파킨슨병 치료제 개발과정 |
라) 당사 제품의 특징
1) 파킨슨병 치료제 특징
- Parkin 단백질은 파킨슨병의 가장 근본적인 병인인 α-Synuclein 제거와 산화스트레스에 의해 손상된 미토콘드리아 제거를 유도할 수 있는 단백질입니다.
- 당사는 파킨슨병에서 치료효능을 가지는 Parkin 단백질에 「약리물질 생체 내 전송기술 TSDT」을 접목하여 혈뇌장벽 (BBB)을 투과할 수 있는 세포/조직 투과성 aMTD-융합 Parkin 재조합단백질인 improved cell-permeable Parkin (iCP-Parkin)을 개발하였습니다.
- iCP-Parkin은 뇌의 도파민성 신경세포 내로 Parkin 단백질을 보충 (replacement) 하여 손상된 미토콘드리아 자가포식 (mitophagy system)을 활성화시켜 도파민성 신경세포의 감소를 막고 응집된 (aggregated) α-Synuclein 단백질을 감소시킴으로써 도파민 신경세포의 사멸을 억제하고 이를 통해 도파민 생성 능력을 개선할 수 있습니다. 따라서, iCP-Parkin은 PD의 근본적 치료가 가능한 first-in-class 파킨슨병 바이오신약 후보물질로 성공화 가능성이 매우 높습니다.
2) 파킨슨병 치료제 효능
- 당사는 다양한 파킨슨병 동물모델에서 iCP-Parkin 치료효능을 검증하였습니다. 다양한 종류의 파킨슨병 유도물질에 의한 질환동물모델에서 iCP-Parkin은 모두 정상 수준의 운동성 개선 및 신경세포 회복효과를 나타냈습니다.
(2) 주력제품 2 : iCP-SOCS3 (Improved Cell-Permeable SOCS3)
(기전특이적 표적 췌장암 치료제)
가) 제품의 주요 사용범위
1) 주요 사용범위/적용증
iCP-SOCS3는 약리물질 생체 내 전송기술 (TSDT)을 적용한 세포/조직투과성 aMTD-융합 SOCS3 재조합단백질로, 암 발현을 유도하는 JAK/STAT signaling이 비정상적으로 활성화된 암세포에 대한 기전특이적 표적 췌장암 치료제 입니다.
2) 적용증: 췌장암
췌장은 길이 약 15 cm, 무게 70 g 정도로 십이지장에 둘러싸여 있고 비장과 가깝게 인접해 있으며, 각종 소화효소와 호르몬을 분비하여 장내 음식물을 분해하고, 혈당조절을 담당합니다.
3) 췌장에 발생하는 종양은 호르몬을 분비하는 내분비 세포에서 발생하는 종양 (5-10%)과 소화효소 분비와 관련된 외분비 세포에서 기원하는 종양 (90% 이상)으로 구분됩니다. 췌장암의 위험인자로는 흡연, 만성 췌장염, 남성, 고령, 방사선, 화학물질, 만성 당뇨병 등이 있습니다.
4) 췌장암은 세계적으로 발병률 9위의 암이며, 2014년 발생한 전체 암의 3%를 차지하고 있습니다 (American Cancer Society, 2019). 췌장암은 초기 증상이 없기 때문에 조기 발견율이 10% 이하로 매우 낮으며, 진행된 췌장암 환자의 대부분에서 복통과 체중감소, 황달, 체중감소, 소화장애, 당뇨병 등이 나타납니다. 췌장암의 수술적 치료는 전체 환자의 10-20% 정도에서만 가능하며, 병기가 진행될수록 수술이 쉽지 않고 초기 합병증이 30% 발생하는 등의 이유로 발병시 4개월~8개월 밖에 살지 못하는 경우가 대부분으로 최악의 사망률과 5 년 생존률 12% 이하를 보이고 있습니다.
나) 췌장암 치료제 시장 및 현황
1) 췌장암 치료제는 진행성 췌장암이나 수술 후 췌장암의 치료에 주로 이용합니다. 췌장암에서 거의 유일하게 사용되던 대표적인 항암제는 플루러유라실 (5-fluorouracil)로 대부분 소화기암의 일차 항암제로 흔히 사용되었으며, 현재는 젬사이타빈 (gemcitabine)이 췌장암의 가장 기본적인 항암제로 인정받고 있습니다.
2) GBI Research 사의 ‘주요 선진국 췌장암 치료제 시장 전망’보고서에 따르면, 췌장암 치료제 시장은 2021년 29억 달러로 확대 될 전망입니다. 그러나 효과적인 치료제와 조기 진단법의 부재로 인해 사망률이 높은 난치암으로 분류되며, 미충족 의료 수요(unmet medical need)가 큽니다.
다) 기존 치료제의 한계점
1) 대부분의 췌장암 치료제는 세포독성에 의해 암세포뿐 아니라 정상 세포까지 파괴하고 약물 저항성이 나타남으로 인해 결국 항암 효능이 저하됩니다. 또한, 현재의 항 췌장암 제제는 치료제의 개념보다는 증상 완화 (relief) 및 생존 기간 연장 (prolongation)에 초점이 맞추어져 있는 상태이기 때문에, 기존 항암제의 한계를 극복할 수 있는 치료제 개발이 필요합니다.
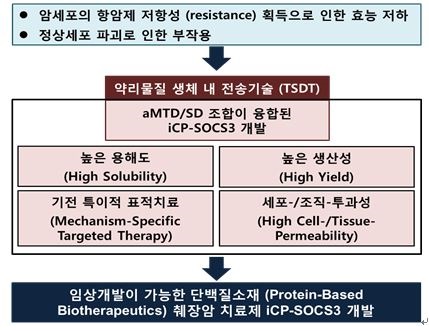
2) 당사는 약리물질 생체 내 전송기술 (TSDT)을 이용하여 단백질과 같은 약리활성물질 (therapeuticmolecule)을 세포 내로 전송할 수 있는 기술을 확보하고 있습니다. 단백질 치료법은 기전특이성이 있고 off-target effect가 낮아 기존 치료제에 비해 부작용이 없거나 적은 새로운 개념의 기전특이적 표적 항암제 (target therapy) 로서 이상적인 항암 치료가 될 수 있습니다.
 |
|
췌장암 치료제 개발과정 |
라) 당사 제품의 특징 _ 췌장암 치료제 특징
1) Suppressor of cytokine signaling 3 (SOCS3)는 췌장암 유발 주요 신호전달체계 JAK/STAT signaling의 억제인자 입니다. 또한, SOCS3는 췌장암 환자에서 불활성화되었으며, 췌장암 세포 성장 및 염증 반응을 통해 췌장암을 촉진합니다.
2) 당사는 췌장암에서 치료효능을 가지는 SOCS3 단백질에 약리물질 생체 내 전송기술 (TSDT)을 접목하여 세포/조직투과성 재조합단백질을 개발하였습니다. iCP-SOCS3는 JAK/STAT signaling을 억제시켜 췌장암 진행을 늦추고, 염증 매개 암 형성 역시 억제합니다. 따라서, 세포 내부에 존재하는 잠재적 항암단백질인 SOCS3를 보충 (replenishing) 함으로써, 새로운 파라다임의 단백질 치료제로서 다양한 암에서 효과적인 항암제 역할을 할 것입니다.
(3) 주력제품(후보물질) 3: CP-BMP2 (Cell-Permeable BMP2)
(골형성 촉진제)
가) 제품의 주요 사용범위
1) 주요 사용범위/적용증
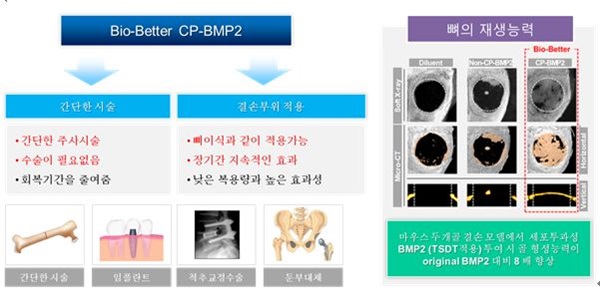
CP-BMP2는 약리물질 생체 내 전송기술 (TSDT)을 적용한 세포/조직투과성 aMTD-융합 BMP2 재조합단백질로, 골 재생 치료를 위한 바이오베터 (bio-better) 의약품 입니다.
 |
|
골형성 촉진제 소개 |
2) 적용증 : 골 질환
골은 형성과 흡수가 반복적으로 일어나는 역동적인 기관이나, 연령이 증가할수록 기능이 저하되고 골절 및 골다공증 같은 골 질환에 의해 integrity가 손상될 수 있습니다. 2013년 골절이 생긴 환자는 15만 4856명임 (건강보험심사 평가원 질병 통계) 으로 2009년 11만 명 대비 5년 만에 약 40% 증가하였습니다.
나) 골 질환 치료제 시장 및 현황
1) 골 질환 치료제제로서 판매되고 있는 bone morphogenic protein 2 (BMP2)는 1988년부터 제작되기 시작된 인간 유래 BMP2를 이용한 인간 BMP2 (recombinant human BMP2: rhBMP2) 재조합 단백질로써, 미국과 유럽 FDA 허가를 받아서 현재 임상에서 골유합을 통한 손상된 뼈나 치조골 복원 등 근골격계 결손부위에 적용하고 있습니다.
2) 골형성단백질 시장은 전 세계 약 1조 5000억 원 규모로 추산되며, 국내 시장은 1000억 원 정도입니다. 또한, 정형외과용 융합바이오소재 (골이식제)는 대부분 BMP류를 포함하는 골재생의 효과를 높인 제품군으로 전 세계 시장은 2015년 50억달러에서 매년 성장률 7.5%에 달할 것으로 예상하고 있습니다.
다) 기존 치료제의 한계점
기존 rhBMP2는 고비용 (high cost) 및 사용 시 낮은 편의성 (low convenience) 때문에 골 형성 촉진제의 개발 및 상용화가 매우 제한적입니다.
라) 당사 제품의 특징
당사는 골 형성능을 가지는 BMP2 단백질에 약리물질 생체 내 전송기술 (TSDT)을 접목하여 운반체 및 이차적 외과 수술 없이 적용가능한 세포/조직투과성 재조합단백질 cell-permeable BMP2 (CP-BMP2)를 개발하였습니다. CP-BMP2는 기존 rhBMP2에 비해 편의성이 획기적으로 개선되었으므로 바이오베터 후보물질로 성공화 가능성이 매우 높습니다.
(4)주력제품(후보물질) 4 : CP-DSOCS3 (Cell-Permeable Truncated SOCS3) (고도비만 치료제)
가) 제품의 주요 사용범위
1) 주요 사용범위/적용증 : 고도비만
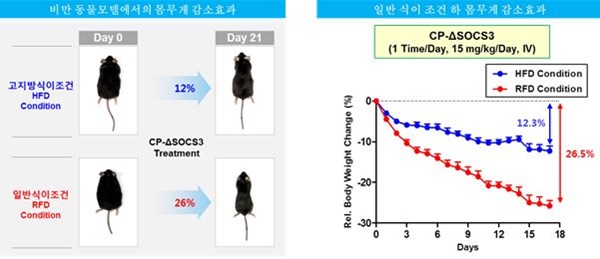
CP-DSOCS3는 「약리물질 생체 내 전송기술 (TSDT)」을 적용한 세포/조직투과성 aMTD-융합 truncated SOCS3 재조합단백질로, 랩틴 저항성 (leptin resistance)으로 촉발된 고도비만치료 [mechanism (leptin-resistance)-specific anti-obesity agent]를 위한 바이오의약품 후보물질 입니다.
 |
|
고도비만 치료제 소개 |
- 식이 유도 비만 쥐 모델에서 일반 식이 조건 하 3 주 간 투여 시 26% 몸무게 감소 효과
- 식이 유도 비만 쥐 모델에서 고지방 식이 조건 하 3 주 간 투여 시 지속적인 고지방 섭취에도 불구하고 12%의 몸무게 감소 효과
- 지방간 감소 (90%), 혈 중 콜레스테롤 감소 (31%) 및 혈당감소 (23%) 효과
나) 고도비만 치료제 시장 및 현황
비만치료약물은 크게 식욕억제제와 지방흡수억제제 두 가지로 나뉘는데, 현재 비만치료제 시장에서는 식욕억제제가 지방흡수 억제제보다 월등히 우세합니다. 전 세계 비만 치료제시장 규모가 2017년 1,760억 달러였으며, 2022년에는 2,455억 달러로 성장할 것이라는 분석이 나오고 있습니다 (MarketsandMarkets, 2017).
다) 기존 치료제의 한계점
|
최근까지 허가 받거나 개발 중인 비만 치료제들은 대부분이 중추신경계에 작용하여 식욕을 억제시키는 화학 조성물 (small molecule)이며, 이들은 경구 투여의 이점이 있음에도 1) 미미한 체중 감소효과 (2.0~8.9 Kg의 감량/년) 및 2) 요요현상, 그리고 3) 비생체물질로 인한 안전성에 대한 우려, 4) 낮은 기전 특이성으로 인한 심각한 부작용 등의 단점이 있습니다. 이로 인하여 극히 일부분의 비만 환자들만이 단기간만 사용하여 시장이 확대 되지 못하고 있습니다 그러나 최근에 비만에 관한 비약적인 연구 및 아래와 같은 새로운 패러다임의 변화로 인하여 다양한 종류의 새로운 비만치료 약물들이 개발되고 있으나 초고도비만 환자에게는 기존 치료제의 낮은 효능과 높은 부작용으로 여전히 혁신적인 치료제가 필요한 실정입니다. 최근 비만 치료제 개발의 패러다임은 식욕 억제뿐 아니라, 지방 세포의 에너지 소모 증가를 유도하는 방향으로 확장되고 있습니다. 또한, 기존 단백질 제제 기반 바이오 신약은 환자 친화적 투여법 개발에 실패하였습니다. 재조합 펩타이드나 단백질 제재 기반의 바이오 신약은 현재 주사 투여를 하고 있으며, 환자들이 선호하는 경구 투여가 가능한 단백질 의약품은 개발 단계에서 대부분 실패하였습니다. 위와 장 등의 소화기를 통과하면서 pH, 효소의 분해 등의 생체 내 요소로 단백질이 분해되기 때문입니다. 이런 이유로 단백질 제재의 비만 치료 신약 개발은 미비하였습니다. |
|
- 심혈관계 및 정서적 불안을 비롯한 부작용이 전혀 없는 안전성 (safety)이 확보된 새로운 기전 특이적 비만 치료제 개발 필요 - 장기 투여가 가능한 치료제 개발 필요 - 식욕 억제뿐만 아니라, 에너지 대사를 증가시켜 고효능의 비만 치료제 개발 필요. - 환자 친화적 투여 경로가 가능한 바이오 비만 치료제 신약 개발 필요 |
라) 당사 제품의 특징
당사는 고도비만에서 leptin resistance를 극복할 수 있는 truncated SOCS3 (ΔSOCS3) 단백질에 「약리물질 생체 내 전송기술 (TSDT)」을 접목하여 혈뇌장벽을 투과할 수 있는 세포/조직투과성 재조합단백질을 개발하였습니다. CP-ΔSOCS3는 뇌의 시상하부 내 신경세포에서 leptin receptor 와 결합하고, 이를 통해 세포 내 leptin receptor와 SOCS3 와의 결합을 억제시켜 leptin resistance를 극복할 수 있는 고도비만치료제 입니다.
(5) 주력제품 5 : iCP-NI (Improved Cell-Permeable Neuclear Import Inhibitor)
가) 제품의 주요 사용범위
iCP-NI는 과도한 급성 염증 상황에서 발생하는 ‘사이토카인’ 폭풍으로 인한 패혈증에 대한 기전 특이적 항염증 치료 후보 물질입니다.
나) 치료제 시장 및 현황
미국의 경우 매년 700,000 명 이상의 패혈증 환자가 발생하고 그 중 225,000 명 정도가 사망하며 13번째 사망원인이고, 중환자실에서 치료중인 환자의 가장 흔한 사망원인임. 시판중인 유일한 치료제인 Xigris가 유효성이 없어 시장에서 철회 되었음.
현재 패혈증 치료제가 없어 항생제 등 대증요법에 따라 치료되고 있음.
2020년 지 매년 1.5-2.0%의 패혈증 환자가 증가할 것으로 예측
다) 기존 치료제의 한계점
기존 치료제 없음
라) 당사 제품의 특징
펩타이드 의약품으로써, NF-κB, AP-1, NFAT, STAT1과 같은 stress related transcription factor (SRTF)의 활성을 억제하는 기전 특이적 항염증 치료 후보 물질임.
(6) 주력제품 5 : 연구용 시약
가) 유전체 조절효소: iCP-Cre (Improved Cell-Permeable Cre)
(형질전환 동물모델 제작용 세포/조직투과성 유전체 조절효소)
1) 주요 사용범위 : iCP-Cre는 간단한 주사만으로 형질전환 마우스모델(genetically engeneered mouse model: GEM) 제작이 가능한 세포/조직투과성 유전체 조절효소 (genome engineering enzymes: GEEs) 입니다. 기존 시스템의 한계를 극복하여 더 정밀하고 정교하게 의생명과학 연구를 할 수 있는 시스템이 「세포/조직투과성 Cre (iCP-Cre)」 입니다. iCP-Cre는 aMTD와 SD를 융합한 차세대 유전체 조절효소로서 기존의 GEEs를 이용한 방법에 비해 높은 효율뿐만 아니라, 시간과 비용 또한 절감할수 있는 연구용 시약 (research reagent) 입니다.
2) 적용 분야 : (1) 유전체 조절기술 (genome engineering technology)은 인위적인 유전체 조절효소를 이용하여 유기체 (organism) 내에 존재하지 않는 새로운 특성을 추가하기 위한 새로운 DNA를 삽입 (insertion) 하거나, 대체 (replacement) 하거나, 기존의 알려진 특성을 제거 (deletion) 하기 위해 유기체 내의 염색체 (chromatin)을 engineering/editing 해주는 기술입니다
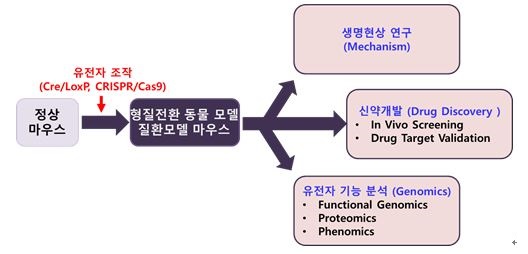
신약 개발에 있어 유전체 조절 기술을 이용한 형질전환 마우스모델은 질병의 다양한 원인과 발병과정 및 진단에 대한 연구용 재료를 제공해주고, 질환모델 동물의 연구를 통해 질병에 관련된 유전자들을 알아내고, 개발된 신약후보물질의 실제 효능 및 독성 검사를 통해 실용화 가능성의 여부를 판단하는 기초 자료를 얻을 수 있기 때문에 신약 개발에 필수적으로 필요합니다
[ 질환모델 동물의 활용 가능 분야 (Applications of GEM) ]
 |
|
질환기술의 활용가능 분야 |
나) 세포분화조절 유도인자군: iCP-RFs _iCP-OCT4, iCP-SOX2, iCP-KLF4, iCP-CMYC, iCP-NANOG, iCP-LIN28 (Improved Cell-Permeable Reprogramming Factors) (유도만능줄기세포 제작용 세포투과성 역분화 유도인자 6종)
1) 주요 사용범위 : iCP-RFs는 virus를 이용하지 않고도 안전하고 높은 효율로 역분화 유도만능 줄기세포 (induced pluripotent stem cells: iPSCs) 제작이 가능한 세포/조직투과성 6종 역분화 유도 인자 (iCP-OCT4, iCP-SOX2, iCP-KLF4, iCP-CMYC, iCP-NANOG, iCP-LIN28) 입니다.
2) 적용 분야 : Virus를 사용하지 않아 돌연변이 문제도 없어 향후 임상적용에도 가능한 iPSC를 개발할 수 있습니다
다) 유전체 조절효소: CP-Cas9 (Cell-Permeable Cas9)
(유전자 교정용 세포/조직투과성 유전체 효소)
1) 주요 사용범위 : CP-Cas9는 기존의 clustered regularly interspaced short palindromic repeats/Cas9 (CRISPR/Cas9) 시스템의 단점인 세포에 대한 물리적 자극 없이 유전자 교정 (gene editing)이 가능한 세포/조직투과성 유전체 교정시약 입니다.
2) 적용 분야 : CRISPR/Cas9은 특정 염기서열을 인식하여 DNA를 자르고 교정하는 기술을 말합니다. 이는, 다양한 연구 및 산업적 활용이 가능하여 농작물이나 가축의 개량 모델을 제작이나 난치성 질환의 근본적 치료방법을 제시 할 수 있습니다.
(나) 공시대상 사업부문의 구분
당사는 한국표준산업분류의 소분류에 따른 의학 및 약학 연구개발업을 영위하고 있으며 주요 제품 및 상품은 "약리물질 생체 내 전송기술 (Therapeuticmolecule Systemic Delivery Technology: TSDT)"플랫폼을 기술 기반우로 하여 신약을 개발하는 단일 사업부문을 영위하고 있습니다
(2) 시장점유율
당사는 현재 "약리물질 생체 내 전송기술 (Therapeuticmolecule Systemic Delivery Technology: TSDT)" 플랫폼 기술 기반 신약 개발중인 회사이므로 제품이나 상품의 판매에 의한 매출은 존재하지 아니하여, 시장점유율에 대한 정보가 존재하지 아니합니다.
(3) 시장의 특성
'가. 업계의 현황' 내용을 참조하시기 바랍니다.
(4) 신규사업 등의 내용 및 전망
해당사항이 없습니다.
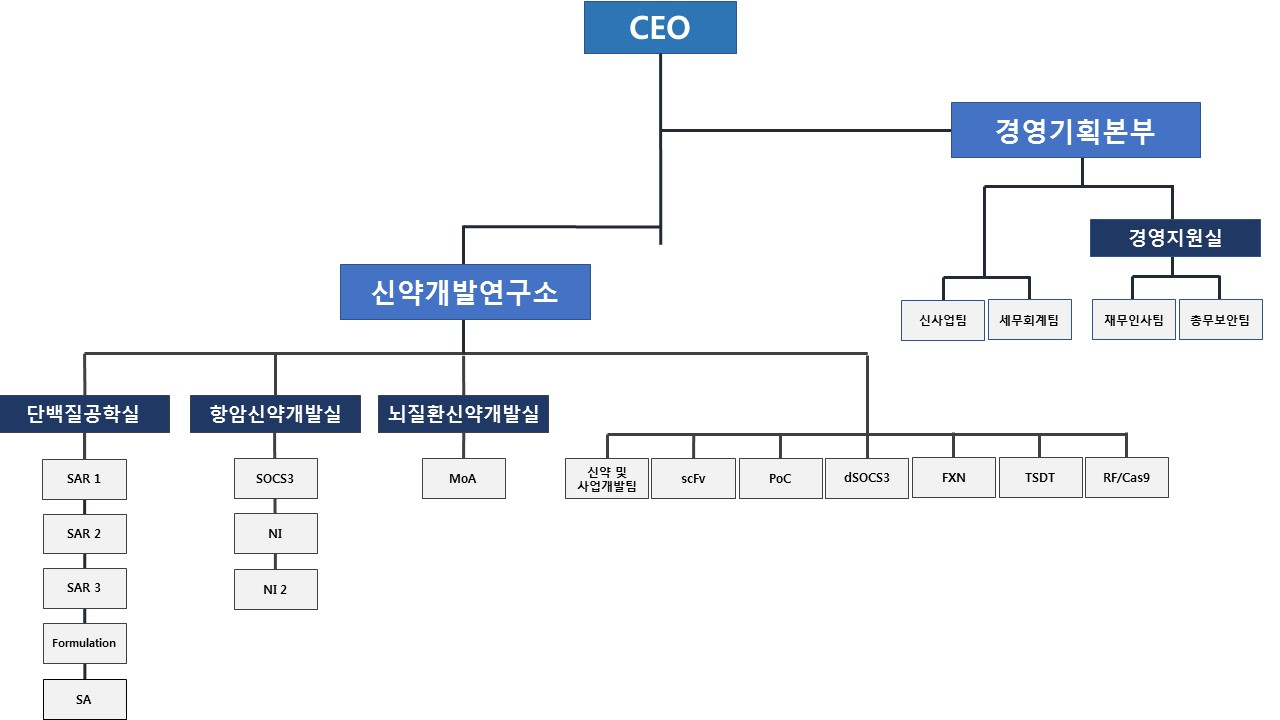
(5) 조직도
 |
|
셀리버리 조직도 |
2. 주주총회 목적사항별 기재사항
□ 재무제표의 승인
가. 해당 사업연도의 영업상황의 개요
나. 해당 사업연도의 대차대조표(재무상태표)ㆍ손익계산서(포괄손익계산서)ㆍ자본변동표ㆍ현금흐름표ㆍ이익잉여금처분계산서(안) 또는 결손금처리계산서(안)ㆍ
- 재무상태표
| 재 무 상 태 표 | |
| 제 6(당) 기 2019년 12월 31일 현재 | |
| 제 5(전) 기 2018년 12월 31일 현재 | |
| 주식회사 셀리버리 | (단위 : 원) |
| 과 목 | 제 6(당) 기말 | 제 5(전) 기말 | ||
|---|---|---|---|---|
| 자 산 | ||||
| I. 유동자산 | 28,364,364,708 | 37,640,702,445 | ||
| 현금및현금성자산(주5,30,32) | 1,245,118,189 | 983,026,732 | ||
| 공정가치측정금융자산(주5,31,32) | 505,470,000 | 13,080,211,920 | ||
| 상각후원가측정금융자산(주5,31,32) | 25,632,109,003 | 22,766,240,238 | ||
| 매출채권(주6,31,32) | 157,468,900 | 539,000,000 | ||
| 단기수취채권(주6,31,32,34) | 662,789,995 | 100,937,680 | ||
| 기타유동자산(주11) | 53,057,701 | 91,545,422 | ||
| 당기법인세자산(주28) | 108,350,920 | 21,087,740 | ||
| 재고자산(주7) | - | 58,652,713 | ||
| Ⅱ. 비유동자산 | 2,493,942,496 | 2,354,603,830 | ||
| 유형자산(주8,12) | 1,421,603,492 | 1,436,402,307 | ||
| 무형자산(주9) | 291,548,845 | 35,939,805 | ||
| 사용권자산(주10) | 165,823,195 | - | ||
| 장기수취채권(주6,31,32) | 1,300,000 | 276,761,203 | ||
| 기타비유동자산(주11) | 613,666,964 | 605,500,515 | ||
| 자 산 총 계 | 30,858,307,204 | 39,995,306,275 | ||
| 부 채 | ||||
| Ⅰ. 유동부채 | 2,083,740,139 | 3,392,679,111 | ||
| 기타채무(주13,26,31,32) | 889,434,003 | 583,943,614 | ||
| 유동성파생금융부채(주15,31,32) | - | 297,696,180 | ||
| 유동성리스부채(주14,31) | 167,363,455 | - | ||
| 기타유동부채(주16,23) | 1,026,942,681 | 2,511,039,317 | ||
| Ⅱ. 비유동부채 | 1,491,144,501 | 776,824,378 | ||
| 기타채무(주13,26,31,32) | 95,833,300 | 25,000,000 | ||
| 확정급여부채(주26) | 1,395,311,201 | 751,824,378 | ||
| 부 채 총 계 | 3,574,884,640 | 4,169,503,489 | ||
| 자 본 | ||||
| Ⅰ. 자본금(주1,18) | 3,910,053,500 | 3,806,303,500 | ||
| Ⅱ. 자본잉여금(주18) | 90,218,760,330 | 80,982,775,900 | ||
| Ⅲ. 기타자본구성요소(주19,22) | 3,417,066,578 | 1,390,404,351 | ||
| Ⅳ. 결손금(주20) | (70,262,457,844) | (50,353,680,965) | ||
| 자 본 총 계 | 27,283,422,564 | 35,825,802,786 | ||
| 부 채 및 자 본 총 계 | 30,858,307,204 | 39,995,306,275 | ||
- 포괄손익계산서
| 포 괄 손 익 계 산 서 | |
| 제 6(당) 기 2019년 1월 1일부터 2019년 12월 31일까지 | |
| 제 5(전) 기 2018년 1월 1일부터 2018년 12월 31일까지 | |
| 주식회사 셀리버리 | (단위 : 원) |
| 과 목 | 제 6(당) 기 | 제 5(전) 기 | ||
|---|---|---|---|---|
| Ⅰ. 매출액(주17,23) | 2,073,694,786 | 4,512,315,508 | ||
| Ⅱ. 매출원가(주22,24,25) | 3,975,896,396 | 2,995,790,107 | ||
| Ⅲ. 매출총이익(손실) | (1,902,201,610) | 1,516,525,401 | ||
| Ⅳ. 판매비와관리비(주22,24,25,34) | 12,682,197,738 | 5,619,023,285 | ||
| Ⅴ. 영업이익(손실) | (14,584,399,348) | (4,102,497,884) | ||
| Ⅵ. 영업외손익(주27) | (4,992,578,211) | (2,548,900,826) | ||
| 기타수익 | 1,414,369 | 3,509,283 | ||
| 기타비용 | (13,268,442) | (507,800) | ||
| 금융수익 | 767,688,666 | 4,678,837,730 | ||
| 금융비용 | (5,748,412,804) | (7,230,740,039) | ||
| Ⅶ. 법인세비용차감전순손실 | (19,576,977,559) | (6,651,398,710) | ||
| Ⅷ. 법인세비용(주28) | 72,995,850 | 46,974,527 | ||
| IX. 당기순이익 | (19,649,973,409) | (6,698,373,237) | ||
| X. 기타포괄손익 | (258,803,470) | (166,546,048) | ||
| - 후속적으로 당기손익으로 재분류되지 않는 항목 | ||||
| 확정급여제도의 재측정요소 | (258,803,470) | (166,546,048) | ||
| XI. 총포괄손익 | (19,908,776,879) | (6,864,919,285) | ||
| XII. 주당손익(주21) | ||||
| 기본주당손실 및 희석주당손실 | (2,529) | (1,300) | ||
- 자본변동표
| 자 본 변 동 표 | |
| 제 6(당) 기 2019년 1월 1일부터 2019년 12월 31일까지 | |
| 제 5(전) 기 2018년 1월 1일부터 2018년 12월 31일까지 | |
| 주식회사 셀리버리 | (단위 : 원) |
| 과 목 | 자본금 | 자본잉여금 | 기타자본구성요소 | 결손금 | 총 계 |
|---|---|---|---|---|---|
| 2018.01.01 (전기초) | 1,849,367,000 | 12,766,234,000 | 437,954,596 | (43,488,761,680) | (28,435,206,084) |
| 당기순손실 | - | - | - | (6,698,373,237) | (6,698,373,237) |
| 전환상환우선주 보통주 전환 | 1,369,836,500 | 41,210,588,100 | - | - | 42,580,424,600 |
| 유상증자 | 587,100,000 | 27,005,953,800 | - | - | 27,593,053,800 |
| 주식기준보상 | - | - | 952,449,755 | - | 952,449,755 |
| 확정급여제도의 재측정요소 | - | - | - | (166,546,048) | (166,546,048) |
| 2018.12.31(전기말) | 3,806,303,500 | 80,982,775,900 | 1,390,404,351 | (50,353,680,965) | 35,825,802,786 |
| 2019.01.01 (당기초) | 3,806,303,500 | 80,982,775,900 | 1,390,404,351 | (50,353,680,965) | 35,825,802,786 |
| 당기순손실 | - | - | - | (19,649,973,409) | (19,649,973,409) |
| 신주인수권 행사 | 57,000,000 | 8,778,139,080 | - | - | 8,835,139,080 |
| 주식매입선택권 행사 | 46,750,000 | 457,845,350 | (37,259,750) | - | 467,335,600 |
| 주식기준보상 | - | - | 2,063,921,977 | - | 2,063,921,977 |
| 확정급여제도의 재측정요소 | - | - | - | (258,803,470) | (258,803,470) |
| 2019.12.31 (당기말) | 3,910,053,500 | 90,218,760,330 | 3,417,066,578 | (70,262,457,844) | 27,283,422,564 |
- 현금흐름표
| 현 금 흐 름 표 |
|
| 제 6(당) 기 2019년 1월 1일부터 2019년 12월 31일까지 | |
| 제 5(전) 기 2018년 1월 1일부터 2018년 12월 31일까지 | |
| 주식회사 셀리버리 | (단위 : 원) |
| 과 목 | 제 6(당) 기 | 제 5(전) 기 | ||
|---|---|---|---|---|
| Ⅰ. 영업활동으로 인한 현금흐름 | (11,580,583,460) | (2,639,290,169) | ||
| 1. 영업활동에서 창출된 현금(주29) | (12,079,865,949) | (2,767,152,792) | ||
| (1) 당기순손실 | (19,649,973,409) | (6,698,373,237) | ||
| (2) 조정 | 8,564,537,228 | 4,295,635,445 | ||
| (3) 영업활동으로 인한 자산부채의 변동 | (994,429,768) | (364,415,000) | ||
| 2. 이자의 수취 | 586,545,669 | 141,696,663 | ||
| 3. 이자의 지급 | - | - | ||
| 4. 법인세의 환급(납부) | (87,263,180) | (13,834,040) | ||
| Ⅱ. 투자활동으로 인한 현금흐름 | 8,866,795,956 | (33,937,761,242) | ||
| 1. 투자활동으로 인한 현금유입액 | 35,824,056,602 | 6,059,992,000 | ||
| 단기금융상품의 감소 | - | 6,049,992,000 | ||
| 당기손익-공정가치 측정 금융자산 처분 | 22,766,240,238 | |||
| 상각후원가 측정 금융자산 처분 | 13,029,000,000 | |||
| 유형자산의 처분 | 13,636,364 | 10,000,000 | ||
| 기타보증금의 감소 | 15,180,000 | - | ||
| 2. 투자활동으로 인한 현금유출액 | (26,957,260,646) | (39,997,753,242) | ||
| 단기금융상품의 증가 | - | 39,272,043,990 | ||
| 당기손익-공정가치 측정 금융자산 취득 | 500,000,000 | - | ||
| 상각후원가 측정 금융자산 취득 | 25,632,109,003 | - | ||
| 유형자산의 취득 | 629,661,643 | 664,726,852 | ||
| 무형자산의 취득 | 95,190,000 | 10,581,000 | ||
| 기타보증금의 증가 | 300,000 | 50,401,400 | ||
| 임차보증금의 증가 | 100,000,000 | - | ||
| Ⅲ. 재무활동으로 인한 현금흐름 | 2,975,878,960 | 34,089,666,710 | ||
| 1. 재무활동으로 인한 현금유입액 | 3,317,500,000 | 35,851,612,910 | ||
| 전환상환우선주 발행 | - | 6,496,612,910 | ||
| 신주인수권 행사 | 2,850,000,000 | - | ||
| 주식매입선택권 행사 | 467,500,000 | - | ||
| 유상증자 | - | 29,355,000,000 | ||
| 2. 재무활동으로 인한 현금유출액 | (341,621,040) | (1,761,946,200) | ||
| 주식발행비용 등 | 438,000 | 1,761,946,200 | ||
| 리스부채의 상환 |
341,183,040 | - | ||
| Ⅳ. 외화표시 현금및현금성자산의 환율변동효과 | 1 | 44 | ||
| Ⅴ. 현금의 증가(감소) (Ⅰ+Ⅱ+Ⅲ+Ⅳ) | 262,091,456 | (2,487,384,657) | ||
| Ⅵ. 기초의 현금 | 983,026,732 | 3,470,411,389 | ||
| Ⅶ. 기말의 현금 | 1,245,118,189 | 983,026,732 | ||
- 결손금처리계산서(안)
| 결 손 금 처 리 계 산 서 | |
| 제 6(당) 기 2019년 1월 1일부터 2019년 12월 31일까지 | |
| 제 5(전) 기 2018년 1월 1일부터 2018년 12월 31일까지 | |
| 주식회사 셀리버리 | (단위 : 천원) |
| 과 목 | 제 6(당) 기 (처리예정일: 2020년 3월 30일) |
제 5(전) 기 | ||
|---|---|---|---|---|
|
Ⅰ. 미처리결손금 |
(70,262,458) | (50,353,681) | ||
|
1. 전기이월미처리결손금 |
(50,353,681) |
(43,058,510) |
||
|
2. 기업회계기준서 제1115호 조정 |
- |
|
(430,252) |
|
|
3. 당기순손실 |
(19,649,973) |
|
(6,698,373) | |
|
4. 확정급여제도의 재측정요소 |
(258,803) |
|
(166,546) | |
|
Ⅱ. 결손금처리액 |
- |
|
- |
|
|
Ⅲ. 차기이월미처리결손금 |
(70,262,458) |
|
(50,353,681) | |
- 최근 2사업연도의 배당에 관한 사항
당사는 최근 2사업연도에 배당이 없습니다.
□ 이사의 선임
가. 후보자의 성명ㆍ생년월일ㆍ추천인ㆍ최대주주와의 관계ㆍ사외이사후보자 여부
| 후보자성명 | 생년월일 | 사외이사 후보자여부 |
최대주주와의 관계 | 추천인 |
|---|---|---|---|---|
| 조대웅 | 1968년 02월 25일 | 사내이사 | 최대주주 본인 | 이사회 |
| 기정욱 | 1970년 04월 22일 | 사내이사 | 특수관계인 | 이사회 |
| 최영실 | 1982년 02월 15일 | 사내이사 | 관계없음 | 이사회 |
| 김형준 | 1960년 09월 30일 | 사외이사 | 관계없음 | 이사회 |
| 총 ( 4 ) 명 | ||||
나. 후보자의 주된직업ㆍ세부경력ㆍ해당법인과의 최근3년간 거래내역
| 후보자성명 | 주된직업 | 세부경력 | 해당법인과의 최근3년간 거래내역 |
|
|---|---|---|---|---|
| 기간 | 내용 | |||
| 조대웅 | (주) 셀리버리 대표이사 | 2014.~현재 | (주) 셀리버리 대표이사 | 2019년 04월 01일자로 당사는 화물용 차량 (FORD TRUCK)을 미국 현지에서구입하여 한국으로 운송하여 현재 사용중입니다. 본 차량에 대해 미국 현지 구입 상 편의를 위해 2019년 4월 1일 미국 영주권을 보유한 대표이사 (최대주주)의 명의로 USD74,000에 매입하고 다음날인 4월 2일 이사회결이를 거쳐 대표이사(최대주주)로 부터 회사가 동일 가격인 USD74,000에 취득하였습니다. |
| 기정욱 | (주) 셀리버리 부사장 | 2017~현재 | (주) 셀리버리 부사장 | 해당사항없음 |
| 최영실 | (주) 셀리버리 연구소장 | 2014~현재 | (주) 셀리버리 연구소장 | 해당사항없음 |
| 김형준 | 전남대학교 의과대학 교수 | 1994~현재 | 전남대학교 의과대학 교수 | 해당사항없음 |
다. 후보자의 체납사실 여부ㆍ부실기업 경영진 여부ㆍ법령상 결격 사유 유무
| 후보자성명 | 체납사실 여부 | 부실기업 경영진 여부 | 법령상 결격 사유 유무 |
|---|---|---|---|
| 조대웅 | 부 | 부 | 무 |
| 기정욱 | 부 | 부 | 무 |
| 최영실 | 부 | 부 | 무 |
| 김형준 | 부 | 부 | 무 |
라. 후보자의 직무수행계획(사외이사 선임의 경우에 한함)
|
1) 전문성
|
마. 후보자에 대한 이사회의 추천 사유
| - 조대웅: 후보자는 (주)셀리버리의 창업자이며 대표이사로 재직 중입니다. 당사의 핵심기술인 『약리물질 생체 내 전송기술 TSDT』의 기술개발자로서 1997년 이후 현재까지 약리물질 생체 내 전송기술을 개발, 진보시켜 왔으며, 1~2세대를 거쳐 융합 재조합단백질의 생산성 (manufacturing yield), 수용성 (recombinant protein solubility) 그리고 안정성 (structural stability) 측면에서 산업화가 가능한 3세대 약리물질 생체 내 전송기술을 완성시킨 동 분야 최고 전문가이고 Impact factor가 35 이상인 저널에 3편, Cancer Research 등 관련분야 전문학술지 (impact factor 10~5)에 8편을 발표한 연구자입니다. 또한 20여년간 학계 (Ph.D. 학위 및 박사후 연구원 경력 9년 및 교수경력 4년 등 13년), 산업계 경력이 있는 핵심 경영자이자 과학자입니다. - 기정욱: 후보자는 (주)셀리버리의 부사장 (경영기획본부장)으로 재직 중입니다. 한국장기신용은행, 현대증권 기업금융부, 현대그룹 전략기획본부를 거친 재무, 전략 전문가로서 당사의 경영기획본부에서 사업개발 및 경영지원업무를 본부장으로서 총괄하고있습니다. - 최영실: 후보자는 (주)셀리버리의 창업멤버이며 연구소장으로 재직 중에 있습니다. 이화여대 세포항상성연구센터 박사 후 연구원으로 재직한 세포생물학 전문가이며 설립 초기부터 조대웅대표이사를 보좌하며 회사의 기술발전에 이바지한 바 있습니다. - 김형준: 후보자는 현재 국립대학교 의대 정교수로 재직중이며 부설병원장으로 재직한 바 있습니다. 특히 혈관종양 분야의 전문가로서 한국조혈모세포은행협회의 이사직을 맡고 있습니다. 그간 쌓아올린 대내외적인 경험과 지식, 산업에 대한 이해를 바탕으로 이사회에 참여함으로써 주주권익을 보호하고 회사의 지속성장과 발전에 기여할 것입니다. |
확인서
 |
|
확인서 - 조대웅 |
 |
|
확인서 - 기정욱 |
 |
|
확인서 - 최영실 |
 |
|
확인서_김형준 |
※ 기타 참고사항
해당사항이 없습니다.
□ 주식매수선택권의 부여
가. 주식매수선택권을 부여하여야 할 필요성의 요지
회사의 경영, 기술혁신 및 사업개발 등에 기여하거나 기여할 수 있는 주요 임직원 등에 대한 동기부여를 통하여 높은 경영성과를 유도하고 이를 통해 회사의 실질적인 가치를 향상시키기 위함.
나. 주식매수선택권을 부여받을 자의 성명
| 성명 | 직위 | 직책 | 교부할 주식 | |
|---|---|---|---|---|
| 주식의종류 | 주식수 | |||
| 황윤서 | 직원 | 과장 | 보통주 | 2,000 |
| 박신영 | 직원 | 과장 | 보통주 | 4,000 |
| 길건희 | 직원 | 과장 | 보통주 | 4,000 |
| 권이슬 | 직원 | 과장 | 보통주 | 2,000 |
| 민성윤 | 직원 | 대리 | 보통주 | 4,000 |
| 김동옥 | 직원 | 과장 | 보통주 | 2,000 |
| 정민용 | 직원 | 차장 | 보통주 | 8,000 |
| 이광환 | 직원 | 과장 | 보통주 | 3,500 |
| 박재형 | 직원 | 차장 | 보통주 | 4,000 |
| 정은나 | 직원 | 부장 | 보통주 | 4,000 |
| 최유진 | 직원 | 과장 | 보통주 | 4,000 |
| 권선홍 | 임원 | 이사 | 보통주 | 15,000 |
| 이준노 | 직원 | 부장 | 보통주 | 3,000 |
| 최강인 | 직원 | 과장 | 보통주 | 3,000 |
| 김미경 | 직원 | 과장 | 보통주 | 3,000 |
| 김성철 | 직원 | 과장 | 보통주 | 2,000 |
| 김규남 | 직원 | 과장 | 보통주 | 3,000 |
| 이재화 | 직원 | 대리 | 보통주 | 3,000 |
| 조정환 | 직원 | 대리 | 보통주 | 3,000 |
| 김선웅 | 직원 | 과장 | 보통주 | 3,500 |
| 이석원 | 직원 | 대리 | 보통주 | 3,000 |
| 곽정훈 | 직원 | 대리 | 보통주 | 2,000 |
| 국용부 | 직원 | 대리 | 보통주 | 3,500 |
| 최용찬 | 직원 | 대리 | 보통주 | 3,500 |
| 유혜민 | 직원 | 대리 | 보통주 | 2,000 |
| 최정헌 | 직원 | 대리 | 보통주 | 3,000 |
| 박지애 | 직원 | 과장 | 보통주 | 2,000 |
| 이수정 | 직원 | 대리 | 보통주 | 2,000 |
| 전지숙 | 직원 | 대리 | 보통주 | 2,000 |
| 이재호 | 직원 | 과장 | 보통주 | 3,000 |
| 최문영 | 직원 | 대리 | 보통주 | 3,000 |
| 이하린 | 직원 | 주임 | 보통주 | 2,250 |
| 조미진 | 직원 | 대리 | 보통주 | 2,250 |
| 정민기 | 직원 | 차장 | 보통주 | 2,000 |
| 김형준 | 임원 | 사외이사 | 보통주 | 5,000 |
| 총(35)명 | - | - | - | 총(120,500 )주 |
김형준 사외이사 후보자는 2020년 03월 30일 예정인 당사의 정기주주총회에서 선임여부가 결정될 사외이사 후보자로 선임이 확정될 시 주식매수선택권 부여 예정.
다. 주식매수선택권의 부여방법, 그 행사에 따라 교부할 주식의 종류 및 수, 그 행사가격, 행사기간 및 기타 조건의 개요
| 구 분 | 내 용 | 비 고 |
|---|---|---|
| 부여방법 | 보통주 신주발행 교부 | - |
| 교부할 주식의 종류 및 수 | 기명식 보통주 120,500주 | - |
| 행사가격 및 행사기간 | 1. 행사가격 상법 제340조의2제4항의 실질가액을 산정하고, 정기주주총회 의결일 전일을 기산일로 하여 자본시장과금융투자업에관한법률시행령 제176조의7제3항의 규정을 준용하여 평가한 시가 2. 행사기간:2022.3.30~2026.03.29 |
- |
| 기타 조건의 개요 | 기타 세부사항은 주식매수선택권과 관련된 제반 법규, 당사 정관, 계약서 등에 정하는 바에 따름. | - |
라. 최근일 현재 잔여주식매수선택권의 내역 및 최근년도 주식매수선택권의 부여, 행사 및 실효내역의 요약
- 최근일 현재 잔여주식매수선택권의 내역
| 총발행 주식수 |
부여가능 주식의 범위 |
부여가능 주식의 종류 |
부여가능 주식수 |
잔여 주식수 |
|---|---|---|---|---|
| 7,820,107 | 발행주식 총수의 15% | 기명식 보통주 | 1,173,016 | 511,516 |
※상기의 잔여주식수는 부여가능주식수(1,173,016주)에서 공시일 현재 기 부여주식수 (927,500주)를 차감하고 실효주식수 (266,000주)를 더한 수량임.
- 최근 2사업연도와 해당사업연도의 주식매수선택권의 부여, 행사 및 실효내역
| 사업년도 | 부여일 | 부여인원 | 주식의 종류 |
부여 주식수 |
행사 주식수 |
실효 주식수 |
잔여 주식수 |
|---|---|---|---|---|---|---|---|
| 2019년 | 2019.03.22 | 14 | 보통주 | 126,000 | - | 5,000 | 121,000 |
| 2018년 | 2018.03.30 | 32 | 보통주 | 229,500 | - | 27,000 | 202,500 |
| 2017년 | 2017.03.30 | 32 | 보통주 | 308,000 | - | 83,500 | 224,500 |
| 2016년 | 2016.03.31 | 39 | 보통주 | 264,000 | 93,500 | 150,500 | 20,000 |
| 계 | - | 총(117)명 | - | 총(927,500)주 | 총(93,500)주 | 총(266,000)주 | 총(568,000)주 |
※ 기타 참고사항
해당사항이 없습니다.
□ 이사의 보수한도 승인
가. 이사의 수ㆍ보수총액 내지 최고 한도액
(당 기)
| 이사의 수 (사외이사수) | 5(1) |
| 보수총액 또는 최고한도액 | 15억원 |
(전 기)
| 이사의 수 (사외이사수) | 4(1) |
| 실제 지급된 보수총액 | 715,322,296 |
| 최고한도액 | 10억원 |
※ 기타 참고사항
해당사항이 없습니다.
□ 감사의 보수한도 승인
가. 감사의 수ㆍ보수총액 내지 최고 한도액
(당 기)
| 감사의 수 | 1 |
| 보수총액 또는 최고한도액 | 6천만원 |
(전 기)
| 감사의 수 | 1 |
| 실제 지급된 보수총액 | 12,225,800 |
| 최고한도액 | 6천만원 |
※ 기타 참고사항
※ 참고사항
| ◇ 주주총회 집중일 개최 사유 신고 - 주주총회 개최(예정)일 : 2020-03-30 - 주주총회 집중(예상)일 개최 사유 : 당사는 코스닥협회의 주주총회 집중일 발표전 증선위 재무제표 제출일자, 결산 이 사회 일자, 외부감사인으로부터 감사보고서 예상 수령일자, 고유사업관련 해외 전 시회 참여 및 고객사 미팅 일정 등을 고려하여 주주총회일을 3월 30일로 결정하였 습니다. 주주총회 집중일 발표 이후 상기 당사의 일정조정이 불가하여 부득이 하게 주주총회 집중일에 주주총회를 개최하게 되었습니다 ◇ 향후 주주총회에서는 주총분산 자율준수프로그램에 적극 참여하여 집중일을 피하여 개최할 수 있도록 노력하겠습니다. ◇ 상기 재무제표는 감사전 개별 재무제표입니다. 외부감사인의 감사의견과 주석을 포함한 최종 재무제표는 추후 전자공시시스템 (http://dart.fss.or.kr)에 공시할 예정입니다. ◇ 코로나바이러스 감염증-19(COVID-19)의 감염 및 전파를 예방하기 위하여, 총회 입장전 '체온측정' 혹은 '문진표'의 결과에 따라 발열이 의심되는 경우 출입이 제한될 수 있음을 알려드립니다. 또한, 질병예방을 위하여 마스크를 반드시 착용하여 주시기 바랍니다. |