 |
|
시장점유율 |
정 정 신 고 (보고)
| 2019년 04월 12일 |
1. 정정대상 공시서류 : 증권신고서
2. 정정대상 공시서류의 최초제출일 : 2019년 04월 02일
3. 정정사항
정정사항 확인의 편의를 위하여 금번 정정사항은 파란글씨로 정정하였습니다
| 항 목 | 정정사유 | 정 정 전 | 정 정 후 |
|---|---|---|---|
| ※ 요약정보는 본문의 정정사항을 반영하였으며, 정오표를 별도로 기재하지 않았습니다. ※ 오타에 대하여 수정하였습니다 |
|||
| 공통 정정사항 | |||
| 유상증자 일정 | 일정 변경에 따른 정정 | (참조 1) | (참조 1) |
| 제1부 모집 또는 매출에 관한 사항 | |||
| Ⅲ. 투자위험요소 | |||
| 1. 사업위험 | |||
| (다) | 경쟁업체 및 점유율 관련 세부내용 추가 | (참조 2) | (참조 2) |
| (마) | 바이오의약품 임상시험 실패에 따른 위험 내용 추가 | (참조 3) | (참조 3) |
| (바) | 연구개발비용 관련 표 정정 | (참조 4) | (참조 4) |
| (사) | 연구개발인력 관련 정정 및 추가 기재 | (참조 5) | (참조 5) |
| (자) | 기술이전 실패에 따른 위험 추가 기재 | - | (참조 6) |
| 2. 회사위험 |
|||
| (가) | 공급계약 관련 세부 작성 | (참조 7) | (참조 7) |
| (마) | KB증권 단기차입금에 따른 시나리오 추가 | (참조 8) | (참조 8) |
| 3. 기타위험 |
|||
| (다) | 전환사채 전환 가능성에 따른 주석희석화 위험 추가 기재 | - | (참조 9) |
| Ⅳ. 인수인의 의견 (분석기관의 평가의견) |
추가 기업실사 일정 | (참조 10) | (참조 10) |
| Ⅴ. 자금의 사용목적 | |||
| 나. 자금의 세부 사용계획 | 자금의 세부 사용계획의 추가 기재 | (참조 11) | (참조 11) |
| 제 2부 발행인에 관한 사항 | |||
| Ⅱ. 사업의 내용 | |||
| 2. 회사의 현황 (1) 사업 현황 및 사업 구분 1) 펩타이드 의약품 개발 기술 (가) 펩타이드 발굴기술 (PEPscovery) |
금융감독원 가이드라인에 의한 수정 기재 | (참조 12) | (참조 12) |
| 5. 매출에 관한 사항 다. 수주현황 |
(참조 13) | (참조 13) | |
| 9. 경영상의 주요 계약 | (참조 14) | (참조 14) | |
| 10. 연구개발 활동 | (참조 15) | (참조 15) | |
| Ⅹ. 그 밖에 투자자 보호를 위하여 필요한 사항 | (참조 16) | (참조 16) | |
(참조 1) - 정정 전
| 일자 | 내용 | 비고 |
|---|---|---|
| 2019년 04월 02일 | 신주발행 이사회결의 | - |
| 2019년 04월 02일 |
증권신고서 제출 | |
| 2019년 04월 03일 |
신주발행 및 기준일 공고 | 당사 인터넷 홈페이지 (http://www.nibec.co.kr) |
| 2019년 04월 16일 |
1차 발행가액 확정 | 신주배정기준일 3거래일 전 |
| 2019년 04월 18일 | 권리락 | - |
| 2019년 04월 19일 | 신주배정 기준일 | (명부폐쇄 4/22~5/2) |
| 2019년 05월 03일 | 신주배정 통지 | - |
| 2019년 05월 13일~ 2019년 05월 17일 |
신주인수권증서 상장 거래기간 | 5거래일 이상 거래 |
| 2019년 05월 20일 |
신주인수권증서 상장 폐지 | 구주주 청약초일 5거래일 전 |
| 2019년 05월 24일 |
확정 발행가액 산정 | 구주주 청약초일 3거래일 전 |
| 2019년 05월 27일 | 확정 발행가액 공고 | 당사 인터넷 홈페이지 (http://www.nibec.co.kr) |
| 2019년 05월 29일~ 2019년 05월 30일 |
구주주 청약 및 초과청약 | - |
| 2019년 06월 03일 | 일반공모 청약 공고 | 당사 인터넷 홈페이지 (http://www.nibec.co.kr) 케이비증권(주) 홈페이지 (http://www.kbsec.com) |
| 2019년 06월 03일~ 2019년 06월 04일 |
일반공모 청약 | 고위험고수익투자신탁, 벤처기업투자신탁 청약 포함 |
| 2019년 06월 07일 |
환불 및 배정 공고 | - |
| 2019년 06월 07일 |
주금 납입 | - |
| 2019년 06월 19일 |
주권 교부 예정일 | - |
| 2019년 06월 20일 |
신주 상장 예정일 | - |
| 주) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정요구 등 조치를 취할 수 있으며, 정정요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다 |
(참조 1) - 정정 후
| 일자 | 내용 | 비고 |
|---|---|---|
| 2019년 04월 02일 | 신주발행 이사회결의 | - |
| 2019년 04월 02일 |
증권신고서 제출 | - |
| 2019년 04월 03일 |
신주발행 및 기준일 공고 | 당사 인터넷 홈페이지 (http://www.nibec.co.kr) |
| 2019년 04월 12일 | (정정)증권신고서 제출 | - |
| 2019년 04월 26일 |
1차 발행가액 확정 | 신주배정기준일 3거래일 전 |
| 2019년 04월 30일 | 권리락 | - |
| 2019년 05월 02일 | 신주배정 기준일 | (명부폐쇄 5/3~5/15) |
| 2019년 05월 16일 | 신주배정 통지 | - |
| 2019년 05월 23일~ 2019년 05월 29일 |
신주인수권증서 상장 거래기간 | 5거래일 이상 거래 |
| 2019년 05월 30일 |
신주인수권증서 상장 폐지 | 구주주 청약초일 5거래일 전 |
| 2019년 06월 04일 |
확정 발행가액 산정 | 구주주 청약초일 3거래일 전 |
| 2019년 06월 05일 | 확정 발행가액 공고 | 당사 인터넷 홈페이지 (http://www.nibec.co.kr) |
| 2019년 06월 10일 | 우리사주조합 청약 | - |
| 2019년 06월 10일~ 2019년 06월 11일 |
구주주 청약 및 초과청약 | - |
| 2019년 06월 13일 | 일반공모 청약 공고 | 당사 인터넷 홈페이지 (http://www.nibec.co.kr) 케이비증권(주) 홈페이지 (http://www.kbsec.com) |
| 2019년 06월 13일~ 2019년 06월 14일 |
일반공모 청약 | 고위험고수익투자신탁, 벤처기업투자신탁 청약 포함 |
| 2019년 06월 18일 |
환불 및 배정 공고 | - |
| 2019년 06월 18일 |
주금 납입 | - |
| 2019년 06월 28일 |
주권 교부 예정일 | - |
| 2019년 07월 01일 |
신주 상장 예정일 | - |
| 주) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정요구 등 조치를 취할 수 있으며, 정정요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다 |
(참조 2) - 정정 전
당사는 펩타이드 공학기술과 약물전달 시스템 및 바이오소재 융합기술을 통하여 제품을 상용화 하고 있습니다. 2018년 12월 12일 펩타이드 기반의 신약 파이프라인에 대한 전임상 및 임상시험과 해외 사업 활성화 촉진을 위해 2019년 1월 미국에 자회사를 설립하고 연구개발을 활성화할 계획에 있습니다. 또한 당사의 치과용 골이식재 제품인 OssGen X-15 는 펩타이드 기반 융합 의료기기로 국내 식약처 허가를 받고 글로벌 임플란트 기업과 판매계약을 맺었으며, 치과 분야뿐 아니라 정형외과 시장에도 확대 적용될 수 있다고 판단하여 미국내 자회사를 통해 FDA 사전승인을 진행하고, 정형외과 시장진입을 준비하고 있습니다.
| [당사의 총 제품 현황] |
|
제품군 |
분야 |
당사 제품명 |
분야의 성격 |
구분 |
세부구분 |
|---|---|---|---|---|---|
| 펩타이드제품군 | 펩타이드 기반 융합바이오소재 |
OssGen-X15 |
전문가 사용 |
의료기기 |
신개발의료기기 |
|
OssGen-X15 Gel |
전문가 사용 |
의료기기 |
신개발의료기기 |
||
|
OssGen Ortho |
전문가 사용 |
의료기기 |
신개발의료기기 |
||
| 펩타이드 치료제 |
NIPEP OSS |
전문가 사용 |
의약품 |
오리지날 |
|
|
NIPEP-Care 1 NIPEP-Care 2 |
전문가 사용 |
의약품 |
오리지날 |
||
|
NIPEP-ACD-Tide |
전문가 사용 |
의약품 |
오리지날 |
||
| 펩타이드 기반 바이오베터 |
OssGen-better |
전문가 사용 |
의약품 |
바이오베터 |
|
|
조직재생용 |
치과용 골이식재 |
OCS-B, OCS-H |
전문가 사용 |
의료기기 |
제네릭 |
|
치주조직재생용쉬트 |
GuidOss |
전문가 사용 |
의료기기 |
신개발의료기기 |
|
|
흡수성치주조직재생유도재 |
Regenomer |
전문가 사용 |
의료기기 |
제네릭 |
|
|
골이식용 복합재료 |
OCS-B Collagen, Equimatrix Collagen |
전문가 사용 |
의료기기 |
신개발의료기기 |
|
|
구강질환 |
개인용 치아미백제 |
Dr.Whitiss |
일반인 사용 |
의약외품 |
오리지날 |
|
전문가용 치아미백제 |
BlanTis Pro(10%) BlanTis Clinic(15%) |
전문가 사용 |
의약품 |
제네릭 |
|
|
시린이 치료제 |
SensBlok |
일반인, 전문가 사용 |
의료기기 |
신개발의료기기 |
|
|
치과용 컨디셔너, 임플란트주위염치료제 |
Clinplant syringe/Floss |
일반인, 전문가 사용 |
의료기기 |
신개발의료기기 |
|
|
치주질환치료제 |
MinoCure |
전문가 사용 |
의약품 |
제네릭 |
|
|
화장품 |
펩타이드 화장품 원료 |
- | - |
화장품 |
오리지날 |
|
미백 주름개선 기능성 화장품 |
Dr.MyYou Solution |
일반인 사용 |
화장품 |
오리지날 |
|
|
항노화 기능성 화장품 |
Eustella Complex Solution |
일반인 사용 |
화장품 |
오리지날 |
|
|
여드름 및 염증 억제 화장품 |
Eustella AC Solution |
일반인 사용 |
화장품 |
오리지날 |
| 주) 오리지날 : 최초 개발되어 허가받은 신약 제네릭 : 오리지널 의약품/의료기기과 용법, 용량, 성능이 동일한 복제약 혹은 의료기기 신개발의료기기 : 신성능, 신구조, 신사용목적 중 하나에 해당하는 의료기기이며, 유사한 의미로 의약품에서는 신약에 해당됨. 신약과 같이 1, 2, 3상의 임상시험이 필요하지 않고, 단상으로 평가함. 바이오베터 : 기존에 허가된 바이오의약품(단백질의약품, 항체의약품, 펩타이드 의약품 등)의 성능을 개선시킨 것. 본질적으로 골격은 기존에 허가된 바이오의약품의 구조를 유지하기 때문에 허가시 기존 바이오의약품과의 동등성 자료를 제출할 것을 요구함. |
구강보건제품 및 조직재생용 바이오소재와 관련하여 당사는 우수한 기술 및 제조공정 노하우 등을 바탕으로 국내시장에서의 시장점유율을 확대해 나가고 있으며 글로벌 임플란트 1위, 2위업체인 Straumann과 Nobel Biocare 등의 유통업체들과의 공급계약을 통해 시장을 넓혀나가고 있습니다. 하지만, 당사의 이러한 노력에도 불구하고 대기업 혹은 글로벌 기업이 당사에 비해 더 나은 제품을 출시하거나 마케팅활동을 강화하는 등 경쟁상황이 악화될 경우 해당 제품에 대한 당사의 영업환경이 악화될 수 있습니다.
또한 당사가 개발 중인 펩타이드 치료제와 펩타이드 기반 바이오베터의 경우, 동 제품과 동일한 효능을 지닌 오리지널 단백질의약품, 바이오시밀러, 펩타이드 치료제 등을 판매 혹은 개발하고 있는 업체가 모두 당사의 경쟁업체에 해당한다고 볼 수 있으므로 경쟁이 더욱 치열해지고 있습니다. 따라서, 당사가 개발 중인 제품보다 안전성 및 효능이 뛰어난 제품이 경쟁업체에 의하여 출시되거나 시장을 선점하게 될 경우에는 펩타이드 치료제의 개발 및 기술이전을 통한 당사의 수익창출 계획에 부정적인 영향을 끼칠 수 있습니다. 당사의 주요 제품 및 추정 시장점유율 등은 다음과 같습니다.
|
제품군 |
분야 |
당사 제품명 |
매출액 (백만원) |
시장점유율(주1) |
주요 경쟁업체 |
주요 경쟁제품 |
|||
|---|---|---|---|---|---|---|---|---|---|
|
2018년 |
2017년 |
2018년 |
2017년 |
2016년 |
|||||
|
조직재생용 |
치과용 골이식재 |
OCS-B, |
4,151 |
4,529 |
18% |
16% |
14% |
Geistlich |
Bio-Oss |
|
치주조직재생용쉬트 |
GuidOss |
40 |
82 |
Geistlich |
Bio-Gide |
||||
|
흡수성치주조직 |
Regenomer |
42 |
21 |
Olympus Terumo |
Teruplug |
||||
|
골이식용 복합재료 |
OCS-B Collagen, Equimatrix Collagen |
663 |
271 |
Geistlich |
Bio-Oss Collagen |
||||
|
구강질환 |
개인용 치아미백제 |
Dr.Whitiss |
59 |
78 |
8% |
12% |
14% |
LG생활건강 |
클라렌세븐데이즈 |
|
아모레퍼시픽 |
메디안퍼페트화이트 |
||||||||
|
시린이 치료제 |
SensBlok |
1 |
2 |
- |
- |
- |
Phoenix Dental |
Super seal |
|
|
Heraeus Kulzer |
Gluma Desensitizer |
||||||||
|
치과용 컨디셔너 |
Clinplant |
51 |
3 |
- |
- |
- |
Straumann |
Prefgel |
|
|
GC America |
Cavity conditioner |
||||||||
|
치주질환치료제 |
MinoCure |
137 |
45 |
- |
- |
- |
동국제약 |
덴타클린 캡슐 |
|
|
Sunstar |
페리오클린 |
||||||||
|
펩타이드 |
펩타이드 기반 |
OssGen-X15 |
- |
- |
- |
- |
- |
Dentsply |
PepGen P-15 |
|
Osteohealth |
GEM21S |
||||||||
|
OssGen-X15 Gel |
- |
- |
- |
- |
- |
Straumann |
Emdogain |
||
|
Medtronic |
INFUSE |
||||||||
|
OssGen Ortho |
- |
- |
- |
- |
- |
Stryker |
OP-1 |
||
|
펩타이드 치료제 |
OsseoTide |
- |
- |
- |
- |
- |
Amgen |
Enbrel |
|
|
NIPEP-Care 1 NIPEP-Care 2 |
- |
- |
- |
- |
- |
||||
|
Nipep-ACD-Tide |
- |
- |
- |
- |
- |
Abbvie |
Humira |
||
|
펩타이드 기반 |
OssGen-better |
- |
- |
- |
- |
- |
Merck |
Fosamax |
|
|
Lilly |
Forteo |
||||||||
|
화장품군 |
미백,주름개선 |
Dr. MyYou skin |
2 |
96 |
- |
- |
- |
kiehl's |
kiehl's |
|
항노화화장품 |
Eustella Complex Solution |
62 |
52 |
- |
- |
- |
Estee Lauder |
Estee Lauder |
|
|
여드름 및 염증억제 화장품 |
Eustella AC Solution |
- |
- |
- |
- |
- |
Proactiv |
Proactiv |
|
|
펩타이드 화장품 원료 |
- |
- |
- |
- |
- |
- |
- |
||
|
기타 |
기술수출 |
- |
1,124 |
- |
- |
- |
- |
- |
|
|
주1) 상기 시장점유율은 회사 추산자료 이므로, 실제와 상이할 수 있음 주3) 경쟁제품이 아직 국내 시장에 미출시되어 시장점유율 산정이 불가함 |
(참조 2) - 정정 후
당사는 펩타이드 공학기술과 약물전달 시스템 및 바이오소재 융합기술을 통하여 제품을 상용화 하고 있습니다. 펩타이드 기반의 신약 파이프라인에 대한 전임상 및 임상시험과 해외 사업 활성화 촉진을 위해 2019년 4월 미국에 자회사를 설립하고 연구개발을 활성화할 계획에 있습니다. 또한 당사의 치과용 골이식재 제품인 OssGen X-15 는 펩타이드 기반 융합 의료기기로 국내 식약처 허가를 받고 글로벌 임플란트 기업과 판매계약을 맺었으며, 치과 분야뿐 아니라 정형외과 시장에도 확대 적용될 수 있다고 판단하여 미국내 자회사를 통해 FDA 사전승인을 진행하고, 정형외과 시장진입을 준비하고 있습니다.
| [당사의 총 제품 현황] |
|
제품군 |
분야 |
당사 제품명 |
분야의 성격 |
구분 |
세부구분 |
|---|---|---|---|---|---|
| 펩타이드제품군 | 펩타이드 기반 융합바이오소재 |
OssGen-X15 |
전문가 사용 |
의료기기 |
신개발의료기기 |
|
OssGen-X15 Gel |
전문가 사용 |
의료기기 |
신개발의료기기 |
||
|
OssGen Ortho |
전문가 사용 |
의료기기 |
신개발의료기기 |
||
| 펩타이드 치료제 |
NIPEP OSS |
전문가 사용 |
의약품 |
오리지날 |
|
|
NIPEP-Care 1 NIPEP-Care 2 |
전문가 사용 |
의약품 |
오리지날 |
||
|
NIPEP-ACD-Tide |
전문가 사용 |
의약품 |
오리지날 |
||
| 펩타이드 기반 바이오베터 |
OssGen-better |
전문가 사용 |
의약품 |
바이오베터 |
|
|
조직재생용 |
치과용 골이식재 |
OCS-B, OCS-H |
전문가 사용 |
의료기기 |
제네릭 |
|
치주조직재생용쉬트 |
GuidOss |
전문가 사용 |
의료기기 |
신개발의료기기 |
|
|
흡수성치주조직재생유도재 |
Regenomer |
전문가 사용 |
의료기기 |
제네릭 |
|
|
골이식용 복합재료 |
OCS-B Collagen, Equimatrix Collagen |
전문가 사용 |
의료기기 |
신개발의료기기 |
|
|
구강질환 |
개인용 치아미백제 |
Dr.Whitiss |
일반인 사용 |
의약외품 |
오리지날 |
|
전문가용 치아미백제 |
BlanTis Pro(10%) BlanTis Clinic(15%) |
전문가 사용 |
의약품 |
제네릭 |
|
|
시린이 치료제 |
SensBlok |
일반인, 전문가 사용 |
의료기기 |
신개발의료기기 |
|
|
치과용 컨디셔너, 임플란트주위염치료제 |
Clinplant syringe/Floss |
일반인, 전문가 사용 |
의료기기 |
신개발의료기기 |
|
|
치주질환치료제 |
MinoCure |
전문가 사용 |
의약품 |
제네릭 |
|
|
화장품 |
펩타이드 화장품 원료 |
- | - |
화장품 |
오리지날 |
|
미백 주름개선 기능성 화장품 |
Dr.MyYou Solution |
일반인 사용 |
화장품 |
오리지날 |
|
|
항노화 기능성 화장품 |
Eustella Complex Solution |
일반인 사용 |
화장품 |
오리지날 |
|
|
여드름 및 염증 억제 화장품 |
Eustella AC Solution |
일반인 사용 |
화장품 |
오리지날 |
| 주) 오리지날 : 최초 개발되어 허가받은 신약 제네릭 : 오리지널 의약품/의료기기과 용법, 용량, 성능이 동일한 복제약 혹은 의료기기 신개발의료기기 : 신성능, 신구조, 신사용목적 중 하나에 해당하는 의료기기이며, 유사한 의미로 의약품에서는 신약에 해당됨. 신약과 같이 1, 2, 3상의 임상시험이 필요하지 않고, 단상으로 평가함. 바이오베터 : 기존에 허가된 바이오의약품(단백질의약품, 항체의약품, 펩타이드 의약품 등)의 성능을 개선시킨 것. 본질적으로 골격은 기존에 허가된 바이오의약품의 구조를 유지하기 때문에 허가시 기존 바이오의약품과의 동등성 자료를 제출할 것을 요구함. |
한편, 당사는 상기 제품들에 대하여 글로벌적으로 조직재생용 바이오소재 기업과 펩타이드 관련 연구개발 및 제조기업들과 경쟁하고 있습니다. 각 기반사업군별 경쟁 현황은 다음과 같습니다.
1) 조직재생용 바이오소재
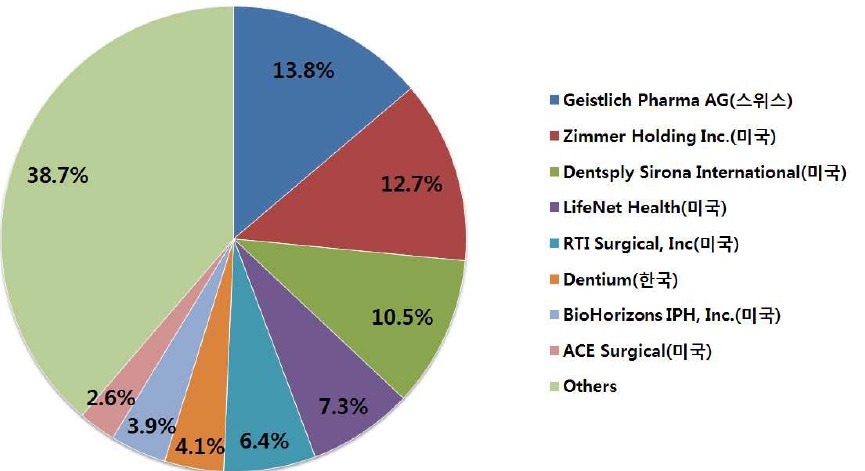
당사가 생산하고 있는 조직재생용 바이오소재는 글로벌적으로 Geistlich Pharma AG(스위스), Zimmer Holding Inc(미국), Dentsply Sirona International(미국) 등과 경쟁하고 있습니다. Marketsandmarkets, Dental Bone Graft Substituetes Market, 2016에 의하면, 치과용 골이식재의 글로벌 시장은 Geistlich Pharma AG(스위스)의 소뼈유래 골이식재인 BioOss를 포함한 상위 5개 업체의 제품이 시장의 대부분을 장악하고 있으며, 특히 Geistlich Pharma AG(스위스)가 2015년 기준 시장점유율 13.8%로 우위를 선점하고 있습니다.
| [글로벌 치과용 골이식 대체물 시장의 주요 업체 및 점유율 현황] |
 |
|
시장점유율 |
자료 : Marketsandmarkets, Dental Bone Graft Substitutes Market, 2016 / 치과용 골이식 대체물 시장, 2018, 연구개발특구진흥재단
또한, 글로벌 치과용 골이식재 시장 중 1, 2, 3위를 차지하고 있는 Giestlich Pharma AG(스위스), Zimmer Holding Inc.(미국), Dentsply Sirona International(미국)에 대한 업계 동향은 다음과 같습니다.
| [글로벌 치과용 골이식 주요 업체의 동향] |
| 업체 명 | 주요 동향 |
|---|---|
| Geistlich Pharma AG(스위스) | - 뼈, 연골, 조직 등의 재생을 위한 생체재료 분야의 전문적인 기업으로 의료용 재료와 의약품을 개발 및 제조하는 업체이며, 주로 치과용 골이식재료와 차폐막 재료를 생산 및 판매 중입니다. - 치과, 정형외과와 같은 특정 분야에 의료기기를 공급하며, Geistlich Biomaterials(치과용 생체재료), Geistlich Surgery(정형외과 생체재료), Geistlich Medical(제약 및 의료용품)의 세 분야를 통해 사업을 운영하고 있습니다. - 2013년 뼈와 연조직의 재생을 유도하는 이중층 콜라겐인‘Bio-Gide’를 출시하였으며, 2015년 연조직 재생을 위한 새로운 콜라겐 매트릭스인 ‘Geistlich Mucograft Seal’을 출시하였습니다. |
| Zimmer Holding Inc.(미국) | - 무릎, 엉덩이, 팔꿈치, 발, 발목, 인공 관절, 치과 보철을 포함하는 정형외과 의료기기 제품을 설계, 개발, 제조 및 판매하는 업체입니다. - 2012년 뼈의 성장을 위하여 높은 마찰계수로 설계된‘Trabecular Metal’인 치아 임플란트를 출시하였고, 2013년 3D 시각화 소프트웨어를 사용하여 의사가 환자에 대한 맞춤형 수술을 계획할 수 있도록 임플란트 배치를 용이하게 하는‘Patient Specific Instruments (PSI) Shouldersystem’을 판매하였습니다. |
| Dentsply Sirona International(미국) | - 전문적인 치과장비 제조 및 치과용 소모품 생산 기업으로 120개국에서 제품을 판매하는 대표적인 치과 용품 제조 및 판매 업체입니다. - 치과 용품 및 장비, CAD/CAM 복원 시스템, 치과 영상기기, 치과 교정용 품 등을 포함한 치과 및 구강 보건 제품을 제조 및 판매 중입니다. |
한편, 국내 치과용 골이식재 시장에서는 당사와 Geistlich Pharma AG(스위스), 오스코텍 등의 업체가 치과용 골이식재 시장을 과점하고 있으며, Geistlich Pharma AG(스위스)의 BioOss가 41.2%, 당사의 OCS-B, OCS-H, GuideOss 등이 12.9%, 오스코텍의 BioCera, SynCera가 8.1%로 국내시장의 점유율을 차지하고 있는 것으로 추정되고 있습니다. 당사의 제품 및 경쟁업체들의 제품의 비교 현황은 다음과 같습니다.
| [국내 치과용 골이식재 경쟁업체들의 제품 비교 현황] |
| 업체 명 | 주요 제품 | 주요 특징 및 장점 |
|---|---|---|
| Geistlich Pharma AG(스위스) |
BioOss | - 소뼈에서 추출된 천연 골이식재. - 유기성분을 제거할때 직접 열을 가하지 않고 화학처리에 의한 특허기술을 이용, 표면구조가 조직 세포의 유착성에 있어서 뛰어남. |
| 나이벡 | OCS-B | - 한우 소뼈에서 추출된 천연의 무기질 재료로써, 높은 순도, 체내 이식 안정성이 높음 - 면역 유발이 가능한 단백성 물질 제거가 완벽하면서도 인체의 뼈와 유사한 표면 구조를 가짐. |
| OCS-H | - 말뼈에서 추출한 골무기질로 인체의 골 구조와 유사 - 인체의 골과 거의 같은 형태의 구조를 가진 말뼈의 형태 및 구조를 그대로 유지 - 광우병 우려 해소 |
|
| 오스코텍 | SynCera | 순수β-TCP로 만든 합성골 제품으로 우수한 생체 친화성과 저렴한 가격 |
| InduCera | 칼슘포스페이트 크리스탈 이중코팅과 새로운 제조 공정으로 신생골 형성 능력을 보다 향상 |
2) 펩타이드 관련 제품
당사가 연구개발중인 펩타이드 관련 제품은 펩타이드 기반 골이식재와 펩타이드 기반의 골다공증 치료제, 관절염치료제, 비알콜성지방간염치료제, 염증성장질환치료제, 펩타이드 기반 바이오베터로, 펩타이드 소재인 점을 제외할 시 다른 소재를 기반으로 경쟁업체들이 연구개발 및 제품출시를 하고 있으며, 이와 관련된 모든 업체들이 경쟁업체라고 할 수 있습니다. 그러나 펩타이드를 기반으로 한 치료제는 글로벌적으로 아직 개발되지 않았기 때문에 시장점유율을 측정할 수 없는 상황입니다. 다만, 펩타이드 기반 골이식재 관련된 제품은 출시되었으며, 이에 대한 내용은 다음과 같습니다.
[펩타이드 기반 골이식재]
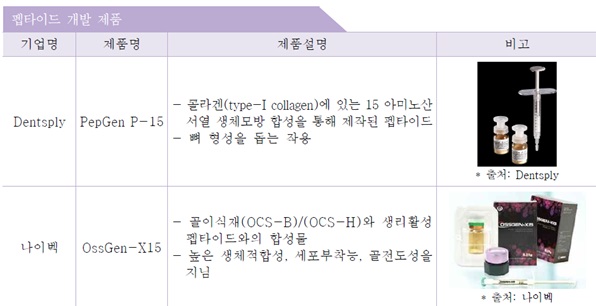
단백질이 지니는 염증 및 면역 원성의 부작용을 줄인 펩타이드를 개발하는 연구 및 이를 이용한 임플란트 제품 개발도 활발하게 연구되고 있으나 아직 연구개발 단계이며, 당사를 제외한 펩타이드 기반 골이식재를 개발한 기업은 Dentsply가 있습니다. 펩타이드 기반 골이식재 제품에 대한 설명은 다음과 같습니다.
 |
|
펩타이드 기반 골이식재 |
(참조 3) - 정정 전
바이오의약품의 특성 상 연구개발에는 오랜 시간과 많은 자금이 소요되는 반면 완제의약품이 시장에 출시되기 전까지는 괄목할만한 수익이 발생하지 않기 때문에 임상 시험이 실패할 경우 개발회사에 미치는 타격은 막대할 수 있습니다. 이러한 위험은 비단 당사뿐 아니라 신약개발 사업을 영위하는 회사들에게는 필연적인 위험입니다.
| [바이오의약품 임상 시험 단계별 성공률] |
|
단계 |
바이오의약품 성공확률 |
|---|---|
|
임상 1상 → 임상 2상 |
66.0% |
|
임상 2상 → 임상 3상 |
34.4% |
|
임상 3상 → 신약허가신청 |
57.2% |
|
신약허가 → 신약승인 |
88.4% |
|
임상 1상부터 신약승인까지 성공 확률 |
11.5% |
| 자료) BIO Biomedtracker Amplion, Clinical Development Success Rates 2006-2015 |
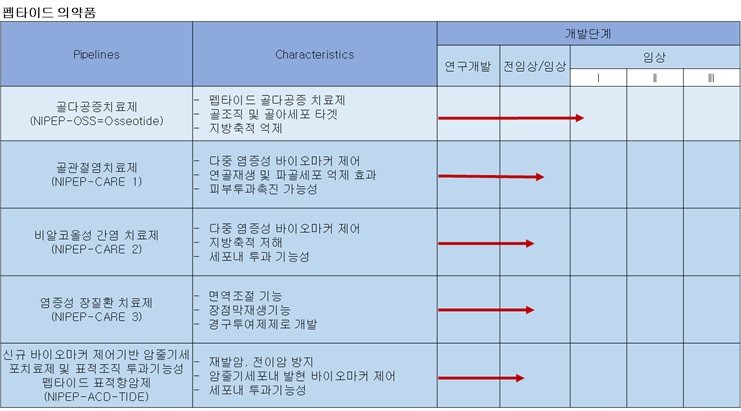
당사의 펩타이드 기반 융합 바이오소재 중 OssGen-X15(골재생 펩타이드가 표면에 고정된 골이식재)는 전임상/임상 완료 및 국내/해외에서 허가 또는 인증을 받아 시판중에 있으며, Regenomer(골재생 펩타이드 함유 주입형 골재생재)는 전임상/임상 완료 및 국내허가까지 완료한 상태로 해외 인증을 준비 중에 있습니다. 반면 펩타이드 기반 치료제인 펩타이드 골다공증치료제(NIPEP-OSS)는 전임상이 완료된 상태로 임상1상 1년, 임상2상 2년, 임상 3상 2년이 진행된 후 2026년에 출시될 것으로 예상되며, 관절염치료제(NIPEP-CARE 1), 항암치료제(NIPEP-ACD Tide)는 전임상이 진행중에 있는 상태로 각각 2027년, 2028년에 출시를 계획하고 있으나, 장기간의 연구개발 플랜으로 이에 대해서 정확히 예측할 수는 없는 상황입니다. 당사의 현재 펩타이드 기반 바이오소재 연구개발단계 및 펩타이드 기반 치료제의 연구개발 진행상황 및 계획은 다음과 같습니다.
| [당사 펩타이드 기반 바이오소재의 연구개발단계] |
 |
|
펩타이드 의약품 연구개발 단계 |
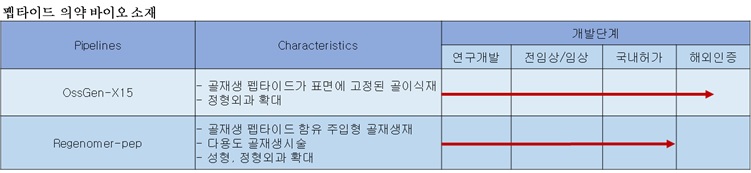 |
|
펩타이드 의약바이오소재 연구개발 단계 |
| [펩타이드 기반 치료제의 연구개발 진행상황 및 향후 계획] |
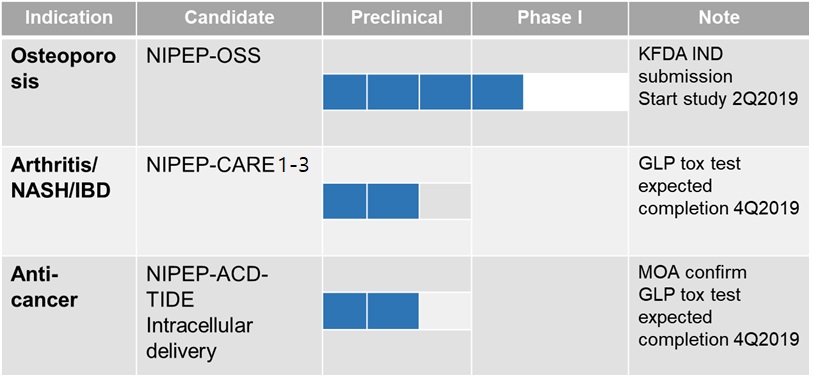 |
|
연구진행 현황 |
당사는 펩타이드 기반 융합바이오소재의 임상단계, 품목허가 과정을 거치면서 최근의 임상시험 절차 및 기준에 대해 상대적으로 잘 인지하고 있고 노하우를 보유하고 있으며, 향후 펩타이드 기반 치료제의 연구개발 또한 당사 연구개발계획에 의거하여
절차를 진행하려고 합니다. 그럼에도 불구하고 당사의 파이프라인이 임상을 진행함에 있어서 유의미한 결과를 도출하지 못할 경우에는 제품화가 불가능하며 투입된 연구비, 연구 역량 등 당사에 높은 기회비용이 발생할 수 있으며 사업계획에 지대한 영향을 미칠 수 있습니다.
특히 금번 주주배정후실권주 일반공모를 통하여 유입되는 자금 중 약 150억원을 향후 연구개발을 위한 자금으로 사용하려고 하고 있습니다. 그러므로 투자자께서는 임상시험 절차, 임상 시험의 단계별 성공률, 당사의 파이프라인 현황 및 개발 단계, 타사 사례 등을 통해 리스크에 대해 충분히 확인 및 인지하시고 투자에 임하시기 바랍니다.
(참조 3) - 정정 후
바이오의약품의 특성 상 연구개발에는 오랜 시간과 많은 자금이 소요되는 반면 완제의약품이 시장에 출시되기 전까지는 괄목할만한 수익이 발생하지 않기 때문에 임상 시험이 실패할 경우 개발회사에 미치는 타격은 막대할 수 있습니다. 일반적으로 바이오의약품의 단계별 성공률은 임상1상에서 임상 2상까지는 66.0%, 임상2상에서 임상3상까지는 34.4%, 임상3상에서 신약허가 신청까지 57.2%, 신약허가에서 신약승인까지는 88.4%로, 임상1상부터 신약승인까지의 성공확률은 11.5%로 상당히 저조합니다. 또한 한국바이오협회가 발표한 임상단계별 특징에 의하면 임상1상에서 임상3상까지 임상대상은 1,000명~5,000명 이상이 필요하며 소요비용은 약 1,250억원을 예상하고 있습니다. 이러한 높은수준의 임상비용과 오랜 소요기간은 비단 당사뿐 아니라 신약개발 사업을 영위하는 회사들에게는 필연적인 위험입니다.
| [바이오의약품 임상 시험 단계별 성공률] |
|
단계 |
바이오의약품 성공확률 |
|---|---|
|
임상 1상 → 임상 2상 |
66.0% |
|
임상 2상 → 임상 3상 |
34.4% |
|
임상 3상 → 신약허가신청 |
57.2% |
|
신약허가 → 신약승인 |
88.4% |
|
임상 1상부터 신약승인까지 성공 확률 |
11.5% |
| 자료) BIO Biomedtracker Amplion, Clinical Development Success Rates 2006-2015 |
| [임상 단계별 소요비용] |
| 임상단계 | 소요비용 |
|---|---|
| 임상1상 | 50억원 내외 |
| 임상2상 | 200억원 내외 |
| 임상3상 | 1,000억원 이상 |
| 자료) 한국바이오협회_2017 |
당사가 연구개발 중인 펩타이드 기반 바이오소재의 현황 및 연구개발단계는 다음과 같습니다.
1) 펩타이드 의약 바이오소재
당사의 펩타이드 의약 바이오 소재 중 OssGen-X15(골재생 펩타이드가 표면에 고정된 골이식재)는 전임상/임상 완료 및 국내/해외에서 허가 또는 인증을 받아 시판중에 있으며, Regenomer-pep(골재생 펩타이드 함유 주입형 골재생제)는 전임상/임상 완료 및 국내허가까지 완료한 상태로 해외 인증을 준비 중에 있습니다. 해외 인증이 완료되는 시점은 2021년 9월로 예상하고 있으며, 인증비용은 약 10억원이 소요될 것으로 예상하고 있습니다.
 |
|
펩타이드 의약바이오소재 연구개발 단계 |
2) 펩타이드 관련 치료제
펩타이드 기반 치료제인 펩타이드 골다공증치료제(NIPEP-OSS)는 전임상이 완료된 상태로 임상1상 1년, 임상2상 2년, 임상 3상 2년이 진행된 후 2026년에 출시될 것으로 예상됩니다. 골관절염치료제(NIPEP-CARE 1), 비알콜성 간염 치료제(NIPEP-CARE2), 염증성 장질환치료제(NIPEP-CARE3), 항암치료제(NIPEP-ACD Tide),는 현재 전임상이 진행중에 있는 상태입니다. 당사는 향후 펩타이드 기반 골다공증치료제 임상 1상 진행비용 35억원, 펩타이드 기반 관절염 치료제의 전임상 및 1상임상비용 각각 30억원, 펩타이드 표적항암제 전임상비용 15억원, 비알콜성지방간염(NASH) 치료제와 장질환 치료제 전임상비용 30억원으로 총 140억원이 소요될 것으로 예상하고 있습니다.
| [펩타이드 기반 치료제의 연구개발 진행상황 및 향후 계획] |
|
구 분 |
진행 상황 및 계획 |
전임상 |
임상 1상 |
임상 2상 |
임상 3상 |
출시예정 |
|---|---|---|---|---|---|---|
| 펩타이드 골다공증치료제 (NIPEP-OSS) |
- 2019년 12월식약처 임상시험 사전검토 제출, 현재 보완사항에 대한 자료 작성 중 - 기술이전 논의중. 임상2상부터는 기술이전 후 공동연구를 통해 진행 |
완료 |
2019.06~ |
2021.01~ |
2023.12~ |
2026 |
| 골관절염치료제(NIPEP-CARE 1), 비알콜성 간염 치료제(NIPEP-CARE2),염증성 장질환치료제(NIPEP-CARE3) |
- 전임상독성시험 진행중 |
진행중 (2019.4Q |
2020.12~ |
2021.06~ |
2024.06~ |
2027 |
| 항암치료제 (NIPEP-AntiCancer) |
- 유방암(Breast cancer)에 대한 유효성 시험 |
진행중 |
2021.01~ |
2022.06~ |
2025.06~ |
2028 |
| [당사 펩타이드 기반 바이오소재의 연구개발단계] |
 |
|
펩타이드 의약품 연구개발 단계 |
당사는 펩타이드 기반 융합바이오소재의 임상단계, 품목허가 과정을 거치면서 최근의 임상시험 절차 및 기준에 대해 상대적으로 잘 인지하고 있고 노하우를 보유하고 있으며, 향후 펩타이드 기반 치료제의 연구개발 또한 당사 연구개발계획에 의거하여
절차를 진행하려고 합니다. 그럼에도 불구하고 당사의 파이프라인이 임상을 진행함에 있어서 유의미한 결과를 도출하지 못할 경우에는 제품화가 불가능하며 투입된 연구비, 연구 역량 등 당사에 높은 기회비용이 발생할 수 있으며 사업계획에 지대한 영향을 미칠 수 있습니다.
특히 금번 주주배정후실권주 일반공모를 통하여 유입되는 자금 중 약 150억원(펩타이드 기반 골다공증치료제 임상 1상 진행비용 35억원, 펩타이드 기반 관절염 치료제의 전임상 및 1상임상비용 각각 30억원, 골이식재 및 골재생제 유럽임상비용 10억, 펩타이드 표적항암제 전임상비용 15억원, 비알콜성지방간염(NASH) 치료제와 장질환 치료제 전임상비용 30억원)을 향후 연구개발을 위한 자금으로 사용하려고 하고 있습니다. 그러나 상기 언급한 바와 같이 임상1상부터 신약승인까지의 성공확률은 11.5%로 상당히 저조하며, 임상시험이 성공하지 못할 경우 자산 및 매출화되지 못하고 모두 비용처리가 될 위험이 있습니다. 그러므로 투자자께서는 임상시험 절차, 임상 시험의 단계별 성공률, 당사의 파이프라인 현황 및 개발 단계, 타사 사례 등을 통해 리스크에 대해 충분히 확인 및 인지하시고 투자에 임하시기 바랍니다.
(참조 4) - 정정 전
| [최근 3년 연구개발비용] |
| (단위 : 천원) |
| 과 목 | 2018년 | 2017년 | 2016년 | |
|---|---|---|---|---|
| 원 재 료 비 | 21,300 | 44,408 | 65,850 | |
| 인 건 비 | 961,774 | 973,219 | 399,181 | |
| 감 가 상 각 비 | 28,865 | 28,346 | 31,076 | |
| 위 탁 용 역 비 | 928,156 | 943,722 | 1,151,919 | |
| 기 타 | 554,482 | 703,993 | 921,086 | |
| 연구개발비용 계 | 2,494,577 | 2,693,688 | 2,569,112 | |
| 정부보조금 | (199,951) | (1,074,296) | (2,058,457) | |
| 회계처리 | 판매비와관리비 | 1,204,012 | 557,939 | 251,727 |
| 제조경비 | 224,004 | 227,645 | 118,368 | |
| 개발비(무형자산) | 1,066,561 | 1,908,104 | 2,199,017 | |
| 연구개발비 / 매출액 비율 [연구개발비용계÷당기매출액×100] |
47.90% | 42.74% | 53.48% | |
매년 매출액의 40% 이상이 발생하고 있는 연구개발비는 구강질환 개선제품, 조직재생용 바이오소재, 펩타이드 제품군, 화장품군의 각 분야 연구개발에 사용되고 있으며, 이에 따른 당사 제품의 특징, 개발단계, 수익창출계획은 다음과 같습니다. 또한 당사가 정부보조금을 받아 정부과제를 수행한 실적은 다음과 같습니다.
| [당사의 전제품 파이프라인] |
|
제품군 |
분야 |
당사 제품명 |
특징 |
개발단계 |
수익창출 계획 |
|---|---|---|---|---|---|
|
펩타이드 |
펩타이드 기반 |
OssGen-X15 |
펩타이드 함유 |
허가완료 |
매출화 |
|
OssGen-X15 Gel |
펩타이드 함유 |
시제품제작 임상준비 |
매출 예정 |
||
|
OssGen Ortho |
펩타이드 함유 |
전임상 진입 준비 단계 |
매출 예정 |
||
|
펩타이드 치료제 |
OsseoTide |
골다공증 치료제 |
전임상 완료, |
임상1상 완료 후 기술이전 예정 |
|
| NIPEP-Care 1 |
관절염치료제염증성장질환치료제 |
전임상 진입 준비 단계 |
임상1상 완료 후 기술이전 예정 |
||
| NIPEP-Care 2 |
비알콜성지방간염치료제 |
전임상 진입 준비 단계 |
임상1상 완료 후 기술이전 예정 |
||
| NIPEP-Care 3 |
염증성장질환치료제 |
전임상 진입 준비 단계 |
임상1상 완료 후 기술이전 예정 |
||
|
NIPEP-ACD-TIDE |
항암치료제 |
전임상 진입준비 단계 |
전임상 완료 후 기술이전 예정 |
||
|
펩타이드 기반 |
OssGen better |
PTH 골다공증바이오베터 |
전임상완료 |
개발완료 후 |
|
|
펩타이드 플랫폼 |
TOPscovery |
세포내 단백질(항체) 전달시스템 |
- |
플랫폼 서비스제공, 기술이전 |
|
|
조직재생용 |
치과용 골이식재 |
OCS-B, |
잇몸뼈 재생 |
허가완료 |
매출화 |
|
치주조직재생용쉬트 |
GuidOss |
치주조직 재생 |
허가완료 |
매출화 |
|
|
Xeno-Gide |
치주조직 재생 |
허가 진행중 |
매출예정 |
||
| 흡수성치주조직 재생유도재 |
Regenomer |
치주 재생 |
허가완료 |
매출화 |
|
|
Regenomatrix Tape, Cote |
치주 재생 |
허가 진행중 |
매출예정 |
||
| 골이식용 복합재료 |
OCS-B Collagen, Equimatrix Collagen |
콜라겐 함유 골이식재 |
허가완료 |
매출화 |
|
|
구강질환 |
개인용 치아미백제 |
Dr.Whitiss (8.6%) |
치아미백 |
허가완료 |
매출화 |
|
전문가용 치아미백제 |
BlancTis Pro (10%) BlancTis Clinic(15%) |
치아미백 |
허가완료 |
||
|
시린이 치료제 |
SensBlok |
시린이 치료 |
허가완료 |
||
|
치과용 컨디셔너 |
Clinplant Syringe/Floss |
치태제거, 치은염, 치주염, |
허가완료 |
||
|
치주질환치료제 |
MinoCure |
치은염, 치주염 치료 |
허가완료 |
||
|
구강케어치약 |
Dr.BlancTis Phosphate |
천연성분치약 |
허가완료 |
||
|
화장품 |
기능성화장품 |
펩타이드 화장품 원료 |
항노화, 염증억제, 미백등 |
ICID 등재 완료 |
매출예정 |
|
Dr.MyYou |
미백, 주름 개선 |
개발완료 |
매출화 |
||
|
Eustella Complex Solution |
항노화 기능 |
재생기능성 펩타이드 국제화장품 원료규격집 (ICID) 등재 완료 |
매출화 |
||
|
Estella AC Solution |
여드름 및 염증 억제 화장품 |
항염증 기능성 펩타이드 국제화장품 원료규격집 (ICID) 등재 완료, 피부임상시험완료 |
매출 예정 |
(참조 4) - 정정 후
| [최근 3년 연구개발비용] |
| (단위 : 천원) |
| 구 분 | 2018년 | 2017년 | 2016년 | |
|---|---|---|---|---|
| 비용의 성격별 분류 | 원재료비 | 21,300 | 44,408 | 65,850 |
| 인건비 | 961,774 | 973,219 | 399,181 | |
| 감가상각비 | 28,865 | 28,346 | 31,076 | |
| 위탁용역비 | 928,156 | 943,722 | 1,151,919 | |
| 기 타 | 554,482 | 703,992 | 921,086 | |
| 연구개발비용 합계 | 2,494,577 | 2,693,687 | 2,569,112 | |
| (정부보조금) | (199,951) | (1,074,296) | (2,058,457) | |
| 보조금 차감 후 금액 | 2,294,626 | 1,619,391 | 510,655 | |
| 회계처리 내역 | 판매비와 관리비 | 1,204,012 | 557,939 | 251,727 |
| 제조경비 | 224,004 | 227,645 | 118,368 | |
| 개발비(무형자산) | 1,066,561 | 1,908,103 | 2,199,017 | |
| 회계처리금액 계 | 2,494,577 | 2,693,687 | 2,569,112 | |
| 연구개발비 / 매출액 비율 [연구개발비용계÷당기매출액×100] |
47.90% | 42.74% | 53.48% | |
매년 매출액의 40% 이상이 발생하고 있는 연구개발비는 구강질환 개선제품, 조직재생용 바이오소재, 펩타이드 제품군, 화장품군의 각 분야 연구개발에 사용되고 있으며, 이에 따른 당사 제품의 특징, 개발단계, 수익창출계획은 다음과 같습니다. 또한 당사가 정부보조금을 받아 정부과제를 수행한 실적은 다음과 같습니다.
| [당사의 전제품 파이프라인] |
|
제품군 |
분야 |
당사 제품명 |
특징 |
개발단계 |
수익창출 계획 |
|---|---|---|---|---|---|
|
펩타이드 |
펩타이드 기반 |
OssGen-X15 |
펩타이드 함유 |
허가완료 |
매출화 |
|
OssGen-X15 Gel |
펩타이드 함유 |
시제품제작 임상준비 |
매출 예정 |
||
|
OssGen Ortho |
펩타이드 함유 |
전임상 진입 준비 단계 |
매출 예정 |
||
|
펩타이드 치료제 |
OsseoTide |
골다공증 치료제 |
전임상 완료, |
임상1상 완료 후 기술이전 예정 |
|
| NIPEP-Care 1 |
관절염치료제염증성장질환치료제 |
전임상 진입 준비 단계 |
임상1상 완료 후 기술이전 예정 |
||
| NIPEP-Care 2 |
비알콜성지방간염치료제 |
전임상 진입 준비 단계 |
임상1상 완료 후 기술이전 예정 |
||
| NIPEP-Care 3 |
염증성장질환치료제 |
전임상 진입 준비 단계 |
임상1상 완료 후 기술이전 예정 |
||
|
NIPEP-ACD-TIDE |
항암치료제 |
전임상 진입준비 단계 |
전임상 완료 후 기술이전 예정 |
||
|
펩타이드 기반 |
OssGen better |
PTH 골다공증바이오베터 |
전임상 진행중 |
임상1상 완료 후 기술이전 예정 |
|
|
펩타이드 플랫폼 |
TOPscovery |
세포내 단백질(항체) 전달시스템 |
- |
플랫폼 서비스제공, 기술이전 예정 |
|
|
조직재생용 |
치과용 골이식재 |
OCS-B, |
잇몸뼈 재생 |
허가완료 |
매출화 |
|
치주조직재생용쉬트 |
GuidOss |
치주조직 재생 |
허가완료 |
매출화 |
|
|
Xeno-Gide |
치주조직 재생 |
허가 진행중 |
매출예정 |
||
| 흡수성치주조직 재생유도재 |
Regenomer |
치주 재생 |
허가완료 |
매출화 |
|
|
Regenomatrix Tape, Cote |
치주 재생 |
허가 진행중 |
매출예정 |
||
| 골이식용 복합재료 |
OCS-B Collagen, Equimatrix Collagen |
콜라겐 함유 골이식재 |
허가완료 |
매출화 |
|
|
구강질환 |
개인용 치아미백제 |
Dr.Whitiss (8.6%) |
치아미백 |
허가완료 |
매출화 |
|
전문가용 치아미백제 |
BlancTis Pro (10%) BlancTis Clinic(15%) |
치아미백 |
매출화 | ||
|
시린이 치료제 |
SensBlok |
시린이 치료 |
매출화 | ||
|
치과용 컨디셔너 |
Clinplant Syringe/Floss |
치태제거, 치은염, 치주염, |
매출화 | ||
|
치주질환치료제 |
MinoCure |
치은염, 치주염 치료 |
매출화 | ||
|
구강케어치약 |
Dr.BlancTis Phosphate |
천연성분치약 |
매출화 | ||
|
화장품 |
기능성화장품 |
펩타이드 화장품 원료 |
항노화, 염증억제, 미백등 |
ICID 등재 완료 |
매출예정 |
|
Dr.MyYou |
미백, 주름 개선 |
개발완료 |
매출화 |
||
|
Eustella Complex Solution |
항노화 기능 |
재생기능성 펩타이드 국제화장품 원료규격집 (ICID) 등재 완료 |
매출화 |
||
|
Estella AC Solution |
여드름 및 염증 억제 화장품 |
항염증 기능성 펩타이드 국제화장품 원료규격집 (ICID) 등재 완료, 피부임상시험완료 |
매출 예정 |
(참조 5) - 정정 전
당사가 영위하고 있는 의약품 및 의료기기 산업은 장기간 연구개발을 통해 기술을 축적한 기업만이 진출할 수 있는 전문시장으로써 고급인력을 통한 지식활용이 필수적으로 요구되고 있습니다. 따라서 우수인력의 확보가 시장경쟁요소에 중요한 요소로 작용합니다. 당사는 2019년 3월 말일기준 전 직원 66명중 총 29명(박사 2명, 박사수료 1명, 석사 10명, 학사 14명, 기타 2 )의 연구개발 인력을 보유하고 있습니다.
| [연구인력 현황] |
|
구분 |
업무 |
인원수 |
|---|---|---|
|
연구소장 |
연구소 총괄, 프로젝트 진행관리, 신규 프로젝트 발굴 |
1 |
|
신제품개발팀 |
제품 연구설계 및 신제품 개발 관련 업무 |
4 |
|
펩타이드개발팀 |
보유 파이프라인 관련 실험 및 연구개발 업무 |
8 |
|
효능평가팀 |
신제품 및 후보물질 등 효능 평가 업무 |
5 |
|
품질관리팀 |
품질검사 업무, 품질 개선 업무, 공정관리 업무 |
7 |
|
품질보증팀 |
소비자가 요구하는 품질 만족을 보증하기 위한 전반적 업무 |
4 |
일반적으로 업계 연구 인력들의 특성이 학계나 국가 연구원 등에서 근무하는 것을 선호하고 있으며, 개인적인 학업 증진을 위한 해외유학 등의 사유로 핵심연구 인력의 이탈이 발생할 수 있습니다. 따라서 당사는 핵심 연구인력의 관리 및 확보를 위하여
핵심인력을 위한 차별화된 대우와 보상(특별 인센티브)을 실시하여 성과와 능력에 따라 승진이 가능하도록 조치하는 한편, 핵심인력이 보유한 능력 및 핵심역량을 육성하기 위한 지속적인 교육을 지원하고 있습니다. 향후에는 핵심인력의 경쟁력을 배가하기 위한 인적자원 관리프로그램을 구축할 예정이며, 국내 대학원 진학, 해외파견 등의 자기개발 프로젝트 또한 운영할 예정입니다. 그러나 이와 같은 각종 보상책에도 불구하고 핵심인력의 이탈 가능성을 배제할 수는 없는 상황입니다. 실제로 상기 노력을 바탕으로 2017년초 26명에 비하여 2019년 현재 연구인력이 29명으로 3명 증가하였으나, 2017년부터 2019년 현재까지 총 16명이 퇴사하였으며, 펩타이드개발팀에서 총 4명이 퇴사하였습니다.
| [연구인력 변동현황] |
|
구분 |
업무 |
2017년 |
2018년 |
2019년 현재 |
구분 |
|||
|---|---|---|---|---|---|---|---|---|
|
부서 |
기초 |
입사 |
퇴사 |
입사 |
퇴사 |
입사 |
퇴사 |
기말 |
|
연구소장 |
1 |
1 |
||||||
|
신제품개발팀 |
3 |
1 |
2 |
4 |
||||
|
펩타이드개발팀 |
2 |
4 |
2 |
5 |
2 |
1 |
8 |
|
|
효능평가팀 |
4 |
1 |
1 |
1 |
5 |
|||
|
품질관리팀 |
12 |
3 |
5 |
2 |
4 |
1 |
7 |
|
|
품질보증팀 |
4 |
|
|
|
4 |
|||
|
합 계 |
26 |
7 |
7 |
8 |
8 |
4 |
1 |
29 |
(참조 5) - 정정 후
당사가 영위하고 있는 의약품 및 의료기기 산업은 장기간 연구개발을 통해 기술을 축적한 기업만이 진출할 수 있는 전문시장으로써 고급인력을 통한 지식활용이 필수적으로 요구되고 있습니다. 따라서 우수인력의 확보가 시장경쟁요소에 중요한 요소로 작용합니다. 당사는 증권신고서 작성일 기준 전 직원 66명중 총 31명(박사 3명, 석사 13명, 학사외 15명)의 연구개발 인력을 보유하고 있습니다.
| [연구인력 현황] |
| (단위 : 명) |
|
구 분 |
인 원 |
||||
|---|---|---|---|---|---|
|
박 사 |
석 사 |
학사 외 |
합 계 |
||
|
첨단소재개발 |
신제품개발팀 |
- |
3 |
1 |
4 |
|
펩타이드개발팀 |
2 |
6 |
1 |
9 |
|
|
효능평가팀 |
- |
1 |
4 |
5 |
|
|
바이오소재 연구팀 |
바이오소재 개발팀 |
1 |
1 |
3 |
4 |
|
바이오소재 최적화, 상용화연구팀 |
- |
2 |
6 |
8 |
|
|
합 계 |
3 |
13 |
15 |
31 |
|
이 중 당사의 핵심 연구인력은 대표이사인 정종평, 연구소 전반의 총괄업무를 담당하고 있는 전무이사 박윤정, 중앙연구소 및 프로젝트 총괄업무를 담당하는 연구소장 이주연등 입니다. 대표이사인 정종평은 서울대학교 치과대학에서 치주학을 전공한 박
사로 치주염증을 비롯한 치과 분야 관련 연구를 계속해왔으며, 치과 임상의로서 다양
한 환자 케이스를 통하여 나이벡의 기반사업인 조직재생용바이오소재 연구개발에 이
바지 하였으며 R&D 및 경영총괄을 맡고 있습니다. 또한 연구소의 총괄업무를 담당
하는 박윤정 전무이사는 현재 서울대학교 치의학대학원 교수 재직중으로 당사의 연구개발 관련 산학협력활동 및 우수한 연구적 네트워크를 구축, 활용하여 우수한 양질의 연구 결과 도출에 이바지하였습니다. 박윤정 전무이사와 중앙연구소 프로젝트 총괄업무를 담당하는 이주연이사는 약학을 전공한 약학박사로 펩타이드를 이용한 약물전달시스템을 비롯한 펩타이드 기반 바이오 의약품 개발 관련하여 다수의 논문 및 특허, 그리고 영향력 있는 바이오 학회 초청 발표 등 활발한 연구 활동을 계속해오고 있는 당사의 핵심인력입니다.
|
<핵심 연구인력 현황> |
||||
|---|---|---|---|---|
|
직 위 |
성 명 |
담당업무 |
주요 경력 |
주요 연구실적(대표논문 5건) |
|
대표이사 |
정종평 |
총괄업무 |
서울대학교 치과대학 치의학 석사(72.02) 서울대학교 치과대학 치의학 박사(79.02) 미국뉴욕주립대학교 교환교수(82.12) 서울대학교 치과대학 교수(11.02) 서울대학교 치과대학 학장(02.02) 지능형생체게면공학 연구센터 센터장(09.03) |
The effect of the surface modification of titanium using a recombinant fragment of fibronectin and vitronectin on cell behavior, Biomaterials (26(25), 5153-5157), 2005
Electrospinning of chitin nanofibers: Degradation behavior and cellular response to normal human keratinocytes and fibroblasts, Biomaterials (27(21), 3934-3944). 2006
Assembly of collagen-binding peptide with collagen as a bioactive scaffold for osteogenesis in vitro and in vivo, Biomaterials (28(29), 4257-4267), 2007
Osteoblastic differentiation of human bone marrow stromal cells in self-assembled BMP-2 receptor-binding peptide-amphiphiles, Biomaterials. (30(21), 3532-3541), 2009
Peptide-mediated intracellular delivery of miRNA-29b for osteogenic stem cell differentiation, Biomaterials. 34(17):4347-59, 2013 |
|
전무이사 |
박윤정 |
연구소 전반 총괄업무 |
이화여자대학교 약학 석사(95.02) 이화여자대학교 약제학 박사(99.02) 미시간대학 약학대학 연구원(02.02) 미시간대학 약학대학 연구교수(03.05) 서울대학교 치의학대학원 교수(현재)
|
Intracellular delivery of cell-penetrating peptide-transcriptional factor fusion protein and its role in selective osteogenesis, Int J Nanomedicine. 9:1153-66, 2014
Simultaneous imaging and restoration of cell function using cell permeable peptide probe, Biomaterials. 35(24):6287-98, 2014
Selective osteogenesis by a synthetic mineral inducing peptide for the treatment of osteoporosis, Biomaterials. 35(37):9747-54, 2014
Identification of cell-penetrating peptide domain from human beta-defensin 3 and characterization of its anti-inflammatory activity, Int J Nanomedicine. 26;10:5423-34., 2015
Dual-function synthetic peptide derived from BMP4 for highly efficient tumor targeting and antiangiogenesis, nt J Nanomedicine. 11;4643-4656, 2016 |
|
이사 (연구소장) |
이주연 |
중앙연구소 프로젝트 총괄업무 |
이화여자대학교 약학 석사(00.02) 이화여자대학교 약제학 박사(04.02) 서울대학교 치과대학 지능형생체계면공학연구센터(IBEC) Post-Doctoral Research Fellowship |
Identification of cell-penetrating peptide domain from human beta-defensin 3 and characterization of its anti-inflammatory activity, Int J Nanomedicine. 26;10:5423-34., 2015
Dual-function synthetic peptide derived from BMP4 for highly efficient tumor targeting and antiangiogenesis, nt J Nanomedicine. 11;4643-4656, 2016
Control of cancer stem cell like population by intracellular target identification followed by the treatment with peptide-siRNA complex, Biochem Biophys Res Commun, 491(3):827-833, 2017
Comparative Study of rhPDGF-BB Plus Equine-Derived Bone Matrix Versus rhPDGF-BB Plus β-TCP in the Treatment of Periodontal Defects, Int J Periodontics Restorative Dent, 37(6):825-832, 2017
A novel calcium-accumulating peptide/gelatin in situ forming hydrogel for enhanced bone regeneration, J Biomed Mater Res A, 106(2):531-542, 2018 |
일반적으로 업계 연구 인력들의 특성이 학계나 국가 연구원 등에서 근무하는 것을 선호하고 있으며, 개인적인 학업 증진을 위한 해외유학 등의 사유로 핵심연구 인력의 이탈이 발생할 수 있습니다. 따라서 당사는 핵심 연구인력의 관리 및 확보를 위하여
핵심인력을 위한 차별화된 대우와 보상(특별 인센티브)을 실시하여 성과와 능력에 따라 승진이 가능하도록 조치하는 한편, 핵심인력이 보유한 능력 및 핵심역량을 육성하기 위한 지속적인 교육을 지원하고 있습니다. 향후에는 핵심인력의 경쟁력을 배가하기 위한 인적자원 관리프로그램을 구축할 예정이며, 국내 대학원 진학, 해외파견 등의 자기개발 프로젝트 또한 운영할 예정입니다. 그러나 이와 같은 각종 보상책에도 불구하고 핵심인력의 이탈 가능성을 배제할 수는 없는 상황입니다. 실제로 상기 노력을 바탕으로 2017년초 26명에 비하여 2019년 현재 연구인력이 31명으로 5명 증가하였으나, 2017년부터 2019년 현재까지 총 16명이 퇴사하였으며, 펩타이드개발팀에서 총 4명이 퇴사하였습니다.
| [연구인력 변동현황] |
|
구분 |
2016년 |
2017년 |
2018년 |
2019년 현재 |
2019년 현재기준 |
|||
|---|---|---|---|---|---|---|---|---|
|
부서 |
입사 |
퇴사 |
입사 |
퇴사 |
입사 |
퇴사 |
||
|
신제품개발팀 |
3 |
- | - | - |
1 |
2 |
- |
4 |
|
펩타이드개발팀 |
2 |
4 |
2 |
5 |
2 |
1 |
- |
9 |
|
효능평가팀 |
4 |
- | - |
1 |
1 |
1 |
- |
5 |
| 바이오소재개발팀 |
12 |
3 |
5 |
2 |
4 |
- |
1 |
5 |
| 바이오소재 최적화, 상용화연구팀 |
4 |
- |
- |
- |
- |
- | - |
8 |
|
합 계 |
28 |
7 |
7 |
8 |
8 |
4 |
1 |
31 |
(참조 6) - 정정 후
일반적으로 신약개발은 후보물질 발굴까지의 연구단계와 비임상시험부터 임상시험까지의 개발단계, 그리고 최종 제품으로 판매하기 위한 허가 및 생산, 마케팅 단계로 나눌 수 있습니다. 각 국가의 규제 당국이 제시하는 단계에 따라 비임상 독성 시험, 임상 시험 (1, 2, 3상), 시판 승인 절차를 거쳐 최종적으로 판매되기까지는 오랜 시간과 많은 비용이 소요되며, 많은 시간과 비용을 투자하였더라도 최종 제품으로 개발이 되는 비율은 매우 낮습니다. 이러한 특성상 많은 바이오중소기업들은 일부 파이프라인에 대해서는 기술이전을 사업모델로 하고 있습니다.
| [2018 국내 제약바이오기업 기술수출 현황] |
| [단위 : 만 USD] |
| 일자 | 회사명 | 제품명 | 계약업체명 | 계약규모 | 계약금 |
|---|---|---|---|---|---|
| 1 | 동아에스티 | DA-9801(당뇨병성신경병증) | 뉴로브파마슈티컬스(미국) | 18,000 | 200 |
| 2 | SK케미칼 | 인틀루엔자백신 생산기술 | 사노피파스퇴르(프랑스) | 15,500 | 1,500 |
| 3 | 크리스탈지노믹스 | CG026806(급성골수성백혈병) | 앱토즈바이오사이언스(미국) | 12,500 | 300 |
| 4 | ABL바이오 | 항암항체신약물질 5종 | TRIGR테라퓨틱스(미국) | 55,000 | 430 |
| 5 | 유한양행 | YH4618(디스크치료제) | 스파인바이오파마(미국) | 21,815 | 65 |
| 6 | JW중외제약 | JW1601(아토피치료제) | 레오파마(덴마크) | 4,200 | 1700 |
| 7 | 앱클론 | AC101(위암 유방암) | 상하이헬리우스바이오텍(중국) | 125,500 | 5,000 |
| 8 | 유한양행 | YH25448(폐암신약) | 얀센바이오텍(미국) | 4,000 | 1,000 |
| 9 | 코오롱생명과학 | 인보사(골관절염치료제) | 먼디파마케이케이(일본) | 59,160 | 2,665 |
| 10 | 인트론바이오 | SAL200(슈퍼박테리아치료제) | 로이반트사이언스(미국) | 66,750 | 1,000 |
| 11 | 크리스탈지노믹스 | 아셀렉스(비스테로이드진통제) | 팜아티스인터내셔날(러시아) | 10,574 | 10 |
| 12 | 에이비엘바이오 | NOV1501(이중항체) | TRIGR테라퓨틱스(미국) | 59,500 | 500 |
2018년 유한양행, 동아에스티, JW중외제약, SK케미칼과 같은 대형제약사는 물론이고 크리스탈지노믹스, 에이비엘바이오, 앱클론, 인트론바이오같은 바이오벤처들도 잇따라 기술수출에 성공하였습니다. 이는 국내기업들의 기술력은 높아지면서 신약개
발의 가능성은 많아지고 있지만 현실적으로 국내에서 이 모든 신약개발 과정을 진행하기가 쉽지 않은 상황때문입니다. 하나의 신약개발에는 평균 10년이라는 개발기간과 신약이 제품으로 출시되기 까지는 조 단위에 해당하는 비용이 필요합니다. 그중 비용의 상당부분을 차지하는 임상시험의 진행은 한 기업이 자체적으로 진행하기에는 어려운것이 현실입니다. 또한 최근 개발되는 신약들은 대부분 글로벌시장을 목표로 하기때문에 다국가 임상이 거의 필수로 여겨지고 있습니다. 이때문에 국내에서만 진행되는 임상에 비해 규모도 크고 환자 모집과정등도 쉽지 않습니다. 이와같은 이유로국내 기업들은 임상 초기단계에서 인프라를 구축한 글로벌 제약사 또는 글로벌 의료기기 업체와 협업하는 경우가 많습니다.
당사는 현재 치과분야에 한정하여 스위스의 Straumann사와 2017년 펩타이드 치과 응용기술 이전 계약을 통해 안정적인 미래 파이프라인 공급 및 신개발 제품의 공급관련 전략적 제휴에 합의한 바 있습니다. 제품에 대한 공동개발을 위한 투자유치를 현재 진행하고 있으며 투자규모 및 방법에 대해서 현재 논의 중에 있습니다.
| <라이센스아웃 계약 총괄표> |
| (단위: 백만원) |
|
품 목 |
계약상대방 |
대상지역 |
계약체결일 |
계약종료일 |
총계약금액* |
수취금액* |
진행단계 |
|---|---|---|---|---|---|---|---|
|
펩타이드 플랫폼 |
Straumann |
전세계 (한국제외) |
2017.03.21 |
각 제품별 및 국가별로 선정된 "제품 출시후 10년" 또는 "특허만료일"중 긴 기간 |
- |
1,125 |
제품개발 논의중 |
|
합 계 |
- |
1,125 |
|||||
주) 초기 기술료를 계약금으로 받았으며 추후 계약에 따라 총계약금액이 정해질 예정입니다.
주2) 외화금액은 최초 공시서류 작성기준일 환율로 환산
| [당사가 개발하는 기술이전 예정 펩타이드기반 파이프라인의 개발 현황] |
|
분야 |
당사 제품명 |
특징 |
세부구분 |
현재 개발단계 |
수익창출 계획 |
|---|---|---|---|---|---|
|
펩타이드 치료제 |
OsseoTide |
골다공증 치료제 |
오리지날 |
전임상 완료, |
임상1상 완료 후 2021년 기술이전 목표 |
| NIPEP-Care 1 |
관절염치료제염증성장질환치료제 |
오리지날 |
전임상 진입 준비 단계 |
임상1상 완료 후 2022년 기술이전 목표 |
|
| NIPEP-Care 2 |
비알콜성지방간염치료제 |
오리지날 |
전임상 진입 준비 단계 |
임상1상 완료 후 2023년 기술이전 목표 |
|
| NIPEP-Care 3 |
염증성장질환치료제 |
오리지날 |
전임상 진입 준비 단계 |
임상1상 완료 후 2023년 기술이전 목표 |
|
|
NIPEP-ACD-TIDE |
항암치료제 |
오리지날 |
전임상 진입준비 단계 |
전임상 완료 후 |
|
|
펩타이드 기반 |
OssGen better |
PTH 골다공증바이오베터 |
바이오베터 |
전임상 진행중 |
임상1상 완료 후 2024년 기술이전 목표 |
|
펩타이드 플랫폼 |
TOPscovery |
세포내 단백질(항체) 전달시스템 |
- |
- |
플랫폼 서비스제공, |
또한 펩타이드 기반한 신약관련(골다공증, 관절염, 항암, 비알콜성지방간염, 염증성 장질환 등)하여, A사를 비롯한 총 네곳의 국내외 제약사와 NDA를 체결하였으며, 이에대한 기술이전에 관한 논의를 계속해서 진행 중에 있니다. 펩타이드기반 바이오베터인 골다공증바이오베터는 전임상을 진행중에 있으며 임상1상 완료후 기술이전을 예상하고 있고,세포내 단백질(항체)를 전달할수있는 기능을 가진 펩타이드플랫폼을 이용하여 기술이전 또는 당사의 펩타이드플랫폼을 사용할수있는 서비스를 제공하여 수익창출할 계획에 있습니다. 이러한 당사의 기술이전계획이 성사될시 일시적으로 수익이 크게 증가할 것으로 기대되고 있습니다.
당사는 당사의 파이프라인에 대해 해외의 다양한 파트너사와 기술이전에 대해 논의하고 있습니다. 파트너사의 임상수행능력, 회사 규모등을 판별하여 기술이전을 시행할 계획이나 당사의 계획과 달리 파트너사와의 협의가 원활히 이루어지지 않아 기술이전 계약이 취소되거나 규모가 축소될 경우 사업에 부정적인 영향이 생길수 있으니 투자자분들께서는 이점 유의하시기 바랍니다.
(참조 7) - 정정 전
당사는 2011년 기술특례상장을 통해 코스닥 시장에 입성한 후 2013년까지 주력 제품이었던 골이식재의 매출 부진 및 해외시장 진출을 위한 인증비용, 시설투자로 인한 감가상각비로 인해 손실이 지속되었습니다. 이후 회사의 새로운 성장동력을 위하여 2014년 홈쇼핑 영업채널을 통해 치아미백제를 판매하면서 매출액이 약 50억원대로 증가하였으나, 높은 수수료와 부가적인 판촉상품때문에 수익성대비 판관비의 비중이 높은 저마진 구조로 인해 -30.3억원의 당기순손실이 발생하였습니다. 2015년에는 마진률이 낮은 치아미백제 판매를 감소시켰으며, 치과용골이식재 매출에 주력하였으며, 화장품 사업을 새로 실시함으로써 전년대비 당기순이익이 약 -12.0억원 감소하였습니다.
(중 략)
당사는 상기 기재된 바와 같이 2011년부터 지속적으로 당기순손실이 이어지고 있으며, 이로 인하여 2018년말 기준 232.3억원의 결손금이 계상되어 있습니다. 그러나 매년 매출액의 약 40~60%의 연구개발비를 사용하면서 누적된 연구개발진들의 기술력과 글로벌 임플란트 업체들로부터의 당사 기술력에 대한 신뢰 향상은 향후 당사의 영업에 긍정적인 요소로 작용할 것으로 기대되고 있습니다. 당사는 다음과 같이 수익성 향상을 위하여 계획하고 있습니다.
1) 대규모 공급계약 체결건
가) Straumann 치과용 골재생 바이오소재 및 콜라겐 바이오소재 대규모 공급계약
당사는 2019년 02월 Staumann과 치과용 골재생 바이오소재 및 콜라겐 바이오소재 등 품목계약의 건으로 수시공시의무관련사항(공정공시)을 공시한 바 있습니다. 상기
공급계약 건은, 총 계약규모 22,000,000CHF으로 약 한화 246.8억원에 따르는 규모이며, 2018년 매출액 대비 473.8%입니다. 이는 기존 치과용 골이식재 파트 외에 구강케어 파트, 콜라겐 파트 등 다양한 품목을 대상으로 한 계약으로 다소 침체되어 있던 구강케어 파트도 성장성을 보일 것으로 기대하고 있습니다.
나) Nobel Biocare 치과용 골이식재의 추가 공급계약
Nobel Biocare와의 기존 계약금액은 6,484천USD이었으며, 2019년 2월 20일 기준 이행금액은 4,716천USD으로 약 73% 이행하였습니다. 금번 계약변경으로 7,442천USD가 증가되어 총 계약금액은 13,926천USD입니다. 남아있던 수주 및 추가 계약으로 인한 수주를 합할 시 2018년 매출액 대비 201.2%에 해당하는 규모입니다, 금번 계약은 2021년 12월 31일까지 납품이며, 2021년에 재계약 체결 시 수주 규모는 더욱 커질 것으로 예상하고 있습니다.
상기 두가지의 대규모 공급계약 체결로 인하여 2019년도부터의 제품 매출 성장은 큰 폭으로 상향될 것으로 기대되고 있습니다. 또한 상기 두 건의 계약은 모두 자동연장되는 계약의 형태이며, 치과용골이식재를 비롯한 치과용 의료기기 제품들은 사용했던 제품들만 사용하는 충성도가 높은 제품군으로, 당사에 CashCow가 될 것으로 전망되고 있습니다.
2) 펩타이드 치료제 개발을 위한 투자 유치
당사는 스위스의 Straumann사와 2017년 펩타이드 치과 응용기술 이전 계약을 통해 안정적인 미래 파이프라인 공급 및 신개발 제품의 공급관련 전략적 제휴에 합의한 바 있습니다. 제품에 대한 공동개발을 위한 투자유치를 현재 진행하고 있으며 투자규모 및 방법에 대해서 현재 논의 중입니다.
3) 펩타이드 기반 연구개발 성과 기술이전
펩타이드 기반한 신약관련(골다공증, 관절염, 항암, 비알콜성지방간염, 염증성 장질환 등)하여, A사를 비롯한 총 네곳의 국내외 제약사와 NDA를 체결하였으며, 이에대한 기술이전에 관한 논의를 계속해서 진행 중에 있습니다. 기술이전에 대한 체결이 완료될 시 일시적으로 수익이 크게 증가할 것으로 기대되고 있습니다.
(참조 7) - 정정 후
당사는 2011년 기술특례상장을 통해 코스닥 시장에 입성한 후 2013년까지 주력 제품이었던 골이식재의 매출 부진 및 해외시장 진출을 위한 인증비용, 시설투자로 인한 감가상각비로 인해 손실이 지속되었습니다. 이후 회사의 새로운 성장동력을 위하여 2014년 홈쇼핑 영업채널을 통해 치아미백제를 판매하면서 매출액이 약 50억원대로 증가하였으나, 높은 수수료와 부가적인 판촉상품때문에 수익성대비 판관비의 비중이 높은 저마진 구조로 인해 36.2억원의 당기순손실이 발생하였습니다. 2015년에는 마진률이 낮은 치아미백제 판매를 감소시켰으며, 치과용골이식재 매출에 주력하였으며, 화장품 사업을 새로 실시함으로써 전년대비 당기순손실이 약 12.0억원 감소하였습니다.
(중 략)
당사는 상기 기재된 바와 같이 2011년부터 지속적으로 당기순손실이 이어지고 있으며, 이로 인하여 2018년말 기준 232.3억원의 결손금이 계상되어 있습니다. 그러나 매년 매출액의 약 40~60%의 연구개발비를 사용하면서 누적된 연구개발진들의 기술력과 글로벌 임플란트 업체들로부터의 당사 기술력에 대한 신뢰 향상은 향후 당사의 영업에 긍정적인 요소로 작용할 것으로 기대되고 있습니다. 또한 당사는 대규모 공급계약 체결을 통하여 수익성 향상을 위한 계획을 진행 중에 있습니다.
가) Straumann 치과용 골재생 바이오소재 및 콜라겐 바이오소재 대규모 공급계약
당사는 2019년 02월 Staumann과 치과용 골재생 바이오소재 및 콜라겐 바이오소재 등 품목계약의 건으로 수시공시의무관련사항(공정공시)을 공시한 바 있습니다.
| 구 분 | 내 용 |
|---|---|
| 공정공시 대상정보 | 치과용 골재생 바이오소재 및 콜라겐 바이오소재 등 품목계약의 건 |
| 계약기간 | 2019년 2월 21일 ~ 2024년 2월 20일 (5년간) |
| 계약품목 | OCS-B, OCS-B Collagen, GuidOss, Regenomer, Clinplant |
| 계약규모 | (1) Contract Year 1 : 2,000,000CHF (2) Contract Year 2 : 3,000,000CHF (3) Contract Year 3 : 4,500,000CHF (4) Contract Year 4 : 5,500,000CHF (5) Contract Tear 5 : 7,000,000CHF 총 계약규모 : 22,000,000CHF (한화 24,677,400,000원) (적용환율은 계약일 최초고시 환율인 1,121.70원을 적용) |
| 기타 | 상기 계약규모는 Straumann이 제시한 예상 계약규모이며, 발주사항이 기재된 발주서에 의해 확정됨 |
상기 공급계약 건은 계약기간이 총 5년으로 1년째 2,000,000CHF, 2년째 3,000,000CHF, 3년째 4,500,000CHF, 4년째 5,500,000CHF, 5년째 7,000,000CHF로 총 계약규모가22,000,000CHF(약 한화 246.8억원)이며, 2018년 매출액 대비 473.8%입니다. 이는 기존 치과용 골이식재 파트 외에 구강케어 파트, 콜라겐 파트 등 다양한 품목을 대상으로 한 계약으로 다소 침체되어 있던 구강케어 파트도 성장성을 보일 것으로 기대하고 있습니다.
(참조 8) - 정정 전
| [최근 3년간 당사 안정성비율 추이] |
| (단위 : 백만원,%, 회) |
| 과목 | 2018년 | 2017년 | 2016년 |
|---|---|---|---|
| 부채비율 | 111.44% | 108.31% | 133.40% |
| 차입금 총계 | 7,823 | 9,392 | 9,527 |
| - 단기차입금 | 870 | 920 | 420 |
| - 유동성장기차입금 | 1.606 | 1,087 | 1,077 |
| - 장기차입금 | 852 | 898 | 1,556 |
| - 사채 | - | 4,012 | 5,141 |
| - 유동성 사채 | 4,495 | 2,474 | 1,332 |
| 차입금의존도 | 35.05% | 36.47% | 41.48% |
(참조 8) - 정정 후
| [최근 3년간 당사 안정성비율 추이] |
| (단위 : 백만원,%, 회) |
| 과목 | KB증권 단기차입금 유입에 따른 시나리오 | 2018년 | 2017년 | 2016년 | |
|---|---|---|---|---|---|
| 5회차 전환사채 상환청구 시 | 5회차 전환사채 미상환 시 | ||||
| 부채비율 | 153.62% | 196.12% | 111.44% | 108.31% | 133.40% |
| 차입금 총계 | 12,328 | 15,219 | 7,823 | 9,392 | 9,527 |
| - 단기차입금 | 9,870 | 9,870 | 870 | 920 | 420 |
| - 유동성장기차입금 | 1.606 | 1.606 | 1.606 | 1,087 | 1,077 |
| - 장기차입금 | 852 | 852 | 852 | 898 | 1,556 |
| - 사채 | - | - | - | 4,012 | 5,141 |
| - 유동성 사채 | - | 4,495 | 4,495 | 2,474 | 1,332 |
| 차입금의존도 | 45.96% | 48.59% | 35.05% | 36.47% | 41.48% |
주) 부채비율 = 부채총계 / 자본총계
주2) 차입금의존도 = 부채총계 / 자산총계
주3) KB증권 단기차입금 유입에 따른 시나리오는 2018년말 재무제표에 단기차입에 따른 자금을 단순 계산한 시나리오로, 실제 자금유입일 기준으로 계산할 시 다를 수 있습니다.
(참조 9) - 정정 후
또한, 당사는 증권신고서 제출일 현재 상환 또는 전환이 이루어지지 않은 제5회 사모 전환사채 46.5억원을 보유하고 있으며, 해당 전환사채의 전환권이 행사 될 경우 최대 465,279주가 잠재적으로 더 증가할 수 있습니다. 현재 당사 주가 하락 등의 이유로 전환권 행사 가능성은 제한적으로 판단되나, 만일 전환이 이루어 질 경우 주식수 증가에 따른 주가 희석이 발생하여 주가가 단기적으로 하락할 수 있으므로 이 점 유의하시기 바랍니다.
| [당사 주식관련사채 발행 현황] |
| (단위 : 백만원, 주) |
|
구분 |
발행일 |
만기일 |
권면 |
이자율 (표면이자율/ 만기이자율) |
조기상환 |
전환청구 |
전환조건 |
미상환사채 |
사채권자 | ||
|---|---|---|---|---|---|---|---|---|---|---|---|
|
전환비율 |
전환 |
권면총액 |
전환가능 |
||||||||
|
제5회 사모 |
17.12.26 |
20.12.26 |
5,000 |
0.0%/4.0% | 19.12.26 ~ 20.09.26 |
18.12.26 ~ 20.11.26 |
100 |
9,994 | 4,650 | 465,279 | 코리아에셋클래식메자닌전문투자형 사모투자신탁제2호 코리아에셋클래식멀티스트래티지 전문투자형사모투자신탁제1호 |
주1) 전환사채권면총액 50억원중 3.5억원(35,021주/주당 9,994원)의 전환청구로 인해 2019년 3월 25일 주식으로 전환되어 상장되었습니다.
(참조 10) - 정정 전
3. 기업실사 일정 및 주요 내용
| 일자 | 실사 내용 |
|---|---|
| 2019.02.18 | * 발행회사 초도 방문 - 발행회사의 유상증자 의사 확인 - 자금조달 희망금액 등 발행회사 의견 청취 |
| 2019.02.19 ~ 2019.02.28 |
* 발행회사의 유상증자 방식결정 협의 * 유상증자 일정 협의 및 확정 * 유상증자를 위한 사전 준비사항 및 진행절차 설명 - 발행가 산정 및 세부일정 설명 * 세부 증자관련 논의 - 유상증자 방식 결정 및 대주주 증자 참여 논의 * 유상증자 진행에 대한 질의/응답 * 실사 사전요청자료 송부 |
| 2019.03.04 ~ 2019.04.01 |
* 증자리스크 검토 - 발행시장 상황, 자금조달규모 적정성, 공모가액 희망 할인율 * 발행사와의 협의 - 발행가액 산정방식, 발행일정, 발행규모, 인수수수료 협의 * 기업실사 진행 및 추가자료 요청 - 기업실사 관련 자료요청 및 절차에 대한 설명 - 기업실사 관련 Q&A * 이사회 등 상법 절차 및 정관 등 검토 * 투자위험요소 실사 1) 사업위험관련 실사 - 기존사업 및 신규사업에 대한 세부사항 등 체크 2) 회사위험관련 실사 - 재무관련 위험 및 우발채무 등의 위험요소 등 체크 3) 기타위험관련 실사 - 주가 희석화관련 위험 등 체크 * 담당자 인터뷰 - 회사개요, 사업의 내용, 주요 재무적 이슈 확인 - 자금사용 계획 파악 - 향후 사업추진계획 및 발행회사의 비전 검토 |
| 2019.04.02 |
* 증권신고서 작성 및 조언 * 이사회의사록 등 검토 * 인수계약서 체결 * 증권신고서 인수인의 의견 완료 * 첨부서류 등 검토 * 증권신고서 업데이트 |
(참조 10) - 정정 후
3. 기업실사 일정 및 주요 내용
| 일자 | 실사 내용 |
|---|---|
| 2019.02.18 | * 발행회사 초도 방문 - 발행회사의 유상증자 의사 확인 - 자금조달 희망금액 등 발행회사 의견 청취 |
| 2019.02.19 ~ 2019.02.28 |
* 발행회사의 유상증자 방식결정 협의 * 유상증자 일정 협의 및 확정 * 유상증자를 위한 사전 준비사항 및 진행절차 설명 - 발행가 산정 및 세부일정 설명 * 세부 증자관련 논의 - 유상증자 방식 결정 및 대주주 증자 참여 논의 * 유상증자 진행에 대한 질의/응답 * 실사 사전요청자료 송부 |
| 2019.03.04 ~ 2019.04.01 |
* 증자리스크 검토 - 발행시장 상황, 자금조달규모 적정성, 공모가액 희망 할인율 * 발행사와의 협의 - 발행가액 산정방식, 발행일정, 발행규모, 인수수수료 협의 * 기업실사 진행 및 추가자료 요청 - 기업실사 관련 자료요청 및 절차에 대한 설명 - 기업실사 관련 Q&A * 이사회 등 상법 절차 및 정관 등 검토 * 투자위험요소 실사 1) 사업위험관련 실사 - 기존사업 및 신규사업에 대한 세부사항 등 체크 2) 회사위험관련 실사 - 재무관련 위험 및 우발채무 등의 위험요소 등 체크 3) 기타위험관련 실사 - 주가 희석화관련 위험 등 체크 * 담당자 인터뷰 - 회사개요, 사업의 내용, 주요 재무적 이슈 확인 - 자금사용 계획 파악 - 향후 사업추진계획 및 발행회사의 비전 검토 |
| 2019.04.02 |
* 증권신고서 작성 및 조언 * 이사회의사록 등 검토 * 인수계약서 체결 * 증권신고서 인수인의 의견 완료 * 첨부서류 등 검토 * 증권신고서 제출 |
| 2019.04.12 | * 정정 증권신고서 제출 |
(참조 11) - 정정 전
2) 차입금 상환
당사는 금번 주주배정후실권주일반공모의 대표주관사인 KB증권으로부터 본 증권신고서 제출일로부터 5영업일 이내에 단기차입금 9,000백만원을 차입할 계획이며, 단기차입금은 연구개발비용 및 제5회차 전환사채의 기한의이익상실 가능성에 대비하는데 사용할 계획입니다. 이후 금번 유상증자를 통한 자금 중 9,133백만원(예상 이자 포함, 상환시점에 따라 이자금액은 변동될 수 있음)을 상환 자금으로 사용할 예정입니다.
| [ 단기자금대출의 주요 금융조건 ] |
| 구분 | 내용 |
|---|---|
| 대주 | 케이비증권 |
| 대출금액 | 금 구십억원(\ 9,000,000,000) |
| 차입일 | 증권신고서 제출일(2019년 04월 02일)로부터 5영업일 이내 |
| 만기 | 차입일로부터 6개월 |
| 대출금리 | 고정 (연) 5.90% |
| 자금사용 목적 | 5회차 전환사채의 상환 청구대비 및 연구개발비용 |
| 의무상환 | 유상증자 대금납입 후 3영업일 이내 조기상환 |
3) 연구개발비 사용
당사는 펩타이드 기반 바이오소재의 연구개발을 진행하고 있으며, 금번 주주배정후실권주 일반공모를 통하여 유입되는 자금 중 15,000백만원으로 펩타이드 관련 의약품 및 바이오소재의 연구개발을 위해 사용할 예정이며, 부족한 자금에 대해서는 자체 자금을 사용하여 연구개발을 진행할 계획입니다.
세부적으로 펩타이드 기반 골다공증치료제 임상 1상비용 약 35억원, 펩타이드 기반 관절염 치료제의 전임상 및 1상임상비용에 각각 30억원 및 35억원, 펩타이드 표적항암제 연구개발비 35억원, 비알콜성지방간염(NASH) 연구개발비 30억원, 염증성 장질환 연구개발비 30억원이 소요될 것으로 예상하고 있습니다. 각 Pipeline별 연구개발 현황 및 자금소요계획은 다음과 같습니다. 바이오의약품 임상시험과 관련된 사항 및 위험은 Ⅲ. 투자위험요소.의 1.사업위험 - (마) 부분에 세부적으로 작성하였으니, 이를 참고하시기 바랍니다.
(참조 11) - 정정 후
2) 차입금 상환
당사는 금번 주주배정후실권주일반공모의 대표주관사인 KB증권으로부터 본 증권신고서 제출일로부터 5영업일 이내에 단기차입금 9,000백만원을 차입할 계획이며, 단기차입금은 유상증자 대금 납입 전에 연구개발비용으로 총 3,400백만원이 사용될 예정이며, 제5회차 전환사채의 기한의이익상실 가능성에 대비하는데 총 5,600백만원(미상환 사채 권면총액 4,650백만원 및 이자비용 약 950백만원)이 사용할 계획입니다. 이후 금번 유상증자를 통한 자금 중 9,133백만원(예상 이자 포함, 상환시점에 따라 이자금액은 변동될 수 있음)을 상환 자금으로 사용할 예정입니다.
| [ 단기자금대출의 주요 금융조건 ] |
| 구분 | 내용 |
|---|---|
| 대주 | 케이비증권 |
| 대출금액 | 금 구십억원(\ 9,000,000,000) |
| 차입일 | 증권신고서 제출일(2019년 04월 02일)로부터 5영업일 이내 |
| 만기 | 차입일로부터 6개월 |
| 대출금리 | 고정 (연) 5.90% |
| 자금사용 목적 | 5회차 전환사채의 상환 청구대비 및 연구개발비용 |
| 의무상환 | 유상증자 대금납입 후 3영업일 이내 조기상환 |
| [ 단기자금대출의 세부 자금사용목적 ] |
| 구 분 | 상세 내역 | 금 액 | 비 고 |
|---|---|---|---|
| 5회차 전환사채 상환 대비 자금 |
미상환 사채 권면총액 | 4,650백만원 | 기한의 이익상실 가능성에 대한 대비 |
| 예상 이자비용 | 950백만원 | ||
| 소 계 | 5,600백만원 | ||
| 연구개발비용 | 펩타이드기반 골다공증치료제 임상1상 비용 | 1,000백만원 |
유상증자 대금 납입 전 연구개발비 사용 |
| 펩타이드기반 관절염치료제 전임상 비용 |
1,400백만원 |
||
| 표적항암치료제 효능평가 비용 |
1,000백만원 |
||
| 소 계 | 3,400백만원 | ||
| 합 계 | 9,000백만원 | - | |
3) 연구개발비 사용
당사는 펩타이드 기반 바이오소재의 연구개발을 진행하고 있으며, 금번 주주배정후실권주 일반공모를 통하여 유입되는 자금 중 15,000백만원으로 펩타이드 관련 의약품 및 바이오소재의 연구개발을 위해 사용할 예정이며, 부족한 자금에 대해서는 자체 자금을 사용하여 연구개발을 진행할 계획입니다.
세부적으로 펩타이드 기반 골다공증치료제 임상 1상 진행비용 35억원, 펩타이드 기반 관절염 치료제의 전임상 및 1상임상비용 각각 30억원, 골이식재 및 치주재생유도제 유럽임상비용 10억, 펩타이드 표적항암제 전임상비용 15억원, 비알콜성지방간염(NASH) 치료제와 장질환 치료제 전임상비용 30억원이 소요될 것으로 예상하고 있습니다. 각 Pipeline별 연구개발 현황 및 자금소요계획은 다음과 같습니다. 바이오의약품 임상시험과 관련된 사항 및 위험은 Ⅲ. 투자위험요소.의 1.사업위험 - (마) 부분에 세부적으로 작성하였으니, 이를 참고하시기 바랍니다.
(참조 12) - 정정 전
<펩타이드 의약품의 특징>
|
구 분 |
제조방법 |
안전성 |
체내 안정성 |
투여경로 |
|
저분자 합성물질 |
합성 |
독성이 큼 |
반감기가 김 |
경구, 주사 |
|
단백질 |
발현 |
면역반응 유발 및 장기간 사용시 약효 감소 우려 |
반감기가 짧음 |
주사 |
|
펩타이드 |
합성 |
면역반응 적음 |
반감기가 짧음. |
주사 |
(참조 12) - 정정 후
<펩타이드 의약품의 특징>
|
구 분 |
제조방법 |
특징 |
투여경로 |
|---|---|---|---|
|
저분자 의약품 |
화학합성 |
약효는 강하나, 수용체에 비가역적으로 결합하여 독성이 큼 |
경구, 주사 |
|
단백질 의약품 |
세포배양 및 발현 |
면역반응 유발 및 장기간 사용시 약 효 감소 우려. 세포내 타겟을 가진 경우, 효과가 없음. 세포주 관리가 매우 중요함. |
주사 |
|
유전자 치료제 |
세포배양 |
세포내로 전달하기 위해 바이러스성 벡터 사용. 바이러스에 의한 염증, 암발생 가능성 있음. 비바이러스성 벡터는 전달 효율이 낮으며, 세포에 대한 독성이 있음. |
주사 |
|
세포치료제 |
세포배양 |
세포가 분리정제가 안 될 경우, 예측할 수 없는 부작용이 발생할 수 있음. 품질관리가 어려움. |
주사 |
|
펩타이드 의약품 |
화학합성 |
면역반응 적음. 수용체에 대한 가역적 결합 및 활성 조절 가능. 품질관리가 용이함. |
경구투여 제형으로 개발 가능. 주사 |
(참조 13) - 정정 전
| (2018년 12월 31일 현재) | (단위 :천미불 ) |
| 품목 | 발주처 | 수주일자 | 납기일자 | 수주총액 | 기납품액 | 수주잔고 |
|---|---|---|---|---|---|---|
| 치과용 골이식재 | 해외업체 | 2012-01-04 | 2020-09-30 | 8,880 | 637 | 8,243 |
| 치과용 골이식재 | 해외업체 | 2014-08-18 | 2020-12-31 | 1,290 | 157 | 1,133 |
| 치과용 골이식재 | 해외업체 | 2014-12-31 | 2020-12-22 | 1,200 | 96 | 1,104 |
| 치과용 골이식재 | 해외업체 | 2015-12-14 | 2021-12-31 | 6,484 | 4,416 | 2,068 |
| 치과용 골이식재 | 해외업체 | 2017-03-13 | 2022-03-09 | 810 | 22 | 788 |
| 치과용 골이식재 | 해외업체 | 2017-03-27 | 2019-12-31 | 700 | 8 | 692 |
| 합 계 | 19,364 | 5,336 | 14,028 | |||
(참조 13) - 정정 후
| (증권신고서 제출일 현재) | (단위 : 천미불) |
|
업 체 명 |
주요계약품목 |
수주일자 |
납기일자 |
수주액 |
기납품액 |
수주잔액 |
|---|---|---|---|---|---|---|
|
Hi-Clearance |
치과용 골이식재 |
2014-08-18 |
2020-12-31 |
1,290 |
157 |
1,133 |
|
Almas Rouyan Pars |
치과용 골이식재 |
2014-12-31 |
2020-12-22 |
1,200 |
96 |
1,104 |
|
Nobel Biocare |
치과용 골이식재 |
2015-12-14 |
2021-12-31 |
13,926 |
4,881 |
9,045 |
|
Araguaney Professional |
치과용 골이식재 |
2017-03-13 |
2022-03-09 |
810 |
22 |
788 |
|
Wright Health Group |
치과용 골이식재 |
2017-03-27 |
2019-12-31 |
700 |
8 |
692 |
|
Straumann |
치과용 골이식재 |
2019-02-21 |
2024-02-20 |
21,982 |
237 |
21,745 |
|
합 계 |
|
|
39,908 |
5,401 |
34,507 |
|
(참조 14) - 정정 전
| (단위 :천미불 ) |
| 계약품목 | 계약상대방 | 계약일자 | 계약기간 | 계약금액 |
|---|---|---|---|---|
| 치과용 골이식재 | 해외업체 | 2014-08-18 | 2020-12-31 | 1,290 |
| 치과용 골이식재 | 해외업체 | 2014-12-31 | 2020-12-22 | 1,200 |
| 치과용 골이식재 | 해외업체 | 2015-12-14 | 2021-12-31 | 13,926 |
| 치과용 골이식재 | 해외업체 | 2017-03-13 | 2022-03-09 | 810 |
| 치과용 골이식재 | 해외업체 | 2017-03-27 | 2019-12-31 | 700 |
| 치과용 골이식재 | 해외업체 | 2019-02-21 | 2024-02-20 | 21,982 |
- 경영상의 주요계약은 보고일 현재 기준입니다.
(참조 14) - 정정 후
(가) 라이센스아웃(License-out) 계약
공시서류 작성기준일 현재 당사가 체결 중인 라이센스아웃(License-out) 계약의현황은 다음과 같습니다
| <라이센스아웃 계약 총괄표> |
| (단위: 백만원) |
|
품 목 |
계약상대방 |
대상지역 |
계약체결일 |
계약종료일 |
총계약금액 |
수취금액 |
진행단계 |
|---|---|---|---|---|---|---|---|
|
펩타이드 플랫폼 |
Straumann |
전세계 (한국제외) |
2017.03.21 |
각 제품별 및 국가별로 선정된 "제품 출시후 10년" 또는 "특허만료일"중 긴 기간 |
1,125 |
제품개발 논의중 |
|
|
합 계 |
1,125 |
||||||
주) 상기 금액은 계약일자의 최초고시환율인 1,124.50원을 적용.
(1) 품 목:펩타이드 플랫폼 기술이전 건.
|
①계약상대방 |
Straumann (유럽) |
|
②계약내용 |
치료용 펩타이드 기술은 현재 전임상 단계로 향후 진행되는 임상비용 및 상업화에 소요되는 경비에 대하여는 별도로 지급받음. 임상완료후 제품을 출시예정이며, 향후 매출발생에 따른 경상기술료(running royalty)는 상기금액과 별도로 지급받음. 이전되는 기술에 대하여 계약상대방은 치과영역(Dental Filed)에서만 활용하는 것으로 제한됨. |
|
③대상지역 |
전세계(한국제외) |
|
④계약기간 |
계약체결일:2017.03.21 계약종료일:각 제품별 및 국가별로 선정된 "제품 출시후 10년" 또는 "특허만료일"중 긴 기간 |
|
⑤총계약금액 |
초기기술료 USD 1,000,000 (한화 1,124,500,000원) |
|
⑥수취금액 |
<반환의무 없는 금액> 계약금(Upfront Payment): USD 1,000,000 (2017.03.30 수취) <반환의무 발생가능 금액> 해당사항 없음 |
|
⑦계약조건 |
계약금(Upfront Payment): USD 1,000,000 - 수취조건: 계약 체결 7일이내
임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급의무는 없음 |
|
⑧회계처리방법 |
계약금 수취액 1,124,500,000원(USD 1,000,000)은 수익 인식 |
|
⑨대상기술 |
치료용 펩타이드 신약 발굴 플랫폼 기술로 치과치료제, 치과재생용 바이오소재 개발 기술 |
|
⑩개발진행경과 |
거래 상대방과 회사는 본 계약 체결 이후 펩타이드 기술을 적용한 제품 개발에 대하여 협의를 진행 중임. |
|
⑪기타사항 |
(나) 판매계약
| (단위: 천미불) |
|
업 체 명 |
주요계약품목 |
계약일자 |
계약만료일 |
계약금액 |
|---|---|---|---|---|
|
Hi-Clearance |
치과용 골이식재 |
2014-08-18 |
2020-12-31 |
1,290 |
|
Almas Rouyan Pars |
치과용 골이식재 |
2014-12-31 |
2020-12-22 |
1,200 |
|
Nobel Biocare |
치과용 골이식재 |
2015-12-14 |
2021-12-31 |
13,926 |
|
Araguaney Professional |
치과용 골이식재 |
2017-03-13 |
2022-03-09 |
810 |
|
Wright Health Group |
치과용 골이식재 |
2017-03-27 |
2019-12-31 |
700 |
|
Straumann |
치과용 골이식재 |
2019-02-21 |
2024-02-20 |
21,982 |
|
합 계 |
|
|
39,908 |
|
보고서 작성일 현재 기준입니다.
(참조 15) - 정정 전
가. 연구개발 담당조직
(주)나이벡의 중앙연구소는 대표이사 총괄 지휘 아래 개발기획 전무이사가 있고, 연구소장을 비롯하여 각 팀으로 구성되어 있습니다.
나. 연구개발 인력현황
당사는 공시자료 제출일 현재 전체임직원수의 약45%의 연구진과 개발인력을 확보하고 있는 R&D기업입니다. 모두 약학, 분자생물학,생화학, 유기합성, 화학공학 등의 전공자들로서 충분한 연구경험을 가지고 있습니다.당사는 당사의 우수연구인력 이외에도, 기타 국내 외 우수 대학 및 기관들과 연구협력 네트워크를 구축하여 기술의 완성도를 높일 수 있도록 제품 성능을 구현하는 기술들의 신뢰성을 확보할 수 있는 연구들을 진행하고 있습니다.
(주)나이벡 중앙연구소에는 5개의 팀이 있으며, 신제품개발팀, 펩타이드 개발팀, 효능평가팀에서 펩타이드 발굴과 응용 및 조직재생용 바이오소재 개발, 의약품 제형설계의 기초 및 효력검증연구를 진행하고 있습니다. 특히 원천기술을 발굴하여 검증하고, 제형을 확립한 후 pilot형태의 시제품을 제작하여 생산본부와의 연계를 이루도록 하고 있습니다.
품질관리팀과 품질보증팀은 제품의 생산, 출하 및 유통이 제조기준 및 관리기준에 의거하여 엄격히 진행하고 있음을 항시 모니터링하여 최전방에서 보증하는 업무를 수행하며 특히 당사의 GMP인증, 각종 규격인증의 업무를 수행하고 있습니다.
다. 연구개발비용
(단위 : 천원)
| 과 목 | 2018년 (제15기) |
2017년 (제14기) |
2016년 (제13기) |
|
| 원 재 료 비 | 21,300 | 44,408 | 65,850 | |
| 인 건 비 | 961,774 | 973,219 | 399,181 | |
| 감 가 상 각 비 | 28,865 | 28,346 | 31,076 | |
| 위 탁 용 역 비 | 928,156 | 943,722 | 1,151,919 | |
| 기 타 | 554,482 | 703,993 | 921,086 | |
| 연구개발비용 계 | 2,494,577 | 2,693,688 | 2,569,112 | |
| 정부보조금 | (199,951) | (1,074,296) | (2,058,457) | |
| 회계처리 | 판매비와관리비 | 1,204,012 | 557,939 | 251,727 |
| 제조경비 | 224,004 | 227,645 | 118,368 | |
| 개발비(무형자산) | 1,066,561 | 1,908,104 | 2,199,017 | |
| 연구개발비 / 매출액 비율 [연구개발비용계÷당기매출액×100] |
47.90% | 42.74% | 53.48% | |
라. 연구개발실적
(참조 15) - 정정 후
가. 연구개발 활동 개요
당사는 펩타이드를 기반으로 하는 바이오 의약품 개발관련 신성장동력사업을 비롯하여 조직재생용바이오소재 기반사업에 대한 연구를 진행 중으로 현재 펩타이드 바이오 의약품 개발 관련 5개의 파이프라인을 구축하여 임상 1상 및 전임상 단계의 연구를 진행하고 있습니다.
|
품목 |
제품 |
제품 설명 |
|---|---|---|
|
펩타이드 의약품 |
골다공증치료제 (NIPEP-OSS= Osseotide) |
골 재생 기능 펩타이드 함유 골다공증 치료제 |
|
관절염 치료제 (NIPEP-CARE 1) |
염증 억제 기능 펩타이드 함유 관절염 치료제 |
|
|
비알콜성지방간염(NASH) 치료제 (NIPEP-CARE 2) |
염증 및 지방 억제 기능 펩타이드 함유 비알콜성지방간염 치료제 |
|
|
염증성 장질환(IBD) 치료제 (NIPEP-CARE 3) |
염증 억제 기능 및 점막 재생 기능 펩타이드 함유 염증성장질환 치료제 |
|
|
항암치료제 (NIPEP-ACD-Tide) |
종양선택적 투과기능이 탑재된 종양 치료 및 전이암, 내성암 치료제 |
나. 연구개발 담당 조직
(1) 연구개발 조직 개요
당사의 중앙연구소는 크게 첨단소재개발과 품질 파트로 나눠지며, 첨단소재개발 관련하여 3개의 팀과 품질 관련 2개팀으로 구분되어 총 5개의 팀으로 이뤄져있으며 연구개발 조직 구성은 아래와 같습니다.
| <연구개발 조직 구성> |
|
연구소 |
팀 |
주요 업무 |
|---|---|---|
|
첨단의약소재 |
신제품개발팀 |
제품 연구설계 및 신제품 개발 관련 업무 |
|
펩타이드개발팀 |
바이오 의약품 관련 실험 및 연구개발 업무 |
|
|
효능평가팀 |
신제품 및 후보물질 등 효능 평가 업무 |
|
|
바이오소재 연구팀 |
바이오소재 개발팀 |
제품 성능 보증 위한 전반적 업무 |
|
바이오소재 최적화, 상용화연구팀 |
품상용화 단계 품질관리 업무 및 중개연구 |
| <연구소 조직도> |
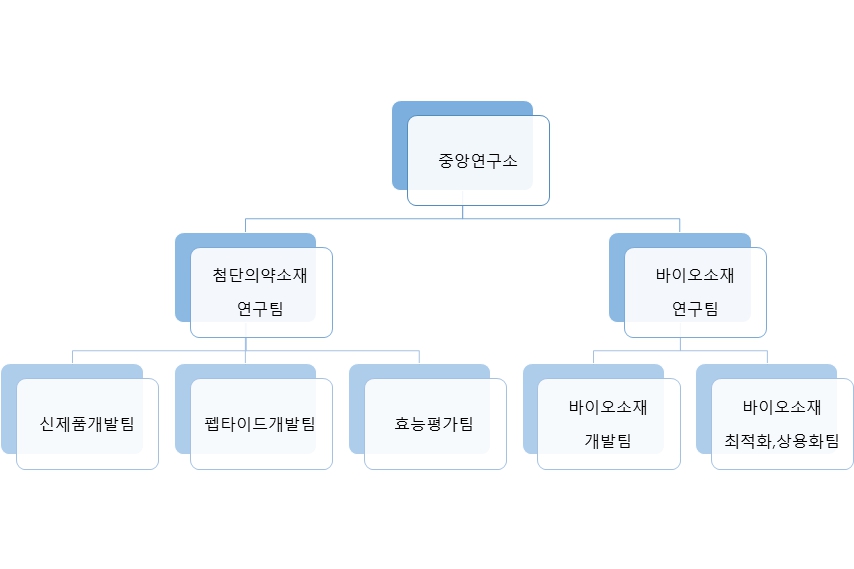 |
|
연구소 조직조 |
(2) 연구개발 인력현황
공시서류 작성기준일 현재 당사는 박사급 3명, 석사급 13명 등 총 31명의 연구인력을 보유하고 있으며, 그 현황은 다음과 같습니다.
| <연구개발 인력 현황> |
| (단위: 명) |
|
구 분 |
인 원 |
||||
|---|---|---|---|---|---|
|
박 사 |
석 사 |
학사 외 |
합 계 |
||
|
첨단의약소재연구팀 |
신제품개발팀 |
3 |
1 |
4 |
|
|
펩타이드개발팀 |
2 |
6 |
1 |
9 |
|
|
효능평가팀 |
1 |
4 |
5 |
||
|
바이오소재 연구팀 |
바이오소재 개발팀 |
1 |
1 |
3 |
4 |
|
바이오소재 최적화, 상용화연구팀 |
2 |
6 |
8 |
||
|
합 계 |
3 |
13 |
15 |
31 |
|
당사는 공시자료 제출일 현재 전체임직원수의 약45%의 연구진과 개발인력을 확보하고 있는 R&D기업입니다. 모두 약학, 분자생물학,생화학, 유기합성, 화학공학 등의 전공자들로서 충분한 연구경험을 가지고 있습니다.당사는 당사의 우수연구인력 이외에도, 기타 국내 외 우수 대학 및 기관들과 연구협력 네트워크를 구축하여 기술의 완성도를 높일 수 있도록 제품 성능을 구현하는 기술들의 신뢰성을 확보할 수 있는 연구들을 진행하고 있습니다.
(주)나이벡 중앙연구소에는 5개의 팀이 있으며, 신제품개발팀, 펩타이드 개발팀, 효능평가팀에서 펩타이드 발굴과 응용 및 조직재생용 바이오소재 개발, 의약품 제형설계의 기초 및 효력검증연구를 진행하고 있습니다. 특히 원천기술을 발굴하여 검증하고, 제형을 확립한 후 pilot형태의 시제품을 제작하여 생산본부와의 연계를 이루도록 하고 있습니다.
바이오소재 연구팀은 제품의 생산, 출하 및 유통이 제조기준 및 관리기준에 의거하여 엄격히 진행하고 있음을 항시 모니터링하여 최전방에서 보증하는 업무를 수행하며 특히 당사의 GMP인증, 각종 규격인증의 업무를 수행하고 있습니다.
(3) 핵심연구인력
이 중 당사의 핵심 연구인력은 대표이사인 정종평, 연구소 전반의 총괄업무를 담당하고 있는 전무이사 박윤정, 중앙연구소 및 프로젝트 총괄업무를 담당하는 연구소장 이주연등 입니다. 대표이사인 정종평은 서울대학교 치과대학에서 치주학을 전공한 박사로 치주염증을 비롯한 치과 분야 관련 연구를 계속해왔으며, 치과 임상의로서 다양한 환자 케이스를 통하여 나이벡의 기반사업인 조직재생용바이오소재 연구개발에 이바지 하였으며 R&D 및 경영총괄을 맡고 있습니다. 또한 연구소의 총괄업무를 담당하는 박윤정 전무이사는 현재 서울대학교 치의학대학원 교수 재직중으로 당사의 연구개발 관련 산학협력활동 및 우수한 연구적 네트워크를 구축, 활용하여 우수한 양질의 연구 결과 도출에 이바지하였습니다. 박윤정 전무이사와 중앙연구소 프로젝트 총괄업무를 담당하는 이주연이사는 약학을 전공한 약학박사로 펩타이드를 이용한 약물전달시스템을 비롯한 펩타이드 기반 바이오 의약품 개발 관련하여 다수의 논문 및 특허, 그리고 영향력 있는 바이오 학회 초청 발표 등 활발한 연구 활동을 계속해오고 있는 당사의 핵심인력입니다.
| <핵심 연구인력 현황> |
|
직 위 |
성 명 |
담당업무 |
주요 경력 |
주요 연구실적(대표논문5건) |
|---|---|---|---|---|
|
대표이사 |
정종평 |
총괄업무 |
서울대학교 치과대학 치의학 석사(‘72.02) 서울대학교 치과대학 치의학 박사(‘79.02) 미국뉴욕주립대학교 교환교수(82.12) 서울대학교 치과대학 교수(11.02) 서울대학교 치과대학 학장(02.02) 지능형생체게면공학 연구센터 센터장(‘09.03) |
The effect of the surface modification of titanium using a recombinant fragment of fibronectin and vitronectin on cell behavior, Biomaterials (26(25), 5153-5157), 2005 Electrospinning of chitin nanofibers: Degradation behavior and cellular response to normal human keratinocytes and fibroblasts, Biomaterials (27(21), 3934-3944). 2006 Assembly of collagen-binding peptide with collagen as a bioactive scaffold for osteogenesis in vitro and in vivo, Biomaterials (28(29), 4257-4267), 2007 Osteoblastic differentiation of human bone marrow stromal cells in self-assembled BMP-2 receptor-binding peptide-amphiphiles, Biomaterials. (30(21), 3532-3541), 2009 Peptide-mediated intracellular delivery of miRNA-29b for osteogenic stem cell differentiation, Biomaterials. 34(17):4347-59, 2013 |
|
전무이사 |
박윤정 |
연구소 전반 총괄업무 |
이화여자대학교 약학 석사(‘95.02) 이화여자대학교 약제학 박사(‘99.02) 미시간대학 약학대학 연구원(‘02.02) 미시간대학 약학대학 연구교수(‘03.05) 서울대학교 치의학대학원 교수(현재) |
Intracellular delivery of cell-penetrating peptide-transcriptional factor fusion protein and its role in selective osteogenesis, Int J Nanomedicine. 9:1153-66, 2014 Simultaneous imaging and restoration of cell function using cell permeable peptide probe, Biomaterials. 35(24):6287-98, 2014 Selective osteogenesis by a synthetic mineral inducing peptide for the treatment of osteoporosis, Biomaterials. 35(37):9747-54, 2014 Identification of cell-penetrating peptide domain from human beta-defensin 3 and characterization of its anti-inflammatory activity, Int J Nanomedicine. 26;10:5423-34., 2015 Dual-function synthetic peptide derived from BMP4 for highly efficient tumor targeting and antiangiogenesis, nt J Nanomedicine. 11;4643-4656, 2016 |
|
이사 (연구소장) |
이주연 |
중앙연구소 프로젝트 총괄업무 |
이화여자대학교 약학 석사(‘00.02) 이화여자대학교 약제학 박사(‘04.02) 서울대학교 치과대학 지능형생체계면공학연구센터(IBEC) Post-Doctoral Research Fellowship |
Identification of cell-penetrating peptide domain from human beta-defensin 3 and characterization of its anti-inflammatory activity, Int J Nanomedicine. 26;10:5423-34., 2015 Dual-function synthetic peptide derived from BMP4 for highly efficient tumor targeting and antiangiogenesis, nt J Nanomedicine. 11;4643-4656, 2016 Control of cancer stem cell like population by intracellular target identification followed by the treatment with peptide-siRNA complex, Biochem Biophys Res Commun, 491(3):827-833, 2017 Comparative Study of rhPDGF-BB Plus Equine-Derived Bone Matrix Versus rhPDGF-BB Plus β-TCP in the Treatment of Periodontal Defects, Int J Periodontics Restorative Dent, 37(6):825-832, 2017 A novel calcium-accumulating peptide/gelatin in situ forming hydrogel for enhanced bone regeneration, J Biomed Mater Res A, 106(2):531-542, 2018 |
다. 연구개발비용
당사는 일반적으로 신약 개발 프로젝트가 임상 3단계를 통과한 이후 발생한 지출을무형자산으로 인식하고, 이전 단계에서 발생한 지출은 당기비용으로 회계처리하고 있습니다.
당사의 최근 3년간 연구개발비용은 다음과 같습니다.
| <연구개발비용 현황> |
| (단위: 천원, %) |
|
구 분 |
2018년 |
2017년 |
2016년 |
|
|---|---|---|---|---|
|
비용의 성격별 분류 |
원재료비 |
21,300 |
44,408 |
65,850 |
|
인건비 |
961,774 |
973,219 |
399,181 |
|
|
감가상각비 |
28,865 |
28,346 |
31,076 |
|
|
위탁용역비 |
928,156 |
943,722 |
1,151,919 |
|
|
기타 |
554,482 |
703,993 |
921,086 |
|
|
연구개발비용 합계 |
2,494,577 |
2,693,688 |
2,569,112 |
|
|
(정부보조금) |
(199,951) |
(1,074,296) |
(2,058,457) |
|
|
보조금 차감 후 금액 |
2,294,626 |
1,619,392 |
510,655 |
|
|
회계처리 내역 |
판매비와 관리비 |
1,204,012 |
557,939 |
251,727 |
|
제조경비 |
224,004 |
227,645 |
118,368 |
|
|
개발비(무형자산) |
1,066,561 |
1,908,104 |
2,199,017 |
|
|
회계처리금액 계 |
2,494,577 |
2,693,687 |
2,569,112 |
|
|
연구개발비 / 매출액 비율 [연구개발비용합계÷당기매출액×100] |
47.90% |
42.74% |
53.48% |
|
라. 연구개발실적
(1)연구개발 진행 현황 및 향후계획
공시서류 작성기준일 현재 당사가 연구개발 진행 중인 신약[개량신약 등 포함]의 현황은 다음과 같습니다.
|
구 분 |
품 목 |
적응증 |
연구시작일 |
현재 진행단계 |
비 고 |
||
|---|---|---|---|---|---|---|---|
|
단계(국가) |
승인일 |
||||||
|
바이오 (식약처 구분 : 화학합성 신약) |
신약 |
NIPEP-OSS (Osseotide) |
골다공증 및 골재생 치료제 |
2011년 |
전임상 완료 |
2019년 예정 |
공동개발 정부보조금 |
|
NIPEP-CARE1 |
관절염 치료제 |
2013년 |
전임상 안전성 시험진입 |
- |
공동개발 정부보조금 |
||
|
NIPEP-CARE2 |
비알코올성간염NASH)치료제 |
2016년 |
전임상 효능시험 중 |
- |
공동개발 정부보조금 |
||
|
NIPEP-CARE3 |
염증성 장질환 치료제 |
2016년 |
전임상 효능시험 중 |
- |
공동개발 정부보조금 |
||
|
NIPEP-ACD-TIDE |
암줄기세포 표적 항암 치료제 |
2008년 |
전임상 효능시험 중 |
- |
공동개발 정부보조금 |
||
|
개량신약 |
OssGen better |
PTH 골다공증치료제 바이오베터 |
2016년 |
전임상 효능시험 중 |
- |
정부보조금 |
|
(가)품 목: NIPEP-OSS (Osseotide)
|
①구 분 |
바이오 신약(화학합성법으로 제조) |
||||||||||||||||||||||||||||||
|
②적응증 |
골다공증,골재생 치료제 |
||||||||||||||||||||||||||||||
|
③작용기전 |
골조직세포외기질에 결합 후,골아세포의 수용체와 결합,세포내 골재생 신호전달 증가,지방분화 신호전달 억제 |
||||||||||||||||||||||||||||||
|
④제품의특성 |
기존의 골다공증 치료제는 골흡수를 억제하는 기전인 비스포스포네이트가 가장 많이 사용되고 있으나, 장기간 사용시 과도하게 골흡수를 억제하여 골질이 약해서 골절 위험이 증가합니다. 유일한 골형성 촉진 기전의 테리파라타이드는 고칼슘혈증을 유 발하거나, 장기간 사용시 골육종을 일으키는 위험성이 있는 것으로 알려져 있음.
|
||||||||||||||||||||||||||||||
|
⑤진행경과 |
현재 전임상 독성시험(독일 소재 GLP 기관, LPT)을 완료하였고, 2018년 12월에 한국 식약처 임상1상 시험 승인을 신청하여, 현재 보완사항 중.2019년 임상1상 진입 예정. |
||||||||||||||||||||||||||||||
|
⑥향후계획 |
임상1상 실시: 2019.06-2020.12,한국 임상1상 후 라이센스 아웃 또는 공동기술개발 임상2상 신청 및 실시:2021.01-2023.01,다국가 임상 임상3상 신청 및 실시:2023.12-2025.12,다국가 임상 |
||||||||||||||||||||||||||||||
|
⑦경쟁제품 |
현재 FDA 승인이 된 골다공증 치료제 리스트
|
||||||||||||||||||||||||||||||
|
⑧관련논문등 |
국내특허등록 (등록번호: 1638775), 국내특허출원 (출원번호: 10-2017-0126876, 등록결정) 및 전세계 특허 (미국, 유럽, 중국, 일본) 논문발표
학회발표
|
||||||||||||||||||||||||||||||
|
⑨시장규모 |
<골다공증 치료제 세계시장 규모> (단위 : 억달러)
자료 : Osteoporosis-Pipeline Assessment & Market Forecast to 2017, Global Data,2010 CAGR 근거 년도 : 2018-2030년: 8.2% |
||||||||||||||||||||||||||||||
|
⑩기타사항 |
참여기관:(주)나이벡, 서울대학교 치의학대학원, 이대목동병원, 충북대학교, 아산병원, 연대 세브란스, 독일 LPT |
(나)품 목: NIPEP-CARE1
|
①구 분 |
바이오 신약 (화학합성법으로 제조) |
||||||||||||||||||||||||||||||||||||||||||||
|
②적응증 |
관절염 치료제 |
||||||||||||||||||||||||||||||||||||||||||||
|
③작용기전 |
세포막을 투과하여 세포핵내 histone deacetylase의 활성을 저해함으로써 염증성 사이토카인의 생성 억제 |
||||||||||||||||||||||||||||||||||||||||||||
|
④제품의특성 |
NIPEP-CARE1는 인체내 면역에 관계하는 단백질로부터 유래한 펩타이드로서, 염증 신호에 관계하는 전사인자를 억제하여 염증성 사이토카인의 생성을 억제함으로써 항 염증 효과를 가지게 됨.관절염 유발 동물 모델에 투여했을 때, 엔브렐 (etanercept)보다 염증지수 완화 및 골소실 억제 연골보호 효과가 우수한 것을 증명하였음. 또한, 세포투과 및 피부로도 투과가 가능하여 주사제 이외의 피부 적용제형으로 개발이 가능함. 관절염 치료제로 많이 사용되는 생물학적 제제로는 TNF-a 차단제가 있으나, 과도하게 면역반응을 차단하여 감염이나 결핵을 유발하는 부작용이 있음.
|
||||||||||||||||||||||||||||||||||||||||||||
|
⑤진행경과 |
전임상 독성시험을 진행 중 |
||||||||||||||||||||||||||||||||||||||||||||
|
⑥향후계획 |
2019년 12월에 전임상 완료 2020년 한국 식약처 임상1상 시험 승인을 신청 계획 전임상 완료 또는 임상1상 후 라이센스 아웃 또는 공동기술개발 |
||||||||||||||||||||||||||||||||||||||||||||
|
⑦경쟁제품 |
현재 개발 중인 관절염 치료제 리스트
|
||||||||||||||||||||||||||||||||||||||||||||
|
⑧관련논문등 |
국내특허등록 (등록번호: 1329774) 및 전세계 특허 (미국, 유럽, 캐나다) 논문발표
학회발표
|
||||||||||||||||||||||||||||||||||||||||||||
|
⑨시장규모 |
<관절염 치료제 세계시장 규모> (단위:억달러)
자료 : Arthritis Therapeutics Market to 2016, GBI research, 2010 CAGR 근거 년도: 골관절염 치료제 2018-2030년 2%, 류마티스 관절염 치료제 2018-2030년 8.6%, 관절염 치료제 2018-2030년 7.7 % |
||||||||||||||||||||||||||||||||||||||||||||
|
⑩기타사항 |
참여기관: (주)나이벡, 서울대학교 치의학대학원, 충북대학교, 아산병원, |
(다)품 목: NIPEP-CARE2
|
①구 분 |
바이오 신약 (화학합성법으로 제조) |
||||||||||||||||||
|
②적응증 |
비알코올성 간염 (NASH) 치료제 |
||||||||||||||||||
|
③작용기전 |
비알코올성 간염의 다중 바이오마커를 제어하여 간조직의 염증,지방 침착 억제 |
||||||||||||||||||
|
④제품의특성 |
NIPEP-CARE2는 인체내 면역에 관계하는 단백질로부터 유래한 펩타이드로서, methionine 결핍 식이에 의해 지방간 유발 동물모델에 투여했을 때, NIPEP-CARE2 에 의한 비알코올성 지방간의 NAS score (ballooning degeneration, lobular inflamm ation, steatosis)가 감소하였고, 간과 혈액에서 염증성 사이토카인의 발현이 감소하였음. |
||||||||||||||||||
|
⑤진행경과 |
전임상 효능시험 진행 중 |
||||||||||||||||||
|
⑥향후계획 |
2019년 12월에 전임상 완료 2021년 한국 식약처 임상1상 시험 승인을 신청 계획 전임상 완료 또는 임상1상 후 라이센스 아웃 또는 공동기술개발 |
||||||||||||||||||
|
⑦경쟁제품 |
현재까지 FDA에 허가 받은 치료제는 없는 상황이며, 개발 중인 비알코올성 간염 치료제 현황은 다음과 같음, 1)혈중 지질감소, 임상3상 2)콜릭액시드 생합성 수용체에 영향을 줌, LDL 증가시킴, 임상 3상 3)Stearoyl-CoA desaturase 1 저해제. 지방침착 저해, 임상 2상에서 계류 중 |
||||||||||||||||||
|
⑧관련논문등 |
- 국내특허출원 (출원번호: 10-2018-0103614) - 국내외 논문 게재 중 |
||||||||||||||||||
|
⑨시장규모 |
<비알코올성 간질환 치료제 세계시장 규모> (단위 : 억달러)
자료 : Allied Market research, NASH market, 2018-2030 CAGR 근거 년도 : 2018-2030년: 25.6% |
||||||||||||||||||
|
⑩기타사항 |
참여기관: (주)나이벡, 서울대학교 치의학대학원, 충북대학교, 아산병원, 질병관리본부 |
(라)품 목: NIPEP-CARE3
|
①구 분 |
바이오 신약 (화학합성법으로 제조) |
|||||||||||||||||||
|
②적응증 |
염증성 장질환 (inflammatory bowel disease) 치료제 |
|||||||||||||||||||
|
③작용기전 |
장점막 조직의 면역조절 펩타이드에 의해 염증성 장질환 치료 및 점막재생 |
|||||||||||||||||||
|
④제품의특성 |
NIPEP-CARE는 HDAC 저해에 의한 염증 감소와 대장 점막에 존재하는 콜라겐에 대한 자가 면역반응을 감소시켜 장점막의 재생을 증가시키는 작용이 있음. 나이벡이 가진 기술로 경구용 제형확립 |
|||||||||||||||||||
|
⑤진행경과 |
전임상 효능시험 진행 중 |
|||||||||||||||||||
|
⑥향후계획 |
2019년 12월에 전임상 완료 2021년 한국 식약처 임상1상 시험 승인을 신청 계획 전임상 완료 또는 임상1상 후 라이센스 아웃 또는 공동기술개발 |
|||||||||||||||||||
|
⑦경쟁제품 |
현재, 1차 치료로 사용하는 약물은 Aminosalicylic acid 로 주로 증상완화에 사용하고 있으며, 이 약에 반응하지 않을 때, 스테로이드를 사용함. 이렇게 해도 효능이 없거나 부작용이 발생하게 되면, 면역제제나 생물학적 제제를 사용함.생물학적 제제인 TNF-a 차단제는 면역반응을 오히려 억제하는 부작용을 가지고 있음. |
|||||||||||||||||||
|
⑧관련논문등 |
- 국내특허출원 (출원번호: 10-2018-0103615 ) - 국내외 논문 게재 중 |
|||||||||||||||||||
|
⑨시장규모 |
(단위 : 억달러)
자료 : Vision gain, Global Inflammatory Bowel Disease drug Market Forecast 2018-2030 CAGR 근거 년도 : 2018-2030년: 2.5% |
|||||||||||||||||||
|
⑩기타사항 |
참여기관:(주)나이벡, 서울대학교 치의학대학원, 충북대학교, 아산병원 |
(마)품 목: NIPEP-ACD-TIDE
|
①구 분 |
바이오 신약(화학합성법으로 제조) |
|||||||||||||||||||||
|
②적응증 |
신규 바이오마커 제어기반 암줄기세포치료제 및 표적조직 투과기능성 펩타이드 표적항암제 |
|||||||||||||||||||||
|
③작용기전 |
암줄기세포발현 바이오마커를 제어하는 세포내투과기능성 펩타이드 및 이를 기반으로 한 표적항 암치료제 |
|||||||||||||||||||||
|
④제품의특성 |
NIPEP-ACD-TIDE는 암줄기세포내 바이오마커를 억제함으로써, 암줄기세포의 이동, 부착과 전이를 억제하는 기능이 있음. 또한, 세포투과기능이 있기 때문에, 항암효과가 있는 단백질 또는 항체와 결합하여 세포내 전달수단 및 병용투여 요법으로 사용가능 함. |
|||||||||||||||||||||
|
⑤진행경과 |
전임상 효능시험 진행 중 |
|||||||||||||||||||||
|
⑥향후계획 |
2020년 전임상 완료. 2022년 한국 식약처 임상1상 시험 승인을 신청 계획 전임상 완료 또는 임상1상 후 라이센스 아웃 또는 공동기술개발 |
|||||||||||||||||||||
|
⑦경쟁제품 |
항암 치료 후에 암이 다시 재발하거나 전이되는 이유는 암세포 중에 암줄기세포가 존재하여, 항암치료에도 살아남아 다시 증식을 하기 때문임. 따라서, 이들 암줄기 세포를 타겟으로 하는 항암제가 개발된다면, 암전이나 재발의 확률이 감소할 것임. 현재, 암줄기세포를 타겟하는 약물을 개발되지 않았음. |
|||||||||||||||||||||
|
⑧관련논문등 |
국내특허등록 (등록번호: 101693533) 및 전세계 특허 (미국, 유럽) 논문발표
학회발표
|
|||||||||||||||||||||
|
⑨시장규모 |
<항암 치료제 세계시장 규모> (단위 : 억달러)
자료: Persistence market research, 항암제 글로벌 마켓 CAGR 근거 년도 : 2018-2030년: 7.4% |
|||||||||||||||||||||
|
⑩기타사항 |
참여기관: (주)나이벡, 서울대학교 치의학대학원, 충북대학교, 아산병원, 프랑스와 영국 바이오텍회사 |
(바)품 목: OssGen Biobetter
|
①구 분 |
바이오 신약 (화학합성법으로 제조) |
||||||||||||||||||||||||
|
②적응증 |
골다공증 치료제 |
||||||||||||||||||||||||
|
③작용기전 |
PTH 골다공증 치료제의 효능과 안전성 증가를 위한 바이오베터 |
||||||||||||||||||||||||
|
④제품의특성 |
PTH는 고칼슘혈증을 일으키고, 2년이상 사용이 제한되어 있음. 또한, 골조직뿐만 아니라 신장에도 영향을 줌. PTH의 골조직으로의 분포를 증가시킴으로써,PTH의 부작용은 감소시키고, 효능은 증가시킴. |
||||||||||||||||||||||||
|
⑤진행경과 |
전임상 효능 및 분포시험 진행 중 |
||||||||||||||||||||||||
|
⑥향후계획 |
2020년 전임상 완료. 2022년 한국 식약처 임상1상 시험 승인을 신청 계획 전임상 완료 또는 임상1상 후 라이센스 아웃 또는 공동기술개발 |
||||||||||||||||||||||||
|
⑦경쟁제품 |
현재 FDA 승인이 된 골다공증 치료제 리스트
|
||||||||||||||||||||||||
|
⑧관련논문등 |
국내특허출원 (출원번호: 10-2017-0126876, 등록결정) 및 전세계 특허 (미국, 유럽, 중국, 일본) 학회발표
|
||||||||||||||||||||||||
|
⑨시장규모 |
<골다공증 치료제 세계시장 규모> (단위 : 억달러)
자료 : Osteoporosis-Pipeline Assessment & Market Forecast to 2017, Global Data,2010 CAGR 근거 년도 : 2018-2030년: 8.2% |
||||||||||||||||||||||||
|
⑩기타사항 |
참여기관:(주)나이벡, 서울대학교 치의학대학원, 이대목동병원, 충북대학교, 아산병원 |
(2)연구개발 완료 실적
| <연구개발 완료 실적> |
|
구 분 |
품 목 |
효능 |
개발완료일 |
현재 현황 |
비 고 |
|---|---|---|---|---|---|
|
조직재생바이오사업 |
치과용 골이식재 (OCS-B/OCS-H) |
골재생촉진 |
2005.09.15. (2007.06.21 정부 판매승인일) |
한국, EU, 미국을 비롯한 전세계 대상으로 판매중 |
-중국 판매허가를 위한 임상시험 완료 -국내 아이비덴탈과 유통계약, 해외는 Straumann, Nobel Biocare 등과의 계약 |
|
치주조직재생용 쉬트 (GuidOss) |
치주조직 재생능 |
2011.04.12 |
한국 판매중 |
-중국 판매허가를 위한 임상시험 진행중 -국내 아이비덴탈과 유통계약, 해외는 Straumann과의 유통계약 |
|
|
치주조직재생용 콜라겐 창상수복재 (Regenomer) |
치주창상대체, 치주조직 형성 촉진 |
2011.08.01 |
한국, 미국, EU 판매중 |
-국내 아이비덴탈과 유통계약 해외는 Straumann과의 유통계약 |
|
|
골재생용 복합소재 (OCS-Collagen) |
골재생촉진을 위한 골미네랄 입자와 콜라겐의 복합이식용 소재 |
2014.07.25 |
한국, EU, 미국을 비롯한 전세계 대상으로 판매중 |
-국내 아이비덴탈과 유통계약, 해외는 Straumann, Nobel Biocare 등과의 계약 |
|
|
펩타이드 융합복합 바이오소재 (OssGen X-15) |
펩타이드가 융합된 골재생바이오소재 |
2011.10.12 |
한국 대상으로 판매중 미국 및 유럽 판매허가 진행중 |
-국내 아이비덴탈과 유통계약 |
|
|
구강보건사업 |
치아미백제 (Dr.Whitiss / |
약물전달시스템 기술 이용한 치아미백제 |
2010.04.20 2015.04.08 |
한국 대상으로 판매중 일반인 사용 가능 의약외품 및 전문가 사용 전문의약품 모두 생산 |
-온라인 판매(의약외품) -치과 유통 판매(전문의약품) |
|
시린이치료제 (Sensblok) |
시린이증상경감 |
2008.08.01 |
한국 대상으로 판매중 |
-온라인 판매 및 치과 유통 판매 |
|
|
치과용항생연고 (Minucure) |
치주염항생제 |
2015.05.29 |
한국 대상으로 판매중 |
-휴온스와 국내 유통계약 -치과 유통 판매 |
|
|
임플란트주위염 예방치료제 (Clinplant) |
항염물질 임플란트 주위염 예방제 |
2009.12.17 |
한국 대상으로 판매중 미국 및 유럽 비롯 전세계 판매중 |
-휴온스와 국내 유통계약 -해외 Straumann 과 유통계약 |
(참조 16) - 정정 전
4. 공모자금의 사용내역
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 백만원) |
| 구 분 | 납입일 | 증권신고서 등의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | |||
| 기업공개(코스닥시장) | 2011.07.07 | 발행제비용 | 380 | 발행제비용 | 360 | - |
| - | - | 시설자금 | 1,196 | 시설자금 | 958 | 시설자금중 일부를 운영 자금으로 집행함. |
| - | - | 운영자금 | 5,764 | 운영자금 | 6,022 | - |
| 소 계 | - | - | 7,340 | - | 7,340 | - |
| 유상증자(제3자배정) | 2015.04.13 | 운영자금 | 999 | 운영자금 | 999 | - |
| 유상증자(주주배정) | 2015.09.10 | 시설자금 | 1,500 | 시설자금 | 1,776 | - |
| - | - | 운영자금 | 4,564 | 운영자금 | 4,288 | 운영자금중 일부를 시설자금으로 집행함 |
| 소 계 | - | - | 6,064 | - | 6,064 | - |
5. 사모자금의 사용내역
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 백만원) |
| 구 분 | 납입일 | 주요사항보고서의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | |||
| 제2회 사모 분리형신주인수권부사채 | 2013.04.12 | 운영자금 | 4,000 | 운영자금 | 4,000 | - |
| 제3회 무보증 국내사모 전환사채 | 2015.03.02 | 시설자금 | 2,000 | 차환자금 | 1,000 | 채권자와 협의하여 제2회 신주인수권부사채 상환 |
| - | - | - | - | 운영자금 | 1,000 | - |
| 소 계 | - | - | 2,000 | - | 2,000 | - |
| 제4회 무보증 국내사모 전환사채 | 2016.03.31 | 시설자금 | 1,000 | 시설자금 | 1,347 | - |
| - | - | 운영자금 | 5,000 | - | 4,653 | 운영자금중 일부를 시설자금으로 집행함 |
| 소 계 | - | - | 6,000 | - | 6,000 | - |
| 제5회 무보증 국내사모 전환사채 | 2017.12.26 | 운영자금 | 5,000 | 운영자금 | 4,186 | 미집행된 납입금액은 제1금융권에 예치중임 |
(참조 16) - 정정 후
4. 공모자금의 사용내역
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 백만원) |
| 구 분 | 납입일 | 증권신고서 등의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | |||
| 기업공개(코스닥시장) | 2011.07.07 | 발행제비용 | 380 | 발행제비용 | 360 | - |
| - | - | 시설자금 | 1,196 | 시설자금 | 958 | 시설자금중 일부를 운영 자금으로 집행함.주1) |
| - | - | 운영자금 | 5,764 | 운영자금 | 6,022 | - |
| 소 계 | - | - | 7,340 | - | 7,340 | - |
| 유상증자(제3자배정) | 2015.04.13 | 운영자금 | 999 | 운영자금 | 999 | - |
| 유상증자(주주배정) | 2015.09.10 | 시설자금 | 1,500 | 시설자금 | 1,776 | - |
| - | - | 운영자금 | 4,564 | 운영자금 | 4,288 | 운영자금중 일부를 시설자금으로 집행함.주2) |
| 소 계 | - | - | 6,064 | - | 6,064 | - |
주1) 증권신고서상 발행제비용(2천만원) 및 시설자금 사용용도 238백만원을 운영자금(제품개발비용)으로 사용하여 차이가 발생하였습니다.
주2) 증권신고서상 운영자금 사용용도 276백만원을 시설자금(제조구역 증설)으로 사용하여 차이가 발생하였습니다.
5. 사모자금의 사용내역
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 백만원) |
| 구 분 | 납입일 | 주요사항보고서의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | |||
| 제2회 사모 분리형신주인수권부사채 | 2013.04.12 | 운영자금 | 4,000 | 운영자금 | 4,000 | - |
| 제3회 무보증 국내사모 전환사채 | 2015.03.02 | 시설자금 | 2,000 | 차환자금 | 1,000 | 채권자와 협의하여 제2회 신주인수권부사채 상환. 주1) |
| - | - | - | - | 운영자금 | 1,000 | - |
| 소 계 | - | - | 2,000 | - | 2,000 | - |
| 제4회 무보증 국내사모 전환사채 | 2016.03.31 | 시설자금 | 1,000 | 시설자금 | 1,347 | - |
| - | - | 운영자금 | 5,000 | - | 4,653 | 운영자금중 일부를 시설자금으로 집행함. 주2) |
| 소 계 | - | - | 6,000 | - | 6,000 | - |
| 제5회 무보증 국내사모 전환사채 | 2017.12.26 | 운영자금 | 5,000 | 운영자금 | 4,186 | 미집행된 납입금액은 제1금융권에 예치중임. 주3) |
주1) 주요사항보고서상 시설자금 사용용도 20억원을 채권자와의 협의하에 제2회 신주인수권부사채 조기상환 10억원, 운영자금(제품개발비 및 원부자재 구입비) 10억원으로 사용하여 차이가 발생하였습니다.
주2) 주요사항보고서상 운영자금 사용용도 347백만원을 시설자금(치과용 골이식재 GMP구축비)으로 사용하여 차이가 발생하였습니다.
주3) 제5회차 전환사채는 펩타이드기반 전임상비용과 원료생산 및 시험비용등 운영자금으로 4,186백만원 집행하였고 잔여 금액은 제1금융권에 예치중입니다.
【 대표이사 등의 확인 】
 |
|
나이벡_대표이사등의 서명_정정 |
증 권 신 고 서
| ( 지 분 증 권 ) |
| [증권신고서 제출 및 정정 연혁] |
| 제출일자 | 문서명 | 비고 |
|---|---|---|
| 2019년 04월 02일 | 증권신고서(지분증권) | 최초 제출일 |
| 2019년 04월 12일 | [기재정정] 증권신고서(지분증권) | 자진정정(파란색) |
| 금융위원회 귀중 | 2019년 4월 12일 |
| 회 사 명 : |
(주)나이벡 |
| 대 표 이 사 : |
정 종 평 |
| 본 점 소 재 지 : |
충북 진천군 이월면 밤디길 116 이월전기전자농공1단지 |
| (전 화) 043) 532-7458 (홈페이지) http://www.nibec.co.kr |
|
| 작 성 책 임 자 : | (직 책) 전무이사 (성 명) 박 윤 정 |
| (전 화) 043-532-7458 | |
| 모집 또는 매출 증권의 종류 및 수 : | 기명식 보통주 | |
| 모집 또는 매출총액 : | 26,565,000,000 | 원 |
| 증권신고서 및 투자설명서 열람장소 |
| 가. 증권신고서 |
| 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 나. 투자설명서 |
| 전자문서 : 금융위(금감원) 전자공시시스템 → http://dart.fss.or.kr |
| 서면문서 : (주)나이벡 : 충북 진천군 이월면 밤디길 116 KB증권(주) : 서울특별시 영등포구 여의나루로 50 |
【 대표이사 등의 확인 】
 |
|
(2019.04.02)대표이사등의 확인서 |
요약정보
1. 핵심투자위험
| 구 분 | 내 용 |
| 사업위험 | 가. 바이오의약품 시장의 변동에 따른 위험 당사가 영위하는 사업은 조직재생용 바이오사업, 구강보건사업 및 펩타이드 기반 사업이며, 상기 사업들은 바이오의약품 산업 내에 속합니다. 2018년 Evaluate Pharma에 따르면 전세계 바이오의약품 시장은 2010년부터 2017년간 연평균 7.7%로 성장하여왔으며, 2018년부터 2024년까지 연평균 9.1% 성장하여 2024년에는 3,830억달러에 달할 것으로 전망하고 있습니다. 한국바이오의약품협회에서 2019년 02월에 발간한 바이오의약품 산업동향보고서에 따르면 국내 바이오의약품 시장은 수출액이 급성장하여 2015년 무역수지 흑자전환 이후 3년 연속 증가하여 왔으며, 2017년 내수산업시장규모는 2조 2,327억원으로 2016년 1조 8,308억원 대비 22% 증가하였습니다. 국내 바이오의약품 시장은 가속화되는 고령화 사회및 만성질환의 증가로 의약품 수요 증가에 따른 바이오의약품 산업의 확대가 지속될 전망입니다. 그러나 이러한 시장조사기관의 전망에도 불구하고 제약시장의 환경 변화, 의약품 관련 지원 및 규제정책의 변화, 다국적 제약사의 바이오의약품 개발과 관련한 투자규모 및 사업전략 변경 등의 영향으로 산업에 부정적인 영향이 있을 경우 당사가 영위하는 사업에도 부정적인 영향을 줄 수 있습니다. 이 점 유의하시어 투자해 주시기 바랍니다. 나. 임플란트 시장 변동에 따른 위험 당사가 영위하는 조직재생용 바이오소재 사업은 치과용 골이식재 및 치주조직재생용 바이오소재로 구분되며, 치과용 임플란트의 필수 재료입니다. 세계 치과용 임플란트 시장은 2016년 기준 45억달러 시장으로 연평균 8.6% 성장하여 2019년에는 59억달러 시장으로 성장할 것으로 예상됩니다. 2018년 기준 세계 치과용 임플란트 시장은 Strauman이 약 전체 시장의 25%를 점유하고 있으며, Danaher(Nobel Biocare) 19%, Dentsply Sirona 12%, Zimmer Biomet 10%, Henry Schein 8%, 오스템임플란트 7% 순으로 상위 5개 기업이 전체 시장의 약 70%를 점유하고 있습니다. 한편, 식품의약품안전처의 KHDI에 의하면 국내 치과용 임플란트 시장규모는 2016년 기준 약 5,587억원 가량으로 최근 5년간 연 12.9%성장 중입니다. 국내 주요 업체로는 오스템임플란트, 덴티움, 네오바이오텍 등이 있으며, 상위 5개 업체가 전체 시장의 약 80%를 점유하고 있습니다. 국내외 치과용 임플란트 관련 시장은 향후 보험정책 완화 및 기술개발성장으로 더 커질것으로 예상되지만, 향후 임플란트의 부작용 발생으로 인한 평판리스크 발생 또는 임플란트를 대체할 기술개발이 될 경우 임플란트 시장에 부정적인 영향이 발생할 소지가 있습니다. 투자자들께서는 이점 유의하시기 바랍니다. 다. 경쟁업체 관련 위험 당사는 크게 조직재생용 바이오소재 및 구강보건제품을 제조 및 판매하는 기반사업군과 펩타이드를 기반으로 한 융합 바이오소재 및 치료제 등 신성장동력사업군으로 구분하고 있습니다. 당사는 각 사업군별 글로벌적으로 조직재생용 바이오소재 기업과 펩타이드 관련 연구개발 및 제조기업들과 경쟁하고 있습니다. 당사가 생산하고 있는 조직재생용 바이오소재는 글로벌적으로 Geistlich Pharma AG(스위스), Zimmer Holding Inc(미국), Dentsply Sirona International(미국) 등과 경쟁하고 있습니다. Marketsandmarkets, Dental Bone Graft Substituetes Market, 2016에 의하면, 치과용 골이식재의 글로벌 시장은 Geistlich Pharma AG(스위스)의 소뼈유래 골이식재인 BioOss를 포함한 상위 5개 업체의 제품이 시장의 대부분을 장악하고 있으며, 특히 Geistlich Pharma AG(스위스)가 2015년 기준 시장점유율 13.8%로 우위를 선점하고 있습니다. 한편, 국내 치과용 골이식재 시장에서는 당사와 Geistlich Pharma AG(스위스), 오스코텍 등의 업체가 치과용 골이식재 시장을 과점하고 있으며, Geistlich Pharma AG(스위스)의 BioOss가 41.2%, 당사의 OCS-B, OCS-H, GuideOss 등이 12.9%, 오스코텍의 BioCera, SynCera가 8.1%로 국내시장의 점유율을 차지하고 있는 것으로 추정되고 있습니다. 한편, 당사가 연구개발중인 펩타이드 관련 제품은 펩타이드 기반 골이식재와 펩타이드 기반의 골다공증 치료제, 관절염치료제, 비알콜성지방간염치료제, 염증성장질환치료제, 펩타이드 기반 바이오베터로, 펩타이드 소재인 점을 제외할 시 다른 소재를 기반으로 경쟁업체들이 연구개발 및 제품출시를 하고 있으며, 이와 관련된 모든 업체들이 경쟁업체라고 할 수 있습니다. 그러나 펩타이드를 기반으로 한 치료제는 글로벌적으로 아직 개발되지 않았기 때문에 시장점유율을 측정할 수 없는 상황입니다. 다만, 펩타이드 기반 골이식재 관련된 제품은 출시되었으며, 당사를 제외한 펩타이드 기반 골이식재를 개발한 기업은 Dentsply가 있습니다. 당사는 글로벌 임플란트 1위, 2위업체인 Straumann과 Nobel Biocare 등의 유통업체들과의 공급계약을 통해 시장점유율을 확대해 나가고 있으며 신성장동력 사업군에서는 현재 펩타이드 기반 제품을 연구개발하여 당사의 수익성을 높이기 위하여 노력하고 있습니다. 그러나 많은 신제품이 연구, 개발되고 있는 경쟁이 치열한 바이오 산업시장에서향후 당사보다 안전성 및 효능이 뛰어난 제품이 경쟁업체에 의하여 출시되어 시장점유율을 확대되고, 당사가 경쟁에서 뒤쳐질 경우에는 당사의 사업성 및 수익성에 부정적인 영향을 끼칠수 있습니다.이 점 유의하여 투자해 주시기 바랍니다. 라. 정부 정책 변동에 따른 위험 의약품 시장은 인간의 생명과 보건에 관련된 제품을 생산하는 산업으로 정부의 의료정책 및 관리제도와 밀접한 관련성을 가지고 있습니다. 당사가 영위하고 있는 상처치유 및 재생의학 사업은 바이오, 의료산업 내에서 높은 성장세를 보이고 있으며, 경제사회적 파급효과가 매우 큰 치료 영역으로 평가되어 정부에서도 '미래 성장을 견인할 수 있는 국가존망기술'로 선정하여 국가적으로 정책적 지원이 확대되고 있습니다. 그러나 동시에 GMP 규정에 따른 제조 및 품질관리 운영에 대한 점검, '세포치료제 제조 및 품질관리기준 가이드라인'의 강화, 임상시험 절차 및 수행 방법에 대한 기준 강화 등 제품의 안전성 및 유효성 등과 관련하여 규제책도 강화하고 있습니다. 이러한 정부 지원의 변화 및 규제 정책의 변화는 당사의 사업을 영위하는데 있어서 커다란 영향으로 작용하고 있으며, 향후 당사에 부정적인 영향을 미치는 정책이 시행될 경우 당사의 수익성 또한 영향이 있으므로 정부의 정책 시행에 대한 모니터링이 필요할 것으로 판단됩니다. 이 점 유의하시어 투자해 주시기 바랍니다. 마. 바이오의약품 임상시험 실패에 따른 위험 당사는 펩타이드 공학기술을 이용한 펩타이드 기반 융합 바이오소재, 펩타이드 치료제, 펩타이드 기반 바이오베타 사업을 위하여 연구개발을 하고 있습니다. 바이오의약품의 개발 과정은 후보물질 선정, 비임상 단계, 임상시험 진행 승인(IND), 임상 1~3상, 품목허가의 단계로 진행됩니다. 일반적으로 바이오의약품의 단계별 성공률은 임상1상에서 임상 2상까지는 66.0%, 임상2상에서 임상3상까지는 34.4%, 임상3상에서 신약허가 신청까지 57.2%, 신약허가에서 신약승인까지는 88.4%로, 임상1상부터 신약승인까지의 성공확률은 11.5%로 상당히 저조합니다. 또한 한국바이오협회가 발표한 임상단계별 특징에 의하면 임상1상에서 임상3상까지 임상대상은 1,000명~5,000명 이상이 필요하며 소요비용은 약 1,250억원을 예상하고 있습니다. 한편, 당사가 연구개발 중인 펩타이드 기반 바이오소재의 현황 및 연구개발단계는 다음과 같습니다. 1) 펩타이드 의약 바이오소재 당사의 펩타이드 의약 바이오 소재 중 OssGen-X15(골재생 펩타이드가 표면에 고정된 골이식재)는 전임상/임상 완료 및 국내/해외에서 허가 또는 인증을 받아 시판중에 있으며, Regenomer-pep(골재생 펩타이드 함유 주입형 골재생제)는 전임상/임상 완료 및 국내허가까지 완료한 상태로 해외 인증을 준비 중에 있습니다. 해외 인증이 완료되는 시점은 2021년 9월로 예상하고 있으며, 인증비용은 약 10억원이 소요될 것으로 예상하고 있습니다. 2) 펩타이드 관련 치료제 펩타이드 기반 치료제인 펩타이드 골다공증치료제(NIPEP-OSS)는 전임상이 완료된 상태로 임상1상 1년, 임상2상 2년, 임상 3상 2년이 진행된 후 2026년에 출시될 것으로 예상됩니다. 골관절염치료제(NIPEP-CARE 1), 비알콜성 간염 치료제(NIPEP-CARE2), 염증성 장질환치료제(NIPEP-CARE3), 항암치료제(NIPEP-ACD Tide),는 현재 전임상이 진행중에 있는 상태입니다. 당사는 향후 펩타이드 기반 골다공증치료제 임상 1상 진행비용 35억원, 펩타이드 기반 관절염 치료제의 전임상 및 1상임상비용 각각 30억원, 펩타이드 표적항암제 전임상비용 15억원, 비알콜성지방간염(NASH) 치료제와 장질환 치료제 전임상비용 30억원으로 총 140억원이 소요될 것으로 예상하고 있습니다. 당사는 펩타이드 기반 융합바이오소재의 임상단계, 품목허가 과정을 거치면서 최근의 임상시험 절차 및 기준에 대해 상대적으로 잘 인지하고 있고 노하우를 보유하고 있으며, 향후 펩타이드 기반 치료제의 연구개발 또한 당사 연구개발계획에 의거하여 절차를 진행하려고 합니다. 그럼에도 불구하고 당사의 파이프라인이 임상을 진행함에 있어서 유의미한 결과를 도출하지 못할 경우에는 제품화가 불가능하며 투입된 연구비, 연구 역량 등 당사에 높은 기회비용이 발생할 수 있으며 사업계획에 지대한 영향을 미칠 수 있습니다. 당사는 금번 주주배정후실권주 일반공모를 통하여 유입되는 자금 중 약 150억원(펩타이드 기반 골다공증치료제 임상 1상 진행비용 35억원, 펩타이드 기반 관절염 치료제의 전임상 및 1상임상비용 각각 30억원, 골이식재 및 골재생제 유럽임상비용 10억, 펩타이드 표적항암제 전임상비용 15억원, 비알콜성지방간염(NASH) 치료제와 장질환 치료제 전임상비용 30억원)을 향후 연구개발을 위한 자금으로 사용하려고 하고 있습니다. 그러나 상기 언급한 바와 같이 임상1상부터 신약승인까지의 성공확률은 11.5%로 상당히 저조하며, 임상시험이 성공하지 못할 경우 자산 및 매출화되지 못하고 모두 비용처리가 될 위험이 있습니다.그러므로 투자자께서는 임상시험 절차, 임상 시험의 단계별 성공률, 당사의 파이프라인 현황 및 개발 단계, 타사 사례 등을 통해 리스크에 대해 충분히 확인 및 인지하시고 투자에 임하시기 바랍니다. 바. 높은 연구개발비 부담에 따른 수익성 위험 당사가 영위하는 바이오제약 사업의 특성상 장시간의 제품의 연구 개발에 대한 투자가 필수적입니다. 향후 보유 파이프라인의 펩타이드 기반 골다공증치료제의 임상 1상 진입비용 및 항염증 파이프라인의 전임상 비용의 증가로 인하여 연구개발비는 이전보다 많이 증가할 것으로 예측하고 있으며 특히 판매관리비의 증가를 초래하여 단기적으로 당사 수익성을 저해할 수 있습니다. 한편, 당사는 펩타이드를 기반으로 하는 의약품 개발비용에 대해서는 임상 3상 이전까지는 비용처리 하고 있으며 개발비를 포함한 한정된 내용연수를 가지는 다음의 무형자산은 사용가능한 시점부터 추정내용 연수동안 정액법으로 상각하고 있습니다. 무형자산화된 개발비의 경우, 향후 제품의 판매중단 등의 이유로 무형자산의 손상이 발생하게 될 경우에는 일시에 자산손상 인식 및 개발비 상각처리 등이 발생할 수 있습니다. 특히 금번 유상증자를 통한 자금조달로 펩타이드기반 의약품 파이프라인에 대해 2020년까지 약 150억원의 연구개발비를 사용할 예정이고, 해당 연구개발비는 성공률이 저조한 임상3상 이전까지 모두 비용화되며, 임상3상 성공 후 무형자산화과 될 시 당사의 회계정책에 의하여 상각처리될 예정입니다. 또한, 산업재산권 또한 특허권 침해 및 분쟁 등으로 손상이 발생하게 될 경우 상각처리 등이 발생으로 당사의 손익에 영향을 줄 수 있습니다. 당사의 예상과 달리 연구개발 진척 상황이 지연되거나 실패하는 등 자금운용 계획의 실행이 불가능해지는 상황이 발생할 경우, 단기적인 재무적 부담이 가중되어 당사의 수익성 및 재무안정성에 부정적인 영향이 있을 수 있습니다. 사. 연구개발인력의 유출에 따른 위험 연구개발 능력은 당사가 속한 산업의 특성상 매우 중요한 요소이며, 지속적인 연구개발을 위해 우수한 인재를 보유/유치하는 것이 회사의 성과를 결정하는 가장 중요한 요소입니다. 당사는 핵심 연구인력의 관리 및 확보를 위하여, 차별화된 대우와 보상, 교육 지원등을 제공하고 있으나, 각종 보상책에도 불구하고 핵심인력의 이탈 가능성을 배제할 수는 없는 상황입니다. 실제로 상기 노력을 바탕으로 2017년초 26명에 비하여 2019년 현재 연구인력이 31명으로 5명 증가하였으나, 2017년부터 2019년 현재까지 총 16명이 퇴사하였으며, 펩타이드개발팀에서 총 4명이 퇴사하였습니다. 당사의 핵심 기술의 특성상 당사 연구개발인력 수준을 대체할 수 있는 인력이 풍부하지 않으며, 대기업, 연구소, 대형병원 등에 비해 우수한 연구개발인력의 유치가 상대적으로 어려울 수 있습니다. 또한 당사는 연구인력들을 대상으로 비밀유지계약을 통해 기술의 유출을 방지하고 있으며, 퇴사 이후에도 적용할수도록 하여 이러한 기술유출의 위험을 최소화하고 있으나, 핵심인력이 이탈할 경우 기술 유출로 인하여 당사의 경쟁력 약화 및 지속적인 성장에 부정적인 영향을 끼칠 수 있으니, 이 점 유의하여 투자해 주시기 바랍니다. 아. 지적재산권 침해에 따른 위험 당사는 기술력 기반의 바이오연구개발회사로서 핵심기술에 대한 지적재산권의 확보가 핵심 경쟁력입니다. 당사는 국내에서 구강질환개선제품 특허 32건(등록 24건, 출원8건), 조직재생용 바이오소재 특허 10건(등록 9건, 출원 1건), 펩타이드 기반 바이오소재 4건(등록 3건, 출원1건)으로 총 46건의 특허를 가지고 있습니다. 또한 PCT(특허협력조약) 출원 32건, 해외특허/출원 62건을 보유 중에 있습니다. 현재 당사의 핵심기술 및 활용기술과 관련한 소송이나 분쟁은 발생한 내역이 없으며 기술보호를 위해 국내뿐만 아니라 해외에서도 특허 등록을 진행하고 있습니다. 또한, 전문 컨설팅 기관으로부터 특허의 침해 여부 및 전략에 관하여 정기적으로 컨설팅을 받고 있습니다. 그럼에도 불구하고 향후 당사가 보유한 지적재산권을 적절히 보호하지 못하거나 당사가 사용하는 기술과 관련한 지적재산권 관련 분쟁이 발생하는 경우 당사의 경쟁력은 약화될 수 있으며 이는 당사의 영업 및 손익에 부정적인 영향을 미칠 수 있습니다. 이점 유의하여 투자해 주시기 바랍니다. 자. 기술이전 실패에 대한 위험 일반적으로 신약개발은 각 국가의 규제 당국이 제시하는 단계에 따라 비임상 독성 시험, 임상 시험 (1, 2, 3상), 시판 승인 절차를 거쳐 최종적으로 판매되기까지는 오랜 시간과 많은 비용이 소요되며, 많은 시간과 비용을 투자하였더라도 최종 제품으로 개발이 되는 비율은 매우 낮습니다. 이러한 특성상 많은 바이오중소기업들은 일부 파이프라인에 대해서는 기술이전을 사업모델로 하고 있습니다. 당사 또한 현재 치과분야에 한정하여 스위스의 Straumann사와 2017년 펩타이드 치과 응용기술 이전 계약을 통해 안정적인 미래 파이프라인 공급 및 신개발 제품의 공급관련 전략적 제휴에 합의한 바 있습니다. 또한 펩타이드 기반한 신약관련(골다공증, 관절염, 항암, 비알콜성지방간염, 염증성 장질환 등)하여, A사를 비롯한 총 네곳의 국내외 제약사와 NDA를 체결하였으며, 이에 대한 기술이전에 관한 논의를 계속해서 진행 중에 있니다. 펩타이드기반 바이오베터인 골다공증바이오베터는 전임상을 진행중에 있으며 임상1상 완료후 기술이전을 예상하고 있고,세포내 단백질(항체)를 전달할수있는 기능을 가진 펩타이드플랫폼을 이용하여 기술이전 또는 당사의 펩타이드플랫폼을 사용할수있는 서비스를 제공하여 수익창출할 계획에 있습니다. 그러나, 당사의 계획과 달리 파트너사와의 협의가 원활히 이루어지지 않아 기술이전 계약이 취소되거나 규모가 축소될 경우 사업에 부정적인 영향이 생길수 있으니 투자자분들께서는 이점 유의하시기 바랍니다. |
| 회사위험 | 가. 지속적인 당기순손실 발생에 따른 위험 당사는 코스닥시장 상장이후 2018년말까지 지속적인 당기순손실이 이어지고 있습니다. 당사는 골이식재 및 구강보건제품으로 약 40~50억원의 꾸준한 매출액을 발생시키고 있으나, 최근 펩타이드 관련 연구개발비 및 임상비용을 위한 지급수수료의 증가로 인해 판매비와 관리비가 증가하였으며, 2016년 -30.3억원, 2017년 -25.7억원, 2018년 -40.4억원의 당기순손실이 누적되고 있습니다. 이로 인하여 2018년말 기준 232.3억원의 결손금이 계상되어 있습니다. 당사는대규모 공급계약 체결의 노력으로 향후 수익성을 개선하고자 하나, 판매비와관리비 및 영업외비용 등을 상회할 만큼의 매출규모가 발생하지 않고 임상 실험의 실패, 연구개발성과의 부진 및 주요 매출처와의 계약해지, 재계약 연장 불가등의 변수가 발생된다면 당사의 수익성에 부정적인 영향을 미칠 수 있습니다. 투자자 분들께서는 이점 유의하시기 바랍니다. 나. 매출처 편중 심화에 따른 위험 당사의 주요 매출처는 글로벌 임플란트 시장의 1,2위인 Straumann과 Noble Biocare이며, 2018년 기준 주요 매출처 상위 3개사에 대한 매출비중이 84.2%를 차지하고 있습니다. 상위 3개사 매출비중은 2016년 62.9%, 2017년 81.6%, 2018년 84.2%로 매출 의존도가 점차 높아지고 있습니다. 주요 매출처에 대한 매출 의존도가 상당히 높은 편이며, 이는 거채처 관리비용의 절감, 매출의 안정적인 성장 및 일정 수준 이익율을 확보하기가 가능하다는 점 등 긍정적인 요소도 존재하나, 주요 거래처의 시장 점유율 하락, 영업활동의 부진, 정책변경 및 당사와 협의과정에서 문제가 발생될 경우 당사의 영업활동 및 수익에도 부정적인 영향을 받을수 있습니다. 당사는 향후 다양한 제품 연구개발을 통하여 기존 주요 매출처 이외에도 신규 매출처 개척을 통해 매출처의 다각화를 진행 및 계획하고 있습니다. 다만, 당사의 계획과는 다르게 신규 매출처의 다각화에 실패하거나 주요 매출처의 영업활동이 부진 등으로 매출이 줄어들 경우 당사의 실적이 급격히 악화될 가능성이 존재하오니 투자자분들께서는 유념하시기 바랍니다. 다. 매출채권 회수 위험 당사의 2018년 매출채권은 1,905백만원으로 2017년 매출채권 1,851백만원 대비 소폭 증가하였으며, 매출채권 중 약 264백만원에 대하여 대손충당금을 설정(매출채권총액 대비 13.86% 수준)하고 있습니다. 주요 매출처를 제외한 기타 매출처들에 대하여 보수적으로 매년 추가 대손충당금 설정하면서 대손충당금설정률은 2016년 9.6%에서 2018년 13.9%로 증가하게 되었습니다. 당사의 매출채권 회전율은 2018년 3.17회, 2017년 3.64회로 한국은행에서 발간한 기업경영분석의 업종평균 3.5회(2017년 기준)과 비슷한 수준을 보이고 있습니다. 당사의 주요 매출처는 세계글로벌 1,2위 임플란트 관련 기업으로, 매출채권이 입금기한 내 100% 회수가 되고 있으며, 이로 인하여 대손충당금 설정에 의한 대손상각비 발생가능성은 적을 것으로 판단되고 있습니다. 그러나 향후 매출처의 영업환경 악화, 주된 거래처와의 거래관계 악화 등이 발생되어 매출채권이 원활하게 회수되지 못하거나, 회수가 지연되어 고령화된 매출채권이 발생할 경우 자금흐름이 악화될 수 있으며, 당사의 수익성 및 재무안정성이 악화될수 있으니 투자자들께서는 이점 유의하시기 바랍니다. 라. 재고자산 증가 및 노후화에 따른 위험 당사의 재고자산은 2016년 17.3억(총자산대비 7.53%), 2017년 24.1억(총자산대비 9.36%), 2018년 25.4억(총자산대비 11.40%)으로 최근 3개년 지속적으로 증가하고 있으며, 재고자산 회전율은 2016년 2.7회, 2017년 2.1회, 2018년 1.92회로 감소하고 있습니다. 당사는 동종업계의 평균 대비 낮은 재고자산 회전율을 보이고 있는데 낮은 재고자산 회전율은 당사의 재고자산 부담이 동종업계 대비 상대적으로 크다는 것을 나타냅니다. 향후 매출증가를 달성하지 못하거나 기술력이 저하되어 당사의 재고자산을 판매하지 못하게 될 경우 재고자산의 추가적인 감액 처리로 인하여 당사의 수익성은 악화될수 있습니다. 당사는 보유 중인 재고자산이 향후 영업계획 및 수주현황에 따라 소진될 것으로 예상하고 있으나, 당사의 개발제품에 대한 임상실험의 지연, 인증지연 또는 주된 거래처와의 거래관계의 악화나 산업의 침체 같은 요인들로 인해 영업환경이 영향을 받게되면 진부화된 재고자산 발생에 따른 재고자산 평가손실등의 인식으로 당사의 현금흐름 및 수익성에 부정적인 영향을 미칠수 있습니다. 이 점 유의하여 투자해 주시기 바랍니다. 마. 재무안정성에 관련 위험 당사의 2018년말 기준 부채규모는 117.4억원이며, 부채비율은 111.4%입니다. 당사의 부채 중 가장 큰 비중을 차지하고 있는 차입금은 2018년 기준 78.2억원으로 유동성 차입금은 69.7억원, 장기차입금은 8.5억원으로 구성되어 있습니다. 총 차입금의존도는 35.05%입니다. 한국은행에 의하면 동종업계의 2017년 부채비율은 91.9%, 차입금의존도는 28.5%로 당사의 재무안정성비율은 동종업계 대비 상대적으로 열위한 수준에 있습니다. 또한 증권신고서 제출일 기준 당사는 차입금 외에 제5회차 사모 전환사채 46.5억이 있습니다. 제5회차 전환사채의 조기상환청구권(Put Option)은 발행일로부터 2년 경과한 날인 2019년 12월 26일부터 가능하나, 기한의이익 상실 조항의 효력이 발생할 경우 즉시 상환에 대한 가능성이 있습니다. 당사는 금번 KB증권으로부터 90억원(고정금리 연 5.9%, 만기 6개월)의 단기자금을 차입하여 연구개발비용 사용 및 동 전환사채에 대한 기한의이익상실 가능성에 대비할 계획입니다. 금번 KB증권으로부터의 단기 차입시 기존 제5회차 전환사채을 상환할 경우 당사의 차입금 의존도는 45.96%, 부채비율을 153.62%(미상환 시 차입금의존도 48.59%, 부채비율 196.12%)로 증가(2018년 재무제표에 단기 차입 및 상환을 단순 합산한 시나리오)하게 됩니다.금번 주주배정후실권주 일반공모 증자가 성공적으로 이루어질 경우 당사의 안정성 지표들은 개선 될 것으로 기대되고 있으나, 2018년말 기준 동종업계 대비 상대적으로 안정성 지표들이 열위한 수준에 있는 점, 주가하락에 따른 공모금액의 축소가능성 및 향후 지속적인 손실로 자본이 감소할경우 다시 채무가 증가할 가능성이 있습니다. 투자자 여러분께서는 추가적인 차입금 발생 여부 및 전환사채의 조기상환청구 가능성에 대하여 유의하여 투자를 고려해 주시기 바랍니다. 바. 음(-)의 영업현금흐름 및 유동성 관련 위험 당사는 최근 3사업연도 중 2016년과 2018년에 음(-)의 "영업활동현금흐름"을 보이고 있으며, 최근 3사업연도동안 지속적으로 음(-)의 "투자활동현금흐름"을 보이고 있습니다. 당사는 이에 대한 현금유출을 충당하기 위하여 재무활동현금흐름을 통하여 조달하고 있으며, 2018년말 보유 현금은 8.6억원입니다. 한편, 2017년말 당사의 유동비율은 175.6%으로 동종업계 2017년 평균 유동비율인 175.6%(한국은행 기업경영분석, C27. 의료, 정밀, 광학기기 및 시계 제조업)와 같았으나, 2018년말 당사의 유동빌윤은 68.3%로 동종업계평균보다 현저히 낮아진 상황입니다. 이는 2018년중 음(-)의 영업활동현금흐름과 투자활동현금흐름이 크게 발생하였음에도, 외부 추가적인 자금조달이 거의 없었기 때문에 당사의 유동성 비율이 전년대비 크게 감소한 것으로 판단됩니다. 이자보상배율도 지속적이 영업손실이 발생하면서 음(-)의 배수를 기록하고 있습니다. 당사는 현금흐름 및 유동성에 대하여 지속적으로 모니터링하면서 유동성 이슈가 발생하지 않도록 대응하고 있으며, 금번 주주배정후실권주일반공모를 통하여 자금이 유입될 시 재무유동성이 개선될 것으로 기대되고 있습니다. 그러나 당사의 예상과는 달리 향후 영업 개선을 통한 영업활동현금흐름이 개선되지 않을 시 장기적으로 회사의 현금흐름에 문제가 발생할 소지가 있습니다. 투자자들께서는 상기의 위험요인을 면밀히 검토하시고 투자에 임해주시기 바랍니다. 사. 최대주주 등의 지분율 감소로 인한 위험 당사의 최대주주는 정종평 대표이사로 1,133,690주(17.71%)의 지분을 보유하고 있으며, 특수관계인을 포함 시 1,406,694주(21.97%)를 보유하고 있습니다. 금번 당사의 주주배정 후 실권주 일반공모 유상증자로 인한 주당 배정비율은 51.928953%로 1주당 0.51928953주의 배정주식(신주인수권증서)를 교부받게 됩니다. 이에 따라 최대주주인 정종평 대표이사는 588,713주, 특수관계인 박윤정은 118,398주를 배정받게 됩니다, 금번 주주배정 청약시 배정받을 주식수내에서 최대주주 및 특수관계인 박윤정은 청약에 100% 참여하여 현재와 같은 경영권 유지 및 일관된 사업진행을 위해 노력할 예정입니다. 당사의 기타 지분은 다수의 소액주주에 분산되어 있어 경영권 유지에는 큰 문제가 없을 것으로 보입니다. 그러나 향후 주식담보 대출후 주가 하락에 의한 담보권 실현 등으로 최대주주 및 특수관계인 지분율이 취약해질 경우, 향후 경영권의 행사가 취약해 질 수 있습니다. 향후 경영권이 취약해질 경우 적대적 M&A 및 외부의 경영권 취득 시도 등의 위험에 노출될 수 있습니다. 이는 최대주주 변경가능성 등에 의한 경영권의 안정성 저하 및 당사의 신뢰도 하락을 유발할 수 있는 등 당사의 장기적인 발전을 저해하는 요소로 작용할 수 있으니 투자자분들께서는 투자시 이러한 점을 깊게 유의하시기 바랍니다. 아. 환율 변동에 따른 위험 당사 2018년 기준 총 매출액 대비 약 78%인 40.9억원이 해외 수출을 통해 발생되고 있습니다. 당사 제품에 필요한 원,부자재의 수입은 2018년기준 43백만원으로 경미한 수준이나, 수출의존도가 높아 이로 인한 환율 변동에 따른 위험에 노출되어 있습니다. 또한 2018년기준 당사의 외화예금 및 외상매출금은 한화기준 9.3억원으로 자산총계 대비 4.17%이며 해외 매출의 경우 대금지급이 주로 USD 및 EUR로 이루어 지고 있기 때문에 환율 변동에 따른 수익성에 영향이 있을수 있습니다. 경영진은 내부적으로 환율 변동에 대한 환위험을 수시로 측정하고 관리하여 환율변동에 따른 환전일을 조정함으로써 환율변동에 따른 위험을 축소하고 있습니다. 그러나 당사에서는 향후 신성장동력으로 기존 제품외에 새로 개발하는 신약에 대해 해외매출을 적극적으로 추진하고 있으며 이로인해 기능통화 이외의 거래가 증가할것으로 예상하고 있는 상황입니다. 예측할수 없는 환율의 급변동 상황 또는 기존 매출처의 경영(제품지급 결제구조) 및 영업악화등의 경우가 발생될 경우 당사의 생산 및 매출에 부정적인 영향을 미칠수 있으니 투자자분들께서는 주의하시기 바랍니다. 자. 관리종목 편입 가능성에 따른 위험 당사는 2011년 7월 펩타이드 기술성 평가를 거쳐 코스닥시장 상장규정 제7조 2항의 기술성장기업의 상장특례를 적용받아 코스닥시장에 상장하였습니다. 기술성장기업으로 상장 시, 재무성과와 관련된 관리종목지정 요건에 대해 기술성장기업에 대한 특례를 받게 됩니다. 특례조항으로는 매출액 30억원 미만시 관리종목으로 지정되는 조건을 상장후 5년간 미적용, 자기자본50%이상(&10억원이상)의 법인세비용차감전 계속사업손실이 최근 3년간 2회이상일시 관리종목지정이 되는 요건을 상장후 3년간 미적용, 최근4사업연도 영업손실일시 관리종목지정이 되는 요건에 대한 미적용을 받고있습니다. 이에 따라, 당사는 상장 이후 지속적으로 영업손실이 발생하고 있음에도 불구하고, 상기와 같은 기술성장기업 특례요건에 의하여 관리종목으로 지정이 안되고 있습니다. 매출액 미달 요건및 법인세비용차감전계속사업손실 요건은 현재 기술성장기업의 특례조건 기간이 만료되어 적용받고 있으나, 최근 3년동안 지속적으로 해당 요건에 대하여 충족하고 있습니다. 당사의 경우 신고서 제출일 현재까지 상기 기준에 해당되는 사항은 없습니다. 그러나 시장 상황이 악화되거나 매출이 현저히 감소할 경우 또는 향후 지속적인 당기순손실에 의하여 자기자본이 감소할 경우 법인세차감전계속사업손실의 요건을 충족하지 못할 위험이 있습니다. 또한, 최근 상장 기업에 대한 금융감독기관 등의 관리감독기준이 엄격해지고 있는 상황으로 관련 규정을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다. 특히, "코스닥시장 상장규정 제28조(관리종목), 코스닥시장 상장규정 제38조(상장의 폐지) 및 코스닥시장 상장규정 제38조의2(실질심사위원회의 심사 등)"에 유의하시기 바랍니다. |
| 기타 투자위험 | 가. 환금 제한 및 원금손실 가능성 금번 유상증자 청약에 참여하여 신주를 배정받을 경우 신주의 추가상장일까지 환금성에 제약이 있으며, 청약 후 추가상장일 사이에 주가가 하락할 경우 원금에 대한 손해가 발생할 가능성이 있습니다. 투자자분들은 투자시 이점 유의하시기 바랍니다. 나. 주가 희석화 위험 당사의 증권신고서 제출일 현재 발행주식총수는 6,402,979주입니다. 금번 주주배정 후 실권주 일반공모 유상증자를 통해 발행예정인 주식수는 3,500,000주이며, 이는 당사 발행주식총수의 약 54.66%에 해당합니다. 금번 유상증자로 인하여 추가 발행 및 상장되는 주식으로 인하여 주가 희석화 및 물량출회에 따른 주가하락 위험이 존재합니다. 신주인수권증서를 매수하는 투자자는 할인율에 의해 발생하는 차익을 단기적으로 실현하기 위해 신주의 매매가 가능한 시점에 즉시 장내에서 매각할 가능성이 높으니 투자자분들은 투자시 이점에 유의하시기 바랍니다. 다. 잔액인수시 주가에 미치는 부정적 영향 우리사주조합 청약, 구주주 청약결과 실권주 및 단수주가 발행하는 경우 동 수량은 일반에게 공모할 예정이며, 일반공모에서도 청약이 미달될 경우 미달된 수량(최종 실권주)은 대표주관회사인 케이비증권이 인수할 계획입니다. 최종 실권주를 인수한 후 대표주관사가 수익 확정을 위해 잔액인수한 물량을 조기에 장내에서 대량 매도할 경우 일시적 물량 출회에 따른 주가 하락의 가능성이 존재하며, 인수한 최종 실권주를 일정 기간 보유하더라도 동 인수물량이 잠재매각물량으로 존재하여 주가 상승에는 부담으로 작용할 가능성이 높습니다. 또한, 대표주관사가 최종 실권주를 인수하게 되면 당사는 실권주 인수금액의 15.0%를 추가수수료로 지급하게 되며, 이를 고려하면 대표주관회사의 실권주 매입단가는 일반청약자들 보다 15.0% 낮은 것과 같은 결과가 초래됩니다. 이에 대표주관회사가 당사 주식을 인수한 후에 조기에 장내에서 매각할 가능성이 높으며, 이 경우 주가가 급락할 수 있습니다.또한, 당사는 증권신고서 제출일 현재 상환 또는 전환이 이루어지지 않은 제5회 사모 전환사채 46.5억원을 보유하고 있으며, 해당 전환사채의 전환권이 행사 될 경우 최대 465,279주가 잠재적으로 더 증가할 수 있습니다. 현재 당사 주가 하락 등의 이유로 전환권 행사 가능성은 제한적으로 판단되나, 만일 전환이 이루어 질 경우 주식수 증가에 따른 주가 희석이 발생하여 주가가 단기적으로 하락할 수 있으므로 이 점 유의하시기 바랍니다. 라. 발행가격 하락 위험 주식시장의 급격한 상황 악화 등으로 인하여 금번 유상증자 발행가격이 하락하면서 모집규모가 크게 줄어들 경우, 당사가 계획했던 사업추진 및 자금운용 등에 차질이 빚어지면서 사업실적 및 재무적 안정성에 부정적 영향을 미칠 수 있습니다. 투자자분들은 투자시 이점에 유의하시기 바랍니다. 마. 잘못된 정보제공 가능성 당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있습니다. 바. 유상증자 일정 변경 가능성 본 증권신고서는 공시심사 과정에서 일부 내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요 내용이 변경될 시에는 본 신고서상의 일정에 차질을 가져올수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있으므로 투자자들께서는 투자시 이러한 점을 감안하시기 바랍니다. 사. 청약자 유형별 배정에 따른 위험 금번 유상증자에서 우리사주조합 청약, 구주주 청약 종료 후 실권주 일반공모 진행 결과 고위험고수익투자신탁(코넥스 고위험고수익투자신탁 포함) 및 코스닥벤처펀드의 청약 수량이 최초 우선 배정된 10%와 30%에 미달하는 경우 해당 미달 수량을 일반 청약자에게 배정하게 되며, 그 결과 일반 청약자의 청약 경쟁률보다 실제 배정받는 물량이 훨씬 많을 수가 있습니다. 일반청약자들께서는 이점 유의하시어 투자 의사 결정하시기 바랍니다. 아. 기타 투자자 유의사항 본 건 유상증자를 통해 취득한 당사의 주식가치가 하락할 수 있으며, 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 투자자 여러분의 독자적인 판단에 의해야 함을 유의하시기 바랍니다. |
2. 모집 또는 매출에 관한 일반사항
| (단위 : 원, 주) |
| 증권의 종류 |
증권수량 | 액면가액 | 모집(매출) 가액 |
모집(매출) 총액 |
모집(매출) 방법 |
|---|---|---|---|---|---|
| 기명식보통주 | 3,500,000 | 500 | 7,590 | 26,565,000,000 | 주주배정후 실권주 일반공모 |
| 인수인 | 증권의 종류 |
인수수량 | 인수금액 | 인수대가 | 인수방법 | |
|---|---|---|---|---|---|---|
| 대표 | 케이비증권 | 기명식보통주 | - | - | 기본수수료 : 모집총액의 2.0% 추가수수료 : 잔액인수금액의 15.0% |
잔액인수 |
| 청약기일 | 납입기일 | 청약공고일 | 배정공고일 | 배정기준일 |
|---|---|---|---|---|
| 2019년 06월 10일 ~ 2019년 06월 11일 | 2019년 06월 18일 | 2019년 06월 13일 | 2019년 06월 18일 | 2019년 05월 02일 |
| 자금의 사용목적 | |
|---|---|
| 구 분 | 금 액 |
| 시설자금 | 2,000,000,000 |
| 차환자금 | 9,132,750,000 |
| 운영자금 | 14,832,588,300 |
| 발행제비용 | 599,661,700 |
| 신주인수권에 관한 사항 | ||
|---|---|---|
| 행사대상증권 | 행사가격 | 행사기간 |
| - | - | - |
| 매출인에 관한 사항 | ||||
|---|---|---|---|---|
| 보유자 | 회사와의 관계 |
매출전 보유증권수 |
매출증권수 | 매출후 보유증권수 |
| - | - | - | - | - |
| 일반청약자 환매청구권 | ||||
|---|---|---|---|---|
| 부여사유 | 행사가능 투자자 | 부여수량 | 행사기간 | 행사가격 |
| - | - | - | - | - |
| 【주요사항보고서】 | [정정] 주요사항보고서(유상증자결정)-2019.04.12 |
| 【기 타】 | 1) 상기 모집가액은 예정가액으로 구주주청약일 3거래일 전인 2019년 06월 04일에 최종발행가액이 확정되어 2019년 06월 05일에 회사의 인터넷 홈페이지(http://www.nibec.co.kr)에 공고되며, 정정 증권신고서(증권발행조건확정)가 금융감독원 전자공시시스템(http://dart.fss.or.kr)에 공시됩니다. 2) 금번 유상증자는 잔액인수방식에 의한 것입니다. 인수방법 및 인수대가에 대한 자세한 내용은'제1부 I. 5 인수등에 관한 사항'을 참고하여 주시기 바랍니다. 3) 상기 청약기일은 구주주청약일이며, 청약공고일은 실권주 일반공모 청약공고일입니다. 실권주 일반공모 청약일은 2019년 06월 10일 ~ 2019년 06월 11일까지 2일간 진행됩니다. 실권주 일반공모 청약의 공고는 회사의 인터넷 홈페이지(http://www.nibec.co.kr) 및 KB증권(주)의 인터넷 홈페이지에 게시됩니다. 4) 상기 모집금액 및 발행제비용은 예정가액을 기준으로 산정된 것으로 향후 변경될 수 있습니다. 발행제비용은 당사의 자체자금으로 사용할 예정입니다. 5) 금융감독원에서 본 증권신고서를 심사하는 과정에서 정정명령 조치를 취할 수 있으며, 만약 정정 명령이 발생할 경우에는 동 신고서에 기재된 일정이 변경될 수 있습니다. 6) 증권신고서의 효력 발생은 본 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. 7) 금번 나이벡 주식회사의 주주배정후 실권주 일반공모 유상증자의 대표주관회사는 KB증권(주)입니다. |
제1부 모집 또는 매출에 관한 사항
Ⅰ. 모집 또는 매출에 관한 일반사항
1. 공모개요
당사는 2019년 04월 02일 최초 이사회 결의 및 2019년 04월 12일 정정 이사회 결의를 통하여 '자본시장과 금융투자업에 관한 법률' 제165조의6 2항 1호에 의거 케이비증권(주)를 대표주관회사로 하여 잔액인수 계약을 체결하고 사전에 그 실권주를 일반에 공모하기로 하여 기명식 보통주 3,500,000주를 주주배정 후 실권주 일반공모 방식으로 발행하기로 결정하였으며, 동 증권의 개요는 다음과 같습니다.
| (단위 : 원, 주) |
| 증권의 종류 | 증권수량 | 액면가액 | 모집(매출)가액 | 모집(매출)총액 | 모집(매출) 방법 |
|---|---|---|---|---|---|
| 기명식보통주 | 3,500,000 | 500 | 7,590 | 26,565,000,000 | 주주배정후 실권주 일반공모 |
| ※ 최초 이사회 결의일: 2019년 04월 02일 정정 이사회 결의일 : 2019년 04월 12일 주) 1주의 모집가액 및 모집총액은 예정금액이며, 확정되지 아니한 금액입니다. |
발행가액은 '증권의발행및공시등에관한규정' 제5-18조 (유상증자의 발행가액 결정)에 의거, 주주배정증자시 할인율 등이 자율화 되어 자유롭게 산정할 수 있으나, 시장혼란 우려 및 기존 관행 등으로 '(구)유가증권의 발행 및 공시 등에 관한 규정' 제57조를 준용하여 산정할 예정입니다.
■ 모집예정가액 산출 근거
본 증권신고서의 모집예정가액은 최초 이사회결의일 직전 거래일(2019년 04월 01일)을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가, 1주일 가중산술평균주가 및 기산일 가중산술평균주가를 산술평균하여 산정한 가액과 기산일 가중산술평균주가 중 낮은 금액을 기준주가로 하여 아래의 산식에 따라 결정하며 할인율은 25%를 적용합니다. 단, 할인율 적용에 따른 모집가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다. (단, 호가단위 미만은 절상함)
| ▶ 모집예정가액 | = | 기준주가 X 【 1 - 할인율(25%) 】 ---------------------------------------- 1 + 【증자비율 X 할인율(25%)】 |
| [발행가액 산정표 (2019. 03. 02 ~ 2019. 04. 01)] | |
| (단위: 주, 원) | |
| 일수 | 일자 | 종가 | 거래량 | 거래대금 |
|---|---|---|---|---|
| 1 | 2019-04-01(월) | 11,600 | 194,725 | 2,239,588,450 |
| 2 | 2019-03-31(일) | |||
| 3 | 2019-03-30(토) | |||
| 4 | 2019-03-29(금) | 11,400 | 348,999 | 4,004,253,950 |
| 5 | 2019-03-28(목) | 12,000 | 878,848 | 10,591,464,700 |
| 6 | 2019-03-27(수) | 12,900 | 1,058,895 | 13,003,202,330 |
| 7 | 2019-03-26(화) | 9,930 | 29,238 | 287,671,950 |
| 8 | 2019-03-25(월) | 9,770 | 72,895 | 714,264,860 |
| 9 | 2019-03-24(일) | |||
| 10 | 2019-03-23(토) | |||
| 11 | 2019-03-22(금) | 10,150 | 38,429 | 388,882,700 |
| 12 | 2019-03-21(목) | 10,200 | 56,097 | 576,754,050 |
| 13 | 2019-03-20(수) | 10,550 | 58,377 | 603,353,500 |
| 14 | 2019-03-19(화) | 10,600 | 169,750 | 1,843,072,700 |
| 15 | 2019-03-18(월) | 10,500 | 36,273 | 378,284,900 |
| 16 | 2019-03-17(일) | |||
| 17 | 2019-03-16(토) | |||
| 18 | 2019-03-15(금) | 10,450 | 61,824 | 650,207,400 |
| 19 | 2019-03-14(목) | 10,750 | 44,924 | 483,357,100 |
| 20 | 2019-03-13(수) | 10,850 | 78,747 | 848,753,250 |
| 21 | 2019-03-12(화) | 10,600 | 85,367 | 889,893,600 |
| 22 | 2019-03-11(월) | 10,250 | 75,446 | 768,910,050 |
| 23 | 2019-03-10(일) | |||
| 24 | 2019-03-09(토) | |||
| 25 | 2019-03-08(금) | 10,450 | 60,292 | 628,985,850 |
| 26 | 2019-03-07(목) | 10,600 | 120,303 | 1,312,420,300 |
| 27 | 2019-03-06(수) | 11,350 | 78,460 | 900,207,200 |
| 28 | 2019-03-05(화) | 11,650 | 115,860 | 1,345,123,800 |
| 29 | 2019-03-04(월) | 11,700 | 193,597 | 2,231,284,200 |
| 30 | 2019-03-03(일) | |||
| 31 | 2019-03-02(토) | |||
| 1개월 가중산술평균주가 (A) | 11,586원 | |||
| 1주일 가중산술평균주가 (B) | 11,999원 | |||
| 기산일 가중산술평균주가 (C) | 11,501원 | |||
| A,B,C의 산술평균 (D) | 11,695원 | [(A)+(B)+(C)]/3 | ||
| 기준주가 (E) | 11,501원 | (C)와 (D)중 낮은 가액 | ||
| 할인율 (F) | 25.0% | |||
| 유상증자비율 (G) | 54.66% | |||
| 예정발행가액(호가단위 미만 절상) | 7,590원 | E x (1 - F) / (1 + (G x F)) | ||
■ 공모일정 등에 관한 사항
| 일자 | 내용 | 비고 |
|---|---|---|
| 2019년 04월 02일 | 신주발행 이사회결의 | - |
| 2019년 04월 02일 |
증권신고서 제출 | |
| 2019년 04월 03일 |
신주발행 및 기준일 공고 | 당사 인터넷 홈페이지 (http://www.nibec.co.kr) |
| 2019년 4월 12일 | (정정) 증권신고서 제출 | - |
| 2019년 04월 26일 |
1차 발행가액 확정 | 신주배정기준일 3거래일 전 |
| 2019년 04월 30일 | 권리락 | - |
| 2019년 05월 02일 | 신주배정 기준일 | (명부폐쇄 5/3~5/15) |
| 2019년 05월 16일 | 신주배정 통지 | - |
| 2019년 05월 23일~ 2019년 05월 29일 |
신주인수권증서 상장 거래기간 | 5거래일 이상 거래 |
| 2019년 05월 30일 |
신주인수권증서 상장 폐지 | 구주주 청약초일 5거래일 전 |
| 2019년 06월 04일 |
확정 발행가액 산정 | 구주주 청약초일 3거래일 전 |
| 2019년 06월 05일 | 확정 발행가액 공고 | 당사 인터넷 홈페이지 (http://www.nibec.co.kr) |
| 2019년 06월 10일 | 우리사주조합 청약 | - |
| 2019년 06월 10일~ 2019년 06월 11일 |
구주주 청약 및 초과청약 | - |
| 2019년 06월 13일 | 일반공모 청약 공고 | 당사 인터넷 홈페이지 (http://www.nibec.co.kr) 케이비증권(주) 홈페이지 (http://www.kbsec.com) |
| 2019년 06월 13일~ 2019년 06월 14일 |
일반공모 청약 | 고위험고수익투자신탁, 벤처기업투자신탁 청약 포함 |
| 2019년 06월 18일 |
환불 및 배정 공고 | - |
| 2019년 06월 18일 |
주금 납입 | - |
| 2019년 06월 28일 |
주권 교부 예정일 | - |
| 2019년 07월 01일 |
신주 상장 예정일 | - |
| 주) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정요구 등 조치를 취할 수 있으며, 정정요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다 |
2. 공모방법
■ 공모방법 : 주주배정후 실권주 일반공모
| [공모방법 : 주주배정후 실권주 일반공모] |
| 모 집 대 상 | 주 수(%) | 비 고 |
|---|---|---|
| 우리사주조합 청약 | 175,000주(5.0%) | - 우리사주조합 청약일 : 2019년 06월 10일(1일간) |
| 구주주 청약 (신주인수권증서 보유자) |
3,325,000(95.0%) | - 구주 1주당 신주 배정비율 : 1주당 0.51928953주 - 신주배정 기준일 : 2019년 05월 02일 - 보유한 신주인수권증서의 수량 한도로 청약가능(구주주에게는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율을 곱한 수량만큼의 신주인수권 증서가 배정됨) |
| 초과 청약 | - | - '자본시장과 금융투자업에 관한 법률' 제165조의6의 제2항 제2호에 의거 초과청약 - 초과청약비율 : 배정신주(신주인수권증서) 1주당 0.2주 - 신주인수권증서 거래를 통해서 신주인수권증서를 매매시 보유자 기준으로 초과청약 가능 |
| 일반모집 청약 (고위험고수익투자신탁 청약 포함) |
- | - 구주주 청약 후 발생하는 단수주 및 실권주에 대해 배정됨 |
| 합 계 | 3,500,000주(100.0%) |
- |
| 주1) | 본 건 유상증자는 주주배정후 실권주 일반공모 방식으로 진행되며, 구주주 청약결과 발생하는 실권주 및 단수주는 우선적으로 초과청약자에게 배정되고 이후 실권이 발생할 경우에 대해서는 일반에게 공모합니다. |
| 주2) | 구주주의 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율인 0.51928953주를 곱하여 산정된 배정주식수로 하되, 1주 미만은 절사합니다. 단, 신주배정기준일 현재 신주배정비율은 자기주식의 변동 등으로 인하여 변경될 수 있습니다. |
| 주4) | 신주인수권증서 보유자는 보유한 신주인수권증서 수량의 한도로 증서청약을 할 수 있고, 동 주식수에 초과청약비율(20%)를 곱한 수량을 한도로 초과청약 할 수 있습니다. 단 1주 미만은 절사합니다. (a) 청약한도 주식수 = 신주인수권증서청약 한도주식수 + 초과청약한도 주식수 (b) 신주인수권증서청약 한도주식수 = 보유한 신주인수권증서의 수량 (c) 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 X 초과청약 비율(20%) |
| 주5) | "코넥스 고위험고수익투자신탁"이란 최초 설정일·설립일로부터 매 3개월마다 코넥스 상장주식의 평균보유비율(코넥스 상장주식의 평가액이 고위험고수익투자신탁의 평가액에서 차지하는 매일의 비율을 3개월 동안 합산하여 같은 기간의 총일수로 나눈 비율을 말한다)이 100분의 2 이상인 고위험고수익투자신탁을 말합니다. 다만, 해당 투자신탁 등의 최초 설정일ㆍ설립일부터 수요예측 참여일까지의 기간이 6개월 미만인 경우에는 수요예측 참여일 직전 영업일의 코넥스 상장주식의 보유비율이 자산총액의 100분의 2 이상이어야 하며, 해당 투자신탁 등의 만기일까지의 잔존기간이 3개월 미만인 경우에는 본문의 평균보유비율을 적용하지 아니합니다. |
| 주6) | 코넥스 고위험고수익투자신탁에 해당되지 않는 고위험고수익투자신탁은 "일반 고위험고수익투자신탁"이라 칭하며, 고위험고수익투자신탁은 일반 고위험고수익투자신탁과 코넥스 고위험고수익투자신탁을 포괄하여 총칭하는 것으로 합니다. |
| 주7) | "벤처기업투자신탁"이란 조세특례제한법 제16조제1항제2호의 벤처기업투자신탁(대통령령 제28636호 조세특례제한법 시행령 일부개정령 시행 이후 설정된 벤처기업투자신탁에 한한다. 이하 같다)을 말합니다. |
| 주8) | 본 건 유상증자는 주권상장법인의 유상증자에 해당되므로, "증권 인수업무 등에 관한 규정" 제9조 제2항 제3호에 의거하여, 고위험고수익투자신탁 총 배정분은 전체 일반공모주식수의 10%를 배정하되, 이 중 코넥스 고위험고수익투자신탁에 대하여 전체 일반공모주식수의 5%를 우대 배정분으로 하며, 잔여 주식은 전체 고위험고수익투자신탁(우대 배정을 받은 코넥스 고위험고수익투자신탁 포함)을 대상으로 배정하기로 합니다. 또한 "증권 인수업무 등에 관한 규정" 제9조 제2항 제4호에 의거하여, 벤처기업투자신탁 총 배정분은 전체 일반공모주식수의 30%를 배정하기로 합니다. 이외 일반청약자 총 배정분은 전체 일반공모주식수의 60%를 배정합니다. ① 1단계: 총 청약물량이 일반공모 배정분 주식수를 초과하는 경우, 각 청약자에 5사6입을 원칙으로 안분 배정하여 잔여주식이 최소화되도록 합니다. 다만, 고위험고수익투자신탁에 대한 공모주식 10%와 벤처기업투자신탁에 대한 공모주식 30%와 개인투자자 및 기관투자자(집합투자업자포함)에 대한 공모주식 60%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정합니다. 다만, 어느 한 그룹에서 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다. ② 2단계: 1단계 배정 후 최종 잔여주식은 최대청약자부터 순차적으로 1주씩 우선배정하되, 동순위 최대청약자가 최종 잔여주식보다 많은 경우에는 대표주관회사가 무작위 추첨방식을 통하여 배정합니다. |
| 주9) | 일반공모 청약을 완료한 주식 수의 합계가 모집하여야 할 주식 수에 미달하는 경우 미달된 잔여주식은 대표주관회사인 케이비증권(주)가 100%를 자기계산으로 이를 인수합니다. |
| 주10) | '증권 인수 업무 등에 관한 규정' 제9조 제2항에 의거 일반청약자(고위험고수익투자신탁 포함)에 대하여 배정하여야 할 주식이 50,000주 이하(액면가 500원 기준)이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 이를 청약자에게 배정하지 아니하고 대표주관회사가 자기 계산으로 인수할 수 있습니다. |
▶ 구주주 1주당 배정비율 산출근거
| 구 분 | 상세내역 |
|---|---|
| A. 보통주식수 | 6,402,979주 |
| B. 우선주식수 | - |
| C. 발행주식총수 (A+B) | 6,402,979주 |
| D. 자기주식수 | - |
| E. 자기주식을 제외한 발행주식총수 (C-D) | 6,402,979주 |
| F. 유상증자 주식수 | 3,500,000주 |
| G. 증자비율 (F/C) | 54.662056% |
| H. 우리사주조합 배정 | 175,000주 |
| H. 구주주 배정주식수 (F) | 3,325,000주 |
| I. 구주주 1주당 배정주식수 (I/E) | 0.51928953 |
3. 공모가격 결정방법
「증권의 발행 및 공시 등에 관한 규정」 제5-18조에 의거 주주배정 증자 시 가격산정 절차 폐지 및 가격산정의 자율화에 따라 발행가액을 자유롭게 산정할 수 있으나, 시장혼란 우려 및 기존 관행 등으로 (舊)「유가증권의 발행 및 공시등에 관한 규정」 제57조를 일부 준용하여 아래와 같이 산정합니다. 다만,「자본시장과 금융투자업에 관한 법률」 제165조의6 및 「증권의 발행 및 공시 등에 관한 규정 제5-15조의2」에 의거하여 1차 발행가액과 2차 발행가액 중 낮은 가액이 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격보다 낮은 경우, 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격을 확정발행가액으로 합니다.(1차 발행가액, 2차 발행가액, 확정발행가액 산정 시 호가 단위 미만은 호가 단위로 절상함) 단, 확정발행가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다.
① 1차 발행가액 산정: 신주배정기준일(2019년 05월 02일)전 제3거래일(2019년 04월 26일)을 기산일로 하여 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1개월 가중산술평균주가, 1주일 가중산술평균주가 및 기산일 가중산술평균주가를 산술평균하여 산정한 가액과 기산일 가중산술평균주가 중 낮은 금액을 기준주가로 하여 할인율은 25%를 적용하여 아래의 산식에 의하여 산정된 발행가액으로 합니다. 단, 할인율 적용에 따른 모집가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다. (단, 주가 호가단위 미만은 절상함)
▶ 1차 발행가액 |
= |
기준주가 X 【 1 - 할인율(25%) 】 ------------------------------------------- 1 + 【증자비율 X 할인율(25%)】 |
② 2차 발행가액 산정: 구주주 청약일(2019년 06월 10일~11일)의 초일 전 제3거래일(2019년 06월 04일)을 기산일로 코스닥시장에서 성립된 거래대금을 거래량으로 가중산술평균한 1주일 가중산술평균주가 및 기산일 가중산술평균주가를 산술평균하여 산정한 가액과 기산일 가중산술평균주가 중 낮은 금액을 기준주가로 하여 할인율은 25%를 적용하여 아래의 산식에 의하여 산정된 발행가액으로 합니다. 단, 할인율 적용에 따른 모집가액이 액면가액 이하일 경우에는 액면가액을 발행가액으로 합니다. (단, 주가호가단위 미만은 절상함)
▶ 2차 발행가액 = 기준주가 ×【1 - 할인율(25%)】
③ 확정 발행가액 산정: 확정 발행가액은 ①의 1차 발행가액과 ②의 2차 발행가액 중 낮은 가액으로 합니다. 단, 『증권의 발행 및 공시 등에 관한 규정』 제5-15조의2에 의거, 청약일 전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가를 기준주가로 할인율 40%를 적용하여 산정한 가액이 확정 발행가액을 초과하는 경우 동 금액을 확정 발행가액으로 합니다.
▶ 확정 발행가액 = MAX[MIN[1차 발행가액, 2차 발행가액], 기준주가의 60%]
④ 모집가액 확정공시에 관한 사항: 1차 발행가액은 2019년 04월 26일에 결정되고, 2019년 04월 29일에 금융감독원 전자공시시스템에 공시됩니다. 확정 발행가액은 2019년 06월 04일에 결정되어 2019년 06월 05일에 금융감독원 전자공시시스템에 공시될 예정이며, 회사의 인터넷 홈페이지(http://www.nibec.co.kr)에 공고됩니다. 확정 발행가액 결정에 따라 정정 증권신고서(증권발행조건확정)가 금융감독원 전자공시시스템(http://dart.fss.or.kr)에 공시됩니다.
※ 일반공모 발행가액은 구주주청약시에 적용된 확정 발행가액을 동일하게 적용합니다.
4. 모집 또는 매출절차 등에 관한 사항
가. 모집 또는 매출 조건
| (단위 : 주, 원) |
| 항 목 | 내 용 | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 모집 또는 매출주식의 수 | 3,500,000 | |||||||||||||||||||||||||||||||
| 주당 모집가액 또는 매출가액 | 예정가액 | 7,590 | ||||||||||||||||||||||||||||||
| 확정가액 | - | |||||||||||||||||||||||||||||||
| 모집총액 또는 매출총액 | 예정가액 | 26,565,000,000 | ||||||||||||||||||||||||||||||
| 확정가액 | - | |||||||||||||||||||||||||||||||
| 청 약 단 위 |
(1) 우리사주조합 / 구주주(신주인수권증서 보유자) : 1주
|
|||||||||||||||||||||||||||||||
| 청약기일 | 우리사주조합 | 개시일 | 2019년 06월 10일 |
| 종료일 | 2019년 06월 10일 |
||
| 구주주 (신주인수권증서 보유자) |
개시일 | 2019년 06월 10일 |
|
| 종료일 | 2019년 06월 11일 |
||
| 일반모집 또는 매출 | 개시일 | 2019년 06월 13일 |
|
| 종료일 | 2019년 06월 14일 | ||
| 청약 증거금 |
우리사주조합 | 청약금액의 100% | |
| 구주주(신주인수권증서 보유자) | 청약금액의 100% | ||
| 초 과 청 약 | 청약금액의 100% | ||
| 일반모집 또는 매출 | 청약금액의 100% | ||
| 납 입 기 일 / 환 불 일 | 2019년 06월 18일 |
||
| 배당기산일(결산일) | 2019년 01월 01일 | ||
| 주1) 본 증권신고서는 금융감독원에서 심사하는 과정에서 정정 요구 등 조치를 취할 수 있으며, 정정 요구 등에 따라 동 신고서에 기재된 일정이 변경될 수 있습니다. 본 증권신고서의 효력 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 유가증권의 가치를 보증 또는 승인한 것이 아니므로 본 유가증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다. 주2) 상기 일정은 유관기관과의 협의 과정에 의하여 변경될 수 있습니다. |
나. 모집 또는 매출의 절차
(1) 공고의 일자 및 방법
| 구 분 | 공고일자 | 공고방법 |
|---|---|---|
| 신주 발행 및 배정기준일(주주확정일) 공고 |
2019년 04월 03일 | 회사 인터넷 홈페이지 (http://www.nibec.co.kr) |
| 모집가액 확정의 공고 | 2019년 06월 05일 | 회사 인터넷 홈페이지 (http://www.nibec.co.kr) |
| 실권주 일반공모 청약공고 | 2019년 06월 13일 | 회사 인터넷 홈페이지 (http://www.nibec.co.kr) KB증권 홈페이지 (http://www.kbsec.co.kr) |
| 실권주 일반공모 배정공고 | 2019년 06월 18일 | KB증권 홈페이지 (http://www.kbsec.co.kr) |
| 주) 청약결과 초과청약금 환불에 대한 통지는 대표주관회사의 홈페이지에 게시함으로써 개별통지에 갈음합니다. |
(2) 청약방법
① 우리사주조합의 청약은 우리사주조합장 명의로 청약사무 취급처에서 일괄 청약합니다.
② 구주주 중 주권을 증권회사에 예탁한 실질주주는 주권을 예탁한 증권회사의 본ㆍ지점 및 "대표주관회사"의 본ㆍ지점에서 청약할 수 있습니다. 다만, 구주주 중 증권회사에 예탁하지 않고 자기명의의 주권을 직접 보유하고 있는 명부상 주주는 신주배정통지서를 첨부하여 실명확인증표를 제시한 후 "대표주관회사"의 본ㆍ지점에서 청약할 수 있습니다. 청약시에는 소정의 청약서 2통에 필요한 사항을 기입하여 청약증거금과 함께 제출하여야 합니다.
③ 신주인수권증서 청약을 한 자에 한하여 신주인수권증서 청약 한도 주식수의 20%를 추가로 청약할 수 있습니다. 이때, 신주인수권증서 청약 한도주식수의 20%에 해당하는 주식 중 소수점 이하인 주식은 청약할 수 없습니다.
④ 일반공모 청약 : 해당 청약사무 취급처에서 사전에 정하여 공시하는 청약방법에 따라 청약사무취급처에 실명확인증표와 소정의 청약서, 청약증거금을 제시하고 청약합니다. 단, 청약증거금은 청약금액의 100%로 하며, 청약증거금은 주금납입일에 납입금으로 대체하되, 청약증거금에 대해서는 무이자로 합니다. 각 청약처별 다중청약은 가능하나, 한개의 청약처에서 이중청약은 불가능하며, 집합투자기구 중 운용주체가 다른 집합투자기구를 제외한 청약자의 한 개의 청약처에 대한 복수청약은 불가능합니다. 고위험고수익투자신탁(코넥스고위험고수익투자신탁 포함)은 청약 시, 청약사무 취급처에 '증권 인수업무 등에 관한 규정' 제2조 제18호(코넥스고위험고수익투자신탁일 경우 동 규정 제2조 제19호)에 따른 요건을 충족하고, 제9조 제4항에 해당하지 않음을 확약하는 서류 및 자산총액이 기재되어 있는 서류를 함께 제출하여야 합니다. 벤처기업투자신탁은 청약 시, 청약사무 취급처에 '증권 인수업무 등에 관한 규정' 제2조 제20호에 따른 요건을 충족하고, 제9조 제10항에 따른 확약서 및 자산총액이 기재되어 있는 서류를 함께 제출하여야 합니다.
⑤ 청약은 청약주식의 단위에 따라 될 수 있으며 1인당 청약한도를 초과하는 청약부분에 대하여는 청약이 없는 것으로 하고 청약사무 취급처는 그 차액을 납입일까지 당해 청약자에게 반환하며, 이때 받은 날부터의 이자는 지급하지 아니합니다.
⑥ 기타
a. 일반공모 배정을 함에 있어 이중청약이 있는 경우에는 그 청약자의 청약 전부를 청약하지 아니한 것으로 봅니다. 단, 구주주가 신주배정비율에 따라 배정받은 주식을 청약한 후 일반공모에 참여하는 경우에는 금지되는 이중청약이 있는 경우로 보지 않습니다.
b. 1인당 청약한도를 초과하는 청약부분에 대하여는 청약이 없는 것으로 합니다.
c. 청약자는 '금융실명거래 및 비밀보장에 관한 법률'에 의거 실지 명의에 의해 청약해야 합니다.
⑦ 청약한도
a. 구주주(신주인수권증서 보유자)의 개인별 청약한도는 신주배정기준일 현재 주주명부에 기재된 소유주식 1주당 신주배정비율인 0.51928953주를 곱하여 산정된 신주인수권증서(단, 1주 미만은 절사)와 초과청약가능 주식수(보유하고 있는 신주인수권증서 1주당 0.2주를 곱하여 산정된 수, 단 1주 미만은 절사)를 합한 주식수로 하되, 자기주식 및 자사주신탁 등의 자기주식 변동으로 인하여 구주주의 1주당 배정 비율은 변동될 수 있습니다.
b.. 일반공모 청약자의 청약한도는 일반공모 총 공모주식 범위 내로 하며, 청약한도를 초과하는 부분에 대해서는 청약이 없는 것으로 간주합니다.
(3) 청약취급처
| 청약대상자 | 청약취급처 | 청약일 | |
|---|---|---|---|
| 우리사주조합 | 케이비증권(주)의 본ㆍ지점 | 2019.06.10 | |
| 구주주 (신주인수권증서 보유자) |
명부주주 (실질주주가 아닌 주주명부 등재 주주) |
케이비증권(주)의 본ㆍ지점 | 2019.06.10 ~ 2019.06.11 |
| 실질주주 | 1) 주주확정일 현재 (주)나이벡의 주식을 예탁하고 있는 당해 증권회사 본ㆍ지점 2) 케이비증권(주)의 본ㆍ지점 |
||
| 일반공모청약 (고위험고수익투자신탁 청약 포함) |
케이비증권(주)의 본ㆍ지점, 홈페이지, HTS | 2019.06.13 ~ 2019.06.14 |
|
(4) 청약결과 배정방법
① 우리사주조합 : 총 발행주식의 5.0%인 175,000주는 우리사주조합에게 우선 배정합니다.
② 구주주 청약 : 신주배정기준일(2019년 05월 02일 예정) 18시 현재 주주명부에 등재된 주주(이하 "구주주"라 한다)에게 본 주식을 1주당 0.51928953주를 곱하여 산정된 배정주식수(단, 1주 미만은 절사함)로 하고, 배정범위 내에서 청약한 수량만큼 배정합니다. 단, 신주배정기준일 전 자기주식 및 자기주식신탁 등의 자기주식 변동으로 인하여 1주당 배정주식수가 변동될 수 있습니다.
② 초과청약에 대한 배정: 구주주(신주인수권증서 보유자) 청약 이후 발생한 실권주가 있는 경우, 실권주를 구주주(신주인수권증서 보유자)가 초과청약(초과청약비율 : 배정 신주 1주당 0.2주)한 주식수에 비례하여 배정하며(단, 초과청약 주식수가 실권주에 미달한 경우 100% 배정), 1주 미만의 주식은 절사하여 배정하지 않습니다.
(i) 청약한도 주식수 = 신주인수권증서청약 한도주식수 + 초과청약 한도주식수
(ii) 신주인수권증서청약 한도주식수 = 보유한 신주인수권 증서의 수량
(iii) 초과청약 한도주식수 = 신주인수권증서청약 한도주식수 X 초과청약 비율(20%)
③ 일반공모 청약: 상기 우리사주조합 청약, 구주주 청약 및 초과청약 결과 발생한 실권주 및 단수주는 대표주관회사가 다음 각호와 같이 일반에게 공모하되, '증권 인수업무 등에 관한 규정' 제9조 제2항 제3호에 따라 고위험고수익투자신탁에 공모주식의 10%를 배정하고, 이 배정분 중 코넥스 고위험고수익투자신탁에는 50%를 우대배정하며, "증권 인수업무 등에 관한 규정" 제9조 제2항 제4호에 따라 벤처기업투자신탁에 공모주식의 30%를 배정합니다. 나머지 60%에 해당하는 주식은 개인청약자 및 기관투자자에게 구분 없이 배정합니다. 고위험고수익투자신탁(코넥스 고위험고수익투자신탁을 포함한다)에 대한 공모주식 10%와 벤처기업투자신탁에 공모주식의 30%와 개인투자자 및 기관투자자에 대한 공모주식 60%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정합니다. 다만, 증권인수업무 등에 관한 규정 제9조 제3항에 따라 어느 한 그룹에서 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다.
(i) 일반공모 청약결과 일반공모 총 청약자의 청약주식수가 공모주식수를 초과하는 경우에는 청약경쟁률에 따라 5사6입을 원칙으로 안분 배정하여 잔여주식이 최소화되도록 합니다. 다만, 고위험고수익투자신탁에 대한 공모주식 10%와 벤처기업투자신탁에 공모주식의 30%와 개인투자자 및 기관투자자(집합투자업자포함)에 대한 공모주식 60%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정합니다. 다만, 어느 한 그룹에서 청약미달이 발생할 경우, 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다. 이후 최종 잔여주식은 최고청약자부터 순차적으로 우선 배정하되, 동순위 최고청약자가 최종 잔여 주식보다 많은 경우에는 "대표주관회사"가 무작위 추첨방식을 통하여 배정합니다.
(ii) 일반공모 청약결과 일반공모 총 청약주식수가 일반공모 주식수에 미달하는 경우에는 청약주식수대로 배정합니다. 배정결과 발생하는 잔여주식은 "대표주관회사"가 잔액인수계약서 내용에 따른 인수비율에 따라 자기계산으로 인수합니다.
④ 단, "대표주관회사"는 '증권 인수업무 등에 관한 규정' 제9조 제2항에 의거 고위험고수익투자신탁 및 일반청약자에 대하여 배정하여야 할 주식이 50,000주(액면가 500원 기준) 이하 이거나, 배정할 주식의 공모금액이 1억원 이하인 경우에는 일반청약자에게 배정하지 아니할 수 있습니다.
(5) 투자설명서 교부에 관한 사항
- '자본시장과 금융투자업에 관한 법률' 제124조에 의거, 본 주식의 청약에 대한 투자설명서 교부 의무는 (주)나이벡, "대표주관회사"가 부담하며, 금번 유상증자의 청약에 참여하시는 투자자께서는 투자설명서를 의무적으로 교부받으셔야 합니다.
- 금번 유상증자에 청약하고자 하는 투자자께서는 (동법 제9조 제5항에 규정된 전문투자자 및 동법 시행령 제132조에 따라 투자설명서의 교부가 면제되는 자 제외) 청약하시기 전 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
- 투자설명서 수령거부 의사표시는 서면, 전화, 전신, 모사전송, 전자우편 및 이와 비슷한 전자통신, 그 밖에 금융위원회가 정하여 고시하는 방법으로 가능합니다.
① 투자설명서 교부 방법 및 일시
|
구분 |
투자설명서 교부 방법 |
교부 일시 |
|---|---|---|
|
우리사주조합 청약자 |
'자본시장과 금융투자업에 관한 법률'시행령 제132조에 의해 |
해당사항 없음 |
|
구주주 |
1), 2), 3)을 병행 |
|
|
1) 우편 송부 |
구주주 청약초일 전까지 수취가능 |
|
|
2) 케이비증권(주)의 본ㆍ지점 교부 |
구주주(신주인수권증서) |
|
|
3) 케이비증권(주)의 홈페이지 및 HTS 교부 |
||
|
일반 |
1), 2)를 병행 |
|
|
1) 케이비증권(주)의 본ㆍ지점 교부 |
일반공모 청약종료일까지 |
|
|
2) 케이비증권(주)의 홈페이지, HTS 교부 |
||
※ 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
② 확인절차
a. 우편을 통한 투자설명서 수령시
- 청약하시기 위해 지점을 방문하셨을 경우, 직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
- HTS를 통한 청약을 원하시는 경우, 청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
- 주주배정 유상증자의 경우 유선청약이 가능합니다. 유선상으로 신분확인을 하신 후, 투자설명서 교부 확인을 해주시고 청약을 진행하여 주시기 바랍니다.
b. 지점 방문을 통한 투자설명서 수령시
직접 투자설명서 교부확인서를 작성하시고 청약을 진행하시기 바랍니다.
c. 홈페이지 또는 HTS를 통한 교부
청약화면에 추가된 투자설명서 다운로드 및 투자설명서 교부 확인에 체크가 선행되어야 청약업무 진행이 가능합니다.
※ 청약취급처, 청약자 유형별 청약방법 요약
[ 청약사무취급처]
(가) 우리사주조합 : 케이비증권(주)의 본, 지점
(나) 구주주 중 실질주주 : 주권을 예탁한 증권회사 및 케이비증권(주) 본, 지점
(다) 구주주 중 명부주주 : 케이비증권(주)의 본, 지점
(라) 일반공모 청약자 : 케이비증권(주)의 본, 지점
| 청약취급처 | 청약방법 | 청약절차 | |
|---|---|---|---|
| 구주주 | 실권주 일반청약자 | ||
| 대표주관회사: 케이비증권(주) |
영업점 내방 청약 | 투자설명서 교부확인 후 청약가능 (단, 투자설명서 수령을 거부할 경우에는 수령거부 확인서류 제출 후 청약) |
투자설명서 교부확인 후 청약가능 (단, 투자설명서 수령을 거부할 경우에는 수령거부 확인서류 제출 후 청약) |
| HTS 및 인터넷 홈페이지를 통한 청약 |
투자설명서를 교부 받은 것에 대한 확인의 절차를 거친 후 청약 | ① 투자설명서를 전자문서의 형태로 다운로드 받는 것에 대한 사전 동의 ② 투자설명서의 다운로드 ③ 투자설명서를 교부 받은 것에 대한 확인상기의 절차를 거친 후 청약 |
|
| 유선청약 | 투자설명서를 교부 받은 것에 대한 확인의 절차를 거친 후 청약(녹취를 통한 확인) | * 실권주 일반공모 청약시 유선청약은 시행하지 않습니다. | |
③ 기타
a. 금번 유상증자의 경우, 본 증권신고서의 효력발생 이후 주주명부상 주주분들에게 투자설명서를 우편으로 발송할 예정입니다. 우편의 반송 등에 의한 사유로 교부를 받지 못하신 투자자께서는, 지점방문을 통해 인쇄물을 받으실 수 있으며, 또한 동일한 내용의 투자설명서를 전자문서의 형태로 케이비증권(주)의 홈페이지에서 다운로드 받으실 수 있습니다. 다만, 전자문서의 형태로 교부받으실 경우, 「자본시장과 금융투자업에 관한 법률」 제124조 제1항 각호의 요건을 모두 충족해야만 청약이 가능합니다.
b. 구주주 청약시 케이비증권(주) 이외의 증권회사를 이용한 청약 방법
해당 증권회사의 청약방법 및 규정에 의해 청약을 진행하시기 바랍니다. 이 경우에도, 본 투자설명서의 교부에 대한 확인 등의 절차를 수행하지 아니하면, 금번 유상증자의 청약에 참여하실 수 없음에 유의하시기 바랍니다.
※ 투자설명서 교부를 받지 않거나, 수령거부의사를 서면 등의 방법으로 표시하지 않을 경우, 본 유상증자의 청약에 참여할 수 없습니다.
| ※ 관련법규 <자본시장과 금융투자업에 관한 법률> 제9조 (그 밖의 용어의 정의) ⑤ 이 법에서 "전문투자자"란 금융투자상품에 관한 전문성 구비 여부, 소유자산규모 등에 비추어 투자에 따른 위험감수능력이 있는 투자자로서 다음 각 호의 어느 하나에 해당하는 자를 말한다. 다만, 전문투자자 중 대통령령으로 정하는 자가 일반투자자와 같은 대우를 받겠다는 의사를 금융투자업자에게 서면으로 통지하는 경우 금융투자업자는 정당한 사유가 있는 경우를 제외하고는 이에 동의하여야 하며, 금융투자업자가 동의한 경우에는 해당 투자자는 일반투자자로 본다. <개정 2009.2.3> 1. 국가 2. 한국은행 3. 대통령령으로 정하는 금융기관 4. 주권상장법인. 다만, 금융투자업자와 장외파생상품 거래를 하는 경우에는 전문투자자와 같은 대우를 받겠다는 의사를 금융투자업자에게 서면으로 통지하는 경우에 한한다. 5. 그 밖에 대통령령으로 정하는 자 제124조 (정당한 투자설명서의 사용) ① 누구든지 증권신고의 효력이 발생한 증권을 취득하고자 하는 자(전문투자자, 그 밖에 대통령령으로 정하는 자를 제외한다)에게 제123조에 적합한 투자설명서(집합투자증권의 경우 투자자가 제123조에 따른 투자설명서의 교부를 별도로 요청하지 아니하는 경우에는 제2항제3호에 따른 간이투자설명서를 말한다. 이하 이 항 및 제132조에서 같다)를 미리 교부하지 아니하면 그 증권을 취득하게 하거나 매도하여서는 아니 된다. 이 경우 투자설명서가 제436조에 따른 전자문서의 방법에 따르는 때에는 다음 각 호의 요건을 모두 충족하는 때에 이를 교부한 것으로 본다.<개정 2013.5.28> 1. 전자문서에 의하여 투자설명서를 받는 것을 전자문서를 받을 자(이하 "전자문서수신자"라 한다)가 동의할 것 2. 전자문서수신자가 전자문서를 받을 전자전달매체의 종류와 장소를 지정할 것 3. 전자문서수신자가 그 전자문서를 받은 사실이 확인될 것 4. 전자문서의 내용이 서면에 의한 투자설명서의 내용과 동일할 것 <자본시장과 금융투자업에 관한 법률 시행령> 제11조 (증권의 모집·매출) ① 법 제9조제7항 및 제9항에 따라 50인을 산출하는 경우에는 청약의 권유를 하는 날 이전 6개월 이내에 해당 증권과 같은 종류의 증권에 대하여 모집이나 매출에 의하지 아니하고 청약의 권유를 받은 자를 합산한다. 다만, 다음 각 호의 어느 하나에 해당하는 자는 합산 대상자에서 제외한다. <개정 2009.10.1, 2010.12.7, 2013.6.21, 2013.8.27> 1. 다음 각 목의 어느 하나에 해당하는 전문가 가. 제10조제1항제1호부터 제4호까지의 자 나. 제10조제3항제12호·제13호에 해당하는 자 중 금융위원회가 정하여 고시하는 자 다. 「공인회계사법」에 따른 회계법인 라. 신용평가회사(법 제335조의3에 따라 신용평가업인가를 받은 자를 말한다. 이하 같다) 마. 발행인에게 회계, 자문 등의 용역을 제공하고 있는 공인회계사·감정인·변호사·변리사·세무사 등 공인된 자격증을 가지고 있는 자 바. 그 밖에 발행인의 재무상황이나 사업내용 등을 잘 알 수 있는 전문가로서 금융위원회가 정하여 고시하는 자 2. 다음 각 목의 어느 하나에 해당하는 연고자 가. 발행인의 최대주주(법 제9조제1항제1호에 따른 최대주주를 말한다. 이하 같다)와 발행주식총수의 100분의 5 이상을 소유한 주주 나. 발행인의 임원(「상법」 제401조의2제1항 각 호의 자를 포함한다. 이하 이 호에서 같다) 및 「근로복지기본법」에 따른 우리사주조합원 다. 발행인의 계열회사와 그 임원 라. 발행인이 주권비상장법인(주권을 모집하거나 매출한 실적이 있는 법인은 제외한다)인 경우에는 그 주주 마. 외국 법령에 따라 설립된 외국 기업인 발행인이 종업원의 복지증진을 위한 주식매수제도 등에 따라 국내 계열회사의 임직원에게 해당 외국 기업의 주식을 매각하는 경우에는 그 국내 계열회사의 임직원 바. 발행인이 설립 중인 회사인 경우에는 그 발기인 사. 그 밖에 발행인의 재무상황이나 사업내용 등을 잘 알 수 있는 연고자로서 금융위원회가 정하여 고시하는 자 제132조 (투자설명서의 교부가 면제되는 자) 법 제124조제1항 각 호 외의 부분 전단에서 "대통령령으로 정하는 자"란 다음 각 호의 어느 하나에 해당하는 자를 말한다. <개정 2009.7.1, 2013.6.21> 1. 제11조 제1항 제1호 다목부터 바목까지 및 같은 항 제2호 각 목의 어느 하나에 해당하는 자 1의2. 제11조제2항제2호 및 제3호에 해당하는 자 2. 투자설명서를 받기를 거부한다는 의사를 서면, 전화·전신·모사전송, 전자우편 및 이와 비슷한 전자통신, 그 밖에 금융위원회가 정하여 고시하는 방법으로 표시한 자 3. 이미 취득한 것과 같은 집합투자증권을 계속하여 추가로 취득하려는 자. 다만, 해당 집합투자증권의 투자설명서의 내용이 직전에 교부한 투자설명서의 내용과 같은 경우만 해당한다. |
(6) 주권교부에 관한 사항
a. 주권교부예정일: 2019년 06월 28일(단, 유관기관과의 업무 협의 과정에서 상기 일정은 변경될 수 있음을 유의하여주시기 바랍니다.)
b. 주권교부장소: 명의개서대행기관(국민은행 증권대행부)
c. '자본시장과 금융투자업에 관한 법률' 제309조 제5항의 규정에 의한 신청을 한 경우, 해당청약자에게 배정된 주식은 한국예탁결제원의 명의로 일괄발행되고 동 주권은 청약취급처의 장부상 계좌에 자동입고됩니다.
| ※ 관련법규 <자본시장과 금융투자업에 관한 법률> 제309조 ⑤ 예탁자 또는 그 투자자가 증권등을 인수 또는 청약하거나, 그 밖의 사유로 새로 증권등의 발행을 청구하는 경우에 그 증권등의 발행인은 예탁자 또는 그 투자자의 신청에 의하여 이들을 갈음하여 예탁결제원을 명의인으로 하여 그 증권등을 발행 또는 등록(「국채법」 또는 「공사채등록법」에 따른 등록을 말한다. 이하 이 절에서 같다)할 수 있다. |
(7) 청약증거금의 대체 및 반환 등에 관한 사항
청약증거금은 청약금액의 100%로 하고, 주금납입기일에 주금납입금으로 대체하며, 청약증거금에 대해서는 무이자로 합니다.
(8) 주금납입장소 : IBK기업은행 대학로지점
다. 신주인수권증서에 관한 사항
| 신주배정기준일 | 신주인수권증서의 매매 금융투자업자 | |
|---|---|---|
| 회사명 | 회사고유번호 | |
| 2019년 05월 02일 | 케이비증권(주) | 00164876 |
(1) 금번과 같이 주주배정방식의 유상증자를 실시할 때, 주주가 소유하고 있는 주식수 비율대로 신주를 인수할 권리인 신주인수권에 대하여 당사는 '자본시장과 금융투자업에 관한 법률' 제165의 6조 3항 및 '증권의발행및공시등에관한규정' 제5-19조에 의거하여 주주에게 신주인수권증서를 발행합니다.
(2) 신주인수권증서 매매의 중개를 할 증권회사는 케이비증권(주)로 합니다.
(3) 청구기간: 신주배정통지일(2019년 05월 16일)로부터 구주주청약 개시일(2019년 06월 10일)의 전영업일(2019년 06월 07일)까지
(4) 신주인수권증서 발행 청구 절차
① 명부주주의 경우 신주인수권증서를 매매하고자 하는 명부주주는 명의개서대리인인 국민은행 증권대행부에 신주인수권증서의 발행을 청구합니다. 신주인수권증서의 매매는 거래상대방과의 신주인수권증서 실물 양도를 통하여 이루어집니다. 신주인수권증서의 매수자는 청약일에 신주인수권증서를 지참하여 케이비증권(주)에 해당 신주인수권증서에 기재되어 있는 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
② 신주인수권증서를 매매하고자 하는 실질주주는 위탁 증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자 계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
(5) 신주인수권증서를 양수한 투자자의 청약방법
신주인수권증서 실물을 보유하고 있는 양수인은 신주인수권증서를 지참하여 케이비증권(주)의 본점 및 지점에서 해당 신주인수권증서에 기재 되어있는 수량만큼 청약할 수 있으며 청약 기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. 또한 신주인수권증서를 증권회사에 예탁하고 있는 양수인은 당해 증권회사 점포 및 케이비증권(주)의 본점 및 지점을 통해 해당 신주인수권증서에 기재되어 있는 수량만큼 청약할 수 있으며 청약 기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다.
(6) 당사는 금번 주주배정후 실권주 일반공모 유상증자 관련 신주인수권증서의 상장을 한국거래소에 신청할 예정입니다. 동 신주인수권증서가 상장될 경우 상장기간은 2019년 05월 23일부터 2019년 05월 29일까지 5거래일간으로 예정하고 있으며, 동 기간 중 상장된 신주인수권증서를 한국거래소에서 매매할 수 있습니다. 동 신주인수권증서는 2019년 05월 30일에 상장폐지될 예정입니다. (코스닥시장상장규정 제150조 "신규상장"에 따라 5거래일 이상 상장되어야 하며,동 규정 제152조 "신주인수권증서의 상장폐지기준"에 따라 주주청약 개시일 5거래일전에 상장폐지되어야 함)
(7) 신주인수권증서의 거래 관련 추가사항
당사는 금번 유상증자의 신주인수권증서를 상장신청할 예정인 바, 현재까지 관계기관과의 협의를 통해 확인된 신주인수권증서 상장시의 제반 거래관련 사항은 다음과 같습니다.
① 상장방식: 실질주주의 신주인수권증서를 일괄예탁 방식으로 발행하여 상장합니다.
② 실질주주의 신주인수권증서 거래
| 구분 | 상장거래방식 | 계좌대체 거래방식 |
|---|---|---|
| 방법 | 실질주주의 신주인수권증서를 일괄예탁 방식으로 발행하여 상장합니다. 위탁자계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. 실질주주의 신주인수권증서는 상장을 위해 일괄예탁되므로 주주 신청에 의한 실물증서 반환은 불가합니다. | 신주인수권증서를 매매하고자 하는 실질주주는 위탁증권회사에 신주인수권증서의 매매를 증명할 수 있는 서류를 첨부하여 거래상대방 명의의 위탁자 계좌로 신주인수권증서의 계좌대체를 청구합니다. 위탁자계좌를 통하여 신주인수권증서를 매수한 자는 그 수량만큼 청약할 수 있으며, 청약기일내에 청약하지 아니하면 그 권리와 효력은 상실됩니다. |
| 기간 | 2019년 05월 23일부터 2019년 05월 29일까지(5거래일간) 거래 |
2019년 05월 16일부터 2019년 05월 31일까지 거래 |
ⅰ) 상장거래 : 2019년 05월 13일부터 05월 17일까지(5영업일간) 거래 가능합니다.
ⅱ) 계좌대체거래 : 2019년 05월 16일(예정)부터 2019년 05월 31일까지 거래 가능합니다.
* 신주인수권증서 상장거래의 결제일인 2019년 05월 31일까지 계좌대체(장외거래) 가능하며, 2019년 06월 01일부터는 신주인수권증서의 청약권리 명세를 확정하므로 신주인수권증서의 계좌대체(장외거래)가 제한됩니다.
ⅲ) 실질주주의 신주인수권증서는 상장을 위해 일괄예탁되므로 주주 신청에 의한 실 물증서 반환은 불가합니다.
③ 명부주주의 신주인수권증서 거래
ⅰ) 신주배정통지일 2019년 05월 16일(예정)로부터 2019년 06월 07일까지 신주인수권증서 실물양도를 통해 거래 가능합니다.
* 신주인수권증서는 당사 명의개서대리인인 국민은행 증권대행부에서 주주 요청시 발급합니다.
ⅱ) 신주배정기준일(2019년 05월 02일) 전일까지 국민은행 증권대행부에 대행예탁(거래증권사 계좌에 입고)신청을 할 경우에는 실질주주와 동일하게 상장거래 및 계좌대체 거래를 할 수 있으며, 이 경우 거래가능기간은 실질 주주와 동일합니다. (단, 신주인수권증서를 입고받을 증권계좌를 보유하고 있어야 합니다.)
라. 주권교부일 이전의 주식양도의 효력에 관한 사항
주식교부일 이전의 주식의 양도는 발행회사에 대하여 효력이 없습니다. 다만, 『자본시장과 금융투자업에 관한 법률』제311조 제4항에 의거 주권발행 전에 증권시장에서의 매매거래를 투자자계좌부 또는 예탁자계좌부상 계좌 간 대체의 방법으로 결제하는 경우에는 「상법」 제335조 제3항에 불구하고 발행인에 대하여 그 효력이 있습니다.
| ※ 『자본시장과 금융투자업에관한 법률』 제 311조 (계좌부기재의 효력) ① 투자자계좌부와 예탁자계좌부에 기재된 자는 각각 그 증권등을 점유하는 것으로 본다. ② 투자자계좌부 또는 예탁자계좌부에 증권등의 양도를 목적으로 계좌 간 대체의 기재를 하거나 질권설정을 목적으로 질물(質物)인 뜻과 질권자를 기재한 경우에는 증권등의 교부가 있었던 것으로 본다. ③ 예탁증권등의 신탁은 예탁자계좌부 또는 투자자계좌부에 신탁재산인 뜻을 기재함으로써 제삼자에게 대항할 수 있다. ④ 주권 발행 전에 증권시장에서의 매매거래를 투자자계좌부 또는 예탁자계좌부상 계좌 간 대체의 방법으로 결제하는 경우에는 「상법」 제335조 제3항에 불구하고 발행인에 대하여 그 효력이 있다. |
마. 기타 모집 또는 매출에 관한 사항
(1) 본 증권신고서는 공시심사과정에서 일부내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요 내용의 변경시에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있으므로 투자자 여러분께서는 투자시 이러한 점을 감안하시기 바랍니다.
(2) 자본시장과 금융투자업에 관한 법률 제120조 3항에 의거 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 주주 및 투자자에게 귀속됩니다.
(3) 본 증권신고서에 기재된 내용은 신고서 제출일 현재까지 발생된 것으로 본 신고서에 기재된 사항 이외에 자산, 부채, 현금흐름 또는 손익상황에 중대한 변동을 가져오거나 중요한 영향을 미치는 사항은 없습니다. 따라서, 주주 및 투자자가 투자의사를 결정함에 있어 유의하여야 할 사항이 본 증권신고서상에 누락되어 있지 않습니다.
(4) 금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서, 반기보고서, 분기보고서 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있사오니 투자의사를 결정하시는 데 참조하시기 바랍니다.
(5) 본 증권신고서의 예정 모집가액은 확정되어 있는 것은 아니며, 추후 2차 발행가액까지 산정함으로써 확정될 예정입니다. 또한, 본 증권신고서의 발행예정금액은 추후 주당 발행가액이 확정되는 내용에 따라 변경될 수 있음을 유의하여 주시기 바랍니다.
5. 인수 등에 관한 사항
| [인수방법: 잔액인수] |
| 인수인 | 인수주식 종류 및 수 | 인수대가 | |
|---|---|---|---|
| 대표주관 | 케이비증권(주) | 인수주식의 종류: 기명식 보통주식 인수주식의 수: 최종 실권주 ×인수비율(100.00%) |
- 인수수수료: 모집총액의 2.0% - 추가수수료: 잔액인수금액의 15.0% |
주1) 잔여주식총수: 우리사주조합청약, 구주주청약 및 일반공모 후 발생한 배정잔여주 또는 청약미달주식
주2) 모집총액 : 최종 발행가액 X 총 발행주식수
Ⅱ. 증권의 주요 권리내용
당사가 금번 주주배정 유상증자를 통하여 발행할 증권은 기명식 보통주이며, 동 증권의 주요 권리내용은 다음과 같습니다.
1. 주식에 관한 사항
제5조 (발행예정주식총수)
이 회사가 발행할 주식의 총수는 100,000,000주로 한다.
제6조 (설립시에 발행하는 주식의 총수)
이 회사가 설립시에 발행하는 주식의 총수는 40,000주(1주의 금액 500원 기준)로 한다.
제7조 (1주의 금액)
이 회사가 발행하는 주식 1주의 금액은 500원으로 한다.
제8조 (주권의 발행과 종류)
① 이 회사가 발행하는 주권은 기명식으로 한다.
② 이 회사의 주권은 1주권, 5주권, 10주권, 50주권, 100주권, 500주권, 1,000주권 및 10,000주권의 8종류로 한다.
제9조 (주식의 종류, 수 및 내용)
① 이 회사는 보통주식과 우선주식을 발행할 수 있다.
② 제5조의 발행예정주식총수 중 우선주식의 발행한도는 2,000,000주로 한다.
③ 우선주식에 대한 최저배당률은 연 액면금액의 0.001%로 한다.
④ 우선주식에 대하여 제 3항의 규정에 의한 배당을 하고, 보통주식에 대하여 우선주식의 배당률과 동룰의 배당을 한 후, 잔여배당가능이익이 있으면 보통주식과 우선주식에 대하여 동등한 비율로 배당한다.
⑤ 우선주식에 대하여 제 3항의 규정에 의한 배당을 하지 못한 사업연도가 있는 경우에는 미배당분은 다음 사업연도로 이연되지 아니한다
⑥ 우선주식의 주주는 의결권이 없는 것으로 한다. 다만, 특별한 경우에 한하여 이사회의 결의에 의해서만 우선 주식 1주당 1개의 의결권을 부여할 수 있다.
⑦ 우선주식은 발행일로부터 10년이 경과하면 보통주식으로 전환된다. 다만, 위 기간 중 소정의 배당을 하지 못한 경우에는 소정의 배당이 완료될 때까지 그 기간은 연장된다.
⑧ 제8항의 규정에 의해 발행되는 신주에 대한 이익의 배당에 관하여는 제 14조의 규정을 준용한다.
⑨ 이 회사가 유상증자 또는 무상증자를 실시하는 경우, 우선주식에 대한 신주의 배정은 유상증자의 경우에는 보통주식으로, 무상증자의 경우에는 동일한 내용의 우선주식으로 한다.
제9조의 1 (A우선주식의 내용)
① 회사는 A우선주식을 발행할 수 있다.
② A우선주식에 대한 최저배당률은 A우선주식 1주당 액면가액의 0.001%로 한다.
③ A우선주식에 대하여 제2항의 규정에 대한 배당을 하고, 잔여배당가능 이익이 있으면 보통주식과 A우선주식에 대하여 동등한 비율로 배당한다.
④ A우선주식에 대하여 제2항의 규정에 의한 배당을 하지 못한 사업연도가 있는 경우에는 미배당분은 다음 사업연도로 이연되지 아니한다.
⑤ A우선주식의 주주는 의결권이 없는 것으로 한다. 다만, 특별한 경우에 한하여 이사회의 결의에 의해서만 A우선주식 1주당 1개의 의결권을 부여할 수 있다.
제9조의 2 (B우선주식의 내용)
① 회사는 B우선주식을 발행할 수 있다.
② 회사가 발행할 B우선주식의 발행한도는 1,000,000주로 한다.
③ B우선주는 이익배당, 잔여재산분배에 있어서 보통주에 대해 우선권이 있고, 전환 및 상환에 관하여 특수한 정함이 있는 전환주식이자 상환주식이며 의결권이 있다.
④ B우선주는 참가적 누적적 우선주로 투자자는 상환전환B우선주를 보유하는 동안 발행가의 1%에 해당하는 금액을 누적적으로 우선 배당 받게 되고, 보통주의 배당률이 B우선주의 배당률을 초과할 경우에는 보통주식과 동일한 배당률로 참가하여 배당을 받는다.
⑤ 피투자기업은 본건 상환전환B우선주식의 적법한 발행을 위하여 상법 등 관계법령이 정하는 바에 따라 주주총회의 결의, 정관 변경 등의 제반 절차를 이행하여야 한다.
⑥ 회사의 B우선주식 주주는 주주총회의 의결에 회부된 모든 사항에 대하여 B우선주식의 의결권을 보통주식의 의결권과 함께 서로 종류를 구분하지 아니하고 행사하며, 전환조건에 따라 보통주로 전환되는 경우에도 전환 후의 보통주식은 1주당 의결권 1표를 갖게 된다.
⑦ 상환전환B우선주에 불리한 주주총회 결의가 있는 때에는 전체 주주총회와 별도로 그 안건에 대하여 본건 상환전환B우선주식 주주들의 종류 주주총회 결의를 거쳐야 한다.
2. 의결권에 관한 사항
제29조 (주주의 의결권)
주주의 의결권은 1주마다 1개로 한다.
제30조 (상호주에 대한 의결권 제한)
회사, 회사와 회사의 자회사 또는 회사의 자회사가 다른 회사의 발행주식 총수의 10분의 1을 초과하는 주식을 가지고 있는 경우, 그 다른 회사가 가지고 있는 이 회사의 주식은 의결권이 없다.
제31조 (의결권의 불통일행사)
① 2 이상의 의결권을 가지고 있는 주주가 의결권의 불통일행사를 하고자 할 때에는 회일의 3일전에 회사에 대하여 서면 또는 전자문서로 그 뜻과 이유를 통지하여야 한다.
② 회사는 주주의 의결권의 불통일행사를 거부할 수 있다. 그러나 주주가 주식의 신탁을 인수하였거나 기타 타인을 위하여 주식을 가지고 있는 경우에는 그러하지 아니하다.
제32조 (의결권의 대리행사)
① 주주는 대리인으로 하여금 그 의결권을 행사하게 할 수 있다.
② 제1항의 대리인은 주주총회 개시전에 그 대리권을 증명하는 서면(위임장)을 제출하여야 한다.
제33조 (주주총회의 결의방법)
주주총회의 결의는 법령과 정관에 다른 정함이 있는 경우를 제외하고는 출석한 주주의 의결권의 과반수와 발행주식의 총수의 4분의 1 이상의 수로써 한다.
3. 신주인수권에 관한 사항
제12조 (신주인수권)
① 주주는 신주발행에 있어서 그가 소유한 주식 수에 비례하여 신주의 배정을 받을 권리를 갖는다.
② 회사는 제1항의 규정에도 불구하고 다음 각 호의 어느 하나에 해당하는 경우는 이사회의 결의로 주주 외의 자에게 신주를 배정할 수 있다.
1. 주주우선공모의 방식으로 신주를 발행하는 경우
2. 발행주식의 총수의 100분의 30을 초과하지 않는 범위 내에서 ?자본시장과 금융투자업에 관한 법률? 제165조의6에 따라 일반공모증자 방식으로 신주를 발행하는 경우
3. [상법] 제542조의3에 따른 주식매수선택권의 행사로 인하여 신주를 발행하는 경우
4. [자본시장과 금융투자업에 관한 법률] 제165조의7에 따라 발행하는 주식 총수의 100분의 20 범위 내에서 우리사주조합원에게 주식을 우선배정하는 경우
5. [중소기업창업지원법]에 의한 중소기업 창업투자회사 및 중소기업창업투자조합에게 발행주식 총수의 100분의 30까지 배정하는 경우
6. 발행주식의 총수의 100분의 30을 초과하지 않는 범위 내에서 경영상 필요로 외국인투자촉진법에 의한 외국인투자를 위하여 신주를 발행하는 경우
7. 외국 및 국내법인, 국내외 금융 기관 등에 발행주식 총수의 100분의 30 범위 내에서 자본참여를 위한 신주를 발행하는 경우
8. [상법] 제418조 제2항의 규정에 따라 국내외 금융기관 또는 기관투자자 등에게 긴급한 자금의 조달, 신기술도입, 신규사업 진출 및 재무구조 개선 등 회사의 경영상 목적을 달성하기 위하여 신주를 발행하는 경우
9. 발행주식 총수의 100분의 30을 초과하지 않는 범위 내에서 사업상 중요한 기술도입, 연구개발, 생산.판매, 자본제휴 등을 위하여 그 상대방에게 신주를 발행하는 경우
10. 주권을 코스닥시장 등 공개시장에 상장하기 위하여 신주를 모집하거나 인수인에게 인수하는 경우
③ 제2항 각 호 중 어느 하나의 규정에 의해 신주를 발행할 경우 발행할 주식의 종류와 수 발행가격 등은 이사회의 결의로 정한다.
④ 신주인수권의 포기 또는 상실에 따른 주식과 신주배정에서 발생한 단주에 대한 처리방법은 이사회의 결의로 정한다.
4. 배당에 관한 사항
제56조 (이익금의 처분)
회사는 매사업년도의 처분전 이익잉여금을 다음과 같이 처분한다.
1. 이익준비금
2. 기타의 법정준비금
3. 배당금
4. 임의적립금
5. 임원상여금
6. 기타의 이익잉여금처분액
제57조 (이익배당)
① 이익의 배당은 금전 또는 금전 외의 재산으로 할 수 있다.
② 이익의 배당을 주식으로 하는 경우 회사가 수종의 주식을 발행한 때에는 주주총회의 결의로 그와 다른 종류의 주식으로도 할 수 있다.
③ 제1항의 배당은 매결산기말 현재의 주주명부에 기재된 주주 또는 등록된 질권자에게 지급하며, 주주총회의 결의로 정한다. 다만, 제54조 제6항에 따라 재무제표를 이사회가 승인하는 경우 이사회 결의로 이익배당을 한다.
④ 미지급 배당금에는 이자를 지급하지 아니한다.
제58조 (배당금 지급청구권의 소멸시효)
배당금의 지급청구권은 5년간 이를 행사하지 아니하면 소멸시효가 완성된다. 소멸시효완성으로 인한 배당금은 본 회사에 귀속한다.
Ⅲ. 투자위험요소
| 【투자자 유의사항】 |
|---|
| * 금번 유상증자를 청약하고자 하는 투자자들은 투자결정을 하기전에 증권신고서의 다른 기재 부분 뿐만 아니라 특히 아래 기재된 투자위험요소를 주의깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 합니다. * 당사는 본 증권신고서를 통하여 청약 전에 투자자께서 숙지하셔야 하는 부분에 대하여 성실히 기재하고자 노력하고 있습니다. 다만, 당사가 현재 알고 있지 못하거나 중요 하지 않다고 판단하여 아래 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수 없으므로, 투자자는 아래 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 투자자 자신의 독자적이고도 세밀한 판단에 의해야 합니다. 따라서 증권신고서에 기재된 사항은 투자 판단 시 참고 자료로 활용하실 것을 권고드리며, 투자자의 투자 판단에 대한 결과는 투자자 본인에게 귀속됨을 다시 한번 알려드립니다. |
1. 사업위험
당사의 사업분야는 크게 조직재생용 바이오소재 및 구강보건제품을 제조 및 판매하는 기반사업군과 펩타이드를 기반으로 한 융합 바이오소재 및 치료제 등 신성장동력사업군으로 구분될 수 있습니다. 사업군별 제품 및 이에 대한 설명, 해당 사업군에 대한 이해를 돕기 위한 주요 용어에 대한 설명은 다음과 같습니다.
[기반사업군]
| 품목 | 제품 | 설명 |
|---|---|---|
| 조직재생용 바이오소재 | 치과용 골이식재 및 콜라겐 바이오소재 |
ㆍ소뼈 및 말뼈의 염증유발 단백질을 제거하여 분말화한 치과용 골이식재 및 콜라겐 바이오소재(치주조직재생용 제품) |
| 구강보건제품 | 치과용 항생연고, 치과용 컨디셔너, 치아미백제 및 시린이 치료제 |
ㆍ 카바마이드 퍼옥사이드와 에센셜오일, 자일리톨을 포함하는 개인용 치아미백제 ㆍ 과산화수소 함유량15%인 전문가용 치아미백제 ㆍ 치아신경완화 성분을 치아내부로 전달해주고, 고분자 코팅과 칼슘 형성 촉진 물질로 치아를 보호할 수 있도록 자극의 전달을 막아주는 시린이 치료제 |
| 화장품 외 | 기능성 화장품 | ㆍ 미백 주름개선 이중기능성 화장품 |
[신성장동력사업군]
| 품목 | 제품 | 설명 |
|---|---|---|
| 펩타이드 치료제 및 펩타이드 기반 바이오베터 |
골다공증 치료제 | ㆍ골재생 기능 펩타이드 함유 골다공증 치료제 ㆍPTH 골다공증 바이오베터 |
| 관절염 치료제 | ㆍ염증 억제 기능 펩타이드 함유 관절염 치료제 |
|
| 비알콜성간염(NASH) 치료제 | ㆍ염증 및 지방 억제 기능 펩타이드 함유 비알콜성지방간염 치료제 |
|
| 염증성 장 질환(IBD) 치료제 | ㆍ염증 억제 및 점막 재생 기능 펩타이드 함유 염증성 장질환 치료제 |
|
| 표적 항암제 | ㆍ종양 선택적 투과기능이 탑재된 종양치료 및 전이암, 내성암치료제 |
|
| 펩타이드기반 융합 바이오소재 |
펩타이드 함유 치과용 골이식재 | ㆍ펩타이드 기반 치과용 골이식재 |
| 정형외과용 골이식재 | ㆍ골재생 기능 펩타이드 함유된 정형외과용 골이식재 ㆍ콜라겐이 함유된 정형외과용 골이식재 |
|
| 주입형 골재생치료제 | ㆍ골재생 기능 펩타이드 함유된 주입형 골재생제 ㆍ콜라겐 젤로 이루어진 주입형 골재생제 |
|
| 정형외과 및 성형외과 적용 가능 조직재생용 시트 | ㆍ콜라겐이 함유된 바이오 조직 재생 시트 및 충전재 |
|
| 펩타이드 치료제 및 펩타이드 기반 바이오베터 |
골다공증 치료제 | ㆍ골재생 기능 펩타이드 함유 골다공증 치료제 ㆍPTH 골다공증 바이오베터 |
| 관절염 치료제 | ㆍ염증 억제 기능 펩타이드 함유 관절염 치료제 |
|
| 비알콜성간염(NASH) 치료제 | ㆍ염증 및 지방 억제 기능 펩타이드 함유 비알콜성지방간염 치료제 |
|
| 염증성 장 질환(IBD) 치료제 | ㆍ염증 억제 및 점막 재생 기능 펩타이드 함유 염증성 장질환 치료제 |
|
| 표적 항암제 | ㆍ종양 선택적 투과기능이 탑재된 종양치료 및 전이암, 내성암치료제 |
|
| 펩타이드 및 기능성 화장품 |
기능성 화장품 | ㆍ펩타이드 기술을 겸비한 항노화 기능성 화장품 ㆍ염증성 피부트러블 증상 개선용 피부면역 증진 소재 함유 화장품 |
[주요 용어 설명]
| 용어 | 설명 |
|---|---|
| 신약 (Original) | 화학구조나 본질 조성이 새로운 신물질 또는 신물질을 유효성분으로 함유한 복합제제 의약품 |
| 바이오베터 (Biobetter) | 바이오 신약의 효능이나 투여 횟수를 개선한 바이오 의약품으로, 기존 바이오 의약품보다 더 낫다(better)는 의미로 바이오베터라고 불림 |
| 펩타이드 (Peptide) | 단백질의 기능적 최소 단위로서 생체 신호전달 및 기능 조절에 관여하는 물질로 2개이상의 아미노산이 사슬처럼 연결되어 있는 물질 |
| 리베이트 (Rebate) | 사전적으로 판매자가 구매자로부터 지불 받은 액수의 일부분을 구매자에게 환불하는 행위 및 그 금액을 의미하며, 판매 촉진을 위한 가격할인 전략. |
| GMP (Good Manufacturing Practice) |
의약품의 안정성과 유효성을 품질면에서 보증하는 기본조건으로서의 우수의약품의 제조·품질관리의 기준. |
| 바이오시밀러 (Biosimilar) | 특허가 만료된 오리지널 바이오의약품(biomedicine)을 복제해 동등한 품질로 만든 의약품 |
| 신약 라이선스 계약 (Licensing) |
단일 회사가 신약개발의 전 과정을 수행하는 것이 아니라, 임상 단계별로 역할을 분담해 신약개발의 리스크(risk, 위험도)를 줄이면서도 빠르게 상업화 할 수 있도록 신약 후보물질의 권리(기술 · 물질 · 제품 · 특허) 등을 도입 또는 이전하는 계약 |
| 라이선스 인 (In-Licensing) | 타사가 보유한 경쟁력 있는 기술 · 물질 · 제품 · 특허 등의 권리를 자사로 들여오는 것 |
| 라이선스 아웃 (Out-Licensing) | 자사가 보유한 기술 · 물질 · 제품 · 특허 · 노하우 등의 권리를 타사에 허여하는 것 |
| 플랫폼 기술 (Platform Technology) |
기존 의약품에 적용하여 다수의 후보 물질을 도출할 수 있는 기반기술을 의미. 플랫폼 기술은 다양한 질환 분야로 적용할 수 있으며, 끊임없는 기술적 진화와 파급효과를 통해 높은 부가가치를 지닌 수익모델을 확보할 수 있음. |
| 전임상 시험 (Pre-Clinical) | 전임상(비임상) 시험은 새로 개발한 신약후보물질을 사람에게 사용하기 전에 동물에게 사용하여 부작용이나 독성, 효과 등을 알아보는 시험임. |
| 임상1상 시험 (Clinical Test - Phase I) |
건강한 사람 20~80명을 대상으로 약물을 안전하게 투여할 수 있는 용량과 인체 내 약물 흡수 정도 등을 평가. 앞서 수행된 전임상 단계에서 독성 시험 등 전임상 시험 결과가 유효한 경우, 시험약을 최초로 사람에 적용하는 단계. |
| 임상2상 시험 (Clinical Test - Phase II) |
100~200명의 소규모 환자들을 대상으로 약물의 약효와 부작용을 평가하고, 유효성을 검증. 단기투약에 따른 흔한 부작용, 약물동태 및 예상 적응증에 대한 효능 효과에 대한 탐색을 위해 실시하는 것으로 대상질환 중 조건에 부합되는 환자를 대상으로 함. 임상3상 시험에 돌입하기 위한 최적용법 용량을 결정하는 단계. |
| 임상3상 시험 (Clinical Test - Phase III) |
신약의 유효성이 어느 정도 확립된 후에 대규모(최소 수백 명에서 수천 명) 환자들을 대상으로 장기 투여시의 안정성 등을 검토하고 확고한 증거를 수집하기 위해 실시. 신약의 유효성이 어느 정도까지 확립된 후에 행해지며 시판허가를 얻기 위한 마지막 단계의 임상시험으로서 비교대조군과 시험처치군을 동시에 설정하여 효능, 효과, 용법, 용량, 사용상의 주의사항 등을 결정. 3상이 성공적으로 끝나면 판매가 가능함. |
| 임상4상 시험 (Clinical Test - Phase IV) |
신약이 시판 사용된 후 장기간의 효능과 안전성에 관한 사항을 평가하기 위한 시험으로, 시판전 제한적인 임상시험에서 파악할 수 없었던 부작용이나 예상하지 못하였던 새로운 적응증을 발견하기 위한 약물역학적인 연구. |
| 가. 바이오의약품 시장의 변동에 따른 위험 당사가 영위하는 사업은 조직재생용 바이오사업, 구강보건사업 및 펩타이드 기반 사업이며, 상기 사업들은 바이오의약품 산업 내에 속합니다. 2018년 Evaluate Pharma에 따르면 전세계 바이오의약품 시장은 2010년부터 2017년간 연평균 7.7%로 성장하여왔으며, 2018년부터 2024년까지 연평균 9.1% 성장하여 2024년에는 3,830억달러에 달할 것으로 전망하고 있습니다. 한국바이오의약품협회에서 2019년 02월에 발간한 바이오의약품 산업동향보고서에 따르면 국내 바이오의약품 시장은 수출액이 급성장하여 2015년 무역수지 흑자전환 이후 3년 연속 증가하여 왔으며, 2017년 내수산업시장규모는 2조 2,327억원으로 2016년 1조 8,308억원 대비 22% 증가하였습니다. 국내 바이오의약품 시장은 가속화되는 고령화 사회및 만성질환의 증가로 의약품 수요 증가에 따른 바이오의약품 산업의 확대가 지속될 전망입니다. 그러나 이러한 시장조사기관의 전망에도 불구하고 제약시장의 환경 변화, 의약품 관련 지원 및 규제정책의 변화, 다국적 제약사의 바이오의약품 개발과 관련한 투자규모 및 사업전략 변경 등의 영향으로 산업에 부정적인 영향이 있을 경우 당사가 영위하는 사업에도 부정적인 영향을 줄 수 있습니다. 이 점 유의하시어 투자해 주시기 바랍니다. |
당사가 영위하는 사업은 조직재생용 바이오사업, 구강보건사업 및 펩타이드 기반 사업이며, 상기 사업들은 전체적인 틀에서 봤을 때 바이오의약품 산업 내에 속합니다. 바이오의약품은 생물의약품으로 불리기도 하며 사람이나 생물체에서 유리된 세포, 조직, 호르몬 등의 유효물질을 이용하여 유전자재조합 또는 세포배양기술을 통해 분자생물학적 기법으로 개발한 의약품을 말합니다.
복제약의 경우, 합성의약품은 화학물질의 합성 비율을 알면 쉽게 제조가 가능한 반면 바이오의약품은 배양기술과 환경, 방법에 따라 전혀 다른 물질이 나올 수 있는 가능성이 있어 복제가 쉽지 않습니다. 이에 따라 바이오의약품은 고부가가치 제품으로써 일반 제약시장보다 빠르게 성장하여 왔습니다.
2018년 Evaluate Pharma에 따르면 전세계 바이오의약품 시장은 2010년부터 2017년간 연평균 7.7%로 성장하여왔으며, 2018년부터 2024년까지 연평균 9.1% 성장하여 2024년에는 3,830억달러에 달할 것으로 전망하고 있습니다. 또한 2017년 기준 전체 의약품 시장은 8,030억원달러이며, 바이오의약품 시장은 2,020억달러로, 전체의약품 대비 25%를 차지하고 있으며, 2010년 매출비중 17% 대비 8% 증가하였습니다. 매출비중이 점차 높아져 2024년 31%까지 증가할 것으로 전망하고 있습니다.
| [글로벌 바이오의약품 시장규모 추이] |
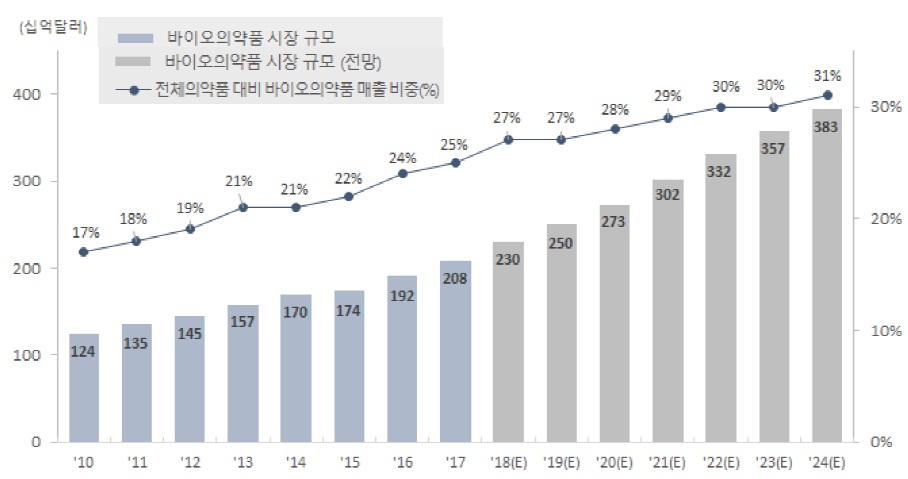 |
|
글로벌 바이오의약품 시장규모 추이 |
자료 : Evaluate pharma World Preview 2018, Outlook to 2024(2018.06), 2018년 바이오의약품 산업동향보고서, 한국바이오의약품협회(2019.02.13)
국내 바이오의약품 시장 또한 빠른 노인인구 증가 및 만성질환의 증가로 의약품 수요 증가에 따른 바이오의약품 산업의 확대가 지속될 전망입니다. 인구구조가 2000년 고령화 사회 (노인 비중 7%) 진입함에 이어 2018년 고령사회(14.3%)에 진입하는 등 고령화 진행속도가 빠른 점을 감안할 때, 향후에도 노인 인구 및 만성질환자 증가에 따라 의약품의 근원 수요는 견고한 확대 추세를 지속할 것으로 전망되고 있습니다.
건강보험심사평가원에 의하면 노인 진료비는 2013년 약 18조원에서 2017년 약 27.1조원까지 증가하였으며, 2018년 3분기 누적 노인진료비는 약 23.1조원으로 전년동기대비 13.1% 증가하였습니다. 전체진료비 대비 노인진료비 비중 또한 2013년 약 35%에서 2018년 3분기 39.9%까지 증가하였습니다.
| [국내 전체 진료비 및 노인진료비 추이] |
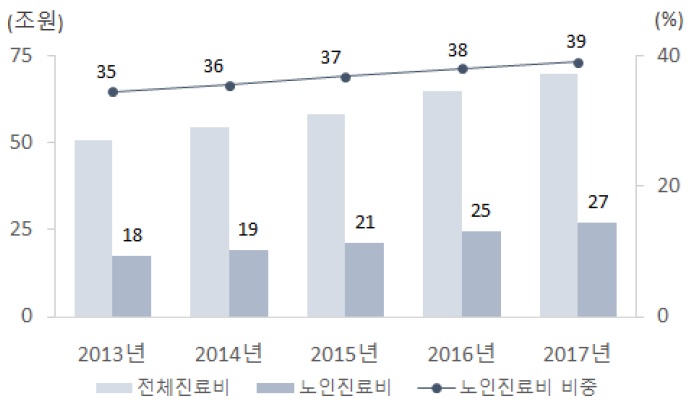 |
|
전체 진료비 및 노인 진료비 비교 |
자료 : 2017년 진료통계지표, 건강보험심사평가원(2018.03)
이에 따라 한국바이오의약품협회에서 2019년 02월에 발간한 바이오의약품 산업동향보고서에 따르면 국내 바이오의약품 시장은 수출액이 급성장하여 2015년 무역수지 흑자전환 이후 3년 연속 증가하여 왔으며, 2017년 내수산업시장규모는 2조 2,327억원으로 2016년 1조 8,308억원 대비 22% 증가하였습니다. 또한, 국내 바이오의약품 시장은 전체의약품 시장(2016년, 21조 7,256억원) 대비 8.4%(2016년)로 전체 시장규모가 미미하여 성장 가능성이 높다고 판단됩니다.
| [국내 바이오의약품 시장규모 추이] |
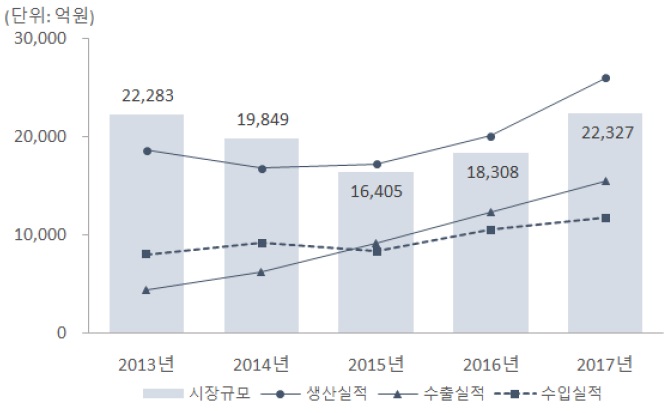 |
|
국내 바이오의약품 시장규모 |
최근 제약산업의 안정적인 성장추세가 다소 둔화되는 모습을 보이는 것에 비해, 신약개발을 위한 높은 수준의 R&D 투자, 생산 및 품질관리 경쟁력 확보를 바탕으로 한 이머징마켓 진출, 높은 치료율과 낮은 부작용을 보이는 바이오의약품 산업은 빠른 성장성을 보이고 있습니다. 그러나 이러한 시장조사기관의 전망에도 불구하고 제약시장의 환경 변화, 의약품 관련 지원 및 규제정책의 변화, 다국적 제약사의 바이오의약품 개발과 관련한 투자규모 및 사업전략 변경 등의 영향으로 산업에 부정적인 영향이 있을 경우 당사가 영위하는 사업에도 부정적인 영향을 줄 수 있습니다. 이 점 유의하시어 투자해 주시기 바랍니다.
| 나. 임플란트 시장 변동에 따른 위험 당사가 영위하는 조직재생용 바이오소재 사업은 치과용 골이식재 및 치주조직재생용 바이오소재로 구분되며, 치과용 임플란트의 필수 재료입니다. 세계 치과용 임플란트 시장은 2016년 기준 45억달러 시장으로 연평균 8.6% 성장하여 2019년에는 59억달러 시장으로 성장할 것으로 예상됩니다. 2018년 기준 세계 치과용 임플란트 시장은 Strauman이 약 전체 시장의 25%를 점유하고 있으며, Danaher(Nobel Biocare) 19%, Dentsply Sirona 12%, Zimmer Biomet 10%, Henry Schein 8%, 오스템임플란트 7% 순으로 상위 5개 기업이 전체 시장의 약 70%를 점유하고 있습니다. 한편, 식품의약품안전처의 KHDI에 의하면 국내 치과용 임플란트 시장규모는 2016년 기준 약 5,587억원 가량으로 최근 5년간 연 12.9%성장 중입니다. 국내 주요 업체로는 오스템임플란트, 덴티움, 네오바이오텍 등이 있으며, 상위 5개 업체가 전체 시장의 약 80%를 점유하고 있습니다. 국내외 치과용 임플란트 관련 시장은 향후 보험정책 완화 및 기술개발성장으로 더 커질것으로 예상되지만, 향후 임플란트의 부작용 발생으로 인한 평판리스크 발생 또는 임플란트를 대체할 기술개발이 될 경우 임플란트 시장에 부정적인 영향이 발생할 소지가 있습니다. 투자자들께서는 이점 유의하시기 바랍니다. |
당사가 영위하는 조직재생용 바이오소재산업은 치과용 골이식재 및 치주조직재생용바이오소재로 치과용 임플란트의 필수 재료입니다. 치과용 골이식재는 치조골 결손 시 결손부를 채우거나 잇몸조직의 재생을 막는 목적으로 사용하며, 주로 치과용 임플란트 시술 시 충분한 양의 골조직을 확보하거나 임플란트의 주변조직과의 결합력을 높이기 위하여 사용되고 있습니다. 치주조직재생용 바이오소재는 쉬트 형태로 치과용 골이식재와 함께 사용하기도 하고 단독으로 차단막 역할로 사용되기도 합니다.
치과용 임플란트는 치아가 결손된 부위에 주변 치아를 손상하지 않고 특수금속으로 만든 인공치근을 치조골에 이식하여 본래 자기 치아와 같은 기능을 수행하는 이식체로, 최근 인구 고령화 및 치과 심미치료 시장 활성화로 인해 높은 시장성을 가지며, 국내 임플란트 제작 기술 및 시술방법은 세계적 수준으로 추후 성장이 기대되는 품목입니다. 식품의약품안전처에서는 신기술과의 융복합으로 기존 한계를 극복하고 새로운 의료서비스를 창출하는 의료기기를 신개념 의료기기로 정의하면서, '2018년 신개발 의료기기 전망 분석 보고서'를 통해 4차 산업혁명 관련 기존의 기술보다 심화되고 제품화에 가까운 치과용 임플란트에 대한 개발현황 및 동향등을 선제적으로 제시하며 추후 바이오 임플란트와 관련된 기술발전과 지속적인 성장을 전망하였습니다.
세계 치과용 임플란트 시장은 2016년 기준 45억달러 시장으로 연평균 8.6% 성장하여 2019년에는 59억달러 시장으로 성장할 것으로 예상되며, 선진국 이외 최근 아시아-태평양, 남미, 특히 중국을 중심으로 고령화가 빠르게 진행되고 있고 무치악 발병률이 높은 고령인구의 지속적인 증가 추세, 소득수준의 향상으로 잠재 소비자가 급격하게 늘어남에 따라 향후 2022년까지 63억달러 규모로 성장할 것으로 예상됩니다.
[치과용 임플란트 국외 시장규모]
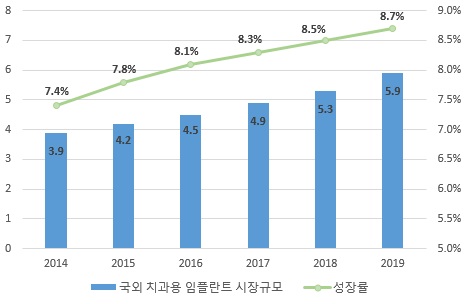 |
|
나이벡_국외치과용임플란트 시장규모 |
출처 : 식약처, KHDI, GlobalData
2018년기준 세계 치과용 임플란트 시장은 Strauman이 약 전체 시장의 25%를 점유하고 있으며, Danaher(Nobel Biocare) 19%, Dentsply Sirona 12%, Zimmer Biomet 10%, Henry Schein 8%, 오스템임플란트 7% 순으로 상위 5개 기업이 전체 시장의 약 70%를 점유하고 있습니다.
| [글로벌 치과용 임플란트 2018년 기준 시장점유율] |
| 순위 | 회사명 | 시장점유율 |
|---|---|---|
| 1 | Straumann | 25% |
| 2 | Danaher(Nobel Biocare) | 19% |
| 3 | Dentsply Sirona | 12% |
| 4 | Henry Schein |
8% |
| 5 | 오스템임플란트 | 7% |
| 6 | Zimmer Biomet | 6% |
| 7 | Dentium | 4% |
| 8 | 기타 | 19% |
| 합 계 | 100.0% | |
자료 : MRG, Straumann 오스템임플란트
한편, 국내 치과용 임플란트 시장은 초기에는 수입제품 위주의 시장이었으나 2000년대 이후 국내 업체들이 빠르게 시장에 진입하면서 90%이상을 국내 제품이 점유하고 있습니다. 식품의약품안전처의 KHDI에 의하면 국내 치과용 임플란트 시장규모는 2016년 기준 약 5,587억원 가량으로 최근 5년간 연 12.9%성장중입니다. 국내 주요 업체로는 오스템임플란트, 덴티움, 네오바이오텍 등이 있으며, 상위 5개 업체가 전체 시장의 약 80%를 점유하고 있습니다.
[국내 치과용임플란트 시장규모]
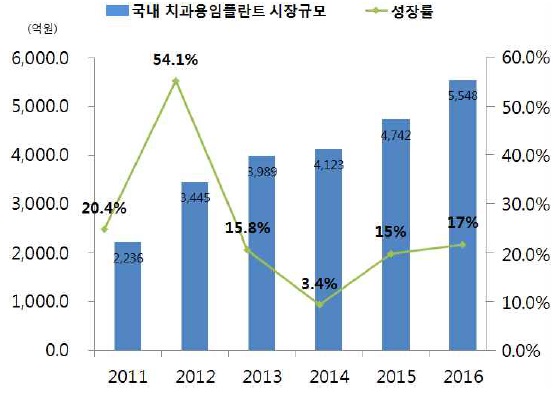 |
|
나이벡_국내치과용임플란트 시장규모 |
출처 : 식약처, KHDI, GlobalData
| [국내 치과용 임플란트 시장점유율] |
| 순위 | 회사명 | 시장점유율 |
|---|---|---|
| 1 | (주)오스템임플란트 | 33.0% |
| 2 | (주)덴티움 | 16.0% |
| 3 | (주)네오바이텍 | 14.0% |
| 4 | (주)디오 | 10.0% |
| 5 | (주)메가젠임플란트 | 7.0% |
| 6 | 기타 | 20.0% |
| 합 계 | 100.0% | |
자료 : 덴티움 사업보고서, 삼성증권, 2017
임플란트는 치과에서 받는 시술 중에서도 특히 고가에 속합니다. 국내 임플란트 시장은 2014년 7월부터 임플란트에 대한 건강보험이 적용되기 시작하며 수요가 증가하기 시작했습니다. 특히 2018년 7월부터는 65세 이상 노인 임플란트에 대한 본인부담금이 50%-30%로 축소 됨에 따라 관련 업체들의 매출상승 기대감이 커지고 있습니다. 보험 정책 변동에 따른 효과성은 하기와 같습니다.
[보험정책 효과]
| 적용일자 | 연령대 | 대상인원 | Market Size 추정 (재료비 평균단가 18만원 적용) |
|---|---|---|---|
| 2014.07.01 | 75세 이상 | 8만명 | 144~288억원 |
| 2015.07.01 | 70세 이상 | 10만명 | 180~260억원 |
| 2016.07.01 | 65세 이상 | 15만명 | 270~540억원 |
| 2018.07.01 | 65세 이상 | 16만명 | 280~550억원 |
주1) 총비용 : 110-128 만원{재료비(9-27만원) + 수술비(101만원)}/개당x70%
주2) 임플란트 평생 1-2개 적용 기준
자료 : 보건복지부, 오스템임플란트
임플란트 시술은 2개까지만 건강보험이 적용되지만 일단 1~2개를 시술하면 그 다음에도 틀니보다는 추가 시술을 원하는 경우가 많아 건강보험 효과가 예상보다 더 커질수 있다고 예상됩니다.
이처럼, 국내외 치과용 임플란트 시장은 향후 지속적으로 보험정책 완화 및 기술개발성장으로 국내외 치과용 임플란트 시장은 더욱더 성장할 것으로 예상되어 당사의 치과용 골이식재 및 치주조직재생용바이오소재 또한 함께 동반성장할 것으로 기대하고 있으나 향후 임플란트의 부작용 발생으로 인한 평판리스크 발생 또는 임플란트를 대체할 기술개발이 될 경우 임플란트 시장에 부정적인 영향이 발생할 소지가 있습니다. 투자자들께서는 이점 유의하시기 바랍니다.
| 다. 경쟁업체 관련 위험 당사는 크게 조직재생용 바이오소재 및 구강보건제품을 제조 및 판매하는 기반사업군과 펩타이드를 기반으로 한 융합 바이오소재 및 치료제 등 신성장동력사업군으로 구분하고 있습니다. 당사는 각 사업군별 글로벌적으로 조직재생용 바이오소재 기업과 펩타이드 관련 연구개발 및 제조기업들과 경쟁하고 있습니다. 당사가 생산하고 있는 조직재생용 바이오소재는 글로벌적으로 Geistlich Pharma AG(스위스), Zimmer Holding Inc(미국), Dentsply Sirona International(미국) 등과 경쟁하고 있습니다. Marketsandmarkets, Dental Bone Graft Substituetes Market, 2016에 의하면, 치과용 골이식재의 글로벌 시장은 Geistlich Pharma AG(스위스)의 소뼈유래 골이식재인 BioOss를 포함한 상위 5개 업체의 제품이 시장의 대부분을 장악하고 있으며, 특히 Geistlich Pharma AG(스위스)가 2015년 기준 시장점유율 13.8%로 우위를 선점하고 있습니다. 한편, 국내 치과용 골이식재 시장에서는 당사와 Geistlich Pharma AG(스위스), 오스코텍 등의 업체가 치과용 골이식재 시장을 과점하고 있으며, Geistlich Pharma AG(스위스)의 BioOss가 41.2%, 당사의 OCS-B, OCS-H, GuideOss 등이 12.9%, 오스코텍의 BioCera, SynCera가 8.1%로 국내시장의 점유율을 차지하고 있는 것으로 추정되고 있습니다. 한편, 당사가 연구개발중인 펩타이드 관련 제품은 펩타이드 기반 골이식재와 펩타이드 기반의 골다공증 치료제, 관절염치료제, 비알콜성지방간염치료제, 염증성장질환치료제, 펩타이드 기반 바이오베터로, 펩타이드 소재인 점을 제외할 시 다른 소재를 기반으로 경쟁업체들이 연구개발 및 제품출시를 하고 있으며, 이와 관련된 모든 업체들이 경쟁업체라고 할 수 있습니다. 그러나 펩타이드를 기반으로 한 치료제는 글로벌적으로 아직 개발되지 않았기 때문에 시장점유율을 측정할 수 없는 상황입니다. 다만, 펩타이드 기반 골이식재 관련된 제품은 출시되었으며, 당사를 제외한 펩타이드 기반 골이식재를 개발한 기업은 Dentsply가 있습니다. 당사는 글로벌 임플란트 1위, 2위업체인 Straumann과 Nobel Biocare 등의 유통업체들과의 공급계약을 통해 시장점유율을 확대해 나가고 있으며 신성장동력 사업군에서는 현재 펩타이드 기반 제품을 연구개발하여 당사의 수익성을 높이기 위하여 노력하고 있습니다. 그러나 많은 신제품이 연구, 개발되고 있는 경쟁이 치열한 바이오 산업시장에서향후 당사보다 안전성 및 효능이 뛰어난 제품이 경쟁업체에 의하여 출시되어 시장점유율을 확대되고, 당사가 경쟁에서 뒤쳐질 경우에는 당사의 사업성 및 수익성에 부정적인 영향을 끼칠수 있습니다.이 점 유의하여 투자해 주시기 바랍니다. |
당사의 사업분야는 크게 조직재생용 바이오소재 및 구강보건제품을 제조 및 판매하는 기반사업군과 펩타이드를 기반으로 한 융합 바이오소재 및 치료제 등 신성장동력사업군으로 구분될 수 있으며, 사업군별 세부 내용 및 매출액/비중은 다음과 같습니다.
[기반사업군]
| (단위 : %, 백만원) |
| 품목 | 제품 | 제품 설명 | 2018년 | 2017년 | 2016년 | |||
|---|---|---|---|---|---|---|---|---|
| 매출액 | 비중 | 매출액 | 비중 | 매출액 | 비중 | |||
| 조직재생용 바이오소재 |
치과용 골이식재 |
소뼈 및 말뼈의 염증유발 단백질을 제거하여 분말화한 치과용 골이식재 |
4,151 |
79.70% |
4,529 |
71.85% |
3,914 |
84.44% |
| 치주조직재생용 바이오소재 | 콜라겐으로 제작된 치주조직재생용 제품 |
745 |
14.30% |
374 |
5.93% |
141 |
3.04% |
|
| 구강보건제품 | 치아미백제 | - 카바마이드 퍼옥사이드와 에센셜오일, 자일리톨을 포함하는 개인용 치아미백제 - 과산화수소 함유량 15%인 전문가용 치아미백제 |
59 |
1.13% |
78 |
1.24% |
479 |
10.33% |
| 시린이치료제외 | 치아신경완화 성분을 치아내부로 전달해주고, 고분자코팅과 칼슘 형성 촉진 물질로 치아를 보호할 수 있도록 자극의 전달을 막아주는 시린이치료제 |
189 |
3.63% |
50 |
0.79% |
41 |
0.88% |
|
| 화장품 외 | 미백 주름개선 이중기능성 화장품 |
64 |
1.23% |
148 |
2.35% |
60 |
1.29% |
|
| 기타수익 및 상품매출 | Straumann 기술이전에 따른 수익 | - | - | 1,124 | 17.83% | - | - | |
| 합 계 |
5,208 |
100.0% |
6,303 |
100.0% |
4,635 |
100.0% |
||
당사의 매출액중 약 90%를 차지하고 있는 조직재생용 바이오소재는 치과용 골이식재 및 치주조직재생용 바이오 소재로 구분합니다. 치과용 골이식재는 임플란트 시술시 골조직을 확보하거나 주변조직과의 결합력을 높이기 위해 사용되는데 당사의 치과용 골이식재는 소뼈 및 말뼈의 염증유발 단백질을 제거하여 분말화한 치과용 골이식재로 면역적 거부반응이 적으며 형태구조학적으로 인체의 골과 같은 구조를 지니고 있어 이식 시 인체의 골 구조 및 세포에 쉽게 융화될수 있는 기능을 가지고 있습니다.
당사의 치주조직재생용 바이오소재는 콜라겐 바이오 소재로 치과용 골이식재와 함께 또는 단독으로 사용합니다. 고순도 돼지 콜라겐을 비화학 가교법으로 제조하여 조직친화성을 가지며 구강 노출시 염증과 세균의 침투를 막고 재생에 도움을 주는 기능을 합니다. 치과용 골이식재 및 치주조직재생용 시트 시장은 치과용 임플란트 시술시 필수재료로 시장의 성장과 함께 임플란트 수요의 증가 등을 바탕으로, 치과용 골이식재 시장은 지속적인 성장세를 유지할것으로 예상됩니다.
[신성장동력사업군]
| 품목 | 제품 | 설명 |
|---|---|---|
| 펩타이드 치료제 및 펩타이드 기반 바이오베터 |
골다공증 치료제 | ㆍ골재생 기능 펩타이드 함유 골다공증 치료제 ㆍPTH 골다공증 바이오베터 |
| 관절염 치료제 | ㆍ염증 억제 기능 펩타이드 함유 관절염 치료제 |
|
| 비알콜성간염(NASH) 치료제 | ㆍ염증 및 지방 억제 기능 펩타이드 함유 비알콜성지방간염 치료제 |
|
| 염증성 장 질환(IBD) 치료제 | ㆍ염증 억제 및 점막 재생 기능 펩타이드 함유 염증성 장질환 치료제 |
|
| 표적 항암제 | ㆍ종양 선택적 투과기능이 탑재된 종양치료 및 전이암, 내성암치료제 |
|
| 펩타이드기반 융합 바이오소재 |
펩타이드 함유 치과용 골이식재 | ㆍ펩타이드 기반 치과용 골이식재 |
| 정형외과용 골이식재 | ㆍ골재생 기능 펩타이드 함유된 정형외과용 골이식재 ㆍ콜라겐이 함유된 정형외과용 골이식재 |
|
| 주입형 골재생치료제 | ㆍ골재생 기능 펩타이드 함유된 주입형 골재생제 ㆍ콜라겐 젤로 이루어진 주입형 골재생제 |
|
| 정형외과 및 성형외과 적용 가능 조직재생용 시트 | ㆍ콜라겐이 함유된 바이오 조직 재생 시트 및 충전재 |
|
| 펩타이드 치료제 및 펩타이드 기반 바이오베터 |
골다공증 치료제 | ㆍ골재생 기능 펩타이드 함유 골다공증 치료제 ㆍPTH 골다공증 바이오베터 |
| 관절염 치료제 | ㆍ염증 억제 기능 펩타이드 함유 관절염 치료제 |
|
| 비알콜성간염(NASH) 치료제 | ㆍ염증 및 지방 억제 기능 펩타이드 함유 비알콜성지방간염 치료제 |
|
| 염증성 장 질환(IBD) 치료제 | ㆍ염증 억제 및 점막 재생 기능 펩타이드 함유 염증성 장질환 치료제 |
|
| 표적 항암제 | ㆍ종양 선택적 투과기능이 탑재된 종양치료 및 전이암, 내성암치료제 |
|
| 펩타이드 및 기능성 화장품 |
기능성 화장품 | ㆍ펩타이드 기술을 겸비한 항노화 기능성 화장품 ㆍ염증성 피부트러블 증상 개선용 피부면역 증진 소재 함유 화장품 |
또한 당사는 펩타이드 기반 융합 바이오소재 및 펩타이드 치료제, 펩타이드 기반 바이오베터를 회사의 신성장동력사업군으로 추진하고 있습니다. 펩타이드란 단백질의 기능적 최소 단위로서 생체 신호전달 및 기능조절에 관여하는 물질로 생물 의약 및 생물화확 분야에서 치료제나 기능성 물질로 사용되는 핵심 소재입니다. 펩타이드 기반 융합바이오소재는 기존의 조직 재생용 바이오소재에 펩타이드를 적용하여 조직재생의 효과를 증진시키는 것이 목적입니다. 과거와 달리 질환의 원인이 다양해지고 여러 원인에 의한 복잡한 조직 결손부의 재건에는 기존의 생체적 합성만으로는 효과를 장담하기 어려워 짐에 따라 생리활성물질, 단백질, 펩타이드의 바이오소재로의 적용이 도입되기 시작하였습니다.
당사는 펩타이드 공학기술과 약물전달 시스템 및 바이오소재 융합기술을 통하여 제품을 상용화 하고 있습니다. 펩타이드 기반의 신약 파이프라인에 대한 전임상 및 임상시험과 해외 사업 활성화 촉진을 위해 2019년 4월 미국에 자회사를 설립하고 연구개발을 활성화할 계획에 있습니다. 또한 당사의 치과용 골이식재 제품인 OssGen X-15 는 펩타이드 기반 융합 의료기기로 국내 식약처 허가를 받고 글로벌 임플란트 기업과 판매계약을 맺었으며, 치과 분야뿐 아니라 정형외과 시장에도 확대 적용될 수 있다고 판단하여 미국내 자회사를 통해 FDA 사전승인을 진행하고, 정형외과 시장진입을 준비하고 있습니다.
| [당사의 총 제품 현황] |
|
제품군 |
분야 |
당사 제품명 |
분야의 성격 |
구분 |
세부구분 |
|---|---|---|---|---|---|
| 펩타이드제품군 | 펩타이드 기반 융합바이오소재 |
OssGen-X15 |
전문가 사용 |
의료기기 |
신개발의료기기 |
|
OssGen-X15 Gel |
전문가 사용 |
의료기기 |
신개발의료기기 |
||
|
OssGen Ortho |
전문가 사용 |
의료기기 |
신개발의료기기 |
||
| 펩타이드 치료제 |
NIPEP OSS |
전문가 사용 |
의약품 |
오리지날 |
|
|
NIPEP-Care 1 NIPEP-Care 2 |
전문가 사용 |
의약품 |
오리지날 |
||
|
NIPEP-ACD-Tide |
전문가 사용 |
의약품 |
오리지날 |
||
| 펩타이드 기반 바이오베터 |
OssGen-better |
전문가 사용 |
의약품 |
바이오베터 |
|
|
조직재생용 |
치과용 골이식재 |
OCS-B, OCS-H |
전문가 사용 |
의료기기 |
제네릭 |
|
치주조직재생용쉬트 |
GuidOss |
전문가 사용 |
의료기기 |
신개발의료기기 |
|
|
흡수성치주조직재생유도재 |
Regenomer |
전문가 사용 |
의료기기 |
제네릭 |
|
|
골이식용 복합재료 |
OCS-B Collagen, Equimatrix Collagen |
전문가 사용 |
의료기기 |
신개발의료기기 |
|
|
구강질환 |
개인용 치아미백제 |
Dr.Whitiss |
일반인 사용 |
의약외품 |
오리지날 |
|
전문가용 치아미백제 |
BlanTis Pro(10%) BlanTis Clinic(15%) |
전문가 사용 |
의약품 |
제네릭 |
|
|
시린이 치료제 |
SensBlok |
일반인, 전문가 사용 |
의료기기 |
신개발의료기기 |
|
|
치과용 컨디셔너, 임플란트주위염치료제 |
Clinplant syringe/Floss |
일반인, 전문가 사용 |
의료기기 |
신개발의료기기 |
|
|
치주질환치료제 |
MinoCure |
전문가 사용 |
의약품 |
제네릭 |
|
|
화장품 |
펩타이드 화장품 원료 |
- | - |
화장품 |
오리지날 |
|
미백 주름개선 기능성 화장품 |
Dr.MyYou Solution |
일반인 사용 |
화장품 |
오리지날 |
|
|
항노화 기능성 화장품 |
Eustella Complex Solution |
일반인 사용 |
화장품 |
오리지날 |
|
|
여드름 및 염증 억제 화장품 |
Eustella AC Solution |
일반인 사용 |
화장품 |
오리지날 |
| 주) 오리지날 : 최초 개발되어 허가받은 신약 제네릭 : 오리지널 의약품/의료기기과 용법, 용량, 성능이 동일한 복제약 혹은 의료기기 신개발의료기기 : 신성능, 신구조, 신사용목적 중 하나에 해당하는 의료기기이며, 유사한 의미로 의약품에서는 신약에 해당됨. 신약과 같이 1, 2, 3상의 임상시험이 필요하지 않고, 단상으로 평가함. 바이오베터 : 기존에 허가된 바이오의약품(단백질의약품, 항체의약품, 펩타이드 의약품 등)의 성능을 개선시킨 것. 본질적으로 골격은 기존에 허가된 바이오의약품의 구조를 유지하기 때문에 허가시 기존 바이오의약품과의 동등성 자료를 제출할 것을 요구함. |
한편, 당사는 상기 제품들에 대하여 글로벌적으로 조직재생용 바이오소재 기업과 펩타이드 관련 연구개발 및 제조기업들과 경쟁하고 있습니다. 각 기반사업군별 경쟁 현황은 다음과 같습니다.
1) 조직재생용 바이오소재
당사가 생산하고 있는 조직재생용 바이오소재는 글로벌적으로 Geistlich Pharma AG(스위스), Zimmer Holding Inc(미국), Dentsply Sirona International(미국) 등과 경쟁하고 있습니다. Marketsandmarkets, Dental Bone Graft Substituetes Market, 2016에 의하면, 치과용 골이식재의 글로벌 시장은 Geistlich Pharma AG(스위스)의 소뼈유래 골이식재인 BioOss를 포함한 상위 5개 업체의 제품이 시장의 대부분을 장악하고 있으며, 특히 Geistlich Pharma AG(스위스)가 2015년 기준 시장점유율 13.8%로 우위를 선점하고 있습니다.
| [글로벌 치과용 골이식 대체물 시장의 주요 업체 및 점유율 현황] |
 |
|
시장점유율 |
자료 : Marketsandmarkets, Dental Bone Graft Substitutes Market, 2016 / 치과용 골이식 대체물 시장, 2018, 연구개발특구진흥재단
또한, 글로벌 치과용 골이식재 시장 중 1, 2, 3위를 차지하고 있는 Giestlich Pharma AG(스위스), Zimmer Holding Inc.(미국), Dentsply Sirona International(미국)에 대한 업계 동향은 다음과 같습니다.
| [글로벌 치과용 골이식 주요 업체의 동향] |
| 업체 명 | 주요 동향 |
|---|---|
| Geistlich Pharma AG(스위스) | - 뼈, 연골, 조직 등의 재생을 위한 생체재료 분야의 전문적인 기업으로 의료용 재료와 의약품을 개발 및 제조하는 업체이며, 주로 치과용 골이식재료와 차폐막 재료를 생산 및 판매 중입니다. - 치과, 정형외과와 같은 특정 분야에 의료기기를 공급하며, Geistlich Biomaterials(치과용 생체재료), Geistlich Surgery(정형외과 생체재료), Geistlich Medical(제약 및 의료용품)의 세 분야를 통해 사업을 운영하고 있습니다. - 2013년 뼈와 연조직의 재생을 유도하는 이중층 콜라겐인‘Bio-Gide’를 출시하였으며, 2015년 연조직 재생을 위한 새로운 콜라겐 매트릭스인 ‘Geistlich Mucograft Seal’을 출시하였습니다. |
| Zimmer Holding Inc.(미국) | - 무릎, 엉덩이, 팔꿈치, 발, 발목, 인공 관절, 치과 보철을 포함하는 정형외과 의료기기 제품을 설계, 개발, 제조 및 판매하는 업체입니다. - 2012년 뼈의 성장을 위하여 높은 마찰계수로 설계된‘Trabecular Metal’인 치아 임플란트를 출시하였고, 2013년 3D 시각화 소프트웨어를 사용하여 의사가 환자에 대한 맞춤형 수술을 계획할 수 있도록 임플란트 배치를 용이하게 하는‘Patient Specific Instruments (PSI) Shouldersystem’을 판매하였습니다. |
| Dentsply Sirona International(미국) | - 전문적인 치과장비 제조 및 치과용 소모품 생산 기업으로 120개국에서 제품을 판매하는 대표적인 치과 용품 제조 및 판매 업체입니다. - 치과 용품 및 장비, CAD/CAM 복원 시스템, 치과 영상기기, 치과 교정용 품 등을 포함한 치과 및 구강 보건 제품을 제조 및 판매 중입니다. |
한편, 국내 치과용 골이식재 시장에서는 당사와 Geistlich Pharma AG(스위스), 오스코텍 등의 업체가 치과용 골이식재 시장을 과점하고 있으며, Geistlich Pharma AG(스위스)의 BioOss가 41.2%, 당사의 OCS-B, OCS-H, GuideOss 등이 12.9%, 오스코텍의 BioCera, SynCera가 8.1%로 국내시장의 점유율을 차지하고 있는 것으로 추정되고 있습니다. 당사의 제품 및 경쟁업체들의 제품의 비교 현황은 다음과 같습니다.
| [국내 치과용 골이식재 경쟁업체들의 제품 비교 현황] |
| 업체 명 | 주요 제품 | 주요 특징 및 장점 |
|---|---|---|
| Geistlich Pharma AG(스위스) |
BioOss | - 소뼈에서 추출된 천연 골이식재. - 유기성분을 제거할때 직접 열을 가하지 않고 화학처리에 의한 특허기술을 이용, 표면구조가 조직 세포의 유착성에 있어서 뛰어남. |
| 나이벡 | OCS-B | - 한우 소뼈에서 추출된 천연의 무기질 재료로써, 높은 순도, 체내 이식 안정성이 높음 - 면역 유발이 가능한 단백성 물질 제거가 완벽하면서도 인체의 뼈와 유사한 표면 구조를 가짐. |
| OCS-H | - 말뼈에서 추출한 골무기질로 인체의 골 구조와 유사 - 인체의 골과 거의 같은 형태의 구조를 가진 말뼈의 형태 및 구조를 그대로 유지 - 광우병 우려 해소 |
|
| 오스코텍 | SynCera | 순수β-TCP로 만든 합성골 제품으로 우수한 생체 친화성과 저렴한 가격 |
| InduCera | 칼슘포스페이트 크리스탈 이중코팅과 새로운 제조 공정으로 신생골 형성 능력을 보다 향상 |
2) 펩타이드 관련 제품
당사가 연구개발중인 펩타이드 관련 제품은 펩타이드 기반 골이식재와 펩타이드 기반의 골다공증 치료제, 관절염치료제, 비알콜성지방간염치료제, 염증성장질환치료제, 펩타이드 기반 바이오베터로, 펩타이드 소재인 점을 제외할 시 다른 소재를 기반으로 경쟁업체들이 연구개발 및 제품출시를 하고 있으며, 이와 관련된 모든 업체들이 경쟁업체라고 할 수 있습니다. 그러나 펩타이드를 기반으로 한 치료제는 글로벌적으로 아직 개발되지 않았기 때문에 시장점유율을 측정할 수 없는 상황입니다. 다만, 펩타이드 기반 골이식재 관련된 제품은 출시되었으며, 이에 대한 내용은 다음과 같습니다.
[펩타이드 기반 골이식재]
단백질이 지니는 염증 및 면역 원성의 부작용을 줄인 펩타이드를 개발하는 연구 및 이를 이용한 임플란트 제품 개발도 활발하게 연구되고 있으나 아직 연구개발 단계이며, 당사를 제외한 펩타이드 기반 골이식재를 개발한 기업은 Dentsply가 있습니다. 펩타이드 기반 골이식재 제품에 대한 설명은 다음과 같습니다.
 |
|
펩타이드 기반 골이식재 |
상기 기재된 바와 같이 적극적인 영위사업에 대한 투자와 계획에도 불구하고 많은 신제품이 연구, 개발되고 있는 경쟁이 치열한 바이오 산업시장에서 당사의 기 출시된 제품을 비롯하여 개발되고 있는 제품들이 유사한 기술을 바탕으로 경쟁업체와의 경쟁이 뒤쳐지거나 혹은 경쟁업체의 우수한 기술을 바탕으로 뛰어난 품질과 가격경쟁력을 보유한 제품들이 개발될 경우, 당사의 영업환경이 급격히 악화될수 있으니 유의하시기 바랍니다.
|
라. 정부 정책 변동에 따른 위험 |
의약품 시장은 정부의 의료 정책 및 관리제도와 밀접한 관련성이 있습니다. 인간의 생명과 보건에 관련된 제품을 생산하는 산업으로 국민의 건강증진 및 건강권 확보 등에 직간접적 영향을 주기 때문에 정부의 정책 및 제도의 변경에 따라 영향을 크게 받습니다.
보건복지부는 범정부 차원으로 수립된 '줄기세포의 연차별 시행계획'에 따라 2007년부터 줄기세포연구의 연차별 시행계획을 수립하고 이를 시행하여 오고 있으며, 2015년 3월에는 '바이오헬스 미래신사업 육성 전략'을 발표하여 암, 관절염, 척수손상 등 난치질환에 대한 바이오의약품(줄기세포, 유전자치료제 등) 개발에 2015년 총 3,400억원을 투자하여 글로벌 시장 선점을 확대하기로 하였습니다.
| [바이오의약품 관련 정부 지원 정책] |
|
시 기 |
내 용 |
|---|---|
|
2015.03 |
'바이오헬스미래신사업 육성 전략' 발표. 2015년 총 3,400억원 투자 |
|
2016~ |
국립 줄기세포재생센터 개소 및 임상 연구용 줄기세포치료제 위탁생산지원 |
|
2017.08 |
'첨단바이오의약품법' 국회 상정 |
|
2017.11 |
'제2차 제약산업 육성 지원 5개년 종합계획’ 바이오의약품 R&D 지원 확대 |
| 2019.03 | '첨단재생의료 및 첨단바이오의약품에 관한 법률안' 심의/의결 |
2017년 11월에는 보건복지부가 '제2차 제약산업 육성 지원 5개년 종합계획' 공청회를 열고 줄기세포 치료제, 유전자 치료제 등 첨단 바이오의약품에 대한 정부 연구개발(R&D) 지원을 늘린다고 발표했으며 1조 7천억원 규모인 민관 R&D 투자금액을 오는 2022년까지 2배로 확대한다고 하였습니다. 또한 2017년 8월 발의되어 11월 국회 상정된 '첨단바이오의약품법(안)'은 원료채취부터 사용단계까지 전주기 맞춤형 안전관리체계 구축하고, 국내 개발 첨단바이오의약품에 대하여 개발 초기부터 밀착지원을 통해 신속한 시장진입을 촉진하고 치료수단이 없는 환자들에 치료기회를 제공하고자 하고 있습니다.
2019년 03월 25일에 정부는 '첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률안'(이하 첨단 바이오법)을 의결하였습니다. 첨단 바이오법은 세포치료, 유전자치료, 조직공학치료 등 첨단재생의료 임상연구를 실시할 수 있는 근거를 마련하고, 첨단바이오의약품에 대한 전(全)주기 안전관리체계를 담았으며, 첨단바이오의약품 조건부 허가와 관련, 당초 비가역적 질병, 만성 또는 재발성 질병 등 포괄적 범위에 해당됐던 조건부 허가 대상이 암 또는 희귀질환 등으로 축소됐습니다. 아울러 재생의료의 경우 관련 분야 활성화 지원과 환자의 안전성 확보가 조화를 이룰 수 있는 방안이 담겼습니다. 이처럼 최근 정부에서는 바이오의약품에 대한 연구개발지원을 확대하고 있고, 글로벌 시장 선점을 위해 정책적으로 지원하고 있습니다.
상기와 같이 정부의 적극적인 지원이 있는 반면, 의약품의 안전관리 강화, 세포치료제의 안전성과 유효성 확보를 위해 가이드라인을 제시하고 있고, 제도적으로 규제정책을 강화하고 있습니다. '세포치료제 제조 및 품질관리기준 가이드라인'의 강화, 약사감시 강화, 매년 '생물의약품 제조업체 정기점검’을 받도록 하는 등 규제를 강화하고 있으며, PIC/S(의약품상호실사협력기구) 가입을 기점으로 '국제조화' 등의 이유로 더욱 강화될 것으로 예상됩니다.
또한 바이오의약품도 다른 의약품과 동일하게 GMP 규정에 따라 제조 및 품질관리를 운영하도록 하고 있습니다. 우리나라 정부는 1977년에 '우수의약품 제조 관리 기준'을 보건사회부 예규로 공포하고 1978년 'KGMP(Korea GMP) 시행 지침'을 발표하였습니다. 이후 KGMP는 1994년 약사법 시행규칙에 '의약품 제조 및 품질 관리 기준'이 규정되면서 의약품 제조업과 품목 허가의 의무 요건이 되었습니다. 2008년 밸리데이션(Validation), 연간 품질 평가, 변경 관리 등 새로운 규정들이 포함되어 선진국의 GMP와 유사한 수준으로 KGMP가 전면 개정되었으며, 국내 제약업체들은 각 분류에 적합한 GMP 생산시설 구비를 위해 GMP 시설설비를 확대함에 따라 시설 및 설비투자 금액이 지속적으로 증가하는 추세를 보였습니다. 다만 KGMP는 아직은 세계 기준인 cGMP에 비해 그 적용 범위가 낮은 것으로 알려져 있습니다. 우수의약품의 제조·관리의 기준으로 상세 설명은 다음과 같습니다.
|
[GMP에 관한 설명] |
|
구분 |
설명 |
승인기관 |
재검토 |
|---|---|---|---|
|
KGMP (Korea Good |
우리나라 약사법 및 의약품등의 안전에 관한 규칙에서 정한 의약품 제조업자가 준수하여야 하는 의약품 제조 및 품질관리 기준 |
식품의약품안전처 (한국) |
매 3년 |
|
cGMP (current Good |
미국 의약품 판매를 위한 품질 및 생산에 관한 기준으로 공장의 구조/ 설비에서부터 원료의 구입, 제조, 품질관리/보증, 포장, 출하 및 유통에 이르는 의약품전반에 관한 관리 기준. 실사를 바탕으로 평가가 이루어지므로 현재 시점에서의 GMP를 평가한다는 의미에서 current를 붙여 cGMP라 칭함. |
미국식품의약국 |
비정기 |
| CE (Conformite Europeene) |
EU시장 내 안전에 관련된 통합 인증마크. 소비자의 건강, 안전, 환경보호 차원에서 위험성이 있다고 판단되는 품목이 유럽시장에서 유통될 때는 CE인증마크를 의무적으로 부착. 유럽시장 진출 시 필수적으로 갖춰야 할 수출상품의 비자(VISA)로 비유 | NB(notified body) - 유럽의 인증기관 | 매년 사후심사 |
당사는 높은 품질의 의약품 생산을 위해 KGMP 인증을 받은 당사의 충북 진천군 공장으로부터 바이오의약품을 생산하고 있으며, SGS, MFDS로부터 인증을 받았습니다. 또한 G-Med(프랑스)와 TFDA(태국)으로부터도 생산시설에 대한 GMP인증을 받았습니다. 증권신고서 제출일 현재 당사 생산시설의 GMP 인증 현황은 다음과 같습니다.
| [(주)나이벡 생산시설 GMP 인증 현황] |
|
최초 인증 일자 |
만기 일자 |
인증 내역 |
인증 기관 |
만기연장 계획 |
|---|---|---|---|---|
|
2018.12.16 |
2021.12.15 |
MDSAP (ISO 13485:2016) Australia; Canada; United States |
SGS(한국) |
3년 마다 갱신 |
|
2015.02.26 |
2021.10.30 |
의약품 제조 및 품질관리기준 적합판정서(의약품 GMP) |
MFDS(한국) |
3년 마다 갱신 |
|
2008.11.26 |
2021.08.30 |
의료기기 제조 및 품질관리기준 적합인정서(의료기기 GMP) |
MFDS(한국) |
3년마다 갱신 |
|
2018.12.12 |
2021.12.21 |
ISO 13485:2016 /EN ISO 13485 International |
G-Med (프랑스) |
3년마다 갱신 |
|
2017.11.15 |
2021.05.05 |
QSD 8571 Taiwan |
TFDA (태국) |
3년마다 갱신 |
당사가 영위하고 있는 상처치유 및 재생의학 사업은 바이오, 의료산업 내에서 높은 성장세를 보이고 있으며, 경제사회적 파급효과가 매우 큰 치료 영역으로 평가되어 정부에서도 '미래 성장을 견인할 수 있는 국가존망기술'로 선정하여 국가적으로 정책적 지원이 확대되고 있습니다. 그러나 동시에 GMP 규정에 따른 제조 및 품질관리 운영에 대한 점검, '세포치료제 제조 및 품질관리기준 가이드라인'의 강화, 임상시험 절차 및 수행 방법에 대한 기준 강화 등 제품의 안전성 및 유효성 등과 관련하여 규제책도 강화하고 있습니다. 이러한 정부 지원의 변화 및 규제 정책의 변화는 당사의 사업을 영위하는데 있어서 커다란 영향으로 작용하고 있으며, 향후 당사에 부정적인 영향을 미치는 정책이 시행될 경우 당사의 수익성 또한 영향이 있으므로 정부의 정책 시행에 대한 모니터링이 필요할 것으로 판단됩니다. 이 점 유의하시어 투자해 주시기 바랍니다.
| 마. 바이오의약품 임상시험 실패에 따른 위험 당사는 펩타이드 공학기술을 이용한 펩타이드 기반 융합 바이오소재, 펩타이드 치료제, 펩타이드 기반 바이오베타 사업을 위하여 연구개발을 하고 있습니다. 바이오의약품의 개발 과정은 후보물질 선정, 비임상 단계, 임상시험 진행 승인(IND), 임상 1~3상, 품목허가의 단계로 진행됩니다. 일반적으로 바이오의약품의 단계별 성공률은 임상1상에서 임상 2상까지는 66.0%, 임상2상에서 임상3상까지는 34.4%, 임상3상에서 신약허가 신청까지 57.2%, 신약허가에서 신약승인까지는 88.4%로, 임상1상부터 신약승인까지의 성공확률은 11.5%로 상당히 저조합니다. 또한 한국바이오협회가 발표한 임상단계별 특징에 의하면 임상1상에서 임상3상까지 임상대상은 1,000명~5,000명 이상이 필요하며 소요비용은 약 1,250억원을 예상하고 있습니다. 한편, 당사가 연구개발 중인 펩타이드 기반 바이오소재의 현황 및 연구개발단계는 다음과 같습니다. 1) 펩타이드 의약 바이오소재 당사의 펩타이드 의약 바이오 소재 중 OssGen-X15(골재생 펩타이드가 표면에 고정된 골이식재)는 전임상/임상 완료 및 국내/해외에서 허가 또는 인증을 받아 시판중에 있으며, Regenomer-pep(골재생 펩타이드 함유 주입형 골재생제)는 전임상/임상 완료 및 국내허가까지 완료한 상태로 해외 인증을 준비 중에 있습니다. 해외 인증이 완료되는 시점은 2021년 9월로 예상하고 있으며, 인증비용은 약 10억원이 소요될 것으로 예상하고 있습니다. 2) 펩타이드 관련 치료제 펩타이드 기반 치료제인 펩타이드 골다공증치료제(NIPEP-OSS)는 전임상이 완료된 상태로 임상1상 1년, 임상2상 2년, 임상 3상 2년이 진행된 후 2026년에 출시될 것으로 예상됩니다. 골관절염치료제(NIPEP-CARE 1), 비알콜성 간염 치료제(NIPEP-CARE2), 염증성 장질환치료제(NIPEP-CARE3), 항암치료제(NIPEP-ACD Tide),는 현재 전임상이 진행중에 있는 상태입니다. 당사는 향후 펩타이드 기반 골다공증치료제 임상 1상 진행비용 35억원, 펩타이드 기반 관절염 치료제의 전임상 및 1상임상비용 각각 30억원, 펩타이드 표적항암제 전임상비용 15억원, 비알콜성지방간염(NASH) 치료제와 장질환 치료제 전임상비용 30억원으로 총 140억원이 소요될 것으로 예상하고 있습니다. 당사는 펩타이드 기반 융합바이오소재의 임상단계, 품목허가 과정을 거치면서 최근의 임상시험 절차 및 기준에 대해 상대적으로 잘 인지하고 있고 노하우를 보유하고 있으며, 향후 펩타이드 기반 치료제의 연구개발 또한 당사 연구개발계획에 의거하여 절차를 진행하려고 합니다. 그럼에도 불구하고 당사의 파이프라인이 임상을 진행함에 있어서 유의미한 결과를 도출하지 못할 경우에는 제품화가 불가능하며 투입된 연구비, 연구 역량 등 당사에 높은 기회비용이 발생할 수 있으며 사업계획에 지대한 영향을 미칠 수 있습니다. 당사는 금번 주주배정후실권주 일반공모를 통하여 유입되는 자금 중 약 150억원(펩타이드 기반 골다공증치료제 임상 1상 진행비용 35억원, 펩타이드 기반 관절염 치료제의 전임상 및 1상임상비용 각각 30억원, 골이식재 및 골재생제 유럽임상비용 10억, 펩타이드 표적항암제 전임상비용 15억원, 비알콜성지방간염(NASH) 치료제와 장질환 치료제 전임상비용 30억원)을 향후 연구개발을 위한 자금으로 사용하려고 하고 있습니다. 그러나 상기 언급한 바와 같이 임상1상부터 신약승인까지의 성공확률은 11.5%로 상당히 저조하며, 임상시험이 성공하지 못할 경우 자산 및 매출화되지 못하고 모두 비용처리가 될 위험이 있습니다.그러므로 투자자께서는 임상시험 절차, 임상 시험의 단계별 성공률, 당사의 파이프라인 현황 및 개발 단계, 타사 사례 등을 통해 리스크에 대해 충분히 확인 및 인지하시고 투자에 임하시기 바랍니다. |
당사는 신성장동력사업군으로 펩타이드 공학기술을 이용한 펩타이드 기반 융합 바이오소재, 펩타이드 치료제, 펩타이드 기반 바이오베타 사업을 위하여 연구개발을 하고 있습니다. 바이오의약품의 개발 과정은 후보물질 선정, 비임상 단계, 임상시험 진행 승인(IND), 임상 1~3상, 품목허가의 단계로 진행됩니다. 당사가 예상하는 펩타이드 관련 제품의 개발 기간 및 타사의 바이오의약품의 개발기간을 고려해 보았을 때 평균 10년 이상의 오랜 기간이 소요되며, 단계별로 비임상 약 3~4년, 임상 5년, 허가 검토에 약 1년 정도의 시간이 소요될 것으로 예상됩니다.
약사법 시행규칙에 따르면 "임상시험(Clinical Trial)"은 의약품의 안전성과 유효성을 증명하기 위하여 사람을 대상으로 해당 약물의 약동ㆍ약력ㆍ약리ㆍ임상적 효과를 확인하고 이상반응을 조사하는 시험을 말합니다. 임상시험은 시판 허가 전의 3단계(1상, 2상, 3상)와 시판 후 임상시험(PMS)을 포함하여 총 4단계로 구분됩니다.
|
구 분 |
내 용 |
|---|---|
|
전 임상시험 |
후보물질의 독성과 유효성을 평가하는 단계로 동물 또는 세포를 대상으로 시험. 후보물질의 부작용 여부 등을 확인 |
|
제1상 임상시험 |
건강한 사람 20~80명을 대상으로 약품을 안전하게 투여할 수 있는 용량과 인체 내 약품 흡수 정도 등을 평가 |
|
제2상 임상시험 |
100~200명의 소규모 환자들을 대상으로 약물의 약효와 부작용을 평가하고, 유효성을 검증 |
|
제3상 임상시험 |
신약의 유효성이 어느 정도 확립된 후에 대규모(최소 수백 명에서 수천 명) 환자들을 대상으로 장기 투여시의 안전성 등 검토와 확고한 증거 수집 위해 실시 |
|
제4상 임상시험 |
신약이 시판 사용된 후 장기간의 효능과 안전성에 관한 사항을 평가하기 위한 시험으로 시판 후 조사(Post-marketing Surveillance) |
|
(자료 : 한국제약산업길라잡이 2014) |
개발사들은 앞 단계의 연구에서 위험(안전성) 대비 이익(유효성)이 충분하다고 판단될 때 다음 단계 임상시험의 진입을 결정하게 되며, 약사법에 따라 적합한 임상시험계획승인(IND) 신청 자료를 마련하여 규제기관의 심사를 받게 됩니다. 규제기관은 위험 대비 이익이 허용 가능하다고 판단되면 IND 승인을 해주며, 개발사는 승인된 계획서와 의약품임상시험관리규정을 준수하여 임상시험을 실시하게 됩니다.
임상시험계획서에서 설정한 가설을 임상시험을 통해 입증했을 때 임상시험이 성공한 것이며, 다음 단계 연구로 나아갈 수 있고, 가설을 입증하지 못하면 임상시험에 실패하게 됩니다. 임상시험의 가설은 단계별 목적과 질환별 치료목적에 따라 설정하며, 통계적 유의성 입증을 위한 대상자 수와 평가방법을 계획서에 명시해야 하며, 시험 진행 도중에 이러한 사항을 변경하기는 어렵습니다. 회사는 임상시험을 위해 자금과 시간을 투자해야 하기 때문에 다음 단계 임상시험에 진입할지 결정할 때 성공 가능성에 대한 면밀한 검토를 하지만, 임상의 단계가 올라갈수록 대상자 조건이 다양해지고 관찰기간이 길어지기 때문에 전단계에서 확인하지 못했던 결과가 나타날 수 있습니다.
1~3상 임상시험은 시험기관윤리위원회 심의 시 임상시험배상책임보험에 의무적으로 가입하도록 되어 있으며, 해당 보험을 통하여 시험 중 개발중인 약으로 인한 부작용 발생 시 대상자에게 적절한 배상을 하게 됩니다. 그로인하여 전임상 단계에서 안전성 및 효능이 검증되었음에도 불구하고 각 임상 단계에서 부작용 등 예상치 못한 결과로 인하여 의약품 개발에 실패할 위험이 상존합니다.
바이오의약품의 특성 상 연구개발에는 오랜 시간과 많은 자금이 소요되는 반면 완제의약품이 시장에 출시되기 전까지는 괄목할만한 수익이 발생하지 않기 때문에 임상 시험이 실패할 경우 개발회사에 미치는 타격은 막대할 수 있습니다. 일반적으로 바이오의약품의 단계별 성공률은 임상1상에서 임상 2상까지는 66.0%, 임상2상에서 임상3상까지는 34.4%, 임상3상에서 신약허가 신청까지 57.2%, 신약허가에서 신약승인까지는 88.4%로, 임상1상부터 신약승인까지의 성공확률은 11.5%로 상당히 저조합니다. 또한 한국바이오협회가 발표한 임상단계별 특징에 의하면 임상1상에서 임상3상까지 임상대상은 1,000명~5,000명 이상이 필요하며 소요비용은 약 1,250억원을 예상하고 있습니다. 이러한 높은수준의 임상비용과 오랜 소요기간은 비단 당사뿐 아니라 신약개발 사업을 영위하는 회사들에게는 필연적인 위험입니다.
| [바이오의약품 임상 시험 단계별 성공률] |
|
단계 |
바이오의약품 성공확률 |
|---|---|
|
임상 1상 → 임상 2상 |
66.0% |
|
임상 2상 → 임상 3상 |
34.4% |
|
임상 3상 → 신약허가신청 |
57.2% |
|
신약허가 → 신약승인 |
88.4% |
|
임상 1상부터 신약승인까지 성공 확률 |
11.5% |
| 자료) BIO Biomedtracker Amplion, Clinical Development Success Rates 2006-2015 |
| [임상 단계별 소요비용] |
| 임상단계 | 소요비용 |
|---|---|
| 임상1상 | 50억원 내외 |
| 임상2상 | 200억원 내외 |
| 임상3상 | 1,000억원 이상 |
| 자료) 한국바이오협회_2017 |
당사가 연구개발 중인 펩타이드 기반 바이오소재의 현황 및 연구개발단계는 다음과 같습니다.
1) 펩타이드 의약 바이오소재
당사의 펩타이드 의약 바이오 소재 중 OssGen-X15(골재생 펩타이드가 표면에 고정된 골이식재)는 전임상/임상 완료 및 국내/해외에서 허가 또는 인증을 받아 시판중에 있으며, Regenomer-pep(골재생 펩타이드 함유 주입형 골재생제)는 전임상/임상 완료 및 국내허가까지 완료한 상태로 해외 인증을 준비 중에 있습니다. 해외 인증이 완료되는 시점은 2021년 9월로 예상하고 있으며, 인증비용은 약 10억원이 소요될 것으로 예상하고 있습니다.
 |
|
펩타이드 의약바이오소재 연구개발 단계 |
2) 펩타이드 관련 치료제
펩타이드 기반 치료제인 펩타이드 골다공증치료제(NIPEP-OSS)는 전임상이 완료된 상태로 임상1상 1년, 임상2상 2년, 임상 3상 2년이 진행된 후 2026년에 출시될 것으로 예상됩니다. 골관절염치료제(NIPEP-CARE 1), 비알콜성 간염 치료제(NIPEP-CARE2), 염증성 장질환치료제(NIPEP-CARE3), 항암치료제(NIPEP-ACD Tide),는 현재 전임상이 진행중에 있는 상태입니다. 당사는 향후 펩타이드 기반 골다공증치료제 임상 1상 진행비용 35억원, 펩타이드 기반 관절염 치료제의 전임상 및 1상임상비용 각각 30억원, 펩타이드 표적항암제 전임상비용 15억원, 비알콜성지방간염(NASH) 치료제와 장질환 치료제 전임상비용 30억원으로 총 140억원이 소요될 것으로 예상하고 있습니다.
| [펩타이드 기반 치료제의 연구개발 진행상황 및 향후 계획] |
|
구 분 |
진행 상황 및 계획 |
전임상 |
임상 1상 |
임상 2상 |
임상 3상 |
출시예정 |
|---|---|---|---|---|---|---|
| 펩타이드 골다공증치료제 (NIPEP-OSS) |
- 2019년 12월식약처 임상시험 사전검토 제출, 현재 보완사항에 대한 자료 작성 중 - 기술이전 논의중. 임상2상부터는 기술이전 후 공동연구를 통해 진행 |
완료 |
2019.06~ |
2021.01~ |
2023.12~ |
2026 |
| 골관절염치료제(NIPEP-CARE 1), 비알콜성 간염 치료제(NIPEP-CARE2),염증성 장질환치료제(NIPEP-CARE3) |
- 전임상독성시험 진행중 |
진행중 (2019.4Q |
2020.12~ |
2021.06~ |
2024.06~ |
2027 |
| 항암치료제 (NIPEP-AntiCancer) |
- 유방암(Breast cancer)에 대한 유효성 시험 |
진행중 |
2021.01~ |
2022.06~ |
2025.06~ |
2028 |
| [당사 펩타이드 기반 바이오소재의 연구개발단계] |
 |
|
펩타이드 의약품 연구개발 단계 |
당사는 펩타이드 기반 융합바이오소재의 임상단계, 품목허가 과정을 거치면서 최근의 임상시험 절차 및 기준에 대해 상대적으로 잘 인지하고 있고 노하우를 보유하고 있으며, 향후 펩타이드 기반 치료제의 연구개발 또한 당사 연구개발계획에 의거하여
절차를 진행하려고 합니다. 그럼에도 불구하고 당사의 파이프라인이 임상을 진행함에 있어서 유의미한 결과를 도출하지 못할 경우에는 제품화가 불가능하며 투입된 연구비, 연구 역량 등 당사에 높은 기회비용이 발생할 수 있으며 사업계획에 지대한 영향을 미칠 수 있습니다.
특히 금번 주주배정후실권주 일반공모를 통하여 유입되는 자금 중 약 150억원(펩타이드 기반 골다공증치료제 임상 1상 진행비용 35억원, 펩타이드 기반 관절염 치료제의 전임상 및 1상임상비용 각각 30억원, 골이식재 및 골재생제 유럽임상비용 10억, 펩타이드 표적항암제 전임상비용 15억원, 비알콜성지방간염(NASH) 치료제와 장질환 치료제 전임상비용 30억원)을 향후 연구개발을 위한 자금으로 사용하려고 하고 있습니다. 그러나 상기 언급한 바와 같이 임상1상부터 신약승인까지의 성공확률은 11.5%로 상당히 저조하며, 임상시험이 성공하지 못할 경우 자산 및 매출화되지 못하고 모두 비용처리가 될 위험이 있습니다. 그러므로 투자자께서는 임상시험 절차, 임상 시험의 단계별 성공률, 당사의 파이프라인 현황 및 개발 단계, 타사 사례 등을 통해 리스크에 대해 충분히 확인 및 인지하시고 투자에 임하시기 바랍니다.
| 바. 높은 연구개발비 부담에 따른 수익성 위험 당사가 영위하는 바이오제약 사업의 특성상 장시간의 제품의 연구 개발에 대한 투자가 필수적입니다. 향후 보유 파이프라인의 펩타이드 기반 골다공증치료제의 임상 1상 진입비용 및 항염증 파이프라인의 전임상 비용의 증가로 인하여 연구개발비는 이전보다 많이 증가할 것으로 예측하고 있으며 특히 판매관리비의 증가를 초래하여 단기적으로 당사 수익성을 저해할 수 있습니다. 한편, 당사는 펩타이드를 기반으로 하는 의약품 개발비용에 대해서는 임상 3상 이전까지는 비용처리 하고 있으며 개발비를 포함한 한정된 내용연수를 가지는 다음의 무형자산은 사용가능한 시점부터 추정내용 연수동안 정액법으로 상각하고 있습니다. 무형자산화된 개발비의 경우, 향후 제품의 판매중단 등의 이유로 무형자산의 손상이 발생하게 될 경우에는 일시에 자산손상 인식 및 개발비 상각처리 등이 발생할 수 있습니다. 특히 금번 유상증자를 통한 자금조달로 펩타이드기반 의약품 파이프라인에 대해 2020년까지 약 150억원의 연구개발비를 사용할 예정이고, 해당 연구개발비는 성공률이 저조한 임상3상 이전까지 모두 비용화되며, 임상3상 성공 후 무형자산화과 될 시 당사의 회계정책에 의하여 상각처리될 예정입니다. 또한, 산업재산권 또한 특허권 침해 및 분쟁 등으로 손상이 발생하게 될 경우 상각처리 등이 발생으로 당사의 손익에 영향을 줄 수 있습니다. 당사의 예상과 달리 연구개발 진척 상황이 지연되거나 실패하는 등 자금운용 계획의 실행이 불가능해지는 상황이 발생할 경우, 단기적인 재무적 부담이 가중되어 당사의 수익성 및 재무안정성에 부정적인 영향이 있을 수 있습니다. |
바이오제약 산업에서는 제도적, 환경적 변화에 따른 신제품 개발능력과 R&D 활성화가 제약회사의 지속적인 성장을 기대하게 하는 중요한 요소로 작용하고 있습니다. 당사가 영위하는 바이오제약 사업의 특성상 제품의 연구 개발에 대한 투자가 필수적이며, 그 기간이 약 10여년 정도로 매우 길게 나타납니다.
당사는 무형자산의 경우 신제품,신기술 등의 개발 비용 중 개별적으로 식별가능하고 미래의 경제적 효익이 유입될 가능성이 매우 높은 비용은 개발비로 계상하고 관련 제품 등의 판매 또는 사용이 가능한 시점부터 상각하고 있습니다. 당사는 대부분이 의료기기 대상이었으며, 의료기기는 임상 없이 제품 판매 허가를 취득할 수 있고, 또한 그 성공률 또한 높아서 의료기기에 대해서는 자산화 하고 있습니다. 다만 펩타이드를 기반으로 하는 의약품 개발비용에 대해서는 임상 3상 이전까지는 비용처리 하고 있습니다. 또한 개발비를 포함한 한정된 내용연수를 가지는 다음의 무형자산은 사용가능한 시점부터추정내용연수동안 정액법으로 상각하고 있습니다.
|
과목 |
추정 내용연수 |
|---|---|
|
산업재산권 |
5~10년 |
|
개발비 |
5년 |
2018년말 무형자산항목에 계상되어 있는 개발비는 치과용 골이식재 및 바이오소재의 개발 및 펩타이드 기반 융합바이오소재 중 OssGen-X15 등의 전임상/임상이 완료되면서 총 취득원가 98.5억원을 계상하였으며, 이 중 감가상각누계 36.2억원, 국고보조금 39.3억원을 제외하고 23.1억원이 장부금액으로 남아있습니다. 이외에도 특허권, 상표권, 의장권 등 산업재산권 13.2억원 및 기타 무형자산 25.7억원이 장부금액으로 계상되어 있습니다. 상기 개발비는 회계상 무형자산으로 분류된 것으로, 향후 제품의 판매중단 등의 이유로 무형자산의 손상이 발생하게 될 경우에는 일시에 자산손상 인식 및 개발비 상각처리 등이 발생할 수 있습니다. 산업재산권 또한 특허권 침해 및 분쟁 등으로 손상이 발생하게 될 경우 상각처리 등이 발생으로 당사의 손익에 영향을 줄 수 있습니다.
| [2018년 당사의 무형자산 내역] |
| (단위: 백만원) |
| 구분 | 취득원가 | 감가상각누계액 | 정부보조금 | 장부금액 |
|---|---|---|---|---|
| 산업재산권 | 2,144 | (824) | - | 1,320 |
| 개발비 | 9,853 | (3,619) | (3,927) | 2,307 |
| 기타무형자산 | 2,589 | (21) | - | 2,568 |
| 합계 | 14,586 | (4,464) | (3,927) | 6,195 |
한편 2018년 기준 당사의 인건비, 위탁용역비, 원재료비 등을 포함한 연구개발비는 24.9억원으로 매출액의 47.9% 수준입니다. 2016년 및 2017년에 발생한 연구개발비는 각각 25.7억원, 26.9억원으로 비슷한 수준이 발생하고 있으며, 매출액 대비 비율은 각각 53.5%, 42.7%로, 2017년에 기술이전으로 인한 일시적 매출액 상승을 제외하면 비슷한 비율을 유지하고 있습니다. 2018년 연구개발비 24.9억원은 판매비와관리비 12.0억원로 회계처리되었으며, 10.7억원은 무형자산(개발비)처리 되었습니다.
| [최근 3년 연구개발비용] |
| (단위 : 천원) |
| 구 분 | 2018년 | 2017년 | 2016년 | |
|---|---|---|---|---|
| 비용의 성격별 분류 | 원재료비 | 21,300 | 44,408 | 65,850 |
| 인건비 | 961,774 | 973,219 | 399,181 | |
| 감가상각비 | 28,865 | 28,346 | 31,076 | |
| 위탁용역비 | 928,156 | 943,722 | 1,151,919 | |
| 기 타 | 554,482 | 703,992 | 921,086 | |
| 연구개발비용 합계 | 2,494,577 | 2,693,687 | 2,569,112 | |
| (정부보조금) | (199,951) | (1,074,296) | (2,058,457) | |
| 보조금 차감 후 금액 | 2,294,626 | 1,619,391 | 510,655 | |
| 회계처리 내역 | 판매비와 관리비 | 1,204,012 | 557,939 | 251,727 |
| 제조경비 | 224,004 | 227,645 | 118,368 | |
| 개발비(무형자산) | 1,066,561 | 1,908,103 | 2,199,017 | |
| 회계처리금액 계 | 2,494,577 | 2,693,687 | 2,569,112 | |
| 연구개발비 / 매출액 비율 [연구개발비용계÷당기매출액×100] |
47.90% | 42.74% | 53.48% | |
매년 매출액의 40% 이상이 발생하고 있는 연구개발비는 구강질환 개선제품, 조직재생용 바이오소재, 펩타이드 제품군, 화장품군의 각 분야 연구개발에 사용되고 있습니다. 이에 따른 당사 제품의 특징, 개발단계, 수익창출계획은 다음과 같습니다. 또한 당사가 정부보조금을 받아 정부과제를 수행한 실적은 다음과 같습니다.
| [당사의 전제품 파이프라인] |
|
제품군 |
분야 |
당사 제품명 |
특징 |
개발단계 |
수익창출 계획 |
|---|---|---|---|---|---|
|
펩타이드 |
펩타이드 기반 |
OssGen-X15 |
펩타이드 함유 |
허가완료 |
매출화 |
|
OssGen-X15 Gel |
펩타이드 함유 |
시제품제작 임상준비 |
매출 예정 |
||
|
OssGen Ortho |
펩타이드 함유 |
전임상 진입 준비 단계 |
매출 예정 |
||
|
펩타이드 치료제 |
OsseoTide |
골다공증 치료제 |
전임상 완료, |
임상1상 완료 후 기술이전 예정 |
|
| NIPEP-Care 1 |
관절염치료제염증성장질환치료제 |
전임상 진입 준비 단계 |
임상1상 완료 후 기술이전 예정 |
||
| NIPEP-Care 2 |
비알콜성지방간염치료제 |
전임상 진입 준비 단계 |
임상1상 완료 후 기술이전 예정 |
||
| NIPEP-Care 3 |
염증성장질환치료제 |
전임상 진입 준비 단계 |
임상1상 완료 후 기술이전 예정 |
||
|
NIPEP-ACD-TIDE |
항암치료제 |
전임상 진입준비 단계 |
전임상 완료 후 기술이전 예정 |
||
|
펩타이드 기반 |
OssGen better |
PTH 골다공증바이오베터 |
전임상 진행중 |
임상1상 완료 후 기술이전 예정 |
|
|
펩타이드 플랫폼 |
TOPscovery |
세포내 단백질(항체) 전달시스템 |
- |
플랫폼 서비스제공, 기술이전 예정 |
|
|
조직재생용 |
치과용 골이식재 |
OCS-B, |
잇몸뼈 재생 |
허가완료 |
매출화 |
|
치주조직재생용쉬트 |
GuidOss |
치주조직 재생 |
허가완료 |
매출화 |
|
|
Xeno-Gide |
치주조직 재생 |
허가 진행중 |
매출예정 |
||
| 흡수성치주조직 재생유도재 |
Regenomer |
치주 재생 |
허가완료 |
매출화 |
|
|
Regenomatrix Tape, Cote |
치주 재생 |
허가 진행중 |
매출예정 |
||
| 골이식용 복합재료 |
OCS-B Collagen, Equimatrix Collagen |
콜라겐 함유 골이식재 |
허가완료 |
매출화 |
|
|
구강질환 |
개인용 치아미백제 |
Dr.Whitiss (8.6%) |
치아미백 |
허가완료 |
매출화 |
|
전문가용 치아미백제 |
BlancTis Pro (10%) BlancTis Clinic(15%) |
치아미백 |
매출화 | ||
|
시린이 치료제 |
SensBlok |
시린이 치료 |
매출화 | ||
|
치과용 컨디셔너 |
Clinplant Syringe/Floss |
치태제거, 치은염, 치주염, |
매출화 | ||
|
치주질환치료제 |
MinoCure |
치은염, 치주염 치료 |
매출화 | ||
|
구강케어치약 |
Dr.BlancTis Phosphate |
천연성분치약 |
매출화 | ||
|
화장품 |
기능성화장품 |
펩타이드 화장품 원료 |
항노화, 염증억제, 미백등 |
ICID 등재 완료 |
매출예정 |
|
Dr.MyYou |
미백, 주름 개선 |
개발완료 |
매출화 |
||
|
Eustella Complex Solution |
항노화 기능 |
재생기능성 펩타이드 국제화장품 원료규격집 (ICID) 등재 완료 |
매출화 |
||
|
Estella AC Solution |
여드름 및 염증 억제 화장품 |
항염증 기능성 펩타이드 국제화장품 원료규격집 (ICID) 등재 완료, 피부임상시험완료 |
매출 예정 |
| [정부과제 수행실적] |
| 번호 | 주관부처 | 과제명 | 연구기간 |
|---|---|---|---|
| 1 | 한국산업기술평가원 | 생리활성펩타이드로표면개질된골재생촉진성골이식재의상용화기술연구 | 2005.04.~2007.03. |
| 2 | 한국보건산업진흥원 | 골재생 촉진기능성 치과용 실크피브로인나노차폐막의 상용화기술연구 | 2005.05.~2006.04. |
| 3 | 한국산업기술진흥협회 | 골재생 촉진성 치과용 키토산 나노차폐막의 상용화기술연구 | 2004.12.~2005.11. |
| 4 | 산업자원부 | 골형성 촉진 펩타이드를 이용한 주입형 골재생재의 개발 | 2007.06.~2011.01. |
| 5 | 한국디자인진흥원 | 골형성 촉진 펩타이드 함유 골이식재의 디자인연구개발 | 2007.11.~2008.04. |
| 6 | 한국보건산업진흥원 | 치주감염제어 및 기능성 조직재생 융합소재개발연구 | 2008.11.~2012.03. |
| 7 | 충청광역경제권선도산업지원단 | 치주조직재생 차폐막 및 조직공학용 콜라겐 지지체의제품화기술 | 2009.10.~2012.04. |
| 8 | 충북도청 | 콜라겐함유치주조직재생제의제품화를위한안전성및유효성평가 | 2010.06.~2011.05. |
| 9 | 중소기업청 | 근골격재생을 위한 펩타이드 기반 신소재 및 약물전달시스템의 사업화 | 2012.03.~2014.02. |
| 10 | 지식경제부 | 성형외과 피하조직수복용 바이오소재 개발 | 2012.08.~2014.04. |
| 11 | 미래창조부 | 노인 맞춤형 차세대 치과용 바이오임플란트 시스템 개발 | 2014.10.~2017.12. |
| 12 | 중소기업기술정보진흥원 | 펩타이드-앱타머 기반 트러블피부용 화장품 개발 | 2016.12.~2018.12 |
| 13 | 과학기술정보통신부 | 줄기세포 치료제 효율 최적화를 위한 기능성생리활성물질(참여기업) | 2017.06.~2022.06 |
| [현재 진행중인 정부과제 수행내용] |
|
과제명 |
줄기세포 치료제 효율 최적화를 위한 기능성생리활성물질 |
|
지원기관 |
과학기술정보통신부 원천기술개발사업 |
|
연구기간 |
2017.06.30 ~ 2022.06.29 (60개월) |
|
정부출연금 |
1,250,000,000원 |
|
민간(기업)부담금 |
435,000,000원 |
|
총 연구비 |
1,685,000,000원 |
|
주관기관 |
서울대학교 산학협력단 |
|
공동연구기관 |
㈜나이벡 |
당사는 향후 보유 파이프라인의 펩타이드 기반 골다공증치료제의 임상 1상 진입비용 및 항염증 파이프라인의 전임상 비용의 증가로 인하여 연구개발비는 이전보다 많이 증가할 것으로 예측하고 있습니다. 이는 특히 판매관리비의 증가를 초래하여 단기적으로 당사 수익성을 저해할 수 있습니다. 당사는 아래와 같이 연구개발비 투자 계획을 수립하고 있으며 금번 유상증자를 통한 자금 조달 계획과 함께 내부적으로 자금운용 계획을 마련하고 있습니다. 그러나 당사의 예상과 달리 연구개발 진척 상황이 지연되거나 실패하는 등 자금운용 계획의 실행이 불가능해지는 상황이 발생할 경우, 단기적인 재무적 부담이 가중되어 당사의 수익성 및 재무안정성에 부정적인 영향이 있을 수 있으니 이 점 유의하여 투자해 주시기 바랍니다.
| 사. 연구개발인력의 유출에 따른 위험 연구개발 능력은 당사가 속한 산업의 특성상 매우 중요한 요소이며, 지속적인 연구개발을 위해 우수한 인재를 보유/유치하는 것이 회사의 성과를 결정하는 가장 중요한 요소입니다. 당사는 핵심 연구인력의 관리 및 확보를 위하여, 차별화된 대우와 보상, 교육 지원등을 제공하고 있으나, 각종 보상책에도 불구하고 핵심인력의 이탈 가능성을 배제할 수는 없는 상황입니다. 실제로 상기 노력을 바탕으로 2017년초 26명에 비하여 2019년 현재 연구인력이 31명으로 5명 증가하였으나, 2017년부터 2019년 현재까지 총 16명이 퇴사하였으며, 펩타이드개발팀에서 총 4명이 퇴사하였습니다. 당사의 핵심 기술의 특성상 당사 연구개발인력 수준을 대체할 수 있는 인력이 풍부하지 않으며, 대기업, 연구소, 대형병원 등에 비해 우수한 연구개발인력의 유치가 상대적으로 어려울 수 있습니다. 또한 당사는 연구인력들을 대상으로 비밀유지계약을 통해 기술의 유출을 방지하고 있으며, 퇴사 이후에도 적용할수도록 하여 이러한 기술유출의 위험을 최소화하고 있으나, 핵심인력이 이탈할 경우 기술 유출로 인하여 당사의 경쟁력 약화 및 지속적인 성장에 부정적인 영향을 끼칠 수 있으니, 이 점 유의하여 투자해 주시기 바랍니다. |
연구개발 능력은 당사가 속한 산업의 특성상 매우 중요한 요소이며, 지속적인 연구개발을 위해 우수한 인재를 보유/유치하는 것이 회사의 성과를 결정하는 가장 중요한 요소입니다. 따라서 주요 연구 인력의 유출이 있을 경우 해당 연구 개발과제가 지연되거나 개발전략을 수정해야 할 가능성이 존재하며, 개발비 부담 등으로 당사의 경쟁력 및 성장 가능성이 악화될 수 있습니다.
당사의 중앙연구소는 5개의 개발팀을 보유하고 있습니다. 신제품개발팀, 펩타이드개발팀, 효능평가팀에서는 펩타이드 발굴과 응용, 조직재생용 바이오소재 개발, 의약품 제형설계의 기초 및 효력검증 연구 등을 수행하고 있으며, 품질관리팀과 품질보증팀은 제품의 생산, 출하 및 유통이 제조 기준 및 관리기준에 의거하여 엄격히 진행하고 있음을 상시 모니터링하는 등 최전방에서 품질을 보증하는 업무를 수행하며, 특히 당사의 GMP인증, 각종 규격인증 등의 취득 업무등도 병행하고 있습니다.
당사가 영위하고 있는 의약품 및 의료기기 산업은 장기간 연구개발을 통해 기술을 축적한 기업만이 진출할 수 있는 전문시장으로써 고급인력을 통한 지식활용이 필수적으로 요구되고 있습니다. 따라서 우수인력의 확보가 시장경쟁요소에 중요한 요소로 작용합니다. 당사는 증권신고서 작성일 기준 전 직원 66명중 총 31명(박사 3명, 석사 13명, 학사외 15명)의 연구개발 인력을 보유하고 있습니다.
| [연구인력 현황] |
| (단위 : 명) |
|
구 분 |
인 원 |
||||
|---|---|---|---|---|---|
|
박 사 |
석 사 |
학사 외 |
합 계 |
||
|
첨단소재개발 |
신제품개발팀 |
- |
3 |
1 |
4 |
|
펩타이드개발팀 |
2 |
6 |
1 |
9 |
|
|
효능평가팀 |
- |
1 |
4 |
5 |
|
|
바이오소재 연구팀 |
바이오소재 개발팀 |
1 |
1 |
3 |
4 |
|
바이오소재 최적화, 상용화연구팀 |
- |
2 |
6 |
8 |
|
|
합 계 |
3 |
13 |
15 |
31 |
|
이 중 당사의 핵심 연구인력은 대표이사인 정종평, 연구소 전반의 총괄업무를 담당하고 있는 전무이사 박윤정, 중앙연구소 및 프로젝트 총괄업무를 담당하는 연구소장 이주연등 입니다. 대표이사인 정종평은 서울대학교 치과대학에서 치주학을 전공한 박
사로 치주염증을 비롯한 치과 분야 관련 연구를 계속해왔으며, 치과 임상의로서 다양
한 환자 케이스를 통하여 나이벡의 기반사업인 조직재생용바이오소재 연구개발에 이
바지 하였으며 R&D 및 경영총괄을 맡고 있습니다. 또한 연구소의 총괄업무를 담당
하는 박윤정 전무이사는 현재 서울대학교 치의학대학원 교수 재직중으로 당사의 연구개발 관련 산학협력활동 및 우수한 연구적 네트워크를 구축, 활용하여 우수한 양질의 연구 결과 도출에 이바지하였습니다. 박윤정 전무이사와 중앙연구소 프로젝트 총괄업무를 담당하는 이주연이사는 약학을 전공한 약학박사로 펩타이드를 이용한 약물전달시스템을 비롯한 펩타이드 기반 바이오 의약품 개발 관련하여 다수의 논문 및 특허, 그리고 영향력 있는 바이오 학회 초청 발표 등 활발한 연구 활동을 계속해오고 있는 당사의 핵심인력입니다.
|
<핵심 연구인력 현황> |
||||
|---|---|---|---|---|
|
직 위 |
성 명 |
담당업무 |
주요 경력 |
주요 연구실적(대표논문 5건) |
|
대표이사 |
정종평 |
총괄업무 |
서울대학교 치과대학 치의학 석사(72.02) 서울대학교 치과대학 치의학 박사(79.02) 미국뉴욕주립대학교 교환교수(82.12) 서울대학교 치과대학 교수(11.02) 서울대학교 치과대학 학장(02.02) 지능형생체게면공학 연구센터 센터장(09.03) |
The effect of the surface modification of titanium using a recombinant fragment of fibronectin and vitronectin on cell behavior, Biomaterials (26(25), 5153-5157), 2005
Electrospinning of chitin nanofibers: Degradation behavior and cellular response to normal human keratinocytes and fibroblasts, Biomaterials (27(21), 3934-3944). 2006
Assembly of collagen-binding peptide with collagen as a bioactive scaffold for osteogenesis in vitro and in vivo, Biomaterials (28(29), 4257-4267), 2007
Osteoblastic differentiation of human bone marrow stromal cells in self-assembled BMP-2 receptor-binding peptide-amphiphiles, Biomaterials. (30(21), 3532-3541), 2009
Peptide-mediated intracellular delivery of miRNA-29b for osteogenic stem cell differentiation, Biomaterials. 34(17):4347-59, 2013 |
|
전무이사 |
박윤정 |
연구소 전반 총괄업무 |
이화여자대학교 약학 석사(95.02) 이화여자대학교 약제학 박사(99.02) 미시간대학 약학대학 연구원(02.02) 미시간대학 약학대학 연구교수(03.05) 서울대학교 치의학대학원 교수(현재)
|
Intracellular delivery of cell-penetrating peptide-transcriptional factor fusion protein and its role in selective osteogenesis, Int J Nanomedicine. 9:1153-66, 2014
Simultaneous imaging and restoration of cell function using cell permeable peptide probe, Biomaterials. 35(24):6287-98, 2014
Selective osteogenesis by a synthetic mineral inducing peptide for the treatment of osteoporosis, Biomaterials. 35(37):9747-54, 2014
Identification of cell-penetrating peptide domain from human beta-defensin 3 and characterization of its anti-inflammatory activity, Int J Nanomedicine. 26;10:5423-34., 2015
Dual-function synthetic peptide derived from BMP4 for highly efficient tumor targeting and antiangiogenesis, nt J Nanomedicine. 11;4643-4656, 2016 |
|
이사 (연구소장) |
이주연 |
중앙연구소 프로젝트 총괄업무 |
이화여자대학교 약학 석사(00.02) 이화여자대학교 약제학 박사(04.02) 서울대학교 치과대학 지능형생체계면공학연구센터(IBEC) Post-Doctoral Research Fellowship |
Identification of cell-penetrating peptide domain from human beta-defensin 3 and characterization of its anti-inflammatory activity, Int J Nanomedicine. 26;10:5423-34., 2015
Dual-function synthetic peptide derived from BMP4 for highly efficient tumor targeting and antiangiogenesis, nt J Nanomedicine. 11;4643-4656, 2016
Control of cancer stem cell like population by intracellular target identification followed by the treatment with peptide-siRNA complex, Biochem Biophys Res Commun, 491(3):827-833, 2017
Comparative Study of rhPDGF-BB Plus Equine-Derived Bone Matrix Versus rhPDGF-BB Plus β-TCP in the Treatment of Periodontal Defects, Int J Periodontics Restorative Dent, 37(6):825-832, 2017
A novel calcium-accumulating peptide/gelatin in situ forming hydrogel for enhanced bone regeneration, J Biomed Mater Res A, 106(2):531-542, 2018 |
일반적으로 업계 연구 인력들의 특성이 학계나 국가 연구원 등에서 근무하는 것을 선호하고 있으며, 개인적인 학업 증진을 위한 해외유학 등의 사유로 핵심연구 인력의 이탈이 발생할 수 있습니다. 따라서 당사는 핵심 연구인력의 관리 및 확보를 위하여
핵심인력을 위한 차별화된 대우와 보상(특별 인센티브)을 실시하여 성과와 능력에 따라 승진이 가능하도록 조치하는 한편, 핵심인력이 보유한 능력 및 핵심역량을 육성하기 위한 지속적인 교육을 지원하고 있습니다. 향후에는 핵심인력의 경쟁력을 배가하기 위한 인적자원 관리프로그램을 구축할 예정이며, 국내 대학원 진학, 해외파견 등의 자기개발 프로젝트 또한 운영할 예정입니다. 그러나 이와 같은 각종 보상책에도 불구하고 핵심인력의 이탈 가능성을 배제할 수는 없는 상황입니다. 실제로 상기 노력을 바탕으로 2017년초 26명에 비하여 2019년 현재 연구인력이 31명으로 5명 증가하였으나, 2017년부터 2019년 현재까지 총 16명이 퇴사하였으며, 펩타이드개발팀에서 총 4명이 퇴사하였습니다.
| [연구인력 변동현황] |
|
구분 |
2016년 |
2017년 |
2018년 |
2019년 현재 |
2019년 현재기준 |
|||
|---|---|---|---|---|---|---|---|---|
|
부서 |
입사 |
퇴사 |
입사 |
퇴사 |
입사 |
퇴사 |
||
|
신제품개발팀 |
3 |
- | - | - |
1 |
2 |
- |
4 |
|
펩타이드개발팀 |
2 |
4 |
2 |
5 |
2 |
1 |
- |
9 |
|
효능평가팀 |
4 |
- | - |
1 |
1 |
1 |
- |
5 |
| 바이오소재개발팀 |
12 |
3 |
5 |
2 |
4 |
- |
1 |
5 |
| 바이오소재 최적화, 상용화연구팀 |
4 |
- |
- |
- |
- |
- | - |
8 |
|
합 계 |
28 |
7 |
7 |
8 |
8 |
4 |
1 |
31 |
핵심 연구인력이 이탈하여 경쟁업체로 이동하는 경우 당사가 사업을 영위함에 있어 큰 문제가 될 수 있습니다. 당사의 핵심 기술의 특성상 당사 연구개발인력 수준을 대체할 수 있는 인력이 풍부하지 않으며, 대기업, 연구소, 대형병원 등에 비해 우수한 연구개발인력의 유치가 상대적으로 어려울 수 있습니다. 또한 당사는 연구인력들을 대상으로 비밀유지계약을 통해 기술의 유출을 방지하고 있으며, 퇴사 이후에도 적용할수도록 하여 이러한 기술유출의 위험을 최소화하고 있으나, 핵심인력이 이탈할 경우 기술 유출로 인하여 당사의 경쟁력 약화 및 지속적인 성장에 부정적인 영향을 끼칠 수 있으니, 이 점 유의하여 투자해 주시기 바랍니다.
| 아. 지적재산권 침해에 따른 위험 당사는 기술력 기반의 바이오연구개발회사로서 핵심기술에 대한 지적재산권의 확보가 핵심 경쟁력입니다. 당사는 국내에서 구강질환개선제품 특허 32건(등록 24건, 출원8건), 조직재생용 바이오소재 특허 10건(등록 9건, 출원 1건), 펩타이드 기반 바이오소재 4건(등록 3건, 출원1건)으로 총 46건의 특허를 가지고 있습니다. 또한 PCT(특허협력조약) 출원 32건, 해외특허/출원 62건을 보유 중에 있습니다. 현재 당사의 핵심기술 및 활용기술과 관련한 소송이나 분쟁은 발생한 내역이 없으며 기술보호를 위해 국내뿐만 아니라 해외에서도 특허 등록을 진행하고 있습니다. 또한, 전문 컨설팅 기관으로부터 특허의 침해 여부 및 전략에 관하여 정기적으로 컨설팅을 받고 있습니다. 그럼에도 불구하고 향후 당사가 보유한 지적재산권을 적절히 보호하지 못하거나 당사가 사용하는 기술과 관련한 지적재산권 관련 분쟁이 발생하는 경우 당사의 경쟁력은 약화될 수 있으며 이는 당사의 영업 및 손익에 부정적인 영향을 미칠 수 있습니다. 이점 유의하여 투자해 주시기 바랍니다. |
당사는 기술력 기반의 바이오연구개발회사로서 핵심기술에 대한 지적재산권의 확보가 핵심 경쟁력입니다. 특허를 확보하지 못한 바이오기업은 원천적으로 사업이 불가능하거나, 특허 소유자로부터 전용실시권을 확보하여야 합니다. 이에 당사는 보유하고 있는 특허기간을 연장 및 보호하기 위해 다양한 전략 및 정책을 도입하고 있으며, 특허 원천기술 및 응용기술에 대한 지속적인 연구개발과 국내, 해외 특허를 출원 및 등록하고 있습니다.
당사는 국내에서 구강질환개선제품 특허 32건(등록 24건, 출원8건), 조직재생용 바이오소재 특허 10건(등록 9건, 출원 1건), 펩타이드 기반 바이오소재 4건(등록 3건, 출원1건)으로 총 46건의 특허를 가지고 있습니다. 또한 PCT(특허협력조약) 출원 32건, 해외특허/출원 62건을 보유 중에 있습니다. 특허를 등록 또는 출원한 제품에 대하여는 제반 권리 및 판매에 관한 유효성을 특허로 보호 받기 때문에 특허 존속기간 동안 배타적인 권리를통해 진입장벽을 형성할 수 있습니다. 당사가 보유한 지적재산권 현황 및 3년간 대표적인 특허 및 출원 중인 특허는 다음과 같습니다.
| [당사 보유 지적재산권 현황] |
| 구분 | 국내특허 | PCT출원(주1) | 해외특허 | |
| 등록 | 출원 | 출원 | ||
| 구강질환개선제품 |
24 |
8 |
21 |
49 |
| 조직재생용 바이오소재 |
9 |
1 |
7 |
7 |
| 펩타이드 기반 융합바이오소재, 펩타이드치료제 및 펩타이드 기반 바이오베터 |
3 |
1 |
4 |
6 |
| 합계 |
36 |
10 |
32 |
62 |
| [3년간 특허 보유 현황(2016~2018년도)] |
|
순번 |
특허의 내용 |
권리자 |
출원/등록 |
국가명 |
출원/등록일 |
출원번호/등록번호 |
|---|---|---|---|---|---|---|
|
1 |
항균 및 항염증 활성을 가지는 펩타이드 및 이를 유효성분으로 함유하는 약제학적 조성물 |
㈜나이벡 |
등록 |
중국 |
2016.01.20 |
ZL 2011 8 0034167.4 |
|
2 |
콜라겐으로 구성된 주입형 피하조직재생용 바이오소재 |
㈜ 나이벡 / |
등록 |
대한민국 |
2016.01.26 |
/10-1590313 |
|
3 |
치아 지각과민 방지용 조성물 |
㈜ 나이벡 / |
등록 |
베트남 |
2016.02.22 |
15186 |
|
4 |
암줄기세포의 성장억제용 항암기능성 펩타이드 및 그 용도 |
㈜ 나이벡 / |
출원 |
PCT |
2016.03.03 |
PCT/KR2016/002109 |
|
㈜ 나이벡 / |
출원 |
유럽 |
2016.07.21 |
16 736 753.1 |
||
|
㈜ 나이벡 / |
출원 |
미국 |
2016.07.23 |
15/113,823 |
||
|
㈜ 나이벡 / |
등록 |
대한민국 |
2017.01.02 |
10-1693533 |
||
|
㈜ 나이벡 / |
등록 |
미국 |
2018.06.12 |
9993519 |
||
|
5 |
지르코니아 결합능을 가지는 펩타이드 |
㈜ 나이벡 / |
출원 |
PCT |
2016.04.05 |
PCT/KR2016/003505 |
|
㈜ 나이벡 / |
등록 |
대한민국 |
2016.11.28 |
10-1681886 |
||
|
㈜ 나이벡 / |
출원 |
유럽 |
2017.02.14 |
16776814.2 |
||
|
㈜ 나이벡 / |
출원 |
미국 |
2017.02.15 |
15/504,035 |
||
|
㈜ 나이벡 / |
등록 |
미국 |
2017.10.31 |
9801973 |
||
|
㈜ 나이벡 / |
출원 |
홍콩 |
2018.08.14 |
18110409.4 |
||
|
6 |
세포외기질 단백질-골미네랄 복합체를 함유하는 조직 구조 모사체 및 그 제조방법 |
㈜ 나이벡 / |
등록 |
대한민국 |
2016.06.02 |
/1628677 |
|
7 |
신규한 지방 축적 억제용 펩타이드 및 이를 포함하는 비만 예방 또는 치료용 약학조성물 |
㈜ 나이벡 / |
등록 |
대한민국 |
2016.07.06 |
/1638775 |
|
㈜ 나이벡 / |
출원 |
미국 |
2017.08.01 |
15/666,506 |
||
|
㈜ 나이벡 / |
출원 |
홍콩 |
2018.01.10 |
18100331.8 |
||
|
㈜ 나이벡 / |
등록 |
미국 |
2018.12.18 |
10,155.022 |
||
|
8 |
합성 펩타이드를 이용한 유도만능줄기세포의 제조방법 |
㈜ 나이벡 / |
출원 |
PCT |
2016.07.19 |
PCT/KR2016/007857 |
|
㈜ 나이벡 / |
출원 |
미국 |
2017.03.24 |
15/514,337 |
||
|
㈜ 나이벡 / |
출원 |
유럽 |
2017.04.27 |
16833217.9 |
||
|
㈜ 나이벡 / |
출원 |
일본 |
2017.04.27 |
2017-543696 |
||
|
㈜ 나이벡 / |
등록 |
미국 |
2018.09.04 |
10066212 |
||
|
㈜ 나이벡 / |
등록 |
대한민국 |
2018.10.02 |
10-1906557 |
||
|
㈜ 나이벡 / |
등록 |
일본 |
2018.12.07 |
6446566 |
||
|
9 |
티타늄 결합능을 가지는 펩타이드 |
㈜ 나이벡 / |
출원 |
대한민국 |
2016.07.26 |
10-2016-0094893 |
|
㈜ 나이벡 / |
출원 |
PCT |
2017.03.07 |
PCT/KR2017/002436 |
||
|
㈜ 나이벡 / |
출원 |
미국 |
2017.07.22 |
15/545,679 |
||
|
㈜ 나이벡 / |
출원 |
유럽 |
2017.08.25 |
17752273.7 |
||
|
㈜ 나이벡 / |
등록 |
대한민국 |
2018.12.24 |
10-1934047 |
||
|
10 |
줄기세포 재생 또는 증식능 향상용 세포 침투성 융합 단백질 |
㈜ 나이벡 / |
등록 |
미국 |
2016.08.09 |
9408920 |
|
㈜ 나이벡 / |
등록 |
대한민국 |
2018.06.14 |
10-1869268 |
||
|
11 |
종양선택적 투과기능성을 가지는 펩타이드 및 그 용도 |
㈜ 나이벡 / |
출원 |
미국 |
2016.08.11 |
15/234,396 |
|
㈜ 나이벡 / |
등록 |
미국 |
2017.12.26 |
9849190 |
||
|
12 |
세포 투과능 및 골조직 재생능을 가지고 있는 이중 기능성 신규 펩타이드 및 이의 용도 |
㈜ 나이벡 / |
출원 |
대한민국 |
2016.12.27 |
10-2016-0180121 |
|
㈜ 나이벡 / |
출원 |
PCT |
2017.12.27 |
PCT/KR2017/015588 |
||
|
13 |
바이오필름 억제용 펩타이드 |
㈜ 나이벡 / |
출원 |
대한민국 |
2017. 04. 05 |
10-2017-0044233 |
|
㈜ 나이벡 / |
출원 |
PCT |
2018.03.19 |
PCT/KR2018/003162 |
||
|
14 |
골 흡수 억제용 펩타이드 |
㈜ 나이벡 / |
출원 |
대한민국 |
2017. 08. 18. |
10-2017-0104939 |
|
㈜ 나이벡 / |
출원 |
PCT |
2018.06.19 |
PCT/KR2018/006874 |
||
|
15 |
노화된 줄기세포 선별용 단백질표지자 GRP78 |
㈜나이벡, |
출원 |
대한민국 |
2017. 10. 13. |
10-2017-0133613 |
|
16 |
노화된 줄기세포 선별용 GRP78 유래 펩타이드 |
(주)나이벡, |
출원 |
대한민국 |
2017. 10. 13. |
10-2017-0133614 |
|
17 |
인간 유래 세포 투과성 펩타이드와 생리활성 펩타이드 결합체 및 그 용도 |
㈜ 나이벡 / |
등록 |
유럽 |
2017.02.22 |
2615105 |
|
18 |
역분화 유도를 위한 세포투과성 융합단백질 및 그 용도 |
㈜ 나이벡 / |
등록 |
미국 |
2017.05.09 |
9644185 |
|
㈜ 나이벡 / |
등록 |
유럽 |
2017.07.05 |
2843052 |
||
|
19 |
표적 선택적 세포/조직 투과기능 활성을 가지는 펩타이드 및 그 용도 |
㈜나이벡 |
등록 |
인도 |
2017.06.29 |
284776 |
|
20 |
아파타이트에 결합하는 골조직 재생능을 가지는 펩타이드 |
㈜ 나이벡 |
등록 |
유럽 |
2017.07.19 |
2813516 |
|
㈜ 나이벡 |
등록 |
이스라엘 |
2017.07.31 |
225150 |
||
|
㈜ 나이벡 |
등록 |
캐나다 |
2018.01.02 |
2811621 |
||
|
21 |
부갑상선호르몬(parathyroid hormone, PTH)에 골조직 선택성 펩타이드가 결합되어 있는 융합 펩타이드를 포함하는 약학 조성물 및 생체재료 |
㈜ 나이벡 / |
출원 |
대한민국 |
2017.09.29 |
10-2017-0126876 |
|
㈜ 나이벡 / |
출원 |
PCT |
2017.11.29 |
PCT/KR2017/013749 |
||
|
22 |
염증감소능 및 줄기세포로부터 연골세포로의 분화 촉진능을 가지는 이중 기능성 펩타이드 및 이의 용도 |
㈜ 나이벡 / |
출원 |
대한민국 |
2018.03.14 |
10-2018-0029912 |
|
23 |
세포 투과능 및 근육 재생능을 가지는 이중 기능성 펩타이드 및 이의 용도 |
㈜ 나이벡 / |
출원 |
대한민국 |
2018.03.14 |
10-2018-0029913 |
|
24 |
골조직 재생을 위한 일체형 바이오소재 및 그 제조방법 |
㈜ 나이벡 / |
출원 |
대한민국 |
2018.06.19 |
10-2017-0077400 |
|
25 |
세포투과성 펩타이드와 형광표지 자성나노입자의 복합체 및 그 용도 |
㈜ 나이벡 / |
등록 |
유럽 |
2018.07.11 |
2197783 |
|
26 |
치은치주염 또는 임플란트 주위염 치료 및 예방용 조성물 및 상기 조성물이 코팅되어 있는 치간칫솔 |
(주)나이벡 |
출원 |
대한민국 |
2018.08.17 |
10-2018-0095971 |
|
(주)나이벡 |
출원 |
PCT |
2018.08.17 |
PCT/KR2018/009469 |
||
|
27 |
염증 및 대사성 질환의 바이오마커에 대한 결합능이 있는 신규한 펩타이드 및 이의 용도 |
㈜ 나이벡 / |
출원 |
대한민국 |
2018.08.31 |
10-2018-0103614 |
|
28 |
다중의 질환 바이오마커의 기능 및 발현을 억제하는 펩타이드의 신규한 용도 |
㈜ 나이벡 / |
출원 |
대한민국 |
2018.08.31 |
10-2018-0103615 |
|
29 |
단백질표지자 GRP78을 이용한 고효율 줄기세포의 선별 방법 |
㈜나이벡, |
출원 |
대한민국 |
2018.10.15 |
/10-2018-0122736 |
|
30 |
고효율 줄기세포 선별을 위한 GRP78 유래 펩타이드 |
㈜나이벡, |
출원 |
대한민국 |
2018.10.15 |
10-2018-0122816 |
|
31 |
펩타이드에 의한 표면활성형 콜라겐 차폐막 |
㈜ 나이벡 / |
등록 |
유럽 |
2018.10.31 |
2700655 |
당사가 영위하고 있는 조직재생용 바이오사업, 구강보건사업 및 펩타이드 기반 사업은은 각 개발사들이 보유한 특화된 기술 및 제품화 능력에 의하여 성패가 결정되는 기술지향형 산업입니다. 현재 당사의 핵심기술 및 활용기술과 관련한 소송이나 분쟁은 발생한 내역이 없으며 기술보호를 위해 국내뿐만 아니라 해외에서도 특허 등록을 진행하고 있습니다. 또한, 전문 컨설팅 기관으로부터 특허의 침해 여부 및 전략에 관하여 정기적으로 컨설팅을 받고 있습니다. 그럼에도 불구하고 향후 당사가 보유한 지적재산권을 적절히 보호하지 못하거나 당사가 사용하는 기술과 관련한 지적재산권 관련 분쟁이 발생하는 경우 당사의 경쟁력은 약화될 수 있으며 이는 당사의 영업 및 손익에 부정적인 영향을 미칠 수 있습니다. 이점 유의하여 투자해 주시기 바랍니다.
| 자. 기술이전 실패에 대한 위험 일반적으로 신약개발은 각 국가의 규제 당국이 제시하는 단계에 따라 비임상 독성 시험, 임상 시험 (1, 2, 3상), 시판 승인 절차를 거쳐 최종적으로 판매되기까지는 오랜 시간과 많은 비용이 소요되며, 많은 시간과 비용을 투자하였더라도 최종 제품으로 개발이 되는 비율은 매우 낮습니다. 이러한 특성상 많은 바이오중소기업들은 일부 파이프라인에 대해서는 기술이전을 사업모델로 하고 있습니다. 당사 또한 현재 치과분야에 한정하여 스위스의 Straumann사와 2017년 펩타이드 치과 응용기술 이전 계약을 통해 안정적인 미래 파이프라인 공급 및 신개발 제품의 공급관련 전략적 제휴에 합의한 바 있습니다. 또한 펩타이드 기반한 신약관련(골다공증, 관절염, 항암, 비알콜성지방간염, 염증성 장질환 등)하여, A사를 비롯한 총 네곳의 국내외 제약사와 NDA를 체결하였으며, 이에 대한 기술이전에 관한 논의를 계속해서 진행 중에 있니다. 펩타이드기반 바이오베터인 골다공증바이오베터는 전임상을 진행중에 있으며 임상1상 완료후 기술이전을 예상하고 있고,세포내 단백질(항체)를 전달할수있는 기능을 가진 펩타이드플랫폼을 이용하여 기술이전 또는 당사의 펩타이드플랫폼을 사용할수있는 서비스를 제공하여 수익창출할 계획에 있습니다. 그러나, 당사의 계획과 달리 파트너사와의 협의가 원활히 이루어지지 않아 기술이전 계약이 취소되거나 규모가 축소될 경우 사업에 부정적인 영향이 생길수 있으니 투자자분들께서는 이점 유의하시기 바랍니다. |
일반적으로 신약개발은 후보물질 발굴까지의 연구단계와 비임상시험부터 임상시험까지의 개발단계, 그리고 최종 제품으로 판매하기 위한 허가 및 생산, 마케팅 단계로 나눌 수 있습니다. 각 국가의 규제 당국이 제시하는 단계에 따라 비임상 독성 시험, 임상 시험 (1, 2, 3상), 시판 승인 절차를 거쳐 최종적으로 판매되기까지는 오랜 시간과 많은 비용이 소요되며, 많은 시간과 비용을 투자하였더라도 최종 제품으로 개발이 되는 비율은 매우 낮습니다. 이러한 특성상 많은 바이오중소기업들은 일부 파이프라인에 대해서는 기술이전을 사업모델로 하고 있습니다.
| [2018 국내 제약바이오기업 기술수출 현황] |
| [단위 : 만 USD] |
| 일자 | 회사명 | 제품명 | 계약업체명 | 계약규모 | 계약금 |
|---|---|---|---|---|---|
| 1 | 동아에스티 | DA-9801(당뇨병성신경병증) | 뉴로브파마슈티컬스(미국) | 18,000 | 200 |
| 2 | SK케미칼 | 인틀루엔자백신 생산기술 | 사노피파스퇴르(프랑스) | 15,500 | 1,500 |
| 3 | 크리스탈지노믹스 | CG026806(급성골수성백혈병) | 앱토즈바이오사이언스(미국) | 12,500 | 300 |
| 4 | ABL바이오 | 항암항체신약물질 5종 | TRIGR테라퓨틱스(미국) | 55,000 | 430 |
| 5 | 유한양행 | YH4618(디스크치료제) | 스파인바이오파마(미국) | 21,815 | 65 |
| 6 | JW중외제약 | JW1601(아토피치료제) | 레오파마(덴마크) | 4,200 | 1700 |
| 7 | 앱클론 | AC101(위암 유방암) | 상하이헬리우스바이오텍(중국) | 125,500 | 5,000 |
| 8 | 유한양행 | YH25448(폐암신약) | 얀센바이오텍(미국) | 4,000 | 1,000 |
| 9 | 코오롱생명과학 | 인보사(골관절염치료제) | 먼디파마케이케이(일본) | 59,160 | 2,665 |
| 10 | 인트론바이오 | SAL200(슈퍼박테리아치료제) | 로이반트사이언스(미국) | 66,750 | 1,000 |
| 11 | 크리스탈지노믹스 | 아셀렉스(비스테로이드진통제) | 팜아티스인터내셔날(러시아) | 10,574 | 10 |
| 12 | 에이비엘바이오 | NOV1501(이중항체) | TRIGR테라퓨틱스(미국) | 59,500 | 500 |
2018년 유한양행, 동아에스티, JW중외제약, SK케미칼과 같은 대형제약사는 물론이고 크리스탈지노믹스, 에이비엘바이오, 앱클론, 인트론바이오같은 바이오벤처들도 잇따라 기술수출에 성공하였습니다. 이는 국내기업들의 기술력은 높아지면서 신약개
발의 가능성은 많아지고 있지만 현실적으로 국내에서 이 모든 신약개발 과정을 진행하기가 쉽지 않은 상황때문입니다. 하나의 신약개발에는 평균 10년이라는 개발기간과 신약이 제품으로 출시되기 까지는 조 단위에 해당하는 비용이 필요합니다. 그중 비용의 상당부분을 차지하는 임상시험의 진행은 한 기업이 자체적으로 진행하기에는 어려운것이 현실입니다. 또한 최근 개발되는 신약들은 대부분 글로벌시장을 목표로 하기때문에 다국가 임상이 거의 필수로 여겨지고 있습니다. 이때문에 국내에서만 진행되는 임상에 비해 규모도 크고 환자 모집과정등도 쉽지 않습니다. 이와같은 이유로국내 기업들은 임상 초기단계에서 인프라를 구축한 글로벌 제약사 또는 글로벌 의료기기 업체와 협업하는 경우가 많습니다.
당사는 현재 치과분야에 한정하여 스위스의 Straumann사와 2017년 펩타이드 치과 응용기술 이전 계약을 통해 안정적인 미래 파이프라인 공급 및 신개발 제품의 공급관련 전략적 제휴에 합의한 바 있습니다. 제품에 대한 공동개발을 위한 투자유치를 현재 진행하고 있으며 투자규모 및 방법에 대해서 현재 논의 중에 있습니다.
| <라이센스아웃 계약 총괄표> |
| (단위: 백만원) |
|
품 목 |
계약상대방 |
대상지역 |
계약체결일 |
계약종료일 |
총계약금액 |
수취금액 |
진행단계 |
|---|---|---|---|---|---|---|---|
|
펩타이드 플랫폼 |
Straumann |
전세계 (한국제외) |
2017.03.21 |
각 제품별 및 국가별로 선정된 "제품 출시후 10년" 또는 "특허만료일"중 긴 기간 |
- |
1,125 |
제품개발 논의중 |
|
합 계 |
- |
1,125 |
|||||
주) 초기 기술료를 계약금으로 받았으며 추후 계약에 따라 총계약금액이 정해질 예정입니다.
주2) 외화금액은 계약일 최초고시 환율인 1,121.70원을 적용하였습니다.
| [당사가 개발하는 기술이전 예정 펩타이드기반 파이프라인의 개발 현황] |
|
분야 |
당사 제품명 |
특징 |
세부구분 |
현재 개발단계 |
수익창출 계획 |
|---|---|---|---|---|---|
|
펩타이드 치료제 |
OsseoTide |
골다공증 치료제 |
오리지날 |
전임상 완료, |
임상1상 완료 후 2021년 기술이전 목표 |
| NIPEP-Care 1 |
관절염치료제염증성장질환치료제 |
오리지날 |
전임상 진입 준비 단계 |
임상1상 완료 후 2022년 기술이전 목표 |
|
| NIPEP-Care 2 |
비알콜성지방간염치료제 |
오리지날 |
전임상 진입 준비 단계 |
임상1상 완료 후 2023년 기술이전 목표 |
|
| NIPEP-Care 3 |
염증성장질환치료제 |
오리지날 |
전임상 진입 준비 단계 |
임상1상 완료 후 2023년 기술이전 목표 |
|
|
NIPEP-ACD-TIDE |
항암치료제 |
오리지날 |
전임상 진입준비 단계 |
전임상 완료 후 |
|
|
펩타이드 기반 |
OssGen better |
PTH 골다공증바이오베터 |
바이오베터 |
전임상 진행중 |
임상1상 완료 후 2024년 기술이전 목표 |
|
펩타이드 플랫폼 |
TOPscovery |
세포내 단백질(항체) 전달시스템 |
- |
- |
플랫폼 서비스제공, |
또한 펩타이드 기반한 신약관련(골다공증, 관절염, 항암, 비알콜성지방간염, 염증성 장질환 등)하여, A사를 비롯한 총 네곳의 국내외 제약사와 NDA를 체결하였으며, 이에대한 기술이전에 관한 논의를 계속해서 진행 중에 있니다. 펩타이드기반 바이오베터인 골다공증바이오베터는 전임상을 진행중에 있으며 임상1상 완료후 기술이전을 예상하고 있고,세포내 단백질(항체)를 전달할수있는 기능을 가진 펩타이드플랫폼을 이용하여 기술이전 또는 당사의 펩타이드플랫폼을 사용할수있는 서비스를 제공하여 수익창출할 계획에 있습니다. 이러한 당사의 기술이전계획이 성사될시 일시적으로 수익이 크게 증가할 것으로 기대되고 있습니다.
당사는 당사의 파이프라인에 대해 해외의 다양한 파트너사와 기술이전에 대해 논의하고 있습니다. 파트너사의 임상수행능력, 회사 규모등을 판별하여 기술이전을 시행할 계획이나 당사의 계획과 달리 파트너사와의 협의가 원활히 이루어지지 않아 기술이전 계약이 취소되거나 규모가 축소될경우 사업에 부정적인 영향이 생길수 있으니 투자자분들께서는 이점 유의하시기 바랍니다.
2. 회사위험
| 가. 지속적인 당기순손실 발생에 따른 위험 당사는 코스닥시장 상장이후 2018년말까지 지속적인 당기순손실이 이어지고 있습니다. 당사는 골이식재 및 구강보건제품으로 약 40~50억원의 꾸준한 매출액을 발생시키고 있으나, 최근 펩타이드 관련 연구개발비 및 임상비용을 위한 지급수수료의 증가로 인해 판매비와 관리비가 증가하였으며, 2016년 -30.3억원, 2017년 -25.7억원, 2018년 -40.4억원의 당기순손실이 누적되고 있습니다. 이로 인하여 2018년말 기준 232.3억원의 결손금이 계상되어 있습니다. 당사는 대규모 공급계약 체결의 노력으로 향후 수익성을 개선하고자 하나, 판매비와관리비 및 영업외비용 등을 상회할 만큼의 매출규모가 발생하지 않고 임상 실험의 실패, 연구개발성과의 부진 및 주요 매출처와의 계약해지, 재계약 연장 불가등의 변수가 발생된다면 당사의 수익성에 부정적인 영향을 미칠 수 있습니다. 투자자 분들께서는 이점 유의하시기 바랍니다. |
당사는 코스닥시장 상장이후 2018년말까지 지속적인 당기순손실이 이어지고 있습니다. 당사는 골이식재 및 구강보건제품으로 약 40~50억원의 꾸준한 매출액을 발생시키고 있으나, 최근 펩타이드 관련 연구개발비 및 임상비용을 위한 지급수수료의 증가로 인해 판매비와 관리비가 증가하였으며, 2016년 -30.3억원, 2017년 -25.7억원, 2018년 -40.4억원의 당기순손실이 누적되고 있습니다. 상장 이후 당사의 실적 추이는 다음과 같습니다.
| [상장 이후 당사 실적추이] |
| (단위 : 백만원) |
| 구분 | 2018년 | 2017년 | 2016년 | 2015년 | 2014년 | 2013년 | 2012년 | 2011년 |
|---|---|---|---|---|---|---|---|---|
| 매출액 | 5,207 | 6,303 | 4,804 | 4,174 | 4,786 | 2,272 | 3,876 | 2,702 |
| 매출원가 | 4,746 | 4,347 | 4,004 | 3,241 | 3,870 | 2,569 | 2,857 | 2,367 |
| 매출총이익 | 462 | 1,956 | 800 | 933 | 916 | -297 | 1,019 | 335 |
| 판매비와관리비 | 3,864 | 3,085 | 3,300 | 2,516 | 3,941 | 2,340 | 1,824 | 2,137 |
| 영업이익 | -3,408 | -1,129 | -2,500 | -1,584 | -3,025 | -2,637 | -805 | -1,802 |
| 기타수익 | 167 | 65 | 128 | 124 | 685 | 36 | 94 | 107 |
| 기타비용 | 34 | 922 | 76 | 586 | 763 | 34 | 241 | 260 |
| 금융수익 | 42 | 14 | 41 | 31 | 31 | 70 | 50 | 50 |
| 금융비용 | 711 | 624 | 713 | 464 | 549 | 521 | 300 | 500 |
| 법인세비용차감전순이익 | -3,944 | -2,595 | -3,120 | -2,479 | -3,621 | -3,086 | -1,202 | -2,406 |
| 법인세비용 | 99 | -28 | -93 | -53 | 0 | 764 | 205 | -571 |
| 당기순이익 | -4,042 | -2,568 | -3,027 | -2,426 | -3,621 | -3,850 | -1,407 | -1,835 |
당사는 2011년 기술특례상장을 통해 코스닥 시장에 입성한 후 2013년까지 주력 제품이었던 골이식재의 매출 부진 및 해외시장 진출을 위한 인증비용, 시설투자로 인한 감가상각비로 인해 손실이 지속되었습니다. 이후 회사의 새로운 성장동력을 위하여 2014년 홈쇼핑 영업채널을 통해 치아미백제를 판매하면서 매출액이 약 50억원대로 증가하였으나, 높은 수수료와 부가적인 판촉상품때문에 수익성대비 판관비의 비중이 높은 저마진 구조로 인해 36.2억원의 당기순손실이 발생하였습니다. 2015년에는 마진률이 낮은 치아미백제 판매를 감소시켰으며, 치과용골이식재 매출에 주력하였으며, 화장품 사업을 새로 실시함으로써 전년대비 당기순손실이 약 12.0억원 감소하였습니다.
2016년을 분기점으로 치과용골이식재가 본격적으로 해외시장에 진출하기 시작하면서 치과용 골이식재 매출이 19.4억원에서 39.1억원까지 증가하였으며, 이에 따라 홈쇼핑 사업을 완전히 중단하였음에도 매출액이 전년대비 15.1% 증가하였습니다. 그러나 일시적인 해외인증비용 및 펩타이드 관련 연구개발의 위탁용역비 증가 및 인건비 상승으로 33.0억원의 판매비와관리비가 발생하였으며, 이로인해 영업손실 25.0억원이 발생하였습니다. 또한 차입금 및 사채 증가에 따른 금융비용이 증가하면서 당기순손실 30.3억원이 발생하였습니다.
2017년 또한 치과용 골이식재의 매출이 39.1억원에서 45.3억원으로, 치주조직재생용 바이오소재의 매출이 1.4억원에서 3.7억원으로 증가하였으며, 2017년 03월 글로벌 임플란트산업의 1위 업체인 Straumann AG(유럽)과 치료용 펩타이드 기술의 치과분야 응용기술을 이전하면서 11.2억원의 일시적인 수익 증가가 있었습니다. 이에 따라 2017년 매출은 63.0억원으로 전년대비 31.2% 증가하였습니다. 그러나 여전히 높은 판매비와관리비로 11.3억원의 영업손실이 발생하였으며, 무형자산(개발비)의 손상차손 8.0억원으로 인한 기타비용 증가, 6.2억원의 금융비용 등의 발생으로 25.7억원의 당기순손실이 발생하였습니다.
2018년의 매출은 52.1억원으로, 2017년의 기술이전으로 인한 일시적인 수익을 제외 시 비슷한 매출 수준을 유지하였습니다. 그러나 연구개발진 및 직원들의 추가 고용 증가에 따른 인건비 상승 및 전임상시험에 따른 연구개발비 증가 등으로 판매비와관리비가 38.6억원이 발생하여 34.1억원의 영업손실이 발생하였습니다. 또한 7.1억원의 금융비용 발생으로 40.4억원의 당기순손실이 이어졌습니다.
당사는 상기 기재된 바와 같이 2011년부터 지속적으로 당기순손실이 이어지고 있으며, 이로 인하여 2018년말 기준 232.3억원의 결손금이 계상되어 있습니다. 그러나 매년 매출액의 약 40~60%의 연구개발비를 사용하면서 누적된 연구개발진들의 기술력과 글로벌 임플란트 업체들로부터의 당사 기술력에 대한 신뢰 향상은 향후 당사의 영업에 긍정적인 요소로 작용할 것으로 기대되고 있습니다. 또한 당사는 대규모 공급계약 체결을 통하여 수익성 향상을 위한 계획을 진행 중에 있습니다.
가) Straumann 치과용 골재생 바이오소재 및 콜라겐 바이오소재 대규모 공급계약
당사는 2019년 02월 Staumann과 치과용 골재생 바이오소재 및 콜라겐 바이오소재 등 품목계약의 건으로 수시공시의무관련사항(공정공시)을 공시한 바 있습니다.
| 구 분 | 내 용 |
|---|---|
| 공정공시 대상정보 | 치과용 골재생 바이오소재 및 콜라겐 바이오소재 등 품목계약의 건 |
| 계약기간 | 2019년 2월 21일 ~ 2024년 2월 20일 (5년간) |
| 계약품목 | OCS-B, OCS-B Collagen, GuidOss, Regenomer, Clinplant |
| 계약규모 | (1) Contract Year 1 : 2,000,000CHF (2) Contract Year 2 : 3,000,000CHF (3) Contract Year 3 : 4,500,000CHF (4) Contract Year 4 : 5,500,000CHF (5) Contract Tear 5 : 7,000,000CHF 총 계약규모 : 22,000,000CHF (한화 24,677,400,000원) (적용환율은 계약일 최초고시 환율인 1,121.70원을 적용) |
| 기타 | 상기 계약규모는 Straumann이 제시한 예상 계약규모이며, 발주사항이 기재된 발주서에 의해 확정됨 |
상기 공급계약 건은 계약기간이 총 5년으로 1년째 2,000,000CHF, 2년째 3,000,000CHF, 3년째 4,500,000CHF, 4년째 5,500,000CHF, 5년째 7,000,000CHF로 총 계약규모가22,000,000CHF(약 한화 246.8억원)이며, 2018년 매출액 대비 473.8%입니다. 이는 기존 치과용 골이식재 파트 외에 구강케어 파트, 콜라겐 파트 등 다양한 품목을 대상으로 한 계약으로 다소 침체되어 있던 구강케어 파트도 성장성을 보일 것으로 기대하고 있습니다.
나) Nobel Biocare 치과용 골이식재의 추가 공급계약
Nobel Biocare와의 기존 계약금액은 6,484천USD이었으며, 2019년 2월 20일 기준 이행금액은 4,716천USD으로 약 73% 이행하였습니다. 금번 계약변경으로 7,442천USD가 증가되어 총 계약금액은 13,926천USD입니다. 남아있던 수주 및 추가 계약으로 인한 수주를 합할 시 2018년 매출액 대비 201.2%에 해당하는 규모입니다, 금번 계약은 2021년 12월 31일까지 납품이며, 2021년에 재계약 체결 시 수주 규모는 더욱 커질 것으로 예상하고 있습니다.
상기 두가지의 대규모 공급계약 체결로 인하여 2019년도부터의 제품 매출 성장은 큰 폭으로 상향될 것으로 기대되고 있습니다. 또한 상기 두 건의 계약은 모두 자동연장되는 계약의 형태이며, 치과용골이식재를 비롯한 치과용 의료기기 제품들은 사용했던 제품들만 사용하는 충성도가 높은 제품군으로, 당사에 CashCow가 될 것으로 전망되고 있습니다.
당사는 주요 매출품목인 조직재생용 바이오소재 및 펩타이드기반 신약에 대해 매출구조의 다각화 및 수익상승을 위해 현재 국내외영업활동을 다각도로 구상하고 대응하고 있으며, 영업활동 외에도 제품의 라인업 다양화, 신제품 파이프라인 확보 등 제품의 연구개발 또한 활발히 진행하고 있습니다. 그러나 이러한 노력에도 불구하고 판매비와관리비 및 영업외비용 등을 상회할 만큼의 매출규모가 발생하지 않고 임상 실험의 실패, 연구개발성과의 부진 및 주요 매출처와의 계약해지, 재계약 연장 불가등의 변수가 발생된다면 당사의 수익성에 부정적인 영향을 미칠 수 있으므로, 투자자 분들께서는 이점 유의하시기 바랍니다.
| 나. 매출처 편중 심화에 따른 위험 당사의 주요 매출처는 글로벌 임플란트 시장의 1,2위인 Straumann과 Noble Biocare이며, 2018년 기준 주요 매출처 상위 3개사에 대한 매출비중이 84.2%를 차지하고 있습니다. 상위 3개사 매출비중은 2016년 62.9%, 2017년 81.6%, 2018년 84.2%로 매출 의존도가 점차 높아지고 있습니다. 주요 매출처에 대한 매출 의존도가 상당히 높은 편이며, 이는 거채처 관리비용의 절감, 매출의 안정적인 성장 및 일정 수준 이익율을 확보하기가 가능하다는 점 등 긍정적인 요소도 존재하나, 주요 거래처의 시장 점유율 하락, 영업활동의 부진, 정책변경 및 당사와 협의과정에서 문제가 발생될 경우 당사의 영업활동 및 수익에도 부정적인 영향을 받을수 있습니다. 당사는 향후 다양한 제품 연구개발을 통하여 기존 주요 매출처 이외에도 신규 매출처 개척을 통해 매출처의 다각화를 진행 및 계획하고 있습니다. 다만, 당사의 계획과는 다르게 신규 매출처의 다각화에 실패하거나 주요 매출처의 영업활동이 부진 등으로 매출이 줄어들 경우 당사의 실적이 급격히 악화될 가능성이 존재하오니 투자자분들께서는 유념하시기 바랍니다. |
당사의 주요 매출처는 글로벌 임플란트 시장의 1,2위인 Straumann과 Noble Biocare이며, 2018년 기준 주요 매출처 상위 3개사에 대한 매출비중이 84.2%를 차지하고 있습니다. 상위 3개사 매출비중은 2016년 62.9%, 2017년 81.6%, 2018년 84.2%로 매출 의존도가 점차 높아지고 있습니다.
| [당사 최근3개년 주요 매출처의 매출액 및 매출비율] |
| (단위 : 백만원) |
|
순번 |
매출처명 |
2018년 | 2017년 | 2016년 | |||
|---|---|---|---|---|---|---|---|
| 매출액 | 비율 | 매출액 | 비율 | 매출액 | 비율 | ||
|
1 |
Nobel Biocare(스위스) |
2,162 |
41.51% |
1,648 | 26.15% | 1,018 | 21.19% |
|
2 |
Straumann(스위스) |
1,378 |
26.45% |
2,724 | 43.23% | 1,591 | 33.12% |
|
3 |
아이비덴탈(한국) |
848 |
16.28% |
767 | 12.17% | 412 | 8.57% |
| 합계 | 4,388 | 84.24% | 5,139 | 81.55% | 3,021 | 62.88% | |
주) 2017년 Straumann사와의 기술이전료(약11억원)가 포함되어 있습니다
| [ 주요 매출처의 개요 ] |
| 구분 | Nobel Biocare | Straumann |
|---|---|---|
| 회사명 | Nobel Biocare Holding AG | Straumann Holding AG |
| 국가 | 스위스 | 스위스 |
| 시가총액(19/03/29) | - | 약 14조 7,128억원 (128.65Billion CHF) |
| 본사 | PO Box CH-8058 Zurich-Airport Glattbrugg, 8152 Switzerland | Straumann Schweiz Peter Merian-Weg 12 4002 Basel |
| 자산총계 | - | 2조 1,329억원(1,865Million CHF) |
| 부채총계 | - | 7,594억원(664Million CHF) |
| 자본총계 | - | 1조 3,735억원(1,201Million CHF) |
| 매출 | - | 1조 5,560억원(1,364Million CHF) |
| 영업이익 | - | 3,923억원(343Million CHF) |
| 당기순이익 | - | 3,179억원(278Million CHF) |
주1) 서울외국환중개 2019년 03월 29일 기준 1CHF=1,143.63원
주2) 각 기업의 요약 재무상태는 2018년말 기준, 요약 손익계산서는 2018년초~말까지의 기준입니다.
주3) Nobel Biocare는 미국 헬스케어그룹인 다나허(Danaher Corp)에 인수됨에 따라 재무정보가 존재하지 않습니다.
Nobel biocare는 1952년에 임플란트 치료를 목적으로 설립되었으며, 세계 최초로 골유착 개념을 기초로 Branemark system을 개발한 기업입니다. 40년 이상의 역사를 보유한 Nobel biocare는 임플란트 PI 브래인마크(Branemark)의 골유착성 발견에서 프로세라(Procera) 디지털 보철 솔루션 및 완전 무치악 환자 치료까지, 치과의학계의 많은 분야에서 선구자로서의 입지를 쌓았습니다. Nobel biocare는 스위스에 상장되었으나, 2014년 12월 미국 헬스케어그룹인 다나허에 인수되면서 상장폐지되었으며, 다나허는 2018년 기준 Dental 분야에서 2,845백만USD(약 3조 2,370억원)가 발생하고 있습니다.
Straumann은 1954년에 설립된 임플란트시장 글로벌 1위 기업으로 스위스 바젤에 본사가 위치하고 있습니다. 1974년 세계 최초로 One-stage 임플란트를 개발한 이후, 35년 이상의 장기 임상 데이터와 연간 100건 이상의 임상 논문을 발표 중에 있습니다. 또한 26개의 해외 법인이 있으며, 약 100여개국에 진출하여 있습니다. 특히 2007년 한국법인을 설립하였으며, 임플란트와 관련하여 국내에서도 인지도가 가장 높은 기업입니다. 2018년 기준 자산 1,865백만CHF(약 2조 1,329억원)에 매출액 1,365백만CHF(약 1조 5,560억원을 기록하였습니다.
당사는 상기 기재된 바와 같이, 주요 매출처에 대한 매출 의존도가 상당히 높은 편이며, 이는 거채처 관리비용의 절감, 매출의 안정적인 성장 및 일정 수준 이익율을 확보하기가 가능하다는 점 등 긍정적인 요소도 존재하나, 주요 거래처의 시장 점유율 하락, 영업활동의 부진, 정책변경 및 당사와 협의과정에서 문제가 발생될 경우 당사의 영업활동 및 수익에도 부정적인 영향을 받을수 있습니다. 당사는 향후 다양한 제품 연구개발을 통하여 기존 주요 매출처 이외에도 신규 매출처 개척을 통해 매출처의 다각화를 진행 및 계획하고 있습니다. 다만, 당사의 계획과는 다르게 신규 매출처의 다각화에 실패하거나 주요 매출처의 영업활동이 부진 등으로 매출이 줄어들 경우 당사의 실적이 급격히 악화될 가능성이 존재하오니 투자자분들께서는 유념하시기 바랍니다.
| 다. 매출채권 회수 위험 당사의 2018년 매출채권은 1,905백만원으로 2017년 매출채권 1,851백만원 대비 소폭 증가하였으며, 매출채권 중 약 264백만원에 대하여 대손충당금을 설정(매출채권총액 대비 13.86% 수준)하고 있습니다. 주요 매출처를 제외한 기타 매출처들에 대하여 보수적으로 매년 추가 대손충당금 설정하면서 대손충당금설정률은 2016년 9.6%에서 2018년 13.9%로 증가하게 되었습니다. 당사의 매출채권 회전율은 2018년 3.17회, 2017년 3.64회로 한국은행에서 발간한 기업경영분석의 업종평균 3.5회(2017년 기준)과 비슷한 수준을 보이고 있습니다. 당사의 주요 매출처는 세계글로벌 1,2위 임플란트 관련 기업으로, 매출채권이 입금기한 내 100% 회수가 되고 있으며, 이로 인하여 대손충당금 설정에 의한 대손상각비 발생가능성은 적을 것으로 판단되고 있습니다. 그러나 향후 매출처의 영업환경 악화, 주된 거래처와의 거래관계 악화 등이 발생되어 매출채권이 원활하게 회수되지 못하거나, 회수가 지연되어 고령화된 매출채권이 발생할 경우 자금흐름이 악화될 수 있으며, 당사의 수익성 및 재무안정성이 악화될수 있으니 투자자들께서는 이점 유의하시기 바랍니다. |
당사는 고객의 지급불능 상태에서 발생하는 추정 손실의 회계처리를 위해 대손충당금 계정을 사용하고 있습니다. 대손충당금의 적정성을 평가시에는 매출채권, 미수금 등 채권의 연령분석을 통하여 각 연령구간별 채권에 대한 거래상대방의 파산여부, 대금지급가능성, 계약서 등을 바탕으로 대금지연, 연체 여부를 검토하여 채권의 손상사건 발생여부를 검토하고 있습니다. 손상사건이 발생한 개별채권 및 중요한 채권에 대하여 개별손상분석을 수행하며, 개별분석에 해당되지 않는 채권은 예상손실율을 적용하고 있습니다.
당사의 매출은 90%이상이 해외매출로 이루어져 있으며 주요 매출처는 글로벌 임플란트 회사이며, 결제조건은 대부분 납품 후 60일 이내 현금결제로 하고 있습니다. 특히 주요 거래처인 Straumann, Nobel Biocare, 아이비덴탈의 채권 회수율은 입금기한 내 100% 회수되고 있습니다. 국내 및 해외 매출의 큰 비중을 차지하는 당사의 주요거래처는 아래와 같으며 향후 동 거래처를 통한 매출채권 회수기한은 다음과 같습니다.
| [2018년 주요 매출처] |
| (단위 : 백만원) |
|
순번 |
매출처명 |
매출처 정보 | 매출금액 | 총 매출비율 | 회수기한 |
|---|---|---|---|---|---|
|
1 |
Nobel Biocare(스위스) |
치과용 의료기기 세계 점유율 2위 |
2,162 |
41.5% |
60일 |
|
2 |
Straumann(스위스) |
치과용 의료기기 세계 점유율 1위 |
1,378 |
26.5% |
60일 |
|
3 |
아이비덴탈(한국) |
국내 치과재료 전문 유통업체 |
848 |
16.3% |
30일 |
| 4 | KEYSTONE DENTAL(미국) | 임플란트 치과재료 전문 유통업체 |
217 |
4.2% |
30일 |
| 5 | TRIDENT S.A.R.L (레바논) |
치과 헬쓰케어 전문기업 |
109 |
2.1% |
30일 |
| 6 | 기 타 | 493 | 9.5% | - | |
| 합 계 | 5,207 | 100.0% | - | ||
당사의 매출채권 내역을 살펴보면, 2018년 매출채권은 1,905백만원으로 2017년 매출채권 1,851백만원 대비 소폭 증가하였으며, 매출채권 중 약 264백만원에 대하여 대손충당금을 설정(매출채권총액 대비 13.86% 수준)하고 있습니다. 주요 매출처를 제외한 기타 매출처들에 대하여 보수적으로 매년 추가 대손충당금 설정하면서 대손충당금설정률은 2016년 9.6%에서 2018년 13.9%로 증가하게 되었습니다. 당사의 매출채권 회전율은 2018년 3.17회, 2017년 3.64회로 한국은행에서 발간한 기업경영분석의 업종평균 3.5회(2017년 기준)과 비슷한 수준을 보이고 있습니다.
1) 당사 매출채권 및 대손충당금 설정 추이
| (단위 : 백만원, 회) |
| 구 분 | 2018년 | 2017년 | 2016년 |
|---|---|---|---|
| 매출액 | 5,208 | 6,303 | 4,804 |
| 매출채권 | 1,905 | 1,851 | 2,003 |
| 대손충당금 | (264) | (201) | (192) |
| 매출채권 순장부가액 | 1,640 | 1,650 | 1,811 |
| 대손충당금 설정률 | 13.9% | 10.9% | 9.6% |
| 매출채권회전율 | 3.17 | 3.64 | 2.38 |
| 산업평균 매출채권회전율 | - | 3.5 | 3.49 |
주) 산업평균 매출채권회전율 : 한국은행 기업경영분석(2017년 기준)의 한국표준 산업분류상 C27(의료, 정밀, 광학기기 및 시계-중소기업)의 매출채권회전율
2) 대손충당금 변동 추이
| (단위: 백만원) | |||
|---|---|---|---|
| 구 분 | 2018년 | 2017년 | 2016년 |
| 기초 | 201 | 192 | 135 |
| 설정(환입) | 63 | 9 | 58 |
| 기말 | 264 | 201 | 192 |
3) 2018년 매출채권 연령분석
| (단위 : 백만원) |
| 구 분 | 3개월 이하 | 3개월 초과 6개월 이하 |
6개월 초과 | 계 | |
|---|---|---|---|---|---|
| 금액 | 일반 | 1,199 | 345 | 97 | 1,640 |
| 특수관계자 | - | - | - | ||
| 계 | 1,199 | 345 | 97 | 1,640 | |
| 구성비율(%) | 73.10% | 21.01% | 5.89% | 100.00% | |
당사의 주요 매출처는 세계글로벌 1,2위 임플란트 관련 기업으로, 매출채권이 입금기한 내 100% 회수가 되고 있으며, 이로 인하여 대손충당금 설정에 의한 대손상각비 발생가능성은 적을 것으로 판단되고 있습니다. 그러나 향후 매출처의 영업환경 악화, 주된 거래처와의 거래관계 악화 등이 발생되어 매출채권이 원활하게 회수되지 못하거나, 회수가 지연되어 고령화된 매출채권이 발생할 경우 자금흐름이 악화될 수 있으며, 당사의 수익성 및 재무안정성이 악화될수 있으니 투자자들께서는 이점 유의하시기 바랍니다.
| 라. 재고자산 증가 및 노후화에 따른 위험 당사의 재고자산은 2016년 17.3억(총자산대비 7.53%), 2017년 24.1억(총자산대비 9.36%), 2018년 25.4억(총자산대비 11.40%)으로 최근 3개년 지속적으로 증가하고 있으며, 재고자산 회전율은 2016년 2.7회, 2017년 2.1회, 2018년 1.92회로 감소하고 있습니다. 당사는 동종업계의 평균 대비 낮은 재고자산 회전율을 보이고 있는데 낮은 재고자산 회전율은 당사의 재고자산 부담이 동종업계 대비 상대적으로 크다는 것을 나타냅니다. 향후 매출증가를 달성하지 못하거나 기술력이 저하되어 당사의 재고자산을 판매하지 못하게 될 경우 재고자산의 추가적인 감액 처리로 인하여 당사의 수익성은 악화될수 있습니다. 당사는 보유 중인 재고자산이 향후 영업계획 및 수주현황에 따라 소진될 것으로 예상하고 있으나, 당사의 개발제품에 대한 임상실험의 지연, 인증지연 또는 주된 거래처와의 거래관계의 악화나 산업의 침체 같은 요인들로 인해 영업환경이 영향을 받게되면 진부화된 재고자산 발생에 따른 재고자산 평가손실등의 인식으로 당사의 현금흐름 및 수익성에 부정적인 영향을 미칠수 있습니다. 이 점 유의하여 투자해 주시기 바랍니다. |
당사는 매월말 자체 재고조사가 실시되고 있으며 독립적인 외부감사인의 입회 하에 실시되는 것은 매년 말 재고조사를 시행하고 있습니다. 전수조사를 기본으로 실지 재고조사를 실시하고 있으며, 일부 중요성이 높지않고 품목수가 많은 품목에 한해서는 샘플링 조사를 실시합니다.
재고자산의 시가가 취득원가보다 하락한 경우에는 저가법을 사용하여 재무상태표가액으로 하고 있습니다. 감액된 재고자산의 시가가 장부금액보다 상승한경우에는 최초의 장부금액을 초과하지 않는 범위 내에서 평가손실을 환입하고 있습니다. 또한 당사는 원칙적으로 원부자제에대해 리뉴얼 혹은, 기재사항 변경등으로 사용이 어려운것데 대해서는 원가로 처리하는 경우가 대부분이며 완제품에 대한 충당금을 쌓는 기준은 제품별 유효기간이 임박한 경우 판매가 어렵기 때문에 이에 대해 충당금을 쌓고 있습니다.
당사의 재고자산은 2016년 17.3억(총자산대비 7.53%), 2017년 24.1억(총자산대비 9.36%), 2018년 25.4억(총자산대비 11.40%)으로 최근 3개년 지속적으로 증가하고 있으며, 재고자산 회전율은 2016년 2.7회, 2017년 2.1회, 2018년 1.92회로 감소하고 있습니다. 당사는 한국은행에서 발표한 '2017년 기업경영분석'에 의한 동종산업(의료, 정밀, 광학기기 및 시계-중소기업 C27)평균 대비 낮은 재고자산 회전율을 보이고 있는데 낮은 재고자산 회전율은 당사의 재고자산 부담이 동종업계 대비 상대적으로 크다는 것을 나타냅니다. 향후 매출증가를 달성하지 못하거나 기술력이 저하되어 당사의 재고자산을 판매하지 못하게 될 경우 재고자산의 추가적인 감액 처리로 인하여 당사의 수익성은 악화될수 있습니다.
| [당사 재고자산 현황] |
| (단위 : 백만원, 회) |
| 구 분 | 2018년 | 2017년 | 2016년 |
|---|---|---|---|
| 제품 | 1,820 | 1,776 | 1,769 |
| 제품 평가충당금 | (408) | (349) | (344) |
| 원재료 | 1,200 | 1,053 | 368 |
| 원재료 평가충당금 | (69) | (69) | (63) |
| 재고자산 순장부금액 | 2,543 | 2,410 | 1,729 |
| 총자산 대비 구성비율 | 11.40% | 9.36% | 7.53% |
| 재고자산회전율 | 1.92 | 2.10 | 2.70 |
| 재고자산회전율 산업평균 | - | 9.30 | 9.46 |
| 매출액대비 재고자산 비율 | 48.83% | 38.25% | 36.01% |
주1) 총자산대비 재고자산구성비율(%) = 재고자산합계÷기말자산합계X100
주2) 재고자산회전율(회수) = 연매출원가÷{(기초재고+기말재고)÷2}
주3) 산업평균 재고자산회전율은 한국은행 기업경영분석(2017년 기준)을 참조함. 업종은 한국표준 산업분류상 C27(의료, 정밀, 광학기기 및 시계-중소기업) (2018년은 집계되지 않음)
당사의 재고자산은 골이식재, 치아미백제, 펩타이드관련 제품 및 원재료등 입니다. 2018년말 기준 완제품의 경우 골이식재 바이오소재가 전체 원재료 중 40.9%를 차지하고 있으며, 원재료의 경우 펩타이드 관련 원재료가 전체 원재료 중 34.76%를 차지하고 있습니다. 당사는 향후 미래성장동력으로써 펩타이드 기반의 의료기기 및 신약을 제품화시키는데 필수 조건인 임상 실험을 위해 필요한 펩타이드 관련 원재료 매입을 증가하여 왔으며, 이에 따라 당사의 재고자산이 지속적으로 증가하여 왔습니다.
| [2018년말 재고자산 내역 및 비중] |
| 구분 | 제품명 | 비중 |
|---|---|---|
| 원재료 | 펩타이드원료 | 34.76% |
| 골이식재 | 4.49% | |
| 미노큐어 | 1.44% | |
| 기타 | 3.79% | |
| 소계 | 44.48% | |
| 완제품 | 골이식재 | 40.94% |
| OCS-B Collagen | 5.56% | |
| 화장품 | 2.55% | |
| 기타 | 6.47% | |
| 소계 | 55.52% |
자료 : 회사자료
당사는 보유 중인 재고자산이 향후 영업계획 및 수주현황에 따라 소진될 것으로 예상하고 있으나, 당사의 개발제품에 대한 임상실험의 지연, 인증지연 또는 주된 거래처와의 거래관계의 악화나 산업의 침체 같은 요인들로 인해 영업환경이 영향을 받게되면 진부화된 재고자산 발생에 따른 재고자산 평가손실등의 인식으로 당사의 현금흐름 및 수익성에 부정적인 영향을 미칠수 있습니다. 이 점 유의하여 투자해 주시기 바랍니다.
| 마. 재무안정성에 관련 위험 당사의 2018년말 기준 부채규모는 117.4억원이며, 부채비율은 111.4%입니다. 당사의 부채 중 가장 큰 비중을 차지하고 있는 차입금은 2018년 기준 78.2억원으로 유동성 차입금은 69.7억원, 장기차입금은 8.5억원으로 구성되어 있습니다. 총 차입금의존도는 35.05%입니다. 한국은행에 의하면 동종업계의 2017년 부채비율은 91.9%, 차입금의존도는 28.5%로 당사의 재무안정성비율은 동종업계 대비 상대적으로 열위한 수준에 있습니다. 또한 증권신고서 제출일 기준 당사는 차입금 외에 제5회차 사모 전환사채 46.5억이 있습니다. 제5회차 전환사채의 조기상환청구권(Put Option)은 발행일로부터 2년 경과한 날인 2019년 12월 26일부터 가능하나, 기한의이익 상실 조항의 효력이 발생할 경우 즉시 상환에 대한 가능성이 있습니다. 당사는 금번 KB증권으로부터 90억원(고정금리 연 5.9%, 만기 6개월)의 단기자금을 차입하여 연구개발비용 사용 및 동 전환사채에 대한 기한의이익상실 가능성에 대비할 계획입니다. 금번 KB증권으로부터의 단기 차입시 기존 제5회차 전환사채을 상환할 경우 당사의 차입금 의존도는 45.96%, 부채비율을 153.62%(미상환 시 차입금의존도 48.59%, 부채비율 196.12%)로 증가(2018년 재무제표에 단기 차입 및 상환을 단순 합산한 시나리오)하게 됩니다.금번 주주배정후실권주 일반공모 증자가 성공적으로 이루어질 경우 당사의 안정성 지표들은 개선 될 것으로 기대되고 있으나, 2018년말 기준 동종업계 대비 상대적으로 안정성 지표들이 열위한 수준에 있는 점, 주가하락에 따른 공모금액의 축소가능성 및 향후 지속적인 손실로 자본이 감소할경우 다시 채무가 증가할 가능성이 있습니다. 투자자 여러분께서는 추가적인 차입금 발생 여부 및 전환사채의 조기상환청구 가능성에 대하여 유의하여 투자를 고려해 주시기 바랍니다. |
당사의 2018년말 기준 부채규모는 117.4억원이며, 부채비율은 111.4%입니다. 당사는 연구개발과 인증, 임상진행을 위하여 외부에서 자금조달을 지속하여 왔으며, 이에따라 부채비율은 2016년 133.4%, 2017년 108.3%, 2018년 111.4%로 변동하여 왔습니다.
한국은행에서 발간한 2017년 기업경영분석 '의료, 정밀, 광학기기 및 시계-중소기업'의 2017년 부채비율은 91.9%, 차입금의존도는 28.5%로 당사의 재무안정성비율은 동종업계 대비 상대적으로 열위한 수준에 있습니다. 최근 3년간 당사의 안정성비율 추이는 다음과 같습니다.
| [최근 3년간 당사 안정성비율 추이] |
| (단위 : 백만원,%, 회) |
| 과목 | KB증권 단기차입금 유입에 따른 시나리오 | 2018년 | 2017년 | 2016년 | |
|---|---|---|---|---|---|
| 5회차 전환사채 상환청구 시 | 5회차 전환사채 미상환 시 | ||||
| 부채비율 | 153.62% | 196.12% | 111.44% | 108.31% | 133.40% |
| 차입금 총계 | 12,328 | 15,219 | 7,823 | 9,392 | 9,527 |
| - 단기차입금 | 9,870 | 9,870 | 870 | 920 | 420 |
| - 유동성장기차입금 | 1.606 | 1.606 | 1.606 | 1,087 | 1,077 |
| - 장기차입금 | 852 | 852 | 852 | 898 | 1,556 |
| - 사채 | - | - | - | 4,012 | 5,141 |
| - 유동성 사채 | - | 4,495 | 4,495 | 2,474 | 1,332 |
| 차입금의존도 | 45.96% | 48.59% | 35.05% | 36.47% | 41.48% |
주) 부채비율 = 부채총계 / 자본총계
주2) 차입금의존도 = 부채총계 / 자산총계
주3) KB증권 단기차입금 유입에 따른 시나리오는 2018년말 재무제표에 단기차입에 따른 자금을 단순 계산한 시나리오로, 실제 자금유입일 기준으로 계산할 시 다를 수 있습니다.
당사의 부채 중 가장 큰 비중을 차지하고 있는 차입금은 2018년 기준 78.2억원으로 유동성 차입금은 69.7억원, 장기차입금은 8.5억원으로 구성되어 있습니다. 총 차입금의존도는 35.05%입니다. 당사의 장.단기 차입금 내역은 금융기관으로부터 일반 운전자금대출, 중소기업 시설자금 및 기자재 리스로 이루어져 있으며, 중소기업은행으로부터의 단기 및 장기차입금은 공장에 대한 담보 및 지급보증의 조건이 있어 만기연장이 가능할 것으로 판단되고 있습니다. 증권신고서 제출일 기준 당사의 차입금 현황 및 상환계획은 다음과 같습니다.
| [당사 차입금 내역 및 상환계획] | |
| (증권신고서 제출일 기준) | (단위 : 백만원,%) |
| 구분 | 대출종별 | 약정일 | 만기일 | 이자율(%) | 금액 | 상환일정 | 비고 | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 19년 | 20년 | 21년 | 22년 | ||||||||
| 단기 차입금 |
중소기업은행 | 운전자금 | 12.12.29 | 19.12.20 | 4.277 | 420 | 420 | - | - | - | 지급보증(357백만원) |
| 운전자금 | 17.10.18 | 19.10.18 | 5.977 | 450 | 450 | - | - | - | |||
| 장기 차입금 |
중소기업은행 | 중소기업시설자금 | 15.06.26 | 20.06.26 | 4.245 | 1,775 | 1,476 | 299 | - | - | 공장(약13.2억원) 지급보증(약15억원) |
| 운전자금 | 19.01.02 | 21.01.02 | 6.407 | 500 | 208 | 292 | - | - | 2019년신규차입 | ||
| IBK캐피탈 | 기자재 리스 | 18.11.20 | 22.11.30 | 4.6 | 682 | 129 | 136 | 142 | 275 | ||
| 합계 | 3,827 | 2,683 | 727 | 142 | 275 | ||||||
또한 증권신고서 제출일 기준 당사는 차입금 외에 제5회차 사모 전환사채 46.5억이 있습니다. 기발행되었던 제3회차 전환사채 및 제 4회차 전환사채는 모두 전환되었으며, 제5회차 사모 전환사채는 2019년 02월 약 3.5억원의 전환청구로 인해 현재 잔존하는 미상환사채는 46.5억원입니다. 제5회차 전환사채의 조기상환청구권(Put Option)은 발행일로부터 2년 경과한 날인 2019년 12월 26일부터 가능하나, 기한의이익 상실 조항의 효력이 발생할 경우 즉시 상환에 대한 가능성이 있습니다. 이에 따라 당사는 KB증권으로부터 단기자금을 차입하여 연구개발비용 사용 및 동 전환사채의 기한의이익상실 가능성에 대비할 계획입니다.
| [당사 주식관련사채 발행 현황] |
| (단위 : 백만원, 주) |
|
구분 |
발행일 |
만기일 |
권면 |
이자율 (표면이자율/ 만기이자율) |
조기상환 |
전환청구 |
전환조건 |
미상환사채 |
사채권자 | ||
|---|---|---|---|---|---|---|---|---|---|---|---|
|
전환비율 |
전환 |
권면총액 |
전환가능 |
||||||||
|
제5회 사모 |
17.12.26 |
20.12.26 |
5,000 |
0.0%/4.0% | 19.12.26 ~ 20.09.26 |
18.12.26 ~ 20.11.26 |
100 |
9,994 | 4,650 | 465,279 | 코리아에셋클래식메자닌전문투자형 사모투자신탁제2호 코리아에셋클래식멀티스트래티지 전문투자형사모투자신탁제1호 |
주1) 전환사채권면총액 50억원중 3.5억원(35,021주/주당 9,994원)의 전환청구로 인해 2019년 3월 25일 주식으로 전환되어 상장되었습니다.
| [ 단기자금대출의 주요 금융조건 ] |
| 구분 | 내용 |
|---|---|
| 대주 | 케이비증권 |
| 대출금액 | 금 구십억원(\ 9,000,000,000) |
| 차입일 | 증권신고서 제출일(2019년 04월 02일)로부터 5영업일 이내 |
| 만기 | 차입일로부터 6개월 |
| 대출금리 | 고정 (연) 5.90% |
| 자금사용 목적 | 5회차 전환사채의 상환 청구대비 및 연구개발비용 |
| 의무상환 | 유상증자 대금납입 후 3영업일 이내 조기상환 |
금번 주주배정후실권주 일반공모 증자가 성공적으로 이루어질 경우 당사의 안정성 지표들은 개선 될 것으로 기대되고 있으나, 2018년말 기준 동종업계 대비 상대적으로 안정성 지표들이 열위한 수준에 있는 점, 주가하락에 따른 공모금액의 축소가능성 및 향후 지속적인 손실로 자본이 감소할경우 다시 채무가 증가할 가능성이 있습니다. 투자자 여러분께서는 추가적인 차입금 발생 여부 및 전환사채의 조기상환청구 가능성에 대하여 유의하여 투자를 고려해 주시기 바랍니다.
| 바. 음(-)의 영업현금흐름 및 유동성 관련 위험 당사는 최근 3사업연도 중 2016년과 2018년에 음(-)의 "영업활동현금흐름"을 보이고 있으며, 최근 3사업연도동안 지속적으로 음(-)의 "투자활동현금흐름"을 보이고 있습니다. 당사는 이에 대한 현금유출을 충당하기 위하여 재무활동현금흐름을 통하여 조달하고 있으며, 2018년말 보유 현금은 8.6억원입니다. 한편, 2017년말 당사의 유동비율은 175.6%으로 동종업계 2017년 평균 유동비율인 175.6%(한국은행 기업경영분석, C27. 의료, 정밀, 광학기기 및 시계 제조업)와 같았으나, 2018년말 당사의 유동비율은 68.3%로 동종업계평균보다 현저히 낮아진 상황입니다. 이는 2018년중 음(-)의 영업활동현금흐름과 투자활동현금흐름이 크게 발생하였음에도, 외부 추가적인 자금조달이 거의 없었기 때문에 당사의 유동성 비율이 전년대비 크게 감소한 것으로 판단됩니다. 이자보상배율도 지속적이 영업손실이 발생하면서 음(-)의 배수를 기록하고 있습니다. 당사는 현금흐름 및 유동성에 대하여 지속적으로 모니터링하면서 유동성 이슈가 발생하지 않도록 대응하고 있으며, 금번 주주배정후실권주일반공모를 통하여 자금이 유입될 시 재무유동성이 개선될 것으로 기대되고 있습니다. 그러나 당사의 예상과는 달리 향후 영업 개선을 통한 영업활동현금흐름이 개선되지 않을 시 장기적으로 회사의 현금흐름에 문제가 발생할 소지가 있습니다. 투자자들께서는 상기의 위험요인을 면밀히 검토하시고 투자에 임해주시기 바랍니다. |
당사는 최근 3사업연도 중 2016년과 2018년에 음(-)의 "영업활동현금흐름"을 보이고 있으며, 최근 3사업연도동안 지속적으로 음(-)의 "투자활동현금흐름"을 보이고 있습니다. 당사는 이에 대한 현금유출을 충당하기 위하여 재무활동현금흐름을 통하여 조달하고 있으며, 2018년말 보유 현금은 8.6억원입니다. 최근 3년간 당사의 요약현금흐름표는 다음과 같습니다.
[요약현금흐름표]
| (단위: 백만원) |
| 구 분 | 2018년 |
2017년 |
2016년 |
|---|---|---|---|
|
영업활동현금흐름 |
(2,307) | 563 | (372) |
|
투자활동현금흐름 |
(2,351) | (4,093) | (2,779) |
|
재무활동현금흐름 |
240 | 4,240 | 5,418 |
|
기초현금및현금성자산 |
5,277 | 4,613 | 2,318 |
|
기말현금및현금성자산 |
859 | 5,277 | 4,613 |
*K-IFRS 연결재무제표 기준
당사는 2016년 30.3억원의 당기순손실이 발생하였으며, 유ㆍ무형 감가상각비 13.2억원, 재고자산평가손실 1.7억원, 재고자산의 증가 6.6억원 등 직접적인 현금의 유출이 없는 비용에 대한 조정과 영업활동으로 인한 자산ㆍ부채의 변동조정에 의하여 실제 영업활동현금은 -3.7억원이 발생하였습니다. 또한 펩타이드 함유 치과용 골이식재인 OssGen-15가 개발이 완료되면서 당사의 충북 진천공장에 펩타이드 구역 시설을 확장하기 시작하였으며, 연구개발의 상용화에따른 무형자산 증가 등으로 -27.8억원의 투자활동현금흐름이 발생하였습니다. 2016년 02월 현대청년펀드 1호 외 4인을 대상으로 4회차 전환사채 60억원을 발행하였으며, 이를 포함하여 54.2억원의 재무활동현금이 유입되어 2016년말 현금및현금성자산이 46.1억원을 보유하게 되었습니다.
2017년 또한 25.7억원의 당기순손실이 발생하였으나, 유ㆍ무형 감가상각비 및 손상차손 21.4억원, 영업활동으로 인한 자산ㆍ부채의 변동조정 등에 의하여 영업활동현금흐름이 5.6억원이 발생할 수 있었습니다. 반면에, 충북 진천공장의 펩타이드 구역 시설투자의 완료 및 연구개발의 상용화에 따른 무형자산 증가 등에 의하여 40.9억원의 음(-)의 투자활동현금흐름이 발생하였습니다. 2017년 12월에는 코리아에셋투자증권(주)를 대상으로 50억원의 5회차 전환사채를 발행하였으며, 이를 포함하여 42.4억원의 재무활동현금흐름이 유입되어 2017년말 현금및현금성자산은 52.8억원 보유하게 되었습니다.
2018년에는 41.5억원의 당기순손실이 발생하였으며, 유ㆍ무형 감가상각비 15.9억원, 영업활동으로 인한 자산ㆍ부채의 변동조정 등에 의하여 23.1억의 음(-)의 영업활동현금흐름이 발생하였습니다. 또한 2017년 대규모 공급계약 성사에 따른 제조공정 개선을 위한 기계장치 도입 7.1억원 및 무형자산의 취득 16.1억원 등에 의하여 -28.6억원의 투자활동현금 유출이 있었으며, 재무활동현금은 2.4억원으로 거의 변동사항이 없었습니다. 이에 따라 2018년 중 현금이 총 44.2억원 감소함에 따라 2018년말 기준 당사가 보유하고 있는 현금및현금성자산은 8.6억원입니다.
2017년말 당사의 유동비율은 175.6%으로 동종업계 2017년 평균 유동비율인 175.6%(한국은행 기업경영분석, C27. 의료, 정밀, 광학기기 및 시계 제조업)와 같았으나, 2018년말 당사의 유동비율은 68.3%로 동종업계평균보다 현저히 낮아진 상황입니다. 당사의 당좌비율 또한 2017년말에는 133.3%로, 동종업계 134.1%와 비슷한 수준이었으나, 2018년말 당좌비율이 35.2%로 전년대비 현저하게 낮아졌습니다. 2018년중 음(-)의 영업활동현금흐름과 투자활동현금흐름이 크게 발생하였음에도, 외부 추가적인 자금조달이 거의 없었기 때문에 당사의 유동성 비율이 전년대비 크게 감소한 것으로 판단됩니다. 이자보상배율도 지속적이 영업손실이 발생하면서 음(-)의 배수를 기록하고 있습니다.
| [최근 3년 당사 및 동종업계 평균 유동성 비율] | |
| (2018년 12월 31일 기준) | |
| 구 분 | 2018년 | 2017년 | 2016년 | 비 고 |
|---|---|---|---|---|
| 유동비율(%) | 68.3% | 175.6% | 187.8% | 유동자산 / 유동부채 |
| 당좌비율(%) | 35.2% | 133.3% | 151.1% | 당좌자산 / 유동부채 |
| 이자보상배율(배) | -4.64 | -1.81 | -3.1 | 영업이익 / 이자비용 |
| 업종평균 유동비율(%) | - | 175.6% | 170.6% | - |
| 업종평균 당좌비율(%) | - | 134.1% | 132.1% | - |
(자료 : 당사 각 사업연도 감사보고서 및 기업경영분석(한국은행, 2018.10)
주) 업종 분류 : C27. 의료, 정밀, 광학기기 및 시계 제조업
상기 기재된 바와 같이 당사는 과거 3년동안 당사는 재무활동현금을 통해 음(-)의 영업활동현금과 투자활동현금을 충당하였으며, 2018년말 기준 동종업계 대비 유동비율과 당좌비율이 열위에 있는 점과 지속적으로 음(-)의 이자보상배율이 기록되고 있는 점을 미루어 보았을 때, 당사의 재무유동성이 유의적 관점에서 안전한 상태에 있다고 할 수는 없습니다. 그러나 당사는 현금흐름 및 유동성에 대하여 지속적으로 모니터링하면서 유동성 이슈가 발생하지 않도록 대응하고 있으며, 금번 주주배정후실권주일반공모를 통하여 자금이 유입될 시 재무유동성이 개선될 것으로 기대되고 있습니다. 그러나 당사의 예상과는 달리 향후 영업 개선을 통한 영업활동현금흐름이 개선되지 않을 시 장기적으로 회사의 현금흐름에 문제가 발생할 소지가 있습니다. 투자자들께서는 상기의 위험요인을 면밀히 검토하시고 투자에 임해주시기 바랍니다.
| 사. 최대주주 등의 지분율 감소로 인한 위험 당사의 최대주주는 정종평 대표이사로 1,133,690주(17.71%)의 지분을 보유하고 있으며, 특수관계인을 포함 시 1,406,694주(21.97%)를 보유하고 있습니다. 금번 당사의 주주배정 후 실권주 일반공모 유상증자로 인한 주당 배정비율은 51.928953%로 1주당 0.51928953주의 배정주식(신주인수권증서)를 교부받게 됩니다. 이에 따라 최대주주인 정종평 대표이사는 588,713주, 특수관계인 박윤정은 118,398주를 배정받게 됩니다, 금번 주주배정 청약시 배정받을 주식수내에서 최대주주 및 특수관계인 박윤정은 청약에 100% 참여하여 현재와 같은 경영권 유지 및 일관된 사업진행을 위해 노력할 예정입니다. 당사의 기타 지분은 다수의 소액주주에 분산되어 있어 경영권 유지에는 큰 문제가 없을 것으로 보입니다. 그러나 향후 주식담보 대출후 주가 하락에 의한 담보권 실현 등으로 최대주주 및 특수관계인 지분율이 취약해질 경우, 향후 경영권의 행사가 취약해 질 수 있습니다. 향후 경영권이 취약해질 경우 적대적 M&A 및 외부의 경영권 취득 시도 등의 위험에 노출될 수 있습니다. 이는 최대주주 변경가능성 등에 의한 경영권의 안정성 저하 및 당사의 신뢰도 하락을 유발할 수 있는 등 당사의 장기적인 발전을 저해하는 요소로 작용할 수 있으니 투자자분들께서는 투자시 이러한 점을 깊게 유의하시기 바랍니다. |
당사의 최대주주는 정종평 대표이사로 1,133,690주(17.71%)의 지분을 보유하고 있으며, 특수관계인을 포함 시 1,406,694주(21.97%)를 보유하고 있습니다. 당사는 증권신고서 제출일 기준 나머지 78.03%의 지분이 소액주주들에게 분산되어 있으며, 회사 설립 이래 최대주주가 변동된 사항이 없습니다. 증권신고서 제출일 현재 최대주주 등의 지분현황은 아래와 같습니다.
| [주주 현황] | |
| (기준일 : 증권신고서 제출일 현재) | (단위 : 주) |
| 구분 | 성 명 | 관 계 | 주식의 종류 |
소유주식수 및 지분율 | |
|---|---|---|---|---|---|
| 주식수 | 지분율 | ||||
| 최대주주 및 특수관계인 |
정종평 | 최대주주 | 보통주 | 1,133,690 | 17.71% |
| 박윤정 | 임원 | 보통주 | 228,000 | 3.56% | |
| 이주연 | 임원 | 보통주 | 18,956 | 0.30% | |
| 김사성 | 사외이사 | 보통주 | 11,048 | 0.17% | |
| 설양조 | 감사 | 보통주 | 2,000 | 0.03% | |
| 장계순 | 처 | 보통주 | 1,000 | 0.02% | |
| 김정빈 | 조카 | 보통주 | 12,000 | 0.19% | |
| 최대주주 등 소계 | - | - | 1,406,694 | 21.97% | |
| 기타 소액주주 | - | 보통주 | 4,996,285 | 78.03% | |
| 합계 | 보통주 | 6,402,979 | 100.00% | ||
금번 당사의 주주배정 후 실권주 일반공모 유상증자로 인한 주당 배정비율은 51.928953%로 1주당 0.51928953주의 배정주식(신주인수권증서)를 교부받게 됩니다. 이에 따라 최대주주인 정종평 대표이사는 588,713주, 특수관계인 박윤정은 118,398주를 배정받게 됩니다, 금번 주주배정 청약시 배정받을 주식수내에서 최대주주 및 특수관계인 박윤정은 청약에 100% 참여하여 현재와 같은 경영권 유지 및 일관된 사업진행을 위해 노력할 예정입니다.
한편, 신고서 제출일 현재 아직 상환이 완료되거나 전환권이 행사되지 않은 제5회 사모 전환사채 46.5억원이 존재하며 전환가능 주식수는 총 465,279주 입니다. 당사의 5회차 전환사채의 전환가액 조정 한도가 최초 발행가액(10,566원)의 70% 수준임과 현재 주가를 고려했을 때, 전환권이 행사 될 가능성은 크지 않을 것으로 예상되나 예상치 못한 주가 변동으로 인해 전환권이 행사 될 경우 최대주주 및 특수관계자 박윤정의 지분율은 19.82%(현재 지분율 : 21.27%)까지 추가 하락할 가능성이 존재합니다.
| [미상환 전환사채 발행현황] |
| (기준일 : | 증권신고서 제출일 현재 | ) | (단위 : 백만원, 주) |
| 종류/구분 | 발행일 | 만기일 | 권면총액 | 전환대상 주식의 종류 |
전환청구 가능기간 |
전환조건 | 미상환사채 | ||
|---|---|---|---|---|---|---|---|---|---|
| 전환비율 | 전환가액 | 권면총액 | 전환가능주식수 | ||||||
| 제5회 무기명식 이권부 무보증 사모 전환사채 |
2017.12.26 |
2020.12.26 |
5,000 |
기명식 보통주 |
18.12.26~ |
100% | 9,994 | 4,650 | 465,279 |
| 합 계 | - | - | 5,000 | - | - | - | - | 4,650 | 465,279 |
한편, 당사 최대주주인 정종평 대표이사는 증권신고서 제출일 현재 보유주식에 대한 주식담보대출 내역이 존재하지 않습니다. 다만 본 유상증자에 참여하기 위해 주식담보대출을 실행한다면 향후 주가 하락 시, 담보권자는 추가 담보를 요구할 가능성이 있으며, 추가 담보 제공이 어려울 경우, 반대 매매를 통한 담보권자의 담보권이 실현될 수 있으며, 이 경우 최대주주의 지분율은 하락할 가능성이 있습니다.
당사의 최대주주인 정종평 대표이사 및 특수관계인들은 현재 21.97%의 지분율을 확보하고 있으며, 기타 지분은 다수의 소액주주에 분산되어 있는 점을 고려해 보았을 때 경영권 유지에는 큰 문제가 없을 것으로 보입니다.그러나 향후 주식담보 대출후 주가 하락에 의한 담보권 실현 등으로 최대주주 및 특수관계인 지분율이 취약해질 경우, 향후 경영권의 행사가 취약해 질 수 있습니다.
또한 당사의 정관에 '적대적 인수합병으로 이사가 비자발적 사임 또는 해임되는 경우 제2항에 의한 퇴직금이외에 퇴직보상금으로 대표이사에게 40억원, 그밖의 이사에게는 20억원을 지급한다.'라는 조항으로 적대적M&A에 대한 방어수단이 있으나, 향후 경영권이 취약해질 경우 적대적 M&A 및 외부의 경영권 취득 시도 등의 위험에 노출될 수 있습니다. 이는 최대주주 변경가능성 등에 의한 경영권의 안정성 저하 및 당사의 신뢰도 하락을 유발할 수 있는 등 당사의 장기적인 발전을 저해하는 요소로 작용할 수 있으니 투자자분들께서는 투자시 이러한 점을 깊게 유의하시기 바랍니다.
| 아. 환율 변동에 따른 위험 당사 2018년 기준 총 매출액 대비 약 78%인 40.9억원이 해외 수출을 통해 발생되고 있습니다. 당사 제품에 필요한 원,부자재의 수입은 2018년기준 43백만원으로 경미한 수준이나, 수출의존도가 높아 이로 인한 환율 변동에 따른 위험에 노출되어 있습니다. 또한 2018년기준 당사의 외화예금 및 외상매출금은 한화기준 9.3억원으로 자산총계 대비 4.17%이며 해외 매출의 경우 대금지급이 주로 USD 및 EUR로 이루어 지고 있기 때문에 환율 변동에 따른 수익성에 영향이 있을수 있습니다. 경영진은 내부적으로 환율 변동에 대한 환위험을 수시로 측정하고 관리하여 환율변동에 따른 환전일을 조정함으로써 환율변동에 따른 위험을 축소하고 있습니다. 그러나 당사에서는 향후 신성장동력으로 기존 제품외에 새로 개발하는 신약에 대해 해외매출을 적극적으로 추진하고 있으며 이로인해 기능통화 이외의 거래가 증가할것으로 예상하고 있는 상황입니다. 예측할수 없는 환율의 급변동 상황 또는 기존 매출처의 경영(제품지급 결제구조) 및 영업악화등의 경우가 발생될 경우 당사의 생산 및 매출에 부정적인 영향을 미칠수 있으니 투자자분들께서는 주의하시기 바랍니다. |
당사 2018년 기준 총 매출액 대비 약 78%인 40.9억원이 해외 수출을 통해 발생되고 있습니다. 당사 제품에 필요한 원,부자재의 수입은 2018년기준 43백만원으로 경미한 수준이나, 수출의존도가 높아 이로 인한 환율 변동에 따른 위험에 노출되어 있습니다.
| [당사 국내외 매출현황] |
| (단위 : 백만원) |
| 구 분 | 구 분 | 2018년 | 2017년 | 2016년 | |||
|---|---|---|---|---|---|---|---|
| 금액 | 비중 | 금액 | 비중 | 금액 | 비중 | ||
| 제품 매출 |
수출 | 4,086 | 78.46% | 5,260 | 83.45% | 3,643 | 75.83% |
| 내수 | 1,122 | 21.54% | 1,042 | 16.53% | 1,162 | 24.19% | |
| 합계 | 5,208 | 100.00% | 6,303 | 100.00% | 4,804 | 100.00% | |
| 원부자재수입 | 국내 | 701 | 94.22% | 1,267 | 99.32% | 682 | 94.69% |
| 수입 | 43 | 5.78% | 9 | 0.68% | 38 | 5.31% | |
| 합계 | 744 | 100.00% | 1,276 | 100.00% | 720 | 100.00% | |
또한 2018년기준 당사의 외화예금 및 외상매출금은 한화기준 9.3억원으로 자산총계 대비 4.17%이며 해외 매출의 경우 대금지급이 주로 USD 및 EUR로 이루어 지고 있기 때문에 환율 변동에 따른 수익성에 영향이 있을수 있습니다. 다만 현재 당사는 외화부채는 없는 상황으로 원부자재등의 수입비중은 2018넌 약 6%정도로 대부분의 제품을 국내에서 조달하여 사용하기 때문에 제품원료에 대한 수입의존도는 매우 낮습니다.
1) 2018년 외화자산 현황
| (단위 : USD, EUR, 천원) |
| 구 분 | 화폐 | 외화금액 | 원화금액 |
|---|---|---|---|
| 외화예금 | USD | 4,259.89 | 4,763 |
| EUR | 63.89 | 82 | |
| 외상매출금 | USD | 830,109.34 | 928,145 |
| 합 계 | - | 932,990 | |
2) 환율 10% 변동 시 세전순손익에 미치는 영향
| (단위 : 천원) |
| 구분 | 2018년 | |
| 10%상승 | 10%하락 | |
| 외환환산손익 | 93,299 | -93,299 |
3) 당사 외환손익 현황
| (단위 : 천원) |
| 구분 | 2018년 | 2017년 | 2016년 |
|---|---|---|---|
| 외환차익 | 48,936 | 21,527 | 44,602 |
| 외화환산이익 | 274 | - | 63,867 |
| 소계 | 49,210 | 21,527 | 108,469 |
| 외환차손 | 12,902 | 86,166 | 48,547 |
| 외화환산손실 | 4,842 | 82,678 | 158 |
| 소계 | 17,744 | 168,844 | 48,705 |
당사가 보유한 외화자산, 매출채권 등의 규모나 외화의 유출입 흐름 등을 감안할 때, 환율 변동에 따른 위험이 있습니다. 다만 당사에서는 주력 상품인 골이식재를 제조하는데 있어 원부자재의 조달을 국내에서 진행하고 있기 때문에 환율 변동에 따른 리스크가 전체 경영에 미치는 영향이 다소 크지 않으며 거래처로부터 매출에 대한 외화가 입금이 되면 경영진은 내부적으로 환율 변동에 대한 환위험을 수시로 측정하고 관리하여 환율변동에 따른 환전일을 조정함으로써 환율변동에 따른 위험을 축소하고 있습니다.
그러나 당사에서는 향후 신성장동력으로 기존 제품외에 새로 개발하는 신약에 대해 해외매출을 적극적으로 추진하고 있으며 이로인해 기능통화 이외의 거래가 증가할것으로 예상하고 있는 상황입니다. 예측할수 없는 환율의 급변동 상황 또는 기존 매출처의 경영(제품지급 결제구조) 및 영업악화등의 경우가 발생될 경우 당사의 생산 및 매출에 부정적인 영향을 미칠수 있으니 투자자분들께서는 주의하시기 바랍니다.
| 자. 관리종목 편입 가능성에 따른 위험 당사는 2011년 7월 펩타이드 기술성 평가를 거쳐 코스닥시장 상장규정 제7조 2항의 기술성장기업의 상장특례를 적용받아 코스닥시장에 상장하였습니다. 기술성장기업으로 상장 시, 재무성과와 관련된 관리종목지정 요건에 대해 기술성장기업에 대한 특례를 받게 됩니다. 특례조항으로는 매출액 30억원 미만시 관리종목으로 지정되는 조건을 상장후 5년간 미적용, 자기자본50%이상(&10억원이상)의 법인세비용차감전 계속사업손실이 최근 3년간 2회이상일시 관리종목지정이 되는 요건을 상장후 3년간 미적용, 최근4사업연도 영업손실일시 관리종목지정이 되는 요건에 대한 미적용을 받고있습니다. 이에 따라, 당사는 상장 이후 지속적으로 영업손실이 발생하고 있음에도 불구하고, 상기와 같은 기술성장기업 특례요건에 의하여 관리종목으로 지정이 안되고 있습니다. 매출액 미달 요건및 법인세비용차감전계속사업손실 요건은 현재 기술성장기업의 특례조건 기간이 만료되어 적용받고 있으나, 최근 3년동안 지속적으로 해당 요건에 대하여 충족하고 있습니다. 당사의 경우 신고서 제출일 현재까지 상기 기준에 해당되는 사항은 없습니다. 그러나 시장 상황이 악화되거나 매출이 현저히 감소할 경우 또는 향후 지속적인 당기순손실에 의하여 자기자본이 감소할 경우 법인세차감전계속사업손실의 요건을 충족하지 못할 위험이 있습니다. 또한, 최근 상장 기업에 대한 금융감독기관 등의 관리감독기준이 엄격해지고 있는 상황으로 관련 규정을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다. 특히, "코스닥시장 상장규정 제28조(관리종목), 코스닥시장 상장규정 제38조(상장의 폐지) 및 코스닥시장 상장규정 제38조의2(실질심사위원회의 심사 등)"에 유의하시기 바랍니다. |
당사는 2011년 7월 펩타이드 기술성 평가를 거쳐 코스닥시장 상장규정 제7조 2항의 기술성장기업의 상장특례를 적용받아 코스닥시장에 상장하였습니다. 기술성장기업으로 상장신청하는 경우 상장심사에 대한 주요 외형요건의 완화 외에 상장후 코스닥시장상장규정에 의거하여 재무성과와 관련된 관리종목지정 요건에 대해 기술성장기업에 대한 특례를 받게 됩니다.
특히, 당사는 상장 이후 지속적으로 영업손실이 발생하고 있음에도 불구하고, 기술성장기업 특례요건에 의하여 관리종목으로 지정이 안되고 있습니다. 매출액 미달 요건및 법인세비용차감전계속사업손실 요건은 현재 기술성장기업의 특례조건 기간이 만료되어 적용받고 있으나, 최근 3년동안 지속적으로 해당 요건에 대하여 충족하고 있습니다. 코스닥시장 관리종목 지정 및 사장폐지 요건에 대한 검토 결과는 다음과 같습니다.
| 【코스닥시장 관리종목 지정 및 상장폐지 요건 검토】 |
|
구분 |
분류 |
요건 |
|---|---|---|
|
매출액 미달 |
관리종목 |
최근년 30억원 미만 (지주회사는 연결기준) * 기술성장기업, 이익미실현기업은 각각 상장후 5년간 미적용 |
|
상장폐지 |
2년 연속 [실질심사] 이익미실현기업 관련, 관리종목지정 유예기간 중 최근 3사업연도 연속으로 매출액이 5억원 미만이면서 전년 대비 100분의 50 이상의 매출액 감소가 공시 등을 통해 확인되는 경우 |
|
|
검토결과 |
2018년 매출액 : 52억, 2017년 매출액 : 63억, 2016년 매출액 : 48억 |
|
|
법인세비용차감전계속사업손실 |
관리종목 |
자기자본50%이상 (&10억원이상)의 법인세비용차감전계속사업손실이 최근3년간 2회 이상 (&최근연도계속사업손실) * 기술성장기업 상장후 3년간 미적용, 이익미실현 기업 상장후 5년 미적용 |
|
상장폐지 |
관리종목 지정후 자기자본50%이상(&10억원이상)의 법인세비용차감전계속사업손실 발생 [실질심사] 이익미실현기업 관련, 관리종목지정 유예기간 중 최근 3사업연도 연속으로 매출액이 5억원 미만이면서 전년 대비 100분의 50 이상의 매출액 감소가 공시 등을 통해 확인되는 경우 |
|
|
검토결과 |
- 2018년 법인세비용차감전손실률 : 37.23%, 2017년 법인세비용차감전손익률 : 21.00%, 2016년 법인세비용차감전손익 률 : 31.70% |
|
|
장기영업손실 |
관리종목 |
최근 4사업연도 영업손실(지주회사는 연결기준) 기술성장기업(기술성장기업부)은 미적용 |
|
상장폐지 |
[실질심사] 관리종목 지정 후 최근 사업연도 영업손실 |
|
|
검토결과 |
기술성장기업에 의한 상장 | |
|
자본잠식/자기자본 |
관리종목 |
(A)사업연도(반기)말 자본잠식률 50%이상 (B)사업연도(반기)말 자기자본 10억원미만 (C)반기보고서 제출기한 경과후 10일내 반기검토(감사)보고서 미제출 or 검토(감사)의견 부적정·의견거절·범위제한한정 |
|
상장폐지 |
최근년말 완전자본잠식 A or C 후 사업연도(반기)말 자본잠식률 50%이상 B or C 후 사업연도(반기)말 자기자본 10억원미만 A or B or C 후 반기말 반기보고서 기한 경과후 10일내 미제출 or 감사의견 부적정·의견거절·범위제한한정 [실질심사] 사업보고서 또는 반기보고서의 법정제출 기한까지 당해 상장폐지 기준 해당사실을 해소하였음을 입증하는 재무제표 및 이에 대한 감사인(정기재무제표에 대한 감사인과 동일한 감사인에 한함)의 감사보고서를 제출하는 경우 |
|
|
검토결과 |
자본잠식 없음. | |
|
감사의견 |
관리종목 |
- |
|
상장폐지 |
감사보고서 부적정·의견거절·범위제한한정 |
|
|
검토결과 |
2018년 감사보고서 적정의견 | |
|
시가총액 |
관리종목 |
보통주시가총액 40억원미만 30일간 지속 |
|
상장폐지 |
관리종목 지정후 90일간 "연속10일 & 누적30일간 40억원이상"의 조건을 미충족 |
|
|
검토결과 |
2019년 04월 01일 시가총액 743억 |
|
|
거래량 |
관리종목 |
분기 월평균거래량이 유동주식수의 1%에 미달 * 월간거래량 1만주, 소액주주 300인이상이 20%이상 지분 보유 등은 적용배제 |
|
상장폐지 |
2분기 연속 |
|
|
검토결과 |
분기 월평균거래량이 유동주식수의 1% 이상 | |
|
지분분산 |
관리종목 |
소액주주200인미만or소액주주지분20%미만 * 300인이상의 소액주주가 유동주식수의 10%이상으로서 100만주이상을 소유하는 경우는 적용배제 |
|
상장폐지 |
2년 연속 |
|
|
검토결과 |
요건 충족 | |
|
불성실공시 |
관리종목 |
- |
|
상장폐지 |
[실질심사] 1년간 불성실공시 벌점 15점 이상 |
|
|
검토결과 |
벌점 없음 | |
|
공시서류 |
관리종목 |
(A)분기,반기, 사업보고서 미제출 (B)정기주총에서 재무제표 미승인 or 정기주총 미개최 |
|
상장폐지 |
2년간 3회 분기,반기,사업보고서 미제출 사업보고서 제출기한후 10일내 미제출 A(미제출상태유지) or B 후 다음회차에 A or B |
|
|
검토결과 |
분기,반기, 사업보고서 제출기한까지 제출 완료 | |
|
사외이사 등 |
관리종목 |
사외이사/감사위원회 요건 미충족 |
|
상장폐지 |
2년 연속 |
|
|
검토결과 |
사외이사/감사위원회 요건 충족 | |
|
회생절차/파산신청 |
관리종목 |
회생절차 개시 신청 또는 파산신청 |
|
상장폐지 |
[실질심사] 개시신청기각,결정취소,회생계획 불인가등 |
|
|
검토결과 |
- | |
|
기타 |
상장폐지 |
최종부도 또는 은행거래정지 해산사유(피흡수합병, 파산선고) 정관 등에 주식양도제한 두는 경우 유가증권시장 상장의 경우 우회상장시 우회상장관련 규정 위반시 (심사종료전 기업결합완료 및 보호예수 위반 등) |
| (자료: 코스닥시장 상장규정) |
당사의 경우 신고서 제출일 현재까지 상기 기준에 해당되는 사항은 없습니다. 그러나 시장 상황이 악화되거나 매출이 현저히 감소할 경우 또는 향후 지속적인 당기순손실에 의하여 자기자본이 감소할 경우 법인세차감전계속사업손실의 요건을 충족하지 못할 위험이 있습니다. 또한, 최근 상장 기업에 대한 금융감독기관 등의 관리감독기준이 엄격해지고 있는 상황으로 관련 규정을 위반할 경우 주권매매정지, 관리종목지정, 상장폐지실질심사, 상장폐지 등의 조치가 취해질 수 있습니다. 특히, "코스닥시장 상장규정 제28조(관리종목), 코스닥시장 상장규정 제38조(상장의 폐지) 및 코스닥시장 상장규정 제38조의2(실질심사위원회의 심사 등)"에 유의하시기 바랍니다.
자세한 금융관련 법규는 "국가법령정보센터(http://law.go.kr)", "금융감독원 금융감독법규정보시스템(http://law.fss.or.kr)", "KRX법규서비스(http://law.krx.co.kr)" 등을 참고하시기 바랍니다.
3. 기타위험
| 가. 환금 제한 및 원금손실 가능성 금번 유상증자 청약에 참여하여 신주를 배정받을 경우 신주의 추가상장일까지 환금성에 제약이 있으며, 청약 후 추가상장일 사이에 주가가 하락할 경우 원금에 대한 손해가 발생할 가능성이 있습니다. 투자자분들은 투자시 이점 유의하시기 바랍니다. |
당사는 코스닥시장 상장법인으로서 이번 유상증자로 발행되는 신주는 코스닥시장에 상장되어 거래될 예정이므로 유동성과 관계된 심각한 환금성 위험은 존재하지 않습니다. 그러나 유상증자 청약에 참여하여 신주를 배정받을 경우, 신주가 상장되어 매매가 가능할 때까지 납입주금에 대한 유동성의 제약이 있습니다.
본 유상증자의 자세한 일정은 본 신고서의 '제1부 모집 또는 매출에 관한 사항 - I. 모집 또는 매출에 관한 일반사항' 중 '1. 공모의 개요'를 참고하시기 바랍니다.
또한 신주가 코스닥시장에 추가 상장될 때까지 당사의 주가가 유상증자로 발행되는 신주의 발행가액 수준으로 유지되지 않을 수 있으며, 당사의 내적인 요인 또는 시장전체의 환경 변화 등에 의해 주가가 급락할 경우, 투자원금에 대한 손실이 발생할 수 있습니다.
당사의 금번 발행되는 주식에 대해서는 전량 보호예수되지 않으므로 상장 후 즉시 물량 출회가 가능하여 주가 하락에 따른 환금성 위험 및 원금손실 위험에 노출될 수 있으니, 이점 투자에 유의하시기 바랍니다.
| 나. 주가 희석화 위험 당사의 증권신고서 제출일 현재 발행주식총수는 6,402,979주입니다. 금번 주주배정 후 실권주 일반공모 유상증자를 통해 발행예정인 주식수는 3,500,000주이며, 이는 당사 발행주식총수의 약 54.66%에 해당합니다. 금번 유상증자로 인하여 추가 발행 및 상장되는 주식으로 인하여 주가 희석화 및 물량출회에 따른 주가하락 위험이 존재합니다. 신주인수권증서를 매수하는 투자자는 할인율에 의해 발생하는 차익을 단기적으로 실현하기 위해 신주의 매매가 가능한 시점에 즉시 장내에서 매각할 가능성이 높으니 투자자분들은 투자시 이점에 유의하시기 바랍니다. |
당사의 금번 유상증자로 인하여 기발행주식 총수 6,402,979주의 54.66%에 해당하는 3,500,000주가 추가로 상장됩니다.
| [유상증자 모집예정 내역] |
| 구 분 | 내 용 |
|---|---|
| 모집예정 주식 종류 | 기명식보통주 |
| 모집예정주식수 | 3,500,000주 |
| 현재 발행주식총수 | 6,402,979주 |
| 증자비율 | 54.662050% |
| 할인율 | 25% |
금번 유상증자에 따른 모집가액은 '(舊)유가증권의 발행 및 공시등에 대한 규정' 제57조에 의해 산출됩니다. 그러나 주식시장의 특성상 향후 주가에 대한 변동성이 있는 관계로 증자에 따른 모집가격 산정시 결정된 1주당 모집가액보다 향후 추가 상장 후 거래 시점의 주가가 낮아져 투자자에게 금전적 손실을 끼칠 가능성이 있습니다.
당사는 본 유상증자의 원활한 신주인수권증서 매매를 위하여 5거래일간 신주인수권증서를 상장하여 신주인수권증서를 통한 구주주 청약률을 제고할 계획입니다. 하지만 신주인수권증서의 원활한 매매 및 청약 참여를 위한 노력에도 불구하고 신주인수권증서를 통한 청약이 부진하여 대규모 실권이 발생할 경우, 투자심리에 악영향을 끼쳐 일반공모 청약에 부정적 영향을 끼칠 수도 있으며 향후 주가하락 가능성도 배제할 수 없습니다.
금번 증자로 인해 추가 발행되는 신주는 보호예수되지 않으므로 일시적인 물량출회에 따른 주가하락의 가능성이 있습니다. 금번 유상증자에 따른 주권의 상장일은 2019년 06월 20일로 예정되어 있습니다. 금번 유상증자에 따른 모집예정주식 3,500,000주가 향후 코스닥 시장에 추가 상장될 경우 유통주식수의 증가로 인하여 주가 희석화 위험이 발생할 수 있습니다.
| 다. 잔액인수시 주가에 미치는 부정적 영향 우리사주조합 청약, 구주주 청약결과 실권주 및 단수주가 발행하는 경우 동 수량은 일반에게 공모할 예정이며, 일반공모에서도 청약이 미달될 경우 미달된 수량(최종 실권주)은 대표주관회사인 케이비증권이 인수할 계획입니다. 최종 실권주를 인수한 후 대표주관사가 수익 확정을 위해 잔액인수한 물량을 조기에 장내에서 대량 매도할 경우 일시적 물량 출회에 따른 주가 하락의 가능성이 존재하며, 인수한 최종 실권주를 일정 기간 보유하더라도 동 인수물량이 잠재매각물량으로 존재하여 주가 상승에는 부담으로 작용할 가능성이 높습니다. 또한, 대표주관사가 최종 실권주를 인수하게 되면 당사는 실권주 인수금액의 15.0%를 추가수수료로 지급하게 되며, 이를 고려하면 대표주관회사의 실권주 매입단가는 일반청약자들 보다 15.0% 낮은 것과 같은 결과가 초래됩니다. 이에 대표주관회사가 당사 주식을 인수한 후에 조기에 장내에서 매각할 가능성이 높으며, 이 경우 주가가 급락할 수 있습니다.또한, 당사는 증권신고서 제출일 현재 상환 또는 전환이 이루어지지 않은 제5회 사모 전환사채 46.5억원을 보유하고 있으며, 해당 전환사채의 전환권이 행사 될 경우 최대 465,279주가 잠재적으로 더 증가할 수 있습니다. 현재 당사 주가 하락 등의 이유로 전환권 행사 가능성은 제한적으로 판단되나, 만일 전환이 이루어 질 경우 주식수 증가에 따른 주가 희석이 발생하여 주가가 단기적으로 하락할 수 있으므로 이 점 유의하시기 바랍니다. |
본 건 유상증자는 주주배정 후 실권주 일반공모 방식으로 진행되며, 우리사주조합 청약, 구주주 청약결과 발생하는 실권주 및 단수주는 우선적으로 초과청약자에게 배정되며, 이후 실권주가 발생할 경우에 대해서는 일반에게 공모(실권주 일반공모)합니다.
실권주 일반공모 청약을 완료한 주식 수의 합계가 모집하여야 할 주식수에 미달하는 경우 미달된 잔여주식(최종 실권주)은 최종적으로 대표주관회사가 자기 계산으로 전부 인수하게 됩니다.
최종 실권주를 인수한 대표주관회사가 수익 확정을 위해 인수한 물량을 조기에 장내에서 대량 매도할 경우 일시적 물량 출회에 따른 주가 하락의 가능성이 존재하며, 인수한 최종 실권주를 일정 기간 보유하더라도 동 인수물량이 잠재 매각물량으로 존재하여 주가 상승에는 부담으로 작용할 가능성이 높습니다. 또한, 금번 유상증자에 따라 당사가 대표주관회사에게 지급할 수수료는 아래와 같습니다.
| [인수방법: 잔액인수] |
| 인수인 | 인수주식 종류 및 수 | 인수대가 | |
|---|---|---|---|
| 대표주관 | 케이비증권(주) | 인수주식의 종류: 기명식 보통주식 인수주식의 수: 최종 실권주 ×인수비율(100.00%) |
- 인수수수료: 모집총액의 2.0% - 추가수수료: 잔액인수금액의 15.0% |
주1) 잔여주식총수: 우리사주조합청약, 구주주청약 및 일반공모 후 발생한 배정잔여주 또는 청약미달주식
주2) 모집총액 : 최종 발행가액 X 총 발행주식수
또한, 당사는 증권신고서 제출일 현재 상환 또는 전환이 이루어지지 않은 제5회 사모 전환사채 46.5억원을 보유하고 있으며, 해당 전환사채의 전환권이 행사 될 경우 최대 465,279주가 잠재적으로 더 증가할 수 있습니다. 현재 당사 주가 하락 등의 이유로 전환권 행사 가능성은 제한적으로 판단되나, 만일 전환이 이루어 질 경우 주식수 증가에 따른 주가 희석이 발생하여 주가가 단기적으로 하락할 수 있으므로 이 점 유의하시기 바랍니다.
| [당사 주식관련사채 발행 현황] |
| (단위 : 백만원, 주) |
|
구분 |
발행일 |
만기일 |
권면 |
이자율 (표면이자율/ 만기이자율) |
조기상환 |
전환청구 |
전환조건 |
미상환사채 |
사채권자 | ||
|---|---|---|---|---|---|---|---|---|---|---|---|
|
전환비율 |
전환 |
권면총액 |
전환가능 |
||||||||
|
제5회 사모 |
17.12.26 |
20.12.26 |
5,000 |
0.0%/4.0% | 19.12.26 ~ 20.09.26 |
18.12.26 ~ 20.11.26 |
100 |
9,994 | 4,650 | 465,279 | 코리아에셋클래식메자닌전문투자형 사모투자신탁제2호 코리아에셋클래식멀티스트래티지 전문투자형사모투자신탁제1호 |
주1) 전환사채권면총액 50억원중 3.5억원(35,021주/주당 9,994원)의 전환청구로 인해 2019년 3월 25일 주식으로 전환되어 상장되었습니다.
즉, 대표주관회사가 최종 실권주를 인수하게 되면 당사는 실권주 인수금액의 15.0%를 추가수수료로 지급하게 되며, 이를 고려하면 대표주관회사의 실권주 매입단가는 일반청약자들 보다 15.0% 낮은 것과 같은 결과가 초래됩니다. 이에 대표주관회사가 당사 주식을 인수한 후에 조기에 장내에서 매각할 가능성이 높으며, 이 경우 주가가 급락할 수 있습니다. 투자자분들은 투자시 이점 유의하시기 바랍니다.
| 라. 발행가격 하락 위험 주식시장의 급격한 상황 악화 등으로 인하여 금번 유상증자 발행가격이 하락하면서 모집규모가 크게 줄어들 경우, 당사가 계획했던 사업추진 및 자금운용 등에 차질이 빚어지면서 사업실적 및 재무적 안정성에 부정적 영향을 미칠 수 있습니다. 투자자분들은 투자시 이점에 유의하시기 바랍니다. |
금번 유상증자의 확정발행가액은 1차 발행가액과 2차 발행가액 중 낮은 가액으로 합니다. 다만 자본시장과 금융투자업에 관한 법률 제165조의6 및 증권의 발행 및 공시등에 관한 규정 제5-15조의2에 의거하여 1차 발행가액과 2차 발행가액 중 낮은 가액이 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격보다 낮은 경우 청약일전 과거 제3거래일부터 제5거래일까지의 가중산술평균주가에서 40% 할인율을 적용하여 산정한 가격을 확정발행가액으로 합니다.(단, 발행가액이 액면가보다 낮을 경우 액면가를 발행가액으로 합니다.)
증자 기간 중 주가가 급락하는 경우에도 일반공모 후 최종실권주에 대해서는 그 전부를 대표주관회사와 인수회사가 인수하므로 청약 미달에 따른 위험은 없습니다.
하지만 주식시장의 급격한 상황 악화 등으로 인하여 금번 유상증자 발행가격이 하락하면서 모집규모가 크게 줄어들 경우, 당사가 계획했던 사업추진 및 자금운용 등에 차질이 빚어지면서 사업실적 및 재무적 안정성에 부정적 영향을 미칠 수 있습니다. 투자자분들은 투자시 이점에 유의하시기 바랍니다.
| 마. 잘못된 정보제공 가능성 당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있습니다. |
'증권관련 집단소송법' 제12조(소송허가 요건)에 따라 50명 이상의 개인이 발행주식총수의 0.01% 이상 보유할 경우 한 명 이상의 대표 당사자가 상기 50인 이상의 당사자들을 대리하여 회사가 발행한 증권의 거래과정에서 발생한 피해에 대하여 소송을 제기할 수 있습니다.
당사가 잘못된 정보를 제공하거나 부실감사 등으로 주주들에게 손해를 끼칠 시 일부 주주들로부터 집단 소송이 제기될 위험이 있습니다. 본 증권신고서 및 투자설명서에서 기재된 잘못된 내용, 잘못된 사업보고서의 공시, 내부자거래에 의한 손해배상청구및 회계부정으로 인한 손해배상 청구 등이 주요한 소송 사유에 포함됩니다. 당사는 향후 이와 같은 집단소송의 대상이 되지 않는다고 확신할 수 없으며, 만약 당사에 대하여 집단소송이 제기될 경우 상당한 소송비용이 발생할 수 있습니다.
| 바. 유상증자 일정 변경 가능성 본 증권신고서는 공시심사 과정에서 일부 내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요 내용이 변경될 시에는 본 신고서상의 일정에 차질을 가져올수 있습니다. 또한, 관계기관과의 업무진행 과정에서 일정이 변경될 수도 있으므로 투자자들께서는 투자시 이러한 점을 감안하시기 바랍니다. |
「자본시장과 금융투자업에 관한 법률」제120조 3항에 의거하여 본 증권신고서의 효력의 발생은 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나, 정부가 이 증권의 가치를 보증 또는 승인한 것이 아니므로 본 증권에 대한 투자는 전적으로 투자자에게 귀속됩니다.
금융감독원 전자공시 홈페이지(http://dart.fss.or.kr)에는 당사의 사업보고서(분기 및 반기보고서 포함) 및 감사보고서 등 기타 정기공시사항과 수시공시사항 등이 전자공시되어 있사오니 투자의사를 결정하시는 데 참조하시기 바랍니다.
본 증권신고서는 공시심사과정에서 일부 내용이 정정될 수 있으며, 투자판단과 밀접하게 연관된 주요 내용이 변경될 경우에는 본 신고서상의 일정에 차질을 가져올 수 있습니다. 또한, 관계기관과의 업무진행과정에서 일정이 변경될 수도 있으므로 투자자들께서는 투자시 이러한 점을 감안하시기 바랍니다.
| 사. 청약자 유형별 배정에 따른 위험 금번 유상증자에서 우리사주조합 청약, 구주주 청약 종료 후 실권주 일반공모 진행 결과 고위험고수익투자신탁(코넥스 고위험고수익투자신탁 포함) 및 코스닥벤처펀드의 청약 수량이 최초 우선 배정된 10%와 30%에 미달하는 경우 해당 미달 수량을 일반 청약자에게 배정하게 되며, 그 결과 일반 청약자의 청약 경쟁률보다 실제 배정받는 물량이 훨씬 많을 수가 있습니다. 일반청약자들께서는 이점 유의하시어 투자 의사 결정하시기 바랍니다. |
금번 당사의 유상증자는 주주배정 후 실권주 일반공모 방식으로 진행됩니다. 구주주 청약 및 초과청약 결과 발생한 실권주 및 단수주는 대표주관회사가 일반청약자에게 공모하게 되는데 일반공모 청약 결과 배정은 '증권 인수업무 등에 관한 규정' 제9조 제2항 제3호에 따라 고위험고수익투자신탁에 공모주식의 10%를 배정하고, 이 배정분 중 코넥스 고위험고수익투자신탁에는 50%를 우대배정하며, "증권 인수업무 등에 관한 규정" 제9조 제2항 제4호에 따라 벤처기업투자신탁에 공모주식의 30%를 배정합니다. 나머지 60%에 해당하는 주식은 개인청약자 및 기관투자자에게 구분 없이 배정합니다.
한편 고위험고수익투자신탁(코넥스 고위험고수익투자신탁 포함)에 대한 공모주식 10%와 벤처기업투자신탁에 공모주식의 30%와 개인투자자 및 기관투자자에 대한 공모주식 60%에 대한 청약경쟁률과 배정은 별도로 산출 및 배정하되, 어느 한 그룹에서 청약미달이 발생할 경우 청약미달에 해당하는 주식은 청약초과 그룹에 배정합니다. 이에 따라 금번 유상증자에서 구주주 청약 종료 후 실권주 일반공모 진행 결과 고위험고수익투자신탁(코넥스 고위험고수익투자신탁 포함) 및 코스닥벤처펀드의 청약 수량이 최초 우선 배정된 10%와 30%에 미달하는 경우 해당 미달 수량을 일반 청약자에게 배정하게 되며, 그 결과 일반 청약자의 청약 경쟁률보다 실제 배정받는 물량이 훨씬 많을 수가 있습니다. 일반청약자들께서는 이점 유의하시어 투자 의사 결정하시기 바랍니다.
| 아. 기타 투자자 유의사항 본 건 유상증자를 통해 취득한 당사의 주식가치가 하락할 수 있으며, 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 투자자 여러분의 독자적인 판단에 의해야 함을 유의하시기 바랍니다. |
금번 유상증자 실시로 당사의 주식가치가 향후 하락할 수 있으므로 투자자 여러분께서는 이점 유의하시기 바랍니다. 이 증권신고서의 효력발생은 정부가 증권신고서의 기재사항이 진실 또는 정확하다는 것을 인정하거나 이 유가증권의 가치를 보증 또는 승인한 것이 아니며, 기재사항은 청약일 이전에 변경될 수 있습니다.
본건 공모주식을 청약하고자 하는 투자자들은 투자결정을 하기 전에 본 증권신고서의 다른 기재 부분뿐만 아니라 상기 투자위험요소를 주의 깊게 검토한 후 이를 고려하여 최종적인 투자판단을 해야 합니다. 다만, 당사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 상기 투자위험요소에 기재하지 않은 사항이라 하더라도 당사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자는 상기 투자위험요소에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 자신의 독자적인 판단에 의해야 합니다.
만일 상기 투자위험요소가 실제로 발생하는 경우 당사의 사업, 재무상태, 기타 운영결과에 중대한 부정적 영향을 미칠 수 있으며, 이에 따라 투자자가 금번 공모 과정에서 취득하게 되는 당사 주식의 시장가격이 하락하여 투자금액의 일부 또는 전부를 잃게 될 수도 있습니다.
본건 공모를 위한 분석 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 여러 가지 요소들의 영향에 따라 애초에 예측했던 것과 다를 수 있다는 점에 유의해야 합니다.
※ 상기 제반 사항을 고려하시어 투자자 제위의 현명한 판단을 바랍니다.
Ⅳ. 인수인의 의견(분석기관의 평가의견)
| 본 장은 자본시장과 금융투자업에 관한 법률 제119조 및 제125조, 금융감독원의 '금융투자회사의 기업실사 모범규준'에 따라 본건 공모 지분증권 인수인이 당해 공모 지분증권에 대한 의견을 기재하고 있는 부분입니다. 따라서 본 장의 작성 주체는 대표주관회사인 케이비증권(주)이며, 발행회사는 (주)나이벡입니다. 본 장에 기재된 분석의견 중에는 예측정보가 포함되어 있습니다. 그러나 예측정보에 대한 실제 결과는 여러가지 요소들의 영향에 따라 예측했던 것과 다를 수 있다는 점을 유의하시기 바랍니다. |
1. 분석기관
| 구 분 | 증 권 회 사 | |
|---|---|---|
| 회 사 명 | 고 유 번 호 | |
| 대표주관회사 | 케이비증권(주) | 00164876 |
2. 분석의 개요
대표주관회사인 케이비증권(주)(이하 "주관회사"라 합니다.)는『자본시장과금융투자업에관한법률』제71조 및 동법시행령 제68조에 의거 공정한 거래질서 확립과 투자자 보호를 위해 다수인을 상대로 한 모집ㆍ매출 등에 관여하는 인수회사로서, 발행인이 제출하는 증권신고서 등에 허위의 기재나 중요한 사항의 누락을 방지하는데 필요한 적절한 주의를 기울였습니다.
대표주관회사인 케이비증권(주)는 인수 또는 모집ㆍ매출의 주선업무를 수행함에 있어 적절한 주의의무를 다하기 위해 금융감독원이 제정한「금융투자회사의 기업실사(Due Diligence) 모범규준」(이하 "모범규준"이라 한다)의 내용을 내부 규정에 반영하여 2012년 02월 01일부터 제출되는 지분증권, 채무증권 증권신고서를 대상(자산유동화증권 등 제외)으로 기업실사를 의무적으로 수행하도록 규정하고 있습니다.
다만, '모범규준' 제3조 제②항에 따라 발행회사의 재무 및 영업현황, 사업 환경, 투자위험, 인수 형태, 신용평가등급 등을 감안하여 강화하거나, 완화할 수 있으며, 동조 제⑤항에 따르면 금융투자회사의 이사회나 리스크관리위원회의 의사결정을 거쳐 '모범규준'의 내용(실사수준)을 생략하거나 강화 또는 완화 적용할 수 있도록 허용하였는 바, 주간회사는 지분증권의 인수 또는 모집·매출의 주선업무를 수행함에 있어서 지분증권의 특성 및 발행회사의 일정요건 충족여부 등에 따라 기업실사 수준을 완화하여 적용할 수 있도록 규정하고 있습니다.
본 지분증권은 대표주관회사 케이비증권(주)의 내부 규정상 기업실사 기준을 적용하여 기업실사 업무를 수행하였습니다.
| <금융투자회사의 기업실사 모범규준> 제3조(적용범위 등) ①이 규준은 법 제119조제3항의 규정에 의한 증권신고서 및 법 제122조의 규정에 의한 정정신고서를 제출하는 경우에 적용하며, 영업의 실체가 있는 발행회사가 제출하는 지분증권, 채무증권 증권신고서를 대상으로 하고 자산유동화증권 등은 적용대상에서 제외된다. ②이 규준은 주간회사가 업무수행 중 참고해야 할 기본적인 지침으로 발행회사의 재무 및 영업 현황, 사업 환경, 투자위험, 인수 형태 등을 감안하여 강화하거나 완화하는 등 탄력적으로 운용할 수 있다. ③기업공개의 경우 기업공개 실사절차의 특성을 감안하여 이 규준의 내용중 한국거래소의 상장심사지침 등에서 의무사항으로 규정하고 있는 내용과 중복되는 부분에 대해서는 이를 생략하거나 완화할 수 있다. ④채무증권의 경우 i)보증유무, 상환조건(만기, 옵션유무), 특약 등 해당 사채의 특성, ii)법 제119조제2항에서 규정하고 있는 일괄신고서에 의한 발행인지 여부, iii)발행회사가 시행령 제121조제6항의 요건을 충족하고 있는지 여부, iv)해당 사채권에 대한 신용평가등급(외부 및 내부) 등을 감안하여 합리적인 기준에 따라 이 규준을 완화할 수 있다. ⑤제2항 내지 제4항에 따라 이 규준을 생략하거나 강화 또는 완화하는 경우에는 이사회나 리스크관리위원회(이하 ‘리스크관리위원회 등’)의 의사결정을 거쳐야 한다. |
3. 기업실사 일정 및 주요 내용
| 일자 | 실사 내용 |
|---|---|
| 2019.02.18 | * 발행회사 초도 방문 - 발행회사의 유상증자 의사 확인 - 자금조달 희망금액 등 발행회사 의견 청취 |
| 2019.02.19 ~ 2019.02.28 |
* 발행회사의 유상증자 방식결정 협의 * 유상증자 일정 협의 및 확정 * 유상증자를 위한 사전 준비사항 및 진행절차 설명 - 발행가 산정 및 세부일정 설명 * 세부 증자관련 논의 - 유상증자 방식 결정 및 대주주 증자 참여 논의 * 유상증자 진행에 대한 질의/응답 * 실사 사전요청자료 송부 |
| 2019.03.04 ~ 2019.04.01 |
* 증자리스크 검토 - 발행시장 상황, 자금조달규모 적정성, 공모가액 희망 할인율 * 발행사와의 협의 - 발행가액 산정방식, 발행일정, 발행규모, 인수수수료 협의 * 기업실사 진행 및 추가자료 요청 - 기업실사 관련 자료요청 및 절차에 대한 설명 - 기업실사 관련 Q&A * 이사회 등 상법 절차 및 정관 등 검토 * 투자위험요소 실사 1) 사업위험관련 실사 - 기존사업 및 신규사업에 대한 세부사항 등 체크 2) 회사위험관련 실사 - 재무관련 위험 및 우발채무 등의 위험요소 등 체크 3) 기타위험관련 실사 - 주가 희석화관련 위험 등 체크 * 담당자 인터뷰 - 회사개요, 사업의 내용, 주요 재무적 이슈 확인 - 자금사용 계획 파악 - 향후 사업추진계획 및 발행회사의 비전 검토 |
| 2019.04.02 |
* 증권신고서 작성 및 조언 * 이사회의사록 등 검토 * 인수계약서 체결 * 증권신고서 인수인의 의견 완료 * 첨부서류 등 검토 * 증권신고서 제출 |
| 2019.04.12 | * 정정 증권신고서 제출 |
4. 기업실사 참여자
[발행회사]
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 |
|---|---|---|---|---|
| (주)나이벡 | 경영총괄 | 박윤정 | 전무이사 | 발행업무총괄 |
| (주)나이벡 | 중앙연구소 | 이주연 | 연구소장 | 발행업무 총괄 |
| (주)나이벡 | 경영지원 | 장영기 | 부장 | 발행업무 실무 |
| (주)나이벡 | 경영지원 | 박희정 | 차장 | 발행업무 실무 |
[대표주관회사]
| 소속기관 | 부서 | 성명 | 직책 | 실사업무분장 | 주요 경력 |
|---|---|---|---|---|---|
| 케이비증권(주) | SME금융2부 | 연대호 | 상무 | 기업실사 총괄 | 기업금융업무 등 21년 |
| 케이비증권(주) | SME금융2부 | 이경재 | 이사 | 기업실사 책임 및 검토 | 기업금융업무 등 19년 |
| 케이비증권(주) | SME금융2부 | 곽민정 | 과장 | 기업실사 실무 | 기업금융업무 등 9년 |
| 케이비증권(주) | SME금융2부 | 엄태호 | 대리 | 기업실사 실무 | 기업금융업무 등 4년 |
5. 기업실사 세부항목 및 점검 결과
- 동 증권신고서에 첨부되어 있는 기업실사 보고서를 참조해 주시기 바랍니다.
6. 종합의견
가. 대표주관회사인 케이비증권(주)는 (주)나이벡이 2019년 04월 02일 이사회에서 결의한 보통주식 3,500,000주에 대한 주주배정 후 실권주 일반공모 증자를 잔액인수 함에 있어 다음과 같이 평가합니다.
| 긍정적요인 |
▶ 동사는 타겟에 결합력을 가진 펩타이드에 대한 서열분석 및 합성을 통하여 420개의 펩타이드 라이브러리를 구축하였으며, 펩타이드의 세포 수준 및 전임상 효능을 검증하였습니다. 이에 따라 기술 이전 및 제품화 등 다양한 매출을 창출할 수 있는 준비를 갖추게 되었습니다.
|
| 부정적요인 | ▶ 동사는 코스닥시장 상장이후 2018년말까지 지속적인 당기순손실이 이어지고 있습니다.최근 3년 또한 2016년 -30.3억원, 2017년 -25.7억원, 2018년 -40.4억원의 당기순손실이 누적되고 있으며, 이로 인하여 2018년말 기준 232.3억원의 결손금이 계상되어 있습니다. ▶ 2018년 기준 주요 매출처 상위 3개사에 대한 매출비중이 84.2%를 차지하고 있습니다. 상위 3개사 매출비중은 2016년 62.9%, 2017년 81.6%, 2018년 84.2%로 매출 의존도가 점차 높아지고 있습니다. ▶ 동사의 재고자산은 2016년 17.3억(총자산대비 7.53%), 2017년 24.1억(총자산대비 9.36%), 2018년 25.4억(총자산대비 11.40%)으로 최근 3개년 지속적으로 증가하고 있으며, 재고자산 회전율은 2016년 2.7회, 2017년 2.1회, 2018년 1.92회로 감소하고 있습니다. 동사는 한국은행에서 발표한 '2017년 기업경영분석'에 의한 동종산업(의료, 정밀, 광학기기 및 시계-중소기업 C27)평균 대비 낮은 재고자산 회전율을 보이고 있는데 낮은 재고자산 회전율은 동사의 재고자산 부담이 동종업계 대비 상대적으로 크다는 것을 나타냅니다. ▶ 동사의 2018년말 기준 부채규모는 117.4억원이며, 부채비율은 111.4%이며, 총 차입금의존도는 35.05%입니다. 한국은행에 의하면 동종업계의 2017년 부채비율은 91.9%, 차입금의존도는 28.5%로 동사의 재무안정성비율은 동종업계 대비 상대적으로 열위한 수준에 있습니다. ▶ 과거 3년동안 동사는 재무활동현금을 통해 음(-)의 영업활동현금과 투자활동현금을 충당하였으며, 2018년말 기준 동종업계 대비 유동비율과 당좌비율이 열위에 있는 점과 지속적으로 음(-)의 이자보상배율이 기록되고 있는 점을 미루어 보았을 때, 동사의 재무유동성이 유의적 관점에서 안전한 상태에 있다고 할 수는 없습니다. |
| 자금조달의 필요성 |
▶ 당사는 금번 유상증자를 통해 조달하는 자금을 차입금 상환 및 연구개발비, 기타 운영자금으로 활용할 계획입니다. |
나. 대표주관회사인 케이비증권(주)은 (주)나이벡이 제출한 자료와 객관적으로 정확하고 신뢰할 수 있다고 믿어지는 자료를 중심으로 실사를 수행하였으며, 객관적인 입장에서 공정을 기하기 위하여 최선의 노력을 다하였습니다.
다. 대표주관회사는 상기 실사를 통해 제공받는 자료들로부터 도출된 결과나 오류, 누락 등에 대하여 책임지지 않으며, 인간적 또는 기계적, 기타 그 외의 다른 요인에 의한 오류발생 가능성으로 인해 본 평가 내용에 대해 명시적으로 혹은 묵시적으로도 증명이나 서명 또는 보증 및 단언을 할 수 없습니다.
라. 동사의 금번 유상증자는 국내외 거시경제 변수 변화로 투자수익에 대한 확실성이 저하될 수 있습니다. 투자자 여러분께서는 상기 검토결과는 물론 동 증권신고서 및 투자설명서에 기재된 동사의 회사 전반에 걸친 현황 및 재무상의 위험과 산업 및 영업상의 위험요인 등을 감안하시어 투자에 유의하시기 바랍니다.
또한, 대표주관회사가 현재 알고 있지 못하거나 중요하지 않다고 판단하여 동 증권신고서 및 투자설명서에 기재하지 않은 사항이라 하더라도 동사의 운영에 중대한 부정적 영향을 미칠 수 있다는 가능성을 배제할 수는 없으므로, 투자자께서는 동 증권신고서 및 투자설명서에 기재된 정보에만 의존하여 투자판단을 해서는 안되며, 독자적이고도 세밀한 판단에 의해 투자결정을 하시기 바랍니다.
| 2019년 04월 12일 |
| 대표주관회사 : 케이비증권주식회사 |
| 대표이사 김 성 현 |
Ⅴ. 자금의 사용목적
1. 모집 또는 매출에 의한 자금조달 내역
가. 자금조달금액
| (단위: 원) |
| 구분 | 금액 |
|---|---|
| 모집 또는 매출총액 (1) | 26,565,000,000 |
| 발 행 제 비 용 (2) | 599,661,700 |
| 순 수 입 금 (1)-(2) | 25,965,338,300 |
주1) 상기 금액은 예정발행가액을 기준으로 산정한 금액입니다.
주2) 상기 모집 또는 매출총액은 우선적으로 아래 자금의 사용 목적에 따라 사용할 예정입니다.
주3) 발행제비용은 공모금액 및 실권규모에 따라 변경될 수 있으며, 상기 기재 금액은 청약 초과로 인하여 실권이 발생하지 않은 상황을 가정하여 산정되었습니다. 또한 상장수수료는 상장신청일 직전일 주가에 따라 변동될 수 있습니다.
나. 발행제비용의 내역
| (단위: 원) |
| 구분 | 금액 | 계산근거 |
|---|---|---|
| 발행분담금 | 4,781,700 | 모집총액의 0.018% (10원 미만 절사) |
| 인수수수료 | 531,300,000 | 모집금액의 2.0% |
| 상장수수료 | 5,180,000 | 430만원+300억원 초과금액 10억당 8만원 |
| 등록면허세 | 7,000,000 | 증자자본금의 0.4% (10원 미만 절사) |
| 지방교육세 | 1,400,000 | 등록세의 20% (10원 미만 절사) |
| 기타비용 | 50,000,000 | 투자설명서 인쇄, 청약서 발송, 등기수임료 등 |
| 합계 | 599,661,700 |
주1) 상기 금액은 예정발행가액을 기준으로 산정한 금액입니다.
주2) 발행제비용은 공모금액 및 실권규모에 따라 변경될 수 있으며, 상기 기재 금액은 청약 초과로 인하여 실권이 발생하지 않은 상황을 가정하여 산정되었습니다. 또한 상장수수료는 상장신청일 직전일 주가에 따라 변동될 수 있습니다.
2. 자금의 사용목적
| (단위: 원) |
| 시설자금 | 운영자금 | 차환자금 | 기타 제비용 | 합계 |
|---|---|---|---|---|
| 2,000,000,000 | 14,832,588,300 | 9,132,750,000 | 599,661,700 | 26,565,000,000 |
주1) 상기 금액은 예상 발행가액을 기준으로 산정한 금액입니다.
가. 자금사용의 개요
당사는 금번 주주배정 후 실권주 일반공모를 통한 납입자금에 대해서 아래와 같은 우선순위로 사용할 예정입니다.
| (단위 : 백만원) |
| 구 분 | 목 적 | 자금 사용 시기 | 사용내역 | 금 액 | 우선순위 |
|---|---|---|---|---|---|
| 시설자금 | 신규라인 구축 및 노후설비 교체 등 | 2019년 06월 ~ 2019년 12월 | 건물 및 시설구축 외 | 2,000 | 3 |
| 차환자금 | 차입금 상환 | 2019년 06월 | KB증권 단기차입금 상환 | 9,133 | 1 |
| 운영자금 | 연구개발비 | 2019년 06월 ~ 2020년 12월 |
펩타이드 관련 연구개발 | 14,832 | 4 |
| 발행비용 | 발행제비용 | - | - | 600 | 2 |
| 총 계 | 26,565 | - | |||
주) 자금 집행시기까지의 미사용금액은 당사 명의의 보통예금에 입금하여 자금을 보유할 계획입니다.
나. 자금의 세부 사용계획
1) 시설자금의 사용
당사는 2016년 펩타이드 함유 치과용 골이식재인 OssGen-15가 개발이 완료되면서 충북 진천공장에 펩타이드 구역 시설을 확장하기 시작하였으며, 지속적으로 수주가 증가하고 있어 생산능력의 증가가 필요할 것으로 예상하고 있습니다. 이와 관련하여 펩타이드 신규 생산라인 신축 및 기계장치 비용으로 2,000백만원을 사용 할 예정입니다.
| [시설자금 세부 사용내역] |
| (단위 : 백만원) |
|
구분 |
목적 |
세부 내역 | 금 액 | 자금집행시기 |
|---|---|---|---|---|
|
기계설비 |
펩타이드 관련 기계설비 |
펩타이드 신규라인 구축 | 1,000 | 2019년 06월~2019년 12월 |
| 기계장치 비용 | 1,000 | |||
| 합 계 | 2,000 | - | ||
2) 차입금 상환
당사는 금번 주주배정후실권주일반공모의 대표주관사인 KB증권으로부터 본 증권신고서 제출일로부터 5영업일 이내에 단기차입금 9,000백만원을 차입할 계획이며, 단기차입금은 유상증자 대금 납입 전에 연구개발비용으로 총 3,400백만원이 사용될 예정이며, 제5회차 전환사채의 기한의이익상실 가능성에 대비하는데 총 5,600백만원(미상환 사채 권면총액 4,650백만원 및 이자비용 약 950백만원)이 사용할 계획입니다. 이후 금번 유상증자를 통한 자금 중 9,133백만원(예상 이자 포함, 상환시점에 따라 이자금액은 변동될 수 있음)을 상환 자금으로 사용할 예정입니다.
| [ 단기자금대출의 주요 금융조건 ] |
| 구분 | 내용 |
|---|---|
| 대주 | 케이비증권 |
| 대출금액 | 금 구십억원(\ 9,000,000,000) |
| 차입일 | 증권신고서 제출일(2019년 04월 02일)로부터 5영업일 이내 |
| 만기 | 차입일로부터 6개월 |
| 대출금리 | 고정 (연) 5.90% |
| 자금사용 목적 | 5회차 전환사채의 상환 청구대비 및 연구개발비용 |
| 의무상환 | 유상증자 대금납입 후 3영업일 이내 조기상환 |
| [ 단기자금대출의 세부 자금사용목적 ] |
| 구 분 | 상세 내역 | 금 액 | 비 고 |
|---|---|---|---|
| 5회차 전환사채 상환 대비 자금 |
미상환 사채 권면총액 | 4,650백만원 | 기한의 이익상실 가능성에 대한 대비 |
| 예상 이자비용 | 950백만원 | ||
| 소 계 | 5,600백만원 | ||
| 연구개발비용 | 펩타이드기반 골다공증치료제 임상1상 비용 | 1,000백만원 |
유상증자 대금 납입 전 연구개발비 사용 |
| 펩타이드기반 관절염치료제 전임상 비용 |
1,400백만원 |
||
| 표적항암치료제 효능평가 비용 |
1,000백만원 |
||
| 소 계 | 3,400백만원 | ||
| 합 계 | 9,000백만원 | - | |
3) 연구개발비 사용
당사는 펩타이드 기반 바이오소재의 연구개발을 진행하고 있으며, 금번 주주배정후실권주 일반공모를 통하여 유입되는 자금 중 15,000백만원으로 펩타이드 관련 의약품 및 바이오소재의 연구개발을 위해 사용할 예정이며, 부족한 자금에 대해서는 자체 자금을 사용하여 연구개발을 진행할 계획입니다.
세부적으로 펩타이드 기반 골다공증치료제 임상 1상 진행비용 35억원, 펩타이드 기반 관절염 치료제의 전임상 및 1상임상비용 각각 30억원, 골이식재 및 치주재생유도제 유럽임상비용 10억, 펩타이드 표적항암제 전임상비용 15억원, 비알콜성지방간염(NASH) 치료제와 장질환 치료제 전임상비용 30억원이 소요될 것으로 예상하고 있습니다. 각 Pipeline별 연구개발 현황 및 자금소요계획은 다음과 같습니다. 바이오의약품 임상시험과 관련된 사항 및 위험은 Ⅲ. 투자위험요소.의 1.사업위험 - (마) 부분에 세부적으로 작성하였으니, 이를 참고하시기 바랍니다.
 |
|
펩타이드 의약품 연구개발 단계 |
 |
|
펩타이드 의약바이오소재 연구개발 단계 |
| [연구개발비 세부 사용내역] |
| (단위 : 백만원) |
| 구 분 | 내 용 | 세부사용금액 | 금액 | 자금 사용시기 |
|---|---|---|---|---|
|
펩타이드 기반 골다공증치료제 임상 1상 진행비용 |
추가 동물실험비 |
500 |
3,500 |
2019년 07월 ~ 2019년 09월 |
|
임상용 시제품 제작비 |
1,000 | 2019년 06월 ~ 2019년 09월 |
||
|
임상시험 기관비 |
1,500 | 2019년 06월 ~ 2019년 09월 |
||
|
CRO비용 |
500 | 2019년 06월 ~ 2019년 09월 |
||
|
펩타이드 기반 관절염치료제 전임상 비용 |
GLP 전임상 기관의 독성시험 및 동물실험비 |
2,000 | 3,000 | 2019년 06월 ~ 2019년 12월 |
|
펩타이드 제작비용 등 |
1,000 | 2019년 06월 ~ 2019년 09월 |
||
| 펩타이드 관련 관절염치료제 임상 1상 진행비용 |
추가 동물실험비 |
200 | 3,000 | 2021년 01월~ 2020년 06월 |
|
임상용 시제품 제작비 |
1,000 | 2021년01월~ 2020년 12월 |
||
|
임상시험 기관비 |
1,500 | 2021년01월~ 2020년 12월 | ||
|
CRO비용 |
300 | 2021년01월~ 2020년 12월 | ||
|
골이식재(OCS-B, OCS-B Collagen), Regenomer 유럽 임상 비용 |
골이식재(OCS-B, OCS-B Collagen) |
700 | 1,000 | 2019년 06월 ~ 2019년 09월 |
|
Regenomer |
300 | 2019년 09월 ~ 2019년 12월 | ||
| Anti-Cancer Peptide | 1,500 | 2019년 07월 ~ 2020년 12월 | ||
| 비알콜성지방간염(NASH) | 1,500 | 2019년 07월 ~ 2020년 12월 |
||
| 염증성 장질환(IBD) | 1,500 | 2019년 07월 ~ 2020년 12월 |
||
|
합 계 |
15,000 | - | ||
Ⅵ. 그 밖에 투자자보호를 위해 필요한 사항
본 건의 경우 시장조성 또는 안정조작에 관한 사항은 해당사항 없습니다.
제2부 발행인에 관한 사항
Ⅰ. 회사의 개요
1. 회사의 개요
가. 회사의 법적, 상업적 명칭
당사의 명칭은 "주식회사 나이벡"이라 칭하고, 영문으로는 "NIBEC Co., Ltd."라 합니다. 단, 약식으로 표기할 경우에는 (주)나이벡이라고 표기합니다.
나. 설립일자
당사는 교육과학기술부(현, 과학기술정보통신부) 한국 연구재단 지정 우수연구센터인 서울대학교 치과대학 소재 지능형 생체계면공학 연구센터 (Intellectual Biointerface Engineering Center, [IBEC])에서의 9년간의 연구결과를 상용화하여 자립기반을 구축함과 동시에 국가의 지원으로 만들어낸 결실을 다시 사회에 환원한다는 목적을 가지고 설립되었습니다. 약물전달시스템, 조직재생용 바이오소재기술, 펩타이드 공학기술의 학문적 성과를 제품개발에 응용하고자 2004년 1월 24일 (주)나이벡을 설립하였으며, 펩타이드 의약품 및 펩타이드 융합바이오 소재, 조직재생용 바이오소재, 조직재생기능성 이식용 의료기기, 구강보건제품 등의 개발 및 제품화를 목적으로 하고 있습니다.
다. 본사의 주소, 전화번호 및 홈페이지
- 본사주소 : 충북 진천군 이월면 밤디길 116 이월전기전자농공1단지
- 전화번호 : 043)532-7458
- 홈페이지 : www.nibec.co.kr
라. 중소기업 해당여부
당사는 보고서 제출일 현재 중소기업기본법 제 2조에 의한 중소기업입니다.
마. 주요사업의 내용
당사는 펩타이드 의약품 및 펩타이드 융합바이오 소재, 조직재생용 바이오소재 및 의료기기, 구강보건제품의 연구 개발 및 제품의 제조, 판매를 진행하고 있습니다. 기타 자세한 사항은 동 보고서 'Ⅱ. 사업의 내용'을 참조하시기 바랍니다.
바. 관계회사에 관한 사항
보고서 제출일 현재 해당사항 없습니다.
사. 회사의 주권상장(또는 등록ㆍ지정)여부 및 특례상장에 관한 사항
| 주권상장 (또는 등록ㆍ지정)여부 |
주권상장 (또는 등록ㆍ지정)일자 |
특례상장 등 여부 |
특례상장 등 적용법규 |
|---|---|---|---|
| 코스닥시장 | 2011년 07월 11일 | 기술성장기업의 코스닥시장 상장 | 코스닥시장상장규정 제7조2항 |
2. 회사의 연혁
가. 회사의 본점소재지 및 그 변경
| 일 자 | 본점소재지 | 비고 |
|---|---|---|
| 2004.01.27 | 서울시 종로구 연건동 28 서울대학교 치과대학내 | 회사설립 |
| 2005.09.07 | 서울시 종로구 연건동 28-22 서울대학교 치의학대학원내 | 본사이전 |
| 2006.04.28 | 서울시 종로구 연건동 28-22 서울대학교 치의학대학원 치과생체재료연구동 107호 |
본사이전 |
| 2009.01.12 | 충북 진천군 이월면 밤디길 116 이월전기전자농공1단지 | 본사이전 |
나. 경영진의 중요한 변동
| 일 자 | 내 용 |
|---|---|
| 2004. 01 | 대표이사 취임 (구영) |
| 2004. 03 | 대표이사 변경 (구영 사임, 정종평 취임) |
| 204. 03 | 경영진 변동 (감사 이승진 취임) |
| 2005. 02 | 경영진 변동 (이사 박윤정 취임) |
| 2007. 03 | 경영진 변동 (사외이사 김사성 취임) |
| 2010. 03 | 경영진 변동 (이사 이주연 취임) |
| 2012. 03 | 경영진 변동 (감사 이승진 사임, 감사 설양조 취임) |
다. 최대주주의 변동
당사의 보고서 제출일 현재 최대주주는 대표이사 정종평입니다. 당사의 설립이후의 최대주주의 변동은 없습니다.
라. 상호의 변경
당사는 설립일로부터 보고서 제출일 현재까지 상호를 변경한 사실이 없습니다.
마. 그 밖에 경영활동과 관련된 중요한 사항의 발생내용
| 구 분 | 내 역 |
|---|---|
| 2000년 | 서울대 치대 교육과학기술부/한국연구재단으로부터 우수연구센터 (ERC Center)로 지정 |
| 2004년 | (주)나이벡 설립 |
| (주)나이벡 중앙연구소 인증 (산업기술진흥협회) | |
| 신기술 벤처기업 지정 (서울지방중소기업청) | |
| 2005년 | 의료기기제조업 허가 |
| 치과용 골이식재 (OCS-B) 제조품목허가 취득 | |
| 2006년 | 치과용 차폐막 (Nanogide-C) 제조품목허가 취득 |
| 2007년 | 이노비즈기업 선정 (중소기업청) |
| 의약외품 제조업 허가 | |
| 치아미백제 (BlancTis) 제조품목허가 취득 | |
| 치과용골이식재 (OCS-H) 제조품목허가 취득 | |
| 2008년 | (주)나이벡 진천 GMP공장, 연구소 준공 |
| 시린이치료제 제조품목허가 취득 | |
| 기술평가보증 벤처기업 지정 (기술보증기금) | |
| 2009년 | 본사이전 : 충북 진천군 이월면 신월리 1127 이월전기전자농공단지 서울지점 : 서울시 종로구 연건동 28 서울대학교 치과대학 치과생체재료연구동 107호 |
| CE 인증획득: OCS-H® (말뼈유래 골이식재) | |
| 치아미백제 블랑티스 (BlancTis) FDA인증 획득 | |
| 치아미백제 블랑티스 포르테 (BlancTis Forte) FDA인증 획득 | |
| 시린이치료제 센스블록 (SensBlok) FDA인증 획득 | |
| 2010년 | 상장예비심사 기술성 평가 통과 |
| 2011년 | GuidOss 제조품목허가 완료 |
| 코스닥 시장 신규 상장 | |
| OCS-H, GuidOss TFDA 허가 승인 획득 | |
| Ossen-X15 KFDA 허가승인 획득 | |
| 2012년 | CE인증 획득: GuidOss (흡수성치주조직재생유도막) |
| TFDA 품목허가 : 치아미백제 블랑티스 포르테 II (BlancTis Forte II) | |
| CE인증 획득: OCS-B (소뼈유래 골이식재) | |
| 태국식양청 품목허가 : OCS-B (소뼈유래 골이식재) | |
| 캐나다식약청 품목허가 : OCS-H (말뼈유래 골이식재) | |
| 2013년 | FDA 품목허가 : OCS-B (소뼈유래 골이식재) |
| KFDA 화장품 제조업, 판매업 허가 | |
| 2014년 | KFDA 품목허가 : Equimatrix-Collagen, OCS-B Collagen, Regenomer |
| 중국식약청 품목허가 : SensBlok (시린이치료제) | |
| FDA 품목허가 : GuidOss (흡수성치주조직재생유도막) | |
| Canada ISO 13485 (CMDCAS) 인증획득 | |
| KFDA 품목허가: 치과용 주사기 | |
| EN ISO 13485 : 2012 갱신 | |
| CE인증 갱신: OCS-H (말뼈유래 골이식재) | |
| 2015년 | 의약품GMP(KGMP) 획득 |
| KFDA 품목허가: 클린티스(ClinTis) | |
| 코스닥시장 유상증자 | |
| 2016년 | 대만식약청 품목허가 : GuidOss(흡수성치주조직재생유도막) |
| 중국식약청 품목허가 : 닥터마이유(기능성화장품) | |
| 러시아 판매허가 : 닥터화이티스(치아미백제) | |
| 2017년 | 펩타이드를 기반으로 하는 치과분야의 응용기술 이전 |
| 중국시장 독점판매권 및 공급계약 | |
| 인도 판매허가 : OCS-B, OCS-B Collagen | |
| 이스라엘 판매허가 : OCS-B, OCS-B Collagen | |
| 캐나다 판매허가 : OCS-B Collagen | |
| 2018년 |
유럽 판매허가 : OCS-B Collagen |
|
세포투과성 펩타이드 및 형광표지 자성나노입자 유럽 특허 등록 |
|
|
줄기세포 재생능 펩타이드 대한민국 특허 등록 |
|
|
암줄기세포 표적 항암 미국 특허 등록 |
|
|
합성 펩타이드 이용한 유도만능 줄기세포 대한민국, 일본, 미국 특허 등록 |
|
|
티타늄 결합능을 가지는 펩타이드 대한민국 특허 등록 |
|
|
충청북도 스타기업 선정 |
|
|
MDSAP(The Medical Device Single Audit Program) 획득 |
|
|
휴온스와 공급계약 : Minocure, Clinplant |
|
|
스트라우만과 제품 공급계약 : OCS-B Collagen, Clinplant, Regenomer |
|
|
펩타이드 골다공증 치료제 전 임상 완료 |
3. 자본금 변동사항
증자(감자)현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 원, 주) |
| 주식발행 (감소)일자 |
발행(감소) 형태 |
발행(감소)한 주식의 내용 | ||||
|---|---|---|---|---|---|---|
| 주식의 종류 | 수량 | 주당 액면가액 |
주당발행 (감소)가액 |
비고 | ||
| 2011.02.28 | 전환권행사 | 보통주 | 499,996 | 500 | - | 전환상환 우선주 |
| 2011.07.13 | 유상증자(일반공모) | 보통주 | 734,000 | 500 | 10,000 | 증자비율 33.33% |
| 2011.08.16 | 전환권행사 | 보통주 | 428,565 | 500 | 3,500 | - |
| 2014.07.28 | 신주인수권행사 | 보통주 | 70,955 | 500 | 4,228 | - |
| 2014.09.11 | 신주인수권행사 | 보통주 | 165,562 | 500 | 4,228 | - |
| 2014.12.09 | 신주인수권행사 | 보통주 | 283,822 | 500 | 4,228 | - |
| 2014.12.11 | 신주인수권행사 | 보통주 | 189,214 | 500 | 4,228 | - |
| 2015.01.07 | 신주인수권행사 | 보통주 | 141,911 | 500 | 4,228 | - |
| 2015.04.14 | 유상증자(제3자배정) | 보통주 | 129,236 | 500 | 7,730 | 증자비율 3.0654% |
| 2015.07.17 | 주식매수선택권행사 | 보통주 | 1,000 | 500 | 1,500 | - |
| 2015.07.17 | 주식매수선택권행사 | 보통주 | 1,000 | 500 | 2,000 | - |
| 2015.07.17 | 주식매수선택권행사 | 보통주 | 1,500 | 500 | 2,300 | - |
| 2015.09.10 | 유상증자(주주배정) | 보통주 | 800,000 | 500 | 7,580 | 증자비율 18.3960% |
| 2015.12.30 | 신주인수권행사 | 보통주 | 70,954 | 500 | 4,228 | - |
| 2016.11.07 | 신주인수권행사 | 보통주 | 23,651 | 500 | 4,228 | - |
| 2016.11.15 | 주식매수선택권행사 | 보통주 | 2,500 | 500 | 1,500 | - |
| 2016.11.15 | 주식매수선택권행사 | 보통주 | 1,000 | 500 | 2,000 | - |
| 2016.11.15 | 주식매수선택권행사 | 보통주 | 2,000 | 500 | 2,300 | - |
| 2016.11.28 | 주식매수선택권행사 | 보통주 | 11,500 | 500 | 1,500 | - |
| 2016.11.28 | 주식매수선택권행사 | 보통주 | 11,000 | 500 | 2,000 | - |
| 2016.11.28 | 주식매수선택권행사 | 보통주 | 14,500 | 500 | 2,300 | - |
| 2016.12.19 | 전환권행사 | 보통주 | 147,710 | 500 | 6,770 | - |
| 2017.04.06 | 전환권행사 | 보통주 | 26,222 | 500 | 7,627 | - |
| 2017.10.23 | 전환권행사 | 보통주 | 314,671 | 500 | 7,627 | - |
| 2017.10.30 | 전환권행사 | 보통주 | 196,669 | 500 | 7,627 | - |
| 2017.11.22 | 전환권행사 | 보통주 | 39,333 | 500 | 7,627 | - |
| 2018.05.21 | 전환권행사 | 보통주 | 147,710 | 500 | 6,770 | - |
| 2018.05.21 | 전환권행사 | 보통주 | 209,779 | 500 | 7,627 | - |
| 2019.03.07 | 전환권행사 | 보통주 | 35,021 | 500 | 9,994 | |
미상환 전환사채 발행현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 백만원, 주) |
| 종류\구분 | 발행일 | 만기일 | 권면총액 | 전환대상 주식의 종류 |
전환청구가능기간 | 전환조건 | 미상환사채 | 비고 | ||
|---|---|---|---|---|---|---|---|---|---|---|
| 전환비율 (%) |
전환가액 | 권면총액 | 전환가능주식수 | |||||||
| 제5회 무보증 국내사모 전환사채 |
2017.12.26 | 2020.12.26 | 5,000 | 보통주 | 2018.12.26~2020.11.26 | 100 | 9,994 | 4,650 | 465.279 | - |
| 합 계 | - | - | - | - | - | - | - | 4,650 | 465.279 | - |
4. 주식의 총수 등
주식의 총수 현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 비고 | |||
|---|---|---|---|---|---|
| 보통주 | 우선주 | 합계 | |||
| Ⅰ. 발행할 주식의 총수 | 98,000,000 | 2,000,000 | 100,000,000 | - | |
| Ⅱ. 현재까지 발행한 주식의 총수 | 6,402,979 | - | 6,402,979 | - | |
| Ⅲ. 현재까지 감소한 주식의 총수 | - | - | - | - | |
| 1. 감자 | - | - | - | - | |
| 2. 이익소각 | - | - | - | - | |
| 3. 상환주식의 상환 | - | - | - | - | |
| 4. 기타 | - | - | - | - | |
| Ⅳ. 발행주식의 총수 (Ⅱ-Ⅲ) | 6,402,979 | - | 6,402,979 | - | |
| Ⅴ. 자기주식수 | - | - | - | - | |
| Ⅵ. 유통주식수 (Ⅳ-Ⅴ) | 6,402,979 | - | 6,402,979 | - | |
5. 의결권 현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 주) |
| 구 분 | 주식의 종류 | 주식수 | 비고 |
|---|---|---|---|
| 발행주식총수(A) | 보통주 | 6,402,979 | - |
| 우선주 | - | - | |
| 의결권없는 주식수(B) | 보통주 | - | - |
| 우선주 | - | - | |
| 정관에 의하여 의결권 행사가 배제된 주식수(C) | 보통주 | - | - |
| 우선주 | - | - | |
| 기타 법률에 의하여 의결권 행사가 제한된 주식수(D) |
보통주 | - | - |
| 우선주 | - | - | |
| 의결권이 부활된 주식수(E) | 보통주 | - | - |
| 우선주 | - | - | |
| 의결권을 행사할 수 있는 주식수 (F = A - B - C - D + E) |
보통주 | 6,402,979 | - |
| 우선주 | - | - |
6. 배당에 관한 사항
주요배당지표
| 구 분 | 주식의 종류 | 당기 | 전기 | 전전기 |
|---|---|---|---|---|
| 제15기 | 제14기 | 제13기 | ||
| 주당액면가액(원) | 500 | 500 | 500 | |
| (연결)당기순이익(백만원) | - | - | - | |
| (별도)당기순이익(백만원) | -4,146 | -2,568 | -3,027 | |
| (연결)주당순이익(원) | -665 | -463 | -578 | |
| 현금배당금총액(백만원) | - | - | - | |
| 주식배당금총액(백만원) | - | - | - | |
| (연결)현금배당성향(%) | - | - | - | |
| 현금배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주식배당수익률(%) | - | - | - | - |
| - | - | - | - | |
| 주당 현금배당금(원) | - | - | - | - |
| - | - | - | - | |
| 주당 주식배당(주) | - | - | - | - |
| - | - | - | - | |
Ⅱ. 사업의 내용
1. 사업의 개요
가. 업계의 현황
(1) 산업의 개요
바이오산업이란 통상 현대 생명공학 기술을 바탕으로 생물체의 기능과 정보를 활용하여 인류의 건강증진, 질병예방, 진단, 치료에 필요한 유용물질과 서비스를 상업적으로 생산하는 산업을 일컫습니다. 즉, 바이오산업은 제품의 특성을 기준으로 분류되는 기존의 타 산업과는 다르게 생명공학기술의 적용 여부를 근거로 분류되는 기술기반의 산업이라고 할 수 있습니다. 우리나라에서는 산업연구원을 중심으로 2003년 이후부터 바이오산업의 범위를 정의하기 위하여 바이오산업기술 분류체계를 구축하고 이에 근거하는 통계작업을 시행하고 있습니다. 이에 따르면 바이오산업 (Bioindustry or Biotechnology industry)의 범위는 의약, 화학, 식품, 환경, 에너지 등으로 구분되며, 특히 바이오 의약품 시장의 경우 생명공학기술 및 의약화학기술을 동시에 이용한제품이 의약품시장의 90%를 차지하고 있습니다.
바이오산업이란 큰 틀 안에서 현재 당사가 영위하는 사업은 조직재생용 바이오산업,구강보건산업 및 펩타이드 기반산업으로 나눌 수 있으며, 이와 관련된 당사의 기반기술은 조직재생 바이오소재기술, 약물 전달시스템 기술 및 펩타이드 공학기술로 특징 지을 수 있습니다.
(가) 펩타이드 의약품 및 의약 바이오 소재 기반 산업
① 펩타이드에 대한 설명
펩타이드(Peptide)란 단백질의 기능적 최소 단위로서 생체 신호전달 및 기능 조절에관여하는 물질입니다. 펩타이드는 두 개 이상의 아미노산이 사슬처럼 연결되어 있는 물질을 말하며, 일반적으로는 길이가 짧은 단백질이나 구성 아미노산의 수가 50개 이하의 사슬로 연결되어 있는 아미노산 중합체를 펩타이드로 구분하여 말하고 있습니다. 이들 펩타이드는 바이오산업에 속하는 생명 과학 소재로서, 생물 의약 및 생물 화학 분야에서 치료제나 기능성 물질로 사용되는 핵심 소재입니다.
펩타이드는 체내에서 유전자로부터 생합성 과정에 의해서도 만들어지지만 체외에서도 아미노산을 합성 방법에 의한 화학적 방법에 의해서도 만들 수 있습니다. 이렇게 만들어진 펩타이드는 단백질-단백질 상호작용을 통한 질병규명, 세포분화 규명, 의약품 제조, 질병의 진단제제, 나노소재의 재료로 사용되는 등 활용성이 넓습니다. 펩타이드를 구성하는 아미노산은 23종인데, 다음의 표와 같이 구성되는 아미노산 수에 따라 만들어질 수 있는 펩타이드의 가짓수는 무궁무진하다고 할 수 있으며 이에 따라 생리활성 펩타이드의 검색범위 또한 넓다고 할 수 있어 개발의 전망이 밝은 분야입니다. 이러한 가능성 외에도 펩타이드가 주목받는 이유는 단백질과 같은 분자량이 높은 물질이나 지용성이 높은 물질이 체내에 적용되었을 때 생체 내에서 간 등에서 축적되는것과 달리 생체 내에서 작용 후 체외로 배출되어 1) 생체 내 독성을 유발할 위험이 없고, 단백질 의약품과 같이 체내 주사 시 2) 면역반응에 의해 항체를 만들어 부작용을 낼 위험이 적고, 3) 표적이 되는 물질과의 특이적인 결합 때문에 높은 활성을 나타내고, 아미노산 종류와 수에 따라 4) 다양한 분자구조가 만들어질 수 있고, 세포내에서만 만들어지는 것이 아니고 합성법으로도 만들어 질 수 있어서 5) 균질한 화합물의 형태로 validation이 가능하기 때문에 의약품이나 바이오메디칼 소재로의 활용 전망이 밝습니다. 또한 기회적인 요소로는 1) 저분자나 천연물 신약개발 비용이 증가하고, 분자생물학이나 의학의 발전으로 2) 신약 개발 표적 (target) 물질이 다양화함에 따라 이에 유연하게 대처할 신물질로 부상하고 있습니다. 합성 공정의 개발이 지속적으로 이루어져 3) 대량생산이 다른 바이오 의약품에 비해 용이하다는 점과 아울러 4) 바이오 신약, 소재의 시장이 성장함에 따라 동반 성장할 가능성이 있기 때문입니다.
② 펩타이드 의약품 및 펩타이드 기반 개량 바이오의약품 (바이오베터) 산업
바이오의약품 산업은 제약회사들이 전통적인 의약품 (합성 신약)을 연구 개발하던 방식과는 차별 되게, 유전자 재조합 기술을 이용하여 단백질 의약품을 연구개발하면서 시작하였습니다. 1973년 캘리포니아 주립대학의 허브 보이어 (Herb Boyer) 교수와 스탠포드 대학교의 스탠 코헨 (Stan Cohen) 교수가 사람의 유전자를 대장균에 이식시켜 대장균에서 단백질을 만들어내는 유전자 재조합기술을 발표하면서 바이오 의약품 제조기술의 산업화가 시작되는 시초를 만들었습니다. 허브 보이어 교수 (Herb Boyer)에 의해 설립된 최초의 바이오 회사인 제넨테크 (GenenTech, 1976년 설립) 이후 카이론 (Chiron), 암젠 (Amgen) 등은 제약 회사들이 채용하지 않았던 유전자 재조합 기술을 이용하여, 새로운 개념의 단백질 치료제들, 진단시약 및 백신들을 상품화하는데 집중한 결과, 과거에는 전혀 없었던 단백질 치료제들이 상품화 되었습니다.
1990년대 말, 2000년의 인간게놈 프로젝트 등의 성과로 단백질 의약품의 연관되는 주변 기술, 즉 고속약효검색, 조합화학, 구조 기반 신약 발굴 등 각종 최첨단 신약연구 방법론이 동원되어 단백질, 항체신약, 펩타이드 합성신약을 연구하고 있으며, 현재는 더 많은 수의 바이오 회사들이 단백질을 활용한 합성신약의 발굴에 집중하고 있습니다. 단백질치료제의 대명사인 Amgen사도 1997년 미국 길포드 (Guilford)사로부터 퇴행성 뇌질환 치료를 위한 합성신약을 도입하는 등 합성신약연구에 매진하고 있습니다. 1990년대 후반까지 바이오산업은 사실상 미국에서만 발달한 산업이었으나 1990년대 후반에서 2000년대 초반에 유럽과 일본 등에서도 다양한 바이오 회사들이 설립되었습니다. 현재는 거의 모든 선진국가들이 바이오산업이 미래성장산업임을 인식하고, 국가적으로 육성하고 있습니다. 아시아에서 국가적으로 바이오산업을 육성하는 가장 대표적인 예는 싱가포르의 바이오 폴리스입니다. 한국에서도 바이오의약품은 국가전략 차원에서 바이오 신약/장기 개발로서 10대 성장 동력 산업으로 지정되어 있습니다. 한국의 바이오의약품 산업은 제약회사들이 단백질 의약품을 개발·생산하면서 본격적으로 도입되었으며, LG생명과학에서 조합화학, 고속약효검색 그리고 구조 기반 신약 발굴 기술을 도입하는 선도적인 역할을 하였습니다. 벤처로서의 바이오기업은 1990년대 후반부터 설립되기 시작하여 2000년도 인간게놈프로젝트를 기점으로 최대 600여 업체들이 설립되었습니다. 초기에는 단백질 신약발굴 보다는 벤처기업의수익을 내기위하여 주변기술에 의한 다양한 사업모델 (새로운 유전자 발굴, DNA 칩, 건강보조식품 등)이 시험되었으나, 최근에는 가장 부가가치가 높은 신약 연구개발 및 그 유관 분야로 수렴하는 경향을 보이고 있습니다.
바이오 의약품 산업은 1세대는 단백질 치료제, 그리고 2세대는 항체를 기반으로 한 단백질 치료제가 주종을 이루고 있습니다. 이들의 생산 방식은 유전자 재조합 미생물에서 만들어진 단백질을 주로 이용하였지만, 최근 펩타이드 합성 기술의 발전으로 인해 필요한 펩타이드를 화학적으로 합성하여 이용 가능하게 되었습니다. 이와 같은 기술을 바탕으로 비천연 합성 펩타이드를 펩타이드 의약품 및 펩타이드 기반 바이오베터의 핵심소재로 이용할 수 있습니다.
현재 기존의 의약품시장은 저분자 합성의약품 (Small molecule) 및 이의 제네릭 의약품시장이 특허 만료로 이미 과포화 되어 성장이 둔화된 것을 볼 때, 바이오 의약품이 미래시장을 주도할 것은 확실합니다 (자료: 2010 바이오경제연구센터 Report V, 바이오시밀러 : 해결해야 할 과제, 한국바이오협회, IMS Health 2009). 특히 항체 기반의 표적지향성 단백질은 치료의 표적을 정확히 조준할 수 있는 능력이 있어 치료의 효율을 증가시킬 것이며 이를 통해 각 국가간 의료비 부담을 줄일 수 있는 계기가 될 것으로 기대됩니다. 또한 기존의 바이오의약품의 특허가 만료되는 2012년을 기점으로 이의 유사 바이오의약품 (바이오시밀러)이 제 3세대 바이오 의약품으로 출시되도록 시장이 재편될 것으로 보이는 점은 많은 것을 시사합니다. 즉, 현재의 의약품 시장은 합성, 제네릭으로는 한계가 있어 성장이 정체되고 성장의 방향은 바이오의약품이지만 이 역시 고가의 치료비 부담이 있습니다. 특허가 만료되고 제네릭 의약품이 출시될 때 그러하듯 저가의 바이오시밀러 의약품에 의해 저렴하면서도 동등한 의료치료를 제공하는 목적으로 초창기 바이오시밀러 연구개발은 무한한 가능성을 제시하였습니다.
이러한 추세에서 최근의 바이오의약품의 개발동향은 바이오시밀러보다는 제 4세대 바이오 의약품이라고도 할 수 있는 바이오베터로 변화하고 있습니다. 후발 단백질 생산업체가 바이오시밀러의 대량생산 자체에 집중하는 반면, 선도 업체들은 여러 가지 화학적인 방법이나 당사슬의 변환, 아미노산 치환 등을 통해 부작용이나 체내 동태를 개선한 동일 단백질 효능 의약품을 개발하기에 이르렀습니다. 이를 개량 바이오의약품, 즉 바이오베터라고 호칭합니다.
|
【바이오 신약, 바이오시밀러, 바이오베터의 개발소요기간, 소용비용, 성공률】 |
|
구 분 |
타겟선정 |
비임상 |
임상시험 |
제품승인 |
|||
|
Ⅰ상 1년 |
Ⅱ상 |
Ⅲ상 |
|||||
|
소요기간 |
바이오신약 |
2년 |
2년 |
5년 |
1년 |
||
|
바이오시밀러 |
0.5~1년 |
1년 |
1~1.5년 |
1년 |
|||
|
펩타이드 의약품 |
0.5년 |
1년 |
5년 |
1년 |
|||
|
바이오베터 |
0.5년 |
1년 |
2.5년 |
1년 |
|||
|
소요비용 |
바이오신약 |
US$ 50M |
US$ 30M |
US$ 120M |
US$0.1M |
||
|
바이오시밀러 |
US$ 1M |
US$ 5M |
US$ 14M |
US$0.1M |
|||
|
펩타이드 의약품 |
US$ 10M |
US$ 3M |
US$ 15M |
US$0.1M |
|||
|
바이오베터 |
US$ 0.5M |
US$ 2M |
US$ 10M |
US$0.1M |
|||
|
성공률 |
바이오신약 |
30% |
〉80% |
30% |
평균 8% |
||
|
바이오시밀러 |
100% |
90% |
80% |
평균 80% |
|||
|
펩타이드 의약품 |
100% |
90% |
80% |
평균 80% |
|||
|
바이오베터 |
100% |
90% |
80% |
평균 80% |
|||
자료: 전국경제인 연합회, 바이오의약산업 현황과 개선과제, 2009.12
원래 펩타이드 의약품은 기존에 사용되고 있는 바이오의약품 중 단백질의약품의 한 종류로 존재하였습니다. 그러나 펩타이드를 바이오베터 (개량 바이오신약)의 관점에서 개발하게 된다면, 기존의 분자량이 큰 단백질의약품의 전체구조 중 활성을 내는데 가장 필수적인 부분만을 찾아 그 자체를 의약품으로 개발하게 되면 바이오베터가 될 수 있습니다. 또한 그 자체를 기존의 투여방식인 주사제 방식을 탈피한 새로운 투여방식에 의한 제제 역시 신약으로 간주됩니다.
전신작용을 요하는 호르몬 펩타이드 제제는 기존제형은 주사제이나, 경구투여, 피부투여, 비강 및 기도 투여에 의해 전신으로 빨리 도달시키는 방법으로 개발 가능합니다. 위의 방법으로 개발된 펩타이드는 그 자체로 펩타이드 기반 바이오베터이며, 이는 넓은 범위에서 단백질의약품 영역에서 사용될 수 있다는 것을 뜻합니다.
③ 펩타이드 기반 의약 바이오 소재 산업
펩타이드 기반 의약 바이오 소재는 기존의 조직 재생용 바이오소재나 의료기기에 펩타이드를 적용하여 조직재생의 효과를 증진시키는 것이 목적입니다. 초기 단계의 바이오소재는 순수한 원료에 의해 생체적합성이 극대화된 상태이며 이로서 현재까지도 조직 재생 시술에 활용되고 있습니다. 그러나 과거와 달리 질환의 원인이 다양하고, 여러 원인에 의한 복잡한 조직 결손부의 재건에는 기존의 생체적합성만으로는 효과를 장담하기 어렵습니다. 또한 정밀의료 시대에 환자의 생체내 환경이 다양하기 때문에 유전자적, 체내 단백환경을 조절하면서 조직재생효율을 극대화하기란 바이오소재 자체만으로는 어렵고, 생체활성물질의 관여가 필요한 상황입니다. 이러한 상황에서1990년대 초 골형성 단백질(Bone Morphogenetic Protein, BMP)이 유전자 재조합으로 제네틱 인스티튜트(Genetic Institute)의 우즈니(Woozney) 박사 그룹에 의해 생산되어 치과, 정형외과를 포함하는 인퓨즈(INFUSE)라는 제품으로 뼈형성 시술에 적용되면서 생리활성물질, 단백질, 펩타이드의 바이오소재로의 적용이 도입되기 시작했습니다. 이후 유사한 골형성 단백질로 이루어진OP-1, 치아 단백질이 첨가된 주입형 의료기기(엠도게인, Emdogain), 혈소판 유래 성장인자가 함유된 골재생재료(젬21에스, GEM21S)입니다. 또한 펩타이드의 중요성이 부각되면서2004년도에 펩타이드가 골재생 재료에 적용된 바이오소재로 펩젠P-15 (PepGen P-15)이 출시되어 임상에서의 활용성이 증대되고 있는 상황입니다. 그러나 해당 산업은 잠재성에 비해 아직 기술이 완성되지 않은 상황으로 활성 펩타이드 도출력, 바이오소재와의 성공적인 결합기법 완성 등의 최적의 기술적인 요건을 도출해내는 기업이나 연구소가 시장을 선점할 수 있는 가능성이 높습니다.
(나) 조직재생용 바이오소재 산업
조직재생용 바이오 소재는 1930년대 비세글리(Bisceglie)에 의해 고분자 합성 막 (필름)위에 생쥐환부의 종양세포를 붙여 돼지 복강내에 이식하고 관찰한 결과 이식된 종양세포가 돼지 체내에서도 살아있음을 확인하게 되었습니다. 이후 체외에서 작업한 생체조직을 다시 이식하는 연구가 시작되어 현재의 조직재생치료의 시작이 되었습니다. 이를 바탕으로 1970년대와 1980년대에 걸쳐 당뇨병 치료에 있어 인슐린을 지속적으로 주사하는 것 보다는 인슐린을 생성하는 췌장소도(pancreatic islet)를 고분자 필름으로 만들어진 캡슐에 넣어서 당뇨병 동물에 이식한 결과 이식 동물의 혈당이조절되는 것을 확인하여 본격적으로 생체에 친화성을 가지면서 세포의 이식이나 조직을 대체할 수 있는 기능성을 지니는 소재를 개발하기 시작했습니다. 이러한 생체 친화성 소재는 초기에 생체조직을 이식하다가 친화성이 있으면서 생체 내에서 흡수되지 않는 고어텍스와 같은 소재를 사용하였고, 이후에는 흡수성 소재, 그리고 더 나아가 천연 소재 가공기술에 의한 흡수성 소재로 개발 변천이 이루어지고 있습니다. 1970년대 후반을 거쳐 1980년대 들어서면서 피부 재생에 관심을 갖던 과학자들이 체내에서 가장 많이 존재하며 피부를 구성하는 주요 성분인 콜라겐 막위에 피부 재생 세포를 깔아 함께 배양시키거나 콜라겐-글리코사미노글리켄 (GAG)복합재 (Collagen-GAG composites)위에 세포를 얹는 방식으로 조직 재건 시술 빈도 1위 시술인 화상 등에 의한 손상부위 재생에 위 기술을 응용하였습니다. 이어 골조직 결손부의 재건을 위한 시술이 2위 다빈도 시술로 자리하였는데 이를 위한 바이오 소재는 초기에는 인체의 뼈를 기증받아 이식하거나 합성물로 미네랄을 제조하여 이식하는 방법을 사용하였습니다. 이종골의 뼈를 가공하는 기술은 초기에는 면역원의 문제로 사용이 제한되다가 최근에는 다양한 가공조건의 개발로 시장에서 최대 점유율을 보이고 있습니다. 이와 함께 트리칼슘인산과 같은 합성 미네랄 역시 다양한 공정기법으로 시장에 진출하고 있습니다. 뼈의 재생에도 피부의 재생과 마찬가지로 조직 재생용 쉬트가 이용되는데 이는 뼈가 생성되어 공간을 차오르는 동안 공간을 확보하기 위해 덮어주는 용도로 필수적이기 때문입니다. 이러한 시술은 1980년대 고어텍스라는 비흡수성 소재로 만들어 활용되다 흡수성 소재인 합성 고분자, 그리고 현재는 순수 콜라겐 기반으로 한 천연 고분자 쉬트가 이러한 목적으로 사용되고 있습니다. 이러한 고분자 쉬트는 치주조직 재생유도 차폐막이라고 불리고 있습니다.
상기와 같이 조직의 재생이나 기능을 복원하는데 사용되는 바이오소재는 조직 공학을 기반으로 한 조직 재생치료에 있어 핵심적인 개념으로 자리잡았는데 이는 1990년대 미국 하버드의대의 조셉 바칸티(Joseph Vacanti)와 미국 MIT 화학공학과의 로버트 랑거(Robert Langer)가 시초라고 할 수 있습니다. 그 이후로, 기술적, 학문적 필요성에 따라 많은 연구를 진행함으로써 연구 성과와 네트워크 발전이 거듭되어 지고 있습니다. 이후 생체조직을 재생하려는 재생의학 개념을 더하여 오늘의 바이오 엔지니어링 분야로 많은 주목을 받고 있고 흔히 ‘세포 치료(cell therapy)’와 “단백질,유전자 치료”라고 하는 용어도 등장하기 시작했습니다. 질병과 사고의 증가와 함께 고령화시대에 삶의 질 향상을 위해 병들거나 훼손된 조직이나 장기를 복원하려는 재생의학의 중요성 및 필요성이 커지면서 미래 산업으로서의 조직재생용 바이오소재의시장성과 경제성이 전 세계적으로 부각되고 있습니다.
(다) 구강보건산업
구강보건의 영역은 치약, 치아미백제 및 가글제품을 포함하는 구강 청정제품 영역과 시린치아 관리, 잇몸질환을 치료하거나 관리하는 구강질환 치료의약품/관리 제품 영역으로 나눌 수 있습니다.
치약으로 통일되었던 구강 청정제품의 시장에서 다양한 욕구를 지니는 소비자 계층에 의해 하얀 치아 및 구취제거를 치약보다 전문적인 제품으로 관리하고자 하는 수요가 증대하면서 치아미백제 및 구강청정제의 시장진출이 시작되었습니다. 초기 시장은 대형 치약 제조사가 주도하였지만, 다양한 소비자의 반응에 능동적으로 대처할 만한 전문지식이 없는 상태에서 해당 제조사의 치아미백제 판매는 한계가 있었습니다. 즉, 수 십년 동안 치과에서 소독제로 사용되거나 치과 전문 미백 시술에서 입증된 효력을 지니는 과산화수소수 및 과산화수소수를 방출하는 물질 (카바마이드 퍼옥사이드)이라는 성분으로 치아를 미백시킬 수 있다는 단순한 논리로서 치약제조사가 치아미백제를 제조하였습니다. 그러나 치아 미백을 원하는 소비자 계층의 눈높이에 맞추기 위해 요구되는 전문성에는 한계가 있었습니다. 따라서 치아미백 전문가인 치과의사 집단에서의 검증된, 그리고 추천이 기반이 되는 치아미백제 및 기타 구강 청정제가 호응을 받으면서 구강 보건제품은 단순히 대형 제조사가 주도하는 시장이 아닌, 치과 진료 등의 전문성이 바탕이 되어 추천되는 제품으로 시장의 주도권이 바뀌는 양상을 보이고 있습니다. 구강질환 치료 및 관리 제품으로는 치주질환 치료제, 시린이 치료제 및 치과용 컨디셔너가 있습니다. 풍치라고 흔히 알려져 있는 치주질환은 충치와 함께 구강 질환의 대표적인 질환으로 자리 잡고 있습니다. 초기 치주질환은 단순히 치주염을 유발하는 세균에 의한 국소적인 질환이라고 인식하고 치과에서 잇몸내 세균막을 기계적으로 제거하고 항생제 처방 등의 치료를 주로 하였으나, 최근 치주질환을 포함하는구강질환과 고혈압, 관절염, 면역질환 및 조산 등을 포함하는 전신 질환과의 상호 연관관계가 지속적으로 보고 (자료: 치주질환과 전신질환, 월간의약정보, 2008.8) 되면서 치주질환 치료에 대한 관심이 증대하고 있어 이에 따라 치료제 개발이 활발한 상황입니다.
풍치와 함께 시린이는 우리나라 성인 7명중 1명꼴로 나타나는 질환으로 이가 시린 것은 여러 구강질환의 전조 증상입니다. 그러나 다빈도 증상으로 많은 소비자들이 필요로하지만 다양한 제품이 나오지 못한 이유는 치아미백제와 같이 치약에 의존하던 초기시장의 성격과, 이러한 제품 역시 전문가 집단에 의한 추천에 의해 성장하는 시장 성격 때문입니다.
(2) 산업의 특성
당사의 당해산업은 사업군의 특징상 공통적으로 평균10%의 높은 연평균 성장률을 보이는 고도의 성장산업이고, 국민의 보건의료 및 삶의 질 향상에 직접적으로 기여하는 산업이라고 할 수 있습니다. 또한 앞서 산업의 성장과정에서 기술한 바대로 하이테크놀로지가 추가되면서 약학, 화학, 생물학, 고분자학, 생화학, 의학, 치의학 및 나노테크놀로지를 기반으로 하는 다학제간 유기적인 네트웍이 필수적이고 기술의 파급력이 큰 첨단산업이라 할 수 있습니다. 이하 세부적인 특성을 다시 기술하였습니다.
(가) 펩타이드 의약품 및 의약 바이오 소재 산업
① 펩타이드 의약품 및 펩타이드 기반 바이오베터 산업
당사의 주력업종인 펩타이드 의약품 사업의 경우 시장 진입의 난이도는 일반화학 의약품과 크게 다르지 않지만 상대적으로 짧은 개발기간 및 높은 성공률에 따라 일반 화학의약품 대비 더 높은 부가가치를 창출할 수 있습니다. 하지만 다른 산업군에 비하면 장기간의 기술 개발과 대규모 개발자금이 병행되어야 하는 시장진입장벽이 있습니다. 바이오산업 전 분야가 그렇듯이 펩타이드 의약품 및 펩타이드 기반 바이오베터는 바이오 의약품으로서 기존 저분자 약물의 시장을 대체할 수 있는 고부가가치를 창출하는 첨단산업 중 하나입니다. 하나의 치료제 또는 바이오베터가 개발되어 세계 시장에서 인정받으면 투자비용의 수백-수천 배의 부가가치를 창출할 수 있습니다. 또한, 제품의 치료효과를 일단 인정받게 되면 의사들로부터 고부가가치 창출 능력을 상당기간 보장 받을 수 있습니다. 현재 정부차원에서 집중 육성되는 바이오 신약, 장기 등 신성장동력분야는 미래 신성장을 이끌 BT산업의 핵심 분야로서 고부가가치를 창출할 수 있는 미래지향적 분야입니다.세계 각 기관의 바이오의약품 시장 보고서에 따르면, 시장규모는 각기 다르게 보고되어 있더라도, 바이오의약품이 의약품 영역 내에서 가장 큰 연평균 성장률을 보이고 있습니다. 글로벌의약품 전문조사기관인 IMS Health에 따르면 파머징마켓으로 통칭되는 7개 국가 (러시아, 한국, 중국, 인도, 멕시코, 터키, 브라질) 의약품시장의 연평균 성장률은 7.5%로 예상됩니다. 선진국시장인 미국, 유럽, 일본 등의 의약품시장 연평균 성장률은 1~2%에불과할 것으로 전망됩니다.
펩타이드 의약품 및 펩타이드 기반 바이오베터를 개발하기 위해서는 의학, 약학, 생명공학 등의 다학제간의 유기적 협조가 필요합니다. 펩타이드 의약품 및 펩타이드 기반 바이오베터는 의약품 원료자체로 조달할 수 있을 뿐만 아니라 의료기기, 기능성화장품 등으로 응용범위를 넓힐 수 있습니다. 이는 기존제품의 성능을 더 업그레이드하여 더 높은 수익을 창출할 수 있는 제품으로 개발할 수 있습니다.
② 펩타이드 기반 의약 바이오 소재 산업
펩타이드 기반 의약 바이오 소재는 조직재생용 바이오소재 산업의 특성과 유사한 국민의 보건의료 및 삶의 질 향상에 직접적으로 기여하는 산업입니다. 조직재생에 효과적인 펩타이드가 포함되어 있어 일반 바이오소재보다 성능이 우수합니다. 따라서 펩타이드 기반 의약 바이오 소재는 일반 바이오소재를 사용하여 재생될 수 없는 심한 조직손상 환자를 치료하기 위해 사용될 제품입니다. 이러한 과정은 단일 소재의 개발만으로는 이룰 수 없고, 재료공학, 고분자공학, 화학공학, 의학, 약학, 생명공학 등의 다학제간의 유기적 협조가 필요합니다. 또한 이러한 기술로 바이오 소재 개발뿐 아니라 의약품의 개발까지도 촉진할 수 있어 기술의 파급력이 높은 산업군입니다.
(나) 조직재생용 바이오소재산업
조직재생용 바이오소재산업은 국민의 보건의료 및 삶의 질 향상에 직접적으로 기여하는 산업입니다. 특히 고령화사회 진입에 따른 조직손상환자, 퇴행성 골격조직 질환및 기능부전성 질환의 비율이 점점 높아져 이들 질환에 대한 의료비 부담이 증대되어이들과 관련한 의료기술 및 치료제에 대한 요구가 증대하고 있는 추세입니다. 노인 인구의 증가로 인해 염증, 근골격조직 손상환자 및 퇴행성 관절질환 환자의 급증으로국내의 이들 질환에 대한 의료비의 부담이 증대되고 있어, 만성염증 및 손상된 조직을 재생을 할 수 있는 기술의 필요성이 증가하고 있습니다.
(다) 구강보건산업
구강보건 산업은 보건산업분야 중에서 빠른 수익성을 창출할 수 있는 가능성이 높은 분야라는 특징을 가지고 있습니다. 특히 현대사회에서는 미 (美)에 대한 욕구의 한 종류로 치아미백에 대한 관심이 점점 증가하고 있습니다. 치과에서 받는 치아 미백술은그 효과가 개인용 치아미백제보다 크기는 하지만 가격이 매우 고가입니다. 일부 개인치과병원에서는 무허가 제품을 사용하기 때문에 전문성을 겸비한 경제적인 제품군에의해 시장이 커질 것으로 전망됩니다. 또한 임플란트 시술빈도가 커짐에 따라 시술후구강관리를 받는 비율도 높아져 (시술인구의 15% 이상) 사용의 증가가 기대됩니다. 또한 고령화 사회로 인한 노인인구의 증가에 따라 시린이, 치주염과 같은 구강질환자가 증가하고 있는 추세입니다. 따라서 구강보건 산업은 지속적인 성장을 보이고 있습니다.
(3) 산업의 성장성
(1) 펩타이드 의약품 및 의약 바이오소재 산업
(가) 펩타이드 의약품 및 펩타이드 기반 바이오베터
전 세계 바이오 개량신약 시장은 빠른 속도로 그 시장을 확대해 나갈 전망입니다.
① 바이오의약품 시장 규모
Biophoenix limited사의 시장보고서에 따르면 바이오의약품 (단백질의약품, 항체의약품, 백신 등) 세계시장은 2018년 3,688억 달러에서 2030년까지 연평균성장률 12.8%로성장하여 2023년 15,650억 달러에 이를 전망입니다.
<바이오의약품 세계시장 규모>
(단위 : 억달러)
|
년도 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
세계시장 |
3,688 |
4,693 |
5.971 |
7.597 |
9.667 |
12.299 |
15.650 |
12.8 |
자료 : Biosimilars and Biobetters: Positioning for a New marke, Biophoenix Limited, 2009
CAGR 근거 년도 : 2018-2030: 12.8%, 2023년까지 12.8%의 CAGR을 적용
펩타이드 의약품 시장은 전 세계적으로 2018년 272.8억 달러에서 2030년까지 연평균성장률 8.9%로 성장하여 2030년 759.2억 달러에 이를 전망입니다.
<펩타이드 의약품 세계시장 규모>
(단위 :억달러)
|
년도 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
세계시장 |
272.8 |
323.6 |
383.8 |
455.2 |
539.8 |
640.1 |
759.2 |
8.9 |
자료 : Biosimilars and Biobetters: Positioning for a New market, Biophoenix Limited, 2009
CAGR 근거 년도 : 2018-2030: 8.9%, 2023년까지 8.9%의 CAGR을 적용
이중에서도 당사의 펩타이드 치료제는 골다공증, 관절염, 비알코올성 간질환, 염증성 대장질환, 항암 (암줄기세포타겟) 을 표적으로 하는데 이의 성장성은 다음과 같습니다.
① 골다공증 치료제 시장
Global Data사에 따르면 골다공증 치료제 세계시장은 8.2%의 연평균 성장률을 보이며 2023년 289억 달러를 전망하였습니다.
Global Data사에 의하면, 골다공증의 시장 증가의 주요 요인은 첫째, 폐경기 이후 여성들의 호르몬 대체 치료법(Hormone Replacement Therapy, HRT) 사용의 감소로 인한 것으로 발표하였습니다. HRT 사용으로 인해 심장마비, 유방암, 발작, 혈전의 증가할 위험이 있다고 보고가 있습니다. HRT 사용 인구의 감소 요인이 복합적으로 작용하여 골다공증 시장이 성장하고 있다고 예상하였습니다.
둘째, 여성위주의 치료 시장에서 남성의 비율이 증가하고 있기 때문입니다. WHO에서 중년의 남성들에게 골다공증 검사에 대하여 인지를 위한 새로운 방침을 발표하였습니다. 따라서 남성들의 골다공증에 대한 인식을 위한 새로운 방침이 골다공증 환자로 진단되는 수의 증가로 이어질 것이며, 골다공증 치료제 시장의 증가로 이어질 것입니다.
마지막으로 선진국인의 라이프스타일이 골다공증 환자를 증가시키는 원인이 되고 있습니다. 고단백질 식품 섭취로 소변으로 칼슘 분비가 증가하고 이로 인해 골절로 인한 위험이 증가하는 것과 관련이 있다고 발표하였습니다.
<골다공증 치료제 세계시장 규모>
(단위 : 억달러)
|
년도 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
세계시장 |
195 |
228 |
267 |
313 |
366 |
428 |
502 |
8.2 |
자료 : Osteoporosis-Pipeline Assessment & Market Forecast to 2017, Global Data,2010
CAGR 근거 년도 : 2018-2030년: 8.2%
② 관절염 치료제 시장
BI Research의 보고서에 따르면 골관절염 치료제의 세계시장 규모는 연평균 성장률 2%로 성장하여 2030년 71억 달러로 예상하였습니다. 골관절염 치료제 시장은 주요 치료제의 특허 만료로 인해 시장규모의 성장이 크지 않을 것으로 보입니다. 이유는 주요 치료제인 볼타렌 (Voltaren) 및 셀레브렉스 (Celebrex)가 2013년과 2014년에 특허가 만료되고 제네릭 치료제로 개발되고 있으며, 처방전 환자들의 감소, 신체 운동과 물리 치료와 같은 대체치료의 선택이 가능해졌기 때문입니다.
류마티스 관절염 치료제 세계시장은 GBI Research의 보고서에 따르면 시장규모는 연평균 성장률 8.6%로 성장하여 2030년에 724억 달러일 것으로 예상하였습니다. 류마티스 관절염 치료제 시장의 성장요인은 류마티스 관절염의 발생율과 유병율이 증가하기 때문입니다. 또한 최첨단 진단기술의 발전으로 류마티스 관절염의 초기 발견이 가능해지면서 이 시장의 규모가 성장할 것으로 예상하였습니다.
<관절염 치료제 세계시장 규모>
(단위 : 억달러)
|
년도 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
골관절염 세계시장 |
57 |
59 |
61 |
63 |
66 |
68 |
71 |
2 |
|
류마티스 관절염 |
269 |
317 |
374 |
441 |
520 |
614 |
724 |
8.6 |
|
합계 |
326 |
376 |
435 |
504 |
586 |
682 |
795 |
7.7 |
자료 : Arthritis Therapeutics Market to 2016, GBI Research, 2010
CAGR 근거 년도: 골관절염 치료제 2018-20303년: 2%
류마티스 관절염 치료제 2018-20303년: 8.6%
관절염 치료제 2018-2030년: 7.7 %
③ 비알코올성 간질환 치료제
Allied Market research에 따르면, 비알코올성 간질환 치료제의 세계시장은 2023년 3.2 천만달러의 규모로 예상되고 있습니다. 비알코올성 간질환은 음주와 관계없이 비만, 지질대사이상으로 인해 간세포에 지방이 축적되어 생기는 질환으로, 지방간(steatosis), 비알코올성 지방간염(NASH, non-alcoholic steatohepatitis)에 이르는 다양한 스펙트럼을 포함합니다. 비만, 인슐린 내성 등 대사증후군과 밀접하게 연관이 되어 있어, 정확한 병기기전과 치료방법이 알려져 있지 않고, 현재까지 FDA에서 승인된 약물이 없습니다.
<비알코올성 간질환 치료제 세계시장 규모>
(단위 : 억달러)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
세계시장 |
0.100 |
0.160 |
0.25 |
0.394 |
0.622 |
0.981 |
1,548 |
25.6 |
자료 : Allied Market research, NASH market, 2018-2030
CAGR 근거 년도 : 2018-2030년: 25.6%
④ 염증성 장질환 치료제
비전게인에 따르면, 염증성 장질환 치료제의 세계시장은 2023년에 7.6천만달러의 규모로 예상되고 있습니다. 현재 주로 사용되는 약물은 amino-salicylate, corticosteroid, 항생제 등이 사용되고 있으나, 증상만 완하시키는 작용을 합니다. 염증성 장질환 치료제로 사용하는 생물학적 제제로서 TNF-a 차단제가 있으나, 염증억제 효과는 있지만, 손상된 장점막을 재생하는 작용은 없기 때문에, 재생에 효과가 있는 약물의 개발이 필요한 상황입니다.
<염증성 장질환 치료제 세계시장 규모>
(단위 : 억달러)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
세계시장 |
0.67 |
0.71 |
0.74 |
0.777 |
0.816 |
0.858 |
0.902 |
2.5 |
자료 : Vision gain, Global Inflammatory Bowel Disease drug Market Forecast 2018-2030
CAGR 근거 년도 : 2018-2030년: 2.5%
⑤ 항암 치료제
퍼시스턴스 마켓리서치에 따르면 글로벌 항암제 시장이 2018~2030년 기간 동안 연평균 7.4%에 달하는 빠른 추세로 확대될 것이라는 예측이 나왔으며, 2018년 1,290억 달러 규모에서 2030년에는 3,038억달러에 도달할 수 있으리라 예상하였습니다. 현재 항암제 연구가 가장 활발하게 진행되고 있는 영역은 면역 항암제로 나타났습니다.
<항암 치료제 세계시장 규모>
(단위 : 억달러)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
세계시장 |
1290 |
1487 |
1716 |
1979 |
2284 |
2634 |
3038 |
7.4 |
자료: Persistence market research, 항암제 글로벌 마켓
CAGR 근거 년도 : 2018-2030년: 7.4%
(나) 펩타이드 기반 의약 바이오 소재
① 치과용 융합바이오소재 (골이식재) 시장규모
펩타이드 기반 치과용 융합 바이오소재 (골이식재)는 조직재생용 바이오소재를 사용했을 때, 충분한 치조골 재생효과를 볼 수 없는 외상이 심한 환자, 치조골 흡수로 조직재생능이 떨어져 있는 고령자에 사용될 예정입니다. 치과용 융합바이오소재 (골이식재)로 현재 상품화 된 것은 스트라우만 (Straumann)사의 엠도게인 (Emdogain) 과 오스테오헬스 (Osteohealth) 사의 GEM21S가 주로 치과용으로 사용되는 제품입니다. 이러한 제품은 단독으로 젤 형태로 시술에 사용되거나 다른 골이식재와 같이 사용하기도 합니다. 융합바이오소재(골이식재)가 본격적으로 시장에 매출을 발생하기 시작한 시기는 2007-2008년 이후로 이후 성장률이 급격히 증가하고 있습니다. 또한 앞으로도 이러한 융합바이오소재(골이식재)의 효과에 대한 인식이 증대되고 있고 시술하는 의사들의 교육을 통하여 시술의 횟수가 증가 할 것으로 예상됩니다.
<치과용 융합바이오소재 (골이식재)의 세계시장 규모>
(단위: 억달러)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
세계시장 |
1.003 |
1.327 |
2.320 |
3.069 |
4.059 |
5.368 |
7.099 |
15 |
자료: US markets for dental biomaterials, Millennium research group, 2010
2019년 치과용 골이식재의 세계시장 규모는 치과용 골이식재 국내시장 규모의 11배로 계상하여 2018년 치과용 융합바이오소재(골이식재)의 국내시장 규모를 79억 원으로 추정하였습니다. 이후 세계시장은 연평균 성장률 15%를 적용하여 2030년에는 424억달러가 될 것으로 예상됩니다.
<치과용 융합바이오소재 (골이식재)의 국내시장 규모>
(단위: 억원)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
국내시장 |
79.35 |
104.94 |
138.78 |
183.54 |
242.73 |
321.01 |
424.53 |
15 |
자료 : US markets for dental biomaterials, Millennium research group, 2010
근거 : 미국시장 규모에서 세계시장의 규모를 추정하기 위하여 치과용 골이식재의 세계시장/국내시장 비율을 근거로 추정하였음.
② 정형외과용 의약 바이오 소재 (골이식재) 시장규모
정형외과용 융합바이오소재(골이식재)는 대부분 BMP류를 포함하는 골재생의 효과를 높인 제품군입니다. 2018년~2030년에는 25%의 연평균 성장률을 나타낼 것으로 예상됩니다.
<정형외과용 융합바이오소재 (골이식재) 세계시장 규모>
(단위: 억달러)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
세계시장 |
59.40 |
75.18 |
117.47 |
183.54 |
286.79 |
448.11 |
700.17 |
25 |
자료 : Orthopedic biomaterials: World market, A Kalorama Information Market Intelligence Report, 2007
CAGR 근거 년도 : 2018-2030년까지 25%의 CAGR을 적용하여 추정하였음.
국내시장의 경우 Medtronic사의 INFUSE는 수입이 허가되어 있지 않으며, 대부분 정형외과 골이식재로는 수입제품인 합성골과 미네랄을 제거한 사람뼈를 주로 사용되고있습니다. 대웅제약의 합성골 이식재와 BMP-2를 융합한 노보시스가 있습니다.
2019년 정형외과용 골이식재의 세계시장 규모는 치과용 골이식재 국내시장 규모의 11배로 계상하여 2018년 정형외과용 융합바이오소재(골이식재)의 국내시장 규모를 539억 원으로 추정하였습니다. 이후 세계시장은 연평균 성장률 12.5%를 적용하여 2030년에는 2214억원이 될 것으로 예상됩니다.
<정형외과용 융합바이오소재 (골이식재)의 국내시장 규모>
(단위: 억원)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
국내시장 |
539 |
682 |
863 |
1092 |
1382 |
1749 |
2214 |
12.5 |
자료 : Orthopedic biomaterials: World market, A Kalorama Information Market Intelligence Report, 2007
CAGR 근거 년도 : 2018-2030년까지 12.5%의 CAGR을 적용하여 추정하였음.
(2) 조직재생용 바이오소재
현재 당사에서는 치과용 골이식재와 치과용 조직재생용 쉬트를 판매하고 있고 이는 정형외과용으로 적용부위를 넓혀서 허가를 거쳐 판매 할 예정입니다.
(가) 치과용 골이식재
치과용 골이식재의 적용을 보면 치조골 결손 시 결손부를 채우거나 잇몸조직의 재생을 막는 목적으로 사용합니다. 또한, 임플란트 시술 시 충분한 양을 골조직을 확보하거나 임플란트의 주변조직과의 결합력을 높이기 위하여 사용되기도 합니다. 치과용 골이식재 시술 예를 보면 치과용 임플란트 시술의 급격한 증가로 인하여 임플란트 시술에 사용되는 골이식재의 수요도 증가하는 것을 알 수 있습니다.
US markets for dental biomaterials등에서의 통계 예측치 보면 치과용 임플란트 시술시 골이식재의 사용이 년 10% 이상 증가 할 것으로 예상됩니다. 기존에는 치과 의사들 중에 골이식재의 사용으로 인한 전염 및 감염을 걱정하는 경우가 있었으나 이식재의 질적 향상 및 시술 기술의 향상으로 이러한 위험이 많이 감소하였습니다. 또한 시술 과정의 발전 및 새로운 임상 적용 기술 개발로 임플란트 시술에서 치과용 골이식재 소재의 사용이 증가할 것으로 예상됩니다.
치과용 골이식재의 세계시장 규모를 보면 다음과 같습니다.
<치과용 골이식재 세계시장 규모>
(단위: 억달러)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
세계시장 |
5.4 |
6.9 |
8.8 |
11.2 |
14.2 |
17.9 |
22.9 |
12.7 |
자료 : Implant-Based Dental Reconstruction: The Worldwide Dental Implant and Bone Graft Market, 2nd Edition, Kalorama Information, 2007
CAGR 근거 년도 : 2018-2030: 12.7%, 2023년까지 12.7%의 CAGR을 적용 .
Millennium Research Group, 2008년 아시아 치과용 바이오소재 보고서에 의하면 치과용 골이식재의 국내시장은 2008년에 186억 원을 차지하였으며, 연 15.6%의 성장을 예측하고 있습니다. 2018년에는594억 원의 시장으로 성장할 전망입니다.
<치과용 골이식재 국내시장 규모>
(단위: 억원)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
국내시장 |
792 |
1059 |
1415 |
1889 |
2524 |
3373 |
4507 |
15.6 |
자료 : Asia pacific markets for dental biomaterials, Millennium Research Group, 2008
CAGR 년도 : 2018-2030년 : 15.6%, 2030년까지 15.6%의 CAGR을 적용
(나) 치주조직재생용 쉬트
치주조직재생용 쉬트는 골이식재와 함께 사용하기도 하고 단독으로 차단막 역할로 사용되기도 합니다. 치주조직재생용 쉬트 시장은 골이식재 사용의 증가 및 임플란트 시장의 성장과 함께 시장의 확대가 예상됩니다.
<치주조직재생용 쉬트의 세계시장 규모>
(단위: 억달러)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
세계시장 |
1.671 |
1,884 |
2.125 |
2.397 |
2.703 |
3.049 |
3.439 |
6.2 |
자료 : US markets for dental biomaterials, Millennium research group, 2010
CAGR 년도 : 2018~2030년 : 6.2% CAGR을 적용
Millennium Research Group에 의하면 치주조직재생용 쉬트의 국내시장의 경우 2018년부터 2030년까지 연평균 성장률 11.5%로 2030년 624억 원의 시장을 예상하고 있습니다. 미국과 같은 선진국에서는 치과용 조직재생용 쉬트가 일찍부터 사용되었으며, 이미 많은 제품이 시장에 출시되어있어 경쟁체제를 보입니다. 국내시장의 경우 현재 성장 중인 시장으로 신제품이 계속 출시되고 있어 골이식재와 유사한 정도의 성장성을 보이고 있는 것을 알 수 있습니다.
<치주조직재생용 쉬트의 국내시장 규모>
(단위: 억원)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
국내시장 |
169 |
210 |
261 |
324 |
403 |
501 |
624 |
11.5 |
자료 : Asia pacific markets for dental biomaterials, Millennium Research Group, 2008
CAGR 근거 년도 : 2018-2030: 11.5%, 2030년까지 11.5%의 CAGR을 적용
(3) 구강보건 제품
전 세계 구강보건 제품시장은 전반적으로 제품의 질을 중요시하는 경향으로 성장하고 있습니다. 당사에서 목표로 하고 있는 구강보건 제품에는 치아미백제, 시린이치료제, 치과용 컨디셔너 및 치주질환 치료제가 있습니다.
(가) 치아미백제
개인용 치아미백제 세계시장 규모를 추정하기 위해 다음과 같은 가정을 하였습니다. 의약품 세계시장 점유율을 살펴보았을 때, 미국이 차지하는 비중은 세계시장의 약 44.7%로 가장 큰 시장을 형성하고 있습니다 (자료: 세계바이오 의약산업, 2011, 생명공학정책연구센터).
미국의 개인용 치아미백시장이 세계시장의 44.7%를 차지하고 있다는 가정하에, 개인용 치아미백제의 2009년 세계시장 규모는 7.5억 달러로 추정하였습니다. 미국의 2009년부터 2014년 사이 연평균 성장률 0.2%를 세계시장의 연평균 성장률에 적용하였습니다.
전문가용 치아미백제 세계시장 규모에 대한 시장조사자료가 존재하지 아니하여, 당사는 다음의 가정을 바탕으로 해당시장의 규모를 추정하였습니다. 국내 치아미백시장의 경우, 전문가에 의한 미백시술이 개인용에 비해 약 3배 높은 수준을 보이고 있으나, 미국 등의해외에서는 개인용 치아미백이 일상화 되어있는 점을 고려하여 보수적으로 전문가용 치아미백제 시장규모가 개인용 치아미백제 시장규모와 동일한 수준의 규모와 성장률을 보인다고 가정하였습니다.
<치아미백제의 세계시장 규모>
(단위;억달러)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
개인용 |
7.31 |
7.34 |
7.37 |
7.38 |
7.42 |
7.44 |
7,47 |
0.2 |
|
전문가용 |
7.41 |
7.44 |
7.47 |
7.48 |
7.51 |
7.54 |
7.57 |
0.2 |
|
세계시장 |
14.83 |
14.89 |
14.95 |
14.86 |
14.93 |
14.98 |
15.04 |
0.2 |
자료 : Oral Care in US, Euromonitor International, 2010
CAGR: 2018-2030: 0.2%의 CAGR을 적용
산출방법: 개인용 치아미백제 미국시장/0.447=개인용 치아미백제 세계시장
전문가용 치아미백제 세계시장은 개인용 치아미백제 세계시장과 동일하게 산정
국내 치아미백제 시장은 2000년대 들어 형성되기 시작하였습니다. 그 후로부터, 우리나라의 경우 치아미백에 대한 여성들의 욕구가 증가하면서 여성들을 타겟으로 하는 치아미백제의 개발이 요구되고 있으며, 우수한 성능의 치아미백제에 대한 국내수요가 증가하고 있습니다.
위의 자료에 따라 2018년도 개인용 치아미백제 734억 원, 전문가용 치아미백제 2205억원에서 생활패턴변화에 따라 더욱 고속 성장이 예상되나, 보수적 연평균 성장률 10%를 적용하여, 2030년까지의 국내시장규모를 예측하였습니다.
<치아미백제 국내시장 규모>
(단위: 억원)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
개인용 |
734 |
899 |
1087 |
1315 |
1591 |
1925 |
2330 |
10 |
|
전문가용 |
2,205 |
2,668 |
3,228 |
3905 |
4726 |
5718 |
6919 |
10 |
|
국내시장 |
2,940 |
3,557 |
4,303 |
5206 |
6300 |
7623 |
9223 |
10 |
자료 : 한국경제 매거진, 2006.9.4
CAGR 근거 년도 : 2018-2030 : 10%
(나) 시린이치료제
당사는 시린이치료제를 일반인용으로 시판할 계획이므로 대체 상품인 시린이치약 시장에 침투하는 전략으로 시린이치약의 규모를 추정하였습니다.
시린이치료제의 세계시장 규모는 일차적으로 미국의 구강청결제 시장규모를 바탕으로 미국이 전세계 의약품 시장에서 차지하는 비중을 고려하여 추정하였습니다. 미국이 차지하는 비율이 전체시장의 약 44.7% 입니다.(자료: 세계바이오 의약산업, 2011 생명공학정책연구센터)
구강청결제 품목별 시장점유율은 치약이 47.3%를 차지해 가장 큰 점유율을 보이고 있으며 이 중 민감성 치아를 위한 치약 (시린이치약)이 차지하는 비율이 11%입니다.
연평균 성장률은 미국의 구강청결제의 성장률인 4.8%로 적용하여 다음과 같이 시장규모를 추정하였습니다. 시린이치약은 성숙단계에 접어들었지만 인구의 고령화로 해당 성장률이 그대로 유지될 것으로 전망됩니다.
<시린이치약의 세계시장 규모>
(단위: 억달러)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
세계시장 |
9.2 |
10.1 |
11.1 |
12.2 |
13.4 |
14.7 |
16.2 |
4.8 |
자료 : 대한무역투자진흥공사, 2006
CAGR 근거 년도 : 2018- 2030: 4.8%, 2030년까지 4.8%의 CAGR을 적용
시린이치료제 국내시장 규모는 아직 보고되어 있지 않으며, 시린이 치료제 관련 제품으로 시장이 완전히 형성되지 않았습니다. 시린이 치료제의 국내시장 규모는 국내 시린이치약의 생산실적과 수입되고 있는 시린이치약의 매출로 추정하였습니다.
시린이치료제 및 시린이치약의 시장이 점점 증가할 것으로 예상되지만, 당사는 시린이치약의 국내시장 연평균 성장률을 세계시장의 연평균 성장률과 동일하게 추정하였습니다.
<시린이 치약의 국내시장 규모>
(단위: 억원)
|
구분 |
2018 |
2020 |
2022 |
2024 |
2026 |
2028 |
2030 |
CAGR(%) |
|
세계시장 |
123 |
135 |
148 |
163 |
178 |
196 |
215 |
4.8 |
자료 : 제약협회 생산실적 보고, 2009, 구강관리용품의 표시 광고 제도에 관한 연구, 문하영
CAGR 근거 년도 : 2016-2023: 4.8%, 2023년까지 4.8%의 CAGR을 적용
(4) 경기변동의 특성
(1) 일반경기변동과의 관계 및 경기변동의 장단 정도
의료산업은 특성상, 경기 흐름과 관계없이 지속적으로 발생하는 환자 수 그리고 그에따른 의약품 및 의료기기의 수요에 의해 경기변동의 영향을 크게 받지 않는 업종입니다. 바이오 신약이나 조직재생재료 등의 제품은 다른 공산품과 비교 했을 때 상대적으로 경기변동과 큰 상관관계가 없는 것으로 나타나 있습니다. 이는 사치재나 대체재가 아니라는 제품의 특성 때문인데 특히 질병 치료를 위한 전문 재료나 신약 매출의 경우 경기 변동이나 계절 요인에 거의 영향을 받지 않습니다. 또한 고령화 시대로 접어들어 조직과 장기의 질환이 증가할 예상이므로 조직재생용 바이오소재, 구강보건제품, 펩타이드 치료제 및 펩타이드 기반 바이오베터의 수요가 계속 증가할 전망입니다. 실제로 전 세계가 경제적 어려움이 있었던 2008년도 글로벌 금융 위기에도 의료산업은 상대적으로 영향을 덜 받은 것으로 나타났습니다.
(2) 계절적 경기변동 여부 및 변동정도
당사에서 목표로 하고 있는 조직재생용 바이오소재, 구강보건제품, 펩타이드 기반 융합바이오소재, 펩타이드 치료제 및 펩타이드 기반 바이오베터의 경우, 인체의 건강에관련된 제품이므로 계절적 경기변동에 영향을 적게 받는 편이지만, 감염 제어와 관련된 감염성 질환의 경우 계절적 경기 변동에 민감할 수 있습니다. 감염성 질환은 병원체의 감염에 의해 나타나는 질병이므로 병원체의 번식 및 전염에 영향을 줄 수 있는 환경에 의해 질병 발생률이 좌우되고 이는 제품경기 변동에 직접 영향을 줄 수 있습니다. 그 예로서 호흡기 질환 치료제의 경우가 있습니다. 그러나 당사의 감염제어 치료제는 호흡기 감염을 제어하는 것이 아니고 국소적인 치주질환을 대상으로 하고 있기 때문에 경로가 한정적이어서 계절과 상관없이 질병이 발생하므로 큰 영향을 주지 않습니다.
(5) 제품의 라이프사이클
(가) 펩타이드 의약품 및 펩타이드 기반 바이오베터
1980년대 후반 펩타이드 합성의 안정화 기술이 개발되어 의약품을 만들 수 있게 됨에 따라 제약사들에 의해 대거 의약품이 만들어지기 시작했습니다. 펩타이드는 바이오산업의 핵심소재로서 고부가가치 산업으로 급부상하고 있습니다. 합성 펩타이드의 적용분야는 항체의 제조, 신약 및 생리활성 물질의 탐색, 기능성 화장품의 주원료, 단백질의 기능 및 구조 연구 등을 비롯한 생명과학 연구에 광범위하게 사용되고 있습니다. 따라서, 펩타이드 의약품 및 펩타이드 기반 바이오베터는 바이오기술과 결합되어도입기에서 성장기로 전환되는 시기라고 판단됩니다. 그리고 펩타이드 의약품 및 펩타이드 기반 바이오베터를 개발하기 위해서는 일반 화학합성물질의 개발 및 바이오시밀러 의약품과 비교해서 많은 연구비와 장기간의 연구기간이 필요합니다. 그러나 일단 개발이 완료된 후에는 제품의 라이프사이클이 긴 면이 있습니다. 이 제품이 최종적으로 인체에 사용되기 위해서는 설정된 가이드라인에 의해 일부는 의약품으로 허가를 받고, 기존의 의료기기에 적용하여 융합의료기기로 개발하는 경우에는 의료기기로 허가를 받아야 합니다. 당사의 펩타이드 발굴 원천기술은 지적재산권에 의해 보호받고 있으며, 펩타이드 의약품 및 펩타이드 기반 바이오베터 그리고 기타 바이오산업에도 응용이 가능하므로 기술 수명주기가 매우 길다는 것을 알 수 있습니다. 즉 펩타이드 의약품 및 펩타이드 기반 바이오베터는 개발하기가 용이하지는 않으나, 일단 허가가 완료된 후에는 제품판매의 라이프사이클이 길며, 제품개발에 소요된 원천 기술은 기술수명주기가 매우 길다는 것을 알 수 있습니다.
(나) 조직재생용 바이오소재
조직재생은 20년전부터 조직공학의 개념이 등장한 이후에 조직공학을 응용하여 손상된 조직을 재생시키려는 재생의학의 개념이 확립되어 오늘의 조직재생용 바이오소재 및 더 나아가 세포치료제까지 개발되었습니다. 이후 재조합단백질 제조기술, 줄기세포치료기술 등을 응용하여 신개념의 조직재생용 신소재들이 개발되고 있습니다. 따라서, 도입기, 성장기, 성숙기, 포화기, 쇠퇴기로 단계를 구분하여 볼 때, 조직재생용 바이오소재는 바이오기술과 결합되어 도입기에서 성장기로 이환되는 과정 중으로 판단됩니다. 그리고 조직재생용 바이오소재의 제품개발에 지속적인 연구비와 일정한연구기간 등이 필요함에 따라 제품의 라이프사이클이 긴 면이 있습니다. 또한 제품 개발에 필요한 기술은 지적재산권에 의해 보호받고 있고, 인체에 사용되기 위해서는 설정된 가이드라인에 의해 의료기기로 허가를 받아야 합니다. 조직재생용 바이오소재는 개발되기가 용이하지는 않으나, 허가가 완료되고, 판매가 시작되어 제품의 효력을 보기까지에는 1년 이상의 관찰기간이 소요됩니다. 따라서 관찰기간을 거쳐서 안전하고 효용성이 높은 재료라는 인식이 자리잡으면 이 소재에 대해서 장기적으로 사용하기 때문에 제품판매의 라이프사이클이 길며, 제품개발에 소요된 기술은 기술수명주기가 매우 길다는 것을 알 수 있습니다.
(다) 구강보건 제품
여성들의 사회활동 증가와 깨끗한 첫인상을 가지고 싶어 하는 현대인들의 욕구로 인하여 치아미백제의 수요가 지속적으로 확대되고 있고 이에 따라 치아미백제 시장은 전 세계적으로 계속 증가하고 있으며, 기존 제품보다 성능이 우수한 신제품 개발의 필요성이 증가하고 있습니다. 또한 시린이 증상과 치주염이 있는 인구층이 노년층에서 30-40대의 중장년층으로 확대되어 시린이 증상 환자의 폭이 넓어지고 있습니다. (자료 : 질병관리본부, 치주질환 유병률, 2014 국민건강통계 결과) 연령별 임플란트 시술건수 역시 40대 이상이 약 70%를 차지하고 있으며, 임플란트시술 5년 이후부터 시술환자의 25% 정도에서 임플란트 주위염이 발생됩니다. 따라서, 이에 대한 시린이치료제, 치과용 컨디셔너, 치주질환 및 임플란트 주위염 치료제와 같은 구강보건 제품의 수요가 증가될 전망입니다. 치아미백제의 경우 일반인의 관심이 점점 증가하고 있고, 기존 제품 대비 성능이 개선된 제품에 대한 욕구와 관련된 시장형성이 증가하고 이에 따라 경쟁제품이 증가함에 맞물려 도입기, 성장기, 성숙기, 포화기, 쇠퇴기로 단계를 구분하여 볼 때 치아미백 제품은 성장기에 접어든 것으로 판단됩니다. 기존의 제품보다 미백성능이 뛰어나며, 미백효과가 지속되는 기간이 향상된 치아미백제를 개발하게 된다면 제품의 라이프사이클을 증가시킬 수 있습니다. 시린이치료제와 치과용 컨디셔너, 치주감염치료용 제품은 효능이 뛰어난 제품을 개발하게 된다면, 전문가가 사용하는 제품의 특성을 고려할 때, 라이프사이클이 깁니다.
(6) 경쟁요소
(가) 펩타이드 의약품 및 의약 바이오소재 사업군
제약 및 바이오 산업의 경우 시장구조는 세분화 되어 있습니다. 특정 제품을 대상으로 할 때 경쟁자수는 타 산업대비 현저하게 적다고 할 수 있고 독점적인 특허가 바탕이 되는 경우 시장점유율이 높을 수 있습니다. 따라서, 이 분야는 기술 개발경쟁이 매우 중요한 요소이며 우수기술을 독점적으로 확보하는 것이 필수입니다.
펩타이드 함유 의약 바이오소재의 경우 일반 조직재생용 바이오소재와 마찬가지로 인체내에 이식되므로, 제품에 적합한 안전성과 유효성이 필요합니다. 또한 추가된 펩타이드에 대한 안전성과 그 성능의 증가를 추가로 증명해야 합니다. 이를 달성하기 위해서는 펩타이드의 개발기술 및 이의 바이오 소재와의 융합기술이 필요하므로, 일반 조직재생용 바이오소재가 펩타이드 기술을 신규로 접목하기에는 기술장벽이 높습니다. 그뿐만 아니라 초기 기술을 완성시키기 위한 자본, 시간, 임상시험 비용이 투입되어야 하는 등의 시장 진입의 난이도가 높습니다.
※ 펩타이드 기반 제품들의 경우 대부분 아직 개발중에 있으며, 개발이 완료되어 현재 판매중인 펩타이드 융합 바이오소재 OssGen-X15의 경우 아직 국내시장에 경쟁제품이 출시되지 않아, 점유율 산정이 불가함.
(나) 조직재생용 바이오소재
조직재생용 바이오소재는 인체 내에 이식되므로, 제품에 적합한 안전성과 유효성이 필요합니다. 제품의 분류는 의료기기에 해당되며, 제품을 판매하기 위해서는 해당 국가의 식약청에서 품목허가를 받아야 합니다. 더불어 일정 규격의 생산 시설, 제조설비에 대한 GMP 시스템 인증을 받아야만 허가를 얻을 수 있으므로 시장 진입의 난이도가 매우 높습니다. 또한 독점적인 특허를 바탕으로 시장에 진입한 경우 시장 점유율은 매우 높은 편입니다.
(다) 구강보건 제품
일반치약과 같은 구강보건 제품의 경우 시장진입의 난이도는 다소 낮습니다. 그러나 당사의 치아미백제, 시린이치료제, 치과용컨디셔너와 같은 제품군은 치약보다는 성능이 높고 이를 단시간 내 입증해야 하므로 기술력에 있어서 시장 진입의 난이도가 치약의 경우보다 다소 높습니다. 그러나 기존의 대기업 주도의 생활용품 업체가 대규모 자본을 투입하여 광고를 하는 등 초기 광고비 투자가 집중되므로 단순히 기술만을 위주로 한 제품이 시장에 진입하기는 어렵습니다. 그러나 이러한 제품은 앞서 기술한 대로 전문가 집단이 주도해야하는 특성 때문에 당사의 기술력과 치과의사 출신 기술진에 의한 제품력으로 시장진입에 성공하였다고 할 수 있습니다.
전문가용 치아미백제, 시린이치료제, 치과용 컨디셔너는 치과의사들이 사용하는 제품이면서, 개인용 치아미백제, 시린이치료제는 일반인이 직접 사용이 가능한 제품입니다. 따라서 전문가인 치과의사의 추천이 있으면 일반 소비자들이 제품을 구매하도록 유도할 수 있습니다.
2. 회사의 현황
(1) 사업 현황 및 사업 구분
당사의 사업 포트폴리오는 펩타이드 의약품 및 의약 바이오소재 사업군, 조직재생용 바이오소재, 구강보건 제품으로 구분할 수 있습니다.
1) 펩타이드 의약품 개발 기술
(가) 펩타이드 발굴기술 (PEPscovery)
질환별 환자의 조직샘플에서 발현이 증가되는 단백질에 대한 빅데이타 및 염증 및 종양과 같은 질환모델을 구축하였습니다. 특정 질환을 유발하는 세포내 또는 세포외 타겟을 선정하고 in vitro 또는 in vivo phage display (파지 디스플레이)를 통해, 세포내/외에 존재하는 특정 타겟에 결합력을 가진 펩타이드를 발굴하였습니다.
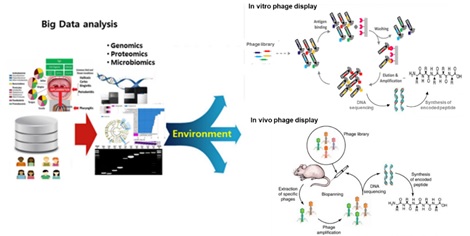 |
|
질환 타겟 결합 펩타이드 발굴 과정 |
타겟에 결합력을 가진 펩타이드에 대한 서열분석 및 합성을 통하여 생리활성 펩타이드 라이브러리를 구축하고, 펩타이드의 세포 수준 및 동물에서의 효능을 검증하였으며, 현재 420여종의 생리활성 펩타이드를 발굴하여 신약후보 물질로 개발 중입니다.
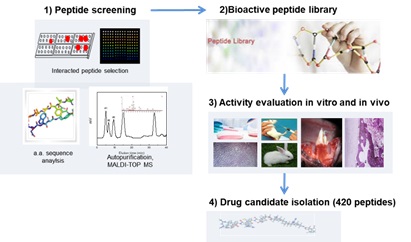 |
|
생리활성 펩타이드의 신약후보물질로 개발과정 |
타겟의 위치를 기준으로 구분했을 때, 질환의 종류에 따라 세포내부 또는 외부에 존재하는 바이오마커가 다릅니다. 각각의 바이오마커에 대한 결합력이 있는 생리활성 펩타이드를 in vitro/in vivo phage display로 발굴함으로써, 마이오마커의 발현을 조절하여 질환을 치료할 수 있습니다. 골질환의 경우 세포외부에 있는 단백질을 타켓으로 하여 골재생을 증가시키며, 염증질환의 경우, 세포내의 염증신호에 관계하는 전사인자를 조절하여 염증을 억제하게 합니다.
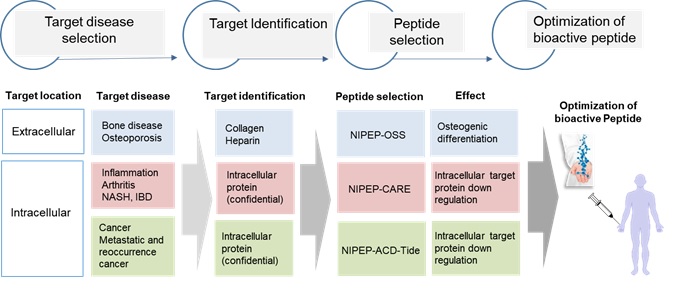 |
|
세포내,외 바이오마커 조절 기술 |
생리활성 펩타이드 의약품은 저분자 합성물질 및 단백질 의약품과 비교했을 때 아래와 같은 특징이 있습니다. 저분자 합성물질의 경우, 타겟에 대한 비가역적인 결합을 함으로써 반감기가 길고 안전성에 대한 문제가 있습니다. 단백질 의약품의 경우, 면역반응의 유발 및 장기간 투여 후 효과가 감소하는 가능성이 있으며, 반감기가 짧습니다. 펩타이드 기반 치료제는 저분자 약물보다 독성이 적으며, 단백질 약물처럼 면역반응을 유발하지 않으며, 타겟에 대한 반응성이 크지만, 가역적인 반응이기 때문에 안전성에 큰 문제가 없습니다.
<펩타이드 의약품의 특징>
|
구 분 |
제조방법 |
특징 |
투여경로 |
|---|---|---|---|
|
저분자 의약품 |
화학합성 |
약효는 강하나, 수용체에 비가역적으로 결합하여 독성이 큼 |
경구, 주사 |
|
단백질 의약품 |
세포배양 및 발현 |
면역반응 유발 및 장기간 사용시 약 효 감소 우려. 세포내 타겟을 가진 경우, 효과가 없음. 세포주 관리가 매우 중요함. |
주사 |
|
유전자 치료제 |
세포배양 |
세포내로 전달하기 위해 바이러스성 벡터 사용. 바이러스에 의한 염증, 암발생 가능성 있음. 비바이러스성 벡터는 전달 효율이 낮으며, 세포에 대한 독성이 있음. |
주사 |
|
세포치료제 |
세포배양 |
세포가 분리정제가 안 될 경우, 예측할 수 없는 부작용이 발생할 수 있음. 품질관리가 어려움. |
주사 |
|
펩타이드 의약품 |
화학합성 |
면역반응 적음. 수용체에 대한 가역적 결합 및 활성 조절 가능. 품질관리가 용이함. |
경구투여 제형으로 개발 가능. 주사 |
(나) 펩타이드 의약품 개발 기술 (TOPscovery)
(1) 세포내 단백질 (항체) 전달
세포내 타겟에서 작용을 하는 단백질 또는 항체는 분자량이 크기 때문에, 세포막을 통과할 수가 없습니다. 따라서, 이들 단백질의 효과를 증가시키기 위해서는 세포내 전달기술이 필요합니다.
세포/조직 투과성 펩타이드는 엔도사이토시스 (endocytosis)와는 다르게 세포막의 인지질(phospholipid)와 펩타이드의 arginine의 상호작용에 의해 세포막을 뚫고 투과되는 것이며, 이는 에너지와 무관하게 일어나는 것으로 낮은 온도에서도 세포막의 투과가 가능합니다.
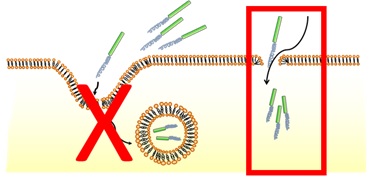 |
|
세포, 조직 투과성 펩타이드 (nipep-tpp)의 작용기전 |
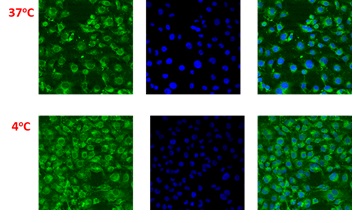 |
|
에너지 비의존적(energy-independent)인 세포 투과 |
나이벡이 개발한 세포/조직 투과성 펩타이드 (NIPEP-TPP)를 이용하여 단백질 또는 항체를 세포 안으로 전달이 가능하게 합니다. 세포 내부로 단백질을 전달하여 단백질의 효과를 증가시키며, 결과적으로 체내 안정성과 생체이용률을 증가시킬 수 있습니다. 이 기술은 세포내 타겟 또는 특정 조직(예: 종양, 뇌혈관 장벽(blood brain barrier)) 에서 작용하는 단백질 의약품에 적용이 가능합니다.
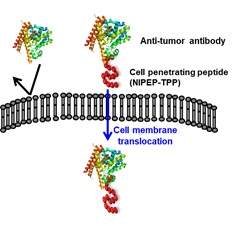 |
|
세포, 조직 투과성 펩타이드(nipep-tpp)에 의한 단백질의 세포 내 전달 원리 |
(2) 제형설계 기술
a. 경구전달 제형 (oral delivery formulation)
펩타이드 또는 단백질은 소화관내 효소에 의해 분해되기 때문에 경구제형으로 투여가 불가능합니다. 이에 따라 대부분의 펩타이드, 단백질 의약품은 주사제형으로 개발 및 적용되고 있습니다. 당뇨, 관절염 같은 만성질환에 사용하는 단백질 의약품의 경우, 장기간 동안 주사를 맞아야 되기 때문에, 환자들의 고통이 많습니다. 경구제형으로 개발이 가능하다면 환자순응도와 적용의 편리성이 증가할 수 있습니다. 나이벡의 소화관내 안정성을 증가시키는 기술에 의해 펩타이드 또는 단백질의 경구전달 제형으로 개발이 가능합니다. 특히, 경구전달 제형은 장에서만 전달될 수 있도록 조절하여 염증성 장질환 (inflammatory bowel disease) 치료제 개발에 응용이 가능합니다.
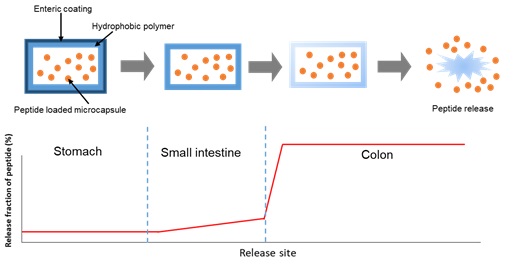 |
|
경구 전달 제형의 설계 |
b. 바이오소재 표면 결합기술
바이오소재에 결합력이 있는 펩타이드 (NIPEP-SBP)를 링커로 사용하여 생리활성 펩타이드를 바이오소재에 결합시킬 수 있습니다. 이를 통해, 바이오소재의 재생 기능과 같은 생리활성을 증가시킬 수 있습니다. 콜라겐, 헤파린, 피브린, 라미닌과 같은 생체고분자, 칼슘포스페이트와 같은 무기질, 임플란트에 사용되는 티타늄, 지르코니아 등 금속에 결합력이 있는 펩타이드를 사용하여 표면에 고정이 가능합니다.
 |
|
바이오 소재 표면 결합 기술 응용 |
바이오소재 표면 결합 펩타이드는 단순한 물리적 흡착의 경우보다 결합력이 강하며, 화학적 가교제를 사용하지 않았기 때문에 잔류 가교제에 의한 독성 문제가 없습니다. 고정하고자 하는 단백질을 변성시키지 않고, 체내에서의 안정성과 국소체류성을 증가시킬 수 있습니다.
<바이오소재 고정방법의 비교>
| 구 분 |
화학적 고정방법 |
물리적 흡착방법 |
당사 바이오소재 표면 결합성 펩타이드 |
|
특성 |
가교제 (cross linker)를 사용하여 소재의 표면에에스터 결합 또는 아마이드 결합과 같은 공유결합을 형성하므로, 장기간 동안 안정하게 결합을 유지가능 |
가교제를 쓰지 않으므로 단백질 소재가 변형될 염려가 없음 |
특정 바이오소재 결합능이 있는 펩타이드를 사용하여 직접 소재에 부착할 수 있으며, 조직재생 효과가 있는 펩타이드와 융합하여 사용이 가능함. 단백질 소재의 변형이 없으며, 추가적인 공정이 필요없음. PEPscovery를 응용하여 다양한 소재에 대한 부착 펩타이드를 발굴가능 |
2) 펩타이드 의약품 파이프라인
가) NIPEP-OSS, 골다공증 치료제
(1) 특징
NIPEP-OSS는 골조직의 세포외기질과 친화성이 있으며, 줄기세포 또는 조골세포에 골조직으로의 분화를 촉진하여 골재생을 증가시킵니다. 또한, 줄기세포에 처리하였을 때, 골조직으로 분화를 촉진시키고, 지방조직으로 분화는 억제합니다. 이는 폐경후 지방조직의 증가로 비만이 증가하는 골다공증 여성에게 유리한 작용입니다. 골다공증 동물 모델에서 골밀도를 증가시켰으며, 반감기는 2-3시간으로, 골조직에 선택적으로 분포하여 효과를 내기 때문에, 안전합니다. 실제로, 단회 피하 주사에서 1700mg/kg까지 부작용이 없었고, 4주 반복투여독성시험에서 NIPEP-OSS에 의한 부작용이 없었으며, 면역반응을 유발하지 않았습니다.
현재 전임상 독성시험(독일 소재 GLP 기관, LPT)을 완료하였고, 2018년 12월에 식약처 임상1상 시험 승인을 신청하여, 2019년에 임상1상을 진입하기 위해 준비 중입니다.
기존의 골다공증 치료제는 골흡수를 억제하는 기전인 비스포스포네이트가 가장 많이 사용되고 있으나, 장기간 사용시 과도하게 골흡수를 억제하여 골질이 약해서 골절 위험이 증가합니다. 유일한 골재생 촉진 기전의 테리파라타이드는 고칼슘혈증을 유발하거나, 장기간 사용시 골육종을 일으키는 위험성이 있는 것으로 알려져 있습니다.
<기존 골다공증 치료제와 비교>
|
구 분 |
Bisphosphonates |
Teriparatide |
NIPEP-OSS |
|
작용기전 |
골흡수 저해 |
골형성 증가 |
골형성 증가, 지방축적 억제, 뼈조직 및 골아세포에 대해 선택적으로 작용 |
|
부작용 |
-소화기계 부작용 -턱뼈 괴사 -저칼슘혈증 -골질이 각화되어 장기간사용시 골절 위험이 증가함 |
-장기간 사용시 골육종위험 -고칼슘혈증 |
현재까지 알려된 부작용없음 |
|
투여간격 |
매일-매주 경구투여 |
매일 피하주사 |
매주 피하주사 |
|
적응증 |
골다공증 |
골다공증 |
골다공증, 국소 골재생 |
나) NIPEP-CARE1, 관절염 치료제
NIPEP-CARE는 인체내 면역에 관계하는 단백질로부터 유래한 펩타이드로서, 염증 신호에 관계하는 전사인자를 억제하여 염증성 사이토카인의 생성을 억제함으로써 항염증 효과를 가지게 됩니다. 관절염 유발 동물 모델에 투여했을 때, 엔브렐 (etanercept)보다 염증지수 완화 및 골소실 억제 연골보호 효과가 우수한 것을 증명하였습니다. 또한, 세포투과 및 피부로도 투과가 가능하여 주사제 이외의 피부 적용제형으로 개발이 가능합니다. 현재 전임상 효능시험을 완료하였고, 전임상 독성시험에 진입할 계획입니다.
관절염 치료제로 많이 사용되는 생물학적 제제로는 TNF-a 차단제가 있는데, 과도하게 면역반응을 차단하여 감염이나 결핵을 유발하는 부작용이 있습니다.
<기존 생물학적 관절염 치료제와 비교>
|
구 분 |
TNF-a Inhibitor |
NIPEP-CARE |
|
작용기전 |
TNF-a에 의한 세포내 신호전달에 의해 유발되는 염증, 면역반응을 차단 |
histone deacetylase (HDAC)을 타겟하여 염증반응을 막음 |
|
부작용 |
감염, 결핵 |
현재까지 밝혀진 부작용 없음, 앞으로 더 규명해야 함 |
|
투여간격 |
피하, 정맥 주사 |
피부 적용, 경구투여 제형으로 개발가능 |
|
적응증 |
염증성 질환에 사용 |
단독 또는 기존의 치료제와 병용가능 TNF-a 에 불감응성 환자에게 사용가능 |
다) NIPEP-CARE2, 비알코올성 지방간염 치료제
비알코올성 간질환은 간내 단순지방침착 (steatosis)부터 지방간염, 간경변에 이르는 다양한 질환을 포괄하며, 비만 또는 인슐린 저항성으로 인한 간세포내 지방침착, 유전적인 원인 등을 그 이유로 보고 있습니다. 현재, 비알코올성 지방간염 치료제로서 FDA 허가를 받은 약물은 존재하지 않는 상황입니다. 일부 개발되는 약물들은 독성 때문에 임상시험 중에 중단이 된 약물들도 있습니다.
methionine 결핍 식이에 의해 지방간 유발 동물모델에 투여했을 때, NIPEP-CARE에 의한 비알코올성 지방간의 NAS score (ballooning degeneration, lobular inflammation, steatosis)가 감소하였고, 간과 혈액에서 염증성 사이토카인의 발현이 감소하였습니다. 현재 다양한 간질환 모델에서 전임상 효능시험을 진행 중입니다.
라) NIPEP-CARE3, 염증성 장질환 치료제
염증성 장질환은 자가면역질환 중 하나이며, 궤양성 대장염과 크론병으로 나눌 수 있습니다. 유전적, 환경적 요인에 의해 발생하며 100가지가 넘는 유전자들과 음식, 스트레스와 같은 요소들이 장내의 세균에 변화를 일으키고 보호 면역기능을 약화시켜 장내에 염증을 일으키게 됩니다. 그 외에도 다른 종류의 감염이나 장내 mucosal integrity가 감소하여 균들이 침투가 깊게 되어 면역반응을 유도하게 되고, 계속된 면역반응은 장 점막 세포를 파괴하여 자가 회복이 불가능하게 됩니다. 현재, 1차 치료로 사용하는 약물은 Aminosalicylic acid 로 주로 증상완화에 사용하고 있으며, 이 약에 반응하지 않을 때, 스테로이드를 사용하게 되나, 효능이 없거나 부작용이 발생하게 되면, 면역제제나 생물학적 제제를 사용하게 됩니다. 생물학적 제제인 TNF-a 차단제는 면역반응을 오히려 억제하는 부작용을 가지고 있습니다. NIPEP-CARE는 HDAC 저해에 의한 염증 감소와 대장 점막에 존재하는 콜라겐에 대한 자가 면역반응을 감소시켜 장점막의 재생을 증가시키는 작용이 있습니다. 현재 다양한 장염 동물모델에서 전임상 효능시험을 진행 중이며, 경구투여 제형으로 시험 중입니다.
마) NIPEP-ACD-TIDE 표적 항암 치료제
항암 치료 후에 암이 다시 재발하거나 전이되는 이유는 암세포 중에 암줄기세포가 존재하여, 항암치료에도 살아남아 다시 증식을 하기 때문입니다. 따라서, 이들 암줄기세포를 타겟으로 하여 치료를 하는 항암제가 개발된다면, 암전이나 재발의 확률이 감소할 것입니다. 현재, 암줄기세포를 타겟하는 약물을 개발되지 않았습니다.
NIPEP-ACD-TIDE는 암줄기세포내 단백질을 억제함으로써, 암줄기세포의 이동, 부착, 전이를 억제하는 기능이 있습니다. 또한, 세포투과기능이 있기 때문에, 항암효과가 있는 단백질 또는 항체와 결합하여 세포내 전달수단으로 사용가능 합니다. 현재, 전임상 효능 시험 중에 있으며, 암자체의 증식과 젼이를 억제하는데 효과가 있는 것을 증명하였습니다. 또한, 면역항암제와 병용투여에 의한 치료효과를 규명할 예정입니다.
3) 펩타이드 의약품 진행 현황 및 예상
 |
|
연구진행 현황 |
4) 가격 경쟁력
기존의 펩타이드 의약품 및 의약 바이오 소재, 조직재생용 바이오소재, 구강보건제품, 바이오의약품 시장은 수입 제품이 주도하고 있습니다. 당사 제품의 시장 점유율을 높이기 위해서는 가격경쟁력이 중요한 역할을 합니다. 현재 유전자재조합 기법으로 제조되는 바이오 의약품은 고가입니다. 당사의 비천연 합성법으로 생산한 펩타이드는 기존 생물학적인 방법으로 생산한 바이오의약품 (단백질, 펩타이드)에 비하여 순도가 높고, 대량생산이 가능하여 생산단가를 낮출 수 있습니다. 또한, 당사만의 독창적인 서열을 가지고 있어서, 기술 수출도 가능합니다.
골이식재의 경우 원료를 국내에서 충당하고, 수율을 증가시킴으로써 생산원가가 낮습니다. 따라서 기존의 고가 수입제품과 비교했을 때 가격 경쟁력이 있습니다. 또한, 당사의 구강보건제품은 코팅형 젤 타입으로 제품화하여 소량 사용으로도 빠른 효과를 보이고 GMP 시설에서 대량 생산 공정을 확립하여 원가율이 낮습니다. 따라서 기존 수입제품이나 생활용품의 가격제한선 이하로 판매가가 책정되더라도 충분한 수익을 얻을 수 있습니다.
5) 수익창출의 지속성
수익을 지속적으로 창출하기 위해서는 시장점유율을 계속 증가해야 합니다. 소비 수준 향상으로 인하여 치아미백 및 구강 질환 치료에 관한 관심이 높아지고 있습니다. 당사의 약물전달시스템기술을 바탕으로 우수한 성능의 제품을 개발하여 시장점유율을 증가 시킬 수 있습니다. 또한 고령화 사회 도래로 인하여 치주질환 환자가 늘고 임플란트 시장의 성장과 더불어 골이식재의 수요는 점점 커지고 있는 있습니다. 또한 당사의 말뼈 기반 골이식재는 광우병 우려로 소뼈를 이용한 골이식재의 사용이 점점 제한되는 점을 감안 할 때 시장의 확대가 기대됩니다. 우수한 성능과 안전성으로 인해 국내시장에서의 점유율을 높여가고 있으며 말뼈 기반 골이식재는 유럽 인증 및 미국 인증을 획득, 이를 교두보로 한 전세계 수출을 목표로 하고 있습니다.
6) 개발 시간 단축
시장 선점을 달성하기 위해서는 제품의 개발 시간을 단축해야 합니다. 당사의PEPscovery 기술을 이용하여 신속하고 효율적인 약효 성분의 스크리닝이 가능합니다. 기존의 바이오 의약품 개발 기술인phage display 및molecule docking 방법과 비교하여 목적 펩타이드를 분리한 후 기능 확인에 있어서도 당사의 조직재생능, 염증제어능, 항균력 등에 대한 시험 프로토콜이 정량화 되어 있어 신속하게 기능을 평가하여 후보물질을 확정하는데 드는 시간, 비용이 절약됩니다. 당사는 연구 네트워크를 구축하고 있어 발굴될 물질에 대한 다양한 동물에서의 성능 시험을 실시할 수 있습니다. 또한 자체 펩타이드 합성 설비가 구축되어 있고, TOPscovery 기술을 응용하여 신속하게 제형을 설계할 수 있습니다.
7) 기술의 응용범위
기술의 응용 범위가 넓어서 의약품 외에 다른 시장으로 응용가능한 경우 빠른 개발로시장의 선점이 가능하고 다양한 수익원이 될 수 있습니다. 당사의 세포/조직 투과성 스마트 펩타이드는 항체, 다른 단백질 의약품의 세포내 투과를 증가시키는 등 약물전달을 위한 플랫폼 기술로 응용이 가능합니다. 또한, 바이오소재 표면 부착성 펩타이드를 이용하여 체내 안정성을 증가시켜 융합 바이오 소재로 개발할 수 있습니다. 당사가 개발한PEPscovery 기술은 의료공학, 조직공학, 생물학, 생화학 등 기초 연구 및 신약개발 등의 바이오산업에도 널리 이용될 수 있기 때문에 개발 기술의 민감성, 재현성, 정확성 등의 장점을 적극 활용할 경우 큰 시장 경쟁력을 갖고 있습니다. 최근 분자진단영역의 산업적 수요가 급격화되는 시점에 당사의PEPscovery 기술을 기반으로 한 빠른 스크리닝 기술을 접목하여 진단제품, 화장품, 백신 등으로도 적용이 가능합니다.
8) 지적재산권
당사의 보유기술에 대한 모방을 방지하기 위해 지적 재산권 확보가 필수적입니다. 당사는2006년부터 특허등록이 이루어졌습니다. 국내 특허의 유효기간은 출원일로부터20년으로 되어 있으므로, 2026-2030년까지 당사 소유기술의 특허권이 유지될 것입니다. 다양한 생리활성을 가진 펩타이드 뱅크를 구축하기에는 장기간의 축적된 연구 데이터와 발굴기술이 필요하므로, 기술복제의 난이도는 높다고 할 수 있습니다. 미국 및 유럽, 일본의 경우에도 기능성 펩타이드에 관련된 지적재산권은 극히 일부만확보하고 있는 실정입니다. 당사의PEPscovery기술은 일련의 조직 재생기능성 펩타이드 서열에 대한 포괄적인 다수의 지적재산권을 이미 등록하여 기술복제가 어려우며 이에 따라 당사의 기술에 대한 독보성을 확립하였습니다. 현재까지 국내 관련업계및 회사에서는 당사 소유의 펩타이드를 적용한 제품이 개발된 사례가 없습니다. 새로운 신규제품기술이 출현하는 것에 대한 대응방안으로, 기존의 지적재산권을 활용함에 있어 대량 생산 및 제품화에 따른 독창적인 특허의 확보가 필요할 경우에는, 현재 당사에서 출원 및 등록된 특허와 기존에 공개된 특허 등을 통합한 패키지 특허를 출원할 계획입니다.
9) 조직도
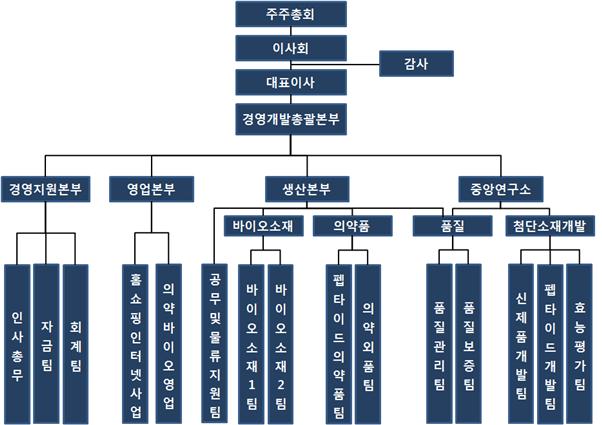 |
|
회사조직도 |
2. 주요 제품 등에 관한 사항
가. 주요 제품 등의 현황
(기반 사업군)
| 품목 | 제품 | 제품 설명 | 매출액 (비율) |
| 조직재생용 바이오소재 |
치과용 골이식재 및 바이오소재 | 소뼈 및 말뼈의 염증유발 단백질을 제거하여 분말화한 치과용 골이식재 및 콜라겐 바이오소재 | 4,896 (94.01%) |
| 구강보건제품 | 치아미백제 및 시린이치료제 |
- 카바마이드 퍼옥사이드와 에센셜오일, 자일리톨을 포함하는 개인용 치아미백제 - 치주질환의 원인균을 억제하는 항생연고제 |
248 (4.76%) |
| 화장품외 | 미백 주름개선 이중기능성 화장품 | 64 (1.23%) |
|
(신성장동력사업군)
| 품목 | 제품 | 제품 설명 |
| 펩타이드 의약품 |
골다공증치료제 (NIPEP-OSS= Osseotide) |
골 재생 기능 펩타이드 함유 골다공증 치료제 |
|
관절염 치료제 (NIPEP-CARE 1) |
염증 억제 기능 펩타이드 함유 관절염 치료제 |
|
|
비알콜성지방간염(NASH) 치료제 (NIPEP-CARE 2) |
염증 및 지방 억제 기능 펩타이드 함유 비알콜성지방간염 치료제 |
|
|
염증성 장질환(IBD) 치료제 (NIPEP-CARE 3) |
염증 억제 기능 및 점막 재생 기능 펩타이드 함유 염증성장질환 치료제 |
|
|
항암치료제 (NIPEP-ACD-Tide) |
종양선택적 투과기능이 탑재된 종양 치료 및 전이암, 내성암 치료제 |
|
| 펩타이드 기반 바이오베터 및 플랫폼 |
OssGen-Better |
PTH 골다공증 바이오 베터 |
|
TOPscovery |
세포내 단백질(항체) 전달시스템 |
나. 주요 제품 등의 가격변동추이
당사의 주요제품 등의 가격과 변동추이는 아래와 같습니다.
(단위: 원)
| 품목 | 제품 | 2018년 (제15기) |
2017년 (제14기) |
2016년 (제13기) |
| 조직재생용 바이오소재 |
치과용 골이식재 |
39,516 | 35,200 | 35,062 |
| 구강보건제품 | 치아미백제 | 10,909 | 10,164 | 10,164 |
| 미노큐어 | 39,091 | 41,538 | 41,775 |
(주1) 가격 산출 기준
가격 산출 = 총 판매금액(원화) ÷ 총 판매수량(개)
※ 총판매수량 : 제품 규격에 상관없이 누적판매수량 적용.
다. 주요 제품 등 관련 각종 산업표준
의약품 또는 의료기기를 판매하기 위해서는 각 제품에 대한 안전 및 성능에 대한 기준을 규정하고 있으며 이 기준을 충족해야 인증기관에서 허가를 받을 수 있습니다. 또한 다른 국가들도 자국민의 안전을 위해 자국 내에 들어오는 제품에 대한 안전 요구사항을 규정하고 있으며, 해외에 제품을 수출하기 위해서는 수출하고자 하는 국가의 규제적 요구사항을 충족해야 합니다. 이러한 규정들은 제품의 수출, 판매허가를 받기 위해 반드시 따라야 하는 것이므로 산업표준과 동일한 성격을 갖는다고 할 수 있습니다.
3. 원재료에 관한 사항
가. 매입현황
(단위 : 천원)
| 품목 | 2018년 (제15기) |
2017년 (제14기) |
2016년 (제13기) |
|
| 치과용 골이식재 |
주재료 | 338,115 | 265,377 | 225,701 |
| 포장재 | 165,363 | 145,828 | 137,339 | |
| 소계 | 503,478 | 411,205 | 363,040 | |
| 치아미백제 | 주재료 | 65,729 | 24,832 | 58,185 |
| 포장재 | 22,557 | 12,609 | 48,311 | |
| 기타 | 120,926 | |||
| 소계 | 88,286 | 37,441 | 227,422 | |
| 기타 | 주재료 | 134,200 | 778,965 | 52,045 |
| 포장재 | 18,423 | 58,813 | 77,742 | |
| 소계 | 152,623 | 837,778 | 129,787 | |
| 합계 | 744,387 | 1,286,424 | 720,249 | |
나. 원재료 가격변동추이
(단위 : 원)
| 구분 | 단위 | 2018년 (제15기) |
2017년 (제14기) |
2016년 (제13기) |
|
| 치과용 골이식재 |
동물뼈 | 마리 | 1,100,000 | 1,100,000 | 1,100,000 |
| 용기 | ea | 930 | 930 | 1,125 | |
| 치아미백제 | 카바마이드 | g | 102 | 140 | 140 |
| PVP | g | 36 | 36 | 36 | |
| 용기 | ea | 1,330 | 192 | 192 | |
(주1) 산출기준
- 산출대상 : 주요 원재료
- 산출단위 및 산출방법: 대상원재료의 산술평균 매입단가
(대상 원재료 매입금액 ÷대상 원재료 매입수량)
4. 생산설비에 관한 사항
(1) 생산설비의 현황
(단위 : 백만원)
|
사업소 |
소유형태 |
소재지 |
자산별 |
기초 |
당기증감 |
당기 |
기말 |
비고 |
|
|
증가 |
감소 |
||||||||
|
진천공장 |
자가 |
충북 진천군 이월면 밤디길 116 |
토지 |
914 | 914 |
1,122 (13,304.40㎡) |
|||
|
자가 |
충북 진천군 이월면 밤디길 116 |
건물 |
5,787 | 174 | 5,613 |
- |
|||
|
자가 |
충북 진천군 이월면 밤디길 116 |
기계장치 |
484 | 756 | 267 | 973 |
- |
||
|
자가 |
충북 진천군 이월면 밤디길 116 |
시설장치 |
2,477 | 47 | 455 | 2,069 |
- |
||
|
연구소 |
자가 |
서울시 종로구 대학로 101(연건동)서울대학교 치의학대학원 치과생체재료동 403호, 404호 |
기계장치 |
67 | 80 | 34 | 113 |
- |
|
|
합 계 |
9,729 | 883 | 930 | 9,682 |
- |
||||
주1) 비고란은 공시지가입니다.
주2) 건물과 시설장치 일부는 차입금 담보로 설정되어 있습니다.
(2) 생산설비의 투자계획 등
(단위 : 백만원)
|
사업부문 |
예상투자총액 |
연도별 예상투자액 |
투자효과 |
비고 |
|||
|
자산형태 |
금 액 |
제14기 |
제15기 |
제16기 |
|||
|
조직재생사업 |
기계장치 |
700 |
300 |
200 |
200 |
생산성향상, 매출증대 |
- |
|
시설장치 |
1,000 |
500 |
300 |
200 |
생산성향상, 매출증대 |
- |
|
|
합 계 |
1,700 |
800 |
500 |
400 |
- |
- |
|
5. 매출에 관한 사항
가. 매출실적
(단위 : 천원)
| 매출 유형 |
품 목 | 2018년 (제15기) |
2017년 (제14기) |
2016년 (제13기) |
|
| 제품매출 | 조직재생용 바이오소재 |
수출 | 4,048,612 | 4,135,692 | 3,641,503 |
| 내수 | 847,025 | 766,625 | 413,546 | ||
| 소계 | 4,895,637 | 4,902,317 | 4,055,049 | ||
| 구강보건제품 | 수출 | 37,239 | 1,047 | ||
| 내수 | 210,877 | 127,846 | 519,346 | ||
| 소계 | 248,116 | 127,846 | 520,393 | ||
| 화장품 | 수출 | ||||
| 내수 | 64,124 | 147,913 | 59,517 | ||
| 소계 | 64,124 | 147,913 | 59,517 | ||
| 기타수익 및 상품매출 | 수출 | 1,124,500 | |||
| 내수 | 169,272 | ||||
| 소계 | 1,124,500 | 169,272 | |||
| 합 계 | 수출 | 4,085,851 | 5,260,192 | 3,642,550 | |
| 내수 | 1,122,026 | 1,042,383 | 1,161,682 | ||
| 합계 | 5,207,877 | 6,302,575 | 4,804,232 | ||
주) 제14기(전기) 및 제13기(전전기) 매출은 종전 기준서인 K-IFRS 1018호에 따라 작성되었습니다.
나. 주요 매출처 등 현황
국내 대기업 및 외국의 다국적 유통회사를 통해 판매를 하고 있습니다.
다. 수주상황
치과용 골이식재의 경우 해외의 유수의 유통업체와 공급계약을 체결하여 판매중에 있습니다.
치아미백제의 경우 온라인, 오프라인에서 판매가 이루어지고 있습니다.
| (증권신고서 제출일 현재) | (단위 : 천미불) |
|
업 체 명 |
주요계약품목 |
수주일자 |
납기일자 |
수주액 |
기납품액 |
수주잔액 |
|---|---|---|---|---|---|---|
|
Hi-Clearance |
치과용 골이식재 |
2014-08-18 |
2020-12-31 |
1,290 |
157 |
1,133 |
|
Almas Rouyan Pars |
치과용 골이식재 |
2014-12-31 |
2020-12-22 |
1,200 |
96 |
1,104 |
|
Nobel Biocare |
치과용 골이식재 |
2015-12-14 |
2021-12-31 |
13,926 |
4,881 |
9,045 |
|
Araguaney Professional |
치과용 골이식재 |
2017-03-13 |
2022-03-09 |
810 |
22 |
788 |
|
Wright Health Group |
치과용 골이식재 |
2017-03-27 |
2019-12-31 |
700 |
8 |
692 |
|
Straumann |
치과용 골이식재 |
2019-02-21 |
2024-02-20 |
21,982 |
237 |
21,745 |
|
합 계 |
|
|
39,908 |
5,401 |
34,507 |
|
라. 향후 매출액의 변동에 영향을 줄 것이라고 인정되는 사항
ⓐ 신제품의 허가 및 출시예정
치주조직재생용 바이오소재는 CE 및 FDA인증을 취득하였고, 또한 생산시설 확충이 2015년 하반기에 완료되어 2016년부터는 매출상승이 발생하였습니다. 전문가미백제는 의약품 GMP 인증은 취득하였고, 매출이 발생되고 있습니다.
그리고, 2018년 8월에 골이식재 콜라겐의 복합 바이오소재 제품의CE인증이 완료되었고, 계약된 판매처로의 매출은 하반기부터 증가될 추세입니다.
ⓑ 해외시장 진출
미국과 유럽시장의 노벨바이오케어사와 수량 개런티와 단가 인상 등의 계약규모의 확대 공급계약과, 스트라우만사와 신규 공급계약을 2019년 2월에 체결하여 전세계적으로 안정적인 판매망을 확보하였으며, 지난해에 출시하여 전세계 바이어들에게 호평을 받은 콜라겐 제품군 등의 신제품이 기존의 판매제품과 더불어 금년도 매출상승에 큰 기여를 할 것으로 사려됩니다.
ⓒ 기술이전 사업 확대
당사는 펩타이드 발굴 및 제품화 기술, 조직재생용 바이오소재기술을 소유하고 있습니다. 이들의 기술이 적용되어 제품화 될 것으로는 펩타이드를 기반으로 한 골다공증 치료제 NIPEP-OSS (OsseoTide)와 관절염 치료제NIPEP-CARE 1을 비롯하여 비알콜성지방간염(NASH)치료제 NIPEP-CARE 2, 염증성 장질환치료제(IBD) NIPEP-CARE 3 그리고 항암치료제인 NIPEP-ACD-Tide가 있습니다. 이러한 제품은 바이오 신약으로 분류되어 전임상 및 임상시험에 있어 막대한 비용과 시간이 소요될 뿐 아니라 생산 역시 매우 엄격한 기준에 의해 진행되어야 하므로 기술집약적 벤처기업이 이를 제품화 하는데는 제약이 있습니다. 2018년도에 전임상을 완료하여 2019년도에 임상1상을 진행 예정인 골다공증 치료제는 임상 1상이 완료 후, 관절염치료제를 비롯한 비알콜성지방간염 및 염증성 장질환치료제도 임상 1상이 완료되는 시점에 국내외 제약사를 통한 기술이전 할 것을 계획하고 있습니다. 또한 항암치료제 같은 경우, 바이오 시장에서의 요구가 큰 편인 점을 감안하여 전임상이 완료된 이후 기술이전 할 것을 계획하고 있습니다.
2017년 1분기에 펩타이드를 응용한 플랫폼 기술에 대한 기술이전이 이루어졌으며, 향후에도 지속적으로 연구계약 및 추가 기술이전을 추진하고 있어 당사의 매출증가에도 기여할 것으로 전망됩니다.
6. 판매경로 등
가. 판매조직
당사의 영업본부는 현재 대표이사가 겸직하고 있는 부분입니다. 당사의 매출은 현재까지는 영업본부에서 직접 영업활동을 통해 일어나는 것이 아닌, 소수의 메이저 판매유통회사와의 제휴로 일어나기 때문에 현 단계에서는 다수의 영업 인력을 요하지 않습니다. 이는 당사의 설립 이념인 지속적인 연구 및 고품질 제품의 생산에 집중할 수 있는 구동력이 되고 있습니다. 즉, 인력, 마케팅 비용 및 시간을 절감하여 연구개발에 매진할 수 있는 계기를 삼고자 하였습니다만 향후 매출이 증대되고 판매처가 다양화하면 영업조직의 확충을 계획하고 있습니다.
나. 판매경로
당사 매출액 대비10% 이상의 매출을 기록한 제품군은 치과용 골이식재로 상기 제품군이 전체매출의90%이상을 차지하고 있습니다. 치과용 골이식재는 세계 유수의 임플란트 글로벌사와 장기계약을 통한 안정적인 매출이 실현되고 있습니다. 치아미백제는 기본적으로 국내외 총판업체 및 이들의 협력 대리점을 통한 영업경로를 채택하고 있습니다. 전문 구강의약품인 미노큐어, 크린플란트는 국내 구강의약품 전문회사인 휴온스와 판매 제휴를 맺어 매출증가에 기여할 것으로 예상되며, 해외 판매처로는 임플란트 글로벌사인 스위스 스트라우만사를 통하여 수출 중에 있습니다.
다. 판매전략
당사는 연구개발전문기업을 지향하는 회사로서 판매는 주로 대기업과 다국적 유통회사를 통한 판매전략을 세우고 있습니다.
7. 시장위험과 위험관리
기준일 현재 회사가 노출된 시장위험에서 가장 중요한 것은 환위험이라고 할 수 있습니다. 그러나 당사가 보유한 외화자산 등의 규모나 외화의 유출입 흐름 등을 감안할 때, 환율 변동에 따른 위험이 전체 경영에 미치는 영향이 크지 않고, 당사 규모나 보유인력 등을 고려하면 파생상품 활용 등을 통한 적극적인 위험관리 노력보다는 본연의 경영에 집중하는 것이 효율적이라고 판단하고 있습니다. 따라서 외화 유입과 유출의 적절한 매칭 등의 위험관리 방법만을 택하고 있습니다. 공시대상기간 동안 외환관련 파생상품 계약을 체결하지 않았으며, 현재로서는 단기간 내에 이러한 계약 등을 체결할 계획이 없습니다. 재무제표에 대한 주석의 위험관리 부분을 참조하시기 바랍니다.
(가) 외환위험관리
연결실체는 외화거래 수행에 따라 다양한 환율변동위험에 노출되어 있습니다. 주요 통화별 환율변동시 민감도 분석내용은 다음과 같습니다.
(단위 : 천원)
| 구분 | 당기말 | 전기말 | ||
| 10%상승 | 10%하락 | 10%상승 | 10%하락 | |
| 외환환산손익 | 93,299 | (93,299) | 114,935 | (114,935) |
(나) 이자율위험관리
연결실체는 고정이자율과 변동이자율로 자금을 차입하고 있으며, 이로 인하여 이자율위험에 노출되어 있습니다. 연결실체는 고정금리차입금과 변동금리차입금의 적절한 균형유지 정책을 수행하는 등 이자율위험을 관리하고 있으며, 이자율위험에 노출된 차입금 내용은 다음과 같습니다.
(단위 : 천원)
| 구분 | 당분기말 | 전기말 |
| 차입금 | 3,327,510 | 2,905,036 |
이자율 1% 변동시 민감도 분석내용은 다음과 같습니다.
(단위 : 천원)
| 구분 | 당분기말 | 전기말 | ||
| 1%상승 | 1%하락 | 1%상승 | 1%하락 | |
| 이자비용 | (33,275) | 33,275 | (29,050) | 29,050 |
(다) 기타 위험 요소
당사는 세계적인 고부가가치 제품을 개발, 제조, 판매하는 회사로서 원재료 비율이 타 제조업에 비해 현저히 낮아 원재료 가격의 변동으로 인한 예상치 못한 손실을 일으킬 가능성이 미미하며, 또한 원재료가 천연물(소뼈, 말뼈 등)인 경우 천재지변 등에 의해 원료수급이 불안정해질수 있으나, 이는 원료 수입 경로를 다양하게 하고 연간 필요 물량을 기확보한 상태로 공정을 진행하므로 크게 문제될 부분은 없습니다.
8. 파생상품거래 현황
당사는 보고서 제출일 현재 당사가 보유하고 있는 파생상품은 없습니다.
9. 경영상의 주요계약
(가) 라이센스아웃(License-out) 계약
공시서류 작성기준일 현재 당사가 체결 중인 라이센스아웃(License-out) 계약의현황은 다음과 같습니다
| <라이센스아웃 계약 총괄표> |
| (단위: 백만원) |
|
품 목 |
계약상대방 |
대상지역 |
계약체결일 |
계약종료일 |
총계약금액 |
수취금액 |
진행단계 |
|---|---|---|---|---|---|---|---|
|
펩타이드 플랫폼 |
Straumann |
전세계 (한국제외) |
2017.03.21 |
각 제품별 및 국가별로 선정된 "제품 출시후 10년" 또는 "특허만료일"중 긴 기간 |
1,125 |
제품개발 논의중 |
|
|
합 계 |
1,125 |
||||||
주) 상기 금액은 계약일자의 최초고시환율인 1,124.50원을 적용.
(1) 품 목:펩타이드 플랫폼 기술이전 건.
|
①계약상대방 |
Straumann (유럽) |
|
②계약내용 |
치료용 펩타이드 기술은 현재 전임상 단계로 향후 진행되는 임상비용 및 상업화에 소요되는 경비에 대하여는 별도로 지급받음. 임상완료후 제품을 출시예정이며, 향후 매출발생에 따른 경상기술료(running royalty)는 상기금액과 별도로 지급받음. 이전되는 기술에 대하여 계약상대방은 치과영역(Dental Filed)에서만 활용하는 것으로 제한됨. |
|
③대상지역 |
전세계(한국제외) |
|
④계약기간 |
계약체결일:2017.03.21 계약종료일:각 제품별 및 국가별로 선정된 "제품 출시후 10년" 또는 "특허만료일"중 긴 기간 |
|
⑤총계약금액 |
초기기술료 USD 1,000,000 (한화 1,124,500,000원) |
|
⑥수취금액 |
<반환의무 없는 금액> 계약금(Upfront Payment): USD 1,000,000 (2017.03.30 수취) <반환의무 발생가능 금액> 해당사항 없음 |
|
⑦계약조건 |
계약금(Upfront Payment): USD 1,000,000 - 수취조건: 계약 체결 7일이내
임상, 등록, 상업화 실패시 계약은 종료될 수 있으며, 계약 종료시에도 회사의 위약금 지급의무는 없음 |
|
⑧회계처리방법 |
계약금 수취액 1,124,500,000원(USD 1,000,000)은 수익 인식 |
|
⑨대상기술 |
치료용 펩타이드 신약 발굴 플랫폼 기술로 치과치료제, 치과재생용 바이오소재 개발 기술 |
|
⑩개발진행경과 |
거래 상대방과 회사는 본 계약 체결 이후 펩타이드 기술을 적용한 제품 개발에 대하여 협의를 진행 중임. |
|
⑪기타사항 |
(나) 판매계약
| (단위: 천미불) |
|
업 체 명 |
주요계약품목 |
계약일자 |
계약만료일 |
계약금액 |
|---|---|---|---|---|
|
Hi-Clearance |
치과용 골이식재 |
2014-08-18 |
2020-12-31 |
1,290 |
|
Almas Rouyan Pars |
치과용 골이식재 |
2014-12-31 |
2020-12-22 |
1,200 |
|
Nobel Biocare |
치과용 골이식재 |
2015-12-14 |
2021-12-31 |
13,926 |
|
Araguaney Professional |
치과용 골이식재 |
2017-03-13 |
2022-03-09 |
810 |
|
Wright Health Group |
치과용 골이식재 |
2017-03-27 |
2019-12-31 |
700 |
|
Straumann |
치과용 골이식재 |
2019-02-21 |
2024-02-20 |
21,982 |
|
합 계 |
|
|
39,908 |
|
보고서 작성일 현재 기준입니다.
10. 연구개발 활동
가. 연구개발 활동 개요
당사는 펩타이드를 기반으로 하는 바이오 의약품 개발관련 신성장동력사업을 비롯하여 조직재생용바이오소재 기반사업에 대한 연구를 진행 중으로 현재 펩타이드 바이오 의약품 개발 관련 5개의 파이프라인을 구축하여 임상 1상 및 전임상 단계의 연구를 진행하고 있습니다.
|
품목 |
제품 |
제품 설명 |
|---|---|---|
|
펩타이드 의약품 |
골다공증치료제 (NIPEP-OSS= Osseotide) |
골 재생 기능 펩타이드 함유 골다공증 치료제 |
|
관절염 치료제 (NIPEP-CARE 1) |
염증 억제 기능 펩타이드 함유 관절염 치료제 |
|
|
비알콜성지방간염(NASH) 치료제 (NIPEP-CARE 2) |
염증 및 지방 억제 기능 펩타이드 함유 비알콜성지방간염 치료제 |
|
|
염증성 장질환(IBD) 치료제 (NIPEP-CARE 3) |
염증 억제 기능 및 점막 재생 기능 펩타이드 함유 염증성장질환 치료제 |
|
|
항암치료제 (NIPEP-ACD-Tide) |
종양선택적 투과기능이 탑재된 종양 치료 및 전이암, 내성암 치료제 |
나. 연구개발 담당 조직
(1) 연구개발 조직 개요
당사의 중앙연구소는 크게 첨단소재개발과 품질 파트로 나눠지며, 첨단소재개발 관련하여 3개의 팀과 품질 관련 2개팀으로 구분되어 총 5개의 팀으로 이뤄져있으며 연구개발 조직 구성은 아래와 같습니다.
| <연구개발 조직 구성> |
|
연구소 |
팀 |
주요 업무 |
|---|---|---|
|
첨단의약소재 |
신제품개발팀 |
제품 연구설계 및 신제품 개발 관련 업무 |
|
펩타이드개발팀 |
바이오 의약품 관련 실험 및 연구개발 업무 |
|
|
효능평가팀 |
신제품 및 후보물질 등 효능 평가 업무 |
|
|
바이오소재 연구팀 |
바이오소재 개발팀 |
제품 성능 보증 위한 전반적 업무 |
|
바이오소재 최적화, 상용화연구팀 |
품상용화 단계 품질관리 업무 및 중개연구 |
| <연구소 조직도> |
 |
|
연구소 조직조 |
(2) 연구개발 인력현황
공시서류 작성기준일 현재 당사는 박사급 3명, 석사급 13명 등 총 31명의 연구인력을 보유하고 있으며, 그 현황은 다음과 같습니다.
| <연구개발 인력 현황> |
| (단위: 명) |
|
구 분 |
인 원 |
||||
|---|---|---|---|---|---|
|
박 사 |
석 사 |
학사 외 |
합 계 |
||
|
첨단의약소재연구팀 |
신제품개발팀 |
3 |
1 |
4 |
|
|
펩타이드개발팀 |
2 |
6 |
1 |
9 |
|
|
효능평가팀 |
1 |
4 |
5 |
||
|
바이오소재 연구팀 |
바이오소재 개발팀 |
1 |
1 |
3 |
4 |
|
바이오소재 최적화, 상용화연구팀 |
2 |
6 |
8 |
||
|
합 계 |
3 |
13 |
15 |
31 |
|
당사는 공시자료 제출일 현재 전체임직원수의 약45%의 연구진과 개발인력을 확보하고 있는 R&D기업입니다. 모두 약학, 분자생물학,생화학, 유기합성, 화학공학 등의 전공자들로서 충분한 연구경험을 가지고 있습니다.당사는 당사의 우수연구인력 이외에도, 기타 국내 외 우수 대학 및 기관들과 연구협력 네트워크를 구축하여 기술의 완성도를 높일 수 있도록 제품 성능을 구현하는 기술들의 신뢰성을 확보할 수 있는 연구들을 진행하고 있습니다.
(주)나이벡 중앙연구소에는 5개의 팀이 있으며, 신제품개발팀, 펩타이드 개발팀, 효능평가팀에서 펩타이드 발굴과 응용 및 조직재생용 바이오소재 개발, 의약품 제형설계의 기초 및 효력검증연구를 진행하고 있습니다. 특히 원천기술을 발굴하여 검증하고, 제형을 확립한 후 pilot형태의 시제품을 제작하여 생산본부와의 연계를 이루도록 하고 있습니다.
바이오소재 연구팀은 제품의 생산, 출하 및 유통이 제조기준 및 관리기준에 의거하여 엄격히 진행하고 있음을 항시 모니터링하여 최전방에서 보증하는 업무를 수행하며 특히 당사의 GMP인증, 각종 규격인증의 업무를 수행하고 있습니다.
(3) 핵심연구인력
이 중 당사의 핵심 연구인력은 대표이사인 정종평, 연구소 전반의 총괄업무를 담당하고 있는 전무이사 박윤정, 중앙연구소 및 프로젝트 총괄업무를 담당하는 연구소장 이주연등 입니다. 대표이사인 정종평은 서울대학교 치과대학에서 치주학을 전공한 박사로 치주염증을 비롯한 치과 분야 관련 연구를 계속해왔으며, 치과 임상의로서 다양한 환자 케이스를 통하여 나이벡의 기반사업인 조직재생용바이오소재 연구개발에 이바지 하였으며 R&D 및 경영총괄을 맡고 있습니다. 또한 연구소의 총괄업무를 담당하는 박윤정 전무이사는 현재 서울대학교 치의학대학원 교수 재직중으로 당사의 연구개발 관련 산학협력활동 및 우수한 연구적 네트워크를 구축, 활용하여 우수한 양질의 연구 결과 도출에 이바지하였습니다. 박윤정 전무이사와 중앙연구소 프로젝트 총괄업무를 담당하는 이주연이사는 약학을 전공한 약학박사로 펩타이드를 이용한 약물전달시스템을 비롯한 펩타이드 기반 바이오 의약품 개발 관련하여 다수의 논문 및 특허, 그리고 영향력 있는 바이오 학회 초청 발표 등 활발한 연구 활동을 계속해오고 있는 당사의 핵심인력입니다.
| <핵심 연구인력 현황> |
|
직 위 |
성 명 |
담당업무 |
주요 경력 |
주요 연구실적(대표논문5건) |
|---|---|---|---|---|
|
대표이사 |
정종평 |
총괄업무 |
서울대학교 치과대학 치의학 석사(‘72.02) 서울대학교 치과대학 치의학 박사(‘79.02) 미국뉴욕주립대학교 교환교수(82.12) 서울대학교 치과대학 교수(11.02) 서울대학교 치과대학 학장(02.02) 지능형생체게면공학 연구센터 센터장(‘09.03) |
The effect of the surface modification of titanium using a recombinant fragment of fibronectin and vitronectin on cell behavior, Biomaterials (26(25), 5153-5157), 2005 Electrospinning of chitin nanofibers: Degradation behavior and cellular response to normal human keratinocytes and fibroblasts, Biomaterials (27(21), 3934-3944). 2006 Assembly of collagen-binding peptide with collagen as a bioactive scaffold for osteogenesis in vitro and in vivo, Biomaterials (28(29), 4257-4267), 2007 Osteoblastic differentiation of human bone marrow stromal cells in self-assembled BMP-2 receptor-binding peptide-amphiphiles, Biomaterials. (30(21), 3532-3541), 2009 Peptide-mediated intracellular delivery of miRNA-29b for osteogenic stem cell differentiation, Biomaterials. 34(17):4347-59, 2013 |
|
전무이사 |
박윤정 |
연구소 전반 총괄업무 |
이화여자대학교 약학 석사(‘95.02) 이화여자대학교 약제학 박사(‘99.02) 미시간대학 약학대학 연구원(‘02.02) 미시간대학 약학대학 연구교수(‘03.05) 서울대학교 치의학대학원 교수(현재) |
Intracellular delivery of cell-penetrating peptide-transcriptional factor fusion protein and its role in selective osteogenesis, Int J Nanomedicine. 9:1153-66, 2014 Simultaneous imaging and restoration of cell function using cell permeable peptide probe, Biomaterials. 35(24):6287-98, 2014 Selective osteogenesis by a synthetic mineral inducing peptide for the treatment of osteoporosis, Biomaterials. 35(37):9747-54, 2014 Identification of cell-penetrating peptide domain from human beta-defensin 3 and characterization of its anti-inflammatory activity, Int J Nanomedicine. 26;10:5423-34., 2015 Dual-function synthetic peptide derived from BMP4 for highly efficient tumor targeting and antiangiogenesis, nt J Nanomedicine. 11;4643-4656, 2016 |
|
이사 (연구소장) |
이주연 |
중앙연구소 프로젝트 총괄업무 |
이화여자대학교 약학 석사(‘00.02) 이화여자대학교 약제학 박사(‘04.02) 서울대학교 치과대학 지능형생체계면공학연구센터(IBEC) Post-Doctoral Research Fellowship |
Identification of cell-penetrating peptide domain from human beta-defensin 3 and characterization of its anti-inflammatory activity, Int J Nanomedicine. 26;10:5423-34., 2015 Dual-function synthetic peptide derived from BMP4 for highly efficient tumor targeting and antiangiogenesis, nt J Nanomedicine. 11;4643-4656, 2016 Control of cancer stem cell like population by intracellular target identification followed by the treatment with peptide-siRNA complex, Biochem Biophys Res Commun, 491(3):827-833, 2017 Comparative Study of rhPDGF-BB Plus Equine-Derived Bone Matrix Versus rhPDGF-BB Plus β-TCP in the Treatment of Periodontal Defects, Int J Periodontics Restorative Dent, 37(6):825-832, 2017 A novel calcium-accumulating peptide/gelatin in situ forming hydrogel for enhanced bone regeneration, J Biomed Mater Res A, 106(2):531-542, 2018 |
다. 연구개발비용
당사는 일반적으로 신약 개발 프로젝트가 임상 3단계를 통과한 이후 발생한 지출을무형자산으로 인식하고, 이전 단계에서 발생한 지출은 당기비용으로 회계처리하고 있습니다.
당사의 최근 3년간 연구개발비용은 다음과 같습니다.
| <연구개발비용 현황> |
| (단위: 천원, %) |
|
구 분 |
2018년 |
2017년 |
2016년 |
|
|---|---|---|---|---|
|
비용의 성격별 분류 |
원재료비 |
21,300 |
44,408 |
65,850 |
|
인건비 |
961,774 |
973,219 |
399,181 |
|
|
감가상각비 |
28,865 |
28,346 |
31,076 |
|
|
위탁용역비 |
928,156 |
943,722 |
1,151,919 |
|
|
기타 |
554,482 |
703,993 |
921,086 |
|
|
연구개발비용 합계 |
2,494,577 |
2,693,688 |
2,569,112 |
|
|
(정부보조금) |
(199,951) |
(1,074,296) |
(2,058,457) |
|
|
보조금 차감 후 금액 |
2,294,626 |
1,619,392 |
510,655 |
|
|
회계처리 내역 |
판매비와 관리비 |
1,204,012 |
557,939 |
251,727 |
|
제조경비 |
224,004 |
227,645 |
118,368 |
|
|
개발비(무형자산) |
1,066,561 |
1,908,104 |
2,199,017 |
|
|
회계처리금액 계 |
2,494,577 |
2,693,687 |
2,569,112 |
|
|
연구개발비 / 매출액 비율 [연구개발비용합계÷당기매출액×100] |
47.90% |
42.74% |
53.48% |
|
라. 연구개발실적
(1)연구개발 진행 현황 및 향후계획
공시서류 작성기준일 현재 당사가 연구개발 진행 중인 신약[개량신약 등 포함]의 현황은 다음과 같습니다.
|
구 분 |
품 목 |
적응증 |
연구시작일 |
현재 진행단계 |
비 고 |
||
|---|---|---|---|---|---|---|---|
|
단계(국가) |
승인일 |
||||||
|
바이오 (식약처 구분 : 화학합성 신약) |
신약 |
NIPEP-OSS (Osseotide) |
골다공증 및 골재생 치료제 |
2011년 |
전임상 완료 |
2019년 예정 |
공동개발 정부보조금 |
|
NIPEP-CARE1 |
관절염 치료제 |
2013년 |
전임상 안전성 시험진입 |
- |
공동개발 정부보조금 |
||
|
NIPEP-CARE2 |
비알코올성간염NASH)치료제 |
2016년 |
전임상 효능시험 중 |
- |
공동개발 정부보조금 |
||
|
NIPEP-CARE3 |
염증성 장질환 치료제 |
2016년 |
전임상 효능시험 중 |
- |
공동개발 정부보조금 |
||
|
NIPEP-ACD-TIDE |
암줄기세포 표적 항암 치료제 |
2008년 |
전임상 효능시험 중 |
- |
공동개발 정부보조금 |
||
|
개량신약 |
OssGen better |
PTH 골다공증치료제 바이오베터 |
2016년 |
전임상 효능시험 중 |
- |
정부보조금 |
|
(가)품 목: NIPEP-OSS (Osseotide)
|
①구 분 |
바이오 신약(화학합성법으로 제조) |
||||||||||||||||||||||||||||||
|
②적응증 |
골다공증,골재생 치료제 |
||||||||||||||||||||||||||||||
|
③작용기전 |
골조직세포외기질에 결합 후,골아세포의 수용체와 결합,세포내 골재생 신호전달 증가,지방분화 신호전달 억제 |
||||||||||||||||||||||||||||||
|
④제품의특성 |
기존의 골다공증 치료제는 골흡수를 억제하는 기전인 비스포스포네이트가 가장 많이 사용되고 있으나, 장기간 사용시 과도하게 골흡수를 억제하여 골질이 약해서 골절 위험이 증가합니다. 유일한 골형성 촉진 기전의 테리파라타이드는 고칼슘혈증을 유 발하거나, 장기간 사용시 골육종을 일으키는 위험성이 있는 것으로 알려져 있음.
|
||||||||||||||||||||||||||||||
|
⑤진행경과 |
현재 전임상 독성시험(독일 소재 GLP 기관, LPT)을 완료하였고, 2018년 12월에 한국 식약처 임상1상 시험 승인을 신청하여, 현재 보완사항 중.2019년 임상1상 진입 예정. |
||||||||||||||||||||||||||||||
|
⑥향후계획 |
임상1상 실시: 2019.06-2020.12,한국 임상1상 후 라이센스 아웃 또는 공동기술개발 임상2상 신청 및 실시:2021.01-2023.01,다국가 임상 임상3상 신청 및 실시:2023.12-2025.12,다국가 임상 |
||||||||||||||||||||||||||||||
|
⑦경쟁제품 |
현재 FDA 승인이 된 골다공증 치료제 리스트
|
||||||||||||||||||||||||||||||
|
⑧관련논문등 |
국내특허등록 (등록번호: 1638775), 국내특허출원 (출원번호: 10-2017-0126876, 등록결정) 및 전세계 특허 (미국, 유럽, 중국, 일본) 논문발표
학회발표
|
||||||||||||||||||||||||||||||
|
⑨시장규모 |
<골다공증 치료제 세계시장 규모> (단위 : 억달러)
자료 : Osteoporosis-Pipeline Assessment & Market Forecast to 2017, Global Data,2010 CAGR 근거 년도 : 2018-2030년: 8.2% |
||||||||||||||||||||||||||||||
|
⑩기타사항 |
참여기관:(주)나이벡, 서울대학교 치의학대학원, 이대목동병원, 충북대학교, 아산병원, 연대 세브란스, 독일 LPT |
(나)품 목: NIPEP-CARE1
|
①구 분 |
바이오 신약 (화학합성법으로 제조) |
||||||||||||||||||||||||||||||||||||||||||||
|
②적응증 |
관절염 치료제 |
||||||||||||||||||||||||||||||||||||||||||||
|
③작용기전 |
세포막을 투과하여 세포핵내 histone deacetylase의 활성을 저해함으로써 염증성 사이토카인의 생성 억제 |
||||||||||||||||||||||||||||||||||||||||||||
|
④제품의특성 |
NIPEP-CARE1는 인체내 면역에 관계하는 단백질로부터 유래한 펩타이드로서, 염증 신호에 관계하는 전사인자를 억제하여 염증성 사이토카인의 생성을 억제함으로써 항 염증 효과를 가지게 됨.관절염 유발 동물 모델에 투여했을 때, 엔브렐 (etanercept)보다 염증지수 완화 및 골소실 억제 연골보호 효과가 우수한 것을 증명하였음. 또한, 세포투과 및 피부로도 투과가 가능하여 주사제 이외의 피부 적용제형으로 개발이 가능함. 관절염 치료제로 많이 사용되는 생물학적 제제로는 TNF-a 차단제가 있으나, 과도하게 면역반응을 차단하여 감염이나 결핵을 유발하는 부작용이 있음.
|
||||||||||||||||||||||||||||||||||||||||||||
|
⑤진행경과 |
전임상 독성시험을 진행 중 |
||||||||||||||||||||||||||||||||||||||||||||
|
⑥향후계획 |
2019년 12월에 전임상 완료 2020년 한국 식약처 임상1상 시험 승인을 신청 계획 전임상 완료 또는 임상1상 후 라이센스 아웃 또는 공동기술개발 |
||||||||||||||||||||||||||||||||||||||||||||
|
⑦경쟁제품 |
현재 개발 중인 관절염 치료제 리스트
|
||||||||||||||||||||||||||||||||||||||||||||
|
⑧관련논문등 |
국내특허등록 (등록번호: 1329774) 및 전세계 특허 (미국, 유럽, 캐나다) 논문발표
학회발표
|
||||||||||||||||||||||||||||||||||||||||||||
|
⑨시장규모 |
<관절염 치료제 세계시장 규모> (단위:억달러)
자료 : Arthritis Therapeutics Market to 2016, GBI research, 2010 CAGR 근거 년도: 골관절염 치료제 2018-2030년 2%, 류마티스 관절염 치료제 2018-2030년 8.6%, 관절염 치료제 2018-2030년 7.7 % |
||||||||||||||||||||||||||||||||||||||||||||
|
⑩기타사항 |
참여기관: (주)나이벡, 서울대학교 치의학대학원, 충북대학교, 아산병원, |
(다)품 목: NIPEP-CARE2
|
①구 분 |
바이오 신약 (화학합성법으로 제조) |
||||||||||||||||||
|
②적응증 |
비알코올성 간염 (NASH) 치료제 |
||||||||||||||||||
|
③작용기전 |
비알코올성 간염의 다중 바이오마커를 제어하여 간조직의 염증,지방 침착 억제 |
||||||||||||||||||
|
④제품의특성 |
NIPEP-CARE2는 인체내 면역에 관계하는 단백질로부터 유래한 펩타이드로서, methionine 결핍 식이에 의해 지방간 유발 동물모델에 투여했을 때, NIPEP-CARE2 에 의한 비알코올성 지방간의 NAS score (ballooning degeneration, lobular inflamm ation, steatosis)가 감소하였고, 간과 혈액에서 염증성 사이토카인의 발현이 감소하였음. |
||||||||||||||||||
|
⑤진행경과 |
전임상 효능시험 진행 중 |
||||||||||||||||||
|
⑥향후계획 |
2019년 12월에 전임상 완료 2021년 한국 식약처 임상1상 시험 승인을 신청 계획 전임상 완료 또는 임상1상 후 라이센스 아웃 또는 공동기술개발 |
||||||||||||||||||
|
⑦경쟁제품 |
현재까지 FDA에 허가 받은 치료제는 없는 상황이며, 개발 중인 비알코올성 간염 치료제 현황은 다음과 같음, 1)혈중 지질감소, 임상3상 2)콜릭액시드 생합성 수용체에 영향을 줌, LDL 증가시킴, 임상 3상 3)Stearoyl-CoA desaturase 1 저해제. 지방침착 저해, 임상 2상에서 계류 중 |
||||||||||||||||||
|
⑧관련논문등 |
- 국내특허출원 (출원번호: 10-2018-0103614) - 국내외 논문 게재 중 |
||||||||||||||||||
|
⑨시장규모 |
<비알코올성 간질환 치료제 세계시장 규모> (단위 : 억달러)
자료 : Allied Market research, NASH market, 2018-2030 CAGR 근거 년도 : 2018-2030년: 25.6% |
||||||||||||||||||
|
⑩기타사항 |
참여기관: (주)나이벡, 서울대학교 치의학대학원, 충북대학교, 아산병원, 질병관리본부 |
(라)품 목: NIPEP-CARE3
|
①구 분 |
바이오 신약 (화학합성법으로 제조) |
|||||||||||||||||||
|
②적응증 |
염증성 장질환 (inflammatory bowel disease) 치료제 |
|||||||||||||||||||
|
③작용기전 |
장점막 조직의 면역조절 펩타이드에 의해 염증성 장질환 치료 및 점막재생 |
|||||||||||||||||||
|
④제품의특성 |
NIPEP-CARE는 HDAC 저해에 의한 염증 감소와 대장 점막에 존재하는 콜라겐에 대한 자가 면역반응을 감소시켜 장점막의 재생을 증가시키는 작용이 있음. 나이벡이 가진 기술로 경구용 제형확립 |
|||||||||||||||||||
|
⑤진행경과 |
전임상 효능시험 진행 중 |
|||||||||||||||||||
|
⑥향후계획 |
2019년 12월에 전임상 완료 2021년 한국 식약처 임상1상 시험 승인을 신청 계획 전임상 완료 또는 임상1상 후 라이센스 아웃 또는 공동기술개발 |
|||||||||||||||||||
|
⑦경쟁제품 |
현재, 1차 치료로 사용하는 약물은 Aminosalicylic acid 로 주로 증상완화에 사용하고 있으며, 이 약에 반응하지 않을 때, 스테로이드를 사용함. 이렇게 해도 효능이 없거나 부작용이 발생하게 되면, 면역제제나 생물학적 제제를 사용함.생물학적 제제인 TNF-a 차단제는 면역반응을 오히려 억제하는 부작용을 가지고 있음. |
|||||||||||||||||||
|
⑧관련논문등 |
- 국내특허출원 (출원번호: 10-2018-0103615 ) - 국내외 논문 게재 중 |
|||||||||||||||||||
|
⑨시장규모 |
(단위 : 억달러)
자료 : Vision gain, Global Inflammatory Bowel Disease drug Market Forecast 2018-2030 CAGR 근거 년도 : 2018-2030년: 2.5% |
|||||||||||||||||||
|
⑩기타사항 |
참여기관:(주)나이벡, 서울대학교 치의학대학원, 충북대학교, 아산병원 |
(마)품 목: NIPEP-ACD-TIDE
|
①구 분 |
바이오 신약(화학합성법으로 제조) |
|||||||||||||||||||||
|
②적응증 |
신규 바이오마커 제어기반 암줄기세포치료제 및 표적조직 투과기능성 펩타이드 표적항암제 |
|||||||||||||||||||||
|
③작용기전 |
암줄기세포발현 바이오마커를 제어하는 세포내투과기능성 펩타이드 및 이를 기반으로 한 표적항 암치료제 |
|||||||||||||||||||||
|
④제품의특성 |
NIPEP-ACD-TIDE는 암줄기세포내 바이오마커를 억제함으로써, 암줄기세포의 이동, 부착과 전이를 억제하는 기능이 있음. 또한, 세포투과기능이 있기 때문에, 항암효과가 있는 단백질 또는 항체와 결합하여 세포내 전달수단 및 병용투여 요법으로 사용가능 함. |
|||||||||||||||||||||
|
⑤진행경과 |
전임상 효능시험 진행 중 |
|||||||||||||||||||||
|
⑥향후계획 |
2020년 전임상 완료. 2022년 한국 식약처 임상1상 시험 승인을 신청 계획 전임상 완료 또는 임상1상 후 라이센스 아웃 또는 공동기술개발 |
|||||||||||||||||||||
|
⑦경쟁제품 |
항암 치료 후에 암이 다시 재발하거나 전이되는 이유는 암세포 중에 암줄기세포가 존재하여, 항암치료에도 살아남아 다시 증식을 하기 때문임. 따라서, 이들 암줄기 세포를 타겟으로 하는 항암제가 개발된다면, 암전이나 재발의 확률이 감소할 것임. 현재, 암줄기세포를 타겟하는 약물을 개발되지 않았음. |
|||||||||||||||||||||
|
⑧관련논문등 |
국내특허등록 (등록번호: 101693533) 및 전세계 특허 (미국, 유럽) 논문발표
학회발표
|
|||||||||||||||||||||
|
⑨시장규모 |
<항암 치료제 세계시장 규모> (단위 : 억달러)
자료: Persistence market research, 항암제 글로벌 마켓 CAGR 근거 년도 : 2018-2030년: 7.4% |
|||||||||||||||||||||
|
⑩기타사항 |
참여기관: (주)나이벡, 서울대학교 치의학대학원, 충북대학교, 아산병원, 프랑스와 영국 바이오텍회사 |
(바)품 목: OssGen Biobetter
|
①구 분 |
바이오 신약 (화학합성법으로 제조) |
||||||||||||||||||||||||
|
②적응증 |
골다공증 치료제 |
||||||||||||||||||||||||
|
③작용기전 |
PTH 골다공증 치료제의 효능과 안전성 증가를 위한 바이오베터 |
||||||||||||||||||||||||
|
④제품의특성 |
PTH는 고칼슘혈증을 일으키고, 2년이상 사용이 제한되어 있음. 또한, 골조직뿐만 아니라 신장에도 영향을 줌. PTH의 골조직으로의 분포를 증가시킴으로써,PTH의 부작용은 감소시키고, 효능은 증가시킴. |
||||||||||||||||||||||||
|
⑤진행경과 |
전임상 효능 및 분포시험 진행 중 |
||||||||||||||||||||||||
|
⑥향후계획 |
2020년 전임상 완료. 2022년 한국 식약처 임상1상 시험 승인을 신청 계획 전임상 완료 또는 임상1상 후 라이센스 아웃 또는 공동기술개발 |
||||||||||||||||||||||||
|
⑦경쟁제품 |
현재 FDA 승인이 된 골다공증 치료제 리스트
|
||||||||||||||||||||||||
|
⑧관련논문등 |
국내특허출원 (출원번호: 10-2017-0126876, 등록결정) 및 전세계 특허 (미국, 유럽, 중국, 일본) 학회발표
|
||||||||||||||||||||||||
|
⑨시장규모 |
<골다공증 치료제 세계시장 규모> (단위 : 억달러)
자료 : Osteoporosis-Pipeline Assessment & Market Forecast to 2017, Global Data,2010 CAGR 근거 년도 : 2018-2030년: 8.2% |
||||||||||||||||||||||||
|
⑩기타사항 |
참여기관:(주)나이벡, 서울대학교 치의학대학원, 이대목동병원, 충북대학교, 아산병원 |
(2)연구개발 완료 실적
| <연구개발 완료 실적> |
|
구 분 |
품 목 |
효능 |
개발완료일 |
현재 현황 |
비 고 |
|---|---|---|---|---|---|
|
조직재생바이오사업 |
치과용 골이식재 (OCS-B/OCS-H) |
골재생촉진 |
2005.09.15. (2007.06.21 정부 판매승인일) |
한국, EU, 미국을 비롯한 전세계 대상으로 판매중 |
-중국 판매허가를 위한 임상시험 완료 -국내 아이비덴탈과 유통계약, 해외는 Straumann, Nobel Biocare 등과의 계약 |
|
치주조직재생용 쉬트 (GuidOss) |
치주조직 재생능 |
2011.04.12 |
한국 판매중 |
-중국 판매허가를 위한 임상시험 진행중 -국내 아이비덴탈과 유통계약, 해외는 Straumann과의 유통계약 |
|
|
치주조직재생용 콜라겐 창상수복재 (Regenomer) |
치주창상대체, 치주조직 형성 촉진 |
2011.08.01 |
한국, 미국, EU 판매중 |
-국내 아이비덴탈과 유통계약 해외는 Straumann과의 유통계약 |
|
|
골재생용 복합소재 (OCS-Collagen) |
골재생촉진을 위한 골미네랄 입자와 콜라겐의 복합이식용 소재 |
2014.07.25 |
한국, EU, 미국을 비롯한 전세계 대상으로 판매중 |
-국내 아이비덴탈과 유통계약, 해외는 Straumann, Nobel Biocare 등과의 계약 |
|
|
펩타이드 융합복합 바이오소재 (OssGen X-15) |
펩타이드가 융합된 골재생바이오소재 |
2011.10.12 |
한국 대상으로 판매중 미국 및 유럽 판매허가 진행중 |
-국내 아이비덴탈과 유통계약 |
|
|
구강보건사업 |
치아미백제 (Dr.Whitiss / |
약물전달시스템 기술 이용한 치아미백제 |
2010.04.20 2015.04.08 |
한국 대상으로 판매중 일반인 사용 가능 의약외품 및 전문가 사용 전문의약품 모두 생산 |
-온라인 판매(의약외품) -치과 유통 판매(전문의약품) |
|
시린이치료제 (Sensblok) |
시린이증상경감 |
2008.08.01 |
한국 대상으로 판매중 |
-온라인 판매 및 치과 유통 판매 |
|
|
치과용항생연고 (Minucure) |
치주염항생제 |
2015.05.29 |
한국 대상으로 판매중 |
-휴온스와 국내 유통계약 -치과 유통 판매 |
|
|
임플란트주위염 예방치료제 (Clinplant) |
항염물질 임플란트 주위염 예방제 |
2009.12.17 |
한국 대상으로 판매중 미국 및 유럽 비롯 전세계 판매중 |
-휴온스와 국내 유통계약 -해외 Straumann 과 유통계약 |
(1) 펩타이드 신약
(가) 골다공증 치료용 펩타이드 의약품
|
제품명 |
NIPEP-OSS (Osseotide) |
|
제품의 내용 |
골조직 선택성이 우수한 펩타이드 19mer로 이루어진 골다공증 및 골재생치료용 주사제 |
|
개발과정 |
- 국내특허등록 (등록번호: 1638775), 국내특허출원 (출원번호: 10-2017-0126876, 등록결정) 및 전세계 특허 (미국, 유럽, 중국, 일본) - 대량생산 공정 확립 - 식약처 임상1상 시험 승인 신청서 제출 |
|
참여기관 |
(주)나이벡, 서울대학교 치의학대학원, 이대목동병원, 충북대학교, 아산병원, 연대 세브란스, 독일 LPT |
(나) 관절염 치료용 펩타이드 의약품
|
제품명 |
NIPEP-CARE 1 |
|
제품의 내용 |
세포투과능이 우수함과 동시에 다중의 염증성 바이오마커를 제어하는 항염 및 연골재생기능성 펩타이드 치료제 |
|
개발과정 |
- 국내특허등록 (등록번호: 1329774) 및 전세계 특허 (미국, 유럽, 캐나다) - 대량생산 공정 확립 |
|
참여기관 |
(주)나이벡, 서울대학교 치의학대학원, 충북대학교, 아산병원, |
(다) 비알콜성 간염 (NASH)치료제
|
제품명 |
NIPEP-CARE2 |
|
제품의 내용 |
비알콜성 간염의 다중 바이오마커를 제어하는 펩타이드 주사제 |
|
개발과정 |
- 국내특허출원 (출원번호: 10-2018-0103614)) - 전임상 효능시험 |
|
참여기관 |
(주)나이벡, 서울대학교 치의학대학원, 충북대학교, 아산병원, 질병관리본부 |
(라) 염증성 장질환 (IBD)치료제
|
제품명 |
NIPEP-CARE3 |
|
제품의 내용 |
장점막조직의 면역조절펩타이드에 의한 염증성 장질환 치료 및 점막재생기능 치료제 |
|
개발과정 |
- 국내특허출원 (출원번호: 10-2018-0103615 ) - 경구용 제형확립 |
|
참여기관 |
(주)나이벡, 서울대학교 치의학대학원, 충북대학교, 아산병원, |
(마) 신규 바이오마커 제어기반 암줄기세포치료제 및 표적조직 투과기능성 펩타이드 표적항암제
|
제품명 |
NIPEP-ACD-TIDE |
|
제품의 내용 |
암줄기세포발현 바이오마커를 제어하는 세포내투과기능성 펩타이드 및 이를 기반으로 한 표적항암치료제 |
|
개발과정 |
- 국내특허등록 (등록번호: 101693533) 및 전세계 특허 (미국, 유럽) - 국내외 논문 게재 (Biomaterials, Int. J. Nanomedicine, BBRC) |
|
참여기관 |
(주)나이벡, 서울대학교 치의학대학원, 충북대학교, 아산병원, 오송첨단의료산업재단 |
(2) 조직재생용 바이오소재
(가) 치과용 골이식재
|
제품명 |
치과용 골이식재 |
|
제품의 내용 |
동물(소뼈 및 말뼈)유래 생체재료로부터 추출된 순수 아파타이트 기반 치과용 골이식재 |
|
개발과정 |
- 국내특허등록 (등록번호: 0635385) 및 PCT국제 특허 출원 (PCT/KR2006/001713) 및 전세계 특허 확보 프라이온-프리 골 이식 대체재의 제조방법 -미국 하버드대학교 임상시험 완료 -중국 임상시험 완료, 중국식약처 허가신청 |
|
참여기관 |
(주)나이벡, 서울대학교 치의학대학원, 서울대학교 치과병원 |
(나) 치주조직재생용 쉬트 (콜라겐)
|
제품명 |
GuidOss |
|
제품의 내용 |
치주조직재생용 콜라겐 차폐막 |
|
사업명 |
지식경제부지원 충청광역경제권선도사업 |
|
개발과정 |
- 국내특허출원 (출원번호:10-2011-0037839,10-2011-0037840) - 단국대학교 치과병원, 원광대학교 치과병원 임상시험완료 - 중국 임상시험 진행중 |
|
참여기관 |
(주)나이벡, 한국생명공학연구원, 서울대학교 치의학대학원, 단국대학교치과병원, 원광대학교치과병원, 서울대학교 치과병원 |
(다) 치주조직재생용 콜라겐 창상수복재
|
제품명 |
Regenomer |
|
제품의 내용 |
발치된 부위에 삽입하여 창상을 대체하고 조직의 형성을 촉진하는 바이오소재 |
|
사업명 |
과학기술정보통신부, 노인 맞춤형 차세대 치과용 바이오임플란트 시스템 개발 |
|
개발과정 |
- 국내특허출원 (출원번호:10-2013-00335850, 10-2017-0077400) |
|
참여기관 |
(주)나이벡, 서울대학교 치의학대학원, 서울대학교 치과병원, 가천대학교 치과병원 |
(라) 골재생용 복합소재
|
제품명 |
OCS-Collagen |
|
제품의 내용 |
골재생촉진을 위한 골미네랄입자와 콜라겐의 복합이식용 골재생소재 |
|
사업명 |
과학기술정보통신부, 노인 맞춤형 차세대 치과용 바이오임플란트 시스템 개발 |
|
개발과정 |
- 국내특허출원 (출원번호:10-2013-00335850, 10-2017-0077400) - 식약처 승인완료 -미국 FDA 승인완료 - 유럽 CE 인증완료 |
|
참여기관 |
(주)나이벡, 서울대학교 치의학대학원, 서울대학교 치과병원, 가천대학교 치과병원 지원기관 : 과학기술정보통신부 |
(마) 바이오임플란트
|
제품명 |
NIB-BIOIMP |
|
제품의 내용 |
골융착을 극대화할 수 있는 약물방출기능성 바이오임플란트 |
|
사업명 |
과학기술정보통신부, 노인 맞춤형 차세대 치과용 바이오임플란트 시스템 개발 |
|
개발과정 |
- 국내특허등록 (1779930), 해외 특허 출원 (미국, 유럽, 중국) - 식약처 승인 신청 |
|
참여기관 |
(주)나이벡, 서울대학교 치의학대학원, 오하이오주립대학교, 서울대학교 치과병원 지원기관 : 과학기술정보통신부 |
(3) 구강보건제품
(가) 치아미백제
|
제품명 |
BlancTis 시리즈 |
|
제품의 내용 |
약물전달시스템 기술을 이용한 젤타입 치아미백제 (의약품,의약외품) |
|
구성요소기술 |
- 투과 촉진형 약물전달시스템 기술 |
|
제품효능 |
기존 치아미백제 대비 4단계 이상의 치아 미백효과 및 장기적인 미백효과 유지 가능 |
|
개발과정 |
- 국내 특허 등록(등록번호: 0870232) 및 해외특허출원 (치아용 미백기능성 물질 전달시스템,Teeth Whitening Functional Materials Delivery System) |
|
참여기관 |
(주)나이벡, 서울대학교 치과병원 보존과 (금기연교수팀) |
(나) 시린이치료제
|
제품명 |
시린이 치료제 SensBlok |
|
제품의 내용 |
다양한 원인에 의해 발생되는 시린이 증상의 경감을 목적으로 한 시린이 치료제 |
|
구성요소기술 |
- 투과 촉진형 약물전달시스템 기술 |
|
제품효능 |
1일3회 3일 적용시 시린증상 경감. 치료효과 3개월간 유지(개인차있음) |
|
개발과정 |
- 국내 특허 출원(출원번호: 10-2008-0098832) 및 해외출원 (치아 지각과민 방지용 조성물, PCT/KR2009/005760, A Composition for Teeth Desensitizing) |
|
참여기관 |
(주)나이벡, 서울대학교 치과병원 (치주과) |
(다) 조절방출시스템 기반 치주염 치료제
|
제품명 |
MinoCure |
|
제품의 내용 |
미노사이클린 조절방출시스템을 탑재한 주입형 치주염 치료제 |
|
구성요소기술 |
- 조절방출형 약물전달시스템 기술 |
|
제품효능 |
치주염의 완화, 치주원인균의 제거 |
|
개발과정 |
- 경희대학교 치과병원 임상시험 진행 - 식약처 승인 획득 |
|
참여기관 |
(주)나이벡, 서울대학교 치의학대학원, 경희대학교 치과병원, 가천대학교 치과병원, 지원기관: 과학기술정보통신부 |
(라) 조절방출시스템 기반 임플란트 주위염 예방치료제
|
제품명 |
Clinplant |
|
제품의 내용 |
항염물질 탑재 임플란트 주위염 예방제 |
|
구성요소기술 |
- 조절방출형 약물전달시스템 기술 |
|
제품효능 |
치주염, 임플란트 주위염의 병용요법, 치태제거 |
|
개발과정 |
- 단국대학교 치과병원 임상완료 - 식약처 승인 획득, CE인증 완료, 미국 FDA등록 - 특허 출원 |
|
참여기관 |
(주)나이벡, 서울대학교 치의학대학원, 단국대학교 치과병원, 가천대학교 치과병원, 지원기관: 과학기술정보통신부 |
(3) 펩타이드 기반 융합 바이오소재
(가) 치과용 골이식재
|
제품명 |
OssGen-X15 |
|
제품의 내용 |
골재생 촉진성 생리활성 펩타이드가 표면에 고정된 융합바이오 의료기기, 치과용 골이식재 |
|
연구실적 |
- 국내특허등록 (등록번호: 0767241, 0739528 (골조직 형성 증진 펩타이드가 함유된 골이식재, 제1형 교원질 부착 유도 펩타이드가 고정된 골이식재 및 조직공학용 지지체) 및 해외 특허 등록 완료 - PCT (출원번호: PCT/KR2007/003687 Bone Graft Containing Osteogenesis Enhancing Peptides) - 식약처 승인 완료, 미국 FDA 및 유럽 CE진행 중 - 한국디자인 진흥원 지원 “골형성 촉진 펩타이드 함유 골이식재의 디자인 연구개발 (연구기간 2007.11~2008.04, 총연구비 50,000천원)” |
|
참여기관 |
(주)나이벡, 서울대학교 치의학대학원, 서울대학교 치과병원, 단국대학교 치과병원, 미국 MCRA 과학기술정보통신부 (바이오임플란트 연구개발사업) |
(4) 펩타이드 기반 화장품
(가) 항염기능성 펩타이드 기반 염증 및 여드름개선용 화장품
|
제품명 |
Eustella AC |
|
제품의 내용 |
당사의 독자적인 항염항균기능성 펩타이드를 함유한 염증 및 여드름 개선용 스킨, 로션 화장품 시스템 |
|
연구실적 |
- 국내(등록번호: 1329774) 및 해외 특허등록 (미국: 8,980,844, 유럽: 2583684) - 충북대학교 미생물학과와 공동연구 - 식약처 승인 완료 - 국내외 논문 게재 중 |
|
참여기관 |
(주)나이벡, 충북대학교 |
< 정부과제 수행실적 >
| 번호 | 주관부처 | 과제명 | 연구기간 |
| 1 | 한국산업기술평가원 | 생리활성펩타이드로표면개질된골재생촉진성골이식재의상용화기술연구 | 2005.04.~2007.03. |
| 2 | 한국보건산업진흥원 | 골재생 촉진기능성 치과용 실크피브로인나노차폐막의 상용화기술연구 | 2005.05.~2006.04. |
| 3 | 한국산업기술진흥협회 | 골재생 촉진성 치과용 키토산 나노차폐막의 상용화기술연구 | 2004.12.~2005.11. |
| 4 | 산업자원부 | 골형성 촉진 펩타이드를 이용한 주입형 골재생재의 개발 | 2007.06.~2011.01. |
| 5 | 한국디자인진흥원 | 골형성 촉진 펩타이드 함유 골이식재의 디자인연구개발 | 2007.11.~2008.04. |
| 6 | 한국보건산업진흥원 | 치주감염제어 및 기능성 조직재생 융합소재개발연구 | 2008.11.~2012.03. |
| 7 | 충청광역경제권선도산업지원단 | 치주조직재생 차폐막 및 조직공학용 콜라겐 지지체의제품화기술 | 2009.10.~2012.04. |
| 8 | 충북도청 | 콜라겐함유치주조직재생제의제품화를위한안전성및유효성평가 | 2010.06.~2011.05. |
| 9 | 중소기업청 | 근골격재생을 위한 펩타이드 기반 신소재 및 약물전달시스템의 사업화 | 2012.03.~2014.02. |
| 10 | 지식경제부 | 성형외과 피하조직수복용 바이오소재 개발 | 2012.08.~2014.04. |
| 11 | 미래창조부 | 노인 맞춤형 차세대 치과용 바이오임플란트 시스템 개발 | 2014.10.~2017.12. |
| 12 | 중소기업기술정보진흥원 | 펩타이드-앱타머 기반 트러블피부용 화장품 개발 | 2016.12.~2018.12 |
|
13 |
과학기술정보통신부 |
줄기세포 치료제 효율 최적화를 위한 기능성생리활성물질 (참여기업) |
2017.06~2022.06 |
마. 향후 연구개발계획
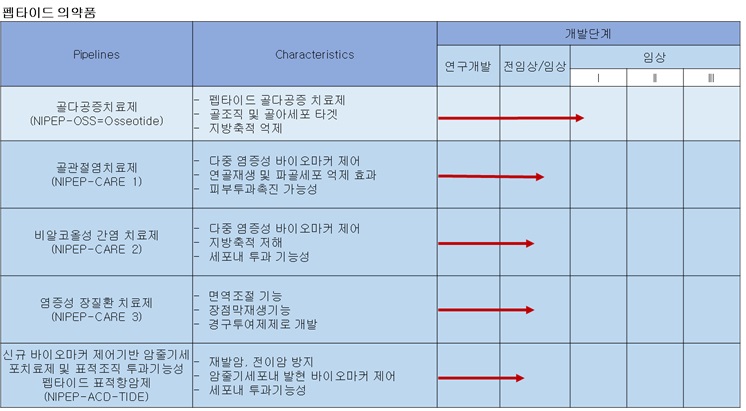 |
|
펩타이드 의약품 연구개발 계획 |
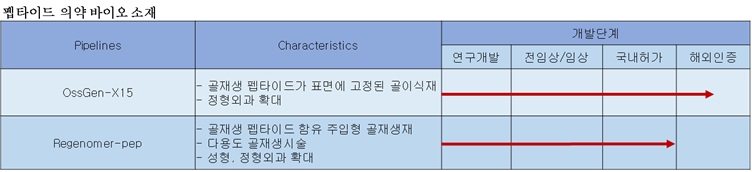 |
|
펩타이드 의약 바이오소재 연구개발 계획 |
11. 그밖에 투자의사결정에 필요한 사항
- 최근3년간 특허 보유사항
|
순번 |
특허의 내용 |
권리자 |
출원/등록 |
국가명 |
출원/등록일 |
출원번호/등록번호 |
|
1 |
항균 및 항염증 활성을 가지는 펩타이드 및 이를 유효성분으로 함유하는 약제학적 조성물 |
㈜나이벡 |
등록 |
중국 |
2016.01.20 |
ZL 2011 8 0034167.4 |
|
2 |
콜라겐으로 구성된 주입형 피하조직재생용 바이오소재 |
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
대한민국 |
2016.01.26 |
/10-1590313 |
|
3 |
치아 지각과민 방지용 조성물 |
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
베트남 |
2016.02.22 |
15186 |
|
4 |
암줄기세포의 성장억제용 항암기능성 펩타이드 및 그 용도 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
PCT |
2016.03.03 |
PCT/KR2016/002109 |
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
유럽 |
2016.07.21 |
16 736 753.1 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
미국 |
2016.07.23 |
15/113,823 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
대한민국 |
2017.01.02 |
10-1693533 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
미국 |
2018.06.12 |
9993519 |
||
|
5 |
지르코니아 결합능을 가지는 펩타이드 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
PCT |
2016.04.05 |
PCT/KR2016/003505 |
|
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
대한민국 |
2016.11.28 |
10-1681886 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
유럽 |
2017.02.14 |
16776814.2 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
미국 |
2017.02.15 |
15/504,035 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
미국 |
2017.10.31 |
9801973 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
홍콩 |
2018.08.14 |
18110409.4 |
||
|
6 |
세포외기질 단백질-골미네랄 복합체를 함유하는 조직 구조 모사체 및 그 제조방법 |
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
대한민국 |
2016.06.02 |
/1628677 |
|
7 |
신규한 지방 축적 억제용 펩타이드 및 이를 포함하는 비만 예방 또는 치료용 약학조성물 |
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
대한민국 |
2016.07.06 |
/1638775 |
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
미국 |
2017.08.01 |
15/666,506 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
홍콩 |
2018.01.10 |
18100331.8 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
미국 |
2018.12.18 |
10,155.022 |
||
|
8 |
합성 펩타이드를 이용한 유도만능줄기세포의 제조방법 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
PCT |
2016.07.19 |
PCT/KR2016/007857 |
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
미국 |
2017.03.24 |
15/514,337 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
유럽 |
2017.04.27 |
16833217.9 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
일본 |
2017.04.27 |
2017-543696 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
미국 |
2018.09.04 |
10066212 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
대한민국 |
2018.10.02 |
10-1906557 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
일본 |
2018.12.07 |
6446566 |
||
|
9 |
티타늄 결합능을 가지는 펩타이드 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
대한민국 |
2016.07.26 |
10-2016-0094893 |
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
PCT |
2017.03.07 |
PCT/KR2017/002436 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
미국 |
2017.07.22 |
15/545,679 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
유럽 |
2017.08.25 |
17752273.7 |
||
|
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
대한민국 |
2018.12.24 |
10-1934047 |
||
|
10 |
줄기세포 재생 또는 증식능 향상용 세포 침투성 융합 단백질 |
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
미국 |
2016.08.09 |
9408920 |
|
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
대한민국 |
2018.06.14 |
10-1869268 |
||
|
11 |
종양선택적 투과기능성을 가지는 펩타이드 및 그 용도 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
미국 |
2016.08.11 |
15/234,396 |
|
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
미국 |
2017.12.26 |
9849190 |
||
|
12 |
세포 투과능 및 골조직 재생능을 가지고 있는 이중 기능성 신규 펩타이드 및 이의 용도 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
대한민국 |
2016.12.27 |
10-2016-0180121 |
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
PCT |
2017.12.27 |
PCT/KR2017/015588 |
||
|
13 |
바이오필름 억제용 펩타이드 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
대한민국 |
2017. 04. 05 |
10-2017-0044233 |
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
PCT |
2018.03.19 |
PCT/KR2018/003162 |
||
|
14 |
골 흡수 억제용 펩타이드? |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
대한민국 |
2017. 08. 18. |
10-2017-0104939 |
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
PCT |
2018.06.19 |
PCT/KR2018/006874 |
||
|
15 |
노화된 줄기세포 선별용 단백질표지자 GRP78? |
㈜나이벡, 충북대학교산학협력단, 서울대학교산학협력단? |
출원 |
대한민국 |
2017. 10. 13. |
10-2017-0133613 |
|
16 |
노화된 줄기세포 선별용 GRP78 유래 펩타이드? |
(주)나이벡, 충북대학교산학협력단, 서울대학교산학협력단? |
출원 |
대한민국 |
2017. 10. 13. |
10-2017-0133614 |
|
17 |
인간 유래 세포 투과성 펩타이드와 생리활성 펩타이드 결합체 및 그 용도 |
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
유럽 |
2017.02.22 |
2615105 |
|
18 |
역분화 유도를 위한 세포투과성 융합단백질 및 그 용도 |
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
미국 |
2017.05.09 |
9644185 |
|
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
유럽 |
2017.07.05 |
2843052 |
||
|
19 |
표적 선택적 세포/조직 투과기능 활성을 가지는 펩타이드 및 그 용도 |
㈜나이벡 |
등록 |
인도 |
2017.06.29 |
284776 |
|
20 |
아파타이트에 결합하는 골조직 재생능을 가지는 펩타이드 |
㈜ 나이벡 |
등록 |
유럽 |
2017.07.19 |
2813516 |
|
㈜ 나이벡 |
등록 |
이스라엘 |
2017.07.31 |
225150 |
||
|
㈜ 나이벡 |
등록 |
캐나다 |
2018.01.02 |
2811621 |
||
|
21 |
부갑상선호르몬(parathyroid hormone, PTH)에 골조직 선택성 펩타이드가 결합되어 있는 융합 펩타이드를 포함하는 약학 조성물 및 생체재료 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
대한민국 |
2017.09.29 |
10-2017-0126876 |
|
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
PCT |
2017.11.29 |
PCT/KR2017/013749 |
||
|
22 |
염증감소능 및 줄기세포로부터 연골세포로의 분화 촉진능을 가지는 이중 기능성 펩타이드 및 이의 용도 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
대한민국 |
2018.03.14 |
10-2018-0029912 |
|
23 |
세포 투과능 및 근육 재생능을 가지는 이중 기능성 펩타이드 및 이의 용도 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
대한민국 |
2018.03.14 |
10-2018-0029913 |
|
24 |
골조직 재생을 위한 일체형 바이오소재 및 그 제조방법 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
대한민국 |
2018.06.19 |
10-2017-0077400 |
|
25 |
세포투과성 펩타이드와 형광표지 자성나노입자의 복합체 및 그 용도 |
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
유럽 |
2018.07.11 |
2197783 |
|
26 |
치은치주염 또는 임플란트 주위염 치료 및 예방용 조성물 및 상기 조성물이 코팅되어 있는 치간칫솔 |
(주)나이벡 |
출원 |
대한민국 |
2018.08.17 |
10-2018-0095971 |
|
(주)나이벡 |
출원 |
PCT |
2018.08.17 |
PCT/KR2018/009469 |
||
|
27 |
염증 및 대사성 질환의 바이오마커에 대한 결합능이 있는 신규한 펩타이드 및 이의 용도 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
대한민국 |
2018.08.31 |
10-2018-0103614 |
|
28 |
다중의 질환 바이오마커의 기능 및 발현을 억제하는 펩타이드의 신규한 용도 |
㈜ 나이벡 / 서울대학교산학협력단 |
출원 |
대한민국 |
2018.08.31 |
10-2018-0103615 |
|
29 |
단백질표지자 GRP78을 이용한 고효율 줄기세포의 선별 방법 |
㈜나이벡, 충북대학교산학협력단, 서울대학교산학협력단? |
출원 |
대한민국 |
2018.10.15 |
/10-2018-0122736 |
|
30 |
고효율 줄기세포 선별을 위한 GRP78 유래 펩타이드 |
㈜나이벡, 충북대학교산학협력단, 서울대학교산학협력단? |
출원 |
대한민국 |
2018.10.15 |
10-2018-0122816 |
|
31 |
펩타이드에 의한 표면활성형 콜라겐 차폐막 |
㈜ 나이벡 / 서울대학교산학협력단 |
등록 |
유럽 |
2018.10.31 |
2700655 |
Ⅲ. 재무에 관한 사항
1. 요약재무정보
| (단위: 천원) |
|||
| 구 분 | 제15기 | 제14기 | 제13기 |
| [유동자산] | 5,289,806 | 9,993,465 | 8,838,096 |
| 현금및현금성자산 | 859,192 | 5,276,939 | 4,613,093 |
| 단기손익금융자산 | - | 503,734 | 10,000 |
| 매출채권 | 1,640,109 | 1,649,949 | 1,811,262 |
| 기타유동자산 | 240,739 | 150,041 | 667,946 |
| 당기법인세자산 | 6,396 | 2,056 | 5,968 |
| 재고자산 | 2,543,370 | 2,410,746 | 1,729,827 |
| [비유동자산] | 17,027,784 | 15,756,908 | 14,131,546 |
| 장기금융상품 | 529,470 | 385,618 | 250,283 |
| 유형자산 | 9,869,111 | 9,869,545 | 9,174,470 |
| 무형자산 | 6,194,651 | 5,210,780 | 4,410,673 |
| 기타비유동자산 | 434,552 | 290,965 | 296,120 |
| 자산총계 | 22,317,590 | 25,750,373 | 22,969,642 |
| [유동부채] | 7,802,804 | 5,690,720 | 4,705,540 |
| [비유동부채] | 3,938,817 | 7,697,784 | 8,422,918 |
| 부채총계 | 11,741,621 | 13,388,514 | 13,128,458 |
| [자본금] | 3,183,979 | 3,005,235 | 2,716,788 |
| [자본잉여금] | 30,619,484 | 28,163,370 | 23,462,063 |
| [자본조정] | 4,965 | 11,955 | 17,317 |
| [이익잉여금] | △23,232,459 | △18,818,701 | △16,354,984 |
| 자본총계 | 10,575,969 | 12,361,859 | 9,841,184 |
| 종속ㆍ관계ㆍ공동기업 투자주식 평가방법 |
해당사항없음 | 해당사항없음 | 해당사항없음 |
| 구 분 | (2018.01.01~ 2018.12.31) |
(2017.01.01~ 2017.12.31) |
(2016.01.01~ 2016.12.31) |
| 매출액 | 5,207,877 | 6,302,575 | 4,804,232 |
| 영업이익(손실) | △3,402,362 | △1,128,739 | △2,499,774 |
| 당기순이익(손실) | △4,146,156 | △2,567,612 | △3,027,189 |
| 기본주당순이익(손실) | △665 원 | △463 원 | △578 원 |
[Δ는 부(-)의 수치]
2. 연결재무제표
"해당사항이 없습니다."
3. 연결재무제표 주석
"해당사항이 없습니다."
4. 재무제표
|
재무상태표 |
|
제 15 기 2018.12.31 현재 |
|
제 14 기 2017.12.31 현재 |
|
제 13 기 2016.12.31 현재 |
|
(단위 : 원) |
|
제 15 기 |
제 14 기 |
제 13 기 |
|
|---|---|---|---|
|
자산 |
|||
|
유동자산 |
5,289,805,899 |
9,993,464,605 |
8,838,096,236 |
|
현금및현금성자산 |
859,191,538 |
5,276,938,987 |
4,613,093,396 |
|
당기손익인식금융자산 |
503,734,244 |
10,000,000 |
|
|
매출채권 및 기타유동채권 |
1,880,847,985 |
1,799,989,827 |
2,479,207,919 |
|
당기법인세자산 |
6,396,320 |
2,056,030 |
5,968,310 |
|
재고자산 |
2,543,370,056 |
2,410,745,517 |
1,729,826,611 |
|
비유동자산 |
17,027,784,254 |
15,756,908,548 |
14,131,545,850 |
|
장기금융상품 |
529,470,194 |
385,618,420 |
250,283,058 |
|
유형자산 |
9,869,111,437 |
9,869,545,234 |
9,174,470,317 |
|
무형자산 |
6,194,650,923 |
5,210,780,194 |
4,410,672,782 |
|
기타비유동채권 |
434,551,700 |
290,964,700 |
296,119,693 |
|
자산총계 |
22,317,590,153 |
25,750,373,153 |
22,969,642,086 |
|
부채 |
|||
|
유동부채 |
7,802,804,486 |
5,690,720,454 |
4,705,539,837 |
|
매입채무 및 기타유동채무 |
7,802,804,486 |
5,690,720,454 |
4,705,539,837 |
|
매입채무 |
121,745,510 |
135,088,300 |
165,507,060 |
|
단기차입금 |
870,000,000 |
920,000,000 |
420,000,000 |
|
미지급금 |
341,272,599 |
668,434,025 |
396,593,296 |
|
미지급비용 |
221,610,667 |
236,648,016 |
191,698,159 |
|
예수금 |
35,192,510 |
32,218,820 |
28,379,770 |
|
선수금 |
14,403,190 |
30,430,604 |
939,044,392 |
|
유동성장기차입금 |
1,605,544,975 |
1,087,256,000 |
1,077,404,000 |
|
유동성전환사채 |
4,495,438,426 |
2,474,348,080 |
1,332,133,068 |
|
유동성장기미지급금 |
97,596,609 |
106,296,609 |
154,780,092 |
|
비유동부채 |
3,938,817,082 |
7,697,794,027 |
8,422,918,445 |
|
장기매입채무 및 기타비유동채무 |
2,274,926,383 |
6,497,938,320 |
7,262,250,748 |
|
장기차입금 |
851,964,985 |
897,780,000 |
1,556,220,000 |
|
전환사채 |
4,012,336,183 |
5,140,997,241 |
|
|
장기미지급금 |
298,461,398 |
463,322,137 |
565,033,507 |
|
장기선수금 |
1,124,500,000 |
1,124,500,000 |
|
|
퇴직급여부채 |
1,663,890,699 |
1,199,855,707 |
1,160,667,697 |
|
부채총계 |
11,741,621,568 |
13,388,514,481 |
13,128,458,282 |
|
자본 |
|||
|
자본금 |
3,183,979,000 |
3,005,234,500 |
2,716,788,000 |
|
자본잉여금 |
30,619,483,940 |
28,163,370,304 |
23,462,062,682 |
|
주식발행초과금 |
29,722,400,740 |
26,743,706,364 |
22,168,918,934 |
|
전환권대가 |
884,731,200 |
1,414,301,940 |
1,293,143,748 |
|
기타자본잉여금 |
12,352,000 |
5,362,000 |
|
|
기타자본구성요소 |
4,965,000 |
11,955,000 |
17,317,000 |
|
기타포괄손익누계액 |
(439,125,129) |
(171,522,410) |
(275,417,359) |
|
이익잉여금(결손금) |
(22,793,334,226) |
(18,647,178,722) |
(16,079,566,519) |
|
자본총계 |
10,575,968,585 |
12,361,858,672 |
9,841,183,804 |
|
자본과부채총계 |
22,317,590,153 |
25,750,373,153 |
22,969,642,086 |
|
포괄손익계산서 |
|
제 15 기 2018.01.01 부터 2018.12.31 까지 |
|
제 14 기 2017.01.01 부터 2017.12.31 까지 |
|
제 13 기 2016.01.01 부터 2016.12.31 까지 |
|
(단위 : 원) |
|
제 15 기 |
제 14 기 |
제 13 기 |
|
|---|---|---|---|
|
매출액 |
5,207,877,219 |
6,302,574,592 |
4,804,231,773 |
|
매출원가 |
4,745,811,934 |
4,346,584,600 |
4,004,453,274 |
|
매출총이익 |
462,065,285 |
1,955,989,992 |
799,778,499 |
|
판매비와관리비 |
3,864,427,020 |
3,084,729,373 |
3,299,552,719 |
|
영업이익(손실) |
(3,402,361,735) |
(1,128,739,381) |
(2,499,774,220) |
|
기타이익 |
127,401,994 |
64,980,520 |
128,412,798 |
|
기타손실 |
93,258,622 |
921,731,966 |
76,450,449 |
|
금융수익 |
54,283,627 |
13,683,330 |
40,644,242 |
|
금융원가 |
733,693,711 |
623,620,262 |
712,936,502 |
|
법인세비용차감전순이익(손실) |
(4,047,628,447) |
(2,595,427,759) |
(3,120,104,131) |
|
법인세비용 |
98,527,057 |
(27,815,556) |
(92,914,974) |
|
당기순이익(손실) |
(4,146,155,504) |
(2,567,612,203) |
(3,027,189,157) |
|
기타포괄손익 |
(267,602,719) |
103,894,949 |
(87,489,158) |
|
당기손익으로 재분류되지 않는항목(세후기타포괄손익) |
(267,602,719) |
103,894,949 |
(87,489,158) |
|
총포괄손익 |
(4,413,758,223) |
(2,463,717,254) |
(3,114,678,315) |
|
주당이익 |
|||
|
기본주당이익(손실) (단위 : 원) |
(665) |
(463) |
(578) |
|
자본변동표 |
|
제 15 기 2018.01.01 부터 2018.12.31 까지 |
|
제 14 기 2017.01.01 부터 2017.12.31 까지 |
|
제 13 기 2016.01.01 부터 2016.12.31 까지 |
|
(단위 : 원) |
|
자본 |
|||||
|---|---|---|---|---|---|
|
자본금 |
자본잉여금 |
기타자본구성요소 |
이익잉여금 |
자본 합계 |
|
|
2016.01.01 (기초자본) |
2,609,857,500 |
21,376,916,027 |
71,925,000 |
(13,240,305,563) |
10,818,393,464 |
|
당기순이익(손실) |
(3,027,189,157) |
(3,027,189,157) |
|||
|
기타포괄손익 |
(87,489,158) |
(87,489,158) |
|||
|
복합금융상품 발행 |
1,041,235,920 |
1,041,235,920 |
|||
|
전환권 행사 |
106,930,500 |
1,043,910,735 |
(54,608,500) |
1,096,232,735 |
|
|
재분류조정 |
|||||
|
자본 증가(감소) 합계 |
106,930,500 |
2,085,146,655 |
(54,608,500) |
(3,114,678,315) |
(977,209,660) |
|
2016.12.31 (기말자본) |
2,716,788,000 |
23,462,062,682 |
17,317,000 |
(16,354,983,878) |
9,841,183,804 |
|
2017.01.01 (기초자본) |
2,716,788,000 |
23,462,062,682 |
17,317,000 |
(16,354,983,878) |
9,841,183,804 |
|
당기순이익(손실) |
(2,567,612,203) |
(2,567,612,203) |
|||
|
기타포괄손익 |
103,894,949 |
103,894,949 |
|||
|
복합금융상품 발행 |
884,731,200 |
884,731,200 |
|||
|
전환권 행사 |
288,446,500 |
3,811,214,422 |
4,099,660,922 |
||
|
재분류조정 |
5,362,000 |
(5,362,000) |
|||
|
자본 증가(감소) 합계 |
288,446,500 |
4,701,307,622 |
(5,362,000) |
(2,463,717,254) |
2,520,674,868 |
|
2017.12.31 (기말자본) |
3,005,234,500 |
28,163,370,304 |
11,955,000 |
(18,818,701,132) |
12,361,858,672 |
|
2018.01.01 (기초자본) |
3,005,234,500 |
28,163,370,304 |
11,955,000 |
(18,818,701,132) |
12,361,858,672 |
|
당기순이익(손실) |
(4,146,155,504) |
(4,146,155,504) |
|||
|
기타포괄손익 |
(267,602,719) |
(267,602,719) |
|||
|
복합금융상품 발행 |
|||||
|
전환권 행사 |
178,744,500 |
2,449,123,636 |
2,627,868,136 |
||
|
재분류조정 |
6,990,000 |
(6,990,000) |
|||
|
자본 증가(감소) 합계 |
178,744,500 |
2,456,113,636 |
(6,990,000) |
(4,413,758,223) |
(1,785,890,087) |
|
2018.12.31 (기말자본) |
3,183,979,000 |
30,618,483,940 |
4,965,000 |
(23,232,459,355) |
10,575,968,585 |
|
현금흐름표 |
|
제 15 기 2018.01.01 부터 2018.12.31 까지 |
|
제 14 기 2017.01.01 부터 2017.12.31 까지 |
|
제 13 기 2016.01.01 부터 2016.12.31 까지 |
|
(단위 : 원) |
|
제 15 기 |
제 14 기 |
제 13 기 |
|
|---|---|---|---|
|
영업활동현금흐름 |
(2,307,210,985) |
563,218,115 |
(372,211,186) |
|
당기순이익(손실) |
(4,146,155,504) |
(2,567,612,203) |
(3,027,189,157) |
|
조정 |
2,831,374,526 |
3,100,789,070 |
2,360,268,442 |
|
퇴직급여 |
330,757,270 |
185,139,098 |
301,412,631 |
|
대손상각비 |
63,188,000 |
9,073,767 |
57,704,329 |
|
감가상각비 |
968,491,450 |
833,718,621 |
756,576,233 |
|
재고자산평가손실 |
58,938,202 |
21,806,824 |
165,855,821 |
|
유형자산처분이익 |
(5,995,000) |
||
|
무형자산상각비 |
627,495,166 |
595,530,467 |
563,051,067 |
|
무형자산손상차손 |
714,023,878 |
||
|
경상연구개발비 |
82,692,440 |
||
|
외화환산이익 |
(274,200) |
(63,866,667) |
|
|
외화환산손실 |
4,841,497 |
82,677,599 |
157,742 |
|
이자수익 |
(42,431,853) |
(9,949,086) |
(40,644,242) |
|
이자비용 |
733,693,711 |
623,620,262 |
712,936,502 |
|
당기손익인식금융자산평가이익 |
(11,851,774) |
(3,734,244) |
|
|
법인세비용 |
98,527,057 |
(27,815,556) |
(92,914,974) |
|
영업활동으로인한자산ㆍ부채의변동 |
(294,319,692) |
165,603,576 |
467,325,918 |
|
매출채권의 감소(증가) |
(58,189,485) |
115,009,668 |
394,219,528 |
|
기타유동자산의 감소(증가) |
(90,698,170) |
276,020,095 |
314,143,403 |
|
재고자산의 감소(증가) |
(191,562,741) |
(702,725,730) |
(660,096,274) |
|
매입채무의 증가(감소) |
(13,342,790) |
(30,418,760) |
(55,848,455) |
|
기타채무의 증가(감소) |
239,926,709 |
304,761,397 |
(67,571,763) |
|
기타유동채무의 증가(감소) |
(13,053,724) |
(904,774,738) |
624,102,959 |
|
장기선수금의 증가(감소) |
1,124,500,000 |
||
|
확정급여채무의의 증가(감소) |
(151,308,860) |
(16,768,356) |
(62,666,061) |
|
사외적립자산의 감소(증가) |
(16,090,631) |
(18,957,419) |
|
|
이자수취 |
42,431,853 |
9,949,086 |
40,850,269 |
|
이자지급 |
(736,201,878) |
(149,423,694) |
(211,847,618) |
|
법인세납부 |
(4,340,290) |
3,912,280 |
(1,619,040) |
|
투자활동현금흐름 |
(2,351,276,304) |
(4,093,448,817) |
(2,778,691,230) |
|
당기손익인식금융자산의 처분 |
503,734,244 |
620,000,000 |
1,141,830,000 |
|
유형자산의 처분 |
6,000,000 |
||
|
보증금의 감소 |
5,154,993 |
207,816,000 |
|
|
당기손익인식금융자산의 증가 |
(1,110,000,000) |
||
|
장기금융상품의 취득 |
(132,000,000) |
(135,335,362) |
(127,514,082) |
|
유형자산의 취득 |
(968,057,653) |
(1,301,188,538) |
(2,233,300,882) |
|
무형자산의 취득 |
(1,611,365,895) |
(2,178,079,910) |
(1,545,522,266) |
|
단기대여금의 증가 |
(100,000,000) |
||
|
보증금의 증가 |
(143,587,000) |
(122,000,000) |
|
|
재무활동현금흐름 |
240,465,640 |
4,239,523,617 |
5,418,074,245 |
|
단기차입금의 증가 |
500,000,000 |
||
|
단기차입금의 상환 |
(50,000,000) |
||
|
장기차입금의 증가 |
692,935,000 |
||
|
유동성장기차입금의 상환 |
(220,461,040) |
(648,588,000) |
(538,886,000) |
|
전환사채의 증가 |
5,000,000,000 |
6,000,000,000 |
|
|
전환권/신주인수권 행사 |
119,385,475 |
||
|
주식선택권행사 |
63,560,953 |
||
|
장기미지급금의 감소 |
(182,008,320) |
(160,225,983) |
(225,986,183) |
|
신주인수권부사채의 감소 |
(451,662,400) |
||
|
현금및현금성자산에 대한 환율변동효과 |
274,200 |
(45,447,324) |
27,582,107 |
|
현금및현금성자산의순증가(감소) |
(4,417,747,449) |
663,845,591 |
2,294,753,936 |
|
기초현금및현금성자산 |
5,276,938,987 |
4,613,093,396 |
2,318,339,460 |
|
기말현금및현금성자산 |
859,191,538 |
5,276,938,987 |
4,613,093,396 |
5. 재무제표 주석
| 제15기 : 2018년 12월 31일 현재 |
| 제14기 : 2017년 12월 31일 현재 |
| 주식회사 나이벡 |
1. 일반사항
주식회사 나이벡(이하"회사")은 바이오소재 융합기술과 약물전달시스템 및 펩타이드 공학기술 관련 제품의 제조 및 판매 등의 사업을 영위할 목적으로 2004년 1월에 설립되어, 충청북도 진천군 이월면에 본사를 두고 당해 사업을 영위하고 있습니다.
회사의 보고기간종료일 현재 수권주식수는 100,000천주(1주당 금액: 500원)이며 설립 이후 수차의 증자를 거쳐 보고기간종료일 현재 회사의 발행주식총수와 납입자본금은 각각 6,367,958주와 3,183,979,000원입니다.
또한, 회사는 주주총회의 특별결의로 발행주식총수의 100분의 15범위 내에서 주식선택권을 부여할 수 있습니다. 부여받은 주식선택권은 이를 부여하는 주주총회 결의일로부터 2년이 경과한 날로부터 7년 내에 권리를 행사할 수 있는 바, 보고기간종료일 현재 회사의 임직원 등에게 부여된 주식선택권은 보통주식 5,000주입니다.
당기말 현재 회사의 주요 주주현황은 다음과 같습니다.
| (단위: 주, %) | |||
|---|---|---|---|
| 구분 | 주주명 | 주식수 | 지분율 |
| 보통주 | 정종평 | 1,133,690 | 17.80 |
| 박윤정 | 228,000 | 3.58 | |
| 기타 | 5,006,268 | 78.62 | |
| 합 계 | 6,367,958 | 100.00 | |
2. 중요한 회계정책
다음은 재무제표 작성에 적용된 중요한 회계정책입니다. 이러한 정책은 별도의 언급이 없다면, 표시된 회계기간에 계속적으로 적용됩니다.
2.1 재무제표 작성기준
회사의 재무제표는 한국채택국제회계기준(이하 기업회계기준)에 따라 작성됐습니다.한국채택국제회계기준은 국제회계기준위원회("IASB")가 발표한 기준서와 해석서 중대한민국이 채택한 내용을 의미합니다.
한국채택국제회계기준은 재무제표 작성 시 중요한 회계추정의 사용을 허용하고 있으며, 회계정책을 적용함에 있어 경영진의 판단을 요구하고 있습니다. 보다 복잡하고 높은 수준의 판단이 필요한 부분이나 중요한 가정 및 추정이 필요한 부분은 주석 3에서 설명하고 있습니다.
2.2 회계정책과 공시의 변경
(1) 회사가 채택한 제ㆍ개정 기준서
회사는 2018년 1월 1일로 개시하는 회계기간부터 다음의 개정 기준서를 신규로 적용하였습니다.
- 기준서 제1028호 '관계기업과 공동기업에 대한 투자' 개정
벤처캐피탈 투자기구, 뮤추얼펀드 등이 보유하는 관계기업이나 공동기업에 대한 투자지분을 지분법이 아닌 공정가치로 평가할 경우, 각각의 지분별로 선택 적용할 수 있음을 명확히 하였습니다. 벤처캐피탈 투자기구 등에 해당하지 않아 상기 면제규정을 적용하지 않으므로, 해당 개정이 재무제표에 미치는 중요한 영향은 없습니다.
- 기준서 제1040호 '투자부동산' 개정
부동산의 투자부동산으로 또는 투자부동산에서의 대체는 용도 변경의 증거가 존재하는 경우에만 가능하며, 동 기준서 문단 57은 이러한 상황의 예시임을 명확히 하였습니다. 또한, 건설중인 부동산도 계정대체 규정 적용 대상에 포함됨을 명확히 하였습니다. 해당 개정이 재무제표 미치는 중요한 영향은 없습니다.
- 기준서 제1102호 '주식기준보상' 개정
현금결제형에서 주식결제형으로 분류변경 시 조건변경 회계처리와 현금결제형 주식기준보상거래의 공정가치 측정방법이 주식결제형 주식기준보상거래와 동일함을 명확히 하였습니다. 해당 개정으로 인해 재무제표에 중요한 영향은 없습니다.
- 해석서 제2122호 '외화 거래와 선지급ㆍ선수취 대가' 제정
제정된 해석서에 따르면, 관련 자산, 비용, 수익(또는 그 일부)의 최초 인식에 적용할 환율을 결정하기 위한 거래일은 대가를 선지급하거나 선수취하여 비화폐성자산이나 비화폐성부채를 최초로 인식하는 날입니다. 해당 해석서의 제정이 재무제표에 미치는 중요한 영향은 없습니다.
- 기준서 제1109호 '금융상품'
회사는 2018년 1월 1일을 최초적용일로 하여 기준서 제1109호 '금융상품'을 적용하였습니다. 기준서 제1109호의 경과규정에 따라 비교 표시된 재무제표는 재작성되지 않았으며, 종전 장부금액과 최초적용일의 장부금액의 차이는 2018년 1월 1일에 이익잉여금(또는 자본)으로 인식하였습니다. 동 기준서의 적용으로 인한 영향의 상세 정보는 주석 38에서 설명하고 있습니다.
-기준서 제1115호 '고객과의 계약에서 생기는 수익'
회사는 기준서 제1115호 '고객과의 계약에서 생기는 수익'을 적용하였습니다. 기준서 제1115호의 경과규정에 따라 비교 표시된 재무제표는 재작성되지 않았으며 최초 적용 누적효과는 2018년 1월 1일에 이익잉여금(또는 자본)에 인식되도록 소급하여 적용하였습니다. 동 기준서의 적용으로 인한 영향의 상세 정보는 주석 38에서 설명하고 있습니다.
(2) 회사가 적용하지 않은 제ㆍ개정 기준서 및 해석서
회사는 제정 또는 공표됐으나 2018년 1월 1일이후 시작하는 회계연도에 시행일이 도래하지 않았고, 조기 적용하지 않은 제ㆍ개정 기준서 및 해석서는 다음과 같습니다.
- 기준서 제1116호 '리스' 제정
2017년 5월 22일 제정된 기준서 제1116호 '리스'는 2019년 1월 1일 이후 최초로 시작되는 회계연도부터 적용하되 조기 적용할 수도 있습니다. 동 기준서는 현행 기준서제1017호 '리스'를 대체할 예정입니다. 회사는 기준서 제1116호를 2019년 1월 1일 이후 시작되는 회계연도부터 적용할 예정입니다.
새로운 기준서는 단일 리스이용자 모형을 도입하여 리스기간이 12개월을 초과하고 기초자산이 소액이 아닌 모든 리스에 대하여 리스이용자가 자산과 부채를 인식하도록 요구합니다. 리스이용자는 사용권자산과 리스료 지급의무를 나타내는 리스부채를인식해야 합니다.
회사는 기준서 제1116호의 최초 적용에 따른 재무적 영향을 평가하기 위하여 현재 상황 및 입수 가능한 정보에 기초하여 2018년 재무제표에 미치는 영향을 분석 중에 있으나, 회사가 이러한 분석을 완료하기 전까지는 재무적 영향에 대한 합리적 추정치를 제공하는 것이 실무상 어렵습니다
- 기준서 제1109호 '금융상품' 개정
부의 보상을 수반하는 일부 중도상환 가능한 금융자산은 상각후원가로 측정될 수 있도록 개정하였으며, 상각후원가로 측정되는 금융부채가 조건변경 되었으나 제거되지는 않은 경우 변경으로 인한 효과는 당기손익으로 인식되어야 합니다. 동 개정 사항은 2019년 1월 1일 이후 시작하는 회계연도 후부터 적용되며, 조기도입이 가능합니다.
- 기준서 제1019호 '종업원급여' 개정
확정급여제도의 변경으로 제도의 개정, 축소, 정산이 되는 경우 제도의 변경 이후 회계기간의 잔여기간에 대한 당기근무원가 및 순이자를 산정하기 위해 순확정급여부채(자산)의 재측정에 사용된 가정을 사용합니다. 또한, 자산인식상한의 영향으로 이전에 인식하지 않은 초과적립액의 감소도 과거근무원가나 정산손익의 일부로 당기손익에 반영합니다. 개정 내용은 2019년 1월 1일 이후 최초로 시작되는 회계연도 이후 발생한 제도의 개정, 축소, 정산에 전진적으로 적용합니다.
- 기준서 제1028호 '관계기업과 공동기업에 대한 투자' 개정
관계기업이나 공동기업에 대한 다른 금융상품(지분법을 적용하지 않는 금융상품)이 기준서 제1109호의 적용대상임을 명확히 하였으며, 관계기업이나 공동기업에 대한순투자의 일부를 구성하는 장기투자지분의 손상 회계처리에 대해서는 기준서 제1109호를 우선하여 적용하도록 개정하였습니다. 동 개정사항은 2019년 1월 1일 이후 시작하는 회계연도 후부터 적용되며, 조기도입이 가능합니다. 또한, 이 기준서의 최초 적용 시 기준서 제1109호의 경과규정을 적용하여 비교정보의 재작성이 요구되지 않으며, 소급적용으로 인한 효과는 최초 적용일의 기초이익잉여금(또는 적절한 다른 자본요소)에 반영합니다.
- 해석서 제2123호 '법인세 처리의 불확실성' 제정
제정된 해석서는 기업이 적용한 법인세 처리가 과세당국에 의해 인정될지에 대한 불확실성이 존재하는 경우 당기법인세와 이연법인세 인식 및 측정에 적용하며, 법인세 처리 불확실성의 회계단위와 재평가가 필요한 상황 등에 대한 지침을 포함하고 있습니다. 해석서는 2019년 1월 1일부터 적용되며 비교재무제표를 소급 재작성하거나 최초 적용연도 기초에 변경 효과를 반영하는 방법 중 선택할 수 있습니다.
- 연차개선 2015-2017
ㆍ 기준서 제1103호 '사업결합'
공동영업과 관련된 자산에 대한 권리와 부채에 대한 의무를 보유하다가 해당 공동영업(사업의 정의 충족)에 대한 지배력을 획득하는 것은 단계적으로 이루어지는 사업결합이므로, 취득자는 공동영업에 대하여 이전에 보유하고 있던 지분 전부를 재측정합니다. 이 개정 내용은 2019년 1월 1일 이후 처음 시작되는 회계연도 이후에 취득일이 속하는 사업결합부터 적용하되 조기 적용할 수 있습니다.
ㆍ 기준서 제1111호 '공동약정'
공동영업에 참여는 하지만 공동지배력을 보유하지 않은 공동영업 당사자가 공동영업에 대한 공동지배력을 획득하는 경우, 공동영업에 대하여 이전에 보유하고 있던 지분은 재측정하지 않습니다. 이 개정 내용은 2019년 1월 1일 이후 처음 시작되는 회계연도 이후에 공동지배력을 획득하는 거래부터 적용하되 조기 적용할 수 있습니다.
ㆍ 기준서 제1012호 '법인세'
기준서 제1012호 문단 57A의 규정(배당의 세효과 인식시점과 인식항목을 규정)은 배당의 법인세효과 모두에 적용되며, 배당의 법인세효과를 원래 인식하였던 항목에 따라 당기손익, 기타포괄손익 또는 자본으로 인식하도록 개정되었습니다. 이 개정 내용은 2019년 1월 1일 이후 처음 시작되는 회계연도부터 적용하되 조기 적용할 수 있습니다.
ㆍ 기준서 제1023호 '차입원가'
적격자산을 의도된 용도로 사용(또는 판매) 가능하게 하는 데 필요한 대부분의 활동이 완료되면, 해당 자산을 취득하기 위해 특정 목적으로 차입한 자금을 일반차입금에포함한다는 사실을 명확히 하였습니다. 이 개정 내용은 해당 개정 내용을 처음 적용하는 회계연도 이후에 생기는 차입원가에 적용하며, 2019년 1월 1일 이후 처음 시작되는 회계연도부터 적용하되 조기 적용할 수 있습니다.
2.3 외화환산
(1) 기능통화와 표시통화
회사는 회사 내 개별기업의 재무제표에 포함되는 항목들을 각각의 영업활동이 이루어지는 주된 경제 환경에서의 통화("기능통화")를 적용하여 측정하고 있습니다. 회사의 기능통화는 대한민국 원화이며 재무제표는 대한민국 원화로 표시되어 있습니다.
(2) 외화거래와 보고기간말의 환산
외화거래는 거래일의 환율 또는 재측정되는 항목인 경우 평가일의 환율을 적용한 기능통화로 인식됩니다. 외화거래의 결제나 화폐성 외화 자산ㆍ부채의 환산에서 발생하는 외환차이는 당기손익으로 인식됩니다. 다만, 조건을 충족하는 현금흐름위험회피나 순투자의 위험회피의 효과적인 부분과 관련되거나 보고기업의 해외사업장에 대한 순투자의 일부인 화폐성항목에서 생기는 손익은 기타포괄손익으로 인식합니다.
차입금과 관련된 외환차이는 손익계산서에 금융원가로 표시되며, 다른 외환차이는 기타수익 또는 기타비용에 표시됩니다.
비화폐성 금융자산ㆍ부채로부터 발생하는 외환차이는 공정가치 변동손익의 일부로 보아 당기손익-공정가치 측정 지분상품으로부터 발생하는 외환차이는 당기손익으로, 기타포괄손익-공정가치 측정 지분상품의 외환차이는 기타포괄손익에 포함하여 인식됩니다.
2.4 금융자산
(1) 분류
2018년 1월 1일부터 회사는 다음의 측정 범주로 금융자산을 분류합니다.
- 당기손익-공정가치 측정 금융자산
- 기타포괄손익-공정가치 금융자산
- 상각후원가 측정 금융자산
금융자산은 금융자산의 관리를 위한 사업모형과 금융자산의 계약상 현금흐름 특성에근거하여 분류합니다.
공정가치로 측정하는 금융자산의 손익은 당기손익 또는 기타포괄손익으로 인식합니다. 채무상품에 대한 투자는 해당 자산을 보유하는 사업모형에 따라 그 평가손익을 당기손익 또는 기타포괄손익으로 인식합니다. 회사는 금융자산을 관리하는 사업모형을 변경하는 경우에만 채무상품을 재분류합니다.
단기매매항목이 아닌 지분상품에 대한 투자는 최초 인식시점에 후속적인 공정가치 변동을 기타포괄손익으로 표시할 것을 지정하는 취소불가능한 선택을 할 수 있습니다. 지정되지 않은 지분상품에 대한 투자의 공정가치 변동은 당기손익으로 인식합니다.
(2) 측정
회사는 최초 인식시점에 금융자산을 공정가치로 측정하며, 당기손익-공정가치 측정 금융자산이 아닌 경우에 해당 금융자산의 취득과 직접 관련되는 거래원가는 공정가치에 가산합니다. 당기손익-공정가치 측정 금융자산의 거래원가는 당기손익으로 비용처리합니다.
내재파생상품을 포함하는 복합계약은 계약상 현금흐름이 원금과 이자로만 구성되어 있는지를 결정할 때 해당 복합계약 전체를 고려합니다.
① 채무상품
금융자산의 후속적인 측정은 금융자산의 계약상 현금흐름 특성과 그 금융자산을 관리하는 사업모형에 근거합니다. 회사는 채무상품을 다음의 세 범주로 분류합니다.
(가) 상각후원가
계약상 현금흐름을 수취하기 위해 보유하는 것이 목적인 사업모형 하에서 금융자산을 보유하고, 계약상 현금흐름이 원리금만으로 구성되어 있는 자산은 상각후원가로 측정합니다. 상각후원가로 측정하는 금융자산으로서 위험회피관계의 적용 대상이 아닌 금융자산의 손익은 해당 금융자산을 제거하거나 손상할 때 당기손익으로 인식합니다. 유효이자율법에 따라 인식하는 금융자산의 이자수익은 '금융수익'에 포함됩니다.
(나) 기타포괄손익-공정가치 측정 금융자산
계약상 현금흐름의 수취와 금융자산의 매도 둘 다를 통해 목적을 이루는 사업모형 하에서 금융자산을 보유하고, 계약상 현금흐름이 원리금만으로 구성되어 있는 금융자산은 기타포괄손익-공정가치로 측정합니다. 손상차손(환입)과 이자수익 및 외환손익을 제외하고는, 공정가치로 측정하는 금융자산의 평가손익은 기타포괄손익으로 인식합니다. 금융자산을 제거할 때에는 인식한 기타포괄손익누계액을 자본에서 당기손익으로 재분류합니다. 유효이자율법에 따라 인식하는 금융자산의 이자수익은 '금융수익'에 포함됩니다. 외환손익은 '기타수익 또는 기타비용'으로 표시하고 손상차손은'기타 비용'으로 표시합니다.
(다) 당기손익-공정가치측정 금융자산
상각후원가 측정이나 기타포괄손익-공정가치 측정 금융자산이 아닌 채무상품은 당기손익-공정가치로 측정됩니다. 위험회피관계가 적용되지 않는 당기손익-공정가치 측정 채무상품의 손익은 당기손익으로 인식하고 발생한 기간에 손익계산서에 '기타수익 또는 기타비용'으로 표시합니다.
② 지분상품
회사는 모든 지분상품에 대한 투자를 후속적으로 공정가치로 측정합니다. 공정가치 변동을 기타포괄손익으로 표시할 것을 선택한 장기적 투자목적 또는 전략적 투자목적의 지분상품에 대해 기타포괄손익으로 인식한 금액은 해당 지분상품을 제거할 때에도 당기손익으로 재분류하지 않습니다. 이러한 지분상품에 대한 배당수익은 회사가 배당을 받을 권리가 확정된 때 '금융수익'으로 당기손익으로 인식합니다.
당기손익-공정가치로 측정하는 금융자산의 공정가치 변동은 손익계산서에 '기타수익 또는 기타비용'으로 표시합니다. 기타포괄손익-공정가치로 측정하는 지분상품에 대한 손상차손(환입)은 별도로 구분하여 인식하지 않습니다.
(3) 손상
회사는 미래전망정보에 근거하여 상각후원가로 측정하거나 기타포괄손익-공정가치로 측정하는 채무상품에 대한 기대신용손실을 평가합니다. 손상 방식은 신용위험의 유의적인 증가 여부에 따라 결정됩니다. 단, 매출채권 및 리스채권에 대해 회사는 채권의 최초 인식시점부터 전체기간 기대신용손실을 인식하는 간편법을 적용합니다.
(4) 인식과 제거
금융자산의 정형화된 매입 또는 매도는 매매일에 인식하거나 제거합니다. 금융자산은 현금흐름에 대한 계약상 권리가 소멸하거나 금융자산을 양도하고 소유에 따른 위험과 보상의 대부분을 이전한 경우에 제거됩니다.
회사가 금융자산을 양도한 경우라도 채무자의 채무불이행시의 소구권 등으로 양도한금융자산의 소유에 따른 위험과 보상의 대부분을 회사가 보유하는 경우에는 이를 제거하지 않고 그 양도자산 전체를 계속하여 인식하되, 수취한 대가를 금융부채로 인식합니다. 해당 금융부채는 재무상태표에 "차입금"으로 분류하고 있습니다.
(5) 금융상품의 상계
금융자산과 부채는 인식한 자산과 부채에 대해 법적으로 집행가능한 상계권리를 현재 보유하고 있고, 순액으로 결제하거나 자산을 실현하는 동시에 부채를 결제할 의도를 가지고 있을 때 상계하여 재무상태표에 순액으로 표시합니다. 법적으로 집행가능한 상계권리는 미래사건에 좌우되지 않으며, 정상적인 사업과정의 경우와 채무불이행의 경우 및 지급불능이나 파산의 경우에도 집행가능한 것을 의미합니다.
2.5 매출채권
매출채권은 정상적인 영업과정에서 판매된 재고자산 및 제공된 용역과 관련하여 고객으로부터 수취할 금액입니다. 매출채권의 회수가 1년 이내에 예상되는 경우 유동자산으로 분류하고 그렇지 아니한 경우 비유동자산으로 분류하고 있습니다. 매출채권은 공정가치로 인식되고 후속적으로 유효이자율법을 적용한 상각후원가에 대손충당금을 차감하여 측정됩니다.
2.6 재고자산
회사는 재고자산을 총평균법에 의해 산정된 취득원가를 재무상태표가액으로 하고 있으며, 연중 계속기록법에 의하여 수량 및 금액을 계산하고 매기말 실지재고조사를 실시하여 그 기록을 조정하고 있습니다. 또한, 보고기간종료일 현재 재고자산의 시가(제품은 순실현가능가액, 원재료는 현행대체원가)가 취득원가보다 하락한 경우에는 시가를 재무상태표가액으로 하고 있습니다. 재고자산의 저가법 적용은 종목별로 하고 있으며 재고자산의 저가법 적용으로 발생하는 평가손실은 당해 재고자산에서 차감하는 형식으로 표시하고 이를 매출원가에 가산하고 있습니다. 한편, 저가법의 적용에 따른 평가손실을 초래했던 상황이 해소되어 새로운 시가가 장부가액보다 상승한 경우에는 최초의 장부가액을 초과하지 않는 범위 내에서 평가손실을 환입하고 있으며, 이러한 재고자산평가손실의 환입은 매출원가에서 차감하고 있습니다
2.7 유형자산
유형자산은 역사적 원가에서 감가상각누계액과 손상차손누계액을 차감하여 표시하고 있습니다. 역사적 원가는 자산의 취득에 직접적으로 관련된 지출을 포함하며, 후속원가는 자산으로부터 발생하는 미래의 경제적 효익이 회사에 유입될 가능성이 높으며 그 원가를 신뢰성있게 측정할 수 있는 경우에 한하여 자산의 장부금액에 포함하거나 별도의 자산으로 인식하고 있습니다.
회사의 유형자산은 취득원가에서 회사가 추정한 추정내용연수에 따라 정액법에 의하여 상각됩니다.
각 자산별로 회사가 사용하고 있는 추정내용연수는 다음과 같습니다.
| 구분 | 내용연수 |
|---|---|
| 건물 | 40년 |
| 시설장치 | 10년 |
| 기계장치 | 5년 |
| 차량운반구 | 5년 |
| 비품 | 5년 |
회사는 매 보고기간말에 유형자산의 감가상각방법, 잔존가치와 경제적 내용연수를 검토하고 필요한 경우 조정을 하고 있습니다. 자산의 장부금액이 추정 회수가능액을 초과하는 경우 자산의 장부금액을 회수가능액으로 즉시 감소시키고 있습니다. 자산의 처분손익은 처분대가와 자산의 장부금액의 차이로 결정되며, 포괄손익계산서의 기타수익(비용)으로 표시하고 있습니다.
2.8 정부보조금
정부보조금은 보조금의 수취와 정부보조금에 부가된 조건의 준수에 대한 합리적인 확신이 있을 때 공정가치로 인식됩니다. 자산관련보조금은 자산의 장부금액을 계산할 때 차감하여 표시되며, 수익관련보조금은 이연하여 정부보조금의 교부 목적과 관련된 비용에서 차감하여 표시됩니다.
2.9 무형자산
영업권을 제외한 무형자산은 역사적 원가로 최초 인식되고, 원가에서 상각누계액과 손상차손누계액을 차감한 금액으로 표시됩니다.
내부적으로 창출한 무형자산인 개발비는 기술적 실현가능성, 미래경제적효익 등을 포함한 자산 인식요건이 충족된 시점 이후에 발생한 지출금액의 합계입니다. 신제품, 신기술 등의 개발 비용 중 개별적으로 식별가능하고 미래의 경제적 효익이 유입될 가능성이 매우 높은 비용은 개발비로 계상하고 관련 제품 등의 판매 또는 사용이 가능한 시점부터 상각하고 있습니다.
개발비를 포함한 한정된 내용연수를 가지는 다음의 무형자산은 사용가능한 시점부터추정내용연수동안 정액법으로 상각됩니다.
|
과목 |
추정 내용연수 |
|---|---|
|
산업재산권 |
5~10년 |
|
개발비 |
5년 |
2.10 비금융자산의 손상
비한정내용연수를 가진 자산은 상각하지 않고 매년 손상검사를 실시하고 있으며 상각하는 자산의 경우는 장부금액이 회수가능하지 않을 수도 있음을 나타내는 환경의 변화나 사건이 있을 때마다 손상검사를 수행하고 있습니다. 손상차손은 회수가능액을 초과하는 장부금액만큼 인식하고 있고 회수가능액은 순공정가치와 사용가치 중 큰 금액으로 결정하고 있습니다. 손상차손을 인식한 경우, 비금융자산은 매 보고기간말에 손상차손의 환입가능성을 검토하고 있습니다.
2.11 매입채무와 기타채무
매입채무는 정상적인 영업과정에서 공급자로부터 취득한 상품 및 제공받은 용역과 관련하여 지급할 의무가 있는 금액입니다. 매입채무의 지급이 1년 이내에 예상되는 경우 유동부채로 분류하고 그렇지 않은 경우 비유동부채로 분류합니다.
매입채무는 최초에 공정가치로 인식하며, 후속적으로 유효이자율법을 사용한 상각후원가로 측정하고 있습니다.
2.12 금융부채
(1) 분류 및 측정
회사의 당기손익-공정가치 측정 금융부채는 단기매매목적의 금융상품입니다. 주로 단기간 내에 재매입할 목적으로 부담하는 금융부채는 단기매매금융부채로 분류됩니다. 또한, 위험회피회계의 수단으로 지정되지 않은 파생상품이나 금융상품으로부터 분리된 내재파생상품도 단기매매금융부채로 분류됩니다.
당기손익-공정가치 측정 금융부채, 금융보증계약, 금융자산의 양도가 제거조건을 충족하지 못하는 경우에 발생하는 금융부채를 제외한 모든 비파생금융부채는 상각후원가로 측정하는 금융부채로 분류되고 있으며, 재무상태표 상 "매입채무", "차입금" 및 "기타금융부채" 등으로 표시됩니다.
특정일에 의무적으로 상환해야 하는 우선주는 부채로 분류됩니다. 이러한 우선주에 대한 유효이자율법에 따른 이자비용은 다른 금융부채에서 인식한 이자비용과 함께 손익계산서 상 "금융원가"로 인식됩니다.
(2) 제거
금융부채는 계약상 의무가 이행, 취소 또는 만료되어 소멸되거나 기존 금융부채의 조건이 실질적으로 변경된 경우에 재무상태표에서 제거됩니다. 소멸하거나 제3자에게 양도한 금융부채의 장부금액과 지급한 대가(양도한 비현금자산이나 부담한 부채를 포함)의 차액은 당기손익으로 인식합니다.
2.13 종업원급여
(1) 퇴직급여
순확정급여부채는 매년 독립적인 계리사에 의해 예측단위적립방식으로 계산되고 있습니다. 확정급여부채의 현재가치에서 사외적립자산의 공정가치를 차감하여 산출된 순액이 자산일 경우, 제도로부터 환급받거나 제도에 대한 미래기여금이 절감되는 방식으로 이용가능한 경제적 효익의 현재가치를 한도로 자산을 인식하고 있습니다. 확정급여부채의 재측정요소는 보험수리적손익, 확정급여부채의 순이자에 포함된 금액을 제외한 사외적립자산의 수익 및 확정급여부채의 순이자에 포함된 금액을 제외한 자산인식상한효과의 변동으로 구성되어 있으며, 즉시 기타포괄손익으로 인식됩니다.회사는 확정급여부채의 순이자를 확정급여부채에 연차보고기간 초에 결정된 할인율을 곱하여 결정되며 보고기간 동안 기여금 납부와 급여지급으로 인한 확정급여부채의 변동을 고려하여 결정하고 있습니다. 확정급여제도와 관련된 순이자비용과 기타비용은 당기손익으로 인식됩니다.
(2) 주식기준보상
주식결제형 주식기준보상거래의 경우 제공받는 재화나 용역의 공정가치로 측정하며,종업원의 용역제공과 같이 제공받는 재화나 용역의 공정가치를 신뢰성 있게 측정할 수 없는 경우에는 부여한 지분상품의 공정가치에 기초하여 재화나 용역의 공정가치로 간접 측정하고 그 금액을 보상원가와 자본조정으로 회계처리하고 있습니다.
2.14 복합금융상품
회사가 발행한 복합금융상품은 보유자의 선택에 의해 지분상품으로 전환될 수 있는 전환사채입니다.
동 복합금융상품의 부채요소는 최초에 동일한 조건의 전환권이 없는 금융부채의 공정가치로 인식되며, 후속적으로 전환일 또는 만기일까지 상각후원가로 인식됩니다. 자본요소는 복합금융상품 전체의 공정가치와 부채요소의 공정가치의 차이로 최초 인식되며, 후속적으로 재측정되지 아니합니다. 복합금융상품의 발행과 직접적으로 관련된 거래원가는 부채요소와 자본요소의 최초 인식 금액에 비례하여 배분됩니다.
2.15 충당부채 및 우발부채
과거사건의 결과로 존재하는 현재의 법적의무 또는 의제의무 이행을 위하여 경제적효익을 갖는 자원이 유출될 가능성이 높으며 그 의무의 이행에 소요되는 금액의 신뢰성 있는 추정이 가능한 경우 충당부채를 인식하고 있습니다.
충당부채로 인식하는 금액은 관련된 사건과 상황에 대한 불가피한 위험과 불확실성을 고려하여 현재 의무를 보고기간말에 이행하기 위하여 소요되는 지출에 대한 최선의 추정치입니다. 화폐의 시간가치 효과가 중요한 경우 충당부채는 의무를 이행하기위하여 예상되는 지출액의 현재가치로 평가하고 있습니다.
또한 과거사건은 발생하였으나 불확실한 미래사건의 발생여부에 의해서 존재여부가 확인되는 잠재적인 의무가 있는 경우 또는 과거사건이나 거래의 결과 현재 의무가 존재하나 자원이 유출될 가능성이 매우 높지 않거나 당해 의무를 이행하여야 할 금액을신뢰성 있게 추정할 수 없는 경우 우발부채로 주석 기재하고 있습니다.
2.16 법인세비용 및 이연법인세
법인세비용은 당기법인세와 이연법인세로 구성됩니다. 법인세는 기타포괄손익이나 자본에 직접 인식된 항목과 관련된 금액을 제외하고는 당기손익으로 인식합니다. 기타포괄손익이나 자본의 특정 항목과 관련된 경우에는 해당 법인세를 각각 기타포괄손익이나 자본에서 직접 부가하거나 차감하여 인식합니다.
회사는 자산과 부채의 장부금액과 세무기준액의 차이로 인해 발생하는 일시적차이에대해 자산부채법을 적용하여 이연법인세를 인식하고 있습니다. 다만, 사업결합 이외의 거래에서 자산, 부채를 최초로 인식할 때 발생하는 이연법인세자산과 부채는 그 거래가 회계이익이나 과세소득에 영향을 미치지 않는다면 인식하지 아니하고 있습니다. 이연법인세는 관련 이연법인세자산이 실현되고 이연법인세부채가 결제될 때 적용될 것으로 예상되는 보고기간말에 제정되었거나 실질적으로 제정될 세율과 세법을적용하여 인식하고 있습니다.
이연법인세자산은 차감할 일시적차이가 사용될 수 있는 미래 과세소득의 발생가능성이 높은 경우에 인식하고 있습니다.
이연법인세자산과 부채는 당기법인세자산과 당기법인세부채를 상계할 수 있는 법적으로 집행가능한 권리를 가지고 있고, 이연법인세자산과 부채가 동일한 과세당국에 의해서 부과되는 법인세와 관련이 있거나 과세대상기업은 다르지만, 당기법인세부채와 자산을 순액으로 결제할 의도가 있거나, 유의적인 금액의 이연법인세부채가 결제되거나 이연법인세자산이 회수될 미래의 각 회계기간마다 자산을 실현하는 동시에 부채를 결제할 의도가 있는 경우에 상계합니다.
2.17 수익인식
- 수행의무의 식별
회사는 바이오소재 융합기술과 약물전달시스템 및 펩타이드 공학기술 관련 제품 등을 제조하여 판매하는 사업을 영위하고 있습니다. 수익은 고객에게 제품을 인도하여 제품의 통제가 이전되었을 때 인식합니다.
또한, 수취채권은 재화를 인도하였을 때 인식합니다. 이는 재화를 인도하는 시점부터는 시간이 지나기만 하면 대가를 지급받게 되므로 대가를 받을 무조건적인 권리가 생기기 때문입니다.
- 변동대가
회사는 받을 권리를 갖게 될 대가를 더 잘 예측할 것으로 예상하는 기댓값 방법을 사용하여 변동 대가를 추정하고, 반품기한이 경과할 때 이미 인식한 누적 수익금액 중 유의적인 부분을 되돌리지 않을 가능성이 매우 높은 금액까지만 변동대가를 거래가격에 포함하여 수익을 인식합니다. 기업이 받았거나 받을 대가 중에서 권리를 갖게 될 것으로 예상하지 않는 금액은 환불부채로 계상합니다.
- 거래가격의 배분
회사는 하나의 계약에서 식별된 여러 수행의무에 상대적 개별 판매가격을 기초로 거래가격을 배분합니다. 각 수행의무의 개별 판매가격을 추정하기 위하여 '시장평가 조정 접근법'을 사용하며, 예외적으로 일부 거래에 대해서는 예상원가를 예측하고 적절한 이윤을 더하는 '예상원가 이윤 가산 접근법'을 사용하였습니다.
- 반품
회사는 고객에게 환불할 것으로 예상되는 총액을 환불부채로 인식하고 수익을 조정하며, 고객이 반품 권리를 행사할 때 고객으로부터 제품을 회수할 권리를 가지므로 그 자산을 인식하고 해당 금액만큼 매출원가를 조정합니다. 제품을 회수할 권리는 제품의 과거장부금액에서 제품을 회수하는데 드는 원가를 차감하여 측정합니다.
2.18 주당이익
기본주당이익은 주주에게 귀속되는 포괄손익계산서상 당기순이익을 보고기간 동안의 회사의 가중평균 유통보통주식수로 나누어 산정한 것입니다.
2.19 영업부문
회사의 영업부문은 단일 영업부문으로 구성되어 있습니다. 따라서, 보고부문별 영업
손익 등에 대한 공시는 생략하였습니다.
2.20 재무제표 승인
회사의 재무제표는 2019년 3월 11일자로 이사회에서 승인됐으며, 정기주주총회에서수정승인 될 수 있습니다.
3. 중요한 회계추정 및 가정
재무제표 작성에는 미래에 대한 가정 및 추정이 요구되며 경영진은 회사의 회계정책을 적용하기 위해 판단이 요구됩니다. 추정 및 가정은 지속적으로 평가되며, 과거 경험과 현재의 상황에 비추어 합리적으로 예측가능한 미래의 사건을 고려하여 이루어집니다. 회계추정의 결과가 실제 결과와 동일한 경우는 드물 것이므로 중요한 조정을유발할 수 있는 유의적인 위험을 내포하고 있습니다.
다음 회계연도에 자산 및 부채 장부금액의 조정에 영향을 미칠 수 있는 경영진 판단과 유의적 위험에 대한 추정 및 가정은 다음과 같습니다. 일부 항목에 대한 유의적인 판단 및 추정에 대한 추가적인 정보는 개별 주석에 포함되어 있습니다.
(1) 법인세
회사의 과세소득에 대한 법인세는 다양한 국가의 세법 및 과세당국의 결정을 적용하여 산정되므로 최종 세효과를 산정하는 데에는 불확실성이 존재합니다.
회사는 특정 기간동안 과세소득의 일정 금액을 투자, 임금증가 등에 사용하지 않았을때 세법에서 정하는 방법에 따라 산정된 법인세를 추가로 부담합니다. 따라서, 해당 기간의 당기법인세와 이연법인세를 측정할 때 이에 따른 세효과를 반영하여야 하고, 이로 인해 회사가 부담할 법인세는 각 연도의 투자, 임금증가 등의 수준에 따라 달라지므로 최종 세효과를 산정하는데에는 불확실성이 존재합니다.
(2) 금융자산의 손상
금융자산의 손실충당금은 부도위험 및 기대손실률 등에 대한 가정에 기초하여 측정됩니다. 회사는 이러한 가정의 설정 및 손상모델에 사용되는 투입변수의 선정에 있어서 회사의 과거 경험, 현재 시장 상황, 재무보고일 기준의 미래전망정보 등을 고려하여 판단합니다.
(3) 순확정급여부채
순확정급여부채의 현재가치는 보험수리적방식에 의해 결정되는 다양한 요소들 특히 할인율의 변동에 영향을 받습니다.
(4) 수익인식
회사는 고객에게 제품 판매 후 고객이 반품할 것으로 예상되는 제품에 대하여 환불부채와 회수할 재화에 대한 권리를 인식하고 있습니다. 판매시점에 포트폴리오 수준에서 누적된 경험에 기초하여 기댓값 방법으로 반품율을 예측하고 있으며, 회사의 수익은 예측된 반품율의 변동에 영향을 받습니다.
4. 공정가치
당기 중 회사의 금융자산과 금융부채의 공정가치에 영향을 미치는 사업환경 및 경제적인 환경의 유의적인 변동은 없습니다.
5. 현금및현금성자산
현금은 회사 보유현금 및 요구불예금(당좌예금, 보통예금)으로, 현금성자산은 유동성이 매우 높으며 확정된 금액으로 전환이 용이하고 가치변동의 위험이 경미한 예금 자산으로 구성되어 있습니다.
보고기간종료일 현재 현금및현금성자산의 구성 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 계정과목 | 당기말 | 전기말 |
| 은행예금 및 보유현금 | 859,192 | 5,276,939 |
6. 사용제한 금융상품
보고기간종료일 현재 사용이 제한된 예금 등의 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 계정과목 | 종류 | 당기말 | 전기말 | 사용제한 사유 |
| 현금및현금성자산 | 보통예금 | 223 | 16,250 | 국책과제 관련 예금 |
7. 매출채권
매출채권은 보고기간종료일로부터 1년 이내에 만기가 도래하여 현재가치할인에 따른 효과가 중요하지 않으므로 공정가치와 장부금액이 일치합니다.
(1) 보고기간종료일 현재 매출채권의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기말 | 전기말 |
| 매출채권 | 1,904,579 | 1,851,231 |
| 대손충당금 | (264,470) | (201,282) |
| 합계 | 1,640,109 | 1,649,949 |
(2) 보고기간종료일 현재 손상되지 않은 매출채권의 연령분석은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기말 | 전기말 |
| 3개월이하 | 1,198,917 | 1,276,093 |
| 3개월 초과 6개월 이하 | 344,624 | 305,667 |
| 6개월 초과 | 96,568 | 68,189 |
| 합계 | 1,640,109 | 1,649,949 |
(3) 당기 및 전기의 매출채권 손실충당금 변동 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당기 | 전기 |
| 기초 | 201,282 | 192,208 |
| 설정(환입) | 63,188 | 9,074 |
| 기말 | 264,470 | 201,282 |
(4) 회사의 손실충당금 설정방법은 개별분석을 통해 산출하고, 개별분석에 해당되지 않는 채권은 예상손실율을 적용하고 있습니다.
8. 금융상품
(1) 금융상품의 범주별 구분 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
|
재무상태표 상 자산 |
당기말 |
전기말 |
|
당기손익-공정가치 금융자산 |
- | 503,734 |
|
상각후원가 금융자산 |
||
| 현금 및 현금성자산 | 859,192 | 5,276,939 |
|
매출채권 |
1,640,109 | 1,649,949 |
|
기타유동금융자산 |
453 | 5,995 |
| 장기금융상품 | 529,470 | 385,618 |
| 기타비유동금융자산 | 434,552 | 290,965 |
| 합계 | 3,463,776 | 8,113,200 |
| (단위: 천원) | ||
|---|---|---|
|
재무상태표 상 부채 |
당기말 |
전기말 |
|
상각후원가 금융부채 |
|
|
| 매입채무 | 121,746 | 135,088 |
| 단기차입금 | 870,000 | 920,000 |
| 기타금융부채 - 유동 | 660,480 | 1,011,379 |
| 유동성장기차입금 | 1,605,545 | 1,087,256 |
| 유동성전환사채 | 4,495,438 | 2,474,348 |
| 장기차입금 | 851,965 | 897,780 |
| 전환사채 | - | 4,012,336 |
| 기타금융부채 - 비유동 | 298,461 | 463,322 |
| 합계 | 8,903,635 | 11,001,509 |
(2) 금융상품 범주별 순손익 내역
당기와 전기 중 금융상품 범주별 순손익 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
|
구분 |
당기 |
전기 |
| 상각후원가 금융자산 | ||
| 이자수익 | 42,432 | 9,949 |
| 외환차익 | 48,936 | 21,527 |
| 당기손익인식금융자산평가이익 | - | 3,734 |
| 장기금융자산평가이익 | 11,852 | - |
| 외화환산이익 | 274 | - |
| 합계 | 103,494 | 35,210 |
| 상각후원가 금융부채 | ||
| 이자비용 | 733,694 | 623,620 |
| 외환차손 | 12,902 | 86,166 |
| 외화환산손실 | 4,842 | 82,678 |
| 합계 | 751,438 | 792,464 |
9. 기타금융자산
보고기간종료일 현재 기타금융자산의 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 당기말 | 전기말 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
| 미수금 | 453 | - | 5,995 | - |
| 보증금 | - | 434,552 | - | 290,965 |
| 합계 | 453 | 434,552 | 5,995 | 290,965 |
10. 기타자산
보고기간종료일 현재 기타자산의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당기말 | 전기말 |
| 선급금 | 145,550 | 29,570 |
| 선급비용 | 28,163 | 28,549 |
| 부가세대급금 | 66,573 | 85,928 |
| 합계 | 240,286 | 144,047 |
11. 재고자산
보고기간종료일 현재 재고자산의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구 분 | 당기말 | 전기말 |
| 제품 | 1,820,191 | 1,775,708 |
| 재고자산평가충당금 | (408,188) | (349,249) |
| 원재료 | 1,200,137 | 1,053,057 |
| 재고자산평가충당금 | (68,770) | (68,770) |
| 합계 | 2,543,370 | 2,410,746 |
회사는 재고자산의 시가가 취득원가보다 하락한 경우에는 저가법을 사용하여 재무상태표가액으로 하고 있습니다. 한편, 감액된 재고자산의 시가가 장부금액보다 상승한 경우에는 최초의 장부금액을 초과하지 않는 범위 내에서 평가손실을 환입하고 있습니다.
12. 유형자산
(1) 보고기간종료일 현재 유형자산 장부금액의 구성 내역은 다음과 같습니다.
<당기말>
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 취득원가 | 감가상각누계액 | 정부보조금 | 장부금액 |
| 토지 | 914,496 | - | - | 914,496 |
| 건물 | 6,960,896 | (1,347,969) | - | 5,612,927 |
| 기계장치 | 4,096,750 | (2,997,264) | (14,082) | 1,085,404 |
| 시설장치 | 4,719,754 | (2,650,698) | - | 2,069,056 |
| 차량운반구 | 13,943 | (11,999) | - | 1,944 |
| 비품 | 425,909 | (293,925) | - | 131,984 |
| 건설중인자산 | 53,300 | - | - | 53,300 |
| 합계 | 17,185,048 | (7,301,855) | (14,082) | 9,869,111 |
<전기말>
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 취득원가 | 감가상각누계액 | 정부보조금 | 장부금액 |
| 토지 | 914,496 | - | - | 914,496 |
| 건물 | 6,960,896 | (1,173,946) | - | 5,786,950 |
| 기계장치 | 3,260,940 | (2,690,259) | (19,431) | 551,250 |
| 시설장치 | 4,672,276 | (2,195,524) | - | 2,476,752 |
| 차량운반구 | 13,943 | (10,705) | - | 3,238 |
| 비품 | 365,740 | (257,581) | - | 108,159 |
| 건설중인자산 | 28,700 | - | - | 28,700 |
| 합계 | 16,216,991 | (6,328,015) | (19,431) | 9,869,545 |
(2) 당기 및 전기 중 회사의 유형자산 장부가액 변동 내역은 다음과 같습니다.
<당기>
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 기초 | 취득 | 감가상각비 | 대체 | 기말 |
| 토지 | 914,496 | - | - | - | 914,496 |
| 건물 | 5,786,950 | - | (174,023) | - | 5,612,927 |
| 기계장치 | 551,250 | 807,040 | (301,656) | 28,770 | 1,085,404 |
| 시설장치 | 2,476,752 | 47,478 | (455,174) | - | 2,069,056 |
| 차량운반구 | 3,238 | - | (1,294) | - | 1,944 |
| 비품 | 108,159 | 60,169 | (36,344) | - | 131,984 |
| 건설중인자산 | 28,700 | 53,370 | - | (28,770) | 53,300 |
| 합계 | 9,869,545 | 968,057 | (968,491) | - | 9,869,111 |
<전기>
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 기초 | 취득 | 처분 | 감가상각비 | 대체 | 기말 |
| 토지 | 914,496 | - | - | - | - | 914,496 |
| 건물 | 4,541,203 | 7,638 | - | (147,891) | 1,386,000 | 5,786,950 |
| 기계장치 | 741,639 | 70,805 | (5) | (273,519) | 12,330 | 551,250 |
| 시설장치 | 1,694,197 | 8,000 | - | (386,745) | 1,161,300 | 2,476,752 |
| 차량운반구 | 4,533 | - | - | (1,295) | - | 3,238 |
| 비품 | 78,102 | 32,125 | - | (32,068) | 30,000 | 108,159 |
| 건설중인자산 | 1,200,300 | 1,418,030 | - | - | (2,589,630) | 28,700 |
| 합계 | 9,174,470 | 1,536,598 | (5) | (841,518) | - | 9,869,545 |
(3) 당기 및 전기의 계정과목별 감가상각 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 과목 | 당기 | 전기 |
| 판매비와관리비 | 14,298 | 20,500 |
| 제조원가 | 919,978 | 784,872 |
| 연구개발비 | 34,215 | 36,146 |
| 합계 | 968,491 | 841,518 |
(4) 보고기간종료일 현재 토지의 소유권은 진천군에 있으며, 분양대금 납부가 완료되는 2022년 7월에 소유권이 이전될 예정입니다. 이와 관련한 미지급 분양대금은 장기미지급금으로 계상되어 있습니다.
(5) 회사는 보고기간종료일 현재 기계장치 중 일부에 대하여 금융리스계약을 체결하고 있으며, 리스계약이 종료되는 2022년 11월에 양수할 예정입니다. 금융리스로 분류된 기계장치의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 |
당기말 |
전기말 |
|
원가- 자본화된 금융리스 |
692,935 | - |
|
감가상각누계액 |
(57,212) | - |
|
순장부금액 |
635,723 | - |
보고기간종료일 현재 기계장치 금융리스계약과 관련하여 리스제공자에게 지급할 최소 리스료는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 |
당기말 |
전기말 |
|
최소리스료 총액 |
||
|
1년 이내 |
158,368 | - |
|
1년 초과 5년 이내 |
600,492 | - |
|
5년 초과 |
- | - |
|
합계 |
758,860 | - |
(6) 당기말과 전기말 현재 회사의 차입금 등과 관련하여 금융기관에 담보(채권최고액: 6,000,000천원)로 제공된 일부 건물, 기계장치 및 시설장치의 장부금액은 각각 3,540,527천원 및 3,663,188천원입니다.
(7) 상기 이외에 회사는 KB캐피탈과 현대캐피탈에 차량운반구 운용리스 계약을 체결하고 있습니다.
13. 무형자산
(1) 보고기간종료일 현재 무형자산 장부금액의 구성 내역은 다음과 같습니다.
<당기말>
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 취득원가 | 감가상각누계액 | 정부보조금 | 장부금액 |
| 산업재산권 | 2,143,542 | (824,032) | - | 1,319,510 |
| 개발비 | 9,853,320 | (3,618,724) | (3,927,380) | 2,307,216 |
| 기타무형자산 | 2,589,185 | (21,260) | - | 2,567,925 |
| 합계 | 14,586,047 | (4,464,016) | (3,927,380) | 6,194,651 |
<전기말>
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 취득원가 | 감가상각누계액 | 정부보조금 | 장부금액 |
| 산업재산권 | 1,782,461 | (622,514) | - | 1,159,947 |
| 개발비 | 8,786,760 | (2,844,541) | (4,091,679) | 1,850,540 |
| 기타무형자산 | 2,205,511 | (5,218) | - | 2,200,293 |
| 합계 | 12,774,732 | (3,472,273) | (4,091,679) | 5,210,780 |
(2) 당기 및 전기 중 무형자산 장부가액 변동 내역은 다음과 같습니다.
<당기>
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구 분 | 기초 | 취득 | 상각 | 정부보조금 | 기말 |
| 산업재산권 | 1,159,947 | 361,082 | (201,519) | - | 1,319,510 |
| 개발비 | 1,850,540 | 1,066,561 | (409,934) | (199,951) | 2,307,216 |
| 기타무형자산 | 2,200,293 | 383,674 | (16,042) | - | 2,567,925 |
| 합계 | 5,210,780 | 1,811,317 | (627,495) | (199,951) | 6,194,651 |
<전기>
| (단위: 천원) | ||||||
|---|---|---|---|---|---|---|
| 구 분 | 기초 | 취득 | 손상 | 상각 | 정부보조금 | 기말 |
| 산업재산권 | 1,115,868 | 224,457 | - | (180,378) | - | 1,159,947 |
| 개발비 | 2,223,383 | 1,908,104 | (796,716) | (409,935) | (1,074,296) | 1,850,540 |
| 기타무형자산 | 1,071,422 | 1,134,089 | - | (5,218) | - | 2,200,293 |
| 합계 | 4,410,673 | 3,266,650 | (796,716) | (595,531) | (1,074,296) | 5,210,780 |
(3) 당기 및 전기의 계정과목별 무형자산 상각 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 과목 | 당기 | 전기 |
| 제조원가 | 409,934 | 409,935 |
| 판매비와관리비 | 217,561 | 185,596 |
| 합계 | 627,495 | 595,531 |
(4) 당기와 전기 중 제조원가로 계상한 경상연구개발비는 각각 224,004천원과 227,645천원입니다.
(5) 보고기간종료일 현재 현재 주요 개발프로젝트별 장부금액 및 잔여상각기간은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 분류 | 단계 | 개별자산명 | 현진행단계 | 장부금액 | 잔여상각기간 |
| 개발비 | 개발완료 | 골재생재(Regenomer) | 제품판매중 | 100,365 | 6개월 |
| 근골격재생용 바이오소재 (OCS-B/H Collagen) |
37,973 | 1년 | |||
| 개발중 | 바이오임플란트 시스템 | 식약청 제품 허가 단계 |
1,262,531 | - | |
| 펩타이드 기반 화장품 | 814,023 | - | |||
| 치주조직재생(XenoGide) | 92,324 | - | |||
| 합계 | 2,307,216 | ||||
| 가. | 골재생재(Regenomer)는 치주조직 재생용 유도재로, 인증취득 후 2014년 부터 판매중입니다. |
| 나. | 근골격재생용 바이오소재(OCS-B/H Collagen)는 골이식용 복합소재로, 인증취득 후 2015년 부터 판매중입니다. |
| 다. | 바이오임플란트 개발은 노인의 구강건강 증진을 위한 노인 맞춤형 치과용 바이오임플란트 시스템의 개발로, 2017년도 하이브리드 임플란트 관련된 국내 특허 등록을 마쳤으며, 현재 시제품 제작을 완료하여 식약처 허가를 진행하고 있는 상황입니다. |
| 라. | 펩타이드 기반 화장품은 피부의 트러블 예방용 기능성 화장품으로, 본 건과 관련하여2건의 특허출원을 완료하였으며, 시제품개발단계는 완료하여 2019년 제품 판매 허가를 목표로 하고 있습니다. |
| 마. | 치주조직재생(XenoGide)은 골이식용 복합소재로, 시제품 개발 단계는 완료하여 2019년 제품 판매 허가를 목표로 하고 있습니다. |
14. 정부보조금
(1) 회사는 바이오소재 개발과 관련하여 중소기업청 등과 과제수행 주관사로서 협약을 체결하여 과제물을 수행하고 있습니다.
(2) 당기와 전기 중 정부보조금의 증감 내역은 다음과 같습니다.
<당기>
| (단위: 천원) | |||
|---|---|---|---|
| 구분 | 개발비 | 기계장치 | 선수금 |
| 기초 | 4,091,679 | 19,431 | 16,250 |
| 수령액 | - | - | 299,830 |
| 자산취득 | 199,951 | - | (199,951) |
| 비용상계 | (364,250) | (5,349) | (115,906) |
| 기말 | 3,927,380 | 14,082 | 223 |
<전기>
| (단위: 천원) | |||
|---|---|---|---|
| 구분 | 개발비 | 기계장치 | 선수금 |
| 기초 | 3,767,202 | 16,981 | 939,044 |
| 수령액 | - | - | 159,302 |
| 자산취득 | 1,074,296 | 7,800 | (1,082,096) |
| 비용상계 | (364,249) | (5,350) | - |
| 손상 | (385,570) | - | - |
| 기말 | 4,091,679 | 19,431 | 16,250 |
15. 기타금융부채
보고기간종료일 현재 회사의 기타금융부채의 구성 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 당기말 | 전기말 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
| 미지급금 | 341,273 | - | 668,434 | - |
| 미지급비용 | 221,611 | - | 236,648 | - |
| 장기미지급금 | 103,042 | 309,127 | 111,743 | 482,436 |
| 차감: 현재가치할인차금 | (5,446) | (10,666) | (5,446) | (19,114) |
| 합계 | 660,480 | 298,461 | 1,011,379 | 463,322 |
16. 기타부채
보고기간종료일 현재 회사의 기타부채의 구성 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 당기말 | 전기말 | ||
| 유동 | 비유동 | 유동 | 비유동 | |
| 선수금 | 14,403 | 1,124,500 | 32,219 | 1,124,500 |
| 예수금 | 35,193 | - | 30,430 | - |
| 합계 | 49,596 | 1,124,500 | 62,649 | 1,124,500 |
17. 단기차입금
보고기간종료일 현재 회사의 단기차입금 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 차입처 | 내역 | 연이자율(%) | 당기말 | 전기말 |
| 중소기업은행 | 일반대출(주1) |
4.03% | 420,000 | 420,000 |
| 일반대출 | 5.89% | 450,000 | 500,000 | |
| 합계 | 870,000 | 920,000 | ||
| (주1) | 상기 차입금에 대하여 기술신용보증기금의 보증서가 담보로 제공되고 있습니다. |
18. 장기차입금
(1) 보고기간종료일 현재 회사의 장기차입금 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 차입처 | 내역 | 연이자율(%) | 당기말 | 전기말 |
| 중소기업은행 | 일반시설자금(주1) |
4.25% | 1,775,116 | 1,925,116 |
| 일반시설자금 | 6.33% | - | 59,920 | |
| IBK캐피탈 | 시설대여(리스) | 4.60% | 682,394 | |
| 소계 | 2,457,510 | 1,985,036 | ||
| 차감: 유동성장기차입금 | (1,605,545) | (1,087,256) | ||
| 장기차입금 잔액 | 851,965 | 897,780 | ||
| (주1) | 상기 차입금에 대하여 회사의 건물 및 기계장치 등과 기술신용보증기금의 보증서가 담보로 제공되고 있습니다. |
(2) 보고기간종료일 현재 회사의 장기차입금의 상환계획은 다음과 같습니다
| (단위: 천원) | ||||
|---|---|---|---|---|
| 내역 | 2020년 | 2021년 | 2022년 | 합계 |
| 중소기업은행 | 299,260 | - | - | 299,260 |
| IBK캐피탈 | 135,782 | 142,161 | 274,762 | 552,705 |
| 합계 | 435,042 | 142,161 | 274,762 | 851,965 |
19. 전환사채
(1) 보고기간종료일 현재 회사의 전환사채 내역은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구분 | 당기말 | 전기말 | ||
| 제5회 전환사채 | 제3회 전환사채 | 제4회 전환사채 | 제5회 전환사채 | |
| 발행일 | 2017-12-26 | 2015-03-02 | 2016-03-31 | 2017-12-26 |
| 상환일 | 2020-12-26(주2) | 2020-03-02 | 2021-03-31 | 2020-12-26 |
| 액면이자율 | 0% | 1% | 0% | 0% |
| 전환가액 | 9,994원(주1) | 6,770원 | 7,627원 | 10,566원 |
| 금액 | 5,000,000 | 1,000,000 | 1,600,000 | 5,000,000 |
| 상환할증금 | 634,125 | 225,621 | 352,304 | 634,125 |
| 전환권조정 | (1,138,687) | (241,118) | (462,459) | (1,621,789) |
| 전환사채 합계 | 4,495,438 | 984,503 | 1,489,845 | 4,012,336 |
| 차감: 유동성전환사채 | 5,000,000 | 1,000,000 | 1,600,000 | - |
| 차감: 유동성상환할증금 | 634,125 | 225,621 | 352,304 | - |
| 차감: 유동성전환권조정 | (1,138,687) | (241,118) | (462,459) | - |
| 차감계 | - | - | - | 4,012,336 |
| (주1) | 전환사채 계약조건에 따라 주식 시가하락으로 인해 2018년 12월 26일자로 전환가액이 조정되었습니다. |
| (주2) | 계약상 상환일은 2020년이나 조기상환청구 행사일자가 2019년으로 유동성전환사채로 분류하였습니다. |
(2) 전환사채의 상환 또는 전환에 관한 조건
| 구분 | 조건 |
|---|---|
| 사채의 명칭 | 제5회 사모전환사채 |
| 액면가액 | 5,000백만원 |
| 발행가액 | 5,000백만원 |
| 만기보장수익률 | 3개월 복리 4.00% |
| 원금상환방법 | 사채 투자자는 사채 발행일 이후 2년이 경과한 날(2019년 12월 26일)부터 매 3개월마다 사채 권면액 전부 또는 일부에 대해 조기 상환을 청구할 수 있다. |
| 전환권 행사기간 | 사채 발행일 이후 이후 1년이 경과한 날(2018년 12월 26일)부터 만기일 1개월 전(2020년 11월 26일) |
| 전환권 행사시 발행할 주식 | 기명식 보통주식 |
| 전환권 행사가액 | 9,994원/1주 |
| 전환가격 조정 | 계약서상 명시되는 사유 발생시 조정(주1) |
| 기한이익 상실에 따른 상환 | 계약서상 기한이익 상실사유 발생시 사채 투자자가 투자한 원금과 투자일로부터 회수일까지 연 복리 15%계산에 의한 이자를 상환한다. |
| 신주의 배당기산일 | 전환에 의하여 발행된 주식은 그 전환을 청구한 날이 속한 영업연도의 직전 영업연도 말에 전환된 것으로 보아 배당의 효력을 가진다. |
| (주1) | 전환권 행사전에 합병, 자본의 감소, 주식분할 및 병합, 시가를 하회하는 발행가액으로 전환사채 신주인수권부사채를 발행하거나, 유상 또는 무상증자, 주식배당, 준비금의 자본전입 등을 함으로써 주식을 발행하는 경우 행사가액을 조정합니다. |
20. 순확정급여부채
(1) 보고기간종료일 현재 순확정급여부채와 관련하여 재무상태표에 인식된 금액은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기말 | 전기말 |
| 확정급여부채의 현재가치 | 1,919,528 | 1,444,452 |
| 사외적립자산의 공정가치 | (255,637) | (244,596) |
| 순확정급여부채 | 1,663,891 | 1,199,856 |
(2) 당기와 전기 중 확정급여부채의 현재가치 변동 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 기초 금액 | 1,444,452 | 1,402,293 |
| 당기근무원가 | 285,009 | 141,149 |
| 이자원가 | 45,749 | 38,518 |
| 보험수리적손익 | 295,627 | (120,740) |
| 퇴직급여 지급액 | (151,309) | (16,768) |
| 기말 금액 | 1,919,528 | 1,444,452 |
(3) 당기와 전기 중 확정급여제도와 관련하여 인식된 손익은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 당기근무원가 | 285,009 | 141,149 |
| 이자비용 | 45,749 | 38,518 |
| 사외적립자산의기대수익 | (7,918) | (6,975) |
| 확정급여제도와 관련하여 인식된 손익 | 322,840 | 172,692 |
(4) 당기와 전기 중 사외적립자산의 공정가치 변동 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 기초금액 | 244,596 | 241,625 |
| 납입액 | 20,000 | - |
| 기대수익 | 7,918 | 6,975 |
| 지급액 | (11,827) | - |
| 보험수리적손익 | (5,050) | (4,004) |
| 기말 금액 | 255,637 | 244,596 |
(5) 당기와 전기 중 확정급여제도 재측정요소의 구성요소는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 확정급여부채 보험수리적손익 | (295,627) | 120,740 |
| 사외적립자산 보험수리적손익 | (5,050) | (4,004) |
| 확정급여제도의 재측정요소 | (300,677) | 116,736 |
| 법인세효과(11%) | 33,074 | (12,841) |
| 세후 확정급여제도의 재측정요소 | (267,603) | 103,895 |
(6) 보고기간종료일 현재 사용한 주요 보험수리적 가정은 다음과 같습니다.
| 구분 | 당기말 | 전기말 |
|---|---|---|
| 할인율 | 2.72% | 3.29% |
| 사외적립자산의 기대수익률 | 2.72% | 3.29% |
| 미래임금상승률 | 6.82% + 승급지수 | 4.20% + 승급지수 |
(7) 보고기간종료일 현재 확정급여부채의 민감도분석 내용은 다음과 같습니다.
| 구분 | 가정의 변동 | 확정급여부채의 변동 |
|---|---|---|
| 할인율 | -1% | 6.10% 증가 |
| +1% | 5.20% 감소 | |
| 임금상승률 | -1% | 5.30% 감소 |
| +1% | 6.30% 증가 |
21. 자본금
(1) 보고기간종료일 현재 자본금의 구성 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기말 | 전기말 |
| 수권주식수 | 100,000,000주 | 100,000,000주 |
| 발행한 주식의 수 | 6,367,958주 | 6,010,469주 |
| 주당액면가액 | 500원 | 500원 |
| 자본금 | 3,183,979 | 3,005,235 |
(2) 당기와 전기 자본금과 주식발행초과금의 변동 내역은 다음과 같습니다.
| (단위: 주,천원) | ||||
|---|---|---|---|---|
|
구분 |
주식수 |
자본금 |
주식발행초과금 |
합 계 |
| 전기초 | 5,433,576 | 2,716,788 | 22,168,919 | 24,885,707 |
| 전환사채의 행사 | 576,893 | 288,447 | 4,574,787 | 4,863,234 |
| 전기말 | 6,010,469 | 3,005,235 | 26,743,706 | 29,748,941 |
| 당기초 | 6,010,469 | 3,005,235 | 26,743,706 | 29,748,941 |
| 전환사채의 행사 | 357,489 | 178,744 | 2,978,695 | 3,157,439 |
| 당기말 | 6,367,958 | 3,183,979 | 29,722,401 | 32,906,380 |
22. 자본잉여금 및 자본조정
보고기간종료일 현재 자본잉여금 및 자본조정 내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 구분 | 당기말 | 전기말 | |
| 자본잉여금 | 주식발행초과금 | 29,722,401 | 26,743,706 |
| 전환권대가 | 884,731 | 1,414,302 | |
| 기타자본잉여금 | 12,352 | 5,362 | |
| 소계 | 30,619,484 | 28,163,370 | |
| 자본조정 | 주식선택권 | 4,965 | 11,955 |
23. 결손금처리계산서
당기 및 전기의 결손금처리계산서의 내용은 다음과 같습니다.
| (단위: 천원) | ||||
|---|---|---|---|---|
| 구 분 | 제 15기(당기) | 제 14기(전기) | ||
| 처리예정일: 2018년 3월 28일 | 처리확정일: 2018년 3월 30일 | |||
| I. 미처리결손금 | 23,232,459 | 18,818,701 | ||
| 전기이월미처리결손금 | 18,818,701 | 16,354,983 | ||
| 당기순손실 | 4,146,155 | 2,567,612 | ||
| 확정급여제도의 재측정요소 | 267,603 | (103,894) | ||
| II.결손금처리액 | - | - | ||
| III.차기이월미처리결손금 | 23,232,459 | 18,818,701 | ||
23. 우발채무와 약정사항
(1) 보고기간종료일 현재 금융기관과 체결한 약정사항 내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 금융기관 | 구분 | 한도액 | 실행금액 |
| 중소기업은행 | 일반대출 | 920,000 | 870,000 |
| 일반시설자금 | 5,000,000 | 1,775,116 | |
| 합계 | 5,920,000 | 2,645,116 | |
회사는 상기 약정사항에 대하여 건물 및 기계장치 등(채권채고액 6,000백만원)을 담보로 제공하고 있으며, 기술신용보증기금으로부터 1,855백만원의 지급보증을 제공받고 있습니다. 또한, 상기 약정사항에 대하여 대표이사로부터 지급보증을 제공받고 있습니다
(2) 회사는 IBK캐피탈과 기계장치 취득에 대한 금융리스계약을 체결하고 있습니다.이와 관련하여 장기차입금은 682,394천원, 금융리스로 분류된 기계장치는 635,723천원을 인식하고 있습니다.
(3) 회사는 바이오벤처기업으로서 그 영업활동의 변동성과 개발비 등 일부 자산의 불확실성은 일반기업보다 클 수 있으며, 현재 자체 수익성모형을 지속적으로 확립하고 있는 상태입니다. 이에 따라 영업환경의 변화나 기술력의 발전상태 등에 따라 향후 회사의 재무상태나 경영성과 등이 큰 폭으로 변동할 가능성이 있으며, 본 재무제표는이러한 변화가능성으로 인하여 발생가능한 조정사항은 반영되지 않았습니다.
(4) 상기 이외에 회사는 서울보증보험으로부터 3백만원의 이행지급보증을 제공받고 있습니다.
25. 법인세비용
(1) 당기 및 전기 중 회사의 손익에 반영된 법인세비용(수익)의 산출 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 당기법인세 부담액 | - | - |
| 전기 이전의 당기법인세에 대한 당기법인세 부담액 등 | - | - |
| 일시적차이 등의 발생과 소멸로 인한 이연법인세비용 | - | - |
| 당기손익 이외로 인식되는 항목과 관련된법인세비용(수익) | 98,527 | (27,816) |
| 법인세비용(수익) | 98,527 | (27,816) |
(2) 당기손익 이외로 인식되는 항목과 관련된 법인세비용(수익)의 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 전환권대가 | 65,453 | (14,975) |
| 확정급여제도의 재측정요소 | 33,074 | (12,841) |
| 합계 | 98,527 | (27,816) |
(3) 법인세비용차감전순손실과 법인세비용간의 관계
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 법인세비용차감전순손실 | (4,047,628) | (2,595,428) |
| 적용세율에 따른 법인세비용 | (445,239) | (285,497) |
| 법인세 효과 | ||
| 불공제비용(수익) 등 | (33,054) | 68,506 |
| 미인식이연법인세효과 | 576,820 | 189,175 |
| 법인세비용(수익) | 98,527 | (27,816) |
(4) 당기 및 전기 중 회사의 이연법인세자산(부채)의 변동 내역은 다음과 같습니다.
<당기>
| (단위: 천원) | |||
|---|---|---|---|
| 계정과목 | 기초 | 증감 | 기말 |
| 퇴직급여충당부채 | 158,890 | 52,258 | 211,148 |
| 대손충당금 | 20,098 | 6,898 | 26,996 |
| 정부보조금 | 513,485 | (79,924) | 433,561 |
| 감가상각비 | 755 | (295) | 460 |
| 퇴직연금 | (26,906) | (1,214) | (28,120) |
| 미지급연차 | 3,763 | - | 3,763 |
| 전환사채 | (122,465) | 66,963 | (55,502) |
| 기타 | 206,391 | (118,634) | 87,757 |
| 미인식이연법인세 | (754,011) | 73,948 | (680,063) |
| 합 계 | - | - | - |
<전기>
| (단위: 천원) | |||
|---|---|---|---|
| 계정과목 | 기초 | 증감 | 기말 |
| 퇴직급여충당부채 | 154,089 | 4,801 | 158,890 |
| 대손충당금 | 18,924 | 1,174 | 20,098 |
| 정부보조금 | 431,237 | 82,248 | 513,485 |
| 감가상각비 | 1,050 | (295) | 755 |
| 퇴직연금 | (26,579) | (327) | (26,906) |
| 신주인수권부사채 | 4,494 | (4,494) | - |
| 미지급연차 | 3,763 | - | 3,763 |
| 전환사채 | (106,449) | (16,016) | (122,465) |
| 기타 | 227,076 | (20,685) | 206,391 |
| 미인식이연법인세 | (707,605) | (46,406) | (754,011) |
| 합 계 | - | - | - |
상기 이외에 이월세액공제 및 이월결손금에 따른 이연법인세 자산이 존재하나 실현가능성이 낮다고 판단하여 미인식하였습니다.
(5) 회사는 전반적인 경제환경과 산업에 대한 전망, 향후 예상수익, 이월세액공제와 이월결손금의 공제가능기간 등 다양한 요소들을 고려하여 매 보고기간말에 이연법인세자산을 평가하며 이연법인세자산의 일부 또는 전부에 대한 혜택이 사용되기에 충분한 과세소득이 발생할 가능성이 더이상 높지 않다면 이연법인세자산을 인식하지 않고 있습니다. 회사는 향후 과세소득의 실현가능성을 합리적으로 확신할 수 없어 차기 이후 각 회계연도에 소멸되는 가산할 일시적차이를 한도로 하여 계산된 차감할 일시적차이 및 이월세액공제를 초과하여 계산되는 이연법인세자산은 인식하지 아니하였습니다.
(6) 보고기간종료일 현재 미사용 결손금의 만료시기는 다음과 같습니다.
| (단위: 천원) | ||||||||
|---|---|---|---|---|---|---|---|---|
| 구분 | 2021년 | 2022년 | 2023년 | 2024년 | 2025년 | 2026년 | 2027년 | 2028년 |
| 금액 | 1,616,827 | 681,544 | 2,733,680 | 2,809,593 | 1,767,337 | 987,247 | 2,501,928 | 4,186,711 |
26. 판매비와 관리비
당기 및 전기의 판매비와 관리비 세부 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 직원급여 | 803,359 | 719,620 |
| 상여금 | 4,900 | 8,680 |
| 퇴직급여 | 67,537 | (95,647) |
| 복리후생비 | 75,487 | 66,753 |
| 여비교통비 | 425,094 | 351,875 |
| 접대비 | 12,690 | 9,098 |
| 통신비 | 3,623 | 3,428 |
| 수도광열비 | 424 | 509 |
| 세금과공과금 | 15,930 | 17,446 |
| 감가상각비 | 14,298 | 20,500 |
| 지급임차료 | 112,853 | 104,414 |
| 수선비 | - | 485 |
| 보험료 | 6,706 | 8,063 |
| 차량유지비 | 17,299 | 10,275 |
| 경상연구개발비 | 1,204,012 | 640,631 |
| 운반비 | 12,870 | 18,867 |
| 교육훈련비 | 2,980 | 2,300 |
| 도서인쇄비 | 6,747 | 2,160 |
| 사무용품비 | 11,956 | 10,448 |
| 소모품비 | 5,178 | 3,613 |
| 지급수수료 | 632,816 | 794,053 |
| 광고선전비 | 98,688 | 145,040 |
| 대손상각비 | 63,188 | 9,074 |
| 건물관리비 | 48,231 | 47,448 |
| 무형고정자산상각 | 217,561 | 185,596 |
| 합계 | 3,864,427 | 3,084,729 |
27. 기타수익 및 기타비용
(1) 당기 및 전기의 기타수익 세부 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 외환차익 | 48,936 | 21,527 |
| 외화환산이익 | 274 | - |
| 유형자산처분이익 | - | 5,995 |
| 잡이익 | 78,192 | 37,459 |
| 합계 | 127,402 | 64,981 |
(2) 당기 및 전기의 기타비용 세부 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 외환차손 | 12,902 | 86,166 |
| 외화환산손실 | 4,842 | 82,678 |
| 기부금 | 9,738 | 13,313 |
| 무형자산손상차손 | - | 714,024 |
| 재고자산평가손실 | 58,938 | 21,807 |
| 잡손실 | 6,839 | 3,744 |
| 합계 | 93,259 | 921,732 |
28. 금융수익 및 금융비용
(1) 당기 및 전기의 금융수익 세부 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 이자수익 | 42,432 | 9,949 |
| 당기손익인식금융자산평가이익 | - | 3,734 |
| 장기금융자산평가이익 | 11,852 | - |
| 합계 | 54,284 | 13,683 |
(2) 당기 및 전기의 금융비용 세부 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 이자비용 | 733,694 | 623,620 |
29. 비용의 성격별 분류
당기 및 전기 중 발생한 비용의 성격별 분류는 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 재고자산의 변동 | (191,563) | (680,919) |
| 재고자산 매입액 등 | 744,387 | 1,275,598 |
| 종업원급여 | 2,248,947 | 1,856,031 |
| 복리후생비 | 226,336 | 216,783 |
| 감가상각비 | 968,491 | 833,719 |
| 운반비 | 13,673 | 19,448 |
| 임차료 | 155,237 | 144,177 |
| 지급수수료 | 1,130,714 | 1,254,690 |
| 광고선전비 | 98,688 | 145,040 |
| 경상연구개발비 | 1,428,016 | 868,277 |
| 무형자산상각비 | 627,495 | 595,530 |
| 기타 | 1,159,818 | 902,942 |
| 합계(주1) | 8,610,239 | 7,431,316 |
| (주1) | 포괄손익계산서상의 매출원가 및 판매비와관리비의 합계액입니다. |
30. 주당손실
(1) 당기 및 전기의 기본주당손실의 산정 내역은 다음과 같습니다.
| (단위: 원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 당기순손실 | 4,146,155,504 | 2,567,612,203 |
| 가중평균유통보통주식수 | 6,230,839주 | 5,551,577주 |
| 기본주당손실 | 665 | 463 |
| (주1) | 회사는 주식선택권 등으로 인한 희석화 효과가 없으므로 희석주당이익을 계산하지 않습니다. |
(2) 가중평균유통보통주식수 산정 내역은 다음과 같습니다.
<당기>
| (단위: 주) | ||||
|---|---|---|---|---|
| 구분 | 일자 | 주식수 | 가중치 | 적수(2) |
| 기초 | 2018-01-01 | 6,010,469 | 365 | 2,193,821,185 |
| 전환권행사 | 2018-05-21 | 357,489 | 225 | 80,435,025 |
| 적용일수(1) | 365 | |||
| 가중평균 유통 보통주식수( = (2) ÷ (1) ) | 6,230,839 | |||
<전기>
| (단위: 주) | ||||
|---|---|---|---|---|
| 구분 | 일자 | 주식수 | 누계 | |
| 가중치 | 적수(2) | |||
| 기초 | 2017-01-01 | 5,433,576 | 365 | 1,983,255,240 |
| 전환권행사 | 2017-04-06 | 26,222 | 270 | 7,079,940 |
| 전환권행사 | 2017-10-23 | 314,669 | 70 | 22,026,830 |
| 전환권행사 | 2017-10-30 | 196,669 | 63 | 12,390,147 |
| 전환권행사 | 2017-11-22 | 39,333 | 40 | 1,573,320 |
| 적용일수(1) | 365 | |||
| 가중평균 유통 보통주식수( = (2) ÷ (1) ) | 5,551,577 | |||
(3) 희석효과가 발생하지 않은 잠재적 보통주
| (단위: 주) | |||||
|---|---|---|---|---|---|
| 구분 | 금액 | 청구기간 | 조건 | 발행될 주식수 | |
| 당기 | 전기 | ||||
| 주식선택권 | 12백만원 | 2011-03-28~2019-03-31 | 주당 1,500원~2,300원 | 5,000 | 10,000 |
| 제3회 전환사채 | 1,000백만원 | 2016-03-02~2020-02-02 | 주당 6,770원 | - | 147,710 |
| 제4회 전환사채 | 1,600백만원 | 2017-03-31~2021-02-28 | 주당 7,627원 | - | 760,456 |
| 제5회 전환사채 | 5,000백만원 | 2018-12-26~2020-11-26 | 주당 9,994원 | 500,300 | - |
31. 주식기준보상
회사는 2010년까지 3회에 걸쳐 임직원 등에게 회사의 주식을 미리 정해진 가격(행사가격)으로 취득할 수 있는 주식선택권을 부여하였으며, 행사 또는 소멸되지 아니한 주식선택권은 아래와 같습니다.
(1) 주식선택권의 내역
| 구분 | 3회차 |
|---|---|
| 부여시점 | 2010-03-30 |
| 가득조건 | 용역제공조건: 3년 |
| 행사가능기간 | 2013-04-01~2019-03-31 |
| 최초 부여 주식수 | 25,000주 |
| 발행할 주식수 | 5,000주 |
| 행사가격 | 2,300원 |
| 부여방법 | 주식교부형 |
(2) 주식선택권 증감내역
| 구분 | 당기 | 전기 |
|---|---|---|
| 기초 잔여주 | 10,000 | 13,500 |
| 행사 및 소멸 | (5,000) | (3,500) |
| 기말 잔여주 | 5,000 | 10,000 |
(3) 주식선택권(자본조정)의 변동
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 기초 | 11,955 | 17,317 |
| 기중 행사 및 소멸분 | (6,990) | (5,362) |
| 기말 | 4,965 | 11,955 |
(4) 회사는 부여된 주식선택권에 대해서 공정가액접근법을 적용하여 보상비용을 산정하였으며, 보상원가 산정에 사용된 제반 가정은 다음과 같습니다.
| 구분 | 3회 |
|---|---|
| 무위험이자율 | 4.56% |
| 기대행사기간 | 6년 |
| 예상주가변동성 | 0.48 |
| 공정가액 | 993원 |
32. 특수관계자와의 거래
당기 및 전기 중 회사가 주요 경영진에 대하여 지급한 분류별 보상 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 계정과목 | 당기 | 전기 |
| 급여 | 609,563 | 512,063 |
| 퇴직급여 | 214,586 | (62,403) |
| 합계 | 824,149 | 449,660 |
상기 이외에 회사의 대표이사는 중속기업은행 등과 체결한 약정과 관련하여 지급보증을제공하고 있습니다(주석 24 참조).
33. 현금흐름표
(1) 당기와 전기 중의 영업활동 현금흐름은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 가. 당기순손실 | (4,146,156) | (2,567,612) |
| 나. 조정 | 2,823,456 | 3,100,789 |
| 퇴직급여 | 322,840 | 185,139 |
| 대손상각비 | 63,188 | 9,074 |
| 감가상각비 | 968,491 | 833,719 |
| 무형자산상각비 | 627,495 | 595,530 |
| 재고자산평가손실 | 58,938 | 21,807 |
| 이자비용 | 733,694 | 623,620 |
| 외화환산손실 | 4,841 | 82,678 |
| 무형자산손상차손 | - | 714,024 |
| 경상연구개발비 | - | 82,692 |
| 이자수익 | (42,432) | (9,949) |
| 외화환산이익 | (274) | - |
| 유형자산처분이익 | - | (5,995) |
| 당기손익인식금융자산평가이익 | - | (3,734) |
| 장기금융자산평가이익 | (11,852) | - |
| 법인세비용 | 98,527 | (27,816) |
| 다. 영업활동으로인한자산부채의변동 | (286,401) | 165,603 |
| 매출채권의 감소(증가) | (58,189) | 115,010 |
| 기타유동자산의 감소(증가) | (90,698) | 276,020 |
| 재고자산의 증가 | (191,563) | (702,726) |
| 매입채무의 감소 | (13,343) | (30,419) |
| 기타채무의 증가 | 239,927 | 304,761 |
| 기타유동부채의 감소 | (13,054) | (904,775) |
| 기타비유동부채의 증가 | - | 1,124,500 |
| 확정급여채무의 감소 | (151,309) | (16,768) |
| 사외적립자산의 증가 | (8,172) | - |
| 영업으로부터 창출된 현금흐름 | (1,609,101) | 698,780 |
(2) 당기와 전기 중 현금의 유입과 유출이 없는 중요한 거래 내역은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기 | 전기 |
| 장기차입금의 유동성대체 | 738,750 | 658,440 |
| 전환사채의 유동성대체 | 4,495,438 | 1,489,845 |
| 전환사채의 행사 | 2,562,416 | 4,863,234 |
| 건설중인자산에서 유형자산으로 대체 | 28,770 | 2,589,630 |
34. 위험관리
회사는 시장위험(환위험, 이자율위험), 신용위험 및 유동성위험과 같은 다양한 금융 위험에 노출되어 있으며, 이러한 위험의 영향을 최소화시키고자 합니다. 회사는 리스크의 유형과 그 측정 방법 등에 대하여 리스크 유형별로 관리원칙 및 관리방법을 규정하고, 지속적으로 정책의 준수와 위험노출 정도를 검토하고 있습니다.
(1) 자본위험 관리
회사의 자본관리는 계속기업으로서의 존속능력을 유지하는 한편, 자본비용을 최소화하여 주주이익을 극대화하며 적정한 자본구조를 유지하는 것을 그 목표로 하고 있습니다. 회사의 자본관리 목적은 계속기업으로서 주주 및 이해당사자들에게 이익을 지속적으로 제공할 수 있는 능력을 보호하고 자본비용을 절감하기 위해 최적 자본구조를 유지하는 것입니다.
보고기간종료일 현재 회사의 부채비율은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 구분 | 당기말 | 전기말 |
| 부채 (A) | 11,741,622 | 13,388,514 |
| 자본 (B) | 10,575,969 | 12,361,859 |
| 부채비율 (A/B) | 111.02% | 108.31% |
(2) 시장위험
1) 외화위험관리
회사는 외화로 표시된 거래를 수행하고 있으므로 환율변동으로 인한 위험에 노출되어 있습니다. 회사는 투기적 외환거래를 금지하고 있으며, 경영진은 내부적으로 원화환율변동에 대한 환위험을 수시로 측정하고 관리하고 있습니다.
보고기간종료일 현재 회사의 화폐성 외화자산과 외화부채의 주요 내역은 다음과 같습니다.
| (단위: USD,EUR,천원) | ||||||
|---|---|---|---|---|---|---|
| 구분 | 계정과목 | 통화 | 당기말 | 전기말 | ||
| 외화 | 원화환산액 | 외화 | 원화환산액 | |||
| 외화자산 |
현금 및 현금성자산 |
USD | 4,259.89 | 4,763 | 157,820.57 | 169,089 |
| EUR | 63.89 | 82 | 571.74 | 731 | ||
| 매출채권 | USD | 830,109.34 | 928,145 | 914,257.00 | 979,535 | |
| 합 계 | USD | 834,369.23 | 932,908 | 1,072,077.57 | 1,148,624 | |
| EUR | 63.89 | 82 | 571.74 | 731 | ||
당기말 현재 다른 모든 변수가 일정하고 미달러화에 대한 원화의 환율 10% 변동시 환율변동이 법인세차감전순이익에 미치는 영향은 다음과 같습니다.
| (단위: 천원) | ||
|---|---|---|
| 통화 | 10% 상승시 | 10% 하락시 |
| USD | 93,291 | (93,291) |
| EUR | 8 | (8) |
2) 이자율위험관리
이자율위험은 시장금리변동으로 인한 재무상태표항목의 가치변동(공정가치)위험과 투자 및 재무활동으로부터 발생하는 이자수익/비용의 현금흐름이 변동될 위험으로 정의할 수 있습니다. 이러한 회사의 이자율변동위험은 주로 변동금리부차입금에서 비롯되며, 회사의 이자율위험 관리의 목표는 이자율 변동으로 인한 불확실성과 금융비용을 최소화하는데 있습니다. 이를 위해 내부 유보자금을 활용한 외부차입의 최소화, 고금리 차입금 감축, 장ㆍ단기 차입구조 개선, 고정 대 변동금리 차입조건의 차입금 적정비율 유지, 정기적인 금리동향 모니터링 실시 및 대응방안 수립 등을 통해 선제적으로 이자율 위험을 관리하고 있습니다.
보고기간종료일 현재 이자율변동위험에 노출된 변동이자부차입금의 내역은 다음과 같습니다.
| (단위:천원) | ||
|---|---|---|
| 구분 | 당기말 | 전기말 |
| 단기차입금 | 870,000 | 920,000 |
| 유동성장기차입금 | 1,605,545 | 1,087,256 |
| 장기차입금 | 851,965 | 897,780 |
| 합계 | 3,327,510 | 2,905,036 |
보고기간종료일 현재 회사가 보유하고 있는 변동이자부차입금의 이자율이 1% 변동할 경우, 이자율변동이 향후 1년간 회사의 현금흐름에 미치는 영향은 다음과 같습니다.
| (단위:천원) | ||
|---|---|---|
| 구분 | 1% 상승시 | 1% 하락시 |
| 이자비용 | (33,275) | 33,275 |
(3) 신용위험관리
신용위험은 계약상대방이 계약상의 의무를 불이행하여 회사에 재무적 손실을 미칠 위험을 의미합니다. 회사는 신용위험을 관리하기 위하여 신용도가 일정 수준 이상인 거래처와 거래하고 있으며, 금융자산의 신용보강을 위한 정책과 절차를 마련하여 운영하고 있습니다. 회사는 신규 거래처와 계약시 거래처의 신용도를 평가하고 이를 근거로 신용거래한도를 결정하고 있습니다. 또한, 회사는 주기적으로 거래처의 신용도를 재평가하여 신용거래한도를 재검토하고 있으며, 회수가 지연되는 금융자산에 대하여는 정기적으로 회수지연 현황 및 회수대책을 보고하고 있으며 지연사유에 따라 적절한 조치를 취하고 있습니다.
신용위험은 금융기관과의 거래에서도 발생할 수 있으며 해당거래는 현금및현금성자산 및 각종 예금 등의 금융상품 거래를 포함합니다. 이러한 위험을 줄이기 위해 회사는 국제 신용등급이 높은 은행들에 대해서만 거래를 하고 있습니다.
회사가 보유한 금융자산 중 매출채권및기타채권의 경우 신용위험에 대한 최대 노출정도는 장부금액과 동일합니다.
(4) 유동성위험관리
유동성위험은 만기도래 시에 금융부채에 관련된 의무를 충족하는데 어려움을 겪게 될 위험입니다. 회사는 정기적인 자금수지계획의 수립을 토대로 영업활동, 투자활동 및 재무활동에서의 자금수지를 미리 예측해 금융부채와 금융자산의 만기구조를 대응시키고 있으며, 이를 통해 필요 유동성 규모를 사전에 확보하고 유지하여 향후에 발생할 수 있는 유동성리스크를 사전에 관리하고 있습니다.
회사는 상기에서 언급한 예측을 통해 여유있는 유동성이 확보될 수 있도록 적절한 만기나 충분한 유동성을 제공해 주는 정기예금, 수시입출금식 예금 등의 금융상품을 통하여 운전자본을 초과하는 자금을 투자하고 있습니다.
보고기간종료일 현재 주요 금융부채의 연도별 상환계획은 다음과 같습니다.
<당기말>
| (단위: 천원) | |||
|---|---|---|---|
| 구분 | 1년 미만 | 1년 이후 | 합계 |
| 매입채무 | 121,746 | - | 121,746 |
| 단기차입금 | 870,000 | - | 870,000 |
| 기타유동금융부채 | 660,480 | - | 660,480 |
| 유동성장기차입금 | 1,605,545 | - | 1,605,545 |
| 유동성전환사채 | 4,495,438 | - | 4,495,438 |
| 장기차입금 | - | 851,965 | 851,965 |
| 기타비유동금융부채 | - | 298,461 | 298,461 |
| 합계 | 7,753,209 | 1,150,426 | 8,903,635 |
<전기말>
| (단위: 천원) | |||
|---|---|---|---|
| 구분 | 1년 미만 | 1년 이후 | 합계 |
| 매입채무 | 135,088 | - | 135,088 |
| 단기차입금 | 920,000 | - | 920,000 |
| 기타금융부채 - 유동 | 1,011,379 | - | 1,011,379 |
| 유동성장기차입금 | 1,087,256 | - | 1,087,256 |
| 유동성전환사채 | 2,474,348 | - | 2,474,348 |
| 장기차입금 | - | 897,780 | 897,780 |
| 전환사채 | - | 4,012,336 | 4,012,336 |
| 기타금융부채 - 비유동 | - | 463,322 | 463,322 |
| 합계 | 5,628,071 | 5,373,438 | 11,001,509 |
35. 보고기간후 사건
회사는 미국내 자회사 설립을 통해 아래와 같은 연구개발업을 진행할 목적으로 신규출자를 계획하고 있습니다. 그 세부내역은 다음과 같습니다.
| 구분 | 내용 |
|---|---|
| 취득목적 | 자회사 설립을 통한 연구개발업 진행 - 파이프라인 전임상, 임상 진행 - 펩타이드 융합 재생 의료기기 FDA 승인 및 이에 대한 대응업무 - 미국 내 제휴회사와의 업무 추진 |
| 출자법인명 | NIBEC Phama. |
| 출자법인 주요사업 | 신약개발업 |
| 출자내역 | 1) 출자예정일: 2019년 3월내 2) 출자금액: USD 300,000 3) 액면가액: 액면가 USD 4) 출자주식수: 300,000주 |
36. 영업손실
회사는 2011년 7월 13일 기술특례 상장 이후 당기말까지 지속적인 영업손실 및 당기순손실을 기록하고 있습니다. 당기 및 과거 4개년 경영성과는 다음과 같습니다.
| (단위: 백만원) | |||||
|---|---|---|---|---|---|
|
구분 |
2014 |
2015 |
2016 |
2017 |
2018 |
|
매출액 |
4,786 |
4,174 |
4,804 |
6,303 |
5,208 |
|
매출총이익 |
916 |
933 |
800 |
1,956 |
462 |
|
영업손실 |
3,025 |
1,584 |
2,500 |
1,129 |
3,402 |
|
법인세차감전순손실 |
2,406 |
2,479 |
3,120 |
2,595 |
4,048 |
|
당기순손실 |
1,835 |
2,426 |
3,027 |
2,568 |
4,146 |
37. 영업의 지역별 특징 및 집중
(1) 지역별 특징
회사는 지역별 영업정보를 검토하고 있습니다. 경영진은 지역적으로 국내와 국외로 구분하여 검토하고 있으며, 그 내역은 다음과 같습니다.
| (단위: 천원) | |||
|---|---|---|---|
| 구분 | 국내 | 해외 | 합계 |
| 제품매출 | 1,122,026 | 4,085,851 | 5,207,877 |
(2) 영업집중
당기 중 전체 매출의 10% 이상을 차지하는 외부고객 3곳에 대한 매출액 합계액은 4,387,311천원(총매출의 84.24%)입니다. 이처럼 회사의 영업은 동 회사들과의 영업관계에 중요하게 의존하고 있으며, 회사의 재무제표는 이러한 영업관계가 당분간 계속될 것이라는 가정하에 작성된 것입니다.
38. 회계정책의 변경
(1) 기준서 제1109호 '금융상품'의 적용
주석 2.2에서 설명한 바와 같이 회사는 2018년 1월 1일을 최초적용일로 하여 기준서제1109호를 적용하였으며, 경과규정에 따라 전기 재무제표는 재작성되지 않았습니다. 기준서 제 1109호의 적용으로 인해 회사의 재무제표에 미치는 영향은 아래와 같습니다.
- 금융상품의 분류
최초적용일인 2018년 1월 1일 현재 기준서 제1109호의 도입으로 인한 금융자산의 재분류 내역은 다음과 같습니다.
| (단위: 천원) | |||||
|---|---|---|---|---|---|
| 구분 |
측정 범주 |
장부금액 |
|||
|
기준서 제1039호 |
기준서 제1109호 |
기준서 제1039호 |
기준서 제1109호 |
차이 |
|
|
유동자산 |
|||||
|
현금 및 현금성자산 |
상각후원가 |
상각후원가 |
5,276,939 |
5,276,939 |
- |
| 당기손익인식금융자산 | 당기손익인식금융자산 |
당기손익-공정가치 |
503,734 | 503,734 | - |
|
매출채권 |
상각후원가 |
상각후원가 |
1,649,949 | 1,649,949 |
- |
|
기타유동금융자산 |
상각후원가 |
상각후원가 |
5,995 | 5,995 |
- |
|
비유동자산 |
|||||
|
장기금융상품 |
상각후원가 |
상각후원가 |
385,618 | 385,618 |
- |
|
기타비유동금융자산 |
상각후원가 |
상각후원가 |
290,965 |
290,965 |
- |
| 유동부채 | |||||
|
매입채무 |
상각후원가 |
상각후원가 |
135,088 | 135,088 |
- |
| 단기차입금 |
상각후원가 |
상각후원가 |
920,000 | 920,000 |
- |
| 기타유동금융부채 |
상각후원가 |
상각후원가 |
1,011,379 | 1,011,379 | - |
| 유동성장기차입금 |
상각후원가 |
상각후원가 |
1,087,256 | 1,087,256 | - |
| 유동성전환사채 | 당기손익인식금융부채 | 당기손익인식금융부채 |
2,474,348 | 2,474,348 |
- |
| 비유동부채 | |||||
| 장기차입금 |
상각후원가 |
상각후원가 |
897,780 | 897,780 |
- |
| 전환사채 | 당기손익인식금융부채 | 당기손익인식금융부채 |
4,012,336 | 4,012,336 |
- |
| 기타비유동금융부채 |
상각후원가 |
상각후원가 |
463,322 | 463,322 | - |
- 금융자산의 손상
회사는 기준서 제1109호의 새로운 기대신용손실 모형 적용대상이 되는 두가지 유형의 금융자산을 보유하고 있습니다.
·재고자산의 매출에 따른 매출채권
·상각후원가로 측정되는 채무상품
회사는 기준서 제1109호의 도입으로 아래와 같은 항목에 대해 손상차손의 인식 관련정책을 변경하였으나 재무제표에 미치는 영향은 없다고 판단하고 있습니다.
① 매출채권
매출채권의 손상 시 간편법을 적용하고 있어 전체 매출채권에 대해 전체 기간 기대신용손실을 사용합니다.
② 채무상품
상각후원가나 기타포괄손익-공정가치로 측정되는 채무상품은 신용위험이 낮은 것으로 판단하여 손실충당금은 12개월 기대신용손실로 인식됩니다.
(2) 기준서 제1115호 '고객과의 계약에서 생기는 수익' 적용
주석 2.2에 기재된 것처럼 회사는 당기부터 기준서 제1115호를 적용하였으며, 경과규정에 따라 비교표시된 전기 재무제표는 재작성되지 않았습니다. 동 기준서의 적용으로 인해 회사의 재무제표에 미치는 영향은 없다고 판단하고 있습니다.
6. 기타 재무에 관한 사항
1) 대손충당금 설정 현황
가. 계정과목별 대손충당금 설정내용
(단위 : 천원)
| 구 분 | 계정과목 | 채권금액 | 대손충당금 | 대손충당금 설정률 |
|---|---|---|---|---|
| 제15기 | 매출채권 | 1,904,573 | 264,470 | 13.89% |
| 제14기 | 매출채권 | 1,851,230 | 201,282 | 10.87% |
| 제13기 | 매출채권 | 2,003,470 | 192,208 | 9.59% |
나. 대손충당금 변동현황 (단위: 천원)
| 구 분 | 제15기 | 제14기 | 제13기 |
|---|---|---|---|
| 1.기초 대손충당금 잔액합계 | 201,282 | 192,208 | 134,504 |
| 2.순대손처리액(①-②±③) | 63,188 | 9,074 | 57,704 |
| ① 대손처리액(상각채권액) | 63,188 | 9,074 | 57,704 |
| ② 상각채권회수액 | - | - | - |
| ③ 기타증감액 | - | - | - |
| 3.대손상각비 계상(환입)액 | - | - | - |
| 4.기말 대손충당금 잔액합계 | 264,470 | 201,282 | 192,208 |
다. 매출채권 관련 대손충당금 설정방침
당사의 대손충당금 설정방법은 개별분석을 통해 산출하고, 개별분석에 해당되지 않는 채권은 과거의 대손경험율에 의한 금액을 대손충당금으로 설정.
라. 보고기간종료일 현재 경과기간별 매출채권 잔액 현황
(단위: 천원)
| 구 분 | 3개월 이하 | 3개월 초과 6개월 이하 |
6개월 초과 | 계 | |
|---|---|---|---|---|---|
| 금액 | 일반 | 1,198,911 | 344,624 | 96,568 | 1,640,103 |
| 특수관계자 | - | - | - | ||
| 계 | 1,198,911 | 344,624 | 96,568 | 1,640,103 | |
| 구성비율(%) | 73.10% | 21.01% | 5.89% | 100.00% | |
2) 재고자산 현황
가. 최근 3사업연도의 재고자산 보유현황
(단위: 천원)
| 계정과목 | 제15기 | 제14기 | 제13기 |
|---|---|---|---|
| 제 품 | 1,412,004 | 1,426,459 | 1,424,960 |
| 원 재 료 | 1,131,366 | 984,287 | 304,867 |
| 합 계 | 2,543,370 | 2,410,746 | 1,729,827 |
| 총자산대비 재고자산구성비율(%) [재고자산합계÷기말자산합계X100] |
11.40% | 9.36% | 7.53% |
| 재고자산회전율(회수) [연매출원가÷{(기초재고+기말재고)÷2}] |
1.92회 | 2.10회 | 2.70회 |
나. 재고자산의 실사내역 등
(1) 재고조사 : 매월말 자체 재고조사가 실시되고 있으며 독립적인 외부감사인의
입회 하에 실시되는 것은 매년 말 재고조사 1회에 한함.
① 재고실사일자 : 2019년 1월 4일
② 재고실사 참여 및 입회자 : 외부감사인, 당사 회계담당 및 재고자산 담당
(2) 조사방법 : 전수조사를 기본으로 실지 재고조사를 실시하고 있으며, 일부 중요성이 높지않고 품목수가 많은 품목에 한해서는 샘플링 조사를 실시합니다.
(3) 장기체화재고 등 현황 : 재고자산의 시가가 취득원가보다 하락한 경우에는 저가법을 사용하여 재무상태표가액으로 하고 있습니다. 한편, 감액된 재고자산의 시가가 장부금액보다 상승한경우에는 최초의 장부금액을 초과하지 않는 범위 내에서 평가손실을 환입하고 있습니다.
당분기말 현재 재고자산에 대한 평가내역은 다음과 같습니다.
(단위: 천원)
| 계정과목 | 보유금액 | 평가손실 | 기말잔액 | 비고 |
|---|---|---|---|---|
| 제 품 | 1,820,192 | 408,188 | 1,412,004 | - |
| 원재료 | 1,200,136 | 68,770 | 1,131,366 | - |
| 합 계 | 3,020,328 | 476,958 | 2,543,370 | - |
3) 공정가치평가 내역
본 사항은 동 공시서류의 "Ⅲ. 재무에 관한 사항-5. 재무제표에 대한 주석-7.금융상품"를 참고하시기 바랍니다.
4) 채무증권 발행실적 등
채무증권 발행실적
| (기준일 : | 2018년 12월 31일 | ) | (단위 : 백만원, %) |
| 발행회사 | 증권종류 | 발행방법 | 발행일자 | 권면 총액 |
이자율 | 평가등급 (평가기관) |
만기일 | 상환 여부 |
주관회사 |
|---|---|---|---|---|---|---|---|---|---|
| 나이벡 | 회사채 | 사모 | 2013.04.12 | 4,000 | 1 | - | 2017.04.12 | 상환완료 | IBK금융그룹 IP Value-up 투자조합 |
| 나이벡 | 회사채 | 사모 | 2015.03.02 | 2,000 | 1 | - | 2020.03.02 | 상환완료 | 현대Agro-Bio 펀드 1호 |
| 나이벡 | 회사채 | 사모 | 2016.03.31 | 6,000 | 0 | - | 2021.03.31 | 상환완료 | 현대Agro-Bio 펀드 1호외 4사 |
| 나이벡 | 회사채 | 사모 | 2017.12.26 | 5,000 | 0 | - | 2020.12.26 | 미상환액 : 50억원 | 한국증권금융외 1사 |
| 합 계 | - | - | - | 17,000 | - | - | - | - | - |
- 보고일 현재 전환권행사(350백만원)로 미상환액은 46.5억원 입니다.
기업어음증권 미상환 잔액
| (기준일 : | 2018년 12월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
1년초과 2년이하 |
2년초과 3년이하 |
3년 초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | |
전자단기사채 미상환 잔액
| (기준일 : | 2018년 12월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 10일 이하 | 10일초과 30일이하 |
30일초과 90일이하 |
90일초과 180일이하 |
180일초과 1년이하 |
합 계 | 발행 한도 | 잔여 한도 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
회사채 미상환 잔액
| (기준일 : | 2018년 12월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | 5,000 | - | - | - | - | 5,000 | |
| 합계 | - | - | 5,000 | - | - | - | - | 5,000 | |
- 보고일 현재 전환권행사(350백만원)로 회사채 미상환액은 46.5억원 입니다.
신종자본증권 미상환 잔액
| (기준일 : | 2008년 12월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 1년 이하 | 1년초과 5년이하 |
5년초과 10년이하 |
10년초과 15년이하 |
15년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | |
조건부자본증권 미상환 잔액
| (기준일 : | 2018년 12월 31일 | ) | (단위 : 백만원) |
| 잔여만기 | 1년 이하 | 1년초과 2년이하 |
2년초과 3년이하 |
3년초과 4년이하 |
4년초과 5년이하 |
5년초과 10년이하 |
10년초과 20년이하 |
20년초과 30년이하 |
30년초과 | 합 계 | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 미상환 잔액 | 공모 | - | - | - | - | - | - | - | - | - | - |
| 사모 | - | - | - | - | - | - | - | - | - | - | |
| 합계 | - | - | - | - | - | - | - | - | - | - | |
Ⅳ. 감사인의 감사의견 등
1. 회계감사인의 명칭 및 감사의견
| 사업연도 | 감사인 | 감사의견 | 감사보고서 특기사항 |
|---|---|---|---|
| 제15기(당기) | 하나회계법인 | 적정 | - |
| 제14기(전기) | 가립회계법인 | 적정 | - |
| 제13기(전전기) | 가립회계법인 | 적정 | - |
2. 감사용역 체결현황
| 사업연도 | 감사인 | 내 용 | 보수 | 총소요시간 |
|---|---|---|---|---|
| 제15기(당기) | 하나회계법인 | 반기검토, 중간감사, 재고실사, 기말감사 | 50,000 | 806 |
| 제14기(전기) | 가립회계법인 | 반기검토, 중간감사, 재고실사, 기말감사 | 48,000 | 749 |
| 제13기(전전기) | 가립회계법인 | 반기검토, 중간감사, 재고실사, 기말감사 | 47,000 | 510 |
3. 회계감사인과의 비감사용역 계약체결 현황
| 사업연도 | 계약체결일 | 용역내용 | 용역수행기간 | 용역보수 | 비고 |
|---|---|---|---|---|---|
| 제15기(당기) | - | - | - | - | - |
| - | - | - | - | - | |
| 제14기(전기) | - | - | - | - | - |
| - | - | - | - | - | |
| 제13기(전전기) | - | - | - | - | - |
| - | - | - | - | - |
Ⅴ. 이사회 등 회사의 기관에 관한 사항
1. 이사회에 관한 사항
가. 이사회 구성 개요
당사는 대표이사 1인을 포함한 4인의 이사로 이사회가 구성되어 있으며, 이 중 1인이 사외이사로 구성되어 있습니다. 이사회는 법령 또는 정관에 정하여진 사항, 주주총회로부터 위임받는 사항, 회사경영의 기본방침 및 업무집행에 관한 중요사항을 의결하고 있으며, 합리적인 의사결정 및 경영의 투명성 확보를 위한 제도적 장치를 확보하고 있습니다.
※ 각 이사의 주요 이력 및 업무분장은 『Ⅷ. 임원 및 직원 등에 관한 사항』"1. 임원 및 직원의 현황" 중 '가. 임원의 현황'을 참고하시기 바랍니다.
나. 이사회의 권한 내용
(1) 이사회의 권한내용
당사의 경영상 의사결정을 위한 이사회는 보고서 제출일 현재 등기이사 4인으로구성되어 있으며, 주요 권한은 다음과 같습니다.
① 주주총회의 소집 및 그 부의 안건의 결정에 관한 사항
② 해산, 영업양도 및 합병 등의 조직의 중요한 변경에 관한 사항
③ 자본금의 변경과 준비금,잉여금,적립금의 자본전입에 관한 사항
④ 임원, 종업원의 보수를 포함한 예산 및 결산에 관한 사항
⑤ 본점의 이전과 사무소, 공장의 설치·이전 및 폐지에 관한 사항
⑥ 중요한 자산의 취득, 처분 및 양도에 관한 사항
⑦ 주식매수선택권의 부여 및 부여취소에 관한 사항
⑧ 대표이사 등의 선임, 해임에 관한 사항
⑨ 명의개서대리인에 관한 사항
⑩ 사채,전환사채,신주인수권부사채 등의 발행 및상환에 관한 사항
⑪ 주식의 발행 및 소각에 관한 사항
(2) 이사회의 운영에 관한 사항
| 【이사회 운영규정의 주요내용】 |
| 제3조【권 한】 ① 이사회는 법령 또는 정관에 정하여진 사항, 주주총회로부터 위임받은 사항, 회사경영의 기본방침 및 업무집행에 관한 중요사항을 의결한다. ② 이사회는 이사의 직무를 감독한다. ③ 이사는 대표이사(사장)으로 하여금 다른 이사 또는 집행간부 직원의 업무에 관하여 이사회에 보고할 것을 요구할 수 있다. ④ 이사는 3개월에 1회 이상 업무의 집행상황을 이사회에 보고하여야 한다. 제4조【구성 및 소집】 ① 이사회의 구성과 소집에 관한 사항은 정관에 명시한 바에 따른다. ② 이사회 의장은 대표이사로 한다. 단, 대표이사 유고시 또는 그 직무의 대행이 필요한 경우 정관의 규정에 의한다. ③ 대표이사는 이사회의 간사로서 1명 또는 그 이상을 선임할 수 있으며, 선임된 간사는 특별한 경우를 제외하고는 이사회에 참석하여야 한다. 제5조【결의 방법】 이사회 결의 방법은 정관에 명시한 바에 따른다. 다만, 이사회 결의에 관하여 특별한 이해관계가 있는 자는 의결권을 행사할 수 없고, 이 경우 당해 이사는 이사회 재적이사의 수에 산입하지 아니한다. 제6조【부의사항】 ① 이사회에서 결의할 사항은 다음 각호와 같다. 1. 영업보고서 승인 2. 주주총회 결의에 관한 다음 각 호의 의안 상정 가. 주주총회의 소집 나. 재무제표의 승인 다. 정관의 변경 라. 자본의 감소 마. 회사의 해산, 합병, 분할합병, 회사의 계속 바. 주식의 소각 사. 회사의 영업 전부 또는 중요한 일부의 양도 및 다른 회사의 영업 전부의 양수 아. 영업 전부의 임대 또는 경영위임, 타인과 영업의 손익 전부를 같이하는 계약, 기타 이에 준할 계약의 체결이나 변경 또는 해약 자. 이사와 감사의 선임 및 해임 차. 주식의 액면미달 발행 카. 이사의 회사에 대한 책임면제 타. 주식배당 결정 파. 이사와 감사의 보수 하. 주식매수선택권의 부여 거. 회사의 최대주주(그의 특수관계인을 포함함) 및 특수관계인과의 거래의 승인 및 주주총회에의 보고 너. 그밖에 주주총회에 부의할 의안 3. 경영에 관한 사항 가. 경영목표의 설정 나. 사업계획, 자금계획 및 예산운용 다. 이사 및 감사의 선임 및 해임안 라. 주식양도의 승인 마. 전사 중장기 사업 전략 및 연구개발 계획 수립/변경 바. 연간 경영계획의 수립/변경 사. 신규 사업 및 신규 투자 계획의 승인 아. 해외 기술협력의 승인 자. 지적재산권의 처분 차. 시설자금을 위한 신규차입 및 회사채 발행의 승인 카. 사내복지기금 조성을 위한 기금의 출연 타. 기타 회사의 중요한 경영정책 결정으로 판단하여 이사회로 상정한 안건 파. 국내 ·외 지점, 출장소, 공장, 사무소 및 현지법인의 설치 이전 및 폐지 하. 중요한 사규, 사칙의 규정 및 개폐 4. 재무에 관한 사항 가. 중요한 재산의 취득, 처분 및 양도 나. 대규모 재산 및 장기차입금의 차입 다. 타법인에 대한 출자 및 출연 라. 결손의 처분 마. 신주의 발행 바. 사채의 모집 사. 전환사채 및 신주인수권부사채의 발행 아. 임의적립금의 사용 자. 준비금의 자본전입 차. 투자 및 중요한 계약의 체결 5. 이사에 관한 사항 가. 이사와 회사간 거래의 승인 나. 타 회사의 임원 겸임 6. 기타 가. 중요한 소송의 제기 나. 주식매수선택권 부여의 취소 다. 당사 업무에 관한 중요사항으로서 각 이사가 이사회결의가 필요하다고 인정하는 사항 라. 기타 법령, 정관 또는 다른 규정에서 정하는 사항, 주주총회에서 위임받은 사항 및 대표이사가 필요하다고 인정하는 사항 ② 이사회는 필요하다고 인정하는 경우 제1항제2호의 사항에 대하여 그 범위를 정하여 대표이사에게 위임할 수 있다. 제7조【보고 사항】 이사회에 보고할 사항은 다음 각호와 같다. ① 이사가 법령 또는 정관에 위반한 행위를 하거나 그 행위를 할 염려가 있다고 감사가 인정한 사항 ② 기타 경영상 중요한 업무집행에 관한 사항 제11조【의사록】 이사회 의사록(별지서식 제1호)의 기록, 보관 등은 정관에 명시한 바에 따른다. 이때 의장은 동 업무의 수행을 동 업무의 수행을 특정 이사 또는 간사에게 명할 수 있다. |
다. 중요 의결사항 등
(1) 이사회의 주요활동내역
| 회차 | 개최일자 | 의 안 내 용 | 가결여부 | 비고 |
|---|---|---|---|---|
| 1 | 2018.02.13 | 2017년 내부회계관리제도 운용실태보고의 건 | 가결 | - |
| 2 | 2018.03.15 | 제14기 재무제표 승인의 건 | 가결 | - |
| 3 | 2018.03.15 | 제14기 정기주주총회 소집에 관한 건 | 가결 | - |
| 4 | 2018.04.09 | 항암의약품시장 진출을 위한 전임상 효력연구 개시의 건 |
가결 | - |
|
5 |
2018.07.30 | 시설대여(리스)계약 체결관련의 건 | 가결 | - |
| 6 | 2018.12.12 | 미국내 자회사 주식취득의 건 | 가결 | - |
(2) 이사회에서의 사외이사의 주요활동내역
| 회차 | 개최일자 | 의 안 내 용 | 가결여부 | 사외이사 참석인원 |
사외이사 김사성 |
|---|---|---|---|---|---|
| 찬반여부 | |||||
| 1 | 2018.02.13 | 2017년 내부회계관리제도 운용실태보고의 건 | 가결 | 1인 (총1인) | 찬성 |
| 2 | 2018.03.15 | 제14기 재무제표 승인의 건 | 가결 | 1인 (총1인) | 찬성 |
| 3 | 2018.03.15 | 제14기 정기주주총회 소집에 관한 건 | 가결 | 1인 (총1인) | 찬성 |
| 4 | 2018.04.09 | 항암의약품시장 진출을 위한 전임상 효력연구 개시의 건 |
가결 | 1인 (총1인) | 찬성 |
|
5 |
2018.07.30 | 시설대여(리스)계약 체결관련의 건 | 가결 | 1인 (총1인) | 찬성 |
| 6 | 2018.12.12 | 미국내 자회사 주식취득의 건 | 가결 | 1인 (총1인) | 찬성 |
라. 사외이사 교육 미실시 내역
| 사외이사 교육 실시여부 | 사외이사 교육 미실시 사유 |
|---|---|
| 미실시 | 외부감사법 개정 이전 교육 미실시 |
2. 감사제도에 관한 사항
가. 감사위원회(감사) 설치여부, 구성방법 등
당사는 1인의 비상근감사로 구성되어 있으며 감사의 권한 및 책임은 아래와 같습니다.
① 감사는 회사의 회계와 업무를 감사한다. 감사는 이사회에 출석하여 의견을 진술할 수 있다.
② 감사는 회의의 목적사항과 소집의 이유를 기재한 서면을 이사회에 제출하여 임시주주총회의 소집을 청구할 수 있다.
③ 감사는 그 직무를 수행하기 위하여 필요한 때에는 자회사에 대하여 영업의 보고를 요구할 수 있다. 이 경우 자회사가 지체없이 보고를 하지 아니할 때 또는 그 보고의 내용을 확인할 필요가 있는 때에는 자회사의 업무와 재산상태를 조사할 수 있다.
④ 감사에 대해서는 정관 제39조 제3항의 규정을 준용한다.
나. 감사위원회(감사)의 인적사항
| 성명 (생년월일) |
주요 경력 | 결격요건 여부 |
비고 |
|---|---|---|---|
| 설양조 (68.05.03) |
- 서울대학교 치과대학 졸업 - 서울대학교대학원(치의학과) 박사 - 서울대학교 치의학대학원 교수(현) - (주)나이벡 감사(현) |
해당사항 없음 |
- |
다. 감사의 독립성
당사의 설양조 감사는 2017년 3월 정기주주총회를 통해 선임하였으며, 보고서 제출일 현재 서울대학교 치의학대학원 교수를 겸직하고 있습니다. 설양조 감사는 이해관계가 전혀 없으며, 업무관련 전문적 지식수준 또한 높은 것으로 판단되어 당사의 경영활동에 대한 독립적인 감시 역할을 수행하는데 문제가 없을 것으로 보입니다.
라. 감사의 주요활동내역
| 회차 | 개최일자 | 의 안 내 용 | 가결여부 | 비고 |
|---|---|---|---|---|
| 1 | 2018.02.13 | 2017년 내부회계관리제도 운용실태보고의 건 | 가결 | - |
| 2 | 2018.03.15 | 제14기 재무제표 승인의 건 | 가결 | - |
| 3 | 2018.03.15 | 제14기 정기주주총회 소집에 관한 건 | 가결 | - |
| 4 | 2018.04.09 | 항암의약품시장 진출을 위한 전임상 효력연구 개시의 건 |
가결 | - |
|
5 |
2018.07.30 | 시설대여(리스)계약 체결관련의 건 | 가결 | - |
| 6 | 2018.12.12 | 미국내 자회사 주식취득의 건 | 가결 | - |
마. 감사 교육 미실시 내역
| 감사 교육 실시여부 | 감사 교육 미실시 사유 |
|---|---|
| 미실시 | 외부감사법 개정 이전 교육 미실시 |
바. 감사 지원조직 현황
| 부서(팀)명 | 직원수(명) | 직위(근속연수) | 주요 활동내역 |
|---|---|---|---|
| 경영지원실 | 4 | 이사 1명, 팀장 3명 (평균 10년) |
- 감사업무지원 - 요청자료 응대 |
사. 준법지원인 지원조직 현황
| 부서(팀)명 | 직원수(명) | 직위(근속연수) | 주요 활동내역 |
|---|---|---|---|
| - | - | - | - |
- 당사는 자산총액 5천억원 미만 상장법인으로 준법지원인을 선임하지 않았습니다.
3. 주주의 의결권 행사에 관한 사항
가. 투표제도
당사는 주주의 의결권 행사와 관련하여 현재 정관상 집중투표제, 서면투표제, 전자투표제를 채택하고 있지 않습니다.
나. 소수주주권의 행사 여부
당사는 보고서 제출일 현재 소수주주권의 행사 사실이 없습니다.
다. 경영권 경쟁 여부
당사는 보고서 제출일 현재 공시대상기간중 경영권과 관련하여 경쟁이 발생한 사실이 없으므로 해당사항이 없습니다.
Ⅵ. 주주에 관한 사항
1. 최대주주 및 특수관계인의 주식소유 현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 주, %) |
| 성 명 | 관 계 | 주식의 종류 |
소유주식수 및 지분율 | 비고 | |||
|---|---|---|---|---|---|---|---|
| 기 초 | 기 말 | ||||||
| 주식수 | 지분율 | 주식수 | 지분율 | ||||
| 정종평 | 본인 | 보통주 | 1,133,690 | 18.86 | 1,133,690 | 17.71 | - |
| 박윤정 | 임원 | 보통주 | 228,000 | 3.79 | 228,000 | 3.56 | - |
| 이주연 | 임원 | 보통주 | 18,956 | 0.32 | 18,956 | 0.30 | - |
| 김사성 | 사외이사 | 보통주 | 11,048 | 0.18 | 11,048 | 0.17 | - |
| 설양조 | 감사 | 보통주 | 5,705 | 0.09 | 2,000 | 0.03 | - |
| 장계순 | 처 | 보통주 | 1,000 | 0.02 | 1,000 | 0.02 | - |
| 김정빈 | 조카 | 보통주 | 12,000 | 0.20 | 12,000 | 0.19 | - |
| 계 | 보통주 | 1,410,399 | 23.46 | 1,406,694 | 21.97 | - | |
| 우선주 | - | - | - | - | - | ||
- 상기 최대주주 및 특수관계인의 지분에 대한 담보제공 사항은 없습니다.
2. 최대주주의 주요경력 및 개요
(1) 최대주주의 주요경력
당사 최대주주의 최근 5년간의 주요직무와 겸직 또는 겸임현황 등을 포함한 경력은 아래와 같으며, 최근 5사업연도 이내에 다른 회사의 최대주주였던 사실이 없습니다.
| 성 명 | 직 위 | 주요경력(최근 5년간) | ||
|---|---|---|---|---|
| 기 간 | 경력사항 | 겸임현황 | ||
| 정종평 | 대표이사 | 2004.03 ~ 현재 | (주)나이벡 대표이사 | - |
(2) 최대주주의 변동을 초래할 수 있는 특정거래
당사의 최대주주는 주식매매의 예약, 주식의 담보제공 등 증권신고서 제출일 현재 최대주주의 변동을 초래하지 않았으며, 기한의 도래 또는 일정조건의 성취 등으로 최대주주의 변동을 초래할 수 있는 거래를 진행하지 않았습니다.
3. 최대주주의 최대주주(법인 또는 단체)의 개요
"해당사항이 없습니다."
4. 최대주주 변동내역
최대주주 변동내역
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 주, %) |
| 변동일 | 최대주주명 | 소유주식수 | 지분율 | 변동원인 | 비 고 |
|---|---|---|---|---|---|
| 2004.01.27 | 정종평 | 1,133,690 | 17.71 | - | - |
5. 주식 소유현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 주) |
| 구분 | 주주명 | 소유주식수 | 지분율 | 비고 |
|---|---|---|---|---|
| 5% 이상 주주 | 정종평 | 1,133,690 | 17.71 | - |
| - | - | - | - | |
| 우리사주조합 | 32,620 | 0.51 | - | |
6. 소액주주현황
소액주주현황
| (기준일 : | 2018년 12월 31일 | ) | (단위 : 주) |
| 구 분 | 주주 | 보유주식 | 비 고 | ||
|---|---|---|---|---|---|
| 주주수 | 비율 | 주식수 | 비율 | ||
| 소액주주 | 6,074 | 99.85 | 4,864,296 | 76.39 | - |
7. 주식의 사무
당사 정관상의 신주인수권 내용, 주식 사무에 관련된 주요사항은 다음과 같습니다.
| 정관상 신주인수권의 내용 |
제12조 (신주인수권) ① 주주는 신주발행에 있어서 그가 소유한 주식 수에 비례하여 신주의 배정을 받을 권리를 갖는다. ② 회사는 제1항의 규정에도 불구하고 다음 각 호의 어느 하나에 해당하는 경우는이사회의 결의로 주주 외의 자에게 신주를 배정할 수 있다. 1. 주주우선공모의 방식으로 신주를 발행하는 경우 2. 발행주식의 총수의 100분의 30을 초과하지 않는 범위 내에서 자본시장과 금융투자업에 관한 법률 제165조의6에 따라 일반공모증자 방식으로 신주를 발행하는경우 3.「상법」 제542조의3에 따른 주식매수선택권의 행사로 인하여 신주를 발행하는 경우 4.「자본시장과 금융투자업에 관한 법률」 제165조의7에 따라 발행하는 주식 총수의 100분의 20 범위 내에서 우리사주조합원에게 주식을 우선배정하는 경우 5.「중소기업창업지원법」에 의한 중소기업 창업투자회사 및 중소기업창업투자조합에게 발행주식 총수의 100분의 30까지 배정하는 경우 6. 발행주식의 총수의 100분의 30을 초과하지 않는 범위 내에서 경영상 필요로 외국인투자촉진법에 의한 외국인투자를 위하여 신주를 발행하는 경우 7. 외국 및 국내법인, 국내외 금융 기관 등에 발행주식 총수의 100분의 30 범위 내에서 자본참여를 위한 신주를 발행하는 경우 8.「상법」 제418조 제2항의 규정에 따라 국내외 금융기관 또는 기관투자자 등에게 긴급한 자금의 조달, 신기술도입, 신규사업 진출 및 재무구조 개선 등 회사의 경영상 목적을 달성하기 위하여 신주를 발행하는 경우 9. 발행주식 총수의 100분의 30을 초과하지 않는 범위 내에서 사업상 중요한 기술도입, 연구개발, 생산·판매·자본제휴 등을 위하여 그 상대방에게 신주를 발행하는 경우 10. 주권을 코스닥시장 등 공개시장에 상장하기 위하여 신주를 모집하거나 인수인에게 인수하는 경우 |
|||
| 결산일 | 12월 31일 | 정기주주총회 | 사업연도 종료 후 3개월 이내 | |
| 주주명부 폐쇠시기 |
매년 1월 1일부터 1월 15일까지 | |||
| 주권의 종류 | 1주권,5주권,10주권,50주권,100주권,500주권,1000주권,10000주권(8종) | |||
| 명의개서대리인 | 국민은행 | |||
| 주주의 특전 | 해당사항 없음 | 공고게재 | 인터넷 홈페이지(www.nibec.co.kr) / 매일경제신문 |
|
8. 최근 6개월간의 주가 및 주식 거래실적
(단위 : 원, 주)
| 종 류 | 18년 7월 | 18년 8월 | 18년 9월 | 18년 10월 | 18년 11월 | 18년 12월 | |
|---|---|---|---|---|---|---|---|
| 보통주 | 최고가(종가) | 15,100 | 13,400 | 14,250 | 13,200 | 9,320 | 11,150 |
| 최저가(종가) | 12,350 | 11,550 | 12,650 | 8,130 | 8,340 | 7,690 | |
| 월간거래량 | 4,689,574 | 1,602,760 | 1,873,251 | 1,626,203 | 662,597 | 1,927,132 | |
Ⅶ. 임원 및 직원 등에 관한 사항
1. 임원 및 직원의 현황
1. 임원 현황
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 주) |
| 성명 | 성별 | 출생년월 | 직위 | 등기임원 여부 |
상근 여부 |
담당 업무 |
주요경력 | 소유주식수 | 최대주주와의 관계 |
재직기간 | 임기 만료일 |
|
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 의결권 있는 주식 |
의결권 없는 주식 |
|||||||||||
| 정종평 | 남 | 1946.01 | 대표이사 | 등기임원 | 상근 | 경영총괄 |
서울대학교 치과대학 치의학과 박사 졸업 |
1,133,690 | - | 본인 | 13년 6개월 | 2019.03.30 |
| 박윤정 | 여 | 1971.02 | 전무이사 | 등기임원 | 상근 | 경영개발 기획총괄 |
이화여대 약학대학 대학원 박사 졸업 현) 서울대학교 치의학대학원 교수 |
228,000 | - | - | 13년 6개월 | 2020.03.31 |
| 이주연 | 여 | 1975.04 | 이사 | 등기임원 | 상근 | 연구개발 |
이화여대 약학대학 대학원 박사 졸업 |
18,956 | - | - | 12년 | 2019.03.30 |
| 김사성 | 남 | 1966.04 | 사외이사 | 등기임원 | 비상근 | 경영지원 |
연세대학교 상경대학 경영학과 학사 졸업 현) 서린회계법인 대표 |
11,048 | - | - | - | 2021.03.29 |
| 설양조 | 남 | 1968.05 | 감사 | 등기임원 | 비상근 | 경영지원 |
서울대학교 대학원 치의학 박사 전) 삼성서울병원 치주과학 교수 현) 서울대학교 치의학대학원 교수 |
2,000 | - | - | - | 2020.03.31 |
2. 직원 현황
| (기준일 : | 2018년 12월 31일 | ) | (단위 : 천원) |
| 사업부문 | 성별 | 직 원 수 | 평 균 근속연수 |
연간급여 총 액 |
1인평균 급여액 |
비고 | ||||
|---|---|---|---|---|---|---|---|---|---|---|
| 기간의 정함이 없는 근로자 |
기간제 근로자 |
합 계 | ||||||||
| 전체 | (단시간 근로자) |
전체 | (단시간 근로자) |
|||||||
| - | 남 | 32 | - | - | - | 32 | 4.03 | 1,184,098 | 37,003 | - |
| - | 여 | 26 | - | - | - | 26 | 3.67 | 943,905 | 36,304 | - |
| 합 계 | 58 | - | - | - | 58 | 3.87 | 2,128,003 | 36,690 | - | |
3. 미등기임원 보수 현황
| (기준일 : | 2018년 12월 31일 | ) | (단위 : 천원) |
| 구 분 | 인원수 | 연간급여 총액 | 1인평균 급여액 | 비고 |
|---|---|---|---|---|
| 미등기임원 | - | - | - | - |
2. 임원의 보수 등
<이사ㆍ감사 전체의 보수현황>
1. 주주총회 승인금액
| (단위 : 천원) |
| 구 분 | 인원수 | 주주총회 승인금액 | 비고 |
|---|---|---|---|
| 이사 | 4 | 900,000 | - |
| 감사 | 1 | 50,000 | - |
2. 보수지급금액
2-1. 이사ㆍ감사 전체
| (단위 : ) |
| 인원수 | 보수총액 | 1인당 평균보수액 | 비고 |
|---|---|---|---|
| 5 | 609,563 | 121,913 | - |
2-2. 유형별
| (단위 : ) |
| 구 분 | 인원수 | 보수총액 | 1인당 평균보수액 |
비고 |
|---|---|---|---|---|
| 등기이사 (사외이사, 감사위원회 위원 제외) |
3 | 574,563 | 191,521 | - |
| 사외이사 (감사위원회 위원 제외) |
1 | 35,000 | 35,000 | - |
| 감사위원회 위원 | - | - | - | - |
| 감사 | 1 | - | - | - |
<이사ㆍ감사의 개인별 보수현황>
1. 개인별 보수지급금액
| (단위 : ) |
| 이름 | 직위 | 보수총액 | 보수총액에 포함되지 않는 보수 |
|---|---|---|---|
| - | - | - | - |
| - | - | - | - |
2. 산정기준 및 방법
이사 및 감사의 개인별 보수 지급액이 5억원 이상에 해당하는 자가 없습니다.
3. 주식매수선택권의 부여 및 행사현황
<표1>
| (단위 : ) |
| 구 분 | 인원수 | 주식매수선택권의 공정가치 총액 | 비고 |
|---|---|---|---|
| 등기이사 | 3 | - | - |
| 사외이사 | 1 | - | - |
| 감사위원회 위원 또는 감사 | 1 | - | - |
| 계 | 5 | - | - |
<표2>
| (기준일 : | 2018년 12월 31일 | ) | (단위 : 원, 주) |
| 부여 받은자 |
관 계 | 부여일 | 부여방법 | 주식의 종류 |
변동수량 | 미행사 수량 |
행사기간 | 행사 가격 |
||
|---|---|---|---|---|---|---|---|---|---|---|
| 부여 | 행사 | 취소 | ||||||||
| 이상철외12명 | 직원 | 2008.03.27 | 신주발행/자기주식 | 보통주 | 24,500 | 15,000 | 9,500 | - | 2011.03.27~2017.03.26 | 1,500 |
| 이상철외23명 | 직원 | 2009.03.27 | 신주발행/자기주식 | 보통주 | 25,000 | 13,000 | 12,000 | - | 2012.03.28~2018.03.27 | 2,000 |
| 이상철외23명 | 직원 | 2010.03.30 | 신주발행/자기주식 | 보통주 | 25,000 | 18,000 | 2,000 | 5,000 | 2013.04.01~2019.03.31 | 2,300 |
| 합 계 | - | - | - | 보통주 | 74,500 | 46,000 | 18,500 | 5,000 | - | - |
Ⅷ. 계열회사 등에 관한 사항
"해당사항 없습니다"
Ⅸ. 이해관계자와의 거래내용
1. 대주주등에 대한 신용공여등
"해당사항 없습니다"
2. 대주주와의 자산양수도등
"해당사항 없습니다"
3. 대주주와의 영업거래
"해당사항 없습니다"
4. 대주주 이외의 이해관계자와의 거래
"해당사항 없습니다"
Ⅹ. 그 밖에 투자자 보호를 위하여 필요한 사항
1. 공시사항의 진행ㆍ변경상황 및 주주총회 현황
가. 주주총회 의사록 요약
| 주총일자 | 안 건 | 결의내용 | 비 고 |
|---|---|---|---|
| 제15기 정기주주총회 (2019.03.28) |
1. 2018 회계연도 재무제표 승인의 건 2. 정관 일부 변경의 건 3. 사내이사 선임의 건 4. 이사 보수한도 승인의 건 5. 감사 보수한도 승인의 건 |
원안대로 승인 | - |
| 제14기 정기주주총회 (2018.03.30) |
1. 2017 회계연도 재무제표 승인의 건 2. 사외이사 선임의 건 3. 이사 보수한도 승인의 건 4. 감사 보수한도 승인의 건 |
원안대로 승인 | - |
| 제13기 정기주주총회 (2017.03.31) |
1. 2016 회계연도 재무제표 승인의 건 2. 사내이사 선임의 건 3. 감사 선임의 건 4. 이사 보수한도 승인의 건 5. 감사 보수한도 승인의 건 |
원안대로 승인 | - |
| 제12기 정기주주총회 (2016.03.30) |
1. 2015 회계연도 재무제표 승인의 건 2. 사내이사 선임의 건 3. 이사 보수한도 승인의 건 4. 감사 보수한도 승인의 건 |
원안대로 승인 | - |
| 제11기 정기주주총회 (2015.03.27) |
1. 2014 회계연도 재무제표 승인의 건 2. 정관 일부 변경의 건 3. 사외이사 선임의 건 4. 이사 보수한도 승인의 건 5. 감사 보수한도 승인의 건 |
원안대로 승인 | - |
2. 우발채무 등
가. 중요한 소송사건 등
"해당사항 없습니다"
나. 견질 또는 담보용 어음·수표 현황
"해당사항 없습니다"
다. 채무보증 현황
"해당사항 없습니다"
라. 채무인수약정 현황
"해당사항 없습니다"
마. 기타의 우발부채
"해당사항 없습니다"
3. 중소기업 검토표
 |
|
중소기업기준검토표_0001 |
 |
|
중소기업기준검토표_0002 |
4. 공모자금의 사용내역
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 백만원) |
| 구 분 | 납입일 | 증권신고서 등의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | |||
| 기업공개(코스닥시장) | 2011.07.07 | 발행제비용 | 380 | 발행제비용 | 360 | - |
| - | - | 시설자금 | 1,196 | 시설자금 | 958 | 시설자금중 일부를 운영 자금으로 집행함.주1) |
| - | - | 운영자금 | 5,764 | 운영자금 | 6,022 | - |
| 소 계 | - | - | 7,340 | - | 7,340 | - |
| 유상증자(제3자배정) | 2015.04.13 | 운영자금 | 999 | 운영자금 | 999 | - |
| 유상증자(주주배정) | 2015.09.10 | 시설자금 | 1,500 | 시설자금 | 1,776 | - |
| - | - | 운영자금 | 4,564 | 운영자금 | 4,288 | 운영자금중 일부를 시설자금으로 집행함.주2) |
| 소 계 | - | - | 6,064 | - | 6,064 | - |
주1) 증권신고서상 발행제비용(2천만원) 및 시설자금 사용용도 238백만원을 운영자금(제품개발비용)으로 사용하여 차이가 발생하였습니다.
주2) 증권신고서상 운영자금 사용용도 276백만원을 시설자금(제조구역 증설)으로 사용하여 차이가 발생하였습니다.
5. 사모자금의 사용내역
| (기준일 : | 증권신고서 제출일 | ) | (단위 : 백만원) |
| 구 분 | 납입일 | 주요사항보고서의 자금사용 계획 |
실제 자금사용 내역 |
차이발생 사유 등 | ||
|---|---|---|---|---|---|---|
| 사용용도 | 조달금액 | 내용 | 금액 | |||
| 제2회 사모 분리형신주인수권부사채 | 2013.04.12 | 운영자금 | 4,000 | 운영자금 | 4,000 | - |
| 제3회 무보증 국내사모 전환사채 | 2015.03.02 | 시설자금 | 2,000 | 차환자금 | 1,000 | 채권자와 협의하여 제2회 신주인수권부사채 상환. 주1) |
| - | - | - | - | 운영자금 | 1,000 | - |
| 소 계 | - | - | 2,000 | - | 2,000 | - |
| 제4회 무보증 국내사모 전환사채 | 2016.03.31 | 시설자금 | 1,000 | 시설자금 | 1,347 | - |
| - | - | 운영자금 | 5,000 | - | 4,653 | 운영자금중 일부를 시설자금으로 집행함. 주2) |
| 소 계 | - | - | 6,000 | - | 6,000 | - |
| 제5회 무보증 국내사모 전환사채 | 2017.12.26 | 운영자금 | 5,000 | 운영자금 | 4,186 | 미집행된 납입금액은 제1금융권에 예치중임. 주3) |
주1) 주요사항보고서상 시설자금 사용용도 20억원을 채권자와의 협의하에 제2회 신주인수권부사채 조기상환 10억원, 운영자금(제품개발비 및 원부자재 구입비) 10억원으로 사용하여 차이가 발생하였습니다.
주2) 주요사항보고서상 운영자금 사용용도 347백만원을 시설자금(치과용 골이식재 GMP구축비)으로 사용하여 차이가 발생하였습니다.
주3) 제5회차 전환사채는 펩타이드기반 전임상비용과 원료생산 및 시험비용등 운영자금으로 4,186백만원 집행하였고 잔여 금액은 제1금융권에 예치중입니다.
【 전문가의 확인 】
1. 전문가의 확인
- 해당사항 없음
2. 전문가와의 이해관계
- 해당사항 없음