 |
|
001.체외진단시장 분류 |
주주총회소집공고
| 2017 년 07월 24일 | ||
| 회 사 명 : | 주식회사 수젠텍 | |
| 대 표 이 사 : | 손미진 | |
| 본 점 소 재 지 : | 대전 유성구 테크노2로 187, 216호 (용산동, 미건테크노월드2차) | |
| (전 화) 042-935-2327 | ||
| (홈페이지)http://www.sugentech.com | ||
| 작 성 책 임 자 : | (직 책) 부사장 | (성 명) 유승범 |
| (전 화) 042-935-2327 | ||
주주총회 소집공고
| (임시) |
주주 여러분의 건승하심과 가정에 만복이 깃드시길 기원합니다.
상법 제365조 및 당사 정관 제22조에 의거 임시주주총회를 다음과 같이 개최하오니 참석하여 주시기 바랍니다.
- 아 래 -
1. 일 시 : 2017년 8월 31일(목) 오후 2시 00분
2. 장 소 : 당사 본점 회의실 (주소 : 대전광역시 유성구 테크노2로 187, 216호 (용산동, 미건테크노월드2차))
3. 회의 목적사항
<부의안건>
가. 제1호 의안 : 정관 개정의 건 (목적 사업 추가)
나. 제2호 의안 : 이사 선임의 건
1-1호 의안 손미진 이사 선임의 건 (재선임)
1-2호 의안 유승범 이사 선임의 건 (재선임)
1-3호 의안 박준우 이사 선임의 건 (신임, 기타비상무이사)
※ 기타 세부내용 : Ⅲ.경영참고사항 2.주주총회 목적사항별 기재사항 참조바랍니다.
4. 주주총회 참석 시 준비물
- 직접행사 : 주총참석장, 신분증
- 간접행사 : 주총참석장, 위임장 (주주와 대리인의 인적사항 기재, 인감날인 및 인감증명서 첨부), 대리인 신분증
2017년 07월 24일
주식회사 수젠텍
대표이사 손미진 (직인생략)
I. 사외이사 등의 활동내역과 보수에 관한 사항
1. 사외이사 등의 활동내역
가. 이사회 출석률 및 이사회 의안에 대한 찬반여부
| 회차 | 개최일자 | 의안내용 | 사외이사 등의 성명 | |||
|---|---|---|---|---|---|---|
| A (출석률: %) |
B (출석률: %) |
C (출석률: %) |
D (출석률: %) |
|||
| 찬 반 여 부 | ||||||
| - | - | - | - | - | - | - |
나. 이사회내 위원회에서의 사외이사 등의 활동내역
| 위원회명 | 구성원 | 활 동 내 역 | ||
|---|---|---|---|---|
| 개최일자 | 의안내용 | 가결여부 | ||
| - | - | - | - | - |
2. 사외이사 등의 보수현황
| (단위 : 원) |
| 구 분 | 인원수 | 주총승인금액 | 지급총액 | 1인당 평균 지급액 |
비 고 |
|---|---|---|---|---|---|
| - | - | - | - | - | - |
II. 최대주주등과의 거래내역에 관한 사항
1. 단일 거래규모가 일정규모이상인 거래
| (단위 : 억원) |
| 거래종류 | 거래상대방 (회사와의 관계) |
거래기간 | 거래금액 | 비율(%) |
|---|---|---|---|---|
| - | - | - | - | - |
2. 해당 사업연도중에 특정인과 해당 거래를 포함한 거래총액이 일정규모이상인 거래
| (단위 : 억원) |
| 거래상대방 (회사와의 관계) |
거래종류 | 거래기간 | 거래금액 | 비율(%) |
|---|---|---|---|---|
| - | - | - | - | - |
III. 경영참고사항
1. 사업의 개요
가. 업계의 현황
(1) 산업의 개요
체외진단(In Vitro Diagnostics) 제품은 생체에서 유래된 혈액, 소변, 타액 등을 이용하여 질병의 진단, 예후, 확진, 모니터링에 사용되는 기기, 시약, 보조기구 등을 통칭합니다. 체외진단 시장은 면역화학 (Immunochemistry), 임상미생물 (Clinical Microbiology), 조직진단(Tissue Diagnostics), 지혈진단(Hemostasis), 혈액진단(Hematology), 분자진단(Molecular Diagnostics), 자가혈당측정(Self-Monitoring Blood Glucose), 현장검사(POCT, Point-of-Care Testing)로 분류할 수 있습니다.
 |
|
001.체외진단시장 분류 |
|
분류 |
설명 |
|
면역화학 |
항원-항체 반응의 원리를 이용한 면역학적 분석 및 효소 반응과 화학적 반응을 이용한 임상화학적 진단 분야 |
|
자가혈당측정 |
개인의 당뇨 관리를 위한 제품 |
|
현장검사 |
현장이나 가정에서 질병에 대한 즉각 대응을 가능하게 하는 목적으로 이용 |
|
분자진단 |
병원체나 세포의 유전정보물질(DNA, RNA)을 분석하는 제품 |
|
혈액진단 |
혈액 내의 적혈구, 백혈구, 혈소판 수, 혈색소 농도를 측정하여 혈액의 변화를 파악하는 방법 |
|
임상미생물 |
미생물 감염을 진단하고, 적절한 항생제 및 투여량을 결정할 수 있는 진단 |
|
조직진단 |
인체의 조직을 떼어내어 질병의 유무 및 상태 등을 판별 |
|
지혈진단 |
혈액응고 진단을 의미하며, 출혈성 질환 및 혈소판 장애, 자가면역 상태를 진단하는데 사용 |
체외진단 산업은 1950년대 말 방사능 동위원소를 표지체(Label)로 이용한 방사면역분석법(Radioimmunoassay)이 개발된 이후 고감도 면역화학진단이 가능해졌으나, 방사능 사용으로 인해 산업적으로 큰 성장을 하지 못하였습니다. 1960년대 들어서 폴리스티렌을 고정체로 이용하는 방법, 효소를 표지체로 이용하는 방법 등이 개발되었고, 1970년대 초에 방사능 동위원소 대신 효소를 표지체로 이용하는 면역화학진단 방법이 개발되면서 체외진단 산업은 급속도로 성장하게 됩니다. 이후 형광, 화학발광 등의 표지체, 자성입자 등이 개발되고, IT 기술의 발달로 인해 자동화가 가능해지면서 1990년대 체외진단 산업은 대용량의 검체를 자동화 시스템으로 처리할 수 있는 기반을 구축하면서 다시 한번 성장하게 됩니다.
1980년대 중반 유전자 증폭할 수 있는 중합효소연쇄반응법(PCR, Polymerase Chain Reaction)이 개발된 이후 2000년대 들어서 체외진단에 본격적으로 도입되었으며, 이러한 분자진단은 현재 가장 빠른 속도로 시장이 성장하고 있습니다. 2000년대 들어서 휴먼 지놈 프로젝트(Human Genome Project)는 인체의 유전자에 대한 정보를 정복하기 위한 디딤돌이 되었으며, 이를 통해 현재까지 질병 관련 유전자 연구가 활발하게 진행되고 있습니다.
1970년대 초반 포도당 산화효소를 이용한 혈당분석기가 개발된 이후 1990년대 들어서 개인이 사용할 수 있는 휴대형 혈당측정기와 바이오센서가 개발되어 자가측정(Self-Testing) 분야가 새롭게 나타나면서 당뇨 환자들은 병원 이외에 가정이나 직장 등 원하는 장소에서 원하는 시간에 혈당을 측정할 수 있게 되었습니다. 또한, 1980년대 말에는 크로마토그래피를 이용한 면역화학 검사 방법의 개발로 임신진단 제품들이 출시되면서 일반 여성들이 가정에서 쉽게 임신 여부를 알 수 있게 되었습니다.
최근까지도 다양한 기술들이 개발되면서 체외진단 제품에 적용되며 산업의 성장을 이끌어가고 있으며, 특히 맞춤형 진단 및 치료를 위한 동반진단(CDx, Companion Diagnostics)과 치료약물모니터링(TDM, Therapeutic Drug Monitoring)과 통신을 이용한 u-헬스 진단이 미래의 체외진단 산업으로 주목 받고 있습니다.
(2) 산업의 특성
체외진단 제품과 관련된 기술은 생명과학, 화학, 물리학과 같은 이학 계열 기술과 기계공학, 전자공학, 재료공학, 화학공학과 같은 공학 기술로 나눌 수 있으며, 각 요소 기술들을 바탕으로 사업화가 가능합니다. 그렇지만 바이오 기술과 공학 기술의 융합과 같은 융합 기술이 가장 활발하게 적용될 수 있는 산업 분야로 세계적인 체외진단 회사들은 바이오 기반의 시약 및 센서, 나노입자, 전자동화 장비 및 소프트웨어에 다양한 기술을 융합시켜 제품을 개발 및 사업화하고 있습니다.
체외진단은 크게 중앙검사실(Central Lab) 검사와 현장검사(POCT)로 나눌 수 있는데, 이에 따라 기업의 특성이 다르게 구분됩니다. 중앙검사실 제품은 전자동화 장비를 비롯하여 여기에 들어가는 시약류로 구분할 수 있으며, 주로 미국, 유럽, 일본 등의 글로벌 체외진단 회사들의 사업 영역에 해당됩니다.
POCT는 바이오센서 단독 또는 바이오센서와 소형 측정기기로 구성되며 원하는 시간, 원하는 장소에서 간단한 작동 방법을 통해 빠르게 검사할 수 있습니다. 이러한 POCT는 글로벌 체외진단 회사들 이외에 국내외의 중소기업들이 사업화하고 있는 영역이기도 합니다.
POCT 중 혈당측정과 임신테스트는 의료와 관련된 지식이 전혀 없는 일반인들도 사용할 수 있는데, 이러한 검사를 자가검사(Self-Testing)이라고 합니다. 자가검사는 병원에서 수행되는 전문가 검사(Professional Test)와 달리 의료 현장이 가정이나 직장에서 일반인들이 수행할 수 있다는 특징이 있습니다.
체외진단 산업은 다른 의료기기 또는 의약품 산업과 마찬가지로 높은 부가가치를 낼 수 있는 산업으로 사업화를 위해서는 각 인허가 기관으로부터 허가나 인증이 필요합니다. 허가 및 인증은 각 국가별로 제도가 유사한 부분이 많지만, 각 국가별로 독특한 부분이 있기 때문에 주의가 필요합니다. 우리나라의 경우 불과 몇 년 전만 하더라도 체외진단 제품은 의약품과 의료기기에 분류되어 있었지만, 현재는 의료기기로 통합되었고, 유럽의 경우는 의료기기로 분류되어 있으며, 미국의 경우 헌혈 스크리닝용 검사는 의료기기가 아닌 생물의약품평가센터에서 인허가를 담당하고 있습니다. 또한, 우리나라, 유럽, 미국 등은 체외진단 분류체계가 다르게 적용되고 있으며, 이에 따라 제품별로 인허가에 차이가 나타나기도 합니다.
체외진단 산업은 대부분 다양한 분야의 기술개발이 필요하고, 사업화를 위해서는 인허가를 받아야 하며, 일부 자가측정 제품을 제외하고는 의사나 임상병리사 등과 같은 의료전문가로 사용자가 한정되어 있는 등 안전성과 유효성이 중시되어야 하기 때문에 시장진입 장벽이 높은 편에 속합니다.
체외진단 산업은 질병의 조기발견, 치료 모니터링, 예후 등에 관련되어 궁극적으로는 국민의 건강 증진 및 삶의 질 향상에 기여하기 때문에 사회적으로 공익성이 큰 사업이라고 볼 수 있습니다. 신종플루나 메르스 등 신종 전염병의 출현은 사회적으로도 큰 혼란을 야기하여 전 산업계에 큰 타격을 주었던 경험이 있는데, 체외진단 산업은 신종 전염병에 대한 조속한 대처에 도움이 됩니다. 또한, 전 세계적으로 고령화 사회가 확대되고 있는 시점에서 질병의 치료 보다는 질병의 조기 발견을 통해 의료비용을 절감하는 것이 효과적이기 때문에 체외진단 산업의 중요성은 매우 크다고 할 수 있습니다.
KEIT PD Issue Report의 체외 진단기기(In Vitro Diagnostics) 현황 및 전망(2014)에 따르면, 글로벌 트렌드로 다음과 같은 특성이 있습니다.
- 기술간 융복합화가 가속화되고 있고 과거 오랫동안 유지되던 검사 분야도 융복합화가 빠르게 진행중임.
- 소형화, 자동화, throughput 증가, 모듈화 등의 변화
- 적은 양의 검체로 빠른 스피드 요구
- IT 접목 u-Health 요구 증대
- 경제성이 가장 중요한 이슈로 등장하고 있음
- 사용자 편의성, 심미성 요구도 증대하고 있음
따라서, 체외진단 산업은 다양한 기술적인 변화와 더불어 경제성과 사용자 요구 사항을 복합적으로 반영하는 방향으로 전개되고 있기 때문에 이러한 특성을 잘 파악하고 대처하는 것이 필요합니다.
(3) 산업의 전망
체외진단 산업은 치료를 위한 질병의 진단에서 출발하여 병세의 진행이나 회복을 예측하는 예후와 관련된 영역이 전통적인 체외진단 산업에 해당되었습니다. 현재는 휴먼 지놈 프로젝트와 분자진단의 발전, 면역화학 검사 기술의 발전 등을 통해 질병의 조기 진단이 중요한 영역으로 자리 잡았으며, 의약품과 연계된 맞춤형 진단/치료와 퍼스널 케어(Personal Care) 등의 영역이 앞으로 체외진단 산업을 이끌어 갈 수 있는 중요한 성장동력이 될 것으로 예상됩니다.
체외진단 산업은 다음과 같은 이유로 지속적인 성장이 예상됩니다.
- 전 세계적인 고령화 사회 확대에 따른 의료비 절감 필요
- ‘삶의 질’에 대한 욕구 증가
- 맞춤형 진단/치료의 필요성 증대
- 세계화 및 지구 온난화에 따른 신규 전염병 창궐/질병 확산 및 이를 억제하기 위한 국가 단위 또는 국제적 차원의 대처
- 바이오 및 IT 기술 등의 발달에 따른 융합 산업분야 부각
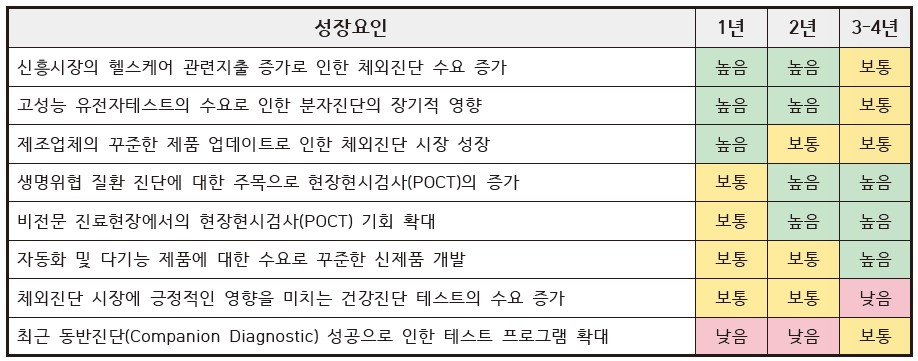
Frost&Sullivan의 Analysis of the Global In Vitro Diagnostic Market(2014)에서는 체외진단 산업의 성장에 대해 다음과 같이 분석하고 있습니다.
●신흥시장의 헬스케어 관련지출 증가로 인한 체외진단 수요 증가
- 아시아 태평양 지역의 헬스케어 관련 지출은 2020년까지 151%가 증가할 것으로 보이며, 중국, 베트남, 인도가 주된 성장요인이 될 전망임.
●고급 유전자테스트로의 수요로 인한 분자진단의 장기적 영향
- 감염병 및 유전질환 테스트의 수요로 인해 분자진단이 현대 헬스케어에서 필수적인 기술로 자리매김하고 있음.
●제조업체의 꾸준한 제품 업데이트로 인한 체외진단 시장 성장
- 경쟁력 있는 체외진단 기업들이 고객니즈를 충족시키기 위한 신제품을 꾸준히 개발하고 있음.
●생명위협 질환 진단에 대한 주목으로 POCT 증가
- 패혈증이나 극심한 심근경색 등 생명을 위협하는 질환의 적절한 진단을 위한 임상적 필요성이 증대되고 있음.
- 높은 사망률을 지닌 심각한 질병은 환자에게 막대한 치료비용 부담과 함께 빠른 POCT의 필요성을 야기함.
●비전문 진료 현장에서의 POCT 기회 확대
- 실직자들은 건강고용보험이 만료되므로 정기적인 건강검진을 받을 수 있는 환경이 필요함.
- 이로 인해 소매 진료소, 약국 및 홈케어 등이 편리함을 장점으로 인기를 얻고 있으며, 빠르고 정확하고 휴대가 가능한 POCT가 비전문 진료현장에서 도움을 줌
●자동화 및 다기능 제품에 대한 수요로 꾸준한 신제품 개발
- 임상 실험실은 숙련된 전문가 고용의 어려움, 수작업에서의 오류 등과 같은 과제를 해결하기 위해 자동화 처리에 의존하고 있음.
- 체외진단제품 제조업체는 임상화학에서 얻어지는 결과물과 같은 수준의 분자처리 자동화를 위해 노력하고 있음.
●체외진단 시장에 긍정적인 영향을 미치는 건강진단 테스트의 수요 증가
- 만성질환의 부담 증가로 체외진단 시장 및 제품의 꾸준한 수요가 이어질 전망임.
- 당뇨병, 천식, 심장병과 같은 만성질환의 비율은 선진국 및 신흥시장에서 증가하는 추세이며, 다수의 만성질환을 겪는 고령인구로 인해 환자집단은 더욱 증가
●동반진단(Companion Diagnostics) 성공으로 인한 테스트 프로그램 확대
- 진단과 제약의 협력을 통해 특정 질병에 대한 진단기술 및 표적 치료제를 동시에 개발하는 ‘Companion Development’ 전략으로 테스트 프로그램이 확대되고 있음.
상기의 체외진단 산업의 성장 요인 중 전망이 좋은 세 가지는 ‘생명위협 질환 진단에 대한 주목으로 POCT 증가’, ‘비전문 진료현장에서의 POCT 기회 확대’, ‘자동화 및 다기능 제품에 대한 수요로 꾸준한 신제품 개발’을 들 수 있습니다. 따라서, POCT 분야는 체외진단 시장에서 향후 전망이 매우 좋을 것으로 예상됩니다.
 |
|
002.체외진단 시장의 성장요인 요약 |
(출처 : Frost&Sullivan, 생명공학연구센터 재가공)
나. 회사의 현황
(1) 영업개황 및 사업부문의 구분
(가) 영업개황
당사는 바이오와IT 융합기술을 기반으로 개인 맞춤형POCT(현장검사, Point-of-Care Testing) 시스템을 구축하여 건강한 사회 구현에 이바지하고자 노력하고 있습니다. 당사는 체외진단(In Vitro Diagnostics) 분야 중 면역화학(Immunochemistry) 기반의POCT 제품을 개발, 제조, 판매하고 있는데, POCT는 체외진단(IVD, In Vitro Diagnostics) 시장 중에서도 규모가 크고 성장성이 높은 영역입니다. 개인 맞춤형POCT 시스템은 가까운 미래에 큰 시장이 형성될 것으로 기대되고 있는데, 이를 위해 당사는 일반 소비자가 직접 검사할 수 있는Self-Testing(자가측정)과 의료 전문가가 현장에서 사용하는Professional POCT(전문가용 현장검사) 기술 및 제품을 개발하고 있고, 맞춤형 진단을 위한TDM(치료약물모니터링, Therapeutic Drug Monitoring) 분야도 기술 개발을 통해 사업화를 추진하고 있습니다. Self-Testing 제품의 경우 캐시카우(Cash Cow)로서의 역할을 위해 디지털 임신테스트 및 배란테스트 등을 출시하였고, Professional POCT 제품은 2016년 하반기에 출시하였습니다.
(나) 공시대상 사업부문의 구분
|
사업부문 |
제품 |
개발 및 사업화 현황 |
|
|
Self-Testing (자가측정) |
디지털 제품군 |
- 슈얼리® 디지털 배란테스트 - 슈얼리® 디지털 임신테스트 Multi - 슈얼리® 디지털 임신테스트 RFU |
- 초소형·저전력 분석시스템을 이용하여 임신/배란 여부를 판정하는 제품 - 3개 제품 국내 허가 및 유럽연합 CE 인증 완료, 2개 제품 미국 FDA 등록 - 매출 발생 |
|
스트립 제품군 |
- 슈얼리® 배란테스트스트립 - 슈얼리® 임신테스트 스트립 |
- 육안으로 배란여부를 판정하는 제품 - 2개 제품 국내 허가, 유럽연합 CE 인증, 미국 FDA 등록 완료 - 매출 발생 |
|
|
고민감도 임신 테스트 |
- 슈얼리® 유-퍼스트 |
- 고민감도로 임신여부를 판정하는 제품 - 국내 허가, 유럽연합 CE 인증 완료 - 매출 발생 |
|
|
Professional POCT (전문가용 현장검사) |
- INCLIX® CRP - INCLIX® PCT - INCLIX® HbA1c - INCLIX® cTn I - INCLIX® PSA |
- 다기능 리더기를 이용하여 다양한 질병과 관련된 바이오마커를 정량적으로 측정하는 제품 - 개발 중 (2016년 4/4분기 이후 순차적으로 제품화 진행 중) |
|
|
TDM (치료약물모니터링) |
- Paclitaxel |
- 약물의 체내 대사 정도를 측정하여 개인에 맞는 용량으로 치료약이 투여될 수 있도록 도움을 주는 제품 - 개발 중 |
|
(2) 시장점유율
국내의 체외진단 관련 회사들은 대부분 규모가 작으며, 국내 의료진들이 글로벌 기업 제품들에 대한 선호도가 크고 상호 경쟁이 심화되고 있는 실정이기 때문에, 많은 회사들이 의료 시장이 확대되고 있는 해외 시장에 주력하고 있는 실정입니다.
그렇지만 임신테스트는 국내 제조사가 시장을 선점하고 있어 수입 제품의 점유율이 크지 않은 상황이고, 배란테스트는 당사의 제품과 저가의 중국 수입 제품이 서로 경쟁하고 있는 상황입니다.
면역화학 기반의 현장검사 제품을 제조하고 있는 국내 업체로는 바디텍메드, 에스디바이오센서, 엑세스바이오, 녹십자엠에스, 휴마시스, 나노엔텍, 에치비아이 등이 있습니다.
해외에서 당사와 유사한 면역화학 기반의 Self-Testing 제품 관련 사업을 전개하는 회사는 미국, 유럽, 일본, 중국 등 각 국에 많이 존재하지만 대부분의 회사들은 국내와 마찬가지로 육안검사에 의한 Rapid Test 제품을 사업화하고 있습니다.
당사와 유사하게 초소형·저전력 분석시스템을 이용한 면역화학 현장검사 제품을 개발하여 사업화한 회사로는 Siemens, SPD(Swiss Precision Diagnostics), Church & Dwight의 3개사가 있습니다. 이 중 SPD는 임신테스트와 배란테스트 1위 기업으로 전 세계 시장 M/S의 36.5%정도를 차지하고 있습니다(Clinica, 2010).
Professional POCT 제품의 경우 디지털 리더기 기반의 사업을 수행하고 있는 회사들은 미국, 유럽, 중국 등에 다수의 회사가 있으며, Siemens와 Roche와 같은 세계적인 헬스케어 기업에서도 면역화학 기반의 현장검사 제품을 사업화하고 있지만, 국내 체외진단 매출 1위 기업이었던 에스디를 비롯하여 Biosite, Axis-Shields 등 현장검사 관련 여러 회사를 인수한 Alere가 전 세계 M/S 1위 기업입니다. 2016년 상반기에 미국의 세계적인 헬스케어 기업인 Abbott는 Alere를 인수하여 세계 최대의 POCT 분야 기업이 되었습니다.
그 밖에 Goungzhou Wondfo Biotech을 비롯한 중국 회사들이 면역화학 기반의 Self-Testing과 Professional POCT 제품들을 개발하여 국내 업체들과 경쟁하고 있습니다.
[국내외 면역화학 기반 POCT 제조사 현황]
|
구분 |
업체명 |
주요 사업영역/제품군 |
비고 |
|
국내 |
바디텍메드 |
- 형광 리더기 기반의 정량분석 - CRP(염증지표), PCT(패혈증지표) 등 |
- |
|
엑세스바이오 |
- 말라리아 Rapid Test 등 감염성 질환 |
- |
|
|
나노엔텍 |
- 마이크로플루이딕스 기반의 정량분석 - 감염성질환 등 Rapid Test 제품 |
바이오포커스 인수 |
|
|
LG생명과학 |
- 알러지 검사 및 감염성 질환 ELISA 검사 |
- |
|
|
녹십자엠에스 |
- ELISA 및 Rapid Test 제품 |
- |
|
|
아산제약 |
- 감염성질환 등 Rapid Test 제품 |
- |
|
|
휴마시스 |
- 임신테스트, 감염성 및 심혈관질환 Rapid Test |
- |
|
|
인포피아 |
- 심혈관질환 정량분석 등 |
- |
|
|
SD 바이오센서 |
- 당화혈색소 정량분석 등 |
- |
|
|
에치비아이 |
- 감염성질환 등 Rapid Test 제품 |
- |
|
|
해외 |
Alere(Abbott) |
- 감염성, 심혈관, 당뇨 등 Rapid Test 및 정량분석 제품군 |
POCT 분야 M/S 세계 1위 |
|
Siemens |
- 당화혈색소 정량분석 제품 등 - 초소형(A1CNow)과 다기능(DCA2000) 형태 |
Bayer 진단사업부분 인수 |
|
|
SPD |
- 디지털 임신/배란테스트 개발 및 사업화 - Clearblue 브랜드 |
Alere와 P&G 합작회사 |
|
|
Church & Dwight |
- 디지털 임신/배란테스트 개발 및 사업화 - First Response 브랜드 |
- |
|
|
Wondfo |
- 임신테스트 및 배란테스트 - 형광 리더기 기반의 정량분석 |
- |
당사에서 현재 사업화를 하고 있는 제품은 임신테스트와 배란테스트 제품으로, 국내 시장에 스트립 제품은 2014년부터, 디지털 제품은 2015년부터 실질적인 판매를 시작하였습니다. 국내에서 임신테스트를 판매하고 있는 회사는 30개 사가 넘을 정도로 매우 많지만 바이오 벤처회사의 ODM 제조와 제약회사 약국 영업이 일반적인 시장 상황입니다. 배란테스트는 난임 부부들의 임신을 돕는 제품으로, 임신테스트와는 달리 온라인 시장이 주요 시장이지만, 임신테스트에 비해 널리 대중화가 되어 있지는 않은 상황입니다.
임신테스트와 배란테스트의 국내 시장은 공식적인 자료가 없어 정확한 파악이 어려우나, 2013년 의약품 생산실적과 업계의 추측으로 보면 다음과 같습니다. 2013년도 임신테스트의 국내 생산실적은 약 70.3억원이었고, 배란테스트는 국내 생산실적 약 4.4억원으로 임신테스트 수입은 국내 생산실적의 10%로, 배란테스트 수입은 국내 생산실적의 50%로 추정하고 연평균시장성장률은 임신테스트 5%, 배란테스트 20%로 가정하여 계산하면 2015년도 임신테스트 시장은 제조사 기준 약 85억원, 배란테스트는 약 13억원 정도 규모로 이는 전 세계 시장의 약 1% 수준에 해당됩니다. 따라서, 당사의 2015년도 국내 시장점유율은 임신테스트 약 0.9%, 배란테스트는 약 35.3% 정도로 추정되고, 2016년 상반기에는 임신테스트 약 1.9%, 배란테스트는 약 41.5% 정도로 추정됩니다. 2016년 9월 당사의 임신테스트 제품 중 전략제품인 고민감도 제품이 동아 제약의 ODM으로 출시 되었고 디지털 임신진단 제품이 온, 오프라인 시장 진출을 본격화 하고 있어 2017년 당사의 임신 진단 시장점유율은 20-30%를 목표로 하고 있습니다.
Professional POCT 제품의 경우 국내 시장은 2014년 약 1.3억 달러 규모(Viosiongain, 2014)로, 이 중 혈당, 임신, 콜레스테롤 등을 제외한 면역화학 분야가 20% 정도를 차지한다고 가정하면 0.26억 달러 규모에 해당되고 이는 전 세계 시장의 8% 정도로 추정됩니다. 당사의 Professional POCT 제품이 순차적으로 출시되면서 국내외 시장에서 시장 점유율을 지속적으로 늘려나갈 계획입니다.
(3) 시장의 특성
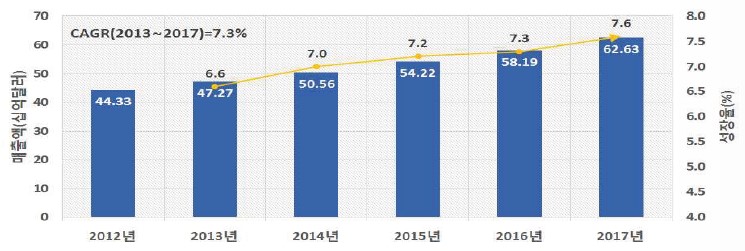
Frost&Sullivan의 Analysis of the Global In Vitro Diagnostic Market(2014) 자료에 따르면 글로벌 체외진단 시장규모는 2013년 472.7억 달러에서 연평균 7.3%로 성장하여 2017년 626.3억 달러 규모로 성장할 것으로 예상하고 있습니다.
 |
|
003.글로벌 체외진단 시장 현황 및 전망 |
(출처 : Frost&Sullivan, 생명공학연구센터 재가공)
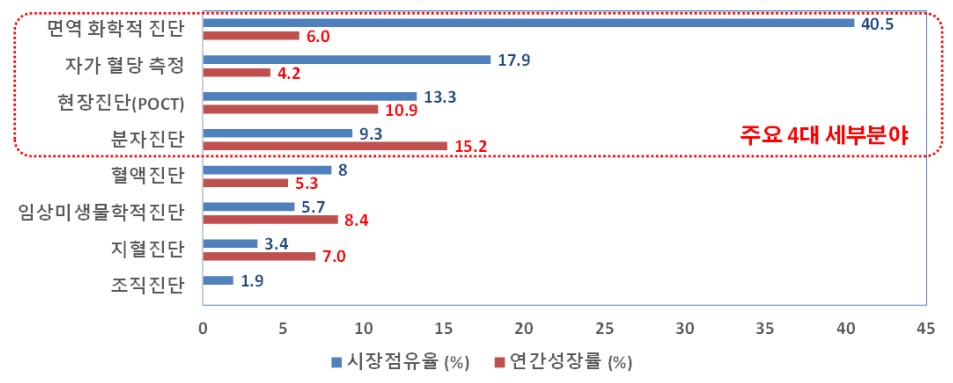
매출액 상위분야는 면역화학 199.5억 달러, 자가혈당측정 85.2억 달러, 현장진단의료기기(POCT) 63.4억 달러이며, 성장률 상위분야는 분자진단 12.7%, 현장진단의료기기(POCT) 8.4%, 지혈진단 8.2%로 분석됩니다. 따라서 POCT 분야는 체외진단 시장 규모 3위 및 성장률 2위에 해당되어 체외진단 분야 중 전망이 매우 밝다고 할 수 있습니다.
 |
|
세계 체외진단 세부 시장점유율('13년 기준) 및 연평균성장률('12년~'17년 기준) |
(출처 : Frost&Sullivan, 연구성과실용화진흥원 재가공)
POCT 시장은 혈당 측정이 약 54%를 차지하고 있고, 임신검사 시장이 약 8.9%, 혈액응고 검사 8.3%, 감염성 질환 검사 6.8%의 순으로 시장이 나누어져 있습니다. 이 중에서 감염성 질환과 심혈관 질환 검사 시장이 가장 높은 성장율을 보이고 있습니다.
[2013년 글로벌 POCT 마켓]
|
Sector |
Market($bn) |
Share(%) |
CAGR(%) |
|
혈당측정 |
8.64 |
54 |
4.8 |
|
임신 |
1.43 |
8.9 |
5.6 |
|
혈액응고 |
1.32 |
8.3 |
11.1 |
|
감염성 질환 |
1.08 |
6.8 |
13.9 |
|
심혈관 질환 |
1.1 |
6.9 |
12.2 |
|
콜레스테롤 |
1.09 |
6.8 |
11.1 |
|
기타 |
1.33 |
8.3 |
9.1 |
|
Total |
15.99 |
100 |
7.7 |
(출처 : Visiongain, 2014)
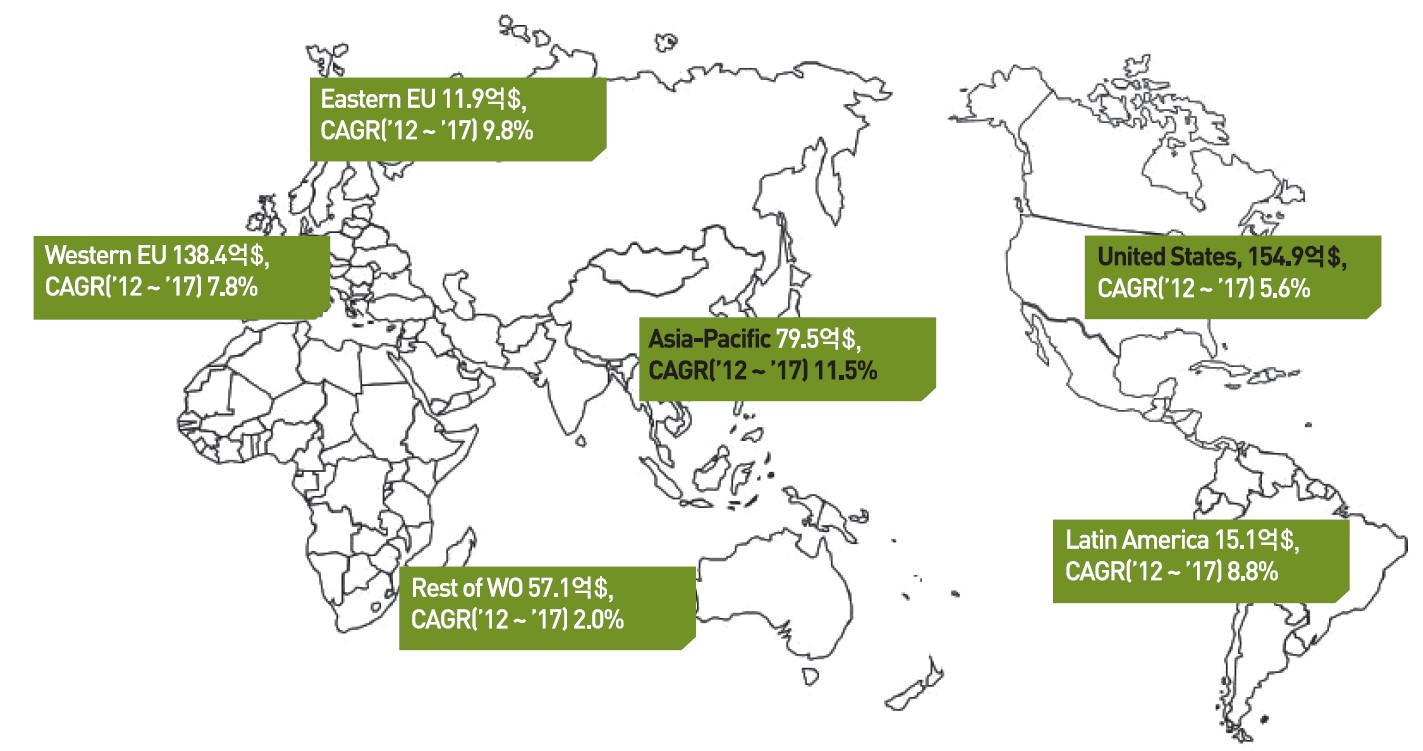
2012년 지역별 시장규모를 보면 미국이 가장 큰 154.9억 달러 규모를 형성하고 있으며, 그 다음으로 서유럽지역이 138.4억 달러, 아시아·태평양지역이 79.5억 달러 규모를 형성하고 있습니다. 2017년 까지 성장전망을 보면 아시아·태평양이 가장 높은 연평균 성장률 11.5%로 향후 큰 시장이 형성 될 것으로 전망됩니다.
 |
|
2012년 지역별 체외진단 시장 규모 및 연평균 성장률 |
(출처 : Frost&Sullivan, KEIT PD Issue Report 인용)
국내의 체외진단 검사 시장은 대부분 중·대형 병원과 검사센터에서 이루어지고 있는데, 소변검사와 일부 Rapid Test를 제외하면 대부분 외국산 제품이 이용되고 있습니다. 이러한 의료기관에서는 대부분 고가의 장비 자동화 장비를 이용하는데, 국내 회사들은 규모가 작아 대형 장비 기반의 사업에 취약하기 때문입니다.
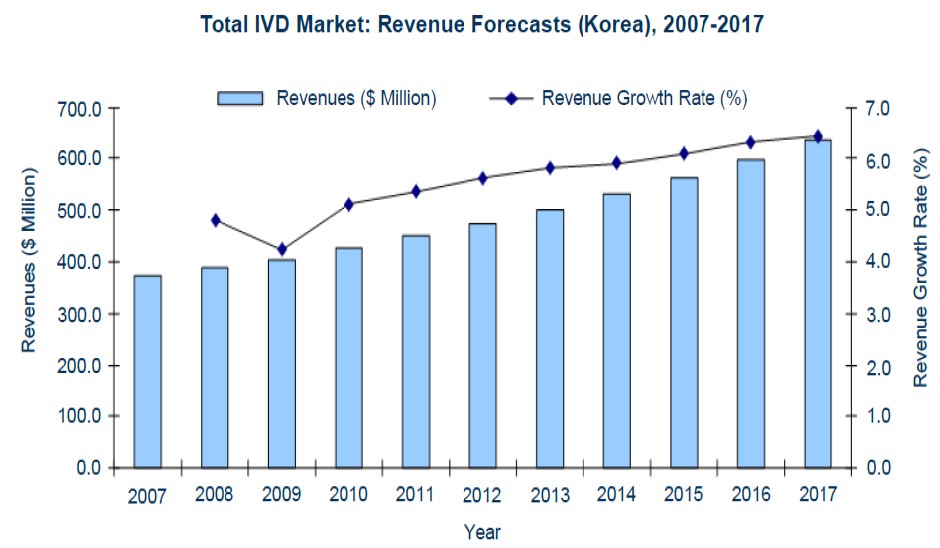
국내 체외진단 시장 규모는 2010년 4,750억 원에서 연평균 5.9%씩 성장하는 것으로 추측되며 (한국보건산업진흥원 보건산업기술이전센터의 체외진단(IVD) 시장 동향(2014)), 이에 따라 2016년에는 약 6,700억 원에 이를 것으로 추정됩니다.
 |
|
국내 체외진단 시장규모 및 성장률 |
[국내 체외진단 시장규모 및 성장률]
(출처 : Frost&Sullivan, 2010, 보건산업진흥원 인용)
국내 POCT 시장은 2014년 1.3억 달러 규모로 2017년 까지 연평균 13.0%로 성장하고, 2018년부터 연평균 15.2%로 성장하여 2021년에는 3.3억 달러 규모에 이를 것으로 추측됩니다(Viosiongain, 2014).
(1) 계절적 경기변동
체외진단 산업은 특성 상 질병의 진단을 목적으로 하고 경기 흐름과 관계없이 지속적으로 환자가 발생하기 때문에 이에 따른 수요가 항상 존재하므로 경기변동의 영향을 비교적 덜 받는 산업입니다.
그렇지만 인플루엔자 진단과 같은 특정 제품의 경우 특정 계절에 발병하는 질병을 진단해야 하기 때문에 계절에 따른 경기변동을 나타내고 있습니다.
일부 제품의 경우 유행하는 질병과 국가 및 세계보건기구의 의료 정책에 따른 영향을 크게 받을 수 있습니다. 따라서 체외진단 산업은 계절적 경기변동 보다는 정책이나 사회적인 환경의 변동에 대해 민감한 산업이라고 할 수 있습니다.
(2) 제품의 라이프 사이클
체외진단 제품은 의약품이나 다른 의료기기와 마찬가지로 라이프 사이클이 다른 산업에 비해 긴 편에 속합니다. 일반적으로 제품의 사업화를 위해서는 기술개발, 성능평가, 인허가, 시스템 인증이 필수적이기 때문에 적어도 2~3년 정도의 시간이 소요됩니다. 이러한 이유로 신기술이나 신제품이 시장에 출시하기 까지 오래 걸려 제품의 개발 및 사업화 사이클이 길 수 밖에 없습니다.
또한 한번 사업화된 제품은 기술의 발전에 따라 일부 업그레이드가 진행되기도 하지만, 인간의 생명과 건강에 대한 제품이기 때문에 시장에서 계속 사용되고 있으며, 20년 이상 사용되는 제품도 상당수 존재합니다.
(3) 대체 시장
질병을 검사하고 모니터링하는 체외진단 제품의 관점에서 볼 때 대체 시장으로 생각해 볼 수 있는 것은 영상진단(Imaging) 시장입니다. 영상진단은 X-ray, 초음파, MRI, CT 등과 같은 장비를 이용하는데, 체외진단과 같은 다양한 질병을 검사할 수는 없지만, 특정 질병과 수술 등의 의료시스템에서 필수적으로 사용되고 있습니다.
의료 현장에서는 영상진단과 체외진단을 경쟁적인 관점에서 사용하기 보다는 상호보완적으로 사용하고 있습니다. 그렇지만 기술의 발전에 따라서는 영상진단이 일부 체외진단 시장을 대체할 가능성도 존재합니다.
체외진단 시장 내에서 볼 때 각 영역별로는 서로 대체 시장 관계에 놓일 수 있습니다. 예를 들어 감염성 질환을 검사하는 분자진단 제품은 면역화학 영역을 침범하여 감염성 질환과 관련된 면역화학 시장을 대체할 수 있습니다. 그렇지만 각 영역별로 검사의 장단점이 있기에 새로운 영역에서 제품이 개발된다고 하더라도 일방적으로 다른 영역을 대체하기 보다는 상호보완적으로 사용되는 경우가 많습니다.
반면, 체외진단 영역 중 POCT는 대형병원이나 검진센터와 같은 중앙검사실(Central Lab)용 제품과 대체 시장 관계에 놓일 수 있습니다. 그 이유는 POCT 제품이 주로 중앙검사실용 제품을 사용할 수 없는 환경에서 사용되기 때문입니다. 즉, POCT는 중앙검사실에서 수행되던 검사를 중소형 병원이나 개인들이 사용할 수 있도록 개발되기 때문입니다. 한편으로 POCT를 사용하다가 일정 수준의 규모가 커지면 중앙검사실용 제품을 사용할 수도 있습니다.
(4) 자원 조달 상황
체외진단 산업의 자원은 크게 원자재와 부자재로 나눌 수 있습니다. 원자재는 제품 제조와 직접적인 관련이 있는 부품, 시약 등 성능 구현에 필수적인 자재를 의미하며, 부자재는 포재, 스티커와 같이 제품 구성에 필요한 자재를 의미합니다.
부자재의 경우 체외진단 기업들은 대부분 아웃소싱을 활용하는 반면 원자재의 경우 아웃소싱을 활용하는 기업들이 있는 반면 주요 원료를 직접 제조하는 기업도 있습니다. 예를 들어 면역화학 제품에 이용되는 항원과 항체는 외부 아웃소싱이 불가능하거나 가격이 비쌀 경우 직접 개발하여 제조하기도 합니다.
(5) 경쟁상황
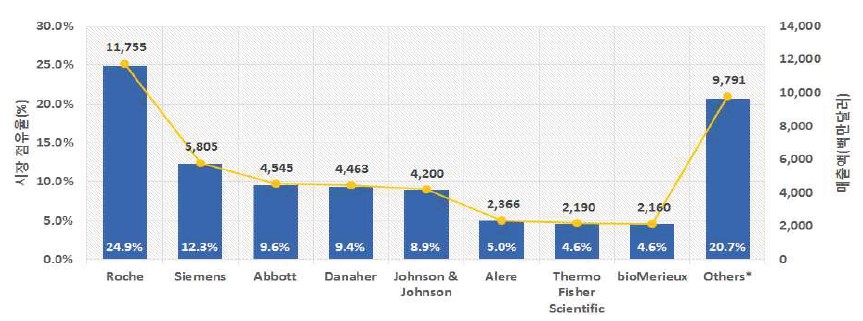
체외진단 시장의 글로벌 기업간 경쟁을 보면, Roche 24.9%, Siemens 12.3%, Abbott 9.6%로 상위 3개 기업이 전체 시장 규모의 46.8%를 차지하고 있고, 상위 8개 기업이 전체 시장의 79.3%를 차지하고 있습니다.
 |
|
글로벌 체외진단 시장 기업별 경쟁구도 |
<그림> 글로벌 체외진단 시장 기업별 경쟁구도(출처 : Frost&Sullivan, Analysis of the Global In Vitro Diagnostic Market(2014), 생명공학연구센터 재가공)
한편, 많은 글로벌 체외진단 기업들은 사업적인 경쟁력 강화와 신규 사업 진출을 위해 M&A를 적극 활용하고 있습니다. Roche는 조직검사에 특화된 기술을 가지고 있는 Ventana 사를, Siemens는 Bayer Healthcare의 체외진단 사업부문을 인수하였고, Danaher는 Beckman Coulter를 Abbott는 2016년도에 세계 최대의 POCT 기업인 Alere를 인수한다고 발표하였습니다. Alere는 경쟁력 있는 POCT 회사들을 많이 인수하였는데, 미세유체 기반의 심혈관 질병 진단회사인 Biosite, 당화혈색소와 CRP 등의 POCT 제품을 사업화하는 Axis-Shields, 콜레스테롤 검사 제품을 사업화하는 Cholestech, Rapid Test 제조사인 국내의 SD 등이 Alere에 인수합병된 회사들입니다. 그 밖에 Thermo Fisher는 세계 최대의 알러지 진단회사인 Phadia와 패혈증 마커인 Procalcitonin에 대한 특허를 보유한 B·R·A·H·M·S 사를 인수하였습니다.
체외진단 분야는 제품 개발에 다양한 기술이 필요하고, 제품군 및 종류도 매우 다양하기 때문에 M&A와 전략적 제휴가 상당히 많이 이루어 지고 있는 실정입니다. 체외진단 기업 이외에도 제약회사와 타 사업분야의 기업 사이에서도 활발하게 진행되고 있습니다. 국내에서는 M&A나 전략적 제휴가 해외에 비해서 많지 않은 상황이지만, 세계 시장에서의 경쟁이 가속화되고 사업력 강화를 위해서는 향후 활성화될 가능성이 높을 것으로 판단됩니다.
국내의 의료환경은 대형병원의 접근성이 매우 좋기 때문에 현재까지 POCT 분야 보다는 중앙검사실 체제가 시장을 주도하고 있습니다. 중앙검사실에서는 대부분 글로벌 기업의 대형장비 제품들이 선점한 상황으로 POCT제품 중심의 국산 제품에 대한 인지도는 아직 높지 않습니다. 현재는 사실상 외산 제품들 사이의 경쟁이 주를 이루고 있습니다. 그러나 최근 로컬병원의 경우 자체의 수익구조의 필요성 및 인플루엔자나 당화혈색소 검사와 같이 진단을 근거로 하는 처방이 필요한 분야가 증가함에 따라 국내의 경우도 로컬병원 중심의 POCT시장이 확대되고 있습니다. 그 이전에는 국내 진단 기업들은 대부분 국내 시장 보다는 해외 시장에 집중하고 있는 상황이었습니다. 이에 비해 임신테스트와 같은 자가측정 제품은 의료기기가 아닌 의약품으로 분류되어 약국중심의 특수한 영역을 형성하고 있었던 국내의 특수성과 결부되어, 가격 경쟁력, 유통 채널을 확보한 국내 업체들이 시장을 장악하고 있습니다.
당사를 비롯하여 국내 체외진단 제조사인 LG생명과학, 씨젠, 바디텍메드, 아이센스, 나노엔텍, 영동제약, 에스디 바이오센서 등은 국내 시장에서 점유율 확대를 위해 노력하고 있으며, 일부 제품군에서는 외산 제품보다 높은 시장 점유율을 나타내고 있습니다.
다른 산업 분야와 마찬가지로 체외진단 제품은 국내외 시장에서 가격 경쟁력을 갖춘 중국 기업과 경쟁이 점점 치열해 지고 있습니다. 그 이유는 중국은 국내 체외진단 기업과 유사하게 대형 종합병원인 3급갑 병원에는 주로 외산 제품들이 납품되고 있는 실정이고, 국내 기업들과 유사한 POCT 분야의 기술개발 업체들이 늘어 나기 때문입니다.
아직까지는 성능 및 신뢰도 측면에서 글로벌 시장에서의 인지도는 한국제품이 중국제품 보다는 다소 우위를 차지하고 있으나 중국 정부의 의료기기 시장에 대한 집중 육성 등 향후 경쟁은 치열해 질 수 있습니다.
(6) 국내/외 규제상황
체외진단 산업은 의료기기 산업에 속하기 때문에 국내?외에서 사업화를 하기 위해서는 다양한 법적 규제를 받고 있습니다. 국내의 경우 의료기기의 성능, 안전성, 안정성 등에 대한 품질이 확보되어야 하기 때문에 연구개발, 원자재 구매, 제조, 품질관리, 출하, 고객 불만 처리 등 일반적인 회사 행정을 제외한 거의 전 사업 분야에 대해 시스템을 구축해야 합니다. 이러한 시스템은 국내에서는 식품의약품안전처로부터 의료기기 GMP를 받아야 제품을 판매할 수 있습니다. 또한 각 제품에 대해서 분석적 성능과 임상적 성능 등에 대한 기술문서를 식품의약품안전처에 제출하여 허가를 받아야 제품 판매가 가능합니다.
해외 시장에서도 국내와 유사하게 시스템 인증과 각 제품에 대한 허가를 받아야 판매가 가능합니다. 유럽연합의 경우 품질 시스템으로 ISO13485 인증을 받아야 하며, 각 제품에 대해서는 기술문서 작성 후 제품에 따라 CE 인증을 받거나 또는 CE 자가선언을 해야 판매가 가능합니다. 미국의 경우는 FDA(Food & Drug Administration)에서 품질 시스템 승인과 기술문서 심사 승인을 받아야 제품 판매가 가능합니다.
국내 및 유럽연합, 미국의 주요 관련 법령은 아래 표와 같습니다.
[체외진단 관련 주요 법령]
|
관련 법령명 |
주요 내용 |
|
의료기기법 |
의료기기의 제조ㆍ수입 및 판매 등에 관한 사항을 규정한 법 |
|
의료기기법 시행령 |
의료기기법에서 위임된 사항과 그 시행에 관하여 필요한 사항을 규정한 명령 |
|
의료기기법 시행규칙 |
「의료기기법」 및 같은 법 시행령에서 위임된 사항과 그 시행에 필요한 사항을 규정한 규칙 |
|
의료기기 제조 및 품질관리 기준 |
의료기기를 제조 또는 수입함에 있어 준수하여야 하는 세부사항과 품질관리심사기관 및 품질책임자 교육실시기관에 대한 지정절차 및 관리방법 등에 관하여 필요한 사항을 정한 고시 |
|
의료기기 품목 및 품목별 등급에 관한 규정 |
의료기기의 품목 및 품목별 등급에 관하여 필요한 사항을 정한 고시 |
|
의료기기 허가·신고·심사 등에 관한 규정 |
의료기기 제조·수입 의료기기의 허가·신고 등에 관한 세부사항 및 의료기기 기술문서 등의 심사에 필요한 세부사항 등에 대한 사항을 정한 고시 |
|
의료기기 안정성시험기준 |
「의료기기법」 및 같은 법 시행규칙에 따라 제출하는 의료기기 기술문서 심사자료와 의료기기 제조 및 품질관리 기준에 따른 의료기기의 안정성시험에 관한 기준을 정한 고시 |
|
DIRECTIVE 98/79/EC OF THE EUROPEAN PARLIAMENT AND OF THE COUNCIL |
체외진단용 제품의 EU 판매를 위한 지침으로 우리나라 의료기기법에 해당 |
|
FD&C (Federal Food, Drug, and Cosmetic Act )의 Section 510(k) |
의료기기의 미국 판매를 위한 미국 연방법으로 우리나라 의료기기법에 해당 |
(4) 주요 제품 소개
1) Self-Testing 제품
당사에서 추구하는 Self-Testing은 초소형·저전력 분석 시스템을 기반으로 한다는 점이 국내외 제조사들과 차별화되는 요소입니다. 이러한 특징은 향후 모바일 헬스케어 (m-Health) 또는 u-헬스케어와 같이 새로운 체외진단 분야로 확대할 수 있는 장점이 있습니다.
Self-Testing 제품으로 처음 개발한 제품은 임신테스트와 배란테스트 제품으로 당사의 캐시카우(Cash Cow) 역할을 담당하는 제품으로 개발되었습니다. 이 제품은 일반 소비자가 스스로 검사할 수 있는 제품으로 브랜드는 Sure + Early의 합성어인 "Surearly (슈얼리)"로 확실하고 빠르게 진단한다는 의미를 지니고 있습니다.
■ 주요 기능 및 특징
디지털 제품은 사용자가 반응 라인을 직접 분석할 필요 없이 바이오센서에 나타나는 반응을 광학적(광원 및 광센서 이용)으로 측정하여 검사 결과를 LCD 창에 나타냅니다.
제품군은 크게 바이오센서가 내장된 일체형으로 RFU(Ready-for-Use) 형태와 바이오센서를 교체하면서 사용할 수 있는 Multiple Use 형태로 구분됩니다. RFU 제품은 바이오센서가 분석기기에 삽입된 일회용으로 여러 번 측정할 필요가 없는 타겟(예 : 임신진단)을, Multiple Use 제품은 여러 번 반복하여 측정할 필요가 있는 타겟(예 : 배란검사)을 대상으로 합니다.
 |
|
슈얼리 디지털 임신테스트 및 배란테스트 |
현재 개발 완료된 제품은 임신테스트와 배란테스트 제품이며, 두 품목에 대해서는 디지털 테스트 이외에 육안으로 검사하는 전통적인 스트립 형태의 제품도 함께 개발하여 저가 제품부터 프리미엄 제품까지의 라인-업을 구축하였습니다. 디지털 임신테스트와 배란테스트를 비롯하여 총 6개 제품이 국내 허가와 CE 인증을 완료하였고, 4개 제품에 대해서 FDA 등록을 완료하였습니다.
■ 차별화 요소
일반적으로 면역화학 POCT의 Self-Testing 제품은 면역크로마토그래피 방식의 제품으로 일반 소비자가 직접 검사를 수행해야 하며, 수행된 결과에 대해서도 직접 판정해야 합니다. 만약 검사 과정 중에 오류가 있거나 제품에 이상이 있을 시에도 전문적인 지식이 없는 일반 소비자가 오류를 인지하지 못하면 잘못된 결과를 판정할 가능성이 높습니다.
면역크로마토그래피 방식의 제품 자체의 정확성은 99%로 우수하지만, 실제 소비자가 검사하는 정확성은 75% 정도로 떨어지는 것으로 알려져 있습니다. 그 주된 이유는 소비자들이 잘못 검사하거나 잘못 판정하기 때문입니다. 이에 비해 당사에서 개발한 초소형·저전력 면역화학 분석시스템을 이용하면 다음과 같은 검사 오류를 검출하여 정확성을 크게 향상시킬 수 있습니다.
① 검사 및 결과 판정 시간이 짧거나 길면 검사 결과가 정확하게 나타나지 않을 수 있습니다. 기존 제품은 일반 소비자가 직접 시간을 측정하여 검사를 수행하고 판정해야 하기 때문에 이를 정확하게 준수하지 않는 경우가 종종 발생합니다. 당사의 초소형·저전력 면역화학 분석시스템은 항상 일정한 검사 시간을 유지할 수 있기 때문에 이러한 오류가 발생하지 않습니다.
② 정확한 검사를 수행하기 위해서는 적정량의 검체가 바이오센서에 유입되어야 합니다. 검체가 너무 적게 유입되면 검사에 필요한 구성성분들이 제대로 반응하지 않고, 반대로 너무 많이 유입되면 Overflow 현상이 발생하여 이상 반응을 유발할 수 있습니다. 기존 제품의 경우 이러한 오류를 일반 소비자들이 직접 인지하고 판정해야 하는데, 현실적으로 어려운 점이 많습니다. 당사의 초소형·저전력 면역화학 분석시스템은 고유의 광학배열과 알고리즘을 통해 검체의 흐름을 인지하여 검체양이 너무 적거나 많은 경우를 감지하여 알려주므로 검사의 정확성을 높일 수 있습니다.
③ 반응 라인이 희미한 경우 육안으로 판정할 때 검사자 마다 주관적으로 해석하는 경우가 발생합니다. 따라서 어떤 사람은 양성으로, 어떤 사람은 음성으로 판정하기 때문에 사람 간 편차가 발생합니다. 당사의 초소형·저전력 면역화학 분석시스템은 디지털로 검사 결과를 알려주기 때문에 검사자의 주관에 의한 판정 오류가 없습니다.
따라서, 슈얼리 디지털 임신테스트 및 배란테스트는 기존 제품과 비교할 때 사용자들에게 디지털 검사 환경을 제공하여 보다 정확한 검사가 가능하다는 기술적인 경쟁 우위를 보이고 있습니다. 또한, 이 제품들은 모바일 헬스케어 및 u-헬스케어에 적용시킬 예정으로 기존 제품들과 기술 및 서비스 등 경쟁우위를 지속적으로 확보할 계획입니다.
2) Professional POCT 제품
체외진단 제품의 판정은 음성/양성과 같이 정성으로 판정하는 제품이 있는 반면 농도를 측정하여 질병의 유무나 병의 진행 정도를 파악할 수 있는 정량분석 제품이 있습니다. 예를 들어 임신테스트는 음성/양성(임신/비임신)의 정성 분석으로 판정되며, 간기능 검사에 사용되는 GOT는 농도로 환산하여 간의 손상 정도를 측정합니다.
당사의 Professional POCT 제품의 브랜드는 INCLIX®이며, 의사나 임상병리사와 같은 의료전문가를 위한 측정기기 및 바이오센서 제품으로, 전문가들이 정확하고 편리하게 사용할 수 있습니다. 본 기술은 면역크로마토그래피 원리를 이용하는 바이오센서와 CMOS 이미지 센서를 이용하여 분석하는 정량분석 현장검사 시스템입니다.
INCLIX®는 감염증 검사, 당뇨 검사, 종양표지자 검사, 패혈증 검사 등 면역화학 기반의 다양한 제품에 적용되며, 치료약물 모니터링(TDM, Therapeutic Drug Monitoring)과 같은 분야에 확장 적용할 수 있는 핵심적인 제품입니다.
■ 주요 기능 및 특징
금 나노입자 기반의 면역크로마토그래피의 분석에 있어서는 그 동안의 기술 개발 결과를 보면 이미지 캡쳐 방식이 민감도 및 재현성이 더 우수한 것으로 나타났으며, 이에 따라 CMOS 이미지 센서 기반의 현장검사 분석기기(INCLIX® 를 개발하게 되었습니다.
즉, 면역크로마토그래피 반응에 의해 나타나는 밴드의 강도를 이미지 캡쳐 후 여러 지점에서 데이터 값을 읽은 후 background noise 값을 제거하여 정량화하는 방식을 통해 측정하는 원리를 이용합니다.
 |
|
면역크로마토그래피 정량분석 기기 |
과거에는 단순하게 검사 결과를 분석하고 프린트하는 기본적인 기능을 수행하였던 것에 비해, 최근에는 기본적인 기능 이외에 환자 정보 입출력, 제품의 lot를 포함한 정보 입력, 바코드 리딩을 이용한 추가 기능, 검사 결과값의 병원 데이터 시스템 연동(LIS), 제품의 자동 인식 또는 코드 프리 기능 등 다양한 기능을 요구하고 있어 이러한 요구사항에 맞춰 제품이 개발되었습니다.
금 나노입자 기반의 정량 현장검사 시스템은 CMOS 이미지 센서를 이용하여 이미지를 촬영한 후 촬영된 이미지로부터 각 pixel별 신호의 세기를 측정하고 기법들을 사용하여 이미지의 특정한 영역에 대한 광학 정보를 얻도록 설계되었습니다.
본 시스템은 이미지 획득을 위한 광 기계부와 하드웨어 제어장치, 소프트웨어 구동을 위한 마이크로프로세서 플랫폼, 주변장치 연결을 위한 인터페이스 등으로 구성되어 개발되었습니다. 마이크로프로세서 플랫폼은 100장의 이미지를 수 초 내에 분석할 수 있도록 고성능의 메인보드가 사용되었고, 안정한 시스템을 위해 리눅스 기반의 OS를 적용하였습니다.
사용자의 오류를 최소화하기 위하여 정량 현장검사 바이오센서 제품 디바이스에 바코드를 부착하고 시스템에서 자동으로 인식하여 테스트 ID를 확인할 수 있도록 하였으며, 사용자가 직관적으로 메뉴를 쉽게 사용할 수 있도록 Graphical User Interface (GUI)를 개발하였습니다.
■ 차별화 요소
중앙검사실에서 수행하는 면역화학 검사는 수 천만~수억 원 이상의 자동화 장비를 사용하고 검사 가격이 비싸며, 한번 검사를 하기 위해서는 시스템상 여러 사람의 검체를 모아야 되기 때문에 시간이 오래 걸리는 등 현장현시 검사 측면에서는 미흡합니다.
이에 반해 면역크로마토그래피 제품은 저렴한 가격에 간편하고 빠르게 검사할 수 있는 장점이 있었지만, 대부분의 제품은 육안으로 검사하는 정성검사(Yes/No 검사) 용도로 사용되어 왔으며, 병의 진행 정도나 치료 정도를 알 수 있는 정량검사(농도를 숫자로 표시하는 검사) 제품에는 적용이 힘들었습니다.
그 이유는 면역크로마토그래피 제품의 정량 검사는 측정장비 개발과 바이오센서의 최적화가 필요한데, 이러한 제품을 개발할 수 있는 능력을 갖추기가 쉽지 않기 때문입니다. 즉, 바이오 기술 기반의 면역크로마토그래피를 IT 기술을 이용하여 분석하기 위해서는 각각의 요소 기술을 확보해야 함은 물론이고 두 기술을 융합시킬 수 있는 기술도 필요합니다. 또한, 의료 현장에서 요구되는 바코드 인식, 의료 시스템 연계, 데이터 표시 및 저장 등 다양한 사항들이 반영되어야 합니다.
면역크로마토그래피 기반의 정량 Professional POCT 제품은 표지체로 금 나노입자 보다는 형광을 많이 사용합니다. 형광을 이용한 면역크로마토그래피는 용액 형태의 시약을 사용하기 때문에 이러한 편차 요인이 적어 정량검사에 사용되었으나, 시약의 냉장보관이 필요하며, 기기 부품이 비싸다는 단점이 있습니다. 금 나노입자를 이용한 면역크로마토그래피는 보편화되고 안정한 기술이며 상온에서 보관 및 운송이 가능하고 사용방법이 용이하다는 장점이 있습니다. 그렇지만 패드를 적셔서 건조시키는 제조 방법이 편차를 발생시킬 수 있는 요인으로 인해 정밀도와 정확성에 영향을 줄 수 있기 때문에 주로 정성 분석에 많이 활용되어 왔습니다.
당사에서는 표지체로 금 나노입자를 사용하는데, 금 나노입자의 장점을 살리고 단점을 개선하기 위한 측정장비 구축 및 고유의 분석 알고리즘을 개발하였습니다. 측정장비는 고감도의 CMOS 이미지 센서를 이용하는데, 부품 소재 및 관련 기술의 발달로 인해 매우 정밀한 분석이 가능해졌습니다. 따라서 반사율 측정 방식 보다는 훨씬 뛰어난 민감도를 나타낼 뿐만 아니라 형광 기반의 제품과 비교하여도 뒤지지 않습니다. 또한 당사에서는 면역 반응의 분석을 위해 검사선과 대조선의 비율을 고유의 방식으로 측정 및 계산하는 알고리즘을 구축하여 보다 정확하고 민감한 정량 분석이 가능하도록 하였습니다. 당사의 면역크로마토그래피 제품은 금 나노입자가 건조된 형태로 제조되는데, 각 요소 성분들의 농도 및 제형 최적화 등을 통해 분석 알고리즘이 적용되도록 개발되었습니다.
당사의 INCLIX® 제품은 모든 제품이 5분-30분 이내에 검사가 완료되는 신속함과 95~99% 이상의 검사 정확성, 그리고 1~2번의 조작으로 검사가 완료되는 편리성을 가지고 있으며, 실온 조건에서 안정하기 때문에 별도의 냉장 시설이 필요하지 않기 때문에 운송이 용이하고 사용환경에 제약이 거의 없습니다.
(5) 신규사업 등의 내용 및 전망
(가) 개인 맞춤형 치료약물 모니터링 (Personalized Therapeutic Drug Monitoring) 개요
전 세계적으로 건강 관련 산업의 기조가 4P (Personalized, Predictive, Preventive, Participatory)라는 핵심 가치를 중심으로 재편되고 있는데, 이 핵심 가치는 서로 긴밀하게 연결된 개념으로 개인 중심, 환자 중심의 의료 효과 극대화가 주목표입니다. 이러한 개인별 맞춤의료 (Personalized Medicine) 시장은 급속한 성장이 예상되며, 의료 산업 전반에 걸쳐 광범위한 영향을 미칠 것으로 보입니다.
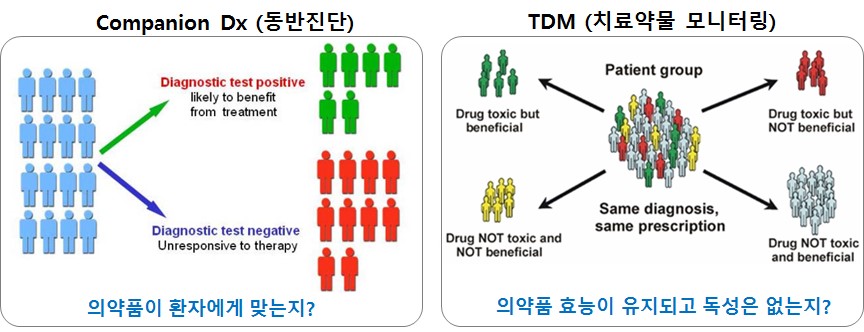
체외진단 분야에서는 맞춤의료에 해당하는 영역이 동반진단(Companion Diagnostics)과 개인맞춤형 치료약물 모니터링(TDM)입니다. 동반진단은 환자에게 표적지향적 치료제(Target-Oriented Therapeutics)를 투여할 수 있는가? 즉, 질병의 원인에 따라 의약품이 맞을 수도 있고 그렇지 않을 수도 있는 표적지향적 치료제가 적용될 수 있는 환자를 선별하기 위해 사용됩니다. 이에 비해 개인맞춤형 치료약물 모니터링(TDM)은 약물의 효과는 충분히 발휘되면서 독성을 일으키지 않는 개인별 최적 약물의 용량을 산출해 치료제 처방에 도움을 주고 건강보험의 비용의 효율성을 높여주는 진단 분야입니다.
 |
|
동반진단과 tdm 개요 비교 |
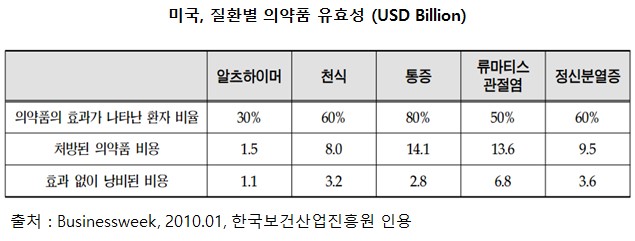
고령 인구의 증가에 따라 의료비용은 각 국가의 보건 당국에게 상당한 부담이 되고 있습니다. 그렇지만 의약품이 환자들에게 효과가 나타나지 않는 경우가 빈번하며, 이로 인해 막대한 비용이 낭비되고 있습니다.
 |
|
미국, 질환별 의약품 유효성 (usd billion) |
의약품이 효과 없이 낭비되는 여러 가지 이유가 있겠지만, 큰 이유 중 하나는 인종, 연령, 성별, 체중, 생활습관 등에 따라 약물의 흡수, 대사, 배설, 효과가 다르기 때문입니다. 따라서 개개인마다 적정량의 약물로 치료 효과를 얻도록 약물농도를 유지하는 것이 필요합니다.적절하지 못한 용량의 약물 복용으로 효과 없이 통원치료만 계속되거나 장기입원을 하게 되고 과도한 약물 투여는 부작용을 일으켜 필요 없는 의료비의 증가가 요구되므로 개인별 맞춤의료는 의료 비용의 절감 측면에서 경제성이 지속적으로 높아질 것으로 보입니다.
노화가 진행됨에 따라 대다수의 일반인들이 겪는 만성질환(고혈압, 고지혈증, 관절염 등)의 경우 오랜 기간 경구용 약물이나 주사제를 처방 받는데, 이러한 화학적 약물(Chemical Drug)은 약물 대사율과 배설에서 개인차가 심하며 치료농도 범위가 좁은 약물의 경우, 약효가 없거나 독성이 나타날 확률이 높기 때문에 약물 복용 중 혈액에서 간단한 POCT장비를 이용하여 약물의 농도를 측정하여 적량의 약물 복용을 하게 하는 것으로서, TDM 진단을 통한 접근은 매우 유용하다고 할 수 있습니다. 한 연구결과(J Clin Oncol. 2008, 26: 2099-105)에 따르면, 개인 맞춤형 약동학에 근거하여 직장암 치료제를 처방하였을 때 대조군에 비해 높은 생존율과 낮은 독성을 보였습니다.
TDM은 의약품의 효능과 부작용을 개선할 수 있기 때문에 체외진단으로서의 가치뿐만 아니라 신약개발에서 임상 성공률을 높일 수 있는 장비로도 활용될 수 있습니다. 특히, 치료 농도 범위가 좁거나 개인간 약물 대사 등의 편차가 큰 의약품들은 임상에서 실패할 가능성이 높은데, 개인 맞춤형 치료약물의 TDM을 적용하게 되면 그 만큼 임상 성공 확률을 높일 수가 있을 것입니다.
(나) TDM 개발 계획
당사에서는 Professional POCT 제품인 INCLIX®에 적용된 기술을 바탕으로 하여 맞춤형 진단에 대한 TDM(Therapeutic Drug Monitoring, 치료약물모니터링) 사업을 계획하고 있습니다.
TDM은 의약품과 연계되어 개발되어야 하는데, 특히, 신약개발과 연계될 경우에는, 임상 및 의약품 개발 과정과 접목시켜야 하기 때문에 일반적인 체외진단 제품에 비해 개발 및 인허가의 난이도가 높을 것으로 판단됩니다. 당사에서는 TDM과 관련된 미국 협력사와 파트너쉽을 맺어 진행하면서 경험 및 노하우를 확보할 계획입니다.
TDM은 현재 미국의 Autotelic 사와 항암제인 Paclitaxel에 대한 TDM 개발 계약을 체결한 상태로, Paclitaxel 개량신약이 미국 FDA의 임상 3상을 진행할 때 체외진단 제품으로 미국 FDA의 PMA(Premarket Approval)를 진행할 계획입니다. Autotelic 사는 Paclitaxel 개량신약 TDM에 대한 전 세계 판권을 가지고 있는 TDM을 전문적으로 사업화하는 회사로 다양한 의약품의 라이센스 인-아웃을 수행한 경험이 있습니다. 핵심 인력들은 대형 제약사에서 의약품 개발 및 인허가를 담당했던 경험을 가지고 있으며, 당사가 TDM 개발과 관련하여 많은 경험과 노하우를 전수받을 수 있는 최적의 회사라 판단됩니다. 향후 FDA 승인을 받으면 당사는 Paclitaxel에 대한 TDM 제품을 Autotelic 사에 독점으로 제공하게 됩니다.
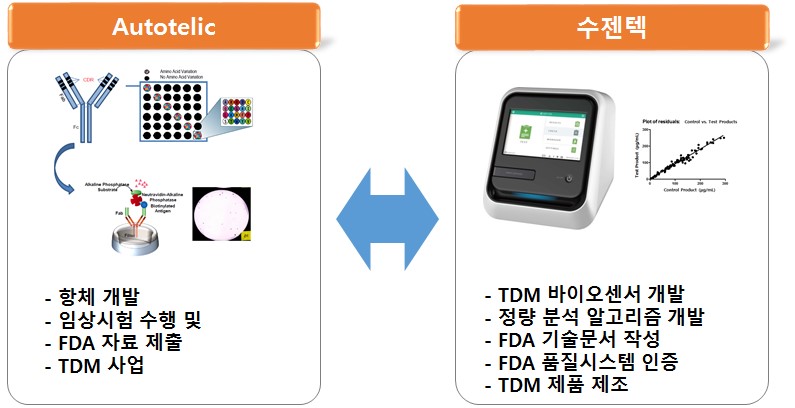 |
|
Autotelic 및 수젠텍의 paclitaxel tdm 개발 및 사업화 개요 |
Autotelic과 TDM 개발이 어느 정도 진행되면 Autotelic 이외에 TDM 사업을 같이 진행할 국내외 의약품 개발회사를 찾을 계획이며, 신약에 대해 공동으로 TDM 개발을 진행하거나 신약개발 과정 중 의약품 분석에 활용될 수 있도록 시스템을 구축할 계획입니다.
(다) TDM 전망
TDM 시장은 연간 12.6%의 높은 성장률로 2019년 26.9억 달러 규모로 성장할 전망이며, 이 중 미국 시장이 18.4억 달러 규모로 예상됩니다.(TriMark Publications, 2013)
TDM은 주로 간질 치료제, 항 부정맥제, 항생제, 항암제, 기관지 확장제, 면역억제제 및 HIV/AIDS 치료제의 모니터링에 사용되어 왔으며, 기존 대형병원, 대형장비 중심의 시장만 존재하고 있습니다. TDM은 약물의 사용 및 처방에 따라 하루에도 여러 번 측정해야 하는 경우도 있고 응급으로 현장에서 신속하게 측정되어야 할 요구가 있어 POCT로 개발될 경우 시장 규모는 커질 것으로 예측됩니다.
2008년 미국 NIH의 조사 결과에 따르면, 맞춤의료로 의료시스템 전환 시 평균 100세 수명의 개인의 경우, 의료비가 10% ~ 30%까지 절감될 수 있음이 보고되었으며, 약물 부작용을 3/4수준으로만 감소시켜도 연간 15% ~ 50%까지 의료비가 절감될 수 있을 것으로 나타났습니다(한국보건산업진흥원, 2013).
선진국일수록 의료비가 차지하는 비용이 지속적으로 확대됨에 따라 이러한 의료 비용 절감은 국가 정책적으로도 맞춤의료의 도입을 이끄는 중요한 동기를 부여합니다. 미국의 경우, 선도적으로 맞춤의료 정책을 논의하며 맞춤의료의 발전을 촉진하기 위해 정부부처에서 법안 제출, 보고서 발표 등 다각도로 접근하고 있으며 FDA는 In Vitro Companion Diagnostic Devices에 관한 Guidance 초안을 2011년에 발표하여 맞춤의료에 관한 정의, 표준, 프로세스 등을 제시함. 또한 맞춤의료의 규제 및 승인을 촉진하기 위해 의약품과 의료기기 담당 조직 간의 협력을 강화하였습니다.
글로벌 맞춤의료 시장은 의료재정 악화 및 의약품의 부작용 사례의 증가로 맞춤의료에 대한 필요성과 수요가 증가하였으며, 현재 환자의 약물 복용순응도(patient compliance)는 약 49% 수준이지만 개인에 맞춰 최적화된 효능과 안전성을 갖춘 맞춤의약의 사용은 이러한 복용순응도가 증가될 것으로 예상됩니다.
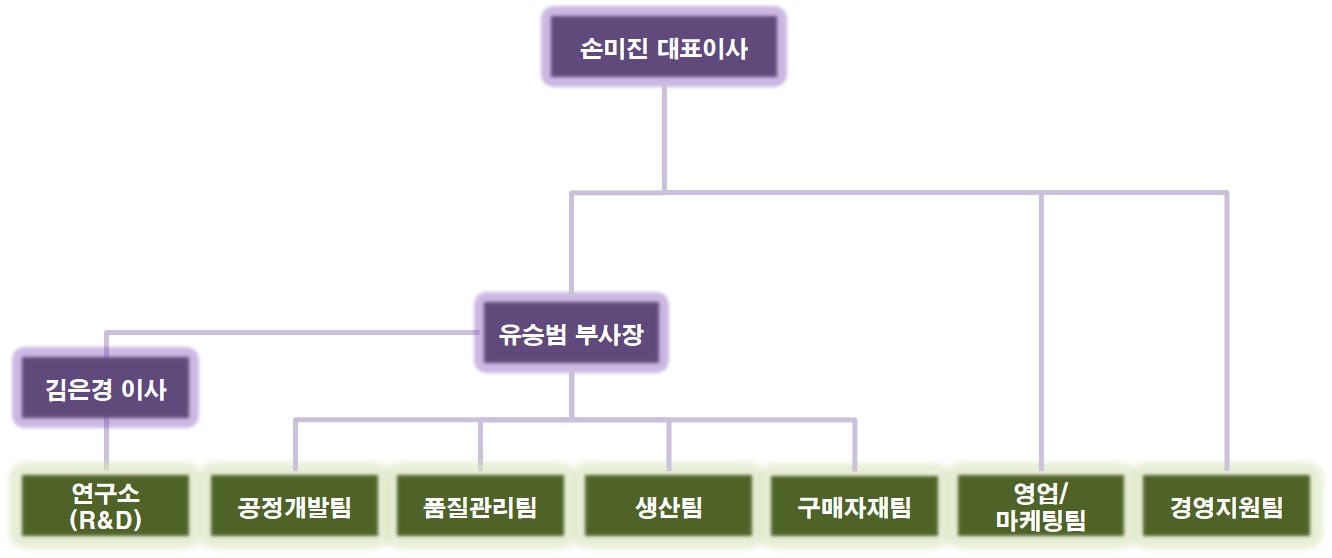
(5) 조직도
 |
|
조직도 |
2. 주주총회 목적사항별 기재사항
□ 정관의 변경
가. 집중투표 배제를 위한 정관의 변경 또는 그 배제된 정관의 변경
| 변경전 내용 | 변경후 내용 | 변경의 목적 |
|---|---|---|
| - | - | - |
나. 그 외의 정관변경에 관한 건
| 변경전 내용 | 변경후 내용 | 변경의 목적 |
|---|---|---|
|
제2조 (목적) 본 회사는 다음 사업을 경영함을 목적으로 한다. 1. 체외진단용 제품, 원료, 보조시약 개발, 제조 및 판매업 1. 의료기기 개발, 제조 및 판매업 1. 생명공학 관련 제품 개발, 제조 및 판매업 1. 체외진단, 의료기기, 생명공학 관련 기술 용역 서비스업 1. 체외진단, 의료기기, 생명공학 관련 전자상거래업 1. 여성용품, 유아용품의 판매업 1. 건물의 임대업 1. 건강보조식품의 개발, 제조 및 판매업 1. 화장품의 개발, 제조 및 판매업 1. 각호에 관련된 수출입업 등 부대사업 일체 |
제2조 (목적) 본 회사는 다음 사업을 경영함을 목적으로 한다. 1.체외진단용 제품, 원료, 보조시약 개발, 제조 및 판매업 1.의료기기 개발, 제조 및 판매업 1.생명공학 관련 제품 개발, 제조 및 판매업 1.체외진단, 의료기기, 생명공학 관련 기술 용역 서비스업 1.체외진단, 의료기기, 생명공학 관련 전자상거래업 1. 여성용품, 유아용품의 판매업 1. 건물의 임대업 1. 건강보조식품의 개발, 제조 및 판매업 1. 화장품의 개발, 제조 및 판매업 1. 바이오 및 이화학용 분석기기 제조 및 판매 |
케이맥바이오센터(주)의 사업 목적을 당사 정관에 추가함. |
※ 기타 참고사항
합병 기일에 앞서 피합병법인의 사업목적을 추가하고자 합니다. (2017년 07월 24일 회사합병 결정 공시 참조)
□ 이사의 선임
가. 후보자의 성명ㆍ생년월일ㆍ추천인ㆍ최대주주와의 관계ㆍ사외이사후보자 여부
| 후보자성명 | 생년월일 | 사외이사 후보자여부 |
최대주주와의 관계 | 추천인 |
|---|---|---|---|---|
| 손미진 | 1965.03.25 | 해당 사항 없음. | 본인. | 이사회 |
| 유승범 | 1967.04.27 | 해당 사항 없음. | 해당 사항 없음. | 이사회 |
| 박준우 | 1976.04.12 | 해당 사항 없음. | 해당 사항 없음. | 이사회 |
| 총 ( 3 ) 명 | ||||
나. 후보자의 주된직업ㆍ약력ㆍ해당법인과의 최근3년간 거래내역
| 후보자성명 | 주된직업 | 약력 | 해당법인과의 최근3년간 거래내역 |
|---|---|---|---|
| 손미진 | (주)수젠텍 대표이사 |
충남대 의과대학 박사 한국생명공학연구원 LG생명과학 기술연구원 현 ㈜수젠텍 대표이사 |
해당 사항 없음. |
| 유승범 | (주)수젠텍 부사장 |
연세대 생화학 석사 LG생명과학 기술연구원 ㈜알테오젠 기술이사 현 ㈜수젠텍 부사장 |
해당 사항 없음. |
| 박준우 | (주)티에스인베스트먼트 이사 |
서울대 화학공학과 학사/석사 대우증권 Asia evolution Korea 안강벤처투자 티에스인베스트먼트 |
해당 사항 없음. |
※ 기타 참고사항
손미진, 유승범 이사는 2017년 12월 09일 임기 만료 예정이나 신규 이사 선임과 함께 재선임하고자 합니다.